DE102010048608A1 - Materialien für organische Elektrolumineszenzvorrichtungen - Google Patents
Materialien für organische Elektrolumineszenzvorrichtungen Download PDFInfo
- Publication number
- DE102010048608A1 DE102010048608A1 DE102010048608A DE102010048608A DE102010048608A1 DE 102010048608 A1 DE102010048608 A1 DE 102010048608A1 DE 102010048608 A DE102010048608 A DE 102010048608A DE 102010048608 A DE102010048608 A DE 102010048608A DE 102010048608 A1 DE102010048608 A1 DE 102010048608A1
- Authority
- DE
- Germany
- Prior art keywords
- aromatic
- group
- radicals
- substituted
- ring system
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 0 CS(c1c(*)cc2)c3c(*)ccc4c(cccc5)c5c2c1c34 Chemical compound CS(c1c(*)cc2)c3c(*)ccc4c(cccc5)c5c2c1c34 0.000 description 6
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/027—Organoboranes and organoborohydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/28—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/32—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings
- C07C13/62—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings with more than three condensed rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/28—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/32—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings
- C07C13/62—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings with more than three condensed rings
- C07C13/66—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings with more than three condensed rings the condensed ring system contains only four rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C13/00—Cyclic hydrocarbons containing rings other than, or in addition to, six-membered aromatic rings
- C07C13/28—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof
- C07C13/32—Polycyclic hydrocarbons or acyclic hydrocarbon derivatives thereof with condensed rings
- C07C13/72—Spiro hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/57—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton
- C07C211/58—Naphthylamines; N-substituted derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/57—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton
- C07C211/61—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton with at least one of the condensed ring systems formed by three or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C49/00—Ketones; Ketenes; Dimeric ketenes; Ketonic chelates
- C07C49/385—Saturated compounds containing a keto group being part of a ring
- C07C49/417—Saturated compounds containing a keto group being part of a ring polycyclic
- C07C49/423—Saturated compounds containing a keto group being part of a ring polycyclic a keto group being part of a condensed ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/90—Benzo [c, d] indoles; Hydrogenated benzo [c, d] indoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/06—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom containing only hydrogen and carbon atoms in addition to the ring nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/44—Radicals substituted by doubly-bound oxygen, sulfur, or nitrogen atoms, or by two such atoms singly-bound to the same carbon atom
- C07D213/53—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/14—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom
- C07D251/24—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom to three ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D313/00—Heterocyclic compounds containing rings of more than six members having one oxygen atom as the only ring hetero atom
- C07D313/02—Seven-membered rings
- C07D313/06—Seven-membered rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0033—Iridium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0086—Platinum compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/025—Silicon compounds without C-silicon linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/0805—Compounds with Si-C or Si-Si linkages comprising only Si, C or H atoms
- C07F7/0807—Compounds with Si-C or Si-Si linkages comprising only Si, C or H atoms comprising Si as a ring atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
- C07F7/0816—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring said ring comprising Si as a ring atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/5022—Aromatic phosphines (P-C aromatic linkage)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/53—Organo-phosphine oxides; Organo-phosphine thioxides
- C07F9/5325—Aromatic phosphine oxides or thioxides (P-C aromatic linkage)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/553—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having one nitrogen atom as the only ring hetero atom
- C07F9/576—Six-membered rings
- C07F9/58—Pyridine rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6568—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms
- C07F9/65683—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms the ring phosphorus atom being part of a phosphine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6568—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms
- C07F9/65685—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms the ring phosphorus atom being part of a phosphine oxide or thioxide
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
- C08G61/124—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds with a five-membered ring containing one nitrogen atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
- C08G61/125—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds with a five-membered ring containing one oxygen atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
- C08G61/126—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds with a five-membered ring containing one sulfur atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B1/00—Dyes with anthracene nucleus not condensed with any other ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/001—Pyrene dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/007—Squaraine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/008—Triarylamine dyes containing no other chromophores
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/10—Metal complexes of organic compounds not being dyes in uncomplexed form
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/623—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing five rings, e.g. pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/625—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing at least one aromatic ring having 7 or more carbon atoms, e.g. azulene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/11—Homopolymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/13—Morphological aspects
- C08G2261/131—Morphological aspects dendritic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/20—Definition of the polymer structure non-conjugated
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/32—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain
- C08G2261/324—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed
- C08G2261/3241—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed containing one or more nitrogen atoms as the only heteroatom, e.g. carbazole
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/32—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain
- C08G2261/324—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed
- C08G2261/3242—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed containing one or more oxygen atoms as the only heteroatom, e.g. benzofuran
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/32—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain
- C08G2261/324—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed
- C08G2261/3243—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed containing one or more sulfur atoms as the only heteroatom, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/32—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain
- C08G2261/324—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed
- C08G2261/3244—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain condensed containing only one kind of heteroatoms other than N, O, S
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/33—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain
- C08G2261/334—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1096—Heterocyclic compounds characterised by ligands containing other heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1408—Carbocyclic compounds
- C09K2211/1416—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1408—Carbocyclic compounds
- C09K2211/1433—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/145—Heterocyclic containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1458—Heterocyclic containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1491—Heterocyclic containing other combinations of heteroatoms
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Indole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Plural Heterocyclic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Led Devices (AREA)
Abstract
Die vorliegende Erfindung betrifft Verbindungen gemäß Formel (1) und (2), welche sich für die Verwendung in elektronischen Vorrichtungen, insbesondere organischen Elektrolumineszenzvorrichtungen, eignen.
Description
- Die vorliegende Erfindung betrifft Materialien für die Verwendung in elektronischen Vorrichtungen, insbesondere in organischen Elektrolumineszenzvorrichtungen.
- Der Aufbau organischer Elektrolumineszenzvorrichtungen (OLEDs), in denen organische Halbleiter als funktionelle Materialien eingesetzt werden, ist beispielsweise in
US 4539507 ,US 5151629 ,EP 0676461 undWO 98/27136 - Die Eigenschaften von phosphoreszierenden OLEDs werden nicht nur von den eingesetzten Triplettemittern bestimmt. Hier sind insbesondere auch die anderen verwendeten Materialien, wie Matrixmaterialien, Lochblockiermaterialien, Elektronentransportmaterialien, Lochtransportmaterialien und Elektronen- bzw. Exzitonenblockiermaterialien von besonderer Bedeutung. Verbesserungen dieser Materialien können somit auch zu deutlichen Verbesserungen der OLED-Eigenschaften führen. Auch für fluoreszierende OLEDs gibt es bei diesen Materialien noch Verbesserungsbedarf.
- Gemäß dem Stand der Technik werden unter anderem Ketone (z. B. gemäß
WO 2004/093207 WO 2010/006680 WO 2005/003253 - Gemäß dem Stand der Technik werden weiterhin Triphenylenderivate als Matrixmaterialien für phosphoreszierende Emitter verwendet, beispielsweise gemäß
JP 2005/071983 WO 2006/038709 - Aufgabe der vorliegenden Erfindung ist die Bereitstellung von Verbindungen, welche sich für den Einsatz in einer fluoreszierenden oder phosphoreszierenden OLED, insbesondere einer phosphoreszierenden OLED, eignen, beispielsweise als Matrixmaterial und/oder als Lochtransport-/Elektronenblockiermaterial bzw. Exzitonenblockiermaterial und/oder als Elektronentransport- bzw. Lochblockiermaterial. Insbesondere ist es die Aufgabe der vorliegenden Erfindung, Matrixmaterialien bereitzustellen, welche sich für grün und rot phosphoreszierende OLEDs eignen.
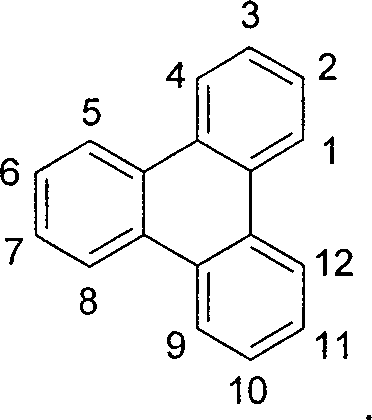
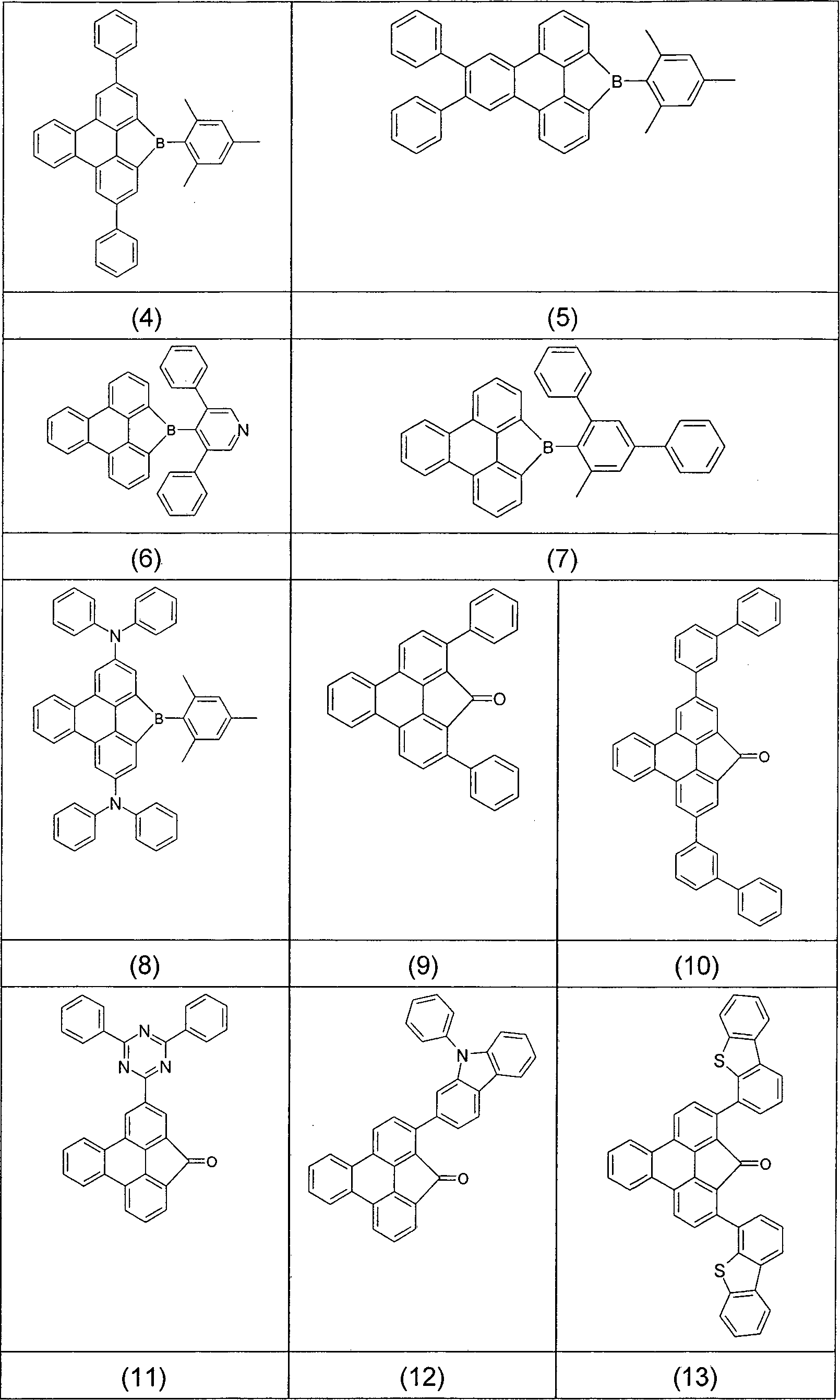
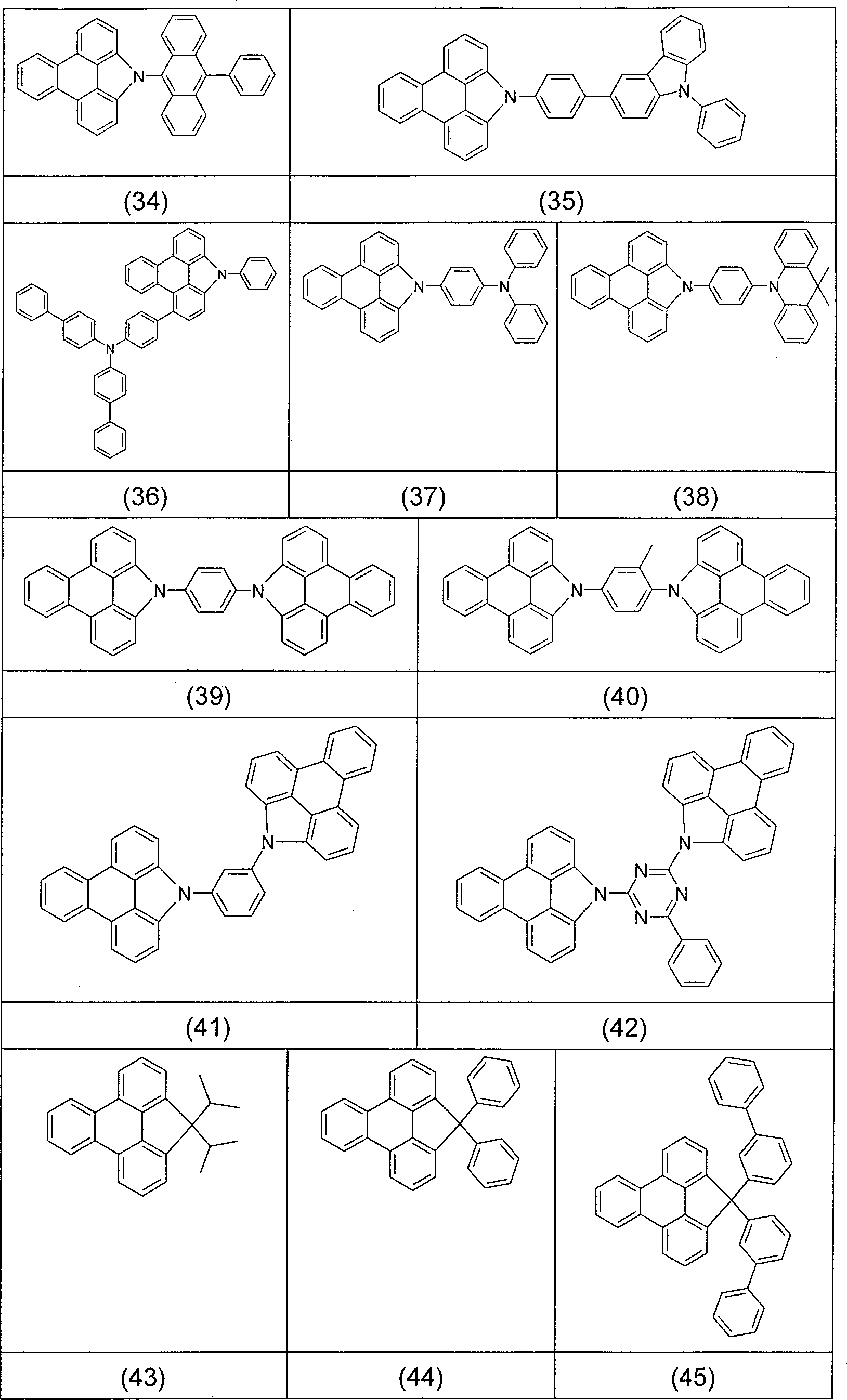
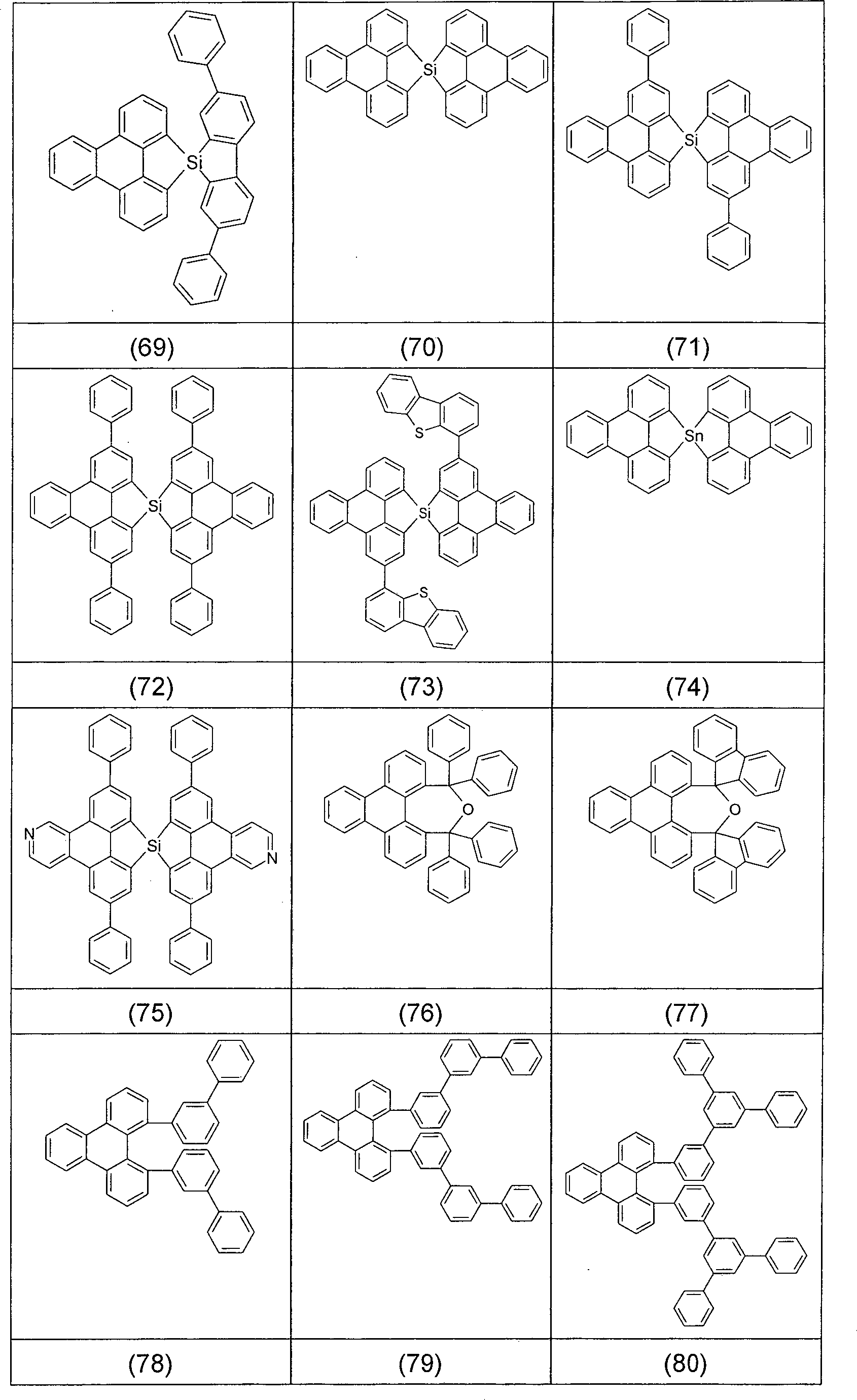
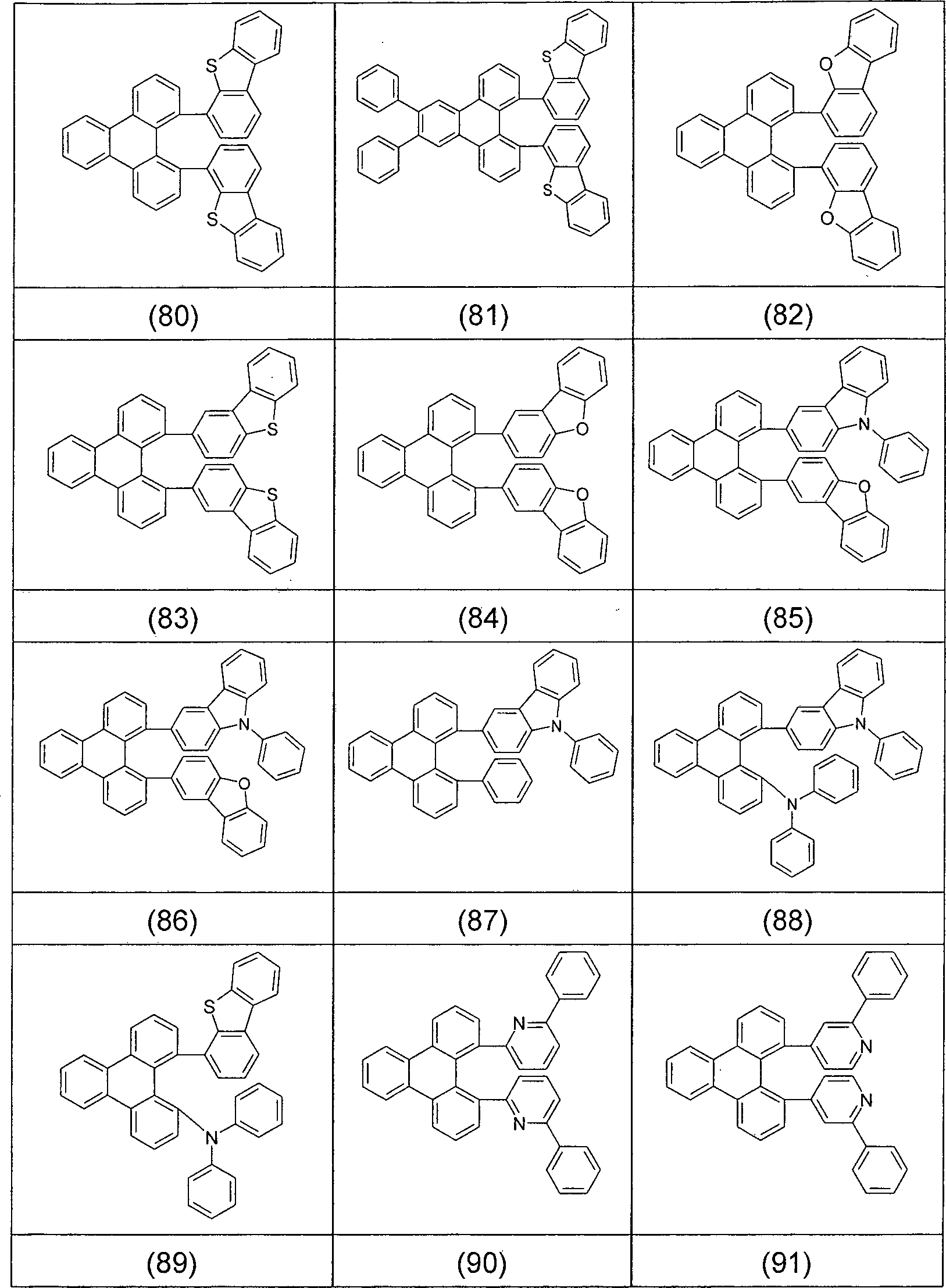
- Überraschend wurde gefunden, dass Triphenylenderivate, die in den Positionen 1 und 12 durch aromatische oder heteroaromatische Ringsysteme, Carbonylgruppen oder Phosphinoxidgruppen substituiert sind bzw. in denen die Positionen 1 und 12 durch eine Gruppe, ausgewählt aus Bor, Kohlenstoff, Silicium, Germanium, Zinn, Stickstoff, Sauerstoff, Schwefel oder Phosphor, verbrückt sind, diese Aufgabe lösen und zu Verbesserungen der organischen Elektrolumineszenzvorrichtung führen, insbesondere hinsichtlich der Lebensdauer, der Effizienz und der Betriebsspannung. Dies gilt insbesondere für rot und grün phosphoreszierende Elektrolumineszenzvorrichtungen, vor allem bei Einsatz der erfindungsgemäßen Verbindungen als Matrixmaterial. Die erfindungsgemäßen Materialien lassen sich in wenigen Schritten und in hoher Ausbeute synthetisieren. Diese Materialien sowie organische Elektrolumineszenzvorrichtungen, welche derartige Verbindungen enthalten, sind daher der Gegenstand der vorliegenden Erfindung.
-
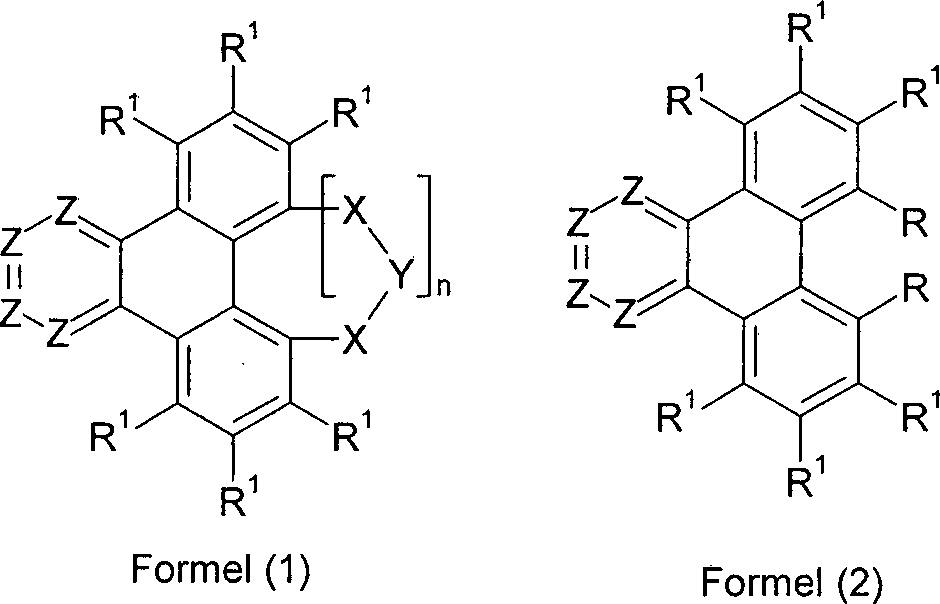
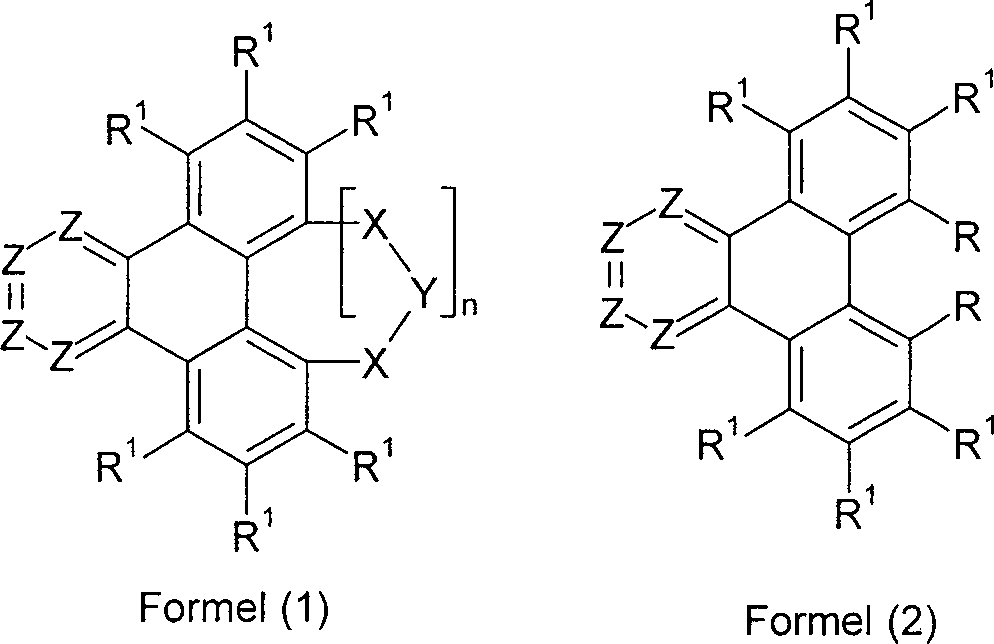
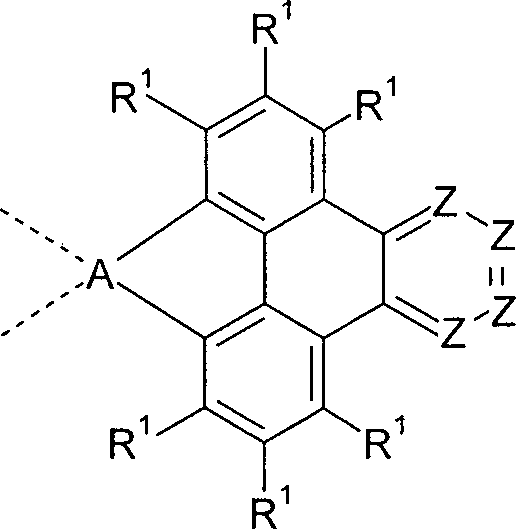
- Gegenstand der vorliegenden Erfindung ist daher eine neutrale Verbindung gemäß der folgenden Formel (1) oder Formel (2), wobei für die verwendeten Symbole und Indizes gilt:
X ist bei jedem Auftreten gleich oder verschieden, bevorzugt gleich BR2, C(R2)2, C=O, Si(R2)2, Ge(R2)2, Sn(R2)2, NR2, O, S, SO, SO2, PR2 oder P(=O)R2;
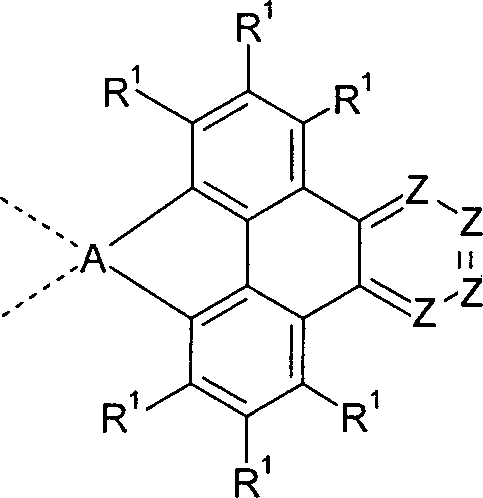
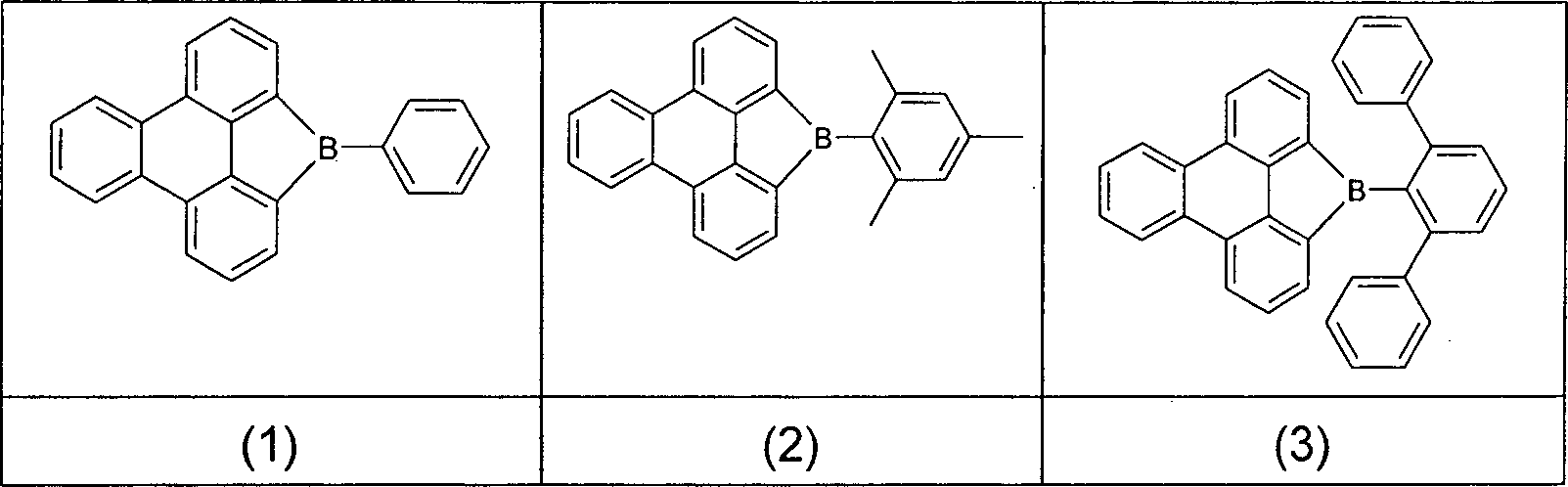
oder X ist für n = 0 eine Gruppe der folgenden Formel (3), Formel (3) A ist C, Si, Ge oder Sn; dabei deuten die gestrichelten Bindungen an A die Bindung an das Triphenylen an;
Y ist BR2, O, S, NR2, PR2 oder P(=O)R2;
Z ist bei jedem Auftreten gleich oder verschieden CR1 oder N mit der Maßgabe, dass maximal zwei Gruppen Z pro Cyclus für N stehen;
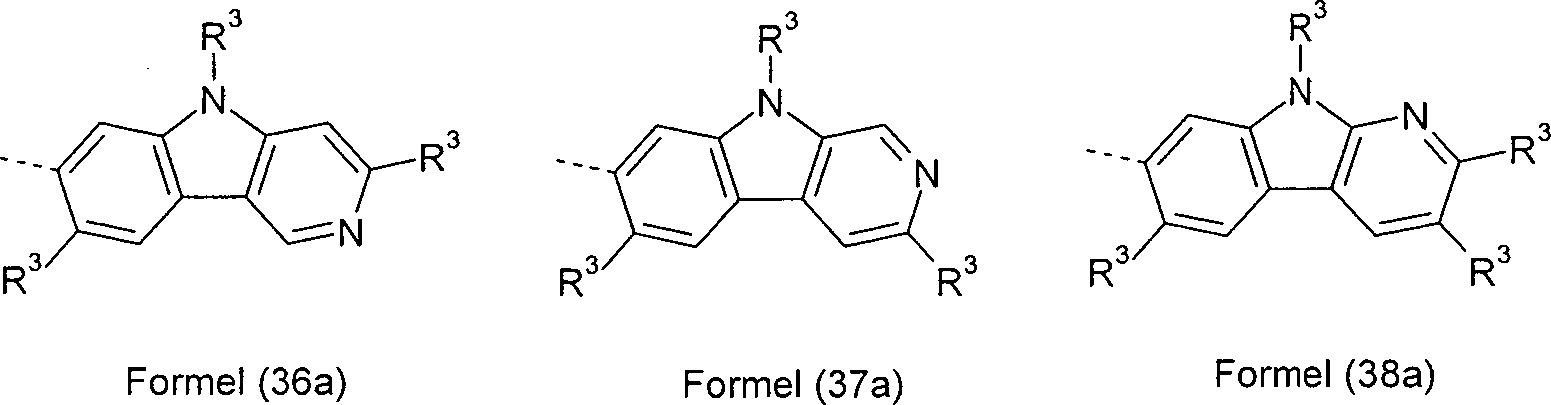
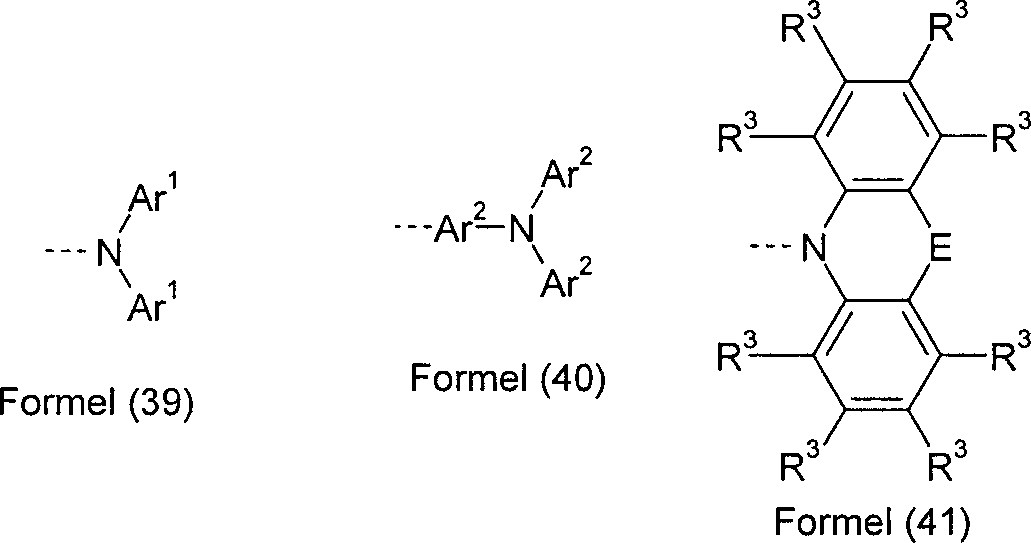
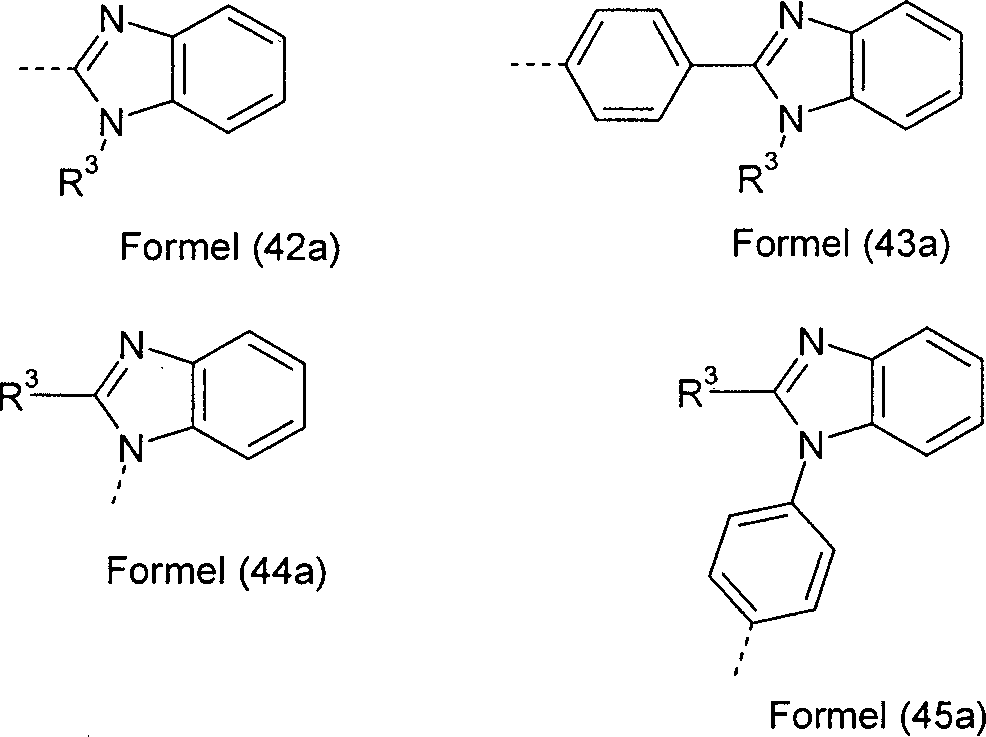
R ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 und einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R1 substituiert sein kann;
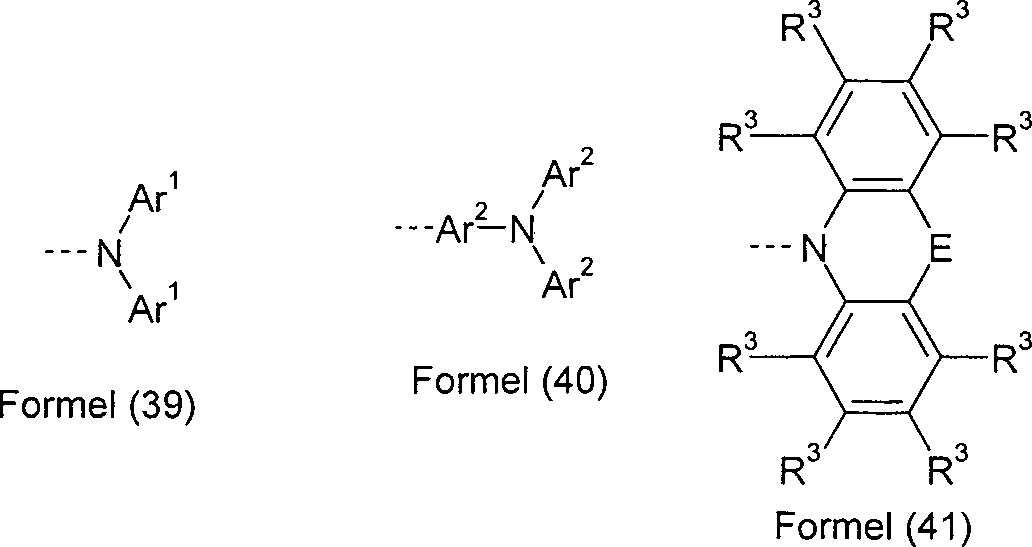
Ar1 ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das mit einem oder mehreren nicht-aromatischen Resten R3 substituiert sein kann; dabei können zwei Reste Ar1, welche an dasselbe N-Atom oder P-Atom binden, auch durch eine Einfachbindung oder eine Brücke, ausgewählt aus N(R4), C(R4)2, O oder S, miteinander verbrückt sein;
R1 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D, F, Cl, Br, I, CN, NO2, N(Ar1)2, N(R3)2, C(=O)Ar1, C(=O)R3, P(=O)(Ar1)2, einer geradkettigen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen oder einer verzweigten oder cyclischen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 40 C-Atomen oder einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, wobei die Alkyl-, Alkoxy-, Thioalkoxy-, Alkenyl- oder Alkinylgruppe jeweils mit einem oder mehreren Resten R3 substituiert sein kann und wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R3C=CR3, C≡C, Si(R3)2, Ge(R3)2, Sn(R3)2, C=O, C=S, C=Se, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S oder CONR3 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann, einer Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die mit einem oder mehreren Resten R3 substituiert sein kann, oder einer Kombination dieser Systeme, wobei optional zwei oder mehr benachbarte Substituenten R1, die an demselben Benzolring gebunden sind, ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können;
R2 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus einer geradkettigen Alkylgruppe mit 1 bis 20 C-Atomen oder einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 20 C-Atomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R3C=CR3, C≡C, Si(R3)2, C=O, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S oder CONR3 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei optional zwei Substituenten R2, welche an dasselbe Kohlenstoff-, Silicium-, Germanium- oder Zinnatom binden, ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem miteinander bilden können, das mit einem oder mehreren Resten R3 substituiert sein kann;
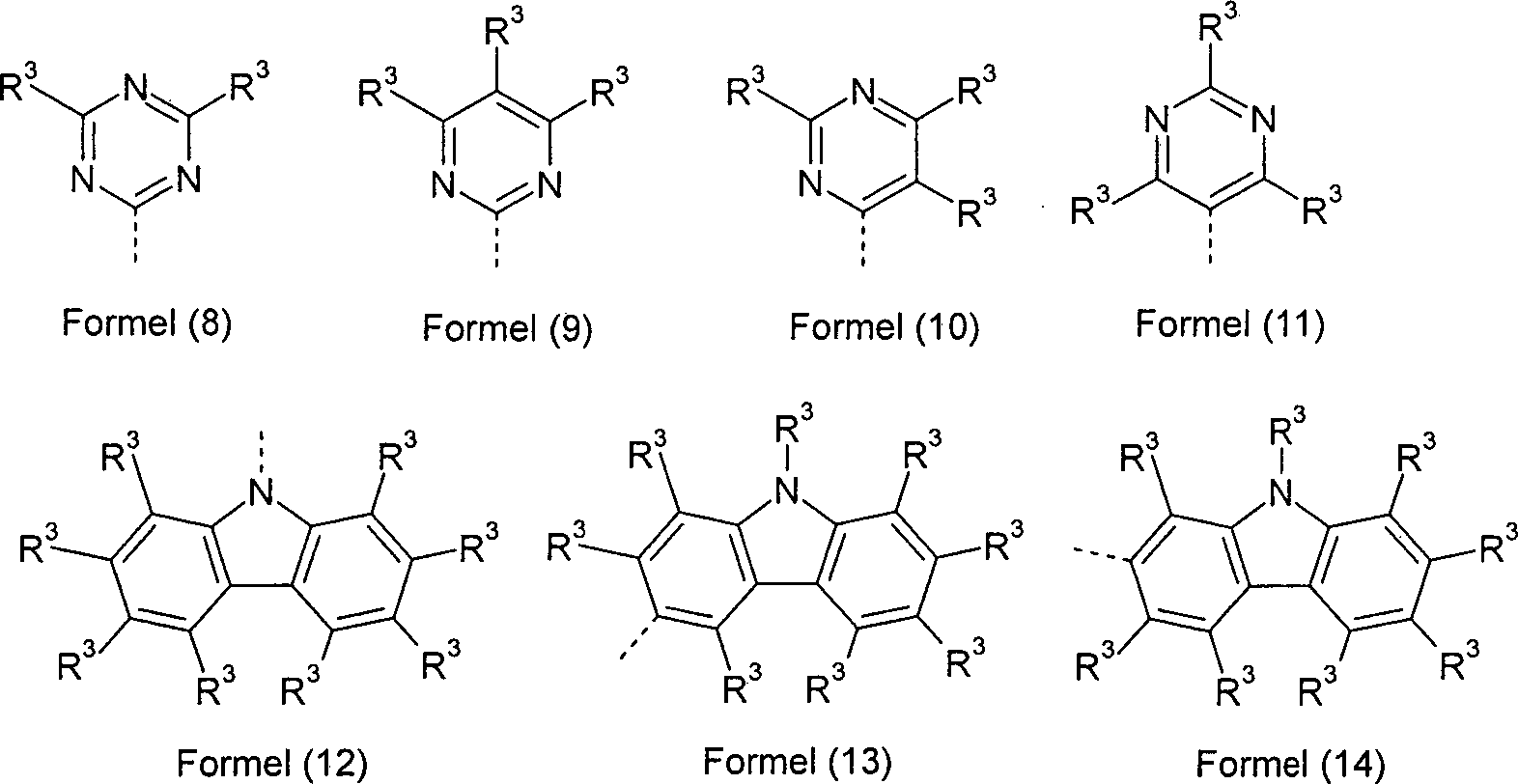
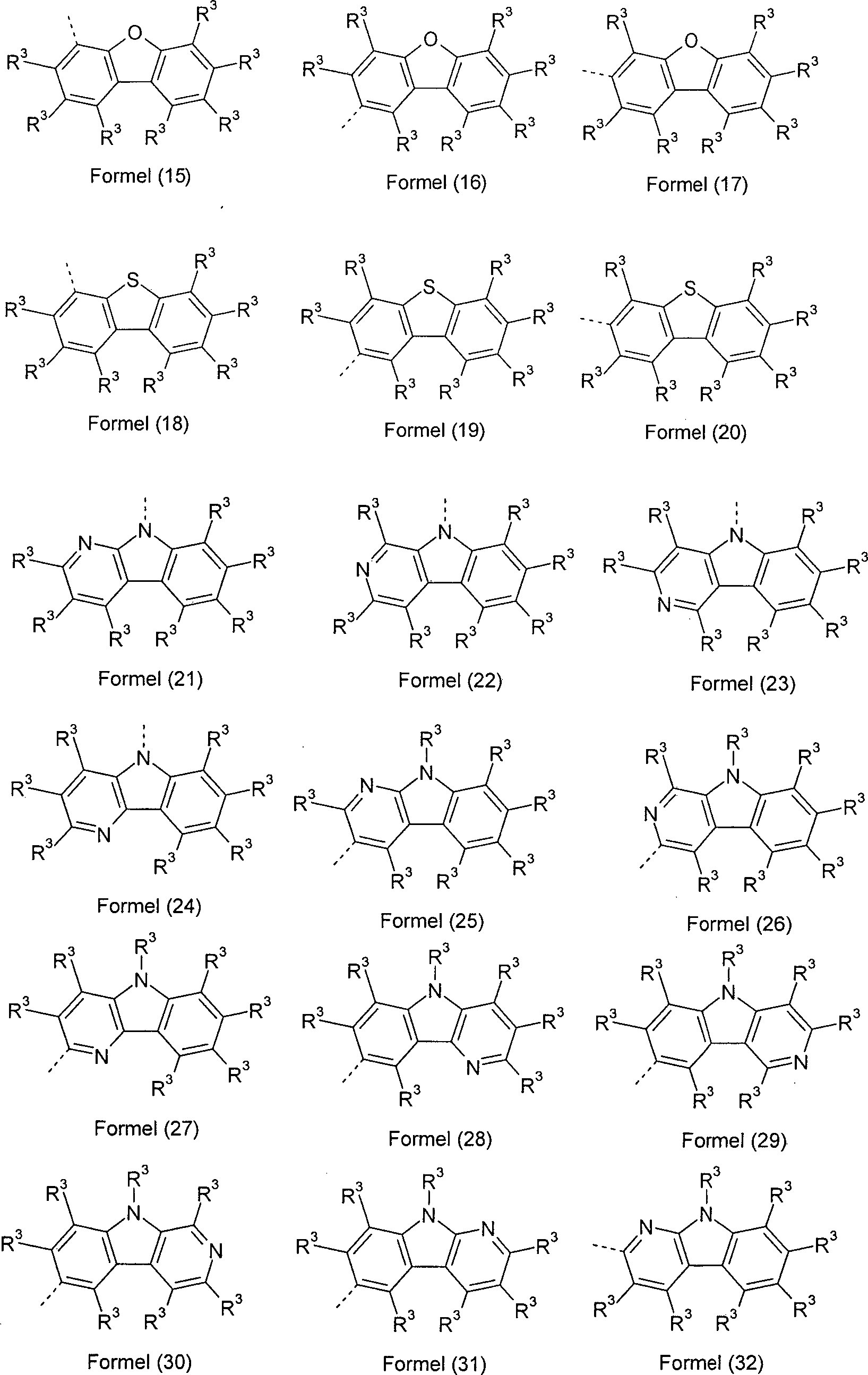
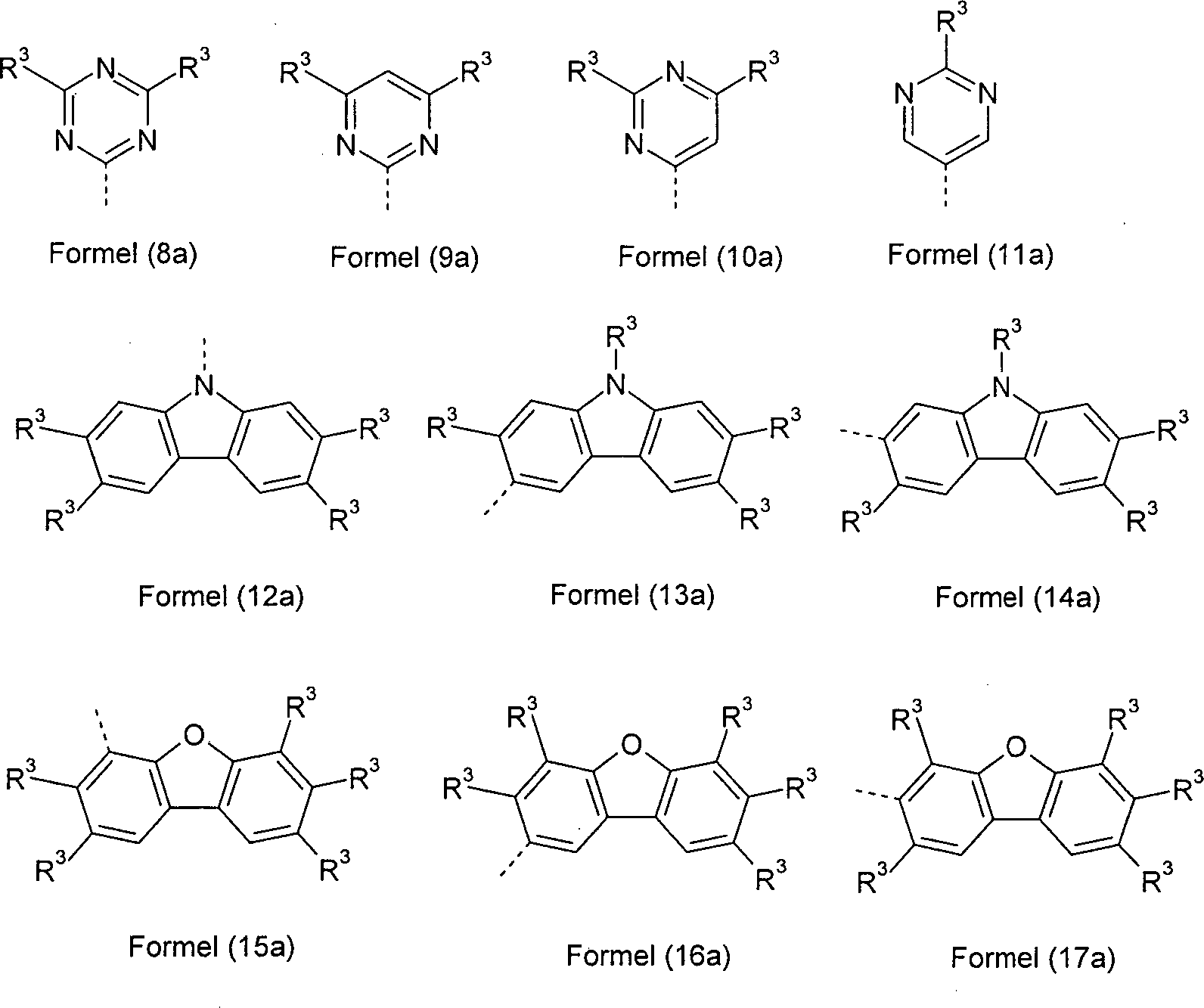
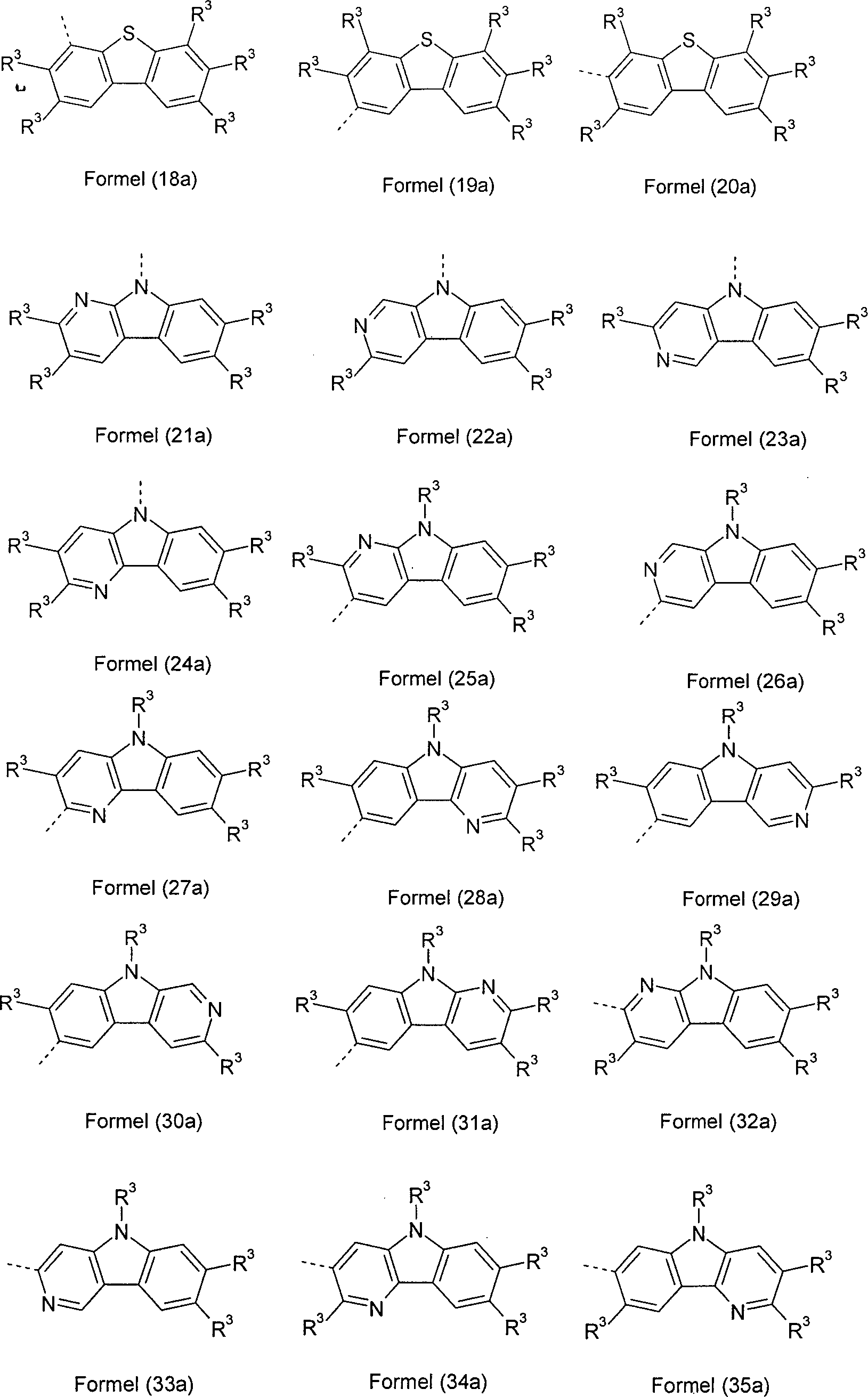
R3 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D, F, Cl, Br, I, CN, NO2, N(R4)2, C(=O)Ar1, C(=O)R4, P(=O)(Ar1)2, einer geradkettigen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen oder einer verzweigten oder cyclischen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 40 C-Atomen oder einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, wobei die Alkyl-, Alkoxy-, Thioalkyl-, Alkenyl- oder Alkinylgruppe mit einem oder mehreren Resten R4 substituiert sein kann und wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R4C=CR4, C≡C, Si(R4)2, C=O, C=NR4, P(=O)(R4), SO, SO2, NR4, O, S oder CONR4 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R4 substituiert sein kann, einer Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die mit einem oder mehreren Resten R4 substituiert sein kann, oder einer Kombination dieser Systeme, wobei optional zwei oder mehr benachbarte Substituenten R3 ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können, das mit einem oder mehreren Resten R4 substituiert sein kann;
R4 ist ausgewählt aus der Gruppe bestehend aus H, D, F, CN, einem aliphatischem Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, einem aromatischem oder heteroaromatischem Ringsystem mit 5 bis 30 aromatischen Ringatomen, in dem ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder eine Alkylgruppe mit 1 bis 5 C-Atomen ersetzt sein können, wobei zwei oder mehr benachbarte Substituenten R4 miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können;
n ist 0 oder 1;
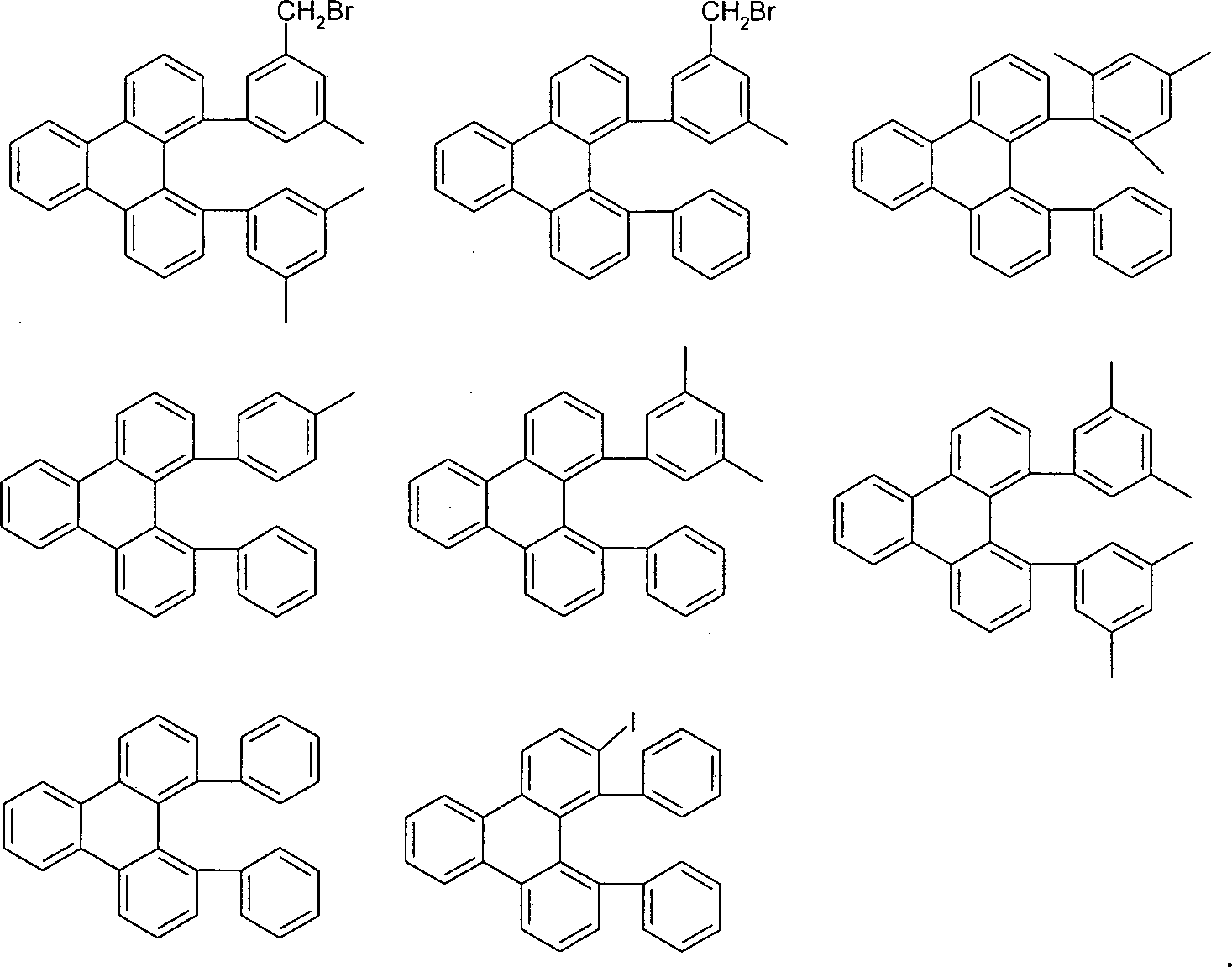
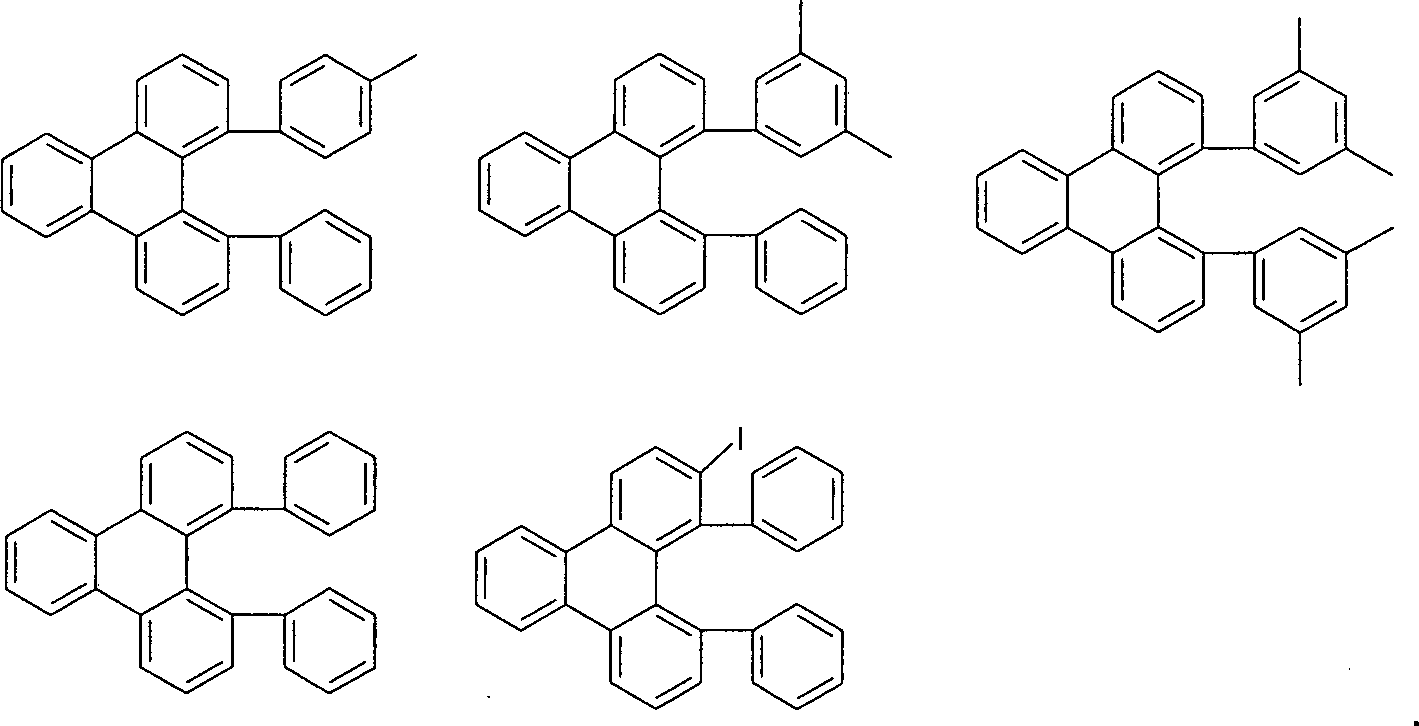
mit der Maßgabe, dass mindestens eine Gruppe R1 in Formel (1) für ein aromatisches oder heteroaromatisches Ringsystem steht, wenn X für C=O, O, S, SO oder SO2 steht und n = 0 ist;
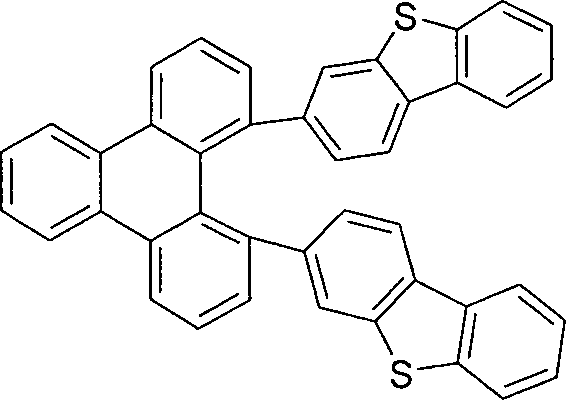
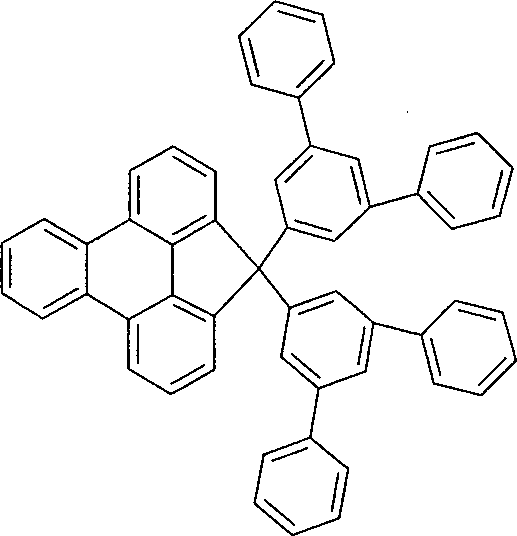
und weiterhin mit der Maßgabe, dass die folgenden Verbindungen von der Erfindung ausgenommen sind: - Ein „nicht-aromatischer Rest” R3, wie er in der Definition von Ar1 aufgeführt ist, ist ein Rest gemäß der Defintion von R3, der keine aromatische oder heteroaromatische Gruppen enthält, also beispielsweise auch keine aromatische Carbonylgruppe.
- Eine Arylgruppe im Sinne dieser Erfindung enthält 6 bis 60 C-Atome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält 2 bis 60 C-Atome und mindestens ein Heteroatom, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Dabei wird unter einer Arylgruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Cyclus, also Benzol, bzw. ein einfacher heteroaromatischer Cyclus, beispielsweise Pyridin, Pyrimidin, Thiophen, etc., oder eine kondensierte (anellierte) Aryl- oder Heteroarylgruppe, beispielsweise Naphthalin, Anthracen, Phenanthren, Chinolin, Isochinolin, etc., verstanden. Miteinander durch Einfachbindung verknüpfte Aromaten, wie zum Beispiel Biphenyl oder Bipyridin, werden dagegen nicht als Aryl- oder Heteroarylgruppe, sondern als aromatisches Ringsystem bezeichnet.
- Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält 6 bis 60 C-Atome im Ringsystem. Ein heteroaromatisches Ringsystem im Sinne dieser Erfindung enthält 2 bis 60 C-Atome und mindestens ein Heteroatom im Ringsystem, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine nicht-aromatische Einheit (bevorzugt weniger als 10% der von H verschiedenen Atome), wie z. B. ein C-, N-, O- oder Si-Atom, verbunden sein können. So sollen beispielsweise auch Systeme wie Fluoren, 9,9'-Spirobifluoren, 9,9-Diarylfluoren, Triarylamin, Diarylether, Stilben, etc. als aromatische Ringsysteme im Sinne dieser Erfindung verstanden werden, und ebenso Systeme, in denen zwei oder mehrere Arylgruppen beispielsweise durch eine Alkylgruppe mit ein bis fünf C-Atomen oder eine Carbonylgruppe verbunden sind.
- Im Rahmen der vorliegenden Erfindung werden unter einem aliphatischen Kohlenwasserstoffrest bzw. einer Alkylgruppe bzw. einer Alkenyl- oder Alkinylgruppe, die typischerweise 1 bis 40 oder auch 1 bis 20 C-Atome enthalten kann, und in der auch einzelne H-Atome oder CH2-Gruppen durch die oben genannten Gruppen substituiert sein können, bevorzugt die Reste Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, neo-Pentyl, Cyclopentyl, n-Hexyl, neo-Hexyl, Cyclohexyl, n-Heptyl, Cycloheptyl, n-Octyl, Cyclooctyl, 2-Ethylhexyl, Trifluormethyl, Pentafluorethyl, 2,2,2-Trifluorethyl, Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclopentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl, Cyclooctenyl, Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl, Heptinyl oder Octinyl verstanden. Unter einer Alkoxygruppe mit 1 bis 40 C-Atomen werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy, n-Pentoxy, s-Pentoxy, 2-Methylbutoxy, n-Hexoxy, Cyclohexyloxy, n-Heptoxy, Cycloheptyloxy, n-Octyloxy, Cyclooctyloxy, 2-Ethylhexyloxy, Pentafluorethoxy und 2,2,2-Trifluorethoxy verstanden. Unter einer Thioalkylgruppe mit 1 bis 40 C-Atomen werden insbesondere Methylthio, Ethylthio, n-Propylthio, i-Propylthio, n-Butylthio, i-Butylthio, s-Butylthio, t-Butylthio, n-Pentylthio, s-Pentylthio, n-Hexylthio, Cyclohexylthio, n-Heptylthio, Cycloheptylthio, n-Octylthio, Cyclooctylthio, 2-Ethylhexylthio, Trifluormethylthio, Pentafluorethyithio, 2,2,2-Trifluorethylthio, Ethenylthio, Propenylthio, Butenylthio, Pentenylthio, Cyclopentenylthio, Hexenylthio, Cyclohexenylthio, Heptenylthio, Cycloheptenylthio, Octenylthio, Cyclooctenylthio, Ethinylthio, Propinylthio, Butinylthio, Pentinylthio, Hexinylthio, Heptinylthio oder Octinylthio verstanden. Allgemein können Alkyl-, Alkoxy- oder Thioalkylgruppen gemäß der vorliegenden Erfindung geradkettig, verzweigt oder cyclisch sein, wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch die oben genannten Gruppen ersetzt sein können; weiterhin können auch ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2, bevorzugt F, Cl oder CN, weiter bevorzugt F oder CN, besonders bevorzugt CN ersetzt sein.
- Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches noch jeweils mit den oben genannten Resten R2 oder einem Kohlenwasserstoffrest substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Benzanthracen, Phenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Triphenylen, Fluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans-Indenofluoren, cis- oder trans-Indenocarbazol, cis- oder trans-Indolocarbazol, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Hexaazatriphenylen, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7-Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diazapyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Phenothiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol oder Gruppen, die abgeleitet sind von Kombinationen dieser Systeme.
- In einer bevorzugten Ausführungsform der Erfindung steht maximal eine Gruppe Z pro Cyclus für N und die anderen Gruppen Z stehen gleich oder verschieden bei jedem Auftreten für CR1. In einer besonders bevorzugten Ausführungsform der Erfindung stehen alle Gruppen Z gleich oder verschieden bei jedem Auftreten für CR1.
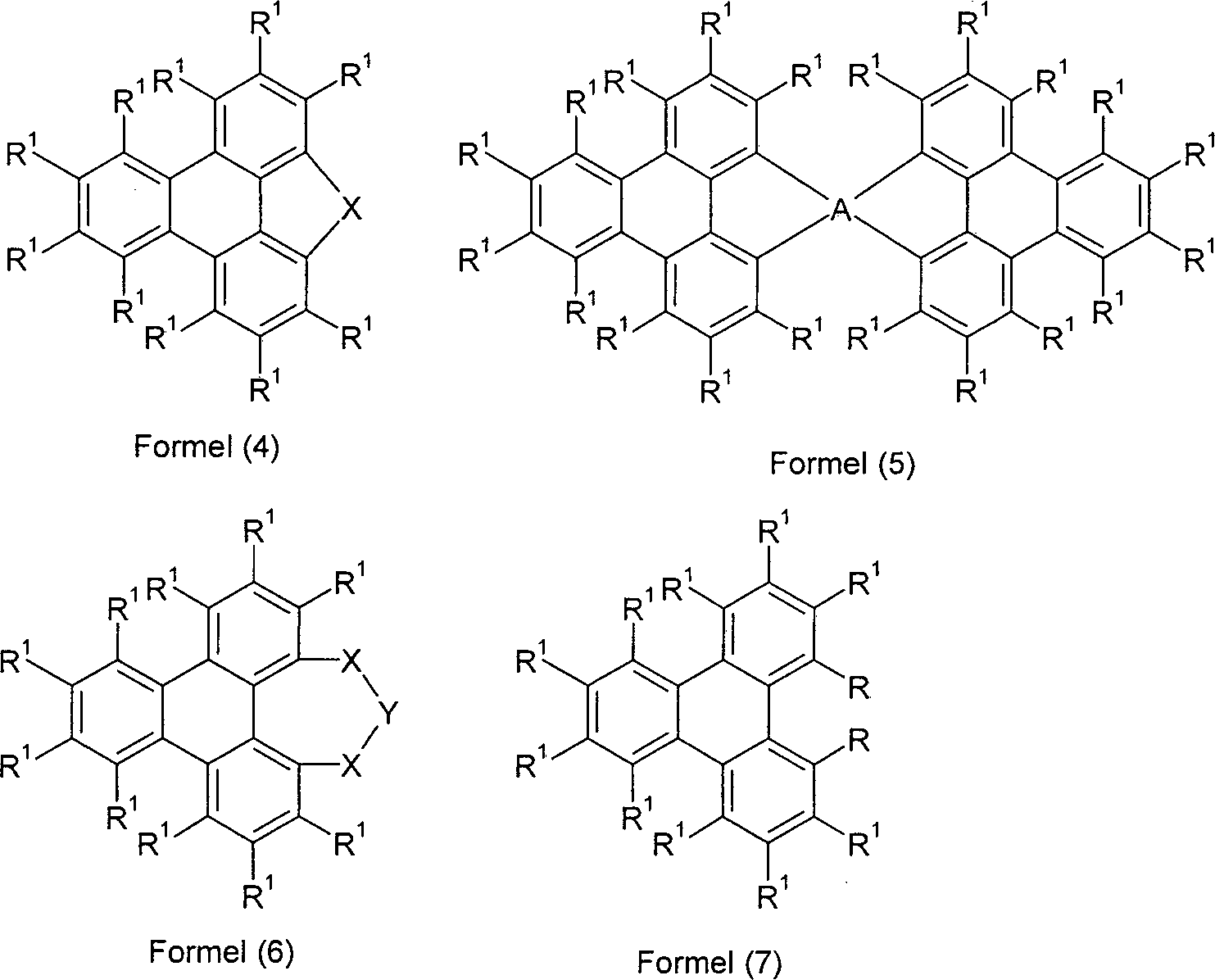
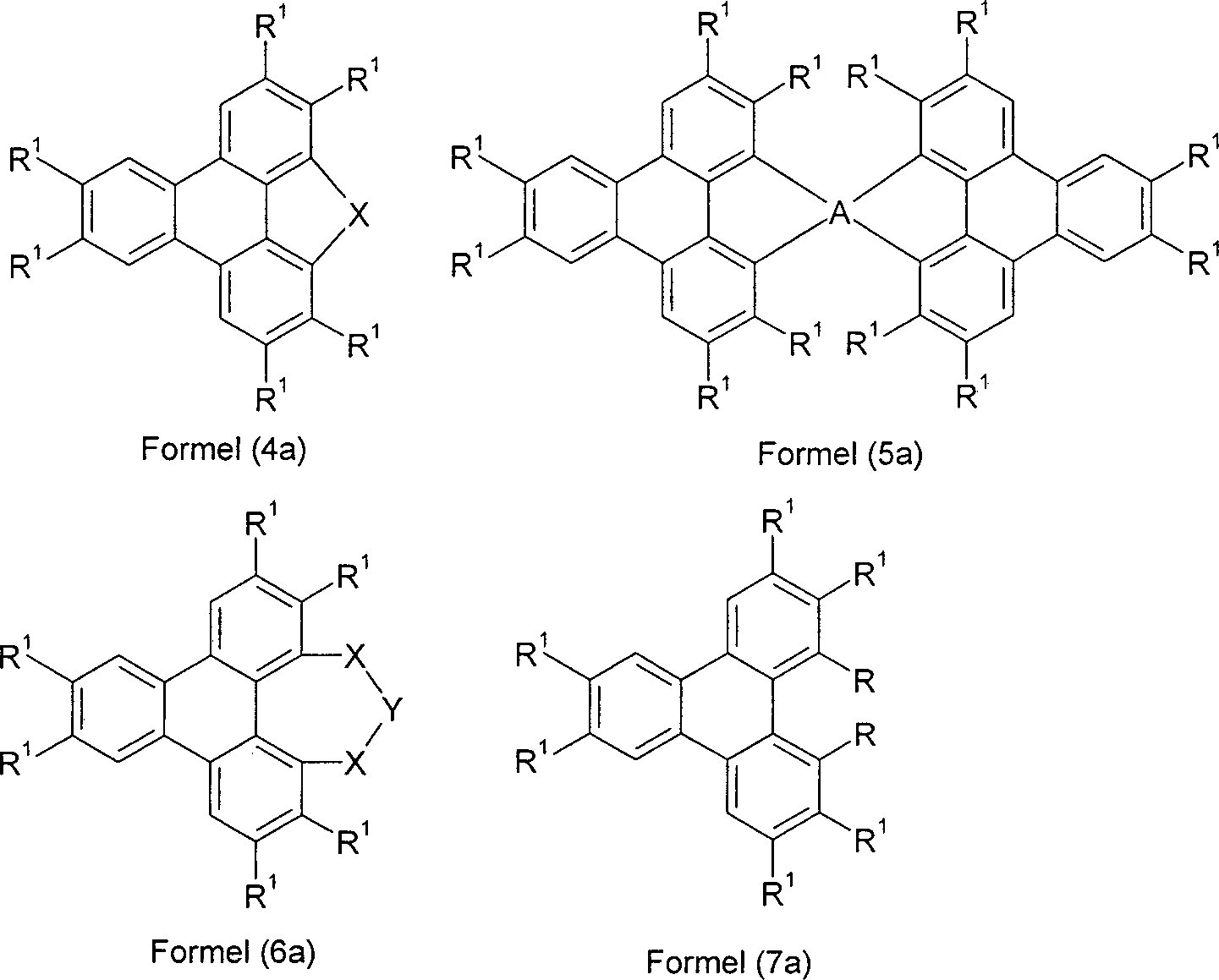
-
-
- In Verbindungen der Formel (1) mit n = 0 bzw. Formel (4) bzw. Formel (4a) ist X bevorzugt ausgewählt aus der Gruppe bestehend aus C(R2)2, Si(R2)2 und N(R2), besonders bevorzugt C(R2)2 und Si(R2)2, ganz besonders bevorzugt C(R2)2.
- R2 steht bevorzugt gleich oder verschieden bei jedem Auftreten für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen, bevorzugt mit 5 bis 24 aromatischen Ringatomen, welches jeweils auch durch einen oder mehrere Reste R3 substituiert sein kann und wobei zwei Reste R2, die an dasselbe Kohlenstoff-, Silicium-, Germanium- oder Zinnatom binden, auch miteinander ein aromatisches Ringsystem bilden können und so ein Spirosystem aufspannen können.
- In einer bevorzugten Ausführungsform der Verbindungen gemäß Formel (1), in der X für eine Gruppe der Formel (3) steht, bzw. Formel (5) bzw. Formel (5a) sind die beiden Triphenylenteilstrukturen, die an A binden, jeweils gleich substituiert. In diesen Verbindungen steht weiterhin bevorzugt A für Kohlenstoff oder Silicium, besonders bevorzugt für Kohlenstoff.
- In Verbindungen der Formel (1) mit n = 1 bzw. Formel (6) bzw. Formel (6a) ist die Gruppe X-Y-X bevorzugt ausgewählt aus der Gruppe bestehend aus C(R2)2-O-C(R2)2, Si(R2)2-O-Si(R2)2, O-BR2-O, O-PR2-O, O-P(=O)R2-O und C(=O)-NR2-C(=O).
- In einer bevorzugten Ausführungsform der Verbindungen gemäß Formel (2) bzw. Formel (7) bzw. Formel (7a) sind die beiden Reste R gleich gewählt.
- In einer bevorzugten Ausführungsform der Erfindung ist R1 in den oben genannten Formeln gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus H, D, F, Cl, Br, CN, N(Ar1)2, C(=O)Ar1, einer geradkettigen Alkyl- oder Alkoxygruppe mit 1 bis 10 C-Atomen oder einer verzweigten oder cyclischen Alkyl- oder Alkoxygruppe mit 3 bis 10 C-Atomen oder einer Alkenyl- oder Alkinylgruppe mit 2 bis 10 C-Atomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch O ersetzt sein können und wobei ein oder mehrere H-Atome durch D oder F ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann.
- In einer besonders bevorzugten Ausführungsform der Erfindung ist R1 in den oben genannten Formeln gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus H, D, F, CN, einer geradkettigen Alkylgruppe mit 1 bis 10 C-Atomen oder einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 10 C-Atomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei ein oder mehrere H-Atome durch D oder F ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 18 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann.
- In einer weiteren Ausführungsform der Erfindung sind die Reste R1, die direkt an das Triphenylen gebunden sind, gleich H.
- Dabei haben für Verbindungen, die durch Vakuumverdampfung verarbeitet werden, die Alkylgruppen bevorzugt nicht mehr als vier C-Atome, besonders bevorzugt nicht mehr als 1 C-Atom. Für Verbindungen, die aus Lösung verarbeitet werden, eignen sich auch Verbindungen, die mit Alkylgruppen mit bis zu 10 C-Atomen substituiert sind oder die mit Oligoarylengruppen, beispielsweise ortho-, meta-, para- oder verzweigten Terphenylgruppen oder Quaterphenylgruppen, substituiert sind.
- Je nach Verwendung der erfindungsgemäßen Verbindungen werden unterschiedliche Substituenten R und R1 gewählt.
- Wenn die Verbindungen der Formeln (1) oder (2) bzw. (4) bis (7) bzw. (4a) bis (7a) als Matrixmaterial für phosphoreszierende Emitter verwendet werden, steht bevorzugt mindestens ein Rest R1 für N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 oder für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann, wobei die Gruppe Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R3 am aromatischen oder heteroaromatischen Ringsystem keine kondensierten Arylgruppen mit mehr als 10 C-Atomen enthalten und keine kondensierten Heteroarylgruppen, in welcher mehr als zwei Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind.
- In einer besonders bevorzugten Ausführungsform der Erfindung enthalten Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R3 am aromatischen bzw. heteroaromatischen Ringsystem keine kondensierten Arylgruppen und keine kondensierten Heteroarylgruppen, in denen zwei oder mehr Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind.
- Besonders bevorzugte Gruppen Ar1 sind ausgewählt aus der Gruppe bestehend aus Phenyl, ortho-, meta- oder para-Biphenyl, ortho-, meta- oder para-Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, Fluoren oder Spirobifluoren, welche jeweils durch einen oder mehrere nicht-aromatische Reste R3 substituiert sein können, bevorzugt jedoch unsubstituiert ist.
- Besonders bevorzugte aromatische Ringsysteme R1 sind ausgewählt aus der Gruppe bestehend aus Phenyl, ortho-, meta- oder para-Biphenyl, ortho-, meta- oder para-Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, Fluoren oder Spirobifluoren, welche jeweils durch einen oder mehrere Reste R3 substituiert sein können, bevorzugt jedoch unsubstituiert ist.
- Besonders bevorzugte heteroaromatische Ringsysteme R1 enthalten als Heteroarylgruppe Triazin, Pyrimidin, Pyrazin, Pyridazin, Pyridin, Benzothiophen, Benzofuran, Indol, Carbazol, Azacarbazol, Diazacarbazol, Dibenzothiophen und/oder Dibenzofuran. Dabei sind die heteroaromatischen Ringsysteme insbesondere ausgewählt aus den Strukturen der folgenden Formeln (8) bis (38), wobei R3 die oben genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt.
- Bevorzugte Ausführungsformen der Gruppen der Formeln (8) bis (38) sind die Strukturen der folgenden Formeln (8a) bis (38a), wobei R3 die oben genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt. Dabei steht in Formel (8a) R3 bevorzugt gleich oder verschieden für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, insbesondere gleich oder verschieden für Phenyl, Biphenyl, Terphenyl oder Quaterphenyl.
- Wenn R1 für eine Gruppe N(Ar1)2 steht oder wenn R1 für ein aromatisches oder heteroaromatisches Ringsystem steht, welches eine Triaryl- bzw. -heteroarylamingruppe ist, dann ist diese Gruppe bevorzugt ausgewählt aus den Strukturen der folgenden Formeln (39) bis (41), wobei die verwendeten Symbole die oben genannten Bedeutungen aufweisen und weiterhin gilt:
Ar2 ist gleich oder verschieden bei jedem Auftreten ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann; dabei ist die Summe der aromatischen Ringatome aller Gruppen Ar2 zusammen nicht größer als 60;
E ist ausgewählt aus der Gruppe bestehend aus C(R4)2, NR4, O oder S. - Dabei steht Ar1 in Formel (39) und Ar2 in Formel (40) bevorzugt gleich oder verschieden bei jedem Auftreten für Phenyl, 1- oder 2-Naphthyl, ortho-, meta- oder para-Biphenyl, ortho-, meta-, para- oder verzweigtes Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, 2-Fluorenyl oder 2-Spirobifluorenyl, welche jeweils durch einen oder mehrere Reste R3 substituiert sein können.
- Wenn die Verbindung der Formel (2) bzw. (7) bzw. (7a) als Matrixmaterial für phosphoreszierende Emitter verwendet wird, steht weiterhin bevorzugt R gleich oder verschieden bei jedem Auftreten für N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches mit einem oder mehreren Resten R1 substituiert sein kann, wobei die Gruppe Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R1 am aromatischen oder heteroaromatischen Ringsystem keine kondensierten Arylgruppen mit mehr als 10 C-Atomen enthält und keine kondensierten Heteroarylgruppen, in welcher mehr als zwei Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind.
- In einer besonders bevorzugten Ausführungsform der Erfindung enthalten Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R1 am aromatischen bzw. heteroaromatischen Ringsystem keine kondensierten Arylgruppen und keine kondensierten Heteroarylgruppen, in denen zwei oder mehr Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind.
- Ganz besonders bevorzugte Gruppen Ar1 sind ausgewählt aus der Gruppe bestehend aus Phenyl, ortho-, meta- oder para-Biphenyl, ortho-, meta- oder para-Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, Fluoren oder Spirobifluoren, welches jeweils durch einen oder mehrere nicht-aromatische Reste R3 substituiert sein kann, bevorzugt jedoch unsubstituiert ist.
- Ganz besonders bevorzugte aromatische bzw. heteroaromatische Ringsysteme R in Formel (2) sind ausgewählt aus der Gruppe bestehend aus Phenyl, ortho-, meta- oder para-Biphenyl, ortho-, meta- oder para-Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, Fluoren, Spirobifluoren, Triazin, Pyridin, Pyrazin, Pyrimidin, Pyridazin oder Carbazol, welches jeweils durch einen oder mehrere Reste R1 substituiert sein kann, bevorzugt jedoch unsubstituiert ist.
- Wenn die Verbindungen der Formeln (1) oder (2) bzw. (4) bis (7) bzw. (4a) bis (7a) als Elektronentransportmaterial verwendet werden, steht bevorzugt mindestens ein Rest R1 und/oder mindestens ein Rest R in den Formeln (2), (7) oder (7a) für C(=O)Ar1, P(=O)(Ar1)2 oder für ein elektronenarmes heteroaromatisches Ringsystem mit 5 bis 40 aromatischen. Ringatomen, bevorzugt mit 5 bis 25 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann; und/oder es steht in Verbindungen der Formel (1) mit n = 0 bevorzugt X für BR2, C=O, SO, SO2 oder P(=O)(R2)2. Ein elektronenarmes heteroaromatisches Ringsystem im Sinne der vorliegenden Erfindung ist ein heteroaromatisches Ringsystem, welches mindestens eine elektronenarme Heteroarylgruppe enthält, wobei es sich dabei entweder um eine 6-Ringheteroarylgruppe mit mindestens einem Stickstoffatom oder um eine 5-Ringheteroarylgruppe mit mindestens zwei Heteroatomen handelt.
- Besonders bevorzugte elektronenarme heteroaromatische Ringsysteme R1 enthalten als Heteroarylgruppe mindestens eine Gruppe gewählt aus Triazin, Pyrimidin, Pyrazin, Pyridazin, Pyridin, Imidazol, Pyrazol, Oxazol, Oxadiazol, Triazol, Thiazol, Thiadiazol, Benzimidazol, Chinolin, Isochinolin und Chinoxalin. Dabei sind die heteroaromatischen Ringsysteme insbesondere ausgewählt aus den Strukturen der oben genannten Formeln (8) bis (11) bzw. (8a) bis (11a) oder aus den folgenden Formeln (42) bis (45), wobei R3 die oben genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt.
- Bevorzugte Ausführungsformen der Gruppen der Formeln (42) bis (45) sind die Strukturen der folgenden Formeln (42a) bis (45a), wobei R3 die oben genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt. Dabei steht R3 bevorzugt gleich oder verschieden für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, insbesondere gleich oder verschieden für Phenyl, Biphenyl, Terphenyl oder Quaterphenyl.
- Wenn die Verbindungen der Formeln (1) oder (2) bzw. (4) bis (7) bzw. (4a) bis (7a) als Lochtransportmaterial oder als emittierende Verbindung verwendet werden, steht bevorzugt mindestens ein Rest R1 und/oder R für N(Ar1)2, für eine Triarylaminogruppe oder für ein elektronenreiches heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen, insbesondere 5 bis 25 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann, insbesondere für einen Rest gemäß einer der oben genannten Formeln (39) bis (41); und/oder es steht in Verbindungen der Formel (1) mit n = 0 X für NR2 oder PR2. Ein elektronenreiches heteroaromatisches Ringsystem im Sinne der vorliegenden Erfindung ist ein heteroaromatisches Ringsystem, welches mindestens eine elektronenreiche Heteroarylgruppe enthält, wobei es sich dabei um eine 5-Ringheteroarylgruppe mit genau einem Heteroatom handelt, an die auch eine oder mehrere Arylgruppen ankondensiert sein können.
- Besonders bevorzugte elektronenreiche heteroaromatische Ringsysteme R1 enthalten als Heteroarylgruppe Pyrrol, Furan, Thiophen, Benzothiophen, Benzofuran, Indol, Carbazol, Dibenzothiophen, Dibenzofuran und/oder Azacarbazol. Dabei sind die elektronenreichen heteroaromatischen Ringsysteme insbesondere ausgewählt aus den Strukturen der oben genannten Formeln (12) bis (38).
- In einer Ausführungsform der Erfindung sind oben genannten Bevorzugungen beliebig miteinander kombinierbar.
- Beispiele für bevorzugte Verbindungen gemäß den oben aufgeführten Ausführungsformen bzw. Verbindungen, wie sie bevorzugt in elektronischen Vorrichtungen eingesetzt werden können, sind die Verbindungen der folgenden Strukturen (1) bis (91).
- Die erfindungsgemäßen Verbindungen können nach dem Fachmann bekannten Syntheseschritten dargestellt werden, wie in Schema 1 bis 3 schematisch dargestellt.
-
- Daneben können entsprechend substituierte Triphenylenderivate nach dem Fachmann geläufigen Methoden der organischen Chemie wie z. B. durch Suzuki-, Stille-, Heck-, Sonogashira-, Yamamoto-, Negishi-, Ullmann- oder Buchwald-Kupplungen zu aromatischen bzw. heteroaromatischen Kohlenwasserstoffen, Aminen, Ethern, Thioethern, etc. umgesetzt werden, wie in Schema 2 exemplarisch gezeigt. Dabei steht <Pd> für einen Palladiumkatalysator. Schema 2:
-
- Ein weiterer Gegenstand der vorliegenden Erfindung ist daher ein Verfahren zur Herstellung einer Verbindung gemäß Formel (1) bzw. (2) durch Umsetzung von 1,12-Dilithio-triphenylen-Derivaten mit Elektrophilen oder durch Umsetzung von Halogen- oder Amino-substituierten Triphenylen-Derivaten in einer metall-katalysierten Kupplungsreaktion.
- Die oben beschriebenen erfindungsgemäßen Verbindungen, insbesondere Verbindungen, welche mit reaktiven Abgangsgruppen, wie Brom, Iod, Chlor, Boronsäure oder Boronsäureester, oder mit reaktiven, polymerisierbaren Gruppen, wie Olefinen oder Oxetanen, substituiert sind, können als Monomere zur Erzeugung entsprechender Oligomere, Dendrimere oder Polymere Verwendung finden. Die Oligomerisation bzw. Polymerisation erfolgt dabei bevorzugt über die Halogenfunktionalität bzw. die Boronsäurefunktionalität bzw. über die polymerisierbare Gruppe. Es ist weiterhin möglich, die Polymere über derartige Gruppen zu vernetzen. Die erfindungsgemäßen Verbindungen und Polymere können als vernetzte oder unvernetzte Schicht eingesetzt werden.
- Weiterer Gegenstand der Erfindung sind daher Oligomere, Polymere oder Dendrimere enthaltend eine oder mehrere der oben aufgeführten. erfindungsgemäßen Verbindungen, wobei ein oder mehrere Bindungen der erfindungsgemäßen Verbindung zum Polymer, Oligomer oder Dendrimer vorhanden sind. Je nach Verknüpfung der erfindungsgemäßen Verbindung bildet diese daher eine Seitenkette des Oligomers oder Polymers oder ist in der Hauptkette verknüpft. Die Polymere, Oligomere oder Dendrimere können konjugiert, teilkonjugiert oder nicht-konjugiert sein. Die Oligomere oder Polymere können linear, verzweigt oder dendritisch sein. Für die Wiederholeinheiten der erfindungsgemäßen Verbindungen in Oligomeren, Dendrimeren und Polymeren gelten dieselben Bevorzugungen, wie oben beschrieben.
- Zur Herstellung der Oligomere oder Polymere werden die erfindungsgemäßen Monomere homopolymerisiert oder mit weiteren Monomeren copolymerisiert. Bevorzugt sind Homopolymere oder Copolymere, wobei die Einheiten gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen zu 0.01 bis 99.9 mol%, bevorzugt 5 bis 90 mol%, besonders bevorzugt 20 bis 80 mol% vorhanden sind. Geeignete und bevorzugte Comonomere, welche das Polymergrundgerüst bilden, sind gewählt aus Fluorenen (z. B. gemäß
EP 842208 WO 2000/022026 EP 707020 EP 894107 WO 2006/061181 WO 92/18552 WO 2004/070772 WO 2004/113468 EP 1028136 ), Dihydrophenanthrenen (z. B. gemäßWO 2005/014689 WO 2004/041901 WO 2004/113412 WO 2005/040302 WO 2005/104264 WO 2007/017066 - Weiterhin können die Verbindungen gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen auch weiter funktionalisiert werden und so zu erweiterten Strukturen umgesetzt werden. Hier ist als Beispiel die Umsetzung mit Arylboronsäuren gemäß Suzuki oder mit primären oder sekundären Aminen gemäß Hartwig-Buchwald zu nennen. So können die Verbindungen gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen auch direkt an phosphoreszierende Metallkomplexe oder auch an andere Metallkomplexe gebunden werden.
- Die erfindungsgemäßen Verbindungen eignen sich für die Verwendung in einer elektronischen Vorrichtung. Dabei wird unter einer elektronischen Vorrichtung eine Vorrichtung verstanden, welche mindestens eine Schicht enthält, die mindestens eine organische Verbindung enthält. Das Bauteil kann dabei aber auch anorganische Materialien enthalten oder auch Schichten, welche vollständig aus anorganischen Materialien aufgebaut sind.
- Ein weiterer Gegenstand der vorliegenden Erfindung ist daher die Verwendung der oben ausgeführten erfindungsgemäßen Verbindungen in einer elektronischen Vorrichtung, insbesondere in einer organischen Elektrolumineszenzvorrichtung.
- Nochmals ein weiterer Gegenstand der vorliegenden Erfindung ist eine elektronische Vorrichtung enthaltend mindestens eine der oben ausgeführten erfindungsgemäßen Verbindungen. Dabei gelten die oben ausgeführten Bevorzugungen ebenso für die elektronischen Vorrichtungen.
- Die elektronische Vorrichtung ist bevorzugt ausgewählt aus der Gruppe bestehend aus organischen Elektrolumineszenzvorrichtungen (OLEDs), organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs), organischen Laserdioden (O-Laser) und „organic plasmon emitting devices” (D. M. Koller et al., Nature Photonics 2008, 1–4), bevorzugt aber organischen Elektrolumineszenzvorrichtungen (OLEDs), besonders bevorzugt phosphoreszierenden OLEDs.
- Die organische Elektrolumineszenzvorrichtung enthält Kathode, Anode und mindestens eine emittierende Schicht. Außer diesen Schichten kann sie noch weitere Schichten enthalten, beispielsweise jeweils eine oder mehrere Lochinjektionsschichten, Lochtransportschichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Exzitonenblockierschichten, Elektronenblockierschichten und/oder Ladungserzeugungsschichten (Charge-Generation Layers). Ebenso können zwischen zwei emittierende Schichten Interlayer eingebracht sein, welche beispielsweise eine exzitonenblockierende Funktion aufweisen. Es sei aber darauf hingewiesen, dass nicht notwendigerweise jede dieser Schichten vorhanden sein muss. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittierende Schicht enthalten, oder sie kann mehrere emittierende Schichten enthalten. Wenn mehrere Emissionsschichten vorhanden sind, weisen diese bevorzugt insgesamt mehrere Emissionsmaxima zwischen 380 nm und 750 nm auf, so dass insgesamt weiße Emission resultiert, d. h. in den emittierenden Schichten werden verschiedene emittierende Verbindungen verwendet, die fluoreszieren oder phosphoreszieren können. Insbesondere bevorzugt sind Systeme mit drei emittierenden Schichten, wobei die drei Schichten blaue, grüne und orange oder rote Emission zeigen (für den prinzipiellen Aufbau siehe z. B.
WO 2005/011013 - Die erfindungsgemäße Verbindung gemäß den oben aufgeführten Ausführungsformen kann dabei in unterschiedlichen Schichten eingesetzt werden, je nach genauer Struktur. Bevorzugt ist eine organische Elektrolumineszenzvorrichtung, enthaltend eine Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen als Matrixmaterial für fluoreszierende oder phosphoreszierende Emitter, insbesondere für phosphoreszierende Emitter, und/oder in einer Lochblockierschicht und/oder in einer Elektronentransportschicht und/oder in einer elektronenblockierenden bzw. exzitonenblockierenden Schicht und/oder in einer Lochtransport- bzw. Lochinjektionsschicht, je nach genauer Substitution. Dabei gelten die oben aufgeführten bevorzugten Ausführungsformen auch für die Verwendung der Materialien in organischen elektronischen Vorrichtungen.
- In einer weiteren Ausführungsform der Erfindung enthält die organische Elektrolumineszenzvorrichtung die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen in einer optischen Auskopplungsschicht. Unter einer optischen Auskopplungsschicht wird dabei eine Schicht verstanden, die nicht zwischen der Anode und der Kathode liegt, sondern die außerhalb der eigentlichen Vorrichtung auf eine Elektrode aufgebracht wird, beispielsweise zwischen einer Elektrode und einem Substrat, um die optische Auskopplung zu verbessern.
- In einer bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen als Matrixmaterial für eine fluoreszierende oder phosphoreszierende Verbindung, insbesondere für eine phosphoreszierende Verbindung, in einer emittierenden Schicht eingesetzt. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittierende Schicht enthalten, oder sie kann mehrere emittierende Schichten enthalten, wobei mindestens eine emittierende Schicht mindestens eine erfindungsgemäße Verbindung als Matrixmaterial enthält.
- Wenn die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen als Matrixmaterial für eine emittierende Verbindung in einer emittierenden Schicht eingesetzt wird, wird sie bevorzugt in Kombination mit einem oder mehreren phosphoreszierenden Materialien (Triplettemitter) eingesetzt. Unter Phosphoreszenz im Sinne dieser Erfindung wird die Lumineszenz aus einem angeregten Zustand mit höherer Spinmultiplizität verstanden, also einem Spinzustand > 1, insbesondere aus einem angeregten Triplettzustand. Im Sinne dieser Anmeldung sollen alle lumineszierenden Komplexe mit Übergangsmetallen oder Lanthaniden, insbesondere alle Iridium-, Platin- und Kupferkomplexe als phosphoreszierende Verbindungen angesehen werden.
- Die Mischung aus der Verbindung gemäß Formel (1) oder (2) bzw. den oben ausgeführten bevorzugten Ausführungsformen und der emittierenden Verbindung enthält zwischen 99 und 1 Vol.-%, vorzugsweise zwischen 98 und 10 Vol.-%, besonders bevorzugt zwischen 97 und 60 Vol.-%, insbesondere zwischen 95 und 80 Vol.-% der Verbindung gemäß Formel (1) oder (2) bzw. der oben ausgeführten bevorzugten Ausführungsformen bezogen auf die Gesamtmischung aus Emitter und Matrixmaterial. Entsprechend enthält die Mischung zwischen 1 und 99 Vol.-%, vorzugsweise zwischen 2 und 90 Vol.-%, besonders bevorzugt zwischen 3 und 40 Vol.-%, insbesondere zwischen 5 und 20 Vol.-% des Emitters bezogen auf die Gesamtmischung aus Emitter und Matrixmaterial.
- Eine weitere bevorzugte Ausführungsform der vorliegenden Erfindung ist der Einsatz der Verbindung gemäß Formel (1) oder (2) bzw. der oben ausgeführten bevorzugten Ausführungsformen als Matrixmaterial für einen phosphoreszierenden Emitter in Kombination mit einem weiteren Matrixmaterial. Besonders geeignete Matrixmaterialien, welche in Kombination mit den Verbindungen gemäß Formel (1) oder (2) bzw. der oben ausgeführten bevorzugten Ausführungsformen eingesetzt werden können, sind aromatische Ketone, aromatische Phosphinoxide oder aromatische Sulfoxide oder Sulfone, z. B. gemäß
WO 2004/013080 WO 2004/093207 WO 2006/005627 WO 2010/006680 WO 2005/039246 US 2005/0069729 JP 2004/288381 EP 1205527 oderWO 2008/086851 WO 2007/063754 WO 2008/056746 DE 102009023155.2 oderDE 102009031021.5 , Azacarbazolderivate, z. B. gemäßEP 1617710 ,EP 1617711 ,EP 1731584 ,JP 2005/347160 WO 2007/137725 WO 2005/111172 WO 2006/117052 WO 2007/063754 WO 2008/056746 WO 2010/015306 DE 102009053382.6 ,DE 102009053644.2 oderDE 102009053645.0 , Zinkkomplexe, z. B. gemäßEP 652273 WO 2009/062578 WO 2010/054729 WO 2010/054730 DE 102009048791.3 undDE 102009053836.4 . Ebenso kann ein weiterer phosphoreszierender Emitter, welcher kürzerwellig als der eigentliche Emitter emittiert, als Co-Host in der Mischung vorhanden sein. - Als phosphoreszierende Verbindung (= Triplettemitter) eignen sich insbesondere Verbindungen, die bei geeigneter Anregung Licht, vorzugsweise im sichtbaren Bereich, emittieren und außerdem mindestens ein Atom der Ordnungszahl größer 20, bevorzugt größer 38 und kleiner 84, besonders bevorzugt größer 56 und kleiner 80 enthalten, insbesondere ein Metall mit dieser Ordnungszahl. Bevorzugt werden als Phosphoreszenzemitter Verbindungen, die Kupfer, Molybdän, Wolfram, Rhenium, Ruthenium, Osmium, Rhodium, Iridium, Palladium, Platin, Silber, Gold oder Europium enthalten, verwendet, insbesondere Verbindungen, die Iridium oder Platin enthalten.
- Beispiele der oben beschriebenen Emitter können den Anmeldungen
WO 00/70655 WO 01/41512 WO 02/02714 WO 02/15645 EP 1191613 ,EP 1191612 ,EP 1191614 ,WO 05/033244 WO 05/019373 US 2005/0258742 - Beispiele für geeignete phosphoreszierende Verbindungen sind in der folgenden Tabelle aufgeführt.
- In einer weiteren Ausführungsform der Erfindung enthält die erfindungsgemäße organische Elektrolumineszenzvorrichtung keine separate Lochinjektionsschicht und/oder Lochtransportschicht und/oder Lochblockierschicht und/oder Elektronentransportschicht, d. h. die emittierende Schicht grenzt direkt an die Lochinjektionschicht oder die Anode an, und/oder die emittierende Schicht grenzt direkt an die Elektronentransportschicht oder die Elektroneninjektionsschicht oder die Kathode an, wie zum Beispiel in
WO 2005/053051 WO 2009/030981 - In einer weiteren bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen als Elektronentransportmaterial in einer Elektronentransport- oder Elektroneninjektionsschicht eingesetzt. Dabei kann die emittierende Schicht fluoreszierend oder phosphoreszierend sein. Wenn die Verbindung als Elektronentransportmaterial eingesetzt wird, kann es bevorzugt sein, wenn sie dotiert ist, beispielsweise mit Alkalimetallkomplexen, wie z. B. LiQ (Lithiumhydroxychinolinat).
- In nochmals einer weiteren bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen in einer Lochblockierschicht eingesetzt, insbesondere in einer phosphoreszierenden OLED. Unter einer Lochblockierschicht wird eine Schicht verstanden, die auf Kathodenseite direkt an eine emittierende Schicht angrenzt.
- Es ist weiterhin möglich, die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen sowohl in einer Lochblockierschicht bzw. Elektronentransportschicht als auch als Matrix in einer emittierenden Schicht zu verwenden.
- In nochmals einer weiteren Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen in einer Lochtransportschicht bzw. in einer Elektronenblockierschicht bzw. Exzitonenblockierschicht eingesetzt.
- In den weiteren Schichten der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung können alle Materialien verwendet werden, wie sie üblicherweise gemäß dem Stand der Technik eingesetzt werden. Der Fachmann kann daher ohne erfinderisches Zutun alle für organische Elektrolumineszenzvorrichtungen bekannten Materialien in Kombination mit den erfindungsgemäßen Verbindungen gemäß Formel (1) oder (2) bzw. den oben ausgeführten bevorzugten Ausführungsformen einsetzen.
- Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck kleiner 10–5 mbar, bevorzugt kleiner 10–6 mbar aufgedampft. Es ist aber auch möglich, dass der Anfangsdruck noch geringer ist, beispielsweise kleiner 10–7 mbar.
- Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10–5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden (z. B. M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301).
- Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie Z. B. Siebdruck, Flexodruck, Offsetdruck, LITI (Light Induced Thermal Imaging, Thermotransferdruck), Ink-Jet Druck (Tintenstrahldruck) oder Nozzle Printing, hergestellt werden. Hierfür sind lösliche Verbindungen nötig, welche beispielsweise durch geeignete Substitution erhalten werden. Diese Verfahren eignen sich insbesondere auch für Oligomere, Dendrimere und Polymere.
- Weiterhin sind Hybridverfahren möglich, bei denen beispielsweise eine oder mehrere Schichten aus Lösung aufgebracht werden und eine oder mehrere weitere Schichten aufgedampft werden. So ist es beispielsweise möglich, dass die emittierende Schicht aus Lösung aufgebracht wird und auf diese Schicht eine Elektronentransportschicht im Vakuum aufgedampft wird.
- Diese Verfahren sind dem Fachmann generell bekannt und können von ihm ohne erfinderisches Zutun auf organische Elektrolumineszenzvorrichtungen enthaltend die erfindungsgemäßen Verbindungen angewandt werden.
- Für die Verarbeitung aus Lösung werden Formulierungen, insbesondere Lösungen, Suspensionen oder Miniemulsionen, der erfindungsgemäßen Verbindungen benötigt. Ein weiterer Gegenstand der vorliegenden Erfindung sind daher Formulierungen, insbesondere Lösungen, Suspensionen oder Miniemulsionen, enthaltend mindestens eine erfindungsgemäße Verbindung und mindestens ein Lösemittel, insbesondere ein organisches Lösemittel.
- Die erfindungsgemäßen Verbindungen und die erfindungsgemäßen organischen Elektrolumineszenzvorrichtungen zeichnen sich durch folgende überraschende Vorteile gegenüber dem Stand der Technik aus:
- 1. Die erfindungsgemäßen Verbindungen bzw. Verbindungen gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen, eingesetzt als Matrixmaterial für fluoreszierende oder phosphoreszierende Emitter, führen zu sehr hohen Effizienzen sowie zu langen Lebensdauern. Dies gilt insbesondere, wenn die Verbindungen als Matrixmaterial für einen phosphoreszierenden Emitter eingesetzt werden.
- 2. Die erfindungsgemäßen Verbindungen bzw. Verbindungen gemäß Formel (1) oder (2) bzw. die oben ausgeführten bevorzugten Ausführungsformen eignen sich nicht nur als Matrix für rot phosphoreszierende Verbindungen, sondern insbesondere auch für grün phosphoreszierende Verbindungen.
- 3. Die erfindungsgemäßen Verbindungen sind in wenigen Reaktionsstufen und mit hohen Ausbeuten einfach synthetisch zugänglich.
- 4. Die erfindungsgemäßen Verbindungen, eingesetzt in organischen Elektrolumineszenzvorrichtungen, führen zu hohen Effizienzen und zu steilen Strom-Spannungs-Kurven mit niedrigen Einsatzspannungen.
- 5. Auch bei Verwendung als Elektronentransportmaterial oder als Lochtransportmaterial führen die erfindungsgemäßen Verbindungen zu sehr guten Eigenschaften in Bezug auf die Effizienz, die Lebensdauer und die Betriebsspannung von organischen Elektrolumineszenzvorrichtungen.
- Diese oben genannten Vorteile gehen nicht mit einer Verschlechterung der weiteren elektronischen Eigenschaften einher.
- Die Erfindung wird durch die nachfolgenden Beispiele näher erläutert, ohne sie dadurch einschränken zu wollen. Der Fachmann kann aus den Schilderungen die Erfindung im gesamten offenbarten Bereich ausführen und ohne erfinderisches Zutun weitere erfindungsgemäße Verbindungen herstellen und diese in elektronischen Vorrichtungen verwenden bzw. das erfindungsgemäße Verfahren anwenden.
- Beispiele:
- A) Synthesebeispiele:
- Die nachfolgenden Synthesen werden, sofern nicht anders angegeben, unter einer Schutzgasatmosphäre in getrockneten Lösungsmitteln durchgeführt. Die Metallkomplexe werden zusätzlich unter Ausschluss von Licht gehandhabt. Die Lösungsmittel und Reagenzien können z. B. von Sigma-ALDRICH bzw. ABCR bezogen werden. In eckigen Klammern sind jeweils die CAS-Nummern der Edukte angegeben. Beispiel 1: 4-(2,4,6-Trimethyl-phenyl)-4H-4-bora-cyclopenta[def]-triphenylen
- A: 1,12-Dilithiotriphenylen·2 TMEDA
- 312.5 ml (500 mmol) n-Butyllithium (1.6 M in n-Hexan) wird tropfenweise mit 58.1 g (500 mmol) N,N-Tetramethylethylendiamin versetzt und 1 h bei Raumtemperatur gerührt. Die Mischung wird tropfenweise mit einer Lösung von 22.8 g (100 mmol) Triphenylen in 150 ml n-Hexan versetzt und anschließend 5 h unter Rückfluss erhitzt. Nach Abdestillieren von ca. 250 ml n-Hexan lässt man die Reaktionsmischung erkalten und kühlt dann für 24 h auf –30°C ab, wobei sich ein brauner Feststoff abscheidet. Man saugt den braunen Feststoff ab, wäscht diesen dreimal mit je 100 ml eiskaltem n-Hexan und trocknet im Vakuum. Ausbeute: 134.7 g (285 mmol), 57%. Vorsicht: 1,12-Dilithiotriphenylen·2 TMEDA ist pyrophor!
- B: 4-(2,4,6-Trimethyl-phenyl)-4H-4-bora-cyclopenta[def]-triphenylen
- Eine Lösung von 47.2 g (100 mmol) 1,12-Dilithiotriphenylen·2 TMEDA in 1500 ml THF wird tropfenweise mit einer Lösung von 20.1 g (100 mmol) Dichlor-2,4,6-trimethylphenylboran [69464-76-2] in 500 ml THF versetzt und 16 h bei Raumtemperatur gerührt. Nach Entfernen des Lösungsmittels im Vakuum wird der Rückstand in 500 ml Dichlormethan aufgenommen und dreimal mit je 200 ml Wasser gewaschen. Nach Trocknen über Natriumsulfat wird die organische Phase eingeengt, der Rückstand wird fünfmal aus Dioxan umkristallisiert und anschließend zweimal im Vakuum (p ca. 10–6 mbar, T ca. 300°C) fraktioniert sublimiert. Ausbeute 13.2 g (37 mmol), 37%. Reinheit: 99.9%ig n. HPLC.
-
- Eine Suspension von 25.8 g (100 mmol) Triphenyleno[1,12-bcd]thiophen [68558-73-6] in 2000 ml n-Hexan wird mit 48.8 g (420 mmol) N,N-Tetramethylethylendiamin und dann tropfenweise mit 250 ml (400 mol) n-Butyllithium (1.6 M in n-Hexan) versetzt und anschließend 4 h bei 60°C gerührt. Nach Erkalten und Abkühlen der Mischung auf –60°C wird diese auf ein Mal unter gutem Rühren mit 46.8 g (450 mmol) Borsäuretrimethylester versetzt. Man rührt 30 min. bei –60°C nach, lässt dann auf Raumtemperatur erwärmen, entfernt das n-Hexan im Vakuum, nimmt den Rückstand in 300 ml THF auf, versetzt mit einer Mischung von 300 ml Wasser und 30 g Eisessig, rührt 2 h nach, saugt vom ausgefallenen Feststoff ab, wäscht diesen zweimal mit je 200 ml Wasser und trocknet im Vakuum. Ausbeute: 30.7 g. Reinheit: ca. 90.0%ig nach NMR, das Rohprodukt wird im Folgenden ohne weitere Reinigung verwendet.
- B) 1,10-Bis-(N-phenyl-carbazol-2-yl)-4H-4-thia-cyclopenta[def]-triphenylen
- Ein Gemisch aus 17.3 g (50 mmol) Triphenyleno[1,12-bcd]thiophen-2,11-diboronsäure, 41.9 g (130 mmol) 2-Brom-9-phenyl-carbazol [94994-62-4] und 31.8 g (150 mmol) Trikaliumphosphat in einem Gemisch aus 200 ml Toluol, 100 ml Ethanol und 300 ml Wasser wird unter Rühren mit 913 mg (3 mmol) Tri-o-tolylphosphin und dann mit 112 mg (0.5 mmol) Palladium(II)acetat versetzt und 16 h unter Rückfluss erhitzt. Nach Erkalten saugt man vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 100 ml eines Gemischs aus Wasser und Ethanol (1:1, v:v) und dann dreimal mit je 100 ml Ethanol und trocknet im Vakuum. Der Feststoff wird fünfmal einer Heißdampfextraktion mit Toluol über Aluminiumoxid (basisch, Aktivitätsstufe 1) unterzogen und dann zweimal im Vakuum (p ca. 10–6 mbar, T ca. 350°C) fraktioniert sublimiert. Ausbeute 12.6 g (34 mmol), 34%. Reinheit: 99.9%ig nach HPLC.
-
- Eine gut gerührte Suspension von 12.1 g (50 mmol) 4H-4-Aza-cyclopenta[def]-triphenylen [109606-75-9], 14.0 g (60 mmol) 4-Brombiphenyl und 7.3 g (65 mmol) Kalium-tert-butylat in 150 ml Toluol wird mit 235 mg (1.3 mmol) Di-tert-butylchlorophosphin und dann mit 225 g (1 mmol) Palladium(II)acetat versetzt und 16 h unter Rückfluss erhitzt. Nach Erkalten auf 60°C gibt man Wasser zu, rührt 30 min. nach, saugt dann vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 100 ml eines Gemischs aus Wasser und Ethanol (1:1, v:v) und dann dreimal mit je 100 ml Ethanol und trocknet im Vakuum. Der Feststoff wird fünfmal einer Heißdampfextraktion mit Toluol über Aluminiumoxid (basisch, Aktivitätsstufe 1) unterzogen und dann zweimal im Vakuum (p ca. 10–6 mbar, T ca. 320°C) fraktioniert sublimiert. Ausbeute: 7.3 g (19 mmol), 37%. Reinheit: 99.9%ig n. HPLC.
-
- Ein Gemisch aus 9.6 g (20 mmol) 1,12-Diiod-triphenylen [130197-34-1], 11.4 g (50 mmol) 2-Dibenzothiophenboronsäure [108847-24-1] und 10.6 g (50 mmol) Trikaliumphosphat in einem Gemisch aus 100 ml Toluol, 50 ml Dioxan und 300 ml Wasser wird unter Rühren mit 304 mg (1 mmol) Tri-o-tolylphosphin und dann mit 45 mg (0.2 mmol) Palladium(II)acetat versetzt und 30 h unter Rückfluss erhitzt. Nach Erkalten saugt man vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 50 ml eines Gemischs aus Wasser und Ethanol (1:1, v:v) und dann dreimal mit je 50 ml Ethanol und trocknet im Vakuum. Der Feststoff wird viermal einer Heißdampfextraktion mit Toluol über Aluminiumoxid (basisch, Aktivitätsstufe 1) unterzogen und dann zweimal im Vakuum (p ca. 10–6 mbar, T ca. 310°C) fraktioniert sublimiert. Ausbeute 5.0 g (8.4 mmol), 41%. Reinheit: 99.9%ig nach HPLC. Beispiel 15: 4,4-Bis-[1,1',3',1'']-terphenyl-5'-yl-4H-cyclopenta[def]-triphenylen
- Eine Lösung von 47.2 g (100 mmol) 1,12-Dilithiotriphenylen·2 TMEDA in 1500 ml THF wird tropfenweise mit einer Lösung von 48.7 g (100 mmol) Bis-[1,1',3',1'']-terphenyl-5'-yl-methanon [1205748-29-3] in 500 ml THF versetzt und dann 2 h unter Rückfluss erhitzt. Nach Quenchen der Reaktionsmischung mit 50 ml Ethanol und Entfernen des Lösungsmittels im Vakuum wird der Rückstand in 500 ml Eisessig aufgenommen, die Suspension wird mit 20 ml konz. Salzsäure und 20 ml Essigsäureanhydrid versetzt und 3 h unter Rückfluss erhitzt. Nach Erkalten saugt man vom ausgefallen Feststoff ab, wäscht diesen dreimal mit je 100 ml Ethanol und trocknet im Vakuum. Der Feststoff wird fünfmal aus DMF umkristallisiert und anschließend zweimal im Vakuum (p ca. 10–6 mbar, T ca. 350°C) fraktioniert sublimiert. Ausbeute: 38.3 g (55 mmol), 55%. Reinheit: 99.9%ig nach HPLC.
- B) Device-Beispiele
- Beispiel 16: Herstellung der OLEDs
- Die Herstellung von erfindungsgemäßen OLEDs sowie OLEDs nach dem Stand der Technik erfolgt nach einem allgemeinen Verfahren gemäß
WO 2004/058911 - In den folgenden Beispielen 17 bis 27 (siehe Tabellen 1, 2 und 3) werden die Ergebnisse verschiedener OLEDs vorgestellt. Glasplättchen, die mit strukturiertem ITO (Indium-Zinn-Oxid) der Dicke 150 nm beschichtet sind, werden zur verbesserten Prozessierung mit 20 nm PEDOT beschichtet (Poly(3,4-ethylendioxy-2,5-thiophen), aus Wasser aufgeschleudert; bezogen von H. C. Starck, Goslar, Deutschland). Diese beschichteten Glasplättchen bilden die Substrate, auf welche die OLEDs aufgebracht werden. Die OLEDs haben prinzipiell folgenden Schichtaufbau: Substrat/Lochinjektionsschicht (HIL1, mit HIL1, 20 nm)/Lochtransportschicht (HTL, mit HTM1 (Referenz) oder den erfindungsgemäßen HTMs, 20 nm)/Elektronenblockierschicht (EBL, 10 nm)/Emissionsschicht (EML mit den erfindungsgemäßen Einzelmatrizes bzw. gemischten Matrices M, 40 nm)/Elektronentransportschicht (ETL, mit ETL1, 20 nm)/Elektroneninjektionsschicht (EIL, mit LiF, 1 nm) und abschließend eine Kathode. Die Kathode wird durch eine 100 nm dicke Aluminiumschicht gebildet. Der genaue Aufbau der OLEDs, insbesondere der Aufbau der Lochleiter- bzw. Emitterschicht, sowie die mit diesen OLEDs erhaltenen Ergebnisse bei Verwendung der erfindungsgemäßen Verbindungen als Matrixmaterialien für phosphoreszierende Emitter ist der Tabelle 1 für grün emittierende OLEDs und der Tabelle 2 für rot emittierende OLEDs zu entnehmen. Dabei beziehen sich die%-Angaben auf Vol.-%. In Tabelle 3 sind die Ergebnisse für die Verwendung von erfindungsgemäßen Verbindungen sowohl als Matrixmaterialien für phosphoreszierende Emitter als auch als Lochtransportmaterialien gezeigt.
- Die zur Herstellung der OLEDs verwendeten Materialien sind in Tabelle 4 aufgeführt.
- Alle Materialien werden in einer Vakuumkammer thermisch aufgedampft. Dabei besteht die Emissionsschicht immer aus mindestens einem Matrixmaterial (Rostmaterial, Wirtsmaterial) und einem emittierenden Dotierstoff (Dotand, Emitter), der dem Matrixmaterial bzw. den Matrixmaterialien durch Coverdampfung in einem bestimmten Volumenanteil beigemischt wird.
- Die noch nicht optimierten OLEDs werden standardmäßig charakterisiert. Hierfür werden die Elektrolumineszenzspektren, die Stromeffizienz (gemessen in cd/A) und die Spannung bestimmt. Die in den Tabellen angegebenen Effizienzen und Spannungen beziehen sich auf die entsprechenden Werte bei einer Betriebshelligkeit von 1000 cd/m2. Tabelle 1: Grün emittierende OLEDs
Bsp. EML Effizienz [cd/A] Spannung [V] CIE, x/y 17 Bsp.1: TEG1 (15%) 40.0 4.7 0.34/0.62 18 Bsp.2: TEG1 (15%) 43.9 4.8 0.33/0.62 19 Bsp5: TEG1 (10%) 51.0 4.6 0.33/0.62 20 Bsp.5: TEG2 (15%) 54.7 4.5 0.32/0.61 21 Bsp.5 (60%): EBL (25): TEG2 (15%) 55.4 4.2 0.32/0.61 22 Bsp.8: TEG2 (15%) 28.0 4.1 0.33/0.61 23 Bsp.14: TEG2 (15%) 45.2 4.2 0.32/0.61 Bsp. EML Effizienz [cd/A] Spannung [V] CIE, x/y 24 Bsp.13: TER1 (15%) 12.4 4.8 0.67/0.33 25 Bsp.11: (20%) Bsp.15: (70%) TER2 (10%) 13.6 4.6 0.67/0.33 Bsp. HTM/EML Effizienz [cd/A] Spannung [V] CIE, x/y 26 Bsp.12/Bsp.8: TER1 (15%) 15.2 4.4 0.67/0.33 27 Bsp.13/Bsp.13: TER2 (10%) 14.3 4.1 0.67/0.33 - Wie aus den oben aufgeführten Beispielen deutlich zu erkennen ist, eignen sich die erfindungsgemäßen Materialien besonders gut für die Verwendung als Matrixmaterialien für phosphoreszierende Emitter und als Lochleiter und führen dort zu hohen Effizienzen und niedrigen Betriebsspannungen.
- ZITATE ENTHALTEN IN DER BESCHREIBUNG
- Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.
- Zitierte Patentliteratur
-
- US 4539507 [0002]
- US 5151629 [0002]
- EP 0676461 [0002]
- WO 98/27136 [0002]
- WO 2004/093207 [0004, 0066]
- WO 2010/006680 [0004, 0066]
- WO 2005/003253 [0004]
- JP 2005/071983 [0005]
- WO 2006/038709 [0005]
- EP 842208 [0054]
- WO 2000/022026 [0054]
- EP 707020 [0054]
- EP 894107 [0054]
- WO 2006/061181 [0054]
- WO 92/18552 [0054]
- WO 2004/070772 [0054]
- WO 2004/113468 [0054]
- EP 1028136 [0054]
- WO 2005/014689 [0054]
- WO 2004/041901 [0054]
- WO 2004/113412 [0054]
- WO 2005/040302 [0054]
- WO 2005/104264 [0054]
- WO 2007/017066 [0054]
- WO 2005/011013 [0060]
- WO 2004/013080 [0066]
- WO 2006/005627 [0066]
- WO 2005/039246 [0066]
- US 2005/0069729 [0066]
- JP 2004/288381 [0066]
- EP 1205527 [0066]
- WO 2008/086851 [0066]
- WO 2007/063754 [0066, 0066]
- WO 2008/056746 [0066, 0066]
- DE 102009023155 [0066]
- DE 102009031021 [0066]
- EP 1617710 [0066]
- EP 1617711 [0066]
- EP 1731584 [0066]
- JP 2005/347160 [0066]
- WO 2007/137725 [0066]
- WO 2005/111172 [0066]
- WO 2006/117052 [0066]
- WO 2010/015306 [0066]
- DE 102009053382 [0066]
- DE 102009053644 [0066]
- DE 102009053645 [0066]
- EP 652273 [0066]
- WO 2009/062578 [0066]
- WO 2010/054729 [0066]
- WO 2010/054730 [0066]
- DE 102009048791 [0066]
- DE 102009053836 [0066]
- WO 00/70655 [0068]
- WO 01/41512 [0068]
- WO 02/02714 [0068]
- WO 02/15645 [0068]
- EP 1191613 [0068]
- EP 1191612 [0068]
- EP 1191614 [0068]
- WO 05/033244 [0068]
- WO 05/019373 [0068]
- US 2005/0258742 [0068]
- WO 2005/053051 [0070]
- WO 2009/030981 [0070]
- WO 2004/058911 [0096]
- Zitierte Nicht-Patentliteratur
-
- M. A. Baldo et al., Appl. Phys. Lett. 1999, 75, 4–6 [0002]
- Chanda et al., Organometallics 2007, 26(7), 1635–1642 [0048]
- Saito et al., J. Organomet. Chem. 2010, 695(7), 1035–1041 [0050]
- D. M. Koller et al., Nature Photonics 2008, 1–4 [0059]
- M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301 [0077]
Claims (15)
- Neutrale Verbindung gemäß Formel (1) oder Formel (2), wobei für die verwendeten Symbole und Indizes gilt: X ist bei jedem Auftreten gleich oder verschieden BR2, C(R2)2, C=O, Si(R2)2, Ge(R2)2, Sn(R2)2, NR2, O, S, SO, SO2, PR2 oder P(=O)R2; oder X ist für n = 0 eine Gruppe der folgenden Formel (3), Formel (3) A ist C, Si, Ge oder Sn; dabei deuten die gestrichelten Bindungen an A die Bindung an das Triphenylen an; Y ist BR2, O, S, NR2, PR2 oder P(=O)R2; Z ist bei jedem Auftreten gleich oder verschieden CR1 oder N mit der Maßgabe, dass maximal zwei Gruppen Z pro Cyclus für N stehen; R ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 und einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R1 substituiert sein kann; Ar1 ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das mit einem oder mehreren nicht-aromatischen Resten R3 substituiert sein kann; dabei können zwei Reste Ar1, welche an dasselbe N-Atom oder P-Atom binden, auch durch eine Einfachbindung oder eine Brücke, ausgewählt aus N(R4), C(R4)2, O oder S, miteinander verbrückt sein; R1 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D, F, Cl, Br, I, CN, NO2, N(Ar1)2, N(R3)2, C(=O)Ar1, C(=O)R3, P(=O)(Ar1)2, einer geradkettigen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen oder einer verzweigten oder cyclischen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 40 C-Atomen oder einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, wobei die Alkyl-, Alkoxy-, Thioalkyl-, Alkenyl- oder Alkinylgruppe mit einem oder mehreren Resten R3 substituiert sein kann und wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R3C=CR3, C≡C, Si(R3)2, Ge(R3)2, Sn(R3)2, C=O, C=S, C=Se, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S oder CONR3 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann, einer Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die mit einem oder mehreren Resten R3 substituiert sein kann, oder einer Kombination dieser Systeme, wobei optional zwei oder mehr benachbarte Substituenten R1, die an demselben Benzolring gebunden sind, ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können; R2 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus einer geradkettigen Alkylgruppe mit 1 bis 20 C-Atomen oder einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 20 C-Atomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R3C=CR3, C≡C, Si(R3)2, C=O, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S oder CONR3 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei optional zwei Substituenten R2, welche an dasselbe Kohlenstoff-, Silicium-, Germanium- oder Zinnatom binden, ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem miteinander bilden können, das mit einem oder mehreren Resten R3 substituiert sein kann; R3 ist bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D, F, Cl, Br, I, CN, NO2, N(R4)2, C(=O)Ar1, C(=O)R4, P(=O)(Ar1)2, einer geradkettigen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen oder einer verzweigten oder cyclischen Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 40 C-Atomen oder einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, wobei die Alkyl-, Alkoxy-, Thioalkyl-, Alkenyl- oder Alkinylgruppe mit einem oder mehreren Resten R4 substituiert sein kann, wobei eine oder mehrere nicht-benachbarte CH2-Gruppen durch R4C=CR4, C≡C, Si(R4)2, C=O, C=NR4, P(=O)(R4), SO, SO2, NR4, O, S oder CONR4 ersetzt sein können und wobei ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, einem aromatischen oder heteroaromatischen Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R4 substituiert sein kann, einer Aryloxy- oder Heteroaryloxygruppe mit 5 bis 60 aromatischen Ringatomen, die mit einem oder mehreren Resten R4 substituiert sein kann, oder einer Kombination dieser Systeme, wobei optional zwei oder mehr benachbarte Substituenten R3 ein monocyclisches oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können, das mit einem oder mehreren Resten R4 substituiert sein kann; R4 ist ausgewählt aus der Gruppe bestehend aus H, D, F, CN, einem aliphatischem Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, einem aromatischem oder heteroaromatischem Ringsystem mit 5 bis 30 aromatischen Ringatomen, in dem ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder eine Alkylgruppe mit 1 bis 5 C-Atomen ersetzt sein können, wobei zwei oder mehr benachbarte Substituenten R4 miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können; n ist 0 oder 1; mit der Maßgabe, dass mindestens eine Gruppe R1 in Formel (1) für ein aromatisches oder heteroaromatisches Ringsystem steht, wenn X für C=O, O, S, SO oder SO2 steht und n = 0 ist; und weiterhin mit der Maßgabe, dass die folgenden Verbindungen von der Erfindung ausgenommen sind:
- Verbindung nach einem oder mehreren der Ansprüche 1 bis 3, dadurch gekennzeichnet, dass in Verbindungen der Formel (1) mit n = 0 bzw. in Verbindungen gemäß Formel (4) bzw. Formel (4a) X ausgewählt ist aus der Gruppe bestehend aus C(R2)2, Si(R2)2 und N(R2) und R2 gleich oder verschieden bei jedem Auftreten für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen steht, welches jeweils auch durch einen oder mehrere Reste R3 substituiert sein kann und wobei zwei Reste R2 auch miteinander ein aromatisches Ringsystem bilden können; und dass in Verbindungen gemäß Formel (1) mit X = Formel (3) bzw. in Verbindungen gemäß Formel (5) bzw. Formel (5a) die beiden Triphenylenteilstrukturen, die an A binden, jeweils gleich substituiert sind und A für Kohlenstoff oder Silicium steht; und dass in Verbindungen der Formel (1) mit n = 1 bzw. in Verbindungen gemäß Formel (6) bzw. Formel (6a) die Gruppe X-Y-X ausgewählt ist aus der Gruppe bestehend aus C(R2)2-O-C(R2)2, Si(R2)2-O-Si(R2)2, O-BR2-O, O-PR2-O, O-P(=O)R2-O und C(=O)-NR2-C(=O); und dass in Verbindungen gemäß Formel (2) bzw. (7) bzw. (7a) die beiden Reste R gleich sind.
- Verfahren zur Herstellung einer Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 durch Umsetzung von 1,12-Dilithio-triphenylen-Derivaten mit Elektrophilen oder durch Umsetzung von Halogen- oder Amino-substituierten Triphenylen-Derivaten in einer metall-katalysierten Kupplungsreaktion.
- Oligomer, Polymer oder Dendrimer enthaltend eine oder mehrere der Verbindungen nach einem oder mehreren der Ansprüche 1 bis 4, wobei ein oder mehrere Bindungen der Verbindung zum Polymer, Oligomer oder Dendrimer vorhanden sind.
- Verwendung einer Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 oder eines Oligomers, Polymers oder Dendrimers nach Anspruch 6 in einer elektronischen Vorrichtung.
- Elektronische Vorrichtung, bevorzugt ausgewählt aus der Gruppe bestehend aus organischen Elektrolumineszenzvorrichtungen (OLEDs), organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs), organischen Laserdioden (O-Laser) und organic plasmon emitting devices, enthaltend mindestens eine Verbindung nach einem oder mehreren der Anprüche 1 bis 4 oder ein Oligomer, Polymer oder Dendrimer gemäß Anspruch 6.
- Elektronische Vorrichtung nach Anspruch 8, dadurch gekennzeichnet, dass es sich um eine organische Elektrolumineszenzvorrichtung handelt und die Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 als Matrixmaterial für fluoreszierende oder phosphoreszierende Emitter und/oder in einer Lochblockierschicht und/oder in einer Elektronentransportschicht und/oder in einer elektronenblockierenden bzw. exzitonenblockierenden Schicht und/oder in einer Lochtransport- bzw. Lochinjektionsschicht und/oder in einer optischen Auskopplungsschicht eingesetzt wird.
- Organische Elektrolumineszenzvorrichtung nach Anspruch 9, dadurch gekennzeichnet, dass die Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 als Matrixmaterial für phosphoreszierende Emitter verwendet wird und dass mindestens ein Rest R1 für N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 steht oder für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann, wobei die Gruppe Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R3 am aromatischen oder heteroaromatischen Ringsystem keine kondensierten Arylgruppen mit mehr als 10 C-Atomen enthält und keine kondensierten Heteroarylgruppen, in welcher mehr als zwei Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind; und/oder dass in der Verbindung der Formel (2) bzw. Formel (7) bzw. Formel (7a) R gleich oder verschieden bei jedem Auftreten für N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2 oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen steht, welches mit einem oder mehreren Resten R1 substituiert sein kann, wobei die Gruppe Ar1 bzw. die Reste an Ar1 bzw. das aromatische oder heteroaromatische Ringsystem bzw. die Reste R1 am aromatischen oder heteroaromatischen Ringsystem keine kondensierten Arylgruppen mit mehr als 10 C-Atomen enthält und keine kondensierten Heteroarylgruppen, in welcher mehr als zwei Aryl- bzw. 6-Ringheteroarylgruppen direkt aneinander ankondensiert sind.
- Organische Elektrolumineszenzvorrichtung nach Anspruch 10, dadurch gekennzeichnet, dass mindestens ein Rest R1 und/oder R ausgewählt ist aus der Gruppe bestehend aus Phenyl, ortho-, meta- oder para-Biphenyl, ortho-, meta- oder para-Terphenyl, ortho-, meta-, para- oder verzweigtes Quaterphenyl, Fluoren oder Spirobifluoren, welche jeweils durch einen oder mehrere Reste R3 substituiert sein können, und/oder dass mindestens ein Rest R1 und/oder R ausgewählt ist aus den Strukturen der Formeln (8) bis (38), wobei R3 die in Anspruch 1 genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt; und/oder dass mindestens ein Rest R1 und/oder R ausgewählt aus den Strukturen der Formeln (39) bis (41), wobei die verwendeten Symbole die in Anspruch 1 genannten Bedeutungen aufweisen und weiterhin gilt: Ar2 ist gleich oder verschieden bei jedem Auftreten ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, welches mit einem oder mehreren Resten R3 substituiert sein kann; dabei ist die Summe der aromatischen Ringatome aller Gruppen Ar2 zusammen nicht größer als 60; E ist ausgewählt aus der Gruppe bestehend aus C(R4)2, NR4, O oder S.
- Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der Ansprüche 9 bis 11, dadurch gekennzeichnet, dass die Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 als Elektronentransportmaterial verwendet wird und mindestens ein Rest R1 und/oder R für C(=O)Ar1, P(=O)(Ar1)2 oder für ein elektronenarmes heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen steht, welches mit einem oder mehreren Resten R3 substituiert sein kann; und/oder X steht für BR2, C=O, SO, SO2 oder P(=O)(R2)2.
- Organische Elektrolumineszenzvorrichtung nach Anspruch 12, dadurch gekennzeichnet, dass das elektronenarme heteroaromatische Ringsystem R1 und/oder R als Heteroarylgruppe Triazin, Pyrimidin, Pyrazin, Pyridazin, Pyridin, Imidazol, Pyrazol, Oxazol, Oxadiazol, Triazol, Thiazol, Thiadiazol, Benzimidazol, Chinolin, Isochinolin oder Chinoxalin enthält und insbesondere ist ausgewählt aus den Strukturen der Formeln (8) bis (11) gemäß Anspruch 11 oder aus den Formeln (42) bis (45), wobei R3 die in Anspruch 1 genannten Bedeutungen aufweist und die gestrichelte Bindung die Bindung an den Triphenylengrundkörper darstellt.
- Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der Ansprüche 9 bis 13, dadurch gekennzeichnet, dass die Verbindung gemäß einem oder mehreren der Ansprüche 1 bis 4 als Lochtransportmaterial oder als emittierende Verbindung verwendet wird mindestens ein Rest R1 und/oder R für N(Ar1)2, für eine Triarylaminogruppe oder für ein elektronenreiches heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen steht, welches mit einem oder mehreren Resten R3 substituiert sein kann; und/oder X steht für NR2 oder PR2.
- Formulierung enthaltend mindestens eine Verbindung nach einem oder mehreren der Ansprüche 1 bis 4 oder ein oder mehrere Polymere, Oligomere oder Dendrimere nach Anspruch 6 und mindestens eine Lösemittel.
Priority Applications (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102010048608A DE102010048608A1 (de) | 2010-10-15 | 2010-10-15 | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2013533106A JP6022462B2 (ja) | 2010-10-15 | 2011-09-16 | 有機エレクトロルミネッセンス素子のためのトリフェニレン系材料 |
| DE112011103450.4T DE112011103450B4 (de) | 2010-10-15 | 2011-09-16 | Materialien auf Basis von Triphenylen für organische Elektrolumineszenzvorrichtungen, Verfahren zu deren Herstellung, deren Verwendung sowie organische elektronische Vorrichtungen |
| KR1020137012415A KR101959575B1 (ko) | 2010-10-15 | 2011-09-16 | 유기 전계발광 디바이스용 트리페닐렌계 재료 |
| CN201180049846.9A CN103180407B (zh) | 2010-10-15 | 2011-09-16 | 用于有机电致发光器件的基于苯并菲的材料 |
| US13/879,530 US9985226B2 (en) | 2010-10-15 | 2011-09-16 | Triphenylene-based materials for organic electroluminescent devices |
| CN201610674734.7A CN106279229B (zh) | 2010-10-15 | 2011-09-16 | 用于有机电致发光器件的基于苯并菲的材料 |
| PCT/EP2011/004654 WO2012048781A1 (de) | 2010-10-15 | 2011-09-16 | Materialien auf basis von triphenylen für organische elektrolumineszenzvorrichtungen |
| JP2016153780A JP6250754B2 (ja) | 2010-10-15 | 2016-08-04 | 有機エレクトロルミネッセンス素子のためのトリフェニレン系材料 |
| US15/985,120 US10971689B2 (en) | 2010-10-15 | 2018-05-21 | Triphenylene-based materials for organic electroluminescent devices |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102010048608A DE102010048608A1 (de) | 2010-10-15 | 2010-10-15 | Materialien für organische Elektrolumineszenzvorrichtungen |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102010048608A1 true DE102010048608A1 (de) | 2012-04-19 |
Family
ID=44719830
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102010048608A Withdrawn DE102010048608A1 (de) | 2010-10-15 | 2010-10-15 | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE112011103450.4T Active DE112011103450B4 (de) | 2010-10-15 | 2011-09-16 | Materialien auf Basis von Triphenylen für organische Elektrolumineszenzvorrichtungen, Verfahren zu deren Herstellung, deren Verwendung sowie organische elektronische Vorrichtungen |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE112011103450.4T Active DE112011103450B4 (de) | 2010-10-15 | 2011-09-16 | Materialien auf Basis von Triphenylen für organische Elektrolumineszenzvorrichtungen, Verfahren zu deren Herstellung, deren Verwendung sowie organische elektronische Vorrichtungen |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US9985226B2 (de) |
| JP (2) | JP6022462B2 (de) |
| KR (1) | KR101959575B1 (de) |
| CN (2) | CN106279229B (de) |
| DE (2) | DE102010048608A1 (de) |
| WO (1) | WO2012048781A1 (de) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013056776A1 (de) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2013064206A1 (de) | 2011-11-01 | 2013-05-10 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| WO2014067614A1 (de) * | 2012-10-31 | 2014-05-08 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2015099483A1 (ko) * | 2013-12-27 | 2015-07-02 | 주식회사 두산 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| WO2018127465A1 (de) * | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| CN116120581A (zh) * | 2023-02-01 | 2023-05-16 | 重庆师范大学 | 稠杂环基mof材料及其制法与在红光led器件制备中的应用 |
| WO2024104934A1 (de) * | 2022-11-16 | 2024-05-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
Families Citing this family (254)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5825846B2 (ja) * | 2010-09-13 | 2015-12-02 | キヤノン株式会社 | 新規縮合多環化合物およびそれを有する有機発光素子 |
| CA2849087A1 (en) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazole derivatives for organic electroluminescent devices |
| CN103946215B (zh) | 2011-11-17 | 2016-09-28 | 默克专利有限公司 | 螺二氢吖啶衍生物和其作为有机电致发光器件用材料的用途 |
| KR102125199B1 (ko) | 2012-07-23 | 2020-06-22 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| JP2015214490A (ja) * | 2012-08-08 | 2015-12-03 | 保土谷化学工業株式会社 | トリフェニレン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| US9741942B2 (en) | 2012-10-11 | 2017-08-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR102086546B1 (ko) * | 2012-10-19 | 2020-03-10 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| KR102098736B1 (ko) * | 2012-10-19 | 2020-04-09 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| JP6407883B2 (ja) * | 2012-12-14 | 2018-10-17 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| EP2941472B1 (de) | 2013-01-03 | 2018-07-25 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| US20150340627A1 (en) | 2013-01-03 | 2015-11-26 | Merck Patent Gmbh | Materials for electronic devices |
| KR102120891B1 (ko) * | 2013-02-22 | 2020-06-10 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| KR20140135525A (ko) | 2013-05-16 | 2014-11-26 | 제일모직주식회사 | 유기 광전자 소자용 발광 재료, 유기 광전자 소자 및 표시 장치 |
| KR20140135532A (ko) * | 2013-05-16 | 2014-11-26 | 제일모직주식회사 | 유기 화합물, 유기 광전자 소자 및 표시 장치 |
| KR101636858B1 (ko) * | 2013-05-29 | 2016-07-06 | 제일모직 주식회사 | 화합물, 이를 포함하는 유기 광전자 소자 및 상기 유기 광전자 소자를 포함하는 표시장치 |
| KR102162792B1 (ko) * | 2013-06-26 | 2020-10-08 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| KR102135243B1 (ko) * | 2013-07-12 | 2020-07-20 | 삼성디스플레이 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| KR102173044B1 (ko) * | 2013-08-22 | 2020-11-03 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| JPWO2015029354A1 (ja) * | 2013-08-27 | 2017-03-02 | 保土谷化学工業株式会社 | トリフェニレン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| KR101702512B1 (ko) * | 2013-09-04 | 2017-02-03 | 제일모직 주식회사 | 유기 화합물, 유기 광전자 소자 및 표시 장치 |
| US9231217B2 (en) | 2013-11-28 | 2016-01-05 | Semiconductor Energy Laboratory Co., Ltd. | Synthesis method of organometallic complex, synthesis method of pyrazine derivative, 5,6-diaryl-2-pyrazyl triflate, light-emitting element, light-emitting device, electronic device, and lighting device |
| KR101706742B1 (ko) * | 2013-12-09 | 2017-02-15 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| CN113527032A (zh) * | 2014-04-16 | 2021-10-22 | 默克专利有限公司 | 用于电子器件的材料 |
| EP3140302B1 (de) | 2014-05-05 | 2019-08-21 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| JP6556764B2 (ja) | 2014-06-25 | 2019-08-07 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| KR101709379B1 (ko) | 2014-10-01 | 2017-02-23 | 주식회사 엘지화학 | 유기 발광 소자 |
| JP2017537085A (ja) | 2014-11-11 | 2017-12-14 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| US9406892B2 (en) * | 2015-01-07 | 2016-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP6772188B2 (ja) | 2015-02-03 | 2020-10-21 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 金属錯体 |
| JP2018525331A (ja) | 2015-06-10 | 2018-09-06 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| KR102556088B1 (ko) | 2015-06-23 | 2023-07-17 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 |
| CN107922359A (zh) | 2015-07-30 | 2018-04-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| JP6862420B2 (ja) | 2015-08-13 | 2021-04-21 | メルク パテント ゲーエムベーハー | ヘキサメチルインダン |
| JP6786591B2 (ja) | 2015-08-14 | 2020-11-18 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 有機エレクトロルミネッセンス素子のためのフェノキサジン誘導体 |
| EP3368520B1 (de) | 2015-10-27 | 2023-04-26 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| WO2017108152A1 (de) * | 2015-12-21 | 2017-06-29 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR102516579B1 (ko) * | 2016-02-05 | 2023-03-31 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR102851400B1 (ko) | 2016-03-03 | 2025-08-29 | 메르크 파텐트 게엠베하 | 유기 전계 발광 장치용 재료 |
| TWI745361B (zh) | 2016-03-17 | 2021-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| CN108884087A (zh) | 2016-04-11 | 2018-11-23 | 默克专利有限公司 | 包含二苯并呋喃和/或二苯并噻吩结构的杂环化合物 |
| US11228003B2 (en) * | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228002B2 (en) * | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JPWO2017209297A1 (ja) * | 2016-06-02 | 2019-04-18 | 国立大学法人名古屋大学 | トリアリーレン化合物及びその製造方法 |
| US10720587B2 (en) * | 2016-07-19 | 2020-07-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957857B2 (en) | 2016-07-27 | 2021-03-23 | Lg Chem Ltd. | Multicyclic compound and organic light emitting device including the same |
| TW201827425A (zh) | 2016-09-14 | 2018-08-01 | 德商麥克專利有限公司 | 具有咔唑結構之化合物 |
| US11447464B2 (en) | 2016-09-14 | 2022-09-20 | Merck Patent Gmbh | Compounds with spirobifluorene-structures |
| US20200028091A1 (en) | 2016-09-30 | 2020-01-23 | Merck Patent Gmbh | Carbazoles with diazadibenzofurane or diazadibenzothiophene structures |
| TWI766884B (zh) | 2016-09-30 | 2022-06-11 | 德商麥克專利有限公司 | 具有二氮雜二苯并呋喃或二氮雜二苯并噻吩結構的化合物、其製法及其用途 |
| TWI764942B (zh) | 2016-10-10 | 2022-05-21 | 德商麥克專利有限公司 | 電子裝置 |
| DE102017008794A1 (de) | 2016-10-17 | 2018-04-19 | Merck Patent Gmbh | Materialien zur Verwendung in elektronischen Vorrichtungen |
| KR102643057B1 (ko) * | 2016-10-26 | 2024-03-04 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| JP2020512273A (ja) | 2016-11-02 | 2020-04-23 | メルク パテント ゲーエムベーハー | 電子デバイス用材料 |
| JP7073388B2 (ja) | 2016-11-08 | 2022-05-23 | メルク パテント ゲーエムベーハー | 電子デバイスのための化合物 |
| US11345687B2 (en) | 2016-11-09 | 2022-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TWI756292B (zh) | 2016-11-14 | 2022-03-01 | 德商麥克專利有限公司 | 具有受體基團與供體基團之化合物 |
| EP3541890B1 (de) | 2016-11-17 | 2020-10-28 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| TW201833118A (zh) | 2016-11-22 | 2018-09-16 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| TW201829385A (zh) | 2016-11-30 | 2018-08-16 | 德商麥克專利有限公司 | 具有戊內醯胺結構之化合物 |
| KR20190086028A (ko) | 2016-12-05 | 2019-07-19 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| EP3548486B1 (de) | 2016-12-05 | 2021-10-27 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| TW201831468A (zh) | 2016-12-05 | 2018-09-01 | 德商麥克專利有限公司 | 含氮的雜環化合物 |
| KR102504432B1 (ko) | 2016-12-22 | 2023-02-27 | 메르크 파텐트 게엠베하 | 적어도 2종의 유기-기능성 화합물을 포함하는 혼합물 |
| US11261291B2 (en) | 2016-12-22 | 2022-03-01 | Merck Patent Gmbh | Materials for electronic devices |
| TW201833300A (zh) | 2017-01-25 | 2018-09-16 | 德商麥克專利有限公司 | 咔唑衍生物 |
| US11407766B2 (en) | 2017-01-30 | 2022-08-09 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN110291064B (zh) | 2017-02-02 | 2023-04-28 | 默克专利有限公司 | 用于电子器件的材料 |
| TW201835075A (zh) | 2017-02-14 | 2018-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| KR20190126097A (ko) | 2017-03-01 | 2019-11-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스 |
| CN110325524A (zh) | 2017-03-02 | 2019-10-11 | 默克专利有限公司 | 用于有机电子器件的材料 |
| TW201843143A (zh) | 2017-03-13 | 2018-12-16 | 德商麥克專利有限公司 | 含有芳基胺結構之化合物 |
| JP7155142B2 (ja) | 2017-03-15 | 2022-10-18 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス用の材料 |
| CN110573515B (zh) | 2017-04-25 | 2023-07-25 | 默克专利有限公司 | 用于电子器件的化合物 |
| EP3621970B1 (de) | 2017-05-11 | 2021-01-13 | Merck Patent GmbH | Bororganische komplexe für organische elektrolumineszente vorrichtungen |
| KR102592390B1 (ko) | 2017-05-11 | 2023-10-20 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 카르바졸계 바디피스 |
| KR102449219B1 (ko) | 2017-05-17 | 2022-09-30 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| JP2020520970A (ja) | 2017-05-22 | 2020-07-16 | メルク パテント ゲーエムベーハー | 電子デバイス用六環性ヘテロ芳香族化合物 |
| TW201920343A (zh) | 2017-06-21 | 2019-06-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| US11767299B2 (en) | 2017-06-23 | 2023-09-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN110770363A (zh) | 2017-06-26 | 2020-02-07 | 默克专利有限公司 | 均质混合物 |
| TW201920070A (zh) | 2017-06-28 | 2019-06-01 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| TWI779067B (zh) | 2017-07-28 | 2022-10-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| CN118405981A (zh) | 2017-09-08 | 2024-07-30 | 默克专利有限公司 | 用于电子器件的材料 |
| CN111065640B (zh) | 2017-09-12 | 2023-04-18 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR102671945B1 (ko) | 2017-10-06 | 2024-06-03 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| CN108675975A (zh) | 2017-10-17 | 2018-10-19 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR102653073B1 (ko) | 2017-10-24 | 2024-03-29 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| JP7002925B2 (ja) * | 2017-11-13 | 2022-01-20 | 東ソー株式会社 | ジナフトテトラフェニレン化合物を含む有機エレクトロルミネッセンス素子 |
| EP4242286A3 (de) | 2017-11-23 | 2023-10-04 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| TWI838352B (zh) | 2017-11-24 | 2024-04-11 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TWI820057B (zh) | 2017-11-24 | 2023-11-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| KR102638811B1 (ko) | 2017-12-15 | 2024-02-21 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 치환된 방향족 아민 |
| TW201938562A (zh) | 2017-12-19 | 2019-10-01 | 德商麥克專利有限公司 | 雜環化合物 |
| KR20200100699A (ko) | 2017-12-20 | 2020-08-26 | 메르크 파텐트 게엠베하 | 헤테로방향족 화합물 |
| US10428269B2 (en) * | 2017-12-27 | 2019-10-01 | Feng-wen Yen | Indenotriphenylene derivative and organic electroluminescence device using the same |
| TWI811290B (zh) | 2018-01-25 | 2023-08-11 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TW201938761A (zh) | 2018-03-06 | 2019-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| TWI802656B (zh) | 2018-03-06 | 2023-05-21 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| US20210020843A1 (en) | 2018-03-16 | 2021-01-21 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US12522608B2 (en) * | 2018-04-13 | 2026-01-13 | Universal Display Corporation | Host materials for electroluminescent devices |
| JP7322075B2 (ja) | 2018-06-07 | 2023-08-07 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンスデバイス |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3823958B1 (de) | 2018-07-20 | 2023-08-23 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| KR102266042B1 (ko) * | 2018-07-27 | 2021-06-17 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| CN108807712B (zh) * | 2018-08-03 | 2020-08-04 | 上海钥熠电子科技有限公司 | 一种oled顶发光器件及显示装置 |
| KR20210052487A (ko) | 2018-08-28 | 2021-05-10 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| TWI837167B (zh) | 2018-08-28 | 2024-04-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TWI823993B (zh) | 2018-08-28 | 2023-12-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TWI826522B (zh) | 2018-09-12 | 2023-12-21 | 德商麥克專利有限公司 | 電致發光裝置 |
| JP7459065B2 (ja) | 2018-09-12 | 2024-04-01 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンスデバイス用の材料 |
| TW202030902A (zh) | 2018-09-12 | 2020-08-16 | 德商麥克專利有限公司 | 電致發光裝置 |
| US12178124B2 (en) | 2018-09-27 | 2024-12-24 | Merck Kgaa | Compounds that can be used in an organic electronic device as active compounds |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| KR20210088597A (ko) | 2018-10-31 | 2021-07-14 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| EP3877369A1 (de) | 2018-11-05 | 2021-09-15 | Merck Patent GmbH | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| KR20210089205A (ko) | 2018-11-06 | 2021-07-15 | 메르크 파텐트 게엠베하 | Oled 용 유기 전계 발광 재료로서 5,6-디페닐-5,6-디히드로디벤즈[c,e][1,2]아자포스포린 및 6-페닐-6h-디벤조[c,e][1,2]티아진-5,5-디옥사이드 유도체 및 유사한 화합물 |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| CN113195500B (zh) | 2018-11-15 | 2024-05-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| TW202039493A (zh) | 2018-12-19 | 2020-11-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| KR102853461B1 (ko) | 2019-01-16 | 2025-09-02 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| TW202035345A (zh) * | 2019-01-17 | 2020-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| US20220127286A1 (en) | 2019-03-04 | 2022-04-28 | Merck Patent Gmbh | Ligands for nano-sized materials |
| US20220162205A1 (en) | 2019-03-12 | 2022-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20210141593A (ko) | 2019-03-20 | 2021-11-23 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN110437241A (zh) * | 2019-07-03 | 2019-11-12 | 浙江华显光电科技有限公司 | 一种红色磷光主体化合物和使用该化合物的有机发光器件 |
| CN110437242A (zh) * | 2019-07-03 | 2019-11-12 | 浙江华显光电科技有限公司 | 一种红色磷光化合物和使用该化合物的有机电致发光器件 |
| CN110330481B (zh) * | 2019-07-03 | 2022-04-08 | 浙江华显光电科技有限公司 | 一种红色磷光化合物和使用该化合物的有机发光器件 |
| CN114222738B (zh) | 2019-08-26 | 2024-05-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| US12108665B2 (en) | 2019-09-02 | 2024-10-01 | Merck Kgaa | Materials for organic electroluminescent devices |
| TW202122558A (zh) | 2019-09-03 | 2021-06-16 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| EP4031546A1 (de) | 2019-09-16 | 2022-07-27 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| CN114401945A (zh) | 2019-09-20 | 2022-04-26 | 默克专利有限公司 | 作为用于电子器件的材料的迫位缩合杂环化合物 |
| KR102413615B1 (ko) * | 2019-09-25 | 2022-06-27 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| CN114641482A (zh) | 2019-11-04 | 2022-06-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| TW202134252A (zh) | 2019-11-12 | 2021-09-16 | 德商麥克專利有限公司 | 有機電致發光裝置用材料 |
| TW202136471A (zh) | 2019-12-17 | 2021-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置用的材料 |
| JP7620631B2 (ja) | 2019-12-18 | 2025-01-23 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のための芳香族化合物 |
| KR20220116008A (ko) | 2019-12-19 | 2022-08-19 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 다환 화합물 |
| CN115052865A (zh) | 2020-01-29 | 2022-09-13 | 默克专利有限公司 | 苯并咪唑衍生物 |
| EP4110884B1 (de) | 2020-02-25 | 2024-11-20 | Merck Patent GmbH | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20220154751A (ko) | 2020-03-17 | 2022-11-22 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| EP4126884B1 (de) | 2020-03-23 | 2025-07-09 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20220158017A (ko) | 2020-03-24 | 2022-11-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| US20230157171A1 (en) | 2020-03-26 | 2023-05-18 | Merck Patent Gmbh | Cyclic compounds for organic electroluminescent devices |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US20230183269A1 (en) | 2020-04-06 | 2023-06-15 | Merck Patent Gmbh | Polycyclic compounds for organic electroluminescent devices |
| US20230234937A1 (en) | 2020-06-18 | 2023-07-27 | Merck Patent Gmbh | Indenoazanaphthalenes |
| CN115916794A (zh) | 2020-06-29 | 2023-04-04 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| JP2023531470A (ja) | 2020-06-29 | 2023-07-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のためのヘテロ芳香族化合物 |
| WO2022017997A1 (en) | 2020-07-22 | 2022-01-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4192832A1 (de) | 2020-08-06 | 2023-06-14 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US12433160B2 (en) | 2020-08-18 | 2025-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4200289A1 (de) | 2020-08-19 | 2023-06-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| TW202229215A (zh) | 2020-09-30 | 2022-08-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置功能層之結構化的化合物 |
| TW202222748A (zh) | 2020-09-30 | 2022-06-16 | 德商麥克專利有限公司 | 用於結構化有機電致發光裝置的功能層之化合物 |
| EP4229145B1 (de) | 2020-10-16 | 2025-07-23 | Merck Patent GmbH | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| US20230389423A1 (en) | 2020-10-16 | 2023-11-30 | Merck Patent Gmbh | Heterocyclic compounds for organic electroluminescent devices |
| CN112625032B (zh) * | 2020-10-19 | 2022-12-09 | 宁波卢米蓝新材料有限公司 | 一种有机化合物及其应用 |
| EP4244228A1 (de) | 2020-11-10 | 2023-09-20 | Merck Patent GmbH | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20230116023A (ko) | 2020-12-02 | 2023-08-03 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| CN112225727B (zh) * | 2020-12-17 | 2021-03-26 | 南京高光半导体材料有限公司 | 一种稠环化合物及有机电致发光器件 |
| EP4263746B1 (de) | 2020-12-18 | 2025-10-01 | Merck Patent GmbH | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| US20240124769A1 (en) | 2020-12-18 | 2024-04-18 | Merck Patent Gmbh | Nitrogenous compounds for organic electroluminescent devices |
| KR20230122094A (ko) | 2020-12-18 | 2023-08-22 | 메르크 파텐트 게엠베하 | Oled에 사용하기 위한 청색 형광 방출체로서의 인돌로[3.2.1-jk]카르바졸-6-카르보니트릴유도체 |
| EP4274827A1 (de) * | 2021-01-05 | 2023-11-15 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| US20220263031A1 (en) * | 2021-02-02 | 2022-08-18 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compound, a plurality of host materials, and organic electroluminescent device comprising the same |
| CN112961145B (zh) * | 2021-02-19 | 2022-12-09 | 南京高光半导体材料有限公司 | 一种化合物及有机电致发光器件 |
| US20240188429A1 (en) | 2021-03-02 | 2024-06-06 | Merck Patent Gmbh | Compounds for organic electroluminescent devices |
| KR20230158657A (ko) | 2021-03-18 | 2023-11-21 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 헤테로방향족 화합물 |
| CN117279902A (zh) | 2021-04-29 | 2023-12-22 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR20240005782A (ko) | 2021-04-29 | 2024-01-12 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| DE112022003409A5 (de) | 2021-07-06 | 2024-05-23 | MERCK Patent Gesellschaft mit beschränkter Haftung | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR20240075888A (ko) | 2021-09-28 | 2024-05-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| KR20240075872A (ko) | 2021-09-28 | 2024-05-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| CN118159623A (zh) | 2021-10-27 | 2024-06-07 | 默克专利有限公司 | 用于有机电致发光器件的含硼和氮的杂环化合物 |
| EP4437814A1 (de) | 2021-11-25 | 2024-10-02 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| EP4448527A1 (de) | 2021-12-13 | 2024-10-23 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20240128020A (ko) | 2021-12-21 | 2024-08-23 | 메르크 파텐트 게엠베하 | 중수소화 유기 화합물의 제조 방법 |
| KR102837128B1 (ko) * | 2021-12-23 | 2025-07-21 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기발광소자 |
| US20250163035A1 (en) | 2022-02-09 | 2025-05-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US20250160204A1 (en) | 2022-02-14 | 2025-05-15 | Merck Patent Gmbh | Materials for electronic devices |
| CN118696106A (zh) | 2022-02-23 | 2024-09-24 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| EP4482843A1 (de) | 2022-02-23 | 2025-01-01 | Merck Patent GmbH | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN114671799B (zh) * | 2022-03-24 | 2024-11-15 | 南京高光半导体材料有限公司 | 一种杂环化合物及有机电致发光器件 |
| EP4519383B1 (de) | 2022-05-06 | 2026-01-14 | Merck Patent GmbH | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4526279A1 (de) | 2022-05-18 | 2025-03-26 | Merck Patent GmbH | Verfahren zur herstellung von deuterierten organischen verbindungen |
| CN119325756A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的杂环化合物 |
| CN119325755A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的有机杂环化合物 |
| EP4544888A1 (de) | 2022-06-24 | 2025-04-30 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| EP4544889A1 (de) | 2022-06-24 | 2025-04-30 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| KR20250037489A (ko) | 2022-07-11 | 2025-03-17 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| CN119894856A (zh) | 2022-09-22 | 2025-04-25 | 默克专利有限公司 | 用于有机电致发光器件的含氮化合物 |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120152954A (zh) | 2022-11-01 | 2025-06-13 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| CN115626914B (zh) * | 2022-11-04 | 2024-04-30 | 冠能光电材料(深圳)有限责任公司 | 一种咔唑类化合物及其应用 |
| WO2024105066A1 (en) * | 2022-11-17 | 2024-05-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024121133A1 (de) | 2022-12-08 | 2024-06-13 | Merck Patent Gmbh | Organische elektronische vorrichtung und spezielle materialien für organische elektronische vorrichtungen |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120569385A (zh) | 2023-01-17 | 2025-08-29 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| WO2024170605A1 (en) | 2023-02-17 | 2024-08-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| EP4683925A1 (de) | 2023-03-20 | 2026-01-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| WO2024251699A1 (de) | 2023-06-07 | 2024-12-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| CN121264197A (zh) | 2023-06-12 | 2026-01-02 | 默克专利有限公司 | 用于光电器件的有机杂环化合物 |
| WO2025003084A1 (de) | 2023-06-28 | 2025-01-02 | Merck Patent Gmbh | Dicyanoarylverbindungen für organische elektrolumineszenzvorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025012253A1 (en) | 2023-07-12 | 2025-01-16 | Merck Patent Gmbh | Materials for electronic devices |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045816A1 (en) | 2023-08-29 | 2025-03-06 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045935A1 (de) | 2023-08-31 | 2025-03-06 | Merck Patent Gmbh | Cyanogruppen-enthaltende aromaten für organische elektrolumineszenzvorrichtungen |
| WO2025073675A1 (en) | 2023-10-04 | 2025-04-10 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2025104058A1 (de) | 2023-11-16 | 2025-05-22 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025119821A1 (en) | 2023-12-05 | 2025-06-12 | Merck Patent Gmbh | Material composition for organic electroluminescent devices |
| WO2025125167A1 (de) | 2023-12-11 | 2025-06-19 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025132547A1 (en) | 2023-12-21 | 2025-06-26 | Merck Patent Gmbh | Mechanochemical method for deuterating organic compounds |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| CN117946044A (zh) * | 2023-12-28 | 2024-04-30 | 南京高光半导体材料有限公司 | 一种带有苯并菲并呋喃基团的胺基化合物及有机发光器件 |
| WO2025168515A1 (de) | 2024-02-06 | 2025-08-14 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025195961A1 (de) | 2024-03-19 | 2025-09-25 | Merck Patent Gmbh | Organische lichtemittierende vorrichtungen |
| WO2025196145A1 (en) | 2024-03-22 | 2025-09-25 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2025210013A1 (de) | 2024-04-04 | 2025-10-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen, insbesondere verbindungen für oleds |
| WO2025228800A1 (de) | 2024-04-30 | 2025-11-06 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026017612A1 (en) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Organic light-emitting device |
| WO2026017611A1 (en) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Organic light emitting device |
| WO2026017608A1 (de) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026017607A1 (en) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Organic light-emitting device |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
Citations (64)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| JP2005071983A (ja) | 2003-08-04 | 2005-03-17 | Fuji Photo Film Co Ltd | 有機電界発光素子 |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| WO2005053051A1 (de) | 2003-11-25 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006038709A1 (ja) | 2004-10-05 | 2006-04-13 | National University Corporation Gunma University | トリフェニレン化合物、その製造方法、およびそれを用いた有機電界発光素子 |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009030981A2 (en) | 2006-12-28 | 2009-03-12 | Universal Display Corporation | Long lifetime phosphorescent organic light emitting device (oled) structures |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053645A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtung |
| DE102009053836A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5077142A (en) | 1989-04-20 | 1991-12-31 | Ricoh Company, Ltd. | Electroluminescent devices |
| US7250226B2 (en) * | 2001-08-31 | 2007-07-31 | Nippon Hoso Kyokai | Phosphorescent compound, a phosphorescent composition and an organic light-emitting device |
| JP4574936B2 (ja) * | 2001-08-31 | 2010-11-04 | 日本放送協会 | 燐光発光性化合物及び燐光発光性組成物 |
| US7282275B2 (en) * | 2002-04-19 | 2007-10-16 | 3M Innovative Properties Company | Materials for organic electronic devices |
| TWI314947B (en) * | 2002-04-24 | 2009-09-21 | Eastman Kodak Compan | Organic light emitting diode devices with improved operational stability |
| JP2004018665A (ja) | 2002-06-17 | 2004-01-22 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料及びそれを使用した有機エレクトロルミネッセンス素子 |
| TW593624B (en) * | 2002-10-16 | 2004-06-21 | Univ Tsinghua | Aromatic compounds and organic LED |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| DE102004008304A1 (de) | 2004-02-20 | 2005-09-08 | Covion Organic Semiconductors Gmbh | Organische elektronische Vorrichtungen |
| TW200613515A (en) | 2004-06-26 | 2006-05-01 | Merck Patent Gmbh | Compounds for organic electronic devices |
| DE102004031000A1 (de) | 2004-06-26 | 2006-01-12 | Covion Organic Semiconductors Gmbh | Organische Elektrolumineszenzvorrichtungen |
| EP1655359A1 (de) | 2004-11-06 | 2006-05-10 | Covion Organic Semiconductors GmbH | Organische Elektrolumineszenzvorrichtung |
| TW200639140A (en) | 2004-12-01 | 2006-11-16 | Merck Patent Gmbh | Compounds for organic electronic devices |
| JP5541859B2 (ja) * | 2005-03-14 | 2014-07-09 | チバ ホールディング インコーポレーテッド | 新規ポリマー |
| WO2006108497A1 (de) | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| DE102005023437A1 (de) | 2005-05-20 | 2006-11-30 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| CN101203583A (zh) * | 2005-05-31 | 2008-06-18 | 通用显示公司 | 发射磷光的二极管中的苯并[9,10]菲基质 |
| JP4029897B2 (ja) * | 2005-10-19 | 2008-01-09 | ソニー株式会社 | ジベンゾアントラセン誘導体、有機電界発光素子、および表示装置 |
| DE102005058543A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| CN101360732A (zh) * | 2006-01-25 | 2009-02-04 | 株式会社德山 | 色烯化合物 |
| US8123987B2 (en) | 2006-01-25 | 2012-02-28 | Tokuyama Corporation | Chromene compounds |
| CN101379110A (zh) * | 2006-02-10 | 2009-03-04 | 西巴控股有限公司 | 新颖聚合物 |
| JP5553993B2 (ja) * | 2006-02-10 | 2014-07-23 | チバ ホールディング インコーポレーテッド | 新規ポリマー |
| DE102006015183A1 (de) | 2006-04-01 | 2007-10-04 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP5317414B2 (ja) | 2006-04-20 | 2013-10-16 | キヤノン株式会社 | ジベンゾアントラセン化合物およびそれを有する有機発光素子 |
| DE102006025846A1 (de) | 2006-06-02 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006031990A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2185532B1 (de) | 2007-08-08 | 2016-11-09 | Universal Display Corporation | Benzokondensierte thiophenverbindungen mit einer triphenylengruppe |
| EP3424918A1 (de) * | 2007-08-08 | 2019-01-09 | Universal Display Corporation | Einzeltriphenylenchromophore in phosphoreszenten leuchtdioden |
| US8628862B2 (en) | 2007-09-20 | 2014-01-14 | Basf Se | Electroluminescent device |
| DE102008008953B4 (de) | 2008-02-13 | 2019-05-09 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| KR101703034B1 (ko) * | 2008-07-18 | 2017-02-06 | 유디씨 아일랜드 리미티드 | 전자 용품을 위한 아자피렌 |
| DE102008035413A1 (de) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| JP2010135406A (ja) * | 2008-12-02 | 2010-06-17 | Mitsui Chemicals Inc | 有機トランジスタ |
| DE102009005746A1 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| TWI541234B (zh) * | 2009-05-12 | 2016-07-11 | 環球展覽公司 | 用於有機發光二極體之2-氮雜聯伸三苯材料 |
| DE102009034625A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2363398B1 (de) * | 2010-03-01 | 2017-10-18 | Semiconductor Energy Laboratory Co., Ltd. | Heterocyclische Verbindung, lichtemittierendes Element, lichtemittierende Vorrichtung, elektronische Vorrichtung und Beleuchtungsvorrichtung |
| US8968887B2 (en) | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| JP5825846B2 (ja) | 2010-09-13 | 2015-12-02 | キヤノン株式会社 | 新規縮合多環化合物およびそれを有する有機発光素子 |
-
2010
- 2010-10-15 DE DE102010048608A patent/DE102010048608A1/de not_active Withdrawn
-
2011
- 2011-09-16 CN CN201610674734.7A patent/CN106279229B/zh active Active
- 2011-09-16 KR KR1020137012415A patent/KR101959575B1/ko active Active
- 2011-09-16 CN CN201180049846.9A patent/CN103180407B/zh active Active
- 2011-09-16 JP JP2013533106A patent/JP6022462B2/ja active Active
- 2011-09-16 WO PCT/EP2011/004654 patent/WO2012048781A1/de not_active Ceased
- 2011-09-16 US US13/879,530 patent/US9985226B2/en active Active
- 2011-09-16 DE DE112011103450.4T patent/DE112011103450B4/de active Active
-
2016
- 2016-08-04 JP JP2016153780A patent/JP6250754B2/ja active Active
-
2018
- 2018-05-21 US US15/985,120 patent/US10971689B2/en active Active
Patent Citations (66)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| JP2005071983A (ja) | 2003-08-04 | 2005-03-17 | Fuji Photo Film Co Ltd | 有機電界発光素子 |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005039246A1 (ja) | 2003-09-30 | 2005-04-28 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、照明装置、表示装置 |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| WO2005053051A1 (de) | 2003-11-25 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006038709A1 (ja) | 2004-10-05 | 2006-04-13 | National University Corporation Gunma University | トリフェニレン化合物、その製造方法、およびそれを用いた有機電界発光素子 |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2009030981A2 (en) | 2006-12-28 | 2009-03-12 | Universal Display Corporation | Long lifetime phosphorescent organic light emitting device (oled) structures |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009053644A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053645A1 (de) | 2009-11-17 | 2011-05-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtung |
| DE102009053836A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
Non-Patent Citations (5)
| Title |
|---|
| Chanda et al., Organometallics 2007, 26(7), 1635-1642 |
| D. M. Koller et al., Nature Photonics 2008, 1-4 |
| M. A. Baldo et al., Appl. Phys. Lett. 1999, 75, 4-6 |
| M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301 |
| Saito et al., J. Organomet. Chem. 2010, 695(7), 1035-1041 |
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013056776A1 (de) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2013064206A1 (de) | 2011-11-01 | 2013-05-10 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| CN104756275B (zh) * | 2012-10-31 | 2017-03-08 | 默克专利有限公司 | 电子器件 |
| CN104756275A (zh) * | 2012-10-31 | 2015-07-01 | 默克专利有限公司 | 电子器件 |
| KR20150079911A (ko) * | 2012-10-31 | 2015-07-08 | 메르크 파텐트 게엠베하 | 전자 디바이스 |
| WO2014067614A1 (de) * | 2012-10-31 | 2014-05-08 | Merck Patent Gmbh | Elektronische vorrichtung |
| US9831441B2 (en) | 2012-10-31 | 2017-11-28 | Merck Patent Gmbh | Electronic device |
| KR101963104B1 (ko) * | 2012-10-31 | 2019-03-28 | 메르크 파텐트 게엠베하 | 전자 디바이스 |
| WO2015099483A1 (ko) * | 2013-12-27 | 2015-07-02 | 주식회사 두산 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20150076602A (ko) * | 2013-12-27 | 2015-07-07 | 주식회사 두산 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| WO2018127465A1 (de) * | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US11495751B2 (en) | 2017-01-04 | 2022-11-08 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2024104934A1 (de) * | 2022-11-16 | 2024-05-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| CN116120581A (zh) * | 2023-02-01 | 2023-05-16 | 重庆师范大学 | 稠杂环基mof材料及其制法与在红光led器件制备中的应用 |
| CN116120581B (zh) * | 2023-02-01 | 2024-06-04 | 重庆师范大学 | 稠杂环基mof材料及其制法与在红光led器件制备中的应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017025067A (ja) | 2017-02-02 |
| US9985226B2 (en) | 2018-05-29 |
| KR101959575B1 (ko) | 2019-03-18 |
| US10971689B2 (en) | 2021-04-06 |
| CN103180407A (zh) | 2013-06-26 |
| JP2014504257A (ja) | 2014-02-20 |
| DE112011103450A5 (de) | 2013-08-14 |
| US20130200359A1 (en) | 2013-08-08 |
| US20180269411A1 (en) | 2018-09-20 |
| JP6250754B2 (ja) | 2017-12-20 |
| CN106279229A (zh) | 2017-01-04 |
| JP6022462B2 (ja) | 2016-11-09 |
| CN103180407B (zh) | 2016-09-07 |
| CN106279229B (zh) | 2018-08-31 |
| DE112011103450B4 (de) | 2023-04-27 |
| KR20140009981A (ko) | 2014-01-23 |
| WO2012048781A1 (de) | 2012-04-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE112011103450B4 (de) | Materialien auf Basis von Triphenylen für organische Elektrolumineszenzvorrichtungen, Verfahren zu deren Herstellung, deren Verwendung sowie organische elektronische Vorrichtungen | |
| EP2344607B1 (de) | Organische elektrolumineszenzvorrichtungen | |
| EP2344609B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP2828266B1 (de) | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen | |
| DE102010019306B4 (de) | Organische Elektrolumineszenzvorrichtungen | |
| DE112010004381B4 (de) | Materialien für elektronische Vorrichtungen | |
| DE102010012738A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| DE102009048791A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP3107977B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| DE102009053836A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| DE102009022858A1 (de) | Organische Elektrolumineszenzvorrichtungen | |
| DE102010033548A1 (de) | Materialien für elektronische Vorrichtungen | |
| DE102009053645A1 (de) | Materialien für organische Elektrolumineszenzvorrichtung | |
| WO2011160757A1 (de) | Materialien für elektronische vorrichtungen | |
| DE102010005697A1 (de) | Verbindungen für elektronische Vorrichtungen | |
| EP2780325A1 (de) | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen | |
| EP2794619B1 (de) | Verbindungen für organische elektrolumineszenzvorrichtungen | |
| EP3130015A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP3110796B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| DE102010013806A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP3016952A1 (de) | Spirokondensierte lact amverbi ndungen für organische elektrolumineszenzvorrichtungen | |
| EP3218368A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| DE102012000064A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| WO2011157346A1 (de) | Verbindungen für elektronische vorrichtungen | |
| WO2011085781A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| R118 | Application deemed withdrawn due to claim for domestic priority |
Effective date: 20130415 |