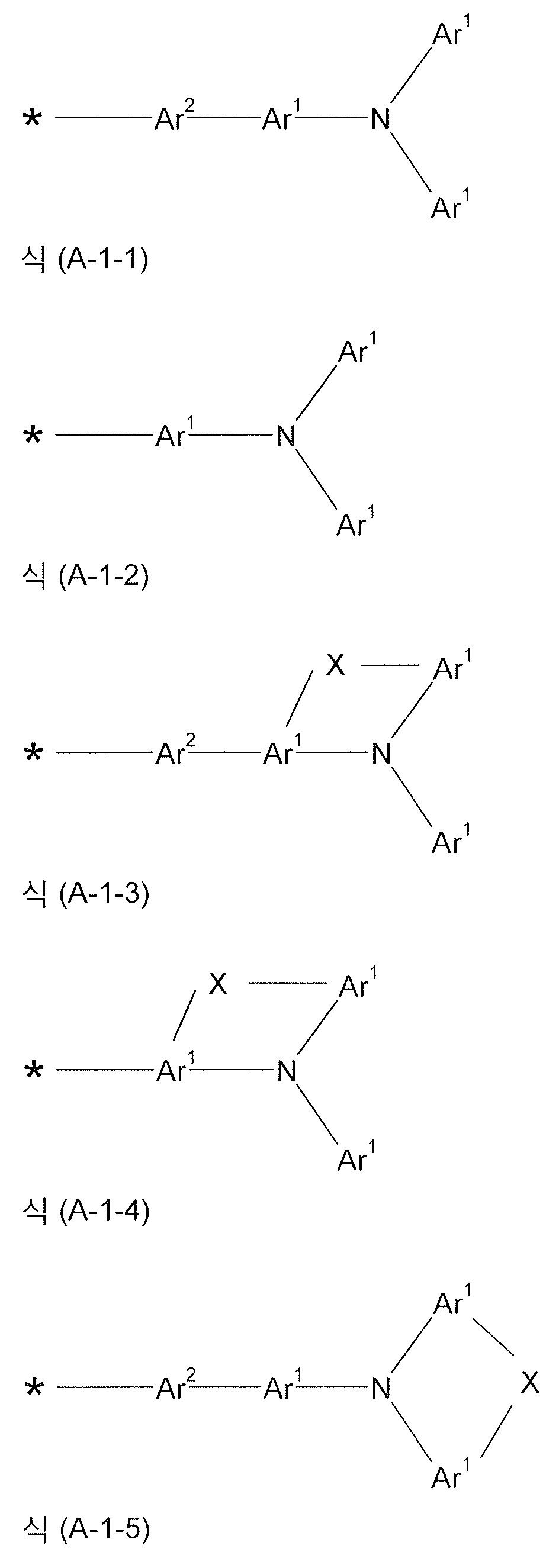KR101963104B1 - 전자 디바이스 - Google Patents
전자 디바이스 Download PDFInfo
- Publication number
- KR101963104B1 KR101963104B1 KR1020157014254A KR20157014254A KR101963104B1 KR 101963104 B1 KR101963104 B1 KR 101963104B1 KR 1020157014254 A KR1020157014254 A KR 1020157014254A KR 20157014254 A KR20157014254 A KR 20157014254A KR 101963104 B1 KR101963104 B1 KR 101963104B1
- Authority
- KR
- South Korea
- Prior art keywords
- groups
- radicals
- substituted
- atoms
- aromatic ring
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- QBLDHQQJEWVUSG-UHFFFAOYSA-N Brc1cccc2c1[o]c1c2cccc1-c(cc1c2c3cccc2)ccc1[n]3-c1ccccc1 Chemical compound Brc1cccc2c1[o]c1c2cccc1-c(cc1c2c3cccc2)ccc1[n]3-c1ccccc1 QBLDHQQJEWVUSG-UHFFFAOYSA-N 0.000 description 1
- QINHFBADADCYKA-UHFFFAOYSA-N OS(c(cc1)ccc1N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c1cccc2c1[o]c1c2cccc1-c(cc1c2c3cccc2)ccc1[n]3-c1ccccc1)O Chemical compound OS(c(cc1)ccc1N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c1cccc2c1[o]c1c2cccc1-c(cc1c2c3cccc2)ccc1[n]3-c1ccccc1)O QINHFBADADCYKA-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/57—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton
- C07C211/61—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton with at least one of the condensed ring systems formed by three or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C225/00—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones
- C07C225/22—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
- C07D311/80—Dibenzopyrans; Hydrogenated dibenzopyrans
- C07D311/82—Xanthenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D495/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
- C07F7/0814—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring said ring is substituted at a C ring atom by Si
-
- H01L51/0059—
-
- H01L51/0072—
-
- H01L51/0073—
-
- H01L51/0074—
-
- H01L51/5012—
-
- H01L51/5056—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/065—Light sources therefor
- A61N2005/0651—Diodes
- A61N2005/0653—Organic light emitting diodes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/06—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members
- C07C2603/08—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing three- or four-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/06—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members
- C07C2603/10—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings
- C07C2603/12—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings only one five-membered ring
- C07C2603/18—Fluorenes; Hydrogenated fluorenes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
- H10K50/155—Hole transporting layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/81—Anodes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/82—Cathodes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Radiology & Medical Imaging (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pathology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Furan Compounds (AREA)
- Pyrane Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
Description
Claims (16)
- 애노드, 캐소드 및 적어도 하나의 유기층을 포함하는 전자 디바이스로서,
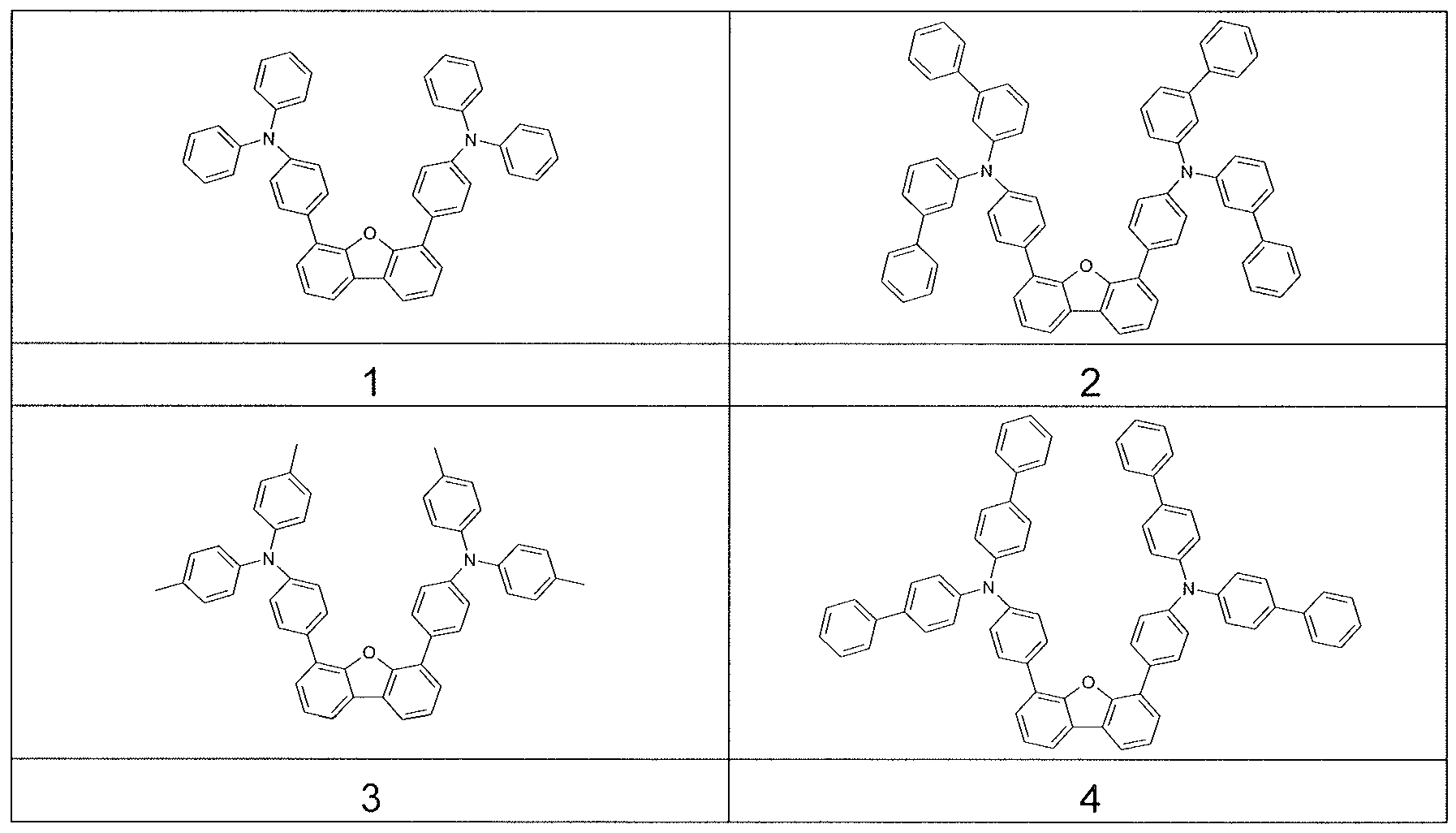
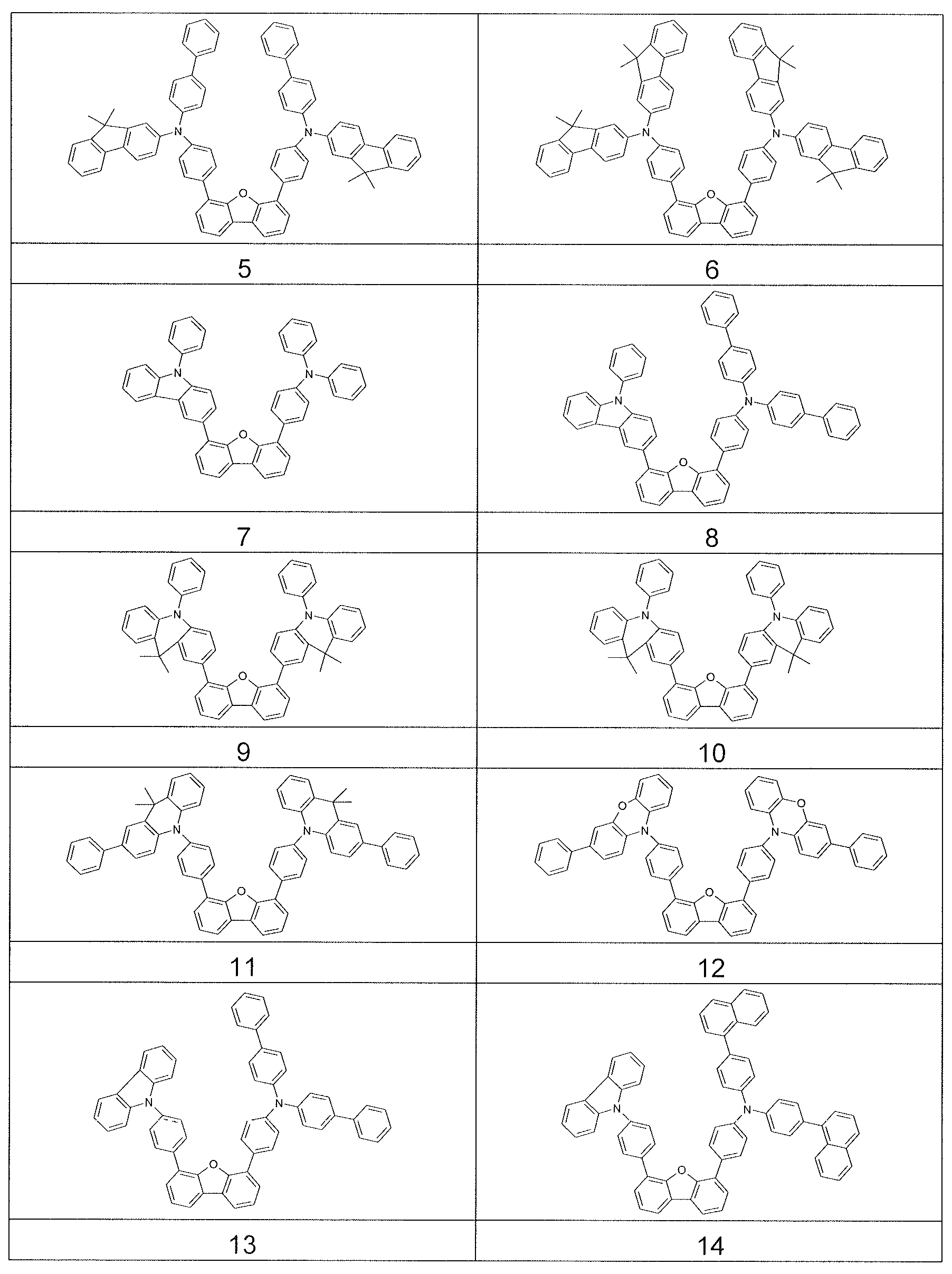
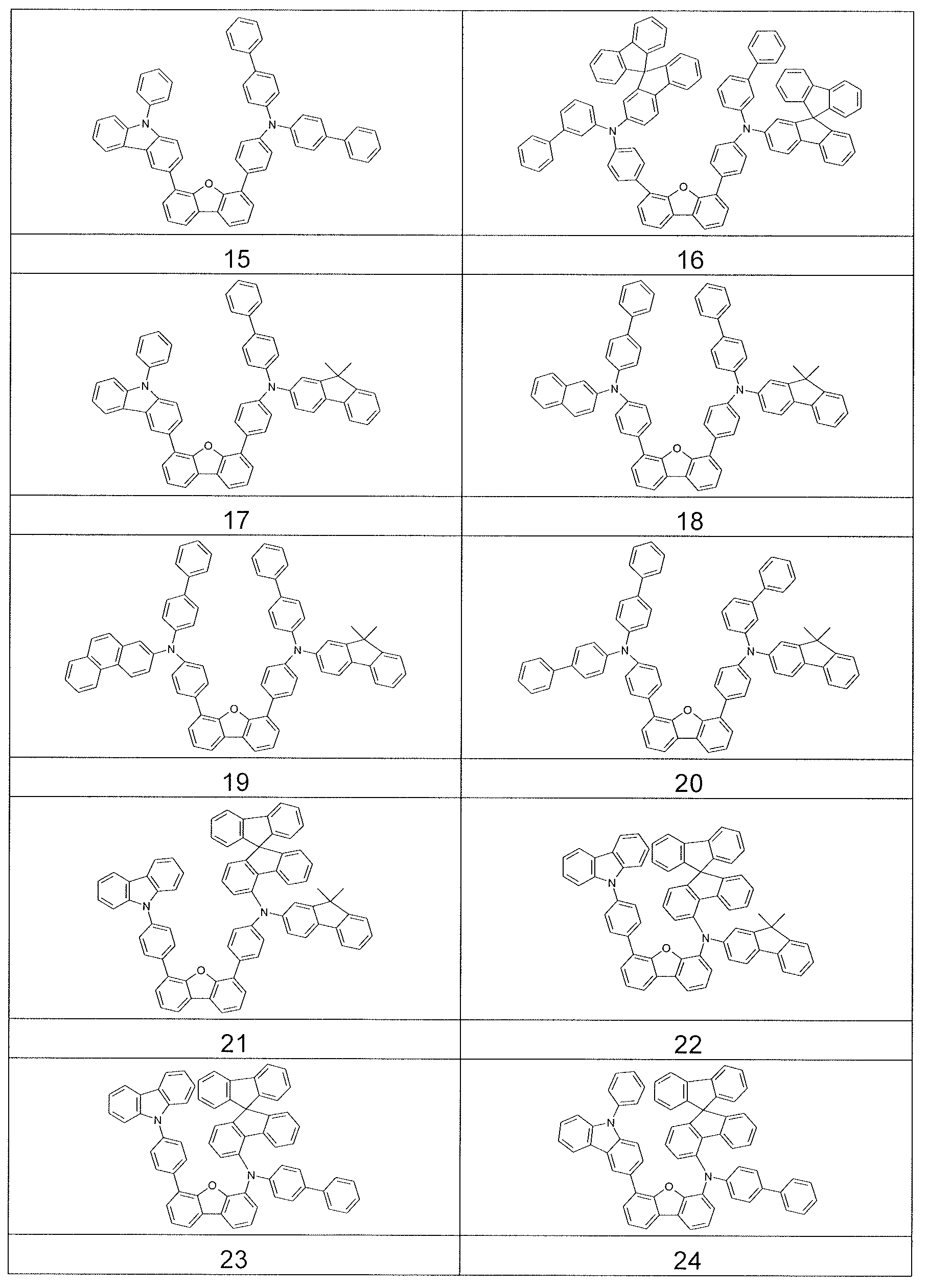
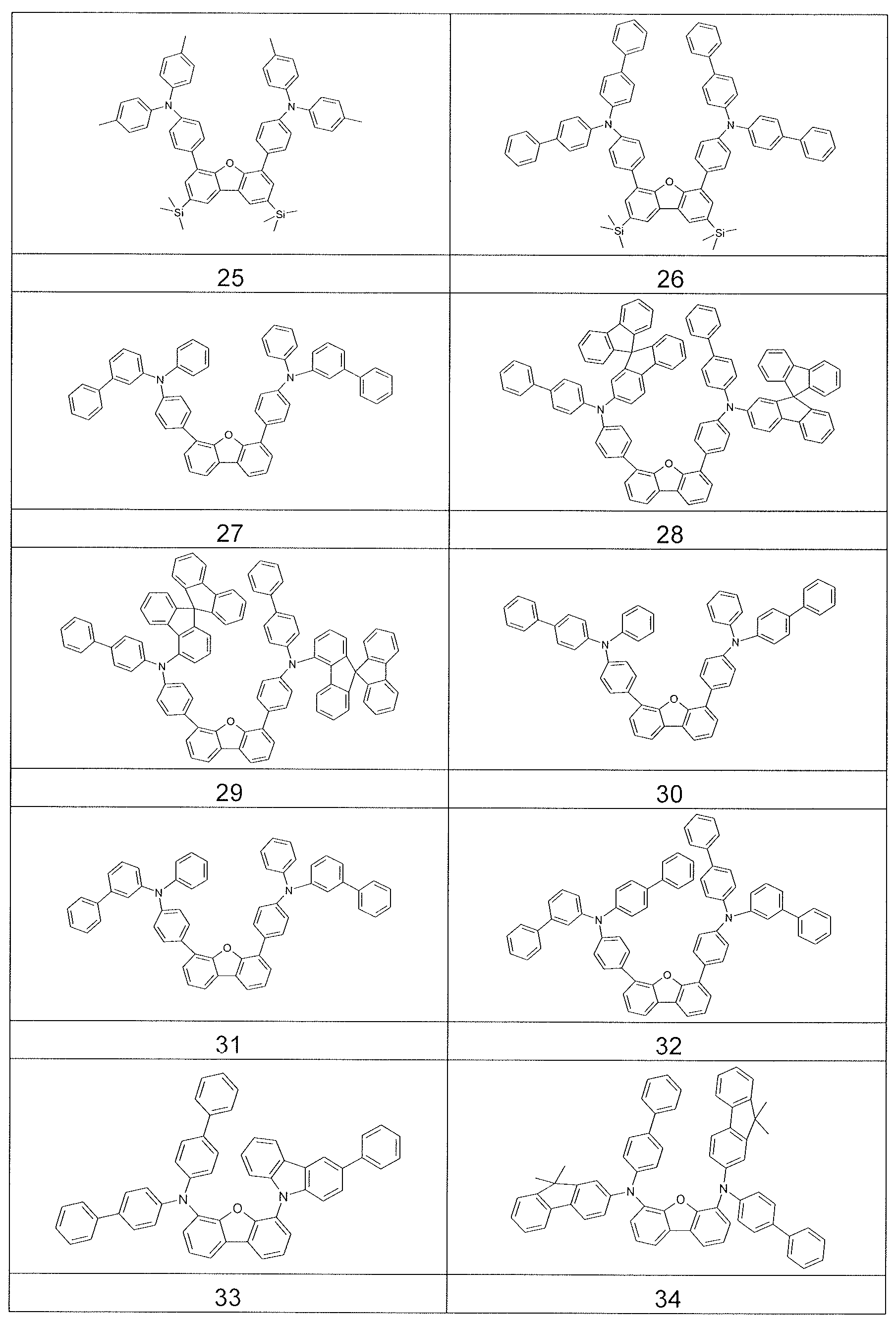
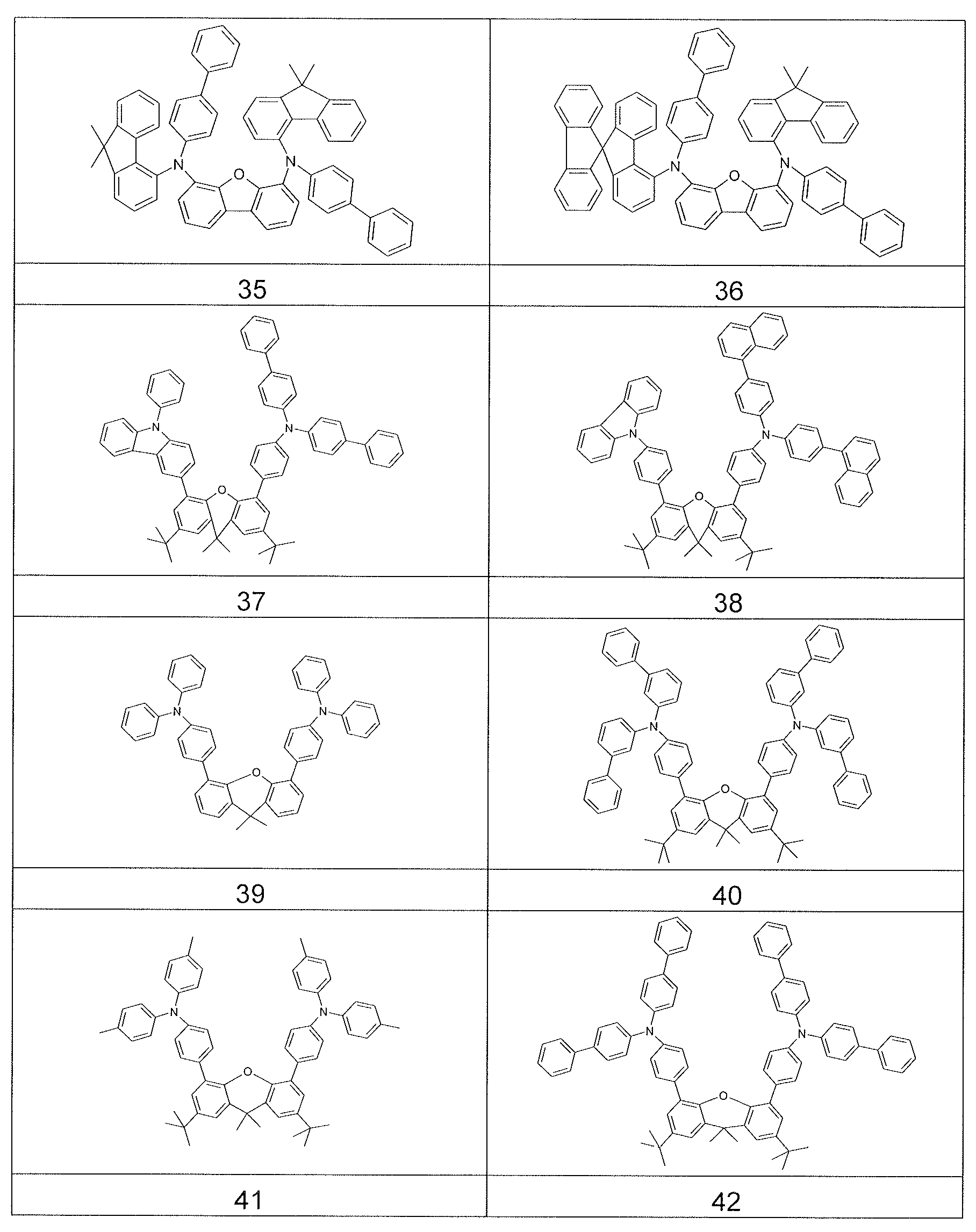
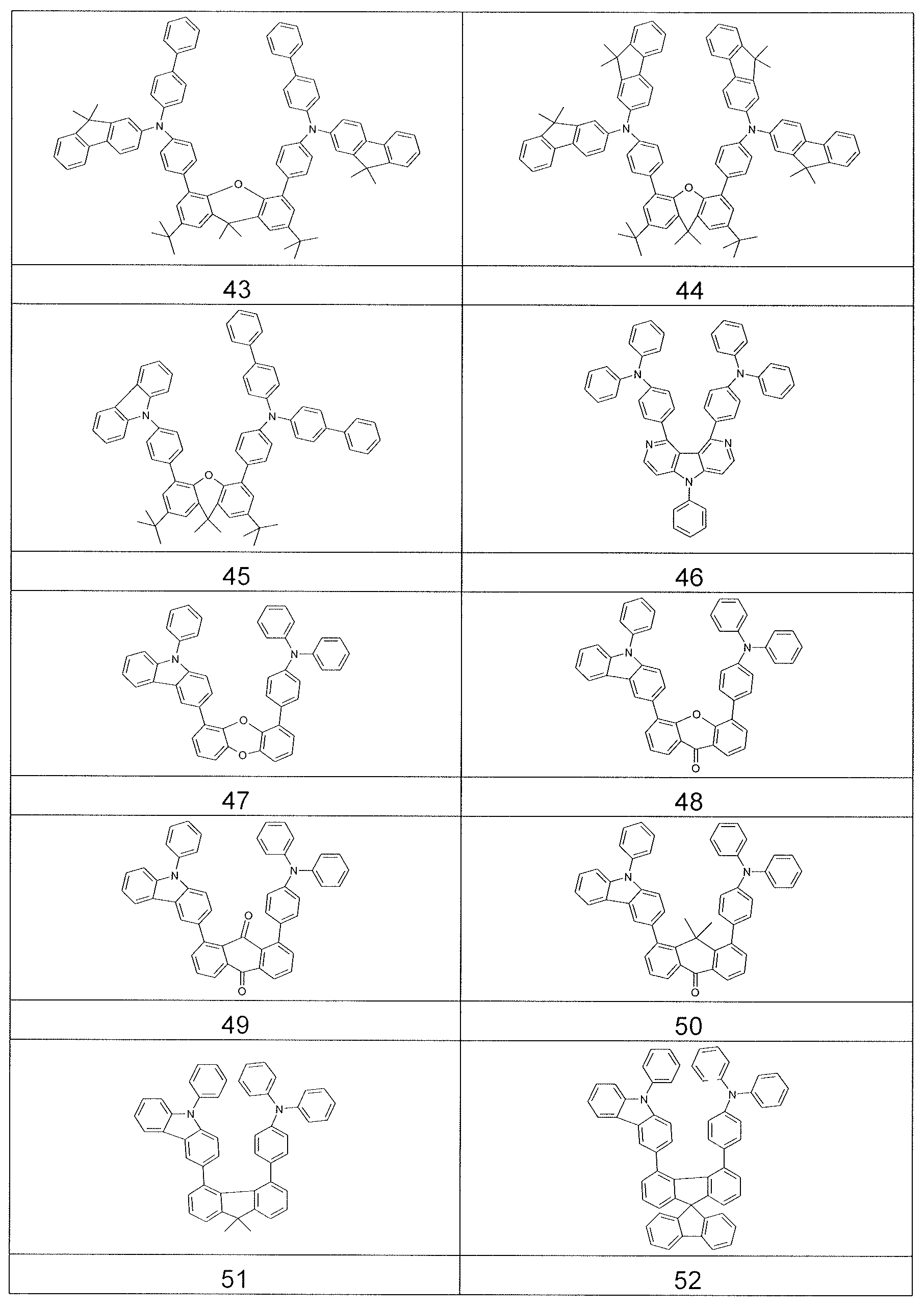
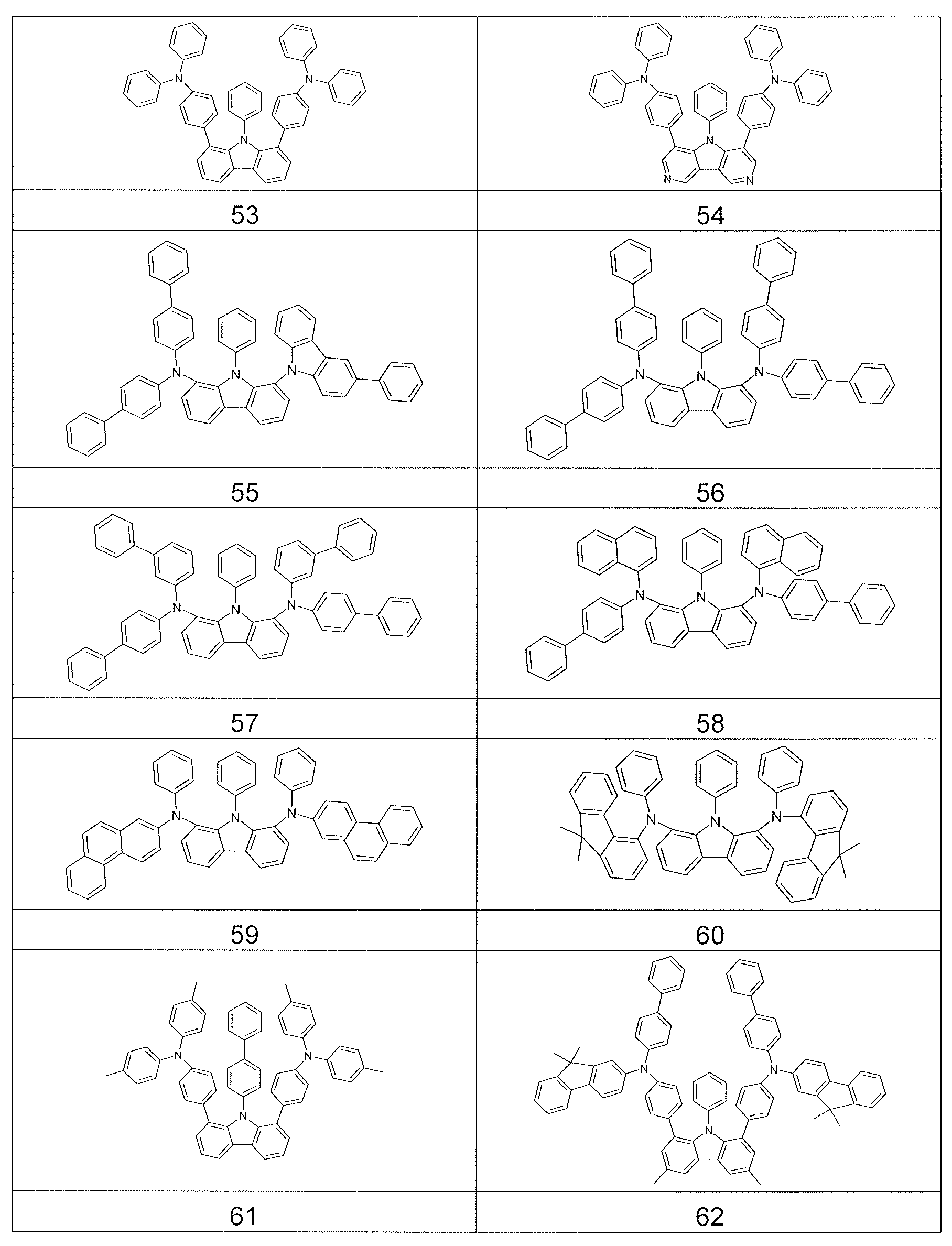
상기 적어도 하나의 유기층은 식 (I-1) 의 화합물을 포함하는, 전자 디바이스.
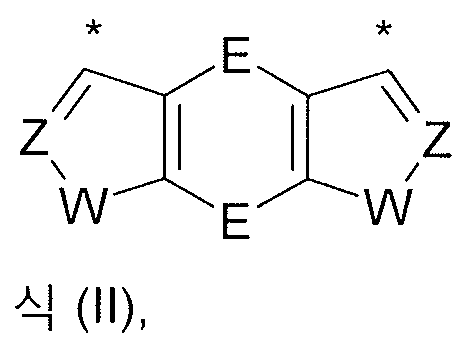
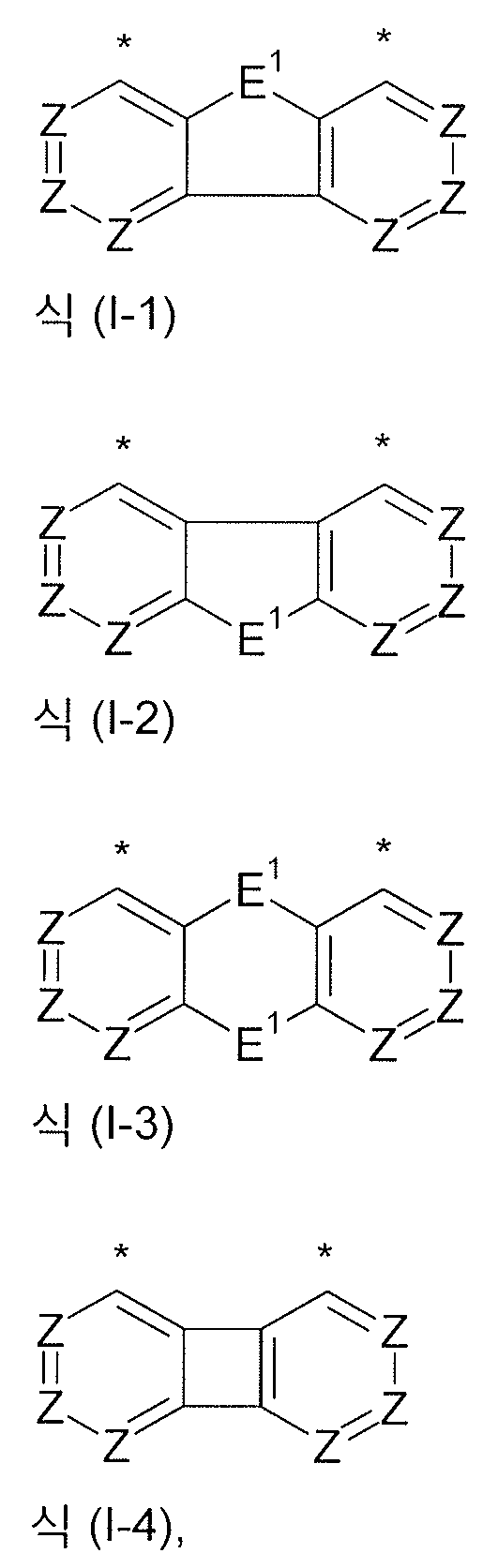
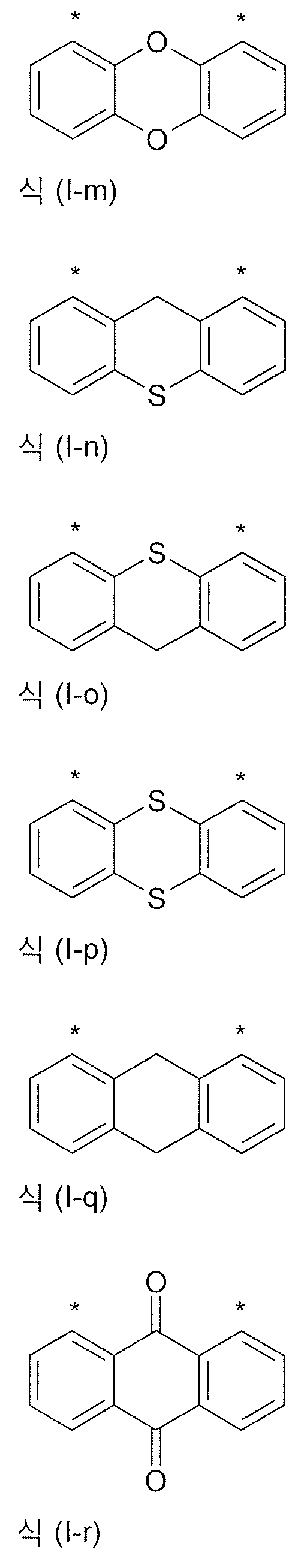
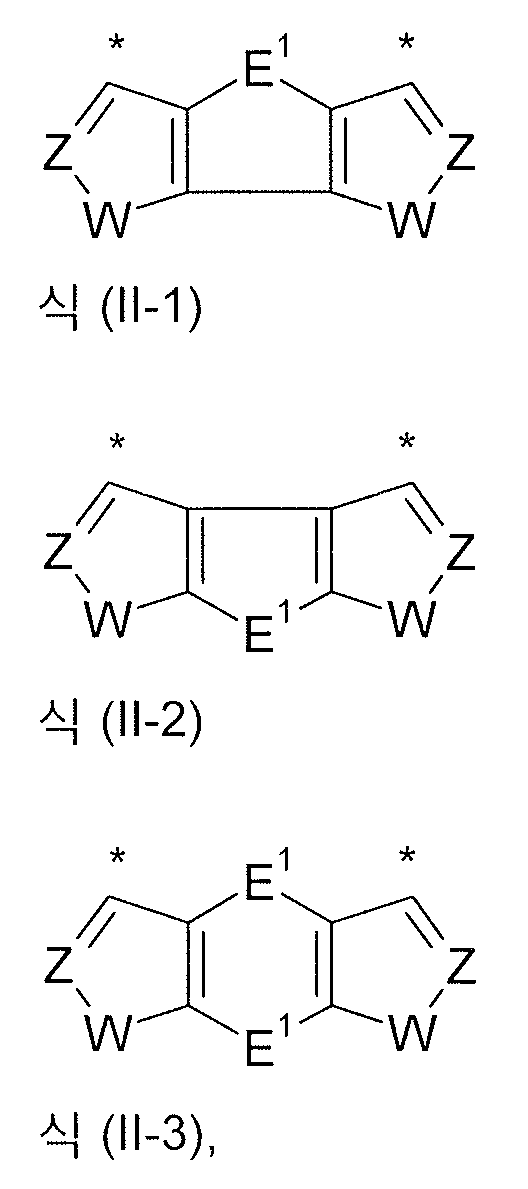
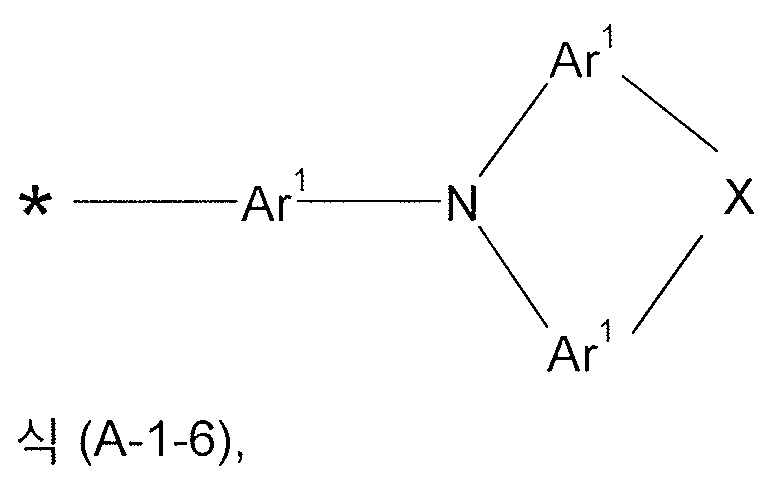
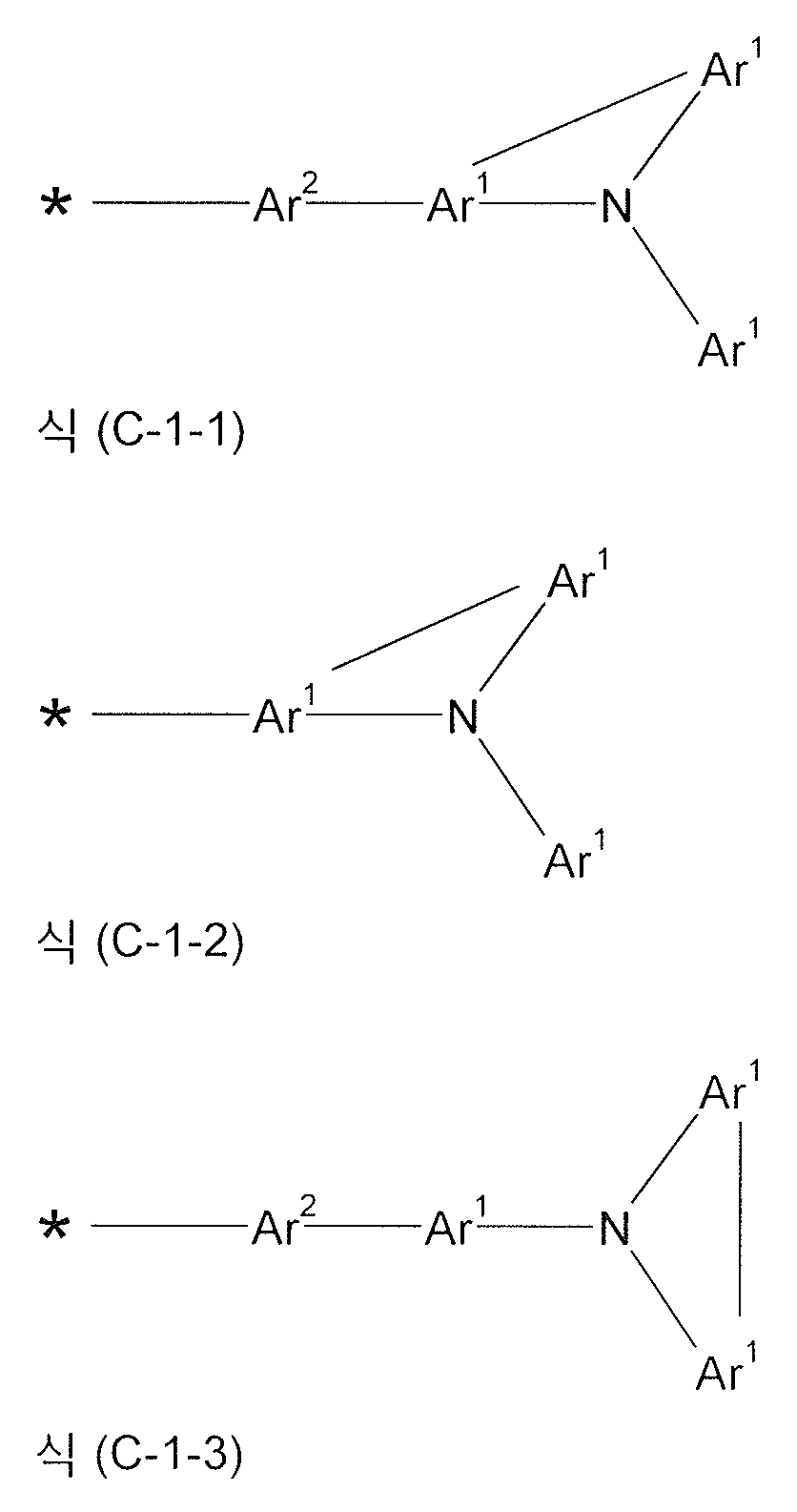
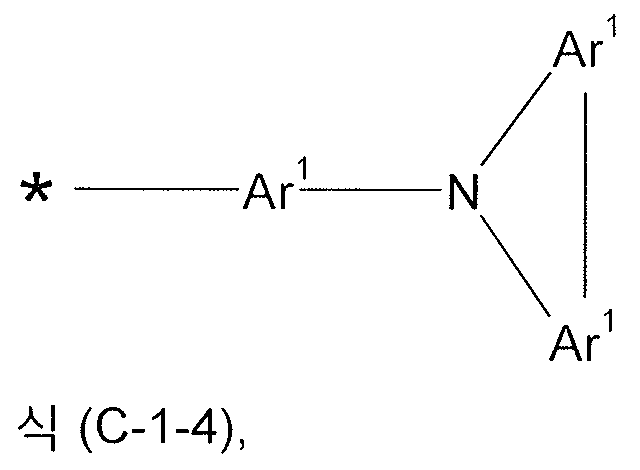
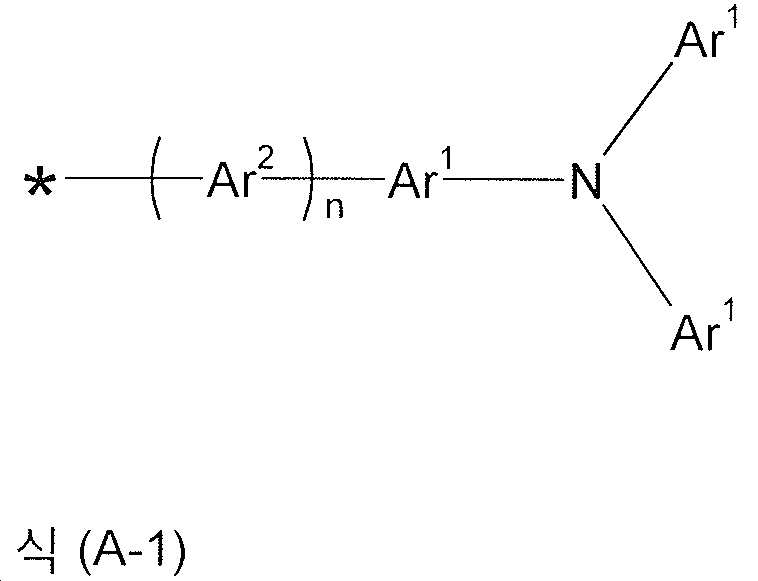
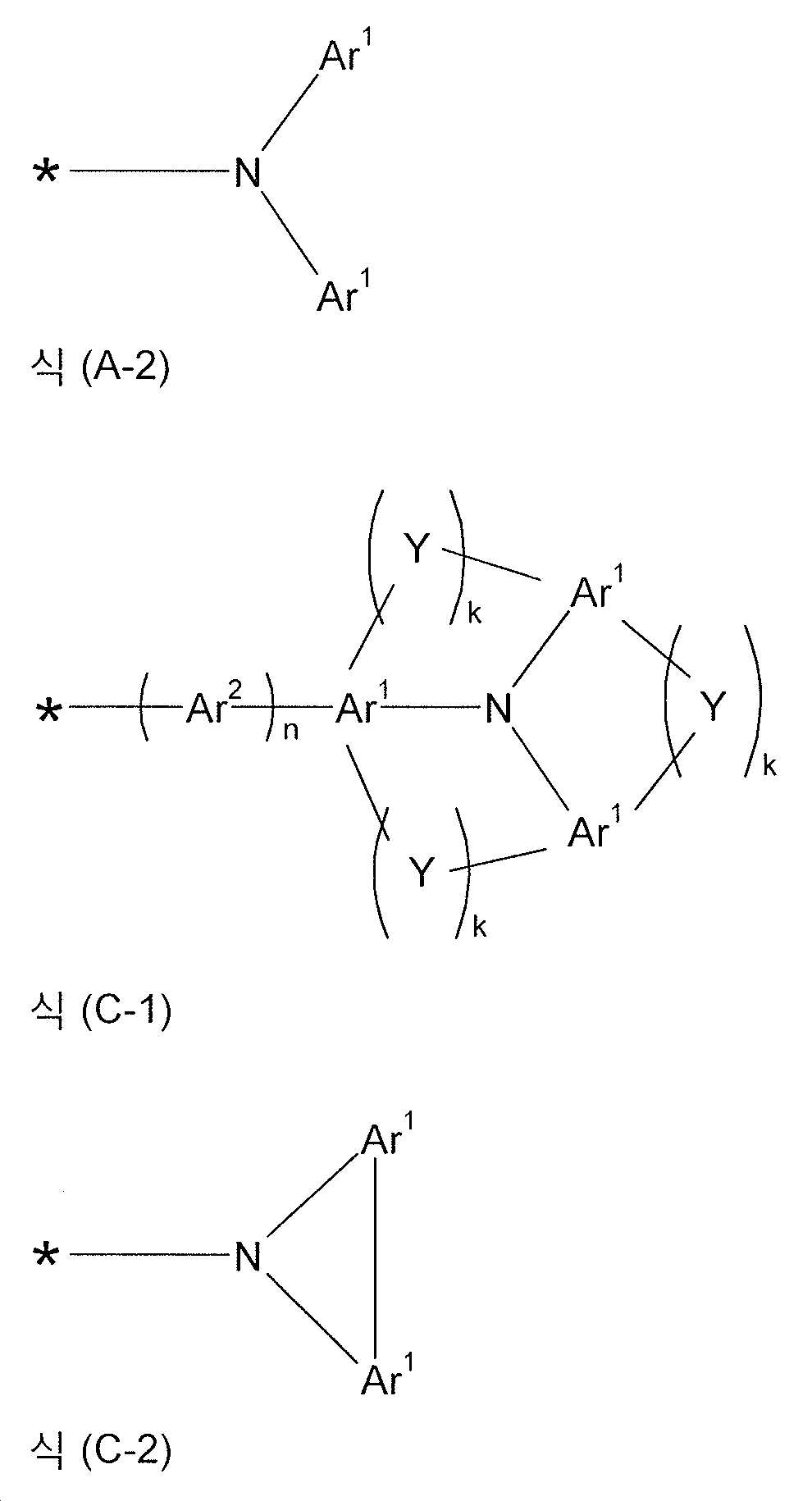
식중 하기 식들의 기들로부터 선택된 기가 * 로 나타낸 위치들에서 결합되고,
식중:
E1 은 O, S 및 NR1 로부터 선택되고;
Z 는 CR1 이고;
Ar1 은 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 13 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되고;
Ar2 는 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 13 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되고;
Y 는 단일 결합이고;
R1 은 각각의 존재시, 동일하거나 또는 상이하게, H, D, F, C(=O)R2, CN, Si(R2)3, N(R2)2, P(=O)(R2)2, S(=O)R2, S(=O)2R2, 1 ~ 20 개의 C 원자들을 갖는 직쇄 알킬 또는 알콕시기 또는 3 ∼ 20 개의 C 원자들을 갖는 분지형 또는 환형 알킬 또는 알콕시기 또는 2 ∼ 20 개의 C 원자들을 갖는 알케닐 또는 알키닐기 (여기서 상기 언급된 기들은 각각 하나 이상의 라디칼들 R2 에 의해 치환될 수 있으며, 상기 언급된 기들 내의 하나 이상의 CH2 기들은 -R2C=CR2-, -C≡C-, Si(R2)2, C=O, C=S, C=NR2, -C(=O)O-, -C(=O)-NR2-, NR2, P(=O)(R2), -O-, -S-, SO 또는 SO2 에 의해 대체될 수 있고, 상기 언급된 기들 내의 하나 이상의 H 원자들은 D, F 또는 CN 에 대체될 수도 있음), 또는 하나 이상의 라디칼들 R2 에 의해 치환될 수도 있는 5 ~ 30 개의 방향족 고리 원자들을 갖는 방향족 고리계, 또는 하나 이상의 라디칼들 R2 에 의해 치환될 수도 있는 5 ~ 30 개의 방향족 고리 원자들을 갖는 아릴옥시 또는 헤테로아릴옥시기이고;
R2 는 각각의 존재시, 동일하거나 또는 상이하게, H, D, F 또는 1 ∼ 20 개의 C 원자들을 갖는 지방족, 방향족 또는 헤테로방향족 유기 라디칼이고, 여기서 부가적으로 하나 이상의 H 원자들은 D 또는 F 에 의해 대체될 수도 있으며;
n 은 각각의 존재시, 동일하거나 또는 상이하게, 0, 1, 2, 3 또는 4 이고;
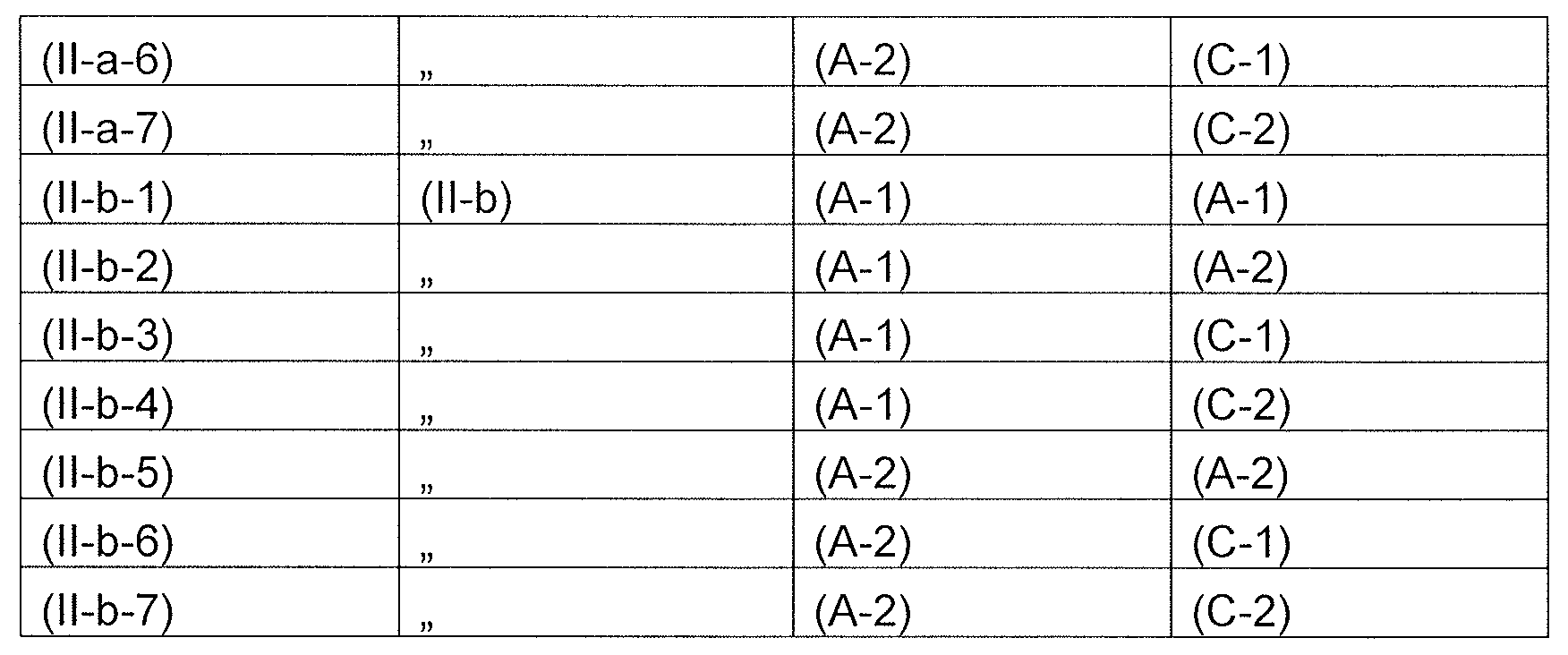
k 는 각각의 존재시, 동일하거나 또는 상이하게, 0 또는 1 이고, 여기서 식 (C-1) 의 기마다의 적어도 하나의 인덱스 k 는 1 과 동일하여야 하며;
식들 (A-1) 및 (A-2) 의 기들로부터 선택된 기는 *로 나타낸 위치들 중 적어도 하나에서 결합되어야 하고,
더욱이 14 개 이상의 방향족 고리 원자들을 갖는 어떠한 축합 아릴 또는 헤테로아릴기도 상기 화합물에 존재하지 않는다. - 삭제
- 제 1 항에 있어서,
상기 기 Ar1 은 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 10 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되는 것을 특징으로 하는 전자 디바이스. - 제 1 항에 있어서,
상기 기 Ar2 는 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 10 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되는 것을 특징으로 하는 전자 디바이스. - 제 1 항에 있어서,
R1 은 각각의 존재시, 동일하거나 또는 상이하게, H, D, F, CN, Si(R2)3, N(R2)2, 1 ~ 20 개의 C 원자들을 갖는 직쇄 알킬 또는 알콕시기 또는 3 ∼ 20 개의 C 원자들을 갖는 분지형 또는 환형 알킬 또는 알콕시기 (여기서 상기 언급된 기들은 각각 하나 이상의 라디칼들 R2 에 의해 치환될 수 있으며, 상기 언급된 기들 내의 하나 이상의 CH2 기들은 -C≡C-, -R2C=CR2-, Si(R2)2, C=O, C=NR2, -NR2-, -O-, -S-, -C(=O)O- 또는 -C(=O)NR2- 에 의해 대체될 수 있음), 또는 하나 이상의 라디칼들 R2 에 의해 치환될 수도 있는 5 ~ 20 개의 방향족 고리 원자들을 갖는 방향족 고리계인 것을 특징으로 하는 전자 디바이스. - 제 1 항에 있어서,
상기 인덱스 n 은 각각의 존재시, 동일하거나 또는 상이하게, 0 또는 1 인 것을 특징으로 하는 전자 디바이스. - 삭제
- 제 1 항 및 제 3 항 내지 제 6 항 중 어느 한 항에 있어서,
식 (I-1) 의 화합물에서, 제 1 항에 기재된 식 (A-1) 및 (A-2) 의 기들로부터 선택된 기가 *로 나타낸 위치들에서 결합되는 것을 특징으로 하는 전자 디바이스. - 제 1 항 및 제 3 항 내지 제 6 항 중 어느 한 항에 있어서,
상기 식 (I-1) 의 화합물이 제 1 항에 기재된 기들 (A-1), (A-2), (C-1) 및 (C-2) 이외에 어떠한 추가 아릴아미노기들도 포함하지 않는 것을 특징으로 하는 전자 디바이스. - 제 1 항 및 제 3 항 내지 제 6 항 중 어느 한 항에 있어서,
상기 식 (I-1) 의 화합물이 제 1 항에 기재된 기들 (A-1), (A-2), (C-1) 및 (C-2) 이외에 어떠한 추가 카르바졸기들도 포함하지 않는 것을 특징으로 하는 전자 디바이스. - 삭제
- 제 1 항 및 제 3 항 내지 제 6 항 중 어느 한 항에 있어서,
상기 전자 디바이스는 유기 집적 회로들 (OICs), 유기 전계효과 트랜지스터들 (OFETs), 유기 박막 트랜지스터들 (OTFTs), 유기 발광 트랜지스터들 (OLETs), 유기 태양 전지들 (OSCs), 유기 광학 검출기들, 유기 광수용체들, 유기 전계 켄치 디바이스들 (OFQDs), 유기 발광 전기화학 셀들 (OLECs), 유기 레이저 다이오드들 (O-lasers) 및 유기 전계발광 디바이스들 (OLEDs) 로부터 선택되는 것을 특징으로 하는 전자 디바이스. - 제 12 항에 있어서,
상기 전자 디바이스는 유기 전계발광 디바이스들로부터 선택되고,
상기 식 (I-1) 의 화합물을 포함하는 상기 유기층이 정공 수송 기능을 갖는 층이거나 또는 방출층인 것을 특징으로 하는 전자 디바이스. - 제 1 항 및 제 3 항 내지 제 6 항 중 어느 한 항에 있어서,
조명 어플리케이션들에서의 광원으로서 및/또는 의료용 또는 미용 어플리케이션들에서의 광원으로서, 및/또는 디스플레이들에서 사용되는, 전자 디바이스. - 제 1 항에 기재된 식 (I-1) 의 화합물로서,
전자 디바이스에서, 정공 수송층 또는 방출층에서 사용되는, 식 (I-1) 의 화합물. - 제 1 항에 있어서,
상기 기 Ar1 은 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 10 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되고;
상기 기 Ar2 는 각각의 존재시, 동일하거나 또는 상이하게, 하나 이상의 라디칼들 R1 에 의해 치환될 수도 있는, 6 ~ 10 개의 방향족 고리 원자들을 갖는 아릴 또는 헤테로아릴기들로부터 선택되고;
R1 은 각각의 존재시, 동일하거나 또는 상이하게, H, D, F, CN, Si(R2)3, N(R2)2, 1 ~ 20 개의 C 원자들을 갖는 직쇄 알킬 또는 알콕시기 또는 3 ∼ 20 개의 C 원자들을 갖는 분지형 또는 환형 알킬 또는 알콕시기 (여기서 상기 언급된 기들은 각각 하나 이상의 라디칼들 R2 에 의해 치환될 수 있으며, 상기 언급된 기들 내의 하나 이상의 CH2 기들은 -C≡C-, -R2C=CR2-, Si(R2)2, C=O, C=NR2, -NR2-, -O-, -S-, -C(=O)O- 또는 -C(=O)NR2- 에 의해 대체될 수 있음), 또는 하나 이상의 라디칼들 R2 에 의해 치환될 수도 있는 5 ~ 20 개의 방향족 고리 원자들을 갖는 방향족 고리계이고;
E1 은 S 및 NR1 로부터 선택되는 것을 특징으로 하는 전자 디바이스.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12007456.2 | 2012-10-31 | ||
| EP12007456 | 2012-10-31 | ||
| PCT/EP2013/003066 WO2014067614A1 (de) | 2012-10-31 | 2013-10-11 | Elektronische vorrichtung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20150079911A KR20150079911A (ko) | 2015-07-08 |
| KR101963104B1 true KR101963104B1 (ko) | 2019-03-28 |
Family
ID=47142883
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157014254A Active KR101963104B1 (ko) | 2012-10-31 | 2013-10-11 | 전자 디바이스 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9831441B2 (ko) |
| EP (2) | EP3806176B1 (ko) |
| JP (1) | JP6469579B2 (ko) |
| KR (1) | KR101963104B1 (ko) |
| CN (1) | CN104756275B (ko) |
| WO (1) | WO2014067614A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190073009A (ko) * | 2017-12-18 | 2019-06-26 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9748492B2 (en) | 2012-11-02 | 2017-08-29 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| JP6452102B2 (ja) * | 2012-12-05 | 2019-01-16 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | アミン誘導体、有機発光材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR20140108117A (ko) * | 2013-02-28 | 2014-09-05 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| US9496503B2 (en) * | 2013-03-25 | 2016-11-15 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| GB2543732A (en) * | 2015-07-20 | 2017-05-03 | Power Oleds Ltd | Heterocyclic compounds and their use in electro-optical or opto-electronic devices |
| GB201306365D0 (en) | 2013-04-09 | 2013-05-22 | Kathirgamanathan Poopathy | Heterocyclic compounds and their use in electro-optical or opto-electronic devices |
| CN105340101B (zh) * | 2013-07-03 | 2017-03-15 | 九州有机光材股份有限公司 | 发光材料、延迟萤光体、有机发光元件及化合物 |
| WO2015014435A1 (de) * | 2013-07-30 | 2015-02-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2015014434A1 (de) | 2013-07-30 | 2015-02-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US10529930B2 (en) | 2013-10-08 | 2020-01-07 | Merck Patent Gmbh | Materials for electronic devices |
| TWI540129B (zh) * | 2013-11-22 | 2016-07-01 | Dic股份有限公司 | 有機電致發光元件用材料及其應用、有機電致發光元件及其應用 |
| WO2015129896A1 (ja) * | 2014-02-28 | 2015-09-03 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 |
| KR102278609B1 (ko) * | 2014-05-14 | 2021-07-19 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| US10461260B2 (en) * | 2014-06-03 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20170170407A1 (en) * | 2014-06-12 | 2017-06-15 | Duk San Neolux Co., Ltd. | Compound for organic electronic element, organic electronic element using same, and electronic device thereof |
| JP6584058B2 (ja) * | 2014-09-25 | 2019-10-02 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | 有機電界発光素子用材料及びこれを用いた有機電界発光素子 |
| JP5848480B1 (ja) * | 2014-10-28 | 2016-01-27 | 三星ディスプレイ株式會社Samsung Display Co., Ltd. | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| US10014480B2 (en) | 2014-11-12 | 2018-07-03 | E-Ray Optoelectronics Technology Co., Ltd. | Heterocyclic compounds and organic electroluminescent devices using the same |
| WO2016078747A1 (de) * | 2014-11-21 | 2016-05-26 | Merck Patent Gmbh | Heterocyclische verbindungen zur verwendung in elektronischen vorrichtungen |
| EP3271364B1 (en) * | 2015-02-20 | 2019-06-12 | Tubitak | Thienothiophene/dithienothiophene - triphenylamine/tetraphenylethylene derivatives for organic light emitting diodes |
| US10000513B2 (en) * | 2015-02-20 | 2018-06-19 | Tubitak | Thienothiophene—boron (donor-acceptor) based materials for organic light emitting diodes |
| KR102624166B1 (ko) * | 2015-06-15 | 2024-01-12 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 |
| US20170025609A1 (en) * | 2015-07-20 | 2017-01-26 | E I Du Pont De Nemours And Company | Electroactive materials |
| US10270041B2 (en) * | 2015-08-28 | 2019-04-23 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element, light-emitting device, electronic device, and lighting device |
| EP3147961A1 (en) * | 2015-09-28 | 2017-03-29 | Novaled GmbH | Organic electroluminescent device |
| KR101614738B1 (ko) * | 2015-11-02 | 2016-04-22 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2017103732A1 (ja) * | 2015-12-17 | 2017-06-22 | 株式会社半導体エネルギー研究所 | 発光素子、発光装置、電子機器、照明装置、照明システムおよび誘導システム |
| WO2017115608A1 (ja) * | 2015-12-28 | 2017-07-06 | コニカミノルタ株式会社 | π共役系化合物、有機エレクトロルミネッセンス素子材料、発光材料、電荷輸送材料、発光性薄膜、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| EP3208861A1 (en) * | 2016-02-19 | 2017-08-23 | Novaled GmbH | Electron transport layer comprising a matrix compound mixture for an organic light-emitting diode (oled) |
| KR102851400B1 (ko) | 2016-03-03 | 2025-08-29 | 메르크 파텐트 게엠베하 | 유기 전계 발광 장치용 재료 |
| KR102710980B1 (ko) * | 2016-06-28 | 2024-09-27 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN106317008A (zh) * | 2016-07-20 | 2017-01-11 | 深圳市华星光电技术有限公司 | 发光材料及其制备方法与使用该发光材料的有机发光二极管 |
| CN106279130A (zh) * | 2016-07-20 | 2017-01-04 | 深圳市华星光电技术有限公司 | 发光材料及其制备方法与使用该发光材料的有机发光二极管 |
| CN106188024A (zh) * | 2016-07-20 | 2016-12-07 | 深圳市华星光电技术有限公司 | 发光材料及其制备方法与使用该发光材料的有机发光二极管 |
| CN105968104A (zh) * | 2016-07-20 | 2016-09-28 | 深圳市华星光电技术有限公司 | 发光材料及其制备方法与使用该发光材料的有机发光二极管 |
| ES2659663B1 (es) * | 2016-08-16 | 2019-01-28 | Abengoa Res Sl | Materiales orgánicos de transporte de huecos para dispositivos opto-electrónicos |
| JP7018895B2 (ja) * | 2016-11-16 | 2022-02-14 | 保土谷化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| WO2018186662A2 (ko) * | 2017-04-07 | 2018-10-11 | 주식회사 엘지화학 | 유기 발광 소자 |
| JP6975959B2 (ja) * | 2017-07-25 | 2021-12-01 | 国立大学法人山形大学 | アリールアミン誘導体、それを用いたホール輸送材料及び有機el素子 |
| KR102121433B1 (ko) * | 2017-09-01 | 2020-06-10 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| KR20190038254A (ko) | 2017-09-29 | 2019-04-08 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102512719B1 (ko) * | 2017-11-07 | 2023-03-23 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| CN110577523B (zh) * | 2018-06-07 | 2021-07-06 | 江苏三月科技股份有限公司 | 一种含三芳胺结构的化合物及其制备的有机电致发光器件 |
| KR102746525B1 (ko) * | 2018-12-18 | 2024-12-26 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102622167B1 (ko) | 2018-12-26 | 2024-01-08 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| JPWO2020175624A1 (ja) * | 2019-02-27 | 2021-12-23 | 国立大学法人九州大学 | 化合物、発光材料および有機半導体レーザー素子 |
| KR102444800B1 (ko) * | 2019-04-17 | 2022-09-19 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102326512B1 (ko) * | 2020-01-14 | 2021-11-16 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN112300055B (zh) * | 2020-10-28 | 2023-02-10 | 陕西莱特光电材料股份有限公司 | 含氮化合物、电子元件和电子装置 |
| CN120383582A (zh) * | 2021-02-09 | 2025-07-29 | 德山新勒克斯有限公司 | 用于有机电子元件的化合物、使用该化合物的有机电子元件及其电子装置 |
| CN117355364A (zh) | 2021-05-21 | 2024-01-05 | 默克专利有限公司 | 用于连续纯化至少一种功能材料的方法和用于连续纯化至少一种功能材料的装置 |
| CN114890981A (zh) * | 2022-05-16 | 2022-08-12 | 内蒙古大学 | 一类胺基取代的二苯并噻吩亚砜衍生物的制备方法 |
| CN114957094A (zh) * | 2022-06-09 | 2022-08-30 | 北京八亿时空液晶科技股份有限公司 | 一种多取代咔唑衍生物及其应用 |
| CN117003741B (zh) * | 2023-10-08 | 2023-12-26 | 吉林奥来德光电材料股份有限公司 | 一种发光辅助材料及其制备方法、发光器件、发光装置 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009267257A (ja) * | 2008-04-28 | 2009-11-12 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2011004639A1 (ja) * | 2009-07-07 | 2011-01-13 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、新規な化合物、照明装置及び表示装置 |
| JP2012049518A (ja) * | 2010-07-27 | 2012-03-08 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、化合物、有機エレクトロルミネッセンス素子、表示装置、並びに照明装置 |
| DE102010048608A1 (de) * | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2012195554A (ja) * | 2011-03-01 | 2012-10-11 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
Family Cites Families (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| JP3278252B2 (ja) | 1993-08-12 | 2002-04-30 | 靖彦 城田 | 有機el素子 |
| DE69432054T2 (de) | 1993-09-29 | 2003-10-09 | Idemitsu Kosan Co | Organische elektrolumineszenzelemente und arylendiaminderivate |
| JPH07133483A (ja) | 1993-11-09 | 1995-05-23 | Shinko Electric Ind Co Ltd | El素子用有機発光材料及びel素子 |
| EP0676461B1 (de) | 1994-04-07 | 2002-08-14 | Covion Organic Semiconductors GmbH | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE19652261A1 (de) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Arylsubstituierte Poly(p-arylenvinylene), Verfahren zur Herstellung und deren Verwendung in Elektroluminszenzbauelementen |
| JP3302945B2 (ja) | 1998-06-23 | 2002-07-15 | ネースディスプレイ・カンパニー・リミテッド | 新規な有機金属発光物質およびそれを含む有機電気発光素子 |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| KR100946314B1 (ko) | 1999-12-01 | 2010-03-09 | 더 트러스티즈 오브 프린스턴 유니버시티 | 인광성 유기금속화합물을 포함하는 유기 발광 장치 |
| KR100377321B1 (ko) | 1999-12-31 | 2003-03-26 | 주식회사 엘지화학 | 피-형 반도체 성질을 갖는 유기 화합물을 포함하는 전기소자 |
| US6660410B2 (en) | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| CN101924190B (zh) | 2000-08-11 | 2012-07-04 | 普林斯顿大学理事会 | 有机金属化合物和发射转换有机电致磷光 |
| JP4154138B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子、表示装置及び金属配位化合物 |
| JP4154140B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 金属配位化合物 |
| JP4154139B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子 |
| KR100691543B1 (ko) | 2002-01-18 | 2007-03-09 | 주식회사 엘지화학 | 새로운 전자 수송용 물질 및 이를 이용한 유기 발광 소자 |
| ITRM20020411A1 (it) | 2002-08-01 | 2004-02-02 | Univ Roma La Sapienza | Derivati dello spirobifluorene, loro preparazione e loro uso. |
| KR100924462B1 (ko) | 2002-08-23 | 2009-11-03 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자 및 안트라센 유도체 |
| EP1549112A4 (en) | 2002-09-20 | 2009-01-07 | Idemitsu Kosan Co | ORGANIC ELECTROLUMINESCENCE ELEMENT |
| JP2006511939A (ja) | 2002-12-23 | 2006-04-06 | コビオン・オーガニック・セミコンダクターズ・ゲーエムベーハー | 有機エレクトロルミネセンス素子 |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| US7851071B2 (en) | 2003-03-13 | 2010-12-14 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| JP4411851B2 (ja) | 2003-03-19 | 2010-02-10 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| JP5318347B2 (ja) | 2003-04-15 | 2013-10-16 | メルク パテント ゲーエムベーハー | 発光可能な、マトリックス材料と有機半導体との混合物、その使用、ならびに前記混合物を含む電子部品 |
| EP2236579B1 (en) | 2003-04-23 | 2014-04-09 | Konica Minolta Holdings, Inc. | Organic electroluminescent element and display |
| DE10333232A1 (de) | 2003-07-21 | 2007-10-11 | Merck Patent Gmbh | Organisches Elektrolumineszenzelement |
| DE10338550A1 (de) | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| DE10345572A1 (de) | 2003-09-29 | 2005-05-19 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| US7795801B2 (en) | 2003-09-30 | 2010-09-14 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| DE102004008304A1 (de) | 2004-02-20 | 2005-09-08 | Covion Organic Semiconductors Gmbh | Organische elektronische Vorrichtungen |
| JP4631386B2 (ja) | 2004-02-25 | 2011-02-16 | 株式会社デンソー | 有機el素子 |
| EP1722602A1 (en) | 2004-03-05 | 2006-11-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device and organic electroluminescent display |
| US7790890B2 (en) | 2004-03-31 | 2010-09-07 | Konica Minolta Holdings, Inc. | Organic electroluminescence element material, organic electroluminescence element, display device and illumination device |
| KR100787425B1 (ko) | 2004-11-29 | 2007-12-26 | 삼성에스디아이 주식회사 | 페닐카바졸계 화합물 및 이를 이용한 유기 전계 발광 소자 |
| DE102004023277A1 (de) | 2004-05-11 | 2005-12-01 | Covion Organic Semiconductors Gmbh | Neue Materialmischungen für die Elektrolumineszenz |
| US7598388B2 (en) | 2004-05-18 | 2009-10-06 | The University Of Southern California | Carbene containing metal complexes as OLEDs |
| EP1749809A4 (en) | 2004-05-27 | 2008-07-02 | Idemitsu Kosan Co | ASYMMETRIC PYRENE DERIVATIVE AND ORGANIC ELECTROLUMINESCENT DEVICE USING THIS |
| JP4862248B2 (ja) | 2004-06-04 | 2012-01-25 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| US7504163B2 (en) | 2004-07-12 | 2009-03-17 | Eastman Kodak Company | Hole-trapping materials for improved OLED efficiency |
| ITRM20040352A1 (it) | 2004-07-15 | 2004-10-15 | Univ Roma La Sapienza | Derivati oligomerici dello spirobifluorene, loro preparazione e loro uso. |
| EP1655359A1 (de) | 2004-11-06 | 2006-05-10 | Covion Organic Semiconductors GmbH | Organische Elektrolumineszenzvorrichtung |
| EP1859005B1 (de) | 2005-03-16 | 2016-04-27 | Merck Patent GmbH | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2006100896A1 (ja) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006108497A1 (de) | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| CN101171320B (zh) | 2005-05-03 | 2013-04-10 | 默克专利有限公司 | 有机电致发光器件 |
| JP5261887B2 (ja) | 2005-05-17 | 2013-08-14 | 三菱化学株式会社 | モノアミン化合物、電荷輸送材料および有機電界発光素子 |
| DE102005023437A1 (de) | 2005-05-20 | 2006-11-30 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| DE102005026651A1 (de) | 2005-06-09 | 2006-12-14 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2007015961A (ja) | 2005-07-06 | 2007-01-25 | Idemitsu Kosan Co Ltd | ピレン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| US20070092755A1 (en) | 2005-10-26 | 2007-04-26 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| EP1956022B1 (en) | 2005-12-01 | 2012-07-25 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent element and organic electroluminescent element |
| JP5420249B2 (ja) | 2005-12-08 | 2014-02-19 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネセンス素子のための新規な材料 |
| DE102005058557A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| EP1968131A4 (en) | 2005-12-27 | 2009-08-19 | Idemitsu Kosan Co | MATERIAL FOR AN ORGANIC ELECTROLUMINESCENCE DEVICE AND ORGANIC ELECTROLUMINESCENCE DEVICE |
| DE102006013802A1 (de) | 2006-03-24 | 2007-09-27 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006025777A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006025846A1 (de) | 2006-06-02 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006031990A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US8062769B2 (en) | 2006-11-09 | 2011-11-22 | Nippon Steel Chemical Co., Ltd. | Indolocarbazole compound for use in organic electroluminescent device and organic electroluminescent device |
| WO2008062636A1 (fr) | 2006-11-24 | 2008-05-29 | Idemitsu Kosan Co., Ltd. | Dérivé d'amine aromatique et élément électroluminescent organique utilisant celui-ci |
| DE102007002714A1 (de) | 2007-01-18 | 2008-07-31 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| CN101139317B (zh) | 2007-05-15 | 2011-09-07 | 南京邮电大学 | 含咔唑单元的有机半导体材料及合成 |
| US8044390B2 (en) | 2007-05-25 | 2011-10-25 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent device, organic electroluminescent device, and organic electroluminescent display |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102007031220B4 (de) | 2007-07-04 | 2022-04-28 | Novaled Gmbh | Chinoide Verbindungen und deren Verwendung in halbleitenden Matrixmaterialien, elektronischen und optoelektronischen Bauelementen |
| EP2045848B1 (en) | 2007-07-18 | 2017-09-27 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device material and organic electroluminescent device |
| DE102007053771A1 (de) | 2007-11-12 | 2009-05-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| US7862908B2 (en) | 2007-11-26 | 2011-01-04 | National Tsing Hua University | Conjugated compounds containing hydroindoloacridine structural elements, and their use |
| JP5329429B2 (ja) | 2007-11-30 | 2013-10-30 | 出光興産株式会社 | アザインデノフルオレンジオン誘導体、有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 |
| KR101450137B1 (ko) * | 2008-01-25 | 2014-10-13 | 삼성전자주식회사 | 유기반도체용 공중합체 및 이를 이용한 유기박막트랜지스터 및 유기 전자소자 |
| DE102008008953B4 (de) | 2008-02-13 | 2019-05-09 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| TWI478624B (zh) | 2008-03-27 | 2015-03-21 | Nippon Steel & Sumikin Chem Co | Organic electroluminescent elements |
| US8057712B2 (en) | 2008-04-29 | 2011-11-15 | Novaled Ag | Radialene compounds and their use |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008035413A1 (de) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| JP2010034465A (ja) * | 2008-07-31 | 2010-02-12 | Sumitomo Chemical Co Ltd | 光電変換素子 |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| US8119037B2 (en) | 2008-10-16 | 2012-02-21 | Novaled Ag | Square planar transition metal complexes and organic semiconductive materials using them as well as electronic or optoelectric components |
| KR101506919B1 (ko) | 2008-10-31 | 2015-03-30 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전자재료용 화합물 및 이를 포함하는 유기 전자 소자 |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR20110097612A (ko) * | 2008-11-11 | 2011-08-31 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자 |
| DE102008064200A1 (de) | 2008-12-22 | 2010-07-01 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009009277B4 (de) | 2009-02-17 | 2023-12-07 | Merck Patent Gmbh | Organische elektronische Vorrichtung, Verfahren zu deren Herstellung und Verwendung von Verbindungen |
| JP5552246B2 (ja) | 2009-03-19 | 2014-07-16 | 三井化学株式会社 | 芳香族アミン誘導体、及びそれらを用いた有機電界発光素子 |
| DE102009014513A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP5709752B2 (ja) | 2009-08-19 | 2015-04-30 | 出光興産株式会社 | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2011055932A2 (ko) * | 2009-11-05 | 2011-05-12 | 덕산하이메탈(주) | 유기화합물 및 이를 이용한 유기전기소자, 그 단말 |
| DE102009053191A1 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| KR101231931B1 (ko) * | 2009-11-13 | 2013-02-08 | 주식회사 엘지화학 | 신규한 축합고리 화합물 및 이를 이용한 유기전자소자 |
| WO2011073149A1 (de) | 2009-12-14 | 2011-06-23 | Basf Se | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds |
| US9353027B2 (en) | 2009-12-21 | 2016-05-31 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element using pyrene derivative |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010013495A1 (de) | 2010-03-31 | 2011-10-06 | Siemens Aktiengesellschaft | Dotierstoff für eine Lochleiterschicht für organische Halbleiterbauelemente und Verwendung dazu |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102010045405A1 (de) | 2010-09-15 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010048607A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| KR101305934B1 (ko) * | 2010-11-19 | 2013-09-12 | 한국과학기술연구원 | 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| EP2663567B1 (de) | 2011-01-13 | 2016-06-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20120109744A (ko) * | 2011-03-25 | 2012-10-09 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전자재료용 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR101979469B1 (ko) | 2011-04-18 | 2019-05-16 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| KR101884496B1 (ko) | 2011-05-05 | 2018-08-01 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| CA2849087A1 (en) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazole derivatives for organic electroluminescent devices |
| CN103946215B (zh) | 2011-11-17 | 2016-09-28 | 默克专利有限公司 | 螺二氢吖啶衍生物和其作为有机电致发光器件用材料的用途 |
-
2013
- 2013-10-11 KR KR1020157014254A patent/KR101963104B1/ko active Active
- 2013-10-11 CN CN201380056910.5A patent/CN104756275B/zh active Active
- 2013-10-11 US US14/439,098 patent/US9831441B2/en active Active
- 2013-10-11 WO PCT/EP2013/003066 patent/WO2014067614A1/de not_active Ceased
- 2013-10-11 JP JP2015540063A patent/JP6469579B2/ja active Active
- 2013-10-11 EP EP20211768.5A patent/EP3806176B1/de active Active
- 2013-10-11 EP EP13776421.3A patent/EP2915199B1/de active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009267257A (ja) * | 2008-04-28 | 2009-11-12 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2011004639A1 (ja) * | 2009-07-07 | 2011-01-13 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、新規な化合物、照明装置及び表示装置 |
| JP2012049518A (ja) * | 2010-07-27 | 2012-03-08 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、化合物、有機エレクトロルミネッセンス素子、表示装置、並びに照明装置 |
| DE102010048608A1 (de) * | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2012195554A (ja) * | 2011-03-01 | 2012-10-11 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190073009A (ko) * | 2017-12-18 | 2019-06-26 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102501667B1 (ko) | 2017-12-18 | 2023-02-21 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104756275B (zh) | 2017-03-08 |
| WO2014067614A1 (de) | 2014-05-08 |
| US20150280133A1 (en) | 2015-10-01 |
| CN104756275A (zh) | 2015-07-01 |
| JP6469579B2 (ja) | 2019-02-13 |
| EP3806176A1 (de) | 2021-04-14 |
| KR20150079911A (ko) | 2015-07-08 |
| EP2915199B1 (de) | 2021-03-31 |
| EP3806176B1 (de) | 2025-06-25 |
| EP2915199A1 (de) | 2015-09-09 |
| US9831441B2 (en) | 2017-11-28 |
| JP2015536567A (ja) | 2015-12-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101963104B1 (ko) | 전자 디바이스 | |
| JP7434406B2 (ja) | フルオレンおよびそれらを含む有機電子素子 | |
| JP6695936B2 (ja) | 化合物および有機エレクトロルミッセンス素子 | |
| KR101928714B1 (ko) | 전자 소자용 화합물 | |
| KR101925192B1 (ko) | 전자 소자용 물질 | |
| KR101929580B1 (ko) | 전자 소자용 화합물 | |
| KR101756611B1 (ko) | 전자 소자용 재료 | |
| KR101772371B1 (ko) | 화합물 및 유기 전자 소자 | |
| JP7543273B2 (ja) | 電子デバイス用の材料 | |
| KR102434545B1 (ko) | 전자 소자용 재료 | |
| JP6367229B2 (ja) | 電子素子のための化合物 | |
| TWI532708B (zh) | 電子裝置用化合物 | |
| KR20180122757A (ko) | 전자 소자용 물질 | |
| KR20150038193A (ko) | 2-디아릴아미노플루오렌의 유도체 및 이를 함유하는 유기 전자 화합물 | |
| KR20160054582A (ko) | 유기 전계발광 디바이스 | |
| KR20150093836A (ko) | 전자 소자용 물질 | |
| JP2023536073A (ja) | 光電子素子用有機分子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |