WO2011157346A1 - Verbindungen für elektronische vorrichtungen - Google Patents
Verbindungen für elektronische vorrichtungen Download PDFInfo
- Publication number
- WO2011157346A1 WO2011157346A1 PCT/EP2011/002547 EP2011002547W WO2011157346A1 WO 2011157346 A1 WO2011157346 A1 WO 2011157346A1 EP 2011002547 W EP2011002547 W EP 2011002547W WO 2011157346 A1 WO2011157346 A1 WO 2011157346A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- groups
- formula
- compounds
- organic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 *(c1nnnnc11)C2=C1N=NII=N2 Chemical compound *(c1nnnnc11)C2=C1N=NII=N2 0.000 description 9
- ILTYGBAZPVOWNK-UHFFFAOYSA-N C(C1C2)C3C2=CC1=C3 Chemical compound C(C1C2)C3C2=CC1=C3 ILTYGBAZPVOWNK-UHFFFAOYSA-N 0.000 description 1
- IMMJHFZDBABZNN-UHFFFAOYSA-N CC(C)(c1ccccc11)c2c(c3ccccc3[n]3-c4cccc5c4cccc5)c3ccc2N1c1c(cccc2)c2ccc1 Chemical compound CC(C)(c1ccccc11)c2c(c3ccccc3[n]3-c4cccc5c4cccc5)c3ccc2N1c1c(cccc2)c2ccc1 IMMJHFZDBABZNN-UHFFFAOYSA-N 0.000 description 1
- YFZQGUKETXDROM-UHFFFAOYSA-N CC1(C)c(c(c2c3cccc2)c(cc2)[n]3-c3ccccc3)c2N(c2ccccc2)c2ccccc12 Chemical compound CC1(C)c(c(c2c3cccc2)c(cc2)[n]3-c3ccccc3)c2N(c2ccccc2)c2ccccc12 YFZQGUKETXDROM-UHFFFAOYSA-N 0.000 description 1
- FYJRXBKVIRDYIQ-UHFFFAOYSA-N CC1(C)c2c(c3ccccc3[nH]3)c3ccc2Nc2ccccc12 Chemical compound CC1(C)c2c(c3ccccc3[nH]3)c3ccc2Nc2ccccc12 FYJRXBKVIRDYIQ-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/14—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom
- C07D251/24—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom to three ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/052—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being six-membered
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Definitions
- the present invention relates to compounds of the formula (I), the use of compounds of the formula (I) in electronic devices and electronic devices comprising one or more compounds of the formula (I). Furthermore, the invention relates to production process for compounds of formula (I) and
- OLEDs organic electroluminescent devices
- the compounds for use as organic semiconductor materials have high thermal stability and high glass transition temperature and sublime indestructible.
- Arylamine derivatives are known in the art as hole transport and
- Vapor deposition or coating process can lead to premature deposition and thus to a complication of the technical process.
- the known hole transporting materials often have low electron stability, resulting in low lifetimes of the electronic devices containing the
- carbazole derivatives e.g. Bis (carbazolyl) biphenyl
- carbazole derivatives e.g. Bis (carbazolyl) biphenyl
- ketones WO 04/093207
- phosphine oxides WO 05/003253
- triazine compounds such as triazinylspirobifluorene
- applications WO 05/053055 and WO 10/015306 are used as matrix materials for phosphorescent emitters.
- ketones low operating voltages and long lifetimes are achieved.
- metal complexes containing ketone ketone ligands such as acetylacetonate.
- metal complexes for example BAIq or bis [2- (2-benzothiazole) phenolatezinc (II), are used as matrix materials for phosphorescent emitters.
- BAIq or bis [2- (2-benzothiazole) phenolatezinc (II) are used as matrix materials for phosphorescent emitters.
- II bis [2- (2-benzothiazole) phenolatezinc
- a mixed-matrix system is understood to mean a system in which two or more different matrix compounds are used together with one or more dopant compounds mixed as the emitting layer. These systems are of particular interest in phosphorescent organic electroluminescent devices. For more detailed information, reference is made to the application WO 10/108579.
- Indenocarbazole and indolocarbazole derivatives with different Linking geometry of the indene or indole and the carbazole unit disclosed.
- the compounds are very suitable for use as functional materials in organic electroluminescent devices, in particular as matrix materials for phosphorescent emitters and as electron-transport materials.
- matrix materials for phosphorescent emitters and as electron-transport materials are very suitable for use as functional materials in organic electroluminescent devices, in particular as matrix materials for phosphorescent emitters and as electron-transport materials.
- EP 1860097, WO 2006/100896, WO 2007/140847, WO 2006/122630 and WO 2008/006449 disclose indenofluorene diamine derivatives for use in electronic devices, in particular as hole transport materials.
- EP 1860097, WO 2006/100896, WO 2007/140847, WO 2006/122630 and WO 2008/006449 disclose indenofluorene diamine derivatives for use in electronic devices, in particular as hole transport materials.
- the present invention describes as a new class of material
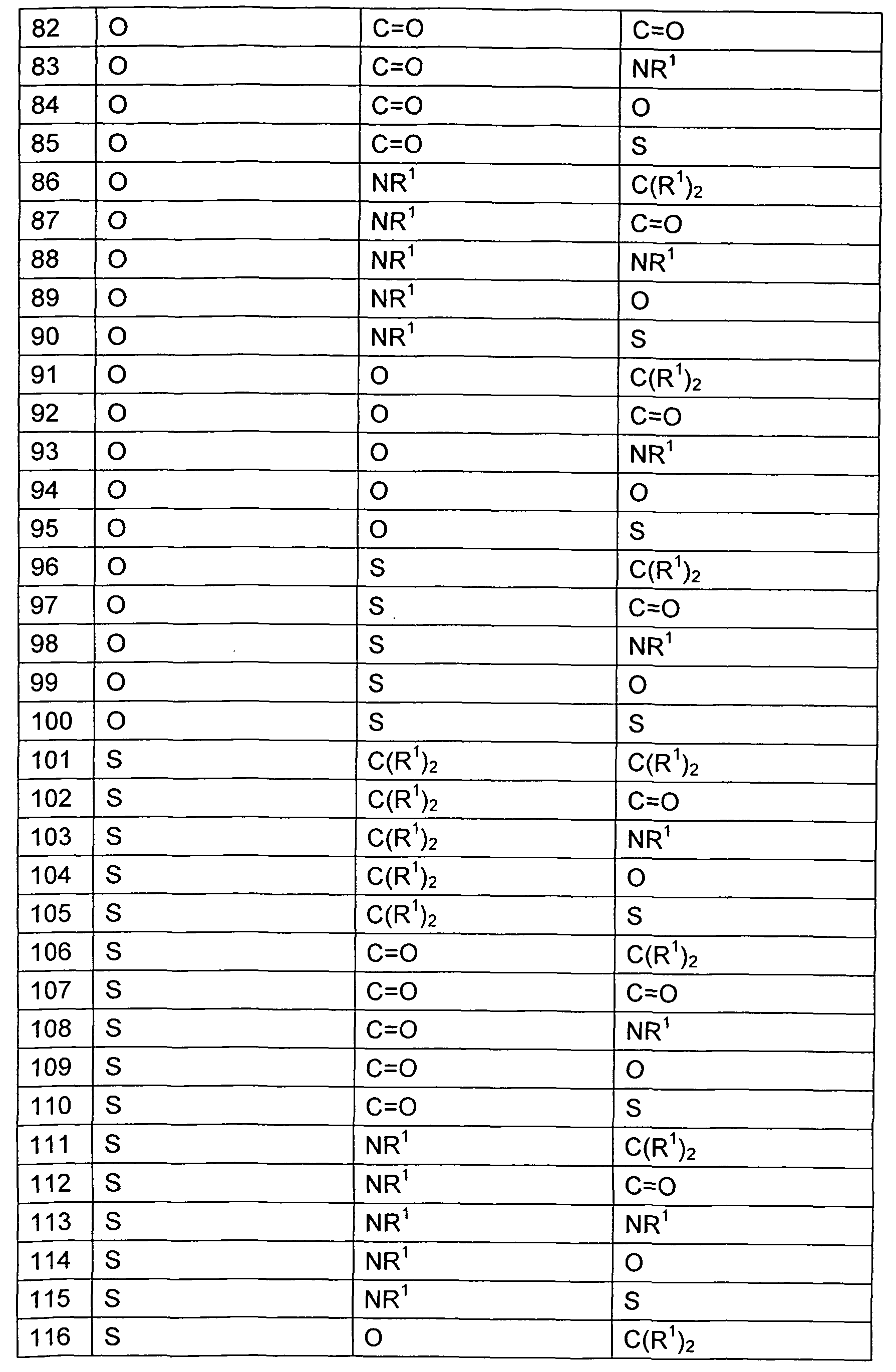
- X, X 2 , X 3 are each a divalent group, the same or
- X 4 , X 5 are identically or differently selected on each occurrence from CR 1 , N and P;
- Z is identically or differently selected from CR 1 and N at each occurrence;
- Ar 1 , Ar 2 are the same or different on each occurrence, an aryl group having 6 to 60 aromatic ring atoms or a heteroaryl group having 5 to 60 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 ;
- Substituents R 4 may also be linked together and form an aliphatic or aromatic ring system; it being excluded that X 2 and X 3 are simultaneously a group of
- an aromatic or heteroaromatic ring can be represented by a central circle ring.
- An aryl group in the sense of this invention contains 6 to 60 C atoms; a heteroaryl group in the context of this invention contains 1 to 60 carbon atoms and at least one heteroatom, with the proviso that the sum of C atoms and heteroatoms gives at least 5.
- the heteroatoms are preferably selected from N, O and / or S.
- an aryl group or heteroaryl group is either a simple aromatic cycle, ie benzene, or a simple heteroaromatic cycle, for example pyridine, pyrimidine, thiophene, etc., or a fused (fused) aryl or heteroaryl group, for example, naphthalene, anthracene, phenanthrene, quinoline, isoquinoline, carbazole, etc. understood.
- An aryl or heteroaryl group which may be substituted in each case by the abovementioned radicals R 1 or R 2 and which may be linked via any position on the aromatic or heteroaromatic compounds is understood in particular to mean groups which are derived from benzene, naphthalene, Anthracene, phenanthrene, pyrene, dihydropyrene, chrysene, perylene, fluoranthene, benzanthracene, benzphenanthrene, tetracene, pentacene, benzpyrene, furan, benzofuran, isobenzofuran, dibenzofuran, thiophene, benzothiophene, isobenzothiophene, dibenzothiophene, pyrrole, indole, isoindole, carbazole, Pyridine, quinoline, isoquinoline, acridine, phenanthridine, benzo-5,6-quinoline,
- An aralkyl group in the context of this invention is an alkyl group substituted by an aryl group, the term aryl group being understood as defined above and the alkyl group having 1 to 20 carbon atoms, wherein in the alkyl group also individual H atoms and / or CH 2 - Groups may be replaced by the groups mentioned above in the definition of R 1 and R 2 and wherein the alkyl group represents the group which binds to the rest of the compound. Accordingly, one represents
- Alkyl group wherein the term heteroaryl group is as defined above and the alkyl group has 1 to 20 carbon atoms, wherein in the alkyl group also single H atoms and / or CH 2 groups by the above in the definition of R 1 and R 2 can be replaced and wherein the alkyl group represents the group which binds to the rest of the compound.
- An aromatic ring system in the sense of this invention contains 6 to 60 carbon atoms in the ring system.
- a heteroaromatic ring system in the context of this invention contains 5 to 60 aromatic ring atoms, at least one of which represents a heteroatom.
- the heteroatoms are preferably selected from N, O and / or S.
- An aromatic or heteroaromatic ring system in the sense of this invention is to be understood as meaning a system which does not necessarily contain only aryl or heteroaryl groups but in which also several aryl or heteroaryl groups a non-aromatic moiety (preferably less than 10% of the atoms other than H), such as e.g. An sp 3 -hybridized C, Si, N or O atom, an sp 2 -hybridized C- or N-
- Atom or a sp-hybridized carbon atom can be connected.
- systems such as 9,9'-spirobifluorene, 9,9'-diarylfluorene, triarylamine, diaryl ethers, stilbene, etc. are to be understood as aromatic ring systems in the context of this invention, and also systems in which two or more aryl groups, for example by a linear or cyclic alkyl, alkenyl or alkynyl group or by a
- Silyl group are connected. Furthermore, systems in which two or more aryl or heteroaryl groups are linked together via one or more single bonds are understood as aromatic or heteroaromatic ring systems in the context of this invention.
- alkoxy or thioalkyl group having 1 to 40 carbon atoms methoxy, trifluoromethoxy, ethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, n-pentoxy, s Pentoxy, 2-methylbutoxy, n-hexoxy, cyclohexyloxy, n-heptoxy, cycloheptyloxy, n-octyloxy, cyclooctyloxy, 2-ethylhexyloxy, pentafluoroethoxy, 2,2,2-trifluoroethoxy, methylthio, ethylthio, n -propylthio, i -propylthio , n-butylthio, i-butylthio, s-butylthio, t-butylthio, n-pentylthi
- X 1 , X 2 and X 3 are each Occurrence identically or differently selected from C (R 1 ) 2 , NR 1 , O and S.
- X 1 represents a group of the formula NR 1 , very particularly preferably a group NR 1 , in which R 1 is an aromatic or heteroaromatic ring system having 5 to 60
- X 4 and X 5 on each occurrence are identically or differently selected from CR 1 and N, whereby not both groups X 4 and X 5 are simultaneously CR 1 .
- one of the two groups X 4 and X 5 is CR 1 and the other is N.
- X 4 is CR 1 and X 5 is N.
- the group R 1 of group NR 1 is not H, D or one
- aromatic ring atoms which may be substituted by one or more radicals R 3 , or a combination of these systems.
- R is as part of the group NR 1 an aromatic or heteroaromatic ring system having 5 to 60 aromatic ring atoms, which with a or a plurality of R 3 may be substituted.
- R 1 in this case is an aryl or heteroaryl group having from 5 to 20 aromatic ring atoms, each of which may be substituted with one or more R 3 groups.
- R 1 is NR 1 which is X 1 , X 2 and / or X 3 selected from phenyl, biphenyl, terphenyl,
- Ar 1 and Ar 2 independently of one another each represent an aryl or
- Heteroaryl group with 5 to 40, particularly preferably with 5 to 20 aromatic ring atoms is.
- R 1 and R 2 are identical or different at each instance and are H, D, F, CN, Si (R 3 ) 3 , N (R 3 ) 2 or a straight-chain alkyl or alkoxy group having 1 to 20
- compounds of the formula (I) can correspond to one of the two formulas (Ia) or (Ib)
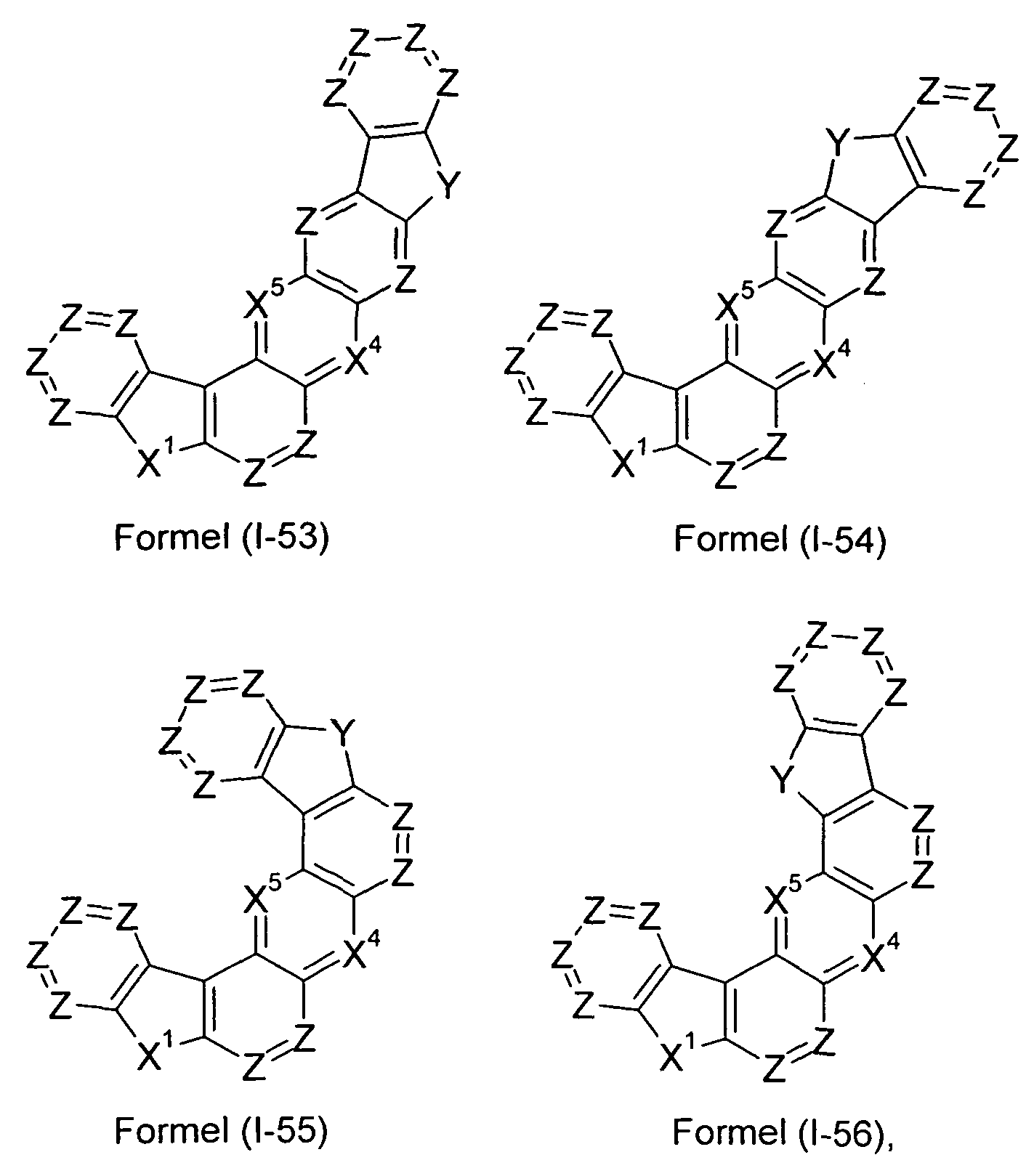
- the groups may be fused via any bond ZZ to the rest of the compound, these Zs not equal to N, Z otherwise being as defined above, and further that Y is the same or different at each occurrence
- Y is selected from C (R 2 ) 2 , NR 2 , O, and S.
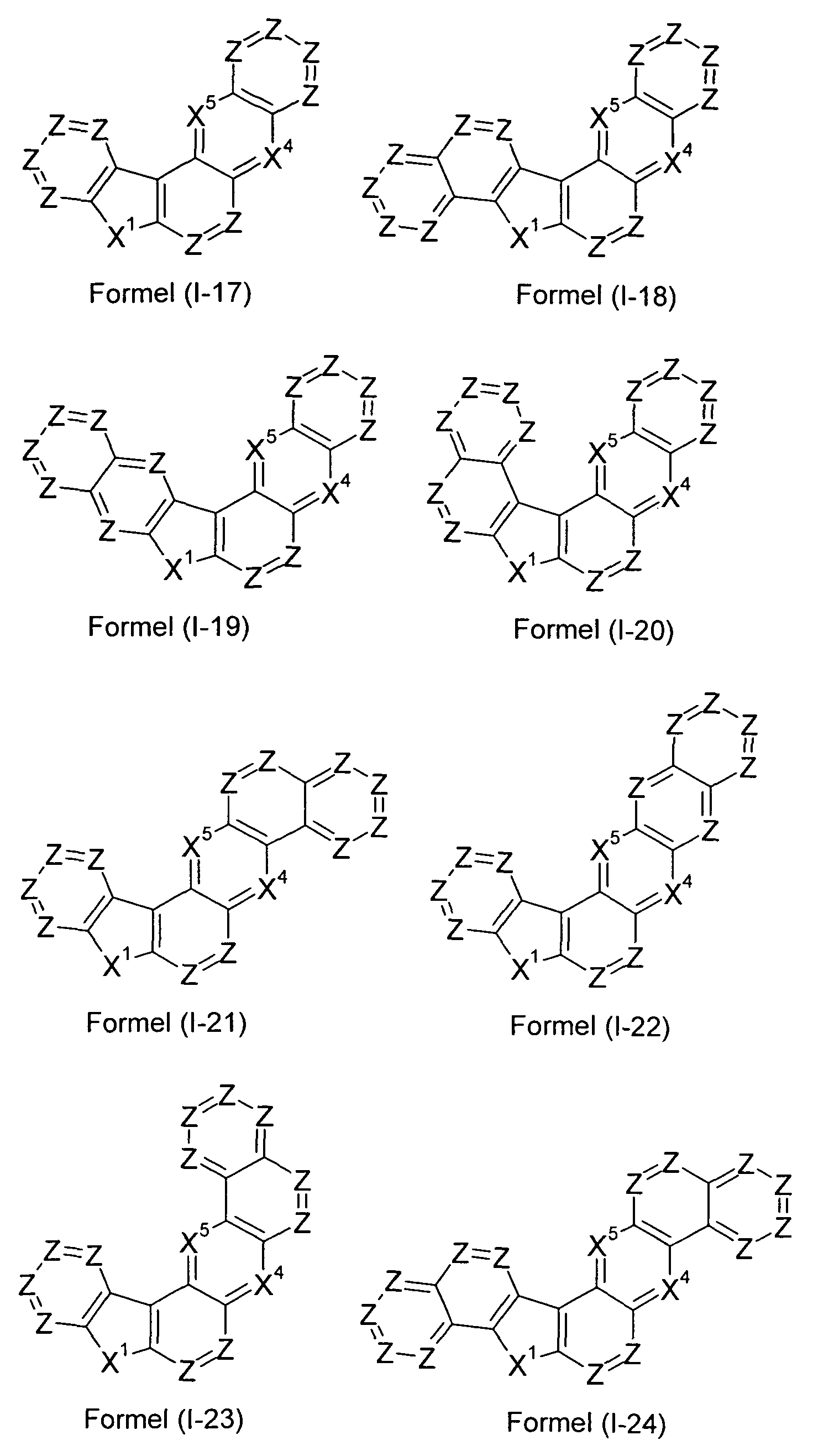
- Particularly preferred embodiments of compounds of the formula (I) are compounds of the following formulas (1-1) to (I-56)
- the compounds according to the invention particularly preferably correspond to one of the abovementioned formulas (1-1) to (I-7) and (1-7) to (I-23).
- not more than two adjacent groups Z are equal to N. It is furthermore preferred that not more than three groups Z per aromatic ring are equal to N and the remaining groups Z are equal to CR 1 . It is particularly preferred that no more than one group Z per aromatic ring is N and the remaining groups Z are CR 1 . Most preferably, all groups Z are equal to CR 1 . Very particular preference is furthermore given to compounds according to the following formulas (1-1 a) to (1-7a) and (1-17a) to (I-23a)
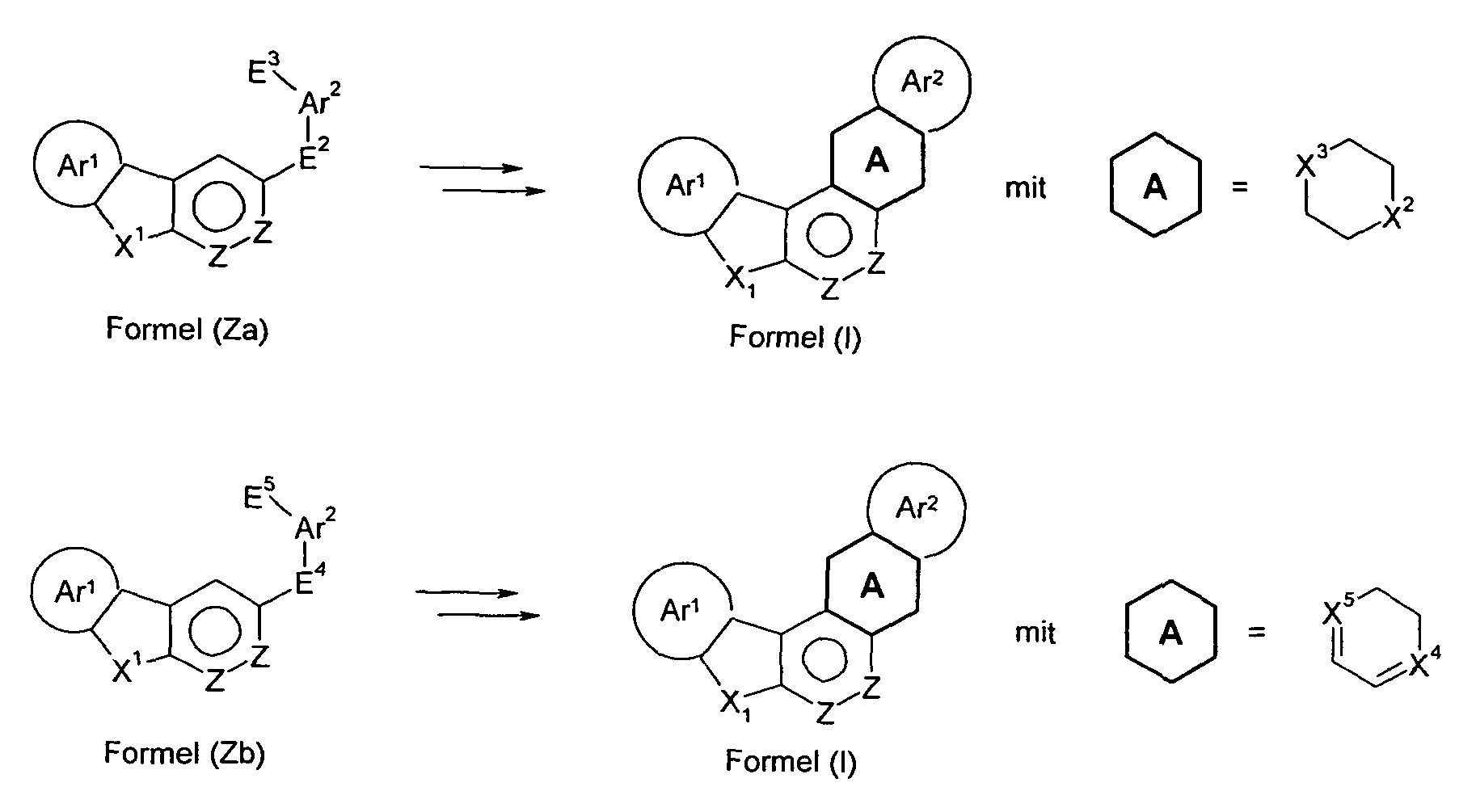
- the compounds of the invention can according to the expert known synthesis steps, such as. As bromination, Suzuki coupling, Hartwig-Buchwald coupling, etc., are shown.
- bridging group C 0 arises as X 3 .
- the resulting compound can be N-arylated in a Hartwig-Buchwald reaction.
- a temperature of about 120 ° C is used, is formed instead of a derivative of type a
- Type of compound b which corresponds to the formula (Ib) according to the invention, with X 4 as nitrogen atom and X 5 as group C-Cl.
- the unfunctionalized compound can be prepared with X 5 as CH via a defunctionalization reaction, or it can be introduced via a coupling reaction, such as a Suzuki coupling, an aryl group at the site of the chlorine atom (see Scheme 1).
- the invention thus provides a process for the preparation of the compounds of the invention according to formula (I), characterized
- Precursor of the divalent group X 2 , E 3 is a precursor of the divalent group X 3 , E 4 is a precursor of the group X 4 and E 5 is a precursor of the group X 5 .
- the compounds according to the invention described above in particular compounds which are substituted by reactive leaving groups, such as bromine, iodine, boronic acid or boronic acid esters, can be used as monomers for producing corresponding oligomers, dendrimers or polymers.
- the oligomerization or polymerization is preferably carried out via the halogen functionality or the boronic acid functionality.
- Another object of the invention are therefore oligomers, polymers or dendrimers containing one or more compounds according to
- Formula (I), wherein the bond (s) to the polymer, oligomer or dendrimer can be located at any, in formula (I) with R 1 or R 2 substituted positions.
- the compound is part of a side chain of the oligomer or polymer or constituent of the main chain.
- An oligomer in the context of this invention is understood as meaning a compound which is composed of at least three monomer units.
- a polymer in the context of the invention is understood as meaning a compound which consists of at least ten monomer units is constructed.
- the polymers, oligomers or dendrimers according to the invention may be conjugated, partially conjugated or non-conjugated.
- the oligomers or polymers of the invention may be linear, branched or dendritic.
- the units of formula (I) may be directly linked together or may be linked together via a divalent group, for example via a substituted or unsubstituted alkylene group, via a heteroatom or via a divalent aromatic or heteroaromatic group.
- three or more units of formula (I) may be linked via a trivalent or higher valent group, for example via a trivalent or higher valent aromatic or heteroaromatic group, to a branched or dendritic oligomer or polymer.
- the repeat units according to formula (I) in oligomers, dendrimers and polymers the same preferences apply as above for
- the monomers according to the invention are homopolymerized or copolymerized with further monomers.
- Suitable and preferred comonomers are selected from fluorenes (eg according to EP 842208 or WO 00/22026), spirobifluorenes (eg according to EP 707020, EP 894107 or WO 06/061 81), paraphenylenes (e.g. according to WO 92/18552), carbazoles (eg according to
- EP 1028136 dihydrophenanthrenes (for example according to WO 05/014689 or WO 07/006383), cis and trans indenofluorenes (for example according to WO
- the polymers, oligomers and dendrimers usually also contain further units, for example emitting (fluorescent or phosphorescent) units, such as e.g. Vinyltriarylamines (for example according to WO 07/068325) or phosphorescent metal complexes (for example according to WO 06/003000), and / or charge transport units, especially those based on triarylamines.
- emitting (fluorescent or phosphorescent) units such as e.g. Vinyltriarylamines (for example according to WO 07/068325) or phosphorescent metal complexes (for example according to WO 06/003000), and / or charge transport units, especially those based on triarylamines.
- the polymers, oligomers and dendrimers according to the invention have advantageous properties, in particular high lifetimes, high efficiencies and good color coordinates.
- the polymers and oligomers according to the invention are generally prepared by polymerization of one or more types of monomer, of which at least one monomer in the polymer leads to repeat units of the formula (I). Suitable polymerization reactions are known in the art and described in the literature. Particularly suitable and preferred polymerization reactions which lead to C-C or C-N linkages are the following:
- the present invention thus also provides a process for the preparation of the polymers, oligomers and dendrimers according to the invention, which is prepared by polymerization according to SUZUKI, polymerization according to YAMAMOTO, polymerization according to SILENCE or polymerization according to HARTWIG-BUCHWALD.
- the dendrimers according to the invention can be prepared according to methods known to the person skilled in the art or in analogy thereto. Suitable methods are described in the literature, such as. In Frechet, Jean M.J .; Hawker, Craig J., "Hyperbranched polyphenylenes and hyperbranched polyesters: new soluble, three-dimensional, reactive polymers", Reactive & Functional Polymers (1995), 26 (1-3), 127-36;
- the compounds of the formula (I) according to the invention are suitable for use in electronic devices, in particular in organic electroluminescent devices (OLEDs). Depending on the substitution, the compounds are used in different functions and layers. For example, compounds containing electron-deficient groups such as six-membered heteroaryl groups having one, preferably more, nitrogen atoms or five-membered heteroaryl groups having two or more nitrogen atoms are particularly suitable for use as a matrix material for phosphorescent dopants
- Electron transport material suitable.
- the compounds according to the invention are preferred in one
- Lochtransport- and / or Lochinjetechnischs slaughter or used in an emitting layer as a matrix material. But they can also be used in other layers and / or functions, for example in an emitting layer as fluorescent dopants or in a
- Electron transport layer as electron transport materials.
- the electronic devices are preferably selected from the group consisting of organic integrated circuits (O-ICs), organic field-effect transistors (O-FETs), organic thin-film transistors (O-TFTs), organic light-emitting transistors (O-LETs), organic solar cells (O-SCs), organic optical detectors, organic photoreceptors, organic field quench devices (O-FQDs), light-emitting electrochemical cells (LECs), organic laser diodes (O-lasers), and most preferably organic electroluminescent devices (OLEDs).
- O-ICs organic integrated circuits
- O-FETs organic field-effect transistors
- OF-TFTs organic thin-film transistors
- O-LETs organic light-emitting transistors
- O-SCs organic solar cells
- organic optical detectors organic photoreceptors
- O-FQDs organic field quench devices
- LECs organic laser diodes
- O-lasers organic laser diodes
- OLEDs organic electroluminescent devices
- At least one compound according to formula (I) or at least one polymer, oligomer or dendrimer comprising at least one unit according to formula (I) and at least one solvent, preferably an organic solvent.
- the formulations of the invention find, for example, in the production of organic electroluminescent devices
- Yet another object of the invention are electronic
- the electronic devices are preferably selected from the above-mentioned devices.
- organic electroluminescent devices comprising the anode, cathode and at least one emitting layer, characterized in that at least one organic layer, which may be an emitting layer, a hole transport layer or another layer, contains at least one compound according to formula (I).
- the organic electroluminescent device may contain further layers. These are, for example, selected from in each case one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, electron blocking layers, exciton blocking layers,
- Charge Generation Layers (IDMC 2003, Taiwan, Session 21 OLED (5), T. Matsumoto, T. Nakada, J. Endo, K. Mori, N. Kawamura, A. Yokoi, J. Kido, Multiphoton Organic EL Device Having Charge Generation Layer), outcoupling layers and / or organic or inorganic p / n junctions. It should be noted, however, that not necessarily each of these layers must be present and the choice of layers always depends on the compounds used and in particular also on the fact that it is a fluorescent or phosphorescent electroluminescent device.
- the organic electroluminescent device may also include a plurality of emitting layers.
- these emission layers particularly preferably have a total of a plurality of emission maxima between 380 nm and 750 nm, so that a total of white emission results, ie in the emitting layers different emitting compounds are used which can fluoresce or phosphoresce and the blue and yellow, orange or emit red light.
- Systems with three emitting layers wherein at least one of these layers contains at least one compound according to formula (I) and wherein the three layers show blue, green and orange or red emission (for the basic structure see, for example, WO 05/011013).
- the compounds according to the invention can also be present in the hole transport layer.
- white emission emitters which have broadband emission bands and thereby show white emission.
- the compound according to formula (I) is used in an electronic device containing one or more phosphorescent dopants. It can the
- Hole transport layer a hole injection layer or in the emitting layer.
- the compound according to formula (I) can also be used according to the invention in an electronic device containing one or more fluorescent dopants.
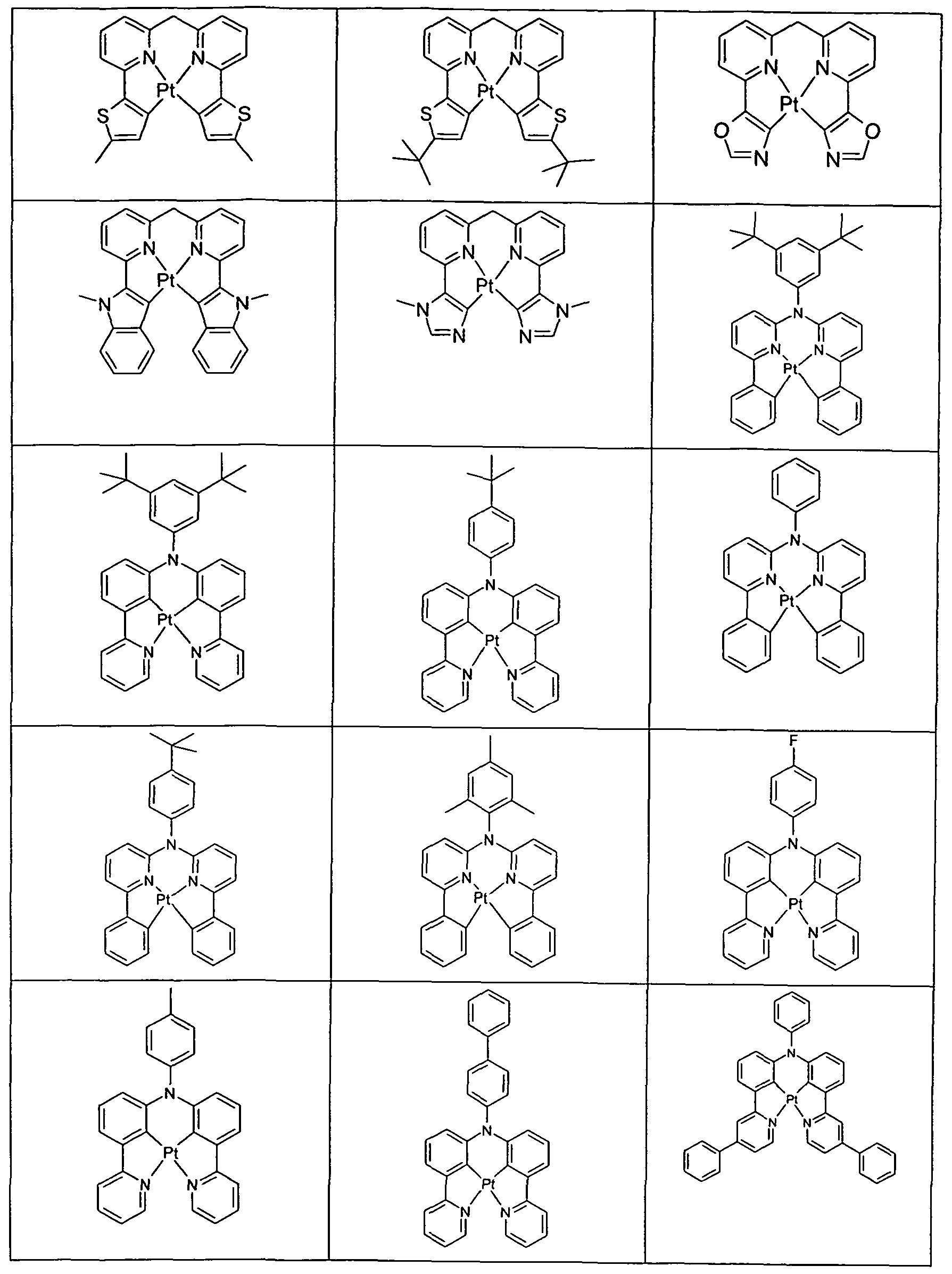
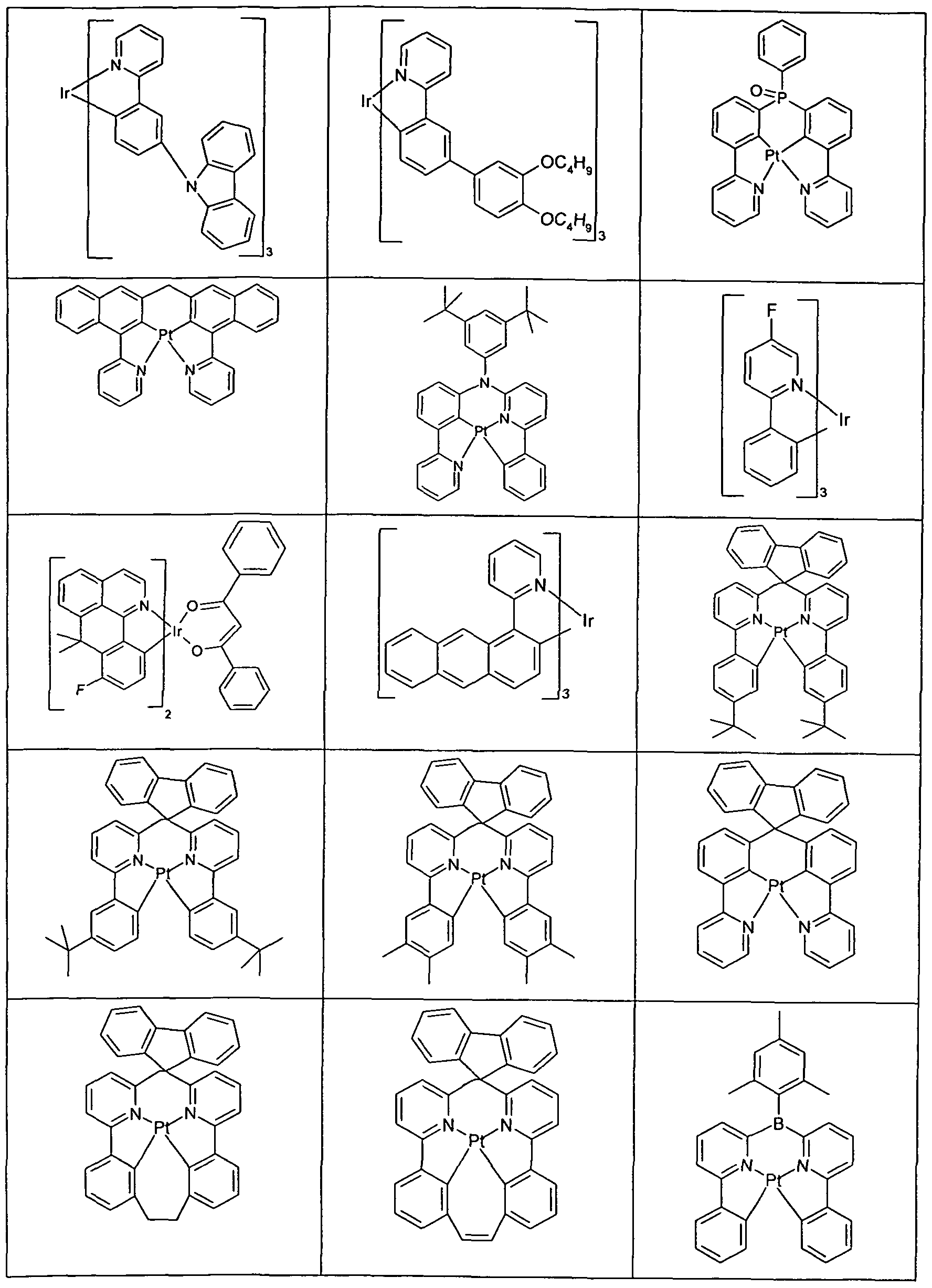
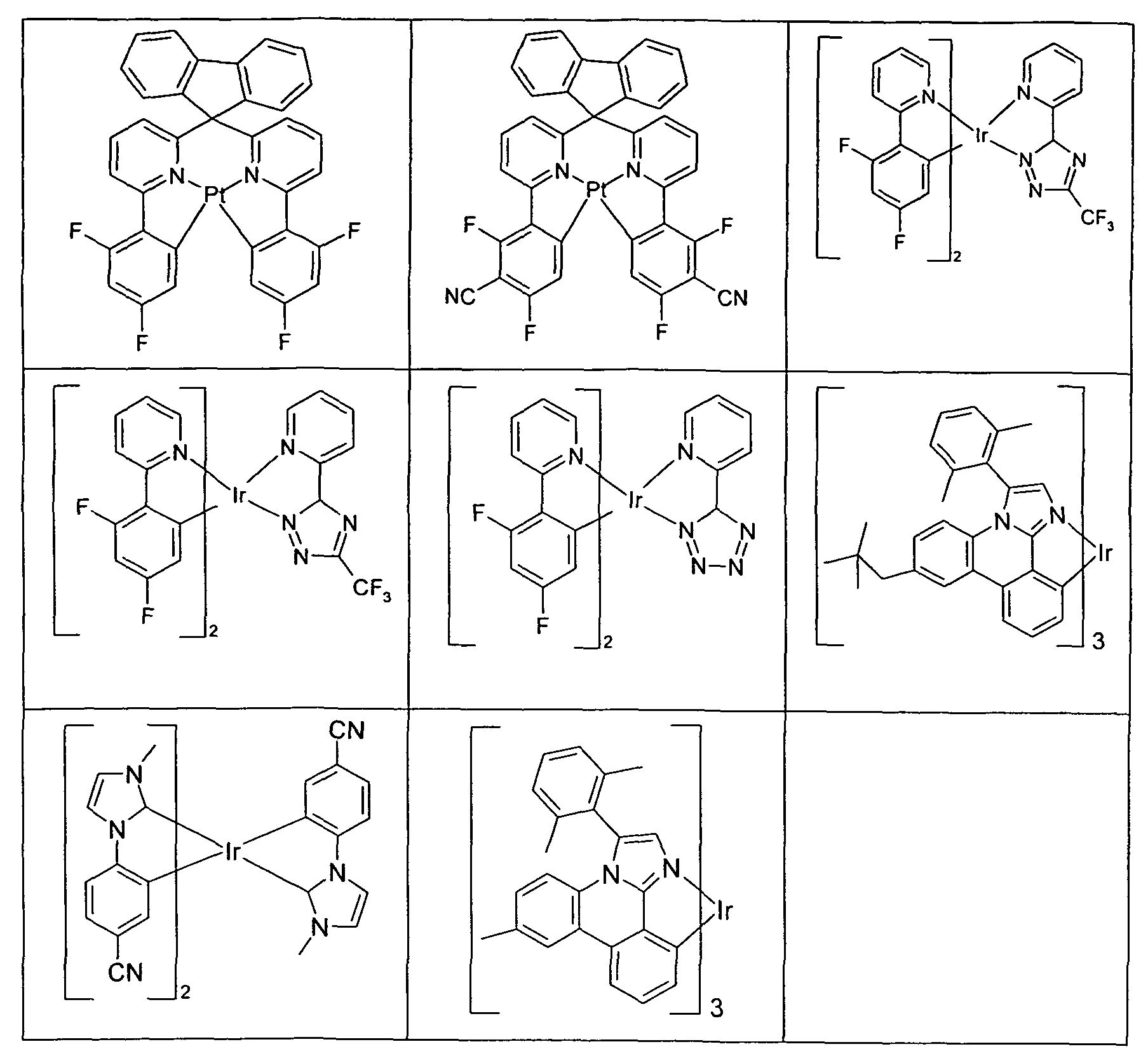
- Particularly suitable phosphorescent dopants are compounds which, when suitably excited, emit light, preferably in the visible range, and also contain at least one atom of atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80.
- phosphorescence emitters as compounds comprising copper, molybdenum, tungsten, rhenium, ruthenium, osmium, rhodium, iridium, palladium, platinum, silver, gold or europium, in particular
- Suitable phosphorescent emitter compounds can furthermore be found in the following table:
- the compounds of the formula (I) are used as hole transport material.
- the compounds are then preferably used in a hole transport layer and / or in a hole injection layer.
- a hole injection layer in the sense of this invention is a layer which is directly adjacent to the anode.
- a hole transport layer in the sense of this invention is a layer that lies between the hole injection layer and the emission layer. The hole transport layer can directly adjoin the emission layer.
- Hole transport material or may be used as hole injection material, it may be preferred if they are doped with electron acceptor compounds, for example with F 4 -TCNQ or with compounds as described in EP 1476881 or EP 1596445.
- the Hexaazatriphenylenderivat is used in a separate layer.
- a structure is preferred which has the following structure: Anode - hexaazatriphenylene derivative - hole transport layer, wherein the hole transport layer comprises one or more compounds according to
- Hole transport layer can be used a plurality of successive hole transport layers, wherein at least one hole transport layer contains at least one compound according to formula (I).
- the compound of the formula (I) is used as a hole transporting material in a hole transporting layer, the compound may be used as a pure material, i. in a proportion of 100% in the hole transport layer or it can be used in combination with one or more further compounds in the hole transport layer.
- the compounds of the formula (I) are used as matrix material in combination with one or more dopants, preferably phosphorescent dopants.
- a dopant is understood to mean the component whose proportion in the mixture is the smaller.
- a matrix material in a system containing a matrix material and a dopant is understood to mean the component whose proportion in the mixture is the larger.
- the proportion of the matrix material in the emitting layer is in this case between 50.0 and 99.9% by volume, preferably between 80.0 and 99.5% by volume and particularly preferred for fluorescent emitting layers between 92.0 and 99.5% by volume and for phosphorescent emitting layers between 85.0 and 97.0 vol.%.
- the proportion of the dopant is between 0.1 and
- Suitable phosphorescent dopants are the phosphorescent emitter compounds mentioned above.
- An emitting layer of an organic electroluminescent device may also contain systems comprising a plurality of matrix materials (mixed-matrix systems) and / or multiple dopants. Also in this case, the dopants are generally those materials whose proportion in the system is smaller and the matrix materials are those materials whose proportion in the system is larger.
- the proportion of a single matrix material in the system may be smaller than the proportion of a single dopant.
- the mixed-matrix systems preferably comprise two or three different matrix materials, more preferably two different matrix materials.
- the two different matrix materials are preferably two different matrix materials.
- Matrix materials may be present in a ratio of 1:10 to 1: 1, preferably in a ratio of 1: 4 to 1: 1.
- the mixed-matrix systems may comprise one or more dopants.
- the dopant compound or the dopant compounds may comprise one or more dopants.
- Particularly suitable matrix materials which can be used in combination with the compounds according to the invention as matrix components of a mixed-matrix system are aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, eg. B. according to WO 04/013080, WO 04/093207, WO 06/005627 or
- JP 2004/288381, EP 1205527 or WO 08/086851 disclosed carbazole derivatives, indolocarbazole derivatives, z. B. according to WO 07/063754 or WO 08/056746, Azacarbazolderivate, z. B. according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160, bipolar matrix materials, for. B. according to WO 07/137725, silanes, z. B. according to WO 05/111172, azaborole or boronic esters, for. B. according to WO 06/1 7052, triazine derivatives, z. B.
- the invention further provides mixtures containing one or more compounds of the formula (I) and one or more further compounds selected from phosphorescent dopants and / or further matrix materials, preferably aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, triarylamines, carbazole derivatives, indolocarbazole derivatives , Azacarbazole derivatives, bipolar matrix materials, silanes, azaboroles or boronic esters, triazine derivatives, zinc complexes, diazasilol or tetraazasilol derivatives, diazaphosphole derivatives and indenocarbazole derivatives.
- phosphorescent dopants and / or further matrix materials preferably aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, triarylamines, carbazole derivatives, indolocarbazole derivatives , Azacarbazole derivatives, bipolar matrix materials, silanes
- Preferred phosphorescent dopants for use in mixed-matrix systems comprising the compounds according to the invention are the phosphorescent dopants listed in the table above.
- the compounds are particularly suitable as emitting compounds if they contain at least one diarylamino group.
- the compounds according to the invention are used in this case as green or blue emitters.
- the proportion of the compound according to formula (I) as dopant in the mixture of the emitting layer in this case is between 0.1 and 50.0% by volume, preferably between 0.5 and 20.0% by volume, particularly preferably between 0.5 and 8.0% by volume. , Accordingly, the share of
- Matrix material between 50.0 and 99.9 vol .-%, preferably between 80.0 and 99.5 vol .-%, particularly preferably between 92.0 and 99.5 vol .-%.
- Preferred matrix materials for use in combination with the compounds of the invention as emitters are listed in one of the following sections. They correspond to the preferred matrix materials for fluorescent emitters.
- Preferred emitter emitter materials are selected from the class of monostyrylamines, distyrylamines, tristyrylamines,
- Tetrastyrylamines Tetrastyrylamines, styrylphosphines, styryl ethers and arylamines.
- a monostyrylamine is meant a compound containing a substituted or unsubstituted styryl group and at least one, preferably aromatic, amine.
- a distyrylamine is meant a compound which is two substituted or unsubstituted Styryl phenomenon and at least one, preferably aromatic, amine.
- a tristyrylamine is understood as meaning a compound which contains three substituted or unsubstituted styryl groups and at least one, preferably aromatic, amine.
- a tetrastyrylamine is meant a compound containing four substituted or unsubstituted styryl groups and at least one, preferably aromatic, amine.
- the styryl groups are particularly preferred stilbenes, which may also be further substituted.
- Corresponding phosphines and ethers are defined in analogy to the amines.
- An arylamine or an aromatic amine in the context of this invention is understood as meaning a compound which contains three substituted or unsubstituted aromatic or heteroaromatic ring systems bonded directly to the nitrogen. At least one of these aromatic or heteroaromatic ring systems is preferably a fused ring system, more preferably at least 14 aromatic ring atoms. Preferred examples of these are aromatic anthraceneamines, aromatic
- Anthracenediamines aromatic pyrenamines, aromatic pyrenediamines, aromatic chrysenamines or aromatic chrysendiamines.
- aromatic anthracene amine is meant a compound in which a diarylamino group is bonded directly to an anthracene group, preferably in the 9-position.
- An aromatic anthracenediamine is understood to mean a compound in which two diarylamino groups are bonded directly to an anthracene group, preferably in the 9,10-position.
- Aromatic pyrenamines, pyrenediamines, chrysenamines and chrysenediamines are defined analogously thereto, the diarylamino groups being preferably attached to the pyrene in the position or in the 1,6-position.
- Further preferred emitter materials are selected from indenofluorenamines or -diamines, for example according to WO 06/122630, benzoindenofluorenamines or -diamines, for example according to WO 08/006449, and dibenzoindenofluorenamines or -diamines, for example according to WO
- Styrylamines are substituted or unsubstituted tristilbenamines or the emitter materials described in WO 06/000388, WO 06/058737, WO 06/000389, WO 07/065549 and WO 07/115610. Further preferred are the condensed hydrocarbons disclosed in the application WO 10/012328. Also preferred as fluorescent emitter materials are the compounds of the formula (I) according to the invention.
- Suitable emitter materials are furthermore the structures depicted in the following table, as well as those described in JP 06/001973, WO 04/047499, US Pat.
- WO 06/098080, WO 07/065678, US 2005/0260442 and WO 04/092111 disclosed derivatives of these structures.
- matrix materials preferably for fluorescent dopants, materials of different classes can be used.
- Preferred matrix materials are selected from the classes of oligoarylenes (for example 2,2 ', 7,7'-tetraphenylspirobifluorene according to EP 676461 or US Pat
- oligoarylenes containing condensed aromatic groups e.g DPVBi or spiro-DPVBi according to EP 676461
- polypodal metal complexes e.g according to WO 04/081017
- hole-conducting compounds eg.
- ketones in particular ketones, phosphine oxides, sulfoxides, etc. (for example according to US Pat
- WO 05/084081 and WO 05/084082 the atropisomers (for example according to WO 06/048268), the boronic acid derivatives (for example according to WO 06/117052) or the benzanthracenes (for example according to WO 08 / 145239).
- suitable matrix materials are preferably the compounds according to the invention. Particularly preferred matrix materials are other than
- oligoarylenes containing naphthalene, anthracene, Benzanthracen and / or pyrene or atropisomers of these compounds, the oligoarylenevinylenes, the ketones, the phosphine oxides and the sulfoxides.
- Very particularly preferred matrix materials selected from the classes of
- Oligoarylenes containing anthracene, benzanthracene, benzphenanthrene and / or pyrene or atropisomers of these compounds are to be understood as meaning a compound in which at least three aryl or arylene groups are bonded to one another.
- Suitable matrix materials are, for example, the materials depicted in the following table, as well as derivatives of these materials, as described in WO 04/018587, WO
- Preferred matrix materials for phosphorescent dopants are carbazole derivatives (eg CBP ( ⁇ , ⁇ -biscarbazolylbiphenyl) or compounds according to WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527 or WO 2008/086851), triarylamines, azacarbazoles (for example according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160), indolocarbazole derivatives, eg.
- CBP ⁇ , ⁇ -biscarbazolylbiphenyl
- triarylamines for example according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160
- indolocarbazole derivatives eg.
- ketones for example according to WO 2004/093207 or WO 2010/006680
- phosphine oxides for example according to WO 2004/093207 or WO 2010/006680
- phosphine oxides for example according to WO 2005/003253
- oligophenylenes for example according to US 2005/0069729
- bipolar matrix materials eg according to WO
- Zinc complexes eg according to WO 2009/062578
- aluminum complexes eg BAIq
- diazasilol and tetraazasilol derivatives e.g. B. according to
- WO 2010/054730 Indenocarbazolderivate, z. B. according to WO 2010/136109 and WO 2011/000455 or diazaphosphole, z. B. according to
- low work function metals, metal alloys or multilayer structures of various metals are preferable, such as
- Alkaline earth metals alkali metals, main group metals or lanthanides (eg Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Furthermore, are suitable
- an alloy of magnesium and silver In multilayer structures, it is also possible, in addition to the metals mentioned, to use further metals which have a relatively high work function, such as, for example, As Ag or Al, which then usually combinations of metals, such as Ca / Ag, Mg / Ag or Ba / Ag are used. It may also be preferred between a metallic one Cathode and the organic semiconductor to introduce a thin intermediate layer of a material with a high dielectric constant. Suitable examples of these are alkali metal or alkaline earth metal fluorides, but also the corresponding oxides or carbonates (eg LiF, Li 2 O, BaF 2 , MgO, NaF, CsF, Cs 2 CO 3 , etc.). Furthermore, for that
- Lithium quinolinate LiQ
- the layer thickness of this layer is preferably between 0.5 and 5 nm.
- the anode high workfunction materials are preferred.
- the anode has a work function greater than 4.5 eV. Vacuum up.
- metals with a high redox potential such as Ag, Pt or Au, are suitable for this purpose.
- metal / metal oxide electrode z. B. AI / Ni7NiO x, Al / PtO x
- at least one of the electrodes must be transparent or
- anode materials are conductive mixed metal oxides. Particularly preferred are indium tin oxide (ITO) or indium zinc oxide (IZO). Preference is furthermore given to conductive, doped organic materials, in particular conductive doped polymers.
- the device is structured accordingly (depending on the application), contacted and finally sealed, since the life of the devices according to the invention is shortened in the presence of water and / or air.
- Organic electroluminescent device characterized in that one or more layers are coated by a sublimation process.
- the materials in vacuum sublimation are "evaporated 6 mbar.
- the initial pressure is even lower, for example less than 10" at an initial pressure less than 10 -5 mbar, preferably less than 10 7 mbar.
- an organic electroluminescent device characterized in that one or more layers are coated with the OVPD (Organic Vapor Phase Deposition) method or with the aid of a carrier gas sublimation. The materials are applied at a pressure between 10 ⁇ 5 mbar and 1 bar.
- OVPD Organic Vapor Phase Deposition
- OVJP Organic Vapor Jet Printing
- the materials are applied directly through a nozzle and thus structured (for example, BMS Arnold et al., Appl. Phys. Lett., 2008, 92, 053301).
- an organic electroluminescent device characterized in that one or more layers of solution, such. B. by spin coating, or with any printing process, such.
- screen printing flexographic printing, nozzle printing or offset printing, but particularly preferably LITI (Light Induced Thermal Imaging,
- Light sources in lighting applications and as light sources in medical and / or cosmetic applications (for example in the
- the compounds of the invention have an excellent
- Hole transport materials suitable.
- the high hole mobility allows a reduction in the operating voltage and an improvement in the operational life of the electronic devices containing the Compounds of the invention.
- the compounds of the present invention result in higher power efficiency of the devices.
- the compounds of formula (I) are characterized by a high oxidation stability in solution, which is advantageous in the purification and handling of the compounds and in their
- the compounds are outstandingly suitable for use as matrix materials in mixed-matrix systems. They preferably lead to a reduction of the operating voltage and to an extension of the life of the electronic devices.
- the compounds of the formula (I) are temperature-stable and can thus be sublimated largely without decomposition.
- Compounds can be obtained in higher purity, which has a positive effect on the performance of electronic devices containing the materials. In particular, devices with longer operational lifetimes can be produced thereby.
- reaction mixture is heated slowly under reflux.
- the cooled reaction solution is carefully added to water and extracted with methylene chloride and dried. This gives a yellow oil, which is stirred hot from heptane and crystallized under ultrasound treatment. 116.1 g (69%) of the product are obtained as a white solid.
- inventive OLEDs and OLEDs according to the prior art is carried out according to a general method according to WO 04/058911, based on the conditions described here
- ITO indium tin oxide
- PEDOT poly (3,4-ethylenedioxy-2,5-thiophene), spun from water for improved processing
- the OLEDs have in principle the following layer structure: Substrate / Optional Hole Injection Layer (HIL) / Hole Transport Layer (HTL) / Optional Interlayer (IL) / Electron Blocking Layer (EBL) /
- HIL Optional Hole Injection Layer
- HTL Hole Transport Layer
- IL Optional Interlayer
- EBL Electron Blocking Layer
- Emission Layer Emission Layer
- HBL Optional Hole Blocking Layer
- Electron transport layer ETL
- cathode is formed by a 100 nm thick aluminum layer.
- Table 1 The to
- the emission layer always consists of at least one matrix material (host material, host material) and an emitting dopant (dopant, emitter), which is admixed to the matrix material or the matrix materials by co-evaporation in a specific volume fraction.
- Electron transport layer consist of a mixture of two materials.
- the OLEDs are characterized by default.
- the electroluminescence spectra are determined at a luminance of 1000 cd / m 2 and from this the CIE 1931 x and y color coordinates are calculated.
- the indication U1000 in Table 2 indicates the voltage required for a luminance of 1000 cd / m 2 .
- SE 000 and LE1000 denote the power efficiency achieved at 1000 cd / m 2 .
- EQE1000 is the external quantum efficiency at an operating luminance of 1000 cd / m 2 .
- the lifetime LD is defined as the time after which the luminance has fallen from the start luminance L0 to a certain amount L1 in a constant-current operation.
- An indication of L0
- the values for the lifetime can be converted to an indication for other starting luminous densities with the aid of conversion formulas known to the person skilled in the art.
- the Lifespan for a starting luminance of 1000 cd / m 2 a usual indication.
- Examples V1-V3 are comparative examples according to the prior art, examples E1-E5 show data from OLEDs
- the OLEDs V1-V3 are comparative examples according to the prior art
- Examples E1-E5 show data from OLEDs in which the compounds A and B according to the invention are used.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020137001317A KR101884034B1 (ko) | 2010-06-18 | 2011-05-23 | 전자 소자용 화합물 |
| CN201180030146.5A CN102947304B (zh) | 2010-06-18 | 2011-05-23 | 用于电子器件的化合物 |
| JP2013514567A JP2013531653A (ja) | 2010-06-18 | 2011-05-23 | 電子デバイス用化合物 |
| DE112011102056.2T DE112011102056B4 (de) | 2010-06-18 | 2011-05-23 | Verbindungen für elektronische Vorrichtungen |
| US13/704,487 US10351557B2 (en) | 2010-06-18 | 2011-05-23 | Compounds for electronic devices |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102010024335A DE102010024335A1 (de) | 2010-06-18 | 2010-06-18 | Verbindungen für elektronische Vorrichtungen |
| DE102010024335.3 | 2010-06-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011157346A1 true WO2011157346A1 (de) | 2011-12-22 |
Family
ID=44227854
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2011/002547 Ceased WO2011157346A1 (de) | 2010-06-18 | 2011-05-23 | Verbindungen für elektronische vorrichtungen |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US10351557B2 (de) |
| JP (1) | JP2013531653A (de) |
| KR (1) | KR101884034B1 (de) |
| CN (1) | CN102947304B (de) |
| DE (2) | DE102010024335A1 (de) |
| WO (1) | WO2011157346A1 (de) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012110182A1 (de) * | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| KR20130115854A (ko) * | 2012-04-13 | 2013-10-22 | 에스에프씨 주식회사 | 축합고리 화합물 및 이를 포함하는 유기전계발광소자 |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012116784A (ja) * | 2010-11-30 | 2012-06-21 | Idemitsu Kosan Co Ltd | 縮合多環化合物、有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP2697226B1 (de) | 2011-04-13 | 2017-01-18 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| US11031562B2 (en) | 2015-08-25 | 2021-06-08 | Merck Patent Gmbh | Metal complexes |
| WO2017056053A1 (en) * | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying benzimidazolo[1,2-a]benzimidazolyl groups, carbazolyl groups, benzofurane groups or benzothiophene groups for organic light emitting diodes |
| EP3150604B1 (de) * | 2015-10-01 | 2021-07-14 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazol mit benzimidazolo[1,2-a]benzimidazolylgruppen, carbazolylgruppen, benzofurangruppen oder benzothiophengruppen für organische leuchtdioden |
| CN105713016B (zh) * | 2016-03-16 | 2018-05-18 | 中节能万润股份有限公司 | 一种新型oled材料及其应用 |
| CA3235146A1 (en) | 2021-10-14 | 2023-04-20 | Incyte Corporation | Quinoline compounds as inhibitors of kras |
| CN119684308B (zh) * | 2025-02-25 | 2025-07-18 | 西安瑞联新材料股份有限公司 | 一种用于有机发光材料的化合物及其应用 |
Citations (102)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB627519A (en) * | 1945-12-22 | 1949-08-10 | Gen Aniline & Film Corp | Dyestuffs of the anthraquinone acridone series |
| US3106563A (en) * | 1960-12-27 | 1963-10-08 | Gen Aniline & Film Corp | Thianthrene vat dyestuffs |
| US3167557A (en) * | 1961-03-07 | 1965-01-26 | Bayer Ag | Process for the production of vat dyestuffs |
| US3244719A (en) * | 1962-08-28 | 1966-04-05 | Basf Ag | Anthraquinone carbazole dyes |
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| JPH061973A (ja) | 1992-06-18 | 1994-01-11 | Konica Corp | 有機エレクトロルミネッセンス素子 |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0681019A2 (de) | 1994-04-26 | 1995-11-08 | TDK Corporation | Phenylanthracenderivat und organisches EL-Element |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| US5935721A (en) | 1998-03-20 | 1999-08-10 | Eastman Kodak Company | Organic electroluminescent elements for stable electroluminescent |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| JP2000273056A (ja) | 1999-01-19 | 2000-10-03 | Idemitsu Kosan Co Ltd | アミノ又はスチリル化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2000315579A (ja) * | 1999-04-28 | 2000-11-14 | Asahi Glass Co Ltd | 有機エレクトロルミネッセンス素子 |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2002067343A1 (en) | 2001-02-20 | 2002-08-29 | Isis Innovation Limited | Aryl-aryl dendrimers |
| WO2003048225A2 (de) | 2001-12-06 | 2003-06-12 | Covion Organic Semiconductors Gmbh | Prozess zur herstellung von aryl-aryl gekoppelten verbindungen |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004018587A1 (ja) | 2002-08-23 | 2004-03-04 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子及びアントラセン誘導体 |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004047499A1 (ja) | 2002-11-18 | 2004-06-03 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| WO2004081017A1 (de) | 2003-03-11 | 2004-09-23 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004092111A1 (ja) | 2003-04-10 | 2004-10-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| EP1476881A2 (de) | 2002-02-20 | 2004-11-17 | Novaled GmbH | Dotiertes organisches halbleitermaterial sowie verfahren zu dessen herstellung |
| US20040247937A1 (en) | 2003-06-03 | 2004-12-09 | Chin-Hsin Chen | Organic electroluminescent devices with a doped co-host emitter |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2005026144A1 (ja) | 2003-09-12 | 2005-03-24 | Sumitomo Chemical Company, Limited | デンドリマー化合物及びそれを用いた有機発光素子 |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| US20050101660A1 (en) * | 2003-11-11 | 2005-05-12 | The Skinny Drink Company | Composition for prevention and treatment of obesity, cardiovascular and coronary artery disease |
| WO2005053055A1 (de) | 2003-11-27 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| US20050181232A1 (en) | 2004-02-17 | 2005-08-18 | Eastman Kodak Company | Anthracene derivative host having ranges of dopants |
| WO2005084081A1 (de) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organische elektronische vorrichtungen |
| US20050211958A1 (en) | 2004-03-25 | 2005-09-29 | Eastman Kodak Company | Electroluminescent device with anthracene derivative host |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| EP1596445A1 (de) | 2003-12-04 | 2005-11-16 | Novaled GmbH | Verfahren zur Dotierung von organischen Halbleitern mit Chinonderivaten |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| US20050260442A1 (en) | 2004-05-24 | 2005-11-24 | Chen-Ping Yu | Anthracene compound for organic electroluminescent device |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| WO2006000388A1 (de) | 2004-06-26 | 2006-01-05 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2006000389A1 (de) | 2004-06-26 | 2006-01-05 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006003000A1 (de) | 2004-07-06 | 2006-01-12 | Merck Patent Gmbh | Elektrolumineszierende polymere |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006048268A1 (de) | 2004-11-06 | 2006-05-11 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2006058737A1 (de) | 2004-12-01 | 2006-06-08 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006098080A1 (ja) | 2005-03-15 | 2006-09-21 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006100896A1 (ja) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| WO2006122630A1 (de) | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2007006383A2 (en) | 2005-07-08 | 2007-01-18 | Unilever N.V. | Food product and process for preparing it |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| US20070092755A1 (en) | 2005-10-26 | 2007-04-26 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007065549A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2007065678A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Neue materialien für organische elektroluminieszenzvorrichtungen |
| WO2007068325A1 (de) | 2005-12-17 | 2007-06-21 | Merck Patent Gmbh | Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung |
| WO2007115610A1 (de) | 2006-04-01 | 2007-10-18 | Merck Patent Gmbh | Materialen für organische elektrolumineszenzvorrichtungen |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2007140847A1 (de) | 2006-06-02 | 2007-12-13 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2008006449A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2008145239A2 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Benzanthracen-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010012328A1 (de) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2010064871A1 (en) * | 2008-12-05 | 2010-06-10 | Gracel Display Inc. | Novel organic electroluminescent compounds and organic electroluminescent device using the same |
| WO2010108579A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2010136109A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011000455A1 (de) | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011021803A2 (ko) * | 2009-08-18 | 2011-02-24 | 덕산하이메탈(주) | 티안트렌 구조를 가지는 화합물 및 이를 이용한 유기전기소자, 그 단말 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3764690A (en) * | 1972-03-03 | 1973-10-09 | Bayer Ag | Substituted n-benzylimidazoles as antimycotic agents |
| DE102009022858A1 (de) | 2009-05-27 | 2011-12-15 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| KR20110102055A (ko) * | 2010-03-10 | 2011-09-16 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
-
2010
- 2010-06-18 DE DE102010024335A patent/DE102010024335A1/de not_active Withdrawn
-
2011
- 2011-05-23 KR KR1020137001317A patent/KR101884034B1/ko active Active
- 2011-05-23 CN CN201180030146.5A patent/CN102947304B/zh active Active
- 2011-05-23 DE DE112011102056.2T patent/DE112011102056B4/de active Active
- 2011-05-23 JP JP2013514567A patent/JP2013531653A/ja active Pending
- 2011-05-23 WO PCT/EP2011/002547 patent/WO2011157346A1/de not_active Ceased
- 2011-05-23 US US13/704,487 patent/US10351557B2/en active Active
Patent Citations (106)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB627519A (en) * | 1945-12-22 | 1949-08-10 | Gen Aniline & Film Corp | Dyestuffs of the anthraquinone acridone series |
| US3106563A (en) * | 1960-12-27 | 1963-10-08 | Gen Aniline & Film Corp | Thianthrene vat dyestuffs |
| US3167557A (en) * | 1961-03-07 | 1965-01-26 | Bayer Ag | Process for the production of vat dyestuffs |
| US3244719A (en) * | 1962-08-28 | 1966-04-05 | Basf Ag | Anthraquinone carbazole dyes |
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| JPH061973A (ja) | 1992-06-18 | 1994-01-11 | Konica Corp | 有機エレクトロルミネッセンス素子 |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0681019A2 (de) | 1994-04-26 | 1995-11-08 | TDK Corporation | Phenylanthracenderivat und organisches EL-Element |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| US5935721A (en) | 1998-03-20 | 1999-08-10 | Eastman Kodak Company | Organic electroluminescent elements for stable electroluminescent |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| JP2000273056A (ja) | 1999-01-19 | 2000-10-03 | Idemitsu Kosan Co Ltd | アミノ又はスチリル化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| JP2000315579A (ja) * | 1999-04-28 | 2000-11-14 | Asahi Glass Co Ltd | 有機エレクトロルミネッセンス素子 |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| WO2002067343A1 (en) | 2001-02-20 | 2002-08-29 | Isis Innovation Limited | Aryl-aryl dendrimers |
| WO2003048225A2 (de) | 2001-12-06 | 2003-06-12 | Covion Organic Semiconductors Gmbh | Prozess zur herstellung von aryl-aryl gekoppelten verbindungen |
| EP1476881A2 (de) | 2002-02-20 | 2004-11-17 | Novaled GmbH | Dotiertes organisches halbleitermaterial sowie verfahren zu dessen herstellung |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004018587A1 (ja) | 2002-08-23 | 2004-03-04 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子及びアントラセン誘導体 |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004047499A1 (ja) | 2002-11-18 | 2004-06-03 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子 |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| WO2004081017A1 (de) | 2003-03-11 | 2004-09-23 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004092111A1 (ja) | 2003-04-10 | 2004-10-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| US20040247937A1 (en) | 2003-06-03 | 2004-12-09 | Chin-Hsin Chen | Organic electroluminescent devices with a doped co-host emitter |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2005026144A1 (ja) | 2003-09-12 | 2005-03-24 | Sumitomo Chemical Company, Limited | デンドリマー化合物及びそれを用いた有機発光素子 |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| WO2005039246A1 (ja) | 2003-09-30 | 2005-04-28 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、照明装置、表示装置 |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| US20050101660A1 (en) * | 2003-11-11 | 2005-05-12 | The Skinny Drink Company | Composition for prevention and treatment of obesity, cardiovascular and coronary artery disease |
| WO2005053055A1 (de) | 2003-11-27 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| EP1596445A1 (de) | 2003-12-04 | 2005-11-16 | Novaled GmbH | Verfahren zur Dotierung von organischen Halbleitern mit Chinonderivaten |
| US20050181232A1 (en) | 2004-02-17 | 2005-08-18 | Eastman Kodak Company | Anthracene derivative host having ranges of dopants |
| WO2005084081A1 (de) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organische elektronische vorrichtungen |
| WO2005084082A1 (de) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organische elektronische vorrichtungen |
| US20050211958A1 (en) | 2004-03-25 | 2005-09-29 | Eastman Kodak Company | Electroluminescent device with anthracene derivative host |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| US20050260442A1 (en) | 2004-05-24 | 2005-11-24 | Chen-Ping Yu | Anthracene compound for organic electroluminescent device |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| WO2006000388A1 (de) | 2004-06-26 | 2006-01-05 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2006000389A1 (de) | 2004-06-26 | 2006-01-05 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006003000A1 (de) | 2004-07-06 | 2006-01-12 | Merck Patent Gmbh | Elektrolumineszierende polymere |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006048268A1 (de) | 2004-11-06 | 2006-05-11 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2006058737A1 (de) | 2004-12-01 | 2006-06-08 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006098080A1 (ja) | 2005-03-15 | 2006-09-21 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006100896A1 (ja) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP1860097A1 (de) | 2005-03-18 | 2007-11-28 | Idemitsu Kosan Co., Ltd. | Aromatisches aminderivat und organisches elektrolumineszenzgerät, bei dem dieses verwendet wird |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| WO2006122630A1 (de) | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2007006383A2 (en) | 2005-07-08 | 2007-01-18 | Unilever N.V. | Food product and process for preparing it |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| US20070092755A1 (en) | 2005-10-26 | 2007-04-26 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007065549A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2007065678A1 (de) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Neue materialien für organische elektroluminieszenzvorrichtungen |
| WO2007068325A1 (de) | 2005-12-17 | 2007-06-21 | Merck Patent Gmbh | Konjugierte polymere enthaltend triarylamin-arylvinylen-einheiten, deren darstellung und verwendung |
| WO2007115610A1 (de) | 2006-04-01 | 2007-10-18 | Merck Patent Gmbh | Materialen für organische elektrolumineszenzvorrichtungen |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2007140847A1 (de) | 2006-06-02 | 2007-12-13 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2008006449A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2008145239A2 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Benzanthracen-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010012328A1 (de) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2010064871A1 (en) * | 2008-12-05 | 2010-06-10 | Gracel Display Inc. | Novel organic electroluminescent compounds and organic electroluminescent device using the same |
| WO2010108579A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2010136109A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011000455A1 (de) | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2011021803A2 (ko) * | 2009-08-18 | 2011-02-24 | 덕산하이메탈(주) | 티안트렌 구조를 가지는 화합물 및 이를 이용한 유기전기소자, 그 단말 |
Non-Patent Citations (13)
| Title |
|---|
| DATABASE CAPLUS [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; KITAHARA, KIYOSHI ET AL: "Synthesis of indole rings fused quinacridones", XP002649599, retrieved from STN Database accession no. 1992:490188 * |
| DATABASE CAPLUS [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; SATO, RYU ET AL: "Chemistry of benzopentathiepin. Reactions of benzopentathiepin with aromatic compounds in the presence of Lewis acid", XP002649598, retrieved from STN Database accession no. 1989:407309 * |
| FRECHET, JEAN M. J., HAWKER, CRAIG J.: "Hyperbranched polyphenylene and hyperbranched polyesters: new soluble, three-dimensional, reactive polymers", REACTIVE & FUNCTIONAL POLYMERS, vol. 26, no. 1-3, 1995, pages 127 - 36, XP004052617, DOI: doi:10.1016/1381-5148(95)00010-D |
| JANSSEN, H. M., MEIJER, E. W.: "The synthesis and characterization of dendritic molecules", MATERIALS SCIENCE AND TECHNOLOGY, vol. 20, 1999, pages 403 - 458 |
| KITAHARA, KIYOSHI ET AL: "Synthesis of indole rings fused quinacridones", NIPPON KAGAKU KAISHI , (6), 662-6 CODEN: NKAKB8; ISSN: 0369-4577, 1992 * |
| LIJUN S ET AL: "The Regiospecific Synthesis of Angularly-Fused Xanthones via the Benzannulation of 1,2-Adducts Derived from 3-(o-Anisoyl)-4-substituted Cyclobutenediones and Their Dithianyl Derivatives", TETRAHEDRON LETTERS, ELSEVIER, AMSTERDAM, NL, vol. 38, no. 21, 26 May 1997 (1997-05-26), pages 3663 - 3666, XP004064005, ISSN: 0040-4039, DOI: DOI:10.1016/S0040-4039(97)00720-X * |
| M. S. ARNOLD ET AL., APPL. PHYS. LETT., vol. 92, 2008, pages 053301 |
| RAMU MEESALA ET AL: "A rapid and efficient entry to synthesis of quino and chromenocarbazoles via Ullmann-Goldberg condensation", TETRAHEDRON, vol. 65, no. 31, 1 August 2009 (2009-08-01), pages 6050 - 6056, XP055002588, ISSN: 0040-4020, DOI: 10.1016/j.tet.2009.05.061 * |
| SATO, RYU ET AL: "Chemistry of benzopentathiepin. Reactions of benzopentathiepin with aromatic compounds in the presence of Lewis acid", HETEROCYCLES , 27(11), 2563-6 CODEN: HTCYAM; ISSN: 0385-5414, 1988 * |
| T. MATSUMOTO, T. NAKADA, J. ENDO, K. MORI, N. KAWAMURA, A. YOKOI, J. KIDO, MULTIPHOTON ORGANIC EL DEVICE HAVING CHARGE GENERATION LAYER |
| TOMALIA, DONALD A.: "Dendrimer molecules", SCIENTIFIC AMERICAN, vol. 272, no. 5, 1995, pages 62 - 6, XP009105348 |
| X XU: "Systematic investigation of the molecular behaviors of heterofullerenes C48X2 (X=B, N)", CHEMICAL PHYSICS, vol. 287, no. 3, 15 February 2003 (2003-02-15), pages 317 - 333, XP055002598, ISSN: 0301-0104, DOI: 10.1016/S0301-0104(02)01020-0 * |
| Y. SHIROTA ET AL., CHEM. REV., vol. 107, no. 4, 2007, pages 953 - 1010 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012110182A1 (de) * | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US9608208B2 (en) | 2011-02-17 | 2017-03-28 | Merck Patent Gmbh | Compounds for electronic devices |
| KR20130115854A (ko) * | 2012-04-13 | 2013-10-22 | 에스에프씨 주식회사 | 축합고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR101897052B1 (ko) | 2012-04-13 | 2018-09-12 | 에스에프씨 주식회사 | 축합고리 화합물 및 이를 포함하는 유기전계발광소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102947304A (zh) | 2013-02-27 |
| CN102947304B (zh) | 2016-06-22 |
| KR101884034B1 (ko) | 2018-07-31 |
| DE112011102056A5 (de) | 2013-03-28 |
| US10351557B2 (en) | 2019-07-16 |
| JP2013531653A (ja) | 2013-08-08 |
| KR20130116069A (ko) | 2013-10-22 |
| US20130092879A1 (en) | 2013-04-18 |
| DE102010024335A1 (de) | 2011-12-22 |
| DE112011102056B4 (de) | 2025-02-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE112011101314B4 (de) | Materialien für elektronische Vorrichtungen | |
| EP3027707B1 (de) | Materialien für elektronische vorrichtungen | |
| EP2705552B1 (de) | Verbindungen für elektronische vorrichtungen | |
| DE112010004381B4 (de) | Materialien für elektronische Vorrichtungen | |
| WO2011160757A1 (de) | Materialien für elektronische vorrichtungen | |
| DE112011102056B4 (de) | Verbindungen für elektronische Vorrichtungen | |
| EP3016952B1 (de) | Spirokondensierte lactamverbindungen für organische elektrolumineszenzvorrichtungen | |
| DE102010048607A1 (de) | Verbindungen für elektronische Vorrichtungen | |
| DE102010009903A1 (de) | Verbindungen für elektronische Vorrichtungen | |
| DE102010005697A1 (de) | Verbindungen für elektronische Vorrichtungen | |
| EP3341349A1 (de) | 6,9,15,18-tetrahydro-s-indaceno[1,2-b:5,6-b']difluoren- derivate und ihre verwendung in elektronischen vorrichtungen | |
| EP2737554A1 (de) | Verbindungen für elektronische vorrichtungen | |
| EP2941472A1 (de) | Materialien für elektronische vorrichtungen | |
| DE102009053836A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| DE102010033548A1 (de) | Materialien für elektronische Vorrichtungen | |
| DE102010019306A1 (de) | Organische Elektrolumineszenzvorrichtungen | |
| DE102009052428A1 (de) | Verbindung für elektronische Vorrichtungen | |
| EP3017016A1 (de) | Materialien für elektronische vorrichtungen | |
| EP2915199A1 (de) | Elektronische vorrichtung | |
| EP2705550A1 (de) | Verbindungen für elektronische vorrichtungen | |
| DE102009048791A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP2697225B1 (de) | Materialien für elektronische vorrichtungen | |
| EP2699641A1 (de) | Verbindungen für elektronische vorrichtungen | |
| DE102010048074A1 (de) | Materialien für elektronische Vorrichtungen | |
| EP2941469A2 (de) | Materialien für elektronische vorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201180030146.5 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11721240 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13704487 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2013514567 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1120111020562 Country of ref document: DE Ref document number: 112011102056 Country of ref document: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20137001317 Country of ref document: KR Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: R225 Ref document number: 112011102056 Country of ref document: DE Effective date: 20130328 |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 11721240 Country of ref document: EP Kind code of ref document: A1 |
|
| WWG | Wipo information: grant in national office |
Ref document number: 112011102056 Country of ref document: DE |