-
Die vorliegende Erfindung betrifft Verbindungen gemäß Formel (I-1), die Verwendung von Verbindungen gemäß Formel (I-1) in elektronischen Vorrichtungen sowie elektronische Vorrichtungen enthaltend eine oder mehrere Verbindungen gemäß Formel (I-1). Weiterhin betrifft die Erfindung Herstellungsverfahren für Verbindungen gemäß Formel (I-1) sowie Formulierungen enthaltend eine oder mehrere Verbindungen gemäß Formel (1-1).
-
Organische Halbleitermaterialien wie die erfindungsgemäßen Verbindungen werden für eine Reihe verschiedenartiger Anwendungen in elektronischen Vorrichtungen entwickelt.
Der Aufbau organischer Elektrolumineszenzvorrichtungen (OLEDs), in denen die erfindungsgemäßen Verbindungen als funktionelle Materialien eingesetzt werden können, ist beispielsweise in
US 4539507 ,
US 5151629 ,
EP 0676461 und
WO 98/27136 beschrieben.
-
Betreffend die Leistungsdaten der organischen Elektrolumineszenzvorrichtungen sind, insbesondere in Hinblick auf eine breite kommerzielle Verwendung, noch weitere Verbesserungen erforderlich. Von besonderer Bedeutung sind in diesem Zusammenhang die Lebensdauer, die Effizienz und die Betriebsspannung der organischen Elektrolumineszenzvorrichtungen sowie die realisierten Farbwerte. Insbesondere bei blau emittierenden Elektrolumineszenzvorrichtungen besteht Verbesserungspotential bezüglich der Lebensdauer der Vorrichtungen.
-
Zudem ist es wünschenswert, dass die Verbindungen zur Verwendung als organische Halbleitermaterialien eine hohe thermische Stabilität und eine hohe Glasübergangstemperatur aufweisen und sich unzersetzt sublimieren lassen.
-
Es besteht in diesem Zusammenhang unter anderem Bedarf an alternativen Lochtransportmaterialien. Bei Lochtransportmaterialien gemäß dem Stand der Technik steigt im Allgemeinen die Spannung mit der Schichtdicke der Lochtransportschicht an. In der Praxis wäre häufig eine höhere Schichtdicke der Lochtransportschicht wünschenswert, dies hat jedoch oftmals eine höhere Betriebsspannung und schlechtere Leistungsdaten zur Folge. In diesem Zusammenhang besteht Bedarf an neuen Lochtransportmaterialien, die eine hohe Ladungsträgerbeweglichkeit aufweisen, so dass dickere Lochtransportschichten mit lediglich geringem Anstieg der Betriebsspannung realisiert werden können.
-
Arylaminderivate sind im Stand der Technik als Lochtransport- und Lochinjektionsmaterialien bekannt. Derartige Materialien basierend auf Indenofluorenen sind beispielsweise in
WO 06/100896 und
WO 06/122630 offenbart. Die oben beschriebenen Indenofluorenamine weisen Nachteile bei der Prozessierbarkeit auf: Während des Aufdampfungs- bzw. Beschichtungsprozesses kann es zur verfrühten Abscheidung und damit zu einer Komplikation des technischen Prozesses kommen. Darüber hinaus weisen die bekannten lochtransportierenden Materialien häufig eine geringe Elektronenstabilität auf, was zu niedrigen Lebensdauern der elektronischen Vorrichtungen enthaltend die Verbindungen führt. Hier besteht weiterer Verbesserungsbedarf.
-
Weiterhin besteht Bedarf an alternativen Matrixmaterialien zur Verwendung in elektronischen Vorrichtungen. Insbesondere besteht Bedarf an Matrixmaterialien für phosphoreszierende Emitter, die gleichzeitig zu guter Effizienz, hoher Lebensdauer und geringer Betriebsspannung führen. Gerade die Eigenschaften der Matrixmaterialien sind häufig limitierend für die Lebensdauer und die Effizienz der organischen Elektrolumineszenzvorrichtung.
-
Gemäß dem Stand der Technik werden häufig Carbazolderivate, z. B. Bis(carbazolyl)biphenyl, als Matrixmaterialien verwendet. Hier besteht noch Verbesserungspotential insbesondere in Bezug auf die Lebensdauer und die Glasübergangstemperatur der Materialien. Weiterhin besteht Verbesserungsbedarf in Bezug auf die Betriebsspannung der elektronischen Vorrichtungen enthaltend die betreffenden Materialien.
-
Weiterhin werden Ketone (
WO 04/093207 ), Phosphinoxide, Sulfone (
WO 05/003253 ) sowie Triazinverbindungen wie Triazinylspirobifluoren (vgl. die Anmeldungen
WO 05/053055 und
WO 10/015306 ) als Matrixmaterialien für phosphoreszierende Emitter verwendet. Insbesondere mit Ketonen werden niedrige Betriebsspannungen und lange Lebensdauern erzielt. Hier besteht noch Verbesserungspotential insbesondere in Bezug auf die Effizienz und die Kompatibilität mit Metallkomplexen, welche Ketoketonat-Liganden enthalten, beispielsweise Acetylacetonat.
-
Weiterhin werden Metallkomplexe, beispielsweise BAlq oder Bis[2-(2-benzothiazol)phenolat]-zink(II), als Matrixmaterialien für phosphoreszierende Emitter verwendet. Hier besteht noch Verbesserungsbedarf insbesondere in Bezug auf die Betriebsspannung und die chemische Stabilität. Rein organische Verbindungen sind häufig stabiler als diese Metallkomplexe. So sind einige dieser Metallkomplexe hydrolyseempfindlich, was die Handhabung der Komplexe erschwert.
-
Von besonderem Interesse ist weiterhin die Bereitstellung von alternativen Materialien als Matrixkomponenten von Mixed-Matrix-Systemen. Unter einem Mixed-Matrix-System wird im Sinne dieser Anmeldung ein System verstanden, in dem zwei oder mehr verschiedene Matrixverbindungen zusammen mit einer (alternativ auch mehreren) Dotandverbindungen gemischt als emittierende Schicht verwendet werden. Diese Systeme sind insbesondere von Interesse bei phosphoreszierenden organischen Elektrolumineszenzvorrichtungen. Für detailliertere Informationen wird auf die Anmeldung
WO 10/108579 verwiesen.
Als im Stand der Technik bekannte Verbindungen als Matrixkomponenten in Mixed-Matrix-Systemen sind unter anderem CBP (Biscarbazolylbiphenyl) und TCTA (Triscarbazolyltriphenylamin) zu nennen. Es besteht jedoch weiterhin Bedarf an alternativen Verbindungen zur Verwendung als Matrixkomponenten in Mixed-Matrix-Systemen. Insbesondere besteht Bedarf an Verbindungen, welche eine Verbesserung der Betriebsspannung und Lebensdauer der elektronischen Vorrichtungen bewirken.
-
In den Anmeldungen
WO 10/136109 und
WO 11/000455 werden Indenocarbazol- und Indolocarbazolderivate mit unterschiedlicher Verknüpfungsgeometrie der Inden- bzw. Indol- und der Carbazoleinheit offenbart. Die Verbindungen eignen sich sehr gut zur Verwendung als Funktionsmaterialien in organischen Elektrolumineszenzvorrichtungen, insbesondere als Matrixmaterialien für phosphoreszierende Emitter sowie als Elektronentransportmaterialien. Es besteht jedoch weiterhin Bedarf an alternativen Verbindungen, insbesondere solchen, mit denen eine Senkung der Betriebsspannung, eine Erhöhung der Leistungseffizienz sowie eine Erhöhung der Lebensdauer erreicht werden kann.
-
-
In
JP 2000-315579 A und in
WO 2010/064871 A1 werden stickstoffhaltige kondensierte heteroaromatische Verbindungen zur Verwendung in organischen Elektrolumineszenzvorrichtungen offenbart. In
R. Meesala et al., Tetrahedron 2009, Vol. 65, S. 6050-6056, in
G. Saint-Ruf et al., Bull. Soc. Chim. France 1974, No. 3-4, p. 521 - 524 und in
R. Sato et al., Heterocycles 1988, Vol. 27, S. 2563-2566, wird die Herstellung bestimmter stickstoffhaltiger kondensierter heteroaromatischer Verbindungen offenbart.
-
Es besteht jedoch weiterhin Bedarf an alternativen Verbindungen, insbesondere solchen, mit denen eine Senkung der Betriebsspannung, eine Erhöhung der Leistungseffizienz sowie eine Erhöhung der Lebensdauer erreicht werden kann.
-
Die vorliegende Erfindung beschreibt als neue Materialklasse Verbindungen der Formel (I-1), welche bei Verwendung in elektronischen Vorrichtungen, bevorzugt organischen Elektrolumineszenzvorrichtungen, vorteilhafte Eigenschaften zeigen. Die Verbindungen finden bevorzugt Verwendung als Lochtransport- oder Lochinjektionsmaterialien, als Matrixmaterialien für fluoreszierende oder phosphoreszierende Emitter oder als Elektronentransportmaterialien.
-
Gegenstand der Erfindung sind somit Verbindungen der Formel (I-1)
wie definiert in Anspruch 1.
-
Es soll der Deutlichkeit halber hervorgehoben werden, dass im Rahmen dieser Anmeldung alternativ zur klassischen Lewis-Schreibweise ein aromatischer bzw. heteroaromatischer Ring durch einen zentralen Kreis im Ring dargestellt werden kann.
-
Eine Arylgruppe im Sinne dieser Erfindung enthält 6 bis 60 C-Atome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält 1 bis 60 C-Atome und mindestens ein Heteroatom, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Dabei wird unter einer Arylgruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Cyclus, also Benzol, bzw. ein einfacher heteroaromatischer Cyclus, beispielsweise Pyridin, Pyrimidin, Thiophen, etc., oder eine kondensierte (annellierte) Aryl- oder Heteroarylgruppe, beispielsweise Naphthalin, Anthracen, Phenanthren, Chinolin, Isochinolin, Carbazol, etc., verstanden.
-
Unter einer Aryl- oder Heteroarylgruppe, die jeweils mit den oben genannten Resten R1 substituiert sein kann und die über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, welche abgeleitet sind von Benzol, Naphthalin, Anthracen, Phenanthren, Pyren, Dihydropyren, Chrysen, Perylen, Fluoranthen, Benzanthracen, Benzphenanthren, Tetracen, Pentacen, Benzpyren, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, Pyrazin, Phenazin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol.
-
Eine Aralkylgruppe im Sinne dieser Erfindung ist eine mit einer Arylgruppe substituierte Alkylgruppe, wobei der Begriff Arylgruppe wie oben definiert zu verstehen ist und die Alkylgruppe 1 bis 20 C-Atome aufweist, wobei in der Alkylgruppe auch einzelne H-Atome und/oder CH2-Gruppen durch die oben bei der Definition von R1 genannten Gruppen ersetzt sein können und wobei die Alkylgruppe diejenige Gruppe darstellt, welche an den Rest der Verbindung bindet. Entsprechend stellt eine Heteroaralkylgruppe eine mit einer Heteroarylgruppe substituierte Alkylgruppe dar, wobei der Begriff Heteroarylgruppe wie oben definiert zu verstehen ist und die Alkylgruppe 1 bis 20 C-Atome aufweist, wobei in der Alkylgruppe auch einzelne H-Atome und/oder CH2-Gruppen durch die oben bei der Definition von R1 genannten Gruppen ersetzt sein können und wobei die Alkylgruppe diejenige Gruppe darstellt, welche an den Rest der Verbindung bindet.
-
Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält 6 bis 60 C-Atome im Ringsystem. Ein heteroaromatisches Ringsystem im Sinne dieser Erfindung enthält 5 bis 60 aromatische Ringatome, von denen mindestens eines ein Heteroatom darstellt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine nicht-aromatische Einheit (bevorzugt weniger als 10 % der von H verschiedenen Atome), wie z. B. ein sp3- hybridisiertes C-, Si-, N- oder O-Atom, ein sp2-hybridisiertes C- oder N-Atom oder ein sp-hybridisiertes C-Atom, verbunden sein können. So sollen beispielsweise auch Systeme wie 9,9'-Spirobifluoren, 9,9'-Diarylfluoren, Triarylamin, Diarylether, Stilben, etc. als aromatische Ringsysteme im Sinne dieser Erfindung verstanden werden, und ebenso Systeme, in denen zwei oder mehrere Arylgruppen beispielsweise durch eine lineare oder cyclische Alkyl-, Alkenyl- oder Alkinylgruppe oder durch eine Silylgruppe verbunden sind. Weiterhin werden auch Systeme, in denen zwei oder mehr Aryl- oder Heteroarylgruppen über eine oder mehrere Einfachbindungen miteinander verknüpft sind, als aromatische oder heteroaromatische Ringsysteme im Sinne dieser Erfindung verstanden.
-
Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5 - 60 aromatischen Ringatomen, welches noch jeweils mit Resten wie oben definiert substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Benzanthracen, Phenanthren, Benzphenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Terphenylen, Fluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans-Indenofluoren, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Indolocarbazol, Indenocarbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7-Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diazapyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Phenothiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol oder Kombinationen dieser Gruppen.
-
Im Rahmen der vorliegenden Erfindung werden unter einer geradkettigen Alkylgruppe mit 1 bis 40 C-Atomen bzw. einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 40 C-Atomen bzw. einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, in der auch einzelne H-Atome oder CH2-Gruppen durch die oben bei der Definition der Reste R1 genannten Gruppen substituiert sein können, bevorzugt die Reste Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, Cyclopentyl, neo-Pentyl, n-Hexyl, Cyclohexyl, neo-Hexyl, n-Heptyl, Cycloheptyl, n-Octyl, Cyclooctyl, 2-Ethylhexyl, Trifluormethyl, Pentafluorethyl, 2,2,2-Trifluorethyl, Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclopentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl, Cyclooctenyl, Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl oder Octinyl verstanden. Unter einer Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy, n-Pentoxy, s-Pentoxy, 2-Methylbutoxy, n-Hexoxy, Cyclohexyloxy, n-Heptoxy, Cycloheptyloxy, n-Octyloxy, Cyclooctyloxy, 2-Ethylhexyloxy, Pentafluorethoxy, 2,2,2-Trifluorethoxy, Methylthio, Ethylthio, n-Propylthio, i-Propylthio, n-Butylthio, i-Butylthio, s-Butylthio, t-Butylthio, n-Pentylthio, s-Pentylthio, n-Hexylthio, Cyclohexylthio, n-Heptylthio, Cycloheptylthio, n-Octylthio, Cyclooctylthio, 2-Ethylhexylthio, Trifluormethylthio, Pentafluorethylthio, 2,2,2-Trifluorethylthio, Ethenylthio, Propenylthio, Butenylthio, Pentenylthio, Cyclopentenylthio, Hexenylthio, Cyclohexenylthio, Heptenylthio, Cycloheptenylthio, Octenylthio, Cyclooctenylthio, Ethinylthio, Propinylthio, Butinylthio, Pentinylthio, Hexinylthio, Heptinylthio oder Octinylthio verstanden.
-
Anspruchsgemäß sind X2 und X3 bei jedem Auftreten gleich oder verschieden ausgewählt aus C(R1)2, NR1, O und S.
-
Bevorzugte Kombinationen der Gruppen X
1, X
2 und X
3 sind weiterhin in der folgenden Tabelle aufgeführt. Nicht anspruchsgemäße Kombinationen sind mit # markiert.
| | X1 | X2 | X3 |
| 1# | C(R1)2 | C(R1)2 | C(R1)2 |
| 2# | C(R1)2 | C(R1)2 | C=O |
| 3# | C(R1)2 | C(R1)2 | NR1 |
| 4# | C(R1)2 | C(R1)2 | O |
| 5# | C(R1)2 | C(R1)2 | S |
| 6# | C(R1)2 | C=O | C(R1)2 |
| 7# | C(R1)2 | C=O | C=O |
| 8# | C(R1)2 | C=O | NR1 |
| 9# | C(R1)2 | C=O | O |
| 10# | C(R1)2 | C=O | S |
| 11# | C(R1)2 | NR1 | C(R1)2 |
| 12# | C(R1)2 | NR1 | C=O |
| 13# | C(R1)2 | NR1 | NR1 |
| 14# | C(R1)2 | NR1 | O |
| 15# | C(R1)2 | NR1 | S |
| 16# | C(R1)2 | O | C(R1)2 |
| 17# | C(R1)2 | O | C=O |
| 18# | C(R1)2 | O | NR1 |
| 19# | C(R1)2 | O | O |
| 20# | C(R1)2 | O | S |
| 21# | C(R1)2 | S | C(R1)2 |
| 22# | C(R1)2 | S | C=O |
| 23# | C(R1)2 | S | NR1 |
| 24# | C(R1)2 | S | O |
| 25# | C(R1)2 | S | S |
| 26# | C=O | C(R1)2 | C(R1)2 |
| 27# | C=O | C(R1)2 | C=O |
| 28# | C=O | C(R1)2 | NR1 |
| 29# | C=O | C(R1)2 | O |
| 30# | C=O | C(R1)2 | S |
| 31# | C=O | C=O | C(R1)2 |
| 32# | C=O | C=O | C=O |
| 33# | C=O | C=O | NR1 |
| 34# | C=O | C=O | O |
| 35# | C=O | C=O | S |
| 36# | C=O | NR1 | C(R1)2 |
| 37# | C=O | NR1 | C=O |
| 38# | C=O | NR1 | NR1 |
| 39# | C=O | NR1 | O |
| 40# | C=O | NR1 | S |
| 41# | C=O | O | C(R1)2 |
| 42# | C=O | O | C=O |
| 43# | C=O | O | NR1 |
| 44# | C=O | O | O |
| 45# | C=O | O | S |
| 46# | C=O | S | C(R1)2 |
| 47# | C=O | S | C=O |
| 48# | C=O | S | NR1 |
| 49# | C=O | S | O |
| 50# | C=O | S | S |
| 51 | NR1 | C(R1)2 | C(R1)2 |
| 52# | NR1 | C(R1)2 | C=O |
| 53 | NR1 | C(R1)2 | NR1 |
| 54 | NR1 | C(R1)2 | O |
| 55 | NR1 | C(R1)2 | S |
| 56# | NR1 | C=O | C(R1)2 |
| 57# | NR1 | C=O | C=O |
| 58# | NR1 | C=O | NR1 |
| 59# | NR1 | C=O | O |
| 60# | NR1 | C=O | S |
| 61 | NR1 | NR1 | C(R1)2 |
| 62# | NR1 | NR1 | C=O |
| 63 | NR1 | NR1 | NR1 |
| 64 | NR1 | NR1 | O |
| 65 | NR1 | NR1 | S |
| 66 | NR1 | O | C(R1)2 |
| 67# | NR1 | O | C=O |
| 68 | NR1 | O | NR1 |
| 69 | NR1 | O | O |
| 70 | NR1 | O | S |
| 71 | NR1 | S | C(R1)2 |
| 72# | NR1 | S | C=O |
| 73 | NR1 | S | NR1 |
| 74 | NR1 | S | O |
| 75 | NR1 | S | S |
| 76# | O | C(R1)2 | C(R1)2 |
| 77# | O | C(R1)2 | C=O |
| 78# | O | C(R1)2 | NR1 |
| 79# | O | C(R1)2 | O |
| 80# | O | C(R1)2 | S |
| 81# | O | C=O | C(R1)2 |
| 82# | O | C=O | C=O |
| 83# | O | C=O | NR1 |
| 84# | O | C=O | O |
| 85# | O | C=O | S |
| 86# | O | NR1 | C(R1)2 |
| 87# | O | NR1 | C=O |
| 88# | O | NR1 | NR1 |
| 89# | O | NR1 | O |
| 90# | O | NR1 | S |
| 91# | O | O | C(R1)2 |
| 92# | O | O | C=O |
| 93# | O | O | NR1 |
| 94# | O | O | O |
| 95# | O | O | S |
| 96# | O | S | C(R1)2 |
| 97# | O | S | C=O |
| 98# | O | S | NR1 |
| 99# | O | S | O |
| 100# | O | S | S |
| 101# | S | C(R1)2 | C(R1)2 |
| 102# | S | C(R1)2 | C=O |
| 103# | S | C(R1)2 | NR1 |
| 104# | S | C(R1)2 | O |
| 105# | S | C(R1)2 | S |
| 106# | S | C=O | C(R1)2 |
| 107# | S | C=O | C=O |
| 108# | S | C=O | NR1 |
| 109# | S | C=O | O |
| 110# | S | C=O | S |
| 111# | S | NR1 | C(R1)2 |
| 112# | S | NR1 | C=O |
| 113# | S | NR1 | NR1 |
| 114# | S | NR1 | O |
| 115# | S | NR1 | S |
| 116# | S | O | C(R1)2 |
| 117# | S | O | C=O |
| 118# | S | O | NR1 |
| 119# | S | O | O |
| 120# | S | O | S |
| 121# | S | S | C(R1)2 |
| 122# | S | S | C=O |
| 123# | S | S | NR1 |
| 124# | S | S | O |
| 125# | S | S | S |
-
Anspruchsgemäß stellt X1 eine Gruppe der Formel NR1 dar, ganz besonders bevorzugt eine Gruppe NR1, in der R1 ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen darstellt, welches mit einem oder mehreren Resten R3 substituiert sein kann.
-
Gemäß einer bevorzugten Ausführungsform steht, wenn eine oder mehrere der Gruppen X1, X2 und X3 eine Gruppe der Formel NR1 darstellen, der Rest R1 der Gruppe NR1 nicht für H, D oder eine Alkylgruppe.
-
Gemäß einer besonders bevorzugten Ausführungsform stellt, wenn eine oder mehrere der Gruppen X1, X2 und X3 eine Gruppe der Formel NR1 darstellen, R1 in NR1 eine Gruppe der Formel C(O)R3, COOR3, CON(R3)2, S(=O)R3, S(=O)2R3, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen dar, das jeweils durch einen oder mehrere Reste R3 substituiert sein kann, oder eine Aryloxy-, Heteroaryloxy-, Aralkyl- oder Heteroaralkylgruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R3 substituiert sein kann, oder eine Kombination dieser Systeme.
-
Ganz besonders bevorzugt stellt, wenn eine oder mehrere der Gruppen X1, X2 und X3 eine Gruppe der Formel NR1 darstellen, R1 als Bestandteil der Gruppe NR1 ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen dar, welches mit einem oder mehreren Resten R3 substituiert sein kann. Noch stärker bevorzugt ist R1 in diesem Fall eine Aryl- oder Heteroarylgruppe mit 5 bis 20 aromatischen Ringatomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann. Am stärksten bevorzugt ist R1 in NR1, welches für X1, X2 und/oder X3 steht, ausgewählt aus Phenyl, Biphenyl, Terphenyl, Quaterphenyl, Naphthyl, Anthracenyl, Pyrenyl, Phenanthrenyl, Benzanthracenyl, Perylenyl, Fluoranthenyl, Benzimidazolyl, Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl und Triazinyl, wobei die genannten Gruppen jeweils mit einer oder mehreren Gruppen R3 substituiert sein können.
-
In einer weiteren bevorzugten Ausführungsform der Erfindung ist R1 bei jedem Auftreten gleich oder verschieden H, D, F, CN, Si(R3)3, N(R3)2 oder eine geradkettige Alkyl- oder Alkoxygruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl- oder Alkoxygruppe mit 3 bis 20 C-Atomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein können, wobei eine oder mehrere CH2-Gruppen durch -C≡C-, -R3C=CR3-, Si(R3)2, C=O, C=NR3, -NR3-, -O-, -S-, -COO- oder -CONR3- ersetzt sein können, oder eine Aryl- oder Heteroarylgruppe mit 5 bis 20 aromatischen Ringatomen, die jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei zwei oder mehrere Reste R1 miteinander verknüpft sein können und ein aliphatisches oder aromatisches Ringsystem bilden können.
-
In einer weiteren bevorzugten Ausführungsform der Erfindung ist R3 bei jedem Auftreten gleich oder verschieden H, D, F, CN, Si(R4)3, N(R4)2 oder eine geradkettige Alkyl- oder Alkoxygruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl- oder Alkoxygruppe mit 3 bis 20 C-Atomen, die jeweils mit einem oder mehreren Resten R4 substituiert sein können, wobei eine oder mehrere CH2-Gruppen durch -C≡C-, -R4C=CR4-, Si(R1)2, C=O, C=NR4, -NR4-, -O-, -S-, -COO- oder -CONR4- ersetzt sein können, oder eine Aryl- oder Heteroarylgruppe mit 5 bis 20 aromatischen Ringatomen, die jeweils mit einem oder mehreren Resten R4 substituiert sein kann, wobei zwei oder mehrere Reste R3 miteinander verknüpft sein können und ein aliphatisches oder aromatisches Ringsystem bilden können.
-
Anspruchsgemäß entspricht die Verbindung der Formel (I-1)
wobei die Gruppen X
1, X
2, X
3, Z wie oben definiert sind.
-
Bevorzugt gilt für die erfindungsgemäßen Verbindungen, dass nicht mehr als zwei benachbarte Gruppen Z gleich N sind. Weiterhin bevorzugt gilt, dass nicht mehr als drei Gruppen Z pro aromatischem Ring gleich N sind und die restlichen Gruppen Z gleich CR1 sind. Besonders bevorzugt ist, dass nicht mehr als eine Gruppe Z pro aromatischem Ring gleich N ist und die restlichen Gruppen Z gleich CR1 sind. Ganz besonders bevorzugt sind alle Gruppen Z gleich CR1.
-
Ganz besonders bevorzugt sind weiterhin Verbindungen gemäß der folgenden Formel (I-1a)
wobei Ar einer Gruppe R
1 entspricht, und X
2, X
3, wie oben definiert sind und weiterhin die Verbindungen gemäß den oben aufgeführten Formeln mit einem oder mehreren Resten R
1 substituiert sein können.
-
Es gelten für die Formel (I-1a) insbesondere die oben genannten bevorzugten Ausführungsformen für die Gruppen X2, X3.
-
Die in den vorangegangenen Abschnitten beschriebenen bevorzugten Ausführungsformen sind erfindungsgemäß beliebig miteinander kombinierbar.
-
Beispiele für erfindungsgemäße Verbindungen werden in der folgenden Tabelle aufgeführt. Verbindungen mit der Markierung # sind nicht anspruchsgemäß.
| | |
| 1 | 2 |
| | |
| 3 | 4 |
| | |
| 5 | 6 |
| | |
| 7 | 8 |
| | |
| 9 | 10 |
| | |
| 11 | 12 |
| | |
| 13 | 14 |
| | |
| 15 | 16 |
| | |
| 17 | 18 # |
| | |
| 19# | 20 # |
| | |
| 21 # | 22 # |
| | |
| 23 | 24 |
| | |
| 25 | 26 |
| | |
| 27 | 28 |
| | |
| 29 | 30 |
| | |
| 31 # | 32 # |
-
Die erfindungsgemäßen Verbindungen können nach dem Fachmann bekannten Syntheseschritten, wie z. B. Bromierung, Suzuki-Kupplung, Hartwig-Buchwald-Kupplung, etc., dargestellt werden.
-
Mögliche Wege zur Synthese von Verbindungen der Formel (I-1) mit einem substituierten Stickstoffatom als Gruppe X1 werden allgemein in den folgenden Schemata 1 bis 4 dargestellt.
-
Auf analoge Weise (nicht anspruchsgemäß) können auch Verbindungen gemäß Formel (I-1), in denen X1 eine andere Gruppe, beispielsweise O, S oder C(R1)2 darstellt, erhalten werden. In diesen Fällen wird statt vom entsprechenden Carbazolderivat von einem Dibenzothiophen-, Dibenzofuran- oder Fluorenderivat ausgegangen.
-
Analog (nicht anspruchsgemäß) können auch Verbindungen hergestellt werden, in denen statt der gezeigten aromatischen Ringe stickstoffanaloge Heterocyclen vorkommen, darunter bevorzugt Pyridin, Pyrimidin, Pyridazin, Pyrazin und Triazin.
-
Im folgenden Schema 1 (nicht anspruchsgemäß) wird unter anderem die Synthese von Verbindungen gemäß Formel (la) mit X2 als Gruppe N-H bzw. N-Ar und X3 als Gruppe C=O dargestellt (Verbindungen Typ a). Dazu wird von einem halogensubstituierten Carbazolderivat ausgegangen, welches in einer Ullmann-Kupplung mit einem Anthranilsäurederivat umgesetzt wird. Das dabei entstehende Derivat wird mit POCl3 bei ca. 60 °C umgesetzt, wobei eine Ringschlussreaktion stattfindet und der Sechsring mit der verbrückenden Gruppe C=O als X3 entsteht. Die entstehende Verbindung kann beispielsweise in einer Hartwig-Buchwald-Reaktion N-aryliert werden.
-
In einer Variante der Umsetzung mit POCl
3, in der eine Temperatur von ca. 120 °C eingesetzt wird, entsteht statt eines Derivats des Typs a ein Verbindungstyp b, der der erfindungsgemäßen Formel (Ib) entspricht, mit X
4 als Stickstoffatom und X
5 als Gruppe C-Cl. Aus diesen Verbindungen kann über eine Defunktionalisierungsreaktion die unfunktionalisierte Verbindung mit X
5 als CH hergestellt werden, oder es kann über eine Kupplungsreaktion, beispielsweise eine Suzuki-Kupplung, eine Arylgruppe an der Stelle des Chloratoms eingeführt werden (vgl. Schema 1).
Weiterhin können ausgehend vom Intermediat, das in der in Schema 1 gezeigten Ullmann-Kupplung entsteht, durch Umsetzung mit einer Alkyllithiumverbindung und anschließender Behandlung mit Säure, beispielsweise Methansulfonsäure oder Polyphosphorsäure, Verbindungen des Typs c mit X
2 als N-H oder N-Ar und X
3 als C(R)
2 erhalten werden (Schema 2).
-
Nochmals weiterhin können, wie in Schema 3 gezeigt, ausgehend von Hydroxyl- bzw. Thiol-substituierten Carbazolderivaten durch Umsetzung mit einem halogensubstituierten Benzoesäurederivat Diarylether- bzw. Diarylthioether-Intermediate erhalten werden.
-
Diese Intermediate können, analog zu dem in Schema 1 Gezeigten, mit POCl
3 zu Verbindungen des Typs d (nicht anspruchsgemäß) (X
2 = O) bzw. des Typs e (nicht anspruchsgemäß) (X
2 = S) umgesetzt werden (Schema 4). Alternativ können die Intermediate, analog zu dem in Schema 2 Gezeigten, durch Addition von Organolithiumverbindungen und anschließender Säurebehandlung zu Verbindungen des Typs f (X
2 = O) bzw. des Typs g (X
2 = S) umgesetzt werden (Schema 4).
-
Gegenstand der Erfindung ist somit ein Verfahren zur Herstellung der erfindungsgemäßen Verbindungen gemäß Formel (I-1), dadurch gekennzeichnet, dass ein Zwischenprodukt gemäß untenstehender Formel (Za) oder (Zb) (nicht anspruchsgemäß) eingesetzt wird
wobei die auftretenden Symbole wie oben definiert sind und E
2 eine Vorstufe der divalenten Gruppe X
2, E
3 eine Vorstufe der divalenten Gruppe X
3, E
4 eine Vorstufe der Gruppe X
4 und E
5 eine Vorstufe der Gruppe X
5 darstellt.
-
Die oben beschriebenen erfindungsgemäßen Verbindungen, insbesondere Verbindungen, welche mit reaktiven Abgangsgruppen, wie Brom, lod, Boronsäure oder Boronsäureester, substituiert sind, können als Monomere zur Erzeugung entsprechender Oligomere, Dendrimere oder Polymere Verwendung finden. Die Oligomerisation bzw. Polymerisation erfolgt dabei bevorzugt über die Halogenfunktionalität bzw. die Boronsäurefunktionalität.
-
Weiterer Gegenstand der Erfindung (nicht anspruchsgemäß) sind daher Oligomere, Polymere oder Dendrimere enthaltend eine oder mehrere Verbindungen gemäß Formel (I-1), wobei die Bindung(en) zum Polymer, Oligomer oder Dendrimer an beliebigen, in Formel (I-1) mit R1 substituierten Positionen lokalisiert sein können. Je nach Verknüpfung der Verbindung gemäß Formel (I-1) ist die Verbindung Bestandteil einer Seitenkette des Oligomers oder Polymers oder Bestandteil der Hauptkette. Unter einem Oligomer im Sinne dieser Erfindung wird eine Verbindung verstanden, welche aus mindestens drei Monomereinheiten aufgebaut ist. Unter einem Polymer im Sinne der Erfindung wird eine Verbindung verstanden, die aus mindestens zehn Monomereinheiten aufgebaut ist. Die erfindungsgemäßen Polymere, Oligomere oder Dendrimere können konjugiert, teilkonjugiert oder nicht-konjugiert sein. Die erfindungsgemäßen Oligomere oder Polymere können linear, verzweigt oder dendritisch sein.
-
In den linear verknüpften Strukturen können die Einheiten gemäß Formel (I-1) direkt miteinander verknüpft sein oder sie können über eine bivalente Gruppe, beispielsweise über eine substituierte oder unsubstituierte Alkylengruppe, über ein Heteroatom oder über eine bivalente aromatische oder heteroaromatische Gruppe miteinander verknüpft sein. In verzweigten und dendritischen Strukturen können beispielsweise drei oder mehrere Einheiten gemäß Formel (I-1) über eine trivalente oder höhervalente Gruppe, beispielsweise über eine trivalente oder höhervalente aromatische oder heteroaromatische Gruppe, zu einem verzweigten bzw. dendritischen Oligomer oder Polymer verknüpft sein.
-
Für die Wiederholeinheiten gemäß Formel (I-1) in Oligomeren, Dendrimeren und Polymeren gelten dieselben Bevorzugungen wie oben für Verbindungen gemäß Formel (I-1) beschrieben.
-
Zur Herstellung der Oligomere oder Polymere werden die erfindungsgemäßen Monomere homopolymerisiert oder mit weiteren Monomeren copolymerisiert. Geeignete und bevorzugte Comonomere sind gewählt aus Fluorenen (z. B. gemäß
EP 842208 oder
WO 00/22026 ), Spirobifluorenen (z. B. gemäß
EP 707020 ,
EP 894107 oder
WO 06/061181 ), Paraphenylenen (z. B. gemäß
WO 92/18552 ), Carbazolen (z. B. gemäß
WO 04/070772 oder
WO 04/113468 ), Thiophenen (z. B. gemäß
EP 1028136 ), Dihydrophenanthrenen (z. B. gemäß
WO 05/014689 oder
WO 07/006383 ), cis- und trans-Indenofluorenen (z. B. gemäß
WO 04/041901 oder
WO 04/113412 ), Ketonen (z. B. gemäß
WO 05/040302 ), Phenanthrenen (z. B. gemäß
WO 05/104264 oder
WO 07/017066 ) oder auch mehreren dieser Einheiten. Die Polymere, Oligomere und Dendrimere enthalten üblicherweise noch weitere Einheiten, beispielsweise emittierende (fluoreszierende oder phosphoreszierende) Einheiten, wie z. B. Vinyltriarylamine (z. B. gemäß
WO 07/068325 ) oder phosphoreszierende Metallkomplexe (z. B. gemäß
WO 06/003000 ), und/oder Ladungstransporteinheiten, insbesondere solche basierend auf Triarylaminen.
-
Die erfindungsgemäßen Polymere, Oligomere und Dendrimere weisen vorteilhafte Eigenschaften, insbesondere hohe Lebensdauern, hohe Effizienzen und gute Farbkoordinaten auf.
-
Die erfindungsgemäßen Polymere und Oligomere werden in der Regel durch Polymerisation von einer oder mehreren Monomersorten hergestellt, von denen mindestens ein Monomer im Polymer zu Wiederholungseinheiten der Formel (I-1) führt. Geeignete Polymerisationsreaktionen sind dem Fachmann bekannt und in der Literatur beschrieben. Besonders geeignete und bevorzugte Polymerisationsreaktionen, die zu C-C- bzw. C-N-Verknüpfungen führen, sind folgende:
- (A) SUZUKI-Polymerisation;
- (B) YAMAMOTO-Polymerisation;
- (C) STILLE-Polymerisation; und
- (D) HARTWIG-BUCHWALD-Polymerisation.
-
Wie die Polymerisation nach diesen Methoden durchgeführt werden kann und wie die Polymere dann vom Reaktionsmedium abgetrennt und aufgereinigt werden können, ist dem Fachmann bekannt und in der Literatur, beispielsweise in
WO 2003/048225 ,
WO 2004/037887 und
WO 2004/037887 , im Detail beschrieben.
-
Gegenstand der vorliegenden Erfindung ist somit auch ein Verfahren zur Herstellung der erfindungsgemäßen Polymere, Oligomere und Dendrimere, das dadurch gekennzeichnet ist, dass sie durch Polymerisation gemäß SUZUKI, Polymerisation gemäß YAMAMOTO, Polymerisation gemäß STILLE oder Polymerisation gemäß HARTWIG-BUCHWALD hergestellt werden. Die erfindungsgemäßen Dendrimere können gemäß dem Fachmann bekannten Verfahren oder in Analogie dazu hergestellt werden. Geeignete Verfahren sind in der Literatur beschrieben, wie z. B. in
Frechet, Jean M. J.; Hawker, Craig J., „Hyperbranched polyphenylene and hyperbranched polyesters: new soluble, three-dimensional, reactive polymers", Reactive & Functional Polymers (1995), 26(1-3), 127-36;
Janssen, H. M.; Meijer, E. W., „The synthesis and characterization of dendritic molecules", Materials Science and Technology (1999), 20 (Synthesis of Polymers), 403-458;
Tomalia, Donald A., „Dendrimer molecules", Scientific American (1995), 272(5), 62-6;
WO 02/067343 A1 und
WO 2005/026144 A1 .
-
Die erfindungsgemäßen Verbindungen gemäß Formel (I-1) eignen sich für den Einsatz in elektronischen Vorrichtungen, insbesondere in organischen Elektrolumineszenzvorrichtungen (OLEDs). Abhängig von der Substitution werden die Verbindungen in unterschiedlichen Funktionen und Schichten eingesetzt. Beispielsweise sind Verbindungen, welche elektronenarme Gruppen wie Sechsring-Heteroarylgruppen mit einem, bevorzugt mehreren, Stickstoffatomen oder Fünfring-Heteroarylgruppen mit zwei oder mehr Stickstoffatomen enthalten, besonders zur Verwendung als Matrixmaterial für phosphoreszierende Dotanden oder als Elektronentransportmaterial geeignet.
-
Bevorzugt werden die erfindungsgemäßen Verbindungen in einer Lochtransport- und/oder Lochinjektionsschicht oder in einer emittierenden Schicht als Matrixmaterial eingesetzt. Sie können aber auch in anderen Schichten und/oder Funktionen eingesetzt werden, beispielsweise in einer emittierenden Schicht als fluoreszierende Dotanden oder in einer Elektronentransportschicht als Elektronentransportmaterialien.
-
Ein weiterer Gegenstand der Erfindung ist daher die Verwendung der erfindungsgemäßen Verbindungen gemäß Formel (I-1) in elektronischen Vorrichtungen. Dabei sind die elektronischen Vorrichtungen bevorzugt ausgewählt aus der Gruppe bestehend aus organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs), organischen Laserdioden (O-Laser) und besonders bevorzugt organischen Elektrolumineszenzvorrichtungen (OLEDs).
-
Gegenstand der Erfindung (nicht anspruchsgemäß) sind auch Formulierungen enthaltend mindestens eine Verbindung gemäß Formel (I-1) oder mindestens ein Polymer, Oligomer oder Dendrimer enthaltend mindestens eine Einheit gemäß Formel (I-1) sowie mindestens ein Lösungsmittel, bevorzugt ein organisches Lösungsmittel.
-
Die erfindungsgemäßen Formulierungen finden beispielsweise bei der Herstellung von organischen Elektrolumineszenzvorrichtungen Verwendung, die in einem folgenden Abschnitt näher beschrieben wird.
-
Nochmals ein weiterer Gegenstand der Erfindung sind elektronische Vorrichtungen (nicht anspruchsgemäß), enthaltend mindestens eine Verbindung gemäß Formel (I-1). Dabei sind die elektronischen Vorrichtungen bevorzugt ausgewählt aus den oben genannten Vorrichtungen. Besonders bevorzugt sind organische Elektrolumineszenzvorrichtungen, enthaltend Anode, Kathode und mindestens eine emittierende Schicht, dadurch gekennzeichnet, dass mindestens eine organische Schicht, die eine emittierende Schicht, eine Lochtransportschicht oder eine andere Schicht sein kann, mindestens eine Verbindung gemäß Formel (I-1) enthält.
-
Außer Kathode, Anode und der emittierenden Schicht kann die organische Elektrolumineszenzvorrichtung noch weitere Schichten enthalten. Diese sind beispielsweise gewählt aus jeweils einer oder mehreren Lochinjektionsschichten, Lochtransportschichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Elektronenblockierschichten, Excitonenblockierschichten, Ladungserzeugungsschichten (Charge-Generation Layers) (IDMC 2003, Taiwan; Session 21 OLED (5), T. Matsumoto, T. Nakada, J. Endo, K. Mori, N. Kawamura, A. Yokoi, J. Kido, Multiphoton Organic EL Device Having Charge Generation Layer), Auskopplungsschichten und/oder organischen oder anorganischen p/n-Übergängen. Es sei aber darauf hingewiesen, dass nicht notwendigerweise jede dieser Schichten vorhanden sein muss und die Wahl der Schichten immer von den verwendeten Verbindungen abhängt und insbesondere auch von der Tatsache, ob es sich um eine fluoreszierende oder phosphoreszierende Elektrolumineszenzvorrichtung handelt.
-
Die organische Elektrolumineszenzvorrichtung kann auch mehrere emittierende Schichten enthalten. Besonders bevorzugt weisen diese Emissionsschichten in diesem Fall insgesamt mehrere Emissionsmaxima zwischen 380 nm und 750 nm auf, so dass insgesamt weiße Emission resultiert, d. h. in den emittierenden Schichten werden verschiedene emittierende Verbindungen verwendet, die fluoreszieren oder phosphoreszieren können und die blaues und gelbes, orange oder rotes Licht emittieren. Insbesondere bevorzugt sind Dreischichtsysteme, also Systeme mit drei emittierenden Schichten, wobei mindestens eine dieser Schichten mindestens eine Verbindung gemäß Formel (I-1) enthält und wobei die drei Schichten blaue, grüne und orange oder rote Emission zeigen (für den prinzipiellen Aufbau siehe z. B.
WO 05/011013 ). Alternativ und/oder zusätzlich können die erfindungsgemäßen Verbindungen auch in der Lochtransportschicht vorhanden sein. Ebenso eignen sich für weiße Emission Emitter, welche breitbandige Emissionsbanden aufweisen und dadurch weiße Emission zeigen.
-
Es ist erfindungsgemäß bevorzugt, dass die Verbindung gemäß Formel (I-1) in einer elektronischen Vorrichtung enthaltend einen oder mehrere phosphoreszierende Dotanden eingesetzt wird. Dabei kann die Verbindung in unterschiedlichen Schichten, bevorzugt in einer Lochtransportschicht, einer Lochinjektionsschicht oder in der emittierenden Schicht verwendet werden. Die Verbindung gemäß Formel (I-1) kann aber auch erfindungsgemäß in einer elektronischen Vorrichtung enthaltend einen oder mehrere fluoreszierende Dotanden eingesetzt werden.
-
Als phosphoreszierende Dotanden (= Triplettemitter) eignen sich insbesondere Verbindungen, die bei geeigneter Anregung Licht, vorzugsweise im sichtbaren Bereich, emittieren und außerdem mindestens ein Atom der Ordnungszahl größer 20, bevorzugt größer 38 und kleiner 84, besonders bevorzugt größer 56 und kleiner 80 enthalten. Bevorzugt werden als Phosphoreszenzemitter Verbindungen, die Kupfer, Molybdän, Wolfram, Rhenium, Ruthenium, Osmium, Rhodium, Iridium, Palladium, Platin, Silber, Gold oder Europium enthalten, verwendet, insbesondere Verbindungen, die Iridium, Platin oder Kupfer enthalten.
-
Dabei werden im Sinne der vorliegenden Erfindung alle lumineszierenden Iridium-, Platin- oder Kupferkomplexe als phosphoreszierende Verbindungen angesehen.
-
Beispiele der oben beschriebenen Emitter können den Anmeldungen
WO 00/70655 ,
WO 01/41512 ,
WO 02/02714 ,
WO 02/15645 ,
EP 1191613 ,
EP 1191612 ,
EP 1191614 ,
WO 05/033244 ,
WO 05/019373 und
US 2005/0258742 entnommen werden. Generell eignen sich alle phosphoreszierenden Komplexe, wie sie gemäß dem Stand der Technik für phosphoreszierende OLEDs verwendet werden und wie sie dem Fachmann auf dem Gebiet der organischen Elektrolumineszenzvorrichtungen bekannt sind. Auch kann der Fachmann ohne erfinderisches Zutun weitere phosphoreszierende Komplexe in Kombination mit den erfindungsgemäßen Verbindungen gemäß Formel (1-1) in organischen Elektrolumineszenzvorrichtungen einsetzen.
-
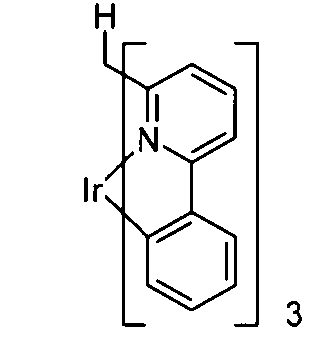
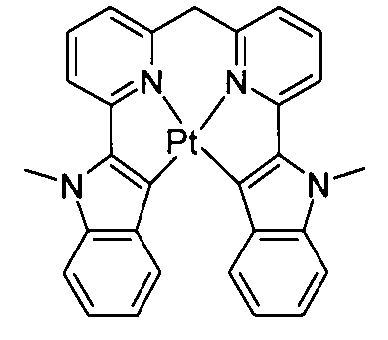
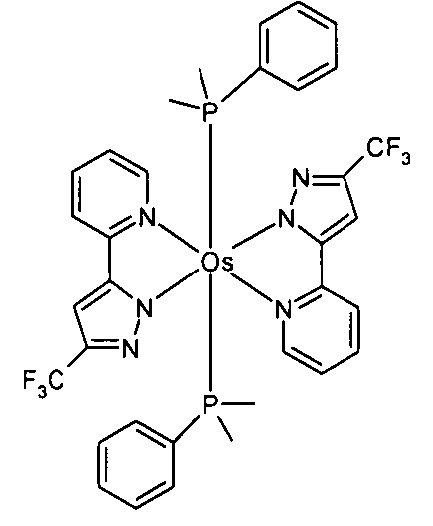
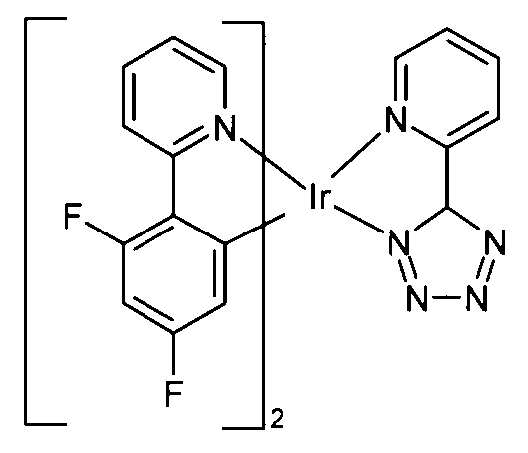
Beispiele für geeignete phosphoreszierende Emitterverbindungen können weiterhin der folgenden Tabelle entnommen werden:
-
In einer bevorzugten Ausführungsform der Erfindung werden die Verbindungen gemäß Formel (I-1) als Lochtransportmaterial eingesetzt. Die Verbindungen werden dann bevorzugt in einer Lochtransportschicht und/oder in einer Lochinjektionsschicht eingesetzt. Eine Lochinjektionsschicht im Sinne dieser Erfindung ist eine Schicht, die direkt an die Anode angrenzt. Eine Lochtransportschicht im Sinne dieser Erfindung ist eine Schicht, die zwischen der Lochinjektionsschicht und der Emissionsschicht liegt. Die Lochtransportschicht kann direkt an die Emissionsschicht angrenzen. Wenn die Verbindungen gemäß Formel (I-1) als Lochtransportmaterial oder als Lochinjektionsmaterial verwendet werden, kann es bevorzugt sein, wenn sie mit Elektronenakzeptor-Verbindungen dotiert sind, beispielsweise mit F
4-TCNQ oder mit Verbindungen, wie sie in
EP 1476881 oder
EP 1596445 beschrieben werden. In einer weiteren bevorzugten Ausführungsform der Erfindung wird eine Verbindung gemäß Formel (I-1) als Lochtransportmaterial in Kombination mit einem Hexaazatriphenylenderivat wie in
US 2007/0092755 beschrieben verwendet. Besonders bevorzugt wird das Hexaazatriphenylenderivat dabei in einer eigenen Schicht eingesetzt.
-
So ist beispielsweise eine Struktur bevorzugt, die folgenden Aufbau besitzt: Anode - Hexaazatriphenylenderivat - Lochtransportschicht, wobei die Lochtransportschicht eine oder mehrere Verbindungen gemäß Formel (I-1) enthält. Ebenso ist es in diesem Aufbau möglich, mehrere aufeinander folgende Lochtransportschichten zu verwenden, wobei wenigstens eine Lochtransportschicht wenigstens eine Verbindung gemäß Formel (I-1) enthält. Der folgende Strukturaufbau ist ebenfalls bevorzugt: Anode - Lochtransportschicht - Hexaazatriphenylenderivat - Lochtransportschicht, wobei wenigstens eine der beiden Lochtransportschichten eine oder mehrere Verbindungen gemäß Formel (I-1) enthält. Ebenso ist es in diesem Aufbau möglich, dass statt einer Lochtransportschicht mehrere aufeinander folgende Lochtransportschichten verwendet werden, wobei wenigstens eine Lochtransportschicht wenigstens eine Verbindung gemäß Formel (I-1) enthält.
-
Wird die Verbindung gemäß Formel (I-1) als Lochtransportmaterial in einer Lochtransportschicht eingesetzt, so kann die Verbindung als Reinmaterial, d.h. in einem Anteil von 100 % in der Lochtransportschicht eingesetzt werden oder sie kann in Kombination mit einer oder mehreren weiteren Verbindungen in der Lochtransportschicht eingesetzt werden.
-
In einer weiteren Ausführungsform der vorliegenden Erfindung werden die Verbindungen der Formel (1-1) als Matrixmaterial in Kombination mit einem oder mehreren Dotanden, vorzugsweise phosphoreszierenden Dotanden, eingesetzt.
-
Unter einem Dotanden wird in einem System enthaltend ein Matrixmaterial und einen Dotanden diejenige Komponente verstanden, deren Anteil in der Mischung der kleinere ist. Entsprechend wird unter einem Matrixmaterial in einem System enthaltend ein Matrixmaterial und einen Dotanden diejenige Komponente verstanden, deren Anteil in der Mischung der größere ist.
-
Der Anteil des Matrixmaterials in der emittierenden Schicht beträgt in diesem Fall zwischen 50.0 und 99.9 Vol.-%, bevorzugt zwischen 80.0 und 99.5 Vol.-% und besonders bevorzugt für fluoreszierende emittierende Schichten zwischen 92.0 und 99.5 Vol.-% sowie für phosphoreszierende emittierende Schichten zwischen 85.0 und 97.0 Vol.-%. Entsprechend beträgt der Anteil des Dotanden zwischen 0.1 und 50.0 Vol.-%, bevorzugt zwischen 0.5 und 20.0 Vol.-% und besonders bevorzugt für fluoreszierende emittierende Schichten zwischen 0.5 und 8.0 Vol.-% sowie für phosphoreszierende emittierende Schichten zwischen 3.0 und 15.0 Vol.-%.
-
Geeignete phosphoreszierende Dotanden sind die weiter vorne genannten phosphoreszierenden Emitterverbindungen.
-
Eine emittierende Schicht einer organischen Elektrolumineszenzvorrichtung kann auch Systeme umfassend mehrere Matrixmaterialien (Mixed-Matrix-Systeme) und/oder mehrere Dotanden enthalten. Auch in diesem Fall sind die Dotanden im Allgemeinen diejenigen Materialien, deren Anteil im System der kleinere ist und die Matrixmaterialien sind diejenigen Materialien, deren Anteil im System der größere ist. In Einzelfällen kann jedoch der Anteil eines einzelnen Matrixmaterials im System kleiner sein als der Anteil eines einzelnen Dotanden.
-
In einer bevorzugten Ausführungsform der Erfindung werden die Verbindungen gemäß Formel (I-1) als eine Komponente von Mixed-Matrix-Systemen verwendet. Die Mixed-Matrix-Systeme umfassen bevorzugt zwei oder drei verschiedene Matrixmaterialien, besonders bevorzugt zwei verschiedene Matrixmaterialien. Die beiden unterschiedlichen Matrixmaterialien können dabei in einem Verhältnis von 1:10 bis 1:1 vorhanden sein, bevorzugt in einem Verhältnis von 1:4 bis 1:1. Die Mixed-Matrix-Systeme können einen oder mehrere Dotanden umfassen. Die Dotandverbindung bzw. die Dotandverbindungen zusammen haben erfindungsgemäß einen Anteil von 0.1 bis 50.0 Vol.-% an der Gesamtmischung und bevorzugt einen Anteil von 0.5 bis 20.0 Vol.- % an der Gesamtmischung. Entsprechend haben die Matrixkomponenten zusammen einen Anteil von 50.0 bis 99.9 Vol-% an der Gesamtmischung und bevorzugt einen Anteil von 80.0 bis 99.5 Vol.-% an der Gesamtmischung.
-
Bevorzugt werden Mixed-Matrix-Systeme in phosphoreszierenden organischen Elektrolumineszenzvorrichtungen eingesetzt.
-
Besonders geeignete Matrixmaterialien, welche in Kombination mit den erfindungsgemäßen Verbindungen als Matrixkomponenten eines Mixed-Matrix-Systems eingesetzt werden können, sind aromatische Ketone, aromatische Phosphinoxide oder aromatische Sulfoxide oder Sulfone, z. B. gemäß
WO 04/013080 ,
WO 04/093207 ,
WO 06/005627 oder
WO 10/006680 , Triarylamine, Carbazolderivate, z. B. CBP (N,N-Bis-carbazolylbiphenyl) oder die in
WO 05/039246 ,
US 2005/0069729 ,
JP 2004/288381 ,
EP 1205527 oder
WO 08/086851 offenbarten Carbazolderivate, Indolocarbazolderivate, z. B. gemäß
WO 07/063754 oder
WO 08/056746 , Azacarbazolderivate, z. B. gemäß
EP 1617710 ,
EP 1617711 ,
EP 1731584 ,
JP 2005/347160 , bipolare Matrixmaterialien, z. B. gemäß
WO 07/137725 , Silane, z. B. gemäß
WO 05/111172 , Azaborole oder Boronester, z. B. gemäß
WO 06/117052 , Triazinderivate, z. B. gemäß
WO 2010/015306 ,
WO 07/063754 oder
WO 08/056746 , Zinkkomplexe, z. B. gemäß
EP 652273 oder
WO 09/062578 , Diazasilol- bzw. Tetraazasilol-Derivate, z. B. gemäß
WO 10/054729 , Diazaphosphol-Derivate, z. B. gemäß
WO 10/054730 , oder Indenocarbazolderivate, z. B. gemäß
WO 10/136109 .
-
Weiterer Gegenstand der Erfindung sind somit Mischungen enthaltend eine oder mehrere Verbindungen gemäß Formel (I-1) sowie eine oder mehrere weitere Verbindungen ausgewählt aus phosphoreszierenden Dotanden und/oder weiteren Matrixmaterialien, bevorzugt aromatischen Ketonen, aromatischen Phosphinoxiden oder aromatischen Sulfoxiden oder Sulfonen, Triarylaminen, Carbazolderivaten, Indolocarbazolderivaten, Azacarbazolderivaten, bipolaren Matrixmaterialien, Silanen, Azaborolen oder Boronestern, Triazinderivaten, Zinkkomplexen, Diazasilol- bzw. Tetraazasilol-Derivaten, Diazaphosphol-Derivaten und Indenocarbazolderivaten.
-
Bevorzugte phosphoreszierende Dotanden zur Verwendung in Mixed-Matrix-Systemen enthaltend die erfindungsgemäßen Verbindungen sind die in der obenstehenden Tabelle aufgeführten phosphoreszierenden Dotanden.
-
In einer weiteren Ausführungsform der Erfindung werden die die Verbindungen gemäß Formel (I-1) als emittierende Materialien in einer emittierenden Schicht eingesetzt. Die Verbindungen sind insbesondere dann als emittierende Verbindungen geeignet, wenn sie mindestens eine Diarylamino-Gruppe enthalten. Insbesondere bevorzugt werden die erfindungsgemäßen Verbindungen in diesem Fall als grüne oder blaue Emitter verwendet.
-
Der Anteil der Verbindung gemäß Formel (I-1) als Dotand in der Mischung der emittierenden Schicht beträgt in diesem Fall zwischen 0.1 und 50.0 Vol.-%, bevorzugt zwischen 0.5 und 20.0 Vol.-%, besonders bevorzugt zwischen 0.5 und 8.0 Vol.-%. Entsprechend beträgt der Anteil des Matrixmaterials zwischen 50.0 und 99.9 Vol.-%, bevorzugt zwischen 80.0 und 99.5 Vol.-%, besonders bevorzugt zwischen 92.0 und 99.5 Vol.-%.
-
Bevorzugte Matrixmaterialien zur Verwendung in Kombination mit den erfindungsgemäßen Verbindungen als Emitter sind in einem der folgenden Abschnitte aufgeführt. Sie entsprechen den als bevorzugt aufgeführten Matrixmaterialien für fluoreszierende Emitter.
-
Im Folgenden werden die in den erfindungsgemäßen elektronischen Vorrichtungen für die jeweiligen Funktionen bzw. in den jeweiligen Funktionsschichten bevorzugt eingesetzten Materialien aufgeführt.
-
Bevorzugte fluoreszierende Emittermaterialien sind ausgewählt aus der Klasse der Monostyrylamine, der Distyrylamine, der Tristyrylamine, der Tetrastyrylamine, der Styrylphosphine, der Styrylether und der Arylamine. Unter einem Monostyrylamin wird eine Verbindung verstanden, die eine substituierte oder unsubstituierte Styrylgruppe und mindestens ein, bevorzugt aromatisches, Amin enthält. Unter einem Distyrylamin wird eine Verbindung verstanden, die zwei substituierte oder unsubstituierte Styrylgruppen und mindestens ein, bevorzugt aromatisches, Amin enthält. Unter einem Tristyrylamin wird eine Verbindung verstanden, die drei substituierte oder unsubstituierte Styrylgruppen und mindestens ein, bevorzugt aromatisches, Amin enthält. Unter einem Tetrastyrylamin wird eine Verbindung verstanden, die vier substituierte oder unsubstituierte Styrylgruppen und mindestens ein, bevorzugt aromatisches, Amin enthält. Die Styrylgruppen sind besonders bevorzugt Stilbene, die auch noch weiter substituiert sein können. Entsprechende Phosphine und Ether sind in Analogie zu den Aminen definiert. Unter einem Arylamin bzw. einem aromatischen Amin im Sinne dieser Erfindung wird eine Verbindung verstanden, die drei substituierte oder unsubstituierte aromatische oder heteroaromatische Ringsysteme direkt an den Stickstoff gebunden enthält. Bevorzugt ist mindestens eines dieser aromatischen oder heteroaromatischen Ringsysteme ein kondensiertes Ringsystem, besonders bevorzugt mit mindestens 14 aromatischen Ringatomen. Bevorzugte Beispiele hierfür sind aromatische Anthracenamine, aromatische Anthracendiamine, aromatische Pyrenamine, aromatische Pyrendiamine, aromatische Chrysenamine oder aromatische Chrysendiamine. Unter einem aromatischen Anthracenamin wird eine Verbindung verstanden, in der eine Diarylaminogruppe direkt an eine Anthracengruppe gebunden ist, vorzugsweise in 9-Position. Unter einem aromatischen Anthracendiamin wird eine Verbindung verstanden, in der zwei Diarylaminogruppen direkt an eine Anthracengruppe gebunden sind, vorzugsweise in 9,10-Position. Aromatische Pyrenamine, Pyrendiamine, Chrysenamine und Chrysendiamine sind analog dazu definiert, wobei die Diarylaminogruppen am Pyren bevorzugt in 1-Position bzw. in 1,6-Position gebunden sind. Weitere bevorzugte Emittermaterialien sind gewählt aus Indenofluorenaminen bzw. -diaminen, beispielsweise gemäß
WO 06/122630 , Benzoindenofluorenaminen bzw. -diaminen, beispielsweise gemäß
WO 08/006449 , und Dibenzoindenofluorenaminen bzw. -diaminen, beispielsweise gemäß
WO 07/140847 . Beispiele für Emittermaterialien aus der Klasse der Styrylamine sind substituierte oder unsubstituierte Tristilbenamine oder die Emittermaterialien, die in
WO 06/000388 ,
WO 06/058737 ,
WO 06/000389 ,
WO 07/065549 und
WO 07/115610 beschrieben sind. Weiterhin bevorzugt sind die in der Anmeldung
WO 10/012328 offenbarten kondensierten Kohlenwasserstoffe.
-
Weiterhin bevorzugt sind als fluoreszierende Emittermaterialien die erfindungsgemäßen Verbindungen gemäß Formel (I-1).
-
Geeignete Emittermaterialien sind weiterhin die in der folgenden Tabelle abgebildeten Strukturen, sowie die in
JP 06/001973 ,
WO 04/047499 ,
WO 06/098080 ,
WO 07/065678 ,
US 2005/0260442 und
WO 04/092111 offenbarten Derivate dieser Strukturen.
-
Als Matrixmaterialien, bevorzugt für fluoreszierende Dotanden, können Materialien verschiedener Stoffklassen verwendet werden. Bevorzugte Matrixmaterialien sind ausgewählt aus den Klassen der Oligoarylene (z. B. 2,2',7,7'-Tetraphenylspirobifluoren gemäß
EP 676461 oder Dinaphthylanthracen), insbesondere der Oligoarylene enthaltend kondensierte aromatische Gruppen, der Oligoarylenvinylene (z. B. DPVBi oder Spiro-DPVBi gemäß
EP 676461 ), der polypodalen Metallkomplexe (z. B. gemäß
WO 04/081017 ), der lochleitenden Verbindungen (z. B. gemäß
WO 04/058911 ), der elektronenleitenden Verbindungen, insbesondere Ketone, Phosphinoxide, Sulfoxide, etc. (z. B. gemäß
WO 05/084081 und
WO 05/084082 ), der Atropisomere (z. B. gemäß
WO 06/048268 ), der Boronsäurederivate (z. B. gemäß
WO 06/117052 ) oder der Benzanthracene (z. B. gemäß
WO 08/145239 ). Weiterhin kommen als Matrixmaterialien bevorzugt die erfindungsgemäßen Verbindungen in Frage. Besonders bevorzugte Matrixmaterialien sind außer den erfindungsgemäßen Verbindungen ausgewählt aus den Klassen der Oligoarylene, enthaltend Naphthalin, Anthracen, Benzanthracen und/oder Pyren oder Atropisomere dieser Verbindungen, der Oligoarylenvinylene, der Ketone, der Phosphinoxide und der Sulfoxide. Ganz besonders bevorzugte Matrixmaterialien ausgewählt aus den Klassen der Oligoarylene, enthaltend Anthracen, Benzanthracen, Benzphenanthren und/oder Pyren oder Atropisomere dieser Verbindungen. Unter einem Oligoarylen im Sinne dieser Erfindung soll eine Verbindung verstanden werden, in der mindestens drei Aryl- bzw. Arylengruppen aneinander gebunden sind.
-
Geeignete Matrixmaterialien, bevorzugt für fluoreszierende Dotanden, sind beispielsweise die in der folgenden Tabelle abgebildeten Materialien, sowie Derivate dieser Materialien, wie sie in
WO 04/018587 ,
WO 08/006449 ,
US 5935721 ,
US 2005/0181232 ,
JP 2000/273056 ,
EP 681019 ,
US 2004/0247937 und
US 2005/0211958 offenbart werden.
-
Bevorzugte Matrixmaterialien für phosphoreszierende Dotanden sind Carbazolderivate (z. B. CBP (N,N-Biscarbazolylbiphenyl) oder Verbindungen gemäß
WO 2005/039246 ,
US 2005/0069729 ,
JP 2004/288381 ,
EP 1205527 oder
WO 2008/086851 ), Triarylamine, Azacarbazole (z. B. gemäß
EP 1617710 ,
EP 1617711 ,
EP 1731584 ,
JP 2005/347160 ), Indolocarbazolderivate, z. B. gemäß
WO 2007/063754 oder
WO 2008/056746 , Ketone (z. B. gemäß
WO 2004/093207 oder
WO 2010/006680 ), Phosphinoxide, Sulfoxide und Sulfone (z. B. gemäß
WO 2005/003253 ), Oligophenylene, aromatische Amine (z. B. gemäß
US 2005/0069729 ), bipolare Matrixmaterialien (z. B. gemäß WO 2007/137725), Silane (z. B. gemäß
WO 2005/111172 ), Azaborole oder Boronester, z. B. gemäß
WO 2006/117052 , Triazinderivate, z. B. gemäß
WO 2010/015306 ,
WO 2007/063754 oder
WO 2008/056746 , Zinkkomplexe (z. B. gemäß
WO 2009/062578 ) Aluminiumkomplexe (z. B. BAlq), Diazasilol- und Tetraazasilol-Derivate, z. B. gemäß
WO 2010/054730 , Indenocarbazolderivate, z. B. gemäß
WO 2010/136109 und
WO 2011/000455 oder Diazaphosphole, z. B. gemäß
WO 2010/054730 .
-
Geeignete Ladungstransportmaterialien, wie sie in der Lochinjektions- bzw. Lochtransportschicht oder in der Elektronentransportschicht der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung verwendet werden können, sind neben den erfindungsgemäßen Verbindungen beispielsweise die in Y. Shirota et al., Chem. Rev. 2007, 107(4), 953-1010 offenbarten Verbindungen oder andere Materialien, wie sie gemäß dem Stand der Technik in diesen Schichten eingesetzt werden.
-
Als Kathode der organischen Elektrolumineszenzvorrichtung sind Metalle mit geringer Austrittsarbeit, Metalllegierungen oder mehrlagige Strukturen aus verschiedenen Metallen bevorzugt, wie beispielsweise Erdalkalimetalle, Alkalimetalle, Hauptgruppenmetalle oder Lanthanoide (z. B. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Weiterhin eignen sich Legierungen aus einem Alkali- oder Erdalkalimetall und Silber, beispielsweise eine Legierung aus Magnesium und Silber. Bei mehrlagigen Strukturen können auch zusätzlich zu den genannten Metallen weitere Metalle verwendet werden, die eine relativ hohe Austrittsarbeit aufweisen, wie z. B. Ag oder Al, wobei dann in der Regel Kombinationen der Metalle, wie beispielsweise Ca/Ag, Mg/Ag oder Ba/Ag verwendet werden. Es kann auch bevorzugt sein, zwischen einer metallischen Kathode und dem organischen Halbleiter eine dünne Zwischenschicht eines Materials mit einer hohen Dielektrizitätskonstante einzubringen. Hierfür kommen beispielsweise Alkalimetall- oder Erdalkalimetallfluoride, aber auch die entsprechenden Oxide oder Carbonate in Frage (z. B. LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3, etc.). Weiterhin kann dafür Lithiumchinolinat (LiQ) verwendet werden. Die Schichtdicke dieser Schicht beträgt bevorzugt zwischen 0.5 und 5 nm.
-
Als Anode sind Materialien mit hoher Austrittsarbeit bevorzugt. Bevorzugt weist die Anode eine Austrittsarbeit größer 4.5 eV vs. Vakuum auf. Hierfür sind einerseits Metalle mit hohem Redoxpotential geeignet, wie beispielsweise Ag, Pt oder Au. Es können andererseits auch Metall/Metalloxid-Elektroden (z. B. Al/Ni/NiOx, Al/PtOx) bevorzugt sein. Für einige Anwendungen muss mindestens eine der Elektroden transparent oder teiltransparent sein, um entweder die Bestrahlung des organischen Materials (organische Solarzelle) oder die Auskopplung von Licht (OLED, O-LASER) zu ermöglichen. Bevorzugte Anodenmaterialien sind hier leitfähige gemischte Metalloxide. Besonders bevorzugt sind Indium-ZinnOxid (ITO) oder Indium-Zink Oxid (IZO). Bevorzugt sind weiterhin leitfähige, dotierte organische Materialien, insbesondere leitfähige dotierte Polymere.
-
Die Vorrichtung wird entsprechend (je nach Anwendung) strukturiert, kontaktiert und schließlich versiegelt, da sich die Lebensdauer der erfindungsgemäßen Vorrichtungen bei Anwesenheit von Wasser und/oder Luft verkürzt.
-
In einer bevorzugten Ausführungsform ist die erfindungsgemäße organische Elektrolumineszenzvorrichtung dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck kleiner 10-5 mbar, bevorzugt kleiner 10-6 mbar aufgedampft. Dabei ist es jedoch auch möglich, dass der Anfangsdruck noch geringer ist, beispielsweise kleiner 10-7 mbar.
-
Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10-5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden (z. B. M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301).
-
Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie z. B. Siebdruck, Flexodruck, Nozzle Printing oder Offsetdruck, besonders bevorzugt aber LITI (Light Induced Thermal Imaging, Thermotransferdruck) oder Ink-Jet Druck (Tintenstrahldruck), hergestellt werden. Hierfür sind lösliche Verbindungen gemäß Formel (I-1) nötig. Hohe Löslichkeit lässt sich durch geeignete Substitution der Verbindungen erreichen.
-
Weiterhin bevorzugt ist es, dass zur Herstellung einer erfindungsgemäßen organischen Elektrolumineszenzvorrichtung eine oder mehrere Schichten aus Lösung und eine oder mehrere Schichten durch ein Sublimationsverfahren aufgetragen werden.
-
Erfindungsgemäß können die elektronischen Vorrichtungen enthaltend eine oder mehrere Verbindungen gemäß Formel (I-1) in Displays, als Lichtquellen in Beleuchtungsanwendungen sowie als Lichtquellen in medizinischen und/oder kosmetischen Anwendungen (z.B. in der Lichttherapie) eingesetzt werden.
-
Die erfindungsgemäßen Verbindungen weisen eine hervorragende Lochbeweglichkeit auf und sind daher sehr gut als Lochtransportmaterialien geeignet. Die hohe Lochbeweglichkeit ermöglicht eine Senkung der Betriebsspannung und eine Verbesserung der operativen Lebensdauer der elektronischen Vorrichtungen enthaltend die erfindungsgemäßen Verbindungen. Weiterhin führen die erfindungsgemäßen Verbindungen bei der Verwendung in elektronischen Vorrichtungen zu einer höheren Leistungseffizienz der Vorrichtungen.
-
Weiterhin zeichnen sich die Verbindungen gemäß Formel (I-1) durch eine hohe Oxidationsstabilität in Lösung aus, was sich vorteilhaft bei der Aufreinigung und Handhabung der Verbindungen sowie bei ihrer Verwendung in elektronischen Vorrichtungen auswirkt.
-
Weiterhin eignen sich die Verbindungen hervorragend zum Einsatz als Matrixmaterialien in Mixed-Matrix-Systemen. Sie führen dabei bevorzugt zu einer Herabsetzung der Betriebsspannung und zu einer Verlängerung der Lebensdauer der elektronischen Vorrichtungen.
-
Ferner sind die Verbindungen gemäß Formel (I-1) temperaturstabil und können somit weitgehend zersetzungsfrei sublimiert werden. Die Aufreinigung der Verbindungen wird dadurch erleichtert und die Verbindungen können in höherer Reinheit erhalten werden, was sich positiv auf die Leistungsdaten der elektronischen Vorrichtungen enthaltend die Materialien auswirkt. Insbesondere können dadurch Vorrichtungen mit längeren operativen Lebensdauern hergestellt werden.
-
Die Erfindung wird durch die nachfolgenden Ausführungsbeispiele näher erläutert, ohne sie dadurch einschränken zu wollen.
-
Anwendungsbeispiele
-
I. Synthesebeispiele
-
A) 5,8-Bis-biphenyl-4-yl-13,13-dimethyl-8,13-dihydro-5H-5,8-diazaindeno[1,2-a]anthracen A
-
1) Synthese von 3-Bromo-carbazol-9-carbonsäure-tert-butylester A1
-
-
Es werden 147.12 g (674.1 mmol) Di-tert-butyl-dicarbonat in 1000 mL entgastem THF gelöst, mit 118.5 g (481.5 mmol) 3-Bromo-9H-carbazol und 5.94 g (48.15 mmol) DMAP versetzt (Vorsicht Gasentwicklung!). Anschließend wird die Reaktionsmischung langsam unter Rückfluss erhitzt. Die abgekühlte Reaktionslösung wird vorsichtig auf Wasser gegeben und mit Methylenchlorid extrahiert und getrocknet. Man erhält ein gelbes Öl, das aus Heptan heiß ausgerührt und unter Ultraschallbehandlung kristallisiert wird. Man erhält 116.1 g (69 %) des Produkts als weißen Feststoff.
-
2) Synthese von 3-(2-Methoxycarbonyl-phenylamino)-carbazol-9-carbonsäure-tert-butylester A2
-
-
63.4 g (183.12 mmol) des Bromids A1 werden mit 39.0 mL (302.15 mmol) Methylanthranilat in 1200 mL trockenem Toluol gelöst und via Spritze mit 27.4 mL (27.4 mmol, 1M in Toluol) Tris-tert-Butylphosphin versetzt. Es wird mit 103.2 g (316.8 mmol) Cs2CO3 und 3.28 g (14.7 mmol) Pd(OAc)2 versetzt und für ca. 2.5 h unter Rückfluss erhitzt. Nach vollständigem Umsatz wird der abgekühlte Ansatz über Kieselgel filtriert und einrotiert. Das erhaltene Öl wird mit MeOH versetzt und 3 min. bei 50 °C gerührt. Der ausfallende Niederschlag wird mehrfach mit wenig MeOH gewaschen. Man erhält 63.1 g (83 %) des Produkts als beigefarbene Kristalle.
-
3) Synthese von 2-(9H-Carbazol-3-ylamino)-benzoesäuremethylester A3
-
-
Es werden 80.5 g (193.3 mmol) des Esters A2 in 600 mL Dichlormethan und 4.2 mL (38.5 mmol) Anisol gelöst. Bei Raumtemperatur wird dann langsam 15.7 mL Trifluoressigsäure zugegeben und die Reaktionsmischung auf 40 °C erhitzt. Es wird anschließend mehrfach portionsweise mit Anisol und Trifluoressigsäure versetzt, bis der Umsatz vollständig ist. Anschließend wird die abgekühlte Reaktionsmischung auf Eiswasser gegeben und vorsichtig, aber möglichst zügig, mit 20 %iger NaOH-Lösung auf pH = 7-8 eingestellt. Es wird mit Methylenchlorid extrahiert, getrocknet, filtriert und eingeengt. Der erhaltene ölige Feststoff wird mit Heptan warm ausgerührt. Man erhält 43.9 g (72 %) des Produkts als Feststoff.
-
4) Synthese von 2-[2-(9H-Carbazol-3-ylamino)-phenyl]-propan-2-ol A4
-
-
Es werden 43.9 g (138.8 mmol) des Esters A3 in trockenem THF gelöst und auf -78 °C gekühlt. Bei dieser Temperatur wird tropfenweise mit 315.4 mL (693.8 mmol, 2.2 M in Diethylether) MeLi versetzt. Nach ca. 5 h und einer Temperatur von -40 °C ist vollständiger Umsatz zu beobachten. Bei -30 °C wird langsam mit 240 mL MeOH versetzt (Vorsicht, es tritt Gasentwicklung ein) und mit Ethylacetat und Wasser extrahiert. Die organische Phase wird getrocknet und der erhaltene gelbe Feststoff wird aus Heptan warm ausgerührt. Man erhält 42.7 g (97 %) des Produkts als gelb-beige Kristalle.
-
5) Synthese von 13,13-Dimethyl-8,13-dihydro-5H-5,8-diaza-indeno[1,2-a]anthracen A5
-
-
Es werden 42.6 g des Alkohols A4 in 1000 mL Dichlormethan gelöst und auf -5 °C gekühlt. Es wird anschließend mit einer Mischung aus 87.4 mL (1.35 mol) Methansufonsäure (10 Äq.) und 118.8 g (1.21 mol) Polyphosphorsäure (9 Äq.) vorsichtig bei -5 °C versetzt. Dabei wird die Reaktionslösung leicht rosa und es scheidet sich ein Öl ab. Die Reaktion wird via DC (Mikroaufarbeitung) kontrolliert und anschließend in der Kälte vorsichtig mit 20 %iger NaOH auf pH = 7-8 eingestellt. Die organische Phase wird abgetrennt, gewaschen, getrocknet und eingeengt. Die beiden entstehenden Isomere werden via Säulenchromatographie (EE:H mit 9:1) getrennt. Das erhaltene Produkt wird nochmals aus Heptan heiß ausgerührt und man erhält 15g (37 %) des Produktes mit einer Reinheit von > 99.5 % als weißen Feststoff.
-
6) Synthese von 5,8-Bis-biphenyl-4-yl-13,13-dimethyl-8,13-dihydro-5H-5,8-diaza-indeno[1,2-a]anthracen A
-
-
Es werden 15 g (50.3 mmol) des Amins A5 in entgastem Toluol gelöst und mit 29.2 g (125.7 mmol) 4-Brombiphenyl versetzt. Es wird anschließend mit 3.5 mL (3.52 mmol, 1M in Toluol) Tri-tert-Butylphosphin, 0.45 g (2.01 mmol) PdOAc2 und 14.4 g (150.8 mmol) NaOtBu versetzt. Es wird für ca. 4 h unter Rückfluss erhitzt und gegebenenfalls nochmals mit 4-Brombiphenyl versetzt. Man lässt die Reaktionslösung abkühlen und versetzt mit Wasser. Dabei fällt das Produkt als grauer Niederschlag aus. Das Rohprodukt wir aus O-Dichlorbenzol kristallisiert. Man erhält 20.3 g (66.9 %) des Produkts als gelblichen Feststoff mit einer Reinheit von 99.99 %.
-
B) Dimethyl-5,8-dinaphthalin-1-yl-8,13-dihydro-5H-5,8-diazaindeno[1,2-a]anthracen B
-
-
Eine Lösung aus 13,13-Dimethyl-8,13-dihydro-5H-5,8-diazaindeno[1,2-a]anthracen A5 (10.0 g, 34 mmol) und 1-Bromnaphthalin (17.4 g, 84 mmol) in entgastem Xylol (200 mL) wird mit Tri-tert-butylphosphin (2.4 mL einer 1 M Lösung in Toluol), Natrium-tert-butylat (9.7 g, 101 mmol) und Palladiumacetat (0.3 g, 1.3 mmol) versetzt und 2 h unter Rückfluss erhitzt. Nach Abkühlen des Reaktionsgemisches auf Raumtemperatur wird der ausgefallene Feststoff abfiltriert und mit Heptan soxhlettiert. Das Rohprodukt wird anschließend viermal aus Toluol umkristallisiert und durch zweimalige Sublimation im Vakuum (p = 5 x 10-5 mbar, T = 270 °C) gereinigt.
-
Ausbeute: 6.6 g (12 mmol), 35 % d. Th., Reinheit >99.9 % laut HPLC, farbloser Feststoff.
-
II. Devicebeispiele
-
Die Herstellung von erfindungsgemäßen OLEDs sowie OLEDs nach dem Stand der Technik erfolgt nach einem allgemeinen Verfahren gemäß
WO 04/058911 , das auf die hier beschriebenen Gegebenheiten (Schichtdickenvariation, Materialien) angepasst wird.
-
In den folgenden Beispielen V1 bis E5 (siehe Tabellen 1 und 2) werden die Daten verschiedener OLEDs vorgestellt. Glasplättchen, die mit strukturiertem ITO (Indium Zinn Oxid) der Dicke 150 nm beschichtet sind, werden zur verbesserten Prozessierung mit 20 nm PEDOT beschichtet (Poly(3,4-ethylendioxy-2,5-thiophen), aus Wasser aufgeschleudert; bezogen von H. C. Starck, Goslar, Deutschland). Diese beschichteten Glasplättchen bilden die Substrate, auf welche die OLEDs aufgebracht werden. Die OLEDs haben prinzipiell folgenden Schichtaufbau: Substrat / Optionale Lochinjektionsschicht (HIL) / Lochtransportschicht (HTL) / Optionale Zwischenschicht (IL) / Elektronenblockierschicht (EBL) / Emissionsschicht (EML) / Optionale Lochblockierschicht (HBL) / Elektronentransportschicht (ETL) und abschließend eine Kathode. Die Kathode wird durch eine 100 nm dicke Aluminiumschicht gebildet. Der genaue Aufbau der OLEDs ist Tabelle 1 zu entnehmen. Die zur Herstellung der OLEDs benötigten Materialien sind in Tabelle 3 gezeigt.
-
Alle Materialien werden in einer Vakuumkammer thermisch aufgedampft. Dabei besteht die Emissionsschicht immer aus mindestens einem Matrixmaterial (Hostmaterial, Wirtsmaterial) und einem emittierenden Dotierstoff (Dotand, Emitter), der dem Matrixmaterial bzw. den Matrixmaterialien durch Coverdampfung in einem bestimmten Volumenanteil beigemischt wird. Eine Angabe wie ST1:TEG1 (90%:10%) bedeutet hierbei, dass das Material ST1 in einem Volumenanteil von 90% und TEG1 in einem Anteil von 10% in der Schicht vorliegt. Analog kann auch die Elektronentransportschicht aus einer Mischung von zwei Materialien bestehen.
-
Die OLEDs werden standardmäßig charakterisiert. Hierfür werden die Elektrolumineszenzspektren, die Stromeffizienz (gemessen in cd/A), die Leistungseffizienz (gemessen in Im/W) und die externe Quanteneffizienz (EQE, gemessen in Prozent) in Abhängigkeit der Leuchtdichte, berechnet aus Strom-Spannungs-Leuchtdichte-Kennlinien (IUL-Kennlinien) sowie die Lebensdauer bestimmt. Die Elektrolumineszenzspektrum werden bei einer Leuchtdichte von 1000 cd/m2 bestimmt und daraus die CIE 1931 x und y Farbkoordinaten berechnet. Die Angabe U1000 in Tabelle 2 bezeichnet die Spannung, die für eine Leuchtdichte von 1000 cd/m2 benötigt wird. SE1000 und LE1000 bezeichnen die Strom- bzw. Leistungseffizienz, die bei 1000 cd/m2 erreicht werden. EQE1000 schließlich ist die externe Quanteneffizienz bei einer Betriebsleuchtdichte von 1000 cd/m2. Als Lebensdauer LD wird die Zeit definiert, nach der die Leuchtdichte bei einem Betrieb mit konstantem Strom von der Startleuchtdichte L0 auf einen gewissen Anteil L1 abgesunken ist. Eine Angabe von L0 = 4000 cd/m2 und L1 = 80% in Tabelle 2 bedeutet, dass die in Spalte LD angegebene Lebensdauer der Zeit entspricht, nach der die Anfangsleuchtdichte der entsprechenden OLED von 4000 cd/m2 auf 3200 cd/m2 abgesunken ist. Die Werte für die Lebensdauer können mit Hilfe dem Fachmann bekannten Umrechnungsformeln auf eine Angabe für andere Startleuchtdichten umgerechnet werden. Hierbei ist die Lebensdauer für eine Startleuchtdichte von 1000 cd/m2 eine übliche Angabe.
-
Die Daten der verschiedenen OLEDs sind in Tabelle 2 zusammengefasst. Die Beispiel V1-V3 sind Vergleichsbeispiele gemäß dem Stand der Technik, die Beispiele E1-E5 zeigen Daten von OLEDs mit erfindungsgemäßen Materialien.
-
Im folgenden werden einige der Beispiele näher erläutert, um die Vorteile der erfindungsgemäßen Verbindungen zu verdeutlichen. Es sei jedoch darauf hingewiesen, dass dies nur eine Auswahl der in Tabelle 2 gezeigten Daten darstellt.
-
Verwendung von erfindungsgemäßen Verbindungen als Lochtransportmaterialien
-
Die OLEDs V1-V3 sind Vergleichsbeispiele gemäß dem Stand der Technik, in denen die Lochtransportmaterialien SpA1 und SpNPB eingesetzt werden. Die Beispiele E1-E5 zeigen Daten von OLEDs, in denen die erfindungsgemäßen Verbindungen A und B eingesetzt werden.
-
Bei Einsatz der Verbindung B in blau fluoreszierenden OLEDs erhält man gegenüber dem Stand der Technik eine um 0.3 V verringerte Betriebsspannung, was mit der fast gleichbleibenden Stromeffizienz zu einer Erhöhung von 7.1 auf 7.5 Im/W führt. Die Lebensdauer erhöht sich durch Einsatz von Verbindung B von 210 auf 240 h (Beispiele V1, E2).
-
In phosphoreszenten grünen OLEDs erzielt man durch Einsatz von erfindungsgemäßen Verbindungen ebenfalls Verbesserungen bezüglich Spannung und Leistungseffizienz. Vor allem ohne HATCN als Zwischenschicht lässt sich durch Verwendung von Verbindung A anstatt SpA1 eine deutliche Steigerung der Leistungseffizienz um fast 15% erzielen, wobei sich gleichzeitig auch die Lebensdauer von 360 auf 410 h erhöht (Beispiele V3, E5).
-
Durch den Einsatz von erfindungsgemäßen Verbindungen auf der Lochtransportseite von OLEDs erhält man also Verbesserungen bezüglich Betriebsspannung, Leistungseffizienz und Lebensdauer.
-
Verwendung von erfindungsgemäßen Verbindungen als Dotanden
-
Bei Einsatz der Verbindung B in der Emissionsschicht von OLEDs erhält man blaue Emission. Verwendet man den Schichtaufbau HATCN 5 nm / SPA1 140 nm / NPB 20 nm / M1:B (95%:5%) 30 nm / ST1:LiQ (50%:50%) 20 nm mit einer 100 nm dicken Aluminiumschicht als Kathode, so erhält man tiefblaue Farbkoordinaten von CIE x/y = 0.15/0.09 sowie eine externe Quanteneffizienz von 5.2% bei 1000 cd/m
2. Die Betriebsspannung beträgt 4.5 V für eine Leuchtdichte von 1000 cd/m
2. Tabelle 1: Aufbau der OLEDs
| Bsp. | HIL Dicke | HTL Dicke | IL Dicke | EBL Dicke | EML Dicke | HBL Dicke | ETL Dicke |
| V1 | HATCN 5nm | SpNPB 40nm | - | NPB 20nm | M1:D1 (98.5%:1.5%) 30nm | - | ST2:LiQ (50%:50%) 20nm |
| V2 | - | SpA1 | HATCN | BPA1 | ST1:TEG1 (90%:10%) | ST1 | ST1:LiQ (50%:50%) |
| | | 70nm | 5nm | 20nm | 30nm | 10nm | 30 nm |
| V3 | - | SpA1 70nm | - | BPA1 90nm | IC1:TEG1 (90%:10%) 30nm | - | ST1:LiQ (50%:50%) 40 nm |
| E1 | HATCN 5nm | A 40nm | - | NPB 20nm | M1:D1 (98.5%:1.5%) 30nm | - | ST2:LiQ (50%:50%) 20nm |
| E2 | HATCN 5nm | B 40nm | - | NPB 20nm | M1:D1 (98.5%:1.5%) 30nm | - | ST2:LiQ (50%:50%) 20nm |
| E3 | - | A 70nm | HATCN 5nm | BPA1 20nm | ST1:TEG1 (90%:10%) 30nm | ST1 10nm | ST1:LiQ (50%:50%) 30 nm |
| E4 | - | B 70nm | HATCN 5nm | BPA1 20nm | ST1:TEG1 (90%:10%) 30nm | ST1 10nm | ST1:LiQ (50%:50%) 30 nm |
| E5 | - | A 70nm | - | BPA1 90nm | IC1:TEG1 (90%:10%) 30nm | - | ST1:LiQ (50%:50%) 40 nm |
Tabelle 2: Daten der OLEDs
| Bsp. | U1000 (V) | SE1000 (cd/A) | LE1000 (Im/W) | EQE 1000 | CIE x/y bei 1000 cd/m2 | L0 (cd/m2) | L1 % | LD (h) |
| V1 | 4.3 | 9.8 | 7.1 | 7.6% | 0.14/0.16 | 6000 | 50 | 210 |
| V2 | 4.2 | 52 | 39 | 14.5% | 0.36/0.60 | 4000 | 80 | 330 |
| V3 | 3.8 | 54 | 45 | 14.9% | 0.36/0.60 | 4000 | 80 | 360 |
| E1 | 4.2 | 9.9 | 7.4 | 7.7% | 0.14/0.16 | 6000 | 50 | 200 |
| E2 | 4.0 | 9.5 | 7.5 | 7.4% | 0.14/0.16 | 6000 | 50 | 240 |
| E3 | 4.0 | 52 | 41 | 14.3% | 0.36/0.60 | 4000 | 80 | 340 |
| E4 | 3.9 | 53 | 43 | 14.6% | 0.36/0.60 | 4000 | 80 | 360 |
| E5 | 3.4 | 55 | 51 | 15.3% | 0.36/0.60 | 4000 | 80 | 410 |
Tabelle 3: Strukturformeln der Materialien für die OLEDs
| | |
| HATCN | SpA1 (Stand der Technik) |
| | |
| NPB | BPA1 |
| | |
| SpNBP (Stand der Technik) | D1 |
| | |
| M1 | ST1 |
| | |
| LiQ | TEG1 |
| | |
| IC1 | A |
| | |
| B | |