DE102005037734B4 - Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen - Google Patents
Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen Download PDFInfo
- Publication number
- DE102005037734B4 DE102005037734B4 DE102005037734.3A DE102005037734A DE102005037734B4 DE 102005037734 B4 DE102005037734 B4 DE 102005037734B4 DE 102005037734 A DE102005037734 A DE 102005037734A DE 102005037734 B4 DE102005037734 B4 DE 102005037734B4
- Authority
- DE
- Germany
- Prior art keywords
- structural units
- occurrence
- different
- same
- atoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- WJNVVLZRPVIRSO-UHFFFAOYSA-N CC1(c(ccc(Br)c2)c2-c2cc(Br)ccc2C1(C)O)O Chemical compound CC1(c(ccc(Br)c2)c2-c2cc(Br)ccc2C1(C)O)O WJNVVLZRPVIRSO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/115—Polyfluorene; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
- C08G61/10—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aromatic carbon atoms, e.g. polyphenylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
- C08G61/126—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds with a five-membered ring containing one sulfur atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/10—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds
- C09B69/105—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing a methine or polymethine dye
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/10—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds
- C09B69/109—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing other specific dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1408—Carbocyclic compounds
- C09K2211/1416—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1408—Carbocyclic compounds
- C09K2211/1433—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Electroluminescent Light Sources (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
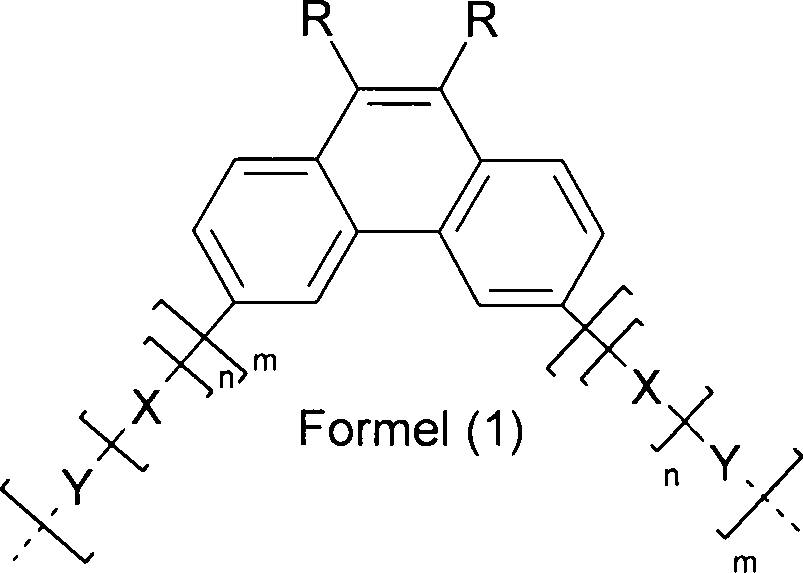
Konjugierte oder teilkonjugierte Polymere, enthaltend mindestens 5 mol% Struktureinheiten der Formel (1),wobei die verwendeten Symbole und Indizes die folgenden Bedeutungen besitzen: R bei jedem Auftreten gleich oder verschieden, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 40 C-Atomen, die durch R1 substituiert sein kann, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CR1=CR1- oder -C≡C- ersetzt sein können, und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches auch durch ein oder mehrere Reste R1 substituiert sein kann; dabei können die beiden Reste R miteinander auch ein weiteres mono- oder polycyclisches, aromatisches oder aliphatisches Ringsystem bilden; X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist; Y bei jedem Auftreten gleich oder verschieden ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder durch ein oder mehrere Reste R1 substituiert sein kann; R1 bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R2, -O-, -S-, -O-CO-O-, -CO-O-, -CR2=CR2- oder -C≡C- ersetzt sein können und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder eine Aryl-, Heteroaryl-, Aryloxy- oder Heteroaryloxygruppe mit 5 bis 40 C-Atomen ist, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann; dabei können auch zwei oder mehrere der Reste R1 miteinander und/oder mit R ein Ringsystem bilden; oder F, Cl, Br, I, CN, N(R2)2, Si(R2)3 oder B(R2)2 bedeuten; R2 bei jedem Auftreten gleich oder verschieden H oder ein aliphatischer oder aromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen ist; Ar bei jedem Auftreten gleich oder verschieden ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder mit R1 substituiert sein kann; ...
Description
- Die vorliegende Erfindung betrifft elektrolumineszierende Polymere, die mindestens 5 mol% Struktureinheiten der Formel (1) enthalten sowie deren Verwendung und bifunktionelle monomere Verbindungen. Die erfindungsgemäßen Polymere zeigen eine verbesserte Effizienz und eine höhere Lebensdauer insbesondere bei Verwendung in polymeren organischen Leuchtdioden.
- Seit mehr als zehn Jahren läuft eine breit angelegte Forschung zur Kommerzialisierung von Anzeige- und Beleuchtungselementen auf Basis polymerer (organischer) Leuchtdioden (PLEDs). Ausgelöst wurde diese Entwicklung durch die Grundlagenentwicklungen, welche in der
WO 90/13148 A1 - Für die Erzeugung aller drei Emissionsfarben ist es notwendig, bestimmte Comonomere in die entsprechenden Polymere einzupolymerisieren (vgl. z. B.
WO 00/46321 A1 WO 03/020790 A2 WO 02/077060 A1 - Als Polymere für vollfarbige Anzeigeelemente (Full-Colour-Displays) wurden bereits verschiedene Materialklassen vorgeschlagen bzw. entwickelt. So kommen sowohl z. B. Poly-Fluoren-Derivate als auch Poly-Spirobifluoren-, Poly-Dihydrophenanthren- und Poly-Indenofluoren-Derivate in Betracht. Auch Polymere, die eine Kombination der genannten Strukturelemente enthalten, wurden bereits vorgeschlagen. Darüber hinaus werden Polymere, welche Poly-para-phenylen (PPP) als Strukturelement enthalten, eingesetzt.
- Die Polymere gemäß dem Stand der Technik zeigen teilweise schon gute Eigenschaften in der Anwendung in PLEDs. Trotz der bereits erzielten Fortschritte entsprechen diese Polymere allerdings noch nicht den Anforderungen, die an sie für hochwertige Anwendungen gesteift werden.
- Insbesondere ist die Lebensdauer der grün und vor allem der blau emittierenden Polymere für viele Anwendungen noch nicht ausreichend. Gleiches gilt für die Effizienz der rot emittierenden Polymeren.
- Es wurde nun überraschenderweise gefunden, dass eine neue Klasse von Polymeren sehr gute und den o. g. Stand der Technik übertreffende Eigenschaften aufweist. Diese Polymere und ihre Verwendung in PLEDs sind daher Gegenstand der vorliegenden Erfindung. Die neuen Struktureinheiten eignen sich insbesondere als Polymer-Grundgerüst, aber je nach Substitutionsmuster auch als Lochleiter, Elektronenleiter und/oder Emitter.
- Die Verwendung von Phenanthrenen in elektrolumineszierenden Polymeren ist bekannt, sie wird beispielsweise in der
WO 02/077060 A1 WO 03/020790 A2 DE 10337346 A1 offenbart. Allerdings ist dort nur allgemein aufgezählt, dass diese Strukturelemente, ebenso wie eine große Vielzahl weiterer Monomere, als mögliche weitere Elemente, neben dem eigentlichen Polymer-Grundgerüst, vorhanden sein können. Besondere Vorteile dieser Einheiten sind nicht beschrieben. Außerdem ist nur ganz allgemein beschrieben, dass diese mit nicht-aromatischen Substituenten substituiert oder unsubstituiert sein können. Die Verwendung unsubstituierter Phenanthren-Einheiten führt jedoch zu unlöslichen Polymeren, so dass diese Einheiten höchstens in einem geringen Anteil verwendet werden können. Welche Substituenten allerdings besonders geeignet sind und an welchen Positionen der Phenanthren-Einheit diese Substituenten vorzugsweise gebunden sein sollten, geht aus diesen Offenbarungen nicht hervor. Ebenso wenig geht daraus hervor, dass sich die neuen Struktureinheiten besonders eignen, in einem höheren Anteil im Polymer eingesetzt zu werden, da sie im Stand der Technik nur als Comonomere in vergleichsweise geringen Anteilen erwähnt sind. Es ist also für den Fachmann nicht ersichtlich, wie diese Einheiten nutzbringend in elektrolumineszierenden Polymeren verwendet werden können. Daher ist die allgemeine Offenbarung von Phenanthren-Einheiten als zufällige Offenbarung zu bewerten. - Ferner werden im Stand der Technik niedermolekulare Verbindungen beschrieben, die ein Phenanthren-Grundgerüst aufweisen:
So werden in derJP 2005/005226 A - Verbindungen mit einem Phenanthroazol-Grundgerüst und deren Verwendung in Licht-emittierenden Elementen werden in der
JP 2001/023777 A - Speziell funktionalisierte Phenanthren-Derivate sowie deren Verwendung als photosensitive Materialien werden in der
JP 05/148211 A - 2-(Phenyl oder heterocyclische)-1H-Phenanthro[9,10-D]imidazole sowie deren Verwendung als Inhibitoren werden in der
WO 2006/063466 A1 - Speziell substituierte Phenanthren-Derivate sowie deren Verwendung als diskotische flüssigkristalline Materialien, werden in der
DE 4307049 A1 beschrieben. - Die Substitution der Phenanthren-Einheiten in 9- bzw. 9,10-Position und die Verknüpfung im Polymer in der 3,6-Position hat sich überraschenderweise als besonders geeignet im Vergleich zur Substitution in anderen Positionen der Phenanthren-Einheit erwiesen. Diese Bevorzugung lässt sich durch die besonders gute synthetische Zugänglichkeit der in diesen Positionen substituierten Einheiten begründen, aber auch durch die besseren optischen und elektronischen Eigenschaften.
- Gegenstand der Erfindung sind konjugierte oder teilkonjugierte Polymere, enthaltend mindestens 5 mol%, vorzugsweise mindestens 10 mol%, besonders bevorzugt mindestens 30 mol% und insbesondere mindestens 50 mol% Struktureinheiten der Formel (1), worin
R bei jedem Auftreten gleich oder verschieden, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 40 C-Atomen, die durch R1 substituiert sein kann, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CR1=CR1- oder -C≡C- ersetzt sein können, vorzugsweise mit der Maßgabe, dass die Heteroatome nicht direkt an die Phenanthren-Einheit gebunden sind, und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder ein aromatisches oder hetero-aromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches auch durch ein oder mehrere Reste R1 substituiert sein kann; dabei können die beiden Reste R miteinander auch ein weiteres mono- oder polycyclisches, aromatisches oder aliphatisches Ringsystem bilden;
X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist;
Y bei jedem Auftreten gleich oder verschieden ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder durch ein oder mehrere Reste R1 substituiert sein kann;
R1 bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R2, -O-, -S-, -O-CO-O-, -CO-O-, -CR2=CR2- oder -C≡C- ersetzt sein können und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder eine Aryl-, Heteroaryl-, Aryloxy- oder Heteroaryloxygruppe mit 5 bis 40 C-Atomen ist, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann; dabei können auch zwei oder mehrere der Reste R1 miteinander und/oder mit R ein Ringsystem bilden; oder F, Cl, Br, I, CN, N(R2)2, Si(R2)3 oder B(R2)2 bedeuten;
R2 bei jedem Auftreten gleich oder verschieden H oder ein aliphatischer oder aromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen ist;
Ar bei jedem Auftreten gleich oder verschieden ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder mit R1 substituiert sein kann;
n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist;
m bei jedem Auftreten gleich oder verschieden 0, 1 oder 2 ist; und
die gestrichelte Bindung dabei in Formel (1) ebenso wie in allen weiteren Formeln die Verknüpfung im Polymer bedeutet. Sie soll hier keine Methylgruppe darstellen. - Auch wenn dies aus der Beschreibung hervorgeht, sei hier nochmals explizit darauf verwiesen, dass die Struktureinheiten gemäß Formel (1) unsymmetrisch substituiert sein können, d. h. dass an einer Einheit unterschiedliche Substituenten R bzw. R1 vorhanden sein können, bzw. dass die Substituenten X und Y, soweit vorhanden, unterschiedlich sein können oder auch nur einseitig auftreten.
- Unter einem aromatischen bzw. heteroaromatischen Ringsystem im Sinne der vorliegenden Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur aromatische bzw. heteroaromatische Gruppen enthält, sondern in dem auch mehrere aromatische bzw. heteroaromatische Gruppen durch eine kurze nicht-aromatische Einheit (< 10% der von H verschiedenen Atome, vorzugsweise < 5% der von H verschiedenen Atome), wie beispielsweise sp3-hybridisierter C, O, N, etc., unterbrochen sein können. So sollen also beispielsweise auch Systeme wie 9,9' Spirobifluoren, 9,9-Diarylfluoren, Triarylamin, etc. als aromatische Ringsysteme verstanden werden.
- In einem Aspekt der Erfindung handelt es sich um konjugierte Polymere. In einem weiteren Aspekt der Erfindung handelt es sich um teilkonjugierte Polymere.
- Konjugierte Polymere im Sinne dieser Erfindung sind Polymere, die in der Hauptkette hauptsächlich sp2-hybridisierte Kohlenstoffatome, die auch durch entsprechende Heteroatome ersetzt sein können, enthalten. Dies bedeutet im einfachsten Fall abwechselndes Vorliegen von Doppel- und Einfachbindungen in der Hauptkette. Hauptsächlich meint, dass natürlich auftretende Defekte, die zu Konjugationsunterbrechungen führen, den Begriff ”konjugiertes Polymer” nicht entwerten. Des Weiteren wird in diesem Anmeldungstext ebenfalls als konjugiert bezeichnet, wenn sich in der Hauptkette beispielsweise Arylamineinheiten und/oder bestimmte Heterocyclen (d. h. Konjugation über N-, O- oder S-Atome) und/oder metallorganische Komplexe (d. h. Konjugation über das Metallatom) befinden. Hingegen werden Einheiten wie beispielsweise einfache Alkylbrücken, (Thio)Ether-, Ester-, Amid- oder Imidverknüpfungen eindeutig als nicht-konjugierte Segmente definiert. Unter einem teilkonjugierten Polymer soll ein Polymer verstanden werden, in dem längere konjugierte Abschnitte in der Hauptkette durch nicht-konjugierte Abschnitte unterbrochen sind, bzw. das längere konjugierte Abschnitte in den Seitenketten eines in der Hauptkette nicht-konjugierten Polymers enthält.
- Die erfindungsgemäßen Polymere können neben den Einheiten gemäß Formel (1) noch weitere Strukturelemente enthalten. Dies sind u. a. solche, wie sie in der
WO 02/077060 A1 DE 10337346 A1 offenbart und umfangreich aufgelistet sind. Diese werden via Zitat als Bestandteil der vorliegenden Erfindung betrachtet. Die weiteren Struktureinheiten können beispielsweise aus den folgenden Klassen stammen:Gruppe 1: Einheiten, welche die Lochinjektions- und/oder -transporteigenschaften der Polymere erhöhen; Gruppe 2: Einheiten, welche die Elektroneninjektions- und/oder -transporteigenschaften der Polymere erhöhen; Gruppe 3: Einheiten, die Kombinationen von Einzeleinheiten der Gruppe 1 und Gruppe 2 aufweisen; Gruppe 4: Einheiten, welche die Emissionscharakteristik insoweit verändern, dass Elektrophosphoreszenz statt Elektrofluoreszenz erhalten werden kann; Gruppe 5: Einheiten, welche den Übergang vom so genannten Singulett- zum Triplettzustand verbessern; Gruppe 6: Einheiten, welche die Morphologie und/oder die Emissionsfarbe der resultierenden Polymere beeinflussen; Gruppe 7: Einheiten, welche typischerweise als Backbone verwendet werden. - Bevorzugte erfindungsgemäße Polymere sind solche, bei denen mindestens ein Strukturelement Ladungstransporteigenschaften aufweist, d. h. die Einheiten aus den Gruppen 1 und/oder 2 enthalten.
- Strukturelemente aus der Gruppe 1, die Lochtransporteigenschaften aufweisen, sind beispielsweise Triarylamin-, Benzidin-, Tetraaryl-para-phenylendiamin-, Triarylphosphin-, Phenothiazin-, Phenoxazin-, Dihydrophenazin-, Thianthren-, Dibenzo-para-dioxin-, Phenoxathiin-, Carbazol-, Azulen-, Thiophen-, Pyrrol- und Furanderivate und weitere O-, S- oder N-haltige Heterocyclen mit hoch liegendem HOMO (HOMO = höchstes besetztes Molekülorbital). Vorzugsweise führen diese Arylamine und Heterocyclen zu einem HOMO im Polymer von mehr als –5,8 eV (gegen Vakuumlevel), besonders bevorzugt von mehr als –5,5 eV.
- Strukturelemente aus der Gruppe 2, die Elektronentransporteigenschaften aufweisen, sind beispielsweise Pyridin-, Pyrimidin-, Pyridazin-, Pyrazin-, Oxadiazol-, Chinolin-, Chinoxalin- und Phenazinderivate, aber auch Triarylborane und weitere O-, S- oder N-haltige Heterocyclen mit niedrig liegendem LUMO (LUMO = niedrigstes unbesetztes Molekülorbital). Vorzugsweise führen diese Einheiten im Polymer zu einem LUMO von weniger als –2,7 eV (gegen Vakuumlevel), besonders bevorzugt von weniger als –3,0 eV.
- Es kann bevorzugt sein, wenn in den erfindungsgemäßen Polymeren Einheiten aus der Gruppe 3 enthalten sind, in denen Strukturen, welche die Lochmobilität und welche die Elektronenmobilität erhöhen (also Einheiten aus Gruppe 1 und 2), direkt aneinander gebunden sind. Einige dieser Einheiten können als Emitter dienen und verschieben die Emissionsfarbe ins Grüne, Gelbe oder Rote. Ihre Verwendung eignet sich also beispielsweise für die Erzeugung anderer Emissionsfarben aus ursprünglich blau emittierenden Polymeren.
- Struktureinheiten gemäß der Gruppe 4 sind solche, welche auch bei Raumtemperatur mit hoher Effizienz aus dem Triplettzustand Licht emittieren können, also Elektrophosphoreszenz statt Elektrofluoreszenz zeigen, was häufig eine Steigerung der Energieeffizienz bewirkt. Hierfür eignen sich zunächst Verbindungen, welche Schweratome mit einer Ordnungszahl von mehr als 36 enthalten. Bevorzugt sind Verbindungen, welche d- oder f-Übergangsmetalle beeinhalten, die die o. g. Bedingung erfüllen. Besonders bevorzugt sind hier entsprechende Struktureinheiten, welche Elemente der Gruppe 8 bis 10 (Ru, Os, Rh, Ir, Pd, Pt) enthalten. Als Struktureinheiten für die erfindungsgemäßen Polymeren kommen hier z. B. verschiedene Komplexe in Frage, wie sie z. B. in der
WO 02/068435 A1 DE 10116962 A1 , derEP 1239526 A2 und derDE 10238903 A1 beschrieben werden. Entsprechende Monomere werden in derWO 02/068435 A1 DE 10350606 A1 beschrieben. - Strukturelemente der Gruppe 5 sind solche, welche den Übergang vom Singulett- zum Triplettzustand verbessern und welche, unterstützend zu den Strukturelementen der Gruppe 4 eingesetzt, die Phosphoreszenzeigenschaften dieser Strukturelemente verbessern. Hierfür kommen insbesondere Carbazol- und überbrückte Carbazoldimereinheiten in Frage, wie sie in der
DE 10304819 A1 und derDE 10328627 A1 beschrieben werden. Weiterhin kommen hierfür Ketone, Phosphinoxide, Sulfoxide und ähnliche Verbindungen in Frage, wie sie in derDE 10349033 A1 beschrieben werden. - Strukturelemente der Gruppe 6, die die Morphologie und/oder die Emissionsfarbe der Polymere beeinflussen, sind neben oben genannten solche, die mindestens noch eine weitere aromatische oder eine andere konjugierte Struktur aufweisen, welche nicht unter die o. g. Gruppen fallen, d. h. die die Ladungsträgermobilitäten nur wenig beeinflussen, die keine metallorganischen Komplexe sind oder die keinen Einfluss auf den Singulett-Triplett-Übergang haben. Derartige Strukturelemente können die Morphologie und/oder die Emissionsfarbe der resultierenden Polymere beeinflussen. Je nach Einheit können sie daher auch als Emitter eingesetzt werden. Bevorzugt sind dabei aromatische Strukturen mit 6 bis 40 C-Atomen oder auch Tolan-, Stilben- oder Bisstyrylarylenderivate, die jeweils mit einem oder mehreren Resten R1 substituiert sein können. Besonders bevorzugt ist dabei der Einbau von 1,4 Phenylen-, 1,4-Naphthylen-, 1,4- oder 9,10-Anthrylen-, 1,6-, 2,7- oder 4,9-Pyrenylen-, 3,9- oder 3,10-Perylenylen-, 4,4'-Biphenylylen-, 4,4'' Terphenylylen, 4,4'-Bi-1,1'-naphthylylen-, 4,4'-Tolanylen-, 4,4'-Stilbenylen- oder 4,4'' Bisstyrylarylenderivaten.
- Strukturelemente der Gruppe 7 sind Einheiten, die aromatische Strukturen mit 6 bis 40 C-Atomen beinhalten, welche typischerweise als Polymergrundgerüst (Backbone) verwendet werden. Dies sind beispielsweise 4,5 Dihydropyrenderivate, 4,5,9,10-Tetrahydropyrenderivate, Fluorenderivate, 9,9' Spirobifluorenderivate, 9,10-Dihydrophenanthrenderivate, 5,7-Dihydrodibenzo-oxepinderivate und cis- und trans-Indenofluorenderivate. Da jedoch der Anteil an Einheiten gemäß Formel (1) ganz besonders bevorzugt mindestens 50 mol% beträgt, werden diese Strukturelemente aus Gruppe 7 hier nicht vorzugsweise als das hauptsächliche Polymergrundgerüst, sondern höchstens als Grundgerüst, das in geringerem Anteil anwesend ist, eingesetzt.
- Bevorzugt sind erfindungsgemäße Polymere, die gleichzeitig neben Struktureinheiten der Formel (1) zusätzlich noch ein oder mehrere Einheiten ausgewählt aus den Gruppen 1 bis 7 enthalten. Es kann ebenfalls bevorzugt sein, wenn gleichzeitig mehr als eine Struktureinheit aus einer Gruppe vorliegt.
- Vorzugsweise beträgt der Anteil an Einheiten der Formel (1) mindestens 10 mol%, besonders bevorzugt mindestens 30 mol% und insbesondere mindestens 50 mol%. Diese Bevorzugung gilt vor allem, wenn es sich bei den Einheiten der Formel (1) um das Polymer-Grundgerüst handelt. Bei anderen Funktionen können andere Anteile bevorzugt sein, beispielsweise ein Anteil in der Größenordnung von 5 bis 20 mol%, wenn es sich um den Lochleiter bzw. den Emitter in einem elektrolumineszierenden Polymer handelt. Für andere Anwendungen, beispielsweise für organische Transistoren, kann der bevorzugte Anteil nochmals unterschiedlich sein, beispielsweise bis zu 100 mol%, wenn es sich um loch- oder elektronenleitende Einheiten handelt.
- Bevorzugt sind erfindungsgemäße Polymere, die außer Struktureinheiten der Formel (1) noch mindestens eine Struktureinheit aus den oben genannten Gruppen enthalten. Besonders bevorzugt sind mindestens zwei Struktureinheiten aus unterschiedlichen der oben genannten Klassen. Wenn vorhanden, ist der Anteil dieser Strukturelemente vorzugsweise jeweils mindestens 5 mol%, besonders bevorzugt jeweils mindestens 10 mol%. Insbesondere ist eine dieser Struktureinheiten aus der Gruppe der lochleitenden Einheiten ausgewählt und die andere Gruppe ist eine emittierende Einheit, wobei diese beiden Funktionen (Lochleitung und Emission) auch von derselben Einheit übernommen werden können.
- Aber auch ein kleinerer Anteil der emittierenden Einheiten, insbesondere grün und rot emittierender Einheiten, kann bevorzugt sein, beispielsweise zur Synthese von weiß emittierenden Copolymeren. Wie weiß emittierende Copolymere synthetisiert werden können, ist im Detail in der
DE 10343606 A1 beschrieben. - Die erfindungsgemäßen Polymere weisen in der Regel 10 bis 10000, vorzugsweise 50 bis 5000 und besonders bevorzugt 50 bis 2000 Wiederholeinheiten auf.
- Die nötige Löslichkeit der Polymere wird u. a. durch die Substituenten R bzw. R1 an den Einheiten der Formel (1) sowie gegebenenfalls an weiteren anwesenden Einheiten gewährleistet. Falls weitere Substituenten vorhanden sind, können auch diese zur Löslichkeit beitragen.
- Um eine ausreichende Löslichkeit zu gewährleisten, ist es bevorzugt, dass im Durchschnitt pro Wiederholeinheit mindestens 2 nicht-aromatische C-Atome in den Substituenten vorhanden sind. Vorzugsweise sind dabei mindestens 4 und besonders bevorzugt mindestens 8 C-Atome. Einzelne dieser C-Atome können auch durch O oder S ersetzt sein. Dies kann aber durchaus bedeuten, dass ein gewisser Anteil von Wiederholeinheiten keine weiteren nicht-aromatischen Substituenten trägt.
- Um die Morphologie des Films nicht zu verschlechtern, ist es bevorzugt, keine langkettigen Substituenten mit mehr als 12 C-Atomen in einer linearen Kette zu haben, besonders bevorzugt keine mit mehr als 8 C-Atomen und insbesondere keine mit mehr als 6 C-Atomen.
- Nicht-aromatische C-Atome sind, wie beispielsweise in der Beschreibung für R und R1 in Formel (1), in entsprechenden geradkettigen, verzweigten oder cyclischen Alkyl- oder Alkoxyketten enthalten.
- Bevorzugt sind erfindungsgemäße Polymere, bei denen für Einheiten der Formel (1) gilt, dass
R bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkylkette mit 2 bis 25 C-Atomen, in der auch ein oder mehrere nicht benachbarte C Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CH=CH- oder C≡C- ersetzt sein können, vorzugsweise mit der Maßgabe, dass die Heteroatome nicht direkt an die Phenanthren-Einheit gebunden sind, und in der auch ein oder mehrere H-Atome durch F oder CN ersetzt sein können, oder eine aromatische oder heteroaromatische Gruppe mit 4 bis 20 C-Atomen ist, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann; dabei können die beiden Reste R zusammen auch ein weiteres mono- oder polycyclisches, aromatisches oder aliphatisches Ringsystem bilden;
X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist;
Y bei jedem Auftreten gleich oder verschieden ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 4 bis 30 C-Atomen ist, welches durch ein oder mehrere Reste R1 substituiert sein kann;
R1 bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R2, -O-, -S-, -O-CO-O-, -CO-O-, -CH=CH- oder -C≡C- ersetzt sein können und in der auch ein oder mehrere H-Atome durch F oder CN ersetzt sein können, oder eine Aryl-, Heteroaryl-, Aryloxy- oder Heteroaryloxygruppe mit 5 bis 40 C-Atomen ist, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann; dabei können auch zwei oder mehrere der Reste R1 miteinander und/oder mit R ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden; oder F, Cl, Br, I, CN, N(R2)2, Si(R2)3 oder B(R2)2 bedeuten;
Ar bei jedem Auftreten gleich oder verschieden ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 4 bis 30 C-Atomen ist, welches unsubstituiert oder mit R1 substituiert sein kann;
m bei jedem Auftreten gleich oder verschieden 0 oder 1 ist; und
die weiteren Symbole und Indizes wie oben unter Formel (1) definiert sind. - Besonders bevorzugt sind erfindungsgemäße Polymere, bei denen für Einheiten der Formel (1) gilt, dass
R bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkylkette mit 4 bis 20 C-Atomen, besonders bevorzugt eine verzweigte Alkylkette ist, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CH=CH- oder -C≡C- ersetzt sein können, vorzugsweise mit der Maßgabe, dass diese nicht direkt an die Phenanthren-Einheit angrenzen, und in der auch ein oder mehrere H-Atome durch F ersetzt sein können; dabei können die beiden Reste R zusammen auch ein weiteres mono- oder polycyclisches Ringsystem bilden;
X bei jedem Auftreten gleich oder verschieden -CH=CH-, -C≡C- oder -N(Ar)-Ar- ist;
Y bei jedem Auftreten gleich oder verschieden ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 6 bis 25 C-Atomen ist, welches durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann;
Ar bei jedem Auftreten gleich oder verschieden eine monovalente Aryl- oder Heteroarylgruppe mit 4 bis 20 C-Atomen ist, welche mit nicht-aromatischen Resten R1 substituiert sein kann;
m bei jedem Auftreten gleich oder verschieden 0 oder 1 ist; und
die weiteren Symbole und Indizes wie oben definiert sind. - Die Bevorzugung aliphatischer Reste R lässt sich durch die nochmals bessere Löslichkeit der resultierenden Polymere und die bessere synthetische Zugänglichkeit begründen.
- Je nach Substitutionsmuster eignen sich die Einheiten der Formel (1) insbesondere für verschiedene Funktionen im Polymer. So können diese Einheiten vorzugsweise als (elektronenleitendes) Polymer-Grundgerüst, als Lochleiter oder als Emitter eingesetzt werden. Welche Verbindungen sich insbesondere für welche Funktion eignen, wird vor allem durch die Substituenten X und Y festgelegt. Die Substituenten R haben einen weniger ausgeprägten Einfluss auf die elektronischen Eigenschaften der Einheiten der Formel (1).
- So gilt für der Verwendung als Polymer-Grundgerüst vorzugsweise, dass
n bei jedem Auftreten gleich 0 ist,
d. h. es sich um eine rein aromatische Struktureinheit handelt. - Für die Verwendung von Einheiten der Formel (1) als lochtransportierende Einheiten gilt vorzugsweise, dass
n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist, wobei mindestens ein n = 1 ist;
m bei jedem Aufteten gleich oder verschieden 0, 1 oder 2 ist, wobei m ungleich 0 ist, wenn das entsprechende n = 1 ist;
X bei jedem Auftreten -N(Ar)-Ar- ist;
d. h. es sich um Triarylaminderivate des Phenanthrens handelt. - Für die Verwendung von Einheiten der Formel (1) als Emitter gilt vorzugsweise, dass
n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist, wobei mindestens ein n = 1 ist;
m bei jedem Auftreten gleich oder verschieden 0, 1 oder 2 ist, wobei m ungleich 0 ist, wenn das entsprechende n = 1 ist;
X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist, wobei mindestens ein X gleich -CR1=CR1- oder -C≡C- ist,
d. h. es sich um Diarylvinylen- oder Diarylacetylenderivate im weitesten Sinne handelt, die auch noch zusätzlich Triarylamineinheiten enthalten können. - Weiterhin bevorzugt sind Einheiten der Formel (1), die in den 9,10-Positionen der Phenanthren-Einheiten symmetrisch substituiert sind.
- Diese Bevorzugung ist durch die bessere synthetische Zugänglichkeit der Monomere zu begründen. Vorzugsweise gilt also, dass in einer Einheit der Formel (1) alle R gleich und besonders bevorzugt auch gleich substituiert sind. Diese Bevorzugung schließt nicht aus, dass die Substituenten X und Y nur einseitig auftreten bzw. auch unterschiedlich sein können.
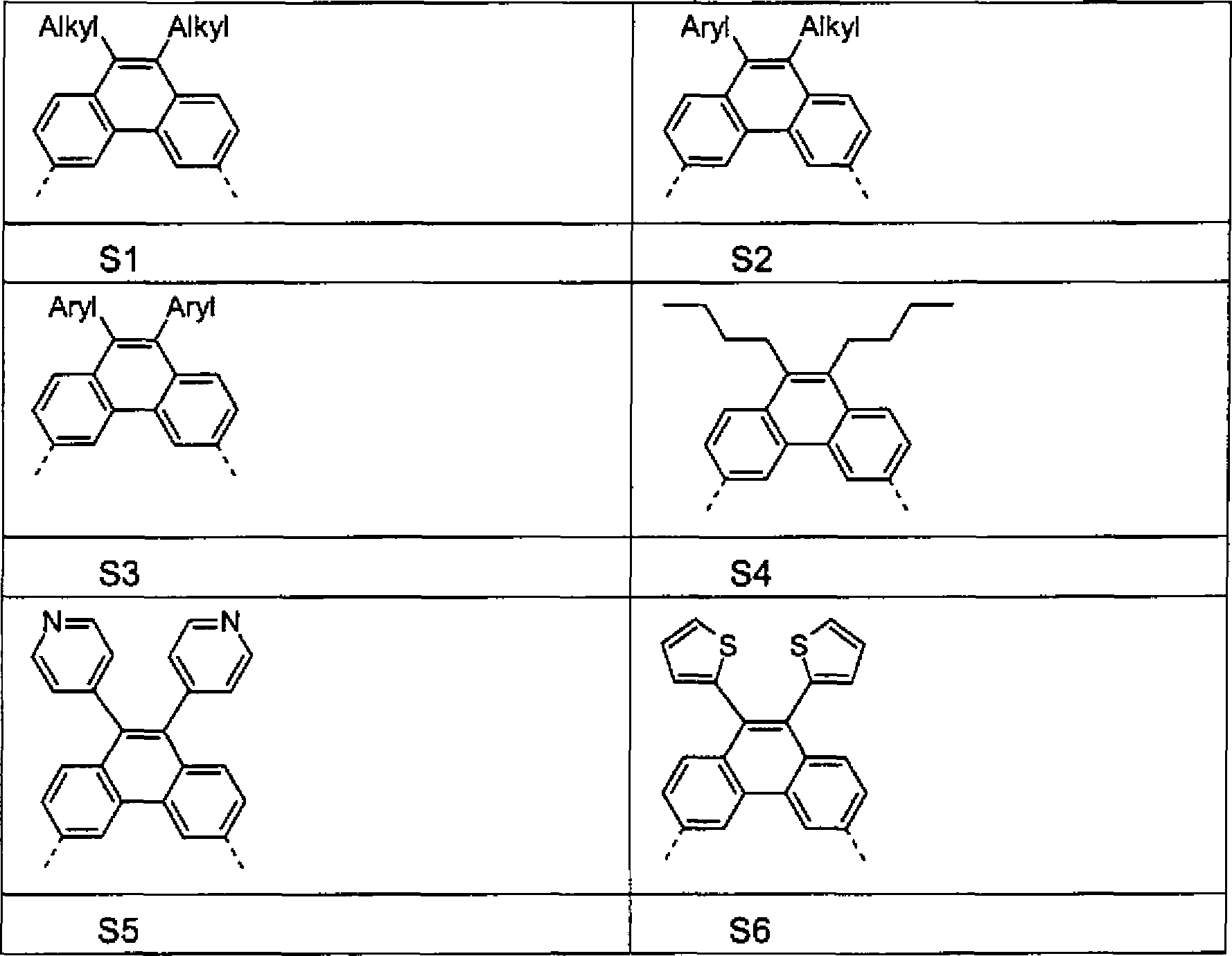
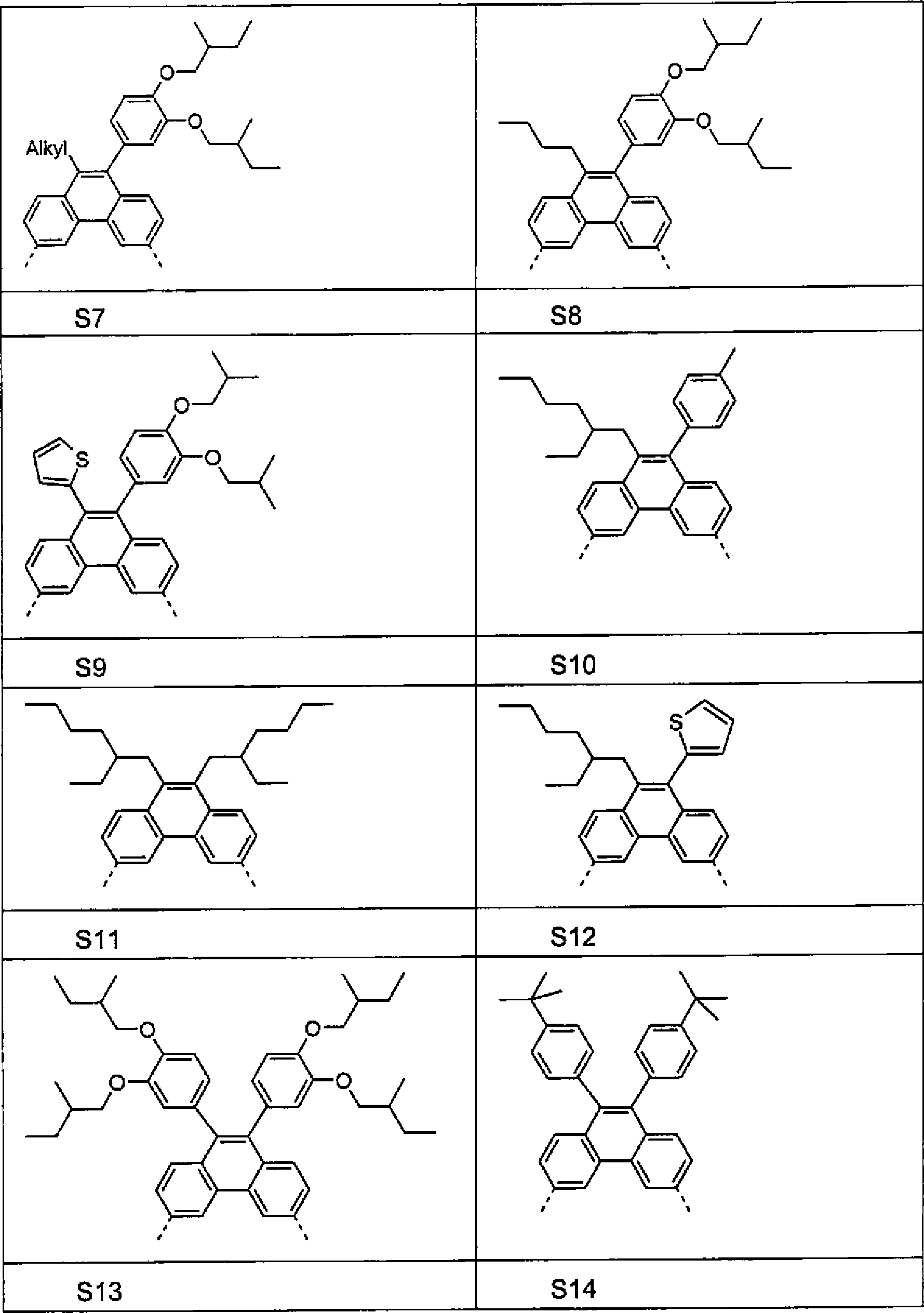
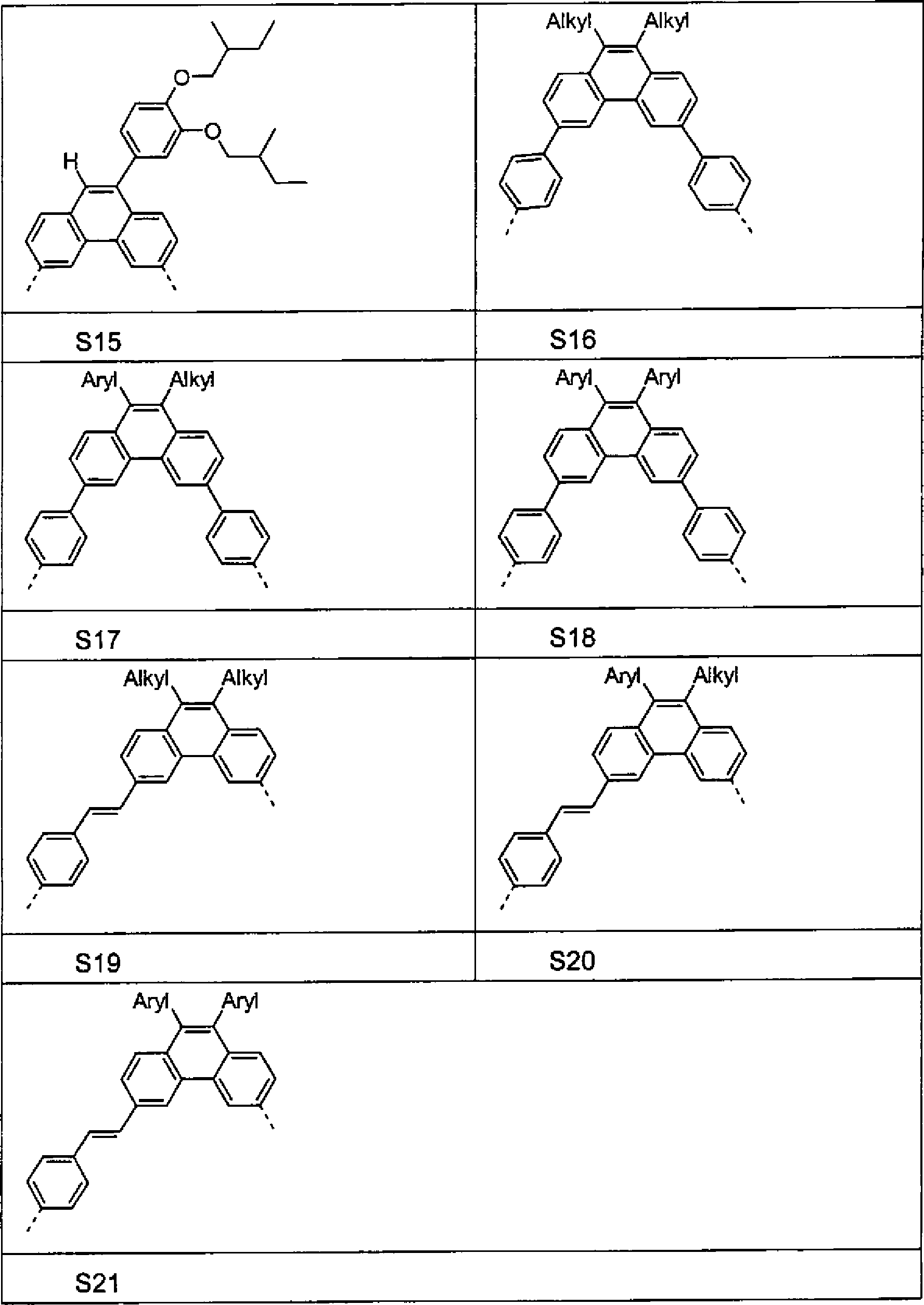
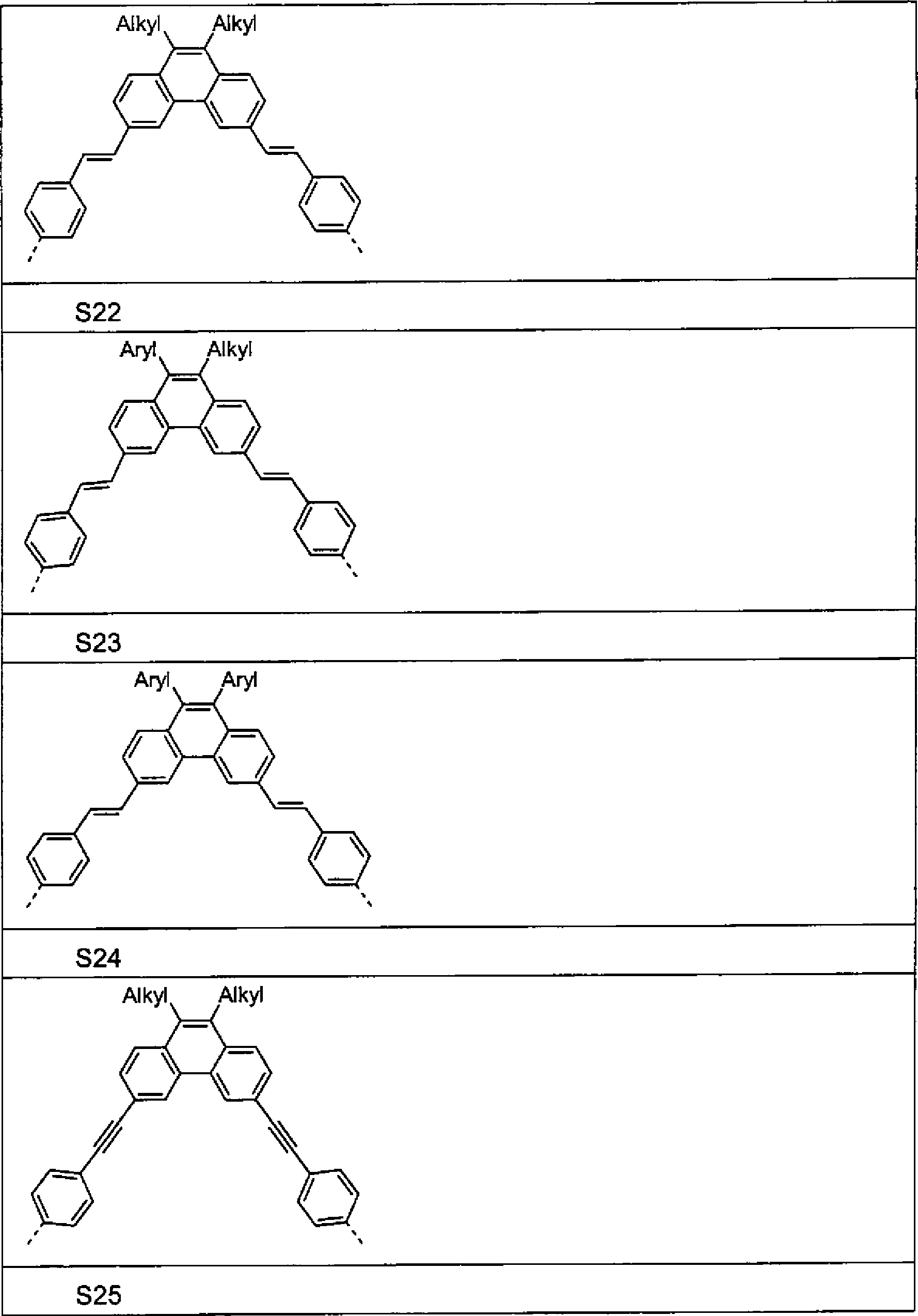
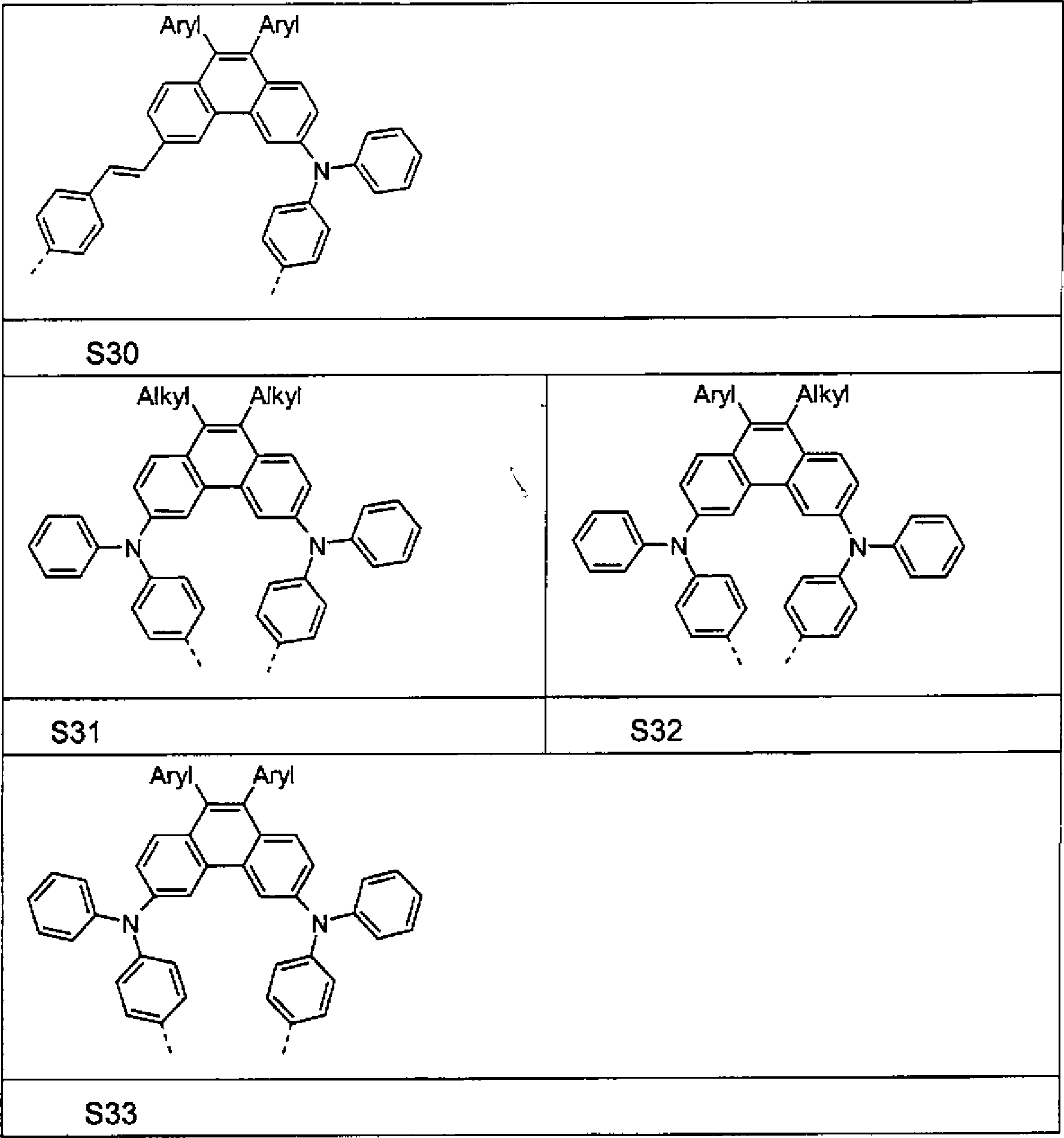
- Beispiele für bevorzugte Einheiten der Formel (1) sind die folgenden Strukturen (S1) bis (S33), wobei die Verknüpfung im Polymer jeweils über die 3,6-Positionen der Phenanthreneinheiten erfolgt, wie über die gestrichelten Bindungen angedeutet. Mögliche Substituenten sind wegen der Übersichtlichkeit im Allgemeinen nicht bzw. nicht überall aufgeführt. Alkyl steht hier allgemein für eine aliphatische Alkylgruppe, Aryl für ein aromatisches oder heteroaromatisches System, wie für R beschrieben. Dabei sind die Strukturen (S1) bis (S18) Beispiele für Grundgerüst-Einheiten, die Strukturen (S19) bis (S30) Beispiele für emittierende Einheiten und die Strukturen (S31) bis (S33) Beispiele für lochleitende Einheiten.
- Die erfindungsgemäßen Polymere sind entweder Homopolymere oder Copolymere. Erfindungsgemäße Copolymere können dabei neben einer oder mehreren Strukturen der Formel (1) potenziell eine oder mehrere weitere Strukturen, beispielsweise aus den oben genannten Gruppen 1 bis 7, aufweisen.
- Die erfindungsgemäßen Copolymere können statistische, alternierende oder blockartige Strukturen aufweisen oder auch mehrere dieser Strukturen abwechselnd besitzen. Wie Copolymere mit blockartigen Strukturen erhalten werden können, ist beispielsweise ausführlich in der
DE 10337077 A1 beschrieben. Diese Offenlegungsschrift ist via Zitat Bestandteil der vorliegenden Anmeldung. - Durch das Verwenden mehrerer verschiedener Strukturelemente können Eigenschaften wie Löslichkeit, Festphasenmorphologie, Farbe, Ladungsinjektions- und -transporteigenschaften, Temperaturstabilität, elektrooptische Charakteristik etc. eingestellt werden.
- Die erfindungsgemäßen Polymere werden in der Regel durch Polymerisation von einer oder mehreren Monomersorten hergestellt, von denen mindestens ein Monomer im Polymer zu Einheiten der Formel (1) führt. Entsprechende Polymerisationsreaktionen gibt es prinzipiell viele. Es haben sich hier jedoch einige Typen besonders bewährt, die zu C-C- bzw. zu C-N-Verknüpfungen führen:
- (A) Polymerisation gemäß SUZUKI;
- (B) Polymerisation gemäß YAMAMOTO;
- (C) Polymerisation gemäß STILLE;
- (D) Polymerisation gemäß HARTWIG-BUCHWALD.
- Wie die Polymerisation nach diesen Methoden durchgeführt werden kann und wie die Polymere vom Reaktionsmedium abgetrennt und aufgereinigt werden können, ist beispielsweise im Detail in der
DE 10249723 A1 beschrieben. - Monomere, die in den erfindungsgemäßen Polymeren zu Struktureinheiten der Formel (1) führen, sind Phenanthren-Derivate, die in der 9- und/oder 10-Position geeignet substituiert sind und an der 3,6-Position (bzw. in einer geeigneten Position an Y, falls vorhanden) geeignete Funktionalitäten aufweisen, die es erlauben, diese Monomereinheit in das Polymer einzubauen.
- Monomere, die im Polymer zu Einheiten der Formel (1) führen, sind neu und daher ebenfalls Gegenstand der vorliegenden Erfindung.
- Weiterhin Gegenstand der Erfindung sind daher bifunktionelle monomere Verbindungen der Formel (2), die dadurch gekennzeichnet sind, dass die beiden funktionellen Gruppen A, gleich oder verschieden sind, ausgewählt aus Cl, Br, I, O-Tosylat, O-Triflat, O-SO2R2, B(OR2)2 und Sn(R2), und unter Bedingungen der C-C- bzw. C-N-Verknüpfungen copolymerisieren, wobei R2 dieselbe Bedeutung hat, wie in Bezug auf Formel (1) beschrieben, und wobei zwei oder mehr Reste R2 auch miteinander ein Ringsystem bilden können,
dass R bei jedem Auftreten gleich oder verschieden, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 40 C-Atomen, die durch R1 substituiert sein kann, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CR1=CR1- oder -C≡C- ersetzt sein können, und in der auch ein oder mehrere H-Atome durch F, CI, Br, I oder CN ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches auch durch ein oder mehrere Reste R1 substituiert sein kann,
und dass die weiteren Symbole und Indizes dieselbe Bedeutung wie in Bezug auf Formel (1) haben. - Vorzugsweise ist A aus Br, I und B(OR2)2 ausgewählt.
- Die C-C-Verknüpfungen sind vorzugsweise ausgewählt aus den Gruppen der SUZUKI-Kupplung, der YAMAMOTO-Kupplung und der STILLE-Kupplung; die C-N-Verknüpfung ist vorzugsweise eine Kupplung gemäß HARTWIG-BUCHWALD.
- Dabei gilt für bifunktionelle monomere Verbindungen der Formel (2) dieselbe Bevorzugung wie sie für die Struktureinheiten der Formel (1) oben beschrieben ist.
- Es kann bevorzugt sein, das erfindungsgemäße Polymer nicht als Reinsubstanz, sondern als Mischung (Blend) zusammen mit weiteren beliebigen polymeren, oligomeren, dendritischen oder niedermolekularen Substanzen zu verwenden. Diese können beispielsweise die elektronischen Eigenschaften verbessern, den Transfer vom Singulett- zum Triplettzustand beeinflussen oder selber aus dem Singulett- oder aus dem Triplettzustand Licht emittieren. Aber auch elektronisch inerte Substanzen können sinnvoll sein, um beispielsweise die Morphologie des gebildeten Polymerfilms oder die Viskosität von Polymerlösungen zu beeinflussen.
- Hergestellt werden können weiterhin Lösungen und Formulierungen aus einem oder mehreren erfindungsgemäßen Polymeren oder Blends in einem oder mehreren Lösungsmitteln. Wie Polymerlösungen hergestellt werden können, ist beispielsweise in der
WO 02/072714 A1 WO 03/019694 A2 - Die erfindungsgemäßen Polymere können in PLEDs verwendet werden. Diese enthalten Kathode, Anode, Emissionsschicht und gegebenenfalls weitere Schichten, wie z. B. vorzugsweise eine Lochinjektionsschicht und gegebenenfalls eine Zwischenschicht zwischen der Lochinjektions- und der Emissionsschicht. Wie PLEDs hergestellt werden können, wird als allgemeines Verfahren ausführlich in der
DE 10304819 A1 beschrieben, das entsprechend für den Einzelfall anzupassen ist. - Wie oben beschrieben, eignen sich die erfindungsgemäßen Polymere ganz besonders als Elektrolumineszenzmaterialien in den derart hergestellten PLEDs oder Displays.
- Als Elektrolumineszenzmaterialien im Sinne der Erfindung gelten Materialien, die als aktive Schicht in einer PLED Verwendung finden können. Aktive Schicht bedeutet, dass die Schicht befähigt ist, bei Anlegen eines elektrischen Feldes Licht abzustrahlen (lichtemittierende Schicht) und/oder dass sie die Injektion und/oder den Transport der positiven und/oder negativen Ladungen verbessert (Ladungsinjektions- oder Ladungstransportschicht). Es kann sich auch um eine Zwischenschicht zwischen einer Lochinjektionsschicht und einer Emissionsschicht handeln.
- Gegenstand der Erfindung ist daher auch die Verwendung eines erfindungsgemäßen Polymers in einer PLED, insbesondere als Elektrolumineszenzmaterial.
- Die PLED weist dabei eine oder mehrere aktive Schichten auf, wobei mindestens eine dieser aktiven Schichten ein oder mehrere erfindungsgemäße Polymere enthält. Die aktive Schicht kann beispielsweise eine lichtemittierende Schicht und/oder eine Transportschicht und/oder eine Ladungsinjektionsschicht und/oder eine Zwischenschicht sein.
- Die erfindungsgemäßen Polymere weisen gegenüber den in der
WO 03/020790 A2 WO 02/077060 A1 - (1) Es wurde gefunden, dass die erfindungsgemäßen Polymere (bei ansonsten gleicher oder ähnlicher Zusammensetzung) höhere Leuchteffizienzen in der Anwendung aufweisen. Dies gilt besonders für die Copolymere, die blaue Emission zeigen. Dies ist von enormer Bedeutung, da somit entweder gleiche Helligkeit bei geringerem Energieverbrauch erzielt werden kann, was vor allem bei mobilen Applikationen (Displays für Handys, Pager, PDA etc.), die auf Batterien und Akkus angewiesen sind, sehr wichtig ist. Umgekehrt erhält man bei gleichem Energieverbrauch höhere Helligkeiten, was beispielsweise für Beleuchtungsanwendungen interessant sein kann.
- (2) Des Weiteren hat sich überraschenderweise gezeigt, dass wiederum im direkten Vergleich die erfindungsgemäßen Polymere höhere operative Lebensdauern aufweisen, insbesondere im Fall von grün und blau emittierenden PLEDs.
- (3) Auch vom Löslichkeitsverhalten (z. B. Gelierungstemperatur bei gegebener Konzentration, Viskosität bei gegebener Konzentration) sind die erfindungsgemäßen Polymere den bekannten Polymeren gleichwertig bzw. weisen z. T. bessere Löslichkeit in einer größeren Bandbreite von Lösungsmitteln auf und eignen sich daher genauso gut oder besser zur Verarbeitung aus Lösung, z. B. durch Drucktechniken.
- (4) Die Zugänglichkeit und die Erzielbarkeit von Farben ist bei den erfindungsgemäßen Polymeren gleichwertig oder besser im Vergleich zum Stand der Technik. Insbesondere bei blau emittierenden Polymeren wird ein verbesserter Farbort und eine gesättigtere blaue Emission beobachtet.
- (5) Die erfindungsgemäßen Polymere sind, auch ohne den Einsatz von elektronenleitenden Comonomeren, gute Elektronenleiter. Elektronenleitende Eigenschaften in Polymeren sind bislang schwierig zu verwirklichen gewesen, da viele Elektronenleiter gemäß dem Stand der Technik für hochwertige Anwendungen nicht ausreichend stabil sind.
- (6) Da das neue Polymergrundgerüst der Formel (1) selber zu tiefblauer Emission führt, ist es leicht möglich, bestimmte emittierende Einheiten einzuführen, die dann im Polymer immer noch zu blauer Emission führen. Dadurch ist es leicht möglich, Ladungstransport- und Emissionseigenschaften im Polymer zu trennen. Dies erscheint nötig, um stabile Polymere zu erhalten. Dies war jedoch bislang nur schwierig möglich, da das Polymergrundgerüst selbst immer gleichzeitig auch emittiert hat.
- Im vorliegenden Anmeldungstext und auch in den im Weiteren folgenden Beispielen wird auf die Verwendung erfindungsgemäßer Polymere oder Blends in Bezug auf PLEDs und die entsprechenden Displays abgezielt. Trotz dieser Beschränkung der Beschreibung ist es für den Fachmann ohne weiteres erfinderisches Zutun möglich, die erfindungsgemäßen Polymere auch für weitere Verwendungen in anderen elektronischen Devices (Vorrichtungen) zu benutzen, z. B. für organische integrierte Schaltungen (O-ICs), organische Feld-Effekt-Transistoren (OFETs), organische Dünnfilmtransistoren (OTFTs), organische Solarzellen (O-SCs) oder auch organische Laserdioden (O-Laser), um nur einige Anwendungen zu nennen.
- Die Verwendung erfindungsgemäßer Polymere in den entsprechenden Vorrichtungen selbst sind ebenfalls Gegenstand der vorliegenden Erfindung.
- Die vorliegende Erfindung wird im folgenden anhand von Ausführungsbeispielen näher erläutert, ohne dadurch jedoch eingeschränkt zu werden.
- Beispiele:
- Beispiel 1:
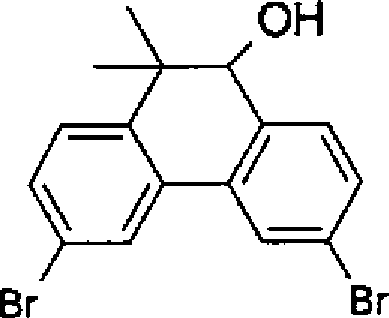
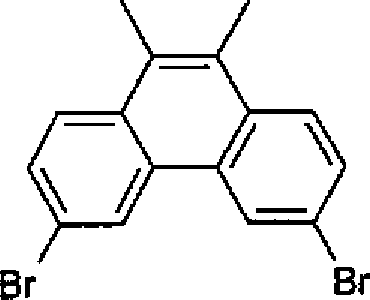
- Synthese von 3,6-Dibrom-9,10-dimethylphenanthren
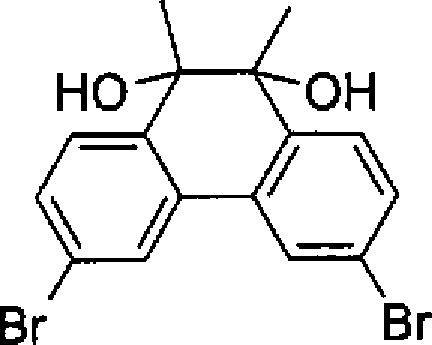
- 34,3 g (94 mmol) 3,6-Dibromphenanthren-9,10-chinon werden unter Argon bei –10°C in 600 ml trockenem THF suspendiert, und es werden 141 ml (282 mmol) Methylmagnesiumchlorid (2 molare Lösung in THF) so zugetropft, dass die Innentemperatur 0°C nicht übersteigt. Anschließend wird über Nacht bei Raumtemperatur gerührt. Dem Ansatz werden unter Eiskühlung 50 ml Eisessig zugegeben, und es wird mit Ethylacetat verdünnt. Nach zweimaligem Waschen mit gesättigter Kochsalzlösung wird über Natriumsulfat getrocknet und die Lösemittel werden entfernt. Man erhält das Produkt, das ohne weitere Aufreinigung in der nächsten Stufe eingesetzt wird.
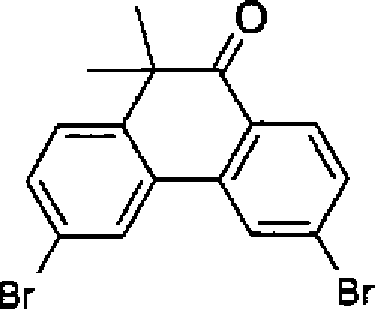
- 132,8 g (294 mmol) 3,6-Dibrom-9,10-dihydroxy-9,10-dimethyl-9,10-dihydrophenanthren werden unter Argon in 420 ml Essigsäure und 210 ml Trifluoressigsäure suspendiert und 3 Stunden unter Rückfluss gerührt. Nach Rühren über Nacht bei Raumtemperatur wird abgesaugt, der Rückstand mit Wasser und Methanol gewaschen, in Toluol gelöst, über Kieselgel filtriert und das Lösemittel entfernt. Man erhält das Produkt, das ohne weitere Aufreinigung in der nächsten Stufe eingesetzt wird.
- Im ausgeheizten Kolben werden 2,16 g (57 mmol) Lithium-aluminiumhydrid vorgelegt. Unter Eiskühlung werden 100 ml THF zugegeben. Danach werden 43,4 g (114 mmol) 3,6-Dibrom-9-keto-10,10-dimethyl-9,10-dihydrophenanthren in 150 ml THF zugetropft und anschließend unter Rückfluss erhitzt. Über Nacht läßt man auf Raumtemperatur abkühlen, dann werden vorsichtig 2 ml Wasser zugegeben. Nach 15 Minuten Rühren werden 2 ml 15%ige NaOH zugegeben, 15 Minuten gerührt, 6 ml Wasser zugetropft und 15 Minuten gerührt. Der entstandene Feststoff wird abgesaugt, mit THF gewaschen und das Lösemittel vom Filtrat entfernt. Man erhält das Produkt, das ohne weitere Aufreinigung in der nächsten Stufe eingesetzt wird.
- 43,4 g (113 mmol) 3,6-Dibrom-9-hydroxy-10,10-dimethyl-9,10-dihydrophenanthren werden in 610 ml Essigsäure suspendiert. Es werden 780 mg Iod und 3,5 ml HBr in Essigsäure zugegeben und die Suspension zum Rückfluss erhitzt. Über Nacht läßt man unter Rühren abkühlen. Man erhält das Produkt, indem der Rückstand abgesaugt und mit Wasser und Methanol gewaschen wird.
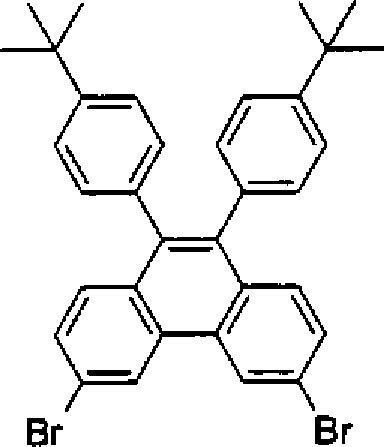
- Die Synthese erfolgt analog zu Beispiel 1 unter Verwendung von 4-tert-Butylphenylmagnesiumchlorid statt Methylmagnesiumchlorid. Das Produkt wird durch mehrfache Umkristallisation aus Toluol und aus Chlorbenzol gereinigt.
Claims (20)
- Konjugierte oder teilkonjugierte Polymere, enthaltend mindestens 5 mol% Struktureinheiten der Formel (1), wobei die verwendeten Symbole und Indizes die folgenden Bedeutungen besitzen: R bei jedem Auftreten gleich oder verschieden, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 40 C-Atomen, die durch R1 substituiert sein kann, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CR1=CR1- oder -C≡C- ersetzt sein können, und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches auch durch ein oder mehrere Reste R1 substituiert sein kann; dabei können die beiden Reste R miteinander auch ein weiteres mono- oder polycyclisches, aromatisches oder aliphatisches Ringsystem bilden; X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist; Y bei jedem Auftreten gleich oder verschieden ein bivalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder durch ein oder mehrere Reste R1 substituiert sein kann; R1 bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R2, -O-, -S-, -O-CO-O-, -CO-O-, -CR2=CR2- oder -C≡C- ersetzt sein können und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder eine Aryl-, Heteroaryl-, Aryloxy- oder Heteroaryloxygruppe mit 5 bis 40 C-Atomen ist, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein kann; dabei können auch zwei oder mehrere der Reste R1 miteinander und/oder mit R ein Ringsystem bilden; oder F, Cl, Br, I, CN, N(R2)2, Si(R2)3 oder B(R2)2 bedeuten; R2 bei jedem Auftreten gleich oder verschieden H oder ein aliphatischer oder aromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen ist; Ar bei jedem Auftreten gleich oder verschieden ein monovalentes aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches unsubstituiert oder mit R1 substituiert sein kann; n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist; m bei jedem Auftreten gleich oder verschieden 0, 1 oder 2 ist; und die gestrichelte Bindung dabei die Verknüpfung im Polymer bedeutet.
- Polymere gemäß Anspruch 1, dadurch gekennzeichnet, dass sie neben den Struktureinheiten der Formel (1) weitere Struktureinheiten enthalten, die die Lochinjektions- und/oder -transporteigenschaften erhöhen, die ausgewählt sind aus den Gruppen der Triarylamine, Benzidine, Tetraaryl-para-phenylendiamine, Triarylphosphine, Phenothiazine, Phenoxazine, Dihydrophenazine, Thianthrene, Dibenzo-para-dioxine, Phenoxathiine, Carbazole, Azulene, Thiophene, Pyrrole und Furane.
- Polymere gemäß Anspruch 1 oder 2, dadurch gekennzeichnet, dass sie neben den Struktureinheiten der Formel (1) weitere Struktureinheiten enthalten, die die Elektroneninjektions- und/oder -transporteigenschaften erhöhen, die ausgewählt sind aus den Gruppen der Pyridine, Pyrimidine, Pyridazine, Pyrazine, Oxadiazole, Chinoline, Chinoxaline und Phenazine, aber auch Triarylborane.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 3, dadurch gekennzeichnet, dass die weiteren Struktureinheiten Kombinationen von Struktureinheiten gemäß Anspruch 2 und 3 aufweisen.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 4, dadurch gekennzeichnet, dass sie neben den Struktureinheiten der Formel (1) weitere Struktureinheiten enthalten, die die Emissionscharakteristik insoweit verändern, dass Elektrophosphoreszenz statt Elektrofluoreszenz erhalten werden kann, die ausgewählt sind aus Struktureinheiten welche Elemente aus der Gruppe Ru, Os, Rh, Ir, Pd, Pt enthalten.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 5, dadurch gekennzeichnet, dass die weiteren Struktureinheiten, die den Übergang vom Singulett- zum Triplettzustand verbessern, ausgewählt sind aus den Klassen der Carbazol- und überbrückten Carbazoldimereinheiten, Ketone, Phosphinoxide, Sulfoxide, Sulfone und Silane.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 6, dadurch gekennzeichnet, dass die weiteren Struktureinheiten, die die Morphologie und/oder die Emissionsfarbe der Polymere beeinflussen, ausgewählt sind aus den Klassen der 1,4-Phenylene, 1,4-Naphthylene, 1,4- oder 9,10-Anthrylene, 1,6-, 2,7- oder 4,9-Pyrenylene, 3,9- oder 3,10-Perylenylene, 4,4'-Biphenylylene, 4,4''-Terphenylylene, 4,4'-Bi-1,1'-naphthylylene, 4,4'-Tolanylene, 4,4'-Stilbenylene oder 4,4''-Bisstyrylarylene.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 7, dadurch gekennzeichnet, dass die weiteren Struktureinheiten, die typischerweise als Backbone verwendet werden, ausgewählt sind aus den Klassen der 4,5-Dihydropyrene, 4,5,9,10-Tetrahydro-pyrene, Fluorene, 9,9'-Spirobifluorene, 9,10-Dihydrophenanthrene, 5,7-Dihydrodibenzooxepine und cis- und trans-Indenofluorene.
- Polymere gemäß mindestens einem der vorhergehenden Ansprüche, dadurch gekennzeichnet, dass der Anteil der Struktureinheiten der Formel (1) mindestens 10 mol% beträgt.
- Polymere gemäß mindestens einem der vorhergehenden Ansprüche, dadurch gekennzeichnet, dass die Polymere außer Struktureinheiten der Formel (1) zwei weitere Struktureinheiten enthalten, wobei eine dieser Struktureinheiten aus der Gruppe der lochleitenden Struktureinheiten gemäß Anspruch 2 und die andere Struktureinheit aus der Gruppe der emittierenden Struktureinheiten gemäß Anspruch 5 ausgewählt ist.
- Polymere gemäß mindestens einem der vorhergehenden Ansprüche, dadurch gekennzeichnet, dass sie Struktureinheiten der Formel (1) als Grundgerüst enthalten und dass n bei jedem Auftreten gleich 0 ist.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 10, dadurch gekennzeichnet, dass sie Struktureinheiten der Formel (1) als lochtransportierende Struktureinheiten enthalten und dass: n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist, wobei mindestens ein n = 1 ist; m bei jedem Aufteten gleich oder verschieden 0, 1 oder 2 ist, wobei m ungleich 0 ist, wenn das entsprechende n = 1 ist; und X bei jedem Auftreten -N(Ar)-Ar- ist.
- Polymere gemäß mindestens einem der Ansprüche 1 bis 10, dadurch gekennzeichnet, dass sie Struktureinheiten der Formel (1) als Emitter enthalten und dass: n bei jedem Auftreten gleich oder verschieden 0 oder 1 ist, wobei mindestens ein n = 1 ist; m bei jedem Auftreten gleich oder verschieden 0, 1 oder 2 ist, wobei m ungleich 0 ist, wenn das entsprechende n = 1 ist; und X bei jedem Auftreten gleich oder verschieden -CR1=CR1-, -C≡C- oder -N(Ar)-Ar- ist, wobei mindestens ein X gleich -CR1=CR1- oder -C≡C- ist.
- Polymere gemäß mindestens einem der vorhergehenden Ansprüche, dadurch gekennzeichnet, dass die Struktureinheiten der Formel (1) in den 9,10-Positionen der Phenanthren-Einheiten symmetrisch substituiert sind.
- Polymere gemäß mindestens einem der vorhergehenden Ansprüche, dadurch gekennzeichnet, dass sie durch Polymerisation gemäß SUZUKI, Polymerisation gemäß YAMAMOTO, Polymerisation gemäß STILLE oder Polymerisation gemäß HARTWIG-BUCHWALD hergestellt werden.
- Bifunktionelle monomere Verbindungen der Formel (2), dadurch gekennzeichnet, dass die beiden funktionellen Gruppen A, gleich oder verschieden sind, ausgewählt aus Cl, Br, I, O-Tosylat, O-Triflat, O-SO2R2, B(OR2)2 und Sn(R2)3, und unter Bedingungen der C-C- bzw. C-N-Verknüpfungen copolymerisieren, wobei R2 dieselbe Bedeutung hat wie in Anspruch 1 angegeben und wobei zwei oder mehr Reste R2 auch miteinander ein Ringsystem bilden können, und dass R bei jedem Auftreten gleich oder verschieden, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 40 C-Atomen, die durch R1 substituiert sein kann, in der auch ein oder mehrere nicht benachbarte C-Atome durch =N-R1, -O-, -S-, -O-CO-O-, -CO-O-, -CR1=CR1- oder -C≡C- ersetzt sein können, und in der auch ein oder mehrere H-Atome durch F, Cl, Br, I oder CN ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 2 bis 40 C-Atomen ist, welches auch durch ein oder mehrere Reste R1 substituiert sein kann und dass die weiteren Symbole und Indizes dieselbe Bedeutung haben wie in Anspruch 1 angegeben.
- Bifunktionelle monomere Verbindungen der Formel (2) gemäß Anspruch 16, dadurch gekennzeichnet, dass die C-C-Verknüpfungen ausgewählt sind aus den Gruppen der SUZUKI-Kupplung, der YAMAMOTO-Kupplung und der STILLE-Kupplung oder dass die C-N-Verknüpfung eine Kupplung gemäß HARTWIG-BUCHWALD ist.
- Verwendung eines Polymers gemäß mindestens einem der Ansprüche 1 bis 15 in organischen elektronischen Bauteilen.
- Verwendung gemäß Anspruch 18, dadurch gekennzeichnet, dass es sich bei den organischen elektronischen Bauteilen um polymere Leuchtdioden (PLED), organische integrierte Schaltungen (O-IC), organische Feld-Effekt-Transistoren (OFET), organische Dünnfilmtransistoren (OTFT), organische Solarzellen (O-SC) oder organische Laserdioden (O-Laser) handelt.
- Verwendung gemäß Anspruch 18 oder 19, dadurch gekennzeichnet, dass es sich bei den organischen elektronischen Bauteilen um polymere Leuchtdioden handelt.
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005037734.3A DE102005037734B4 (de) | 2005-08-10 | 2005-08-10 | Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen |
| US12/063,363 US20100288974A1 (en) | 2005-08-10 | 2006-07-19 | Electroluminescent polymers and use thereof |
| CN2006800287734A CN101238756B (zh) | 2005-08-10 | 2006-07-19 | 电致发光聚合物和其用途 |
| PCT/EP2006/007105 WO2007017066A1 (de) | 2005-08-10 | 2006-07-19 | Elektrolumineszierende polymere und ihre verwendung |
| KR1020087005616A KR101318070B1 (ko) | 2005-08-10 | 2006-07-19 | 전계발광 중합체 및 이의 용도 |
| JP2008525414A JP5474348B2 (ja) | 2005-08-10 | 2006-07-19 | エレクトロルミネセントポリマー及びそれの使用 |
| EP06762700A EP1913797A1 (de) | 2005-08-10 | 2006-07-19 | Elektrolumineszierende polymere und ihre verwendung |
| TW095128870A TW200720371A (en) | 2005-08-10 | 2006-08-07 | Electroluminescent polymers, and the use thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005037734.3A DE102005037734B4 (de) | 2005-08-10 | 2005-08-10 | Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE102005037734A1 DE102005037734A1 (de) | 2007-02-22 |
| DE102005037734B4 true DE102005037734B4 (de) | 2018-02-08 |
Family
ID=37072963
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102005037734.3A Expired - Lifetime DE102005037734B4 (de) | 2005-08-10 | 2005-08-10 | Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20100288974A1 (de) |
| EP (1) | EP1913797A1 (de) |
| JP (1) | JP5474348B2 (de) |
| KR (1) | KR101318070B1 (de) |
| CN (1) | CN101238756B (de) |
| DE (1) | DE102005037734B4 (de) |
| TW (1) | TW200720371A (de) |
| WO (1) | WO2007017066A1 (de) |
Families Citing this family (171)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102005040411A1 (de) | 2005-08-26 | 2007-03-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| WO2008012250A1 (en) | 2006-07-28 | 2008-01-31 | Ciba Holding Inc. | Novel polymers |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008015526B4 (de) | 2008-03-25 | 2021-11-11 | Merck Patent Gmbh | Metallkomplexe |
| DE102008017591A1 (de) | 2008-04-07 | 2009-10-08 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008018670A1 (de) | 2008-04-14 | 2009-10-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008027005A1 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Organische elektronische Vorrichtung enthaltend Metallkomplexe |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008050841B4 (de) | 2008-10-08 | 2019-08-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008054141A1 (de) | 2008-10-31 | 2010-05-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009022858A1 (de) | 2009-05-27 | 2011-12-15 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR20110097612A (ko) | 2008-11-11 | 2011-08-31 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자 |
| DE102008057051B4 (de) | 2008-11-13 | 2021-06-17 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008057050B4 (de) | 2008-11-13 | 2021-06-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009005746A1 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009009277B4 (de) | 2009-02-17 | 2023-12-07 | Merck Patent Gmbh | Organische elektronische Vorrichtung, Verfahren zu deren Herstellung und Verwendung von Verbindungen |
| DE102009010714A1 (de) | 2009-02-27 | 2010-09-02 | Merck Patent Gmbh | Vernetzbare und vernetzte Polymere, Verfahren zu deren Herstellung sowie deren Verwendung |
| DE102009011223A1 (de) | 2009-03-02 | 2010-09-23 | Merck Patent Gmbh | Metallkomplexe |
| DE102009013041A1 (de) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009033371A1 (de) | 2009-07-16 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009034625A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053644B4 (de) | 2009-11-17 | 2019-07-04 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009042693A1 (de) | 2009-09-23 | 2011-03-24 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053191A1 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009053836A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010004803A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent GmbH, 64293 | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| CN102812573B (zh) | 2010-03-23 | 2015-09-30 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102010024335A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010024897A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010033548A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010048607A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010048608A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2663567B1 (de) | 2011-01-13 | 2016-06-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| DE102012000064B4 (de) | 2011-01-21 | 2026-01-22 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| CN103476774B (zh) | 2011-04-13 | 2017-02-15 | 默克专利有限公司 | 用于电子器件的材料 |
| EP2697226B1 (de) | 2011-04-13 | 2017-01-18 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| EP2699641B1 (de) | 2011-04-18 | 2017-05-17 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| JP6195823B2 (ja) | 2011-05-05 | 2017-09-13 | メルク パテント ゲーエムベーハー | 電子素子のための化合物 |
| KR101884496B1 (ko) | 2011-05-05 | 2018-08-01 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| US9780311B2 (en) | 2011-07-29 | 2017-10-03 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2013017192A1 (de) | 2011-08-03 | 2013-02-07 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| JP6223984B2 (ja) | 2011-10-27 | 2017-11-01 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| CN103946215B (zh) | 2011-11-17 | 2016-09-28 | 默克专利有限公司 | 螺二氢吖啶衍生物和其作为有机电致发光器件用材料的用途 |
| EP2791105B1 (de) | 2011-12-12 | 2020-03-18 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| DE102012022880B4 (de) | 2011-12-22 | 2024-12-24 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| KR102357439B1 (ko) | 2012-02-14 | 2022-02-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 스피로비플루오렌 화합물 |
| JP6105040B2 (ja) | 2012-03-23 | 2017-03-29 | メルク パテント ゲーエムベーハー | エレクトロルミネッセンス素子のための9,9’−スピロビキサンテン誘導体 |
| DE102012011335A1 (de) * | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| EP2872590B1 (de) | 2012-07-13 | 2018-11-14 | Merck Patent GmbH | Metallkomplexe |
| CN108054293B (zh) | 2012-07-23 | 2020-05-22 | 默克专利有限公司 | 2-二芳基氨基芴的衍生物和含有所述2-二芳基氨基芴衍生物的有机电子复合体 |
| KR20210076207A (ko) | 2012-07-23 | 2021-06-23 | 메르크 파텐트 게엠베하 | 플루오렌 및 이를 함유하는 전자 소자 |
| CN110444694B (zh) | 2012-07-23 | 2023-04-07 | 默克专利有限公司 | 化合物以及有机电致发光器件 |
| JP6363075B2 (ja) | 2012-08-07 | 2018-07-25 | メルク パテント ゲーエムベーハー | 金属錯体 |
| WO2014044347A1 (de) | 2012-09-20 | 2014-03-27 | Merck Patent Gmbh | Metallkomplexe |
| WO2014072017A1 (de) | 2012-11-12 | 2014-05-15 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR102173856B1 (ko) | 2012-11-30 | 2020-11-04 | 메르크 파텐트 게엠베하 | 전자 소자 |
| EP2941472B1 (de) | 2013-01-03 | 2018-07-25 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| US20150340627A1 (en) | 2013-01-03 | 2015-11-26 | Merck Patent Gmbh | Materials for electronic devices |
| CN103254044B (zh) * | 2013-05-22 | 2015-08-26 | 河南省科学院化学研究所有限公司 | 2,7-二溴-9,10取代-菲衍生物 |
| GB201313699D0 (en) * | 2013-07-31 | 2013-09-11 | Cambridge Display Tech Ltd | Polymer and organic electronic device |
| CN105612164A (zh) | 2013-10-02 | 2016-05-25 | 默克专利有限公司 | 用于oled中的含硼化合物 |
| WO2015082056A1 (de) | 2013-12-06 | 2015-06-11 | Merck Patent Gmbh | Verbindungen und organische elektronische vorrichtungen |
| EP3080229B1 (de) | 2013-12-12 | 2018-01-17 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| KR102618668B1 (ko) | 2013-12-19 | 2023-12-27 | 메르크 파텐트 게엠베하 | 헤테로시클릭 스피로 화합물 |
| JP2017537085A (ja) | 2014-11-11 | 2017-12-14 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| EP3250658B1 (de) | 2015-01-30 | 2019-06-19 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| JP6772188B2 (ja) | 2015-02-03 | 2020-10-21 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 金属錯体 |
| KR101668419B1 (ko) | 2015-02-06 | 2016-10-21 | 김효영 | 워터 캡슐식 물티슈 패키지 |
| JP2018525331A (ja) | 2015-06-10 | 2018-09-06 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| US20180219156A1 (en) | 2015-07-22 | 2018-08-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| GB201513037D0 (en) | 2015-07-23 | 2015-09-09 | Merck Patent Gmbh | Phenyl-derived compound for use in organic electronic devices |
| WO2017016632A1 (en) | 2015-07-29 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN107922359A (zh) | 2015-07-30 | 2018-04-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| JP6786591B2 (ja) | 2015-08-14 | 2020-11-18 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 有機エレクトロルミネッセンス素子のためのフェノキサジン誘導体 |
| US20180327339A1 (en) | 2015-08-28 | 2018-11-15 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| TWI745361B (zh) | 2016-03-17 | 2021-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| CN108884087A (zh) | 2016-04-11 | 2018-11-23 | 默克专利有限公司 | 包含二苯并呋喃和/或二苯并噻吩结构的杂环化合物 |
| US12486230B2 (en) | 2016-06-03 | 2025-12-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US11192909B2 (en) | 2016-06-30 | 2021-12-07 | Merck Patent Gmbh | Method for the separation of enantiomeric mixtures from metal complexes |
| US11365167B2 (en) | 2016-07-08 | 2022-06-21 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP7039549B2 (ja) | 2016-07-14 | 2022-03-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 金属錯体 |
| TW201827425A (zh) | 2016-09-14 | 2018-08-01 | 德商麥克專利有限公司 | 具有咔唑結構之化合物 |
| US11447464B2 (en) | 2016-09-14 | 2022-09-20 | Merck Patent Gmbh | Compounds with spirobifluorene-structures |
| US20200028091A1 (en) | 2016-09-30 | 2020-01-23 | Merck Patent Gmbh | Carbazoles with diazadibenzofurane or diazadibenzothiophene structures |
| TWI766884B (zh) | 2016-09-30 | 2022-06-11 | 德商麥克專利有限公司 | 具有二氮雜二苯并呋喃或二氮雜二苯并噻吩結構的化合物、其製法及其用途 |
| TWI764942B (zh) | 2016-10-10 | 2022-05-21 | 德商麥克專利有限公司 | 電子裝置 |
| JP2020512273A (ja) | 2016-11-02 | 2020-04-23 | メルク パテント ゲーエムベーハー | 電子デバイス用材料 |
| JP7073388B2 (ja) | 2016-11-08 | 2022-05-23 | メルク パテント ゲーエムベーハー | 電子デバイスのための化合物 |
| TWI756292B (zh) | 2016-11-14 | 2022-03-01 | 德商麥克專利有限公司 | 具有受體基團與供體基團之化合物 |
| TW201833118A (zh) | 2016-11-22 | 2018-09-16 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| JP7101670B2 (ja) | 2016-11-25 | 2022-07-15 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子(oled)の材料としてのビスベンゾフラン縮合2,8-ジアミノインデノ[1,2-b]フルオレン誘導体およびその関連化合物 |
| US11453680B2 (en) | 2016-11-25 | 2022-09-27 | Merck Patent Gmbh | Bisbenzofuran-fused indeno[1,2-B]fluorene derivatives and related compounds as materials for organic electroluminescent devices (OLED) |
| TW201829385A (zh) | 2016-11-30 | 2018-08-16 | 德商麥克專利有限公司 | 具有戊內醯胺結構之化合物 |
| TW201831468A (zh) | 2016-12-05 | 2018-09-01 | 德商麥克專利有限公司 | 含氮的雜環化合物 |
| KR102504432B1 (ko) | 2016-12-22 | 2023-02-27 | 메르크 파텐트 게엠베하 | 적어도 2종의 유기-기능성 화합물을 포함하는 혼합물 |
| CN110177855A (zh) | 2017-01-23 | 2019-08-27 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| TW201833300A (zh) | 2017-01-25 | 2018-09-16 | 德商麥克專利有限公司 | 咔唑衍生物 |
| CN110291064B (zh) | 2017-02-02 | 2023-04-28 | 默克专利有限公司 | 用于电子器件的材料 |
| CN110325524A (zh) | 2017-03-02 | 2019-10-11 | 默克专利有限公司 | 用于有机电子器件的材料 |
| TW201843143A (zh) | 2017-03-13 | 2018-12-16 | 德商麥克專利有限公司 | 含有芳基胺結構之化合物 |
| CN110573515B (zh) | 2017-04-25 | 2023-07-25 | 默克专利有限公司 | 用于电子器件的化合物 |
| JP2020520970A (ja) | 2017-05-22 | 2020-07-16 | メルク パテント ゲーエムベーハー | 電子デバイス用六環性ヘテロ芳香族化合物 |
| US11767299B2 (en) | 2017-06-23 | 2023-09-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TW201920070A (zh) | 2017-06-28 | 2019-06-01 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| TWI779067B (zh) | 2017-07-28 | 2022-10-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| CN118405981A (zh) | 2017-09-08 | 2024-07-30 | 默克专利有限公司 | 用于电子器件的材料 |
| EP4242286A3 (de) | 2017-11-23 | 2023-10-04 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| KR102638811B1 (ko) | 2017-12-15 | 2024-02-21 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 치환된 방향족 아민 |
| TW201938562A (zh) | 2017-12-19 | 2019-10-01 | 德商麥克專利有限公司 | 雜環化合物 |
| KR20200100699A (ko) | 2017-12-20 | 2020-08-26 | 메르크 파텐트 게엠베하 | 헤테로방향족 화합물 |
| US20210020843A1 (en) | 2018-03-16 | 2021-01-21 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| US12178124B2 (en) | 2018-09-27 | 2024-12-24 | Merck Kgaa | Compounds that can be used in an organic electronic device as active compounds |
| EP3877369A1 (de) | 2018-11-05 | 2021-09-15 | Merck Patent GmbH | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| JP7620631B2 (ja) | 2019-12-18 | 2025-01-23 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のための芳香族化合物 |
| KR20220116008A (ko) | 2019-12-19 | 2022-08-19 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 다환 화합물 |
| CN115052865A (zh) | 2020-01-29 | 2022-09-13 | 默克专利有限公司 | 苯并咪唑衍生物 |
| EP4110884B1 (de) | 2020-02-25 | 2024-11-20 | Merck Patent GmbH | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20220154751A (ko) | 2020-03-17 | 2022-11-22 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| US20230157171A1 (en) | 2020-03-26 | 2023-05-18 | Merck Patent Gmbh | Cyclic compounds for organic electroluminescent devices |
| US20230183269A1 (en) | 2020-04-06 | 2023-06-15 | Merck Patent Gmbh | Polycyclic compounds for organic electroluminescent devices |
| US20230234937A1 (en) | 2020-06-18 | 2023-07-27 | Merck Patent Gmbh | Indenoazanaphthalenes |
| CN115916794A (zh) | 2020-06-29 | 2023-04-04 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| JP2023531470A (ja) | 2020-06-29 | 2023-07-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のためのヘテロ芳香族化合物 |
| TW202222748A (zh) | 2020-09-30 | 2022-06-16 | 德商麥克專利有限公司 | 用於結構化有機電致發光裝置的功能層之化合物 |
| TW202229215A (zh) | 2020-09-30 | 2022-08-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置功能層之結構化的化合物 |
| US20230389423A1 (en) | 2020-10-16 | 2023-11-30 | Merck Patent Gmbh | Heterocyclic compounds for organic electroluminescent devices |
| EP4229145B1 (de) | 2020-10-16 | 2025-07-23 | Merck Patent GmbH | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| US20240124769A1 (en) | 2020-12-18 | 2024-04-18 | Merck Patent Gmbh | Nitrogenous compounds for organic electroluminescent devices |
| KR20230122094A (ko) | 2020-12-18 | 2023-08-22 | 메르크 파텐트 게엠베하 | Oled에 사용하기 위한 청색 형광 방출체로서의 인돌로[3.2.1-jk]카르바졸-6-카르보니트릴유도체 |
| EP4263746B1 (de) | 2020-12-18 | 2025-10-01 | Merck Patent GmbH | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| CN118159623A (zh) | 2021-10-27 | 2024-06-07 | 默克专利有限公司 | 用于有机电致发光器件的含硼和氮的杂环化合物 |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| CN118696106A (zh) | 2022-02-23 | 2024-09-24 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| EP4482843A1 (de) | 2022-02-23 | 2025-01-01 | Merck Patent GmbH | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN114853586B (zh) * | 2022-04-21 | 2024-03-15 | 扬州市职业大学(扬州开放大学) | 一种菲酮衍生物的制备方法 |
| EP4519383B1 (de) | 2022-05-06 | 2026-01-14 | Merck Patent GmbH | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| CN119325756A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的杂环化合物 |
| CN119325755A (zh) | 2022-06-20 | 2025-01-17 | 默克专利有限公司 | 用于光电器件的有机杂环化合物 |
| CN119894856A (zh) | 2022-09-22 | 2025-04-25 | 默克专利有限公司 | 用于有机电致发光器件的含氮化合物 |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120152954A (zh) | 2022-11-01 | 2025-06-13 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120569385A (zh) | 2023-01-17 | 2025-08-29 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025003084A1 (de) | 2023-06-28 | 2025-01-02 | Merck Patent Gmbh | Dicyanoarylverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025045935A1 (de) | 2023-08-31 | 2025-03-06 | Merck Patent Gmbh | Cyanogruppen-enthaltende aromaten für organische elektrolumineszenzvorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05148211A (ja) * | 1991-11-29 | 1993-06-15 | Mita Ind Co Ltd | フエナントレン誘導体およびそれを用いた感光体 |
| DE4307049A1 (de) * | 1993-03-08 | 1994-09-15 | Hoechst Ag | Diskotische Flüssigkristalle |
| JP2001023777A (ja) * | 1999-07-08 | 2001-01-26 | Toray Ind Inc | 発光素子 |
| JP2005005226A (ja) * | 2003-06-16 | 2005-01-06 | Sony Corp | 有機電界発光素子 |
| DE10337346A1 (de) * | 2003-08-12 | 2005-03-31 | Covion Organic Semiconductors Gmbh | Konjugierte Polymere enthaltend Dihydrophenanthren-Einheiten und deren Verwendung |
| WO2006063466A1 (en) * | 2004-12-17 | 2006-06-22 | Merck Frosst Canada Ltd. | 2-(phenyl or heterocyclic)-1h-phenantrho[9,10-d]imidazoles as mpges-1 inhibitors |
Family Cites Families (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3980640A (en) * | 1974-12-20 | 1976-09-14 | E. I. Du Pont De Nemours And Company | Schiff bases derived from phenanthrene-9,10-diamines and ortho-hydroxy aldehydes |
| US5609970A (en) * | 1995-01-12 | 1997-03-11 | Polaroid Corporation | Electroluminescent device with polymeric charge injection layer |
| KR100280707B1 (ko) * | 1998-11-12 | 2001-02-01 | 김순택 | 발광 화합물 및 이를 발색재료로서 채용하고있는 표시소자 |
| JP4158078B2 (ja) * | 2001-01-30 | 2008-10-01 | ソニー株式会社 | アミノスチリルフェナントレン化合物及びその合成中間体 |
| DE10109027A1 (de) * | 2001-02-24 | 2002-09-05 | Covion Organic Semiconductors | Rhodium- und Iridium-Komplexe |
| EP1370619B1 (de) * | 2001-03-10 | 2006-06-21 | MERCK PATENT GmbH | Lösung und dispersionen organischer halbleiter |
| KR100888910B1 (ko) * | 2001-03-24 | 2009-03-16 | 메르크 파텐트 게엠베하 | 스피로비플루오렌 단위와 플루오렌 단위를 함유하는 공액중합체 및 이의 용도 |
| DE10116962A1 (de) * | 2001-04-05 | 2002-10-10 | Covion Organic Semiconductors | Rhodium- und Iridium-Komplexe |
| DE10141624A1 (de) * | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors | Lösungen polymerer Halbleiter |
| US7250226B2 (en) * | 2001-08-31 | 2007-07-31 | Nippon Hoso Kyokai | Phosphorescent compound, a phosphorescent composition and an organic light-emitting device |
| DE10143353A1 (de) * | 2001-09-04 | 2003-03-20 | Covion Organic Semiconductors | Konjugierte Polymere enthaltend Spirobifluoren-Einheiten und deren Verwendung |
| DE10159946A1 (de) * | 2001-12-06 | 2003-06-18 | Covion Organic Semiconductors | Prozess zur Herstellung von Aryl-Aryl gekoppelten Verbindungen |
| SG128438A1 (en) * | 2002-03-15 | 2007-01-30 | Sumitomo Chemical Co | Polymer compound and polymer light emitting deviceusing the same |
| TWI314947B (en) * | 2002-04-24 | 2009-09-21 | Eastman Kodak Compan | Organic light emitting diode devices with improved operational stability |
| JP4161262B2 (ja) * | 2002-06-26 | 2008-10-08 | ソニー株式会社 | 有機電界発光素子、及びそれを用いた発光又は表示装置 |
| DE10392958T5 (de) * | 2002-07-22 | 2005-08-11 | Sumitomo Chemical Co., Ltd. | Copolymer und polymere lichtemittierende Vorrichtung unter Verwendung desselben |
| DE10238903A1 (de) * | 2002-08-24 | 2004-03-04 | Covion Organic Semiconductors Gmbh | Rhodium- und Iridium-Komplexe |
| DE10249723A1 (de) * | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-Einheiten enthaltende konjugierte Polymere, deren Darstellung und Verwendung |
| TWI267545B (en) * | 2003-06-17 | 2006-12-01 | Univ Tsinghua | Electroluminescent conjugated polymers containing phosphorescent moieties and the application thereof in LED |
| DE10328627A1 (de) * | 2003-06-26 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Neue Materialien für die Elektrolumineszenz |
| JP4329437B2 (ja) | 2003-07-14 | 2009-09-09 | ソニー株式会社 | ビス(アミノスチリル)フェナントレン化合物及びその合成中間体、並びに有機電界発光素子 |
| DE10337077A1 (de) * | 2003-08-12 | 2005-03-10 | Covion Organic Semiconductors | Konjugierte Copolymere, deren Darstellung und Verwendung |
| JP2005075731A (ja) * | 2003-08-28 | 2005-03-24 | Institute Of Physical & Chemical Research | フェナントレン化合物およびその製造方法 |
| DE10343606A1 (de) * | 2003-09-20 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Weiß emittierende Copolymere, deren Darstellung und Verwendung |
| US7211208B2 (en) * | 2004-01-13 | 2007-05-01 | Aircraft Braking Systems Corporation | Carbon brake disk having noncarbonic material therein and method for making same |
| DE102004020298A1 (de) * | 2004-04-26 | 2005-11-10 | Covion Organic Semiconductors Gmbh | Elektrolumineszierende Polymere und deren Verwendung |
| CN101203583A (zh) * | 2005-05-31 | 2008-06-18 | 通用显示公司 | 发射磷光的二极管中的苯并[9,10]菲基质 |
| CN101443928A (zh) * | 2006-05-12 | 2009-05-27 | 默克专利有限公司 | 茚并芴聚合物基有机半导体材料 |
| CN101490862B (zh) * | 2006-07-25 | 2013-03-13 | 默克专利有限公司 | 聚合物共混物和它们在有机发光器件中的用途 |
| EP2435496A1 (de) * | 2009-05-29 | 2012-04-04 | Merck Patent GmbH | Konjugierte polymere und ihre verwendung als organische halbleiter |
-
2005
- 2005-08-10 DE DE102005037734.3A patent/DE102005037734B4/de not_active Expired - Lifetime
-
2006
- 2006-07-19 KR KR1020087005616A patent/KR101318070B1/ko active Active
- 2006-07-19 CN CN2006800287734A patent/CN101238756B/zh active Active
- 2006-07-19 EP EP06762700A patent/EP1913797A1/de not_active Withdrawn
- 2006-07-19 WO PCT/EP2006/007105 patent/WO2007017066A1/de not_active Ceased
- 2006-07-19 US US12/063,363 patent/US20100288974A1/en not_active Abandoned
- 2006-07-19 JP JP2008525414A patent/JP5474348B2/ja not_active Expired - Fee Related
- 2006-08-07 TW TW095128870A patent/TW200720371A/zh unknown
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05148211A (ja) * | 1991-11-29 | 1993-06-15 | Mita Ind Co Ltd | フエナントレン誘導体およびそれを用いた感光体 |
| DE4307049A1 (de) * | 1993-03-08 | 1994-09-15 | Hoechst Ag | Diskotische Flüssigkristalle |
| JP2001023777A (ja) * | 1999-07-08 | 2001-01-26 | Toray Ind Inc | 発光素子 |
| JP2005005226A (ja) * | 2003-06-16 | 2005-01-06 | Sony Corp | 有機電界発光素子 |
| DE10337346A1 (de) * | 2003-08-12 | 2005-03-31 | Covion Organic Semiconductors Gmbh | Konjugierte Polymere enthaltend Dihydrophenanthren-Einheiten und deren Verwendung |
| WO2006063466A1 (en) * | 2004-12-17 | 2006-06-22 | Merck Frosst Canada Ltd. | 2-(phenyl or heterocyclic)-1h-phenantrho[9,10-d]imidazoles as mpges-1 inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| US20100288974A1 (en) | 2010-11-18 |
| KR20080033523A (ko) | 2008-04-16 |
| DE102005037734A1 (de) | 2007-02-22 |
| EP1913797A1 (de) | 2008-04-23 |
| CN101238756A (zh) | 2008-08-06 |
| JP2009504811A (ja) | 2009-02-05 |
| JP5474348B2 (ja) | 2014-04-16 |
| TW200720371A (en) | 2007-06-01 |
| WO2007017066A1 (de) | 2007-02-15 |
| CN101238756B (zh) | 2010-10-06 |
| KR101318070B1 (ko) | 2013-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE102005037734B4 (de) | Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen | |
| EP2038241B1 (de) | Elektrolumineszierende polymere und ihre verwendung | |
| DE102004020298A1 (de) | Elektrolumineszierende Polymere und deren Verwendung | |
| EP1641894B1 (de) | Neue materialien für die elektrolumineszenz | |
| EP1668058B1 (de) | Konjugierte polymere, deren darstellung und verwendung | |
| EP1656408B1 (de) | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung | |
| EP1592729B1 (de) | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung | |
| EP1558662B1 (de) | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung | |
| EP1741148B1 (de) | Elektrolumineszierende polymere enthaltend planare arylamin-einheiten, deren darstellung und verwendung | |
| EP1427768B1 (de) | Konjugierte polymere enthaltend spirobifluoren-einheiten und deren verwendung | |
| EP1819749B1 (de) | Teilkonjugierte polymere, deren darstellung und verwendung | |
| EP1709699B1 (de) | Konjugierte polymere, deren darstellung und verwendung | |
| EP1831326B1 (de) | Elektrolumineszierende polymere und deren verwendung | |
| EP1745113B1 (de) | Neue materialmischungen für die elektrolumineszenz | |
| DE10357317A1 (de) | Konjugierte Polymere, deren Darstellung und Verwendung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OP8 | Request for examination as to paragraph 44 patent law | ||
| R016 | Response to examination communication | ||
| R016 | Response to examination communication | ||
| R016 | Response to examination communication | ||
| R079 | Amendment of ipc main class |
Free format text: PREVIOUS MAIN CLASS: C09B0069100000 Ipc: C09K0011060000 |
|
| R018 | Grant decision by examination section/examining division | ||
| R020 | Patent grant now final | ||
| R071 | Expiry of right |