DE102009057167A1 - Elektronische Vorrichtung enthaltend Metallkomplexe - Google Patents
Elektronische Vorrichtung enthaltend Metallkomplexe Download PDFInfo
- Publication number
- DE102009057167A1 DE102009057167A1 DE102009057167A DE102009057167A DE102009057167A1 DE 102009057167 A1 DE102009057167 A1 DE 102009057167A1 DE 102009057167 A DE102009057167 A DE 102009057167A DE 102009057167 A DE102009057167 A DE 102009057167A DE 102009057167 A1 DE102009057167 A1 DE 102009057167A1
- Authority
- DE
- Germany
- Prior art keywords
- group
- substituted
- aromatic
- occurrence
- organic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 229910052751 metal Inorganic materials 0.000 title claims abstract description 44
- 239000002184 metal Substances 0.000 title claims abstract description 44
- 125000003118 aryl group Chemical group 0.000 claims description 68
- 239000003446 ligand Substances 0.000 claims description 57
- 150000001875 compounds Chemical class 0.000 claims description 51
- 125000004432 carbon atom Chemical group C* 0.000 claims description 40
- -1 1,2-vinylene Chemical group 0.000 claims description 39
- 229910052698 phosphorus Inorganic materials 0.000 claims description 29
- 125000004122 cyclic group Chemical group 0.000 claims description 27
- 229910052799 carbon Inorganic materials 0.000 claims description 25
- 239000000463 material Substances 0.000 claims description 24
- 229910052757 nitrogen Inorganic materials 0.000 claims description 24
- 229910052717 sulfur Inorganic materials 0.000 claims description 24
- 230000007935 neutral effect Effects 0.000 claims description 22
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 21
- 125000001072 heteroaryl group Chemical group 0.000 claims description 20
- 239000011159 matrix material Substances 0.000 claims description 20
- 229910052760 oxygen Inorganic materials 0.000 claims description 19
- 125000001931 aliphatic group Chemical group 0.000 claims description 18
- 125000004429 atom Chemical group 0.000 claims description 16
- 238000000034 method Methods 0.000 claims description 13
- 229910002091 carbon monoxide Inorganic materials 0.000 claims description 12
- 125000000217 alkyl group Chemical group 0.000 claims description 11
- 230000000903 blocking effect Effects 0.000 claims description 11
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 claims description 10
- 125000003545 alkoxy group Chemical group 0.000 claims description 10
- 125000000623 heterocyclic group Chemical group 0.000 claims description 10
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 9
- 125000001424 substituent group Chemical group 0.000 claims description 9
- 229910052739 hydrogen Inorganic materials 0.000 claims description 8
- 125000002950 monocyclic group Chemical group 0.000 claims description 8
- 125000005309 thioalkoxy group Chemical group 0.000 claims description 8
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 7
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 7
- 239000011574 phosphorus Substances 0.000 claims description 7
- 239000011593 sulfur Substances 0.000 claims description 7
- 150000001408 amides Chemical class 0.000 claims description 6
- 150000001412 amines Chemical class 0.000 claims description 6
- 125000006165 cyclic alkyl group Chemical group 0.000 claims description 6
- 230000005525 hole transport Effects 0.000 claims description 6
- 238000002347 injection Methods 0.000 claims description 6
- 239000007924 injection Substances 0.000 claims description 6
- 230000008569 process Effects 0.000 claims description 6
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 claims description 5
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 claims description 5
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 claims description 5
- 125000003342 alkenyl group Chemical group 0.000 claims description 5
- 125000000304 alkynyl group Chemical group 0.000 claims description 5
- RBFQJDQYXXHULB-UHFFFAOYSA-N arsane Chemical class [AsH3] RBFQJDQYXXHULB-UHFFFAOYSA-N 0.000 claims description 5
- 150000007942 carboxylates Chemical class 0.000 claims description 5
- XLJMAIOERFSOGZ-UHFFFAOYSA-M cyanate Chemical compound [O-]C#N XLJMAIOERFSOGZ-UHFFFAOYSA-M 0.000 claims description 5
- 150000004678 hydrides Chemical class 0.000 claims description 5
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 claims description 5
- 239000012948 isocyanate Substances 0.000 claims description 5
- 150000002513 isocyanates Chemical class 0.000 claims description 5
- 150000002540 isothiocyanates Chemical class 0.000 claims description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 5
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 claims description 5
- 238000002360 preparation method Methods 0.000 claims description 5
- OUULRIDHGPHMNQ-UHFFFAOYSA-N stibane Chemical class [SbH3] OUULRIDHGPHMNQ-UHFFFAOYSA-N 0.000 claims description 5
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 4
- 125000004104 aryloxy group Chemical group 0.000 claims description 4
- 125000004986 diarylamino group Chemical group 0.000 claims description 4
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 4
- HZVOZRGWRWCICA-UHFFFAOYSA-N methanediyl Chemical class [CH2] HZVOZRGWRWCICA-UHFFFAOYSA-N 0.000 claims description 4
- 125000003367 polycyclic group Chemical group 0.000 claims description 4
- 229920006395 saturated elastomer Polymers 0.000 claims description 4
- 229910052802 copper Inorganic materials 0.000 claims description 3
- 125000005240 diheteroarylamino group Chemical group 0.000 claims description 3
- 230000005669 field effect Effects 0.000 claims description 3
- 150000004820 halides Chemical class 0.000 claims description 3
- 125000004475 heteroaralkyl group Chemical group 0.000 claims description 3
- 230000003287 optical effect Effects 0.000 claims description 3
- 150000003003 phosphines Chemical class 0.000 claims description 3
- 108091008695 photoreceptors Proteins 0.000 claims description 3
- 238000010791 quenching Methods 0.000 claims description 3
- 125000006413 ring segment Chemical group 0.000 claims description 3
- 150000003839 salts Chemical class 0.000 claims description 3
- 239000010409 thin film Substances 0.000 claims description 3
- 125000005259 triarylamine group Chemical group 0.000 claims description 3
- 229910052727 yttrium Inorganic materials 0.000 claims description 3
- 239000011701 zinc Substances 0.000 claims description 3
- 125000001989 1,3-phenylene group Chemical group [H]C1=C([H])C([*:1])=C([H])C([*:2])=C1[H] 0.000 claims description 2
- LPHIYKWSEYTCLW-UHFFFAOYSA-N 1h-azaborole Chemical class N1B=CC=C1 LPHIYKWSEYTCLW-UHFFFAOYSA-N 0.000 claims description 2
- 239000004215 Carbon black (E152) Substances 0.000 claims description 2
- 150000002148 esters Chemical class 0.000 claims description 2
- 229910052737 gold Inorganic materials 0.000 claims description 2
- 229930195733 hydrocarbon Natural products 0.000 claims description 2
- WUNJCKOTXFSWBK-UHFFFAOYSA-N indeno[2,1-a]carbazole Chemical class C1=CC=C2C=C3C4=NC5=CC=CC=C5C4=CC=C3C2=C1 WUNJCKOTXFSWBK-UHFFFAOYSA-N 0.000 claims description 2
- VVVPGLRKXQSQSZ-UHFFFAOYSA-N indolo[3,2-c]carbazole Chemical class C1=CC=CC2=NC3=C4C5=CC=CC=C5N=C4C=CC3=C21 VVVPGLRKXQSQSZ-UHFFFAOYSA-N 0.000 claims description 2
- 150000002576 ketones Chemical class 0.000 claims description 2
- 229910052745 lead Inorganic materials 0.000 claims description 2
- 229910052759 nickel Inorganic materials 0.000 claims description 2
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical class [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 claims description 2
- 229910052763 palladium Inorganic materials 0.000 claims description 2
- 229910052697 platinum Inorganic materials 0.000 claims description 2
- 229910052709 silver Inorganic materials 0.000 claims description 2
- 150000003457 sulfones Chemical class 0.000 claims description 2
- 150000003462 sulfoxides Chemical class 0.000 claims description 2
- 229910052718 tin Inorganic materials 0.000 claims description 2
- 150000003918 triazines Chemical class 0.000 claims description 2
- 229910052720 vanadium Inorganic materials 0.000 claims description 2
- 229910052725 zinc Inorganic materials 0.000 claims description 2
- 150000003751 zinc Chemical class 0.000 claims description 2
- 125000000609 carbazolyl group Chemical class C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims 1
- 150000007858 diazaphosphole derivatives Chemical class 0.000 claims 1
- 238000004246 ligand exchange chromatography Methods 0.000 claims 1
- 150000004756 silanes Chemical class 0.000 claims 1
- 239000010410 layer Substances 0.000 description 49
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 45
- 239000010949 copper Substances 0.000 description 29
- 239000000203 mixture Substances 0.000 description 20
- 239000000243 solution Substances 0.000 description 19
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 18
- 150000003254 radicals Chemical class 0.000 description 18
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 239000007787 solid Substances 0.000 description 15
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 14
- 238000005160 1H NMR spectroscopy Methods 0.000 description 13
- 239000012074 organic phase Substances 0.000 description 12
- 239000011541 reaction mixture Substances 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 8
- 229910021645 metal ion Inorganic materials 0.000 description 8
- 150000002739 metals Chemical class 0.000 description 8
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 6
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 125000005842 heteroatom Chemical group 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 229960000583 acetic acid Drugs 0.000 description 5
- 239000012362 glacial acetic acid Substances 0.000 description 5
- 229910052741 iridium Inorganic materials 0.000 description 5
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 5
- 239000011133 lead Substances 0.000 description 5
- NROKBHXJSPEDAR-UHFFFAOYSA-M potassium fluoride Chemical compound [F-].[K+] NROKBHXJSPEDAR-UHFFFAOYSA-M 0.000 description 5
- 239000002904 solvent Substances 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- 239000011135 tin Substances 0.000 description 5
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 5
- NLMDJJTUQPXZFG-UHFFFAOYSA-N 1,4,10,13-tetraoxa-7,16-diazacyclooctadecane Chemical compound C1COCCOCCNCCOCCOCCN1 NLMDJJTUQPXZFG-UHFFFAOYSA-N 0.000 description 4
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 4
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 4
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 4
- 239000008346 aqueous phase Substances 0.000 description 4
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 4
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 4
- 239000002739 cryptand Substances 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 4
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 4
- 235000019341 magnesium sulphate Nutrition 0.000 description 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 4
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 4
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
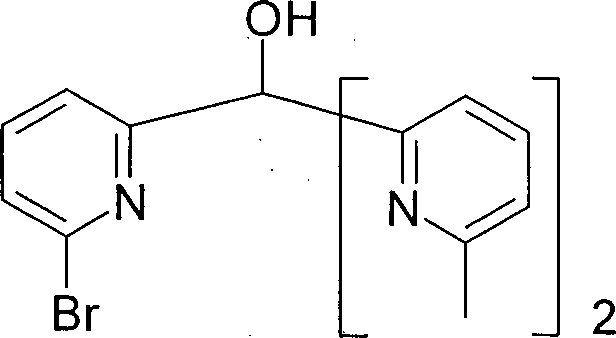
- AELPIDFIURROQN-UHFFFAOYSA-N (6-bromopyridin-2-yl)-bis(6-methylpyridin-2-yl)methanol Chemical compound CC1=CC=CC(C(O)(C=2N=C(C)C=CC=2)C=2N=C(Br)C=CC=2)=N1 AELPIDFIURROQN-UHFFFAOYSA-N 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 3
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- 150000004696 coordination complex Chemical group 0.000 description 3
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 3
- 239000010931 gold Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 3
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 3
- 238000007639 printing Methods 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- 238000001953 recrystallisation Methods 0.000 description 3
- 238000000859 sublimation Methods 0.000 description 3
- 230000008022 sublimation Effects 0.000 description 3
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- TZMSYXZUNZXBOL-UHFFFAOYSA-N 10H-phenoxazine Chemical compound C1=CC=C2NC3=CC=CC=C3OC2=C1 TZMSYXZUNZXBOL-UHFFFAOYSA-N 0.000 description 2
- SZXUTTGMFUSMCE-UHFFFAOYSA-N 2-(1h-imidazol-2-yl)pyridine Chemical compound C1=CNC(C=2N=CC=CC=2)=N1 SZXUTTGMFUSMCE-UHFFFAOYSA-N 0.000 description 2
- TZXCNVCUQLKGGQ-UHFFFAOYSA-N 2-(methoxymethyl)-6-methylpyridine Chemical compound COCC1=CC=CC(C)=N1 TZXCNVCUQLKGGQ-UHFFFAOYSA-N 0.000 description 2
- KQJYQGMOBWPQGQ-UHFFFAOYSA-N 2-[1-(methoxymethyl)imidazol-2-yl]pyridine Chemical compound COCN1C=CN=C1C1=CC=CC=N1 KQJYQGMOBWPQGQ-UHFFFAOYSA-N 0.000 description 2
- DDCWJZNXVVQWAJ-UHFFFAOYSA-N 2-[6-[fluoro-bis(6-methylpyridin-2-yl)methyl]pyridin-2-yl]-1h-benzimidazole Chemical compound CC1=CC=CC(C(F)(C=2N=C(C)C=CC=2)C=2N=C(C=CC=2)C=2NC3=CC=CC=C3N=2)=N1 DDCWJZNXVVQWAJ-UHFFFAOYSA-N 0.000 description 2
- BSGAESOHSGRPLH-UHFFFAOYSA-N 2-[fluoro-bis(6-phenylpyridin-2-yl)methyl]-6-phenylpyridine Chemical compound C=1C=CC(C=2C=CC=CC=2)=NC=1C(C=1N=C(C=CC=1)C=1C=CC=CC=1)(F)C(N=1)=CC=CC=1C1=CC=CC=C1 BSGAESOHSGRPLH-UHFFFAOYSA-N 0.000 description 2
- GWMLSAPXHRPDFW-UHFFFAOYSA-N 2-bis(6-phenylpyridin-2-yl)phosphoryl-6-phenylpyridine Chemical compound C=1C=CC(C=2C=CC=CC=2)=NC=1P(C=1N=C(C=CC=1)C=1C=CC=CC=1)(=O)C(N=1)=CC=CC=1C1=CC=CC=C1 GWMLSAPXHRPDFW-UHFFFAOYSA-N 0.000 description 2
- MUXNWJXFXNMPCZ-UHFFFAOYSA-N 2-bromo-6-[methoxy-bis(6-methylpyridin-2-yl)methyl]pyridine Chemical compound C=1C=CC(C)=NC=1C(C=1N=C(Br)C=CC=1)(OC)C1=CC=CC(C)=N1 MUXNWJXFXNMPCZ-UHFFFAOYSA-N 0.000 description 2
- NFJATBBHQFVLPX-UHFFFAOYSA-N 2-methyl-6-[(6-methylpyridin-2-yl)-(2-pyridin-2-yl-1h-imidazol-5-yl)methyl]pyridine Chemical compound CC1=CC=CC(C(C=2NC(=NC=2)C=2N=CC=CC=2)C=2N=C(C)C=CC=2)=N1 NFJATBBHQFVLPX-UHFFFAOYSA-N 0.000 description 2
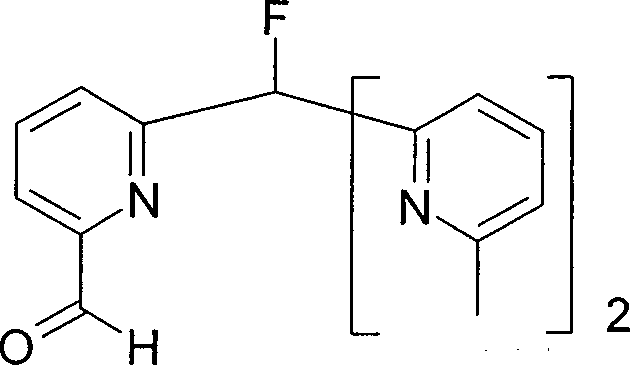
- NBRLFFJBURVXCQ-UHFFFAOYSA-N 6-[fluoro-bis(6-methylpyridin-2-yl)methyl]pyridine-2-carbaldehyde Chemical compound CC1=CC=CC(C(F)(C=2N=C(C)C=CC=2)C=2N=C(C=O)C=CC=2)=N1 NBRLFFJBURVXCQ-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 229920000144 PEDOT:PSS Polymers 0.000 description 2
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- HZOBODSAPPCATO-UHFFFAOYSA-N bis(6-methylpyridin-2-yl)methanone Chemical compound CC1=CC=CC(C(=O)C=2N=C(C)C=CC=2)=N1 HZOBODSAPPCATO-UHFFFAOYSA-N 0.000 description 2
- 150000001716 carbazoles Chemical class 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 2
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 239000003574 free electron Substances 0.000 description 2
- 238000007429 general method Methods 0.000 description 2
- 239000011261 inert gas Substances 0.000 description 2
- 238000007641 inkjet printing Methods 0.000 description 2
- 229960004592 isopropanol Drugs 0.000 description 2
- 125000002524 organometallic group Chemical group 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- RDOWQLZANAYVLL-UHFFFAOYSA-N phenanthridine Chemical compound C1=CC=C2C3=CC=CC=C3C=NC2=C1 RDOWQLZANAYVLL-UHFFFAOYSA-N 0.000 description 2
- 229940031826 phenolate Drugs 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- 150000003057 platinum Chemical class 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000011698 potassium fluoride Substances 0.000 description 2
- 235000003270 potassium fluoride Nutrition 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 2
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- 229930192474 thiophene Natural products 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- HTDIUWINAKAPER-UHFFFAOYSA-N trimethylarsine Chemical compound C[As](C)C HTDIUWINAKAPER-UHFFFAOYSA-N 0.000 description 2
- YWWDBCBWQNCYNR-UHFFFAOYSA-N trimethylphosphine Chemical compound CP(C)C YWWDBCBWQNCYNR-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- BUHVIAUBTBOHAG-FOYDDCNASA-N (2r,3r,4s,5r)-2-[6-[[2-(3,5-dimethoxyphenyl)-2-(2-methylphenyl)ethyl]amino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound COC1=CC(OC)=CC(C(CNC=2C=3N=CN(C=3N=CN=2)[C@H]2[C@@H]([C@H](O)[C@@H](CO)O2)O)C=2C(=CC=CC=2)C)=C1 BUHVIAUBTBOHAG-FOYDDCNASA-N 0.000 description 1
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 1
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 1
- ICPSWZFVWAPUKF-UHFFFAOYSA-N 1,1'-spirobi[fluorene] Chemical compound C1=CC=C2C=C3C4(C=5C(C6=CC=CC=C6C=5)=CC=C4)C=CC=C3C2=C1 ICPSWZFVWAPUKF-UHFFFAOYSA-N 0.000 description 1
- HQDYNFWTFJFEPR-UHFFFAOYSA-N 1,2,3,3a-tetrahydropyrene Chemical compound C1=C2CCCC(C=C3)C2=C2C3=CC=CC2=C1 HQDYNFWTFJFEPR-UHFFFAOYSA-N 0.000 description 1
- ZFXBERJDEUDDMX-UHFFFAOYSA-N 1,2,3,5-tetrazine Chemical compound C1=NC=NN=N1 ZFXBERJDEUDDMX-UHFFFAOYSA-N 0.000 description 1
- FNQJDLTXOVEEFB-UHFFFAOYSA-N 1,2,3-benzothiadiazole Chemical compound C1=CC=C2SN=NC2=C1 FNQJDLTXOVEEFB-UHFFFAOYSA-N 0.000 description 1
- UGUHFDPGDQDVGX-UHFFFAOYSA-N 1,2,3-thiadiazole Chemical compound C1=CSN=N1 UGUHFDPGDQDVGX-UHFFFAOYSA-N 0.000 description 1
- HTJMXYRLEDBSLT-UHFFFAOYSA-N 1,2,4,5-tetrazine Chemical compound C1=NN=CN=N1 HTJMXYRLEDBSLT-UHFFFAOYSA-N 0.000 description 1
- BBVIDBNAYOIXOE-UHFFFAOYSA-N 1,2,4-oxadiazole Chemical compound C=1N=CON=1 BBVIDBNAYOIXOE-UHFFFAOYSA-N 0.000 description 1
- YGTAZGSLCXNBQL-UHFFFAOYSA-N 1,2,4-thiadiazole Chemical compound C=1N=CSN=1 YGTAZGSLCXNBQL-UHFFFAOYSA-N 0.000 description 1
- FYADHXFMURLYQI-UHFFFAOYSA-N 1,2,4-triazine Chemical compound C1=CN=NC=N1 FYADHXFMURLYQI-UHFFFAOYSA-N 0.000 description 1
- UDGKZGLPXCRRAM-UHFFFAOYSA-N 1,2,5-thiadiazole Chemical compound C=1C=NSN=1 UDGKZGLPXCRRAM-UHFFFAOYSA-N 0.000 description 1
- DXBHBZVCASKNBY-UHFFFAOYSA-N 1,2-Benz(a)anthracene Chemical compound C1=CC=C2C3=CC4=CC=CC=C4C=C3C=CC2=C1 DXBHBZVCASKNBY-UHFFFAOYSA-N 0.000 description 1
- UUSUFQUCLACDTA-UHFFFAOYSA-N 1,2-dihydropyrene Chemical compound C1=CC=C2C=CC3=CCCC4=CC=C1C2=C43 UUSUFQUCLACDTA-UHFFFAOYSA-N 0.000 description 1
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- FKASFBLJDCHBNZ-UHFFFAOYSA-N 1,3,4-oxadiazole Chemical compound C1=NN=CO1 FKASFBLJDCHBNZ-UHFFFAOYSA-N 0.000 description 1
- MBIZXFATKUQOOA-UHFFFAOYSA-N 1,3,4-thiadiazole Chemical compound C1=NN=CS1 MBIZXFATKUQOOA-UHFFFAOYSA-N 0.000 description 1
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical compound C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- USYCQABRSUEURP-UHFFFAOYSA-N 1h-benzo[f]benzimidazole Chemical compound C1=CC=C2C=C(NC=N3)C3=CC2=C1 USYCQABRSUEURP-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- PFRPMHBYYJIARU-UHFFFAOYSA-N 2,3-diazatetracyclo[6.6.2.04,16.011,15]hexadeca-1(14),2,4,6,8(16),9,11(15),12-octaene Chemical compound C1=CC=C2N=NC3=CC=CC4=CC=C1C2=C43 PFRPMHBYYJIARU-UHFFFAOYSA-N 0.000 description 1
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 1
- FEYDZHNIIMENOB-UHFFFAOYSA-N 2,6-dibromopyridine Chemical compound BrC1=CC=CC(Br)=N1 FEYDZHNIIMENOB-UHFFFAOYSA-N 0.000 description 1
- ZMVVDBASCHDMMS-UHFFFAOYSA-N 2-[bis(6-bromopyridin-2-yl)-fluoromethyl]-6-bromopyridine Chemical compound C=1C=CC(Br)=NC=1C(C=1N=C(Br)C=CC=1)(F)C1=CC=CC(Br)=N1 ZMVVDBASCHDMMS-UHFFFAOYSA-N 0.000 description 1
- KFTFTNLNHUOACP-UHFFFAOYSA-N 2-[fluoro-(6-methylpyridin-2-yl)methyl]-6-methylpyridine Chemical compound CC1=CC=CC(C(F)C=2N=C(C)C=CC=2)=N1 KFTFTNLNHUOACP-UHFFFAOYSA-N 0.000 description 1
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical compound C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 1
- LYTMVABTDYMBQK-UHFFFAOYSA-N 2-benzothiophene Chemical compound C1=CC=CC2=CSC=C21 LYTMVABTDYMBQK-UHFFFAOYSA-N 0.000 description 1
- ZOMHRMUGNHXRCG-UHFFFAOYSA-N 2-bis(6-bromopyridin-2-yl)phosphoryl-6-bromopyridine Chemical compound BrC1=CC=CC(P(=O)(C=2N=C(Br)C=CC=2)C=2N=C(Br)C=CC=2)=N1 ZOMHRMUGNHXRCG-UHFFFAOYSA-N 0.000 description 1
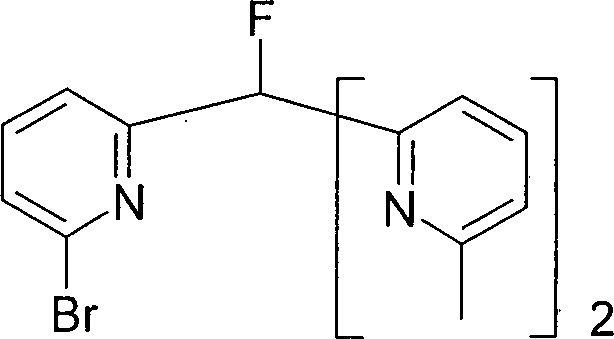
- LXUMAKZUJPMEBL-UHFFFAOYSA-N 2-bromo-6-[fluoro-bis(6-methylpyridin-2-yl)methyl]pyridine Chemical compound CC1=CC=CC(C(F)(C=2N=C(C)C=CC=2)C=2N=C(Br)C=CC=2)=N1 LXUMAKZUJPMEBL-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- CPDDXQJCPYHULE-UHFFFAOYSA-N 4,5,14,16-tetrazapentacyclo[9.7.1.12,6.015,19.010,20]icosa-1(18),2,4,6,8,10(20),11(19),12,14,16-decaene Chemical group C1=CC(C2=CC=CC=3C2=C2C=NN=3)=C3C2=CC=NC3=N1 CPDDXQJCPYHULE-UHFFFAOYSA-N 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- IUKNPBPXZUWMNO-UHFFFAOYSA-N 5,12-diazatetracyclo[6.6.2.04,16.011,15]hexadeca-1(15),2,4,6,8(16),9,11,13-octaene Chemical compound N1=CC=C2C=CC3=NC=CC4=CC=C1C2=C43 IUKNPBPXZUWMNO-UHFFFAOYSA-N 0.000 description 1
- NHWJSCHQRMCCAD-UHFFFAOYSA-N 5,14-diazatetracyclo[6.6.2.04,16.011,15]hexadeca-1(14),2,4,6,8(16),9,11(15),12-octaene Chemical compound C1=CN=C2C=CC3=NC=CC4=CC=C1C2=C43 NHWJSCHQRMCCAD-UHFFFAOYSA-N 0.000 description 1
- PODJSIAAYWCBDV-UHFFFAOYSA-N 5,6-diazatetracyclo[6.6.2.04,16.011,15]hexadeca-1(14),2,4(16),5,7,9,11(15),12-octaene Chemical compound C1=NN=C2C=CC3=CC=CC4=CC=C1C2=C43 PODJSIAAYWCBDV-UHFFFAOYSA-N 0.000 description 1
- KJCRNHQXMXUTEB-UHFFFAOYSA-N 69637-93-0 Chemical compound C1=CC=C2N=C(N=C3NC=4C(=CC=CC=4)NC3=N3)C3=NC2=C1 KJCRNHQXMXUTEB-UHFFFAOYSA-N 0.000 description 1
- SNFCXVRWFNAHQX-UHFFFAOYSA-N 9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=CC=C21 SNFCXVRWFNAHQX-UHFFFAOYSA-N 0.000 description 1
- BPMFPOGUJAAYHL-UHFFFAOYSA-N 9H-Pyrido[2,3-b]indole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=N1 BPMFPOGUJAAYHL-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 239000005964 Acibenzolar-S-methyl Substances 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- FMMWHPNWAFZXNH-UHFFFAOYSA-N Benz[a]pyrene Chemical compound C1=C2C3=CC=CC=C3C=C(C=C3)C2=C2C3=CC=CC2=C1 FMMWHPNWAFZXNH-UHFFFAOYSA-N 0.000 description 1
- VMPLMOXGWULJTH-UHFFFAOYSA-N C1=CC(C)=CC=C1N(C=1C=C2C3(C4=CC(=CC=C4C2=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC(=CC=C1C1=CC=C(C=C13)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 Chemical compound C1=CC(C)=CC=C1N(C=1C=C2C3(C4=CC(=CC=C4C2=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC(=CC=C1C1=CC=C(C=C13)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 VMPLMOXGWULJTH-UHFFFAOYSA-N 0.000 description 1
- ZPIPUFJBRZFYKJ-UHFFFAOYSA-N C1=NC=C2C=CC3=CN=CC4=CC=C1C2=C34 Chemical compound C1=NC=C2C=CC3=CN=CC4=CC=C1C2=C34 ZPIPUFJBRZFYKJ-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 0 Cc1nc(*(*)C(c2nc(Br)ccc2)F)ccc1 Chemical compound Cc1nc(*(*)C(c2nc(Br)ccc2)F)ccc1 0.000 description 1
- XJUZRXYOEPSWMB-UHFFFAOYSA-N Chloromethyl methyl ether Chemical compound COCCl XJUZRXYOEPSWMB-UHFFFAOYSA-N 0.000 description 1
- 239000005749 Copper compound Substances 0.000 description 1
- 229910021589 Copper(I) bromide Inorganic materials 0.000 description 1
- 101000801643 Homo sapiens Retinal-specific phospholipid-transporting ATPase ABCA4 Proteins 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Natural products P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 102100033617 Retinal-specific phospholipid-transporting ATPase ABCA4 Human genes 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 1
- DPOPAJRDYZGTIR-UHFFFAOYSA-N Tetrazine Chemical compound C1=CN=NN=N1 DPOPAJRDYZGTIR-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- FEFUFYZCRKRQBK-UHFFFAOYSA-N [3-(methoxymethyl)-2-pyridin-2-yl-1,2-dihydroimidazol-5-yl]-bis(6-methylpyridin-2-yl)methanol Chemical compound COCN1C=C(C(O)(C=2N=C(C)C=CC=2)C=2N=C(C)C=CC=2)NC1C1=CC=CC=N1 FEFUFYZCRKRQBK-UHFFFAOYSA-N 0.000 description 1
- VGRJHHLDEYYRNF-UHFFFAOYSA-N ac1lasce Chemical compound C1C2=CC=CC=C2C(C=2C3=CC=CC=C3CC=22)=C1C1=C2CC2=CC=CC=C21 VGRJHHLDEYYRNF-UHFFFAOYSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- GUNJVIDCYZYFGV-UHFFFAOYSA-K antimony trifluoride Chemical compound F[Sb](F)F GUNJVIDCYZYFGV-UHFFFAOYSA-K 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- WMUIZUWOEIQJEH-UHFFFAOYSA-N benzo[e][1,3]benzoxazole Chemical compound C1=CC=C2C(N=CO3)=C3C=CC2=C1 WMUIZUWOEIQJEH-UHFFFAOYSA-N 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 1
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 239000012159 carrier gas Substances 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229940061627 chloromethyl methyl ether Drugs 0.000 description 1
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 150000001880 copper compounds Chemical class 0.000 description 1
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 150000001987 diarylethers Chemical class 0.000 description 1
- UZBQIPPOMKBLAS-UHFFFAOYSA-N diethylazanide Chemical compound CC[N-]CC UZBQIPPOMKBLAS-UHFFFAOYSA-N 0.000 description 1
- XXPBFNVKTVJZKF-UHFFFAOYSA-N dihydrophenanthrene Natural products C1=CC=C2CCC3=CC=CC=C3C2=C1 XXPBFNVKTVJZKF-UHFFFAOYSA-N 0.000 description 1
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 1
- QKIUAMUSENSFQQ-UHFFFAOYSA-N dimethylazanide Chemical compound C[N-]C QKIUAMUSENSFQQ-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000001194 electroluminescence spectrum Methods 0.000 description 1
- DNJIEGIFACGWOD-UHFFFAOYSA-N ethanethiol Chemical compound CCS DNJIEGIFACGWOD-UHFFFAOYSA-N 0.000 description 1
- HHFAWKCIHAUFRX-UHFFFAOYSA-N ethoxide Chemical compound CC[O-] HHFAWKCIHAUFRX-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- JKFAIQOWCVVSKC-UHFFFAOYSA-N furazan Chemical compound C=1C=NON=1 JKFAIQOWCVVSKC-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 150000002344 gold compounds Chemical class 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- JBFYUZGYRGXSFL-UHFFFAOYSA-N imidazolide Chemical compound C1=C[N-]C=N1 JBFYUZGYRGXSFL-UHFFFAOYSA-N 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 150000002466 imines Chemical class 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- 239000011229 interlayer Substances 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical compound C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 239000008204 material by function Substances 0.000 description 1
- LSDPWZHWYPCBBB-UHFFFAOYSA-M methanethiolate Chemical compound [S-]C LSDPWZHWYPCBBB-UHFFFAOYSA-M 0.000 description 1
- NBTOZLQBSIZIKS-UHFFFAOYSA-N methoxide Chemical compound [O-]C NBTOZLQBSIZIKS-UHFFFAOYSA-N 0.000 description 1
- ADUFDSSCDCLUFT-UHFFFAOYSA-N n-[4-(4-aminophenyl)phenyl]-n-phenylnaphthalen-1-amine Chemical group C1=CC(N)=CC=C1C1=CC=C(N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 ADUFDSSCDCLUFT-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- SAVQQRYWWAGSQW-UHFFFAOYSA-N n-methyl-n-(trifluoro-$l^{4}-sulfanyl)methanamine Chemical compound CN(C)S(F)(F)F SAVQQRYWWAGSQW-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- 125000005069 octynyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C#C* 0.000 description 1
- 238000007645 offset printing Methods 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- SLIUAWYAILUBJU-UHFFFAOYSA-N pentacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C21 SLIUAWYAILUBJU-UHFFFAOYSA-N 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- 150000004707 phenolate Chemical class 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-M phenolate Chemical compound [O-]C1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-M 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical compound O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- WKFBZNUBXWCCHG-UHFFFAOYSA-N phosphorus trifluoride Chemical compound FP(F)F WKFBZNUBXWCCHG-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- IKNCGYCHMGNBCP-UHFFFAOYSA-N propan-1-olate Chemical compound CCC[O-] IKNCGYCHMGNBCP-UHFFFAOYSA-N 0.000 description 1
- OGHBATFHNDZKSO-UHFFFAOYSA-N propan-2-olate Chemical compound CC(C)[O-] OGHBATFHNDZKSO-UHFFFAOYSA-N 0.000 description 1
- SUVIGLJNEAMWEG-UHFFFAOYSA-N propane-1-thiol Chemical compound CCCS SUVIGLJNEAMWEG-UHFFFAOYSA-N 0.000 description 1
- KJRCEJOSASVSRA-UHFFFAOYSA-N propane-2-thiol Chemical compound CC(C)S KJRCEJOSASVSRA-UHFFFAOYSA-N 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- GDISDVBCNPLSDU-UHFFFAOYSA-N pyrido[2,3-g]quinoline Chemical compound C1=CC=NC2=CC3=CC=CN=C3C=C21 GDISDVBCNPLSDU-UHFFFAOYSA-N 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 239000010944 silver (metal) Substances 0.000 description 1
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical compound C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 238000005092 sublimation method Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 125000006836 terphenylene group Chemical group 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- JRMUNVKIHCOMHV-UHFFFAOYSA-M tetrabutylammonium bromide Chemical compound [Br-].CCCC[N+](CCCC)(CCCC)CCCC JRMUNVKIHCOMHV-UHFFFAOYSA-M 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- 230000008646 thermal stress Effects 0.000 description 1
- 238000001931 thermography Methods 0.000 description 1
- 150000007944 thiolates Chemical class 0.000 description 1
- 238000010023 transfer printing Methods 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical group 0.000 description 1
- PMZLFYBZWYRRAZ-UHFFFAOYSA-N tricyclohexylarsane Chemical compound C1CCCCC1[As](C1CCCCC1)C1CCCCC1 PMZLFYBZWYRRAZ-UHFFFAOYSA-N 0.000 description 1
- WLPUWLXVBWGYMZ-UHFFFAOYSA-N tricyclohexylphosphine Chemical compound C1CCCCC1P(C1CCCCC1)C1CCCCC1 WLPUWLXVBWGYMZ-UHFFFAOYSA-N 0.000 description 1
- AVYPTBDUFIEJDP-UHFFFAOYSA-N tricyclohexylstibane Chemical compound C1CCCCC1[Sb](C1CCCCC1)C1CCCCC1 AVYPTBDUFIEJDP-UHFFFAOYSA-N 0.000 description 1
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- CYTQBVOFDCPGCX-UHFFFAOYSA-N trimethyl phosphite Chemical compound COP(OC)OC CYTQBVOFDCPGCX-UHFFFAOYSA-N 0.000 description 1
- PORFVJURJXKREL-UHFFFAOYSA-N trimethylstibine Chemical compound C[Sb](C)C PORFVJURJXKREL-UHFFFAOYSA-N 0.000 description 1
- BPLUKJNHPBNVQL-UHFFFAOYSA-N triphenylarsine Chemical compound C1=CC=CC=C1[As](C=1C=CC=CC=1)C1=CC=CC=C1 BPLUKJNHPBNVQL-UHFFFAOYSA-N 0.000 description 1
- SLGBZMMZGDRARJ-UHFFFAOYSA-N triphenylene Chemical compound C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 1
- HVYVMSPIJIWUNA-UHFFFAOYSA-N triphenylstibine Chemical compound C1=CC=CC=C1[Sb](C=1C=CC=CC=1)C1=CC=CC=C1 HVYVMSPIJIWUNA-UHFFFAOYSA-N 0.000 description 1
- QZBJYTDDWVXFDF-UHFFFAOYSA-N tris(2,3,4,5,6-pentafluorophenyl)arsane Chemical compound FC1=C(F)C(F)=C(F)C(F)=C1[As](C=1C(=C(F)C(F)=C(F)C=1F)F)C1=C(F)C(F)=C(F)C(F)=C1F QZBJYTDDWVXFDF-UHFFFAOYSA-N 0.000 description 1
- FQLSDFNKTNBQLC-UHFFFAOYSA-N tris(2,3,4,5,6-pentafluorophenyl)phosphane Chemical compound FC1=C(F)C(F)=C(F)C(F)=C1P(C=1C(=C(F)C(F)=C(F)C=1F)F)C1=C(F)C(F)=C(F)C(F)=C1F FQLSDFNKTNBQLC-UHFFFAOYSA-N 0.000 description 1
- QYWFCUVQKBNIRJ-UHFFFAOYSA-N tris(2,3,4,5,6-pentafluorophenyl)stibane Chemical compound FC1=C(F)C(F)=C(F)C(F)=C1[Sb](C=1C(=C(F)C(F)=C(F)C=1F)F)C1=C(F)C(F)=C(F)C(F)=C1F QYWFCUVQKBNIRJ-UHFFFAOYSA-N 0.000 description 1
- YSPBORFVJLIOMX-UHFFFAOYSA-N tritert-butylarsane Chemical compound CC(C)(C)[As](C(C)(C)C)C(C)(C)C YSPBORFVJLIOMX-UHFFFAOYSA-N 0.000 description 1
- NZJQTVDLVPHKGY-UHFFFAOYSA-N tritert-butylstibane Chemical compound CC(C)(C)[Sb](C(C)(C)C)C(C)(C)C NZJQTVDLVPHKGY-UHFFFAOYSA-N 0.000 description 1
- YGPLLMPPZRUGTJ-UHFFFAOYSA-N truxene Chemical compound C1C2=CC=CC=C2C(C2=C3C4=CC=CC=C4C2)=C1C1=C3CC2=CC=CC=C21 YGPLLMPPZRUGTJ-UHFFFAOYSA-N 0.000 description 1
- 238000002061 vacuum sublimation Methods 0.000 description 1
- 238000001947 vapour-phase growth Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/331—Metal complexes comprising an iron-series metal, e.g. Fe, Co, Ni
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/10—Metal complexes of organic compounds not being dyes in uncomplexed form
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/30—Doping active layers, e.g. electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/346—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising platinum
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/371—Metal complexes comprising a group IB metal element, e.g. comprising copper, gold or silver
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/381—Metal complexes comprising a group IIB metal element, e.g. comprising cadmium, mercury or zinc
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1033—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1037—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/187—Metal complexes of the iron group metals, i.e. Fe, Co or Ni
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/188—Metal complexes of other metals not provided for in one of the previous groups
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Inorganic Chemistry (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Photovoltaic Devices (AREA)
- Semiconductor Lasers (AREA)
Abstract
Die vorliegende Erfindung betrifft elektronische Vorrichtungen, insbesondere organische Elektrolumineszenzvorrichtungen enthaltend Metallkomplexe gemäß der Formel (1) sowie die bevorzugten Metallkomplexe.
Description
- Die vorliegende Anmeldung betrifft elektronische Vorrichtungen, insbesondere organische Elektrolumineszenzvorrichtungen, enthaltend Metallkomplexe sowie die für die Verwendung bevorzugten Metallkomplexe.
- Der Aufbau organischer Elektrolumineszenzvorrichtungen (OLEDs), in denen organische Halbleiter als funktionelle Materialien eingesetzt werden, ist beispielsweise in
US 4539507 ,US 5151629 ,EP 0676461 undWO 98/27136 - Gemäß dem Stand der Technik werden in phosphoreszierenden OLEDs als Triplettemitter insbesondere Iridium- und Platinkomplexe eingesetzt. Diese haben jedoch den Nachteil, dass es sich dabei um Metalle mit einer sehr geringen Häufigkeit und daher auch entsprechend um teure Metalle handelt. Zur Schonung der natürlichen Ressourcen dieser Metalle wäre es daher wünschenswert, Emitter auf Basis anderer Metalle zur Verfügung zu haben. Ein weiterer Nachteil der üblicherweise verwendeten Iridium- und Platinkomplexe besteht darin, dass es sich üblicherweise um organometallische Komplexe mit Metall-Kohlenstoff-Bindungen handelt. Solche Metall-Kohlenstoff-Bindungen sind teilweise nur schwierig synthetisch zugänglich. Weiterhin weisen diese Komplexe teilweise nur eine geringe thermische Stabilität auf.
- Aufgabe der vorliegenden Erfindung ist daher die Bereitstellung weiterer Metallkomplexe, welche sich als Emitter oder auch als Matrixmaterialien oder in anderen Funktionen für die Verwendung in OLEDs eignen und dort zu hohen Effizienzen und hohen Lebensdauern führen und welche synthetisch einfach zugänglich sind.
- Überraschend wurde gefunden, dass bestimmte, unten näher beschriebene Metallchelatkomplexe diese Aufgabe lösen und sich sehr gut für die Verwendung in organischen Elektrolumineszenzvorrichtungen eignen, insbesondere bei der Verwendung als emittierendes Material. Dabei zeigen sie eine hohe Lebensdauer, eine hohe Effizienz und eine gute Stabilität gegenüber Temperaturbelastung. Weiterhin ist das Zentralatom dieser Komplexe nicht Iridium als seltenes Metall. Ein weiterer Vorteil dieser Komplexe ist, dass diese synthetisch einfach zugänglich sind. Organische Elektrolumineszenzvorrichtungen, welche diese Komplexe enthalten, sowie die bevorzugten Metallkomplexe sind daher der Gegenstand der vorliegenden Erfindung.
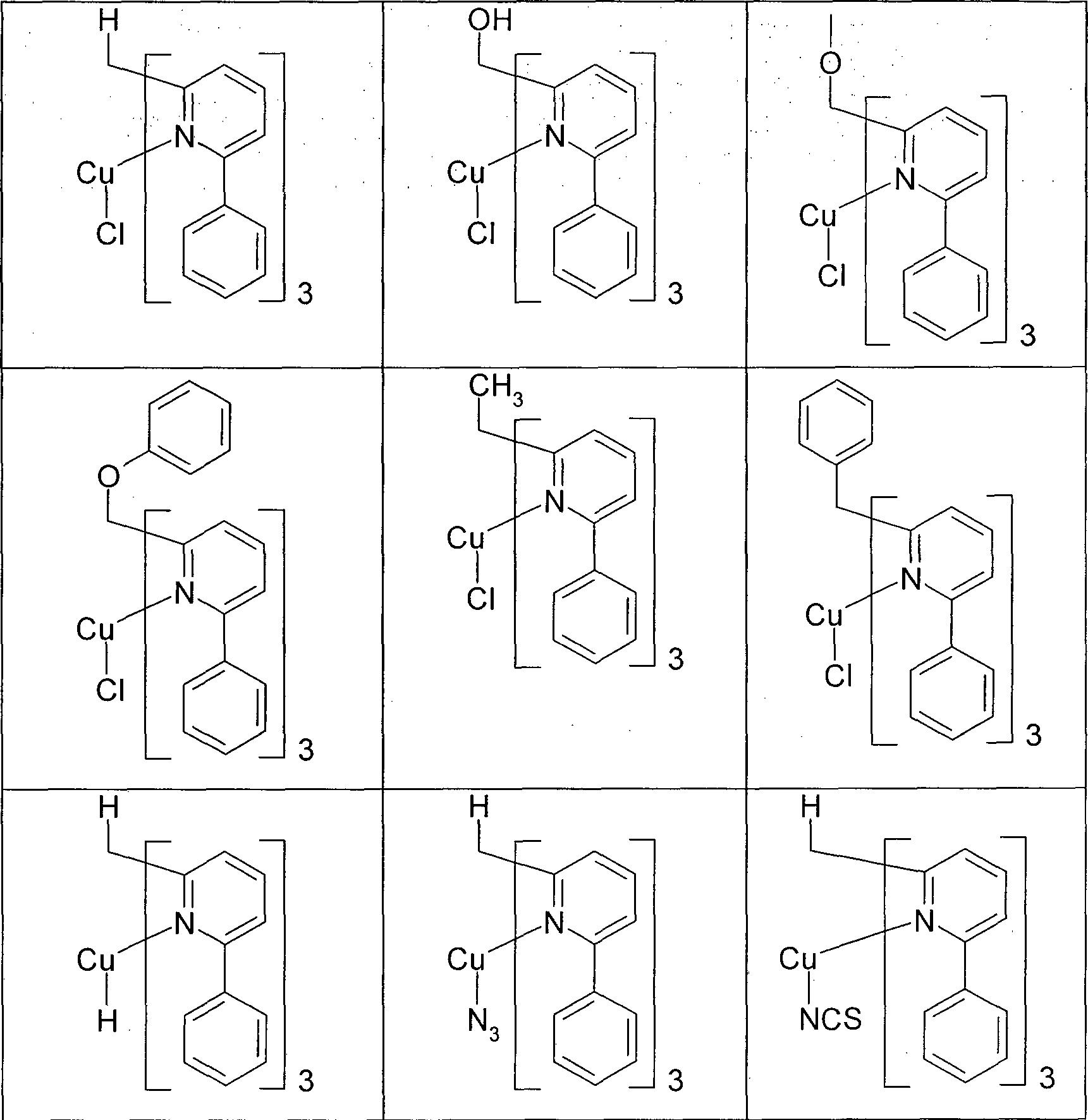
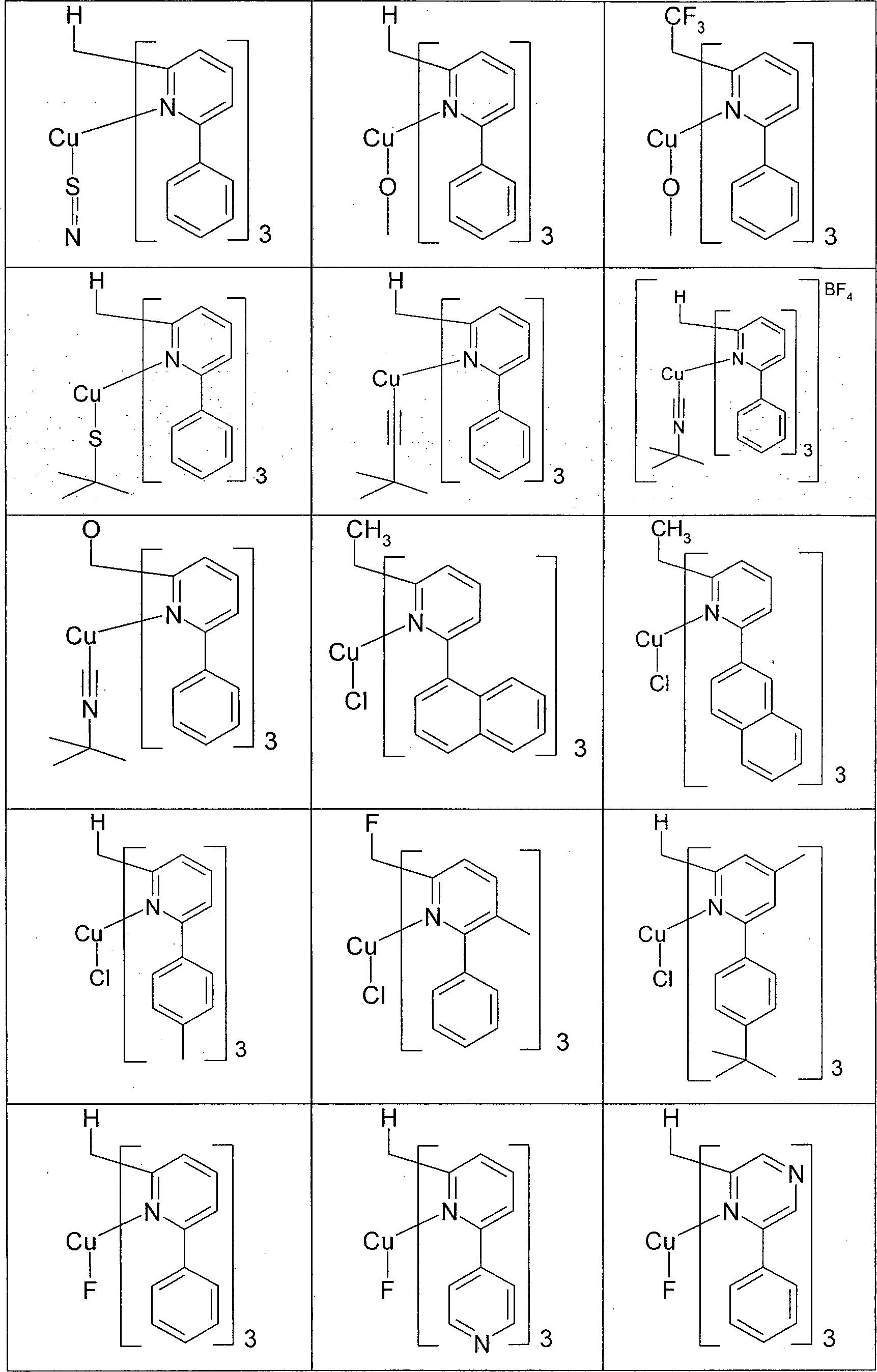
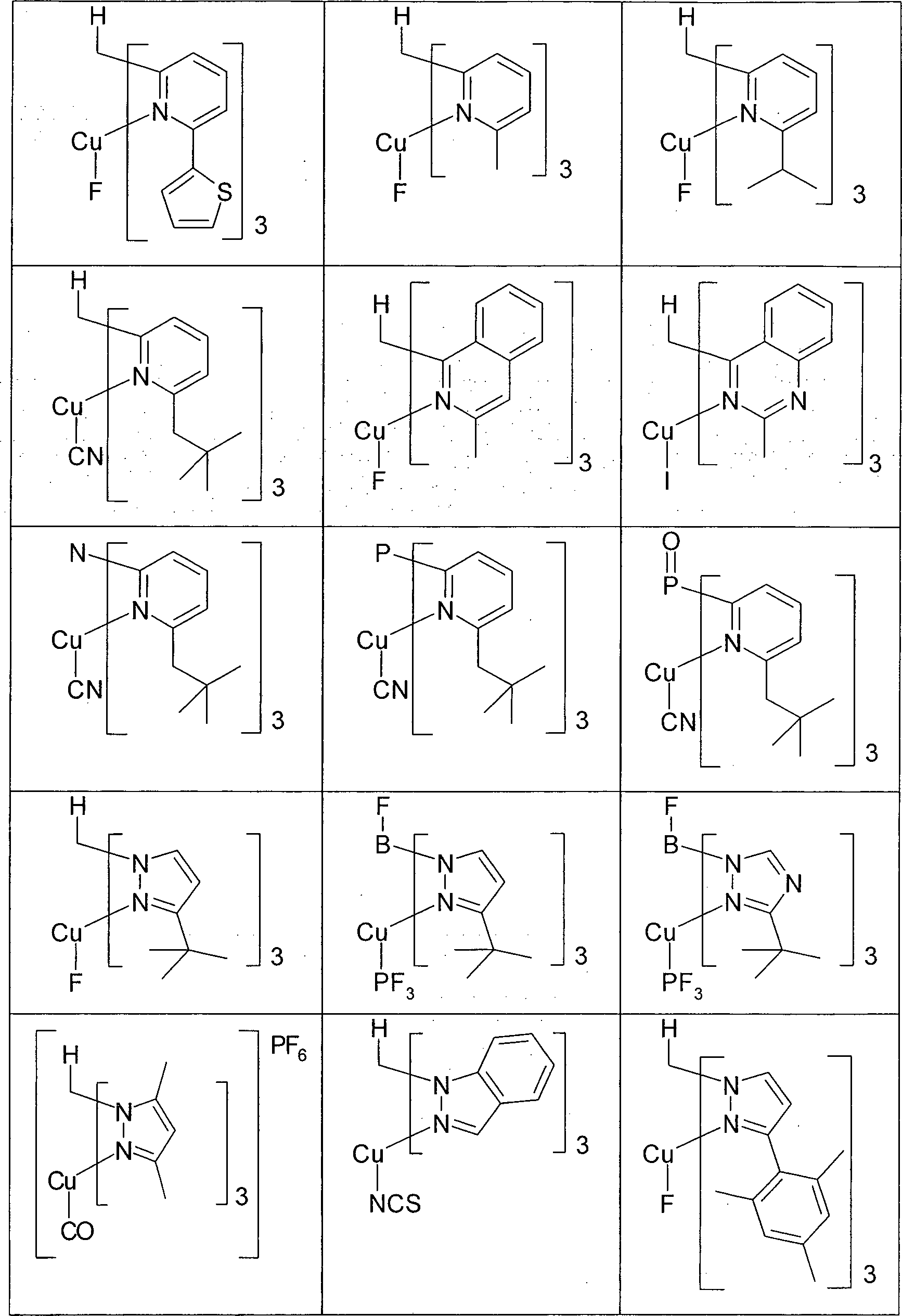
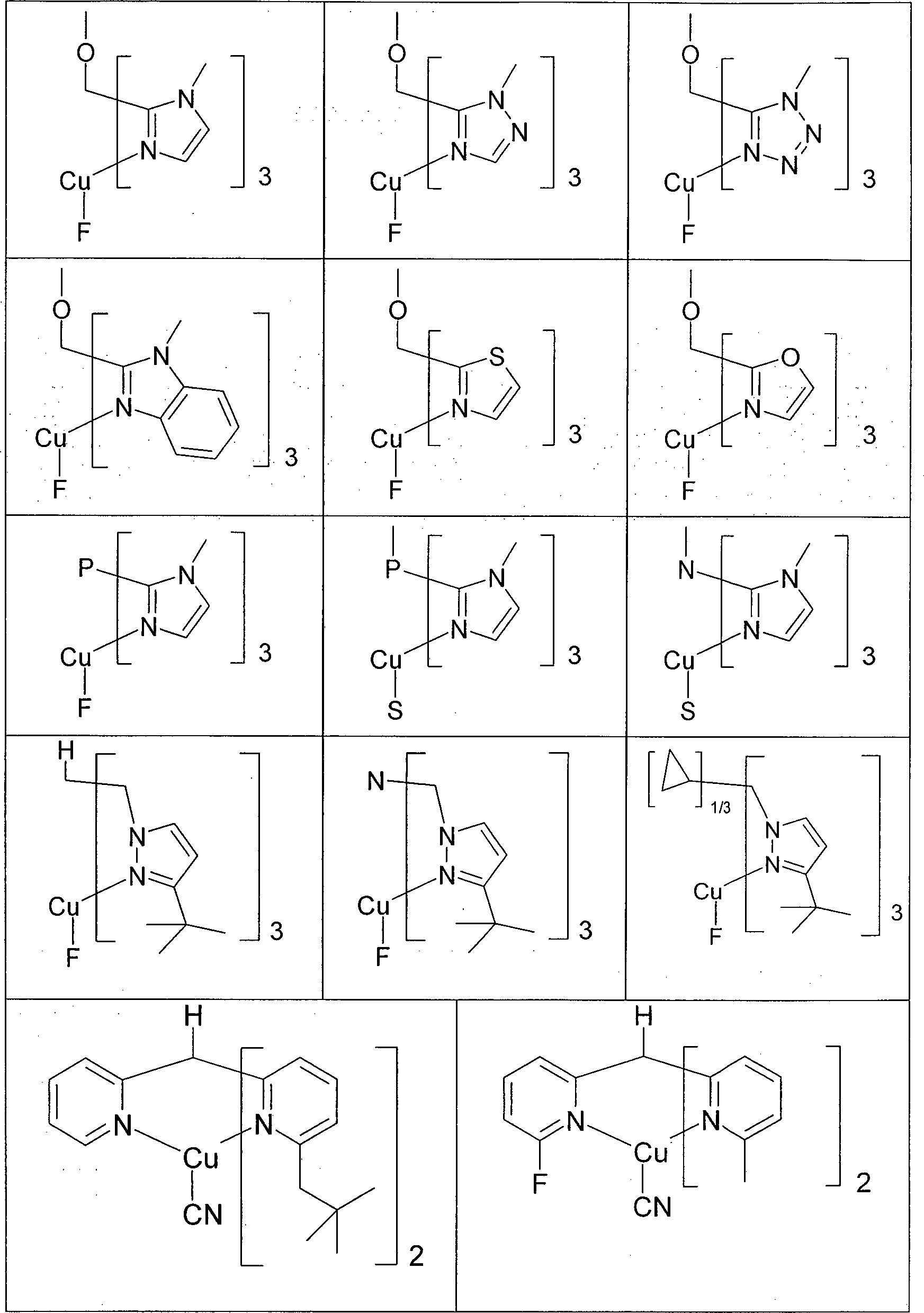
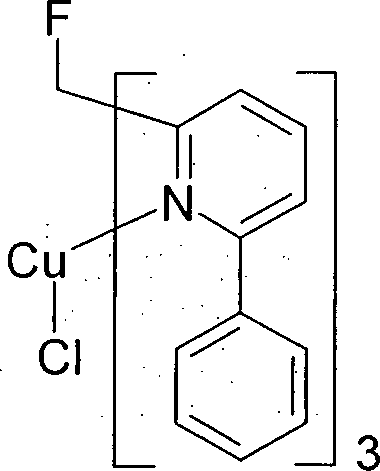
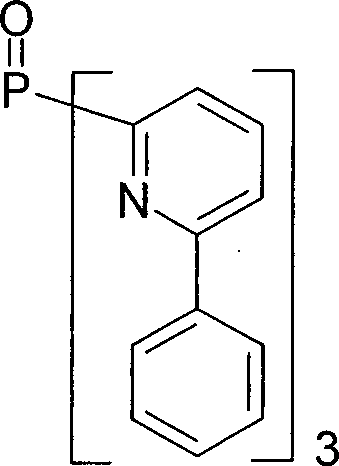
- Gegenstand der vorliegenden Erfindung ist somit eine elektronische Vorrichtung enthaltend Anode, Kathode und mindestens eine Verbindung gemäß Formel (1), Formel (1) enthaltend ein Metall M, koordiniert an einen Liganden L gemäß Formel (2), Formel (2) wobei für die verwendeten Symbole und Indizes gilt:
M ist ausgewählt aus Cu, Ag, Au, Zn, Sn, Pb, Ni, Pd oder Pt;
V ist ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P, PR+, P(=O), As, AsR+, As(=O), Sb, SbR+, Sb(=O) oder S+; oder V ist eine aliphatische, aromatische oder heteroaromatische cyclische Gruppe mit 3 bis 6 Ringatomen, die die Teilliganden L1, L2 und L3, gegebenenfalls über die Gruppe Y, kovalent miteinander verbindet und die durch einen oder mehrere Reste R substituiert sein kann;
Y ist bei jedem Auftreten gleich oder verschieden eine bivalente Gruppe, ausgewählt aus CR2, BR, SiR2, NR, PR, P(=O)R, AsR, As(=O)R, SbR, Sb(=O)R, O, S, 1,2-Vinylen oder 1,2- oder 1,3-Phenylen, welches jeweils mit einem oder mehreren Resten R substituiert sein kann;
a ist 0 oder 1;
b ist 1, 2 oder 3, wobei für b 2 oder 3 der Index a = 1 ist;
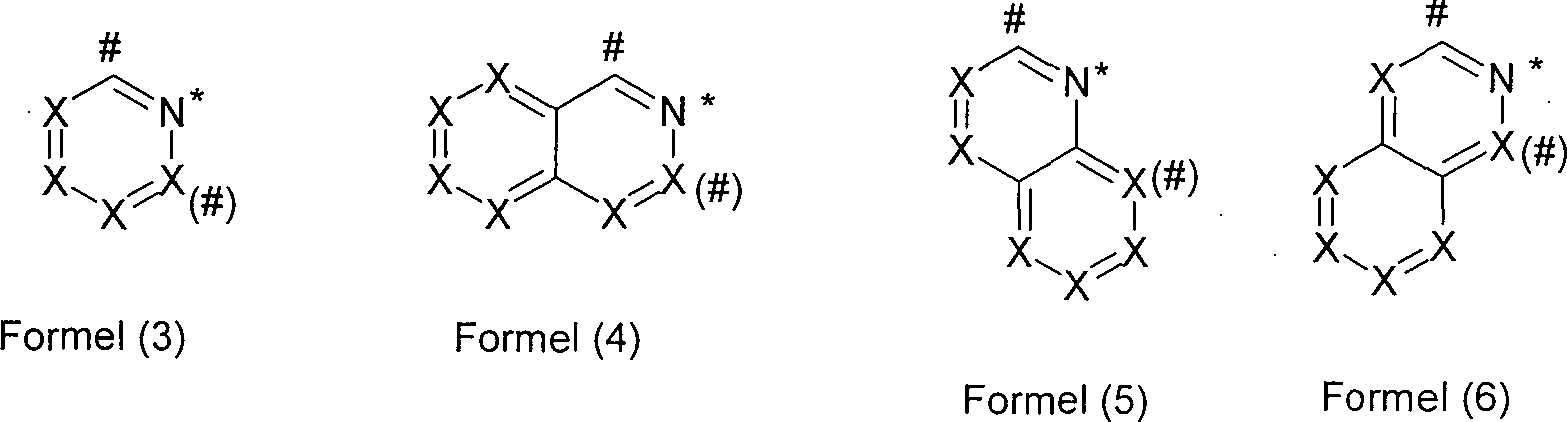
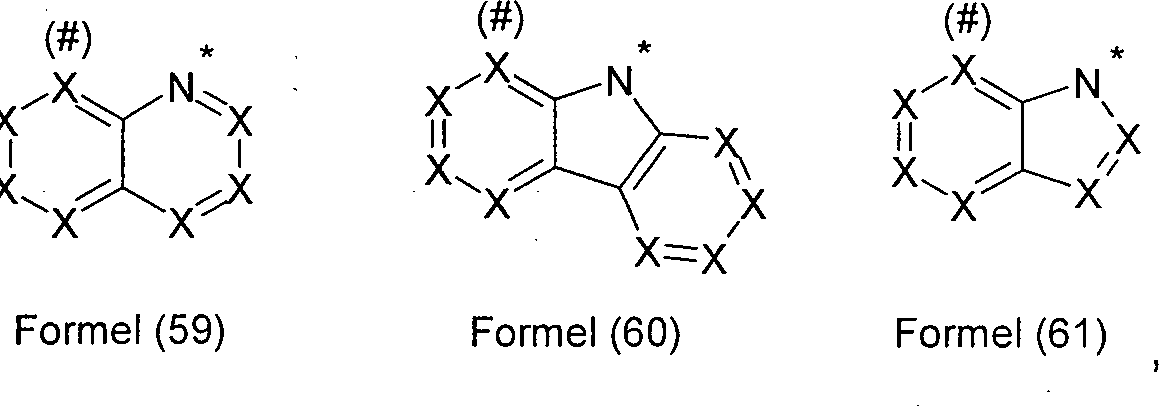
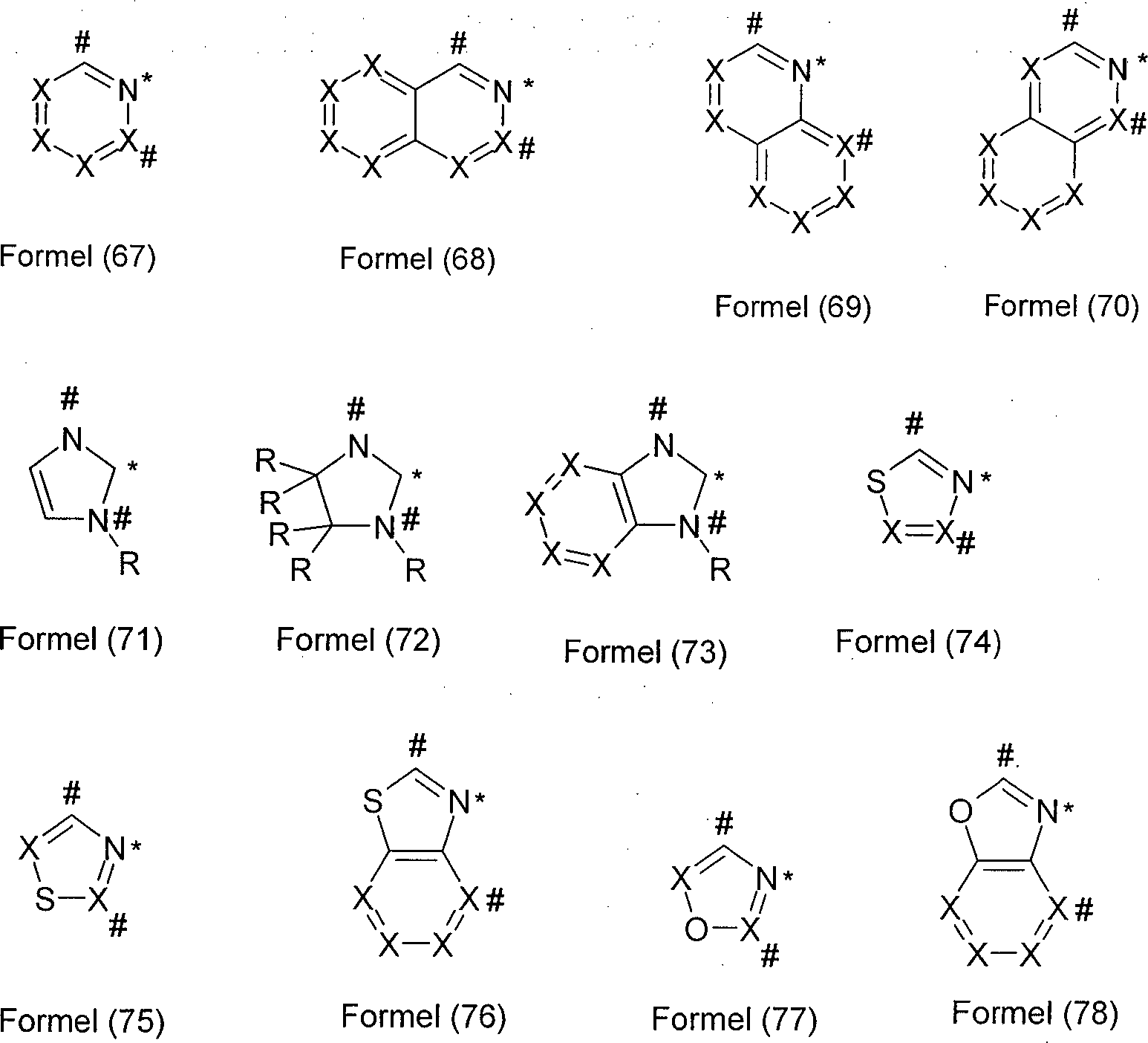
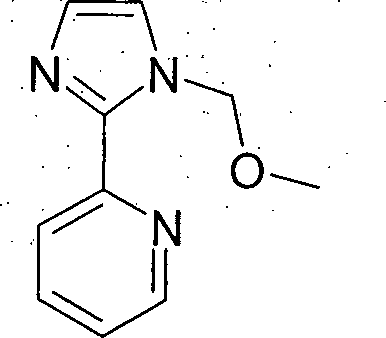
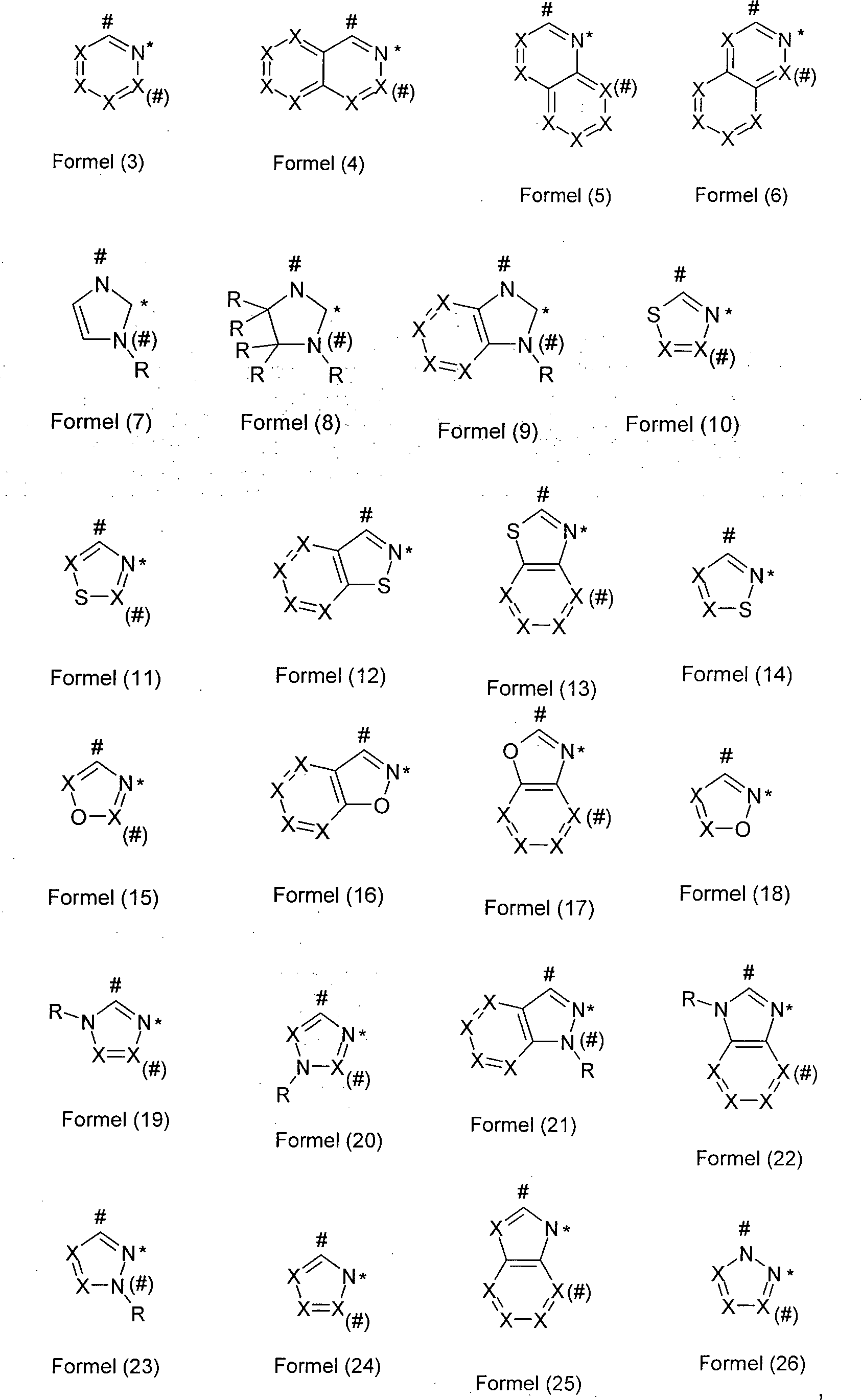
L1 ist eine heterocyclische Gruppe mit 1 bis 20 C-Atomen und mindestens einem N-Atom, welche durch einen oder mehrere Reste R substituiert sein kann und welche über ein neutrales oder anionisches Stickstoffatom oder über ein neutrales Kohlenstoffatom, welches jeweils Teil der heterocyclischen Gruppe ist, an M bindet; oder ist eine cyclische oder heterocyclische Gruppe mit 1 bis 20 C-Atomen, welche über ein exocyclisches Donoratom an M bindet und welche durch einen oder mehrere Reste R substituiert sein kann;
L2, L3 sind gleich oder verschieden bei jedem Auftreten eine koordinierende Gruppe, welche durch einen oder mehrere Reste R substituiert sein kann und welche über Stickstoff, Phosphor, Schwefel oder ein neutrales Kohlenstoffatom an M bindet, wobei L2 und/oder L3 auch gleich oder verschieden L1 sein können;
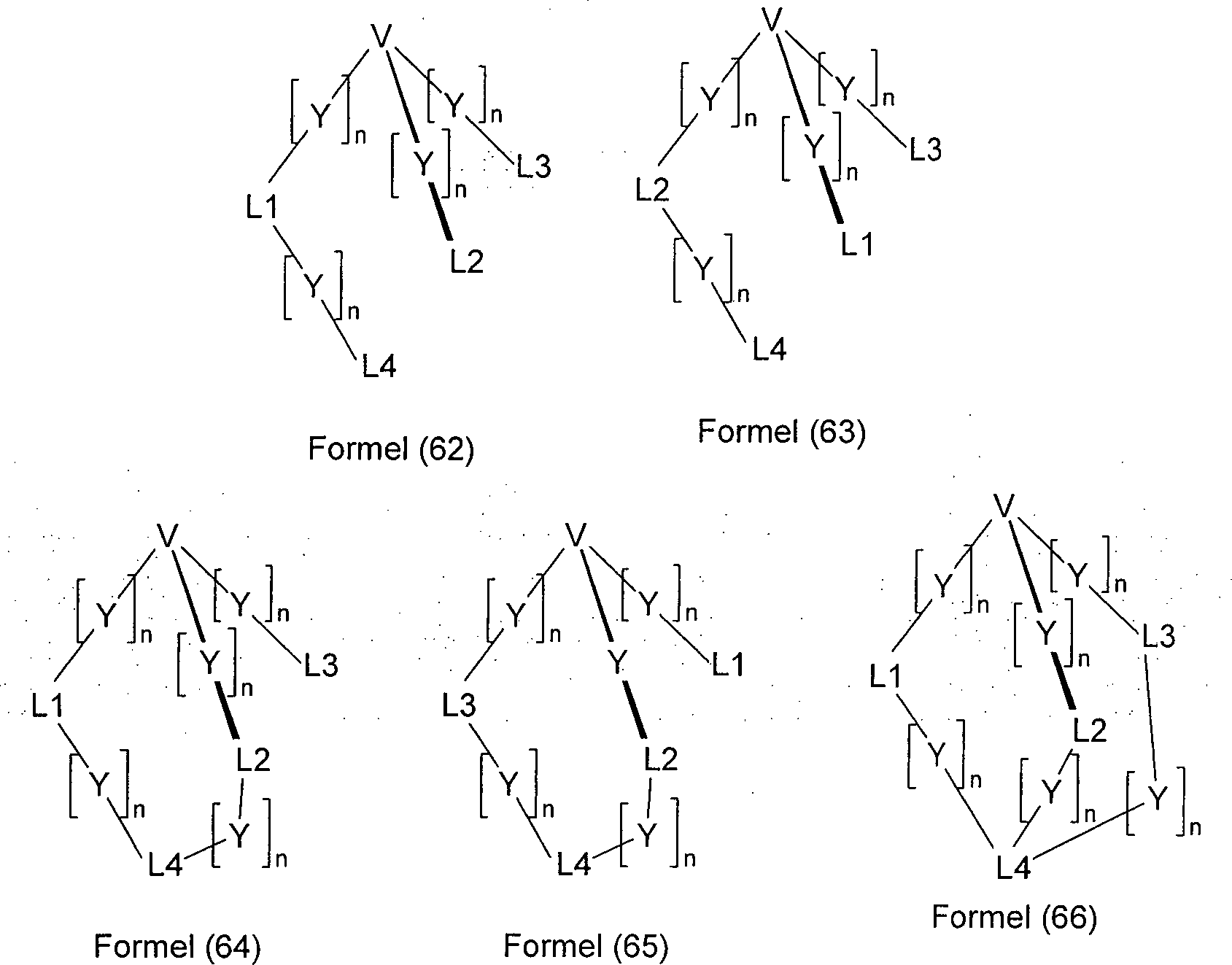
L4 ist ein beliebiger Ligand, welcher an das Metall M koordiniert und welcher durch einen oder mehrere Reste R substituiert sein kann; dabei kann L4 auch durch eine direkte Bindung oder durch eine bivalente Gruppe -(Y)n- mit einem oder mehreren der Teilliganden L1, L2 und/oder L3 verknüpft sein;
n ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3;
R ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, N(R1)2, CN, NO2, OH, Si(R1)3, B(OR1)2, C(=O)R1, P(=O)(R1)2, S(=O)R1, S(=O)2R1, OSO2R1, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, die jeweils mit einem oder mehreren Resten R1 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R1C=CR1, C≡C, Si(R1)2, Ge(R1)2, Sn(R1)2, C=O, C=S, C=Se, C=NR1, P(=O)(R1), SO, SO2, NR1, O, S oder CONR1 ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Aryloxy-, Heteroaryloxy-, Aralkyl- oder Heteroaralkylgruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Diarylaminogruppe, Diheteroarylaminogruppe oder Arylheteroarylaminogruppe mit 10 bis 40 aromatischen Ringatomen, welche durch einen oder mehrere Reste R1 substituiert sein kann; dabei können zwei oder mehrere Substituenten R auch miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches, heteroaromatisches und/oder benzoannelliertes Ringsystem bilden;
R1 ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, N(R2)2, CN, NO2, OH, Si(R2)3, B(OR2)2, C(=O)R2, P(=O)(R2)2, S(=O)R2, S(=O)2R2, OSO2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, die jeweils mit einem oder mehreren Resten R2 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S oder CONR2 ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Aryloxy-, Heteroaryloxy-, Aralkyl- oder Heteroaralkylgruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Diarylaminogruppe, Diheteroarylaminogruppe oder Arylheteroarylaminogruppe mit 10 bis 40 aromatischen Ringatomen, welche durch einen oder mehrere Reste R2 substituiert sein kann; dabei können zwei oder mehrere Substituenten R1 auch miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches, heteroaromatisches und/oder benzoannelliertes Ringsystem bilden;
R2 ist bei jedem Auftreten gleich oder verschieden H, D, F oder ein aliphatischer, aromatischer und/oder heteroaromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, in dem auch ein oder mehrere H-Atome durch F ersetzt sein können; dabei können zwei oder mehrere Substituenten R2 auch miteinander ein mono- oder polycyclisches aliphatisches, aromatisches, heteroaromatisches und/oder benzoannelliertes Ringsystem bilden. - Unter einem Teilliganden im Sinne der vorliegenden Erfindung werden in dem Liganden der Formel (2) die Gruppen L1, L2 und L3 verstanden, also jeweils die einzelnen Arme des polypodalen Liganden, welche jeweils an das Metall M koordinieren und über den Brückenkopf V und gegebenenfalls über Y verknüpft werden.
- In der Struktur der Formel (1) bedeutet ein Index b = 2 oder 3, dass jeweils 2 oder 3 der Metallkomplex-Einheiten über einen Liganden L4 verknüpft sind. Der Ligand L4 bindet dann entsprechend gleichzeitig an 2 oder 3 Metalle M.
- Unter einem Donoratom im Sinne der vorliegenden Erfindung wird ein Atom verstanden, welches mindestens ein freies Elektronenpaar aufweist und dadurch in der Lage ist, an ein Metallatom bzw. Metallion zu binden. Dabei kann das Donoratom neutral oder negativ geladen sein.
- Unter einem exocyclischen Donoratom im Sinne dieser Erfindung wird ein Donoratom verstanden, welches nicht Teil der cyclischen oder heterocyclischen Gruppe L1 ist, sondern welches als Substituent an L1 gebunden ist und welches mindestens ein freies Elektronenpaar aufweist und dadurch in der Lage ist, an ein Metallatom zu binden. Beispiele für exocyclische Donoratome sind Sauerstoff in Form eines Phenolats, Schwefel in Form eines Thiolats, Stickstoff in Form eines Amins, Imins, Amids oder Imids und Phosphor in Form eines Phosphins.
- Eine Arylgruppe im Sinne dieser Erfindung enthält 6 bis 60 C-Atome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält 2 bis 60 C-Atome und mindestens ein Heteroatom, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Dabei wird unter einer Arylgruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Cyclus, also Benzol, bzw. ein einfacher heteroaromatischer Cyclus, beispielsweise Pyridin, Pyrimidin, Thiophen, etc., oder eine kondensierte Aryl- oder Heteroarylgruppe, beispielsweise Naphthalin, Anthracen, Phenanthren, Chinolin, Isochinolin, etc., verstanden. Ein cyclisches Carben im Sinne dieser Erfindung ist eine cyclische Gruppe, welche über ein neutrales C-Atom an das Metall bindet. Dabei kann die cyclische Gruppe gesättigt oder ungesättigt sein. Bevorzugt sind hierbei Arduengo-Carbene, also solche Carbene, bei welchen an das Carben-C-Atom zwei Stickstoffatome gebunden sind.
- Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält 6 bis 60 C-Atome im Ringsystem. Ein heteroaromatisches Ringsystem im Sinne dieser Erfindung enthält 2 bis 60 C-Atome und mindestens ein Heteroatom im Ringsystem, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine nicht-aromatische Einheit (bevorzugt weniger als 10% der von H verschiedenen Atome), wie z. B. ein sp3-hybridisiertes C-, N- oder O-Atom, unterbrochen sein können. So sollen beispielsweise auch Systeme wie 9,9'-Spirobifluoren, 9,9-Diarylfluoren, Triarylamin, Diarylether, Stilben, etc. als aromatische Ringsysteme im Sinne dieser Erfindung verstanden werden, und ebenso Systeme, in denen zwei oder mehrere Arylgruppen beispielsweise durch eine lineare oder cyclische Alkylgruppe oder durch eine Silylgruppe unterbrochen sind.
- Im Rahmen der vorliegenden Erfindung werden unter einer C1- bis C40-Alkylgruppe, in der auch einzelne H-Atome oder CH2-Gruppen durch die oben genannten Gruppen substituiert sein können, bevorzugt die Reste Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, Cyclopentyl, n-Hexyl, Cyclohexyl, n-Heptyl, Cycloheptyl, n-Octyl, Cyclooctyl, 2-Ethylhexyl, Trifluormethyl, Pentafluorethyl und 2,2,2-Trifluorethyl verstanden. Unter einer Alkenylgruppe werden bevorzugt die Reste Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclopentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl und Cyclooctenyl verstanden. Unter einer Alkinylgruppe werden bevorzugt Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl, Heptinyl und Octinyl verstanden. Unter einer C1- bis C40-Alkoxygruppe werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy oder 2-Methylbutoxy verstanden. Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5–60 aromatischen Ringatomen, welches noch jeweils mit den oben genannten Resten R substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Phenanthren, Benzanthracen, Benzphenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Terphenylen, Fluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans-Indenofluoren, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7-Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diazapyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Phenothiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol.
- Die Metallkomplexe gemäß Formel (1) können Komplexe polypodaler Liganden oder Kryptate sein, abhängig davon, ob der Ligand L4 mit den Teilliganden L1, L2 und L3 verknüpft ist oder nicht. Unter einem polypodalen Liganden im Sinne dieser Erfindung wird ein Ligand verstanden, in welchem drei koordinierende Teilliganden L1, L2 und L3 durch eine Gruppe V aneinander gebunden sind. Unter einem Kryptat im Sinne dieser Erfindung wird eine Verbindung zwischen einem Kryptanden und einem Metallion verstanden, in der das Metallion von den Brücken des komplexbildenden Kryptanden dreidimensional umgeben ist. Unter einem Kryptanden im Sinne dieser Erfindung wird ein makrocyclischer tripodaler Ligand verstanden. Dabei kann ein Kryptand entstehen, wenn der Ligand L4 mit zwei oder mit allen drei der Teilliganden L1, L2 und/oder L3 verknüpft ist.
- Außerdem kann in Metallkomplexen gemäß Formel (1) auch die Gruppe V an M koordiniert sein, wenn die Gruppe V ein freies Elektronenpaar aufweist, wenn sie also beispielsweise N oder P darstellt.
- In einer bevorzugten Ausführungsform der Erfindung ist a = 0 und die Gruppe V koordiniert an M. In einer weiteren bevorzugten Ausführungsform der Erfindung ist a = 1, d. h. es ist ein Ligand L4 vorhanden, und V koordiniert nicht an M. Wie oben definiert, ist der Teilligand L1 eine heterocyclische Gruppe mit mindestens einem N-Atom, welche über ein neutrales oder anionisches Stickstoffatom oder über ein neutrales Kohlenstoffatom, welches jeweils Teil der heterocyclischen Gruppe ist, an M bindet, oder es ist eine cyclische Gruppe mit einem exocyclischen Donoratom, welches an M bindet. Die Bindung über ein neutrales Kohlenstoffatom ist möglich in Form eines Carbens. Dabei weist die cyclische bzw. heterocyclische Gruppe mindestens 5 und maximal 20 Ringatome auf. Es kann sich dabei auch um eine kondensierte Gruppe handeln, also eine Gruppe, in der mehrere Ringe über eine gemeinsame Kante miteinander verknüpft sind. Die Gruppe L1 kann dabei gesättigt, ungesättigt oder aromatisch bzw. heteroaromatisch sein. In einer bevorzugten Ausführungsform der Erfindung handelt es sich bei L1 um eine bzw. Heteroarylgruppe bzw. um eine Arylgruppe mit einem exocyclischen Donoratom, oder es handelt sich um ein cyclisches, gesättigtes oder ungesättigtes Carben. In einer besonders bevorzugten Ausführungsform der Erfindung weist die Aryl- bzw. Heteroarylgruppe 5 bis 14 aromatische Ringatome auf, besonders bevorzugt 5 bis 10 aromatische Ringatome.
- In einer bevorzugten Ausführungsform der Erfindung ist der Index b = 1.
- Bevorzugt sind Verbindungen gemäß Formel (1), dadurch gekennzeichnet, dass diese nicht geladen, d. h. elektrisch neutral, sind. Dies wird dadurch erreicht, dass die Ladung der Teilliganden L1, L2 und L3 sowie des Liganden L4 und der verbrückenden Einheit V so gewählt wird, dass sie die Ladung des komplexierten Metallions M kompensieren.
- Bevorzugt sind weiterhin Verbindungen gemäß Formel (1), dadurch gekennzeichnet, dass die Summe der Valenzelektronen, d. h. die Elektronen der äußersten Schale, um das Metallatom, wenn es sich um ein Übergangsmetall handelt, 18 beträgt. Diese Bevorzugung ist durch die besondere Stabilität dieser Metallkomplexe begründet.
- Bei den Metallen M handelt es sich um die oben beschriebenen Metalle, wobei bevorzugt Cu als Cu(I), Ag als Ag(I), Au als Au(I), Zn als Zn(II), Sn als Sn(IV), Pb als Pb(IV), Ni als Ni(0), Pd als Pd(0) und Pt als Pt(0) vorliegt. Dabei bezeichnet der Wert in Klammern hinter dem Metall jeweils die Oxidationsstufe des Metalls. Bevorzugt sind die Metalle M ausgewählt aus der Gruppe bestehend aus Cu(I), Ag(I), Ni(0), Pd(0) und Pt(0), besonders bevorzugt Cu(I) und Ag(I), ganz besonders bevorzugt Cu(I).
- In einer bevorzugten Ausführungsform der Erfindung ist L1 ausgewählt aus den Gruppen gemäß den Formeln (3) bis (30): wobei die verwendeten Symbole dieselbe Bedeutung haben, wie oben beschrieben, und weiterhin gilt:
X steht bei jedem Auftreten gleich oder verschieden für CR oder N;
D steht bei jedem Auftreten gleich oder verschieden für O–, S–, NR–, PR–, NR2, PR2, COO–, SO3 –, -C(=O)R, -CR(=NR) oder -N(=CR2). - Bevorzugt stehen maximal drei Symbole X in jeder Gruppe für N, besonders bevorzugt stehen maximal zwei Symbole X in jeder Gruppe für N, ganz besonders bevorzugt steht maximal ein Symbol X in jeder Gruppe für N. Insbesondere bevorzugt stehen alle Symbole X für C. Dabei koordinieren die Gruppen der Formeln (3) bis (30) an das Metall M über die durch * gekennzeichnete Position. Die durch # gekennzeichnete Position gibt die Position an, an der der Teilligand an Y bzw. an V gebunden ist. Die durch (#) gekennzeichnete Position gibt die Position an, an der der Teilligand gegebenenfalls an Y bzw. an L4 gebunden ist. Wenn eine solche weitere Bindung an Y bzw. an L4 vorhanden ist, steht das entsprechende Symbol X für C und in den Formeln (7), (8), (9), (21) und (23) ist keine Gruppe Ran den Stickstoff gebunden.
- L2 und L3 sind definitionsgemäß koordinierende Gruppen, welche auch durch einen oder mehrere Reste R substituiert sein können und welche über Stickstoff, Phosphor, Schwefel, Sauerstoff oder ein neutrales Kohlenstoffatom an M binden, wobei L2 und L3 auch gleich oder verschieden L1 sein können. In einer bevorzugten Ausführungsform der Erfindung sind L2 und L3 gleich oder verschieden bei jedem Auftreten eine koordinierende Gruppe, welche über Stickstoff, Phosphor oder Schwefel an M bindet, oder sind gleich oder verschieden L1.
- Bevorzugte koordinierende Gruppen, welche über Stickstoff an M binden, sind ausgewählt aus der Gruppe bestehend aus -NR2, -NR–, -CR1=NR1 und -N=C(R1)2, wobei R und R1 die oben genannten Bedeutungen aufweisen. Besonders bevorzugt sind R und R1 gleich oder verschieden bei jedem Auftreten eine Alkylgruppe mit 1 bis 10 C-Atomen, welche mit einem oder mehreren Resten R1 bzw. R2 substituiert sein kann.
- Bevorzugte koordinierende Gruppen, welche über Phosphor an M binden, sind ausgewählt aus der Gruppe bestehend aus -PR2, -PR(OR) und P(OR)2, wobei R die oben genannten Bedeutungen aufweist. Besonders bevorzugt ist R gleich oder verschieden bei jedem Auftreten ein aromatisches oder heteroaromatisches Ringsystem, welches mit einem oder mehreren Resten R1 substituiert sein kann.
- Bevorzugte koordinierende Gruppen, welche über Schwefel an M binden, sind ausgewählt aus der Gruppe bestehend aus -S- oder -SR, wobei R die oben genannten Bedeutungen aufweist. Besonders bevorzugt ist R gleich oder verschieden bei jedem Auftreten eine Alkylgruppe mit 1 bis 10 C-Atomen, welche mit einem oder mehreren Resten R1 substituiert sein kann, oder ein aromatisches oder heteroaromatisches Ringsystem, welches mit einem oder mehreren Resten R1 substituiert sein kann.
- Besonders bevorzugt sind Verbindungen gemäß Formel (1), dadurch gekennzeichnet, dass L2 gleich oder verschieden bei jedem Auftreten L1 ist. Ganz besonders bevorzugt sind Verbindungen gemäß Formel (1), dadurch gekennzeichnet, dass L2 und L3 gleich oder verschieden bei jedem Auftreten L1 sind.
- In einer weiteren bevorzugten Ausführungsform der Erfindung ist Y gleich oder verschieden bei jedem Auftreten eine bivalente Gruppe, ausgewählt aus CR2, BR, SiR2, NR, PR, P(=O)R, O oder S, besonders bevorzugt CR2, SiR2, NR, O oder S, ganz besonders bevorzugt CR2.
- In einer weiteren bevorzugten Ausführungsform der Erfindung ist der Index n gleich oder verschieden bei jedem Auftreten 0, 1 oder 2. Dabei ist der Index n = 0 oder 1, insbesondere 0, dann bevorzugt, wenn die Gruppe V nicht an M koordiniert. Weiterhin ist n = 1 oder 2 insbesondere dann bevorzugt, wenn die Gruppe V an M koordiniert.
- Die verbrückende Einheit V kann neutral oder einfach negativ oder einfach positiv geladen sein. Dabei wird die Ladung von V bevorzugt so gewählt, dass insgesamt ein neutraler Komplex entsteht. So ist z. B. eine neutrale verbrückende Einheit V bevorzugt, wenn es sich um ein einwertiges Metallion M+ und drei neutrale und einen einfach negativen (Teil)Liganden L1, L2, L3 und L4 handelt. Weiterhin ist eine einfach negative verbrückende Einheit V bevorzugt, wenn es sich um ein einwertiges Metallion M+ und vier neutrale (Teil)Liganden L1, L2, L3 und L4 handelt. Weiterhin ist eine einfach positive verbrückende Einheit V bevorzugt, wenn es sich um ein einwertiges Metallion M+ und zwei einfach negative und zwei neutrale (Teil)Liganden L1, L2, L3 und L4 handelt. Entsprechendes gilt, wenn das Metallion eine andere Wertigkeit aufweist.
- In einer weiteren bevorzugten Ausführungsform der Erfindung ist die verbrückende Einheit V ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der Formeln (31) bis (34), wobei die gestrichelten Bindungen jeweils die Bindung zu den Teilliganden L1, L2 und L3 bzw. zu Y andeuten.
- In einer besonders bevorzugten Ausführungsform der Erfindung ist die verbrückende Einheit V ausgewählt aus CR, N, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der oben genannten Formeln (31) bis (34).
- In einer weiteren bevorzugten Ausführungsform der Erfindung ist L4 ausgewählt aus der Gruppe bestehend aus Kohlenmonoxid, Stickstoffmonoxid, Alkylcyaniden, wie z. B. Acetonitril, Arylcyaniden, wie z. B. Benzonitril, Alkylisocyaniden, wie z. B. Methylisonitril, Arylisocyaniden, wie z. B. Benzoisonitril, Aminen, wie z. B. Trimethylamin, Triethylamin, Morpholin, Phosphinen, insbesondere Halogenphosphine, Trialkylphosphine, Triarylphosphine oder Alkylarylphosphine, wie z. B. Trifluorphosphin, Trimethylphosphin, Tricyclohexylphosphin, Tri-tert-butylphosphin, Triphenylphosphin, Tris(pentafluorphenyl)phosphin, Phosphiten, wie z. B. Trimethylphosphit, Triethylphosphit, Arsinen, wie z. B. Trifluorarsin, Trimethylarsin, Tricyclohexylarsin, Tri-tert-butylarsin, Triphenylarsin, Tris(pentafluorphenyl)arsin, Stibinen, wie z. B. Trifluorstibin, Trimethylstibin, Tricyclohexylstibin, Tri-tert-butylstibin, Triphenylstibin, Tris(pentafluorphenyl)stibin, stickstoffhaltigen Heterocyclen, wie z. B. Pyridin, Pyridazin, Pyrazin, Pyrimidin, Triazin, Carbenen, insbesondere Arduengo Carbenen, Hydrid, Deuterid, den Halogeniden F–, Cl–, Br– und I–, Alkylacetyliden, wie z. B. Methyl-C≡C–, tert-Butyl-C≡C–, Arylacetyliden, wie z. B. Phenyl-C≡C–, Cyanid, Cyanat, Isocyanat, Thiocyanat, Isothiocyanat, aliphatischen oder aromatischen Alkoholaten, wie z. B. Methanolat, Ethanolat, Propanolat, iso-Propanolat, tert-Butylat, Phenolat, aliphatischen oder aromatischen Thioalkoholaten, wie z. B. Methanthiolat, Ethanthiolat, Propanthiolat, iso-Propanthiolat, tert-Thiobutylat, Thiophenolat, Amiden, wie z. B. Dimethylamid, Diethylamid, Di-iso-propylamid, Morpholid, Carboxylaten, wie z. B. Acetat, Trifluoracetat, Propionat, Benzoat, anionischen, stickstoffhaltigen Heterocyclen, wie Pyrrolid, Imidazolid, Pyrazolid. Dabei sind die Alkylgruppen in diesen Gruppen bevorzugt C1-C20-Alkylgruppen, besonders bevorzugt C1-C10-Alkylgruppen, ganz besonders bevorzugt C1-C4-Alkylgruppen. Unter einer Arylgruppe werden auch Heteroarylgruppen verstanden. Diese Gruppen sind wie oben definiert.
- Bevorzugte Liganden L4 sind weiterhin die Liganden der folgenden Formeln (35) bis (61), wobei die verwendeten Symbole und Indizes die oben genannten Bedeutungen haben und * die Position der Koordination an M andeutet. Die durch (#) gekennzeichnete Position gibt die Position an, an der L4, gegebenenfalls über -(Y)n-, an einen der Teilliganden L1, L2 oder L3 gebunden sein kann. Wenn eine solche Bindung an Y bzw. an L1, L2 oder L3 vorhanden ist, steht das entsprechende Symbol X für C und in den Formeln (38), (39), (40) und (55) ist keine Gruppe R an den Stickstoff gebunden.
- Bevorzugte Strukturen gemäß Formel (1) sind Strukturen, in denen die oben genannten Bevorzugungen gleichzeitig auftreten, also Strukturen, in denen gilt:
L1 ist ausgewählt aus den oben genannten Gruppen gemäß den Formeln (3) bis (30);
L2, L3 sind gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus -NR2, -NR–, -N=C(R1)2, -PR2, -PR(OR), P(OR)2, -S– und -SR oder L1;
Y ist gleich oder verschieden bei jedem Auftreten eine bivalente Gruppe, ausgewählt aus CR2, BR, SiR2, NR, PR, P(=O)R, O oder S,;
n ist gleich oder verschieden bei jedem Auftreten 0, 1 oder 2;
V ist ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der oben genannten Formeln (31) bis (34);
L4 ist ausgewählt aus der Gruppe bestehend aus Kohlenmonoxid, Stickstoffmonoxid, Alkylcyaniden, Arylcyaniden, Alkylisocyaniden, Arylisocyaniden, Aminen, Halogenphosphinen, Trialkylphosphinen, Triarylphosphinen, Alkylarylphosphine, Phosphiten, Arsinen, Stibinen, neutralen oder anionischen stickstoffhaltigen Heterocyclen, Carbenen, Hydrid, Deuterid, F–, Cl–, Br und I–, Alkylacetyliden, Arylacetyliden, Cyanid, Cyanat, Isocyanat, Thiocyanat, Isothiocyanat, aliphatischen oder aromatischen Alkoholaten, aliphatischen oder aromatischen Thioalkoholaten, Amiden, Carboxylaten oder Liganden der oben genannten Formeln (35) bis (61);
b ist gleich 1. - Besonders bevorzugte Strukturen gemäß Formel (1) sind Strukturen, in denen gilt:
L1 ist ausgewählt aus den oben genannten Gruppen gemäß den Formeln (3) bis (30);
L2, L3 sind gleich oder verschieden bei jedem Auftreten L1;
Y ist gleich oder verschieden bei jedem Auftreten eine bivalente Gruppe, ausgewählt aus CR2, SiR2, NR, O oder S, bevorzugt CR2;
n ist gleich oder verschieden bei jedem Auftreten 0 oder 1;
V ist ausgewählt aus CR, CO–, N, NR+, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der oben genannten Formeln (31) bis (34);
L4 ist ausgewählt aus der Gruppe bestehend aus Kohlenmonoxid, Stickstoffmonoxid, Alkylcyaniden, Arylcyaniden, Alkylisocyaniden, Arylisocyaniden, Aminen, Halogenphosphinen, Trialkylphosphinen, Triarylphosphinen, Alkylarylphosphine, Phosphiten, Arsinen, Stibinen, neutralen oder anionischen stickstoffhaltigen Heterocyclen, Carbenen, Hydrid, Deuterid, F–, Cl–, Br und I–, Alkylacetyliden, Arylacetyliden, Cyanid, Cyanat, Isocyanat, Thiocyanat, Isothiocyanat, aliphatischen oder aromatischen Alkoholaten, aliphatischen oder aromatischen Thioalkoholaten, Amiden, Carboxylaten oder Liganden der oben genannten Formeln (35) bis (61);
b ist gleich 1. - Die weiteren verwendeten Symbole und Indizes haben jeweils die oben genannten Bedeutungen.
- In einer bevorzugten Ausführungsform der Erfindung ist der Ligand L4 über eine direkte Bindung oder über eine Gruppe -(Y)n- mit mindestens einem der Teilliganden L1, L2 und/oder L3 verknüpft. Dadurch weist der Ligand L eine Struktur gemäß einer der Formeln (62) bis (66) auf, wobei die verwendeten Symbole und Indizes die oben genannten Bedeutungen haben:
- Dabei gelten für die oben genannten Strukturen der Formel (62) bis (66) dieselben Bevorzugungen, wie oben für Strukturen der Formel (1) genannt.
- Besonders bevorzugt ist der Teilligand L4 in Strukturen der Formel (62) oder (63) gleich oder verschieden definiert wie die obige Definition der Teilliganden L1 bis L3 bzw. wie oben die Strukturen (35) bis (61).
-
- Besonders bevorzugt ist der Teilligand L4 in Strukturen der Formel (66) N oder P.
- Bevorzugt sind weiterhin Verbindungen gemäß Formel (1) bzw. gemäß Formel (62) bis (66) bzw. gemäß den oben aufgeführten bevorzugten Ausführungsformen, in denen R bei jedem Auftreten gleich oder verschieden für H, D, F, CN, eine geradkettige Alkyl- oder Alkoxygruppe mit 1 bis 6 C-Atomen oder eine verzweigte oder cyclische Alkyl- oder Alkoxygruppe mit 3 bis 6 C-Atomen, die jeweils mit einem oder mehreren Resten R1 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R1C=CR1, O oder S ersetzt sein können und ein oder mehrere H-Atome durch D oder F ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 18 aromatischen Ringatomen, welche jeweils durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Diarylaminogruppe mit 10 bis 20 aromatischen Ringatomen, welche durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Kombination dieser Systeme steht; dabei können zwei oder mehrere Substituenten R auch miteinander ein mono- oder polycyclisches aliphatisches, aromatisches und/oder benzoannelliertes Ringsystem bilden. Besonders bevorzugt steht das Symbol R in diesen Verbindungen, gleich oder verschieden bei jedem Auftreten, für H, D, F, eine geradkettige Alkylgruppe mit 1 bis 4 C-Atomen oder eine verzweigte Alkylgruppe mit 3 oder 4 C-Atomen, die jeweils mit einem oder mehreren Resten R1 substituiert sein kann, wobei ein oder mehrere H-Atome durch F ersetzt sein können, oder eine Arylgruppe mit 6 bis 10 aromatischen Ringatomen oder ein aromatisches Ringsystem mit 12 bis 18 aromatischen Ringatomen, welche jeweils durch einen oder mehrere Reste R1 substituiert sein kann; dabei können zwei oder mehrere Substituenten R auch miteinander ein mono- oder polycyclisches aliphatisches, aromatisches und/oder benzoannelliertes Ringsystem bilden.
- Weiterhin bevorzugt sind symmetrische Verbindungen, insbesondere Verbindungen, in denen die Teilliganden L1 und L2 gleich sind und auch gleich substituiert sind oder in denen die Teilliganden L1, L2 und L3 gleich sind und auch gleich substituiert sind.
- Die Komplexe gemäß Formel (1) bzw. gemäß Formel (62) bis (66) bzw. gemäß den oben aufgeführten bevorzugten Ausführungsformen sind prinzipiell durch verschiedene Verfahren herstellbar, wobei sich jedoch die im Folgenden beschriebenen Verfahren als besonders gut geeignet herausgestellt haben.
- Daher ist ein weiterer Gegenstand der vorliegenden Erfindung ein Verfahren zur Herstellung der Komplexe gemäß Formel (1) durch Umsetzung der Liganden L gemäß Formel (2) mit Metallsalzen bzw. Metallkomplexen des entsprechenden Metalls M. Beispiele für geeignete Kupferverbindungen sind CuF, CuCi, CuBr, Cul, Cu(OAc), Cu2(CO3) oder Cu(CH3CN)PF6. Beispiele für geeignete Goldverbindungen sind AuHal·SR2, wobei Hal für ein Halogenid steht und R für eine Alkylgruppe mit 1 bis 5 C-Atomen.
- Die Synthese kann auch thermisch, photochemisch oder durch Mikrowellenstrahlung aktiviert werden. Durch diese Verfahren lassen sich die Komplexe in hoher Reinheit, bevorzugt in einer Reinheit von > 99% nach 1H-NMR oder HPLC, erhalten.
- Beispiele für bevorzugte Verbindungen gemäß Formel (1) sind die im Folgenden abgebildeten Verbindungen. Diese Komplexe lassen sich unter anderem mit den oben erläuterten Synthesemethoden herstellen.
- Die oben beschriebenen Komplexe werden erfindungsgemäß als aktive Komponente in elektronischen Vorrichtungen verwendet, wie z. B. organischen Elektrolumineszenzvorrichtungen (= organische Leuchtdioden, OLEDs, PLEDs), organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs) oder auch organischen Laserdioden (O-Laser).
- Aktive Komponenten sind beispielsweise Ladungsinjektions-, Ladungstransport- oder Ladungsblockiermaterialien, insbesondere aber Emissionsmaterialien und Matrixmaterialien. Für diese Funktionen zeigen die Verbindungen gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen besonders gute Eigenschaften, insbesondere als Emissionsmaterial, wie vorne schon erläutert und im Folgenden noch näher ausgeführt wird.
- In einer bevorzugten Ausführungsform der Erfindung ist die elektronische Vorrichtung daher ausgewählt aus der Gruppe bestehend aus organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs) oder organischen Laserdioden (O-Laser), insbesondere aber organischen Elektrolumineszenzvorrichtungen (OLEDs, PLEDs), enthaltend eine oder mehrere Verbindungen gemäß Formel (1). Bevorzugt sind elektronische Vorrichtungen, enthaltend eine oder mehrere Verbindungen der Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen.
- Die organische Elektrolumineszenzvorrichtung enthält Kathode, Anode und mindestens eine emittierende Schicht. Außer diesen Schichten kann sie noch weitere Schichten enthalten, beispielsweise jeweils eine oder mehrere Lochinjektionsschichten, Lochtransportschichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Exzitonenblockierschichten, Elektronenblockierschichten und/oder Ladungserzeugungsschichten (Charge-Generation Layer). Ebenso können zwischen zwei emittierende Schichten Interlayers eingebracht sein, welche. beispielsweise eine Exzitonen-blockierende Funktion aufweisen. Es sei aber darauf hingewiesen, dass nicht notwendigerweise jede dieser Schichten vorhanden sein muss.
- In einer bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als emittierende Verbindung in einer emittierenden Schicht eingesetzt. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittierende Schicht enthalten, oder sie kann mehrere emittierende Schichten enthalten, wobei mindestens eine emittierende Schicht mindestens eine Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen enthält. Wenn mehrere Emissionsschichten vorhanden sind, weisen diese bevorzugt insgesamt mehrere Emissionsmaxima zwischen 380 nm und 750 nm auf, so dass insgesamt weiße Emission resultiert, d. h. in den emittierenden Schichten werden verschiedene emittierende Verbindungen verwendet, die fluoreszieren oder phosphoreszieren können. Insbesondere bevorzugt sind Dreischichtsysteme (drei emittierende Schichten), wobei die drei Schichten blaue, grüne und orange oder rote Emission zeigen (für den prinzipiellen Aufbau siehe z. B.
WO 05/011013 - Wenn die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als emittierende Verbindung in einer emittierenden Schicht eingesetzt wird, wird sie bevorzugt in Kombination mit einem oder mehreren Matrixmaterialien eingesetzt. Die Mischung aus der Verbindung gemäß Formel (1) bzw. den oben genannten bevorzugten Ausführungsformen und dem Matrixmaterial enthält zwischen 1 und 99 Gew.-%, vorzugsweise zwischen 2 und 90 Gew.-%, besonders bevorzugt zwischen 3 und 40 Gew.-%, insbesondere zwischen 5 und 15 Gew.-% der Verbindung gemäß Formel (1) bzw. den oben genannten bevorzugten Ausführungsformen bezogen auf die Gesamtmischung aus Emitter und Matrixmaterial. Entsprechend enthält die Mischung zwischen 99 und 1 Gew.-%, vorzugsweise zwischen 98 und 10 Gew.-%, besonders bevorzugt zwischen 97 und 60 Gew.-%, insbesondere zwischen 95 und 85 Gew.-% des Matrixmaterials bezogen auf die Gesamtmischung aus Emitter und Matrixmaterial.
- Geeignete Matrixmaterialien für die erfindungsgemäßen Verbindungen, welche einzeln oder als Mischung von zwei oder mehr dieser Materialien eingesetzt werden können, sind Ketone, Phosphinoxide, Sulfoxide und Sulfone, z. B. gemäß
WO 04/013080 WO 04/093207 WO 06/005627 DE 10 2008 033 943.1 , Triarylamine, Carbazolderivate, z. B. CBP (N,N-Biscarbazolylbiphenyl) oder die inWO 05/039246 US 2005/0069729 JP 2004/288381 EP 1205527 oderWO 08/086851 WO 07/063754 WO 08/056746 DE 10 2009 023 155.2 undDE 10 2009 031 021.5 , Azacarbazole, z. B. gemäßEP 1617710 ,EP 1617711 ,EP 1731584 ,JP 2005/347160 WO 07/137725 WO 05/111172 WO 06/117052 DE 10 2008 036 982.9 undDE 10 2009 048 791.3 ,WO 07/063754 WO 08/056746 EP 652273 WO 09/062578 DE 10 2008 056 688.8 , oder Diazaphospholderivate, z. B. gemäß der nicht offen gelegten AnmeldungDE 10 2009 022 858.6 . - Es können auch zwei oder mehr lumineszierende Metallkomplexe eingesetzt werden, wobei der kürzerwellig emittierende Metallkomplex als Co-Host für den längerwellig emittierenden Metallkomplex dient.
- Es kann weiterhin auch bevorzugt sein, ein ladungstransportierendes Hostmaterial zusammen mit einem Hostmaterial, welches nicht am Ladungstransport beteiligt ist, einzusetzen, z. B. gemäß der nicht offen gelegten Anmeldung
DE 10 2009 014 513.3 . - In einer weiteren bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als Matrixmaterial für eine emittierende Verbindung in einer emittierenden Schicht eingesetzt. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittierende Schicht enthalten, oder sie kann mehrere emittierende Schichten enthalten, wobei mindestens eine emittierende Schicht mindestens eine Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als Matrixmaterial enthält. Wenn mehrere Emissionsschichten vorhanden sind, gilt hierfür das oben ausgeführte. Wenn die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als Matrixmaterial für eine emittierende Verbindung in einer emittierenden Schicht eingesetzt wird, wird sie bevorzugt in Kombination mit einem oder mehreren fluoreszierenden oder phosphoreszierenden Materialien eingesetzt.
- In einer weiteren bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als Lochblockiermaterial in einer Lochblockierschicht und/oder als Elektronentransportmaterial in einer Elektronentransportschicht eingesetzt. Dabei kann die emittierende Schicht fluoreszierend oder phosphoreszierend sein.
- In einer weiteren bevorzugten Ausführungsform der Erfindung wird die Verbindung gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen als Lochtransportmaterial in einer Lochtransport- bzw. -injektionsschicht und/oder als Elektronenblockiermaterial in einer Elektronenblockierschicht eingesetzt. Dabei kann die emittierende Schicht fluoreszierend oder phosphoreszierend sein.
- Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck von üblicherweise kleiner 10–5 mbar, bevorzugt kleiner 10–6 mbar aufgedampft. Es ist aber auch möglich, dass der Anfangsdruck noch geringer ist, beispielsweise kleiner 10–7 mbar.
- Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10–5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden (z. B. M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301).
- Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie z. B. Siebdruck, Flexodruck oder Offsetdruck, besonders bevorzugt aber LITI (Light Induced Thermal Imaging, Thermotransferdruck) oder Ink-Jet Druck (Tintenstrahldruck), hergestellt werden. Hierfür sind lösliche Verbindungen nötig, welche beispielsweise durch geeignete Substitution erhalten werden.
- Ebenso möglich sind Hybridverfahren, bei denen beispielsweise eine oder mehrere Schichten aus Lösung aufgebracht werden und eine oder mehrere andere Schichten aufgedampft werden.
- Diese Verfahren sind dem Fachmann generell bekannt und können von ihm ohne Probleme auf elektronische Vorrichtungen enthaltend Verbindungen gemäß Formel (1) bzw. die oben genannten bevorzugten Ausführungsformen angewandt werden.
- Die oben genannten bevorzugten Verbindungen, in denen der Ligand L4 mit mindestens einem der Teilliganden L1, L2 und/oder L3 verknüpft ist, sind neu und sind daher ein weiterer Gegenstand der vorliegenden Erfindung.
-
- Ein weiterer Gegenstand der Erfindung ist die Verwendung einer Verbindung gemäß einer der Formeln (62) bis (66) in einer elektronischen Vorrichtung.
- Die erfindungsgemäßen organischen Elektrolumineszenzvorrichtungen und die erfindungsgemäßen Verbindungen zeichnen sich durch folgende überraschende Vorteile gegenüber dem Stand der Technik aus:
- 1. Im Gegensatz zu vielen Metallkomplexen gemäß dem Stand der Technik, die der teilweisen oder vollständigen pyrolytischen Zersetzung bei Sublimation unterliegen, weisen die erfindungsgemäßen Verbindungen eine hohe thermische Stabilität auf.
- 2. Organische Elektrolumineszenzvorrichtungen enthaltend Verbindungen gemäß Formel (1) als emittierende Materialien weisen eine hohe Lebensdauer auf.
- 3. Es sind blau lumineszierende Komplexe zugänglich, welche bei Verwendung in organischen Elektrolumineszenzvorrichtungen eine hohe Lebensdauer aufweisen. Dies ist ein deutlicher Fortschritt gegenüber dem Stand der Technik, da bislang blau lumineszierende Metallkomplexe nur mit schlechten Farbkoordinaten und insbesondere einer sehr schlechten Lebensdauer zugänglich waren.
- 4. Die erfindungsgemäßen Verbindungen, eingesetzt in organischen Elektrolumineszenzvorrichtungen, führen zu hohen Effizienzen und zu steilen Strom-Spannungs-Kurven.
- 5. Die Verbindungen gemäß Formel (1) basieren nicht auf dem seltenen Metall Iridium, was zur Ressourcenschonung dieses Metalls beiträgt.
- 6. Da es sich nicht um ortho-metallierte Komplexe handelt, sind die Komplexe gemäß Formel (1) bzw. gemäß der oben aufgeführten bevorzugten Ausführungsformen gut und in hohen Ausbeuten und hohen Reinheiten synthetisch zugänglich.
- Die oben genannten Vorteile gehen nicht mit einer Verschlechterung der weiteren elektronischen Eigenschaften einher.
- Die Erfindung wird durch die nachfolgenden Beispiele näher erläutert, ohne sie dadurch einschränken zu wollen. Der Fachmann kann aus den Schilderungen ohne erfinderisches Zutun weitere erfindungsgemäße Komplexe herstellen und diese in organischen elektronischen Vorrichtungen verwenden bzw. das erfindungsgemäße Verfahren anwenden und so die Erfindung im gesamten beanspruchten Bereich ausführen.
- Beispiele:
-
- Eine Mischung von 50.2 g (100 mmol) Tris(6-brom-pyridin-2-yl)fluormethan [760177-68-2], 61.0 g (500 mmol) Phenylboronsäure, 58.1 g (1 mol) Kaliumfluorid, wasserfrei in 1000 ml THF wird mit 809 mg (4 mmol) Tris-tert-butyl-phosphin und dann 674 mg (3 mmol) Palladium(II)acetat versetzt und anschließend 5 h unter Rückfluss gerührt. Nach Erkalten wird die Reaktionsmischung mit 300 ml Wasser versetzt, die wässrige Phase wird abgetrennt, die organische Phase wird über Celite filtriert und zur Trockene eingeengt. Der so erhaltene Feststoff wird zweimal aus Chloroform (ca. 50 ml) unter Zusatz von Ethanol (ca. 200 ml) umkristallisiert. Ausbeute: 38.5 g (78 mmol), 78%, 99.0%ig nach 1H-NMR.
- B): Cu-Komplex 1
- Eine Mischung von 4.9 g (10 mmol) Tris(6-phenyl-pyridin-2-yl)fluormethan, 1.0 g (10 mmol) Kupfer(I)chlorid in 50 ml THF wird 24 h bei 60°C gerührt. Man engt die Reaktionsmischung im Vakuum auf ein Volumen von 5 ml ein, gibt 20 ml Methanol zu, saugt vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 10 ml Methanol und trocknet im Vakuum. Ausbeute: 3.9 g (6.6 mmol), 66%, 99.5%-ig nach 1H-NMR.
-
- Eine auf –78°C gekühlte Suspension von 26.1 g (110 mmol) 2,6-Dibrompyridin in 150 ml Diethylether wird tropfenweise mit 40.0 ml (100 mmol) n-Butyllithium (2.5 N) versetzt und so lange bei –78°C gerührt, bis eine gelbe Lösung entsteht. Diese Lösung wird tropfenweise mit 200 ml Diethylether verdünnt und dann unter gutem Rühren auf ein Mal mit einer Lösung von 23.3 g (110 mmol) Bis(6-methyl-2-pyridinyl)-methanon in 80 ml THF versetzt. Nach Erwärmen auf 0°C gibt man tropfenweise ein Gemisch aus 50 ml Wasser und 6 ml Eisessig zu, saugt dann vom ausgefallenen Feststoff ab, wäscht diesen einmal mit 25 ml Diethylether und einmal mit 25 ml Ethanol und trocknet im Vakuum. Ausbeute: 17.8 g (48 mmol), 48%, 98%ig nach 1H-NMR. B): (6-Brom-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)methoxy-methan
- Eine Suspension von 1.4 g (60 mmol) Natriumhydrid in 50 ml DMF wird bei 40°C mit einer Lösung von 18.5 g (50 mmol) (6-Brom-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)methanol in 50 ml DMF versetzt und 30 min. nachgerührt. Dann gibt man ein Gemisch von 8.5 g (60 mmol) Methyliodid und 10 ml DMF zu, rührt 20 h bei Raumtemperatur nach, gibt tropfenweise 5 ml Ethanol zu, verdünnt mit 500 ml Dichlormethan, wäscht die org. Phase fünfmal mit je 300 ml Wasser, trocknet die organische Phase über Magnesiumsulfat und zieht dann das Lösungsmittel im Vakuum komplett ab. Der Rückstand wird aus Ethanol unter Zusatz von wenig Essigsäureethylester umkristallisiert. Ausbeute: 16.5 g (43 mmol), 86%-ig nach 1H-NMR. C): (6-(Phenyl-2-thiol)-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)methoxymethan
- Eine Mischung von 38.4 g (100 mmol) (6-Brom-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)methoxy-methan, 41.9 g (130 mmol) [2-Tetrahyro-2H-pyran-2-yl]thio]phenyl-boronsäure-di-iso-proplylester [620988-03-6], 19.2 g (330 mol) Kaliumfluorid (wasserfrei) in 500 ml THF wird mit 405 mg (2 mmol) Tris-tert-butyl-phosphin und dann mit 337 mg (1.5 mmol) Palladium(II)acetat versetzt und anschließend 5 h unter Rückfluss gerührt. Nach Erkalten wird die Reaktionsmischung mit 300 ml Wasser und 15 ml Eisessig versetzt, die Mischung wird 2 h bei 50°C gerührt, die wässrige Phase wird abgetrennt, die organische Phase wird über Celite filtriert und zur Trockene eingeengt. Der so erhaltene Feststoff wird aus Aceton (20 ml) unter Zusatz von Ethanol (150 ml) umkristallisiert. Ausbeute: 27.3 g (66 mmol), 66%, 99.0%ig nach 1H-NMR.
- D): Cu-Komplex 7
- Eine Lösung von 4.1 g (10 mmol) (6-(Phenyl-2-thiol)-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)methoxy-methan in 50 ml THF wird mit 10.0 ml (10 mmol) Natriummethanolat-Lösung, 1 N in Methanol, versetzt und 1 h bei 40°C gerührt. Dann gibt man 1.0 g (10 mmol) Kupfer(I)chlorid fest zu und rührt weitere 24 h nach. Man engt die Reaktionsmischung im Vakuum auf ein Volumen von 5 ml ein, gibt 50 ml Methanol zu, saugt vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 10 ml Methanol und trocknet im Vakuum. Nach zweimaliger Umkristallisation aus DMSO/iso-Propanol wird im Hochvakuum (p = 1 × 10–6 mbar, T = 320°C) sublimiert. Ausbeute: 3.4 g (7.0 mmol), 71%, 99.8%ig nach HPLC. Beispiel 8: Cu-Komplex 8 A): (6-Brom-pyridin-2-yl)-bis-(6-methl-pyridin2-yl)fluormethan
- Eine Lösung von 37.0 g (100 mmol) (6-Brom-pyridin-2-yl)-bis-(6-methyl-pyridin2-yl)methanol in 300 ml Chloroform wird unter Rühren mit 46.6 g (350 mmol) Dimethylaminoschwefeltrifluorid versetzt und dann 1 h unter Rückfluss gerührt. Nach Erkalten und Abkühlen der Reaktionsmischung auf + 5°C gibt man eine Lösung von 65 g Natriumhydroxid in 500 ml Wasser zu langsam (Achtung: exotherm!), rührt 30 min. nach, trennt die wässrige Phase ab und trocknet die organische Phase über Calciumchlorid. Nach Entfernen des Lösungsmittels im Vakuum nimmt man das Öl in 100 ml heißem Methanol auf, saugt nach Erkalten vom farblosen Feststoff ab, wäscht diesen einmal mit 30 ml Methanol und trocknet im Vakuum. Ausbeute: 33.1 g (8.9 mmol), 89%, 97%-ig nach 1H-NMR. B): (6-Formyl-pyridin-2-yl)-bis-(6-methyl-pyridin2-yl)fluormethan
- Eine auf –78°C gekühlte Lösung von 16.6 g (50 mmol) 6-Brom-pyridin-2-yl)-bis-(6-methyl-pyridin2-yl)fluormethan in 200 ml THF wird zügig mit 20 ml (50 mmol) n-Butyllithium (2.5 N in Hexan) versetzt und 10 min. bei –78°C gerührt. Dann gibt man 4.4 g (60 mmol) DMF in 10 ml THF auf ein Mal zu, rührt 30 min. nach und lässt dann auf Raumtemperatur erwärmen. Man gibt 55 ml 1 N Salzsäure zu, rührt 1 h nach und engt im Vakuum zur Trockene ein. Man nimmt den Rückstand in 500 ml Dichlormnethan auf, wäscht mit 100 ml 1 N Natronlauge und dann mit 100 ml Wasser, trocknet die organische Phase über Magnesiumsulfat, engt die organische Phase im Vakuum auf ca. 30 ml ein, gibt 100 ml iso-Propanol zu, rührt 1 h nach, saugt vom ausgefallenen Feststoff ab, wäscht diesen mit Methanol und trocknet im Vakuum. Ausbeute: 10.3 g (32 mmol), 64%, 95.0%-ig nach 1H-NMR. C): (6-(Benzimidazol-2-yl)-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)fluormethan
- Eine Suspension von 12.0 g Kieselgel in 50 ml Dichlormethan wird tropfenweise mit 3.0 ml Thionylchlirid versetzt und dann 1 h bei Raumtemperatur gerührt. Anschließend tropft man eine Lösung von 6.4 g (20 mmol) (6-Formyl-pyridin-2-yl)-bis-(6-methyl-pyridin2-yl)fluormethan und 2.4 g (22 mmol) o-Phenylendiamin zu und rührt 6 h bei nach. Man versetzt mit 50 ml Dichlormethan und 50 ml Ethanol, saugt über Kieselgel ab, wäscht dieses mit Dichlormethan nach, engt die organische Phase im Vakuum ein und kristallisiert den Rückstand aus ca. 50 ml Ethanol unter Zusatz von 5 ml Triethylamin um. Ausbeute: 4.9 g (12 mmol), 60%, 99.0%-ig nach 1H-NMR.
- D): Cu-Komplex 8
- Eine Mischung von 4.1 g (10 mmol) (6-(Benzimidazol-2-yl)-pyridin-2-yl)-bis-(6-methyl-pyridin-2-yl)fluormethan und 1.0 g (10 mmol) Kupfer(I)chlorid in 50 ml THF wird mit 1.3 g (10 mmol) Diisopropylethylamin versetzt und 24 h bei 40°C gerührt. Man engt die Reaktionsmischung im Vakuum auf ein Volumen von 5 ml ein, gibt 30 ml Methanol zu, saugt vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 10 ml Methanol und trocknet im Vakuum. Nach zweimaliger Umkristallisation aus Acetonitril wird im Hochvakuum (p = 1 × 10–6 mbar, T = 310°C) sublimiert. Ausbeute: 3.3 g (7.0 mmol), 70%, 99.9%-ig nach HPLC. Beispiel 9: Cu-Komplex 9 A): 2-(1-Methoxymethyl-1H-imidazol-2-yl)-pyridin
- Zu einer Lösung von 400.0 g (10 mol) Natruimhydroxid in 400 ml Wasser gibt man unter gutem Rühren bei Raumtemperatur 600 ml Toluol, 84.2 g (580 mmol) 1H-Imidazol-2-yl-pyridin [18653-75-3] und 14.8 g (40 mmol) Tetrabutylammoniumbromid zu, tropft dann ein Gemisch von 50.0 g (621 mmol) Chiormethyl-methyl-ether und 100 ml Toluol langsam zu, und rührt 16 h bei Raumtemperatur nach. Man erweitert die Reaktionsmischung mit 800 ml Toluol und 800 ml Wasser, trennt die organische Phase ab, trocknet diese über Magnesiumsulfat und entfernt das Lösungsmittel im Vakuum. Ausbeute: 99.0 g (90 mmol), 98%, 96%-ig nach 1H-NMR. B): Bis-(6-methyl-pyridin-2-yl)-(1-methoxymethyl-2-pyridin-2-yl-3H-imidazol-4-yl)methanol
- Eine auf –78°C gekühlte Lösung von 18.9 g (100 mmol) 2-(1-Methoxymethyl-1H-imidazol-2-yl)-pyridin in 500 ml THF wird tropfenweise mit 40 ml (100 mmol) n-Butyllithium (2.5 M in Hexan) versetzt und 30 min. nachgerührt. Anschließend gibt man eine Lösung von 21.2 g (100 mmol) Bis(6-methyl-2-pyridinyl)-methanon in 50 ml THF auf ein Mal zu und lässt die Reaktionsmischung auf Raumtemperatur erwärmen. Nach Zugabe eines Gemischs von 100 ml Wasser und 6.0 ml Eisessig rührt man 1 h nach, trennt dann die organische Phase ab, trocknet diese über Kaliumcarbonat und engt dann im Vakuum zur Trockene ein. Ausbeute: 23.0 g (57 mmol), 57%, 95.0%-ig nach 1H-NMR. C): Bis-(6-methyl-pyridin-2-yl)-(2-pyridin-2-yl-3H-imidazol-4-yl)methan
- 20.1 g (50 mmol) Bis-(6-methyl-pyridin-2-yl)-(1-methoxymethyl-2-pyridin-2-yl-3H-imidazol-4-yl)methan werden in 300 ml Eisessig suspendiert. Man versetzt die Suspension mit 20 ml wässriger hypophosphoriger Säure (50 Gew.-%ig) und 40 ml wässriger Iodwasserstoffsäure (57 Gew.-%ig) und rührt die Reaktionsmischung 24 h bei 80°C. Nach Erkalten saugt man vom ausgefallenen Feststoff ab, wäscht diesen einmal mit 20 ml Eisessig und dreimal mit je 20 ml Methanol. Man suspendiert den Feststoff in 300 ml Dichlormethan, gibt 100 ml gesättigte Ammoniumchlorid-Lösung und dann 50 ml Ammoniaklösung zu, rührt, bis sich der Feststoff gelöst hat, trennt die organische Phase ab, wäscht diese mit gesättigter Kochsalzlösung, trocknet die organische Phase über Magnesiumsulfat und engt dann im Vakuum ein. Der Rückstand wird zweimal aus Essigsäureethylester umkristallisiert. Ausbeute: 10.9 g (32 mmol), 64%, 99.0%-ig nach 1H-NMR.
- D): Cu-Komplex 9
- Eine Mischung von 3.4 g (10 mmol) Bis-(6-methyl-pyridin-2-yl)-(2-pyridin-2-yl-3H-imidazol-4-yl)methan und 1.0 g (10 mmol) Kupfer(I)chlorid in 50 ml THF wird mit 1.3 g (10 mmol) Diisopropylethylamin versetzt und 24 h bei 40°C gerührt. Man engt die Reaktionsmischung im Vakuum auf ein Volumen von 5 ml ein, gibt 30 ml Methanol zu, saugt vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 10 ml Methanol und trocknet im Vakuum. Nach zweimaliger Umkristallisation aus DMF/EtOH wird im Hochvakuum (p = 1 × 10–6 mbar, T = 320°C) sublimiert. Ausbeute: 2.1 g (5.2 mmol), 52%, 99.8%-ig nach HPLC. Beispiel 10: Cu-Komplex 10 A): Tris(6-phenyl-pyridin-2-yl)phosphinoxid
- Eine Mischung von 51.8 g (100 mmol) Tris(6-brom-pyridin-2-yl)phosphinoxid [197776-47-9], 61.0 g (500 mmol) Phenylboronsäure, 58.1 g (1 mol) Kaliumfluorid (wasserfrei) in 1000 ml THF wird mit 809 mg (4 mmol) Tris-tert-butyl-phosphin und dann 674 g (3 mmol) Palladium(II)acetat versetzt und anschließend 5 h unter Rückfluss gerührt. Nach Erkalten wird die Reaktionsmischung mit 300 ml Wasser versetzt, die wässrige Phase wird abgetrennt, die organische Phase wird über Celite filtriert und zur Trockene eingeengt. Der so erhaltene Feststoff wird aus Chloroform (50 ml) unter Zusatz von Ethanol (250 ml) umkristallisiert. Ausbeute: 38.4 g (75 mmol), 75%, 99.0%-ig nach 1H-NMR.
- B): Cu-Komplex 10
- Eine Mischung von 5.1 g (10 mmol) Tris(6-phenyl-pyridin-2-yl)phosphinoxid und 891 mg (10 mmol) Kupfer(I)cyanid in 50 ml THF wird 24 h bei 60°C gerührt. Man engt die Reaktionsmischung im Vakuum auf ein Volumen von 5 ml ein, gibt 20 ml Methanol zu, saugt vom ausgefallenen Feststoff ab, wäscht diesen dreimal mit je 10 ml Methanol und trocknet im Vakuum. Ausbeute: 3.7 g (6.2 mmol), 62%, 99.0%-ig nach 1H-NMR.
- Beispiel 11: Herstellung und Charakterisierung von organischen Elektrolumineszenzvorrichtungen aus der Gasphase
- Erfindungsgemäße Elektrolumineszenzvorrichtungen können, wie beispielsweise in
WO 05/003253 - Dabei wird der folgende Device-Aufbau verwendet:
Lochinjektionsschicht (HIL) 20 nm 2,2',7,7'-Tetrakis(di-para-tolylamino)spiro-9,9'-bifluoren Lochtransportschicht (HTL1) 5 nm NPB (N-Naphthyl-N-phenyl-4,4'-diaminobiphenyl) Elektronenblockierschicht (EBL) EBL1, 10 nm oder EBL2, 10 nm Emissionsschicht (EML) Matrix M1, M2, M3 oder M4 oder Kombinationen davon, 40 nm; Emitter: 10 Vol.-% Dotierung; Verbindungen: s. Tabelle 1. Elektronenleiter (ETL) 20 nm BAlq Kathode 1 nm LiF, darauf 100 nm Al. - Die Strukturen von EBL, M und TEB sind der Übersichtlichkeit halber im Folgenden abgebildet.
- Diese noch nicht optimierten OLEDs werden standardmäßig charakterisiert; hierfür werden die Elektrolumineszenzspektren, die externe Quanteneffizienz (gemessen in %) in Abhängigkeit von der Helligkeit, berechnet aus Strom-Spannungs-Helligkeit-Kennlinien (IUL-Kennlinien) bestimmt. Tabelle 1: Device-Ergebnisse
Bsp. EBL Matrix Emitter EQE bei 100 cd/m2 [%] Spannung bei 100 cd/m2 [V] CIE x/y 12 EBL1 M3 Cu-Komplex 7 7.8 6.3 0.24/0.62 13 EBL1 M1 (40%) M3 (50%) Cu-Komplex 7 6.8 5.7 0.25/0.59 14 EBL2 M3 Cu-Komplex 8 9.5 5.5 0.17/0.46 15 EBL2 M3 (50%) M4 (40%) Cu-Komplex 8 8.9 5.8 0.19/0.48 16 EBL2 M3 Bsp. 27 Cu-Komplex 9 7.5 6.1 0,17/0.39 17 EBL1 M2 Cu-Komplex 9 8.3 7.4 0.17/0.38 - Beispiel 18: Herstellung und Charakterisierung von organischen Elektrolumineszenzvorrichtungen aus Lösung
- Die Herstellung von LEDs erfolgt nach dem im Folgenden skizzierten allgemeinen Verfahren. Dieses muss natürlich im Einzelfall auf die jeweiligen Gegebenheiten (z. B. Schichtdickenvariation, um optimale Effizienz bzw. Farbe zu erreichen) angepasst werden.
- Allgemeines Verfahren zur Herstellung der OLEDs:
- Die Herstellung solcher Bauteile lehnt sich an die Herstellung polymerer Leuchtdioden (PLEDs) an, die in der Literatur bereits vielfach beschrieben ist (z. B. in der
WO 2004/037887 A2 - Analog dem o. g. allgemeinen Verfahren werden OLEDs mit folgendem Aufbau erzeugt:
PEDOT 20 nm (aus Wasser aufgeschleudert; PEDOT bezogen von BAYER AG; Poly-[3,4-ethylendioxy-2,5-thiophen] Matrix + Emitter 80 nm, 5 Gew.-% Emitterkonzentration (aus Toluol, Chlorbenzol oder DMF aufgeschleudert), Ba/Ag 10 nm Ba/150 nm Ag als Kathode. - Strukturierte ITO-Substrate und das Material für die sogenannte Pufferschicht (PEDOT, eigentlich PEDOT:PSS) sind käuflich erhältlich (ITO von Technoprint und anderen, PEDOT:PPS als wässrige Dispersion Clevios Baytron P von H. C. Starck). Die Emissionsschicht wird in einer Inertgasatmosphäre, im vorliegenden Fall. Argon, aufgeschleudert und 10 min bei 120°C ausgeheizt. Zuletzt wird eine Kathode aus Barium und Aluminium im Vakuum aufgedampft. Die lösungsprozessierten Devices werden standardmäßig charakterisiert, die genannten OLED-Beispiele sind noch nicht optimiert. In Tabelle 2 sind die Effizienz und die Spannung bei 100 cd/m2 sowie die Farbe aufgeführt. Tabelle 2: Device-Ergebnisse
Bsp. Matrix Emitter EQE bei 100 cd/m2 [%] Spannung bei 100 cd/m2 [V] CIE x/y 19 M1 (30%) M4 (60%) Cu-Komplex 1 2,1 8,9 0.35/0.61 20 M3 (45%) M4 (45%) Cu-Komplex 6 3.4 6.2 0.17/0.55 21 M1 (30%) M4 (60%) Cu-Komplex 10 4.9 7.7 0.30/0.42 - ZITATE ENTHALTEN IN DER BESCHREIBUNG
- Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.
- Zitierte Patentliteratur
-
- US 4539507 [0002]
- US 5151629 [0002]
- EP 0676461 [0002]
- WO 98/27136 [0002]
- WO 05/011013 [0053]
- WO 04/013080 [0055]
- WO 04/093207 [0055]
- WO 06/005627 [0055]
- DE 102008033943 [0055]
- WO 05/039246 [0055]
- US 2005/0069729 [0055]
- JP 2004/288381 [0055]
- EP 1205527 [0055]
- WO 08/086851 [0055]
- WO 07/063754 [0055, 0055]
- WO 08/056746 [0055, 0055]
- DE 102009023155 [0055]
- DE 102009031021 [0055]
- EP 1617710 [0055]
- EP 1617711 [0055]
- EP 1731584 [0055]
- JP 2005/347160 [0055]
- WO 07/137725 [0055]
- WO 05/111172 [0055]
- WO 06/117052 [0055]
- DE 102008036982 [0055]
- DE 102009048791 [0055]
- EP 652273 [0055]
- WO 09/062578 [0055]
- DE 102008056688 [0055]
- DE 102009022858 [0055]
- DE 102009014513 [0057]
- WO 05/003253 [0090]
- WO 2004/037887 A2 [0095]
- Zitierte Nicht-Patentliteratur
-
- M. A. Baldo et al., Appl. Phys. Lett. 1999, 75, 4– 6 [0002]
- M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301 [0062]
Claims (16)
- Elektronische Vorrichtung enthaltend Anode, Kathode und mindestens eine Verbindung gemäß Formel (1), Formel (1) enthaltend ein Metall M, koordiniert an einen Liganden L gemäß Formel (2), Formel (2) wobei für die verwendeten Symbole und Indizes gilt: M ist ausgewählt aus Cu, Ag, Au, Zn, Sn, Pb, Ni, Pd oder Pt; V ist ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P, PR+, P(=O), As, AsR+, As(=O), Sb, SbR+, Sb(=O) oder S+; oder V ist eine aliphatische, aromatische oder heteroaromatische cyclische Gruppe mit 3 bis 6 Ringatomen, die die Teilliganden L1, L2 und L3, gegebenenfalls über die Gruppe Y, kovalent miteinander verbindet und die durch einen oder mehrere Reste R substituiert sein kann; Y ist bei jedem Auftreten gleich oder verschieden eine bivalente Gruppe, ausgewählt aus CR2, BR, SiR2, NR, PR, P(=O)R, AsR, As(=O)R, SbR, Sb(=O)R, O, S, 1,2-Vinylen oder 1,2- oder 1,3-Phenylen, welches jeweils mit einem oder mehreren Resten R substituiert sein kann; a ist 0 oder 1; b ist 1, 2 oder 3, wobei für b = 2 oder 3 der Index a = 1 ist; L1 ist eine heterocyclische Gruppe mit 1 bis 20 C-Atomen und mindestens einem N-Atom, welche durch einen oder mehrere Reste R substituiert sein kann und welche über ein neutrales oder anionisches Stickstoffatom oder über ein neutrales Kohlenstoffatom, welches jeweils Teil der heterocyclischen Gruppe ist, an M bindet; oder ist eine cyclische oder heterocyclische Gruppe mit 1 bis 20 C-Atomen, welche über ein exocyclisches Donoratom an M bindet und welche durch einen oder mehrere Reste R substituiert sein kann; L2, L3 sind gleich oder verschieden bei jedem Auftreten eine koordinierende Gruppe, welche durch einen oder mehrere Reste R substituiert sein kann und welche über Stickstoff, Phosphor, Schwefel oder ein neutrales Kohlenstoffatom an M bindet, wobei L2 und/oder L3 auch gleich oder verschieden L1 sein können; L4 ist ein beliebiger Ligand, welcher an das Metall M koordiniert und welcher durch einen oder mehrere Reste R substituiert sein kann; dabei kann L4 auch durch eine direkte Bindung oder durch eine bivalente Gruppe -(Y)n- mit einem oder mehreren der Teilliganden L1, L2 und/oder L3 verknüpft sein; n ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3; R ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, N(R1)2, CN, NO2, OH, Si(R1)3, B(OR1)2, C(=O)R1, P(=O)(R1)2, S(=O)R1, S(=O)2R1, OSO2R1, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomeng die jeweils mit einem oder mehreren Resten R1 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R1C=CR1, C≡C, Si(R1)2, Ge(R1)2, Sn(R1)2, C=O, C=S, C=Se, C=NR1, P(=O)(R1), SO, SO2, NR1, O, S oder CONR1 ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Aryloxy-, Heteroaryloxy-, Aralkyl- oder Heteroaralkylgruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R1 substituiert sein kann, oder eine Diarylaminogruppe, Diheteroarylaminogruppe oder Arylheteroarylaminogruppe mit 10 bis 40 aromatischen Ringatomen, welche durch einen oder mehrere Reste R1 substituiert sein kann; dabei können zwei oder mehrere Substituenten R auch miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches, heteroaromatisches und/oder benzoannelliertes Ringsystem bilden; R1 ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, N(R2)2, CN, NO2, OH, Si(R2)3, B(OR2)2, C(=O)R2, P(=O)(R2)2, S(=O)R2, S(=O)2R2, OSO2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 3 bis 40 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, die jeweils mit einem oder mehreren Resten R2 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S oder CONR2 ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Aryloxy-, Heteroaryloxy-, Aralkyl- oder Heteroaralkylgruppe mit 5 bis 60 aromatischen Ringatomen, die durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Diarylaminogruppe, Diheteroarylaminogruppe oder Arylheteroarylaminogruppe mit 10 bis 40 aromatischen Ringatomen, welche durch einen oder mehrere Reste R2 substituiert sein kann; dabei können zwei oder mehrere Substituenten R1 auch miteinander ein mono- oder polycyclisches, aliphatisches, aromatisches, heteroaromatisches und/oder benzoannelliertes Ringsystem bilden; R2 ist bei jedem Auftreten gleich oder verschieden H, D, F oder ein aliphatischer, aromatischer und/oder heteroaromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen, in dem auch ein oder mehrere H-Atome durch F ersetzt sein können; dabei können zwei oder mehrere Substituenten R2 auch miteinander ein mono- oder polycyclisches aliphatisches oder aromatisches Ringsystem bilden.
- Elektronische Vorrichtung nach Anspruch 1, dadurch gekennzeichnet, dass L1 eine Heteroarylgruppe ist oder eine Aryl- bzw. Heteroarylgruppe mit einem exocyclischen Donoratom oder ein cyclisches, gesättigtes oder ungesättigtes Carben, wobei diese Gruppen jeweils mit einem oder mehreren Resten R substituiert sein können.
- Elektronische Vorrichtung nach Anspruch 1 oder 2, dadurch gekennzeichnet, dass L1 ausgewählt ist aus den Gruppen gemäß den Formeln (3) bis (30): wobei die verwendeten Symbole dieselbe Bedeutung haben, wie in Anspruch 1 beschrieben, und weiterhin gilt: X steht bei jedem Auftreten gleich oder verschieden für CR oder N; D steht bei jedem Auftreten gleich oder verschieden für O–, S–, NR–, PR–, NR2, PR2, COO–, SO3 –, -C(=O)R, -CR(=NR) oder -N(=CR2); dabei koordinieren die Gruppen an das Metall M über die durch * gekennzeichnete Position, die durch # gekennzeichnete Position gibt die Position an, an der der Teilligand an Y bzw. an V gebunden ist, und die durch (#) gekennzeichnete Position gibt die Position an, an der der Teilligand gegebenenfalls an Y bzw. an L4 gebunden ist.
- Elektronische Vorrichtung nach einem oder mehreren der Ansprüche 1 bis 3, dadurch gekennzeichnet, dass L2 und L3 koordinierende Gruppen sind, welche auch durch einen oder mehrere Reste R substituiert sein können und welche über Stickstoff, Phosphor oder Schwefel an M bindet oder welche gleich oder verschieden L1 sind.
- Elektronische Vorrichtung nach einem oder mehreren der Ansprüche 1 bis 4, dadurch gekennzeichnet, dass Y gleich oder verschieden bei jedem Auftreten eine bivalente Gruppe ist, ausgewählt aus CR2, BR, SiR2, NR, PR, P(=O)R, O oder S.
- Elektronische Vorrichtung nach einem oder mehreren der Ansprüche 1 bis 5, dadurch gekennzeichnet, dass V ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der Formeln (31) bis (34), wobei die gestrichelten Bindungen jeweils die Bindung zu den Teilliganden L1, L2 und L3 bzw. zu Y andeuten und R wie in Anspruch 1 definiert ist.
- Elektronische Vorrichtung nach einem oder mehreren der Ansprüche 1 bis 6, dadurch gekennzeichnet, dass L4 ausgewählt ist aus der Gruppe bestehend aus Kohlenmonoxid, Stickstoffmonoxid, Alkyl cyaniden, Arylcyaniden, Alkylisocyaniden, Arylisocyaniden, Aminen, Phosphinen, Phosphiten, Arsinen, Stibinen, stickstoffhaltigen Heterocyclen, Carbenen, Hydrid, Deuterid, den Halogeniden F–, Cl–, Br und I–, Alkylacetyliden, Arylacetyliden, Cyanid, Cyanat, Isocyanat, Thiocyanat, Isothiocyanat, aliphatischen oder aromatischen Alkoholaten, aliphatischen oder aromatischen Thioalkoholaten, Amiden, Carboxylaten oder Gruppen der folgenden Formeln (35) bis (61), wobei die verwendeten Symbole und Indizes die in Anspruch 1 und 3 genannten Bedeutungen haben, * die Position der Koordination an M andeutet und die durch (#) gekennzeichnete Position die Position angibt, an der L4, gegebenenfalls über -(Y)n-, an einen der Teilliganden L1, L2 oder L3 gebunden sein kann.
- Elektronische Vorrichtung nach einem oder mehreren der Ansprüche 1 bis 7, dadurch gekennzeichnet, dass für die verwendeten Symbole und Indizes gilt: L1 ist ausgewählt aus den oben genannten Gruppen gemäß den Formeln (3) bis (30) gemäß Anspruch 3; L2, L3 sind gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus -NR2, -NR–, -N=C(R1)2, -PR2, -PR(OR), P(OR)2, -S– und -SR oder L1; Y ist gleich oder verschieden bei jedem Auftreten eine bivalente Gruppe, ausgewählt aus CR2, BR, SiR2, NR, PR, P(O)R, O oder S; n ist gleich oder verschieden bei jedem Auftreten 0, 1 oder 2; V ist ausgewählt aus B, BR–, CR, CO–, SiR, N, NR+, P oder P(=O); oder V ist eine cyclische Gruppe gemäß einer der Formeln (31) bis (34) gemäß Anspruch 6; L4 ist ausgewählt aus der Gruppe bestehend aus Kohlenmonoxid, Stickstoffmonoxid, Alkylcyaniden, Arylcyaniden, Alkylisocyaniden, Arylisocyaniden, Aminen, Halogenphosphinen, Trialkylphosphinen, Triarylphosphinen, Alkylarylphosphine, Phosphiten, Arsinen, Stibinen, neutralen oder anionischen stickstoffhaltigen Heterocyclen, Carbenen, Hydrid, Deuterid, F–, Cl–, Br und I–, Alkylacetyliden, Arylacetyliden, Cyanid, Cyanat, Isocyanat, Thiocyanat, Isothiocyanat, aliphatischen oder aromatischen Alkoholaten, aliphatischen oder aromatischen Thioalkoholaten, Amiden, Carboxylaten oder Liganden der oben genannten Formeln (35) bis (61) gemäß Anspruch 7; b ist gleich 1; die weiteren verwendeten Symbole und Indizes haben die in Anspruch 1 genannten Bedeutungen.
- Elektronische Vorrichtung gemäß einem oder mehreren der Ansprüche 1 bis 9, ausgewählt aus der Gruppe bestehend aus organischen Elektrolumineszenzvorrichtungen (= organische Leuchtdioden, OLEDs, PLEDs), organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektrochemischen Zellen (LECs) und organischen Laserdioden (O-Laser).
- Organische Elektrolumineszenzvorrichtung nach einem oder mehreren der Ansprüche 1 bis 10, dadurch gekennzeichnet, dass die Verbindung gemäß Formel (1) als emittierende Verbindung in einer emittierenden Schicht eingesetzt wird.
- Organische Elektrolumineszenzvorrichtungnach Anspruch 11, dadurch gekennzeichnet, dass die Verbindung gemäß Formel (1) im Kombination mit einem oder mehreren Matrixmaterialien eingesetzt werden, welche ausgewählt sind aus der Gruppe bestehend aus Ketonen, Phosphinoxiden, Sulfoxiden, Sulfonen, Triarylaminen, Carbazolderivaten, Indolocarbazolderivaten, Indenocarbazolderivaten, Azacarbazolen, bipolaren Matrixmaterialien, Silanen, Azaborolen, Boronestern, Triazinderivaten, Zinkkomplexen, Diaza- oder Tetraazasilolderivate oder Diazaphospholderivate.
- Organische Elektrolumineszenzvorrichtung nach Anspruch 11 oder 12, dadurch gekennzeichnet, dass die Verbindung gemäß Formel (1) als Matrixmaterial für eine emittierende Verbindung in einer emittierenden Schicht eingesetzt wird und/oder als Lochblockiermaterial in einer Lochblockierschicht und/oder als Elektronentransportmaterial in einer Elektronentransportschicht und/oder als Lochtransportmaterial in einer Lochtransport- bzw. -injektionsschicht und/oder als Elektronenblockiermaterial in einer Elektronenblockierschicht.
- Verwendung einer Verbindung nach Anspruch 14 in einer elektronischen Vorrichtung.
- Verfahren zur Herstellung einer Verbindung nach Anspruch 14, dadurch gekennzeichnet, dass die entsprechenden freien Liganden mit Metallsalzen bzw. Metallkomplexen des entsprechenden Metalls M umgesetzt werden.
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102009057167A DE102009057167A1 (de) | 2009-12-05 | 2009-12-05 | Elektronische Vorrichtung enthaltend Metallkomplexe |
| US13/513,592 US9634268B2 (en) | 2009-12-05 | 2010-11-09 | Electronic device comprising metal complexes |
| CN201080055085.3A CN102648540B (zh) | 2009-12-05 | 2010-11-09 | 包含金属络合物的电子器件 |
| JP2012541333A JP5766712B2 (ja) | 2009-12-05 | 2010-11-09 | 金属錯体を含む電子素子 |
| KR1020127017578A KR20120091443A (ko) | 2009-12-05 | 2010-11-09 | 금속 착물을 포함하는 전자 소자 |
| DE112010004687T DE112010004687A5 (de) | 2009-12-05 | 2010-11-09 | Elektronische vorrichtung enthaltend metallkomplexe |
| PCT/EP2010/006821 WO2011066898A1 (de) | 2009-12-05 | 2010-11-09 | Elektronische vorrichtung enthaltend metallkomplexe |
| TW099141714A TW201137083A (en) | 2009-12-05 | 2010-12-01 | Electronic device comprising metal complexes |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102009057167A DE102009057167A1 (de) | 2009-12-05 | 2009-12-05 | Elektronische Vorrichtung enthaltend Metallkomplexe |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102009057167A1 true DE102009057167A1 (de) | 2011-06-09 |
Family
ID=43501416
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102009057167A Withdrawn DE102009057167A1 (de) | 2009-12-05 | 2009-12-05 | Elektronische Vorrichtung enthaltend Metallkomplexe |
| DE112010004687T Withdrawn DE112010004687A5 (de) | 2009-12-05 | 2010-11-09 | Elektronische vorrichtung enthaltend metallkomplexe |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE112010004687T Withdrawn DE112010004687A5 (de) | 2009-12-05 | 2010-11-09 | Elektronische vorrichtung enthaltend metallkomplexe |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9634268B2 (de) |
| JP (1) | JP5766712B2 (de) |
| KR (1) | KR20120091443A (de) |
| CN (1) | CN102648540B (de) |
| DE (2) | DE102009057167A1 (de) |
| TW (1) | TW201137083A (de) |
| WO (1) | WO2011066898A1 (de) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012143080A2 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9799840B2 (en) | 2011-10-17 | 2017-10-24 | Osram Oled Gmbh | Organic electronic component with dopant, use of a dopant and method for the production of the dopant |
Families Citing this family (184)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103228647B (zh) | 2010-11-24 | 2017-02-15 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| CN103619986B (zh) | 2011-06-03 | 2017-02-08 | 默克专利有限公司 | 有机电致发光器件 |
| CA2849087A1 (en) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazole derivatives for organic electroluminescent devices |
| EP2768808B1 (de) | 2011-10-20 | 2017-11-15 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US9231218B2 (en) * | 2012-07-10 | 2016-01-05 | Universal Display Corporation | Phosphorescent emitters containing dibenzo[1,4]azaborinine structure |
| CN104471020B (zh) | 2012-07-10 | 2017-03-08 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR102125199B1 (ko) | 2012-07-23 | 2020-06-22 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| DE102012020167A1 (de) * | 2012-10-13 | 2014-04-17 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| DE102012021650A1 (de) | 2012-11-03 | 2014-05-08 | Eberhard Karls Universität Tübingen | Metallkomplexe |
| JP2016516731A (ja) * | 2013-03-16 | 2016-06-09 | メルク パテント ゲーエムベーハー | 金属錯体 |
| DE102013215342B4 (de) * | 2013-08-05 | 2023-05-04 | Novaled Gmbh | Verfahren zur Herstellung organisch phosphoreszenter Schichten unter Zusatz schwerer Hauptgruppenmetallkomplexe, damit hergestellte Schicht, deren Verwendung und organisches Halbleiterbauelement diese umfassend |
| EP3140302B1 (de) | 2014-05-05 | 2019-08-21 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102014114224A1 (de) | 2014-09-30 | 2016-03-31 | Osram Oled Gmbh | Organisches elektronisches Bauteil, Verwendung eines Zinkkomplexes als p-Dotierungsmittel für organische elektronische Matrixmaterialien |
| EP3204463B1 (de) | 2014-10-08 | 2019-04-17 | cynora GmbH | Metall-komplexe mit tridentaten liganden für optoelektronische anwendungen |
| RS61013B1 (sr) | 2014-10-24 | 2020-11-30 | Landos Biopharma Inc | Terapeutski preparati zasnovani na lantionin sintetazi c- sličnom proteinu-2 |
| JP6862420B2 (ja) | 2015-08-13 | 2021-04-21 | メルク パテント ゲーエムベーハー | ヘキサメチルインダン |
| JP6044695B2 (ja) * | 2015-11-16 | 2016-12-14 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それが具備された表示装置及び照明装置 |
| KR102851400B1 (ko) | 2016-03-03 | 2025-08-29 | 메르크 파텐트 게엠베하 | 유기 전계 발광 장치용 재료 |
| TWI745361B (zh) | 2016-03-17 | 2021-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| CN108884087A (zh) | 2016-04-11 | 2018-11-23 | 默克专利有限公司 | 包含二苯并呋喃和/或二苯并噻吩结构的杂环化合物 |
| WO2017186760A1 (en) | 2016-04-29 | 2017-11-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP7039549B2 (ja) | 2016-07-14 | 2022-03-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 金属錯体 |
| US11447464B2 (en) | 2016-09-14 | 2022-09-20 | Merck Patent Gmbh | Compounds with spirobifluorene-structures |
| TW201827425A (zh) | 2016-09-14 | 2018-08-01 | 德商麥克專利有限公司 | 具有咔唑結構之化合物 |
| US20200028091A1 (en) | 2016-09-30 | 2020-01-23 | Merck Patent Gmbh | Carbazoles with diazadibenzofurane or diazadibenzothiophene structures |
| TWI766884B (zh) | 2016-09-30 | 2022-06-11 | 德商麥克專利有限公司 | 具有二氮雜二苯并呋喃或二氮雜二苯并噻吩結構的化合物、其製法及其用途 |
| US11345687B2 (en) | 2016-11-09 | 2022-05-31 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TWI756292B (zh) | 2016-11-14 | 2022-03-01 | 德商麥克專利有限公司 | 具有受體基團與供體基團之化合物 |
| EP3541890B1 (de) | 2016-11-17 | 2020-10-28 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| TW201829385A (zh) | 2016-11-30 | 2018-08-16 | 德商麥克專利有限公司 | 具有戊內醯胺結構之化合物 |
| KR20190086028A (ko) | 2016-12-05 | 2019-07-19 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| EP3548486B1 (de) | 2016-12-05 | 2021-10-27 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| TW201831468A (zh) | 2016-12-05 | 2018-09-01 | 德商麥克專利有限公司 | 含氮的雜環化合物 |
| KR102504432B1 (ko) | 2016-12-22 | 2023-02-27 | 메르크 파텐트 게엠베하 | 적어도 2종의 유기-기능성 화합물을 포함하는 혼합물 |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| TW201833300A (zh) | 2017-01-25 | 2018-09-16 | 德商麥克專利有限公司 | 咔唑衍生物 |
| US11407766B2 (en) | 2017-01-30 | 2022-08-09 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TW201835075A (zh) | 2017-02-14 | 2018-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| TW201843143A (zh) | 2017-03-13 | 2018-12-16 | 德商麥克專利有限公司 | 含有芳基胺結構之化合物 |
| JP7155142B2 (ja) | 2017-03-15 | 2022-10-18 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス用の材料 |
| KR102395784B1 (ko) | 2017-03-27 | 2022-05-10 | 삼성전자주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| WO2018189134A1 (de) | 2017-04-13 | 2018-10-18 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| EP3621970B1 (de) | 2017-05-11 | 2021-01-13 | Merck Patent GmbH | Bororganische komplexe für organische elektrolumineszente vorrichtungen |
| KR102592390B1 (ko) | 2017-05-11 | 2023-10-20 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 카르바졸계 바디피스 |
| US11767299B2 (en) | 2017-06-23 | 2023-09-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN110785415A (zh) | 2017-07-05 | 2020-02-11 | 默克专利有限公司 | 用于有机电子器件的组合物 |
| WO2019007867A1 (de) | 2017-07-05 | 2019-01-10 | Merck Patent Gmbh | Zusammensetzung für organische elektronische vorrichtungen |
| CN111065640B (zh) | 2017-09-12 | 2023-04-18 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR102671945B1 (ko) | 2017-10-06 | 2024-06-03 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| KR102653073B1 (ko) | 2017-10-24 | 2024-03-29 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| TWI785142B (zh) | 2017-11-14 | 2022-12-01 | 德商麥克專利有限公司 | 用於有機電子裝置之組成物 |
| CA3083442A1 (en) | 2017-11-30 | 2019-06-06 | Landos Biopharma, Inc. | Therapies with lanthionine c-like protein 2 ligands and cells prepared therewith |
| TW201938562A (zh) | 2017-12-19 | 2019-10-01 | 德商麥克專利有限公司 | 雜環化合物 |
| TWI811290B (zh) | 2018-01-25 | 2023-08-11 | 德商麥克專利有限公司 | 用於有機電致發光裝置的材料 |
| US20210020843A1 (en) | 2018-03-16 | 2021-01-21 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3802520A1 (de) | 2018-05-30 | 2021-04-14 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| JP7322075B2 (ja) | 2018-06-07 | 2023-08-07 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンスデバイス |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3823958B1 (de) | 2018-07-20 | 2023-08-23 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| JP7459065B2 (ja) | 2018-09-12 | 2024-04-01 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンスデバイス用の材料 |
| TWI826522B (zh) | 2018-09-12 | 2023-12-21 | 德商麥克專利有限公司 | 電致發光裝置 |
| TW202030902A (zh) | 2018-09-12 | 2020-08-16 | 德商麥克專利有限公司 | 電致發光裝置 |
| WO2020064662A2 (de) | 2018-09-27 | 2020-04-02 | Merck Patent Gmbh | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| US12178124B2 (en) | 2018-09-27 | 2024-12-24 | Merck Kgaa | Compounds that can be used in an organic electronic device as active compounds |
| EP3877369A1 (de) | 2018-11-05 | 2021-09-15 | Merck Patent GmbH | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| KR20210089205A (ko) | 2018-11-06 | 2021-07-15 | 메르크 파텐트 게엠베하 | Oled 용 유기 전계 발광 재료로서 5,6-디페닐-5,6-디히드로디벤즈[c,e][1,2]아자포스포린 및 6-페닐-6h-디벤조[c,e][1,2]티아진-5,5-디옥사이드 유도체 및 유사한 화합물 |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| CN113195500B (zh) | 2018-11-15 | 2024-05-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| TW202039493A (zh) | 2018-12-19 | 2020-11-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| KR102853461B1 (ko) | 2019-01-16 | 2025-09-02 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| TW202035345A (zh) | 2019-01-17 | 2020-10-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| US20230080974A1 (en) | 2019-02-18 | 2023-03-16 | Merck Patent Gmbh | Composition for organic electronic devices |
| JP2022521096A (ja) * | 2019-02-22 | 2022-04-05 | マトリックス センサーズ,インコーポレイテッド | 配向性冷光エミッタを有する結晶質フィルムおよび発光デバイス |
| US20220127286A1 (en) | 2019-03-04 | 2022-04-28 | Merck Patent Gmbh | Ligands for nano-sized materials |
| US20220162205A1 (en) | 2019-03-12 | 2022-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20210141593A (ko) | 2019-03-20 | 2021-11-23 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021013775A1 (de) | 2019-07-22 | 2021-01-28 | Merck Patent Gmbh | Verfahren zur herstellung ortho-metallierter metallverbindungen |
| CN114222738B (zh) | 2019-08-26 | 2024-05-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| US12108665B2 (en) | 2019-09-02 | 2024-10-01 | Merck Kgaa | Materials for organic electroluminescent devices |
| TW202122558A (zh) | 2019-09-03 | 2021-06-16 | 德商麥克專利有限公司 | 用於有機電致發光裝置之材料 |
| EP4031546A1 (de) | 2019-09-16 | 2022-07-27 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| CN114342103B (zh) | 2019-09-19 | 2025-12-23 | 默克专利有限公司 | 两种主体材料的混合物和包含所述混合物的有机电致发光器件 |
| CN114401945A (zh) | 2019-09-20 | 2022-04-26 | 默克专利有限公司 | 作为用于电子器件的材料的迫位缩合杂环化合物 |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| TW202130783A (zh) | 2019-11-04 | 2021-08-16 | 德商麥克專利有限公司 | 有機電致發光裝置 |
| CN114641482A (zh) | 2019-11-04 | 2022-06-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| TW202134252A (zh) | 2019-11-12 | 2021-09-16 | 德商麥克專利有限公司 | 有機電致發光裝置用材料 |
| TW202136181A (zh) | 2019-12-04 | 2021-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置用的材料 |
| TW202136471A (zh) | 2019-12-17 | 2021-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置用的材料 |
| JP7620631B2 (ja) | 2019-12-18 | 2025-01-23 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のための芳香族化合物 |
| KR20220116008A (ko) | 2019-12-19 | 2022-08-19 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 다환 화합물 |
| CA3135502C (en) | 2019-12-20 | 2024-01-09 | Josep Bassaganya-Riera | Lanthionine c-like protein 2 ligands, cells prepared therewith, and therapies using same |
| US12234578B2 (en) | 2020-01-29 | 2025-02-25 | Wisconsin Alumni Research Foundation | Tannin composite fibers |
| CN115052865A (zh) | 2020-01-29 | 2022-09-13 | 默克专利有限公司 | 苯并咪唑衍生物 |
| EP4110884B1 (de) | 2020-02-25 | 2024-11-20 | Merck Patent GmbH | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| TW202146625A (zh) | 2020-03-11 | 2021-12-16 | 德商麥克專利有限公司 | 有機電致發光裝置 |
| KR20220151192A (ko) | 2020-03-11 | 2022-11-14 | 메르크 파텐트 게엠베하 | 유기 전계 발광 장치 |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20220154751A (ko) | 2020-03-17 | 2022-11-22 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| EP4126884B1 (de) | 2020-03-23 | 2025-07-09 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20220158017A (ko) | 2020-03-24 | 2022-11-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| US20230157171A1 (en) | 2020-03-26 | 2023-05-18 | Merck Patent Gmbh | Cyclic compounds for organic electroluminescent devices |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US20230183269A1 (en) | 2020-04-06 | 2023-06-15 | Merck Patent Gmbh | Polycyclic compounds for organic electroluminescent devices |
| US20230255106A1 (en) | 2020-05-29 | 2023-08-10 | Merck Patent Gmbh | Organic electroluminescent apparatus |
| US20230234937A1 (en) | 2020-06-18 | 2023-07-27 | Merck Patent Gmbh | Indenoazanaphthalenes |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| CN115916794A (zh) | 2020-06-29 | 2023-04-04 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| JP2023531470A (ja) | 2020-06-29 | 2023-07-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のためのヘテロ芳香族化合物 |
| EP4192832A1 (de) | 2020-08-06 | 2023-06-14 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| EP4196486B1 (de) | 2020-08-13 | 2025-07-09 | UDC Ireland Limited | Metallkomplexe |
| US12433160B2 (en) | 2020-08-18 | 2025-09-30 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4200289A1 (de) | 2020-08-19 | 2023-06-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US20240101552A1 (en) | 2020-09-18 | 2024-03-28 | Shanghai Pharmaceuticals Holding Co., Ltd. | Carbonyl heterocyclic compound and application thereof |
| TW202229215A (zh) | 2020-09-30 | 2022-08-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置功能層之結構化的化合物 |
| TW202222748A (zh) | 2020-09-30 | 2022-06-16 | 德商麥克專利有限公司 | 用於結構化有機電致發光裝置的功能層之化合物 |
| EP4229145B1 (de) | 2020-10-16 | 2025-07-23 | Merck Patent GmbH | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| US20230389423A1 (en) | 2020-10-16 | 2023-11-30 | Merck Patent Gmbh | Heterocyclic compounds for organic electroluminescent devices |
| CN112209916B (zh) * | 2020-10-23 | 2021-06-01 | 河北师范大学 | 一种钌配合物、制备方法和催化用途 |
| EP4244228A1 (de) | 2020-11-10 | 2023-09-20 | Merck Patent GmbH | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20230116023A (ko) | 2020-12-02 | 2023-08-03 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 복소환 화합물 |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20230122094A (ko) | 2020-12-18 | 2023-08-22 | 메르크 파텐트 게엠베하 | Oled에 사용하기 위한 청색 형광 방출체로서의 인돌로[3.2.1-jk]카르바졸-6-카르보니트릴유도체 |
| US20240124769A1 (en) | 2020-12-18 | 2024-04-18 | Merck Patent Gmbh | Nitrogenous compounds for organic electroluminescent devices |
| EP4263746B1 (de) | 2020-12-18 | 2025-10-01 | Merck Patent GmbH | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| EP4274827A1 (de) | 2021-01-05 | 2023-11-15 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| US20240188429A1 (en) | 2021-03-02 | 2024-06-06 | Merck Patent Gmbh | Compounds for organic electroluminescent devices |
| KR20230158657A (ko) | 2021-03-18 | 2023-11-21 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 헤테로방향족 화합물 |
| CN117279902A (zh) | 2021-04-29 | 2023-12-22 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR20240005782A (ko) | 2021-04-29 | 2024-01-12 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 재료 |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| CN117355364A (zh) | 2021-05-21 | 2024-01-05 | 默克专利有限公司 | 用于连续纯化至少一种功能材料的方法和用于连续纯化至少一种功能材料的装置 |
| DE112022003409A5 (de) | 2021-07-06 | 2024-05-23 | MERCK Patent Gesellschaft mit beschränkter Haftung | Materialien für organische elektrolumineszenzvorrichtungen |
| CN117917983A (zh) | 2021-09-13 | 2024-04-23 | 默克专利有限公司 | 有机电致发光器件的材料 |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| KR20240075872A (ko) | 2021-09-28 | 2024-05-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR20240075888A (ko) | 2021-09-28 | 2024-05-29 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| CN118159623A (zh) | 2021-10-27 | 2024-06-07 | 默克专利有限公司 | 用于有机电致发光器件的含硼和氮的杂环化合物 |
| EP4437814A1 (de) | 2021-11-25 | 2024-10-02 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| EP4448527A1 (de) | 2021-12-13 | 2024-10-23 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20240128020A (ko) | 2021-12-21 | 2024-08-23 | 메르크 파텐트 게엠베하 | 중수소화 유기 화합물의 제조 방법 |
| US20250163035A1 (en) | 2022-02-09 | 2025-05-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| US20250160204A1 (en) | 2022-02-14 | 2025-05-15 | Merck Patent Gmbh | Materials for electronic devices |
| CN118696106A (zh) | 2022-02-23 | 2024-09-24 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| EP4482843A1 (de) | 2022-02-23 | 2025-01-01 | Merck Patent GmbH | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| EP4519383B1 (de) | 2022-05-06 | 2026-01-14 | Merck Patent GmbH | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4526279A1 (de) | 2022-05-18 | 2025-03-26 | Merck Patent GmbH | Verfahren zur herstellung von deuterierten organischen verbindungen |
| EP4544888A1 (de) | 2022-06-24 | 2025-04-30 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| EP4544889A1 (de) | 2022-06-24 | 2025-04-30 | Merck Patent GmbH | Zusammensetzung für organische elektronische vorrichtungen |
| KR20250037489A (ko) | 2022-07-11 | 2025-03-17 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| WO2024033282A1 (en) | 2022-08-09 | 2024-02-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN119894856A (zh) | 2022-09-22 | 2025-04-25 | 默克专利有限公司 | 用于有机电致发光器件的含氮化合物 |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120152954A (zh) | 2022-11-01 | 2025-06-13 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| WO2024105066A1 (en) | 2022-11-17 | 2024-05-23 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| TW202438505A (zh) | 2022-12-19 | 2024-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置之材料 |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN120569385A (zh) | 2023-01-17 | 2025-08-29 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| EP4683925A1 (de) | 2023-03-20 | 2026-01-28 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
Citations (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009014513A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100937900B1 (ko) * | 2001-08-29 | 2010-01-21 | 유니버시티 오브 서던 캘리포니아 | 금속착물을 포함하는 캐리어수송층을 구비한 유기발광장치 |
| DE10310887A1 (de) * | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| DE102004046665A1 (de) * | 2004-09-24 | 2006-07-27 | Basf Ag | Verwendung von Kupfer(I)-Komplexen in organischen lichtemittierenden Dioden |
| US20060073360A1 (en) * | 2004-09-28 | 2006-04-06 | Fuji Photo Film Co., Ltd. | Organic electroluminescent device |
| JP5080729B2 (ja) * | 2004-09-28 | 2012-11-21 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP2006310479A (ja) * | 2005-04-27 | 2006-11-09 | Fuji Photo Film Co Ltd | 有機電界発光素子 |
| DE102008015526B4 (de) * | 2008-03-25 | 2021-11-11 | Merck Patent Gmbh | Metallkomplexe |
| KR20110097612A (ko) | 2008-11-11 | 2011-08-31 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자 |
-
2009
- 2009-12-05 DE DE102009057167A patent/DE102009057167A1/de not_active Withdrawn
-
2010
- 2010-11-09 DE DE112010004687T patent/DE112010004687A5/de not_active Withdrawn
- 2010-11-09 CN CN201080055085.3A patent/CN102648540B/zh not_active Expired - Fee Related
- 2010-11-09 WO PCT/EP2010/006821 patent/WO2011066898A1/de not_active Ceased
- 2010-11-09 JP JP2012541333A patent/JP5766712B2/ja not_active Expired - Fee Related
- 2010-11-09 US US13/513,592 patent/US9634268B2/en active Active
- 2010-11-09 KR KR1020127017578A patent/KR20120091443A/ko not_active Ceased
- 2010-12-01 TW TW099141714A patent/TW201137083A/zh unknown
Patent Citations (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004037887A2 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005039246A1 (ja) | 2003-09-30 | 2005-04-28 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、照明装置、表示装置 |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009014513A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
Non-Patent Citations (2)
| Title |
|---|
| M. A. Baldo et al., Appl. Phys. Lett. 1999, 75, 4- 6 |
| M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012143080A2 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US9799840B2 (en) | 2011-10-17 | 2017-10-24 | Osram Oled Gmbh | Organic electronic component with dopant, use of a dopant and method for the production of the dopant |
| US10158092B2 (en) | 2011-10-17 | 2018-12-18 | Osram Oled Gmbh | Organic electronic component with dopant, use of a dopant and method for the production of the dopant |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102648540B (zh) | 2016-03-16 |
| KR20120091443A (ko) | 2012-08-17 |
| JP5766712B2 (ja) | 2015-08-19 |
| US9634268B2 (en) | 2017-04-25 |
| US20120286254A1 (en) | 2012-11-15 |
| DE112010004687A5 (de) | 2012-09-20 |
| JP2013513225A (ja) | 2013-04-18 |
| CN102648540A (zh) | 2012-08-22 |
| TW201137083A (en) | 2011-11-01 |
| WO2011066898A1 (de) | 2011-06-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE102008015526B4 (de) | Metallkomplexe | |
| DE102009057167A1 (de) | Elektronische Vorrichtung enthaltend Metallkomplexe | |
| EP2742054B1 (de) | Metallkomplexe | |
| EP2344609B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP2294160B1 (de) | Elektronische vorrichtung enthaltend metallkomplexe | |
| DE112011102366B4 (de) | Metallkomplexe | |
| DE102008057051B4 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| DE102008057050B4 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP2344607B1 (de) | Organische elektrolumineszenzvorrichtungen | |
| EP2726490B1 (de) | Metallkomplexe | |
| DE102009053645A1 (de) | Materialien für organische Elektrolumineszenzvorrichtung | |
| DE102010012738A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP2714704A1 (de) | Metallkomplexe | |
| DE102009022858A1 (de) | Organische Elektrolumineszenzvorrichtungen | |
| DE102009048791A1 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| WO2010099852A1 (de) | Metallkomplexe mit azaborol-liganden und elektronische vorrichtung damit | |
| DE102007002714A1 (de) | Neue Materialien für organische Elektrolumineszenzvorrichtungen | |
| DE102010019306A1 (de) | Organische Elektrolumineszenzvorrichtungen | |
| WO2011160757A1 (de) | Materialien für elektronische vorrichtungen | |
| DE102012000064B4 (de) | Materialien für organische Elektrolumineszenzvorrichtungen | |
| EP2828266A1 (de) | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen | |
| DE102012020167A1 (de) | Metallkomplexe | |
| WO2022029096A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| R118 | Application deemed withdrawn due to claim for domestic priority |
Effective date: 20120605 |