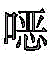CN110785415A - 用于有机电子器件的组合物 - Google Patents
用于有机电子器件的组合物 Download PDFInfo
- Publication number
- CN110785415A CN110785415A CN201880039441.9A CN201880039441A CN110785415A CN 110785415 A CN110785415 A CN 110785415A CN 201880039441 A CN201880039441 A CN 201880039441A CN 110785415 A CN110785415 A CN 110785415A
- Authority
- CN
- China
- Prior art keywords
- atoms
- aromatic
- groups
- organic
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/06—Peri-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/06—Peri-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/90—Multiple hosts in the emissive layer
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
- H10K2102/10—Transparent electrodes, e.g. using graphene
- H10K2102/101—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO]
- H10K2102/103—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO] comprising indium oxides, e.g. ITO
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
- H10K71/12—Deposition of organic active material using liquid deposition, e.g. spin coating
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
- H10K71/16—Deposition of organic active material using physical vapour deposition [PVD], e.g. vacuum deposition or sputtering
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Manufacturing & Machinery (AREA)
- Plural Heterocyclic Compounds (AREA)
- Electroluminescent Light Sources (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Photovoltaic Devices (AREA)
- Indole Compounds (AREA)
- Electrodes Of Semiconductors (AREA)
- Thin Film Transistor (AREA)
Abstract
本发明涉及一种包含电子传输主体和空穴传输主体的组合物,涉及其在电子器件中的用途以及包含所述组合物的电子器件。所述电子传输主体最优选选自三嗪‑二苯并呋喃‑咔唑体系的类别或三嗪‑二苯并噻吩‑咔唑体系的类别。所述空穴传输主体优选选自联咔唑类别。
Description
技术领域
本发明涉及一种包含电子传输主体和空穴传输主体的组合物,涉及其在电子器件中的用途以及包含所述组合物的电子器件。电子传输主体特别优选选自三嗪-二苯并呋喃-咔唑体系的类别或三嗪-二苯并噻吩-咔唑体系的类别。空穴传输主体优选选自联咔唑类别。
背景技术
例如在US 4539507、US 5151629、EP 0676461和WO 98/27136中描述了其中将有机半导体用作功能材料的有机电致发光器件(例如,OLED-有机发光二极管,或OLEC-有机发光电化学电池)的结构。除荧光发光体之外,在此采用的发光材料越来越多地是表现出磷光而不是荧光的有机金属络合物(M.A.Baldo等,Appl.Phys.Lett.1999,75,4~6)。由于量子力学的原因,使用有机金属化合物作为磷光发光体,能量和功率效率可以增加高达四倍。然而,一般而言,在OLED的情况下,特别是在表现出三重态发光(磷光)的OLED的情况下,仍然需要例如在效率、工作电压和寿命方面进行改善。
有机电致发光器件的性质不仅仅由所使用的发光体决定。在此同样特别重要的是所使用的其它材料,诸如主体和基质材料、空穴阻挡材料、电子传输材料、空穴传输材料以及电子或激子阻挡材料,并且其中特别重要的是主体或基质材料。这些材料的改善可以引起电致发光器件的显著改善。
用于有机电子器件中的主体材料是本领域技术人员众所周知的。术语基质材料在现有技术中经常也用于指磷光发光体用主体材料。所述术语的这种使用也适用于本发明。同时,已经开发出用于荧光电子器件和磷光电子器件两者的多种主体材料。
根据现有技术,尤其使用酮(例如,根据WO 2004/093207或WO 2010/006680)或氧化膦(例如,根据WO 2005/003253)作为磷光发光体用基质材料。根据现有技术的另外的基质材料是三嗪(例如,WO 2008/056746、EP 0906947、EP 0908787、EP 0906948)和内酰胺(例如,WO 2011/116865或WO 2011/137951)。另外,根据现有技术尤其使用咔唑衍生物(例如,根据WO 2005/039246、US 2005/0069729或WO 2014/015931)、吲哚并咔唑衍生物(例如,根据WO 2007/063754或WO 2008/056746)或茚并咔唑衍生物(例如,根据WO 2010/136109或WO2011/000455),特别是被缺电子的杂芳族基团取代的那些,诸如三嗪,作为磷光发光体用基质材料。WO 2011/057706公开了咔唑衍生物,其被两个三苯基三嗪基团取代。WO 2011/046182公开了咔唑-芳亚基-三嗪衍生物,其在三嗪上被芴基基团取代。WO 2009/069442公开了作为主体材料的三环化合物,诸如咔唑、二苯并呋喃或二苯并噻吩,其被缺电子的杂芳族基团(例如,吡啶、嘧啶或三嗪)高程度取代。WO 2011/057706、WO 2015/014434和WO2015/169412公开了另外的主体材料,这些主体材料尤其包括三嗪-二苯并呋喃-咔唑衍生物和三嗪-二苯并噻吩-咔唑衍生物,其中所述三嗪通过连接基的方式任选地与二苯并呋喃或二苯并噻吩键合。
用于改善电子器件,特别是有机电致发光器件的性能数据的另一可行性在于使用两种或更多种材料,特别是主体材料或基质材料的组合物。
US 6,392,250B1公开了在OLED的发光层中使用由电子传输材料、空穴传输材料和荧光发光体组成的混合物。与现有技术相比,借助于这种混合物,可以改善OLED的寿命。
US 6,803,720B1公开了在OLED的发光层中使用包含磷光发光体和空穴传输材料以及电子传输材料的混合物。空穴传输材料和电子传输材料都是有机小分子。
US 9,601,698公开了在OLED的发光层中使用两种主体材料和磷光发光体的混合物,例如吡啶-咔唑-二苯并噻吩衍生物与三芳基氨基取代的联咔唑的混合物。
根据WO 2015/156587,特定的咔唑衍生物与联咔唑的混合物可以用作主体材料。
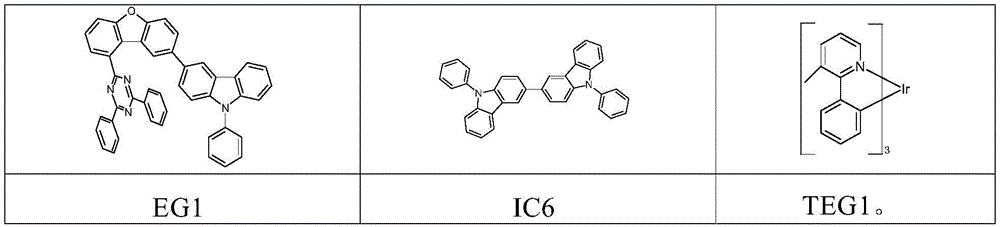
根据WO 2015/169412,例如,三嗪-二苯并呋喃-咔唑衍生物和三嗪-二苯并噻吩-咔唑衍生物同样可以混合物形式使用。因此,例如描述了名称为E34的OLED的制造,其在发光层中包含主体材料EG1、IC6和磷光发光体TEG1。所用化合物的结构如下所示:
专利KR101744248B1描述了器件中两个发光层的特定顺序,其中每个发光层包含两种主体材料。第一发光层包含主体1-1和主体1-2。第二发光层包含主体2-1和主体2-2,其中主体1-2和主体2-1是相同的材料。权利要求7描述了具体的1-2主体材料。权利要求10描述了以上缩写为EG1的化合物作为2-2主体材料。
根据在本申请的优先权日之后公开的专利申请KR20170113320,可以将在文献H-6中提到的以上缩写为EG1的化合物与二(1,3-联苯)-取代的联咔唑混合在一起使用。所述文献中将相应的联咔唑(3-(9'-1,3-联苯-9H-咔唑-3'-基)-9-(1,3-联苯)-9H-咔唑)称为H-2。
然而,特别是在有机电子器件的寿命方面,关于这些材料的使用或关于这些材料的混合物的使用,仍然需要改善。
发明内容
因此,本发明的目的是提供以下材料:所述材料适用于有机电子器件中,特别是有机电致发光器件中,并且特别是荧光或磷光OLED中,并且导致特别是关于改善的寿命的良好器件性质,以及提供相应的电子器件。
此时已经发现,如下的组合物实现了该目的并且克服了现有技术的缺点,所述组合物包含式(1)的化合物,例如特别优选三嗪-二苯并呋喃-咔唑衍生物或三嗪-二苯并噻吩-咔唑衍生物,和式(2)的空穴传输主体,优选联咔唑。这种类型的组合物导致有机电子器件,特别是有机电致发光器件的非常好的性质,特别是在寿命方面情况如此,并且特别是在发光层中存在浓度为2重量%与15重量%之间的发光组分的情况下导致非常好的性质。
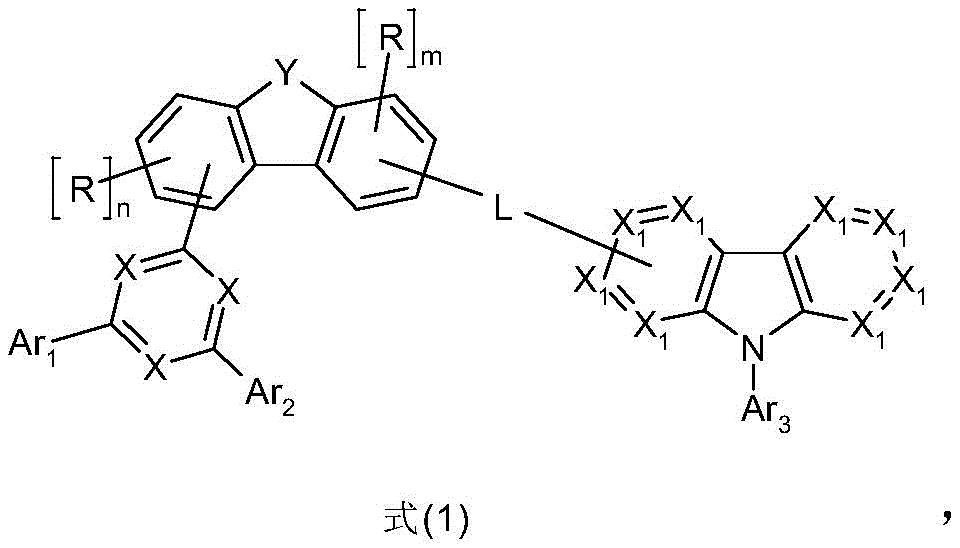
因此,本发明首先涉及一种包含至少一种式(1)的化合物和至少一种式(2)的化合物的组合物
其中以下适用于所使用的符号和标记:
X在每次出现时相同或不同地是CR0或N,条件是至少一个基团X代表N;
X1在每次出现时相同或不同地是CR或N;
X2在每次出现时相同或不同地是CR1或N;
Y选自O或S;
L在每次出现时相同或不同地是单键或具有5至30个芳族环原子的芳族或杂芳族环系,其可以被一个或多个基团R3取代,优选具有6至18个C原子的芳族或杂芳族环系,其可以被一个或多个基团R3取代;
Ar1、Ar2在每种情况下在每次出现时彼此独立地是具有5至40个芳族环原子的芳基或杂芳基基团,其可以被一个或多个基团R3取代;
Ar3是具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代;
Ar4和Ar5在每种情况下彼此独立地是具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不能同时为苯基;
R0、R、R1在每次出现时相同或不同地选自H,D,F,Cl,Br,I,CN,NO2,N(Ar)2,N(R2)2,C(=O)Ar,C(=O)R2,P(=O)(Ar)2,P(Ar)2,B(Ar)2,Si(Ar)3,Si(R2)3,具有1至20个C原子的直链的烷基、烷氧基或硫代烷基基团,或具有3至20个C原子的支链或环状的烷基、烷氧基或硫代烷基基团,或具有2至20个C原子的烯基基团,其在每种情况下可以被一个或多个基团R2取代,其中一个或多个不相邻的CH2基团可以被R2C=CR2、Si(R2)2、C=O、C=S、C=NR2、P(=O)(R2)、SO、SO2、NR2、O、S或CONR2替换,并且其中一个或多个H原子可以被D、F、Cl、Br、I、CN或NO2替换,具有5至40个芳族环原子的芳族或杂芳族环系,其在每种情况下可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳氧基或杂芳氧基基团,其可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳烷基或杂芳烷基基团,其可以被一个或多个R2取代;键合到同一碳原子或相邻碳原子的两个取代基R0和/或R和/或R1可以任选地形成可以被一个或多个基团R2取代的单环或多环的脂族、芳族或杂芳族环系;
R2在每次出现时相同或不同地选自H,D,F,Cl,Br,I,CN,NO2,N(Ar)2,NH2,N(R3)2,C(=O)Ar,C(=O)H,C(=O)R3,P(=O)(Ar)2,具有1至40个C原子的直链的烷基、烷氧基或硫代烷基基团,或具有3至40个C原子的支链或环状的烷基、烷氧基或硫代烷基基团,或具有2至40个C原子的烯基或炔基基团,其在每种情况下可以被一个或多个基团R3取代,其中一个或多个不相邻的CH2基团可以被HC=CH、R3C=CR3、C≡C、Si(R3)2、Ge(R3)2、Sn(R3)2、C=O、C=S、C=Se、C=NR3、P(=O)(R3)、SO、SO2、NH、NR3、O、S、CONH或CONR3替换,并且其中一个或多个H原子可以被D、F、Cl、Br、I、CN或NO2替换,具有5至60个芳族环原子的芳族或杂芳族环系,其在每种情况下可以被一个或多个基团R3取代,或具有5至60个芳族环原子的芳氧基或杂芳氧基基团,其可以被一个或多个基团R3取代,或这些体系的组合,其中两个或更多个相邻取代基R2可以任选地形成可以被一个或多个基团R3取代的单环或多环的脂族、芳族或杂芳族环系;
R3在每种情况下相同或不同地选自H,D,F,CN,具有1至20个C原子的脂族烃基或具有5至30个芳族环原子的芳族或杂芳族环系,其中一个或多个H原子可以被D、F、Cl、Br、I或CN替换且其可以被一个或多个各自具有1至4个碳原子的烷基基团取代;两个或更多个相邻取代基R3可以彼此形成单或多环的脂族环系;
Ar在每次出现时相同或不同地是具有5至30个芳族环原子的芳族或杂芳族环系,其可以被一个或多个非芳族的基团R3取代;与同一N原子、P原子或B原子键合的两个基团Ar也可以通过单键或选自N(R3)、C(R3)2、O或S的桥连基彼此桥连;并且
n和m彼此独立地表示0、1、2或3。
根据本发明,L优选是具有6至18个C原子的芳族或杂芳族环系,其可以被一个或多个基团R3取代。具有6至18个C原子的芳族或杂芳族环系优选是选自如下所述的L-1至L-40的连接基,其可以被一个或多个基团R3取代。根据本发明,L特别优选是具有6至18个C原子的芳族环系,其可以被一个或多个基团R3取代,非常特别优选选自苯亚基、萘亚基、联二苯叉、菲亚基或联三苯叉亚基,其中与其它取代基的键合不受限制。具有6至18个C原子的芳族环系优选为苯亚基,其中与其它取代基的键合不受限制。在此,苯亚基可以在邻、间或对位与二苯并呋喃/二苯并噻吩单元和咔唑单元连接。作为苯亚基的L优选在间位连接。
本发明另外涉及包含此类组合物的制剂,涉及这些组合物在有机电子器件中的用途,涉及包含此类组合物并且优选在一个层中包含所述组合物的有机电子器件,优选电致发光器件,以及涉及制造此类器件的方法。如下所述,本发明同样涉及相应的优选实施方式。通过对已知材料的具体选择,特别是涉及对式(1)的电子传导材料和式(2)的空穴传输材料的选择,实现了令人惊讶且有利的效果。
如上所述或优选如下所述,包括包含至少一种式(1)的化合物和至少一种式(2)的化合物的组合物的层特别是发光层(EML)、电子传输层(ETL)、电子注入层(EIL)和/或空穴阻挡层(HBL)。
在发光层的情况下,这优选是磷光层,其特征在于,如上所述,除了包含式(1)和式(2)的基质材料的组合物之外,其还包含磷光发光体。
在本发明的意义上,相邻的碳原子是彼此直接连接的碳原子。
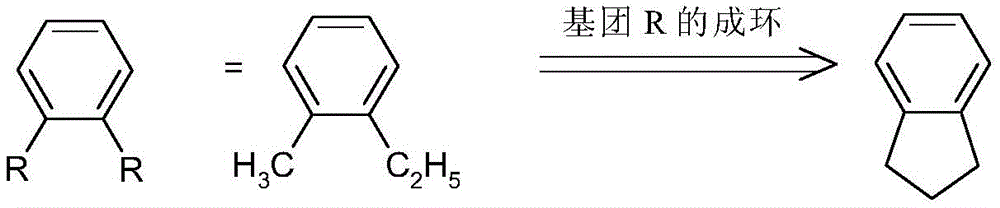
出于本说明书的目的,两个或更多个基团可以彼此形成环的表述旨在用以特别指这两个基团通过化学键彼此连接,形式上消除了两个氢原子。这通过以下方案说明:
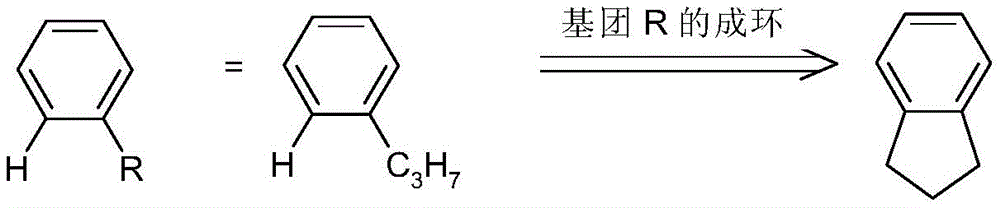
另外,然而,上述表述也旨在用以指在这两个基团中的一个代表氢的情况下,第二个基团在与氢原子键合的位置键合,从而形成环。
这旨在通过以下方案说明:
在本发明的意义上,芳基基团含有6至40个芳族环原子,优选C原子。在本发明的意义上,杂芳基基团含有5至40个碳原子;其中所述环原子包括C原子和至少一个杂原子,条件是C原子和杂原子的总和为至少5。杂原子优选选自N、O和/或S。在此,芳基基团或杂芳基基团是简单的芳族环,即苯基、衍生自苯的芳族环,或简单的杂芳族环,例如衍生自吡啶、嘧啶或噻吩的杂芳族环,或稠合的芳基或杂芳基基团,例如衍生自萘、蒽、菲、喹啉或异喹啉的基团。因此,具有6至10个C原子的芳基基团优选为苯基或萘基,其中作为取代基的芳基基团的键合不受限制。因此,具有6至10个C原子的芳亚基基团优选为苯亚基或萘亚基,其中芳亚基基团作为连接基的连接不受限制。
在本发明的意义上,芳族环系在环系中含有6至40个C原子,并且可以被一个或多个基团R3取代,其中R3具有下述含义。如上所述,芳族环系还包含芳基基团。
在本发明的意义上,杂芳族环系包含5至40个环原子和至少一个杂原子,并且可以被一个或多个基团R3取代,其中R3具有下述含义。优选的杂芳族环系具有10至40个环原子和至少一个杂原子,并且可以被一个或多个基团R3取代,其中R3具有下述含义。如上所述,杂芳族环系还包含杂芳基基团。杂芳族环系中的杂原子优选选自N、O和/或S。
在本发明的意义上,芳族或杂芳族环系用以指以下体系,其不必仅含有芳基或杂芳基基团,而是其中多个芳基或杂芳基基团还可以被非芳族单元(优选少于10%的除H外的原子)诸如C、N或O原子或羰基间断。因此,例如,诸如9,9'-螺二芴、9,9'-二芳基芴、三芳基胺、二芳基醚、均二苯乙烯等的体系在本发明的意义上旨在用以指芳族或杂芳族环系,其中两个或更多个芳基基团例如通过直链或环状的烷基基团或通过甲硅烷基基团间断的体系也是如此。另外,其中两个或更多个芳基或杂芳基基团彼此直接键合的体系,例如联苯、三联苯、四联苯或联吡啶,同样被芳族或杂芳族环系的定义所涵盖。
具有5至40个芳族环原子并且在每种情况下也可以被所述基团R3取代且可以通过任何所需位置连接到芳族或杂芳族环系的芳族或杂芳族环系,用以指例如衍生自以下物质的基团:苯、萘、蒽、苯并蒽、菲、苯并菲、芘、苣、苝、荧蒽、苯并荧蒽、并四苯、并五苯、苯并芘、联苯、联二苯叉、三联苯、联三苯叉、芴、螺二芴、二氢菲、二氢芘、四氢芘、顺式或反式茚并芴、顺式或反式单苯并茚并芴、顺式或反式二苯并茚并芴、三聚茚、异三聚茚、螺三聚茚、螺异三聚茚、呋喃、苯并呋喃、异苯并呋喃、二苯并呋喃、噻吩、苯并噻吩、异苯并噻吩、二苯并噻吩、吡咯、吲哚、异吲哚、咔唑、吲哚并咔唑、茚并咔唑、吡啶、喹啉、异喹啉、吖啶、菲啶、苯并-5,6-喹啉、苯并-6,7-喹啉、苯并-7,8-喹啉、吩噻嗪、吩嗪、吡唑、吲唑、咪唑、苯并咪唑、萘并咪唑、菲并咪唑、吡啶并咪唑、吡嗪并咪唑、喹喔啉并咪唑、唑、苯并唑、萘并唑、蒽并唑、菲并唑、异唑、1,2-噻唑、1,3-噻唑、苯并噻唑、哒嗪、苯并哒嗪、嘧啶、苯并嘧啶、喹喔啉、1,5-二氮杂蒽、2,7-二氮杂芘、2,3-二氮杂芘、1,6-二氮杂芘、1,8-二氮杂芘、4,5-二氮杂芘、4,5,9,10-四氮杂苝、吡嗪、吩嗪、吩嗪、吩噻嗪、荧红环、萘啶、氮杂咔唑、苯并咔啉、菲咯啉、1,2,3-三唑、1,2,4-三唑、苯并三唑、1,2,3-二唑、1,2,4-二唑、1,2,5-二唑、1,3,4-二唑、1,2,3-噻二唑、1,2,4-噻二唑、1,2,5-噻二唑、1,3,4-噻二唑、1,3,5-三嗪、1,2,4-三嗪、1,2,3-三嗪、四唑、1,2,4,5-四嗪、1,2,3,4-四嗪、1,2,3,5-四嗪、嘌呤、喋啶、吲哚嗪和苯并噻二唑。
缩写Ar在每次出现时相同或不同地是具有5至30个芳族环原子的芳族或杂芳族环系,其可以被一个或多个非芳族的基团R3取代;与同一N原子、P原子或B原子键合的两个基团Ar也可以通过单键或选自N(R3)、C(R3)2、O或S的桥连基彼此桥连。取代基R3已经在以上描述或优选地在以下描述。
在本发明的意义上,环状的烷基、烷氧基或硫代烷氧基基团用以指单环、双环或多环基团。
出于本发明的目的,其中个别H原子或CH2基团还可以被上述基团取代的C1-至C20-烷基基团,用以指例如基团甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、2-甲基丁基、正戊基、仲戊基、叔戊基、2-戊基、新戊基、环戊基、正己基、仲己基、叔己基、2-己基、3-己基、新己基、环己基、1-甲基环戊基、2-甲基戊基、正庚基、2-庚基、3-庚基、4-庚基、环庚基、1-甲基环己基、正辛基、2-乙基己基、环辛基、1-双环[2.2.2]辛基、2-双环[2.2.2]辛基、2-(2,6-二甲基)辛基、3-(3,7-二甲基)辛基、金刚烷基、三氟甲基、五氟乙基、2,2,2-三氟乙基、1,1-二甲基-正己-1-基、1,1-二甲基-正庚-1-基、1,1-二甲基-正辛-1-基、1,1-二甲基-正癸-1-基、1,1-二甲基-正十二碳-1-基、1,1-二甲基-正十四碳-1-基、1,1-二甲基-正十六碳-1-基、1,1-二甲基-正十八碳-1-基、1,1-二乙基-正己-1-基、1,1-二乙基-正庚-1-基、1,1-二乙基-正辛-1-基、1,1-二乙基-正癸-1-基、1,1-二乙基-正十二烷-1-基、1,1-二乙基-正十四碳-1-基、1,1-二乙基-正十六碳-1-基、1,1-二乙基-正十八碳-1-基、1-(正丙基)环己-1-基、1-(正丁基)环己-1-基、1-(正己基)环己-1-基、1-(正辛基)环己-1-基和1-(正癸基)环己-1-基。
烯基基团用以指例如乙烯基、丙烯基、丁烯基、戊烯基、环戊烯基、己烯基、环己烯基、庚烯基、环庚烯基、辛烯基、环辛烯基或环辛二烯基。
炔基基团用以指例如乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基或辛炔基。
C1-至C20-烷氧基基团用以指例如甲氧基、三氟甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基或2-甲基丁氧基。
C1-至C20-硫代烷基基团用以指例如S-烷基基团,例如硫代甲基、1-硫代乙基、1-硫代异丙基、1-硫代正丙基、1-硫代异丁基、1-硫代正丁基或1-硫代叔丁基。
具有5至40个芳族环原子的芳氧基或杂芳氧基基团表示O-芳基或O-杂芳基,并且是指芳基或杂芳基基团分别通过氧原子键合。
具有5至40个芳族环原子的芳烷基或杂芳烷基基团是指如上所述的烷基基团被芳基基团或杂芳基基团取代。
在本发明的意义上,磷光发光体是表现出来自具有相对高的自旋多重性的激发态(即自旋态>1),特别是来自激发的三重态的发光的化合物。出于本申请的目的,所有包含过渡金属或镧系元素的发光络合物被认为是磷光发光体。以下给出了更精确的定义。
如果包含至少一种如上所述或优选如下所述的式(1)的化合物和至少一种如上所述或以下所述的式(2)的化合物的组合物用作磷光发光体的基质材料,其三重态能量优选不显著小于磷光发光体的三重态能量。以下优选适用于三重态能级:T1(发光体)-T1(基质)≤0.2eV,特别优选≤0.15eV,非常特别优选≤0.1eV。在此,T1(基质)是发光层中的基质材料的三重态能级,其中此条件适用于两种基质材料中的每一种,并且T1(发光体)是磷光发光体的三重态能级。如果发光层包含多于两种的基质材料,则上述关系优选地也适用于每种另外的基质材料。
式(1)的电子传输主体:
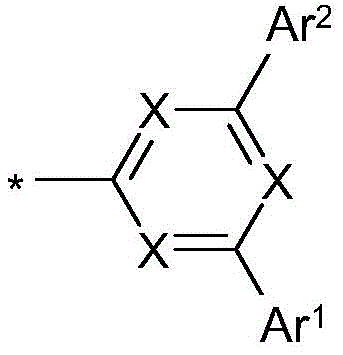
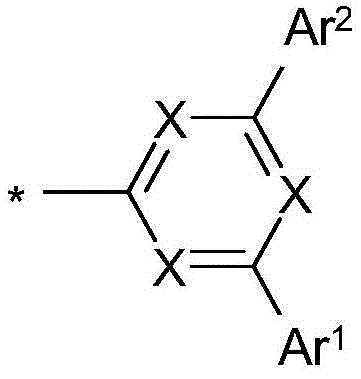
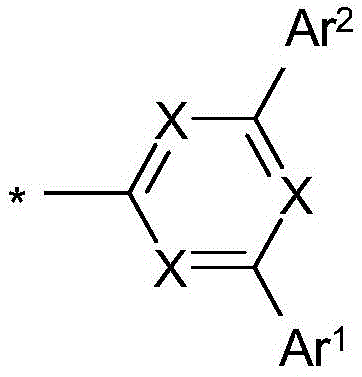
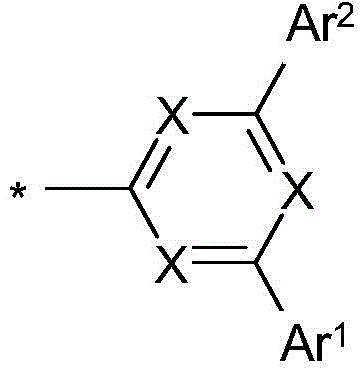
在本发明的一个实施方式中,选择如下的式(1)的化合物,其中Y选自O或S,并且取代基
在二苯并呋喃或二苯并噻吩的位置1、2、3或4上键合,其中X、X1、Y、L、Ar1、Ar2、Ar3、R、n和m具有以上指示的含义或以下指示的含义,并且*表示与二苯并呋喃或二苯并噻吩的连接位点。
式(1)的化合物中的符号X1优选代表N两次,特别优选代表N一次,并且其余的基团X1则代表CR,其中R在每种情况下彼此独立地具有以上指示的含义或优选以下指示的含义。式(1)的化合物中的X1非常特别优选地是CR。
式(1)的化合物由式(1a)和(1b)代表,其中X1在每次出现时相同或不同地表示CR,并且取代基
位于二苯并呋喃或二苯并噻吩的1或2位上,
其中X、Y、L、Ar1、Ar2、Ar3、R、n和m具有如上指示的含义或如下指示的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
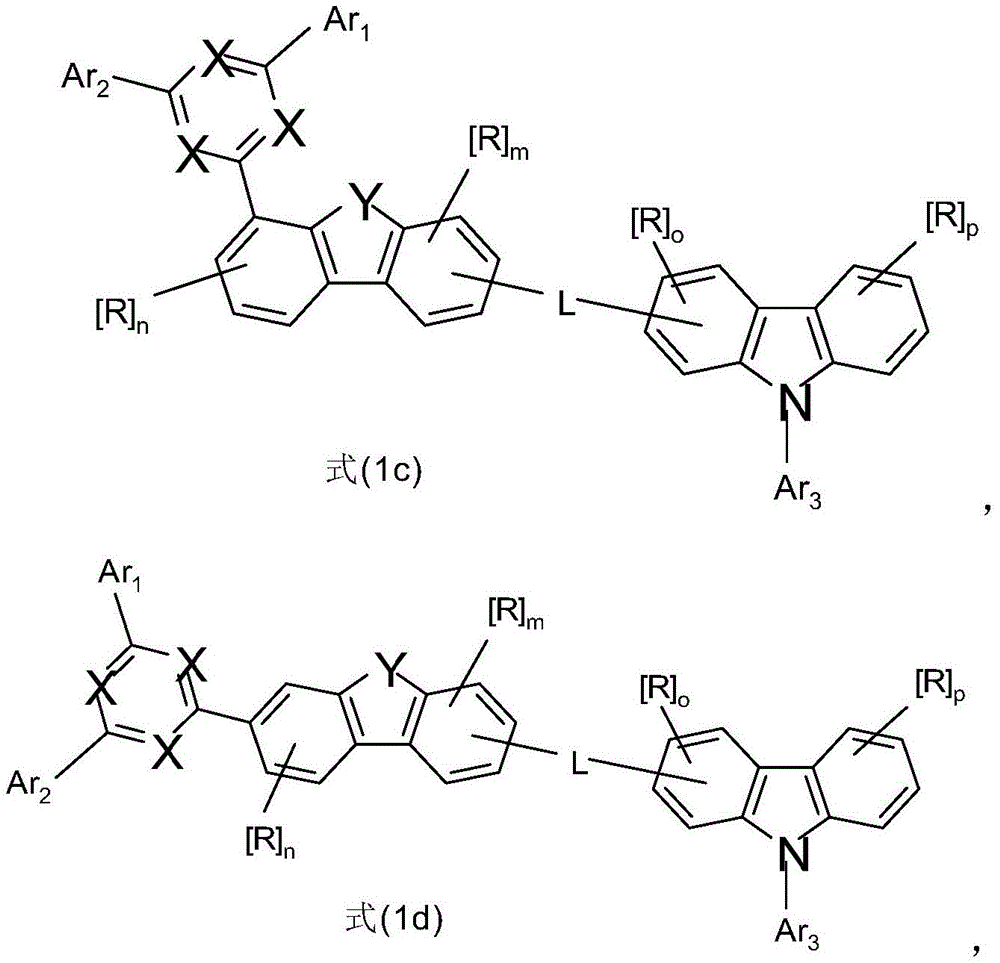
式(1)的化合物由式(1c)和(1d)代表,其中X1在每次出现时相同或不同地表示CR,并且取代基
位于二苯并呋喃或二苯并噻吩的3或4位上,
其中X、Y、L、Ar1、Ar2、Ar3、R、n和m具有如上指示的含义或如下指示的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
对于所述组合物,优选地选择至少一种具有上述或优选下述的取代基的式(1a)化合物。
对于所述组合物,优选地选择至少一种具有上述或优选下述的取代基的式(1b)化合物。
对于所述组合物,优选地选择至少一种具有上述或优选下述的取代基的式(1c)化合物。
对于所述组合物,优选地选择至少一种具有上述或优选下述的取代基的式(1d)化合物。
因此,本发明另外涉及如上所述的组合物,其中式(1)的化合物符合式(1a)、(1b)、(1c)或(1d)的化合物,优选式(1b)或(1c)的化合物。
式(1)、(1a)、(1b)、(1c)或(1d)的化合物中的符号X优选代表N至少一次,特别优选代表N两次,并且非常特别优选所有符号X代表N。其余基团X则代表CR0,特别代表CH。
R0优选地在每次出现时相同或不同地选自H、D、F或具有5至40个芳族环原子的芳族或杂芳族环系。R0在每次出现时特别优选地是H。
因此,对于所述组合物,特别优选地选择其中取代基
表示三嗪的式(1)、(1a)、(1b)、(1c)或(1d)的化合物。
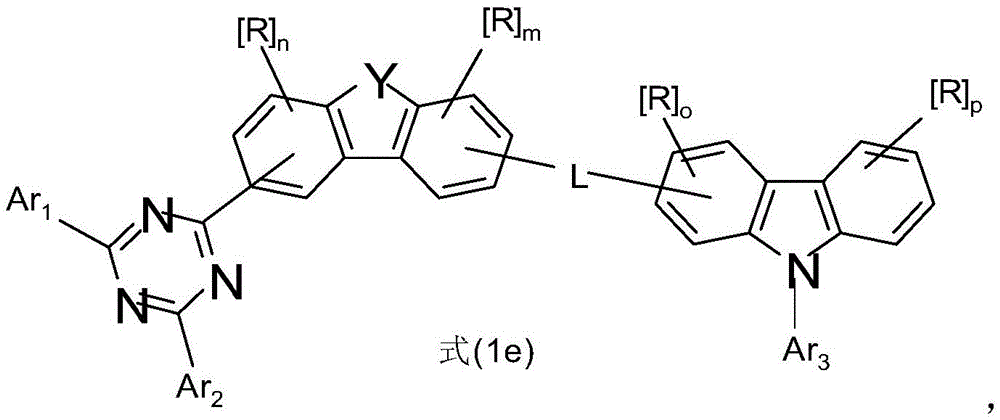
在所述实施方式中,对于所述组合物,优选地选择式(1e)的化合物,
其中Y、L、Ar1、Ar2、Ar3、R、n和m具有如上指示的含义或如下指示的含义,
三嗪取代基在1、2、3或4位连接,并且p和o在每种情况下彼此独立地表示0、1、2或3。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,Ar1和Ar2在每种情况下彼此独立地优选代表所述或优选如上所述的具有6至40个C原子的芳基基团,其可以被一个或多个基团R3取代。特别优选地,至少一个Ar1和Ar2代表苯基,另一个芳族取代基代表具有6至40个C原子的芳基基团,其可以被一个或多个基团R3取代。特别优选地,至少一个Ar1和Ar2代表苯基,另一个芳族取代基代表苯基基团,其可以被一个或多个基团R3取代。非常特别优选地,这两个基团Ar1和Ar2是相同的。非常特别优选地,基团Ar1和Ar2均代表苯基。
如果在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,所述或优选如上所述的Ar1和Ar2表示被一个或多个基团R3取代的芳基或杂芳基基团,则所述取代基R3优选地在每次出现时相同或不同地选自D、F或具有5至40个芳族环原子的芳族或杂芳族环系。对于这种/这些取代基R3,具有5至40个芳族环原子的杂芳族环系优选地衍生自二苯并呋喃或二苯并噻吩。对于这种/这些取代基R3,具有6至40个芳族环原子的芳族环系优选是苯基、联苯基或三联苯基,特别优选地是苯基或[1,1',2',1”]-三联苯-5'-基。Ar1和Ar2中的芳基基团或杂芳基基团在每种情况下彼此独立地优选被R3单取代。Ar1和Ar2中的芳基基团或杂芳基基团特别优选被R3单取代。Ar1和Ar2中的芳基基团或杂芳基基团非常特别优选未被取代。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,Y选自O或S。Y特别优选代表O。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,n优选是0或1,其中R具有以上指示的含义或以下指示的含义。n特别优选是0。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中或在优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,m优选是0或1,其中R具有以上指示的含义或以下指示的含义。m特别优选是0。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中或在优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,n和m的总和(缩写为(n+m))优选是0、1或2,其中R具有以上指示的含义或以下指示的含义。(n+m)特别优选是0或1。(n+m)非常特别优选是0。
如果在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中或在优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,n和m大于0或者n或m大于0,则取代基R优选地在每次出现时相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系。对于所述取代基R,所述具有5至40个芳族环原子的杂芳族环系优选地衍生自二苯并呋喃或二苯并噻吩。对于所述取代基R,所述具有6至40个芳族环原子的芳族环系优选是苯基、联苯基或三联苯基,特别优选地是苯基或[1,1',2',1”]-三联苯-5'-基。对于所述取代基R,具有1至40个C原子的烷基基团优选是具有1至4个C原子的直链或支链烷基基团,特别优选是甲基、乙基、正丙基或正丁基,非常特别优选是甲基。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,L优选地在每种情况下相同或不同地是单键或具有6至18个C原子的芳族或杂芳族环系,其可以被一个或多个基团R3取代。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,L特别优选地是具有6至18个C原子的芳族或杂芳族环系,其可以被一个或多个基团R3取代。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,L非常特别优选地是具有6至18个C原子的芳族环系,其可以被一个或多个基团R3取代。在此,R3优选选自D或苯基。
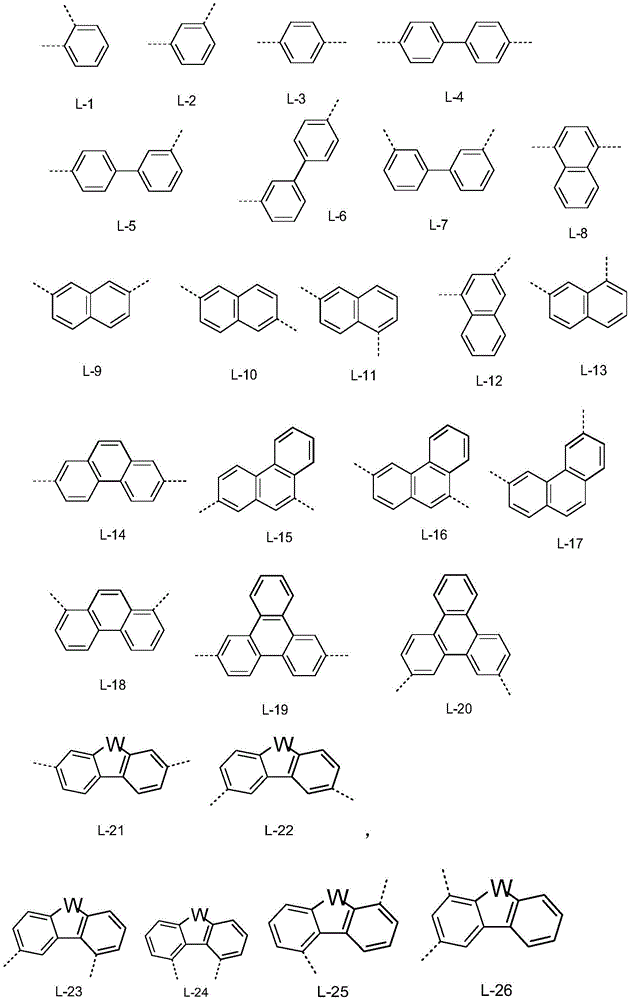
所述具有6至18个C原子的芳族或杂芳族环系优选是选自L-1至L-40的连接基,其可以未被取代或者可以被如上所述的R3取代。
其中W表示N-R0、O、S或C(R0)2,并且R0具有以上指示或优选指示的含义。W优选是O或S。W特别优选是C(R0)2,其中R0特别优选表示甲基或苯基。
具有6至18个C原子的芳族环系且因此连接基L特别优选选自苯亚基、萘亚基、联二苯叉、菲亚基或联三苯叉亚基,其中与其它取代基的键合不受限制。所述具有6至18个C原子的芳族环系特别为苯亚基,其中与其它取代基的键合不受限制。在此,苯亚基可以在邻、间或对位连接到二苯并呋喃/二苯并噻吩单元和咔唑单元。作为苯亚基的L优选在间位连接。
L或连接基L-1至L-40之一优选未被取代。
在式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)或(1e)的化合物中,L可以在二苯并呋喃环或二苯并噻吩环的6、7、8或9位连接。如上所述或如优选描述的L优选在二苯并呋喃环或二苯并噻吩环的6位或8位连接。如上所述或如优选描述的L特别优选在二苯并呋喃环或二苯并噻吩环的8位连接。
在所述实施方式中,如果L在二苯并呋喃环或二苯并噻吩环的8位连接,则对于所述组合物,优选选择式(1f)的化合物,
其中Y、L、Ar1、Ar2、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,所述三嗪取代基在1、2、3或4位连接,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
如果L是单键,则对于所述组合物,优选选择式(1g)的化合物,
其中Y、Ar1、Ar2、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,所述三嗪取代基在1、2、3或4位连接,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)或(1g)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)或(1g)的化合物中,L可以在任何期望位置与杂芳基,优选咔唑键合。如上所述或如优选描述的L优选在咔唑的3位连接。
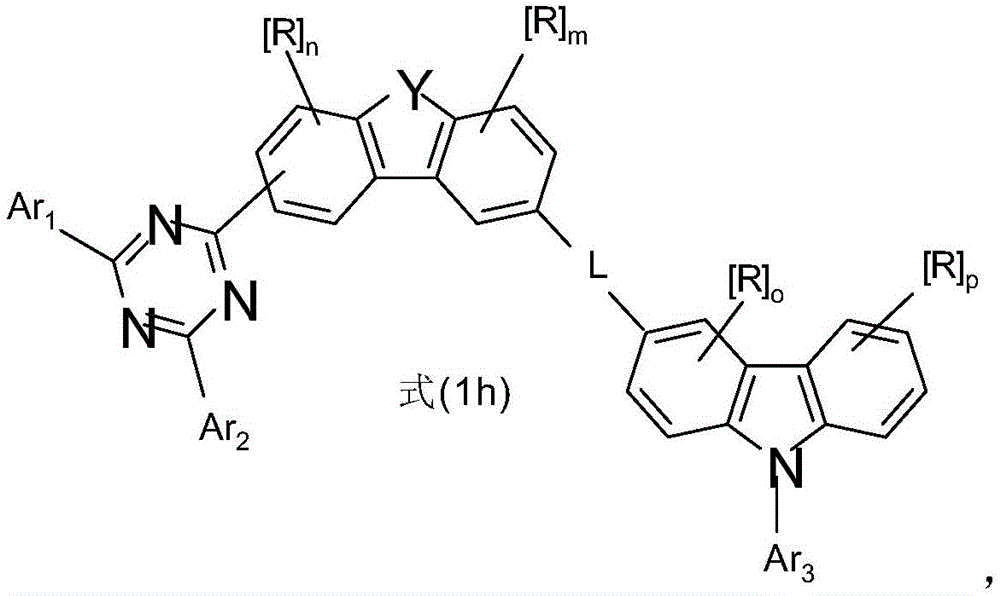
在所述实施方式中,对于所述组合物,优选地选择式(1h)的化合物,
其中Y、Ar1、Ar2、L、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,所述三嗪取代基在1、2、3或4位连接,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
如上所述或优选描述的特别优选选择的式(1)化合物符合式(1i),
其中Y、Ar1、Ar2、L、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
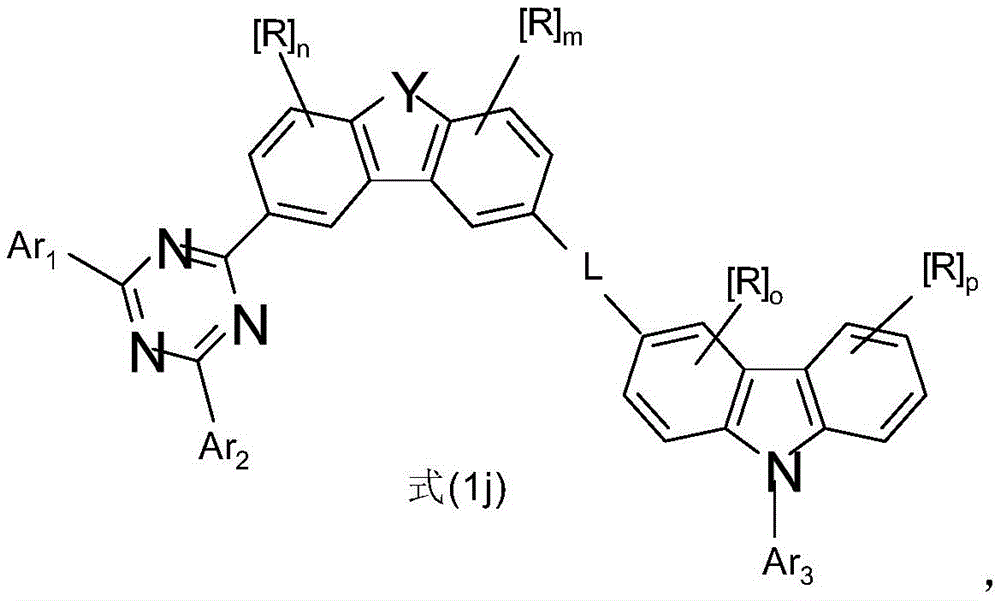
如上所述或优选描述的特别优选选择的式(1)化合物符合式(1j),
其中Y、Ar1、Ar2、L、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
如上所述或优选描述的特别优选选择的式(1)化合物符合式(1k),
其中Y、Ar1、Ar2、L、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
如上所述或优选描述的特别优选选择的式(1)化合物符合式(1l),
其中Y、Ar1、Ar2、L、n和m具有以上指示或优选指示的含义,R具有以上或以下指示的含义,Ar3具有以上指示或以下描述为优选的含义,并且p和o在每种情况下彼此独立地表示0、1、2或3。
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,o优选是0或1,其中R具有以上指示的含义或以下指示的含义。o特别优选是0。
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,p优选是0、1或2,其中R在每种情况下彼此独立地具有以上指示的含义或以下指示的含义。p特别优选是0或1。p非常特别优选是0。
如果在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,p大于0,则取代基R优选地在每种情况下相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系,或者键合到相邻碳原子的两个取代基R形成芳族或杂芳族环系。在所述R中具有5至40个芳族环原子的芳族或杂芳族环系优选对应于Ar3。Ar3的优选含义如下所述。由两个取代基R形成的芳族或杂芳族环系特别优选地对应于螺二芴。
如果在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,p大于0,则取代基R在每次出现时相同或不同地特别优选地衍生自来自咔唑、9-苯基咔唑、二苯并呋喃、二苯并噻吩、芴、三联苯或螺二芴的芳族或杂芳族环系,非常特别优选地来自9-苯基咔唑和螺二芴。
咔唑上的一起形成芳族或杂芳族环系的两个取代基R优选符合式(A)
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,Ar3优选选自具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代,不同之处在于具有10至40个芳族环原子的杂芳族环系含有N。
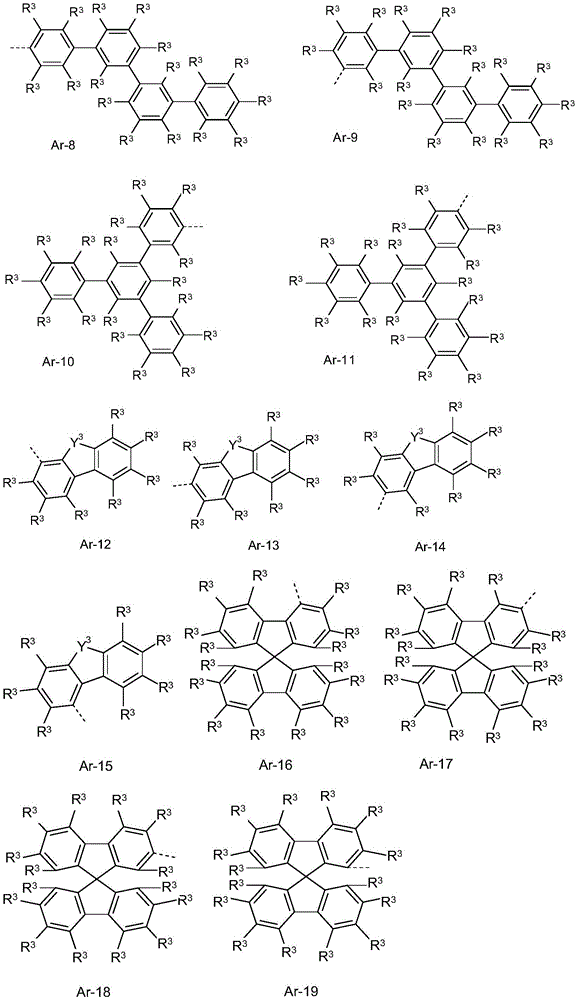
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,Ar3优选选自芳族或杂芳族环系Ar-1至Ar-22,
其中Y3在每次出现时相同或不同地表示O、S或C(R#)2,其中R3具有以上给出的含义或以下的优选含义,并且虚线键代表与N原子的键,并且其中作为Ar3的取代基的R3不包括具有5至30个芳族环原子的杂芳族环系。
基团R#在每次出现时相同或不同地是H,D,F,Cl,Br,I,CN,NO2,N(Ar)2,N(R2)2,C(=O)Ar,C(=O)R2,P(=O)(Ar)2,P(Ar)2,B(Ar)2,Si(Ar)3,Si(R2)3,具有1至20个C原子的直链的烷基、烷氧基或硫代烷基基团,或具有3至20个C原子的支链或环状的烷基、烷氧基或硫代烷基基团,或具有2至20个C原子的烯基基团,其在每种情况下可以被一个或多个基团R2取代,其中一个或多个不相邻的CH2基团可以被R2C=CR2、Si(R2)2、C=O、C=S、C=NR2、P(=O)(R2)、SO、SO2、NR2、O、S或CONR2替换,并且其中一个或多个H原子可以被D、F、Cl、Br、I、CN或NO2替换,具有5至40个芳族环原子的芳族或杂芳族环系,其在每种情况下可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳氧基或杂芳氧基基团,其可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳烷基或杂芳烷基基团,其可以被一个或多个基团R2取代;键合到同一碳原子或相邻碳原子的两个取代基R#可以任选地形成可以被一个或多个基团R2取代的单环或多环的脂族、芳族或杂芳族环系。
Y3优选是O、S或C(CH3)2。Y3特别优选是O。Y3非常特别优选是C(CH3)2。
结构Ar-1至Ar-22中的取代基R3在每种情况下相同或不同地选自H,D,F,CN,具有1至20个C原子的脂族烃基或具有6至30个芳族环原子的芳族环系,其中一个或多个H原子可以被D、F、Cl、Br、I或CN替换且其可以被一个或多个各自具有1至4个碳原子的烷基基团取代;两个或更多个相邻取代基R3可以彼此形成单或多环的脂族环系。结构Ar-1至Ar-22中的取代基R3优选在每次出现时相同或不同地选自H、F、CN、具有1至10个C原子的脂族烃基或具有6至30个芳族环原子的芳族环系。结构Ar-1至Ar-22中的取代基R3优选在每次出现时相同或不同地选自H或如上所述的具有6至30个芳族环原子的芳族环系,但优选二苯并呋喃、二苯并噻吩或螺二芴。
两个取代基R和R3,其中R在咔唑上具有取代基并且R3作为Ar3上的取代基,同样可以一起形成芳族或杂芳族环系,其中它们通过连接基,例如通过-O-、-S-或-C(R0)2-相应地彼此连接,其中R0具有以上指示的含义或优选的含义,优选经由-O-或-C(CH3)2-相应地彼此连接。
结构Ar-1至Ar-22中的取代基R3特别优选地在每次出现时是H。
在式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物中,Ar3特别优选选自芳族或杂芳族环系Ar-1、Ar-2、Ar-3、Ar-7、Ar-10、Ar-11、Ar-14、Ar-15、Ar-20、Ar-21和Ar-22,其中取代基R3和Y3具有以上给出或描述为优选的含义。
根据本发明选择的特别合适的化合物的实例是式(1f)、(1h)或(1i)的化合物,其中L具有优选或特别优选指示的含义。
根据本发明选择的特别合适的化合物的实例是式(1i)的化合物,其中L具有优选或特别优选指示的含义。
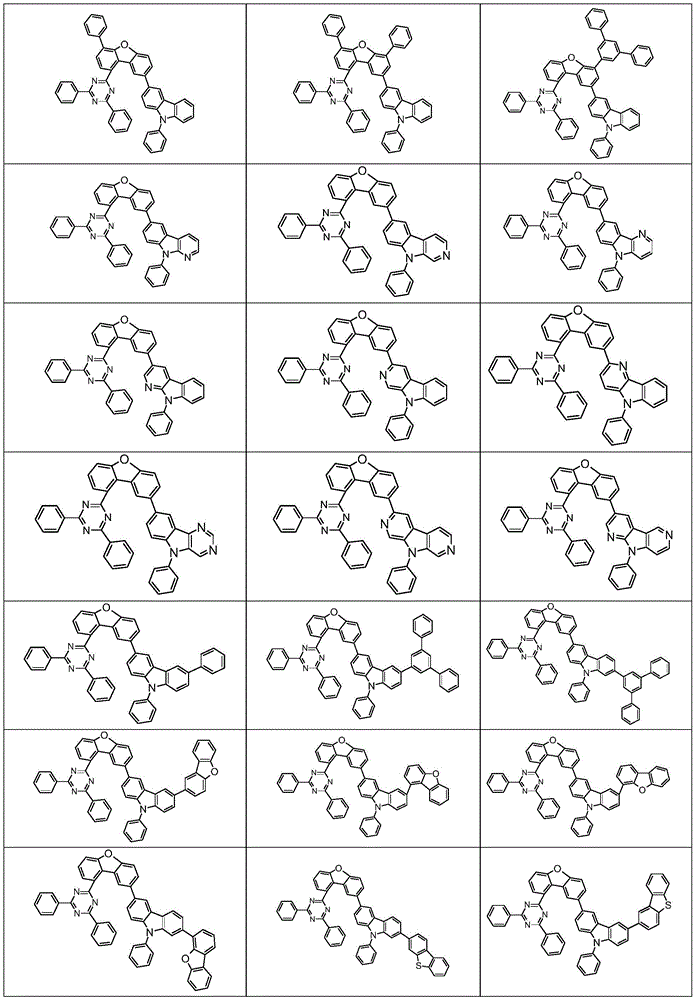
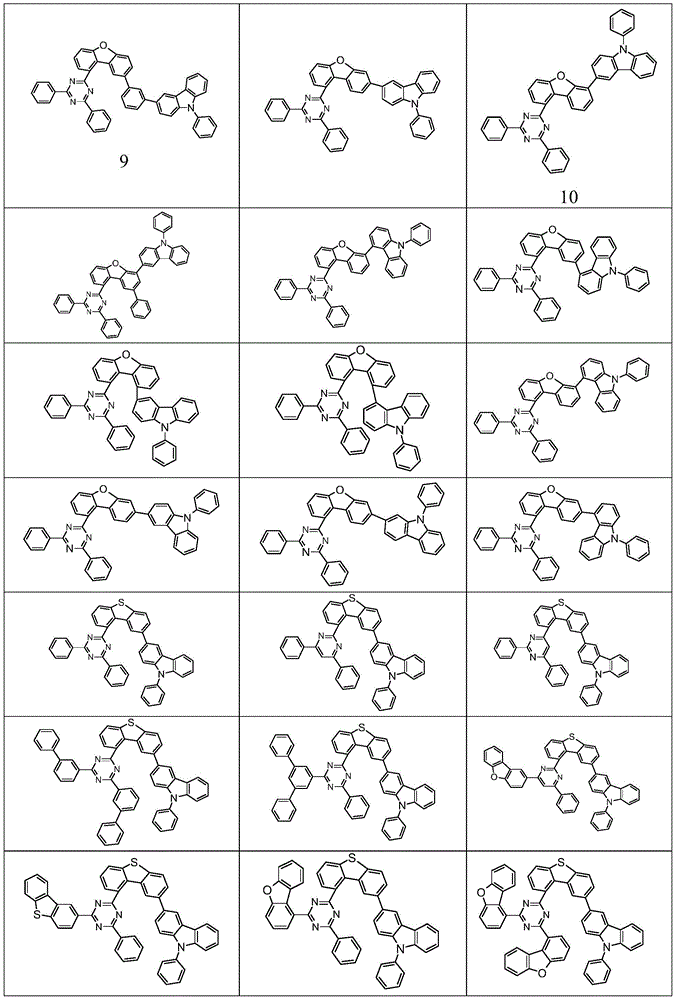
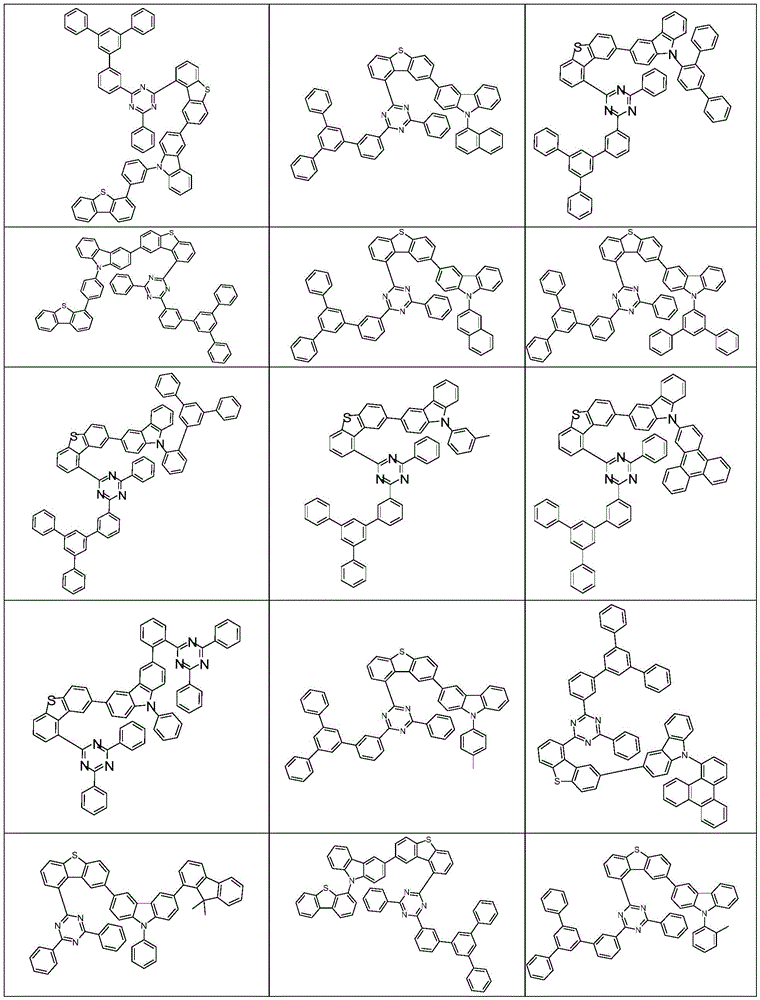
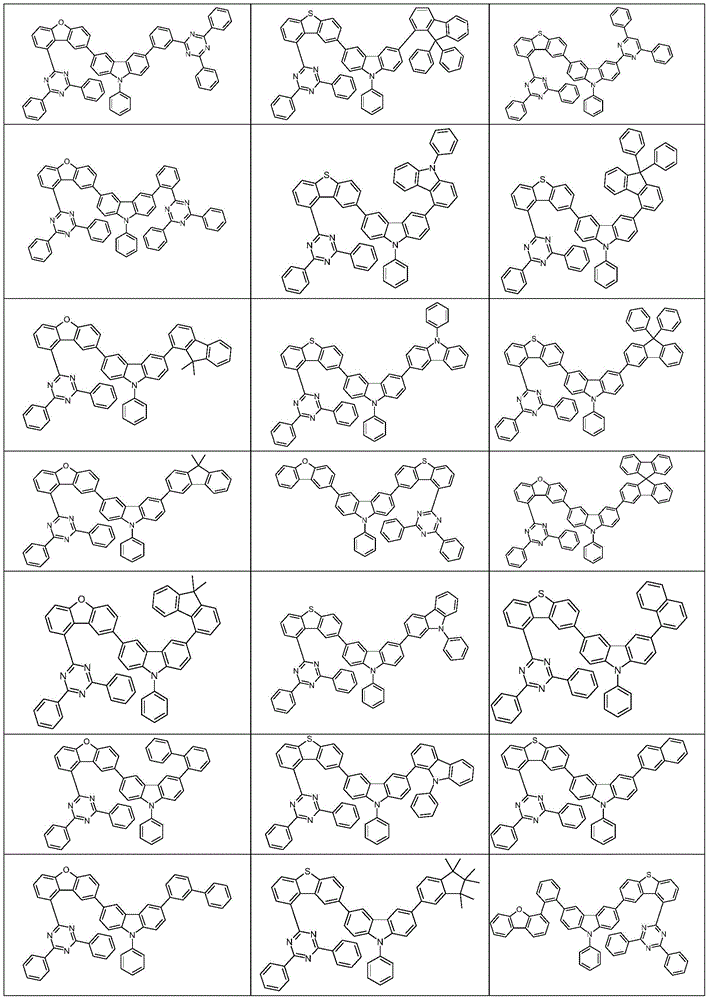
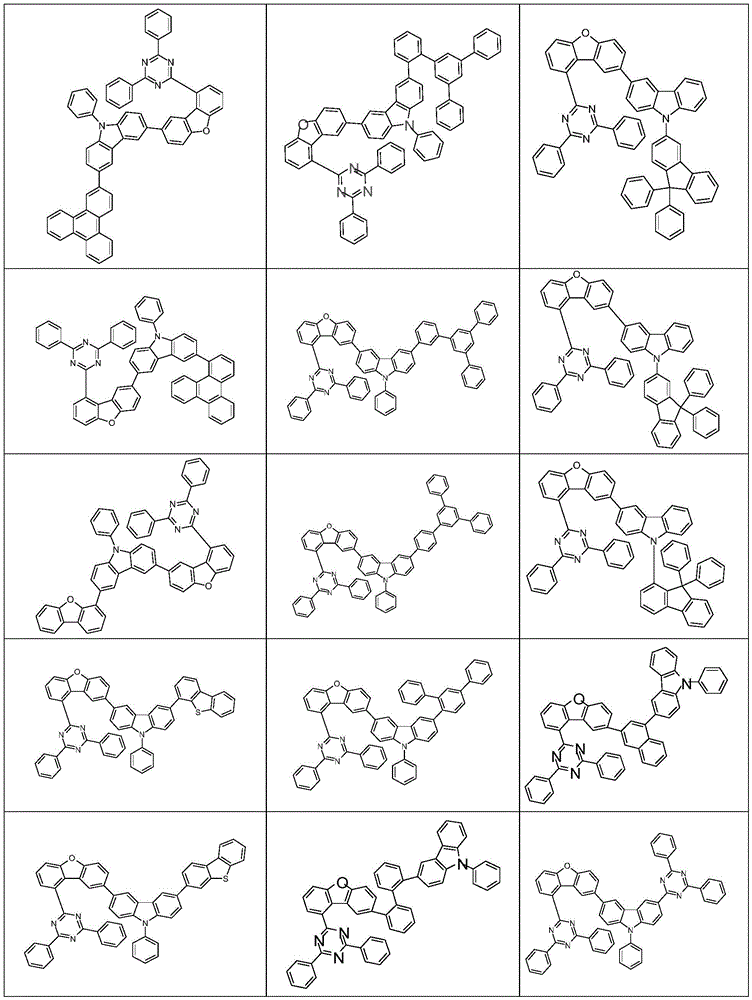
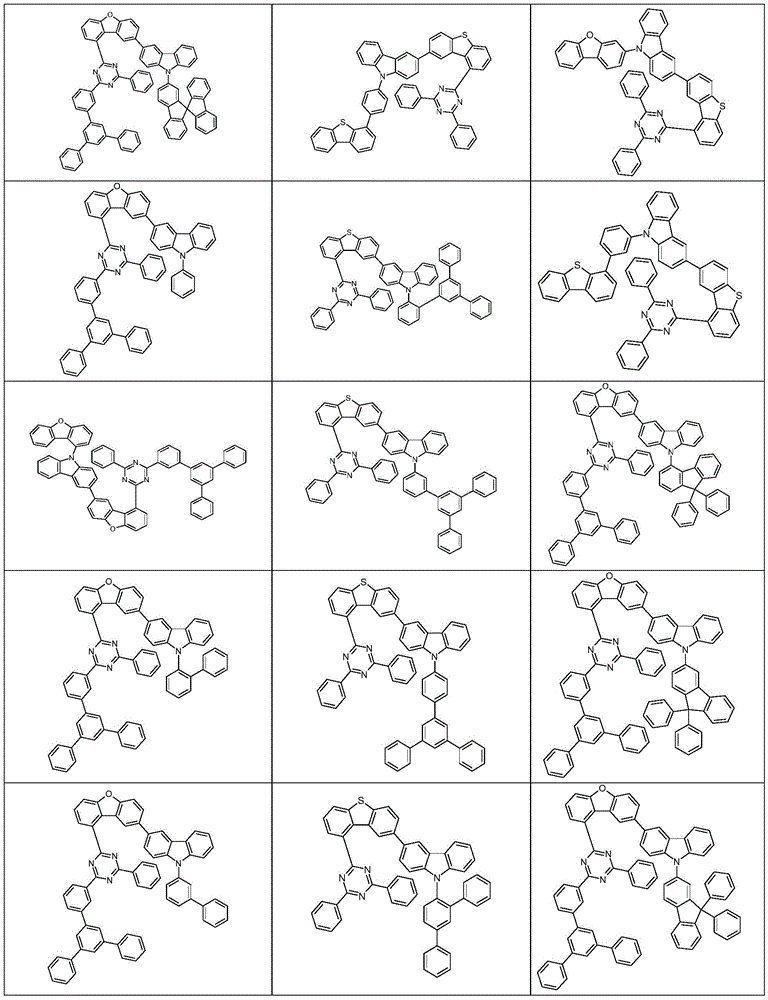
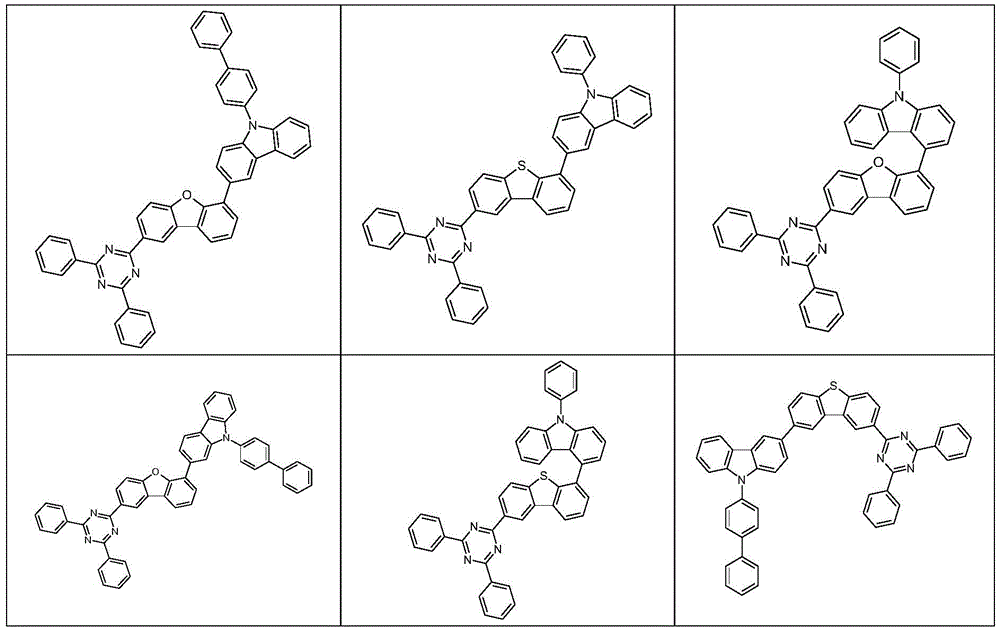
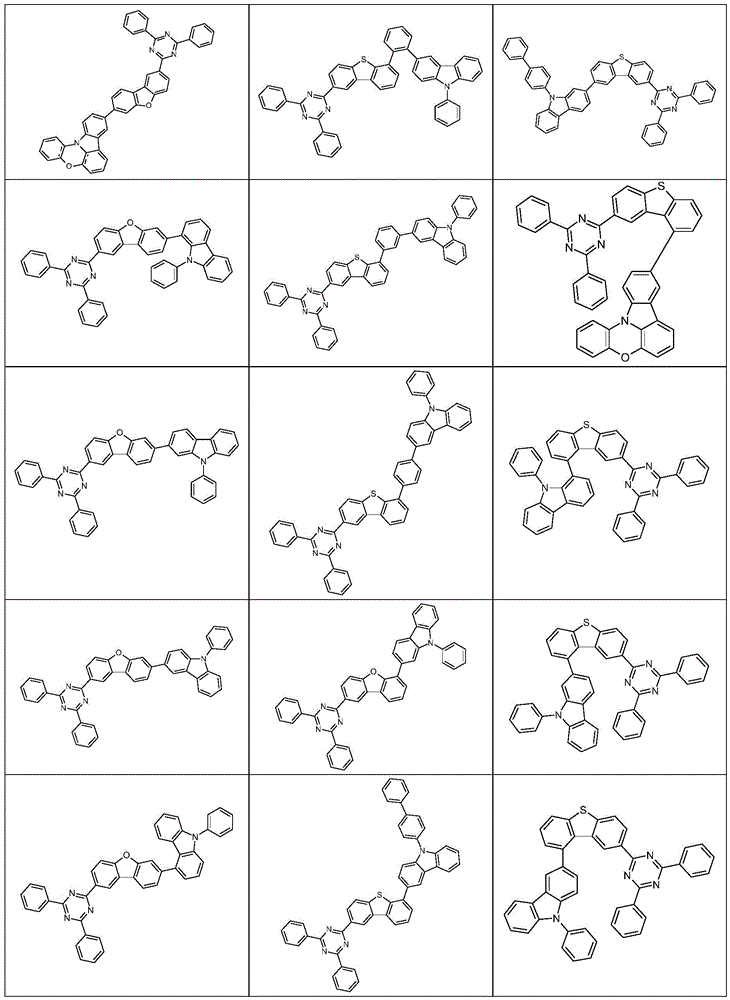
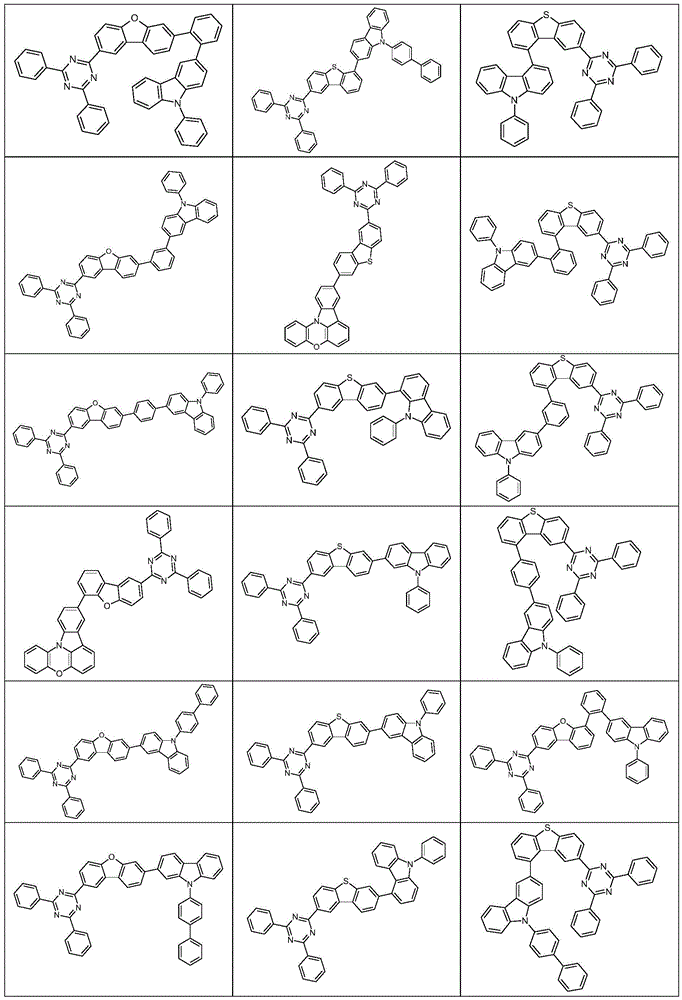
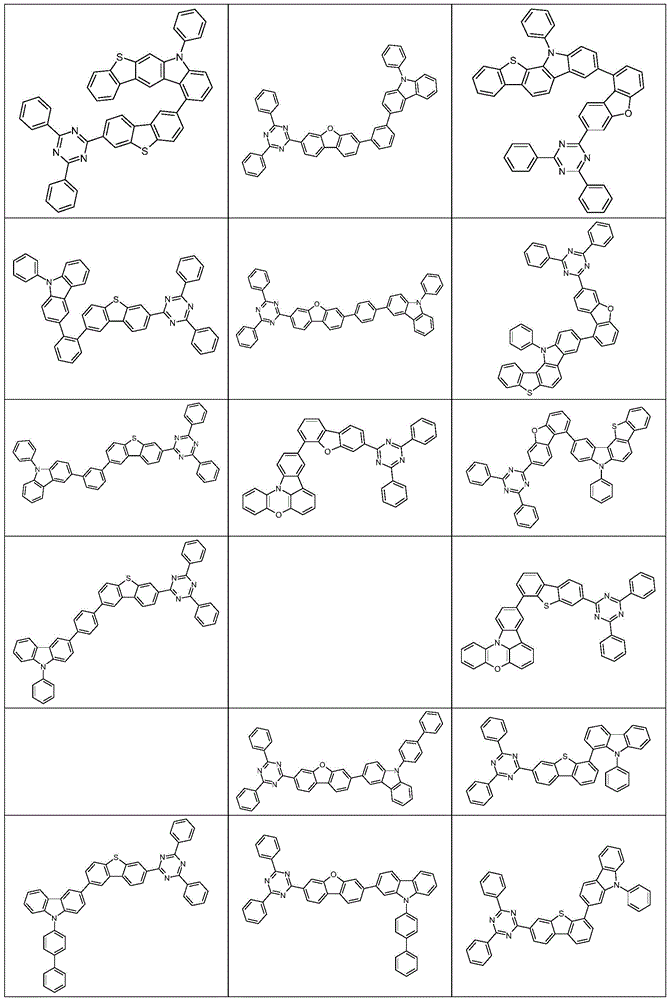
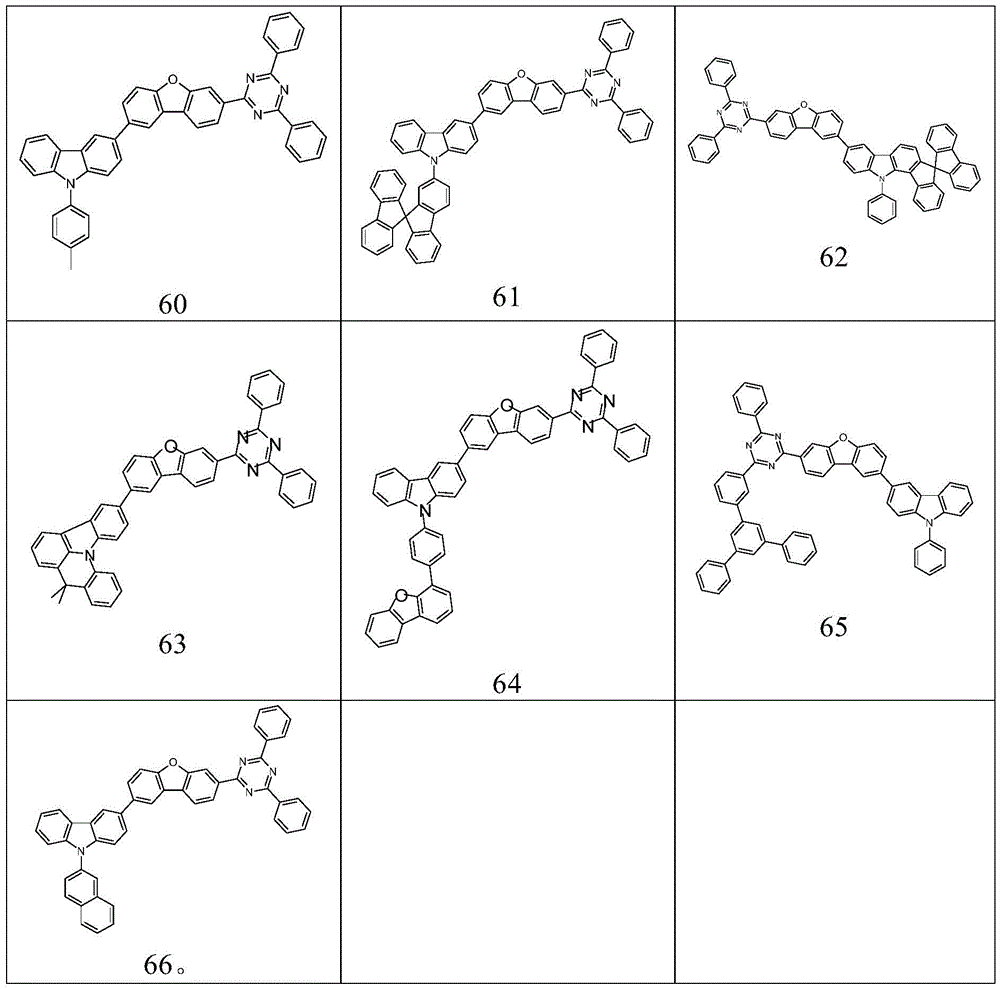
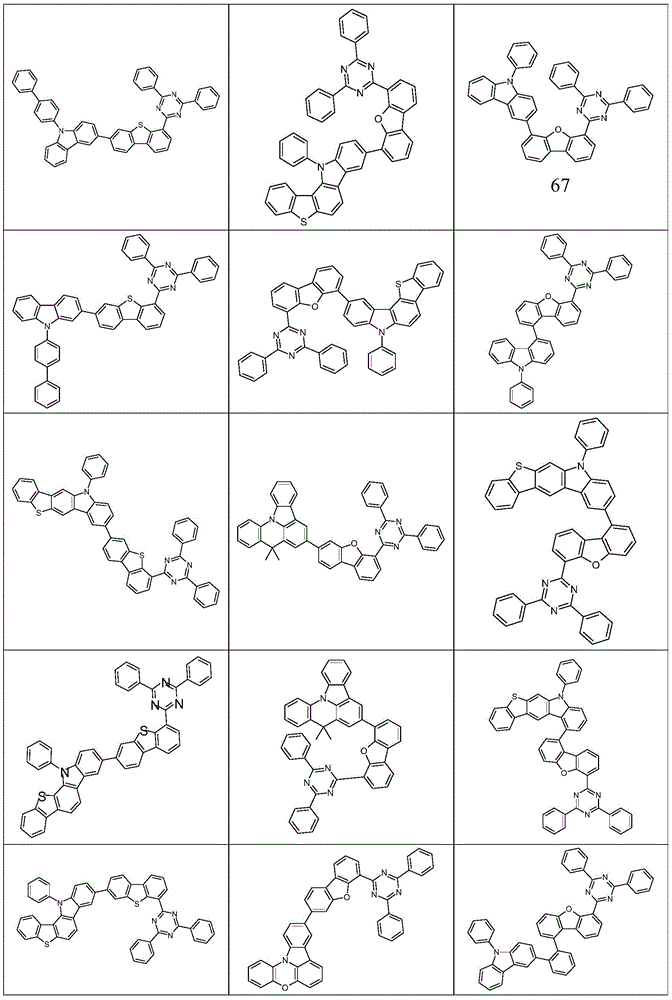
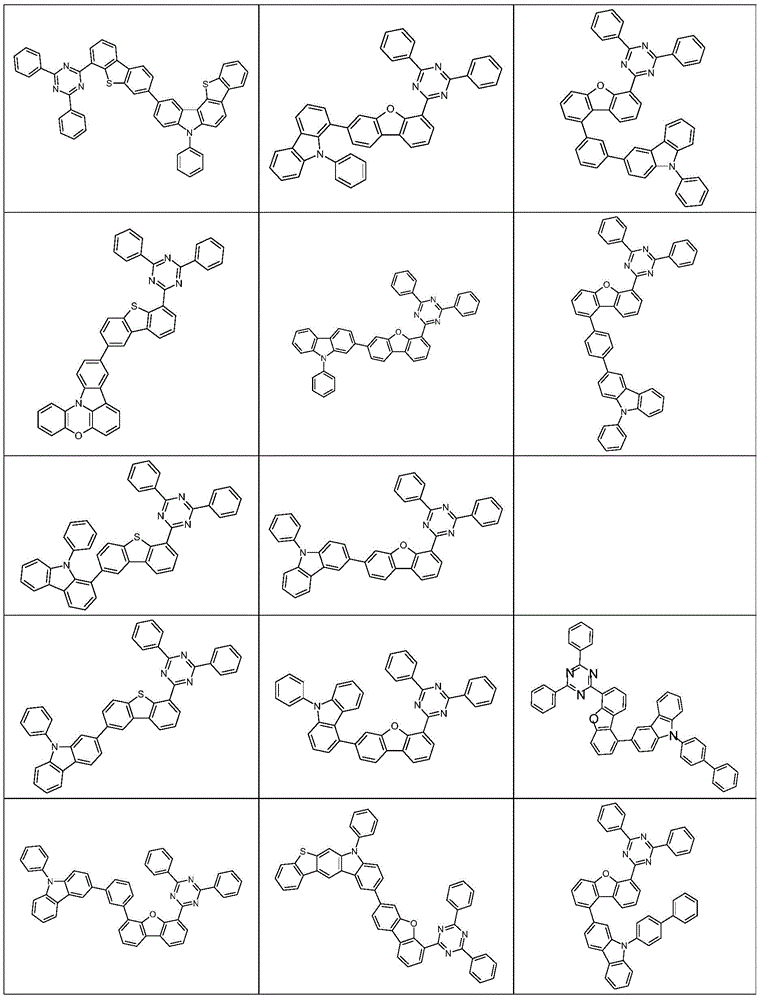
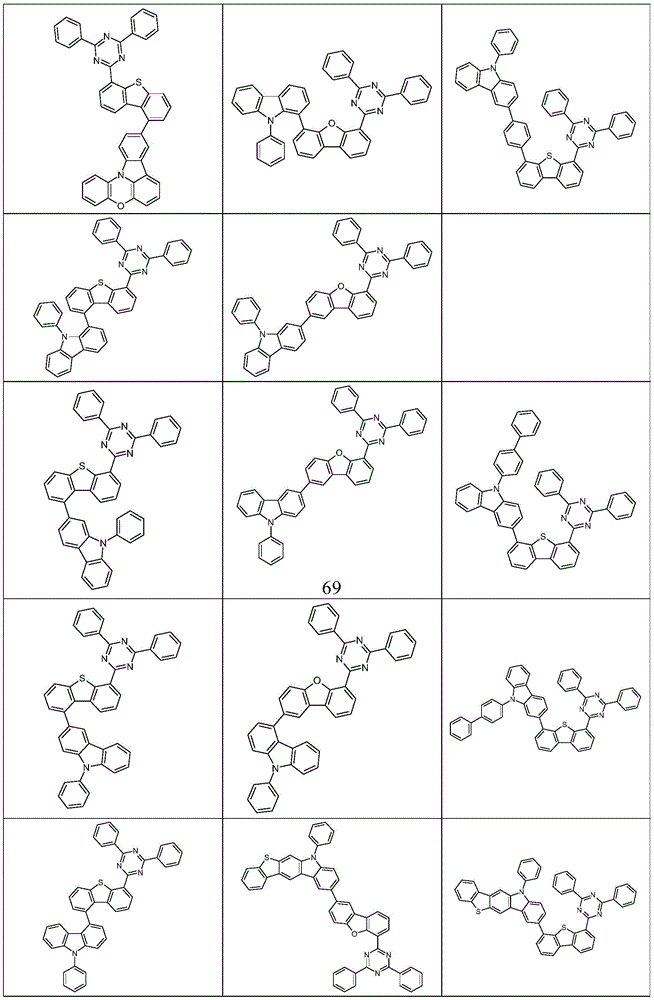
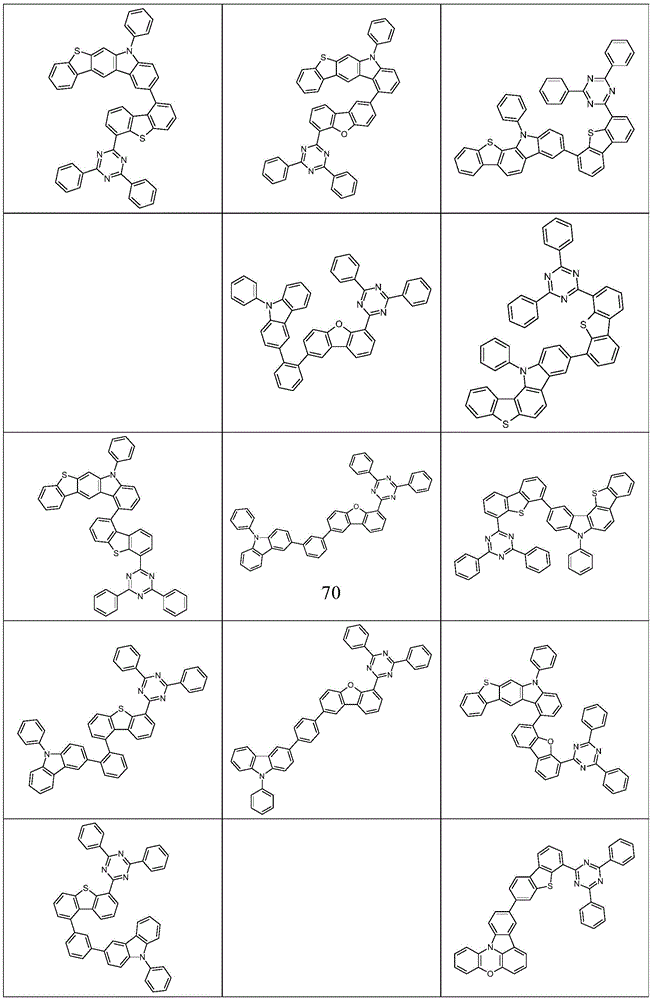
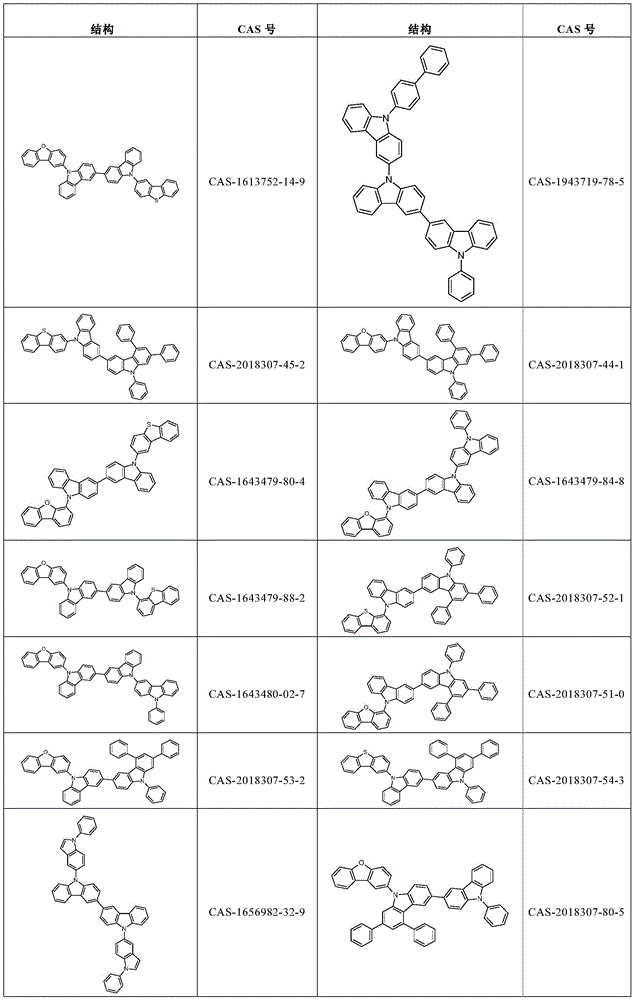
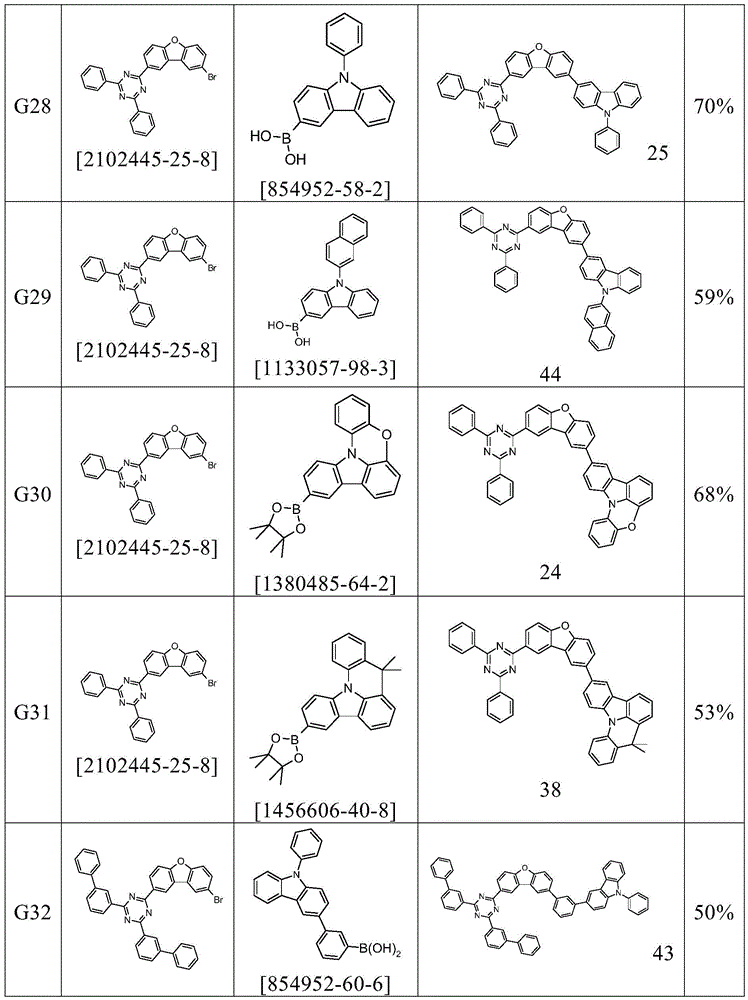
根据本发明选择的合适的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)或(1l)的化合物的实例是下表1、2、3和4中给出的结构。
表1:
表2:
表3:
表4:
根据本发明选择的特别合适的式(1)、(1b)、(1e)、(1f)、(1g)、(1h)或(1i)的化合物是表5中的化合物1至21。对于根据本发明的组合物而言,非常特别合适的化合物是式(1b)或(1i)的化合物,其中L具有优选提及或特别优选提及的含义之一。
表5:
根据本发明选择的特别合适的式(1)、(1a)、(1e)、(1f)、(1g)、(1h)或(1j)的化合物是表6中的化合物23至44。
表6:
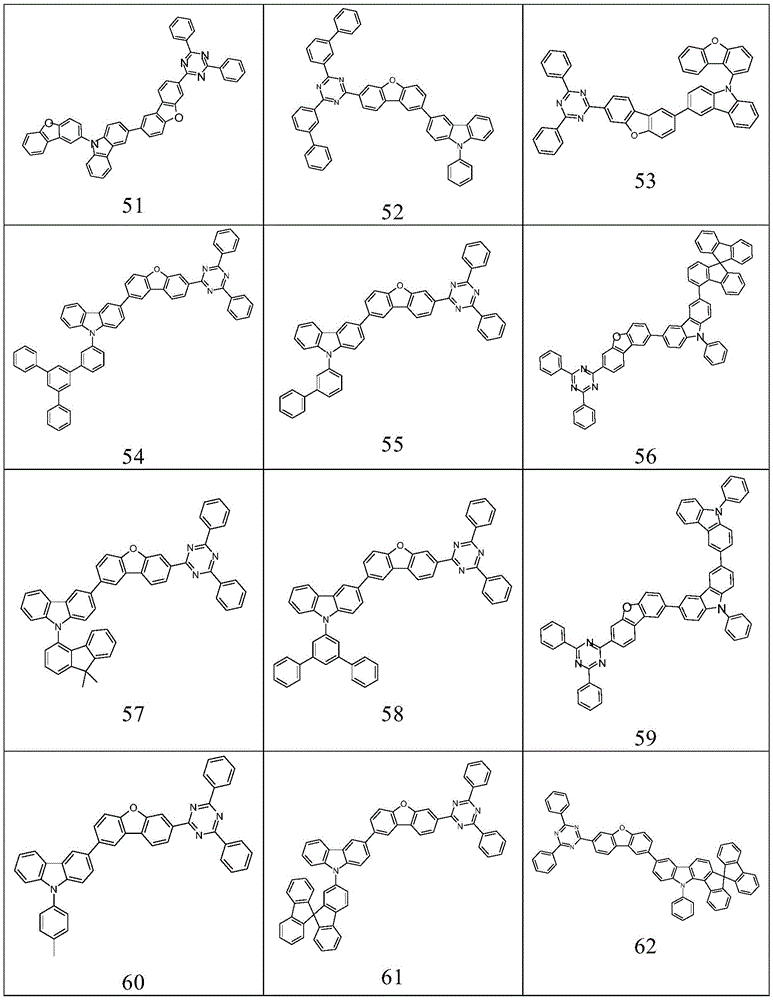
根据本发明选择的特别合适的式(1)、(1d)、(1e)、(1f)、(1g)、(1h)或(1k)的化合物是表7中的化合物45至66。
表7:
根据本发明选择的特别合适的式(1)、(1c)、(1e)、(1f)、(1g)、(1h)或(1l)的化合物是表8中的化合物67至88。
表8:
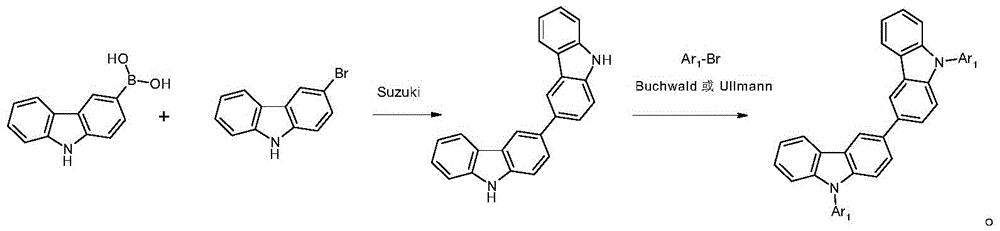
式(1)的化合物或优选的式(1a)至(1l)的化合物以及化合物1至88的制备是本领域技术人员已知的。化合物可以通过本领域技术人员已知的合成步骤,例如卤化,优选溴化,以及后续有机金属偶联反应,例如Suzuki偶联、Heck偶联或Hartwig-Buchwald偶联来制备。式(1)的化合物或优选的式(1a)至(1l)的化合物以及化合物1至88的制备特别地从WO2015/169412,特别是第63页和第77页至第114页上的合成实施例,以及WO 2011/057706,特别是第92页至第94页上的合成实施例已知。
式(1)或(1l)的化合物的制备可以根据以下方案1进行,其中X、Y、Ar1、Ar2和Ar3具有以上指示的含义之一,并且方案1中的R表示具有1至4个C原子的烷基基团。
方案1:
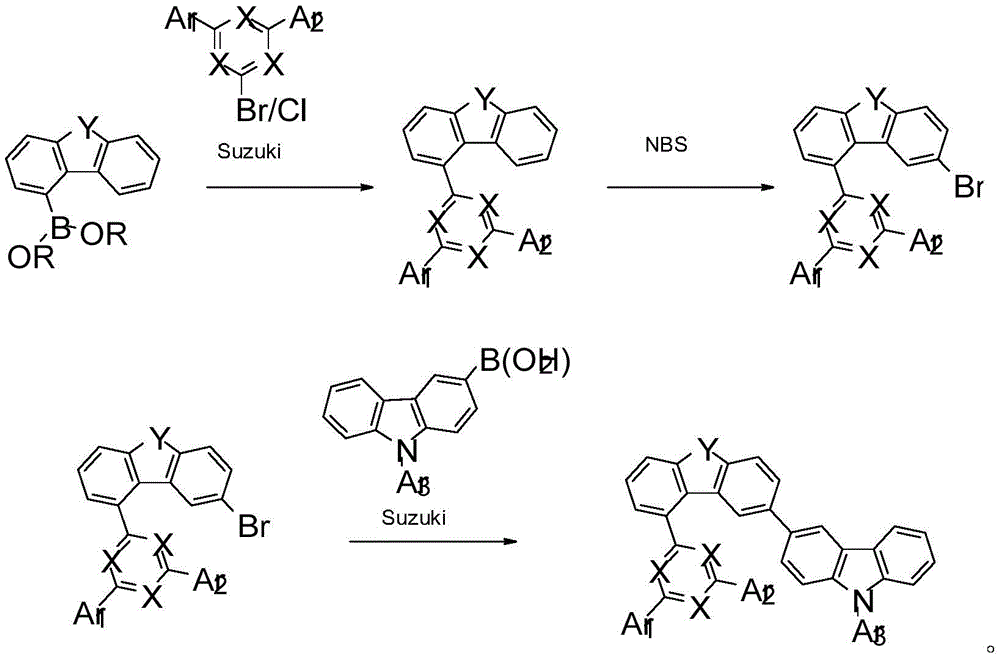
式(1)或(1k)的化合物的制备可以根据以下方案2进行,其中X、Y、Ar1、Ar2和Ar3具有以上指示的含义之一,并且方案2中的R表示具有1至4个C原子的烷基基团。
方案2:
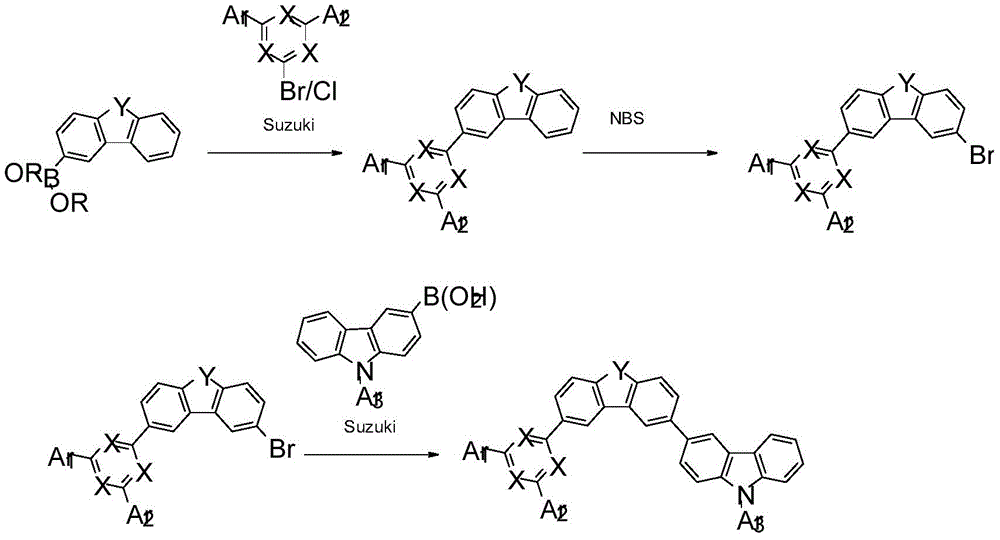
式(1)或(1j)的化合物的制备可以根据以下方案3进行,其中X、Y、Ar1、Ar2和Ar3具有以上指示的含义之一,并且方案3中的R表示具有1至4个C原子的烷基基团。
方案3:
式(1)或(1i)的化合物的制备可以根据以下方案4进行,其中X、Y、Ar1、Ar2和Ar3具有以上指示的含义之一,并且方案4中的R表示具有1至4个C原子的烷基基团。式(1)、(1b)或(1i)的化合物的制备同样可以根据以下方案5进行,其中X、Y、Ar1、Ar2和Ar3具有以上指示的含义之一。
方案4:
方案5
式(2)的空穴传输主体:
在本发明的一个实施方式中,如上所述选择式(2)的化合物,其与如上所述或优选描述的式(1)、(1a)、(1b)、(1c)、(1d)、(1e)、(1f)、(1g)、(1h)、(1i)、(1j)、(1k)和(1l)的化合物或者与化合物1至88一起用于所述组合物中。
式(2)的化合物中的符号X2优选代表N两次,特别优选代表N一次,并且其余的基团X2则代表CR1,其中R1在每种情况下彼此独立地具有以上指示的含义或优选以下指示的含义。式(2)的化合物中的X2非常特别优选地是CR1。
式(2)的化合物由式(2a)代表,其中X2在每次出现时相同或不同地表示CR1,
其中R1、Ar4和Ar5具有以上给出的含义或以下描述的优选含义,并且q和t在每种情况下彼此独立地表示0、1、2、3或4,并且r和s在每种情况下彼此独立地表示0、1、2或3。
在式(2a)的化合物中,H被从取代基R1的定义中排除。此排除相应地适用于以下所有出现q、t、s和r的式。
因此,本发明另外涉及一种如上所述的组合物,其中式(2)的化合物符合式(2a)的化合物。
在式(2)或(2a)的化合物的一个优选的实施方式中,所述两个咔唑在每种情况下在3位彼此连接。所述实施方式由式(2b)的化合物代表,
其中R1、Ar4和Ar5具有以上给出的含义或以下描述的优选含义,并且q和t在每种情况下彼此独立地表示0、1、2、3或4,并且r和s在每种情况下彼此独立地表示0、1、2或3。
因此,本发明另外涉及一种如上所述的组合物,其中式(2)的化合物符合式(2b)的化合物。
在式(2)、(2a)或(2b)的化合物中,q优选是0、1或2,其中R1具有以上指示的含义或以下指示的含义。q特别优选是0或1。q非常特别优选是0。
如果在式(2)、(2a)或(2b)的化合物中,q大于0,则取代基R1优选地在每次出现时相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系,其可以被一个或多个基团R2取代。在所述R1中具有5至40个芳族环原子的芳族或杂芳族环系优选衍生自苯、二苯并呋喃、二苯并噻吩、9-苯基咔唑、联苯或三联苯,其可以被一个或多个基团R2取代。取代基[R1]q的优选位置是1、2、3或4位或者1位和4位的组合或者1位和3位的组合,特别优选是1位和3位、2位或3位,非常特别优选是3位,其中R1具有以上指示的优选含义之一,并且q大于0。[R1]q中特别优选的取代基R1是苯基和联苯基。
在式(2)、(2a)或(2b)的化合物中,r优选是0、1或2,其中R1具有以上指示的含义或以下指示的含义。r特别优选是0或1,非常特别优选是0。
如果在式(2)、(2a)或(2b)的化合物中,r大于0,则取代基R1优选地在每次出现时相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系,其可以被一个或多个基团R2取代。在所述R1中具有5至40个芳族环原子的芳族或杂芳族环系优选衍生自苯、二苯并呋喃、二苯并噻吩、9-苯基咔唑、联苯和三联苯,其可以被一个或多个基团R2取代。取代基[R1]r的优选位置是1或2位,特别优选是1位,其中R1具有以上指示的优选含义之一,并且r大于0。[R1]r中特别优选的取代基R1是苯基、9-苯基咔唑和9H-咔唑-9-基。
在式(2)、(2a)或(2b)的化合物中,s优选是0、1或2,其中R1具有以上指示的含义或以下指示的含义。s特别优选是0或1,非常特别优选是0。
如果在式(2)、(2a)或(2b)的化合物中,s大于0,则取代基R1优选地在每次出现时相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系,其可以被一个或多个基团R2取代。在所述R1中具有5至40个芳族环原子的芳族或杂芳族环系优选衍生自苯、二苯并呋喃、二苯并噻吩、9-苯基咔唑、联苯或三联苯,其可以被一个或多个基团R2取代。取代基[R1]s的优选位置是1或2位,特别优选是1位,其中R1具有以上指示的优选含义之一,并且s大于0。[R1]r中特别优选的取代基R1是苯基、9-苯基咔唑和9H-咔唑-9-基。
在式(2)、(2a)或(2b)的化合物中,t优选是0、1或2,其中R1具有以上指示的含义或以下指示的含义。t特别优选是0或1。t非常特别优选是0。
如果在式(2)、(2a)或(2b)的化合物中,t大于0,则取代基R1优选地在每次出现时相同或不同地选自D、F、具有1至40个C原子的烷基基团或具有5至40个芳族环原子的芳族或杂芳族环系,其可以被一个或多个基团R2取代。在所述R1中具有5至40个芳族环原子的芳族或杂芳族环系优选衍生自苯、二苯并呋喃、二苯并噻吩、9-苯基咔唑、联苯或三联苯,其可以被一个或多个基团R2取代。取代基[R1]q的优选位置是1、2、3或4位或者1位和4位、1位和3位、1位和2位以及3位和4位的组合,特别优选是1位和3位、2位或3位,非常特别优选是2位或3位,其中R1具有以上指示的优选含义之一,并且t大于0。[R1]t中特别优选的取代基R1是苯基、联苯基和三联苯基。
取代基R2优选地在每次出现时相同或不同地选自D,F,Cl,Br,I,CN,NO2,N(Ar)2,NH2,N(R3)2,C(=O)Ar,C(=O)H,C(=O)R3,P(=O)(Ar)2,具有1至40个C原子的直链的烷基、烷氧基或硫代烷基基团或具有3至40个C原子的支链或环状的烷基、烷氧基或硫代烷基基团或具有2至40个C原子的烯基或炔基基团,其在每种情况下可以被一个或多个基团R3取代,或者是具有5至60个芳族环原子的芳族或杂芳族环系,其在每种情况下可以被一个或多个基团R3取代,或者是具有5至60个芳族环原子的芳氧基或杂芳氧基基团,其可以被一个或多个基团R3取代。取代基R2在其出现时特别优选地是如上所述的芳族或杂芳族环系,优选选自咔唑、9-苯基咔唑、二苯并呋喃、二苯并噻吩、芴、三联苯或螺二芴,非常特别优选衍生自二苯并呋喃。
在如上所述的取代基R2之一被取代基R3取代的情况下,适用如上所述或优选描述的R3的含义。
在如上所述的式(2)、(2a)或(2b)的化合物中,Ar4和Ar5在每种情况下彼此独立地是具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不能同时是苯基。由于指示的条件,根据本发明的组合物不同于WO 2015/169412的组合物。
如果根据本发明将式(1f)、(1h)和(1i)的化合物与式(2)、(2a)或(2b)的化合物一起使用,并且式(1f)、(1h)和(1i)的化合物中的L不表示单键,则除了以上指示的定义之外,Ar4和Ar5都可以表示苯基。
在可以被一个或多个取代基R3取代的具有10至40个C原子的杂芳族环系的情况下,特别优选富电子环系,其中任选被R3取代的环系优选包含总共仅一个N原子,或者任选被R3取代的环系总共包含一个或多个O和/或S原子。
在式(2)、(2a)或(2b)的化合物或优选描述的式(2)、(2a)或(2b)的化合物中,Ar4和Ar5优选选自如上所述的芳族或杂芳族环系Ar-1至Ar-22,其中关于基团R#、Y3和R3的注释也适用,条件是Ar4和Ar5不同时是苯基,并且优选地,任选被R3取代的由Ar-12、Ar-13、Ar-14、Ar-15、Ar-20和Ar-21代表的杂芳族环系总共仅包含一个N原子。
如果根据本发明将式(1f)、(1h)和(1i)的化合物与式(2)、(2a)或(2b)的化合物一起使用,并且式(1f)、(1h)和(1i)的化合物中的L不表示单键,则除了以上指示的定义之外,Ar4和Ar5都可以表示苯基。
在本发明的一个优选的实施方式中,选择式(2)、(2a)或(2b)的化合物,其中取代基Ar4和Ar5之一表示具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代,并且另一个取代基表示具有6至40个芳族环原子的芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不同时是苯基。所述条件不适用于如上所述的其中L不表示单键的式(1f)、(1h)或(1i)的化合物。
因此,本发明另外涉及一种如上所述或优选描述的组合物,其中式(2)或(2a)或(2b)的化合物中的取代基Ar4和Ar5之一表示具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,其可以被一个或多个基团R3取代,并且另一个取代基表示具有6至40个芳族环原子的芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不同时是苯基。
在所述实施方式中,优选地,如果一个取代基Ar4或Ar5对应于如上所述或优选描述的结构Ar-1至Ar-22中的一种,并且另一个取代基符合结构Ar-1至Ar-11或Ar-16至Ar-19或Ar-22中的一种,条件是Ar4和Ar5不同时是苯基,并且优选地,任选被R3取代的由Ar-12、Ar-13、Ar-14、Ar-15、Ar-20和Ar-21代表的杂芳族环系总共仅包含一个N原子。
在本发明的一个特别优选的实施方式中,选择式(2)、(2a)或(2b)的化合物,其中取代基Ar4和Ar5在每种情况下彼此独立地表示具有6至40个芳族环原子的芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不同时是苯基。
当在所述实施方式中存在时,取代基R3优选是芳族的,并且如果Ar4和Ar5表示具有6至40个环原子的芳族环系,则取代基R3不包含杂原子。
因此,本发明另外涉及一种如上所述或优选描述的组合物,其中式(2)或(2a)或(2b)的化合物中的取代基Ar4和Ar5在每种情况下彼此独立地表示具有6至40个芳族环原子的芳族环系,其可以被一个或多个基团R3取代,条件是Ar4和Ar5不同时是苯基。
在所述实施方式中,优选地,如果两个取代基Ar4和Ar5在每种情况下彼此独立地符合如上所述或优选描述的结构Ar-1至Ar-11或Ar-16至Ar-19或Ar-22中的一种,条件是Ar4和Ar5不同时是苯基,并且优选地,选择任选地被R3取代的芳族环系中的取代基R3,使其不包含杂原子。
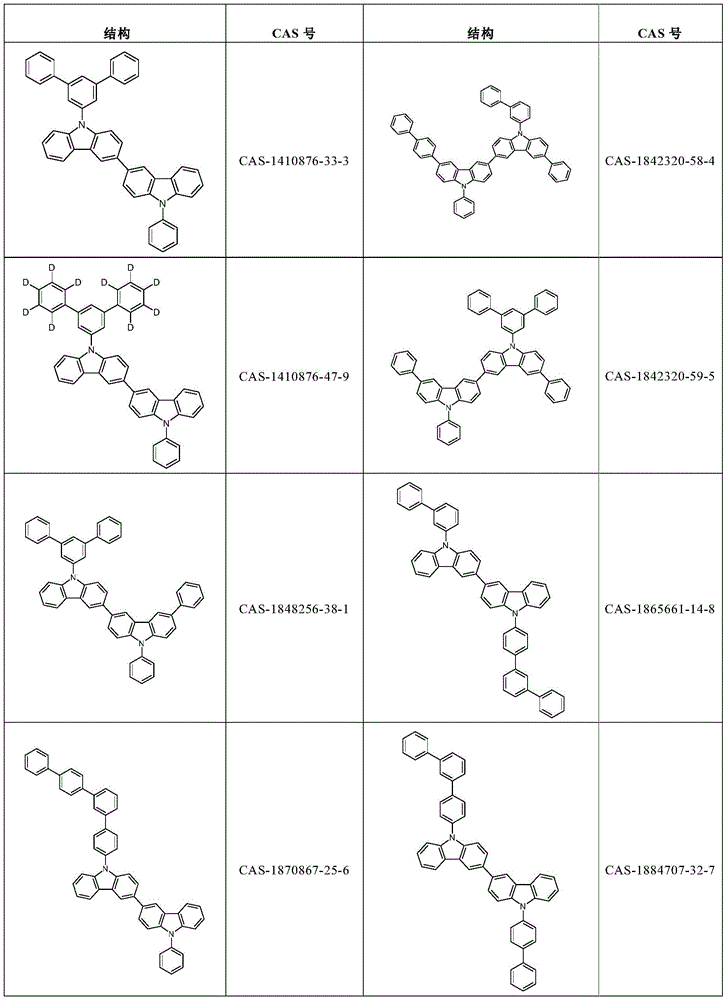
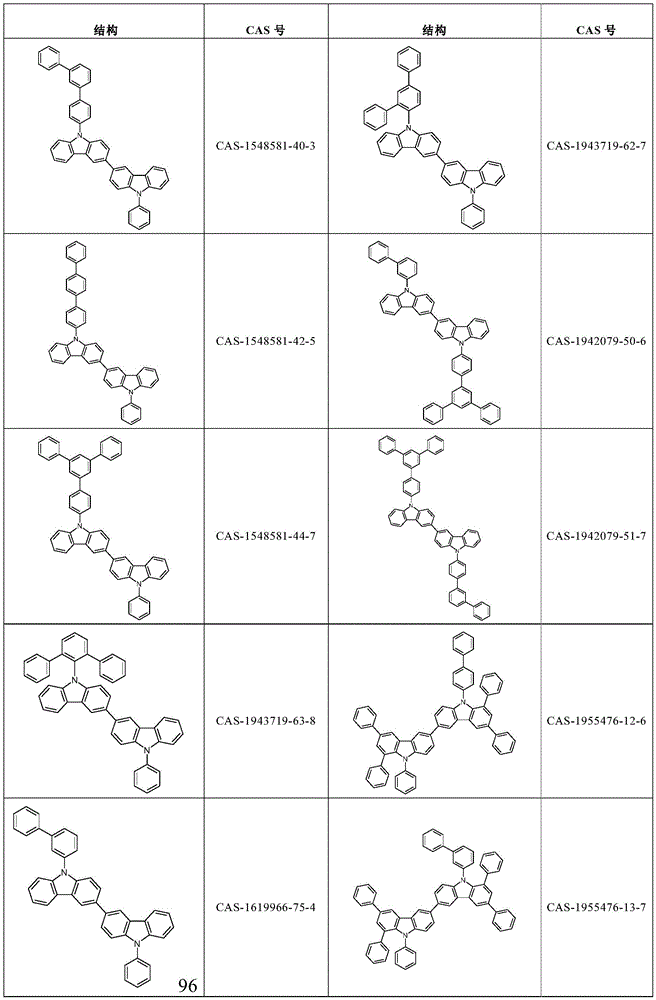
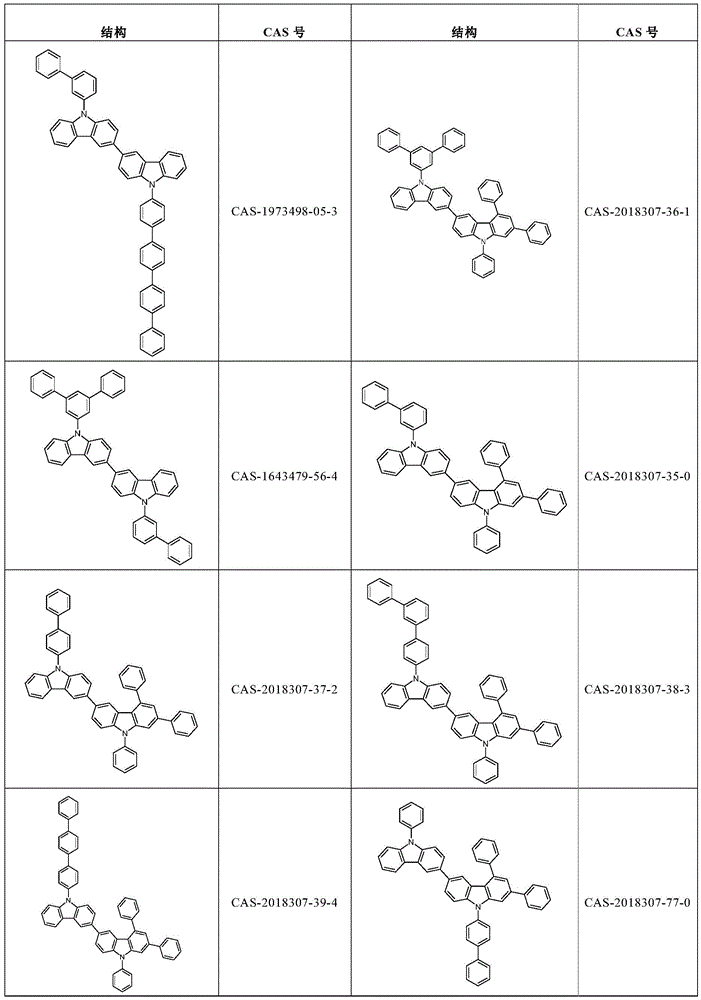
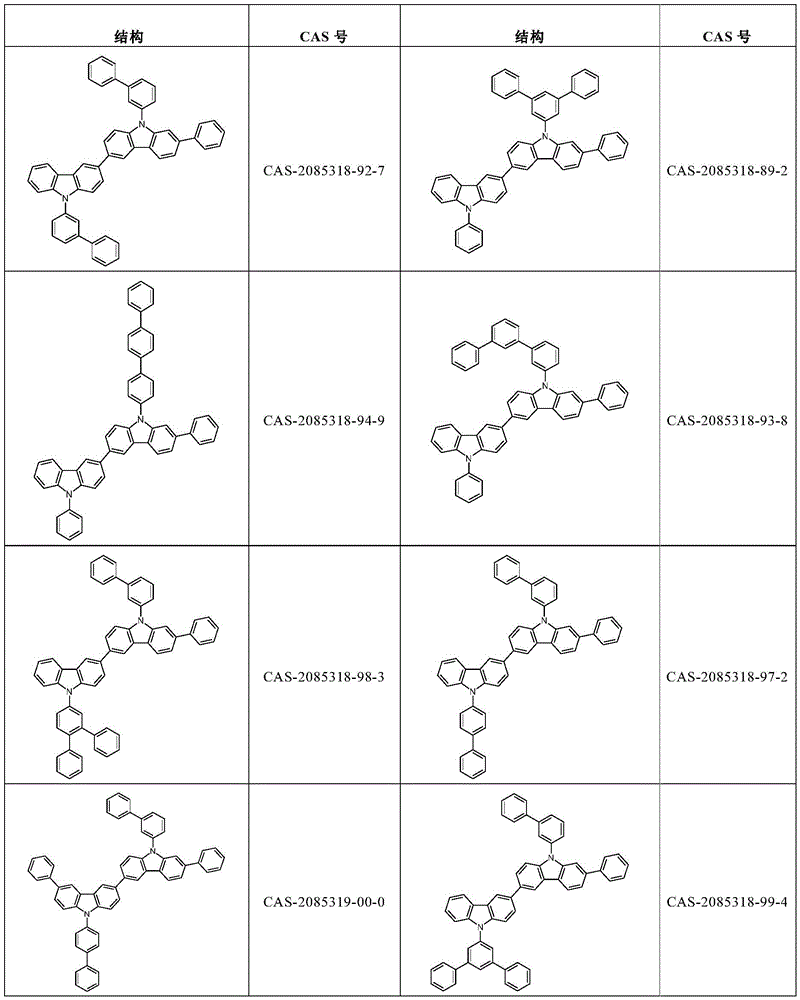
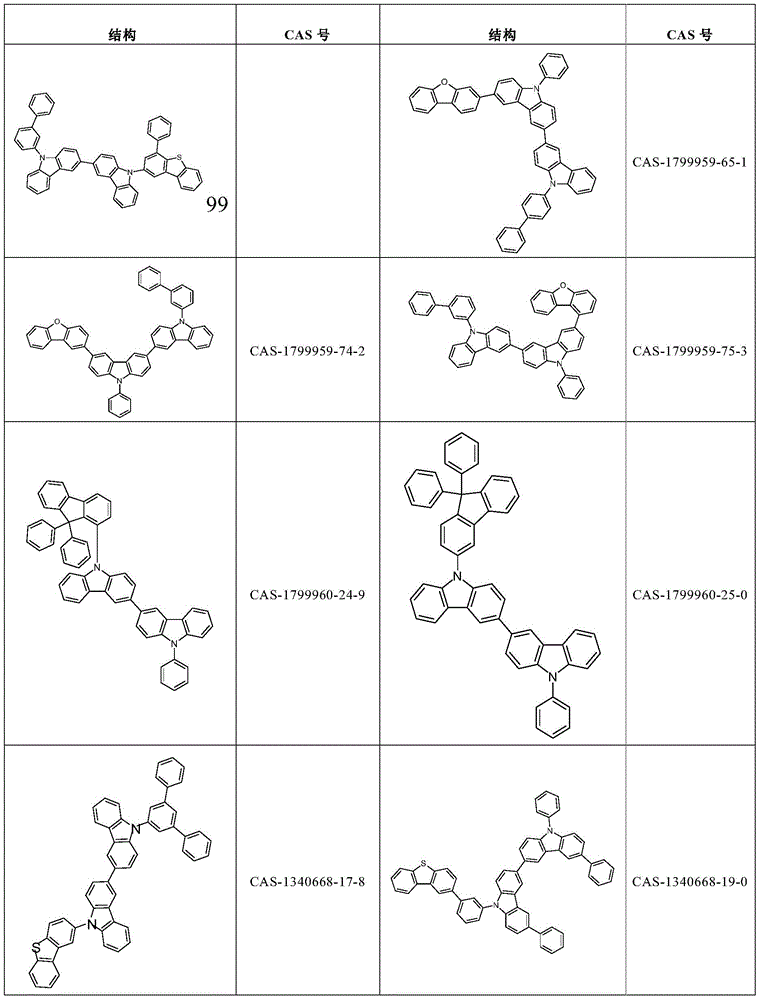
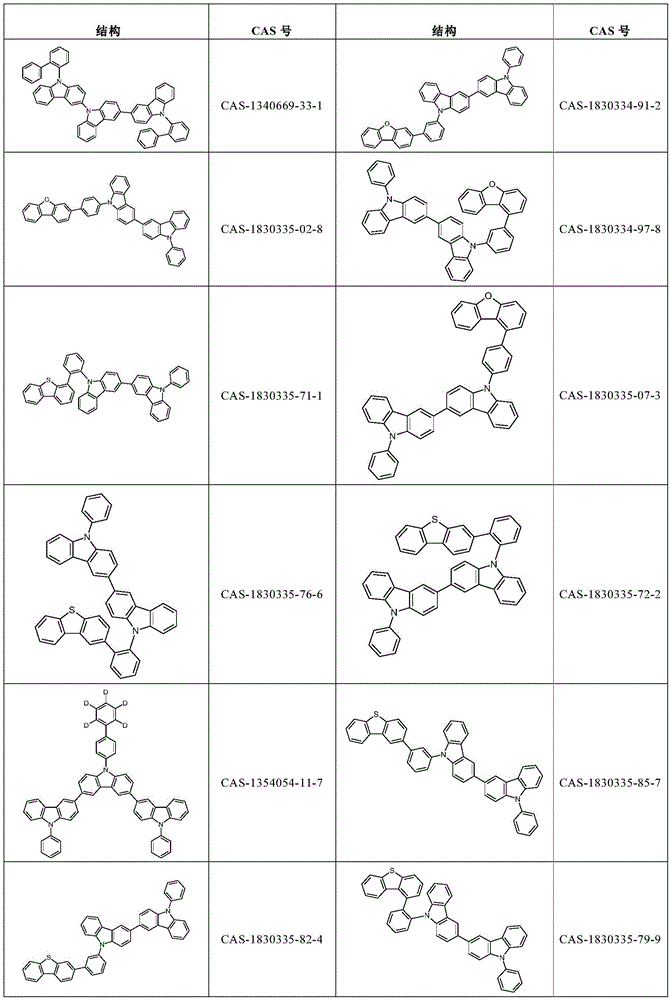
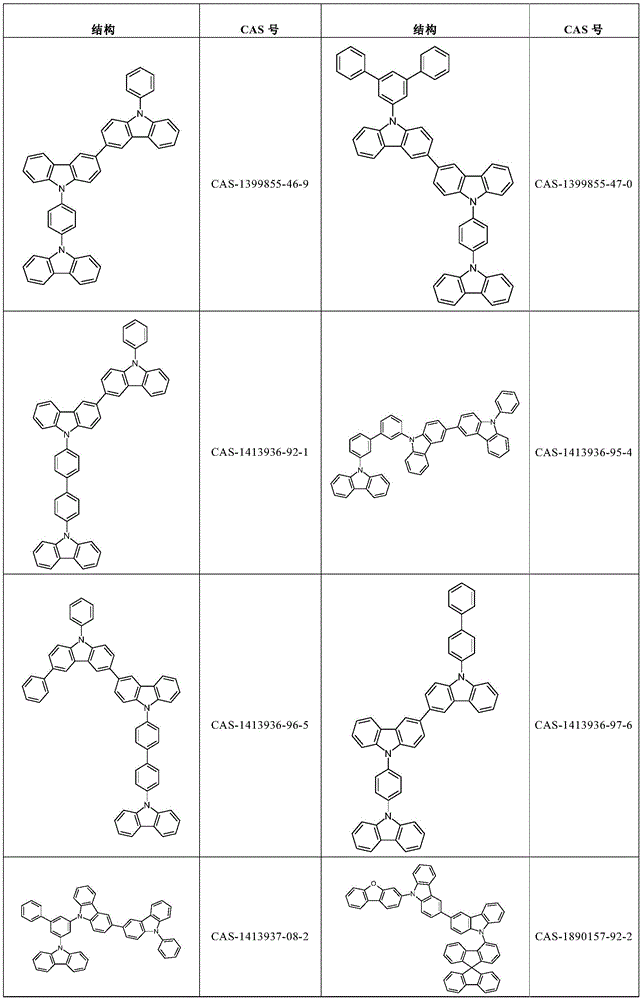
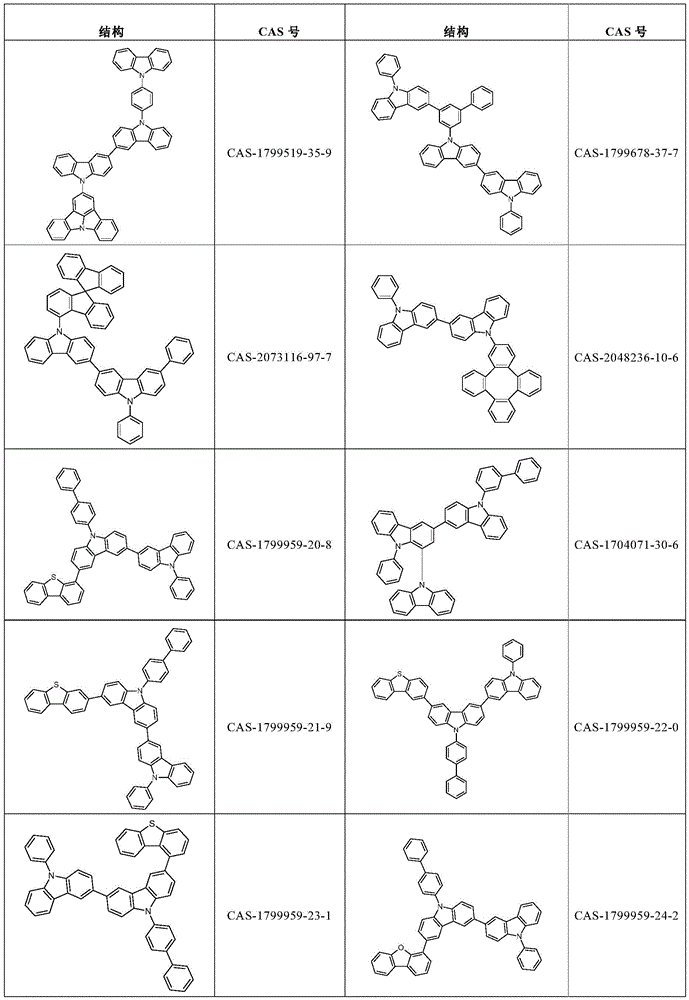
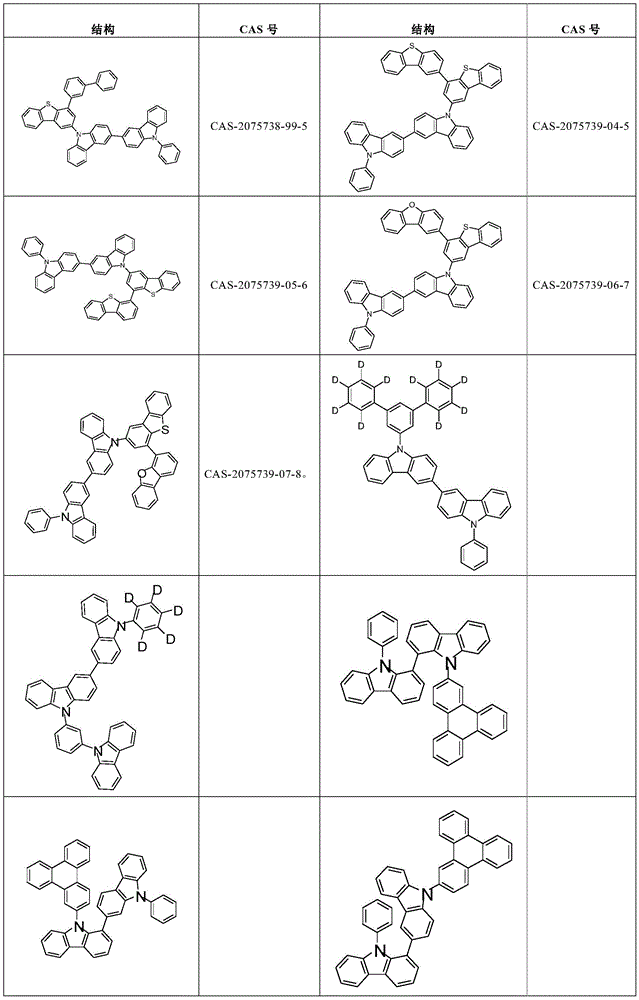
根据本发明选择的合适的式(2)、(2a)或(2b)的化合物的实例是下表9中所示的结构。
表9:
根据本发明选择的式(2)、(2a)或(2b)的化合物的特别合适的实例是如上所述的化合物89至101。
式(2)的化合物或式(2a)和(2b)的优选化合物以及来自表9的化合物的制备是本领域技术人员已知的。化合物可以通过本领域技术人员已知的合成步骤,例如卤化,优选溴化,以及后续的有机金属偶联反应,例如Suzuki偶联、Heck偶联或Hartwig-Buchwald偶联来制备。式(2)的联咔唑中的一些是可商购获得的。
式(2)的化合物或式(2a)和(2b)的优选化合物可以例如根据方案6或方案7制备。
方案6,用于制备式(2)、(2a)或(2b)的不对称联咔唑:
方案7,用于制备式(2)、(2a)或(2b)的对称联咔唑(在该方案中,Ar1和Ar2相同并且缩写为Ar1):
在实验部分中描述了有关合成的其它细节和其它文献引用。
根据本发明,以上提到的式(1)、(1a)至(1l)的主体材料及其优选描述的实施方式或来自表1至8的化合物可以根据需要与所述的式(2)、(2a)和(2b)的主体材料及其优选描述的实施方式或来自表9的化合物进行组合。
对于根据本发明的组合物,式(1)的主体材料与式(2)的主体材料的特别优选的混合物是通过将来自表5至8的化合物1至88与来自表9的化合物组合而获得。
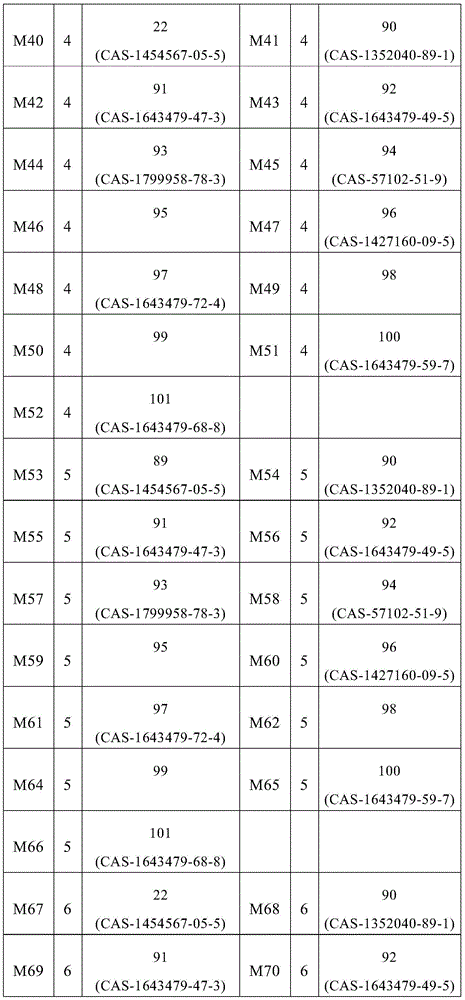
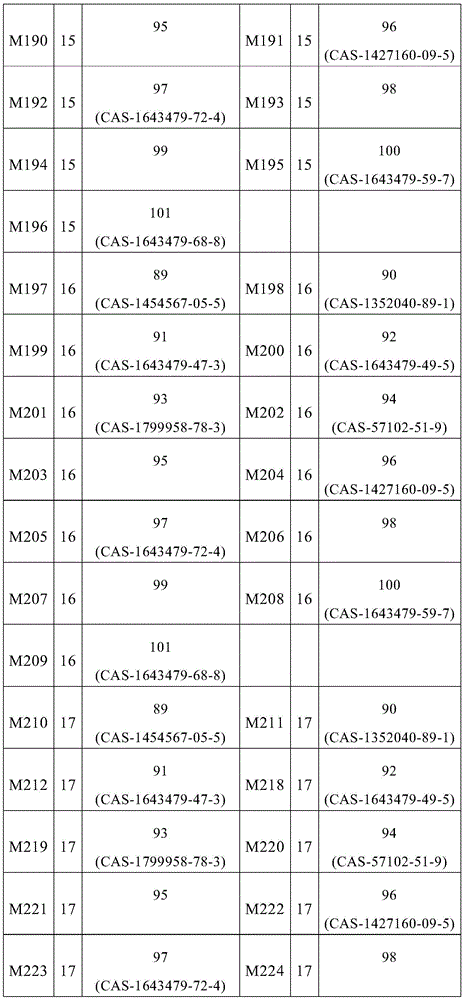
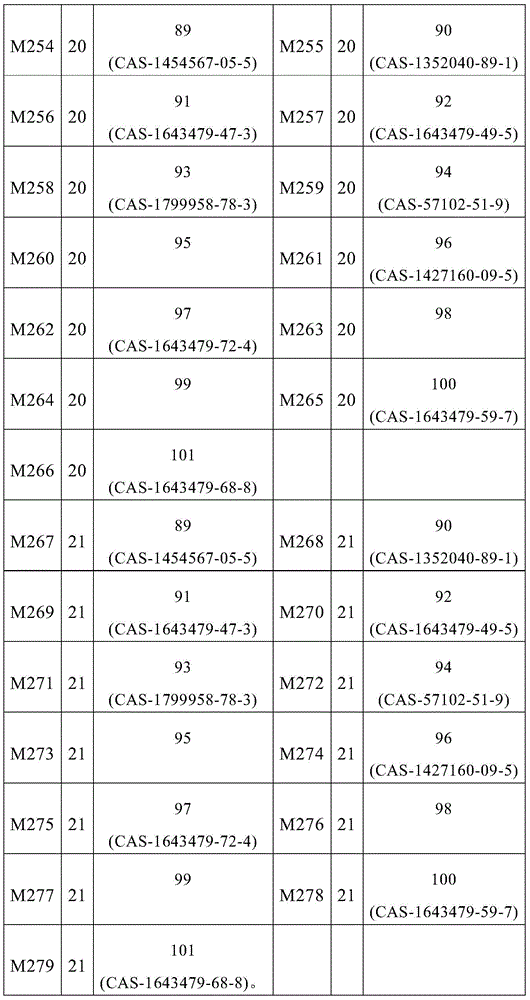
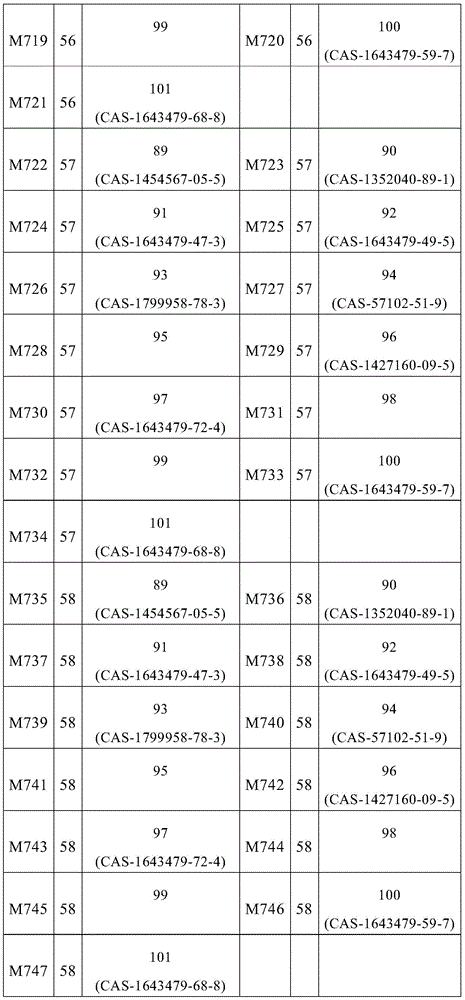
式(1)的主体材料与式(2)的主体材料的非常特别优选的混合物M1至M279是通过将来自表5的化合物1至21与来自表9的化合物89至101组合而获得,如下表10所示的。
表10:
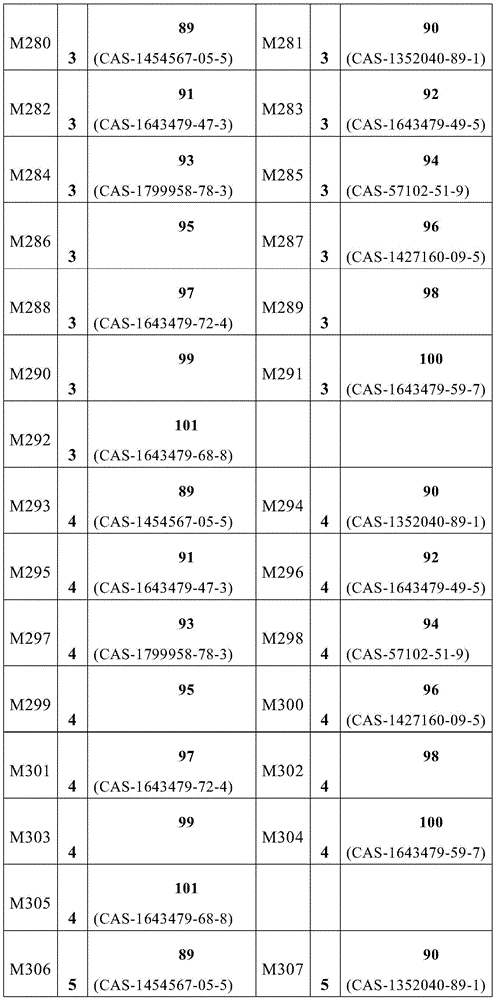
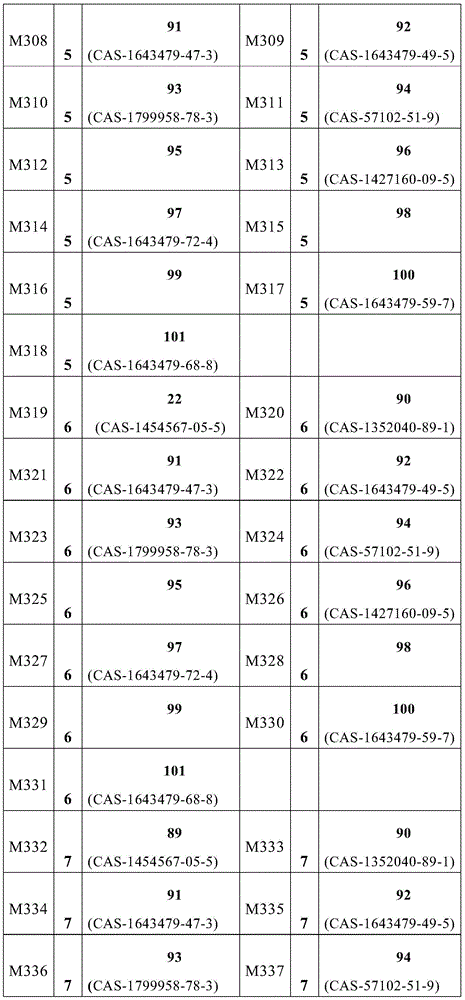
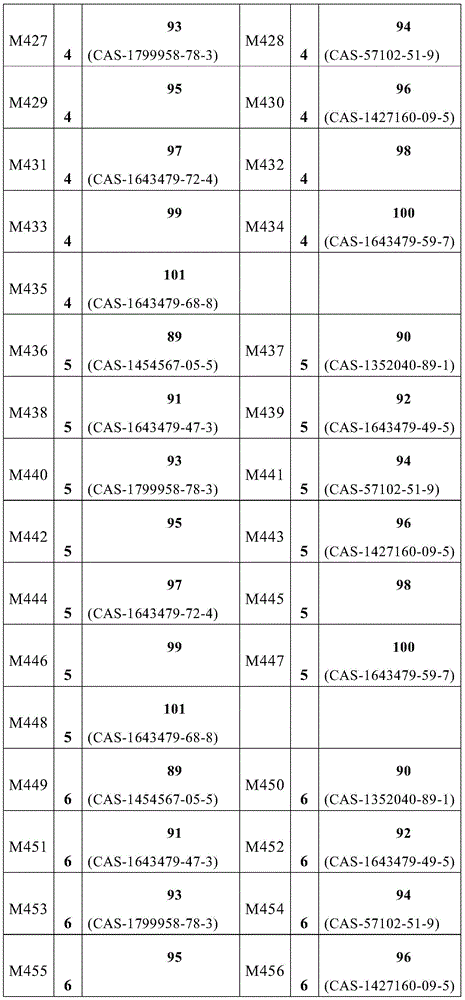
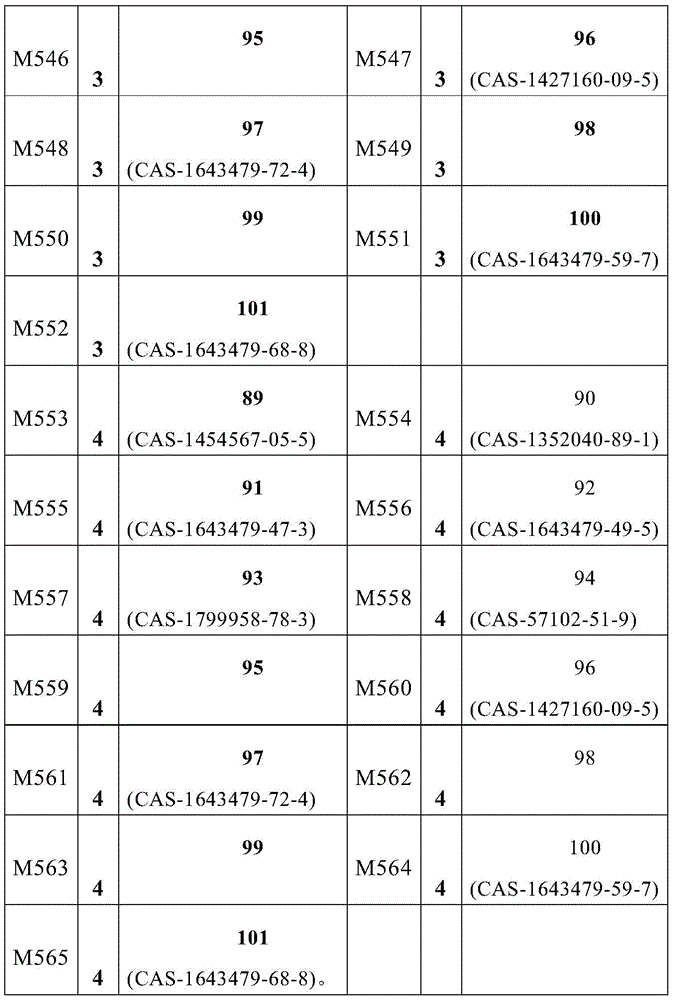
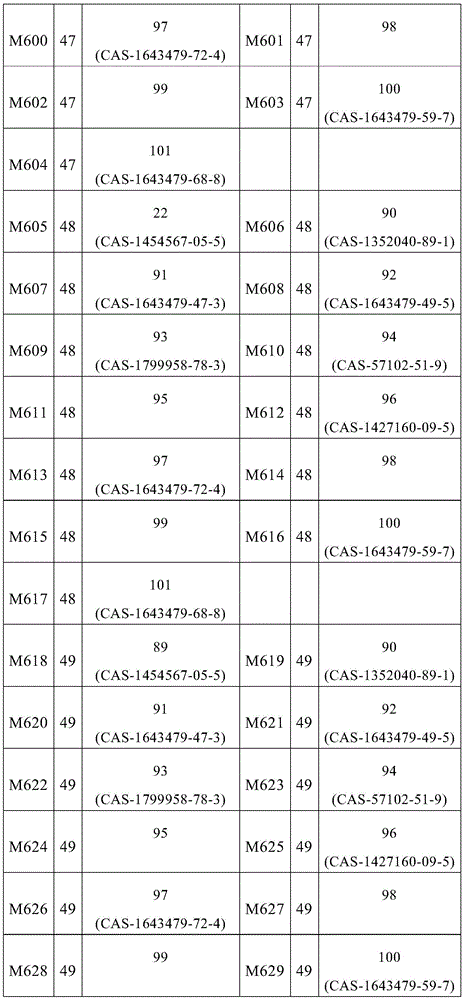
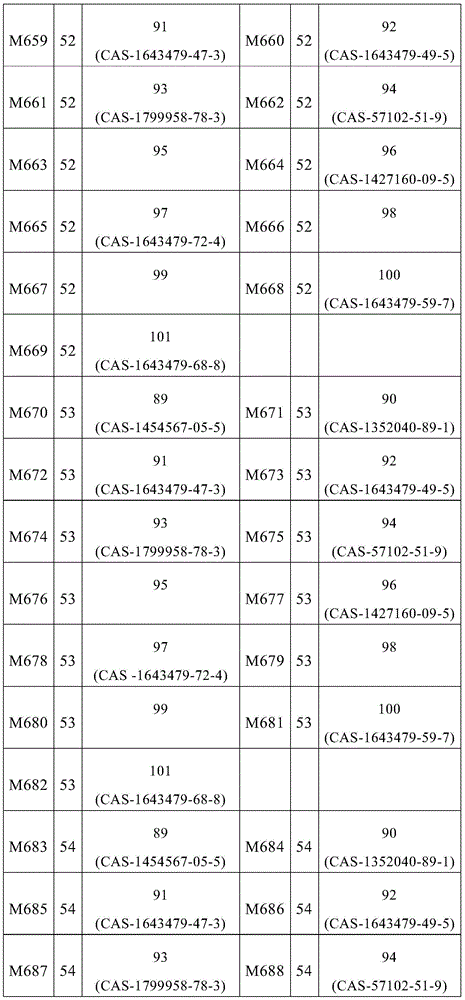
式(1)的主体材料与式(2)的主体材料的非常特别优选的混合物M280至M565是通过将来自表6的化合物23至44与来自表9的化合物89至101组合而获得,如下表11所示的。
表11:
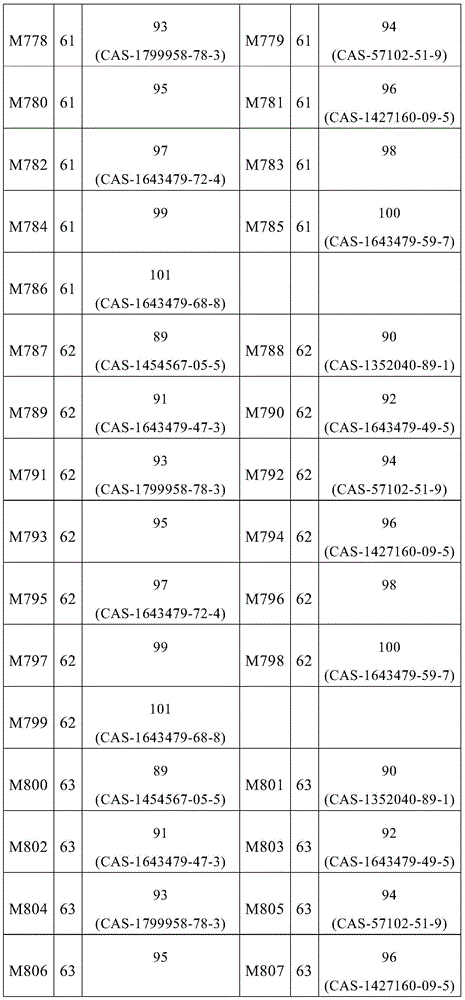
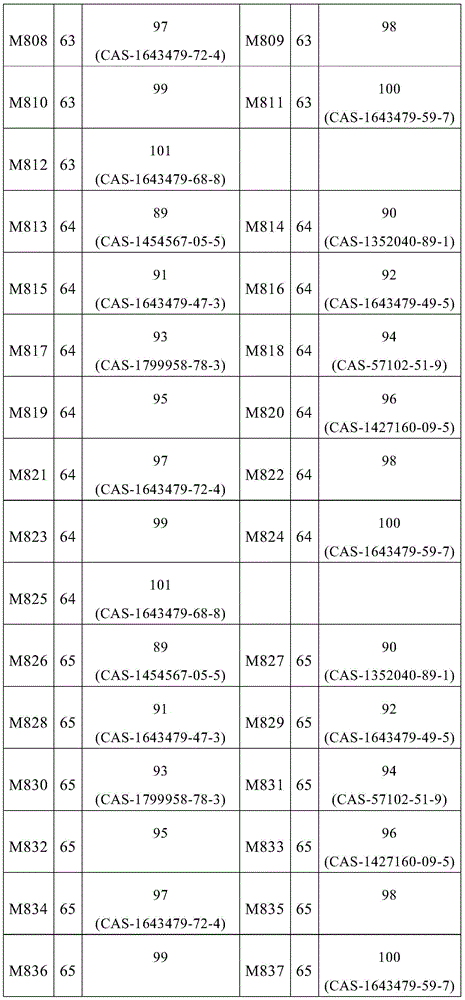
式(1)的主体材料与式(2)的主体材料的非常特别优选的混合物M566至M851是通过将来自表7的化合物45至66与来自表9的化合物89至101组合而获得,如下表12所示的。
表12:
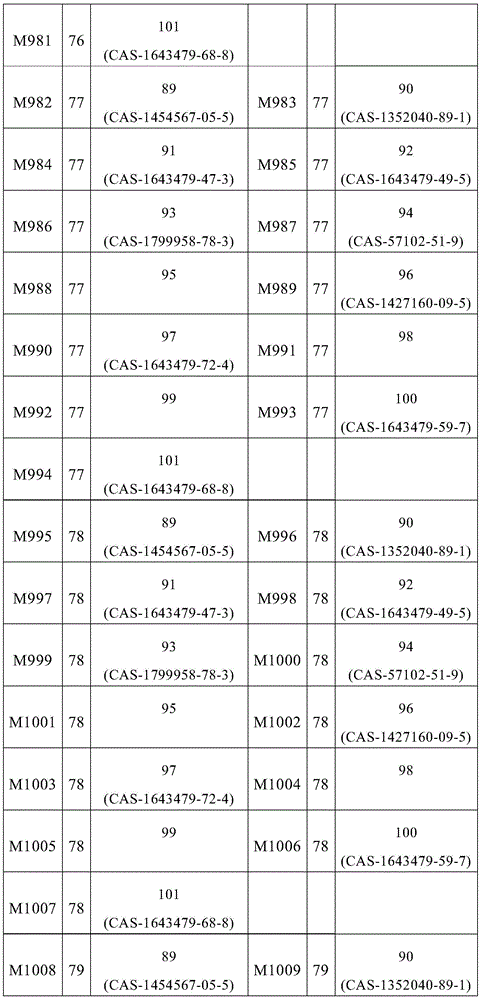
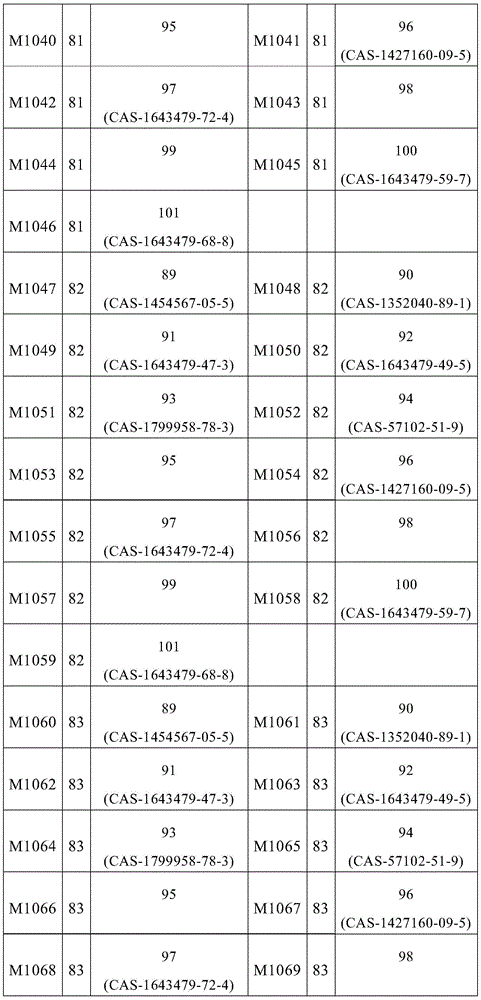
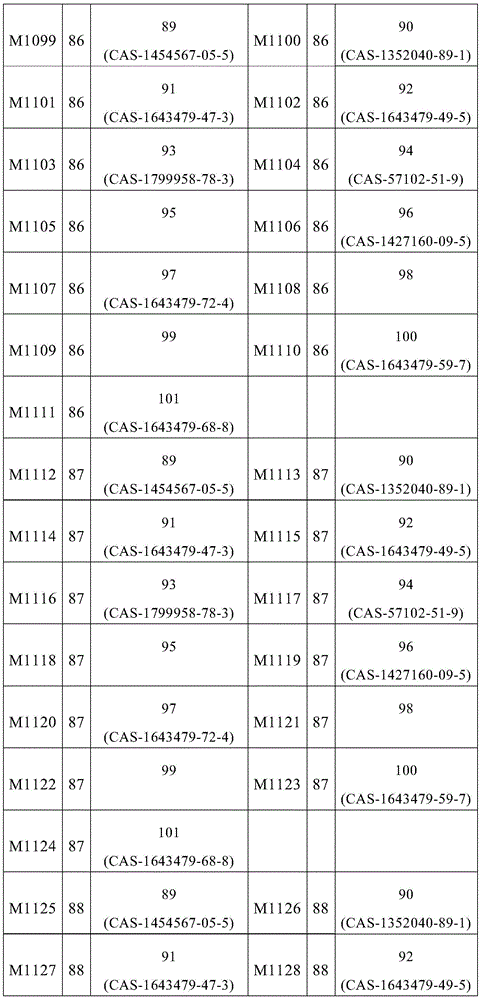
式(1)的主体材料与式(2)的主体材料的非常特别优选的混合物M852至M1137是通过将来自表8的化合物67至88与来自表9的化合物89至101组合而获得,如下表13所示的。
表13:
基于整个组合物计,如上所述或如优选描述的式(1)的电子传输主体在根据本发明的组合物中的浓度是在5重量%至90重量%范围内,优选在10重量%至85重量%范围内,更优选在20重量%至85重量%范围内,甚至更优选在30重量%至80重量%范围内,非常特别优选在20重量%至60重量%范围内,并且最优选在30重量%至50重量%范围内。
基于整个组合物计,如上所述或如优选描述的式(2)的电子传输主体在所述组合物中的浓度是在10重量%至95重量%范围内,优选在15重量%至90重量%范围内,更优选在15重量%至80重量%范围内,甚至更优选在20重量%至70重量%范围内,非常特别优选在40重量%至80重量%范围内,并且最优选在50重量%至70重量%范围内。
基于发光层的全部成分计,如上所述或如优选描述的式(2)的空穴传输主体在发光层中的浓度优选是在40体积%至45体积%范围内;基于发光层的全部成分计,如上所述或如优选描述的式(1)的电子传输主体在发光层中的浓度优选是在40体积%至45体积%范围内。
基于发光层的全部成分计,在发光层中的发光体浓度小于10体积%的情况下,式(2)的空穴传输化合物的体积比例优选高于如上所述或优选描述的式(1)的电子传输化合物的体积比例。基于发光层的全部成分计,在所述实施方式中如上所述或优选描述的式(2)的空穴传输化合物的体积比例优选为65%至75%。
在另一个优选的实施方式中,除了至少一种如上所述或如优选描述的式(1)化合物作为电子传输主体或电子传输基质材料并且至少一种如上所述或如优选描述的式(2)化合物作为空穴传输主体或空穴传输基质材料以外,根据本发明的组合物还可以包含其它化合物,特别是有机功能材料。所述实施方式中的组合物优选形成如下所述的电子器件中的有机层。
因此,本发明还涉及一种组合物,除以上提到的材料以外,所述组合物还包含至少一种选自空穴注入材料、空穴传输材料、空穴阻挡材料、宽带隙材料、荧光发光体、磷光发光体、主体材料、电子阻挡材料、电子传输材料和电子注入材料、n型掺杂剂和p型掺杂剂的另外的化合物。从本领域技术人员已知的多种材料中选择这些材料绝对没有困难。
在此,n型掺杂剂用以指还原剂,即电子给体。n型掺杂剂的优选实例是W(hpp)4和根据WO 2005/086251 A2的其它富电子金属络合物、P=N化合物(例如WO 2012/175535 A1、WO 2012/175219 A1)、萘亚基碳化二亚胺(例如WO 2012/168358 A1)、芴(例如WO 2012/031735 A1)、自由基和双自由基(例如EP 1837926 A1、WO 2007/107306 A1)、吡啶(例如EP2452946 A1、EP 2463927 A1)、N-杂环化合物(例如WO 2009/000237 A1)和吖啶以及吩嗪(例如US 2007/145355 A1)。
在此,p型掺杂剂用以指氧化剂,即电子受体。p型掺杂剂的优选实例是F4-TCNQ、F6-TNAP、NDP-2(诺瓦尔德(Novaled))、NDP-9(诺瓦尔德)、醌(例如EP 1538684 A1、WO 2006/081780 A1、WO 2009/003455 A1、WO 2010/097433 A1)、轴烯(例如EP 1988587 A1、US2010/102709 A1、EP 2180029 A1、WO 2011/131185 A1、WO 2011134458 A1、US 2012/223296 A1)、含S的过渡金属络合物(例如WO 2007/134873 A1、WO 2008/061517 A2、WO2008/061518 A2、DE 102008051737 A1、WO 2009/089821 A1、US 2010/096600 A1)、联咪唑(例如WO 2008/138580 A1)、酞菁(例如WO 2008/058525 A2)、硼杂四氮杂并环戊二烯(例如WO 2007/115540 A1)、富勒烯(例如DE 102010046040 A1)和主族卤化物(例如WO 2008/128519 A2)。
在US 7,294,849的公开内容的意义上,宽带隙材料用以指以至少3.5eV的带隙为特征的材料,其中带隙用以指材料的HOMO能量与LUMO能量之间的间隔。
根据本发明的包含双极性主体和电子传输主体的组合物优选另外包含至少一种发光化合物或发光体,其中磷光发光体是特别优选的。
术语磷光发光体通常涵盖如下化合物,其中通过从具有相对高的自旋多重性的激发态(即自旋态>1)的自旋禁阻跃迁而发光,例如通过从三重态或具有甚至更高的自旋量子数的态(例如,五重态)的跃迁而发光。这优选地用以指从三重态的跃迁。
合适的磷光发光体(=三重态发光体)特别是在合适的激发下优选在可见光区发光的化合物,并且此外含有至少一个原子序数大于20,优选大于38且小于84,特别优选大于56且小于80的原子,特别是具有所述原子序数的金属。所用的磷光发光体优选是含有铜、钼、钨、铼、钌、锇、铑、铱、钯、铂、银、金或铕的化合物,特别是含有铱或铂的化合物。出于本发明的目的,所有包含以上提到的金属的发光化合物都被视为磷光化合物。
通常,合适的磷光络合物是如根据现有技术用于磷光OLED并且如本领域技术人员在有机电致发光器件领域中已知的所有磷光络合物。
所述发光体的实例由申请WO 2016/015815、WO 00/70655、WO 2001/41512、WO2002/02714、WO 2002/15645、EP 1191613、EP 1191612、EP 1191614、WO 05/033244、WO 05/019373、US 2005/0258742、WO 2009/146770、WO 2010/015307、WO 2010/031485、WO 2010/054731、WO 2010/054728、WO 2010/086089、WO 2010/099852、WO 2010/102709、WO 2011/032626、WO 2011/066898、WO 2011/157339、WO 2012/007086、WO 2014/008982、WO 2014/023377、WO 2014/094961、WO 2014/094960、WO 2015/036074、WO 2015/104045、WO 2015/117718、WO 2016/015815、WO 2016/124304、WO 2017/032439、WO 2015/036074、WO 2015/117718和WO 2016/015815揭示。
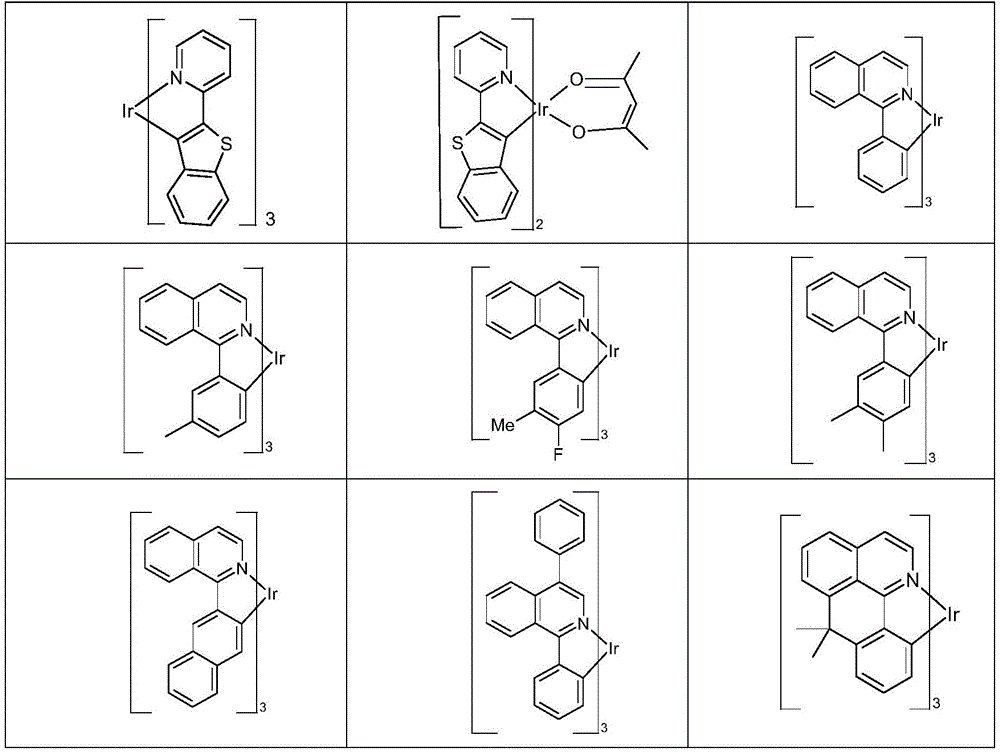
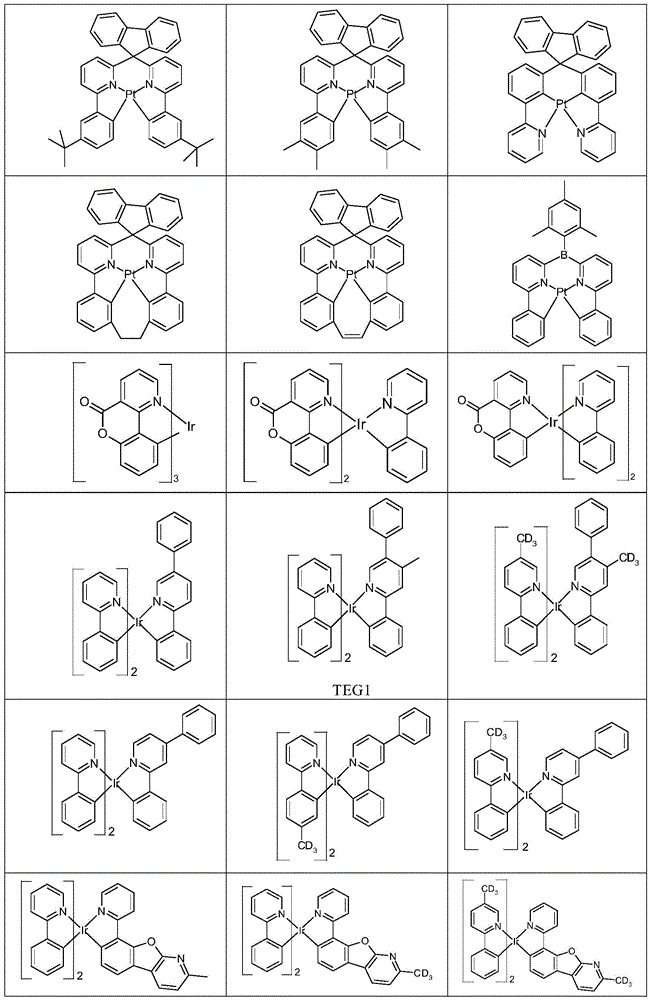
磷光发光体的优选实例在下表14中示出。
表14:
多足磷光发光体的优选实例在下表15中示出。
表15:
在根据本发明的组合物中,每种混合物M1、M2、M3、M4、M5、M6、M7、M8、M9、M10、M11、M12、M13、M14、M15、M16、M17、M18、M19、M20、M21、M22、M23、M24、M25、M26、M27、M28、M29、M30、M31、M32、M33、M34、M35、M36、M37、M38、M39、M40、M41、M42、M43、M44、M45、M46、M47、M48、M49、M50、M51、M52、M53、M54、M55、M56、M57、M58、M59、M60、M61、M62、M63、M64、M65、M66、M67、M68、M69、M70、M71、M72、M73、M74、M75、M76、M77、M78、M79、M80、M81、M82、M83、M84、M85、M86、M87、M88、M89、M90、M91、M92、M93、M94、M95、M96、M97、M98、M99、M100、M101、M102、M103、M104、M105、M106、M107、M108、M109、M110、M111、M112、M113、M114、M115、M116、M117、M118、M119、M120、M121、M122、M123、M124、M125、M126、M127、M128、M129、M130、M131、M132、M133、M134、M135、M136、M137、M138、M139、M140、M141、M142、M143、M144、M145、M146、M147、M148、M149、M150、M151、M152、M153、M154、M155、M156、M157、M158、M159、M160、M161、M162、M163、M164、M165、M166、M167、M168、M169、M170、M171、M172、M173、M174、M175、M176、M177、M178、M179、M180、M181、M182、M183、M184、M185、M186、M187、M188、M189、M190、M191、M192、M193、M194、M195、M196、M197、M198、M199、M200、M201、M202、M203、M204、M205、M206、M207、M208、M209、M210、M211、M212、M213、M214、M215、M216、M217、M218、M219、M220、M221、M222、M223、M224、M225、M226、M227、M228、M229、M230、M231、M232、M233、M234、M235、M236、M237、M238、M239、M240、M241、M242、M243、M244、M245、M246、M247、M248、M249、M250、M251、M252、M253、M254、M255、M256、M257、M258、M259、M260、M261、M262、M263、M264、M265、M266、M267、M268、M269、M270、M271、M272、M273、M274、M275、M276、M277、M278、M279、M280、M281、M282、M283、M284、M285、M286、M287、M288、M289、M290、M291、M292、M293、M294、M295、M296、M297、M298、M299、M300、M301、M302、M303、M304、M305、M306、M307、M308、M309、M310、M311、M312、M313、M314、M315、M316、M317、M318、M319、M320、M321、M322、M323、M324、M325、M326、M327、M328、M329、M330、M331、M332、M333、M334、M335、M336、M337、M338、M339、M340、M341、M342、M343、M344、M345、M346、M347、M348、M349、M350、M351、M352、M353、M354、M355、M356、M357、M358、M359、M360、M361、M362、M363、M364、M365、M366、M367、M368、M369、M370、M371、M372、M373、M374、M375、M376、M377、M378、M379、M380、M381、M382、M383、M384、M385、M386、M387、M388、M389、M390、M391、M392、M393、M394、M395、M396、M397、M398、M399、M400、M401、M402、M403、M404、M405、M406、M407、M408、M409、M410、M411、M412、M413、M414、M415、M416、M417、M418、M419、M420、M421、M422、M423、M424、M425、M426、M427、M428、M429、M430、M431、M432、M433、M434、M435、M436、M437、M438、M439、M440、M441、M442、M443、M444、M445、M446、M447、M448、M449、M450、M451、M452、M453、M454、M455、M456、M457、M458、M459、M460、M461、M462、M463、M464、M465、M466、M467、M468、M469、M470、M471、M472、M473、M474、M475、M476、M477、M478、M479、M480、M481、M482、M483、M484、M485、M486、M487、M488、M489、M490、M491、M492、M493、M494、M495、M496、M497、M498、M499、M500、M501、M502、M503、M504、M505、M506、M507、M508、M509、M510、M511、M512、M513、M514、M515、M516、M517、M518、M519、M520、M521、M522、M523、M524、M525、M526、M527、M528、M529、M530、M531、M532、M533、M534、M535、M536、M537、M538、M539、M540、M541、M542、M543、M544、M545、M546、M547、M548、M549、M550、M551、M552、M553、M554、M555、M556、M557、M558、M559、M560、M561、M562、M563、M564、M565、M566、M567、M568、M569、M570、M571、M572、M573、M574、M575、M576、M577、M578、M579、M580、M581、M582、M583、M584、M585、M586、M587、M588、M589、M590、M591、M592、M593、M594、M595、M596、M597、M598、M599、M600、M601、M602、M603、M604、M605、M606、M607、M608、M609、M610、M611、M612、M613、M614、M615、M616、M617、M618、M619、M620、M621、M622、M623、M624、M625、M626、M627、M628、M629、M630、M631、M632、M633、M634、M635、M636、M637、M638、M639、M640、M641、M642、M643、M644、M645、M646、M647、M648、M649、M650、M651、M652、M653、M654、M655、M656、M657、M658、M659、M660、M661、M662、M663、M664、M665、M666、M667、M668、M669、M670、M671、M672、M673、M674、M675、M676、M677、M678、M679、M680、M681、M682、M683、M684、M685、M686、M687、M688、M689、M690、M691、M692、M693、M694、M695、M696、M697、M698、M699、M700、M701、M702、M703、M704、M705、M706、M707、M708、M709、M710、M711、M712、M713、M714、M715、M716、M717、M718、M719、M720、M721、M722、M723、M724、M725、M726、M727、M728、M729、M730、M731、M732、M733、M734、M735、M736、M737、M738、M739、M740、M741、M742、M743、M744、M745、M746、M747、M748、M749、M750、M751、M752、M753、M754、M755、M756、M757、M758、M759、M760、M761、M762、M763、M764、M765、M766、M767、M768、M769、M770、M771、M772、M773、M774、M775、M776、M777、M778、M779、M780、M781、M782、M783、M784、M785、M786、M787、M788、M789、M790、M791、M792、M793、M794、M795、M796、M797、M798、M799、M800、M801、M802、M803、M804、M805、M806、M807、M808、M809、M810、M811、M812、M813、M814、M815、M816、M817、M818、M819、M820、M821、M822、M823、M824、M825、M826、M827、M828、M829、M830、M831、M832、M833、M834、M835、M836、M837、M838、M839、M840、M841、M842、M843、M844、M845、M846、M847、M848、M849、M850、M851、M852、M853、M854、M855、M856、M857、M858、M859、M860、M861、M862、M863、M864、M865、M866、M867、M868、M869、M870、M871、M872、M873、M874、M875、M876、M877、M878、M879、M880、M881、M882、M883、M884、M885、M886、M887、M888、M889、M890、M891、M892、M893、M894、M895、M896、M897、M898、M899、M900、M901、M902、M903、M904、M905、M906、M907、M908、M909、M910、M911、M912、M913、M914、M915、M916、M917、M918、M919、M920、M921、M922、M923、M924、M925、M926、M927、M928、M929、M930、M931、M932、M933、M934、M935、M936、M937、M938、M939、M940、M941、M942、M943、M944、M945、M946、M947、M948、M949、M950、M951、M952、M953、M954、M955、M956、M957、M958、M959、M960、M961、M962、M963、M964、M965、M966、M967、M968、M969、M970、M971、M972、M973、M974、M975、M976、M977、M978、M979、M980、M981、M982、M983、M984、M985、M986、M987、M988、M989、M990、M991、M992、M993、M994、M995、M996、M997、M998、M999、M1000、M1001、M1002、M1003、M1004、M1005、M1006、M1007、M1008、M1009、M1010、M1011、M1012、M1013、M1014、M1015、M1016、M1017、M1018、M1019、M1020、M1021、M1022、M1023、M1024、M1025、M1026、M1027、M1028、M1029、M1030、M1031、M1032、M1033、M1034、M1035、M1036、M1037、M1038、M1039、M1040、M1041、M1042、M1043、M1044、M1045、M1046、M1047、M1048、M1049、M1050、M1051、M1052、M1053、M1054、M1055、M1056、M1057、M1058、M1059、M1060、M1061、M1062、M1063、M1064、M1065、M1066、M1067、M1068、M1069、M1070、M1071、M1072、M1073、M1074、M1075、M1076、M1077、M1078、M1079、M1080、M1081、M1082、M1083、M1084、M1085、M1086、M1087、M1088、M1089、M1090、M1091、M1092、M1093、M1094、M1095、M1096、M1097、M1098、M1099、M1100、M1101、M1102、M1103、M1104、M1105、M1106、M1107、M1108、M1109、M1110、M1111、M1112、M1113、M1114、M1115、M1116、M1117、M1118、M1119、M1120、M1121、M1122、M1123、M1124、M1125、M1126、M1127、M1128、M1129、M1130、M1131、M1132、M1133、M1134、M1135、M1136或M1137优选与选自表14或15的化合物组合。
根据本发明的包含至少一种磷光发光体的组合物优选形成发红外光、黄光、橙光、红光、绿光、蓝光或紫外光的层,特别优选形成发黄光或绿光的层,并且非常特别地优选形成发绿光的层。
在此,发黄光的层用以指其光致发光最大值在540nm至570nm范围内的层。发橙光的层用以指其光致发光最大值在570nm至600nm范围内的层。发红光的层用以指其光致发光最大值在600nm至750nm范围内的层。发绿光的层用以指其光致发光最大值在490nm至540nm范围内的层。发蓝光的层用以指其光致发光最大值在440nm至490nm范围内的层。在此,通过在室温下测量层厚度为50nm的层的光致发光光谱来确定所述层的光致发光,其中所述层包含根据本发明的组合物,即包含发光体和基质。
例如,使用可商购获得的光致发光光谱仪来记录所述层的光致发光光谱。
通常在10-5摩尔浓度的无氧溶液中测量所选发光体的光致发光光谱,其中测量在室温下进行,并且所选发光体以所述浓度溶解于其中的任何溶剂都是合适的。特别合适的溶剂通常是甲苯或2-甲基-THF,还有二氯甲烷。使用可商购获得的光致发光光谱仪进行测量。由发光体的光致发光光谱确定以eV计的三重态能量T1。首先,确定光致发光光谱的最大峰值Pl最大(nm)。然后,根据E(T1,eV)=1240/E(T1,nm)=1240/Pl最大(nm),将最大峰值Pl最大(nm)转化成以eV计。
因此,优选的磷光发光体是红外发光体,优选来自表14或15,其三重态能量T1优选是约1.9eV至约1.0eV。
因此,优选的磷光发光体是红色发光体,优选来自表14或15,其三重态能量T1优选是约2.1eV至约1.9eV。
因此,优选的磷光发光体是黄色发光体,优选来自表14或15,其三重态能量T1优选是约2.3eV至约2.1eV。
因此,优选的磷光发光体是绿色发光体,优选来自表14或15,其三线态能量T1优选是约2.5eV至约2.3eV。
因此,优选的磷光发光体是蓝色发光体,优选来自表14或15,其三线态能量T1优选是约3.1eV至约2.5eV。
因此,优选的磷光发光体是紫外发光体,优选来自表14或15,其三线态能量T1优选是约4.0eV至约3.1eV。
因此,特别优选的磷光发光体是绿色或黄色发光体,优选来自表14或15,如上所述。
因此,非常特别优选的磷光发光体是绿色发光体,优选来自表14或15,其三线态能量T1优选为约2.5eV至约2.3eV。
对于根据本发明的组合物或根据本发明的发光层,非常特别优选选择如上所述的优选来自表14或15的绿色发光体。
优选的荧光发光体选自芳基胺类。在本发明意义上,芳基胺或芳族胺用以指含有三个与氮直接键合的取代或未取代的芳族或杂芳族环系的化合物。这些芳族或杂芳族环系中的至少一个优选是稠合环系,特别优选具有至少14个芳族环原子的稠合环系。其优选实例是芳族蒽胺、芳族蒽二胺、芳族芘胺、芳族芘二胺、芳族苣胺或芳族苣二胺。芳族蒽胺用以指其中一个二芳基氨基基团优选在9位与蒽基团直接键合的化合物。芳族蒽二胺用以指其中两个二芳基氨基基团优选在9,10-位上与蒽基团直接键合的化合物。以与此类似的方式定义芳族芘胺、芳族芘二胺、芳族苣胺和芳族苣二胺,其中所述二芳基氨基基团优选在1位或在1,6位与芘键合。其它优选的荧光发光体是茚并芴胺或茚并芴二胺,例如根据WO 2006/108497或WO 2006/122630;苯并茚并芴胺或苯并茚并芴二胺,例如根据WO 2008/006449;和二苯并茚并芴胺或二苯并茚并芴二胺,例如根据WO 2007/140847;以及具有稠合芳基基团的茚并芴衍生物,其公开在WO 2010/012328中。
在本发明的另一个优选的实施方式中,根据本发明的组合物用作混合基质体系的组分。所述混合基质体系优选包含三种或四种不同的基质材料,特别优选三种不同的基质材料(即,除了根据本发明的组合物以外的其它基质组分)。可以与根据本发明的组合物组合用作混合基质体系的基质组分的特别合适的基质材料选自宽带隙材料、电子传输材料(ETM)和空穴传输材料(HTM)。
混合基质体系优选用于磷光有机电致发光器件中。关于混合基质体系的更精确的细节尤其在申请WO 2010/108579中给出。可以与根据本发明的组合物组合用作磷光或荧光有机电致发光器件中的混合基质体系的基质组分的特别合适的基质材料选自以下对于磷光发光体指示的优选基质材料或对于荧光发光体指示的优选基质材料,这取决于所使用的发光体的类型。所述混合基质体系优选对于表14或15中的发光体进行优化。
除特别优选包含选自M1至M1137的材料的混合物的如上所述的根据本发明的组合物以外,优选用于荧光发光体的合适的其它主体材料是各种类别的物质。优选的其它主体材料选自以下类别:低聚芳亚基(例如,根据EP 676461的2,2',7,7'-四苯基螺二芴,或二萘基蒽),特别是含有稠合芳族基团的低聚芳亚基,低聚芳亚基乙烯亚基(例如,DPVBi或螺-DPVBi,根据EP 676461),多足金属络合物(例如,根据WO 2004/081017),空穴传导化合物(例如,根据WO 2004/058911),电子传导化合物,特别是酮、氧化膦、亚砜等(例如,根据WO2005/084081和WO 2005/084082),阻转异构体(例如,根据WO 2006/048268),硼酸衍生物(例如,根据WO 2006/117052)或苯并蒽(例如,根据WO 2008/145239)。特别优选的基质材料选自以下类别:包含萘、蒽、苯并蒽和/或芘的低聚芳亚基或这些化合物的阻转异构体,低聚芳亚基乙烯亚基,酮,氧化膦和亚砜。非常特别优选的基质材料选自包含蒽、苯并蒽、苯并菲和/或芘的低聚芳亚基类或这些化合物的阻转异构体。在本发明的意义上,低聚芳亚基旨在用以指其中至少三个芳基或芳亚基基团彼此键合的化合物。
除特别优选包含选自M1至M1137的材料的混合物的如上所述的根据本发明的组合物以外,优选用于磷光发光体的合适的其它基质材料是各种类别的物质。优选的其它基质材料选自以下类别:芳族胺,特别是三芳基胺,例如根据US 2005/0069729;咔唑衍生物(例如,CBP、N,N-双咔唑基联苯)或化合物,根据WO 2005/039246、US 2005/0069729、JP 2004/288381、EP 1205527或WO 2008/086851,桥连咔唑衍生物,例如根据WO 2011/088877和WO2011/128017,茚并咔唑衍生物,例如根据WO 2010/136109和WO 2011/000455,氮杂咔唑衍生物,例如根据EP 1617710、EP 1617711、EP 1731584、JP 2005/347160,吲哚并咔唑衍生物,例如根据WO 2007/063754或WO 2008/056746;酮,例如根据WO 2004/093207或WO 2010/006680;氧化膦、亚砜和砜,例如根据WO 2005/003253;低聚苯亚基;双极性基质材料,例如根据WO 2007/137725;硅烷,例如根据WO 2005/111172;硼氮杂环戊熳或硼酸酯,例如根据WO 2006/117052;三嗪衍生物,例如根据WO 2010/015306、WO 2007/063754或WO 2008/056746;锌络合物,例如根据EP 652273或WO 2009/062578;铝络合物,例如BAlq;硅二氮杂环戊熳和硅四氮杂环戊熳衍生物,例如,根据WO 2010/054729;磷二氮杂环戊熳衍生物,例如根据WO 2010/054730;以及铝络合物,例如BAlQ。
根据本发明的一个可替代的实施方式,除电子传输主体和空穴传输主体的组分以外,所述组合物不包含其它组分,即功能材料。所述实施方式涉及按原样用于制造有机层的材料混合物。所述体系也称为预混体系,所述体系是在气相沉积期间用作唯一的材料源。这使得能够以简单且快速的方式实现具有组分的更均匀分布的层的气相沉积,而无需精确地控制多种必要材料源。
因此,本发明另外涉及一种由式(1)、(1a)至(1l)的化合物或选自1至88的化合物和式(2)、(2a)、(2b)的化合物或选自89至101的化合物组成的组合物。
如上所述或优选描述的根据本发明的组合物适合用于有机电子器件中。在此,有机电子器件用以指包括至少一个包含至少一种有机化合物的层的器件。然而,所述器件还可以包含无机材料或者还包括完全由无机材料构成的层。
因此,本发明另外涉及如上所述或优选描述的组合物,特别是选自M1至M1137的混合物在有机电子器件中的用途。
所述组合物的组分或成分可以通过气相沉积或从溶液中进行处理。如果组合物是从溶液中施用的,则根据本发明的组合物的制剂必须包含至少一种其它溶剂。这些制剂可以是例如溶液、分散体或乳液。为此目的,可以优选使用两种或更多种溶剂的混合物。
因此,本发明另外涉及一种包含根据本发明的组合物和至少一种溶剂的制剂。
合适且优选的溶剂例如是甲苯,苯甲醚,邻-、间-或对-二甲苯,苯甲酸甲酯,均三甲苯,四氢化萘,藜芦醚,THF,甲基-THF,THP,氯苯,二烷,苯氧基甲苯、特别是3-苯氧基甲苯,(-)-葑酮,1,2,3,5-四甲基苯,1,2,4,5-四甲基苯,1-甲基萘,2-甲基苯并噻唑,2-苯氧基乙醇,2-吡咯烷酮,3-甲基苯甲醚,4-甲基苯甲醚,3,4-二甲基苯甲醚,3,5-二甲基苯甲醚,苯乙酮,α-萜品醇,苯并噻唑,苯甲酸丁酯,异丙苯,环己醇,环己酮,环己基苯,十氢化萘,十二烷基苯,苯甲酸乙酯,茚满,苯甲酸甲酯,NMP,对伞花烃,苯乙醚,1,4-二异丙基苯,二苄基醚,二乙二醇丁基甲基醚,三乙二醇丁基甲基醚,二乙二醇二丁基醚,三乙二醇二甲基醚,二乙二醇单丁基醚,三丙二醇二甲基醚,四乙二醇二甲基醚,2-异丙基萘,戊基苯,己基苯,庚基苯,辛基苯,1,1-双(3,4-二甲基苯基)乙烷、六甲基二氢化茚或这些溶剂的混合物。
在此,所述制剂还可以包含至少一种其它有机或无机化合物,所述化合物同样用于电子器件中,例如发光化合物,特别是磷光发光体,和/或其它基质材料。以上已经提到了合适的发光化合物和其它基质材料。
本发明还涉及根据本发明的组合物在有机电子器件中,优选在电子传输和/或发光层中的用途。
有机电子器件优选选自有机集成电路(OIC)、有机场效应晶体管(OFET)、有机薄膜晶体管(OTFT)、有机电致发光器件、有机太阳能电池(OSC)、有机光学检测器和有机光感受器,其中特别优选有机电致发光器件。
使用根据本发明的组合物的非常特别优选的有机电致发光器件是有机发光晶体管(OLET)、有机场猝熄器件(OFQD)、有机发光电化学电池(OLEC、LEC、LEEC)、有机激光二极管(O-laser)和有机发光二极管(OLED),特别优选OLEC和OLED,并且最优选OLED。
如上所述或如优选描述的根据本发明的组合物优选在电子器件中在具有电子传输功能的层中使用。所述层优选是电子注入层(EIL)、电子传输层(ETL)、空穴阻挡层(HBL)和/或发光层(EML),特别优选是ETL、EIL和/或EML。根据本发明的组合物特别优选在EML中特别是用作基质材料。
因此,本发明另外还涉及一种有机电子器件,所述有机电子器件特别选自以上提到的电子器件之一,并且优选在发光层(EML)中,在电子传输层(ETL)中,在电子注入层(EIL)中和/或在空穴阻挡层(HBL)中,非常优选在EML、EIL和/或ETL中并且非常特别优选在EML中包含如上所述或优选描述的根据本发明的组合物。
在发光层的情况下,这特别优选是磷光层,所述磷光层的特征在于,除如上所述或优选描述的组合物以外,其还包含磷光发光体,特别地连同来自表14或15的发光体或如上所述的优选发光体一起。
因此,在本发明的一个特别优选的实施方式中,所述电子器件是有机电致发光器件,非常特别优选地是有机发光二极管(OLED),其在发光层(EML)中包含如上所述或优选描述的根据本发明的组合物以及磷光发光体。
基于包含发光体和基质材料的整体组合物,根据优选实施方式的根据本发明的组合物和发光化合物优选包含99.9至1体积%,进一步优选99至10体积%,特别优选98至60体积%,非常特别优选97至80体积%的根据优选实施方式包含至少一种式(1)的化合物和至少一种式(2)的化合物的基质材料。相应地,基于包含发光体和基质材料的整体组合物,所述组合物优选包含0.1至99体积%,进一步优选1至90体积%,特别优选2至40体积%,非常特别优选3至20体积%的发光体。如果化合物是从溶液中处理的,则优选使用相应的以重量%计的量,而不是以上提到的以体积%计的量。
除了阴极、阳极和包含根据本发明的组合物的层之外,电子器件还可以包括其它层。这些层在每种情况下选自例如一个或多个空穴注入层、空穴传输层、空穴阻挡层、发光层、电子传输层、电子注入层、电子阻挡层、激子阻挡层、中间层、电荷产生层(IDMC 2003,台湾(Taiwan);会议21OLED(5),T.Matsumoto,T.Nakada,J.Endo,K.Mori,N.Kawamura,A.Yokoi,J.Kido,具有电荷产生层的多光子有机EL器件(Multiphoton Organic EL DeVice Having Charge Generation Layer)和/或有机或无机p/n结。然而,应该指出,并非必须存在这些层中的每个层。
有机电致发光器件中的层的顺序优选如下:
阳极/空穴注入层/空穴传输层/发光层/电子传输层/电子注入层/阴极。
所述层顺序是优选的顺序。
在此应当再次指出,并非必须存在所有的所述层,和/或可以另外存在其它层。
根据本发明的包含根据本发明的组合物的有机电致发光器件可以包括多个发光层。在这种情况下,这些发光层特别优选总共具有在380nm与750nm之间的多个发射最大值,总体上产生白色发光,即在发光层中使用能够发荧光或发磷光并且发射蓝色或黄色或橙色或红色光的多种发光化合物。特别优选三层体系,即,具有三个发光层的体系,其中这三个层表现出蓝色、绿色和橙色或红色发光(对于基本结构,参见例如WO 2005/011013)。应当注意,为了产生白光,代替多种发出颜色的发光体化合物,一种单独使用的在宽波长范围内发射的发光体化合物也可以是合适的。
可用于根据本发明的有机电致发光器件的空穴注入或空穴传输层或电子阻挡层或电子传输层中的合适的电荷传输材料例如是公开在Y.Shirota等,Chem.Rev.2007,107(4),953-1010中的化合物,或如在根据现有技术在这些层中使用的其它材料。
可以用于电子传输层的材料是如根据现有技术作为电子传输层中的电子传输材料使用的所有材料。特别合适的是铝络合物,例如Alq3;锆络合物,例如Zrq4;苯并咪唑衍生物;三嗪衍生物;嘧啶衍生物;吡啶衍生物;吡嗪衍生物;喹喔啉衍生物;喹啉衍生物;二唑衍生物;芳族酮;内酰胺;硼烷;磷二氮杂环戊熳衍生物和氧化膦衍生物。其它合适的材料是如JP 2000/053957、WO 2003/060956、WO 2004/028217、WO 2004/080975和WO 2010/072300中公开的以上提到的化合物的衍生物。
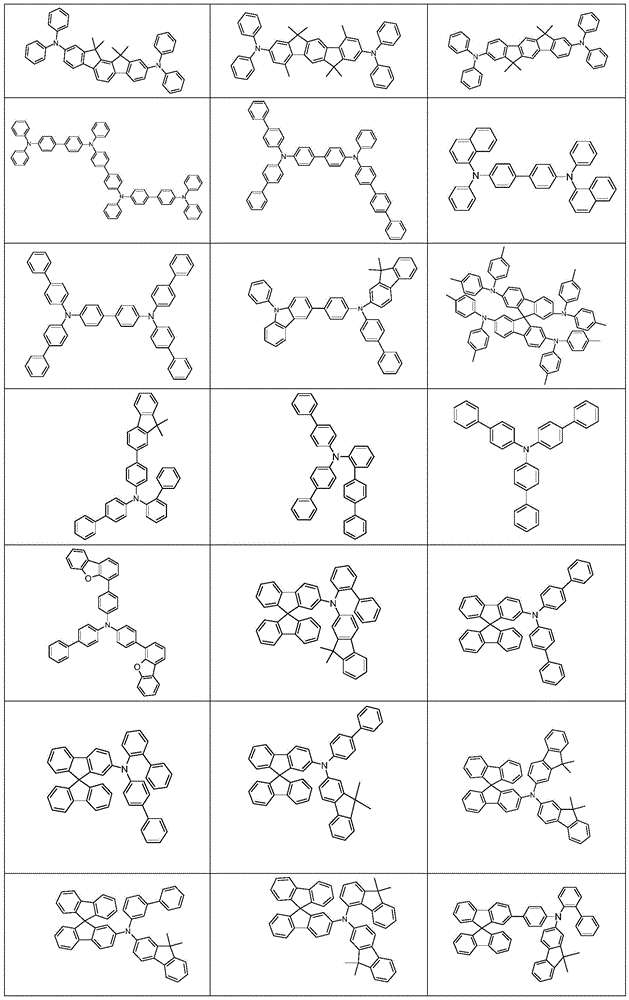
优选的空穴传输材料特别是可以用于空穴传输、空穴注入或电子阻挡层中的材料,诸如茚并芴胺衍生物(例如根据WO 06/122630或WO 06/100896),EP 1661888中公开的胺衍生物,六氮杂苯并菲衍生物(例如根据WO 01/049806),含有稠合芳族环的胺衍生物(例如根据US 5,061,569),WO 95/09147中公开的胺衍生物,单苯并茚并芴胺(例如根据WO 08/006449),二苯并茚并芴胺(例如根据WO 07/140847),螺二芴胺(例如根据WO 2012/034627或仍未公开的EP 12000929.5),芴胺(例如根据WO 2014/015937、WO 2014/015938和WO2014/015935),螺二苯并吡喃胺(例如根据WO 2013/083216)和二氢吖啶衍生物(例如根据WO 2012/150001)。
其它合适的空穴传输材料是以下化合物:
电子器件的阴极优选包含具有低逸出功的金属、包含多种金属的金属合金或多层结构,这些金属诸如为碱土金属、碱金属、主族金属或镧系元素(例如Ca、Ba、Mg、Al、In、Mg、Yb、Sm等)。另外合适的是包含碱金属或碱土金属和银的合金,例如包含镁和银的合金。在多层结构的情况下,除了所述金属之外,还可以使用具有相对高逸出功的其它金属,例如Ag和Al,在这种情况下,通常使用金属的组合,诸如Ca/Ag、Mg/Ag或Ba/Ag。也可以优选在金属阴极与有机半导体之间引入具有高介电常数的材料的薄中间层。适合于这个目的的例如是碱金属氟化物或碱土金属氟化物,也可以是相应的氧化物或碳酸盐(例如LiF、Li2O、BaF2、MgO、NaF、CsF、Cs2CO3等)。另外,对于此目的,可以使用喹啉锂(LiQ)。所述层的层厚度优选在0.5nm与5nm之间。
阳极优选包含具有高逸出功的材料。阳极优选相对于真空具有大于4.5eV的逸出功。一方面,适于该目的的是具有高氧化还原电位的金属,例如Ag、Pt或Au。另一方面,也可以优选金属/金属氧化物电极(例如Al/Ni/NiOx、Al/PtOx)。对于一些应用,至少一个电极必须是透明或部分透明的,以便于有机材料的照射(有机太阳能电池)或光的耦合输出(OLED、O-laser)。在此优选的阳极材料是导电的混合金属氧化物。特别优选的是氧化锡铟(ITO)或氧化铟锌(IZO)。另外优选导电掺杂的有机材料,特别导电掺杂的聚合物。另外,阳极也可以由多层组成,例如由ITO的内层和金属氧化物,优选氧化钨、氧化钼或氧化钒的外层组成。
在制造期间,所述有机电子器件被适当地(根据应用)结构化,设置接触点并最终密封,因为根据本发明的器件的寿命在存在水和/或空气的情况下缩短。
在另一个优选的实施方式中,包含根据本发明的组合物的有机电子器件的特征在于一个或多个包含根据本发明的组合物的层是借助于升华工艺施加,其中所述材料通过在真空升华单元中在小于10-5毫巴,优选小于10-6毫巴的初始压力下气相沉积而施加。然而,在此初始压力也可以甚至更低,例如小于10-7毫巴。
同样优选的是一种有机电致发光器件,其特征在于一个或多个层是借助于OVPD(有机气相沉积)工艺或借助载气升华施加,其中材料是在10-5毫巴与1巴之间的压力下施加。所述方法的一个特例是OVJP(有机蒸气喷射印刷)工艺,其中材料直接通过喷嘴施加并因此结构化(例如M.S.Arnold等,Appl.Phys.Lett.2008,92,053301)。
此外优选一种有机电致发光器件,其特征在于,一个或多个层是自溶液中例如通过旋涂,或通过任何所需印刷工艺如丝网印刷、柔版印刷、喷嘴印刷或胶版印刷,但是特别优选LITI(光诱导热成像、热转移印刷)或喷墨印刷来制造。为此目的,需要根据本发明的组合物的组分的可溶性化合物。通过适当取代相应化合物可以实现高溶解性。从溶液中处理的优点在于,可以非常简单且廉价地施加包含根据本发明的组合物的层。所述技术特别适合批量制造有机电子器件。
混合工艺也是可行的,其中例如一个或多个层是从溶液中施加,并且一个或多个另外的层是通过气相沉积施加。
这些工艺对于本领域技术人员来说通常是已知的,并且可以应用到有机电致发光器件。
因此,本发明另外涉及一种用于制造包含如上所述或优选描述的根据本发明的组合物的有机电子器件的方法,其特征在于至少一个包含根据本发明的组合物的有机层是通过气相沉积,特别是通过升华工艺和/或通过OVPD(有机气相沉积)工艺和/或借助于载气升华,或者从溶液中,特别是通过旋涂或通过印刷工艺来施加的。
在通过气相沉积制造有机电子器件的情况下,对于可以如何将旨在包含根据本发明的组合物并且可以包含多种不同成分的有机层施加或气相沉积在任何所需基底上,基本上有两种可行性。一方面,所用的材料可以各自存在于一个材料源中,并且最终从多个材料源中蒸发(“共蒸发”)。另一方面,可以将多种材料预混合,并且所述混合物可以在单个材料源中提供,最终将其自此蒸发(“预混合物蒸发”)。这使得能够以简单且快速的方式实现具有组分的均匀分布的层的气相沉积,而无需精确控制多种所需材料源。
因此,本发明另外涉及一种方法,所述方法的特征在于,至少一种如上所述或优选描述的式(1)的化合物和至少一种如上所述或优选描述的式(2)的化合物,任选地与如上所述或优选描述的其它材料一起,依次或同时地从至少两个材料源进行气相沉积,并且形成有机层。
在本发明的一个优选的实施方式中,通过气相沉积施加至少一个有机层,其中将组合物的成分预混合并从单一材料源蒸发。
因此,本发明另外涉及一种方法,所述方法的特征在于,如上所述或优选描述的根据本发明的组合物被用作气相沉积的材料源,并且任选地与其它材料一起形成有机层。
本发明还涉及一种用于制造包含如上所述或优选描述的根据本发明的组合物的有机电子器件的方法,其特征在于,使用如上所述的根据本发明的制剂来施加有机层。
根据本发明的组合物或根据本发明的器件与现有技术的区别在于以下令人惊讶的优点:
根据本发明的组合物在有机电子器件中,特别是在有机电致发光器件中,并且特别是在OLED或OLEC中的使用导致器件寿命显著增加。
如在以下指示的实施例1中可以看出的,通过使用根据现有技术的化合物,例如化合物V1,可以以10%的在EML中的平均发光体浓度实现良好的电压和效率。然而,组件的寿命很短。
通过如上所述的式(1)的化合物与如上所述的式(2)的化合物的根据本发明的组合,可以实现大于2倍的寿命改善以及相当的组件电压和相当的或改善的组件效率。
通过如上所述的式(1)的化合物与如上所述的式(2)的化合物的根据本发明的组合以及发光层中2至15重量%的发光体浓度,可以优选实现大约大于2倍的寿命改善以及相当的组件电压和相当的或改善的组件效率。
通过在实施例E1和E2中在12%的发光体浓度下使用作为式(1)化合物代表的化合物1(缩写为CbzT1)和联咔唑89(缩写为BisC2)或90(缩写为BisC3)证明了该优点。
即使在EML中只有7%的较低发光体浓度,在所述发光体浓度下,OLED的寿命通常下降,但与现有技术相比,根据本发明的组合所实现的寿命仍显著改善。分别地在7%的发光体浓度下,在实施例E3和E4中通过使用化合物1(缩写为CbzT1)和联咔唑89(缩写为BisC2)或90(缩写为BisC3)以及在实施例E5、E6和E7中通过使用化合物9、13或15与联咔唑91作为式(1)化合物的代表证明了这一点。
代表式(1)、(1f)、(1h)和(1i)的化合物的化合物9与如上所述根据本发明的式(2)的化合物组合显示了最佳结果。
在实施例E8中在7%的发光体浓度下通过使用作为式(1)化合物代表的化合物69和联咔唑91,同样证明了这一点。
与比较例的区别在于,式(2)的联咔唑中的取代基Ar4和Ar5的电子结构不同时为苯基。本领域技术人员不能预见,作为具有10至40个环原子,特别是12至40个环原子的芳族环系,或作为具有10至40个环原子的杂芳族富电子环系,取代基Ar4和Ar5中至少一个的较高电子密度引起改善的气相沉积行为,并因此导致电子器件,特别是OLED的寿命的改善。由于与现有技术相比寿命增加,特别是增加大约大于1.5倍,特别地大约大于2倍,非常特别地2至3倍,因此改善变得明显。
不受理论的束缚,认为选定取代基Ar4和Ar5的共轭也有影响。这是因为如果将苯基变为联苯基,则共轭也得到改善,并且所述器件表现出如上所述的有利性质。如果将联苯基变为杂芳族环系,例如二苯并呋喃、二苯并噻吩或咔唑,则体系由于通过O原子、S原子或N原子的桥连而平面化,并且共轭得到另外改善。因此,使用富电子杂芳族环系也获得了这些优点。
与现有技术的其它区别在于选择式(1)的具体化合物,其中连接基L表示具有6至18个C原子的芳族环系,其中寿命再次得到惊人地改善。
根据本发明的组合物非常适用于发光层,并且与如上所述的来自现有技术的化合物相比,其表现出改善的性能数据,特别是关于寿命的改善的数据。
根据本发明的组合物可以容易地处理,因此非常适于商业应用中的大规模制造。
根据本发明的组合物可以预混合并由单一材料源气相沉积,从而可以简单且快速的方式制造具有所用组分的均匀分布的有机层。
这些以上提到的优点不会伴随电子器件的其它电子性质的损害。
应该指出,本发明中描述的实施方式的变化落在本发明的范围内。除非明确排除,否则本发明中公开的每个特征可以被提供相同、等效或类似目的的替代特征替换。因此,除非另有说明,否则本发明中公开的每个特征被认为是通用系列的实例或者是等效或类似的特征。
本发明的所有特征可以以任何方式彼此组合,除非某些特征和/或步骤是相互排斥的。这特别适用于本发明的优选特征。同样,非必要组合的特征可以单独使用(而不是组合使用)。
可以对关于本发明公开的技术动作的教导进行提炼并与其它实施例组合。
具体实施方式
通过以下实施例更详细地解释本发明,而不希望由此限制本发明。
通用方法:
轨道能量和电子态的确定
材料的HOMO和LUMO能量以及三重态能级和单重态能级通过量子化学计算确定。为此,在本申请中使用“Gaussian09,修订版D.01”软件包(高斯有限公司(Gaussian Inc.))。为了计算不含金属的有机物质(用“org.”方法表示),首先使用半经验方法AM1(高斯输入行“#AM1opt”)以电荷0和多重性1进行几何优化。然后,基于优化的几何形状对电子基态和三重态能级进行能量计算(单点)。在此使用TDDFT(时变密度泛函理论)方法B3PW91和6-31G(d)基集(高斯输入行“#B3PW91/6-31G(d)td=(50-50,n态=4)”)(电荷0,多重性1)。对于有机金属化合物(由“Org.m”方法表示),使用Hartree-Fock方法和LanL2MB基集(高斯输入行"#HF/LanL2MB opt")(电荷0,多重性1)优化几何形状。类似于如上所述的对于有机物质,进行能量计算,不同之处在于对于金属原子使用使用“LanL2DZ”基集,并且对于配体使用“6-31G(d)”基集(高斯输入行“#B3PW91/gen Pseudo=lanl2 td=(50-50,n态=4)”)。能量计算以哈特里为单位给出作为两个电子占据的最后一个轨道的HOMO(α占据特征值)和作为第一未占轨道的LUMO(α未占特征值),其中HEh和LEh分别代表以哈特里为单位的HOMO能量和以哈特里为单位的LUMO能量。参照循环伏安法测量校准的以电子伏特为单位的HOMO值和LUMO值,如下确定:
HOMO(eV)=(HEh*27.212)*0.8308-1.118;
LUMO(eV)=(LEh*27.212)*1.0658-0.5049。
材料的三重态T1被定义为具有由量子化学能量计算产生的最低能量的三重态的相对激发能量(eV)。
单重态能级S1定义为具有由量子化学能量计算产生的第二低的能量的单重态的相对激发能量(eV)。
最低能量的单重态称为S0。
本文所述的方法与所使用的软件包无关,并且始终给出相同的结果。为此目的常用的程序的实例为“Gaussian09”(高斯有限公司(Gaussian Inc.))和Q-Chem 4.1(量子化学有限公司(Q-Chem,Inc.))。在本申请中,“Gaussian09,修订版D.01”软件包用于计算能量。
实施例1:OLED的制造
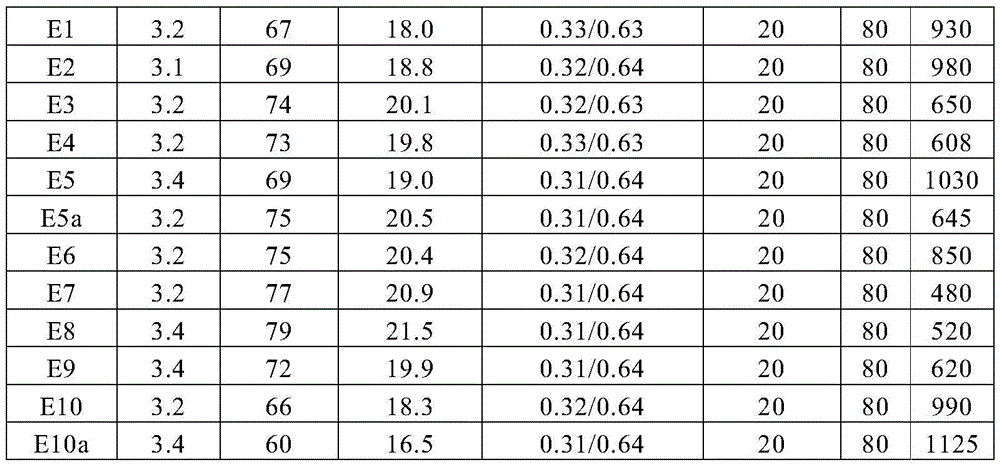
在以下的实施例E1至E10a中给出了根据本发明的材料组合在OLED中的用途(参见表16)。
实施例E1-E10a的预处理:首先,在涂覆之前对涂覆有厚度为50nm的结构化ITO(氧化锡铟)的玻璃板用氧等离子体处理,然后用氩等离子体处理。这些经等离子体处理的玻璃板形成对其施加OLED的基底。
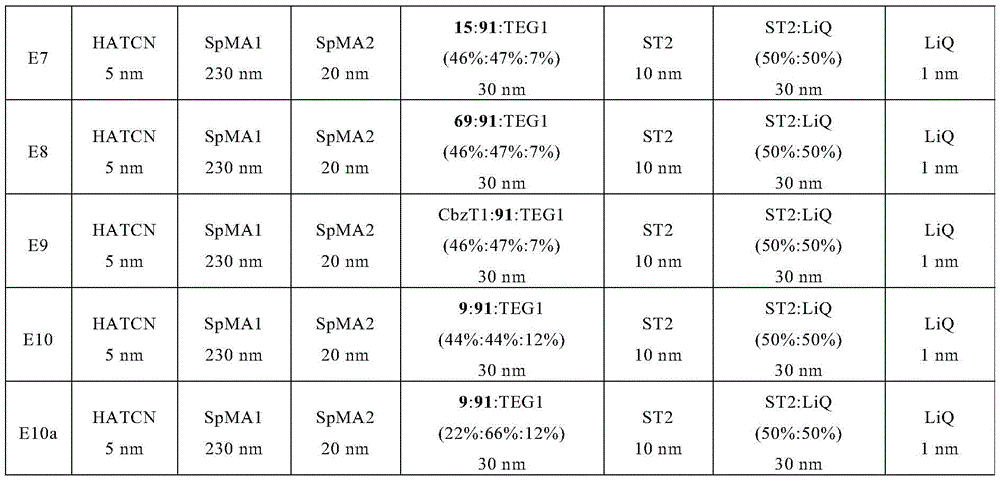
OLED基本上具有以下层结构:基底/空穴注入层(HIL)/空穴传输层(HTL)/电子阻挡层(EBL)/发光层(EML)/任选的空穴阻挡层(HBL)/电子传输层(ETL)/任选的电子注入层(EIL),且最后是阴极。阴极由厚度为100nm的铝层形成。OLED的精确结构示于表16中。表17中显示了制造OLED所需的材料。OLED的数据列于表18中。实施例V1是根据WO 2015/169412的比较例,实施例E1至E10a显示根据本发明的OLED的数据。实施例E5、E10和E10a显示根据本发明的优选的OLED。
所有材料都通过在真空室中热气相沉积施加。这里的发光层总是由至少一种基质材料(主体材料),在本发明的意义上,至少两种基质材料,和发光掺杂剂(发光体)组成,所述发光体通过共蒸发以一定体积比例与一种或多种基质材料混合。这里的表达如CbzT1:BisC1:TEG1(45%:45%:10%)意指材料CbzT1以45%的体积比例存在于层中,BisC1以45%的比例存在于层中,并且TEG1以10%的比例存在于层中。类似地,电子传输层也可以由两种材料的混合物组成。
OLED通过标准方法表征。为此目的,确定电致发光光谱、电流效率(CE,以cd/A实测)和外量子效率(EQE,以%计量),其作为发光密度的函数,是从假定郎伯发光特性的电流/电压/发光密度特性线计算,并且确定寿命。电致发光光谱在1000cd/m2的发光密度下确定,并由此计算CIE 1931x和y色坐标。表18中的术语U1000表示发光密度为1000cd/m2所需的电压。CE1000和EQE1000分别表示在1000cd/m2时达到的电流效率和外量子效率。
寿命LD定义了在以恒定电流密度j0工作时发光密度从初始发光密度下降到一定比率L1之后的时间。表18中的表达式L1=80%是指在列LD中指示的寿命对应于发光密度下降到其初始值的80%之后的时间。
根据本发明的混合物在OLED中的用途
根据本发明的材料组合可以用于磷光OLED中的发光层中。在实施例E1至E4中,将化合物CbzT1(对应于化合物1)与BisC2(对应于化合物89)或BisC3(对应于化合物90)的根据本发明的组合物用作发光层中的基质材料。在实施例E5、E5a、E6、E7、E10和E10a中,将化合物9、13和15分别与化合物91的根据本发明的组合物用作发光层中的基质材料。在实施例E8中,将化合物69与化合物91的根据本发明的组合物用作发光层中的基质材料。
表16:OLED的结构
表17:OLED用材料的结构式
表18:OLED的数据
实施例2:化合物1(CbzT1)的合成
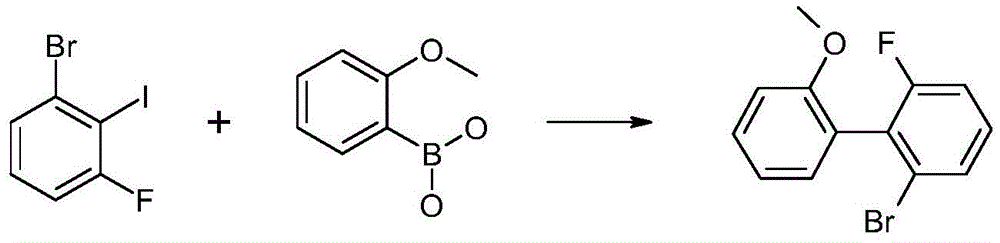
a)6-溴-2-氟-2'-甲氧基联苯
将200g(664mmol)的1-溴-3-氟-2-碘苯、101g(664mmol)的2-甲氧基苯基硼酸和137.5g(997mmol)的四硼酸钠溶解在1000ml THF和600ml水中并脱气。添加9.3g(13.3mmol)的双(三苯基膦)氯化钯(II)和1g(20mmol)的氢氧化肼。随后将反应混合物在保护气体气氛下在70℃下搅拌48小时。将甲苯添加到冷却的溶液中,将其用水洗涤多次,干燥并蒸发。产物通过硅胶柱色谱法用甲苯/庚烷(1:2)纯化。收率:155g(553mmol),理论值的83%。
b)6'-溴-2'-氟联苯-2-醇
将112g(418mmol)的6-溴-2-氟-2’-甲氧基联苯溶解在2l二氯甲烷中,并冷却至5℃。在90分钟内,将41.01ml(431mmol)三溴化硼滴加到该溶液中,并且继续搅拌过夜。随后将水缓慢添加到混合物中,将有机相用水洗涤三次,用Na2SO4干燥并在旋转蒸发仪中蒸发,并通过色谱法纯化产物。收率:104g(397mmol),理论值的98%。
c)1-溴二苯并呋喃
将111g(416mmol)的6'-溴-2'-氟联苯-2-醇溶解在2l DMF(最多0.003%的H2O)中并冷却至5℃。将20g(449mmol)的氢化钠(在石蜡油中的60%悬浮液)添加到该溶液中,继续搅拌另外20分钟。添加完成后,然后将混合物在100℃下加热45分钟。冷却后,将500ml乙醇缓慢添加到混合物中,将混合物在旋转蒸发仪中蒸发,然后通过色谱法纯化产物。收率:90g(367mmol),理论值的88.5%。
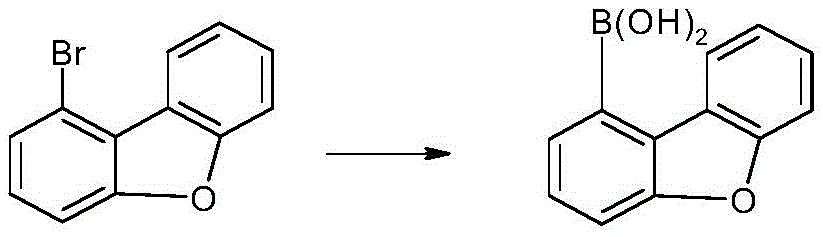
d)二苯并呋喃-1-硼酸
将180g(728mmol)的1-溴苯并呋喃溶解在1500ml的干燥THF中,并且冷却至-78℃。在此温度下,在约5分钟内添加305ml(764mmol/在己烷中2.5M)的正丁基锂,随后将混合物在-78℃下再搅拌2.5小时。在此温度下,尽可能迅速地添加151g(1456mmol)硼酸三甲酯,并使反应物缓慢升至室温(约18小时)。将反应溶液用水洗涤,并将沉淀的固体和有机相与甲苯进行共沸干燥。在约40℃下在搅拌下用甲苯/二氯甲烷洗涤粗产物,并抽滤。收率:146g(690mmol),理论值的95%。
e)2-二苯并呋喃-1-基-4,6-二苯基-1,3,5-三嗪
将23g(110.0mmol)二苯并呋喃-1-硼酸、29.5g(110.0mmol)2-氯-4,6-二苯基-1,3,5-三嗪和21g(210.0mmol)碳酸钠悬浮在500ml乙二醇二胺醚和500ml水中。向该悬浮液中添加913mg(3.0mmol)三邻甲苯基膦,然后添加112mg(0.5mmol)乙酸钯(II),并将反应混合物加热回流16小时。冷却后,分离出有机相,通过硅胶过滤,用200ml水洗涤三次,随后浓缩至干燥。将残余物从甲苯和二氯甲烷/庚烷中重结晶。收率为37g(94mmol),对应于理论值的87%。
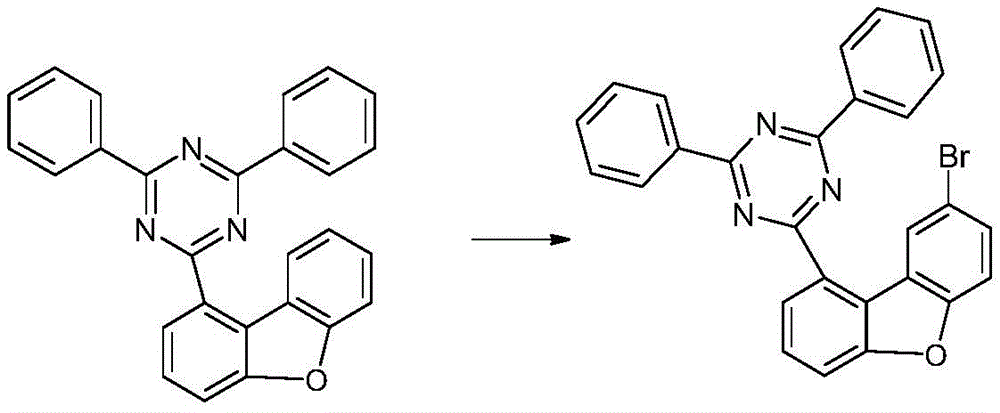
f)2-(8-溴二苯并呋喃-1-基)-4,6-二苯基-1,3,5-三嗪
将70g(190.0mmol)的2-二苯并呋喃-1-基-4,6-二苯基-1,3,5-三嗪悬浮在2000ml乙酸(100%)和2000ml硫酸(95-98%)中。将34g(190mmol)NBS逐份添加到该悬浮液中,并将混合物在黑暗中搅拌2小时。此后,添加水/冰,分离出固体,并用乙醇冲洗。将残余物从甲苯中重结晶。收率为80g(167mmol),对应于理论值的87%。
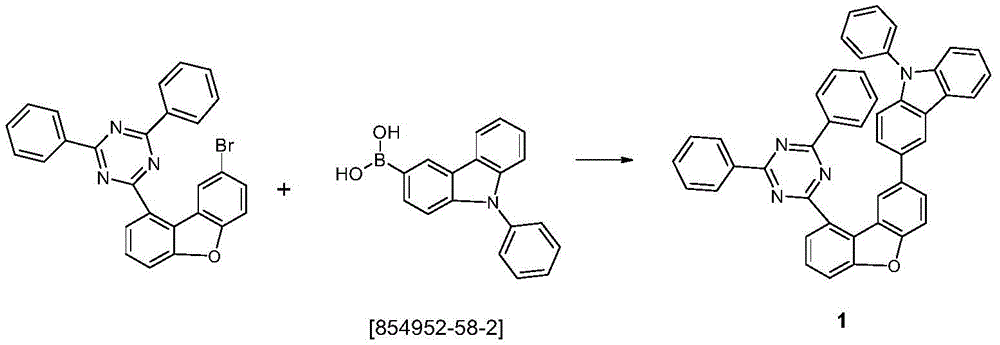
g)3-[9-(4,6-二苯基-1,3,5-三嗪-2-基)二苯并呋喃-2-基]-9-苯基-9H-咔唑
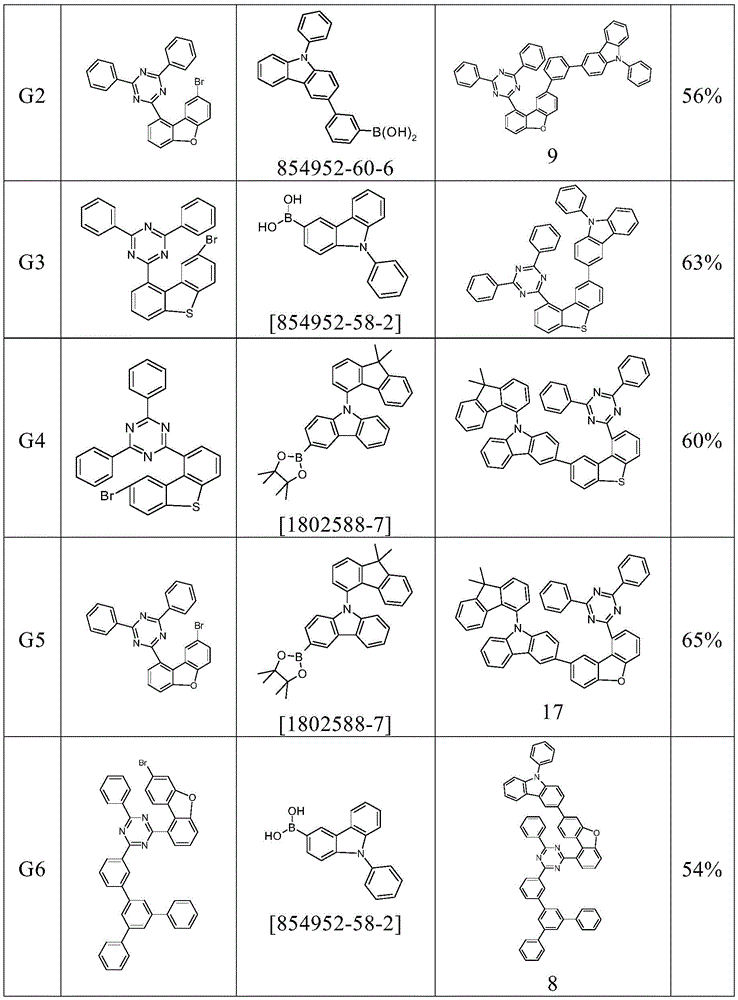
将75g(156mmol)2-(8-溴二苯并呋喃-1-基)-4,6-二苯基-1,3,5-三嗪、50g(172mmol)N-苯基咔唑-3-硼酸[854952-58-2]和36g(340mmol)碳酸钠悬浮在1000ml乙二醇二胺醚和280ml水中。向该悬浮液中添加1.8g(1.5mmol)四(三苯基膦)钯(0),并将反应混合物加热回流16小时。冷却后,分离出有机相,通过硅胶过滤,用200ml水洗涤三次,随后浓缩至干燥。通过在硅胶上用甲苯/庚烷(1:2)进行柱色谱法纯化产物,随后在高真空(p=5×10-7毫巴)中升华(纯度99.9%)。收率为50g(78mmol),对应于理论值的50%。
以下化合物可以类似方式制备。这里的纯化也可以使用柱色谱法或其它常用溶剂进行,例如对于重结晶或热萃取,可以使用正庚烷、丁醇、丙酮、乙酸乙酯、乙腈、甲苯、二甲苯、二氯甲烷、甲醇、N,N-二甲基甲酰胺、四氢呋喃、乙酸乙酯、乙酸正丁酯或1,4-二烷。
实施例3:化合物89(BisC2)和90(BisC3)的合成
化合物89从文献中已知,并且类似于US 20150001488制备。
化合物90从文献中已知,并且类似于Physical Chemistry Chemical Physics,17(37),2015,24468-24474制备。
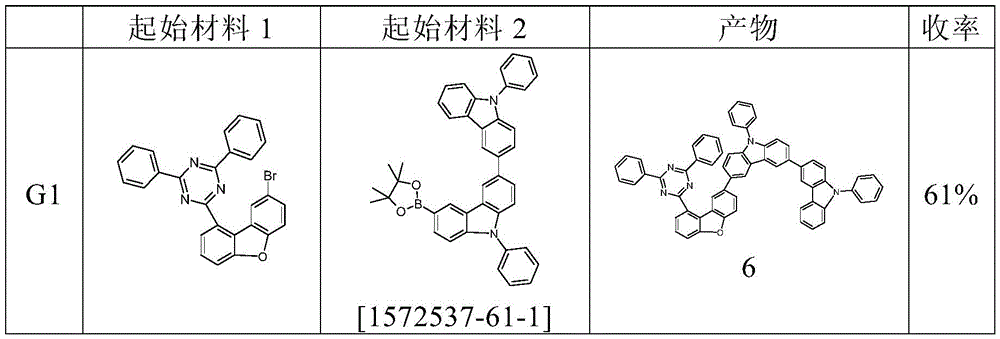
实施例4:
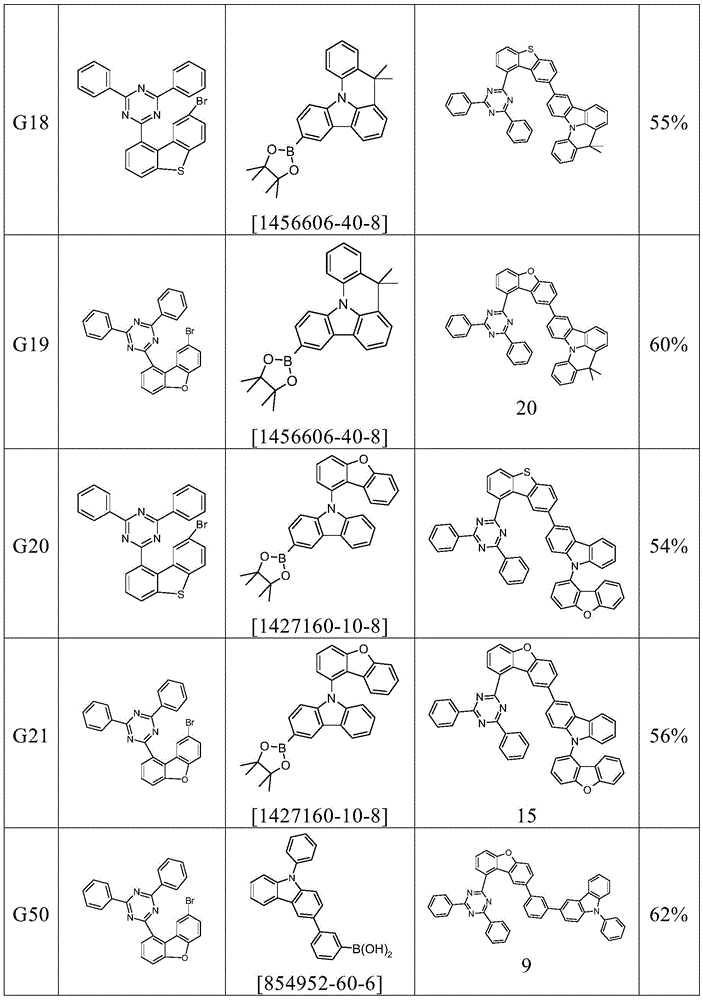
以下化合物可以类似于实施例2g)制备。这里的纯化也可以使用柱色谱法或其它常用溶剂进行,例如对于重结晶或热萃取,可以使用正庚烷、丁醇、丙酮、乙酸乙酯、乙腈、甲苯、二甲苯、二氯甲烷、甲醇、N,N-二甲基甲酰胺、四氢呋喃、乙酸乙酯、乙酸正丁酯或1,4-二烷。
实施例5:
A)
从2-(二苯并[b,d]呋喃-3-基)-4,6-二苯基-1,3,5-三嗪[1651203-47-2]开始,类似于实施例2f)制备溴中间体。收率83%。
B)
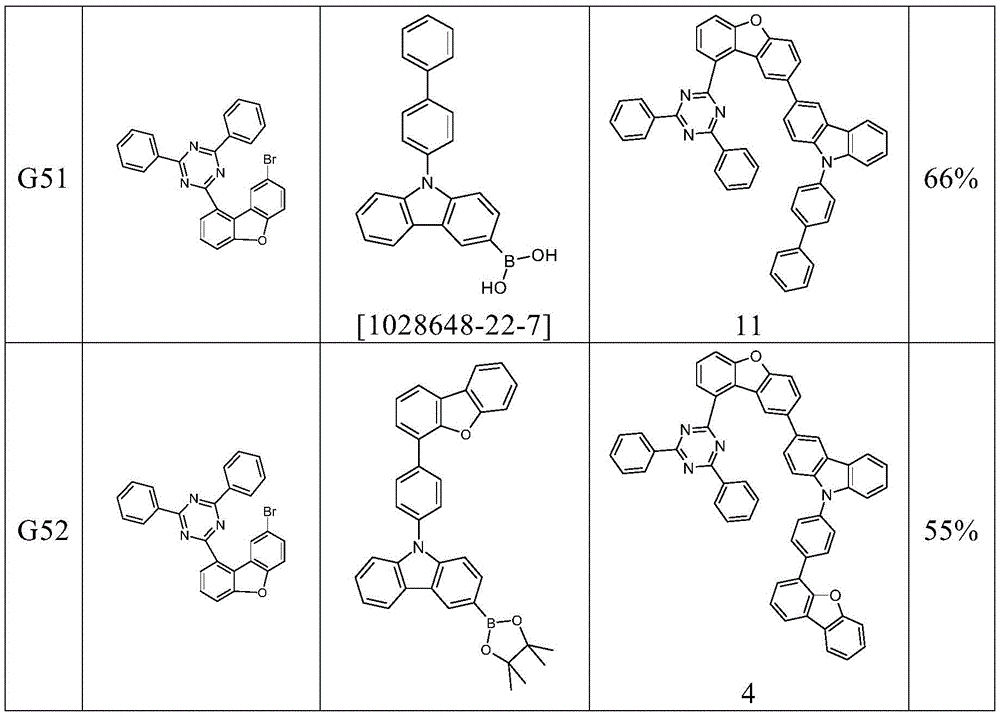
以下化合物可以类似于实施例2g)制备。这里的纯化也可以使用柱色谱法或其它常用溶剂进行,例如对于重结晶或热萃取,可以使用正庚烷、丁醇、丙酮、乙酸乙酯、乙腈、甲苯、二甲苯、二氯甲烷、甲醇、N,N-二甲基甲酰胺、四氢呋喃、乙酸乙酯、乙酸正丁酯或1,4-二烷。
实施例6:
以下化合物可以类似于实施例2g)制备。这里的纯化也可以使用柱色谱法或其它常用溶剂进行,例如对于重结晶或热萃取,可以使用正庚烷、丁醇、丙酮、乙酸乙酯、乙腈、甲苯、二甲苯、二氯甲烷、甲醇、N,N-二甲基甲酰胺、四氢呋喃、乙酸乙酯、乙酸正丁酯或1,4-二烷。
Claims (18)
1.一种组合物,所述组合物包含至少一种式(1)的化合物和至少一种式(2)的化合物
其中以下适用于所使用的符号和标记:
X在每次出现时相同或不同地是CR0或N,条件是至少一个基团X代表N;
X1在每次出现时相同或不同地是CR或N;
X2在每次出现时相同或不同地是CR1或N;
Y选自O或S;
L在每次出现时相同或不同地是单键或具有5至30个芳族环原子的芳族或杂芳族环系,所述芳族或杂芳族环系可以被一个或多个基团R3取代,优选具有6至18个C原子的芳族或杂芳族环系,所述芳族或杂芳族环系可以被一个或多个基团R3取代;
Ar1、Ar2在每种情况下在每次出现时彼此独立地是具有5至40个芳族环原子的芳基或杂芳基基团,所述芳基或杂芳基基团可以被一个或多个基团R3取代;
Ar3是具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,所述芳族环系和所述杂芳族环系可以被一个或多个基团R3取代;
Ar4和Ar5在每种情况下彼此独立地是具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,所述芳族环系和所述杂芳族环系可以被一个或多个基团R3取代,条件是Ar4和Ar5不能同时为苯基;
R0、R、R1在每次出现时相同或不同地选自H,D,F,Cl,Br,I,CN,NO2,N(Ar)2,N(R2)2,C(=O)Ar,C(=O)R2,P(=O)(Ar)2,P(Ar)2,B(Ar)2,Si(Ar)3,Si(R2)3,具有1至20个C原子的直链的烷基、烷氧基或硫代烷基基团,或具有3至20个C原子的支链或环状的烷基、烷氧基或硫代烷基基团,或具有2至20个C原子的烯基基团,所述基团在每种情况下可以被一个或多个基团R2取代,其中一个或多个不相邻的CH2基团可以被R2C=CR2、Si(R2)2、C=O、C=S、C=NR2、P(=O)(R2)、SO、SO2、NR2、O、S或CONR2替换,并且其中一个或多个H原子可以被D、F、Cl、Br、I、CN或NO2替换,具有5至40个芳族环原子的芳族或杂芳族环系,所述芳族或杂芳族环系在每种情况下可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳氧基或杂芳氧基基团,所述芳氧基或杂芳氧基基团可以被一个或多个基团R2取代,或具有5至40个芳族环原子的芳烷基或杂芳烷基基团,所述芳烷基或杂芳烷基基团可以被一个或多个基团R2取代;键合到同一碳原子或相邻碳原子的两个取代基R0和/或R和/或R1可以任选地形成可以被一个或多个基团R2取代的单环或多环的脂族、芳族或杂芳族环系;
R2在每次出现时相同或不同地选自H,D,F,Cl,Br,I,CN,NO2,N(Ar)2,NH2,N(R3)2,C(=O)Ar,C(=O)H,C(=O)R3,P(=O)(Ar)2,具有1至40个C原子的直链的烷基、烷氧基或硫代烷基基团,或具有3至40个C原子的支链或环状的烷基、烷氧基或硫代烷基基团,或具有2至40个C原子的烯基或炔基基团,所述基团在每种情况下可以被一个或多个基团R3取代,其中一个或多个不相邻的CH2基团可以被HC=CH、R3C=CR3、C≡C、Si(R3)2、Ge(R3)2、Sn(R3)2、C=O、C=S、C=Se、C=NR3、P(=O)(R3)、SO、SO2、NH、NR3、O、S、CONH或CONR3替换,并且其中一个或多个H原子可以被D、F、Cl、Br、I、CN或NO2替换,具有5至60个芳族环原子的芳族或杂芳族环系,所述芳族或杂芳族环系在每种情况下可以被一个或多个基团R3取代,或具有5至60个芳族环原子的芳氧基或杂芳氧基基团,所述芳氧基或杂芳氧基基团可以被一个或多个基团R3取代,或这些体系的组合,其中两个或更多个相邻取代基R2可以任选地形成可以被一个或多个基团R3取代的单环或多环的脂族、芳族或杂芳族环系;
R3在每种情况下相同或不同地选自H,D,F,CN,具有1至20个C原子的脂族烃基或具有5至30个芳族环原子的芳族或杂芳族环系,其中一个或多个H原子可以被D、F、Cl、Br、I或CN替换且其可以被一个或多个各自具有1至4个碳原子的烷基基团取代;两个或更多个相邻取代基R3可以彼此形成单环或多环的脂族环系;
Ar在每次出现时相同或不同地是具有5至30个芳族环原子的芳族或杂芳族环系,所述芳族或杂芳族环系可以被一个或多个非芳族的基团R3取代;与同一N原子、P原子或B原子键合的两个基团Ar也可以通过单键或选自N(R3)、C(R3)2、O或S的桥连基彼此桥连;并且
n和m彼此独立地表示0、1、2或3。
3.根据权利要求1或2所述的组合物,其特征在于,所述式(2)的化合物符合式(2a),
其中所用的符号和标记具有在权利要求1中给出的含义,q和t在每种情况下彼此独立地表示0、1、2、3或4,并且r和s在每种情况下彼此独立地表示0、1、2或3。
4.根据权利要求1至3中的一项或多项所述的组合物,其特征在于,取代基Ar4或Ar5之一表示具有6至40个芳族环原子的芳族环系或具有10至40个芳族环原子的杂芳族环系,所述芳族环系和所述杂芳族环系可以被一个或多个基团R3取代,并且另一个取代基表示具有6至40个芳族环原子的芳族环系,所述芳族环系可以被一个或多个基团R3取代,条件是Ar4和Ar5不能同时是苯基。
5.根据权利要求1至4中的一项或多项所述的组合物,其特征在于,取代基Ar4和Ar5在每种情况下彼此独立地表示具有6至40个芳族环原子的芳族环系,所述芳族环系可以被一个或多个基团R3取代,条件是Ar4和Ar5不同时是苯基。
6.根据权利要求1至5中的一项或多项所述的组合物,其特征在于,所述组合物包含至少一种另外的化合物,所述另外的化合物选自空穴注入材料、空穴传输材料、空穴阻挡材料、宽带隙材料、荧光发光体、磷光发光体、主体材料、电子阻挡材料、电子传输材料和电子注入材料、n型掺杂剂和p型掺杂剂。
7.一种制剂,所述制剂包含根据权利要求1至6中的一项或多项所述的组合物和至少一种溶剂。
8.根据权利要求1至6中的一项或多项所述的组合物在有机电子器件中的用途。
9.根据权利要求8所述的用途,其特征在于,所述有机电子器件选自有机集成电路(OIC)、有机场效应晶体管(OFET)、有机薄膜晶体管(OTFT)、有机电致发光器件、有机太阳能电池(OSC)、有机光学检测器和有机光感受器。
10.一种有机电子器件,所述有机电子器件包含至少一种根据权利要求1至6中的一项或多项所述的组合物。
11.根据权利要求10所述的器件,其特征在于,所述器件选自有机集成电路(OIC)、有机场效应晶体管(OFET)、有机薄膜晶体管(OTFT)、有机电致发光器件、有机太阳能电池(OSC)、有机光学检测器和有机光感受器。
12.根据权利要求10或11所述的器件,其特征在于,所述器件是选自有机发光晶体管(OLET)、有机场猝熄器件(OFQD)、有机发光电化学电池(OLEC、LEC、LEEC)、有机激光二极管(O-laser)和有机发光二极管(OLED)的电致发光器件。
13.根据权利要求10至12中的一项或多项所述的器件,其特征在于,所述器件在发光层(EML)中、在电子传输层(ETL)中、在电子注入层(EIL)中和/或在空穴阻挡层(HBL)中包含根据权利要求1至6中的一项或多项所述的组合物。
14.根据权利要求10至13中的一项或多项所述的器件,其特征在于,所述器件在发光层中包含根据权利要求1至6中的一项或多项所述的组合物以及磷光发光体。
15.一种用于制造根据权利要求10至14中的一项或多项所述的器件的方法,其特征在于,通过气相沉积或从溶液中施加至少一个包含根据权利要求1至6中的一项或多项所述的组合物的有机层。
16.根据权利要求15所述的方法,其特征在于,在权利要求1至6中的一项中所述的至少一种式(1)的化合物和至少一种式(2)的化合物,任选与其它材料一起,从至少两种材料源依次或同时地进行气相沉积,并形成所述有机层。
17.根据权利要求15所述的方法,其特征在于,根据权利要求1至6中的一项或多项所述的组合物用作所述气相沉积的材料源,并形成所述有机层。
18.根据权利要求15所述的方法,其特征在于,使用根据权利要求7所述的制剂以施加所述有机层。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17179775 | 2017-07-05 | ||
| EP17179775.6 | 2017-07-05 | ||
| EP17195036 | 2017-10-05 | ||
| EP17195036.3 | 2017-10-05 | ||
| PCT/EP2018/067732 WO2019007866A1 (de) | 2017-07-05 | 2018-07-02 | Zusammensetzung für organische elektronische vorrichtungen |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN110785415A true CN110785415A (zh) | 2020-02-11 |
Family
ID=62816553
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880039441.9A Pending CN110785415A (zh) | 2017-07-05 | 2018-07-02 | 用于有机电子器件的组合物 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US11591320B2 (zh) |
| EP (2) | EP3649123B1 (zh) |
| JP (3) | JP7135012B2 (zh) |
| KR (4) | KR102594782B1 (zh) |
| CN (1) | CN110785415A (zh) |
| TW (1) | TWI808980B (zh) |
| WO (1) | WO2019007866A1 (zh) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113292545A (zh) * | 2021-06-28 | 2021-08-24 | 南京高光半导体材料有限公司 | 一种含有三嗪及三嗪衍生物的化合物及有机电致发光器件 |
| CN113801109A (zh) * | 2021-08-17 | 2021-12-17 | 南京高光半导体材料有限公司 | 一种含有双咔唑结构的化合物及有机电致发光器件 |
| CN113950474A (zh) * | 2019-11-05 | 2022-01-18 | Lt素材株式会社 | 杂环化合物以及包括其的有机发光装置 |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102038031B1 (ko) * | 2017-09-15 | 2019-10-30 | 엘티소재주식회사 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102511183B1 (ko) * | 2017-12-01 | 2023-03-20 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR102392657B1 (ko) * | 2019-01-14 | 2022-04-28 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| US20230080974A1 (en) * | 2019-02-18 | 2023-03-16 | Merck Patent Gmbh | Composition for organic electronic devices |
| CN109928945B (zh) * | 2019-04-11 | 2022-11-04 | 西安欧得光电材料有限公司 | 一种1-溴二苯并呋喃及其合成方法 |
| KR102298235B1 (ko) * | 2019-10-08 | 2021-09-07 | 엘티소재주식회사 | 헤테로고리 화합물, 이를 포함하는 유기 발광 소자, 유기 발광 소자의 유기물층용 조성물 및 유기 발광 소자의 제조 방법 |
| TW202146625A (zh) | 2020-03-11 | 2021-12-16 | 德商麥克專利有限公司 | 有機電致發光裝置 |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| KR102859823B1 (ko) * | 2022-03-26 | 2025-09-16 | 베이징 썸머 스프라우트 테크놀로지 컴퍼니 리미티드 | 유기 전계발광소자 |
| KR20250152618A (ko) | 2023-02-17 | 2025-10-23 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| WO2025228800A1 (de) | 2024-04-30 | 2025-11-06 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2026017611A1 (en) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Organic light emitting device |
| WO2026017607A1 (en) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Organic light-emitting device |
| WO2026017608A1 (de) | 2024-07-15 | 2026-01-22 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140158992A1 (en) * | 2012-12-07 | 2014-06-12 | Universal Display Corporation | Carbazole Compounds For Delayed Fluorescence |
| WO2015165563A1 (de) * | 2014-04-30 | 2015-11-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US20150318487A1 (en) * | 2014-05-02 | 2015-11-05 | Samsung Display Co., Ltd. | Organic light-emitting device |
| WO2015169412A1 (de) * | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR101744248B1 (ko) * | 2016-09-06 | 2017-06-07 | 주식회사 엘지화학 | 유기발광 소자 |
| CN108779392A (zh) * | 2016-11-29 | 2018-11-09 | 株式会社Lg化学 | 有机发光器件 |
Family Cites Families (142)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| DE69432054T2 (de) | 1993-09-29 | 2003-10-09 | Idemitsu Kosan Co | Organische elektrolumineszenzelemente und arylendiaminderivate |
| JPH07133483A (ja) | 1993-11-09 | 1995-05-23 | Shinko Electric Ind Co Ltd | El素子用有機発光材料及びel素子 |
| EP0676461B1 (de) | 1994-04-07 | 2002-08-14 | Covion Organic Semiconductors GmbH | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE19652261A1 (de) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Arylsubstituierte Poly(p-arylenvinylene), Verfahren zur Herstellung und deren Verwendung in Elektroluminszenzbauelementen |
| US5942340A (en) | 1997-10-02 | 1999-08-24 | Xerox Corporation | Indolocarbazole electroluminescent devices |
| US5952115A (en) | 1997-10-02 | 1999-09-14 | Xerox Corporation | Electroluminescent devices |
| US5843607A (en) | 1997-10-02 | 1998-12-01 | Xerox Corporation | Indolocarbazole photoconductors |
| JP3302945B2 (ja) | 1998-06-23 | 2002-07-15 | ネースディスプレイ・カンパニー・リミテッド | 新規な有機金属発光物質およびそれを含む有機電気発光素子 |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| KR100946314B1 (ko) | 1999-12-01 | 2010-03-09 | 더 트러스티즈 오브 프린스턴 유니버시티 | 인광성 유기금속화합물을 포함하는 유기 발광 장치 |
| KR100377321B1 (ko) | 1999-12-31 | 2003-03-26 | 주식회사 엘지화학 | 피-형 반도체 성질을 갖는 유기 화합물을 포함하는 전기소자 |
| US6660410B2 (en) | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| US6392250B1 (en) | 2000-06-30 | 2002-05-21 | Xerox Corporation | Organic light emitting devices having improved performance |
| CN101924190B (zh) | 2000-08-11 | 2012-07-04 | 普林斯顿大学理事会 | 有机金属化合物和发射转换有机电致磷光 |
| JP4154140B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 金属配位化合物 |
| JP4154139B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子 |
| JP4154138B2 (ja) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | 発光素子、表示装置及び金属配位化合物 |
| US6803720B2 (en) | 2000-12-15 | 2004-10-12 | Universal Display Corporation | Highly stable and efficient OLEDs with a phosphorescent-doped mixed layer architecture |
| CN100379049C (zh) | 2001-03-14 | 2008-04-02 | 普林斯顿大学理事会 | 用于蓝色磷光基有机发光二极管的材料与器件 |
| KR100691543B1 (ko) | 2002-01-18 | 2007-03-09 | 주식회사 엘지화학 | 새로운 전자 수송용 물질 및 이를 이용한 유기 발광 소자 |
| EP1549112A4 (en) | 2002-09-20 | 2009-01-07 | Idemitsu Kosan Co | ORGANIC ELECTROLUMINESCENCE ELEMENT |
| JP2006511939A (ja) | 2002-12-23 | 2006-04-06 | コビオン・オーガニック・セミコンダクターズ・ゲーエムベーハー | 有機エレクトロルミネセンス素子 |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| US7851071B2 (en) | 2003-03-13 | 2010-12-14 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| JP4411851B2 (ja) | 2003-03-19 | 2010-02-10 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| JP5318347B2 (ja) | 2003-04-15 | 2013-10-16 | メルク パテント ゲーエムベーハー | 発光可能な、マトリックス材料と有機半導体との混合物、その使用、ならびに前記混合物を含む電子部品 |
| EP2236579B1 (en) | 2003-04-23 | 2014-04-09 | Konica Minolta Holdings, Inc. | Organic electroluminescent element and display |
| KR101105619B1 (ko) | 2003-07-07 | 2012-01-18 | 메르크 파텐트 게엠베하 | 유기 방출형 반도체 및 매트릭스 물질의 혼합물, 이들의용도 및 상기 물질을 함유하는 전자 부품 |
| DE10333232A1 (de) | 2003-07-21 | 2007-10-11 | Merck Patent Gmbh | Organisches Elektrolumineszenzelement |
| DE10338550A1 (de) | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| DE10345572A1 (de) | 2003-09-29 | 2005-05-19 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| US7795801B2 (en) | 2003-09-30 | 2010-09-14 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| DE10357044A1 (de) | 2003-12-04 | 2005-07-14 | Novaled Gmbh | Verfahren zur Dotierung von organischen Halbleitern mit Chinondiiminderivaten |
| DE102004008304A1 (de) | 2004-02-20 | 2005-09-08 | Covion Organic Semiconductors Gmbh | Organische elektronische Vorrichtungen |
| DE102004010954A1 (de) | 2004-03-03 | 2005-10-06 | Novaled Gmbh | Verwendung eines Metallkomplexes als n-Dotand für ein organisches halbleitendes Matrixmaterial, organisches Halbleitermaterial und elektronisches Bauteil |
| US7790890B2 (en) | 2004-03-31 | 2010-09-07 | Konica Minolta Holdings, Inc. | Organic electroluminescence element material, organic electroluminescence element, display device and illumination device |
| KR100787425B1 (ko) | 2004-11-29 | 2007-12-26 | 삼성에스디아이 주식회사 | 페닐카바졸계 화합물 및 이를 이용한 유기 전계 발광 소자 |
| DE102004023277A1 (de) | 2004-05-11 | 2005-12-01 | Covion Organic Semiconductors Gmbh | Neue Materialmischungen für die Elektrolumineszenz |
| US7598388B2 (en) | 2004-05-18 | 2009-10-06 | The University Of Southern California | Carbene containing metal complexes as OLEDs |
| JP4862248B2 (ja) | 2004-06-04 | 2012-01-25 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| EP1655359A1 (de) | 2004-11-06 | 2006-05-10 | Covion Organic Semiconductors GmbH | Organische Elektrolumineszenzvorrichtung |
| WO2006081780A1 (de) | 2005-02-04 | 2006-08-10 | Novaled Ag | Dotanden für organische halbleiter |
| WO2006100896A1 (ja) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2006108497A1 (de) | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| CN101171320B (zh) | 2005-05-03 | 2013-04-10 | 默克专利有限公司 | 有机电致发光器件 |
| DE102005023437A1 (de) | 2005-05-20 | 2006-11-30 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| EP1956022B1 (en) | 2005-12-01 | 2012-07-25 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent element and organic electroluminescent element |
| US7919010B2 (en) | 2005-12-22 | 2011-04-05 | Novaled Ag | Doped organic semiconductor material |
| ATE394800T1 (de) | 2006-03-21 | 2008-05-15 | Novaled Ag | Heterocyclisches radikal oder diradikal, deren dimere, oligomere, polymere, dispiroverbindungen und polycyclen, deren verwendung, organisches halbleitendes material sowie elektronisches bauelement |
| EP1837927A1 (de) | 2006-03-22 | 2007-09-26 | Novaled AG | Verwendung von heterocyclischen Radikalen zur Dotierung von organischen Halbleitern |
| WO2007115540A1 (de) | 2006-03-30 | 2007-10-18 | Novaled Ag | Verwendung von bora-tetraazapentalenen |
| EP1860709B1 (de) | 2006-05-24 | 2012-08-08 | Novaled AG | Verwendung von quadratisch planaren Übergangsmetallkomplexen als Dotand |
| DE102006025777A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006025846A1 (de) | 2006-06-02 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102006031990A1 (de) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US8062769B2 (en) | 2006-11-09 | 2011-11-22 | Nippon Steel Chemical Co., Ltd. | Indolocarbazole compound for use in organic electroluminescent device and organic electroluminescent device |
| DE102006053320B4 (de) | 2006-11-13 | 2012-01-19 | Novaled Ag | Verwendung einer Koordinationsverbindung zur Dotierung organischer Halbleiter |
| DE102006054524B4 (de) | 2006-11-20 | 2022-12-22 | Novaled Gmbh | Verwendung von Dithiolenübergangsmetallkomplexen und Selen- analoger Verbindungen als Dotand |
| DE102006054523B4 (de) | 2006-11-20 | 2009-07-23 | Novaled Ag | Dithiolenübergangsmetallkomplexe und Selen-analoge Verbindungen, deren Verwendung als Dotand, organisches halbleitendes Material enthaltend die Komplexe, sowie elektronische oder optoelektronisches Bauelement enthaltend einen Komplex |
| DE102007002714A1 (de) | 2007-01-18 | 2008-07-31 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102007018456B4 (de) | 2007-04-19 | 2022-02-24 | Novaled Gmbh | Verwendung von Hauptgruppenelementhalogeniden und/oder -pseudohalogeniden, organisches halbleitendes Matrixmaterial, elektronische und optoelektronische Bauelemente |
| EP3457451B1 (de) | 2007-04-30 | 2019-07-17 | Novaled GmbH | Die verwendung von oxokohlenstoff-, pseudooxokohlenstoff- und radialenverbindungen |
| EP1990847B1 (de) | 2007-05-10 | 2018-06-20 | Novaled GmbH | Verwendung von chinoiden Bisimidazolen und deren Derivaten als Dotand zur Dotierung eines organischen halbleitenden Matrixmaterials |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2009014B1 (de) | 2007-06-22 | 2018-10-24 | Novaled GmbH | Verwendung eines Precursors eines n-Dotanden zur Dotierung eines organischen halbleitenden Materials, Precursor und elektronisches oder optoelektronisches Bauelement |
| DE102007031220B4 (de) | 2007-07-04 | 2022-04-28 | Novaled Gmbh | Chinoide Verbindungen und deren Verwendung in halbleitenden Matrixmaterialien, elektronischen und optoelektronischen Bauelementen |
| DE102008051737B4 (de) | 2007-10-24 | 2022-10-06 | Novaled Gmbh | Quadratisch planare Übergangsmetallkomplexe, organische halbleitende Materialien sowie elektronische oder optoelektronische Bauelemente, die diese umfassen und Verwendung derselben |
| DE102007053771A1 (de) | 2007-11-12 | 2009-05-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| WO2009069442A1 (ja) | 2007-11-26 | 2009-06-04 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| DE112009000621A5 (de) | 2008-01-15 | 2010-12-16 | Novaled Ag | Dithiolenübergangsmetallkomplexe und elektronische oder optoelektronische Bauelemente |
| US8057712B2 (en) | 2008-04-29 | 2011-11-15 | Novaled Ag | Radialene compounds and their use |
| DE102008027005A1 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Organische elektronische Vorrichtung enthaltend Metallkomplexe |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008035413A1 (de) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| DE102008036247A1 (de) | 2008-08-04 | 2010-02-11 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend Metallkomplexe |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102008048336A1 (de) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Einkernige neutrale Kupfer(I)-Komplexe und deren Verwendung zur Herstellung von optoelektronischen Bauelementen |
| US8119037B2 (en) | 2008-10-16 | 2012-02-21 | Novaled Ag | Square planar transition metal complexes and organic semiconductive materials using them as well as electronic or optoelectric components |
| ES2370120T3 (es) | 2008-10-23 | 2011-12-12 | Novaled Ag | Compuesto de radialeno y su utilización. |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR20110097612A (ko) | 2008-11-11 | 2011-08-31 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자 |
| DE102008057050B4 (de) | 2008-11-13 | 2021-06-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008057051B4 (de) | 2008-11-13 | 2021-06-17 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008064200A1 (de) | 2008-12-22 | 2010-07-01 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009007038A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
| US8592806B2 (en) | 2009-02-26 | 2013-11-26 | Novaled Ag | Quinone compounds as dopants in organic electronics |
| DE102009011223A1 (de) | 2009-03-02 | 2010-09-23 | Merck Patent Gmbh | Metallkomplexe |
| DE102009013041A1 (de) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009014513A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009041414A1 (de) | 2009-09-16 | 2011-03-17 | Merck Patent Gmbh | Metallkomplexe |
| JPWO2011046182A1 (ja) | 2009-10-16 | 2013-03-07 | 出光興産株式会社 | 含フルオレン芳香族化合物、有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009057167A1 (de) | 2009-12-05 | 2011-06-09 | Merck Patent Gmbh | Elektronische Vorrichtung enthaltend Metallkomplexe |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| WO2011131185A1 (de) | 2010-04-21 | 2011-10-27 | Novaled Ag | Mischung zur herstellung einer dotierten halbleiterschicht |
| CN102892859B (zh) | 2010-04-27 | 2016-03-09 | 诺瓦莱德公开股份有限公司 | 有机半导体材料和电子构件 |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE112011102008B4 (de) | 2010-06-15 | 2022-04-21 | Merck Patent Gmbh | Metallkomplexe |
| DE102010027317A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metallkomplexe |
| US20140144509A1 (en) | 2010-09-10 | 2014-05-29 | Novaled Ag | Compounds for Organic Photovoltaic Devices |
| DE102010045405A1 (de) | 2010-09-15 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010046040B4 (de) | 2010-09-22 | 2021-11-11 | Novaled Gmbh | Verfahren zur Herstellung von Fulleren-Derivaten |
| EP2452946B1 (en) | 2010-11-16 | 2014-05-07 | Novaled AG | Pyridylphosphinoxides for organic electronic device and organic electronic device |
| EP2463927B1 (en) | 2010-12-08 | 2013-08-21 | Novaled AG | Material for organic electronic device and organic electronic device |
| TWI526418B (zh) | 2011-03-01 | 2016-03-21 | 諾瓦發光二極體股份公司 | 有機半導體材料及有機組成物 |
| KR101884496B1 (ko) | 2011-05-05 | 2018-08-01 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| US9142781B2 (en) | 2011-06-09 | 2015-09-22 | Novaled Ag | Compound for organic electronic device |
| WO2012175535A1 (de) | 2011-06-22 | 2012-12-27 | Novaled Ag | Organisches elektronisches bauelement |
| JP6461599B2 (ja) | 2011-06-22 | 2019-01-30 | ノヴァレッド ゲーエムベーハー | 電子装置 |
| CN103946215B (zh) | 2011-11-17 | 2016-09-28 | 默克专利有限公司 | 螺二氢吖啶衍生物和其作为有机电致发光器件用材料的用途 |
| EP2872590B1 (de) | 2012-07-13 | 2018-11-14 | Merck Patent GmbH | Metallkomplexe |
| CN110444694B (zh) | 2012-07-23 | 2023-04-07 | 默克专利有限公司 | 化合物以及有机电致发光器件 |
| KR20210076207A (ko) | 2012-07-23 | 2021-06-23 | 메르크 파텐트 게엠베하 | 플루오렌 및 이를 함유하는 전자 소자 |
| CN108054293B (zh) | 2012-07-23 | 2020-05-22 | 默克专利有限公司 | 2-二芳基氨基芴的衍生物和含有所述2-二芳基氨基芴衍生物的有机电子复合体 |
| KR102125199B1 (ko) | 2012-07-23 | 2020-06-22 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| JP6363075B2 (ja) | 2012-08-07 | 2018-07-25 | メルク パテント ゲーエムベーハー | 金属錯体 |
| EP2935292B1 (de) | 2012-12-21 | 2019-04-10 | Merck Patent GmbH | Metallkomplexe |
| WO2014094960A1 (de) | 2012-12-21 | 2014-06-26 | Merck Patent Gmbh | Metallkomplexe |
| EP2821459B1 (en) | 2013-07-01 | 2017-10-04 | Cheil Industries Inc. | Composition and organic optoelectric device and display device |
| WO2015014434A1 (de) | 2013-07-30 | 2015-02-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP3044284B1 (de) | 2013-09-11 | 2019-11-13 | Merck Patent GmbH | Metallkomplexe |
| US10529930B2 (en) * | 2013-10-08 | 2020-01-07 | Merck Patent Gmbh | Materials for electronic devices |
| US11005050B2 (en) | 2014-01-13 | 2021-05-11 | Merck Patent Gmbh | Metal complexes |
| KR102177213B1 (ko) | 2014-01-20 | 2020-11-11 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| CN105980519B (zh) | 2014-02-05 | 2019-06-14 | 默克专利有限公司 | 金属络合物 |
| WO2015156587A1 (en) | 2014-04-08 | 2015-10-15 | Rohm And Haas Electronic Materials Korea Ltd. | Multi-component host material and organic electroluminescent device comprising the same |
| WO2016015815A1 (de) | 2014-07-28 | 2016-02-04 | Merck Patent Gmbh | Metallkomplexe |
| CN106661006B (zh) * | 2014-07-29 | 2019-11-08 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| KR20160028254A (ko) * | 2014-09-03 | 2016-03-11 | 현대자동차주식회사 | 카메라를 이용한 제진재 도포 품질 검사 시스템 및 그 품질 검사 방법 |
| JP6772188B2 (ja) | 2015-02-03 | 2020-10-21 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 金属錯体 |
| US11031562B2 (en) | 2015-08-25 | 2021-06-08 | Merck Patent Gmbh | Metal complexes |
| KR101982715B1 (ko) | 2016-03-28 | 2019-05-27 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102061246B1 (ko) | 2016-09-28 | 2020-02-20 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| WO2018101691A1 (ko) * | 2016-11-29 | 2018-06-07 | 주식회사 엘지화학 | 유기 발광 소자 |
-
2018
- 2018-07-02 CN CN201880039441.9A patent/CN110785415A/zh active Pending
- 2018-07-02 EP EP18737229.7A patent/EP3649123B1/de active Active
- 2018-07-02 KR KR1020207002898A patent/KR102594782B1/ko active Active
- 2018-07-02 KR KR1020247031924A patent/KR102840663B1/ko active Active
- 2018-07-02 EP EP23150252.7A patent/EP4186898A1/de active Pending
- 2018-07-02 KR KR1020237036164A patent/KR102616338B1/ko active Active
- 2018-07-02 JP JP2019572031A patent/JP7135012B2/ja active Active
- 2018-07-02 WO PCT/EP2018/067732 patent/WO2019007866A1/de not_active Ceased
- 2018-07-02 TW TW107122748A patent/TWI808980B/zh active
- 2018-07-02 US US16/628,280 patent/US11591320B2/en active Active
- 2018-07-02 KR KR1020237043180A patent/KR102717279B1/ko active Active
-
2022
- 2022-08-31 JP JP2022137893A patent/JP7302080B2/ja active Active
- 2022-08-31 JP JP2022137892A patent/JP7293474B2/ja active Active
- 2022-12-29 US US18/090,711 patent/US12435070B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140158992A1 (en) * | 2012-12-07 | 2014-06-12 | Universal Display Corporation | Carbazole Compounds For Delayed Fluorescence |
| WO2015165563A1 (de) * | 2014-04-30 | 2015-11-05 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US20150318487A1 (en) * | 2014-05-02 | 2015-11-05 | Samsung Display Co., Ltd. | Organic light-emitting device |
| WO2015169412A1 (de) * | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR101744248B1 (ko) * | 2016-09-06 | 2017-06-07 | 주식회사 엘지화학 | 유기발광 소자 |
| CN108779392A (zh) * | 2016-11-29 | 2018-11-09 | 株式会社Lg化学 | 有机发光器件 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113950474A (zh) * | 2019-11-05 | 2022-01-18 | Lt素材株式会社 | 杂环化合物以及包括其的有机发光装置 |
| CN113292545A (zh) * | 2021-06-28 | 2021-08-24 | 南京高光半导体材料有限公司 | 一种含有三嗪及三嗪衍生物的化合物及有机电致发光器件 |
| CN113801109A (zh) * | 2021-08-17 | 2021-12-17 | 南京高光半导体材料有限公司 | 一种含有双咔唑结构的化合物及有机电致发光器件 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230152167A (ko) | 2023-11-02 |
| TW201920156A (zh) | 2019-06-01 |
| JP2020526027A (ja) | 2020-08-27 |
| KR102616338B1 (ko) | 2023-12-20 |
| KR102717279B1 (ko) | 2024-10-15 |
| KR102840663B1 (ko) | 2025-07-30 |
| US20200231578A1 (en) | 2020-07-23 |
| US12435070B2 (en) | 2025-10-07 |
| EP3649123A1 (de) | 2020-05-13 |
| US11591320B2 (en) | 2023-02-28 |
| EP3649123B1 (de) | 2023-03-15 |
| EP4186898A1 (de) | 2023-05-31 |
| KR20200024879A (ko) | 2020-03-09 |
| JP2022177049A (ja) | 2022-11-30 |
| JP7302080B2 (ja) | 2023-07-03 |
| WO2019007866A1 (de) | 2019-01-10 |
| KR20230174290A (ko) | 2023-12-27 |
| JP2022177050A (ja) | 2022-11-30 |
| KR20240148441A (ko) | 2024-10-11 |
| JP7293474B2 (ja) | 2023-06-19 |
| TWI808980B (zh) | 2023-07-21 |
| US20230150987A1 (en) | 2023-05-18 |
| KR102594782B1 (ko) | 2023-10-27 |
| JP7135012B2 (ja) | 2022-09-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7302080B2 (ja) | 有機電子デバイスのための組成物 | |
| JP7794753B2 (ja) | 有機エレクトロルミネッセント装置 | |
| KR102804818B1 (ko) | 유기 전자 디바이스용 조성물 | |
| CN115280538A (zh) | 有机电致发光器件 | |
| KR102803370B1 (ko) | 유기 전자 디바이스용 조성물 | |
| KR102653984B1 (ko) | 유기 전자 디바이스용 조성물 | |
| CN115669281A (zh) | 有机电致发光器件 | |
| JP7693654B2 (ja) | 2種のホスト材料の混合物、およびこれを含む有機エレクトロルミネッセントデバイス | |
| KR102786661B1 (ko) | 유기 전자 디바이스용 조성물 | |
| CN118202815A (zh) | 用于有机电子器件的组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |