JP2022090057A - 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート - Google Patents
抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート Download PDFInfo
- Publication number
- JP2022090057A JP2022090057A JP2022070921A JP2022070921A JP2022090057A JP 2022090057 A JP2022090057 A JP 2022090057A JP 2022070921 A JP2022070921 A JP 2022070921A JP 2022070921 A JP2022070921 A JP 2022070921A JP 2022090057 A JP2022090057 A JP 2022090057A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- amino acid
- acid sequence
- seq
- cdh6
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68033—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a maytansine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68037—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a camptothecin [CPT] or derivatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6861—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from kidney or bladder cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6869—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from a cell of the reproductive system: ovaria, uterus, testes, prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0021—Intradermal administration, e.g. through microneedle arrays, needleless injectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
- C12N5/12—Fused cells, e.g. hybridomas
- C12N5/16—Animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
- C12N5/12—Fused cells, e.g. hybridomas
- C12N5/16—Animal cells
- C12N5/163—Animal cells one of the fusion partners being a B or a T lymphocyte
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/40—Immunoglobulins specific features characterized by post-translational modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/40—Immunoglobulins specific features characterized by post-translational modification
- C07K2317/41—Glycosylation, sialylation, or fucosylation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/02—Cells for production
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Cell Biology (AREA)
- Genetics & Genomics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Dermatology (AREA)
- Molecular Biology (AREA)
- Reproductive Health (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Urology & Nephrology (AREA)
- General Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Endocrinology (AREA)
- Gynecology & Obstetrics (AREA)
- Oncology (AREA)
- Pregnancy & Childbirth (AREA)
- Mycology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
瘍活性を有する薬物との抗体-薬物コンジュゲート、該抗体-薬物コンジュゲートを用い
た腫瘍に対する治療効果を有する医薬品、及び、該抗体、該抗体-薬物コンジュゲート又
は該医薬品を用いた腫瘍の治療方法等を提供することである。
【解決手段】 内在化活性を有する抗CDH6抗体、及び、該抗体と抗腫瘍活性を有する
薬物との抗体-薬物コンジュゲートにより上記課題の解決が図れる。
【選択図】なし
Description
抗体に、細胞傷害活性を有する薬物を結合させたものである。ADCは、がん細胞に効率的に薬物を送達できることによって、がん細胞内に薬物を蓄積させ、がん細胞を死滅させることが期待できる(非特許文献10、特許文献1及び2)。ADCとして例えば、抗CD30モノクローナル抗体にモノメチルアウリスタチンEを結合させたアドセトリス(商標)(ブレンツキシマブ ベドチン)がホジキンリンパ腫と未分化大細胞リンパ腫の治療薬として認可されている。また、抗HER2モノクローナル抗体にエムタンシンを結合させたカドサイラ(商標)(トラスツズマブ エムタンシン)がHER2陽性の進行、再発乳癌の治療に用いられている。
[1]配列番号4に記載のアミノ酸配列に特異的に結合し、細胞内に取り込まれる内在化能を有する、抗体又は当該抗体の機能性断片;
[2]配列番号4に記載のアミノ酸配列への結合に対して、以下の(1)~(5):
(1)配列番号53の21~233番目に記載のアミノ酸配列からなる軽鎖及び配列番号56の20~471番目に記載のアミノ酸配列からなる重鎖を有する抗体、
(2)配列番号61の21~233番目に記載のアミノ酸配列からなる軽鎖及び配列番号69の20~471番目に記載のアミノ酸配列からなる重鎖を有する抗体、
(3)配列番号61の21~233番目に記載のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目に記載のアミノ酸配列からなる重鎖を有する抗体、
(4)配列番号65の21~233番目に記載のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目に記載のアミノ酸配列からなる重鎖を有する抗体、及び
(5)配列番号61の21~233番目に記載のアミノ酸配列からなる軽鎖及び配列番号77の20~471番目に記載のアミノ酸配列からなる重鎖を有する抗体、
からなる群から選択される抗体のうち少なくともいずれか1つと競合阻害活性を有する[1]に記載の抗体又は当該抗体の機能性断片;
[3]以下の(1)~(4):
(1)配列番号12に記載のアミノ酸配列からなるCDRL1、配列番号13に記載のアミノ酸配列からなるCDRL2及び配列番号14に記載のアミノ酸配列からなるCDRL3、
(2)配列番号22に記載のアミノ酸配列からなるCDRL1、配列番号23に記載のアミノ酸配列からなるCDRL2及び配列番号24に記載のアミノ酸配列からなるCDRL3、
(3)配列番号32に記載のアミノ酸配列からなるCDRL1、配列番号33に記載のアミノ酸配列からなるCDRL2及び配列番号34に記載のアミノ酸配列からなるCDRL3、及び
(4)配列番号42に記載のアミノ酸配列からなるCDRL1、配列番号43に記載のアミノ酸配列からなるCDRL2及び配列番号44に記載のアミノ酸配列からなるCDRL3、
からなる群から選択されるいずれか1つに記載のCDRL1、CDRL2及びCDRL3、並びに、
以下の(5)~(9):
(5)配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号18に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3、
(6)配列番号27に記載のアミノ酸配列からなるCDRH1、配列番号28に記載のアミノ酸配列からなるCDRH2及び配列番号29に記載のアミノ酸配列からなるCDRH3、
(7)配列番号37に記載のアミノ酸配列からなるCDRH1、配列番号38に記載のアミノ酸配列からなるCDRH2及び配列番号39に記載のアミノ酸配列からなるCDRH3、
(8)配列番号47に記載のアミノ酸配列からなるCDRH1、配列番号48に記載のアミノ酸配列からなるCDRH2及び配列番号49に記載のアミノ酸配列からなるCDRH3、及び
(9)配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号60に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3、
からなる群から選択されるいずれか1つに記載のCDRH1、CDRH2及びCDRH3を含む、
[1]又は[2]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[4]以下の(1)~(5):
(1)配列番号12に記載のアミノ酸配列からなるCDRL1、配列番号13に記載のアミノ酸配列からなるCDRL2及び配列番号14に記載のアミノ酸配列からなるCDRL3、及び、配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号18に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3、
(2)配列番号22に記載のアミノ酸配列からなるCDRL1、配列番号23に記載のアミノ酸配列からなるCDRL2及び配列番号24に記載のアミノ酸配列からなるCDRL3、及び、配列番号27に記載のアミノ酸配列からなるCDRH1、配列番号28に記載のアミノ酸配列からなるCDRH2及び配列番号29に記載のアミノ酸配列からなるCDRH3、
(3)配列番号32に記載のアミノ酸配列からなるCDRL1、配列番号33に記載のアミノ酸配列からなるCDRL2及び配列番号34に記載のアミノ酸配列からなるCDRL3、及び、配列番号37に記載のアミノ酸配列からなるCDRH1、配列番号38に記載のアミノ酸配列からなるCDRH2及び配列番号39に記載のアミノ酸配列からなるCDRH3、
(4)配列番号42に記載のアミノ酸配列からなるCDRL1、配列番号43に記載のアミノ酸配列からなるCDRL2及び配列番号44に記載のアミノ酸配列からなるCDRL3、及び、配列番号47に記載のアミノ酸配列からなるCDRH1、配列番号48に記載のアミノ酸配列からなるCDRH2及び配列番号49に記載のアミノ酸配列からなるCDRH3、及び
(5)配列番号12に記載のアミノ酸配列からなるCDRL1、配列番号13に記載のアミノ酸配列からなるCDRL2及び配列番号14に記載のアミノ酸配列からなるCDRL3、及び、配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号60に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3、
からなる群から選択されるCDRL1、CDRL2及びCDRL3、並びに、CDRH1、CDRH2及びCDRH3を含む、
[1]~[3]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[5]ヒト化されている[1]~[4]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[6]以下の(1)~(4):
(1)配列番号63に記載のアミノ酸配列からなる軽鎖可変領域、
(2)配列番号67に記載のアミノ酸配列からなる軽鎖可変領域、
(3)(1)~(2)のアミノ酸配列において各CDR配列以外のフレームワーク領域の配列に対して少なくとも95%以上の配列同一性を有するアミノ酸配列、及び
(4)(1)~(3)のアミノ酸配列において各CDR配列以外のフレームワーク領域の配列において1又は数個のアミノ酸が欠失、置換又は付加されたアミノ酸配列
からなる群から選択されるいずれか1つに記載の軽鎖可変領域、並びに、
以下の(5)~(9):
(5)配列番号71に記載のアミノ酸配列からなる重鎖可変領域、
(6)配列番号75に記載のアミノ酸配列からなる重鎖可変領域、
(7)配列番号79に記載のアミノ酸配列からなる重鎖可変領域、
(8)(5)~(7)のアミノ酸配列において各CDR配列以外のフレームワーク領域の配列に対して少なくとも95%以上の配列相同性を有するアミノ酸配列、及び
(9)(5)~(8)のアミノ酸配列において各CDR配列以外のフレームワーク領域の配列において1又は数個のアミノ酸が欠失、置換又は付加されたアミノ酸配列
からなる群から選択されるいずれか1つに記載の重鎖可変領域、
を有する[1]~[5]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[7]以下の(1)~(4):
(1)配列番号63に記載のアミノ酸配列からなる軽鎖可変領域及び配列番号71に記載のアミノ酸配列からなる重鎖可変領域、
(2)配列番号63に記載のアミノ酸配列からなる軽鎖可変領域及び配列番号75に記載のアミノ酸配列からなる重鎖可変領域、
(3)配列番号67に記載のアミノ酸配列からなる軽鎖可変領域及び配列番号75に記載のアミノ酸配列からなる重鎖可変領域、又は
(4)配列番号63に記載のアミノ酸配列からなる軽鎖可変領域及び配列番号79に記載のアミノ酸配列からなる重鎖可変領域、
のいずれかの軽鎖可変領域及び重鎖可変領域、
を含む[1]~[6]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[8]以下の(1)~(4):
(1)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69の20~471番目のアミノ酸配列からなる重鎖、
(2)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列からなる重鎖、
(3)配列番号65の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列からなる重鎖、又は
(4)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77の20~471番目のアミノ酸配列からなる重鎖、
のいずれかを有する[1]~[7]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[9]配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69の20~471番目のアミノ酸配列からなる重鎖を有する[8]に記載の抗体又は当該抗体の機能性断片;
[10]配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列からなる重鎖を有する[8]に記載の抗体又は当該抗体の機能性断片;
[11]配列番号65の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列からなる重鎖を有する[8]に記載の抗体又は当該抗
体の機能性断片;
[12]配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77の20~471番目のアミノ酸配列からなる重鎖を有する[8]に記載の抗体又は当該抗体の機能性断片;
[13]機能性断片がFab、F(ab’)2、Fab’及びFvからなる群から選択される[1]~[12]のいずれか1項に記載の抗体の機能性断片;
[14][1]~[13]のいずれか1項に記載の抗体又は当該抗体の機能性断片をコードするポリヌクレオチド;
[15]以下の(1)~(5):
(1)配列番号12に記載のアミノ酸配列からなるCDRL1、配列番号13に記載のアミノ酸配列からなるCDRL2及び配列番号14に記載のアミノ酸配列からなるCDRL3を含む軽鎖可変領域をコードするポリヌクレオチド、及び、配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号18に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3を含む重鎖可変領域をコードするポリヌクレオチド、
(2)配列番号22に記載のアミノ酸配列からなるCDRL1、配列番号23に記載のアミノ酸配列からなるCDRL2及び配列番号24に記載のアミノ酸配列からなるCDRL3を含む軽鎖可変領域をコードするポリヌクレオチド、及び、配列番号27に記載のアミノ酸配列からなるCDRH1、配列番号28に記載のアミノ酸配列からなるCDRH2及び配列番号29に記載のアミノ酸配列からなるCDRH3を含む重鎖可変領域をコードするポリヌクレオチド、
(3)配列番号32に記載のアミノ酸配列からなるCDRL1、配列番号33に記載のアミノ酸配列からなるCDRL2及び配列番号34に記載のアミノ酸配列からなるCDRL3を含む軽鎖可変領域をコードするポリヌクレオチド、及び、配列番号37に記載のアミノ酸配列からなるCDRH1、配列番号38に記載のアミノ酸配列からなるCDRH2及び配列番号39に記載のアミノ酸配列からなるCDRH3を含む重鎖可変領域をコードするポリヌクレオチド、
(4)配列番号42に記載のアミノ酸配列からなるCDRL1、配列番号43に記載のアミノ酸配列からなるCDRL2及び配列番号44に記載のアミノ酸配列からなるCDRL3を含む軽鎖可変領域をコードするポリヌクレオチド、及び、配列番号47に記載のアミノ酸配列からなるCDRH1、配列番号48に記載のアミノ酸配列からなるCDRH2及び配列番号49に記載のアミノ酸配列からなるCDRH3を含む重鎖可変領域をコードするポリヌクレオチド、並びに
(5)配列番号12に記載のアミノ酸配列からなるCDRL1、配列番号13に記載のアミノ酸配列からなるCDRL2及び配列番号14に記載のアミノ酸配列からなるCDRL3を含む軽鎖可変領域をコードするポリヌクレオチド、及び、配列番号17に記載のアミノ酸配列からなるCDRH1、配列番号60に記載のアミノ酸配列からなるCDRH2及び配列番号19に記載のアミノ酸配列からなるCDRH3を含む重鎖可変領域をコードするポリヌクレオチド、
からなる群から選択されるいずれか1つに記載のポリヌクレオチドを含む[14]に記載のポリヌクレオチド;
[16]配列番号61の21~233番目のアミノ酸配列からなる軽鎖をコードするポリヌクレオチド及び配列番号69の20~471番目のアミノ酸配列からなる重鎖をコードするポリヌクレオチドを含む[14]又は[15]に記載のポリヌクレオチド;
[17]配列番号61の21~233番目のアミノ酸配列からなる軽鎖をコードするポリヌクレオチド及び配列番号73の20~471番目のアミノ酸配列からなる重鎖をコードするポリヌクレオチドを含む[14]又は[15]に記載のポリヌクレオチド;
[18]配列番号65の21~233番目のアミノ酸配列からなる軽鎖をコードするポリヌクレオチド及び配列番号73の20~471番目のアミノ酸配列からなる重鎖をコードするポリヌクレオチドを含む[14]又は[15]に記載のポリヌクレオチド;
[19]配列番号61の21~233番目のアミノ酸配列からなる軽鎖をコードするポリヌクレオチド及び配列番号77の20~471番目のアミノ酸配列からなる重鎖をコードするポリヌクレオチドを含む[14]又は[15]に記載のポリヌクレオチド;
[20][14]~[19]のいずれか1項に記載のポリヌクレオチドを含有する発現ベクター;
[21][20]に記載の発現ベクターにより形質転換された宿主細胞;
[22]宿主細胞が真核細胞である[21]に記載の宿主細胞;
[23][21]又は[22]に記載の宿主細胞を培養する工程、及び当該工程で得られた培養物から目的の抗体又は当該抗体の機能性断片を採取する工程を含むことを特徴とする当該抗体又は当該抗体の機能性断片の製造方法;
[24]重鎖又は軽鎖が、N-結合への糖鎖付加、O-結合への糖鎖付加、N末のプロセッシング、C末のプロセッシング、脱アミド化、アスパラギン酸の異性化、メチオニンの酸化、N末にメチオニン残基の付加、プロリン残基のアミド化、N末グルタミンもしくはN末グルタミン酸のピログルタミン酸化、及びカルボキシル末端における1つ又は2つのアミノ酸欠失からなる群より選択される1又は2以上の修飾をうけた、[1]~[13]のいずれか1項に記載の抗体又は当該抗体の機能性断片;
[25]重鎖のカルボキシル末端において1つ又は2つのアミノ酸が欠失している[24]に記載の抗体;
[26]2本の重鎖の双方でカルボキシル末端において1つのアミノ酸が欠失している[25]に記載の抗体;
[27]重鎖のカルボキシル末端のプロリン残基が更にアミド化されている[24]~[26]のいずれか1項に記載の抗体;
[28]抗体依存性細胞傷害活性を増強させるために糖鎖修飾が調節されている[1]~[13]及び[24]~[27]からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片;
[29][1]~[13]及び[24]~[28]からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片に薬物が結合している抗体-薬物コンジュゲート;
[30]薬物が抗腫瘍性化合物である、[29]に記載の抗体-薬物コンジュゲート;
[31]抗腫瘍性化合物が次式:
[32]抗体と薬物が、次式(a)~(f):
(a)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
(b)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
(c)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
(d)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
(e)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、及び
(f)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
からなる群から選択されるいずれかの構造のリンカーを介して結合している、[29]~[31]のいずれか1項に記載の抗体-薬物コンジュゲート。
(ここで、抗体は、-(Succinimid-3-yl-N)の末端において結合する。抗腫瘍性化合物は、1位のアミノ基の窒素原子を結合部位として、(a)、(b)、(e)又は(f)の-CH2CH2CH2-C(=O)-部分、(c)のCH2-O-CH2-C(=O)-部分又は(d)のCH2CH2-O-CH2-C(=O)-部分のカルボニル基に結合する。上記式中GGFGは、グリシン-グリシン-フェニルアラニン-グリシンからなるペプチド結合でつながっているアミノ酸配列を示す。
-(Succinimid-3-yl-N)-は次式:
[33]リンカーが以下の(c)、(d)及び(e)からなる群から選択されるいずれかの式で示される[29]~[32]のいずれか1項に記載の抗体-薬物コンジュゲート:(c)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
(d)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
(e)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-;
[34]リンカーが以下の(c)又は(e)の式で示される[29]~[33]のいずれか1項に記載の抗体-薬物コンジュゲート:
(c)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
(e)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-;
[35]以下の式:
ここで、ABは抗体又は該抗体の機能性断片を示す。nは抗体と結合している薬物-リンカー構造の1抗体あたりの平均結合数を示す。抗体とリンカーは抗体由来のスルフヒドリル基を介して結合している;
[36]以下の式:
ここで、ABは抗体又は該抗体の機能性断片を示す。nは抗体と結合している薬物-リンカー構造の1抗体あたりの平均結合数を示す。抗体とリンカーは抗体由来のスルフヒドリル基を介して結合している;
[37]抗体が以下の(1)~(4):
(1)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69の20~471番目のアミノ酸配列からなる重鎖、
(2)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列からなる重鎖、
(3)配列番号65の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73の
20~471番目のアミノ酸配列からなる重鎖、又は
(4)配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77の20~471番目のアミノ酸配列からなる重鎖、
からなる群から選択されるいずれか1つに記載の軽鎖及び重鎖を含む抗体又は当該抗体の機能性断片である、[29]~[36]のいずれか1項に記載の抗体-薬物コンジュゲート;
[38]抗体が、配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69の20~471番目のアミノ酸配列からなる重鎖を含む抗体又は当該抗体の機能性断片である、[37]に記載の抗体-薬物コンジュゲート;
[39]抗体が、配列番号61の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77の20~471番目のアミノ酸配列からなる重鎖を含む抗体又は当該抗体の機能性断片である、[37]に記載の抗体-薬物コンジュゲート;
[40]重鎖又は軽鎖が、N-結合への糖鎖付加、O-結合への糖鎖付加、N末のプロセッシング、C末のプロセッシング、脱アミド化、アスパラギン酸の異性化、メチオニンの酸化、N末にメチオニン残基の付加、プロリン残基のアミド化、N末グルタミンもしくはN末グルタミン酸のピログルタミン酸化及びカルボキシル末端における1つ又は2つのアミノ酸欠失からなる群から選択される1又は2以上の修飾をうけた、[29]~[39]のいずれか1項に記載の抗体-薬物コンジュゲート;
[41]選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が1~10個の範囲である[29]~[40]のいずれか1項に記載の抗体-薬物コンジュゲート;
[42]選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が2~8個の範囲である[41]に記載の抗体-薬物コンジュゲート;
[43]選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が5~8個の範囲である[42]に記載の抗体-薬物コンジュゲート;
[44]選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が7~8個である[43]に記載の抗体-薬物コンジュゲート;
[45][29]~[44]のいずれか1項に記載の抗体-薬物コンジュゲート、その塩、又はそれらの水和物を含むことを特徴とする医薬組成物;
[46]抗腫瘍薬であることを特徴とする、[45]に記載の医薬組成物;
[47]腫瘍がCDH6を発現する腫瘍であることを特徴とする、[46]に記載の医薬組成物;
[48]腫瘍が、腎細胞癌、腎淡明細胞癌、乳頭状腎細胞癌、卵巣癌、卵巣漿液性腺癌、甲状腺癌、胆管癌、肺癌、小細胞肺癌、神経膠芽腫、中皮腫、子宮癌、膵臓癌、ウィルムス腫瘍又は神経芽腫であることを特徴とする、[46]又は[47]に記載の医薬組成物;
[49][29]~[44]のいずれか1項に記載の抗体-薬物コンジュゲート、その塩、又はそれらの水和物から選択されるいずれかを個体に投与することを特徴とする腫瘍の治療方法;
[50]腫瘍がCDH6が発現している腫瘍であることを特徴とする、[49]に記載の治療方法;
[51]腫瘍が、腎細胞癌、腎淡明細胞癌、乳頭状腎細胞癌、卵巣癌、卵巣漿液性腺癌、甲状腺癌、胆管癌、肺癌、小細胞肺癌、神経膠芽腫、中皮腫、子宮癌、膵臓癌、ウィルムス腫瘍又は神経芽腫であることを特徴とする、[49]又は[50]に記載の治療方法;[52][29]~[44]のいずれか1項に記載の抗体-薬物コンジュゲート、その塩、又はそれらの水和物から選択される少なくとも一つを含む医薬組成物及び少なくとも一つの抗腫瘍薬を、同時に、別々に又は連続して個体に投与することを特徴とする腫瘍の治療方法;
[53][1]~[13]及び[24]~[28]からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片或いは[23]に記載の製造方法で得られる抗体又は当該抗体の機能性断片と、薬物-リンカー中間化合物を反応させる工程を含むこと
を特徴とする、抗体-薬物コンジュゲートの製造方法;又は
[54][21]又は[22]に記載の宿主細胞を培養する工程、当該工程で得られた培養物から目的の抗体又は当該抗体の機能性断片を採取する工程、及び当該工程で得られた抗体又は当該抗体の機能性断片と薬物-リンカー中間化合物を反応させる工程を含むことを特徴とする、抗体-薬物コンジュゲートの製造方法。
ず、抗原の様々な部分構造を作製する。部分構造の作製にあたっては、公知のオリゴヌクレオチド合成技術を用いることができる。例えば、CDH6のC末端又はN末端から適当な長さで順次短くした一連のポリペプチドを当業者に周知の遺伝子組み換え技術を用いて作製した後、それらに対する抗体の反応性を検討し、大まかな認識部位を決定した後に、更に短いペプチドを合成してそれらのペプチドとの反応性を検討することによって、エピトープを決定することができる。また、複数の細胞外ドメインからなる膜タンパク質に結合する抗体が、複数のドメインからなる立体構造をエピトープとしている場合は、特定の細胞外ドメインのアミノ酸配列を改変することによって、立体構造を改変することによってどのドメインと結合するかを決定することができる。特定の抗体の結合する抗原の部分立体構造であるエピトープは、X線構造解析によって抗体と隣接する抗原のアミノ酸残基を特定することによっても決定することができる。
カドヘリンは、細胞膜表面に存在する糖タンパク質で、カルシウムイオン依存的にN末端側の細胞外ドメイン同士が結合することで、細胞間接着分子として、また細胞間相互作用を担うシグナル分子として機能する。カドヘリンスーパーファミリーの内、クラシック
カドヘリンに分類される分子群は、細胞外に5個の細胞外ドメイン(ECドメイン)と1個の膜貫通領域、及び細胞内ドメインから構成される1回膜貫通タンパク質である。
本発明の抗CDH6抗体の一例として、配列番号4に示すアミノ酸配列を含むアミノ酸配列を認識し、かつ内在化活性を有する抗CDH6抗体を挙げることができる。本発明の抗CDH6抗体の一例として、配列番号4に示すアミノ酸配列を含むアミノ酸配列を特異的に認識し、かつ内在化活性を有する抗CDH6抗体を挙げることができる。本発明の抗CDH6抗体の一例として、配列番号4に示すアミノ酸配列からなるアミノ酸配列を認識し、かつ内在化活性を有する抗CDH6抗体を挙げることができる。本発明の抗CDH6抗体の一例として、配列番号4に示すアミノ酸配列からなるアミノ酸配列を特異的に認識し、かつ内在化活性を有する抗CDH6抗体を挙げることができる。抗体が「配列番号4に示すアミノ酸配列を含むアミノ酸配列を特異的に認識」する又は「EC3ドメインを特異的に認識」するとは、抗体が、CDH6のEC3ドメインをCDH6の他の細胞外ドメインと比較して強く認識する又は強く結合することをいう。
Differentiation,2008,15,751-761)、(2)治療抗体に結合する二次抗体(蛍光標識)を用いて細胞内に取り込まれた蛍光量を測定するアッセイ(Molecular Biology of the Cell Vol.15,5268-5282,December 2004)又は(3)治療抗体に結合するイムノトキシンを用いて、細胞内に取り込まれると毒素が放出されて細胞増殖が抑制されるというMab-ZAPアッセイ(Bio Techniques 28:162-165,January 2000)を用いて確認できる。イムノトキシンとしては、ジフテテリア毒素の触媒領域とプロテインGとのリコンビナント複合タンパク質タンパク質も使用可能である。
抗原は抗原タンパク質をコードする遺伝子を遺伝子操作によって宿主細胞に産生させることによって得ることができる。具体的には、抗原遺伝子を発現可能なベクターを作製し、これを宿主細胞に導入して該遺伝子を発現させ、発現した抗原を精製すればよい。上記の遺伝子操作による抗原発現細胞、あるいは抗原を発現している細胞株を動物に免疫する方法を用いることによっても抗体を取得できる。
本発明で使用される抗CDH6抗体は、特に制限はないが、例えば、本願の配列表で示されたアミノ酸配列で特定される抗体を好適に使用することができる。本発明において使用される抗CDH6抗体としては、以下の特性を有するものが望ましい。
(1)以下の特性を有することを特徴とする抗体;
(a)CDH6に特異的に結合する
(b)CDH6と結合することによってCDH6発現細胞に内在化する活性を有する
(2)CDH6がヒトCDH6である上記(1)に記載の抗体又は当該抗体。
(3)ヒトCDH6のEC3を特異的に認識し、かつ内在化活性を有する
本発明のCDH6に対する抗体の取得方法は、抗CDH6抗体を取得できる限りにおいて、特に制限されないが、高次構造を保持したCDH6を抗原として用いることが好ましい。
MF,Gehl J,Rangara R,Rouy D,Caillaud JM,Delaere P,Branellec D,Schwartz B,Scherman D.Proc Natl Acad Sci USA.1999 Apr 13;96(8):4262-7.)。本手法はプラスミドの筋注前にヒアルロニダーゼで筋肉を処理することにより、さらに発現量が向上する(McMahon JM1, Signori E,Wells KE,Fazio VM,Wells DJ.Gene Ther.2001 Aug;8(16):1264-70)。また、ハイブリドーマの作製は公知の方法によって行うことができ、例えば、Hybrimune Hybridoma Production System(Cyto Pulse Sciences社)を用いて行うこともできる。
(a)CDH6のcDNAを発現ベクター(例えば、pcDNA3.1:Thermo Fisher Scientific)に組み込み、エレクトロポレーションや遺伝子銃
等の方法によって、そのベクターを直接被免疫動物(例えば、ラットやマウス)に投与することによって、動物体内においてCDH6を発現させることによって、免疫反応を誘起させることができる。エレクトロポレーション等によるベクターの投与は抗体価を上げるために必要であれば、1回でも複数回でもよく、好ましくは複数回である;
(b)免疫反応を誘起された上述の動物より、抗体産生細胞を含む組織(例えばリンパ節)を採取する;
(c)骨髄腫細胞(以下「ミエローマ」という)(例えば、マウスミエローマSP2/0-ag14細胞)の調製;
(d)抗体産生細胞とミエローマとの細胞融合;
(e)目的とする抗体を産生するハイブリドーマ群の選別;
(f)単一細胞クローンへの分割(クローニング);
(g)場合によっては、モノクローナル抗体を大量に製造するためのハイブリドーマの培養、又はハイブリドーマを移植した動物の飼育;及び/又は
(h)このようにして製造されたモノクローナル抗体の生理活性(内在化活性)、及びその結合特異性の検討、あるいは標識試薬としての特性の検定。
本発明の抗体には、上記CDH6に対するモノクローナル抗体に加え、ヒトに対する異種抗原性を低下させること等を目的として人為的に改変した遺伝子組換え型抗体、例えば、キメラ(Chimeric)抗体、ヒト化(Humanized)抗体又はヒト抗体等も含まれる。これらの抗体は、既知の方法を用いて製造することができる。
6855,(1984)参照)。
ルタミン酸;塩基性グループ=リシン、アルギニン、ヒスチジン;非極性グループ=アラニン、バリン、ロイシン、イソロイシン、プロリン、フェニルアラニン、メチオニン、トリプトファン;及び非帯電極性ファミリー=グリシン、アスパラギン、グルタミン、システイン、セリン、スレオニン、チロシン。他の好適なアミノ酸グループは次のとおりである:脂肪族ヒドロキシグループ=セリン及びスレオニン;アミド含有グループ=アスパラギン及びグルタミン;脂肪族グループ=アラニン、バリン、ロイシン及びイソロイシン;並びに芳香族グループ=フェニルアラニン、トリプトファン及びチロシン。かかるアミノ酸置換は元のアミノ酸配列を有する物質の特性を低下させない範囲で行うのが好ましい。
アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;又は、配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体が挙げられる。より好ましい例としては、配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体(本明細書中、「H01L02抗体」又は「H01L02」とも称する);配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体(本明細書中、「H02L02抗体」又は「H02L02」とも称する);配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体(本明細書中、「H04L02抗体」又は「H04L02」とも称する);又は、配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体(本明細書中、「H02L03抗体」又は「H02L03」とも称する)が挙げられる。H01L02抗体、H02L02抗体、H02L03抗体又はH04L02抗体の配列を表1に示す。
R, McGettigan PA, McWilliam H, Valentin
F, Wallace IM, Wilm A, Lopez R, Thompson JD, Gibson TJ and Higgins DG(2007),「Clustal W and Clustal X version 2.0」, Bioinformatics.23(21):2947-2948)のデフォルトパラメーターを使用して配列を整列させることによって決定することができる。
、61~384番目のヌクレオチドからなるヌクレオチド配列は可変領域をコードし、385~699番目のヌクレオチドからなるヌクレオチド配列は定常領域をコードしている。
本発明の抗体としては、さらに、CDH6に結合する、ヒト抗体を挙げることができる。抗CDH6ヒト抗体とは、ヒト染色体由来の抗体の遺伝子配列のみを有するヒト抗体を意味する。抗CDH6ヒト抗体は、ヒト抗体の重鎖と軽鎖の遺伝子を含むヒト染色体断片を有するヒト抗体産生マウスを用いた方法(Tomizuka,K.et al.,Nature Genetics(1997)16,p.133-143,;Kuroiwa,Y.et.al.,Nucl.Acids Res.(1998)26,p.3447-3448;Yoshida,H.et.al.,Animal Cell Technology:Basic and Applied Aspects vol.10,p.69-73(Kitagawa,Y.,Matsuda,T.and Iijima,S.eds.),Kluwer Academic Publishers,1999.;Tomizuka,K.et.al.,Proc.Natl.Acad.Sci.USA(2000)97,p.722-727等を参照。)によって取得することができる。
の抗体を培養上清中から得ることもできる。
-1650)、マウス線維芽細胞NIH3T3(ATCC No.CRL-1658)やチャイニーズ・ハムスター卵巣細胞(CHO細胞、ATCC CCL-61)のジヒドロ葉酸還元酵素欠損株(Urlaub,G.and Chasin,L.A.Proc.Natl.Acad.Sci.U.S.A.(1980)77,p.4126-4220)、FreeStyle 293F細胞(Invitrogen社)を挙げることができる。
等電点電気泳動等を適宜選択、組み合わせれば、抗体を分離、精製することができる(Strategies for Protein Purification and Characterization:A Laboratory Course Manual,Daniel R.Marshak et al.eds.,Cold Spring Harbor Laboratory Press(1996);Antibodies:A Laboratory Manual.Ed Harlow and David Lane,Cold Spring Harbor Laboratory(1988))が、これらに限定されるものではない。
(1)薬物
上記「2.抗CDH6抗体の製造」にて取得された抗CDH6抗体はリンカー構造部分を介して薬物を結合させることによって、抗CDH6抗体-薬物コンジュゲートとすることができる。薬物としては、リンカー構造に結合できる置換基、部分構造を有するものであれば特に制限はない。抗CDH6抗体-薬物コンジュゲートは結合する薬物に応じて種々の用途に用いることができる。そのような薬物の例としては、抗腫瘍活性を有する物質、血液疾患に対する効果を有する物質、自己免疫疾患に対する効果を有する物質、抗炎症物質、抗菌物質、抗真菌物質、抗寄生虫物質、抗ウイルス物質、抗麻酔物質等を挙げることができる。
本発明の抗CDH6抗体-薬物コンジュゲートに結合される化合物として抗腫瘍性化合物を用いる例について以下に述べる。抗腫瘍性化合物としては、抗腫瘍効果を有する化合物であって、リンカー構造に結合できる置換基、部分構造を有するものであれば特に制限はない。抗腫瘍性化合物は、リンカーの一部又は全部が腫瘍細胞内で切断されて抗腫瘍性化合物部分が遊離されて抗腫瘍効果が発現される。リンカーが薬物との結合部分で切断されれば抗腫瘍性化合物が本来の構造で遊離され、その本来の抗腫瘍効果が発揮される。
6,7]インドリジノ[1,2-b]キノリン-10,13(9H,15H)-ジオン;次式:)
本発明の抗CDH6抗体-薬物コンジュゲートにおいて薬物を抗CDH6抗体に結合させるリンカー構造について述べる。
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
さらにより好ましくは、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
を挙げることができる。
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=
O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)。
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-(NH-DX)、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)。
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-(NH-DX)
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-(NH-DX)。
本発明の抗体ー薬物コンジュゲートに用いることができる抗体は、上記「2.抗CDH6抗体の製造」の項及び実施例に記載の内在化活性を有する抗CDH6抗体及び該抗体の機能性断片であれば特に制限がない。
下記式(1)で示される抗体-薬物コンジュゲートのうち、チオエーテルを介して抗CDH6抗体とリンカー構造が結合しているものは抗CDH6抗体を還元してジスルフィド結合をスルヒドリル基に変換した抗体に対して、既知の方法によって入手しうる化合物(2)(例えば、US2016/297890号公開特許公報に記載の方法(例えば段落[0336]~[0374]に記載の方法)で入手可能)を反応させることによって製造することができる。例えば下記の方法によって製造することができる。
ここで、L1は、
-(Succinimid-3-yl-N)-の構造で示される。
L1’は次式で示される、マレイミジル基を示す。]
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。
製造した抗体-薬物コンジュゲート(1)は、以下の共通操作によって濃縮、バッファー交換、精製、抗体濃度及び抗体一分子あたりの薬物平均結合数の測定を行い、抗体-薬物コンジュゲート(1)の同定を行うことができる。
Amicon Ultra(50,000 MWCO,Millipore Corporation)の容器内に抗体もしくは抗体-薬物コンジュゲート溶液を入れ、遠心機(Allegra X-15R,Beckman Coulter,Inc.)を用いた遠心操作(2000G乃至3800Gにて5乃至20分間遠心)にて、抗体もしくは抗体-薬物コンジュゲート溶液を濃縮した。
UV測定器(Nanodrop 1000,Thermo Fisher Scientific Inc.)を用いて、メーカー規定の方法に従い、抗体濃度の測定を行った。その際に、抗体ごとに異なる280nm吸光係数(1.3mLmg-1cm-1乃至1.8mLmg-1cm-1)を用いた。
Sephadex G-25担体を使用したNAP-25カラム(Cat.No.17-0852-02,GE Healthcare Japan Corporation)を、メーカー規定の方法に従い、塩化ナトリウム(50mM)及びEDTA(2mM)を含むリン酸緩衝液(50mM,pH6.0)(本明細書でPBS6.0/EDTAと称する。)にて平衡化させた。このNAP-25カラム一本につき、抗体水溶液2.5mLをのせたのち、PBS6.0/EDTA3.5mLで溶出させた画分(3.5mL)を分取した。この画分を共通操作Aによって濃縮し、共通操作Bを用いて抗体濃度の測定を行ったのちに、PBS6.0/EDTAを用いて20mg/mLに抗体濃度を調整した。
市販のSorbitol(5%)を含む酢酸緩衝液(10mM,pH5.5;本明細書でABSと称する。)のいずれかの緩衝液でNAP-25カラムを平衡化させた。このNAP-25カラムに、抗体-薬物コンジュゲート反応水溶液(約2.5mL)をのせ、メーカー規定の量の緩衝液で溶出させることで、抗体画分を分取した。この分取画分を再びNAP-25カラムにのせ緩衝液で溶出させるゲルろ過精製操作を計2乃至3回繰り返すことで、未結合の薬物リンカーや低分子化合物(トリス(2-カルボキシエチル)ホスフィン塩酸塩(TCEP),N-アセチル-L-システイン(NAC),ジメチルスルホキシド)を除いた抗体-薬物コンジュゲートを得た。
抗体-薬物コンジュゲートにおける結合薬物濃度は、抗体-薬物コンジュゲート水溶液の280nm及び370nmの二波長におけるUV吸光度を測定したのちに下記の計算を行うことで、算出することができる。
A280=AD,280+AA,280=εD,280CD+εA,280CA 式(1)
A370=AD,370+AA,370=εD,370CD+εA,370CA 式(2)
ここで、A280は280nmにおける抗体-薬物コンジュゲート水溶液の吸光度を示し、A370は370nmにおける抗体-薬物コンジュゲート水溶液の吸光度を示し、AA,280は280nmにおける抗体の吸光度を示し、AA,370は370nmにおける抗体の吸光度を示し、AD,280は280nmにおけるコンジュゲート前駆体の吸光度を示し、AD,370は370nmにおけるコンジュゲート前駆体の吸光度を示し、εA,280は280nmにおける抗体のモル吸光係数を示し、εA,370は370nmにおける抗体のモル吸光係数を示し、εD,280は280nmにおけるコンジュゲート前駆体のモル吸光係数を示し、εD,370は370nmにおけるコンジュゲート前駆体のモル吸光係数を示し、CAは抗体-薬物コンジュゲートにおける抗体濃度を示し、CDは抗体-薬物コンジュゲートにおける薬物濃度を示す。
抗体-薬物コンジュゲートにおける抗体一分子あたりの薬物平均結合数は、前述の「(4)-5 共通操作E」に加え、以下の方法を用いる高速液体クロマトグラフィー(HPLC)分析によっても求めることができる。以下に、抗体と薬物リンカーがジスルフィド結合している場合のHPLCによる薬物平均結合数の測定方法を記載する。当業者は、この方法を参照して、抗体と薬物リンカーとの結合様式に依存して適宜、HPLCにより薬物平均結合数を測定し得る。
抗体-薬物コンジュゲート溶液(約1mg/mL、60μL)をジチオトレイトール(DTT)水溶液(100mM、15μL)と混合する。混合物を37℃で30分インキュベートすることで、抗体-薬物コンジュゲートの軽鎖及び重鎖間のジスルフィド結合を切断したサンプルを、HPLC分析に用いる。
HPLC分析を、下記の測定条件にて行う。
検出器:紫外吸光度計(測定波長:280nm)
カラム:ACQUITY UPLC BEH Phenyl(2.1×50mm、1.7μm、130Å;Waters、P/N 186002884)
カラム温度:80℃
移動相A:0.10%トリフルオロ酢酸(TFA)、15%2-プロパノールを含む水溶液
移動相B:0.075%TFA、15%2-プロパノールを含むアセトニトリル溶液
グラジエントプログラム:14%-36%(0分-15分)、36%-80%(15分-17分)、80%-14%(17分―17.01分)、14%(17.01分―25分)
サンプル注入量:10μL
F-3.データ解析
F-3-1 薬物の結合していない抗体の軽鎖(L0)及び重鎖(H0)に対して、薬物の結合した軽鎖(薬物がi個結合した軽鎖:Li)及び重鎖(薬物がi個結合した重鎖:Hi)は、結合した薬物の数に比例して疎水性が増し保持時間が大きくなることから、例えば、L0、L1、H0、H1、H2、H3の順に溶出される。L0及びH0との保持時間比較により検出ピークをL0、L1、H0、H1、H2、H3のいずれかに割り当てることができる。薬物結合数は、当業者によって定義され得るが、好ましくは、L0、L1、H0、H1、H2、H3である。
なお、抗体-薬物コンジュゲートの量を確保するために、同様な条件で作製して得られた平均薬物数が同程度の複数の抗体-薬物コンジュゲート(例えば±1程度)を混合して新たなロットにすることができる。その場合、平均薬物数は混合前の平均薬物数の間に収まる。
(a)配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69に示される重鎖全長アミノ酸配列の20~471番目のア
ミノ酸配列からなる重鎖からなる抗体;
(b)配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;
(c)配列番号61に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;
(d)配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号69に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;
(e)配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号73に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;
(f)配列番号65に示される軽鎖全長アミノ酸配列の21~233番目のアミノ酸配列からなる軽鎖及び配列番号77に示される重鎖全長アミノ酸配列の20~471番目のアミノ酸配列からなる重鎖からなる抗体;又は
(g)重鎖又は軽鎖がN-結合への糖鎖付加、O-結合への糖鎖付加、N末のプロセッシング、C末のプロセッシング、脱アミド化、アスパラギン酸の異性化、メチオニンの酸化、N末にメチオニン残基の付加、プロリン残基のアミド化、N末グルタミンやN末グルタミン酸のピログルタミン酸化などに代表される翻訳後修飾、及びカルボキシル末端における1つ又は2つのアミノ酸欠失からなる群より選択される1又は2以上の修飾を含む、(a)~(f)からなる群から選択されるいずれか1つに記載の抗体。
上記、「2.抗CDH6抗体の製造」の項及び実施例に記載された本発明の抗CDH6抗体及び当該抗体の機能性断片は、腫瘍細胞表面のCDH6に結合し、内在化活性を有することから、単独であるいは他の薬剤と組み合わせて、医薬として、腎細胞腫瘍及び卵巣腫瘍等のがん、例えば、腎細胞癌、腎淡明細胞癌、乳頭状腎細胞癌、卵巣癌、卵巣漿液性腺癌、甲状腺癌、胆管癌、肺癌(例えば、小細胞肺癌又は非小細胞肺癌)、神経膠芽腫、中皮腫、子宮癌、膵臓癌、ウィルムス腫瘍又は神経芽腫の治療剤として用いることができる。
合、所望により薬理学的に許容され得る酸付加塩を形成することができる。そのような酸付加塩としては、例えばフッ化水素酸塩、塩酸塩、臭化水素酸塩、ヨウ化水素酸塩などのハロゲン化水素酸塩;硝酸塩、過塩素酸塩、硫酸塩、燐酸塩などの無機酸塩;メタンスルホン酸塩、トリフルオロメタンスルホン酸塩、エタンスルホン酸塩などの低級アルカンスルホン酸塩;ベンゼンスルホン酸塩、p-トルエンスルホン酸塩などのアリ-ルスルホン酸塩;蟻酸塩、酢酸塩、トリフルオロ酢酸塩、りんご酸塩、フマル酸塩、コハク酸塩、クエン酸塩、酒石酸塩、シュウ酸塩、マレイン酸塩などの有機酸塩;又はオルニチン酸塩、グルタミン酸塩、アスパラギン酸塩などのアミノ酸塩などを挙げることができる。
癌、甲状腺癌、胆管癌、肺癌(例えば、小細胞肺癌又は非小細胞肺癌)、神経膠芽腫、中皮腫、子宮癌、膵臓癌、ウィルムス腫瘍又は神経芽腫を挙げることができるが、CDH6を発現している限りこれらに制限されない。より好ましいがんの例としては、腎細胞癌(例えば、腎淡明細胞癌、乳頭状腎細胞癌)又は卵巣癌を挙げることができる。
1)-1 ヒト、マウス、ラットおよびカニクイザルCDH6発現ベクターの構築
ヒトCDH6タンパク質(NP_004923)をコードするcDNA発現ベクター(OriGene社、RC217889)を用いて、当業者に公知な方法に従い哺乳動物発現用ベクターに組み込むことによってヒトCDH6発現ベクターpcDNA3.1-hCDH6が作製された。ヒトCDH6 ORF(Open Reading Frame)のアミノ酸配列を配列番号1に示す。
法に従い哺乳動物発現用ベクターに組み込むことによってヒトCDH6発現ベクターpcDNA3.1-rCDH6、及びp3xFLAG-CMV-9-rCDH6が作製された。ラットCDH6 ORFのアミノ酸配列を配列番号8に示す。
免疫にはWKY/Izmラットの雌(日本エスエルシー社)を使用した。まずラット両足下腿部をHyaluronidase(SIGMA-ALDRICH社)にて前処理後、同部位に実施例1)- 1で作製したヒトCDH6発現ベクターpcDNA3.1-hCDH6を筋肉内注射した。続けて、ECM830(BTX社)を使用し、2ニードル電極を用いて、同部位にインビボエレクトロポレーションを実施した。約二週間に一度、同様のインビボエレクトロポーレーションを繰り返した後、ラットのリンパ節又は脾臓を採取しハイブリドーマ作製に用いた。
リンパ節細胞あるいは脾臓細胞とマウスミエローマSP2/0-ag14細胞(ATCC, No.CRL-1 581)とをLF301 Cell Fusion Unit(BEX社)を用いて電気細胞融合した後、ClonaCell-HY Selection Medium D(StemCell Technologies社)に懸濁し、希釈して37℃、5% CO2の条件下で培養した。出現した各々のハイブリドーマコロニーは、モノクローンとして回収され、ClonaCell-HY Selection
Medium E(StemCell Technologies社)に懸濁して37℃、5% CO2の条件下で培養した。適度に細胞が増殖した後、各々のハイブリドーマ細胞の凍結ストックを作製すると共に、得られたハイブリドーマ培養上清を抗ヒトCDH6抗体産生ハイブリドーマのスクリーニングに用いた。
1)-4-1 Cell-ELISA用抗原遺伝子発現細胞の調製
293α細胞(インテグリンαv及びインテグリンβ3を発現するHEK293由来の安定発現細胞株)を10% FBS含有DMEM培地中5x105細胞/mLになるよう調製した。Lipofectamine 2000(Thermo Fisher Scienftific社)を用いた形質移入手順に従って、この293α細胞に対して、pcDNA3.1-hCDH6もしくはpcDNA3.1-cynoCDH6または、陰性コントロールとしてpcDNA3.1のDNAを導入し、96-well plate(Corning社)に100μLずつ分注後、10% FBS含有DMEM培地中で37℃、5% CO2の条件下で24から27時間培養した。得られた形質移入細胞を接着状態のまま、Cell-ELISAに使用した。
実施例1)-4-1で調製した発現ベクター導入293α細胞の培養上清を除去後、pcDNA3.1-hCDH6もしくはpcDNA3.1-cynoCDH6またはpcDNA3.1導入293α細胞の各々に対しハイブリドーマ培養上清を添加し、4℃で1時間静置した。well中の細胞を5% FBS含有PBS(+)で1回洗浄後、5% FBS含有PBS(+)で500倍に希釈したAnti-Rat IgG-Peroxidase antibody produced in rabbit(SIGMA社)を加えて、4℃で1時間静置した。well中の細胞を5% FBS含有PBS(+)で3回洗浄した後、OPD発色液(OPD溶解液(0.05 M クエン酸3ナトリウム、0.1M リン酸水素2ナトリウム・12水 pH4.5)にo-フェニレンジアミン二塩酸塩(和光純薬社)、H2O2をそれぞれ0.4mg/mL、0.6%(v/v)になるように溶解)を100μL/wellで添加した。時々攪拌しながら発色反応を行い、1M HClを100μL/wellで添加して発色反応を停止させた後、プレートリーダー(ENVISION:PerkinElmer社)で490nmの吸光度を測定した。コントロールのpcDNA3.1導入293α細胞と比較し、pcDNA3.1-hCDH6ならびにpcDNA3.1-cynoCDH6発現ベクター導入293α細胞の方でより高い吸光度を示す培養上清を産生するハイブリドーマをヒト、かつ、カニクイサルCDH6に結合する抗体産生ハイブリドーマとして選択した。
1)-5-1 フローサイトメトリー解析用抗原遺伝子発現細胞の調製
293T細胞を5×104細胞/cm2になるよう225cm2フラスコ(住友ベークライト社)に播種し、10% FBS含有DMEM培地中で37℃、5% CO2の条件下で一晩培養した。この293T細胞に、pcDNA3.1-cynoCDH6または、陰性コントロールとしてpcDNA3.1をLipofectamine 2000を用いて導入し、37℃、5% CO2の条件下でさらに一晩培養した。各ベクターを導入した293T細胞をTrypLE Express(Thermo Fisher Scienftific社)で処理し、10% FBS含有DMEMで細胞を洗浄した後、5%
FBS含有PBSに懸濁した。得られた細胞懸濁液をフローサイトメトリー解析に使用した。
実施例1)-4のCell-ELISAで選択されたヒト、かつ、カニクイサルCDH6に結合する抗体産生ハイブリドーマが産生する抗体のカニクイサルCDH6に対する結合特異性をフローサイトメトリー法によりさらに確認した。実施例1)-5-1で調製した一過性発現293T細胞の懸濁液を遠心し、上清を除去した後、各々に対しハイブリドーマ培養上清を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで500倍に希釈したAnti-Rat IgG FITC conjugate(SIGMA社)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、2μg/mL 7-aminoactinomycin D(Molecular Probes社)を含む5% FBS含有PBSに再懸濁し、フローサイトメーター(FC500:BeckmanCoulter社)で検出した。データ解析はFlowJo(TreeStar社)で行った。7-aminoactinomycin D陽性の死細胞をゲートで除外した後、生細胞のFITC蛍光強度のヒストグラムを作成した。コントロールであるpcDNA3.1導入293T細胞の蛍光強度ヒストグラムに対しpcDNA3.1-cynoCDH6導入293T細胞のヒストグラムが強蛍光強度側にシフトしている抗体を産生するハイブリドーマを細胞膜表面上に発現するカニクイサルCDH6に特異的に結合する抗体産生ハイブリドーマとして選択した。
実施例1)- 5で選択したラット抗CDH6抗体産生ハイブリドーマの中から、ヒトならびにサルCDH6に強く特異的に結合することが示唆されたクローンrG019、rG055、rG056、rG061を選抜し、各抗体のアイソタイプを同定した。抗体の重鎖のサブクラス、軽鎖のタイプは、RAT MONOCLONAL ANTIBODY
ISOTYPING TEST KIT(DSファーマバイオメディカル社)により決定された。その結果、rG019、rG055、rG056、rG061の4クローンともサブクラスは、IgG2b、タイプはκ鎖であることが確認された。
1)-7-1 培養上清作製
ラット抗ヒトCDH6モノクローナル抗体は、ハイブリドーマ培養上清から精製した。まず、ラット抗CDH6モノクローナル抗体産生ハイブリドーマをClonaCell-HY Selection Medium E(StemCell Technologies社)で充分量まで増殖させた後、Ultra Low IgG FBS(Thermo Fisher Scienftific社)を20%添加したHybridoma
SFM(Thermo Fisher Scienftific社)に培地交換し、4-5日間培養した。本培養上清を回収し、0.8μmのフィルターに通した後、さらに0.2μmのフィルターに通して不溶物を除去した。
実施例1)-7-1で作製したハイブリドーマの培養上清から抗体(ラット抗CDH6抗体(rG019,rG055,rG056,rG061))をProtein Gアフィニティークロマトグラフィーで精製した。Protein Gカラム(GE Healthcare Bioscience社)に抗体を吸着させ、PBSでカラムを洗浄後に0.1M グリシン/塩酸水溶液(pH2.7)で溶出した。溶出液に1M Tris-HCl(pH9.0)を加えてpH7.0~7.5に調整した後に、Centrifugal UF Filter Device VIVASPIN20(分画分子量UF30K、Sartorius社)にてHBSor(25mM ヒスチジン/5% ソルビトール、pH6.0)へのバッファー置換を行うとともに抗体の濃縮を行い、抗体濃度を1mg/mLに調製した。最後にMinisart-Plus filter(Sartorius社)でろ過し、精製サンプルとした。
2)-1 フローサイトメトリーによるラット抗CDH6抗体の結合能評価
実施例1)-7で作製したラット抗CDH6抗体のヒトCDH6結合性をフローサイトメトリー法により評価した。実施例1)-1で作製したpcDNA3.1-hCDH6を293T細胞(ATCC)にLipofectamine 2000(Thermo Fisher Scientific)を用いて一過性に導入し、37℃、5% CO2の条件下で一晩培養した後、細胞懸濁液を調製した。遺伝子導入した293T細胞懸濁液を遠心し、上清を除去した後、実施例1)-7で調製したラット抗CDH6モノクローナル抗体4種(クローン番号は、rG019、rG055、rG056及びrG061)又はラットIgGコントロール(R&D Systems)を終濃度10ng/mL加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで50倍に希釈したAnti-Rat IgG(whole molecule)-FITC antibody produced in rabbit(SIGMA)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後
、フローサイトメーター(FC500:Beckman Coulter)で検出を行った。データ解析はFlowJo(TreeStar)で行った。その結果を図1に示す。図1のヒストグラムにおいて、横軸は抗体結合量を表すFITCの蛍光強度、縦軸は細胞数を示す。網掛けで示すヒストグラムはhCDH6を導入していない陰性コントロール293T細胞を用いた場合を示し、白抜き実線で示すヒストグラムは、hCDH6導入293T細胞を用いた場合を示す。細胞表面のhCDH6に抗体が結合したことによって蛍光強度が増強したことを示す。ラットIgGコントロールはいずれの細胞にも結合しない。この結果、作製したラット抗CDH6モノクローナル抗体4種はpcDNA3.1-hCDH6導入293T細胞に結合することを確認した。
2)-2-1 ヒトCDH6各ドメイン欠失体発現ベクターの構築
ヒトCDH6の細胞外全長には5つの細胞外ドメイン、EC1(配列番号2)、EC2(配列番号3)、EC3(配列番号4)、EC4(配列番号5)、EC5(配列番号6)が存在する。ヒトCDH6全長から、5つのECドメインを各一箇所ずつ欠失発現した遺伝子をGeneArt社で合成し、当業者に公知な方法に従い哺乳動物発現用ベクターp3xFLAG-CMV-9ベクター(SIGMA-ALDRICH社)へ組み込み、EC1からEC5をそれぞれ欠失した、各ドメイン欠失体発現ベクターを作製した。
各ECドメイン欠失ベクターを導入した293α細胞株を用いたフローサイトメトリー解析により、ラット抗ヒトCDH6抗体の結合エピトープを同定した。インテグリンαvおよびインテグリンβ3発現ベクターをHEK293細胞内に安定形質移入した細胞株293α細胞株に対して、実施例2)-2-1で作成した各ドメイン欠失体発現ベクター、及び全長ヒトCDH6を発現するpcDNA3.1-hCDH6をLipofectamine 2000(Thermo Fisher Scientific)を用いて一過性に導入し、37℃、5% CO2の条件下で一晩培養した後、細胞懸濁液を調製した。導入293α細胞懸濁液を遠心し、上清を除去した後、実施例1)-7で調製したラット抗CDH6モノクローナル抗体4種(クローン番号は、rG019、rG055、rG056及びrG061)又はラットIgGコントロール(R&D Systems)を終濃度20nMで加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで50倍に希釈したAnti-Rat IgG(whole molecule)-FITC antibody produced in rabbit(SIGMA)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。その結果を図2-1~図2-6に示す。図2-1~図2-6のヒストグラムにおいて、横軸は抗体結合量を表すFITCの蛍光強度、縦軸は細胞数を示す。網掛けで示すヒストグラムは遺伝子を導入していない陰性コントロール293α細胞を用いた場合を示し、白抜き実線で示すヒストグラムは、全長hCDH6又は各ECドメイン欠失293細胞を用いた場合を示す。細胞表面の全長hCDH6又は各ECドメイン欠失体に抗体が結合した場合は、蛍光強度が増強する。ラットIgGコントロールはいずれの導入細胞にも結合しない。作製したラット抗CDH6モノクローナル抗体4種は、全長hCDH6、EC1欠失体、EC2欠失体、EC4欠失体、及びEC5欠失体には結合するが、EC3欠失体には結合しない。この結果から、ラット抗CDH6モノクローナル抗体4種はhCDH6のEC3をエピトープとして特異的に結合することが示された。
2)-3-1 ヒト腫瘍細胞株におけるCDH6の発現確認
取得抗体の評価に用いるCDH6陽性ヒト腫瘍細胞株を選抜するため、公知データベースからCDH6発現情報を検索し、フローサイトメトリー法により細胞膜表面でのCDH6の発現を評価した。ヒト卵巣腫瘍細胞株NIH:OVCAR-3,PA-1,ES-2及びヒト腎細胞腫瘍細胞株786-O(全てATCCから入手)を37℃、5% CO2の条件下で培養した後、細胞懸濁液を調製した。細胞を遠心し、上清を除去した後、市販抗ヒトCDH6抗体(MABU2715,R&D Systems)又は陰性コントロールとしてマウスIgG1(BD Pharmingen)を終濃度50ug/mL加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで50倍に希釈したF(ab’)2 Fragment of FITC-conjugated Goat Anti-mouse immunoglobulins(Dako)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。その結果を図3に示す。図3のヒストグラムにおいて、横軸は抗体結合量を表すFITCの蛍光強度、縦軸は細胞数を示す。網掛けで示すヒストグラムは陰性コントロールmIgG1で染色した場合を示し、白抜き実線で示すヒストグラムは抗ヒトCDH6抗体で染色した場合を示す。細胞表面のhCDH6に抗体が結合したことによって蛍光強度が増強したことを示す。mIgG1コントロールはいずれの細胞にも結合しない。この結果、NIH:OVCAR-3,PA-1及び786-O細胞株は、内在的にCDH6を細胞表面上に発現することが示された。一方、ES-2細胞株はCDH6を全く発現しないことが示された。
ラット抗CDH6抗体の内在化活性は、タンパク質合成を阻害する毒素(サポリン)を結合させた抗ラットIgG試薬Rat-ZAP(ADVANCED TARGETING SYSTEMS)を用いて評価した。すなわち、ヒトCDH6陽性卵巣腫瘍細胞株NIH:OVCAR-3(ATCC)を4x103 cells/wellで96wellプレートに播種して37℃、5% CO2の条件下で一晩培養した。ヒトCDH6陽性腎細胞腫瘍細胞株786-O(ATCC)は1x103 cells/wellで96wellプレートに播種して一晩培養した。翌日、ラット抗CDH6抗体(終濃度:1nM)又は、陰性コントロール抗体としてラットIgG2b抗体(R&D Systems)を添加した。さらに、Rat-ZAP(終濃度:0.5nM)または、陰性コントロールとして毒素を結合していないGoat Anti-Rat IgG, Fc(gamma) Fragment Specific(JACKSON IMMUNORESEARCH)(終濃度:0.5nM)を添加し、3日間37℃、5%CO2条件下で培養した。生存細胞数は、CellTiter-GloTM Luminescent Cell Viability Assay(Promega)によるATP活性(RLU)の定量で測定した。この評価では、ラット抗CDH6抗体の内在化活性に依存してRat-ZAPが細胞内に取り込まれ、タンパク合成を阻害するサポリンが細胞内に放出されることで、細胞増殖が抑制される。抗CDH6抗体添加による細胞増殖抑制作用は、Rat-ZAPの代わりに陰性コントロールを添加したウェルの生存細胞数を100%とした相対生存率で表記した。図4にグラフおよび細胞生存率の表を示す。この結果、ラット抗CDH6抗体はCDH6に結合して内在化を引き起こすことが示された。
3)-1 rG019重鎖可変領域及び軽鎖可変領域の遺伝子断片の増幅および配列決定
3)-1-1 G019からのtotal RNAの調製
rG019の可変領域を含むcDNAを増幅するためG019よりTRIzol Re
agent(Ambion社)を用いてtotal RNAを調製した。
重鎖可変領域を含むcDNAの増幅は、実施例3)-1-1で調製したtotal RNAの約1μgとSMARTer RACE cDNA Amplification Kit(Clontech社)を用いて実施した。rG019の重鎖遺伝子の可変領域のcDNAをPCRで増幅するためのプライマーとして、UPM (Universal Primer A Mix:SMARTer RACE cDNA Amplification Kitに付属)、及び公知のラット重鎖の定常領域の配列から設計したプライマーを用いた。
実施例3)-1-2と同様の方法で実施した。ただし、rG019の軽鎖遺伝子の可変領域のcDNAをPCRで増幅するためのプライマーとして、UPM (Universal Primer A Mix:SMARTer RACE cDNA Amplification Kitに付属)、及び公知のラット軽鎖の定常領域の配列から設計したプライマーを用いた。
実施例3)-1と同様の方法で配列を決定した。
実施例3)-1と同様の方法で配列を決定した。
実施例3)-1と同様の方法で配列を決定した。
4)-1 ヒトキメラ化抗CDH6抗体chG019の発現ベクターの構築
4)-1-1 キメラ及びヒト化軽鎖発現ベクターpCMA-LKの構築
プラスミドpcDNA3.3-TOPO/LacZ(Invitrogen社)を制限酵素XbaI及びPmeIで消化して得られる約5.4kbのフラグメントと、配列番号50に示すヒト軽鎖シグナル配列及びヒトκ鎖定常領域をコードするDNA配列を含むDNA断片をIn-Fusion Advantage PCRクローニングキット(Clontech社)を用いて結合して、pcDNA3.3/LKを作製した。
pCMA-LKをXbaI及びPmeIで消化して軽鎖シグナル配列及びヒトκ鎖定常領域を取り除いたDNA断片と、配列番号51で示されるヒト重鎖シグナル配列及びヒトIgG1定常領域をコードするDNA配列を含むDNA断片をIn-Fusion Advantage PCRクローニングキット(Clontech社)を用いて結合して、pCMA-G1を構築した。
配列番号57に示すchG019重鎖のヌクレオチド配列のヌクレオチド番号36乃至440に示されるDNA断片を合成した(GENEART社)。In-Fusion HD PCRクローニングキット(Clontech社)を用いて、pCMA-G1を制限酵素BlpIで切断した箇所に合成したDNA断片を挿入することによりchG019重鎖発現ベクターを構築した。なお、chG019重鎖は予期せぬジスルフィド結合を防ぐため、CDR中のシステインをプロリンに置換した配列を用いた。
配列番号52に示すchG019軽鎖をコードするDNA配列を含むDNA断片を合成した(GENEART社)。In-Fusion HD PCRクローニングキット(Clontech社)を用いて、合成したDNA断片とpCMA-LKをXbaI及びPmeIで消化して軽鎖シグナル配列及びヒトκ鎖定常領域を取り除いたDNA断片を結合することにより、chG019軽鎖発現ベクターを構築した。
4)-2-1 chG019の生産
FreeStyle 293F細胞(Invitrogen社)はマニュアルに従い、継代、培養をおこなった。対数増殖期の1.2×109個のFreeStyle 293F細胞(Invitrogen社)を3L Fernbach Erlenmeyer Flask(CORNING社)に播種し、FreeStyle293 expression medium(Invitrogen社)で希釈して2.0×106細胞/mlに調製した。40mlのOpti-Pro SFM培地(Invitrogen社)に0
.24mgの重鎖発現ベクターと0.36mgの軽鎖発現ベクターと1.8mgのPolyethyleneimine(Polyscience #24765)を加えて穏やかに攪拌し、さらに5分間放置した後にFreeStyle 293F細胞に添加した。37℃、8%CO2インキュベーターで4時間、90rpmで振とう培養後に600mlのEX-CELL VPRO培地(SAFC Biosciences社)、18mlのGlutaMAX I(GIBCO社)、及び30mlのYeastolate Ultrafiltrate(GIBCO社)を添加し、37℃、8%CO2インキュベーターで7日間、90rpmで振とう培養して得られた培養上清をDisposable Capsule Filter (Advantec #CCS-045-E1H)でろ過した。
実施例4)-2-1で得られた培養上清をrProtein Aアフィニティークロマトグラフィーの1段階工程で精製した。培養上清をPBSで平衡化したMabSelectSuReが充填されたカラム(GE Healthcare Bioscience社製)にアプライしたのちに、カラム容量の2倍以上のPBSでカラムを洗浄した。次に2Mアルギニン塩酸塩溶液(pH4.0)で溶出し、抗体の含まれる画分を集めた。その画分を透析(Thermo Scientific社、Slide-A-Lyzer Dialysis Cassette)によりHBSor(25mM ヒスチジン/5% ソルビトール、pH6.0)へのバッファー置換を行った。Centrifugal UF
Filter Device VIVASPIN20(分画分子量UF10K,Sartorius社)で抗体を濃縮し、IgG濃度を5mg/ml以上に調製した。最後にMinisart-Plus filter(Sartorius社)でろ過し、精製サンプルとした。
4)-2で精製したヒトキメラ化抗CDH6抗体chG019のCDH6結合性をフローサイトメトリー法により確認した。実施例1)-1で作製したpcDNA3.1-hCDH6、又はpcDNA3.1-cynoCDH6、又はpcDNA3.1をそれぞれ293α細胞にLipofectamine 2000を用いて一過性に導入し、37℃、5% CO2の条件下で一晩培養した後、細胞懸濁液を調製した。これらの細胞懸濁液にchG019を加えて4℃で1時間静置した後、5% FBS含有PBSで2回洗浄し、5% FBS含有PBSで500倍に希釈したPE標識F(ab’)2 Fragment抗ヒトIgG,Fcγ抗体(JACKSON IMMUNORESEARCH)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSに再懸濁し、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。図5に示すとおり、chG019は陰性コントロールであるpcDNA3.1導入293T細胞には結合せず、pcDNA3.1-hCDH6及びpcDNA3.1-cynoCDH6導入293T細胞に抗体濃度依存的に結合した。図5において横軸は抗体濃度を示し、縦軸は結合量をMeanFluorescent Intensity(平均蛍光強度)で示す。この結果から、chG019が、ヒトおよびカニクイザルCDH6に対して特異的に結合し、結合活性はほぼ同等であることがわかる。
5)-1 抗CDH6抗体のヒト化体デザイン
5)-1-1 chG019の可変領域の分子モデリング
chG019の可変領域の分子モデリングは、ホモロジーモデリングとして公知の方法(Methods in Enzymology,203,121-153,(1991))を利用した。chG019の重鎖と軽鎖の可変領域に対して高い配列同一性を有するProtein Data Bank(Nuc.Acid Res.35,D301-D303(2007))に登録されている構造(PDB ID:2I9L)を鋳型に、市販のタンパク質立体構造解析プログラムBioLuminate(Schrodinger社製)を用いて行った。
chG019は、CDRグラフティング(Proc.Natl.Acad.Sci.USA 86,10029-10033(1989))によりヒト化した。KABAT et al.(Sequences of Proteins of Immunological Interest,5th Ed.Public Health Service National Institutes of Health,Bethesda,MD.(1991))において既定されるヒトのgamma鎖サブグループ1およびkappa鎖サブグループ1のコンセンサス配列が、chG019のフレームワーク領域に対して高い同一性を有することから、それぞれ、重鎖と軽鎖のアクセプターとして選択された。アクセプター上に移入すべきドナー残基は、Queen et al.(Proc.Natl.Acad.Sci.USA 86,10029-10033(1989))によって与えられる基準などを参考に三次元モデルを分析することで選択された。
設計された3種の重鎖をhH01、hH02及びhH04と命名した。hH01の重鎖全長アミノ酸配列を、配列番号69に記載する。配列番号69のアミノ酸配列をコードするヌクレオチド配列を、配列番号70に記載する。hH02の重鎖全長アミノ酸配列を、配列番号73に記載する。配列番号73のアミノ酸配列をコードするヌクレオチド配列を、配列番号74に記載する。hH04の重鎖全長アミノ酸配列を、配列番号77に記載する。配列番号77のアミノ酸配列をコードするヌクレオチド配列を、配列番号78に記載する。
設計された2種の軽鎖をhL02およびhL03と命名した。hL02の軽鎖全長アミノ酸配列を、配列番号61に記載する。配列番号61のアミノ酸配列をコードするヌクレオチド配列を、配列番号62に記載する。hL03の軽鎖全長アミノ酸配列を、配列番号65に記載する。配列番号65のアミノ酸配列をコードするヌクレオチド配列は、配列番号66に記載する。
hH01及びhL02からなる抗体を「H01L02抗体」又は「H01L02」と称する。hH02及びhL02からなる抗体を「H02L02抗体」又は「H02L02」と称する。hH02及びhL03からなる抗体を「H02L03抗体」又は「H02L03」と称する。hH04及びhL02からなる抗体を「H04L02抗体」又は「H04L02」と称する。
5)-5-1 ヒト化hG019の重鎖発現ベクターの構築
5)-5-1-1 ヒト化hG019-H01タイプ重鎖発現ベクターの構築
配列番号70に示すヒト化hG019-H01タイプ重鎖のヌクレオチド配列のヌクレオチド番号36乃至440に示されるDNA断片を合成した(GENEART社)。実施例4)-1-3と同様の方法でヒト化hG019-H01タイプ重鎖発現ベクターを構築した。
配列番号74に示すヒト化hG019-H02タイプ重鎖のヌクレオチド配列のヌクレオチド番号36乃至440に示されるDNA断片を合成した(GENEART社)。実施例4)-1-3と同様の方法でヒト化hG019-H02タイプ重鎖発現ベクターを構築した。
配列番号78に示すヒト化hG019-H04タイプ重鎖のヌクレオチド配列のヌクレオチド番号36乃至440に示されるDNA断片を合成した(GENEART社)。実施例4)-1-3と同様の方法でヒト化hG019-H04タイプ重鎖発現ベクターを構築した。
5)-5-2-1 ヒト化hG019-L02タイプ軽鎖発現ベクターの構築
配列番号62に示すヒト化hG019-L02タイプ軽鎖のヌクレオチド配列のヌクレオチド番号37乃至399に示されるヒト化hG019-L02タイプ軽鎖の可変領域をコードするDNA配列を含むDNA断片を合成した(GENEART社)。In-Fusion HD PCRクローニングキット(Clontech社)を用いて、pCMA-LKを制限酵素BsiWIで切断した箇所に合成したDNA断片を挿入することによりヒト化hG019-L02タイプ軽鎖発現ベクターを構築した。
配列番号66に示すヒト化hG019-L03タイプ軽鎖のヌクレオチド配列のヌクレオチド番号37乃至399に示されるヒト化hG019-L03タイプ軽鎖の可変領域をコードするDNA配列を含むDNA断片を合成した(GENEART社)。実施例5)-5-2-1と同様の方法でヒト化hG019-L03タイプ軽鎖発現ベクターを構築した。
5)-5-3-1 H01L02、H02L02、H02L03、H04L02の生産
実施例4)-2-1と同様の方法で生産した。実施例5)-4に示した重鎖と軽鎖の組み合わせにより、H01L02、H02L02、H02L03、H04L02を生産した。
実施例5)-5-3-1で得られた培養上清をrProtein Aアフィニティークロマトグラフィーとセラミックハイドロキシアパタイトの2段階工程で精製した。培養上清をPBSで平衡化したMabSelectSuReが充填されたカラム(GE Healthcare Bioscience社製)にアプライした後に、カラム容量の2倍以上のPBSでカラムを洗浄した。次に2Mアルギニン塩酸塩溶液(pH4.0)で抗体を溶出した。抗体の含まれる画分を透析(Thermo Scientific社、Slide-A-Lyzer Dialysis Cassette)によりPBSへのバッファー置換を行い、5mMリン酸ナトリウム/50mM MES/pH7.0のバッファーで5倍希釈した後に、5mM NaPi/50mM MES/30mM NaCl/pH7.0のバッファーで平衡化したセラミックハイドロキシアパタイトカラム(日本バイオラッド、Bio-Scale CHT Type―1 Hydroxyapatite Column)にアプライした。塩化ナトリウムによる直線的濃度勾配溶出を実施し、抗体の含まれる画分を集めた。その画分を透析(Thermo Scientific社、Slide-A-Lyzer Dialysis Cassette)によりHBSor(25mM ヒスチジン/5% ソルビトール、pH6.0)へのバッファー置換を行った。Centrifugal UF Filter Device VIVASPIN20(分画分子量UF10K,Sartorius社)にて抗体を濃縮し、IgG濃度を20mg/mlに調製した。最後にMinisart-Plus filter(Sartorius社)でろ過し、精製サンプルとした。
実施例で用いた抗CDH6抗体NOV0712は、国際公開第2016/024195号に記載のNOV0712の軽鎖全長、及び重鎖全長のアミノ酸配列(それぞれ、国際公開第2016/024195の配列番号235及び配列番号234)を参照して作製した。
参考例1)-1-1 抗CDH6抗体NOV0712の重鎖発現ベクターの構築
配列番号84に示すNOV0712の重鎖のヌクレオチド配列のヌクレオチド番号36乃至428に示されるNOV0712の重鎖の可変領域を含むDNA断片を合成した(GENEART社)。実施例4)-1-3と同様の方法でNOV0712の重鎖発現ベクターを構築した。当該NOV0712の重鎖発現ベクターにより発現するNOV0712の重鎖のアミノ酸配列を、配列番号83に示す。配列番号83に示されるアミノ酸配列中、1~19番目のアミノ酸残基からなるアミノ酸配列はシグナル配列である。
配列番号82に示すNOV0712の軽鎖のヌクレオチド配列のヌクレオチド番号37乃至405に示されるNOV0712の軽鎖の可変領域をコードするDNA配列を含むDNA断片を合成した(GENEART社)。実施例5)-5-2-1と同様の方法でNOV0712の軽鎖発現ベクターを構築した。当該NOV0712の軽鎖発現ベクターにより発現するNOV0712の軽鎖のアミノ酸配列を、配列番号81に示す。配列番号81に示されるアミノ酸配列中、1~20番目のアミノ酸残基からなるアミノ酸配列はシグナル配列である。
参考例1)-2-1 抗CDH6抗体NOV0712の生産
実施例4)-2-1と同様の方法でNOV0712を生産した。
参考例1)-2-1で得られた培養上清から実施例4)-2-2と同様の方法で抗CDH6抗体NOV0712を精製した(抗体濃度HBSorで5mg/l)。
6)-1 ヒト化hG019の結合性評価
6)-1-1 ヒト化hG019のヒトCDH6抗原結合能
抗体と抗原(Recombinant Human CDH6 Fc His chimera, R&D Systems)との解離定数測定は、Biacore T200(GEヘルスケアバイオサイエンス)を使用し、固定化した抗His抗体に抗原をリガンドとして捕捉(キャプチャー)し、抗体をアナライトとして測定するキャプチャー法にて行った。抗ヒスチジン抗体(His capture kit、GEヘルスケアバイオサイエンス)は、センサーチップCM5(GEヘルスケアバイオサイエンス)へ、アミンカップリング法にて約1000RU共有結合させた。リファレンスセルにも同様に固定化した。ランニングバッファーとして1mM CaCl2を添加したHBS-P+(10mM HEPES pH7.4、0.15M NaCl、0.05% Surfactant P20)を用いた。抗ヒスチジン抗体を固定化したチップ上に、抗原を60秒間添加した後、抗体の希釈系列溶液(0.391-100nM)を流速30μl/分で300秒間添加し、引き続き600秒間の解離相をモニターした。再生溶液として、5M MgCl2を添加したGlycine溶液pH1.5を流速10μl/分で30秒間、2回添加した。データの解析は、分析ソフトウェア(BIAevaluation software, version 4.1)のSteady State Affinityモデルを用いて、解離定数(KD)を算出した。結果を表2に示す。
実施例1)-1で作製したpcDNA3.1-hCDH6、pcDNA3.1-cynoCDH6、p3xFLAG-CMV-9-mCDH6、p3xFLAG-CMV-9-rCDH6を、293α細胞にLipofectamine 2000を用いて一過性に導入し、37℃、5% CO2の条件下で一晩培養した後、細胞懸濁液を調製した。陰性コントロールとして、遺伝子導入していない293α細胞を用いた。上記にて作製した293α細胞懸濁液を遠心し、上清を除去した後、実施例5)-5-3で調製したヒト化hG019抗体4種(クローン番号は、H01L02、H02L02、H02L03およびH04L02)、又は、ヒトIgG1コントロール(Calbiochem)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで500倍に希釈したanti-human Fcg PE goat F(ab’)(Jackson laboratory)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。図6-1及び図6-2において横軸は抗体濃度を示し、縦軸は結合量をMeanFluorescent Intensity(平均蛍光強度)で示す。図6-1及び図6-2に示すとおり、陰性コントロールであるヒトIgG1コントロールは、いずれのCDH6遺伝子導入細胞に対しても結合しない。ヒト化hG019抗体4種(クローン番号は、H01L02、H02L02、H02L03およびH04L02)はヒト及びカニクイザルCDH6に結合するが、マウス及びラットCDH6には結合しない。いずれの抗体も、陰性コントロールである空ベクターpcDNA3.1導入細胞には結合しない。一方、NOV0712抗体はヒト、カニクイザル、マウス、及びラットCDH6全てに結合活性を示すことが国際公開第2016/024195号に示されている。この結果、本明細書で取得したヒト化hG019抗体4種は、NOV0712抗体と異なる結合性質を示す抗CDH6抗体であることが示された。
6)-2-1 ドメイン欠失体を用いたエピトープ解析
実施例2)-2-1で作成した各ドメイン欠失体発現ベクター、及び全長hCDH6を発現するpcDNA3.1-hCDH6をLipofectamine 2000(Th
ermo Fisher Scientific)を用いて一過性に導入し、37℃、5% CO2の条件下で一晩培養した後、細胞懸濁液を調製した。遺伝子導入した293α細胞懸濁液を遠心し、上清を除去した後、実施例5)-5-3で調製したヒト化hG019抗体4種(クローン番号は、H01L02、H02L02、H02L03およびH04L02)、又は、参考例1で調製した抗CDH6抗体NOV0712、又は、陰性コントロールとしてヒトIgG1(Calbiochem)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、5% FBS含有PBSで500倍に希釈したAPC-anti-human IgG goat F(ab’)2(Jackson laboratory)を加えて懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。その結果を図7-1~図7-6に示す。図7-1~図7-6のヒストグラムにおいて、横軸は抗体結合量を表すAPCの蛍光強度、縦軸は細胞数を示す。網掛けで示すヒストグラムは遺伝子を導入していない陰性コントロール293α細胞を用いた場合を示し、白抜き実線で示すヒストグラムは、全長hCDH6又は各ECドメイン欠失293α細胞を用いた場合を示す。細胞表面の全長hCDH6又は各ECドメイン欠失体に抗体が結合した場合は、蛍光強度が増強する。ヒトIgG1コントロールはいずれの導入細胞にも結合しない。ヒト化hG019抗体4種(クローン番号は、H01L02、H02L02、H02L03およびH04L02)は、全長hCDH6、EC1欠失体、EC2欠失体、EC4欠失体、及びEC5欠失体には結合するが、EC3欠失体には結合しない。すなわち、ヒト化hG019抗体4種はhCDH6のEC3をエピトープとして特異的に結合することが示された。一方、抗CDH6抗体NOV0712は、全長hCDH6、EC1欠失体、EC2欠失体、EC3欠失体、及びEC4欠失体には結合するが、EC5欠失体には結合しない。すなわち、抗CDH6抗体NOV0712抗体はhCDH6のEC5をエピトープとして特異的に結合することが示され、国際公開第2016/024195号に記載されているNOV0712のエピトープ情報と一致する。この結果から、NOV0712と本明細書で取得したヒト化hG019抗体4種は、異なる性質を示す抗CDH6抗体であることが示された。
6)-2-2-1 786-O/hCDH6安定発現細胞株の作製
786-O/hCDH6安定発現細胞株は、786-O細胞(ATCC)にヒトCDH6全長発現用組換えレトロウイルスを感染させることにより作製した。ヒトCDH6発現レトロウイルスベクター(pQCXIN-hCDH6)は、ヒトCDH6タンパク質(NP_004923)をコードするcDNA発現ベクター(OriGene社RC217889)を用いて、当業者に公知な方法に従いレトロウイルスベクターpQCXIN(CLONTECH)に組み込むことにより作製された。FuGene HD(Promega)を用いてレトロウイルスパッケージング細胞RetroPack PT67(CLONTECH)にpQCXIN-hCDH6を一過性に導入し、48時間後に組換えレトロウイルスを含む培養上清を回収し、786-O細胞培養系に添加することで同細胞に感染させた。感染3日後から、G418(Gibco)を終濃度50mg/mLで添加した培地で37℃、5% CO2の条件下で培養を行い感染細胞の薬剤選抜を行うことで、ヒトCDH6を安定的に発現する細胞株786-O/hCDH6を樹立した。実施例2)-3-1と同様にフローサイトメトリーにて安定発現株でのヒトCDH6の高発現を確認した(図8)。検出用抗体には5% FBS含有PBSで500倍に希釈したGoat anti-Mouse IgG1 Secondary Antibody Alexa Fluor 647(Thermo Fisher Scientific)を使用した。その結果を図8に示す。図8のヒストグラムにおいて、横軸は抗体結合量を表すAlexa Fluor 647の蛍光強度、縦軸は細胞数を示す。網掛けで示すヒストグラムは陰性コントロールmIgG1で染色した場合を示し、白抜き実線で示すヒストグラムは抗ヒトCDH6抗体で染色した場合を示す。細胞表面のhCDH6に抗体が結合したことによって蛍光強度が増強したことを示す。mIgG1コントロールはいずれの細胞にも結合しない。この結果、786-O/hCDH6安定発現細胞株では親株786-O細胞と比較して、ヒトCDH6を高発現することが示された。
Alexa Fluor 488 Monoclonal Antibody Labeling Kit(Thermo Fisher)を用いて、ラベル化H01L02及びラベル化NOV0712を作製した。7)-2-2-1で作製した786-O/hCDH6安定発現細胞株の細胞懸濁液を遠心し、上清を除去した後、ラベル化NOV0712又はラベル化H01L02を終濃度5nMで添加し、さらに実施例5)-5-3で調製したヒト化hG019抗体4種(クローン番号は、H01L02、H02L02、H02L03およびH04L02)、又は、参考例1で調製した抗CDH6抗体NOV0712、又は、陰性コントロールとしてヒトIgG1(Calbiochem)を図9の横軸で示す終濃度で添加して懸濁し、4℃で1時間静置した。5% FBS含有PBSで2回洗浄した後、フローサイトメーター(CantoII:BD Biosciences)で検出を行った。データ解析はFlowJo(TreeStar)で行った。その結果を図9に示す。横軸はラベル化していない抗体の添加時の終濃度を示し、縦軸は結合量をMeanFluorescent Intensity(平均蛍光強度)で示す。ラベル化NOV0712を添加した細胞にラベル化していないNOV0712を添加した場合は、同じエピトープを持ち結合が競合するため、添加濃度依存的にラベル化していない抗体に置き換わりラベル化抗体の結合量が減少する。一方、ラベル化NOV0712を添加した細胞にヒト化hG019抗体4種、又は陰性コントロールとしてヒトIgG1を添加しても、ラベル化抗体の結合量に変化は無いことから、これらの抗体はエピトープが異なり結合が競合しないことが示される。同様に、ラベル化H01L02を添加した細胞にラベル化していないヒト化hG019抗体4種を添加した場合は、同じエピトープを持ち結合が競合するため、添加濃度依存的にラベル化していない抗体に置き換わりラベル化抗体の結合量が減少する。一方、ラベル化H01L02を添加した細胞にNOV0712、又は陰性コントロールとしてヒトIgG1を添加しても、ラベル化抗体の結合量に変化は無いことから、これらの抗体はエピトープが異なり結合が競合しないことが示される。
ヒト化hG019およびNOV0712の内在化活性は、タンパク質合成を阻害する毒素(サポリン)を結合させた抗ヒトIgG試薬Hum-ZAP(ADVANCED TARGETING SYSTEMS)を用いて評価した。すなわち、ヒトCDH6陽性卵巣腫瘍細胞株NIH:OVCAR-3(ATCC)を4x103 cells/wellで96wellプレートに播種して37℃、5% CO2の条件下で一晩培養した。ヒトCDH6陽性腎細胞腫瘍細胞株786-O(ATCC)は1x103 cells/wellで96wellプレートに播種して一晩培養した。ヒトCDH6陽性卵巣腫瘍細胞株PA-1(ATCC)を1x103 cells/wellで96wellプレートに播種して37℃、5% CO2の条件下で一晩培養した。翌日、抗CDH6抗体(終濃度:1nM)、又は、陰性コントロール抗体としてヒトIgG1抗体(Calbiochem)を添加した。さらにHum-ZAP(終濃度:0.5nM)または、陰性コントロールとして毒素を結合していないF(ab’)2 Fragment Goat Anti-human IgG,Fc(gamma) Fragment Specific(JACKSON IMMUNORESEARCH)(終濃度:0.5nM)を添加し、3日間37℃、5%CO2条件下で培養した。生存細胞数は、CellTiter-GloTM Luminescent Cell Viability AssayによるATP活性(RLU)の定量で測定した。この評価では、ヒト化抗CDH6抗体の内在化活性に依存してHum-ZAPが細胞内に取り込まれ、タンパク合成を阻害するサポリンが細胞内に放出されることで、細胞増殖が抑制される。抗CDH6抗体添加による細胞増殖抑制作用は、Hum-ZAPの代わりに陰性コントロールを添加したウェルの生存細胞数を100%とした相対生存率で表記した。図10-1~図10-3にグラフおよび細胞生存率の表を示す。本実験において内在化活性が強い抗体は低い細胞生存率を示すと考えられる。この結果、NOV0712はヒト化hG019抗体4種は3種の細胞株いずれにおいても細胞生存率から予測される内在化率は約50~75%であり、非常に高い内在化活性を示し、NOV0712と比較して、さらに高い内在活性を示す。ADCの薬効メカニズムから、高い内在化活性を有する抗体は、ADC化抗体をして、より適していると考えられる。
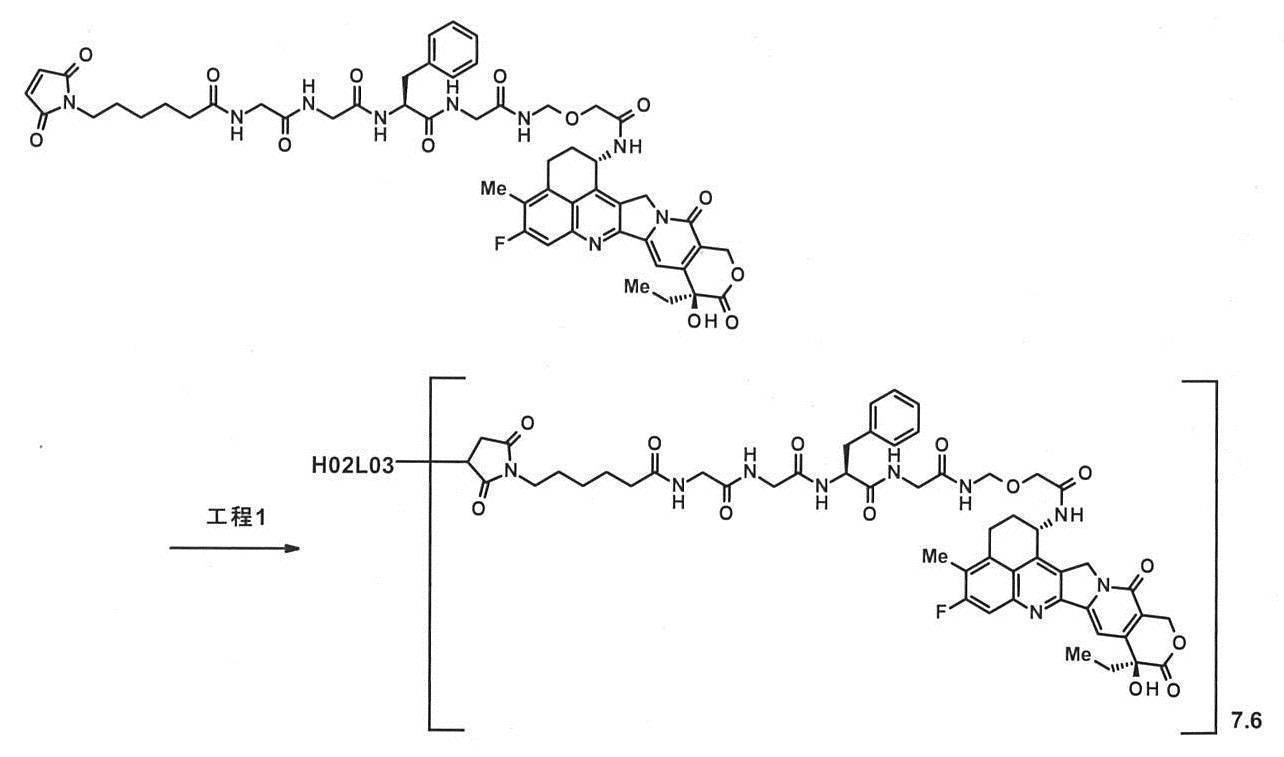
7)-1 抗体-薬物コンジュゲートの作製 H01L02-DXd
工程1:抗体-薬物コンジュゲート(1)
抗体濃度:2.26mg/mL,抗体収量:42.9mg(76%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):5.9;共通操作Fにて測定された抗体一分子あたりの薬物平均結合数(n):7.7。
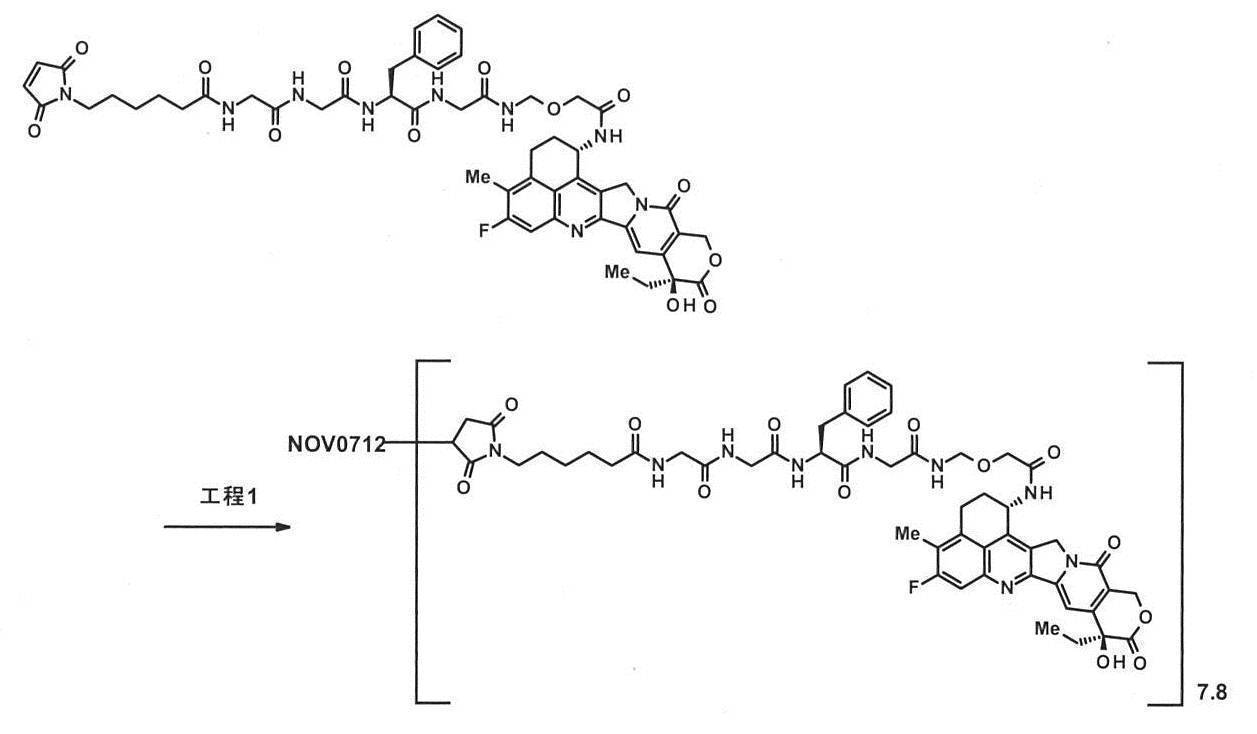
工程1:抗体-薬物コンジュゲート(2)
-イル)ヘキサノイル]グリシルグリシル-L-フェニルアラニル-N-[(2-{[(1S,9S)-9-エチル-5-フルオロ-9-ヒドロキシ-4-メチル-10,13-ジオキソ-2,3,9,10,13,15-ヘキサヒドロ-1H,12H-ベンゾ[de]ピラノ[3’,4’:6,7]インドリジノ[1,2-b]キノリン-1-イル]アミノ}-2-オキソエトキシ)メチル]グリシンアミドの10mM ジメチルスルホキシド溶液(0.389mL;抗体一分子に対して10当量)を加え、15℃で1時間インキュベートし、薬物リンカーを抗体へ結合させた。次に、100mM NAC(Sigma-Aldrich Co.LLC)水溶液(0.0350mL;抗体一分子に対して9当量)を加え、さらに室温にて20分間撹拌し、薬物リンカーの反応を停止させた。
抗体濃度:2.61mg/mL,抗体収量:49.6mg(87%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):5.9;共通操作Fにて測定された抗体一分子あたりの薬物平均結合数(n):7.6。
工程1:抗体-薬物コンジュゲート(3)
ィド結合を還元した。
抗体濃度:2.71mg/mL,抗体収量:51.4mg(91%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):5.7;共通操作Fにて測定された抗体一分子あたりの薬物平均結合数(n):7.6。
工程1:抗体-薬物コンジュゲート(4)
mM TCEP(東京化成工業株式会社)水溶液(0.232mL;抗体一分子に対して6.0当量)及び1Mリン酸水素二カリウム水溶液(Nacalai Tesque,Inc.;0.0855mL)を加えた。本溶液のpHが7.0±0.1内であることを確認した後に、37℃で2時間インキュベートすることによって、抗体内鎖間部のジスルフィド結合を還元した。
抗体濃度:2.56mg/mL,抗体収量:48.7mg(87%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):5.8;共通操作Fにて測定された抗体一分子あたりの薬物平均結合数(n):7.6。
参考例2)-1 抗体-薬物コンジュゲートの作製 NOV0712-DM4
抗体-薬物コンジュゲート(5)
抗体と薬物リンカーのコンジュゲーション:参考例1にて作製したNOV0712を、
製造方法1に記載した共通操作B(280nm吸光係数として1.51mLmg-1cm-1を使用)及びCを用いて、20mM HEPES8.1(LIFE TECHNOLOGIES社製 HEPES, 1M Buffer Solution(20mL)を1M水酸化ナトリウムでpH8.1とした後、蒸留水にて1Lとした)にて9.7mg/mLに調製し、20℃で10分間インキュベートした。次いでWO2016/024195号公開特許公報に記載の10mM 1-(2,5-ジオキソピロリジン-1-イルオキシ)-1-オキソ-4-(ピリジン-2-イルジスルファニル)ブタン-2-スルフォン酸のDMA溶液(0.366mL;抗体一分子に対して5.2当量)、10mM N2-デアセチル-デアセチル-N2-(4-メチル-4-メルカプト-1-オキソペンチル)-メイタンシン(DM4)のDMA溶液(0.366mL;抗体一分子に対して6.8当量)、及び0.243mLのDMAを加え、20℃で16時間インキュベートし、薬物リンカーを抗体へ結合させた。次に、1M 酢酸水溶液を加えpH5.0とし、さらに室温にて20分間撹拌し、薬物リンカーの反応を停止させた。
を使用して、下記の特性値を得た。
抗体濃度:2.58mg/mL,抗体収量:72.2mg(93%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):3.0。
工程1:抗体-薬物コンジュゲート(6)
抗体濃度:2.26mg/mL,抗体収量:56.4mg(92%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):6.4;共通操作Fにて測定された抗体一分子あたりの薬物平均結合数(n):7.8。
参考例3)-1 抗体-薬物コンジュゲートの作製 H01L02-DM4
抗体-薬物コンジュゲート(7)
抗体と薬物リンカーのコンジュゲーション:実施例5にて作製したH01L02を、製造方法1に記載した共通操作B(280nm吸光係数として1.53mLmg-1cm-1を使用)及びCを用いて、20mM HEPES8.1(LIFE TECHNOLOGIES社製 HEPES, 1M Buffer Solution(20mL)を1M水酸化ナトリウムでpH8.1とした後、蒸留水にて1Lとした)にて9.8mg/mLに調製し、20℃で10分間インキュベートした。次いでWO2016/024195号公開特許公報に記載の10mM 1-(2,5-ジオキソピロリジン-1-イルオキシ)-1-オキソ-4-(ピリジン-2-イルジスルファニル)ブタン-2-スルフォン酸のDMA溶液(0.062mL;抗体一分子に対して11.5当量)、10mM N2-デアセチル-N2-(4-メチル-4-メルカプト-1-オキソペンチル)-メイタンシン(DM4)のDMA溶液(0.082mL;抗体一分子に対して15.1当量)を加え、20℃で18時間インキュベートし、薬物リンカーを抗体へ結合させた。次に、1M 酢酸水溶液を加えpH5.0とし、さらに室温にて20分間撹拌し、薬物リンカーの反応を停止させた。
抗体濃度:1.97mg/mL,抗体収量:6.90mg(88%),共通操作Eにて測定された抗体一分子あたりの薬物平均結合数(n):3.6。
8)-1 CDH6陽性ヒト腫瘍細胞株に対する抗体-薬物コンジュゲートのin vitro細胞増殖抑制活性評価
CDH6陽性ヒト卵巣腫瘍細胞株PA-1を10% FBS含有MEM培地中2x103細胞/100μL/wellになるよう96ウェルプレートに播種し、37℃、5% CO2の条件下で一晩培養した。翌日、実施例7で作製したヒト化hG019-薬物コンジュゲート4種(クローン名は、H01L02-DXd、H02L02-DXd、H02L03-DXd及びH04L02-DXd)、又は参考例2で作製したNOV0712-薬物コンジュゲート(NOV0712-DM4)を終濃度0.0001(nM)から100(nM)となるように添加した。4日間培養後に生存細胞数をCellTiter-GloTM Luminescent Cell Viability Assay(Promega)によるATPの定量で測定した。図11に抗体-薬物コンジュゲートを各々添加した際の濃度依存的な細胞増殖抑制活性を示す。この結果、ヒト化hG019-薬物コンジュゲート4種は、NOV0712-薬物コンジュゲートと比較して、より低い添加濃度から腫瘍細胞の増殖抑制活性を示し、抗腫瘍活性が高いことが示される。
抗体-薬物コンジュゲートの抗腫瘍効果は、CDH6陽性ヒト腫瘍細胞株の細胞を免疫不全マウスに移植した動物モデルを用いて評価した。4-5週齢のBALB/c ヌードマウス(CAnN.Cg-Foxnl[nu]/CrlCrlj[Foxnlnu/Foxnlnu]、日本チャールス・リバー)及び、SCIDマウス(CB17/Icr-Prkdc[scid]/CrlCrlj、日本チャールス・リバー)を実験使用前にSPF条件化で3日間以上馴化した。マウスには滅菌した固形飼料(FR-2,Funabashi Farms Co.,Ltd)を給餌し、滅菌した水道水(5-15ppm次亜塩素酸ナトリウム溶液を添加して調製)を与えた。移植した腫瘍の長径及び短径を電子式デジタルノギス(CD-15CX,Mitutoyo Corp.)で1週間に2回測定し、以下に示す計算式により腫瘍体積を算出した。
腫瘍体積(mm3)=1/2×長径(mm)×[短径(mm)]2
抗体-薬物コンジュゲートは全てABS緩衝液(10mM-Acetate Buffer, 5% Sorbitol, pH5.5)(NACALAI)で希釈し、各実施例に示す用量にて尾静脈内投与した。また、コントロール群(Vehicle群)としてABS緩衝液を同様に投与した。1群あたり6匹のマウスを実験に用いた。
実施例2)-3-1にてCDH6発現を確認した、CDH6陽性ヒト腎細胞腫瘍細胞株786-O(ATCC)をマトリゲル(コーニング社)に懸濁し、5×106cellsを雄SCIDマウスの右側腹部に皮下移植し(Day0)、Day18に無作為に群分けを実施した。群分け実施日に、実施例7で作製した抗体-薬物コンジュゲート4種(クローン名は、H01L02-DXd、H02L02-DXd、H02L03-DXd及びH04L02-DXd)、又は参考例2で作製したNOV0712-DM4を3mg/kgの用量で尾静脈内投与した。結果を図12に示す。横軸は日数、縦軸は腫瘍体積、誤差範囲はSE値を示す。
実施例2)-3-1にてCDH6発現を確認した、CDH6陽性ヒト卵巣腫瘍細胞株PA-1(ATCC)をマトリゲル(コーニング社)に懸濁し、8.5×106cellsを雌ヌードマウスの右側腹部に皮下移植し(Day0)、Day11に無作為に群分けを実施した。群分け実施日に、実施例7で作製した抗体-薬物コンジュゲートH01L02-DXd又は参考例2で作製したNOV0712-DM4もしくはNOV0712-DXdを、1及び3mg/kgの用量で尾静脈内投与した。結果を図13に示す。横軸は日数、縦軸は腫瘍体積、誤差範囲はSE値を示す。
実施例2)-3-1にてCDH6発現を確認した、CDH6陽性ヒト卵巣腫瘍細胞株NIH:OVCAR-3(ATCC)をマトリゲル(コーニング社)に懸濁し、1×107cellsを雌ヌードマウスの右側腹部に皮下移植し(Day0)、Day22に無作為に群分けを実施した。群分け実施日に、実施例7で作製した抗体-薬物コンジュゲートH01L02-DXd又は参考例2で作製したNOV0712-DM4を、1及び3mg/kgの用量で尾静脈内投与した。結果を図14に示す。横軸は日数、縦軸は腫瘍体積、誤差範囲はSE値を示す。
実施例2)-3-1にてCDH6発現を確認した、CDH6陽性ヒト腎細胞腫瘍細胞株786-O(ATCC)をマトリゲル(コーニング社)に懸濁し、5×106cellsを雄SCIDマウスの右側腹部に皮下移植し(Day0)、Day20に無作為に群分けを実施した。群分け実施日に、実施例7で作製した抗体-薬物コンジュゲートH01L02-DXd又は参考例2で作製したNOV0712-DM4を、1及び3mg/kgの用量で尾静脈内投与した。結果を図15に示す。横軸は日数、縦軸は腫瘍体積、誤差範囲はSE値を示す。
実施例2)-3-1にてCDH6を発現しないことを確認した、CDH6陰性ヒト卵巣腫瘍細胞株ES-2(ATCC)を生理食塩水に懸濁し、1×106cellsを雌ヌードマウスの右側腹部に皮下移植し(Day0)、Day7に無作為に群分けを実施した。群分け実施日に、実施例7で作成した抗体-薬物コンジュゲートH01L02-DXd又は参考例2で作製したNOV0712-DM4を、1及び3mg/kgの用量で尾静脈内投与した。結果を図16に示す。横軸は日数、縦軸は腫瘍体積、誤差範囲はSE値を示す。
Claims (29)
- 配列番号4に記載のアミノ酸配列に特異的に結合し、細胞内に取り込まれる内在化能を有する、抗体又は当該抗体の機能性断片。
(当該抗体又は当該抗体の機能性断片は、配列番号63に記載のアミノ酸配列に対して95%以上の同一性を有するアミノ酸配列からなる軽鎖可変領域及び配列番号75に記載のアミノ酸配列に対して95%以上の同一性を有するアミノ酸配列からなる重鎖可変領域を含む。) - 配列番号61の21~233番目のアミノ酸配列に対して95%以上の同一性を有するアミノ酸配列からなる軽鎖及び配列番号73の20~471番目のアミノ酸配列に対して95%以上の同一性を有するアミノ酸配列からなる重鎖を含む、請求項1に記載の抗体又は当該抗体の機能性断片。
- 機能性断片がFab、F(ab’)2、Fab’及びFvからなる群から選択される請求項1又は2に記載の抗体の機能性断片。
- 請求項1~3のいずれか1項に記載の抗体又は当該抗体の機能性断片に含まれるアミノ酸配列をコードするヌクレオチド配列を含むポリヌクレオチド。
- 請求項4に記載のポリヌクレオチドを含有する発現ベクター。
- 請求項5に記載の発現ベクターにより形質転換された宿主細胞。
- 宿主細胞が真核細胞である請求項6に記載の宿主細胞。
- 請求項6又は7に記載の宿主細胞を培養する工程、及び当該工程で得られた培養物から目的の抗体又は当該抗体の機能性断片を採取する工程を含むことを特徴とする当該抗体又は当該抗体の機能性断片の製造方法。
- 重鎖又は軽鎖が、N-結合への糖鎖付加、O-結合への糖鎖付加、N末のプロセッシング、C末のプロセッシング、脱アミド化、アスパラギン酸の異性化、メチオニンの酸化、N末にメチオニン残基の付加、プロリン残基のアミド化、N末グルタミンもしくはN末グルタミン酸のピログルタミン酸化、及びカルボキシル末端における1つ又は2つのアミノ酸欠失からなる群より選択される1又は2以上の修飾をうけた、請求項1~3のいずれか1項に記載の抗体又は当該抗体の機能性断片。
- 重鎖のカルボキシル末端において1つ又は2つのアミノ酸が欠失している請求項9に記載の抗体。
- 2本の重鎖の双方でカルボキシル末端において1つのアミノ酸が欠失している請求項10に記載の抗体。
- 重鎖のカルボキシル末端のプロリン残基が更にアミド化されている請求項9~11のいずれか1項に記載の抗体。
- 抗体依存性細胞傷害活性を増強させるために糖鎖修飾が調節されている請求項1~3及び請求項9~12からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片。
- 請求項1~3及び請求項9~13からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片に薬物が結合している抗体-薬物コンジュゲート。
- 薬物が抗腫瘍性化合物である、請求項14に記載の抗体-薬物コンジュゲート。
- 抗体と薬物が、次式(a)~(f):
(a)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
(b)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
(c)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
(d)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2CH2-O-CH2-C(=O)-、
(e)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、及び
(f)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-、
からなる群から選択されるいずれかの構造のリンカーを介して結合している、請求項14~16のいずれか1項に記載の抗体-薬物コンジュゲート。
(ここで、抗体は、-(Succinimid-3-yl-N)の末端において結合する。抗腫瘍性化合物は、1位のアミノ基の窒素原子を結合部位として、(a)、(b)、(e)又は(f)の-CH2CH2CH2-C(=O)-部分、(c)のCH2-O-CH2-C(=O)-部分又は(d)のCH2CH2-O-CH2-C(=O)-部分のカルボニル基に結合する。上記式中GGFGは、グリシン-グリシン-フェニルアラニン-グリシンからなるペプチド結合でつながっているアミノ酸配列を示す。
-(Succinimid-3-yl-N)-は次式:
- リンカーが以下の(c)又は(e)の式で示される請求項14~17のいずれか1項に記載の抗体-薬物コンジュゲート:
(c)-(Succinimid-3-yl-N)-CH2CH2CH2CH2CH2-C(=O)-GGFG-NH-CH2-O-CH2-C(=O)-、
(e)-(Succinimid-3-yl-N)-CH2CH2-C(=O)-NH-CH2CH2O-CH2CH2O-CH2CH2-C(=O)-GGFG-NH-CH2CH2CH2-C(=O)-。 - 選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が1~10個の範囲である請求項14~20のいずれか1項に記載の抗体-薬物コンジュゲート。
- 選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が2~8個の範囲である請求項21に記載の抗体-薬物コンジュゲート。
- 選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が5~8個の範囲である請求項22に記載の抗体-薬物コンジュゲート。
- 選択された1種の薬物-リンカー構造の1抗体あたりの平均結合数が7~8個である請求項23に記載の抗体-薬物コンジュゲート。
- 請求項14~24のいずれか1項に記載の抗体-薬物コンジュゲート、その塩、又はそれらの水和物を含むことを特徴とする医薬組成物。
- 抗腫瘍薬であることを特徴とする、請求項25に記載の医薬組成物。
- 腫瘍がCDH6を発現する腫瘍であることを特徴とする、請求項26に記載の医薬組成物。
- 腫瘍が、腎細胞癌、腎淡明細胞癌、乳頭状腎細胞癌、卵巣癌、卵巣漿液性腺癌、甲状腺癌、胆管癌、肺癌、小細胞肺癌、神経膠芽腫、中皮腫、子宮癌、膵臓癌、ウィルムス腫瘍又は神経芽腫であることを特徴とする、請求項26又は27に記載の医薬組成物。
- 請求項1~3及び請求項9~13からなる群から選択されるいずれか1項に記載の抗体又は当該抗体の機能性断片或いは請求項8に記載の製造方法で得られる抗体又は当該抗体の機能性断片と、薬物-リンカー中間化合物を反応させる工程を含むことを特徴とする、抗体-薬物コンジュゲートの製造方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024026117A JP7776555B2 (ja) | 2017-05-15 | 2024-02-26 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
| JP2025157162A JP2026001062A (ja) | 2017-05-15 | 2025-09-22 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017096749 | 2017-05-15 | ||
| JP2017096749 | 2017-05-15 | ||
| JP2021002874A JP7064629B2 (ja) | 2017-05-15 | 2021-01-12 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021002874A Division JP7064629B2 (ja) | 2017-05-15 | 2021-01-12 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024026117A Division JP7776555B2 (ja) | 2017-05-15 | 2024-02-26 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022090057A true JP2022090057A (ja) | 2022-06-16 |
| JP7445699B2 JP7445699B2 (ja) | 2024-03-07 |
Family
ID=64273811
Family Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019518773A Active JP6827534B2 (ja) | 2017-05-15 | 2018-05-14 | 抗cdh6抗体及び抗cdh6抗体−薬物コンジュゲート |
| JP2021002874A Active JP7064629B2 (ja) | 2017-05-15 | 2021-01-12 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
| JP2022070921A Active JP7445699B2 (ja) | 2017-05-15 | 2022-04-22 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
| JP2024026117A Active JP7776555B2 (ja) | 2017-05-15 | 2024-02-26 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
| JP2025157162A Pending JP2026001062A (ja) | 2017-05-15 | 2025-09-22 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019518773A Active JP6827534B2 (ja) | 2017-05-15 | 2018-05-14 | 抗cdh6抗体及び抗cdh6抗体−薬物コンジュゲート |
| JP2021002874A Active JP7064629B2 (ja) | 2017-05-15 | 2021-01-12 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024026117A Active JP7776555B2 (ja) | 2017-05-15 | 2024-02-26 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
| JP2025157162A Pending JP2026001062A (ja) | 2017-05-15 | 2025-09-22 | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート |
Country Status (25)
| Country | Link |
|---|---|
| US (4) | US11446386B2 (ja) |
| EP (2) | EP4374852A3 (ja) |
| JP (5) | JP6827534B2 (ja) |
| KR (2) | KR102768694B1 (ja) |
| CN (1) | CN110651045A (ja) |
| AU (2) | AU2018270961B9 (ja) |
| BR (1) | BR112019023832A2 (ja) |
| CA (1) | CA3063827A1 (ja) |
| CO (1) | CO2019013020A2 (ja) |
| DK (1) | DK3626825T3 (ja) |
| ES (1) | ES2991607T3 (ja) |
| FI (1) | FI3626825T3 (ja) |
| HR (1) | HRP20241458T1 (ja) |
| HU (1) | HUE070023T2 (ja) |
| IL (2) | IL318785A (ja) |
| LT (1) | LT3626825T (ja) |
| MX (2) | MX2023001685A (ja) |
| PH (1) | PH12019502545A1 (ja) |
| PL (1) | PL3626825T3 (ja) |
| PT (1) | PT3626825T (ja) |
| RS (1) | RS66163B1 (ja) |
| SI (1) | SI3626825T1 (ja) |
| SM (1) | SMT202400472T1 (ja) |
| TW (16) | TW202530220A (ja) |
| WO (1) | WO2018212136A1 (ja) |
Families Citing this family (44)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW202530220A (zh) * | 2017-05-15 | 2025-08-01 | 日商第一三共股份有限公司 | 抗體-藥物結合物之製造方法 |
| TWI885539B (zh) | 2017-09-29 | 2025-06-01 | 日商第一三共股份有限公司 | 抗體-吡咯并苯二氮呯衍生物複合體 |
| SG11202100653YA (en) | 2018-07-25 | 2021-02-25 | Daiichi Sankyo Co Ltd | Effective method for manufacturing antibody-drug conjugate |
| US12358999B2 (en) | 2018-07-27 | 2025-07-15 | Daiichi Sankyo Company, Limited | Protein recognizing drug moiety of antibody-drug conjugate |
| KR102894505B1 (ko) | 2018-07-31 | 2025-12-02 | 다이이찌 산쿄 가부시키가이샤 | 항체-약물 콘주게이트 투여에 의한 전이성 뇌종양의 치료 |
| JP7458981B2 (ja) | 2018-08-06 | 2024-04-01 | 第一三共株式会社 | 抗体-薬物コンジュゲートとチューブリン阻害剤の組み合わせ |
| JP7481255B2 (ja) | 2018-08-23 | 2024-05-10 | 第一三共株式会社 | 抗体薬物複合体の感受性マーカー |
| SMT202500141T1 (it) | 2018-09-06 | 2025-05-12 | Daiichi Sankyo Co Ltd | Coniugati farmaco-anticorpo di derivati dinucleotidici ciclici |
| US20220016257A1 (en) * | 2018-11-14 | 2022-01-20 | Daiichi Sankyo Company, Limited | Anti-cdh6 antibody-pyrrolobenzodiazepine derivative conjugate |
| EA202191641A1 (ru) | 2018-12-11 | 2021-09-13 | Дайити Санкио Компани, Лимитед | Комбинация конъюгата антитело-лекарственное средство с ингибитором parp |
| KR20210107069A (ko) | 2018-12-21 | 2021-08-31 | 다이이찌 산쿄 가부시키가이샤 | 항체-약물 컨쥬게이트와 키나아제 저해제의 조합 |
| KR102679892B1 (ko) | 2019-03-29 | 2024-07-02 | 메디뮨 리미티드 | 화합물 및 이의 접합체 |
| WO2021260583A1 (en) | 2020-06-24 | 2021-12-30 | Astrazeneca Uk Limited | Combination of antibody-drug conjugate and dna-pk inhibitor |
| EP4171651A1 (en) | 2020-06-24 | 2023-05-03 | AstraZeneca UK Limited | Combination of antibody-drug conjugate and atm inhibitor |
| JP7793556B2 (ja) | 2020-06-24 | 2026-01-05 | アストラゼネカ ユーケー リミテッド | 抗体-薬物コンジュゲートとatr阻害剤との組み合わせ |
| US20230233540A1 (en) | 2020-06-24 | 2023-07-27 | Astrazeneca Uk Limited | Combination of antibody-drug conjugate and cdk9 inhibitor |
| WO2021260582A1 (en) | 2020-06-24 | 2021-12-30 | Astrazeneca Uk Limited | Combination of antibody-drug conjugate and aurora b inhibitor |
| BR112023006337A2 (pt) | 2020-10-09 | 2023-05-09 | Astrazeneca Uk Ltd | Produto farmacêutico, uso de um conjugado anticorpo anti-her2-fármaco ou um inibidor seletivo de parp1, e, método de tratamento do câncer |
| IL302812A (en) | 2020-11-11 | 2023-07-01 | Daiichi Sankyo Co Ltd | Antibody-drug conjugate combinations with anti-SIRP alpha antibody |
| TW202241454A (zh) | 2021-02-01 | 2022-11-01 | 日商第一三共股份有限公司 | 抗體-免疫賦活化劑共軛物之新穎製造方法 |
| IL305816A (en) | 2021-03-12 | 2023-11-01 | Daiichi Sankyo Co Ltd | Glycan and a method for preparing a medicine containing it |
| WO2022228494A1 (zh) | 2021-04-29 | 2022-11-03 | 上海汇连生物医药有限公司 | 抗体偶联药物的制备方法及应用 |
| US20250179196A1 (en) * | 2021-07-30 | 2025-06-05 | Janssen Biotech, Inc. | Materials and methods of making or using il-23r binding proteins |
| TW202508643A (zh) | 2021-09-15 | 2025-03-01 | 日商第一三共股份有限公司 | 抗體-藥物結合物之用途 |
| WO2023102875A1 (en) * | 2021-12-10 | 2023-06-15 | Multitude Therapeutics Inc. | Anti-cdh6 antibody drug conjugate |
| CA3239715A1 (en) * | 2021-12-10 | 2023-06-15 | Xun Meng | Anti-cdh6 antibodies and antibody-drug conjugates thereof |
| WO2023126822A1 (en) | 2021-12-28 | 2023-07-06 | Astrazeneca Uk Limited | Combination of antibody-drug conjugate and rasg12c inhibitor |
| WO2023143387A1 (en) * | 2022-01-26 | 2023-08-03 | Beigene , Ltd. | ANTI-DXd ANTIBODIES AND METHODS OF USE |
| IL315341A (en) | 2022-03-02 | 2024-10-01 | Daiichi Sankyo Co Ltd | METHOD FOR PRODUCING Fc-CONTAINING MOLECULE |
| US20250276079A1 (en) | 2022-04-27 | 2025-09-04 | Daiichi Sankyo Company, Limited | COMBINATION OF ANTIBODY-DRUG CONJUGATE WITH EZH1 and/or EZH2 INHIBITOR |
| CN119403829A (zh) | 2022-05-11 | 2025-02-07 | 第一三共株式会社 | 对于肿瘤抗原特异性的抗体和cd47抑制剂的组合 |
| US20250304717A1 (en) | 2022-05-12 | 2025-10-02 | Hainan Simcere Zaiming Pharmaceutical Co., Ltd. | Camptothecin derivative and ligand-drug conjugate |
| KR20250012631A (ko) | 2022-05-24 | 2025-01-24 | 다이이찌 산쿄 가부시키가이샤 | 항-cdh6 항체-약물 접합체의 투약 |
| KR20250040960A (ko) | 2022-07-28 | 2025-03-25 | 아스트라제네카 유케이 리미티드 | 항체-약물 접합체 및 이중특이적 체크포인트 억제제의 조합 |
| WO2024048490A1 (ja) | 2022-08-29 | 2024-03-07 | 第一三共株式会社 | 変異Fc領域を含む抗体薬物コンジュゲート |
| CN119855836A (zh) | 2022-09-09 | 2025-04-18 | 第一三共株式会社 | 新型寡糖、该寡糖的制造中间体、以及它们的制造方法 |
| TW202434310A (zh) | 2023-01-27 | 2024-09-01 | 日商第一三共股份有限公司 | 抗lrrc15抗體 |
| WO2024165049A1 (zh) | 2023-02-10 | 2024-08-15 | 山东先声生物制药有限公司 | 抗cdh6的抗体及其用途 |
| AU2024236246A1 (en) | 2023-03-14 | 2025-10-30 | Daiichi Sankyo Company, Limited | Combination of anti-CDH6 antibody-drug conjugate and VEGF inhibitor |
| EP4687998A1 (en) * | 2023-03-28 | 2026-02-11 | Hansoh Bio LLC | Ligand-cytotoxicity drug conjugates and pharmaceutical uses thereof |
| KR20250164708A (ko) * | 2023-03-29 | 2025-11-25 | 다이이찌 산쿄 가부시키가이샤 | 항 cd25 항체 및 항 cd25 항체-약물 콘주게이트 |
| CN120916791A (zh) | 2023-03-31 | 2025-11-07 | 第一三共株式会社 | 抗CDH6抗体-药物缀合物与HIF-2α抑制剂的组合 |
| KR20250169610A (ko) | 2023-04-14 | 2025-12-03 | 하이난 심시어 자이밍 파마슈티컬 컴퍼니 리미티드 | 항-cdh6 항체-약물 접합체 및 이의 용도 |
| TW202542193A (zh) * | 2023-12-29 | 2025-11-01 | 大陸商上海翰森生物醫藥科技有限公司 | 抗原結合分子、其藥物偶聯物及其醫藥用途 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014057687A1 (ja) * | 2012-10-11 | 2014-04-17 | 第一三共株式会社 | 抗体-薬物コンジュゲート |
| WO2016024195A1 (en) * | 2014-08-12 | 2016-02-18 | Novartis Ag | Anti-cdh6 antibody drug conjugates |
| JP6827534B2 (ja) * | 2017-05-15 | 2021-02-10 | 第一三共株式会社 | 抗cdh6抗体及び抗cdh6抗体−薬物コンジュゲート |
Family Cites Families (87)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1989006692A1 (en) | 1988-01-12 | 1989-07-27 | Genentech, Inc. | Method of treating tumor cells by inhibiting growth factor receptor function |
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| US5183884A (en) | 1989-12-01 | 1993-02-02 | United States Of America | Dna segment encoding a gene for a receptor related to the epidermal growth factor receptor |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| ATE185601T1 (de) | 1990-07-10 | 1999-10-15 | Cambridge Antibody Tech | Verfahren zur herstellung von spezifischen bindungspaargliedern |
| US5637770A (en) | 1991-01-16 | 1997-06-10 | Daiichi Pharmaceutical Co., Ltd. | Hexa-cyclic compound |
| JP3008226B2 (ja) | 1991-01-16 | 2000-02-14 | 第一製薬株式会社 | 六環性化合物 |
| JP4124480B2 (ja) | 1991-06-14 | 2008-07-23 | ジェネンテック・インコーポレーテッド | 免疫グロブリン変異体 |
| WO1993006213A1 (en) | 1991-09-23 | 1993-04-01 | Medical Research Council | Production of chimeric antibodies - a combinatorial approach |
| DE69233782D1 (de) | 1991-12-02 | 2010-05-20 | Medical Res Council | Herstellung von Autoantikörpern auf Phagenoberflächen ausgehend von Antikörpersegmentbibliotheken |
| JP3507073B2 (ja) | 1992-03-24 | 2004-03-15 | ケンブリッジ アンティボディー テクノロジー リミティド | 特異的結合対の成員の製造方法 |
| US6214345B1 (en) | 1993-05-14 | 2001-04-10 | Bristol-Myers Squibb Co. | Lysosomal enzyme-cleavable antitumor drug conjugates |
| GB9313509D0 (en) | 1993-06-30 | 1993-08-11 | Medical Res Council | Chemisynthetic libraries |
| CA2177367A1 (en) | 1993-12-03 | 1995-06-08 | Andrew David Griffiths | Recombinant binding proteins and peptides |
| US6504029B1 (en) | 1995-04-10 | 2003-01-07 | Daiichi Pharmaceutical Co., Ltd. | Condensed-hexacyclic compounds and a process therefor |
| JPH08337584A (ja) | 1995-04-10 | 1996-12-24 | Dai Ichi Seiyaku Co Ltd | 縮合六環式アミノ化合物、これを含有する医薬及びその製法 |
| SG50747A1 (en) | 1995-08-02 | 1998-07-20 | Tanabe Seiyaku Co | Comptothecin derivatives |
| CA2192725C (en) | 1995-12-28 | 2004-04-20 | Kenji Tsujihara | Camptothecin derivatives |
| JPH1095802A (ja) | 1995-12-28 | 1998-04-14 | Tanabe Seiyaku Co Ltd | カンプトテシン誘導体 |
| US5968511A (en) | 1996-03-27 | 1999-10-19 | Genentech, Inc. | ErbB3 antibodies |
| TW409058B (en) | 1996-06-06 | 2000-10-21 | Daiichi Seiyaku Co | Method for preparation of a drug complex |
| TW527183B (en) | 1996-06-06 | 2003-04-11 | Daiichi Seiyaku Co | Drug complex |
| JPH1171280A (ja) | 1997-06-26 | 1999-03-16 | Tanabe Seiyaku Co Ltd | 医薬組成物 |
| JPH1192405A (ja) | 1997-09-19 | 1999-04-06 | Dai Ichi Seiyaku Co Ltd | 薬物複合体 |
| PT1071700E (pt) | 1998-04-20 | 2010-04-23 | Glycart Biotechnology Ag | Modificação por glicosilação de anticorpos para melhorar a citotoxicidade celular dependente de anticorpos |
| KR100581443B1 (ko) | 1998-05-22 | 2006-05-23 | 다이이찌 세이야꾸 가부시기가이샤 | 약물복합체 |
| CA2348931A1 (en) | 1998-10-30 | 2000-05-11 | Daiichi Pharmaceutical Co., Ltd. | Dds compound and method for measurement thereof |
| ES2601882T5 (es) | 1999-04-09 | 2021-06-07 | Kyowa Kirin Co Ltd | Procedimiento para controlar la actividad de una molécula inmunofuncional |
| PT2283866E (pt) | 1999-06-25 | 2015-07-20 | Genentech Inc | Métodos de tratamento utilizando conjugados de anticorpo anti-erbb-maitansinóide |
| JP2002060351A (ja) | 2000-03-22 | 2002-02-26 | Dai Ichi Seiyaku Co Ltd | 水酸基を有する薬物を含むdds化合物 |
| KR20030031502A (ko) | 2000-06-29 | 2003-04-21 | 다이이찌 세이야꾸 가부시기가이샤 | 디디에스 화합물 및 그의 제조방법 |
| KR20030023697A (ko) | 2000-07-13 | 2003-03-19 | 다이이찌 세이야꾸 가부시기가이샤 | Dds 화합물을 함유하는 의약 조성물 |
| HU231090B1 (hu) | 2000-10-06 | 2020-07-28 | Kyowa Kirin Co., Ltd. | Antitest-kompozíciót termelő sejt |
| EP1283053A1 (en) | 2001-08-09 | 2003-02-12 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Inhibitors of HER3 activity |
| TWI313609B (en) | 2001-08-21 | 2009-08-21 | Mitsubishi Tanabe Pharma Corp | Pharmaceutical composition for inhibiting the metastasis or preventing the recurrence of malignant tumor |
| US20050123536A1 (en) | 2001-11-20 | 2005-06-09 | Che-Leung Law | Treatment of immunological disorders using anti-dc30 antibodies |
| US8877901B2 (en) | 2002-12-13 | 2014-11-04 | Immunomedics, Inc. | Camptothecin-binding moiety conjugates |
| US7585491B2 (en) | 2002-12-13 | 2009-09-08 | Immunomedics, Inc. | Immunoconjugates with an intracellularly-cleavable linkage |
| US9745380B2 (en) | 2002-03-01 | 2017-08-29 | Immunomedics, Inc. | RS7 antibodies |
| US20050276812A1 (en) | 2004-06-01 | 2005-12-15 | Genentech, Inc. | Antibody-drug conjugates and methods |
| US20040202666A1 (en) | 2003-01-24 | 2004-10-14 | Immunomedics, Inc. | Anti-cancer anthracycline drug-antibody conjugates |
| MXPA06009701A (es) | 2004-02-26 | 2007-03-26 | Inotek Pharmaceuticals Corp | Derivados de isoquinolina y metodos de uso de los mismos. |
| ES2533695T3 (es) | 2004-03-02 | 2015-04-14 | Seattle Genetics, Inc. | Anticuerpos cargados parcialmente y métodos para su conjugación |
| CA2564076C (en) | 2004-05-19 | 2014-02-18 | Medarex, Inc. | Chemical linkers and conjugates thereof |
| KR20180091967A (ko) | 2004-07-22 | 2018-08-16 | 제넨테크, 인크. | Her2 항체 조성물 |
| US8802820B2 (en) | 2004-11-12 | 2014-08-12 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| AU2005316844A1 (en) | 2004-11-29 | 2006-06-22 | Seattle Genetics, Inc. | Engineered antibodies and immunoconjugates |
| UA94899C2 (ru) | 2005-01-21 | 2011-06-25 | Дженентек, Инк. | Фиксированное дозирование антител к her |
| DE102005009099A1 (de) | 2005-02-28 | 2006-08-31 | Ktb Tumorforschungsgesellschaft Mbh | Proteinbindende Camptothecin-Peptid-Derivate und diese enthaltende Arzneimittel |
| DE102005009084A1 (de) | 2005-02-28 | 2006-08-31 | Ktb Tumorforschungsgesellschaft Mbh | Proteinbindende Anthrazyklin-Peptid-Derivate und diese enthaltende Arzneimittel |
| US7833979B2 (en) | 2005-04-22 | 2010-11-16 | Amgen Inc. | Toxin peptide therapeutic agents |
| AR056857A1 (es) | 2005-12-30 | 2007-10-24 | U3 Pharma Ag | Anticuerpos dirigidos hacia her-3 (receptor del factor de crecimiento epidérmico humano-3) y sus usos |
| US20080131428A1 (en) | 2006-02-24 | 2008-06-05 | Arius Research, Inc. | Cytotoxicity mediation of cells evidencing surface expression of TROP-2 |
| RS54163B1 (sr) | 2006-05-30 | 2015-12-31 | Genentech Inc. | Anti-cd22 antitela, njihovi imunokonjugati i njihova upotreba |
| UA95958C2 (en) | 2006-05-30 | 2011-09-26 | Дженентек, Инк. | Antibody that binds to cd22, immunoconjugates and uses therefor |
| ITMI20061473A1 (it) | 2006-07-26 | 2008-01-27 | Indena Spa | Derivati della camptotecina ad attivita antitumorale |
| JP2010513524A (ja) | 2006-12-21 | 2010-04-30 | シェーリング コーポレイション | Kspキネシン活性を阻害するためのピロロ[3,2−a]ピリジン誘導体 |
| DK2716301T3 (en) | 2007-02-16 | 2017-07-31 | Merrimack Pharmaceuticals Inc | ANTIBODIES AGAINST ERBB3 AND APPLICATIONS THEREOF |
| US20100143245A1 (en) | 2007-03-22 | 2010-06-10 | Sloan-Kettering Institute For Cancer Research | Uses of monoclonal antibody 8h9 |
| CN104524590B (zh) | 2008-04-30 | 2019-06-21 | 伊缪诺金公司 | 交联剂和它们的用途 |
| ES2544971T3 (es) | 2008-05-13 | 2015-09-07 | Genentech, Inc. | Análisis de conjugados de fármacos y anticuerpos mediante espectrometría de masas con captura por afinidad basada en esferas |
| JP5677972B2 (ja) | 2008-11-18 | 2015-02-25 | メリマック ファーマシューティカルズ インコーポレーティッド | ヒト血清アルブミンリンカーおよびそのコンジュゲート |
| LT3903829T (lt) | 2009-02-13 | 2023-06-12 | Immunomedics, Inc. | Imunokonjugatai su viduląsteliniu būdu skaldoma jungtimi |
| US20120171201A1 (en) | 2009-07-22 | 2012-07-05 | Enzon Pharmaceuticals, Inc. | Methods of treating her2 positive cancer with her2 receptor antagonist in combination with multi-arm polymeric conjugates of 7-ethyl-10-hydroxycamptothecin |
| JP5829520B2 (ja) | 2009-08-20 | 2015-12-09 | 国立大学法人 千葉大学 | コルヒチン誘導体 |
| EP2480230A4 (en) | 2009-09-24 | 2015-06-10 | Seattle Genetics Inc | DR5 Ligand-HEILMITTELKONJUGATE |
| CN105999263B (zh) | 2009-11-13 | 2021-06-29 | 第一三共欧洲有限公司 | 用于治疗或预防人表皮生长因子受体-3(her-3)相关疾病的材料和方法 |
| WO2011068845A1 (en) | 2009-12-02 | 2011-06-09 | Immunomedics, Inc. | Combining radioimmunotherapy and antibody-drug conjugates for improved cancer therapy |
| ES2661228T3 (es) | 2010-05-13 | 2018-03-28 | Indiana University Research And Technology Corporation | Péptidos de la superfamilia de glucagón que muestran actividad de receptor nuclear de hormona |
| EA031043B1 (ru) | 2010-05-17 | 2018-11-30 | Ливтех, Инк. | Антитело против trop-2 человека, обладающее противоопухолевой активностью in vivo |
| EP2571525A4 (en) | 2010-05-18 | 2016-04-27 | Cerulean Pharma Inc | Compositions and methods for treating autoimmune and other diseases |
| JPWO2011155579A1 (ja) | 2010-06-10 | 2013-08-15 | 北海道公立大学法人 札幌医科大学 | 抗Trop−2抗体 |
| CA2804185C (en) | 2010-07-12 | 2017-03-21 | Covx Technologies Ireland Limited | Multifunctional antibody conjugates |
| WO2012019024A2 (en) | 2010-08-04 | 2012-02-09 | Immunogen, Inc. | Her3-binding molecules and immunoconjugates thereof |
| CA2815154A1 (en) | 2010-08-06 | 2012-02-09 | U3 Pharma Gmbh | Use of her3 binding agents in prostate treatment |
| JP6014596B2 (ja) | 2010-11-09 | 2016-10-25 | メディミューン,エルエルシー | 均一コンジュゲーションのための抗体足場 |
| CN103313990B (zh) | 2010-11-17 | 2016-07-20 | 基因泰克公司 | 丙氨酰美登醇抗体偶联物 |
| CN104053672A (zh) | 2011-11-11 | 2014-09-17 | 瑞纳神经科学公司 | Trop-2特异性抗体及其用途 |
| US9427464B2 (en) | 2011-11-22 | 2016-08-30 | Chiome Bioscience Inc. | Anti-human TROP-2 antibody having an antitumor activity in vivo |
| KR20140114826A (ko) | 2011-12-14 | 2014-09-29 | 시애틀 지네틱스, 인크. | Fgfr 항체 약물 콘주게이트 (adcs) 및 그의 용도 |
| US20130280282A1 (en) | 2012-04-24 | 2013-10-24 | Daiichi Sankyo Co., Ltd. | Dr5 ligand drug conjugates |
| WO2013188740A1 (en) | 2012-06-14 | 2013-12-19 | Ambrx, Inc. | Anti-psma antibodies conjugated to nuclear receptor ligand polypeptides |
| WO2014061277A1 (ja) | 2012-10-19 | 2014-04-24 | 第一三共株式会社 | 親水性構造を含むリンカーで結合させた抗体-薬物コンジュゲート |
| US9814784B2 (en) | 2013-01-03 | 2017-11-14 | Celltrion, Inc. | Antibody-linker-drug conjugate, preparation method therefor, and anticancer drug composition containing same |
| KR102444529B1 (ko) | 2013-12-25 | 2022-09-19 | 다이이찌 산쿄 가부시키가이샤 | 항 trop2 항체-약물 컨쥬게이트 |
| AU2015245122B2 (en) * | 2014-04-10 | 2019-10-24 | Daiichi Sankyo Company, Limited | Anti-HER3 antibody-drug conjugate |
| WO2018185618A1 (en) | 2017-04-03 | 2018-10-11 | Novartis Ag | Anti-cdh6 antibody drug conjugates and anti-gitr antibody combinations and methods of treatment |
-
2018
- 2018-05-11 TW TW114109579A patent/TW202530220A/zh unknown
- 2018-05-11 TW TW114109578A patent/TW202532105A/zh unknown
- 2018-05-11 TW TW114109582A patent/TW202530221A/zh unknown
- 2018-05-11 TW TW114109576A patent/TW202532104A/zh unknown
- 2018-05-11 TW TW114109573A patent/TW202532102A/zh unknown
- 2018-05-11 TW TW114109571A patent/TW202532101A/zh unknown
- 2018-05-11 TW TW113130333A patent/TWI904805B/zh active
- 2018-05-11 TW TW114109581A patent/TW202542161A/zh unknown
- 2018-05-11 TW TW107116035A patent/TWI794230B/zh active
- 2018-05-11 TW TW113130332A patent/TWI904804B/zh active
- 2018-05-11 TW TW114109575A patent/TW202530271A/zh unknown
- 2018-05-11 TW TW112104379A patent/TWI855528B/zh active
- 2018-05-11 TW TW114109574A patent/TW202532103A/zh unknown
- 2018-05-11 TW TW114109572A patent/TW202530218A/zh unknown
- 2018-05-11 TW TW114109577A patent/TW202530219A/zh unknown
- 2018-05-11 TW TW114109580A patent/TW202532106A/zh unknown
- 2018-05-14 US US16/613,203 patent/US11446386B2/en active Active
- 2018-05-14 AU AU2018270961A patent/AU2018270961B9/en active Active
- 2018-05-14 EP EP24164945.8A patent/EP4374852A3/en active Pending
- 2018-05-14 KR KR1020197033607A patent/KR102768694B1/ko active Active
- 2018-05-14 WO PCT/JP2018/018572 patent/WO2018212136A1/ja not_active Ceased
- 2018-05-14 PT PT188025365T patent/PT3626825T/pt unknown
- 2018-05-14 PL PL18802536.5T patent/PL3626825T3/pl unknown
- 2018-05-14 FI FIEP18802536.5T patent/FI3626825T3/fi active
- 2018-05-14 HR HRP20241458TT patent/HRP20241458T1/hr unknown
- 2018-05-14 DK DK18802536.5T patent/DK3626825T3/da active
- 2018-05-14 SI SI201831157T patent/SI3626825T1/sl unknown
- 2018-05-14 ES ES18802536T patent/ES2991607T3/es active Active
- 2018-05-14 BR BR112019023832-8A patent/BR112019023832A2/pt unknown
- 2018-05-14 RS RS20241225A patent/RS66163B1/sr unknown
- 2018-05-14 IL IL318785A patent/IL318785A/en unknown
- 2018-05-14 CN CN201880032336.2A patent/CN110651045A/zh active Pending
- 2018-05-14 IL IL270635A patent/IL270635B2/en unknown
- 2018-05-14 KR KR1020257004599A patent/KR20250025511A/ko active Pending
- 2018-05-14 JP JP2019518773A patent/JP6827534B2/ja active Active
- 2018-05-14 HU HUE18802536A patent/HUE070023T2/hu unknown
- 2018-05-14 CA CA3063827A patent/CA3063827A1/en active Pending
- 2018-05-14 LT LTEPPCT/JP2018/018572T patent/LT3626825T/lt unknown
- 2018-05-14 SM SM20240472T patent/SMT202400472T1/it unknown
- 2018-05-14 EP EP18802536.5A patent/EP3626825B1/en active Active
-
2019
- 2019-11-13 MX MX2023001685A patent/MX2023001685A/es unknown
- 2019-11-13 MX MX2023001686A patent/MX2023001686A/es unknown
- 2019-11-14 PH PH12019502545A patent/PH12019502545A1/en unknown
- 2019-11-21 CO CONC2019/0013020A patent/CO2019013020A2/es unknown
-
2020
- 2020-09-02 US US17/010,162 patent/US11077202B2/en active Active
-
2021
- 2021-01-12 JP JP2021002874A patent/JP7064629B2/ja active Active
-
2022
- 2022-04-22 JP JP2022070921A patent/JP7445699B2/ja active Active
- 2022-07-26 US US17/874,239 patent/US12233155B2/en active Active
-
2024
- 2024-02-26 JP JP2024026117A patent/JP7776555B2/ja active Active
-
2025
- 2025-01-21 US US19/033,419 patent/US20250228766A1/en active Pending
- 2025-04-23 AU AU2025202863A patent/AU2025202863A1/en active Pending
- 2025-09-22 JP JP2025157162A patent/JP2026001062A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014057687A1 (ja) * | 2012-10-11 | 2014-04-17 | 第一三共株式会社 | 抗体-薬物コンジュゲート |
| WO2016024195A1 (en) * | 2014-08-12 | 2016-02-18 | Novartis Ag | Anti-cdh6 antibody drug conjugates |
| JP6827534B2 (ja) * | 2017-05-15 | 2021-02-10 | 第一三共株式会社 | 抗cdh6抗体及び抗cdh6抗体−薬物コンジュゲート |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7064629B2 (ja) | 抗cdh6抗体及び抗cdh6抗体-薬物コンジュゲート | |
| JP7064635B2 (ja) | 抗gpr20抗体及び抗gpr20抗体-薬物コンジュゲート | |
| JP2025090684A (ja) | 化学療法抵抗性癌の治療方法における使用のための抗体-薬物コンジュゲート | |
| HK40027154B (en) | Anti-cdh6 antibody and anti-cdh6 antibody-drug conjugate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220510 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230509 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230629 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230904 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230928 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231108 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231207 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240115 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240213 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240226 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7445699 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |