WO2024218109A1 - Materials for electronic devices - Google Patents
Materials for electronic devices Download PDFInfo
- Publication number
- WO2024218109A1 WO2024218109A1 PCT/EP2024/060343 EP2024060343W WO2024218109A1 WO 2024218109 A1 WO2024218109 A1 WO 2024218109A1 EP 2024060343 W EP2024060343 W EP 2024060343W WO 2024218109 A1 WO2024218109 A1 WO 2024218109A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- aromatic
- atoms
- radicals
- formula
- compounds
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C23/00—Compounds containing at least one halogen atom bound to a ring other than a six-membered aromatic ring
- C07C23/18—Polycyclic halogenated hydrocarbons
- C07C23/20—Polycyclic halogenated hydrocarbons with condensed rings none of which is aromatic
- C07C23/46—Polycyclic halogenated hydrocarbons with condensed rings none of which is aromatic with more than three condensed rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/52—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton to carbon atoms of six-membered aromatic rings being part of condensed ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/14—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom
- C07D251/24—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom to three ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/40—Ortho- or ortho- and peri-condensed systems containing four condensed rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/52—Ortho- or ortho- and peri-condensed systems containing five condensed rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/93—Spiro compounds
- C07C2603/94—Spiro compounds containing "free" spiro atoms
Definitions
- the present invention relates to materials for use in electronic devices, in particular in organic electroluminescent devices, and to electronic devices, in particular organic electroluminescent devices containing these materials.
- Electronic devices which contain organic, organometallic and/or polymeric semiconductors are becoming increasingly important, and these are used in many commercial products for cost reasons and due to their performance. Examples include organic-based charge transport materials (e.g. triarylamine-based hole transporters) in copiers, organic or polymeric light-emitting diodes (OLEDs or PLEDs) in indicator and display devices, or organic photoreceptors in copiers.
- organic-based charge transport materials e.g. triarylamine-based hole transporters
- OLEDs or PLEDs organic or polymeric light-emitting diodes
- Organic solar cells O-SC
- organic field-effect transistors O-FET
- organic thin-film transistors O-TFT
- organic switching elements O-IC
- organic optical amplifiers O-lasers
- Electronic devices in the sense of this invention are understood to be organic electronic devices which contain organic semiconductor materials as functional materials.
- the electronic devices are electroluminescent devices such as OLEDs.
- the structure of OLEDs in which organic compounds are used as functional materials is known to the person skilled in the art from the prior art.
- OLEDs are understood to be electronic devices which have one or more layers which comprise organic compounds and emit light when a voltage is applied.
- Electronic devices in particular OLEDs, there is a great need to improve the performance data, in particular service life, efficiency and operating voltage. No satisfactory solution has yet been found for these aspects.
- Electronic devices usually comprise a cathode, an anode and at least one functional, preferably emitting layer. In addition to these layers, they can contain further layers, for example one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, exciton blocking layers, electron blocking layers and/or charge generation layers.
- the hole transport layers and electron transport layers, as well as the matrix materials of the emitting layer have a major influence on the performance data of electronic devices.
- the object of the present invention is to provide compounds which are suitable for use in an electronic device, in particular an OLED, in particular as material for electron transport layers or matrix materials, and which lead to good properties there.
- an OLED in particular as material for electron transport layers or matrix materials
- certain pentaphenanthrenes described in more detail below, solve this problem and are well suited for use in electronic devices, in particular OLEDs.
- the OLEDs in particular have a long service life, high efficiency and a lower operating voltage.
- These compounds and electronic devices, in particular organic electroluminescent devices, which contain these compounds are therefore the subject of the present invention.
- the compounds are also easier to process.
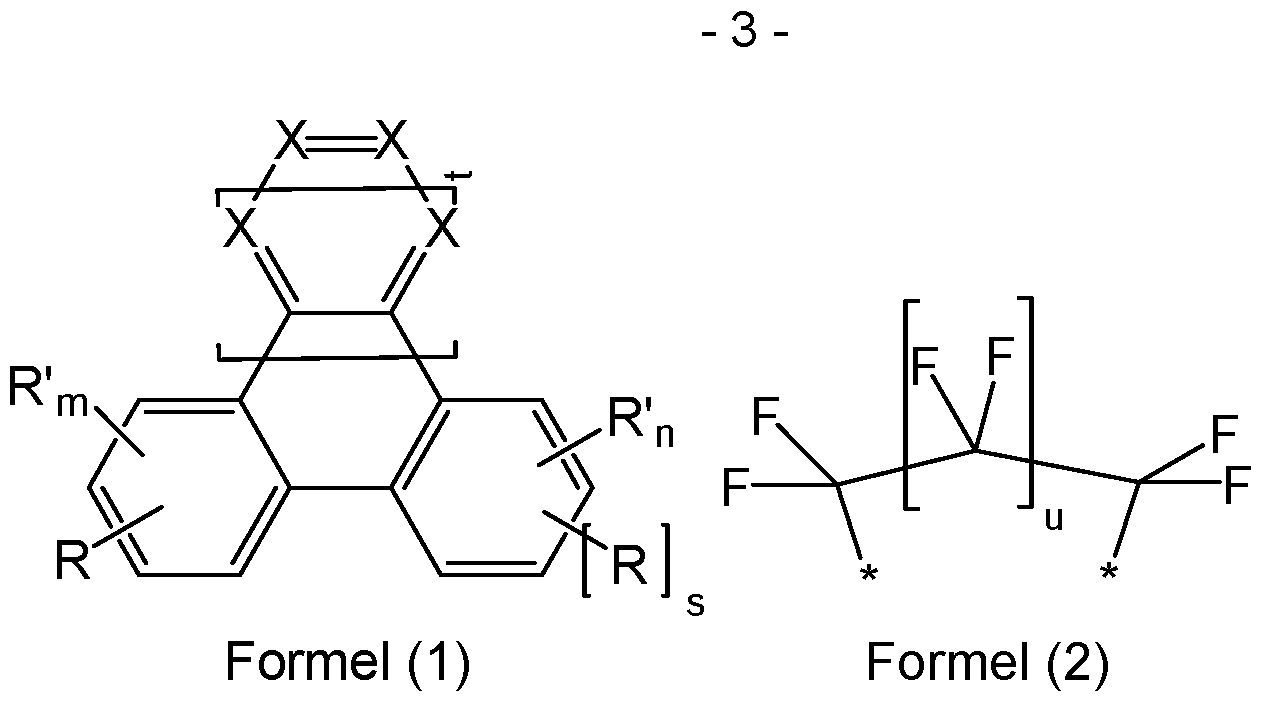
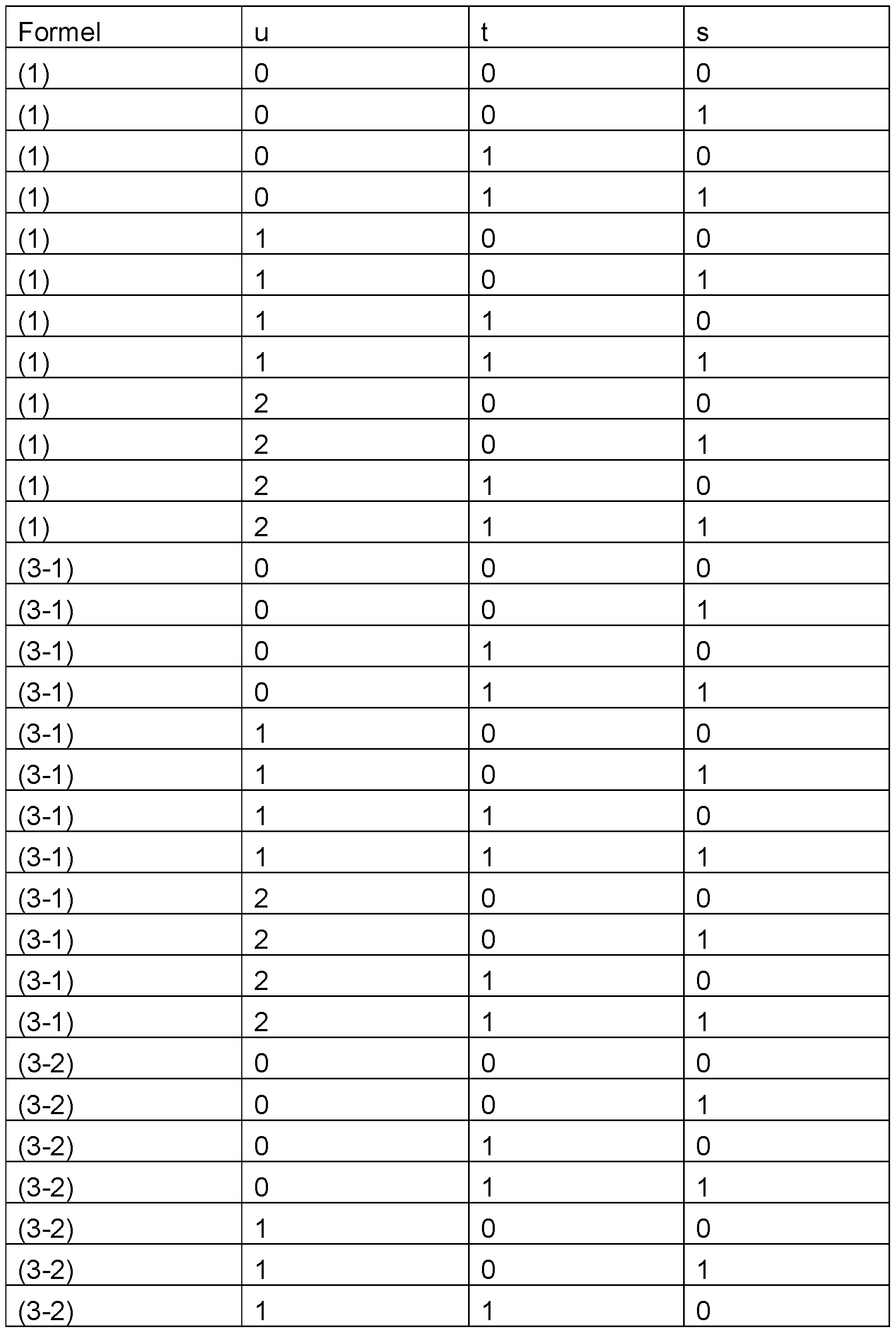
- the subject of the present invention is a compound according to formulas (1) and (2), where the following applies to the symbols used: X is the same or different on each occurrence and is CR' or N, with the proviso that a maximum of two groups X per cycle stand for N; u is 0, 1 or 2, preferably 0 or 1, particularly preferably 1; t is 0 or 1, preferably 0; m is 0, 1, 2 or 3; n is an integer value between 0 and 4-s; s is 0 or 1; R is, on each occurrence, identically or differently, an aromatic or heteroaromatic ring system having 5 to 60 aromatic ring atoms, preferably having 5 to 40 aromatic ring atoms, which may each be substituted by one or more radicals R 1 , where two radicals R bonded to different cycles or two radicals R and R' bonded to different cycles can together form an aliphatic, heteroaliphatic, aromatic or heteroaromatic ring system, which may be substituted by one or more radicals R 1 ; R' is
- An aryl group in the sense of this invention contains 6 to 40 C atoms; a heteroaryl group in the sense of this invention contains 5 to 40 C atoms and at least one heteroatom, with the proviso that the sum of C atoms and heteroatoms is at least 5.
- the heteroatoms are preferably selected from N, O and/or S.
- An aryl group or heteroaryl group is understood to be either a simple aromatic cycle, i.e.
- Aromatics linked to one another by a single bond, such as biphenyl, are not referred to as aryl or heteroaryl groups, but as aromatic ring systems.
- An aromatic ring system in the sense of this invention contains 6 to 60 C atoms, preferably 6 to 40 C atoms in the ring system.
- a heteroaromatic ring system in the sense of this invention contains 1 to 60 C atoms, preferably 1 to 40 C atoms and at least one heteroatom in the ring system, with the proviso that the sum of C atoms and heteroatoms is at least 5.
- the heteroatoms are preferably selected from N, O and/or S.
- An aromatic or heteroaromatic ring system in the sense of this invention is to be understood as a system which does not necessarily only contain aryl or heteroaryl groups, but in which several aryl or heteroaryl groups can also be connected by a non-aromatic unit (preferably less than 10% of the atoms other than H), such as a C, N or O atom or carbonyl group.
- This also includes systems in which two or more aryl or heteroaryl groups are directly linked to one another, such as biphenyl, terphenyl, bipyridine or phenylpyridine.
- systems such as fluorene, 9,9'-spirobifluorene, 9,9-diarylfluorene, triarylamine, diaryl ether, stilbene, etc. are also to be understood as aromatic ring systems in the sense of this invention, as are systems in which two or more aryl groups are linked, for example, by a linear or cyclic alkyl group or by a silyl group.
- Preferred aromatic or heteroaromatic ring systems are simple aryl or heteroaryl groups and groups in which two or more aryl or heteroaryl groups are directly linked to one another, for example biphenyl, terphenyl, quaterphenyl or bipyridine, and also fluorene or spirobifluorene.
- An electron-rich heteroaromatic ring system is characterized by the fact that it is a heteroaromatic ring system that does not contain any electron-poor heteroaryl groups.
- An electron-poor heteroaryl group is a six-membered ring heteroaryl group with at least one nitrogen atom or a five-membered ring heteroaryl group with at least two heteroatoms, one of which is a nitrogen atom and the other oxygen, sulfur or a substituted nitrogen atom, where further aryl or heteroaryl groups can be condensed onto these groups.
- electron-rich Heteroaryl groups Five-membered ring heteroaryl groups with exactly one hetero atom, selected from oxygen, sulfur or substituted nitrogen, to which further aryl groups and/or further electron-rich five-membered ring heteroaryl groups can be condensed.
- electron-rich heteroaryl groups examples include pyrrole, furan, thiophene, indole, benzofuran, benzothiophene, carbazole, dibenzofuran, dibenzothiophene or indenocarbazole.
- An electron-rich heteroaryl group is also referred to as an electron-rich heteroaromatic radical.
- An electron-poor heteroaromatic ring system is characterized in that it contains at least one electron-poor heteroaryl group, and particularly preferably no electron-rich heteroaryl groups.
- alkyl group is used as a generic term for both linear or branched alkyl groups and for cyclic alkyl groups.
- alkenyl group or alkynyl group are used as generic terms for both linear or branched alkenyl or alkynyl groups and for cyclic alkenyl or alkynyl groups.
- a cyclic alkyl, alkoxy or thioalkoxy group in the sense of this invention is understood to mean a monocyclic, a bicyclic or a polycyclic group.
- an aliphatic hydrocarbon radical or an alkyl group or an alkenyl or alkynyl group which can contain 1 to 40 C atoms and in which individual H atoms or CH2 groups can also be substituted by the abovementioned groups, preferably the radicals methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, s-butyl, t-butyl, 2-methylbutyl, n-pentyl, s-pentyl, t-pentyl, 2-pentyl, neo-pentyl, cyclopentyl, n-hexyl, s-hexyl, t-hexyl, 2-hexyl, 3-hexyl, neo-hexyl, cyclohexyl, 1-methylcyclopentyl, 2-methylpentyl, n-hepty
- alkoxy group OR 1 with 1 to 40 carbon atoms, preference is given to methoxy, trifluoromethoxy, ethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, n-pentoxy, s-pentoxy, 2-methylbutoxy, n-hexoxy, cyclohexyloxy, n-heptoxy, cycloheptyloxy, n-Octyloxy, cyclooctyloxy, 2-ethylhexyloxy, pentafluoroethoxy and 2,2,2-trifluoroethoxy are understood.
- a thioalkyl group SR 1 with 1 to 40 carbon atoms includes, in particular, methylthio, ethylthio, n-propylthio, i-propylthio, n-butylthio, i-butylthio, s-butylthio, t-butylthio, n-pentylthio, s-pentylthio, n-hexylthio, cyclohexylthio, n-heptylthio, cycloheptylthio, n-octylthio, cyclooctylthio, 2-ethylhexylthio, trifluoromethylthio, pentafluoroethylthio, 2,2,2-trifluoroethylthio, ethenylthio, propenylthio, butenylthio, pentenylthio, cyclopenten
- alkyl, alkoxy or thioalkyl groups according to the present invention can be straight-chain, branched or cyclic, where one or more non-adjacent CH2 groups can be replaced by the above-mentioned groups; furthermore, one or more H atoms can be replaced by D, F, Cl, Br, I, CN or NO2, preferably F, Cl or CN, particularly preferably F or CN.
- An aromatic or heteroaromatic ring system with 5 - 60 aromatic ring atoms, preferably 5 - 40 aromatic ring atoms, which can also be substituted with the above-mentioned radicals or a Hydrocarbon residue which can be substituted and which can be linked to the aromatic or heteroaromatic via any position are understood to mean in particular groups which are derived from benzene, naphthalene, anthracene, benzanthracene, phenanthrene, pyrene, chrysene, perylene, fluoranthene, naphthacene, pentacene, benzopyrene, biphenyl, biphenylene, terphenyl, triphenylene, fluorene, spirobifluorene, dihydrophenanthrene, dihydropyrene, tetrahydropyrene, cis- or trans- indenofluorene, cis- or trans- indenocarbazole, c
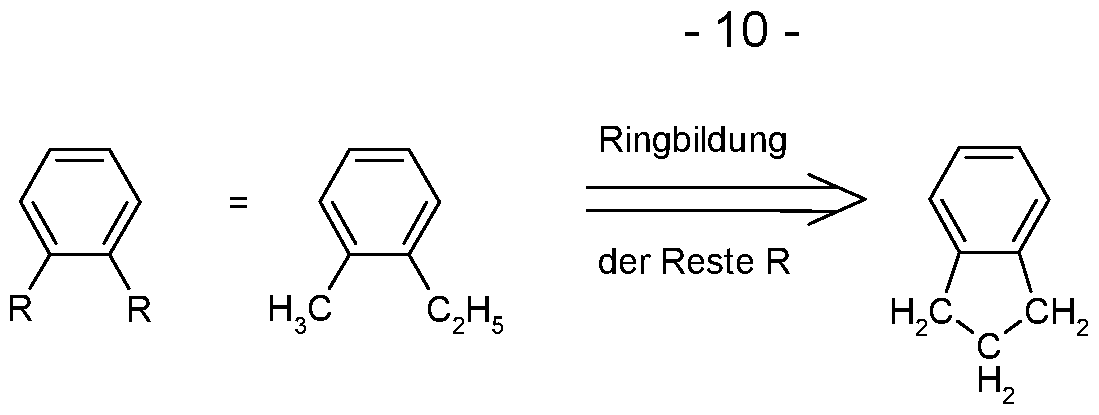
- the phrase that two or more residues can form a ring system with one another is to be understood to mean, among other things, that the two residues are linked to one another by a chemical bond with the formal elimination of two hydrogen atoms. This is illustrated by the following scheme: .
- the above formulation should also be understood to mean that if one of the two residues represents hydrogen, the second residue binds to the position to which the hydrogen atom was bound, forming a ring. This is illustrated by the following scheme: .
- R and R' are on the same ring if they comprise an aromatic ring system which consists of two aryl groups with 6 C atoms which are connected to one another via a single bond and a monoatomic bridge, this bridge is not an aliphatic carbon atom, unless the carbon is a spiro atom. Therefore, R and/or R', if they comprise an aromatic ring system, is not a fluorene, but can be spirobifluorene.
- R and/or R' comprise an aromatic or heteroaromatic ring system which consists of two aryl groups with 6 C atoms which are connected to one another via a single bond and a monoatomic bridge, this bridge is not an aliphatic carbon atom, unless the carbon is a spiro atom. Therefore, R and/or R', if they comprise an aromatic ring system, is not a fluorene, but can be a spirobifluorene.
- R and/or R' comprise an aromatic or heteroaromatic ring system consisting of two aryl groups having 6 C atoms which are connected via a Single bond and a monoatomic bridge are connected to each other, this bridge selected from a B, N, O, or S atom.
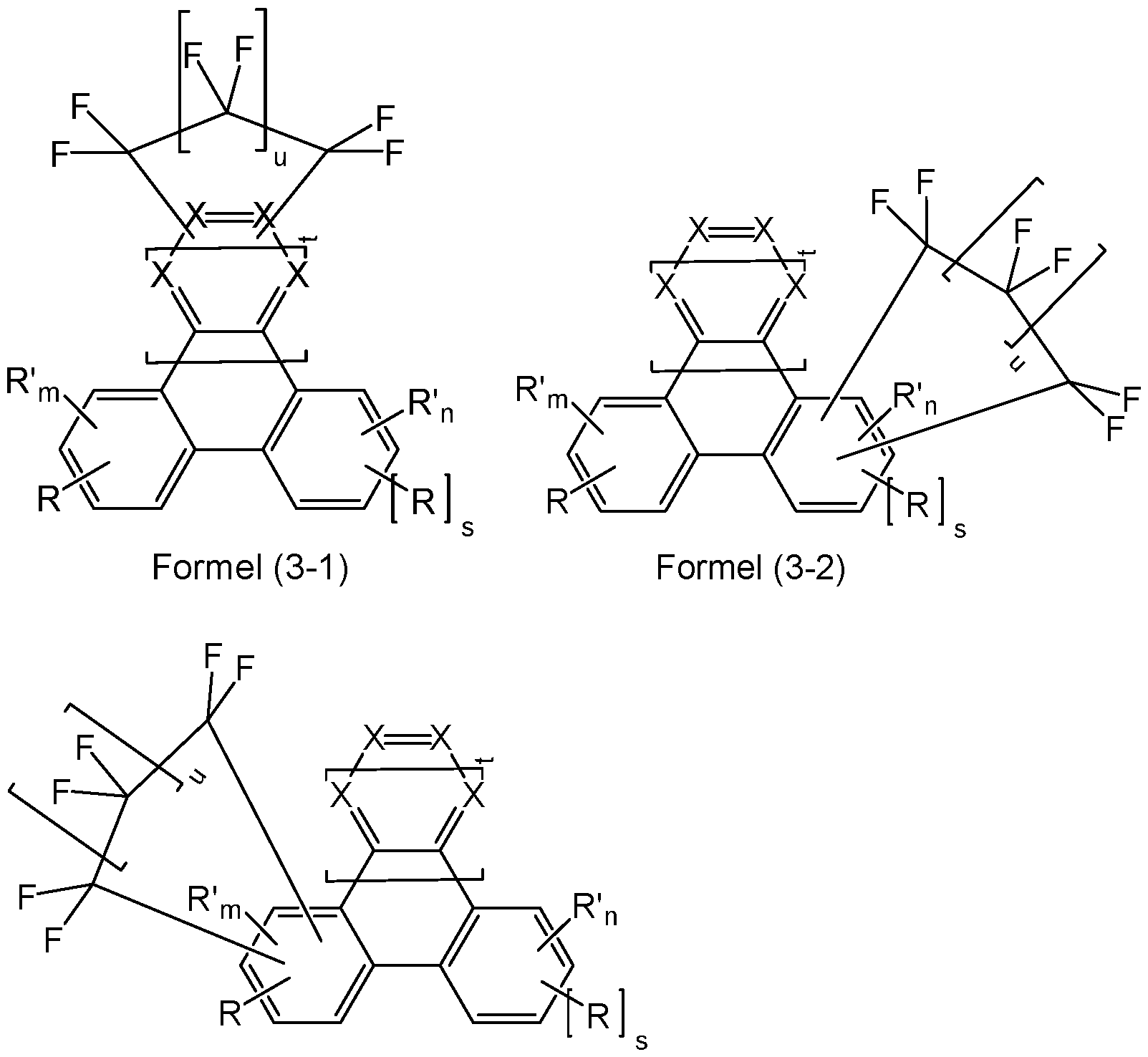
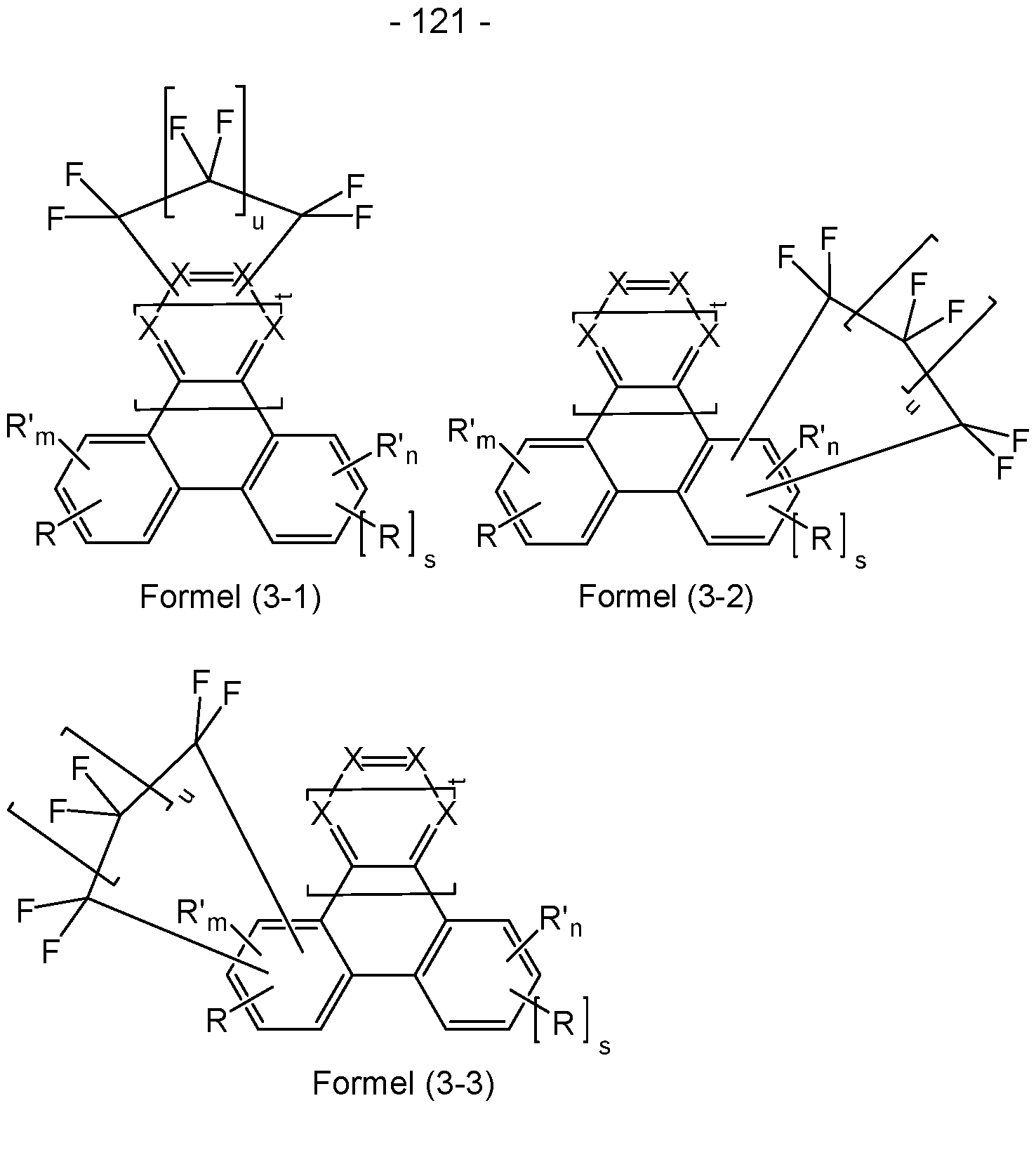
- formulas (3-1), (3-2) or (3-3) where the symbols used have the meanings given above for formula (1), with the additional rule that in formulas (3-2) and (3-3) two preferably adjacent R' stand for the structure -CF2-(CF2)u-CF2- and m in formula (3-2) stands for 2 or 3 and n in formula (3-3) stands for an integer value between 2 and 3-s.
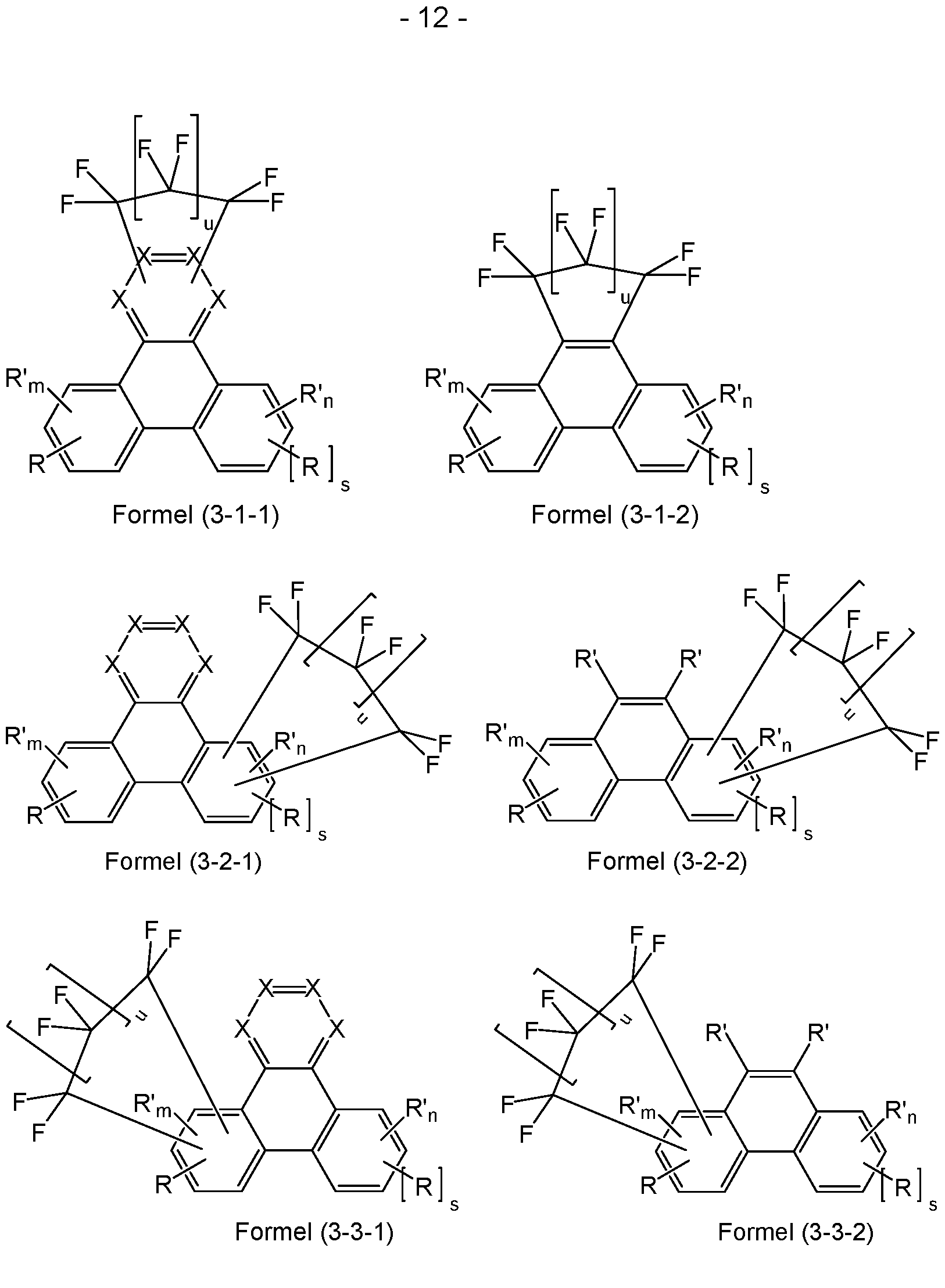
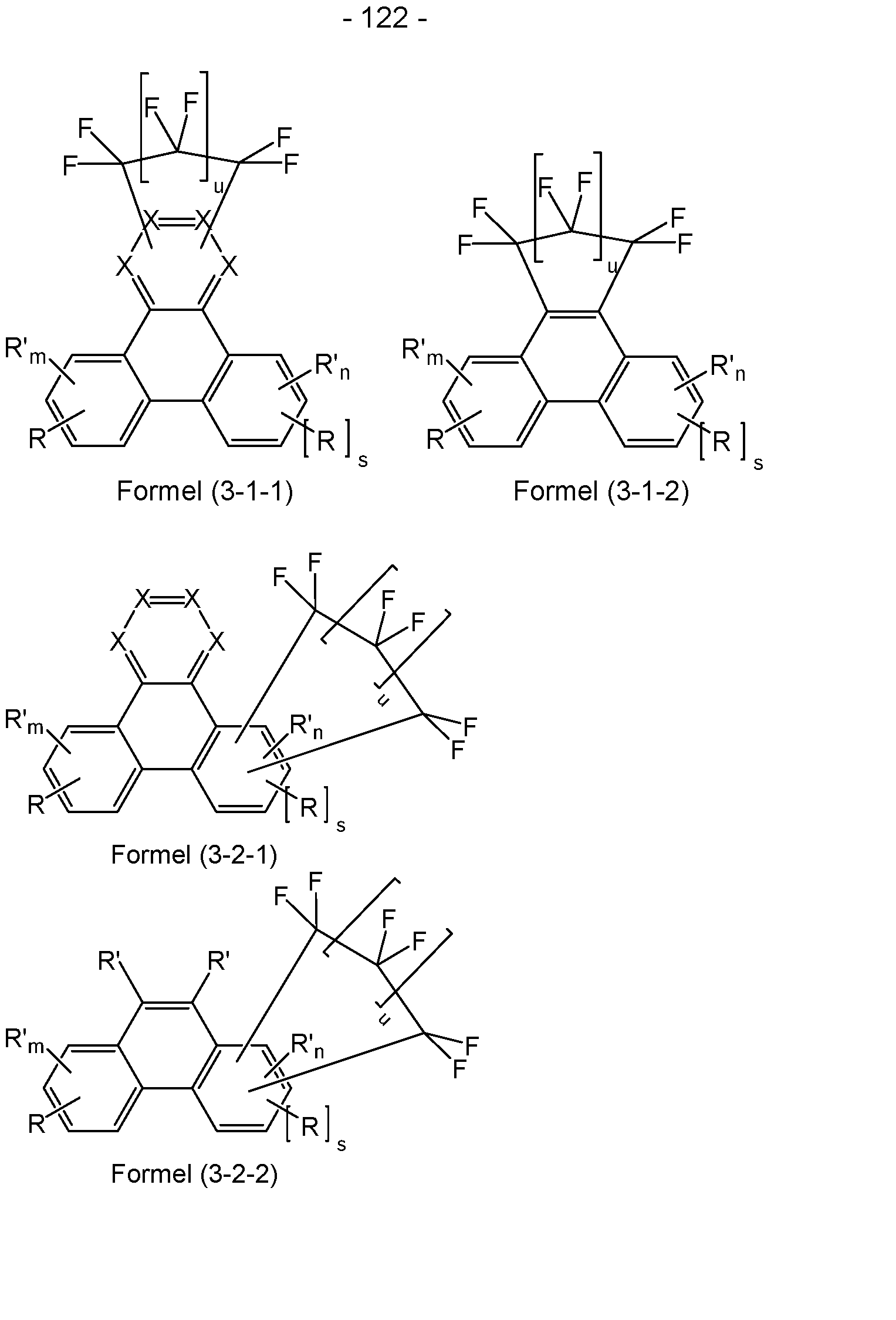
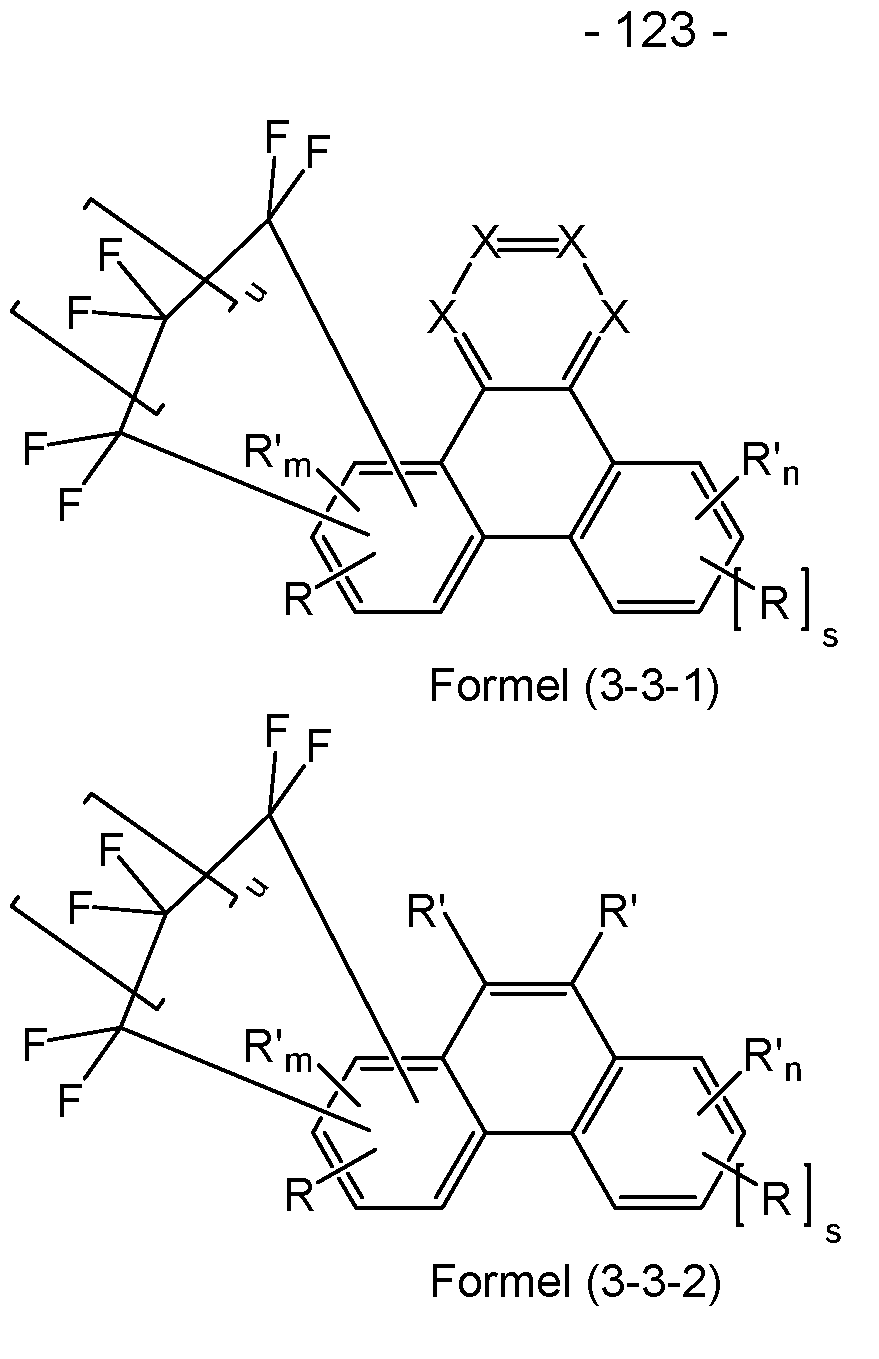
- formulas (3-1), (3-2) and (3-3) are shown by the following formulas (3-1-1), (3-1-2), (3-2-1), (3-2-2), (3-3-1) or (3-3-2):
- Formula (3 Formula (3-3-2) where the symbols used have the meanings given above for formula (1) and where it additionally applies that in the formulas (3- 2-1), (3-2-2), (3-3-1) and (3-3-2) two preferably adjacent R' stand for the structure -CF2-(CF2) u -CF2- and m in formula (3-2-1) and (3-2-2) stands for 2 or 3 and n in formula (3-3-1) and (3-3-2) stands for an integer value between 2 and 3-s.
- a preferred embodiment of the compound of formula (3-1-1) is a compound of formula (3-1-1a): -1-1a) where the S used symbols have the meanings given above for formula (3-1-1).
- X is CR'.
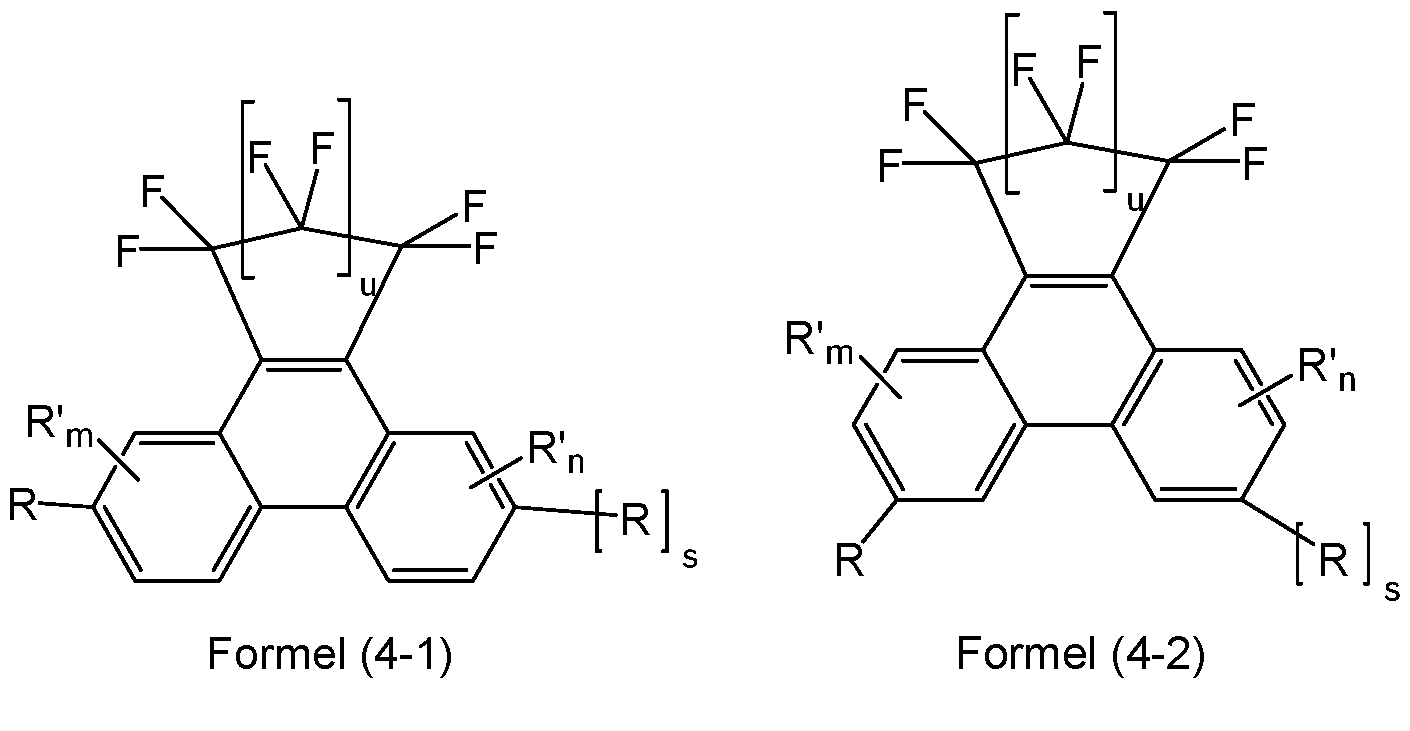
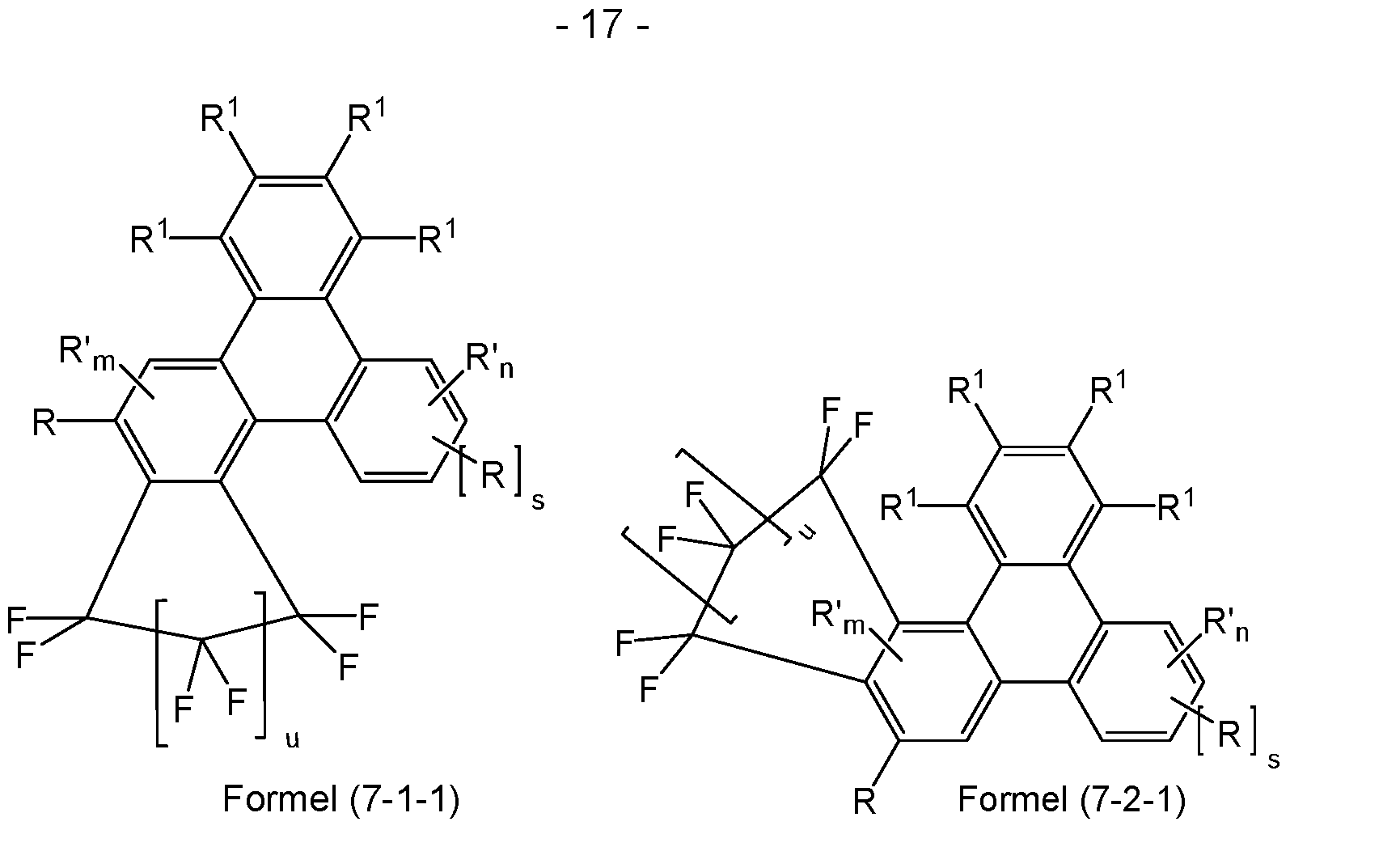
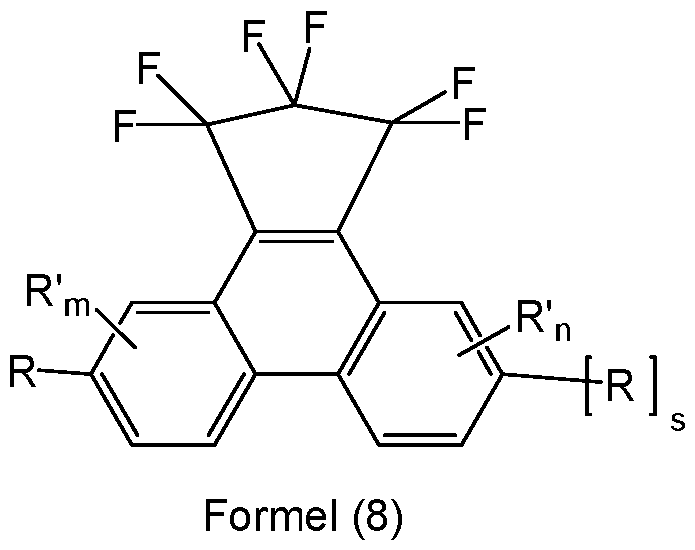
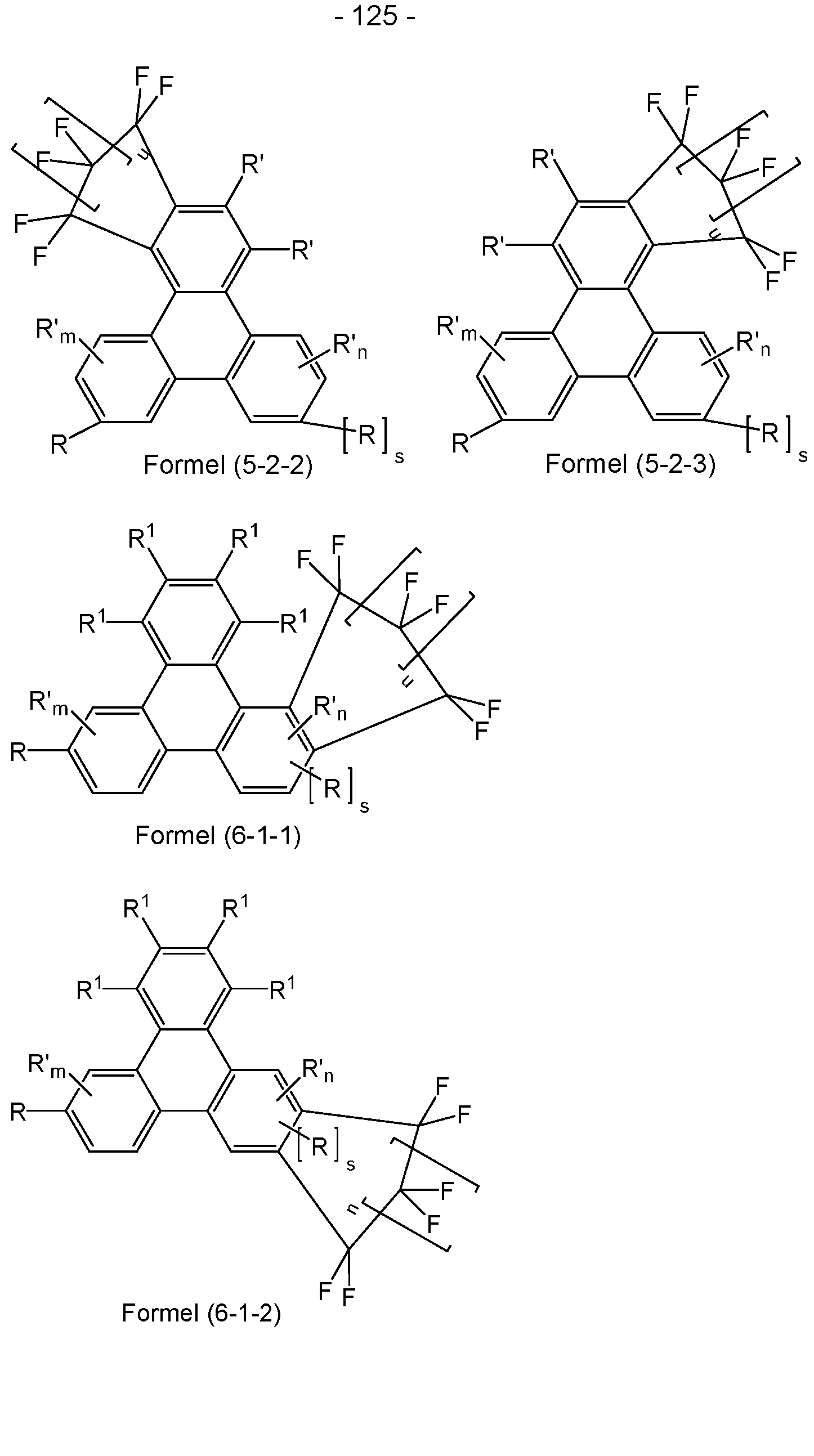
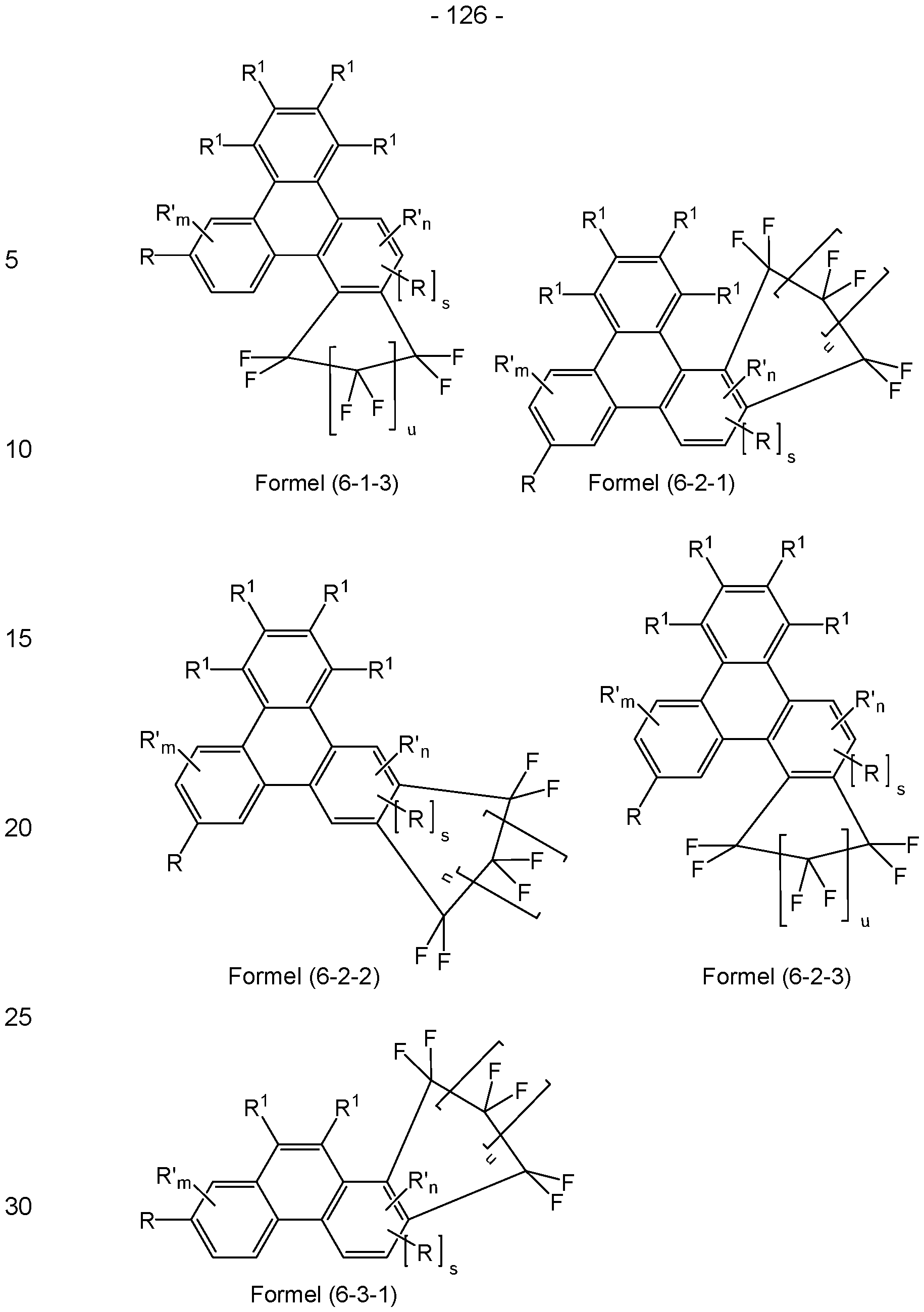
- Further preferred embodiments are shown by the following formulas (4-1), (4-2), (5-1-1), (5-1-2), (5-1-3), (5-2-1), (5-2-2), (5-2-3), (6-1-1), (6-1-2), (6-1-3), (6-2-1), (6-2-2), (6-2-3), (6-3-1), (6-3-2), (6-3-3), (6-4-1), (6-4-2), (6-4-3), (7-1-1) or (7-2-1):
- R' is selected on each occurrence, identically or differently, from the group consisting of H, D, F, CN, OR 1 , a straight-chain alkyl group having 1 to 10 C atoms or an alkenyl group having 2 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, where the alkyl or alkenyl group can each be substituted by one or more radicals R 1 , but is preferably unsubstituted, and where one or more non-adjacent CH2 groups can be replaced by O, or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, which can each be substituted by one or more radicals R 1 ; two radicals R' or two each R and R' radicals bonded to different rings also form an aliphatic, aromatic or heteroaromatic ring system with one another.
- R' is particularly preferably selected, identically or differently on each occurrence, from the group consisting of H, F, CN, a straight-chain alkyl group having 1 to 6 C atoms, in particular having 1, 2, 3 or 4 C atoms, or a branched or cyclic alkyl group having 3 to 6 C atoms, where the alkyl group can be substituted in each case by one or more R 1 radicals, but is preferably unsubstituted, or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, which can be substituted in each case by one or more R 1 radicals, preferably non-aromatic R 1 radicals.
- R' is very particularly preferably selected on each occurrence, identically or differently, from the group consisting of H, D or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , preferably non-aromatic radicals R 2 .
- R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 ; two radicals R or two radicals R and R' each bound to different cycles can also form an aliphatic, aromatic or heteroaromatic ring system with one another.
- R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 24, preferably 6 to 18 and particularly preferably 6 to 13 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 , preferably non-aromatic radicals R 1 .
- R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 24, preferably 6 to 18 and particularly preferably 6 to 13 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , preferably non-aromatic radicals R 2 .
- two radicals R and R' which are bonded to different cycles do not form an aliphatic, aromatic or heteroaromatic ring system with one another.
- two radicals R, or R and R' which are bonded to different cycles do not form an aliphatic, aromatic or heteroaromatic ring system with one another.
- Suitable aromatic or heteroaromatic ring systems R or R' are selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorene, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorene, which can be linked via the 1-, 2-, 3- or 4-position, naphthalene, which can be linked via the 1- or 2-position, indole, benzofuran, benzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, indenocarbazole, indolocarbazole
- R is a heteroaryl group, in particular triazine, pyrimidine or quinazoline
- aromatic or heteroaromatic radicals R 1 on this heteroaryl group can also be preferred.
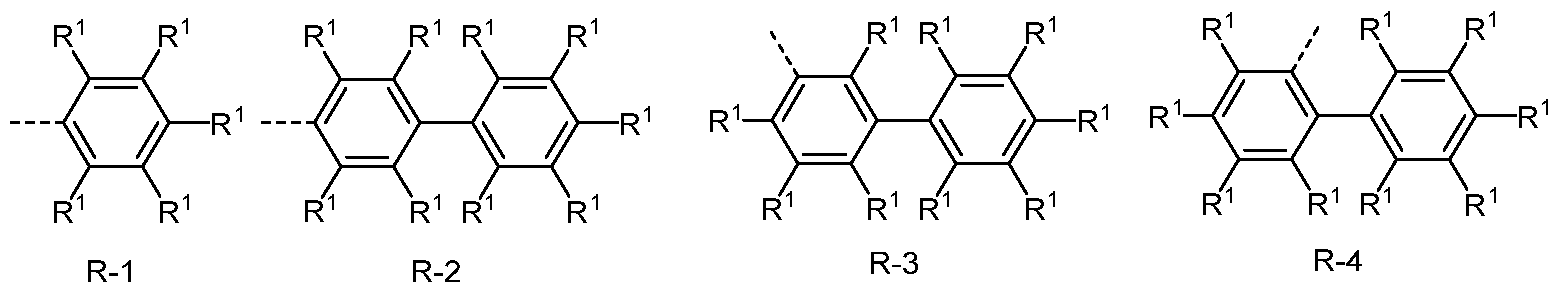
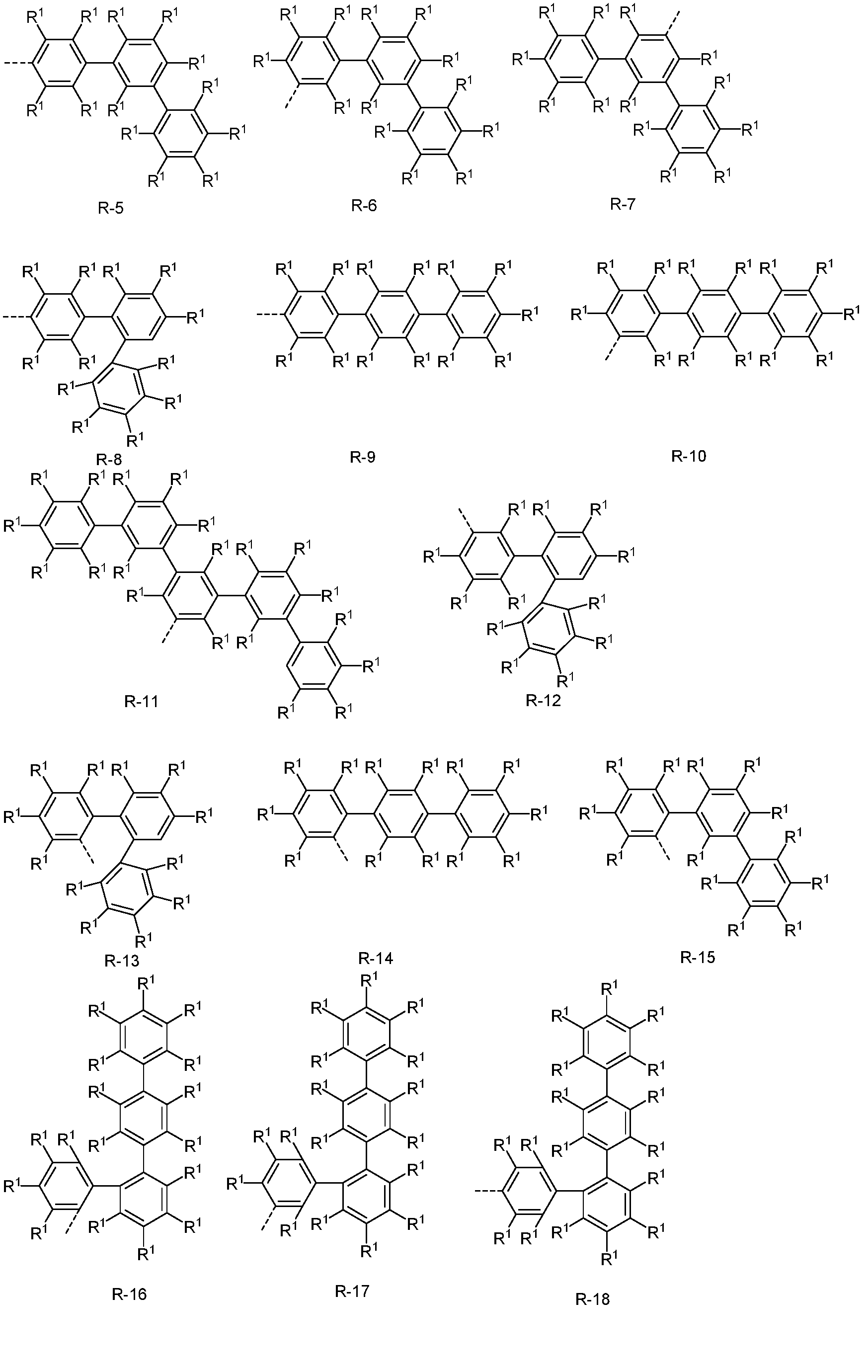
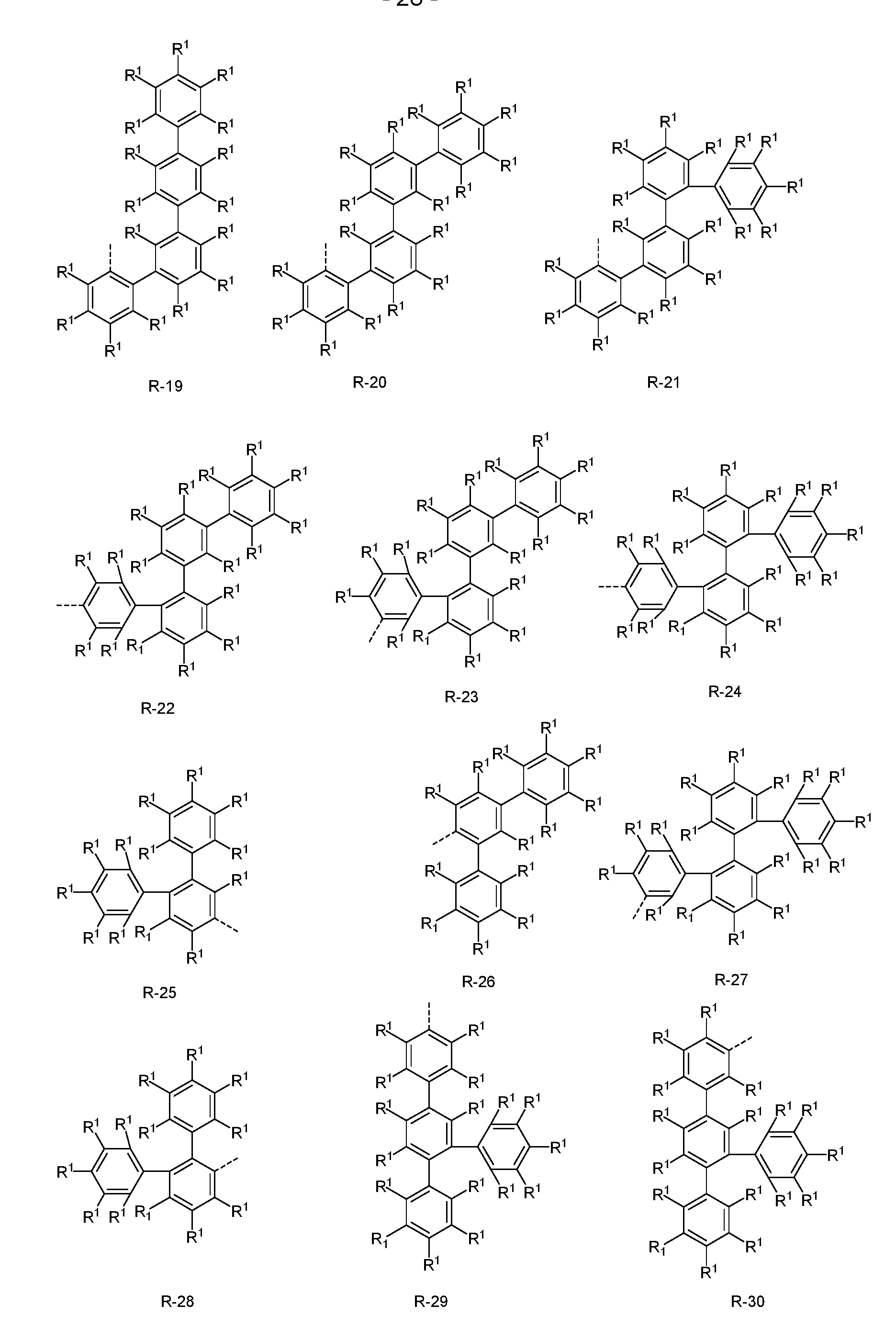
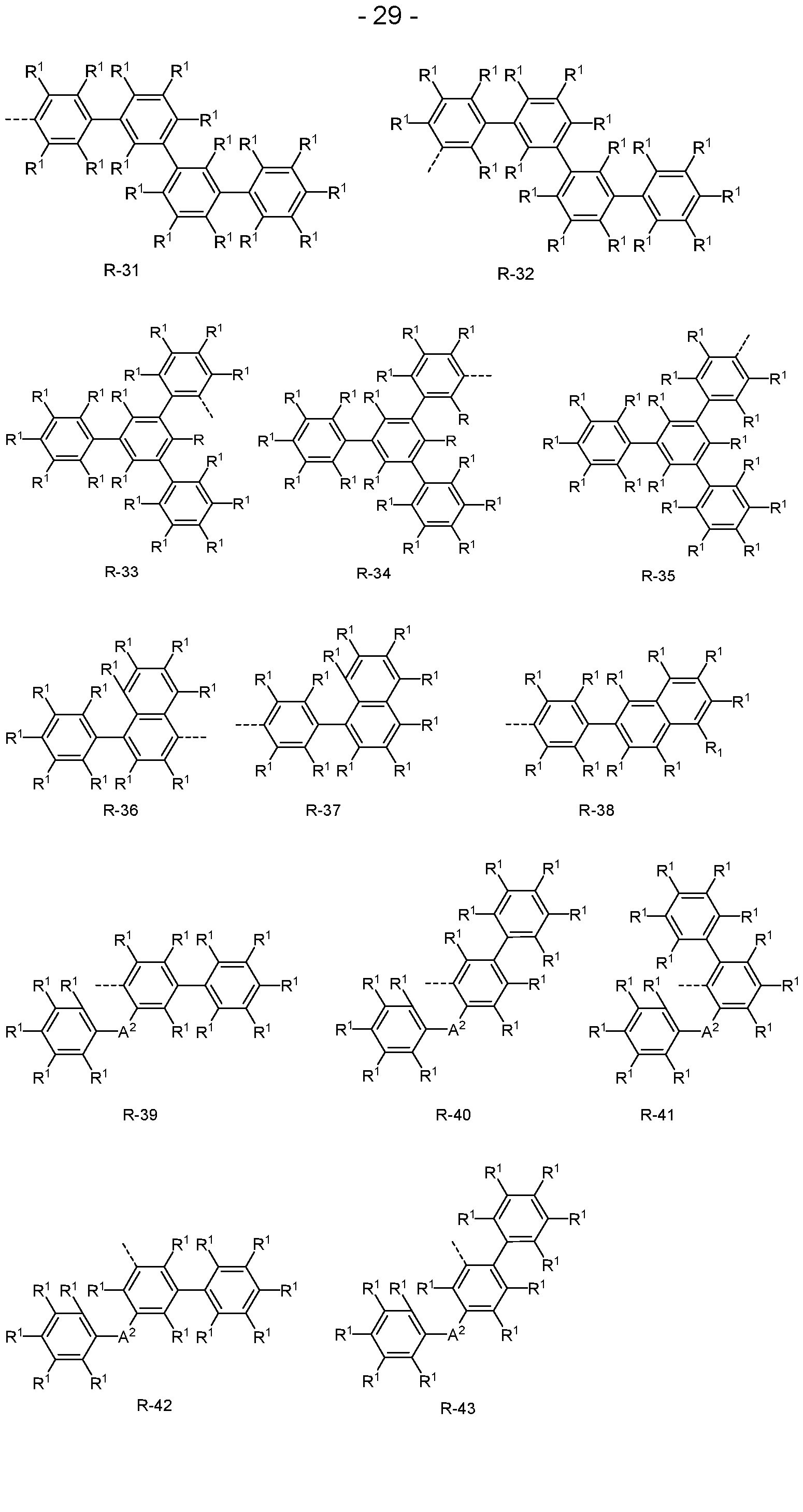
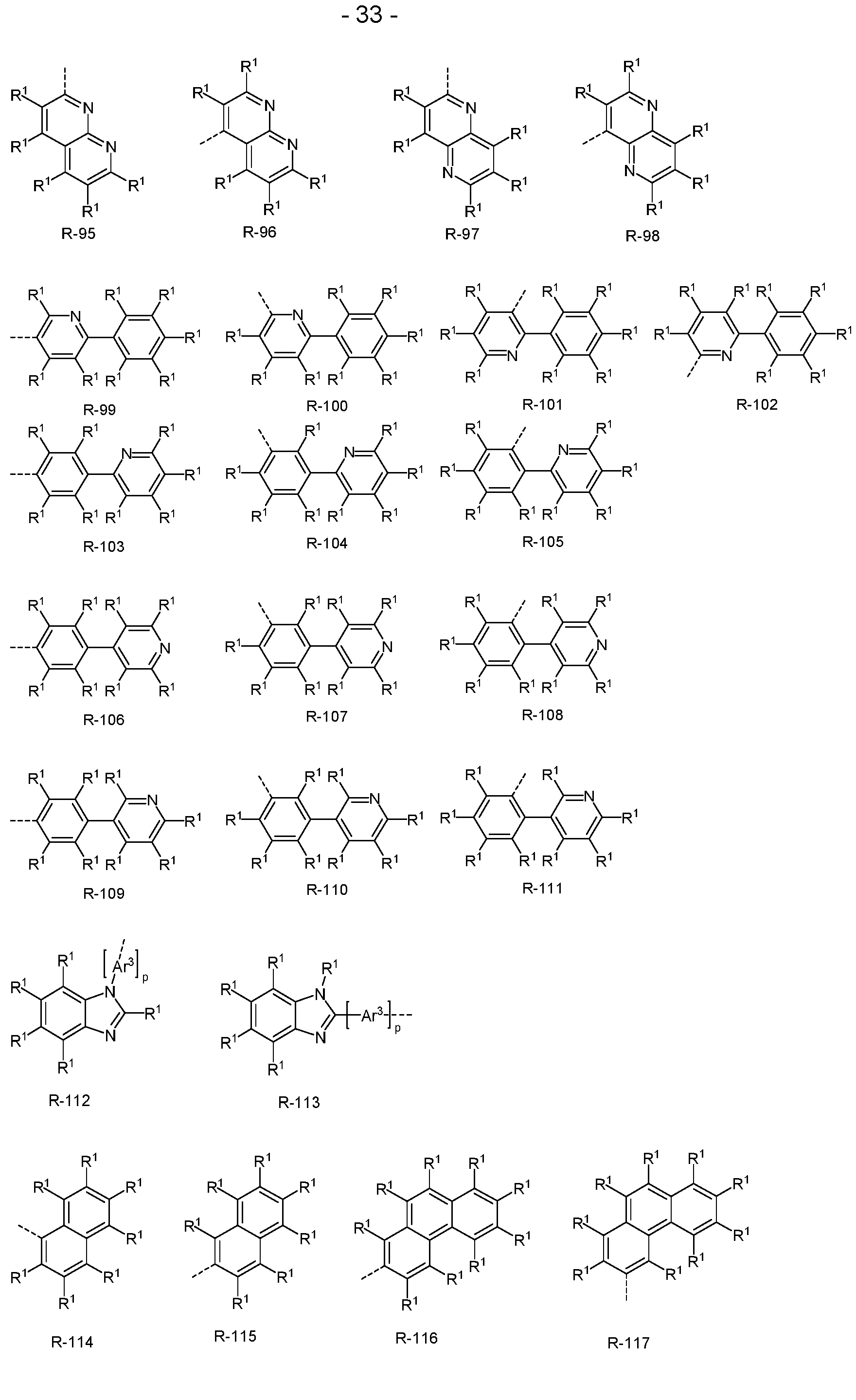
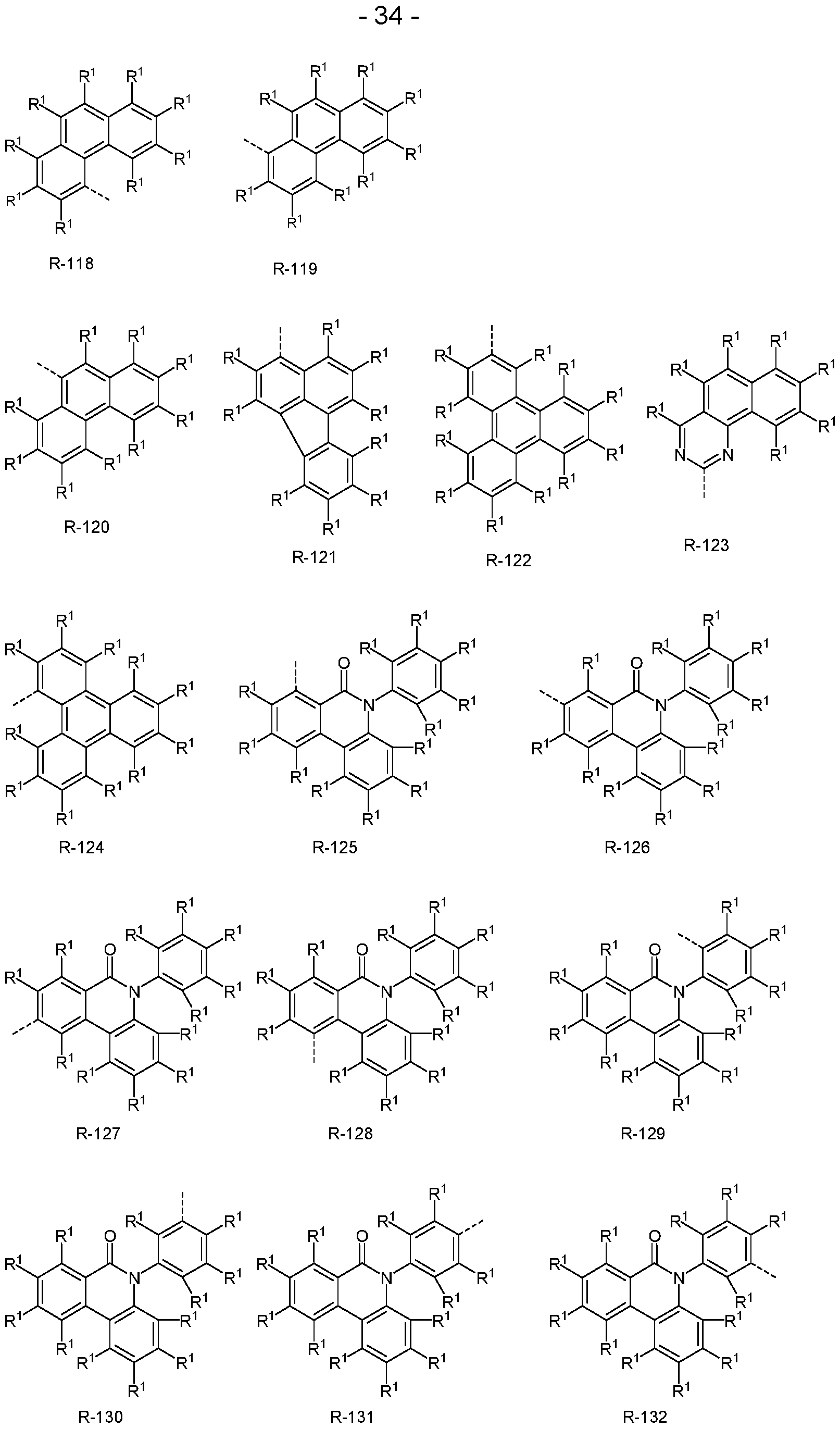
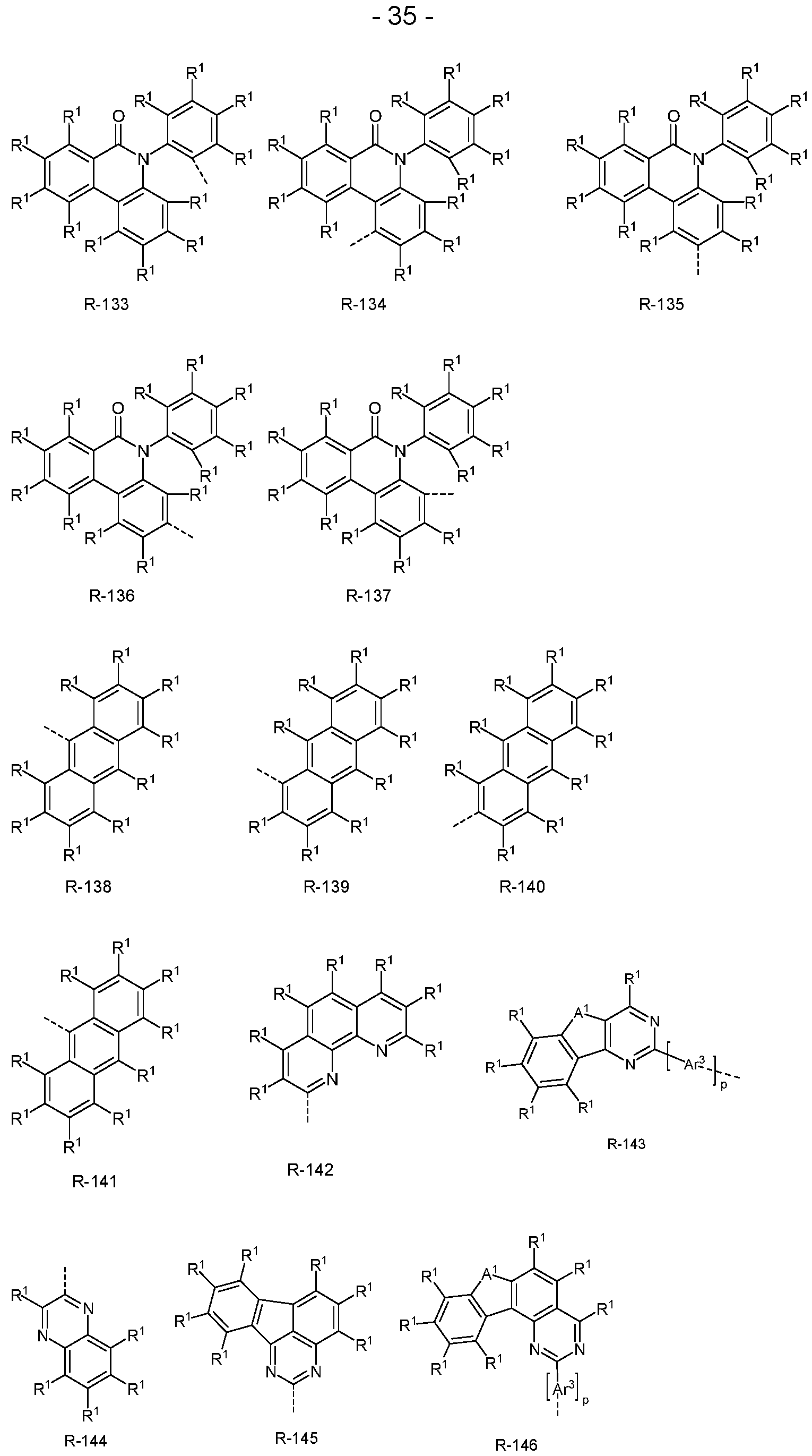
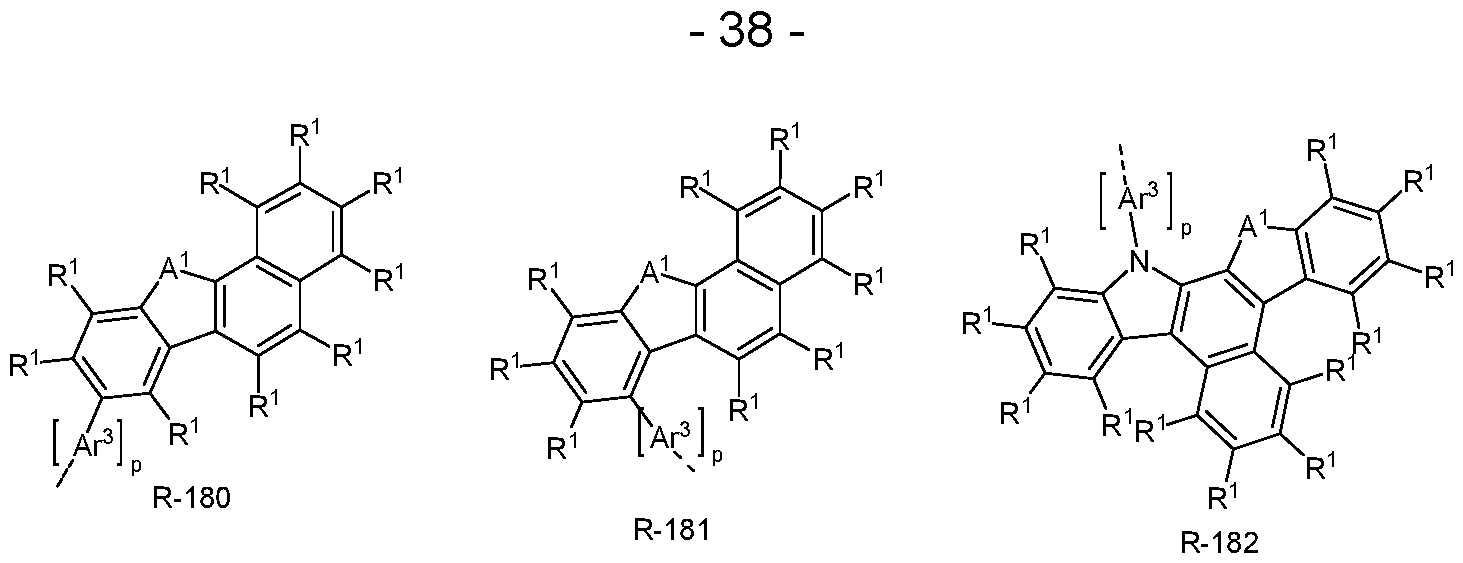
- the groups R or R', if they represent an aromatic or heteroaromatic ring system, are preferably selected from the groups of the following formulas R-1 to R-182,
- R 1 has the meanings given above, the dashed bond represents the bond to formula (1) and the following also applies:
- Ar 3 is, identically or differently on each occurrence, a divalent aromatic or heteroaromatic ring system having 6 to 18 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 ;
- a 1 is, identically or differently on each occurrence, BR 1 , C(R 1 ) 2 , NR 1 , O or S, where A 1 in the formulas R-45, R-46, R-47, R-48 stands for BR 1 , NR 1 , O or S, preferably C(R 1 ) 2 , NR 1 , O or S, where A 1 in the formulas R-45, R-46, R-47, R-48 stands for NR 1 , O or S;
- a 2 is, identically or differently on each occurrence, C(R 1 ) 2 , NR 1 , O or S;
- p is 0 or 1, where
- Ar 3 comprises bivalent aromatic or heteroaromatic ring systems based on the groups of R-1 to R-182, where p is 0 and the dashed bond and an R 1 represent the bond to the aromatic or heteroaromatic group after R-1 to R-182. If the above-mentioned groups R-1 to R-182 have several groups A 1 for R, all combinations from the definition of A 1 are possible. Preferred embodiments are then those in which one group A 1 represents C(R 1 ) 2 , NR 1 , O or S and the other group A 1 represents C(R 1 ) 2 or in which both groups A 1 represent S or O or in which both groups A 1 represent O or S.
- the substituent R 1 which is bonded to the nitrogen atom preferably represents an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 2 .
- this substituent R 1 is the same or different on each occurrence and represents an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, preferably having 6 to 12 aromatic ring atoms, and which in each case may also be substituted by one or more radicals R 2 .
- phenyl, biphenyl, terphenyl and quaterphenyl with linkage patterns as listed above for R-1 to R-35 where these structures may be substituted by one or more radicals R 1 , but are preferably unsubstituted.
- a 1 is C(R 1 ) 2
- the substituents R 1 which are bonded to this carbon atom are preferably identical or different on each occurrence and represent a linear alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms or an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 2 .
- R 1 is very particularly preferably a methyl group or a phenyl group.
- the radicals R 1 can also form a ring system with one another, resulting in a spiro system.
- R' is selected on each occurrence, identically or differently, from the group consisting of D, F, CN, OR 1 or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 .
- R' is particularly preferably selected on each occurrence, identically or differently, from the group consisting of D, F, CN or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, particularly preferably having 6 to 12 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 , preferably non-aromatic radicals R 1 .
- Suitable aromatic or heteroaromatic ring systems R' are selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorene, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorene, which can be linked via the 1-, 2-, 3- or 4-position, naphthalene, which can be linked via the 1- or 2-position, indole, benzofuran, benzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, indenocarbazole, indolocarbazole,
- R' is a heteroaryl group, in particular triazine, pyrimidine or quinazoline
- aromatic or heteroaromatic radicals R 1 on this heteroaryl group can also be preferred.
- the groups R', if they represent an aromatic or heteroaromatic ring system, are preferably selected from the groups of the above formulas R-1 to R-182, particularly preferably selected from the groups of the above formulas R-1 to R-182, where A 1 is C(R 1 ) 2 , NR 1 , O or S.
- R' is the same or different on each occurrence and is selected from the group consisting of H, D, F, CN, N(R 2 ) 2 , OR 2 , a straight-chain alkyl group having 1 to 10 C atoms.
- R 1 is the same or different on each occurrence and is selected from the group consisting of H, D, F, CN, N(R 2 ) 2 , OR 2 , a straight-chain alkyl group having 1 to 10 C atoms or an alkenyl group having 2 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, where the alkyl or alkenyl group can each be substituted by one or more radicals R 2 and where one or more non-adjacent CH2 groups can be replaced by O, or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, which can each be substituted by one or more radicals R 2 ; two or more radicals R 1 can form an aliphatic ring system with one another.
- R 1 is the same or different on each occurrence and is selected from the group consisting of H, a straight-chain alkyl group having 1 to 6 C atoms, in particular having 1, 2, 3 or 4 C atoms, or a branched or cyclic alkyl group having 3 to 6 C atoms, where the alkyl group may be substituted by one or more radicals R 2 , but is preferably unsubstituted, or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , but is preferably unsubstituted.
- R 2 is the same or different on each occurrence and is H, F, an alkyl group having 1 to 4 C atoms or an aryl group having 6 to 10 C atoms, which may be substituted by an alkyl group having 1 to 4 C atoms, but is preferably unsubstituted.
- all radicals R 1 , insofar as they represent an aromatic or heteroaromatic ring system, or R 2 , insofar as they represent aromatic or heteroaromatic groups are selected from the groups R-1 to R-182, which are then each substituted accordingly with R 2 or the groups mentioned under R 2 .
- all aromatic or heteroaromatic groups of the radicals R, R', R 1 or R 2 are selected from the corresponding groups R-1 to R-182, preferably selected from the groups R-1 to R-182, where A 1 stands for O, S, NR 1 or C(R 1 ) 2 or the corresponding radicals NR 2 , or C(R 2 ) 2 or NR 3 , or C(R 3 ) 2 .
- the radicals R and/or R' do not form any further aromatic or heteroaromatic groups fused to the basic structure of formula (1).
- R is the same or different on each occurrence and is a group selected from the groups R-1 to R-182 and R 1 in these groups is H, D, F or CN.
- R' is the same or different on each occurrence and is H, D, F or CN, preferably H or D, in all cycles of the compound of formula (1).
- the invention also relates to an oligomer, polymer or dendrimer containing one or more compounds according to formula (1) or the preferred embodiments, where the bond(s) to the oligomer, polymer or dendrimer can be made at any position in formula (1).
- the compound according to the invention is preferably not part of a polymer, oligomer or copolymer.
- the alkyl groups in compounds according to the invention which are processed by vacuum evaporation preferably have no more than five C atoms, particularly preferably no more than 4 C atoms, very particularly preferably no more than 1 C atom.
- compounds which are substituted with alkyl groups, in particular branched alkyl groups, with up to 10 C atoms or which are substituted with oligoarylene groups, for example ortho-, meta-, para- or branched terphenyl or quaterphenyl groups are also suitable.
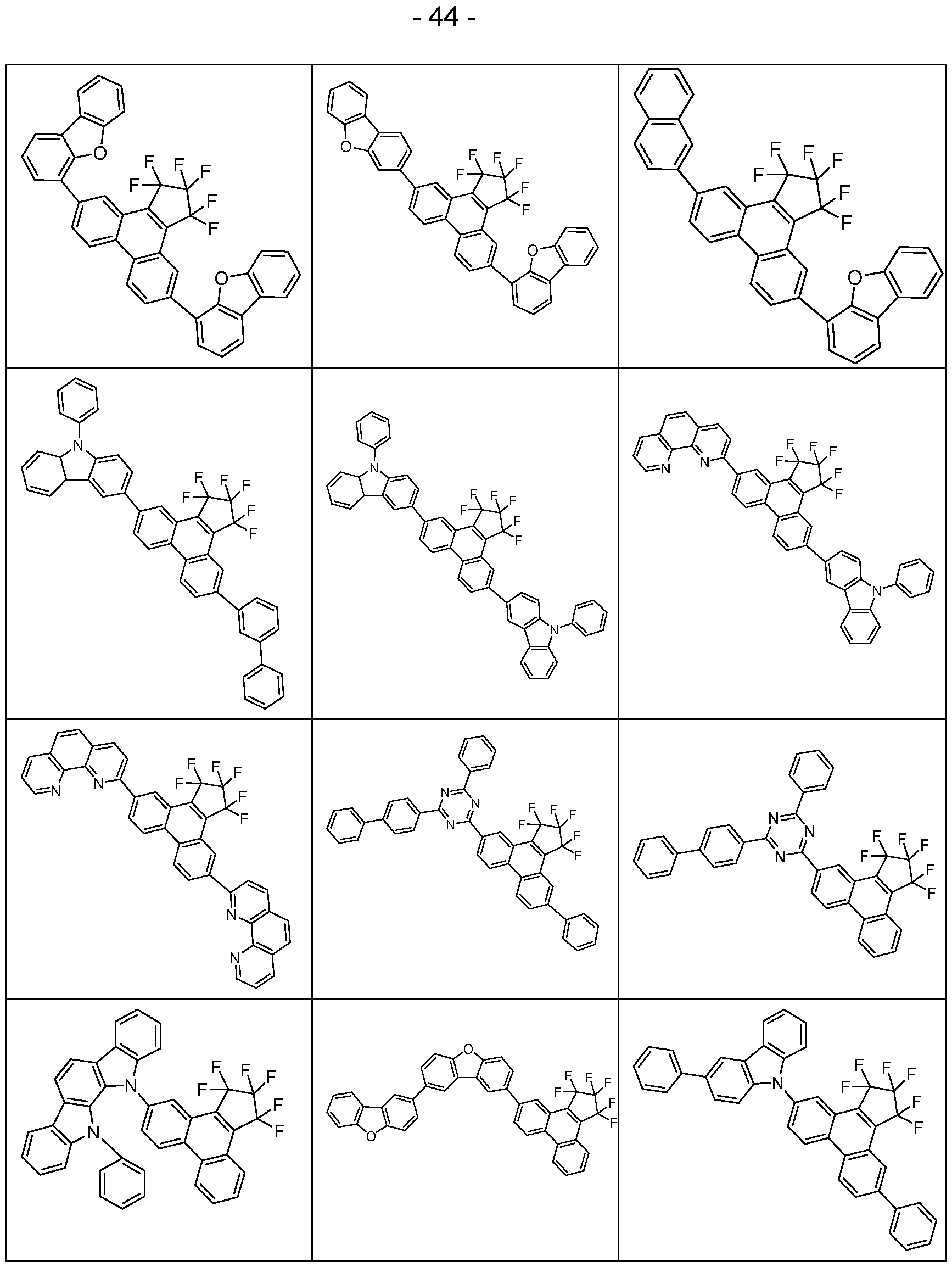
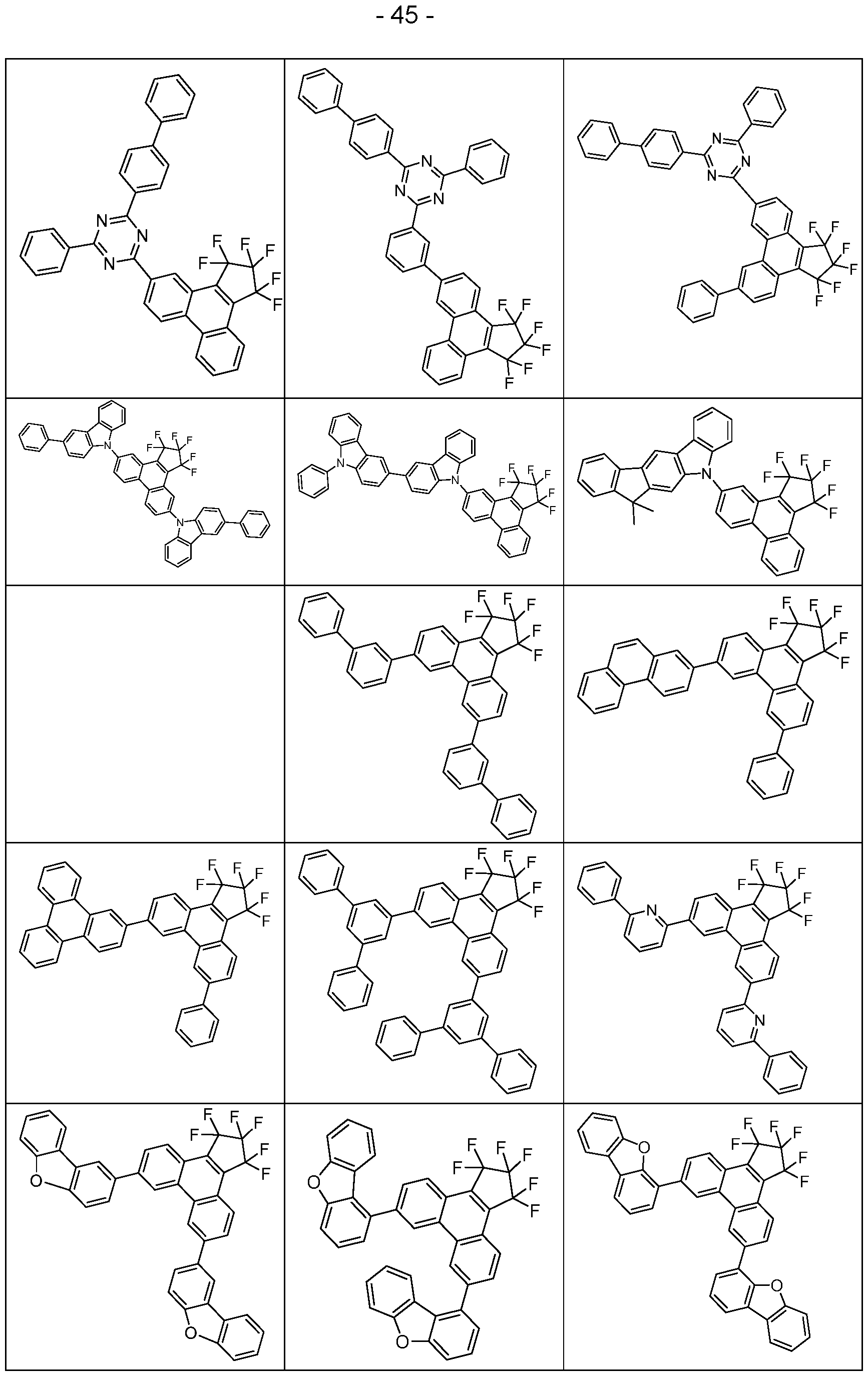
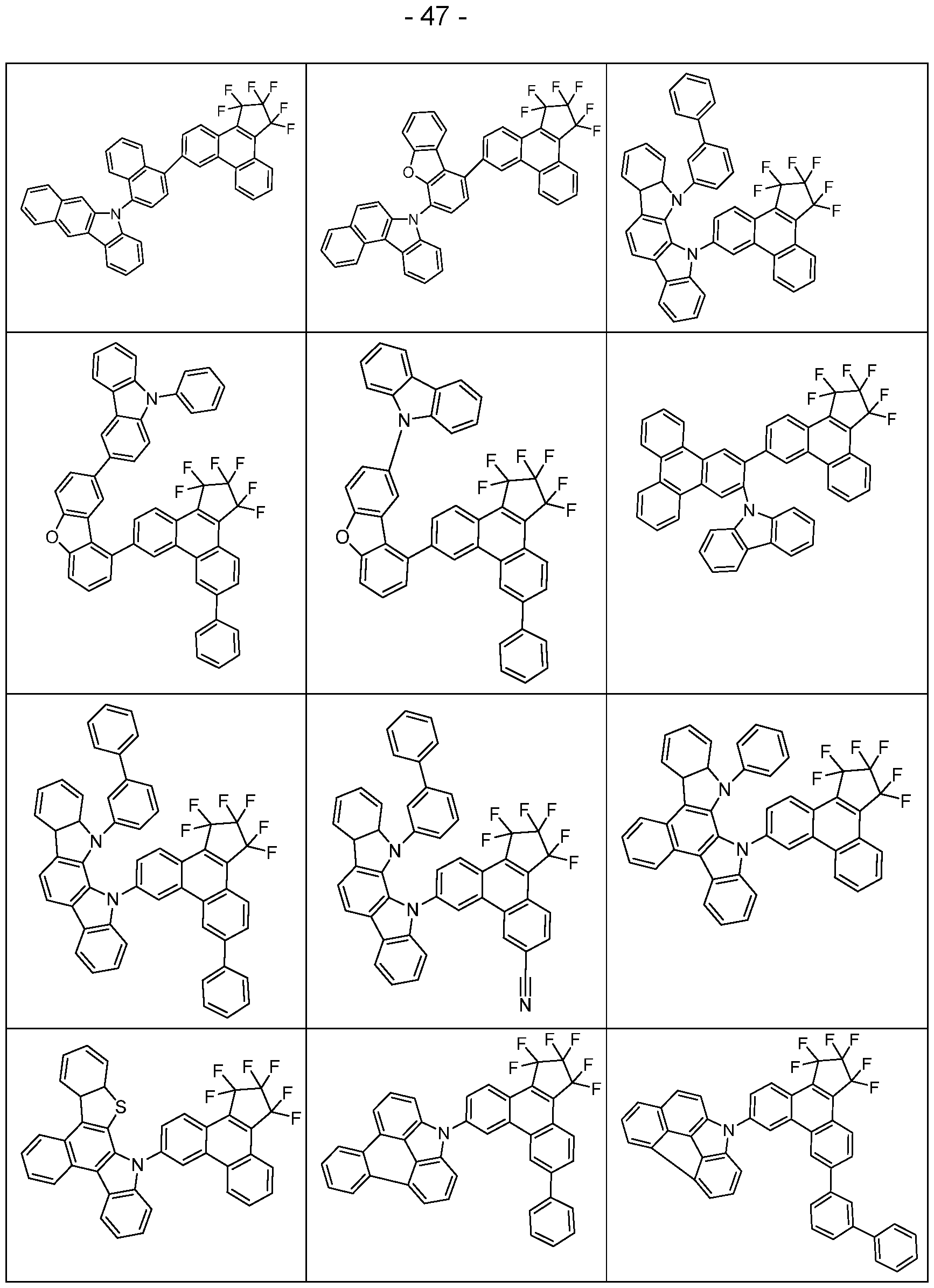
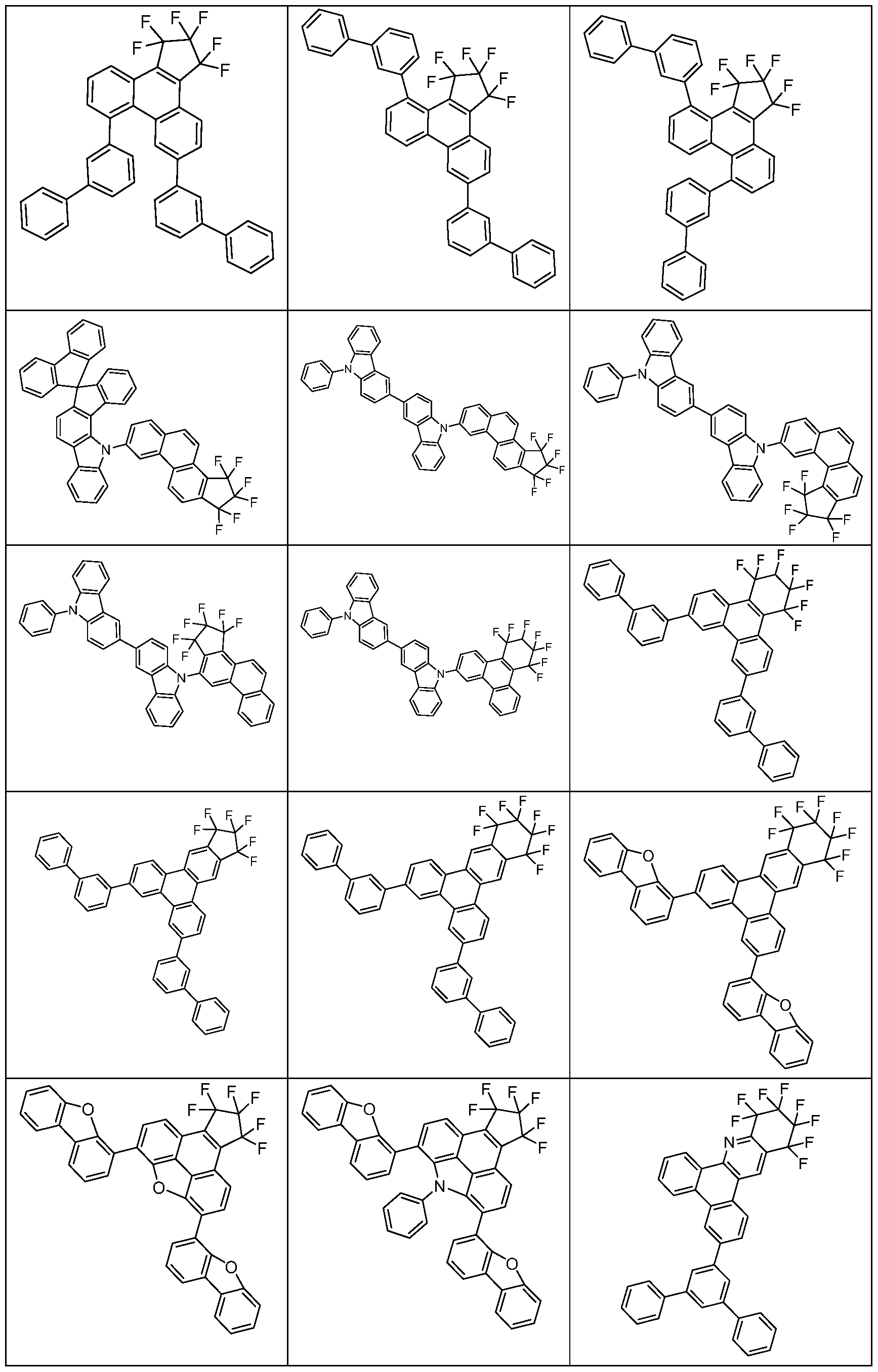
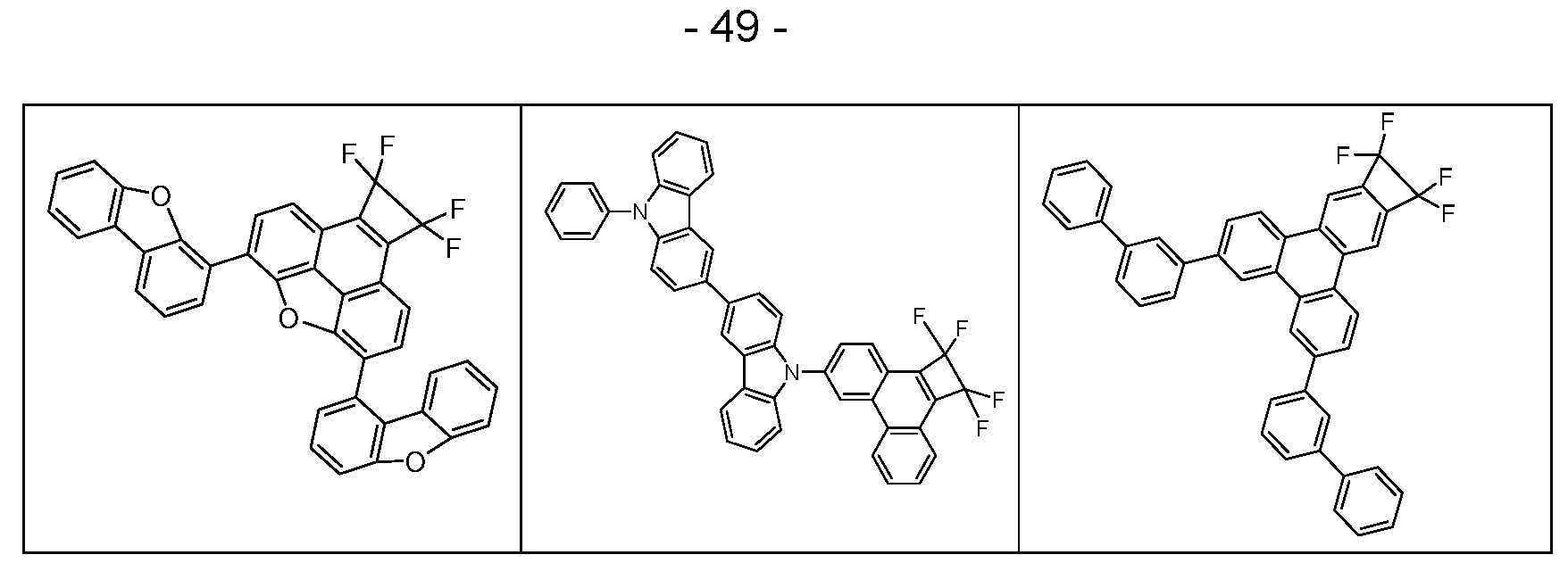
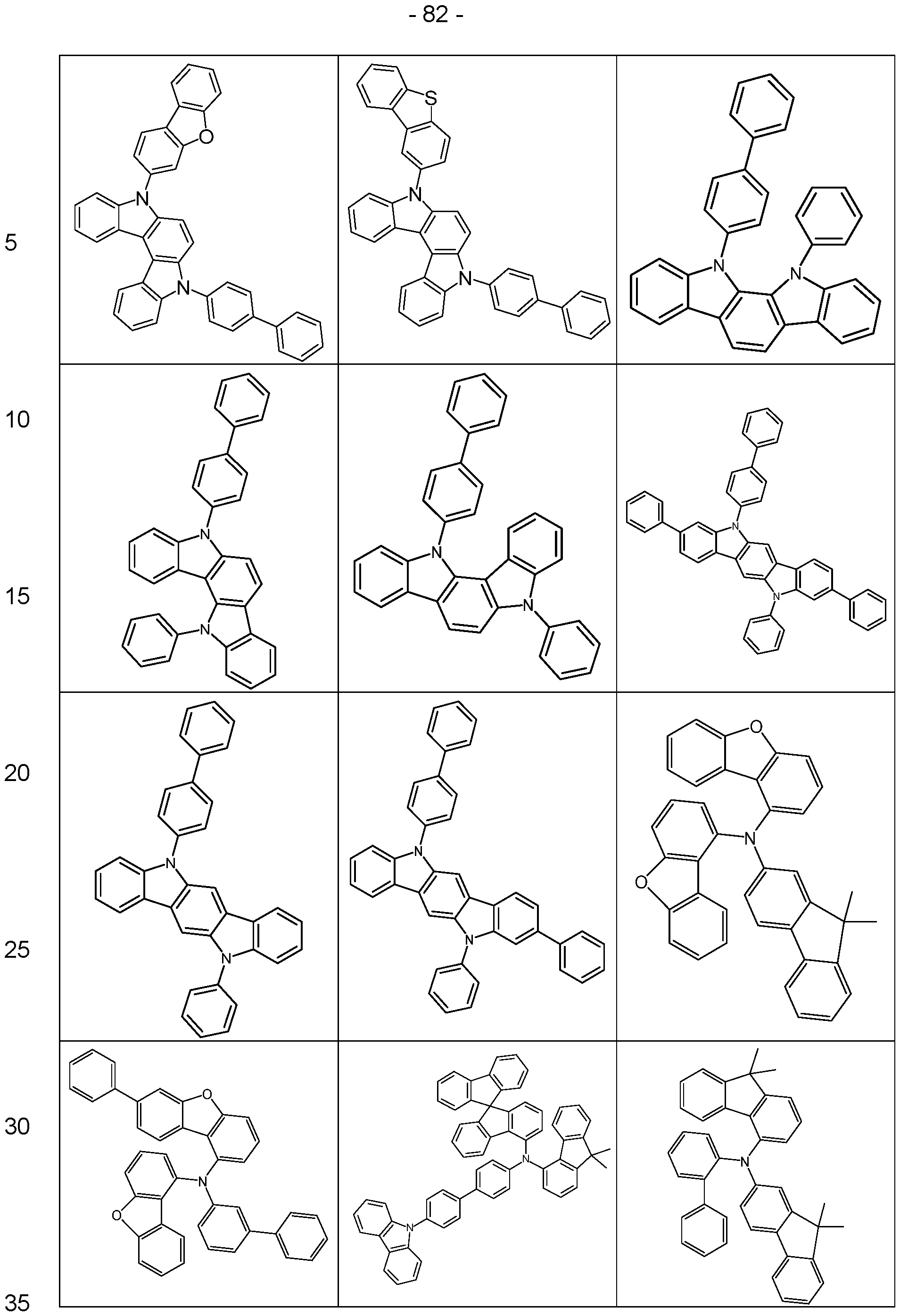
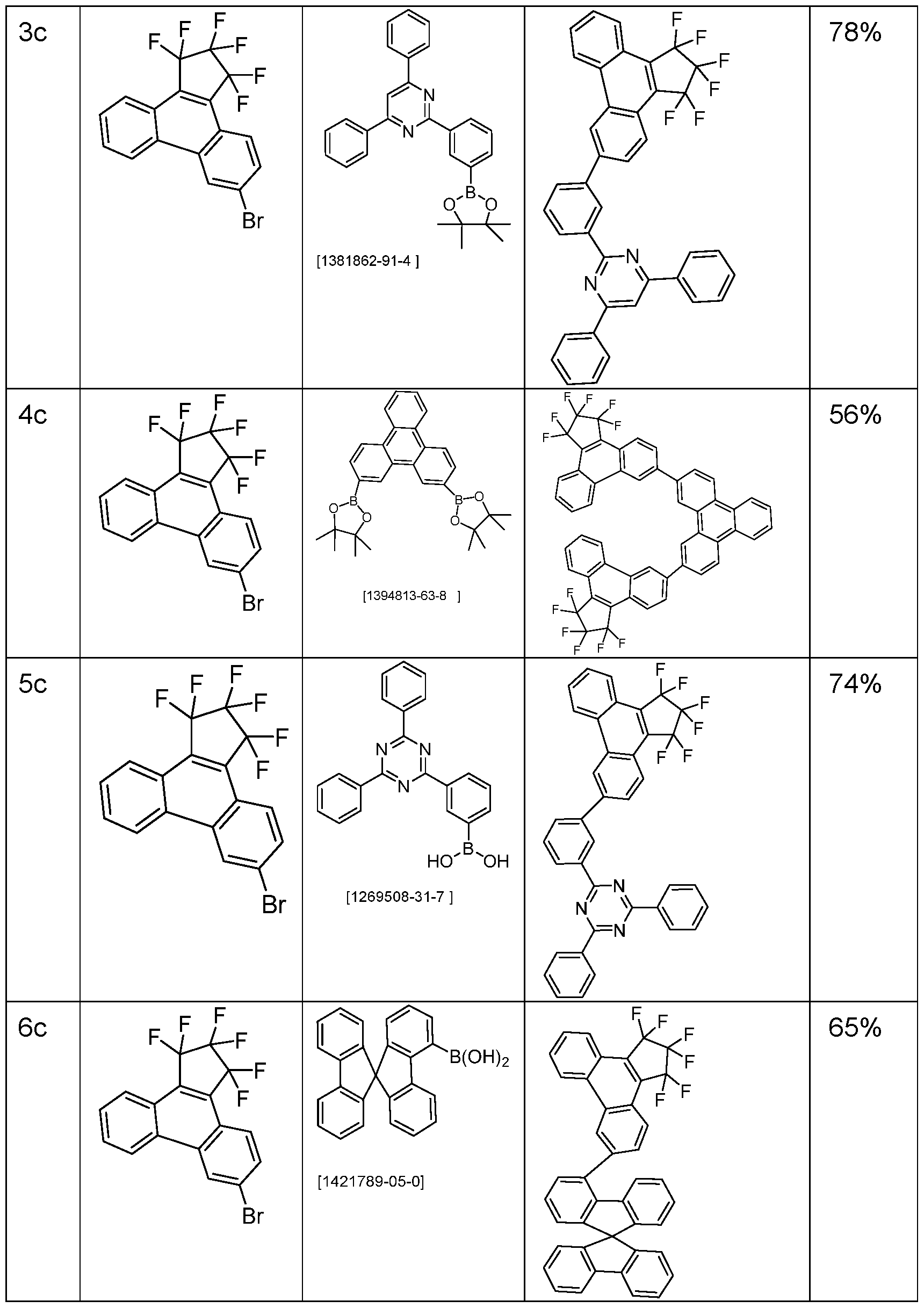
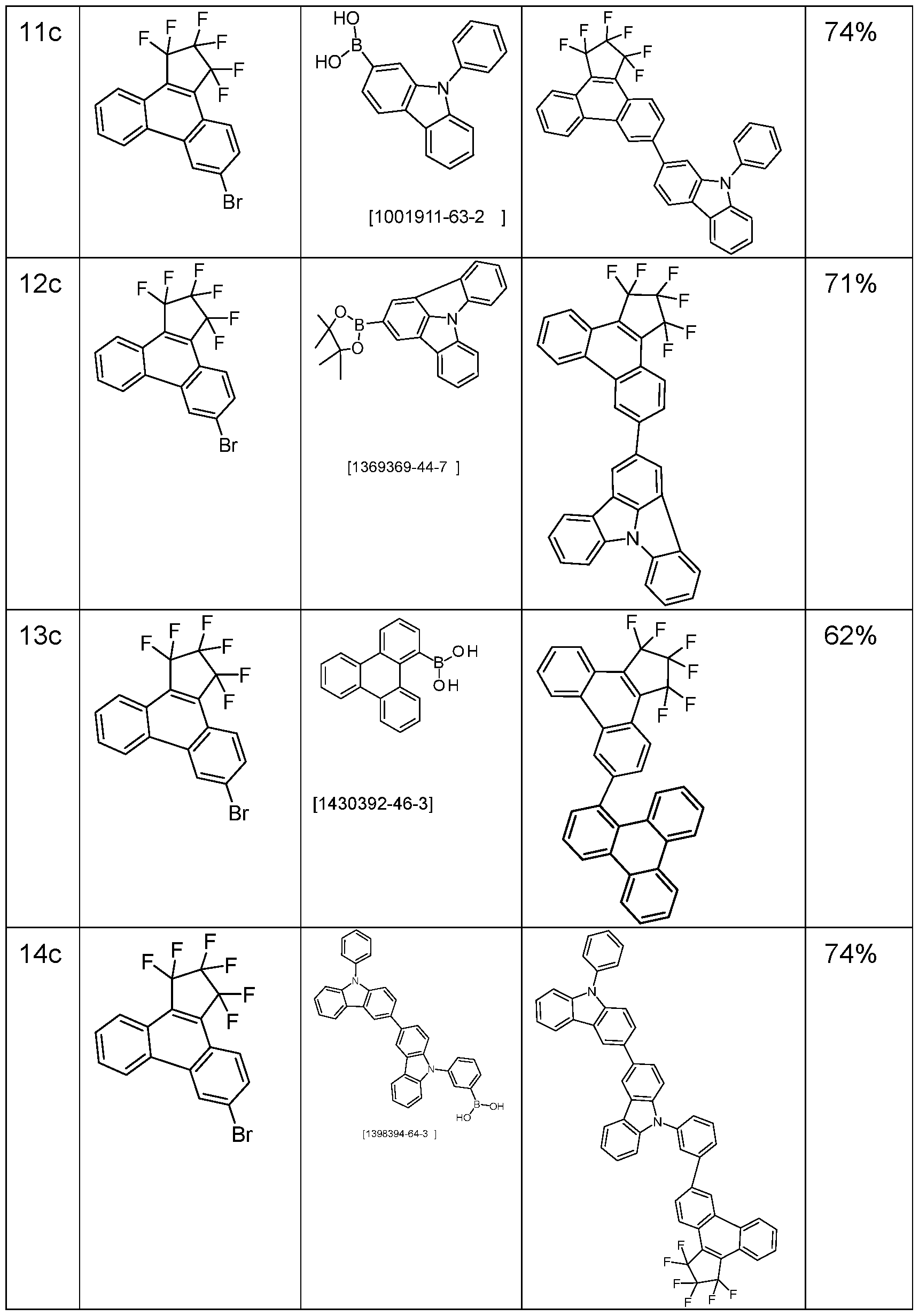
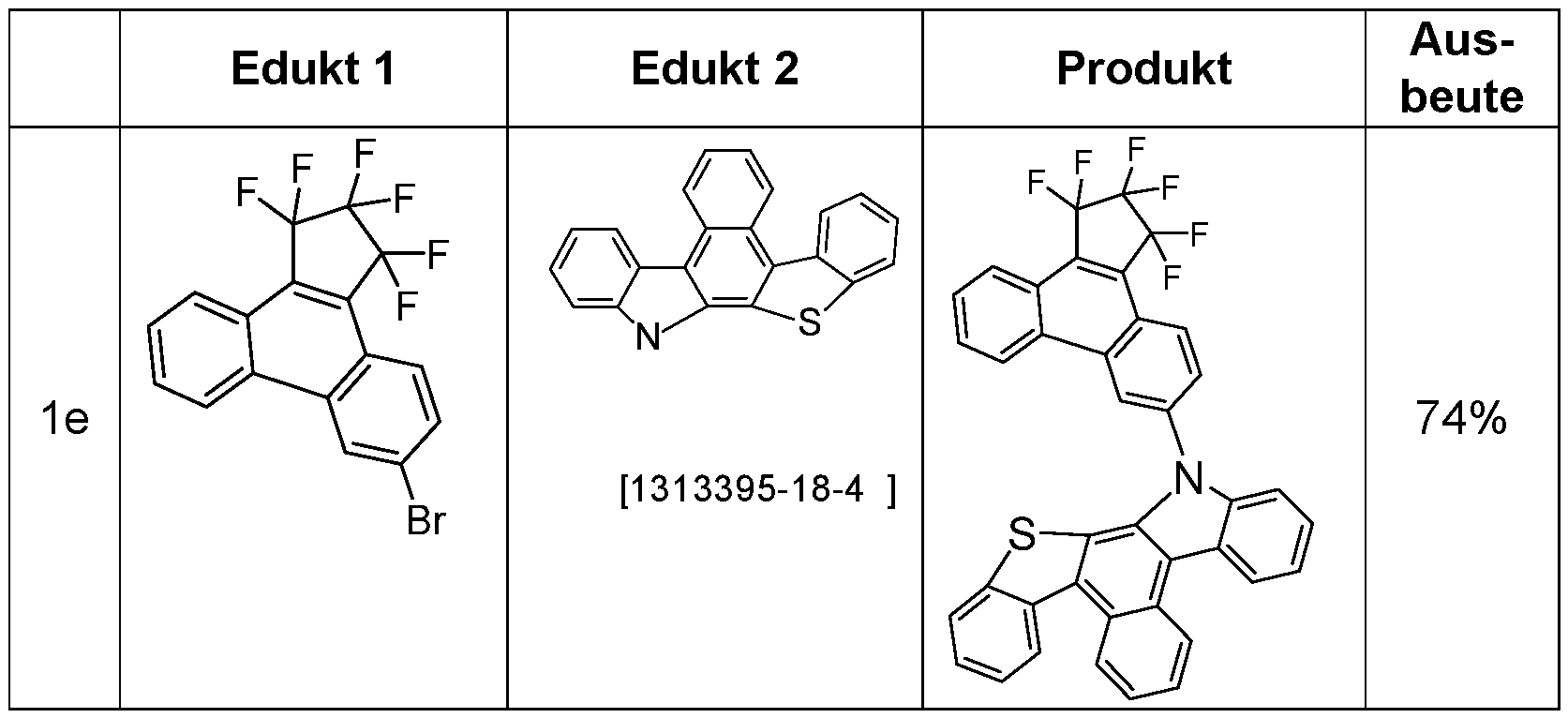
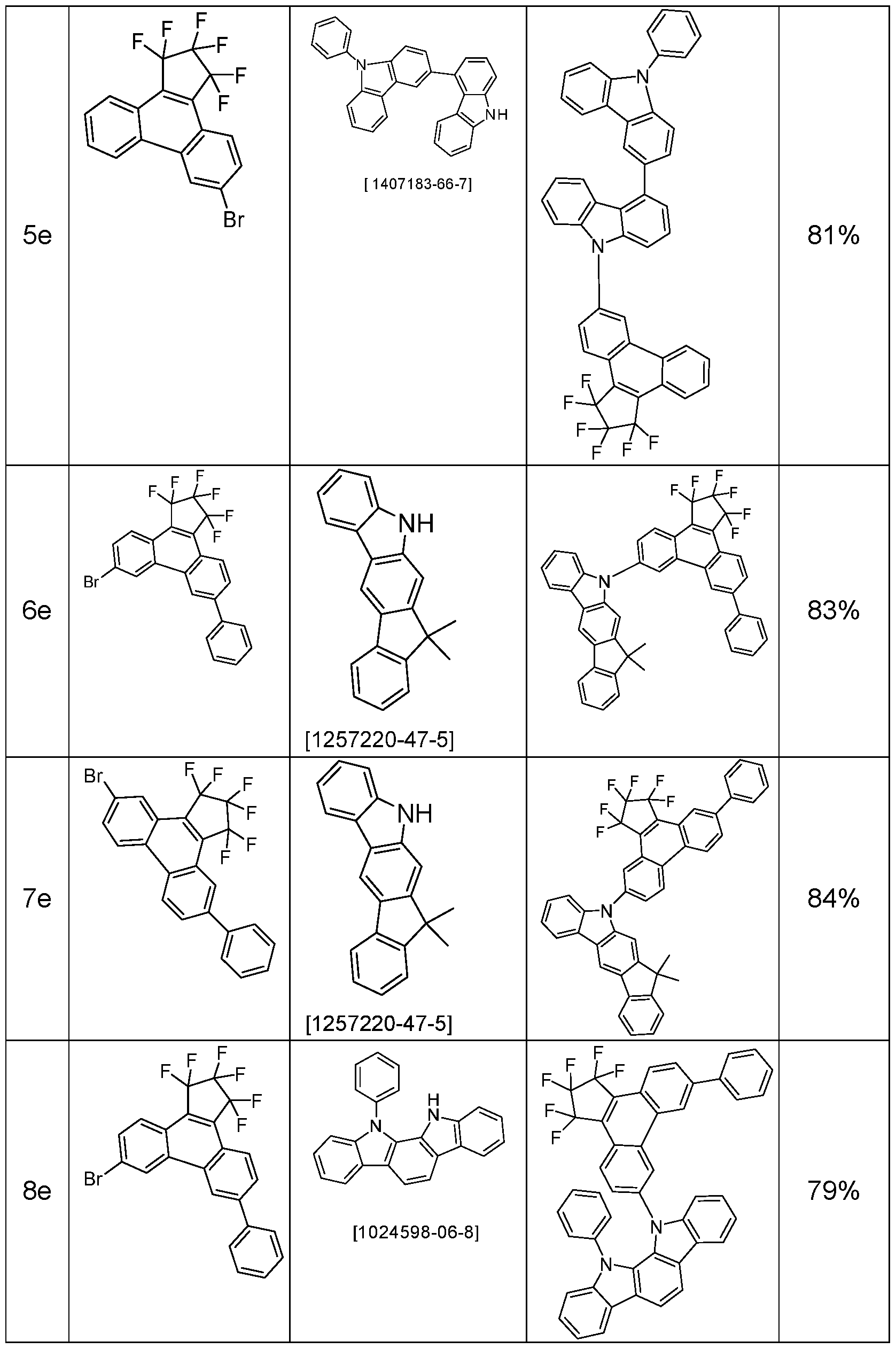
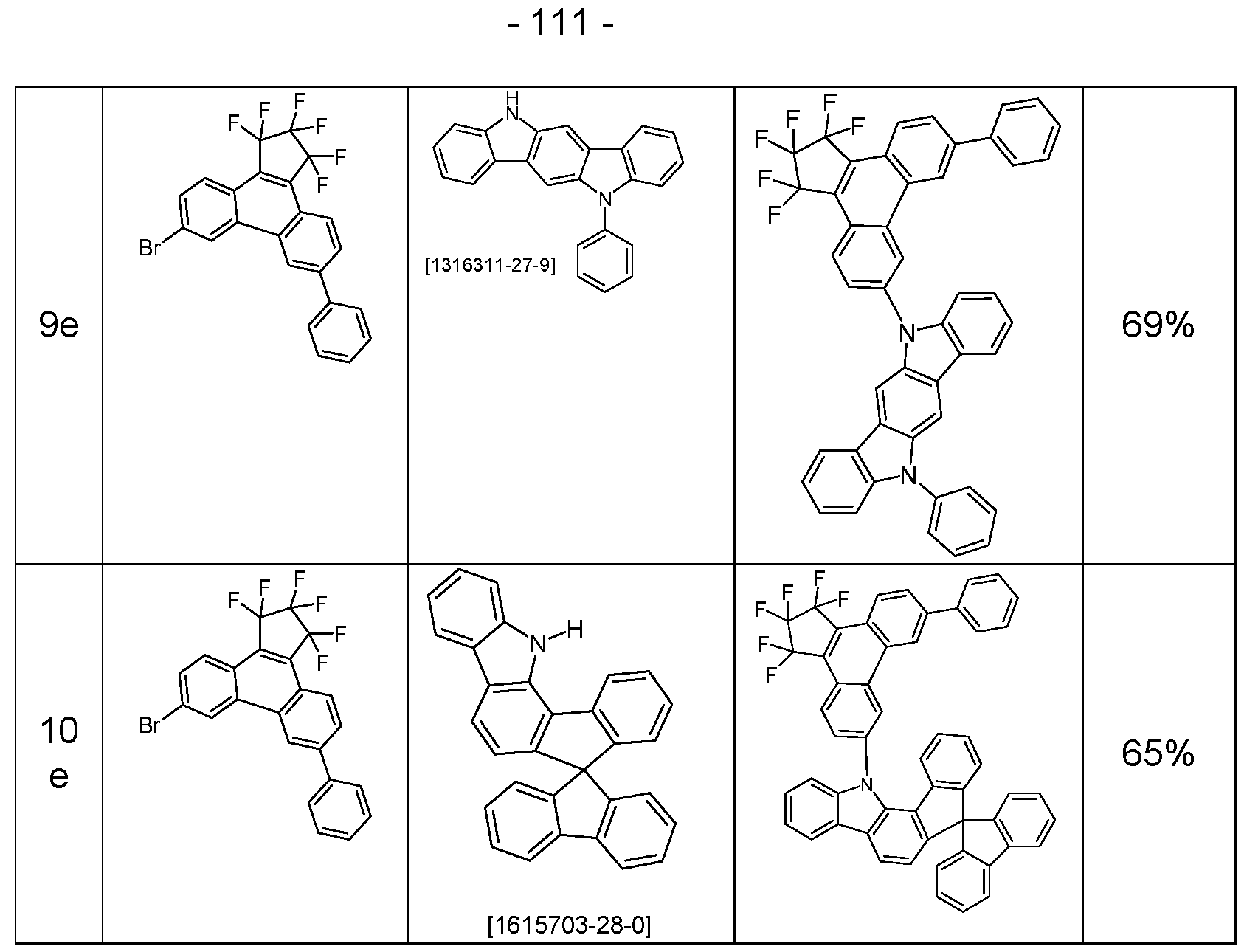
- the above-mentioned preferred embodiments can be combined with one another as desired within the restrictions defined in claim 1. In a particularly preferred embodiment of the invention, the above-mentioned preferences occur simultaneously. Examples of preferred compounds according to the above-mentioned embodiments are the compounds listed in the following table.
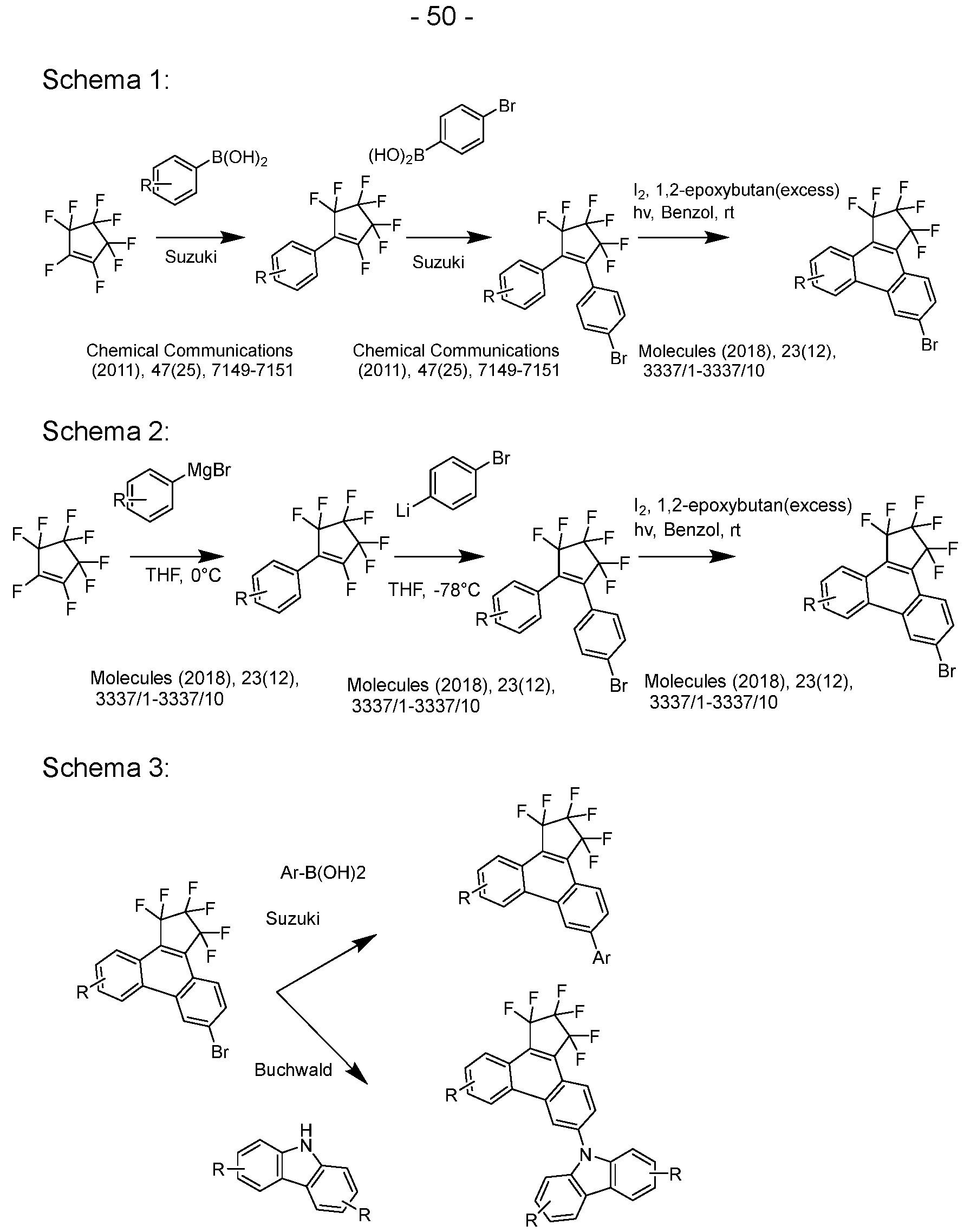
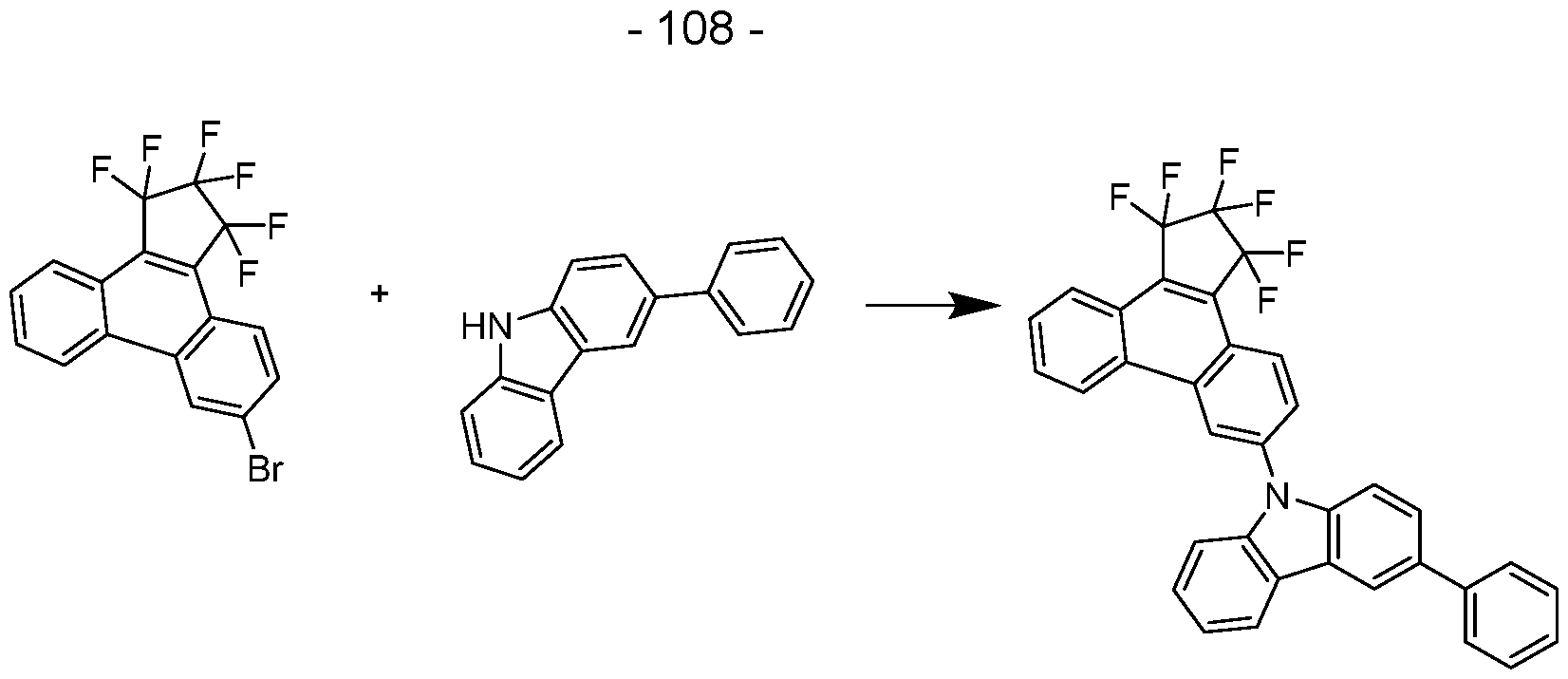
- the compounds according to the invention can be prepared by synthesis steps known to the person skilled in the art, such as bromination, Suzuki coupling, Ullmann coupling, Heck reaction, Hartwig-Buchwald coupling, etc.
- the present invention therefore further relates to a process for preparing the compounds according to the invention, characterized by the following steps: (A) synthesis of the condensed basic structure according to formula (1); (B) introduction of the aromatic or heteroaromatic groups R by coupling reactions.
- the compounds according to the invention can therefore be prepared starting from compounds known from the literature according to Fukumoto et al., Macromolecules 2017, 50, 865 or Gotsu et al., Molecules 2018, 23, 3337. In Schemes 1 and 2, this is shown using the example of the brominated basic structure, which is prepared by a sequence of Suzuki couplings or organometallic coupling reactions. Additional groups can be added to this basic scaffold by further coupling reactions, as shown in Scheme 3.
- formulations of the compounds according to the invention are required. These formulations can be, for example, solutions, dispersions or emulsions. It may be preferable to use mixtures of two or more solvents for this purpose.
- Suitable and preferred Solvents are, for example, toluene, anisole, o-, m- or p-xylene, methyl benzoate, mesitylene, tetralin, veratrol, THF, methyl-THF, THP, chlorobenzene, dioxane, phenoxytoluene, especially 3-phenoxytoluene, (-)-fenchone, 1,2,3,5-tetramethylbenzene, 1,2,4,5-Te tramethylbenzene, 1-methyl-naphthalene, 2-methylbenzothiazole, 2-phenoxyethanol, 2-pyrrolidinone, 3-methylanisole, 4-methylanisole, 3,4-dimethylanisole, 3,5-dimethylanisole, acetophenone, ⁇ -terpineol, benzothiazole, butyl benzoate, cumene, cyclohexanol, cyclohexanone, cyclohexylbene zol, Decalin
- a further subject matter of the present invention is therefore a formulation, in particular a solution, dispersion or emulsion, comprising at least one compound according to the invention and at least one further compound.
- the further compound can be, for example, a solvent, in particular one of the abovementioned solvents or a mixture of these solvents. The preparation of such solutions is known to the person skilled in the art and is described, for example, in WO 2002/072714, WO 2003/019694 and the literature cited therein.
- the further compound can also be at least one further organic or inorganic compound which is also used in the electronic device, for example an emitting compound and/or a matrix material. This further compound can also be polymeric.
- the compounds according to the invention are suitable for use in an electronic device, in particular in an organic electroluminescent device (OLED). Depending on the substitution the compounds can be used in different functions and layers.
- a further subject of the present invention is therefore the use of a compound according to the invention in an electronic device.
- a still further subject of the present invention is an electronic device containing at least one compound according to the invention.
- An electronic device in the sense of the present invention is a device which contains at least one layer which contains at least one organic compound.
- the component can also contain inorganic materials or layers which are made up entirely of inorganic materials.
- the electronic device is preferably selected from the group consisting of organic electroluminescent devices (OLEDs), organic integrated circuits (O-ICs), organic field-effect transistors (O-FETs), organic thin-film transistors (O-TFTs), organic light-emitting transistors (O-LETs), organic solar cells (O-SCs), dye-sensitized organic solar cells (DSSCs), organic optical detectors, organic photoreceptors, organic field quench devices (O-FQDs), light-emitting electrochemical cells (LECs), organic laser diodes (O-lasers) and organic plasmon emitting devices, but preferably organic electroluminescent devices (OLEDs).
- O-ICs organic integrated circuits
- O-FETs organic field-effect transistors
- OF-TFTs organic thin-film transistors
- O-LETs organic light-emitting transistors
- O-SCs organic solar cells
- DSSCs dye-sensitized organic solar cells
- organic optical detectors organic photo
- the device is particularly preferably an organic electroluminescent device comprising a cathode, anode and at least one emitting layer, wherein at least one organic layer, which can be an emitting layer, hole transport layer, electron transport layer, hole blocking layer, electron blocking layer or another functional layer, contains at least one inventive compound.
- the layer depends on the substitution of the compound.
- the organic electroluminescent device can contain further layers, for example one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, exciton blocking layers, electron blocking layers, charge generation layers and/or organic or inorganic p/n junctions. Interlayers can also be introduced between two emitting layers, which, for example, have an exciton blocking function.
- the organic electroluminescent device can contain one emitting layer, or it can contain several emitting layers. If several emission layers are present, these preferably have a total of several emission maxima between 380 nm and 750 nm, so that overall white emission results, ie different emitting compounds that can fluoresce or phosphoresce are used in the emitting layers. Systems with three emitting layers are particularly preferred, with the three layers showing blue, green and orange or red emission (the basic structure is described, for example, in WO 2005/011013).
- the organic electroluminescent device according to the invention can also be a tandem OLED, in particular for white-emitting OLEDs.
- the compound according to formula (1) is preferably used in an organic electroluminescent device which comprises one or more phosphorescent emitters.
- the compound according to the invention according to the embodiments listed above can be used in different layers, depending on the precise structure.
- the organic electroluminescent device can contain one emitting layer, or it can contain several emitting layers, with at least one layer containing at least one compound according to the invention.
- the compound according to the invention can also be used in an electron transport layer and/or in a hole blocking layer and/or in a hole transport layer and/or in an exciton blocking layer and/or as a matrix material.
- the compound according to the invention is particularly preferably used as a matrix material in an emitting layer and/or as an electron transport material in an electron transport or hole blocking layer, in particular as a matrix material in a phosphorescent layer.
- phosphorescent compound typically refers to compounds in which the emission of light occurs through a spin-forbidden transition, e.g. a transition from an excited triplet state or a state with a higher spin quantum number, e.g. a quintet state.
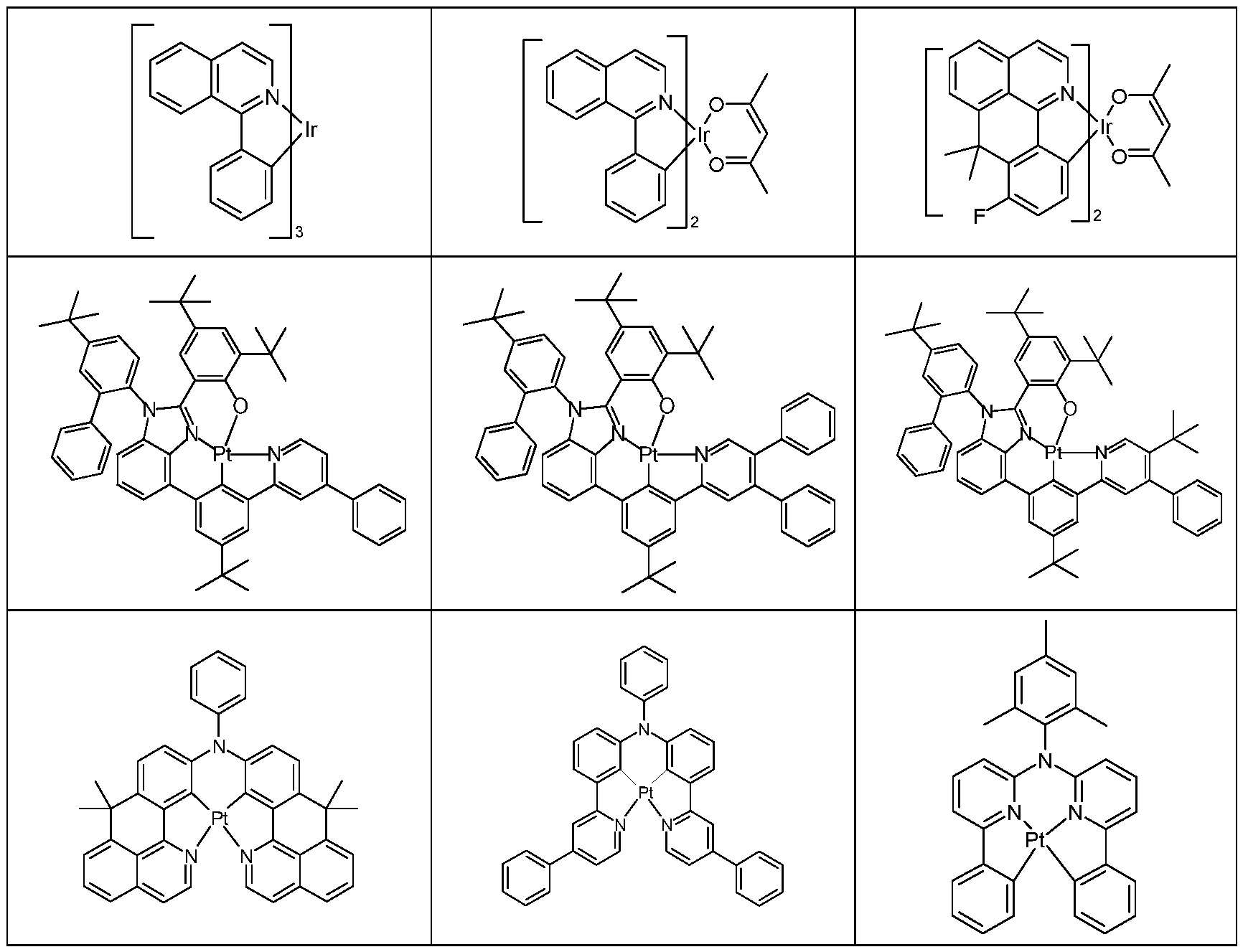
- Suitable phosphorescent compounds are in particular compounds which emit light, preferably in the visible range, when suitably excited and also contain at least one atom with an atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80. All luminescent complexes with transition metals or lanthanides are preferably regarded as phosphorescent compounds, in particular if they contain copper, molybdenum, tungsten, rhenium, ruthenium, osmium, rhodium, iridium, palladium, platinum, silver, gold or europium, in particular compounds which contain iridium, platinum or copper.
- all luminescent iridium, platinum or copper complexes are regarded as phosphorescent emitting compounds.
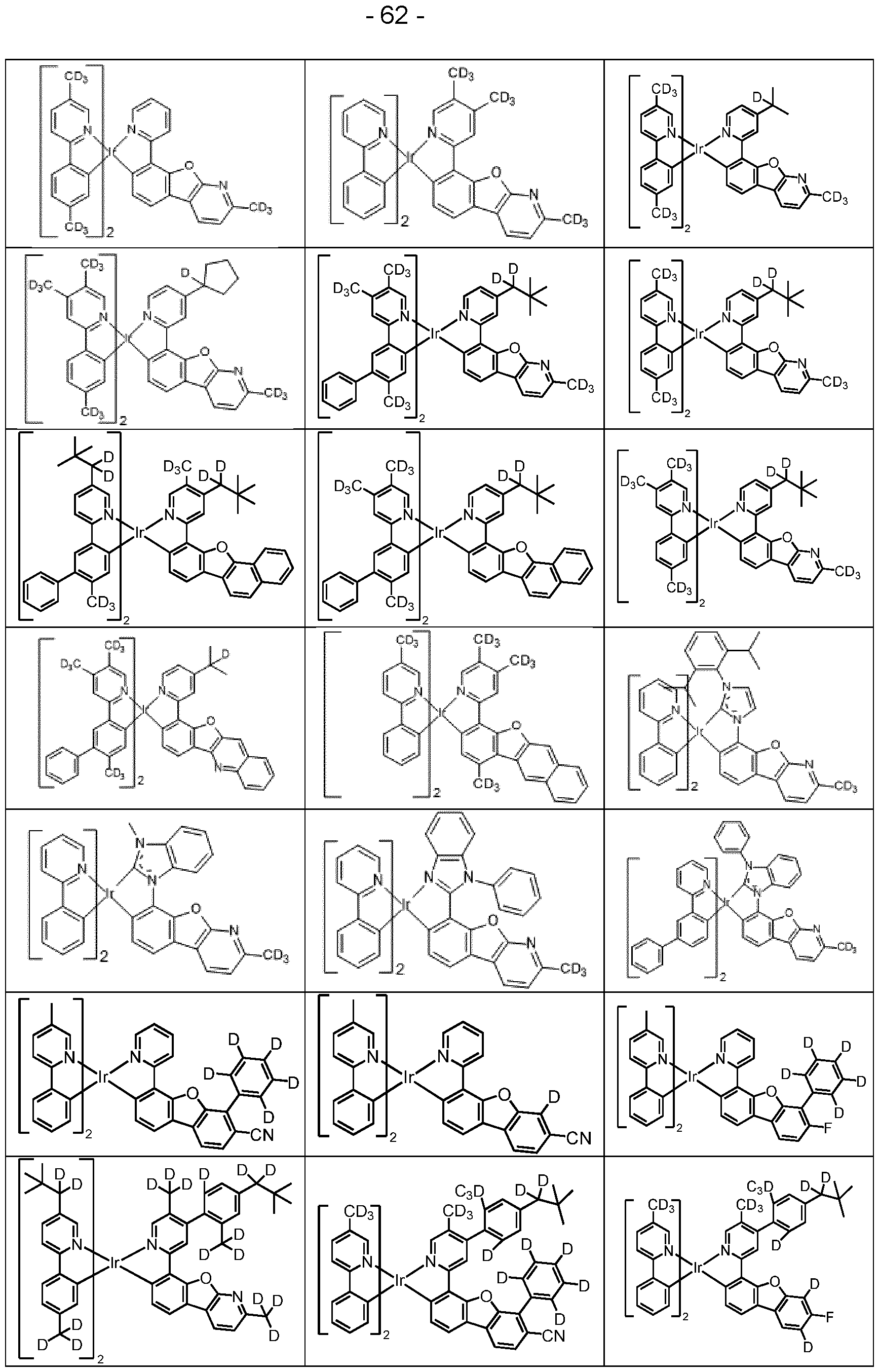
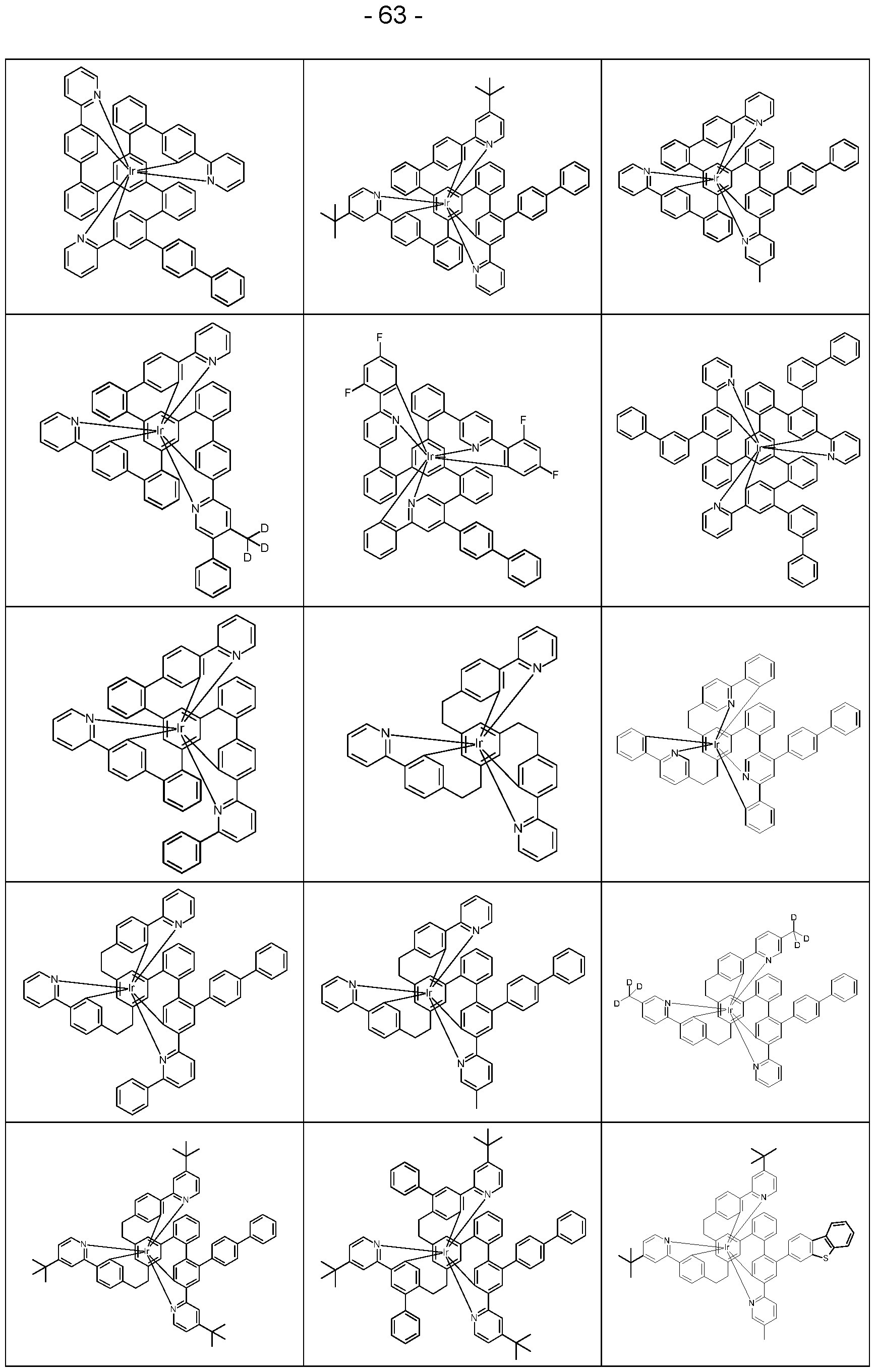
- Examples of the emitters described above can be found in applications WO 00/70655, WO 2001/41512, WO 2002/02714, WO 2002/15645, EP 1191613, EP 1191612, EP 1191614, WO 05/033244, WO 05/019373, US 2005/0258742, WO 2009/146770, WO 2010/015307, WO 2010/031485, WO 2010/054731, WO 2010/054728, WO 2010/086089, WO 2010/099852, WO 2010/102709, WO 2011/032626, WO 2011/066898, WO 2011/157339, WO 2012/007086, WO 2014/008982, WO 2014/023377, WO 2014/094961, WO 2014/094960, WO 2015/036074, WO 2015/10
- all phosphorescent complexes as used according to the prior art for phosphorescent OLEDs and as known to the person skilled in the art in the field of organic electroluminescence are suitable, and the person skilled in the art can use further phosphorescent complexes without inventive step. It is possible for the person skilled in the art, even without inventive activity, to use further phosphorescent complexes in combination with the compounds of formula (1) in organic electroluminescent devices. Further examples are listed in a table below. According to the invention, it is also possible to use the compound of formula (1) in an electronic device that contains one or more fluorescent emitting compounds. In a preferred embodiment of the invention, the compounds of formula (1) are used as electron-transporting material.
- the compounds are preferably contained in an electron-transport layer or a hole-blocking layer or an electron-conducting or bipolar host material.
- Use in an electron-transport layer or host material is particularly preferred.
- An electron-transport layer in the sense of the present application is a layer with an electron-transporting function between the cathode and the emitting layer.
- electron injection layers and hole blocking layers are understood to mean certain embodiments of electron transport layers.
- an electron injection layer is an electron transport layer that directly borders the cathode or is only separated from it by a single coating of the cathode.
- a hole blocking layer is the electron transport layer that directly borders the emitting layer on the cathode side.
- the OLED according to the invention preferably comprises two, three or four electron-transporting layers between the cathode and the emitting layer, of which preferably at least one, particularly preferably exactly one or two, contain compounds of the formula (1). If the compound of formula (1) is used as an electron transport material in an electron transport layer, an electron injection layer or a hole blocking layer, the compound can be used as a pure material, ie in a proportion of 100% in the electron transport layer, or it can be used in combination with one or more other compounds.
- Hole transport layers or electron blocking layers of the electronic devices according to the invention can additionally comprise one or more p-dopants.
- p-dopants used according to the present invention are preferably those organic electron acceptor compounds which are capable of oxidizing one or more of the other compounds in the mixture.
- Particularly preferred embodiments of p-dopants are the compounds disclosed in WO 2011/073149, EP 1968131, EP 2276085, EP 2213662, EP 1722602, EP 2045848, DE 102007031220, US 8044390, US 8057712, WO 2009/003455, WO 2010/094378, WO 2011/120709, US 2010/0096600, WO 2012/095143 and DE 102012209523.
- Particularly preferred p-dopants are quinodimethane compounds, azaindenofluorenediones, azaphenylenes, azatriphenylenes, I2, metal halides, preferably transition metal halides, metal oxides, preferably metal oxides containing at least one transition metal or a metal of the 3rd main group, and transition metal complexes, preferably complexes of Cu, Co, Ni, Pd and Pt with ligands containing at least one oxygen atom as a bonding site.
- preferred dopants are transition metal oxides, preferably oxides of rhenium, molybdenum and tungsten, particularly preferably Re2O7, MoO3, WO3 and ReO3.
- the p-dopants are preferably present in a substantially homogeneous distribution in the p-doped layers. This can be achieved, for example, by coevaporation of the p-dopant and the hole transport material matrix.
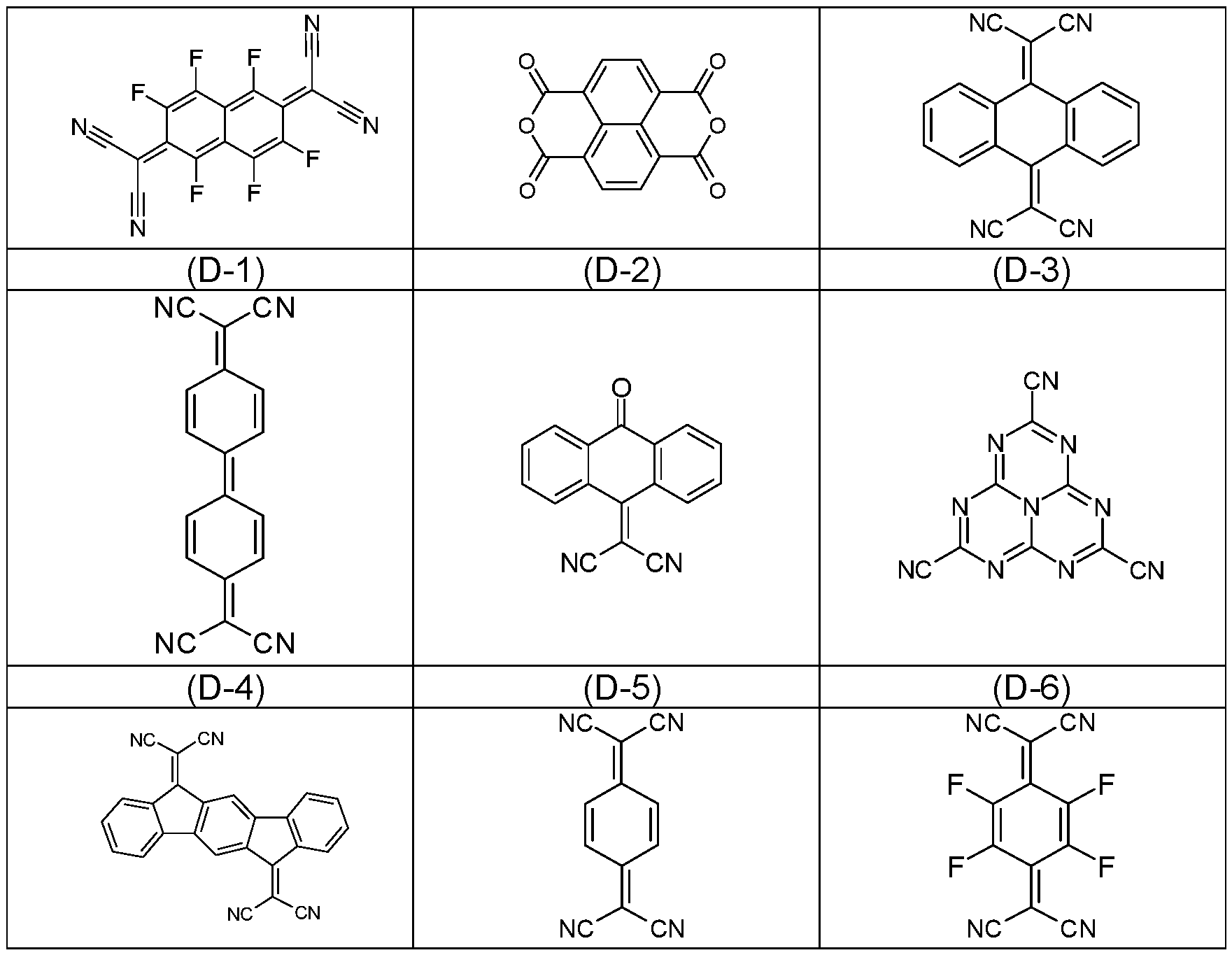
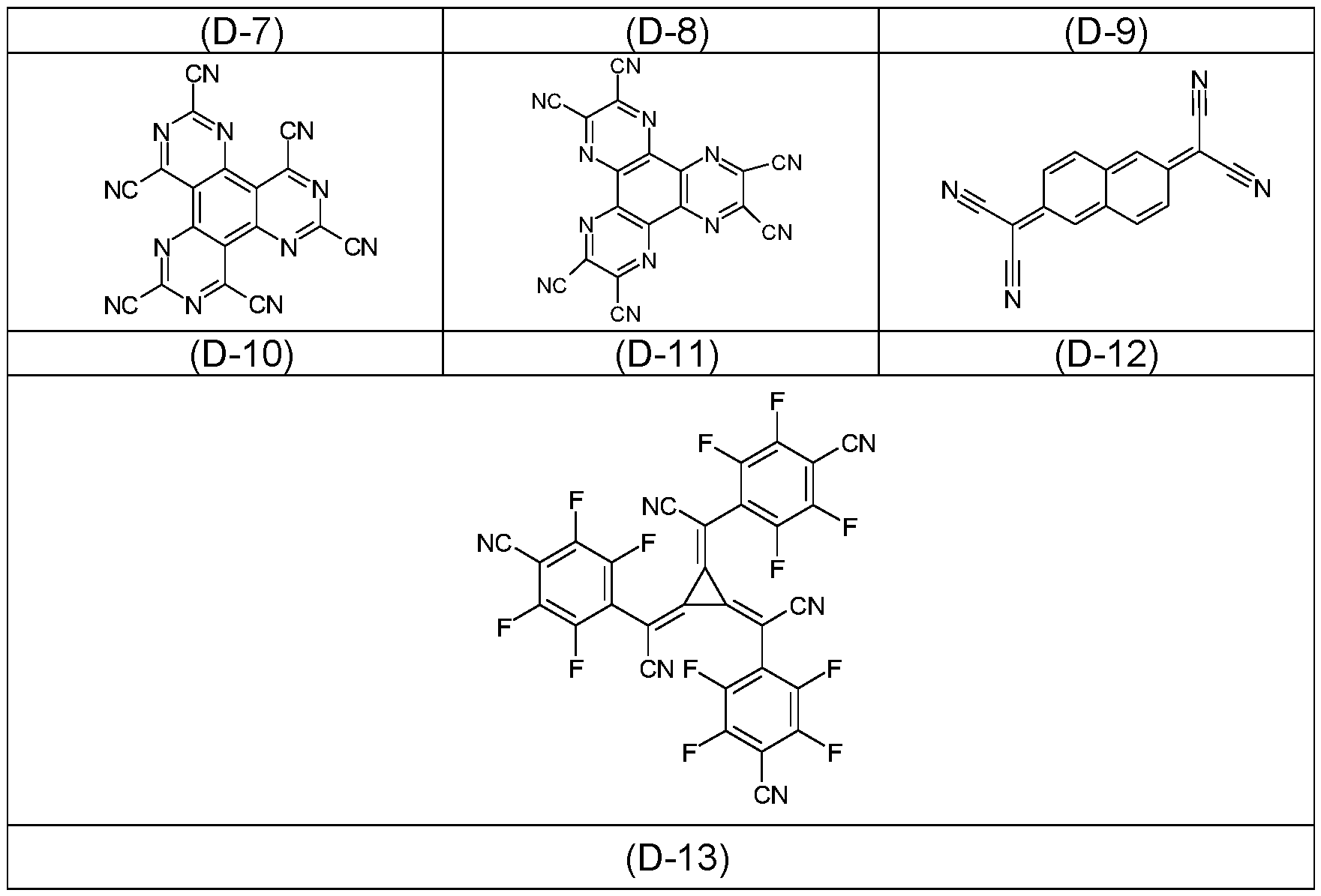
- Preferred p-dopants are in particular the following compounds:
- the hole transport materials used can be used in combination with a hexaazatriphenylene derivative, as described in US 2007/0092755.
- the hexaazatriphenylene derivative is particularly preferably used in a separate layer.
- the compound of formula (1) is used in an emitting layer as a matrix material in combination with one or more emitting compounds, preferably phosphorescent compounds.
- the proportion of matrix material in the emitting layer in this case is between 50.0 and 99.9 vol. %, preferably between 80.0 and 99.5 vol. %, particularly preferably between 92.0 and 99.5 vol. %, for fluorescent emitting layers and between 85.0 and 97.0 vol. % for phosphorescent emitting layers.
- the proportion of the emitting compound is between 0.1 and 50.0 vol.%, preferably between 0.5 and 20.0 vol.%, particularly preferably between 0.5 and 8.0 vol.% for fluorescent emitting Layers and between 3.0 and 15.0 vol.% for phosphorescent emitting layers.
- An emitting layer of an organic electroluminescent device can also comprise systems that contain a large number of matrix materials (mixed matrix systems) and/or a large number of emitting compounds. In this case too, the emitting compounds are generally those that have the smaller proportion in the system and the matrix materials are those that have the larger proportion in the system. In individual cases, however, the proportion of an individual matrix material in the system can be lower than the proportion of an individual emitting compound.
- the compounds of formula (1) are used as a component of mixed matrix systems.
- the mixed matrix systems preferably consist of two or three different matrix materials, particularly preferably of two different matrix materials.
- one of the two materials is preferably a material with hole-transporting properties and the other material is a material with electron-transporting properties.
- the compound of formula (1) is preferably the matrix material with electron-transporting properties.
- the desired electron-transporting and hole-transporting properties of the mixed matrix components can also be predominantly or completely combined in a single mixed matrix component, with the other mixed matrix component(s) fulfilling other functions.
- the two different matrix materials can be present in a ratio of 1:50 to 1:1, preferably 1:20 to 1:1, even more preferably 1:10 to 1:1 and most preferably 1:4 to 1:1.
- Mixed matrix systems are preferably used in phosphorescent organic electroluminescent devices.
- a source for more detailed information on mixed matrix systems is the application WO 2010/108579.
- the mixed matrix systems can contain one or more emitting compounds, preferably one or more phosphorescent compounds.
- mixed matrix systems are preferably used in phosphorescent organic electroluminescent devices.
- Particularly suitable matrix materials which can be used in combination with the compounds according to the invention as matrix components of a mixed matrix system are selected from the preferred matrix materials for phosphorescent compounds or the preferred matrix materials for fluorescent compounds mentioned below, depending on which type of emitting compound is used in the mixed matrix system.
- Preferred phosphorescent compounds for use in mixed matrix systems are the same as those described above as generally preferred phosphorescent emitter materials.
- Preferred fluorescent emitting compounds are selected from the class of arylamines.
- an arylamine or an aromatic amine is understood to mean a compound which contains three substituted or unsubstituted aromatic or heteroaromatic ring systems which are bonded directly to the nitrogen.
- at least one of these aromatic or heteroaromatic ring systems is a condensed ring system, particularly preferably with at least 14 aromatic ring atoms.
- Preferred examples of these are aromatic anthraceneamines, aromatic anthracenediamines, aromatic pyrenamines, aromatic pyrenediamines, aromatic chrysenamines or aromatic chrysenediamines.
- aromatic anthraceneamine is understood to mean a compound in which a diarylamino group is bonded directly to an anthracene group, preferably in position 9.
- An aromatic anthracenediamine is understood to mean a compound in which two diarylamino groups are directly bonded to an anthracene group, preferably in positions 9, 10.
- Aromatic pyrenamines, pyrenediamines, chrysenamines and chrysenediamines are defined analogously, in which the diarylamino groups are preferably bonded to the pyrene in the 1-position or 1,6-position.
- indenofluorenamines or fluorenediamines for example according to WO 2006/108497 or WO 2006/122630
- benzoindenofluorenamines or fluorenediamines for example according to WO 2008/006449
- dibenzoindenofluorenamines or diamines for example according to WO 2007/140847
- the indenofluorene derivatives with condensed aryl groups disclosed in WO 2010/012328 are preferred.
- pyrenearylamines disclosed in WO 2012/048780 and in WO 2013/185871.
- benzoindenofluorenamines disclosed in WO 2014/037077 are also preferred.
- the benzofluorenamines disclosed in WO 2014/106522 are also preferred.
- the extended benzoindenofluorenes disclosed in WO 2014/111269 and in WO 2017/036574 are also preferred.
- the phenoxazines disclosed in WO 2017/028940 and in WO 2017/028941 are used.
- boron compounds according to WO2020208051, WO2015102118, WO2016152418, WO2018095397, WO2019004248, WO2019132040, US20200161552, WO2021089450 are used.
- Useful matrix materials include materials from various substance classes.
- Preferred matrix materials are selected from the classes of oligoaryls (e.g. 2,2',7,7'-tetraphenylspirobifluorene according to EP 676461 or dinaphthylanthracene), in particular oligoaryls with fused aromatic groups, oligoarylenevinylenes (e.g. DPVBi or spiro-DPVBi according to EP 676461), polypodal metal complexes (e.g. according to WO 2004/081017), hole-conducting compounds (e.g.
- electron-conducting compounds in particular ketones, phosphine oxides, sulfoxides etc. (for example according to WO 2005/084081 and WO 2005/084082), atropisomers (for example according to WO 2006/048268), boronic acid derivatives (for example according to WO 2006/117052) or the benzanthracenes (for example according to WO 2008/145239).
- Particularly preferred matrix materials are selected from the classes of oligoarylenes with naphthalene, anthracene, benzanthracene and/or pyrene or atropisomers of these compounds, the oligoarylenevinylenes, the ketones, the phosphine oxides and the sulfoxides.
- Very particularly preferred matrix materials are selected from the classes of oligoarylenes which include anthracene, benzanthracene, benzophenanthrene and/or pyrene or atropisomers of these compounds.
- an oligoarylene is understood to mean a compound in which at least three aryl or arylene groups are connected to one another.
- Preferred matrix materials for phosphorescent compounds are, as well as compounds according to formula (1), aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, e.g. according to WO 2004/013080, WO 2004/093207, WO 2006/005627 or WO 2010/006680, triarylamines, carbazole derivatives, e.g. CBP (N,N-biscarbazolylbiphenyl) or WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527, WO 2008/086851 or WO 2013/041176, indolocarbazole derivatives, e.g. B.
- aromatic ketones aromatic phosphine oxides or aromatic sulfoxides or sulfones
- triarylamines e.g. CBP (N,N-biscarbazolylbiphenyl) or WO 2005/039246, US 2005/
- indenocarbazole derivatives e.g. according to WO 2010/136109, WO 2011/000455, WO 2013/041176 or WO 2013/056776, azacarbazole derivatives, e.g. according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160, bipolar matrix materials, e.g. according to WO 2007/137725, silanes, e.g. according to WO 2005/111172, azaboroles or boronic esters, e.g. according to WO 2006/117052, triazine derivatives, e.g. B.
- WO 2012/048781 lactams, e.g. according to WO 2011/116865 or WO 2011/137951, or dibenzofuran derivatives, e.g. according to WO 2015/169412, WO 2016/015810, WO 2016/023608, WO 2017/148564 or WO 2017/148565.
- a further phosphorescent emitter which emits at a shorter wavelength than the actual emitter can be present in the mixture as a co-host or a compound which does not participate in charge transport or does not participate to a significant extent, as described for example in WO 2010/108579. Since the compounds according to the invention are electron-transporting compounds, they are preferably combined with a hole-transporting matrix material.
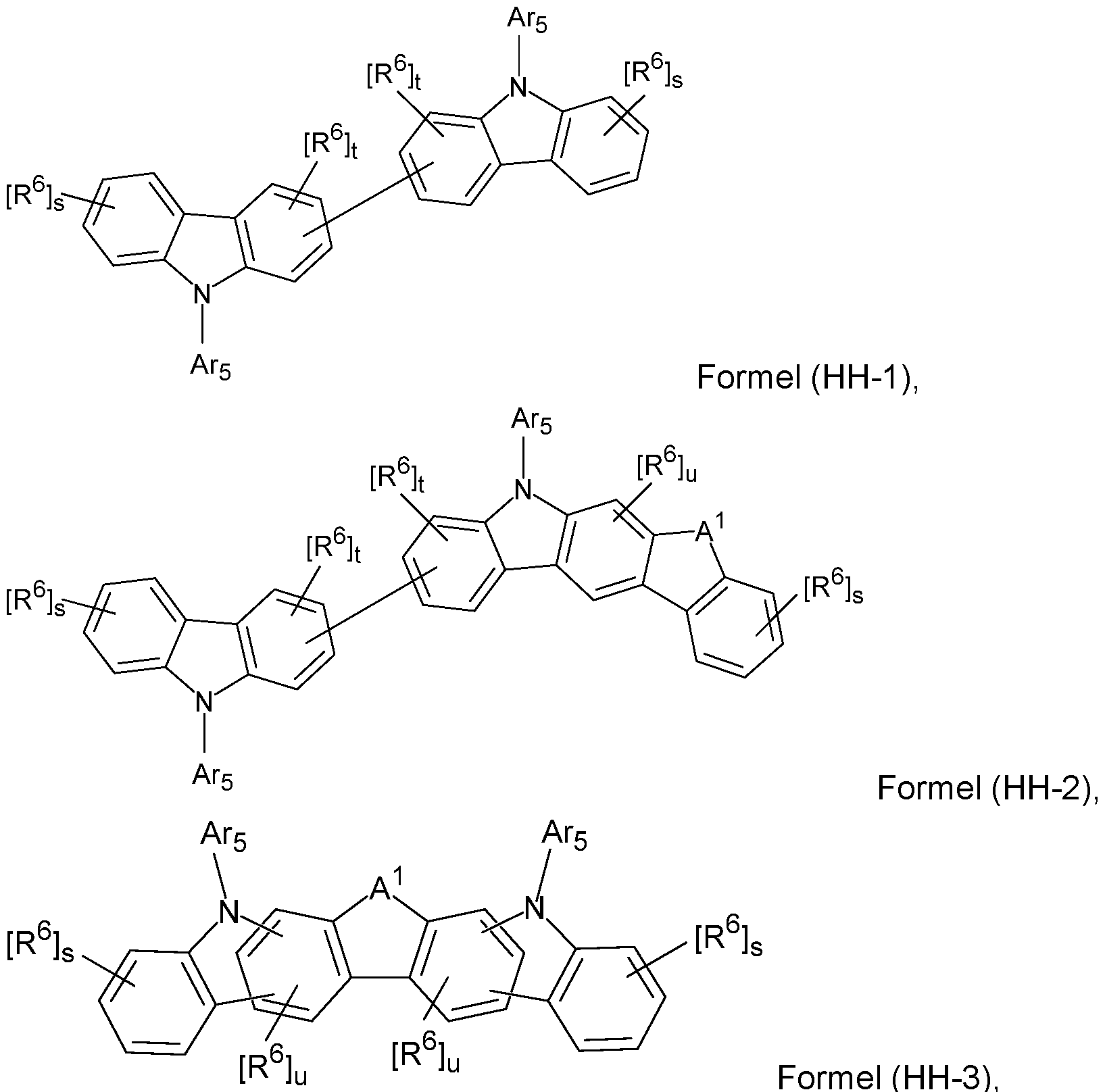
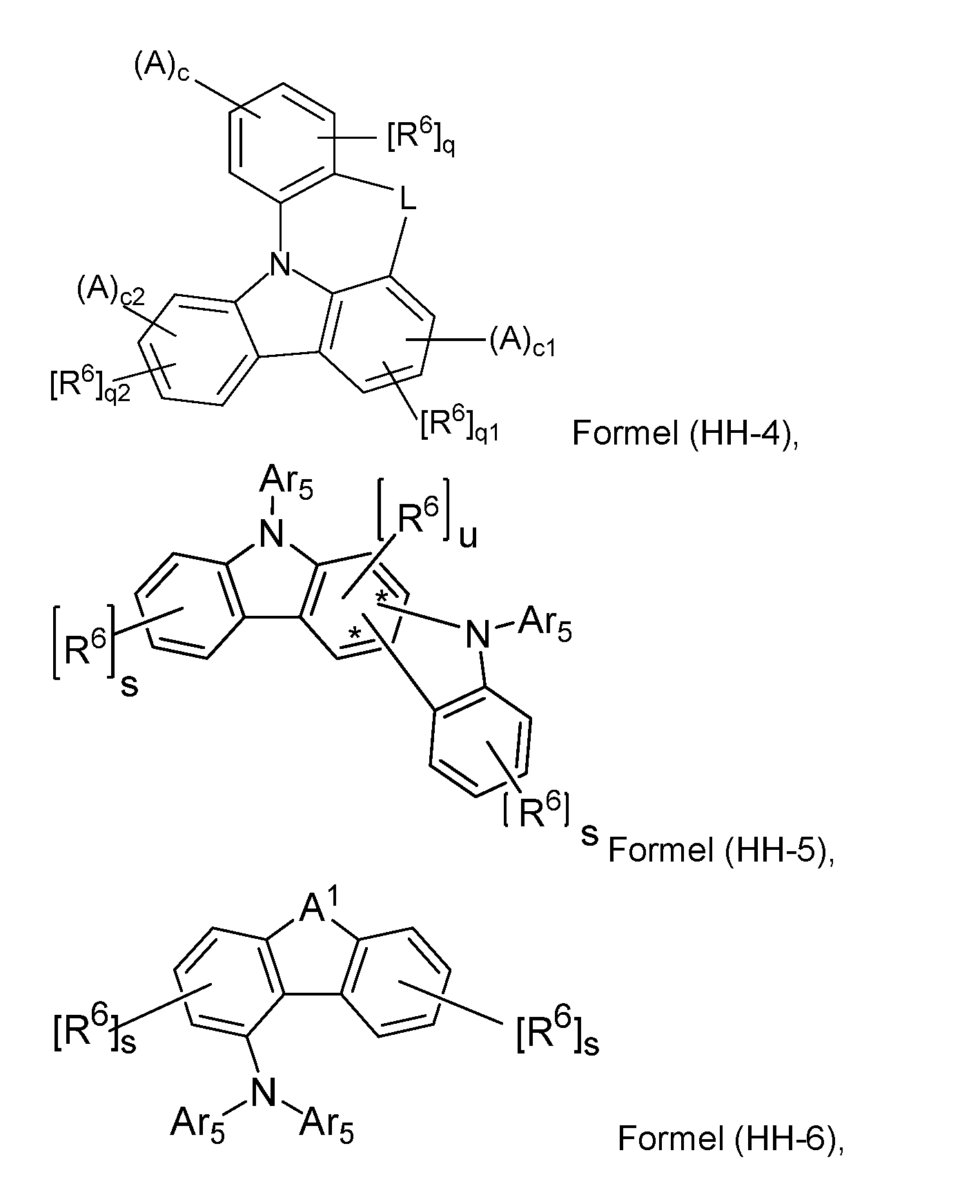
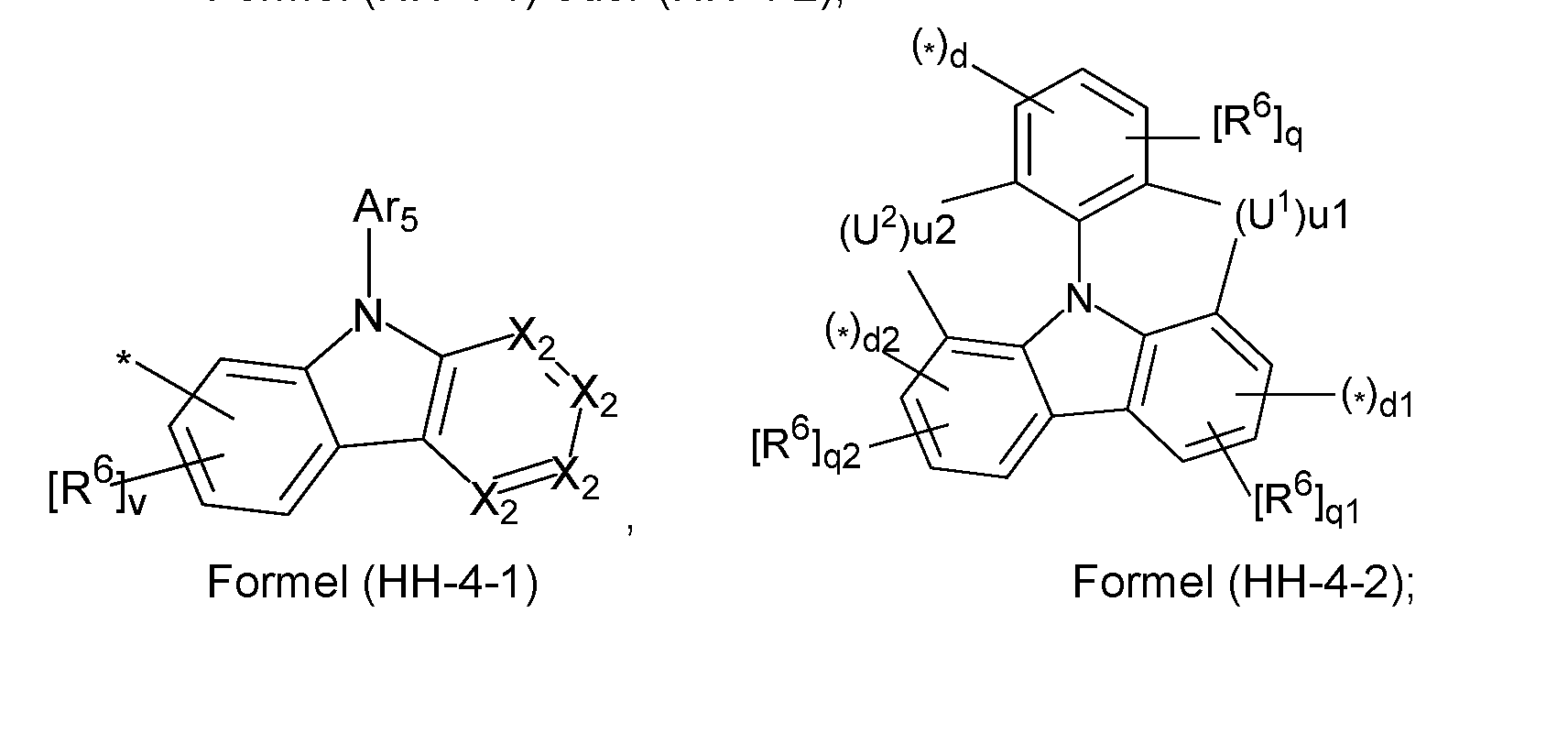
- Particularly suitable hole-transporting matrix materials which are advantageously combined with compounds of the formula (1), as described above or preferably described, in a mixed matrix system, can be selected from the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), as described below.
- a further subject matter of the invention is therefore an organic electronic device comprising an anode, a cathode and at least one organic layer containing at least one light-emitting layer, wherein the at least one light-emitting layer contains at least one compound of the formula (1) as matrix material 1, as described above or as preferred, and at least one compound of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6) as matrix material 2, , - 70 - where the symbols and indices used are: A 1 is C(R 7 ) 2 , NR 7 , O or S; L is a bond, O, S, C(R 7 ) 2 or NR 7 ; A is at each occurrence independently a group of the formula (HH-4-1) or (HH-4-2), X2 is, on each occurrence, the same or different, CH, CR 6 or N, where a maximum of 2 symbols X2 can be N; * indicates the bonding site to the formula (HH-4); U 1 , U
- s is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0.
- t is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0.
- u is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0.
- the sum of the indices s, t and u in compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-5) or (HH-6) is preferably at most 6, particularly preferably at most 4 and particularly preferably at most 2. This preferably applies if R 6 is different from D.
- c, c1, c2 each independently represent 0 or 1 at each occurrence, where the sum of the indices on each occurrence means c+c1+c21.
- c2 has the meaning 1.
- L is preferably a single bond or C(R 7 ) 2 , where R 7 has a meaning given above, particularly preferably L is a single bond.
- v is preferably 0 or 1 if the radical R 6 is different from D.
- U 1 or U 2 on each occurrence are preferably a single bond or C(R 7 ) 2 , where R 7 has a meaning given above, particularly preferably U 1 or U 2 on each occurrence are a single bond.
- q, q1, q2 are preferably 0 or 1 if the radical R 6 is different from D.
- R 6 is the same or different on each occurrence and is selected from the group consisting of D, F, CN, a straight-chain alkyl group having 1 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl group can be substituted in each case by one or more radicals R 7 , or an aromatic or heteroaromatic ring system having 5 to 60 ring atoms, preferably having 5 to 40 ring atoms, which can be substituted in each case by one or more radicals R 7 .
- R 6 is the same or different on each occurrence and is selected from the group consisting of D or an aromatic or heteroaromatic ring system having 6 to 30 ring atoms, which may be substituted by one or more radicals R 7.
- Ar5 in compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-5) or (HH-6) is selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorenyl, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorenyl, which can be linked via the 1-, 2-, 3- or 4-position, naphthyl, in particular 1- or 2-linked naphthyl, or residues derived from indole, benzofuran, benzothiophene, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked
- Ar5 is preferably not substituted. If A 1 in formula (HH-2) or (HH-3) or (HH-6) is NR 7 , the substituent R 7 which is bonded to the nitrogen atom preferably represents an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 8 . In a particularly preferred embodiment, this substituent R 7 is the same or different on each occurrence and represents an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, in particular having 6 to 18 aromatic ring atoms.
- R 7 Preferred embodiments for R 7 are phenyl, biphenyl, terphenyl and quaterphenyl, which are preferably unsubstituted, and radicals derived from triazine, pyrimidine and quinazoline, which can be substituted by one or more radicals R 8 .
- a 1 in formula (HH-2) or (HH-3) or (HH-6) is C(R 7 ) 2
- the substituents R 7 which are bonded to this carbon atom are preferably identical or different on each occurrence and represent a linear alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms or an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which can also be substituted by one or more radicals R 8 .
- R 7 is very particularly preferably a methyl group or for a phenyl group.
- the radicals R 7 can also form a ring system with one another, which leads to a spiro system.
- these compounds are partially or fully deuterated, particularly preferably fully deuterated.
- the preparation of the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6) are generally known and some of the compounds are commercially available.
- Compounds of the formula (HH-4) are disclosed, for example, in WO2021/180614, pages 110 to 119, in particular as examples on pages 120 to 127. Their preparation is disclosed in WO2021/180614 A1 on page 128 and in the synthesis examples on pages 214 to 218.
- the preparation of the triarylamines of the formula (HH-6) is known to the person skilled in the art and some of the compounds are commercially available.
- the at least one further matrix material is a deuterated compound, it is possible that this at least one matrix material is a mixture of deuterated compounds with the same basic chemical structure, which differ only in the degree of deuteration.
- this is a mixture of deuterated compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), as described above, the degree of deuteration of these compounds being at least 50% to 90%, preferably 70% to 100%.
- this is a mixture of deuterated compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and/or (HH-6), as described above, wherein the degree of deuteration of these compounds is at least 50% to 90%, preferably 70% to 100%.
- Corresponding deuteration methods are known to the person skilled in the art and are described, for example, in KR2016041014 A, WO2017/122988 A1, KR2020052820 A, KR101978651 B1 and WO2018/110887 A1 or in Bulletin of the Chemical Society of Japan, 2021, 94(2), 600-605 or Asian Journal of Organic Chemistry, 2017, 6(8), 1063-1071.
- suitable further matrix materials for a combination with compounds of the formula (1) are the compounds described in WO2019/229011 A1, Table 3, pages 137 to 203, which can also be partially or completely deuterated.
- suitable further matrix materials for a combination with compounds of the formula (1) or preferred compounds of the formula (1), as previously described or preferably described are the compounds described in WO2021/180625 A1, Table 3, pages 131 to 127 and in Table 4, pages 137 to 139, which may also be partially or fully deuterated.
- Suitable further matrix materials for a combination with compounds of the formula (1) or preferred compounds of the formula (1) are the compounds described in KR20230034896 A, on pages 42 to 47, compounds [2-1] to [2-110], or on pages 49 to 51, compounds [3-1] to [3-26].
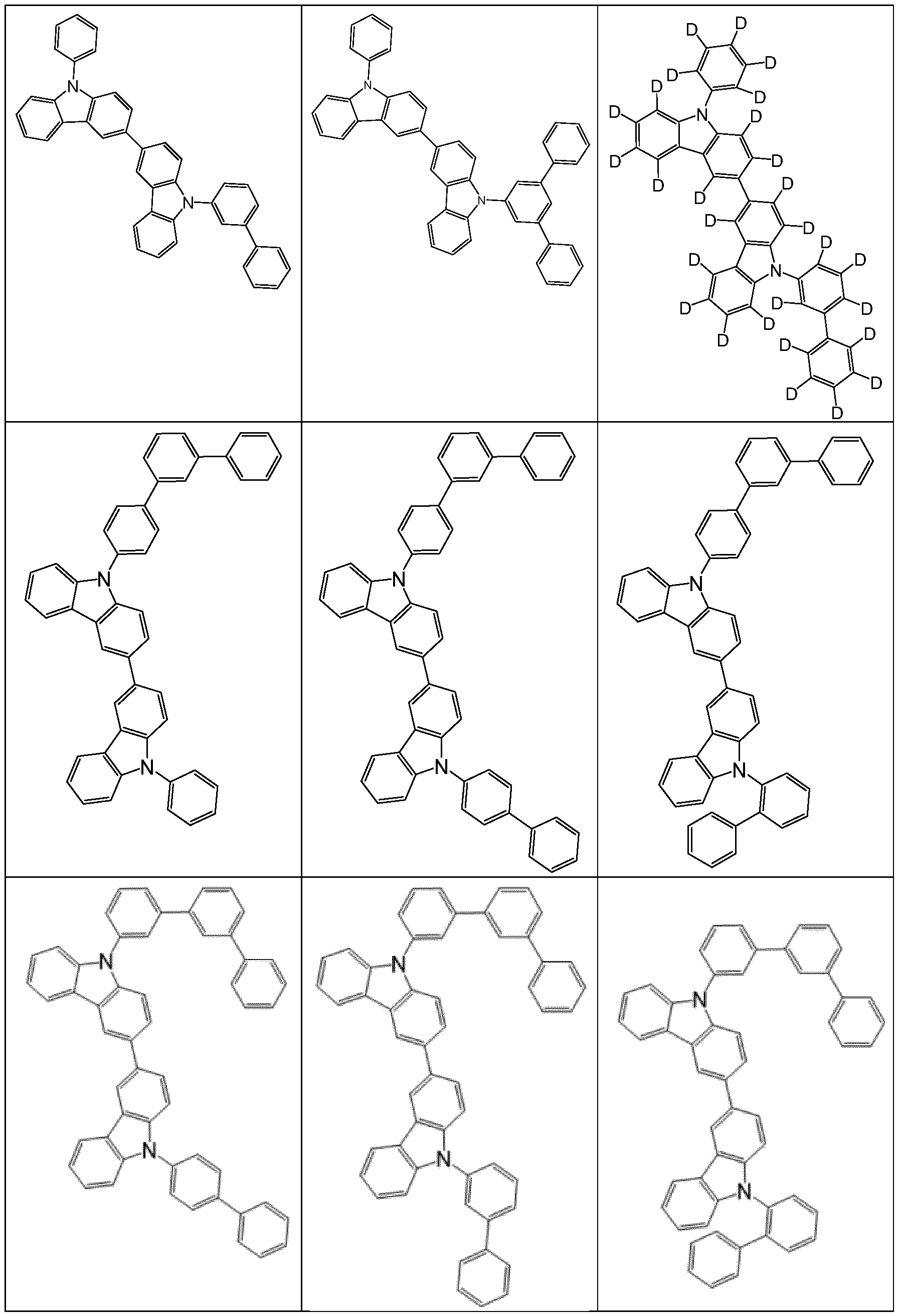
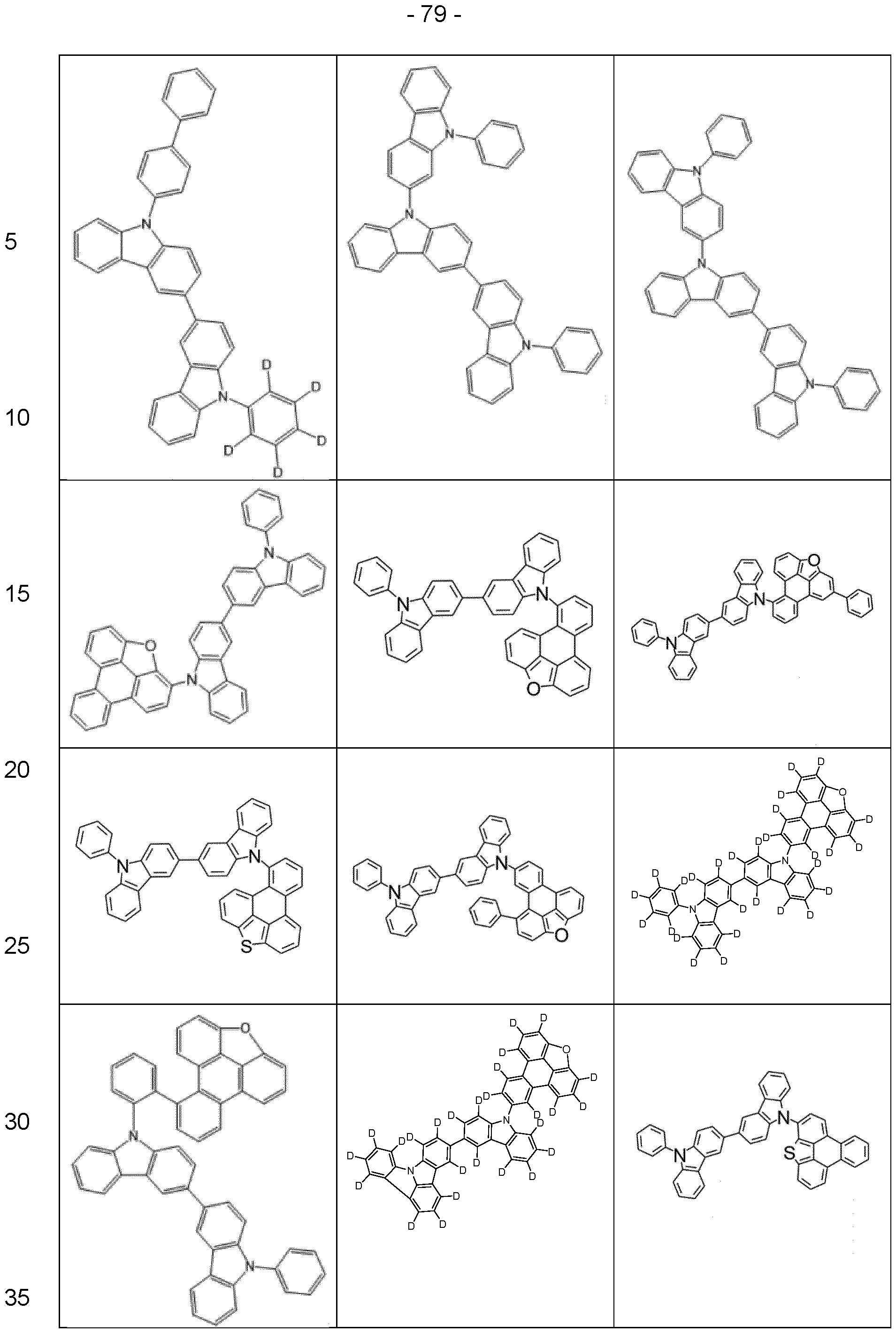
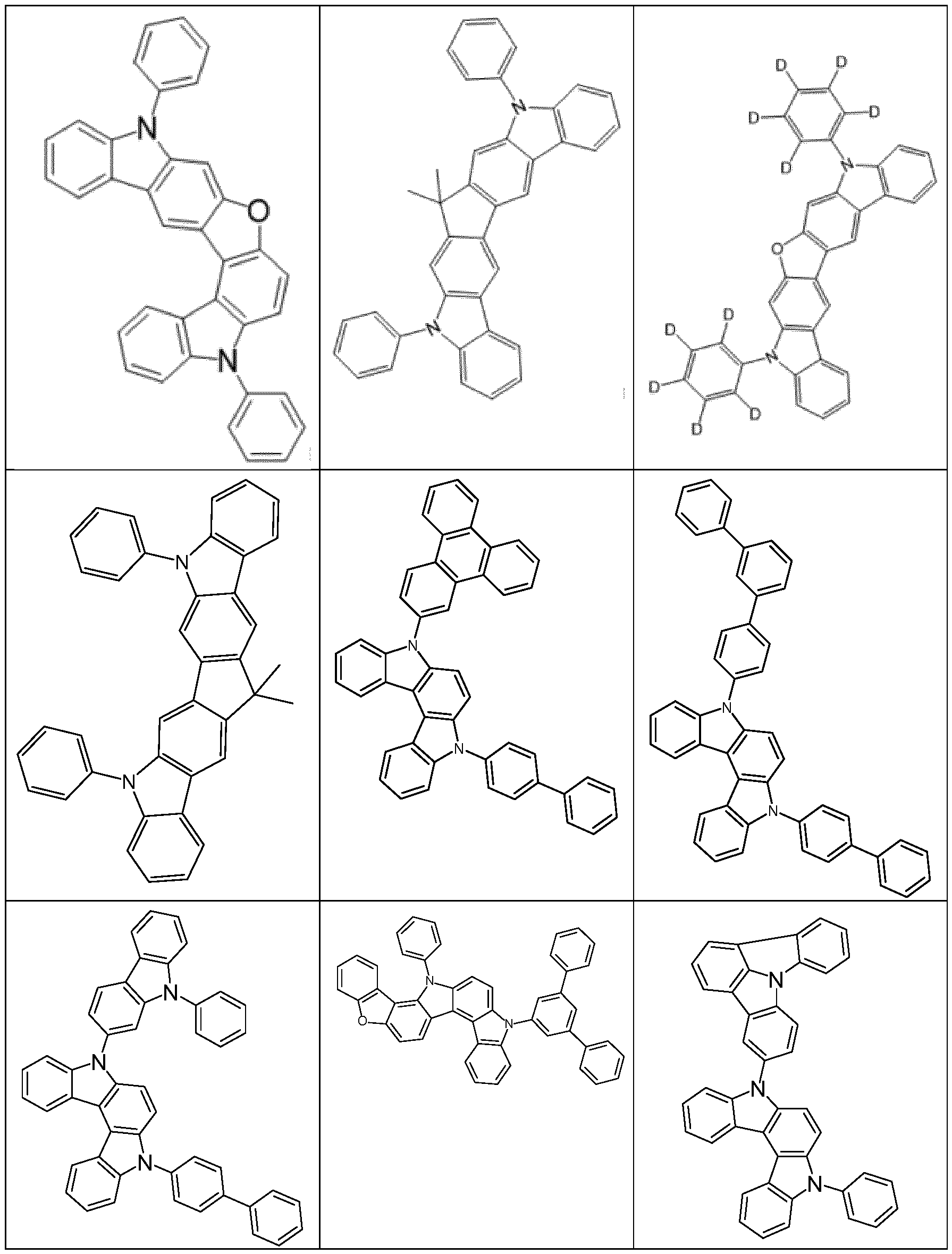
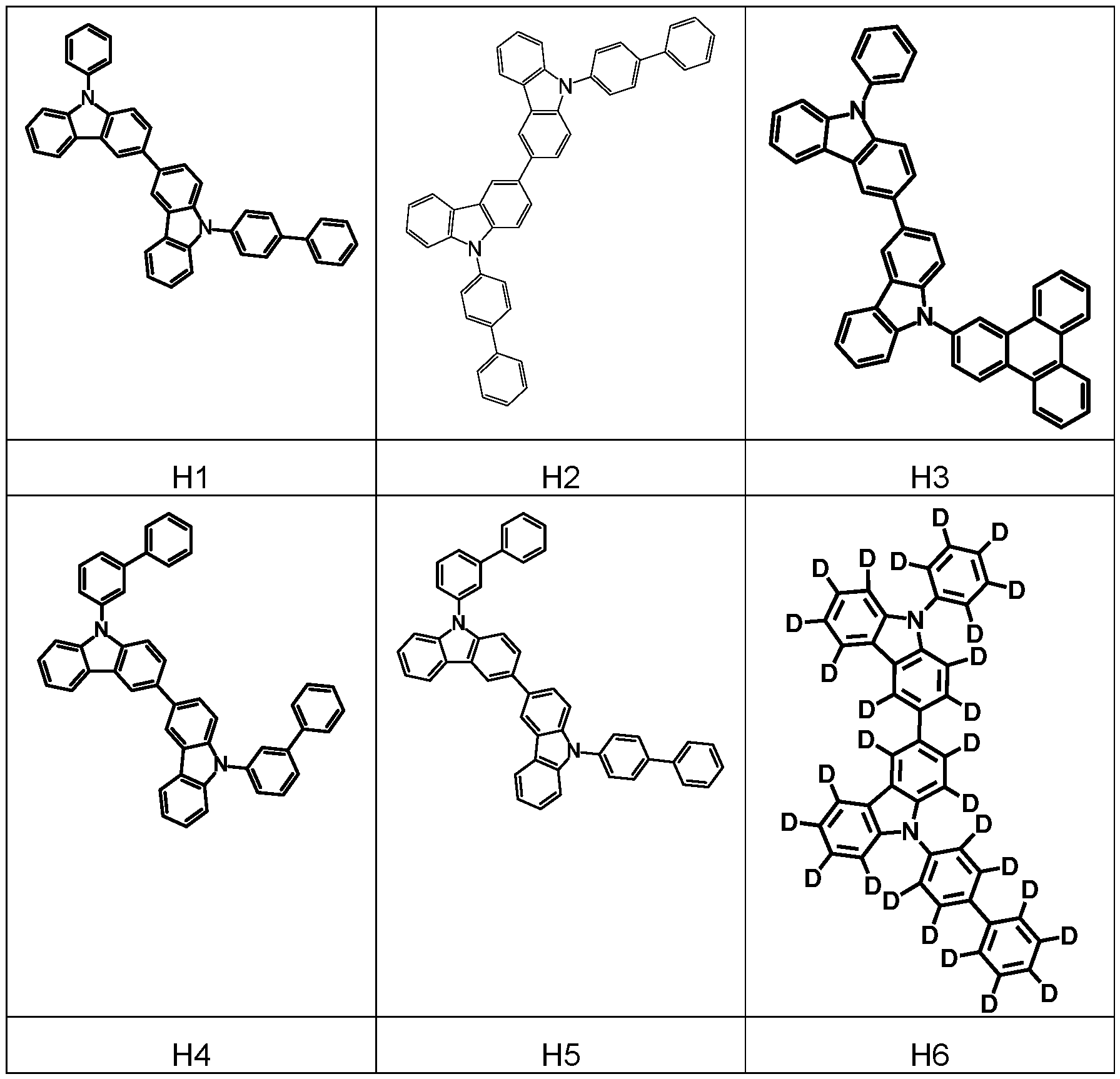
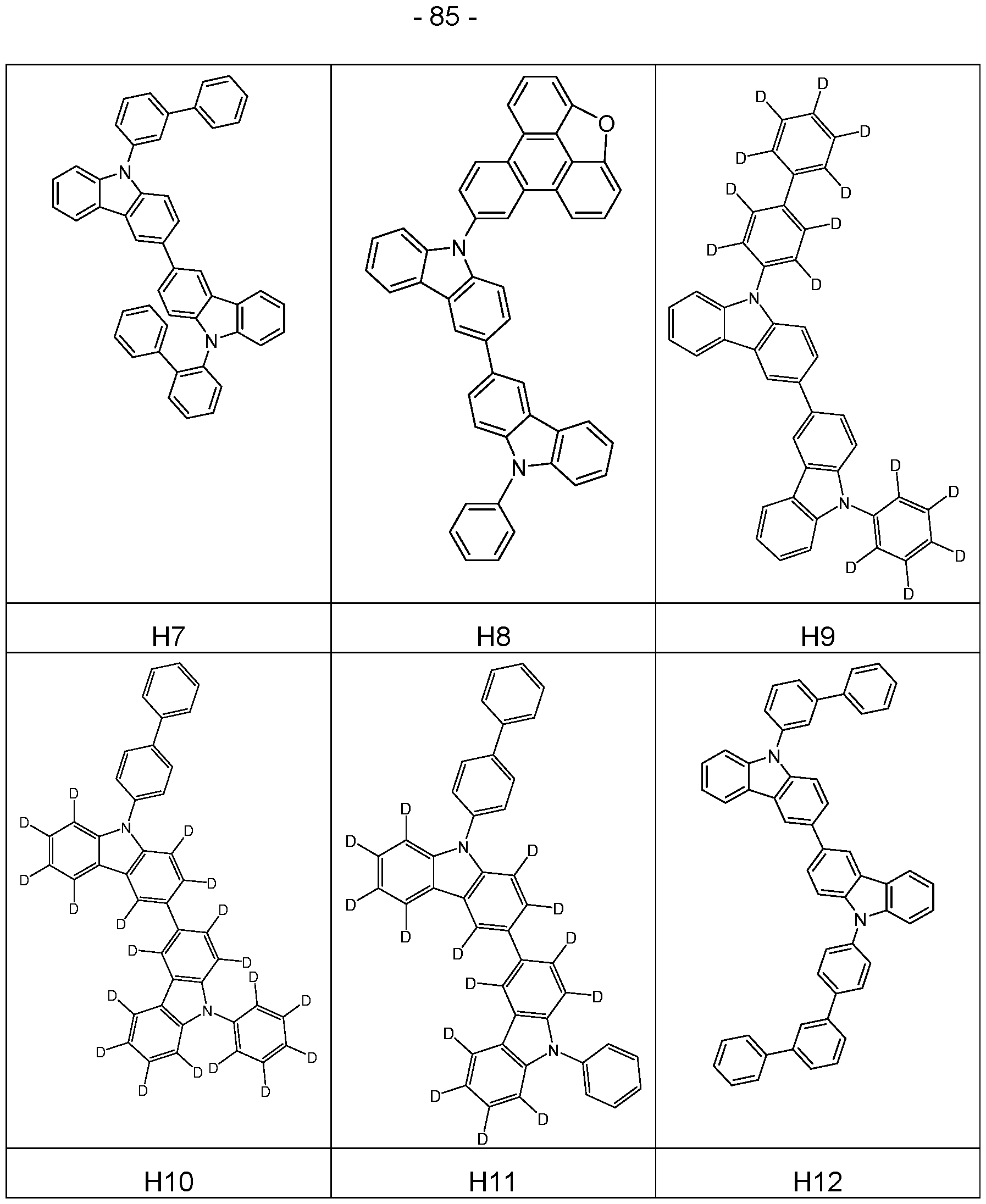
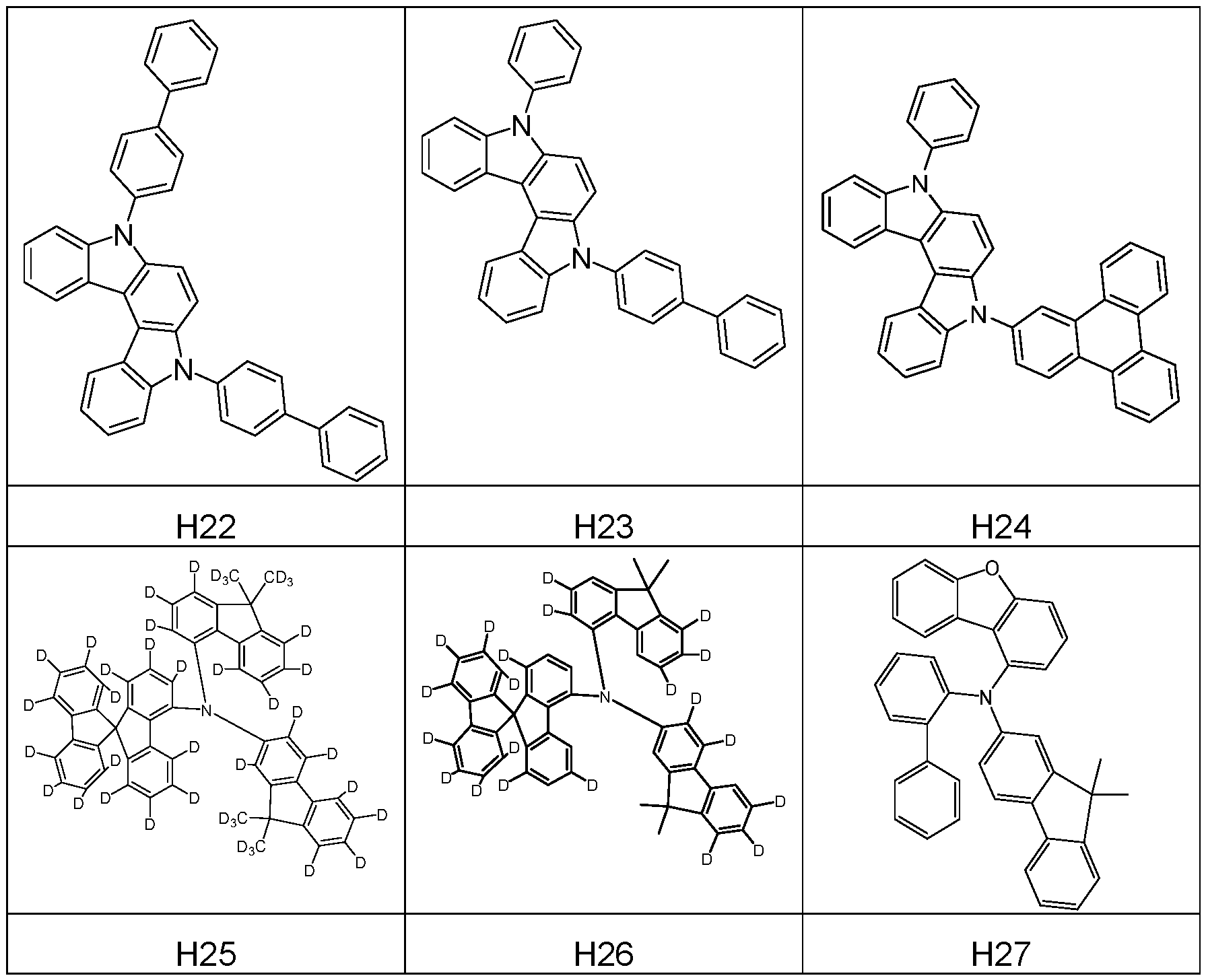
- suitable host materials of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6) for combination with compounds of the formula (1) or preferred embodiments are the structures listed in Tables 1 and 2 below. Table 1:
- Particularly suitable compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), which are selected according to the invention and are preferably used in combination with at least one compound of the formula (1) in the electroluminescent device according to the invention, are the compounds of Table 2.
- the above-mentioned host materials of formula (1) and their preferred embodiments can be combined as desired in the device according to the invention with the previously mentioned matrix materials/host materials, the matrix materials/host materials of formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6) and their preferred embodiments in Table 1 or the compounds H1 to H27.
- the concentration of the host material of formula (1), as described above or preferably described, in the mixture according to the invention or in the light-emitting layer of the device according to the invention is usually in the range from 5% by weight to 90% by weight, preferably in the range from 10% by weight to 85% by weight, more preferably in the range from 20% by weight to 85% by weight, even more preferably in the range from 30% by weight to 80% by weight, very particularly preferably in the range from 20% by weight to 60% by weight and most preferably in the range from 30 wt. % to 50 wt. %, based on the entire mixture or based on the entire composition of the light-emitting layer.
- the concentration of the sum of all host materials of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), as described above or described as preferred, in the mixture according to the invention or in the light-emitting layer of the device according to the invention is usually in the range from 10 wt. % to 95 wt. %, preferably in the range from 15 wt. % to 90 wt. %, more preferably in the range from 15 wt. % to 80 wt. %, even more preferably in the range from 20 wt. % to 70 wt. %, very particularly preferably in the range from 40 wt. % to 80 wt.
- the present invention also relates to a mixture which, in addition to the above-mentioned host materials of the formula (1), hereinafter referred to as host material 1, and the host material of at least one of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), hereinafter referred to as host material 2, as previously described or preferably described, contains at least one phosphorescent emitter.
- the present invention also relates to an organic electroluminescent device, as previously described or preferably described, wherein the light-emitting layer contains, in addition to the above-mentioned host materials of the formula (1) and at least one of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), as previously described or preferably described, in particular the material combinations M1 to M729, at least one phosphorescent emitter.
- Suitable charge transport materials as can be used in the hole injection or hole transport layer or in the electron barrier layer or in the electron transport layer of the electronic component according to the invention, are, in addition to the compounds of formula (1), for example those mentioned in Y. Shirota et al., Chem.
- indenofluorenamine derivatives for example according to WO 06/122630 or WO 06/100896
- the amine derivatives disclosed in EP 1661888 hexaazatriphenylene derivatives (for example according to WO 01/049806), amine derivatives with fused aromatics (for example according to US 5,061,569), the amine derivatives disclosed in WO 95/09147, monobenzoindenofluorenamines (for example according to WO 08/006449), dibenzoindenofluorenamines (for example according to WO 07/140847), spirobifluorenamines (for example according to WO 2012/034627 or WO 2013/120577), fluorenamines (for example according to WO 2014/015937, WO 2014/015938, WO 2014/015935 and WO 2015/082056), spirodibenzopyranamines (for example
- the OLED according to the invention preferably comprises two or more different electron-transporting layers.
- the compound of the formula (1) can be used in one or more or in all electron-transporting layers.
- the compound of the formula (1) is used in exactly one or exactly two electron-transporting layers, and other compounds are used in the other electron-transporting layers present.
- Other compounds which can be used in addition to the compounds of the formula (1) are all materials which are used according to the prior art as electron-transport materials in the electron-transport layer.
- Particularly suitable are aluminum complexes, e.g. Alq3, zirconium complexes, e.g. Zrq4, lithium complexes, e.g.
- Liq Liq, benzimidazole derivatives, triazine derivatives, pyrimidine derivatives, pyridine derivatives, pyrazine derivatives, quinoxaline derivatives, quinoline derivatives, oxadiazole derivatives, aromatic ketones, lactams, boranes, diazaphosphole derivatives and phosphine oxide derivatives.
- Other suitable materials are derivatives of the aforementioned compounds, as disclosed in JP 2000/053957, WO 2003/060956, WO 2004/028217, WO 2004/080975 and WO 2010/072300.
- Preferred cathodes of the electronic component are metals with a low work function, metal alloys or multilayer structures made of different metals, e.g. B.
- alkaline earth metals alkali metals, main group metals or lanthanides (e.g. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Alloys of an alkali or alkaline earth metal and silver are also suitable, e.g. an alloy of magnesium and silver.
- other metals with a relatively high work function can also be used, e.g. Ag or Al, whereby combinations of the metals such as Ca/Ag, Mg/Ag or Ba/Ag are generally used. It can also be advantageous to use a thin intermediate layer made of a material with a high dielectric constant between a metallic cathode and the organic semiconductors.
- suitable materials are alkali or alkaline earth metal fluorides, but also the corresponding oxides or carbonates (e.g. LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3, etc.). It is also possible to use lithium quinolinate (LiQ) for this purpose.
- the layer thickness of this layer is preferably between 0.5 and 5 nm.
- Preferred anodes are materials with a high work function.
- the anode preferably has a work function of more than 4.5 eV against vacuum.
- metals with a high redox potential are suitable for this, e.g. Ag, Pt or Au.
- metal/metal oxide electrodes e.g.
- Al/Ni/NiOx, Al/PtOx can also be preferred.
- at least one of the electrodes must be transparent or partially transparent in order to enable the irradiation of the organic material (organic solar cell) or the emission of light (OLED, O laser).
- Preferred anode materials here are conductive metal mixed oxides. Indium tin oxide (ITO) or indium zinc oxide (IZO) are particularly preferred. Conductively doped organic materials, in particular conductively doped polymers, are further preferred.
- the anode can also consist of two or more layers, for example an inner layer of ITO and an outer layer of a metal oxide, preferably tungsten oxide, molybdenum oxide or vanadium oxide.
- the device is structured accordingly (depending on the application), contacted and finally sealed to exclude harmful influences from water and air.
- all materials can be used as are usually used according to the prior art.
- the person skilled in the art can therefore, without inventive step, use all materials known for organic electroluminescent devices in combination with the compounds according to the invention according to formula (1) or the preferred embodiments set out above.
- an organic electroluminescent device characterized in that one or more layers are coated using a sublimation process.
- the materials are vapor-deposited in vacuum sublimation systems at an initial pressure of less than 10 -5 mbar, preferably less than 10 -6 mbar.
- the initial pressure is even lower, for example less than 10 -7 mbar.
- an organic electroluminescent device characterized in that one or more layers are coated using the OVPD (Organic Vapour Phase Deposition) process or with the aid of carrier gas sublimation. The materials are applied at a pressure of between 10 -5 mbar and 1 bar.
- OVPD Organic Vapour Phase Deposition
- a special case of this process is the OVJP (Organic Vapour Jet Printing) process, in which the materials are applied directly through a nozzle and thus structured.
- an organic electroluminescent device characterized in that one or more layers are coated from solution, such as by spin coating, or using any printing process, such as B.
- the electronic devices containing one or more compounds of formula (1) can be used in displays, as light sources in lighting applications and as light sources in medical and/or cosmetic applications (e.g. light therapy).
- the compounds according to the invention and the organic electroluminescent devices according to the invention are characterized by one or more of the following properties: 1.
- the compounds according to the invention lead to long lifetimes. 2.
- the compounds according to the invention lead to high efficiencies, in particular to a high EQE. 3.
- the compounds according to the invention lead to low operating voltages. 4.
- the compounds according to the invention show improved oxidation stability in solution, which has a positive effect on the handling of the compounds, for example when processing in printing processes. 5.
- the compounds according to the invention show high temperature stability, so that they can be evaporated without decomposition in a high vacuum. The invention is explained in more detail by the following examples, without wishing to restrict it thereby.
- the person skilled in the art can carry out the invention in the entire disclosed area and, without inventive step, produce further compounds according to the invention and use them in electronic devices or apply the method according to the invention.
- the reactants can be obtained from ALDRICH or ABCR (palladium(II) acetate, tri-o-tolylphosphine, inorganics, solvents).
- the information for the reactants known from the literature are the CAS numbers.
- Example a 2-(2 ⁇ chloro ⁇ 3,3,4,4,5,5 ⁇ hexafluorocyclopent ⁇ 1 ⁇ en ⁇ 1 ⁇ yl)biphenyl Under an argon atmosphere, 1,1'-biphenyl-3-boronic acid (14.8 g, 75 mmol, 1.5 equiv.), Pd 2 dba 3 ⁇ CHCl 3 (2.5, 0.0025 mol, 1 mol% Pd), X-Phos (4.7 mg, 0.001 mol, 2 mol%) and K 3 PO 4 (300 g, 150 mmol, 3 equiv.) are initially charged.
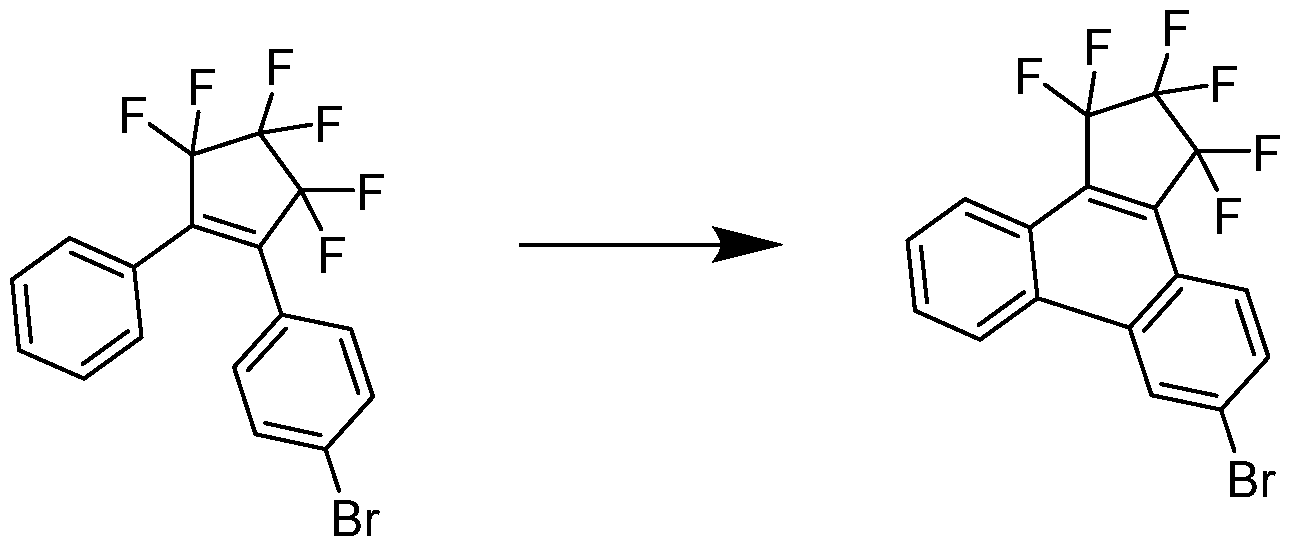
- Example b 6 ⁇ Bromo ⁇ 1,1,2,2,3,3 ⁇ hexafluoro ⁇ 1H,2H,3H ⁇ cyclopenta[l]phenanthrene
- iodine 2.9 g, 12 mmol
- benzene 300 ml
- 1,2-epoxybutane 300 ml, 350 mmol
- Example c 2 ⁇ 1,1,2,2,3,3 ⁇ Hexafluoro ⁇ 1H,2H,3H ⁇ cyclopenta[l]phenanthren ⁇ 6 ⁇ yl ⁇ triphenylene
- Triphenylene-2-boronic acid 35 g, 130 mmol
- 6-bromo-1,1,2,2,3,3-hexa-fluoro-1H,2H,3H-cyclopenta[l]phenanthrene (44.5 g, 110 mmol)
- tripotassium phosphate (44.6 g, 210.0 mmol) are suspended in 500 mL toluene, 500 mL dioxane and 500 mL water.
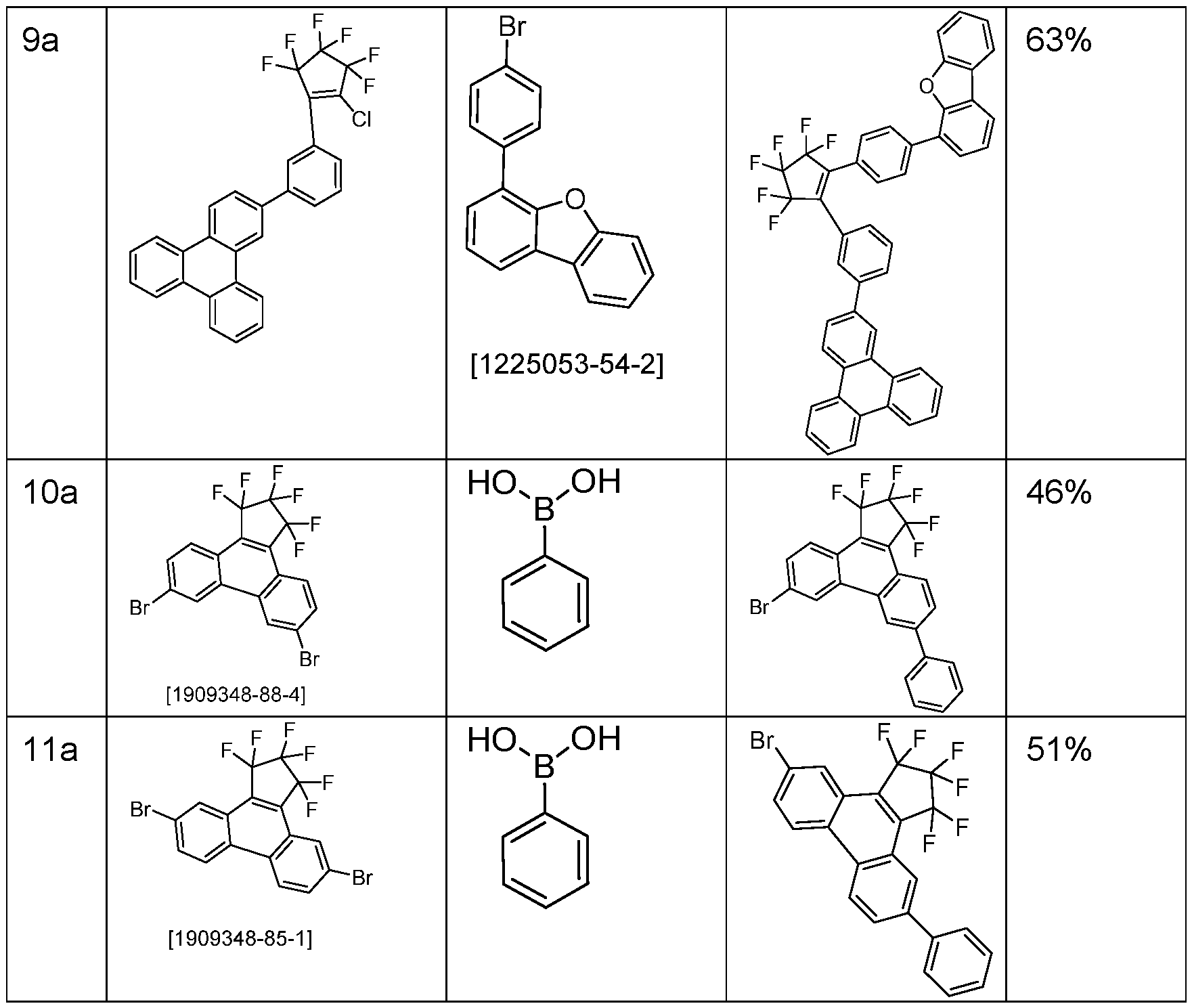
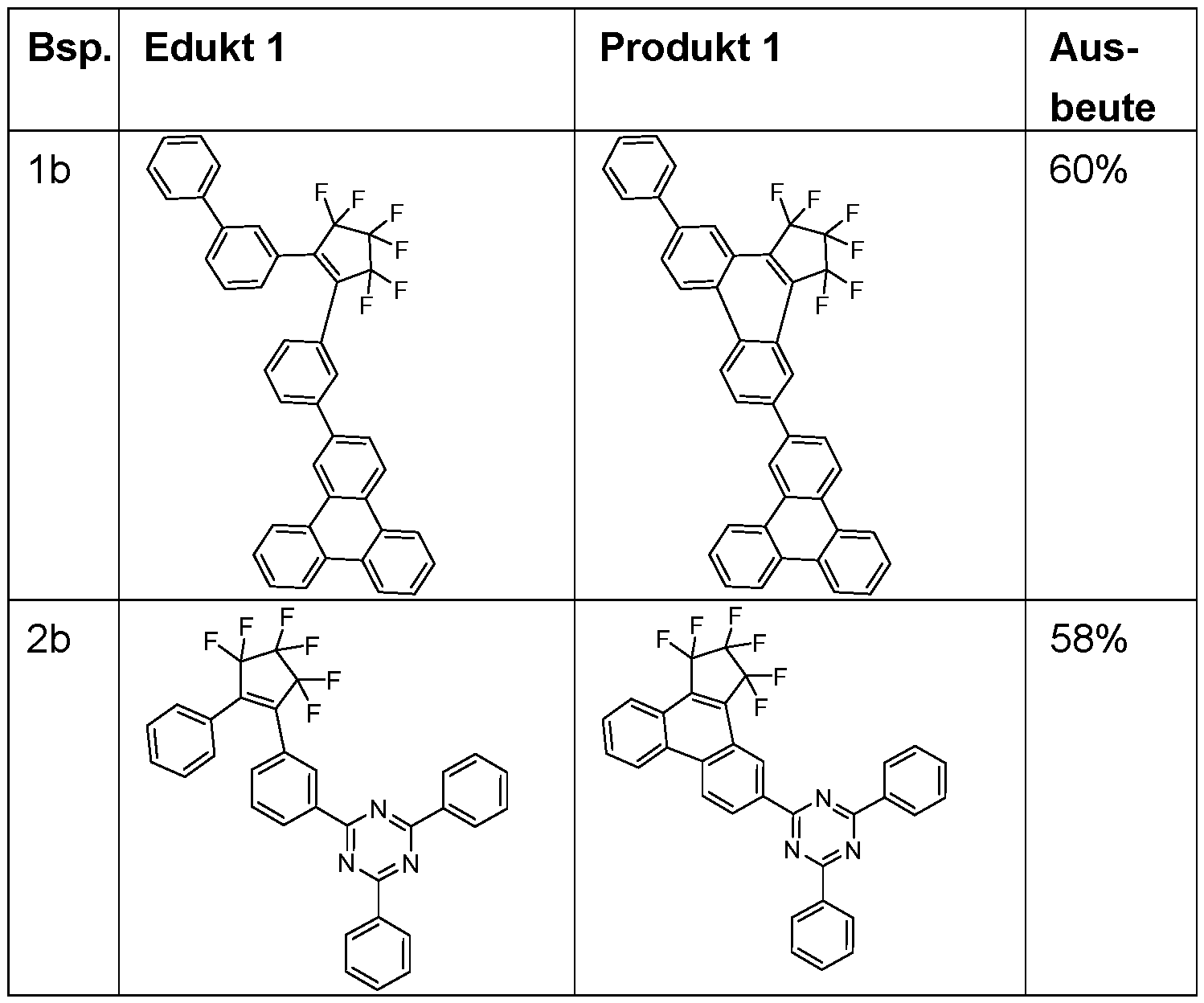
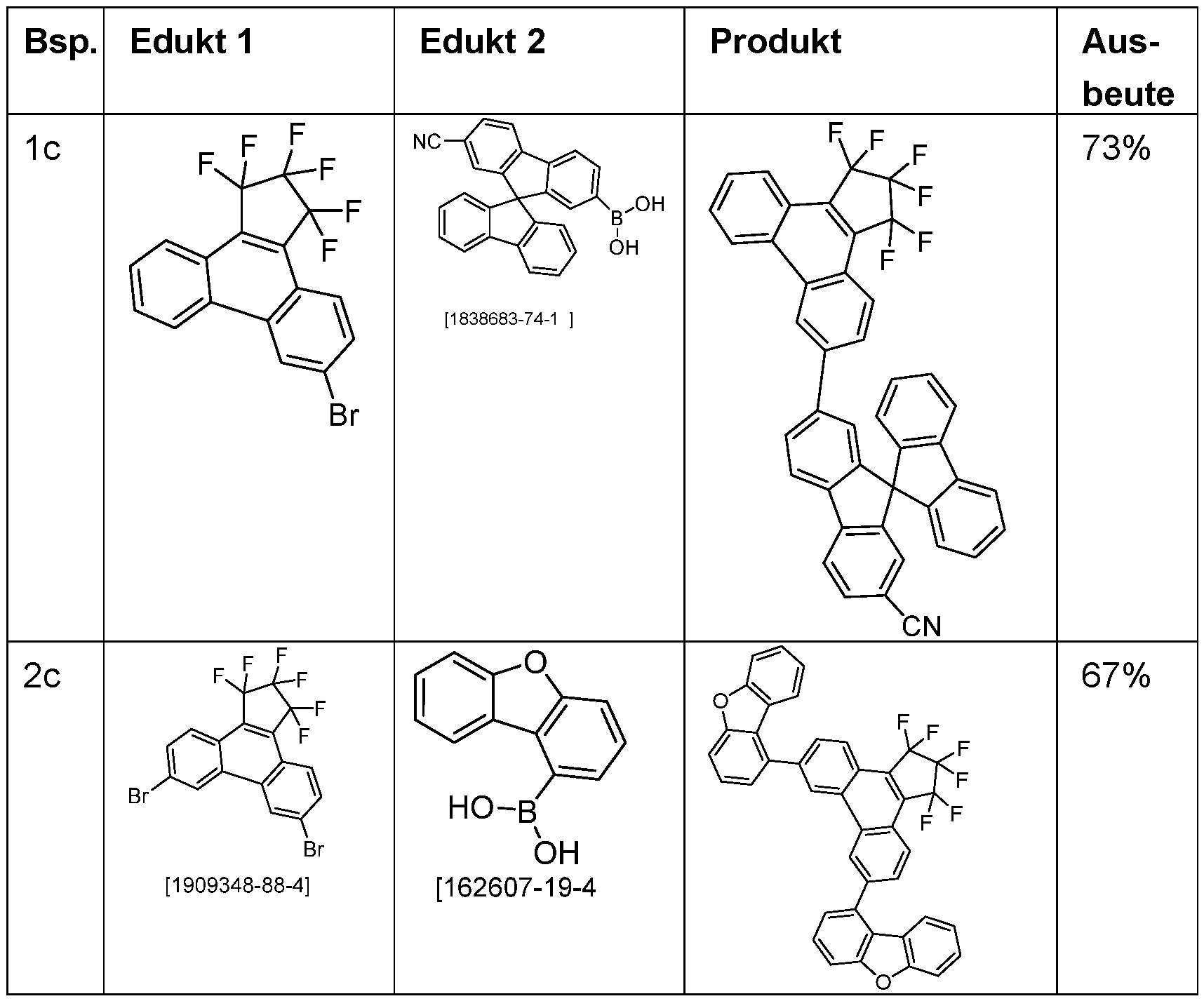
- Tri-o-tolylphosphine (913 mg, 3.0 mmol) and then palladium(II) acetate (112 mg, 0.5 mmol) are added to this suspension and the reaction mixture is heated under reflux for 16 h. After cooling, the organic phase is separated, filtered through silica gel, washed three times with 200 mL water each time and then concentrated. The residue is recrystallized from toluene and from dichloromethane/isopropanol and finally sublimed under high vacuum. The purity is 99.9%. The yield is 42 g (77 mmol), corresponding to 71% of theory. The following compounds are obtained analogously:
- the following examples E1 to E10 present the use of the materials according to the invention in OLEDs.
- Pretreatment for examples E1 to E13 Glass plates coated with structured ITO (indium tin oxide) with a thickness of 50 nm are treated with an oxygen plasma, followed by an argon plasma, before coating. These plasma-treated glass plates form the substrates onto which the OLEDs are applied.
- the OLEDs basically have the following layer structure: substrate / optional interlayer (IL) / hole injection layer (HIL) / hole transport layer (HTL) / electron blocking layer (EBL) / emission layer (EML) / optional hole blocking layer (HBL) / electron transport layer (ETL) / optional electron injection layer (EIL) and finally a cathode.
- the cathode is formed by a 100 nm thick aluminum layer.
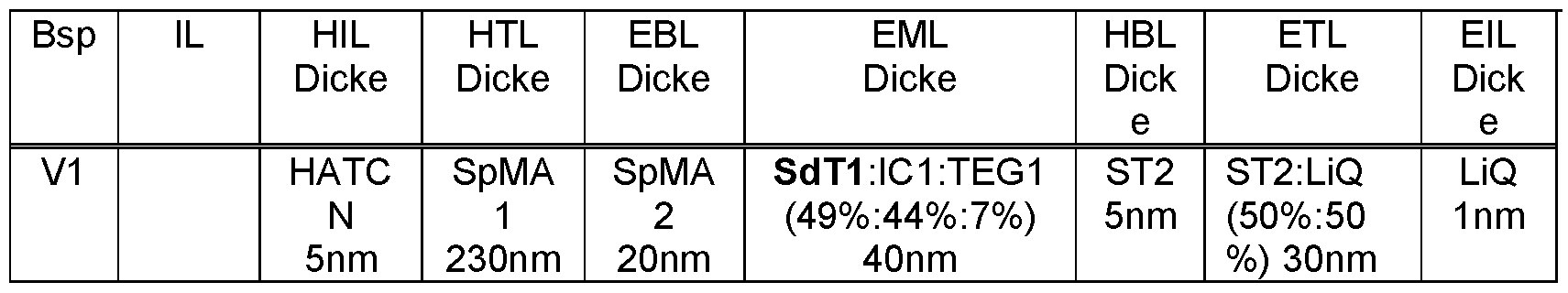
- Table 1 The exact structure of the OLEDs can be found in Table 1.
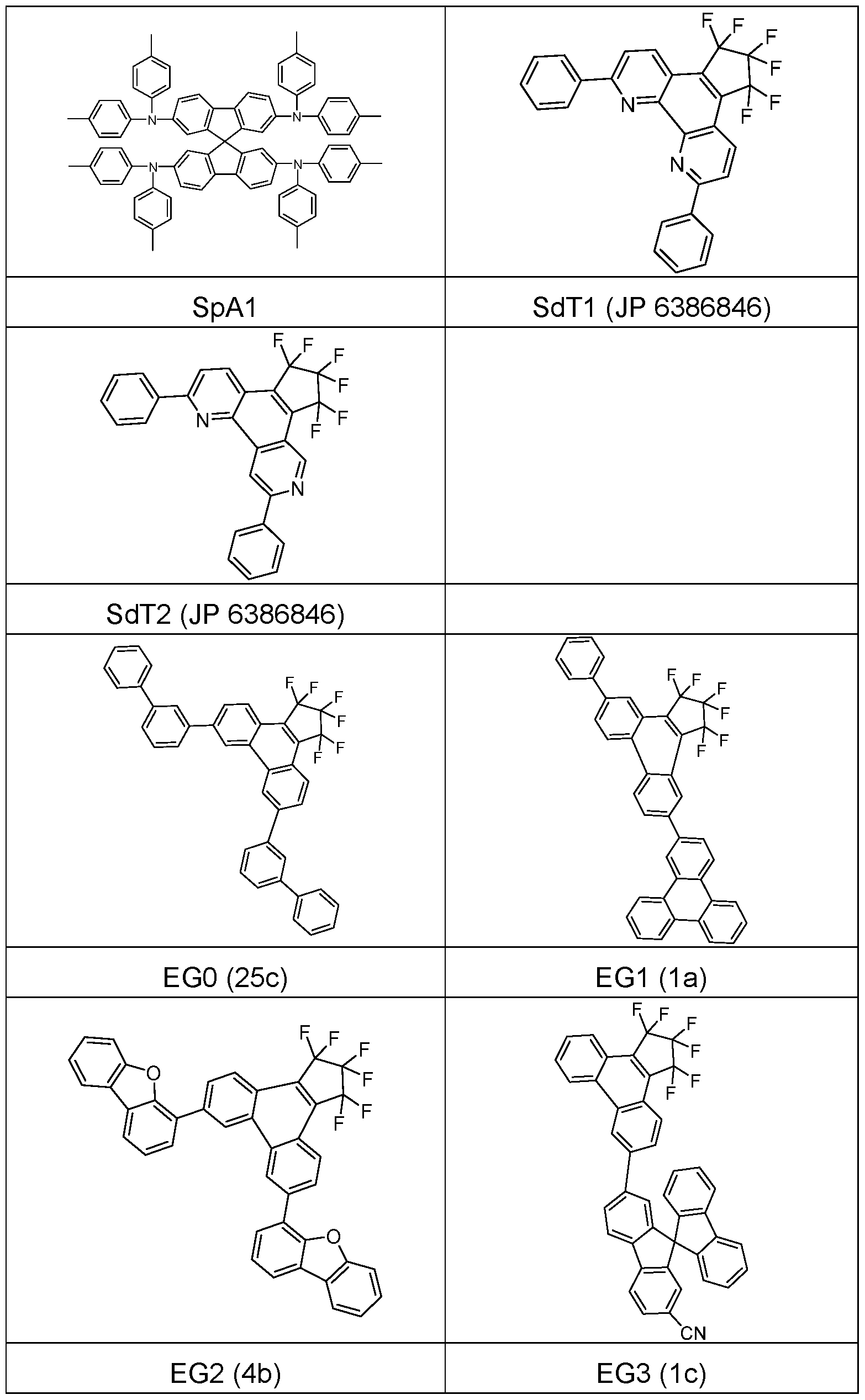
- the materials required to manufacture the OLEDs are shown in Table 2.
- the data for the OLEDs are listed in Tables 3 and 4. All materials are thermally vapor-deposited in a vacuum chamber.
- the emission layer always consists of at least one matrix material (host material) and an emitting dopant (dopant, emitter), which is mixed into the matrix material or materials by co-evaporation in a certain volume proportion.
- a specification such as IC1:EG1:TEG1 (45%:45%:10%) means that the material IC1 is present in the layer in a volume proportion of 45%, EG1 in a volume proportion of 45% and TEG1 in a volume proportion of 10%.
- the electron transport layer can also consist of a mixture of two materials.
- the OLEDs are characterized as standard.
- the electroluminescence spectra, the current efficiency (SE, measured in cd/A) and the external quantum efficiency (EQE, measured in %) are determined as a function of the luminance, calculated from current-voltage-luminance characteristics assuming a Lambertian radiation characteristic.
- the electroluminescence spectra are determined at a luminance of 1000 cd/m2 and the CIE 1931 x and y color coordinates are calculated from this. The results obtained in this way can be found in Table 3.
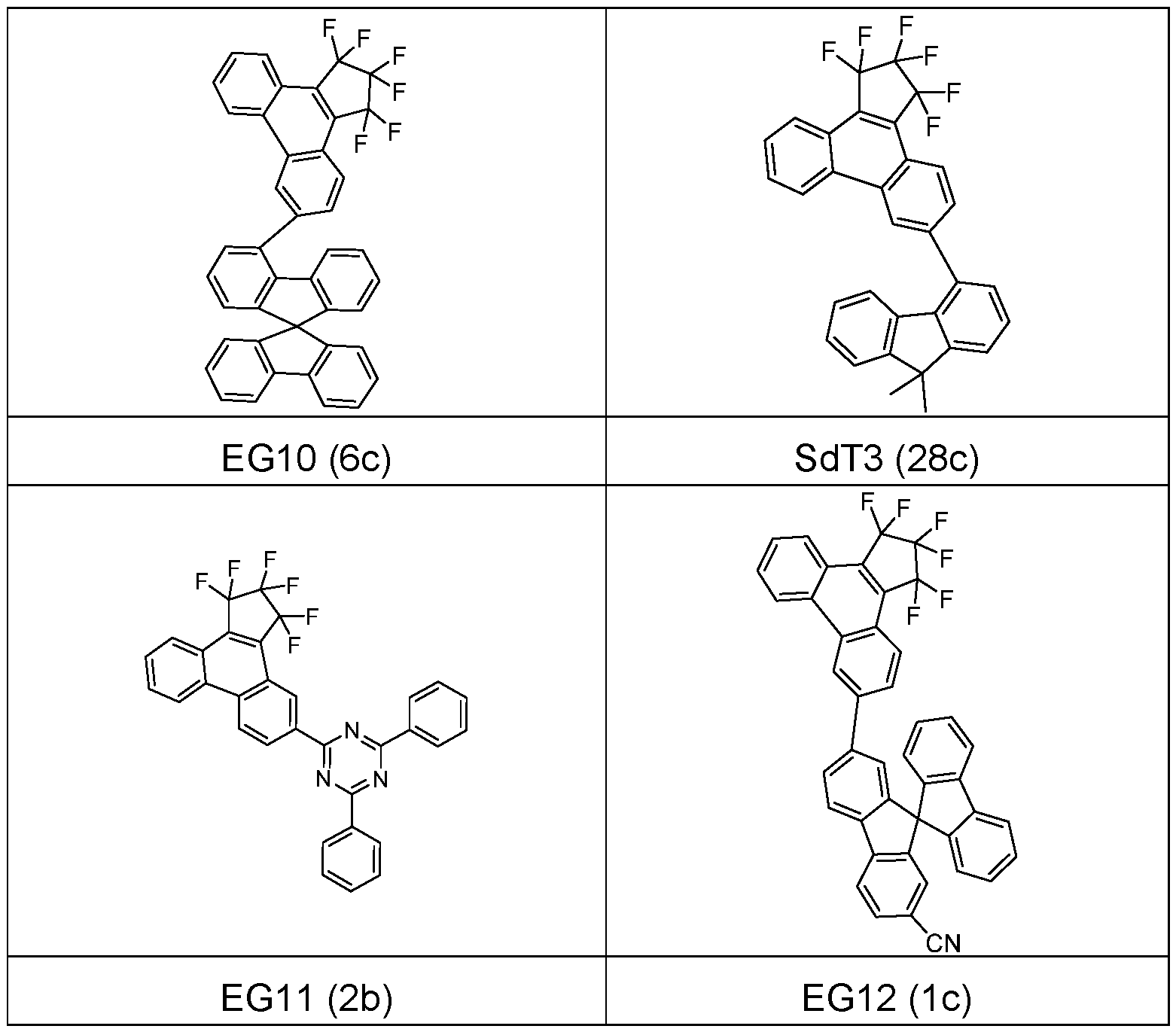
- the compounds EG0 to EG10 according to the invention can be used in Examples E1 to E11 as matrix material in the emission layer of phosphorescent green OLEDs and EG11 and EG12 in Examples E12 to E13 as electron transport material in the emission layer of phosphorescent green OLEDs.
- Table 1 Structure of the OLEDs
- Table 2 Structural formulas of the materials for the OLEDs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
Materialien für elektronische Vorrichtungen Die vorliegende Erfindung betrifft Materialien für die Verwendung in elektronischen Vorrichtungen, insbesondere in organischen Elektrolumi- neszenzvorrichtungen, sowie elektronische Vorrichtungen, insbesondere organische Elektrolumineszenzvorrichtungen enthaltend diese Materialien. Elektronische Vorrichtungen, welche organische, metallorganische und/oder polymere Halbleiter enthalten, gewinnen zunehmend an Bedeutung, wobei diese aus Kostengründen und aufgrund ihrer Leistungs- fähigkeit in vielen kommerziellen Produkten eingesetzt werden. Als Bei- spiele seien hier Ladungstransportmaterialien auf organischer Basis (z.B. Lochtransporter auf Triarylamin-Basis) in Kopiergeräten, organischen oder polymeren Leuchtdioden (OLEDs oder PLEDs) in Anzeige- und Display- vorrichtungen oder organische Photorezeptoren in Kopierern genannt. Organische Solarzellen (O-SC), organische Feldeffekt-Transistoren (O- FET), organische Dünnfilm-Transistoren (O-TFT), organische Schalt- elemente (O-IC), organische optische Verstärker und organische Laser- dioden (O-Laser) sind in einem fortgeschrittenen Entwicklungsstand und können in der Zukunft große Bedeutung erlangen. Als elektronische Vorrichtungen im Sinne dieser Erfindung werden organische elektronische Vorrichtungen verstanden, welche organische Halbleitermaterialien als funktionelle Materialien enthalten. Insbesondere stehen die elektronischen Vorrichtungen für Elektrolumineszenzvor- richtungen wie OLEDs. Der Aufbau von OLEDs, in welchen organische Verbindungen als funktionelle Materialien verwendet werden, ist dem Fachmann aus dem Stand der Technik bekannt. Im Allgemeinen werden unter OLEDs elektronische Vorrichtungen verstanden, welche eine oder mehrere Schichten haben, welche organische Verbindungen umfassen, und beim Anlegen einer Spannung Licht emittieren. In elektronischen Vorrichtungen, insbesondere OLEDs, gibt es einen großen Bedarf, die Leistungsdaten, insbesondere Lebensdauer, Effizienz und Betriebsspannung zu verbessern. Für diese Aspekte konnte bisher keine zufriedenstellende Lösung gefunden werden. Elektronische Vorrichtungen umfassen üblicherweise Kathode, Anode und mindestens eine funktionale, bevorzugt emittierende Schicht. Außer diesen Schichten können sie noch weitere Schichten enthalten, beispiels- weise jeweils eine oder mehrere Lochinjektionsschichten, Lochtransport- schichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Exzitonenblockierschichten, Elektronen- blockierschichten und/oder Ladungserzeugungsschichten (Charge- Generation Layers). Einen großen Einfluss auf die Leistungsdaten von elektronischen Vorrichtungen haben die Lochtransportschichten und Elektronentrans- portschichten, aber auch die Matrixmaterialien der emittierenden Schicht. Aufgabe der vorliegenden Erfindung ist die Bereitstellung von Verbin- dungen, welche sich für den Einsatz in einer elektronischen Vorrichtung, insbesondere einer OLED, eignen, insbesondere als Material von Elektronentransportschichten oder Matrixmaterialien, und dort zu guten Eigenschaften führen. Überraschend wurde gefunden, dass bestimmte, unten näher beschrie- bene Pentaphenanthrene diese Aufgabe lösen und sich gut für die Ver- wendung in elektronischen Vorrichtungen, insbesondere OLEDs eignen. Dabei weisen die OLEDs insbesondere eine lange Lebensdauer, eine hohe Effizienz und eine geringere Betriebsspannung auf. Diese Verbin- dungen sowie elektronische Vorrichtungen, insbesondere organische Elektrolumineszenzvorrichtungen, welche diese Verbindungen enthalten, sind daher der Gegenstand der vorliegenden Erfindung. Auch lassen sich die Verbindungen besser verarbeiten. Gegenstand der vorliegenden Erfindung ist eine Verbindung gemäß Formeln (1) und (2), wobei für die verwendeten Symbole gilt: X ist gleich oder verschieden bei jedem Auftreten CR‘ oder N mit der Maßgabe, dass maximal zwei Gruppen X pro Zyklus für N stehen; u ist 0, 1 oder 2, bevorzugt 0 oder 1, besonders bevorzugt 1; t ist 0 oder 1, bevorzugt 0; m ist 0, 1, 2 oder 3; n ist ein ganzzahliger Wert zwischen 0 und 4-s; s ist 0 oder 1; R ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ringatomen, bevorzugt mit 5 bis 40 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann, wobei zwei an verschiedene Zyklen gebundene Reste R oder zwei je an verschiedene Zyklen gebundene Reste R und R‘ miteinander ein aliphatisches, heteroaliphatisches, aromatisches oder heteroaroma- tisches Ringsystem bilden können, das mit einem oder mehreren Resten R1 substituiert sein kann; R‘ ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, N(R1)2, NAr‘2, OAr‘, SAr‘, B(OR1)2, CHO, C(=O)R1, CR1=C(R1)2, CN, C(=O)OR1, C(=O)NR1, Si(R1)3, NO2, P(=O)(R1)2, OSO2R1, OR1, S(=O)R1, S(=O)2R1, SR1, eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C- Atomen oder eine verzweigte oder zyklische Alkylgruppe mit 3 bis 20 C-Atomen, wobei die Alkyl-, Alkenyl- oder Alkinylgruppe jeweils mit einem oder mehreren Resten R1 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch -R1C=CR1- , -C≡C-, Si(R1)2, CONR1, C=O, C=S, -C(=O)O-, P(=O)(R1), -NR1-, -O- , -S-, SO oder SO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 aromatischen Ring- atomen, bevorzugt mit 5 bis 40 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann, wobei zwei oder mehr an verschiedene Zyklen gebundene Reste R‘ oder zwei je an verschiedene Zyklen gebundene Reste R und R‘ miteinander ein aliphatisches, heteroaliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können, das mit einem oder mehreren Resten R1 substituiert sein kann; mit der Maßgabe, dass zwei benachbarte R‘ zusammen für eine Struktur der Formel (2) stehen, wobei * eine Bindung zum C in C-R‘ darstellt, wobei die zwei benachbarten R‘ bevorzugt an zwei benach- barten X gebunden sind; Ar‘ ist bei jedem Auftreten gleich oder verschieden ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 aromatischen Ringatomen, das durch einen oder mehrere Reste R1 substituiert sein kann, wobei zwei oder mehr R1 miteinander ein aromatisches oder heteroaromatisches Ringsystem bilden können; R1 ist bei jedem Auftreten gleich oder verschieden H, D, F, I, N(R2)2, B(OR2)2, CHO, C(=O)R2, CR2=C(R2)2, CN, C(=O)OR2, Si(R2)3, NO2, P(=O)(R2)2, OSO2R2, SR2, OR2, S(=O)R2, S(=O)2R2, eine gerad- kettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen oder eine verzweigte oder zyklische Alkylgruppe mit 3 bis 20 C-Atomen, wobei die Alkyl-, Alkenyl- oder Alkinylgruppe jeweils mit einem oder mehreren Resten R2 substituiert sein kann und wobei eine oder mehrere CH2-Gruppen in den oben genannten Gruppen durch -R2C=CR2-, -C≡C-, Si(R2)2, C=O, C=S, -C(=O)O-, CONR2, P(=O)(R2), -NR2-, -O-, -S-, SO oder SO2 ersetzt sein können und wobei ein oder mehrere H-Atome in den oben genannten Gruppen durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, wobei zwei oder mehr Reste R1 miteinander ein aliphatisches, hetero- aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden können; R2 ist bei jedem Auftreten gleich oder verschieden H, D, F, CN oder ein aliphatischer, aromatischer oder heteroaromatischer organischer Rest mit 1 bis 20 C-Atomen, in dem auch ein oder mehrere H-Atome durch D oder F ersetzt sein können; dabei können zwei oder mehr Substituenten R2 miteinander verknüpft sein und einen Ring bilden; wobei R, sowie R‘ am gleichen Zyklus, wenn diese ein aromatisches Ring- system umfassen, kein Fluoren ist, ausgenommen ein Fluoren mit einem Spiroatom als Brückenkohlenstoff. Eine Arylgruppe im Sinne dieser Erfindung enthält 6 bis 40 C-Atome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält 5 bis 40 C-Atome und mindestens ein Heteroatom, mit der Maßgabe, dass die Summe aus C-Atomen und Heteroatomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Dabei wird unter einer Aryl- gruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Zyklus, also Benzol, bzw. ein einfacher heteroaromatischer Zyklus, beispielsweise Pyridin, Pyrimidin, Thiophen, etc., oder eine kondensierte (anellierte) Aryl- oder Heteroarylgruppe, beispielsweise Naphthalin, Anthracen, Phenanthren, Chinolin, Isochinolin, etc., verstanden. Mitein- ander durch Einfachbindung verknüpfte Aromaten, wie zum Beispiel Biphenyl, werden dagegen nicht als Aryl- oder Heteroarylgruppe, sondern als aromatisches Ringsystem bezeichnet. Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält 6 bis 60 C-Atome, bevorzugt 6 bis 40 C-Atome im Ringsystem. Ein heteroaroma- tisches Ringsystem im Sinne dieser Erfindung enthält 1 bis 60 C-Atome, bevorzugt 1 bis 40 C-Atome und mindestens ein Heteroatom im Ring- system, mit der Maßgabe, dass die Summe aus C-Atomen und Hetero- atomen mindestens 5 ergibt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine nicht-aromatische Einheit (bevorzugt weniger als 10 % der von H verschiedenen Atome), wie z. B. ein C-, N- oder O-Atom oder Carbonyl- gruppe, verbunden sein können. Ebenso sollen hierunter Systeme verstanden werden, in denen zwei oder mehr Aryl- bzw. Heteroaryl- gruppen direkt miteinander verknüpft sind, wie z. B. Biphenyl, Terphenyl, Bipyridin oder Phenylpyridin. So sollen beispielsweise auch Systeme wie Fluoren, 9,9‘-Spirobifluoren, 9,9-Diarylfluoren, Triarylamin, Diarylether, Stilben, etc. als aromatische Ringsysteme im Sinne dieser Erfindung ver- standen werden, und ebenso Systeme, in denen zwei oder mehrere Aryl- gruppen beispielsweise durch eine lineare oder cyclische Alkylgruppe oder durch eine Silylgruppe verbunden sind. Bevorzugte aromatische bzw. heteroaromatische Ringsysteme sind einfache Aryl- bzw. Heteroaryl- gruppen sowie Gruppen, in denen zwei oder mehr Aryl- bzw. Heteroaryl- gruppen direkt miteinander verknüpft sind, beispielsweise Biphenyl, Terphenyl, Quaterphenyl oder Bipyridin, sowie Fluoren oder Spirobi- fluoren. Ein elektronenreiches heteroaromatisches Ringsystem ist dadurch ge- kennzeichnet, dass es sich dabei um ein heteroaromatisches Ringsystem handelt, das keine elektronenarmen Heteroarylgruppen enthält. Eine elektronenarme Heteroarylgruppe ist eine Sechsring-Heteroarylgruppe mit mindestens einem Stickstoffatom oder eine Fünfring-Heteroarylgruppe mit mindestens zwei Heteroatomen, von denen eines ein Stickstoffatom und das andere Sauerstoff, Schwefel oder ein substituiertes Stickstoffatom ist, wobei an diese Gruppen jeweils noch weitere Aryl- oder Heteroaryl- gruppen ankondensiert sein können. Dagegen sind elektronenreiche Heteroarylgruppen Fünfring-Heteroarylgruppen mit genau einem Hetero- atom, ausgewählt aus Sauerstoff, Schwefel oder substituiertem Stickstoff, an welche noch weitere Arylgruppen und/oder weitere elektronenreiche Fünfring-Heteroarylgruppen ankondensiert sein können. So sind Beispiele für elektronenreiche Heteroarylgruppen Pyrrol, Furan, Thiophen, Indol, Benzofuran, Benzothiophen, Carbazol, Dibenzofuran, Dibenzothiophen oder Indenocarbazol. Eine elektronenreiche Heteroarylgruppe wird auch als elektronenreicher heteroaromatischer Rest bezeichnet. Ein elektronenarmes heteroaromatisches Ringsystem ist dadurch gekenn- zeichnet, dass es mindestens eine elektronenarme Heteroarylgruppe enthält, und insbesondere bevorzugt keine elektronenreiche Heteroaryl- gruppen. Im Rahmen der vorliegenden Erfindung wird der Begriff Alkylgruppe als Oberbegriff sowohl für lineare oder verzweigte Alkylgruppen wie auch für zyklische Alkylgruppen verwendet. Analog werden die Begriffe Alkenyl- gruppe bzw. Alkinylgruppe als Oberbegriffe sowohl für lineare oder ver- zweigte Alkenyl- bzw. Alkinylgruppen wie auch für zyklische Alkenyl- bzw. Alkinylgruppen verwendet. Unter einer cyclischen Alkyl-, Alkoxy- oder Thioalkoxygruppe im Sinne dieser Erfindung wird eine monocyclische, eine bicyclische oder eine polycyclische Gruppe verstanden. Im Rahmen der vorliegenden Erfindung werden unter einem aliphatischen Kohlenwasserstoffrest bzw. einer Alkylgruppe bzw. einer Alkenyl- oder Alkinylgruppe, die 1 bis 40 C-Atome enthalten kann, und in der auch einzelne H-Atome oder CH2-Gruppen durch die oben genannten Gruppen substituiert sein können, bevorzugt die Reste Methyl, Ethyl, n-Propyl, i- Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, t- Pentyl, 2-Pentyl, neo-Pentyl, Cyclopentyl, n-Hexyl, s-Hexyl, t-Hexyl, 2-Hexyl, 3-Hexyl, neo-Hexyl, Cyclohexyl, 1-Methylcyclopentyl, 2-Methyl- pentyl, n-Heptyl, 2-Heptyl, 3-Heptyl, 4-Heptyl, Cycloheptyl, 1-Methylcyclo- hexyl, n-Octyl, Cyclooctyl, 2-Ethylhexyl, 1-Bicyclo[2,2,2]octyl, 2-Bicyclo- [2,2,2]octyl, 2-(2,6-Dimethyl)octyl, 3-(3,7-Dimethyl)octyl, Adamantyl, Trifluormethyl, Pentafluorethyl, 2,2,2-Trifluorethyl, 1,1-Dimethyl-n-hex-1-yl, 1,1-Dimethyl-n-hept-1-yl, 1,1-Dimethyl-n-oct-1-yl, 1,1-Dimethyl-n-dec-1-yl, 1,1-Dimethyl-n-dodec-1-yl, 1,1-Dimethyl-n-tetradec-1-yl, 1,1-Dimethyl-n- hexadec-1-yl, 1,1-Dimethyl-n-octadec-1-yl, 1,1-Diethyl-n-hex-1-yl, 1,1- Diethyl-n-hept-1-yl, 1,1-Diethyl-n-oct-1-yl, 1,1-Diethyl-n-dec-1-yl, 1,1- Diethyl-n-dodec-1-yl, 1,1-Diethyl-n-tetradec-1-yl, 1,1-Diethyl-n-hexadec-1- yl, 1,1-Diethyl-n-octadec-1-yl, 1-(n-Propyl)-cyclohex-1-yl, 1-(n-Butyl)- cyclohex-1-yl, 1-(n-Hexyl)-cyclohex-1-yl, 1-(n-Octyl)-cyclohex-1-yl und 1- (n-Decyl)-cyclohex-1-yl, Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclo- pentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl, Cyclooctenyl, Cyclooctadienyl, Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl, Heptinyl oder Octinyl verstanden. Unter einer Alkoxygruppe OR1 mit 1 bis 40 C-Atomen werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy, n-Pentoxy, s-Pentoxy, 2-Methylbutoxy, n-Hexoxy, Cyclohexyloxy, n-Heptoxy, Cyclo- heptyloxy, n-Octyloxy, Cyclooctyloxy, 2-Ethylhexyloxy, Pentafluorethoxy und 2,2,2-Trifluorethoxy verstanden. Unter einer Thioalkylgruppe SR1 mit 1 bis 40 C-Atomen werden insbesondere Methylthio, Ethylthio, n-Propyl- thio, i-Propylthio, n-Butylthio, i-Butylthio, s-Butylthio, t-Butylthio, n-Pentyl- thio, s-Pentylthio, n-Hexylthio, Cyclohexylthio, n-Heptylthio, Cycloheptyl- thio, n-Octylthio, Cyclooctylthio, 2-Ethylhexylthio, Trifluormethylthio, Pentafluorethylthio, 2,2,2-Trifluorethylthio, Ethenylthio, Propenylthio, Butenylthio, Pentenylthio, Cyclopentenylthio, Hexenylthio, Cyclohexenyl- thio, Heptenylthio, Cycloheptenylthio, Octenylthio, Cyclooctenylthio, Ethinylthio, Propinylthio, Butinylthio, Pentinylthio, Hexinylthio, Heptinylthio oder Octinylthio verstanden. Allgemein können Alkyl-, Alkoxy- oder Thio- alkylgruppen gemäß der vorliegenden Erfindung geradkettig, verzweigt oder zyklisch sein, wobei eine oder mehrere nicht-benachbarte CH2- Gruppen durch die oben genannten Gruppen ersetzt sein können; weiterhin können auch ein oder mehrere H-Atome durch D, F, Cl, Br, I, CN oder NO2, bevorzugt F, Cl oder CN, besonders bevorzugt F oder CN ersetzt sein. Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5 - 60 aromatischen Ringatomen, vorzugsweise 5 - 40 aromatischen Ring- atomen, welches noch jeweils mit den oben genannten Resten oder einem Kohlenwasserstoffrest substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Benzanthracen, Phenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Triphenylen, Fluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans- Indenofluoren, cis- oder trans-Indenocarbazol, cis- oder trans-Indolo- carbazol, cis- oder trans-Monobenzoindenofluoren, cis- oder trans- Dibenzoindenofluoren, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothio- phen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carba- zol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chino- lin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimi- dazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benz- oxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2- Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Hexaazatriphenylen, Benzo- pyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7- Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diaza- pyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Pheno- thiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenan- throlin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4- Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thia- diazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol oder Gruppen, die abgeleitet sind von Kombinationen dieser Systeme. Unter der Formulierung, dass zwei oder mehr Reste miteinander ein Ring- system bilden können, soll im Rahmen der vorliegenden Beschreibung unter anderem verstanden werden, dass die beiden Reste miteinander durch eine chemische Bindung unter formaler Abspaltung von zwei Wasserstoffatomen verknüpft sind. Dies wird durch das folgende Schema verdeutlicht: . Weiterhin soll unter der oben genannten Formulierung aber auch ver- standen werden, dass für den Fall, dass einer der beiden Reste Wasser- stoff darstellt, der zweite Rest unter Bildung eines Rings an die Position, an die das Wasserstoffatom gebunden war, bindet. Dies soll durch das folgende Schema verdeutlicht werden: . In einer bevorzugten Ausführungsform ist R, sowie R‘ am gleichen Zyklus, wenn diese ein aromatisches Ringsystem umfassen, welches aus zwei Arylgruppen mit 6 C-Atomen besteht, welche über eine Einfachbindung und eine einatomige Brücke miteinander verbunden sind, diese Brücke kein aliphatisches Kohlenstoffatom ist, ausgenommen der Kohlenstoff ein Spiroatom ist. Daher ist R und/oder R‘, wenn diese ein aromatisches Ringsystem umfassen, kein Fluoren, kann jedoch Spirobifluoren sein. In einer bevorzugten Ausführungsform ist, wenn R und/oder R‘ ein aromatisches oder heteroaromatisches Ringsystem umfassen, welches aus zwei Arylgruppen mit 6 C-Atomen besteht, welche über eine Einfach- bindung und eine einatomige Brücke miteinander verbunden sind, diese Brücke kein aliphatisches Kohlenstoffatom, ausgenommen das Kohlen- stoff ist ein Spiroatom. Daher ist R und/oder R‘, wenn diese ein aroma- tisches Ringsystem umfassen, kein Fluoren, kann jedoch ein Spirobi- fluoren sein. In einer bevorzugten Ausführungsform ist, wenn R und/oder R‘ ein aromatisches oder heteroaromatisches Ringsystem umfassen, welches aus zwei Arylgruppen mit 6 C-Atomen besteht, welche über eine Einfachbindung und eine einatomige Brücke miteinander verbunden sind, diese Brücke ausgewählt aus einem B-, N-, O-, oder S-Atom. Weitere bevorzugte Ausführungsformen zeigen die folgenden Formeln (3-1), (3-2) oder (3-3): Formel (3-3) wobei die verwendeten Symbole die oben für Formel (1) genannten Bedeutungen aufweisen, wobei zusätzlich gilt, dass in den Formeln (3-2) und (3-3) zwei bevorzugt benachbarte R‘ für die Struktur -CF2-(CF2)u-CF2- stehen und m in Formel (3-2) für 2 oder 3 und n in Formel (3-3) für einen ganzzahligen Wert zwischen 2 und 3-s stehen. Weitere bevorzugte Ausführungsformen der Formeln (3-1), (3-2) und (3-3) zeigen die folgenden Formeln (3-1-1), (3-1-2), (3-2-1), (3-2-2), (3-3-1) oder (3-3-2): Formel (3 Formel (3-3-2) wobei die verwendeten Symbole die oben für Formel (1) genannten Bedeutungen aufweisen und wobei zusätzlich gilt, dass in den Formeln (3- 2-1), (3-2-2), (3-3-1) und (3-3-2) zwei bevorzugt benachbarte R‘ für die Struktur -CF2-(CF2)u-CF2- stehen und m in Formel (3-2-1) und (3-2-2) für 2 oder 3 und n in Formel (3-3-1) und (3-3-2) für einen ganzzahligen Wert zwischen 2 und 3-s stehen. Eine bevorzugte Ausführungsform der Verbindung der Formel (3-1-1) ist eine Verbindung der Formel (3-1-1a): -1-1a) wobei die verwendeten S ymbole die oben für Formel (3-1-1) genannten Bedeutungen aufweisen. In einer bevorzugten Ausführungsform der Erfindung steht X für CR‘. Weitere bevorzugte Ausführungsformen zeigen die folgenden Formeln (4- 1), (4-2), (5-1-1), (5-1-2), (5-1-3), (5-2-1), (5-2-2), (5-2-3), (6-1-1), (6-1-2), (6-1-3), (6-2-1), (6-2-2), (6-2-3), (6-3-1), (6-3-2), (6-3-3), (6-4-1), (6-4-2), (6-4-3), (7-1-1) oder (7-2-1): For 2) Formel (7-1-1) R Formel (7-2-1) wobei die verwendeten Symbole die oben für Formel (1) genannten Bedeutungen aufweisen, wobei zusätzlich gilt, dass im Fall von s = 0 in den Formeln (4-1), (4-2), (5-1-1), (5-1-2), (5-1-3), (5-2-1), (5-2-2) und (5-2- 3) an diesem Kohlenstoffatom R‘ gebunden ist, sowie m in Formel (7-1-1) und (7-2-1) für 0 oder 1 und n in den Formeln (6-1-1), (6-1-2), (6-1-3), (6- 2-1), (6-2-2), (6-2-3), (6-3-1), (6-3-2), (6-3-3), (6-4-1), (6-4-2), (6-4-3) für einen ganzzahligen Wert zwischen 0 und 2-s stehen. Eine weitere bevorzugte Ausführungsform zeigt die folgende Formel (8): wobei die verwendeten Symbole die oben für Formel (1) genannten Bedeutungen aufweisen, wobei zusätzlich gilt, dass im Fall von s = 0 an diesem Kohlenstoffatom R‘ gebunden ist. In einer bevorzugten Ausführungsform ist die erfindungsgemäße Verbindung ausgewählt aus einer der folgenden Verbindungen: Materials for electronic devices The present invention relates to materials for use in electronic devices, in particular in organic electroluminescent devices, and to electronic devices, in particular organic electroluminescent devices containing these materials. Electronic devices which contain organic, organometallic and/or polymeric semiconductors are becoming increasingly important, and these are used in many commercial products for cost reasons and due to their performance. Examples include organic-based charge transport materials (e.g. triarylamine-based hole transporters) in copiers, organic or polymeric light-emitting diodes (OLEDs or PLEDs) in indicator and display devices, or organic photoreceptors in copiers. Organic solar cells (O-SC), organic field-effect transistors (O-FET), organic thin-film transistors (O-TFT), organic switching elements (O-IC), organic optical amplifiers, and organic laser diodes (O-lasers) are at an advanced stage of development and may become very important in the future. Electronic devices in the sense of this invention are understood to be organic electronic devices which contain organic semiconductor materials as functional materials. In particular, the electronic devices are electroluminescent devices such as OLEDs. The structure of OLEDs in which organic compounds are used as functional materials is known to the person skilled in the art from the prior art. In general, OLEDs are understood to be electronic devices which have one or more layers which comprise organic compounds and emit light when a voltage is applied. In electronic devices, in particular OLEDs, there is a great need to improve the performance data, in particular service life, efficiency and operating voltage. No satisfactory solution has yet been found for these aspects. Electronic devices usually comprise a cathode, an anode and at least one functional, preferably emitting layer. In addition to these layers, they can contain further layers, for example one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, exciton blocking layers, electron blocking layers and/or charge generation layers. The hole transport layers and electron transport layers, as well as the matrix materials of the emitting layer, have a major influence on the performance data of electronic devices. The object of the present invention is to provide compounds which are suitable for use in an electronic device, in particular an OLED, in particular as material for electron transport layers or matrix materials, and which lead to good properties there. Surprisingly, it has been found that certain pentaphenanthrenes, described in more detail below, solve this problem and are well suited for use in electronic devices, in particular OLEDs. The OLEDs in particular have a long service life, high efficiency and a lower operating voltage. These compounds and electronic devices, in particular organic electroluminescent devices, which contain these compounds are therefore the subject of the present invention. The compounds are also easier to process. The subject of the present invention is a compound according to formulas (1) and (2), where the following applies to the symbols used: X is the same or different on each occurrence and is CR' or N, with the proviso that a maximum of two groups X per cycle stand for N; u is 0, 1 or 2, preferably 0 or 1, particularly preferably 1; t is 0 or 1, preferably 0; m is 0, 1, 2 or 3; n is an integer value between 0 and 4-s; s is 0 or 1; R is, on each occurrence, identically or differently, an aromatic or heteroaromatic ring system having 5 to 60 aromatic ring atoms, preferably having 5 to 40 aromatic ring atoms, which may each be substituted by one or more radicals R 1 , where two radicals R bonded to different cycles or two radicals R and R' bonded to different cycles can together form an aliphatic, heteroaliphatic, aromatic or heteroaromatic ring system, which may be substituted by one or more radicals R 1 ; R' is, on each occurrence, identically or differently, H, D, F, Cl, Br, I, N(R 1 ) 2 , NAr'2, OAr', SAr', B(OR 1 ) 2 , CHO, C(=O)R 1 , CR 1 =C(R 1 ) 2 , CN, C(=O)OR 1 , C(=O)NR 1 , Si(R 1 ) 3 , NO2, P(=O)(R 1 ) 2 , OSO2R 1 , OR 1 , S(=O)R 1 , S(=O) 2 R 1 , SR 1 , a straight-chain alkyl group having 1 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl, alkenyl or alkynyl group can each be substituted by one or more radicals R 1 , where one or more non-adjacent CH2 groups are substituted by -R 1 C=CR 1 - , -C≡C-, Si(R 1 ) 2 , CONR 1 , C=O, C=S, -C(=O)O-, P(=O)(R 1 ), -NR 1 -, -O-, -S-, SO or SO2, or an aromatic or heteroaromatic ring system with 5 to 60 aromatic ring atoms, preferably with 5 to 40 aromatic ring atoms, each of which can be substituted by one or more radicals R 1 , where two or more radicals R 'bonded to different cycles or two radicals R and R' each bonded to different cycles can together form an aliphatic, heteroaliphatic, aromatic or heteroaromatic ring system, which can be substituted by one or more radicals R 1 ; with the proviso that two adjacent R' together represent a structure of the formula (2), where * represents a bond to C in CR', where the two adjacent R' are preferably bonded to two adjacent X; Ar' is on each occurrence, identically or differently, an aromatic or heteroaromatic ring system having 5 to 40 aromatic ring atoms which may be substituted by one or more radicals R 1 , where two or more R 1s may together form an aromatic or heteroaromatic ring system; R 1 is, identically or differently on each occurrence, H, D, F, I, N(R 2 ) 2 , B(OR 2 ) 2 , CHO, C(=O)R 2 , CR 2 =C(R 2 ) 2 , CN, C(=O)OR 2 , Si(R 2 ) 3 , NO2, P(=O)(R 2 ) 2 , OSO2R 2 , SR 2 , OR 2 , S(=O)R 2 , S(=O) 2 R 2 , a straight-chain alkyl group having 1 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl, alkenyl or alkynyl group is each substituted with one or more R 2 and wherein one or more CH2 groups in the abovementioned groups can be replaced by -R 2 C=CR 2 -, -C≡C-, Si(R 2 ) 2 , C=O, C=S, -C(=O)O-, CONR 2 , P(=O)(R 2 ), -NR 2 -, -O-, -S-, SO or SO2 and where one or more H atoms in the abovementioned groups can be replaced by D, F, Cl, Br, I, CN or NO2, or an aromatic or heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 2 , where two or more radicals R 1 can form an aliphatic, heteroaliphatic, aromatic or heteroaromatic ring system with one another; R 2 is, on each occurrence, identically or differently, H, D, F, CN or an aliphatic, aromatic or heteroaromatic organic radical having 1 to 20 C atoms, in which one or more H atoms can also be replaced by D or F; two or more substituents R 2 can be linked to one another and form a ring; where R and R' on the same ring, if they comprise an aromatic ring system, are not fluorene, except for a fluorene with a spiro atom as a bridging carbon. An aryl group in the sense of this invention contains 6 to 40 C atoms; a heteroaryl group in the sense of this invention contains 5 to 40 C atoms and at least one heteroatom, with the proviso that the sum of C atoms and heteroatoms is at least 5. The heteroatoms are preferably selected from N, O and/or S. An aryl group or heteroaryl group is understood to be either a simple aromatic cycle, i.e. benzene, or a simple heteroaromatic cycle, for example pyridine, pyrimidine, thiophene, etc., or a condensed (fused) aryl or heteroaryl group, for example naphthalene, anthracene, phenanthrene, quinoline, isoquinoline, etc. Aromatics linked to one another by a single bond, such as biphenyl, are not referred to as aryl or heteroaryl groups, but as aromatic ring systems. An aromatic ring system in the sense of this invention contains 6 to 60 C atoms, preferably 6 to 40 C atoms in the ring system. A heteroaromatic ring system in the sense of this invention contains 1 to 60 C atoms, preferably 1 to 40 C atoms and at least one heteroatom in the ring system, with the proviso that the sum of C atoms and heteroatoms is at least 5. The heteroatoms are preferably selected from N, O and/or S. An aromatic or heteroaromatic ring system in the sense of this invention is to be understood as a system which does not necessarily only contain aryl or heteroaryl groups, but in which several aryl or heteroaryl groups can also be connected by a non-aromatic unit (preferably less than 10% of the atoms other than H), such as a C, N or O atom or carbonyl group. This also includes systems in which two or more aryl or heteroaryl groups are directly linked to one another, such as biphenyl, terphenyl, bipyridine or phenylpyridine. For example, systems such as fluorene, 9,9'-spirobifluorene, 9,9-diarylfluorene, triarylamine, diaryl ether, stilbene, etc. are also to be understood as aromatic ring systems in the sense of this invention, as are systems in which two or more aryl groups are linked, for example, by a linear or cyclic alkyl group or by a silyl group. Preferred aromatic or heteroaromatic ring systems are simple aryl or heteroaryl groups and groups in which two or more aryl or heteroaryl groups are directly linked to one another, for example biphenyl, terphenyl, quaterphenyl or bipyridine, and also fluorene or spirobifluorene. An electron-rich heteroaromatic ring system is characterized by the fact that it is a heteroaromatic ring system that does not contain any electron-poor heteroaryl groups. An electron-poor heteroaryl group is a six-membered ring heteroaryl group with at least one nitrogen atom or a five-membered ring heteroaryl group with at least two heteroatoms, one of which is a nitrogen atom and the other oxygen, sulfur or a substituted nitrogen atom, where further aryl or heteroaryl groups can be condensed onto these groups. In contrast, electron-rich Heteroaryl groups Five-membered ring heteroaryl groups with exactly one hetero atom, selected from oxygen, sulfur or substituted nitrogen, to which further aryl groups and/or further electron-rich five-membered ring heteroaryl groups can be condensed. Examples of electron-rich heteroaryl groups are pyrrole, furan, thiophene, indole, benzofuran, benzothiophene, carbazole, dibenzofuran, dibenzothiophene or indenocarbazole. An electron-rich heteroaryl group is also referred to as an electron-rich heteroaromatic radical. An electron-poor heteroaromatic ring system is characterized in that it contains at least one electron-poor heteroaryl group, and particularly preferably no electron-rich heteroaryl groups. In the context of the present invention, the term alkyl group is used as a generic term for both linear or branched alkyl groups and for cyclic alkyl groups. Analogously, the terms alkenyl group or alkynyl group are used as generic terms for both linear or branched alkenyl or alkynyl groups and for cyclic alkenyl or alkynyl groups. A cyclic alkyl, alkoxy or thioalkoxy group in the sense of this invention is understood to mean a monocyclic, a bicyclic or a polycyclic group. In the context of the present invention, an aliphatic hydrocarbon radical or an alkyl group or an alkenyl or alkynyl group which can contain 1 to 40 C atoms and in which individual H atoms or CH2 groups can also be substituted by the abovementioned groups, preferably the radicals methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, s-butyl, t-butyl, 2-methylbutyl, n-pentyl, s-pentyl, t-pentyl, 2-pentyl, neo-pentyl, cyclopentyl, n-hexyl, s-hexyl, t-hexyl, 2-hexyl, 3-hexyl, neo-hexyl, cyclohexyl, 1-methylcyclopentyl, 2-methylpentyl, n-heptyl, 2-heptyl, 3-heptyl, 4-heptyl, cycloheptyl, 1-methylcyclohexyl, n-octyl, cyclooctyl, 2-ethylhexyl, 1-bicyclo[2,2,2]octyl, 2-bicyclo[2,2,2]octyl, 2-(2,6-dimethyl)octyl, 3-(3,7-dimethyl)octyl, Adam antyl, Trifluoromethyl, pentafluoroethyl, 2,2,2-trifluoroethyl, 1,1-dimethyl-n-hex-1-yl, 1,1-dimethyl-n-hept-1-yl, 1,1-dimethyl-n-oct-1-yl, 1,1-dimethyl-n-dec-1-yl, 1,1-dimethyl-n-dodec-1-yl, 1,1-dimethyl-n-tetradec-1-yl , 1,1-Dimethyl-n-hexadec-1-yl, 1,1-Dimethyl-n-octadec-1-yl, 1,1-Diethyl-n-hex-1-yl, 1,1-Diethyl-n-hept-1-yl, 1,1-Diethyl-n-oct-1-yl, 1,1-Diethyl-n-dec-1-yl, 1,1- Diethyl-n-dodec-1-yl, 1,1-Diethyl-n-tetradec-1-yl, 1,1-Diethyl-n-hexadec-1- yl, 1,1-Diethyl-n-octadec-1-yl, 1-(n-Propyl)-cyclohex-1-yl, 1-(n-Butyl)- cyclohex-1-yl, 1-(n-Hexyl)-cyclohex-1-yl, 1-(n-Octyl)-cyclohex-1-yl und 1- (n-Decyl)-cyclohex-1-yl, Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclo- pentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl, Cyclooctenyl, Cyclooctadienyl, Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl, Heptynyl or octynyl understood. Among an alkoxy group OR 1 with 1 to 40 carbon atoms, preference is given to methoxy, trifluoromethoxy, ethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, n-pentoxy, s-pentoxy, 2-methylbutoxy, n-hexoxy, cyclohexyloxy, n-heptoxy, cycloheptyloxy, n-Octyloxy, cyclooctyloxy, 2-ethylhexyloxy, pentafluoroethoxy and 2,2,2-trifluoroethoxy are understood. A thioalkyl group SR 1 with 1 to 40 carbon atoms includes, in particular, methylthio, ethylthio, n-propylthio, i-propylthio, n-butylthio, i-butylthio, s-butylthio, t-butylthio, n-pentylthio, s-pentylthio, n-hexylthio, cyclohexylthio, n-heptylthio, cycloheptylthio, n-octylthio, cyclooctylthio, 2-ethylhexylthio, trifluoromethylthio, pentafluoroethylthio, 2,2,2-trifluoroethylthio, ethenylthio, propenylthio, butenylthio, pentenylthio, cyclopentenylthio, hexenylthio, cyclohexenylthio, heptenylthio , Cycloheptenylthio, Octenylthio, Cyclooctenylthio, Ethynylthio, Propynylthio, butynylthio, pentynylthio, hexynylthio, heptynylthio or octynylthio. In general, alkyl, alkoxy or thioalkyl groups according to the present invention can be straight-chain, branched or cyclic, where one or more non-adjacent CH2 groups can be replaced by the above-mentioned groups; furthermore, one or more H atoms can be replaced by D, F, Cl, Br, I, CN or NO2, preferably F, Cl or CN, particularly preferably F or CN. An aromatic or heteroaromatic ring system with 5 - 60 aromatic ring atoms, preferably 5 - 40 aromatic ring atoms, which can also be substituted with the above-mentioned radicals or a Hydrocarbon residue which can be substituted and which can be linked to the aromatic or heteroaromatic via any position are understood to mean in particular groups which are derived from benzene, naphthalene, anthracene, benzanthracene, phenanthrene, pyrene, chrysene, perylene, fluoranthene, naphthacene, pentacene, benzopyrene, biphenyl, biphenylene, terphenyl, triphenylene, fluorene, spirobifluorene, dihydrophenanthrene, dihydropyrene, tetrahydropyrene, cis- or trans- indenofluorene, cis- or trans- indenocarbazole, cis- or trans- indolocarbazole, cis- or trans- monobenzoindenofluorene, cis- or trans- dibenzoindenofluorene, truxene, isotruxene, spirotruxene, spiroisotruxene, furan, benzofuran, isobenzofuran, dibenzofuran, thiophene, benzothio- phen, isobenzothiophene, dibenzothiophene, pyrrole, indole, isoindole, carbazole, pyridine, quinoline, isoquinoline, acridine, phenanthridine, benzo-5,6-quinoline, benzo-6,7-quinoline, benzo-7,8-quinoline, phenothiazine, phenoxazine, pyrazole, indazole, imidazole, benzimidazole, naph thimidazole, phenanthrimidazole, pyridimidazole, pyrazinimidazole, quinoxalinimidazole, oxazole, benzo-oxazole, naphthoxazole, anthroxazole, phenanthroxazole, isoxazole, 1,2-thiazole, 1,3-thiazole, benzothiazole, pyridazine, hexaazatriphenylene, benzopyridazine, pyrimidine, benzopyrimidine, quinoxaline, 1,5-diazaanthracene, 2,7-diazapyrene, 2,3-diazapyrene, 1,6-diazapyrene, 1,8-diazapyrene, 4,5-diazapyrene, 4,5,9,10-tetraazaperylene, pyrazine, phenazine, phenoxazine, phenothiazine, fluorubin, naphthyridine, azacar bazol, benzocarboline, phenanthroline, 1,2,3-triazole, 1,2,4-triazole, benzotriazole, 1,2,3-oxadiazole, 1,2,4-oxadiazole, 1,2,5-oxadiazole, 1,3,4-oxadiazole, 1,2,3-thiadiazole, 1,2,4-thiadiazole, 1,2,5-thiadiazole azole, 1,3,4-thiadiazole, 1,3,5-triazine, 1,2,4-triazine, 1,2,3-triazine, tetrazole, 1,2,4,5-tetrazine, 1,2,3,4-tetrazine, 1,2,3,5-tetrazine, purine, pteridine, indolizine and benzothiadiazole or groups derived from combinations of these systems. In the context of the present description, the phrase that two or more residues can form a ring system with one another is to be understood to mean, among other things, that the two residues are linked to one another by a chemical bond with the formal elimination of two hydrogen atoms. This is illustrated by the following scheme: . Furthermore, the above formulation should also be understood to mean that if one of the two residues represents hydrogen, the second residue binds to the position to which the hydrogen atom was bound, forming a ring. This is illustrated by the following scheme: . In a preferred embodiment, R and R' are on the same ring if they comprise an aromatic ring system which consists of two aryl groups with 6 C atoms which are connected to one another via a single bond and a monoatomic bridge, this bridge is not an aliphatic carbon atom, unless the carbon is a spiro atom. Therefore, R and/or R', if they comprise an aromatic ring system, is not a fluorene, but can be spirobifluorene. In a preferred embodiment, if R and/or R' comprise an aromatic or heteroaromatic ring system which consists of two aryl groups with 6 C atoms which are connected to one another via a single bond and a monoatomic bridge, this bridge is not an aliphatic carbon atom, unless the carbon is a spiro atom. Therefore, R and/or R', if they comprise an aromatic ring system, is not a fluorene, but can be a spirobifluorene. In a preferred embodiment, when R and/or R' comprise an aromatic or heteroaromatic ring system consisting of two aryl groups having 6 C atoms which are connected via a Single bond and a monoatomic bridge are connected to each other, this bridge selected from a B, N, O, or S atom. Further preferred embodiments are shown by the following formulas (3-1), (3-2) or (3-3): Formula (3-3) where the symbols used have the meanings given above for formula (1), with the additional rule that in formulas (3-2) and (3-3) two preferably adjacent R' stand for the structure -CF2-(CF2)u-CF2- and m in formula (3-2) stands for 2 or 3 and n in formula (3-3) stands for an integer value between 2 and 3-s. Further preferred embodiments of formulas (3-1), (3-2) and (3-3) are shown by the following formulas (3-1-1), (3-1-2), (3-2-1), (3-2-2), (3-3-1) or (3-3-2): Formula (3 Formula (3-3-2) where the symbols used have the meanings given above for formula (1) and where it additionally applies that in the formulas (3- 2-1), (3-2-2), (3-3-1) and (3-3-2) two preferably adjacent R' stand for the structure -CF2-(CF2) u -CF2- and m in formula (3-2-1) and (3-2-2) stands for 2 or 3 and n in formula (3-3-1) and (3-3-2) stands for an integer value between 2 and 3-s. A preferred embodiment of the compound of formula (3-1-1) is a compound of formula (3-1-1a): -1-1a) where the S used symbols have the meanings given above for formula (3-1-1). In a preferred embodiment of the invention, X is CR'. Further preferred embodiments are shown by the following formulas (4-1), (4-2), (5-1-1), (5-1-2), (5-1-3), (5-2-1), (5-2-2), (5-2-3), (6-1-1), (6-1-2), (6-1-3), (6-2-1), (6-2-2), (6-2-3), (6-3-1), (6-3-2), (6-3-3), (6-4-1), (6-4-2), (6-4-3), (7-1-1) or (7-2-1): For 2) Formula (7-1-1) R Formula (7-2-1) where the symbols used have the meanings given above for formula (1), with the additional fact that in the case of s = 0 in the formulas (4-1), (4-2), (5-1-1), (5-1-2), (5-1-3), (5-2-1), (5-2-2) and (5-2-3), R' is bonded to this carbon atom, and m in formulas (7-1-1) and (7-2-1) is 0 or 1 and n in the formulas (6-1-1), (6-1-2), (6-1-3), (6-2-1), (6-2-2), (6-2-3), (6-3-1), (6-3-2), (6-3-3), (6-4-1), (6-4-2), (6-4-3) is an integer value between 0 and 2-s. A further preferred embodiment is shown by the following formula (8): where the symbols used have the meanings given above for formula (1), with the additional feature that in the case of s = 0, R' is bonded to this carbon atom. In a preferred embodiment, the compound according to the invention is selected from one of the following compounds:
Im Folgenden werden bevorzugte Substituenten R, Ar‘, R‘, R1 und R2 beschrieben. In einer besonders bevorzugten Ausführungsform der Erfin- dung treten die nachfolgend genannten Bevorzugungen für R, Ar‘, R‘, R1 und R2 gleichzeitig auf und gelten für die Strukturen der Formel (1) sowie für alle oben aufgeführten bevorzugten Ausführungsformen. In einer bevorzugten Ausführungsform der Erfindung ist R‘ bei jedem Auf- treten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D, F, CN, OR1, einer geradkettigen Alkylgruppe mit 1 bis 10 C-Atomen oder einer Alkenylgruppe mit 2 bis 10 C-Atomen oder einer verzweigten oder zyklischen Alkylgruppe mit 3 bis 10 C-Atomen, wobei die Alkyl- bzw. Alkenylgruppe jeweils mit einem oder mehreren Resten R1 substituiert sein kann, bevorzugt jedoch unsubstituiert ist, und wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch O ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann; dabei können zwei Reste R‘ oder zwei je an verschiedene Zyklen gebundene Reste R und R‘ auch miteinander ein aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden. Besonders bevorzugt ist R‘ bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, F, CN, einer geradkettigen Alkylgruppe mit 1 bis 6 C-Atomen, insbesondere mit 1, 2, 3 oder 4 C- Atomen, oder einer verzweigten oder zyklischen Alkylgruppe mit 3 bis 6 C- Atomen, wobei die Alkylgruppe jeweils mit einem oder mehreren Resten R1 substituiert sein kann, bevorzugt aber unsubstituiert ist, oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 24 aroma- tischen Ringatomen, das jeweils durch einen oder mehrere Reste R1, bevorzugt nicht-aromatische Reste R1, substituiert sein kann. Ganz besonders bevorzugt ist R‘ bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus H, D oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 24 aromatischen Ring- atomen, das jeweils durch einen oder mehrere Reste R2, bevorzugt nicht- aromatische Reste R2, substituiert sein kann. In einer bevorzugten Ausführungsform der Erfindung ist R bei jedem Auf- treten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann; dabei können zwei Reste R oder zwei je an verschiedene Zyklen gebundene Reste R und R‘ auch miteinander ein aliphatisches, aromatisches oder heteroaromatisches Ringsystem bilden. Besonders bevorzugt ist R bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 24, bevorzugt mit 6 bis 18 und besonders bevorzugt mit 6 bis 13 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1, bevorzugt nicht-aromatische Reste R1, substituiert sein kann. Ganz besonders bevorzugt ist R bei jedem Auf- treten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 24, bevorzugt mit 6 bis 18 und besonders bevorzugt mit 6 bis 13 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2, bevorzugt nicht-aromatische Reste R2, substituiert sein kann. In einer bevorzugten Ausführungsform bilden zwei Reste R und R‘, welche an verschiedene Zyklen gebunden sind, miteinander kein aliphatisches, aromatisches oder heteroaromatisches Ringsystem. In einer weiteren bevorzugten Ausführungsform bilden zwei Reste R, bzw. R und R‘, welche an verschiedene Zyklen gebunden sind, miteinander kein aliphatisches, aromatisches oder heteroaromatisches Ringsystem. Geeignete aromatische bzw. heteroaromatische Ringsysteme R oder R‘ sind ausgewählt aus Phenyl, Biphenyl, insbesondere ortho-, meta- oder para-Biphenyl, Terphenyl, insbesondere ortho-, meta-, para- oder ver- zweigtem Terphenyl, Quaterphenyl, insbesondere ortho-, meta-, para- oder verzweigtem Quaterphenyl, Fluoren, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Spirobifluoren, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Naphthalin, welches über die 1- oder 2-Position verknüpft sein kann, Indol, Benzofuran, Benzothiophen, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Dibenzo- furan, Carbazol, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Dibenzothiophen, welches über die 1-, 2-, 3- oder 4-Position ver- knüpft sein kann, Indenocarbazol, Indolocarbazol, Pyridin, Pyrimidin, Pyrazin, Pyridazin, Triazin, Chinolin, Chinazolin, Benzimidazol, Phenanthren, Triphenylen oder einer Kombination aus zwei oder drei dieser Gruppen, welche jeweils mit einem oder mehreren Resten R1 sub- stituiert sein können. Wenn R für eine Heteroarylgruppe, insbesondere für Triazin, Pyrimidin oder Chinazolin steht, können auch aromatische oder heteroaromatische Reste R1 an dieser Heteroarylgruppe bevorzugt sein. Dabei sind die Gruppen R oder R‘, wenn sie für ein aromatisches bzw. heteroaromatisches Ringsystem stehen, bevorzugt gewählt aus den Gruppen der folgenden Formeln R-1 bis R-182, Preferred substituents R, Ar', R', R 1 and R 2 are described below. In a particularly preferred embodiment of the invention, the preferences for R, Ar', R', R 1 and R 2 mentioned below occur simultaneously and apply to the structures of formula (1) as well as to all preferred embodiments listed above. In a preferred embodiment of the invention, R' is selected on each occurrence, identically or differently, from the group consisting of H, D, F, CN, OR 1 , a straight-chain alkyl group having 1 to 10 C atoms or an alkenyl group having 2 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, where the alkyl or alkenyl group can each be substituted by one or more radicals R 1 , but is preferably unsubstituted, and where one or more non-adjacent CH2 groups can be replaced by O, or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, which can each be substituted by one or more radicals R 1 ; two radicals R' or two each R and R' radicals bonded to different rings also form an aliphatic, aromatic or heteroaromatic ring system with one another. R' is particularly preferably selected, identically or differently on each occurrence, from the group consisting of H, F, CN, a straight-chain alkyl group having 1 to 6 C atoms, in particular having 1, 2, 3 or 4 C atoms, or a branched or cyclic alkyl group having 3 to 6 C atoms, where the alkyl group can be substituted in each case by one or more R 1 radicals, but is preferably unsubstituted, or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, which can be substituted in each case by one or more R 1 radicals, preferably non-aromatic R 1 radicals. R' is very particularly preferably selected on each occurrence, identically or differently, from the group consisting of H, D or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , preferably non-aromatic radicals R 2 . In a preferred embodiment of the invention, R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 ; two radicals R or two radicals R and R' each bound to different cycles can also form an aliphatic, aromatic or heteroaromatic ring system with one another. Particularly preferably, R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 24, preferably 6 to 18 and particularly preferably 6 to 13 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 , preferably non-aromatic radicals R 1 . Very particularly preferably, R is selected on each occurrence, identically or differently, from the group consisting of an aromatic or heteroaromatic ring system having 6 to 24, preferably 6 to 18 and particularly preferably 6 to 13 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , preferably non-aromatic radicals R 2 . In a preferred embodiment, two radicals R and R' which are bonded to different cycles do not form an aliphatic, aromatic or heteroaromatic ring system with one another. In a further preferred embodiment, two radicals R, or R and R' which are bonded to different cycles do not form an aliphatic, aromatic or heteroaromatic ring system with one another. Suitable aromatic or heteroaromatic ring systems R or R' are selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorene, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorene, which can be linked via the 1-, 2-, 3- or 4-position, naphthalene, which can be linked via the 1- or 2-position, indole, benzofuran, benzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, indenocarbazole, indolocarbazole, pyridine, pyrimidine, pyrazine, pyridazine, triazine, quinoline, quinazoline, benzimidazole, phenanthrene, triphenylene or a combination of two or three of these groups, each of which can be substituted by one or more radicals R 1. If R is a heteroaryl group, in particular triazine, pyrimidine or quinazoline, aromatic or heteroaromatic radicals R 1 on this heteroaryl group can also be preferred. The groups R or R', if they represent an aromatic or heteroaromatic ring system, are preferably selected from the groups of the following formulas R-1 to R-182,
R-16 R-18 R-58 R-114 -117 R-16 R-18 R-58 R-114 -117
wobei R1 die oben genannten Bedeutungen aufweist, die gestrichelte Bindung die Bindung zu Formel (1) darstellt und weiterhin gilt: Ar3 ist bei jedem Auftreten gleich oder verschieden ein bivalentes aroma- tisches oder heteroaromatisches Ringsystem mit 6 bis 18 aroma- tischen Ringatomen, welches jeweils mit einem oder mehreren Resten R1 substituiert sein kann; A1 ist bei jedem Auftreten gleich oder verschieden BR1, C(R1)2, NR1, O oder S, wobei A1 in den Formeln R-45, R-46, R-47, R-48 für BR1, NR1, O oder S steht, bevorzugt C(R1)2, NR1, O oder S, wobei A1 in den Formeln R-45, R-46, R-47, R-48 für NR1, O oder S steht; A2 ist bei jedem Auftreten gleich oder verschieden C(R1)2, NR1, O oder S; p ist 0 oder 1, wobei p = 0 bedeutet, dass die Gruppe Ar3 nicht vorhan- den ist und dass die entsprechende aromatische bzw. heteroaroma- tische Gruppe direkt an das zugehörige Atom, beispielsweise ein Kohlenstoffatom oder an ein Heteroatom wie ein Stickstoff gebunden ist, wobei im Fall von Bindung an ein Heteroatom für die Formeln R- 44, R-49, R-53, R-57, R-58, R-62, R-66, R-70, R-71, R-112, R-152 bis R-160, R-167, R-172, R-177, R-182 p gleich 1 ist; r ist 0 oder 1, wobei r = 0 bedeutet, dass an dieser Position keine Gruppe A1 gebunden ist und an die entsprechenden Kohlenstoffatome stattdessen Reste R1 gebunden sind. In einer bevorzugten Ausführungsform umfasst Ar3 bivalente aromatische oder heteroaromatische Ringsysteme basierend auf den Gruppen der R-1 bis R-182, wobei p gleich 0 gilt und die gestrichelte Bindung und ein R1 für die Bindung zur aromatischen oder heteroaromatischen Gruppe nach R-1 bis R-182 steht. Wenn die oben genannten Gruppen R-1 bis R-182 für R mehrere Gruppen A1 aufweisen, so kommen hierfür alle Kombinationen aus der Definition von A1 in Frage. Bevorzugte Ausführungsformen sind dann solche, in denen eine Gruppe A1 für C(R1)2, NR1, O oder S und die andere Gruppe A1 für C(R1)2 steht oder in denen beide Gruppen A1 für S oder O stehen oder in denen beide Gruppen A1 für O bzw. S stehen. Wenn A1 für NR1 steht, steht der Substituent R1, der an das Stickstoffatom gebunden ist, bevorzugt für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, welches auch durch einen oder mehrere Reste R2 substituiert sein kann. In einer besonders bevorzugten Ausführungsform steht dieser Substituent R1 gleich oder ver- schieden bei jedem Auftreten für ein aromatisches oder heteroaroma- tisches Ringsystem mit 6 bis 24 aromatischen Ringatomen, bevorzugt mit 6 bis 12 aromatischen Ringatomen, und welches jeweils auch durch einen oder mehrere Reste R2 substituiert sein kann. Besonders bevorzugt sind Phenyl, Biphenyl, Terphenyl und Quaterphenyl mit Verknüpfungsmustern, wie vorne für R-1 bis R-35 aufgeführt, wobei diese Strukturen durch einen oder mehrere Reste R1 substituiert sein können, bevorzugt aber unsubstituiert sind. Wenn A1 für C(R1)2 steht, stehen die Substituenten R1, die an dieses Kohlenstoffatom gebunden sind, bevorzugt gleich oder verschieden bei jedem Auftreten für eine lineare Alkylgruppe mit 1 bis 10 C-Atomen oder für eine verzweigte oder zyklische Alkylgruppe mit 3 bis 10 C-Atomen oder für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, welches auch durch einen oder mehrere Reste R2 substituiert sein kann. Ganz besonders bevorzugt steht R1 für eine Methylgruppe oder für eine Phenylgruppe. Dabei können die Reste R1 auch miteinander ein Ringsystem bilden, was zu einem Spirosystem führt. In einer bevorzugten Ausführungsform der Erfindung ist R‘ bei jedem Auf- treten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus D, F, CN, OR1 oder einem aromatischen oder heteroaromatischen Ring- system mit 6 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1 substituiert sein kann. Besonders bevorzugt ist R‘ bei jedem Auftreten gleich oder verschieden ausgewählt aus der Gruppe bestehend aus D, F, CN oder einem aroma- tischen oder heteroaromatischen Ringsystem mit 6 bis 24 aromatischen Ringatomen, besonders bevorzugt mit 6 bis 12 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R1, bevorzugt nicht- aromatische Reste R1, substituiert sein kann. Geeignete aromatische bzw. heteroaromatische Ringsysteme R‘ sind aus- gewählt aus Phenyl, Biphenyl, insbesondere ortho-, meta- oder para- Biphenyl, Terphenyl, insbesondere ortho-, meta-, para- oder verzweigtem Terphenyl, Quaterphenyl, insbesondere ortho-, meta-, para- oder ver- zweigtem Quaterphenyl, Fluoren, welches über die 1-, 2-, 3- oder 4- Position verknüpft sein kann, Spirobifluoren, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Naphthalin, welches über die 1- oder 2-Position verknüpft sein kann, Indol, Benzofuran, Benzothiophen, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Dibenzo- furan, Carbazol, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Dibenzothiophen, welches über die 1-, 2-, 3- oder 4-Position ver- knüpft sein kann, Indenocarbazol, Indolocarbazol, Pyridin, Pyrimidin, Pyrazin, Pyridazin, Triazin, Chinolin, Chinazolin, Benzimidazol, Phenanthren, Triphenylen oder einer Kombination aus zwei oder drei dieser Gruppen, welche jeweils mit einem oder mehreren Resten R1 sub- stituiert sein können. Wenn R‘ für eine Heteroarylgruppe, insbesondere für Triazin, Pyrimidin oder Chinazolin steht, können auch aromatische oder heteroaromatische Reste R1 an dieser Heteroarylgruppe bevorzugt sein. Dabei sind die Gruppen R‘, wenn sie für ein aromatisches bzw. heteroaro- matisches Ringsystem stehen, bevorzugt gewählt aus den Gruppen der vorstehenden Formeln R-1 bis R-182, besonders bevorzugt gewählt aus den Gruppen der vorstehenden Formeln R-1 bis R-182, wobei A1 für C(R1)2, NR1, O oder S steht. In einer bevorzugten Ausführungsform der Erfindung ist R‘ gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus H, D, F, CN, N(R2)2, OR2, einer geradkettigen Alkylgruppe mit 1 bis 10 C-Atomen. In einer weiteren bevorzugten Ausführungsform der Erfindung ist R1 gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe be- stehend aus H, D, F, CN, N(R2)2, OR2, einer geradkettigen Alkylgruppe mit 1 bis 10 C-Atomen oder einer Alkenylgruppe mit 2 bis 10 C-Atomen oder einer verzweigten oder zyklischen Alkylgruppe mit 3 bis 10 C-Atomen, wobei die Alkyl- bzw. Alkenylgruppe jeweils mit einem oder mehreren Resten R2 substituiert sein kann und wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch O ersetzt sein können, oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 30 aroma- tischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 sub- stituiert sein kann; dabei können zwei oder mehrere Reste R1 miteinander ein aliphatisches Ringsystem bilden. In einer besonders bevorzugten Ausführungsform der Erfindung ist R1 gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus H, einer gerad- kettigen Alkylgruppe mit 1 bis 6 C-Atomen, insbesondere mit 1, 2, 3 oder 4 C-Atomen, oder einer verzweigten oder zyklischen Alkylgruppe mit 3 bis 6 C-Atomen, wobei die Alkylgruppe mit einem oder mehreren Resten R2 substituiert sein kann, bevorzugt aber unsubstituiert ist, oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 24 aroma- tischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 sub- stituiert sein kann, bevorzugt aber unsubstituiert ist. In einer weiteren bevorzugten Ausführungsform der Erfindung ist R2 gleich oder verschieden bei jedem Auftreten H, F, eine Alkylgruppe mit 1 bis 4 C- Atomen oder eine Arylgruppe mit 6 bis 10 C-Atomen, welche mit einer Alkylgruppe mit 1 bis 4 C-Atomen substituiert sein kann, bevorzugt aber unsubstituiert ist. In einer weiteren bevorzugten Ausführungsform der Erfindung sind alle Reste R1, soweit sie für ein aromatisches oder heteroaromatisches Ring- system, bzw. R2 soweit sie für aromatische oder heteroaromatische Gruppen stehen, ausgewählt aus den Gruppen R-1 bis R-182, welche allerdings dann jeweils entsprechend mit R2, bzw. den bei R2 genannten Gruppen substituiert sind. In einer bevorzugten Ausführungsform der Erfindung sind alle aroma- tischen oder heteroaromatischen Gruppen der Reste R, R‘, R1 oder R2 ausgewählt aus den entsprechenden Gruppen R-1 bis R-182, bevorzugt ausgewählt aus den Gruppen R-1 bis R-182, wobei A1 für O, S, NR1 oder C(R1)2 bzw. die entsprechenden Reste NR2, bzw. C(R2)2 oder NR3, bzw. C(R3)2 steht. In einer bevorzugten Ausführungsform bilden die Reste R und/oder R‘ keine weiteren an das Grundgerüst der Formel (1) ankondensierten aromatischen oder heteroaromatischen Gruppen. In einer bevorzugten Ausführungsform der Erfindung steht R bei jedem Auftreten gleich oder verschieden für eine Gruppe ausgewählt aus den Gruppen R-1 bis R-182 und R1 steht in diesen Gruppen für H, D, F oder CN. In einer bevorzugten Ausführungsform steht R‘ bei jedem Auftreten gleich oder verschieden an allen Zyklen der Verbindung der Formel (1) für H, D, F oder CN, bevorzugt H oder D. Die Erfindung betrifft außerdem ein Oligomer, Polymer oder Dendrimer enthaltend eine oder mehrere Verbindungen gemäß Formel (1) oder der bevofzguten Ausführungsformen, wobei die Bindung(en) zu dem Oligomer, Polymer oder Dendrimer an beliebigen Positionen in Formel (1) erfolgen kann (können). Die erfindungsgemäße Verbindung ist bevorzugt nicht Teil eines Polymers, Oligomers oder Copolymers. Bevorzugt haben die Alkylgruppen in erfindungsgemäßen Verbindungen, die durch Vakuumverdampfung verarbeitet werden, bevorzugt nicht mehr als fünf C-Atome, besonders bevorzugt nicht mehr als 4 C-Atome, ganz besonders bevorzugt nicht mehr als 1 C-Atom. Für Verbindungen, die aus Lösung verarbeitet werden, eignen sich auch Verbindungen, die mit Alkyl- gruppen, insbesondere verzweigten Alkylgruppen, mit bis zu 10 C-Atomen substituiert sind oder die mit Oligoarylengruppen, beispielsweise ortho-, meta-, para- oder verzweigten Terphenyl- oder Quaterphenylgruppen, substituiert sind. Die oben genannten bevorzugten Ausführungsformen können beliebig innerhalb der in Anspruch 1 definierten Einschränkungen miteinander kombiniert werden. In einer besonders bevorzugten Ausführungsform der Erfindung treten die oben genannten Bevorzugungen gleichzeitig auf. Beispiele für bevorzugte Verbindungen gemäß den oben aufgeführten Ausführungsformen sind die in der folgenden Tabelle aufgeführten Verbin- dungen. where R 1 has the meanings given above, the dashed bond represents the bond to formula (1) and the following also applies: Ar 3 is, identically or differently on each occurrence, a divalent aromatic or heteroaromatic ring system having 6 to 18 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 ; A 1 is, identically or differently on each occurrence, BR 1 , C(R 1 ) 2 , NR 1 , O or S, where A 1 in the formulas R-45, R-46, R-47, R-48 stands for BR 1 , NR 1 , O or S, preferably C(R 1 ) 2 , NR 1 , O or S, where A 1 in the formulas R-45, R-46, R-47, R-48 stands for NR 1 , O or S; A 2 is, identically or differently on each occurrence, C(R 1 ) 2 , NR 1 , O or S; p is 0 or 1, where p = 0 means that the group Ar 3 is not present and that the corresponding aromatic or heteroaromatic group is bonded directly to the associated atom, for example a carbon atom or to a heteroatom such as nitrogen, where in the case of bonding to a heteroatom for the formulas R- 44, R-49, R-53, R-57, R-58, R-62, R-66, R-70, R-71, R-112, R-152 to R-160, R-167, R-172, R-177, R-182 p is 1; r is 0 or 1, where r = 0 means that no group A 1 is bonded at this position and instead radicals R 1 are bonded to the corresponding carbon atoms. In a preferred embodiment, Ar 3 comprises bivalent aromatic or heteroaromatic ring systems based on the groups of R-1 to R-182, where p is 0 and the dashed bond and an R 1 represent the bond to the aromatic or heteroaromatic group after R-1 to R-182. If the above-mentioned groups R-1 to R-182 have several groups A 1 for R, all combinations from the definition of A 1 are possible. Preferred embodiments are then those in which one group A 1 represents C(R 1 ) 2 , NR 1 , O or S and the other group A 1 represents C(R 1 ) 2 or in which both groups A 1 represent S or O or in which both groups A 1 represent O or S. If A 1 represents NR 1 , the substituent R 1 which is bonded to the nitrogen atom preferably represents an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 2 . In a particularly preferred embodiment, this substituent R 1 is the same or different on each occurrence and represents an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, preferably having 6 to 12 aromatic ring atoms, and which in each case may also be substituted by one or more radicals R 2 . Particularly preferred are phenyl, biphenyl, terphenyl and quaterphenyl with linkage patterns as listed above for R-1 to R-35, where these structures may be substituted by one or more radicals R 1 , but are preferably unsubstituted. If A 1 is C(R 1 ) 2 , the substituents R 1 which are bonded to this carbon atom are preferably identical or different on each occurrence and represent a linear alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms or an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 2 . R 1 is very particularly preferably a methyl group or a phenyl group. The radicals R 1 can also form a ring system with one another, resulting in a spiro system. In a preferred embodiment of the invention, R' is selected on each occurrence, identically or differently, from the group consisting of D, F, CN, OR 1 or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 . R' is particularly preferably selected on each occurrence, identically or differently, from the group consisting of D, F, CN or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, particularly preferably having 6 to 12 aromatic ring atoms, each of which may be substituted by one or more radicals R 1 , preferably non-aromatic radicals R 1 . Suitable aromatic or heteroaromatic ring systems R' are selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorene, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorene, which can be linked via the 1-, 2-, 3- or 4-position, naphthalene, which can be linked via the 1- or 2-position, indole, benzofuran, benzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, indenocarbazole, indolocarbazole, pyridine, pyrimidine, pyrazine, pyridazine, triazine, quinoline, quinazoline, benzimidazole, phenanthrene, triphenylene or a combination of two or three of these groups, each of which can be substituted by one or more radicals R 1. If R' is a heteroaryl group, in particular triazine, pyrimidine or quinazoline, aromatic or heteroaromatic radicals R 1 on this heteroaryl group can also be preferred. The groups R', if they represent an aromatic or heteroaromatic ring system, are preferably selected from the groups of the above formulas R-1 to R-182, particularly preferably selected from the groups of the above formulas R-1 to R-182, where A 1 is C(R 1 ) 2 , NR 1 , O or S. In a preferred embodiment of the invention, R' is the same or different on each occurrence and is selected from the group consisting of H, D, F, CN, N(R 2 ) 2 , OR 2 , a straight-chain alkyl group having 1 to 10 C atoms. In a further preferred embodiment of the invention, R 1 is the same or different on each occurrence and is selected from the group consisting of H, D, F, CN, N(R 2 ) 2 , OR 2 , a straight-chain alkyl group having 1 to 10 C atoms or an alkenyl group having 2 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, where the alkyl or alkenyl group can each be substituted by one or more radicals R 2 and where one or more non-adjacent CH2 groups can be replaced by O, or an aromatic or heteroaromatic ring system having 6 to 30 aromatic ring atoms, which can each be substituted by one or more radicals R 2 ; two or more radicals R 1 can form an aliphatic ring system with one another. In a particularly preferred embodiment of the invention, R 1 is the same or different on each occurrence and is selected from the group consisting of H, a straight-chain alkyl group having 1 to 6 C atoms, in particular having 1, 2, 3 or 4 C atoms, or a branched or cyclic alkyl group having 3 to 6 C atoms, where the alkyl group may be substituted by one or more radicals R 2 , but is preferably unsubstituted, or an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , but is preferably unsubstituted. In a further preferred embodiment of the invention, R 2 is the same or different on each occurrence and is H, F, an alkyl group having 1 to 4 C atoms or an aryl group having 6 to 10 C atoms, which may be substituted by an alkyl group having 1 to 4 C atoms, but is preferably unsubstituted. In a further preferred embodiment of the invention, all radicals R 1 , insofar as they represent an aromatic or heteroaromatic ring system, or R 2 , insofar as they represent aromatic or heteroaromatic groups, are selected from the groups R-1 to R-182, which are then each substituted accordingly with R 2 or the groups mentioned under R 2 . In a preferred embodiment of the invention, all aromatic or heteroaromatic groups of the radicals R, R', R 1 or R 2 are selected from the corresponding groups R-1 to R-182, preferably selected from the groups R-1 to R-182, where A 1 stands for O, S, NR 1 or C(R 1 ) 2 or the corresponding radicals NR 2 , or C(R 2 ) 2 or NR 3 , or C(R 3 ) 2 . In a preferred embodiment, the radicals R and/or R' do not form any further aromatic or heteroaromatic groups fused to the basic structure of formula (1). In a preferred embodiment of the invention, R is the same or different on each occurrence and is a group selected from the groups R-1 to R-182 and R 1 in these groups is H, D, F or CN. In a preferred embodiment, R' is the same or different on each occurrence and is H, D, F or CN, preferably H or D, in all cycles of the compound of formula (1). The invention also relates to an oligomer, polymer or dendrimer containing one or more compounds according to formula (1) or the preferred embodiments, where the bond(s) to the oligomer, polymer or dendrimer can be made at any position in formula (1). The compound according to the invention is preferably not part of a polymer, oligomer or copolymer. The alkyl groups in compounds according to the invention which are processed by vacuum evaporation preferably have no more than five C atoms, particularly preferably no more than 4 C atoms, very particularly preferably no more than 1 C atom. For compounds which are processed from solution, compounds which are substituted with alkyl groups, in particular branched alkyl groups, with up to 10 C atoms or which are substituted with oligoarylene groups, for example ortho-, meta-, para- or branched terphenyl or quaterphenyl groups, are also suitable. The above-mentioned preferred embodiments can be combined with one another as desired within the restrictions defined in claim 1. In a particularly preferred embodiment of the invention, the above-mentioned preferences occur simultaneously. Examples of preferred compounds according to the above-mentioned embodiments are the compounds listed in the following table.
Die erfindungsgemäßen Verbindungen können nach dem Fachmann bekannten Syntheseschritten, wie z. B. Bromierung, Suzuki-Kupplung, Ullmann-Kupplung, Heck-Reaktion, Hartwig-Buchwald-Kupplung, etc., dargestellt werden. Ein weiterer Gegenstand der vorliegenden Erfindung ist daher ein Ver- fahren zur Herstellung der erfindungsgemäßen Verbindungen, gekenn- zeichnet durch die folgenden Schritte: (A) Synthese des kondensierten Grundgerüsts nach Formel (1); (B) Einführen der aromatischen oder heteroaromatischen Gruppen R durch Kupplungsreaktionen. Die erfindungsgemäßen Verbindungen können daher ausgehend von literaturbekannten Verbindungen nach Fukumoto et al., Macromolecules 2017, 50, 865 oder Gotsu et al., Molecules 2018, 23, 3337 dargestellt werden. In Schema 1 und 2 ist dies am Beispiel des bromierten Grundgerüsts gezeigt, welches durch eine Folge von Suzuki-Kupplungen oder metall- organischen Kupplungsreaktionen hergestellt wird. An dieses Grundgerüst können durch weitere Kupplungsreaktionen, wie in Schema 3 gezeigt, weitere Gruppen hinzugefügt werden. The compounds according to the invention can be prepared by synthesis steps known to the person skilled in the art, such as bromination, Suzuki coupling, Ullmann coupling, Heck reaction, Hartwig-Buchwald coupling, etc. The present invention therefore further relates to a process for preparing the compounds according to the invention, characterized by the following steps: (A) synthesis of the condensed basic structure according to formula (1); (B) introduction of the aromatic or heteroaromatic groups R by coupling reactions. The compounds according to the invention can therefore be prepared starting from compounds known from the literature according to Fukumoto et al., Macromolecules 2017, 50, 865 or Gotsu et al., Molecules 2018, 23, 3337. In Schemes 1 and 2, this is shown using the example of the brominated basic structure, which is prepared by a sequence of Suzuki couplings or organometallic coupling reactions. Additional groups can be added to this basic scaffold by further coupling reactions, as shown in Scheme 3.
Für die Verarbeitung der erfindungsgemäßen Verbindungen aus flüssiger Phase, beispielsweise durch Spin-Coating oder durch Druckverfahren, sind Formulierungen der erfindungsgemäßen Verbindungen erforderlich. Diese Formulierungen können beispielsweise Lösungen, Dispersionen oder Emulsionen sein. Es kann bevorzugt sein, hierfür Mischungen aus zwei oder mehr Lösemitteln zu verwenden. Geeignete und bevorzugte Lösemittel sind beispielsweise Toluol, Anisol, o-, m- oder p-Xylol, Methyl- benzoat, Mesitylen, Tetralin, Veratrol, THF, Methyl-THF, THP, Chlor- benzol, Dioxan, Phenoxytoluol, insbesondere 3-Phenoxytoluol, (-)- Fenchon, 1,2,3,5-Tetramethylbenzol, 1,2,4,5-Tetramethylbenzol, 1-Methyl- naphthalin, 2-Methylbenzothiazol, 2-Phenoxyethanol, 2-Pyrrolidinon, 3- Methylanisol, 4-Methylanisol, 3,4-Dimethylanisol, 3,5-Dimethylanisol, Acetophenon, ^-Terpineol, Benzothiazol, Butylbenzoat, Cumol, Cyclo- hexanol, Cyclohexanon, Cyclohexylbenzol, Decalin, Dodecylbenzol, Ethyl- benzoat, Indan, NMP, p-Cymol, Phenetol, 1,4-Diisopropylbenzol, Di- benzylether, Diethylenglycolbutylmethylether, Triethylenglycolbutylmethyl- ether, Diethylenglycoldibutylether, Triethylenglycoldimethylether, Di- ethylenglycolmonobutylether, Tripropyleneglycoldimethylether, Tetra- ethylenglycoldimethylether, 2-Isopropylnaphthalin, Pentylbenzol, Hexyl- benzol, Heptylbenzol, Octylbenzol, 1,1-Bis(3,4-dimethylphenyl)ethan, 2- Methylbiphenyl, 3-Methylbiphenyl, 1-Methylnaphthalin, 1-Ethylnaphthalin, Ethyloctanoat, Sebacinsäure-diethylester, Octyloctanoat, Heptylbenzol, Menthyl-isovalerat, Cyclohexylhexanoat oder Mischungen dieser Löse- mittel. Ein weiterer Gegenstand der vorliegenden Erfindung ist daher eine For- mulierung, insbesondere eine Lösung, Dispersion oder Emulsion, umfassend mindestens eine erfindungsgemäße Verbindung und mindes- tens eine weitere Verbindung. Die weitere Verbindung kann beispiels- weise ein Lösemittel sein, insbesondere eines der oben genannten Löse- mittel oder eine Mischung dieser Lösemittel. Die Herstellung solcher Lösungen ist dem Fachmann bekannt und ist beispielsweise beschrieben in WO 2002/072714, WO 2003/019694 und der darin zitierten Literatur. Die weitere Verbindung kann aber auch mindestens eine weitere organische oder anorganische Verbindung sein, die ebenfalls in der elektronischen Vorrichtung eingesetzt wird, beispielsweise eine emittierende Verbindung und/oder ein Matrixmaterial. Diese weitere Verbindung kann auch polymer sein. Die erfindungsgemäßen Verbindungen eignen sich für die Verwendung in einer elektronischen Vorrichtung, insbesondere in einer organischen Elektrolumineszenzvorrichtung (OLED). Abhängig von der Substitution können die Verbindungen in unterschiedlichen Funktionen und Schichten verwendet werden. Ein weiterer Gegenstand der vorliegenden Erfindung ist daher die Verwen- dung einer erfindungsgemäßen Verbindung in einer elektronischen Vor- richtung. Ein nochmals weiterer Gegenstand der vorliegenden Erfindung ist eine elektronische Vorrichtung enthaltend mindestens eine erfindungsgemäße Verbindung. Eine elektronische Vorrichtung im Sinne der vorliegenden Erfindung ist eine Vorrichtung, welche mindestens eine Schicht enthält, die mindestens eine organische Verbindung enthält. Das Bauteil kann dabei auch anorga- nische Materialien enthalten oder auch Schichten, welche vollständig aus anorganischen Materialien aufgebaut sind. Die elektronische Vorrichtung ist bevorzugt ausgewählt aus der Gruppe bestehend aus organischen Elektrolumineszenzvorrichtungen (OLEDs), organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt- Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solar- zellen (O-SCs), farbstoffsensibilisierten organischen Solarzellen (DSSCs), organischen optischen Detektoren, organischen Photorezeptoren, orga- nischen Feld-Quench-Devices (O-FQDs), lichtemittierenden elektro- chemischen Zellen (LECs), organischen Laserdioden (O-Laser) und „organic plasmon emitting devices“, bevorzugt aber organischen Elektro- lumineszenzvorrichtungen (OLEDs). Die Vorrichtung ist besonders bevorzugt eine organische Elektrolumines- zenzvorrichtung umfassend Kathode, Anode und mindestens eine emittierende Schicht, wobei mindestens eine organische Schicht, welche eine emittierende Schicht, Lochtransportschicht, Elektronentransport- schicht, Lochblockierschicht, Elektronenblockierschicht oder eine andere funktionelle Schicht sein kann, mindestens eine erfindungsgemäße Verbindung umfasst. Die Schicht ist abhängig von der Substitution der Verbindung. Außer diesen Schichten kann die organische Elektrolumineszenzvor- richtung noch weitere Schichten enthalten, beispielsweise jeweils eine oder mehrere Lochinjektionsschichten, Lochtransportschichten, Loch- blockierschichten, Elektronentransportschichten, Elektroneninjektions- schichten, Exzitonenblockierschichten, Elektronenblockierschichten, Ladungserzeugungsschichten (Charge-Generation Layers) und/oder organische oder anorganische p/n Übergänge. Ebenso können zwischen zwei emittierende Schichten Interlayer eingebracht sein, welche beispiels- weise eine exzitonenblockierende Funktion aufweisen. Es sei aber darauf hingewiesen, dass nicht notwendigerweise jede dieser Schichten vorhanden sein muss. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittierende Schicht enthalten, oder sie kann mehrere emittierende Schichten enthalten. Wenn mehrere Emissionsschichten vorhanden sind, weisen diese bevorzugt insgesamt mehrere Emissionsmaxima zwischen 380 nm und 750 nm auf, sodass insgesamt weiße Emission resultiert, d. h. in den emittierenden Schichten werden verschiedene emittierende Verbin- dungen verwendet, die fluoreszieren oder phosphoreszieren können. Insbesondere bevorzugt sind Systeme mit drei emittierenden Schichten, wobei die drei Schichten blaue, grüne und orange oder rote Emission zeigen (Der prinzipielle Aufbau ist beispielsweise in WO 2005/011013 beschrieben). Es kann sich bei der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung auch um eine Tandem-OLED handeln, insbesondere für weiß emittierende OLEDs. Bevorzugt wird die Verbindung gemäß Formel (1) in einer organischen Elektrolumineszenzvorrichtung verwendet, welche einen oder mehrere phosphoreszierende Emitter umfasst. Die erfindungsgemäße Verbindung gemäß den oben aufgeführten Ausführungsformen kann dabei in unter- schiedlichen Schichten eingesetzt werden, je nach genauer Struktur. Dabei kann die organische Elektrolumineszenzvorrichtung eine emittieren- de Schicht enthalten, oder sie kann mehrere emittierende Schichten ent- halten, wobei mindestens eine Schicht mindestens eine erfindungs- gemäße Verbindung enthält. Weiterhin kann die erfindungsgemäße Verbindung auch in einer Elektronentransportschicht und/oder in einer Lochblockierschicht und/oder in einer Lochtransportschicht und/oder in einer Exzitonenblockierschicht und/oder als Matrixmaterial eingesetzt werden. Besonders bevorzugt wird die erfindungsgemäße Verbindung als Matrixmaterial in einer emittierenden Schicht und/oder als Elektronen- transportmaterial in einer Elektronentransport- oder Lochblockierschicht eingesetzt, insbesondere als Matrixmaterial in einer phosphoreszierenden Schicht. Der Ausdruck „phosphoreszierende Verbindung“ bezeichnet typischer- weise Verbindungen, bei denen die Aussendung von Licht durch einen spin-verbotenen Übergang erfolgt, z. B. einen Übergang von einem angeregten Triplett-Zustand oder einem Zustand mit einer höheren Spin- Quantenzahl, z. B. einem Quintett-Zustand. Geeignete phosphoreszierende Verbindungen (= Triplett-Emitter) sind ins- besondere Verbindungen, die bei geeigneter Anregung Licht, vorzugs- weise im sichtbaren Bereich, emittieren und außerdem mindestens ein Atom der Ordnungszahl größer als 20, vorzugsweise größer als 38 und kleiner als 84, besonders bevorzugt größer als 56 und kleiner als 80 enthalten. Bevorzugt werden als phosphoreszierende Verbindungen alle lumineszierenden Komplexe mit Übergangsmetallen oder Lanthaniden angesehen, insbesondere wenn sie Kupfer, Molybdän, Wolfram, Rhenium, Ruthenium, Osmium, Rhodium, Iridium, Palladium, Platin, Silber, Gold oder Europium enthalten, insbesondere Verbindungen, die Iridium, Platin oder Kupfer enthalten. Im Rahmen der vorliegenden Erfindung werden alle lumineszierenden Iridium-, Platin- oder Kupferkomplexe als phosphores- zierende emittierende Verbindungen betrachtet. Beispiele der oben beschriebenen Emitter können den Anmeldungen WO 00/70655, WO 2001/41512, WO 2002/02714, WO 2002/15645, EP 1191613, EP 1191612, EP 1191614, WO 05/033244, WO 05/019373, US 2005/0258742, WO 2009/146770, WO 2010/015307, WO 2010/031485, WO 2010/054731, WO 2010/054728, WO 2010/086089, WO 2010/099852, WO 2010/102709, WO 2011/032626, WO 2011/066898, WO 2011/157339, WO 2012/007086, WO 2014/008982, WO 2014/023377, WO 2014/094961, WO 2014/094960, WO 2015/036074, WO 2015/104045, WO 2015/117718, WO 2016/015815, WO 2016/124304, WO 2017/032439, WO 2018/011186, WO 2018/041769, WO 2019/020538, WO 2018/178001, WO 2019/115423 und WO 2019/158453 entnommen werden. Generell eignen sich alle phospho- reszierenden Komplexe, wie sie gemäß dem Stand der Technik für phos- phoreszierende OLEDs verwendet werden und wie sie dem Fachmann auf dem Gebiet der organischen Elektrolumineszenz bekannt sind, und der Fachmann kann ohne erfinderisches Zutun weitere phosphoreszierende Komplexe verwenden. Für den Fachmann ist es auch ohne erfinderische Tätigkeit möglich, weitere phosphoreszierende Komplexe in Kombination mit den Verbindungen der Formel (1) in organischen Elektrolumineszenz- vorrichtungen zu verwenden. Weitere Beispiele sind in einer nach- folgenden Tabelle aufgeführt. Erfindungsgemäß ist es auch möglich, die Verbindung der Formel (1) in einer elektronischen Vorrichtung zu verwenden, die eine oder mehrere fluoreszierende emittierende Verbindungen enthält. In einer bevorzugten Ausführungsform der Erfindung werden die Verbin- dungen der Formel (1) als elektronentransportierendes Material verwen- det. In diesem Fall sind die Verbindungen vorzugsweise in einer Elektronentransportschicht oder einer Lochblockierschicht oder einem elektronenleitendem oder bipolaren Hostmaterial enthalten. Besonders bevorzugt ist die Verwendung in einer Elektronentransportschicht oder Hostmaterial. Eine Elektronentransportschicht im Sinne der vorliegenden Anmeldung ist eine Schicht mit elektronentransportierender Funktion zwischen der Kathode und der emittierenden Schicht. Unter Elektroneninjektionsschichten und Lochblockierschichten werden im Rahmen der vorliegenden Anmeldung bestimmte Ausführungsformen von Elektronentransportschichten verstanden. Eine Elektroneninjektions- schicht ist im Falle einer Mehrzahl von Elektronentransportschichten zwischen Kathode und emittierender Schicht eine Elektronentransport- schicht, die direkt an die Kathode angrenzt oder nur durch eine einzige Beschichtung der Kathode von dieser getrennt ist. Eine Lochblockier- schicht ist im Falle mehrerer Elektronentransportschichten zwischen Kathode und emittierender Schicht diejenige Elektronentransportschicht, die kathodenseitig direkt an die emittierende Schicht angrenzt. Vorzugs- weise umfasst die erfindungsgemäße OLED zwischen Kathode und emittierender Schicht zwei, drei oder vier elektronentransportierende Schichten, von denen vorzugsweise mindestens eine, besonders bevorzugt genau eine oder zwei Verbindungen der Formel (1) enthalten. Wird die Verbindung der Formel (1) als Elektronentransportmaterial in einer Elektronentransportschicht, einer Elektroneninjektionsschicht oder einer Lochblockierschicht verwendet, so kann die Verbindung als reines Material, d.h. in einem Anteil von 100 %, in der Elektronentransportschicht eingesetzt werden, oder sie kann in Kombination mit einer oder mehreren weiteren Verbindungen verwendet werden. Lochtransportschichten oder Elektronenblockierschichten der erfindungs- gemäßen elektronischen Vorrichtungen können zusätzlich ein oder mehrere p-Dotiermittel umfassen. p-Dotiermittel, die gemäß der vor- liegenden Erfindung verwendet werden, sind vorzugsweise solche organischen Elektronenakzeptorverbindungen, die in der Lage sind, eine oder mehrere der anderen Verbindungen in der Mischung zu oxidieren. Besonders bevorzugte Ausführungsformen von p-Dotiermitteln sind die in WO 2011/073149, EP 1968131, EP 2276085, EP 2213662, EP 1722602, EP 2045848, DE 102007031220, US 8044390, US 8057712, WO 2009/003455, WO 2010/094378, WO 2011/120709, US 2010/0096600, WO 2012/095143 und DE 102012209523 offenbarten Verbindungen. Besonders bevorzugte p-Dotiermittel sind Chinodimethanverbindungen, Azaindenofluorendione, Azaphenylene, Azatriphenylene, I2, Metall- halogenide, vorzugsweise Übergangsmetallhalogenide, Metalloxide, vorzugsweise Metalloxide, die mindestens ein Übergangsmetall oder ein Metall der 3. Hauptgruppe enthalten, und Übergangsmetallkomplexe, vorzugsweise Komplexe von Cu, Co, Ni, Pd und Pt mit Liganden, die mindestens ein Sauerstoffatom als Bindungsstelle enthalten. Bevorzugt werden ferner Übergangsmetalloxide als Dotiermittel, vorzugsweise Oxide von Rhenium, Molybdän und Wolfram, besonders bevorzugt Re2O7, MoO3, WO3 und ReO3. Die p-Dotiermittel liegen vorzugsweise in einer im Wesentlichen homo- genen Verteilung in den p-dotierten Schichten vor. Dies kann z. B. durch Coevaporation des p-Dotiermittels und der Lochtransportmaterialmatrix erreicht werden. Bevorzugte p-Dotiermittel sind insbesondere die folgenden Verbindungen: For processing the compounds according to the invention from the liquid phase, for example by spin coating or by printing processes, formulations of the compounds according to the invention are required. These formulations can be, for example, solutions, dispersions or emulsions. It may be preferable to use mixtures of two or more solvents for this purpose. Suitable and preferred Solvents are, for example, toluene, anisole, o-, m- or p-xylene, methyl benzoate, mesitylene, tetralin, veratrol, THF, methyl-THF, THP, chlorobenzene, dioxane, phenoxytoluene, especially 3-phenoxytoluene, (-)-fenchone, 1,2,3,5-tetramethylbenzene, 1,2,4,5-Te tramethylbenzene, 1-methyl-naphthalene, 2-methylbenzothiazole, 2-phenoxyethanol, 2-pyrrolidinone, 3-methylanisole, 4-methylanisole, 3,4-dimethylanisole, 3,5-dimethylanisole, acetophenone, ^-terpineol, benzothiazole, butyl benzoate, cumene, cyclohexanol, cyclohexanone, cyclohexylbene zol, Decalin, dodecylbenzene, ethyl benzoate, indane, NMP, p-cymene, phenetol, 1,4-diisopropylbenzene, dibenzyl ether, diethylene glycol butyl methyl ether, triethylene glycol butyl methyl ether, diethylene glycol dibutyl ether, triethylene glycol dimethyl ether, diethylene glycol monobutyl ether, tripropylene glycol dimethyl ether, ethylene glycol dimethyl ether, 2-isopropylnaphthalene, pentylbenzene, hexylbenzene, heptylbenzene, octylbenzene, 1,1-bis(3,4-dimethylphenyl)ethane, 2-methylbiphenyl, 3-methylbiphenyl, 1-methylnaphthalene, 1-ethylnaphthalene, ethyl octanoate, sebacic acid diethyl ester, Heptylbenzene, menthyl isovalerate, cyclohexylhexanoate or mixtures of these solvents. A further subject matter of the present invention is therefore a formulation, in particular a solution, dispersion or emulsion, comprising at least one compound according to the invention and at least one further compound. The further compound can be, for example, a solvent, in particular one of the abovementioned solvents or a mixture of these solvents. The preparation of such solutions is known to the person skilled in the art and is described, for example, in WO 2002/072714, WO 2003/019694 and the literature cited therein. The further compound can also be at least one further organic or inorganic compound which is also used in the electronic device, for example an emitting compound and/or a matrix material. This further compound can also be polymeric. The compounds according to the invention are suitable for use in an electronic device, in particular in an organic electroluminescent device (OLED). Depending on the substitution the compounds can be used in different functions and layers. A further subject of the present invention is therefore the use of a compound according to the invention in an electronic device. A still further subject of the present invention is an electronic device containing at least one compound according to the invention. An electronic device in the sense of the present invention is a device which contains at least one layer which contains at least one organic compound. The component can also contain inorganic materials or layers which are made up entirely of inorganic materials. The electronic device is preferably selected from the group consisting of organic electroluminescent devices (OLEDs), organic integrated circuits (O-ICs), organic field-effect transistors (O-FETs), organic thin-film transistors (O-TFTs), organic light-emitting transistors (O-LETs), organic solar cells (O-SCs), dye-sensitized organic solar cells (DSSCs), organic optical detectors, organic photoreceptors, organic field quench devices (O-FQDs), light-emitting electrochemical cells (LECs), organic laser diodes (O-lasers) and organic plasmon emitting devices, but preferably organic electroluminescent devices (OLEDs). The device is particularly preferably an organic electroluminescent device comprising a cathode, anode and at least one emitting layer, wherein at least one organic layer, which can be an emitting layer, hole transport layer, electron transport layer, hole blocking layer, electron blocking layer or another functional layer, contains at least one inventive compound. The layer depends on the substitution of the compound. In addition to these layers, the organic electroluminescent device can contain further layers, for example one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, exciton blocking layers, electron blocking layers, charge generation layers and/or organic or inorganic p/n junctions. Interlayers can also be introduced between two emitting layers, which, for example, have an exciton blocking function. It should be noted, however, that not all of these layers necessarily have to be present. The organic electroluminescent device can contain one emitting layer, or it can contain several emitting layers. If several emission layers are present, these preferably have a total of several emission maxima between 380 nm and 750 nm, so that overall white emission results, ie different emitting compounds that can fluoresce or phosphoresce are used in the emitting layers. Systems with three emitting layers are particularly preferred, with the three layers showing blue, green and orange or red emission (the basic structure is described, for example, in WO 2005/011013). The organic electroluminescent device according to the invention can also be a tandem OLED, in particular for white-emitting OLEDs. The compound according to formula (1) is preferably used in an organic electroluminescent device which comprises one or more phosphorescent emitters. The compound according to the invention according to the embodiments listed above can be used in different layers, depending on the precise structure. The organic electroluminescent device can contain one emitting layer, or it can contain several emitting layers, with at least one layer containing at least one compound according to the invention. Furthermore, the compound according to the invention can also be used in an electron transport layer and/or in a hole blocking layer and/or in a hole transport layer and/or in an exciton blocking layer and/or as a matrix material. The compound according to the invention is particularly preferably used as a matrix material in an emitting layer and/or as an electron transport material in an electron transport or hole blocking layer, in particular as a matrix material in a phosphorescent layer. The term "phosphorescent compound" typically refers to compounds in which the emission of light occurs through a spin-forbidden transition, e.g. a transition from an excited triplet state or a state with a higher spin quantum number, e.g. a quintet state. Suitable phosphorescent compounds (= triplet emitters) are in particular compounds which emit light, preferably in the visible range, when suitably excited and also contain at least one atom with an atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80. All luminescent complexes with transition metals or lanthanides are preferably regarded as phosphorescent compounds, in particular if they contain copper, molybdenum, tungsten, rhenium, ruthenium, osmium, rhodium, iridium, palladium, platinum, silver, gold or europium, in particular compounds which contain iridium, platinum or copper. In the context of the present invention, all luminescent iridium, platinum or copper complexes are regarded as phosphorescent emitting compounds. Examples of the emitters described above can be found in applications WO 00/70655, WO 2001/41512, WO 2002/02714, WO 2002/15645, EP 1191613, EP 1191612, EP 1191614, WO 05/033244, WO 05/019373, US 2005/0258742, WO 2009/146770, WO 2010/015307, WO 2010/031485, WO 2010/054731, WO 2010/054728, WO 2010/086089, WO 2010/099852, WO 2010/102709, WO 2011/032626, WO 2011/066898, WO 2011/157339, WO 2012/007086, WO 2014/008982, WO 2014/023377, WO 2014/094961, WO 2014/094960, WO 2015/036074, WO 2015/104045, WO 2015/117718, WO 2016/015815, WO 2016/124304, WO 2017/032439, WO 2018/011186, WO 2018/041769, WO 2019/020538, WO 2018/178001, WO 2019/115423 and WO 2019/158453. In general, all phosphorescent complexes as used according to the prior art for phosphorescent OLEDs and as known to the person skilled in the art in the field of organic electroluminescence are suitable, and the person skilled in the art can use further phosphorescent complexes without inventive step. It is possible for the person skilled in the art, even without inventive activity, to use further phosphorescent complexes in combination with the compounds of formula (1) in organic electroluminescent devices. Further examples are listed in a table below. According to the invention, it is also possible to use the compound of formula (1) in an electronic device that contains one or more fluorescent emitting compounds. In a preferred embodiment of the invention, the compounds of formula (1) are used as electron-transporting material. In this case, the compounds are preferably contained in an electron-transport layer or a hole-blocking layer or an electron-conducting or bipolar host material. Use in an electron-transport layer or host material is particularly preferred. An electron-transport layer in the sense of the present application is a layer with an electron-transporting function between the cathode and the emitting layer. In the context of the present application, electron injection layers and hole blocking layers are understood to mean certain embodiments of electron transport layers. In the case of a plurality of electron transport layers between the cathode and the emitting layer, an electron injection layer is an electron transport layer that directly borders the cathode or is only separated from it by a single coating of the cathode. In the case of several electron transport layers between the cathode and the emitting layer, a hole blocking layer is the electron transport layer that directly borders the emitting layer on the cathode side. The OLED according to the invention preferably comprises two, three or four electron-transporting layers between the cathode and the emitting layer, of which preferably at least one, particularly preferably exactly one or two, contain compounds of the formula (1). If the compound of formula (1) is used as an electron transport material in an electron transport layer, an electron injection layer or a hole blocking layer, the compound can be used as a pure material, ie in a proportion of 100% in the electron transport layer, or it can be used in combination with one or more other compounds. Hole transport layers or electron blocking layers of the electronic devices according to the invention can additionally comprise one or more p-dopants. p-dopants used according to the present invention are preferably those organic electron acceptor compounds which are capable of oxidizing one or more of the other compounds in the mixture. Particularly preferred embodiments of p-dopants are the compounds disclosed in WO 2011/073149, EP 1968131, EP 2276085, EP 2213662, EP 1722602, EP 2045848, DE 102007031220, US 8044390, US 8057712, WO 2009/003455, WO 2010/094378, WO 2011/120709, US 2010/0096600, WO 2012/095143 and DE 102012209523. Particularly preferred p-dopants are quinodimethane compounds, azaindenofluorenediones, azaphenylenes, azatriphenylenes, I2, metal halides, preferably transition metal halides, metal oxides, preferably metal oxides containing at least one transition metal or a metal of the 3rd main group, and transition metal complexes, preferably complexes of Cu, Co, Ni, Pd and Pt with ligands containing at least one oxygen atom as a bonding site. Furthermore, preferred dopants are transition metal oxides, preferably oxides of rhenium, molybdenum and tungsten, particularly preferably Re2O7, MoO3, WO3 and ReO3. The p-dopants are preferably present in a substantially homogeneous distribution in the p-doped layers. This can be achieved, for example, by coevaporation of the p-dopant and the hole transport material matrix. Preferred p-dopants are in particular the following compounds:
Die verwendeten Lochtransportmaterialien können in Kombination mit einem Hexaazatriphenylenderivat, wie in US 2007/0092755 beschrieben, eingesetzt werden. Besonders bevorzugt wird hier das Hexaaza- triphenylenderivat in einer separaten Schicht eingesetzt. In einer weiteren Ausführungsform der vorliegenden Erfindung wird die Verbindung der Formel (1) in einer emittierenden Schicht als Matrix- material in Kombination mit einer oder mehreren emittierenden Verbin- dungen, vorzugsweise phosphoreszierenden Verbindungen, eingesetzt. Der Anteil des Matrixmaterials in der emittierenden Schicht liegt in diesem Fall zwischen 50,0 und 99,9 Vol.-%, bevorzugt zwischen 80,0 und 99,5 Vol.-%, besonders bevorzugt zwischen 92,0 und 99,5 Vol-%. für fluores- zierende emittierende Schichten und zwischen 85,0 und 97,0 Vol.-% für phosphoreszierende emittierende Schichten. Entsprechend liegt der Anteil der emittierenden Verbindung zwischen 0,1 und 50,0 Vol.-%, bevorzugt zwischen 0,5 und 20,0 Vol.-%, besonders bevorzugt zwischen 0,5 und 8,0 Vol.-% für fluoreszierende emittierende Schichten und zwischen 3,0 und 15,0 Vol.-% für phosphoreszierende emittierende Schichten. Eine emittierende Schicht einer organischen Elektrolumineszenzvor- richtung kann auch Systeme umfassen, die eine Vielzahl von Matrix- materialien (Mischmatrixsysteme) und/oder eine Vielzahl von emittierenden Verbindungen enthalten. Auch in diesem Fall sind in der Regel die emittierenden Verbindungen diejenigen, die den kleineren Anteil im System haben und die Matrixmaterialien diejenigen, die den größeren Anteil im System haben. In Einzelfällen kann jedoch der Anteil eines einzelnen Matrixmaterials im System geringer sein als der Anteil einer einzelnen emittierenden Verbindung. Vorzugsweise werden die Verbindungen der Formel (1) als Bestandteil von Mischmatrixsystemen eingesetzt. Die Mischmatrixsysteme bestehen vorzugsweise aus zwei oder drei verschiedenen Matrixmaterialien, besonders bevorzugt aus zwei verschiedenen Matrixmaterialien. Vorzugs- weise ist in diesem Fall eines der beiden Materialien ein Material mit löchertransportierenden Eigenschaften und das andere Material ist ein Material mit elektronentransportierenden Eigenschaften. Die Verbindung der Formel (1) ist vorzugsweise das Matrixmaterial mit elektronentranspor- tierenden Eigenschaften. Die gewünschten elektronentransportierenden und löchertransportierenden Eigenschaften der gemischten Matrix- komponenten können jedoch auch überwiegend oder vollständig in einer einzigen gemischten Matrixkomponente kombiniert sein, wobei die weitere(n) gemischte(n) Matrixkomponente(n) andere Funktionen erfüllt (erfüllen). Die beiden unterschiedlichen Matrixmaterialien können in einem Verhältnis von 1:50 bis 1:1, bevorzugt 1:20 bis 1:1, noch bevorzugter 1:10 bis 1:1 und am meisten bevorzugt 1:4 bis 1:1 vorliegen. Bevorzugt werden Mischmatrixsysteme in phosphoreszierenden organischen Elektrolumines- zenzvorrichtungen eingesetzt. Eine Quelle für detailliertere Informationen über Mischmatrixsysteme ist die Anmeldung WO 2010/108579. Die Mischmatrixsysteme können eine oder mehrere emittierende Verbin- dungen enthalten, vorzugsweise eine oder mehrere phosphoreszierende Verbindungen. Im Allgemeinen werden Mischmatrixsysteme bevorzugt in phosphoreszierenden organischen Elektrolumineszenzvorrichtungen eingesetzt. Besonders geeignete Matrixmaterialien, die in Kombination mit den erfindungsgemäßen Verbindungen als Matrixbestandteile eines Misch- matrixsystems verwendet werden können, werden aus den unten genannten bevorzugten Matrixmaterialien für phosphoreszierende Verbin- dungen oder den bevorzugten Matrixmaterialien für fluoreszierende Ver- bindungen ausgewählt, je nachdem, welche Art von emittierender Verbin- dung in dem Mischmatrixsystem verwendet wird. Bevorzugte phosphoreszierende Verbindungen zur Verwendung in gemischten Matrixsystemen sind die gleichen, wie weiter oben als allge- mein bevorzugte phosphoreszierende Emittermaterialien beschrieben. Beispiele für phosphoreszierende Verbindungen sind nachfolgend aufgeführt. Bevorzugte fluoreszierende emittierende Verbindungen sind ausgewählt aus der Klasse der Arylamine. Unter einem Arylamin oder einem aromatischen Amin wird im Rahmen der vorliegenden Erfindung eine Verbindung verstanden, die drei substituierte oder unsubstituierte aromatische oder heteroaromatische Ringsysteme enthält, die direkt an den Stickstoff gebunden sind. Vorzugsweise ist mindestens eines dieser aromatischen oder heteroaromatischen Ringsysteme ein kondensiertes Ringsystem, besonders bevorzugt mit mindestens 14 aromatischen Ringatomen. Bevorzugte Beispiele hierfür sind aromatische Anthracen- amine, aromatische Anthracendiamine, aromatische Pyrenamine, aromatische Pyrenediamine, aromatische Chrysenamine oder aromatische Chrysendiamine. Unter einem aromatischen Anthracenamin versteht man eine Verbindung, bei der eine Diarylaminogruppe direkt an eine Anthracengruppe, vorzugsweise in Position 9, gebunden ist. Unter einem aromatischen Anthracendiamin ist eine Verbindung zu verstehen, in der zwei Diarylaminogruppen direkt an eine Anthracengruppe gebunden sind, vorzugsweise in den Positionen 9, 10. Analog sind aromatische Pyrenamine, Pyrendiamine, Chrysenamine und Chrysendiamine definiert, bei denen die Diarylaminogruppen vorzugsweise in 1-Position oder 1,6- Position an das Pyren gebunden sind. Weitere bevorzugte emittierende Verbindungen sind Indenofluorenamine oder Fluorendiamine, beispiels- weise nach WO 2006/108497 oder WO 2006/122630, Benzoindeno- fluorenamine oder -fluorendiamine, beispielsweise nach WO 2008/006449, und Dibenzoindenofluorenamine oder -diamine, beispiels- weise nach WO 2007/140847, sowie die in WO 2010/012328 offenbarten Indenofluorenderivate mit kondensierten Arylgruppen. Ebenso bevorzugt sind die in WO 2012/048780 und in WO 2013/185871 offenbarten Pyrenearylamine. Ebenfalls bevorzugt sind die in WO 2014/037077 offenbarten Benzoindenofluorenamine, die in WO 2014/106522 offen- barten Benzofluorenamine, die in WO 2014/111269 und in WO 2017/036574 offenbarten verlängerten Benzoindenofluorene, die in WO 2017/028940 und in WO 2017/028941 offenbarten Phenoxazine und die in WO 2016/150544 offenbarten an Furaneinheiten oder an Thiophen- einheiten gebundenen Fluorderivate. Weiterhin können Bor-Verbindung gemäß WO2020208051, WO2015102118, WO2016152418 , WO2018095397, WO2019004248 , WO2019132040, US20200161552, WO2021089450 Verwendung finden. Nützliche Matrixmaterialien, vorzugsweise für fluoreszierende Verbindungen, umfassen Materialien verschiedener Substanzklassen. Bevorzugte Matrixmaterialien sind ausgewählt aus den Klassen der Oligoaryle (z.B.2,2',7,7'-Tetraphenylspirobifluoren nach EP 676461 oder Dinaphthylanthracen), insbesondere der Oligoaryle mit anellierten aromatischen Gruppen, der Oligoarylenvinylene (z.B. DPVBi oder Spiro- DPVBi gemäß EP 676461), der polypodalen Metallkomplexe (z.B. gemäß WO 2004/081017), der lochleitenden Verbindungen (z.B. gemäß WO 2004/058911), der elektronenleitenden Verbindungen, insbesondere Ketone, Phosphinoxide, Sulfoxide etc. (zum Beispiel nach WO 2005/084081 und WO 2005/084082), die Atropisomere (zum Beispiel nach WO 2006/048268), die Boronsäurederivate (zum Beispiel nach WO 2006/117052) oder die Benzanthracene (zum Beispiel nach WO 2008/145239). Besonders bevorzugte Matrixmaterialien sind ausgewählt aus den Klassen der Oligoarylene mit Naphthalin, Anthracen, Benzanthracen und/oder Pyren oder Atropisomeren dieser Verbindungen, den Oligoarylenvinylenen, den Ketonen, den Phosphinoxiden und den Sulfoxiden. Ganz besonders bevorzugte Matrixmaterialien sind ausge- wählt aus den Klassen der Oligoarylene, die Anthracen, Benzanthracen, Benzophenanthren und/oder Pyren oder Atropisomere dieser Verbin- dungen umfassen. Unter einem Oligoarylen ist im Rahmen der vorliegen- den Erfindung eine Verbindung zu verstehen, in der mindestens drei Aryl- oder Arylengruppen miteinander verbunden sind. Weiter bevorzugt sind die in WO 2006/097208, WO 2006/131192, WO 2007/065550, WO 2007/110129, WO 2007/065678, WO 2008/145239, WO 2009/100925, WO 2011/054442 und EP 1553154 offenbarten Anthracenderivate, die in EP 1749809, EP 1905754 und US 2012/0187826 offenbarten Pyrenver- bindungen, die in WO 2015/158409 offenbarten Benzanthracenyl- anthracenverbindungen, die in WO 2017/025165 offenbarten Indeno- benzofurane und die in WO 2017/036573 offenbarten Phenanthryl- anthracene. Bevorzugte Matrixmaterialien für phosphoreszierende Verbindungen sind, ebenso wie Verbindungen gemäß Formel (1), aromatische Ketone, aromatische Phosphinoxide oder aromatische Sulfoxide oder Sulfone, z. B. gemäß WO 2004/013080, WO 2004/093207, WO 2006/005627 oder WO 2010/006680, Triarylamine, Carbazolderivate, z. B. CBP (N,N-Bis- carbazolylbiphenyl) oder WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527, WO 2008/086851 oder WO 2013/041176, Indolocarbazolderivate, z. B. gemäß WO 2007/063754 oder WO 2008/056746, Indenocarbazolderivate, z. B. gemäß WO 2010/136109, WO 2011/000455, WO 2013/041176 oder WO 2013/056776, Azacarbazol- derivate, z. B. gemäß EP 1617710, EP 1617711, EP 1731584, JP 2005/347160, bipolare Matrixmaterialien, z. B. gemäß WO 2007/137725, Silane, z. B. gemäß WO 2005/111172, Azaborole oder Boronester, z. B. gemäß WO 2006/117052, Triazinderivate, z. B. gemäß WO 2007/063754, WO 2008/056746, WO 2010/015306, WO 2011/057706, WO 2011/060859 oder WO 2011/060877, Zinkkomplexe, z. B. gemäß EP 652273 oder WO 2009/062578, Diazasilol- bzw. Tetraazasilol-Derivate, z. B. gemäß WO 2010/054729, Diazaphosphol-Derivate, z. B. gemäß WO 2010/054730, verbrückte Carbazol-Derivate, z. B. gemäß WO 2011/042107, WO 2011/060867, WO 2011/088877 und WO 2012/143080, Triphenylen- derivate, z. B. gemäß WO 2012/048781, Lactame, z. B. gemäß WO 2011/116865 oder WO 2011/137951, oder Dibenzofuranderivate, z. B. gemäß WO 2015/169412, WO 2016/015810, WO 2016/023608, WO 2017/148564 oder WO 2017/148565. Ebenso kann ein weiterer phos- phoreszierender Emitter, welcher kürzerwellig als der eigentliche Emitter emittiert, als Co-Host in der Mischung vorhanden sein oder eine Verbin- dung, die nicht oder nicht in wesentlichem Umfang am Ladungstransport teilnimmt, wie beispielsweise in WO 2010/108579 beschrieben. Da es sich bei den erfindungsgemäßen Verbindungen um elektronentransportierende Verbindungen handelt, werden diese bevorzugt mit einem lochtranspor- tierenden Matrixmaterial kombiniert. Besonders geeignete lochtransportierende Matrixmaterialien, die vorteilhaft mit Verbindungen der Formel (1), wie zuvor beschrieben oder bevorzugt beschrieben, in einem Mixed-Matrix-System kombiniert werden, können aus den Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH- 4), (HH-5) oder (HH-6) ausgewählt werden, wie nachfolgend beschrieben. Ein weiterer Gegenstand der Erfindung ist demzufolge eine organische elektronische Vorrichtung umfassend eine Anode, eine Kathode und mindestens eine organische Schicht, enthaltend mindestens eine licht- emittierende Schicht, wobei die mindestens eine lichtemittierende Schicht mindestens eine Verbindung der Formel (1) als Matrixmaterial 1, wie zuvor beschrieben oder als bevorzugt beschrieben, und mindestens eine Verbindung der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH- 6) als Matrixmaterial 2 enthält, , - 70 - wobei für die verwendeten Symbole und Indizes gilt: A1 ist C(R7)2, NR7, O oder S; L ist eine Bindung, O, S, C(R7)2 oder NR7; A ist bei jedem Auftreten unabhängig voneinander eine Gruppe der Formel (HH-4-1) oder (HH-4-2), X2 ist bei jedem Auftreten gleich oder verschieden CH, CR6 oder N, wobei maximal 2 Symbole X2 N bedeuten können; * kennzeichnet die Bindungsstelle an die Formel (HH-4); U1, U2 sind bei Auftreten eine Bindung, O, S, C(R7)2 oder NR7; R6 ist bei jedem Auftreten gleich oder verschieden D, F, CN, eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen, wobei die Alkyl- , Alkenyl- oder Alkinylgruppe jeweils mit einem oder mehreren Resten R7 substituiert sein kann und wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch Si(R7)2, C=O, NR7, O, S oder CONR7 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 Ringatomen, das jeweils durch einen oder mehrere Reste R7 substituiert sein kann; dabei können zwei Reste R6 auch miteinander ein aromatisches, heteroaromatisches, aliphatisches oder heteroaliphatisches Ring- system bilden; Ar5 steht gleich oder verschieden bei jedem Auftreten unabhängig für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 Ringatomen, welches mit einem oder mehreren Resten R7 substi- tuiert sein kann; R7 ist bei jedem Auftreten gleich oder verschieden D, F, Cl, Br, I, N(R8)2, CN, NO2, OR8, SR8, Si(R8)3, B(OR8)2, C(=O)R8, P(=O)(R8)2, S(=O)R8, S(=O)2R8, OSO2R8, eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C-Atomen, wobei die Alkyl-, Alkenyl- oder Alkinylgruppe jeweils mit einem oder mehreren Resten R8 substituiert sein kann, wobei eine oder mehrere nicht benachbarte CH2-Gruppen durch Si(R8)2, C=O, NR8, O, S oder CONR8 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 40 Ringatomen, das jeweils durch einen oder mehrere Reste R8 substituiert sein kann; dabei können zwei oder mehrere Reste R7 miteinander ein aromatisches, heteroaromatisches, aliphatisches oder heteroaliphatisches Ringsystem bilden, vorzugsweise bilden die Reste R7 kein solches Ringsystem; R8 ist bei jedem Auftreten gleich oder verschieden H, D, F oder ein aliphatischer, aromatischer oder heteroaromatischer organischer Rest, insbesondere ein Kohlenwasserstoffrest, mit 1 bis 20 C- Atomen, in dem auch ein oder mehrere H-Atome durch F ersetzt sein können; c, c1, c2 bedeuten jeweils unabhängig voneinander bei jedem Auftreten 0 oder 1, wobei die Summe der Indizes bei jedem Auftreten c+c1+c2 = 1 bedeutet; d, d1, d2 bedeuten jeweils unabhängig voneinander bei jedem Auftreten 0 oder 1, wobei die Summe der Indizes bei jedem Auftreten d+d1+d2 = 1 bedeutet; q, q1, q2 bedeuten jeweils unabhängig bei jedem Auftreten 0, 1, 2, 3 oder 4; s ist bei jedem Auftreten gleich oder verschieden 0, 1, 2, 3 oder 4; t ist bei jedem Auftreten gleich oder verschieden 0, 1, 2, oder 3; u ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2; u1, u2 bedeuten jeweils unabhängig voneinander bei jedem Auftreten 0 oder 1, wobei die Summe u1 + u2 = 1 bedeutet; und v ist 0, 1, 2 oder 3. In Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-5) oder (HH-6) ist s bevorzugt 0 oder 1, wenn der Rest R6 von D verschieden ist, oder besonders bevorzugt 0. In Verbindungen der Formeln (HH-1), (HH-2) oder (HH-3) ist t bevorzugt 0 oder 1, wenn der Rest R6 von D verschieden ist, oder besonders bevorzugt 0. In Verbindungen der Formeln (HH-1), (HH-2), (HH-3) oder (HH-5) ist u bevorzugt 0 oder 1, wenn der Rest R6 von D verschieden ist, oder besonders bevorzugt 0. Die Summe der Indices s, t und u in Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-5) oder (HH-6) beträgt vorzugsweise höchstens 6, insbesondere bevorzugt höchstens 4 und besonders bevorzugt höchstens 2. Dies gilt bevorzugt, wenn R6 verschieden von D ist. In Verbindungen der Formel (HH-4) bedeuten c, c1, c2 jeweils unabhängig voneinander bei jedem Auftreten 0 oder 1, wobei die Summe der Indizes bei jedem Auftreten c+c1+c21 bedeutet. Bevorzugt hat c2 die Bedeutung 1. In Verbindungen der Formel (HH-4) ist L bevorzugt eine Einfachbindung oder C(R7)2, wobei R7 eine zuvor genannte Bedeutung hat, besonders bevorzugt ist L eine Einfachbindung. In Formel (HH-4-1) ist v bevorzugt 0 oder 1, wenn der Rest R6 von D verschieden ist. In Formel (HH-4-2) sind U1 oder U2 bei Auftreten bevorzugt eine Ein- fachbindung oder C(R7)2, wobei R7 eine zuvor genannte Bedeutung hat, besonders bevorzugt sind U1 oder U2 bei Auftreten eine Einfachbindung. In Formel (HH-4-2) sind q, q1, q2 bevorzugt 0 oder 1, wenn der Rest R6 von D verschieden ist. In einer bevorzugten Ausführungsform der Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH-6), die erfindungsgemäß mit Verbindungen der Formel (1) oder bevorzugten Verbindungen der Formel (1) kombiniert werden können, wie zuvor beschrieben, ist R6 gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus D, F, CN, eine geradkettige Alkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkylgruppe mit 3 bis 20 C- Atomen, wobei die Alkylgruppe jeweils mit einem oder mehreren Resten R7 substituiert sein kann, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 60 Ringatomen, bevorzugt mit 5 bis 40 Ringatomen, das jeweils durch einen oder mehrere Reste R7 substituiert sein kann. In einer bevorzugten Ausführungsform der Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH-6), die erfindungsgemäß mit Verbindungen der Formel (1) oder bevorzugten Verbindungen der Formel (1) kombiniert werden können, wie zuvor beschrieben, ist R6 gleich oder verschieden bei jedem Auftreten ausgewählt aus der Gruppe bestehend aus D oder einem aromatischen oder heteroaromatischen Ringsystem mit 6 bis 30 Ringatomen, welches mit einem oder mehreren Resten R7 substituiert sein kann. Bevorzugt wird Ar5 in Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-5) oder (HH-6) ausgewählt aus Phenyl, Biphenyl, insbesondere ortho-, meta- oder para-Biphenyl, Terphenyl, insbesondere ortho-, meta-, para- oder verzweigtem Terphenyl, Quaterphenyl, insbesondere ortho-, meta-, para- oder verzweigtem Quaterphenyl, Fluorenyl, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Spirobifluorenyl, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Naphthyl, insbeson- dere 1- oder 2-verknüpftes Naphthyl, oder Reste abgeleitet von Indol, Benzofuran, Benzothiophen, Carbazol, welches über die 1-, 2-, 3- oder 4- Position verknüpft sein kann, Dibenzofuran, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Dibenzothiophen, welches über die 1-, 2-, 3- oder 4-Position verknüpft sein kann, Indenocarbazol, Indolo- carbazol, Pyridin, Pyrimidin, Pyrazin, Pyridazin, Triazin, Chinolin, Isochinolin, Chinazolin, Chinoxalin, Phenanthren oder Triphenylen, welche jeweils mit einem oder mehreren Resten R7 substituiert sein können. Bevorzugt ist Ar5 nicht substituiert. Wenn A1 in Formel (HH-2) oder (HH-3) oder (HH-6) für NR7 steht, steht der Substituent R7, der an das Stickstoffatom gebunden ist, bevorzugt für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ringatomen, welches auch durch einen oder mehrere Reste R8 substituiert sein kann. In einer besonders bevorzugten Ausführungs- form steht dieser Substituent R7 gleich oder verschieden bei jedem Auf- treten für ein aromatisches oder heteroaromatisches Ringsystem mit 6 bis 24 aromatischen Ringatomen, insbesondere mit 6 bis 18 aromatischen Ringatomen. Bevorzugte Ausführungsformen für R7 sind Phenyl, Biphenyl, Terphenyl und Quaterphenyl, die bevorzugt unsubstituiert sind, sowie Reste abgeleitet von Triazin, Pyrimidin und Chinazolin, die durch einen oder mehrere Reste R8 substituiert sein können. Wenn A1 in Formel (HH-2) oder (HH-3) oder (HH-6) für C(R7)2 steht, stehen die Substituenten R7, die an dieses Kohlenstoffatom gebunden sind, bevorzugt gleich oder verschieden bei jedem Auftreten für eine lineare Alkylgruppe mit 1 bis 10 C-Atomen oder für eine verzweigte oder cyclische Alkylgruppe mit 3 bis 10 C-Atomen oder für ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 24 aromatischen Ring- atomen, welches auch durch einen oder mehrere Reste R8 substituiert sein kann. Ganz besonders bevorzugt steht R7 für eine Methylgruppe oder für eine Phenylgruppe. Dabei können die Reste R7 auch miteinander ein Ringsystem bilden, was zu einem Spirosystem führt. In einer bevorzugten Ausführungsform der Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) und (HH-6) sind diese Verbin- dungen teilweise oder vollständig deuteriert, besonders bevorzugt voll- ständig deuteriert. Die Herstellung der Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) und (HH-6) sind generell bekannt und einige der Verbin- dungen sind kommerziell erhältlich. Verbindungen der Formel (HH-4) sind beispielsweise in WO2021/180614, Seiten 110 bis 119, insbesondere als Beispiele auf den Seiten 120 bis 127 offenbart. Deren Herstellung ist in WO2021/180614 A1 auf Seite 128 sowie in den Synthesebeispielen auf Seite 214 bis 218 offenbart. Die Herstellung der Triarylamine der Formel (HH-6) ist dem Fachmann bekannt und einige der Verbindungen sind kommerziell erhältlich. Handelt es sich bei dem mindestens einen weiteren Matrixmaterial um eine deuterierte Verbindung, so ist es möglich, dass dieses mindestens eine Matrixmaterial eine Mischung an deuterierten Verbindungen gleicher chemischer Grundstruktur ist, die sich lediglich durch den Deuterierungs- grad unterscheiden. In einer bevorzugten Ausführungsform des mindestens einen weiteren Matrixmaterials ist dieses ein Gemisch aus deuterierten Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH-6), wie zuvor beschrieben, wobei der Deuterierungsgrad dieser Verbindungen mindestens 50% bis 90% beträgt, bevorzugt 70% bis 100 % beträgt. In einer bevorzugten Ausführungsform des mindestens einen weiteren Matrixmaterials ist dieses ein Gemisch aus deuterierten Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) und/oder (HH-6), wie zuvor beschrieben, wobei der Deuterierungsgrad dieser Verbindungen mindestens 50% bis 90% beträgt, bevorzugt 70% bis 100 % beträgt. Entsprechende Deuterierungsmethoden sind dem Fachmann bekannt und beispielsweise in KR2016041014 A, WO2017/122988 A1, KR2020052820 A, KR101978651 B1 und WO2018/110887 A1 oder in Bulletin of the Chemical Society of Japan, 2021, 94(2), 600-605 oder Asian Journal of Organic Chemistry, 2017, 6(8), 1063-1071 beschrieben. Beispiele für geeignete weitere Matrixmaterialien für eine Kombination mit Verbindungen der Formel (1), wie zuvor beschrieben oder bevorzugt beschrieben, sind die Verbindungen, beschrieben in WO2019/229011 A1, Tabelle 3, Seiten 137 bis 203, die auch teilweise oder vollständig deuteriert sein können. Beispiele für geeignete weitere Matrixmaterialien für eine Kombination mit Verbindungen der Formel (1) oder bevorzugten Verbindungen der Formel (1), wie zuvor beschrieben oder bevorzugt beschrieben, sind die Verbindungen, beschrieben in WO2021/180625 A1, Tabelle 3, Seiten 131 bis 127 und in Tabelle 4, Seiten 137 bis 139, die auch teilweise oder vollständig deuteriert sein können. Beispiele für geeignete weitere Matrixmaterialien für eine Kombination mit Verbindungen der Formel (1) oder bevorzugten Verbindungen der Formel (1), wie zuvor beschrieben oder bevorzugt beschrieben, sind die Verbindungen, beschrieben in KR20230034896 A, auf den Seiten 42 bis 47, Verbindungen [2-1] bis [2-110], oder auf den Seiten 49 bis 51, Verbindungen [3-1] bis [3-26]. Weitere Beispiele für geeignete Hostmaterialien der Formeln (HH-1), (HH- 2), (HH-3), (HH-4), (HH-5) und (HH-6) für eine Kombination mit Verbin- dungen der Formel (1) oder bevorzugten Ausführungsformen sind die in den nachstehenden Tabellen 1 und 2 genannten Strukturen. Tabelle 1: The hole transport materials used can be used in combination with a hexaazatriphenylene derivative, as described in US 2007/0092755. The hexaazatriphenylene derivative is particularly preferably used in a separate layer. In a further embodiment of the present invention, the compound of formula (1) is used in an emitting layer as a matrix material in combination with one or more emitting compounds, preferably phosphorescent compounds. The proportion of matrix material in the emitting layer in this case is between 50.0 and 99.9 vol. %, preferably between 80.0 and 99.5 vol. %, particularly preferably between 92.0 and 99.5 vol. %, for fluorescent emitting layers and between 85.0 and 97.0 vol. % for phosphorescent emitting layers. Accordingly, the proportion of the emitting compound is between 0.1 and 50.0 vol.%, preferably between 0.5 and 20.0 vol.%, particularly preferably between 0.5 and 8.0 vol.% for fluorescent emitting Layers and between 3.0 and 15.0 vol.% for phosphorescent emitting layers. An emitting layer of an organic electroluminescent device can also comprise systems that contain a large number of matrix materials (mixed matrix systems) and/or a large number of emitting compounds. In this case too, the emitting compounds are generally those that have the smaller proportion in the system and the matrix materials are those that have the larger proportion in the system. In individual cases, however, the proportion of an individual matrix material in the system can be lower than the proportion of an individual emitting compound. Preferably, the compounds of formula (1) are used as a component of mixed matrix systems. The mixed matrix systems preferably consist of two or three different matrix materials, particularly preferably of two different matrix materials. In this case, one of the two materials is preferably a material with hole-transporting properties and the other material is a material with electron-transporting properties. The compound of formula (1) is preferably the matrix material with electron-transporting properties. However, the desired electron-transporting and hole-transporting properties of the mixed matrix components can also be predominantly or completely combined in a single mixed matrix component, with the other mixed matrix component(s) fulfilling other functions. The two different matrix materials can be present in a ratio of 1:50 to 1:1, preferably 1:20 to 1:1, even more preferably 1:10 to 1:1 and most preferably 1:4 to 1:1. Mixed matrix systems are preferably used in phosphorescent organic electroluminescent devices. A source for more detailed information on mixed matrix systems is the application WO 2010/108579. The mixed matrix systems can contain one or more emitting compounds, preferably one or more phosphorescent compounds. In general, mixed matrix systems are preferably used in phosphorescent organic electroluminescent devices. Particularly suitable matrix materials which can be used in combination with the compounds according to the invention as matrix components of a mixed matrix system are selected from the preferred matrix materials for phosphorescent compounds or the preferred matrix materials for fluorescent compounds mentioned below, depending on which type of emitting compound is used in the mixed matrix system. Preferred phosphorescent compounds for use in mixed matrix systems are the same as those described above as generally preferred phosphorescent emitter materials. Examples of phosphorescent compounds are listed below. Preferred fluorescent emitting compounds are selected from the class of arylamines. In the context of the present invention, an arylamine or an aromatic amine is understood to mean a compound which contains three substituted or unsubstituted aromatic or heteroaromatic ring systems which are bonded directly to the nitrogen. Preferably, at least one of these aromatic or heteroaromatic ring systems is a condensed ring system, particularly preferably with at least 14 aromatic ring atoms. Preferred examples of these are aromatic anthraceneamines, aromatic anthracenediamines, aromatic pyrenamines, aromatic pyrenediamines, aromatic chrysenamines or aromatic chrysenediamines. An aromatic anthraceneamine is understood to mean a compound in which a diarylamino group is bonded directly to an anthracene group, preferably in position 9. An aromatic anthracenediamine is understood to mean a compound in which two diarylamino groups are directly bonded to an anthracene group, preferably in positions 9, 10. Aromatic pyrenamines, pyrenediamines, chrysenamines and chrysenediamines are defined analogously, in which the diarylamino groups are preferably bonded to the pyrene in the 1-position or 1,6-position. Further preferred emitting compounds are indenofluorenamines or fluorenediamines, for example according to WO 2006/108497 or WO 2006/122630, benzoindenofluorenamines or fluorenediamines, for example according to WO 2008/006449, and dibenzoindenofluorenamines or diamines, for example according to WO 2007/140847, and the indenofluorene derivatives with condensed aryl groups disclosed in WO 2010/012328. Likewise preferred are the pyrenearylamines disclosed in WO 2012/048780 and in WO 2013/185871. Also preferred are the benzoindenofluorenamines disclosed in WO 2014/037077, the benzofluorenamines disclosed in WO 2014/106522, the extended benzoindenofluorenes disclosed in WO 2014/111269 and in WO 2017/036574, the phenoxazines disclosed in WO 2017/028940 and in WO 2017/028941 and the fluorine derivatives bound to furan units or to thiophene units disclosed in WO 2016/150544. Furthermore, boron compounds according to WO2020208051, WO2015102118, WO2016152418, WO2018095397, WO2019004248, WO2019132040, US20200161552, WO2021089450 are used. Useful matrix materials, preferably for fluorescent compounds, include materials from various substance classes. Preferred matrix materials are selected from the classes of oligoaryls (e.g. 2,2',7,7'-tetraphenylspirobifluorene according to EP 676461 or dinaphthylanthracene), in particular oligoaryls with fused aromatic groups, oligoarylenevinylenes (e.g. DPVBi or spiro-DPVBi according to EP 676461), polypodal metal complexes (e.g. according to WO 2004/081017), hole-conducting compounds (e.g. according to WO 2004/058911), electron-conducting compounds, in particular ketones, phosphine oxides, sulfoxides etc. (for example according to WO 2005/084081 and WO 2005/084082), atropisomers (for example according to WO 2006/048268), boronic acid derivatives (for example according to WO 2006/117052) or the benzanthracenes (for example according to WO 2008/145239). Particularly preferred matrix materials are selected from the classes of oligoarylenes with naphthalene, anthracene, benzanthracene and/or pyrene or atropisomers of these compounds, the oligoarylenevinylenes, the ketones, the phosphine oxides and the sulfoxides. Very particularly preferred matrix materials are selected from the classes of oligoarylenes which include anthracene, benzanthracene, benzophenanthrene and/or pyrene or atropisomers of these compounds. In the context of the present invention, an oligoarylene is understood to mean a compound in which at least three aryl or arylene groups are connected to one another. Further preferred are the anthracene derivatives disclosed in WO 2006/097208, WO 2006/131192, WO 2007/065550, WO 2007/110129, WO 2007/065678, WO 2008/145239, WO 2009/100925, WO 2011/054442 and EP 1553154, the pyrene compounds disclosed in EP 1749809, EP 1905754 and US 2012/0187826, the benzanthracenyl-anthracene compounds disclosed in WO 2015/158409, the indenobenzofurans disclosed in WO 2017/025165 and the pyrene compounds disclosed in WO 2017/036573 disclosed phenanthryl-anthracenes. Preferred matrix materials for phosphorescent compounds are, as well as compounds according to formula (1), aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, e.g. according to WO 2004/013080, WO 2004/093207, WO 2006/005627 or WO 2010/006680, triarylamines, carbazole derivatives, e.g. CBP (N,N-biscarbazolylbiphenyl) or WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527, WO 2008/086851 or WO 2013/041176, indolocarbazole derivatives, e.g. B. according to WO 2007/063754 or WO 2008/056746, indenocarbazole derivatives, e.g. according to WO 2010/136109, WO 2011/000455, WO 2013/041176 or WO 2013/056776, azacarbazole derivatives, e.g. according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160, bipolar matrix materials, e.g. according to WO 2007/137725, silanes, e.g. according to WO 2005/111172, azaboroles or boronic esters, e.g. according to WO 2006/117052, triazine derivatives, e.g. B. according to WO 2007/063754, WO 2008/056746, WO 2010/015306, WO 2011/057706, WO 2011/060859 or WO 2011/060877, zinc complexes, e.g. according to EP 652273 or WO 2009/062578, diazasilole or tetraazasilole derivatives, e.g. according to WO 2010/054729, diazaphosphole derivatives, e.g. according to WO 2010/054730, bridged carbazole derivatives, e.g. B. according to WO 2011/042107, WO 2011/060867, WO 2011/088877 and WO 2012/143080, triphenylene derivatives, e.g. according to WO 2012/048781, lactams, e.g. according to WO 2011/116865 or WO 2011/137951, or dibenzofuran derivatives, e.g. according to WO 2015/169412, WO 2016/015810, WO 2016/023608, WO 2017/148564 or WO 2017/148565. Likewise, a further phosphorescent emitter which emits at a shorter wavelength than the actual emitter can be present in the mixture as a co-host or a compound which does not participate in charge transport or does not participate to a significant extent, as described for example in WO 2010/108579. Since the compounds according to the invention are electron-transporting compounds, they are preferably combined with a hole-transporting matrix material. Particularly suitable hole-transporting matrix materials which are advantageously combined with compounds of the formula (1), as described above or preferably described, in a mixed matrix system, can be selected from the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), as described below. A further subject matter of the invention is therefore an organic electronic device comprising an anode, a cathode and at least one organic layer containing at least one light-emitting layer, wherein the at least one light-emitting layer contains at least one compound of the formula (1) as matrix material 1, as described above or as preferred, and at least one compound of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6) as matrix material 2, , - 70 - where the symbols and indices used are: A 1 is C(R 7 ) 2 , NR 7 , O or S; L is a bond, O, S, C(R 7 ) 2 or NR 7 ; A is at each occurrence independently a group of the formula (HH-4-1) or (HH-4-2), X2 is, on each occurrence, the same or different, CH, CR 6 or N, where a maximum of 2 symbols X2 can be N; * indicates the bonding site to the formula (HH-4); U 1 , U 2 are, on each occurrence, a bond, O, S, C(R 7 ) 2 or NR 7 ; R 6 is, identically or differently on each occurrence, D, F, CN, a straight-chain alkyl group having 1 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl, alkenyl or alkynyl group may in each case be substituted by one or more radicals R 7 and where one or more non-adjacent CH 2 groups may be replaced by Si(R 7 ) 2 , C=O, NR 7 , O, S or CONR 7 , or an aromatic or heteroaromatic ring system having 5 to 60 ring atoms, which may in each case be substituted by one or more radicals R 7 ; two radicals R 6 can also form an aromatic, heteroaromatic, aliphatic or heteroaliphatic ring system with one another; Ar5, identical or different at each occurrence, independently represents an aromatic or heteroaromatic ring system having 5 to 40 ring atoms, which may be substituted by one or more radicals R7 ; R 7 is, identically or differently on each occurrence, D, F, Cl, Br, I, N(R 8 ) 2 , CN, NO2, OR 8 , SR 8 , Si(R 8 ) 3 , B(OR 8 ) 2 , C(=O)R 8 , P(=O)(R 8 ) 2 , S(=O)R 8 , S(=O) 2 R 8 , OSO2R 8 , a straight-chain alkyl group having 1 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl, alkenyl or alkynyl group may each be substituted by one or more radicals R 8 , where one or more non-adjacent CH2 groups are replaced by Si(R 8 ) 2 , C=O, NR 8 , O, S or CONR 8 , or an aromatic or heteroaromatic ring system having 5 to 40 ring atoms, each of which may be substituted by one or more radicals R 8 ; two or more radicals R 7 can form an aromatic, heteroaromatic, aliphatic or heteroaliphatic ring system with one another, preferably the radicals R 7 do not form such a ring system; R 8 is, identically or differently on each occurrence, H, D, F or an aliphatic, aromatic or heteroaromatic organic radical, in particular a hydrocarbon radical, having 1 to 20 C atoms, in which one or more H atoms can also be replaced by F; c, c1, c2 each independently on each occurrence is 0 or 1, where the sum of the indices on each occurrence is c+c1+c2 = 1; d, d1, d2 each independently on each occurrence is 0 or 1, where the sum of the indices on each occurrence is d+d1+d2 = 1; q, q1, q2 each independently on each occurrence is 0, 1, 2, 3 or 4; s is, identically or differently on each occurrence, 0, 1, 2, 3 or 4; t is, identically or differently on each occurrence, 0, 1, 2, or 3; u is the same or different at each occurrence and is 0, 1 or 2; u1, u2 each independently mean 0 or 1 at each occurrence, where the sum u1 + u2 = 1; and v is 0, 1, 2 or 3. In compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-5) or (HH-6), s is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0. In compounds of the formulas (HH-1), (HH-2) or (HH-3), t is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0. In compounds of the formulas (HH-1), (HH-2), (HH-3) or (HH-5), u is preferably 0 or 1 if the radical R 6 is different from D, or particularly preferably 0. The sum of the indices s, t and u in compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-5) or (HH-6) is preferably at most 6, particularly preferably at most 4 and particularly preferably at most 2. This preferably applies if R 6 is different from D. In compounds of the formula (HH-4), c, c1, c2 each independently represent 0 or 1 at each occurrence, where the sum of the indices on each occurrence means c+c1+c21. Preferably c2 has the meaning 1. In compounds of the formula (HH-4), L is preferably a single bond or C(R 7 ) 2 , where R 7 has a meaning given above, particularly preferably L is a single bond. In formula (HH-4-1), v is preferably 0 or 1 if the radical R 6 is different from D. In formula (HH-4-2), U 1 or U 2 on each occurrence are preferably a single bond or C(R 7 ) 2 , where R 7 has a meaning given above, particularly preferably U 1 or U 2 on each occurrence are a single bond. In formula (HH-4-2), q, q1, q2 are preferably 0 or 1 if the radical R 6 is different from D. In a preferred embodiment of the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), which can be combined according to the invention with compounds of the formula (1) or preferred compounds of the formula (1), as described above, R 6 is the same or different on each occurrence and is selected from the group consisting of D, F, CN, a straight-chain alkyl group having 1 to 20 C atoms or a branched or cyclic alkyl group having 3 to 20 C atoms, where the alkyl group can be substituted in each case by one or more radicals R 7 , or an aromatic or heteroaromatic ring system having 5 to 60 ring atoms, preferably having 5 to 40 ring atoms, which can be substituted in each case by one or more radicals R 7 . In a preferred embodiment of the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), which can be combined according to the invention with compounds of the formula (1) or preferred compounds of the formula (1), as described above, R 6 is the same or different on each occurrence and is selected from the group consisting of D or an aromatic or heteroaromatic ring system having 6 to 30 ring atoms, which may be substituted by one or more radicals R 7. Preferably, Ar5 in compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-5) or (HH-6) is selected from phenyl, biphenyl, in particular ortho-, meta- or para-biphenyl, terphenyl, in particular ortho-, meta-, para- or branched terphenyl, quaterphenyl, in particular ortho-, meta-, para- or branched quaterphenyl, fluorenyl, which can be linked via the 1-, 2-, 3- or 4-position, spirobifluorenyl, which can be linked via the 1-, 2-, 3- or 4-position, naphthyl, in particular 1- or 2-linked naphthyl, or residues derived from indole, benzofuran, benzothiophene, carbazole, which can be linked via the 1-, 2-, 3- or 4-position, dibenzofuran, which can be linked via the 1-, 2-, 3- or 4-position, dibenzothiophene, which can be linked via the 1-, 2-, 3- or 4-position, indenocarbazole, Indolocarbazole, pyridine, pyrimidine, pyrazine, pyridazine, triazine, quinoline, isoquinoline, quinazoline, quinoxaline, phenanthrene or triphenylene, each of which may be substituted by one or more radicals R 7 . Ar5 is preferably not substituted. If A 1 in formula (HH-2) or (HH-3) or (HH-6) is NR 7 , the substituent R 7 which is bonded to the nitrogen atom preferably represents an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may also be substituted by one or more radicals R 8 . In a particularly preferred embodiment, this substituent R 7 is the same or different on each occurrence and represents an aromatic or heteroaromatic ring system having 6 to 24 aromatic ring atoms, in particular having 6 to 18 aromatic ring atoms. Preferred embodiments for R 7 are phenyl, biphenyl, terphenyl and quaterphenyl, which are preferably unsubstituted, and radicals derived from triazine, pyrimidine and quinazoline, which can be substituted by one or more radicals R 8 . If A 1 in formula (HH-2) or (HH-3) or (HH-6) is C(R 7 ) 2 , the substituents R 7 which are bonded to this carbon atom are preferably identical or different on each occurrence and represent a linear alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms or an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which can also be substituted by one or more radicals R 8 . R 7 is very particularly preferably a methyl group or for a phenyl group. The radicals R 7 can also form a ring system with one another, which leads to a spiro system. In a preferred embodiment of the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), these compounds are partially or fully deuterated, particularly preferably fully deuterated. The preparation of the compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6) are generally known and some of the compounds are commercially available. Compounds of the formula (HH-4) are disclosed, for example, in WO2021/180614, pages 110 to 119, in particular as examples on pages 120 to 127. Their preparation is disclosed in WO2021/180614 A1 on page 128 and in the synthesis examples on pages 214 to 218. The preparation of the triarylamines of the formula (HH-6) is known to the person skilled in the art and some of the compounds are commercially available. If the at least one further matrix material is a deuterated compound, it is possible that this at least one matrix material is a mixture of deuterated compounds with the same basic chemical structure, which differ only in the degree of deuteration. In a preferred embodiment of the at least one further matrix material, this is a mixture of deuterated compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), as described above, the degree of deuteration of these compounds being at least 50% to 90%, preferably 70% to 100%. In a preferred embodiment of the at least one further matrix material, this is a mixture of deuterated compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and/or (HH-6), as described above, wherein the degree of deuteration of these compounds is at least 50% to 90%, preferably 70% to 100%. Corresponding deuteration methods are known to the person skilled in the art and are described, for example, in KR2016041014 A, WO2017/122988 A1, KR2020052820 A, KR101978651 B1 and WO2018/110887 A1 or in Bulletin of the Chemical Society of Japan, 2021, 94(2), 600-605 or Asian Journal of Organic Chemistry, 2017, 6(8), 1063-1071. Examples of suitable further matrix materials for a combination with compounds of the formula (1), as described above or preferably described, are the compounds described in WO2019/229011 A1, Table 3, pages 137 to 203, which can also be partially or completely deuterated. Examples of suitable further matrix materials for a combination with compounds of the formula (1) or preferred compounds of the formula (1), as previously described or preferably described, are the compounds described in WO2021/180625 A1, Table 3, pages 131 to 127 and in Table 4, pages 137 to 139, which may also be partially or fully deuterated. Examples of suitable further matrix materials for a combination with compounds of the formula (1) or preferred compounds of the formula (1), as previously described or preferably described, are the compounds described in KR20230034896 A, on pages 42 to 47, compounds [2-1] to [2-110], or on pages 49 to 51, compounds [3-1] to [3-26]. Further examples of suitable host materials of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6) for combination with compounds of the formula (1) or preferred embodiments are the structures listed in Tables 1 and 2 below. Table 1:
Besonders geeignete Verbindungen der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH-6), die erfindungsgemäß ausgewählt werden und bevorzugt in Kombination mit mindestens einer Verbindung der Formel (1) in der erfindungsgemäßen elektrolumineszierenden Vorrichtung verwendet werden, sind die Verbindungen der Tabelle 2. Particularly suitable compounds of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6), which are selected according to the invention and are preferably used in combination with at least one compound of the formula (1) in the electroluminescent device according to the invention, are the compounds of Table 2.
Tabelle 2: Table 2:
Die vorstehend genannten Hostmaterialien der Formel (1) sowie deren bevorzugt beschriebene Ausführungsformen können in der erfindungs- gemäßen Vorrichtung beliebig mit den zuvor genannten Matrixmaterialien/ Hostmaterialien, den Matrixmaterialien/Hostmaterialien der Formeln (HH- 1), (HH-2), (HH-3), (HH-4), (HH-5) oder (HH-6) sowie deren bevorzugt beschriebenen Ausführungsformen der Tabelle 1 oder den Verbindungen H1 bis H27 kombiniert werden. Die Konzentration des Hostmaterials der Formel (1), wie zuvor beschrieben oder bevorzugt beschrieben, in der erfindungsgemäßen Mischung oder in der lichtemittierenden Schicht der erfindungsgemäßen Vorrichtung liegt üblicherweise im Bereich von 5 Gew.-% bis 90 Gew.-%, bevorzugt im Bereich von 10 Gew.-% bis 85 Gew.-%, mehr bevorzugt im Bereich von 20 Gew.-% bis 85 Gew.-%, noch mehr bevorzugt im Bereich von 30 Gew.-% bis 80 Gew.-%, ganz besonders bevorzugt im Bereich von 20 Gew.-% bis 60 Gew.-% und am meisten bevorzugt im Bereich von 30 Gew.-% bis 50 Gew.-%, bezogen auf die gesamte Mischung oder bezogen auf die gesamte Zusammensetzung der lichtemittierenden Schicht. Die Konzentration der Summe aller Hostmaterialien der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) und (HH-6), wie zuvor beschrieben oder als bevorzugt beschrieben, in der erfindungsgemäßen Mischung oder in der lichtemittierenden Schicht der erfindungsgemäßen Vorrichtung liegt üblicherweise im Bereich von 10 Gew.-% bis 95 Gew.-%, bevorzugt im Bereich von 15 Gew.-% bis 90 Gew.-%, mehr bevorzugt im Bereich von 15 Gew.-% bis 80 Gew.-%, noch mehr bevorzugt im Bereich von 20 Gew.- % bis 70 Gew.-%, ganz besonders bevorzugt im Bereich von 40 Gew.-% bis 80 Gew.-% und am meisten bevorzugt im Bereich von 50 Gew.-% bis 70 Gew.-%, bezogen auf die gesamte Mischung oder bezogen auf die gesamte Zusammensetzung der lichtemittierenden Schicht. Die vorliegende Erfindung betrifft auch eine Mischung, die neben den vorstehend genannten Hostmaterialien der Formel (1), zukünftig Hostmaterial 1 genannt, und des Hostmaterials mindestens einer der Formeln (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) und (HH-6), zukünftig Hostmaterial 2 genannt, wie zuvor beschrieben oder bevorzugt beschrieben, mindestens noch einen phosphoreszierenden Emitter enthält. Die vorliegende Erfindung betrifft auch eine organische elektrolumines- zierende Vorrichtung, wie zuvor beschrieben oder bevorzugt beschrieben, wobei die lichtemittierende Schicht neben den vorstehend genannten Hostmaterialien der Formeln (1) und mindestens einer der Formeln (HH- 1), (HH-2), (HH-3), (HH-4), (HH-5) und (HH-6), wie zuvor beschrieben oder bevorzugt beschrieben, insbesondere den Materialkombinationen M1 bis M729, mindestens noch einen phosphoreszierenden Emitter enthält. Geeignete Ladungstransportmaterialien, wie sie in der Lochinjektions- oder Lochtransportschicht oder in der Elektronensperrschicht oder in der Elektronentransportschicht des erfindungsgemäßen elektronischen Bauelements verwendet werden können, sind neben den Verbindungen der Formel (1) zum Beispiel die in Y. Shirota et al., Chem. Rev.2007, 107(4), 953-1010 genannten, oder andere Materialien, wie sie in diesen Schichten gemäß dem Stand der Technik verwendet werden. Als Materialien für die Löchertransportschicht können alle Materialien verwendet werden, die nach dem Stand der Technik als Lochtransportmaterialien in der Lochtransportschicht eingesetzt werden. Es können aromatische Aminverbindungen eingesetzt werden. Weitere Verbindungen, die vorzugsweise in löchertransportierenden Schichten der erfindungsgemäßen OLEDs eingesetzt werden, sind insbesondere Indenofluorenamin-Derivate (z.B. nach WO 06/122630 oder WO 06/100896), die in EP 1661888 offenbarten Aminderivate, Hexaazatriphenylen-Derivate (z.B. nach WO 01/049806), Aminderivate mit anellierten Aromaten (zum Beispiel nach US 5,061,569), die in WO 95/09147 offenbarten Aminderivate, Monobenzoindenofluorenamine (zum Beispiel nach WO 08/006449), Dibenzoindenofluorenamine (zum Beispiel nach WO 07/140847), Spirobifluorenamine (zum Beispiel nach WO 2012/034627 oder WO 2013/120577), Fluorenamine (zum Beispiel nach WO 2014/015937, WO 2014/015938, WO 2014/015935 und WO 2015/082056), Spirodibenzopyranamine (zum Beispiel gemäß WO 2013/083216), Dihydroacridin-Derivate (zum Beispiel gemäß WO 2012/150001), Spirodibenzofurane und Spirodibenzothiophene (zum Beispiel nach WO 2015/022051, WO 2016/102048 und WO 2016/131521), Phenanthrendiarylamine (zum Beispiel nach WO 2015/131976), Spirotribenzotropolone (zum Beispiel gemäß WO 2016/087017), Spirobifluorene mit meta-Phenyldiamingruppen (zum Beispiel gemäß WO 2016/078738), Spirobisacridine (zum Beispiel gemäß WO 2015/158411), Xanthendiarylamine (zum Beispiel gemäß WO 2014/072017), und 9,10-Dihydroanthracen-Spiroverbindungen mit Diarylaminogruppen gemäß WO 2015/086108. Ganz besonders bevorzugt ist die Verwendung von durch Diarylaminogruppen in 4-Position substituierten Spirobifluorenen als löchertransportierende Verbindungen, insbesondere die Verwendung derjenigen Verbindungen, die in WO 2013/120577 beansprucht und offenbart sind, und die Verwendung von durch Diarylaminogruppen in 2- Position substituierten Spirobifluorenen als löchertransportierende Verbindungen, insbesondere die Verwendung derjenigen Verbindungen, die in WO 2012/034627 beansprucht und offenbart sind. Vorzugsweise umfasst die erfindungsgemäße OLED zwei oder mehr verschiedene elektronentransportierende Schichten. Die Verbindung der Formel (1) kann dabei in einer oder mehreren oder in allen elektronen- transportierenden Schichten verwendet werden. In einer bevorzugten Ausführungsform wird die Verbindung der Formel (1) in genau einer oder genau zwei elektronentransportierenden Schichten eingesetzt, und in den weiteren vorhandenen elektronentransportierenden Schichten werden andere Verbindungen eingesetzt. Weitere Verbindungen, die neben den Verbindungen der Formel (1) verwendet werden können, sind alle Materialien, die nach dem Stand der Technik als Elektronentransport- materialien in der Elektronentransportschicht eingesetzt werden. Besonders geeignet sind Aluminiumkomplexe, z.B. Alq3, Zirkonium- komplexe, z.B. Zrq4, Lithiumkomplexe, z.B. Liq, Benzimidazol-Derivate, Triazin-Derivate, Pyrimidin-Derivate, Pyridin-Derivate, Pyrazin-Derivate, Chinoxalin-Derivate, Chinolin-Derivate, Oxadiazol-Derivate, aromatische Ketone, Lactame, Borane, Diazaphosphol-Derivate und Phosphinoxid- Derivate. Weitere geeignete Materialien sind Derivate der vorgenannten Verbindungen, wie sie in JP 2000/053957, WO 2003/060956, WO 2004/028217, WO 2004/080975 und WO 2010/072300 offenbart sind. Bevorzugte Kathoden des elektronischen Bauelements sind Metalle mit geringer Austrittsarbeit, Metalllegierungen oder Mehrschichtstrukturen aus verschiedenen Metallen, z. B. Erdalkalimetallen, Alkalimetallen, Haupt- gruppenmetallen oder Lanthanoiden (z. B. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Zusätzlich geeignet sind Legierungen aus einem Alkali- oder Erd- alkalimetall und Silber, z. B. eine Legierung aus Magnesium und Silber. Bei Mehrschichtstrukturen können neben den genannten Metallen auch weitere Metalle mit einer relativ hohen Austrittsarbeit verwendet werden, z. B. Ag oder Al, wobei in der Regel Kombinationen der Metalle wie z. B. Ca/Ag, Mg/Ag oder Ba/Ag eingesetzt werden. Es kann auch vorteilhaft sein, eine dünne Zwischenschicht aus einem Material mit einer hohen Dielektrizitätskonstante zwischen einer metallischen Kathode und dem organischen Halbleiter einzuführen. Beispiele für geeignete Materialien sind Alkali- oder Erdalkalimetallfluoride, aber auch die entsprechenden Oxide oder Carbonate (z. B. LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3 usw.). Es ist auch möglich, Lithiumchinolinat (LiQ) zu diesem Zweck zu verwenden. Die Schichtdicke dieser Schicht liegt vorzugsweise zwischen 0,5 und 5 nm. Bevorzugte Anoden sind Materialien mit einer hohen Austrittsarbeit. Vorzugsweise hat die Anode eine Austrittsarbeit von mehr als 4,5 eV gegen Vakuum. Dazu eignen sich erstens Metalle mit hohem Redox- potential, z. B. Ag, Pt oder Au. Zum anderen können auch Metall/Metall- oxid-Elektroden (z. B. Al/Ni/NiOx, Al/PtOx) bevorzugt werden. Für einige Anwendungen muss mindestens eine der Elektroden transparent oder teiltransparent sein, um die Bestrahlung des organischen Materials (organische Solarzelle) oder die Emission von Licht (OLED, O-Laser) zu ermöglichen. Bevorzugte Anodenmaterialien sind hier leitfähige Metall- mischoxide. Besonders bevorzugt werden Indiumzinnoxid (ITO) oder Indiumzinkoxid (IZO). Weiter bevorzugt werden leitfähig dotierte organische Materialien, insbesondere leitfähig dotierte Polymere. Darüber hinaus kann die Anode auch aus zwei oder mehr Schichten bestehen, zum Beispiel aus einer inneren Schicht aus ITO und einer äußeren Schicht aus einem Metalloxid, vorzugsweise Wolframoxid, Molybdänoxid oder Vanadiumoxid. Die Vorrichtung wird entsprechend (je nach Anwendung) strukturiert, kontaktiert und abschließend versiegelt, um schädliche Einflüsse durch Wasser und Luft auszuschließen. In den weiteren Schichten der erfindungsgemäßen organischen Elektro- lumineszenzvorrichtung können alle Materialien verwendet werden, wie sie üblicherweise gemäß dem Stand der Technik eingesetzt werden. Der Fachmann kann daher ohne erfinderisches Zutun alle für organische Elektrolumineszenzvorrichtungen bekannten Materialien in Kombination mit den erfindungsgemäßen Verbindungen gemäß Formel (1) bzw. den oben ausgeführten bevorzugten Ausführungsformen einsetzen. Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck kleiner 10-5 mbar, bevorzugt kleiner 10-6 mbar aufgedampft. Es ist aber auch möglich, dass der Anfangsdruck noch geringer ist, beispielsweise kleiner 10-7 mbar. Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10-5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden. Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie z. B. Siebdruck, Flexodruck, Offsetdruck, LITI (Light Induced Thermal Imaging, Thermotransferdruck), Ink-Jet Druck (Tintenstrahldruck) oder Nozzle Printing, hergestellt werden. Hierfür sind lösliche Verbindungen nötig, welche beispielsweise durch geeignete Substitution erhalten werden. Weiterhin sind Hybridverfahren möglich, bei denen beispielsweise eine oder mehrere Schichten aus Lösung aufgebracht werden und eine oder mehrere weitere Schichten aufgedampft werden. Diese Verfahren sind dem Fachmann generell bekannt und können von ihm ohne erfinderisches Zutun auf organische Elektrolumineszenzvor- richtungen enthaltend die erfindungsgemäßen Verbindungen angewandt werden. Erfindungsgemäß können die elektronischen Vorrichtungen, die eine oder mehrere Verbindungen der Formel (1) enthalten, in Displays, als Licht- quellen in Beleuchtungsanwendungen und als Lichtquellen in medizi- nischen und/oder kosmetischen Anwendungen (z.B. Lichttherapie) eingesetzt werden. Die erfindungsgemäßen Verbindungen und die erfindungsgemäßen orga- nischen Elektrolumineszenzvorrichtungen zeichnen sich durch einen oder mehrere der folgenden Eigenschaften aus: 1. Die erfindungsgemäßen Verbindungen führen zu langen Lebens- dauern. 2. Die erfindungsgemäßen Verbindungen führen zu hohen Effizienzen, insbesondere zu einer hohen EQE. 3. Die erfindungsgemäßen Verbindungen führen zu geringen Betriebs- spannungen. 4. Die erfindungsgemäßen Verbindungen zeigen eine verbesserte Oxidationsstabilität in Lösung, was sich positiv auf die Handhabung der Verbindungen beispielsweise bei Verarbeitung in Druckverfahren auswirkt. 5. Die erfindungsgemäßen Verbindungen zeigen eine hohe Temperatur- stabilität, so dass sie im Hochvakuum unzersetzt verdampft werden können. Die Erfindung wird durch die nachfolgenden Beispiele näher erläutert, ohne sie dadurch einschränken zu wollen. Der Fachmann kann aus den Schilderungen die Erfindung im gesamten offenbarten Bereich ausführen und ohne erfinderisches Zutun weitere erfindungsgemäße Verbindungen herstellen und diese in elektronischen Vorrichtungen verwenden bzw. das erfindungsgemäße Verfahren anwenden. Beispiele: Die nachfolgenden Synthesen werden, sofern nicht anders angegeben, unter einer Schutzgasatmosphäre durchgeführt. Die Edukte können von den Firmen ALDRICH bzw. ABCR (Palladium(II)acetat, Tri-o-tolyl- phosphin, Anorganika, Lösemittel) bezogen werden. Die Angaben bei den literaturbekannten Edukten sind die CAS-Nummern. Beispiel a: 2-(2‐Chloro‐3,3,4,4,5,5‐hexafluorocyclopent‐1‐en‐1‐yl)biphenyl Unter Argon-Atmosphäre werden 1,1‘-Biphenyl-3-boronsäure (14.8 g, 75 mmol, 1.5 Äquiv.), Pd2dba3·CHCl3 (2.5, 0.0025 mol, 1 Mol-% Pd), X-Phos (4.7 mg, 0.001 mol, 2 Mol-%) und K3PO4 (300 g, 150 mmol, 3 Äquiv.) vorgelegt. Dann wird 1,2-Dichlorhexafluorcyclopenten (12.5 g, 50 mmol) und von Sauerstoff befreites trockenes Dioxan (1500 ml) zugegeben. Die resultierende Suspension wird 16 h unter Rückfluss erhitzt. Nachdem die Reaktion abgeschlossen ist, wird die Mischung durch ein kurzes Celite- Kissen mit Hexan filtriert und das Filtrat wird eingedampft. Reinigung durch Säulenchromatographie an Kieselgel mit Hexan als Elutionsmittel liefert das entsprechende Produkt. Die Ausbeute beträgt 13.5 g (37 mmol), entsprechend 75 % der Theorie. Analog werden die folgenden Verbindungen erhalten: The above-mentioned host materials of formula (1) and their preferred embodiments can be combined as desired in the device according to the invention with the previously mentioned matrix materials/host materials, the matrix materials/host materials of formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) or (HH-6) and their preferred embodiments in Table 1 or the compounds H1 to H27. The concentration of the host material of formula (1), as described above or preferably described, in the mixture according to the invention or in the light-emitting layer of the device according to the invention is usually in the range from 5% by weight to 90% by weight, preferably in the range from 10% by weight to 85% by weight, more preferably in the range from 20% by weight to 85% by weight, even more preferably in the range from 30% by weight to 80% by weight, very particularly preferably in the range from 20% by weight to 60% by weight and most preferably in the range from 30 wt. % to 50 wt. %, based on the entire mixture or based on the entire composition of the light-emitting layer. The concentration of the sum of all host materials of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), as described above or described as preferred, in the mixture according to the invention or in the light-emitting layer of the device according to the invention is usually in the range from 10 wt. % to 95 wt. %, preferably in the range from 15 wt. % to 90 wt. %, more preferably in the range from 15 wt. % to 80 wt. %, even more preferably in the range from 20 wt. % to 70 wt. %, very particularly preferably in the range from 40 wt. % to 80 wt. % and most preferably in the range from 50 wt. % to 70 wt. %, based on the entire mixture or based on the entire composition of the light-emitting layer. The present invention also relates to a mixture which, in addition to the above-mentioned host materials of the formula (1), hereinafter referred to as host material 1, and the host material of at least one of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), hereinafter referred to as host material 2, as previously described or preferably described, contains at least one phosphorescent emitter. The present invention also relates to an organic electroluminescent device, as previously described or preferably described, wherein the light-emitting layer contains, in addition to the above-mentioned host materials of the formula (1) and at least one of the formulas (HH-1), (HH-2), (HH-3), (HH-4), (HH-5) and (HH-6), as previously described or preferably described, in particular the material combinations M1 to M729, at least one phosphorescent emitter. Suitable charge transport materials, as can be used in the hole injection or hole transport layer or in the electron barrier layer or in the electron transport layer of the electronic component according to the invention, are, in addition to the compounds of formula (1), for example those mentioned in Y. Shirota et al., Chem. Rev.2007, 107(4), 953-1010, or other materials as used in these layers according to the prior art. All materials that are used according to the prior art as hole transport materials in the hole transport layer can be used as materials for the hole transport layer. Aromatic amine compounds can be used. Further compounds which are preferably used in hole-transporting layers of the OLEDs according to the invention are in particular indenofluorenamine derivatives (for example according to WO 06/122630 or WO 06/100896), the amine derivatives disclosed in EP 1661888, hexaazatriphenylene derivatives (for example according to WO 01/049806), amine derivatives with fused aromatics (for example according to US 5,061,569), the amine derivatives disclosed in WO 95/09147, monobenzoindenofluorenamines (for example according to WO 08/006449), dibenzoindenofluorenamines (for example according to WO 07/140847), spirobifluorenamines (for example according to WO 2012/034627 or WO 2013/120577), fluorenamines (for example according to WO 2014/015937, WO 2014/015938, WO 2014/015935 and WO 2015/082056), spirodibenzopyranamines (for example according to WO 2013/083216), dihydroacridine derivatives (for example according to WO 2012/150001), spirodibenzofurans and spirodibenzothiophenes (for example according to WO 2015/022051, WO 2016/102048 and WO 2016/131521), phenanthrenedarylamines (for example according to WO 2015/131976), spirotribenzotropolones (for example according to WO 2016/087017), spirobifluorenes with meta-phenyldiamine groups (for example according to WO 2016/078738), spirobisacridines (for example according to WO 2015/158411), xanthenediarylamines (for example according to WO 2014/072017), and 9,10-dihydroanthracene spiro compounds with diarylamino groups according to WO 2015/086108. Very particular preference is given to the use of spirobifluorenes substituted by diarylamino groups in the 4-position as hole-transporting compounds, in particular the use of those compounds claimed and disclosed in WO 2013/120577, and the use of spirobifluorenes substituted by diarylamino groups in 2- Position-substituted spirobifluorenes as hole-transporting compounds, in particular the use of those compounds which are claimed and disclosed in WO 2012/034627. The OLED according to the invention preferably comprises two or more different electron-transporting layers. The compound of the formula (1) can be used in one or more or in all electron-transporting layers. In a preferred embodiment, the compound of the formula (1) is used in exactly one or exactly two electron-transporting layers, and other compounds are used in the other electron-transporting layers present. Other compounds which can be used in addition to the compounds of the formula (1) are all materials which are used according to the prior art as electron-transport materials in the electron-transport layer. Particularly suitable are aluminum complexes, e.g. Alq3, zirconium complexes, e.g. Zrq4, lithium complexes, e.g. Liq, benzimidazole derivatives, triazine derivatives, pyrimidine derivatives, pyridine derivatives, pyrazine derivatives, quinoxaline derivatives, quinoline derivatives, oxadiazole derivatives, aromatic ketones, lactams, boranes, diazaphosphole derivatives and phosphine oxide derivatives. Other suitable materials are derivatives of the aforementioned compounds, as disclosed in JP 2000/053957, WO 2003/060956, WO 2004/028217, WO 2004/080975 and WO 2010/072300. Preferred cathodes of the electronic component are metals with a low work function, metal alloys or multilayer structures made of different metals, e.g. B. alkaline earth metals, alkali metals, main group metals or lanthanides (e.g. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Alloys of an alkali or alkaline earth metal and silver are also suitable, e.g. an alloy of magnesium and silver. In multilayer structures, in addition to the metals mentioned, other metals with a relatively high work function can also be used, e.g. Ag or Al, whereby combinations of the metals such as Ca/Ag, Mg/Ag or Ba/Ag are generally used. It can also be advantageous to use a thin intermediate layer made of a material with a high dielectric constant between a metallic cathode and the organic semiconductors. Examples of suitable materials are alkali or alkaline earth metal fluorides, but also the corresponding oxides or carbonates (e.g. LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3, etc.). It is also possible to use lithium quinolinate (LiQ) for this purpose. The layer thickness of this layer is preferably between 0.5 and 5 nm. Preferred anodes are materials with a high work function. The anode preferably has a work function of more than 4.5 eV against vacuum. Firstly, metals with a high redox potential are suitable for this, e.g. Ag, Pt or Au. Secondly, metal/metal oxide electrodes (e.g. Al/Ni/NiOx, Al/PtOx) can also be preferred. For some applications, at least one of the electrodes must be transparent or partially transparent in order to enable the irradiation of the organic material (organic solar cell) or the emission of light (OLED, O laser). Preferred anode materials here are conductive metal mixed oxides. Indium tin oxide (ITO) or indium zinc oxide (IZO) are particularly preferred. Conductively doped organic materials, in particular conductively doped polymers, are further preferred. In addition, the anode can also consist of two or more layers, for example an inner layer of ITO and an outer layer of a metal oxide, preferably tungsten oxide, molybdenum oxide or vanadium oxide. The device is structured accordingly (depending on the application), contacted and finally sealed to exclude harmful influences from water and air. In the other layers of the organic electroluminescent device according to the invention, all materials can be used as are usually used according to the prior art. The person skilled in the art can therefore, without inventive step, use all materials known for organic electroluminescent devices in combination with the compounds according to the invention according to formula (1) or the preferred embodiments set out above. Also preferred is an organic electroluminescent device, characterized in that one or more layers are coated using a sublimation process. The materials are vapor-deposited in vacuum sublimation systems at an initial pressure of less than 10 -5 mbar, preferably less than 10 -6 mbar. However, it is also possible for the initial pressure to be even lower, for example less than 10 -7 mbar. Also preferred is an organic electroluminescent device, characterized in that one or more layers are coated using the OVPD (Organic Vapour Phase Deposition) process or with the aid of carrier gas sublimation. The materials are applied at a pressure of between 10 -5 mbar and 1 bar. A special case of this process is the OVJP (Organic Vapour Jet Printing) process, in which the materials are applied directly through a nozzle and thus structured. Also preferred is an organic electroluminescent device, characterized in that one or more layers are coated from solution, such as by spin coating, or using any printing process, such as B. Screen printing, flexographic printing, offset printing, LITI (Light Induced Thermal Imaging, thermal transfer printing), ink-jet printing or nozzle printing. Soluble compounds are required for this, which are obtained, for example, by suitable substitution. Hybrid processes are also possible in which, for example, one or more layers are applied from solution and one or more further layers are vapor-deposited. These processes are generally known to the person skilled in the art and can be applied by him without inventive step to organic electroluminescent devices containing the compounds according to the invention. According to the invention, the electronic devices containing one or more compounds of formula (1) can be used in displays, as light sources in lighting applications and as light sources in medical and/or cosmetic applications (e.g. light therapy). The compounds according to the invention and the organic electroluminescent devices according to the invention are characterized by one or more of the following properties: 1. The compounds according to the invention lead to long lifetimes. 2. The compounds according to the invention lead to high efficiencies, in particular to a high EQE. 3. The compounds according to the invention lead to low operating voltages. 4. The compounds according to the invention show improved oxidation stability in solution, which has a positive effect on the handling of the compounds, for example when processing in printing processes. 5. The compounds according to the invention show high temperature stability, so that they can be evaporated without decomposition in a high vacuum. The invention is explained in more detail by the following examples, without wishing to restrict it thereby. From the descriptions, the person skilled in the art can carry out the invention in the entire disclosed area and, without inventive step, produce further compounds according to the invention and use them in electronic devices or apply the method according to the invention. Examples: The following syntheses are carried out under a protective gas atmosphere unless otherwise stated. The reactants can be obtained from ALDRICH or ABCR (palladium(II) acetate, tri-o-tolylphosphine, inorganics, solvents). The information for the reactants known from the literature are the CAS numbers. Example a: 2-(2‐chloro‐3,3,4,4,5,5‐hexafluorocyclopent‐1‐en‐1‐yl)biphenyl Under an argon atmosphere, 1,1'-biphenyl-3-boronic acid (14.8 g, 75 mmol, 1.5 equiv.), Pd 2 dba 3 ·CHCl 3 (2.5, 0.0025 mol, 1 mol% Pd), X-Phos (4.7 mg, 0.001 mol, 2 mol%) and K 3 PO 4 (300 g, 150 mmol, 3 equiv.) are initially charged. Then 1,2-dichlorohexafluorocyclopentene (12.5 g, 50 mmol) and deoxygenated dry dioxane (1500 mL) are added. The resulting suspension is heated under reflux for 16 h. After the reaction is complete, the mixture is filtered through a short pad of Celite with hexane and the filtrate is evaporated. Purification by column chromatography on silica gel with hexane as eluent yields the corresponding product. The yield is 13.5 g (37 mmol), corresponding to 75% of theory. The following compounds are obtained analogously:
Beispiel b: 6‐Bromo‐1,1,2,2,3,3‐hexafluoro‐1H,2H,3H‐cyclopenta[l]phenanthren Unter Argon-Atmosphäre wird zu einer Mischung aus 1-(4-Bromophenyl)- 2-phenyl-3,3,4,4,5,5-hexafluorocyclopenten (3 g, 7.3 mmol) und Benzol (300 ml) bei RT Jod (2.9 g, 12 mmol) hinzugefügt. Nach 30-minütigem Rühren wird 1,2-Epoxybutan (300 ml, 350 mmol) zugegeben. Die Mischung wird unter Lichteinstrahlung bei RT für 3 h gerührt. Das Reaktionsgemisch wird in gesättigte wässrige Natriumthiosulfatlösung (10 ml) gegossen und die resultierende organische Schicht getrennt und mit destilliertem Wasser (100 ml) und Salzlösung (100 ml) gewaschen. Nach Abtrennung und Trocknung der organischen Schicht wird das Lösungs- mittel bei vermindertem Druck eingedampft. Der Rückstand wird durch Säulenchromatographie an Kieselgel getrennt (Laufmittel: Ethylacetat/ Hexan = 1/4). Der Rückstand wird aus Toluol und aus Dichlormethan / iso- Propanol umkristallisiert und abschließend im Hochvakuum sublimiert. Die Reinheit beträgt 99.9 %. Die Ausbeute beträgt 1.8 g (4.5 mmol), entsprechend 61 % der Theorie. Analog werden die folgenden Verbindungen erhalten: Beispiel c: 2‐{1,1,2,2,3,3‐Hexafluoro‐1H,2H,3H‐cyclopenta[l]phenanthren‐6‐ yl}triphenylen Triphenylen-2-boronsäure (35 g, 130 mmol), 6‐Bromo‐1,1,2,2,3,3‐hexa- fluoro‐1H,2H,3H‐cyclopenta[l]phenanthren (44.5 g, 110 mmol) und Trikaliumphosphat (44.6 g, 210.0 mmol) werden in 500 mL Toulol, 500 mL Dioxan und 500 mL Wasser suspendiert. Zu dieser Suspension werden Tri-o-tolylphosphin (913 mg, 3.0 mmol) und dann Palladium(II)acetat (112 mg, 0.5 mmol) gegeben, und die Reaktionsmischung wird 16 h unter Rückfluss erhitzt. Nach Erkalten wird die organische Phase abgetrennt, über Kieselgel filtriert, dreimal mit je 200 mL Wasser gewaschen und anschließend eingeengt. Der Rückstand wird aus Toluol und aus Dichlor- methan / iso-Propanol umkristallisiert und abschließend im Hochvakuum sublimiert. Die Reinheit beträgt 99.9 %. Die Ausbeute beträgt 42 g (77 mmol), entsprechend 71 % der Theorie. Analog werden die folgenden Verbindungen erhalten: Example b: 6‐Bromo‐1,1,2,2,3,3‐hexafluoro‐1H,2H,3H‐cyclopenta[l]phenanthrene Under argon atmosphere, iodine (2.9 g, 12 mmol) is added to a mixture of 1-(4-bromophenyl)-2-phenyl-3,3,4,4,5,5-hexafluorocyclopentene (3 g, 7.3 mmol) and benzene (300 ml) at RT. After stirring for 30 minutes, 1,2-epoxybutane (300 ml, 350 mmol) is added. The mixture is stirred under light irradiation at RT for 3 h. The The reaction mixture is poured into saturated aqueous sodium thiosulfate solution (10 ml) and the resulting organic layer is separated and washed with distilled water (100 ml) and brine (100 ml). After separating and drying the organic layer, the solvent is evaporated under reduced pressure. The residue is separated by column chromatography on silica gel (mobile phase: ethyl acetate/hexane = 1/4). The residue is recrystallized from toluene and from dichloromethane/isopropanol and finally sublimed under high vacuum. The purity is 99.9%. The yield is 1.8 g (4.5 mmol), corresponding to 61% of theory. The following compounds are obtained analogously: Example c: 2‐{1,1,2,2,3,3‐Hexafluoro‐1H,2H,3H‐cyclopenta[l]phenanthren‐6‐yl}triphenylene Triphenylene-2-boronic acid (35 g, 130 mmol), 6-bromo-1,1,2,2,3,3-hexa-fluoro-1H,2H,3H-cyclopenta[l]phenanthrene (44.5 g, 110 mmol) and tripotassium phosphate (44.6 g, 210.0 mmol) are suspended in 500 mL toluene, 500 mL dioxane and 500 mL water. Tri-o-tolylphosphine (913 mg, 3.0 mmol) and then palladium(II) acetate (112 mg, 0.5 mmol) are added to this suspension and the reaction mixture is heated under reflux for 16 h. After cooling, the organic phase is separated, filtered through silica gel, washed three times with 200 mL water each time and then concentrated. The residue is recrystallized from toluene and from dichloromethane/isopropanol and finally sublimed under high vacuum. The purity is 99.9%. The yield is 42 g (77 mmol), corresponding to 71% of theory. The following compounds are obtained analogously:
Beispiel d: 9‐{1,1,2,2,3,3‐Hexafluorocyclopenta[l]phenanthren‐6‐yl}‐3‐ phenylcarbazol Example d: 9‐{1,1,2,2,3,3‐Hexafluorocyclopenta[l]phenanthren‐6‐yl}‐3‐phenylcarbazole
3-Phenylcarbazol (24.3 g,100 mmol), 6‐Bromo‐1,1,2,2,3,3‐hexafluoro‐ 1H,2H,3H‐cyclopenta[l]phenanthren (48 g ,120 mmol), Brombenzol und 50.5 g NaOtBu werden in 1.5 L p-Xylol vorgelegt. Dann werden Pd(OAc)2 (0.5 g, 2.11 mmol) und 4.2 ml 1 M Tri-tert.-butylphosphin zugegeben. Das Reaktionsgemisch wird 16 h unter Rückfluss erhitzt. Nach dem Abkühlen wird die organische Phase abgetrennt. Es wird dreimal mit je 200 ml Wasser gewaschen und anschließend zur Trockene eingedampft. Der Rückstand wird mit heißem Toluol extrahiert, aus Toluol umkristallisiert und schließlich im Hochvakuum sublimiert. Ausbeute: 52 g (92 mmol), 78 % d. Th.; Reinheit: 99.9 % n. HPLC. Analog können folgende Verbindungen hergestellt werden: 3-Phenylcarbazole (24.3 g, 100 mmol), 6-bromo-1,1,2,2,3,3-hexafluoro-1H,2H,3H-cyclopenta[l]phenanthrene (48 g, 120 mmol), bromobenzene and 50.5 g NaOtBu are placed in 1.5 L p-xylene. Then Pd(OAc) 2 (0.5 g, 2.11 mmol) and 4.2 ml 1 M tri-tert-butylphosphine are added. The reaction mixture is heated under reflux for 16 h. After cooling, the organic phase is separated. It is washed three times with 200 ml water each time and then evaporated to dryness. The residue is extracted with hot toluene, recrystallized from toluene and finally sublimated under high vacuum. Yield: 52 g (92 mmol), 78% of theory; purity: 99.9% by HPLC. The following compounds can be prepared analogously:
Beispiel: Herstellung der OLEDs In den folgenden Beispielen E1 bis E10 (siehe Tabelle 1) wird der Einsatz der erfindungsgemäßen Materialien in OLEDs vorgestellt. Vorbehandlung für die Beispiele E1 bis E13: Glasplättchen, die mit strukturiertem ITO (Indium Zinn Oxid) der Dicke 50 nm beschichtet sind, werden vor der Beschichtung mit einem Sauer- stoffplasma, gefolgt von einem Argonplasma, behandelt. Diese mit Plasma behandelten Glasplättchen bilden die Substrate, auf welche die OLEDs aufgebracht werden. Die OLEDs haben prinzipiell folgenden Schichtaufbau: Substrat / optionale Interlayer (IL) /Lochinjektionsschicht (HIL) / Lochtransportschicht (HTL) / Elektronenblockierschicht (EBL) / Emissionsschicht (EML) / optionale Lochblockierschicht (HBL) / Elektronentransportschicht (ETL) / optionale Elektroneninjektionsschicht (EIL) und abschließend eine Kathode. Die Kathode wird durch eine 100 nm dicke Aluminiumschicht gebildet. Der genaue Aufbau der OLEDs ist Tabelle 1 zu entnehmen. Die zur Herstellung der OLEDs benötigten Materialien sind in Tabelle 2 gezeigt. Die Daten der OLEDs sind in Tabelle 3 und 4 aufgelistet. Alle Materialien werden in einer Vakuumkammer thermisch aufgedampft. Dabei besteht die Emissionsschicht immer aus mindestens einem Matrix- material (Hostmaterial, Wirtsmaterial) und einem emittierenden Dotierstoff (Dotand, Emitter), der dem Matrixmaterial bzw. den Matrixmaterialien durch Coverdampfung in einem bestimmten Volumenanteil beigemischt wird. Eine Angabe wie IC1:EG1:TEG1 (45%:45%:10%) bedeutet hierbei, dass das Material IC1 in einem Volumenanteil von 45%, EG1 in einem Volumenanteil von 45% und TEG1 in einem Volumenanteil von 10% in der Schicht vorliegt. Analog kann auch die Elektronentransportschicht aus einer Mischung von zwei Materialien bestehen. Die OLEDs werden standardmäßig charakterisiert. Hierfür werden die Elektrolumineszenzspektren, die Stromeffizienz (SE, gemessen in cd/A) und die externe Quanteneffizienz (EQE, gemessen in %) in Abhängigkeit der Leuchtdichte, berechnet aus Strom-Spannungs-Leuchtdichte- Kennlinien unter Annahme einer lambertschen Abstrahlcharakteristik bestimmt. Die Elektrolumineszenzspektren werden bei einer Leuchtdichte von 1000 cd/m² bestimmt und daraus die CIE 1931 x und y Farb- koordinaten berechnet. Die so erhaltenen Ergebnisse sind Tabelle 3 zu entnehmen. Verwendung der erfindungsgemäßen Materialien in OLEDs Die erfindungsgemäßen Verbindungen EG0 bis EG10 können in den Beispielen E1 bis E11 als Matrixmaterial in der Emissionsschicht von phosphoreszierenden grünen OLEDs und EG11 und EG12 in Beispiel E12 bis E13 als Elektrontransportmaterial in der Emissionsschicht von phosphoreszierenden grünen OLEDs eingesetzt werden. Tabelle 1: Aufbau der OLEDs Tabelle 2: Strukturformeln der Materialien für die OLEDs Example: Production of OLEDs The following examples E1 to E10 (see Table 1) present the use of the materials according to the invention in OLEDs. Pretreatment for examples E1 to E13: Glass plates coated with structured ITO (indium tin oxide) with a thickness of 50 nm are treated with an oxygen plasma, followed by an argon plasma, before coating. These plasma-treated glass plates form the substrates onto which the OLEDs are applied. The OLEDs basically have the following layer structure: substrate / optional interlayer (IL) / hole injection layer (HIL) / hole transport layer (HTL) / electron blocking layer (EBL) / emission layer (EML) / optional hole blocking layer (HBL) / electron transport layer (ETL) / optional electron injection layer (EIL) and finally a cathode. The cathode is formed by a 100 nm thick aluminum layer. The exact structure of the OLEDs can be found in Table 1. The The materials required to manufacture the OLEDs are shown in Table 2. The data for the OLEDs are listed in Tables 3 and 4. All materials are thermally vapor-deposited in a vacuum chamber. The emission layer always consists of at least one matrix material (host material) and an emitting dopant (dopant, emitter), which is mixed into the matrix material or materials by co-evaporation in a certain volume proportion. A specification such as IC1:EG1:TEG1 (45%:45%:10%) means that the material IC1 is present in the layer in a volume proportion of 45%, EG1 in a volume proportion of 45% and TEG1 in a volume proportion of 10%. Analogously, the electron transport layer can also consist of a mixture of two materials. The OLEDs are characterized as standard. For this purpose, the electroluminescence spectra, the current efficiency (SE, measured in cd/A) and the external quantum efficiency (EQE, measured in %) are determined as a function of the luminance, calculated from current-voltage-luminance characteristics assuming a Lambertian radiation characteristic. The electroluminescence spectra are determined at a luminance of 1000 cd/m² and the CIE 1931 x and y color coordinates are calculated from this. The results obtained in this way can be found in Table 3. Use of the materials according to the invention in OLEDs The compounds EG0 to EG10 according to the invention can be used in Examples E1 to E11 as matrix material in the emission layer of phosphorescent green OLEDs and EG11 and EG12 in Examples E12 to E13 as electron transport material in the emission layer of phosphorescent green OLEDs. Table 1: Structure of the OLEDs Table 2: Structural formulas of the materials for the OLEDs
Tabelle 3: Daten der OLEDs Table 3: OLED data
Claims
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP23168839.1 | 2023-04-20 | ||
| EP23168839 | 2023-04-20 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2024218109A1 true WO2024218109A1 (en) | 2024-10-24 |
Family
ID=86095754
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2024/060343 Pending WO2024218109A1 (en) | 2023-04-20 | 2024-04-17 | Materials for electronic devices |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2024218109A1 (en) |
Citations (175)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| WO1995009147A1 (en) | 1993-09-29 | 1995-04-06 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element and arylenediamine derivative |
| EP0652273A1 (en) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organic material for electroluminescent device and electroluminescent device |
| EP0676461A2 (en) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiro compounds and their application as electroluminescence materials |
| JP2000053957A (en) | 1998-06-23 | 2000-02-22 | Koto Gijutsu Kenkyuin Kenkyu Kumiai | Novel organometallic luminescent material and organic electroluminescent device containing the same |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2001049806A1 (en) | 1999-12-31 | 2001-07-12 | Lg Chemical Co., Ltd | Electronic device comprising organic compound having p-type semiconducting characteristics |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191614A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device and metal coordination compound therefor |
| EP1191613A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device, display apparatus and metal coordination compound |
| EP1191612A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device, display apparatus and metal coordination compound |
| EP1205527A1 (en) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2002072714A1 (en) | 2001-03-10 | 2002-09-19 | Covion Organic Semiconductors Gmbh | Solutions and dispersions of organic semiconductors |
| WO2002002714A3 (en) | 2000-06-30 | 2002-10-24 | Du Pont | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2003019694A2 (en) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors Gmbh | Solutions of polymer semiconductors |
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004028217A1 (en) | 2002-09-20 | 2004-04-01 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| WO2004058911A2 (en) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organic electroluminescent element |
| WO2004080975A1 (en) | 2003-03-13 | 2004-09-23 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| WO2004081017A1 (en) | 2003-03-11 | 2004-09-23 | Covion Organic Semiconductors Gmbh | Metal complexes |
| JP2004288381A (en) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | Organic electroluminescent element |
| WO2004093207A2 (en) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mixtures of matrix materials and organic semiconductors capable of emission, use of the same and electronic components containing said mixtures |
| WO2005011013A1 (en) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organic electroluminescent element |
| WO2005019373A2 (en) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (oled's) |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005033244A1 (en) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metal complexes |
| EP1553154A1 (en) | 2002-08-23 | 2005-07-13 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and anthracene derivative |
| WO2005084082A1 (en) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organic electronic devices |
| WO2005111172A2 (en) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Novel material mixtures for use in electroluminescence |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| JP2005347160A (en) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | Organic electroluminescence element, lighting device and display device |
| EP1617711A1 (en) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organic electroluminescent device and display |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006048268A1 (en) | 2004-11-06 | 2006-05-11 | Merck Patent Gmbh | Organic electroluminescent device |
| EP1661888A1 (en) | 2004-11-29 | 2006-05-31 | Samsung SDI Co., Ltd. | Phenylcarbazole-based compound and organic electroluminescent device employing the same |
| WO2006097208A1 (en) | 2005-03-16 | 2006-09-21 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| WO2006100896A1 (en) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescence device utilizing the same |
| WO2006108497A1 (en) | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Compounds for organic electronic devices |
| WO2006117052A1 (en) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organic electroluminescent device and boric acid and borinic acid derivatives used therein |
| EP1722602A1 (en) | 2004-03-05 | 2006-11-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device and organic electroluminescent display |
| WO2006122630A1 (en) | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Compounds for organic electronic devices |
| EP1731584A1 (en) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organic electroluminescent device material, organic electroluminescent device, display and illuminating device |
| WO2006131192A1 (en) | 2005-06-09 | 2006-12-14 | Merck Patent Gmbh | New materials for organic electroluminescence devices |
| EP1749809A1 (en) | 2004-05-27 | 2007-02-07 | Idemitsu Kosan Co., Ltd. | Asymmetric pyrene derivative and organic electroluminescent device using same |
| US20070092755A1 (en) | 2005-10-26 | 2007-04-26 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| WO2007063754A1 (en) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent element and organic electroluminescent element |
| WO2007065678A1 (en) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Novel materials for organic electroluminiescent devices |
| WO2007065550A1 (en) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| WO2007110129A1 (en) | 2006-03-24 | 2007-10-04 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| WO2007137725A1 (en) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| WO2007140847A1 (en) | 2006-06-02 | 2007-12-13 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2008006449A1 (en) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| EP1905754A1 (en) | 2005-07-06 | 2008-04-02 | Idemitsu Kosan Co., Ltd. | Pyrene derivative and organic electroluminescence device making use of the same |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (en) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazole derivatives for organc electroluminescent devices |
| EP1968131A1 (en) | 2005-12-27 | 2008-09-10 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent device and organic electroluminescent device |
| WO2008145239A2 (en) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Benzanthracene derivatives for organic electroluminescent devices |
| DE102007031220A1 (en) | 2007-07-04 | 2009-01-08 | Novaled Ag | Chinoid compounds and their use in semiconducting matrix materials, electronic and optoelectronic devices |
| EP2045848A1 (en) | 2007-07-18 | 2009-04-08 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device material and organic electroluminescent device |
| WO2009062578A1 (en) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organic electroluminescent devices comprising azomethine-metal complexes |
| WO2009100925A1 (en) | 2008-02-13 | 2009-08-20 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| WO2009146770A2 (en) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Electronic device comprising metal complexes |
| WO2010006680A1 (en) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010012328A1 (en) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2010015307A1 (en) | 2008-08-04 | 2010-02-11 | Merck Patent Gmbh | Electronic devices comprising metal complexes having isonitrile ligands |
| WO2010015306A1 (en) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organic electroluminescence device |
| WO2010031485A1 (en) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| US20100096600A1 (en) | 2008-10-16 | 2010-04-22 | Novaled Ag | Square Planar Transition Metal Complexes and Organic Semiconductive Materials Using Them as Well as Electronic or Optoelectric Components |
| WO2010054730A1 (en) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organic electroluminescent devices |
| WO2010054731A1 (en) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2010054729A2 (en) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010054728A1 (en) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2010072300A1 (en) | 2008-12-22 | 2010-07-01 | Merck Patent Gmbh | Organic electroluminescent device comprising triazine derivatives |
| EP2213662A1 (en) | 2007-11-30 | 2010-08-04 | Idemitsu Kosan Co., Ltd. | Azaindenofluorenedione derivative, organic electroluminescent device material, and organic electroluminescent device |
| WO2010086089A1 (en) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metal complexes |
| WO2010094378A1 (en) | 2009-02-17 | 2010-08-26 | Merck Patent Gmbh | Organic electronic device |
| WO2010099852A1 (en) | 2009-03-02 | 2010-09-10 | Merck Patent Gmbh | Metal complexes having azaborol ligands and electronic device having the same |
| WO2010102709A1 (en) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010108579A1 (en) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organic electroluminescent device |
| WO2010136109A1 (en) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011000455A1 (en) | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| EP2276085A1 (en) | 2008-03-27 | 2011-01-19 | Nippon Steel Chemical Co., Ltd. | Organic electroluminescent device |
| WO2011032626A1 (en) | 2009-09-16 | 2011-03-24 | Merck Patent Gmbh | Metal complexes |
| WO2011042107A2 (en) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011054442A2 (en) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materials for electronic devices |
| WO2011057706A2 (en) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materials for electronic devices |
| WO2011060867A1 (en) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Nitrogen-containing condensed heterocyclic compounds for oleds |
| WO2011060877A2 (en) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2011060859A1 (en) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011066898A1 (en) | 2009-12-05 | 2011-06-09 | Merck Patent Gmbh | Electronic device containing metal complexes |
| WO2011073149A1 (en) | 2009-12-14 | 2011-06-23 | Basf Se | Metal complexes comprising diazabenzimidazol carbene-ligands and the use thereof in oleds |
| WO2011088877A1 (en) | 2010-01-25 | 2011-07-28 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2011116865A1 (en) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2011120709A1 (en) | 2010-03-31 | 2011-10-06 | Osram Opto Semiconductors Gmbh | Dopant for a hole conductor layer for organic semiconductor components, and use thereof |
| US8044390B2 (en) | 2007-05-25 | 2011-10-25 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent device, organic electroluminescent device, and organic electroluminescent display |
| WO2011137951A1 (en) | 2010-05-04 | 2011-11-10 | Merck Patent Gmbh | Organic electroluminescence devices |
| US8057712B2 (en) | 2008-04-29 | 2011-11-15 | Novaled Ag | Radialene compounds and their use |
| WO2011157339A1 (en) | 2010-06-15 | 2011-12-22 | Merck Patent Gmbh | Metal complexes |
| WO2012007086A1 (en) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metal complexes |
| WO2012034627A1 (en) | 2010-09-15 | 2012-03-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2012048781A1 (en) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Triphenylene-based materials for organic electroluminescent devices |
| WO2012048780A1 (en) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2012095143A1 (en) | 2011-01-13 | 2012-07-19 | Merck Patent Gmbh | Compounds for organic electroluminescent devices |
| US20120187826A1 (en) | 2009-12-21 | 2012-07-26 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element using pyrene derivative |
| WO2012143080A2 (en) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2012150001A1 (en) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2013041176A1 (en) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazole derivatives for organic electroluminescence devices |
| WO2013056776A1 (en) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2013083216A1 (en) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro dihydroacridine derivatives and the use thereof as materials for organic electroluminescence devices |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| DE102012209523A1 (en) | 2012-06-06 | 2013-12-12 | Osram Opto Semiconductors Gmbh | Main group metal complexes as p-dopants for organic electronic matrix materials |
| WO2013185871A1 (en) | 2012-06-12 | 2013-12-19 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2014008982A1 (en) | 2012-07-13 | 2014-01-16 | Merck Patent Gmbh | Metal complexes |
| WO2014015935A2 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Compounds and organic electronic devices |
| WO2014015938A1 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivatives of 2-diarylaminofluorene and organic electronic compounds containing them |
| WO2014015937A1 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Compounds and organic electroluminescent devices |
| WO2014023377A2 (en) | 2012-08-07 | 2014-02-13 | Merck Patent Gmbh | Metal complexes |
| WO2014037077A1 (en) | 2012-09-04 | 2014-03-13 | Merck Patent Gmbh | Connections for electronic devices |
| WO2014072017A1 (en) | 2012-11-12 | 2014-05-15 | Merck Patent Gmbh | Materials for electronic devices |
| WO2014094961A1 (en) | 2012-12-21 | 2014-06-26 | Merck Patent Gmbh | Metal complexes |
| WO2014094960A1 (en) | 2012-12-21 | 2014-06-26 | Merck Patent Gmbh | Metal complexes |
| WO2014106522A1 (en) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materials for electronic devices |
| WO2014111269A2 (en) | 2013-10-14 | 2014-07-24 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015022051A1 (en) | 2013-08-15 | 2015-02-19 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015036074A1 (en) | 2013-09-11 | 2015-03-19 | Merck Patent Gmbh | Metal complexes |
| WO2015082056A1 (en) | 2013-12-06 | 2015-06-11 | Merck Patent Gmbh | Compounds and organic electronic devices |
| WO2015086108A1 (en) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015102118A1 (en) | 2014-02-18 | 2015-07-09 | 学校法人関西学院 | Polycyclic aromatic compound |
| WO2015104045A1 (en) | 2014-01-13 | 2015-07-16 | Merck Patent Gmbh | Metal complexes |
| WO2015117718A1 (en) | 2014-02-05 | 2015-08-13 | Merck Patent Gmbh | Metal complexes |
| WO2015131976A1 (en) | 2014-03-07 | 2015-09-11 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015158411A1 (en) | 2014-04-14 | 2015-10-22 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015158409A1 (en) | 2014-04-16 | 2015-10-22 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015169412A1 (en) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2016015810A1 (en) | 2014-07-29 | 2016-02-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016015815A1 (en) | 2014-07-28 | 2016-02-04 | Merck Patent Gmbh | Metal complexes |
| WO2016023608A1 (en) | 2014-08-13 | 2016-02-18 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20160041014A (en) | 2014-10-06 | 2016-04-15 | 유니버셜 디스플레이 코포레이션 | Organic electroluminescent materials and devices |
| WO2016068162A1 (en) * | 2014-10-29 | 2016-05-06 | 国立大学法人茨城大学 | Polymer having condensed polycyclic aromatic skeleton, and light-emitting element and electrode each manufactured using same |
| WO2016078738A1 (en) | 2014-11-18 | 2016-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016087017A1 (en) | 2014-12-01 | 2016-06-09 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016102048A1 (en) | 2014-12-22 | 2016-06-30 | Merck Patent Gmbh | Materials for electronic devices |
| WO2016124304A1 (en) | 2015-02-03 | 2016-08-11 | Merck Patent Gmbh | Metal complexes |
| WO2016131521A1 (en) | 2015-02-16 | 2016-08-25 | Merck Patent Gmbh | Spirobifluorene derivative-based materials for electronic devices |
| WO2016150544A1 (en) | 2015-03-25 | 2016-09-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016152418A1 (en) | 2015-03-25 | 2016-09-29 | 学校法人関西学院 | Polycyclic aromatic compound and light emission layer-forming composition |
| WO2017025165A1 (en) | 2015-08-12 | 2017-02-16 | Merck Patent Gmbh | Materials for electronic devices |
| WO2017028941A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017032439A1 (en) | 2015-08-25 | 2017-03-02 | Merck Patent Gmbh | Metal complexes |
| WO2017036574A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | 6,9,15,18-tetrahydro-s-indaceno[1,2-b:5,6-b']difluorene derivatives and use thereof in electronic devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2017122988A1 (en) | 2016-01-13 | 2017-07-20 | 덕산네오룩스 주식회사 | Compound for organic electric element, organic electric element using same, and electronic device thereof |
| WO2017148565A1 (en) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2018011186A1 (en) | 2016-07-14 | 2018-01-18 | Merck Patent Gmbh | Metal complexes |
| WO2018041769A1 (en) | 2016-08-30 | 2018-03-08 | Merck Patent Gmbh | Binuclear and trinuclear metal complexes composed of two inter-linked tripodal hexadentate ligands for use in electroluminescent devices |
| WO2018095397A1 (en) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | Organic compound containing boron and uses thereof, organic mixture, and organic electronic device |
| WO2018110887A1 (en) | 2016-12-14 | 2018-06-21 | 주식회사 엘지화학 | Heterocyclic compound, and organic light-emitting element comprising same |
| WO2018178001A1 (en) | 2017-03-29 | 2018-10-04 | Merck Patent Gmbh | Metal complexes |
| WO2019004248A1 (en) | 2017-06-30 | 2019-01-03 | 住友化学株式会社 | Macromolecular compound and light-emitting element using same |
| WO2019020538A1 (en) | 2017-07-25 | 2019-01-31 | Merck Patent Gmbh | METALLIC COMPLEXES |
| KR101978651B1 (en) | 2018-10-30 | 2019-05-15 | 머티어리얼사이언스 주식회사 | Method for preparing deuterated orgarnic compounds and deuterated orgarnic compounds produced by the same |
| WO2019115423A1 (en) | 2017-12-13 | 2019-06-20 | Merck Patent Gmbh | Metal complexes |
| WO2019132040A1 (en) | 2017-12-28 | 2019-07-04 | 出光興産株式会社 | Novel compound and organic electroluminescence element |
| WO2019158453A1 (en) | 2018-02-13 | 2019-08-22 | Merck Patent Gmbh | Metal complexes |
| WO2019229011A1 (en) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Composition for organic electronic devices |
| KR20200052820A (en) | 2018-11-07 | 2020-05-15 | 머티어리얼사이언스 주식회사 | An organic compound and an organic light emitting diode |
| US20200161552A1 (en) | 2018-11-21 | 2020-05-21 | Sfc Co., Ltd. | Indolocarbazole derivatives and organic electroluminescent devices using the same |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021180614A1 (en) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organic electroluminescent apparatus |
| WO2021180625A1 (en) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organic electroluminescent apparatus |
| KR20230034896A (en) | 2021-09-03 | 2023-03-10 | 삼성에스디아이 주식회사 | Composition for optoelectronic device and organic optoelectronic device and display device |
-
2024
- 2024-04-17 WO PCT/EP2024/060343 patent/WO2024218109A1/en active Pending
Patent Citations (180)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| WO1995009147A1 (en) | 1993-09-29 | 1995-04-06 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element and arylenediamine derivative |
| EP0652273A1 (en) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organic material for electroluminescent device and electroluminescent device |
| EP0676461A2 (en) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiro compounds and their application as electroluminescence materials |
| JP2000053957A (en) | 1998-06-23 | 2000-02-22 | Koto Gijutsu Kenkyuin Kenkyu Kumiai | Novel organometallic luminescent material and organic electroluminescent device containing the same |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2001049806A1 (en) | 1999-12-31 | 2001-07-12 | Lg Chemical Co., Ltd | Electronic device comprising organic compound having p-type semiconducting characteristics |
| EP1205527A1 (en) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2002002714A3 (en) | 2000-06-30 | 2002-10-24 | Du Pont | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191613A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device, display apparatus and metal coordination compound |
| EP1191612A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device, display apparatus and metal coordination compound |
| EP1191614A2 (en) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Luminescence device and metal coordination compound therefor |
| WO2002072714A1 (en) | 2001-03-10 | 2002-09-19 | Covion Organic Semiconductors Gmbh | Solutions and dispersions of organic semiconductors |
| WO2003019694A2 (en) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors Gmbh | Solutions of polymer semiconductors |
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| EP1553154A1 (en) | 2002-08-23 | 2005-07-13 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and anthracene derivative |
| WO2004028217A1 (en) | 2002-09-20 | 2004-04-01 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| WO2004058911A2 (en) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organic electroluminescent element |
| WO2004081017A1 (en) | 2003-03-11 | 2004-09-23 | Covion Organic Semiconductors Gmbh | Metal complexes |
| WO2004080975A1 (en) | 2003-03-13 | 2004-09-23 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| JP2004288381A (en) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | Organic electroluminescent element |
| WO2004093207A2 (en) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mixtures of matrix materials and organic semiconductors capable of emission, use of the same and electronic components containing said mixtures |
| EP1617710A1 (en) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material for organic electroluminescent device, organic electroluminescent device, illuminating device and display |
| EP1617711A1 (en) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organic electroluminescent device and display |
| WO2005011013A1 (en) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organic electroluminescent element |
| WO2005019373A2 (en) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Transition metal complexes comprising carbene ligands serving as emitters for organic light-emitting diodes (oled's) |
| WO2005033244A1 (en) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metal complexes |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005039246A1 (en) | 2003-09-30 | 2005-04-28 | Konica Minolta Holdings, Inc. | Organic electroluminescent device, illuminating device, and display |
| WO2005084082A1 (en) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organic electronic devices |
| WO2005084081A1 (en) | 2004-02-20 | 2005-09-09 | Merck Patent Gmbh | Organic electronic devices |
| EP1722602A1 (en) | 2004-03-05 | 2006-11-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device and organic electroluminescent display |
| EP1731584A1 (en) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organic electroluminescent device material, organic electroluminescent device, display and illuminating device |
| WO2005111172A2 (en) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Novel material mixtures for use in electroluminescence |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| EP1749809A1 (en) | 2004-05-27 | 2007-02-07 | Idemitsu Kosan Co., Ltd. | Asymmetric pyrene derivative and organic electroluminescent device using same |
| JP2005347160A (en) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | Organic electroluminescence element, lighting device and display device |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006048268A1 (en) | 2004-11-06 | 2006-05-11 | Merck Patent Gmbh | Organic electroluminescent device |
| EP1661888A1 (en) | 2004-11-29 | 2006-05-31 | Samsung SDI Co., Ltd. | Phenylcarbazole-based compound and organic electroluminescent device employing the same |
| WO2006097208A1 (en) | 2005-03-16 | 2006-09-21 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| WO2006100896A1 (en) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescence device utilizing the same |
| WO2006108497A1 (en) | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Compounds for organic electronic devices |
| WO2006117052A1 (en) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organic electroluminescent device and boric acid and borinic acid derivatives used therein |
| WO2006122630A1 (en) | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Compounds for organic electronic devices |
| WO2006131192A1 (en) | 2005-06-09 | 2006-12-14 | Merck Patent Gmbh | New materials for organic electroluminescence devices |
| EP1905754A1 (en) | 2005-07-06 | 2008-04-02 | Idemitsu Kosan Co., Ltd. | Pyrene derivative and organic electroluminescence device making use of the same |
| US20070092755A1 (en) | 2005-10-26 | 2007-04-26 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| WO2007063754A1 (en) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent element and organic electroluminescent element |
| WO2007065678A1 (en) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Novel materials for organic electroluminiescent devices |
| WO2007065550A1 (en) | 2005-12-08 | 2007-06-14 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| EP1968131A1 (en) | 2005-12-27 | 2008-09-10 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent device and organic electroluminescent device |
| WO2007110129A1 (en) | 2006-03-24 | 2007-10-04 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| WO2007137725A1 (en) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| WO2007140847A1 (en) | 2006-06-02 | 2007-12-13 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2008006449A1 (en) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (en) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazole derivatives for organc electroluminescent devices |
| US8044390B2 (en) | 2007-05-25 | 2011-10-25 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent device, organic electroluminescent device, and organic electroluminescent display |
| WO2008145239A2 (en) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Benzanthracene derivatives for organic electroluminescent devices |
| DE102007031220A1 (en) | 2007-07-04 | 2009-01-08 | Novaled Ag | Chinoid compounds and their use in semiconducting matrix materials, electronic and optoelectronic devices |
| WO2009003455A1 (en) | 2007-07-04 | 2009-01-08 | Novaled Ag | Quinoid compounds and the use thereof in semiconducting matrix materials, electronic and optoelectronic components |
| EP2045848A1 (en) | 2007-07-18 | 2009-04-08 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device material and organic electroluminescent device |
| WO2009062578A1 (en) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organic electroluminescent devices comprising azomethine-metal complexes |
| EP2213662A1 (en) | 2007-11-30 | 2010-08-04 | Idemitsu Kosan Co., Ltd. | Azaindenofluorenedione derivative, organic electroluminescent device material, and organic electroluminescent device |
| WO2009100925A1 (en) | 2008-02-13 | 2009-08-20 | Merck Patent Gmbh | Novel materials for organic electroluminescent devices |
| EP2276085A1 (en) | 2008-03-27 | 2011-01-19 | Nippon Steel Chemical Co., Ltd. | Organic electroluminescent device |
| US8057712B2 (en) | 2008-04-29 | 2011-11-15 | Novaled Ag | Radialene compounds and their use |
| WO2009146770A2 (en) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Electronic device comprising metal complexes |
| WO2010006680A1 (en) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010012328A1 (en) | 2008-07-29 | 2010-02-04 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2010015307A1 (en) | 2008-08-04 | 2010-02-11 | Merck Patent Gmbh | Electronic devices comprising metal complexes having isonitrile ligands |
| WO2010015306A1 (en) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organic electroluminescence device |
| WO2010031485A1 (en) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| US20100096600A1 (en) | 2008-10-16 | 2010-04-22 | Novaled Ag | Square Planar Transition Metal Complexes and Organic Semiconductive Materials Using Them as Well as Electronic or Optoelectric Components |
| WO2010054730A1 (en) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organic electroluminescent devices |
| WO2010054729A2 (en) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010054728A1 (en) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2010054731A1 (en) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2010072300A1 (en) | 2008-12-22 | 2010-07-01 | Merck Patent Gmbh | Organic electroluminescent device comprising triazine derivatives |
| WO2010086089A1 (en) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metal complexes |
| WO2010094378A1 (en) | 2009-02-17 | 2010-08-26 | Merck Patent Gmbh | Organic electronic device |
| WO2010099852A1 (en) | 2009-03-02 | 2010-09-10 | Merck Patent Gmbh | Metal complexes having azaborol ligands and electronic device having the same |
| WO2010102709A1 (en) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2010108579A1 (en) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organic electroluminescent device |
| WO2010136109A1 (en) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011000455A1 (en) | 2009-06-30 | 2011-01-06 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2011032626A1 (en) | 2009-09-16 | 2011-03-24 | Merck Patent Gmbh | Metal complexes |
| WO2011042107A2 (en) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011054442A2 (en) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materials for electronic devices |
| WO2011057706A2 (en) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materials for electronic devices |
| WO2011060877A2 (en) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2011060859A1 (en) | 2009-11-17 | 2011-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2011060867A1 (en) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Nitrogen-containing condensed heterocyclic compounds for oleds |
| WO2011066898A1 (en) | 2009-12-05 | 2011-06-09 | Merck Patent Gmbh | Electronic device containing metal complexes |
| WO2011073149A1 (en) | 2009-12-14 | 2011-06-23 | Basf Se | Metal complexes comprising diazabenzimidazol carbene-ligands and the use thereof in oleds |
| US20120187826A1 (en) | 2009-12-21 | 2012-07-26 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element using pyrene derivative |
| WO2011088877A1 (en) | 2010-01-25 | 2011-07-28 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2011116865A1 (en) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2011120709A1 (en) | 2010-03-31 | 2011-10-06 | Osram Opto Semiconductors Gmbh | Dopant for a hole conductor layer for organic semiconductor components, and use thereof |
| WO2011137951A1 (en) | 2010-05-04 | 2011-11-10 | Merck Patent Gmbh | Organic electroluminescence devices |
| WO2011157339A1 (en) | 2010-06-15 | 2011-12-22 | Merck Patent Gmbh | Metal complexes |
| WO2012007086A1 (en) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metal complexes |
| WO2012034627A1 (en) | 2010-09-15 | 2012-03-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2012048781A1 (en) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Triphenylene-based materials for organic electroluminescent devices |
| WO2012048780A1 (en) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2012095143A1 (en) | 2011-01-13 | 2012-07-19 | Merck Patent Gmbh | Compounds for organic electroluminescent devices |
| WO2012143080A2 (en) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2012150001A1 (en) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2013041176A1 (en) | 2011-09-21 | 2013-03-28 | Merck Patent Gmbh | Carbazole derivatives for organic electroluminescence devices |
| WO2013056776A1 (en) | 2011-10-20 | 2013-04-25 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2013083216A1 (en) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro dihydroacridine derivatives and the use thereof as materials for organic electroluminescence devices |
| WO2013120577A1 (en) | 2012-02-14 | 2013-08-22 | Merck Patent Gmbh | Spirobifluorene compounds for organic electroluminescent devices |
| DE102012209523A1 (en) | 2012-06-06 | 2013-12-12 | Osram Opto Semiconductors Gmbh | Main group metal complexes as p-dopants for organic electronic matrix materials |
| WO2013185871A1 (en) | 2012-06-12 | 2013-12-19 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2014008982A1 (en) | 2012-07-13 | 2014-01-16 | Merck Patent Gmbh | Metal complexes |
| WO2014015935A2 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Compounds and organic electronic devices |
| WO2014015938A1 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Derivatives of 2-diarylaminofluorene and organic electronic compounds containing them |
| WO2014015937A1 (en) | 2012-07-23 | 2014-01-30 | Merck Patent Gmbh | Compounds and organic electroluminescent devices |
| WO2014023377A2 (en) | 2012-08-07 | 2014-02-13 | Merck Patent Gmbh | Metal complexes |
| WO2014037077A1 (en) | 2012-09-04 | 2014-03-13 | Merck Patent Gmbh | Connections for electronic devices |
| WO2014072017A1 (en) | 2012-11-12 | 2014-05-15 | Merck Patent Gmbh | Materials for electronic devices |
| WO2014094961A1 (en) | 2012-12-21 | 2014-06-26 | Merck Patent Gmbh | Metal complexes |
| WO2014094960A1 (en) | 2012-12-21 | 2014-06-26 | Merck Patent Gmbh | Metal complexes |
| WO2014106522A1 (en) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015022051A1 (en) | 2013-08-15 | 2015-02-19 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015036074A1 (en) | 2013-09-11 | 2015-03-19 | Merck Patent Gmbh | Metal complexes |
| WO2014111269A2 (en) | 2013-10-14 | 2014-07-24 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015082056A1 (en) | 2013-12-06 | 2015-06-11 | Merck Patent Gmbh | Compounds and organic electronic devices |
| WO2015086108A1 (en) | 2013-12-12 | 2015-06-18 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015104045A1 (en) | 2014-01-13 | 2015-07-16 | Merck Patent Gmbh | Metal complexes |
| WO2015117718A1 (en) | 2014-02-05 | 2015-08-13 | Merck Patent Gmbh | Metal complexes |
| WO2015102118A1 (en) | 2014-02-18 | 2015-07-09 | 学校法人関西学院 | Polycyclic aromatic compound |
| WO2015131976A1 (en) | 2014-03-07 | 2015-09-11 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015158411A1 (en) | 2014-04-14 | 2015-10-22 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015158409A1 (en) | 2014-04-16 | 2015-10-22 | Merck Patent Gmbh | Materials for electronic devices |
| WO2015169412A1 (en) | 2014-05-05 | 2015-11-12 | Merck Patent Gmbh | Materials for organic light emitting devices |
| WO2016015815A1 (en) | 2014-07-28 | 2016-02-04 | Merck Patent Gmbh | Metal complexes |
| WO2016015810A1 (en) | 2014-07-29 | 2016-02-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016023608A1 (en) | 2014-08-13 | 2016-02-18 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20160041014A (en) | 2014-10-06 | 2016-04-15 | 유니버셜 디스플레이 코포레이션 | Organic electroluminescent materials and devices |
| WO2016068162A1 (en) * | 2014-10-29 | 2016-05-06 | 国立大学法人茨城大学 | Polymer having condensed polycyclic aromatic skeleton, and light-emitting element and electrode each manufactured using same |
| WO2016078738A1 (en) | 2014-11-18 | 2016-05-26 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016087017A1 (en) | 2014-12-01 | 2016-06-09 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016102048A1 (en) | 2014-12-22 | 2016-06-30 | Merck Patent Gmbh | Materials for electronic devices |
| WO2016124304A1 (en) | 2015-02-03 | 2016-08-11 | Merck Patent Gmbh | Metal complexes |
| WO2016131521A1 (en) | 2015-02-16 | 2016-08-25 | Merck Patent Gmbh | Spirobifluorene derivative-based materials for electronic devices |
| WO2016150544A1 (en) | 2015-03-25 | 2016-09-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2016152418A1 (en) | 2015-03-25 | 2016-09-29 | 学校法人関西学院 | Polycyclic aromatic compound and light emission layer-forming composition |
| WO2017025165A1 (en) | 2015-08-12 | 2017-02-16 | Merck Patent Gmbh | Materials for electronic devices |
| WO2017028941A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017028940A1 (en) | 2015-08-14 | 2017-02-23 | Merck Patent Gmbh | Phenoxazine derivatives for organic electroluminescent devices |
| WO2017032439A1 (en) | 2015-08-25 | 2017-03-02 | Merck Patent Gmbh | Metal complexes |
| WO2017036574A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | 6,9,15,18-tetrahydro-s-indaceno[1,2-b:5,6-b']difluorene derivatives and use thereof in electronic devices |
| WO2017036573A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Compounds for electronic devices |
| WO2017122988A1 (en) | 2016-01-13 | 2017-07-20 | 덕산네오룩스 주식회사 | Compound for organic electric element, organic electric element using same, and electronic device thereof |
| WO2017148565A1 (en) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materials for organic electroluminescence devices |
| WO2017148564A1 (en) | 2016-03-03 | 2017-09-08 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2018011186A1 (en) | 2016-07-14 | 2018-01-18 | Merck Patent Gmbh | Metal complexes |
| WO2018041769A1 (en) | 2016-08-30 | 2018-03-08 | Merck Patent Gmbh | Binuclear and trinuclear metal complexes composed of two inter-linked tripodal hexadentate ligands for use in electroluminescent devices |
| WO2018095397A1 (en) | 2016-11-23 | 2018-05-31 | 广州华睿光电材料有限公司 | Organic compound containing boron and uses thereof, organic mixture, and organic electronic device |
| WO2018110887A1 (en) | 2016-12-14 | 2018-06-21 | 주식회사 엘지화학 | Heterocyclic compound, and organic light-emitting element comprising same |
| WO2018178001A1 (en) | 2017-03-29 | 2018-10-04 | Merck Patent Gmbh | Metal complexes |
| WO2019004248A1 (en) | 2017-06-30 | 2019-01-03 | 住友化学株式会社 | Macromolecular compound and light-emitting element using same |
| WO2019020538A1 (en) | 2017-07-25 | 2019-01-31 | Merck Patent Gmbh | METALLIC COMPLEXES |
| WO2019115423A1 (en) | 2017-12-13 | 2019-06-20 | Merck Patent Gmbh | Metal complexes |
| WO2019132040A1 (en) | 2017-12-28 | 2019-07-04 | 出光興産株式会社 | Novel compound and organic electroluminescence element |
| WO2019158453A1 (en) | 2018-02-13 | 2019-08-22 | Merck Patent Gmbh | Metal complexes |
| WO2019229011A1 (en) | 2018-05-30 | 2019-12-05 | Merck Patent Gmbh | Composition for organic electronic devices |
| KR101978651B1 (en) | 2018-10-30 | 2019-05-15 | 머티어리얼사이언스 주식회사 | Method for preparing deuterated orgarnic compounds and deuterated orgarnic compounds produced by the same |
| KR20200052820A (en) | 2018-11-07 | 2020-05-15 | 머티어리얼사이언스 주식회사 | An organic compound and an organic light emitting diode |
| US20200161552A1 (en) | 2018-11-21 | 2020-05-21 | Sfc Co., Ltd. | Indolocarbazole derivatives and organic electroluminescent devices using the same |
| WO2020208051A1 (en) | 2019-04-11 | 2020-10-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021089450A1 (en) | 2019-11-04 | 2021-05-14 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021180614A1 (en) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organic electroluminescent apparatus |
| WO2021180625A1 (en) | 2020-03-11 | 2021-09-16 | Merck Patent Gmbh | Organic electroluminescent apparatus |
| KR20230034896A (en) | 2021-09-03 | 2023-03-10 | 삼성에스디아이 주식회사 | Composition for optoelectronic device and organic optoelectronic device and display device |
Non-Patent Citations (5)
| Title |
|---|
| ASIAN JOURNAL OF ORGANIC CHEMISTRY, vol. 6, no. 8, 2017, pages 1063 - 1071 |
| BULLETIN OF THE CHEMICAL SOCIETY OF JAPAN, vol. 94, no. 2, 2021, pages 600 - 605 |
| FUKUMOTO ET AL., MACROMOLECULES, vol. 50, 2017, pages 865 |
| GOTSU ET AL., MOLECULES, vol. 23, 2018, pages 3337 |
| Y. SHIROTA ET AL., CHEM. REV., vol. 107, no. 4, 2007, pages 953 - 1010 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3080229B1 (en) | Materials for electronic devices | |
| EP3423543A1 (en) | Materials for organic electroluminescence devices | |
| EP2705552A1 (en) | Compounds for electronic devices | |
| WO2013087142A1 (en) | Compounds for electronic devices | |
| WO2016045765A1 (en) | Materials for organic electroluminescent devices | |
| WO2017041874A1 (en) | Materials for organic electroluminescent devices | |
| EP4437814A1 (en) | Materials for electronic devices | |
| WO2023052272A1 (en) | Materials for electronic devices | |
| WO2024013004A1 (en) | Materials for electronic devices | |
| EP4631325A1 (en) | Organic electronic device and special materials for organic electronic devices | |
| WO2023052314A1 (en) | Materials for electronic devices | |
| EP4410074A1 (en) | Materials for electronic devices | |
| EP4452909A1 (en) | Process for preparing deuterated organic compounds | |
| EP4192832A1 (en) | Materials for organic electroluminescent devices | |
| EP4244228A1 (en) | Sulfurous compounds for organic electroluminescent devices | |
| WO2024218109A1 (en) | Materials for electronic devices | |
| WO2025132551A1 (en) | Materials for electronic devices | |
| WO2024240725A1 (en) | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazine derivatives for use in organic electroluminescent devices | |
| EP4573098A1 (en) | Materials for organic electroluminescent devices | |
| WO2024133211A1 (en) | Novel materials for organic electroluminescent devices | |
| EP4573099A1 (en) | Materials for organic electroluminescent devices | |
| WO2023152346A1 (en) | Materials for electronic devices | |
| WO2023052275A1 (en) | Materials for electronic devices | |
| EP4619383A1 (en) | Materials for organic electroluminescent devices | |
| WO2025021855A1 (en) | Materials for organic light-emitting devices and organic sensors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 24717739 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |