JP7520870B2 - がんの治療における使用のための、アゼチドベンゾジアゼピン二量体及びこれを含む複合体 - Google Patents
がんの治療における使用のための、アゼチドベンゾジアゼピン二量体及びこれを含む複合体 Download PDFInfo
- Publication number
- JP7520870B2 JP7520870B2 JP2021555569A JP2021555569A JP7520870B2 JP 7520870 B2 JP7520870 B2 JP 7520870B2 JP 2021555569 A JP2021555569 A JP 2021555569A JP 2021555569 A JP2021555569 A JP 2021555569A JP 7520870 B2 JP7520870 B2 JP 7520870B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- compound
- alkyl
- mmol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/542—Carboxylic acids, e.g. a fatty acid or an amino acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/55—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being also a pharmacologically or therapeutically active agent, i.e. the entire conjugate being a codrug, i.e. a dimer, oligomer or polymer of pharmacologically or therapeutically active compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6863—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from stomach or intestines cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Description
(Gregson,S.J.,et al.,Chem.Commun.,1999,797-798.doi:10.1039/A809791G;
Gregson,S.,et al.,J.Med.Chem.,44,737-748(2001);Alley,M.C.,et al.,Cancer Research,64,6700-6706(2004);及びHartley,J.A.,et al.,Cancer Research,64,6693-6699(2004))は、スタンドアロン薬剤、例えば、NCT02034227として臨床検査に関与しており、急性骨髄性白血病及び慢性リンパ性白血病を治療する際のその使用を調査している(https://www.clinicaltrials.gov/ct2/show/NCT02034227を参照)。
及びWO2006/111759に開示されており、このようなPBD化合物の亜硫酸水素塩は、例えば、SG2285(ZC-423):
である。
ならびにその塩及び溶媒和物を提供し、
式中:
R2及びR2’は、Hであり;
R6及びR9は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから独立して選択され;
ここでR及びR’は、任意選択的に置換されているC1-12アルキル、C3-20ヘテロシクリル及びC5-20アリール基から独立して選択され;
(a)R7は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択され;
R7’は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択されるか;又は
(b)R7及びR7’は、一緒になって:(i)nが7~16である-O-(CH2)n-O-;若しくは(ii)mが2~5である-O-(CH2CH2O)m-を形成するか;
のいずれかであり;
R”は、C3-12アルキレン基であり、かかる鎖は、1つ以上のヘテロ原子、例えば、O、S、NRN2(ここで、RN2は、H若しくはC1-4アルキルである)、及び/又は芳香族環、例えば、ベンゼン若しくはピリジンによって中断されていてよく;
Y及びY’は、O、S、又はNHから選択され;
R6’及びR9’は、それぞれ、R6及びR9と同じ基から選択され;
(i-a)R10及びR11は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(i-b)R10はHであり、R11は、OH及びORAから選択され、ここで、RAは、C1-4アルキルであるか;又は
(i-c)R10及びR11は、両方がHである;
のいずれかであり;
(ii-a)R20及びR21は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(ii-b)R20は、Hであり、R21は、OH及びORBから選択され、ここで、RBはC1-4アルキルであるか;又は
(ii-c)R20及びR21は、両方がHである;
のいずれかである。
ならびにその塩及び溶媒和物を含み、
式中:
Y、Y’、R”、R2、R2’、R6、R6’、R7、R7’、R9及びR9’は、本発明の第1の態様に定義されている通りであり;
R11bは、OH、ORAから選択され、ここでRAは、C1-4アルキルであり;
RLは:
(iiia):
(Qは:
であり、QXは、Qが、アミノ酸残基、ジペプチド残基又はトリペプチド残基であるようになっており;
Xは:
であり、a=0~5、b=0~16、c=0又は1、d=0~5であり;
GLは、リガンド単位に接続するためのリンカーである);ならびに
(iiib):
(RL1及びRL2は、H及びメチルから独立して選択され、又は、これらが結合している炭素原子と一緒になって、シクロプロピレン若しくはシクロブチレン基を形成し;
eが0又は1である);
から選択される、細胞結合剤への接続のためのリンカーであり;
(a)R30及びR31は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(b)R30は、Hであり、R31は、OH及びORBから選択され、ここでRBはC1-4アルキルであるか;
(c)R30及びR31は、両方がHであるか;又は
(d)R31は、OH若しくはORBであり、ここでRBは、C1-4アルキルであり、R30は:
(i)
;
(ii)
;
(iii)
、
(RZは:
(z-i)
;
(z-ii)OC(=O)CH3;
(z-iii)NO2;
(z-iv)OMe;
(z-v)グルクロニド;
(z-vi)NH-C(=O)-X1-NHC(=O)X2-NH-C(=O)-RZC、ここで、-C(=O)-X1-NH-及びC(=O)-X2-NH-は、天然アミノ酸残基を表し、RZCは、Me、OMe、CH2CH2OMe、及び(CH2CH2O)2Meから選択される)
から選択される;
のいずれかである。
L-(DL)p (II)
を提供し、
式中、Lは、リガンド単位(すなわち、標的薬剤)であり、DLは、式I’の薬物リンカー単位であり:
式中、R2、R2’、R6、R7、R9、R11b、Y、R”、Y’、R6’、R7’、R9’、R30及びR31は、本発明の第2の態様に定義されている通りであり;
RLLは:
(iiia):
(Q及びXは、第1の態様に定義されている通りであり、GLLは、リガンド単位に接続されているリンカーである);ならびに
(iiib):
(RL1及びRL2は、第1の態様に定義されている通りである);
から選択される、細胞結合剤への接続のためのリンカーであり;
pは、1~20の整数である。
置換基
「任意選択的に置換されている」という句は、本明細書中で使用される場合、非置換であっても置換されていてもよい親基に関する。
飽和単環式炭化水素化合物:
シクロプロパン(C3)、シクロブタン(C4)、シクロペンタン(C5)、シクロヘキサン(C6)、シクロヘプタン(C7)、メチルシクロプロパン(C4)、ジメチルシクロプロパン(C5)、メチルシクロブタン(C5)、ジメチルシクロブタン(C6)、メチルシクロペンタン(C6)、ジメチルシクロペンタン(C7)及びメチルシクロヘキサン(C7)、
不飽和単環式炭化水素化合物:
シクロプロペン(C3)、シクロブテン(C4)、シクロペンテン(C5)、シクロヘキセン(C6)、メチルシクロプロペン(C4)、ジメチルシクロプロペン(C5)、メチルシクロブテン(C5)、ジメチルシクロブテン(C6)、メチルシクロペンテン(C6)、ジメチルシクロペンテン(C7)及びメチルシクロヘキセン(C7)、ならびに
飽和多環式炭化水素化合物:
ノルカラン(C7)、ノルピナン(C7)、ノルボルナン(C7)。
N1:アジリジン(C3)、アゼチジン(C4)、ピロリジン(テトラヒドロピロール)(C5)、ピロリン(例えば、3-ピロリン、2,5-ジヒドロピロール)(C5)、2H-ピロール又は3H-ピロール(イソピロール、イソアゾール)(C5)、ピペリジン(C6)、ジヒドロピリジン(C6)、テトラヒドロピリジン(C6)、アゼピン(C7)、
O1:オキシラン(C3)、オキセタン(C4)、オキソラン(テトラヒドロフラン)(C5)、オキソール(ジヒドロフラン)(C5)、オキサン(テトラヒドロピラン)(C6)、ジヒドロピラン(C6)、ピラン(C6)、オキセピン(C7)、
S1:チイラン(C3)、チエタン(C4)、チオラン(テトラヒドロチオフェン)(C5)、チアン(テトラヒドロチオピラン)(C6)、チエパン(C7)、
O2:ジオキソラン(C5)、ジオキサン(C6)、及びジオキセパン(C7)、
O3:トリオキサン(C6)、
N2:イミダゾリジン(C5)、ピラゾリジン(ジアゾリジン)(C5)、イミダゾリン(C5)、ピラゾリン(ジヒドロピラゾール)(C5)、ピペラジン(C6)、
N1O1:テトラヒドロオキサゾール(C5)、ジヒドロオキサゾール(C5)、テトラヒドロイソオキサゾール(C5)、ジヒドロイソオキサゾール(C5)、モルホリン(C6)、テトラヒドロオキサジン(C6)、ジヒドロオキサジン(C6)、オキサジン(C6)、
N1S1:チアゾリン(C5)、チアゾリジン(C5)、チオモルホリン(C6)、
N2O1:オキサジアジン(C6)、
O1S1:オキサチオール(C5)及びオキサチアン(チオキサン)(C6)、ならびに、
N1O1S1:オキサチアジン(C6)。
N1:ピロール(アゾール)(C5)、ピリジン(アジン)(C6)、
O1:フラン(オキソール)(C5)、
S1:チオフェン(チオール)(C5)、
N1O1:オキサゾール(C5)、イソオキサゾール(C5)、イソキサジン(C6)、
N2O1:オキサジアゾール(フラザン)(C5)、
N3O1:オキサトリアゾール(C5)、
N1S1:チアゾール(C5)、イソチアゾール(C5)、
N2:イミダゾール(1,3-ジアゾール)(C5)、ピラゾール(1,2-ジアゾール)(C5)、ピリダジン(1,2-ジアジン)(C6)、ピリミジン(1,3-ジアジン)(C6)(例えば、シトシン、チミン、ウラシル)、ピラジン(1,4-ジアジン)(C6)、
N3:トリアゾール(C5)、トリアジン(C6)、及び、
N4:テトラゾール(C5)。
ベンゾフラン(O1)、イソベンゾフラン(O1)、インドール(N1)、イソインドール(N1)、インドリジン(N1)、インドリン(N1)、イソインドリン(N1)、プリン(N4)(例えば、アデニン、グアニン)、ベンズイミダゾール(N2)、インダゾール(N2)、ベンズオキサゾール(N1O1)、ベンズイソオキサゾール(N1O1)、ベンゾジオキソール(O2)、ベンゾフラザン(N2O1)、ベンゾトリアゾール(N3)、ベンゾチオフラン(S1)、ベンゾチアゾール(N1S1)、ベンゾチアジアゾール(N2S)に由来する(2つの縮合環を含む)C9、
クロメン(O1)、イソクロメン(O1)、クロマン(O1)、イソクロマン(O1)、ベンゾジオキサン(O2)、キノリン(N1)、イソキノリン(N1)、キノリジン(N1)、ベンゾキサジン(N1O1)、ベンゾジアジン(N2)、ピリドピリジン(N2)、キノキサリン(N2)、キナゾリン(N2)、シンノリン(N2)、フタラジン(N2)、ナフチリジン(N2)、プテリジン(N4)に由来する(2つの縮合環を含む)C10、
ベンゾジアゼピン(N2)に由来する(2つの縮合環を含む)C11、
カルバゾール(N1)、ジベンゾフラン(O1)、ジベンゾチオフェン(S1)、カルボリン(N2)、ペリミジン(N2)、ピリドインドール(N2)に由来する(3つの縮合環を含む)C13、ならびに、
アクリジン(N1)、キサンテン(O1)、チオキサンテン(S1)、オキサントレン(O2)、フェノキサチイン(O1S1)、フェナジン(N2)、フェノキサジン(N1O1)、フェノチアジン(N1S1)、チアントレン(S2)、フェナントリジン(N1)、フェナントロリン(N2)、フェナジン(N2)に由来する(3つの縮合環を含む)C14
が挙げられるが、これらに限定されない。
スクシンイミジル マレイミジル フタルイミジル
におけるように、一緒になって環式構造を形成していてよい。
C3-12アルキレン:「C3-12アルキレン」という用語は、本明細書中で使用される場合、脂肪族であっても脂環式であってもよく、また、飽和、部分不飽和、又は完全不飽和であってよい、3~12個の炭素原子(他に特定されない限り)を有する炭化水素化合物の2つの水素原子であって、両方が同じ炭素原子からであるか、2つの異なる炭素原子のそれぞれからのものであるかのいずれかである当該2つの水素原子を除去することによって得られる二座部分に関する。ゆえに、「アルキレン」という用語には、以下に考察されている、サブクラスのアルケニレン、アルキニレン、シクロアルキレンなどが含まれる。
は、C5基である。
上付きの標識C(=O)及びNHは、原子が結合している基を示す。例えば、NH基は、カルボニル(示されている部分の一部ではない)に結合しているとして示され、当該カルボニルは、NH基(示されている部分の一部ではない)に結合しているとして示されている。
リガンド単位は、任意の種類であってよく、標的分子に特異的に結合するタンパク質、ポリペプチド、ペプチド及び非ペプチド性剤を挙げることができる。いくつかの実施形態において、リガンド単位は、タンパク質、ポリペプチド又はペプチドであってよい。いくつかの実施形態において、リガンド単位は、環式ポリペプチドであってよい。これらのリガンド単位は、抗体、若しくは少なくとも1つの標的分子-結合部位を含有する抗体の断片、リンホカイン、ホルモン、増殖因子、又は標的に特異的に結合し得る任意の他の細胞結合分子若しくは物質を含むことができる。
細胞結合剤は、任意の種類のものが可能であり、ペプチド及び非ペプチドを挙げることができる。細胞結合剤として、少なくとも1つの結合部位を有する抗体又は抗体断片、リンホカイン、ホルモン、ホルモン模倣物、ビタミン、増殖因子、栄養輸送分子、又は任意の他の細胞結合分子若しくは物質を挙げることができる。
1つの実施形態において、細胞結合剤は、4~30、好ましくは6~20の、連続アミノ酸残基を含む直鎖又は環状ペプチドである。この実施形態において、1つの細胞結合剤が1つの単量体又は二量体アゼチドベンゾジアゼピン化合物と連結されていることが好ましい。
「抗体」という用語は、本明細書中、最も広義の意味で用いられ、具体的には、モノクローナル抗体、ポリクローナル抗体、二量体、多量体、多特異性抗体(例えば、二特異性抗体)、多価抗体及び抗体断片を包含するが、ただし、それらが所望の生物活性を示す限りにおいてである(Miller et al(2003)Jour.of Immunology 170:4854-4861)。抗体は、マウス抗体、ヒト抗体、ヒト化抗体、キメラ抗体、又は他の種由来抗体が可能である。抗体とは、免疫系により産生される、特定の抗原を認識してそれに結合することができるタンパク質である。(Janeway,C.,Travers,P.,Walport,M.,Shlomchik(2001)Immuno Biology,5th Ed.,Garland Publishing,New York)。標的抗原は、一般に、複数の抗体のCDRで認識される多数の結合部位(エピトープとも呼ばれる)を有する。異なるエピトープに特異的に結合する抗体は、それぞれ異なる構造を有する。したがって、1つの抗原は、1つより多い対応する抗体を有する可能性がある。抗体として、全長免疫グロブリン分子又は全長免疫グロブリン分子の免疫学的活性部分、すなわち、注目している標的の抗原に免疫学的に結合する抗原結合部位又はその一部分を有する分子が挙げられ、そのような標的として、癌細胞又は自己免疫疾患に関連した自己免疫抗体を産生する細胞が挙げられるが、これらに限定されない。免疫グロブリンは、任意の型(例えばIgG、IgE、IgM、IgD、及びIgA)、クラス(例えばIgG1、IgG2、IgG3、IgG4、IgA1、及びIgA2)又はサブクラスの免疫グロブリン分子が可能である。免疫グロブリンは、任意の種由来のものが可能であり、ヒト、マウス、又はウサギ起原が挙げられる。
(2)E16(LAT1、SLC7A5)
(3)STEAP1(前立腺の6回膜貫通型上皮抗原)
(4)0772P(CA125、MUC16)
(5)MPF(MPF、MSLN、SMR、巨核球増強因子、メソテリン)
(6)Napi3b(NAPI-3B、NPTIIb、SLC34A2、溶質輸送体ファミリー34(リン酸ナトリウム)、
メンバー2、II型ナトリウム依存性リン酸輸送体3b)
(7)Sema 5b(FLJ10372、KIAA1445、Mm.42015、SEMA5B、SEMAG、セマフォリン5b Hlog、25semaドメイン、7回トロンボスポンジン反復配列(seven thrombospondin repeats)(1型及び1型様)、膜貫通ドメイン(TM)、及び短細胞質ドメイン、(セマフォリン)5B)
(8)PSCA hlg(2700050C12Rik、C530008O16Rik、RIKEN cDNA 2700050C12、RIKEN cDNA
2700050C12遺伝子)
(9)ETBR(エンドセリンB型受容体)
(10)MSG783(RNF124、仮想タンパク質FLJ20315)
(11)STEAP2(HGNC_8639、IPCA-1、PCANAP1、STAMP1、STEAP2、STMP、前立腺癌関連遺伝子1、前立腺癌関連タンパク質1、前立腺の6回膜貫通型上皮抗原2、6回膜貫通型前立腺タンパク質)
(12)TrpM4(BR22450、FLJ20041、TRPM4、TRPM4B、一過性受容器電位カチオン5チャンネル、サブファミリーM、メンバー4)
(13)CRIPTO(CR、CR1、CRGF、CRIPTO、TDGF1、奇形腫由来増殖因子)
(14)CD21(CR2(補体受容体2)又はC3DR(C3d/エプスタイン・バーウイルス受容体)又はHs.73792)
(15)CD79b(CD79B、CD79β、IGb(免疫グロブリン関連β)、B29)
(16)FcRH2(IFGP4、IRTA4、SPAP1A(SH2ドメイン含有ホスファターゼアンカータンパク質 1a)、SPAP1B、SPAP1C)
(17)HER2(ErbB2)
(18)NCA(CEACAM6)
(19)MDP(DPEP1)
(20)IL20R-α(IL20Ra、ZCYTOR7)
(21)ブレビカン(BCAN、BEHAB)
(22)EphB2R(DRT、ERK、Hek5、EPHT3、Tyro5)
(23)ASLG659(B7h)
(24)PSCA(前立腺幹細胞抗原前駆体)
(25)GEDA
(26)BAFF-R(B細胞活性化因子受容体、BLyS受容体3、BR3)
(27)CD22(B細胞受容体CD22-Bアイソフォーム、BL-CAM、Lyb-8、Lyb8、SIGLEC-2、FLJ22814)
(27a)CD22(CD22分子)
(28)CD79a(CD79A、CD79α)、免疫グロブリン関連α、B細胞特異的タンパク質(Igβ(CD79B)と共有結合で相互作用し、表面でIgM分子と複合体を形成し、B細胞分化に関与するシグナルを伝達する)、pI:4.84、MW:25028、TM:2[P]、遺伝子染色体:19q13.2)
(29)CXCR5(バーキットリンパ腫受容体1、CXCL13ケモカインにより活性化されるGタンパク質共役受容体、このGタンパク質共役受容体は、リンパ球遊走及び体液性防御において機能し、HIV-2感染、ならびに恐らくはAIDS、リンパ腫、骨髄腫、及び白血病の発症において役割を果たす)。372aa、pl:8.54、MW:41959、TM:7[P]、遺伝子染色体:11q23.3、
(30)HLA-DOB(ペプチドに結合して、そのペプチドをCD4+Tリンパ球に提供するMHCクラスII分子のβサブユニット(Ia抗原))、273aa、pI:6.56、MW:30820、TM:1[P]、遺伝子染色体:6p21.3)
(31)P2X5(プリン作動性受容体P2Xリガンド開口型イオンチャンネル5、細胞外ATPにより開口するイオンチャンネルであり、このチャンネルは、シナプス伝達及び神経新生に関与している可能性があり、この不全が突発性排尿筋不安定という病態生理の一因である可能性がある)、422aa)、pI:7.63、MW:47206、TM:1[P]、遺伝子染色体:17p13.3)。
(32)CD72(B細胞分化抗原CD72、Lyb-2);359aa、pI:8.66、MW:40225、TM:15[P]、遺伝子染色体:9p13.3)。
(33)LY64(リンパ球抗原64(RP105)、ロイシンに富む反復配列(LRR)ファミリーのI型膜タンパク質であり、B細胞活性化及びアポトーシスを制御し、この機能喪失は、全身性エリトマトーデスの患者で疾患活性の上昇を伴う)。661aa、pI:6.20、MW:74147、TM:1[P]、遺伝子染色体:5q12)。
(34)FcRH1(Fc受容体様タンパク質1、免疫グロブリンFcドメインの推定受容体であり、C2型Ig様ドメイン及びITAMドメインを含有し、Bリンパ球分化において役割を果たす可能性がある);429aa、pI:5.28、MW:46925 TM:1[P]、遺伝子染色体:1q21-1q22)
(35)IRTA2(免疫グロブリンスーパーファミリー受容体転座関連2、B細胞発達及びリンパ腫形成で役割を担っている可能性がある推定免疫受容体である。転位置による遺伝子の調節解除が、ある種のB細胞悪性腫瘍で生じる)。977aa、pI:6.88、MW:106468、TM:1[P]遺伝子染色体:1q21)
(36)TENB2(TMEFF2、トモレギュリン(tomoregulin)、TPEF、HPP1、TR、推定膜貫通プロテオグリカン、増殖因子及びフォリスタチンのEGF/ヘレグリンファミリーと関連)。374aa)
(37)PSMA-FOLH1(葉酸ヒドロラーゼ(前立腺特異的膜抗原)1)
(38)SST(ソマトスタチン受容体;注、5つのサブタイプが存在する)
(38.1)SSTR2(ソマトスタチン受容体2)
(38.2)SSTR5(ソマトスタチン受容体5)
(38.3)SSTR1
(38.4)SSTR3
(38.5)SSTR4
AvB6-両方のサブユニット(39+40)
(39)ITGAV(インテグリン、αV)
(40)ITGB6(インテグリン、β6)
(41)CEACAM5(癌胎児抗原関連細胞接着分子5)
(42)MET(met癌原遺伝子;肝細胞増殖因子受容体)
(43)MUC1(ムチン1、細胞表面関連)
(44)CA9(炭酸脱水酵素IX)
(45)EGFRvIII(上皮増殖因子受容体(EGFR)、転写物変異型3、
(46)CD33(CD33分子)
(47)CD19(CD19分子)
(48)IL2RA(インターロイキン2受容体、α);NCBI参照配列:NM_000417.2);
(49)AXL(AXL受容体チロシンキナーゼ)
(50)CD30-TNFRSF8(腫瘍壊死因子受容体スーパーファミリー、メンバー8)
(51)BCMA(B細胞成熟抗原)-TNFRSF17(腫瘍壊死因子受容体スーパーファミリー、メンバー17)
(52)CT Ags-CTA(癌精巣抗原)
(53)CD174(ルイス式Y)-FUT3(フコシルトランスフェラーゼ3(ガラクトシド3(4)-L-フコシルトランスフェラーゼ、ルイス式血液型群)
(54)CLEC14A(C型レクチンドメインファミリー14、メンバーA;Genbank受入番号NM175060)
(55)GRP78-HSPA5(熱ショック70kDaタンパク質5(グルコース制御タンパク質、78kDa)
(56)CD70(CD70分子)L08096
(57)幹細胞特異的抗原。例えば:
・5T4(以下のエントリー(63)を参照)
・CD25(上記エントリー(48)を参照)
・CD32
・LGR5/GPR49
・プロミニン(Prominin)/CD133
(58)ASG-5
(59)ENPP3(エクトヌクレオチドピロホスファターゼ/ホスホジエステラーゼ3)
(60)PRR4(プロリンリッチ4(涙腺))
(61)GCC-GUCY2C(グアニル酸シクラーゼ2C(熱安定性エンテロトキシン受容体)
(62)Liv-1-SLC39A6(溶質担体ファミリー39(亜鉛輸送体)、メンバー6)
(63)5T4、トロホブラスト糖タンパク質、TPBG-TPBG(トロホブラスト糖タンパク質)
(64)CD56-NCMA1(神経細胞接着分子1)
(65)CanAg(腫瘍関連抗原CA242)
(66)FOLR1(葉酸受容体1)
(67)GPNMB(糖タンパク質(膜貫通型)nmb)
(68)TIM-1-HAVCR1(A型肝炎ウイルス細胞受容体1)
(69)RG-1/前立腺腫瘍標的ミンディン-ミンディン/RG-1
(70)B7-H4-VTCN1(V-setドメイン含有T細胞活性化インヒビター1
(71)PTK7(PTK7タンパク質チロシンキナーゼ7)
(72)CD37(CD37分子)
(73)CD138-SDC1(シンデカン1)
(74)CD74(CD74分子、主要組織適合遺伝子複合体、クラスIIインバリアント鎖)
(75)クローディン-CL(クローディン)
(76)EGFR(上皮増殖因子受容体)
(77)Her3(ErbB3)-ERBB3(v-erb-b2赤芽球性白血病ウイルス性癌遺伝子ホモログ3(トリ))
(78)RON-MST1R(マクロファージ刺激1受容体(c-met関連チロシンキナーゼ))
(79)EPHA2(EPH受容体A2)
(80)CD20-MS4A1(膜貫通の4つのドメイン(membrane-spanning 4-domains)、サブファミリーA、メンバー1)
(81)テネイシンC-TNC(テネイシンC)
(82)FAP(線維芽細胞活性化タンパク質、α)
(83)DKK-1(Dickkopf1ホモログ(アフリカツメガエル))
(84)CD52(CD52分子)
(85)CS1-SLAMF7(SLAMファミリーメンバー7)
(86)エンドグリン-ENG(エンドグリン)
(87)アネキシンA1-ANXA1(アネキシンA1)
(88)V-CAM(CD106)-VCAM1(血管細胞接着分子1)
(89)ASCT2(SLC1A5としても知られているASC輸送体2)である。
ASCT2抗体は、WO2018/089393に記載されており、WO2018/089393は、本明細書に援用される。
本発明の化合物は、治療方法で使用することができる。治療方法も提供され、本方法は、治療を必要としている治療対象に、治療上有効量の式IIの複合体を投与することを含む。「治療上有効量」という用語は、患者で有益性を示すのに十分な量である。そのような有益性とは、少なくとも1種の症状の少なくとも改善であってもよい。実際に投与される量ならびに投与の速度及び時間経過は、治療されようとしているものの性質及び重篤度に依存するだろう。治療の処方(例えば、投薬量の決定)は、一般医及び他の医師の責任能力の範囲内である。
薬物積載量(p)は、細胞結合剤(例えば抗体)あたりのABD薬物の平均数である。本発明の化合物がシステインと結合している場合、薬物積載量は、細胞結合剤あたり1~8つの薬物(D)の範囲が可能である、すなわち1、2、3、4、5、6、7、及び8つの薬物部分が細胞結合剤と共有結合している。複合体の組成として、1~8つの範囲の薬物と複合している細胞結合剤(例えば抗体)を集めたものが含まれる。本発明の化合物がリシンと結合している場合、薬物積載量は、細胞結合剤あたり1~80つの薬物(D)の範囲が可能であるが、上限を40、20、10、又は8とするのが好適であり得る。複合体の組成として、1~80、1~40、1~20、1~10、又は1~8の範囲の薬物と複合している細胞結合剤(例えば抗体)を集めたものが含まれる。
多数の好適なN-ProtN、O-ProtO及びY-ProtY保護基が、本明細書に援用される、Greene、T.W.and Wuts,G.M.,Protective Groups in Organic Synthesis,3rd Edition、John Wiley & Sons、Inc.,1999に記載されている。
本発明の第1の態様の化合物、特に、式IVの化合物の合成における可能性のあるステップをスキーム1に示す。これは、N10保護ABD二量体(d1A)から開始する。
スキーム1
スキーム2
スキーム3
スキーム4
スキーム5
本発明の第2の態様の化合物、特に、式Iの化合物の合成における可能性のあるステップをスキーム6に示す。これは、2つの環化されたABD単量体:ProtN保護されたN10位を有するm2A及びRL付加されたN10-窒素を有するm6A;によって開始される。
スキーム6
スキーム7
スキーム8
スキーム9
本発明の第3の態様の複合体、特に、式IIの構成薬物リンカー単位(DL)の合成における可能性のあるステップは、リガンド単位へのリンカーの接続により、(式Iの化合物のように)基RLを(式I’の化合物のように)基RLLに変換することを含む。
本発明の第1、第2及び第3の態様のいくつかの実施形態において、R7及びR7’置換基は、一緒になって、基:(i)-O-(CH2)n-O-、ここで、nは、7~16である;又は(ii)-O-(CH2CH2O)m-、ここで、mは、2~5である;を形成して、大環状ABD二量体を与えることができる。
スキーム10
N10-C11基が-NH-CH2-(すなわち第2級アミン)である化合物は、上記の手順の変形例によって合成され得る。特に、化合物3B*の還元アミノ化は、さらなるステップにおける使用のためのm2A又はd1Aの変性されたバージョンを生じ得る:
複合体は、先に記載されているように調製され得る。抗体は、Doronina et al.,Nature Biotechnology,2003,21,778-784)に記載されているように薬物リンカー化合物に複合体化され得る。簡潔には、pH7.4で50mMのホウ酸ナトリウムを含有するPBSにおける抗体(4~5mg/mL)は、37℃でトリス(カルボキシエチル)ホスフィン塩酸塩(TCEP)によって還元される。鎖間ジスルフィドを還元する反応の進行は、5,5’-ジチオビス(2-ニトロ安息香酸)との反応によってモニタリングされ、所望のチオール/mAbレベルが達成されるまで続行される。還元された抗体は、次いで、0℃まで冷却され、抗体チオールあたり1.5当量のマレイミド薬物-リンカーによってアルキル化される。1時間後、反応は、5当量のN-アセチルシステインの添加によってクエンチされる。クエンチされた薬物-リンカーは、PD-10カラム上でのゲル濾過によって除去される。ADCは、次いで、0.22μmシリンジフィルタを通して滅菌される。タンパク質濃度は、それぞれ280nm及び329nmでのスペクトル分析により、280nmでの薬物吸光度の寄与を補正して決定され得る。サイズ排除クロマトグラフィーは、抗体凝集の程度を決定するのに使用され得、RP-HPLCは、残存するNACクエンチ薬物-リンカーのレベルを決定するのに使用され得る。
以下の優先事項は、上述の本発明の全ての態様に適用されてよく、又は、単一の態様に関していてよい。優先事項は、任意の組み合わせで一つに組み合わされてよい。
いくつかの実施形態において、Y及びY’は、両方がOである。
式中、rは、1又は2である。
いくつかの実施形態において、R9は、Hである。
いくつかの実施形態において、R10及びR11は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成する。これらの実施形態のいくつかにおいて、R20及びR21は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成する。これらの実施形態の他のものにおいて、R20及びR21は、両方がHである。
いくつかの実施形態において、R30及びR31は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成する。
-Phe-Lys-,
-Val-Ala-,
-Val-Lys-,
-Ala-Lys-,
-Val-Cit-,
-Phe-Cit-,
-Leu-Cit-,
-Ile-Cit-,
-Phe-Arg-、
-Trp-Cit-
ここで、Citはシトルリンである。
-Phe-Lys-,
-Val-Ala-,
-Val-Lys-,
-Ala-Lys-,
-Val-Cit-。
Arg:Z、Mtr、Tos;
Asn:Trt、Xan;
Asp:Bzl、t-Bu;
Cys:Acm、Bzl、Bzl-OMe、Bzl-Me、Trt;
Glu:Bzl、t-Bu;
Gln:Trt、Xan;
His:Boc、Dnp、Tos、Trt;
Lys:Boc、Z-Cl、Fmoc、Z、Alloc;
Ser:Bzl、TBDMS、TBDPS;
Thr:Bz;
Trp:Boc;
Tyr:Bzl、Z、Z-Br。
。
及び
。
R11b(式I及びI*)
本発明の第1の態様のいくつかの実施形態において、式IVa、IVb又はIVcのものである:
式中、R1aは、メチル及びベンジルから選択され;
R10、R11、R20及びR21は、上記に定義されている通りである。
式中、R1aは、メチル及びベンジルから選択され;
R30、R31、RL及びR11bは、上記に定義されている通りである。
いくつかの実施形態において、RLは、式IIIaのものである。
GLは、以下から選択され得、式中、Arは、C5-6アリーレン基、例えば、フェニレンを表す。
GLLは、以下から選択され得、式中、Arは、C5-6アリーレン基、例えば、フェニレンを表す。
Xは:
であり、
式中、a=0~5、b=0~16、c=0又は1、d=0~5である。
1つの実施形態において、Qは、アミノ酸残基である。アミノ酸は、天然アミノ酸又は非天然アミノ酸であってよい。
CO-Phe-Lys-NH,
CO-Val-Ala-NH,
CO-Val-Lys-NH,
CO-Ala-Lys-NH,
CO-Val-Cit-NH,
CO-Phe-Cit-NH,
CO-Leu-Cit-NH,
CO-Ile-Cit-NH,
CO-Phe-Arg-NH、及び
CO-Trp-Cit-NH;
から選択され、
Citはシトルリンである。
CO-Phe-Lys-NH,
CO-Val-Ala-NH,
CO-Val-Lys-NH,
CO-Ala-Lys-NH,
CO-Val-Cit-NH
から選択される。
CO-Gly-Gly-NH,
CO-Pro-Pro-NH、及び
CO-Val-Glu-NH
が挙げられる。
CO-Glu-Val-Ala-NH
CO-Glu-Val-Cit-NH
CO-αGlu-Val-Ala-NH
CO-αGlu-Val-Cit-NH
である。
式中、Qは、以下:
(a)-CH2-;
(b)-C3H6-;及び
(c)
から選択される。
手動フラッシュクロマトグラフィーを、Merck Kieselgel 60 F254シリカゲルを使用して実施した。抽出及びクロマトグラフィーの溶媒は、Fisher Scientific,U.Kから購入し、さらに精製することなく使用した。全ての化学薬品をAldrich、Lancaster又はBDHから購入した。
逆相超高速液体クロマトグラフィー(UFLC)を、Phenomenex(登録商標)Gemini NX 5μC18カラム(50℃)寸法:150×21.2mmを使用したShimazdzu Prominence(登録商標)機において行った。使用した溶出液は、溶媒A(0.1%ギ酸を含むH2O)及び溶媒B(0.1%ギ酸を含むCH3CN)であった。全てのUFLC実験を以下の勾配条件で実施した:初期組成の13%Bを15分の期間をかけて60%Bに増加させ、次いで2分間かけて100%Bに増加させた。組成を100%Bで1分間保持し、次いで0.1分で13%Bに戻し、そこで1.9分間保持した。勾配実行の合計継続時間は20.0分であった。流速は20.0mL/分であり、検出は254及び280nmであった。
a)1-((ベンジルオキシ)カルボニル)アゼチジン-2-カルボン酸(2)
(2S)-アゼチジン-2-カルボン酸1(3g、29.674mmol)及び重炭酸ナトリウム(6.3g、75mmol)をH2O(25mL、1387.75mmol)に可溶化し、THF(25mL、307mmol、100質量%)中のN-(ベンジルオキシカルボニル)スクシンイミド(8.5g、34mmol)を滴加した。室温で12時間撹拌後、2つの相を分離させた。水相をジエチルエーテル(50mL)で洗浄し、氷浴において冷却し、次いで、濃HClによってpH=2まで酸性化した。水相を酢酸エチル(2×50mL)で抽出し、合わせた有機抽出物を乾燥し(MgSO4)、過剰な溶媒を真空蒸発させて、粗生成物を透明な油として得た。粗製材料を精製することなく次のステップにおいて使用した。LCMS 3分:ES+=1.34分、m/z258.2[M+Na]+。
乾燥丸底フラスコにおいて、(2S)-1-ベンジルオキシカルボニルアゼチジン-2-カルボン酸2(6.98g、29.7mmol)をMeOH(65mL)に可溶化し、硫酸(3mL)を添加した。混合物を加熱還流し、一晩中撹拌したままにした。混合物を室温まで冷却したままにして、Net3(pH=7まで)によってクエンチした後、1時間撹拌した。メタノールを真空中で除去した。残渣をEtOAc中で採取し、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過した。有機物を真空中で除去して、粗生成物3(8.004g、32.11mmol)を透明な油として得た。LCMS 3分:ES+=1.53分、m/zイオン化なし
O1-ベンジル O2-メチル (2S)-アゼチジン-1,2-ジカルボキシラート3(7.6g、30mMol)をTHF(75mL、922mmol)に可溶化し、0℃に冷却し、LiBH4(1g、45mMol,)を添加した。混合物を室温まで加温させ、さらなる時間撹拌し、この時点で、反応が完了した。反応混合物を0℃に冷却した後、H2O及び1M HClでクエンチした。揮発性物質を真空中で除去した。残渣をEtOAc中で採取し、ブライン(2×50mL)で洗浄し、MgSO4で乾燥し、濾過し、溶媒を減圧下で回転蒸発によって除去した。シリカゲルカラムクロマトグラフィーによる精製により(Hex/EtOAc、100%から1:2)、生成物4を透明な油として得た(4.076g、3ステップで60%の収率)。LCMS 3分:ES+=1.36分、m/z222.3[M+H]+。
ベンジル (2S)-2-(ヒドロキシメチル)アゼチジン-1-カルボキシラート4(4.0766g、18.425mmol)を乾燥CH2Cl2(20mL、312.0mmol)に可溶化し、混合物を0℃に冷却した後、イミダゾール(2.508g、36.84mmol)及びTBS-Cl(4.16g、27.6mmol)を添加した。混合物を室温まで加温させ、撹拌したままにした。LCMSは、反応が5分以内に完了したことを示す。有機物を飽和NH4Cl、水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、揮発性物質を真空中で除去した。シリカゲルカラムクロマトグラフィーによる精製により(Hex/EtOAc、100%から9:1)、生成物5を得た(6.90g、完全に乾燥していない、定量)。LCMS 3分:ES+=2.15分、m/z336.9[M+H]+。
パラジウム担持炭素(10%)(100mg、0.93mMol)を、EtOAc(5mL)で滴下して処理し、得られたスラリーを、Parr水素化ボトルにおいて、5(6.9027g、20.57mmol)をEtOH(100mL)に懸濁させた懸濁液に室温で添加した。反応混合物を20psiでH2ガスに供し、次いで、ボトルを(3回繰り返して)真空引きした。次いでボトルの蓋をして38psiのH2とし、1時間振とうした。この時間の間、圧力を約30psiに降下させ、ボトルの蓋をして40psiまで戻し、さらなる時間振とうした。さらなる圧力減少が観察されず、反応が完了したようであった。このことをLC-MSによって確認した。混合物を、セライトを通して濾過し、濾液を真空蒸発させ、粗生成物6を褐色油として得た(3.761g、90%の収率)。LCMS 3分:ES+=1.70分、m/zイオン化なし。
DCC(3.8g、18mmol)を、7(3.9g、7.9mmol)及びHOBt(2.3g、17mMol)をCH2Cl2(200mL)に溶解させた溶液に0℃で添加した。冷浴を除去し、反応を室温で30分間進行させ、このとき、6(3.65g、18mmol)及びトリエチルアミン(3.2mL、23mmol)をCH2Cl2(200mL)に溶解させた溶液を、アルゴン下、-10℃で迅速に添加した。反応混合物を室温で撹拌させ、LC/MSによってモニタリングした。2分後、反応が完了した。固体をセライト上での濾過によって除去し、有機相を、低温の水性0.1M HClによって、pHが2と測定されるまで洗浄した。有機相を次いで水、続いて、飽和水性重炭酸ナトリウム、ブラインで洗浄し、MgSO4で乾燥し、濾過し、急速減圧した。シリカゲルカラムクロマトグラフィーによる精製により(Hex/EtOAc/CH2Cl2、100%から1:2:1)、生成物8を得た(5.9g、87%の収率)。生成物は、いくらかのモノカップリング生成物(不純物はクロマトグラフィーにて分離していない)によって汚染されている。LCMS 3分:ES+=2.35分、m/z862.2[M+H]+。
亜鉛(4.65g、71.1mmol)を、8(2.45g、2.85mmol)をMeOH/H2O/ギ酸の90:5:5(66mL)の混合物に溶解させた溶液にゆっくり添加した。生じた発熱を、氷浴を使用して制御し、反応混合物の温度を40℃未満に維持した。完了の際、固体をセライト上での濾過によって除去し、有機相を水及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。粗製材料9(2.28g、定量)をそのまま次のステップにおいて使用した。LCMS 3分:ES+=2.32分、m/z802.3[M+H]+。
化合物9(2.23g、2.78mmol)をアルゴン雰囲気下CH2Cl2(50mL)に可溶化した。混合物を-78℃に冷却した後、ピリジン(0.99mL、12.3mmol)及びクロロギ酸アリル(0.738mL、2.49mmol)を添加した。反応を-78℃において10分間撹拌したままにした後、室温まで加温させた。15分後、反応が完了した。有機物を飽和CuSO4、H2O、ブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。粗生成物10(1.47g、1.52mMol、定量)をそのまま次のステップにおいて使用した。LCMS 3分:ES+=2.53分、m/z970.3[M+H]+。
化合物11(850mg、1.14mMol)をCH2Cl2(60mL)に可溶化した。1-ヒドロキシ-2,2,6,6-テトラメチル-ピペリジン;1-メチルイミダゾール;2-(2-ピリジル)ピリジン(0.7mL、1140mmol、0.2mMl/L)及びテトラキスアセトニトリル銅(I)トリフラート(55mg、0.145mMol)を順次添加し、混合物を、空気を圧入した2バルーンで35℃にて撹拌した。反応を一晩中撹拌したままにした後、ロータリーエバポレーターによって真空乾固した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から95:5)、生成物12を得た(346g、0.47mMol、41%の収率)。LCMS 3分:ES+=1.48分、m/z737.9[M+H]+。
化合物12(335mg、0.45mmol)を、アルゴン下、フラスコにおいて、CH2Cl2(20mL)に可溶化した。ピロリジン(650μL、7.8mmol)及びPd(PPh3)4(50mg、0.004mMol)を続いて添加し、完了するまで混合物を室温で撹拌したままにした。有機物を飽和NH4Cl、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。Isoleraクロマトグラフィーによる精製(CH2Cl2/(CH2Cl2+10%MeOH)92:7から10:90。生成物を含有する2つのフラクションを単離したが、不十分な純度であった。フラクションを合わせ、手動クロマトグラフィーによって再精製し、純粋な生成物Ex1を単離した(146mg、0.27mMol、24%の収率)。LCMS 3分:ES+=1.32分、m/z533.8[M+H]+。LCMS 15分:ES+=4.83分、m/z533.9[M+H]+。
a)((S)-(2-(((tert-ブチルジメチルシリル)オキシ)メチル)アゼチジン-1-イル)(5-メトキシ-2-ニトロ-4-((トリイソプロピルシリル)オキシ)フェニル)メタノン(13)
DCC(4.021g、19.49mmol)を、5-メトキシ-2-ニトロ-4-トリイソプロピルシリルオキシ-安息香酸13(6g、16.24mmol)及びHOPO(1.984g、17.86mMol)をCH2Cl2(100mL)に溶解させた溶液に0℃で添加した。冷浴を除去し、反応を室温で30分間進行させ、このとき、[(2S)-アゼチジン-2-イル]メトキシ-tert-ブチル-ジメチル-シラン6(3.761g、18.68mmol)及びトリエチルアミン(3.39mL、33.5mmol)をCH2Cl2(100mL)に溶解させた溶液を、アルゴン下、-10℃で迅速に添加した。反応混合物を室温で撹拌させ、LC/MSによってモニタリングした。2分後、反応が完了した。固体をセライト上での濾過によって除去し、有機相を、低温の水性0.1M HClによって、pHが2と測定されるまで洗浄した。有機相を次いで水、続いて飽和水性重炭酸ナトリウム、ブラインで洗浄し、MgSO4で乾燥し、急速減圧した。シリカゲルカラムクロマトグラフィーによる精製により(Hex/EtOAc、100%から1:1)、生成物14を得た(8.6737g、96.63%の収率)。LCMS 3分:ES+=2.44分、m/z554.2[M+H]+。
亜鉛(10g、152.9mMol)を、14(8.6737g、15.69mMol)をMeOH/H2O/ギ酸の90:5:5の混合物(200mL)に溶解させた溶液にゆっくり添加した。生じた発熱を、氷浴を使用して制御し、反応混合物の温度を40℃未満に維持した。完了の際、固体をセライト上での濾過によって除去し、有機相を水及びブラインで洗浄した後、MgSO4で乾燥し、揮発性物質を減圧下で除去した。粗製材料15(7.6343g、14.6mMol、93.05%の収率)をそのまま次のステップにおいて使用した。LCMS 3分:ES+=2.42分、m/z524.4[M+H]+。
化合物15(7.6343g、14.60mMol)を、アルゴン雰囲気下、CH2Cl2(100mL)に可溶化した。混合物を-78℃に冷却した後、ピリジン(2.6mL、32mmol)及びクロロギ酸アリル(1.7mL、16mMol)を添加した。反応を-78℃において10分間撹拌したままにした後、室温まで加温させた。15分後、反応が完了した。有機物を飽和CuSO4、H2O、ブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。粗生成物16(8.9129g、14.69mMol、定量)をそのまま次のステップにおいて使用した。LCMS 3分:ES+=2.53分、m/z608.2[M+H]+。
化合物16(8.9129g、14.69mMol)をH2O/THF/酢酸の3:1:1混合物(80mL)に可溶化し、反応を週末にかけて撹拌したままにした。混合物をCH2Cl2で抽出し、飽和NaHCO3、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(Hex/EtOAc、100%から1:1)、生成物17を得た(5.5572g、76.80%の収率)を透明な油として得た。LCMS 3分:ES+=1.97分、m/z494.0[M+H]+。
化合物17(5.5572g、11.28mMol)をCH2Cl2(40mL)に可溶化した。1-ヒドロキシ-2,2,6,6-テトラメチル-ピペリジン;1-メチルイミダゾール;2-(2-ピリジル)ピリジン(6mL、1mmol)及びテトラキスアセトニトリル銅(I)トリフラート(425mg、1.1279mMol)を順次添加し、混合物を、空気を圧入した2バルーンで35℃にて撹拌した。反応を一晩中撹拌したままにした後、ロータリーエバポレーターによって真空乾固した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から97:3)、生成物18(5.3835g、10.97mMol、97.27%の収率)を淡橙色発泡体として得た。LCMS 3分:ES+=2.00分、m/z491.8[M+H]+。
化合物18(5.3835g、10.97mMol)をCH2Cl2(50mL)に可溶化し、-78℃に冷却した。2,6-ルチジン(2.55mL、21.9mmol)及びTBS-OTf(3.78mL、16.4mMol)を順次添加した。混合物を10分間放置した後、冷却浴を除去し、室温まで加温させ、有機物をH2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から95:5)、生成物19を得た(6.8532g、定量)。LCMS 3分:ES+=2.47分、m/z606.0[M+H]+。
化合物19(6.8g、14mMol)をDMF(10mL)に可溶化した。LiOAc.2H2O(1.4g、14mmMl)及びH2O(3mL又は可能な限り)を添加した。溶液が再び透明になったら、数滴の水を添加した。プロセスを、反応が完了するまで繰り返し続けた。有機物をCHCl3で希釈し、クエン酸溶液(pH=3)、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から95:5)、生成物20を得た(5.2885g、11.79mMol、85%の収率)を黄色油として得た。LCMS 3分:ES+=1.86分、m/z449.8[M+H]+。
1,3-ジブロモプロパン(204.9mg、1.015mMol)及び化合物20(1g、2.030mMol)をアルゴン雰囲気下でCH2Cl2(50mL)に可溶化した。K2CO3(280mg、2.026mmol)及びTBAI(149mg、0.2mMol)を順次添加し、完了するまで混合物を40℃で撹拌させた。混合物を一晩中撹拌したままにしたが、反応は完了まで行かず、代わりに、不純物が形成された。有機物をH2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から97:3)、生成物21を得(482mg、0.471mMol、46.50%の収率)、これは、分離不能な不純物(LCMS 15分において室温で9.95分)によって汚染されていた。LCMS 15分:ES+=9.86分、m/z938.3[M+H]+。
化合物21(482mg、0.5143mMol)を、アルゴン下、フラスコにおいて、CH2Cl2(20mL)に可溶化した。ピロリジン(786μL、9.44mmol)及びPd(PPh3)4(54mg、0.046mMol)を続いて添加し、完了するまで混合物を室温で撹拌したままにした。有機物を飽和NH4Cl、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。Isoleraクロマトグラフィーによる精製(CH2Cl2/(CH2Cl2+10%MeOH)98:2から30:70。生成物を含有する2つのフラクションを単離したが、不十分な純度であった。フラクションを合わせ、Isoleraクロマトグラフィーによって再精製し(同じ溶媒系)、純粋な生成物Ex2Aを単離した(35.1mg、0.135mMol、13.5%の収率)。LCMS 3分:ES+=1.23分、m/z505.8[M+H]+。
1,3-ビス(ブロモメチル)ベンゼン(267.9mg、1.011mMol)及び化合物20(1g、2.030mMol)をアルゴン雰囲気下でDMF(5mL)に可溶化した。K2CO3(280mg、2.026mmol)及びTBAI(749mg、2.027mMol)を順次添加し、完了するまで混合物を40℃で撹拌させた。混合物を一晩中撹拌したままにしたが、反応は完了まで行かず、不純物が形成された。混合物をCH2Cl2で希釈し、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から97:3)、生成物22(467mg、0.43mMol、42.47%の収率)+398mgの混合フラクションを得た。LCMS 3分:ES+=2.30分、m/z1000.5[M+H]+。
化合物22(455mg、0.419mMol)を、アルゴン下、フラスコにおいて、CH2Cl2(20mL)に可溶化した。ピロリジン(600μL、7.2mmol)及びPd(PPh3)4(48mg、0.041mMol)を続いて添加し、完了するまで混合物を室温で撹拌したままにした。有機物を飽和NH4Cl、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。Isoleraクロマトグラフィーによる精製(CH2Cl2/(CH2Cl2+10%MeOH)98:2から30:70。生成物を含有する2つのフラクションを単離したが、不十分な純度であった。フラクションを合わせ、Isoleraクロマトグラフィーによって再精製し(同じ溶媒系)、純粋な生成物Ex2Bを白色固体として単離した(214.5mg、0.378mMol、90.5%の収率)。LCMS 3分:ES+=1.38分、m/z567.8[M+H]+。
a)アリル (5-((5-(5-アミノ-4-((S)-2-(((tert-ブチルジメチルシリル)オキシ)メチル)アゼチジン-1-カルボニル)-2-メトキシフェノキシ)ペンチル)オキシ)-2-((S)-2-(((tert-ブチルジメチルシリル)オキシ)メチル)アゼチジン-1-カルボニル)-4-メトキシフェニル)カルバマート(23)
化合物9(1.192g、1.488mMol)をアルゴン雰囲気下でCH2Cl2(250mL)に可溶化した。混合物を-78℃に冷却した後、ピリジン(0.241mL、2.98mmol)及びクロロギ酸アリル(0.158mL、1.484mMol)を添加した。反応を-78℃において10分間撹拌したままにした後、室温まで加温させた。15分後、反応が完了した。有機物を飽和CuSO4、H2O、ブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH)、モノ及びビス-allocの混合物を得、これを第2のカラム(Hex/EtOAc)によってさらに精製して、純粋な生成物23を得た(499.2g、50%の生じ得るもののうち37.9%の収率)。LCMS 3分:ES+=2.41分、m/z886.6[M+H]+。
トリホスゲン(68.8mg、0.232mMol)を、0℃において、CH2Cl2(50mL)中の23(620mg、0.7mmol)及びTEA(203μL、1.46mMol)の混合物に少しずつ添加した。氷浴を除去し、15分後、Alloc-Val-Ala-PAB-OH(275mg、0.728mMol)を微粉末として少しずつ添加し、続いて、さらなるTEA(73μL、0.524mMol)及びジラウリン酸ジブチルスズ(39.6μL、0.07mMol)を添加した。反応混合物を37℃で4時間撹拌させ、続いて、室温で一晩中撹拌した。有機物をH2O、飽和NH4Cl及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH)、純粋な生成物24を得た(414g、45.9%の収率)。LCMS 3分:ES+=2.43分、m/z1289.5[M+H]+。
化合物24(414mg、0.32mMol)をH2O/THF/酢酸の3:1:1混合物(10mL)に可溶化し、反応を週末にかけて撹拌したままにした。混合物をCH2Cl2で抽出し、飽和NaHCO3、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から94:6)、生成物25を得た(326mg、95.7%の収率)。LCMS 3分:ES+=1.80分、m/z1060.1[M+H]+。
化合物25(202.4mg、0.3mMol)をCH2Cl2(20mL)に可溶化した。1-ヒドロキシ-2,2,6,6-テトラメチル-ピペリジン;1-メチルイミダゾール;2-(2-ピリジル)ピリジン(0.4mL、0.03mmol)及びテトラキスアセトニトリル銅(I)トリフラート(11mg、0.03mMol)を順次添加し、混合物を、空気を圧入した2バルーンで35℃にて撹拌した。反応を一晩中撹拌したままにした後、ロータリーエバポレーターによって真空乾固した。シリカゲルカラムクロマトグラフィーによる精製により(CHCl3/MeOH、100%から97:3)、生成物26を得た(313mg、0.19mMol、64.5%の収率)。LCMS 3分:ES+=1.59分、m/z1057.1[M+H]+。
化合物26(195mg、0.184mMol)を、アルゴン下、フラスコにおいて、CH2Cl2(10mL)に可溶化した。ピロリジン(262μL、3.15mmol)及びPd(PPh3)4(21mg、0.018mMol)を続いて添加し、完了するまで混合物を室温で撹拌したままにした。有機物を飽和NH4Cl、H2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。Isoleraクロマトグラフィーによる精製(CH2Cl2/(CH2Cl2+10%MeOH)98:2から30:70により、生成物27を得た(141mg、0.16mMol、87.7%の収率)。LCMS 3分:ES+=1.23分、m/z870.9[M+H]+。
反応をグローブボックスにおいて行った。化合物27(70mg、0.080mMol)を、フラスコにおいて室温でアルゴン下、CH2Cl2(10mL)に可溶化した。Mal-dPEG8-OH(50mg、0.084mmol)及びEDCI.HCl(15.4mg、0.080mMol)を添加し、完了まで混合物を撹拌した。有機物をH2O及びブラインで洗浄した後、MgSO4で乾燥し、濾過し、揮発性物質を減圧下で除去した。Isoleraクロマトグラフィーによる精製(CH2Cl2/(CH2Cl2+10%MeOH)98:2から30:70により、純粋でない生成物を得た。逆相Isoleraによるさらなる精製により、純粋なEx3(4mg、0.027mMol、3.4%の収率)及びいくらかの不透明なフラクション(22mg)を得た。LCMS 3分:ES+=1.51分、m/z1445.6[M+H]+。
ConjA(Her2-Ex3)
リン酸緩衝食塩水(pH7.4)(PBS)にトリス(2-カルボキシエチル)ホスフィン(TCEP)を溶解させた10mM溶液を(50モル当量/抗体、7.6マイクロモル、762.7μL)、トラスツズマブ(22.9mg、153ナノモル)を、30mMヒスチジン/ヒスチジンHCl、30mMアルギニン(pH6.8)及び1mMのエチレンジアミン四酢酸(EDTA)を含有する還元緩衝液に溶解した、抗体濃度が1.1mg/mLの、20.8mLの溶液に添加した。還元混合物を、オービタルシェーカーにおいて、穏やかに(60rpm)振とうしながら、37℃で2時間(又は完全な還元がUHPLCによって観察されるまで)反応させた。還元された抗体溶液を、スピンフィルター遠心分離を介して、30mMヒスチジン/ヒスチジンHCl、30mMアルギニン及び1mM EDTAを含有する、最終抗体濃度が1.1mg/mLの複合化緩衝液に緩衝液交換した(過剰な還元剤を全て除去するため)。Ex3をDMSO溶液(12.5モル当量/抗体、2.1mL DMSO中1.9マイクロモル)として18.6mLのこの還元された抗体溶液(20.5mg、136ナノモル)に添加して、10%(v/v)の最終DMSO濃度とした。溶液を室温で17時間混合し、次いで、複合化を、N-アセチルシステイン(8.5マイクロモル、100mMで68μL)の添加によってクエンチし、次いで、15mL Amicon Ultracell 30KDa MWCOスピンフィルターを使用したスピンフィルター遠心分離を介して精製し、滅菌濾過し、分析した。
分子の効能を、がん細胞株NCI-N87におけるin vitro細胞毒性アッセイを介して測定した。
サブ密集(80-90%の密集度)T75フラスコからの細胞の濃度及び生存度を、トリパンブルー染色によって測定し、LUNA-II(商標)Automated Cell Counterを使用してカウントする。細胞を2×105/mlに希釈し、96-ウェル平底プレートに分配した(ウェルあたり50μl)。
NCI-N87異種移植マウス
雌性重症複合免疫不全マウス(Fox Chase SCID(登録商標)、CB17/Icr-Prkdcscid/IcrIcoCrl、Charles River)は、研究の1日目で、体重(BW)範囲が16.5~21.6グラムで8週齢であった。動物に自由飲水(逆浸透、1ppm Cl)させ、18.0%の粗タンパク質、5.0%の粗脂肪及び5.0%の粗繊維からなるNIH 31Modified and Irradiated Lab Diet(登録商標)を自由摂食させた。マウスを、静圧マイクロアイソレーターにおける照射Enricho’cobs(商標)Laboratory Animal Beddingにおいて、12時間の明サイクルにて20~22℃(68~72°F)及び40~60%の湿度で飼育した。CR Discovery Servicesは、具体的には、拘束、畜産、外科手術、試料及び流体規制、ならびに獣医医療に関するGuide for Care and Use of Laboratory Animalsの勧告を遵守している。CR Discovery Servicesの動物管理及び使用プログラムは、実験動物の管理及び使用に対する承認規格の遵守を保証する、Association for Assessment and Accreditation of Laboratory Animal Care International(AAALAC)によって公認されている。
ヒトNCI-N87胃癌リンパ腫細胞を、10%ウシ胎仔血清、2mMグルタミン、100単位/mLペニシリンGナトリウム、100μg/mL硫酸ストレプトマイシン及び25μg/mLゲンタマイシンを補充したRPMI-1640培地において培養した。細胞を、5%CO2及び95%空気の雰囲気において37℃で加湿インキュベーターにおいて組織培養フラスコ中で増殖させた。
移植に使用したNCI-N87細胞を対数期増殖の間に摘出し、50%Matrigel(商標)(BD Biosciences)を含有するリン酸緩衝食塩水(PBS)に再懸濁した。腫瘍移植の日に、各試験マウスに、1×107細胞(0.1mL細胞懸濁液)を右側腹に皮下注射し、腫瘍成長を、100~150mm3の標的範囲に近づいた平均サイズとしてモニタリングした。研究の1日目に指定した14日後に、マウスを、それぞれ、108~144mm3の範囲の個々の腫瘍体積、及び115mm3の群平均腫瘍体積を有する10匹の動物からなる群に、計算した腫瘍サイズに従って分類した
式中、腫瘍のmmでのw=幅、及びl=長さである。腫瘍重量を、1mgが腫瘍体積の1mm3と同等であると仮定して、推定してよい。
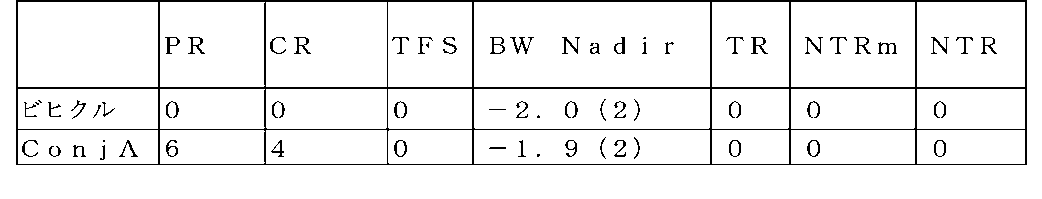
処置を、確立された皮下NCI-N87腫瘍(108~144mm3)を有する10匹のマウス(n=10)において1日目に開始した。ConjA(4mg/kg)を1日目(qd×1)に1回静脈投与した。ビヒクル処置群を効力分析の対照群とした。研究が79日目に終了するまで腫瘍を1週間に2回測定した。各マウスを、腫瘍がエンドポイント体積の800mm3に達したとき、又は最終日のいずれか早く到達したときに安楽死させた。エンドポイントまでの時間(TTE)を各マウスについて計算した。
腫瘍を、カリパーを使用して1週間に2回測定し、各動物を、その腫瘍がエンドポイント体積の800mm3に達したとき、又は最終日(79日目)のいずれか早く到達したときに安楽死させた。腫瘍体積エンドポイントに関する研究から外す動物を、腫瘍進行(TP)のために安楽死させたことを、安楽死の日付と共に記録した。解析についてのエンドポイント(TTE)までの時間を、各マウスについて、以下の式によって計算した:
TTE=(log10(エンドポイント体積)-b)/m
式中、TTEは、日数で表され、エンドポイント体積は、mm3で表され、bは、切片であり、mは、対数変換された腫瘍成長データセットの線形回帰により得られる直線の傾きである。データセットは、解析において使用されるエンドポイント体積を超えた最初の観察と、このエンドポイント体積への到達の直前の3回連続の観察とからなった。計算されたTTEは、腫瘍サイズのために動物を安楽死させた日であるTPの日よりも通常は少ない。エンドポイント体積に到達しなかった腫瘍を有する動物には、研究の最終日(79日目)と等しいTTE値を割り当てた。対数変換された計算されたTTEが、エンドポイントに到達する前の日より先であるか、又は腫瘍体積エンドポイントに到達する日を超える場合には、線形補間を実施してTTEを概算した。事故に起因するNTR(処置と関連しない)原因(NTRa)又は未知の病因に起因するNTR原因(NTRu)により死亡したと分類されるいずれの動物も、TTEの計算(及び全てのさらなる解析)から除外した。TR(処置関連)死亡又はNTRm(転移に起因する、処置と関連しない死亡)と分類される動物には、死亡の日と等しいTTE値を割り当てた。処置効果は、対照群と比較した、処置群におけるエンドポイント(TTE)までの時間中央値の増加として定義される、腫瘍成長遅延(TGD):
TGD=T-C(日数で表される)
又は、対照群のTTE中央値のパーセンテージとしての:
式中:
T=処置群についてのTTE中央値、及び
C=指定の対照群についてのTTE中央値
から評価した。
腫瘍成長阻害(TGI)解析では、処置及び対照マウスの腫瘍体積中央値(MTV)の差を評価する。この研究では、TGIを求めるエンドポイントは、全ての評価可能な対照マウスが研究に残っていた最終日である19日目であった。TGI解析の日における、動物の数nでの腫瘍体積の中央値、MTV(n)を各群について求めた。パーセント腫瘍成長阻害(%TGI)を、指定の対照群のMTVと、薬物処置群のMTVとの間の差として定義し、対照群のMTVのうちのパーセンテージとして表記した:
%TGI=((MTV対照-MTV薬物処置)/MTV対照)×100=[1-(MTV薬物処置/MTV対照)]×100
処置効力は、最終日に研究に残っている動物の腫瘍体積から求めることができる。MTV(n)は、腫瘍がエンドポイント体積に到達せずに残っている動物の数(n)における、研究の最終日での腫瘍体積の中央値として定義した。処置効力はまた、研究の際に観察される縮小反応の発生及び大きさからも求めることができる。処置により、動物における腫瘍の部分縮小(PR)又は完全縮小(CR)を引き起こし得る。PR反応において、腫瘍体積は、研究の過程で、3回連続の測定値について、その1日目の体積の50%以下であり、かつ、これらの3回の測定値のうちの1以上について13.5mm3以上であった。CR反応において、腫瘍体積は、研究の過程で、3回連続の測定値について、13.5mm3未満であった。動物について、PR又はCR事象については研究の際に1回のみ、また、PR及びCRの両方の基準が満たされたときにはCRとしてのみスコアリングした。研究の終了時にCR反応を伴う動物は、加えて、無腫瘍生存動物(TFS)として分類した。動物を縮小反応についてモニタリングした。
動物について、1~5日目には毎日、次いで、研究の完了までは1週間に2回体重測定した。マウスを、任意の有害な処置関連(TR)副作用の明白な徴候について頻繁に観察し、臨床徴候は、観察されたときに記録した。個々の体重をプロトコールによってモニタリングし、1回の測定で30%を超える、又は、3回連続の測定で25%を超える体重減少を伴った動物をTR死亡として安楽死させた。群平均体重減少も、CR Discovery Servicesプロトコールに従ってモニタリングした。許容可能な毒性を、研究の際の群平均体重(BW)減少が20%未満であること及びTR死が10%以下であることとして定義した。投与は、平均体重減少が許容可能な限界を超えたいずれの群においても中断した。群平均体重が許容レベルに回復したときには、投与を、より低いレベル及び/又は低減した頻度に変更して再開した。死亡は、臨床徴候及び/又は剖検により証拠立てられるように処置副作用に帰せられるときには、TRと分類した。TR分類には、投与期間の間又は最後の投与の14日以内の未知の原因による死亡もまた割り当てられた。死亡は、死亡が処置副作用と関連するという証拠がないときには、処置と関連しない(NTR)と分類した。NTR死亡は、以下のようにさらにカテゴライズされる:NTRaは、事故又はヒューマンエラーに起因する死亡を記載している;NTRmは、剖検結果に基づいて浸潤及び/又は転移による腫瘍の播種から生じたとされる死亡に割り当てられる;NTRuは、転移、腫瘍進行、事故又はヒューマンエラーに関連する死亡についての利用可能な証拠を欠いている未知の原因の死亡を記載している。処置副作用は、NTRuと分類される死亡から除外され得ないことが注意されるべきである。
Windows用GraphPad Prism8.0を全ての統計的解析及びグラフ表示に使用した。許容可能な限界を超える毒性(>20%群平均体重減少又は10%超の処置関連死亡)を経験する、又は、評価可能な観察が5つ未満である研究群を、統計的解析に含まなかった。ログランク検定を用いて、2つの全生存経験群の間の有意差を査定した。ログランク検定は、NTR死亡に起因する研究に属していないものを除いて、群における全ての動物について個々のTTEを分析する。対照及び処置群の19日目の腫瘍体積の中央値(MTV)間の差の統計的解析を、マンホイットニーのU検定を使用して達成した。統計的解析のために、両側検定をP=0.05の有意水準で行った。Prismでは、試験結果を、P>0.05では非有意(ns)、0.01<P≦0.05では有意(「*」の記号で表す)、0.001<P≦0.01では非常に有意(「**」)、及びP≦0.001では極めて有意(「***」)とまとめる。統計的有意性の検定は、群間の差の大きさについての推定値を提供するものではないため、この報告の文脈内では、有意性の全ての水準を、有意又は非有意として記載した。
1.式IVの化合物:
式中:
R2及びR2’は、Hであり;
R6及びR9は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから独立して選択され;
ここでR及びR’は、任意選択的に置換されているC1-12アルキル、C3-20ヘテロシクリル及びC5-20アリール基から独立して選択され;
(a)R7は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択され;
R7’は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択されるか;又は
(b)R7及びR7’は、一緒になって:(i)nが7~16である-O-(CH2)n-O-;若しくは(ii)mが2~5である-O-(CH2CH2O)m-を形成するか;
のいずれかであり;
R”は、C3-12アルキレン基であり、かかる鎖は、1つ以上のヘテロ原子、例えば、O、S、NRN2(ここで、RN2は、H若しくはC1-4アルキルである)、及び/又は芳香族環、例えば、ベンゼン若しくはピリジンによって中断されていてよく;
Y及びY’は、O、S、又はNHから選択され;
R6’及びR9’は、それぞれ、R6及びR9と同じ基から選択され;
(i-a)R10及びR11は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(i-b)R10はHであり、R11は、OH及びORAから選択され、ここで、RAは、C1-4アルキルであるか;又は
(i-c)R10及びR11は、両方がHである;
のいずれかであり;
(ii-a)R20及びR21は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(ii-b)R20は、Hであり、R21は、OH及びORBから選択され、ここで、RBはC1-4アルキルであるか;又は
(ii-c)R20及びR21は、両方がHである;
のいずれかである;
前記化合物、ならびにその塩及び溶媒和物。
式中、rは、1又は2である
の基である、記述1又は記述2のいずれかに記載の化合物。
R1aは、メチル及びベンジルから選択される
記述1に記載の化合物。
であって、
式中:
Y、Y’、R”、R2、R2’、R6、R6’、R7、R7’、R9及びR9’は、記述1から18のいずれか1つに定義されている通りであり;
R11bは、OH、ORAから選択され、ここでRAは、C1-4アルキルであり;
RLは:
(iiia):
、
(Qは:
、
であり、QXは、Qが、アミノ酸残基、ジペプチド残基又はトリペプチド残基であるようになっており;
Xは:
であり、a=0~5、b=0~16、c=0又は1、d=0~5であり;
GLは、リガンド単位に接続するためのリンカーである);ならびに
(iiib):
(RL1及びRL2は、H及びメチルから独立して選択され、又は、これらが結合している炭素原子と一緒になって、シクロプロピレン若しくはシクロブチレン基を形成し;
eが0又は1である);
から選択される、細胞結合剤への接続のためのリンカーであり;
(a)R30及びR31は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(b)R30は、Hであり、R31は、OH及びORBから選択され、ここでRBはC1-4アルキルであるか;又は
(c)R30及びR31は、両方がHであるか;又は
(d)R31は、OH若しくはORBであり、ここでRBは、C1-4アルキルであり、R30は:
(i)
;
(ii)
;
(iii)
、
(RZは:
(z-i)
;
(z-ii)OC(=O)CH3;
(z-iii)NO2;
(z-iv)OMe;
(z-v)グルクロニド;
(z-vi)NH-C(=O)-X1-NHC(=O)X2-NH-C(=O)-RZC、ここで、-C(=O)-X1-NH-及びC(=O)-X2-NH-は、天然アミノ酸残基を表し、RZCは、Me、OMe、CH2CH2OMe、及び(CH2CH2O)2Meから選択される)
から選択される;
のいずれかである、
前記化合物、ならびにその塩及び溶媒和物。
(R1aは、メチル及びベンジルから選択される)。
CO-Phe-Lys-NH,
CO-Val-Ala-NH,
CO-Val-Lys-NH,
CO-Ala-Lys-NH,
CO-Val-Cit-NH,
CO-Phe-Cit-NH,
CO-Leu-Cit-NH,
CO-Ile-Cit-NH,
CO-Phe-Arg-NH、及び
CO-Trp-Cit-NH
から選択されるジペプチド残基である、記述19から31のいずれか1つに記載の化合物。
CO-Glu-Val-Ala-NH,
CO-Glu-Val-Cit-NH,
CO-αGlu-Val-Ala-NH、及び
CO-αGlu-Val-Cit-NH
から選択されるトリペプチド残基である、記述19から31のいずれか1つに記載の化合物。
(式中、Arは、C5-6アリーレン基を表す)。
式中、Qは、以下:
(a)-CH2-;
(b)-C3H6-;及び
(c)
から選択される、記述19に記載の化合物。
L-(DL)p (II)
であって、
式中、Lは、リガンド単位(すなわち、標的薬剤)であり、DLは、式I’の薬物リンカー単位であり:
式中:
Y、Y’、R”、R2、R2’、R6、R6’、R7、R7’、R9及びR9’は、記述1から18のいずれか1つに定義されている通りであり;
R11b、R30及びR31は、記述19から27及び29から31のいずれか1つに定義されている通りであり;
RLLは:
(iiia):
(Q及びXは、記述19及び32から43に定義されている通りであり、GLLは、リガンド単位に接続されているリンカーである);ならびに
(iiib):
(RL1及びRL2は、記述19及び48から52に定義されている通りである);
から選択される、細胞結合剤への接続のためのリンカーであり;
pは、1~20の整数である;
前記複合体。
(式中、Arは、C5-6アリーレン基を表す)。
式中、Qは、以下:
(a)-CH2-;
(b)-C3H6-;及び
(c)
から選択される、記述57に記載の複合体。
(1)BMPR1B;
(2)E16;
(3)STEAP1;
(4)0772P;
(5)MPF;
(6)Napi3b;
(7)Sema 5b;
(8)PSCA hlg;
(9)ETBR;
(10)MSG783;
(11)STEAP2;
(12)TrpM4;
(13)CRIPTO;
(14)CD21;
(15)CD79b;
(16)FcRH2;
(17)HER2;
(18)NCA;
(19)MDP;
(20)IL20R-α;
(21)ブレビカン;
(22)EphB2R;
(23)ASLG659;
(24)PSCA;
(25)GEDA;
(26)BAFF-R;
(27)CD22;
(28)CD79a;
(29)CXCR5;
(30)HLA-DOB;
(31)P2X5;
(32)CD72;
(33)LY64;
(34)FcRH1;
(35)IRTA2;
(36)TENB2;
(37)PSMA-FOLH1;
(38)SST;
(38.1)SSTR2;
(38.2)SSTR5;
(38.3)SSTR1;
(38.4)SSTR3;
(38.5)SSTR4;
(39)ITGAV;
(40)ITGB6;
(41)CEACAM5;
(42)MET;
(43)MUC1;
(44)CA9;
(45)EGFRvIII;
(46)CD33;
(47)CD19;
(48)IL2RA;
(49)AXL;
(50)CD30-TNFRSF8;
(51)BCMA-TNFRSF17;
(52)CT Ags-CTA;
(53)CD174(ルイスY)-FUT3;
(54)CLEC14A;
(55)GRP78-HSPA5;
(56)CD70;
(57)幹細胞特異的抗原;
(58)ASG-5;
(59)ENPP3;
(60)PRR4;
(61)GCC-GUCY2C;
(62)Liv-1-SLC39A6;
(63)5T4;
(64)CD56-NCMA1;
(65)CanAg;
(66)FOLR1;
(67)GPNMB;
(68)TIM-1-HAVCR1;
(69)RG-1/前立腺腫瘍標的ミンディン-ミンディン/RG-1;
(70)B7-H4-VTCN1;
(71)PTK7;
(72)CD37;
(73)CD138-SDC1;
(74)CD74;
(75)クローディン-CLs;
(76)EGFR;
(77)Her3;
(78)RON-MST1R;
(79)EPHA2;
(80)CD20-MS4A1;
(81)テネイシンC-TNC;
(82)FAP;
(83)DKK-1;
(84)CD52;
(85)CS1-SLAMF7;
(86)エンドグリン-ENG;
(87)アネキシンA1-ANXA1;
(88)V-CAM(CD106)-VCAM1;
(89)ASCT2(SLC1A5)。
Claims (24)
- 式IVの化合物:
であって、
式中:
R2及びR2’は、Hであり;
R6及びR9は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから独立して選択され;
ここでR及びR’は、任意選択的に置換されているC1-12アルキル、C3-20ヘテロシクリル、C 6-10 カルボアリール基及びC5-14 ヘテロアリール基から独立して選択され;
(a)R7は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択され;
R7’は、H、R、OH、OR、SH、SR、NH2、NHR、NRR’、ニトロ、Me3Sn及びハロから選択されるか;又は
(b)R7及びR7’は、一緒になって:(i)nが7~16である-O-(CH2)n-O-;若しくは(ii)mが2~5である-O-(CH2CH2O)m-を形成するか;
のいずれかであり;
R”は、C3-12アルキレン基であり、かかる鎖は、O、S、NRN2(ここで、RN2は、H若しくはC1-4アルキルである)から選択される1つ以上のヘテロ原子、及び/又はベンゼン若しくはピリジンから選択される芳香族環によって中断されていてよく;
Y及びY’は、O、S、又はNHから選択され;
R6’及びR9’は、それぞれ、R6及びR9と同じ基から選択され;
(i-a)R10及びR11は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(i-b)R10はHであり、R11は、OH及びORAから選択され、ここで、RAは、C1-4アルキルであるか;又は
(i-c)R10及びR11は、両方がHである;
のいずれかであり;
(ii-a)R20及びR21は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(ii-b)R20は、Hであり、R21は、OH及びORBから選択され、ここで、RBはC1-4アルキルであるか;又は
(ii-c)R20及びR21は、両方がHである;
のいずれかである;
前記化合物、ならびにその塩及び溶媒和物。 - Y及びY’は、両方がOである、請求項1に記載の化合物。
- R”は、C3-7アルキレンである、請求項1又は請求項2のいずれかに記載の化合物。
- R”は、式:
式中、rは、1又は2である
の基である、請求項1又は請求項2のいずれかに記載の化合物。 - R9は、Hであり、R6は、Hであり、R7及びR7’は、独立して、C1-4アルキルオキシ基である、請求項1から4のいずれか一項に記載の化合物。
- R6’は、R6と同じ基であり、R7’は、R7と同じ基であり、R9’は、R9と同じ基であり、Y’は、Yと同じ基である、請求項1から4のいずれか一項に記載の化合物。
- 式IVa、IVb又はIVcのものである:
式中、R1aは、メチル及びベンジルから選択される
請求項1に記載の化合物。 - 式Iの化合物:
であって、
式中:
Y、Y’、R”、R2、R2’、R6、R6’、R7、R7’、R9及びR9’は、請求項1から9のいずれか一項に定義されている通りであり;
R11bは、OH、ORAから選択され、ここでRAは、C1-4アルキルであり;
RLは:
(iiia):
(Qは:
であり、QXは、Qが、アミノ酸残基、ジペプチド残基又はトリペプチド残基であるようになっており;
Xは:
であり、a=0~5、b=0~16、c=0又は1、d=0~5であり;
GLは、リガンド単位に接続するためのリンカーである);ならびに
(iiib):
(RL1及びRL2は、H及びメチルから独立して選択され、又は、これらが結合している炭素原子と一緒になって、シクロプロピレン若しくはシクロブチレン基を形成し;
eが0又は1である);
から選択される、細胞結合剤への接続のためのリンカーであり;
(a)R30及びR31は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成するか;又は
(b)R30は、Hであり、R31は、OH及びORBから選択され、ここでRBはC1-4アルキルであるか
(c)R30及びR31は、両方がHであるか;又は
(d)R31は、OH若しくはORBであり、ここでRBは、C1-4アルキルであり、R30は:
(i)
;
(ii)
;
(iii)
、
(RZは:
(z-i)
;
(z-ii)OC(=O)CH3;
(z-iii)NO2;
(z-iv)OMe;
(z-v)グルクロニド;
(z-vi)NH-C(=O)-X1-NHC(=O)X2-NH-C(=O)-RZC、ここで、-C(=O)-X1-NH-及びC(=O)-X2-NH-は、天然アミノ酸残基を表し、RZCは、Me、OMe、CH2CH2OMe、及び(CH2CH2O)2Meから選択される)
から選択される;
のいずれかである
前記化合物、ならびにその塩及び溶媒和物。 - R30及びR31は、一緒になって、これらが結合しているN及びC原子間に二重結合を形成する、請求項8に記載の化合物。
- 式Ia、Ib又はIcのものである:
式中、R1aは、メチル及びベンジルから選択される
請求項8に記載の化合物。 - RLが、式IIIaのものであり、Qが:
CO-Phe-Lys-NH,
CO-Val-Ala-NH,
CO-Val-Lys-NH,
CO-Ala-Lys-NH,
CO-Val-Cit-NH,
CO-Phe-Cit-NH,
CO-Leu-Cit-NH,
CO-Ile-Cit-NH,
CO-Phe-Arg-NH、及び
CO-Trp-Cit-NH
から選択されるジペプチド残基である、請求項8から10のいずれか一項に記載の化合物。 - RLは、式IIIaのものであり、aは、0であり、cは、1であり、dは、2であり、bは、0~8である、請求項8から10のいずれか一項に記載の化合物。
- bは、0、4又は8である、請求項12に記載の化合物。
- RLは、式IIIaのものであり、GLは以下から選択される、請求項8から13のいずれか一項に記載の化合物。
(式中、Arは、フェニレン基を表す)。 - GLは、GL1-1である、請求項14に記載の化合物。
- 式Idのものであり:
式中、Qは、以下:
(a)-CH2-;
(b)-C3H6-;及び
(c)
から選択される、請求項8に記載の化合物。 - 式IIの複合体:
L-(DL)p (II)
であって、
式中、Lは、リガンド単位(すなわち、標的薬剤)であり、DLは、式I’の薬物リンカー単位であり:
式中:
Y、Y’、R”、R2、R2’、R6、R6’、R7、R7’、R9及びR9’は、請求項1から6のいずれか一項に定義されている通りであり;
R11b、R30及びR31は、請求項8及び9のいずれかに定義されている通りであり;
RLLは:
(iiia):
(Q及びXは、請求項8及び11から13のいずれかに定義されている通りであり、GLLは、リガンド単位に接続されているリンカーである);ならびに
(iiib):
(RL1及びRL2は、請求項8に定義されている通りである);
から選択される、細胞結合剤への接続のためのリンカーであり;
pは、1~20の整数である;
前記複合体。 - GLLが以下から選択される、請求項17に記載の複合体:
(式中、Arは、フェニレン基を表し、CBAはリガンド単位を表す。)。 - DLが式(Id’)のものであり:
式中、Qは、以下:
(a)-CH2-;
(b)-C3H6-;及び
(c)
から選択される、請求項17に記載の複合体。 - 請求項17~19のいずれか一項に記載の複合体の混合物を含む組成物であって、複合体の混合物中の平均pは、約1~約8である、前記組成物。
- 療法に用いるための、請求項17~19のいずれか一項に記載の複合体。
- 請求項17~19のいずれか一項に記載の複合体、及び薬学的に許容可能な希釈剤、担体又は賦形剤を含む、医薬組成物。
- 治療対象の増殖性疾患の治療に用いるための、請求項17~19のいずれか一項に記載の複合体。
- 治療対象の増殖性疾患の治療に用いるための、請求項22に記載の医薬組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1903541.9A GB201903541D0 (en) | 2019-03-15 | 2019-03-15 | Compounds and conjugates |
| GB1903541.9 | 2019-03-15 | ||
| GBGB2000121.0A GB202000121D0 (en) | 2020-01-06 | 2020-01-06 | Compounds and conjugates |
| GB2000121.0 | 2020-01-06 | ||
| PCT/EP2020/056761 WO2020187721A1 (en) | 2019-03-15 | 2020-03-13 | Azetidobenzodiazepine dimers and conjugates comprising them for use in the treatment of cancer |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022524880A JP2022524880A (ja) | 2022-05-10 |
| JP7520870B2 true JP7520870B2 (ja) | 2024-07-23 |
Family
ID=69845376
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021555569A Active JP7520870B2 (ja) | 2019-03-15 | 2020-03-13 | がんの治療における使用のための、アゼチドベンゾジアゼピン二量体及びこれを含む複合体 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US12209099B2 (ja) |
| EP (1) | EP3938372B1 (ja) |
| JP (1) | JP7520870B2 (ja) |
| KR (1) | KR102890251B1 (ja) |
| CN (1) | CN113631560B (ja) |
| AU (1) | AU2020242747B2 (ja) |
| BR (1) | BR112021018260A2 (ja) |
| CA (1) | CA3130174A1 (ja) |
| ES (1) | ES2967878T3 (ja) |
| IL (1) | IL286326B2 (ja) |
| MX (1) | MX2021010477A (ja) |
| SG (1) | SG11202108900WA (ja) |
| WO (1) | WO2020187721A1 (ja) |
| ZA (1) | ZA202105931B (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018192944A1 (en) | 2017-04-18 | 2018-10-25 | Medimmune Limited | Pyrrolobenzodiazepine conjugates |
Family Cites Families (440)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3361742A (en) | 1964-12-07 | 1968-01-02 | Hoffmann La Roche | 5-oxo-1h-pyrrolo-[2, 1-c][1, 4]-benzodiazepin-2-crylamides |
| US3523941A (en) | 1967-03-06 | 1970-08-11 | Hoffmann La Roche | Benzodiazepine compounds and process for their preparation |
| US3524849A (en) | 1967-10-27 | 1970-08-18 | Hoffmann La Roche | Process for the preparation of pyrrolo-benzodiazepine acrylamides and intermediates useful therein |
| DE1965304A1 (de) | 1968-12-30 | 1970-07-23 | Fujisawa Pharmaceutical Co | Benzdiazepinon-Verbindungen und Verfahren zu ihrer Herstellung |
| JPS4843755B1 (ja) | 1969-06-26 | 1973-12-20 | ||
| IL33558A (en) | 1968-12-30 | 1973-10-25 | Fujisawa Pharmaceutical Co | Antibiotic pyrrolo-benzodiazepine compound,its derivatives and processes for their production |
| JPS5382792U (ja) | 1976-12-10 | 1978-07-08 | ||
| JPS585916B2 (ja) | 1977-12-27 | 1983-02-02 | 株式会社ミドリ十字 | 新規ベンゾジアゼピン系化合物 |
| JPS5615289A (en) | 1979-07-17 | 1981-02-14 | Green Cross Corp:The | Novel benzodiazepinnbased compound 3 |
| JPS57131791A (en) | 1980-12-31 | 1982-08-14 | Fujisawa Pharmaceut Co Ltd | Benzodiazepine derivative and its preparation |
| CA1184175A (en) | 1981-02-27 | 1985-03-19 | Walter Hunkeler | Imidazodiazepines |
| CA1185602A (en) | 1981-02-27 | 1985-04-16 | Emilio Kyburz | Imidazodiazepines |
| CA1173441A (en) | 1981-02-27 | 1984-08-28 | Hoffmann-La Roche Limited | Imidazodiazepines |
| JPS58180487A (ja) | 1982-04-16 | 1983-10-21 | Kyowa Hakko Kogyo Co Ltd | 抗生物質dc−81およびその製造法 |
| US4427588A (en) | 1982-11-08 | 1984-01-24 | Bristol-Myers Company | Process for conversion of oxotomaymycin to tomaymycin |
| US4427587A (en) | 1982-11-10 | 1984-01-24 | Bristol-Myers Company | Total synthesis of antitumor antibiotics BBM-2040A and BBM-2040B |
| JPS59152329A (ja) | 1983-02-17 | 1984-08-31 | Green Cross Corp:The | 局所障害抑制剤 |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| FR2586683B1 (fr) | 1985-08-29 | 1988-07-01 | Centre Nat Rech Scient | Nouveaux derives de neothramycine, leur procede de preparation et leur application en tant que medicaments |
| US5583024A (en) | 1985-12-02 | 1996-12-10 | The Regents Of The University Of California | Recombinant expression of Coleoptera luciferase |
| JP2660201B2 (ja) | 1988-08-05 | 1997-10-08 | 塩野義製薬株式会社 | 新規ピロロ[1,4]ベンゾジアゼピン誘導体および老人性痴呆薬 |
| CA2023779A1 (en) | 1989-08-23 | 1991-02-24 | Margaret D. Moore | Compositions and methods for detection and treatment of epstein-barr virus infection and immune disorders |
| JPH053790A (ja) | 1990-04-19 | 1993-01-14 | Fujisawa Pharmaceut Co Ltd | デヒドロペプチダーゼ−i |
| US5256643A (en) | 1990-05-29 | 1993-10-26 | The Government Of The United States | Human cripto protein |
| AU9016591A (en) | 1990-10-25 | 1992-05-26 | Tanox Biosystems, Inc. | Glycoproteins associated with membrane-bound immunoglobulins as antibody targets on B cells |
| US5440021A (en) | 1991-03-29 | 1995-08-08 | Chuntharapai; Anan | Antibodies to human IL-8 type B receptor |
| WO1992017497A1 (en) | 1991-03-29 | 1992-10-15 | Genentech, Inc. | Human pf4a receptors and their use |
| US5543503A (en) | 1991-03-29 | 1996-08-06 | Genentech Inc. | Antibodies to human IL-8 type A receptor |
| FR2676058B1 (fr) | 1991-04-30 | 1994-02-25 | Hoechst Lab | Prodrogues glycosylees, leur procede de preparation et leur utilisation dans le traitement des cancers. |
| FR2676230B1 (fr) | 1991-05-07 | 1993-08-27 | Centre Nat Rech Scient | Nouveaux derives de pyrrolo [1,4]-benzodiazepines, leur procede de preparation et medicaments les contenant. |
| JP3050424B2 (ja) | 1991-07-12 | 2000-06-12 | 塩野義製薬株式会社 | ヒトエンドセリンリセプター |
| US5264557A (en) | 1991-08-23 | 1993-11-23 | The United States Of America As Represented By The Department Of Health And Human Services | Polypeptide of a human cripto-related gene, CR-3 |
| US5362852A (en) | 1991-09-27 | 1994-11-08 | Pfizer Inc. | Modified peptide derivatives conjugated at 2-hydroxyethylamine moieties |
| US6011146A (en) | 1991-11-15 | 2000-01-04 | Institut Pasteur | Altered major histocompatibility complex (MHC) determinant and methods of using the determinant |
| US6153408A (en) | 1991-11-15 | 2000-11-28 | Institut Pasteur And Institut National De La Sante Et De La Recherche Medicale | Altered major histocompatibility complex (MHC) determinant and methods of using the determinant |
| GB9205051D0 (en) | 1992-03-09 | 1992-04-22 | Cancer Res Campaign Tech | Pyrrolobenzodiazepine derivatives,their preparation,and compositions containing them |
| FR2696176B1 (fr) | 1992-09-28 | 1994-11-10 | Synthelabo | Dérivés de pipéridine, leur préparation et leur application en thérapeutique. |
| IL107366A (en) | 1992-10-23 | 2003-03-12 | Chugai Pharmaceutical Co Ltd | Genes coding for megakaryocyte potentiator |
| US5644033A (en) | 1992-12-22 | 1997-07-01 | Health Research, Inc. | Monoclonal antibodies that define a unique antigen of human B cell antigen receptor complex and methods of using same for diagnosis and treatment |
| US5869445A (en) | 1993-03-17 | 1999-02-09 | University Of Washington | Methods for eliciting or enhancing reactivity to HER-2/neu protein |
| US5801005A (en) | 1993-03-17 | 1998-09-01 | University Of Washington | Immune reactivity to HER-2/neu protein for diagnosis of malignancies in which the HER-2/neu oncogene is associated |
| US6214345B1 (en) | 1993-05-14 | 2001-04-10 | Bristol-Myers Squibb Co. | Lysosomal enzyme-cleavable antitumor drug conjugates |
| GB9316162D0 (en) | 1993-08-04 | 1993-09-22 | Zeneca Ltd | Fungicides |
| US5773223A (en) | 1993-09-02 | 1998-06-30 | Chiron Corporation | Endothelin B1, (ETB1) receptor polypeptide and its encoding nucleic acid methods, and uses thereof |
| EP0647450A1 (en) | 1993-09-09 | 1995-04-12 | BEHRINGWERKE Aktiengesellschaft | Improved prodrugs for enzyme mediated activation |
| US5750370A (en) | 1995-06-06 | 1998-05-12 | Human Genome Sciences, Inc. | Nucleic acid encoding human endothlein-bombesin receptor and method of producing the receptor |
| JPH08336393A (ja) | 1995-04-13 | 1996-12-24 | Mitsubishi Chem Corp | 光学活性なγ−置換−β−ヒドロキシ酪酸エステルの製造法 |
| US5707829A (en) | 1995-08-11 | 1998-01-13 | Genetics Institute, Inc. | DNA sequences and secreted proteins encoded thereby |
| US20020193567A1 (en) | 1995-08-11 | 2002-12-19 | Genetics Institute, Inc. | Secreted proteins and polynucleotides encoding them |
| JP3646191B2 (ja) | 1996-03-19 | 2005-05-11 | 大塚製薬株式会社 | ヒト遺伝子 |
| US6218519B1 (en) | 1996-04-12 | 2001-04-17 | Pro-Neuron, Inc. | Compounds and methods for the selective treatment of cancer and bacterial infections |
| NZ332598A (en) | 1996-05-17 | 2000-04-28 | Schering Corp | Human BAS-1 protein, and use as an antagonist for modulating physiology or development of a cell |
| AU739028B2 (en) | 1996-09-27 | 2001-10-04 | Bristol-Myers Squibb Company | Hydrolyzable prodrugs for delivery of anticancer drugs to metastatic cells |
| US6759509B1 (en) | 1996-11-05 | 2004-07-06 | Bristol-Myers Squibb Company | Branched peptide linkers |
| US5945511A (en) | 1997-02-20 | 1999-08-31 | Zymogenetics, Inc. | Class II cytokine receptor |
| US20030185830A1 (en) | 1997-02-25 | 2003-10-02 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of prostate cancer |
| US7033827B2 (en) | 1997-02-25 | 2006-04-25 | Corixa Corporation | Prostate-specific polynucleotide compositions |
| US6261791B1 (en) | 1997-03-10 | 2001-07-17 | The Regents Of The University Of California | Method for diagnosing cancer using specific PSCA antibodies |
| AU739407C (en) | 1997-03-10 | 2002-08-08 | Regents Of The University Of California, The | PSCA: prostate stem cell antigen |
| US6541212B2 (en) | 1997-03-10 | 2003-04-01 | The Regents Of The University Of California | Methods for detecting prostate stem cell antigen protein |
| US6555339B1 (en) | 1997-04-14 | 2003-04-29 | Arena Pharmaceuticals, Inc. | Non-endogenous, constitutively activated human protein-coupled receptors |
| US6319688B1 (en) | 1997-04-28 | 2001-11-20 | Smithkline Beecham Corporation | Polynucleotide encoding human sodium dependent phosphate transporter (IPT-1) |
| WO1998051824A1 (en) | 1997-05-15 | 1998-11-19 | Abbott Laboratories | Reagents and methods useful for detecting disease of the urinary tract |
| US6890749B2 (en) | 1997-05-15 | 2005-05-10 | Abbott Laboratories | Reagents and methods useful for detecting diseases of the prostate |
| US6602677B1 (en) | 1997-09-19 | 2003-08-05 | Promega Corporation | Thermostable luciferases and methods of production |
| US20030060612A1 (en) | 1997-10-28 | 2003-03-27 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| US20020034749A1 (en) | 1997-11-18 | 2002-03-21 | Billing-Medel Patricia A. | Reagents and methods useful for detecting diseases of the breast |
| US6110695A (en) | 1997-12-02 | 2000-08-29 | The Regents Of The University Of California | Modulating the interaction of the chemokine, B Lymphocyte Hemoattractant, and its Receptor, BLR1 |
| ES2313779T3 (es) | 1998-03-13 | 2009-03-01 | The Burnham Institute | Moleculas que migran a diversos organos o tejidos seleccionados. |
| WO1999058658A2 (en) | 1998-05-13 | 1999-11-18 | Epimmune, Inc. | Expression vectors for stimulating an immune response and methods of using the same |
| US20020187472A1 (en) | 2001-03-09 | 2002-12-12 | Preeti Lal | Steap-related protein |
| KR100581443B1 (ko) | 1998-05-22 | 2006-05-23 | 다이이찌 세이야꾸 가부시기가이샤 | 약물복합체 |
| US20030064397A1 (en) | 1998-05-22 | 2003-04-03 | Incyte Genomics, Inc. | Transmembrane protein differentially expressed in prostate and lung tumors |
| WO2002016429A2 (en) | 2000-08-24 | 2002-02-28 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| ATE349722T1 (de) | 1998-07-08 | 2007-01-15 | E Ink Corp | Verbesserte farbige mikroverkapselte elektrophoretische anzeige |
| DE69907977T2 (de) | 1998-08-27 | 2004-07-22 | Spirogen Ltd., Ryde | Pyrrolobenzodiazepine |
| WO2000012130A1 (en) | 1998-08-27 | 2000-03-09 | Smithkline Beecham Corporation | Rp105 agonists and antagonists |
| GB9818732D0 (en) | 1998-08-27 | 1998-10-21 | Univ Portsmouth | Collection of compounds |
| GB9818730D0 (en) | 1998-08-27 | 1998-10-21 | Univ Portsmouth | Collections of compounds |
| GB9818731D0 (en) | 1998-08-27 | 1998-10-21 | Univ Portsmouth | Compounds |
| JP4689781B2 (ja) | 1998-09-03 | 2011-05-25 | 独立行政法人科学技術振興機構 | アミノ酸輸送蛋白及びその遺伝子 |
| AU5963699A (en) | 1998-10-02 | 2000-04-26 | Mcmaster University | Spliced form of (erb)b-2/neu oncogene |
| US20020119158A1 (en) | 1998-12-17 | 2002-08-29 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| US6858710B2 (en) | 1998-12-17 | 2005-02-22 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| US6468546B1 (en) | 1998-12-17 | 2002-10-22 | Corixa Corporation | Compositions and methods for therapy and diagnosis of ovarian cancer |
| US6962980B2 (en) | 1999-09-24 | 2005-11-08 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| US20030091580A1 (en) | 2001-06-18 | 2003-05-15 | Mitcham Jennifer L. | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| HK1041009B (en) | 1998-12-30 | 2009-05-08 | Beth Israel Deaconess Medical Center, Inc. | Characterization of the soc/crac calcium channel protein family |
| US20030187196A1 (en) | 1998-12-30 | 2003-10-02 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| ES2348708T3 (es) | 1999-01-29 | 2010-12-13 | Corixa Corporation | Proteinas de fusion de her-2/neu. |
| GB9905124D0 (en) | 1999-03-05 | 1999-04-28 | Smithkline Beecham Biolog | Novel compounds |
| AU3395900A (en) | 1999-03-12 | 2000-10-04 | Human Genome Sciences, Inc. | Human lung cancer associated gene sequences and polypeptides |
| US7304126B2 (en) | 1999-05-11 | 2007-12-04 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US6268488B1 (en) | 1999-05-25 | 2001-07-31 | Barbas, Iii Carlos F. | Prodrug activation using catalytic antibodies |
| AU4952600A (en) | 1999-06-03 | 2000-12-28 | Takeda Chemical Industries Ltd. | Screening method with the use of cd100 |
| PT2283866E (pt) | 1999-06-25 | 2015-07-20 | Genentech Inc | Métodos de tratamento utilizando conjugados de anticorpo anti-erbb-maitansinóide |
| US6302318B1 (en) | 1999-06-29 | 2001-10-16 | General Electric Company | Method of providing wear-resistant coatings, and related articles |
| US7589172B2 (en) | 1999-07-20 | 2009-09-15 | Genentech, Inc. | PRO256 polypeptides |
| US7297770B2 (en) | 1999-08-10 | 2007-11-20 | Genentech, Inc. | PRO6496 polypeptides |
| US7294696B2 (en) | 1999-08-17 | 2007-11-13 | Genentech Inc. | PRO7168 polypeptides |
| US6909006B1 (en) | 1999-08-27 | 2005-06-21 | Spirogen Limited | Cyclopropylindole derivatives |
| JP3951035B2 (ja) | 1999-09-01 | 2007-08-01 | ジェネンテック・インコーポレーテッド | 分泌及び膜貫通ポリペプチドとそれをコードしている核酸 |
| US20030129192A1 (en) | 1999-09-10 | 2003-07-10 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| US20030206918A1 (en) | 1999-09-10 | 2003-11-06 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| US20030232056A1 (en) | 1999-09-10 | 2003-12-18 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of ovarian cancer |
| AU778199B2 (en) | 1999-10-29 | 2004-11-25 | Genentech Inc. | Anti-prostate stem cell antigen (PSCA) antibody compositions and methods of use |
| EP2363403B1 (en) | 1999-11-29 | 2016-04-20 | The Trustees of Columbia University in the City of New York | Isolation of five novel genes coding for new fc receptors-type melanoma involved in the pathogenesis of lymphoma/melanoma |
| CA2392510A1 (en) | 1999-11-30 | 2001-06-07 | Corixa Corporation | Compositions and methods for therapy and diagnosis of breast cancer |
| WO2001041787A1 (en) | 1999-12-10 | 2001-06-14 | Epimmune Inc. | INDUCING CELLULAR IMMUNE RESPONSES TO HER2/neu USING PEPTIDE AND NUCLEIC ACID COMPOSITIONS |
| DE60040240D1 (de) | 1999-12-23 | 2008-10-23 | Zymogenetics Inc | Löslicher interleukin-20 rezeptor |
| EP1743648B1 (en) | 1999-12-23 | 2010-03-03 | ZymoGenetics, Inc. | Method for treating inflammation |
| US6610286B2 (en) | 1999-12-23 | 2003-08-26 | Zymogenetics, Inc. | Method for treating inflammation using soluble receptors to interleukin-20 |
| NZ502058A (en) | 1999-12-23 | 2003-11-28 | Ovita Ltd | Isolated mutated nucleic acid molecule for regulation of ovulation rate |
| US20040001827A1 (en) | 2002-06-28 | 2004-01-01 | Dennis Mark S. | Serum albumin binding peptides for tumor targeting |
| AU784285B2 (en) | 1999-12-24 | 2006-03-02 | Genentech Inc. | Methods and compositions for prolonging elimination half-times of bioactive compounds |
| US7294695B2 (en) | 2000-01-20 | 2007-11-13 | Genentech, Inc. | PRO10268 polypeptides |
| US20030224379A1 (en) | 2000-01-21 | 2003-12-04 | Tang Y. Tom | Novel nucleic acids and polypeptides |
| AU2001234493A1 (en) | 2000-01-21 | 2001-07-31 | Corixa Corporation | Compounds and methods for prevention and treatment of her-2/neu associated malignancies |
| AU2001243142A1 (en) | 2000-02-03 | 2001-08-14 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| US20030104562A1 (en) | 2000-02-11 | 2003-06-05 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| WO2001062794A2 (en) | 2000-02-22 | 2001-08-30 | Millennium Pharmaceuticals, Inc. | 18607, a human calcium channel |
| US20030219806A1 (en) | 2000-02-22 | 2003-11-27 | Millennium Pharmaceuticals, Inc. | Novel 18607, 15603, 69318, 12303, 48000, 52920, 5433, 38554, 57301, 58324, 55063, 52991, 59914, 59921 and 33751 molecules and uses therefor |
| US20040052793A1 (en) | 2001-02-22 | 2004-03-18 | Carter Paul J. | Caspase activivated prodrugs therapy |
| US20040005561A1 (en) | 2000-03-01 | 2004-01-08 | Corixa Corporation | Compositions and methods for the detection, diagnosis and therapy of hematological malignancies |
| US20040002068A1 (en) | 2000-03-01 | 2004-01-01 | Corixa Corporation | Compositions and methods for the detection, diagnosis and therapy of hematological malignancies |
| CA2402293A1 (en) | 2000-03-07 | 2001-09-13 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| AU4941101A (en) | 2000-03-24 | 2001-10-08 | Fahri Saatcioglu | Novel prostate-specific or testis-specific nucleic acid molecules, polypeptides,and diagnostic and therapeutic methods |
| WO2001072830A2 (de) | 2000-03-31 | 2001-10-04 | Ipf Pharmaceuticals Gmbh | Diagnostik- und arzneimittel zur untersuchung des zelloberflächenproteoms von tumor- und entzündungszellen sowie zur behandlung von tumorerkrankungen und entzündlichen erkrankungen vorzugsweise mit hilfe einer spezifischen chemokinrezeptor-analyse und der chemokinrezeptor-ligand-interaktion |
| AU2001253140A1 (en) | 2000-04-03 | 2001-10-15 | The Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services | Tumor markers in ovarian cancer |
| IL152136A0 (en) | 2000-04-07 | 2003-05-29 | Arena Pharm Inc | Non-endogenous, constitutively activated known g protein-coupled receptors |
| AU2001263105A1 (en) | 2000-05-18 | 2001-11-26 | Lexicon Genetics Incorporated | Human semaphorin homologs and polynucleotides encoding the same |
| WO2001090304A2 (en) | 2000-05-19 | 2001-11-29 | Human Genome Sciences, Inc. | Nucleic acids, proteins, and antibodies |
| WO2001094641A2 (en) | 2000-06-09 | 2001-12-13 | Idec Pharmaceuticals Corporation | Gene targets and ligands that bind thereto for treatment and diagnosis of ovarian carcinomas |
| CA2409776A1 (en) | 2000-06-16 | 2001-12-27 | Incyte Genomics, Inc. | G-protein coupled receptors |
| AU2001271714A1 (en) | 2000-06-30 | 2002-01-14 | Human Genome Sciences, Inc. | B7-like polynucleotides, polypeptides, and antibodies |
| JP2004528003A (ja) | 2000-06-30 | 2004-09-16 | インサイト・ゲノミックス・インコーポレイテッド | 細胞外マトリクスおよび細胞接着分子 |
| US20020165347A1 (en) | 2000-06-30 | 2002-11-07 | Amgen, Inc. | B7-like molecules and uses thereof |
| AU2002214531A1 (en) | 2000-07-03 | 2002-01-30 | Curagen Corporation | Proteins and nucleic acids encoding same |
| US20040044179A1 (en) | 2000-07-25 | 2004-03-04 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| AU2001283507A1 (en) | 2000-07-27 | 2002-02-13 | Mayo Foundation For Medical Education And Research | B7-h3 and b7-h4, novel immunoregulatory molecules |
| EP1366158B1 (en) | 2000-07-28 | 2008-05-21 | Ulrich Wissenbach | Trp8 markers for cancer |
| US7229623B1 (en) | 2000-08-03 | 2007-06-12 | Corixa Corporation | Her-2/neu fusion proteins |
| AU2001283360A1 (en) | 2000-08-14 | 2002-02-25 | Corixa Corporation | Methods for diagnosis and therapy of hematological and virus-associated malignancies |
| JP2004522412A (ja) | 2000-08-14 | 2004-07-29 | コリクサ コーポレイション | Her−2/neu−関連悪性腫瘍の治療および診断のための組成物および方法 |
| GB0020953D0 (en) | 2000-08-24 | 2000-10-11 | Smithkline Beecham Biolog | Vaccine |
| EP1346040A2 (en) | 2000-09-11 | 2003-09-24 | Nuvelo, Inc. | Novel nucleic acids and polypeptides |
| US7582293B2 (en) | 2000-09-15 | 2009-09-01 | Genentech, Inc. | Anti-PRO6308 antibodies |
| ATE333888T1 (de) | 2000-09-15 | 2006-08-15 | Zymogenetics Inc | Verwendung eines polypeptids, welches die extrazelluläre domäne von il-20ra und il-20rb enthält, zur behandlung von entzündungen |
| US6613567B1 (en) | 2000-09-15 | 2003-09-02 | Isis Pharmaceuticals, Inc. | Antisense inhibition of Her-2 expression |
| CA2422814A1 (en) | 2000-09-18 | 2002-03-21 | Biogen, Inc. | Cripto mutant and uses thereof |
| UA83458C2 (uk) | 2000-09-18 | 2008-07-25 | Байоджен Айдек Ма Інк. | Виділений поліпептид baff-r (рецептор фактора активації в-клітин сімейства tnf) |
| JP5010089B2 (ja) | 2000-09-19 | 2012-08-29 | スピロジェン リミテッド | Cc−1065およびデュオカルマイシンのアキラルアナログの組成物およびその使用方法 |
| AU2002215345A1 (en) | 2000-10-13 | 2002-04-22 | Eos Biotechnology, Inc. | Methods of diagnosis of prostate cancer, compositions and methods of screening for modulators of prostate cancer |
| ATE432986T1 (de) | 2000-11-07 | 2009-06-15 | Zymogenetics Inc | Menschlicher rezeptor für tumor necrosis factor |
| US20020150573A1 (en) | 2000-11-10 | 2002-10-17 | The Rockefeller University | Anti-Igalpha-Igbeta antibody for lymphoma therapy |
| US20040018194A1 (en) | 2000-11-28 | 2004-01-29 | Francisco Joseph A. | Recombinant anti-CD30 antibodies and uses thereof |
| WO2002061087A2 (en) | 2000-12-19 | 2002-08-08 | Lifespan Biosciences, Inc. | Antigenic peptides, such as for g protein-coupled receptors (gpcrs), antibodies thereto, and systems for identifying such antigenic peptides |
| AU2002243495A1 (en) | 2001-01-12 | 2002-07-24 | University Of Medicine And Dentistry Of New Jersey | Bone morphogenetic protein-2 in the treatment and diagnosis of cancer |
| US20030119133A1 (en) | 2001-01-16 | 2003-06-26 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US20030119125A1 (en) | 2001-01-16 | 2003-06-26 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| WO2002059377A2 (en) | 2001-01-24 | 2002-08-01 | Protein Design Labs | Methods of diagnosis of breast cancer, compositions and methods of screening for modulators of breast cancer |
| AU2002251841A1 (en) | 2001-01-30 | 2002-08-12 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of pancreatic cancer |
| WO2002064775A1 (en) | 2001-02-12 | 2002-08-22 | Bionomics Limited | Identification of genes involved in the tumourigenic process |
| US20030087250A1 (en) | 2001-03-14 | 2003-05-08 | Millennium Pharmaceuticals, Inc. | Nucleic acid molecules and proteins for the identification, assessment, prevention, and therapy of ovarian cancer |
| EP1243276A1 (en) | 2001-03-23 | 2002-09-25 | Franciscus Marinus Hendrikus De Groot | Elongated and multiple spacers containing activatible prodrugs |
| US20040236091A1 (en) | 2001-03-28 | 2004-11-25 | Chicz Roman M. | Translational profiling |
| US6362331B1 (en) | 2001-03-30 | 2002-03-26 | Council Of Scientific And Industrial Research | Process for the preparation of antitumor agents |
| WO2003008537A2 (en) | 2001-04-06 | 2003-01-30 | Mannkind Corporation | Epitope sequences |
| US6820011B2 (en) | 2001-04-11 | 2004-11-16 | The Regents Of The University Of Colorado | Three-dimensional structure of complement receptor type 2 and uses thereof |
| AU2002254615A1 (en) | 2001-04-17 | 2002-10-28 | The Board Of Trustees Of The University Of Arkansas | Repeat sequences of the ca125 gene and their use for diagnostic and therapeutic interventions |
| JP2005527180A (ja) | 2001-04-18 | 2005-09-15 | プロテイン デザイン ラブス, インコーポレイテッド | 肺がんの診断方法、肺がんの修飾因子の組成及びスクリーニングの方法 |
| HUP0501113A3 (en) | 2001-04-26 | 2007-12-28 | Biogen Idec Inc | Cripto blocking antibodies and uses thereof |
| US6884869B2 (en) | 2001-04-30 | 2005-04-26 | Seattle Genetics, Inc. | Pentapeptide compounds and uses related thereto |
| JP2005504513A (ja) | 2001-05-09 | 2005-02-17 | コリクサ コーポレイション | 前立腺癌の治療及び診断のための組成物及び方法 |
| WO2002092836A2 (en) | 2001-05-11 | 2002-11-21 | Sloan-Kettering Institute For Cancer Research | Nucleic acid sequence encoding ovarian antigen, ca125, and uses thereof |
| ATE446771T1 (de) | 2001-05-24 | 2009-11-15 | Zymogenetics Inc | Taci-immunoglobulin-fusionsproteine |
| US7157558B2 (en) | 2001-06-01 | 2007-01-02 | Genentech, Inc. | Polypeptide encoded by a polynucleotide overexpresses in tumors |
| AU2002314901A1 (en) | 2001-06-04 | 2002-12-16 | Eos Biotechnology, Inc. | Methods of diagnosis and treatment of androgen-dependent prostate cancer, prostate cancer undergoing androgen-withdrawal, and androgen-independent prostate cancer |
| WO2003000842A2 (en) | 2001-06-04 | 2003-01-03 | Curagen Corporation | Novel proteins and nucleic acids encoding same |
| EP1572872A2 (en) | 2001-06-05 | 2005-09-14 | Exelixis, Inc. | Igs as modifiers of the p53 pathway and methods of use |
| WO2002099140A1 (en) | 2001-06-05 | 2002-12-12 | Exelixis, Inc. | GLRAs AS MODIFIERS OF THE p53 PATHWAY AND METHODS OF USE |
| US7235358B2 (en) | 2001-06-08 | 2007-06-26 | Expression Diagnostics, Inc. | Methods and compositions for diagnosing and monitoring transplant rejection |
| US7125663B2 (en) | 2001-06-13 | 2006-10-24 | Millenium Pharmaceuticals, Inc. | Genes, compositions, kits and methods for identification, assessment, prevention, and therapy of cervical cancer |
| US7189507B2 (en) | 2001-06-18 | 2007-03-13 | Pdl Biopharma, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| CA2451465A1 (en) | 2001-06-18 | 2002-12-27 | Eos Biotechnology Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| US7705120B2 (en) | 2001-06-21 | 2010-04-27 | Millennium Pharmaceuticals, Inc. | Compositions, kits, and methods for identification, assessment, prevention, and therapy of breast cancer |
| US20030108958A1 (en) | 2001-06-28 | 2003-06-12 | Rene De Waal Malefyt | Biological activity of AK155 |
| AU2002314433A1 (en) | 2001-07-02 | 2003-01-21 | Licentia Ltd. | Ephrin-tie receptor materials and methods |
| US20040076955A1 (en) | 2001-07-03 | 2004-04-22 | Eos Biotechnology, Inc. | Methods of diagnosis of bladder cancer, compositions and methods of screening for modulators of bladder cancer |
| WO2003003984A2 (en) | 2001-07-05 | 2003-01-16 | Curagen Corporation | Novel proteins and nucleic acids encoding same |
| US7446185B2 (en) | 2001-07-18 | 2008-11-04 | The Regents Of The University Of California | Her2/neu target antigen and use of same to stimulate an immune response |
| US20030108963A1 (en) | 2001-07-25 | 2003-06-12 | Millennium Pharmaceuticals, Inc. | Novel genes, compositions, kit, and methods for identification, assessment, prevention and therapy of prostate cancer |
| EA007984B1 (ru) | 2001-08-03 | 2007-02-27 | Дженентек, Инк. | ПОЛИПЕПТИДЫ TACIs И BR3 И ИХ ПРИМЕНЕНИЕ |
| WO2003016475A2 (en) | 2001-08-14 | 2003-02-27 | The General Hospital Corporation | Nucleic acid and amino acid sequences involved in pain |
| US20030092013A1 (en) | 2001-08-16 | 2003-05-15 | Vitivity, Inc. | Diagnosis and treatment of vascular disease |
| AU2002313559A1 (en) | 2001-08-23 | 2003-03-10 | Oxford Biomedica (Uk) Limited | Genes |
| WO2003029262A2 (en) | 2001-08-29 | 2003-04-10 | Vanderbilt University | The human mob-5 (il-24) receptors and uses thereof |
| US20030124579A1 (en) | 2001-09-05 | 2003-07-03 | Eos Biotechnology, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| EP1429793B1 (en) | 2001-09-06 | 2015-02-25 | Agensys, Inc. | Nucleic acid and corresponding protein entitled steap-1 useful in treatment and detection of cancer |
| AU2002330039A1 (en) | 2001-09-17 | 2003-04-01 | Eos Biotechnology, Inc. | Methods of diagnosis of cancer compositions and methods of screening for modulators of cancer |
| IL160933A0 (en) | 2001-09-18 | 2004-08-31 | Proteologics Inc | Methods and compositions for treating ?cap associated diseases |
| EP2143438B1 (en) | 2001-09-18 | 2011-07-13 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumors |
| CA2460621A1 (en) | 2001-09-19 | 2003-03-27 | Nuvelo, Inc. | Novel nucleic acids and polypeptides |
| US7091186B2 (en) | 2001-09-24 | 2006-08-15 | Seattle Genetics, Inc. | p-Amidobenzylethers in drug delivery agents |
| WO2003026577A2 (en) | 2001-09-24 | 2003-04-03 | Seattle Genetics, Inc. | P-amidobenzylethers in drug delivery agents |
| AU2002327792A1 (en) | 2001-09-28 | 2003-04-07 | Bing Yang | Diagnosis and treatment of diseases caused by mutations in cd72 |
| WO2003029421A2 (en) | 2001-10-03 | 2003-04-10 | Origene Technologies, Inc. | Regulated breast cancer genes |
| AU2002362436A1 (en) | 2001-10-03 | 2003-04-14 | Rigel Pharmaceuticals, Inc. | Modulators of lymphocyte activation and migration |
| CA2675409A1 (en) | 2001-10-19 | 2003-05-01 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of inflammatory bowel disorders |
| US20040241703A1 (en) | 2002-08-19 | 2004-12-02 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| US20050123925A1 (en) | 2002-11-15 | 2005-06-09 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| EP1525213B1 (en) | 2001-10-24 | 2012-06-27 | National Jewish Health | Three-dimensional structures of tall-1 and its cognate receptors and modified proteins and methods related thereto |
| US7405192B2 (en) | 2001-10-31 | 2008-07-29 | Alcon, Inc. | Bone morphogenic proteins (BMP), BMP receptors and BMP binding proteins and their use in the diagnosis and treatment of glaucoma |
| WO2003042661A2 (en) | 2001-11-13 | 2003-05-22 | Protein Design Labs, Inc. | Methods of diagnosis of cancer, compositions and methods of screening for modulators of cancer |
| US20030232350A1 (en) | 2001-11-13 | 2003-12-18 | Eos Biotechnology, Inc. | Methods of diagnosis of cancer, compositions and methods of screening for modulators of cancer |
| US20050123536A1 (en) | 2001-11-20 | 2005-06-09 | Che-Leung Law | Treatment of immunological disorders using anti-dc30 antibodies |
| EP1448226A1 (en) | 2001-11-29 | 2004-08-25 | Genset S.A. | Agonists and antagonists of prolixin for the treatment of metabolic disorders |
| WO2003048202A2 (en) | 2001-12-03 | 2003-06-12 | Asahi Kasei Pharma Corporation | Nf-kappab activating genes |
| PT1461428E (pt) | 2001-12-03 | 2012-05-29 | Alexion Pharma Inc | Método para produção de anticorpos híbridos |
| WO2003054152A2 (en) | 2001-12-10 | 2003-07-03 | Nuvelo, Inc. | Novel nucleic acids and polypeptides |
| WO2003057730A1 (en) | 2002-01-07 | 2003-07-17 | Euroscreen S.A. | Ligand for g-protein coupled receptor gpr43 and uses thereof |
| US20030134790A1 (en) | 2002-01-11 | 2003-07-17 | University Of Medicine And Dentistry Of New Jersey | Bone Morphogenetic Protein-2 And Bone Morphogenetic Protein-4 In The Treatment And Diagnosis Of Cancer |
| JP4133832B2 (ja) | 2002-01-16 | 2008-08-13 | 独立行政法人科学技術振興機構 | カラー動画ホログラフィ再生装置 |
| US7452675B2 (en) | 2002-01-25 | 2008-11-18 | The Queen's Medical Center | Methods of screening for TRPM4b modulators |
| CN1646161A (zh) | 2002-02-21 | 2005-07-27 | 杜克大学 | 自身免疫疾病的药剂和治疗方法 |
| JP2005535290A (ja) | 2002-02-22 | 2005-11-24 | ジェネンテック・インコーポレーテッド | 免疫関連疾患の治療のための組成物と方法 |
| WO2003074662A2 (en) | 2002-03-01 | 2003-09-12 | Exelixis, Inc. | SCDs AS MODIFIERS OF THE p53 PATHWAY AND METHODS OF USE |
| WO2003101400A2 (en) | 2002-06-04 | 2003-12-11 | Avalon Pharmaceuticals, Inc. | Cancer-linked gene as target for chemotherapy |
| US6660856B2 (en) | 2002-03-08 | 2003-12-09 | Kaohsiung Medical University | Synthesis of pyrrolo[2,1-c][1,4]benzodiazepine analogues |
| EP2258712A3 (en) | 2002-03-15 | 2011-05-04 | Multicell Immunotherapeutics, Inc. | Compositions and Methods to Initiate or Enhance Antibody and Major-histocompatibility Class I or Class II-restricted T Cell Responses by Using Immunomodulatory, Non-coding RNA Motifs |
| CA2486490A1 (en) | 2002-03-19 | 2003-12-31 | Curagen Corporation | Therapeutic polypeptides, nucleic acids encoding same, and methods of use |
| EP1579186A4 (en) | 2002-03-21 | 2008-10-08 | Sunesis Pharmaceuticals Inc | IDENTIFYING KINASE INHIBITORS |
| US7193069B2 (en) | 2002-03-22 | 2007-03-20 | Research Association For Biotechnology | Full-length cDNA |
| EP1494693B1 (en) | 2002-03-22 | 2010-12-08 | Biogen Idec MA Inc. | Cripto-specific antibodies |
| EP1490085A2 (en) | 2002-03-25 | 2004-12-29 | Uab Research Foundation | Fc receptor homolog, reagents, and uses thereof |
| WO2003083074A2 (en) | 2002-03-28 | 2003-10-09 | Idec Pharmaceuticals Corporation | Novel gene targets and ligands that bind thereto for treatment and diagnosis of colon carcinomas |
| US20030194704A1 (en) | 2002-04-03 | 2003-10-16 | Penn Sharron Gaynor | Human genome-derived single exon nucleic acid probes useful for gene expression analysis two |
| CA2481503A1 (en) | 2002-04-05 | 2003-10-23 | Agensys, Inc. | Nucleic acid and corresponding protein entitled 98p4b6 useful in treatment and detection of cancer |
| WO2003087768A2 (en) | 2002-04-12 | 2003-10-23 | Mitokor | Targets for therapeutic intervention identified in the mitochondrial proteome |
| AU2003230874A1 (en) | 2002-04-16 | 2003-11-03 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| WO2003089904A2 (en) | 2002-04-17 | 2003-10-30 | Baylor College Of Medicine | Aib1 as a prognostic marker and predictor of resistance to encocrine therapy |
| AU2003228869A1 (en) | 2002-05-03 | 2003-11-17 | Incyte Corporation | Transporters and ion channels |
| EP1572925A4 (en) | 2002-05-15 | 2007-08-15 | Avalon Pharmaceuticals | CANCER-ASSOCIATED GENE AS A TARGET FOR CHEMOTHERAPY |
| AU2003232453A1 (en) | 2002-05-30 | 2003-12-19 | David K. Bol | Human solute carrier family 7 member 11 (hslc7a11) |
| WO2003101283A2 (en) | 2002-06-04 | 2003-12-11 | Incyte Corporation | Diagnostics markers for lung cancer |
| AU2003241179C1 (en) | 2002-06-06 | 2010-11-25 | Oncotherapy Science, Inc. | Genes and polypeptides relating to human colon cancers |
| AU2003242633A1 (en) | 2002-06-06 | 2003-12-22 | Molecular Engines Laboratories | Dudulin genes, non-human animal model: uses in human hematological disease |
| AU2003249691A1 (en) | 2002-06-07 | 2003-12-22 | Avalon Pharmaceuticals, Inc | Cancer-linked gene as target for chemotherapy |
| AU2003245441A1 (en) | 2002-06-12 | 2003-12-31 | Avalon Pharmaceuticals, Inc. | Cancer-linked gene as target for chemotherapy |
| JP2005533794A (ja) | 2002-06-18 | 2005-11-10 | アーケミックス コーポレイション | アプタマー−毒素分子およびこれを使用する方法 |
| US20040249130A1 (en) | 2002-06-18 | 2004-12-09 | Martin Stanton | Aptamer-toxin molecules and methods for using same |
| US7304149B2 (en) | 2002-06-20 | 2007-12-04 | Washington University In St. Louis | BTLA nucleic acids |
| EP1534331B1 (en) | 2002-06-21 | 2014-10-29 | Johns Hopkins University School of Medicine | Membrane associated tumor endothelium markers |
| DE10229834A1 (de) | 2002-07-03 | 2004-01-29 | Zinser Textilmaschinen Gmbh | Streckwerk für Spinnmaschinen mit nachgeordneter Verdichtungsvorrichtung |
| AU2003281515A1 (en) | 2002-07-19 | 2004-02-09 | Cellzome Ag | Protein complexes of cellular networks underlying the development of cancer and other diseases |
| MXPA05000940A (es) | 2002-07-25 | 2005-05-16 | Genentech Inc | Anticuerpos taci y su uso. |
| EP2353611B1 (en) | 2002-07-31 | 2015-05-13 | Seattle Genetics, Inc. | Drug conjugates and their use for treating cancer, an autoimmune disease or an infectious disease |
| WO2004032828A2 (en) | 2002-07-31 | 2004-04-22 | Seattle Genetics, Inc. | Anti-cd20 antibody-drug conjugates for the treatment of cancer and immune disorders |
| WO2004015426A1 (en) | 2002-08-06 | 2004-02-19 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with human cxc chemokine receptor 5(cxcr5) |
| JP2004121218A (ja) | 2002-08-06 | 2004-04-22 | Jenokkusu Soyaku Kenkyusho:Kk | 気管支喘息または慢性閉塞性肺疾患の検査方法 |
| WO2004020583A2 (en) | 2002-08-27 | 2004-03-11 | Bristol-Myers Squibb Company | Polynucleotide predictor set for identifying protein tyrosine kinase modulators |
| WO2004020595A2 (en) | 2002-08-29 | 2004-03-11 | Five Prime Therapeutics, Inc. | Novel human polypeptides encoded by polynucleotides |
| AU2003256038A1 (en) | 2002-08-30 | 2004-03-19 | Ramot At Tel Aviv University Ltd. | Self-immolative dendrimers releasing many active moieties upon a single activating event |
| AU2002951346A0 (en) | 2002-09-05 | 2002-09-26 | Garvan Institute Of Medical Research | Diagnosis of ovarian cancer |
| EP1545610A4 (en) | 2002-09-06 | 2006-11-08 | Mannkind Corp | EPITOPE SEQUENCES |
| WO2004040000A2 (en) | 2002-09-09 | 2004-05-13 | Nura, Inc | G protein coupled receptors and uses thereof |
| JP2004113151A (ja) | 2002-09-27 | 2004-04-15 | Sankyo Co Ltd | 癌遺伝子及びその用途 |
| CA2500978A1 (en) | 2002-10-03 | 2004-04-15 | Mcgill University | Antibodies and cyclic peptides which bind cea (carcinoembryonic antigen) and their use as cancer therapeutics |
| US20060183120A1 (en) | 2002-10-04 | 2006-08-17 | Teh Bin T | Molecular sub-classification of kidney tumors and the discovery of new diagnostic markers |
| US20040138269A1 (en) | 2002-10-11 | 2004-07-15 | Sugen, Inc. | Substituted pyrroles as kinase inhibitors |
| EP1581169A4 (en) | 2002-11-08 | 2008-09-17 | Genentech Inc | COMPOSITIONS AND METHODS FOR THE TREATMENT OF DISEASES RELATED TO NATURAL KILLER CELLS |
| WO2004044178A2 (en) | 2002-11-13 | 2004-05-27 | Genentech, Inc. | Methods and compositions for diagnosing dysplasia |
| GB0226593D0 (en) | 2002-11-14 | 2002-12-24 | Consultants Ltd | Compounds |
| AU2003282624A1 (en) | 2002-11-14 | 2004-06-03 | Syntarga B.V. | Prodrugs built as multiple self-elimination-release spacers |
| WO2004045520A2 (en) | 2002-11-15 | 2004-06-03 | Musc Foundation For Research Development | Complement receptor 2 targeted complement modulators |
| MXPA05005237A (es) | 2002-11-15 | 2005-08-16 | Univ Arkansas | Gen ca125 y su uso para diagnostico e intervenciones terapeuticas. |
| AU2003297300A1 (en) | 2002-11-20 | 2004-06-15 | Biogen Idec Inc. | Novel gene targets and ligands that bind thereto for treatment and diagnosis of carcinomas |
| US7557092B2 (en) | 2002-11-21 | 2009-07-07 | University Of Utah Research Foundation | Purinergic modulation of smell |
| AU2003298786A1 (en) | 2002-11-26 | 2004-06-18 | Protein Design Labs, Inc. | Methods of detecting soft tissue sarcoma, compositions and methods of screening for soft tissue sarcoma modulators |
| AU2003302774A1 (en) | 2002-12-06 | 2004-06-30 | Diadexus, Inc. | Compositions, splice variants and methods relating to ovarian specific genes and proteins |
| US20040157278A1 (en) | 2002-12-13 | 2004-08-12 | Bayer Corporation | Detection methods using TIMP 1 |
| EP1581171B1 (en) | 2002-12-20 | 2012-06-27 | Abbott Biotherapeutics Corp. | Antibodies against gpr64 and uses thereof |
| AU2003299819A1 (en) | 2002-12-23 | 2004-07-22 | Human Genome Sciences, Inc. | Neutrokine-alpha conjugate, neutrokine-alpha complex, and uses thereof |
| JP2007520995A (ja) | 2003-01-08 | 2007-08-02 | ブリストル−マイヤーズ スクイブ カンパニー | 上皮増殖因子受容体モデュレーターに対する感受性を決定するためのバイオマーカーおよび方法 |
| WO2004063355A2 (en) | 2003-01-10 | 2004-07-29 | Protein Design Labs, Inc. | Novel methods of diagnosis of metastatic cancer, compositions and methods of screening for modulators of matastatic cancer |
| US20050227301A1 (en) | 2003-01-10 | 2005-10-13 | Polgen | Cell cycle progression proteins |
| US20040171823A1 (en) | 2003-01-14 | 2004-09-02 | Nadler Steven G. | Polynucleotides and polypeptides associated with the NF-kappaB pathway |
| JP2007520996A (ja) | 2003-01-15 | 2007-08-02 | ミレニアム・ファーマシューティカルズ・インコーポレイテッド | 44390、54181、211、5687、884、1405、636、4421、5410、30905、2045、16405、18560、2047、33751、52872、14063、20739、32544、43239、44373、51164、53010、16852、1587、2207、22245、2387、52908、69112、14990、18547、115、579、15985、15625、760、18603、2395、2554、8675、32720、4809、14303、16816、17827、32620、577、619、1423、2158、8263、15402、16209、16386、21165、30911、41897、1643、2543、9626、13231、32409、84260、2882、8203、32678または55053を用いて泌尿器科障害を処置するための方法および組成物 |
| EP1594893A2 (en) | 2003-02-14 | 2005-11-16 | Sagres Discovery, Inc. | Therapeutic targets in cancer |
| US20030224411A1 (en) | 2003-03-13 | 2003-12-04 | Stanton Lawrence W. | Genes that are up- or down-regulated during differentiation of human embryonic stem cells |
| DE60326060D1 (de) | 2003-03-31 | 2009-03-19 | Council Scient Ind Res | Nichtvernetzende pyrroloä2,1-cüä1,4übenzodiazepine als potentielle antitumor-agentien und ihre herstellung |
| GB0321295D0 (en) | 2003-09-11 | 2003-10-15 | Spirogen Ltd | Synthesis of protected pyrrolobenzodiazepines |
| GB0416511D0 (en) | 2003-10-22 | 2004-08-25 | Spirogen Ltd | Pyrrolobenzodiazepines |
| ATE516288T1 (de) | 2003-10-22 | 2011-07-15 | Us Gov Health & Human Serv | Pyrrolobenzodiazepinderivate, zusammensetzungen, die diese enthalten, und damit in zusammenhang stehende verfahren |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| AU2005214988A1 (en) | 2004-02-17 | 2005-09-01 | Absalus, Inc. | Super-humanized antibodies against respiratory syncytial virus |
| CA2556752C (en) | 2004-02-23 | 2016-02-02 | Genentech, Inc. | Heterocyclic self-immolative linkers and conjugates |
| GB0404574D0 (en) | 2004-03-01 | 2004-04-07 | Spirogen Ltd | Amino acids |
| GB0404578D0 (en) | 2004-03-01 | 2004-04-07 | Spirogen Ltd | Pyrrolobenzodiazepines |
| GB0404577D0 (en) | 2004-03-01 | 2004-04-07 | Spirogen Ltd | Pyrrolobenzodiazepines |
| EP1720881B9 (en) | 2004-03-01 | 2013-04-17 | Spirogen Sàrl | 11-hydroxy-5h-pyrrolo[2,1-c][1,4]benzodiazepin-5-one derivatives as key intermediates for the preparation of c2 substituted pyrrolobenzodiazepins |
| DE102004010943A1 (de) | 2004-03-03 | 2005-09-29 | Degussa Ag | Verfahren zur Herstellung von N-geschützten 4-Ketprolinderivaten |
| US7528126B2 (en) | 2004-03-09 | 2009-05-05 | Spirogen Limited | Pyrrolobenzodiazepines |
| FR2869231B1 (fr) | 2004-04-27 | 2008-03-14 | Sod Conseils Rech Applic | Composition therapeutique contenant au moins un derive de la pyrrolobenzodiazepine et la fludarabine |
| EP1750614B1 (en) | 2004-05-11 | 2017-09-27 | The General Hospital Corporation | Methods for making oxidation resistant polymeric material |
| GB0410725D0 (en) | 2004-05-13 | 2004-06-16 | Spirogen Ltd | Pyrrolobenzodiazepine therapeutic agents |
| NZ553500A (en) | 2004-09-23 | 2009-11-27 | Genentech Inc Genentech Inc | Cysteine engineered antibodies and conjugates withCysteine engineered antibodies and conjugates with a free cysteine amino acid in the heavy chain a free cysteine amino acid in the heavy chain |
| AU2005316844A1 (en) | 2004-11-29 | 2006-06-22 | Seattle Genetics, Inc. | Engineered antibodies and immunoconjugates |
| EP1831418A2 (en) | 2004-12-24 | 2007-09-12 | Showa Denko Kabushiki Kaisha | Production method of thermoelectric semiconductor alloy, thermoelectric conversion module and thermoelectric power generating device |
| ES2417133T3 (es) | 2005-02-03 | 2013-08-06 | Antitope Limited | Anticuerpos y proteínas humanas |
| EP2511299A1 (en) | 2005-04-19 | 2012-10-17 | Seattle Genetics, Inc. | Humanized anti-CD70 binding agents and uses thereof |
| EP1879901B1 (en) | 2005-04-21 | 2009-12-23 | Spirogen Limited | Pyrrolobenzodiazepines |
| GB0508084D0 (en) | 2005-04-21 | 2005-06-01 | Spirogen Ltd | Pyrrolobenzodiazepines |
| US20070154906A1 (en) | 2005-10-05 | 2007-07-05 | Spirogen Ltd. | Methods to identify therapeutic candidates |
| WO2007039752A1 (en) | 2005-10-05 | 2007-04-12 | Spirogen Limited | Alkyl 4- [4- (5-oxo-2, 3, 5, 11a-tetrahyd0-5h-pyrr0l0 [2, 1-c] [1, 4] benzodiazepine-8-yloxy) -butyrylamino]-1h-pyrrole-2-carboxylate derivatives and related compounds for the treatment of a proliferative disease |
| SI1934174T1 (sl) | 2005-10-07 | 2011-08-31 | Exelixis Inc | Inhibitorji MEK in postopki za njihovo uporabo |
| EP1813614B1 (en) | 2006-01-25 | 2011-10-05 | Sanofi | Cytotoxic agents comprising new tomaymycin derivatives |
| WO2008010101A2 (en) | 2006-07-18 | 2008-01-24 | Sanofi-Aventis | Antagonist antibody against epha2 for the treatment of cancer |
| HRP20140331T1 (hr) | 2006-08-14 | 2014-05-09 | Xencor, Inc. | Optimizirana antitijela usmjerena na cd19 |
| US20080112961A1 (en) | 2006-10-09 | 2008-05-15 | Macrogenics, Inc. | Identification and Engineering of Antibodies with Variant Fc Regions and Methods of Using Same |
| EP1914242A1 (en) | 2006-10-19 | 2008-04-23 | Sanofi-Aventis | Novel anti-CD38 antibodies for the treatment of cancer |
| WO2008050140A2 (en) | 2006-10-27 | 2008-05-02 | Spirogen Limited | Compounds for treatment of parasitic infection |
| PT2099823E (pt) | 2006-12-01 | 2014-12-22 | Seattle Genetics Inc | Agentes de ligação ao alvo variantes e suas utilizações |
| CL2008001334A1 (es) | 2007-05-08 | 2008-09-22 | Genentech Inc | Anticuerpo anti-muc16 disenado con cisteina; conjugado que lo comprende; metodo de produccion; formulacion farmaceutica que lo comprende; y su uso para tratar el cancer. |
| PT2019104E (pt) | 2007-07-19 | 2013-12-03 | Sanofi Sa | Agentes citotóxicos compreendendo novos derivados de tomaimicina e sua utilização terapêutica |
| AU2008312457B2 (en) | 2007-10-19 | 2014-04-17 | Genentech, Inc. | Cysteine engineered anti-TENB2 antibodies and antibody drug conjugates |
| GB0722088D0 (en) | 2007-11-09 | 2007-12-19 | Spirogen Ltd | Pyrrolobenzodiazepines |
| GB0722087D0 (en) | 2007-11-09 | 2007-12-19 | Spirogen Ltd | Polyamides |
| PL2265283T3 (pl) | 2008-03-18 | 2015-03-31 | Seattle Genetics Inc | Koniugaty aurystatyny lek łącznik |
| EP2109244A1 (de) | 2008-04-09 | 2009-10-14 | Siemens Aktiengesellschaft | Verfahren zur sicherheitsgerichteten Übertragung Sicherheitsschaltgerät und Kontrolleinheit |
| CN104524590B (zh) | 2008-04-30 | 2019-06-21 | 伊缪诺金公司 | 交联剂和它们的用途 |
| AU2009271401A1 (en) | 2008-06-16 | 2010-01-21 | Immunogen Inc. | Novel synergistic effects |
| GB0813432D0 (en) | 2008-07-22 | 2008-08-27 | Spirogen Ltd | Pyrrolobenzodiazepines |
| GB0819097D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| GB0819095D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| AU2010210646B2 (en) | 2009-02-05 | 2015-10-29 | Immunogen, Inc. | Novel benzodiazepine derivatives |
| KR20110122859A (ko) | 2009-02-23 | 2011-11-11 | 그렌마크 파머수티칼스 에스. 아. | Cd19에 결합하는 인간화된 항체 및 그것의 용도 |
| JP5382792B2 (ja) | 2009-08-14 | 2014-01-08 | 独立行政法人理化学研究所 | 光2次非線形薄膜における1次及び2次光感受率異方性同時測定方法、当該方法を実行する装置及び当該方法をコンピュータに実行させるプログラム |
| FR2949469A1 (fr) | 2009-08-25 | 2011-03-04 | Sanofi Aventis | Derives anticancereux, leur preparation et leur application en therapeutique |
| NZ598929A (en) | 2009-09-01 | 2014-05-30 | Abbvie Inc | Dual variable domain immunoglobulins and uses thereof |
| US20110070227A1 (en) | 2009-09-18 | 2011-03-24 | Anna-Marie Novotney-Barry | Treatment of Autoimmune and Inflammatory Diseases |
| EP2480230A4 (en) | 2009-09-24 | 2015-06-10 | Seattle Genetics Inc | DR5 Ligand-HEILMITTELKONJUGATE |
| US20110269956A1 (en) | 2009-11-11 | 2011-11-03 | Bristol-Myers Squibb Company | Hepatitis C Virus Inhibitors |
| US9040526B2 (en) | 2010-02-09 | 2015-05-26 | Bristol-Myers Squibb Company | Benzylpyrrolidinone derivatives as modulators of chemokine receptor activity |
| KR20130009760A (ko) | 2010-02-10 | 2013-01-23 | 이뮤노젠 아이엔씨 | Cd20 항체 및 이의 용도 |
| WO2011100398A1 (en) | 2010-02-10 | 2011-08-18 | Immunogen, Inc. | Cd20 antibodies and uses thereof |
| NZ602933A (en) | 2010-04-15 | 2014-09-26 | Seattle Genetics Inc | Pyrrolobenzodiazepines used to treat proliferative diseases |
| WO2011130615A2 (en) | 2010-04-15 | 2011-10-20 | Dr. Reddy's Laboratories Ltd. | Preparation of lacosamide |
| GB201006340D0 (en) | 2010-04-15 | 2010-06-02 | Spirogen Ltd | Synthesis method and intermediates |
| JP5870400B2 (ja) | 2010-04-15 | 2016-03-01 | シアトル ジェネティクス,インコーポレーテッド | 標的化ピロロベンゾジアゼピンコンジュゲート |
| MA34277B1 (fr) | 2010-04-15 | 2013-06-01 | Spirogen Developments Sarl | Pyrrolobenzodiazépines et conjugués de celles-ci |
| CN106749665B (zh) | 2010-04-21 | 2021-03-26 | 辛塔佳有限公司 | Cc-1065类似物和双功能接头的缀合物 |
| FR2963007B1 (fr) | 2010-07-26 | 2013-04-05 | Sanofi Aventis | Derives anticancereux, leur preparation et leur application therapeutique |
| CN103153986B (zh) | 2010-08-04 | 2014-11-05 | 百时美施贵宝公司 | 丙型肝炎病毒抑制剂 |
| CN103249730A (zh) | 2010-09-24 | 2013-08-14 | 百时美施贵宝公司 | 丙型肝炎病毒抑制剂 |
| JP6014596B2 (ja) | 2010-11-09 | 2016-10-25 | メディミューン,エルエルシー | 均一コンジュゲーションのための抗体足場 |
| MY183977A (en) | 2011-02-15 | 2021-03-17 | Immunogen Inc | Cytotoxic benzodiazepine derivatives |
| US9135118B2 (en) | 2011-03-07 | 2015-09-15 | Aptare, Inc. | System to catalog and search point-in-time instances of a file system |
| WO2013041606A1 (en) | 2011-09-20 | 2013-03-28 | Spirogen Sàrl | Pyrrolobenzodiazepines as unsymmetrical dimeric pbd compounds for inclusion in targeted conjugates |
| DK2750713T3 (en) | 2011-10-14 | 2015-12-21 | Medimmune Ltd | PYRROLOBENZODIAZEPINS AND CONJUGATES THEREOF |
| JP6393617B2 (ja) | 2011-10-14 | 2018-09-19 | シアトル ジェネティクス,インコーポレーテッド | ピロロベンゾジアゼピンおよび標的コンジュゲート |
| US9102704B2 (en) | 2011-10-14 | 2015-08-11 | Spirogen Sarl | Synthesis method and intermediates useful in the preparation of pyrrolobenzodiazepines |
| EP2751111B1 (en) | 2011-10-14 | 2017-04-26 | MedImmune Limited | Asymmetrical bis-(5H-Pyrrolo[2,1-c][1,4]benzodiazepin-5-one) derivatives for the treatment of proliferative or autoimmune diseases |
| WO2013053871A1 (en) | 2011-10-14 | 2013-04-18 | Spirogen Sàrl | Pyrrolobenzodiazepines |
| AU2012322613B2 (en) | 2011-10-14 | 2016-04-21 | Medimmune Limited | Pyrrolobenzodiazepines and targeted conjugates |
| JP2013194140A (ja) | 2012-03-19 | 2013-09-30 | Fuji Xerox Co Ltd | トナー用ポリエステル樹脂、静電荷像現像用トナー、静電荷像現像剤、トナーカートリッジ、プロセスカートリッジ、画像形成装置及び画像形成方法 |
| BR112014027143B1 (pt) | 2012-04-30 | 2020-06-09 | Medimmune Ltd | pirrolobenzodiazepinas |
| IN2014MN02175A (ja) | 2012-04-30 | 2015-08-28 | Ucl Business Plc | |
| US9062577B2 (en) | 2012-05-14 | 2015-06-23 | Southwest Research Institute | Diesel engine operation for fast transient response and low emissions |
| WO2013177481A1 (en) | 2012-05-25 | 2013-11-28 | Immunogen, Inc. | Benzodiazepines and conjugates thereof |
| KR20150027829A (ko) | 2012-07-09 | 2015-03-12 | 제넨테크, 인크. | 항-cd22 항체를 포함하는 면역접합체 |
| SG11201500093TA (en) | 2012-07-09 | 2015-02-27 | Genentech Inc | Immunoconjugates comprising anti-cd79b antibodies |
| US9464141B2 (en) | 2012-08-02 | 2016-10-11 | Genentech, Inc. | Anti-ETBR antibodies and immunoconjugates |
| HK1211208A1 (zh) | 2012-08-22 | 2016-05-20 | Immunogen, Inc. | 細胞毒性苯並二氮呯衍生物 |
| DK2906248T3 (en) | 2012-10-12 | 2019-03-04 | Medimmune Ltd | Pyrrolobenzodiazepines and their conjugates |
| EP2906249B1 (en) | 2012-10-12 | 2018-06-27 | MedImmune Limited | Synthesis and intermediates of pyrrolobenzodiazepine derivatives for conjugation |
| WO2014057118A1 (en) | 2012-10-12 | 2014-04-17 | Adc Therapeutics Sarl | Pyrrolobenzodiazepine-anti-cd22 antibody conjugates |
| CN104955485B (zh) | 2012-10-12 | 2018-01-30 | Adc疗法责任有限公司 | 吡咯并苯并二氮杂卓‑抗her2抗体结合物 |
| WO2014057114A1 (en) | 2012-10-12 | 2014-04-17 | Adc Therapeutics Sàrl | Pyrrolobenzodiazepine-anti-psma antibody conjugates |
| US9931414B2 (en) | 2012-10-12 | 2018-04-03 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| EP2906296B1 (en) | 2012-10-12 | 2018-03-21 | ADC Therapeutics SA | Pyrrolobenzodiazepine-antibody conjugates |
| US10695433B2 (en) | 2012-10-12 | 2020-06-30 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| JP6270859B2 (ja) | 2012-10-12 | 2018-01-31 | エイディーシー・セラピューティクス・エス・アー・エール・エルAdc Therapeutics Sarl | ピロロベンゾジアゼピン−抗体結合体 |
| JP5993093B2 (ja) | 2012-10-12 | 2016-09-14 | メドイミューン・リミテッドMedImmune Limited | ピロロベンゾジアゼピン類およびその複合体 |
| KR101995621B1 (ko) * | 2012-10-12 | 2019-07-03 | 에이디씨 테라퓨틱스 에스에이 | 피롤로벤조디아제핀-항-cd22 항체 컨주게이트 |
| BR102013027577A2 (pt) | 2012-10-25 | 2016-03-29 | Memorialsloan Kettering Cancer Ct | método de detecção de um nível aumentado de axl ou gas6 e método de identificação de um paciente com câncer resistente a inibidor de egfr |
| JP6133431B2 (ja) | 2012-11-24 | 2017-05-24 | ハンジョウ ディーエーシー バイオテック シーオー.,エルティディ.Hangzhou Dac Biotech Co.,Ltd. | 親水性連結体及び薬物分子と細胞結合分子との共役反応における親水性連結体の使用 |
| AU2013366493B2 (en) | 2012-12-21 | 2017-08-24 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof |
| HK1216176A1 (zh) | 2012-12-21 | 2016-10-21 | Medlmmune Limited | 用於治疗增殖性和自身免疫疾病的非对称吡咯并苯并二氮杂卓二聚物 |
| SMT201900339T1 (it) | 2013-02-22 | 2019-07-11 | Medimmune Ltd | Coniugati anticorpo anti-dll3/pbd e loro usi |
| AU2014230735B2 (en) | 2013-03-13 | 2018-03-15 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof |
| WO2014159981A2 (en) | 2013-03-13 | 2014-10-02 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| AU2014229529B2 (en) | 2013-03-13 | 2018-02-15 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof |
| JP2016518382A (ja) | 2013-04-26 | 2016-06-23 | ピエール、ファーブル、メディカマン | Axl抗体薬物複合体および癌の治療のためのその使用 |
| CA2922544A1 (en) | 2013-08-28 | 2015-03-05 | Stemcentrx, Inc. | Engineered anti-dll3 conjugates and methods of use |
| NZ717003A (en) | 2013-09-02 | 2019-05-31 | Hangzhou Dac Biotech Co Ltd | Novel cytotoxic agents for conjugation of drugs to cell binding molecule |
| NL2011583C2 (en) | 2013-10-10 | 2015-04-13 | Wwinn B V | Module, system and method for detecting acoustical failure of a sound source. |
| GB201317982D0 (en) | 2013-10-11 | 2013-11-27 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| GB201317981D0 (en) | 2013-10-11 | 2013-11-27 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| US9956299B2 (en) | 2013-10-11 | 2018-05-01 | Medimmune Limited | Pyrrolobenzodiazepine—antibody conjugates |
| GB201318069D0 (en) | 2013-10-11 | 2013-11-27 | Maersk Olie & Gas | Seismic data processing method and apparatus |
| DE102013220528B4 (de) | 2013-10-11 | 2015-05-07 | Continental Automotive Gmbh | Einspritzventil und Verfahren zum Betreiben eines Einspritzventils |
| US20160355875A1 (en) | 2013-10-11 | 2016-12-08 | Cellectis | Methods and kits for detecting nucleic acid sequences of interest using dna-binding protein domain |
| EP3054985B1 (en) | 2013-10-11 | 2018-12-26 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| WO2015052533A1 (en) | 2013-10-11 | 2015-04-16 | Spirogen Sàrl | Pyrrolobenzodiazepine-antibody conjugates |
| US10010624B2 (en) | 2013-10-11 | 2018-07-03 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| BR112016014126B1 (pt) | 2013-12-16 | 2023-02-14 | Medimmune Limited | Composto não-peptídico, conjugados de anticorpo-fármaco do mesmo, uso dos ditos conjugados para o tratamento de câncer e composição farmacêutica que compreende os mesmos |
| WO2015112822A1 (en) | 2014-01-24 | 2015-07-30 | Kolltan Pharmaceuticals, Inc. | Antibody-drug conjugates targeting kit receptor and uses thereof |
| ES2719584T3 (es) | 2014-04-11 | 2019-07-11 | Medimmune Llc | Compuestos conjugados que comprenden anticuerpos modificados por ingeniería genética con cisteína |
| GB201406767D0 (en) | 2014-04-15 | 2014-05-28 | Cancer Rec Tech Ltd | Humanized anti-Tn-MUC1 antibodies anf their conjugates |
| CN106687141A (zh) | 2014-09-10 | 2017-05-17 | 麦迪穆有限责任公司 | 吡咯并苯并二氮杂卓及其缀合物 |
| GB201416112D0 (en) | 2014-09-12 | 2014-10-29 | Medimmune Ltd | Pyrrolobenzodiazepines and conjugates thereof |
| BR112017004802A2 (pt) | 2014-09-12 | 2017-12-12 | Genentech Inc | anticorpos anti-cll-1 e imunoconjugados |
| BR112017004953A2 (pt) | 2014-09-17 | 2017-12-05 | Genentech Inc | imunoconjugado, formulação farmacêutica, método de tratamento e método de inibição da proliferação de uma célula |
| SG11201702079UA (en) | 2014-09-17 | 2017-04-27 | Genentech Inc | Pyrrolobenzodiazepines and antibody disulfide conjugates thereof |
| WO2016053107A1 (en) | 2014-10-03 | 2016-04-07 | Synaffix B.V. | Sulfamide linker, conjugates thereof, and methods of preparation |
| GB201506407D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201506388D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Cancer Res Technology Ltd And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201506399D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201506394D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201506402D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201506409D0 (en) | 2015-04-15 | 2015-05-27 | Williams David G And Berkel Patricius H C Van And Howard Philip W | Humanized anti-axl antibodies and their conjugates |
| GB201506393D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| TW201709932A (zh) | 2015-06-12 | 2017-03-16 | 西雅圖遺傳學公司 | Cd123抗體及其共軛物 |
| CN108391434A (zh) | 2015-06-23 | 2018-08-10 | 百时美施贵宝公司 | 大环苯并二氮杂*二聚体、其缀合物、制备和用途 |
| AR106018A1 (es) | 2015-08-26 | 2017-12-06 | Achillion Pharmaceuticals Inc | Compuestos de arilo, heteroarilo y heterocíclicos para el tratamiento de trastornos médicos |
| MA43345A (fr) | 2015-10-02 | 2018-08-08 | Hoffmann La Roche | Conjugués anticorps-médicaments de pyrrolobenzodiazépine et méthodes d'utilisation |
| GB201602359D0 (en) * | 2016-02-10 | 2016-03-23 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| GB201602356D0 (en) | 2016-02-10 | 2016-03-23 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| GB201607478D0 (en) | 2016-04-29 | 2016-06-15 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| WO2017201132A2 (en) | 2016-05-18 | 2017-11-23 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepines and conjugates thereof |
| JP7093767B2 (ja) | 2016-08-11 | 2022-06-30 | ジェネンテック, インコーポレイテッド | ピロロベンゾジアゼピンプロドラッグ及びその抗体コンジュゲート |
| GB201617466D0 (en) | 2016-10-14 | 2016-11-30 | Medimmune Ltd | Pyrrolobenzodiazepine conjugates |
| KR20190083654A (ko) | 2016-11-10 | 2019-07-12 | 메디뮨 엘엘씨 | Asct2에 특이적인 결합 분자 및 이의 용도 |
| GB201702031D0 (en) | 2017-02-08 | 2017-03-22 | Medlmmune Ltd | Pyrrolobenzodiazepine-antibody conjugates |
| WO2018182341A1 (ko) | 2017-03-29 | 2018-10-04 | 주식회사 레고켐 바이오사이언스 | 피롤로벤조디아제핀 이량체 전구체 및 이의 리간드-링커 접합체 화합물 |
| AR111963A1 (es) | 2017-05-26 | 2019-09-04 | Univ California | Método y moléculas |
| TWI885539B (zh) | 2017-09-29 | 2025-06-01 | 日商第一三共股份有限公司 | 抗體-吡咯并苯二氮呯衍生物複合體 |
| AU2018430758B2 (en) | 2018-07-05 | 2022-01-27 | Hangzhou Dac Biotech Co., Ltd | Cross-linked pyrrolobenzodiazepine dimer (PBD) derivative and its conjugates |
-
2020
- 2020-03-13 MX MX2021010477A patent/MX2021010477A/es unknown
- 2020-03-13 WO PCT/EP2020/056761 patent/WO2020187721A1/en not_active Ceased
- 2020-03-13 BR BR112021018260A patent/BR112021018260A2/pt unknown
- 2020-03-13 IL IL286326A patent/IL286326B2/en unknown
- 2020-03-13 SG SG11202108900WA patent/SG11202108900WA/en unknown
- 2020-03-13 EP EP20711857.1A patent/EP3938372B1/en active Active
- 2020-03-13 ES ES20711857T patent/ES2967878T3/es active Active
- 2020-03-13 CA CA3130174A patent/CA3130174A1/en active Pending
- 2020-03-13 AU AU2020242747A patent/AU2020242747B2/en active Active
- 2020-03-13 JP JP2021555569A patent/JP7520870B2/ja active Active
- 2020-03-13 CN CN202080021224.4A patent/CN113631560B/zh active Active
- 2020-03-13 US US17/439,639 patent/US12209099B2/en active Active
- 2020-03-13 KR KR1020217029628A patent/KR102890251B1/ko active Active
-
2021
- 2021-08-18 ZA ZA2021/05931A patent/ZA202105931B/en unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018192944A1 (en) | 2017-04-18 | 2018-10-25 | Medimmune Limited | Pyrrolobenzodiazepine conjugates |
Non-Patent Citations (2)
| Title |
|---|
| Bioorg. Med. Chem.,2004年,12,5427-5436 |
| Tetrahedron Letters,1997年,Vol.38, No.33,5839-5842 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102890251B1 (ko) | 2025-11-25 |
| IL286326B1 (en) | 2025-06-01 |
| IL286326A (en) | 2021-10-31 |
| EP3938372B1 (en) | 2023-10-25 |
| US12209099B2 (en) | 2025-01-28 |
| CN113631560B (zh) | 2025-02-18 |
| US20220160881A1 (en) | 2022-05-26 |
| CN113631560A (zh) | 2021-11-09 |
| ES2967878T3 (es) | 2024-05-06 |
| CA3130174A1 (en) | 2020-09-24 |
| EP3938372A1 (en) | 2022-01-19 |
| SG11202108900WA (en) | 2021-09-29 |
| AU2020242747A1 (en) | 2021-09-16 |
| BR112021018260A2 (pt) | 2021-11-23 |
| IL286326B2 (en) | 2025-10-01 |
| AU2020242747B2 (en) | 2025-09-18 |
| ZA202105931B (en) | 2024-01-31 |
| MX2021010477A (es) | 2021-10-01 |
| KR20210139270A (ko) | 2021-11-22 |
| WO2020187721A1 (en) | 2020-09-24 |
| JP2022524880A (ja) | 2022-05-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102312910B1 (ko) | 피롤로벤조디아제핀 컨쥬게이트 | |
| US20210283141A1 (en) | Pyrrolobenzodiazepine conjugates | |
| US20210380605A1 (en) | Pyrrolobenzodiazepine conjugates | |
| JP7520870B2 (ja) | がんの治療における使用のための、アゼチドベンゾジアゼピン二量体及びこれを含む複合体 | |
| JP7259024B2 (ja) | ピロロベンゾジアゼピン複合体 | |
| HK40058926A (en) | Azetidobenzodiazepine dimers and conjugates comprising them for use in the treatment of cancer | |
| HK40058926B (en) | Azetidobenzodiazepine dimers and conjugates comprising them for use in the treatment of cancer | |
| EA045942B1 (ru) | Азетидобензодиазепиновые димеры и конъюгаты, содержащие их, для применения для лечения рака | |
| TW202308697A (zh) | 吡咯并苯并二氮呯共軛物 | |
| WO2022218970A2 (en) | Pyrrolobenzodiazepine conjugates | |
| HK40025650B (en) | Pyrrolobenzodiazepine conjugates | |
| HK40025650A (en) | Pyrrolobenzodiazepine conjugates | |
| BR112019007612B1 (pt) | Compostos e conjugados de pirrolobenzodiazepina, composições que compreendem ditos conjugados e uso dos mesmos para tratar uma doença proliferativa |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230313 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240222 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240319 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240618 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240702 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240710 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7520870 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |