KR20150027829A - 항-cd22 항체를 포함하는 면역접합체 - Google Patents
항-cd22 항체를 포함하는 면역접합체 Download PDFInfo
- Publication number
- KR20150027829A KR20150027829A KR20157003046A KR20157003046A KR20150027829A KR 20150027829 A KR20150027829 A KR 20150027829A KR 20157003046 A KR20157003046 A KR 20157003046A KR 20157003046 A KR20157003046 A KR 20157003046A KR 20150027829 A KR20150027829 A KR 20150027829A
- Authority
- KR
- South Korea
- Prior art keywords
- antibody
- seq
- amino acid
- acid sequence
- hvr
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 229940127121 immunoconjugate Drugs 0.000 claims abstract description 190
- 238000000034 method Methods 0.000 claims abstract description 109
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 215
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 claims description 137
- 206010028980 Neoplasm Diseases 0.000 claims description 137
- 239000003814 drug Substances 0.000 claims description 129
- 102100038080 B-cell receptor CD22 Human genes 0.000 claims description 122
- 210000004027 cell Anatomy 0.000 claims description 104
- -1 fluoro-substituted phenyl Chemical group 0.000 claims description 100
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 claims description 95
- 241000282414 Homo sapiens Species 0.000 claims description 93
- 125000005647 linker group Chemical group 0.000 claims description 89
- 230000027455 binding Effects 0.000 claims description 67
- 238000009739 binding Methods 0.000 claims description 67
- 125000003118 aryl group Chemical group 0.000 claims description 64
- 125000000217 alkyl group Chemical group 0.000 claims description 54
- 125000000623 heterocyclic group Chemical group 0.000 claims description 53
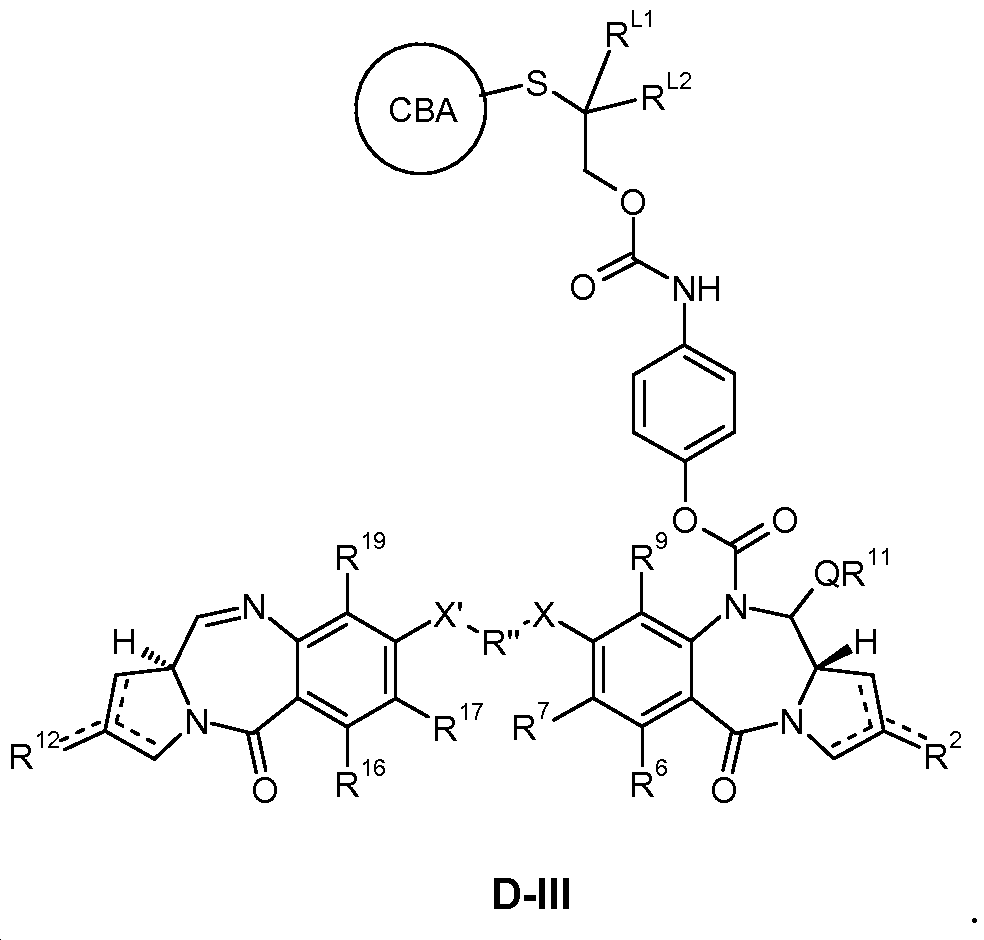
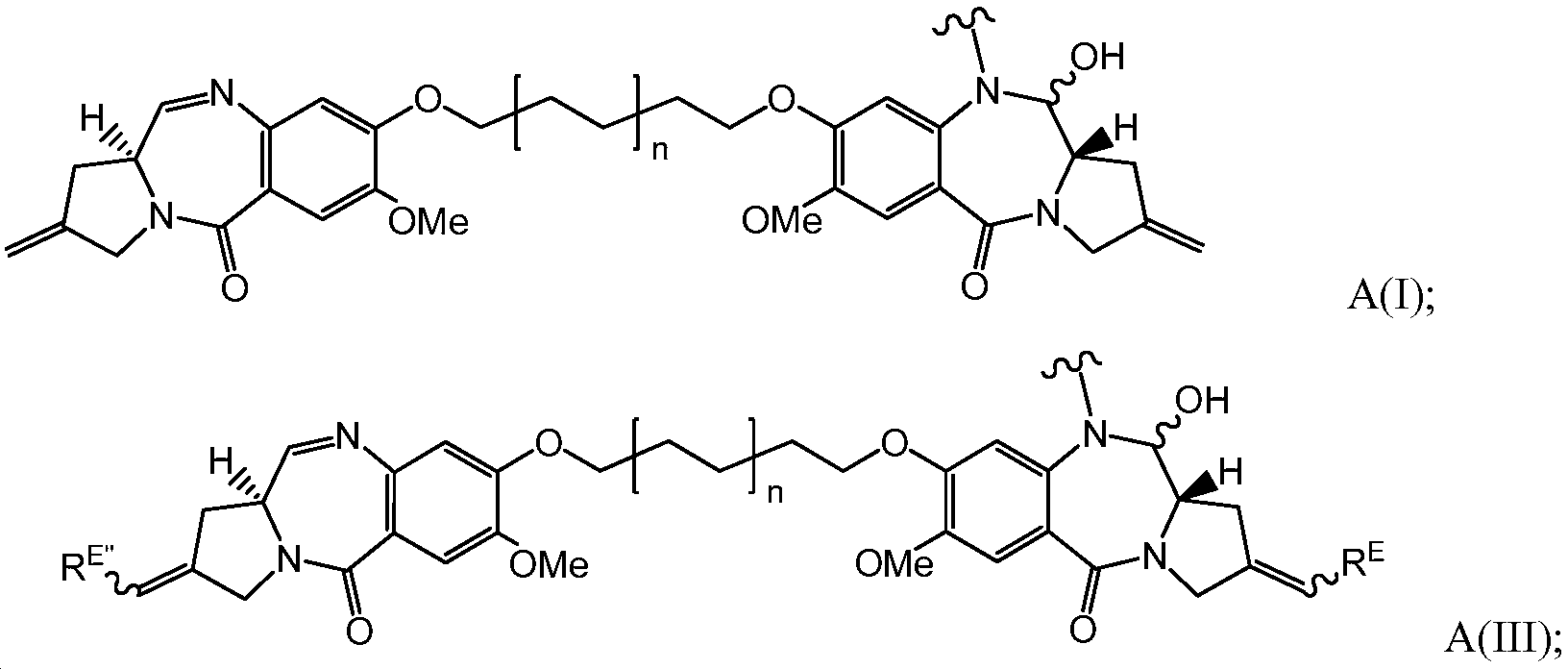
- YUOCYTRGANSSRY-UHFFFAOYSA-N pyrrolo[2,3-i][1,2]benzodiazepine Chemical group C1=CN=NC2=C3C=CN=C3C=CC2=C1 YUOCYTRGANSSRY-UHFFFAOYSA-N 0.000 claims description 51
- 206010025323 Lymphomas Diseases 0.000 claims description 40
- 201000011510 cancer Diseases 0.000 claims description 38
- 150000001413 amino acids Chemical class 0.000 claims description 33
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 28
- 229940127089 cytotoxic agent Drugs 0.000 claims description 27
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 claims description 25
- 150000001875 compounds Chemical class 0.000 claims description 24
- 239000002254 cytotoxic agent Substances 0.000 claims description 24
- 231100000599 cytotoxic agent Toxicity 0.000 claims description 24
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 claims description 23
- 125000005843 halogen group Chemical group 0.000 claims description 22
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 21
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 21
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 21
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 20
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 20
- 229940124597 therapeutic agent Drugs 0.000 claims description 20
- 239000000126 substance Substances 0.000 claims description 19
- 201000009277 hairy cell leukemia Diseases 0.000 claims description 18
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 claims description 16
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 claims description 16
- 102000044389 human CD22 Human genes 0.000 claims description 15
- 208000032839 leukemia Diseases 0.000 claims description 14
- 229910052757 nitrogen Inorganic materials 0.000 claims description 14
- 125000004432 carbon atom Chemical group C* 0.000 claims description 13
- 125000005842 heteroatom Chemical group 0.000 claims description 13
- 229910052760 oxygen Inorganic materials 0.000 claims description 13
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 claims description 12
- 108091005804 Peptidases Proteins 0.000 claims description 12
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 claims description 12
- 239000004365 Protease Substances 0.000 claims description 12
- 125000002947 alkylene group Chemical group 0.000 claims description 12
- 230000001472 cytotoxic effect Effects 0.000 claims description 12
- 230000000306 recurrent effect Effects 0.000 claims description 12
- 229910052717 sulfur Inorganic materials 0.000 claims description 12
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 claims description 11
- 231100000433 cytotoxic Toxicity 0.000 claims description 11
- 230000014509 gene expression Effects 0.000 claims description 11
- 239000003937 drug carrier Substances 0.000 claims description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 8
- 230000002401 inhibitory effect Effects 0.000 claims description 8
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 7
- 229910052751 metal Inorganic materials 0.000 claims description 6
- 239000002184 metal Substances 0.000 claims description 6
- 239000000825 pharmaceutical preparation Substances 0.000 claims description 6
- 125000001544 thienyl group Chemical group 0.000 claims description 6
- AGGWFDNPHKLBBV-YUMQZZPRSA-N (2s)-2-[[(2s)-2-amino-3-methylbutanoyl]amino]-5-(carbamoylamino)pentanoic acid Chemical compound CC(C)[C@H](N)C(=O)N[C@H](C(O)=O)CCCNC(N)=O AGGWFDNPHKLBBV-YUMQZZPRSA-N 0.000 claims description 5
- 230000035755 proliferation Effects 0.000 claims description 5
- 125000004076 pyridyl group Chemical group 0.000 claims description 5
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims description 4
- 150000001768 cations Chemical class 0.000 claims description 4
- 125000002541 furyl group Chemical group 0.000 claims description 4
- 230000001613 neoplastic effect Effects 0.000 claims description 4
- 230000001225 therapeutic effect Effects 0.000 claims description 4
- ALBODLTZUXKBGZ-JUUVMNCLSA-N (2s)-2-amino-3-phenylpropanoic acid;(2s)-2,6-diaminohexanoic acid Chemical compound NCCCC[C@H](N)C(O)=O.OC(=O)[C@@H](N)CC1=CC=CC=C1 ALBODLTZUXKBGZ-JUUVMNCLSA-N 0.000 claims description 3
- 125000004980 cyclopropylene group Chemical group 0.000 claims description 3
- FADYJNXDPBKVCA-UHFFFAOYSA-N L-Phenylalanyl-L-lysin Natural products NCCCCC(C(O)=O)NC(=O)C(N)CC1=CC=CC=C1 FADYJNXDPBKVCA-UHFFFAOYSA-N 0.000 claims description 2
- 239000000611 antibody drug conjugate Substances 0.000 description 132
- 229940049595 antibody-drug conjugate Drugs 0.000 description 132
- 229940079593 drug Drugs 0.000 description 104
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 69
- 229920002857 polybutadiene Polymers 0.000 description 53
- 239000000243 solution Substances 0.000 description 51
- 239000000203 mixture Substances 0.000 description 47
- 125000006701 (C1-C7) alkyl group Chemical group 0.000 description 42
- 235000001014 amino acid Nutrition 0.000 description 42
- 239000000427 antigen Substances 0.000 description 41
- 238000011282 treatment Methods 0.000 description 41
- 102000036639 antigens Human genes 0.000 description 38
- 108091007433 antigens Proteins 0.000 description 38
- 241001465754 Metazoa Species 0.000 description 37
- 241000699670 Mus sp. Species 0.000 description 35
- 238000006467 substitution reaction Methods 0.000 description 34
- 229940024606 amino acid Drugs 0.000 description 33
- 230000002829 reductive effect Effects 0.000 description 33
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 description 31
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 30
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 29
- 235000018417 cysteine Nutrition 0.000 description 29
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 28
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 27
- 239000003153 chemical reaction reagent Substances 0.000 description 27
- 102000039446 nucleic acids Human genes 0.000 description 27
- 108020004707 nucleic acids Proteins 0.000 description 27
- 150000007523 nucleic acids Chemical class 0.000 description 27
- 230000000694 effects Effects 0.000 description 26
- 239000011541 reaction mixture Substances 0.000 description 26
- 239000000047 product Substances 0.000 description 24
- 125000001424 substituent group Chemical group 0.000 description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 24
- 229940093499 ethyl acetate Drugs 0.000 description 23
- 235000019439 ethyl acetate Nutrition 0.000 description 23
- 229910052739 hydrogen Inorganic materials 0.000 description 22
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 22
- OMRPLUKQNWNZAV-CONSDPRKSA-N (6as)-3-[3-[[(6as)-2-methoxy-8-(4-methoxyphenyl)-11-oxo-6a,7-dihydropyrrolo[2,1-c][1,4]benzodiazepin-3-yl]oxy]propoxy]-8-(4-aminophenyl)-2-methoxy-6a,7-dihydropyrrolo[2,1-c][1,4]benzodiazepin-11-one Chemical compound C1=CC(OC)=CC=C1C1=CN2C(=O)C3=CC(OC)=C(OCCCOC=4C(=CC=5C(=O)N6C=C(C[C@H]6C=NC=5C=4)C=4C=CC(N)=CC=4)OC)C=C3N=C[C@@H]2C1 OMRPLUKQNWNZAV-CONSDPRKSA-N 0.000 description 20
- 239000000562 conjugate Substances 0.000 description 20
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 19
- 125000003277 amino group Chemical group 0.000 description 19
- 108090000623 proteins and genes Proteins 0.000 description 19
- 108060003951 Immunoglobulin Proteins 0.000 description 17
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 17
- 102000018358 immunoglobulin Human genes 0.000 description 17
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 16
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 16
- 102000004196 processed proteins & peptides Human genes 0.000 description 16
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 15
- 239000012634 fragment Substances 0.000 description 15
- 235000018102 proteins Nutrition 0.000 description 15
- 102000004169 proteins and genes Human genes 0.000 description 15
- 239000013598 vector Substances 0.000 description 15
- WNQJTLATMXYSEL-OEAJRASXSA-N Thr-Phe-Leu Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(C)C)C(O)=O WNQJTLATMXYSEL-OEAJRASXSA-N 0.000 description 14
- 125000000539 amino acid group Chemical group 0.000 description 14
- 201000010099 disease Diseases 0.000 description 14
- 208000035475 disorder Diseases 0.000 description 14
- 239000001257 hydrogen Substances 0.000 description 14
- 230000004048 modification Effects 0.000 description 14
- 238000012986 modification Methods 0.000 description 14
- GVNVAWHJIKLAGL-UHFFFAOYSA-N 2-(cyclohexen-1-yl)cyclohexan-1-one Chemical compound O=C1CCCCC1C1=CCCCC1 GVNVAWHJIKLAGL-UHFFFAOYSA-N 0.000 description 13
- 101150065749 Churc1 gene Proteins 0.000 description 13
- 102000004190 Enzymes Human genes 0.000 description 13
- 108090000790 Enzymes Proteins 0.000 description 13
- 102100038239 Protein Churchill Human genes 0.000 description 13
- HTONZBWRYUKUKC-RCWTZXSCSA-N Val-Thr-Val Chemical compound CC(C)[C@H](N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(O)=O HTONZBWRYUKUKC-RCWTZXSCSA-N 0.000 description 13
- 239000002253 acid Substances 0.000 description 13
- 238000013459 approach Methods 0.000 description 13
- 229910052799 carbon Inorganic materials 0.000 description 13
- 229940088598 enzyme Drugs 0.000 description 13
- 238000003818 flash chromatography Methods 0.000 description 13
- 239000006260 foam Substances 0.000 description 13
- 108010078144 glutaminyl-glycine Proteins 0.000 description 13
- 238000003780 insertion Methods 0.000 description 13
- 230000037431 insertion Effects 0.000 description 13
- 238000004519 manufacturing process Methods 0.000 description 13
- 238000005259 measurement Methods 0.000 description 13
- 125000006413 ring segment Chemical group 0.000 description 13
- 229920006395 saturated elastomer Polymers 0.000 description 13
- 238000011579 SCID mouse model Methods 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 12
- 238000003556 assay Methods 0.000 description 12
- 230000037396 body weight Effects 0.000 description 12
- 150000002148 esters Chemical class 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 12
- 238000012447 xenograft mouse model Methods 0.000 description 12
- 230000008859 change Effects 0.000 description 11
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 11
- 108010017391 lysylvaline Proteins 0.000 description 11
- 108010051242 phenylalanylserine Proteins 0.000 description 11
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 10
- XQJCEKXQUJQNNK-ZLUOBGJFSA-N Ser-Ser-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O XQJCEKXQUJQNNK-ZLUOBGJFSA-N 0.000 description 10
- 230000021615 conjugation Effects 0.000 description 10
- 238000012217 deletion Methods 0.000 description 10
- 230000037430 deletion Effects 0.000 description 10
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 10
- 125000000524 functional group Chemical group 0.000 description 10
- 238000001727 in vivo Methods 0.000 description 10
- 230000000670 limiting effect Effects 0.000 description 10
- 238000011068 loading method Methods 0.000 description 10
- 229920001184 polypeptide Polymers 0.000 description 10
- 230000002285 radioactive effect Effects 0.000 description 10
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 10
- FRBAHXABMQXSJQ-FXQIFTODSA-N Arg-Ser-Ser Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O FRBAHXABMQXSJQ-FXQIFTODSA-N 0.000 description 9
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- SXFPZRRVWSUYII-KBIXCLLPSA-N Gln-Ser-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(=O)N)N SXFPZRRVWSUYII-KBIXCLLPSA-N 0.000 description 9
- 108010065920 Insulin Lispro Proteins 0.000 description 9
- 241000880493 Leptailurus serval Species 0.000 description 9
- HQYVQDRYODWONX-DCAQKATOSA-N Val-His-Ser Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N[C@@H](CO)C(=O)O)N HQYVQDRYODWONX-DCAQKATOSA-N 0.000 description 9
- 150000001299 aldehydes Chemical class 0.000 description 9
- 230000004071 biological effect Effects 0.000 description 9
- 230000004540 complement-dependent cytotoxicity Effects 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 230000035772 mutation Effects 0.000 description 9
- 239000012038 nucleophile Substances 0.000 description 9
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 9
- 230000004044 response Effects 0.000 description 9
- 238000003756 stirring Methods 0.000 description 9
- 210000001519 tissue Anatomy 0.000 description 9
- 230000004614 tumor growth Effects 0.000 description 9
- DJQYYYCQOZMCRC-UHFFFAOYSA-N 2-aminopropane-1,3-dithiol Chemical compound SCC(N)CS DJQYYYCQOZMCRC-UHFFFAOYSA-N 0.000 description 8
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 8
- JVTHIXKSVYEWNI-JRQIVUDYSA-N Thr-Asn-Tyr Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O JVTHIXKSVYEWNI-JRQIVUDYSA-N 0.000 description 8
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 8
- 239000012472 biological sample Substances 0.000 description 8
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 8
- 125000004122 cyclic group Chemical group 0.000 description 8
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 8
- 108010015792 glycyllysine Proteins 0.000 description 8
- 238000001990 intravenous administration Methods 0.000 description 8
- 229920001223 polyethylene glycol Polymers 0.000 description 8
- 125000003396 thiol group Chemical class [H]S* 0.000 description 8
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 7
- WBDWQKRLTVCDSY-WHFBIAKZSA-N Asp-Gly-Asp Chemical compound OC(=O)C[C@H](N)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(O)=O WBDWQKRLTVCDSY-WHFBIAKZSA-N 0.000 description 7
- OCQUNKSFDYDXBG-QXEWZRGKSA-N Gly-Arg-Ile Chemical compound CC[C@H](C)[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)CN)CCCN=C(N)N OCQUNKSFDYDXBG-QXEWZRGKSA-N 0.000 description 7
- PDUHNKAFQXQNLH-ZETCQYMHSA-N Gly-Lys-Gly Chemical compound NCCCC[C@H](NC(=O)CN)C(=O)NCC(O)=O PDUHNKAFQXQNLH-ZETCQYMHSA-N 0.000 description 7
- UVTSZKIATYSKIR-RYUDHWBXSA-N Gly-Tyr-Glu Chemical compound [H]NCC(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CCC(O)=O)C(O)=O UVTSZKIATYSKIR-RYUDHWBXSA-N 0.000 description 7
- 208000017604 Hodgkin disease Diseases 0.000 description 7
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 7
- GILLQRYAWOMHED-DCAQKATOSA-N Lys-Val-Ser Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](N)CCCCN GILLQRYAWOMHED-DCAQKATOSA-N 0.000 description 7
- XMBSYZWANAQXEV-UHFFFAOYSA-N N-alpha-L-glutamyl-L-phenylalanine Natural products OC(=O)CCC(N)C(=O)NC(C(O)=O)CC1=CC=CC=C1 XMBSYZWANAQXEV-UHFFFAOYSA-N 0.000 description 7
- WEDZFLRYSIDIRX-IHRRRGAJSA-N Phe-Ser-Arg Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC1=CC=CC=C1 WEDZFLRYSIDIRX-IHRRRGAJSA-N 0.000 description 7
- 239000002202 Polyethylene glycol Substances 0.000 description 7
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 7
- WSTIOCFMWXNOCX-YUMQZZPRSA-N Ser-Gly-Lys Chemical compound C(CCN)C[C@@H](C(=O)O)NC(=O)CNC(=O)[C@H](CO)N WSTIOCFMWXNOCX-YUMQZZPRSA-N 0.000 description 7
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 7
- SZEIFUXUTBBQFQ-STQMWFEESA-N Tyr-Pro-Gly Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N1CCC[C@H]1C(=O)NCC(O)=O SZEIFUXUTBBQFQ-STQMWFEESA-N 0.000 description 7
- OWFGFHQMSBTKLX-UFYCRDLUSA-N Val-Tyr-Tyr Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC1=CC=C(C=C1)O)C(=O)N[C@@H](CC2=CC=C(C=C2)O)C(=O)O)N OWFGFHQMSBTKLX-UFYCRDLUSA-N 0.000 description 7
- 108010086434 alanyl-seryl-glycine Proteins 0.000 description 7
- 239000002246 antineoplastic agent Substances 0.000 description 7
- 108010038850 arginyl-isoleucyl-tyrosine Proteins 0.000 description 7
- 239000012267 brine Substances 0.000 description 7
- 238000004113 cell culture Methods 0.000 description 7
- 229960004397 cyclophosphamide Drugs 0.000 description 7
- 238000001514 detection method Methods 0.000 description 7
- 230000008030 elimination Effects 0.000 description 7
- 238000003379 elimination reaction Methods 0.000 description 7
- 230000006870 function Effects 0.000 description 7
- XKUKSGPZAADMRA-UHFFFAOYSA-N glycyl-glycyl-glycine Natural products NCC(=O)NCC(=O)NCC(O)=O XKUKSGPZAADMRA-UHFFFAOYSA-N 0.000 description 7
- 108010018006 histidylserine Proteins 0.000 description 7
- 210000004408 hybridoma Anatomy 0.000 description 7
- 150000002431 hydrogen Chemical class 0.000 description 7
- 150000002482 oligosaccharides Chemical class 0.000 description 7
- 239000002243 precursor Substances 0.000 description 7
- 238000000746 purification Methods 0.000 description 7
- 230000009467 reduction Effects 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 238000010186 staining Methods 0.000 description 7
- 150000003573 thiols Chemical class 0.000 description 7
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 7
- 229960004528 vincristine Drugs 0.000 description 7
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 7
- YYSWCHMLFJLLBJ-ZLUOBGJFSA-N Ala-Ala-Ser Chemical compound C[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(O)=O YYSWCHMLFJLLBJ-ZLUOBGJFSA-N 0.000 description 6
- VKKYFICVTYKFIO-CIUDSAMLSA-N Arg-Ala-Glu Chemical compound OC(=O)CC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CCCN=C(N)N VKKYFICVTYKFIO-CIUDSAMLSA-N 0.000 description 6
- KMSHNDWHPWXPEC-BQBZGAKWSA-N Arg-Asp-Gly Chemical compound NC(N)=NCCC[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)NCC(O)=O KMSHNDWHPWXPEC-BQBZGAKWSA-N 0.000 description 6
- HUZGPXBILPMCHM-IHRRRGAJSA-N Asn-Arg-Phe Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O HUZGPXBILPMCHM-IHRRRGAJSA-N 0.000 description 6
- MKJBPDLENBUHQU-CIUDSAMLSA-N Asn-Ser-Leu Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(O)=O MKJBPDLENBUHQU-CIUDSAMLSA-N 0.000 description 6
- MNQMTYSEKZHIDF-GCJQMDKQSA-N Asp-Thr-Ala Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C)C(O)=O MNQMTYSEKZHIDF-GCJQMDKQSA-N 0.000 description 6
- GHAHOJDCBRXAKC-IHPCNDPISA-N Asp-Trp-Tyr Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CC3=CC=C(C=C3)O)C(=O)O)NC(=O)[C@H](CC(=O)O)N GHAHOJDCBRXAKC-IHPCNDPISA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- SHZGCJCMOBCMKK-UHFFFAOYSA-N D-mannomethylose Natural products CC1OC(O)C(O)C(O)C1O SHZGCJCMOBCMKK-UHFFFAOYSA-N 0.000 description 6
- SBJKKFFYIZUCET-JLAZNSOCSA-N Dehydro-L-ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(=O)C1=O SBJKKFFYIZUCET-JLAZNSOCSA-N 0.000 description 6
- SBJKKFFYIZUCET-UHFFFAOYSA-N Dehydroascorbic acid Natural products OCC(O)C1OC(=O)C(=O)C1=O SBJKKFFYIZUCET-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 6
- PNNNRSAQSRJVSB-SLPGGIOYSA-N Fucose Natural products C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C=O PNNNRSAQSRJVSB-SLPGGIOYSA-N 0.000 description 6
- OYTPNWYZORARHL-XHNCKOQMSA-N Gln-Ala-Pro Chemical compound C[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@H](CCC(=O)N)N OYTPNWYZORARHL-XHNCKOQMSA-N 0.000 description 6
- FQCILXROGNOZON-YUMQZZPRSA-N Gln-Pro-Gly Chemical compound NC(=O)CC[C@H](N)C(=O)N1CCC[C@H]1C(=O)NCC(O)=O FQCILXROGNOZON-YUMQZZPRSA-N 0.000 description 6
- YQPFCZVKMUVZIN-AUTRQRHGSA-N Glu-Val-Gln Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O YQPFCZVKMUVZIN-AUTRQRHGSA-N 0.000 description 6
- MIIVFRCYJABHTQ-ONGXEEELSA-N Gly-Leu-Val Chemical compound [H]NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(O)=O MIIVFRCYJABHTQ-ONGXEEELSA-N 0.000 description 6
- ZZWUYQXMIFTIIY-WEDXCCLWSA-N Gly-Thr-Leu Chemical compound [H]NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(O)=O ZZWUYQXMIFTIIY-WEDXCCLWSA-N 0.000 description 6
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 6
- PMGDADKJMCOXHX-UHFFFAOYSA-N L-Arginyl-L-glutamin-acetat Natural products NC(=N)NCCCC(N)C(=O)NC(CCC(N)=O)C(O)=O PMGDADKJMCOXHX-UHFFFAOYSA-N 0.000 description 6
- SHZGCJCMOBCMKK-DHVFOXMCSA-N L-fucopyranose Chemical compound C[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O SHZGCJCMOBCMKK-DHVFOXMCSA-N 0.000 description 6
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 6
- LZDNBBYBDGBADK-UHFFFAOYSA-N L-valyl-L-tryptophan Natural products C1=CC=C2C(CC(NC(=O)C(N)C(C)C)C(O)=O)=CNC2=C1 LZDNBBYBDGBADK-UHFFFAOYSA-N 0.000 description 6
- AXZGZMGRBDQTEY-SRVKXCTJSA-N Leu-Gln-Met Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCSC)C(O)=O AXZGZMGRBDQTEY-SRVKXCTJSA-N 0.000 description 6
- FEHQLKKBVJHSEC-SZMVWBNQSA-N Leu-Glu-Trp Chemical compound C1=CC=C2C(C[C@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CC(C)C)C(O)=O)=CNC2=C1 FEHQLKKBVJHSEC-SZMVWBNQSA-N 0.000 description 6
- KIZIOFNVSOSKJI-CIUDSAMLSA-N Leu-Ser-Cys Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O)N KIZIOFNVSOSKJI-CIUDSAMLSA-N 0.000 description 6
- AIMGJYMCTAABEN-GVXVVHGQSA-N Leu-Val-Glu Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(O)=O AIMGJYMCTAABEN-GVXVVHGQSA-N 0.000 description 6
- 208000028018 Lymphocytic leukaemia Diseases 0.000 description 6
- GQZMPWBZQALKJO-UWVGGRQHSA-N Lys-Gly-Arg Chemical compound [H]N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(O)=O GQZMPWBZQALKJO-UWVGGRQHSA-N 0.000 description 6
- SPSSJSICDYYTQN-HJGDQZAQSA-N Met-Thr-Gln Chemical compound CSCC[C@H](N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@H](C(O)=O)CCC(N)=O SPSSJSICDYYTQN-HJGDQZAQSA-N 0.000 description 6
- 241000699666 Mus <mouse, genus> Species 0.000 description 6
- SITLTJHOQZFJGG-UHFFFAOYSA-N N-L-alpha-glutamyl-L-valine Natural products CC(C)C(C(O)=O)NC(=O)C(N)CCC(O)=O SITLTJHOQZFJGG-UHFFFAOYSA-N 0.000 description 6
- 108010066427 N-valyltryptophan Proteins 0.000 description 6
- FRPVPGRXUKFEQE-YDHLFZDLSA-N Phe-Asp-Val Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(O)=O FRPVPGRXUKFEQE-YDHLFZDLSA-N 0.000 description 6
- FGWUALWGCZJQDJ-URLPEUOOSA-N Phe-Thr-Ile Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O FGWUALWGCZJQDJ-URLPEUOOSA-N 0.000 description 6
- QKWYXRPICJEQAJ-KJEVXHAQSA-N Pro-Tyr-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)NC(=O)[C@@H]2CCCN2)O QKWYXRPICJEQAJ-KJEVXHAQSA-N 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 108010076504 Protein Sorting Signals Proteins 0.000 description 6
- GWMXFEMMBHOKDX-AVGNSLFASA-N Ser-Gln-Phe Chemical compound OC[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 GWMXFEMMBHOKDX-AVGNSLFASA-N 0.000 description 6
- FMDHKPRACUXATF-ACZMJKKPSA-N Ser-Gln-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(O)=O FMDHKPRACUXATF-ACZMJKKPSA-N 0.000 description 6
- YMTLKLXDFCSCNX-BYPYZUCNSA-N Ser-Gly-Gly Chemical compound OC[C@H](N)C(=O)NCC(=O)NCC(O)=O YMTLKLXDFCSCNX-BYPYZUCNSA-N 0.000 description 6
- UIGMAMGZOJVTDN-WHFBIAKZSA-N Ser-Gly-Ser Chemical compound OC[C@H](N)C(=O)NCC(=O)N[C@@H](CO)C(O)=O UIGMAMGZOJVTDN-WHFBIAKZSA-N 0.000 description 6
- QYSFWUIXDFJUDW-DCAQKATOSA-N Ser-Leu-Arg Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O QYSFWUIXDFJUDW-DCAQKATOSA-N 0.000 description 6
- BMKNXTJLHFIAAH-CIUDSAMLSA-N Ser-Ser-Leu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(O)=O BMKNXTJLHFIAAH-CIUDSAMLSA-N 0.000 description 6
- DKGRNFUXVTYRAS-UBHSHLNASA-N Ser-Ser-Trp Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(O)=O DKGRNFUXVTYRAS-UBHSHLNASA-N 0.000 description 6
- VRUFCJZQDACGLH-UVOCVTCTSA-N Thr-Leu-Thr Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(O)=O VRUFCJZQDACGLH-UVOCVTCTSA-N 0.000 description 6
- SGAOHNPSEPVAFP-ZDLURKLDSA-N Thr-Ser-Gly Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)NCC(O)=O SGAOHNPSEPVAFP-ZDLURKLDSA-N 0.000 description 6
- IQPWNQRRAJHOKV-KATARQTJSA-N Thr-Ser-Lys Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@H](C(O)=O)CCCCN IQPWNQRRAJHOKV-KATARQTJSA-N 0.000 description 6
- SVGAWGVHFIYAEE-JSGCOSHPSA-N Trp-Gly-Gln Chemical compound C1=CC=C2C(C[C@H](N)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(O)=O)=CNC2=C1 SVGAWGVHFIYAEE-JSGCOSHPSA-N 0.000 description 6
- RCMHSGRBJCMFLR-BPUTZDHNSA-N Trp-Met-Asn Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(O)=O)=CNC2=C1 RCMHSGRBJCMFLR-BPUTZDHNSA-N 0.000 description 6
- MBLJBGZWLHTJBH-SZMVWBNQSA-N Trp-Val-Arg Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O)=CNC2=C1 MBLJBGZWLHTJBH-SZMVWBNQSA-N 0.000 description 6
- 208000025865 Ulcer Diseases 0.000 description 6
- 108010008685 alanyl-glutamyl-aspartic acid Proteins 0.000 description 6
- 108010069020 alanyl-prolyl-glycine Proteins 0.000 description 6
- 108010008355 arginyl-glutamine Proteins 0.000 description 6
- 108010052670 arginyl-glutamyl-glutamic acid Proteins 0.000 description 6
- 238000009835 boiling Methods 0.000 description 6
- 150000001720 carbohydrates Chemical group 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 238000002648 combination therapy Methods 0.000 description 6
- 235000020960 dehydroascorbic acid Nutrition 0.000 description 6
- 239000011615 dehydroascorbic acid Substances 0.000 description 6
- 238000010494 dissociation reaction Methods 0.000 description 6
- 230000005593 dissociations Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 239000000284 extract Substances 0.000 description 6
- 108010067216 glycyl-glycyl-glycine Proteins 0.000 description 6
- 150000002430 hydrocarbons Chemical class 0.000 description 6
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 6
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 6
- 208000003747 lymphoid leukemia Diseases 0.000 description 6
- 210000003563 lymphoid tissue Anatomy 0.000 description 6
- GTCAXTIRRLKXRU-UHFFFAOYSA-N methyl carbamate Chemical compound COC(N)=O GTCAXTIRRLKXRU-UHFFFAOYSA-N 0.000 description 6
- 244000005700 microbiome Species 0.000 description 6
- 210000005170 neoplastic cell Anatomy 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 229920001542 oligosaccharide Polymers 0.000 description 6
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 6
- 238000003752 polymerase chain reaction Methods 0.000 description 6
- 108010020755 prolyl-glycyl-glycine Proteins 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- 108010072986 threonyl-seryl-lysine Proteins 0.000 description 6
- 239000003053 toxin Substances 0.000 description 6
- 231100000765 toxin Toxicity 0.000 description 6
- 108700012359 toxins Proteins 0.000 description 6
- 238000013518 transcription Methods 0.000 description 6
- 231100000397 ulcer Toxicity 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 5
- WLVLIYYBPPONRJ-GCJQMDKQSA-N Asn-Thr-Ala Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C)C(O)=O WLVLIYYBPPONRJ-GCJQMDKQSA-N 0.000 description 5
- XYBJLTKSGFBLCS-QXEWZRGKSA-N Asp-Arg-Val Chemical compound NC(N)=NCCC[C@@H](C(=O)N[C@@H](C(C)C)C(O)=O)NC(=O)[C@@H](N)CC(O)=O XYBJLTKSGFBLCS-QXEWZRGKSA-N 0.000 description 5
- QNFRBNZGVVKBNJ-PEFMBERDSA-N Asp-Ile-Gln Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CC(=O)O)N QNFRBNZGVVKBNJ-PEFMBERDSA-N 0.000 description 5
- 101100505161 Caenorhabditis elegans mel-32 gene Proteins 0.000 description 5
- GEEXORWTBTUOHC-FXQIFTODSA-N Cys-Arg-Ser Chemical compound C(C[C@@H](C(=O)N[C@@H](CO)C(=O)O)NC(=O)[C@H](CS)N)CN=C(N)N GEEXORWTBTUOHC-FXQIFTODSA-N 0.000 description 5
- BBQIWFFTTQTNOC-AVGNSLFASA-N Cys-Phe-Gln Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CS)N BBQIWFFTTQTNOC-AVGNSLFASA-N 0.000 description 5
- 241000196324 Embryophyta Species 0.000 description 5
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical group OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 5
- CGWHAXBNGYQBBK-JBACZVJFSA-N Glu-Trp-Tyr Chemical compound C([C@H](NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CCC(O)=O)N)C(O)=O)C1=CC=C(O)C=C1 CGWHAXBNGYQBBK-JBACZVJFSA-N 0.000 description 5
- SOEGEPHNZOISMT-BYPYZUCNSA-N Gly-Ser-Gly Chemical compound NCC(=O)N[C@@H](CO)C(=O)NCC(O)=O SOEGEPHNZOISMT-BYPYZUCNSA-N 0.000 description 5
- XHVONGZZVUUORG-WEDXCCLWSA-N Gly-Thr-Lys Chemical compound NCC(=O)N[C@@H]([C@H](O)C)C(=O)N[C@H](C(O)=O)CCCCN XHVONGZZVUUORG-WEDXCCLWSA-N 0.000 description 5
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 5
- JCGMFFQQHJQASB-PYJNHQTQSA-N Ile-Val-His Chemical compound N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC1=CNC=N1)C(=O)O JCGMFFQQHJQASB-PYJNHQTQSA-N 0.000 description 5
- PWWVAXIEGOYWEE-UHFFFAOYSA-N Isophenergan Chemical compound C1=CC=C2N(CC(C)N(C)C)C3=CC=CC=C3SC2=C1 PWWVAXIEGOYWEE-UHFFFAOYSA-N 0.000 description 5
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 5
- CQGSYZCULZMEDE-UHFFFAOYSA-N Leu-Gln-Pro Natural products CC(C)CC(N)C(=O)NC(CCC(N)=O)C(=O)N1CCCC1C(O)=O CQGSYZCULZMEDE-UHFFFAOYSA-N 0.000 description 5
- NRFGTHFONZYFNY-MGHWNKPDSA-N Leu-Ile-Tyr Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 NRFGTHFONZYFNY-MGHWNKPDSA-N 0.000 description 5
- IRMLZWSRWSGTOP-CIUDSAMLSA-N Leu-Ser-Ala Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(O)=O IRMLZWSRWSGTOP-CIUDSAMLSA-N 0.000 description 5
- 239000004472 Lysine Substances 0.000 description 5
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 5
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical group OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 5
- RMODQFBNDDENCP-IHRRRGAJSA-N Pro-Lys-Leu Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(O)=O RMODQFBNDDENCP-IHRRRGAJSA-N 0.000 description 5
- LVVBAKCGXXUHFO-ZLUOBGJFSA-N Ser-Ala-Asp Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(O)=O)C(O)=O LVVBAKCGXXUHFO-ZLUOBGJFSA-N 0.000 description 5
- XXXAXOWMBOKTRN-XPUUQOCRSA-N Ser-Gly-Val Chemical compound [H]N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C(C)C)C(O)=O XXXAXOWMBOKTRN-XPUUQOCRSA-N 0.000 description 5
- JZRYFUGREMECBH-XPUUQOCRSA-N Ser-Val-Gly Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(=O)NCC(O)=O JZRYFUGREMECBH-XPUUQOCRSA-N 0.000 description 5
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 5
- KRPKYGOFYUNIGM-XVSYOHENSA-N Thr-Asp-Phe Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)O)N)O KRPKYGOFYUNIGM-XVSYOHENSA-N 0.000 description 5
- GXUWHVZYDAHFSV-FLBSBUHZSA-N Thr-Ile-Thr Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(O)=O GXUWHVZYDAHFSV-FLBSBUHZSA-N 0.000 description 5
- YOPQYBJJNSIQGZ-JNPHEJMOSA-N Thr-Tyr-Tyr Chemical compound C([C@H](NC(=O)[C@@H](N)[C@H](O)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)C1=CC=C(O)C=C1 YOPQYBJJNSIQGZ-JNPHEJMOSA-N 0.000 description 5
- VCAWFLIWYNMHQP-UKJIMTQDSA-N Val-Glu-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](C(C)C)N VCAWFLIWYNMHQP-UKJIMTQDSA-N 0.000 description 5
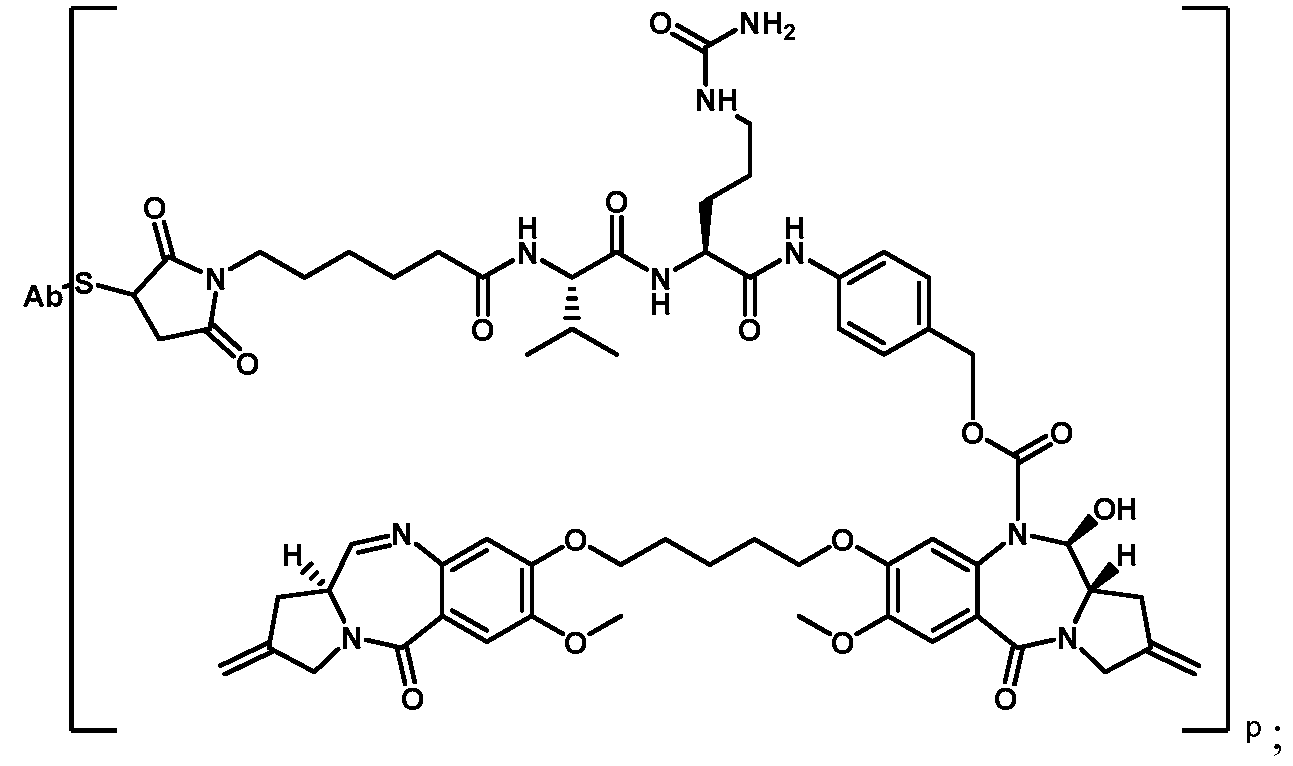
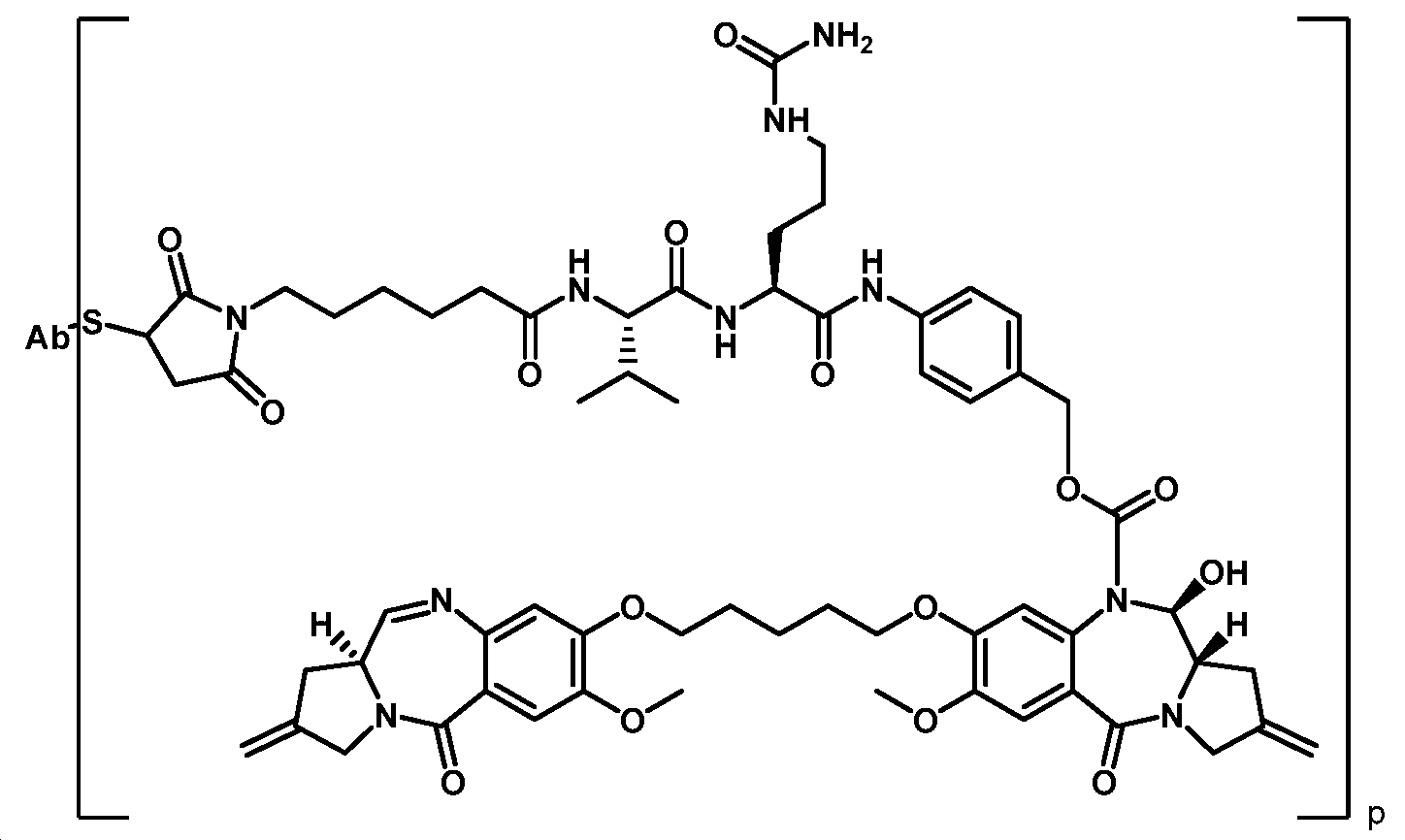
- IEDXPSOJFSVCKU-HOKPPMCLSA-N [4-[[(2S)-5-(carbamoylamino)-2-[[(2S)-2-[6-(2,5-dioxopyrrolidin-1-yl)hexanoylamino]-3-methylbutanoyl]amino]pentanoyl]amino]phenyl]methyl N-[(2S)-1-[[(2S)-1-[[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-3-[[(1S,2R)-1-hydroxy-1-phenylpropan-2-yl]amino]-1-methoxy-2-methyl-3-oxopropyl]pyrrolidin-1-yl]-3-methoxy-5-methyl-1-oxoheptan-4-yl]-methylamino]-3-methyl-1-oxobutan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]-N-methylcarbamate Chemical compound CC[C@H](C)[C@@H]([C@@H](CC(=O)N1CCC[C@H]1[C@H](OC)[C@@H](C)C(=O)N[C@H](C)[C@@H](O)c1ccccc1)OC)N(C)C(=O)[C@@H](NC(=O)[C@H](C(C)C)N(C)C(=O)OCc1ccc(NC(=O)[C@H](CCCNC(N)=O)NC(=O)[C@@H](NC(=O)CCCCCN2C(=O)CCC2=O)C(C)C)cc1)C(C)C IEDXPSOJFSVCKU-HOKPPMCLSA-N 0.000 description 5
- 108010081404 acein-2 Proteins 0.000 description 5
- 125000000304 alkynyl group Chemical group 0.000 description 5
- 125000003368 amide group Chemical group 0.000 description 5
- 230000000259 anti-tumor effect Effects 0.000 description 5
- 230000001580 bacterial effect Effects 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 238000003745 diagnosis Methods 0.000 description 5
- 239000000539 dimer Substances 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 108010089804 glycyl-threonine Proteins 0.000 description 5
- 108010037850 glycylvaline Proteins 0.000 description 5
- 125000001072 heteroaryl group Chemical group 0.000 description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 5
- 230000016784 immunoglobulin production Effects 0.000 description 5
- 238000003364 immunohistochemistry Methods 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 230000005917 in vivo anti-tumor Effects 0.000 description 5
- 239000012948 isocyanate Substances 0.000 description 5
- 150000002513 isocyanates Chemical class 0.000 description 5
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 5
- 230000000269 nucleophilic effect Effects 0.000 description 5
- 238000002823 phage display Methods 0.000 description 5
- 239000002953 phosphate buffered saline Substances 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 108010053725 prolylvaline Proteins 0.000 description 5
- 125000006239 protecting group Chemical group 0.000 description 5
- 238000012216 screening Methods 0.000 description 5
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 5
- 210000004881 tumor cell Anatomy 0.000 description 5
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 4
- IORKCNUBHNIMKY-CIUDSAMLSA-N Ala-Pro-Glu Chemical compound C[C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(O)=O)C(O)=O IORKCNUBHNIMKY-CIUDSAMLSA-N 0.000 description 4
- SNDBKTFJWVEVPO-WHFBIAKZSA-N Asp-Gly-Ser Chemical compound [H]N[C@@H](CC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(O)=O SNDBKTFJWVEVPO-WHFBIAKZSA-N 0.000 description 4
- GYWQGGUCMDCUJE-DLOVCJGASA-N Asp-Phe-Ala Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](C)C(O)=O GYWQGGUCMDCUJE-DLOVCJGASA-N 0.000 description 4
- 208000003950 B-cell lymphoma Diseases 0.000 description 4
- 108090000317 Chymotrypsin Proteins 0.000 description 4
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 4
- MADFVRSKEIEZHZ-DCAQKATOSA-N Gln-Gln-Lys Chemical compound C(CCN)C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](CCC(=O)N)N MADFVRSKEIEZHZ-DCAQKATOSA-N 0.000 description 4
- HMIXCETWRYDVMO-GUBZILKMSA-N Gln-Pro-Glu Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(O)=O)C(O)=O HMIXCETWRYDVMO-GUBZILKMSA-N 0.000 description 4
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 4
- YOKVEHGYYQEQOP-QWRGUYRKSA-N Leu-Leu-Gly Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)NCC(O)=O YOKVEHGYYQEQOP-QWRGUYRKSA-N 0.000 description 4
- 108060001084 Luciferase Proteins 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- YBAFDPFAUTYYRW-UHFFFAOYSA-N N-L-alpha-glutamyl-L-leucine Natural products CC(C)CC(C(O)=O)NC(=O)C(N)CCC(O)=O YBAFDPFAUTYYRW-UHFFFAOYSA-N 0.000 description 4
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 4
- MBLBDJOUHNCFQT-LXGUWJNJSA-N N-acetylglucosamine Natural products CC(=O)N[C@@H](C=O)[C@@H](O)[C@H](O)[C@H](O)CO MBLBDJOUHNCFQT-LXGUWJNJSA-N 0.000 description 4
- YYKZDTVQHTUKDW-RYUDHWBXSA-N Phe-Gly-Gln Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)NCC(=O)N[C@@H](CCC(=O)N)C(=O)O)N YYKZDTVQHTUKDW-RYUDHWBXSA-N 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- 241000288906 Primates Species 0.000 description 4
- UIMCLYYSUCIUJM-UWVGGRQHSA-N Pro-Gly-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H]1CCCN1 UIMCLYYSUCIUJM-UWVGGRQHSA-N 0.000 description 4
- GMJDSFYVTAMIBF-FXQIFTODSA-N Pro-Ser-Asp Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(O)=O GMJDSFYVTAMIBF-FXQIFTODSA-N 0.000 description 4
- PRKWBYCXBBSLSK-GUBZILKMSA-N Pro-Ser-Val Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O PRKWBYCXBBSLSK-GUBZILKMSA-N 0.000 description 4
- 102000001708 Protein Isoforms Human genes 0.000 description 4
- 108010029485 Protein Isoforms Proteins 0.000 description 4
- QGMLKFGTGXWAHF-IHRRRGAJSA-N Ser-Arg-Phe Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O QGMLKFGTGXWAHF-IHRRRGAJSA-N 0.000 description 4
- BEZTUFWTPVOROW-KJEVXHAQSA-N Thr-Tyr-Arg Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC1=CC=C(C=C1)O)C(=O)N[C@@H](CCCN=C(N)N)C(=O)O)N)O BEZTUFWTPVOROW-KJEVXHAQSA-N 0.000 description 4
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 4
- NXRAUQGGHPCJIB-RCOVLWMOSA-N Val-Gly-Asn Chemical compound CC(C)[C@H](N)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(O)=O NXRAUQGGHPCJIB-RCOVLWMOSA-N 0.000 description 4
- 150000001241 acetals Chemical class 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 125000002252 acyl group Chemical group 0.000 description 4
- 235000004279 alanine Nutrition 0.000 description 4
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 125000003545 alkoxy group Chemical group 0.000 description 4
- 150000001412 amines Chemical class 0.000 description 4
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 4
- 108010044540 auristatin Proteins 0.000 description 4
- 238000001574 biopsy Methods 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 210000004899 c-terminal region Anatomy 0.000 description 4
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 4
- 239000000544 cholinesterase inhibitor Substances 0.000 description 4
- 230000002759 chromosomal effect Effects 0.000 description 4
- 229960002376 chymotrypsin Drugs 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 239000012230 colorless oil Substances 0.000 description 4
- 125000004093 cyano group Chemical group *C#N 0.000 description 4
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 4
- 231100000673 dose–response relationship Toxicity 0.000 description 4
- 238000001962 electrophoresis Methods 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 230000013595 glycosylation Effects 0.000 description 4
- 238000006206 glycosylation reaction Methods 0.000 description 4
- 108010050848 glycylleucine Proteins 0.000 description 4
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 4
- 125000004404 heteroalkyl group Chemical group 0.000 description 4
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 4
- 239000013067 intermediate product Substances 0.000 description 4
- 108010073472 leucyl-prolyl-proline Proteins 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 4
- 108010064235 lysylglycine Proteins 0.000 description 4
- 230000035800 maturation Effects 0.000 description 4
- WSFSSNUMVMOOMR-BJUDXGSMSA-N methanone Chemical compound O=[11CH2] WSFSSNUMVMOOMR-BJUDXGSMSA-N 0.000 description 4
- 229960000485 methotrexate Drugs 0.000 description 4
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 4
- 239000003094 microcapsule Substances 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 239000008194 pharmaceutical composition Substances 0.000 description 4
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 230000002062 proliferating effect Effects 0.000 description 4
- 125000004548 quinolin-3-yl group Chemical group N1=CC(=CC2=CC=CC=C12)* 0.000 description 4
- 125000004550 quinolin-6-yl group Chemical group N1=CC=CC2=CC(=CC=C12)* 0.000 description 4
- 238000012552 review Methods 0.000 description 4
- 229960004641 rituximab Drugs 0.000 description 4
- 238000002390 rotary evaporation Methods 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 4
- WYWHKKSPHMUBEB-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 4
- 230000009261 transgenic effect Effects 0.000 description 4
- IESDGNYHXIOKRW-YXMSTPNBSA-N (2s)-2-[[(2s)-1-[(2s)-6-amino-2-[[(2s,3r)-2-amino-3-hydroxybutanoyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCCNC(N)=N)C(O)=O IESDGNYHXIOKRW-YXMSTPNBSA-N 0.000 description 3
- DIBLBAURNYJYBF-XLXZRNDBSA-N (2s)-2-[[(2s)-2-[[2-[[(2s)-6-amino-2-[[(2s)-2-amino-3-methylbutanoyl]amino]hexanoyl]amino]acetyl]amino]-3-phenylpropanoyl]amino]-3-(4-hydroxyphenyl)propanoic acid Chemical compound C([C@H](NC(=O)CNC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)C(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)C1=CC=CC=C1 DIBLBAURNYJYBF-XLXZRNDBSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- OYJCVIGKMXUVKB-GARJFASQSA-N Ala-Leu-Pro Chemical compound C[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N1CCC[C@@H]1C(=O)O)N OYJCVIGKMXUVKB-GARJFASQSA-N 0.000 description 3
- WQLDNOCHHRISMS-NAKRPEOUSA-N Ala-Pro-Ile Chemical compound [H]N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(O)=O WQLDNOCHHRISMS-NAKRPEOUSA-N 0.000 description 3
- XWFWAXPOLRTDFZ-FXQIFTODSA-N Ala-Pro-Ser Chemical compound C[C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CO)C(O)=O XWFWAXPOLRTDFZ-FXQIFTODSA-N 0.000 description 3
- SLKLLQWZQHXYSV-CIUDSAMLSA-N Asn-Ala-Lys Chemical compound NC(=O)C[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(O)=O SLKLLQWZQHXYSV-CIUDSAMLSA-N 0.000 description 3
- DXVMJJNAOVECBA-WHFBIAKZSA-N Asn-Gly-Asn Chemical compound NC(=O)C[C@H](N)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(O)=O DXVMJJNAOVECBA-WHFBIAKZSA-N 0.000 description 3
- LGCVSPFCFXWUEY-IHPCNDPISA-N Asn-Trp-Tyr Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CC3=CC=C(C=C3)O)C(=O)O)NC(=O)[C@H](CC(=O)N)N LGCVSPFCFXWUEY-IHPCNDPISA-N 0.000 description 3
- AHWRSSLYSGLBGD-CIUDSAMLSA-N Asp-Pro-Glu Chemical compound OC(=O)C[C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(O)=O)C(O)=O AHWRSSLYSGLBGD-CIUDSAMLSA-N 0.000 description 3
- SQIARYGNVQWOSB-BZSNNMDCSA-N Asp-Tyr-Phe Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O SQIARYGNVQWOSB-BZSNNMDCSA-N 0.000 description 3
- 208000004736 B-Cell Leukemia Diseases 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 208000026310 Breast neoplasm Diseases 0.000 description 3
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 3
- 241000282693 Cercopithecidae Species 0.000 description 3
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 3
- ZXCAQANTQWBICD-DCAQKATOSA-N Cys-Lys-Val Chemical compound CC(C)[C@@H](C(=O)O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CS)N ZXCAQANTQWBICD-DCAQKATOSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 3
- 108010087819 Fc receptors Proteins 0.000 description 3
- 102000009109 Fc receptors Human genes 0.000 description 3
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 3
- 241000233866 Fungi Species 0.000 description 3
- DHNWZLGBTPUTQQ-QEJZJMRPSA-N Gln-Asp-Trp Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)O)NC(=O)[C@H](CC(=O)O)NC(=O)[C@H](CCC(=O)N)N DHNWZLGBTPUTQQ-QEJZJMRPSA-N 0.000 description 3
- XKPACHRGOWQHFH-IRIUXVKKSA-N Gln-Thr-Tyr Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O XKPACHRGOWQHFH-IRIUXVKKSA-N 0.000 description 3
- FITIQFSXXBKFFM-NRPADANISA-N Gln-Val-Ser Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CO)C(O)=O FITIQFSXXBKFFM-NRPADANISA-N 0.000 description 3
- ITYRYNUZHPNCIK-GUBZILKMSA-N Glu-Ala-Leu Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(O)=O ITYRYNUZHPNCIK-GUBZILKMSA-N 0.000 description 3
- GLWXKFRTOHKGIT-ACZMJKKPSA-N Glu-Asn-Asn Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O GLWXKFRTOHKGIT-ACZMJKKPSA-N 0.000 description 3
- HNVFSTLPVJWIDV-CIUDSAMLSA-N Glu-Glu-Gln Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O HNVFSTLPVJWIDV-CIUDSAMLSA-N 0.000 description 3
- KASDBWKLWJKTLJ-GUBZILKMSA-N Glu-Glu-Met Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCSC)C(O)=O KASDBWKLWJKTLJ-GUBZILKMSA-N 0.000 description 3
- ALMBZBOCGSVSAI-ACZMJKKPSA-N Glu-Ser-Asn Chemical compound C(CC(=O)O)[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(=O)N)C(=O)O)N ALMBZBOCGSVSAI-ACZMJKKPSA-N 0.000 description 3
- MFYLRRCYBBJYPI-JYJNAYRXSA-N Glu-Tyr-Lys Chemical compound C1=CC(=CC=C1C[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CCC(=O)O)N)O MFYLRRCYBBJYPI-JYJNAYRXSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- VSVZIEVNUYDAFR-YUMQZZPRSA-N Gly-Ala-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)CN VSVZIEVNUYDAFR-YUMQZZPRSA-N 0.000 description 3
- GRIRDMVMJJDZKV-RCOVLWMOSA-N Gly-Asn-Val Chemical compound [H]NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(O)=O GRIRDMVMJJDZKV-RCOVLWMOSA-N 0.000 description 3
- PABFFPWEJMEVEC-JGVFFNPUSA-N Gly-Gln-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CCC(=O)N)NC(=O)CN)C(=O)O PABFFPWEJMEVEC-JGVFFNPUSA-N 0.000 description 3
- IKAIKUBBJHFNBZ-LURJTMIESA-N Gly-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)CN IKAIKUBBJHFNBZ-LURJTMIESA-N 0.000 description 3
- WCORRBXVISTKQL-WHFBIAKZSA-N Gly-Ser-Ser Chemical compound NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O WCORRBXVISTKQL-WHFBIAKZSA-N 0.000 description 3
- FFJQHWKSGAWSTJ-BFHQHQDPSA-N Gly-Thr-Ala Chemical compound [H]NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C)C(O)=O FFJQHWKSGAWSTJ-BFHQHQDPSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- WMKXFMUJRCEGRP-SRVKXCTJSA-N His-Asn-His Chemical compound C1=C(NC=N1)C[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CC2=CN=CN2)C(=O)O)N WMKXFMUJRCEGRP-SRVKXCTJSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- MKWSZEHGHSLNPF-NAKRPEOUSA-N Ile-Ala-Val Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](C(C)C)C(=O)O)N MKWSZEHGHSLNPF-NAKRPEOUSA-N 0.000 description 3
- FADXGVVLSPPEQY-GHCJXIJMSA-N Ile-Cys-Asn Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(=O)N)C(=O)O)N FADXGVVLSPPEQY-GHCJXIJMSA-N 0.000 description 3
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 3
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 3
- OIARJGNVARWKFP-YUMQZZPRSA-N Leu-Asn-Gly Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(O)=O OIARJGNVARWKFP-YUMQZZPRSA-N 0.000 description 3
- GPICTNQYKHHHTH-GUBZILKMSA-N Leu-Gln-Ser Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(O)=O GPICTNQYKHHHTH-GUBZILKMSA-N 0.000 description 3
- QJUWBDPGGYVRHY-YUMQZZPRSA-N Leu-Gly-Cys Chemical compound CC(C)C[C@@H](C(=O)NCC(=O)N[C@@H](CS)C(=O)O)N QJUWBDPGGYVRHY-YUMQZZPRSA-N 0.000 description 3
- HYMLKESRWLZDBR-WEDXCCLWSA-N Leu-Gly-Thr Chemical compound CC(C)C[C@H](N)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(O)=O HYMLKESRWLZDBR-WEDXCCLWSA-N 0.000 description 3
- SBANPBVRHYIMRR-UHFFFAOYSA-N Leu-Ser-Pro Natural products CC(C)CC(N)C(=O)NC(CO)C(=O)N1CCCC1C(O)=O SBANPBVRHYIMRR-UHFFFAOYSA-N 0.000 description 3
- AIQWYVFNBNNOLU-RHYQMDGZSA-N Leu-Thr-Val Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(O)=O AIQWYVFNBNNOLU-RHYQMDGZSA-N 0.000 description 3
- YQFZRHYZLARWDY-IHRRRGAJSA-N Leu-Val-Lys Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(O)=O)CCCCN YQFZRHYZLARWDY-IHRRRGAJSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- XNKDCYABMBBEKN-IUCAKERBSA-N Lys-Gly-Gln Chemical compound NCCCC[C@H](N)C(=O)NCC(=O)N[C@H](C(O)=O)CCC(N)=O XNKDCYABMBBEKN-IUCAKERBSA-N 0.000 description 3
- WQDKIVRHTQYJSN-DCAQKATOSA-N Lys-Ser-Arg Chemical compound C(CCN)C[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCN=C(N)N)C(=O)O)N WQDKIVRHTQYJSN-DCAQKATOSA-N 0.000 description 3
- IOQWIOPSKJOEKI-SRVKXCTJSA-N Lys-Ser-Leu Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(O)=O IOQWIOPSKJOEKI-SRVKXCTJSA-N 0.000 description 3
- IEVXCWPVBYCJRZ-IXOXFDKPSA-N Lys-Thr-His Chemical compound NCCCC[C@H](N)C(=O)N[C@@H]([C@H](O)C)C(=O)N[C@H](C(O)=O)CC1=CN=CN1 IEVXCWPVBYCJRZ-IXOXFDKPSA-N 0.000 description 3
- DLCAXBGXGOVUCD-PPCPHDFISA-N Lys-Thr-Ile Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O DLCAXBGXGOVUCD-PPCPHDFISA-N 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical compound ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 3
- OVRNDRQMDRJTHS-RTRLPJTCSA-N N-acetyl-D-glucosamine Chemical compound CC(=O)N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-RTRLPJTCSA-N 0.000 description 3
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 108090000854 Oxidoreductases Proteins 0.000 description 3
- 102000004316 Oxidoreductases Human genes 0.000 description 3
- 229930012538 Paclitaxel Natural products 0.000 description 3
- MSHZERMPZKCODG-ACRUOGEOSA-N Phe-Leu-Phe Chemical compound C([C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CC=CC=C1 MSHZERMPZKCODG-ACRUOGEOSA-N 0.000 description 3
- JDMKQHSHKJHAHR-UHFFFAOYSA-N Phe-Phe-Leu-Tyr Natural products C=1C=C(O)C=CC=1CC(C(O)=O)NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)CC1=CC=CC=C1 JDMKQHSHKJHAHR-UHFFFAOYSA-N 0.000 description 3
- JLLJTMHNXQTMCK-UBHSHLNASA-N Phe-Pro-Ala Chemical compound OC(=O)[C@H](C)NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)CC1=CC=CC=C1 JLLJTMHNXQTMCK-UBHSHLNASA-N 0.000 description 3
- WWPAHTZOWURIMR-ULQDDVLXSA-N Phe-Pro-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)CC1=CC=CC=C1 WWPAHTZOWURIMR-ULQDDVLXSA-N 0.000 description 3
- IIEOLPMQYRBZCN-SRVKXCTJSA-N Phe-Ser-Cys Chemical compound N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O IIEOLPMQYRBZCN-SRVKXCTJSA-N 0.000 description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 description 3
- IHCXPSYCHXFXKT-DCAQKATOSA-N Pro-Arg-Glu Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(O)=O IHCXPSYCHXFXKT-DCAQKATOSA-N 0.000 description 3
- TUYWCHPXKQTISF-LPEHRKFASA-N Pro-Cys-Pro Chemical compound C1C[C@H](NC1)C(=O)N[C@@H](CS)C(=O)N2CCC[C@@H]2C(=O)O TUYWCHPXKQTISF-LPEHRKFASA-N 0.000 description 3
- UAYHMOIGIQZLFR-NHCYSSNCSA-N Pro-Gln-Val Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(O)=O UAYHMOIGIQZLFR-NHCYSSNCSA-N 0.000 description 3
- LGSANCBHSMDFDY-GARJFASQSA-N Pro-Glu-Pro Chemical compound C1C[C@H](NC1)C(=O)N[C@@H](CCC(=O)O)C(=O)N2CCC[C@@H]2C(=O)O LGSANCBHSMDFDY-GARJFASQSA-N 0.000 description 3
- VPEVBAUSTBWQHN-NHCYSSNCSA-N Pro-Glu-Val Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(O)=O VPEVBAUSTBWQHN-NHCYSSNCSA-N 0.000 description 3
- ZLXKLMHAMDENIO-DCAQKATOSA-N Pro-Lys-Asp Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(O)=O ZLXKLMHAMDENIO-DCAQKATOSA-N 0.000 description 3
- PCWLNNZTBJTZRN-AVGNSLFASA-N Pro-Pro-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@H]1NCCC1 PCWLNNZTBJTZRN-AVGNSLFASA-N 0.000 description 3
- GOMUXSCOIWIJFP-GUBZILKMSA-N Pro-Ser-Arg Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O GOMUXSCOIWIJFP-GUBZILKMSA-N 0.000 description 3
- OWQXAJQZLWHPBH-FXQIFTODSA-N Pro-Ser-Asn Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(O)=O OWQXAJQZLWHPBH-FXQIFTODSA-N 0.000 description 3
- OYEDZGNMSBZCIM-XGEHTFHBSA-N Ser-Arg-Thr Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(O)=O OYEDZGNMSBZCIM-XGEHTFHBSA-N 0.000 description 3
- VGNYHOBZJKWRGI-CIUDSAMLSA-N Ser-Asn-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](N)CO VGNYHOBZJKWRGI-CIUDSAMLSA-N 0.000 description 3
- ZOHGLPQGEHSLPD-FXQIFTODSA-N Ser-Gln-Glu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(O)=O ZOHGLPQGEHSLPD-FXQIFTODSA-N 0.000 description 3
- BPMRXBZYPGYPJN-WHFBIAKZSA-N Ser-Gly-Asn Chemical compound [H]N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(O)=O BPMRXBZYPGYPJN-WHFBIAKZSA-N 0.000 description 3
- GZFAWAQTEYDKII-YUMQZZPRSA-N Ser-Gly-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H](N)CO GZFAWAQTEYDKII-YUMQZZPRSA-N 0.000 description 3
- YUJLIIRMIAGMCQ-CIUDSAMLSA-N Ser-Leu-Ser Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(O)=O YUJLIIRMIAGMCQ-CIUDSAMLSA-N 0.000 description 3
- GZSZPKSBVAOGIE-CIUDSAMLSA-N Ser-Lys-Ala Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(O)=O GZSZPKSBVAOGIE-CIUDSAMLSA-N 0.000 description 3
- FPCGZYMRFFIYIH-CIUDSAMLSA-N Ser-Lys-Ser Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(O)=O FPCGZYMRFFIYIH-CIUDSAMLSA-N 0.000 description 3
- VGQVAVQWKJLIRM-FXQIFTODSA-N Ser-Ser-Val Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O VGQVAVQWKJLIRM-FXQIFTODSA-N 0.000 description 3
- PCJLFYBAQZQOFE-KATARQTJSA-N Ser-Thr-Lys Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CO)N)O PCJLFYBAQZQOFE-KATARQTJSA-N 0.000 description 3
- RCOUFINCYASMDN-GUBZILKMSA-N Ser-Val-Met Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCSC)C(O)=O RCOUFINCYASMDN-GUBZILKMSA-N 0.000 description 3
- SIEBDTCABMZCLF-XGEHTFHBSA-N Ser-Val-Thr Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(O)=O SIEBDTCABMZCLF-XGEHTFHBSA-N 0.000 description 3
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 3
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 3
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 3
- ASJDFGOPDCVXTG-KATARQTJSA-N Thr-Cys-Leu Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(C)C)C(O)=O ASJDFGOPDCVXTG-KATARQTJSA-N 0.000 description 3
- KWQBJOUOSNJDRR-XAVMHZPKSA-N Thr-Cys-Pro Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CS)C(=O)N1CCC[C@@H]1C(=O)O)N)O KWQBJOUOSNJDRR-XAVMHZPKSA-N 0.000 description 3
- DSLHSTIUAPKERR-XGEHTFHBSA-N Thr-Cys-Val Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](C(C)C)C(O)=O DSLHSTIUAPKERR-XGEHTFHBSA-N 0.000 description 3
- FIFDDJFLNVAVMS-RHYQMDGZSA-N Thr-Leu-Met Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(O)=O FIFDDJFLNVAVMS-RHYQMDGZSA-N 0.000 description 3
- NCXVJIQMWSGRHY-KXNHARMFSA-N Thr-Leu-Pro Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N1CCC[C@@H]1C(=O)O)N)O NCXVJIQMWSGRHY-KXNHARMFSA-N 0.000 description 3
- BDGBHYCAZJPLHX-HJGDQZAQSA-N Thr-Lys-Asn Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(O)=O BDGBHYCAZJPLHX-HJGDQZAQSA-N 0.000 description 3
- UKINEYBQXPMOJO-UBHSHLNASA-N Trp-Asn-Ser Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CO)C(=O)O)N UKINEYBQXPMOJO-UBHSHLNASA-N 0.000 description 3
- DQDXHYIEITXNJY-BPUTZDHNSA-N Trp-Gln-Gln Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CCC(=O)N)C(=O)O)N DQDXHYIEITXNJY-BPUTZDHNSA-N 0.000 description 3
- SCCKSNREWHMKOJ-SRVKXCTJSA-N Tyr-Asn-Ser Chemical compound N[C@@H](Cc1ccc(O)cc1)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(O)=O SCCKSNREWHMKOJ-SRVKXCTJSA-N 0.000 description 3
- SINRIKQYQJRGDQ-MEYUZBJRSA-N Tyr-Lys-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CC1=CC=C(O)C=C1 SINRIKQYQJRGDQ-MEYUZBJRSA-N 0.000 description 3
- MQGGXGKQSVEQHR-KKUMJFAQSA-N Tyr-Ser-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC1=CC=C(O)C=C1 MQGGXGKQSVEQHR-KKUMJFAQSA-N 0.000 description 3
- NHOVZGFNTGMYMI-KKUMJFAQSA-N Tyr-Ser-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC1=CC=C(O)C=C1 NHOVZGFNTGMYMI-KKUMJFAQSA-N 0.000 description 3
- RIVVDNTUSRVTQT-IRIUXVKKSA-N Tyr-Thr-Gln Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)N)O RIVVDNTUSRVTQT-IRIUXVKKSA-N 0.000 description 3
- GNWUWQAVVJQREM-NHCYSSNCSA-N Val-Asn-His Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CC1=CN=CN1)C(=O)O)N GNWUWQAVVJQREM-NHCYSSNCSA-N 0.000 description 3
- QHDXUYOYTPWCSK-RCOVLWMOSA-N Val-Asp-Gly Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)NCC(=O)O)N QHDXUYOYTPWCSK-RCOVLWMOSA-N 0.000 description 3
- UEHRGZCNLSWGHK-DLOVCJGASA-N Val-Glu-Val Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(O)=O UEHRGZCNLSWGHK-DLOVCJGASA-N 0.000 description 3
- ZIGZPYJXIWLQFC-QTKMDUPCSA-N Val-His-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CC1=CN=CN1)NC(=O)[C@H](C(C)C)N)O ZIGZPYJXIWLQFC-QTKMDUPCSA-N 0.000 description 3
- XTDDIVQWDXMRJL-IHRRRGAJSA-N Val-Leu-His Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)O)NC(=O)[C@H](C(C)C)N XTDDIVQWDXMRJL-IHRRRGAJSA-N 0.000 description 3
- SYSWVVCYSXBVJG-RHYQMDGZSA-N Val-Leu-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C(C)C)N)O SYSWVVCYSXBVJG-RHYQMDGZSA-N 0.000 description 3
- HPANGHISDXDUQY-ULQDDVLXSA-N Val-Lys-Phe Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)O)N HPANGHISDXDUQY-ULQDDVLXSA-N 0.000 description 3
- KRAHMIJVUPUOTQ-DCAQKATOSA-N Val-Ser-His Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CC1=CN=CN1)C(=O)O)N KRAHMIJVUPUOTQ-DCAQKATOSA-N 0.000 description 3
- ZLNYBMWGPOKSLW-LSJOCFKGSA-N Val-Val-Asp Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(O)=O)C(O)=O ZLNYBMWGPOKSLW-LSJOCFKGSA-N 0.000 description 3
- LLJLBRRXKZTTRD-GUBZILKMSA-N Val-Val-Ser Chemical compound CC(C)[C@@H](C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CO)C(=O)O)N LLJLBRRXKZTTRD-GUBZILKMSA-N 0.000 description 3
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 3
- 230000009824 affinity maturation Effects 0.000 description 3
- 125000002723 alicyclic group Chemical group 0.000 description 3
- 125000004450 alkenylene group Chemical group 0.000 description 3
- 125000004414 alkyl thio group Chemical group 0.000 description 3
- 125000004419 alkynylene group Chemical group 0.000 description 3
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 3
- 108010050025 alpha-glutamyltryptophan Proteins 0.000 description 3
- 230000004075 alteration Effects 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 229940088710 antibiotic agent Drugs 0.000 description 3
- 239000012300 argon atmosphere Substances 0.000 description 3
- 108010077245 asparaginyl-proline Proteins 0.000 description 3
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 235000014633 carbohydrates Nutrition 0.000 description 3
- 150000001721 carbon Chemical group 0.000 description 3
- 230000004663 cell proliferation Effects 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 238000004590 computer program Methods 0.000 description 3
- 125000000753 cycloalkyl group Chemical group 0.000 description 3
- 125000002993 cycloalkylene group Chemical group 0.000 description 3
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 3
- 125000002228 disulfide group Chemical group 0.000 description 3
- 230000009977 dual effect Effects 0.000 description 3
- 229960002949 fluorouracil Drugs 0.000 description 3
- 230000033581 fucosylation Effects 0.000 description 3
- 108010000434 glycyl-alanyl-leucine Proteins 0.000 description 3
- 108010050475 glycyl-leucyl-tyrosine Proteins 0.000 description 3
- 150000004820 halides Chemical class 0.000 description 3
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 230000005847 immunogenicity Effects 0.000 description 3
- 238000007901 in situ hybridization Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 125000004551 isoquinolin-3-yl group Chemical group C1=NC(=CC2=CC=CC=C12)* 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 210000003292 kidney cell Anatomy 0.000 description 3
- 108010044311 leucyl-glycyl-glycine Proteins 0.000 description 3
- 201000007270 liver cancer Diseases 0.000 description 3
- 208000014018 liver neoplasm Diseases 0.000 description 3
- 210000001165 lymph node Anatomy 0.000 description 3
- 125000005439 maleimidyl group Chemical group C1(C=CC(N1*)=O)=O 0.000 description 3
- 230000036210 malignancy Effects 0.000 description 3
- 229960004961 mechlorethamine Drugs 0.000 description 3
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical class ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 3
- 229960004857 mitomycin Drugs 0.000 description 3
- 125000002950 monocyclic group Chemical group 0.000 description 3
- OWIUPIRUAQMTTK-UHFFFAOYSA-M n-aminocarbamate Chemical compound NNC([O-])=O OWIUPIRUAQMTTK-UHFFFAOYSA-M 0.000 description 3
- 239000002773 nucleotide Substances 0.000 description 3
- 125000003729 nucleotide group Chemical group 0.000 description 3
- 239000012044 organic layer Substances 0.000 description 3
- 150000002923 oximes Chemical class 0.000 description 3
- 229960001592 paclitaxel Drugs 0.000 description 3
- 239000008177 pharmaceutical agent Substances 0.000 description 3
- 108010024654 phenylalanyl-prolyl-alanine Proteins 0.000 description 3
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 108010070643 prolylglutamic acid Proteins 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- 238000003127 radioimmunoassay Methods 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 238000010188 recombinant method Methods 0.000 description 3
- 230000000717 retained effect Effects 0.000 description 3
- HXCHCVDVKSCDHU-PJKCJEBCSA-N s-[(2r,3s,4s,6s)-6-[[(2r,3s,4s,5r,6r)-5-[(2s,4s,5s)-5-(ethylamino)-4-methoxyoxan-2-yl]oxy-4-hydroxy-6-[[(2s,5z,9r,13e)-9-hydroxy-12-(methoxycarbonylamino)-13-[2-(methyltrisulfanyl)ethylidene]-11-oxo-2-bicyclo[7.3.1]trideca-1(12),5-dien-3,7-diynyl]oxy]-2-m Chemical compound C1[C@H](OC)[C@@H](NCC)CO[C@H]1O[C@H]1[C@H](O[C@@H]2C\3=C(NC(=O)OC)C(=O)C[C@@](C/3=C/CSSSC)(O)C#C\C=C/C#C2)O[C@H](C)[C@@H](NO[C@@H]2O[C@H](C)[C@@H](SC(=O)C=3C(=C(OC)C(O[C@H]4[C@@H]([C@H](OC)[C@@H](O)[C@H](C)O4)O)=C(I)C=3C)OC)[C@@H](O)C2)[C@@H]1O HXCHCVDVKSCDHU-PJKCJEBCSA-N 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 108010048397 seryl-lysyl-leucine Proteins 0.000 description 3
- 108010026333 seryl-proline Proteins 0.000 description 3
- 239000012453 solvate Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 235000000346 sugar Nutrition 0.000 description 3
- 125000005420 sulfonamido group Chemical group S(=O)(=O)(N*)* 0.000 description 3
- 125000001273 sulfonato group Chemical group [O-]S(*)(=O)=O 0.000 description 3
- 150000003457 sulfones Chemical class 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 108010080629 tryptophan-leucine Proteins 0.000 description 3
- 108010052774 valyl-lysyl-glycyl-phenylalanyl-tyrosine Proteins 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- JXLYSJRDGCGARV-CFWMRBGOSA-N vinblastine Chemical compound C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-CFWMRBGOSA-N 0.000 description 3
- 108010027345 wheylin-1 peptide Proteins 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- WGMMKWFUXPMTRW-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-[(2-bromoacetyl)amino]propanoate Chemical compound BrCC(=O)NCCC(=O)ON1C(=O)CCC1=O WGMMKWFUXPMTRW-UHFFFAOYSA-N 0.000 description 2
- QNNVICQPXUUBSN-GSVOUGTGSA-N (2r)-2-sulfanylpropan-1-ol Chemical compound C[C@@H](S)CO QNNVICQPXUUBSN-GSVOUGTGSA-N 0.000 description 2
- SLURUCSFDHKXFR-WWMWMSKMSA-N (7s,9s)-7-[[(1s,3r,4as,9s,9ar,10as)-9-methoxy-1-methyl-3,4,4a,6,7,9,9a,10a-octahydro-1h-pyrano[1,2][1,3]oxazolo[3,4-b][1,4]oxazin-3-yl]oxy]-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione Chemical compound O=C1C2=CC=CC(OC)=C2C(=O)C(C(O)=C23)=C1C(O)=C3C[C@@](O)(C(=O)CO)C[C@@H]2O[C@H]1C[C@@H]2N3CCO[C@H](OC)[C@H]3O[C@@H]2[C@H](C)O1 SLURUCSFDHKXFR-WWMWMSKMSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 2
- RVRLFABOQXZUJX-UHFFFAOYSA-N 1-[1-(2,5-dioxopyrrol-1-yl)ethyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C(C)N1C(=O)C=CC1=O RVRLFABOQXZUJX-UHFFFAOYSA-N 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical compound C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- CTMHWPIWNRWQEG-UHFFFAOYSA-N 1-methylcyclohexene Chemical compound CC1=CCCCC1 CTMHWPIWNRWQEG-UHFFFAOYSA-N 0.000 description 2
- DGHHQBMTXTWTJV-BQAIUKQQSA-N 119413-54-6 Chemical compound Cl.C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 DGHHQBMTXTWTJV-BQAIUKQQSA-N 0.000 description 2
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Chemical compound C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- AETVBWZVKDOWHH-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-(1-ethylazetidin-3-yl)oxypyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)OC1CN(C1)CC AETVBWZVKDOWHH-UHFFFAOYSA-N 0.000 description 2
- SCVJRXQHFJXZFZ-KVQBGUIXSA-N 2-amino-9-[(2r,4s,5r)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-3h-purine-6-thione Chemical compound C1=2NC(N)=NC(=S)C=2N=CN1[C@H]1C[C@H](O)[C@@H](CO)O1 SCVJRXQHFJXZFZ-KVQBGUIXSA-N 0.000 description 2
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 2
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 2
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 2
- 125000001963 4 membered heterocyclic group Chemical group 0.000 description 2
- 125000002373 5 membered heterocyclic group Chemical group 0.000 description 2
- 125000004070 6 membered heterocyclic group Chemical group 0.000 description 2
- 125000003341 7 membered heterocyclic group Chemical group 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- CXRCVCURMBFFOL-FXQIFTODSA-N Ala-Ala-Pro Chemical compound C[C@H](N)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(O)=O CXRCVCURMBFFOL-FXQIFTODSA-N 0.000 description 2
- KUDREHRZRIVKHS-UWJYBYFXSA-N Ala-Asp-Tyr Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O KUDREHRZRIVKHS-UWJYBYFXSA-N 0.000 description 2
- MDNAVFBZPROEHO-UHFFFAOYSA-N Ala-Lys-Val Natural products CC(C)C(C(O)=O)NC(=O)C(NC(=O)C(C)N)CCCCN MDNAVFBZPROEHO-UHFFFAOYSA-N 0.000 description 2
- ARHJJAAWNWOACN-FXQIFTODSA-N Ala-Ser-Val Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O ARHJJAAWNWOACN-FXQIFTODSA-N 0.000 description 2
- IOFVWPYSRSCWHI-JXUBOQSCSA-N Ala-Thr-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](C)N IOFVWPYSRSCWHI-JXUBOQSCSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- XRNXPIGJPQHCPC-RCWTZXSCSA-N Arg-Thr-Val Chemical compound CC(C)[C@H](NC(=O)[C@@H](NC(=O)[C@@H](N)CCCNC(N)=N)[C@@H](C)O)C(O)=O XRNXPIGJPQHCPC-RCWTZXSCSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- XYOVHPDDWCEUDY-CIUDSAMLSA-N Asn-Ala-Leu Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(O)=O XYOVHPDDWCEUDY-CIUDSAMLSA-N 0.000 description 2
- GXMSVVBIAMWMKO-BQBZGAKWSA-N Asn-Arg-Gly Chemical compound NC(=O)C[C@H](N)C(=O)N[C@H](C(=O)NCC(O)=O)CCCN=C(N)N GXMSVVBIAMWMKO-BQBZGAKWSA-N 0.000 description 2
- SNYCNNPOFYBCEK-ZLUOBGJFSA-N Asn-Ser-Ser Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O SNYCNNPOFYBCEK-ZLUOBGJFSA-N 0.000 description 2
- NVFSJIXJZCDICF-SRVKXCTJSA-N Asp-Lys-Lys Chemical compound C(CCN)C[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CC(=O)O)N NVFSJIXJZCDICF-SRVKXCTJSA-N 0.000 description 2
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 2
- 230000003844 B-cell-activation Effects 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 206010006187 Breast cancer Diseases 0.000 description 2
- 125000004648 C2-C8 alkenyl group Chemical group 0.000 description 2
- 125000004649 C2-C8 alkynyl group Chemical group 0.000 description 2
- KLWPJMFMVPTNCC-UHFFFAOYSA-N Camptothecin Natural products CCC1(O)C(=O)OCC2=C1C=C3C4Nc5ccccc5C=C4CN3C2=O KLWPJMFMVPTNCC-UHFFFAOYSA-N 0.000 description 2
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- 241000699802 Cricetulus griseus Species 0.000 description 2
- 239000004971 Cross linker Substances 0.000 description 2
- VIRYODQIWJNWNU-NRPADANISA-N Cys-Glu-Val Chemical compound CC(C)[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](CS)N VIRYODQIWJNWNU-NRPADANISA-N 0.000 description 2
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- 102220472268 Eukaryotic translation initiation factor 4E transporter_N28V_mutation Human genes 0.000 description 2
- 108010015133 Galactose oxidase Proteins 0.000 description 2
- JXFLPKSDLDEOQK-JHEQGTHGSA-N Gln-Gly-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H](N)CCC(N)=O JXFLPKSDLDEOQK-JHEQGTHGSA-N 0.000 description 2
- IULKWYSYZSURJK-AVGNSLFASA-N Gln-Leu-Lys Chemical compound NC(=O)CC[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(O)=O IULKWYSYZSURJK-AVGNSLFASA-N 0.000 description 2
- JJKKWYQVHRUSDG-GUBZILKMSA-N Glu-Ala-Lys Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(O)=O JJKKWYQVHRUSDG-GUBZILKMSA-N 0.000 description 2
- CLROYXHHUZELFX-FXQIFTODSA-N Glu-Gln-Asp Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(O)=O CLROYXHHUZELFX-FXQIFTODSA-N 0.000 description 2
- NNCSJUBVFBDDLC-YUMQZZPRSA-N Gly-Leu-Ser Chemical compound NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(O)=O NNCSJUBVFBDDLC-YUMQZZPRSA-N 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- QQFSKBMCAKWHLG-UHFFFAOYSA-N Ile-Phe-Pro-Pro Chemical compound C1CCC(C(=O)N2C(CCC2)C(O)=O)N1C(=O)C(NC(=O)C(N)C(C)CC)CC1=CC=CC=C1 QQFSKBMCAKWHLG-UHFFFAOYSA-N 0.000 description 2
- 102000016844 Immunoglobulin-like domains Human genes 0.000 description 2
- 108050006430 Immunoglobulin-like domains Proteins 0.000 description 2
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- DBVWMYGBVFCRBE-CIUDSAMLSA-N Leu-Asn-Asn Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O DBVWMYGBVFCRBE-CIUDSAMLSA-N 0.000 description 2
- PVMPDMIKUVNOBD-CIUDSAMLSA-N Leu-Asp-Ser Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(O)=O PVMPDMIKUVNOBD-CIUDSAMLSA-N 0.000 description 2
- JIHDFWWRYHSAQB-GUBZILKMSA-N Leu-Ser-Glu Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@H](C(O)=O)CCC(O)=O JIHDFWWRYHSAQB-GUBZILKMSA-N 0.000 description 2
- AMSSKPUHBUQBOQ-SRVKXCTJSA-N Leu-Ser-Lys Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)O)N AMSSKPUHBUQBOQ-SRVKXCTJSA-N 0.000 description 2
- BRTVHXHCUSXYRI-CIUDSAMLSA-N Leu-Ser-Ser Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O BRTVHXHCUSXYRI-CIUDSAMLSA-N 0.000 description 2
- FGMHXLULNHTPID-KKUMJFAQSA-N Lys-His-Lys Chemical compound NCCCC[C@H](N)C(=O)N[C@H](C(=O)N[C@@H](CCCCN)C(O)=O)CC1=CN=CN1 FGMHXLULNHTPID-KKUMJFAQSA-N 0.000 description 2
- PDIDTSZKKFEDMB-UWVGGRQHSA-N Lys-Pro-Gly Chemical compound [H]N[C@@H](CCCCN)C(=O)N1CCC[C@H]1C(=O)NCC(O)=O PDIDTSZKKFEDMB-UWVGGRQHSA-N 0.000 description 2
- CTJUSALVKAWFFU-CIUDSAMLSA-N Lys-Ser-Cys Chemical compound C(CCN)C[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O)N CTJUSALVKAWFFU-CIUDSAMLSA-N 0.000 description 2
- SQXZLVXQXWILKW-KKUMJFAQSA-N Lys-Ser-Phe Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O SQXZLVXQXWILKW-KKUMJFAQSA-N 0.000 description 2
- QLFAPXUXEBAWEK-NHCYSSNCSA-N Lys-Val-Asp Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(O)=O)C(O)=O QLFAPXUXEBAWEK-NHCYSSNCSA-N 0.000 description 2
- UGCIQUYEJIEHKX-GVXVVHGQSA-N Lys-Val-Glu Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(O)=O UGCIQUYEJIEHKX-GVXVVHGQSA-N 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 241001529936 Murinae Species 0.000 description 2
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- KLYYKKGCPOGDPE-OEAJRASXSA-N Phe-Thr-Leu Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(O)=O KLYYKKGCPOGDPE-OEAJRASXSA-N 0.000 description 2
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Natural products OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- NBBJYMSMWIIQGU-UHFFFAOYSA-N Propionic aldehyde Chemical compound CCC=O NBBJYMSMWIIQGU-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- 241000283984 Rodentia Species 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 206010039491 Sarcoma Diseases 0.000 description 2
- FTVRVZNYIYWJGB-ACZMJKKPSA-N Ser-Asp-Glu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(O)=O FTVRVZNYIYWJGB-ACZMJKKPSA-N 0.000 description 2
- SFTZWNJFZYOLBD-ZDLURKLDSA-N Ser-Gly-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H](N)CO SFTZWNJFZYOLBD-ZDLURKLDSA-N 0.000 description 2
- KCGIREHVWRXNDH-GARJFASQSA-N Ser-Leu-Pro Chemical compound CC(C)C[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@H](CO)N KCGIREHVWRXNDH-GARJFASQSA-N 0.000 description 2
- PPNPDKGQRFSCAC-CIUDSAMLSA-N Ser-Lys-Asp Chemical compound NCCCC[C@H](NC(=O)[C@@H](N)CO)C(=O)N[C@@H](CC(O)=O)C(O)=O PPNPDKGQRFSCAC-CIUDSAMLSA-N 0.000 description 2
- HHJFMHQYEAAOBM-ZLUOBGJFSA-N Ser-Ser-Ala Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(O)=O HHJFMHQYEAAOBM-ZLUOBGJFSA-N 0.000 description 2
- HNDMFDBQXYZSRM-IHRRRGAJSA-N Ser-Val-Phe Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O HNDMFDBQXYZSRM-IHRRRGAJSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- CYVQBKQYQGEELV-NKIYYHGXSA-N Thr-His-Gln Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N[C@@H](CCC(=O)N)C(=O)O)N)O CYVQBKQYQGEELV-NKIYYHGXSA-N 0.000 description 2
- YOOAQCZYZHGUAZ-KATARQTJSA-N Thr-Leu-Ser Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(O)=O YOOAQCZYZHGUAZ-KATARQTJSA-N 0.000 description 2
- DXPURPNJDFCKKO-RHYQMDGZSA-N Thr-Lys-Val Chemical compound CC(C)[C@H](NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)[C@@H](C)O)C(O)=O DXPURPNJDFCKKO-RHYQMDGZSA-N 0.000 description 2
- MROIJTGJGIDEEJ-RCWTZXSCSA-N Thr-Pro-Pro Chemical compound C[C@@H](O)[C@H](N)C(=O)N1CCC[C@H]1C(=O)N1[C@H](C(O)=O)CCC1 MROIJTGJGIDEEJ-RCWTZXSCSA-N 0.000 description 2
- CYCGARJWIQWPQM-YJRXYDGGSA-N Thr-Tyr-Ser Chemical compound C[C@@H](O)[C@H]([NH3+])C(=O)N[C@H](C(=O)N[C@@H](CO)C([O-])=O)CC1=CC=C(O)C=C1 CYCGARJWIQWPQM-YJRXYDGGSA-N 0.000 description 2
- AUZADXNWQMBZOO-JYJNAYRXSA-N Tyr-Pro-Arg Chemical compound C([C@H](N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O)C1=CC=C(O)C=C1 AUZADXNWQMBZOO-JYJNAYRXSA-N 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- LHADRQBREKTRLR-DCAQKATOSA-N Val-Cys-Leu Chemical compound CC(C)C[C@@H](C(=O)O)NC(=O)[C@H](CS)NC(=O)[C@H](C(C)C)N LHADRQBREKTRLR-DCAQKATOSA-N 0.000 description 2
- OXVPMZVGCAPFIG-BQFCYCMXSA-N Val-Gln-Trp Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)O)N OXVPMZVGCAPFIG-BQFCYCMXSA-N 0.000 description 2
- WDIGUPHXPBMODF-UMNHJUIQSA-N Val-Glu-Pro Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)N1CCC[C@@H]1C(=O)O)N WDIGUPHXPBMODF-UMNHJUIQSA-N 0.000 description 2
- VHIZXDZMTDVFGX-DCAQKATOSA-N Val-Ser-Leu Chemical compound CC(C)C[C@@H](C(=O)O)NC(=O)[C@H](CO)NC(=O)[C@H](C(C)C)N VHIZXDZMTDVFGX-DCAQKATOSA-N 0.000 description 2
- QPJSIBAOZBVELU-BPNCWPANSA-N Val-Tyr-Ala Chemical compound C[C@@H](C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)NC(=O)[C@H](C(C)C)N QPJSIBAOZBVELU-BPNCWPANSA-N 0.000 description 2
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 2
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 2
- CWRYPZZKDGJXCA-UHFFFAOYSA-N acenaphthene Chemical compound C1=CC(CC2)=C3C2=CC=CC3=C1 CWRYPZZKDGJXCA-UHFFFAOYSA-N 0.000 description 2
- 125000004036 acetal group Chemical group 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 229960004308 acetylcysteine Drugs 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 125000004423 acyloxy group Chemical group 0.000 description 2
- 229940009456 adriamycin Drugs 0.000 description 2
- 238000012867 alanine scanning Methods 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 2
- 150000001409 amidines Chemical class 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 230000001093 anti-cancer Effects 0.000 description 2
- 108010009111 arginyl-glycyl-glutamic acid Proteins 0.000 description 2
- 150000001491 aromatic compounds Chemical class 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- 229940120638 avastin Drugs 0.000 description 2
- CUFNKYGDVFVPHO-UHFFFAOYSA-N azulene Chemical compound C1=CC=CC2=CC=CC2=C1 CUFNKYGDVFVPHO-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- 125000002619 bicyclic group Chemical group 0.000 description 2
- 230000003115 biocidal effect Effects 0.000 description 2
- 210000001185 bone marrow Anatomy 0.000 description 2
- 125000001246 bromo group Chemical group Br* 0.000 description 2
- 229930195731 calicheamicin Natural products 0.000 description 2
- 229940127093 camptothecin Drugs 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 238000012054 celltiter-glo Methods 0.000 description 2
- 239000002738 chelating agent Substances 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 238000002512 chemotherapy Methods 0.000 description 2
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 2
- 229960004630 chlorambucil Drugs 0.000 description 2
- 150000001805 chlorine compounds Chemical class 0.000 description 2
- NEHMKBQYUWJMIP-UHFFFAOYSA-N chloromethane Chemical compound ClC NEHMKBQYUWJMIP-UHFFFAOYSA-N 0.000 description 2
- 229960002173 citrulline Drugs 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000012875 competitive assay Methods 0.000 description 2
- 230000002860 competitive effect Effects 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- COFJBSXICYYSKG-OAUVCNBTSA-N cph2u7dndy Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(N)=O)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 COFJBSXICYYSKG-OAUVCNBTSA-N 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- PSNOPSMXOBPNNV-VVCTWANISA-N cryptophycin 1 Chemical compound C1=C(Cl)C(OC)=CC=C1C[C@@H]1C(=O)NC[C@@H](C)C(=O)O[C@@H](CC(C)C)C(=O)O[C@H]([C@H](C)[C@@H]2[C@H](O2)C=2C=CC=CC=2)C/C=C/C(=O)N1 PSNOPSMXOBPNNV-VVCTWANISA-N 0.000 description 2
- PSNOPSMXOBPNNV-UHFFFAOYSA-N cryptophycin-327 Natural products C1=C(Cl)C(OC)=CC=C1CC1C(=O)NCC(C)C(=O)OC(CC(C)C)C(=O)OC(C(C)C2C(O2)C=2C=CC=CC=2)CC=CC(=O)N1 PSNOPSMXOBPNNV-UHFFFAOYSA-N 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- IMBXRZKCLVBLBH-OGYJWPHRSA-N cvp protocol Chemical compound ClCCN(CCCl)P1(=O)NCCCO1.O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1.C([C@H](C[C@]1(C(=O)OC)C=2C(=C3C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C=O)=CC=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 IMBXRZKCLVBLBH-OGYJWPHRSA-N 0.000 description 2
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 125000001295 dansyl group Chemical group [H]C1=C([H])C(N(C([H])([H])[H])C([H])([H])[H])=C2C([H])=C([H])C([H])=C(C2=C1[H])S(*)(=O)=O 0.000 description 2
- ILLHQJIJCRNRCJ-UHFFFAOYSA-N dec-1-yne Chemical compound CCCCCCCCC#C ILLHQJIJCRNRCJ-UHFFFAOYSA-N 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 239000003405 delayed action preparation Substances 0.000 description 2
- 238000001212 derivatisation Methods 0.000 description 2
- 238000002405 diagnostic procedure Methods 0.000 description 2
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 2
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 2
- QWHNJUXXYKPLQM-UHFFFAOYSA-N dimethyl cyclopentane Natural products CC1(C)CCCC1 QWHNJUXXYKPLQM-UHFFFAOYSA-N 0.000 description 2
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical compound [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- VSJKWCGYPAHWDS-UHFFFAOYSA-N dl-camptothecin Natural products C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)C5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-UHFFFAOYSA-N 0.000 description 2
- 229960003668 docetaxel Drugs 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 2
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 2
- 150000002222 fluorine compounds Chemical class 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 229960003082 galactose Drugs 0.000 description 2
- CHPZKNULDCNCBW-UHFFFAOYSA-N gallium nitrate Chemical compound [Ga+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O CHPZKNULDCNCBW-UHFFFAOYSA-N 0.000 description 2
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000036252 glycation Effects 0.000 description 2
- VPZXBVLAVMBEQI-UHFFFAOYSA-N glycyl-DL-alpha-alanine Natural products OC(=O)C(C)NC(=O)CN VPZXBVLAVMBEQI-UHFFFAOYSA-N 0.000 description 2
- 108010010147 glycylglutamine Proteins 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 125000001976 hemiacetal group Chemical group 0.000 description 2
- 150000002373 hemiacetals Chemical class 0.000 description 2
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 2
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 238000013537 high throughput screening Methods 0.000 description 2
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 2
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- DOUHZFSGSXMPIE-UHFFFAOYSA-N hydroxidooxidosulfur(.) Chemical compound [O]SO DOUHZFSGSXMPIE-UHFFFAOYSA-N 0.000 description 2
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 150000002466 imines Chemical class 0.000 description 2
- 125000001841 imino group Chemical group [H]N=* 0.000 description 2
- 230000002163 immunogen Effects 0.000 description 2
- 229940072221 immunoglobulins Drugs 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- KLEAIHJJLUAXIQ-JDRGBKBRSA-N irinotecan hydrochloride hydrate Chemical compound O.O.O.Cl.C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 KLEAIHJJLUAXIQ-JDRGBKBRSA-N 0.000 description 2
- HEBMCVBCEDMUOF-UHFFFAOYSA-N isochromane Chemical compound C1=CC=C2COCCC2=C1 HEBMCVBCEDMUOF-UHFFFAOYSA-N 0.000 description 2
- 238000001155 isoelectric focusing Methods 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 125000001810 isothiocyanato group Chemical group *N=C=S 0.000 description 2
- 125000000468 ketone group Chemical group 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 108010034529 leucyl-lysine Proteins 0.000 description 2
- 238000004020 luminiscence type Methods 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 2
- 229960001924 melphalan Drugs 0.000 description 2
- 229960001428 mercaptopurine Drugs 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 108010085203 methionylmethionine Proteins 0.000 description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 2
- BDJAEZRIGNCQBZ-UHFFFAOYSA-N methylcyclobutane Chemical compound CC1CCC1 BDJAEZRIGNCQBZ-UHFFFAOYSA-N 0.000 description 2
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 2
- GDOPTJXRTPNYNR-UHFFFAOYSA-N methylcyclopentane Chemical compound CC1CCCC1 GDOPTJXRTPNYNR-UHFFFAOYSA-N 0.000 description 2
- 238000002703 mutagenesis Methods 0.000 description 2
- 231100000350 mutagenesis Toxicity 0.000 description 2
- 208000025113 myeloid leukemia Diseases 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 239000002088 nanocapsule Substances 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 210000000822 natural killer cell Anatomy 0.000 description 2
- 229930014626 natural product Natural products 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 229960001420 nimustine Drugs 0.000 description 2
- VFEDRRNHLBGPNN-UHFFFAOYSA-N nimustine Chemical compound CC1=NC=C(CNC(=O)N(CCCl)N=O)C(N)=N1 VFEDRRNHLBGPNN-UHFFFAOYSA-N 0.000 description 2
- 125000000449 nitro group Chemical class [O-][N+](*)=O 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 210000001672 ovary Anatomy 0.000 description 2
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 description 2
- 229960001756 oxaliplatin Drugs 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- AQIXEPGDORPWBJ-UHFFFAOYSA-N pentan-3-ol Chemical compound CCC(O)CC AQIXEPGDORPWBJ-UHFFFAOYSA-N 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 238000010647 peptide synthesis reaction Methods 0.000 description 2
- PTMHPRAIXMAOOB-UHFFFAOYSA-N phosphoramidic acid Chemical group NP(O)(O)=O PTMHPRAIXMAOOB-UHFFFAOYSA-N 0.000 description 2
- 210000004180 plasmocyte Anatomy 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 229940068977 polysorbate 20 Drugs 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 230000004481 post-translational protein modification Effects 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 210000001236 prokaryotic cell Anatomy 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 238000000159 protein binding assay Methods 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 125000004159 quinolin-2-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C([H])C(*)=NC2=C1[H] 0.000 description 2
- 125000004549 quinolin-4-yl group Chemical group N1=CC=C(C2=CC=CC=C12)* 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 238000001959 radiotherapy Methods 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 238000010839 reverse transcription Methods 0.000 description 2
- 238000004007 reversed phase HPLC Methods 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 108010069117 seryl-lysyl-aspartic acid Proteins 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- JJAHTWIKCUJRDK-UHFFFAOYSA-N succinimidyl 4-(N-maleimidomethyl)cyclohexane-1-carboxylate Chemical compound C1CC(CN2C(C=CC2=O)=O)CCC1C(=O)ON1C(=O)CCC1=O JJAHTWIKCUJRDK-UHFFFAOYSA-N 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 125000001010 sulfinic acid amide group Chemical group 0.000 description 2
- 229910021653 sulphate ion Inorganic materials 0.000 description 2
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- DUYAAUVXQSMXQP-UHFFFAOYSA-M thioacetate Chemical compound CC([S-])=O DUYAAUVXQSMXQP-UHFFFAOYSA-M 0.000 description 2
- SRVJKTDHMYAMHA-WUXMJOGZSA-N thioacetazone Chemical compound CC(=O)NC1=CC=C(\C=N\NC(N)=S)C=C1 SRVJKTDHMYAMHA-WUXMJOGZSA-N 0.000 description 2
- 125000000858 thiocyanato group Chemical group *SC#N 0.000 description 2
- 150000003568 thioethers Chemical class 0.000 description 2
- CNHYKKNIIGEXAY-UHFFFAOYSA-N thiolan-2-imine Chemical compound N=C1CCCS1 CNHYKKNIIGEXAY-UHFFFAOYSA-N 0.000 description 2
- 229960001196 thiotepa Drugs 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 229960003087 tioguanine Drugs 0.000 description 2
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- PYHOFAHZHOBVGV-UHFFFAOYSA-N triazane Chemical compound NNN PYHOFAHZHOBVGV-UHFFFAOYSA-N 0.000 description 2
- ILWRPSCZWQJDMK-UHFFFAOYSA-N triethylazanium;chloride Chemical compound Cl.CCN(CC)CC ILWRPSCZWQJDMK-UHFFFAOYSA-N 0.000 description 2
- 125000004044 trifluoroacetyl group Chemical group FC(C(=O)*)(F)F 0.000 description 2
- 108010079202 tyrosyl-alanyl-cysteine Proteins 0.000 description 2
- 108010071635 tyrosyl-prolyl-arginine Proteins 0.000 description 2
- 229940035893 uracil Drugs 0.000 description 2
- 238000003828 vacuum filtration Methods 0.000 description 2
- 229960003048 vinblastine Drugs 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 229920003169 water-soluble polymer Polymers 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- JKHVDAUOODACDU-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(2,5-dioxopyrrol-1-yl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCN1C(=O)C=CC1=O JKHVDAUOODACDU-UHFFFAOYSA-N 0.000 description 1
- JWDFQMWEFLOOED-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(pyridin-2-yldisulfanyl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCSSC1=CC=CC=N1 JWDFQMWEFLOOED-UHFFFAOYSA-N 0.000 description 1
- PVGATNRYUYNBHO-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-(2,5-dioxopyrrol-1-yl)butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O PVGATNRYUYNBHO-UHFFFAOYSA-N 0.000 description 1
- VLARLSIGSPVYHX-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-(2,5-dioxopyrrol-1-yl)hexanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCN1C(=O)C=CC1=O VLARLSIGSPVYHX-UHFFFAOYSA-N 0.000 description 1
- WCMOHMXWOOBVMZ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-[3-(2,5-dioxopyrrol-1-yl)propanoylamino]hexanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCNC(=O)CCN1C(=O)C=CC1=O WCMOHMXWOOBVMZ-UHFFFAOYSA-N 0.000 description 1
- IHVODYOQUSEYJJ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-[[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]amino]hexanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCNC(=O)C(CC1)CCC1CN1C(=O)C=CC1=O IHVODYOQUSEYJJ-UHFFFAOYSA-N 0.000 description 1
- BSPMWFRGZQDRIU-UHFFFAOYSA-N (2-amino-1h-imidazol-5-yl)methanol Chemical class NC1=NC(CO)=CN1 BSPMWFRGZQDRIU-UHFFFAOYSA-N 0.000 description 1
- GJLXVWOMRRWCIB-MERZOTPQSA-N (2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-5-(diaminomethylideneamino)pentanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanoyl]amino]-6-aminohexanamide Chemical compound C([C@H](NC(=O)[C@H](CCCN=C(N)N)NC(=O)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(N)=O)C1=CC=C(O)C=C1 GJLXVWOMRRWCIB-MERZOTPQSA-N 0.000 description 1
- YXJBAUJMORGGEG-SSDOTTSWSA-N (2r)-2-(pyridin-2-yldisulfanyl)propan-1-ol Chemical compound OC[C@@H](C)SSC1=CC=CC=N1 YXJBAUJMORGGEG-SSDOTTSWSA-N 0.000 description 1
- YXTKHLHCVFUPPT-YYFJYKOTSA-N (2s)-2-[[4-[(2-amino-5-formyl-4-oxo-1,6,7,8-tetrahydropteridin-6-yl)methylamino]benzoyl]amino]pentanedioic acid;(1r,2r)-1,2-dimethanidylcyclohexane;5-fluoro-1h-pyrimidine-2,4-dione;oxalic acid;platinum(2+) Chemical compound [Pt+2].OC(=O)C(O)=O.[CH2-][C@@H]1CCCC[C@H]1[CH2-].FC1=CNC(=O)NC1=O.C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 YXTKHLHCVFUPPT-YYFJYKOTSA-N 0.000 description 1
- URLVCROWVOSNPT-XOTOMLERSA-N (2s)-4-[(13r)-13-hydroxy-13-[(2r,5r)-5-[(2r,5r)-5-[(1r)-1-hydroxyundecyl]oxolan-2-yl]oxolan-2-yl]tridecyl]-2-methyl-2h-furan-5-one Chemical compound O1[C@@H]([C@H](O)CCCCCCCCCC)CC[C@@H]1[C@@H]1O[C@@H]([C@H](O)CCCCCCCCCCCCC=2C(O[C@@H](C)C=2)=O)CC1 URLVCROWVOSNPT-XOTOMLERSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- TVIRNGFXQVMMGB-OFWIHYRESA-N (3s,6r,10r,13e,16s)-16-[(2r,3r,4s)-4-chloro-3-hydroxy-4-phenylbutan-2-yl]-10-[(3-chloro-4-methoxyphenyl)methyl]-6-methyl-3-(2-methylpropyl)-1,4-dioxa-8,11-diazacyclohexadec-13-ene-2,5,9,12-tetrone Chemical compound C1=C(Cl)C(OC)=CC=C1C[C@@H]1C(=O)NC[C@@H](C)C(=O)O[C@@H](CC(C)C)C(=O)O[C@H]([C@H](C)[C@@H](O)[C@@H](Cl)C=2C=CC=CC=2)C/C=C/C(=O)N1 TVIRNGFXQVMMGB-OFWIHYRESA-N 0.000 description 1
- AXKGIPZJYUNAIW-UHFFFAOYSA-N (4-aminophenyl)methanol Chemical compound NC1=CC=C(CO)C=C1 AXKGIPZJYUNAIW-UHFFFAOYSA-N 0.000 description 1
- LTDQGCFMTVHZKP-UHFFFAOYSA-N (4-bromophenyl)-(4,6-dimethoxy-3-methyl-1-benzofuran-2-yl)methanone Chemical compound O1C2=CC(OC)=CC(OC)=C2C(C)=C1C(=O)C1=CC=C(Br)C=C1 LTDQGCFMTVHZKP-UHFFFAOYSA-N 0.000 description 1
- IEUUDEWWMRQUDS-UHFFFAOYSA-N (6-azaniumylidene-1,6-dimethoxyhexylidene)azanium;dichloride Chemical compound Cl.Cl.COC(=N)CCCCC(=N)OC IEUUDEWWMRQUDS-UHFFFAOYSA-N 0.000 description 1
- FPVKHBSQESCIEP-UHFFFAOYSA-N (8S)-3-(2-deoxy-beta-D-erythro-pentofuranosyl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol Natural products C1C(O)C(CO)OC1N1C(NC=NCC2O)=C2N=C1 FPVKHBSQESCIEP-UHFFFAOYSA-N 0.000 description 1
- 125000006652 (C3-C12) cycloalkyl group Chemical group 0.000 description 1
- AGNGYMCLFWQVGX-AGFFZDDWSA-N (e)-1-[(2s)-2-amino-2-carboxyethoxy]-2-diazonioethenolate Chemical compound OC(=O)[C@@H](N)CO\C([O-])=C\[N+]#N AGNGYMCLFWQVGX-AGFFZDDWSA-N 0.000 description 1
- OFZYBEBWCZBCPM-UHFFFAOYSA-N 1,1-dimethylcyclobutane Chemical compound CC1(C)CCC1 OFZYBEBWCZBCPM-UHFFFAOYSA-N 0.000 description 1
- PBIJFSCPEFQXBB-UHFFFAOYSA-N 1,1-dimethylcyclopropane Chemical compound CC1(C)CC1 PBIJFSCPEFQXBB-UHFFFAOYSA-N 0.000 description 1
- FNQJDLTXOVEEFB-UHFFFAOYSA-N 1,2,3-benzothiadiazole Chemical compound C1=CC=C2SN=NC2=C1 FNQJDLTXOVEEFB-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- PUAKTHBSHFXVAG-UHFFFAOYSA-N 1,2-dimethylcyclobutene Chemical compound CC1=C(C)CC1 PUAKTHBSHFXVAG-UHFFFAOYSA-N 0.000 description 1
- SZZWLAZADBEDQP-UHFFFAOYSA-N 1,2-dimethylcyclopentene Chemical compound CC1=C(C)CCC1 SZZWLAZADBEDQP-UHFFFAOYSA-N 0.000 description 1
- BGJSXRVXTHVRSN-UHFFFAOYSA-N 1,3,5-trioxane Chemical compound C1OCOCO1 BGJSXRVXTHVRSN-UHFFFAOYSA-N 0.000 description 1
- FTNJQNQLEGKTGD-UHFFFAOYSA-N 1,3-benzodioxole Chemical compound C1=CC=C2OCOC2=C1 FTNJQNQLEGKTGD-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 1
- OGYGFUAIIOPWQD-UHFFFAOYSA-N 1,3-thiazolidine Chemical compound C1CSCN1 OGYGFUAIIOPWQD-UHFFFAOYSA-N 0.000 description 1
- YNGDWRXWKFWCJY-UHFFFAOYSA-N 1,4-Dihydropyridine Chemical compound C1C=CNC=C1 YNGDWRXWKFWCJY-UHFFFAOYSA-N 0.000 description 1
- VILFTWLXLYIEMV-UHFFFAOYSA-N 1,5-difluoro-2,4-dinitrobenzene Chemical compound [O-][N+](=O)C1=CC([N+]([O-])=O)=C(F)C=C1F VILFTWLXLYIEMV-UHFFFAOYSA-N 0.000 description 1
- VMLKTERJLVWEJJ-UHFFFAOYSA-N 1,5-naphthyridine Chemical compound C1=CC=NC2=CC=CN=C21 VMLKTERJLVWEJJ-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- MYBLAOJMRYYKMS-RTRLPJTCSA-N 1-(2-chloroethyl)-1-nitroso-3-[(3r,4r,5s,6r)-2,4,5-trihydroxy-6-(hydroxymethyl)oxan-3-yl]urea Chemical compound OC[C@H]1OC(O)[C@H](NC(=O)N(CCCl)N=O)[C@@H](O)[C@@H]1O MYBLAOJMRYYKMS-RTRLPJTCSA-N 0.000 description 1
- ZGEGCLOFRBLKSE-UHFFFAOYSA-N 1-Heptene Chemical group CCCCCC=C ZGEGCLOFRBLKSE-UHFFFAOYSA-N 0.000 description 1
- AASYSXRGODIQGY-UHFFFAOYSA-N 1-[1-(2,5-dioxopyrrol-1-yl)hexyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C(CCCCC)N1C(=O)C=CC1=O AASYSXRGODIQGY-UHFFFAOYSA-N 0.000 description 1
- DIYPCWKHSODVAP-UHFFFAOYSA-N 1-[3-(2,5-dioxopyrrol-1-yl)benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1=CC=CC(N2C(C=CC2=O)=O)=C1 DIYPCWKHSODVAP-UHFFFAOYSA-N 0.000 description 1
- VNJBTKQBKFMEHH-UHFFFAOYSA-N 1-[4-(2,5-dioxopyrrol-1-yl)-2,3-dihydroxybutyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1CC(O)C(O)CN1C(=O)C=CC1=O VNJBTKQBKFMEHH-UHFFFAOYSA-N 0.000 description 1
- WXXSHAKLDCERGU-UHFFFAOYSA-N 1-[4-(2,5-dioxopyrrol-1-yl)butyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1CCCCN1C(=O)C=CC1=O WXXSHAKLDCERGU-UHFFFAOYSA-N 0.000 description 1
- XQUPVDVFXZDTLT-UHFFFAOYSA-N 1-[4-[[4-(2,5-dioxopyrrol-1-yl)phenyl]methyl]phenyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C(C=C1)=CC=C1CC1=CC=C(N2C(C=CC2=O)=O)C=C1 XQUPVDVFXZDTLT-UHFFFAOYSA-N 0.000 description 1
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 1
- VYBULKYOUJBBPW-UHFFFAOYSA-N 1-amino-3-iminothiourea Chemical compound NNC(=S)N=N VYBULKYOUJBBPW-UHFFFAOYSA-N 0.000 description 1
- MUPYMRJBEZFVMT-UHFFFAOYSA-N 1-chloro-4-dimethoxyphosphorylsulfanylbenzene Chemical compound COP(=O)(OC)SC1=CC=C(Cl)C=C1 MUPYMRJBEZFVMT-UHFFFAOYSA-N 0.000 description 1
- AVPHQXWAMGTQPF-UHFFFAOYSA-N 1-methylcyclobutene Chemical compound CC1=CCC1 AVPHQXWAMGTQPF-UHFFFAOYSA-N 0.000 description 1
- ATQUFXWBVZUTKO-UHFFFAOYSA-N 1-methylcyclopentene Chemical compound CC1=CCCC1 ATQUFXWBVZUTKO-UHFFFAOYSA-N 0.000 description 1
- SHDPRTQPPWIEJG-UHFFFAOYSA-N 1-methylcyclopropene Chemical compound CC1=CC1 SHDPRTQPPWIEJG-UHFFFAOYSA-N 0.000 description 1
- CEEDNDKFZGTXOZ-VIFPVBQESA-N 1-o-tert-butyl 2-o-methyl (2s)-4-methylidenepyrrolidine-1,2-dicarboxylate Chemical compound COC(=O)[C@@H]1CC(=C)CN1C(=O)OC(C)(C)C CEEDNDKFZGTXOZ-VIFPVBQESA-N 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- CJEZLXXESOYJHS-UHFFFAOYSA-N 1-pyridin-2-ylisoquinoline Chemical compound N1=CC=CC=C1C1=NC=CC2=CC=CC=C12 CJEZLXXESOYJHS-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- IEMAOEFPZAIMCN-UHFFFAOYSA-N 1H-pyrazole Chemical compound C=1C=NNC=1.C=1C=NNC=1 IEMAOEFPZAIMCN-UHFFFAOYSA-N 0.000 description 1
- MREIFUWKYMNYTK-UHFFFAOYSA-N 1H-pyrrole Chemical compound C=1C=CNC=1.C=1C=CNC=1 MREIFUWKYMNYTK-UHFFFAOYSA-N 0.000 description 1
- SVUOLADPCWQTTE-UHFFFAOYSA-N 1h-1,2-benzodiazepine Chemical compound N1N=CC=CC2=CC=CC=C12 SVUOLADPCWQTTE-UHFFFAOYSA-N 0.000 description 1
- HUEXNHSMABCRTH-UHFFFAOYSA-N 1h-imidazole Chemical compound C1=CNC=N1.C1=CNC=N1 HUEXNHSMABCRTH-UHFFFAOYSA-N 0.000 description 1
- AWBOSXFRPFZLOP-UHFFFAOYSA-N 2,1,3-benzoxadiazole Chemical compound C1=CC=CC2=NON=C21 AWBOSXFRPFZLOP-UHFFFAOYSA-N 0.000 description 1
- FARGFPCUTAMIMN-UHFFFAOYSA-N 2,2-bis(2,5-dioxopyrrolidin-1-yl)octanedioic acid Chemical compound O=C1CCC(=O)N1C(C(O)=O)(CCCCCC(=O)O)N1C(=O)CCC1=O FARGFPCUTAMIMN-UHFFFAOYSA-N 0.000 description 1
- LSIXBBPOJBJQHN-UHFFFAOYSA-N 2,3-Dimethylbicyclo[2.2.1]hept-2-ene Chemical compound C1CC2C(C)=C(C)C1C2 LSIXBBPOJBJQHN-UHFFFAOYSA-N 0.000 description 1
- BTOTXLJHDSNXMW-POYBYMJQSA-N 2,3-dideoxyuridine Chemical compound O1[C@H](CO)CC[C@@H]1N1C(=O)NC(=O)C=C1 BTOTXLJHDSNXMW-POYBYMJQSA-N 0.000 description 1
- ZABMHLDQFJHDSC-UHFFFAOYSA-N 2,3-dihydro-1,3-oxazole Chemical compound C1NC=CO1 ZABMHLDQFJHDSC-UHFFFAOYSA-N 0.000 description 1
- FLNPFFMWAPTGOT-UHFFFAOYSA-N 2,3-dihydro-1h-pyrazole Chemical compound C1NNC=C1.C1NNC=C1 FLNPFFMWAPTGOT-UHFFFAOYSA-N 0.000 description 1
- JKTCBAGSMQIFNL-UHFFFAOYSA-N 2,3-dihydrofuran Chemical compound C1CC=CO1 JKTCBAGSMQIFNL-UHFFFAOYSA-N 0.000 description 1
- KGLPWQKSKUVKMJ-UHFFFAOYSA-N 2,3-dihydrophthalazine-1,4-dione Chemical compound C1=CC=C2C(=O)NNC(=O)C2=C1 KGLPWQKSKUVKMJ-UHFFFAOYSA-N 0.000 description 1
- GPWNWKWQOLEVEQ-UHFFFAOYSA-N 2,4-diaminopyrimidine-5-carbaldehyde Chemical compound NC1=NC=C(C=O)C(N)=N1 GPWNWKWQOLEVEQ-UHFFFAOYSA-N 0.000 description 1
- FYEWLNDAMUOKTG-UHFFFAOYSA-N 2-(1H-imidazol-2-yl)-1H-benzimidazole Chemical compound C1=CNC(C=2NC3=CC=CC=C3N=2)=N1 FYEWLNDAMUOKTG-UHFFFAOYSA-N 0.000 description 1
- PORTXTUJPQINJC-UHFFFAOYSA-N 2-(pyridin-2-yldisulfanyl)ethanol Chemical compound OCCSSC1=CC=CC=N1 PORTXTUJPQINJC-UHFFFAOYSA-N 0.000 description 1
- FZDFGHZZPBUTGP-UHFFFAOYSA-N 2-[[2-[bis(carboxymethyl)amino]-3-(4-isothiocyanatophenyl)propyl]-[2-[bis(carboxymethyl)amino]propyl]amino]acetic acid Chemical compound OC(=O)CN(CC(O)=O)C(C)CN(CC(O)=O)CC(N(CC(O)=O)CC(O)=O)CC1=CC=C(N=C=S)C=C1 FZDFGHZZPBUTGP-UHFFFAOYSA-N 0.000 description 1
- HGKUPDZBTAQFGJ-UHFFFAOYSA-N 2-amino-2-phenylpropanamide Chemical compound NC(=O)C(N)(C)C1=CC=CC=C1 HGKUPDZBTAQFGJ-UHFFFAOYSA-N 0.000 description 1
- BMUXBWLKTHLRQC-UHFFFAOYSA-N 2-azanylethanoic acid Chemical compound NCC(O)=O.NCC(O)=O.NCC(O)=O BMUXBWLKTHLRQC-UHFFFAOYSA-N 0.000 description 1
- JUIKUQOUMZUFQT-UHFFFAOYSA-N 2-bromoacetamide Chemical compound NC(=O)CBr JUIKUQOUMZUFQT-UHFFFAOYSA-N 0.000 description 1
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical compound C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- WZBZLXHSUKNNEF-UHFFFAOYSA-N 2-propan-2-yl-1-benzofuran Chemical compound C1=CC=C2OC(C(C)C)=CC2=C1 WZBZLXHSUKNNEF-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- RSEBUVRVKCANEP-UHFFFAOYSA-N 2-pyrroline Chemical compound C1CC=CN1 RSEBUVRVKCANEP-UHFFFAOYSA-N 0.000 description 1
- KGIGUEBEKRSTEW-UHFFFAOYSA-N 2-vinylpyridine Chemical compound C=CC1=CC=CC=N1 KGIGUEBEKRSTEW-UHFFFAOYSA-N 0.000 description 1
- BQTJMKIHKULPCZ-UHFFFAOYSA-N 2H-indene Chemical compound C1=CC=CC2=CCC=C21 BQTJMKIHKULPCZ-UHFFFAOYSA-N 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 1
- JZIBVTUXIVIFGC-UHFFFAOYSA-N 2H-pyrrole Chemical compound C1C=CC=N1 JZIBVTUXIVIFGC-UHFFFAOYSA-N 0.000 description 1
- CMLFRMDBDNHMRA-UHFFFAOYSA-N 2h-1,2-benzoxazine Chemical compound C1=CC=C2C=CNOC2=C1 CMLFRMDBDNHMRA-UHFFFAOYSA-N 0.000 description 1
- QMEQBOSUJUOXMX-UHFFFAOYSA-N 2h-oxadiazine Chemical compound N1OC=CC=N1 QMEQBOSUJUOXMX-UHFFFAOYSA-N 0.000 description 1
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 1
- BOLMDIXLULGTBD-UHFFFAOYSA-N 3,4-dihydro-2h-oxazine Chemical compound C1CC=CON1 BOLMDIXLULGTBD-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- JVQIKJMSUIMUDI-UHFFFAOYSA-N 3-pyrroline Chemical compound C1NCC=C1 JVQIKJMSUIMUDI-UHFFFAOYSA-N 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- ZMRMMAOBSFSXLN-UHFFFAOYSA-N 4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanehydrazide Chemical compound C1=CC(CCCC(=O)NN)=CC=C1N1C(=O)C=CC1=O ZMRMMAOBSFSXLN-UHFFFAOYSA-N 0.000 description 1
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 description 1
- WCVPFJVXEXJFLB-UHFFFAOYSA-N 4-aminobutanamide Chemical class NCCCC(N)=O WCVPFJVXEXJFLB-UHFFFAOYSA-N 0.000 description 1
- TVZGACDUOSZQKY-LBPRGKRZSA-N 4-aminofolic acid Chemical compound C1=NC2=NC(N)=NC(N)=C2N=C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 TVZGACDUOSZQKY-LBPRGKRZSA-N 0.000 description 1
- 125000006418 4-methylphenylsulfonyl group Chemical group 0.000 description 1
- BBEQQKBWUHCIOU-UHFFFAOYSA-N 5-(dimethylamino)-1-naphthalenesulfonic acid(dansyl acid) Chemical compound C1=CC=C2C(N(C)C)=CC=CC2=C1S(O)(=O)=O BBEQQKBWUHCIOU-UHFFFAOYSA-N 0.000 description 1
- WYXSYVWAUAUWLD-SHUUEZRQSA-N 6-azauridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=N1 WYXSYVWAUAUWLD-SHUUEZRQSA-N 0.000 description 1
- 102100031126 6-phosphogluconolactonase Human genes 0.000 description 1
- 108010029731 6-phosphogluconolactonase Proteins 0.000 description 1
- NJBMMMJOXRZENQ-UHFFFAOYSA-N 6H-pyrrolo[2,3-f]quinoline Chemical compound c1cc2ccc3[nH]cccc3c2n1 NJBMMMJOXRZENQ-UHFFFAOYSA-N 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- ZGXJTSGNIOSYLO-UHFFFAOYSA-N 88755TAZ87 Chemical compound NCC(=O)CCC(O)=O ZGXJTSGNIOSYLO-UHFFFAOYSA-N 0.000 description 1
- FUXVKZWTXQUGMW-FQEVSTJZSA-N 9-Aminocamptothecin Chemical compound C1=CC(N)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 FUXVKZWTXQUGMW-FQEVSTJZSA-N 0.000 description 1
- 208000002008 AIDS-Related Lymphoma Diseases 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- 208000010507 Adenocarcinoma of Lung Diseases 0.000 description 1
- JBGSZRYCXBPWGX-BQBZGAKWSA-N Ala-Arg-Gly Chemical compound OC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](N)C)CCCN=C(N)N JBGSZRYCXBPWGX-BQBZGAKWSA-N 0.000 description 1
- BUDNAJYVCUHLSV-ZLUOBGJFSA-N Ala-Asp-Ser Chemical compound C[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(O)=O BUDNAJYVCUHLSV-ZLUOBGJFSA-N 0.000 description 1
- PUBLUECXJRHTBK-ACZMJKKPSA-N Ala-Glu-Ser Chemical compound C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O PUBLUECXJRHTBK-ACZMJKKPSA-N 0.000 description 1
- NHLAEBFGWPXFGI-WHFBIAKZSA-N Ala-Gly-Asn Chemical compound C[C@@H](C(=O)NCC(=O)N[C@@H](CC(=O)N)C(=O)O)N NHLAEBFGWPXFGI-WHFBIAKZSA-N 0.000 description 1
- OBVSBEYOMDWLRJ-BFHQHQDPSA-N Ala-Gly-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)CNC(=O)[C@H](C)N OBVSBEYOMDWLRJ-BFHQHQDPSA-N 0.000 description 1
- FOHXUHGZZKETFI-JBDRJPRFSA-N Ala-Ile-Cys Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CS)C(=O)O)NC(=O)[C@H](C)N FOHXUHGZZKETFI-JBDRJPRFSA-N 0.000 description 1
- LNNSWWRRYJLGNI-NAKRPEOUSA-N Ala-Ile-Val Chemical compound C[C@H](N)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(O)=O LNNSWWRRYJLGNI-NAKRPEOUSA-N 0.000 description 1
- HHRAXZAYZFFRAM-CIUDSAMLSA-N Ala-Leu-Asn Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(O)=O HHRAXZAYZFFRAM-CIUDSAMLSA-N 0.000 description 1
- AWNAEZICPNGAJK-FXQIFTODSA-N Ala-Met-Ser Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CO)C(O)=O AWNAEZICPNGAJK-FXQIFTODSA-N 0.000 description 1
- OMNVYXHOSHNURL-WPRPVWTQSA-N Ala-Phe Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 OMNVYXHOSHNURL-WPRPVWTQSA-N 0.000 description 1
- YCRAFFCYWOUEOF-DLOVCJGASA-N Ala-Phe-Ser Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)C)CC1=CC=CC=C1 YCRAFFCYWOUEOF-DLOVCJGASA-N 0.000 description 1
- MAZZQZWCCYJQGZ-GUBZILKMSA-N Ala-Pro-Arg Chemical compound [H]N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCCNC(N)=N)C(O)=O MAZZQZWCCYJQGZ-GUBZILKMSA-N 0.000 description 1
- CREYEAPXISDKSB-FQPOAREZSA-N Ala-Thr-Tyr Chemical compound [H]N[C@@H](C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O CREYEAPXISDKSB-FQPOAREZSA-N 0.000 description 1
- PXAFZDXYEIIUTF-LKTVYLICSA-N Ala-Trp-Glu Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(=O)N[C@@H](CCC(O)=O)C(O)=O PXAFZDXYEIIUTF-LKTVYLICSA-N 0.000 description 1
- YJHKTAMKPGFJCT-NRPADANISA-N Ala-Val-Glu Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(O)=O YJHKTAMKPGFJCT-NRPADANISA-N 0.000 description 1
- VHAQSYHSDKERBS-XPUUQOCRSA-N Ala-Val-Gly Chemical compound C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)NCC(O)=O VHAQSYHSDKERBS-XPUUQOCRSA-N 0.000 description 1
- OMSKGWFGWCQFBD-KZVJFYERSA-N Ala-Val-Thr Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(O)=O OMSKGWFGWCQFBD-KZVJFYERSA-N 0.000 description 1
- 108010012934 Albumin-Bound Paclitaxel Proteins 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 102100021266 Alpha-(1,6)-fucosyltransferase Human genes 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- DBKNLHKEVPZVQC-LPEHRKFASA-N Arg-Ala-Pro Chemical compound NC(N)=NCCC[C@H](N)C(=O)N[C@@H](C)C(=O)N1CCC[C@@H]1C(O)=O DBKNLHKEVPZVQC-LPEHRKFASA-N 0.000 description 1
- MAISCYVJLBBRNU-DCAQKATOSA-N Arg-Asn-Lys Chemical compound C(CCN)C[C@@H](C(=O)O)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H](CCCN=C(N)N)N MAISCYVJLBBRNU-DCAQKATOSA-N 0.000 description 1
- PBSOQGZLPFVXPU-YUMQZZPRSA-N Arg-Glu-Gly Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(O)=O PBSOQGZLPFVXPU-YUMQZZPRSA-N 0.000 description 1
- JQFJNGVSGOUQDH-XIRDDKMYSA-N Arg-Glu-Trp Chemical compound C1=CC=C2C(C[C@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCN=C(N)N)N)C(O)=O)=CNC2=C1 JQFJNGVSGOUQDH-XIRDDKMYSA-N 0.000 description 1
- ZATRYQNPUHGXCU-DTWKUNHWSA-N Arg-Gly-Pro Chemical compound C1C[C@@H](N(C1)C(=O)CNC(=O)[C@H](CCCN=C(N)N)N)C(=O)O ZATRYQNPUHGXCU-DTWKUNHWSA-N 0.000 description 1
- OTZMRMHZCMZOJZ-SRVKXCTJSA-N Arg-Leu-Glu Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(O)=O OTZMRMHZCMZOJZ-SRVKXCTJSA-N 0.000 description 1
- VIINVRPKMUZYOI-DCAQKATOSA-N Arg-Met-Glu Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(O)=O VIINVRPKMUZYOI-DCAQKATOSA-N 0.000 description 1
- LXMKTIZAGIBQRX-HRCADAONSA-N Arg-Phe-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CC2=CC=CC=C2)NC(=O)[C@H](CCCN=C(N)N)N)C(=O)O LXMKTIZAGIBQRX-HRCADAONSA-N 0.000 description 1
- YCYXHLZRUSJITQ-SRVKXCTJSA-N Arg-Pro-Pro Chemical compound NC(=N)NCCC[C@H](N)C(=O)N1CCC[C@H]1C(=O)N1[C@H](C(O)=O)CCC1 YCYXHLZRUSJITQ-SRVKXCTJSA-N 0.000 description 1
- ICRHGPYYXMWHIE-LPEHRKFASA-N Arg-Ser-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CO)NC(=O)[C@H](CCCN=C(N)N)N)C(=O)O ICRHGPYYXMWHIE-LPEHRKFASA-N 0.000 description 1
- HRCIIMCTUIAKQB-XGEHTFHBSA-N Arg-Thr-Cys Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CS)C(=O)O)NC(=O)[C@H](CCCN=C(N)N)N)O HRCIIMCTUIAKQB-XGEHTFHBSA-N 0.000 description 1
- LYJXHXGPWDTLKW-HJGDQZAQSA-N Arg-Thr-Gln Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CCCN=C(N)N)N)O LYJXHXGPWDTLKW-HJGDQZAQSA-N 0.000 description 1
- JBQORRNSZGTLCV-WDSOQIARSA-N Arg-Trp-Lys Chemical compound C1=CC=C2C(C[C@@H](C(=O)N[C@@H](CCCCN)C(O)=O)NC(=O)[C@@H](N)CCCN=C(N)N)=CNC2=C1 JBQORRNSZGTLCV-WDSOQIARSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DJHGAFSJWGLOIV-UHFFFAOYSA-K Arsenate3- Chemical compound [O-][As]([O-])([O-])=O DJHGAFSJWGLOIV-UHFFFAOYSA-K 0.000 description 1
- XQQVCUIBGYFKDC-OLHMAJIHSA-N Asn-Asp-Thr Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O XQQVCUIBGYFKDC-OLHMAJIHSA-N 0.000 description 1
- KUYKVGODHGHFDI-ACZMJKKPSA-N Asn-Gln-Ser Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(O)=O KUYKVGODHGHFDI-ACZMJKKPSA-N 0.000 description 1
- WONGRTVAMHFGBE-WDSKDSINSA-N Asn-Gly-Gln Chemical compound C(CC(=O)N)[C@@H](C(=O)O)NC(=O)CNC(=O)[C@H](CC(=O)N)N WONGRTVAMHFGBE-WDSKDSINSA-N 0.000 description 1
- PBSQFBAJKPLRJY-BYULHYEWSA-N Asn-Gly-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)CNC(=O)[C@H](CC(=O)N)N PBSQFBAJKPLRJY-BYULHYEWSA-N 0.000 description 1
- OLVIPTLKNSAYRJ-YUMQZZPRSA-N Asn-Gly-Lys Chemical compound C(CCN)C[C@@H](C(=O)O)NC(=O)CNC(=O)[C@H](CC(=O)N)N OLVIPTLKNSAYRJ-YUMQZZPRSA-N 0.000 description 1
- NLRJGXZWTKXRHP-DCAQKATOSA-N Asn-Leu-Arg Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O NLRJGXZWTKXRHP-DCAQKATOSA-N 0.000 description 1
- KHCNTVRVAYCPQE-CIUDSAMLSA-N Asn-Lys-Asn Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(O)=O KHCNTVRVAYCPQE-CIUDSAMLSA-N 0.000 description 1
- YXVAESUIQFDBHN-SRVKXCTJSA-N Asn-Phe-Ser Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CO)C(O)=O YXVAESUIQFDBHN-SRVKXCTJSA-N 0.000 description 1
- YUOXLJYVSZYPBJ-CIUDSAMLSA-N Asn-Pro-Glu Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(O)=O)C(O)=O YUOXLJYVSZYPBJ-CIUDSAMLSA-N 0.000 description 1
- UWFOMGUWGPRVBW-GUBZILKMSA-N Asn-Pro-Met Chemical compound CSCC[C@@H](C(=O)O)NC(=O)[C@@H]1CCCN1C(=O)[C@H](CC(=O)N)N UWFOMGUWGPRVBW-GUBZILKMSA-N 0.000 description 1
- VCJCPARXDBEGNE-GUBZILKMSA-N Asn-Pro-Pro Chemical compound NC(=O)C[C@H](N)C(=O)N1CCC[C@H]1C(=O)N1[C@H](C(O)=O)CCC1 VCJCPARXDBEGNE-GUBZILKMSA-N 0.000 description 1
- UGXYFDQFLVCDFC-CIUDSAMLSA-N Asn-Ser-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O UGXYFDQFLVCDFC-CIUDSAMLSA-N 0.000 description 1
- NCXTYSVDWLAQGZ-ZKWXMUAHSA-N Asn-Ser-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O NCXTYSVDWLAQGZ-ZKWXMUAHSA-N 0.000 description 1
- JBDLMLZNDRLDIX-HJGDQZAQSA-N Asn-Thr-Leu Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(O)=O JBDLMLZNDRLDIX-HJGDQZAQSA-N 0.000 description 1
- ZAESWDKAMDVHLL-RCOVLWMOSA-N Asn-Val-Gly Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(O)=O ZAESWDKAMDVHLL-RCOVLWMOSA-N 0.000 description 1
- LMIWYCWRJVMAIQ-NHCYSSNCSA-N Asn-Val-Lys Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CC(=O)N)N LMIWYCWRJVMAIQ-NHCYSSNCSA-N 0.000 description 1
- PQKSVQSMTHPRIB-ZKWXMUAHSA-N Asn-Val-Ser Chemical compound [H]N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CO)C(O)=O PQKSVQSMTHPRIB-ZKWXMUAHSA-N 0.000 description 1
- MRQQMVZUHXUPEV-IHRRRGAJSA-N Asp-Arg-Phe Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O MRQQMVZUHXUPEV-IHRRRGAJSA-N 0.000 description 1
- BFOYULZBKYOKAN-OLHMAJIHSA-N Asp-Asp-Thr Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O BFOYULZBKYOKAN-OLHMAJIHSA-N 0.000 description 1
- NYQHSUGFEWDWPD-ACZMJKKPSA-N Asp-Gln-Ala Chemical compound C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](CC(=O)O)N NYQHSUGFEWDWPD-ACZMJKKPSA-N 0.000 description 1
- JUWZKMBALYLZCK-WHFBIAKZSA-N Asp-Gly-Asn Chemical compound OC(=O)C[C@H](N)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(O)=O JUWZKMBALYLZCK-WHFBIAKZSA-N 0.000 description 1
- PZXPWHFYZXTFBI-YUMQZZPRSA-N Asp-Gly-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H](N)CC(O)=O PZXPWHFYZXTFBI-YUMQZZPRSA-N 0.000 description 1
- SVABRQFIHCSNCI-FOHZUACHSA-N Asp-Gly-Thr Chemical compound [H]N[C@@H](CC(O)=O)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(O)=O SVABRQFIHCSNCI-FOHZUACHSA-N 0.000 description 1
- HOBNTSHITVVNBN-ZPFDUUQYSA-N Asp-Ile-Leu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)O)NC(=O)[C@H](CC(=O)O)N HOBNTSHITVVNBN-ZPFDUUQYSA-N 0.000 description 1
- DWOGMPWRQQWPPF-GUBZILKMSA-N Asp-Leu-Glu Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(O)=O DWOGMPWRQQWPPF-GUBZILKMSA-N 0.000 description 1
- AYFVRYXNDHBECD-YUMQZZPRSA-N Asp-Leu-Gly Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(O)=O AYFVRYXNDHBECD-YUMQZZPRSA-N 0.000 description 1
- XWSIYTYNLKCLJB-CIUDSAMLSA-N Asp-Lys-Asn Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(O)=O XWSIYTYNLKCLJB-CIUDSAMLSA-N 0.000 description 1
- WMLFFCRUSPNENW-ZLUOBGJFSA-N Asp-Ser-Ala Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(O)=O WMLFFCRUSPNENW-ZLUOBGJFSA-N 0.000 description 1
- KGHLGJAXYSVNJP-WHFBIAKZSA-N Asp-Ser-Gly Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CO)C(=O)NCC(O)=O KGHLGJAXYSVNJP-WHFBIAKZSA-N 0.000 description 1
- MGSVBZIBCCKGCY-ZLUOBGJFSA-N Asp-Ser-Ser Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O MGSVBZIBCCKGCY-ZLUOBGJFSA-N 0.000 description 1
- ITGFVUYOLWBPQW-KKHAAJSZSA-N Asp-Thr-Val Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(O)=O ITGFVUYOLWBPQW-KKHAAJSZSA-N 0.000 description 1
- NVXLFIPTHPKSKL-UBHSHLNASA-N Asp-Trp-Asn Chemical compound C1=CC=C2C(C[C@H](NC(=O)[C@H](CC(O)=O)N)C(=O)N[C@@H](CC(N)=O)C(O)=O)=CNC2=C1 NVXLFIPTHPKSKL-UBHSHLNASA-N 0.000 description 1
- GFYOIYJJMSHLSN-QXEWZRGKSA-N Asp-Val-Arg Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O GFYOIYJJMSHLSN-QXEWZRGKSA-N 0.000 description 1
- VXEORMGBKTUUCM-KWBADKCTSA-N Asp-Val-Gly-Pro Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N1CCC[C@H]1C(O)=O VXEORMGBKTUUCM-KWBADKCTSA-N 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 108091008875 B cell receptors Proteins 0.000 description 1
- 208000036170 B-Cell Marginal Zone Lymphoma Diseases 0.000 description 1
- 108020003591 B-Form DNA Proteins 0.000 description 1
- 208000037914 B-cell disorder Diseases 0.000 description 1
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 1
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 240000008564 Boehmeria nivea Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- YFSNBQBDMHKKQP-UHFFFAOYSA-N C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.N(=C=S)C1(CNCC(NCCN)C)CC=CC=C1 Chemical compound C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.N(=C=S)C1(CNCC(NCCN)C)CC=CC=C1 YFSNBQBDMHKKQP-UHFFFAOYSA-N 0.000 description 1
- OYMXIQOPIIXDSM-UHFFFAOYSA-N C(CCCCC)(=O)OSC Chemical compound C(CCCCC)(=O)OSC OYMXIQOPIIXDSM-UHFFFAOYSA-N 0.000 description 1
- XRGUZUWNIIFDHP-ZSCHJXSPSA-N C1=CC=C2NC=CC2=C1.NCCCC[C@H](N)C(O)=O Chemical compound C1=CC=C2NC=CC2=C1.NCCCC[C@H](N)C(O)=O XRGUZUWNIIFDHP-ZSCHJXSPSA-N 0.000 description 1
- 102100024217 CAMPATH-1 antigen Human genes 0.000 description 1
- 108010065524 CD52 Antigen Proteins 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 102000005600 Cathepsins Human genes 0.000 description 1
- 108010084457 Cathepsins Proteins 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- JWBOIMRXGHLCPP-UHFFFAOYSA-N Chloditan Chemical compound C=1C=CC=C(Cl)C=1C(C(Cl)Cl)C1=CC=C(Cl)C=C1 JWBOIMRXGHLCPP-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 241000282552 Chlorocebus aethiops Species 0.000 description 1
- 108010023736 Chondroitinases and Chondroitin Lyases Proteins 0.000 description 1
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229930188224 Cryptophycin Natural products 0.000 description 1
- PMPVIKIVABFJJI-UHFFFAOYSA-N Cyclobutane Chemical compound C1CCC1 PMPVIKIVABFJJI-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- LVZWSLJZHVFIQJ-UHFFFAOYSA-N Cyclopropane Chemical compound C1CC1 LVZWSLJZHVFIQJ-UHFFFAOYSA-N 0.000 description 1
- AMRLSQGGERHDHJ-FXQIFTODSA-N Cys-Ala-Arg Chemical compound [H]N[C@@H](CS)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O AMRLSQGGERHDHJ-FXQIFTODSA-N 0.000 description 1
- SZQCDCKIGWQAQN-FXQIFTODSA-N Cys-Arg-Ala Chemical compound [H]N[C@@H](CS)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(O)=O SZQCDCKIGWQAQN-FXQIFTODSA-N 0.000 description 1
- CPTUXCUWQIBZIF-ZLUOBGJFSA-N Cys-Asn-Ser Chemical compound SC[C@H](N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(O)=O CPTUXCUWQIBZIF-ZLUOBGJFSA-N 0.000 description 1
- UUERSUCTHOZPMG-SRVKXCTJSA-N Cys-Asn-Tyr Chemical compound SC[C@H](N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 UUERSUCTHOZPMG-SRVKXCTJSA-N 0.000 description 1
- IIGHQOPGMGKDMT-SRVKXCTJSA-N Cys-Asp-Phe Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)O)NC(=O)[C@H](CC(=O)O)NC(=O)[C@H](CS)N IIGHQOPGMGKDMT-SRVKXCTJSA-N 0.000 description 1
- HIPHJNWPLMUBQQ-ACZMJKKPSA-N Cys-Cys-Gln Chemical compound SC[C@H](N)C(=O)N[C@@H](CS)C(=O)N[C@H](C(O)=O)CCC(N)=O HIPHJNWPLMUBQQ-ACZMJKKPSA-N 0.000 description 1
- KXUKWRVYDYIPSQ-CIUDSAMLSA-N Cys-Leu-Ala Chemical compound [H]N[C@@H](CS)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(O)=O KXUKWRVYDYIPSQ-CIUDSAMLSA-N 0.000 description 1
- WVLZTXGTNGHPBO-SRVKXCTJSA-N Cys-Leu-Leu Chemical compound [H]N[C@@H](CS)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O WVLZTXGTNGHPBO-SRVKXCTJSA-N 0.000 description 1
- HJGUQJJJXQGXGJ-FXQIFTODSA-N Cys-Met-Ser Chemical compound CSCC[C@@H](C(=O)N[C@@H](CO)C(=O)O)NC(=O)[C@H](CS)N HJGUQJJJXQGXGJ-FXQIFTODSA-N 0.000 description 1
- BOMGEMDZTNZESV-QWRGUYRKSA-N Cys-Tyr-Gly Chemical compound SC[C@H](N)C(=O)N[C@H](C(=O)NCC(O)=O)CC1=CC=C(O)C=C1 BOMGEMDZTNZESV-QWRGUYRKSA-N 0.000 description 1
- ATFSDBMHRCDLBV-BPUTZDHNSA-N Cys-Val-Trp Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)O)NC(=O)[C@H](CS)N ATFSDBMHRCDLBV-BPUTZDHNSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- WQZGKKKJIJFFOK-CBPJZXOFSA-N D-Gulose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-CBPJZXOFSA-N 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- CYCGRDQQIOGCKX-UHFFFAOYSA-N Dehydro-luciferin Natural products OC(=O)C1=CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 CYCGRDQQIOGCKX-UHFFFAOYSA-N 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 102100024746 Dihydrofolate reductase Human genes 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- BUDQDWGNQVEFAC-UHFFFAOYSA-N Dihydropyran Chemical compound C1COC=CC1 BUDQDWGNQVEFAC-UHFFFAOYSA-N 0.000 description 1
- WQOXQRCZOLPYPM-UHFFFAOYSA-N Dimethyl disulfide Natural products CSSC WQOXQRCZOLPYPM-UHFFFAOYSA-N 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 206010014733 Endometrial cancer Diseases 0.000 description 1
- 206010014759 Endometrial neoplasm Diseases 0.000 description 1
- SAMRUMKYXPVKPA-VFKOLLTISA-N Enocitabine Chemical compound O=C1N=C(NC(=O)CCCCCCCCCCCCCCCCCCCCC)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 SAMRUMKYXPVKPA-VFKOLLTISA-N 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- OBMLHUPNRURLOK-XGRAFVIBSA-N Epitiostanol Chemical compound C1[C@@H]2S[C@@H]2C[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CC[C@H]21 OBMLHUPNRURLOK-XGRAFVIBSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 206010073306 Exposure to radiation Diseases 0.000 description 1
- 206010061850 Extranodal marginal zone B-cell lymphoma (MALT type) Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 108090000331 Firefly luciferases Proteins 0.000 description 1
- BJGNCJDXODQBOB-UHFFFAOYSA-N Fivefly Luciferin Natural products OC(=O)C1CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 BJGNCJDXODQBOB-UHFFFAOYSA-N 0.000 description 1
- 108010019236 Fucosyltransferases Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- XOKGKOQWADCLFQ-GARJFASQSA-N Gln-Arg-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CCC(=O)N)N)C(=O)O XOKGKOQWADCLFQ-GARJFASQSA-N 0.000 description 1
- GMGKDVVBSVVKCT-NUMRIWBASA-N Gln-Asn-Thr Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O GMGKDVVBSVVKCT-NUMRIWBASA-N 0.000 description 1
- XKBASPWPBXNVLQ-WDSKDSINSA-N Gln-Gly-Asn Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(O)=O XKBASPWPBXNVLQ-WDSKDSINSA-N 0.000 description 1
- FTIJVMLAGRAYMJ-MNXVOIDGSA-N Gln-Ile-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@@H](N)CCC(N)=O FTIJVMLAGRAYMJ-MNXVOIDGSA-N 0.000 description 1
- VZRAXPGTUNDIDK-GUBZILKMSA-N Gln-Leu-Asn Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)O)NC(=O)[C@H](CCC(=O)N)N VZRAXPGTUNDIDK-GUBZILKMSA-N 0.000 description 1
- LGIKBBLQVSWUGK-DCAQKATOSA-N Gln-Leu-Gln Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O LGIKBBLQVSWUGK-DCAQKATOSA-N 0.000 description 1
- CAXXTYYGFYTBPV-IUCAKERBSA-N Gln-Leu-Gly Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(O)=O CAXXTYYGFYTBPV-IUCAKERBSA-N 0.000 description 1
- XZUUUKNKNWVPHQ-JYJNAYRXSA-N Gln-Phe-Leu Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(C)C)C(O)=O XZUUUKNKNWVPHQ-JYJNAYRXSA-N 0.000 description 1
- CVRUVYDNRPSKBM-QEJZJMRPSA-N Gln-Trp-Ser Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CO)C(=O)O)NC(=O)[C@H](CCC(=O)N)N CVRUVYDNRPSKBM-QEJZJMRPSA-N 0.000 description 1
- WPJDPEOQUIXXOY-AVGNSLFASA-N Gln-Tyr-Asn Chemical compound C1=CC(=CC=C1C[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)O)NC(=O)[C@H](CCC(=O)N)N)O WPJDPEOQUIXXOY-AVGNSLFASA-N 0.000 description 1
- ZFBBMCKQSNJZSN-AUTRQRHGSA-N Gln-Val-Gln Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O ZFBBMCKQSNJZSN-AUTRQRHGSA-N 0.000 description 1
- GJLXZITZLUUXMJ-NHCYSSNCSA-N Gln-Val-Met Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCSC)C(=O)O)NC(=O)[C@H](CCC(=O)N)N GJLXZITZLUUXMJ-NHCYSSNCSA-N 0.000 description 1
- LKDIBBOKUAASNP-FXQIFTODSA-N Glu-Ala-Glu Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(O)=O LKDIBBOKUAASNP-FXQIFTODSA-N 0.000 description 1
- VPKBCVUDBNINAH-GARJFASQSA-N Glu-Arg-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CCC(=O)O)N)C(=O)O VPKBCVUDBNINAH-GARJFASQSA-N 0.000 description 1
- RDPOETHPAQEGDP-ACZMJKKPSA-N Glu-Asp-Ala Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(O)=O RDPOETHPAQEGDP-ACZMJKKPSA-N 0.000 description 1
- PAQUJCSYVIBPLC-AVGNSLFASA-N Glu-Asp-Phe Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 PAQUJCSYVIBPLC-AVGNSLFASA-N 0.000 description 1
- LGYZYFFDELZWRS-DCAQKATOSA-N Glu-Glu-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CCC(O)=O LGYZYFFDELZWRS-DCAQKATOSA-N 0.000 description 1
- QJCKNLPMTPXXEM-AUTRQRHGSA-N Glu-Glu-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CCC(O)=O QJCKNLPMTPXXEM-AUTRQRHGSA-N 0.000 description 1
- AIGROOHQXCACHL-WDSKDSINSA-N Glu-Gly-Ala Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](C)C(O)=O AIGROOHQXCACHL-WDSKDSINSA-N 0.000 description 1
- MTAOBYXRYJZRGQ-WDSKDSINSA-N Glu-Gly-Asp Chemical compound OC(=O)CC[C@H](N)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(O)=O MTAOBYXRYJZRGQ-WDSKDSINSA-N 0.000 description 1
- GJBUAAAIZSRCDC-GVXVVHGQSA-N Glu-Leu-Val Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(O)=O GJBUAAAIZSRCDC-GVXVVHGQSA-N 0.000 description 1
- OFIHURVSQXAZIR-SZMVWBNQSA-N Glu-Lys-Trp Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(O)=O OFIHURVSQXAZIR-SZMVWBNQSA-N 0.000 description 1
- NPMSEUWUMOSEFM-CIUDSAMLSA-N Glu-Met-Asn Chemical compound CSCC[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)O)NC(=O)[C@H](CCC(=O)O)N NPMSEUWUMOSEFM-CIUDSAMLSA-N 0.000 description 1
- XNOWYPDMSLSRKP-GUBZILKMSA-N Glu-Met-Gln Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(N)=O)C(O)=O XNOWYPDMSLSRKP-GUBZILKMSA-N 0.000 description 1
- RFTVTKBHDXCEEX-WDSKDSINSA-N Glu-Ser-Gly Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)NCC(O)=O RFTVTKBHDXCEEX-WDSKDSINSA-N 0.000 description 1
- RGJKYNUINKGPJN-RWRJDSDZSA-N Glu-Thr-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(=O)O)N RGJKYNUINKGPJN-RWRJDSDZSA-N 0.000 description 1
- YOTHMZZSJKKEHZ-SZMVWBNQSA-N Glu-Trp-Lys Chemical compound C1=CC=C2C(C[C@@H](C(=O)N[C@@H](CCCCN)C(O)=O)NC(=O)[C@@H](N)CCC(O)=O)=CNC2=C1 YOTHMZZSJKKEHZ-SZMVWBNQSA-N 0.000 description 1
- BKMOHWJHXQLFEX-IRIUXVKKSA-N Glu-Tyr-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)NC(=O)[C@H](CCC(=O)O)N)O BKMOHWJHXQLFEX-IRIUXVKKSA-N 0.000 description 1
- VIPDPMHGICREIS-GVXVVHGQSA-N Glu-Val-Leu Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O VIPDPMHGICREIS-GVXVVHGQSA-N 0.000 description 1
- QXUPRMQJDWJDFR-NRPADANISA-N Glu-Val-Ser Chemical compound CC(C)[C@H](NC(=O)[C@@H](N)CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O QXUPRMQJDWJDFR-NRPADANISA-N 0.000 description 1
- WGYHAAXZWPEBDQ-IFFSRLJSSA-N Glu-Val-Thr Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(O)=O WGYHAAXZWPEBDQ-IFFSRLJSSA-N 0.000 description 1
- 108010073178 Glucan 1,4-alpha-Glucosidase Proteins 0.000 description 1
- 102100022624 Glucoamylase Human genes 0.000 description 1
- 239000004366 Glucose oxidase Substances 0.000 description 1
- 108010015776 Glucose oxidase Proteins 0.000 description 1
- 108010018962 Glucosephosphate Dehydrogenase Proteins 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- MFVQGXGQRIXBPK-WDSKDSINSA-N Gly-Ala-Glu Chemical compound NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(O)=O MFVQGXGQRIXBPK-WDSKDSINSA-N 0.000 description 1
- UPOJUWHGMDJUQZ-IUCAKERBSA-N Gly-Arg-Arg Chemical compound NC(=N)NCCC[C@H](NC(=O)CN)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O UPOJUWHGMDJUQZ-IUCAKERBSA-N 0.000 description 1
- GWCRIHNSVMOBEQ-BQBZGAKWSA-N Gly-Arg-Ser Chemical compound [H]NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(O)=O GWCRIHNSVMOBEQ-BQBZGAKWSA-N 0.000 description 1
- DTPOVRRYXPJJAZ-FJXKBIBVSA-N Gly-Arg-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)CN)CCCN=C(N)N DTPOVRRYXPJJAZ-FJXKBIBVSA-N 0.000 description 1
- XCLCVBYNGXEVDU-WHFBIAKZSA-N Gly-Asn-Ser Chemical compound NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(O)=O XCLCVBYNGXEVDU-WHFBIAKZSA-N 0.000 description 1
- BYYNJRSNDARRBX-YFKPBYRVSA-N Gly-Gln-Gly Chemical compound NCC(=O)N[C@@H](CCC(N)=O)C(=O)NCC(O)=O BYYNJRSNDARRBX-YFKPBYRVSA-N 0.000 description 1
- GNPVTZJUUBPZKW-WDSKDSINSA-N Gly-Gln-Ser Chemical compound [H]NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(O)=O GNPVTZJUUBPZKW-WDSKDSINSA-N 0.000 description 1
- YWAQATDNEKZFFK-BYPYZUCNSA-N Gly-Gly-Ser Chemical compound NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O YWAQATDNEKZFFK-BYPYZUCNSA-N 0.000 description 1
- HAXARWKYFIIHKD-ZKWXMUAHSA-N Gly-Ile-Ser Chemical compound NCC(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(O)=O HAXARWKYFIIHKD-ZKWXMUAHSA-N 0.000 description 1
- LLZXNUUIBOALNY-QWRGUYRKSA-N Gly-Leu-Lys Chemical compound NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(O)=O)CCCCN LLZXNUUIBOALNY-QWRGUYRKSA-N 0.000 description 1
- NTBOEZICHOSJEE-YUMQZZPRSA-N Gly-Lys-Ser Chemical compound [H]NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(O)=O NTBOEZICHOSJEE-YUMQZZPRSA-N 0.000 description 1
- CVFOYJJOZYYEPE-KBPBESRZSA-N Gly-Lys-Tyr Chemical compound [H]NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O CVFOYJJOZYYEPE-KBPBESRZSA-N 0.000 description 1
- WNZOCXUOGVYYBJ-CDMKHQONSA-N Gly-Phe-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CC1=CC=CC=C1)NC(=O)CN)O WNZOCXUOGVYYBJ-CDMKHQONSA-N 0.000 description 1
- ZZJVYSAQQMDIRD-UWVGGRQHSA-N Gly-Pro-His Chemical compound NCC(=O)N1CCC[C@H]1C(=O)N[C@@H](Cc1cnc[nH]1)C(O)=O ZZJVYSAQQMDIRD-UWVGGRQHSA-N 0.000 description 1
- CSMYMGFCEJWALV-WDSKDSINSA-N Gly-Ser-Gln Chemical compound NCC(=O)N[C@@H](CO)C(=O)N[C@H](C(O)=O)CCC(N)=O CSMYMGFCEJWALV-WDSKDSINSA-N 0.000 description 1
- FKYQEVBRZSFAMJ-QWRGUYRKSA-N Gly-Ser-Tyr Chemical compound NCC(=O)N[C@@H](CO)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 FKYQEVBRZSFAMJ-QWRGUYRKSA-N 0.000 description 1
- NVTPVQLIZCOJFK-FOHZUACHSA-N Gly-Thr-Asp Chemical compound [H]NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(O)=O NVTPVQLIZCOJFK-FOHZUACHSA-N 0.000 description 1
- TVTZEOHWHUVYCG-KYNKHSRBSA-N Gly-Thr-Thr Chemical compound [H]NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O TVTZEOHWHUVYCG-KYNKHSRBSA-N 0.000 description 1
- BAYQNCWLXIDLHX-ONGXEEELSA-N Gly-Val-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H](C(C)C)NC(=O)CN BAYQNCWLXIDLHX-ONGXEEELSA-N 0.000 description 1
- MUGLKCQHTUFLGF-WPRPVWTQSA-N Gly-Val-Met Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCSC)C(=O)O)NC(=O)CN MUGLKCQHTUFLGF-WPRPVWTQSA-N 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- JBCLFWXMTIKCCB-UHFFFAOYSA-N H-Gly-Phe-OH Natural products NCC(=O)NC(C(O)=O)CC1=CC=CC=C1 JBCLFWXMTIKCCB-UHFFFAOYSA-N 0.000 description 1
- JIUYRPFQJJRSJB-QWRGUYRKSA-N His-His-Gly Chemical compound C([C@H](N)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)NCC(O)=O)C1=CN=CN1 JIUYRPFQJJRSJB-QWRGUYRKSA-N 0.000 description 1
- GIRSNERMXCMDBO-GARJFASQSA-N His-Ser-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CO)NC(=O)[C@H](CC2=CN=CN2)N)C(=O)O GIRSNERMXCMDBO-GARJFASQSA-N 0.000 description 1
- 101000819490 Homo sapiens Alpha-(1,6)-fucosyltransferase Proteins 0.000 description 1
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 1
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 1
- 101000935587 Homo sapiens Flavin reductase (NADPH) Proteins 0.000 description 1
- 101001041117 Homo sapiens Hyaluronidase PH-20 Proteins 0.000 description 1
- 101000878605 Homo sapiens Low affinity immunoglobulin epsilon Fc receptor Proteins 0.000 description 1
- 108010003272 Hyaluronate lyase Proteins 0.000 description 1
- 102000001974 Hyaluronidases Human genes 0.000 description 1
- LELOWRISYMNNSU-UHFFFAOYSA-N Hydrocyanic acid Natural products N#C LELOWRISYMNNSU-UHFFFAOYSA-N 0.000 description 1
- VSNHCAURESNICA-UHFFFAOYSA-N Hydroxyurea Chemical compound NC(=O)NO VSNHCAURESNICA-UHFFFAOYSA-N 0.000 description 1
- 206010020649 Hyperkeratosis Diseases 0.000 description 1
- MPBVHIBUJCELCL-UHFFFAOYSA-N Ibandronate Chemical compound CCCCCN(C)CCC(O)(P(O)(O)=O)P(O)(O)=O MPBVHIBUJCELCL-UHFFFAOYSA-N 0.000 description 1
- KMBPQYKVZBMRMH-PEFMBERDSA-N Ile-Gln-Asn Chemical compound CC[C@H](C)[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O KMBPQYKVZBMRMH-PEFMBERDSA-N 0.000 description 1
- HOLOYAZCIHDQNS-YVNDNENWSA-N Ile-Gln-Glu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CCC(=O)O)C(=O)O)N HOLOYAZCIHDQNS-YVNDNENWSA-N 0.000 description 1
- KUHFPGIVBOCRMV-MNXVOIDGSA-N Ile-Gln-Leu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CC(C)C)C(=O)O)N KUHFPGIVBOCRMV-MNXVOIDGSA-N 0.000 description 1
- SLQVFYWBGNNOTK-BYULHYEWSA-N Ile-Gly-Asn Chemical compound CC[C@H](C)[C@@H](C(=O)NCC(=O)N[C@@H](CC(=O)N)C(=O)O)N SLQVFYWBGNNOTK-BYULHYEWSA-N 0.000 description 1
- IGJWJGIHUFQANP-LAEOZQHASA-N Ile-Gly-Gln Chemical compound CC[C@H](C)[C@@H](C(=O)NCC(=O)N[C@@H](CCC(=O)N)C(=O)O)N IGJWJGIHUFQANP-LAEOZQHASA-N 0.000 description 1
- CMNMPCTVCWWYHY-MXAVVETBSA-N Ile-His-Leu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N[C@@H](CC(C)C)C(=O)O)N CMNMPCTVCWWYHY-MXAVVETBSA-N 0.000 description 1
- LNJLOZYNZFGJMM-DEQVHRJGSA-N Ile-His-Pro Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N2CCC[C@@H]2C(=O)O)N LNJLOZYNZFGJMM-DEQVHRJGSA-N 0.000 description 1
- KEKTTYCXKGBAAL-VGDYDELISA-N Ile-His-Ser Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC1=CN=CN1)C(=O)N[C@@H](CO)C(=O)O)N KEKTTYCXKGBAAL-VGDYDELISA-N 0.000 description 1
- FZWVCYCYWCLQDH-NHCYSSNCSA-N Ile-Leu-Gly Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)O)N FZWVCYCYWCLQDH-NHCYSSNCSA-N 0.000 description 1
- GAZGFPOZOLEYAJ-YTFOTSKYSA-N Ile-Leu-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)O)N GAZGFPOZOLEYAJ-YTFOTSKYSA-N 0.000 description 1
- GLYJPWIRLBAIJH-FQUUOJAGSA-N Ile-Lys-Pro Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N1CCC[C@@H]1C(=O)O)N GLYJPWIRLBAIJH-FQUUOJAGSA-N 0.000 description 1
- GLYJPWIRLBAIJH-UHFFFAOYSA-N Ile-Lys-Pro Natural products CCC(C)C(N)C(=O)NC(CCCCN)C(=O)N1CCCC1C(O)=O GLYJPWIRLBAIJH-UHFFFAOYSA-N 0.000 description 1
- SVZFKLBRCYCIIY-CYDGBPFRSA-N Ile-Pro-Arg Chemical compound CC[C@H](C)[C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCCNC(N)=N)C(O)=O SVZFKLBRCYCIIY-CYDGBPFRSA-N 0.000 description 1
- VISRCHQHQCLODA-NAKRPEOUSA-N Ile-Pro-Cys Chemical compound CC[C@H](C)[C@@H](C(=O)N1CCC[C@H]1C(=O)N[C@@H](CS)C(=O)O)N VISRCHQHQCLODA-NAKRPEOUSA-N 0.000 description 1
- JODPUDMBQBIWCK-GHCJXIJMSA-N Ile-Ser-Asn Chemical compound [H]N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(O)=O JODPUDMBQBIWCK-GHCJXIJMSA-N 0.000 description 1
- FBGXMKUWQFPHFB-JBDRJPRFSA-N Ile-Ser-Cys Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O)N FBGXMKUWQFPHFB-JBDRJPRFSA-N 0.000 description 1
- JNLSTRPWUXOORL-MMWGEVLESA-N Ile-Ser-Pro Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CO)C(=O)N1CCC[C@@H]1C(=O)O)N JNLSTRPWUXOORL-MMWGEVLESA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical class C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical compound C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 1
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 1
- 238000012695 Interfacial polymerization Methods 0.000 description 1
- 229930194542 Keto Natural products 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- LHSGPCFBGJHPCY-UHFFFAOYSA-N L-leucine-L-tyrosine Natural products CC(C)CC(N)C(=O)NC(C(O)=O)CC1=CC=C(O)C=C1 LHSGPCFBGJHPCY-UHFFFAOYSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 1
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 1
- 102100038609 Lactoperoxidase Human genes 0.000 description 1
- 108010023244 Lactoperoxidase Proteins 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 229920001491 Lentinan Polymers 0.000 description 1
- CZCSUZMIRKFFFA-CIUDSAMLSA-N Leu-Ala-Asn Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(N)=O)C(O)=O CZCSUZMIRKFFFA-CIUDSAMLSA-N 0.000 description 1
- HXWALXSAVBLTPK-NUTKFTJISA-N Leu-Ala-Trp Chemical compound C[C@@H](C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)O)NC(=O)[C@H](CC(C)C)N HXWALXSAVBLTPK-NUTKFTJISA-N 0.000 description 1
- DUBAVOVZNZKEQQ-AVGNSLFASA-N Leu-Arg-Val Chemical compound CC(C)C[C@H](N)C(=O)N[C@H](C(=O)N[C@@H](C(C)C)C(O)=O)CCCN=C(N)N DUBAVOVZNZKEQQ-AVGNSLFASA-N 0.000 description 1
- FGNQZXKVAZIMCI-CIUDSAMLSA-N Leu-Asp-Cys Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CS)C(=O)O)N FGNQZXKVAZIMCI-CIUDSAMLSA-N 0.000 description 1
- ULXYQAJWJGLCNR-YUMQZZPRSA-N Leu-Asp-Gly Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)NCC(O)=O ULXYQAJWJGLCNR-YUMQZZPRSA-N 0.000 description 1
- QCSFMCFHVGTLFF-NHCYSSNCSA-N Leu-Asp-Val Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(O)=O QCSFMCFHVGTLFF-NHCYSSNCSA-N 0.000 description 1
- VPKIQULSKFVCSM-SRVKXCTJSA-N Leu-Gln-Arg Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O VPKIQULSKFVCSM-SRVKXCTJSA-N 0.000 description 1
- ZYLJULGXQDNXDK-GUBZILKMSA-N Leu-Gln-Asp Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(O)=O ZYLJULGXQDNXDK-GUBZILKMSA-N 0.000 description 1
- KAFOIVJDVSZUMD-DCAQKATOSA-N Leu-Gln-Gln Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O KAFOIVJDVSZUMD-DCAQKATOSA-N 0.000 description 1
- KAFOIVJDVSZUMD-UHFFFAOYSA-N Leu-Gln-Gln Natural products CC(C)CC(N)C(=O)NC(CCC(N)=O)C(=O)NC(CCC(N)=O)C(O)=O KAFOIVJDVSZUMD-UHFFFAOYSA-N 0.000 description 1
- ZTLGVASZOIKNIX-DCAQKATOSA-N Leu-Gln-Glu Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CCC(=O)O)C(=O)O)N ZTLGVASZOIKNIX-DCAQKATOSA-N 0.000 description 1
- FQZPTCNSNPWHLJ-AVGNSLFASA-N Leu-Gln-Lys Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(O)=O FQZPTCNSNPWHLJ-AVGNSLFASA-N 0.000 description 1
- HPBCTWSUJOGJSH-MNXVOIDGSA-N Leu-Glu-Ile Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O HPBCTWSUJOGJSH-MNXVOIDGSA-N 0.000 description 1
- YFBBUHJJUXXZOF-UWVGGRQHSA-N Leu-Gly-Pro Chemical compound CC(C)C[C@H](N)C(=O)NCC(=O)N1CCC[C@H]1C(O)=O YFBBUHJJUXXZOF-UWVGGRQHSA-N 0.000 description 1
- VGPCJSXPPOQPBK-YUMQZZPRSA-N Leu-Gly-Ser Chemical compound CC(C)C[C@H](N)C(=O)NCC(=O)N[C@@H](CO)C(O)=O VGPCJSXPPOQPBK-YUMQZZPRSA-N 0.000 description 1
- QNBVTHNJGCOVFA-AVGNSLFASA-N Leu-Leu-Glu Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(O)=O)CCC(O)=O QNBVTHNJGCOVFA-AVGNSLFASA-N 0.000 description 1
- KTOIECMYZZGVSI-BZSNNMDCSA-N Leu-Phe-His Chemical compound C([C@H](NC(=O)[C@@H](N)CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(O)=O)C1=CC=CC=C1 KTOIECMYZZGVSI-BZSNNMDCSA-N 0.000 description 1
- MUCIDQMDOYQYBR-IHRRRGAJSA-N Leu-Pro-His Chemical compound CC(C)C[C@@H](C(=O)N1CCC[C@H]1C(=O)N[C@@H](CC2=CN=CN2)C(=O)O)N MUCIDQMDOYQYBR-IHRRRGAJSA-N 0.000 description 1
- LJBVRCDPWOJOEK-PPCPHDFISA-N Leu-Thr-Ile Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O LJBVRCDPWOJOEK-PPCPHDFISA-N 0.000 description 1
- 239000012448 Lithium borohydride Substances 0.000 description 1
- GQYIWUVLTXOXAJ-UHFFFAOYSA-N Lomustine Chemical compound ClCCN(N=O)C(=O)NC1CCCCC1 GQYIWUVLTXOXAJ-UHFFFAOYSA-N 0.000 description 1
- 102100038007 Low affinity immunoglobulin epsilon Fc receptor Human genes 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- DDWFXDSYGUXRAY-UHFFFAOYSA-N Luciferin Natural products CCc1c(C)c(CC2NC(=O)C(=C2C=C)C)[nH]c1Cc3[nH]c4C(=C5/NC(CC(=O)O)C(C)C5CC(=O)O)CC(=O)c4c3C DDWFXDSYGUXRAY-UHFFFAOYSA-N 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010052178 Lymphocytic lymphoma Diseases 0.000 description 1
- 208000030289 Lymphoproliferative disease Diseases 0.000 description 1
- IXHKPDJKKCUKHS-GARJFASQSA-N Lys-Ala-Pro Chemical compound C[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@H](CCCCN)N IXHKPDJKKCUKHS-GARJFASQSA-N 0.000 description 1
- UWKNTTJNVSYXPC-CIUDSAMLSA-N Lys-Ala-Ser Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CCCCN UWKNTTJNVSYXPC-CIUDSAMLSA-N 0.000 description 1
- NTSPQIONFJUMJV-AVGNSLFASA-N Lys-Arg-Val Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(O)=O NTSPQIONFJUMJV-AVGNSLFASA-N 0.000 description 1
- WLCYCADOWRMSAJ-CIUDSAMLSA-N Lys-Asn-Cys Chemical compound NCCCC[C@H](N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(O)=O WLCYCADOWRMSAJ-CIUDSAMLSA-N 0.000 description 1
- HQVDJTYKCMIWJP-YUMQZZPRSA-N Lys-Asn-Gly Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(O)=O HQVDJTYKCMIWJP-YUMQZZPRSA-N 0.000 description 1
- HIIZIQUUHIXUJY-GUBZILKMSA-N Lys-Asp-Gln Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O HIIZIQUUHIXUJY-GUBZILKMSA-N 0.000 description 1
- AAORVPFVUIHEAB-YUMQZZPRSA-N Lys-Asp-Gly Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)NCC(O)=O AAORVPFVUIHEAB-YUMQZZPRSA-N 0.000 description 1
- VEGLGAOVLFODGC-GUBZILKMSA-N Lys-Glu-Ser Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O VEGLGAOVLFODGC-GUBZILKMSA-N 0.000 description 1
- HGNRJCINZYHNOU-LURJTMIESA-N Lys-Gly Chemical compound NCCCC[C@H](N)C(=O)NCC(O)=O HGNRJCINZYHNOU-LURJTMIESA-N 0.000 description 1
- NKKFVJRLCCUJNA-QWRGUYRKSA-N Lys-Gly-Lys Chemical compound NCCCC[C@H](N)C(=O)NCC(=O)N[C@H](C(O)=O)CCCCN NKKFVJRLCCUJNA-QWRGUYRKSA-N 0.000 description 1
- OJDFAABAHBPVTH-MNXVOIDGSA-N Lys-Ile-Gln Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(O)=O OJDFAABAHBPVTH-MNXVOIDGSA-N 0.000 description 1
- ZXFRGTAIIZHNHG-AJNGGQMLSA-N Lys-Ile-Leu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)O)NC(=O)[C@H](CCCCN)N ZXFRGTAIIZHNHG-AJNGGQMLSA-N 0.000 description 1
- WAIHHELKYSFIQN-XUXIUFHCSA-N Lys-Ile-Val Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(O)=O WAIHHELKYSFIQN-XUXIUFHCSA-N 0.000 description 1
- AIRZWUMAHCDDHR-KKUMJFAQSA-N Lys-Leu-Leu Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O AIRZWUMAHCDDHR-KKUMJFAQSA-N 0.000 description 1
- QQPSCXKFDSORFT-IHRRRGAJSA-N Lys-Lys-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CCCCN QQPSCXKFDSORFT-IHRRRGAJSA-N 0.000 description 1
- LUAJJLPHUXPQLH-KKUMJFAQSA-N Lys-Phe-Ser Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)N[C@@H](CO)C(=O)O)NC(=O)[C@H](CCCCN)N LUAJJLPHUXPQLH-KKUMJFAQSA-N 0.000 description 1
- DIBZLYZXTSVGLN-CIUDSAMLSA-N Lys-Ser-Ser Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O DIBZLYZXTSVGLN-CIUDSAMLSA-N 0.000 description 1
- MEQLGHAMAUPOSJ-DCAQKATOSA-N Lys-Ser-Val Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O MEQLGHAMAUPOSJ-DCAQKATOSA-N 0.000 description 1
- ZFNYWKHYUMEZDZ-WDSOQIARSA-N Lys-Trp-Val Chemical compound CC(C)[C@@H](C(=O)O)NC(=O)[C@H](CC1=CNC2=CC=CC=C21)NC(=O)[C@H](CCCCN)N ZFNYWKHYUMEZDZ-WDSOQIARSA-N 0.000 description 1
- RIPJMCFGQHGHNP-RHYQMDGZSA-N Lys-Val-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCCCN)N)O RIPJMCFGQHGHNP-RHYQMDGZSA-N 0.000 description 1
- 201000003791 MALT lymphoma Diseases 0.000 description 1
- 241000282567 Macaca fascicularis Species 0.000 description 1
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 229930126263 Maytansine Natural products 0.000 description 1
- IIPHCNKHEZYSNE-DCAQKATOSA-N Met-Arg-Gln Chemical compound CSCC[C@H](N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(O)=O IIPHCNKHEZYSNE-DCAQKATOSA-N 0.000 description 1
- VOOINLQYUZOREH-SRVKXCTJSA-N Met-Gln-Leu Chemical compound CC(C)C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](CCSC)N VOOINLQYUZOREH-SRVKXCTJSA-N 0.000 description 1
- KQBJYJXPZBNEIK-DCAQKATOSA-N Met-Glu-Arg Chemical compound CSCC[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@H](C(O)=O)CCCNC(N)=N KQBJYJXPZBNEIK-DCAQKATOSA-N 0.000 description 1
- MTBVQFFQMXHCPC-CIUDSAMLSA-N Met-Glu-Asp Chemical compound CSCC[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(O)=O MTBVQFFQMXHCPC-CIUDSAMLSA-N 0.000 description 1
- TZHFJXDKXGZHEN-IHRRRGAJSA-N Met-His-Leu Chemical compound [H]N[C@@H](CCSC)C(=O)N[C@@H](CC1=CNC=N1)C(=O)N[C@@H](CC(C)C)C(O)=O TZHFJXDKXGZHEN-IHRRRGAJSA-N 0.000 description 1
- WSPQHZOMTFFWGH-XGEHTFHBSA-N Met-Thr-Cys Chemical compound CSCC[C@H](N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(O)=O WSPQHZOMTFFWGH-XGEHTFHBSA-N 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M Methanesulfonate Chemical compound CS([O-])(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 229930192392 Mitomycin Natural products 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 102000016943 Muramidase Human genes 0.000 description 1
- 108010014251 Muramidase Proteins 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 1
- OVBPIULPVIDEAO-UHFFFAOYSA-N N-Pteroyl-L-glutaminsaeure Natural products C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-UHFFFAOYSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- 102100031688 N-acetylgalactosamine-6-sulfatase Human genes 0.000 description 1
- AJHCSUXXECOXOY-UHFFFAOYSA-N N-glycyl-L-tryptophan Natural products C1=CC=C2C(CC(NC(=O)CN)C(O)=O)=CNC2=C1 AJHCSUXXECOXOY-UHFFFAOYSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- 108010047562 NGR peptide Proteins 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 101100342977 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) leu-1 gene Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 241000238413 Octopus Species 0.000 description 1
- 108020005187 Oligonucleotide Probes Proteins 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- WYNCHZVNFNFDNH-UHFFFAOYSA-N Oxazolidine Chemical compound C1COCN1 WYNCHZVNFNFDNH-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000609499 Palicourea Species 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 206010033645 Pancreatitis Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 102000007079 Peptide Fragments Human genes 0.000 description 1
- 108010033276 Peptide Fragments Proteins 0.000 description 1
- 244000146510 Pereskia bleo Species 0.000 description 1
- 208000027190 Peripheral T-cell lymphomas Diseases 0.000 description 1
- CSYVXYQDIVCQNU-QWRGUYRKSA-N Phe-Asp-Gly Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(O)=O)C(=O)NCC(O)=O CSYVXYQDIVCQNU-QWRGUYRKSA-N 0.000 description 1
- OJUMUUXGSXUZJZ-SRVKXCTJSA-N Phe-Asp-Ser Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(O)=O OJUMUUXGSXUZJZ-SRVKXCTJSA-N 0.000 description 1
- CUMXHKAOHNWRFQ-BZSNNMDCSA-N Phe-Asp-Tyr Chemical compound C([C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)C1=CC=CC=C1 CUMXHKAOHNWRFQ-BZSNNMDCSA-N 0.000 description 1
- LLGTYVHITPVGKR-RYUDHWBXSA-N Phe-Gln-Gly Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(O)=O LLGTYVHITPVGKR-RYUDHWBXSA-N 0.000 description 1
- AKJAKCBHLJGRBU-JYJNAYRXSA-N Phe-Glu-His Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H](CC2=CN=CN2)C(=O)O)N AKJAKCBHLJGRBU-JYJNAYRXSA-N 0.000 description 1
- NAXPHWZXEXNDIW-JTQLQIEISA-N Phe-Gly-Gly Chemical compound OC(=O)CNC(=O)CNC(=O)[C@@H](N)CC1=CC=CC=C1 NAXPHWZXEXNDIW-JTQLQIEISA-N 0.000 description 1
- KDYPMIZMXDECSU-JYJNAYRXSA-N Phe-Leu-Glu Chemical compound OC(=O)CC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CC1=CC=CC=C1 KDYPMIZMXDECSU-JYJNAYRXSA-N 0.000 description 1
- YCCUXNNKXDGMAM-KKUMJFAQSA-N Phe-Leu-Ser Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(O)=O YCCUXNNKXDGMAM-KKUMJFAQSA-N 0.000 description 1
- GRVMHFCZUIYNKQ-UFYCRDLUSA-N Phe-Phe-Val Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](C(C)C)C(O)=O GRVMHFCZUIYNKQ-UFYCRDLUSA-N 0.000 description 1
- ZJPGOXWRFNKIQL-JYJNAYRXSA-N Phe-Pro-Pro Chemical compound C([C@H](N)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(O)=O)C1=CC=CC=C1 ZJPGOXWRFNKIQL-JYJNAYRXSA-N 0.000 description 1
- BPCLGWHVPVTTFM-QWRGUYRKSA-N Phe-Ser-Gly Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CO)C(=O)NCC(O)=O BPCLGWHVPVTTFM-QWRGUYRKSA-N 0.000 description 1
- MCIXMYKSPQUMJG-SRVKXCTJSA-N Phe-Ser-Ser Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O MCIXMYKSPQUMJG-SRVKXCTJSA-N 0.000 description 1
- LTAWNJXSRUCFAN-UNQGMJICSA-N Phe-Thr-Arg Chemical compound [H]N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O LTAWNJXSRUCFAN-UNQGMJICSA-N 0.000 description 1
- YTGGLKWSVIRECD-JBACZVJFSA-N Phe-Trp-Glu Chemical compound C([C@H](N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(O)=O)C1=CC=CC=C1 YTGGLKWSVIRECD-JBACZVJFSA-N 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 206010065857 Primary Effusion Lymphoma Diseases 0.000 description 1
- 206010036711 Primary mediastinal large B-cell lymphomas Diseases 0.000 description 1
- LNLNHXIQPGKRJQ-SRVKXCTJSA-N Pro-Arg-Arg Chemical compound NC(N)=NCCC[C@@H](C(O)=O)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@@H]1CCCN1 LNLNHXIQPGKRJQ-SRVKXCTJSA-N 0.000 description 1
- XJROSHJRQTXWAE-XGEHTFHBSA-N Pro-Cys-Thr Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CS)C(=O)N[C@@H]([C@@H](C)O)C(O)=O XJROSHJRQTXWAE-XGEHTFHBSA-N 0.000 description 1
- UEHYFUCOGHWASA-HJGDQZAQSA-N Pro-Glu-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H]1CCCN1 UEHYFUCOGHWASA-HJGDQZAQSA-N 0.000 description 1
- ULIWFCCJIOEHMU-BQBZGAKWSA-N Pro-Gly-Asp Chemical compound OC(=O)C[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H]1CCCN1 ULIWFCCJIOEHMU-BQBZGAKWSA-N 0.000 description 1
- JMVQDLDPDBXAAX-YUMQZZPRSA-N Pro-Gly-Gln Chemical compound NC(=O)CC[C@@H](C(O)=O)NC(=O)CNC(=O)[C@@H]1CCCN1 JMVQDLDPDBXAAX-YUMQZZPRSA-N 0.000 description 1
- VWXGFAIZUQBBBG-UWVGGRQHSA-N Pro-His-Gly Chemical compound C([C@@H](C(=O)NCC(=O)[O-])NC(=O)[C@H]1[NH2+]CCC1)C1=CN=CN1 VWXGFAIZUQBBBG-UWVGGRQHSA-N 0.000 description 1
- MCWHYUWXVNRXFV-RWMBFGLXSA-N Pro-Leu-Pro Chemical compound CC(C)C[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@@H]2CCCN2 MCWHYUWXVNRXFV-RWMBFGLXSA-N 0.000 description 1
- XQPHBAKJJJZOBX-SRVKXCTJSA-N Pro-Lys-Glu Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(O)=O XQPHBAKJJJZOBX-SRVKXCTJSA-N 0.000 description 1
- MHHQQZIFLWFZGR-DCAQKATOSA-N Pro-Lys-Ser Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(O)=O MHHQQZIFLWFZGR-DCAQKATOSA-N 0.000 description 1
- ANESFYPBAJPYNJ-SDDRHHMPSA-N Pro-Met-Pro Chemical compound CSCC[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@@H]2CCCN2 ANESFYPBAJPYNJ-SDDRHHMPSA-N 0.000 description 1
- RFWXYTJSVDUBBZ-DCAQKATOSA-N Pro-Pro-Glu Chemical compound OC(=O)CC[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@H]1NCCC1 RFWXYTJSVDUBBZ-DCAQKATOSA-N 0.000 description 1
- LNICFEXCAHIJOR-DCAQKATOSA-N Pro-Ser-Leu Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(O)=O LNICFEXCAHIJOR-DCAQKATOSA-N 0.000 description 1
- KWMZPPWYBVZIER-XGEHTFHBSA-N Pro-Ser-Thr Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(O)=O KWMZPPWYBVZIER-XGEHTFHBSA-N 0.000 description 1
- RJTUIDFUUHPJMP-FHWLQOOXSA-N Pro-Trp-His Chemical compound C1C[C@H](NC1)C(=O)N[C@@H](CC2=CNC3=CC=CC=C32)C(=O)N[C@@H](CC4=CN=CN4)C(=O)O RJTUIDFUUHPJMP-FHWLQOOXSA-N 0.000 description 1
- AWJGUZSYVIVZGP-YUMQZZPRSA-N Pro-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1 AWJGUZSYVIVZGP-YUMQZZPRSA-N 0.000 description 1
- IIRBTQHFVNGPMQ-AVGNSLFASA-N Pro-Val-Lys Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@@H]1CCCN1 IIRBTQHFVNGPMQ-AVGNSLFASA-N 0.000 description 1
- YDTUEBLEAVANFH-RCWTZXSCSA-N Pro-Val-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H]1CCCN1 YDTUEBLEAVANFH-RCWTZXSCSA-N 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 108010079005 RDV peptide Proteins 0.000 description 1
- 239000012891 Ringer solution Substances 0.000 description 1
- GNSXDDLDAGAXTL-UHFFFAOYSA-N S1OCCCC1.O1SCCCC1 Chemical compound S1OCCCC1.O1SCCCC1 GNSXDDLDAGAXTL-UHFFFAOYSA-N 0.000 description 1
- 239000002262 Schiff base Substances 0.000 description 1
- QEDMOZUJTGEIBF-FXQIFTODSA-N Ser-Arg-Asp Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(O)=O QEDMOZUJTGEIBF-FXQIFTODSA-N 0.000 description 1
- HBOABDXGTMMDSE-GUBZILKMSA-N Ser-Arg-Val Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(O)=O HBOABDXGTMMDSE-GUBZILKMSA-N 0.000 description 1
- KNZQGAUEYZJUSQ-ZLUOBGJFSA-N Ser-Asp-Ala Chemical compound C[C@@H](C(=O)O)NC(=O)[C@H](CC(=O)O)NC(=O)[C@H](CO)N KNZQGAUEYZJUSQ-ZLUOBGJFSA-N 0.000 description 1
- GRRAECZXRONTEE-UBHSHLNASA-N Ser-Cys-Trp Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(O)=O GRRAECZXRONTEE-UBHSHLNASA-N 0.000 description 1
- IXUGADGDCQDLSA-FXQIFTODSA-N Ser-Gln-Gln Chemical compound C(CC(=O)N)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CO)N IXUGADGDCQDLSA-FXQIFTODSA-N 0.000 description 1
- VMVNCJDKFOQOHM-GUBZILKMSA-N Ser-Gln-Lys Chemical compound C(CCN)C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](CO)N VMVNCJDKFOQOHM-GUBZILKMSA-N 0.000 description 1
- YQQKYAZABFEYAF-FXQIFTODSA-N Ser-Glu-Gln Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O YQQKYAZABFEYAF-FXQIFTODSA-N 0.000 description 1
- LALNXSXEYFUUDD-GUBZILKMSA-N Ser-Glu-Leu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(O)=O LALNXSXEYFUUDD-GUBZILKMSA-N 0.000 description 1
- GRSLLFZTTLBOQX-CIUDSAMLSA-N Ser-Glu-Met Chemical compound CSCC[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](CO)N GRSLLFZTTLBOQX-CIUDSAMLSA-N 0.000 description 1
- UQFYNFTYDHUIMI-WHFBIAKZSA-N Ser-Gly-Ala Chemical compound OC(=O)[C@H](C)NC(=O)CNC(=O)[C@@H](N)CO UQFYNFTYDHUIMI-WHFBIAKZSA-N 0.000 description 1
- MUARUIBTKQJKFY-WHFBIAKZSA-N Ser-Gly-Asp Chemical compound [H]N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(O)=O MUARUIBTKQJKFY-WHFBIAKZSA-N 0.000 description 1
- KDGARKCAKHBEDB-NKWVEPMBSA-N Ser-Gly-Pro Chemical compound C1C[C@@H](N(C1)C(=O)CNC(=O)[C@H](CO)N)C(=O)O KDGARKCAKHBEDB-NKWVEPMBSA-N 0.000 description 1
- WEQAYODCJHZSJZ-KKUMJFAQSA-N Ser-His-Tyr Chemical compound C([C@H](NC(=O)[C@H](CO)N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)C1=CN=CN1 WEQAYODCJHZSJZ-KKUMJFAQSA-N 0.000 description 1
- UIPXCLNLUUAMJU-JBDRJPRFSA-N Ser-Ile-Ser Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(O)=O UIPXCLNLUUAMJU-JBDRJPRFSA-N 0.000 description 1
- GJFYFGOEWLDQGW-GUBZILKMSA-N Ser-Leu-Gln Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)O)NC(=O)[C@H](CO)N GJFYFGOEWLDQGW-GUBZILKMSA-N 0.000 description 1
- XNCUYZKGQOCOQH-YUMQZZPRSA-N Ser-Leu-Gly Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)NCC(O)=O XNCUYZKGQOCOQH-YUMQZZPRSA-N 0.000 description 1
- UBRMZSHOOIVJPW-SRVKXCTJSA-N Ser-Leu-Lys Chemical compound OC[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(O)=O UBRMZSHOOIVJPW-SRVKXCTJSA-N 0.000 description 1
- LRZLZIUXQBIWTB-KATARQTJSA-N Ser-Lys-Thr Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)O)C(O)=O LRZLZIUXQBIWTB-KATARQTJSA-N 0.000 description 1
- KZPRPBLHYMZIMH-MXAVVETBSA-N Ser-Phe-Ile Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O KZPRPBLHYMZIMH-MXAVVETBSA-N 0.000 description 1
- XZKQVQKUZMAADP-IMJSIDKUSA-N Ser-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CO)C(O)=O XZKQVQKUZMAADP-IMJSIDKUSA-N 0.000 description 1
- WLJPJRGQRNCIQS-ZLUOBGJFSA-N Ser-Ser-Asn Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(O)=O WLJPJRGQRNCIQS-ZLUOBGJFSA-N 0.000 description 1
- VFWQQZMRKFOGLE-ZLUOBGJFSA-N Ser-Ser-Cys Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O)N)O VFWQQZMRKFOGLE-ZLUOBGJFSA-N 0.000 description 1
- XJDMUQCLVSCRSJ-VZFHVOOUSA-N Ser-Thr-Ala Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C)C(O)=O XJDMUQCLVSCRSJ-VZFHVOOUSA-N 0.000 description 1
- NADLKBTYNKUJEP-KATARQTJSA-N Ser-Thr-Leu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(O)=O NADLKBTYNKUJEP-KATARQTJSA-N 0.000 description 1
- SNXUIBACCONSOH-BWBBJGPYSA-N Ser-Thr-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H]([C@H](O)C)C(=O)N[C@@H](CO)C(O)=O SNXUIBACCONSOH-BWBBJGPYSA-N 0.000 description 1
- UQGAAZXSCGWMFU-UBHSHLNASA-N Ser-Trp-Asp Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)O)NC(=O)[C@H](CO)N UQGAAZXSCGWMFU-UBHSHLNASA-N 0.000 description 1
- FRPNVPKQVFHSQY-BPUTZDHNSA-N Ser-Trp-Met Chemical compound CSCC[C@@H](C(=O)O)NC(=O)[C@H](CC1=CNC2=CC=CC=C21)NC(=O)[C@H](CO)N FRPNVPKQVFHSQY-BPUTZDHNSA-N 0.000 description 1
- MFQMZDPAZRZAPV-NAKRPEOUSA-N Ser-Val-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CO)N MFQMZDPAZRZAPV-NAKRPEOUSA-N 0.000 description 1
- LGIMRDKGABDMBN-DCAQKATOSA-N Ser-Val-Lys Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CO)N LGIMRDKGABDMBN-DCAQKATOSA-N 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 208000009359 Sezary Syndrome Diseases 0.000 description 1
- 208000021388 Sezary disease Diseases 0.000 description 1
- 108010032838 Sialoglycoproteins Proteins 0.000 description 1
- 102000007365 Sialoglycoproteins Human genes 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 241000256251 Spodoptera frugiperda Species 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 1
- BXFOFFBJRFZBQZ-QYWOHJEZSA-N T-2 toxin Chemical compound C([C@@]12[C@]3(C)[C@H](OC(C)=O)[C@@H](O)[C@H]1O[C@H]1[C@]3(COC(C)=O)C[C@@H](C(=C1)C)OC(=O)CC(C)C)O2 BXFOFFBJRFZBQZ-QYWOHJEZSA-N 0.000 description 1
- 208000031672 T-Cell Peripheral Lymphoma Diseases 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 229940123237 Taxane Drugs 0.000 description 1
- YPWFISCTZQNZAU-UHFFFAOYSA-N Thiane Chemical compound C1CCSCC1 YPWFISCTZQNZAU-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- NJEMRSFGDNECGF-GCJQMDKQSA-N Thr-Ala-Asp Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@H](C(O)=O)CC(O)=O NJEMRSFGDNECGF-GCJQMDKQSA-N 0.000 description 1
- DWYAUVCQDTZIJI-VZFHVOOUSA-N Thr-Ala-Ser Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(O)=O DWYAUVCQDTZIJI-VZFHVOOUSA-N 0.000 description 1
- VFEHSAJCWWHDBH-RHYQMDGZSA-N Thr-Arg-Leu Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(O)=O VFEHSAJCWWHDBH-RHYQMDGZSA-N 0.000 description 1
- UNURFMVMXLENAZ-KJEVXHAQSA-N Thr-Arg-Tyr Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O UNURFMVMXLENAZ-KJEVXHAQSA-N 0.000 description 1
- UTCFSBBXPWKLTG-XKBZYTNZSA-N Thr-Cys-Gln Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(=O)N)C(=O)O)N)O UTCFSBBXPWKLTG-XKBZYTNZSA-N 0.000 description 1
- DHPPWTOLRWYIDS-XKBZYTNZSA-N Thr-Cys-Glu Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(O)=O)C(O)=O DHPPWTOLRWYIDS-XKBZYTNZSA-N 0.000 description 1
- NIEWSKWFURSECR-FOHZUACHSA-N Thr-Gly-Asp Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(O)=O NIEWSKWFURSECR-FOHZUACHSA-N 0.000 description 1
- VYEHBMMAJFVTOI-JHEQGTHGSA-N Thr-Gly-Gln Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(O)=O VYEHBMMAJFVTOI-JHEQGTHGSA-N 0.000 description 1
- XOWKUMFHEZLKLT-CIQUZCHMSA-N Thr-Ile-Ala Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O XOWKUMFHEZLKLT-CIQUZCHMSA-N 0.000 description 1
- FQPDRTDDEZXCEC-SVSWQMSJSA-N Thr-Ile-Ser Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(O)=O FQPDRTDDEZXCEC-SVSWQMSJSA-N 0.000 description 1
- MECLEFZMPPOEAC-VOAKCMCISA-N Thr-Leu-Lys Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)O)N)O MECLEFZMPPOEAC-VOAKCMCISA-N 0.000 description 1
- BIBYEFRASCNLAA-CDMKHQONSA-N Thr-Phe-Gly Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@H](C(=O)NCC(O)=O)CC1=CC=CC=C1 BIBYEFRASCNLAA-CDMKHQONSA-N 0.000 description 1
- DEGCBBCMYWNJNA-RHYQMDGZSA-N Thr-Pro-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)[C@@H](C)O DEGCBBCMYWNJNA-RHYQMDGZSA-N 0.000 description 1
- GFRIEEKFXOVPIR-RHYQMDGZSA-N Thr-Pro-Lys Chemical compound C[C@@H](O)[C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCCCN)C(O)=O GFRIEEKFXOVPIR-RHYQMDGZSA-N 0.000 description 1
- IEZVHOULSUULHD-XGEHTFHBSA-N Thr-Ser-Val Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O IEZVHOULSUULHD-XGEHTFHBSA-N 0.000 description 1
- LECUEEHKUFYOOV-ZJDVBMNYSA-N Thr-Thr-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](N)[C@@H](C)O LECUEEHKUFYOOV-ZJDVBMNYSA-N 0.000 description 1
- UMFLBPIPAJMNIM-LYARXQMPSA-N Thr-Trp-Phe Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)N[C@@H](CC3=CC=CC=C3)C(=O)O)N)O UMFLBPIPAJMNIM-LYARXQMPSA-N 0.000 description 1
- NDLHSJWPCXKOGG-VLCNGCBASA-N Thr-Trp-Tyr Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)N[C@@H](CC3=CC=C(C=C3)O)C(=O)O)N)O NDLHSJWPCXKOGG-VLCNGCBASA-N 0.000 description 1
- MNYNCKZAEIAONY-XGEHTFHBSA-N Thr-Val-Ser Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CO)C(O)=O MNYNCKZAEIAONY-XGEHTFHBSA-N 0.000 description 1
- BPGDJSUFQKWUBK-KJEVXHAQSA-N Thr-Val-Tyr Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 BPGDJSUFQKWUBK-KJEVXHAQSA-N 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- UMILHIMHKXVDGH-UHFFFAOYSA-N Triethylene glycol diglycidyl ether Chemical compound C1OC1COCCOCCOCCOCC1CO1 UMILHIMHKXVDGH-UHFFFAOYSA-N 0.000 description 1
- OKJPEAGHQZHRQV-UHFFFAOYSA-N Triiodomethane Natural products IC(I)I OKJPEAGHQZHRQV-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- FYAMXEPQQLNQDM-UHFFFAOYSA-N Tris(1-aziridinyl)phosphine oxide Chemical compound C1CN1P(N1CC1)(=O)N1CC1 FYAMXEPQQLNQDM-UHFFFAOYSA-N 0.000 description 1
- AVYVKJMBNLPWRX-WFBYXXMGSA-N Trp-Ala-Ser Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(O)=O)=CNC2=C1 AVYVKJMBNLPWRX-WFBYXXMGSA-N 0.000 description 1
- IQGJAHMZWBTRIF-UBHSHLNASA-N Trp-Asp-Asn Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CC(=O)N)C(=O)O)N IQGJAHMZWBTRIF-UBHSHLNASA-N 0.000 description 1
- JZHJLBPBQKPTNX-UBHSHLNASA-N Trp-Cys-Ser Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CO)C(O)=O)=CNC2=C1 JZHJLBPBQKPTNX-UBHSHLNASA-N 0.000 description 1
- FEZASNVQLJQBHW-CABZTGNLSA-N Trp-Gly-Ala Chemical compound C1=CC=C2C(C[C@H](N)C(=O)NCC(=O)N[C@@H](C)C(O)=O)=CNC2=C1 FEZASNVQLJQBHW-CABZTGNLSA-N 0.000 description 1
- CCZXBOFIBYQLEV-IHPCNDPISA-N Trp-Leu-Leu Chemical compound CC(C)C[C@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)Cc1c[nH]c2ccccc12)C(O)=O CCZXBOFIBYQLEV-IHPCNDPISA-N 0.000 description 1
- RRVUOLRWIZXBRQ-IHPCNDPISA-N Trp-Leu-Lys Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CC1=CNC2=CC=CC=C21)N RRVUOLRWIZXBRQ-IHPCNDPISA-N 0.000 description 1
- HTGJDTPQYFMKNC-VFAJRCTISA-N Trp-Thr-Leu Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@H](C(=O)N[C@@H](CC(C)C)C(O)=O)[C@@H](C)O)=CNC2=C1 HTGJDTPQYFMKNC-VFAJRCTISA-N 0.000 description 1
- UIRVSEPRMWDVEW-RNXOBYDBSA-N Trp-Tyr-Phe Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)O)NC(=O)[C@H](CC2=CC=C(C=C2)O)NC(=O)[C@H](CC3=CNC4=CC=CC=C43)N UIRVSEPRMWDVEW-RNXOBYDBSA-N 0.000 description 1
- UOXPLPBMEPLZBW-WDSOQIARSA-N Trp-Val-Lys Chemical compound C1=CC=C2C(C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(O)=O)=CNC2=C1 UOXPLPBMEPLZBW-WDSOQIARSA-N 0.000 description 1
- VCXWRWYFJLXITF-AUTRQRHGSA-N Tyr-Ala-Ala Chemical compound OC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC1=CC=C(O)C=C1 VCXWRWYFJLXITF-AUTRQRHGSA-N 0.000 description 1
- FBVGQXJIXFZKSQ-GMVOTWDCSA-N Tyr-Ala-Trp Chemical compound C[C@@H](C(=O)N[C@@H](CC1=CNC2=CC=CC=C21)C(=O)O)NC(=O)[C@H](CC3=CC=C(C=C3)O)N FBVGQXJIXFZKSQ-GMVOTWDCSA-N 0.000 description 1
- QOIKZODVIPOPDD-AVGNSLFASA-N Tyr-Cys-Gln Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(O)=O QOIKZODVIPOPDD-AVGNSLFASA-N 0.000 description 1
- QUILOGWWLXMSAT-IHRRRGAJSA-N Tyr-Gln-Gln Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O QUILOGWWLXMSAT-IHRRRGAJSA-N 0.000 description 1
- ZRPLVTZTKPPSBT-AVGNSLFASA-N Tyr-Glu-Ser Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O ZRPLVTZTKPPSBT-AVGNSLFASA-N 0.000 description 1
- SOEGLGLDSUHWTI-STECZYCISA-N Tyr-Pro-Ile Chemical compound CC[C@H](C)[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)CC1=CC=C(O)C=C1 SOEGLGLDSUHWTI-STECZYCISA-N 0.000 description 1
- VXFXIBCCVLJCJT-JYJNAYRXSA-N Tyr-Pro-Pro Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N1CCC[C@H]1C(=O)N1CCC[C@H]1C(O)=O VXFXIBCCVLJCJT-JYJNAYRXSA-N 0.000 description 1
- KWKJGBHDYJOVCR-SRVKXCTJSA-N Tyr-Ser-Cys Chemical compound C1=CC(=CC=C1C[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CS)C(=O)O)N)O KWKJGBHDYJOVCR-SRVKXCTJSA-N 0.000 description 1
- SYFHQHYTNCQCCN-MELADBBJSA-N Tyr-Ser-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CO)NC(=O)[C@H](CC2=CC=C(C=C2)O)N)C(=O)O SYFHQHYTNCQCCN-MELADBBJSA-N 0.000 description 1
- KLQPIEVIKOQRAW-IZPVPAKOSA-N Tyr-Thr-Thr Chemical compound C[C@H]([C@@H](C(=O)N[C@@H]([C@@H](C)O)C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)N)O KLQPIEVIKOQRAW-IZPVPAKOSA-N 0.000 description 1
- DTWMJYGOUWNWEC-IHPCNDPISA-N Tyr-Trp-Cys Chemical compound C([C@H](N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CS)C(O)=O)C1=CC=C(O)C=C1 DTWMJYGOUWNWEC-IHPCNDPISA-N 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000002495 Uterine Neoplasms Diseases 0.000 description 1
- 208000016599 Uterine disease Diseases 0.000 description 1
- 244000000188 Vaccinium ovalifolium Species 0.000 description 1
- YFOCMOVJBQDBCE-NRPADANISA-N Val-Ala-Glu Chemical compound C[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)O)NC(=O)[C@H](C(C)C)N YFOCMOVJBQDBCE-NRPADANISA-N 0.000 description 1
- PAPWZOJOLKZEFR-AVGNSLFASA-N Val-Arg-Lys Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCCCN)C(=O)O)N PAPWZOJOLKZEFR-AVGNSLFASA-N 0.000 description 1
- BYOHPUZJVXWHAE-BYULHYEWSA-N Val-Asn-Asn Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CC(=O)N)C(=O)O)N BYOHPUZJVXWHAE-BYULHYEWSA-N 0.000 description 1
- BMGOFDMKDVVGJG-NHCYSSNCSA-N Val-Asp-Lys Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CCCCN)C(=O)O)N BMGOFDMKDVVGJG-NHCYSSNCSA-N 0.000 description 1
- IWZYXFRGWKEKBJ-GVXVVHGQSA-N Val-Gln-His Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CC1=CN=CN1)C(=O)O)N IWZYXFRGWKEKBJ-GVXVVHGQSA-N 0.000 description 1
- VFOHXOLPLACADK-GVXVVHGQSA-N Val-Gln-Leu Chemical compound CC(C)C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](C(C)C)N VFOHXOLPLACADK-GVXVVHGQSA-N 0.000 description 1
- JXGWQYWDUOWQHA-DZKIICNBSA-N Val-Gln-Phe Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)O)N JXGWQYWDUOWQHA-DZKIICNBSA-N 0.000 description 1
- AAOPYWQQBXHINJ-DZKIICNBSA-N Val-Gln-Tyr Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)N)C(=O)N[C@@H](CC1=CC=C(C=C1)O)C(=O)O)N AAOPYWQQBXHINJ-DZKIICNBSA-N 0.000 description 1
- FOADDSDHGRFUOC-DZKIICNBSA-N Val-Glu-Phe Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)O)N FOADDSDHGRFUOC-DZKIICNBSA-N 0.000 description 1
- PMXBARDFIAPBGK-DZKIICNBSA-N Val-Glu-Tyr Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 PMXBARDFIAPBGK-DZKIICNBSA-N 0.000 description 1
- DLMNFMXSNGTSNJ-PYJNHQTQSA-N Val-His-Ile Chemical compound CC[C@H](C)[C@@H](C(=O)O)NC(=O)[C@H](CC1=CN=CN1)NC(=O)[C@H](C(C)C)N DLMNFMXSNGTSNJ-PYJNHQTQSA-N 0.000 description 1
- KVRLNEILGGVBJX-IHRRRGAJSA-N Val-His-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)CC1=CN=CN1 KVRLNEILGGVBJX-IHRRRGAJSA-N 0.000 description 1
- LYERIXUFCYVFFX-GVXVVHGQSA-N Val-Leu-Glu Chemical compound CC(C)C[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)O)NC(=O)[C@H](C(C)C)N LYERIXUFCYVFFX-GVXVVHGQSA-N 0.000 description 1
- KSFXWENSJABBFI-ZKWXMUAHSA-N Val-Ser-Asn Chemical compound [H]N[C@@H](C(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(O)=O KSFXWENSJABBFI-ZKWXMUAHSA-N 0.000 description 1
- PZTZYZUTCPZWJH-FXQIFTODSA-N Val-Ser-Ser Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)O)N PZTZYZUTCPZWJH-FXQIFTODSA-N 0.000 description 1
- LCHZBEUVGAVMKS-RHYQMDGZSA-N Val-Thr-Leu Chemical compound CC(C)C[C@H](NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)[C@@H](C)O)C(O)=O LCHZBEUVGAVMKS-RHYQMDGZSA-N 0.000 description 1
- PGBMPFKFKXYROZ-UFYCRDLUSA-N Val-Tyr-Phe Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC1=CC=C(C=C1)O)C(=O)N[C@@H](CC2=CC=CC=C2)C(=O)O)N PGBMPFKFKXYROZ-UFYCRDLUSA-N 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 229940122803 Vinca alkaloid Drugs 0.000 description 1
- 235000009754 Vitis X bourquina Nutrition 0.000 description 1
- 235000012333 Vitis X labruscana Nutrition 0.000 description 1
- 240000006365 Vitis vinifera Species 0.000 description 1
- 235000014787 Vitis vinifera Nutrition 0.000 description 1
- 238000012452 Xenomouse strains Methods 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- PVNFMCBFDPTNQI-UIBOPQHZSA-N [(1S,2R,5S,6S,16E,18E,20R,21S)-11-chloro-21-hydroxy-12,20-dimethoxy-2,5,9,16-tetramethyl-8,23-dioxo-4,24-dioxa-9,22-diazatetracyclo[19.3.1.110,14.03,5]hexacosa-10,12,14(26),16,18-pentaen-6-yl] acetate [(1S,2R,5S,6S,16E,18E,20R,21S)-11-chloro-21-hydroxy-12,20-dimethoxy-2,5,9,16-tetramethyl-8,23-dioxo-4,24-dioxa-9,22-diazatetracyclo[19.3.1.110,14.03,5]hexacosa-10,12,14(26),16,18-pentaen-6-yl] 3-methylbutanoate [(1S,2R,5S,6S,16E,18E,20R,21S)-11-chloro-21-hydroxy-12,20-dimethoxy-2,5,9,16-tetramethyl-8,23-dioxo-4,24-dioxa-9,22-diazatetracyclo[19.3.1.110,14.03,5]hexacosa-10,12,14(26),16,18-pentaen-6-yl] 2-methylpropanoate [(1S,2R,5S,6S,16E,18E,20R,21S)-11-chloro-21-hydroxy-12,20-dimethoxy-2,5,9,16-tetramethyl-8,23-dioxo-4,24-dioxa-9,22-diazatetracyclo[19.3.1.110,14.03,5]hexacosa-10,12,14(26),16,18-pentaen-6-yl] propanoate Chemical compound CO[C@@H]1\C=C\C=C(C)\Cc2cc(OC)c(Cl)c(c2)N(C)C(=O)C[C@H](OC(C)=O)[C@]2(C)OC2[C@H](C)[C@@H]2C[C@@]1(O)NC(=O)O2.CCC(=O)O[C@H]1CC(=O)N(C)c2cc(C\C(C)=C\C=C\[C@@H](OC)[C@@]3(O)C[C@H](OC(=O)N3)[C@@H](C)C3O[C@@]13C)cc(OC)c2Cl.CO[C@@H]1\C=C\C=C(C)\Cc2cc(OC)c(Cl)c(c2)N(C)C(=O)C[C@H](OC(=O)C(C)C)[C@]2(C)OC2[C@H](C)[C@@H]2C[C@@]1(O)NC(=O)O2.CO[C@@H]1\C=C\C=C(C)\Cc2cc(OC)c(Cl)c(c2)N(C)C(=O)C[C@H](OC(=O)CC(C)C)[C@]2(C)OC2[C@H](C)[C@@H]2C[C@@]1(O)NC(=O)O2 PVNFMCBFDPTNQI-UIBOPQHZSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- NLMBVBUNULOTNS-HOKPPMCLSA-N [4-[[(2s)-5-(carbamoylamino)-2-[[(2s)-2-[6-(2,5-dioxopyrrol-1-yl)hexanoylamino]-3-methylbutanoyl]amino]pentanoyl]amino]phenyl]methyl n-[(2s)-1-[[(2s)-1-[[(3r,4s,5s)-1-[(2s)-2-[(1r,2r)-3-[[(1s,2r)-1-hydroxy-1-phenylpropan-2-yl]amino]-1-methoxy-2-methyl-3-o Chemical compound C1([C@H](O)[C@@H](C)NC(=O)[C@H](C)[C@@H](OC)[C@@H]2CCCN2C(=O)C[C@H]([C@H]([C@@H](C)CC)N(C)C(=O)[C@@H](NC(=O)[C@H](C(C)C)N(C)C(=O)OCC=2C=CC(NC(=O)[C@H](CCCNC(N)=O)NC(=O)[C@@H](NC(=O)CCCCCN3C(C=CC3=O)=O)C(C)C)=CC=2)C(C)C)OC)=CC=CC=C1 NLMBVBUNULOTNS-HOKPPMCLSA-N 0.000 description 1
- USDJGQLNFPZEON-UHFFFAOYSA-N [[4,6-bis(hydroxymethylamino)-1,3,5-triazin-2-yl]amino]methanol Chemical compound OCNC1=NC(NCO)=NC(NCO)=N1 USDJGQLNFPZEON-UHFFFAOYSA-N 0.000 description 1
- GXVKHKJETWAWRR-UHFFFAOYSA-N a805143 Chemical compound C1CCNC1.C1CCNC1 GXVKHKJETWAWRR-UHFFFAOYSA-N 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 229940028652 abraxane Drugs 0.000 description 1
- QUHYUSAHBDACNG-UHFFFAOYSA-N acerogenin 3 Natural products C1=CC(O)=CC=C1CCCCC(=O)CCC1=CC=C(O)C=C1 QUHYUSAHBDACNG-UHFFFAOYSA-N 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- HXGDTGSAIMULJN-UHFFFAOYSA-N acetnaphthylene Natural products C1=CC(C=C2)=C3C2=CC=CC3=C1 HXGDTGSAIMULJN-UHFFFAOYSA-N 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 229930183665 actinomycin Natural products 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 125000004442 acylamino group Chemical group 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 230000000274 adsorptive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 150000001295 alanines Chemical class 0.000 description 1
- 108010011559 alanylphenylalanine Proteins 0.000 description 1
- HAXFWIACAGNFHA-UHFFFAOYSA-N aldrithiol Chemical compound C=1C=CC=NC=1SSC1=CC=CC=N1 HAXFWIACAGNFHA-UHFFFAOYSA-N 0.000 description 1
- 125000005257 alkyl acyl group Chemical group 0.000 description 1
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 1
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 1
- KOSRFJWDECSPRO-UHFFFAOYSA-N alpha-L-glutamyl-L-glutamic acid Natural products OC(=O)CCC(N)C(=O)NC(CCC(O)=O)C(O)=O KOSRFJWDECSPRO-UHFFFAOYSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229960000473 altretamine Drugs 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001408 amides Chemical group 0.000 description 1
- 125000000320 amidine group Chemical group 0.000 description 1
- 229940064734 aminobenzoate Drugs 0.000 description 1
- 229960003437 aminoglutethimide Drugs 0.000 description 1
- ROBVIMPUHSLWNV-UHFFFAOYSA-N aminoglutethimide Chemical compound C=1C=C(N)C=CC=1C1(CC)CCC(=O)NC1=O ROBVIMPUHSLWNV-UHFFFAOYSA-N 0.000 description 1
- 229960002749 aminolevulinic acid Drugs 0.000 description 1
- 229960003896 aminopterin Drugs 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 229960001220 amsacrine Drugs 0.000 description 1
- XCPGHVQEEXUHNC-UHFFFAOYSA-N amsacrine Chemical compound COC1=CC(NS(C)(=O)=O)=CC=C1NC1=C(C=CC=C2)C2=NC2=CC=CC=C12 XCPGHVQEEXUHNC-UHFFFAOYSA-N 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003817 anthracycline antibiotic agent Substances 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 238000010913 antigen-directed enzyme pro-drug therapy Methods 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000008209 arabinosides Chemical class 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 108010013835 arginine glutamate Proteins 0.000 description 1
- 108010091092 arginyl-glycyl-proline Proteins 0.000 description 1
- 108010007483 arginyl-leucyl-tyrosyl-glutamic acid Proteins 0.000 description 1
- 108010029539 arginyl-prolyl-proline Proteins 0.000 description 1
- 108010068380 arginylarginine Proteins 0.000 description 1
- 229940000489 arsenate Drugs 0.000 description 1
- 125000005251 aryl acyl group Chemical group 0.000 description 1
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 125000000613 asparagine group Chemical group N[C@@H](CC(N)=O)C(=O)* 0.000 description 1
- 108010069205 aspartyl-phenylalanine Proteins 0.000 description 1
- 108010092854 aspartyllysine Proteins 0.000 description 1
- 229930184293 auramycin Natural products 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- 229950011321 azaserine Drugs 0.000 description 1
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical compound C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 description 1
- MQTOSJVFKKJCRP-BICOPXKESA-N azithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)N(C)C[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 MQTOSJVFKKJCRP-BICOPXKESA-N 0.000 description 1
- 229960004099 azithromycin Drugs 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- UREZNYTWGJKWBI-UHFFFAOYSA-M benzethonium chloride Chemical compound [Cl-].C1=CC(C(C)(C)CC(C)(C)C)=CC=C1OCCOCC[N+](C)(C)CC1=CC=CC=C1 UREZNYTWGJKWBI-UHFFFAOYSA-M 0.000 description 1
- 229960001950 benzethonium chloride Drugs 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- XSCHRSMBECNVNS-UHFFFAOYSA-N benzopyrazine Natural products N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 238000013357 binding ELISA Methods 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- HUTDDBSSHVOYJR-UHFFFAOYSA-H bis[(2-oxo-1,3,2$l^{5},4$l^{2}-dioxaphosphaplumbetan-2-yl)oxy]lead Chemical compound [Pb+2].[Pb+2].[Pb+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O HUTDDBSSHVOYJR-UHFFFAOYSA-H 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 210000001772 blood platelet Anatomy 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 150000001649 bromium compounds Chemical class 0.000 description 1
- 229960005520 bryostatin Drugs 0.000 description 1
- MJQUEDHRCUIRLF-TVIXENOKSA-N bryostatin 1 Chemical compound C([C@@H]1CC(/[C@@H]([C@@](C(C)(C)/C=C/2)(O)O1)OC(=O)/C=C/C=C/CCC)=C\C(=O)OC)[C@H]([C@@H](C)O)OC(=O)C[C@H](O)C[C@@H](O1)C[C@H](OC(C)=O)C(C)(C)[C@]1(O)C[C@@H]1C\C(=C\C(=O)OC)C[C@H]\2O1 MJQUEDHRCUIRLF-TVIXENOKSA-N 0.000 description 1
- MUIWQCKLQMOUAT-AKUNNTHJSA-N bryostatin 20 Natural products COC(=O)C=C1C[C@@]2(C)C[C@]3(O)O[C@](C)(C[C@@H](O)CC(=O)O[C@](C)(C[C@@]4(C)O[C@](O)(CC5=CC(=O)O[C@]45C)C(C)(C)C=C[C@@](C)(C1)O2)[C@@H](C)O)C[C@H](OC(=O)C(C)(C)C)C3(C)C MUIWQCKLQMOUAT-AKUNNTHJSA-N 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- LRHPLDYGYMQRHN-UHFFFAOYSA-N butyl alcohol Substances CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 1
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N butyric aldehyde Natural products CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 229940088954 camptosar Drugs 0.000 description 1
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical compound C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 1
- 239000003560 cancer drug Substances 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 238000005251 capillar electrophoresis Methods 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 125000003739 carbamimidoyl group Chemical group C(N)(=N)* 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- SKOLWUPSYHWYAM-UHFFFAOYSA-N carbonodithioic O,S-acid Chemical compound SC(S)=O SKOLWUPSYHWYAM-UHFFFAOYSA-N 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- BBZDXMBRAFTCAA-AREMUKBSSA-N carzelesin Chemical compound C1=2NC=C(C)C=2C([C@H](CCl)CN2C(=O)C=3NC4=CC=C(C=C4C=3)NC(=O)C3=CC4=CC=C(C=C4O3)N(CC)CC)=C2C=C1OC(=O)NC1=CC=CC=C1 BBZDXMBRAFTCAA-AREMUKBSSA-N 0.000 description 1
- 229950007509 carzelesin Drugs 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000005341 cation exchange Methods 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 210000004534 cecum Anatomy 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000011748 cell maturation Effects 0.000 description 1
- 238000003570 cell viability assay Methods 0.000 description 1
- 210000002711 centrocyte Anatomy 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 230000000973 chemotherapeutic effect Effects 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 229920005556 chlorobutyl Polymers 0.000 description 1
- 229960001480 chlorozotocin Drugs 0.000 description 1
- VZWXIQHBIQLMPN-UHFFFAOYSA-N chromane Chemical compound C1=CC=C2CCCOC2=C1 VZWXIQHBIQLMPN-UHFFFAOYSA-N 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 230000004186 co-expression Effects 0.000 description 1
- 238000005354 coacervation Methods 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 230000024203 complement activation Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 230000001268 conjugating effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 108010006226 cryptophycin Proteins 0.000 description 1
- 108010089438 cryptophycin 1 Proteins 0.000 description 1
- 108010090203 cryptophycin 8 Proteins 0.000 description 1
- GICLSALZHXCILJ-UHFFFAOYSA-N ctk5a5089 Chemical compound NCC(O)=O.NCC(O)=O GICLSALZHXCILJ-UHFFFAOYSA-N 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 125000001651 cyanato group Chemical class [*]OC#N 0.000 description 1
- CFBGXYDUODCMNS-UHFFFAOYSA-N cyclobutene Chemical compound C1CC=C1 CFBGXYDUODCMNS-UHFFFAOYSA-N 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- 125000004956 cyclohexylene group Chemical group 0.000 description 1
- 125000004979 cyclopentylene group Chemical group 0.000 description 1
- OOXWYYGXTJLWHA-UHFFFAOYSA-N cyclopropene Chemical compound C1C=C1 OOXWYYGXTJLWHA-UHFFFAOYSA-N 0.000 description 1
- 108010069495 cysteinyltyrosine Proteins 0.000 description 1
- 229960000684 cytarabine Drugs 0.000 description 1
- 230000001120 cytoprotective effect Effects 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 238000002784 cytotoxicity assay Methods 0.000 description 1
- 231100000263 cytotoxicity test Toxicity 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- CYQFCXCEBYINGO-IAGOWNOFSA-N delta1-THC Chemical compound C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 CYQFCXCEBYINGO-IAGOWNOFSA-N 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 238000009795 derivation Methods 0.000 description 1
- URLVCROWVOSNPT-QTTMQESMSA-N desacetyluvaricin Natural products O=C1C(CCCCCCCCCCCC[C@@H](O)[C@H]2O[C@@H]([C@@H]3O[C@@H]([C@@H](O)CCCCCCCCCC)CC3)CC2)=C[C@H](C)O1 URLVCROWVOSNPT-QTTMQESMSA-N 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 229940039227 diagnostic agent Drugs 0.000 description 1
- 239000000032 diagnostic agent Substances 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 108020001096 dihydrofolate reductase Proteins 0.000 description 1
- 125000005442 diisocyanate group Chemical group 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 150000002019 disulfides Chemical class 0.000 description 1
- 239000003534 dna topoisomerase inhibitor Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- ZWAOHEXOSAUJHY-ZIYNGMLESA-N doxifluridine Chemical compound O[C@@H]1[C@H](O)[C@@H](C)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ZWAOHEXOSAUJHY-ZIYNGMLESA-N 0.000 description 1
- 229950005454 doxifluridine Drugs 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- VLCYCQAOQCDTCN-UHFFFAOYSA-N eflornithine Chemical compound NCCCC(N)(C(F)F)C(O)=O VLCYCQAOQCDTCN-UHFFFAOYSA-N 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000012039 electrophile Substances 0.000 description 1
- 229940120655 eloxatin Drugs 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 229950011487 enocitabine Drugs 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- 229950002973 epitiostanol Drugs 0.000 description 1
- 229930013356 epothilone Natural products 0.000 description 1
- 150000003883 epothilone derivatives Chemical class 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 229960001842 estramustine Drugs 0.000 description 1
- FRPJXPJMRWBBIH-RBRWEJTLSA-N estramustine Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 FRPJXPJMRWBBIH-RBRWEJTLSA-N 0.000 description 1
- RQIFXTOWUNAUJC-UHFFFAOYSA-N ethanesulfinic acid Chemical compound CCS(O)=O RQIFXTOWUNAUJC-UHFFFAOYSA-N 0.000 description 1
- 125000001033 ether group Chemical group 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 229960005237 etoglucid Drugs 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 235000019152 folic acid Nutrition 0.000 description 1
- 239000011724 folic acid Substances 0.000 description 1
- 229960000304 folic acid Drugs 0.000 description 1
- 150000002224 folic acids Chemical class 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- WCVXAYSKMJJPLO-UHFFFAOYSA-N furan Chemical compound C=1C=COC=1.C=1C=COC=1 WCVXAYSKMJJPLO-UHFFFAOYSA-N 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 229940044658 gallium nitrate Drugs 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- 229940020967 gemzar Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229940116332 glucose oxidase Drugs 0.000 description 1
- 235000019420 glucose oxidase Nutrition 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 108010085059 glutamyl-arginyl-proline Proteins 0.000 description 1
- 108010080575 glutamyl-aspartyl-alanine Proteins 0.000 description 1
- 108010042598 glutamyl-aspartyl-glycine Proteins 0.000 description 1
- 108010057083 glutamyl-aspartyl-leucine Proteins 0.000 description 1
- 108010055341 glutamyl-glutamic acid Proteins 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 1
- XBGGUPMXALFZOT-UHFFFAOYSA-N glycyl-L-tyrosine hemihydrate Natural products NCC(=O)NC(C(O)=O)CC1=CC=C(O)C=C1 XBGGUPMXALFZOT-UHFFFAOYSA-N 0.000 description 1
- 108010072405 glycyl-aspartyl-glycine Proteins 0.000 description 1
- 108010079413 glycyl-prolyl-glutamic acid Proteins 0.000 description 1
- 108010081551 glycylphenylalanine Proteins 0.000 description 1
- 108010084389 glycyltryptophan Proteins 0.000 description 1
- 108010087823 glycyltyrosine Proteins 0.000 description 1
- 210000000224 granular leucocyte Anatomy 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000003966 growth inhibitor Substances 0.000 description 1
- 125000002795 guanidino group Chemical group C(N)(=N)N* 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 201000003911 head and neck carcinoma Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- UUVWYPNAQBNQJQ-UHFFFAOYSA-N hexamethylmelamine Chemical compound CN(C)C1=NC(N(C)C)=NC(N(C)C)=N1 UUVWYPNAQBNQJQ-UHFFFAOYSA-N 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 108010028295 histidylhistidine Proteins 0.000 description 1
- 108010085325 histidylproline Proteins 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229960002773 hyaluronidase Drugs 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 229940088013 hycamtin Drugs 0.000 description 1
- 229940042795 hydrazides for tuberculosis treatment Drugs 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 150000007857 hydrazones Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 238000004191 hydrophobic interaction chromatography Methods 0.000 description 1
- 229920001600 hydrophobic polymer Polymers 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 229960001330 hydroxycarbamide Drugs 0.000 description 1
- 229920003063 hydroxymethyl cellulose Polymers 0.000 description 1
- 229940031574 hydroxymethyl cellulose Drugs 0.000 description 1
- 229940044700 hylenex Drugs 0.000 description 1
- 229940015872 ibandronate Drugs 0.000 description 1
- MTNDZQHUAFNZQY-UHFFFAOYSA-N imidazoline Chemical compound C1CN=CN1 MTNDZQHUAFNZQY-UHFFFAOYSA-N 0.000 description 1
- 125000000879 imine group Chemical group 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 230000007154 intracellular accumulation Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 230000002601 intratumoral effect Effects 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- PGLTVOMIXTUURA-UHFFFAOYSA-N iodoacetamide Chemical compound NC(=O)CI PGLTVOMIXTUURA-UHFFFAOYSA-N 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 125000002510 isobutoxy group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])O* 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001261 isocyanato group Chemical group *N=C=O 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical compound C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 150000004715 keto acids Chemical class 0.000 description 1
- 229940057428 lactoperoxidase Drugs 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 229940115286 lentinan Drugs 0.000 description 1
- 108010083708 leucyl-aspartyl-valine Proteins 0.000 description 1
- 108010057821 leucylproline Proteins 0.000 description 1
- 108010012058 leucyltyrosine Proteins 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 229960002247 lomustine Drugs 0.000 description 1
- 201000005249 lung adenocarcinoma Diseases 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 210000005265 lung cell Anatomy 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 230000002132 lysosomal effect Effects 0.000 description 1
- 239000004325 lysozyme Substances 0.000 description 1
- 229960000274 lysozyme Drugs 0.000 description 1
- 235000010335 lysozyme Nutrition 0.000 description 1
- 108010003700 lysyl aspartic acid Proteins 0.000 description 1
- 108010054155 lysyllysine Proteins 0.000 description 1
- 108010038320 lysylphenylalanine Proteins 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 229940099262 marinol Drugs 0.000 description 1
- 230000008774 maternal effect Effects 0.000 description 1
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 1
- WKPWGQKGSOKKOO-RSFHAFMBSA-N maytansine Chemical compound CO[C@@H]([C@@]1(O)C[C@](OC(=O)N1)([C@H]([C@@H]1O[C@@]1(C)[C@@H](OC(=O)[C@H](C)N(C)C(C)=O)CC(=O)N1C)C)[H])\C=C\C=C(C)\CC2=CC(OC)=C(Cl)C1=C2 WKPWGQKGSOKKOO-RSFHAFMBSA-N 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- TWXDDNPPQUTEOV-FVGYRXGTSA-N methamphetamine hydrochloride Chemical compound Cl.CN[C@@H](C)CC1=CC=CC=C1 TWXDDNPPQUTEOV-FVGYRXGTSA-N 0.000 description 1
- XNEFVTBPCXGIRX-UHFFFAOYSA-N methanesulfinic acid Chemical compound CS(O)=O XNEFVTBPCXGIRX-UHFFFAOYSA-N 0.000 description 1
- XMYQHJDBLRZMLW-UHFFFAOYSA-N methanolamine Chemical group NCO XMYQHJDBLRZMLW-UHFFFAOYSA-N 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 1
- 108010056582 methionylglutamic acid Proteins 0.000 description 1
- JLEJCNOTNLZCHQ-VKHMYHEASA-N methyl (2s)-2-chloropropanoate Chemical compound COC(=O)[C@H](C)Cl JLEJCNOTNLZCHQ-VKHMYHEASA-N 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- VNXBKJFUJUWOCW-UHFFFAOYSA-N methylcyclopropane Chemical compound CC1CC1 VNXBKJFUJUWOCW-UHFFFAOYSA-N 0.000 description 1
- WPHGSKGZRAQSGP-UHFFFAOYSA-N methylenecyclohexane Natural products C1CCCC2CC21 WPHGSKGZRAQSGP-UHFFFAOYSA-N 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 239000004530 micro-emulsion Substances 0.000 description 1
- 108010029942 microperoxidase Proteins 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- MXWHMTNPTTVWDM-NXOFHUPFSA-N mitoguazone Chemical compound NC(N)=N\N=C(/C)\C=N\N=C(N)N MXWHMTNPTTVWDM-NXOFHUPFSA-N 0.000 description 1
- 229960003539 mitoguazone Drugs 0.000 description 1
- 229960000350 mitotane Drugs 0.000 description 1
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 125000006518 morpholino carbonyl group Chemical group [H]C1([H])OC([H])([H])C([H])([H])N(C(*)=O)C1([H])[H] 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 201000005962 mycosis fungoides Diseases 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229940086322 navelbine Drugs 0.000 description 1
- 230000035407 negative regulation of cell proliferation Effects 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 125000006501 nitrophenyl group Chemical group 0.000 description 1
- 125000000018 nitroso group Chemical group N(=O)* 0.000 description 1
- OSTGTTZJOCZWJG-UHFFFAOYSA-N nitrosourea Chemical compound NC(=O)N=NO OSTGTTZJOCZWJG-UHFFFAOYSA-N 0.000 description 1
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 125000001736 nosyl group Chemical group S(=O)(=O)(C1=CC=C([N+](=O)[O-])C=C1)* 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 239000002751 oligonucleotide probe Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- GHCAUEMXBSLMGU-UHFFFAOYSA-N oxadiazole;1,2,5-oxadiazole Chemical compound C=1C=NON=1.C1=CON=N1 GHCAUEMXBSLMGU-UHFFFAOYSA-N 0.000 description 1
- GUVKYQNSMXSMMU-UHFFFAOYSA-N oxane Chemical compound C1CCOCC1.C1CCOCC1 GUVKYQNSMXSMMU-UHFFFAOYSA-N 0.000 description 1
- AZHVQJLDOFKHPZ-UHFFFAOYSA-N oxathiazine Chemical compound O1SN=CC=C1 AZHVQJLDOFKHPZ-UHFFFAOYSA-N 0.000 description 1
- CQDAMYNQINDRQC-UHFFFAOYSA-N oxatriazole Chemical compound C1=NN=NO1 CQDAMYNQINDRQC-UHFFFAOYSA-N 0.000 description 1
- ATYBXHSAIOKLMG-UHFFFAOYSA-N oxepin Chemical compound O1C=CC=CC=C1 ATYBXHSAIOKLMG-UHFFFAOYSA-N 0.000 description 1
- AHHWIHXENZJRFG-UHFFFAOYSA-N oxetane Chemical compound C1COC1 AHHWIHXENZJRFG-UHFFFAOYSA-N 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 description 1
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N p-hydroxybenzoic acid methyl ester Natural products COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 208000003154 papilloma Diseases 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 125000000538 pentafluorophenyl group Chemical group FC1=C(F)C(F)=C(*)C(F)=C1F 0.000 description 1
- 125000004817 pentamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 229960002340 pentostatin Drugs 0.000 description 1
- FPVKHBSQESCIEP-JQCXWYLXSA-N pentostatin Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC[C@H]2O)=C2N=C1 FPVKHBSQESCIEP-JQCXWYLXSA-N 0.000 description 1
- 125000004115 pentoxy group Chemical group [*]OC([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 201000002628 peritoneum cancer Diseases 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 210000001986 peyer's patch Anatomy 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229960003742 phenol Drugs 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 108010070409 phenylalanyl-glycyl-glycine Proteins 0.000 description 1
- 108010073025 phenylalanylphenylalanine Proteins 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 125000003170 phenylsulfonyl group Chemical group C1(=CC=CC=C1)S(=O)(=O)* 0.000 description 1
- FVZVCSNXTFCBQU-UHFFFAOYSA-N phosphanyl Chemical group [PH2] FVZVCSNXTFCBQU-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical compound O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 1
- 125000001476 phosphono group Chemical group [H]OP(*)(=O)O[H] 0.000 description 1
- PTMHPRAIXMAOOB-UHFFFAOYSA-L phosphoramidate Chemical compound NP([O-])([O-])=O PTMHPRAIXMAOOB-UHFFFAOYSA-L 0.000 description 1
- 150000008300 phosphoramidites Chemical class 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- LFSXCDWNBUNEEM-UHFFFAOYSA-N phthalazine Chemical compound C1=NN=CC2=CC=CC=C21 LFSXCDWNBUNEEM-UHFFFAOYSA-N 0.000 description 1
- 125000005545 phthalimidyl group Chemical group 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- LYKMMUBOEFYJQG-UHFFFAOYSA-N piperoxan Chemical compound C1OC2=CC=CC=C2OC1CN1CCCCC1 LYKMMUBOEFYJQG-UHFFFAOYSA-N 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229920000191 poly(N-vinyl pyrrolidone) Polymers 0.000 description 1
- 229920001583 poly(oxyethylated polyols) Polymers 0.000 description 1
- 108010054442 polyalanine Proteins 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 206010036596 premature ejaculation Diseases 0.000 description 1
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 description 1
- 229960000624 procarbazine Drugs 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 108010015796 prolylisoleucine Proteins 0.000 description 1
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 230000007026 protein scission Effects 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- 150000003214 pyranose derivatives Chemical class 0.000 description 1
- CRTBNOWPBHJICM-UHFFFAOYSA-N pyrazine Chemical compound C1=CN=CC=N1.C1=CN=CC=N1 CRTBNOWPBHJICM-UHFFFAOYSA-N 0.000 description 1
- KOUKXHPPRFNWPP-UHFFFAOYSA-N pyrazine-2,5-dicarboxylic acid;hydrate Chemical compound O.OC(=O)C1=CN=C(C(O)=O)C=N1 KOUKXHPPRFNWPP-UHFFFAOYSA-N 0.000 description 1
- DNXIASIHZYFFRO-UHFFFAOYSA-N pyrazoline Chemical compound C1CN=NC1 DNXIASIHZYFFRO-UHFFFAOYSA-N 0.000 description 1
- IOXGEAHHEGTLMQ-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1.C1=CC=NN=C1 IOXGEAHHEGTLMQ-UHFFFAOYSA-N 0.000 description 1
- WHMDPDGBKYUEMW-UHFFFAOYSA-N pyridine-2-thiol Chemical compound SC1=CC=CC=N1 WHMDPDGBKYUEMW-UHFFFAOYSA-N 0.000 description 1
- YMXFJTUQQVLJEN-UHFFFAOYSA-N pyrimidine Chemical compound C1=CN=CN=C1.C1=CN=CN=C1 YMXFJTUQQVLJEN-UHFFFAOYSA-N 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- ZVJHJDDKYZXRJI-UHFFFAOYSA-N pyrroline Natural products C1CC=NC1 ZVJHJDDKYZXRJI-UHFFFAOYSA-N 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- UOWVMDUEMSNCAV-WYENRQIDSA-N rachelmycin Chemical compound C1([C@]23C[C@@H]2CN1C(=O)C=1NC=2C(OC)=C(O)C4=C(C=2C=1)CCN4C(=O)C1=CC=2C=4CCN(C=4C(O)=C(C=2N1)OC)C(N)=O)=CC(=O)C1=C3C(C)=CN1 UOWVMDUEMSNCAV-WYENRQIDSA-N 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 210000001350 reed-sternberg cell Anatomy 0.000 description 1
- 239000012925 reference material Substances 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 229930002330 retinoic acid Natural products 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- MBABCNBNDNGODA-WPZDJQSSSA-N rolliniastatin 1 Natural products O1[C@@H]([C@@H](O)CCCCCCCCCC)CC[C@H]1[C@H]1O[C@@H]([C@H](O)CCCCCCCCCC[C@@H](O)CC=2C(O[C@@H](C)C=2)=O)CC1 MBABCNBNDNGODA-WPZDJQSSSA-N 0.000 description 1
- VHXNKPBCCMUMSW-FQEVSTJZSA-N rubitecan Chemical compound C1=CC([N+]([O-])=O)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VHXNKPBCCMUMSW-FQEVSTJZSA-N 0.000 description 1
- 238000013391 scatchard analysis Methods 0.000 description 1
- 125000005920 sec-butoxy group Chemical group 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 1
- 210000000717 sertoli cell Anatomy 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 108010048818 seryl-histidine Proteins 0.000 description 1
- 208000012201 sexual and gender identity disease Diseases 0.000 description 1
- 208000015891 sexual disease Diseases 0.000 description 1
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 201000000307 small intestine lymphoma Diseases 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- MKNJJMHQBYVHRS-UHFFFAOYSA-M sodium;1-[11-(2,5-dioxopyrrol-1-yl)undecanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCCCCCCN1C(=O)C=CC1=O MKNJJMHQBYVHRS-UHFFFAOYSA-M 0.000 description 1
- ULARYIUTHAWJMU-UHFFFAOYSA-M sodium;1-[4-(2,5-dioxopyrrol-1-yl)butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O ULARYIUTHAWJMU-UHFFFAOYSA-M 0.000 description 1
- VUFNRPJNRFOTGK-UHFFFAOYSA-M sodium;1-[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1CCC(CN2C(C=CC2=O)=O)CC1 VUFNRPJNRFOTGK-UHFFFAOYSA-M 0.000 description 1
- YYMWVZQRBNARFZ-UHFFFAOYSA-M sodium;2-[2,3-bis(sulfanyl)propoxy]ethanesulfonate Chemical compound [Na+].[O-]S(=O)(=O)CCOCC(S)CS YYMWVZQRBNARFZ-UHFFFAOYSA-M 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- ICXJVZHDZFXYQC-UHFFFAOYSA-N spongistatin 1 Natural products OC1C(O2)(O)CC(O)C(C)C2CCCC=CC(O2)CC(O)CC2(O2)CC(OC)CC2CC(=O)C(C)C(OC(C)=O)C(C)C(=C)CC(O2)CC(C)(O)CC2(O2)CC(OC(C)=O)CC2CC(=O)OC2C(O)C(CC(=C)CC(O)C=CC(Cl)=C)OC1C2C ICXJVZHDZFXYQC-UHFFFAOYSA-N 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 208000017572 squamous cell neoplasm Diseases 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- SFVFIFLLYFPGHH-UHFFFAOYSA-M stearalkonium chloride Chemical compound [Cl-].CCCCCCCCCCCCCCCCCC[N+](C)(C)CC1=CC=CC=C1 SFVFIFLLYFPGHH-UHFFFAOYSA-M 0.000 description 1
- 238000011476 stem cell transplantation Methods 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- KZNICNPSHKQLFF-UHFFFAOYSA-N succinimide Chemical class O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 1
- NVBFHJWHLNUMCV-UHFFFAOYSA-N sulfamide Chemical compound NS(N)(=O)=O NVBFHJWHLNUMCV-UHFFFAOYSA-N 0.000 description 1
- BUUPQKDIAURBJP-UHFFFAOYSA-N sulfinic acid Chemical compound OS=O BUUPQKDIAURBJP-UHFFFAOYSA-N 0.000 description 1
- 150000003453 sulfinic acid esters Chemical class 0.000 description 1
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 1
- IWOKCMBOJXYDEE-UHFFFAOYSA-N sulfinylmethane Chemical group C=S=O IWOKCMBOJXYDEE-UHFFFAOYSA-N 0.000 description 1
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 125000001174 sulfone group Chemical group 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical class ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000003319 supportive effect Effects 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- RCINICONZNJXQF-XAZOAEDWSA-N taxol® Chemical compound O([C@@H]1[C@@]2(CC(C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3(C21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-XAZOAEDWSA-N 0.000 description 1
- 229940063683 taxotere Drugs 0.000 description 1
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 1
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 1
- BPEWUONYVDABNZ-DZBHQSCQSA-N testolactone Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(OC(=O)CC4)[C@@H]4[C@@H]3CCC2=C1 BPEWUONYVDABNZ-DZBHQSCQSA-N 0.000 description 1
- 229960005353 testolactone Drugs 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- KHVCOYGKHDJPBZ-WDCZJNDASA-N tetrahydrooxazine Chemical compound OC[C@H]1ONC[C@@H](O)[C@@H]1O KHVCOYGKHDJPBZ-WDCZJNDASA-N 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 238000011285 therapeutic regimen Methods 0.000 description 1
- GVIJJXMXTUZIOD-UHFFFAOYSA-N thianthrene Chemical compound C1=CC=C2SC3=CC=CC=C3SC2=C1 GVIJJXMXTUZIOD-UHFFFAOYSA-N 0.000 description 1
- CBDKQYKMCICBOF-UHFFFAOYSA-N thiazoline Chemical compound C1CN=CS1 CBDKQYKMCICBOF-UHFFFAOYSA-N 0.000 description 1
- XSROQCDVUIHRSI-UHFFFAOYSA-N thietane Chemical compound C1CSC1 XSROQCDVUIHRSI-UHFFFAOYSA-N 0.000 description 1
- 125000005300 thiocarboxy group Chemical group C(=S)(O)* 0.000 description 1
- 150000003566 thiocarboxylic acids Chemical class 0.000 description 1
- 125000000101 thioether group Chemical group 0.000 description 1
- ATGUDZODTABURZ-UHFFFAOYSA-N thiolan-2-ylideneazanium;chloride Chemical compound Cl.N=C1CCCS1 ATGUDZODTABURZ-UHFFFAOYSA-N 0.000 description 1
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 1
- 125000005505 thiomorpholino group Chemical group 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- QERYCTSHXKAMIS-UHFFFAOYSA-N thiophene-2-carboxylic acid Chemical compound OC(=O)C1=CC=CS1 QERYCTSHXKAMIS-UHFFFAOYSA-N 0.000 description 1
- 125000000341 threoninyl group Chemical group [H]OC([H])(C([H])([H])[H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- YFTWHEBLORWGNI-UHFFFAOYSA-N tiamiprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC(N)=NC2=C1NC=N2 YFTWHEBLORWGNI-UHFFFAOYSA-N 0.000 description 1
- 229950011457 tiamiprine Drugs 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- RUELTTOHQODFPA-UHFFFAOYSA-N toluene 2,6-diisocyanate Chemical compound CC1=C(N=C=O)C=CC=C1N=C=O RUELTTOHQODFPA-UHFFFAOYSA-N 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 229940044693 topoisomerase inhibitor Drugs 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 229950001353 tretamine Drugs 0.000 description 1
- IUCJMVBFZDHPDX-UHFFFAOYSA-N tretamine Chemical compound C1CN1C1=NC(N2CC2)=NC(N2CC2)=N1 IUCJMVBFZDHPDX-UHFFFAOYSA-N 0.000 description 1
- 229960001727 tretinoin Drugs 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 108010014563 tryptophyl-cysteinyl-serine Proteins 0.000 description 1
- 108010044292 tryptophyltyrosine Proteins 0.000 description 1
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 1
- 108010029599 tyrosyl-glutamyl-tryptophan Proteins 0.000 description 1
- 108010003137 tyrosyltyrosine Proteins 0.000 description 1
- 241000701447 unidentified baculovirus Species 0.000 description 1
- 241001515965 unidentified phage Species 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 206010046766 uterine cancer Diseases 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 125000002987 valine group Chemical group [H]N([H])C([H])(C(*)=O)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 108010073969 valyllysine Proteins 0.000 description 1
- 229960004355 vindesine Drugs 0.000 description 1
- GBABOYUKABKIAF-IELIFDKJSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-IELIFDKJSA-N 0.000 description 1
- 229960002066 vinorelbine Drugs 0.000 description 1
- CILBMBUYJCWATM-PYGJLNRPSA-N vinorelbine ditartrate Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.OC(=O)[C@H](O)[C@@H](O)C(O)=O.C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC CILBMBUYJCWATM-PYGJLNRPSA-N 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000011345 viscous material Substances 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 229940053867 xeloda Drugs 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
- A61K31/5517—1,4-Benzodiazepines, e.g. diazepam or clozapine condensed with five-membered rings having nitrogen as a ring hetero atom, e.g. imidazobenzodiazepines, triazolam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6867—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from a cell of a blood cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6807—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug or compound being a sugar, nucleoside, nucleotide, nucleic acid, e.g. RNA antisense
- A61K47/6809—Antibiotics, e.g. antitumor antibiotics anthracyclins, adriamycin, doxorubicin or daunomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6875—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody being a hybrid immunoglobulin
- A61K47/6877—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody being a hybrid immunoglobulin the antibody being an immunoglobulin containing regions, domains or residues from different species
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- Organic Chemistry (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 항-CD22 항체와 면역접합체 그리고 이를 이용하는 방법을 제시한다.
Description
본 발명은 항-CD22 항체를 포함하는 면역접합체(immunoconjucates) 및 이를 이용하는 방법들에 관계된다.
B-세포항원, 이를 테면 CD19, CD22, 및 CD52는 임파종 치료를 위한 치료 가능성 표적을 나타낸다(Grillo-Lopez A.J. et al., Curr Pharm Biotechnol, 2:301-11, (2011). CD22는 분화의 성숙 단계에서만 오직 B-세포 표면상에서 발현되는 135-kDa B-세포-제한된 시알로당단백질이다(Dorken, B. et al., J. Immunol. 136:4470-4479(1986)). 인간에서 CD22의 주요 형태는 세포밖 도메인에 7개 면역글로블린 슈퍼패밀리 도메인이 포함된 CD22베타이다(Wilson, G.L. et al., J. Exp. Med. 173:137-146 (1991)). 변이 형태, CD22 알파는 면역글로블린 슈퍼패밀리 도메인 3 및 4가 부족하다(Stamenkovic, I. and Seed, B., Nature 345:74-77 (1990)). 인간 CD22에 리간드-결합은 면역글로블린 슈퍼패밀리 도메인 1과 2 (또한 에피토프 1과 2라고도 불림)와 연관된 것으로 나타났다(Engel, P. et al., J. Exp. Med. 181:1581-1586, 1995).
B 세포-관련된 장애는 악성 임파종 (비-호지킨(Hodgkin) 임파종, NHL), 다발성 골수종, 그리고 만성 림프모구 백혈병 (CLL, B 세포 백혈병 (CD5+ B 림프구)을 포함하나 이에 한정되지 않는다. B 림프구로부터 주로 발생되는 이질성 암 집단인 비-호지킨 임파종(NHLs)은 새로 진단을 받은 모든 암의 대략적으로 4%를 나타낸다( Jemal, A. et al., CA-Cancer J Clin, 52: 23-47, (2002)). 공격적인 NHL은 성인 NHL의 대략적으로 30 - 40%를 포함하고(Harris, N.L. et al., Hematol. J. 1:53-66 (2001)) 미만성 거대 B-세포 임파종 (DLBCL), 맨틀 세포 임파종 (MCL), 말초 T-세포 임파종, 그리고 역형성 거대 세포 임파종을 포함한다. 프론트라인 복합 화학요법은 공격성 NHL 환자의 절반도 치료하지 못하고, 대부분 환자들은 결국 이들의 병에 굴복하게 된다(Fisher, R.I. Semin. Oncol. 27(suppl 12): 2-8 (2000)).
B-세포 NHL에서, CD22 발현은 공격적 집단과 무기력 집단에서 각각 91% 내지 99% 범위에 이른다(Cesano, A. et al., Blood 100:350a(2002)). CD22는 B-세포 활성화 복합체의 성분 (Sato, S. et al., Semin. Immunol. 10:287-296 (1998)) 그리고 흡착 분자(Engl, Pl t al., Immunol. 150:4719-4732(1993))로써 모두 기능을 할 수 있다. CD22-결함 마우스의 B 세포들은 더 짧아진 수명과 강화된 세포자가사멸을 가지며, 이는 B-세포 생존에서 이 항원의 역할을 제안한다 (Otipoby, K.L. et al., Nature (Lond) 384:634-637(1996)). 이의 천연 리간드(들) 또는 항체와 결합된 후, CD22는 신속하게 내화되며(internalized), 주요 B 세포와 신형성 B 세포에서 전-자가사멸성 신호에서 공동-자극 신호를 제공한다(Sato, S. et al., Immunity 5:551-562(1996)).
CD22-연합된 상태, 이를 테면 암의 진단 및 치료를 위하여 CD22를 표적으로 하는 물질이 당업계에서 요구된다. 본 발명은 이러한 수요를 충족시키고, 다른 장점들도 제공한다.
발명의 요약
본 발명은 항-CD22 항체 및 면역접합체 그리고 이를 이용하는 방법들을 제시한다.
일부 구체예들에 있어서, 세포독성 물질에 공유적으로 부착된 CD22에 결합되는 항체를 포함하는 면역접합체가 제공되며, 이때 상기 항체는 서열 번호: 28의 아미노산 20 내지 240 안에 있는 에피토프에 결합된다. 일부 구체예들에 있어서, 상기 세포독성 물질은 피롤로벤조디아제핀이다.
일부 구체예들에 있어서, 상기 항체는 (i) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3, (ii) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3, 그리고 (iii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2를 포함한다. 일부 구체예들에 있어서, 상기 항체는 (i) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2, 그리고 (iii) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3을 포함한다. 일부 구체예들에 있어서, 상기 항체는 다음을 포함한다: a) (i) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3, (iv) 서열 번호: 12 그리고 15 내지 22의 아미노산 서열로부터 선택된 아미노산 서열을 포함하는 HVR-L1, (v) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2 그리고 (vi) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3, 또는 b) (i) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3, (iv) 서열 번호: 15의 아미노산 서열을 포함하는 HVR-L1, (v) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2, 그리고 (vi) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3. 일부 구체예들에 있어서, 상기 항체는 다음을 포함한다: a) (i) 서열 번호: 12 그리고 15 내지 22로부터 선택된 아미노산 서열을 포함하는 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2, 그리고 (iii) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3; 또는 b) (i) 서열 번호: 15의 아미노산 서열을 포함하는 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2, 그리고 (iii) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3. 일부 구체예들에 있어서, 상기 항체는 다음을 포함한다: a) 서열 번호: 7의 아미노산 서열에 최소한 95% 서열 동일성을 보유하는 VH 서열; 또는 b) 서열 번호: 8의 아미노산 서열에 최소한 95% 서열 동일성을 보유하는 VL 서열; 또는 c) (a)에서와 같은 VH 서열 그리고 (b)에서와 같은 VL 서열. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 7의 아미노산 서열을 보유하는 VH 서열을 포함한다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 6의 아미노산 서열을 보유하는 VL 서열 또는 서열 번호: 8의 아미노산 서열을 보유하는 VL 서열을 포함한다. 일부 구체예들에 있어서, 상기 항체는 IgG1, IgG2a 또는 IgG2b 항체다.
일부 구체예들에 있어서, 세포독성 물질에 공유적으로 부착된 CD22에 결합되는 항체를 포함하는 면역접합체가 제공되며, 이때 상기 항체는 (a) 서열 번호: 7의 아미노산 서열을 보유하는 VH 서열과 서열 번호: 8의 아미노산 서열을 보유하는 VL 서열을 포함하며, 그리고 이때 상기 세포독성 물질은 피롤로벤조디아제핀이다.
일부 구체예들에 있어서, 상기 면역접합체는 식(formula) Ab-(L-D)p를 보유하며, 이때: (a) Ab는 항체이며; (b) L은 링커이며; (c) D는 세포독성 물질이며; 그리고 (d) p는 1-8이다. 이러한 일부 구체예들에 있어서, D는 화학식 A의 피롤로벤조디아제핀이다:
이때 점선은 C1과 C2 또는 C2와 C3 사이에 이중 결합의 임의선택적 존재를 나타내며;
R2는 H, OH, =O, =CH2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R 그리고 COR로부터 독립적으로 선택되며, 그리고 할로 또는 디할로로부터 임의선택적으로 더 선택되며, 이때 RD는 R, CO2R, COR, CHO, CO2H, 그리고 할로로부터 독립적으로 선택되며;
R6과 R9는 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
R7은 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
Q는 O, S 그리고 NH로부터 독립적으로 선택되며;
R11은 H, 또는 R이거나 또는, Q가 O일 때, SO3M이며, 여기에서 M은 금속 양이온이고;
R 및 R'는 임의선택적으로 치환된 C1-8 알킬, C3-8 헤테로시클일 그리고 C5-20 아릴 기로부터 각각 독립적으로 선택되며, 그리고 NRR'기와 관련하여 임의선택적으로, R 및 R'는 이들에 부착된 질소 원자와 함께 임의선택적으로 치환된 4-, 5-, 6- 또는 7-원(membered) 헤테로사이클 고리를 형성하고;
R12, R16, R19 및 R17은 R2, R6, R9 및 R7에 대해 차례로 정의된 바와 같고;
R″는 C3-12 알킬렌 기이며, 이의 쇄는 하나 또는 그 이상의 이형원자 및/또는 임의선택적으로 치환된 방향족 고리에 의해 차단될 수 있으며; 그리고
X와 X'는 O, S 그리고 N(H)로부터 독립적으로 선택된다.
일부 구체예들에 있어서, D는 하기 구조를 가진다:
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, D는 다음에서 선택된 구조를 가진다:
이때 RE 및 RE"는 H 또는 RD로부터 각각 독립적으로 선택되며, 이때 RD 는 R, CO2R, COR, CHO, CO2H, 그리고 할로로부터 독립적으로 선택되며;
이때 Ar1 및 Ar2는 각각 임의선택적으로 치환된 C5-20 아릴이며; 그리고
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, D는 구조식 B의 피롤로벤조디아제핀이다:
이때 수평 파동선은 링커에 공유적 부착 부위를 나타내고;
RV1 및 RV2는 H, 메틸, 에틸, 페닐, 플루오로-치환된 페닐, 그리고 C5-6 헤테로시클일로부터 독립적으로 선택되며; 그리고
n은 0 또는 1이다.
일부 구체예들에 있어서, 상기 면역접합체는 프로테아제에 의해 절단가능한 링커를 포함한다. 이러한 일부 구체예들에 있어서, 상기 링커는 val-cit 이펩티드 또는 Phe-homoLys 이펩티드를 포함한다. 일부 구체예들에 있어서, 면역접합체는 다음 식을 가진다:
일부 구체예들에 있어서, p는 1-3이다.
일부 구체예들에 있어서, 상기 면역접합체는 하기 구조를 포함한다:
이때 CBA는 항체 (Ab)를 나타낸다. 일부 구체예들에 있어서, RL1 및 RL2는각각 H와 메틸로부터 독립적으로 선택되며, 또는 이들이 결합된 탄소원자와 함께 시클로프로필렌 기를 형성한다. 일부 구체예들에 있어서, Y는 단일 결합, (a1), 그리고 (a2)으로부터 선택된다:
이때 N은 상기 기(group)가 PBD 모이어티의 N10에 결합됨을 보여준다.
일부 구체예들에 있어서, 상기 면역접합체는 다음으로부터 선택된 구조를 포함한다:
일부 구체예들에 있어서, 상기 면역접합체는 다음의 구조를 포함한다:
이때 RE 및 RE"는 각각 H 및 RD로부터 독립적으로 선택된다.
일부 구체예들에 있어서, 상기 면역접합체는 다음 구조를 포함한다:
이때 Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 C5-20 아릴이다. 일부 구체예들에 있어서, Ar1 및 Ar2는 임의선택적으로 치환된 페닐, 퓨라닐, 티오페닐 그리고 피리딜로부터 각각 독립적으로 선택된다.
일부 구체예들에 있어서, 상기 면역접합체는 다음 구조를 포함한다:
이때 RV1 및 RV2는 H, 메틸, 에틸, 임의선택적으로 치환된 페닐, 그리고 C5-6 헤테로시클일로부터 각각 독립적으로 선택된다. 일부 구체예들에 있어서, RV1 및 RV2는 H, 페닐, 그리고 4-플루오로페닐로부터 각각 독립적으로 선택된다.
일부 구체예들에 있어서, 다음으로부터 선택된 화학식을 가지는 면역접합체가 제공된다:
이때 Ab는 (i) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3, (iv) 서열 번호: 15의 아미노산 서열을 포함하는 HVR-L1, (v) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2 그리고 (vi) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3을 포함하는 항체이며; 그리고 이때 p는 1 내지 3이다.
일부 구체예들에 있어서, 면역접합체가 제공되며, 이때 상기 면역접합체는 다음 화학식을 보유한다:
이때 Ab는 (i) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3, (iv) 서열 번호: 15의 아미노산 서열을 포함하는 HVR-L1, (v) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2, 그리고 (vi) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3을 포함하는 항체이며; 그리고 이때 p는 1 내지 3이다. 이러한 일부 구체예들에 있어서, 상기 항체는 서열 번호: 7의 아미노산 서열을 보유하는 VH 서열 그리고 서열 번호: 8의 아미노산 서열을 보유하는 VL 서열을 포함한다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 26의 중쇄와 서열 번호: 23의 경쇄를 포함한다.
본 명세서에서 논의된 임의의 구체예들에 있어서, 상기 항체는 단클론 항체일 수 있다. 일부 구체예들에 있어서, 상기 항체는 인간, 인간화된, 또는 키메라 항체다. 일부 구체예들에 있어서, 상기 항체는 CD22에 결합하는 항체 단편이다. 일부 구체예들에 있어서, 상기 항체는 인간 CD22에 결합한다. 이러한 일부 구체예들에 있어서, 인간 CD22는 서열 번호: 28 또는 서열 번호: 29의 서열을 보유한다.
일부 구체예들에 있어서, 약학 제제(formulation)가 제공되며, 이때 제제는 본 명세서에서 설명된 면역접합체와 약학적으로 수용가능한 운반체를 포함한다. 일부 구체예들에 있어서, 이 약학 제제는 추가 치료제를 포함한다.
일부 구체예들에 있어서, CD22-양성 암에 걸린 개체를 치료하는 방법들이 제시된다. 일부 구체예들에 있어서, 이 방법은 본 명세서에서 설명된 면역접합체의 유효량을 상기 개체에 투여하는 것을 포함한다. 일부 구체예들에 있어서, CD22-양성 암은 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포 백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷(Burkitt) 임파종, 그리고 맨틀 세포 임파종으로부터 선택된다. 일부 구체예들에 있어서, 이 방법은 상기 개체에게 추가 치료물질을 투여하는 것을 더 포함한다. 이러한 일부 구체예들에 있어서, 추가 치료물질은 CD79b에 결합하는 항체를 포함한다. 일부 구체예들에 있어서, 추가 치료물질은 세포독성 물질에 공유적으로 부착된 CD79b에 결합되는 항체가 포함된 면역접합체다.
일부 구체예들에 있어서, CD22-양성 세포의 증식을 저해시키는 방법이 제시된다. 이러한 일부 구체예들에 있어서, 이 방법은 세포 표면 상에서 CD22에 상기 면역접합체의 결합을 허용하는 조건하에서 본 명세서에서 설명된 면역접합체에 세포를 노출시키고, 이로 인하여 이 세포의 증식이 억제되는 것을 포함한다. 일부 구체예들에 있어서, 이 세포는 신생물 B 세포다. 일부 구체예들에 있어서, 이 세포는 임파종 세포다.
도 1a-1b: 도 1a는 인간 하위군 III 서열과 나란히 배열된, 뮤린 10F4 항-CD22 항체 (m10F4)의 중쇄 가변 영역, 인간화된 10F4 버젼 1 (hu10F4v1) 중쇄 가변 영역 그리고 인간화된 10F4 버젼 3 (hu10F4v3) 중쇄 가변 영역의 아미노산 서열들을 나타낸다. HVRs들은 네모상자로 표시된다(HVR-H1, HVR-H2, HVR-H3). HVRs을 묶는 서열은 골격 서열 (FR-H1 내지 FR-H4)이다. Kabat 넘버링에 따라 서열에 번호가 부여된다. Kabat, Chothia, 그리고 접촉 CDRs은 상자로 표시된 HVRs 부근에 표시된다. 도 1b는 인간 카파 I 서열과 나란하게 배열된, 뮤린 10F4 항-CD22 항체 (m10F4)의 경쇄 가변 영역, 인간화된 10F4 버젼 1 (hu10F4v1) 경쇄 가변 영역 그리고 인간화된 10F4 버젼 3 (hu10F4v3) 경쇄 가변 영역의 아미노산 서열들을 나타낸다. 상기 항체 hu10F4v3은 HVR-L1 (N28V)의 아미노산 28에서 hu10F4v1과 상이하다. HVRs들은 네모상자로 표시된다. FR-L1, FR-L2, FR-L3, 그리고 FR-L4 서열은 HVRs (HVR-L1, HVR-L2, HVR-L3)를 묶는다. Kabat 넘버링에 따라 서열에 번호가 부여된다. Kabat, Chothia, 그리고 접촉 CDRs은 상자로 표시된 HVRs 부근에 표시된다.
도 2는 IgG1의 이소타입인 인간화된 항-CD22 항체 10F4v3의 경쇄 및 중쇄의 전장 아미노산 서열(가변 및 불변 영역)을 나타낸다. 밑줄 부분은 불변 도메인들이다.
도 3은 항-CD22 시스테인 조작된(engineered) 항체의 아미노산 서열을 나타내는데, 이때 경쇄 또는 중쇄 또는 Fc 영역은 선택된 아미노산 위치들에서 아미노산이 시스테인으로 대체되어 변경된다. 제시된 시스테인 조작된 이러한 항체는 Kabat 위치 205에서 발린(서열 위치 발린 210)은 시스테인으로 변경된 항-CD22 10F4 변이 경쇄("항-CD22 V205C h10Fv3 시스테인 조작된 경쇄"); EU 위치 118 (서열 위치 알라닌 121)에서 알라닌이 시스테인으로 변경된 항-CD22 10F4 변이 중쇄("항-CD22 A118C h10Fv3 시스테인 조작된 중쇄"); 그리고 EU 위치 400 (서열 위치 세린 403)에서 세린이 시스테인으로 변경된 항-CD22 10F4 변이 Fc 영역 ("항-CD22 S400C h10Fv3 시스테인 조작된 Fc 영역")을 포함한다. 각 도면에서, 변경된 아미노산은 두 줄 밑줄이 쳐진 굵은 글씨로 나타낸다. 한줄 밑줄은 불변 영역을 나타낸다. 가변 영역들은 밑줄이 없다.
도 4는 실시예 A에서 설명되는 (A) 10F4v3-PBD, (B) 10F4v3-SS-PBD, 그리고 (C) 10F4v3-SSMe-PBD의 링커 및 약물 구조를 나타낸다.
도 5는 실시예 B에서 설명된, WSU-DLCL2 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 6은 실시예 C에서 설명된, Granta-519 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 7은 실시예 D에서 설명된, SuDHL4-luc 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 8은 실시예 E에서 설명된, SuDHL4-luc 마우스 이종이식편 모델에서 10F4v3-PBD에 의한 종양 성장의 약량-의존성 저해를 나타낸다.
도 9는 실시예 F에서 설명된, Bjab-luc 마우스 이종이식편 모델에서 10F4v3-PBD에 의한 종양 성장의 약량-의존성 저해를 나타낸다.
도 10은 실시예 G에서 설명된, WSU-DLCL2 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 보여준다.
도 2는 IgG1의 이소타입인 인간화된 항-CD22 항체 10F4v3의 경쇄 및 중쇄의 전장 아미노산 서열(가변 및 불변 영역)을 나타낸다. 밑줄 부분은 불변 도메인들이다.
도 3은 항-CD22 시스테인 조작된(engineered) 항체의 아미노산 서열을 나타내는데, 이때 경쇄 또는 중쇄 또는 Fc 영역은 선택된 아미노산 위치들에서 아미노산이 시스테인으로 대체되어 변경된다. 제시된 시스테인 조작된 이러한 항체는 Kabat 위치 205에서 발린(서열 위치 발린 210)은 시스테인으로 변경된 항-CD22 10F4 변이 경쇄("항-CD22 V205C h10Fv3 시스테인 조작된 경쇄"); EU 위치 118 (서열 위치 알라닌 121)에서 알라닌이 시스테인으로 변경된 항-CD22 10F4 변이 중쇄("항-CD22 A118C h10Fv3 시스테인 조작된 중쇄"); 그리고 EU 위치 400 (서열 위치 세린 403)에서 세린이 시스테인으로 변경된 항-CD22 10F4 변이 Fc 영역 ("항-CD22 S400C h10Fv3 시스테인 조작된 Fc 영역")을 포함한다. 각 도면에서, 변경된 아미노산은 두 줄 밑줄이 쳐진 굵은 글씨로 나타낸다. 한줄 밑줄은 불변 영역을 나타낸다. 가변 영역들은 밑줄이 없다.
도 4는 실시예 A에서 설명되는 (A) 10F4v3-PBD, (B) 10F4v3-SS-PBD, 그리고 (C) 10F4v3-SSMe-PBD의 링커 및 약물 구조를 나타낸다.
도 5는 실시예 B에서 설명된, WSU-DLCL2 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 6은 실시예 C에서 설명된, Granta-519 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 7은 실시예 D에서 설명된, SuDHL4-luc 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 나타낸다.
도 8은 실시예 E에서 설명된, SuDHL4-luc 마우스 이종이식편 모델에서 10F4v3-PBD에 의한 종양 성장의 약량-의존성 저해를 나타낸다.
도 9는 실시예 F에서 설명된, Bjab-luc 마우스 이종이식편 모델에서 10F4v3-PBD에 의한 종양 성장의 약량-의존성 저해를 나타낸다.
도 10은 실시예 G에서 설명된, WSU-DLCL2 마우스 이종이식편 모델에서 다양한 항체-약물 접합체의 효과를 보여준다.
I. 정의
본 명세서의 목적을 위한 "수용자 인간 골격(acceptor human framework)"이란 하기에서 정의된 바와 같이, 인간 면역글로블린 골격으로부터 유도된 경쇄 가변 도메인 (VL) 골격 또는 중쇄 가변 도메인 (VH) 골격의 아미노산 서열이 포함된 골격 또는 인간 공통(consensus) 골격이다. 인간 면역글로블린 골격 또는 인간 공통 골격"으로부터 유도된 "수용자 인간 골격은 이의 동일한 아미노산 서열을 포함할 수 있거나, 또는 아미노산 서열 변화를 포함할 수 있다. 일부 구체예들에 있어서, 아미노산 변화 수는 10 또는 그 미만, 9 또는 그 미만, 8 또는 그 미만, 7 또는 그 미만, 6 또는 그 미만, 5 또는 그 미만, 4 또는 그 미만, 3 또는 그 미만, 또는 2 또는 그 미만이 된다. 일부 구체예들에 있어서, VL 수용자 인간 골격은 VL 인간 면역글로블린 골격 서열 또는 인간 공통 골격 서열에 대해 서열이 동일하다.
"친화력(Affinity)"은 한 분자(예컨데, 항체)의 단일 결합 부위와 이의 결합 짝 (예컨데, 항원) 사이의 비공유 상호작용의 총 강도를 말한다. 다른 언급이 없는 한, 본 명세서에서 사용된 바와 같이, "결합 친화력"은 결합 쌍(예컨데, 항체와 항원)의 구성요소 간 1:1 상호작용을 반영하는 고유의 결합 친화력을 말한다. 분자 X가 이의 짝 Y에 대한 친화력은 일반적으로 해리 상수 (Kd)로 나타낼 수 있다. 친화력은 본 명세서에서 설명된 것들을 포함하여 당업계에 공지된 통상적인 방법들에 의해 측정될 수 있다. 결합 친화력을 측정하는 특정한 설명된 예시적인 구체예들은 다음에서 기술된다.
"친화력 숙성된(matured)" 항체란 하나 또는 그 이상의 초가변 영역 (HVRs)내 하나 또는 그 이상의 변경을 보유하여, 이러한 변경이 없는 부모 항체와 비교하였을 때, 이러한 변경이 항원에 대한 상기 항체의 친화력을 개선시키게 만드는, 항체를 지칭한다.
용어 "항-CD22 항체" 그리고 "CD22에 결합하는 항체"란 충분한 친화력으로 CD22에 결합할 수 있는 항체를 말하며, 이러한 항체는 CD22를 표적으로 하는 진단 및/또는 치료 물질로 유용하다. 한 구체예에 있어서, 무관한, 비-CD22 단백질에 대한 항-CD22 항체의 결합 정도는 예컨데, 방사능면역분석 (RIA)에 의해 측정되었을 때 CD22에 대한 상기 항체의 결합의 약 10% 미만이 된다. 특정 구체예들에 있어서, CD22에 결합하는 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, , ≤ 5 Nm, , ≤ 4 nM, , ≤ 3 nM, , ≤ 2 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM (예컨데, 10-8 M 또는 그 미만, 예컨데 10-8 M 내지 10-13 M, 예컨데, 10-9 M 내지 10-13 M)의 해리 상수 (Kd)를 가진다. 특정 구체예들에 있어서, 항-CD22 항체는 상이한 종간에 CD22 가운데 보존된 CD22의 에피토프에 결합한다.
용어 "항체"는 광범위한 의미에서 본 명세서에서 이용되는데, 단클론 항체, 다클론 항체, 다중특이적 항체 (예컨데, 이중특이적 항체), 그리고 바람직한 항원-결합 활성을 나타내는 항체 단편들을 포함하나 이에 한정되지 않는 다양한 항체 구조들이 포괄된다.
"항체 단편"은 고유한 항체의 일부분이 포함된, 그리고 고유한 항체가 결합하는 항원에 결합하는 고유한 항체가 아닌 분자를 지칭한다. 항체 단편의 예로는 Fv, Fab, Fab', Fab'-SH, F(ab')2; 디아바디(diabodies); 선형 항체; 단일-쇄 항체 분자(예컨데 scFv); 그리고 항체 단편들로부터 형성된 다중특이적 항체들을 포함하나 이에 한정되지 않는다.
기준 항체로써, "동일한 에피토프에 결합하는 항체"는 경쟁 분석에서 기준 항체가 이의 항원에 결합하는 것을 50% 또는 그 이상으로 차단하는 항체를 지칭하고, 그리고 역으로, 기준 항체는 경쟁 분석에서 항체가 이의 항원에 결합하는 것을 50% 또는 그 이상으로 차단시킨다. 예시적인 경쟁 분석이 본 명세서에서 제시된다.
용어 "암" 및 "암의(cancerous)"란 통제안된 세포 성장/증식을 전형적으로 특징으로 하는 포유류의 생리학적 상태를 지칭하거나 또는 설명한다. 암의 예로는 흑색종, 암종, 임파종 (예컨데, 호지킨 및 비-호지킨 임파종), 아세포종, 육종, 그리고 백혈병을 포함하나 이에 한정되지 않는다. 좀더 구체적으로 암의 예로는 B-세포 연합된 암, 예로써, 고등급, 중등급 그리고 저등급의 임파종(B 세포 임파종 이를 테면, 예로써, 점막-연합된-림프 조직 B 세포 임파종 그리고 비-호지킨 임파종 (NHL), 맨틀 세포 임파종, 버킷 임파종, 소림프구성 임파종, 변연부 임파종, 미만성 거대 세포 임파종, 소포 임파종, 그리고 호지킨 임파종 그리고 T 세포 임파종을 포함) 그리고 백혈병(2차 백혈병, 만성 림프모구 백혈병 (CLL), 이를 테면 B 세포백혈병 (CD5+ B 림프구), 골수성 백혈병, 이를 테면 급성 골수성 백혈병, 만성 골수성 백혈병, 림프 백혈병, 이를 테면 급성 임파아구성 백혈병 (ALL) 그리고 골수이형성을 포함), 그리고 다른 조혈 및/또는 B 세포- 또는 T-세포-연합된 암을 포함한다. 다형핵 백혈구, 이를 테면 호염기성, 호산구, 호중구, 그리고 단세포, 수상돌기세포, 혈소판, 적혈구 그리고 천연 킬러 세포가 포함된 추가 조혈 세포의 암도 또한 포함된다. 다음에서 선택된 암성 B 세포 증식성 장애들이 또한 포함된다: 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 그리고맨틀 세포 임파종. B-세포암의 기원은 다음을 포함한다: 변연부, 소포 임파종 그리고 미만성 거대 B-세포 임파종에서 기억 B-세포에서 변연부 B-세포 임파종의 기원은 배중심의 밝은 영역에 있는 중심세포(centrocytes)에서 유래되고, 만성 림프모구 백혈병과 소임파성 백혈병은 B1 세포 (CD5+)에서 유래되고, 맨틀 세포 임파종은 맨틀 영역내 고유 B-세포에서 유래되고, 그리고 버킷 임파종은 배중심의 어두운 영역내 중심아세포에서 유래된다. 본 명세서에서 "조혈 세포 조직"으로 언급된 조혈 세포를 포함하는 조직은 흉선과 골수 그리고 말초 림프 조직, 이를 테면 비장, 림프절, 점막과 연합된 림프 조직, 이를 테면 장-연합된 림프 조직, 편도선, Peyer의 패취(patches) 그리고 맹장 그리고 다른 점막 조직과 연합된 림프 조직, 예로써, 기관지 내벽을 포함한다. 이러한 암의 추가 특정 예로는 편평 세포 암, 소(small)-세포 폐암, 비-소 세포 폐암, 폐의 선암, 폐의 편명 암종, 복막의 암, 간세포 암, 위장 암, 췌장 암, 신경교종, 경부암, 난소암, 간암, 방광암, 간종양, 유방암, 결장암, 결장직장암, 내막암 또는 자궁 암종, 타액선 암종, 신장암, 간암, 전립선암, 음문암, 갑상선암, 간의 암종, 백혈병 그리고 다른 임파증식성 장애, 그리고 다양한 유형의 두경부암을 포함한다.
본 명세서에서 "B-세포 악성"은 낮은 등급/소포 NHL, 소림프구성 (SL) NHL, 중간 등급/소포 NHL, 중간 등급 미만성 NHL, 높은 등급의 면역아세포 NHL, 높은 등급 임파아구성 NHL, 높은 등급 소(small) 비-절단된 세포 NHL, 거대 질환(bulky disease) NHL, 맨틀 세포 임파종, AIDS-관련된 임파종, 그리고 발덴스트롬 마크로글로불린혈증, 비-호지킨 임파종 (NHL), 림프구 현저 호지킨 질환(LPHD), 소림프구성 임파종 (SLL), 만성 림프모구 백혈병 (CLL), 재발된 무기력한 NHL 그리고 리투시맙(rituximab)-난치성 무기력한 NHL이 포함된 무기력한 NHL을 포함하는 비-호지킨 임파종 (NHL); 급성 임파아구성 백혈병 (ALL), 만성 림프모구 백혈병 (CLL), 털모양 세포 백혈병, 만성 골수아구성 백혈병을 포함하는 백혈병; 버킷 임파종; 맨틀 세포 임파종; 그리고 기타 혈액 악성을 포함한다. 이러한 악성은 B-세포 표면 지표, 이를 테면 CD22에 대하여 지향된 항체로 치료될 수 있다. 이러한 질환은 B 세포 표면 지표, 이를 테면 CD22에 대항하여 지향된 항체의 투여에 의해 치료되는 것으로 고려되며, 그리고 접합안된 ("네이키드(naked)") 항체 또는 본 명세서에서 공개된 세포독성 물질에 접합된 항체의 투여를 포함한다. 이러한 질환은 본 발명의 항-CD22 항체 또는 또다른 항체 또는 항체 약물 접합체, 또다른 세포 독성 물질, 방사능 또는 다른 치료와 병용하여 동시에 또는 연속적으로 본 발명의 항-CD22 항체 약물 접합체가 포함된 복합 요법에 의해 치료될 수 있는 것으로 고려된다. 예시적인 치료 방법에서, 항-CD22 면역접합체는 항-CD79b 항체, 면역글로블린, 또는 이의 CD79b 결합 단편과 복합되어 동시에 또는 순차적으로 투여된다. 항- CD79b 항체는 네이키드 항체 또는 항체 약물 접합체일 수 있다. 또다른 예시적인 치료 방법에서, 항-CD22 면역접합체는 항-CD20 항체, 면역글로블린, 또는 이의 CD20 결합 단편과 복합되어, 함께 또는 순차적으로 투여된다. 항-CD20 항체는 네이키드 항체 또는 항체 약물 접합체일 수 있다. 복합 요법의 일부 구체예들에 있어서, 항-CD22 면역접합체는 Rituxan® (리투시맙)과 함께 투여된다.
본원 명세서에서 이용된 바와 같이, 용어 "비-호지킨 임파종" 또는 "NHL"는 호지킨 임파종 이외의 임파계의 암을 지칭한다. 호지킨 임파종은 일반적으로 호지킨 임파종에서 Reed-Sternberg 세포의 존재와 비-호지킨 임파종에서 상기 세포들의 부재로 비-호지킨 임파종으로부터 구별될 수 있다. 본 명세서에서 이용된 이 용어에 포괄되는 비-호지킨 임파종의 예로는 당업계에 공지된 분류 체계 이를 테면 Revised European-American Lymphoma (REAL) scheme as described in Color Atlas of Clinical Hematology (3rd edition), A. Victor Hoffbrand and John E. Pettit (eds.) (Harcourt Publishers Ltd., 2000)에 따라 당업자(예컨대, 종양학자 또는 병리학자)에 의해 확인되는 임의의 것들을 포함한다. 특히, 도. 11.57, 11.58 그리고 11.59에 있는 목록 참고. 좀더 구체적인 예들은 재발된 또는 난치성 NHL, 프론트 라인 낮은 등급 NHL, 단계 III/IV NHL, 화학요법 저항성 NHL, 전구물질 B 임파아구성 백혈병 및/또는 임파종, 소림프구성 임파종, B 세포만성 림프모구 백혈병 및/또는 전림프구 백혈병 및/또는 소림프구성 임파종, B-세포전림프구 임파종, 면역종 및/또는 림프구형질세포성 임파종, 림프구형질세포성 임파종, 변연부 B 세포 임파종, 비장의 변연부 임파종, 외부결절성 변연부 - MALT 임파종, 결절성 변연부 임파종, 털모양 세포백혈병, 형질구종 및/또는 혈장 세포 골수종, 낮은 등급/소포 임파종, 중간 등급/소포 NHL, 맨틀 세포 임파종, 여포 중심 임파종 (소포), 중간 등급 미만성 NHL, 미만성 거대 B-세포 임파종, 공격성 NHL (공격성 프론트-라인 NHL 및 공격성 재발된 NHL을 포함), 자가 줄기세포 이식 후 재발된 또는 자가줄기세포 이식에 대해 난치성 NHL, 원발성 종격동 거대 B-세포 임파종, 원발성 삼출액 임파종, 높은 등급 면역아세포 NHL, 높은 등급 임파아구성 NHL, 높은 등급 소(small) 비-절단된 세포NHL, 거대 질환(bulky disease) NHL, 버킷 임파종, 전구물질 (말초) 거대 과립 림프구 백혈병, 균상식육종 및/또는 세자리 증후군(Sezary syndrome), 피부(cutaneous) 임파종, 역형성 거대 세포 임파종, 혈관중심성 임파종을 포함하나 이에 한정되지 않는다.
용어 "키메라(chimeric)" 항체는 항체의 중쇄 및/또는 경쇄의 일부가 특정 원료 또는 종으로부터 유도되며, 중쇄 및/또는 경쇄의 나머지는 상이한 원료 또는 종으로부터 유도된 항체를 지칭한다.
항체의 "분류(class)"는 불변 도메인의 유형 또는 이의 중쇄가 보유하는 불변 영역의 유형을 지칭한다. 항체에는 5가지 주요 분류가 있다: IgA, IgD, IgE, IgG, 및 IgM, 그리고 이들중 일부는 하위분류(이소타입)으로 더 세분될 수 있는데, 예컨데, IgG1, IgG2, IgG3, IgG4, IgA1, 그리고 IgA2. 면역글로블린의 상이한 분류에 대응하는 중쇄 불변 도메인은 차례로 α, δ, ε, γ 그리고 μ로 불린다.
본 명세서에서 이용된 바와 같이, 용어 "세포독성 물질"은 세포 기능을 저해 또는 막거나 및/또는 세포 사멸 또는 파괴를 야기하는 물질을 지칭한다. 세포독성 물질은 방사능 동위원소(예컨데, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 그리고 Lu의 방사능활성 동위원소); 화학요법 물질 또는 약물 (예컨데, 메토트렉세이트, 아드리아마이신, 빈카 알칼로이드 (빈크리스틴, 빈블라스틴, 에토포시드), 옥소루비신, 멜파란, 미토마이신 C, 클로람부칠, 다우노루비친 또는 다른 삽입(intercalating) 물질); 성장 저해 물질; 효소 및 이의 단편들 이를 테면 핵산분해 효소; 항생제; 톡신 이를 테면, 세균, 곰팡이, 식물 또는 동물 기원의 소(small) 분자 톡신 또는 효소적으로 활성 톡신, 이의 단편 및/또는 변이 포함; 그리고 하기에서 논의되는 다양한 항종양 또는 항암 물질들을 포함하나 이에 한정되지 않는다.
"화학요법 물질"은 암의 치료에 유용한 화학 화합물이다. 화학요법 물질의 예로는 알킬화 물질, 이를 테면 티오테파 및 사이클로포스파미드 (CYTOXAN®); 알킬 술포네이트 이를 테면 부술판, 임프로술판 그리고 피포술판; 아지리딘 이를 테면 벤조도파, 칼보쿠온, 메투레도파, 그리고 우레도파; 에틸렌이민 그리고 알트레타민, 트리에틸렌멜라민, 트리에틸렌포스포라미드, 트리에틸렌티오포스포라미드 및 트리메틸로멜라민을 포함하는 메알아멜라민; 아세토게닌(특히 불라타신 및 불라타시논); 델타-9-테트라히드로카나비놀(드로나비놀, MARINOL®); 베타-라파촌; 라파촐; 콜치시넨; 베툴리닌산; 캄포테신(합성 유사체 토포테칸 포함(HYCAMTIN®), CPT-11 (이리도테칸, CAMPTOSAR®), 아세틸캄포테신, 스코포렉틴, 그리고 9-아미노캄포테신); 브리오스타틴; 칼리스타틴; CC-1065(이의 아도켈레신, 카르젤레신 및 비젤레신 합성 유사체 포함); 포도필라톡신; 포도필린산; 테니포시드; 크립토피신 (특히 크립토피신 1과 크립토피신 8); 도라스태틴; 듀오카르마이신 (합성 유사체 포함, KW-2189 및 CB1-TM1); 에루테로빈; 판크라티스태틴; 사르코딕틴; 스폰기스태틴; 질소 무스타드, 이를 테면 클로람부칠, 클로르나파진, 클로로포스파미드, 에스트라무스틴, 이포스파미드, 메클로레타민, 메클로레타민 옥스드 히드로클로라이드, 멜파란, 노벰비친, 페네스테린, 프레디니무스틴, 트로포스파미드, 우라실 무스타드; 니트로소우레아 이를 테면 카르무스틴, 클로로조토신, 포테무스틴, 로무스틴, 니무스틴, 그리고 라님무스틴; 항생제 이를 테면 에네디네(enediyne) 항생제 (가령, 칼리케아미, 특히 칼리케아미신 감마 1I 그리고 칼리케아미신 오메가 I1 (예컨데, Agnew, Chem Intl. Ed. Engl., 33: 183-186 (1994) 참조); 디네미신 A를 포함하는 디네미신; 에스페라미신; 뿐만 아니라 네오카르지노스태틴 발색단 그리고 관련된 색소단백질 에네디네 항생제 발색단), 아클라시노미신, 악티노마이신, 아우트라마이신, 아자세린, 블레오마이신, 카티노마이신, 카라비신, 카르미노마이신, 카르지노필린, 크로모미신, 닥티노마이신, 다우노루비친, 데토루비신, 6-디아조-5-옥소-L-노르류신, 옥소루비신 (몰포리노-옥소루비신, 시아노몰포리노-옥소루비신, 2-피롤리노-옥소루비신 그리고 데옥시옥소루비신을 포함), 에피루비신, 에소르루비신, 이다루비신, 마르셀로마이신, 미토마이신 이를 테면 미토마이신 C, 미코페놀산, 노갈라마이신, 올리보마이신, 페플로마이신, 포르피로마이신, 퓨로마이신, 퀘라마이신, 로도루비신, 스트렙토니그린, 스트렙조신, 부베르시딘, 우베니멕스, 지노스태틴, 조루비신; 항-대사물질 이를 테면 메토트렉세이트 및 5-플루오로우라실 (5-FU); 엽산 유사체 이를 테면 데노프테린, 메토트렉세이트, 테로프테린, 트렘트렉세이트; 퓨린 유사체 이를 테면 플루다라빈, 6-멀캅토퓨린, 티아미프린, 티오구아닌; 피리미딘 유사체 이를 테면 안시타빈, 아자시티빈, 6-아자우리딘, 카르보푸르, 시타라빈, 디데옥시우리딘, 독시플루리딘, 에노시타빈, 플록우리딘; 그리고로겐 이를 테면 칼루스테론, 드로모스타놀론 프로피오네이트, 에피티오스타놀, 메피티오스탄, 테스톨락톤; 항-아드레날 이를 테면 아미노글루테티미드, 미토탄, 트리로스탄; 엽산 보충물 이를 테면 프로리닌산; 아세갈톤; 알도포스파미드 글리코시드; 아미노레불리닌산; 에니루라실; 암사크린; 베스트라부칠; 비산트렌; 에다트락세이트; 데포파민; 데메콜친; 디아지퀴논; 엘포르니틴; 엘리프티니움 아세테이트; 에포티론; 에토글루시드; 갈리늄 니트레이트; 히드록시우레아; 렌티난; 로니다닌; 메이탄시노이드 이를 테면 메이탄신 및 안사미토신; 미토구아존; 미토산트론; 모피단몰; 니트라에린; 펜토스태틴; 페나메트; 피라루비친; 로스옥산트론; 2-에틸히드라지드; 프로카르바진; PSK® 폴리사카라이드 복합체 (JHS Natural Products, Eugene, OR); 라족산; 리조신; 시조피란; 스피로게르마니움; 테나우아존산; 트리아지퀴온; 2,2',2"-트리클로로트리에틸아민; 트리초테센(특히 T-2 톡신, 베라쿠린 A, 로리딘 A 및 아구니딘); 우레탄; 벤데신(ELDISINE®, FILDESIN®); 다크라바진; 만노무스틴; 미토브로니톨; 미토락톨; 피포브로만; 가시토신; 아라비노시드 ("Ara-C"); 티오테파; 탁소이드, 예컨데, 파클리탁셀(TAXOL®; Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANETM Cremophor-프리, 파클리탁셀의 알부민-조작된 나노입자 제제(American Pharmaceutical Partners, Schaumberg, Illinois), 그리고 도세탁셀 (TAXOTERE®; Rhne-Poulenc Rorer, Antony, France); 클로라부칠; 겜시타빈(GEMZAR®); 6-티오구아닌; 멀캅토퓨린; 메토트렉세이트; 플라티늄 유사체 이를 테면 시스플라틴과 카르보플라틴; 빈블라스틴 (VELBAN®); 플라티늄; 에토포시드 (VP-16); 이포스파미드; 미톡산트론; 빈크리스틴 (ONCOVIN®); 옥살리플라틴; 류코보빈; 비노렐빈(NAVELBINE®); 노반트론; 에다트렉세이트; 다우노마이신; 아미노프테린; 이반드로네이트; 토포이소메라제 저해제 RFS 2000; 디플루오로메틸오르니틴(DMFO); 레티노이드 이를 테면 레티논산; 카페시타빈(XELODA®); 상기중 임의의 것의 약학적으로 수용가능한 염, 산 또는 유도체; 뿐만 아니라 상기의 2개 또는 그 이상의 조합 이를 테면 CHOP, 사이클로포스파미드, 옥소루비신, 빈크리스틴, 그리고 프레디솔론의 복합 치료제의 약어; CVP, 사이클로포스파미드, 빈크리스틴, 그리고 프레디솔론의 복합 치료제의 약어; 그리고 FOLFOX, 옥살리플라틴 (ELOXATINTM)과 5-FU 및루코보린이 복합된 치료 섭생의 약어를 포함한다.
"작용기 (Effector) 기능"이란 항체의 Fc 영역에 기여하는 생물학적 활성을 지칭하는데, 상기 항체 이소타입에 따라 변화된다. 항체 작용기 기능의 예로는 다음을 포함한다; C1q 결합 및 보체 의존적 세포독성 (CDC); Fc 수용체 결합; 항체-의존적 세포-중개된 세포독성 (ADCC); 식작용; 세포표면 수용체 (예컨데 B 세포 수용체)의 하향 조절; 그리고 B 세포 활성화.
물질, 예컨데, 약학 제제의 "유효량"이란 바람직한 치료 또는 예방 결과를 획득하기 위하여 필요한 약량 및 시간 동안 효과적인 양을 지칭한다.
용어 "에피토프"는 항체가 결합되는 항원 분자상의 특정 부위를 말한다.
본원 명세서에서 용어 "Fc 영역"은 불변 영역의 최소한 일부분이 포함된 면역글로블린 중쇄의 C-말단 영역을 정의하는데 이용된다. 이 용어는 고유한 서열 Fc 영역과 변이 Fc 영역을 포함한다. 한 구체예에 있어서, 인간 IgG 중쇄 Fc 영역은 Cys226, 또는 Pro230으로부터 중쇄의 카르복시-말단까지 이어진다. 그러나, Fc 영역의 C-말단 리신 (Lys447)은 존재할 수 있거나 또는 존재하지 않을 수 있다. 본 명세서에서 특별히 언급되지 않는 한, Fc 영역 또는 불변 영역에서 아미노산 잔기의 번호 매김은 Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991에서 설명된 것과 같이 EU 색인이라고도 불리는 EU 넘버링 체계에 따른다.
"골격(Framework)" 또는 "FR"은 초가변 영역 (HVR) 잔기이외의 가변 도메인 잔기를 지칭한다. 가변 도메인의 FR은 4개의 FR 도메인들: FR1, FR2, FR3, 그리고 FR4로 구성된다. 따라서, HVR 및 FR 서열은 일반적으로 VH (또는 VL)에서 다음의 서열로 나타난다: FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
용어 "전장(full length) 항체", "고유한 항체" 그리고 "전체 항체"는 본 명세서에서 서로 호환되며, 고유한 항체 구조에 실질적으로 유사한 구조를 가지는 항체 또는 본 명세서에서 정의된 바와 같이 Fc 영역이 포함된 중쇄를 보유하는 항체를 지칭한다.
용어 "CD22의 당화된 형태(glycosylated forms)"는 탄수화물 잔기의 추가에 의해 해독후 변형된 CD22의 자연 발생 형태를 지칭한다.
용어 "숙주 세포", "숙주 세포 계통", 그리고 "숙주 세포 배양물"은 호환되며, 외생 핵산이 도입된 세포를 지칭하며, 이러한 세포의 자손도 포함된다. 숙주 세포는 "형질변환체(transformants)" 및 "형질변환 세포"를 포함하는데, 이들은 1차 형질변환 세포와 계대수에 무관하게 이로부터 유도된 자손을 포함한다. 자손은 부모 세포와 핵산 함량에서 완전하게 일치하지 않을 수 있지만, 돌연변이를 포함할 수 있다. 원래 형질변환 세포에서 선별 또는 선택된 것과 동일한 기능 또는 생물학적 활성을 보유한 돌연변이 자손이 본 명세서에서 포함된다.
"인간 항체"는 인간 또는 인간 세포에 의해 생산된 항체 또는 인간 항체 레퍼토리를 이용하는 비-인간 원료 또는 다른 인간 항체-인코딩 서열로부터 유도된 항체의 것에 대응하는 아미노산 서열을 보유하는 항체다. 인간 항체의 이러한 정의에서 비-인간 항원-결합 잔기가 포함된 인간화된 항체는 특별히 배제된다.
"인간 공통 골격(human consensus framework)"은 인간 면역글로블린 VL 또는 VH 골격 서열의 선별에서 가장 흔하기 발생되는 아미노산 잔기를 나타내는 골격이다. 일반적으로, 인간 면역글로블린 VL 또는 VH 서열의 선별은 가변 도메인 서열들의 하위군(subgroup)로부터 한다. 일반적으로, 서열의 하위군은 Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols. 1-3에서 설명된 하위군이다. 한 구체예에 있어서, VL의 경우, 하위군은 Kabat et al., supra에서 설명된 것과 같은 카파 I 하위군이다. 한 구체예에 있어서, VH의 경우, 하위군은 Kabat et al., supra에서 설명된 것과 같은 하위군 III이다.
"인간화된(humanized)" 항체란 비-인간 HVRs의 아미노산 잔기와 인간 FRs의 아미노산 잔기가 포함된 키메라 항체를 지칭한다. 특정 구체예들에 있어서, 인간화된 항체는 최소한 하나, 그리고 전형적으로 2개의 가변 도메인들을 실질적으로 포함하는데, 이때 모든 또는 실질적으로 모든 HVRs (예컨데, CDRs)은 비-인간 항체의 것들에 대응되며, 그리고 모든 또는 실질적으로 모든 FRs은 인간 항체의 것에 대응된다. 인간화된 항체는 임의선택적으로 인간 항체로부터 유도된 항체 불변 영역의 최소한 일부분을 포함할 수 있다. 항체의 "인간화된 형태", 예컨데, 비-인간 항체는 인간화를 겪은 항체를 지칭한다.
본 명세서에서 이용된 바와 같이 용어 "초가변 영역" 또는 "HVR"은 서열에서 초가변적인 및/또는 구조적으로 특정된 루프("초가변 루프")를 만드는 항체 가변 도메인의 영역을 지칭한다. 일반적으로, 고유한 4개-쇄 항체는 6개의 HVRs를 포함하는데; VH에서 3개 (H1, H2, H3), 그리고 VL에서 3개 (L1, L2, L3). HVRs는 일반적으로 초가변 루프의 아미노산을 포함하거나 및/또는 "상보성 결정 영역" (CDRs)의 아미노산을 포함하는데, 후자의 경우 최대 서열 가변성이고 및/또는 항원 인식에 관련된다. 예시적인 초가변 루프는 아미노산 잔기 26-32 (L1), 50-52 (L2), 91-96 (L3), 26-32 (H1), 53-55 (H2), 그리고 96-101 (H3)에서 발생된다. (Chothia and Lesk, J. Mol. Biol. 196:901-917 (1987).) 예시적인 CDRs (CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2, 그리고 CDR-H3)은 L1의 아미노산 잔기 24-34, L2의 50-56, L3의 89-97, H1의 31-35B, H2의 50-65, 그리고 H3의 95-102에서 발생된다. (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991).) VH에서 CDR1를 제외하고, CDRs는 초가변 루프를 형성하는 아미노산 잔기를 일반적으로 포함한다. CDRs는 또한 "특이성 결정 잔기" 또는 "SDRs"를 포함하는데, 이것은 항원과 접촉되는 잔기들이다. SDRs는 단축된(abbreviated)-CDRs, 또는 a-CDRs로 불리는 CDRs의 영역내에 포함된다. 예시적인 a-CDRs (a-CDR-L1, a-CDR-L2, a-CDR-L3, a-CDR-H1, a-CDR-H2, 그리고 a-CDR-H3)는 L1의 아미노산 잔기 31-34, L2의 50-55, L3의 89-96, H1의 31-35B, H2의 50-58, 그리고 H3의 95-102에서 발생된다. (Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008).) 다른 언급이 없는 한, 가변 도메인에서 HVR 잔기 및 잔기들(예컨데, FR 잔기)는 Kabat et al., supra에 따라 번호매김된다.
"면역접합체"는 세포독성 물질을 포함하나 이에 한정되지 않는 하나 또는 그 이상의 이종성 분자(들)에 접합된 항체다.
"개체" 또는 "대상"은 포유류다. 포유류는 길들여진 동물들(예컨데, 소, 양, 고양이, 개 그리고 말), 영장류(예컨데, 인간과 인간이 아닌 영장류 이를 테면 원숭이), 토끼 그리고 설치류(예컨데, 마우스 및 렛)을 포함하나 이에 한정되지 않는다. 특정 구체예들에 있어서, 개체 또는 대상는 인간이다.
"단리된(isolated) 항체"는 이 항체의 자연적 환경 성분으로부터 분리된 항체다. 일부 구체예들에 있어서, 항체는 예로써, 전기영동 (예컨데, SDS-PAGE, 등전성 포커싱(IEF), 모세관 전기영동) 또는 크로마토그래피(예컨데, 이온 교환 또는 역상 HPLC)에 의해 측정되었을 때 95% 이상 또는 99% 순도로 정제된다. 항체 순도를 평가하는 방법들에 대한 검토는 예컨데, Flatman et al., J. Chromatogr. B 848:79-87 (2007)를 참고한다.
"단리된 핵산"은 이의 자연적 환경으로부터 분리된 핵산 분자를 지칭한다. 단리된 핵산은 이 핵산 분자가 보통 포함된 세포안에 내포된 핵산 분자를 포함하지만, 그러나 이 핵산 분자는 염색체외 또는 이의 자연적 염색체 위치와는 상이한 염색체 위치에 존재된다.
"항-CD22 항체를 인코드하는 단리된 핵산"은 항체 중쇄 및 경쇄(또는 이의 단편)를 인코드하는 하나 또는 그 이상의 핵산 분자를 지칭하는데, 단일 벡터 또는 별도 벡터에 있는 이러한 핵산 분자(들), 그리고 숙주 세포 안에 하나 또는 그 이상의 위치에 존재하는 이러한 핵산 분자(들)들도 포함된다.
본 명세서에서 이용된 바와 같이, 용어 "CD22"는 다른 언급이 없는 한, 포유류 이를 테면 영장류 (예컨데 인간, 시노몰구스 원숭이 (cyno)) 그리고 설치류 (예컨데, 마우스와 렛)이 포함된 임의의 척추동물 기원의 임의의 고유한 CD22를 지칭한다. 이 용어는 가공안된 "전장" CD22 뿐만 아니라 세포 안에서 가공되어 생성된 임의의 형태의 CD22를 포괄한다. 이 용어는 또한 자연적으로 생성된 CD22의 변이, 예컨데, 접합(splice) 변이, 대립형질 변이, 그리고 이소폼(isoforms) 또한 포괄한다. CD22의 주요 이소폼 (CD22베타)은 847개의 아미노산과 세포밖 도메인 안에 7개의 면역글로블린-유사 영역을 포함한다(Wilson, G.L. et al., J. Exp. Med. 173:137-146 (1991)). 소수의 이소폼인 CD22알파는 647개의 아미노산을 포함하고, 세포밖 도메인 안에 면역글로블린-유사 도메인 3 및 4가 부족하다(Stamenkovic, I. and Seed, B., Nature 345:74-77 (1990)) 그리고 Wilson et al. (1991), 상기를 참고). 예시적인 인간 CD22베타 전구물질의 아미노산 서열 (신호 서열과 함께)은 서열 번호: 28에 나타낸다. 예시적인 인간 성숙 CD22베타의 아미노산 서열(신호 서열 없이)은 서열 번호: 29에 나타낸다. 예시적인 인간 CD22알파 전구물질의 아미노산 서열 (신호 서열과 함께)은 서열 번호: 30에 나타낸다. 예시적인 인간 성숙 CD22알파의 아미노산 서열(신호 서열 없이)은 서열 번호: 31에 나타낸다.
용어 "CD22-양성 암"은 이들의 표면에 CD22를 발현시키는 세포들이 포함된 암을 지칭한다.
용어 "CD22-양성 세포"는 이의 표면에서 CD22를 발현시키는 세포를 지칭한다.
본 명세서에서 이용된 바와 같이 용어 "단클론 항체"는 실질적으로 상동성 항체, 가령, 동일한 집단 및/또는 동일한 에피토프에 결합되는 항체 집단에서 획득된 항체를 지칭하는데, 있을 수 있는 변이 항체, 예컨데, 자연적으로 발생되는 돌연변이 또는 단클론 항체 집단의 생산 동안 생성된 변이 항체는 제외되며, 이러한 변이는 일반적으로 소량으로 존재한다. 상이한 결정부(에피토프)를 지향하는 상이한 항체가 일반적으로 포함된 다클론 항체 제제와 대조적으로, 단클론 항체 집단의 각 단클론 항체는 항원 상에 단일 결정부위를 지향한다. 따라서, 변형자( modifier) "단클론"은 실질적으로 상동성 항체 집단으로부터 획득된 항체의 특징을 나타내고, 그리고 임의의 특정 방법으로 항체 생산이 필요한 것으로 간주되지는 않는다. 예로써, 본 발명에 따라 이용되는 단클론 항체는 하이브리도마 방법, 재조합 DNA 방법, 파아지-디스플레이, 그리고 인간 면역글로블린 좌(loci)의 전부 또는 일부가 포함된 유전자전이 동물을 이용하는 방법을 포함하나 이에 한정되지 않는 다양한 기술에 의해 만들어질 수 있고, 단클론 항체를 만드는 이러한 방법 및 다른 예시적인 방법들은 본 명세서에서 설명된다.
"네이키드(naked) 항체"는 이질성 모이어티 (예컨데, 세포독성 모이어티) 또는 방사능라벨에 접합되지 않은 항체를 지칭한다. 네이키드 항체는 약학 제제 안에 존재할 수 있다.
"고유한 항체"는 다양한 구조를 가진 자연 발생적 면역글로블린 분자들을 지칭한다. 예로써, 고유한 IgG 항체는 2개의 동일한 경쇄와 2개의 동일한 중쇄가 이황화결합된 약 150,000 달톤의 이형사합체 당단백질이다. N-말단에서 C-말단으로, 각 중쇄는 가변 중쇄 도메인 또는 중쇄 가변 도메인이라고 불리는 가변 영역(VH), 이어서 3개의 불변 도메인들 (CH1, CH2, 그리고 CH3)을 보유한다. 유사하게, N-말단에서 C-말단으로, 각 경쇄는 가변 경쇄 도메인 또는 경쇄 가변 도메인으로 불리는 가변 영역(VL), 이어서 불변 경쇄 (CL) 도메인을 보유한다. 항체의 경쇄는 이의 불변 도메인의 아미노산 서열에 기초하여 카파 (κ) 및 람다 (λ)로 불리는 두 가지 유형중 하나에 해당될 수 있다.
용어 "포장 삽입물(package insert)"은 징후, 용도, 용량, 투여, 복합 요법, 금기 및/또는 이러한 치료 산물의 사용과 관련된 경고에 관련된 정보가 포함된, 치료제의 시판 포장에 관례적으로 포함되는 지시사항을 이를 때 사용된다.
기준 폴리펩티드서열에 대하여 "아미노산 서열 동일성 백분율(%)"은 최대 서열 상동성 비율을 얻기 위하여 서열들을 배열하고, 필요에 따라 갭을 도입시킨 후, 기본 폴리펩티드 서열에서 아미노산 잔기와 동일한 후보 서열 안에 있는 아미노산 잔기의 비율로 정의되는데, 임의의 보존적 치환은 서열 동일성으로 간주되지 않는다. 아미노산 서열 동일성 백분율을 결정하기 위한 목적으로 하는 배열은 당업계 숙지된 범위내 다양한 방식으로 이루어질 수 있으며, 예를 들면, 공개적으로 이용가능한 컴퓨터 소프트웨어 이를 테면 BLAST, BLAST-2, ALIGN 또는 Megalign (DNASTAR) 소프트웨어를 이용한다. 당업계 숙련자는 비교되는 서열의 전장에 걸쳐 최대 배열을 획득하는데 요구되는 임의의 알고리즘이 포함된 서열을 배열하기 위한 적절한 매개변수를 결정할 수 있다. 그러나, 본 명세서에 기재된 목적을 위하여, 아미노산 서열 동일성 % 값은 서열 비교 컴퓨터 프로그램 ALIGN-2를 이용하여 생성된다. ALIGN-2 서열 비교 컴퓨터 프로그램은 Genentech, Inc.에 의해 기획되었으며, 그리고 원천 코드는 U.S. Copyright Office, Washington D.C., 20559에 사용자 서류와 함께 기록되어 있고, 이는 미국 저작권 등록 번호 TXU510087로 등록되어 있다. ALIGN-2 프로그램은 Genentech, Inc., South San Francisco, California으로부터 공개적으로 이용가능하며, 또는 원천 코드로부터 적성될 수도 있다. ALIGN-2 프로그램은 디지탈 UNIX V4.0D를 포함하는 UNIX 운용 체계상에서 이용될 수 있도록 작성되어야 한다. 모든 서열 비교 매개변수들은 ALIGN-2 프로그램에 의해 설정되며, 변화되지 않는다.
ALIGN-2가 아미노산 서열 비교를 위하여 이용되는 상황에서, 주어진 아미노산 서열 B에 대한 주어진 아미노산 서열 A의 아미노산 서열 동일성 % (이것은 주어진 아미노산 서열 B에 대한 특정 %의 아미노산 서열 동일성을 보유 또는 포함하는 주어진 아미노산 서열 A로 대체 표현될 수도 있음)은 다음과 같이 산출된다:
분수 X/Y 에 곱하기 100
여기에서 X는 A 및 B의 프로그램 배열에서 서열 배열 프로그램 ALIGN-2에 의해 동일한 합치로 기록된 아미노산 잔기의 수를 나타내며, 그리고 Y는 B에 있는 전체 아미노산 잔기의 수를 나타낸다. 아미노산 서열 A의 길이가 B의 아미노산 서열 의 길이와 대등하지 않을 때, B에 대한 A의 아미노산 서열 동일성 %은 A에 대한 B의 아미노산 서열 동일성 %과는 대등하지 않을 것이라는 것을 인지할 수 있다. 구체적으로 명시되지 않는 한, 본 명세서에서 이용된 모든 아미노산 서열 동일성 % 값은 ALIGN-2 컴퓨터 프로그램을 이용하여 바로 앞 단락에서 설명된 것과 같이 획득된다.
용어 "약학 제제"는 제제안에 내포된 활성 성분의 생물학적 활성이 효과가 있도록 허용하는 형태 그리고 제제가 대상에게 투여될 때 수용불가능한 독성이 있는 추가 성분들이 포함되지 않는 제제를 말한다.
"약학적으로 수용가능한 운반체"는 대상에게 비독성이면서, 활성 성분이 아닌 약학 제제 안에 있는 성분을 지칭한다. 약학적으로 수용가능한 운반체는 완충액, 부형제, 안정화제, 또는 보존제를 포함하나 이에 한정되지 않는다.
본 명세서에서 이용된 바와 같이, "치료" (그리고 이의 문법적으로 변화된 형태 이를 테면 "치료하다" 또는 "치료하는")는 치료되는 개체의 치료될 개체의 자연 과정을 변경시키는 시도와, 예방을 위한 또는 임상 병리 과정 동안에 실행될 수 있는 임상적 중재를 말한다. 치료의 바람직한 효과는 질환의 발생 또는 재발을 방지, 증상의 완화, 질환의 병리학적 임의의 직접 또는 간접적 결과의 감소, 전이 방지, 질병 진행 속도의 감소, 질병 상태의 개선 또는 완화, 그리고 차도 또는 개선된 예후를 포함하나 이에 한정되지 않는다. 일부 구체예들에 있어서, 본 발명의 면역접합체는 질환의 발달을 지연 또는 질환의 진행을 느리게 하는데 이용된다.
용어 "가변 영역" 또는 "가변 도메인"은 항원에 항체의 결합에 관련되는 항체 중쇄 또는 경쇄의 도메인을 지칭한다. 고유한 항체의 중쇄 및 경쇄 (차례로 VH 및 VL)의 가변 도메인들은 유사한 구조를 보유하는데, 각 도메인은 4개의 보존된 골격 영역(FRs)과 3개의 초가변 영역(HVRs)을 포함한다. (예컨데, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007).) 단일 VH 또는 VL 도메인은 항원-결합 특이성을 부여하는데 충분할 수 있다. 더욱이, 특정 항원에 결합하는 항체는 상보성 VL 또는 VH 도메인들의 라이브러리를 각각 스크리닝하기 위하여 항원에 결합되는 항체의 VH 또는 VL 도메인을 이용하여 단리될 수 있다. 예컨데, Portolano et al., J. Immunol. 150:880-887 (1993); Clarkson et al., Nature 352:624-628 (1991).
본 명세서에서 이용된 바와 같이, 용어 "벡터"는 연결된 또다른 핵산의 증식시킬 수 있는 핵산 분자를 말한다. 이 용어는 자체-복제가능한 핵산구조로써의 벡터 구조 뿐만 아니라 벡터가 도입된 숙주 세포의 게놈 안에 통합된 벡터도 포함한다. 특정 벡터는 기능적으로 연계된 핵산의 발현을 지시할 수 있다. 이러한 벡터는 본원 명세서에서 "발현 벡터"라고 한다.
본 명세서에서 이용된 바와 같이, 구절 "임의선택적으로 치환된"이란 치환되거나 치환되지 않을 수 있을 수 있는 부모 기와 관계된다.
다른 언급이 없는 한, 본 명세서에서 이용된 용어 "치환된"이란 하나 또는 그 이상의 치환체를 보유하는 부모 기에 관련된 것이다. 용어 "치환체"는 통상적인 의미로 본 명세서에서 이용되며, 부모기에 적절하게 융합되거나 공유적으로 부착된 화학 모이어티를 지칭한다. 광범위한 치환체들이 공지되어 있으며, 그리고 이의 형성 및 다양한 부모기로의 도입 방법 또한 공지되어 있다.
일부 구체예들에 있어서, 본 명세서에서 설명된 치환체(임의선택적 치환체 포함)는 상기 항체에 비반응성인 기들에 한정된다. 일부 구체예들에 있어서, 링커 (L)을 통하여 PBD 화합물의 N10 위치에서 상기 항체에 연결이 형성된다. 일부 경우에서 PBD 구조의 다른 부분에 위치된 반응성 기능기는 상기 항체에 추가 결합을 형성할 수 있다(이를 교차연결(crosslinking)이라고 부를 수 있다). 일부 경우에서 이러한 추가 결합은 접합체의 운반 및 생물학적 활성을 변경시킬 수 있다. 따라서, 일부 구체예들에 있어서, 추가 치환체는 반응 기능성이 부족한 것들에 제한된다.
일부 구체예들에 있어서, 치환체는 R, OR, SR, NRR', NO2, 할로, CO2R, COR, CONH2, CONHR, 그리고 CONRR'에서 선택된다. 일부 구체예들에 있어서, 치환체는 R, OR, SR, NRR', NO2, CO2R, COR, CONH2, CONHR, 그리고 CONRR'에서 선택된다. 일부 구체예들에 있어서, 치환체는 R, OR, SR, NRR', NO2, 그리고 할로에서 선택된다. 일부 구체예들에 있어서, 치환체는 R, OR, SR, NRR', 그리고 NO2로 구성된 그룹에서 선택된다.
상기에서 논의된 임의의 구체예들은 본 명세서에서 설명된 임의의 치환체에 적용될 수 있다. 대안으로, 치환체는 하기에서 논의되는 하나 또는 그 이상의 기로부터 선택될 수 있다.
본 명세서에서 이용된 바와 같이, 용어 "C1-12 알킬"은 1 내지 12개의 탄소원자를 가지는 탄화수소 화합물의 탄소원자로부터 수소를 제거함으로써 획득되는 단가(monovalent) 모이어티에 관계되며, 이때 탄화수소 화합물은 지방족이며, 고리 또는 비고리(acyclic)일 수 있으며, 포화 또는 불포화(예컨데 부분적으로 불포화, 완전하게 불포화)될 수 있다. 따라서, 용어 "알킬"은 하기에서 논의되는 바와 같이, 하위-부류 알케닐, 알키닐, 시클로알킬, 등을 포함한다.
포화 알킬 기의 예는 메틸 (C1), 에틸 (C2), 프로필 (C3), 부틸 (C4), 펜틸 (C5), 헥실 (C6) 그리고 헵틸 (C7)을 포함하나 이에 한정되지 않는다.
포화 선형 알킬 기의 예는 메틸 (C1), 에틸 (C2), n-프로필 (C3), n-부틸 (C4), n-펜틸 (아밀) (C5), n-헥실 (C6) 그리고 n-헵틸 (C7)을 포함하나 이에 한정되지 않는다.
포화 분기화된 알킬 기의 예로는 이소-프로필 (C3), 이소부틸 (C4), sec-부틸 (C4), tert-부틸 (C4), 이소-펜틸 (C5), 그리고 네오-펜틸 (C5)을 포함하나 이에 한정되지 않는다.
알킬 기는 O, N(H) 그리고 S로부터 선택된 하나 또는 그 이상의 이형원자에 의해 임의선택적으로 중단될 수 있다. 이러한 기를 "헤테로알킬"이라고 할 수 있다.
본 명세서에서 이용된 바와 같이, 용어 "C2-12 헤테로알킬"은 2 내지 12개의 탄소원자를 가지는 탄화수소 화합물의 탄소원자로부터 수소를 제거함으로써 획득되는 단가(monovalent) 모이어티에 관계되며, 그리고 하나 또는 그 이상의 헤테로원자는 O, N(H) 그리고 S, 바람직하게는 O 및 S로부터 선택된다.
헤테로알킬 기의 예로는 하나 또는 그 이상의 에틸렌 글리콜 단위 -(OCH2CH2)-를 포함하나 이에 국한되지 않는다. 헤테로알킬 가의 말단은 헤테로원자의 주요 형태, 예컨데 -OH, -SH 또는 -NH2일 수 있다. 바람직한 구체예에 있어서, 말단은 -CH3이다.
본 명세서에서 이용된 바와 같이 용어 "C2-12 알케닐"은 하나 또는 그 이상의 탄소-탄소 이중 결합을 보유하는 알킬 기에 관계된다.
불포화 알케닐 기의 예로는 에테닐 (비닐, -CH=CH2), 1-프로페닐 (-CH=CH-CH3), 2-프로페닐 (아릴, CHCH=CH2), 이소프로페닐 (1-메틸비닐, -C(CH3)=CH2), 부테닐 (C4), 펜테닐 (C5), 그리고 헥세닐(C6)을 포함하나 이에 한정되지 않는다.
본 명세서에서 이용된 바와 같이, 용어 "C2-12 알키닐"은 하나 또는 그 이상의 탄소-탄소 삼중 결합을 보유하는 알킬 기에 관계된다.
불포화 알키닐 기의 예로는 에티닐 (-C≡CH) 그리고 2-프로피닐(프로파르길, -CH2C≡CH)을 포함하나 이에 한정되지 않는다.
본 명세서에서 이용된 바와 같이, 용어 "C3-12 시클로알킬"은 시클일 기이기도 한 알킬 기에 관계되는데; 즉, 3개 내지 7개 탄소 원자를 보유하는 모이어티와 3 내지 7개 고리 원자가 포함된 고리 탄화수소(카르보사이클) 화합물의 지환식 고리로부터 수소 원자를 제거함으로써 획득된 단가 모이어티이다.
시클로알킬 기의 예로는 다음으로부터 유도된 것들을 포함하나 이에 한정되지 않는다:
(i) 포화 모노사이클 탄화수소 화합물들:
시클로프로판 (C3), 시클로부탄 (C4), 시클로펜탄 (C5), 시클로헥산 (C6), 시클로헵탄 (C7), 메틸시클로프로판 (C4), 디메틸시클로프로판 (C5), 메틸시클로부탄 (C5), 디메틸시클로부탄 (C6), 메틸시클로펜탄 (C6), 디메틸시클로펜탄 (C7) 그리고메틸시클로헥산 (C7);
(ii) 불포화 모노사이클 탄화수소 화합물들:
시클로프로펜 (C3), 시클로부텐 (C4), 시클로펜텐 (C5), 시클로헥센 (C6), 메틸시클로프로펜 (C4), 디메틸시클로프로펜 (C5), 메틸시클로부텐 (C5), 디메틸시클로부텐 (C6), 메틸시클로펜텐 (C6), 디메틸시클로펜텐 (C7) 그리고메틸시클로헥센 (C7); 그리고
(iii) 포화 폴리사이클 탄화수소 화합물들:
노르카란(C7), 노르피난(C7), 노르보난(C7).
본 명세서에서 이용된 것과 같이, 용어 "C3-20 헤테로시클일"은 헤테로사이클 화합물의 고리 원자로부터 수소 원자를 제거함으로써 획득되는 단가 모이어티에 관계되는데, 이 모이어티는 3 내지 20개 고리 원자를 보유하며, 이들중 1 내지 10개는 고리 헤테로원자다. 일부 구체예들에 있어서, 각 고리는 3 내지 7개 고리 원자를 보유하며, 이들중 1 내지 4개는 고리 헤테로원자다.
본 명세서에서 이용된 것과 같이, 접두부 (예컨데 C3-20, C3-7, C5-6, 등.)는 고리 원자의 수, 또는 고리 원자의 수의 범위, 탄소 원자 또는 헤테로 원자를 나타낸다. 예로써, 본 명세서에서 이용된 것과 같이, 용어 "C5-6 헤테로시클일"은 5 또는 6개의 고리 원자를 보유한 헤테로시클일 기에 관계된다.
모노사이클 헤테로시클일 기의 예들은 다음으로부터 유도된 것들을 포함하나 이에 한정되지 않는다:
(i) N1: 아지리딘 (C3), 아제티딘(C4), 피롤리딘(테트라히드로피롤) (C5), 피롤린(예컨데, 3-피롤린, 2,5-디히드로피롤) (C5), 2H-피롤 또는 3H-피롤 (이소피롤, 이소아졸) (C5), 피페리딘 (C6), 디히드로피리딘 (C6), 테트라히드로피리딘 (C6), 아제핀(C7);
(ii) O1: 옥시란 (C3), 옥세탄(C4), 옥소란(테트라히드로퓨란) (C5), 옥솔(디히드로퓨란) (C5), 옥산(테트라히드로피란) (C6), 디히드로피란 (C6), 피란 (C6), 옥세핀(C7);
(iii) S1: 티이란(C3), 티에탄(C4), 티오란(테트라히드로티오펜) (C5), 티안 (테트라히드로티오피란) (C6), 티에판(C7);
(iv) O2: 디옥소란 (C5), 디옥산 (C6), 그리고 디옥세판 (C7);
(v) O3: 트리옥산(C6);
(vi) N2: 이미다졸리딘 (C5), 피라졸리딘(디아졸리딘) (C5), 이미다졸린 (C5), 피라졸린(디히드로피라졸) (C5), 피페라진(C6);
(vii) N1O1: 테트라히드로옥사졸 (C5), 디히드로옥사졸 (C5), 테트라히드로이소옥사졸 (C5), 디히드로이소옥사졸 (C5), 몰포린 (C6), 테트라히드로옥사진 (C6), 디히드로옥사진 (C6), 옥사진 (C6);
(viii) N1S1: 티아졸린(C5), 티아졸리딘 (C5), 티오몰포린 (C6);
(ix) N2O1: 옥사디아진(C6);
(x) O1S1: 옥사티올(C5) 그리고 옥사티안(티옥산) (C6); 그리고,
(xi) N1O1S1: 옥사티아진(C6).
치환된 모노사이클 헤테로시클일 기의 예로는 고리형태의 사카라이드로부터 유도된 것들, 예로써, 퓨란노스(C5), 이를 테면 아라비노퓨라노스, 릭소퓨라노스, 리보퓨라노스, 그리고 크실로퓨란, 그리고 피라노스(C6), 이를 테면 알로피라노스, 알트로피라노스, 글루코피라노스, 만노피라노스, 굴로피라노스, 이도피라노스, 갈락토피라노스, 그리고 탈로피라노스를 포함하나 이에 한정되지 않는다.
본 명세서에서 이용된 바와 같이, 용어 "C5-20 아릴"은 방향족 화합물의 방향족 고리 원자로부터 수소 원자를 제거함으로써 획득된 단가 모이어티에 관계되는데, 이 모이어티는 3 내지 20개 고리 원자를 가진다. 일부 구체예들에 있어서, 각 고리는 5 내지 7개의 고리 원자를 가진다.
일부 구체예들에 있어서, 고리 원자들은 "카르보아릴 기"에서와 같이 모두 탄소 원자다. 카르보아릴 기의 예로는 벤젠 (가령, 페닐) (C6), 나프탈렌 (C10), 아줄렌 (C10), 안트라센(C14), 페난트렌(C14), 나프타센(C18), 그리고 피렌(C16)으로부터 유도된 것들을 포함하나 이에 한정되지 않는다.
융합된 고리를 포함하고, 이 고리중 최소한 하나는 방향족 고리인 아릴 기의 예로는 인단(예컨데 2,3-디히드로-1H-인덴) (C9), 인덴 (C9), 이소인덴 (C9), 테트라린(1,2,3,4-테트라히드로나프탈렌 (C10), 아세나프텐(C12), 플루오렌(C13), 페날렌(C13), 아세페난트렌(C15), 그리고 아세안트렌(C16)으로부터 유도된 것들을 포함하나 이에 한정되지 않는다.
일부 구체예들에 있어서, 고리 원자들은 "헤테로아릴 기"에서와 같이 하나 또는 그 이상의 헤테로 원자를 포함할 수 있다. 모노사이클 헤테로아릴 기의 예로는 다음으로부터 유도된 것들을 포함하나 이에 한정되지 않는다:
(i) N1: 피롤 (아졸) (C5), 피리딘 (아진) (C6);
(ii) O1: 퓨란 (옥솔) (C5);
(iii) S1: 티오펜 (티올) (C5);
(iv) N1O1: 옥사졸 (C5), 이소옥사졸 (C5), 이소옥사진 (C6);
(v) N2O1: 옥사디아졸(퓨라잔) (C5);
(vi) N3O1: 옥사트리아졸(C5);
(vii) N1S1: 티아졸(C5), 이소티아졸(C5);
(viii) N2: 이미다졸(1,3-디아졸) (C5), 피라졸 (1,2-디아졸) (C5), 피리다진(1,2-디아진) (C6), 피리미딘 (1,3-디아진) (C6) (예컨데, 시토신, 티민, 우라실), 피라진(1,4-디아진) (C6);
(ix) N3: 트리아졸(C5), 트리아진(C6); 그리고,
(x) N4: 테트라졸(C5).
융합된 고리를 포함하는 헤테로아릴의 예로는 다음을 포함하나 이에 한정되지 않는다:
(i) 벤조퓨란 (O1), 이소벤조퓨란 (O1), 인돌 (N1), 이소인돌 (N1), 인돌리진(N1), 인돌린 (N1), 이소인돌린 (N1), 퓨린 (N4) (예컨데, 아데닌, 구아닌), 벤지이미다졸(N2), 인다졸 (N2), 벤즈옥사졸 (N1O1), 벤즈이소옥사졸 (N1O1), 벤조디옥솔(O2), 벤조퓨라잔(N2O1), 벤조트리아졸 (N3), 벤조티오퓨란 (S1), 벤조티아졸 (N1S1), 벤조티아디아졸 (N2S)로부터 유도된 C9 (2개의 융합된 고리와 함께);
(ii) 크로멘 (O1), 이소크로멘 (O1), 크로만 (O1), 이소크로만 (O1), 벤조디옥산(O2), 퀴놀린(N1), 이소퀴놀린(N1), 퀴놀리진(N1), 벤즈옥사진 (N1O1), 벤조디아진 (N2), 피리도피리딘 (N2), 퀴노옥살린(N2), 퀴나졸린(N2), 씨놀린(N2), 프탈라진(N2), 나프티리딘(N2), 프테리딘(N4)으로부터 유도된 C10 (2개의 융합된 고리와 함께);
(iii) 벤조디아제핀(N2)으로부터 유도된 C11 (2개의 융합된 고리와 함께);
(iv) 카르바졸(N1), 디벤조퓨란 (O1), 디벤조티오펜 (S1), 카르보린(N2), 페리미딘(N2), 피리도인돌 (N2)로부터 유도된 C13(3개의 융합된 고리와 함께); 그리고,
(v) 아크리딘(N1), 산텐(O1), 티오산텐(S1), 옥산트렌(O2), 페녹산틴(O1S1), 페나진(N2), 펜옥사진 (N1O1), 페노티아진(N1S1), 티안트렌(S2), 펜난트리딘(N1), 페난트롤린(N2), 페나진(N2)로부터 유도된 C14(3개의 융합된 고리와 함께).
상기 기들은 단독으로 또는 또다른 치환체와 함께, 상기 기들로부터 또는 하기에서 열거된 추가 치환체로부터 선택된 하나 또는 그 이상의 기로 임의선택적으로 치환될 수 있다.
할로: -F, -Cl, -Br, 그리고 -I.
히드록시: -OH.
에테르: -OR, 이때 R은 에테르 치환체, 예로써, C1-7 알킬 기 (하기에서 논의되는 바와 같이 C1-7 알콕시 기로 불리기도 함), C3-20 헤테로시클일 기 (C3-20 헤테로시클일옥시 기로 불리기도 함), 또는 C5-20 아릴 기 (C5-20 아릴옥시 기로 불리기도 함). 일부 구체예들에 있어서, R은 C1-7 알킬 기다.
알콕시: -OR, 이때 R은 알킬 기, 예로써, C1-7 알킬 기다. C1-7알콕시 기의 예로는 -OMe (메톡시), -OEt (에톡시), -O(nPr) (n-프로폭시), -O(iPr) (이소프로폭시), -O(nBu) (n-부톡시), -O(sBu) (sec-부톡시), -O(iBu) (이소부톡시), 그리고-O(tBu) (tert-부톡시)을 포함하나 이에 한정되지 않는다.
아세탈: -CH(OR1)(OR2), 이때 R1 및 R2는 독립적으로 아세탈 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기. 일부 구체예들에 있어서, R1 및/또는 R2는 독립적으로 C1-7 알킬 기다. 일부 구체예들에 있어서, "사이클" 아세탈 기의 경우, R1와 R2는 이들에 부착된 2개의 산소 원자와 함께 4 내지 8개의 고리 원자를 보유하는 헤테로사이클 고리를 형성한다. 아세탈 기의 예는 -CH(OMe)2, -CH(OEt)2, 그리고 -CH(OMe)(OEt)을 포함하나 이에 한정되지 않는다.
헤미아세탈: -CH(OH)(OR1), 이때 R1은 헤미아세탈 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기. 일부 구체예들에 있어서, R1은 C1-7 알킬 기다. 헤미아세탈 기의 예로는 -CH(OH)(OMe) 그리고 -CH(OH)(OEt)을 포함하나 이에 한정되지 않는다.
케탈: -CR(OR1)(OR2), 이때 R1 및 R2는 아세탈의 경우에 대해 정의된 바와 같고, 그리고 R은 수소 이외의 케탈 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 케탈 기의 예로는 -C(Me)(OMe)2, -C(Me)(OEt)2, -C(Me)(OMe)(OEt), -C(Et)(OMe)2, -C(Et)(OEt)2, 그리고 -C(Et)(OMe)(OEt)을 포함하나 이에 한정되지 않는다.
헤미케탈: -CR(OH)(OR1), 여기에서 R1은 헤미아세탈에 대해 정의된 바와 같고, 그리고 R은 수소 이외의 헤미케탈 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 헤미케탈 기의 예로는 -C(Me)(OH)(OMe), -C(Et)(OH)(OMe), -C(Me)(OH)(OEt), 그리고 -C(Et)(OH)(OEt)을 포함하나 이에 한정되지 않는다.
옥소(케토, -온): =O.
티온(티오케톤): =S.
이미노 (이민): =NR, 이때 R은 이미노 치환체, 예로써, 수소, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 수소 또는 C1-7 알킬 기다. 이미노 기의 예로는 =NH, =NMe, =NEt, 그리고 =NPh을 포함하나 이에 한정되지 않는다.
포르밀 (카르브알데히드, 카르복시알데히드): -C(=O)H.
아실 (케토): -C(=O)R, 이때 R은 아실 치환체, 예로써, C1-7 알킬 기 (C1-7 알킬아실 또는 C1-7 알카노일이라고도 부름), C3-20 헤테로시클일 기 (C3-20 헤테로시클일아실이라고도 부름), 또는 C5-20 아릴 기 (C5-20 아릴아실이라고도 부름)이다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 아실 기의 예로는 -C(=O)CH3 (아세틸), -C(=O)CH2CH3 (프로피오닐), -C(=O)C(CH3)3 (t-부티릴), 그리고 -C(=O)Ph (벤조일, 페논)을 포함하나 이에 한정되지 않는다.
카르복시(카르복실산): -C(=O)OH.
티오카르복시 (티오카르복실산): -C(=S)SH.
티올카르복시 (티올카르복실산): -C(=O)SH.
티오노카르복시 (티오노카르복실산): -C(=S)OH.
이미딘산: -C(=NH)OH.
히드록사민산: -C(=NOH)OH.
에스테르 (카르복실레이트, 카르복실산 에스테르, 옥시카르보닐): -C(=O)OR, 이때 R은 에스테르 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 에스테르 기의 예로는 -C(=O)OCH3, -C(=O)OCH2CH3, -C(=O)OC(CH3)3, 그리고 -C(=O)OPh을 포함하나 이에 한정되지 않는다.
아실옥시(역 에스테르): -OC(=O)R, 이때 R은 아실옥시 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 아실옥시 기의 예로는 -OC(=O)CH3 (아세톡시), -OC(=O)CH2CH3, -OC(=O)C(CH3)3, -OC(=O)Ph, 그리고 -OC(=O)CH2Ph을 포함하나 이에 한정되지 않는다.
옥시카르보닐옥시: -OC(=O)OR, 이때 R은 에스테르 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 옥시카르보닐옥시 기의 예로는 -OC(=O)OCH3, -OC(=O)OCH2CH3, -OC(=O)OC(CH3)3, 그리고 -OC(=O)OPh을 포함하나 이에 한정되지 않는다.
아미노: -NR1R2, 이때 R1 및 R2는 독립적으로 아미노 치환체, 예로써, 수소, C1-7 알킬 기 (C1-7 알킬아미노 또는 디-C1-7 알킬아미노라고도 함), C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R1 및 R2는 독립적으로 H 또는 C1-7 알킬 기다. 일부 구체예들에 있어서, "사이클" 아미노 기의 경우, R1 및 R2는 이들이 부착된 질소 원자와 함께, 4 내지 8개의 고리 원자를 가진 헤테로사이클 고리를 형성한다. 아미노 기는 1차(-NH2), 2차(-NHR1), 또는 3차 (-NHR1R2)일 수 있으며, 그리고 양이온 형태에서 4차 (-+NR1R2R3)일 수 있다. 아미노 기의 예로는 -NH2, -NHCH3, -NHC(CH3)2, -N(CH3)2, -N(CH2CH3)2, 그리고 -NHPh을 포함하나 이에 한정되지 않는다. 사이클 아미노 기의 예로는 아지리디노, 아제티디노, 피롤리디노, 피페리디노, 피페라지노, 몰포리노, 그리고 티오몰포리노를 포함하나 이에 한정되지 않는다.
아미도 (카르바모일, 카르바밀, 아미노카르보닐, 카르복사미드): C(=O)NR1R2는, 이때 R1 및 R2는 아미노기의 경우에서 정의된 바와 같이 독립적으로 아미노 치환체다. 아미도 기의 예로는 -C(=O)NH2, -C(=O)NHCH3, -C(=O)N(CH3)2, -C(=O)NHCH2CH3, 그리고 -C(=O)N(CH2CH3)2, 뿐만 아니라 아미도 기, 여기에서 R1 및 R2는 이들이 부착된 질소원자와 함께 헤테로사이클 구조를 형성하는 아미도기, 예로써, 피페리디노카르보닐, 몰포리노카르보닐, 티오몰포리노카르보닐, 그리고 피페라지노카르보닐을 포함하나 이에 한정되지 않는다.
티오아미도 (티오카르바밀): -C(=S)NR1R2, 이때 R1 및 R2는 아미노기의 경우에서 정의된 바와 같이 독립적으로 아미노 치환체다. 티오아미도 기의 예로는 -C(=S)NH2, -C(=S)NHCH3, -C(=S)N(CH3)2, 그리고 -C(=S)NHCH2CH3을 포함하나 이에 한정되지 않는다.
아실아미도 (아실아미노): -NR1C(=O)R2, 이때 R1은 아미드 치환체, 예로써, 수소, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기이며, 그리고 R2는 아실 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20아릴 기다. 일부 구체예들에 있어서, R1 및/또는 R2는 수소 또는 C1-7 알킬 기다. 아실아미드 기의 예로는 -NHC(=O)CH3, -NHC(=O)CH2CH3, 그리고 -NHC(=O)Ph을 포함하나 이에 한정되지 않는다. R1 및 R2는 함께 사이클 구조를 형성할 수 있는데, 예로써, 숙시니미딜, 말레이미딜 그리고 프탈리미딜을 형성할 수 있다:
아미노카르보닐옥시: -OC(=O)NR1R2, 이때 R1 및 R2는 아미노기의 경우에서 정의된 바와 같이, 독립적으로 아미노 치환체다. 아미노카르보닐옥시 기의 예로는 -OC(=O)NH2, -OC(=O)NHMe, -OC(=O)NMe2, 그리고 -OC(=O)NEt2을 포함하나 이에 한정되지 않는다.
우레도: -N(R1)CONR2R3 이때 R2 및 R3은 아미노기에서 정의된 바와 같이 독립적으로 아미노 치환체이며, 그리고 R1은 우레도 치환체, 예로써, 수소, C1-7 알킬 기, C3-20헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R1은 수소 또는 C1-7 알킬 기다. 우레도 기의 예로는 -NHCONH2, -NHCONHMe, -NHCONHEt, -NHCONMe2, -NHCONEt2, -NMeCONH2, -NMeCONHMe, -NMeCONHEt, -NMeCONMe2, 그리고 -NMeCONEt2을 포함하나 이에 한정되지 않는다.
구아니디노: -NH-C(=NH)NH2.
테트라졸일: 4개의 질소 원자와 1개의 탄소 원자를 가지는 5원 방향족 고리,
아미딘(아미디노): -C(=NR)NR2, 이때 각 R은 아미딘 치환체, 예로써, 수소, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, 각 R은 H 또는 C1-7 알킬 기다. 아미딘 기의 예로는 -C(=NH)NH2, -C(=NH)NMe2, 그리고 -C(=NMe)NMe2을 포함하나 이에 한정되지 않는다.
니트로: -NO2.
니트로소: -NO.
아지도: -N3.
시아노 (니트릴, 카르보니트릴): -CN.
이소시아노: -NC.
시아나토: -OCN.
이소시아나토: -NCO.
티오시아노 (티오시아나토): -SCN.
이소티오시아노 (이소티오시아나토): -NCS.
술퍼히드릴(티올, 멀캅토): -SH.
티오에테르 (술피드): -SR, 이때 R은 티오에테르 치환체, 예로써, C1-7 알킬 기 (C1-7 알킬티오 기라고도 함), C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 티오에테르 기의 예로는 -SCH3 그리고 -SCH2CH3을 포함하나 이에 한정되지 않는다.
디설피드: -SS-R, 이때 R은 디설피드 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기 (C1-7 알킬 디설피드라고도 함)다. 디설피드 기의 예로는 -SSCH3 그리고 -SSCH2CH3을 포함하나 이에 한정되지 않는다.
술핀(술피닐, 술폭시드): -S(=O)R, 이때 R은 술핀 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술핀 기의 예로는 -S(=O)CH3 그리고 -S(=O)CH2CH3을 포함하나 이에 한정되지 않는다.
술폰 (술포닐): -S(=O)2R, 이때 R은 술폰 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기, 예로써, 불소첨가된 또는 과불소첨가된 C1-7 알킬 기다. 술폰 기의 예로는 -S(=O)2CH3 (메탄술포닐, 메실), -S(=O)2CF3 (트리플일), -S(=O)2CH2CH3 (에실), -S(=O)2C4F9 (노나플일), -S(=O)2CH2CF3 (트레실), -S(=O)2CH2CH2NH2 (타우릴), -S(=O)2Ph (페닐술포닐, 베실), 4-메틸페닐술포닐 (토실), 4-클로로페닐술포닐 (클로실), 4-브로모페닐술포닐 (브로실), 4-니트로페닐 (노실), 2-나프탈렌술포네이트 (냅실), 그리고 5-디메틸아미노-나프탈렌-1-일술포네이트 (단실)을 포함하나 이에 한정되지 않는다.
술핀산 (술피노): -S(=O)OH, -SO2H.
술폰산 (술포): -S(=O)2OH, -SO3H.
술피네이트(술피닌산 에스테르): -S(=O)OR; 이때 R은 술피네이트 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술피네이트 기의 예로는 -S(=O)OCH3 (메톡시술피닐; 메틸 술피네이트) 그리고 -S(=O)OCH2CH3 (에톡시술피닐; 에틸 술피네이트)을 포함하나 이에 한정되지 않는다.
술포네이트 (술포닌산 에스테르): -S(=O)2OR, 이때 R은 술포네이트 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술포네이트 기의 예로는 -S(=O)2OCH3 (메톡시술포닐; 메틸 술포네이트) 그리고 -S(=O)2OCH2CH3 (에톡시술포닐; 에틸 술포네이트)을 포함하나 이에 한정되지 않는다.
술피닐옥시: -OS(=O)R, 이때 R은 술피닐옥시 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술피닐옥시기의 예로는 -OS(=O)CH3 그리고 -OS(=O)CH2CH3을 포함하나 이에 한정되지 않는다.
술포닐옥시: -OS(=O)2R, 이때 R은 술포닐옥시 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술포닐옥시 기의 예로는 -OS(=O)2CH3 (메실레이트) 그리고 -OS(=O)2CH2CH3 (에실레이트)을 포함하나 이에 한정되지 않는다.
술페이트: -OS(=O)2OR; 이때 R은 술페이트 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술페이트 기의 예로는 -OS(=O)2OCH3 그리고 -SO(=O)2OCH2CH3을 포함하나 이에 한정되지 않는다.
술파밀(술파모일; 술핀산 아미드; 술핀아미드): -S(=O)NR1R2, 이때 R1 및 R2는 아미노기에 대해 정의된 바와 같이 독립적으로 아미노 치환체다. 술파밀 기의 예로는 -S(=O)NH2, -S(=O)NH(CH3), -S(=O)N(CH3)2, -S(=O)NH(CH2CH3), -S(=O)N(CH2CH3)2, 그리고 -S(=O)NHPh을 포함하나 이에 한정되지 않는다.
술폰아미도 (술피나모일; 술폰산 아미드; 술폰아미드): -S(=O)2NR1R2, 이때 R1 및 R2는 아미노기에 대해 정의된 바와 같이 독립적으로 아미노 치환체다. 술폰아미도 기의 예로는 -S(=O)2NH2, -S(=O)2NH(CH3), -S(=O)2N(CH3)2, -S(=O)2NH(CH2CH3), -S(=O)2N(CH2CH3)2, 그리고 -S(=O)2NHPh을 포함하나 이에 한정되지 않는다.
술프아미노: -NR1S(=O)2OH, 이때 R1은 아미노기에 대해 정의된 바와 같이 아미노 치환체다. 술프아미노 기의 예로는 -NHS(=O)2OH 그리고 -N(CH3)S(=O)2OH을 포함하나 이에 한정되지 않는다.
술폰아미노: -NR1S(=O)2R, 이때 R1은 아미노기에 대해 정의된 바와 같이 아미노 치환체이며, 그리고 R은 술폰아미노 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술폰아미노 기의 예로는 -NHS(=O)2CH3 그리고 -N(CH3)S(=O)2C6H5를 포함하나 이에 한정되지 않는다.
술핀아미노: -NR1S(=O)R, 이때 R1은 아미노기에 대해 정의된 바와 같이 아미노 치환체이며, 그리고 R은 술핀아미노 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 C1-7 알킬 기다. 술핀아미노 기의 예로는 -NHS(=O)CH3 그리고 -N(CH3)S(=O)C6H5를 포함하나 이에 한정되지 않는다.
포스피노 (포스핀): -PR2, 이때 R은 포스피노 치환체, 예로써, -H, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스피노 기의 예로는 -PH2, -P(CH3)2, -P(CH2CH3)2, -P(t-Bu)2, 그리고 -P(Ph)2을 포함하나 이에 한정되지 않는다.
포스포: -P(=O)2.
포스피닐 (포스핀 옥시드): -P(=O)R2, 이때 R은 포스피닐 치환체, 예로써, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기. 일부 구체예들에 있어서, R은 C1-7 알킬 기 또는 C5-20 아릴 기다. 포스피닐 기의 예로는 -P(=O)(CH3)2, -P(=O)(CH2CH3)2, -P(=O)(tBu)2, 그리고 -P(=O)(Ph)2을 포함하나 이에 한정되지 않는다.
포스핀산 (포스포노): -P(=O)(OH)2.
포스포네이트 (포스포노 에스테르): -P(=O)(OR)2, 여기에서 R은 포스포네이트 치환체, 예로써, -H, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스포네이트 기의 예로는 -P(=O)(OCH3)2, -P(=O)(OCH2CH3)2, -P(=O)(O-tBu)2, 그리고 -P(=O)(OPh)2을 포함하나 이에 한정되지 않는다.
포스포린산(포스포노옥시): -OP(=O)(OH)2.
포스페이트 (포스포노옥시 에스테르): -OP(=O)(OR)2, 여기에서 R은 포스페이트 치환체, 예로써, -H, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스페이트 기의 예로는 -OP(=O)(OCH3)2, -OP(=O)(OCH2CH3)2, -OP(=O)(OtBu)2, 그리고 -OP(=O)(OPh)2을 포함하나 이에 한정되지 않는다.
포스포러스산: -OP(OH)2
포스피트: -OP(OR)2, 여기에서 R은 포스피트 치환체, 예로써, -H, C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스피트 기의 예로는 -OP(OCH3)2, -OP(OCH2CH3)2, -OP(OtBu)2, 그리고 -OP(OPh)2을 포함하나 이에 한정되지 않는다.
포스포라미디트: -OP(OR1)-NR2 2, 여기에서 R1 및 R2는 포스포라미드트 치환체, 예로써, -H, (임의선택적으로 치환된) C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R은 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스포라미드트 기의 예로는 -OP(OCH2CH3)-N(CH3)2, -OP(OCH2CH3)-N(i-Pr)2, 그리고 -OP(OCH2CH2CN)-N(i-Pr)2을 포함하나 이에 한정되지 않는다.
포스포라미데이트: -OP(=O)(OR1)-NR2 2, 여기에서 R1 및 R2는 포스포라미데이트 치환체, 예로써, -H, (임의선택적으로 치환된) C1-7 알킬 기, C3-20 헤테로시클일 기, 또는 C5-20 아릴 기다. 일부 구체예들에 있어서, R1 및 R2는 -H, C1-7 알킬 기, 또는 C5-20 아릴 기다. 포스포라미데이트 기의 예로는 -OP(=O)(OCH2CH3)-N(CH3)2, -OP(=O)(OCH2CH3)-N(i-Pr)2, 그리고 -OP(=O)(OCH2CH2CN)-N(i-Pr)2을 포함하나 이에 한정되지 않는다.
본 명세서에서 용어 "C3-12 알킬렌"은 3 내지 12개의 탄소 원자(명시적으로 다른 언급이 없는 한)를 보유하는, 지방족이며, 사이클 또는 비사이클일 수 있는 탄화 수소 화합물의 동일한 탄소 원자, 또는 2개의 상이한 탄소 원자 각각으로부터 2개의 수소원자를 제거함으로써 획득되는 이좌배위자(bidentate) 모이어티에 관계한다. 따라서, 용어 "알킬렌"은 아래에서 논의되는 바와 같이 하위부류 알케닐렌, 알키닐렌, 시클로알킬렌, 등을 포함한다.
선형 포화 C3-12 알킬렌 기의 예로는 -(CH2)n- (여기에서 n은 3 내지 12의 정수), 예로써, -CH2CH2CH2- (프로필렌), -CH2CH2CH2CH2- (부틸렌), -CH2CH2CH2CH2CH2- (펜틸렌) 그리고 -CH2CH2CH2CH2CH2CH2CH2- (헵틸렌)을 포함하나 이에 한정되지 않는다.
분기화된 포화 C3-12 알킬렌 기의 예로는 -CH(CH3)CH2-, -CH(CH3)CH2CH2-, -CH(CH3)CH2CH2CH2-, -CH2CH(CH3)CH2-, -CH2CH(CH3)CH2CH2-, -CH(CH2H3)-, -CH(CH2H3)CH2-, 그리고 -CH2CH(CH2H3)CH2-을 포함하나 이에 한정되지 않는다.
선형 부분적으로 불포화 C3-12 알킬렌 기 (C3-12 알케닐렌, 그리고 알키닐렌 기)의 예로는 -CH=CHCH2-, -CH2-CH=CH2-, -CH=CHCH2CH2-, -CH=CHCH2CH2CH2-, -CH=CHCH=CH-, -CH=CHCH=CH-CH2-, -CH=CH-CH=CH-CH2CH2-, -CH=CH-CH2CH=CH-, -CH=CHCH2CH2CH=CH-, 그리고 -CH2-C≡C-CH2-을 포함하나 이에 한정되지 않는다.
분기화된 부분적으로 불포화 C3-12 알킬렌 기 (C3-12 알케닐렌 그리고 알키닐렌 기)의 예로는 -C(CH3)=CH-, -C(CH3)=CHCH2-, -CH=CHCH(CH3)- 그리고 -C≡C-CH(CH3)-을 포함하나 이에 한정되지 않는다.
알리사이클 포화 C3-12 알킬렌 기 (C3-12 시클로알킬렌)의 예로는 시클로펜틸렌(예컨데 시클로펜트-1,3-일렌), 그리고 시클로헥실렌 (예컨데 시클로헥스-1,4-일렌)을 포함하나 이에 한정되지 않는다.
알리사이클 부분적으로 불포화 C3-12 알킬렌 기 (C3-12 시클로알킬렌)의 예로는 시클로펜테닐렌(예컨데 4-시클로펜텐-1,3-일렌), 시클로헥센일렌(예컨데 2-시클로헥센-1,4-일렌; 3-시클로헥센-1,2-일렌; 2,5-시클로헥사디엔-1,4-일렌)을 포함하나 이에 한정되지 않는다.
"링커"는 공유 결합 또는 약물 모이어티에 항체가 공유적으로 부탁되는 원자의 쇄를 포함하는 화학적 모이어티를 지칭한다. 비제한적인 예시적인 링커들은 본 명세서에서 설명된다.
용어 "키랄(chiral)"은 거울상 짝의 겹쳐지지 않은 성질을 보유하는 분자를 지칭하고, 한편 용어 "아키랄(achiral)"은 이들의 거울상 짝에 겹쳐질 수 있는 분자를 지칭한다.
용어 "입체이성질체(stereoisomer)"는 동일한 화학적 구성을 보유하지만, 그러나 공간에서 원자 또는 기의 배열이 상이한 화합물들을 말한다.
"부분입체이성질체(diastereomer)"는 하나 또는 그 이상의 키랄성을 가지지만, 이들 분자는 서로 거울상이 아닌 입체이성질체를 말한다. 부분입체이성질체들은 상이한 물리적 성질, 예컨데 용융점, 끓는점, 스펙트럼 성질, 및 반응성을 보유한다. 부분입체이성질체 혼합물들은 고해상 분석 과정, 이를 테면 전기영동 및 크로마토그래피에 의해 분리될 수 있다.
"거울상이성질체(enantiomers)"는 서로 겹쳐질 수 없는 거울 상인 화합물의 두 입체이성질체를 말한다.
본 명세서에서 이용된 입체적 정의 및 관례는 일반적으로 S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; 그리고 Eliel, E. and Wilen, S., Stereocchemistry of Organic Compounds (1994) John Wiley & Sons, Inc., New York에 따른다. 많은 유기 화합물들은 광학적으로 활성 형태로 존재하는데, 가령, 화합물들은 편광 면을 회전하는 능력을 보유한다. 광학적으로 활성 화합물이 설명될 때, 접두어 D 그리고 L, 또는 R 그리고 S는 이의 키랄 중심(들)에 대해 분자의 절대적인 배치를 나타내는데 이용된다. 접두어 d 그리고 l 또는 (+) 그리고 (-)은 화합물에 의해 편광의 회전 신호를 나타내는데 이용되는데, (-) 또는 l은 이 화합물이 좌회선성임을 의미한다. (+) 또는 d가 앞에 붙은 화합물은 우회전성이다. 주어진 화학 구조에서, 이러한 입체이성질체들은 서로 거울상인 것을 제외하고 동일하다. 특정 입체이성질체는 거울상체라고도 하는데, 이러한 이성질체의 혼합물은 거울상체 혼합물이라고도 한다. 거울상체의 50:50 혼합물은 라셈 혼합물 또는 라셈체라고도 하는데, 화학 반응 또는 공정에서 입체선택 또는 입체특이성이 없을 때 발생될 수 있다. 용어 "라셈(racemic) 혼합물" 그리고 "라셈체(racemate)"는 광학적 활성없이 2개의 거울상체의 등몰(equimolar) 혼합물을 말한다.
"이탈(Leaving) 기"는 또다른 기능기에 의해 치환될 수 있는 기능기를 말한다. 특정 이탈기는 당분야에 공지되어 있으며, 예로는 할로겐화물(예컨데, 염소화물, 브롬화물, 요오드화물), 메탄술포닐 (메실), p-톨루엔술포닐 (토실), 트리플루오로메틸술포닐 (트리플레이트), 그리고 트리플루오로메틸술포네이트를 포함하나 이에 한정되지 않는다.
용어 "보호(protecting) 기"는 화합물상에 있는 다른 반응기가 반응하는 동안 특정 반응기를 차단 또는 보호하는 치환체를 말한다. 예로써, "아미노-보호 기"는 화합물에 있는 아미노 기능기를 차단 또는 보호하는 아미노 기에 부착된 치환체다. 적절한 아미노-보호 기는 아세틸, 트리플루오로아세틸, t-부톡시카르보닐 (BOC), 벤질옥시카르보닐 (CBZ) 그리고 9-플루오레닐메틸렌옥시카르보닐 (Fmoc)을 포함하나 이에 한정되지 않는다. 보호 기와 이들의 용도에 대한 전반적인 설명은 T. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991, 또는 이후 편집물을 참고한다.
II. 조성물 및 방법
한 측면에서, 본 발명은 CD22에 결합하는 항체 및 이러한 항체가 포함된 면역접합체에 일부 기초된다. 본 발명의 항체 및 면역접합체는 예컨데, CD22-양성 암의 진단 또는 치료에 유용하다.
A. 예시적인 항-CD22 항체
일부 구체예들에 있어서, CD22에 결합하는 단리된 항체가 제공된다. CD22는 분화의 성숙 단계에서 B-세포 표면에서 발현되는 135-kDa의 B-세포-제한된 시알로당단백질이다. CD22는 다양한 B-세포 관련된 장애 및 다양한 임파종들, 이를 테면 비-호지킨 임파종이 포함된 암에서 발현된다.
신호 서열 (아미노산 1 내지 19)을 가진, 예시적인 자연 발생적 인간 CD22 전구물질 서열은 서열 번호: 28에 제공되며, 그리고 대응하는 성숙 CD22 서열은 서열 번호: 29 (서열 번호: 28의 아미노산 20 내지 847에 대응)에서 제공된다. 신호 서열 (아미노산 1 내지 19)을 가진, 추가적인 예시적인 자연 발생적 인간 CD22 전구물질 서열은 서열 번호: 30에 제공되며, 그리고 대응하는 성숙 CD22 서열은 서열 번호: 31 (서열 번호: 30의 아미노산 20 내지 670에 대응)에서 제공된다.
특정 구체예들에 있어서, 항-CD22 항체는 서열 번호: 28의 아미노산 20 내지 240 내에 있는 에피토프에 결합한다. 이러한 항체의 비-제한적 예시로는 10F4 및 이의 인간화된 버전이 포함된다. 일부 구체예들에 있어서, 항-CD22 항체는 인간 CD22에 결합한다. 일부 구체예들에 있어서, 항-CD22 항체는 인간 CD22 및 시노몰구스 원숭이 CD22에 결합한다.
일부 구체예들에 있어서, 항-CD22 항체는 ≤ 10 nM, 또는 ≤ 5 nM, 또는 ≤ 4 nM, 또는 ≤ 3 nM, 또는 ≤ 2 nM의 친화력 그리고 임의선택적으로 ≥ 0.0001 nM, 또는 ≥ 0.001 nM, 또는 ≥ 0.01 nM의 친화력으로 인간 CD22에 결합한다. 이러한 항체의 비-제한적 예시로는 차례로 2.4 nM, 1.1-1.7 nM, 그리고 1.6 nM의 친화력으로 인간 CD22에 결합하는 mu10F4, hu10F4v1, 그리고 hu10F4v3이 포함되는데, 예컨데, US 2008/0050310 참고.
분석(Assays)
항-CD22 항체가 "서열 번호: 28의 아미노산 20 내지 240 내에 있는 에피토프에 결합하는 지"를 판단하기 위하여, N- 및 C-말단 결손을 가진 CD22 폴리펩티드는 CHO 세포에서 발현되며, 그리고 절두된 폴리펩티드에 상기 항체의 결합되는지는 이미 설명된 바와 같이 FACS에 의해 테스트된다. 예컨데, US 2008/0050310 참고. CHO 세포에서 발현된 전장의 CD22에 대한 결합과 비교하여 절두된 폴리펩티드에 대한 상기 항체의 결합의 실질적인 감소(≥ 70% 감소) 또는 배제는 상기 항체가 절두된 폴리펩티드에 결합하지 않음을 나타낸다.
항-CD22 항체가 ≤ 10 nM, 또는 ≤ 5 nM, 또는 ≤ 4 nM, 또는 ≤ 3 nM, 또는 ≤ 2 nM의 "친화력으로 결합"하는지의 판단은 연속적으로 희석된, 라벨안된 항-CD22 항체를 이용한 경쟁 분석에서 표면상에 CD22를 발현시키는 CHO 세포를 이용하여 결정된다. 예컨데, US 2008/0050310 참고. 이 항체의 결합 친화력, KD는 비-선형 곡선 피팅 프로그램을 이용하여 실행되는 표준 Scatchard 분석에 따라 결정될 수 있다(예로써, Munson et al., Anal Biochem, 107: 220-239, 1980 참고).
항체 10F4 및 다른 구체예들
일부 구체예들에 있어서, 본 발명은 (a) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3으로부터 선택된 최소한 1, 2, 3, 4, 5, 또는 6개의 HVRs가 포함된 항-CD22 항체 또는 면역접합체를 제공한다. 일부 구체예들에 있어서, 본 발명은 (a) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 15의 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 13의 아미노산 서열을 포함하는 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열을 포함하는 HVR-L3으로부터 선택된 최소한 1, 2, 3, 4, 5, 또는 6개의 HVRs가 포함된 항-CD22 항체 또는 면역접합체를 제공한다.
한 측면에서, 본 발명은 (a) 서열 번호: 9의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 10의 아미노산 서열을 포함하는 HVR-H2; 그리고 (c) 서열 번호: 11의 아미노산 서열을 포함하는 HVR-H3으로부터 선택된 최소한 1개, 최소한 2개 또는 3개 VH HVR 서열이 모두 포함된 항체 또는 면역접합체를 제공한다. 한 구체예에 있어서, 상기 항체는 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3을 포함한다. 또다른 구체예에 있어서, 상기 항체는 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3을 포함하고, 그리고 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함한다. 추가 구체예에 있어서, 상기 항체는 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3을 포함하고, 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함하고, 그리고 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2를 포함한다. 추가 구체예에 있어서, 상기 항체는 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1; (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2; 그리고 (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3을 포함한다.
또다른 측면에서, 본 발명은 (a) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VL HVR 모두가 포함된 항체 또는 면역접합체를 제공한다. 또다른 측면에서, 본 발명은 (a) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VL HVR 모두가 포함된 항체 또는 면역접합체를 제공한다. 한 구체예에 있어서, 상기 항체는 (a) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함한다. 한 구체예에 있어서, 상기 항체는 (a) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함한다.
또다른 측면에서, 본 발명의 항체 또는 면역접합체는 (a) (i) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, 그리고 (iii) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VH HVR 서열 모두가 포함된 VH 도메인; 그리고 (b) (i) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VL HVR 서열 모두가 포함된 VL 도메인을 포함한다. 또다른 측면에서, 본 발명의 항체 또는 면역접합체는 (a) (i) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, 그리고 (iii) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VH HVR 서열 모두가 포함된 VH 도메인; 그리고 (b) (i) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고(c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 최소한 1개, 최소한 2개 또는 3개의 VL HVR 서열 모두가 포함된 VL 도메인을 포함한다.
또다른 측면에서, 본 발명은 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1; (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2; (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3; (d) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1; (e) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함하는 항체 또는 면역접합체를 제공한다. 또다른 측면에서, 본 발명은 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1; (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2; (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3; (d) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1; (e) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함하는 항체 또는 면역접합체를 제공한다..
상기 구체예들중 임의의 것에 있어서, 항-CD22 항체는 인간화된다. 한 구체예에 있어서, 항-CD22 항체는 상기 구체예들중 임의의 것에서와 같이 HVRs을 포함하고, 인간 수용 골격, 예컨데 인간 면역글로블린 골격 또는 인간 공통 골격을 더 포함한다. 특정 구체예들에 있어서, 인간 수용체 골격은 인간 VL 카파 1 (VLKI) 골격 및/또는 VH 골격 VHIII이다. 일부 구체예들에 있어서, 인간화된 항-CD22 항체는 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1; (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2; (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3; (d) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1; (e) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함한다. 일부 구체예들에 있어서, 인간화된 항-CD22 항체는 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1; (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2; (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3; (d) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1; (e) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (f) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3을 포함한다.
또다른 측면에서, 항-CD22 항체는 서열 번호: 7의 아미노산 서열에 대하여 최소한 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100% 서열 동일성을 보유한 중쇄 가변 도메인 (VH) 서열을 포함한다. 특정 구체예들에 있어서, 서열 번호: 7의 아미노산 서열에 대하여 최소한 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99% 서열 동일성을 보유한 VH 서열은 기준 서열과 비교하여 치환 (예컨데, 보존적 치환), 삽입, 또는 결손을 포함하지만, 항-CD22 항체는 CD22에 결합하는 능력을 유지하는 서열을 포함한다. 특정 구체예들에 있어서, 서열 번호: 7에서 총 1 내지 10개의 아미노산이 치환되거나, 삽입되거나 및/또는 결손되었다. 특정 구체예들에 있어서, 서열 번호: 7에서 총 1 내지 5개의 아미노산이 치환되거나, 삽입되거나 및/또는 결손되었다. 특정 구체예들에 있어서, 치환, 삽입, 또는 결손은 HVRs 밖의 영역(이를 테면, FRs)에서 일어난다.
임의선택적으로, 항-CD22 항체는 서열 번호: 5 또는 서열 번호: 7의 해독후 변형이 포함된, 서열 번호: 5 또는 서열 번호: 7의 VH 서열을 포함한다. 특정 구체예에 있어서, VH는 (a) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (b) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, 그리고 (c) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3로부터 선택된 하나, 둘 또는 세 개의 HVRs을 포함한다.
일부 구체예들에 있어서, 항-CD22 항체가 제공되는데, 이때 상기 항체는 서열 번호: 8의 아미노산 서열에 대하여 최소한 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100% 서열 동일성을 갖는 경쇄 가변 도메인 (VL)을 포함한다. 특정 구체예들에 있어서, 서열 번호: 8의 아미노산 서열에 대하여 최소한 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99% 서열 동일성을 보유한 VL 서열은 기준 서열과 비교하여 치환 (예컨데, 보존적 치환), 삽입, 또는 결손을 포함하지만, 항-CD22 항체는 CD22에 결합하는 능력을 유지하는 서열을 포함한다. 특정 구체예들에 있어서, 서열 번호: 8에서 총 1 내지 10개의 아미노산이 치환되거나, 삽입되거나 및/또는 결손되었다. 특정 구체예들에 있어서, 서열 번호: 8에서 총 1 내지 5개의 아미노산이 치환되거나, 삽입되거나 및/또는 결손되었다. 특정 구체예들에 있어서, 치환, 삽입, 또는 결손은 HVRs 밖의 영역(이를 테면, FRs)에서 일어난다. 임의선택적으로, 항-CD22 항체는 서열 번호: 6 또는 서열 번호: 8의 해독후 변형이 포함된, 서열 번호: 6 또는 서열 번호: 8의 VL 서열을 포함한다. 특정 구체예에 있어서, VL은 (a) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고 (c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 하나, 둘 또는 세 개의 HVRs을 포함한다. 일부 구체예들에 있어서, VL은 (a) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1; (b) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2; 그리고(c) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3에서 선택된 하나, 둘 또는 세 개의 HVRs을 포함한다.
또다른 측면에서, 항-CD22 항체가 제공되는데, 이때 상기 항체는 상기에서 제공된 임의의 구체예들에서와 같은 VH와 상기에서 제공된 임의의 구체예들에서와 같은 VL을 포함한다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 7 및 서열 번호: 8의 차례로 VH 및 VL 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 5 및 서열 번호: 6의 차례로 VH 및 VL 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 24 및 서열 번호: 23의 차례로 중쇄 및 경쇄 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 26 및 서열 번호: 23의 차례로 중쇄 및 경쇄 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 25 및 서열 번호: 23의 차례로 중쇄 및 경쇄 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다. 일부 구체예들에 있어서, 상기 항체는 서열 번호: 27 및 서열 번호: 23의 차례로 중쇄 및 경쇄 서열을 포함하는데, 이때 이들의 전사 후 변형도 포함된다.
추가 측면에 있어서, 본 발명은 본 명세서에서 제공되는 항-CD22 항체와 동일한 에피토프에 결합되는 항체 또는 면역접합체를 제공한다. 예로써, 특정 구체예들에 있어서, 서열 번호: 7의 VH 서열과 서열 번호: 8의 VL 서열이 포함된 항-CD22 항체와 동일한 에피토프에 결합되는 항체 또는 면역접합체가 제공된다. 특정 구체예들에 있어서, 서열 번호: 28의 아미노산 20 내지 240으로부터, 이내에 또는 이와 중첩되는 에피토프에 결합하는 항체가 제공된다.
본 발명의 추가 측면에 있어서, 상기 구체예들중 임의의 것에 따른 항-CD22 항체는 키메라, 인간화된 또는 인간 항체가 포함된 단클론 항체다. 한 구체예에 있어서, 항-CD22 항체는 항체 단편, 예컨데, a Fv, Fab, Fab', scFv, 디아바디(diabody), 또는 F(ab')2 단편이다. 또다른 구체예에 있어서, 상기 항체는 실질적으로 전장 항체, 예컨대, IgG1 항체 또는 본 명세서에서 정의된 바와 같은 다른 항체 분류 또는 이소타입이다.
상기에서 설명된 임의의 면역접합체에서, 상기 항체는 약물 모이어티에 접합될 수 있다. 일부 구체예들에 있어서, 상기 항체는 세포독성 물질에 접합된다. 이러한 일부 구체예들에 있어서, 상기 세포독성 물질은 피롤로벤조디아제핀 (PBD), 이를 테면 PBD 이합체다. 다양한 비제한적인 예시적인 PBD 이합체는 본 명세서에서 논의된다.
추가 측면에 있어서, 상기 구체예들중 임의의 것에 따른 항-CD22 항체 또는 면역접합체는 하기 섹션 1-7에서 설명된 바와 같이 특징들중 임의의 것을 단독, 또는 조합하여 포함할 수 있다.
1. 항체 친화력
특정 구체예들에 있어서, 본 명세서에서 제공된 항체는 ≤ 1μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM의 해리 상수 (Kd)를 보유하고 그리고 임의선택적으로 ≥ 10-13 M. (예컨데 10-8 M 또는 그 미만, 예컨데 10-8 M 내지 10-13 M, 예컨데, 10-9 M 내지 10-13 M)이다.
한 구체예에 있어서, Kd는 다음의 분석에서 설명된 것과 같이 관심 항체의 Fab 버전과 이의 항원으로 실행된 방사능라벨된 항원 결합 분석(RIA)에 의해 측정된다. 항원에 대한 Fabs의 용액 결합 친화력은 라벨안된 항원의 적정(titration) 시리즈 존재하에 최소 농도의 (125I)-라벨된 항원과 평형화(equilibrating)되고, 그 다음 항-Fab 항체-피복된 플레이트에 결합된 항원을 포집함으로써 측정된다(예컨데, Chen et al., J. Mol. Biol. 293:865-881(1999) 참고). 분석 조건을 확립하기 위하여, MICROTITER® 다중-웰 플레이트 (Thermo Scientific)는 50 mM 탄산나트륨 (pH 9.6)내에서 5 μg/ml의 포획 항-Fab 항체 (Cappel Labs)로 하룻밤 동안 피복되며, 그리고 후속적으로 실온(대략적으로 23℃)에서 2 내지 5시간 동안 PBS에서 2% (w/v) 소의 혈청 알부민으로 차단된다. 비-흡착성 플레이트 (Nunc #269620)에서, 100 pM 또는 26 pM [125I]-항원은 관심 Fab(예컨데, 항-VEGF 항체, Fab-12의 평가와 일관된, Presta et al., Cancer Res. 57:4593-4599 (1997))의 일련의 희석물과 혼합된다. 그 다음 관심 Fab는 하룻밤동안 항온처리되며; 그러나, 항온처리는 평형에 확실히 도달되도록 더 오랜 기간(예컨데, 약 65 시간)동안 지속될 수 있다. 그 이후, 혼합물은 실온에서 항온처리를 위하여(예컨대, 한 시간) 포획 플레이트로 옮겨진다. 그 다음 용액이 제거되고, 플레이트는 PBS 안에서 0.1% 폴리소르베이트 20 (TWEEN-20®)로 8회 세척되었다. 플레이트가 건조되었을 때, 150 μl/웰의 섬광물질 (MICROSCINT-20™; Packard)이 추가되며, 그리고 플레이트는 10분간 TOPCOUNT™ 감마 카운터(Packard) 상에서 카운트된다. 최대 결합의 20% 미만 또는 20%를 제공하는 각 Fab 농도는 경쟁 결합 분석에 사용하기 위하여 선택된다.
또다른 구체예에 따르면, Kd는 25℃에서 ~10 반응 단위(RU)에서 고정된 항원 CM5 칩(chips)과 함께 BIACORE®-2000 또는 BIACORE®-3000 (BIAcore, Inc., Piscataway, NJ)을 이용하여 표면 플라스몬 공명 분석에 의해 측정된다. 간략하게 설명하자면, 카르복시메틸화된 덱스트란 바이오센스 칩(CM5, BIACORE, Inc.)은 공급업자의 지침에 따라 N-에틸-N'-(3-디메틸아미노프로필)-카르보디이미드 히드로클로라이드 (EDC) 그리고 N-히드록시숙시니미드 (NHS)로 활성화된다. 항원은 10 mM 아세테이트 나트륨, pH 4.8로 5 μg/ml (~0.2 μM)으로 희석된 후 결합 단백질의 대략적으로 10 반응 단위(RU)를 획득하기 위하여 분당 5 μl의 유속으로 주사된다. 항원 주사 후, 1 M 에탄올아민은 반응안된 기를 차단하기 위하여 주사된다. 역학 측정을 위하여, Fab의 2배 연속 희속물(0.78 nM 내지 500 nM)은 25℃에서 0.05% 폴리소르베이트 20 (TWEEN-20™) 계면활성제 (PBST)와 함께 PBS로 대략적으로 분당 25 μl의 유속으로 주사된다. 결합율 (kon) 및 해리율(koff)은 결합 및 해리 센서그램(sensorgram)을 동시에 피팅함으로써 단순 1 대 1 Langmuir 결합 모델 (BIACORE® Evaluation Software 버젼 3.2)로 산출된다. 평형 해리 상수 (Kd)는 koff/kon의 비율로 산출된다. 예컨데, Chen et al., J. Mol. Biol. 293:865-881 (1999) 참고. 결합율이 상기 표면 플라스몬 공명 분석에 따라 106 M-1 s-1을 초과하는 경우, 결합율은 25℃에서 분광계, 이를 테면 정지-유동(stop-flow) 구비된 분광광도계(Aviv Instruments) 또는 교반(stirred) 큐벳을 갖춘 8000-시리즈 SLM-AMINCO TM 분광광도계(ThermoSpectronic)에서 측정되었을 때 항원의 농도가 증가되는 조건하에서 PBS, pH 7.2에서 20 nM 항-항원 항체 (Fab 형태)의 형광 방출 강도의 증가 또는 감소를 측정하는 형광 담금질 기술을 이용하여 측정될 수 있다(여기 = 295 nm; 방출 = 340 nm, 16 nm 밴드-패스)
2. 항체 단편들
특정 구체예들에 있어서, 본 명세서에서 제시되는 항체는 항체 단편이다. 항체 단편들은 Fab, Fab', Fab'-SH, F(ab')2, Fv, 그리고 scFv 단편, 그리고 하기에서 설명되는 다른 단편을 포함하나 이에 한정되지 않는다. 특정 항체 단편에 대한 검토는 Hudson et al. Nat. Med. 9:129-134 (2003)을 참고한다. scFv 단편에 대한 검토는 예컨데, Pluckthuen, in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994)을 참고하고; 또한 WO 93/16185; 그리고 U.S. 특허 5,571,894 그리고5,587,458를 또한 참고한다. 구조 수용체 결합 에피토프 잔기를 포함하고, 생체내 반감기가 증가된 Fab 및 F(ab')2 단편에 대한 논의는 U.S. 특허 5,869,046을 참고한다.
디아바디는 이가(bivalent) 또는 이중특이적인 2개의 항원-결합 부위를 가진 항체 단편이다. 예로써, EP 404,097; WO 1993/01161; Hudson et al., Nat. Med. 9:129-134 (2003); 그리고 Hollinger et al., Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993)을 참고한다. 트리아바디(triabodies) 및 테트라바디(tetrabodies) 또한 Hudson et al., Nat. Med. 9:129-134 (2003)에서 설명된다.
단일-도메인 항체는 항체의 중쇄 가변 도메인의 전부 또는 일부 또는 경쇄 가변 도메인의 전부 또는 일부가 포함된 항체 단편이다. 특정 구체예들에 있어서, 단일-도메인 항체는 인간 단일-도메인 항체 (Domantis, Inc., Waltham, MA; 예컨데, U.S. 특허 6,248,516 B1 참고)다.
항체 단편은 하기에서 설명된 것과 같이, 고유한 항체의 단백질 절단 뿐만 아니라 재조합 숙주 세포(예컨데 대장균(E. coli) 또는 파아지)에 의해 생산되는 것을 포함하나 이에 한정되지 않는 다양한 기술에 의해 만들어질 수 있다.
3. 키메라 및 인간화된 항체
특정 구체예들에 있어서, 본 명세서에서 제공된 항체는 키메라 항체다. 특정 키메라 항체는 예컨데, U.S. 특허 4,816,567; 그리고 Morrison et al., Proc. Natl. Acad. Sci. USA, 81:6851-6855 (1984))에서 설명된다. 한 실시예에서, 키메라 항체는 비-인간 가변 영역 (예컨데, 마우스, 렛, 헴스터, 토끼, 또는 비-인간 영장류, 이를 테면 원숭이로부터 유도된 가변 영역)과 인간 불변 영역을 포함한다. 추가 실시예에서, 키메라 항체는 분류 또는 아류가 부모 항체의 것으로부터 변화된 "분류 전환된(class switched)" 항체다. 키메라 항체는 이의 항원-결합 단편을 포함한다.
특정 구체예들에 있어서, 키메라 항체는 인간화된 항체다. 전형적으로, 비-인간 항체는 인간에 대한 면역원성이 감소되도록 인간화되며, 한편, 부모의 비-인간 항체의 특이성 및 친화력은 유지된다. 일반적으로, 인간화된 항체는 HVRs, 예컨데, CDRs(또는 이의 일부분)은 비-인간 항체로부터 유도되며, FRs (또는 이의 일부분)은 인간 항체 서열로부터 유도된 하나 또는 그 이상의 가변 도메인들을 포함한다. 인간화된 항체는 임의선택적으로 인간 불변 영역의 최소한 일부분을 또한 포함할 수 있다. 일부 구체예들에 있어서, 항체 특이성 또는 친화력을 복원 또는 개선시키기 위하여, 인간화된 항체에서 일부 FR 잔기는 비-인간 항체 (예컨데, HVR 잔기가 유도된 상기 항체)의 대응하는 잔기로 치환된다.
인간화된 항체 및 이의 제법은 예컨데, Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008)에서 검토되며, 예컨데, Riechmann et al., Nature 332:323-329 (1988); Queen et al., Proc. Nat'l Acad. Sci. USA 86:10029-10033 (1989); US 특허 5, 821,337, 7,527,791, 6,982,321, 그리고 7,087,409; Kashmiri et al., Methods 36:25-34 (2005) (SDR (a-CDR) 접목을 설명); Padlan, Mol. Immunol. 28:489-498 (1991) ("재표면화(resurfacing)" 설명); Dall'Acqua et al., Methods 36:43-60 (2005) ("FR 셔플링(shuffling)"설명); 그리고 Osbourn et al., Methods 36:61-68 (2005) 그리고 Klimka et al., Br. J. Cancer, 83:252-260 (2000) (FR 셔플링에 대한 "유도된 선별" 방식을 설명)에서 추가 설명된다.
인간화를 위하여 이용되는 인간 골격 영역들은 다음을 포함하나 이에 한정되지 않는다: "베스트-핏(best-fit)" 방법을 이용하여 선별된 골격 영역 (예컨데, Sims et al. J. Immunol. 151:2296 (1993)); 경쇄 또는 중쇄 가변 영역의 특정 하위군의 인간 항체의 공통 서열로부터 유도된 골격 영역 (예컨데, Carter et al. Proc. Natl. Acad. Sci. USA, 89:4285 (1992); 그리고 Presta et al. J. Immunol., 151:2623 (1993) 참고); 인간 성숙 (체세포적으로 돌연변이된) 골격 영역 또는 인간 생식계역 골격 영역 (예컨데, Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008) 참고); 그리고 스크리닝 FR 라이브러리로부터 유도된 골격 영역(예컨데, Baca et al., J. Biol. Chem. 272:10678-10684 (1997) 그리고 Rosok et al., J. Biol. Chem. 271:22611-22618 (1996) 참고).
4. 인간 항체
특정 구체예들에 있어서, 본 명세서에서 제공되는 항체는 인간 항체다. 인간 항체는 당분야에 공지된 다양한 기술을 이용하여 생산될 수 있다. 인간 항체는 van Dijk and van de Winkel, Curr. Opin. Pharmacol. 5: 368-74 (2001) 그리고 Lonberg, Curr. Opin. Immunol. 20:450-459 (2008)에서 전반적으로 설명된다.
인간 항체는 항원 공격에 반응하여 고유한 인간 항체 또는 인간 가변 영역을 가진 고유한 항체를 만들기 위하여 변형된 유전자전이 동물에게 면역원을 투여함으로써 제조될 수 있다. 이러한 동물은 전형적으로 내생적 면역글로블린 좌를 대체한, 또는 염색체 외적으로 존재하거나 동물의 염색체 안에 무작위로 통합된 인간 면역글로블린 좌의 전부 또는 일부를 함유한다. 이러한 유전자전이 마우스에서, 내생적 면역글로블린 좌는 일반적으로 비활성화되어 있다. 유전자전이 동물로부터 인간 항체를 획득하는 방법에 대한 검토는 Lonberg, Nat. Biotech. 23:1117-1125 (2005)을 참고한다. 또한 예컨데, XENOMOUSETM 기술을 설명하는 U.S. 특허 6,075,181 및 6,150,584; HUMAB® 기술을 설명하는 U.S. 특허 5,770,429; K-M MOUSE® 기술을 설명하는 U.S. 특허 7,041,870, 그리고 VELOSCIMOUSE® 기술을 설명하는 U.S. 특허 출원 공개 US 2007/0061900을 참고한다). 이러한 동물에 의해 생성된 고유한 항체의 인간 가변 영역은 예컨데, 상이한 인간 불변 영역과 복합됨으로써 더 변형될 수 있다.
인간 항체는 하이브리도마-기반 방법에 의해 또한 만들어질 수 있다. 인간 단클론 항체 생산을 위하여 인간 골수종과 마우스-인간 헤테로골수종 세포 계통에 대해 설명되었다(예컨데, Kozbor J. Immunol., 133: 3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, pp. 51-63 (Marcel Dekker, Inc., New York, 1987); 그리고 Boerner et al., J. Immunol., 147: 86 (1991).) 인간 B-세포하이브리도마 기술을 통하여 생성된 인간 항체는 Li et al., Proc. Natl. Acad. Sci. USA, 103:3557-3562 (2006)에서 또한 설명된다. 추가 방법은 예로써, U.S. 특허 7,189,826 (하이브리도마 세포 계통으로부터 단클론 인간 IgM 항체를 생산하는 것을 설명) 그리고 Ni, Xiandai Mianyixue, 26(4):265-268 (2006) (인간-인간 하이브리도마를 설명)에서 설명된 것들을 포함한다. 인간 하이브리도마 기술 (Trioma technology)은 Vollmers and Brandlein, Histology and Histopathology, 20(3):927-937 (2005) 그리고 Vollmers and Brandlein, Methods and Findings in Experimental and Clinical Pharmacology, 27(3):185-91 (2005)에서 설명된다.
인간 항체는 인간-유도된 파아지 디스플레이 라이브러리로부터 선택된 Fv 클론 가변 도메인 서열을 단리함으로써 또한 생성될 수 있다. 이러한 가변 도메인 서열은 바람직한 인간 불변 도메인과 복합될 수 있다. 항체 라이브러리로부터 인간 항체를 선별하는 기술은 하기에서 설명된다.
5. 라이브러리-유도된 항체
항체는 바람직한 활성 또는 활성을 가지는 항체에 대하여 복합 라이브러리를 스크리닝함으로써 단리될 수 있다. 예로써, 파아지 디스플레이 라이브러리를 만들고, 바람직한 결합 특징을 보유한 항체에 대하여 이러한 라이브러리를 스크리닝하는 다양한 방법들이 당분야에 공지되어 있다. 이러한 방법들은 예컨데, Hoogenboom et al. in Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, 2001)에서 검토되며, 그리고 예컨데, McCafferty et al., Nature 348:552-554; Clackson et al., Nature 352: 624-628 (1991); Marks et al., J. Mol. Biol. 222: 581-597 (1992); Marks and Bradbury, Methods in Molecular Biology 248:161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004); Lee et al., J. Mol. Biol. 340(5): 1073-1093 (2004); Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004); 그리고 Lee et al., J. Immunol. Methods 284(1-2): 119-132(2004)에서 추가 설명된다.
특정 파아지 디스플레이 방법에서, VH 및 VL 유전자들의 레퍼토리는 폴리메라제 쇄 반응 (PCR)에 의해 별도로 클론되고, 파아지 라이브러리에서 무작위로 조합되며, 그 다음 Winter et al., Ann. Rev. Immunol., 12: 433-455 (1994)에서 설명된 것과 같이 항원-결합 파이지에 대하여 선별될 수 있다. 파아지는 전형적으로 단일-쇄 Fv (scFv) 단편 또는 Fab 단편으로던 항체 단편을 드러낸다. Libraries from 면역화된 원료로부터 라이브러리는 하이브리도마의 구축 없이도 면역원에 대한 고-친화력 항체를 제공한다. 대안으로, Griffiths et al., EMBO J, 12: 725-734 (1993)에서 설명된 바와 같이 임의의 면역화 없지 광범위한 비-자체 및 자체 항원에 대하여 항체의 단일 원료를 제공하기 위하여 (예컨대, 인간으로부터) 고유 레퍼토리(naive repertoire)가 클론될 수 있다. 끝으로, 고유 라이브러리는 Hoogenboom and Winter, J. Mol. Biol., 227: 381-388 (1992)에서 설명된 것과 같이 상당한 가변 CDR3 영역을 인코드하고, 시험관내에서 재배열을 이루기 위하여 무작위 서열이 포함된 PCR 프라이머를 이용하여, 줄기 세포로부터 재배열 안된 V-유전자 세그먼트를 클로닝함으로써 합성에 의해 만들어질 수 있다. 인간 항체 파아지 라이브러리를 설명하는 특허 공개는 예로써 다음의 것들을 포함한다: US 특허 5,750,373, 그리고 US 특허 공개 번호 2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936, 그리고 2009/0002360.
인간 항체 라이브러리로부터 단리된 항체 또는 항체 단편은 본 명세서에서 인간 항체 또는 인간 항체 단편으로 간주된다.
6. 다중특이적 항체
특정 구체예들에 있어서, 본 명세서에서 제공되는 항체는 다중특이적 항체, 예컨데 이중특이적 항체다. 다중특이적 항체는 최소한 2가지 다른 부위에 대하여 결합 특이성을 보유하는 단클론 항체다. 특정 구체예들에 있어서, 결합 특이성중 하나는 CD22에 대한 특이성이며, 다른 하나는 임의의 다른 항원에 대한 특이성이다. 특정 구체예들에 있어서, 이중특이적 항체는 CD22의 상이한 2개의 에피토프에 결합될 수 있다. 이중특이적 항체는 CD22를 발현시키는 세포에게 세포독성 물질을 국소화시키는데 또한 이용될 수 있다. 이중특이적 항체는 전장 항체 또는 항체 단편으로 준비될 수 있다.
다중특이적 항체를 만드는 기술은 상이한 특이성을 보유한 2개의 면역글로블린 중쇄-경쇄 쌍의 재조합 공동-발현(Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, 그리고 Traunecker et al., EMBO J. 10: 3655 (1991) 참고), 그리고 "노브-인-홀(knob-in-hole)" 조작 (예컨데, U.S. 특허 5,731,168 참고)을 포함하나 이에 한정되지 않는다. 다중-특이성 항체는 항체 Fc-헤테로이합체 분자를 만들기 위한 정전기적 스티어링 효과를 만들거나(WO 2009/089004A1); 2개 또는 그 이상 항체 또는 단편의 가교 (예컨데, US 특허 4,676,980, 그리고 Brennan et al., Science, 229: 81 (1985)); 이중-특이성 항체를 만들기 위하여 류신 지퍼를 이용하거나(예컨데, Kostelny et al., J. Immunol., 148(5):1547-1553 (1992)); 이중특이적 항체 단편을 만들기 위하여 "디아바디" 기술을 이용하거나 (예컨데, Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993)); 그리고단일-쇄 Fv (sFv) 이합체를 이용하거나(예컨대, Gruber et al., J. Immunol., 152:5368 (1994)); 그리고 예컨데, Tutt et al. J. Immunol. 147: 60 (1991)에서 설명된 것과 같이 삼중특이적 항체를 만들어서 또한 만들어질 수 있다.
"옥토퍼스(Octopus) 항체"를 포함하는 3개 또는 그 이상의 기능적 항원 결합 부위를 가진 조작된 항체 또한 설명된다(예컨데 US 2006/0025576A1 참고).
본 명세서에서 상기 항체 또는 단편은 CD22 뿐만 아니라 또다른, 상이한 항원에 결합하는 항원 결합 부위가 포함된 "이중 작용(Dual Acting) FAb" 또는 "DAF"를 포함한다(예로써, US 2008/0069820 참고).
7. 항체 변이체(Variants)
특정 구체예들에 있어서, 본 명세서에서 제공되는 항체의 아미노산 서열 변이가 고려된다. 예로써, 상기 항체의 결합 친화력 및/또는 기타 생물학적 성질들을 개선시키는 것이 바람직할 수 있다. 항체의 아미노산 서열 변이는 상기 항체를 인코드하는 뉴클레오티드 서열 안에 적절한 변형을 도입시키거나, 또는 펩티드 합성에 의해 제조될 수 있다. 이러한 변형은 상기 항체의 아미노산 서열로부터 잔기의 결손 및/또는 서열 안에 잔기의 삽입 또는 치환이 포함된다. 최종 구조물이 바람직한 성질, 예컨대, 항원-결합을 보유한다면, 이러한 최종 구조물에 도달되도록 결손, 삽입, 그리고 치환의 임의의 조합이 만들어질 수 있다.
a)
치환, 삽입, 그리고 결손 변이체
특정 구체예들에 있어서, 하나 또는 그 이상의 아미노산 치환을 보유하는 항체 변이체들이 제공된다. 치환에 의한 돌연변이생성에 관심 부위는 HVRs 및 FRs을 포함한다. 보존적 치환은 "바람직한 치환"이라는 제목으로 표 1에 나타낸다. 좀더 실질적인 변화는 "예시적인 치환"이라는 제목으로 표 1에 제공되며, 그리고 아미노산 측쇄 분류에 대하여 하기에서 더 논의된다. 아미노산 치환은 관심 항체 안으로 도입될 수 있으며, 바람직한 활성, 예컨데, 유지된/개선된 항원 결합, 면역원성 감소, 또는 개선된 ADCC 또는 CDC에 대하여 생성물이 선별될 수 있다.
공통 측쇄 성질에 따라 아미노산들이 분류될 수 있다:
(1) 소수성: 노르류신, Met, Ala, Val, Leu, Ile;
(2) 중성 친수성: Cys, Ser, Thr, Asn, Gln;
(3) 산성: Asp, Glu;
(4) 염기성: His, Lys, Arg;
(5) 쇄 방향에 영향을 주는 잔기: Gly, Pro;
(6) 방향족: Trp, Tyr, Phe.
비-보존적 치환은 이들 부류중 하나의 구성요소가 또다른 부류의 것으로 교환이 수반될 것이다.
치환성 변이중 한 가지 유형은 부모 항체의 하나 또는 그 이상의 초가변 영역 잔기의 치환 (예컨데 인간화된 또는 인간 항체)과 관련된다. 일반적으로, 추가 연구를 위하여 선택된 생성된 변이(들)은 부무 항체와 비교하여 특정 생물학적 성질에서 변화(예컨데, 개선) (예컨데, 증가된 친화력, 감소된 면역원성)를 가질 수 있거나 및/또는 부모 항체의 특정 생물학적 성질을 실질적으로 유지할 것이다. 예시적인 치환성 변이는 예컨데, 이를 테면 본 명세서에서 설명된 것과 같은, 파아지 디스플레이-기반된 친화력 성숙 기술을 이용하여 통상적으로 생성되는, 친화력 숙성된 항체다. 간략하게 설명하자면, 하나 또는 그 이상의 HVR 잔기는 돌연변이되고, 그리고 변이 항체는 파아지 상에서 드러나게 되며, 특정 생물학적 활성(예컨데 결합 친화력)에 대하여 선별된다.
예컨데, 항체 친화력을 개선시키기 위하여 HVRs에 변경 (예컨데, 치환)이 만들어질 수 있다. 이러한 변경은 HVR "핫스팟(hotspots)" 이를 테면, 체세포 성숙과정 동안 높은 빈도로 돌연변이되는 코돈에 의해 인코드되는 잔기에서 만들어질 수 있고 (예컨데, Chowdhury, Methods Mol. Biol. 207:179-196 (2008)), 및/또는 SDRs (a-CDRs)에 만들어질 수 있으며, 생성된 변이 VH 또는 VL은 결합 친화력에 대하여 테스트된다. 2차 라이브러리로부터 구축 및 재선별에 의한 친화력 성숙은 예컨데, Hoogenboom et al. Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, (2001).)에 설명되어 있다. 친화력 성숙의 일부 구체예들에 있어서, 다양성(diversity)은 임의의 다양한 방법 (예컨데, 에러-유발(error-prone) PCR, 쇄 셔플링(chain shuffling), 또는 올리고뉴클레오티드-지향된 돌연변이생성)에 의해 성숙에 대하여 선택된 가변 유전자 안으로 도입된다. 2차 라이브러리가 만들어진다. 이 라이브러리는 바람직한 친화력을 가진 임의의 항체 변이를 확인하기 위하여 스크리닝된다. 다양성을 도입하는 또다른 방법은 HVR-지향된 방법과 관련되는데, 이때 몇 가지 HVR 잔기 (예컨데, 한 번에 4-6개의 잔기 )가 무작위화된다. 항원 결합에 관련된 HVR 잔기는 예컨데, 알라닌 스캐닝 돌연변이생성 또는 모델링을 이용하여 특이적으로 확인될 수 있다. 특히, CDR-H3 및 CDR-L3이 대개 표적화된다.
특정 구체예들에 있어서, 치환, 삽입, 또는 결손은 이러한 변경이 항체가 항원에 결합하는 능력을 실질적으로 감소시키지 않는 한, 하나 또는 그 이상의 HVRs에서 발생될 수 있다. 예로써, 실질적으로 결합 친화력을 감소시키지 않는 보존적 변경 (예컨데, 본 명세서에서 제시된 보존적 치환)이 HVRs 안에 만들어질 수 있다. 이러한 변경은 HVR "핫스팟" 또는 SDRs 외부에서 일어날 수 있다. 상기에서 제공된 변이 VH와 VL 서열의 특정 구체예들에 있어서, 각 HVR은 변경되지 않거나, 또는 단지 하나, 둘 또는 세 개의 아미노산 치환을 포함할 수 있다.
돌연변이생성을 표적으로 하는 항체의 잔기 또는 영역을 확인하는 유용한 방법은 Cunningham and Wells (1989) Science, 244:1081-1085에서 설명된 것과 같은 "알라닌 스캐닝(scanning) 돌연변이생성"이라고도 한다. 이 방법에서, 표적 잔기의 잔기 또는 기(예컨데, 하전된 잔기 이를 테면 arg, asp, his, lys, 그리고 glu)가 확인되며, 그리고 중성 또는 음 하전된 아미노산 (예컨데, 알라닌 또는 폴리알라닌)에 의해 대체되어 상기 항체와 항원과의 상호작용이 영향을 받았는지를 확인한다. 최초 치환에 대한 기능적 감응성을 설명하기 위하여 아미노산 위치들에 추가 치환이 도입될 수 있다. 대안으로, 또는 추가적으로, 항원-항체 복합체의 결정 구조는 상기 항체 와 항원 사이에 접촉 점을 확인하는데 이용된다. 이러한 접촉 잔기와 이웃 잔기는 치환을 위한 후보로 표적이 될 수 있거나 또는 제거될 수 있다. 이들이 바람직한 성질을 보유하는지를 결정하기 위하여 변이체들이 스크리닝될 수 있다.
아미노산 서열 삽입은 길이가 1개의 잔기에서부터 수백 또는 그 이상의 잔기가 포함된 폴리펩티드 범위의 아미노- 및/또는 카르복시-말단, 뿐만 아니라 단일 또는 다중 아미노산 잔기의 서열내 삽입을 포함한다. 말단 삽입의 예로는 N-말단 메티오닐 잔기를 가진 항체를 포함한다. 상기 항체 분자의 다른 삽입 변이는 상기 항체의 N- 또는 C-말단을 효소 (예컨데 ADEPT용 효소) 또는 항체의 혈청 반감기를 증가시키는 폴리펩티드에 융합을 포함한다.
b)
당화(glycosylation) 변이체
특정 구체예들에 있어서, 본 명세서에서 제공되는 항체는 이 항체의 당화된 정도를 증가 또는 감소시키기 위하여 변경된다. 항체에 당화 부위의 추가 또는 결손은 하나 또는 그 이상의 당화 부위가 만들어지거나 또는 제거되도록, 아미노산 서열을 변경시켜 통상적으로 이루어질 수 있다.
여기에서 상기 항체는 Fc 영역을 포함하는데, 여기에 탄수화물이 변경될 수 있다. 포유류 세포에 의해 생산되는 고유한 항체는 전형적으로 분기화된, 바이안테너리 올리고사카라이드를 포함하는데, 이는 일반적으로 Fc 영역의 CH2 도메인의 Asn297에 N-링키지에 의해 부착된다. 예컨데, Wright et al. TIBTECH 15:26-32 (1997). 올리고사카라이드는 다양한 탄수화물, 예컨데, 만노즈, N-아세틸 글루코사민 (GlcNAc), 갈락토즈, 그리고 시알산, 뿐만 아니라 바이안테너리 올리고사카라이드 구조의 "줄기(stem)"에 있는 GlcNAc에 부착된 퓨코즈를 포함할 수 있다. 일부 구체예들에 있어서, 특정 개량된 성질을 가지는 항체 변이체를 만들기 위하여 항체내 올리고사카라이드의 변형이 만들어질 수 있다.
한 구체예에 있어서, Fc 영역에 부착된(직접 또는 간접적으로) 퓨코즈가 없는 탄수화물 구조를 보유한 항체 변이체가 제공된다. 예로써, 이러한 항체에서 퓨코즈의 양은 1% 내지 80%, 1% 내지 65%, 5% 내지 65% 또는 20% 내지 40%가 될 수 있다. 퓨코즈의 양은 예로써 WO 2008/077546에서 설명된 것과 같이, MALDI-TOF 질량 분석법에 의해 측정되었을 때, Asn 297에 부착된 모든 당구조(가령, 복합체, 하이브리드, 많은 만노즈 구조)의 합에 비교하여, Asn297에서 슈가 쇄 안에 있는 퓨코즈의 평균 양을 산출함으로써, 퓨코즈의 양이 결정된다. Asn297는 Fc 영역 안에 대략 위치 297에 위치한 아스파라진 잔기를 말한다 (Fc 영역 잔기의 Eu 넘버링); 그러나, Asn297는 약간의 서열 변이로 인하여 위치 297의 대략 ± 3개 아미노산 위 또는 아래, 이를 테면, 위치 294와 300 사이에 위치할 수 있다. 이러한 퓨코실화(fucosylation) 변이는 ADCC 기능을 개선시킬 수 있다. 예컨데, US 특허 공개 번호US 2003/0157108 (Presta, L.); US 2004/0093621 (Kyowa Hakko Kogyo Co., Ltd) 참고. "탈-퓨코실화된" 또는 "퓨코즈-결핍" 항체 변이체에 관련된 공개의 예로는 다음을 포함한다: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki et al. J. Mol. Biol. 336:1239-1249 (2004); Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004). 탈-퓨코실화 항체를 생산할 수 있는 세포 계통의 예로는 단백질 퓨코실화가 결핍된 Lec13 CHO 세포 (Ripka et al. Arch. Biochem. Biophys. 249:533-545 (1986); US 특허 출원 번호 US 2003/0157108 A1, Presta, L; 그리고 WO 2004/056312 A1, Adams et al., 특히 실시예 11), 그리고 녹아웃 세포 계통, 이를 테면 알파-1,6-퓨코실전이효소 유전자, FUT8, 녹아웃 CHO 세포(예컨데, Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004); Kanda, Y. et al., Biotechnol. Bioeng., 94(4):680-688 (2006); 그리고 WO2003/085107)를 포함한다 .
이등분된 올리고사카라이드를 가진 항체 변이체가 더 제공되는데, 예컨데, 상기 항체의 Fc 영역에 부착된 바이안테너리 올리고사카라이드는 GlcNAc에 의해 이등분된다. 이러한 항체 변이체는 감소된 퓨코실화 및/또는 개선된 ADCC 기능을 보유할 수 있다. 이러한 항체 변이체의 예는 예컨데, WO 2003/011878 (Jean-Mairet et al.); US 특허 6,602,684 (Umana et al.); 그리고 US 2005/0123546 (Umana et al.)에서 설명된다. Fc 영역에 부착된 올리고사카라이드 안에 최소한 한 개의 갈락토즈 잔기를 가진 항체 변이체가 또한 제공된다. 이러한 항체 변이체는 개선된 CDC 기능을 보유할 수 있다. 이러한 항체 변이체는 예컨데, WO 1997/30087 (Patel et al.); WO 1998/58964 (Raju, S.); 그리고 WO 1999/22764 (Raju, S.)에서 설명된다.
c)
Fc 영역 변이체
특정 구체예들에 있어서, 하나 또는 그 이상의 아미노산 변형은 본 명세서에서 제공되는 항체의 Fc 영역 안에 도입되고, 이로 인하여 Fc 영역 변이를 만들 수 있다. Fc 영역 변이체는 하나 또는 그 이상의 아미노산 위치에서 아미노산 변형 (예컨데 치환)이 포함된 인간 Fc 영역 서열 (예컨데, 인간 IgG1, IgG2, IgG3 또는 IgG4 Fc 영역)을 포함할 수 있다.
특정 구체예들에 있어서, 본 발명은 모든 작용기 기능은 아니지만 일부를 보유하는 항체 변이를 고려하는데, 이로써 생체내 항체의 반감기가 중요하지만, 특정 작용기 기능(이를 테면 보체 및 ADCC)은 불피요하거나 또는 유해한 용도를 위한 바람직한 후보물질을 만들 수 있다. CDC 및/또는 ADCC 활성의 감소/고갈을 확인하기 위하여 시험관내 및/또는 생체내 세포독성 분석이 실행될 수 있다. 예로써, Fc 수용체 (FcR) 결합 분석은 항체가 FcγR 결합 (그런 이유로 ADCC 활성이 없을 것 같은)은 없지만, FcRn 결합 능력은 유지하는 지를 확인하기 위하여 실행될 수 있다. ADCC를 중개하는 주요 세포, NK 세포는 오직 FcγRIII 만을 발현시키지만, 반면 단세포는 FcγRI, FcγRII 그리고 FcγRIII을 발현시킨다. 조혈 세포 상에서 FcR 발현은 Ravetch and Kinet, Annu. Rev. Immunol. 9:457-492 (1991)의 페이지 464의 표 3에 요약된다. 관심 분자의 관심 ADCC 활성을 평가하기 위한 시험관내 분석의 비-제한적 예는 U.S. 특허 5,500,362 (예컨데 Hellstrom, I. et al. Proc. Nat'l Acad. Sci. USA 83:7059-7063 (1986)) 그리고 Hellstrom, I et al., Proc. Nat'l Acad. Sci. USA 82:1499-1502 (1985); 5,821,337 (Bruggemann, M. et al., J. Exp. Med. 166:1351-1361 (1987))에서 설명된다. 대안으로, 비-방사능활성 분석 방법이 이용될 수 있다(예로써, 유동 세포분석을 위한 ACTI™ 비-방사능활성 세포독성(CellTechnology, Inc. Mountain View, CA; 그리고 CytoTox 96® 비-방사능활성 세포독성 분석(Promega, Madison, WI). 분석에 유용한 작용기 세포는 말초 혈액 단핵 세포(PBMC)와 Natural Killer (NK) 세포를 포함한다. 대안으로, 또는 추가적으로, 관심 분자의 ADCC 활성은 이를 테면, Clynes et al. Proc. Nat'l Acad. Sci. USA 95:652-656 (1998)에서 공개된 것과 같은 동물 모델안에서 생체내 평가될 수 있다. 항체가 C1q에 결합할 수 없고, 따라서 CDC 활성이 부족하다는 것을 확인하기 위하여 C1q 결합 분석이 또한 실행될 수 있다. 예컨데, WO 2006/029879와 WO 2005/100402에서 C1q 및 C3c 결합 ELISA. 보체 활성화를 평가하기 위하여, CDC 분석이 실행될 수 있다(예로써, Gazzano-Santoro et al., J. Immunol. Methods 202:163 (1996); Cragg, M.S. et al., Blood 101:1045-1052 (2003); 그리고 Cragg, M.S. 그리고 M.J. Glennie, Blood 103:2738-2743 (2004) 참고). FcRn 결합 및 생체내 제거/반감기 결정은 당분야에 공지된 방법을 이용하여 또한 실행될 수 있다(예컨데, Petkova, S.B. et al., Int'l. Immunol. 18(12):1759-1769 (2006) 참고).
감소된 작용기 기능을 가진 항체는 하나 또는 그 이상의 Fc 영역 잔기 238, 265, 269, 270, 297, 327 그리고 329의 치환을 가진 것들을 포함한다 (U.S. 특허 6,737,056). 이러한 Fc 돌연변이체는 잔기 265 및 297이 알라닌으로 치환된 "DANA" Fc 돌연변이체가 포함된, 아미노산 위치 265, 269, 270, 297 그리고 327중 2개 또는 그 이상에서 치환을 가진 Fc 돌연변이체를 포함한다(US 특허 7,332,581).
FcRs에 개선된 또는 감소된 결합을 가진 특정 항체 변이체가 설명된다(See, 예컨데, U.S. 특허 6,737,056; WO 2004/056312, 그리고 Shields et al., J. Biol. Chem. 9(2): 6591-6604 (2001).)
특정 구체예들에 있어서, 항체 변이체는 ADCC를 개선시키는 하나 또는 그 이상의 아미노산 치환, 예컨데, Fc 영역의 위치 298, 333, 및/또는 334(잔기의 EU 번호매김)에서 치환을 가진 Fc 영역을 포함한다.
일부 구체예들에 있어서, 예컨데, US 특허 6,194,551, WO 99/51642, 그리고 Idusogie et al. J. Immunol. 164: 4178-4184 (2000)에서 설명된 것과 같이, Fc 영역 안에서 변경이 만들어지고, 이로써 C1q 결합 및/또는 보체 의존적 세포독성 (CDC)이 변경된다(이를 테면 개선 또는 감소).
태아에게 모체 IgGs의 전달을 담당하는 신생아 Fc 수용체(FcRn)(Guyer et al., J. Immunol. 117:587 (1976) 그리고 Kim et al., J. Immunol. 24:249 (1994))에 개선된 결합 및 증가된 반감기를 가진 항체는 US2005/0014934A1 (Hinton et al.)에서 설명된다. 이들 항체는 FcRn에 Fc 영역의 결합을 개선시키는 하나 또는 그 이상의 치환을 가진 Fc 영역을 포함한다. 이러한 Fc 변이체는 Fc 영역 잔기중 하나 또는 그 이상에서 치환을 가진 것들을 포함한다: 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 또는 434, 예컨데, Fc 영역 잔기 434의 치환 (US 특허 7,371,826).
Fc 영역 변이체의 다른 실시예와 관련하여 Duncan & Winter, Nature 322:738-40 (1988); U.S. 특허 5,648,260; U.S. 특허 5,624,821; 그리고 WO 94/29351 참고.
d)
시스테인 조작된 항체 변이체
특정 구체예들에 있어서, 항체의 하나 또는 그 이상의 잔기가 시스테인 잔기으로 치환된, 시스테인 조작된 항체, 예컨데, "티오MAbs(thioMAbs)"를 만드는 것이 바람직할 수 있다. 특정 구체예들에 있어서, 치환된 잔기는 상기 항체의 접근가능한 부위에서 일어난다. 이들 잔기가 시스테인으로 대체됨으로써, 이로 인하여 반응성 티올 기는 상기 항체의 접근가능한 부위에 위치되며, 그리고 다른 모이어티, 이를 테면 약물 모이어티 또는 링커-약물 모이어티에 항체를 접합시켜, 본 명세서에서 더 설명되는 면역접합체가 탄생될 수 있다. 특정 구체예들에 있어서, 다음 잔기들중 임의의 하나 또는 그 이상의 잔기는 시스테인으로 치환될 수 있다: 경쇄의 V205 (Kabat 번호매김); 중쇄의 A118 (EU 번호매김); 그리고 중쇄 Fc 영역의 S400 (EU 번호매김). 항-CD22 항체의 비제한적인 예시적인 시스테인 조작된 중쇄 및 경쇄는 도 3 (서열 번호: 25 내지 27)에 나타낸다. 시스테인 조작된 항체는 예컨데, U.S. 특허 7,521,541에서 설명된 것과 같이 만들어질 수 있다.
e)
항체 유도체
특정 구체예들에 있어서, 본 명세서에서 제공되는 항체는 당분야에 공지되어 있고, 바로 이용가능한 추가적인 비단백질성 모이어티가 포함되도록 추가 변형될 수 있다. 상기 항체의 유도화에 적절한 모이어티는 수용성 폴리머가 포함되나 이에 국한되지 않는다. 수용성 폴리머의 비-제한적인 실시예는 폴리에틸렌 글리콜 (PEG), 에틸렌 글리콜/프로필렌글리콜의 코폴리머, 카르복시메틸 셀룰로오즈, 덱스트란, 폴리비닐 알코올, 폴리비닐 피롤리돈, 폴리-1,3-디옥소란, 폴리-1,3,6-트리옥산, 에틸렌/말레 무수물 코폴리머, 폴리아미노산 (동종폴리머 또는 무작위 코폴리머), 그리고덱스트란 또는 폴리(n-비닐 피롤리돈)폴리에틸렌 글리콜, 프로프로필렌글리콜 동종폴리머, 프롤리프로필렌옥시드/에틸렌 옥시드 코-폴리머, 폴리옥시에틸화된 폴리올 (예컨데, 글리세롤), 폴리비닐 알코올, 그리고 이의 혼합물을 포함하나 이에 한정되지 않는다. 폴리에틸렌 글리콜 프로피온알데히드는 물에서 이의 안정성으로 인하여 제작에 유리할 수 있다. 폴리머는 임의의 분자량을 가지며, 그리고 분기화된 또는 분기화안된 것일 수 있다. 상기 항체에 부착된 폴리머의 수는 가변적일 수 있으며, 그리고 하나 이상의 폴리머가 부착된 경우, 이들 폴리머는 동일하거나 또는 상이한 분자일 수 있다. 일반적으로, 유도화에 이용된 폴리머의 수 및/또는 유형은 개선되어야 하는 항체의 특정 성질 또는 기능, 항체 유도체가 명시된 상태하에 치료제로 이용될 것인지의 여부를 포함하나 이에 한정되지 않는 고려사항에 근거하여 결정될 수 있다.
또다른 구체예에 있어서, 방사선에 노출됨으로써 선택적으로 가열될 수 있는 항체와 비단백질 모이어티의 접합체가 제공된다. 한 구체예에 있어서, 비단백질성 모이어티는 탄소 나노튜브다(Kam et al., Proc. Natl. Acad. Sci. USA 102: 11600-11605 (2005)). 방사선은 임의의 파장일 수 있고, 보통의 세포에게는 해가없지만, 상기 항체-비단백질성 모이어티에 근접한 세포를 죽이는 온도로 비단백질 모이어티를 가열시키는 파장이 포함되나 이에 한정되지 않는다.
B. 재조합 방법 및 조성물
예컨데, U.S. 특허 4,816,567에서 설명된 것과 같은 재조합 방법 및 조성물을 이용하여 항체가 만들어질 수 있다. 한 구체예에 있어서, 본 명세서에서 설명된 항-CD22 항체를 인코드하는 단리된 핵산이 제공된다. 이러한 핵산은 상기 항체의 VL이 포함된 아미노산 서열 및/또는 상기 항체의 VH가 포함된 아미노산 서열(예컨데, 상기 항체의 경쇄 및/또는 중쇄)을 인코드할 수 있다. 추가 구체예에 있어서, 이러한 핵산이 포함된 하나 또는 그 이상의 벡터 (예컨데, 발현 벡터)가 제공된다. 추가 구체예에 있어서, 이러한 핵산이 포함된 숙주 세포가 제공된다. 이러한 한 가지 구체예에서, 숙주 세포는 (1) 항체의 VL이 포함된 아미노산 서열 및/또는 상기 항체의 VH가 포함된 아미노산 서열을 인코드하는 핵산을 포함하는 벡터, 또는 (2) 항체의 VL이 포함된 아미노산 서열을 인코드하는 핵산을 포함하는 제 1 벡터와 상기 항체의 VH가 포함된 아미노산 서열을 인코드하는 핵산을 포함하는 제 2 벡터를 포함한다(예컨데, 이들 벡터로 형질변환되었다). 한 구체예에 있어서, 숙주 세포는 진핵세포, 예컨데 중국 헴스터 난소(Chinese Hamster Ovary (CHO)) 세포 또는 림프 세포(예컨데, Y0, NS0, Sp20 세포)다. 한 구체예에 있어서, 항-CD22 항체를 만드는 방법이 제공되는데, 이때 이 방법은 상기에서 제공된 바와 같은 항체가 인코드된 핵산이 포함된 숙주 세포를 항체의 발현에 적절한 조건하에서 배양하고, 그리고 숙주 세포(또는 숙주 세포 배양 배지)로부터 상기 항체를 임의선택적으로 회수하는 것을 포함한다.
항-CD22 항체의 재조합 생산을 위하여, 예컨데, 상기에서 설명된 바와 같이, 항체를 인코드하는 핵산이 단리되고, 그리고 추가 클로닝 및/또는 숙주 세포 안에서 발현을 위하여 하나 또는 그 이상의 벡터 안으로 삽입된다. 이러한 핵산은 용이하게 단리되고, 통상의 과정을 이용하여 서열화될 수 있다(예컨데, 항체의 중쇄 및 경쇄를 인코드하는 유전자에 특이적으로 결합될 수 있는 올리고뉴클레오티드 프로브를 이용함으로써).
항체-인코딩 벡터의 클로닝 또는 발현을 위한 적절한 숙주 세포는 본 명세서에서 설명된 원핵 또는 진핵 세포를 포함한다. 예로써, 항체는 당화 및 Fc 작용기 기능이 필요없을 때 특히 세균 안에서 만들어질 수 있다. 세균 안에서 항체 단편 및 폴리펩티드의 발현을 위하여, 예컨데, U.S. 특허 5,648,237, 5,789,199, 그리고5,840,523를 참고한다. (Charlton, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ, 2003), pp. 245-254, 대장균(E. coli)에서 항체 단편의 발현을 설명) 발현 후, 상기 항체는 가용성 분획물 안에 세균 세포 페스트로부터 단리될 수 있고, 그리고 추가 정제될 수 있다.
원핵세포에 추가하여, 진핵 미생물, 이를 테면 사상균 또는 효모는 당화 경로가 "인간화되고", 부분적으로 또는 완전하게 인간 당화 패턴을 가진 항체가 만들어지는 곰팡이 및 효모가 포함된 항체-인코딩 벡터를 위한 적절한 클로닝 또는 발현 숙주다. Gerngross, Nat. Biotech. 22:1409-1414 (2004), 그리고 Li et al., Nat. Biotech. 24:210-215 (2006) 참고.
당화된 항체의 발현을 위한 적절한 숙주 세포는 다중 유기체(무척추동물 및 척추동물)로부터 또한 유도될 수 있다. 무척추동물 세포의 예로는 식물 및 곤충 세포를 포함한다. 다수의 베큘로바이러스 균주는 곤충 세포와 함께 이용될 수 있는 것으로 확인되었는데, 특히 스포도프테라 푸르기페르다(Spodoptera frugiperda) 세포의 형질감염에 확인되었다.
식물 세포 배양물 또한 숙주로 이용될 수 있다. 예컨데, US 특허 5,959,177, 6,040,498, 6,420,548, 7,125,978, 그리고 6,417,429 (유전자전이 식물에서 항체를 생산하기 위한 PLANTIBODIES™ 기술을 설명)를 참고.
척추동물 세포가 숙주로 또한 이용될 수 있다. 예로써, 현탁액에서 성장하도록 적응된 포유류 세포 계통이 유용할 수 있다. 유용한 포유류 숙주 세포 계통의 다른 예는 SV40 (COS-7)에 의하여 형질변환된 원숭이 신장 CV1 계통; 인간 배아 신장 계통 (예컨데, Graham et al., J. Gen Virol. 36:59 (1977)에서 설명된 것과 같은 293 또는 293 세포들); 아기 헴스터 신장 세포(BHK); 마우스 세르톨리 세포 (예컨데, Mather, Biol. Reprod. 23:243-251 (1980)에서 설명된 것과 같은 TM4 세포); 원숭이 신장 세포(CV1); 아프리카 녹색 원숭이 신장 세포(VERO-76); 인간 경부 암종 세포(HELA); 개의 신장 세포(MDCK; 버팔로 렛 간 세포(BRL 3A); 인간 폐 세포(W138); 인간 간 세포(Hep G2); 마우스 유방 종양(MMT 060562); TRI 세포, 예컨데, Mather et al., Annals N.Y. Acad. Sci. 383:44-68 (1982)에서 설명된 것과 같은; MRC 5 세포; 그리고 FS4 세포들이다. 다른 유용한 포유류 숙주 세포 계통은 DHFR-CHO 세포(Urlaub et al., Proc. Natl. Acad. Sci. USA 77:4216 (1980)); 그리고 골수종 세포 계통 이를 테면 Y0, NS0 그리고 Sp2/0을 포함하는 중국 헴스터 난소(CHO) 세포를 포함한다. 항체 생산을 위하여 적절한 포유류 숙주 세포 계통의 검토는 예컨데, Yazaki and Wu, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ), pp. 255-268 (2003)를 참고한다.
C. 분석
본 명세서에서 제공되는 항-CD22 항체는 당분야에 공지된 다양한 분석에 의해 이들의 물리적/화학적 성질 및/또는 생물학적 활성에 대해 확인되고, 스크리닝되며, 또는 특징화될 수 있다.
한 측면에서, 항체는 예컨데, 공지의 방법 이를 테면 ELISA, BIACore®, FACS, 또는 Western blot에 의해 항체의 항원 결합 활성에 대하여 테스트된다.
또다른 측면에서, 경쟁 분석을 이용하여 CD22에 결합하는 본 명세서에서 설명된 임의의 항체와 경쟁하는 항체를 확인할 수 있다. 특정 구체예들에 있어서, 이러한 경쟁 항체는 본 명세서에서 설명된 항체가 결합하는 동일한 에피토프(예컨대, 선형 또는 입체 에피토프)에 결합한다. 항체가 결합하는 에피토프 멥핑을 위한 상세한 예시적인 방법은 Morris (1996) "Epitope Mapping Protocols,"in Methods in Molecular Biology vol. 66 (Humana Press, Totowa, NJ)에서 설명된다.
예시적인 경쟁 분석에서, 고정된 CD22는 CD22에 결합하는 라벨된 제 1 항체 (예컨데, 본원 명세서에서 설명되는 임의의 항체)와 CD22에 결합하기 위하여 제 1 항체와 경쟁하는 능력에 대하여 테스트되는 라벨안된 제 2 항체가 포함된 용액 안에서 항온처리된다. 제 2 항체는 하이브리도마 상청액 안에 존재할 수 있다. 대조으로, 고정된 CD22는 제 1 라벨된 제 1 항체가 포함된, 그러나 라벨안된 제 2 항체는 포함되지 않은 용액 안에서 항온처리된다. CD22에 제 1 항체의 결합이 허용되는 조건하에서 항온처리된 후, 과량의 결합안된 항체는 제거되고, 그리고 고정된 CD22와 연합된 라벨의 양이 측정된다. 고정된 CD22와 연합된 라벨의 양이 대조 시료와 비교하여 테스트 시료에서 실질적으로 감소된 경우, 이는 제 2 항체가 CD22에 결합하는 것에 대하여 제 1 항체와 경쟁한다는 것을 나타낸다. Harlow and Lane (1988) Antibodies: A Laboratory Manual ch.14 (Cold Spring Harbor Laboratory, Cold Spring Harbor, NY).
D. 면역접합체
본 발명은 하나 또는 그 이상의 세포독성 물질, 이를 테면 화학요법 물질 또는 약물, 성장 저해 물질, 톡신 (예컨데, 단백질 톡신, 세균, 곰팡이, 식물, 또는 동물 기원의 효소적으로 활성 톡신, 또는 이의 단편), 또는 방사능활성 동위원소 (이를 테면, 방사능접합체)에 접합된 본 명세서의 항-CD22 항체가 포함된 면역접찹체를 또한 제공한다.
면역접합체는 종양으로 약물 모이어티의 표적화 전달과 그리고 일부 구체예들에 있어서 세포내 축적을 허용하는데, 여기에서 접합안된 약물의 전신 투여는 정상 세포로 독성의 수용불가능한 수준을 초래할 수 있다(Polakis P. (2005) Current Opinion in Pharmacology 5:382-387).
항체-약물 접합체(ADC)는 잠재적 세포독성 약물을 항원-발현시키는 종양 세포에 표적화시키고(Teicher, B.A. (2009) Current Cancer Drug Targets 9:982-1004), 이로써 효과를 최대화시키고, 표적을 벗어난 독성을 최소화시킴으로써, 치료 지수가 강화되는, 항체 및 세포독성 약물 모두의 성질을 복합시킨 표적화된 화학요법 분자다(Carter, P.J. and Senter P.D. (2008) The Cancer Jour. 14(3):154-169; Chari, R.V. (2008) Acc. Chem. Res. 41:98-107.
본 발명의 ADC 화합물들은 항암 활성을 가진 것들을 포함한다. 일부 구체예들에 있어서, ADC 화합물들은 약물 모이어티에 접합된, 가령, 공유적으로 부착된 항체를 포함한다. 일부 구체예들에 있어서, 상기 항체는 링커를 통하여 약물 모이어티에 공유적으로 부착된다. 본 발명의 상기 항체-약물 접합체 (ADC)는 종양 조직에 약물의 유효량을 선택적으로 전달하고, 여기에서 치료 지수는 증가시키면서 ("치료 윈도우") 더 큰 선택성, 이를 테면, 더 낮은 유효한 투여 분량이 획득될 수 있다.
상기 항체-약물 접합체(ADC)의 약물 모이어티(D)는 세포독성 또는 세포억제성 효과를 보유하는 임의의 화합물, 모이어티 또는 기를 포함한다. 예시적인 약물 모이어티는 피롤로벤조디아제핀 (PBD) 및 세포독성 활성을 보유한 이의 유도체를 포함하나 이에 한정되지 않는다. 이러한 면역접합체의 비제한적 예들은 하기에 더 상세하게 논의된다.
1. 예시적인 항체-약물 접합체
항체-약물 접합체 (ADC) 화합물의 예시적인 구체예는 종양 세포를 표적으로 하는 항체(Ab), 약물 모이어티 (D), 그리고 Ab를 D에 부착시키는 링커 모이어티 (L)를 포함한다. 일부 구체예들에 있어서, 상기 항체는 하나 또는 그 이상의 아미노산 잔기, 이를 테면 리신 및/또는 시스테인을 통하여 링커 모이어티(L)에 부착된다.
예시적인 ADC는 공식 I을 가진다:
여기에서 p는 1 내지 약 20이다. 일부 구체예들에 있어서, 항체에 접합될 수 있는 약물 모이어티의 수는 자유 시스테인 잔기 수에 의해 제한된다. 일부 구체예들에 있어서, 자유 시스테인 잔기는 본 명세서에서 설명된 방법에 의해 항체 아미노산 서열 안으로 도입된다. 공식 I의 예시적인 ADC는 1, 2, 3, 또는 4개의 조작된 시스테인 아미노산을 보유한 항체를 포함하나 이에 한정되지 않는다 (Lyon, R. et al (2012) Methods in Enzym. 502:123-138). 일부 구체예들에 있어서, 하나 또는 그 이상의 자유 시스테인 잔기가 조작하지 않아도 항체 안에 이미 존재할 수 있고, 이런 경우 기존의 자유 시스테인 잔기가 이용되어 상기 항체를 약물에 접합시킬 수 있다. 일부 구체예들에 있어서, 항체는 하나 또는 그 이상의 자유 시스테인 잔기를 만들기 위하여 항체 접합에 앞서 환원 조건에 노출된다.
a) 예시적인 링커
"링커" (L)는 공식 I의 항체-약물 접합체 (ADC)를 형성하기 위하여 하나 또는 그 이상의 약물 모이어티(D)를 항체(Ab)에 연결시키는데 이용되는 이중기능 또는 다중기능 모이어티다. 일부 구체예들에 있어서, 항체-약물 접합체 (ADC)는 약물과 상기 항체에 공유적으로 부착되는 반응 기능을 보유한 링커를 이용하여 만들 수 있다. 예로써, 일부 구체예들에 있어서, 항체 (Ab)의 시스테인 티올은 링커 또는 약물-링커 중간생성물의 반응 기능기와 결합을 형성하여 ADC를 만들 수 있다.
한 측면에서, 링커는 공유 결합을 형성하기 위하여 항체 상에 존재하는 자유 시스테인과 반응할 수 있는 기능을 보유한다. 이러한 반응 기능기의 비제한적인 예시는 말레이미드, 할로아세타아미드, α-할로아세틸, 활성화된 에스테르 이를 테면 숙시니미드 에스테르, 4-니트로페닐 에스테르, 펜타플루오로페닐 에스테르, 테트라플루오로페닐 에스테르, 무수물, 산 염화물, 술포닐 염화물, 이소시아네이트, 트기로 이소티오시아네이트를 포함한다. 예컨데, Klussman, et al (2004), Bioconjugate Chemistry 15(4):765-773의 페이지 766의 접합 방법 및 본 명세서에서 실시예들을 참고.
일부 구체예들에 있어서, 링커는 항체 상에 존재하는 친전자(electrophilic) 기와 반응할 수 있는 기능기를 가진다. 예시적인 이러한 친전자 기는 알데히드 그리고 케톤 카르보닐 기를 포함하나 이에 한정되지 않는다. 일부 구체예들에 있어서, 링커의 반응 기능기의 헤테로 원자는 항체 상에서 친전자 기와 반응하여 항체 단위에 공유 결합을 형성할 수 있다. 이러한 반응 기능기의 비제한적인 예로는 하이드라지드, 옥심, 아미노, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트, 그리고 아릴하이드라지드를 포함한다.
링커는 하나 또는 그 이상의 링커 성분을 포함할 수 있다. 예시적인 링커 성분은 6-말레이미도카프로일 ("MC"), 말레이미도프로파노일 ("MP"), 발린-시투룰린 ("val-cit" 또는 "vc"), 알라닌-페닐알라닌 ("ala-phe"), p-아미노벤질옥시카르보닐 ("PAB"), N-숙시니미딜 4-(2-피리딜티오) 펜타노에이트 ("SPP"), 그리고 4-(N-말레이미도메틸) 시클로헥산-1 카르복실레이트 ("MCC")를 포함한다. 다양한 링커 성분은 당분야에 공지되어 있고, 이들중 일부는 하기에서 설명된다.
링커는 약물의 방출을 용이하게 하는 절단가능한 링커"일 수 있다. 비제한적인 예시적인 절단가능한 링커는 산-불안정한 링커 (예컨데, 하이드라존이 포함된), 프로테아제-민감성 (예컨데, 펩티다제-민감성) 링커, 광불안정한 링커, 또는 디설피드-함유 링커를 포함한다(Chari et al., Cancer Research 52:127-131 (1992); US 5208020).
특정 구체예들에 있어서, 링커는 식 II를 보유한다:
이때 A는 "스트레쳐(stretcher) 단위"이며, 그리고 a는 0 내지 1의 정수이고; W는 "아미노산 단위"이며, 그리고 w는 0 내지 12의 정수이며; Y는 "스페이스 단위"이고, 그리고 y는 0, 1, 또는 2이다. 식 II의 링커가 포함된 ADC는 공식 I(A): Ab-(Aa-Ww-Yy-D)p를 보유하며, 이때 Ab, D, 그리고 p는 상기 공식 I에서 정의된 바와 같다. 이러한 링커의 예시적인 구체예들은 U.S. 특허 7,498,298에서 설명되며, 이들은 명시적으로 명세서의 참고자료에 편입된다.
일부 구체예들에 있어서, 링커 성분은 항체를 또다른 링커 성분 또는 약물 모이어티에 연계시키는 "스트레쳐 단위" (A)를 포함한다. 비제한적인 예시적인 스트레쳐 단위는 하기에서 나타낸다(이때 물결선은 항체, 약물, 또는 추가 링커 성분에 공유 부착 부위를 나타낸다):
일부 구체예들에 있어서, 링커 성분은 "아미노산 단위" (W)를 포함한다. 이러한 일부 구체예들에 있어서, 아미노산 단위는 프로테아제, 이를 테면 리소좀 효소에 의한 링커의 절단을 허용함으로써, 세포내 프로테아제에 노출될 때 상기 면역접합체로부터 약물의 방출이 용이하게 된다(Doronina et al. (2003) Nat. Biotechnol. 21:778-784). 예시적인 아미노산 단위는 이펩티드, 삼펩티드, 사펩티드, 그리고 오펩티드를 포함하나 이에 한정되지 않는다. 예시적인 이펩티드는 발린-시투룰린 (vc 또는 val-cit), 알라닌-페닐알라닌 (af 또는 ala-phe); 페닐알라닌-리신 (fk 또는 phe-lys); 페닐알라닌-호모리신 (phe-homolys); 그리고N-메틸-발린-시투룰린 (Me-val-cit)을 포함하나 이에 한정되지 않는다. 예시적인 삼펩티드는 글리신-발린-시투룰린 (gly-val-cit) 그리고글리신-글리신-글리신 (gly-gly-gly)을 포함하나 이에 한정되지 않는다. 아미노산 단위는 자연적으로 발생되는 아미노산 잔기 및/또는 소수 아미노산 및/또는 비-자연 발생적 아미노산 유사체, 이를 테면 시투룰린을 포함할 수 있다. 아미노산 단위는 특정 효소, 예로써, 종양-연합된 프로테아제, 카텝신 B, C 그리고 D, 또는 플라스민 프로테아제에 의해 효소 절단되고 최적화되도록 기획된다.
전형적으로, 펩티드-유형 링커는 2개 또는 그 이상 아미노산 및/또는 펩티드 단편 사이에 펩티드 결합이 형성됨으로써 준비될 수 있다. 이러한 펩티드 결합은 액상 합성 방법 (예컨데, E. Schroeder 그리고 K. Luebke (1965) "The Peptides", volume 1, pp 76-136, Academic Press)에 따라 준비될 수 있다.
일부 구체예들에 있어서, 링커 성분은 상기 항체를 약물 모이어티에 직접적으로 연계하거나 또는 스트레쳐 단위 및/또는 아미노산 단위를 통하여 연계하는 "스페이스" 단위를 포함한다. 스페이스 단위는 "자가-희생적(self-immolative)" 또는 "비-자가-희생적"일 수 있다. "비-자가-희생적" 스페이스 단위는 ADC가 절단될 때 약물 모이어티 상에 일부 또는 모든 스페이스 단위가 남아있다. 비-자가-희생적 스페이스 단위의 예로는 글리신 스페이스 단위 그리고 글리신-글리신 스페이스 단위를 포함하나 이에 한정되지 않는다. 일부 구체예들에 있어서, 종양-세포 연합된 프로테아제에 의해 글리신-글리신 스페이스 단위가 포함된 ADC의 효소 절단으로 ADC의 나머지로부터 글리신-글리신-약물 모이어티거 방출된다. 이러한 일부 구체예들에 있어서, 글리신-글리신-약물 모이어티는 종양 세포 안에서 가수분해 단계를 거치게 되고, 따라서 약물 모이어티로부터 글리신-글리신 스페이스 단위가 절단된다.
"자가-희생적" 스페이스 단위는 약물 모이어티의 방출을 허용한다. 특정 구체예들에 있어서, 링커의 스페이스 단위는 p-아미노벤질 단위를 포함한다. 이러한 일부 구체예들에 있어서, p-아미노벤질 알코올은 아미드 결합을 통하여 아미노산 단위에 부착되고, 그리고 카르바메이트, 메틸카르바메이트, 또는 카르보네이트가 벤질 알코올과 약물 사이에 만들어진다 (Hamann et al. (2005) Expert Opin. Ther. Patents (2005) 15:1087-1103). 일부 구체예들에 있어서, 스페이스 단위는 p-아미노벤질옥시카르보닐 (PAB)을 포함한다. 일부 구체예들에 있어서, 자가-희생적 링커가 포함된 ADC는 다음 구조를 보유한다:
이때 Q는 -C1-C8 알킬, -O-(C1-C8 알킬), -할로겐, -니트로, 또는 -시아노이며; m은 0 내지 4 범위의 정수이고; X는 하나 또는 그 이상의 추가 스페이스 단위이거나 또는 존재하지 않을 수 있고; 그리고 p는 1 내지 약 20 범위가 된다. 일부 구체예들에 있어서, p는 1 내지 10, 1 내지 7, 1 내지 5, 또는 1 내지4의 범위가 된다. 비제한적인 예시적인 X 스페이스 단위는 다음을 포함한다:
자가-희생적 스페이스의 다른 예들은 PAB 기와 전자적으로 유사한 방향족 화합물, 이를 테면 2-아미노이미다졸-5-메탄올 유도체 (U.S. 특허 7,375,078; Hay et al. (1999) Bioorg. Med. Chem. Lett. 9:2237) 그리고 오르소- 또는 파라-아미노벤질아세탈을 포함하나 이에 한정되지 않는다. 일부 구체예들에 있어서, 스페이스는 아미드 결합 가수분해시 고리화를 겪는데 이용될 수 있는데, 이를 테면 치환된 그리고 치환안된 4-아미노부틸산 아미드 (Rodrigues et al (1995) Chemistry Biology 2:223), 적절하게 치환된 비시클로[2.2.1] 그리고 비시클로[2.2.2] 고리계 (Storm et al (1972) J. Amer. Chem. Soc. 94:5815) 그리고 2-아미노페닐프로피온산 아미드 (Amsberry, et al (1990) J. Org. Chem. 55:5867)가 이용될 수 있다. 약물을 글리신 잔기의 α-탄소에 연계는 ADC에서 유용할 수 있는 자가-희생적 스페이스의 또다른 예가 된다 (Kingsbury et al (1984) J. Med. Chem. 27:1447).
일부 구체예들에 있어서, 링커 L은 분기된(branching), 다중기능성 링커 모이어티를 통하여 하나이상의 약물 모이어티를 항체에 공유적으로 부착시키기 위한 가지돌기(dendritic) 유형 링커일 수 있다 (Sun et al (2002) Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun et al (2003) Bioorganic & Medicinal Chemistry 11:1761-1768). 가지돌기 링커는 항체에 대한 약물의 몰 비율, 즉, 로딩(로딩)을 증가시키고, 이는 ADC의 효능과 관련된다. 따라서, 여기에서 항체는 오직 한 개의 반응 시스테인 티올 기를 가지면, 다수의 약물 모이어티는 가지돌기 링커를 통하여 부착될 수 있다.
비제한적인 예시적인 링커는 식 I의 ADC 내용에서 나타낸다:
이때 n은 0 내지 12이다. 일부 구체예들에 있어서, n은 2 내지 10이다. 일부 구체예들에 있어서, n은 4 내지 8이다.
추가 비제한적인 예시적인 ADCs는 다음 구조들을 포함한다:
여기에서 X는 다음과 같다:
Y는
각 R은 독립적으로 H 또는 C1-C6 알킬이며; 그리고 n은 1 내지 12다.
일부 구체예들에 있어서, 링커는 용해도 및/또는 반응성을 조정하는 기로 치환된다. 비제한적인 실시예로써, 하전된 치환체 이를 테면, 술포네이트 (-SO3 -) 또는 암모늄은 링커 시약의 물 용해도를 증가시킬 수 있고, 그리고 링커 시약과 상기 항체 및/또는 약물 모이어티의 결합 반응을 촉진시키고, 또는 ADC를 준비하는데 이용되는 합성 경로에 따라 Ab-L (항체-링커 중간생성물)과 D, 또는 D-L (약물-링커 중간생성물)과 Ab의 결합 반응을 촉진시킨다. 일부 구체예들에 있어서, 링커의 일부분은 상기 항체에 결합되고, 링커의 일부분은 약물에 결합되어, 그 다음 Ab-(링커 일부분)a는 약물-(링커 일부분)b에 결합되어, 식 I의 ADC가 형성된다.
본 발명의 화합물들은 다음의 링커 시약으로 준비된 ADC를 명백하게 고려하지만 이에 국한되지 않는다: 비스-말레이미도-트리옥시에틸렌 글리콜 (BMPEO), N-(β-말레이미도프로필옥시)-N-히드록시 숙시니미드 에스테르 (BMPS), N-(ε-말레이미도카프로일옥시) 숙시니미드 에스테르 (EMCS), N-[γ-말레이미도부티릴옥시]숙시니미드 에스테르 (GMBS), 1,6-헥산-비스-비닐술폰 (HBVS), 숙시니미딜 4-(N-말레이미도메틸)시클로헥산-1-카르복시-(6-아미도카프로에이트) (LC-SMCC), m-말레이미도벤조일-N-히드록시숙시니미드 에스테르 (MBS), 4-(4-N-말레이미도페닐)부틸산 하이드라지드 (MPBH), 숙시니미딜 3-(브로모아세트아미도)프로피오네이트 (SBAP), 숙시니미딜 요오드아세테이트(SIA), 숙시니미딜 (4-요오드아세틸)아미노벤조에이트 (SIAB), N-숙시니미딜-3-(2-피리딜디티오) 프로피오네이트(SPDP), N-숙시니미딜-4-(2-피리딜티오)펜타노에이트 (SPP), 숙시니미딜 4-(N-말레이미도메틸)시클로헥산-1-카르복실레이트 (SMCC), 숙시니미딜 4-(p-말레이미도페닐)부티레이트(SMPB), 숙시니미딜 6-[(베타-말레이미도프로피온아미도)헥사노에이트] (SMPH), 이미노티올란(IT), 술포-EMCS, 술포-GMBS, 술포-KMUS, 술포-MBS, 술포-SIAB, 술포-SMCC, 그리고술포-SMPB, 그리고 숙시니미딜-(4-비닐술폰)벤조에이트 (SVSB), 그리고 다음의 비스-말레이미드 시약를 포함하고: 디티오비스말레이미도에탄 (DTME), 1,4-비스말레이미도부탄 (BMB), 1,4 비스말레이미딜-2,3-디히드록시부탄 (BMDB), 비스말레이미도헥산 (BMH), 비스말레이미도에탄 (BMOE), BM(PEG)2 (하기에 나타냄), 그리고 BM(PEG)3 (하기에 나타냄); 이미도에스테르의 이중기능기 유도체 (이를 테면 디메틸 아디피이미데이트 HCl), 활성 에스테르 (이를 테면 디숙시니미딜 수베레이트), 알데히드 (이를 테면 글루타르알데히드), 비스-아지도 화합물들 (이를 테면 비스 (p-아지도벤조일) 헥산디아민), 비스-디아조니움 유도체 (이를 테면 비스-(p-디아조니움벤조일)-에틸렌디아민), 디이소시아네이트 (이를 테면 톨루엔 2,6-디이소시아네이트), 그리고비스-활성 플루오린 화합물들 (이를 테면 1,5-디플루오로-2,4-디니트로벤젠). 일부 구체예들에 있어서, 비스-말레이미드 시약은티올-함유 약물 모이어티, 링커, 또는 링커-약물 중간생성물에게 항체내 시스테인의 티올기 부착을 허용한다. 티올 기와 반응성이 있는 다른 기능기는 요오드아세트아미드, 브로모아세트아미드, 비닐 피리딘, 디설피드, 피리딜 디설피드, 이소시아네이트, 그리고 이소티오시아네이트를 포함하나 이에 한정되지 않는다.
특정 유용한 링커 시약은 다양한 시판되는 원료, 이를 테면 Pierce Biotechnology, Inc. (Rockford, IL), Molecular Biosciences Inc.(Boulder, CO)로부터 구입하거나, 또는 당분야에서 설명된 절차에 따라 합성되거나; 예로써, Toki et al (2002) J. Org. Chem. 67:1866-1872; Dubowchik, et al. (1997) Tetrahedron Letters, 38:5257-60; Walker, M.A. (1995) J. Org. Chem. 60:5352-5355; Frisch et al (1996) Bioconjugate Chem. 7:180-186; US 6214345; WO 02/088172; US 2003130189; US2003096743; WO 03/026577; WO 03/043583; 그리고 WO 04/032828에서 설명된 절차에 따라 합성된다.
탄소-14-라벨된 1-이소티오시아나토벤질-3-메틸디에틸렌 트리아민펜타아세트산(MX-DTPA)은 항체에 방사능뉴클레오티드를 접합시키기 위한 예시적인 킬레이팅 물질이다. 예컨데, WO94/11026 참고.
b) 예시적인 약물 모이어티
일부 구체예들에 있어서, ADC는 피롤로벤조디아제핀 (PBD)을 포함한다. 일부 구체예들에 있어서, PBD 이합체는 특이적 DNA 서열을 인지하고 이에 결합된다. 천연 산물 안트라마이신, PBD는 1965년 처음으로 보고되었다(Leimgruber, et al., (1965) J. Am. Chem. Soc., 87:5793-5795; Leimgruber, et al., (1965) J. Am. Chem. Soc., 87:5791-5793). 그 이후, 트리사이클 PBD 스캐폴드의 이합체를 포함하는 자연 생성 및 유사체 모두를 포함한 다수의 PBDs가 보고되었다(Thurston, et al., (1994) Chem. Rev. 1994, 433-465) (US 6884799; US 7049311; US 7067511; US 7265105; US 7511032; US 7528126; US 7557099). 임의의 특정 이론에 국한되지 않고, 이합체 구조는 B-형태의 DNA의 작은 홈을 가진 등나선도(isohelicity)를 위한 적절한 3차원 모양을 부여함으로써, 결합 부위에 꼭 맞게 된다(Kohn, In Antibiotics III. Springer-Verlag, New York, pp. 3-11 (1975); Hurley and Needham-VanDevanter, (1986) Acc. Chem. Res., 19:230-237). C2 아릴 치환체를 보유한 이합체 PBD 화합물은 세포독성 물질로써 유용한 것으로 나타났다(Hartley et al (2010) Cancer Res. 70(17):6849-6858; Antonow (2010) J. Med. Chem. 53(7):2927-2941; Howard et al (2009) Bioorganic and Med. Chem. Letters 19(22):6463-6466).
PBD 이합체는 항체에 접합되며, 생성된 ADC는 항암 성질을 보유하는 것으로 드러났다. PBD 이합체 상에 비제한적인 예시적인 링키지 부위는 5-원(membered) 피롤로 고리, PBD 단위 사이에 묶음, 그리고 N10-C11 이민 기 (WO 2009/016516; US 2009/304710; US 2010/047257; US 2009/036431; US 2011/0256157; WO 2011/130598)를 포함한다.
ADCs의 비제한적인 예시적인 PBD 이합체 성분은 식 A의 성분 및 이의 염과 용매화합물들이며, 여기에서:
파동선은 링커에 공유 부착 부위를 나타내고;
점선은 C1과 C2 또는 C2와 C3 사이에 이중 결합의 임의선택적 존재를 나타내며;
R2는 H, OH, =O, =CH2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R 그리고 COR로부터 독립적으로 선택되며, 그리고 임의선택적으로 할로 또는 디할로로부터 추가 선택되며, 이때 RD는 R, CO2R, COR, CHO, CO2H, 그리고 할로로부터 독립적으로 선택되며;
R6과 R9는 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
R7은 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
Q는 O, S 그리고 NH로부터 독립적으로 선택되며;
R11은 H, 또는 R이거나 또는, Q가 O일 때, SO3M이며, 여기에서 M은 금속 양이온이고;
R 및 R'는 임의선택적으로 치환된 C1-12 알킬, C3-20 헤테로시클일 그리고 C5-20 아릴 기로부터 각각 독립적으로 선택되며, 그리고 기 NRR'와 관련되어 임의선택적으로, R 및 R'는 이들이 부착된 질소 원자와 함께 임의선택적으로 치환된 4-, 5-, 6- 또는 7-원 헤테로사이클 고리를 형성하고;
R12, R16, R19 및 R17은 R2, R6, R9 및 R7에 대해 차례로 정의된 바와 같고;
R″는 C3-12알킬렌 기이며, 각 쇄는 하나 또는 그 이상의 헤테로원자, 예컨데 O, S, N(H), NMe 및/또는 방향족 고리, 예컨데 벤젠 또는 피리딘에 의해 중단될 수 있으며, 이때 고리는 임의선택적으로 치환되며; 그리고
X와 X'는 O, S 그리고 N(H)로부터 독립적으로 선택된다.
일부 구체예들에 있어서, R9 및 R19는 H다.
일부 구체예들에 있어서, R6 및 R16는 H다.
일부 구체예들에 있어서, R7 및 R17은 모두 OR7A이며, 여기에서 R7A는 임의선택적으로 치환된 C1-4 알킬이다. 일부 구체예들에 있어서, R7A는 Me다. 일부 구체예들에 있어서, R7A는 CH2Ph이며, 여기에서 Ph는 페닐 기다.
일부 구체예들에 있어서, X는 O이다.
일부 구체예들에 있어서, R11은 H다.
일부 구체예들에 있어서, 각 단량체 단위에서 C2와 C3 사이에 이중 결합이 있다.
일부 구체예들에 있어서, R2 및 R12는 H 및 R로부터 독립적으로 선택된다. 일부 구체예들에 있어서, R2 및 R12는 독립적으로 R이다. 일부 구체예들에 있어서, R2 및 R12는 독립적으로 임의선택적으로 치환된 C5-20 아릴 또는 C5-7 아릴 또는 C8-10 아릴이다. 일부 구체예들에 있어서, R2 및 R12는 독립적으로 임의선택적으로 치환된 페닐, 티에닐, 나프틸, 피리딜, 퀴놀리닐, 또는 이소퀴놀리닐이다. 일부 구체예들에 있어서, R2 및 R12는 =O, =CH2, =CH-RD, 그리고 =C(RD)2로부터 독립적으로 선택된다. 일부 구체예들에 있어서, R2 및 R12는 각각 =CH2이다. 일부 구체예들에 있어서, R2 및 R12는 각각 H다. 일부 구체예들에 있어서, R2 및 R12는 각각 =O이다. 일부 구체예들에 있어서, R2 및 R12는 각각 =CF2이다. 일부 구체예들에 있어서, R2 및/또는 R12는 독립적으로 =C(RD)2이다. 일부 구체예들에 있어서, R2 및/또는 R12는 독립적으로 =CH-RD이다.
일부 구체예들에 있어서, R2 및/또는 R12가 각각 =CH-RD일 때, 각 기는 다음에 나타낸 배위를 독립적으로 보유할 수 있다:
일부 구체예들에 있어서, =CH-RD는 배위(I)에 있다.
일부 구체예들에 있어서, R″는 C3 알킬렌 기 또는 C5 알킬렌 기다.
일부 구체예들에 있어서, ADC의 예시적인 PBD 이합체 성분은 식 A(I)의 구조를 가진다:
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, ADC의 예시적인 PBD 이합체 성분은 식 A(II)의 구조를 가진다:
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, ADC의 예시적인 PBD 이합체 성분은 식 A(III)의 구조를 가진다:
이때 RE 및 RE"는 H 또는 RD로부터 각각 독립적으로 선택되며, 이때 RD 는 상기에서 정의된 바와 같고; 그리고
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, n은 0이다. 일부 구체예들에 있어서, n은 1이다. 일부 구체예들에 있어서, RE 및/또는 RE"는 H이다. 일부 구체예들에 있어서, RE 및 RE"는 H이다. 일부 구체예들에 있어서, RE 및/또는 RE"는 RD이며, 이때 RD는 임의선택적으로 치환된 C1-12 알킬이다. 일부 구체예들에 있어서, RE 및/또는 RE"는 RD이며, 이때 RD는 메틸이다.
일부 구체예들에 있어서, ADC의 예시적인 PBD 이합체 성분은 식 A(IV)의 구조를 가진다:
이때 Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 C5-20 아릴이며; 이때 Ar1 및 Ar2는 동일하거나 또는 상이할 수 있고; 그리고
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, ADC의 예시적인 PBD 이합체 성분은 식 A(V)의 구조를 가진다:
이때 Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 C5-20 아릴이며; 이때 Ar1 및 Ar2는 동일하거나 또는 상이할 수 있고; 그리고
이때 n은 0 또는 1이다.
일부 구체예들에 있어서, Ar1 및 Ar2는 임의선택적으로 치환된 페닐, 퓨라닐, 티오페닐 그리고 피리딜으로부터 각각 독립적으로 선택된다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 페닐이다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 티엔-2-일 또는 티엔-3-일이다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 퀴놀리닐 또는 이소퀴놀리닐이다. 퀴놀리닐 또는 이소퀴놀리닐 기는 임의의 이용가능한 고리 위치를 통하여 PBD 코어에 결합될 수 있다. 예로써, 퀴놀리닐은 퀴놀린-2-일, 퀴놀린-3-일, 퀴놀린-4일, 퀴놀린-5-일, 퀴놀린-6-일, 퀴놀린-7-일 및 퀴놀린-8-일일 수 있다. 일부 구체예들에 있어서, 퀴놀리닐은 퀴놀린-3-일과 퀴놀린-6-일에서 선택된다. 이소퀴놀리닐은 이소퀴놀린-1-일, 이소퀴놀린-3-일, 이소퀴놀린-4일, 이소퀴놀린-5-일, 이소퀴놀린-6-일, 이소퀴놀린-7-일 그리고 이소퀴놀린-8-일일 수 있다. 일부 구체예들에 있어서, 이소퀴놀리닐은 이소퀴놀린-3-일과 이소퀴놀린-6-일로부터 선택된다.
ADCs의 추가 비제한적인 예시적인 PBD 이합체 성분은 식 B의 성분 및 이의 염 및 용매화합물이며:
이때:
파동선은 링커에 공유 부착 부위를 나타내고;
OH에 연결된 파동선은 S 또는 R 배열을 나타내며;
RV1 및 RV2는 H, 메틸, 에틸, 그리고 페닐 (이때 페닐은 특히 위치 4에서 임의선택적으로 플루오로로 치환되며) 그리고 C5-6 헤테로시클일로부터 독립적으로 선택되며; 이때 RV1 및 RV2는 동일하거나 또는 상이할 수 있으며; 그리고
n은 0 또는 1이다.
일부 구체예들에 있어서, RV1 및 RV2는 H, 페닐, 그리고 4-플루오로페닐로부터 독립적으로 선택된다.
일부 구체예들에 있어서, 링커는 B 고리의 N10 이민, C 고리의 C-2 엔도/엑소 위치, 또는 A 고리를 연결시키는 묶음 단위(아래 구조 C(I) 및 C(II) 참고)를 포함하는 PBD 이합체 약물 모이어티의 다양한 부위중 하나에 부착될 수 있다.
ADCs의 비제한적인 예시적인 PBD 이합체 성분은 식 C(I) 및 C(II)를 포함한다:
식 C(I) 및 C(II)는 이들의 N10-C11 이민 형에서 나타난다. 예시적인 PBD 약물 모이어티는 하기 표에 나타낸 것과 같은 또한 카르비놀아민 그리고 보호된 카르비놀아민 형태를 포함한다:
이때:
X는 CH2 (n = 1 내지 5), N, 또는 O이며;
Z 및 Z'는 OR 및 NR2로부터 독립적으로 선택되며, 여기에서 R은 1 내지 5개 탄소원자를 포함하는 1차, 2차 또는 3차 알킬이다;
R1, R'1, R2 및 R'2는 각각 H, C1-C8 알킬, C2-C8 알케닐, C2-C8 알키닐, C5-20 아릴 (치환된 아릴을 포함), C5-20 헤테로아릴 기, -NH2, -NHMe, -OH, 그리고 -SH로부터 독립적으로 선택되며, 여기에서, 일부 구체예들에 있어서, 알킬, 알케닐 그리고 알키닐 쇄는 최대 5개 탄소 원자를 포함하고;
R3 및 R'3은 H, OR, NHR, 그리고 NR2로부터 독립적으로 선택되며, 여기에서 R은 1 내지 5개의 탄소 원자를 함유하는 1차, 2차 또는 3차 알킬이며;
R4 및 R'4는 H, Me, 그리고 OMe로부터 독립적으로 선택되며;
R5는 C1-C8 알킬, C2-C8 알케닐, C2-C8 알키닐, C5-20 아릴 (할로, 니트로, 시아노, 알콕시, 알킬, 헤테로시클일에 의해 치환된 아릴 포함) 그리고 C5-20 헤테로아릴 기로부터 선택되며, 여기에서, 일부 구체예들에 있어서, 알킬, 알케닐 그리고알키닐 쇄는 최대 5개의 탄소 원자를 포함하고;
R11은 H, C1-C8 알킬, 또는 보호 기 (이를 테면 아세틸, 트리플루오로아세틸, t-부톡시카르보닐 (BOC), 벤질옥시카르보닐 (CBZ), 9-플루오레닐메틸렌옥시카르보닐 (Fmoc), 또는 자가-희생 단위 이를 테면, 발린-시투룰린-PAB을 포함하는 모이어티)이고;
R12는 H, C1-C8 알킬, 또는 보호 기이며;
이때 R1, R'1, R2, R'2, R5, 또는 R12 중 하나의 수소 또는 A 고리 사이에 있는 -OCH2CH2(X)nCH2CH2O- 스페이스의 수소는 ADC의 링커에 연결된 결합으로 대체된다.
ADC의 예시적인 PBD 이합체 일부분은 다음을 포함하나 이에 한정되지 않는다(파동선은 링커에 공유 부착 부위를 나타낸다):
일부 구체예들에 있어서, PBD 이합체를 포함하는 항체-약물 접합체는 식 (D) 그리고 이의 염 및 용매화합물의 구조를 가진다:
이때:
점선은 C1과 C2 또는 C2와 C3 사이에 이중 결합의 임의선택적 존재를 나타내며;;
R2는 H, OH, =O, =CH2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R 그리고 COR로부터 독립적으로 선택되며, 그리고 임의선택적으로 할로 또는 디할로로부터 추가 선택되며; 여기에서 RD 는 R, CO2R, COR, CHO, CO2H, 그리고 할로로부터 독립적으로 선택되며;
R6과 R9는 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
R7은 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
Y는 단일 결합, 그리고 식 a1 또는 a2의 기로부터 선택되며:
여기에서 N은 기들이 PBD 모이어티의 N10에 결합되는 것을 나타낸다;
RL1 및 RL2는 H 그리고 메틸로부터 독립적으로 선택되거나, 또는 이들이 부착된 탄소와 함께 시클로프로필렌 기를 형성하고;
CBA는 항체를 나타내며;
Q는 O, S 그리고 NH로부터 독립적으로 선택되며;
R11은 H, 또는 R이거나 또는, Q가 O일 때, SO3M이며, 여기에서 M은 금속 양이온이고;
R 및 R'는 임의선택적으로 치환된 C1-12 알킬, C3-20 헤테로시클일 그리고 C5-20 아릴 기로부터 독립적으로 각각 선택되며, 그리고 임의선택적으로 기 NRR'와 관련된 경우, R 및 R'는 이들이 부착된 질소 원자와 함께 임의선택적으로 치환된 4-, 5-, 6- 또는 7-원 헤테로사이클 고리를 형성하며;
이때 R12, R16, R19 및 R17은 R2, R6, R9 및 R7에 대해 차례로 정의된 바와 같고;
이때 R″는 C3-12 알킬렌 기이며, 이의 쇄는 하나 또는 그 이상의 헤테로원자, 예컨데 O, S, N(H), NMe 및/또는 방향족 고리, 예컨데 벤젠 또는 피리딘에 의해 중단될 수 있으며, 이들 고리는 임의선택적으로 치환되며;
X와 X'는 O, S 그리고 N(H)로부터 독립적으로 선택된다.
일부 구체예들에 있어서, 상기 항체는 시스테인을 통하여 PBD 이합체에 연계되어 디설피드 링키지를 형성하는데, 이는 예컨데, 도 4b 및 4c에 나타낸다.
일부 구체예들에 있어서, 식 D는 Y에 따라 식 D-I, D-II 및 D-III로부터 선택된다:
식 A의 화합물들에서:
는 황 연결기다.
일부 구체예들에 있어서, ADC는 다음 구조를 포함하고:
그리고 일부 구체예들에 있어서, ADC는 다음 구조를 포함한다:
이때 CBA는 항체이며, 그리고 n은 0 또는 1이다. Y, RL1 및 RL2는 기존에 정의된 바와 같고, 그리고 RE 및 RE"는 각각 H 또는 RD로부터 독립적으로 선택된다.
상기에서 설명된 임의의 구체예들에 있어서, 특정 치환체는 다음과 같이 정의되며, 여기에서 다음과 같다:
n은 0이며;
n은 1이며;
RE는 H이며;
RE는 RD이고, 여기에서 RD 는 임의선택적으로 치환된 알킬이며;
RE는 RD이고, 여기에서 RD 는 메틸이며;
RL1 및 RL2는 H이고;
RL1 및 RL2는 Me이다.
일부 구체예들에 있어서, ADC는 다음 구조를 포함하고:
그리고 일부 구체예들에 있어서, ADC는 다음 구조를 포함한다:
이때 CBA는 항체이며, 그리고 n은 0 또는 1이다. Y, RL1 및 RL2는 앞서 정의된 바와 같고, 그리고 Ar1 및 Ar2는 각각 독립적으로 임의선택적으로 치환된 C5-20 아릴이며. Ar1 및 Ar2는 동일하거나 또는 상이할 수 있다.
일부 구체예들에 있어서, Ar1 및 Ar2는 각각 임의선택적으로 치환된 페닐, 퓨라닐, 티오페닐 그리고 피리딜로부터 독립적으로 선택된다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 임의선택적으로 치환된 페닐이다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 임의선택적으로 치환된 티엔-2-일 또는 티엔-3-일이다. 일부 구체예들에 있어서, Ar1 및 Ar2는 각각 임의선택적으로 치환된 퀴놀리닐 또는 이소퀴놀리닐이다.
다양한 구체예들에 있어서, 퀴놀리닐 또는 이소퀴놀리닐 기는 임의의 이용가능한 고리 위치를 통하여 PBD 코어에 결합될 수 있다. 예로써, 퀴놀리닐은 퀴놀린-2-일, 퀴놀린-3-일, 퀴놀린-4일, 퀴놀린-5-일, 퀴놀린-6-일, 퀴놀린-7-일 그리고퀴놀린-8-일일 수 있다. 이들 중 퀴놀린-3-일 그리고 퀴놀린-6-일이 바람직할 수 있다. 이소퀴놀리닐은 이소퀴놀린-1-일, 이소퀴놀린-3-일, 이소퀴놀린-4일, 이소퀴놀린-5-일, 이소퀴놀린-6-일, 이소퀴놀린-7일 그리고 이소퀴놀린-8-일일 수 있다. 이들 중 이소퀴놀린-3-일 그리고 이소퀴놀린-6-일이 바람직할 수 있다.
일부 구체예들에 있어서, ADC는 다음 구조를 포함하고:
그리고 일부 구체예들에 있어서, ADC는 다음 구조를 포함한다:
이때 CBA는 항체이며, 그리고 n은 0 또는 1이다. Y, RL1 및 RL2는 앞서 정의된 바와 같고, 그리고 RV1 및 RV2는 H, 메틸, 에틸 그리고 페닐 (페닐은 일부 구체예들에 있어서, 위치 4에서 플로오르로 임의선택적으로 치환될 수 있다) 그리고 C5-6 헤테로시클일로부터 독립적으로 선택된다. RV1 및 RV2는 동일하거나 또는 상이할 수 있으며. 일부 구체예들에 있어서, RV1 및 RV2는 H, 페닐, 그리고 4-플루오로페닐로부터 독립적으로 선택될 수 있다.
PBD 이합체를 포함하는 비제한적인 예시적인 ADCs의 구체예는 다음 구조를 가진다:
PBD 이합체-val-cit-PAB-Ab;
PBD 이합체-Phe-Lys-PAB-Ab, 이때:
n은 0 내지 12이다. 일부 구체예들에 있어서, n은 2 내지 10이다. 일부 구체예들에 있어서, n은 4 내지 8이다. 일부 구체예들에 있어서, n은 4, 5, 6, 7, 및 8로부터 선택된다.
PBD 이합체-val-cit-PAB-Ab 및 PBD 이합체-Phe-Lys-PAB-Ab의 링커는 프로테아제 절단가능하다.
PBD 이합체를 포함하는 ADCs의 비제한적인 예시적 구체예들은 다음 구조를 보유한다:
PBD 이합체-디설피드-Ab; 그리고
PBD 이합체-디설피드 메틸-Ab.
PBD 이합체 및 PBD 이합체가 포함된 ADC는 당분야에 공지된 방법에 따라 그리고 본 명세서에서 설명된 방법에 따라 제조될 수 있다. 예컨데, WO 2009/016516; US 2009/304710; US 2010/047257; US 2009/036431; US 2011/0256157; WO 2011/130598 참고.
c)
약물 로딩
약물 로딩은 식 I의 분자에서 항체 당 약물 모이어티의 평균 수, p로 나타낸다. 약물 로딩은 항체당 1 내지 20개의 약물 모이어티(D) 범위가 될 수 있다. 식 I의 ADCs는 약 1 내지 20개의 약물 모이어티 범위로 접합된 항체 집합을 포함한다. 접합 반응에서 ADC의 준비물내 항체당 약물 모이어티의 평균 수는 통상적인 수단, 이를 테면 질량 분석, ELISA 분석, 그리고 HPLC에 의해 특징화될 수 있다. p 측면에서 ADC의 정량적 분포 또한 측정될 수 있다. 일부 경우들에 있어서, 상동성 ADC의 분리, 정제 및 특징화는 이를 테면 역상 HPLC 또는 전기영동 수단에 의해 획득될 수 있으며, 여기에서 p는 또다른 약물이 로딩된 ADC의 특정 값이 된다.
일부 항체-약물 접합체의 경우, p는 항체 상에 있는 부착 부위의 수로 제한될 수 있다. 예로써, 여기에서 부착은 시스테인 티올이며, 상기의 특정 예시적인 구체예들에 있어서, 항체는 오직 한개 또는 몇 개의 시스테인 티올 기를 보유할 수 있거나, 또는 링커에 부착될 수 있는 오직 한 개 또는 몇 개의 충분한 반응성 티올기를 보유할 수 있다. 특정 구체예들에 있어서, 약물 로딩이 높을 수록, 예컨데 p >5일 경우 특정 항체-약물 접합체의 응집(aggregation), 불용성, 독성 또는 세포 침투 능력의 상실을 야기할 수 있다. 특정 구체예들에 있어서, ADC의 경우 평균 약물 로딩은 1 내지 약 8; 약 2 내지 약 6; 또는 약 3 내지 약 5의 범위가 된다. 또한, 특정 ADCs의 경우, 항체당 약물 모이어티의 최적 비율은 8 미만일 수 있고, 그리고 약 2 내지 약 5 일 수 있는 것으로 나타났다 (US 7498298).
특정 구체예들에 있어서, 이론적인 최대치보다 적은 약물 모이어티가 접합 반응 동안 항체에 접합된다. 항체는 하기에서 논의되는 바와 같이, 약물-링커 중간생성물 또는 링커 시약과 반응하지 않는 예를 들면, 리신 잔기를 보유할 수 있다. 일반적으로, 항체는 약물 모이어티에 연결될 수도 있는 많은 자유 그리고 반응성 시스테인 티올 기를 포함하지 않고; 실제로 항체내 대부분 시스테인 티올 잔기는 디설피드 다리로 존재한다. 특정 구체예들에 있어서, 항체는 부분적 또는 전체 환원 조건하에서 반응성 시스테인 티올기를 만들기 위하여 환원 물질 이를 테면 디티오트레톨 (DTT) 또는 트리카르보닐에틸포스핀 (TCEP)으로 환원될 수 있다. 특정 구체예들에 있어서, 항체는 반응성 친핵 기 이를 테면 리신 또는 시스테인를 드러내기 위하여 변성 조건을 거친다.
ADC의 로딩 (약물/항체 비율)은 여러 방법으로 조절될 수 있으며 그리고 예로써, (i) 항체에 대한 약물-링커 중간생성물 또는 링커 시약의 몰 초과량을 제한하고, (ii) 접합 반응 시간 또는 온도를 제한하고, 그리고 (iii) 시스테인 티올 변형에 대한 환원 상태를 부분적 또는 제한함으로써, 조절될 수 있다.
여기에서 하나 이상의 친핵 기는 약물-링커 중간생성물 또는 링커 시약과 반응하고, 그 다음 생성 산물은 항체에 부착된 하나 또는 그 이상의 약물 모이어티 분포를 가진 ADC 화합물의 혼합물이 된다는 것으로 이해된다. 항체당 평균 약물의 수는 항체에 특이적이며, 그리고 약물에 대해 특이적인 이중 ELISA 항체 분석에 의해 혼합물로부터 산출될 수 있다. 개체 ADC 분자는 질량 분석에 의해 혼합물에서 확인될 수 있고 HPLC, 예컨데 소수성 상호작용 크로마토그래피에 의해 분리될 수 있다(예컨데, McDonagh et al (2006) Prot. Engr. Design & Selection 19(7):299-307; Hamblett et al (2004) Clin. Cancer Res. 10:7063-7070; Hamblett, K.J., et al. "Effect of drug loading on the pharmacology, pharmacokinetics, and toxicity of an anti-CD30 antibody-drug conjugates," Abstract No. 624, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004; Alley, S.C., et al. "Controlling the location of drug attachment in antibody-drug conjugates," Abstract No. 627, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004 참고). 특정 구체예들에 있어서, 단일 로딩 값을 가진 상동성 ADC는 전기영동 또는 크로마토그래피에 의해 접합 혼합물로부터 단리될 수 있다.
d)
면역접합체를 준비하는 특정 방법들
식 I의 ADC는 당분야에 공지된 유기 화학 반응, 조건 그리고 시약을 이용하는 몇 가지 경로에 의해 제조될 수 있는데, 다음이 포함된다: (1) 공유 결합을 통하여 Ab-L을 만들기 위하여 이가 링커 시약과 항체의 친핵 기의 반응, 이어서 약물 모이어티 D의 반응; 그리고 (2) 공유 결합을 통하여 D-L을 만들기 위하여 이가 링커 시약과 약물 모이어티의 친핵 기의 반응, 이어서 항체의 친핵기와의 반응. 후자 경로를 통하여 식 I의 ADC를 제조하는 예시적인 방법은 이의 전문이 명세서의 참고자료에 편입된 US 7498298에서 설명된다.
항체 상의 친핵 기는 다음을 포함하나 이에 한정되지 않는다: (i) N-말단 아민 기, (ii) 측쇄 아민 기, 예컨데 리신, (iii) 측쇄 티올 기, 예컨데 시스테인, 그리고 (iv) 슈가 히드록실 또는 아미노 기, 여기에서 상기 항체는 당화된다. 아민, 티올, 그리고히드록실 기는 친핵기이며, 링커 모이어티 상에 친전자기와 반응하여 공유 결합을 형성할 수 있고, 그리고 링커 시약은 다음을 포함한다: (i) 활성 에스테르 이를 테면 NHS 에스테르, HOBt 에스테르, 할로포르메이트, 그리고 산 할로겐화물; (ii) 알킬 그리고벤질 할로겐화물 이를 테면 할로아세트아미드; 그리고 (iii) 알데히드, 케톤, 카르복시, 그리고 말레이미드 기. 특정 항체는 환원가능한 쇄간 디설피드, 가령, 시스테인 다리를 가진다. 항체는 환원 물질 이를 테면 DTT (디티오트레톨) 또는 트리카르보닐에틸포스핀 (TCEP)로 처리됨으로써 링커 시약과의 접합에 반응성이 될 수 있고, 따라서 상기 항체는 완전하게 또는 부분적으로 환원된다. 각 시스테인 다리는 따라서 이론적으로 2개의 반응성 티올 친핵체를 형성할 것이다. 추가 친핵 기는 예컨데, 리신 잔기과 2-이미노티올란 (Traut의 시약)이 반응하여, 아민이 티올로 전환됨으로써, 리신 잔기 변형을 통하여 항체 안으로 도입될 수 있다. 반응성 티올 기는 또한 1, 2, 3, 4개 또는 그 이상 시스테인 잔기를 도입시킴으로써(예컨데, 하나 또는 그 이상의 비-고유한 시스테인 아미노산 잔기가 포함된 변이체 항체를 만듦으로써), 항체 안으로 도입될 수 있다.
본 발명의 항체-약물 접합체는 항체 상의 친전자 기 이를 테면 알데히드 또는 케톤 카르보닐 기와 링커 시약 또는 약물의 친핵 기와의 반응에 의해 또한 만들어질 수 있다. 링커 시약 상에 유용한 친핵 기는 하이드라지드, 옥심, 아미노, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트, 그리고 아릴하이드라지드를 포함하나 이에 한정되지 않는다. 한 구체예에 있어서, 항체는 링커 시약 또는 약물 상에 친핵 치환체와 반응할 수 있는 친전자 모이어티를 도입시키기 위하여 변형된다. 또다른 구체예에 있어서, 당화된 항체의 슈가는 예컨데 과옥소산염 산화 시약으로 산화되어, 알데히드 또는 케톤 기를 형성할 수 있고, 이는 링커 시약 또는 약물 모이어티의 아민기와 반응할 수 있다. 생성된 이민 Schiff 염기 기는 안정적인 링키지를 형성할 수 있거나, 또는 예컨데 수소화붕소시약에 의해 환원되어 안정적인 아민 링키지를 형성할 수 있다. 한 구체예에 있어서, 당화된 항체의 탄수화물 부분은 갈락토즈 산화효소 또는 메타-과옥소산 나트륨염과 반응으로 항체에서 카르보닐 (알데히드 그리고 케톤) 기를 만들 수 있고, 이는 약물에 있는 적절한 기와 반응할 수 있다(Hermanson, Bioconjugate Techniques). 또다른 구체예에 있어서, N-말단 세린 또는 트레오닌 잔기를 함유하는 항체는 메타-과옥소산 나트륨염과 반응할 수 있고, 제 1 아미노산을 대신하여 알데히드를 생산하게 된다 (Geoghegan & Stroh, (1992) Bioconjugate Chem. 3:138-146; US 5362852). 이러한 알데히드는 약물 모이어티 또는 링커 친핵체와 반응될 수 있다.
약물 모이어티 상의 예시적인 친핵 기는 다음을 포함하나 이에 한정되지 않는다: 링커 모이어티 상에 있는 친전자 기와 공유 결합을 형성하기 위하여 반응할 수 있는 아민, 티올, 히드록실, 하이드라지드, 옥심, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트, 그리고 아릴하이드라지드 기, 그리고 링커 시약은 다음을 포함한다: (i) 활성 에스테르 이를 테면 NHS 에스테르, HOBt 에스테르, 할로포르메이트, 그리고 산 할로겐화물; (ii) 알킬 그리고 벤질 할로겐화물 이를 테면 할로아세트아미드; (iii) 알데히드, 케톤, 카르복시, 그리고 말레이미드 기.
ADC를 만드는데 이용될 수 있는 비제한적인 예시적인 교차-링커 시약은 본 명세서 안에 "예시적인 링커"라는 제목의 부분에서 설명된다. 단백질성 모이어티와 화학 모이어티가 포함된 2개 모이어티를 연계시키기 위하여 교차-링커 시약을 사용하는 방법은 당분야에 공지되어 있다. 일부 구체예들에 있어서, 항체 및 세포독성 물질이 포함된 융합 단백질은 예컨대, 재조합 기술 또는 펩티드 합성에 의해 만들어질 수 있다. 재조합 DNA 분자는 항체를 인코드하는 영역과 접합체의 세포독성 부분을 인코드하는 영역을 포함할 수 있는데, 이들 영역은 서로 인접해있거나 또는 접합체의 바람직한 성질을 파괴하지 않은 링커 펩티드를 인코드하는 영역에 의해 분리되어 있을 수 있다.
여전히 또다른 구체예에 있어서, 항체는 종양 사전-표적화에서 이용을 위한 "수용체"(이를 테면 스트렙타아비딘)에 접합될 수 있으며, 이때 상기 항체-수용체 접합체는 환자에게 투여되고, 이어서 제거 물질을 이용하여 순환계로부터 결합안된 접합체가 제거되고, 그리고 세포독성 물질에 접합된 "리간드" (예컨데, 약물 또는 방사능뉴클레오티드)가 투여된다.
E.
진단 및 탐지를 위한 방법 및 조성물
특정 구체예들에 있어서, 항-CD22 본 명세서에서 제공되는 임의의 항체는 생물학적 시료 안에 CD22의 존재를 탐지하는데 유용하다. 본 명세서에서 이용된 바와 같이, 용어 "탐지"는 정량적 또는 정성적 탐지를 포괄한다. "생물학적 시료"는 예컨데, 세포 또는 조직 (예컨데, 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷 임파종, 그리고 맨틀 세포 임파종을 포함하나 이에 한정되지 않는 B 세포 장애 및/또는 B 세포 증식성 장애를 가진 또는 가진 것으로 의심이 되는 대상의 조직이 포함된 암 또는 암 가능성이 있는 임파 조직이 포함된 생검 물질을 포함한다.
한 구체예에 있어서, 진단 또는 탐지 방법에 이용되기 위한 항-CD22 항체가 제공된다. 추가 측면에 있어서, 생물학적 시료 안에 CD22의 존재에 대한 탐지 방법이 제공된다. 특정 구체예들에 있어서, 이 방법은 본 명세서에서 설명된 항-CD22 항체를 항-CD22 항체가 CD22에 결합이 허용되는 조건하에서 생물학적 시료에 접촉시키고, 그리고 생물학적 시료 안에서 항-CD22 항체와 CD22 사이에 복합체가 형성되었는지를 탐지하는 것을 포함한다. 이러한 방법은 시험관내 또는 생체내 방법일 수 있다. 한 구체예에 있어서, 항-CD22 항체는 항-CD22 항체를 이용한 치료에 적격인 대상을 선택하는데 이용되며, 예컨데 여기에서 CD22는 환자 선별을 위한 생물지표다. 추가 구체예에 있어서, 생물학적 시료는 세포 또는 조직 (예컨데, 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷 임파종, 그리고 맨틀 세포 임파종을 포함하나 이에 한정되지 않는 B 세포 장애 및/또는 B 세포 증식성 장애를 가진 또는 가진 것으로 의심이 되는 대상의 조직이 포함된 암 또는 암 가능성이 있는 임파 조직이 포함된 생검 물질을 포함한다)이다.
추가 구체예에 있어서, 항-CD22 항체는 예컨데, 암의 진단, 예후, 단계를 결정하기 위한 목적, 적절한 치료 과정을 결정하기 위한 목적, 또는 치료에 대한 암의 반응을 모니터하기 위한 목적으로, 생체내 영상화(imaging)에 의해 대상에서 CD22-양성 암을 탐지하기 위하여 생체내에서 이용된다. 생체내 탐지를 위하여 당분야에 공지된 한 가지 방법은 예컨데, van Dongen et al., The Oncologist 12:1379-1389 (2007) 그리고 Verel et al., J. Nucl. Med. 44:1271-1281 (2003)에서 설명된 것과 같은 면역-양전자 방출 단층촬영술 (면역-PET)이다. 이러한 구체들에 있어서, 대상에서 CD22-양성 암을 탐지하는 방법이 제공되는데, 이 방법은 라벨된 항-CD22 항체를 CD22-양성 암을 가진 또는 가진 것으로 의심되는 대상에게 투여하고, 그리고 대상에서 라벨된 항-CD22 항체를 탐지하는 것을 포함하며, 이때 라벨된 항-CD22 항체의 탐지는 대상에 CD22-양성 암이 있음을 나타낸다. 이러한 구체예들에 있어서, 라벨된 항-CD22 항체는 양전자 방출자, 이를 테면 68Ga, 18F, 64Cu, 86Y, 76Br, 89Zr, 그리고 124I에 접합된 항-CD22 항체를 포함한다. 특정 구체예에 있어서, 양전자 방출자는 89Zr이다.
추가 구체예들에 있어서, 진단 또는 탐지 방법은 기질에 고정된 제 1 항-CD22 항체를 CD22의 존재에 대하여 테스트되는 생물학적 시료와 접촉시키고, 이 기질을 제 2 항-CD22 항체에 노출시키고, 그리고 제 2 항-CD22가 생물학적 시료 안에 제 1 항-CD22와 CD 22 사이의 복합체에 결합되어 있는 지를 탐지하는 것을 포함한다. 기질은 임의의 지지성 매체, 예컨대, 유리, 금속, 세라믹, 폴리머 비드, 슬라이드, 칩 또는 다른 기질이 될 수 있다. 특정 구체예들에 있어서, 생물학적 시료는 세포 또는 조직 (예컨데, 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷 임파종, 그리고 맨틀 세포 임파종을 포함하나 이에 한정되지 않는 B 세포 장애 및/또는 B 세포 증식성 장애를 가진 또는 가진 것으로 의심이 되는 대상의 조직이 포함된 암 또는 암 가능성이 있는 임파 조직이 포함된 생검 물질을 포함한다)이다. 특정 구체예들에 있어서, 제 1 또는 제 2 항-CD22 항체는 본 명세서에서 설명된 임의의 항체다.
상기 구체예들중 임의의 것에 따라 진단 또는 탐지될 수 있는 예시적인 장애는 CD22-양성 암, 이를 테면 CD22-양성 임파종, CD22-양성 비-호지킨 임파종 (NHL; CD22-양성 공격성 NHL, CD22-양성 재발된 공격성 NHL, CD22-양성 재발된 무기력한 NHL, CD22-양성 난치성 NHL, 그리고 CD22-양성 난치성 무기력한 NHL을 포함하나 이에 한정되지 않는다), CD22-양성 만성 림프모구 백혈병 (CLL), CD22-양성 소림프구성 임파종, CD22-양성 백혈병, CD22-양성 털모양 세포백혈병 (HCL), CD22-양성 급성 림프구성 백혈병 (ALL), CD22-양성 버킷 임파종, 그리고 CD22-양성 맨틀 세포 임파종을 포함한다. 일부 구체예들에 있어서, CD22-양성 암은 종양 세포 >90% 이상에서 매우 약하거나 또는 착색이 없는 것에 상응하는 "0"이상의 항-CD22 면역조직화학(IHC) 점수를 받은 암이다. 일부 구체예들에 있어서, CD22-양성 암은 1+, 2+ 또는 3+ 수준에서 CD22를 발현시키고, 이때 1+은 신생물 세포 >50%에서 약한 착색에 상응하며, 2+는 >50% 신생물 세포에서 중간수준의 착색에 상응하며, 그리고 3+는 신생물 세포의 >50%에서 강력한 착색에 상응한다. 일부 구체예들에 있어서, CD22-양성 암은 즉석(in situ) 혼성화(ISH) 분석에 따라 CD22를 발현시키는 암이다. 이러한 일부 구체예들에 있어서, IHC에 이용되는 것과 유사한 득점 시스템이 이용된다. 일부 구체예들에 있어서, CD22-양성 암은 CD22 mRNA를 탐지하는 역-전사효소 PCR (RT-PCR) 분석에 따라 CD22를 발현시키는 암이다. 일부 구체예들에 있어서, RT-PCR은 정량적 RT-PCR이다.
특정 구체예들에 있어서, 라벨된 항-CD22 항체가 제공된다. 라벨은 직접적으로 탐지되는 라벨 또는 모이어티 (이를 테면 형광, 발색단, 전자-밀도, 화학적 발광, 그리고 방사능활성 라벨), 뿐만 아니라 예컨데, 효소 반응 또는 분자 상호작용을 통하여 간접적으로 탐지되는 이를 테면 효소 또는 리간드와 같은 모이어티를 포함하나 이에 한정되지 않는다. 염료 전구물질 이를 테면 HRP, 락토퍼옥시다제, 또는 마이크로퍼옥시다제, 바이오틴/아비딘, 스핀 라벨, 박테리오파아지 라벨, 안정적인 자유 라디칼 및 이와 유사한 것들을 산화시키는 과산화수소를 이용하는 효소와 결합된, 예시적인 라벨은 방사능동위원소 32P, 14C, 125I, 3H, 그리고 131I, 플루오르 이를 테면, 희토 킬레이트 또는 플루오레신 및 이의 유도체, 로다민 및 이의 유도체, 단실, 움벨리페론, 루세리페라제, 예컨데, 반딧불이 발광효소 및 세균성 발광효소 (U.S. 특허 4,737,456), 루시페린, 2,3-디히드로 프탈라진디온, 양소추냉이 과산화효소(HRP), 알칼리 포스파타제, β-갈락토시다제, 글루코아밀라제, 리소자임, 사카라이드 옥시다제, 예컨데, 글루코즈 옥시다제, 갈락토즈 옥시다제, 그리고 글루코즈-6-포스페이트 탈수소효소, 헤테로사이클 옥시다제 이를 테면 우리카제 및 산틴 옥시다제를 포함하나 이에 한정되지 않는다. 또다른 구체예에 있어서, 라벨은양전자 방출자다. 양전자 방출자는 68Ga, 18F, 64Cu, 86Y, 76Br, 89Zr, 그리고 124I를 포함하나 이에 한정되지 않는다. 특정 구체예에 있어서, 양전자 방출자는 89Zr이다.
F.
약학 제제
본원 명세서에서 설명된 항-CD22 항체 또는 면역접합체의 약학 제제는 하나 또는 그 이상의 임의선택적 약학적으로 수용가능한 운반체에 바람직한 수준의 순도를 가진 이러한 항체 또는 면역접합체를 혼합하여 동결건조된 제제 또는 수성 용액 형태로 만들어진다(Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)). 약학적으로 수용가능한 운반체는 이용된 약량 및 농도에서 수용자에게 일반적으로 비독성이며, 그리고 다음을 포함하나 이에 한정되지 않는다: 완충액 이를 테면 포스페이트, 구연산염, 그리고 다른 유기 산; 아스크로브산 및 메티오닌이 포함된 항산화제; 보존제 (이를 테면 옥타데실디메틸벤질 암모늄 클로라이드; 헥사메토니움 클로라이드; 벤잘코니움 클로라이드; 벤제토니움 클로라이드; 페놀, 부틸 또는 벤질 알코올; 알킬 파라벤 이를 테면 메틸 또는 프로필 파라벤; 카테콜; 레소르시놀; 시클로헥사놀; 3-펜타놀; 그리고 m-크레졸); 저분자량 (약 10개 잔기 미만) 폴리펩티드; 단백질, 이를 테면 혈청 알부민, 젤라틴, 또는 면역글로블린; 친수성 폴리머 이를 테면 폴리비닐피롤리돈; 아미노산 이를 테면 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌, 또는 리신; 모노사카라이드, 디사카라이드, 그리고 포도당, 만노즈, 또는 덱스트린이 포함된 기타 탄수화물; 킬레이팅 물질 이를 테면 EDTA; 슈가 이를 테면 슈크로즈, 만니톨, 트레할로즈 또는 솔비톨; 염-형성 카운터-이온 이를 테면 나트륨; 금속 복합체 (예컨데 Zn-단백질 복합체); 그리고/또는 비-이온성 계면활성제 이를 테면 폴리에틸렌 글리콜 (PEG). 본원 명세서에서 예시적인 약학적으로 수용가능한 운반체는 침입형(insterstitial) 약물 분산 물질 이를 테면 가용성 중성-활성 히알루로니다제 당단백질 (sHASEGP), 예로써, 인간 가용성 PH-20 히알루로니다제 당단백질, 이를 테면 rHuPH20 (HYLENEX®, Baxter International, Inc.)을 포함한다. rHuPH20을 포함하는 특정 예시적인 sHASEGPs 및 이용 방법은 US 특허 공개 번호 2005/0260186 및 2006/0104968에서 설명된다. 한 측면에서, sHASEGP는 하나 또는 그 이상의 추가 글리코사미노글리칸 이를 테면 콘드로이티나제와 복합된다.
예시적인 동결건조된 항체 또는 면역접합체 제제는 US 특허 6,267,958에서 설명된다. 수성 항체 또는 면역접합체 제제는 US 특허 6,171,586 그리고 WO2006/044908에서 설명된 것들을 포함하고, 후자의 제제는 히스티딘-아세테이트 완충액을 포함한다.
본 명세서의 제제는 치료될 특정 질환에 필수적인, 바람직하게는 서로 불리하게 영향을 주지 않는 상보성 활성을 가진 하나 또는 그 이상의 활성 성분을 또한 포함할 수 있다.
활성 성분은 코아세르베이션 기술 또는 인터페이스(interfacial) 중합화에 의해 준비된 미소캡슐 안에 포집될 수 있는데, 예로써, 콜로이드성 약물 운반 시스템(예로써, 리포좀, 알부민 미소구체, 미세유액, 나노-입자 그리고 나노캡슐) 또는 거대유액 안에 각각 히드록시메틸셀룰로오즈 또는 젤라틴-미소캡슐 그리고 폴리-(메틸메타아실레이트) 미소캡슐로 준비될 수 있다. 이러한 기술은 Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)에서 기술된다.
지속적-방출 조제물이 만들어질 수 있다. 지속적-방출 조제물의 적절한 예로는 고체의 소수성 폴리머 함유 상기 항체 또는 면역접합체의 반침투성 매트릭스를 포함하는데, 이 매트릭스는 모양을 갖춘 물품, 예컨데 필름, 또는 미소캡슐의 형태다.
생체내 투여에 이용되는 제제는 일반적으로 살균된다. 살균은 살균 여과 막을 통하여 여과에 의해 용이하게 이루어질 수 있다.
G. 치료 방법 및 조성물
본 명세서에서 제공되는 임의의 항-CD22 항체 또는 면역접합체는 방법, 예컨데, 치료 방법에 이용될 수 있다.
한 측면에서, 본 명세서에서 제공되는 항-CD22 항체 또는 면역접합체는 CD22-양성 세포의 증식을 억제하는 방법에 이용되는데, 이 방법은 세포의 표면 상에 있는 CD22에 항-CD22 항체 또는 면역접합체의 결합을 허용하는 조건하에서 세포를 항-CD22 항체 또는 면역접합체에 노출시키는 것을 포함하고, 이로 인하여 세포의 증식이 억제된다. 특정 구체예들에 있어서, 이 방법은 시험관내 또는 생체내 방법이다. 일부 구체예들에 있어서, 이 세포는 B 세포다. 일부 구체예들에 있어서, 이 세포는 신생물 B 세포, 이를 테면 임파종 세포 또는 백혈병 세포다.
세포증식 시험관내의 억제는 Promega (Madison, WI)에서 시판하는 CellTiter-GloTM Luminescent Cell Viability Assay를 이용하여 분석될 수 있다. 이 분석은 존재하는 ATP의 양에 근거하여 배양물에서 살아있는 세포의 수를 결정하는데, 이는 대사적으로 활성 세포를 나타낸다. Crouch et al. (1993) J. Immunol. Meth. 160:81-88, US Pat. No. 6602677 참고. 이 분석은 96- 또는 384-웰 포맷에서 실행되어, 자동화된 고-처리량 스크리닝(HTS)에 적합하게 된다. Cree et al. (1995) AntiCancer Drugs 6:398-404. 이 분석 과정은 배양된 세포에 직접단일 시약 (CellTiter-Glo® 시약)을 첨가하는 것과 관련된다. 이로써 세포가 용해되고, 루시페라제 반응에 의해 생성되는 발광 신호가 생성된다. 이 발광 신호는 존재하는 ATP의 양에 비례하며, 이는 배양물에 존재하는 살아있는 세포의 수에 직접적으로 비례한다. 발광계 또는 CCD 카메라 영상 장치에 의해 데이터가 기록될 수 있다. 발광 출력은 상대적인 광 단위(RLU)로 나타낸다.
또다른 측면에서, 약물로써 아용하기 위한 항-CD22 항체 또는 면역접합체가 제공된다. 추가 측면에서, 치료 방법에 사용하기 위한 항-CD22 항체 또는 면역접합체가 제공된다. 특정 구체예들에 있어서, CD22-양성 암 치료에 사용하기 위한 항-CD22 항체 또는 면역접합체가 제공된다. 특정 구체예들에 있어서, 본 발명은 CD22-양성 암을 가진 개체를 치료하는 방법에 이용하기 위한 항-CD22 항체 또는 면역접합체를 제공하는데, 이 방법은 이 개체에게 유효량의 항-CD22 항체 또는 면역접합체를 투여하는 것을 포함한다. 이러한 한 가지 구체예에서, 이 방법은 하기에서 설명되는 최소한 한 가지 추가 치료 물질의 유효량을 이 개체에게 투여하는 것을 더 포함한다.
추가 측면에 있어서, 약물의 제조 또는 준비에서 본 발명은 항-CD22 항체 또는 면역접합체의 용도를 제공한다. 한 구체예에 있어서, 이 약물은 CD22-양성 암의 치료용이다. 추가 구체예에 있어서, 이 약물은 CD22-양성 암을 치료하는 방법에 이용되는데, 이 방법은 CD22-양성 암을 가진 개체에게 이 약물의 유효량을 투여하는 것을 포함한다. 이러한 한 가지 구체예에서, 이 방법은 하기에서 설명되는 최소한 한 가지 추가 치료 물질의 유효량을 이 개체에게 투여하는 것을 더 포함한다.
추가 측면에 있어서, 본 발명은 CD22-양성 암을 치료하는 방법을 제공한다. 한 구체예에 있어서, 이 방법은 이러한 CD22-양성 암을 가진 개체에게 유효량의 항-CD22 항체 또는 면역접합체를 투여하는 것을 포함한다. 이러한 한 가지 구체예에서, 이 방법은 하기에서 설명되는 최소한 한 가지 추가 치료 물질의 유효량을 이 개체에게 투여하는 것을 더 포함한다.
상기 구체예들중 임의의 한 구체예에 따른 CD22-양성 암은 예컨데, 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷 임파종, 그리고 맨틀 세포 임파종일 수 있다. 일부 구체예들에 있어서, CD22-양성 암은 종양 세포 >90% 이상에서 매우 약하거나 또는 착색이 없는 것에 상응하는 "0"이상의 항-CD22 면역조직화학(IHC) 또는 즉석 혼성화(ISH) 점수를 받은 암이다. 또다른 구체예들에 있어서, CD22-양성 암은 1+, 2+ 또는 3+ 수준에서 CD22를 발현시키고, 이때 1+은 신생물 세포 >50%에서 약한 착색에 상응하며, 2+는 >50% 신생물 세포에서 중간수준의 착색에 상응하며, 그리고 3+는 신생물 세포의 >50%에서 강력한 착색에 상응한다. 일부 구체예들에 있어서, CD22-양성 암은 CD22 mRNA를 탐지하는 역-전사효소 PCR (RT-PCR) 분석에 따라 CD22를 발현시키는 암이다. 일부 구체예들에 있어서, RT-PCR은 정량적 RT-PCR이다.
일부 구체예들에 있어서, 피롤로벤조디아제핀 세포독성 모이어티가 포함된 면역접합체는 예로써, 실시예 B 및 D에서 나타낸 것과 같은 이종이식편 모델에서 증명된 것과 같이, 미만성 거대 B-세포 임파종을 치료하는데 유용하다. 일부 구체예들에 있어서, 미만성 거대 B-세포 임파종을 치료하는데 사용하기 위한 면역접합체는 다음 구조를 보유한 PBD 이합체를 포함한다:
이때 n은 0 또는 1이다. 일부 구체예들에 있어서, PBD 이합체는프로테아제 절단가능한 링커를 통하여 항체에 공유적으로 부착되는데, 이를 테면, 예로써, 도 4a에 나타낸 상기 면역접합체다. 일부 구체예들에 있어서, PBD 이합체는 디설피드 링커를 통하여 항체에 공유적으로 부착되는데, 이를 테면, 예로써, 도 4b 및 4c에 나타낸 상기 면역접합체다. 일부 구체예들에 있어서, 피롤로벤조디아제핀 세포독성 모이어티가 포함된 면역접합체는 맨틀 세포 임파종 그리고 버킷 임파종을 치료하는데 유용하다.
상기 구체예들중 임의의 한 구체예에 따른"개체"는 인간일 수 있다.
추가 측면에 있어서, 본 발명은 상기 치료 방법들중 임의의 것에 사용하기 위하여 본 명세서에서 제공된 항-CD22 항체 또는 면역접합체가 포함된 약학 제제를 제공한다. 한 구체예에 있어서, 약학 제제는 본 명세서에서 제공된 항-CD22 항체 또는 면역접합체와 약학적으로 수용가능한 운반체를 포함한다. 또다른 구체예에 있어서, 약학 제제는 본 명세서에서 제공된 임의의 항-CD22 항체 또는 면역접합체와 최소한 한 가지 추가 치료 물질, 예컨데, 하기에서 설명되는 것을 포함한다.
본 발명의 항체 또는 면역접합체는 단독으로 또는 치료법에서 다른 물질과 복합되어 이용될 수 있다. 예를 들면, 본 발명의 항체 또는 면역접합체는 최소한 한 가지 추가 치료 물질과 함께 공동-투여될 수 있다.
일부 구체예들에 있어서, 항-CD22 면역접합체는 항-CD79b 항체 또는 면역접합체와 함께 투여된다. 비제한적인 예시적인 항-CD79b 항체 또는 면역접합체는 huMA79bv28의 초가변 영역을 포함하는데, 이러한 항-CD79b 항체 또는 면역접합체는 (i) 서열 번호: 32의 서열을 가진 HVR-H1, (ii) 서열 번호: 33의 서열을 가진 HVR-H2, (iii) 서열 번호: 34의 서열을 가진 HVR-H3, (iv) 서열 번호: 35의 서열을 가진 HVR-L1, (v) 서열 번호: 36의 서열을 가진 HVR-L2, 그리고 (vi) 서열 번호: 37의 서열을 가진 HVR-L3을 포함한다. 일부 구체예들에 있어서, 항-CD79b 항체 또는 면역접합체는 huMA79bv28의 중쇄 가변 영역 및 경쇄 가변 영역을 포함한다. 이러한 일부 구체예들에 있어서, 항-CD79b 항체 또는 면역접합체는 서열 번호: 38의 서열을 보유한 중쇄 가변 영역과 서열 번호: 39의 서열을 보유한 경쇄 가변 영역을 포함ㅎ나다. 일부 구체예들에 있어서, 항-CD79b 면역접합체는 아우리스태틴, 네모루비친 유도체, 그리고 피롤로벤조디아제핀으로부터 선택된 세포 독성 물질을 포함한다. 일부 구체예들에 있어서, 항-CD79b 면역접합체는 MMAE, PNU-159682, 그리고 다음 구조를 보유한 PBD 이합체로부터 선택된 세포독성 물질을 포함한다:
이때 n은 0 또는 1이다. 일부 구체예들에 있어서, 항-CD79b 면역접합체는 예컨데, US 8,088,378 B2에서 설명된 티오 huMA79bv28 HC A118C-MC-val-cit-PAB-MMAE 면역접합체; 티오 huMA79bv28 HC S400C-MC-val-cit-PAB-MMAE 면역접합체, 티오 huMA79bv28 LC V205C-MC-val-cit-PAB-MMAE 면역접합체, 티오 huMA79bv28 HC A118C-MC-val-cit-PAB-PNU-159682, 티오 huMA79bv28 HC A118C-MC-아세탈-PNU-159682, 티오 huMA79bv28 HC A118C-MC-val-cit-PAB-PBD, 티오 huMA79bv28 HC S400C-MC-val-cit-PAB-PNU-159682, 티오 huMA79bv28 HC S400C-MC-아세탈-PNU-159682, 티오 huMA79bv28 HC S400C-MC-val-cit-PAB-PBD, 티오 huMA79bv28 LC V205C-MC-val-cit-PAB-PNU-159682, 티오 huMA79bv28 LC V205C-MC-아세탈-PNU-159682, 그리고 티오 huMA79bv28 LC V205C-MC-val-cit-PAB-PBD로부터 선택된다. 티오 huMA79bv28 HC A118C의 중쇄 및 경쇄 서열은 각각 서열 번호: 40과 41에 나타낸다. 티오 huMA79bv28 HC S400C의 중쇄 및 경쇄 서열은 각각 서열 번호: 43과 41에 나타낸다. 티오 huMA79bv28 LC V205C의 중쇄 및 경쇄 서열은 각각 서열 번호: 42와 44에 나타낸다. 특이적 항체 서열과는 별도로, 항-CD79b 면역접합체의 구조는 본 명세서와 US 2008/0050310에서 설명된 항-CD22 면역접합체의 구조와 유사하다. PNU-159682를 포함하는 비제한적인 예시적인 면역접합체는 다음 구조들을 보유한다:
Ab-MC-아세탈-PNU-159682
Ab-MC-val-cit-PAB-PNU-159682
일부 구체예들에 있어서, 항-CD22 면역접합체는 항-CD20 항체 (네이키드 항체 또는 ADC)와 복합 투여된다. 일부 구체예들에 있어서, 항-CD20 항체는 리투시맙 (Rituxan®) 또는 2H7 (Genentech, Inc., South San Francisco, CA)이다. 일부 구체예들에 있어서, 항-CD22 면역접합체는 항-VEGF 항체 (가령 베비시주맙, 상표명 Avastin®)와 복합 투여된다.
다른 치료 섭생이 항-CD22 면역접합체의 투여와 복합될 수 있는데, 방사선 요법 및/또는 골수 및 말초 혈액 이식물, 및/또는 세포독성 물질을 포함하나 이에 한정되지 않는다. 일부 구체예들에 있어서, 세포독성 물질은 물질 또는 물질의 조합 이를 테면, 예로써, 사이클로포스파미드, 히드록시다우노루비친, 아드리아마이신, 독소루비신, 빈크리스틴 (Oncovin™), 프레디솔론, CHOP (사이클로포스파미드, 옥소루비신, 빈크리스틴, 그리고 프레디솔론의 조합), CVP (사이클로포스파미드, 빈크리스틴, 그리고 프레디솔론의 조합), 또는 면역치료법 이를 테면 항-CD20 (예컨데, 리투시맙, 상표명 Rituxan®), 항-VEGF (예컨데, 베비시주맙, 상표명 Avastin®), 탁산 (이를 테면 파클리탁셀 그리고 도세탁셀) 그리고 안트라사이클린 항생제다.
상기에서 명시된 이러한 복합 요법은 복합 투여(여기에서 2개 또는 그 이상 치료 물질이 동일한 또는 별도 제제 안에 포함됨), 그리고 별도 투여가 포함된되며, 이 경우 본 발명의 상기 항체 또는 면역접합체의 투여는 추가 치료물질 및/또는 어쥬번트의 투여 전, 동시 또는 투여 이후가 될 수 있다. 본 발명의 항체 또는 면역접합체는 방사선 요법과 복합되어 또한 이용될 수 있다.
본 발명의 항체 또는 면역접합체(그리고 임의의 추가 치료 물질)는 장관외, 폐내, 그리고 비강내 및 국소 투여가 바람직한 경우, 병소내 투여가 포함된 임의의 적절한 수단에 의해 투여될 수 있다. 장관외 주입은 근육, 정맥, 동맥내, 복막내, 또는 피하 투여를 포함한다. 복용은 투여가 잠시 또는 오래 지속되는지에 일부 의존적으로, 이를 테면 정맥 또는 파하 주사와 같은 주사에 의한 임의 경로에 의해 이루어질 수 있다. 다양한 투약 일정은 1회 투여 또는 다양한 시간-시점에 걸쳐 다중 투여, 볼루스(bolus) 투여를 포함하나 이에 한정되지 않으며, 펄스 주입이 본 명세서에서 고려된다.
본 발명의 항체 또는 면역접합체는 우수한 의학적 관행에 일치되는 방식으로 제형화되고, 투약 및 투여될 수 있다. 본 발명의 내용에서 고려되는 인자들은 치료될 특정 장애, 치료될 특정 포유류, 개체 환자의 임상적 상태, 장애의 원인, 물질 운반 부위, 투여 방법, 투여 일정, 그리고 의료진에게 알려진 다른 인자들을 포함한다.
상기 항체 또는 면역접합체는 해당 장애를 예방 또는 치료하는데 있이서 현재 이용되는 하나 또는 그 이상의 물질과 함께 제형화될 필요는 없지만, 임의선택적으로 조제될 수 있다. 이러한 다른 물질의 유효량은 제제에 존재하는 항체 또는 면역접합체의 양, 장애 또는 치료 유형, 그리고 상기에서 논의된 다른 인자들에 따라 달라진다. 이들은 일반적으로 동일한 투약형내에 그리고 본 명세서에서 설명된 투여 경로를 이용하여, 또는 본 명세서에서 설명된 투약량의 약 1 내지 99%, 또는 임상적으로 적절하다고 판단되는 임의의 투약량과 경로에 의해 투여될 수 있다.
질환의 예방 또는 치료를 위하여, 본 발명의 항체 또는 면역접합체의 적절한 투약량(단독으로 또는 하나 또는 그 이상의 다른 추가 치료 물질과 복합되어 이용될 때)은 치료될 질환의 유형, 항체 또는 면역접합체의 유형, 상기 항체 또는 면역접합체가 예방 또는 치료 목적으로 투여되는지, 기존 요법, 환자의 병력 및 상기 항체 또는 면역접합체에 대한 반응, 그리고 주치의의 판단에 따라 달라진다. 상기 항체 또는 면역접합체는 1회 또는 일련의 치료 과정에 걸쳐 적절하게 환자에게 투여된다. 질환의 유형 및 중증도에 따라, 약 1 ㎍/kg 내지 15 mg/kg (예컨데 0.1mg/kg - 10mg/kg)의 항체 또는 면역접합체가 1회 또는 그 이상의 별도 투여,또는 연속 주입에 의해 환자에게 투여를 위한 최초 후보 투약량이 될 수 있다. 전형적으로 1일 1회 투약량은 상기에서 언급된 인자들에 따라 약 1 ㎍/kg 내지 100 mg/kg 또는 그 이상이 될 수 있다. 수일 또는 그 이상 동안 반복 투여를 위하여, 상태에 따라, 치료는 질환 증상의 바람작한 억제가 일어날 때까지 일반적으로 지속될 것이다. 상기 항체 또는 면역접합체의 한 가지 예시적인 투약량은 약 0.05 mg/kg 내지 약 10 mg/kg의 범위가 될 것이다. 따라서, 약 0.5 mg/kg, 2.0 mg/kg, 4.0 mg/kg 또는 10 mg/kg (또는 이의 임의의 조합)의 1회 또는 그 이상의 투약분량이 환자에게 투여될 수 있다. 이러한 투약분량은 간헐적으로 예컨데 매주 또는 3주마다 한번씩(예컨대 환자는 항체의 약 2 내지 약 20의 투여 분량, 또는 예컨대 약 6회의 투여분량을 제공받는다) 투여될 수 있다. 처음 높은 로딩 투여 분량, 이어서 1회 또는 그 이상의 더 낮은 투여분량이 투여될 수 있다. 그러나, 다른 섭생들이 유용할 수 있다. 이 요법의 진행은 통상적인 기술 및 분석을 통하여 용이하게 관찰된다.
일부 구체예들에 있어서, 피롤로벤조디아제핀 (PBD) 이합체가 포함된 저투여용량의 10F4v3 ADC는 MMAE 모이어티가 포함된 고투여용량의 10F4v3 ADC와 동일한 효과를 획득하는데 이용될 수 있다.
상기 임의의 본 발명의 면역접합체와 항-CD22 항체 모두를 이용하여 실행될 수 있다.
H. 제조 물품
본 발명의 또다른 측면에서, 상기에서 설명된 장애의 치료, 예방 및/또는 진단에 유용한 물질들이 함유된 제조 물품이 제공된다. 제조 물품은 용기, 라벨 또는 용기 상에 또는 용기에 연합된 포장 삽입물을 포함한다. 적절한 용기는 예로써, 병, 바이알, 주사기, IV 용액 주머니 등을 포함한다. 용기는 다양한 재료, 이를 테면 유리 또는 플라스틱으로부터 만들어진다. 용기는 자체에 조성물을 보유하거나 또는 장애의 치료, 예방 및/또는 진단하는데 효과적인 또다른 조성물과 복합될 수 있고, 그리고 살균 접근 포트 (예로써 용기는 정맥 용액 주머니일 수 있거나 또는 피하 주사 바늘에 의해 찌를 수 있는 마개를 가진 바이알일 수 있다)를 가질 수 있다. 조성물내 최소한 한 가지 활성 물질은 본 발명의 항체 또는 면역접합체다. 라벨 또는 포장 삽입물에는 이 조성물이 선택된 상태를 치료하는데 이용된다라고 명시된다. 더욱이, 제조 물품은 (a) 여기에 포함된 조성물을 가진 제 1 용기; 그리고 (b) 추가 세포독성 또는 다른 치료 물질이 포함된 조성물을 가진 제 2 용기를 포함할 수 있다. 본 발명의 구체예에서 제조 물품은 이 조성물이 특정 상태를 치료하는데 이용될 수 있음을 표시한 포장 삽입물을 더 포함할 수 있다. 대안으로, 또는 추가적으로, 제조 물품은 약학적으로-수용가능한 완충액, 이를 테면 주사용 정균수(BWFI), 포스페이트-완충된 염수, Ringer 용액 또는 덱스트로즈 용액이 포함된 제 2 (또는 제 3) 용기를 더 포함할 수 있다. 다른 완충액, 희석액, 필터, 바늘 및 주사기를 포함하는 상업적 그리고 사용자 입장에서 바람직한 다른 재료들이 더 포함될 수 있다.
III. 실시예
다음은 본 발명의 방법 및 조성물의 실시예다. 상기에서 제공된 전반적인 설명이 제공된다면 다양한 다른 구체예들이 실시될 수 있음을 이해해야 한다.
A. 항-CD22 항체 약물 접합체의 생산
인간화 변이체 hu10F4v1 및 hu10F4v3을 포함하는 항-CD22 항체 10F4 및 특정 변이체들은 예컨데, US 2008/0050310에서 설명된다. 항체 10F4, hu10F4v1, 그리고hu10F4v3은 서열 번호: 9, 10, 및 11 (각각 차례로 HVR H1, HVR H2, 및 HVR H3)의 중쇄 HVRs를 포함한다. 항체 10F4 및 hu10F4v1는 서열 번호: 12, 13, 그리고 14 (각각 차례로 HVR L1, HVF L2, 및 HVR L3)의 경쇄 HVRs를 포함한다. Hu10F4v3은 서열 번호: 15, 13, 그리고 14 (각각 차례로 HVR L1, HVF L2, 및 HVR L3)의 경쇄 HVRs를 포함하며, 이때 hu10F4v3의 HVR-L1은 10F4 그리고 10F4v1의 HVR L1과 비교하였을 때 단일 아미노산 변화(N28V)를 포함한다. 인간 CD22에 대한 3개 항체의 결합 친화력은 유사한 것으로 밝혀졌다(1.4 nM 내지 2.3 nM의 범위). hu10F4v1의 HVR L1에서 특정 추가 아미노산 치환이 있었고, 서열 번호: 16 내지 22에 나타낸다. 이들 각 HVR L1 서열이 포함된 항체는 인간 CD22에 대한 결합 친화력을 보유하는데, 이 친화력은 hu10F4v1의 결합 친화력보다 2-배 미만으로 변화된다. 예컨데, US 2008/0050310 참고.
더 큰 규모의 항체 생산을 위하여, 항체는 CHO 세포에서 만들어졌다. VL 및 VH를 코딩하는 벡터는 CHO 세포 안으로 형질감염되었으며, IgG는 단백질 A 친화력 크로마토그래피에 의해 세포 배양 배지로부터 정제되었다.
항-CD22 항체-약물 접합체 (ADCs)는 티오 Hu 항-CD22 10F4v3 HC A118C 항체를 특정 약물 모이어티 접합시켜 만들었다. 티오 Hu 항-CD22 10F4v3 HC A118C는 접합가능한 티올 기를 추가하는 중쇄의 A118C 돌연변이를 가진 인간화된 항-CD22 10F4v3 항체다. 예컨데, US 2008/0050310 참고. 티오 Hu 항-CD22 10F4v3 HC A118C의 중쇄 아미노산 서열은 서열 번호: 26 (도 3 참고)에 나타내며, 그리고 티오 Hu 항-CD22 10F4v3 HC A118C의 경쇄 아미노산 서열은 서열 번호: 23 (도 2 참고)에 나타낸다. 면역접합체는 다음과 같이 준비되었다.
티오 Hu 항-CD22 10F4v3 HC A118C-MC-val-cit-PAB-PBD ("10F4v3-PBD")
접합에 앞서, 상기 항체는 디티오트레톨 (DTT)로 환원되어 티오-항체의 조작된 시스테인으로부터 차단 기(예컨대 시스테인)을 제거하였다. 이 과정은 항체의 쇄간(interchain) 디설피드 결합을 또한 환원시킨다. 환원된 항체는 방출된 차단기를 제거하기 위하여 정제되었고, 쇄간 디설피드는 데히드로-아스크로브산 (dhAA)을 이용하여 재산화되었다. 그 다음 고유한 항체는 약물-링커 모이어티 MC-val-cit-PAB-PBD ("val-cit"는 본 명세서에서 "vc"로 불릴 수 있다)와 복합되어 항체의 조작된 시스테인 잔기에 약물-링커 모이어티의 접합이 허용되었다. 접합 반응은 임의의 자유 링커-약물 모이어티와 반응되도록 과량의 N-아세틸-시스테인이 첨가됨으로써 진정되었고, 그리고 ADC는 정제되었다. ADC의 약물 로드 (항체당 평균 약물 모이어티의 수)는 하기 실시예에서 나타낸 것과 같이, 약 1.7 내지 약 1.9개 범위였다. 10F4v3-PBD는 도 4a (p = 약물 로드)에 나타낸 구조를 보유한다.
티오 Hu 항-CD22 10F4v3 HC A118C-MC-val-cit-PAB-MMAE ("10F4v3-MMAE")
접합에 앞서, 상기 항체는 디티오트레톨 (DTT)로 환원되어 티오-항체의 조작된 시스테인으로부터 차단 기(예컨대 시스테인)을 제거하였다. 이 과정은 항체의 쇄간(interchain) 디설피드 결합을 또한 환원시킨다. 환원된 항체는 방출된 차단기를 제거하기 위하여 정제되었고, 쇄간 디설피드는 데히드로-아스크로브산 (dhAA)을 이용하여 재산화되었다. 그 다음 고유한 항체는 약물-링커 모이어티 MC-val-cit-PAB-MMAE ("val-cit"는 본 명세서에서 "vc"로 불릴 수 있다)와 복합되어 항체의 조작된 시스테인 잔기에 약물-링커 모이어티의 접합이 허용되었다. 접합 반응은 임의의 자유 링커-약물 모이어티와 반응되도록 과량의 N-아세틸-시스테인이 첨가됨으로써 진정되었고, 그리고 ADC는 정제되었다. ADC의 약물 로드 (항체당 평균 약물 모이어티의 수)는 하기 실시예에서 나타낸 것과 같이, 약 2로 측정되었다. 티오 Hu 항-CD22 10F4v3 HC A118C-MC-val-cit-PAB-MMAE는 예컨데, US 2008/0050310에서 설명된다.
티오 Hu 항-CD22 10F4v3 HC A118C-디설피드-PBD ("10F4v3-SS-PBD")와 티오 Hu 항-CD22 10F4v3 HC A118C-디설피드 메틸-PBD ("10F4v3-SSMe-PBD")
접합에 앞서, 상기 항체는 디티오트레톨 (DTT)로 환원되어 티오-항체의 조작된 시스테인으로부터 차단 기(예컨대 시스테인)을 제거하였다. 이 과정은 항체의 쇄간(interchain) 디설피드 결합을 또한 환원시킨다. 환원된 항체는 방출된 차단기를 제거하기 위하여 정제되었고, 쇄간 디설피드는 데히드로-아스크로브산 (dhAA)을 이용하여 재산화되었다.
그 다음 고유한 항체는 50 mM Tris, pH 8에서 16 내지 24 시간 동안 6-8배 몰 과량의 약물-링커 모이어티 (실시예 H 또는 I에서 차례로 14 또는 22)과 복합되었다. 그 다음 ADC는 양이온 교환 컬럼에 의해 정제되었다. ADC의 약물 로드 (항체당 평균 약물 모이어티 수)는 하기 실시예에서 나타낸 것과 같이 약 1.7 내지 약 1.9 범위다. 10F4v3-SS-PBD는 도 4b (p = 약물 로드)에 나타낸 구조를 가진다. 10F4v3-SSMe-PBD는 도 4c (p = 약물 로드)에 나타낸 구조를 가진다.
B. WSU-DLCL2 이종이식편 모델에서 인간화된 항-CD22 항체 약물 접합체의 생체내 항-종양 활성
PBD와 티오 Hu 항-CD22 10F4v3 HC A118C 접합체 효과를 테스트하기 위하여 WSU-DLCL2 종양 (미만성 거대 B-세포 임파종 세포 계통)의 마우스 이종이식편 모델에서 접합된 항체의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (12-13 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 WSU-DLCL2 세포 (DSMZ, German Collection of Microorganisms and Cell Cultures, Braunschweig, Germany)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro J, et al. nlme: linear and nonlinear mixed effects models. 2009; R 패키지, 버젼 3.1-96 참고). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율(modest dropout rates)을 모두 해결할 수 있다. 입방 회귀 키(cubic regression splines)를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
9마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 0.5 또는 2 또는 8 mg ADC/kg의 티오 Hu 항-CD22 10F4v3 HC A118C 면역접합체 또는 대조 항체-약물 접합체 (대조 ADCs)로 처리되었다. 대조 ADCs는 WSU-DLCL2 세포의 표면 상에서 발현되지 않는 단백질에 결합된다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 2 및 도 5에 나타낸다. 표 2는 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 2에서 나타낸 약물 접합체와 투여 분량으로 35 일 일정에서, 프로테아제 절단가능한 링커를 통하여 PBD에 접합된 10F4v3 ADCs ("10F4v3-PBD")는 운반체와 대조 ADC ("대조-PBD")과 비교하였을 때, WSU-DLCL2 종양을 가진 SCID 마우스에서 종양 성장이 저해되었음을 나타낸다. 도 5 참고.
더욱이, 2 mg/kg의 10F4v3-PBD는 아우리스태틴 약물 MMAE에 접합된 8 mg/kg의 인간화된 항-CD22 티오mab ("10F4v3-MMAE")와 필적가능한 항-종양 활성을 나타내었다. 도 5 참고. 표 2에서 나타낸 것과 같이, 2 mg/kg 10F4v3-PBD를 제공받은 마우스는 9가지 완전한 반응을 보였고, 반면 8 mg/kg 10F4v3-MMAE를 제공받은 마우스는 6가지 부분적인 반응과 3가지 완전한 반응을 보였다.
이 연구에서, 각 투약형 집단에서 체중 변화 비율을 측정하였다. 그 결과는 10F4v3 ADCs의 투여는 연구 동안 체중의 상당한 증가를 야기하지 않았음을 나타내었다.
C. Granta-519 이종이식편 모델에서 인간화된 항-CD22 항체 약물 접합체의 생체내 항-종양 활성
PBD와 티오 Hu 항-CD22 10F4v3 HC A118C 접합체("10F4v3-PBD") 효과를 테스트하기 위하여 Granta-519 종양 (인간 맨틀 세포 임파종 세포 계통)의 마우스 이종이식편 모델에서 접합된 항체의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (10-11 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 Granta-519 세포(DSMZ, German Collection of Microorganisms and Cell Cultures, Braunschweig, Germany)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro et al. 2009 참고). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율을 모두 해결할 수 있다. 입방 회귀 키를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
9마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 1 mg ADC/kg의 10F4v3 면역접합체 또는 대조 항체-약물 접합체 (대조 ADCs)로 처리되었다. 대조 ADCs는 Grant-519 세포의 표면 상에서 발현되지 않는 단백질에 결합된다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 3 및 도 6에 나타낸다. 표 3은 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 3에서 나타낸 약물 접합체와 1 mg ADC/kg의 투여 분량으로 29 일 일정에서, 프로테아제 절단가능한 링커를 통하여 PBD에 접합된 티오 Hu 항-CD22 ADC("10F4v3-PBD")는 운반체와 비교하였을 때, Granta-519 종양을 가진 SCID 마우스에서 종양 성장이 저해되었음을 나타낸다. 그러나, PBD에 접합된 대조 ADC("대조-PBD") 또한 항-종양 활성을 보여주었고, 이는 이 종양 모델이 PBD에 매우 민감함을 나타낸다. 끝으로, 1 mg/kg으로 제공될 때, 10F4v3-PBD는 아우리스태틴 약물 MMAE ("10F4v3-MMAE")에 접합된 인간화된 항-CD22 티오mab보다 종양 성장을 더 억제하였다.
10F4v3-PBD를 제공받은 마우스는 종양 퇴행을 모두 나타내었지만, 10F4v3-MMAE로 처리된 대부분의 마우스는 그렇지 않았다. 단일 투여 분량의 10F4v3-PBD는 한 가지 부분적 반응과 8가지 완전한 반응을 결과하였다.
본 연구에서 각 투약량 집단에서 체중 변화 비율이 측정되었다. 결과에 따르면, 10F4v3 ADCs의 투여는 연구 동안 체중의 심각한 증가를 야기하지 않았다.
D. SuDHL4-luc 이종이식편 모델에서 인간화된 항-CD22 항체 약물 접합체의 생체내 항-종양 활성
PBD와 티오 Hu 항-CD22 10F4v3 HC A118C 접합체("10F4v3-PBD") 효과를 테스트하기 위하여 SuDHL4-luc 종양 (미만성 거대 B-세포 임파종 세포 계통)의 마우스 이종이식편 모델에서 접합된 항체의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (11-12 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 SuDHL4-luc 세포(DSMZ, German Collection of Microorganisms and Cell Cultures, Braunschweig, Germany, 그리고 루시퍼라제 유전자를 안정적으로 발현하도록 Genentech에서 조작됨)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro et al. 2008 참고). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율을 모두 해결할 수 있다. 입방 회귀 키를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
8마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 2 또는 8 mg ADC/kg의 10F4v3 면역접합체 또는 대조 항체-약물 접합체 (대조 ADCs)로 처리되었다. 대조 ADCs는 SuDHL4-luc 세포의 표면 상에서 발현되지 않는 단백질에 결합된다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 4 및 도 7에 나타낸다. 표 4는 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 4에서 나타낸 약물 접합체와 투여 분량으로 35 일 일정에서, 프로테아제 절단가능한 링커를 통하여 PBD에 접합된 티오 Hu 항-CD22 ADC("10F4v3-PBD")는 운반체와 대조 ADC("대조-PBD")과 비교하였을 때, SuDHL4-luc 종양을 가진 SCID 마우스에서 종양 성장이 저해되었음을 나타낸다. 도 7 참고.
더욱이, 2 mg/kg의 10F4v3-PBD는 아우리스태틴 약물 MMAE에 접합된 8 mg/kg의 인간화된 항-CD22 티오mab ("10F4v3-MMAE")와 필적가능한 항-종양 활성을 나타내었다; 처리된 모든 동물에서 완전한 반응을 보였다. 도 7 및 표 4 참고.
이 연구에서, 각 투약형 집단에서 체중 변화 비율을 측정하였다. 그 결과는 10F4v3 ADCs의 투여는 연구 동안 체중의 상당한 증가를 야기하지 않았음을 나타내었다.
E. SuDHL4-luc 이종이식편 모델에서 10F4v3-PBD의 투여 분량 단계적 증가 연구
SuDHL4-luc 종양 (미만성 거대 B-세포 임파종 세포 계통)의 마우스 이종이식편 모델에서 다양한 투여 분량 수준에서 10F4v3-PBD의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (9-10 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 SuDHL4-luc 세포(DSMZ, German Collection of Microorganisms and Cell Cultures, Braunschweig, Germany, 그리고 루시퍼라제 유전자를 안정적으로 발현하도록 Genentech에서 조작됨)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro et al. 2008 참고). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율을 모두 해결할 수 있다. 입방 회귀 키를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
8마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 0.2, 0.5, 1, 또는 2 mg ADC/kg의 10F4v3-PBD 또는 SuDHL4-luc 세포의 표면 상에서 발현되지 않는 단백질에 결합되는 대조-PBD로 처리되었다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 5 및 도 8에 나타낸다. 표 5는 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 5에서 나타낸 약물 접합체와 투여 분량으로 31일 일정에서, 10F4v3-PBD는 SuDHL4-luc 종양을 가진 SCID 마우스에서 투여 분량 의존적으로 종양 성장을 저해하였다. 0.5 mg/kg 또는 더 높은 약량에서 투여될 때, 10F4v3-PBD는 운반체 또는 대조 ADC와 비교하여 명백한 저해 활성을 나타내었다. 도 8 참고. 또한, 단일 투여 분량의 2 mg/kg 10F4v3-PBD는 모든 처리된 동물에서 완벽한 종양 감소를 초래하였다.
이 연구에서, 각 투약형 집단에서 체중 변화 비율을 측정하였다. 그 결과는 10F4v3-PBD의 투여는 연구 동안 체중의 상당한 증가를 야기하지 않았음을 나타내었다.
F. Bjab-luc 이종이식편 모델에서 10F4v3-PBD의 투여 분량 단계적 증가 연구
Bjab-luc 종양 (버킷 임파종 세포 계통)의 마우스 이종이식편 모델에서 다양한 투여 분량 수준에서 10F4v3-PBD의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (11-12 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 Bjab-luc 세포 (예컨데, Lonza, Basel, Switzerland로부터 이용가능하며, 그리고 루시퍼라제 유전자를 안정적으로 발현하도록 Genentech에서 조작됨)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro et al. 2008 참고). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율을 모두 해결할 수 있다. 입방 회귀 키를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
9마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 0.05, 0.2, 0.5, 또는 1mg ADC/kg의 10F4v3-PBD 또는 Bjab-luc 세포의 표면 상에서 발현되지 않는 단백질에 결합되는 대조-PBD로 처리되었다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 6 및 도 9에 나타낸다. 표 6은 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 6에서 나타낸 약물 접합체와 투여 분량으로 35 일 일정에서, 10F4v3-PBD는 Bjab-luc 종양을 가진 SCID 마우스에서 투여 분량 의존적으로 종양 성장을 저해하였다. 0.2 mg/kg 또는 더 높은 약량에서 투여될 때, 10F4v3-PBD는 운반체 또는 대조 ADC와 비교하여 명백한 저해 활성을 나타내었다. 도 9 참고. 또한, 단일 투여 분량의 0.5 또는 1 mg/kg 10F4v3-PBD는 모든 처리된 동물에서 완벽한 종양 감소를 초래하였다. 1 mg/kg에서 대조-PBD 또한 실질적인 항-종양 활성을 나타나고, 이는 이 모델이 PBD에 매우 민감하다는 것을 나타낸다.
이 연구에서, 각 투약형 집단에서 체중 변화 비율을 측정하였다. 그 결과는 10F4v3-PBD의 투여는 연구 동안 체중의 상당한 증가를 야기하지 않았음을 나타내었다.
G. WSU-DLCL2 이종이식편 모델에서 생체내 항-종양 활성 of 인간화된 항-CD22 항체 약물 접합체의 생체내 항-종양 활성
PBD와 티오 Hu 항-CD22 10F4v3 HC A118C 접합체 효과를 테스트하기 위하여 WSU-DLCL2 종양 (미만성 거대 B-세포 임파종 세포 계통)의 마우스 이종이식편 모델에서 접합된 항체의 효과가 검사되었다.
암컷 CB17 ICR SCID 마우스 (9-10 주령, Charles Rivers Laboratories; Hollister, CA)에게 2 x 107 WSU-DLCL2 세포(DSMZ, German Collection of Microorganisms and Cell Cultures, Braunschweig, Germany)로 측면 피하로 각각 접종되었다. 이종이식편 종양이 150-300 mm3의 평균 종양 크기에 도달될 때(0 일 시점으로 칭함), 처음의 그리고 유일한 치료 투여 분량이 투여되었다. 종양 체적은 칼리퍼를 이용하여 측정된 2차원에 근거하여 산출되었으며, 다음의 식에 따라 mm3로 표현된다: V= 0.5a x b2, 이때 a 및 b는 종양의 각각 긴 직경과 짧은 직경을 나타낸다. 시간을 두고 동일한 동물에서 종양 체적의 반복 측정을 분석하기 위하여, 혼합형 모델링 방식이 이용되었다(예컨데, Pinheiro J, et al. nlme: linear and nonlinear mixed effects models. 2009; R 패키지, 버젼 3.1-96). 이 방식은 반복된 측정과 연구 종료 전에 동물에서 치료와 무관한 제거로 인한 보통의 탈락비율을 모두 해결할 수 있다. 입방 회귀 키를 이용하여 각 투여 분량 수준에서 log2 종양 용적의 시간 과정에 대해 비-선형 프로파일을 피팅하였다. 그 다음 이들 비-선형 프로파일은 혼합 모델 안에서 투여 분량과 관련있었다.
9마리의 마우스 집단은 단일 정맥(i.v.) 투여 분량인 0.5, 또는 2 또는 10mg ADC/kg의 티오 Hu 항-CD22 10F4v3 HC A118C 면역접합체 또는 대조 항체-약물 접합체 (대조 ADCs)로 처리되었다. 대조 ADCs는 WSU-DLCL2 세포의 표면 상에서 발현되지 않는 단백질에 결합된다. 마우스의 종양 및 체중은 실험 동안 주당 1-2회 측정되었다. 마우스는 3000 mm3에 도달되기 전 또는 종양이 임박한 궤양 신호를 보일 때 안락사시켰다. 모든 동물 프로토콜은 Institutional Animal Care and Use Committee (IACUC)에 의해 승인되었다.
실험 결과는 표 7 및 도 10에 나타낸다. 표 2는 각 치료 집단, 연구 종료시 관측가능한 종양을 가진 마우스의 수("TI"), 부분 반응을 보이는 마우스의 수("PR"; 여기에서 투여 후 임의의 시간에서 종양 체적은 0일 시점에서 측정된 종양 체적의 50% 미만으로 떨어짐), 완전한 반응을 보이는 마우스의 수("CR"; 여기에서 투여 후 임의의 시간에서 종양 체적이 0 mm3으로 떨어짐), 각 집단에 대한 약물 투여 분량, 그리고 투여된 각 ADC에 대한 약물 로드를 나타낸다.
표 7에서 나타낸 약물 접합체와 투여 분량으로 28 일 일정에서, 10F4v3-PBD 그리고 10F4v3-SSMe-PBD는 운반체와 대조 ADCs와 비교하였을 때, WSU-DLCL2 종양을 가진 SCID 마우스에서 0.5 mg/kg에서 종양 성장이 저해되었음을 나타낸다. 도 7 참고.
더욱이, 2 mg/kg 10F4v3-SSMe-PBD는 거의 완벽한 종양 성장 억제를 보여주었다. 도 7 참고. 표 2에 나타낸 바와 같이, 2 μg/kg 10F4v3-SSMe-PBD를 제공받은 2마리 마우스와 0.5 μg/kg 10F4v3-SSMe-PBD를 제공받은 한 마리 마우스는 이 요법에 부분적인 반응을 보였다.
이 연구에서, 각 투약형 집단에서 체중 변화 비율을 측정하였다. 그 결과는 10F4v3 ADCs의 투여는 연구 동안 체중의 상당한 증가를 야기하지 않았음을 나타내었다.
H. 디설피드 PBD 시약의 합성
(a) (
S
)-2-(메톡시카르보닐)-4-메틸렌피롤리디니움 클로라이드 (
3
)
(i) (
S
)-1-tert-부틸 2-메틸 4-메틸렌피롤리딘-1,2-디카르복실레이트 (
2
)
탄산칼륨 (19.92 g, 14 mmol, 3 eq.)은 DMF (270 mL)에서 교반된 카르복실산 (1) (10.92 g, 48 mmol, 1 eq.) 용액에 첨가되었다. 생성된 백색 현탁액은 30분간 실온에서 교반되었고, 이때 요오드메탄 (21.48 g, 9.5 mL, 151 mmol, 3.15 eq.)이 첨가되었다. 반응 혼합물은 실온에서 3일간 교반되도록 두었다. 감압 하에서 회전 증발에 의해 DMF가 제거되면 에틸아세테이트와 물 사이에서 분할되는 황색 잔류물이 획득되었다. 유기 층은 분리되었고, 수성 상은 에틸아세테이트로 추출되었다. 복합된 유기 층들은 물, 염수로 세척되었고, 그리고 황산 마그네슘 상에서 건조되었다. 에틸아세테이트는 감압하에서 회전 증발에 제거되면 황색 오일로 된 비정제 산물이 수득되었다. 비정제 산물은 섬광 크로마토그래피 [85% n-헥산/15% 에틸아세테이트]에 의해 정제되어, 무색 오일로 된 산물을 수득하였다. (공지 화합물 F et al., J. Org. Chem. 1992, 57, 2060-2065)
(ii) (
S
)-2-(메톡시카르보닐)-4-메틸렌피롤리디니움 클로라이드 (
3
)
실온에서 디옥산 (63 mL, 254.4 mmol, 4.5 eq.)에서 4M 염화수소산 용액은 Boc 보호된 C-고리 단편 (2) (13.67 g, 56.6 mmol, 1 eq.)에 첨가되었다. 비등이 관찰되는데, 이는 CO2의 유리 및 Boc 기의 제거를 나타낸다. 산물은 백색 고체로 침전되었고, 추가 디옥산이 첨가되어 교반을 용이하게 하였다. 반응 혼합물은 한 시간 동안 교반되도록 두었고, 그 다음 에테르로 희석되었다. 침전된 산물은 진공 여과에 의해 수집되며, 추가 에테르로 세척되었다. 대기 건조에 의해 백색 분말의 바람직한 산물이 수득되었다(9.42 g, 94%) (P Herdwijn et al., Canadian Journal of Chemistry. 1982, 60, 2903-7)
(b) tert-부틸 (5-((5-(5-아미노-4-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-2-메톡시펜옥시)펜틸)옥시)-2-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시페닐)카르바메이트 (
9
)
(i) (
S
)-(4,4'-(펜탄-1,5-디일비스(옥시))비스(5-메톡시-2-니트로-4,1-페닐렌))비스(((
S
)-2-(메톡시카르보닐)-4-메틸렌피롤리딘-1-일)메타논) (
5
)
촉매량의 무수 DMF (0.5 mL)는 실온에서 무수 DCM (180 mL) 안에 옥살일 클로라이드 (9.1 g, 6.25 mL, 71.7 mmol, 3 eq.)와 이합체 코어(4) (11.82 g, 23.9 mmol, 1 eq.)의 교반된 현탁액에 첨가되었다. DMF를 첨가한 후 활발한 비등이 관찰되었고, 반응 혼합물은 염화칼슘 건조 튜브가 고정된 밑둥근 플라스크 안에서 18 시간 동안 교반되도록 두었다. 생성된 맑은 용액은 감압하에서 증발되었으며, 고체는 에테르로 저작되었다(triturate). 고형 산물은 진공 여과에 의해 수거되었으며, 추가 에테르로 세척되었고, 40℃에서 1.5시간 동안 진공에서 건조되었다. 이 고체는 TEA (12.08 g, 119.6 mmol, 5 eq.)안에 C-고리 (3) (9.35 g, 52.6 mmol, 2.2 eq.)와 건조 DCM (110 mL)의 현탁액에 부분적으로 추가되었고, 온도는 드라이아이스/아세토니트릴 조의 도움으로 -40 내지 -50℃ 사이의 온도에서 유지된다. 반응 혼합물은 -40℃에서 교반되도록 허용된 후, 실온으로 데워지도록 두었으며, 이때 LCMS는 출발 물질의 완전한 소비를 나타내었다. 반응 혼합물은 추가 DCM로 희석되었고, 수성 염화수소산 (1M, 2 x 200 mL), 포화 수성 중탄산 나트륨 (2 x 250 mL), 물(250 mL), 염수 (250 mL)로 순차적으로 세척되었고, 건조되었다(MgSO4). DCM은 감압하에서 회전 증발에 의해 제거되어 황색 포말의 산물이 수득되었다(13.94 g, 79 %). 분석 데이터: RT 3.95 min; MS (ES+) m/z (상대적 강도) 741 ([M + 1]+., 100).
(ii) (
S
)-(4,4'-(펜탄-1,5-디일비스(옥시))비스(5-메톡시-2-니트로-4,1-페닐렌))비스(((
S
)-2-(히드록시메틸)-4-메틸렌피롤리딘-1-일)메타논) (
6
)
고형 리튬 수소화붕소(0.093 g, 4.3 mmol, 3 eq.)는 0℃(얼음조)에서 질소 대기하에 건조 THF(10 mL)에서 에스테르 (5) (1.05 g, 142 mmol, 1 eq.)의 용액에 일부분으로 추가되었다. 반응 혼합물은 30분간 0℃에서 교반되도록 하였고, 그 다음 실온으로 데워지도록 두었으며, 이때 오랜지색 점성(gum) 침전물이 관찰되었다. 반응 혼합물은 추가 2시간 동안 실온에서 교반되도록 두었고, 그 다음 얼음조 안에서 냉각되었으며, 물(20 mL)로 처리되어 황색 현탁액이 제공되었다. 염화수소산 (1M)이 비등이 중단될 때까지 신중하게 추가되었다(격렬한 비등!). 반응 혼합물은 에틸아세테이트 (4 x 50 mL)로 추출되었고, 그리고 복합된 유기 층들은 물(100 mL), 염수 (100 mL)로 세척되었고, 건조되었다(MgSO4). 에틸아세테이트는 감압하에서 회전 증발에 의해 제거되고, 황색 포말의 산물이 획득되었다(0.96 g, 99%). 이 반응은 12.4 g 규모에서 반복되어 11.06 g의 산물이 생성되었다(96%). 분석 데이터: RT 3.37 min; MS (ES+) m/z (상대적 강도) 685 ([M + H]+., 100).
(iii) (
S
)-((펜탄-1,5-디일비스(옥시))비스(5-메톡시-2-니트로-4,1-페닐렌))비스(((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-일)메타논) (
7
)
아르곤 대기하에서 무수 DMF (100 mL) 안에 비스-니트로 알코올 (6) (7.94 g, 11.6 mmol, 1 eq), tert-부틸디메틸실일클로라이드 (4.54 g, 30.15 mmol, 2.6 eq) 그리고 이미다졸(4.1 g, 60.3 mmol, 5.2 eq)의 용액은 실온에서 3시간 동안 교반되었다. 반응 혼합물은 물(250 mL)로 희석되었고, DCM (4 x 100 mL)으로 추출되었다. 복합된 추출물은 물(200 mL), 포화 염수 (200 mL)로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되었다. 잔기는 섬광 컬럼 크로마토그래피 [50% 에틸아세테이트/50% n-헥산 내지 100% 에틸아세테이트- 10%씩 증분]에서 정제되어 황색 포말로된 산물이 획득되었다(10.0 g, 94%). 분석 데이터: RT 4.57 min; MS (ES+) m/z (상대적 강도) 913 [M + H]+., 100).
(iv) (
S
)-((펜탄-1,5-디일비스(옥시))비스(2-아미노-5-메톡시-4,1-페닐렌))비스(((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-일)메타논) (
8
)
포름산 용액 (5% v/v, 15 mL)은 에틸아세테이트/에탄올 (80 mL/150 mL)에서 아연 분말(29.56 g, 0.45 mol, 40 eq.)과 화합물 (7) (10.34 g, 11.32 mmol, 1 eq.)의 혼합물에 한 부분으로 추가되었다. 12℃의 발열이 관찰되었다. 15분 후, 반응 혼합물은 에틸아세테이트 (과량)으로 세척되면서 셀라이트를 통하여 여과되었다. 여과물은 포화 중탄산 나트륨 (3 x 150 mL), 물(200 mL), 포화 염수 (200 mL)로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되었다. 섬광 컬럼 크로마토그래피 [에틸아세테이트]에 의해 정제되면 백색 포말로 된 산물이 수득되었다 (8.09 g, 84%). 분석 데이터: RT 4.43 min; MS (ES+) m/z (상대적 강도) 853 ([M + H]+., 100).
(v) tert-부틸 (5-((5-(5-아미노-4-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-2-메톡시펜옥시)펜틸)옥시)-2-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시페닐)카르바메이트 (
9
)
무수 THF (50 mL)에서 비스-아닐린 (8) (6.02 g, 7.1 mmol, 1 eq.)과 디-t-부틸-디카르보네이트 (1.54 g, 7.1 mmol, 1 eq.)의 용액은 16시간 동안 재환류에서 가열되었다. 용매는 감압하에서 기화되었고, 잔류물은 섬광 컬럼 크로마토그래피 [40% 에틸아세테이트/60% n-헥산 내지 60% 에틸아세테이트/40% n-헥산 내지 100% 에틸아세테이트]로 정제되어 백색 포말로 된 산물이 제공되었다(3.22 g, 48%). 분석 데이터: RT 4.27 min MS (ES+) m/z (상대적 강도) 953 ([M + H]+., 100), MS (ES-) m/z (상대적 강도) 951 ([M - H])-., 100).
(c) (11
S
,11a
S
)-2-(피리딘-2-일디술파닐)에틸 11-히드록시-7-메톡시-8-((5-(((
S
)-7-메톡시-2-메틸렌-5-옥소-2,3,5,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
14
)
화합물 10은 Jones et al, J. Am. Chem. Soc., 2006, 128, 6526-6527에 따라 준비되었다.
(i) tert-부틸 (2-(피리딘-2-일디술파닐)에틸) ((
S
)-(펜탄-1,5-디일비스(옥시))비스(2-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시-5,1-페닐렌))디카르바메이트 (
11
)
트리에틸아민 (0.25 g, 0.34 mL, 2.42 mmol, 2.2 eq.)은 실온에서 아르곤 대기하에 건조 THF (10 mL) 안에서 모노-Boc 보호된 비스-아닐린 (9) (1.05 g, 1.1 mmol, 1.0 eq.)과 트리포스포겐(0.117 g, 0.4 mmol, 0.36 eq.)의 교반된 용액에 추가되었다. 반응 혼합물은 40℃로 가열되었고, 5분 후 시료는 메탄올로 처리되었고, LCMS에 의해 메틸 카르바메이트로 분석되었다. 분석 데이터: RT 4.37 min MS (ES+) m/z (상대적 강도) 1011 ([M + H]+., 100).
건조 THF (10 mL)에서 2-(피리딘-2-일디술파닐)에탄올 (10) (0.31 g, 1.65 mmol, 1.5 eq.)와 트리에틸아민 (0.17 g, 0.23 mL, 1.65 mmol, 1.5 eq.)의 용액은 새로 준비된 이소시아네이트에 점적되었다. 반응 혼합물은 40℃에서 1.5시간 동안 가열되었고, 그 다음 추가 부분의 트리포스포겐 (0.058 g, 0.2 mmol, 0.18 eq.)이 첨가되었다. 추가 30분 후, 반응 혼합물은 냉각되도록 둔 다음, 여과시켜 트리에틸아민 히드로클로라이드를 제거하였고, 여과물은 건조되도록 기화되어 황색 오일로된 미정제 산물이 제공되었고, 이는 섬광 컬럼 크로마토그래피 [60% n-헥산/40% 에틸아세테이트에서 55% n-헥산/45% 에틸아세테이트로 변화]에 의해 정제되어 무색 오일로 된 원하는 산물이 제공되었다(0.63 g, 49%). 분석 데이터: RT 4.50 min; MS (ES+) m/z (상대적 강도) 1166 ([M + H]+., 100), MS (ES-) m/z (상대적 강도) 1164 ([M - H])-., 70).
(ii) tert-부틸 (2-(피리딘-2-일디술파닐)에틸) ((
S
)-(펜탄-1,5-디일비스(옥시))비스(2-((
S
)-2-(히드록시메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시-5,1-페닐렌))디카르바메이트 (
12
)
AcOH/H2O (3/1/) (8 mL)은 THF(2 mL)에 화합물 (11) (0.37 g, 0.32 mmol, 1 eq) in THF (2 mL)의 용액에 첨가되었고, 생성된 용액은 18시간 동안 실온에서 교반되었다. 반응 혼합물의 pH는 포화 NaHCO3 용액을 이용하여 pH8로 조정되었다. 혼합물은 에틸아세테이트 (3 x 100 mL)로 추출되었고, 복합된 추출물은 포화 NaHCO3 용액 (100 mL), 물(100 mL), 포화 염수 (100 mL)로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되었다. 섬광 컬럼 크로마토그래피 [그라디언트 용리 클로로포름 /메탄올 0% 내지 5%, 1%씩 증분]에 의한 잔류물의 정제로 백색 포말로 된 산물이 제공되었다(0.24 g, 81%). 분석 데이터: RT 3.08 min; MS (ES+) m/z (상대적 강도) 938 ([M + H]+., 100), MS (ES-) m/z (상대적 강도) 936 ([M - H])-., 100).
(iii) (11
S
,11a
S
)-tert-부틸 11-히드록시-8-((5-(((11
S
,11a
S
)-11-히드록시-7-메톡시-2-메틸렌-5-옥소-10-((2-(피리딘-2-일디술파닐)에톡시)카르보닐)-2,3,5,10,11,11a-헥사히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-7-메톡시-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
13
)
DCM (5 mL)내 DMSO (79 mg, 72 μL, 1.0 mmol, 4.4 eq) 용액은 -78℃(드라이아이스/아세톤)에서 아르곤 대기하에 DCM (5 mL)내 옥살일 클로라이드 (62 mg, 42 μL, 0.49 mmol, 2.15 eq.)의 용액에 점적되었다. 이 용액은 -78℃에서 15분간 교반되었다. DCM (6 mL)내 화합물 (12) (0.214 g, 0.23 mmol, 1.0 eq.)의 용액이 점적되었고, 혼합물은 -78℃에서 45분간 교반되었다. 트리에틸아민 (0.23 g, 0.32 mL, 2.28 mmol, 10 eq.)이 첨가되었고, 5분 후 반응 혼합물은 실온에 도달되도록 두었다. 반응 혼합물은 포화 NH4Cl 용액 (15 mL)으로 처리되었고, 유기 부분은 분리되었고, 1M 구연산 용액 (3 x 50 mL), 포화 NaHCO3 용액 (100 mL), 물(100mL), 포화 염수 (100 mL)으로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되어 옅은 황색 오일이 제공되었다. 섬광 컬럼 크로마토그래피에 의한 정제로 백색 포말로 된 산물이 제공되었다(68 mg, 32%). 분석 데이터: RT 2.90 min; MS (ES+) m/z(상대적 강도) 933 ([M + H]+., 50), MS (ES-) m/z (상대적 강도) 935 ([M - H])-., 55).
(iv) (11
S
,11a
S
)-2-(피리딘-2-일디술파닐)에틸 11-히드록시-7-메톡시-8-((5-(((
S
)-7-메톡시-2-메틸렌-5-옥소-2,3,5,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
14
)
95% 트리플루오로아세트산 (1 mL)의 차가운(얼음조) 용액은 얼음조에서 냉각된 화합물 13에 첨가되었다. 용액은 0℃에서 15분간 교반되었고, 이때 LCMS에 의해 완료된 것으로 나타났다. 이 반응 혼합물은 차가운 포화 NaHCO3 용액의 혼합물에 점적되어 트리플루오로아세트산 용액이 중화되었다. 혼합물은 DCM (4 x 50 mL)으로 추출되었고, 복합된 추출물은 포화 염수 (100 mL)로 세척되었고, 건조되었다(MgSO4) 그리고 감압하에서 기화되어 백색 포말로 된 산물이 제공되었다(26 mg, 96%). 분석 데이터: RT 2.72 min; MS (ES+) m/z (상대적 강도) 816 ([M + H]+., 70), MS (ES-) m/z (상대적 강도) 814 ([M - H])-., 40).
1. 디설피드 메틸 PBD 시약의 합성
(a) (
R
)-2-(피리딘-2-일디술파닐)프로판-1-올 (
18
)
(i) (
R
)-메틸 2-(아세틸티오)프로파노에이트 (
16
)
티오아세트산 (1.99 g, 1.86 mL, 26.1 mmol, 1.1 eq.)은 건조 DMF (40 mL)에 탄산 세슘(7.73 g, 23.72 mmol, 1.0 eq.)의 현탁액에 추가되었다. 30 분 후 (S)-메틸 2-클로로프로파노에이트 (15)가 추가되었고, 혼합물은 실온에서 1시간 동안 교반되도록 두었다. 반응 혼합물은 디에틸 에테르 (150 mL)과 물(150 mL) 사이에서 분할되었다; 물이 분리되었고, 추가 디에틸 에테르 (150 mL) 부분에 의해 세척되었다. 복합된 유기 부분들은 물(6 x 100 mL), 염수 (200 mL)로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되었다. 섬광 컬럼 크로마토그래피 [10% 에틸아세테이트/90% n-헥산]에 의한 정제에 의해 무색 오일로 된 산물이 수득되었다(3.01 g, 82%). 분석 데이터: RT 2.25 min; MS (ES+) m/z (상대적 강도) 163 ([M + H]+., 10), 185([M + Na]+., 65); [α]t d = [+141]17.8℃ d (c, 2.26 CHCl3).
(ii) (
R
)-2-멀캅토프로판-1-올(
17
)
건조 THF (10 mL)에서 티오아세테이트 (16) (0.57 g, 3.54 mmol, 1.0 eq.)의 용액은 아르곤 대기하에 재환류에서 건조 THF(20mL)에서 수산화리튬 알루미늄(0.54 g, 14.15 mmol, 4.0 eq.) 현탁액에 점적되었다. 1시간 후, 반응 혼합물은 0℃도 냉각되었고, 2M HCl은 비등이 중단될 때까지 30℃ 미만으로 온도를 유지시키면서 점적되었다. 생성된 혼합물은 실온에서 1시간 동안 교반되도록 두었고, 그 다음 THF (40 mL)로 세척되면서 셀라이트를 통하여 여과되었다. 용매는 기화되었다; 잔류물은 DCM에 다시 용해되었고, 건조되었다(MgSO4). 감암하에 DCM의 기화와 이어서 잔류물의 컬럼 크로마토그래피[60% n-헥산/40% 에틸아세테이트]에 의해 옅은 황색 오일로 된 산물이 수득되었다(0.193 g, 58%). 분석 데이터: [α]t d = [-22]17.2℃(c, 0.972 CHCl3).
(iii) (
R
)-2-(피리딘-2-일디술파닐)프로판-1-올 (
18
)
술푸릴 클로라이드 (DCM내에서 1M, 2.0 mL, 2.0 mmol, 1.1 eq.)는 아르곤 대기하에 0℃에서 건조 DCM(5mL)내에 2-멀캅토피리딘 (0.2 g, 1.81 mmol, 1.0 eq.)의 용액에 점적되었다. 생성된 용액은 실온에서 2시간 교반되었고, DCM은 감압하에서 기화되어 황색 고체가 수득되었다. 고체는 건조 DCM (10 mL)에 현탁되었고, 건조 DCM (5 mL)내 (R)-2-멀캅토프로판-1-올 (17)(0.18 g, 1.95 mmol, 1.08 eq.)의 용액이 점적되었다. 혼합물은 아르곤 대기하에 실온에서 18시간 동안 교반되었다. 반응 혼합물은 여과되었고, 여과물은 감압하에서 기화되어 황색 점성물이 수득되었다. 점성 물질은 물에 다시 용해되었고, 용액은 수산화 암모늄 용액으로 염기화되었고, DCM (3 x 50 mL)으로 추출되었고, 그리고 복합된 추출물은 물(100 mL), 염수 (100 mL)로 세척되었고, 건조되었다(MgSO4) 그리고 기화되어 황색 오일이 수득되었다. 섬광 컬럼 크로마토그래피 [80% n-헥산/20% 에틸아세테이트 내지 60 % n-헥산/40% 에틸아세테이트, 5%씩 증분]에 의해 무색 오일로 된 산물이 수득되었다 (0.213 g, 59%). 분석 데이터: RT 2.43 min; MS (ES+) m/z (상대적 강도) 202 ([M + H]+., 50); [α]t d = [+273]26.2℃ d (c, 0.28 CHCl3).
(b) (11
S
,11a
S
)-(
R
)-2-(피리딘-2-일디술파닐)프로필 11-히드록시-7-메톡시-8-((5-(((
S
)-7-메톡시-2-메틸렌-5-옥소-2,3,5,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
22
)
(i) tert-부틸 ((
R
)-2-(피리딘-2-일디술파닐)프로필) ((
S
)-(펜탄-1,5-디일비스(옥시))비스(2-((
S
)-2-(((tert-부틸디메틸실일)옥시)메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시-5,1-페닐렌))디카르바메이트 (
19
)
트리에틸아민 (0.28 g, 0.39 mL, 2.8 mmol, 2.2 eq.)은 아르곤 대기하 실온에서 건조 THF(15mL)내 모노-boc 보호된 비스-아닐린 (9) (1.21 g, 1.27 mmol, 1.0 eq.)와 트리포스포겐 (0.136 g, 0.46 mmol, 0.36 eq.)의 교반된 용액에 첨가되었다. 반응 혼합물은 40℃로 가열되었고, 5분 후 시료는 메탄올로 처리되었고, 그리고 LCMS에 의해 메틸 카르바메이트로 분석되었다. 분석 데이터: RT 4.30 min MS (ES+) m/z (상대적 강도) 1011 ([M + H]+., 100).
건조 THF (10 mL)내에 (R)-2-(피리딘-2-일디술파닐)프로판-1-올(18) (0.38 g, 1.91 mmol, 1.5 eq.) 및 트리에틸아민 (0.19 g, 0.27 mL, 1.91 mmol, 1.5 eq.)의 용액은 새로 준비된 이소시아네이트에 점적되었다. 반응 혼합물은 40℃에서 4 시간동안 가열되었고, 실온에서 18시간 동안 교반되었다. 반응 혼합물은 여과되어 트리에틸아민 히드로클로라이드가 제거되었고, 여과물은 건조되도록 기화되어 황색 오일의 미정제 산물이 획득되었고, 이는 섬광 컬럼 크로마토그래피 [60% n-헥산/40% 에틸아세테이트 내지 40% n-헥산/60% 에틸아세테이트, 5%씩 증분]에 의해 정제되어 백색 포말로 된 바람직한 산물이 수득되었다(0.75 g, 50%). 분석 데이터: RT 4.50 min; MS (ES+) m/z (상대적 강도) 1180 ([M + H]+., 60); [α]t d = [-18]21℃ d (c, 0.28 CHCl3).
(ii) tert-부틸 ((
R
)-2-(피리딘-2-일디술파닐)프로필) ((
S
)-(펜탄-1,5-디일비스(옥시))비스(2-((
S
)-2-(히드록시메틸)-4-메틸렌피롤리딘-1-카르보닐)-4-메톡시-5,1-페닐렌))디카르바메이트 (
20
)
아세트산/H2O (3/1, 16 mL)는 THF(4mL)내 비스-실일 에테르 (19) (0.72 g, 0.61 mmol, 1 eq.)의 용액에 추가되었다. 생성된 용액은 실온에서 16 시간 동안 교반되었다. 반응 혼합물의 pH는 포화 중탄산 나트륨 용액에 의해 pH8로 조정되었다. 혼합물은 에틸아세테이트 (4 x 150 mL)로 추출되었고, 복합된 추출물은 포화 중탄산 나트륨 용액 (2 x 150 mL), 물(150 mL), 염수 (150 mL)로 세척되었고, 건조되었고(MgSO4), 감압하에서 기화되었다. 섬광 컬럼 크로마토그래피에 의한 정제에 의해 백색 포말로 된 산물이 수득되었다(0.56 g, 96%). 분석 데이터: RT 3.15 min; MS (ES+) m/z (상대적 강도) 953 ([M + H]+., 100); [α]t d = [-13.5]26℃ d (c, 0.22 CHCl3).
(iii) (11
S
,11a
S
)-tert-부틸 11-히드록시-8-((5-(((11S,11a
S
)-11-히드록시-7-메톡시-2-메틸렌-5-옥소-10-(((
R
)-2-(피리딘-2-일디술파닐)프로폭시)카르보닐)-2,3,5,10,11,11a-헥사히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-7-메톡시-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
21
)
무수 DCM (5 mL)내 DMSO (91 mg, 83 μL, 1.16 mmol, 4.4 eq.)의 용액은 아르곤 대기하에 -40℃에서 무수 DCM (5 mL)내 옥살일 클로라이드 (DCM내 2.0M, 318 μL, 0.635 mmol, 2.4 eq.)의 용액에 점적되었다. 용액은 -40℃에서 15분간 교반되었다. 무수 DCM (10 mL)내 비스-알코올 (20) (0.252 g, 0.26 mmol, 1 eq.)의 용액이 점적되었고, 생성된 혼합물은 -40℃에서 45분간 교반되었다. 이 시간 동안 온도는 -25℃에 도달되도록 두었다. 온도는 -35℃로 낮추고, 트리에틸아민 (0.27 g, 0.36 mL, 2.6 mmol, 10 eq.)이 점적되었다. 5분 후, 온도는 실온에 도달되도록 두었다. 반응 혼합물은 DCM (50 mL)으로 희석되었고, 1M 구연산 용액 (3 x 150 mL), 포화 중탄산 나트륨 용액 (150 mL), 물(200 mL), 염수 (200 mL)로 추출되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되어 황색 포말이 수득되었다. 섬광 컬럼 크로마토그래피 [클로로포름/메탄올 0% 내지 2%, 0.5%씩 증분]에 의한 정제로 백색 포말이 획득되었다 (0.137 g, 53%). 분석 데이터: RT 3.17 min; MS (ES+) m/z (상대적 강도) 948 ([M + H]+., 100); [α]t d = [+170]26℃ d (c, 0.25 CHCl3).
(iv) (11S,11a
S
)-(
R
)-2-(피리딘-2-일디술파닐)프로필 11-히드록시-7-메톡시-8-((5-(((
S
)-7-메톡시-2-메틸렌-5-옥소-2,3,5,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-8-일)옥시)펜틸)옥시)-2-메틸렌-5-옥소-2,3,11,11a-테트라히드로-1H-피롤로[2,1-c][1,4]벤조디아제핀-10(5H)-카르복실레이트 (
22
)
95% 트리플루오로아세트산 (8.5 mL)의 차가운 용액(얼음조)은 얼음조 안에서 냉각된 화합물 (21) (0.221 g, 0.23 mmol, 1 eq.)에 추가되었다. 용액은 0℃에서 25분간 교반되었고, LCMS에 의해 완료되었음이 볼 수 있었다. 반응 혼합물은 차가운 그리고 포화 중탄산 나트륨 용액 (200 mL)의 혼합물에 점적되어, 트리플루오로아세트산 용액이 중화되었다. 혼합물은 DCM (4 x 75 mL)으로 추출되었고, 복합된 추출물은 물(100 mL) 포화 염수 (100 mL)로 세척되었고, 건조되었고(MgSO4) 그리고 감압하에서 기화되어 미정제 산물이 수득되었다. 섬광 컬럼 크로마토그래피 [클로로포름/메탄올 0% 내지 3%, 1%씩 증분]에 의한 정제로 백색 포말로 된 산물이 획득되었다 (0.192 g, 99%). 분석 데이터: RT 3.00 min; MS (ES+) m/z (상대적 강도) 830 ([M + H]+., 75); [α]t d = [+444]22℃ d (c, 0.26 CHCl3).
전술한 발명은 명백한 이해를 위한 목적으로 설명 및 실시예에 의해 일부 상세하게 설명되었지만, 본 발명의 범위를 설명 및 실시예들로 제한되어서는 안된다. 본 명세서에서 언급된 모든 특허 및 과학 문헌은 이들의 전문이 명세서의 참고자료에 편입된다.
SEQUENCE LISTING
<110> Genentech, Inc.
<120> ANTI-CD22 ANTIBODIES AND IMMUNOCONJUGATES
<130> GENE-32632/WO-1/ORD
<150> US 61/669,272
<151> 2012-07-09
<150> US 61/777,113
<151> 2013-03-12
<160> 52
<170> PatentIn version 3.5
<210> 1
<211> 113
<212> PRT
<213> Homo sapiens
<400> 1
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Asp Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser
<210> 2
<211> 107
<212> PRT
<213> Homo sapiens
<400> 2
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 3
<211> 120
<212> PRT
<213> Mus musculus
<400> 3
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Arg Glu Trp Ile
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Val Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Ala
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 4
<211> 112
<212> PRT
<213> Mus musculus
<400> 4
Asp Ile Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Phe Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Gln Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 5
<211> 120
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 5
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 112
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 6
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Phe Leu Glu Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Gln Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 7
<211> 120
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 7
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 8
<211> 112
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 8
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Val Gly Asn Thr Phe Leu Glu Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Gln Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 9
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 9
Gly Tyr Glu Phe Ser Arg Ser Trp Met Asn
1 5 10
<210> 10
<211> 18
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 10
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
1 5 10 15
Lys Gly
<210> 11
<211> 11
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 11
Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 12
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 12
Arg Ser Ser Gln Ser Ile Val His Ser Asn Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 13
<211> 7
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 13
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 14
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 14
Phe Gln Gly Ser Gln Phe Pro Tyr Thr
1 5
<210> 15
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 15
Arg Ser Ser Gln Ser Ile Val His Ser Val Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 16
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 16
Arg Ser Ser Gln Ser Ile Val His Ser Ala Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 17
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 17
Arg Ser Ser Gln Ser Ile Val His Ser Gln Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 18
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 18
Arg Ser Ser Gln Ser Ile Val His Ser Ser Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 19
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 19
Arg Ser Ser Gln Ser Ile Val His Ser Asp Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 20
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 20
Arg Ser Ser Gln Ser Ile Val His Ser Ile Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 21
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 21
Arg Ser Ser Gln Ser Ile Val His Ser Asn Gly Ile Thr Phe Leu Glu
1 5 10 15
<210> 22
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 22
Arg Ser Ser Gln Ser Ile Val His Ser Asn Gly Gln Thr Phe Leu Glu
1 5 10 15
<210> 23
<211> 219
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Val Gly Asn Thr Phe Leu Glu Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Gln Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 24
<211> 450
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 24
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 25
<211> 219
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Val Gly Asn Thr Phe Leu Glu Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Gln Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Cys Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 26
<211> 450
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 26
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Cys Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 27
<211> 450
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Glu Phe Ser Arg Ser
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Cys Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 28
<211> 847
<212> PRT
<213> Homo sapiens
<400> 28
Met His Leu Leu Gly Pro Trp Leu Leu Leu Leu Val Leu Glu Tyr Leu
1 5 10 15
Ala Phe Ser Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu
20 25 30
Tyr Ala Trp Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala
35 40 45
Leu Asp Gly Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr
50 55 60
Asn Lys Asn Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr
65 70 75 80
Lys Asp Gly Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly
85 90 95
Asp Lys Asn Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn
100 105 110
Asp Ser Gly Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp
115 120 125
Met Glu Arg Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His
130 135 140
Ile Gln Leu Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr
145 150 155 160
Cys Leu Leu Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp
165 170 175
Leu Leu Glu Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser
180 185 190
Leu Thr Ile Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro
195 200 205
Gln Trp Ser His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala
210 215 220
Asp Gly Lys Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His
225 230 235 240
Thr Pro Lys Leu Glu Ile Lys Val Thr Pro Ser Asp Ala Ile Val Arg
245 250 255
Glu Gly Asp Ser Val Thr Met Thr Cys Glu Val Ser Ser Ser Asn Pro
260 265 270
Glu Tyr Thr Thr Val Ser Trp Leu Lys Asp Gly Thr Ser Leu Lys Lys
275 280 285
Gln Asn Thr Phe Thr Leu Asn Leu Arg Glu Val Thr Lys Asp Gln Ser
290 295 300
Gly Lys Tyr Cys Cys Gln Val Ser Asn Asp Val Gly Pro Gly Arg Ser
305 310 315 320
Glu Glu Val Phe Leu Gln Val Gln Tyr Ala Pro Glu Pro Ser Thr Val
325 330 335
Gln Ile Leu His Ser Pro Ala Val Glu Gly Ser Gln Val Glu Phe Leu
340 345 350
Cys Met Ser Leu Ala Asn Pro Leu Pro Thr Asn Tyr Thr Trp Tyr His
355 360 365
Asn Gly Lys Glu Met Gln Gly Arg Thr Glu Glu Lys Val His Ile Pro
370 375 380
Lys Ile Leu Pro Trp His Ala Gly Thr Tyr Ser Cys Val Ala Glu Asn
385 390 395 400
Ile Leu Gly Thr Gly Gln Arg Gly Pro Gly Ala Glu Leu Asp Val Gln
405 410 415
Tyr Pro Pro Lys Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile
420 425 430
Arg Glu Gly Asp Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn
435 440 445
Pro Ser Val Thr Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu
450 455 460
Pro Ser Leu Gly Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr
465 470 475 480
Thr Ile Ala Cys Ala Arg Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro
485 490 495
Val Ala Leu Asn Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys
500 505 510
Ile Lys Pro Leu Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln
515 520 525
Cys Asp Phe Ser Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu
530 535 540
Lys Asn Gly Arg Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser
545 550 555 560
Ile Ser Pro Glu Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser
565 570 575
Ile Gly Gln Thr Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala
580 585 590
Pro Arg Arg Leu Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu
595 600 605
Gly Lys Ser Ala Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val
610 615 620
Ser His Tyr Thr Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro His His
625 630 635 640
Ser Gln Lys Leu Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala
645 650 655
Tyr Trp Cys Gln Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu
660 665 670
Ser Thr Leu Thr Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg Val
675 680 685
Ala Val Gly Leu Gly Ser Cys Leu Ala Ile Leu Ile Leu Ala Ile Cys
690 695 700
Gly Leu Lys Leu Gln Arg Arg Trp Lys Arg Thr Gln Ser Gln Gln Gly
705 710 715 720
Leu Gln Glu Asn Ser Ser Gly Gln Ser Phe Phe Val Arg Asn Lys Lys
725 730 735
Val Arg Arg Ala Pro Leu Ser Glu Gly Pro His Ser Leu Gly Cys Tyr
740 745 750
Asn Pro Met Met Glu Asp Gly Ile Ser Tyr Thr Thr Leu Arg Phe Pro
755 760 765
Glu Met Asn Ile Pro Arg Thr Gly Asp Ala Glu Ser Ser Glu Met Gln
770 775 780
Arg Pro Pro Arg Thr Cys Asp Asp Thr Val Thr Tyr Ser Ala Leu His
785 790 795 800
Lys Arg Gln Val Gly Asp Tyr Glu Asn Val Ile Pro Asp Phe Pro Glu
805 810 815
Asp Glu Gly Ile His Tyr Ser Glu Leu Ile Gln Phe Gly Val Gly Glu
820 825 830
Arg Pro Gln Ala Gln Glu Asn Val Asp Tyr Val Ile Leu Lys His
835 840 845
<210> 29
<211> 828
<212> PRT
<213> Homo sapiens
<400> 29
Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu Tyr Ala Trp
1 5 10 15
Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala Leu Asp Gly
20 25 30
Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr Asn Lys Asn
35 40 45
Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr Lys Asp Gly
50 55 60
Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly Asp Lys Asn
65 70 75 80
Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn Asp Ser Gly
85 90 95
Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp Met Glu Arg
100 105 110
Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His Ile Gln Leu
115 120 125
Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr Cys Leu Leu
130 135 140
Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp Leu Leu Glu
145 150 155 160
Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser Leu Thr Ile
165 170 175
Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro Gln Trp Ser
180 185 190
His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala Asp Gly Lys
195 200 205
Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His Thr Pro Lys
210 215 220
Leu Glu Ile Lys Val Thr Pro Ser Asp Ala Ile Val Arg Glu Gly Asp
225 230 235 240
Ser Val Thr Met Thr Cys Glu Val Ser Ser Ser Asn Pro Glu Tyr Thr
245 250 255
Thr Val Ser Trp Leu Lys Asp Gly Thr Ser Leu Lys Lys Gln Asn Thr
260 265 270
Phe Thr Leu Asn Leu Arg Glu Val Thr Lys Asp Gln Ser Gly Lys Tyr
275 280 285
Cys Cys Gln Val Ser Asn Asp Val Gly Pro Gly Arg Ser Glu Glu Val
290 295 300
Phe Leu Gln Val Gln Tyr Ala Pro Glu Pro Ser Thr Val Gln Ile Leu
305 310 315 320
His Ser Pro Ala Val Glu Gly Ser Gln Val Glu Phe Leu Cys Met Ser
325 330 335
Leu Ala Asn Pro Leu Pro Thr Asn Tyr Thr Trp Tyr His Asn Gly Lys
340 345 350
Glu Met Gln Gly Arg Thr Glu Glu Lys Val His Ile Pro Lys Ile Leu
355 360 365
Pro Trp His Ala Gly Thr Tyr Ser Cys Val Ala Glu Asn Ile Leu Gly
370 375 380
Thr Gly Gln Arg Gly Pro Gly Ala Glu Leu Asp Val Gln Tyr Pro Pro
385 390 395 400
Lys Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile Arg Glu Gly
405 410 415
Asp Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn Pro Ser Val
420 425 430
Thr Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu Pro Ser Leu
435 440 445
Gly Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr Thr Ile Ala
450 455 460
Cys Ala Arg Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro Val Ala Leu
465 470 475 480
Asn Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys Ile Lys Pro
485 490 495
Leu Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln Cys Asp Phe
500 505 510
Ser Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu Lys Asn Gly
515 520 525
Arg Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser Ile Ser Pro
530 535 540
Glu Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser Ile Gly Gln
545 550 555 560
Thr Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala Pro Arg Arg
565 570 575
Leu Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu Gly Lys Ser
580 585 590
Ala Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val Ser His Tyr
595 600 605
Thr Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro His His Ser Gln Lys
610 615 620
Leu Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala Tyr Trp Cys
625 630 635 640
Gln Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu Ser Thr Leu
645 650 655
Thr Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg Val Ala Val Gly
660 665 670
Leu Gly Ser Cys Leu Ala Ile Leu Ile Leu Ala Ile Cys Gly Leu Lys
675 680 685
Leu Gln Arg Arg Trp Lys Arg Thr Gln Ser Gln Gln Gly Leu Gln Glu
690 695 700
Asn Ser Ser Gly Gln Ser Phe Phe Val Arg Asn Lys Lys Val Arg Arg
705 710 715 720
Ala Pro Leu Ser Glu Gly Pro His Ser Leu Gly Cys Tyr Asn Pro Met
725 730 735
Met Glu Asp Gly Ile Ser Tyr Thr Thr Leu Arg Phe Pro Glu Met Asn
740 745 750
Ile Pro Arg Thr Gly Asp Ala Glu Ser Ser Glu Met Gln Arg Pro Pro
755 760 765
Arg Thr Cys Asp Asp Thr Val Thr Tyr Ser Ala Leu His Lys Arg Gln
770 775 780
Val Gly Asp Tyr Glu Asn Val Ile Pro Asp Phe Pro Glu Asp Glu Gly
785 790 795 800
Ile His Tyr Ser Glu Leu Ile Gln Phe Gly Val Gly Glu Arg Pro Gln
805 810 815
Ala Gln Glu Asn Val Asp Tyr Val Ile Leu Lys His
820 825
<210> 30
<211> 670
<212> PRT
<213> Homo sapiens
<400> 30
Met His Leu Leu Gly Pro Trp Leu Leu Leu Leu Val Leu Glu Tyr Leu
1 5 10 15
Ala Phe Ser Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu
20 25 30
Tyr Ala Trp Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala
35 40 45
Leu Asp Gly Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr
50 55 60
Asn Lys Asn Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr
65 70 75 80
Lys Asp Gly Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly
85 90 95
Asp Lys Asn Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn
100 105 110
Asp Ser Gly Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp
115 120 125
Met Glu Arg Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His
130 135 140
Ile Gln Leu Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr
145 150 155 160
Cys Leu Leu Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp
165 170 175
Leu Leu Glu Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser
180 185 190
Leu Thr Ile Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro
195 200 205
Gln Trp Ser His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala
210 215 220
Asp Gly Lys Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His
225 230 235 240
Pro Pro Lys Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile Arg
245 250 255
Glu Gly Asp Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn Pro
260 265 270
Ser Val Thr Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu Pro
275 280 285
Ser Leu Gly Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr Thr
290 295 300
Ile Ala Cys Ala Ala Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro Val
305 310 315 320
Ala Leu Asn Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys Ile
325 330 335
Lys Pro Leu Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln Cys
340 345 350
Asp Phe Ser Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu Lys
355 360 365
Asn Gly Arg Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser Ile
370 375 380
Ser Pro Glu Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser Ile
385 390 395 400
Gly Gln Thr Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala Pro
405 410 415
Arg Arg Leu Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu Gly
420 425 430
Lys Ser Ala Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val Ser
435 440 445
His Tyr Thr Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro Tyr His Ser
450 455 460
Gln Lys Leu Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala Tyr
465 470 475 480
Trp Cys Gln Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu Ser
485 490 495
Thr Leu Thr Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg Val Ala
500 505 510
Val Gly Leu Gly Ser Cys Leu Ala Ile Leu Ile Leu Ala Ile Cys Gly
515 520 525
Leu Lys Leu Gln Arg Arg Trp Lys Arg Thr Gln Ser Gln Gln Gly Leu
530 535 540
Gln Glu Asn Ser Ser Gly Gln Ser Phe Phe Val Arg Asn Lys Lys Val
545 550 555 560
Arg Arg Ala Pro Leu Ser Glu Gly Pro His Ser Leu Gly Cys Tyr Asn
565 570 575
Pro Met Met Glu Asp Gly Ile Ser Tyr Thr Thr Leu Arg Phe Pro Glu
580 585 590
Met Asn Ile Pro Arg Thr Gly Asp Ala Glu Ser Ser Glu Met Gln Arg
595 600 605
Pro Pro Pro Asp Cys Asp Asp Thr Val Thr Tyr Ser Ala Leu His Lys
610 615 620
Arg Gln Val Gly Asp Tyr Glu Asn Val Ile Pro Asp Phe Pro Glu Asp
625 630 635 640
Glu Gly Ile His Tyr Ser Glu Leu Ile Gln Phe Gly Val Gly Glu Arg
645 650 655
Pro Gln Ala Gln Glu Asn Val Asp Tyr Val Ile Leu Lys His
660 665 670
<210> 31
<211> 651
<212> PRT
<213> Homo sapiens
<400> 31
Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu Tyr Ala Trp
1 5 10 15
Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala Leu Asp Gly
20 25 30
Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr Asn Lys Asn
35 40 45
Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr Lys Asp Gly
50 55 60
Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly Asp Lys Asn
65 70 75 80
Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn Asp Ser Gly
85 90 95
Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp Met Glu Arg
100 105 110
Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His Ile Gln Leu
115 120 125
Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr Cys Leu Leu
130 135 140
Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp Leu Leu Glu
145 150 155 160
Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser Leu Thr Ile
165 170 175
Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro Gln Trp Ser
180 185 190
His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala Asp Gly Lys
195 200 205
Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His Pro Pro Lys
210 215 220
Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile Arg Glu Gly Asp
225 230 235 240
Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn Pro Ser Val Thr
245 250 255
Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu Pro Ser Leu Gly
260 265 270
Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr Thr Ile Ala Cys
275 280 285
Ala Ala Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro Val Ala Leu Asn
290 295 300
Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys Ile Lys Pro Leu
305 310 315 320
Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln Cys Asp Phe Ser
325 330 335
Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu Lys Asn Gly Arg
340 345 350
Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser Ile Ser Pro Glu
355 360 365
Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser Ile Gly Gln Thr
370 375 380
Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala Pro Arg Arg Leu
385 390 395 400
Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu Gly Lys Ser Ala
405 410 415
Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val Ser His Tyr Thr
420 425 430
Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro Tyr His Ser Gln Lys Leu
435 440 445
Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala Tyr Trp Cys Gln
450 455 460
Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu Ser Thr Leu Thr
465 470 475 480
Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg Val Ala Val Gly Leu
485 490 495
Gly Ser Cys Leu Ala Ile Leu Ile Leu Ala Ile Cys Gly Leu Lys Leu
500 505 510
Gln Arg Arg Trp Lys Arg Thr Gln Ser Gln Gln Gly Leu Gln Glu Asn
515 520 525
Ser Ser Gly Gln Ser Phe Phe Val Arg Asn Lys Lys Val Arg Arg Ala
530 535 540
Pro Leu Ser Glu Gly Pro His Ser Leu Gly Cys Tyr Asn Pro Met Met
545 550 555 560
Glu Asp Gly Ile Ser Tyr Thr Thr Leu Arg Phe Pro Glu Met Asn Ile
565 570 575
Pro Arg Thr Gly Asp Ala Glu Ser Ser Glu Met Gln Arg Pro Pro Pro
580 585 590
Asp Cys Asp Asp Thr Val Thr Tyr Ser Ala Leu His Lys Arg Gln Val
595 600 605
Gly Asp Tyr Glu Asn Val Ile Pro Asp Phe Pro Glu Asp Glu Gly Ile
610 615 620
His Tyr Ser Glu Leu Ile Gln Phe Gly Val Gly Glu Arg Pro Gln Ala
625 630 635 640
Gln Glu Asn Val Asp Tyr Val Ile Leu Lys His
645 650
<210> 32
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 32
Gly Tyr Thr Phe Ser Ser Tyr Trp Ile Glu
1 5 10
<210> 33
<211> 18
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 33
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
1 5 10 15
Lys Gly
<210> 34
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 34
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr
1 5 10
<210> 35
<211> 15
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 35
Lys Ala Ser Gln Ser Val Asp Tyr Glu Gly Asp Ser Phe Leu Asn
1 5 10 15
<210> 36
<211> 7
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 36
Ala Ala Ser Asn Leu Glu Ser
1 5
<210> 37
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 37
Gln Gln Ser Asn Glu Asp Pro Leu Thr
1 5
<210> 38
<211> 117
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 38
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
50 55 60
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 39
<211> 112
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 39
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly Asp Ser Phe Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
<210> 40
<211> 446
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 40
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
50 55 60
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Cys Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 41
<211> 218
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 41
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly Asp Ser Phe Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 42
<211> 218
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 42
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly Asp Ser Phe Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Cys Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 43
<211> 447
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 43
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
50 55 60
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Cys
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 44
<211> 446
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 44
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
50 55 60
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 45
<211> 25
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 45
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser
20 25
<210> 46
<211> 13
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 46
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
1 5 10
<210> 47
<211> 32
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 47
Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr Leu Gln
1 5 10 15
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
20 25 30
<210> 48
<211> 11
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 48
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 49
<211> 23
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 49
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys
20
<210> 50
<211> 15
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 50
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
1 5 10 15
<210> 51
<211> 32
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 51
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
20 25 30
<210> 52
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> Synthetic
<400> 52
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
1 5 10
Claims (45)
- 세포독성 물질에 공유적으로 부착된 CD22에 결합되는 항체가 포함된 면역접합체에 있어서, 이때 상기 항체는 서열 번호: 28의 아미노산 20 내지 240내에 있는 에피토프에 결합되며, 그리고 이때 상기 세포독성 물질은 피롤로벤조디아제핀인, 면역접합체.
- 청구항 1에 있어서, 이때 상기 항체는 (i) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3, (ii) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3, 그리고 (iii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2를 포함하는, 면역접합체.
- 청구항 1 또는 2에 있어서, 이때 상기 항체는 (i) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, 그리고 (iii) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3을 포함하는, 면역접합체.
- 청구항 1에 있어서, 이때 상기 항체는 다음을 포함하는, 면역접합체:
a) (i) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3, (iv) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1, (v) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고 (vi) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3; 또는
b) (i) 서열 번호: 9의 아미노산 서열이 포함된 HVR-H1, (ii) 서열 번호: 10의 아미노산 서열이 포함된 HVR-H2, (iii) 서열 번호: 11의 아미노산 서열이 포함된 HVR-H3, (iv) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1, (v) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고 (vi) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3. - 청구항 1 내지 3중 임의의 한 항에 있어서, 이때 상기 항체는 다음을 포함하는 면역접합체:
a) (i) 서열 번호: 12 그리고 15 내지 22에서 선택된 아미노산 서열이 포함된 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고 (iii) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3; 또는
b) (i) 서열 번호: 15의 아미노산 서열이 포함된 HVR-L1, (ii) 서열 번호: 13의 아미노산 서열이 포함된 HVR-L2, 그리고 (iii) 서열 번호: 14의 아미노산 서열이 포함된 HVR-L3. - 청구항 1 내지 5중 임의의 한 항에 있어서, 이때 상기 항체는 다음을 포함하는 면역접합체:
a) 서열 번호: 7의 아미노산 서열에 최소한 95% 서열 동일성을 보유하는 VH 서열; 또는
b) 서열 번호: 8의 아미노산 서열에 최소한 95% 서열 동일성을 보유하는 VL 서열; 또는
c) (a)에서와 같은 VH 서열과 (b)에서와 같은 VL 서열. - 청구항 6에 있어서, 서열 번호: 7의 아미노산 서열을 보유한 VH 서열을 포함하는, 면역접합체.
- 청구항 6에 있어서, 서열 번호: 6의 아미노산 서열을 보유한 VL 서열 또는 서열 번호:8의 아미노산 서열을 보유한 VL 서열을 포함하는, 면역접합체.
- 세포독성 물질에 공유적으로 부착된 CD22에 결합하는 항체를 포함하는 면역접합체에 있어서, 이때 상기 항체는 (a) 서열 번호: 7의 아미노산 서열을 보유하는 VH 서열과 서열 번호: 8의 아미노산 서열을 보유하는 VL 서열을 포함하고, 이때 상기 세포독성 물질은 피롤로벤조디아제핀인, 면역접합체.
- 청구항 1 내지 9중 임의의 한 항에 있어서, 상기 항체는 IgG1, IgG2a 또는 IgG2b 항체인, 면역접합체.
- 청구항 1 내지 10중 임의의 한 항에 있어서, 상기 면역접합체는 식 Ab-(L-D)p을 보유하며, 이때:
(a) Ab는 항체이며;
(b) L은 링커이며;
(c) D는 세포독성 물질이며; 그리고
(d) p는 1-8의 범위인, 면역접합체 - 청구항 11에 있어서, 이때 D는 식 A의 피롤로벤조디아제핀인, 면역접합체:
이때 파동선은 링커에 공유 부착 부위를 나타내며;
점선은 C1과 C2 또는 C2와 C3 사이에 이중 결합의 임의선택적 존재를 나타내며;;
R2는 H, OH, =O, =CH2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R 그리고 COR로부터 독립적으로 선택되며, 그리고 할로 또는 디할로로부터 임의선택적으로 추가 선택되며, 이때 RD는 R, CO2R, COR, CHO, CO2H, 그리고 할로로부터 독립적으로 선택되며;
R6과 R9는 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
R7은 H, R, OH, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn 그리고 할로로부터 독립적으로 선택되며;
Q는 O, S 그리고 NH로부터 독립적으로 선택되며;
R11은 H, 또는 R이거나 또는, Q가 O일 때, SO3M이며, 여기에서 M은 금속 양이온이고;
R 및 R'는 각각 임의선택적으로 치환된 C1-12 알킬, C3-20 헤테로시클일 그리고 C5-20 아릴 기로부터 독립적으로 선택되며, 그리고 임의선택적으로 기 NRR'와 관련하여, R 및 R'는 이들이 부착된 질소 원자와 함께 임의선택적으로 치환된 4-, 5-, 6- 또는 7-원(membered) 헤테로사이클 고리를 형성하고;
R12, R16, R19 및 R17은 R2, R6, R9 및 R7에 대해 차례로 정의된 바와 같고;
R″는 C3-12 알킬렌 기이며, 이의 쇄는 하나 또는 그 이상의 이형원자 및/또는 임의선택적으로 치환된 방향족 고리에 의해 차단될 수 있으며; 그리고
X와 X'는 O, S 그리고 N(H)로부터 독립적으로 선택된다. - 청구항 11 내지 15중 임의의 한 항에 있어서, 링커는 프로테아제에 절단가능한, 면역접합체.
- 청구항 16에 있어서, 링커는 val-cit 이펩티드 또는 Phe-Lys 이펩티드를 포함하는, 면역접합체.
- 청구항 11 내지 18중 임의의 한 항에 있어서, p는 1-3의 범위가 되는, 면역접합체.
- 청구항 23에 있어서, Ar1 및 Ar2는 각각 임의선택적으로 치환된 페닐, 퓨라닐, 티오페닐 그리고 피리딜로부터 독립적으로 선택되는, 면역접합체.
- 청구항 25에 있어서, RV1 및 RV2는 각각 H, 페닐, 그리고 4-플루오로페닐로부터 독립적으로 선택되는, 면역접합체.
- 청구항 27 또는 28에 있어서, 이때 상기 항체는 서열 번호: 7의 VH 서열과 서열 번호: 8의 VL 서열을 포함하는, 면역접합체.
- 청구항 29에 있어서, 이때 상기 항체는 서열 번호: 26의 중쇄와 서열 번호: 23의 경쇄를 포함하는, 면역접합체.
- 전술한 임의의 한 항에 있어서, 이때 상기 항체는 단클론 항체인, 면역접합체.
- 전술한 임의의 한 항에 있어서, 이때 상기 항체는 인간, 인간화된, 또는 키메라 항체인, 면역접합체.
- 전술한 임의의 한 항에 있어서, 이때 상기 항체는 CD22에 결합하는 항체 단편인, 면역접합체.
- 전술한 임의의 한 항에 있어서, 이때 상기 항체는 인간 CD22에 결합하는, 면역접합체.
- 청구항 34에 있어서, 이때 인간 CD22는 서열 번호: 28 또는 서열 번호: 29의 서열을 보유하는, 면역접합체.
- 전술한 임의의 한 항에 따른 면역접합체와 약학적으로 수용가능한 운반체를 포함하는 약학 제제.
- 청구항 36에 있어서, 추가 치료 물질를 더 포함하는, 약학 제제.
- CD22-양성 암을 가진 개체를 치료하는 방법에 있어서, 이 방법은 청구항 1 내지 35중 임의의 한 항에 따른 상기 면역접합체의 유효량을 개체에게 투여하는 것을 포함하는 방법.
- 청구항 38에 있어서, 이때 CD22-양성 암은 임파종, 비-호지킨 임파종 (NHL), 공격성 NHL, 재발된 공격성 NHL, 재발된 무기력한 NHL, 난치성 NHL, 난치성 무기력한 NHL, 만성 림프모구 백혈병 (CLL), 소림프구성 임파종, 백혈병, 털모양 세포백혈병 (HCL), 급성 림프구성 백혈병 (ALL), 버킷 임파종, 그리고 맨틀 세포 임파종으로부터 선택되는, 방법.
- 청구항 39에 있어서, 추가 치료 물질을 개체에게 투여하는 것을 더 포함하는, 방법.
- 청구항 40에 있어서, 이때 추가 치료물질은 CD79b에 결합하는 항체가 포함된, 방법.
- 청구항 41에 있어서, 이때 추가 치료물질은 세포독성 물질에 공유적으로 부착된 CD79b에 결합하는 항체가 포함된 면역접합체인, 방법.
- CD22-양성 세포의 증식을 억제하는 방법에 있어서, 이 방법은 세포 표면 상에 있는 CD22에게 면역접합체의 결합을 허용하는 조건하에서 청구항 1 내지 35중 임의의 한 항에 따른 면역접합체에 상기 세포를 노출시키는 것을 포함하며, 이로 인하여 상기 세포의 증식이 억제되는, 방법.
- 청구항 43에 있어서, 이때 세포는 신생물 B 세포인, 방법.
- 청구항 44에 있어서, 이때 세포는 임파종 세포인, 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261669272P | 2012-07-09 | 2012-07-09 | |
| US61/669,272 | 2012-07-09 | ||
| US201361777113P | 2013-03-12 | 2013-03-12 | |
| US61/777,113 | 2013-03-12 | ||
| PCT/US2013/049515 WO2014011518A1 (en) | 2012-07-09 | 2013-07-08 | Immunoconjugates comprising anti-cd22 antibodies |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150027829A true KR20150027829A (ko) | 2015-03-12 |
Family
ID=48803621
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR20157003046A Withdrawn KR20150027829A (ko) | 2012-07-09 | 2013-07-08 | 항-cd22 항체를 포함하는 면역접합체 |
Country Status (21)
| Country | Link |
|---|---|
| US (2) | US20140030279A1 (ko) |
| EP (1) | EP2869849A1 (ko) |
| JP (1) | JP2015527318A (ko) |
| KR (1) | KR20150027829A (ko) |
| CN (1) | CN104540524A (ko) |
| AR (1) | AR091703A1 (ko) |
| AU (1) | AU2013288929A1 (ko) |
| BR (1) | BR112015000441A2 (ko) |
| CA (1) | CA2873889A1 (ko) |
| CL (1) | CL2015000027A1 (ko) |
| CR (1) | CR20150048A (ko) |
| EA (1) | EA201590174A1 (ko) |
| HK (1) | HK1209043A1 (ko) |
| IL (1) | IL235985A0 (ko) |
| IN (1) | IN2014DN10510A (ko) |
| MX (1) | MX2015000357A (ko) |
| PE (1) | PE20150615A1 (ko) |
| PH (1) | PH12014502797A1 (ko) |
| SG (1) | SG11201500087VA (ko) |
| TW (1) | TW201406785A (ko) |
| WO (1) | WO2014011518A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20180054849A (ko) * | 2015-10-02 | 2018-05-24 | 제넨테크, 인크. | 피롤로벤조디아제핀 항체 약물 콘쥬게이트 및 이의 사용 방법 |
Families Citing this family (79)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0819095D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| JP5870400B2 (ja) | 2010-04-15 | 2016-03-01 | シアトル ジェネティクス,インコーポレーテッド | 標的化ピロロベンゾジアゼピンコンジュゲート |
| NZ602933A (en) | 2010-04-15 | 2014-09-26 | Seattle Genetics Inc | Pyrrolobenzodiazepines used to treat proliferative diseases |
| US9000130B2 (en) | 2010-06-08 | 2015-04-07 | Genentech, Inc. | Cysteine engineered antibodies and conjugates |
| WO2013041606A1 (en) | 2011-09-20 | 2013-03-28 | Spirogen Sàrl | Pyrrolobenzodiazepines as unsymmetrical dimeric pbd compounds for inclusion in targeted conjugates |
| EP2751111B1 (en) | 2011-10-14 | 2017-04-26 | MedImmune Limited | Asymmetrical bis-(5H-Pyrrolo[2,1-c][1,4]benzodiazepin-5-one) derivatives for the treatment of proliferative or autoimmune diseases |
| AU2012322613B2 (en) | 2011-10-14 | 2016-04-21 | Medimmune Limited | Pyrrolobenzodiazepines and targeted conjugates |
| WO2013053871A1 (en) | 2011-10-14 | 2013-04-18 | Spirogen Sàrl | Pyrrolobenzodiazepines |
| JP6393617B2 (ja) | 2011-10-14 | 2018-09-19 | シアトル ジェネティクス,インコーポレーテッド | ピロロベンゾジアゼピンおよび標的コンジュゲート |
| WO2014057118A1 (en) * | 2012-10-12 | 2014-04-17 | Adc Therapeutics Sarl | Pyrrolobenzodiazepine-anti-cd22 antibody conjugates |
| EP2906296B1 (en) | 2012-10-12 | 2018-03-21 | ADC Therapeutics SA | Pyrrolobenzodiazepine-antibody conjugates |
| US10695433B2 (en) | 2012-10-12 | 2020-06-30 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| KR101995621B1 (ko) | 2012-10-12 | 2019-07-03 | 에이디씨 테라퓨틱스 에스에이 | 피롤로벤조디아제핀-항-cd22 항체 컨주게이트 |
| JP5993093B2 (ja) | 2012-10-12 | 2016-09-14 | メドイミューン・リミテッドMedImmune Limited | ピロロベンゾジアゼピン類およびその複合体 |
| EP2906249B1 (en) | 2012-10-12 | 2018-06-27 | MedImmune Limited | Synthesis and intermediates of pyrrolobenzodiazepine derivatives for conjugation |
| JP6270859B2 (ja) | 2012-10-12 | 2018-01-31 | エイディーシー・セラピューティクス・エス・アー・エール・エルAdc Therapeutics Sarl | ピロロベンゾジアゼピン−抗体結合体 |
| DK2906248T3 (en) | 2012-10-12 | 2019-03-04 | Medimmune Ltd | Pyrrolobenzodiazepines and their conjugates |
| US9931414B2 (en) | 2012-10-12 | 2018-04-03 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| WO2014057114A1 (en) | 2012-10-12 | 2014-04-17 | Adc Therapeutics Sàrl | Pyrrolobenzodiazepine-anti-psma antibody conjugates |
| AU2013366493B2 (en) | 2012-12-21 | 2017-08-24 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof |
| HK1216176A1 (zh) | 2012-12-21 | 2016-10-21 | Medlmmune Limited | 用於治疗增殖性和自身免疫疾病的非对称吡咯并苯并二氮杂卓二聚物 |
| AU2014229529B2 (en) | 2013-03-13 | 2018-02-15 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof |
| WO2014159981A2 (en) | 2013-03-13 | 2014-10-02 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| US9790282B2 (en) | 2013-03-25 | 2017-10-17 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Anti-CD276 polypeptides, proteins, and chimeric antigen receptors |
| US10442836B2 (en) | 2013-08-12 | 2019-10-15 | Genentech, Inc. | 1-(chloromethyl)-2,3-dihydro-1H-benzo[E]indole dimer antibody-drug conjugate compounds, and methods of use and treatment |
| GB201317981D0 (en) | 2013-10-11 | 2013-11-27 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| US10010624B2 (en) | 2013-10-11 | 2018-07-03 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| GB201317982D0 (en) | 2013-10-11 | 2013-11-27 | Spirogen Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| US9956299B2 (en) | 2013-10-11 | 2018-05-01 | Medimmune Limited | Pyrrolobenzodiazepine—antibody conjugates |
| EP3054985B1 (en) | 2013-10-11 | 2018-12-26 | Medimmune Limited | Pyrrolobenzodiazepine-antibody conjugates |
| BR112016013258A2 (pt) | 2013-12-16 | 2018-01-16 | Genentech Inc | composto conjugado anticorpo-droga, composição farmacêutica, método para tratar câncer e kit |
| GB201409558D0 (en) | 2014-05-29 | 2014-07-16 | Ucb Biopharma Sprl | Method |
| GB201409653D0 (en) * | 2014-05-30 | 2014-07-16 | Stell Dr Anneliese | Pyrrolobenzodiazepine therapeutic agents |
| GB201412659D0 (en) | 2014-07-16 | 2014-08-27 | Ucb Biopharma Sprl | Molecules |
| GB201412658D0 (en) | 2014-07-16 | 2014-08-27 | Ucb Biopharma Sprl | Molecules |
| CN106687141A (zh) | 2014-09-10 | 2017-05-17 | 麦迪穆有限责任公司 | 吡咯并苯并二氮杂卓及其缀合物 |
| MX2017003123A (es) | 2014-09-12 | 2017-05-12 | Genentech Inc | Anticuerpos y conjugados modificados geneticamente con cisteina. |
| PE20170935A1 (es) | 2014-09-12 | 2017-07-13 | Genentech Inc | Anticuerpos anti-her2 e inmunoconjugados |
| GB201416112D0 (en) | 2014-09-12 | 2014-10-29 | Medimmune Ltd | Pyrrolobenzodiazepines and conjugates thereof |
| SG11201702079UA (en) * | 2014-09-17 | 2017-04-27 | Genentech Inc | Pyrrolobenzodiazepines and antibody disulfide conjugates thereof |
| EP3193933B1 (en) | 2014-09-17 | 2021-04-28 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Anti-cd276 antibodies (b7h3) |
| BR112017011111A2 (pt) | 2014-11-25 | 2017-12-26 | Adc Therapeutics Sa | conjugados de pirrolobenzodiazepina-anticorpo |
| GB201506411D0 (en) | 2015-04-15 | 2015-05-27 | Bergenbio As | Humanized anti-axl antibodies |
| GB201506402D0 (en) | 2015-04-15 | 2015-05-27 | Berkel Patricius H C Van And Howard Philip W | Site-specific antibody-drug conjugates |
| GB201601075D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibodies molecules |
| GB201601073D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibodies |
| GB201601077D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibody molecule |
| MA43354A (fr) | 2015-10-16 | 2018-08-22 | Genentech Inc | Conjugués médicamenteux à pont disulfure encombré |
| CN105288639A (zh) * | 2015-11-23 | 2016-02-03 | 中国药科大学 | 一种载阿霉素的主动靶向白蛋白纳米载体的制备及其应用 |
| GB201521391D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| GB201521393D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| GB201521389D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Method |
| GB201521382D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| GB201521383D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl And Ucb Celltech | Method |
| GB201601431D0 (en) | 2016-01-26 | 2016-03-09 | Medimmune Ltd | Pyrrolobenzodiazepines |
| GB201602359D0 (en) * | 2016-02-10 | 2016-03-23 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| GB201602356D0 (en) | 2016-02-10 | 2016-03-23 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| GB201607478D0 (en) | 2016-04-29 | 2016-06-15 | Medimmune Ltd | Pyrrolobenzodiazepine Conjugates |
| WO2017201132A2 (en) | 2016-05-18 | 2017-11-23 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepines and conjugates thereof |
| WO2017223275A1 (en) | 2016-06-24 | 2017-12-28 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepines and conjugates thereof |
| JP7050770B2 (ja) * | 2016-10-05 | 2022-04-08 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | 抗体薬物コンジュゲートの調製方法 |
| GB201617466D0 (en) | 2016-10-14 | 2016-11-30 | Medimmune Ltd | Pyrrolobenzodiazepine conjugates |
| HUE054689T2 (hu) | 2017-02-08 | 2021-09-28 | Adc Therapeutics Sa | Pirrolobenzodiazepin-antitest konjugátumok |
| GB201702031D0 (en) | 2017-02-08 | 2017-03-22 | Medlmmune Ltd | Pyrrolobenzodiazepine-antibody conjugates |
| SI3612537T1 (sl) | 2017-04-18 | 2022-10-28 | Medimmune Limited | Konjugati pirolobenzodiazepina |
| EP3612234B1 (en) | 2017-04-20 | 2024-03-13 | ADC Therapeutics SA | Combination therapy with an anti-axl antibody-drug conjugate |
| CA3064804A1 (en) | 2017-06-14 | 2018-12-20 | Adc Therapeutics Sa | Dosage regimes for the administration of an anti-cd19 adc |
| SG11202000358YA (en) | 2017-08-18 | 2020-02-27 | Medimmune Ltd | Pyrrolobenzodiazepine conjugates |
| TWI885539B (zh) | 2017-09-29 | 2025-06-01 | 日商第一三共股份有限公司 | 抗體-吡咯并苯二氮呯衍生物複合體 |
| EP3717021A1 (en) | 2017-11-27 | 2020-10-07 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepine antibody conjugates |
| EP3727463A1 (en) | 2017-12-21 | 2020-10-28 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepine antibody conjugates |
| GB201721802D0 (en) * | 2017-12-22 | 2018-02-07 | Almac Discovery Ltd | Ror1-specific antigen binding molecules |
| GB201803342D0 (en) | 2018-03-01 | 2018-04-18 | Medimmune Ltd | Methods |
| GB201806022D0 (en) | 2018-04-12 | 2018-05-30 | Medimmune Ltd | Pyrrolobenzodiazepines and conjugates thereof |
| JP2021532116A (ja) * | 2018-07-23 | 2021-11-25 | マジェンタ セラピューティクス インコーポレイテッドMagenta Therapeutics, Inc. | 同種異系の細胞療法における抗−cd5抗体薬物コンジュゲート(adc)の使用 |
| KR20210081350A (ko) * | 2018-10-19 | 2021-07-01 | 메드임뮨 리미티드 | 피롤로벤조디아제핀 컨쥬게이트 |
| EP3670530A1 (en) | 2018-12-18 | 2020-06-24 | Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft | Cd22-specific t cell receptors and adoptive t cell therapy for treatment of b cell malignancies |
| MX2021010477A (es) | 2019-03-15 | 2021-10-01 | Medimmune Ltd | Dimeros de azetidobenzodiazepina y conjugados que los comprenden para uso en el tratamiento de cancer. |
| WO2021021846A1 (en) * | 2019-07-29 | 2021-02-04 | The Children's Hospital Of Philadelphia | Antibodies for the diagnosis and treatment of b-cell acute lymphoblastic leukemia |
Family Cites Families (107)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4737456A (en) | 1985-05-09 | 1988-04-12 | Syntex (U.S.A.) Inc. | Reducing interference in ligand-receptor binding assays |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| US6548640B1 (en) | 1986-03-27 | 2003-04-15 | Btg International Limited | Altered antibodies |
| IL85035A0 (en) | 1987-01-08 | 1988-06-30 | Int Genetic Eng | Polynucleotide molecule,a chimeric antibody with specificity for human b cell surface antigen,a process for the preparation and methods utilizing the same |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| WO1990005144A1 (en) | 1988-11-11 | 1990-05-17 | Medical Research Council | Single domain ligands, receptors comprising said ligands, methods for their production, and use of said ligands and receptors |
| DE3920358A1 (de) | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5959177A (en) | 1989-10-27 | 1999-09-28 | The Scripps Research Institute | Transgenic plants expressing assembled secretory antibodies |
| US6075181A (en) | 1990-01-12 | 2000-06-13 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US6150584A (en) | 1990-01-12 | 2000-11-21 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US5770429A (en) | 1990-08-29 | 1998-06-23 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| DE69129154T2 (de) | 1990-12-03 | 1998-08-20 | Genentech, Inc., South San Francisco, Calif. | Verfahren zur anreicherung von proteinvarianten mit geänderten bindungseigenschaften |
| US5571894A (en) | 1991-02-05 | 1996-11-05 | Ciba-Geigy Corporation | Recombinant antibodies specific for a growth factor receptor |
| JP4124480B2 (ja) | 1991-06-14 | 2008-07-23 | ジェネンテック・インコーポレーテッド | 免疫グロブリン変異体 |
| GB9114948D0 (en) | 1991-07-11 | 1991-08-28 | Pfizer Ltd | Process for preparing sertraline intermediates |
| WO1993006217A1 (en) | 1991-09-19 | 1993-04-01 | Genentech, Inc. | EXPRESSION IN E. COLI OF ANTIBODY FRAGMENTS HAVING AT LEAST A CYSTEINE PRESENT AS A FREE THIOL, USE FOR THE PRODUCTION OF BIFUNCTIONAL F(ab')2 ANTIBODIES |
| US5362852A (en) | 1991-09-27 | 1994-11-08 | Pfizer Inc. | Modified peptide derivatives conjugated at 2-hydroxyethylamine moieties |
| FI941572L (fi) | 1991-10-07 | 1994-05-27 | Oncologix Inc | Anti-erbB-2-monoklonaalisten vasta-aineiden yhdistelmä ja käyttömenetelmä |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| ATE503496T1 (de) | 1992-02-06 | 2011-04-15 | Novartis Vaccines & Diagnostic | Biosynthetisches bindeprotein für tumormarker |
| ATE139900T1 (de) | 1992-11-13 | 1996-07-15 | Idec Pharma Corp | Therapeutische verwendung von chimerischen und markierten antikörper gegen menschlichen b lymphozyt beschränkter differenzierung antigen für die behandlung von b-zell-lymphoma |
| US6214345B1 (en) | 1993-05-14 | 2001-04-10 | Bristol-Myers Squibb Co. | Lysosomal enzyme-cleavable antitumor drug conjugates |
| CA2163345A1 (en) | 1993-06-16 | 1994-12-22 | Susan Adrienne Morgan | Antibodies |
| US5789199A (en) | 1994-11-03 | 1998-08-04 | Genentech, Inc. | Process for bacterial production of polypeptides |
| US5840523A (en) | 1995-03-01 | 1998-11-24 | Genetech, Inc. | Methods and compositions for secretion of heterologous polypeptides |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US6267958B1 (en) | 1995-07-27 | 2001-07-31 | Genentech, Inc. | Protein formulation |
| GB9603256D0 (en) | 1996-02-16 | 1996-04-17 | Wellcome Found | Antibodies |
| US6171586B1 (en) | 1997-06-13 | 2001-01-09 | Genentech, Inc. | Antibody formulation |
| ES2244066T3 (es) | 1997-06-24 | 2005-12-01 | Genentech, Inc. | Procedimiento y composiciones de glicoproteinas galactosiladas. |
| US6040498A (en) | 1998-08-11 | 2000-03-21 | North Caroline State University | Genetically engineered duckweed |
| US6602677B1 (en) | 1997-09-19 | 2003-08-05 | Promega Corporation | Thermostable luciferases and methods of production |
| WO1999022764A1 (en) | 1997-10-31 | 1999-05-14 | Genentech, Inc. | Methods and compositions comprising glycoprotein glycoforms |
| US6610833B1 (en) | 1997-11-24 | 2003-08-26 | The Institute For Human Genetics And Biochemistry | Monoclonal human natural antibodies |
| WO1999029888A1 (en) | 1997-12-05 | 1999-06-17 | The Scripps Research Institute | Humanization of murine antibody |
| US6194551B1 (en) | 1998-04-02 | 2001-02-27 | Genentech, Inc. | Polypeptide variants |
| ATE375365T1 (de) | 1998-04-02 | 2007-10-15 | Genentech Inc | Antikörper varianten und fragmente davon |
| PT1071700E (pt) | 1998-04-20 | 2010-04-23 | Glycart Biotechnology Ag | Modificação por glicosilação de anticorpos para melhorar a citotoxicidade celular dependente de anticorpos |
| DE69907977T2 (de) | 1998-08-27 | 2004-07-22 | Spirogen Ltd., Ryde | Pyrrolobenzodiazepine |
| US6737056B1 (en) | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| EP1141024B1 (en) | 1999-01-15 | 2018-08-08 | Genentech, Inc. | POLYPEPTIDE COMPRISING A VARIANT HUMAN IgG1 Fc REGION |
| ES2601882T5 (es) | 1999-04-09 | 2021-06-07 | Kyowa Kirin Co Ltd | Procedimiento para controlar la actividad de una molécula inmunofuncional |
| KR100797667B1 (ko) | 1999-10-04 | 2008-01-23 | 메디카고 인코포레이티드 | 외래 유전자의 전사를 조절하는 방법 |
| US7125978B1 (en) | 1999-10-04 | 2006-10-24 | Medicago Inc. | Promoter for regulating expression of foreign genes |
| CA2388245C (en) | 1999-10-19 | 2012-01-10 | Tatsuya Ogawa | The use of serum-free adapted rat cells for producing heterologous polypeptides |
| AU784983B2 (en) | 1999-12-15 | 2006-08-17 | Genentech Inc. | Shotgun scanning, a combinatorial method for mapping functional protein epitopes |
| DK2857516T3 (en) | 2000-04-11 | 2017-08-07 | Genentech Inc | Multivalent antibodies and uses thereof |
| HU231090B1 (hu) | 2000-10-06 | 2020-07-28 | Kyowa Kirin Co., Ltd. | Antitest-kompozíciót termelő sejt |
| US6946292B2 (en) | 2000-10-06 | 2005-09-20 | Kyowa Hakko Kogyo Co., Ltd. | Cells producing antibody compositions with increased antibody dependent cytotoxic activity |
| US7064191B2 (en) | 2000-10-06 | 2006-06-20 | Kyowa Hakko Kogyo Co., Ltd. | Process for purifying antibody |
| US6596541B2 (en) | 2000-10-31 | 2003-07-22 | Regeneron Pharmaceuticals, Inc. | Methods of modifying eukaryotic cells |
| EP1916303B1 (en) | 2000-11-30 | 2013-02-27 | Medarex, Inc. | Nucleic acids encoding rearranged human immunoglobulin sequences from transgenic transchromosomal mice |
| US6884869B2 (en) | 2001-04-30 | 2005-04-26 | Seattle Genetics, Inc. | Pentapeptide compounds and uses related thereto |
| EP1423510A4 (en) | 2001-08-03 | 2005-06-01 | Glycart Biotechnology Ag | ANTIBODY GLYCOSYLATION VARIANTS WITH INCREASED ANTIBODY-DEPENDENT CELLULAR CYTOTOXICITY |
| US7091186B2 (en) | 2001-09-24 | 2006-08-15 | Seattle Genetics, Inc. | p-Amidobenzylethers in drug delivery agents |
| WO2003026577A2 (en) | 2001-09-24 | 2003-04-03 | Seattle Genetics, Inc. | P-amidobenzylethers in drug delivery agents |
| HUP0600342A3 (en) | 2001-10-25 | 2011-03-28 | Genentech Inc | Glycoprotein compositions |
| US20050123536A1 (en) | 2001-11-20 | 2005-06-09 | Che-Leung Law | Treatment of immunological disorders using anti-dc30 antibodies |
| US20040093621A1 (en) | 2001-12-25 | 2004-05-13 | Kyowa Hakko Kogyo Co., Ltd | Antibody composition which specifically binds to CD20 |
| CN1646161A (zh) * | 2002-02-21 | 2005-07-27 | 杜克大学 | 自身免疫疾病的药剂和治疗方法 |
| WO2003084569A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Drug containing antibody composition |
| CA2481837A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Production process for antibody composition |
| CA2481656A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Cells in which activity of the protein involved in transportation of gdp-fucose is reduced or lost |
| CN102911987B (zh) | 2002-04-09 | 2015-09-30 | 协和发酵麒麟株式会社 | 基因组被修饰的细胞 |
| US20050031613A1 (en) | 2002-04-09 | 2005-02-10 | Kazuyasu Nakamura | Therapeutic agent for patients having human FcgammaRIIIa |
| WO2003085119A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | METHOD OF ENHANCING ACTIVITY OF ANTIBODY COMPOSITION OF BINDING TO FcϜ RECEPTOR IIIa |
| CA2488441C (en) | 2002-06-03 | 2015-01-27 | Genentech, Inc. | Synthetic antibody phage libraries |
| WO2004032828A2 (en) | 2002-07-31 | 2004-04-22 | Seattle Genetics, Inc. | Anti-cd20 antibody-drug conjugates for the treatment of cancer and immune disorders |
| US7361740B2 (en) | 2002-10-15 | 2008-04-22 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| DK2289936T3 (en) | 2002-12-16 | 2017-07-31 | Genentech Inc | IMMUNGLOBULIN VARIATIONS AND APPLICATIONS THEREOF |
| EP1585767A2 (en) | 2003-01-16 | 2005-10-19 | Genentech, Inc. | Synthetic antibody phage libraries |
| US20060104968A1 (en) | 2003-03-05 | 2006-05-18 | Halozyme, Inc. | Soluble glycosaminoglycanases and methods of preparing and using soluble glycosaminogly ycanases |
| US7871607B2 (en) | 2003-03-05 | 2011-01-18 | Halozyme, Inc. | Soluble glycosaminoglycanases and methods of preparing and using soluble glycosaminoglycanases |
| DE60326060D1 (de) | 2003-03-31 | 2009-03-19 | Council Scient Ind Res | Nichtvernetzende pyrroloä2,1-cüä1,4übenzodiazepine als potentielle antitumor-agentien und ihre herstellung |
| WO2005035586A1 (ja) | 2003-10-08 | 2005-04-21 | Kyowa Hakko Kogyo Co., Ltd. | 融合蛋白質組成物 |
| WO2005035778A1 (ja) | 2003-10-09 | 2005-04-21 | Kyowa Hakko Kogyo Co., Ltd. | α1,6-フコシルトランスフェラーゼの機能を抑制するRNAを用いた抗体組成物の製造法 |
| ATE516288T1 (de) | 2003-10-22 | 2011-07-15 | Us Gov Health & Human Serv | Pyrrolobenzodiazepinderivate, zusammensetzungen, die diese enthalten, und damit in zusammenhang stehende verfahren |
| DK2380910T3 (en) | 2003-11-05 | 2015-10-19 | Roche Glycart Ag | Antigen binding molecules with increased Fc receptor binding affinity and effector function |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| WO2005053742A1 (ja) | 2003-12-04 | 2005-06-16 | Kyowa Hakko Kogyo Co., Ltd. | 抗体組成物を含有する医薬 |
| CA2556752C (en) | 2004-02-23 | 2016-02-02 | Genentech, Inc. | Heterocyclic self-immolative linkers and conjugates |
| GB0404577D0 (en) | 2004-03-01 | 2004-04-07 | Spirogen Ltd | Pyrrolobenzodiazepines |
| US7528126B2 (en) | 2004-03-09 | 2009-05-05 | Spirogen Limited | Pyrrolobenzodiazepines |
| MXPA06011199A (es) | 2004-03-31 | 2007-04-16 | Genentech Inc | Anticuerpos anti-tgf-beta humanizados. |
| US7785903B2 (en) | 2004-04-09 | 2010-08-31 | Genentech, Inc. | Variable domain library and uses |
| PL1737891T3 (pl) | 2004-04-13 | 2013-08-30 | Hoffmann La Roche | Przeciwciała przeciw selektynie p |
| TWI380996B (zh) | 2004-09-17 | 2013-01-01 | Hoffmann La Roche | 抗ox40l抗體 |
| NZ553500A (en) | 2004-09-23 | 2009-11-27 | Genentech Inc Genentech Inc | Cysteine engineered antibodies and conjugates withCysteine engineered antibodies and conjugates with a free cysteine amino acid in the heavy chain a free cysteine amino acid in the heavy chain |
| JO3000B1 (ar) | 2004-10-20 | 2016-09-05 | Genentech Inc | مركبات أجسام مضادة . |
| EP1957531B1 (en) | 2005-11-07 | 2016-04-13 | Genentech, Inc. | Binding polypeptides with diversified and consensus vh/vl hypervariable sequences |
| US20070237764A1 (en) | 2005-12-02 | 2007-10-11 | Genentech, Inc. | Binding polypeptides with restricted diversity sequences |
| EP1813614B1 (en) | 2006-01-25 | 2011-10-05 | Sanofi | Cytotoxic agents comprising new tomaymycin derivatives |
| AR060871A1 (es) | 2006-05-09 | 2008-07-16 | Genentech Inc | Union de polipeptidos con supercontigos optimizados |
| RS54163B1 (sr) * | 2006-05-30 | 2015-12-31 | Genentech Inc. | Anti-cd22 antitela, njihovi imunokonjugati i njihova upotreba |
| UA95958C2 (en) * | 2006-05-30 | 2011-09-26 | Дженентек, Инк. | Antibody that binds to cd22, immunoconjugates and uses therefor |
| WO2008010101A2 (en) | 2006-07-18 | 2008-01-24 | Sanofi-Aventis | Antagonist antibody against epha2 for the treatment of cancer |
| WO2008027236A2 (en) | 2006-08-30 | 2008-03-06 | Genentech, Inc. | Multispecific antibodies |
| EP1914242A1 (en) | 2006-10-19 | 2008-04-23 | Sanofi-Aventis | Novel anti-CD38 antibodies for the treatment of cancer |
| US20080226635A1 (en) | 2006-12-22 | 2008-09-18 | Hans Koll | Antibodies against insulin-like growth factor I receptor and uses thereof |
| CN100592373C (zh) | 2007-05-25 | 2010-02-24 | 群康科技(深圳)有限公司 | 液晶显示面板驱动装置及其驱动方法 |
| DK2176296T3 (da) | 2007-07-16 | 2012-05-21 | Genentech Inc | Anti-CD79B-antistoffer og immunkonjugater og anvendelsesfremgangsmåder. |
| PT2019104E (pt) | 2007-07-19 | 2013-12-03 | Sanofi Sa | Agentes citotóxicos compreendendo novos derivados de tomaimicina e sua utilização terapêutica |
| SI2235064T1 (sl) | 2008-01-07 | 2016-04-29 | Amgen Inc. | Metoda za izdelavo heterodimernih molekul - protitelesa fc z uporabo elektrostatičnih usmerjevalnih učinkov |
| MA34277B1 (fr) * | 2010-04-15 | 2013-06-01 | Spirogen Developments Sarl | Pyrrolobenzodiazépines et conjugués de celles-ci |
-
2013
- 2013-07-08 KR KR20157003046A patent/KR20150027829A/ko not_active Withdrawn
- 2013-07-08 HK HK15109754.0A patent/HK1209043A1/xx unknown
- 2013-07-08 WO PCT/US2013/049515 patent/WO2014011518A1/en not_active Ceased
- 2013-07-08 PE PE2015000032A patent/PE20150615A1/es not_active Application Discontinuation
- 2013-07-08 EP EP13739331.0A patent/EP2869849A1/en not_active Withdrawn
- 2013-07-08 AU AU2013288929A patent/AU2013288929A1/en not_active Abandoned
- 2013-07-08 SG SG11201500087VA patent/SG11201500087VA/en unknown
- 2013-07-08 AR ARP130102425 patent/AR091703A1/es unknown
- 2013-07-08 US US13/936,279 patent/US20140030279A1/en not_active Abandoned
- 2013-07-08 BR BR112015000441A patent/BR112015000441A2/pt not_active IP Right Cessation
- 2013-07-08 MX MX2015000357A patent/MX2015000357A/es unknown
- 2013-07-08 JP JP2015521674A patent/JP2015527318A/ja active Pending
- 2013-07-08 IN IN10510DEN2014 patent/IN2014DN10510A/en unknown
- 2013-07-08 CN CN201380035861.7A patent/CN104540524A/zh active Pending
- 2013-07-08 CA CA2873889A patent/CA2873889A1/en not_active Abandoned
- 2013-07-08 TW TW102124395A patent/TW201406785A/zh unknown
- 2013-07-08 EA EA201590174A patent/EA201590174A1/ru unknown
-
2014
- 2014-11-30 IL IL235985A patent/IL235985A0/en unknown
- 2014-12-15 PH PH12014502797A patent/PH12014502797A1/en unknown
-
2015
- 2015-01-07 CL CL2015000027A patent/CL2015000027A1/es unknown
- 2015-02-04 CR CR20150048A patent/CR20150048A/es not_active Application Discontinuation
-
2017
- 2017-04-26 US US15/497,656 patent/US20170290920A1/en not_active Abandoned
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20180054849A (ko) * | 2015-10-02 | 2018-05-24 | 제넨테크, 인크. | 피롤로벤조디아제핀 항체 약물 콘쥬게이트 및 이의 사용 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20140030279A1 (en) | 2014-01-30 |
| CL2015000027A1 (es) | 2015-07-10 |
| JP2015527318A (ja) | 2015-09-17 |
| EP2869849A1 (en) | 2015-05-13 |
| HK1209043A1 (en) | 2016-03-24 |
| CN104540524A (zh) | 2015-04-22 |
| MX2015000357A (es) | 2015-05-12 |
| PE20150615A1 (es) | 2015-05-28 |
| CA2873889A1 (en) | 2014-01-16 |
| WO2014011518A1 (en) | 2014-01-16 |
| BR112015000441A2 (pt) | 2017-12-19 |
| PH12014502797A1 (en) | 2015-02-09 |
| AU2013288929A1 (en) | 2014-12-04 |
| TW201406785A (zh) | 2014-02-16 |
| US20170290920A1 (en) | 2017-10-12 |
| SG11201500087VA (en) | 2015-02-27 |
| EA201590174A1 (ru) | 2015-09-30 |
| IN2014DN10510A (ko) | 2015-08-21 |
| CR20150048A (es) | 2015-04-14 |
| AR091703A1 (es) | 2015-02-25 |
| IL235985A0 (en) | 2015-01-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20150027829A (ko) | 항-cd22 항체를 포함하는 면역접합체 | |
| EP2869850B1 (en) | Immunoconjugates comprising anti-cd79b antibodies | |
| JP6242865B2 (ja) | 抗pmel17抗体および免疫複合体 | |
| JP6404811B2 (ja) | 抗lgr5抗体および免疫複合体 | |
| JP6297550B2 (ja) | 抗cd79b抗体を含む免疫複合体 | |
| US9464141B2 (en) | Anti-ETBR antibodies and immunoconjugates | |
| JP6297549B2 (ja) | 抗cd22抗体および免疫複合体 | |
| RU2727663C2 (ru) | Иммуноконъюгаты, содержащие антитела против her2 и пирролбензодиазепины | |
| KR20170057280A (ko) | 항-her2 항체 및 면역콘주게이트 | |
| US10246515B2 (en) | Methods of treating hedgehog-related diseases with an anti-LGR5 antibody | |
| JP2015529656A (ja) | 抗etbr抗体および免疫複合体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20150204 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PN2301 | Change of applicant |
Patent event date: 20161214 Comment text: Notification of Change of Applicant Patent event code: PN23011R01D |
|
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |