JP7307231B2 - 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) - Google Patents
酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) Download PDFInfo
- Publication number
- JP7307231B2 JP7307231B2 JP2022072343A JP2022072343A JP7307231B2 JP 7307231 B2 JP7307231 B2 JP 7307231B2 JP 2022072343 A JP2022072343 A JP 2022072343A JP 2022072343 A JP2022072343 A JP 2022072343A JP 7307231 B2 JP7307231 B2 JP 7307231B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- antibodies
- tpp
- seq
- antigen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6855—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from breast cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
X1はNを表し、
X2はNを表し、
X3はCを表す;
または
X1はNを表し、
X2はCを表し、
X3はNを表す;
または
X1はCHもしくはCFを表し、
X2はCを表し、
X3はNを表す;
または
X1はNHを表し、
X2はCを表し、
X3はCを表す;
または
X1はCHを表し、
X2はNを表し、
X3はCを表し、
R1は水素またはメチルを表し、
R2はメチル、エチル、-CH2-CH(CH3)2、-CH2-C(=O)OHまたはイソプロピルを表し、
R3はメチル、エチル、-CH2-CH(CH3)2または-CH2-C(=O)-NH2を表し、
Mは
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH、
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH、
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W、
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH、
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH、
#-C(=O)-CH2-W、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)2~8-C(=O)-###、
#-C(=O)-(CH2)3-C(=O)-###、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##または
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)1~8-(CH2)2-NH-C(=O)-CH2-##
基を表し、
Wは
nは1~50の数を表し、
AKは結合剤またはその誘導体、好ましくは抗体または抗原結合フラグメントを表し、
#は化合物との結合を表し、
##は結合剤のシステイン側鎖の硫黄原子との結合を表し、
###は結合剤のリジン側鎖の窒素原子との結合を表す)
ならびにその塩、溶媒和物および溶媒和物の塩が、公知のコンジュゲートと比較して優れた特性を有することが分かった。
X2がCを表し、
X3がNを表し、
R1が水素またはメチルを表し、
R2がメチル、-CH2-CH(CH3)2、-CH2-C(=O)OHまたはイソプロピルを表し、
R3がメチル、-CH2-CH(CH3)2または-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH、
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH、
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W、
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH、
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH、
#-C(=O)-CH2-W、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###、
#-C(=O)-(CH2)3-C(=O)-###、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W、
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##または
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)4-(CH2)2-NH-C(=O)-CH2-##
基を表し、
Wが
nが1~50の数を表し、
AKが結合剤またはその誘導体、好ましくは抗体または抗原結合フラグメントを表し、
#が化合物との結合を表し、
##が結合剤のシステイン側鎖の硫黄原子との結合を表し、
###が結合剤のリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が好ましい。
R2がメチルまたはイソプロピルを表し、
R3がメチルまたは-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###
基を表し、
nが1~50の数を表し、
AKが結合剤またはその誘導体、好ましくは抗体または抗原結合フラグメントを表し、
#が化合物との結合を表し、
###が結合剤のリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が特に好ましい。
R2がメチルを表し、
R3が-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###
基を表し、
nが1~50の数を表し、
AKが結合剤またはその誘導体、好ましくは抗体または抗原結合フラグメントを表し、
#が化合物との結合を表し、
###が結合剤のリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が極めて特に好ましい。
R2がメチルを表し、
R3が-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###
基を表し、
nが1~20の数を表し、
AKが結合剤またはその誘導体、好ましくは抗体または抗原結合フラグメントを表し、
#が化合物との結合を表し、
###が結合剤のリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が特別に好ましい。
R2がメチルを表し、
R3が-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###
基を表し、
nが1~20の数を表し、
AKが抗CD123抗体、抗CXCR5抗体、抗B7H3抗体、抗TWEAKR抗体、抗Her2抗体もしくは抗EGFR抗体を表す、またはこれらの抗原結合抗体フラグメントを表し、
#が化合物との結合を表し、
###が抗体(AK)またはその抗原結合抗体フラグメントのリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が選択される。
R2がメチルを表し、
R3が-CH2-C(=O)-NH2を表し、
Mが
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###
基を表し、
nが1~20の数を表し、
AKが、TPP-9476、TPP-8988、TPP-8987およびTPP-6013からなる群から選択される抗CD123抗体を表す、TPP-9574およびTPP-9580からなる群から選択される抗CXCR5抗体を表す、抗B7H3抗体TPP-8382を表す、TPP-7006およびTPP-7007からなる群から選択される抗TWEAKR抗体を表す、抗Her2抗体TPP-1015を表す、もしくは抗EGFR抗体TPP-981を表す、またはこれらの抗原結合抗体フラグメントを表し、
#が化合物との結合を表し、
###が抗体(AK)またはその抗原結合抗体フラグメントのリジン側鎖の窒素原子との結合を表す、
式(I)の結合剤-薬物コンジュゲートならびにその塩、溶媒和物およびこれらの溶媒和物の塩が選択される。
本発明によると、AK(AK1、AK2)が結合剤またはその誘導体(好ましくは抗体)を表し、nが1~20、好ましくは1~8、より好ましくは4~8の数を表す、以下のKSP阻害剤コンジュゲートが特に好ましい。AK1は、好ましくはシステイン残基を介してKSP阻害剤と結合した抗体を表し;AK2は、好ましくはリジン残基を介してKSP阻害剤と結合した抗体を表す。ここで使用される結合剤または抗体は、好ましくは本明細書で好ましいとして記載される結合剤および抗体である。
本発明によるコンジュゲートは、最初にその低分子量KSP阻害剤にリンカーを提供することによって調製される。次いで、このようにして得られた中間体を結合剤(好ましくは抗体)と反応させる。
最も広い意味では、「結合剤」という用語は、結合剤-薬物コンジュゲートによって対処されるべき一定の標的細胞集団に存在する標的分子に結合する分子を意味すると理解される。結合剤という用語は、その最も広い意味で理解されるべきであり、例えばレクチン、一定の糖鎖に結合することができるタンパク質、またはリン脂質結合タンパク質も含む。このような結合剤には、例えば、高分子量タンパク質(結合タンパク質)、ポリペプチドまたはペプチド(結合ペプチド)、非ペプチド(例えば、アプタマー(米国特許第5270163号明細書)、Keefe AD.ら、Nat.Rev.Drug Discov.2010;9:537~550による概説)またはビタミン)、および他の全ての細胞結合分子または物質が含まれる。結合タンパク質は、例えば、抗体および抗体フラグメントまたは抗体模倣物、例えば、アフィボディ、アドネクチン、アンチカリン(登録商標)、DARPins、アビマー、ナノボディである(Gebauer M.ら、Curr.Opinion in Chem.Biol.2009;13:245~255;Nuttall S.D.ら、Curr.Opinion in Pharmacology 2008;8:608~617による概説)。結合ペプチドは、例えば、リガンド/受容体ペアのリガンド、例えばリガンド/受容体ペアVEGF/KDRのVEGF、例えばリガンド/受容体ペアトランスフェリン/トランスフェリン受容体のトランスフェリン、またはサイトカイン/サイトカイン受容体、例えばリガンド/受容体ペアTNFα/TNFα受容体のTNFαである。
結合剤、例えば抗体またはその抗原結合断片が向けられる標的分子は、好ましくはがん標的分子である。「がん標的分子」という用語は、同じ組織型の非がん細胞よりも1つまたは複数のがん細胞種上に豊富に存在する標的分子を記載する。好ましくは、がん標的分子は、同じ組織型の非がん細胞と比較して1つまたは複数のがん細胞種上に選択的に存在し、選択的にとは同じ組織型の非がん細胞と比較してがん細胞上に少なくとも2倍豊富であることを記載する(「選択的がん標的分子」)。がん標的分子の使用により、本発明によるコンジュゲートを使用したがん細胞の選択的治療が可能になる。
(1)EGFR(EGF受容体、NCBI参照配列NP_005219.2、NCBI遺伝子ID:1956)
(2)メソテリン(SwissProt参照Q13421-3)、メソテリンはアミノ酸296~598によってコードされる。アミノ酸37~286は巨核球増強因子をコードする。メソテリンは、GPIアンカーによって細胞膜に固定されており、細胞外に局在化している。
(3)カルボアンヒドラーゼIX(CA9、SwissProt参照Q16790)、NCBI遺伝子ID:768)
(4)C4.4a(NCBI参照配列NP_055215.2;同義語LYPD3、NCBI遺伝子ID:27076)
(5)CD52(NCBI参照配列NP_001794.2)
(6)Her2(ERBB2;NCBI参照配列NP_004439.2;NCBI遺伝子ID:2064)
(7)CD20(NCBI参照配列NP_068769.2)
(8)リンパ球活性化抗原CD30(SwissProt ID P28908)
(9)リンパ球接着分子CD22(SwissProt ID P20273;NCBI遺伝子ID:933)
(10)骨髄細胞表面抗原CD33(SwissProt ID P20138;NCBI遺伝子ID:945)
(11)膜貫通型糖タンパク質NMB(GPNMB、SwissProt ID Q14956、NCBI遺伝子ID:10457)
(12)接着分子CD56(SwissProt ID P13591)
(13)表面分子CD70(SwissProt ID P32970、NCBI遺伝子ID:970)。
(14)表面分子CD74(SwissProt ID P04233、NCBI遺伝子ID:972)。
(15)Bリンパ球抗原CD19(SwissProt ID P15391、NCBI遺伝子ID:930)
(16)表面タンパク質ムチン-1(MUC1、SwissProt ID P15941、NCBI遺伝子ID:4582)。
(17)表面タンパク質CD138(SwissProt ID P18827)
(18)インテグリンαV(NCBI参照配列:NP_002201.1、NCBI遺伝子ID:3685)
(19)奇形癌腫由来増殖因子1タンパク質TDGF1(NCBI参照配列:NP_003203.1、NCBI遺伝子ID:6997)
(20)前立腺特異的膜抗原PSMA(Swiss Prot ID:Q04609;NCBI遺伝子ID:2346)。
(21)チロシンプロテインキナーゼEPHA2(Swiss Prot ID:P29317、NCBI遺伝子ID:1969)。
(22)表面タンパク質SLC44A4(NCBI参照配列:NP_001171515.1、NCBI遺伝子ID:80736)
(23)表面タンパク質BMPR1B(SwissProt:O00238)
(24)輸送タンパク質SLC7A5(SwissProt:Q01650)
(25)上皮前立腺抗原STEAP1(SwissProt:Q9UHE8、遺伝子ID:26872)
(26)卵巣癌抗原MUC16(SwissProt:Q8WXI7、遺伝子ID:94025)。
(27)輸送タンパク質SLC34A2(SwissProt:O95436、遺伝子ID:10568)
(28)表面タンパク質SEMA5b(SwissProt:Q9P283)
(29)表面タンパク質LYPD1(SwissProt:Q8N2G4)
(30)エンドセリン受容体B型EDNRB(SwissProt:P24530、NCBI遺伝子ID:1910)。
(31)RINGフィンガータンパク質RNF43(SwissProt:Q68DV7)
(32)前立腺癌関連タンパク質STEAP2(SwissProt:Q8NFT2)
(33)陽イオンチャネルTRPM4(SwissProt:Q8TD43)
(34)補体受容体CD21(SwissProt:P20023)
(35)B細胞抗原受容体複合体関連タンパク質CD79b(SwissProt:P40259、NCBI遺伝子ID:974)
(36)細胞接着抗原CEACAM6(SwissProt:P40199)
(37)ジペプチダーゼDPEP1(SwissProt:P16444)
(38)インターロイキン受容体IL20Rα(SwissProt:Q9UHF4、NCBI遺伝子ID:3559)
(39)プロテオグリカンBCAN(SwissProt:Q96GW7)
(40)エフリン受容体EPHB2(SwissProt:P29323)
(41)前立腺幹細胞関連タンパク質PSCA(NCBI参照配列:NP_005663.2)
(42)表面タンパク質LHFPL3(SwissProt:Q86UP9)
(43)受容体タンパク質TNFRSF13C(SwissProt:Q96RJ3)
(44)B細胞抗原受容体複合体関連タンパク質CD79a(SwissProt:P11912)
(45)受容体タンパク質CXCR5(CD185;SwissProt:P32302;NCBI遺伝子ID643、NCBI参照配列:NP_001707.1)
(46)イオンチャネルP2X5(SwissProt:Q93086)
(47)リンパ球抗原CD180(SwissProt:Q99467)
(48)受容体タンパク質FCRL1(SwissProt:Q96LA6)
(49)受容体タンパク質FCRL5(SwissProt:Q96RD9)
(50)MHCクラスII分子Ia抗原HLA-DOB(NCBI参照配列:NP_002111.1)
(51)T細胞タンパク質VTCN1(SwissProt:Q7Z7D3)
(52)TWEAKR(FN14、TNFRSF12A、NCBI参照配列:NP_057723.1、NCBI遺伝子ID:51330)
(53)リンパ球抗原CD37(Swiss Prot:P11049、NCBI遺伝子ID:951)
(54)FGF受容体2;FGFR2(NCBI遺伝子ID:2263;正式記号:FGFR2)。FGFR2受容体は様々なスプライス変異体(α、β、IIIb、IIIc)に存在する。全てのスプライス変異体が標的分子として作用することができる。
(55)膜貫通糖タンパク質B7H3(CD276;NCBI遺伝子ID:80381 NCBI参照配列:NP_001019907.1、Swiss Prot:Q5ZPR3-1)。
(56)B細胞受容体BAFFR(CD268;NCBI遺伝子ID:115650)
(57)受容体タンパク質ROR 1(NCBI遺伝子ID:4919)
(58)表面受容体CD123(IL3RA;NCBI遺伝子ID:3563;NCBI参照配列:NP_002174.1;Swiss-Prot:P26951)
(59)受容体タンパク質シンシチン(NCBI遺伝子ID 30816)
(60)アスパラギン酸β-ヒドロキシラーゼ(ASPH;NCBI遺伝子ID 444)
(61)細胞表面糖タンパク質CD44(NCBI遺伝子ID:960)
(62)CDH15(カドヘリン15、NCBI遺伝子ID:1013)
(63)細胞表面糖タンパク質CEACAM5(NCBI遺伝子ID:1048)
(64)細胞接着分子L1様(CHL1、NCBI遺伝子ID:10752)
(65)受容体チロシンキナーゼc-Met(NCBI遺伝子ID:4233)
(66)ノッチリガンドDLL3(NCBI遺伝子ID:10683)
(67)エフリンA4(EFNA4、NCBI遺伝子ID:1945)
(68)エクトヌクレオチドピロホスファターゼ/ホスホジエステラーゼ3(ENPP3、NCBI遺伝子ID:5169)
(69)凝固因子III(F3、NCBI遺伝子ID:2152)
(70)FGF受容体3(FGFR3、NCBI遺伝子ID:2261)
(71)葉酸ヒドロラーゼFOLH1(NCBI遺伝子ID:2346)
(72)葉酸受容体1(FOLR1;NCBI遺伝子ID:2348)
(73)グアニル酸シクラーゼ2C(GUCY2C、NCBI遺伝子ID:2984)
(74)KIT癌原遺伝子受容体チロシンキナーゼ(NCBI遺伝子ID:3815)
(75)リソソーム関連膜タンパク質1(LAMP1、NCBI遺伝子ID:3916)
(76)リンパ球抗原6複合体、遺伝子座E(LY6E、NCBI遺伝子ID:4061)
(77)タンパク質NOTCH3(NCBI遺伝子ID:4854)
(78)タンパク質チロシンキナーゼ7(PTK7、NCBI遺伝子ID:5754)
(79)ネクチン細胞接着分子4(PVRL4、NECTIN4、NCBI遺伝子ID:81607)
(80)膜貫通タンパク質シンデカン1(SDC1、NCBI遺伝子ID:6382)
(81)SLAMファミリーメンバー7(SLAMF7、NCBI遺伝子ID:57823)
(82)輸送タンパク質SLC39A6(NCBI遺伝子ID:25800)
(83)SLIT様およびNTRK様ファミリーメンバー6(SLITRK6、NCBI遺伝子ID:84189)
(84)細胞表面受容体TACSTD2(NCBI遺伝子ID:4070)
(85)受容体タンパク質TNFRSF8(NCBI遺伝子ID:943)
(86)受容体タンパク質TNFSF13B(NCBI遺伝子ID:10673)
(87)糖タンパク質TPBG(NCBI遺伝子ID:7162)
(88)細胞表面受容体TROP2(TACSTD2、NCBI遺伝子ID:4070)
(89)ガラニン様Gタンパク質共役受容体KISS1R(GPR54、NCBI遺伝子ID:84634)
(90)輸送タンパク質SLAMF6(NCBI遺伝子ID:114836)
当業者であれば、抗体、その抗原結合フラグメントまたはその変異体を細菌発現の助けを借りて産生することができる方法を知っている。
当業者であれば、抗体、その抗原結合フラグメントまたはその変異体を哺乳動物細胞発現の助けを借りて産生することができる方法を知っている。
抗体、その抗原結合フラグメントまたはその変異体は、例として硫酸アンモニウムまたはエタノール沈殿、酸抽出、プロテインAクロマトグラフィー、プロテインGクロマトグラフィー、陰イオンまたは陽イオン交換クロマトグラフィー、ホスホセルロースクロマトグラフィー、疎水性相互作用クロマトグラフィー(HIC)、アフィニティークロマトグラフィー、ヒドロキシアパタイトクロマトグラフィーおよびレクチンクロマトグラフィーが挙げられる周知の方法によって組換え細胞培養物から回収および精製することができる。高速液体クロマトグラフィー(「HPLC」)も同様に精製に使用することができる。例えば、Colligan、Current Protocols in Immunology、またはCurrent Protocols in Protein Science、John Wiley&Sons、NY、N.Y.、(1997~2001)、例えば、第1、4、6、8、9、10章を参照されたい。
本発明によると、抗CD123抗体を使用することが可能である。
本発明によると、抗CXCR5抗体を使用することが可能である。
本発明によると、抗B7H3抗体を使用することが可能である。
本発明によると、抗TWEAKR抗体を使用することが可能である。
本発明によると、抗HER2抗体を使用することが可能である。
本発明によると、抗EGFR抗体を使用することが可能である。
・ザルツムマブ/2F8/HuMax-EGFr、Genmab A/S製(国際公開第02/100348号パンフレット、国際公開第2004/056847号パンフレット、INN番号8605)
・ネシツムマブ/11F8、ImClone/IMC-11F8、ImClone Systems Inc.[Eli Lilly&Co]製[(国際公開第2005/090407号パンフレット(欧州特許第01735348号明細書、米国特許出願公開第2007/0264253号明細書、米国特許第7598350号明細書、国際公開第2005/090407号パンフレット)、INN番号9083)
・マツズマブ/抗EGFR MAb、Merck KGaA/抗EGFR MAb、Takeda/EMD 72000/EMD-6200/EMD-72000およびEMD-55900/MAb 425/モノクローナル抗体425、Merck KGaA/Takeda製(国際公開第92/15683号パンフレット、INN番号8103(マツズマブ))
・RG-7160/GA-201/GA 201/R-7160/R7160/RG 7160/RO-4858696/RO-5083945/RO-48838696/RO 5083945、Glycart Biotechnology AG製(Roche Holding AG)(国際公開第2010/112413号パンフレット、国際公開第2010/115554号パンフレット)
・GT-MAB 5.2-GEX/CetuGEX、Glycotope GmbH製(国際公開第2008/028686号パンフレット(欧州特許第01900750号明細書、欧州特許第01911766号明細書、欧州特許第02073842号明細書、米国特許出願公開第2010/0028947号明細書)
・ISU-101、Isu Abxis Inc(ISU Chemical Co.Ltd)/Scancell製(国際公開第2008/004834号パンフレット)
・ABT-806/mAb-806/ch-806/抗EGFRモノクローナル抗体806、Ludwig Institute for Cancer Research/Abbott/Life Science Pharmaceuticals製(国際公開第02/092771号パンフレット、国際公開第2005/081854号パンフレットおよび国際公開第2009/023265号パンフレット)
・SYM-004(2つのキメラIgG1抗体(992および1024)からなる)、Symphogen A/S製(国際公開第2010/022736号パンフレット)
・MR1-1/MR1-1KDEL、IVAX Corp(Teva Pharmaceutical Industries Ltd)(Duke大学)製(特許:国際公開第2001/062931号パンフレット)
・欠失突然変異体、EGFRvIIIに対する抗体、Amgen/Abgenix製(国際公開第2005/010151号パンフレット、米国特許第7628986号明細書)
・SC-100、Scancell Ltd製(国際公開第01/088138号パンフレット)
・MDX-447/EMD 82633/BAB-447/H 447/MAb、EGFR、Medarex/Merck KgaA、Bristol-Myers Squibb(米国)/Merck KGaA(ドイツ)/Takeda(日本)製(国際公開第91/05871号パンフレット、国際公開第92/15683号パンフレット)
・抗EGFR-Mab、Xencor製(国際公開第2005/056606号パンフレット)
・DXL-1218/抗EGFRモノクローナル抗体(がん)、InNexus、InNexus Biotechnology Inc製、Pharmaprojects PH048638
がん標的分子カルボアンヒドラーゼIXに結合する抗体の例は、国際公開第2007/070538号パンフレットに記載されている(例えば、請求項1~16)。
C4.4a抗体および抗原結合フラグメントの例は、国際公開第2012/143499号パンフレットに記載されている。抗体の配列は、国際公開第2012/143499号パンフレットの表1に示されており、各行は、列1に列挙される抗体の可変軽鎖または可変重鎖のそれぞれのCDRアミノ酸配列を示している。
がん標的分子CD20に結合する抗体の例は、リツキシマブ(Genentech)である。リツキシマブ(CAS番号:174722-31-7)は、非ホジキンリンパ腫の治療に使用されるキメラ抗体である。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD52に結合する抗体の例はアレムツズマブ(Genzyme)である。アレムツズマブ(CAS番号:216503-57-0)は、慢性リンパ性白血病の治療に使用されるヒト化抗体である。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
抗メソテリン抗体の例は、例えば、国際公開第2009/068204号パンフレットに記載されている。国際公開第2009/068204号パンフレットに開示されている抗体および抗原結合フラグメントは全て、本明細書に開示される本発明の文脈において使用することができる。より好ましくは、国際公開第2009/068204号パンフレットに開示されている抗体はMF-Tである。
がん標的分子CD30に結合し、がん、例えばホジキンリンパ腫の治療に使用することができる抗体の例は、ブレンツキシマブ、イラツムマブ、および国際公開第2008/092117号パンフレット、国際公開第2008/036688号パンフレットまたは国際公開第2006/089232号パンフレットに開示されている抗体である。抗CD30コンジュゲートの例は、ブレンツキシマブベドチン(INN番号9144)である。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD22に結合し、がん、例えばリンパ腫の治療に使用することができる抗体の例は、イノツズマブおよびエプラツズマブである。抗CD22コンジュゲートの例は、イノツズマブオザガマイシン(INN番号8574)または抗CD22-MMAEおよび抗CD22-MC-MMAE(それぞれCAS RN:139504-50-0および474645-27-7)である。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD33に結合し、がん、例えば白血病の治療に使用することができる抗体の例は、ゲムツズマブおよびリンツズマブ(INN 7580)である。抗CD33コンジュゲートの例は、ゲムツズマブ-オザガマイシンである。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子NMBに結合し、がん、例えば黒色腫または乳がんの治療に使用することができる抗体の例は、グレンバツムマブ(INN 9199)である。抗NMBコンジュゲートの例は、グレンバツマムベドチン(CAS RN:474645-27-7)である。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD56に結合し、がん、例えば多発性骨髄腫、小細胞肺癌、MCCまたは卵巣癌の治療に使用することができる抗体の例は、ロルボツズマブ(lorvotuzumab)である。抗CD57コンジュゲートの例は、ロルボツズマブメルタンシン(lorvotuzumab mertansine)(CAS RN:139504-50-0)である。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD70に結合し、がん、例えば、非ホジキンリンパ腫または腎細胞がんの治療に使用することができる抗体の例は、国際公開第2007/038637号パンフレットおよび国際公開第2008/070593号パンフレットに開示されている。抗CD70コンジュゲートの例はSGN-75(CD70 MMAF)である。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD74に結合し、がん、例えば多発性骨髄腫の治療に使用することができる抗体の例は、ミラツズマブである。抗CD74コンジュゲートの例は、ミラツズマブ-ドキソルビシン(CAS RN:23214-92-8)である。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD19に結合し、がん、例えば非ホジキンリンパ腫の治療に使用することができる抗体の例は、国際公開第2008/031056号パンフレットに開示されている。さらなる抗体および抗CD19コンジュゲート(SAR3419)の例は、国際公開第2008/047242号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子ムチン-1に結合し、がん、例えば非ホジキンリンパ腫の治療に使用することができる抗体の例は、クリバツズマブおよび国際公開第2003/106495号パンフレット、国際公開第2008/028686号パンフレットに開示されている抗体である。抗ムチンコンジュゲートの例は、国際公開第2005/009369号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子CD138およびそのコンジュゲートに結合し、がん、例えば多発性骨髄腫の治療に使用することができる抗体の例は、国際公開第2009/080829号パンフレット、国際公開第2009/080830号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子インテグリンαVに結合し、がん、例えば黒色腫、肉腫または癌腫の治療に使用することができる抗体の例は、インテツムマブ(CAS RN:725735-28-4)、アブシキシマブ(CAS RN:143653-53-6)、エタラシズマブ(CAS RN:892553-42-3)ならびに米国特許第7465449号明細書、欧州特許第719859号明細書、国際公開第2002/012501号パンフレットおよび国際公開第2006/062779号パンフレットに開示される抗体である。抗インテグリンαVコンジュゲートの例は、インテツムマブ-DM 4および国際公開第2007/024536号パンフレットに開示されている他のADCである。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子TDGF1に結合し、がんの治療に使用することができる抗体の例は、国際公開第02/077033号パンフレット、米国特許第7318924号明細書、国際公開2003/083041号パンフレットおよび国際公開第2002/088170号パンフレットに開示される抗体である。抗TDGF1コンジュゲートの例は、国際公開第2002/088170号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子PSMAに結合し、がん、例えば前立腺癌の治療に使用することができる抗体の例は、国際公開第97/35616号パンフレット、国際公開第99/47554号パンフレット、国際公開第01/009192号パンフレットおよび国際公開第2003/034903号パンフレットに開示される抗体である。抗PSMAコンジュゲートの例は、国際公開第2009/026274号パンフレットおよび国際公開第2007/002222号パンフレットに開示されている。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子EPHA2に結合し、コンジュゲートを調製するためおよびがんの治療に使用することができる抗体の例は、国際公開第2004/091375号パンフレットに開示されている。これらの抗体および抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子SLC44A4に結合し、コンジュゲートを調製するためおよびがん、例えば膵臓または前立腺癌の治療に使用することができる抗体の例は、国際公開第2009/033094号パンフレットおよび米国特許出願公開第2009/0175796号明細書に開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子HLA-DOBに結合する抗体の例は、がん、例えば非ホジキンリンパ腫の治療に使用することができる抗体Lym-1(CAS RN:301344-99-0)である。抗HLA-DOBコンジュゲートの例は、例えば、国際公開第2005/081711号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
がん標的分子VTCN1に結合し、コンジュゲートを調製するためおよびがん、例えば卵巣癌、膵臓がん、肺がんまたは乳がんの治療に使用することができる抗体の例は、国際公開第2006/074418号パンフレットに開示されている。これらの抗体およびその抗原結合フラグメントを本発明の文脈において使用することができる。
抗FGFR2抗体および抗原結合フラグメントの例は、国際公開第2013076186号パンフレットに記載されている。抗体の配列は、国際公開第2013076186号パンフレットの表9および表10に示されている。M048-D01およびM047-D08と呼ばれる抗体に由来する抗体、抗原結合フラグメントおよび抗体の変異体が好ましい。
本出願において、結合剤-薬物コンジュゲートの文脈において、以下の表に示される以下の好ましい抗体が参照される:TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574およびTPP-9580。
本発明はまた、本発明の化合物の全ての適当な同位体変種も包含する。本発明の化合物の同位体変種は、ここでは、本発明の化合物中の少なくとも1個の原子が同じ原子番号であるが通常または主に自然に生じる原子質量とは異なる原子質量を有する別の原子と交換された化合物を意味すると理解される。本発明の化合物に組み込まれ得る同位体の例としては、水素、炭素、窒素、酸素、リン、硫黄、フッ素、塩素、臭素およびヨウ素の同位体、例えば、2H(重水素)、3H(トリチウム)、13C、14C、15N、17O、18O、32P、33P、33S、34S、35S、36S、18F、36Cl、82Br、123I、124I、129Iおよび131Iがある。本発明による化合物の特定の同位体変種、特に1種または複数の放射性同位元素が組み込まれたものは、例えば、体内での作用機構または有効成分分布の調査に有益となり得、比較的容易な調製性および検出性のために、特に3Hまたは14Cで標識された化合物がこの目的に適している。さらに、同位体、例えば、重水素の組込みにより、化合物のより大きな代謝安定性の結果としての特定の治療上の利益、例えば、体内での半減期の延長または要求される活性剤用量の減少がもたらされ得るので、本発明による化合物のこのような修飾も、いくつかの場合、本発明の好ましい実施形態を構成し得る。本発明による化合物の同位体変種は、当業者に既知の方法、例えば、以下にさらに記載される方法および実施例に記載の手順によって、それぞれの試薬および/または出発化合物の対応する同位体修飾を用いることにより調製することができる。
その治療に本発明による化合物が使用され得る過増殖性疾患には、特に、がんおよび腫瘍疾患の群が含まれる。本発明の文脈において、これらは、それだけに限らないが、以下の疾患を特に意味すると理解される:乳癌および乳腫瘍(乳腺管および小葉形態、原位置も含む乳癌)、気道の腫瘍(小細胞および非小細胞癌、気管支癌)、脳腫瘍(例えば、脳幹および視床下部のもの、星細胞腫、上衣腫、膠芽腫、神経膠腫、髄芽腫、髄膜腫および神経外胚葉性腫瘍および松果体腫瘍)、消化器官の腫瘍(食道、胃、胆嚢、小腸、大腸、直腸の癌および肛門癌)、肝臓腫瘍(とりわけ、肝細胞癌、胆管癌および混合肝細胞性胆管癌)、頭頸部領域の腫瘍(喉頭、下咽頭、上咽頭、中喉頭、口唇および口腔癌、口腔黒色腫)、皮膚腫瘍(基底細胞腫、棘細胞癌、扁平上皮細胞癌、カポジ肉腫、悪性黒色腫、非黒色腫性皮膚がん、メルケル細胞皮膚がん、肥満細胞腫瘍)、結合組織の腫瘍(とりわけ、軟組織肉腫、骨肉腫、悪性線維性組織球腫、軟骨肉腫、線維肉腫、血管肉腫、平滑筋肉腫、脂肪肉腫、リンパ肉腫および横紋筋肉腫)、眼の腫瘍(とりわけ、眼内黒色腫および網膜芽細胞腫)、内分泌腺および外分泌腺の腫瘍(例えば、甲状腺および副甲状腺、膵臓および唾液腺癌、腺癌)、尿路の腫瘍(膀胱、陰茎、腎臓、腎盂および尿管の腫瘍)ならびに生殖器官の腫瘍(女性の子宮内膜、子宮頸部、卵巣、膣、外陰および子宮ならびに男性の前立腺および精巣の癌)。これらにはまた、固形および循環細胞としての血液、リンパ系および脊髄の増殖性疾患、例えば、白血病、リンパ腫および骨髄増殖性疾患、例えば急性骨髄性、急性リンパ芽球性、慢性リンパ球性、慢性骨髄性および有毛細胞白血病ならびにAIDS関連リンパ腫、ホジキンリンパ腫、非ホジキンリンパ腫、皮膚T細胞リンパ腫、バーキットリンパ腫および中枢神経系のリンパ腫も含まれる。
131I-chTNT、アバレリクス、アビラテロン、アクラルビシン、アダリムマブ、Ado-トラスツズマブ・エムタンシン、アファチニブ、アフリベルセプト、アルデスロイキン、アレムツズマブ、アレンドロン酸、アリトレチノイン、アルトレタミン、アミホスチン、アミノグルテチミド、ヘキシル-5-アミノレブリン酸、アムルビシン、アムサクリン、アナストロゾール、アンセスチム、アネトールジチオールチオン、アネツマブ・ラブタンシン、アンギオテンシンII、アンチトロンビンIII、アプレピタント、アルシツモマブ、アルグラビン、三酸化ヒ素、アスパラギナーゼ、アテゾリズマブ、アベルマブ、アキシチニブ、アザシチジン、ベロテカン、ベンダムスチン、ベシレソマブ、ベリノスタット、ベバシズマブ、ベキサロテン、ビカルタミド、ビサントレン、ブレオマイシン、ブリナツモマブ、ボルテゾミブ、ブセレリン、ボスチニブ、ブレンツキシマブベドチン、ブスルファン、カバジタキセル、カボザンチニブ、カルシトニン、ホリナートカルシウム、レボホリナートカルシウム、カペシタビン、カプロマブ、カルボマゼピン、カルボプラチン、カルボコン、カーフィルゾミブ、カルモフール、カルムスチン、カツマキソマブ、セレコキシブ、セルモロイキン、セリチニブ、セツキシマブ、クロラムブシル、クロルマジノン、クロルメチン、シドフォビル、シナカルセト、シスプラチン、クラドリビン、クロドロン酸、クロファラビン、コビメチニブ、コパンリシブ、クリサンタスパーゼ、クリゾチニブ、シクロホスファミド、シプロテロン、シタラビン、ダカルバジン、ダクチノマイシン、ダラツムマブ、ダブラフェニブ、ダロルタミド、ダサチニブ、ダウノルビシン、デシタビン、デガレリクス、デニロイキンジフチトクス、デノスマブ、デプレオチド、デスロレリン、デクスラゾキサン、塩化ジブロスピジウム、ジアンヒドロガラクチトール、ジクロフェナク、ドセタキセル、ドラセトロン、ドキシフルリジン、ドキソルビシン、ドキソルビシン+エストロン、ドロナビノール、デュルバルマブ、エドレコロマブ、酢酸エリプチニウム、エンドスタチン、エノシタビン、エンザルタミド、エパカドスタット、エピルビシン、エピチオスタノール、エポエチンα、エポエチンβ、エポエチンζ、エプタプラチン、エリブリン、エルロチニブ、エソメプラゾール、エストラムスチン、エトポシド、エチニルエストラジオール、エベロリムス、エキセメスタン、ファドロゾール、フェンタニル、フルオキシメステロン、フロクスウリジン、フルダラビン、フルオロウラシル、フルタミド、葉酸、フォルメスタン、ホスアプレピタント、フォテムスチン、フルベストラント、ガドブトロール、ガドテリドール、ガドテル酸メグルミン塩、ガドベルセタミド、ガドキセト酸二ナトリウム塩(gd-EOB-DTPA二ナトリウム塩)、硝酸ガリウム、ガニレリクス、ゲフィチニブ、ゲムシタビン、ゲムツズマブ、グルカルピダーゼ、グルトキシム、ゴセレリン、グラニセトロン、顆粒球コロニー刺激因子(G-CSF)、顆粒球マクロファージコロニー刺激因子(GM-CSF)、ヒスタミン二塩酸塩、ヒストレリン、ヒドロキシカルバミド、I-125種、イバンドロン酸、イブリツモマブ・チウキセタン、イブルチニブ、イダルビシン、イホスファミド、イマチニブ、イミキモド、インプロスルファン、インジセトロン、インカドロン酸、インゲノールメブテート、インターフェロンα、インターフェロンβ、インターフェロンγ、イオビトリドール、イオベングアン(123I)、イオメプロール、イピリムマブ、イリノテカン、イトラコナゾール、イクサベピロン、イキサゾミブ、ランレオチド、ランソプラゾール、ラパチニブ、ラソコリン、レナリドミド、レンバチニブ、レノグラスチム、レンチナン、レトロゾール、リュープロレリン、レバミソール、レボノルゲストレル、レボチロキシンナトリウム、リペグフィルグラスチム、リスリド、ロバプラチン、ロムスチン、ロニダミン、マソプロコール、メドロキシプロゲステロン、メゲストロール、メラルソプロール、メルファラン、メピチオスタン、メルカプトプリン、メスナ、メタドン、メトトレキサート、メトキサレン、アミノレブリン酸メチル、メチルプレドニゾロン、メチルテストステロン、メチロシン、ミファムルチド、ミルテフォシン、ミリプラチン、ミトブロニトール、ミトグアゾン、ミトラクトール、マイトマイシン、ミトタン、ミトキサントロン、モガムリズマブ、モルグラモスチム、モピダモール、塩酸モルヒネ、硫酸モルヒネ、ナビロン、ナビキシモルス、ナファレリン、ナロキソン+ペンタゾシン、ナルトレキソン、ナルトグラスチム、ネシツムマブ、ネダプラチン、ネララビン、ネリドロン酸、ネツピタント/パロノセトロン、ニボルマブ、ニボルマブ、ペンテトレオチド、ニロチニブ、ニルタミド、ニモラゾール、ニモツズマブ、ニムスチン、ニンテダニブ、ニトラクリン、ニボルマブ、オビヌツズマブ、オクトレオチド、オファツムマブ、オラパリブ、オララツマブ、オマセタキシン・メペサクシネート、オメプラゾール、オンダンセトロン、オルゴテイン、オリロチモド、オシメルチニブ、オキサリプラチン、オキシコドン、オキシメトロン、オゾガマイシン、p53遺伝子療法、パクリタキセル、パルボシクリブ、パリフェルミン、パラジウム103種、パロノセトロン、パミドロン酸、パニツムマブ、パノビノスタット、パントプラゾール、パゾパニブ、ペガスパルガーゼ、ペンブロリズマブ、ペグインターフェロンα-2b、ペンブロリズマブ、ペメトレキセド、ペントスタチン、ペプロマイシン、ペルフルブタン、ペルホスファミド、ペルツズマブ、ピシバニール、ピロカルピン、ピラルビシン、ピキサントロン、プレリキサフォール、プリカマイシン、ポリグルサム、リン酸ポリエストラジオール、ポリビニルピロリドン+ヒアルロン酸ナトリウム、ポリサッカリド-K、ポマリドマイド、ポナチニブ、ポルフィマーナトリウム、プララトレキサート、プレドニムスチン、プレドニゾン、プロカルバジン、プロコダゾール、プロプラノロール、キナゴリド、ラベプラゾール、ラコツモマブ、塩化ラジウム-223、ラドチニブ、ラロキシフェン、ラルチトレキセド、ラモセトロン、ラムシルマブ、ラニムスチン、ラスブリカーゼ、ラゾキサン、レファメチニブ、レゴラフェニブ、リセドロン酸、レニウム-186エチドロネート、リツキシマブ、ロガラチニブ、ロラピタント、ロミデプシン、ロムルチド、ロニシクリブ、サマリウム(153Sm)レキシドロナム、サツモマブ、セクレチン、シルツキシマブ、シプレウセル-T、シゾフィラン、ソブゾキサン、グリシダゾールナトリウム、ソニデジブ、ソラフェニブ、スタノゾロール、ストレプトゾシン、スニチニブ、タラポルフィン、タリモジーン・ラハーパレプベック、タミバロテン、タモキシフェン、タペンタドール、タソネルミン、テセロイキン、テクネチウム(99mTc)ノフェツモマブメルペンタン、99mTc-HYNIC-[Tyr3]-オクトレオチド、テガフール、テガフール+ギメラシル+オテラシル、テモポルフィン、テモゾロミド、テムシロリムス、テニポシド、テストステロン、テトロフォスミン、サリドマイド、チオテパ、チマルファシン、サイロトロピンα、チオグアニン、トシリズマブ、トポテカン、トレミフェン、トシツモマブ、トラベクテジン、トラメチニブ、トラマドール、トラスツズマブ、トレオスルファン、トレチノイン、トリフルリジン+チピラシル、トラメチニブ、トリロスタン、トリプトレリン、トロホスファミド、トロンボポエチン、ウベニメクス、バルルビシン、バンデタニブ、バプレオチド、バタラニブ、ベムラフェニブ、ビンブラスチン、ビンクリスチン、ビンデシン、ビンフルニン、ビノレルビン、ビスモデギブ、ボリノスタット、イットリウム90ガラスマイクロビーズ、ジノスタチン、ジノスタチンスチマラマー、ゾレドロン酸、ゾルビシン。
・個々の有効成分による治療と比較して、腫瘍の成長を遅くし、そのサイズを縮小し、またはそれを完全に排除する有効性の改善;
・単独療法の場合よりも低投与量で使用される化学療法剤を使用する可能性;
・個々の投与と比較してより少ない副作用でのより耐容性のある療法の可能性;
・より広範囲の新生物障害の治療の可能性;
・療法に対するより高い反応率の達成;
・現在の標準療法と比較してより長い患者の生存時間。
以下の実施例は、本発明を例示する。本発明はこれらの実施例に制限されない。
実施例の例として、以下のスキームは、実施例に至る例示的合成経路を示す:
スキーム1:レグマイン切断可能リンカーを用いたリジン結合ADCの合成
略語および頭字語:
ABCB1 ATP結合カセットサブファミリーBメンバー1(P-gpおよびMDR1の同義語)
abs. 無水
Ac アセチル
ACN アセトニトリル
aq. 水性、水溶液
ATP アデノシン三リン酸
BCRP 乳がん耐性タンパク質、流出輸送体
BEP 2-ブロモ-1-エチルピリジニウムテトラフルオロボレート
Boc tert-ブトキシカルボニル
br. ブロードな(NMRにおける)
Ex. 実施例
BxPC3 ヒト腫瘍細胞株
C 濃度
ca. およそ、約
CI 化学イオン化(MSにおける)
DAR 薬物対抗体比
d 二重項(NMRにおける)
d 日
TLC 薄層クロマトグラフィー
DCI 直接化学イオン化(MSにおける)
DCM ジクロロメタン
dd 二重項の二重項(NMRにおける)
DMAP 4-N,N-ジメチルアミノピリジン
DME 1,2-ジメトキシエタン
DMEM ダルベッコ改変イーグル培地(細胞培養のための標準栄養培地)
DMF N,N-ジメチルホルムアミド
DMSO ジメチルスルホキシド
D/P 色素(蛍光色素)/タンパク質比
DPBS,D-PBS, ダルベッコリン酸緩衝塩溶液
DSMZ Deutsche Sammlung von Mikroorganismen und Zellkulturen(ドイツ微生物細胞培養コレクション)
PBS PBS=DPBS=D-PBS、pH7.4、Sigma、番号D8537
組成:
KCl 0.2g
KH2PO4(無水物) 0.2g
NaCl 8.0g
Na2HPO4(無水物) 1.15g
H2Oを用いて1lにした
dt 三重項の二重項(NMRにおける)
DTT DL-ジチオトレイトール
EDC N’-(3-ジメチルアミノプロピル)-N-エチルカルボジイミド塩酸塩
EGFR 上皮成長因子受容体
EI 電子衝突イオン化(MSにおける)
ELISA 酵素結合免疫吸着測定法
eq. 当量
ESI エレクトロスプレーイオン化(MSにおける)
ESI-MicroTofq ESI-MicroTofq(Tof=飛行時間およびq=四重極による質量分析計の名称)
FCS ウシ胎仔血清
Fmoc (9H-フルオレン-9-イルメトキシ)カルボニル
sat. 飽和
GTP グアノシン-5’-三リン酸
H 時間
HATU O-(7-アザベンゾトリアゾール-1-イル)-N,N,N’,N’-テトラメチルウロニウムヘキサフルオロホスフェート
HEPES 4-(2-ヒドロキシエチル)ピペラジン-1-エタンスルホン酸
HOAc 酢酸
HOAt 1-ヒドロキシ-7-アザベンゾトリアゾール
HOBt 1-ヒドロキシ-1H-ベンゾトリアゾール水和物
HOSu N-ヒドロキシスクシンイミド
HPLC 高圧、高速液体クロマトグラフィー
IC50 最大半数阻害濃度
i.m. 筋肉内、筋肉への投与
i.v. 静脈内、静脈内への投与
conc. 濃縮
KPL-4 ヒト腫瘍細胞株
KU-19-19 ヒト腫瘍細胞株
LC-MS 液体クロマトグラフィー結合質量分析
LLC-PK1 cells ルイス肺癌ブタ腎臓細胞株
L-MDR ヒトMDR1トランスフェクトLLC-PK1細胞
LoVo ヒト腫瘍細胞株
M 多重項(NMRにおける)
Me メチル
MDR1 多剤耐性タンパク質1
MeCN アセトニトリル
min 分
MOLM-13 ヒト腫瘍細胞株
MS 質量分析
MTT 3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニル-2H-テトラゾリウムブロミド
MV-4-11 ヒト腫瘍細胞株
NB4 ヒト腫瘍細胞株
NCI-H292 ヒト腫瘍細胞株
NMM N-メチルモルホリン
NMP N-メチル-2-ピロリジノン
NMR 核磁気共鳴分光法
NMRI 海軍医学研究所(NMRI)に由来するマウス系統
Nude mice 実験動物
NSCLC 非小細胞肺がん
PBS リン酸緩衝塩溶液
Pd/C パラジウム活性炭
P-gp P-糖タンパク質、トランスポータータンパク質
PNGaseF 糖を切断する酵素
quant. 定量的(収率における)
quart 四重項(NMRにおける)
quint 五重項(NMRにおける)
Rec-1 ヒト腫瘍細胞株
Rf 保持指数(TLCにおける)
RT 室温
Rt 保持時間(HPLCにおける)
s 一重項(NMRにおける)
s.c. 皮下投与、皮膚下への投与
SCID mice 重度の複合免疫不全を有する試験マウス
SK-HEP-1 ヒト腫瘍細胞株
t 三重項(NMRにおける)
TBAF テトラ-n-ブチルアンモニウムフルオリド
TCEP トリス(2-カルボキシエチル)ホスフィン
TEMPO (2,2,6,6-テトラメチルピペリジン-1-イル)オキシル
Teoc トリメチルシリルエトキシカルボニル
tert 第三級
TFA トリフルオロ酢酸
THF テトラヒドロフラン
T3P(登録商標) 2,4,6-トリプロピル-1,3,5,2,4,6-トリオキサトリホスフィナン2,4,6-トリオキシド
U251 ヒト腫瘍細胞株
UV 紫外分光法
v/v (溶液の)体積対体積の比
Z ベンジルオキシカルボニル
方法1(LC-MS):
機器:Waters ACQUITY SQD UPLCシステム;カラム:Waters Acquity UPLC HSS T3 1.8μ5 0×1mm;移動相A:水1l+99%濃度ギ酸0.25ml;移動相B:アセトニトリル1l+99%濃度ギ酸0.25ml;勾配:0.0分90%A→1.2分5%A→2.0分5%A;オーブン:50℃;流量:0.40ml/分;UV検出:208~400nm。
MS機器型:Waters Synapt G2S;UPLC機器型:Waters Acquity I-CLASS;カラム:Waters、BEH300、2.1×150mm、C18 1.7μm;移動相A:水1l+0.01%ギ酸;移動相B:アセトニトリル1l+0.01%ギ酸;勾配:0.0分2%B→1.5分2%B→8.5分95%B→10.0分95%B;オーブン:50℃;流量:0.50ml/分;UV検出:220nm
MS機器:Waters(Micromass)QM;HPLC機器:Agilent 1100シリーズ;カラム:Agilent ZORBAX Extend-C18 3.0×50mm 3.5ミクロン;移動相A:水1l+0.01molの炭酸アンモニウム、移動相B:アセトニトリル1l;勾配:0.0分98%A→0.2分98%A→3.0分5%A→4.5分5%A;オーブン:40℃;流量:1.75ml/分;UV検出:210nm
MS機器型:Waters Synapt G2S;UPLC機器型:Waters Acquity I-CLASS;カラム:Waters、HSST3、2.1×50mm、C18 1.8μm;移動相A:水1l+0.01%ギ酸;移動相B:アセトニトリル1l+0.01%ギ酸;勾配:0.0分10%B→0.3分10%B→1.7分95%B→2.5分95%B;オーブン:50℃;流量:1.20ml/分;UV検出:210nm
機器:Waters ACQUITY SQD UPLCシステム;カラム:Waters Acquity UPLC HSS T3 1.8μ 50×1mm;移動相A:水1l+99%濃度ギ酸0.25ml;移動相B:アセトニトリル1l+99%濃度ギ酸0.25ml;勾配:0.0分95%A→6.0分5%A→7.5分5%A;オーブン:50℃;流量:0.35ml/分;UV検出:210~400nm。
機器:Micromass Quattro Premier with Waters UPLC Acquity;カラム:Thermo Hypersil GOLD 1.9μ、50×1mm;移動相A:水1l+50%濃度ギ酸0.5ml;移動相B:アセトニトリル1l+50%濃度ギ酸0.5ml;勾配:0.0分97%A→0.5分97%A→3.2分5%A→4.0分5%Aオーブン:50℃;流量:0.3ml/分;UV検出:210nm。
機器:Agilent MS Quad 6150;HPLC:Agilent 1290;カラム:Waters Acquity UPLC HSS T3 1.8μ50×2.1mm;移動相A:水1l+99%濃度ギ酸0.25ml;移動相B:アセトニトリル1l+99%濃度ギ酸0.25ml;勾配:0.0分90%A→0.3分90%A→1.7分5%A→3.0分5%A オーブン:50℃;流量:1.20ml/分;UV検出:205~305nm。
MS機器型:Waters Synapt G2S;UPLC機器型:Waters Acquity I-CLASS;カラム:Waters、HSST3、2.1×50mm、C18 1.8μm;移動相A:水1l+0.01%ギ酸;移動相B:アセトニトリル1l+0.01%ギ酸;勾配:0.0分2%B→2.0分2%B→13.0分90%B→15.0分90%B;オーブン:50℃;流量:1.20ml/分;UV検出:210nm。
MS機器:Waters;HPLC機器:Waters(カラムWaters X-Bridge C18、19mm×50mm、5μm、溶離液A:水+0.05%アンモニア、移動相B:アセトニトリル(ULC)、勾配;流量:40ml/分;UV検出:DAD;210~400nm)
または
MS機器:Waters、HPLC機器:Waters(カラムPhenomenex Luna 5μC18(2)100A、AXIA Tech.50×21.2mm、溶離液A:水+0.05%ギ酸、溶離液B:アセトニトリル(ULC)、勾配;流量:40ml/分;UV検出:DAD;210~400nm)。
MS機器:Waters SQD;HPLC機器:Waters UPLC;カラム:Zorbax SB-Aq(Agilent)、50mm×2.1mm、1.8μm;移動相A:水+0.025%ギ酸、溶離液B:アセトニトリル(ULC)+0.025%ギ酸;勾配:0.0分98%A-0.9分25%A-1.0分5%A-1.4分5%A-1.41分98%A-1.5分98%A;オーブン:40℃;流量:0.600ml/分;UV検出:DAD;210nm。
機器:HP1100シリーズ
カラム:Merck Chromolith SpeedROD RP-18e、50~4.6mm、カタログ番号1.51450.0001、プレカラムChromolith Guardカートリッジキット、RP-18e、5~4.6mm、カタログ番号1.51470.0001
勾配:流量5ml/分
注入体積5μl
溶媒A:水中HClO4(70%)(4ml/l)
溶媒B:アセトニトリル
開始20%B
0.50分20%B
3.00分90%B
3.50分90%B
3.51分20%B
4.00分20%B
カラム温度:40℃
波長:210nm
MS機器型:Thermo Scientific FT-MS;機器型:UHPLC+:Thermo Scientific UltiMate 3000;カラム:Waters、HSST3、2.1×75mm、C18 1.8μm;移動相A:水1l+0.01%ギ酸;移動相B:アセトニトリル1l+0.01%ギ酸;勾配:0.0分10%B→2.5分95%B→3.5分95%B;オーブン:50℃;流量:0.90ml/分;UV検出:210nm/最適積分路210~300nm。
MS機器:Waters(Micromass)Quattro Micro;機器Waters UPLC Acquity;カラム:Waters BEH C18 1.7μ50×2.1mm;移動相A:水1l+0.01molのギ酸アンモニウム、移動相B:アセトニトリル1l;勾配:0.0分95%A→0.1分95%A→2.0分15%A→2.5分15%A→2.51分10%A→3.0分10%A;オーブン:40℃;流量:0.5ml/分;UV検出:210nm。
MS機器型:ThermoFisherScientific LTQ-Orbitrap-XL;HPLC機器型:Agilent 1200SL;カラム:Agilent、POROSHELL 120、3×150mm、SB-C18 2.7μm;移動相A:水1l+0.1%トリフルオロ酢酸;移動相B:アセトニトリル1l+0.1%トリフルオロ酢酸;勾配:0.0分2%B→0.3分2%B→5.0分95%B→10.0分95%B;オーブン:40℃;流量:0.75ml/分;UV検出:210nm
中間体C52
(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロパン-1-アミン
LC-MS(方法1):Rt=1.18分;MS(ESIpos):m/z=295[M+H]+。
LC-MS(方法7):Rt=1.59分;MS(ESIpos):m/z=328[M+H]+。
LC-MS(方法7):Rt=1.48分;MS(ESIpos):m/z=298[M+H]+。
LC-MS(方法7):Rt=1.63分;MS(ESIpos):m/z=401[M+H]+。
LC-MS(方法6):Rt=2.97分;MS(ESIpos):m/z=459[M+H]+。
LC-MS(方法6):Rt=2.10分;MS(ESIpos):m/z=338[M-NH2]+、709[2M+H]+。
1H-NMR(400 MHz,DMSO-d6):δ[ppm]=0.87(s,9H),1.53(s,2H),3.59(s,1H),5.24(d,2H),6.56(s,1H),6.94(m,1H),7.10(d,2H),7.20(m,1H),7.26(m,2H),7.34(m,2H),7.46(m,1H).
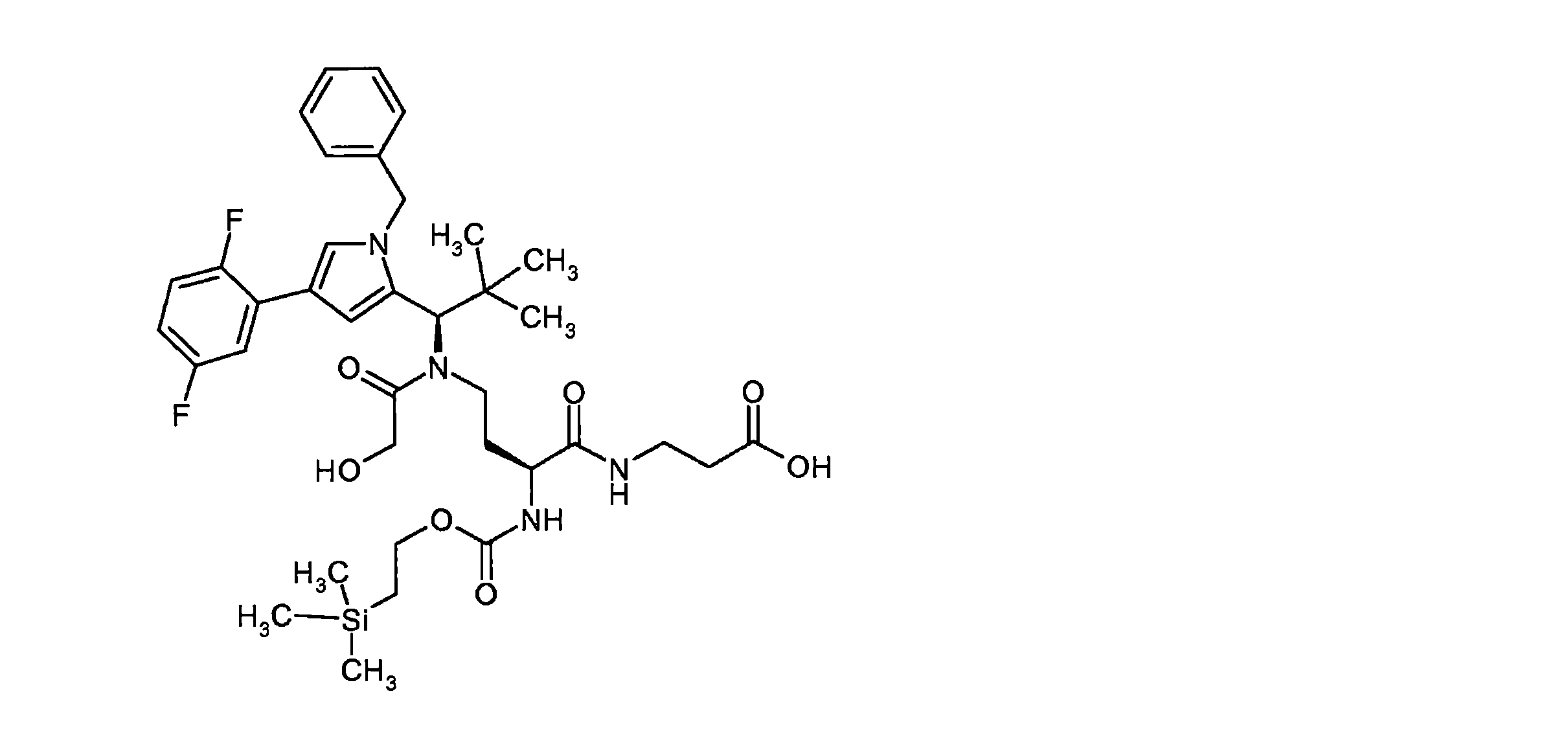
(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-2-({[2-(トリメチルシリル)エトキシ]カルボニル}アミノ)ブタン酸
LC-MS(方法12)Rt=1.97分;MS(ESIpos):m/z=614(M+H)+。
LC-MS(方法1)Rt=1.48分;MS(ESIpos):m/z=714(M+H)+。
LC-MS(方法1):Rt=1.34分;MS(ESIpos):m/z=656(M-H)-。
1H-NMR(400 MHz,DMSO-d6):δ[ppm]=0.03(s,9H),0.58(m,1H),0.74-0.92(m,11H),1.40(m,1H),3.3(m,2H),3.7(m,1H),3.8-4.0(m,2H),4.15(q,2H),4.9 and 5.2(2d,2H),5.61(s,1H),6.94(m,2H),7.13-7.38(m,7H),7.48(s,1H),7.60(m,1H),12.35(s,1H).
N-[(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-2-({[2-(トリメチルシリル)エトキシ]カルボニル}アミノ)ブタノイル]-β-アラニン
LC-MS(方法1):Rt=1.29分;MS(ESIpos):m/z=729(M+H)+。
(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ)-2-{[(ベンジルオキシ)カルボニル]アミノ}ブタン酸
LC-MS(方法1):Rt=1.31分;MS(ESIpos):m/z=646(M-H)-。
ジベンジルN-{(2S)-2-アミノ-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル{(グリコロイル)アミノ]ブタノイル}-β-アラニル-D-グルタメート
LC-MS(方法1):Rt=1.08分;MS(ESIpos):m/z=894[M+H]+。
ジ-tert-ブチルN-{(2S)-2-アミノ-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル{(グリコロイル)アミノ]ブタノイル}-β-アラニル-D-グルタメート
LC-MS(方法1):Rt=1.06分;MS(ESIpos):m/z=826[M+H]+。
トリフルオロ酢酸ジベンジルN-{(2S)-2-(L-アスパラギニルアミノ)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]ブタノイル}-β-アラニル-D-グルタミン酸塩
メチル(2S)-4-オキソ-2-({[2-(トリメチルシリル)エトキシ]カルボニル}アミノ)ブタノエート
LC-MS(方法1):Rt=0.89分;MS(ESIneg):m/z=290(M-H)-。
LC-MS(方法1)Rt=0.87分;MS(ESIpos):m/z=278(M+H)+。
1H-NMR(400 MHz,DMSO-d6):δ[ppm]=0.03(s,9H),0.91(m,2H),2.70-2.79(m,1H),2.88(dd,1H),3.63(s,3H),4.04(m,2H),4.55(m,1H),7.54(d,1H),9.60(t,1H).
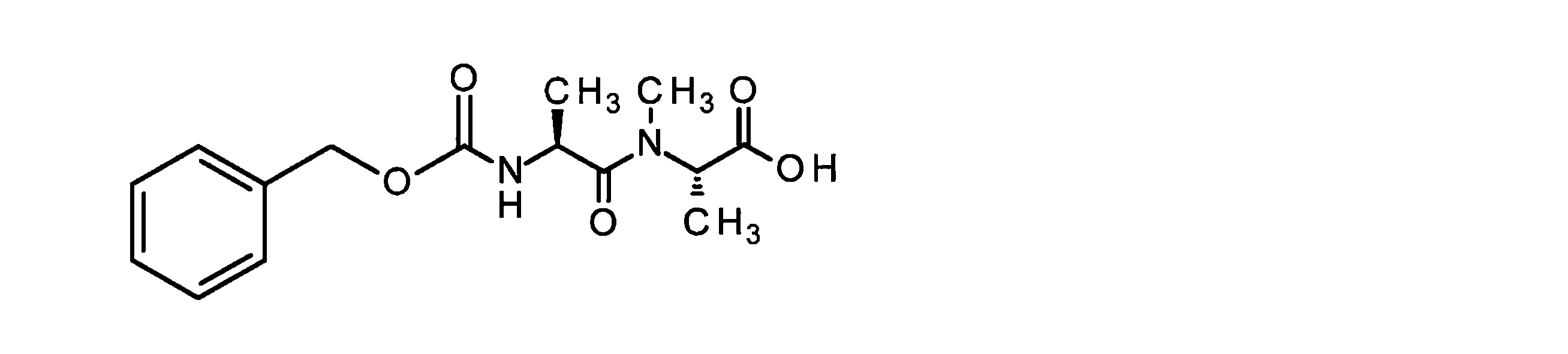
N-[(ベンジルオキシ)カルボニル]-L-バリル-L-アラニン
LC-MS(方法12):Rt=1.34分;MS(ESIpos):m/z=323.16(M+H)+。
N-(ピリジン-4-イルアセチル)-L-アラニル-L-アラニル-L-アスパラギントリフルオロアセテート
LC-MS(方法1):Rt=0.15分;MS(ESIpos):m/z=394(M+H)+。
N-[(ベンジルオキシ)カルボニル]-L-アラニル-N-メチル-L-アラニン
LC-MS(方法1):Rt=0.68分;MS(ESIpos):m/z=309[M+H]+。
N-[(ベンジルオキシ)カルボニル]-L-アラニル-N-メチル-L-アラニル-L-アスパラギントリフルオロ酢酸塩
LC-MS(方法1):Rt=0.57分;MS(ESIneg):m/z=421[M-H]-。
N-[(ベンジルオキシ)カルボニル]-L-アラニル-N-メチル-L-アラニル-L-アラニン
LC-MS(方法12):Rt=1.25分;MS(ESIneg):m/z=378[M-H]-。
N-[(ベンジルオキシ)カルボニル]-L-アラニル-N-メチル-L-アラニル-L-ロイシン
LC-MS(方法12):Rt=0.83分;MS(ESIneg):m/z=420[M-H]-。
(5S,8S,11S)-11-(2-アミノ-2-オキソエチル)-8-[2-(ベンジルオキシ)-2-オキソエチル]-5-メチル-3,6,9-トリオキソ-1-フェニル-2-オキサ-4,7,10-トリアザドデカン-12-酸
LC-MS(方法1):Rt=0.76分;MS(ESIpos):m/z=543[M+H]+。
1-ブロモ-2-オキソ-6,9,12,15-テトラオキサ-3-アザオクタデカン-18-酸
LC-MS(方法5):Rt=1.05分;MS(ESIpos):m/z=386および388(M+H)+。
N-[(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)アセチル]-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法12):Rt=1.66分;MS(ESIneg):m/z=1119[M-H]-。
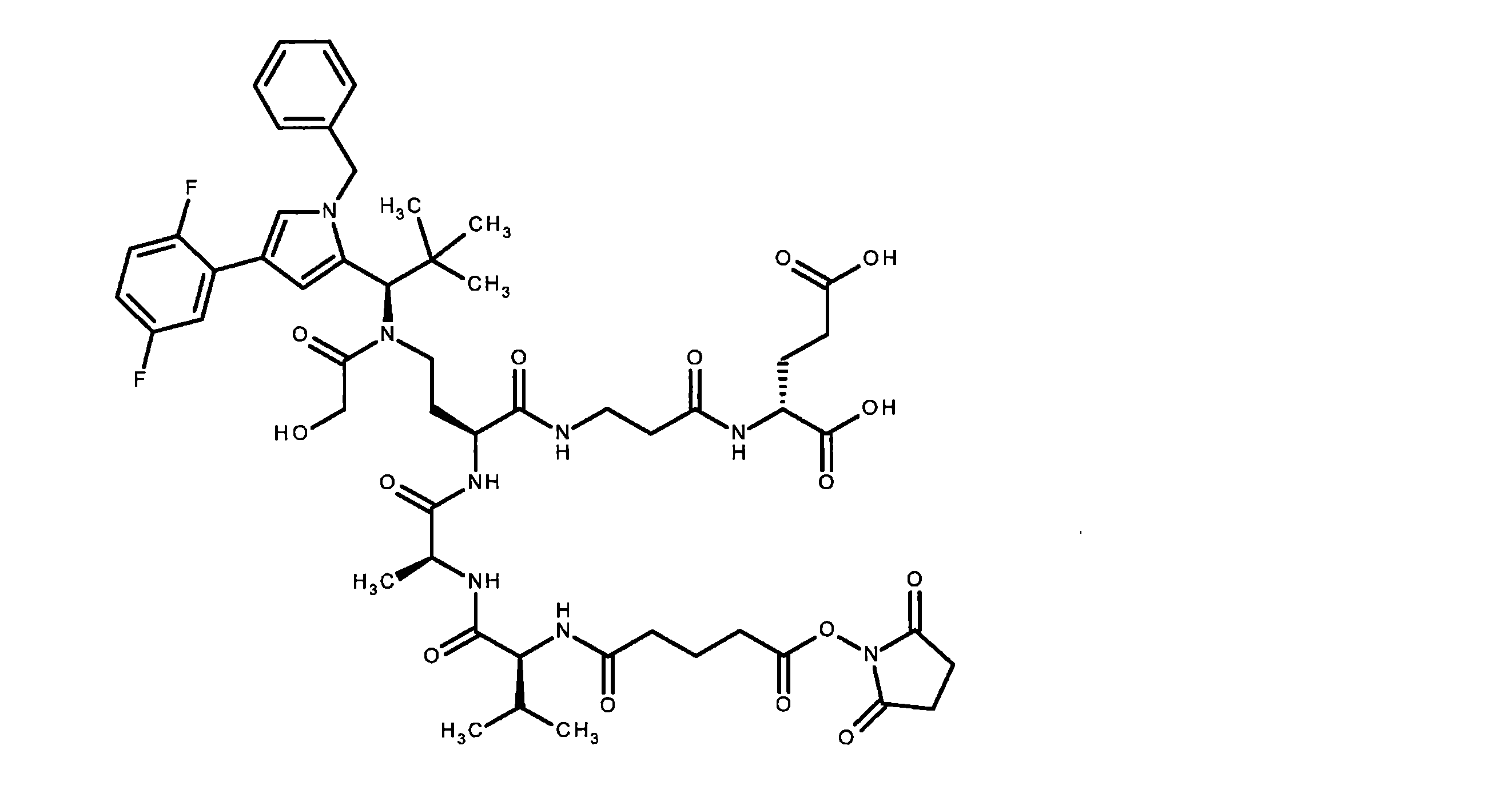
N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法1):Rt=0.93分;MS(ESIpos):m/z=1195[M+H]+。
N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-アラニル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法1):Rt=0.90分;MS(ESIneg):m/z=1181[M-H]-。
N-[(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)ヘキサノイル]-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法1):Rt=3.2分;MS(ESIpos):m/z=1177[M+H]+。
N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-アラニル-N-メチル-L-アラニル-N-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アラニンアミド
LC-MS(方法1):Rt=0.96分;MS(ESIpos):m/z=1152[M+H]+。
N-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-2-[(N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-バリル-L-アラニル)アミノ]ブタノイル}-β-アラニル-D-グルタミン酸
LC-MS(方法1):Rt=0.98分;MS(ESIpos):m/z=1095[M+H]+。
N-[(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-2-({N-[(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)アセチル]-L-バリル-L-アラニル}アミノ)ブタノイル]-β-アラニル-D-グルタミン酸
LC-MS(方法1):Rt=0.98分;MS(ESIpos):m/z=1021[M+H]+。
N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-ロイシンアミド
LC-MS(方法1):Rt=1.02分;MS(ESIpos):m/z=1194[M+H]+。
N-{5-[(2,5-ジオキソピロリジン-1-イル)オキシ]-5-オキソペンタノイル}-L-アラニル-N-メチル-L-α-アスパルチル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法1):Rt=0.89分;MS(ESIpos):m/z=1225[M+H]+。
N-(ブロモアセチル)-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-]-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法1):Rt=0.95分;MS(ESIpos):m/z=1104および1106[M+H]+。
N-(18-ブロモ-17-オキソ-4,7,10,13-テトラオキサ-16-アザオクタデカン-1-オイル)-L-アラニル-N-メチル-L-アラニル-N1-{(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-[(3-{[(1R)-1,3-ジカルボキシプロピル]アミノ}-3-オキソプロピル)アミノ]-1-オキソブタン-2-イル}-L-アスパルトアミド
LC-MS(方法8):Rt=4.06分;MS(ESI-pos):m/z=1353[M+H]+。
B-1.抗体作製の一般的方法
使用した抗体、例えばTPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574およびTPP-9580のタンパク質配列(アミノ酸配列)を、当業者に公知の方法によって対応するタンパク質をコードするDNA配列に変換し、一過性哺乳動物細胞培養に適した発現ベクターに挿入する(Tomら、Methods Express:Expression Systemsの第12章、Michael R.DysonおよびYves Durocher編、Scion Publishing Ltd、2007に記載されているように)。
抗体、例えばTPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574およびTPP-9580を、Tomら、Methods Express:Expression Systemsの第12章、Michael R.DysonおよびYves Durocher編、Scion Publishing Ltd、2007に記載されるように、一過性哺乳動物細胞培養で作製した。
抗体、例えばTPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574およびTPP-9580を、細胞培養物上清から得た。細胞上清を細胞の遠心分離によって清澄化した。次いで、細胞上清を、MabSelect Sure(GE Healthcare)クロマトグラフィーカラムでのアフィニティークロマトグラフィーによって精製した。この目的のために、カラムをDPBS pH7.4(Sigma/Aldrich)で平衡化し、細胞上清をアプライし、カラムを約10カラム容量のDPBS pH7.4+500mM塩化ナトリウムで洗浄した。抗体を50mM酢酸ナトリウムpH3.5+500mM塩化ナトリウムに溶出し、次いで、DPBS pH7.4中Superdex 200カラム(GE Healthcare)でゲル濾過クロマトグラフィーによってさらに精製した。
以下の抗体をカップリング反応に使用した:
実施例a:TPP-981セツキシマブ(抗EGFR AK)
実施例c:TPP-6013(抗CD123 AK)
TPP-8987(抗CD123 AK)
TPP-8988(抗CD123 AK)
TPP-9476(抗CD123 AK)
実施例h:TPP-8382(抗B7H3 AK)
実施例e:TPP-1015(抗Her2 AK)
実施例k:TPP-7006(抗TWEAKR AK)
TPP-7007(抗TWEAKR AK)
実施例x:TPP-9574(抗CXCR5 AK)
TPP-9580(抗CXCR5 AK)
カップリング反応は、通常、アルゴン下で実施した。
アルゴン下で、PBS緩衝液中2~7当量、好ましくは3当量のTCEP溶液(c約0.2~0.8mg/ml、好ましくは0.5mg/ml)を、PBS緩衝液中当の抗体20~200mg(c約5~15mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSOに溶解した2~20当量、好ましくは5~10当量のマレイミド前駆体化合物を添加した。より高いDARを達成するために、15~20当量を使用することも可能である。室温でさらに1.5時間~2時間撹拌した後、混合物を予めpH8に調整したPBS緩衝液で希釈した。次いで、この溶液を、PBS緩衝液pH8で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液pH8で溶出した。溶出液をPBS緩衝液pH8で2~7mg/mlの濃度に希釈した。この溶液をアルゴン下室温で一晩撹拌した。次いで、必要であれば、溶液をpH7.2に再緩衝化した。ADC溶液を超遠心分離によって濃縮し、PBS緩衝液(pH7.2)で再希釈し、次いで、場合により再び約10mg/mlの濃度に濃縮した。
実施例a:TPP-981セツキシマブ(部分還元)-S§1
実施例c:TPP-6013(抗CD123 AK)(部分還元)-S§1
TPP-8987(抗CD123 AK)(部分還元)-S§1
TPP-8988(抗CD123 AK)(部分還元)-S§1
TPP-9476(抗CD123 AK)(部分還元)-S§1
実施例e:TPP-1015(抗Her2 AK)(部分還元)-S§1
実施例h:TPP-8382(抗B7H3 AK)(部分還元)-S§1
実施例k:TPP-7006(抗TWEAKR)(部分還元)-S§1
TPP-7007(抗TWEAKR)(部分還元)-S§1
実施例x:TPP-9574(抗CXCR5 AK)(部分還元)-S§1
TPP-9580(抗CXCR5 AK)(部分還元)-S§1
(式中、
§1は、スクシンイミド基または任意の異性体加水分解開鎖スクシンアミドまたはそれから生じるアルキレン基との結合を表し、
Sは部分還元抗体のシステイン残基の硫黄原子を表す)。
以下の抗体をカップリング反応に使用した:
実施例a:TPP-981セツキシマブ(抗EGFR AK)
実施例c:TPP-6013(抗CD123 AK)
TPP-8987(抗CD123 AK)
TPP-8988(抗CD123 AK)
TPP-9476(抗CD123 AK)
実施例e:TPP-1015(抗Her2 AK)
実施例k:TPP-7006(抗TWEAKR AK)
TPP-7007(抗TWEAKR AK)
実施例x:TPP-9574(抗CXCR5 AK)
TPP-9580(抗CXCR5 AK)
カップリング反応は、通常、アルゴン下で実施した。
実施例a:TPP-981セツキシマブ(抗EGFR AK)-NH§2
実施例c:TPP-6013(抗CD123 AK)-NH§2
TPP-8987(抗CD123 AK)-NH§2
TPP-8988(抗CD123 AK)-NH§2
TPP-9476(抗CD123 AK)-NH§2
実施例e:TPP-1015(抗Her2 AK)-NH§2
実施例k:TPP-7006(抗TWEAKR AK)-NH§2
TPP-7007(抗TWEAKR AK)-NH§2
実施例x:TPP-9574(抗CXCR5 AK)-NH§2
TPP-9580(抗CXCR5 AK)-NH§2
(式中、
§2はカルボニル基との結合を表し、
NHは抗体のリジン残基の側鎖アミノ基を表す)。
反応後、場合によって、反応混合物を、例えば限外濾過によって濃縮し、次いで、例えばSephadex(登録商標)G-25カラムを使用してクロマトグラフィーによって脱塩および精製した。溶出を、例えば、リン酸緩衝生理食塩水(PBS)を用いて行った。次いで、溶液を滅菌濾過し、凍結させた。あるいは、コンジュゲートを凍結乾燥することができる。
脱グリコシル化および/または変性後の分子量決定に加えてタンパク質識別のために、トリプシン消化を行って、変性、還元および誘導体化後に、発見されたトリプシン性ペプチドを介したタンパク質の識別を確認した。
個々のコンジュゲート種の分子量の質量分析測定によって、リジン結合ADCの担毒体負荷の決定を行った。ここで、抗体コンジュゲートをまずPNGaseFで脱グリコシル化し、試料を酸性化し、HPLC分離/脱塩後、ESI-MicroTofQ(Bruker Daltonik)を用いた質量分析によって分析した。TIC(全イオンクロマトグラム)中のシグナル上の全てのスペクトルを加え、MaxEnt逆重畳積分に基づいて異なるコンジュゲート種の分子量を計算した。次いで、DAR(=薬物/抗体比)を、異なる種のシグナル積分後に計算した。この目的のために、担毒体数によって重み付けされた全ての種についての積分結果の合計を、全ての種について単純に重み付けされた積分結果の合計で割った。
カップリングが行われた後、結合剤が標的分子に結合する能力を確認した。当業者であれば、この目的のために使用することができる種々の方法に精通している;例えば、コンジュゲートの親和性を、ELISA技術または表面プラズモン共鳴分析(BIAcore(商標)測定)を用いて確認することができる。コンジュゲート濃度は、例えばタンパク質決定によって抗体コンジュゲートのための慣用的な方法を用いて当業者によって測定され得る(Doroninaら;Nature Biotechnol.2003;21:778~784およびPolsonら、Blood 2007;1102:616~623も参照)。
実施例M1
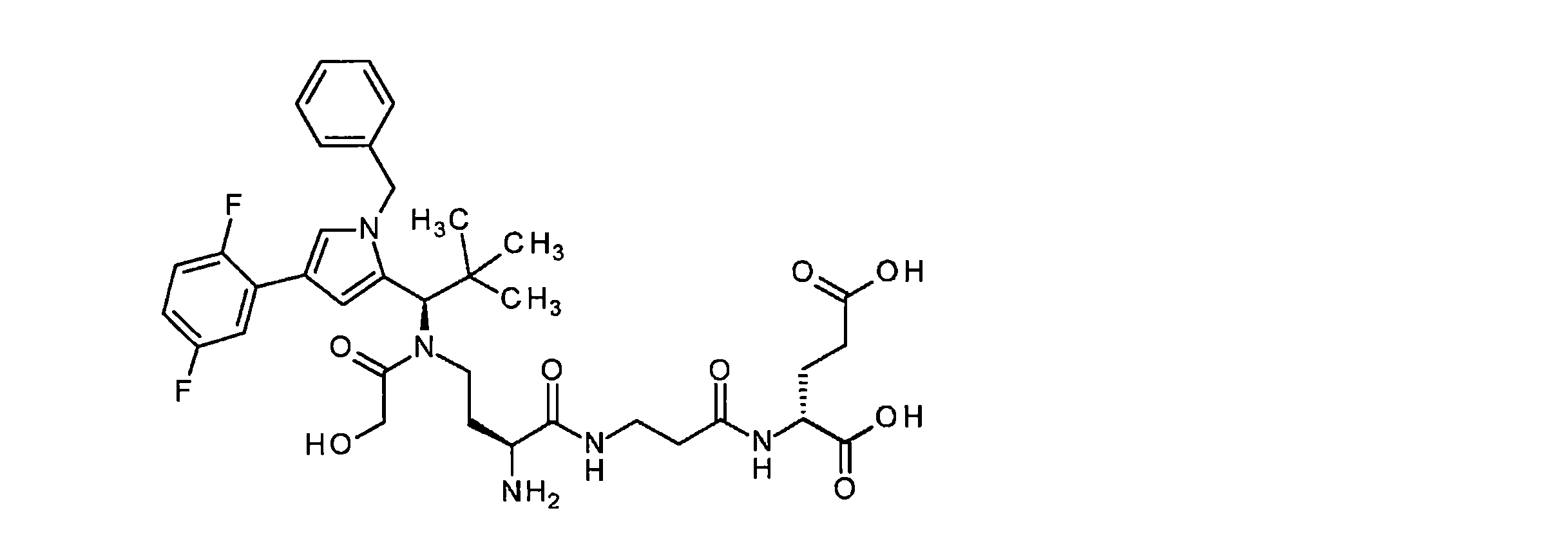
N-{(2S)-2-アミノ-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]ブタノイル}-β-アラニル-D-グルタミン酸
LC-MS(方法1):Rt=1.78分;MS(ESIpos):m/z=714[M+H]+。
マレイミド基を介して抗体のシステイン側鎖にカップリングした実施例の構造式に示されるADCは、リンカーおよびカップリング手順に応じて、主に各場合に示される開環または閉環形態で存在する。しかしながら、調製物は、少量のそれぞれの他の形態を含んでもよい。
アルゴン下、TCEP0.029mgのPBS緩衝液0.05ml中溶液を、PBS0.5ml中当の抗体5mg(c=10mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q1 0.26mg(0.00023mmol)を添加した。室温でさらに90分間撹拌した後、混合物を予めpH8に調整したPBS緩衝液で2.5ml容量に希釈し、次いで、PBS緩衝液pH8で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)を通過させ、PBS緩衝液pH8で溶出した。溶出液をアルゴン下室温で一晩撹拌した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
アルゴン下、TCEP0.172mgのPBS緩衝液0.3ml中溶液を、PBS3ml中当の抗体30mg(c=10mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO300μlに溶解した中間体Q1 1.57mg(0.0014mmol)を添加した。室温でさらに90分間撹拌した後、混合物を予めpH8に調整したPBS緩衝液で5ml容量に希釈し、次いで、PBS緩衝液pH8で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)を通過させ、PBS緩衝液pH8で溶出した。溶出液をPBS緩衝液pH8で7.5ml容量に希釈し、アルゴン下室温で一晩撹拌した。次いで、この溶液を、PBS緩衝液pH7.2で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液pH7.2で溶出した。次いで、溶出液を超遠心分離によって濃縮し、PBS緩衝液(pH7.2)で再希釈し、再濃縮し、再び滅菌濾過した。
アルゴン下で、DMSO50μlに溶解した5当量(0.2mg)の中間体Q2をPBS0.5ml中の当の抗体5mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下で、DMSO50μlに溶解した4当量(1mg)の中間体Q2をPBS緩衝液(pH7.2)3ml中の当の抗体30mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。次いで、混合物をPBS緩衝液(pH7.2)で5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈し、再濃縮し、再び滅菌濾過した。
アルゴン下で、DMSO250μlに溶解した2.5当量(1mg)の中間体Q2をPBS緩衝液(pH7.2)5ml中の当の抗体50mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。次いで、混合物をPBS緩衝液(pH7.2)で7.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈し、再濃縮し、再び滅菌濾過した。
アルゴン下で、DMSO7.5mlに溶解した4.5当量(36mg)の中間体Q2をPBS緩衝液(pH7.2)150ml中の当の抗体1000mgに添加した(c=6.7mg/ml)。
アルゴン下で、DMSO50μlに溶解した5当量(0.2mg)の中間体Q3をPBS0.5ml中の当の抗体5mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下で、DMSO50μlに溶解した4当量(1mg)の中間体Q3をPBS緩衝液(pH7.2)3ml中の当の抗体30mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。次いで、混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈し、再濃縮し、再び滅菌濾過した。
アルゴン下、TCEP0.029mgのPBS緩衝液0.05ml中溶液を、PBS緩衝液(pH7.2)0.4ml中当の抗体5mg(c=12.5mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q4 0.275mg(0.00023mmol)を添加した。室温でさらに90分間撹拌した後、反応物をPBS緩衝液で総容量2.5mlに希釈した。次いで、この溶液を、PBS緩衝液(pH7.2)で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液(pH7.2)で溶出した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
アルゴン下で、DMSO50μlに溶解した5当量(0.2mg)の中間体Q5をPBS0.5ml中の当の抗体5mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下で、DMSO50μlに溶解した5当量(0.18mg)の中間体Q6をPBS0.4ml中の当の抗体5mgに添加した(c=12.5mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下、TCEP0.029mgのPBS緩衝液0.05ml中溶液を、PBS0.4ml中当の抗体5mg(c=12.5mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q7 0.24mg(0.00023mmol)を添加した。室温でさらに90分間撹拌した後、混合物を予めpH8に調整したPBS緩衝液で2.5ml容量に希釈し、次いで、PBS緩衝液pH8で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)を通過させ、PBS緩衝液pH8で溶出した。溶出液をアルゴン下室温で一晩撹拌した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
アルゴン下で、DMSO50μlに溶解した5当量(0.2mg)の中間体Q8をPBS0.5ml中の当の抗体5mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下で、DMSO50μlに溶解した5当量(0.2mg)の中間体Q9をPBS0.5ml中の当の抗体5mgに添加した(c=10mg/ml)。室温で1時間撹拌した後、再び同量を添加し、混合物を室温でさらに1時間撹拌した。その後、反応混合物をPBS緩衝液(pH7.2)で2.5mlに希釈し、Sephadexカラムで精製し、次いで、超遠心分離によって濃縮し、PBS(pH7.2)で再希釈した。
アルゴン下、TCEP0.029mgのPBS緩衝液0.05ml中溶液を、PBS緩衝液(pH7.2)0.5ml中当の抗体5mg(c=10mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q10 0.295mg(0.00023mmol)を添加した。室温でさらに20時間撹拌した後、反応物をPBS緩衝液で総容量2.5mlに希釈した。次いで、この溶液を、PBS緩衝液(pH7.2)で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液(pH7.2)で溶出した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
アルゴン下、TCEP0.057mgのPBS緩衝液0.05ml中溶液を、PBS緩衝液(pH7.2)0.5ml中当の抗体5mg(c=10mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q10 0.59mg(0.00053mmol)を添加した。室温でさらに20時間撹拌した後、反応物をPBS緩衝液で総容量2.5mlに希釈した。次いで、この溶液を、PBS緩衝液(pH7.2)で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液(pH7.2)で溶出した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
アルゴン下、TCEP0.029mgのPBS緩衝液0.05ml中溶液を、PBS緩衝液(pH7.2)0.4ml中当の抗体5mg(c=12.5mg/ml)に添加した。混合物を室温で30分間撹拌し、次いで、DMSO50μlに溶解した中間体Q11 0.32mg(0.00023mmol)を添加した。室温でさらに20時間撹拌した後、反応物をPBS緩衝液で総容量2.5mlに希釈した。次いで、この溶液を、PBS緩衝液(pH7.2)で平衡化したPD10カラム(Sephadex(登録商標)G-25、GE Healthcare)にアプライし、PBS緩衝液(pH7.2)で溶出した。これに続いて超遠心分離による濃縮およびPBS緩衝液(pH7.2)による再希釈を行った。
参照実施例R1:
N-(3-アミノプロピル)-N-{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}-2-ヒドロキシアセトアミド
本発明による化合物の生物学的活性を以下に記載されるアッセイで示すことができる:
a.C-1a ADCの細胞傷害性効果の決定
ADCの細胞傷害効果の分析を、種々の細胞株を用いて行った:
NCI-H292:ヒト粘表皮肺癌細胞、ATCC-CRL-1848、標準培地:RPMI 1640(Biochrom;番号FG1215、stab.グルタミン)+10%FCS(Sigma;番号F2442)、TWEAKR陽性;EGFR陽性。
細胞を、C-1に指定されている増殖培地を用いて標準的な方法によって培養した。トリプシン(0.05%)およびEDTA(0.02%)のPBS(Biochrom AG番号L2143)中溶液で細胞を剥離し、ペレット化し、培養培地に再懸濁し、計数し、白色底の96ウェル培養プレート(Costar番号3610)に播種し(75μl/ウェルで、1ウェルあたり以下の細胞数である:NCI-H292:2500細胞/ウェル、BxPC3 2500細胞/ウェル、LoVo 3000細胞/ウェル)、37℃および5%二酸化炭素でインキュベーター中でインキュベートすることによって、試験を行った。懸濁細胞を計数し、白色底を有する96ウェル培養プレート(Costar番号3610)(75μl/ウェル、1ウェル当たり以下の細胞数:Rec-1:3000細胞/ウェル、HBL-1:6000細胞/ウェル)に播種した。24時間後、抗体薬物コンジュゲートを、25μlの培養培地(4倍濃縮)中細胞に添加して、細胞上3×10-7M~3×10-11Mの最終抗体薬物コンジュゲート濃度を得た(3連)。次いで、細胞を37℃および5%二酸化炭素のインキュベーター内でインキュベートした。並列プレート上で、薬物処理開始時(0日目)の細胞活性を、Cell Titer Glow(CTG)発光細胞生存率アッセイ(Promega番号G7573および番号G7571)を使用して決定した。この目的のために、1細胞バッチ当たり100μlの基質を添加し、次いで、プレートをアルミ箔で覆い、プレートシェーカー上180rpmで2分間振盪し、実験室ベンチに8分間放置し、次いで、ルミノメーター(Victor X2、Perkin Elmer)を使用して測定した。基質は、その強度が細胞の生存率に正比例する発光シグナルを生成する生細胞中のATP含量を検出する。次いで、抗体薬物コンジュゲートとの72時間のインキュベーション後、これらの細胞の生存率も、上記のCell Titer Glow発光細胞生存率アッセイを使用して決定した。測定されたデータから、増殖阻害のIC50を、0日目と比較して、DRC(用量反応曲線)分析スプレッドシートおよび4パラメータ当てはめを使用して計算した。DRC分析スプレッドシートは、IDBS E-WorkBook Suiteプラットフォーム(IDBS:ID Business Solutions Ltd.、Guildford、英国)でBayer Pharma AGおよびBayer Business Servicesによって開発されたバイオブックスプレッドシートである。
細胞を、C-1に指定されている増殖培地を用いて標準的な方法によって培養した。細胞をAccutase(登録商標)のPBS中溶液(Biochrom AG製 番号L2143)で剥離し、ペレット化し、培養培地に再懸濁し、計数し、白色底の96ウェル培養プレート(Costar製 番号3610)に播種することによって(NCI H292:2500細胞/ウェル;SK-HEP-1:1000細胞/ウェル;KPL-4:1200細胞/ウェル;総容量100μl)、試験を行った。次いで、細胞を37℃および5%二酸化炭素のインキュベーター内でインキュベートした。48時間後、培地を交換した。次いで、10-5M~10-13Mの濃度の培養培地10μl中の抗体薬物コンジュゲートを細胞にピペットで分注し(3連で)、次いで、アッセイを37℃および5%二酸化炭素のインキュベーター内でインキュベートした。懸濁細胞を計数し、白色底の96ウェルプレート(Costar製 番号3610)(番号3610)に播種した(総容量100μl中MOLM-13:2000細胞/ウェル;NB4:7000細胞/ウェル;MV-4-11:5000細胞/ウェル)。37℃および5%二酸化炭素で6時間インキュベートした後、培地を交換し、抗体-薬物コンジュゲートまたは代謝産物を、90μl中細胞に(3連)、10-5M~10-13Mの濃度で培養培地10μlにピペットによって添加した。バッチをインキュベーター中、37℃および5%二酸化炭素でインキュベートした。96時間後、MTTアッセイ(ATCC、Manassas、Virginia、米国、カタログ番号30-1010K)を用いて細胞増殖を検出した。この目的のために、MTT試薬を細胞と共に4時間インキュベートし、引き続いて界面活性剤を添加して細胞を一晩溶解させた。形成された色素を570nmで検出した(Infinite M1000 pro、Tecan)。測定したデータを使用して、DRC(用量応答曲線)を用いて増殖阻害のIC50を計算した。試験物質で処理しなかったが、それ以外は同様に処理した細胞の増殖を100%の数値として定義した。
ヒトキネシンスピンドルタンパク質KSP/Eg5(tebu-bio/Cytoskeleton Inc、番号027EG01-XL)のモータードメインを、10nMの濃度で、50μg/mlのタキソール(Sigma番号T7191-5MG)で安定化した微小管(ウシまたはブタ、tebu-bio/Cytoskeleton Inc)と共に、15mM PIPES、pH6.8(5mM MgCl2および10mM DTT、Sigma)中室温で5分間インキュベートした。新たに調製した混合物を、384MTP(Corning製)に等分した。次いで、1.0×10-6M~1.0×10-13Mの濃度で試験する阻害剤およびATP(最終濃度500μM、Sigma)を添加した。インキュベーションを室温で2時間行った。マラカイトグリーン(Biomol)を用いて形成された無機リン酸塩を検出することによってATPアーゼ活性を検出した。試薬の添加後、アッセイを室温で50分間インキュベートした後、620nmの波長での吸収を検出した。使用した陽性対照は、モナストロール(Sigma、M8515-1mg)およびイスピネシブ(AdooQ Bioscience A10486)であった。用量-活性曲線の個々のデータは、8倍の測定値である。IC50値は、2つの独立した実験の平均である。100%対照は阻害剤で処理しなかった試料とした。
a:カテプシンBアッセイ
試験する全てのカテプシンB切断可能プロドラッグについて、混合物を微小反応容器(0.5ml、エッペンドルフ製)で作製した。ここで使用した酵素はヒト肝組織から得た。2μgのカテプシンB(Sigma C8571 25μg)を最初に装入し、200μlの50mMリン酸Na緩衝液、pH6.0、2mM DTTで総容量200μlにした。次いで、試験する基質溶液50μlをピペットで入れた。混合物をサーモブロック(Thermo Fisher Scientific製)中、40℃で300rpmで一定撹拌しながらインキュベートした。酵素反応を速度論的に制御した。このために、10μlの試料を様々な時間に採取した。酵素反応を停止させるために、採取した試料を直ちに20μlの氷冷メタノールと混和し、次いで、-20℃で凍結した。サンプリングのために選択した時間は、10分後、2時間後、4時間後および24時間後であった。試料をRP-HPLC分析(逆相HPLC、Agilent Technologies 1200シリーズ)によって調べた。放出された担毒体の決定によって、酵素反応の半減期t1/2の決定が可能になった。
組換えヒト酵素を用いてレグマインアッセイを行った。レグマイン酵素溶液(カタログ番号2199-CY、R&D Systems)を50mM酢酸ナトリウム緩衝液/100mM NaCl、pH4.0に所望の濃度に希釈し、37℃で2時間プレインキュベートした。次いで、rhレグマインを、50mM MES緩衝液、250mM NaCl、pH5.0中1ng/μlの最終濃度に調整した。試験する全てのレグマイン切断可能プロドラッグについて、混合物を微小反応容器(0.5ml、エッペンドルフ製)で作製した。このために、基質溶液を50mM MES緩衝液、250mM NaCl、pH5.0で所望の濃度(2倍濃度)に調整した。酵素反応の速度論的測定のために、250μlのレグマイン溶液を最初に装入し、250μlの基質溶液を添加することによって酵素反応を開始した(最終濃度:単一濃度;3μM)。種々の時点で、50μlの試料を採取した。直ちに、酵素反応を停止させるために100μlの氷冷メタノールをこの試料に添加、次いで、試料を-20℃で凍結した。サンプリングのために選択した時間は、0.5時間後、1時間後、3時間後および24時間後であった。次いで、試料をRP-HPLC分析およびLC-MS分析によって分析した。放出された担毒体の決定によって、酵素反応の半減期t1/2の決定が可能になった。
N-(ピリジン-4-イルアセチル)-L-アラニル-L-アラニル-N1-[(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-(メチルアミノ)-1-オキソブタン-2-イル]-L-アスパルトアミド
LC-MS(方法1):Rt=0.86分;MS(ESIpos):m/z=902[M+H]+。
N-(ピリジン-4-イルアセチル)-L-アラニル-N-メチル-L-アラニル-N1-[(2S)-4-[{(1R)-1-[1-ベンジル-4-(2,5-ジフルオロフェニル)-1H-ピロール-2-イル]-2,2-ジメチルプロピル}(グリコロイル)アミノ]-1-(メチルアミノ)-1-オキソブタン-2-イル]-L-アスパルトアミド
LC-MS(方法1):Rt=0.83分;MS(ESIpos):m/z=916[M+H]+。
内在化は、抗体薬物コンジュゲート(ADC)を介した抗原発現がん細胞における細胞傷害性ペイロードの特異的かつ効率的な提供を可能にする重要な過程である。この過程を、特異的抗体の蛍光標識およびアイソタイプ対照抗体を介して監視する。まず、蛍光色素を抗体のリジンにコンジュゲートした。コンジュゲーションは、2倍~10倍モル過剰のCypHer 5EモノNHSエステル(バッチ357392、GE Healthcare)を用いてpH8.3で行った。カップリング後、反応混合物をゲルクロマトグラフィー(Zeba Spin Desalting Columns、40K、Thermo Scientific、番号87768;溶出緩衝液:ダルベッコPBS、Sigma-Aldrich、番号D8537)によって精製して、過剰の色素を除去し、pHを調整した。タンパク質溶液をVIVASPIN 500カラム(Sartorius stedim biotec)を用いて濃縮した。抗体の色素負荷を、分光光度分析(NanoDrop製)およびその後の計算(D/P=A色素εタンパク質:(A280-0.16A色素)ε色素)によって決定した。
蛍光色素のカップリングを、C2に記載されるように行った。調査する抗原を造血懸濁細胞によって発現させる;結果として、内在化をFACSベースの内在化アッセイで調査した。
リンカーのおかげで、抗体-薬物コンジュゲートの活性代謝産物がリソソーム分解によって産生される。したがって、内在化が起こった後の細胞内輸送は本質的に重要である。リソソームオルガネラに特異的な標識(例えば、表面分子または小型GTPアーゼ)を用いた抗体の共局在化に関する研究により、所望のプロファイルを有する抗体の選択が可能になる。この目的のために、全量100μlの標的陽性細胞(5×104/ウェル)を96-MTP(Greiner bio-one、CELLSTAR、650 180、U底)に播種した。CypHer5E標識抗標的抗体(最終濃度20μg/ml)を添加した後、バッチ(1時点あたり複製)をインキュベーター(5%CO2)内で37℃で30分間、2時間および6時間インキュベートした。選択されたインキュベーション時間の終了の30分前に、リソソーム特異的標識を試験するバッチに添加した。CytoPainter LysoGreen指示薬(最終濃度1:2000;abcam、ab176826)を用いて、リソソームを染色した。インキュベーション後、氷冷FACS緩衝液200μl(ダルベッコPBS、Sigma-Aldrich、番号D8537+3%FBS熱不活性化FBS、Gibco、番号10500-064)を添加し、細胞懸濁液を400×gおよび4℃で5分間遠心分離した。細胞ペレットを氷冷FACS緩衝液300μlに再懸濁し、再度遠心分離した(4分間、4℃で400×g)。遠心分離後、上清を捨て、細胞ペレットを氷冷FACS緩衝液30μlに溶解した。次いで、試料を直ちにFACS/画像分析(FlowSight amnis、Millipore)に供した。特別なソフトウェア(共局在ソフトウェアIDEAS Application v6.1)を用いて共局在を評価した。表3は、抗CD123抗体について例示的な方法でこのアッセイからの結果を要約している。
Caco-2細胞を用いるフラックスアッセイでのインビトロ試験によって、物質の細胞透過性を調査することができる[M.D.TroutmanおよびD.R.Thakker、Pharm.Res.20(8)、1210~1224(2003)]。この目的のために、細胞を24ウェルフィルタープレート上で15~16日間培養した。透過性を測定するために、それぞれの試験物質をHEPES緩衝液中で細胞に頂端に(A)または基底に(B)適用し、2時間インキュベートした。0時間後および2時間後、試料をシスおよびトランス区画から採取した。試料を逆相カラムを用いてHPLC(Agilent 1200、Boblingen、ドイツ)によって分離した。HPLCシステムを、ターボイオンスプレーインターフェースを介してトリプル四重極質量分析計API 4000(AB SCIEX Deutschland GmbH、Darmstadt、ドイツ)に連結した。透過性を、Schwabら[D.Schwabら、J.Med.Chem.46、1716~1725(2003)]によって公開された式を用いて計算したPapp値に基づいて評価した。Papp(B-A)とPapp(A-B)の比(流出比)が2超または0.5未満である場合、物質が能動的に輸送されたと分類した。
多くの腫瘍細胞は薬物のためにトランスポータータンパク質を発現し、これはしばしば細胞増殖抑制剤に対する耐性の発達を伴う。したがって、例えば、P-糖タンパク質(P-gp)またはBCRPなどの、このようなトランスポータータンパク質の基質ではない物質は、改善された活性プロファイルを示すことができるだろう。
5mg/kgの実施例2c-9476(DAR6.3)および実施例2c-9476(DAR3.4)の雄ウィスターラットへの静脈内投与後に、ADCの血漿濃度をELISAによって測定し、クリアランス(CL)、曲線下面積(AUC)および半減期(t1/2)などの薬物動態パラメータを計算した。
ADCの抗体部分を、血漿試料および腫瘍溶解液中の全IgG濃度として、リガンド結合アッセイ(ELISA)を用いて測定した。ここでは、サンドイッチELISAフォーマットを使用した。このELISAは、血漿および腫瘍試料における測定のために適格であり、有効であった。ELISAプレートを抗ヒトヤギIgG Fc抗体でコーティングした。試料とのインキュベーションの後、プレートを洗浄し、サル抗ヒトIgG(H+L)抗体および西洋ワサビペルオキシダーゼ(HRP)の検出コンジュゲートとインキュベートした。さらなる洗浄ステップの後、HRP基質をOPDに添加し、発色を490nmでの吸収を介して監視した。既知のIgG濃度を有する標準試料を、4パラメータ方程式を用いて当てはめた。定量下限(LLOQ)および上限(ULOQ)内で、未知の濃度を内挿によって決定した。
方法の説明:
イムノコンジュゲート(immunoconjugate)による内在化試験を行って、細胞内で形成される代謝産物を分析する。この目的のために、ヒト肺腫瘍細胞NCI H292(3×105個/ウェル)を6ウェルプレートに播種し、一晩(37℃、5%CO2)インキュベートする。細胞を、10μg/ml(66nM)の試験するADCで処理する。内在化を、37℃および5%CO2で行った。細胞試料を種々の時点(0、4、24、48、72時間)でさらなる分析のために採取する。まず、上清(約5ml)を収穫し、遠心分離(2分間、室温、1000rpm、Heraeus Variofuge 3.0R)後、-80℃で保存する。細胞をPBSで洗浄し、Accutase(登録商標)で剥離し、細胞数を決定する。さらなる洗浄後、規定の数の細胞(2×105個)を溶解緩衝液100ml(Mammalian Cell Lysis Kit(Sigma MCL1))で処理し、連続振盪(Thermomixer、15分間、4℃、650rpm)しながら、Protein LoBindチューブ(Eppendorfカタログ番号0030 108.116)中でインキュベートする。インキュベーション後、溶解液を遠心分離し(10分間、4℃、12000g、eppendorf 5415R)、上清を収穫する。得られた上清を-80℃で保存する。次いで、全ての試料を以下のように分析する。
3~30mg/kgの様々なADCの静脈内投与後に、ADCおよび生じる任意の代謝産物の血漿および腫瘍濃度を測定することができ、クリアランス(CL)、曲線下面積(AUC)および半減期(t1/2)などの薬物動態パラメータを計算することができる。
血漿、腫瘍、肝臓および腎臓中の化合物の分析は、トリプル四重極質量分析計(MS)に連結された高圧液体クロマトグラフィー(HPLC)によって、一般的にメタノールによるタンパク質の沈殿後に行われる。
本発明によるコンジュゲートの活性を、例えば異種移植片モデルを用いてインビボで試験した。当業者であれば、本発明による化合物の活性を試験することを可能にする先行技術の方法に精通している(例えば、国際公開第2005/081711号パンフレット;Polsonら、Cancer Res.2009年3月15日;69(6):2358-64参照)。この目的のために、結合剤の標的分子を発現する腫瘍細胞株をげっ歯類(例えばマウス)に接種した。次いで、本発明によるコンジュゲート、アイソタイプ抗体対照コンジュゲート、対照抗体または等張食塩水を接種動物に投与した。投与を2回以上行った。数日のインキュベーション期間後、コンジュゲート処置動物と対照群を比較することによって、腫瘍サイズを決定した。コンジュゲート処置動物はより小さい腫瘍サイズを示した。
抗体-薬物コンジュゲートの抗原を発現するヒト腫瘍細胞を、免疫抑制マウス、例えばNMRiヌードマウスまたはSCIDマウスの側腹部に皮下接種する。100万~1000万個の細胞を細胞培養液から剥離し、遠心分離し、培地または培地/matrigelに再懸濁する。細胞懸濁液をマウスの皮下に注射する。
腫瘍細胞(例えば、NCI-H292、REC-1、MOLM-13およびMV-4-11)を雌NMRIヌードマウス(Janvier)の側腹部に皮下接種する。約40mm2の腫瘍サイズで、抗体-薬物コンジュゲートを用いて静脈内処置を行う。処置後、適切ならば腫瘍増殖の監視を続ける。
Claims (9)
- CXCR5に結合する抗体又は抗原結合抗体フラグメントであって、
配列番号92によって示される重鎖の可変CDR1配列、配列番号93によって示される重鎖の可変CDR2配列、および配列番号94によって示される重鎖の可変CDR3配列を含む可変重鎖、ならびに配列番号96によって示される軽鎖の可変CDR1配列、配列番号97によって示される軽鎖の可変CDR2配列、および配列番号98によって示される軽鎖の可変CDR3配列を含む可変軽鎖を含む、抗体又は抗原結合抗体フラグメント。 - 可変重鎖が配列番号91を含む、請求項1に記載の抗体又は抗原結合抗体フラグメント。
- 可変軽鎖が配列番号95を含む、請求項1又は2に記載の抗体又は抗原結合抗体フラグメント。
- 配列番号99を含む重鎖を含む、請求項1から3のいずれか一項に記載の抗体又は抗原結合抗体フラグメント。
- 配列番号100を含む軽鎖を含む、請求項1から4のいずれか一項に記載の抗体又は抗原結合抗体フラグメント。
- CXCR5発現に関連する疾患の治療のための医薬であって、請求項1から5のいずれか一項に記載の抗体又は抗原結合抗体フラグメントを含む医薬。
- 請求項1から5のいずれか一項に記載の抗体又は抗原結合抗体フラグメントと、化学療法剤とを含む、コンジュゲート。
- 化学療法剤がキネシンスピンドルタンパク質の阻害剤を含む、請求項7に記載のコンジュゲート。
- CXCR5発現に関連する疾患の治療のための医薬であって、請求項7又は8に記載のコンジュゲートを含む医薬。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16205868 | 2016-12-21 | ||
| EP16205868.9 | 2016-12-21 | ||
| JP2019533395A JP7066714B2 (ja) | 2016-12-21 | 2017-12-14 | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) |
| PCT/EP2017/082789 WO2018114578A1 (de) | 2016-12-21 | 2017-12-14 | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019533395A Division JP7066714B2 (ja) | 2016-12-21 | 2017-12-14 | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022093432A JP2022093432A (ja) | 2022-06-23 |
| JP7307231B2 true JP7307231B2 (ja) | 2023-07-11 |
Family
ID=57614197
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019533395A Active JP7066714B2 (ja) | 2016-12-21 | 2017-12-14 | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) |
| JP2022072343A Active JP7307231B2 (ja) | 2016-12-21 | 2022-04-26 | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019533395A Active JP7066714B2 (ja) | 2016-12-21 | 2017-12-14 | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) |
Country Status (14)
| Country | Link |
|---|---|
| US (3) | US11660351B2 (ja) |
| EP (1) | EP3558388A1 (ja) |
| JP (2) | JP7066714B2 (ja) |
| KR (3) | KR102556826B1 (ja) |
| CN (2) | CN110312534B (ja) |
| AR (1) | AR110418A1 (ja) |
| AU (3) | AU2017380871C1 (ja) |
| CA (1) | CA3047489A1 (ja) |
| IL (3) | IL291308B2 (ja) |
| MX (3) | MX2019007641A (ja) |
| PE (1) | PE20191235A1 (ja) |
| RU (1) | RU2761390C2 (ja) |
| TW (2) | TWI781125B (ja) |
| WO (1) | WO2018114578A1 (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016207089A1 (de) | 2015-06-22 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) und binder-prodrug-konjugate (apdcs) mit enzymatisch spaltbaren gruppen |
| US10973923B2 (en) | 2015-06-23 | 2021-04-13 | Bayer Pharma Aktiengesellschaft | Site specific homogeneous with KSP inhibitors |
| CA2990398A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-cd123-antibodies |
| KR20180123047A (ko) | 2016-03-24 | 2018-11-14 | 바이엘 파마 악티엔게젤샤프트 | 효소적으로 절단가능한 기를 갖는 세포독성 활성제의 전구약물 |
| WO2017216028A1 (en) | 2016-06-15 | 2017-12-21 | Bayer Pharma Aktiengesellschaft | Specific antibody-drug-conjugates (adcs) with ksp inhibitors and anti-cd123-antibodies |
| US12059472B2 (en) | 2016-12-21 | 2024-08-13 | Bayer Aktiengesellschaft | Prodrugs of cytotoxic active agents having enzymatically cleavable groups |
| WO2018114578A1 (de) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| CA3047522A1 (en) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Specific antibody drug conjugates (adcs) having ksp inhibitors |
| EP3658172A4 (en) | 2017-07-25 | 2021-05-05 | TrueBinding, Inc. | TREATING CANCER BY BLOCKING THE INTERACTION OF TIM-3 AND HIS LIGAND |
| KR102804751B1 (ko) * | 2017-08-23 | 2025-05-13 | 막스-델부뤽-센트럼 퓌어 몰레쿨라레 메디친 인 데어 헬름홀츠-게마인샤프트 | Cxcr5에 결합하는 키메라 항원 수용체 및 car-t 세포 |
| WO2019243159A1 (de) * | 2018-06-18 | 2019-12-26 | Bayer Aktiengesellschaft | Gegen cxcr5 gerichtete binder-wirkstoff-konjugate mit enzymatisch spaltbaren linkern und verbessertem wirkungsprofil |
| CN120058944A (zh) | 2019-01-30 | 2025-05-30 | 真和制药有限公司 | 抗gal3抗体及其用途 |
| MX2022014786A (es) | 2020-05-26 | 2023-01-16 | Truebinding Inc | Metodos para tratar enfermedades inflamatorias mediante el bloqueo de galectina-3. |
| WO2022175595A1 (en) * | 2021-02-16 | 2022-08-25 | Glykos Finland Oy | Linker-payloads and conjugates thereof |
| TW202320857A (zh) | 2021-07-06 | 2023-06-01 | 美商普方生物製藥美國公司 | 連接子、藥物連接子及其結合物及其使用方法 |
| WO2024105205A1 (en) | 2022-11-17 | 2024-05-23 | Bayer Aktiengesellschaft | Antibody-drug conjugates (a2dcs) with enzymatically cleavable groups |
| WO2025027529A1 (en) | 2023-07-31 | 2025-02-06 | Advesya | Anti-il-1rap antibody drug conjugates and methods of use thereof |
| TW202530255A (zh) | 2023-12-15 | 2025-08-01 | 法商亞維西亞有限公司 | 抗il-1rap結合結構域及其抗體-藥物偶聯物 |
| WO2025149667A1 (en) | 2024-01-12 | 2025-07-17 | Pheon Therapeutics Ltd | Antibody drug conjugates and uses thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010537636A (ja) | 2007-08-29 | 2010-12-09 | サノフィ−アベンティス | ヒト化抗cxcr5抗体、その誘導体及びそれらの使用 |
| WO2012010582A1 (en) | 2010-07-21 | 2012-01-26 | Roche Glycart Ag | Anti-cxcr5 antibodies and methods of use |
| JP2016524595A (ja) | 2013-05-02 | 2016-08-18 | アレス トレーディング ソシエテ アノニム | Cxcr5に対するモノクローナル抗体 |
Family Cites Families (149)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CU22545A1 (es) | 1994-11-18 | 1999-03-31 | Centro Inmunologia Molecular | Obtención de un anticuerpo quimérico y humanizado contra el receptor del factor de crecimiento epidérmico para uso diagnóstico y terapéutico |
| US5179017A (en) | 1980-02-25 | 1993-01-12 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4634665A (en) | 1980-02-25 | 1987-01-06 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4399216A (en) | 1980-02-25 | 1983-08-16 | The Trustees Of Columbia University | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4714681A (en) | 1981-07-01 | 1987-12-22 | The Board Of Reagents, The University Of Texas System Cancer Center | Quadroma cells and trioma cells and methods for the production of same |
| US4474893A (en) | 1981-07-01 | 1984-10-02 | The University of Texas System Cancer Center | Recombinant monoclonal antibodies |
| US4510245A (en) | 1982-11-18 | 1985-04-09 | Chiron Corporation | Adenovirus promoter system |
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US5168062A (en) | 1985-01-30 | 1992-12-01 | University Of Iowa Research Foundation | Transfer vectors and microorganisms containing human cytomegalovirus immediate-early promoter-regulatory DNA sequence |
| US4968615A (en) | 1985-12-18 | 1990-11-06 | Ciba-Geigy Corporation | Deoxyribonucleic acid segment from a virus |
| DE8808645U1 (de) | 1988-07-06 | 1988-08-25 | Hofer, Daniel, 7730 Villingen-Schwenningen | Anzeigeeinrichtung für Feuerlöscher |
| US4925648A (en) | 1988-07-29 | 1990-05-15 | Immunomedics, Inc. | Detection and treatment of infectious and inflammatory lesions |
| US5601819A (en) | 1988-08-11 | 1997-02-11 | The General Hospital Corporation | Bispecific antibodies for selective immune regulation and for selective immune cell binding |
| ES2096590T3 (es) | 1989-06-29 | 1997-03-16 | Medarex Inc | Reactivos biespecificos para la terapia del sida. |
| DK0595798T3 (da) | 1989-10-20 | 1999-09-27 | Medarex Inc | Bispecifikke heteroantistoffer med dobbelte effektorfunktioner |
| US5270163A (en) | 1990-06-11 | 1993-12-14 | University Research Corporation | Methods for identifying nucleic acid ligands |
| CA2093022C (en) | 1990-10-05 | 2005-02-22 | Michael W. Fanger | Targeted immunostimulation with bispecific reagents |
| EP0557300B1 (en) | 1990-10-29 | 1997-11-19 | Chiron Corporation | Bispecific antibodies, method of production, and uses thereof |
| DE69233153T2 (de) | 1991-03-06 | 2004-05-27 | Merck Patent Gmbh | Humanisierte monoklonale antikörper |
| WO1992019973A1 (en) | 1991-04-26 | 1992-11-12 | Surface Active Limited | Novel antibodies, and methods for their use |
| ES2193143T3 (es) | 1992-03-05 | 2003-11-01 | Univ Texas | Uso de inmunoconjugados para la diagnosis y/o terapia de tumores vascularizaos. |
| ATE188874T1 (de) | 1992-08-18 | 2000-02-15 | Centro Inmunologia Molecular | Monoklonale antikörper gegen den epidermalen wachstumsfaktorrezeptor, zellen und verfahren zur ihrer herstellung und sie erhaltende zusammensetzungen |
| DE69531187T2 (de) | 1994-12-20 | 2004-04-22 | Merck Patent Gmbh | Monoklonaler Antikörper gegen das Alpha-V-Integrin |
| DK1143006T3 (da) | 1995-08-18 | 2008-07-14 | Morphosys Ip Gmbh | Vektorer/DNA-sekvenser fra humane kombinatoriske antistofbiblioteker |
| WO1997024373A1 (en) | 1995-12-29 | 1997-07-10 | Medvet Science Pty. Limited | Monoclonal antibody antagonists to haemopoietic growth factors |
| AU725583B2 (en) | 1996-03-25 | 2000-10-12 | E. R. Squibb & Sons, L.L.C. | Monoclonal antibodies specific for the extracellular domain of prostate specific membrane antigen |
| US6150508A (en) | 1996-03-25 | 2000-11-21 | Northwest Biotherapeutics, Inc. | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen |
| NZ517331A (en) | 1999-07-29 | 2004-02-27 | Medarex Inc | Human monoclonal antibodies to prostate specific membrane antigen and a transgenic mouse to produce the antibody |
| SK12232002A3 (sk) | 2000-02-25 | 2003-03-04 | The Government Of The United States, As Represented By The | Anti-ERGFRvIII scFv so zlepšenou cytotoxicitou a výťažkom, imunotoxíny a spôsoby ich použitia |
| JP2003533987A (ja) | 2000-05-19 | 2003-11-18 | イス ケミカル カンパニー リミテッド | 表皮成長因子収容体に対するヒト化抗体 |
| US6884446B1 (en) | 2000-07-27 | 2005-04-26 | Red Arrow Products Co., Llc | Article for browning and flavoring foodstuffs |
| US7288390B2 (en) | 2000-08-07 | 2007-10-30 | Centocor, Inc. | Anti-dual integrin antibodies, compositions, methods and uses |
| AUPR395801A0 (en) | 2001-03-26 | 2001-04-26 | Austin Research Institute, The | Antibodies against cancer |
| HUP0501113A3 (en) | 2001-04-26 | 2007-12-28 | Biogen Idec Inc | Cripto blocking antibodies and uses thereof |
| PT1392359E (pt) | 2001-05-11 | 2010-01-27 | Ludwig Inst For Cancer Res Ltd | Proteínas de ligação específica e suas utilizações |
| US7595378B2 (en) | 2001-06-13 | 2009-09-29 | Genmab A/S | Human monoclonal antibodies to epidermal growth factor receptor (EGFR) |
| CN100497389C (zh) | 2001-06-13 | 2009-06-10 | 根马布股份公司 | 表皮生长因子受体(egfr)的人单克隆抗体 |
| WO2003060064A2 (en) | 2001-07-12 | 2003-07-24 | Incyte Genomics, Inc. | Intracellular signaling molecules |
| SG114505A1 (en) | 2001-10-17 | 2005-09-28 | First Cube Pte Ltd | System and method for facilitating delivery and return service |
| EP2360169B1 (en) | 2001-10-23 | 2015-10-14 | Psma Development Company, L.L.C. | PSMA antibodies |
| DE60232994D1 (de) | 2001-12-06 | 2009-08-27 | Merck & Co Inc | Inhibitoren von mitotischem kinesin |
| US20080193445A1 (en) | 2002-01-18 | 2008-08-14 | Liliane Goetsch | Novel anti-IGF-IR antibodies and uses thereof |
| US7282567B2 (en) | 2002-06-14 | 2007-10-16 | Immunomedics, Inc. | Monoclonal antibody hPAM4 |
| CA2478833C (en) | 2002-03-13 | 2015-11-10 | Biogen, Inc. | Anti-.alpha.v.beta.6 antibodies |
| EP1494693B1 (en) | 2002-03-22 | 2010-12-08 | Biogen Idec MA Inc. | Cripto-specific antibodies |
| MXPA05003830A (es) | 2002-10-11 | 2005-06-23 | Cytokinetics Inc | Compuestos, composiciones y metodos. |
| US8658377B2 (en) * | 2002-11-15 | 2014-02-25 | Morehouse School Of Medicine | Detecting cancer with anti-CCL25 and anti-CCR9 antibodies |
| US8512701B2 (en) * | 2002-11-15 | 2013-08-20 | Morehouse School Of Medicine | Anti-CXCL13 and anti-CXCR5 antibodies for the prevention and treatment of cancer and cancer cell migration |
| JP2006524693A (ja) | 2003-04-11 | 2006-11-02 | メディミューン,インコーポレーテッド | EphA2および非腫瘍性過増殖性細胞障害 |
| WO2004100873A2 (en) | 2003-05-07 | 2004-11-25 | Cytokinetics, Inc. | Compounds, compositions, and methods |
| BRPI0411803A (pt) | 2003-06-27 | 2006-05-23 | Abgenix Inc | anticorpos dirigidos aos mutantes de deleção de receptor de fator de crescimento epidérmico e seus usos |
| FR2857811A1 (fr) | 2003-07-16 | 2005-01-21 | St Microelectronics Sa | Methode de chiffrage d'un flux audio ou video compresse a tolerance d'erreurs |
| WO2005009369A2 (en) | 2003-07-21 | 2005-02-03 | Immunogen, Inc. | A ca6 antigen-specific cytotoxic conjugate and methods of using the same |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| KR20060127413A (ko) | 2003-11-25 | 2006-12-12 | 카이론 코포레이션 | 항암제로서의 퀴나졸리논 화합물 |
| EP1701979A2 (en) | 2003-12-03 | 2006-09-20 | Xencor, Inc. | Optimized antibodies that target the epidermal growth factor receptor |
| US7662581B1 (en) | 2003-12-18 | 2010-02-16 | Novartis Vaccines And Diagnostics, Inc. | Eg5 co-crystals |
| US7767792B2 (en) | 2004-02-20 | 2010-08-03 | Ludwig Institute For Cancer Research Ltd. | Antibodies to EGF receptor epitope peptides |
| US7598350B2 (en) | 2004-03-19 | 2009-10-06 | Imclone Llc | Human anti-epidermal growth factor receptor antibody |
| KR101170925B1 (ko) | 2004-06-18 | 2012-08-07 | 노바티스 백신즈 앤드 다이아그노스틱스 인코포레이티드 | 암 치료용 키네신 방추 단백질 (ksp) 억제제로서의n-(1-(1-벤질-4-페닐-1h-이미다졸-2-일)-2,2-디메틸프로필)벤자미드 유도체 및 관련 화합물 |
| EP1773884B1 (en) | 2004-08-03 | 2012-03-07 | Innate Pharma | Therapeutic and diagnostic methods and compositions targeting 4ig-b7-h3 and its counterpart nk cell receptor |
| US7449486B2 (en) | 2004-10-19 | 2008-11-11 | Array Biopharma Inc. | Mitotic kinesin inhibitors and methods of use thereof |
| US20100093767A1 (en) | 2004-12-03 | 2010-04-15 | Takeda San Diego, Inc. | Mitotic Kinase Inhibitors |
| EA013323B1 (ru) | 2004-12-09 | 2010-04-30 | Сентокор, Инк. | Иммуноконъюгаты против интегрина, способы и варианты применения |
| GB0428250D0 (en) | 2004-12-23 | 2005-01-26 | Novartis Ag | Organic compounds |
| EP2230517A1 (en) | 2005-01-07 | 2010-09-22 | Diadexus, Inc. | OVR110 antibody compositions and methods of use |
| US8207303B2 (en) | 2005-02-18 | 2012-06-26 | Medarex, Inc. | Monoclonal antibodies against CD30 lacking in fucosyl residues |
| GB0505969D0 (en) | 2005-03-23 | 2005-04-27 | Novartis Ag | Organic compounds |
| CN103127523A (zh) | 2005-06-20 | 2013-06-05 | Psma开发有限公司 | Psma抗体-药物缀合物 |
| TW200800951A (en) | 2005-08-09 | 2008-01-01 | Novartis Ag | Substituted imidazole compounds as KSP inhibitors |
| CA2893252C (en) | 2005-08-24 | 2018-05-29 | Immunogen, Inc. | Process for preparing antibody maytansinoid conjugates |
| EA016186B1 (ru) | 2005-09-26 | 2012-03-30 | Медарекс, Инк. | Человеческие моноклональные антитела к cd70 и их применение |
| EP1790664A1 (en) | 2005-11-24 | 2007-05-30 | Ganymed Pharmaceuticals AG | Monoclonal antibodies against claudin-18 for treatment of cancer |
| CN101374856A (zh) * | 2005-11-29 | 2009-02-25 | 斯克里普斯研究学院 | 抑制肿瘤细胞浸润、转移和血管生成 |
| DOP2006000277A (es) | 2005-12-12 | 2007-08-31 | Bayer Pharmaceuticals Corp | Anticuerpos anti mn y métodos para su utilización |
| WO2008004834A1 (en) | 2006-07-06 | 2008-01-10 | Isu Abxis Co., Ltd | Humanized monoclonal antibody highly binding to epidermal growth factor receptor, egf receptor |
| EP2066349B1 (en) | 2006-09-08 | 2012-03-28 | MedImmune, LLC | Humanized anti-cd19 antibodies and their use in treatment of tumors, transplantation and autoimmune diseases |
| AU2007294122B2 (en) | 2006-09-10 | 2013-03-07 | Glycotope Gmbh | Use of human cells of myeloid leukaemia origin for expression of antibodies |
| EP1900750A1 (en) | 2006-09-18 | 2008-03-19 | Glycotope Gmbh | Fully human high yield production system for improved antibodies |
| EP1911766A1 (en) | 2006-10-13 | 2008-04-16 | Glycotope Gmbh | Use of human cells of myeloid leukaemia origin for expression of antibodies |
| WO2008036688A2 (en) | 2006-09-18 | 2008-03-27 | Xencor, Inc. | Optimized antibodies that target hm1.24 |
| EP1914242A1 (en) | 2006-10-19 | 2008-04-23 | Sanofi-Aventis | Novel anti-CD38 antibodies for the treatment of cancer |
| PT2099823E (pt) | 2006-12-01 | 2014-12-22 | Seattle Genetics Inc | Agentes de ligação ao alvo variantes e suas utilizações |
| WO2008140603A2 (en) | 2006-12-08 | 2008-11-20 | Macrogenics, Inc. | METHODS FOR THE TREATMENT OF DISEASE USING IMMUNOGLOBULINS HAVING FC REGIONS WITH ALTERED AFFINITIES FOR FCγR ACTIVATING AND FCγR INHIBITING |
| GEP20125415B (en) | 2007-01-05 | 2012-03-12 | Novartis Ag | Imidazole derivatives as kinesin spindle protein inhibitors (eg-5) |
| WO2008092117A2 (en) | 2007-01-25 | 2008-07-31 | Xencor, Inc. | Immunoglobulins with modifications in the fcr binding region |
| US20100143245A1 (en) | 2007-03-22 | 2010-06-10 | Sloan-Kettering Institute For Cancer Research | Uses of monoclonal antibody 8h9 |
| KR20090122403A (ko) | 2007-03-29 | 2009-11-27 | 노파르티스 아게 | 증식성 질환의 치료를 위한 3-이미다졸릴-인돌 |
| US8163279B2 (en) | 2007-04-13 | 2012-04-24 | Stemline Therapeutics, Inc. | IL3Rα antibody conjugates and uses thereof |
| NZ556142A (en) | 2007-06-25 | 2009-11-27 | Novartis Ag | Animal remedy dispensing means |
| KR20100029099A (ko) | 2007-06-28 | 2010-03-15 | 톰슨 라이센싱 | 비디오 믹서 교차점 매트릭스의 2중 사용 |
| JP5409628B2 (ja) | 2007-08-03 | 2014-02-05 | アッヴィ・バイオセラピューティクス・インコーポレイテッド | 抗tweak受容体抗体の治療上の使用 |
| JP5532486B2 (ja) | 2007-08-14 | 2014-06-25 | ルードヴィッヒ インスティテュート フォー キャンサー リサーチ | Egf受容体を標的とするモノクローナル抗体175ならびにその誘導体および用途 |
| US8865875B2 (en) | 2007-08-22 | 2014-10-21 | Medarex, L.L.C. | Site-specific attachment of drugs or other agents to engineered antibodies with C-terminal extensions |
| HRP20130649T1 (hr) | 2007-09-07 | 2013-08-31 | Agensys, Inc. | Protutijela i povezane molekule koje se vežu za 24p4c12 proteine |
| US8039597B2 (en) | 2007-09-07 | 2011-10-18 | Agensys, Inc. | Antibodies and related molecules that bind to 24P4C12 proteins |
| US9023351B2 (en) | 2007-11-26 | 2015-05-05 | Bayer Intellectual Property Gmbh | Anti-mesothelin antibodies and uses thereof |
| EA201070687A1 (ru) | 2007-12-06 | 2010-12-30 | Си Эс Эл ЛИМИТЕД | Способ ингибирования лейкозных стволовых клеток |
| US8252832B2 (en) | 2007-12-14 | 2012-08-28 | Novartis Ag | Kinesin inhibitors as cancer therapeutics |
| ES2526433T3 (es) | 2007-12-26 | 2015-01-12 | Biotest Ag | Inmunoconjugados dirigidos a CD138 y usos de los mismos |
| EP2238168B8 (en) | 2007-12-26 | 2014-07-23 | Biotest AG | Agents targeting cd138 and uses thereof |
| AU2009231991B2 (en) | 2008-04-02 | 2014-09-25 | Macrogenics, Inc. | HER2/neu-specific antibodies and methods of using same |
| CA2723973A1 (en) | 2008-05-15 | 2009-11-19 | Biogen Idec Ma Inc. | Anti-fn14 antibodies and uses thereof |
| EP2331577B1 (en) | 2008-08-29 | 2017-06-07 | Symphogen A/S | Recombinant anti-epidermal growth factor receptor antibody compositions |
| WO2010084186A1 (en) | 2009-01-26 | 2010-07-29 | Novartis Ag | Salts and polymorphs of a kinesin inhibitor compound |
| SG174963A1 (en) | 2009-03-31 | 2011-11-28 | Roche Glycart Ag | Treatment of cancer with a humanized anti-egfr igg1 antibody and irinotecan |
| AR075982A1 (es) | 2009-03-31 | 2011-05-11 | Roche Glycart Ag | Terapia de combinacion de un anticuerpo afucosilado y una o mas de las citoquinas seleccionadas de gm- csf humano, m -csf humano y/o il-3 humano y composicion |
| EP2426148B1 (en) | 2009-04-27 | 2015-08-05 | Kyowa Hakko Kirin Co., Ltd. | Anti-il-3ra antibody for use in treatment of blood tumor |
| CN101959216B (zh) | 2009-07-20 | 2014-06-18 | 电信科学技术研究院 | 一种分载波配置增强cell_fach的方法、系统和设备 |
| PL2486141T3 (pl) | 2009-10-07 | 2018-07-31 | Macrogenics, Inc. | Polipeptydy zawierające regiony fc i mające w wyniku zmian w zakresie fukozylacji ulepszoną funkcję efektorową, i sposoby zastosowania tych polipeptydów |
| NZ604510A (en) | 2010-08-17 | 2013-10-25 | Csl Ltd | Dilutable biocidal compositions and methods of use |
| AR086363A1 (es) | 2011-04-21 | 2013-12-11 | Bayer Ip Gmbh | Conjugados de principio activo-ligante (adc) y el uso de los mismos |
| KR102087854B1 (ko) | 2011-06-10 | 2020-03-12 | 메르사나 테라퓨틱스, 인코포레이티드 | 단백질-중합체-약물 접합체 |
| US9726666B2 (en) * | 2011-06-13 | 2017-08-08 | Tla Targeted Immunotherapies Ab | Diagnosing and treating inflammatory diseases |
| AR088941A1 (es) | 2011-11-23 | 2014-07-16 | Bayer Ip Gmbh | Anticuerpos anti-fgfr2 y sus usos |
| UA112096C2 (uk) | 2011-12-12 | 2016-07-25 | Байєр Інтеллектуал Проперті Гмбх | Заміщені триазолопіридини та їх застосування як інгібіторів ttk |
| AU2013222935B2 (en) * | 2012-02-24 | 2016-03-10 | Alteogen Inc. | Modified antibody in which motif comprising cysteine residue is bound, modified antibody-drug conjugate comprising the modified antibody, and production method for same |
| PT2850106T (pt) | 2012-05-18 | 2022-07-18 | Aptevo Res & Development Llc | Imunofusão biespecífica (bif) de scfv de ligação a cd123 e cd3 |
| WO2014061277A1 (ja) | 2012-10-19 | 2014-04-24 | 第一三共株式会社 | 親水性構造を含むリンカーで結合させた抗体-薬物コンジュゲート |
| WO2014093640A1 (en) | 2012-12-12 | 2014-06-19 | Mersana Therapeutics,Inc. | Hydroxy-polmer-drug-protein conjugates |
| TW201437211A (zh) | 2013-03-01 | 2014-10-01 | Bayer Pharma AG | 經取代咪唑并嗒□ |
| US9498532B2 (en) | 2013-03-13 | 2016-11-22 | Novartis Ag | Antibody drug conjugates |
| US9498540B2 (en) | 2013-03-15 | 2016-11-22 | Novartis Ag | Cell proliferation inhibitors and conjugates thereof |
| CN105451773A (zh) * | 2013-03-15 | 2016-03-30 | 诺华股份有限公司 | 细胞增殖抑制剂及其缀合物 |
| CN105308070A (zh) | 2013-06-14 | 2016-02-03 | 拜耳制药股份公司 | 抗tweakr抗体及其用途 |
| KR102087850B1 (ko) | 2013-10-11 | 2020-03-12 | 메르사나 테라퓨틱스, 인코포레이티드 | 단백질-고분자-약물 접합체 |
| CA2932476A1 (en) | 2013-12-12 | 2015-06-18 | Stemcentrx, Inc. | Novel anti-dpep3 antibodies and methods of use |
| KR102329024B1 (ko) | 2013-12-23 | 2021-11-19 | 바이엘 파마 악티엔게젤샤프트 | 키네신 스핀들 단백질(ksp)과의 항체 약물 접합체 (adcs) |
| AU2015229463A1 (en) | 2014-03-12 | 2016-09-15 | Novartis Ag | Specific sites for modifying antibodies to make immunoconjugates |
| WO2015189143A1 (en) | 2014-06-12 | 2015-12-17 | Bayer Pharma Aktiengesellschaft | Aglycosyl anti-tweakr antibodies and uses thereof |
| US10786578B2 (en) | 2014-08-05 | 2020-09-29 | Novartis Ag | CKIT antibody drug conjugates |
| JP2017525710A (ja) | 2014-08-22 | 2017-09-07 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Cxcr5に結合する抗原結合タンパク質 |
| MX2017003123A (es) * | 2014-09-12 | 2017-05-12 | Genentech Inc | Anticuerpos y conjugados modificados geneticamente con cisteina. |
| JP6743015B2 (ja) | 2014-12-15 | 2020-08-19 | バイエル ファーマ アクチエンゲゼルシャフト | Ksp阻害剤の脱グリコシル化抗tweakr抗体との抗体薬物複合体(adc類) |
| TW201709932A (zh) | 2015-06-12 | 2017-03-16 | 西雅圖遺傳學公司 | Cd123抗體及其共軛物 |
| WO2016207089A1 (de) | 2015-06-22 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) und binder-prodrug-konjugate (apdcs) mit enzymatisch spaltbaren gruppen |
| US10973923B2 (en) * | 2015-06-23 | 2021-04-13 | Bayer Pharma Aktiengesellschaft | Site specific homogeneous with KSP inhibitors |
| CN108025085A (zh) | 2015-06-23 | 2018-05-11 | 拜耳制药股份公司 | Ksp抑制剂与抗b7h3抗体的抗体药物缀合物(adc) |
| JP2018525334A (ja) | 2015-06-23 | 2018-09-06 | バイエル ファーマ アクチエンゲゼルシャフト | キネシンスピンドルタンパク質(ksp)阻害剤の抗tweakr抗体との抗体薬物複合体 |
| CA2990411A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-b7h3-antibodies |
| CA2990398A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-cd123-antibodies |
| KR20180123047A (ko) | 2016-03-24 | 2018-11-14 | 바이엘 파마 악티엔게젤샤프트 | 효소적으로 절단가능한 기를 갖는 세포독성 활성제의 전구약물 |
| WO2017216028A1 (en) | 2016-06-15 | 2017-12-21 | Bayer Pharma Aktiengesellschaft | Specific antibody-drug-conjugates (adcs) with ksp inhibitors and anti-cd123-antibodies |
| CA3047522A1 (en) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Specific antibody drug conjugates (adcs) having ksp inhibitors |
| WO2018114578A1 (de) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| US12059472B2 (en) | 2016-12-21 | 2024-08-13 | Bayer Aktiengesellschaft | Prodrugs of cytotoxic active agents having enzymatically cleavable groups |
| WO2019243159A1 (de) | 2018-06-18 | 2019-12-26 | Bayer Aktiengesellschaft | Gegen cxcr5 gerichtete binder-wirkstoff-konjugate mit enzymatisch spaltbaren linkern und verbessertem wirkungsprofil |
| IL282748B2 (en) | 2018-11-05 | 2025-07-01 | Bayer Pharma AG | Cytostatic conjugates with integrin ligands |
-
2017
- 2017-12-14 WO PCT/EP2017/082789 patent/WO2018114578A1/de not_active Ceased
- 2017-12-14 EP EP17837949.1A patent/EP3558388A1/de active Pending
- 2017-12-14 MX MX2019007641A patent/MX2019007641A/es unknown
- 2017-12-14 JP JP2019533395A patent/JP7066714B2/ja active Active
- 2017-12-14 IL IL291308A patent/IL291308B2/en unknown
- 2017-12-14 KR KR1020197020706A patent/KR102556826B1/ko active Active
- 2017-12-14 KR KR1020237018668A patent/KR102583006B1/ko active Active
- 2017-12-14 CN CN201780087040.6A patent/CN110312534B/zh active Active
- 2017-12-14 US US16/472,749 patent/US11660351B2/en active Active
- 2017-12-14 CN CN202310307417.1A patent/CN116327974A/zh active Pending
- 2017-12-14 PE PE2019001293A patent/PE20191235A1/es unknown
- 2017-12-14 RU RU2019122802A patent/RU2761390C2/ru active
- 2017-12-14 AU AU2017380871A patent/AU2017380871C1/en active Active
- 2017-12-14 KR KR1020237018663A patent/KR102628678B1/ko active Active
- 2017-12-14 CA CA3047489A patent/CA3047489A1/en active Pending
- 2017-12-19 TW TW106144529A patent/TWI781125B/zh active
- 2017-12-19 TW TW111134796A patent/TWI823564B/zh active
- 2017-12-21 AR ARP170103619A patent/AR110418A1/es unknown
-
2019
- 2019-06-18 IL IL267473A patent/IL267473B/en unknown
- 2019-06-21 MX MX2024008464A patent/MX2024008464A/es unknown
- 2019-06-21 MX MX2023009205A patent/MX2023009205A/es unknown
-
2021
- 2021-09-01 US US17/464,565 patent/US11478554B2/en active Active
-
2022
- 2022-04-26 JP JP2022072343A patent/JP7307231B2/ja active Active
-
2023
- 2023-03-10 US US18/182,093 patent/US20230338559A1/en active Pending
-
2024
- 2024-01-31 IL IL310558A patent/IL310558B2/en unknown
- 2024-09-27 AU AU2024220179A patent/AU2024220179A1/en active Pending
- 2024-09-27 AU AU2024220178A patent/AU2024220178A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010537636A (ja) | 2007-08-29 | 2010-12-09 | サノフィ−アベンティス | ヒト化抗cxcr5抗体、その誘導体及びそれらの使用 |
| WO2012010582A1 (en) | 2010-07-21 | 2012-01-26 | Roche Glycart Ag | Anti-cxcr5 antibodies and methods of use |
| JP2016524595A (ja) | 2013-05-02 | 2016-08-18 | アレス トレーディング ソシエテ アノニム | Cxcr5に対するモノクローナル抗体 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7307231B2 (ja) | 酵素的に切断可能な基を有する抗体薬物コンジュゲート(adc) | |
| US11806404B2 (en) | Site specific homogeneous with KSP inhibitors | |
| US12059472B2 (en) | Prodrugs of cytotoxic active agents having enzymatically cleavable groups | |
| KR20210033470A (ko) | 효소에 의해 절단 가능한 링커 및 개선된 활성 프로파일을 갖는, cxcr5에 대해 유도된 결합제-약물 접합체 | |
| HK40096469A (zh) | 具有酶促可裂解基团的抗体-药物-缀合物(adc) | |
| BR112019012883B1 (pt) | Conjugados de anticorpo-fármaco, uso dos mesmos e composição farmacêutica | |
| HK40016986A (en) | Antibody drug conjugates (adcs) having enzymatically cleavable groups | |
| HK40016986B (en) | Antibody drug conjugates (adcs) having enzymatically cleavable groups |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220427 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230410 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230524 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230605 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230629 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7307231 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |