CN116327974A - 具有酶促可裂解基团的抗体-药物-缀合物(adc) - Google Patents
具有酶促可裂解基团的抗体-药物-缀合物(adc) Download PDFInfo
- Publication number
- CN116327974A CN116327974A CN202310307417.1A CN202310307417A CN116327974A CN 116327974 A CN116327974 A CN 116327974A CN 202310307417 A CN202310307417 A CN 202310307417A CN 116327974 A CN116327974 A CN 116327974A
- Authority
- CN
- China
- Prior art keywords
- antibody
- tpp
- antibodies
- group
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6855—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from breast cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明涉及具有改善性质的新型结合剂‑活性物质‑缀合物(ADC)、这些ADC的活性代谢物及其制备方法。本发明还涉及这些缀合物用于治疗和/或预防疾病的用途以及这些缀合物用于制备用于治疗和/或预防疾病、特别是过度增生病症和/或血管生成病症,例如癌症的药剂的用途。
Description
本申请是申请日为2017年12月14日、申请号为201780087040.6、发明名称为“具有酶促可裂解基团的抗体-药物-缀合物(ADC)”的中国专利申请(其对应PCT申请的申请日为2017年12月14日、申请号为PCT/EP2017/082789)的分案申请。
引言和现有技术
本发明涉及具有改善性质的新型结合剂-活性物质-缀合物(ADC)、这些ADC的活性代谢物及其制备方法。本发明还涉及这些缀合物用于治疗和/或预防疾病的用途和这些缀合物用于制备用于治疗和/或预防疾病,特别是过度增生和/或血管生成病症,例如癌症的药剂的用途。此类治疗可作为单一疗法或另外与其它药剂或其它治疗措施联合实施。根据本发明,所述结合剂优选为抗体。
癌症是多种多样的组织的不受控细胞生长的后果。在许多情况下,新的细胞渗透到现有组织中(浸润性生长(invasives Wachstum))或它们转移到远端器官中。癌症发生在多种多样的器官中并通常具有组织特异性病程。因此,术语癌症作为上位概念描述不同器官、组织和细胞类型的一大类特定病症。
肿瘤在初期可任选通过手术和放射治疗措施除去。转移的肿瘤通常用化疗药物只能姑息治疗。此处的目标是实现改善生活品质和延长寿命的最佳组合。
结合剂蛋白与一个或多个活性物质分子的缀合物是已知的,特别是以所谓“抗体药物缀合物”(ADC)的形式,其中针对肿瘤相关抗原的内化抗体经连接单元(Verknüpfungseinheit)共价连接至细胞毒性剂。在将ADC引入肿瘤细胞中和该缀合物随后裂解后,然后在肿瘤细胞内释放细胞毒性剂本身或由其形成的其它的细胞毒性有效代谢物且可在其内直接和选择性展现其作用。以该方式,相比于癌症的传统化疗,可将对正常组织的损伤保持在明显较窄的界限内[参见例如J.M.Lambert,Curr.Opin.Pharmacol.5,543-549(2005);A.M.Wu和P.D.Senter,Nat.Biotechnol.23,1137-1146(2005);P.D.Senter,Curr.Opin.Chem.Biol.13,235-244(2009);L.Ducry和B.Stump,Bioconjugate Chem.21,5-13(2010)]。因此,WO2012/171020描述了ADC,其中多个毒簇分子经聚合物接头连接至抗体。作为可能的毒簇,WO2012/171020尤其提到物质SB 743921、SB 715992(伊斯平斯(Ispinesib))、MK-0371、AZD8477、AZ3146和ARRY-520。
最后提到的物质是所谓的驱动蛋白纺锤体蛋白抑制剂。驱动蛋白纺锤体蛋白(KSP,也称作Eg5、HsEg5、KNSL1或KIF11)是双极有丝分裂纺锤体发挥作用所必需的驱动蛋白样马达蛋白。KSP的抑制导致有丝分裂阻滞并较长时间导致细胞凋亡(Tao等人,CancerCell 2005Jul 8(1),39-59)。在发现最早的细胞穿透KSP抑制剂Monastrol后,KSP抑制剂已确立为一类新型化疗药物(Mayer等人,Science 286:971-974,1999),且是一系列专利申请的主题(例如WO2006/044825;WO2006/002236;WO2005/051922;WO2006/060737;WO03/060064;WO03/040979和WO03/049527)。但是,由于KSP仅在有丝分裂阶段的短时期内是活性的,KSP抑制剂在该阶段期间必须以足够高的浓度存在。WO2014/151030公开了包含某些KSP抑制剂的ADC。具有KSP抑制剂的ADC也公开于专利申请WO2015/096982和WO2016/096610中,所述KSP抑制剂还包含酶促可裂解的接头,然而其不具有最佳作用概况。
豆荚蛋白(Legumain)是肿瘤相关的天冬酰胺酰内肽酶(S.Ishii,MethodsEnzymol.1994,244,604;J.M.Chen等人J.Biol.Chem.1997,272,8090),并且已用于加工小细胞毒性分子例如多柔比星和依托泊苷衍生物等的前药(W.Wu等人Cancer Res.2006,66,970;L.Stern等人Bioconjugate Chem.2009,20,500;K.M.Bajjuri等人ChemMedChem 2011,6,54)。
其它溶酶体酶是例如组织蛋白酶或糖苷酶,例如β-葡糖醛酸糖苷酶,其也已用于通过前药的酶促裂解而释放活性的活性物质。在体内酶促可裂解的基团尤其是2-8-寡肽基团或糖苷。肽裂解位点公开于Bioconjugate Chem.2002,13,855-869和Bioorganic&Medicinal Chemistry Letters 8(1998)3341-3346以及Bioconjugate Chem.1998,9,618-626。这些包括例如缬氨酸-丙氨酸、缬氨酸-赖氨酸、缬氨酸-瓜氨酸、丙氨酸-赖氨酸和苯丙氨酸-赖氨酸(任选地具有额外的酰胺基团)。
发明概述
现有技术公开了各种具有酶促可裂解接头的抗体-活性物质-缀合物,然而其没有例如关于其对不同细胞的广泛效用的最佳作用概况。因此,本发明的目的是提供在以相对低的浓度施用后展现持久的细胞凋亡作用并因此用于癌症治疗的更有效的化合物。此处,在一个方面,从ADC细胞内释放的代谢物的概况发挥重要作用。通常,由ADC形成的代谢物为流出泵的底物和/或具有穿过细胞膜的高渗透性。两种现象可能造成短的保留时间且因此造成在肿瘤细胞内的次优的细胞凋亡作用。
因此,本发明的主题是具有特定毒簇-接头组合物的结合剂-活性物质-缀合物(ADC),所述特定毒簇-接头组合物与抗体结合着在作用强度和作用宽度方面具有特别令人感兴趣的作用概况。为了进一步改善ADC及其代谢物的肿瘤选择性,已经为结合剂缀合物提供肽接头,所述肽接头可以通过肿瘤相关的溶酶体酶诸如豆荚蛋白或组织蛋白酶释放。因此,肿瘤选择性不仅通过抗体的选择来确定,而且还通过肽衍生物的酶促裂解,例如通过肿瘤相关的酶诸如豆荚蛋白来确定。此外,在肿瘤细胞中从根据本发明的结合剂-活性物质-缀合物(ADC)释放的代谢物的特征还在于特别令人感兴趣的性质概况。它们表现出来自肿瘤细胞的低流出并导致肿瘤中的高活性物质暴露。因此,在肿瘤细胞中实现了高作用,相反,由于渗透性差所致,仅存在低全身细胞毒性作用,这导致较低的脱靶毒性。
根据本发明使用的驱动蛋白纺锤体蛋白抑制剂具有对该作用必不可少的氨基。通过用肽衍生物修饰该氨基,阻断对驱动蛋白纺锤体蛋白的作用,且因此也抑制细胞毒性作用的发展。这些肽衍生物也可以是抗体的接头的组成部分。然而,如果该肽残基或肽接头可以通过肿瘤相关酶诸如豆荚蛋白或组织蛋白酶从活性物质裂解出来,则可以在肿瘤组织中有针对性地重建该作用。通过在不同于分子中的氨基的其它位置进一步修饰驱动蛋白纺锤体蛋白抑制剂来确保在肿瘤中形成的代谢物的特别的性质概况,然而,所述进一步修饰不损害靶标处的高功效。
此外,对于某些实施方案,根据本发明的ADC的结构实现抗体的高载量(称为DAR,药物与抗体比率),其在此令人惊讶地对ADC的物理化学和药物动力学行为没有负面影响。
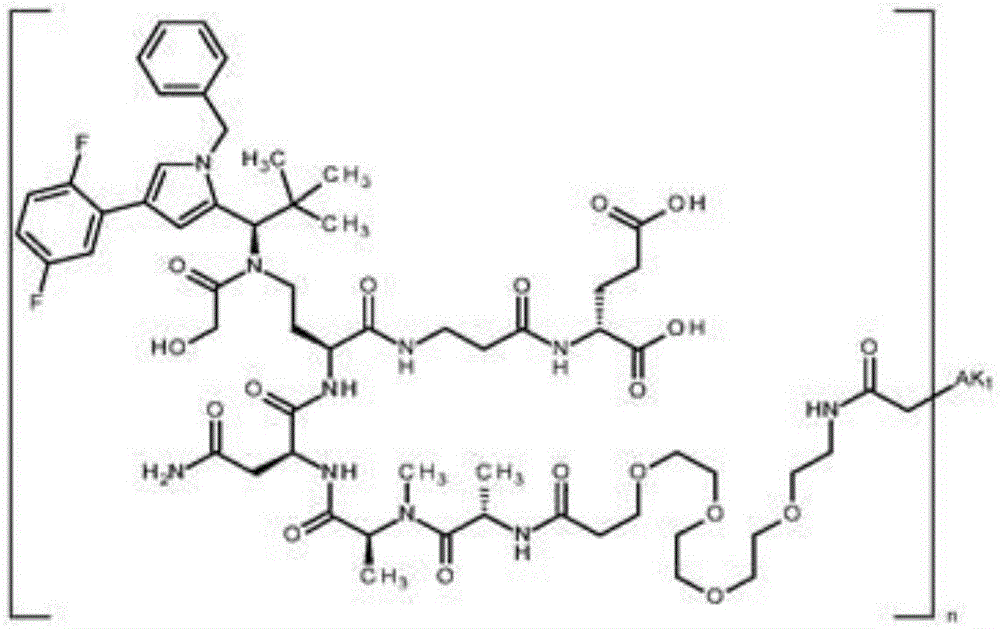
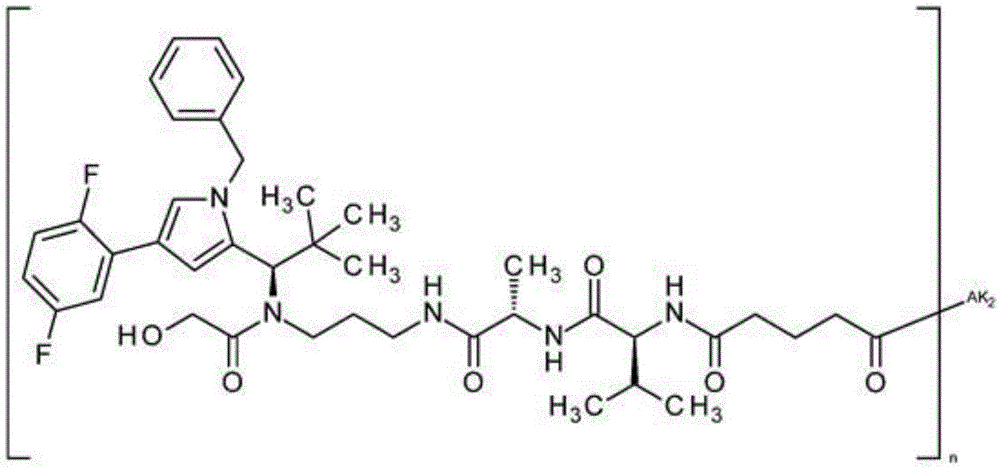
令人惊讶地,现在我们已发现式(I)的结合剂-活性物质-缀合物
其中
X1 代表N,
X2 代表N,且
X3 代表C;
或
X1 代表N,
X2 代表C,且
X3 代表N;
或
X1 代表CH或CF,
X2 代表C,且
X3 代表N;
或
X1 表示NH,
X2 代表C,且
X3 代表C;
或
X1 代表CH,
X2 代表N,且
X3 代表C,
R1 代表氢或甲基,
R2 代表甲基、乙基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,
R3 代表甲基、乙基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)2-8-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)1-8-(CH2)2-NH-C(=O)-CH2-##,
W 代表以下基团
n 代表1至50的数目,
AK 代表结合剂或其衍生物,优选抗体或结合抗原的片段,
# 代表连接至所述化合物的键,
## 代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
### 代表连接至所述结合剂的赖氨酸侧链的氮原子的键,以及其盐、溶剂化物和这些溶剂化物的盐具有与已知缀合物相比优异的性质。
优选那些式(I)的结合剂-活性物质-缀合物,
其中
X1 代表CH,
X2 代表C,
X3 代表N,
R1 代表氢或甲基,
R2 代表甲基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,
R3 代表甲基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)4-(CH2)2-NH-C(=O)-CH2-##,
W 代表以下基团
n 代表1至50的数目,
AK 代表结合剂或其衍生物,优选抗体或结合抗原的片段,
# 代表连接至所述化合物的键,
## 代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
### 代表连接至所述结合剂的赖氨酸侧链的氮原子的键,以及其盐、溶剂化物和这些溶剂化物的盐。
尤其优选那些式(I)的结合剂-活性物质-缀合物,
其中
R1 代表氢或甲基,
R2 代表甲基或异丙基,
R3 代表甲基或–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n 代表1至50的数目,
AK 代表结合剂或其衍生物,优选抗体或结合抗原的片段,
# 代表连接至所述化合物的键,
### 代表连接至所述结合剂的赖氨酸侧链的氮原子的键,以及其盐、溶剂化物和这些溶剂化物的盐。
非常尤其优选那些式(I)的结合剂-活性物质-缀合物,其中
R1 代表甲基,
R2 代表甲基,
R3 代表–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n 代表1至50的数目,
AK 代表结合剂或其衍生物,优选抗体或结合抗原的片段,
# 代表连接至所述化合物的键,
### 代表连接至所述结合剂的赖氨酸侧链的氮原子的键,以及其盐、溶剂化物和这些溶剂化物的盐。
特别优选那些式(I)的结合剂-活性物质-缀合物,其中
R1 代表甲基,
R2 代表甲基,
R3 代表–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n 代表1至20的数目,
AK 代表结合剂或其衍生物,优选抗体或结合抗原的片段,
# 代表连接至所述化合物的键,
### 代表连接至所述结合剂的赖氨酸侧链的氮原子的键,
以及其盐、溶剂化物和这些溶剂化物的盐。
选择的是那些式(I)的结合剂-活性物质-缀合物,
其中
R1 代表甲基,
R2 代表甲基,
R3 代表–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n 代表1至20的数目,且
AK 代表抗-CD123抗体、抗-CXCR5抗体、抗-B7H3抗体、抗-TWEAKR抗体、抗-Her2抗体或抗-EGFR抗体或代表它们的结合抗原的抗体片段,
# 代表连接至所述化合物的键,
### 代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键,
以及其盐、溶剂化物和这些溶剂化物的盐。
选择的尤其是那些式(I)的结合剂-活性物质-缀合物,其中
R1 代表甲基,
R2 代表甲基,
R3 代表–CH2-C(=O)-NH2,
M 代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n 代表1至20的数目,且
AK 代表选自TPP-9476、TPP-8988、TPP-8987和TPP-6013的抗-CD123抗体,代表选自TPP-9574和TPP-9580的抗-CXCR5抗体,代表抗-B7H3抗体TPP-8382,代表选自TPP-7006和TPP-7007的抗-TWEAKR抗体,代表抗-Her2抗体TPP-1015或代表抗-EGFR抗体TPP-981或代表它们的结合抗原的抗体片段,
# 代表连接至所述化合物的键,
### 代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键,
以及其盐、溶剂化物和这些溶剂化物的盐。
优选上述式的那些结合剂-活性物质-缀合物,其中AK代表特异性结合至细胞外癌症靶分子的结合剂。在一个优选实施方案中,所述结合剂在结合至其在靶细胞上的细胞外靶分子之后通过结合被所述靶细胞内化。优选地,所述结合剂是抗体或结合抗原的片段。
在本发明的一个优选主题中,所述细胞外癌症靶分子选自癌症靶分子EGFR、CD123、HER2、B7H3、TWEAKR和CXCR5;尤其优选CD123、CXCR5和B7H3。
在本发明的一个优选主题中,所述结合剂AK是抗-CD123抗体、抗-CXCR5抗体、抗-B7H3抗体、抗-TWEAKR抗体、抗-Her2抗体或抗-EGFR抗体或它们的结合抗原的抗体片段。
特别优选的是所述式的那些结合剂-活性物质-缀合物,其中AK(AK1、AK2)代表选自TPP-8382(抗B7H3)、TPP-6013(抗-CD123)、TPP-8987(抗-CD123)、TPP-8988(抗-CD123)、TPP-9476(抗-CD123)、TPP-9574(抗-CXCR5)和TPP-9580(抗-CXCR5)的抗体,或它们的结合抗原的片段。此处,优选抗体TPP-6013、TPP-8987、TPP-8988和TPP-9476(在每种情况下,抗-CD123)。这些抗体的确切结构(序列)可见于表:抗体的蛋白序列、该表后的文字和序列表。
特别优选的是那些式(I)的结合剂-活性物质-缀合物,其中AK代表选自TPP-8382(抗B7H3)、TPP-6013(抗-CD123)、TPP-8987(抗-CD123)、TPP-8988(抗-CD123)、TPP-9476(抗-CD123)、TPP-9574(抗-CXCR5)和TPP-9580(抗-CXCR5)的抗体。此处,优选抗体(AK)TPP-6013、TPP-8987、TPP-8988和TPP-9476(在每种情况下,抗-CD123)。
附图说明
图1A-1L:结合剂-活性物质-缀合物的优选抗体的注释序列。所显示的是IgG的重链和轻链的蛋白序列,以及这些抗体的VH和VL区。在序列下方注释重要区域(IgG中的VH和VL区,以及CDR区(H-CDR1、H-CDR2、H-CDR3、L-CDR1、L-CDR2、L-CDR3))。注释序列的SEQ IDNO如下:TPP-981VH(PRT)-SEQ ID NO:1、TPP-981VL(PRT)-SEQ ID NO:5、TPP-981重链(PRT)-SEQ ID NO:9、TPP-981轻链(PRT)-SEQ ID NO:10、TPP-1015VH(PRT)-SEQ ID NO:11、TPP-1015VL(PRT)-SEQ ID NO:15、TPP-1015重链(PRT)-SEQ ID NO:19、TPP-1015轻链(PRT)-SEQ ID NO:20、TPP-6013VH(PRT)-SEQ ID NO:21、TPP-6013VL(PRT)-SEQ ID NO:25、TPP-6013重链(PRT)-SEQ ID NO:29、TPP-6013轻链(PRT)-SEQ ID NO:30、TPP-7006VH(PRT)-SEQ ID NO:31、TPP-7006VL(PRT)-SEQ ID NO:35、TPP-7006重链(PRT)-SEQ ID NO:39、TPP-7006轻链(PRT)-SEQ ID NO:40、TPP-7007VH(PRT)-SEQ ID NO:41、TPP-7007VL(PRT)-SEQ ID NO:45、TPP-7007重链(PRT)-SEQ ID NO:49、TPP-7007轻链(PRT)-SEQ IDNO:50、TPP-8382VH(PRT)-SEQ ID NO:51、TPP-8382VL(PRT)-SEQ ID NO:55、TPP-8382重链(PRT)-SEQ ID NO:59、TPP-8382轻链(PRT)-SEQ ID NO:60、TPP-8987VH(PRT)-SEQ ID NO:61、TPP-8987VL(PRT)-SEQ ID NO:65、TPP-8987重链(PRT)-SEQ ID NO:69、TPP-8987轻链(PRT)-SEQ ID NO:70、TPP-8988VH(PRT)-SEQ ID NO:71、TPP-8988VL(PRT)-SEQ ID NO:75、TPP-8988重链(PRT)-SEQ ID NO:79、TPP-8988轻链(PRT)-SEQ ID NO:80、TPP-9476VH(PRT)-SEQ ID NO:81、TPP-9476VL(PRT)-SEQ ID NO:85、TPP-9476重链(PRT)-SEQ ID NO:89、TPP-9476轻链(PRT)-SEQ ID NO:90、TPP-9574VH(PRT)-SEQ ID NO:91、TPP-9574VL(PRT)-SEQ ID NO:95、TPP-9574重链(PRT)-SEQ ID NO:99、TPP-9574轻链(PRT)-SEQ IDNO:100、TPP-9580VH(PRT)-SEQ ID NO:101、TPP-9580VL(PRT)-SEQ ID NO:105、TPP-9580重链(PRT)-SEQ ID NO:109和TPP-9580轻链(PRT)-SEQ ID NO:110。
图2A-2K:结合剂-活性物质-缀合物的优选抗体的序列以及靶蛋白的序列的序列表。
发明详述
本发明提供了结合剂或其衍生物与一个或多个活性物质分子的缀合物,其中该活性物质分子是驱动蛋白纺锤体蛋白抑制剂(KSP抑制剂)。
下面描述了可以根据本发明使用的结合剂、其可以根据本发明使用的KSP抑制剂和可以根据本发明使用的接头,它们可以不受限制地组合使用。特别地,在每种情况下表示为优选或特别优选的结合剂可以与在每种情况下表示为优选或特别优选的KSP抑制剂组合使用,任选地与在每种情况下表示为优选或特别优选的接头组合使用。
特别优选的KSP抑制剂-缀合物(结合剂-活性物质-缀合物)
根据本发明,特别优选下面的KSP抑制剂-缀合物,其中AK(AK1、AK2)代表结合剂或其衍生物(优选抗体),并且n代表1至50,优选1至20,优选1至8,特别优选4至8的数目。AK1优选代表经由半胱氨酸残基结合至KSP抑制剂的抗体;AK2优选代表经由赖氨酸残基结合至KSP抑制剂的抗体。此处使用的结合剂或抗体优选是在说明书中描述为优选的结合剂和抗体。
此处,特别优选以下结合剂-活性物质-缀合物:
优选所述式的那些结合剂-活性物质-缀合物,其中AK(AK1、AK2)代表特异性结合至细胞外癌症靶分子的结合剂。在一个优选实施方案中,所述结合剂在结合至其在靶细胞上的细胞外靶分子之后通过结合被所述靶细胞内化。
在本发明的一个优选主题中,所述细胞外癌症靶分子选自癌症靶分子EGFR、CD123、Her2、B7H3、TWEAKR和CXCR5,尤其是CD123、CXCR5和B7H3。
在本发明的一个优选主题中,所述结合剂AK(AK1、AK2)是抗-CD123抗体、抗-CXCR5抗体、抗-B7H3抗体、抗-TWEAKR抗体、抗-Her2抗体或抗-EGFR抗体或它们的结合抗原的抗体片段。
特别优选的是所述式的那些结合剂-活性物质-缀合物,其中AK(AK1、AK2)代表选自TPP-8382(抗B7H3)、TPP-6013(抗-CD123)、TPP-8987(抗-CD123)、TPP-8988(抗-CD123)、TPP-9476(抗-CD123)、TPP 9574(抗-CXCR5)和TPP-9580(抗-CXCR5)的抗体,或它们的结合抗原的片段。此处,优选抗体TPP-6013、TPP-8987、TPP-8988和TPP-9476(在每种情况下,抗-CD123)。这些抗体的确切结构(序列)可见于表:抗体的蛋白序列、该表后的文字和序列表。
KSP抑制剂-接头-中间体和缀合物的制备根据本发明的缀合物如下制备:通过首先为其低分子量KSP抑制剂提供接头。然后使以这种方式获得的中间体与结合剂(优选抗体)反应。
对于与赖氨酸残基偶联的中间体和随后与抗体偶联,反应可以如下说明:
在上述反应方案中,X1、X2、X3、R1、R2、R3和AK2具有式(I)中给出的含义,并且此处R4代表甲基,且n代表0或1。
构建块A的合成已描述于WO2015/096982中。肽衍生物B和C通过肽化学的经典方法制备。在室温下,在N,N-二异丙基乙胺存在的情况下,使用HATU在DMF中偶联中间体C和D。随后,在活性炭上的10%钯上以氢解的方式裂解出苄基氧基羰基保护基和苄基酯。然后在N,N-二异丙基乙胺存在的情况下,使完全脱保护的中间体与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮在DMF中在室温下反应,以得到ADC前体分子E。然后,如章节B-5中所述,将该活化的酯与相应的抗体偶联。
对于与半胱氨酸残基偶联的中间体和随后与抗体偶联,反应可以如下说明:
在上述反应方案中,X1、X2、X3、R1、R2、R3和AK1具有式(I)中
给出的含义,并且此处R4代表甲基,且n代表1。
使用类似的操作方式,也可制备其中n代表0的化合物。
构建块A的合成已描述于WO2015/096982中。肽衍生物B和C通过肽化学的经典方法制备。在室温下,在N,N-二异丙基乙胺存在的情况下,使用HATU在DMF中偶联中间体C和D。随后,在活性炭上的10%钯上以氢解的方式裂解出苄基氧基羰基保护基和苄基酯。然后在N,N-二异丙基乙胺存在的情况下,使完全脱保护的中间体与1-{6-[(2,5-二氧代吡咯烷-1-基)氧基]-6-氧代己基}-1H-吡咯-2,5-二酮在DMF中在室温下反应,以得到ADC前体分子E。然后,如章节B-4中所述,将该马来酰亚胺衍生物与相应的抗体偶联。
取决于接头,琥珀酰亚胺连接的ADC在缀合后可以转化成开链琥珀酰胺,其具有有利的稳定性概况。
该反应(开环)可以在pH 7.5至9,优选pH 8在25℃至37℃的温度下例如通过搅拌实现。优选的搅拌时间为8至30小时。
对于与半胱氨酸残基偶联的中间体和随后与抗体偶联和随后琥珀酰亚胺环的开环,反应可以如下说明:
在上述反应方案中,X1、X2、X3、R1、R2、R3和AK1具有式(I)中给出的含义,并且此处R4代表甲基,且n代表0或1。
构建块A的合成已描述于WO2015/096982中。肽衍生物B和C通过肽化学的经典方法制备。在室温下,在N,N-二异丙基乙胺存在的情况下,使用HATU在DMF中偶联中间体C和D。随后,在活性炭上的10%钯上以氢解的方式裂解出苄基氧基羰基保护基和苄基酯。然后在N,N-二异丙基乙胺存在的情况下,使完全脱保护的中间体与1-{2-[(2,5-二氧代吡咯烷-1-基)氧基]-2-氧代乙基}-1H-吡咯-2,5-二酮在室温下反应,以得到ADC前体分子E。然后,如章节B-4中所述,将该马来酰亚胺衍生物与相应的抗体在小规模偶联或中等规模偶联下进行偶联。
结合剂
在最广义上,术语“结合剂”被理解为是指结合至存在于该结合剂-活性物质-缀合物指向的特定靶细胞群上的靶分子的分子。术语结合剂应以其最广的含义理解并且也包括例如凝集素、能够结合特定糖链的蛋白或磷脂结合蛋白。此类结合剂包括例如高分子量蛋白(结合蛋白)、多肽或肽(结合肽)、非肽(例如适体(US5,270,163)(Keefe AD.等人的综述,Nat.Rev.Drug Discov.2010;9:537-550)或维生素)和所有其它细胞结合分子或物质。结合蛋白是例如抗体和抗体片段或拟抗体,例如亲和体(Affibodies)、Adnectin、Anticalin、DARPin、Avimer、纳米抗体(Gebauer M.等人的综述,Curr.Opinion in Chem.Biol.2009;13:245-255;Nuttall S.D.等人,Curr.Opinion in Pharmacology 2008;8:608-617)。结合肽是例如配体/受体对的配体,例如配体/受体对VEGF/KDR的VEGF,如配体/受体对转铁蛋白/转铁蛋白受体的转铁蛋白,或细胞因子/细胞因子受体,如配体/受体对TNFα/TNFα受体的TNFα。
所述结合剂可以是结合蛋白。结合剂的优选的实施方案为抗体、结合抗原的抗体片段、多特异性抗体或拟抗体。
文献还公开了有机分子共价偶联(缀合)至结合剂和尤其抗体的各种可能性。根据本发明优选的是毒簇经由抗体的半胱氨酸残基的一个或多个硫原子和/或经由抗体的赖氨酸残基的一个或多个NH基团缀合至抗体。但是,也可以经由抗体的游离羧基或经由糖残基使毒簇结合至抗体。
“靶分子”在最广义上被理解为是指存在于靶细胞群中的分子并且可以是蛋白(例如生长因子的受体)或非肽分子(例如糖或磷脂)。其优选是受体或抗原。
术语“细胞外”靶分子描述位于细胞外部的连接至细胞上的靶分子,或位于细胞外部的靶分子的一部分,即结合剂可以在完整的细胞上结合至其细胞外靶分子。细胞外靶分子可锚定在细胞膜中或是细胞膜的组成部分。本领域技术人员了解识别细胞外靶分子的方法。对于蛋白,这可以通过(一个或多个)跨膜域的测定和蛋白在该膜中的取向来进行。这些数据通常存放在蛋白数据库(例如SwissProt)中。
术语“癌症靶分子”描述与相同组织类型的非癌细胞相比更大量存在于一种或多种癌细胞种类上的靶分子。优选地,癌症靶分子与相同组织类型的非癌细胞相比选择性存在于一种或多种癌细胞种类上,其中选择性描述与相同组织类型的非癌细胞相比至少两倍富集在癌细胞上(“选择性癌症靶分子”)。癌症靶分子的使用允许通过根据本发明的缀合物选择性治疗癌细胞。
结合剂可经由键与接头连接。结合剂可经由所述结合剂的杂原子连接。根据本发明的结合剂的可用于连接的杂原子是硫(在一个实施方案中经由结合剂的巯基)、氧(根据本发明借助结合剂的羧基或羟基)和氮(在一个实施方案中经由结合剂的伯或仲胺基或酰胺基)。这些杂原子可存在于天然结合剂中或通过化学方法或分子生物学方法引入。根据本发明,结合剂与毒簇的连接对于结合剂对靶分子的结合活性而言只有轻微影响。在一个优选实施方案中,该连接对于结合剂对靶分子的结合活性而言没有影响。
根据本发明,术语“抗体”应以其最广的含义理解并包括免疫球蛋白分子,例如完整或经修饰的单克隆抗体、多克隆抗体或多特异性抗体(例如双特异性抗体)。免疫球蛋白分子优选包含具有通常通过二硫桥连接的四个多肽链(两个重链(H链)和两个轻链(L链))的分子。各重链包含重链可变结构域(缩写为VH)和重链恒定结构域。重链恒定结构域可以例如包含三个结构域CH1、CH2和CH3。各轻链包含可变结构域(缩写为VL)和恒定结构域。轻链恒定结构域包含结构域(缩写为CL)。VH和VL结构域可进一步细分成高变区,也称作互补决定区("complementarity determining region",缩写为CDR),和具有低序列变异性的区("框架区",缩写为FR)。通常,各VH和VL区由三个CDR和最多四个FR构成。例如以下列顺序从氨基末端到羧基末端:FR1、CDR1、FR2、CDR2、FR3、CDR3、FR4。抗体可获自每个对此合适的物种,例如兔、美洲驼、骆驼、小鼠或大鼠。在一个实施方案中,该抗体为人或鼠来源的。该抗体可以例如是人、人源化或嵌合的。
术语“单克隆”抗体是指获自一群基本同质抗体的抗体,即该群的各个抗体除天然存在的突变(其可以少数出现)外是相同的。单克隆抗体以高特异性识别单个抗原结合位点。术语单克隆抗体不涉及特定制备方法。
术语“完整”抗体是指包含结合抗原的结构域以及轻链和重链的恒定结构域的抗体。恒定结构域可以是天然存在的结构域或其多个氨基酸位置发生变化的变体,并且也可以是无糖基化的。
术语“经修饰的完整”抗体是指借助共价键(例如肽键)经由它们的氨基末端或羧基末端与不源自抗体的另一多肽或蛋白融合的完整抗体。此外,可以如下修饰抗体,以使得在特定的位置处引入反应性半胱氨酸以使偶联至毒簇变容易(参见Junutula等人,NatBiotechnol.2008Aug;26(8):925-32)。
“氨基酸修饰”或“突变”在此处是指在多肽序列中的氨基酸取代、插入和/或缺失。此处优选的氨基酸修饰为取代。“氨基酸取代”或“取代”在此处是指在蛋白序列的给定位置的氨基酸被另一氨基酸替换。例如,取代Y50W描述亲本多肽的变体,其中在位置50的酪氨酸被色氨酸替换。多肽的“变体”描述具有与参比多肽、典型地天然或“亲本”多肽基本上相同的氨基酸序列的多肽。多肽变体可在天然氨基酸序列的特定位置具有一个或多个氨基酸置换、缺失和/或插入。
术语“人”抗体是指可获自人类或为合成人抗体的抗体。“合成”人抗体是部分或甚至完全地可由基于人抗体序列分析的合成序列经由计算机模拟获得的抗体。人抗体可以例如由从人源性抗体序列库中分离的核酸编码。此类抗体的实例可见于等人,Nature Biotech.2000,18:853-856。此类“人类”和“合成”抗体还包括通过由PNGaseF去糖基化或通过重链的N297(kabat编号)突变成任意其它氨基酸所制备的无糖基化变体。
术语“人源化”或“嵌合”抗体描述由序列的非人部分和人部分组成的抗体。在这些抗体中,人免疫球蛋白的一部分序列(受体)被非人免疫球蛋白的序列部分(供体)替换。在许多情况下,该供体是鼠免疫球蛋白。在人源化抗体的情况下,受体的CDR的氨基酸被供体的氨基酸替换。有时,框架的氨基酸也被供体的相应氨基酸替换。在一些情况下,该人源化抗体含有既不包含于受体中又不包含于供体中且在抗体的优化过程中引入的氨基酸。在嵌合抗体的情况下,供体免疫球蛋白的可变结构域与人抗体的恒定区融合。此类“人源化”和“嵌合”抗体还包括通过由PNGaseF去糖基化或通过重链的N297(Kabat编号)突变成任意其它氨基酸所制备的无糖基化变体。
如本文所用的术语互补决定区(CDR)是指对于结合至抗原所需的可变抗体结构域的那些氨基酸。通常,各可变区具有三个CDR区,其被称作CDR1、CDR2和CDR3。各CDR区可包含根据Kabat定义的氨基酸和/或根据Chotia定义的高变环的氨基酸。根据Kabat的定义包含例如可变轻链/结构域(VL)的大致氨基酸位置24-34(CDR1)、50-56(CDR2)和89-97(CDR3)的区域和可变重链/结构域(VH)的大致氨基酸位置31-35(CDR1)、50-65(CDR2)和95-102(CDR3)的区域(Kabat等人,Sequences of Proteins of Immunological Interest,第5版,Public Health Service,National Institutes of Health,Bethesda,MD.(1991))。根据Chotia的定义包含例如可变轻链(VL)的大致氨基酸位置26-32(CDR1)、50-52(CDR2)和91–96(CDR3)的区域和可变重链(VH)的大致氨基酸位置26-32(CDR1)、53-55(CDR2)和96-101(CDR3)的区域(Chothia和Lesk;JMol Biol 196:901-917(1987))。在一些情况下,CDR可包含来自根据Kabat和Chotia定义的CDR区的氨基酸。
根据重链恒定结构域的氨基酸序列,可以将抗体分成不同种类。完整抗体有五大类:IgA、IgD、IgE、IgG和IgM,其中几种可分成进一步的亚类(同种型),例如IgG1、IgG2、IgG3、IgG4、IgA1和IgA2。与不同种类对应的重链恒定结构域被称作[alpha/α]、[delta/δ]、[epsilon/ε]、[gamma/γ]和[my/μ]。抗体的三维结构和亚基结构都是已知的。
抗体/免疫球蛋白的术语“功能片段”或“结合抗原的抗体片段”被定义为仍包含抗体/免疫球蛋白的结合抗原的结构域的抗体/免疫球蛋白片段(例如IgG的可变结构域)。抗体的“结合抗原的结构域”通常包含抗体的一个或多个高变区,例如CDR、CDR2和/或CDR3区。但是,抗体的“框架”或“骨架”区对于抗体结合至抗原而言也可起到作用。框架区构成CDR的骨架。结合抗原的结构域优选至少包含可变轻链的氨基酸4至103和可变重链的氨基酸5至109,更优选可变轻链的氨基酸3至107和可变重链的4至111,特别优选为完整的可变轻链和重链,即VL的氨基酸1-109和VH的1至113(根据WO97/08320编号)。
本发明的“功能片段”或“结合抗原的抗体片段”非穷举地包括Fab、Fab'、F(ab')2和Fv片段、双价抗体、单结构域抗体(DAb)、线性抗体、单链抗体(单链Fv,缩写为scFv);和多特异性抗体,如双和三特异性抗体,其由抗体片段形成,C.A.K Borrebaeck编辑(1995)Antibody Engineering(Breakthroughs in Molecular Biology),Oxford UniversityPress;R.Kontermann&S.Duebel,编辑(2001)Antibody Engineering(SpringerLaboratory Manual),Springer Verlag)。不同于“多特异性”或“多功能”的其它抗体的抗体是具有相同结合位点的那些。多特异性抗体可对抗原的不同表位是特异性的或可对多于一种抗原的表位是特异性的(参见例如WO 93/17715;WO 92/08802;WO 91/00360;WO 92/05793;Tutt,等人,1991,J.Immunol.147:60 69;美国专利号4,474,893;4,714,681;4,925,648;5,573,920;5,601,819;或Kostelny等人,1992,J.Immunol.148:1547 1553)。可以构建F(ab')2或Fab分子,以使得可以减少或完全防止在Ch1和CL结构域之间发生的分子间二硫化物相互作用的数量。
“表位”是指能与免疫球蛋白或T细胞受体发生特异性结合的蛋白决定簇。表位决定簇通常由分子的化学活性表面基团如氨基酸或糖侧链或其组合构成,并通常具有特定的三维结构性质以及特定的电荷性质。
“功能片段”或“结合抗原的抗体片段”可借助共价键(例如肽键)经由其氨基末端或羧基末端与不源自抗体的另一多肽或蛋白融合。此外,可如下修饰抗体和结合抗原的片段,以使得在特定位置引入反应性半胱氨酸以使偶联至毒簇变容易(参见Junutula等人,Nat Biotechnol.2008Aug;26(8):925-32)。
多克隆抗体可通过本领域普通技术人员已知的方法制备。单克隆抗体可通过本领域普通技术人员已知的方法制备(和Milstein,Nature,256,495-497,1975)。人和人源化单克隆抗体可通过本领域普通技术人员已知的方法制备(Olsson等人,MethEnzymol.92,3-16,或Cabilly等人,US 4,816,567,或Boss等人,US 4,816,397)。
本领域普通技术人员了解制备人抗体及其片段的各种方法,例如借助转基因小鼠(N Lonberg和D Huszar,Int Rev Immunol.1995;13(1):65-93)或噬菌体展示技术(Clackson等人,Nature.1991年8月15日;352(6336):624-8)。本发明的抗体可获自例如基于由大量健康志愿者建立的多种抗体的氨基酸序列组成的重组抗体库。抗体也可借助已知的重组DNS技术制备。抗体的核酸序列可通过常规测序获得或可获自可公开访问的数据库。
“分离的”抗体或结合剂已经纯化以除去细胞的其它成分。可能干扰诊断或治疗用途的细胞的污染成分是例如酶、激素或细胞的其它肽或非肽成分。优选已以基于该抗体或结合剂计大于95重量%(例如通过Lowry法、UV-Vis光谱学或通过SDS毛细管凝胶电泳测定)的程度纯化的抗体或结合剂。此外,已纯化以使得可以决定氨基末端或内部氨基酸序列的至少15个氨基酸或已纯化至同质性的抗体,其中同质性通过SDS-PAGE在还原或非还原条件下测定(可以借助考马斯蓝染色或优选通过银着色进行检测)。但是,通常通过一个或多个纯化步骤制备抗体。
术语“特异性结合”或“特异性地结合”是指结合至预定抗原/靶分子的抗体或结合剂。抗体或结合剂的特异性结合通常描述具有至少10-7M的亲和力(作为Kd值;即优选为具有比10-7M更小的Kd值的那些)的抗体或结合剂,其中该抗体或结合剂对预定抗原/靶分子的亲和力为对不是预定抗原/靶分子或密切相关抗原/靶分子的非特异性抗原/靶分子(例如牛血清白蛋白或酪蛋白)的至少两倍。抗体或结合剂的特异性结合不排除抗体或结合剂结合至多种抗原/靶分子(例如不同物种的直系同源物)。该抗体优选具有至少10-7M(作为Kd值;即优选为具有比10-7M更小的Kd值的那些),优选至少10-8M,特别优选10-9M至10-11M的亲和力。可以例如借助表面等离子体共振波谱法测定Kd值。
本发明的抗体-活性物质-缀合物同样表现出在这些范围内的亲和力。该亲和力优选基本不受活性物质缀合的影响(一般而言,该亲和力降低小于一个量级,换言之,例如最多从10-8M降低至10-7M)。
根据本发明使用的抗体也优选以高选择性为特征。当根据本发明的抗体对靶蛋白表现出的亲和力为对非依赖性的其它抗原,例如人血清白蛋白的至少2倍,优选5倍或特别优选10倍(可以例如借助表面等离子体共振波谱法测定亲和力),则存在高选择性。
此外,根据本发明使用的抗体优选是交叉反应性的。为了能够简化和更好地解释临床前研究,例如毒理学或效用研究(例如在异种移植小鼠中),有利的是根据本发明使用的抗体不仅结合人靶蛋白,而且还在用于研究的物种中结合物种靶蛋白。在一个实施方案中,根据本发明使用的抗体除人靶蛋白外还对至少一个其它物种的靶蛋白呈交叉反应性。对于毒理学和效用研究,优选使用啮齿科、犬科和非人灵长科的物种。优选的啮齿物种是小鼠和大鼠。优选的非人灵长类动物是猕猴、猩猩和长尾猕猴。
在一个实施方案中,根据本发明使用的抗体除人靶蛋白外还对选自小鼠、大鼠和长尾猕猴(食蟹猴)的至少一个其它物种的靶蛋白呈交叉反应性。尤其优选的是除人靶蛋白外至少对小鼠靶蛋白呈交叉反应性的根据本发明使用的抗体。优选的是对其它非人物种的靶蛋白的亲和力与对人靶蛋白的亲和力相差不大于50倍,特别是不大于10倍的交叉反应性抗体。
针对癌症靶分子的抗体
结合剂,例如抗体或其结合抗原的片段所针对的靶分子优选是癌症靶分子。术语“癌症靶分子”描述与相同组织类型的非癌细胞相比更大量存在于一种或多种癌细胞种类上的靶分子。优选地,癌症靶分子与相同组织类型的非癌细胞相比选择性存在于一种或多种癌细胞种类上,其中选择性描述与相同组织类型的非癌细胞相比至少两倍富集在癌细胞上(“选择性癌症靶分子”)。癌症靶分子的使用允许通过根据本发明的缀合物选择性治疗癌细胞。
对抗原,例如癌细胞抗原特异性的抗体可以由本领域普通技术人员借助他已知的方法(例如重组表达)制备或可商业获得(例如获自Merck KGaA,德国)。癌症疗法中的已知市售抗体的实例是(西妥昔单抗,Merck KGaA)、(贝伐单抗,Roche)和(曲妥珠单抗,Genentech)。曲妥珠单抗是IgG1κ型重组人源化单克隆抗体,其在细胞基检测中以高亲和力(Kd=5nM)结合人表皮生长受体的细胞外结构域。该抗体在CHO细胞中重组制成。所有这些抗体也可通过借助PNGase F去糖基化或通过重链的N297(Kabat编号)突变成任意氨基酸而作为这些抗体的无糖基化变体来制备。
在一个优选实施方案中,该靶分子是选择性癌症靶分子。
在一个特别优选的实施方案中,该靶分子是蛋白。
在一个实施方案中,该靶分子是细胞外靶分子。在一个优选实施方案中,该细胞外靶分子是蛋白。
癌症靶分子是本领域技术人员已知的。下面列出它们的实例。
癌症靶分子的实例是:
(1)EGFR(EGF受体,NCBI参考序列NP_005219.2,NCBI Gene ID:1956)
(2)间皮素(SwissProt Reference Q13421-3),其中间皮素由氨基酸296-598编码。氨基酸37-286编码巨核细胞-增强因子。间皮素通过GPI锚而锚定在细胞膜中,且在细胞外局部化。
(3)碳酸酐酶IX(CA9,SwissProt Reference Q16790),NCBI Gene ID:768)
(4)C4.4a(NCBI参考序列NP_055215.2;同义词LYPD3,NCBI Gene ID:27076)
(5)CD52(NCBI参考序列NP_001794.2)
(6)Her2(ERBB2;NCBI参考序列NP_004439.2;NCBI Gene ID:2064)
(7)CD20(NCBI参考序列NP_068769.2)
(8)淋巴细胞活化抗原CD30(SwissProt ID P28908)
(9)淋巴细胞粘附分子CD22(SwissProt ID P20273;NCBI Gene ID:933)
(10)骨髓细胞表面抗原CD33(SwissProt ID P20138;NCBI Gene ID:945)
(11)跨膜糖蛋白NMB(GPNMB,SwissProt ID Q14956,NCBI Gene ID:10457)
(12)粘附分子CD56(SwissProt ID P13591)
(13)表面分子CD70(SwissProt ID P32970,NCBI Gene ID:970)
(14)表面分子CD74(SwissProt ID P04233,NCBI Gene ID:972)
(15)B-淋巴细胞抗原CD19(SwissProt ID P15391,NCBI Gene ID:930)
(16)表面蛋白粘蛋白-1(MUC1,SwissProt ID P15941,NCBI Gene ID:4582)
(17)表面蛋白CD138(SwissProt ID P18827)
(18)整联蛋白αV(NCBI参考序列:NP_002201.1,NCBI Gene ID:3685)
(19)畸胎癌衍生的生长因子1蛋白TDGF1(NCBI参考序列:NP_003203.1,NCBI GeneID:6997)
(20)前列腺特异性的膜抗原PSMA(Swiss Prot ID:Q04609;NCBI GeneID:2346)
(21)酪氨酸蛋白激酶EPHA2(Swiss Prot ID:P29317,NCBI Gene ID:1969)
(22)表面蛋白SLC44A4(NCBI参考序列:NP_001171515.1,NCBI GeneID:80736)
(23)表面蛋白BMPR1B(SwissProt:O00238)
(24)转运蛋白SLC7A5(SwissProt:Q01650)
(25)上皮前列腺抗原STEAP1(SwissProt:Q9UHE8,Gene ID:26872)
(26)卵巢癌抗原MUC16(SwissProt:Q8WXI7,Gene ID:94025)
(27)转运蛋白SLC34A2(SwissProt:O95436,Gene ID:10568)
(28)表面蛋白SEMA5b(SwissProt:Q9P283)
(29)表面蛋白LYPD1(SwissProt:Q8N2G4)
(30)内皮素受体B型EDNRB(SwissProt:P24530,NCBI Gene ID:1910)
(31)环指蛋白RNF43(SwissProt:Q68DV7)
(32)前列腺癌相关的蛋白STEAP2(SwissProt:Q8NFT2)
(33)阳离子通道TRPM4(SwissProt:Q8TD43)
(34)补体受体CD21(SwissProt:P20023)
(35)B-细胞抗原受体复合物相关蛋白CD79b(SwissProt:P40259,NCBI Gene ID:974)
(36)细胞粘附抗原CEACAM6(SwissProt:P40199)
(37)二肽酶DPEP1(SwissProt:P16444)
(38)白介素受体IL20Rα(SwissProt:Q9UHF4,NCBI Gene ID:3559)
(39)蛋白聚糖BCAN(SwissProt:Q96GW7)
(40)肝配蛋白受体EPHB2(SwissProt:P29323)
(41)前列腺干细胞相关蛋白PSCA(NCBI参考序列:NP_005663.2)
(42)表面蛋白LHFPL3(SwissProt:Q86UP9)
(43)受体蛋白TNFRSF13C(SwissProt:Q96RJ3)
(44)B-细胞抗原受体复合物相关蛋白CD79a(SwissProt:P11912)
(45)受体蛋白CXCR5(CD185;SwissProt:P32302;NCBI Gene ID 643,NCBI参考序列:NP_001707.1)
(46)离子通道P2X5(SwissProt:Q93086)
(47)淋巴细胞抗原CD180(SwissProt:Q99467)
(48)受体蛋白FCRL1(SwissProt:Q96LA6)
(49)受体蛋白FCRL5(SwissProt:Q96RD9)
(50)MHC II类分子Ia抗原HLA-DOB(NCBI参考序列:NP_002111.1)
(51)T-细胞蛋白VTCN1(SwissProt:Q7Z7D3)
(52)TWEAKR(FN14,TNFRSF12A,NCBI参考序列:NP_057723.1,NCBI Gene ID:51330)
(53)淋巴细胞抗原CD37(Swiss Prot:P11049,NCBI Gene ID:951)
(54)FGF受体2;FGFR2(NCBI Gene ID:2263;官方符号:FGFR2)。FGFR2受体发生在不同的剪接变体(α、β、IIIb、IIIc)中。所有剪接变体均可充当靶分子。
(55)跨膜糖蛋白B7H3(CD276;NCBI Gene ID:80381NCBI参考序列:NP_001019907.1,Swiss Prot:Q5ZPR3-1)
(56)B细胞受体BAFFR(CD268;NCBI Gene ID:115650)
(57)受体蛋白ROR 1(NCBI Gene ID:4919)
(58)表面受体CD123(IL3RA;NCBI Gene ID:3563;NCBI参考序列:NP_002174.1;Swiss-Prot:P26951)
(59)受体蛋白合胞素(NCBI Gene ID 30816)
(60)天冬氨酸β-羟化酶(ASPH;NCBI Gene ID 444)
(61)细胞表面糖蛋白CD44(NCBI Gene ID:960)
(62)CDH15(钙粘素15,NCBI Gene ID:1013)
(63)细胞表面糖蛋白CEACAM5(NCBI Gene ID:1048)
(64)细胞粘附分子L1样(CHL1,NCBI Gene ID:10752)
(65)体酪氨酸激酶c-Met(NCBI Gene ID:4233)
(66)notch配体DLL3(NCBI Gene ID:10683)
(67)肝配蛋白A4(EFNA4,NCBI Gene ID:1945)
(68)异核苷酸焦磷酸酶/磷酸二酯酶3(ENPP3,NCBI Gene ID:5169)
(69)凝血因子III(F3,NCBI Gene ID:2152)
(70)FGF受体3(FGFR3,NCBI Gene ID:2261)
(71)叶酸水解酶FOLH1(NCBI Gene ID:2346)
(72)叶酸受体1(FOLR1;NCBI Gene ID:2348)
(73)鸟苷酸环化酶2C(GUCY2C,NCBI Gene ID:2984)
(74)KIT原癌基因受体酪氨酸激酶(NCBI Gene ID:3815)
(75)溶酶体相关膜蛋白1(LAMP1,NCBI Gene ID:3916)
(76)淋巴细胞抗原6复合物,基因座E(LY6E,NCBI Gene ID:4061)
(77)蛋白NOTCH3(NCBI Gene ID:4854)
(78)蛋白酪氨酸激酶7(PTK7,NCBI Gene ID:5754)
(79)结合素细胞粘附分子4(PVRL4,NECTIN4,NCBI Gene ID:81607)
(80)跨膜蛋白多配体聚糖1(SDC1,NCBI Gene ID:6382)
(81)SLAM家族成员7(SLAMF7,NCBI Gene ID:57823)
(82)转运蛋白SLC39A6(NCBI Gene ID:25800)
(83)SLIT-和NTRK-样家族成员6(SLITRK6,NCBI Gene ID:84189)
(84)细胞表面受体TACSTD2(NCBI Gene ID:4070)
(85)受体蛋白TNFRSF8(NCBI Gene ID:943)
(86)受体蛋白TNFSF13B(NCBI Gene ID:10673)
(87)糖蛋白TPBG(NCBI Gene ID:7162)
(88)细胞表面受体TROP2(TACSTD2,NCBI Gene ID:4070)
(89)甘丙肽样G蛋白偶联受体KISS1R(GPR54,NCBI Gene ID:84634)
(90)转运蛋白SLAMF6(NCBI Gene ID:114836)。
在本发明的一个优选主题中,该癌症靶分子选自癌症靶分子EGFR、CD123、Her2、B7H3、TWEAKR和CXCR5,尤其是CD123、CXCR5和B7H3。
在本发明的另一个特别优选的主题中,该结合剂结合至选自以下的细胞外癌症靶分子:癌症靶分子EGFR、CD123、Her2、B7H3、TWEAKR和CXCR5,尤其是CD123、CXCR5和B7H3。
在本发明的另一个特别优选的主题中,该结合剂特异性结合至选自癌症靶分子EGFR、CD123、Her2、B7H3、TWEAKR和CXCR5、特别是CD123、CXCR5和B7H3的细胞外癌症靶分子。在一个优选实施方案中,该结合剂在结合至其在靶细胞上的细胞外靶分子后通过该结合被靶细胞内化。这导致该结合剂-活性物质-缀合物(其可以是免疫缀合物或ADC)被靶细胞吸收。随后优选在细胞内,优选借助溶酶体处理该结合剂。
在一个实施方案中,该结合剂是结合蛋白。在一个优选实施方案中,该结合剂是抗体、结合抗原的抗体片段、多特异性抗体或拟抗体。
优选的拟抗体是亲和体、Adnectin、Anticalin、DARPin、Avimer或纳米抗体。优选的多特异性抗体是双特异性和三特异性抗体。
在一个优选实施方案中,该结合剂是抗体或结合抗原的抗体片段,更优选分离的抗体或分离的结合抗原的抗体片段。
优选的结合抗原的抗体片段是Fab、Fab'、F(ab')2和Fv片段、双价抗体、DAb、线性抗体和scFv。特别优选的是Fab、双价抗体和scFv。
在一个特别优选的实施方案中,该结合剂是抗体。特别优选的是单克隆抗体或其结合抗原的抗体片段。更特别优选的是人、人源化或嵌合抗体或其结合抗原的抗体片段。
结合癌症靶分子的抗体或结合抗原的抗体片段可由本领域普通技术人员使用已知方法制备,例如化学合成或重组表达。用于癌症靶分子的结合剂可以商业获得或可以由本领域普通技术人员使用已知方法制备,例如化学合成或重组表达。在WO 2007/070538(参见第22页“抗体”)中描述了用于制备抗体或结合抗原的抗体片段的其它方法。本领域技术人员知道如何可以建立所谓的噬菌体展示库(例如Morphosys HuCAL Gold)并用于发现抗体或结合抗原的抗体片段(参见WO 2007/070538,第24页及其后和第70页中的AK实施例1、第72页中的AK实施例2)。例如在第26页中(WO 2007/070538)描述了使用来自B细胞的DNA库制备抗体的其它方法。抗体的人源化方法描述在WO2007070538的第30-32页中并详细描述在Queen等人,Pros.Natl.Acad.Sci.USA86:10029-10033,1989或WO 90/0786中。此外,通常蛋白,特别是抗体的重组表达方法是本领域技术人员已知的(参见例如Berger和Kimrnel(Guide to Molecular Cloning Techniques,Methods in Enzymology,第152卷,AcademicPress,Inc.);Sambrook,等人,(Molecular Cloning:ALaboratory Manual,(第二版,ColdSpring Harbor Laboratory Press;Cold Spring Harbor,N.Y.;1989)第1-3卷);CurrentProtocols in Molecular Biology,(F.M.Ausabel等人[编],Current Protocols,GreenPublishing Associates,Inc./John Wiley&Sons,Inc.);Harlow等人,(MonoclonalAntibodies:ALaboratory Manual,Cold Spring Harbor Laboratory Press(19881,Paul[编]);Fundamental Immunology,(Lippincott Williams&Wilkins(1998));和Harlow等人,(Using Antibodies:A Laboratory Manual,Cold Spring Harbor Laboratory Press(1998))。本领域技术人员知道对于蛋白/抗体的表达而言所必需的相应载体、启动子和信号肽。常见方法也描述在WO 2007/070538第41-45页中。例如在WO 2007/070538第74页及其后的实施例6中描述了制备IgG1抗体的方法。可用于测定抗体在结合至其抗原后的内化的方法是本领域技术人员已知的并例如描述在WO 2007/070538第80页中。本领域技术人员能够使用WO 2007/070538中描述的方法,其已用于与具有其它靶分子特异性的抗体的制备类似地制备碳酸酐酶IX(Mn)抗体。
细菌表达
本领域技术人员知悉可以何种方式借助细菌表达来制备抗体、其结合抗原的片段或其变体。
适合用于所需蛋白的细菌表达的表达载体通过在功能阅读框架内插入编码所需蛋白的DNA序列与合适的翻译起始信号和翻译终止信号和与功能性启动子一起来构建。所述载体包含一个或多个表型上可选择的标记和复制起点,以使得能够保留载体、且在需要的情况下在宿主内进行自身扩增。适合用于转化的原核细胞宿主包括但不限于大肠杆菌、枯草芽孢杆菌(Bacillus subtilis)、鼠伤寒沙门氏菌(Salmonella typhimurium)和来自假单孢菌属(Pseudomonas)、链霉菌属(Streptomyces)和葡萄球菌属(Staphylococcus)的各种菌种。细菌载体可例如基于噬菌体、质粒或噬菌粒。这些载体可含有可选择标记和细菌复制起点,其可衍生自市售的质粒。许多市售的质粒通常含有众所周知的克隆载体pBR322(ATCC 37017)的元件。在细菌系统中,可以基于待表达的蛋白的目标用途,选择许多有利的表达载体。
在将合适的宿主菌株转化以及宿主菌株生长至适当的细胞密度后,通过合适的手段(例如改变温度或化学诱导)将所选的启动子去-抑制(de-reprimiert)/诱导,并将细胞再培养一段时间。通常通过离心来收获细胞,如果需要以物理方式或化学手段消化(aufgeschlossen),并保留所得的粗提取物用于进一步纯化。
因此,本发明的另一实施方案是表达载体,其包含编码本发明的新型抗体的核酸。
本发明的抗体或其结合抗原的片段包括天然纯化的产物、源自化学合成的产物以及通过重组技术在原核细胞宿主,例如大肠杆菌、枯草芽孢杆菌、鼠伤寒沙门氏菌和来自假单孢菌属、链霉菌属和葡萄球菌属的各种菌种,优选大肠杆菌中所产生的产物。
哺乳动物细胞表达
本领域技术人员知悉可以何种方式借助哺乳动物细胞表达来制备抗体、其结合抗原的片段或其变体。
用于在哺乳动物细胞宿主中表达的优选的调控序列包括在哺乳动物细胞中导致高表达的病毒元件,例如衍生自巨细胞病毒(CMV)(例如CMV启动子/增强子)、猿猴病毒40(SV40)(例如SV40启动子/增强子)、腺病毒(例如腺病毒主要晚期启动子(AdMLP))和多瘤病毒的启动子和/或表达扩增子。抗体的表达可以是组成型或调控型的(例如通过加入或移除小分子诱导剂,例如四环霉素与Tet系统的组合来诱导)。
对于病毒调控元件和其序列的进一步说明参照例如Stinski的U.S.5,168,062、Bell等人的U.S.4,510,245以及Schaffner等人的U.S.4,968,615。重组表达载体同样地可包括复制起点和可选择标记(参见例如U.S.4,399,216、4,634,665和U.S.5,179,017)。合适的可选择标记包括赋予对物质,例如G418、嘌呤霉素、潮霉素、杀稻瘟素、吉欧霉素(Zeocin)/博莱霉素(Bleomycin)或甲氨喋呤的抗性的基因,或当该载体已引入细胞时导致宿主细胞营养缺陷的可选择标记,例如谷氨酰胺合成酶(Bebbington等人,Biotechnology(N Y).1992Feb;10(2):169-75)。
例如,二氢叶酸还原酶(DHFR)基因赋予对甲氨喋呤的抗性,neo基因赋予对G418的抗性,来自土曲菌(Aspergillus terreus)的bsd基因赋予对杀稻瘟素的抗性,嘌呤霉素N-乙酰基移转酶赋予对嘌呤霉素的抗性,Sh ble基因产物赋予对吉欧霉素的抗性,且大肠杆菌潮霉素抗性基因(hyg或hph)赋予对潮霉素的抗性。可选择标记,例如DHFR或谷氨酰胺合成酶也有助于结合MTX和MSX的扩增技术。
将表达载体转染至宿主细胞中可借助标准技术来执行,尤其是借助电穿孔、核转染、磷酸钙沉淀、脂质转染、基于聚阳离子的转染,例如基于聚乙烯亚胺(PEI)的转染和DEAE-葡聚糖转染。
适合用于抗体、其结合抗原的片段或其变体的表达的哺乳动物宿主细胞包括中国仓鼠卵巢(CHO细胞),例如CHO-K1、CHO-S、CHO-K1SV[包括DHFR-CHO细胞,描述于Urlaub和Chasin,(1980)Proc.Natl.Acad.Sci.USA 77:4216-4220和Urlaub等人,Cell.1983Jun;33(2):405-12,与DHFR可选择标记一起使用,如R.J.Kaufman和P.A.Sharp(1982)Mol.Biol.159:601-621中所述,以及其它敲除细胞,如详述于Fan等人,BiotechnolBioeng.2012Apr;109(4):1007-15中),NS0骨髓瘤细胞、COS细胞、HEK293细胞、HKB11细胞、BHK21细胞、CAP细胞、EB66细胞和SP2细胞。
抗体、其结合抗原的片段或其变体的表达也可在表达系统例如HEK293、HEK293T、HEK293-EBNA、HEK293E、HEK293-6E、HEK293-Freestyle、HKB11、Expi293F、293EBNALT75、CHO-Freestyle、CHO-S、CHO-K1、CHO-K1SV、CHOEBNALT85、CHOS-XE、CHO-3E7或CAP-T细胞(例如,如Durocher等人,Nucleic Acids Res.2002Jan 15;30(2):E9)中以瞬时或半稳定方式来进行。
在一些实施方案中,表达载体以如下方式构建,以使得待表达的蛋白分泌至其中宿主细胞生长的细胞培养基中。抗体、其结合抗原的片段或其变体也可借助本领域技术人员已知的蛋白纯化方法从细胞培养基中获得。
纯化
抗体、其结合抗原的片段或其变体可从重组的细胞培养物中借助众所周知的方法来获得并纯化,该方法例如包括硫酸铵沉淀或乙醇沉淀、酸萃取、蛋白A色谱、蛋白G色谱、阴离子或阳离子交换色谱、磷酸纤维素色谱、疏水作用色谱(HIC)、亲和色谱、羟磷灰石色谱和凝集素色谱。高效液相色谱(“HPLC”)同样可用来纯化。参见例如Colligan,CurrentProtocols in Immunology,或Current Protocols in Protein Science,John Wiley&Sons,NY,N.Y.,(1997-2001),例如第1、4、6、8、9、10章。
本发明的抗体或其结合抗原的片段或其变体包括天然纯化产物、化学合成法的产物和借助重组技术在原核或真核宿主细胞中所制成的产物。真核细胞宿主包括例如酵母细胞、高等植物细胞、昆虫细胞和哺乳动物细胞。根据对于重组表达所选择的宿主细胞,所表达的蛋白可以是糖基化或非糖基化形式。
在一个优选的实施方案中,该抗体以(1)高于95重量%(例如通过Lowry法、通过UV-Vis光谱或通过SDS毛细管凝胶电泳法(例如使用Caliper LabChip GXII,GX 90或Biorad Bioanalyzer仪器)测量),和在更优选的实施方案中以大于99重量%的程度纯化,(2)以适合于决定N-末端或内部氨酸序列的至少15个残基的程度纯化,或(3)纯化至同质性(通过SDS-PAGE在还原或非还原条件下借助马考斯蓝染色或优选银染色所测定)。
通常,分离的抗体借助至少一个蛋白纯化步骤获得。
抗-CD123抗体
根据本发明,可使用抗-CD123抗体。
术语“抗-CD123抗体”或“特异性结合至CD123的抗体”是指结合癌症靶分子CD123((IL3RA;NCBI-Gene ID:3563;NCBI参考序列:NP_002174.1;Swiss-Prot:P26951;SEQ IDNO:111)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合CD123。
Sun等人(Sun等人,1996,Blood 87(1):83-92)描述了结合IL-3Rα的N-末端结构域、CD123的单克隆抗体7G3的生成和性质。美国专利号6,177,078(Lopez)涉及抗-CD123抗体7G3。该抗体的嵌合变体(CSL360)描述于WO 2009/070844,以及人源化版本(CSL362)描述于WO 2012/021934中。7G3抗体的序列公开于EP2426148。此序列构成由CDR移植("CDR嫁接")获得的人源化抗体的起始点。
在细胞表面抗原结合后被特别好地内化的抗体是Kuo等人所公开的抗-CD123抗体12F1(Kuo等人,2009,Bioconjug Chem.20(10):1975-82)。抗体12F1以比抗体7G3更高的亲和力与CD123结合,并在细胞表面抗原结合后比7G3明显更快内化。基于12F1的双特异性scFv免疫融合蛋白公开于WO 2013/173820。抗体TPP-6013是12F1的嵌合变体。
本发明尤其涉及具有归因于源自小鼠的抗体7G3(Sun等人,1996,Blood 87(1):83-92)和12F1(Kuo等人,2009,Bioconjug Chem.20(10):1975-82)的抗体或其结合抗原的片段或其变体的缀合物,或具有归因于源自小鼠的抗体12F1(Kuo等人,2009,BioconjugChem.20(10):1975-82)的抗体或其结合抗原的片段或其变体的缀合物。
鼠7G3抗体以及鼠12F1抗体的人源化变体基于CDR移植("CDR嫁接")至人框架中并随后优化来生成,并且是本发明上下文中的优选实例。
在本发明的上下文中特别优选抗-CD123抗体TPP-9476、TPP-8988、TPP-8987和TPP-6013。
抗-CXCR5抗体
根据本发明,可使用抗-CXCR5抗体。
术语“抗-CXCR5抗体”或“特异性结合至CXCR5的抗体”是指结合癌靶分子CXCR5(NCBI参考序列:NP_001707.1;SEQ ID NO:112)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合CXCR5。
结合至CXCR5的抗体和结合抗原的片段的实例是本领域技术人员已知的并例如描述于EP2195023中。
用于大鼠抗体RF8B2(ACC2153)的杂交瘤细胞购自DSMZ并通过标准方法鉴定该抗体的序列。该序列构成通过CDR移植("CDR嫁接")所获得的人源化抗体的起始点。
基于CDR移植("CDR嫁接")至种系序列中来生成该抗体的人源化变体。
这些抗体和结合抗原的片段可用于本发明的上下文中。
在本发明的上下文中特别优选抗-CXCR5抗体TPP-9574和TPP-9580。
抗-B7H3抗体
根据本发明,可使用抗-B7H3抗体。
术语“抗-B7H3抗体”或“特异性结合至B7H3的抗体”是指结合癌靶标分子B7H3(NCBI参考序列:NP_001019907.1SEQ ID NO:113)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合B7H3。
结合至B7H3的抗体和结合抗原的片段的实例是本领域技术人员已知的,并且描述于例如WO201109400、EP1773884和WO2014061277中。EP2121008描述了抗-B7H3抗体8H9及其CDR序列。
这些抗体和结合抗原的片段可用于本发明的上下文中。
通过针对表达小鼠的重组B7H3(小鼠CD276;基因ID:102657)和人B7H3(人CD276;基因ID:80381)的细胞筛选抗体噬菌体展示文库来获得抗-B7H3抗体的优选实施方案。将获得的抗体转化为人IgG1形式。抗-B7H3抗体TPP-8382是优选的实例。
在本发明的上下文中特别优选抗-B7H3抗体TPP-8382。
抗-TWEAKR抗体
根据本发明,可使用抗-TWEAKR抗体。
术语“抗-TWEAKR抗体”或“特异性结合至TWEAKR的抗体”是指结合癌靶标分子TWEAKR(NCBI参考序列:NP_057723.1SEQ ID NO:114)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合TWEAKR。
结合至TWEAKR的抗体的实例公开于例如WO2009/020933(A2)、WO2009/140177(A2)、WO 2014/198817(A1)和WO 2015/189143(A1)中。这些抗体和结合抗原的片段可用于本发明的上下文中。
ITEM-4是抗-TWEAKR抗体,其由Nakayama等人(Nakayama,等人,2003,BiochemBiophy Res Comm,306:819-825)描述。Zhou等人(Zhou等人,2013,J Invest Dermatol.133(4):1052-62)和WO 2009/020933中描述了基于CDR移植("CDR嫁接")的该抗体的人源化变体。这些抗体和结合抗原的片段可用于本发明的上下文中。
在本发明的上下文中特别优选抗-TWEAKR抗体TPP-7006和TPP-7007。这些是抗体ITEM-4的人源化变体。这些抗体和结合抗原的片段优选可用于本发明的上下文中。
抗-HER2抗体:
根据本发明,可使用抗-HER2抗体。
术语“抗-HER2抗体”或“特异性结合至HER2的抗体”是指结合癌靶标分子HER2(NCBI参考序列:NP_004439.2SEQ ID NO:115)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合HER2。
结合癌症靶分子Her2的抗体的实例是曲妥珠单抗(Genentech)。曲妥珠单抗是人源化抗体,其尤其用于治疗乳腺癌。在一个特别优选的实施方案中,抗-HER2抗体是TPP-1015(曲妥珠单抗类似物)。
除了曲妥珠单抗(INN 7637,CAS编号:RN:180288-69-1)和帕妥珠单抗(CAS编号:380610-27-5)以外,结合至HER2的抗体的其它实例是如WO 2009/123894-A2、WO 200/8140603-A2或WO 2011/044368-A2中公开的抗体。抗-HER2缀合物的实例是曲妥珠单抗-Emtansine(INN编号9295)。这些抗体和结合抗原的片段可用于本发明的上下文中。
在本发明的上下文中特别优选抗-HER2抗体TPP-1015(类似于曲妥珠单抗)。
抗-EGFR抗体
根据本发明,可使用抗-EGFR抗体。
术语“抗-EGFR抗体”或“特异性结合至EGFR的抗体”是指结合癌靶标分子EGFR(NCBI参考序列:NP_005219.2SEQ ID NO:116)的抗体,优选地以足够用于诊断和/或治疗应用的亲和力结合。在特定实施方案中,所述抗体以≤1μM、≤100nM、≤10nM、≤1nM、≤0.1nM、≤0.01nM或≤0.001nM的解离常数(KD)结合EGFR。
在一个优选实施方案中,所述抗-EGFR抗体选自TPP-981、西妥昔单抗、帕尼单抗、尼妥珠单抗。在一个特别优选的实施方案中,所述抗-EGFR抗体是TPP-981。
EGFR抗体的其它实施方案是:
·扎芦木单抗/2F8/HuMax-EGFr,来自Genmab A/S公司(WO 02/100348,WO 2004/056847,INN编号8605)
·奈昔木单抗/11F8,ImClone/IMC-11F8,来自ImClone Systems Inc.[EliLilly&Co]公司(WO 2005/090407(EP 01735348-A1、US 2007/0264253-A1、US 7,598,350、WO 2005/090407-A1),INN编号9083)·马妥珠单抗/抗-EGFR MAb,Merck KGaA/抗-EGFRMAb,Takeda/EMD 72000/EMD-6200/EMD-72000和EMD-55900/MAb 425/单克隆抗体425,来自Merck KGaA/Takeda公司(WO 92/15683,INN编号8103(马妥珠单抗))
·RG-7160/GA-201/GA201/R-7160/R7160/RG7160/RO-4858696/RO-5083945/RO4858696/RO5083945,来自Glycart Biotechnology AG(Roche Holding AG)公司(WO2010/112413-A1、WO 2010/115554)
·GT-MAB 5.2-GEX/CetuGEX,来自Glycotope GmbH公司(WO 2008/028686-A2(EP01900750-A1、EP 01911766-A1、EP 02073842-A2、US 2010/0028947-A1)
·ISU-101,来自Isu Abxis Inc(ISU Chemical Co Ltd)公司/Scancell(WO2008/004834-A1)
·ABT-806/mAb-806/ch-806/抗-EGFR单克隆抗体806,来自Ludwig Institutefor Cancer Research公司/Abbott/Life Science Pharmaceuticals(WO 02/092771、WO2005/081854和WO 2009/023265)
·SYM-004(由两个嵌合IgG1抗体(992和1024)组成),来自Symphogen A/S公司(WO2010/022736-A2)
·MR1-1/MR1-1KDEL,来自IVAX Corp(Teva Pharmaceutical Industries Ltd)公司(杜克大学),(专利:WO2001/062931-A2)
·针对缺失突变体EGFRvIII的抗体,来自Amgen/Abgenix公司(WO 2005/010151、US 7,628,986)
·SC-100,来自Scancell Ltd公司(WO 01/088138-A1)
·MDX-447/EMD 82633/BAB-447/H 447/MAb,EGFR,Medarex/Merck KgaA,来自Bristol-Myers Squibb(US)/Merck KGaA(DE)/Takeda(JP)公司(WO 91/05871、WO 92/15683)
·抗-EGFR-Mab,来自Xencor公司(WO 2005/056606)
·DXL-1218/抗-EGFR单克隆抗体(癌症),InNexus,来自InNexus BiotechnologyInc公司,Pharmaprojects PH048638。
抗-碳酸酐酶IX抗体
结合癌症靶分子碳酸酐酶IX的抗体的实例描述于WO 2007/070538-A2(例如权利要求1-16)中。
抗-C4.4a抗体:
C4.4a抗体和结合抗原的片段的实例描述于WO 2012/143499 A2中。抗体的序列在WO 2012/143499 A2的表1中给出,其中每行显示第1列中列出的抗体的可变轻链或可变重链的各自的CDR氨基酸序列。
抗-CD20抗体:
结合癌症靶分子CD20的抗体的实例是利妥昔单抗(Genentech)。利妥昔单抗(CAS编号:174722-31-7)是用于治疗非霍奇金氏淋巴瘤的嵌合抗体。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-CD52抗体:
结合癌症靶分子CD52的抗体的实例是阿仑单抗(Genzyme)。阿仑单抗(CAS编号:216503-57-0)是用于治疗慢性淋巴细胞白血病的人源化抗体。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-间皮素抗体:
抗-间皮素抗体的实例描述于例如WO2009/068204中。WO2009/068204公开的所有抗体和结合抗原的片段可用于本文公开的本发明的上下文中。特别优选地,WO2009/068204中公开的抗体是MF-T。
抗-CD30抗体
结合癌症靶分子CD30且可用于治疗癌症(例如霍奇金氏淋巴瘤)的抗体的实例是Brentuximab、伊妥木单抗和如WO 2008/092117、WO 2008/036688或WO 2006/089232中公开的抗体。抗-CD30缀合物的实例是Brentuximab Vedotin(INN编号9144)。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-CD22抗体
结合癌症靶分子CD22且可用于治疗癌症(例如淋巴瘤)的抗体的实例是Inotuzumab和依帕珠单抗。抗-CD22缀合物的实例是Inotuzumab Ozagamycin(INN编号8574)或抗-CD22-MMAE和抗-CD22-MC-MMAE(CAS编号分别为:139504-50-0和474645-27-7)。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-CD33抗体
结合癌症靶分子CD33且可用于治疗癌症(例如白血病)的抗体的实例是吉姆单抗和林妥珠单抗(INN 7580)。抗-CD33缀合物的实例是吉姆单抗-奥扎格霉素。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-NMB抗体
结合癌症靶分子NMB且可用于治疗癌症(例如黑色素瘤或乳腺癌)的抗体的实例是Glembatumumab(INN 9199)。抗-NMB缀合物的实例是Glembatumumab Vedotin(CAS编号:474645-27-7)。这些抗体和抗其原结合片段可用于本发明的上下文中。
抗-CD56抗体
结合癌症靶分子CD56且可用于治疗癌症(例如多发性骨髓瘤、小细胞肺癌、MCC或卵巢癌)的抗体的实例是洛伐单抗。抗-CD57缀合物的实例是洛伐珠单抗美登素(CAS编号:139504-50-0)。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-CD70抗体
结合癌症靶分子CD70且可用于治疗癌症(例如非霍奇金氏淋巴瘤或肾细胞癌)的抗体的实例公开于WO 2007/038637-A2和WO 2008/070593-A2中。抗-CD70缀合物的实例是SGN-75(CD70 MMAF)。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-CD74抗体
结合癌症靶分子CD74且可用于治疗癌症(例如多发性骨髓瘤)的抗体的实例是米拉珠单抗。抗-CD74缀合物的实例是米拉珠单抗-多柔比星(CAS号:23214-92-8)。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-CD19抗体
结合癌症靶分子CD19且可用于治疗癌症(例如非霍奇金氏淋巴瘤)的抗体的实例公开于WO 2008/031056-A2中。其它抗体和抗-CD19缀合物(SAR3419)的实例公开于WO2008/047242-A2中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-粘蛋白抗体
结合癌症靶分子粘蛋白-1且可用于治疗癌症(例如非霍奇金氏淋巴瘤)的抗体的实例是Clivatuzumab或WO 2003/106495-A2、WO 2008/028686-A2中公开的抗体。抗-粘蛋白缀合物的实例公开于WO 2005/009369-A2中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-CD138抗体
可用于治疗癌症(例如多发性骨髓瘤)的结合癌症靶分子CD138的抗体及其缀合物的实例公开于WO 2009/080829-A1、WO 2009/080830-A1中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-整联蛋白-αV抗体
结合癌症靶分子整联蛋白αV且可用于治疗癌症(例如黑素瘤、肉瘤或癌)的抗体的实例是英妥木单抗(CAS编号:725735-28-4)、阿昔单抗(CAS编号:143653-53-6)、埃达珠单抗(CAS编号:892553-42-3)或US 7,465,449、EP 719859-A1、WO 2002/012501-A1或WO2006/062779-A2中公开的抗体。抗-整联蛋白αV缀合物的实例是Intetumumab-DM4和WO2007/024536-A2中公开的其它ADC。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-TDGF1抗体
结合癌症靶分子TDGF1且可以用于治疗癌症的抗体的实例是WO 02/077033-A1、US7,318,924、WO 2003/083041-A2和WO 2002/088170-A2中公开的抗体。抗-TDGF1缀合物的实例公开于WO 2002/088170-A2中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-PSMA抗体
结合癌症靶分子PSMA且可以用于治疗癌症(例如前列腺癌)的抗体的实例是WO97/35616-A1、WO 99/47554-A1、WO 01/009192-A1和WO2003/034903中公开的抗体。抗-PSMA缀合物的实例公开于WO 2009/026274-A1和WO 2007/002222中。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-EPHA2抗体
结合癌症靶分子EPHA2且可用于制备缀合物和用于治疗癌症的抗体的实例公开于WO 2004/091375-A2中。这些抗体和结合抗原的片段可用于本发明的上下文中。
抗-SLC44A4抗体
结合癌症靶分子SLC44A4且可用于制备缀合物和用于治疗癌症(例如胰腺或前列腺癌)的抗体的实例公开于WO2009/033094-A2和US2009/0175796-A1中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-HLA-DOB抗体
结合癌症靶分子HLA-DOB的抗体的实例是抗体Lym-1(CAS编号:301344-99-0),其可用于治疗癌症例如非霍奇金氏淋巴瘤。抗-HLA-DOB缀合物的实例公开于例如WO 2005/081711-A2中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-VTCN1抗体
结合癌症靶分子VTCN1且可用于制备缀合物和用于治疗癌症(例如卵巢癌、胰腺癌、肺癌或乳腺癌)的抗体的实例公开于WO 2006/074418-A2中。这些抗体和其结合抗原的片段可用于本发明的上下文中。
抗-FGFR2抗体
抗-FGFR2抗体和结合抗原的片段的实例描述于WO2013076186中。抗体的序列显示于WO2013076186的表9和表10中。优选衍生自称为M048-D01和M047-D08的抗体的抗体、结合抗原的片段和抗体的变体。
用于根据本发明的结合剂-活性物质-缀合物的优选的抗体和结合抗原的抗体片段
在本申请中,结合剂-活性物质-缀合物参考如下表中所示的下列优选的抗体:TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574和TPP-9580。
表:抗体的蛋白序列:
TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574和TPP-9580是包含一个或多个上表中所给出的重链可变区(VH)或轻链可变区(VL)的CDR序列(H-CDR1、H-CDR2、H-CDR3、L-CDR1、L-CDR2、L-CDR3)的抗体。优选地,所述抗体包含给出的重链可变区(VH)和/或轻链可变区(VL)。优选地,所述抗体包含给出的重链区(IgG重链)和/或给出的轻链区(IgG轻链)。
TPP-981是包含重链可变区(VH)和轻链可变区(VL)的抗-EGFR抗体,所述重链可变区包含如SEQ ID NO:2所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:3所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:4所示的重链可变CDR3序列(H-CDR3),所述轻链可变区包含如SEQ ID NO:6所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:7所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:8所示的轻链可变CDR3序列(L-CDR3)。
TPP-1015是包含重链可变区(VH)和轻链可变区(VL)的抗-HER2抗体,所述重链可变区包含如SEQ ID NO:12所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:13所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:14所示的重链可变CDR3序列(H-CDR3),所述轻链可变区包含如SEQ ID NO:16所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:17所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:18所示的轻链可变CDR3序列(L-CDR3)。
TPP-6013是包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:22所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:23所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:24所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:26所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:27所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:28所示的轻链可变CDR3序列(L-CDR3)。
TPP-7006是包含重链可变区(VH)和轻链可变区(VL)的抗-TWEAKR抗体,所述重链可变区包含如SEQ ID NO:32所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:33所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:34所示的重链可变CDR3序列(H-CDR3),所述轻链可变区包含如SEQ ID NO:36所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:37所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:38所示的轻链可变CDR3序列(L-CDR3)。
TPP-7007是包含重链可变区(VH)和轻链可变区(VL)的抗-TWEAKR抗体,所述重链可变区包含如SEQ ID NO:42所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:43所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:44所示的重链可变CDR3序列(H-CDR3),所述轻链可变区包含如SEQ ID NO:46所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:47所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:48所示的轻链可变CDR3序列(L-CDR3)。
TPP-8382是包含重链可变区(VH)和轻链可变区(VL)的抗-B7H3抗体,所述重链可变区包含如SEQ ID NO:52所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:53所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:54所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:56所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:57所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:58所示的轻链可变CDR3序列(L-CDR3)。
TPP-8987是包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:62所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:63所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:64所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:66所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:67所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:68所示的轻链可变CDR3序列(L-CDR3)。
TPP-8988是包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:72所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:73所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:74所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:76所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:77所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:78所示的轻链可变CDR3序列(L-CDR3)。
TPP-9476是包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:82所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:83所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:84所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:86所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:87所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:88所示的轻链可变CDR3序列(L-CDR3)。
TPP-9574是包含重链可变区(VH)和轻链可变区(VL)的抗-CXCR5抗体,所述重链可变区包含如SEQ ID NO:92所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:93所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:94所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:96所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:97所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:98所示的轻链可变CDR3序列(L-CDR3)。
TPP-9580是包含重链可变区(VH)和轻链可变区(VL)的抗-CXCR5抗体,所述重链可变区包含如SEQ ID NO:102所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:103所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:104所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:106所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:107所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:108所示的轻链可变CDR3序列(L-CDR3)。
TPP-981是优选包含如SEQ ID NO:1中所示的重链可变区(VH)和如SEQ ID NO:5中所示的轻链可变区(VL)的抗-EGFR抗体。
TPP-1015是优选包含如SEQ ID NO:11所示的重链可变区(VH)和如SEQ ID NO:15所示的轻链可变区(VL)的抗-HER2抗体。
TPP-6013是优选包含如SEQ ID NO:21中所示的重链可变区(VH)和如SEQ ID NO:25中所示的轻链可变区(VL)的抗-CD123抗体。
TPP-7006是优选包含如SEQ ID NO:31中所示的重链可变区(VH)和如SEQ ID NO:35中所示的轻链可变区(VL)的抗-TWEAKR抗体。
TPP-7007是优选包含如SEQ ID NO:41中所示的重链可变区(VH)和如SEQ ID NO:45中所示的轻链可变区(VL)的抗-TWEAKR抗体。
TPP-8382是优选包含如SEQ ID NO:51中所示的重链可变区(VH)和如SEQ ID NO:55中所示的轻链可变区(VL)的抗-B7H3抗体。
TPP-8987是优选包含如SEQ ID NO:61中所示的重链可变区(VH)和如SEQ ID NO:65中所示的轻链可变区(VL)的抗-CD123抗体。
TPP-8988是优选包含如SEQ ID NO:71中所示的重链可变区(VH)和如SEQ ID NO:75中所示的轻链可变区(VL)的抗-CD123抗体。
TPP-9476是优选包含如SEQ ID NO:81中所示的重链可变区(VH)和如SEQ ID NO:85中所示的轻链可变区(VL)的抗-CD123抗体。
TPP-9574是优选包含如SEQ ID NO:91中所示的重链可变区(VH)和如SEQ ID NO:95中所示的轻链可变区(VL)的抗-CXCR5抗体。
TPP-9580是优选包含如SEQ ID NO:101中所示的重链可变区(VH)和如SEQ ID NO:105中所示的轻链可变区(VL)的抗-CXCR5抗体。
TPP-981是优选包含如SEQ ID NO:9中所示的重链区和如SEQ ID NO:10中所示的轻链区的抗-CD123抗体。
TPP-1015是优选包含如SEQ ID NO:19所示的重链区和如SEQ ID NO:20所示的轻链区的抗-HER2抗体。
TPP-6013是优选包含如SEQ ID NO:29中所示的重链区和如SEQ ID NO:30中所示的轻链区的抗-CD123抗体。
TPP-7006是优选包含如SEQ ID NO:39中所示的重链区和如SEQ ID NO:40中所示的轻链区的抗-TWEAKR抗体。
TPP-7007是优选包含如SEQ ID NO:49中所示的重链区和如SEQ ID NO:50中所示的轻链区的抗-TWEAKR抗体。
TPP-8382是优选包含如SEQ ID NO:59中所示的重链区和如SEQ ID NO:60中所示的轻链区的抗-B7H3抗体。
TPP-8987是优选包含如SEQ ID NO:69中所示的重链区和如SEQ ID NO:70中所示的轻链区的抗-CD123抗体。
TPP-8988是优选包含如SEQ ID NO:79中所示的重链区和如SEQ ID NO:80中所示的轻链区的抗-CD123抗体。
TPP-9476是优选包含如SEQ ID NO:89中所示的重链区和如SEQ ID NO:90中所示的轻链区的抗-CD123抗体。
TPP-9574是优选包含如SEQ ID NO:99中所示的重链区和如SEQ ID NO:100中所示的轻链区的抗-CXCR5抗体。
TPP-9580是优选包含如SEQ ID NO:109中所示的重链区和如SEQ ID NO:110中所示的轻链区的抗-CXCR5抗体。
同位素、盐、溶剂化物、同位素变体
本发明还涵盖本发明的化合物的所有合适的同位素变体。本发明的化合物的同位素变体在此被理解为指其中本发明的化合物内的至少一个原子已经被交换为原子序数相同、但原子质量与自然界中通常或主要存在的原子质量不同的另一个原子。可以掺入本发明的化合物的同位素的实例是氢、碳、氮、氧、磷、硫、氟、氯、溴和碘的同位素,诸如2H(氘)、3H(氚)、13C、14C、15N、17O、18O、32P、33P、33S、34S、35S、36S、18F、36Cl、82Br、123I、124I、129I和131I。本发明的化合物的特定同位素变体,特别是其中掺入一种或多种放射性同位素的那些可能是有利的,例如用于检查作用机制或活性物质在体内的分布;由于相对容易的可制备性和可检测性,特别是用3H或14C同位素标记的化合物适合于此目的。此外,由于化合物的代谢稳定性较高,同位素(例如氘)的掺入可导致特定治疗益处,例如体内半衰期延长或所需活性剂量减少;因此,本发明的化合物的此类修饰任选地也可构成本发明的优选实施方案。本发明的化合物的同位素变体可以通过本领域技术人员已知的方法制备,例如通过下文进一步描述的方法和实施例中所述的规程,通过使用各自试剂和/或起始化合物的相应同位素变体。
在本发明的上下文中优选的盐是本发明的化合物的生理学上可接受的盐。还涵盖本身不适用于药物应用但可用于例如分离或纯化本发明的化合物的盐。
本发明的化合物的生理学上可接受的盐包括无机酸、羧酸和磺酸的酸加成盐,例如如下酸的盐:盐酸、氢溴酸、硫酸、磷酸、甲磺酸、乙磺酸、苯磺酸、甲苯磺酸、萘二磺酸、乙酸、三氟乙酸、丙酸、乳酸、酒石酸、苹果酸、柠檬酸、富马酸、马来酸和苯甲酸。
本发明化合物的生理学上可接受的盐还包括常规碱的盐,例如且优选碱金属盐(例如钠盐和钾盐),碱土金属盐(例如钙盐和镁盐)和衍生自氨或具有1-16个碳原子的有机胺的铵盐,所述有机胺例如且优选乙胺、二乙胺、三乙胺、乙基二异丙胺、单乙醇胺、二乙醇胺、三乙醇胺、二环己胺、二甲基氨基乙醇、普鲁卡因、二苄胺、N-甲基哌啶、N-甲基吗啉、精氨酸、赖氨酸和1,2-乙二胺。
在本发明的上下文中的溶剂化物被描述为本发明的化合物的如下形式,其通过以固态或液态与溶剂分子配位而形成络合物。水合物是溶剂化物的特定形式,其中与水配位。在本发明的上下文中优选的溶剂化物是水合物。
治疗用途
本发明的化合物可用于治疗的过度增生病症特别包括癌症和肿瘤病症类。在本发明上下文中,这些被理解为尤其是指下列病症,但不限于它们:乳腺癌和乳腺肿瘤(乳腺癌包括导管和小叶形式,以及原位(in situ))、呼吸道肿瘤(小细胞和非小细胞癌、支气管癌)、脑肿瘤(例如脑干肿瘤和下丘脑肿瘤、星形细胞瘤、室管膜瘤、胶质母细胞瘤、胶质瘤、髓母细胞瘤、脑膜瘤和神经外胚层和松果体瘤)、消化器官肿瘤(食道、胃、胆囊、小肠、大肠、直肠和肛门癌)、肝肿瘤(尤其是肝细胞癌、胆管细胞癌和混合肝细胞胆管细胞癌)、头颈区的肿瘤(喉、下咽部、鼻咽、口咽、嘴唇和口腔癌,口腔黑色素瘤)、皮肤瘤(基底细胞瘤、Spinaliome、鳞状细胞癌、卡波西肉瘤、恶性黑色素瘤、非黑色素瘤皮肤癌、梅克尔细胞皮肤癌、肥大细胞瘤)、支持和结缔组织肿瘤(尤其是软组织肉瘤、骨肉瘤、恶性纤维组织细胞瘤、软骨肉瘤、纤维肉瘤、血管肉瘤、平滑肌肉瘤、脂肪肉瘤、淋巴肉瘤和横纹肌肉瘤)、眼睛肿瘤(尤其是眼内黑色素瘤和成视网膜细胞瘤)、内分泌和外分泌腺的肿瘤(例如甲状腺和甲状旁腺、胰腺和唾液腺癌、腺癌)、尿道肿瘤(膀胱、阴茎、肾、肾盂和输尿管的肿瘤)和生殖器官肿瘤(女性的子宫内膜癌、子宫颈癌、卵巢癌、阴道癌、外阴癌和子宫癌,男性的前列腺癌和睾丸癌)。这些还包括实体形式和作为循环细胞的血液、淋巴系统和脊髓的增殖性病症,如白血病、淋巴瘤和骨髓增生病症,例如急性髓性白血病、急性成淋巴细胞性白血病、慢性淋巴细胞性白血病、慢性髓细胞性白血病和毛细胞性白血病和AIDS相关淋巴瘤、霍奇金淋巴瘤、非霍奇金淋巴瘤、皮肤T-细胞淋巴瘤、伯基特氏淋巴瘤和中枢神经系统中的淋巴瘤。
人类的这些已充分表征的疾病也可能在其它哺乳动物中以可比拟的病因学发生,并在此同样可用本发明的化合物治疗。
本文所述针对CD123的结合剂-或抗体-活性物质-缀合物(ADC)可优选用于治疗CD123表达病症,例如CD123表达癌症。通常,此类癌细胞在蛋白(例如使用免疫测定)或RNA水平上具有可测定量的CD123。相比于相同类型的非癌组织,这些癌症组织中的一些显示升高的CD123水平,优选地在相同的患者中测量。任选地,在以根据本发明的抗体-活性物质-缀合物(ADC)治疗癌症开始之前测量CD123含量(患者阶层化)。针对CD123的结合剂-活性物质-缀合物(ADC)可优选用于治疗CD123表达病症,例如CD123表达癌症,例如造血和淋巴组织的肿瘤或造血和淋巴恶性肿瘤。与CD123表达相关的癌症的实例包括骨髓疾病,例如急性髓性白血病(AML)和骨髓增生不良综合征(MDS)。其它类型的癌症包括B-细胞急性淋巴母细胞白血病(B-ALL)、毛细胞白血病、母细胞胞浆性树突细胞瘤(BPDCN)、霍奇金氏淋巴瘤、未成熟T-细胞急性淋巴性白血病(未成熟T-ALL)、伯基特氏淋巴瘤、滤泡淋巴瘤、慢性淋巴性白血病(CLL)、套细胞淋巴瘤(MCL)。所述本发明的方法包括治疗患有CD123-表达癌症的患者,其中所述方法包括施用根据本发明的抗体-活性物质-缀合物(ADC)。
用本发明的化合物治疗上述癌症包括实体瘤的治疗及其转移或循环形式的治疗。
在本发明上下文中,术语“治疗”或“治疗”在传统意义上使用并且是指为了对抗、减轻、减弱或缓解疾病或健康异常和改善例如在癌症的情况下因该疾病受损的生存状况而照料、护理和看护患者。
本发明的其它主题因此在于本发明的化合物用于治疗和/或预防病症,特别是上文提到的病症的用途。
本发明的其它主题在于本发明的化合物用于制备用于治疗和/或预防病症,特别是上文提到的病症的药剂的用途。
本发明的其它主题在于本发明的化合物在治疗和/或预防病症,特别是上文提到的病症的方法中的用途。
本发明的其它主题在于使用有效量的至少一种本发明的化合物治疗和/或预防病症,特别是上文提到的病症的方法。
本发明的化合物可以独自使用或如果需要,与一种或多种其它药理活性物质组合使用,只要这种组合不造成不合意和不可接受的副作用。因此,本发明的其它主题在于含有至少一种本发明的化合物和一种或多种其它活性物质的药剂,其特别是用于治疗和/或预防上文提到的病症。
例如,本发明的化合物可以与用于治疗癌症的已知抗过度增生、细胞生长抑制、细胞毒性或免疫治疗性物质组合。作为合适的组合活性物质,示例性提到:
131I-chTNT、阿倍瑞克(Abarelix)、阿比特龙、阿柔比星、阿达木单抗、Ado-Trastuzumab Emtansin、阿法替尼、阿柏西普、阿地白介素、阿仑单抗(Alemtuzumab)、阿仑棒酸、阿利维A酸(Alitretinoin)、六甲蜜胺、氨磷汀、氨鲁米特、己基-5-氨基乙酰丙酸酯、氨柔比星、安吖啶、阿那曲唑、安西司亭、茴三硫、Anetumab ravtansine、血管紧张素II、抗凝血酶III、阿瑞吡坦、阿西莫单抗、Arglabin、三氧化二砷、门冬酰胺酶、阿特珠单抗、阿维鲁单抗、阿西替尼、阿扎胞苷、贝洛替康(Belotecan)、苯达莫司汀、贝索单抗、贝利司他、贝伐单抗(Bevacizumab)、贝沙罗汀(Bexaroten)、比卡鲁胺、比生群、博来霉素、博纳吐单抗、硼替佐米、布舍瑞林、博舒替尼、Brentuximab vedotin、白消安、卡巴他赛(Cabazitaxel)、卡博替尼、降血钙素、亚叶酸钙、左亚叶酸钙、卡培他滨、卡罗单抗、卡巴咪嗪、卡铂、Carboquon、卡菲偌米布、卡莫氟、卡莫司汀、卡妥索单抗(Catumaxomab)、西乐葆、西莫白介素、色瑞替尼、西妥昔单抗、苯丁酸氮芥、氯地孕酮、氮芥、西多福韦、西那卡塞、顺铂、克拉屈滨、氯膦酸、氯法拉滨(Clofarabin)、考比替尼、Copanlisib、克立他酶(Crisantaspase)、克唑替尼、环磷酰胺、环丙孕酮、阿糖胞苷、达卡巴嗪、放线菌素、达雷木单抗、达拉非尼、Darolutamide、达沙替尼、柔红霉素、地西他滨、地加瑞克、地尼白介素(Denileukin-Diftitox)、地诺塞麦(Denosumab)、地普奥肽、地洛瑞林、右丙亚胺、二溴螺氯铵、二去水矛醇、双氯芬酸、多西他赛、多拉司琼、去氧氟尿苷、多柔比星、多柔比星+雌酮、屈大麻酚、Durvalumab、依决洛单抗、依利醋铵、血管内皮抑素、依诺他滨、恩扎鲁胺、Epacadostat、表柔比星、环硫雄醇、依泊汀α、依泊汀β、依泊汀ζ、依他铂、艾日布林(Eribulin)、埃洛替尼、埃索美拉唑、雌莫司汀、依托泊苷、乙炔雌二醇、依维莫司、依西美坦、法屈唑、芬太尼、氟羚甲基睾丸素、氟尿苷、氟达拉滨、氟尿嘧啶、氟他胺、叶酸、福美坦、福沙吡坦、福莫司汀、氟维司群、钆布醇、加多利道、钆特酸葡胺盐、钆弗塞胺、钆塞酸二钠盐(Gd-EOB-DTPA二钠盐)、硝酸镓、加尼瑞克、吉非替尼、吉西他滨、吉妥单抗(Gemtuzumab)、羧肽酶、谷胱甘肽(Glutoxim)、戈舍瑞林、格兰西龙、粒细胞集落刺激因子(G-CSF)、粒细胞巨噬细胞集落刺激因子(GM-CSF)、二盐酸组胺、组氨瑞林(Histrelin)、羟基脲、I-125粒子、兰索拉唑、依班膦酸-替伊莫单抗(Ibritumomab-Tiuxetan)、依鲁替尼、伊达比星、异环磷酰胺、伊马替尼、咪喹莫特、英丙舒凡(Improsulfan)、吲地司琼、英卡膦酸、巨大戟醇甲基丁烯酸酯、干扰素α、干扰素β、干扰素γ、碘比醇、碘苄胍(123I)、碘美普尔、易普利姆玛(Ipilimumab)、伊立替康、伊曲康唑、伊沙匹隆(Ixabepilon)、伊沙佐米、兰瑞肽、兰索拉唑、Lansoprazol、拉帕替尼(Lapatinib)、Lasocholine、来那度胺(Lenalidomid)、乐伐替尼、来格司亭、蘑菇多糖、来曲唑、亮丙瑞林、左旋四咪唑、左炔诺孕酮、左甲状腺素钠、Lipegfilgrastim、麦角乙脲、乐铂、环己亚硝脲、氯尼达明、马索罗酚、甲羟孕酮、甲地孕酮、美拉胂醇、苯丙氨酸氮芥、美雄烷、巯基嘌呤、美司钠、美沙酮、氨甲喋呤、甲氧呋豆素、甲基氨基酮戊酸盐、甲基泼尼松龙、甲基睾酮、Metirosin、米伐木肽(Mifamurtid)、米特福辛、米铂(Miriplatin)、二溴甘露醇、丙脒腙、二溴卫矛醇、丝裂霉素、米托坦、米托蒽醌、Mogamulizumab、莫拉司亭、莫哌达醇、盐酸吗啡、硫酸吗啡、大麻隆、Nabiximols、那法瑞林、纳洛酮+戊唑辛、纳曲酮、那托司亭、Necitumumab、奈达铂、奈拉滨(Nelarabin)、奈立膦酸、奈妥吡坦/palonosetron、纳武单抗、纳武单抗喷曲肽、尼洛替尼(Nilotinib)、尼鲁米特、尼莫唑、尼妥珠单抗(Nimotuzumab)、嘧啶亚硝脲、尼达尼布、二胺硝吖啶(Nitracrin)、纳武单抗、阿托珠单抗、奥曲肽、奥法木单抗(Ofatumumab)、奥拉帕尼、Olaratumab、高三尖杉酯碱、奥美拉唑、奥坦西隆、奥古蛋白、Orilotimod、奥希替尼、奥沙利铂、羟考酮、羟甲烯龙、Ozogamicin、p53-基因疗法、紫杉醇、帕博西尼、帕利夫明、钯-103粒子、帕洛诺司琼、帕米膦酸、帕尼单抗(Panitumumab)、帕比司他、泮托拉唑、帕唑帕尼(Pazopanib)、培加帕酶、帕母单抗、聚乙二醇干扰素α-2b、派姆单抗、培美曲唑、喷司他丁、培洛霉素、全氟丁烷、培磷酰胺、帕妥株单抗、溶链菌制剂(Picibanil)、毛果芸香碱、吡柔比星、匹克生琼、普乐沙福(Plerixafor)、普卡霉素、聚氨葡糖(Poliglusam)、磷酸聚雌二醇、聚乙烯吡咯烷酮+透明质酸钠、多糖-K、泊马度胺、帕纳替尼、卟吩姆钠、普拉曲沙(Pralatrexat)、松龙苯芥、泼尼松、甲基苄肼、丙考达唑、普萘洛尔、喹高利特(Quinagolid)、雷贝拉唑、Racotumomab、氯化镭223、拉多替尼、雷诺昔酚、雷替曲塞(Raltitrexed)、雷莫司琼、雷莫芦单抗、雷莫司汀(Ranimustin)、拉布立酶、丙亚胺、Refametinib、瑞戈非尼(Regorafenib)、利塞膦酸、铼-186依替膦酸盐、利妥昔单抗(Rituximab)、Rogaratinib、罗拉吡坦、罗米地辛(Romidepsin)、罗莫肽、瑞博西尼、来昔决南钐(153Sm)、沙妥莫单抗、分泌素、司妥昔单抗、Sipuleucel-T、西佐喃、索布佐生、甘氨双唑钠(Natriumglycididazol)、索尼德吉、索拉非尼(Sorafenib)、康力龙、链脲霉素、舒尼替尼、他拉泊芬(Talaporfin)、Talimogen Laherparepvec、他米巴罗汀(Tamibaroten)、他莫昔芬、他喷他多、他索纳明(Tasonermin)、替西白介素(Teceleukin)、锝[99mTc]巯诺莫单抗、99mTc-HYNIC-[Tyr3]-奥曲肽、替加氟、替加氟+吉美嘧啶(Gimeracil)+奥替拉西(Oteracil)、替莫卟吩、替莫唑胺、西罗莫司(Temsirolimus)、表鬼臼毒噻吩糖苷、睾酮、替曲膦(Tetrofosmin)、反应停、硫替派、胸腺法新(Thymalfasin)、促甲状腺素α、硫鸟嘌呤(Tioguanin)、托珠单抗(Tocilizumab)、托泊替康、托瑞米芬、托西莫单抗(Tositumomab)、曲贝替定(Trabectedin)、曲美替尼、曲马多、曲妥珠单抗、曲奥舒凡(Treosulfan)、维甲酸、曲氟尿苷+Tipiracil、曲美替尼、曲洛司坦、曲普瑞林、氯乙环磷酰胺、促血小板生成素、乌苯美司、戊柔比星(Valrubicin)、凡德他尼(Vandetanib)、伐普肽、瓦他拉尼、维罗非尼(Vemurafenib)、长春碱、长春新碱、长春地辛、长春氟宁、长春瑞宾、维莫德吉、伏立诺他(Vorinostat)、钇-90-玻璃微球、新制癌菌素、净司他丁斯酯、唑来膦酸、佐柔比星。
此外,本发明的化合物可以例如与可例如结合至下列靶标的结合剂(例如抗体)组合:OX-40、CD137/4-1BB、DR3、IDO1/IDO2、LAG-3、CD40。
由于结合剂-活性物质-缀合物(ADC)的非细胞可渗透毒簇代谢物应当对于适应性免疫系统的细胞无损害作用,所以根据本发明的结合剂-活性物质-缀合物(ADC)与癌症免疫治疗的组合以用于治疗癌症或肿瘤是本发明的另一主题。细胞毒性结合剂-活性物质-缀合物的内在作用机制包括直接触发肿瘤细胞的细胞死亡和因此释放可刺激免疫反应的肿瘤抗原。此外,有迹象表明KSP抑制剂毒簇类别在体外诱导所谓免疫细胞死亡[immunogeniccell death(ICD])的标记。因此,本发明的抗体-活性物质-缀合物(ADC)与一种或多种用于癌症免疫治疗的治疗配药或与一种或多种活性物质,优选地针对癌症免疫治疗的分子靶标的抗体的组合代表用于治疗癌症或肿瘤的优选方法。i)用于癌症免疫治疗的治疗配药的实例包括免疫调节单克隆抗体和针对癌症免疫治疗的靶标的低分子量物质、疫苗、CAR T细胞、双特异性T-细胞-招募抗体、溶瘤病毒、基于细胞的疫苗接种配药。ii)适用于免疫调节单克隆抗体的所选的癌症免疫治疗的靶标的实例包括CTLA-4、PD-1/PDL-1、OX-40、CD137、DR3、IDO1、IDO2、TDO2、LAG-3、TIM-3CD40.,ICOS/ICOSL、TIGIT;GITR/GITRL、VISTA、CD70、CD27、HVEM/BTLA、CEACAM1、CEACAM6、ILDR2、CD73、CD47、B7H3、TLR's。因此,根据本发明的结合剂-活性物质-缀合物(ADC)与癌症治疗的组合在一个方面可使具有微弱的免疫原性的肿瘤具有更大的免疫原性并增强癌症免疫治疗的效用,并进一步发挥持久的治疗作用。
此外,根据本发明的化合物也可以与放射疗法和/或外科手术联合使用。
通常,用本发明的化合物与其它的细胞生长抑制、细胞毒性或免疫治疗活性剂的组合追求下列目标:
·与用单一活性物质治疗相比,在减慢肿瘤生长、减小其尺寸或甚至完全消除其方面改进的效用;
·以比单一疗法的情况中更低的剂量使用所用化疗药物的可能性;
·与单独施用相比,具有较少副作用的更耐受治疗的可能性;
·治疗更广谱的肿瘤病症的可能性;
·实现更高的治疗响应率;
·与当今标准疗法相比,更长的患者存活时间。
此外,本发明的化合物也可以与放射疗法和/或外科手术联合使用。
本发明的其它主题在于包含至少一种本发明化合物通常与一种或多种惰性、无毒、药学上合适的助剂的药剂,及其用于上文提到的目的的用途。
本发明的化合物可以全身和/或局部发挥作用。为此,它们可通过合适方式,例如肠道外、可能吸入或作为植入物或支架施用。
本发明的化合物可以以适合这些施用途径的施用形式施用。
肠道外施用可以绕开再吸收步骤(例如静脉内、动脉内、心脏内、脊柱内或腰内)或包括再吸收(例如肌肉内、皮下、皮内、经皮或腹膜内)进行。适合肠道外施用的施用形式尤其包括溶液剂、混悬剂、乳剂或冻干产物形式的注射和输液制剂。优选的是肠道外施用,尤其是静脉施用。
通常已经发现,在肠道外施用的情况下有利的是施用约0.1至20mg/kg,优选约0.3至7mg/kg体重的量以实现有效结果。
尽管如此,任选地可能必需偏离所示的量,尤其取决于体重、施用途径、个体对活性物质的响应、制剂类型和施用时间点或时间间隔。因此,在一些情况下,少于上述最低量可能是足够的,而在另一些情况下,必须超过所提到的上限。在施用更大量的情况下,可能最好将它们在一天内分成几个单剂。
本发明提供了包括但不限于以下实施方式:
1.式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐
其中
X1代表N,
X2代表N,且X3代表C;
或
X1代表N,
X2代表C,且X3代表N;
或
X1代表CH或CF,X2代表C,且X3代表N;
或
X1表示NH,
X2代表C,且
X3代表C;
或
X1代表CH,
X2代表N,且
X3代表C,
R1代表氢或甲基,
R2代表甲基、乙基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,
R3代表甲基、乙基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)2-8-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)1-8-(CH2)2-NH-C(=O)-CH2-##,
W代表以下基团
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
##代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
2.根据实施方式1所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
X1代表CH,
X2代表C,
X3代表N;
R1代表氢或甲基,
R2代表甲基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,
R3代表甲基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)4-(CH2)2-NH-C(=O)-CH2-##,
W代表以下基团
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
##代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
3.根据实施方式1和2所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,
其中
R1代表氢或甲基,
R2代表甲基或异丙基,
R3代表甲基或–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
4.根据实施方式1至3所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
5.根据实施方式1至4所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
6.根据实施方式1至5所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,且
AK代表抗-CD123抗体、抗-CXCR5抗体、抗-B7H3抗体、抗-TWEAKR抗体、抗-Her2抗体或抗-EGFR抗体或代表它们的结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键。
7.根据实施方式1至6所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,且
AK代表选自TPP-9476、TPP-8988、TPP-8987和TPP-6013的抗-CD123抗体,代表选自TPP-9574和TPP-9580的抗-CXCR5抗体,代表抗-B7H3抗体TPP-8382,代表选自TPP-7006和TPP-7007的抗-TWEAKR抗体,代表抗-Her2抗体TPP-1015或代表抗-EGFR抗体TPP-981或代表它们的结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键。
8.根据实施方式1至7所述的具有以下结构的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐
其中
AK1代表经由半胱氨酸侧链的硫原子连接的抗体,
AK2代表经由赖氨酸侧链的氮原子连接的抗体,且
n代表1至50。
9.根据实施方式8所述的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
n代表1至20。
10.根据实施方式8和9所述的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
n代表1至8。
11.根据实施方式8至10所述的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
n代表4至8。
12.根据实施方式1至11中一项或多项所述的结合剂-活性物质-缀合物,其中
AK(AK1、AK2)代表选自TPP-8382(抗B7H3)、TPP-6013(抗-CD123)、TPP-8987(抗-CD123)、TPP-8988(抗-CD123)、TPP 9476(抗-CD123)、TPP-9580(抗-CXCR5)和TPP 9574(抗-CXCR5)的抗体,或它们的结合抗原的片段。
13.根据实施方式1至12中一项或多项所述的结合剂-活性物质-缀合物,其中
AK(AK1、AK2)代表抗-CD123抗体TPP-6013,
代表抗-CD123抗体TPP-8987,
代表抗-CD123抗体TPP-8988或
代表抗-CD123抗体TPP-9476,
或它们的结合抗原的片段。
14.根据实施方式1至13中一项或多项所述的结合剂-活性物质-缀合物,其中AK(AK1、AK2)
(i)代表包含重链可变区(VH)和轻链可变区(VL)的抗-B7H3抗体,所述重链可变区包含如SEQ ID NO:52所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:53所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:54所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:56所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:57所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:58所示的轻链可变CDR3序列(L-CDR3),
(ii)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:22所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:23所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:24所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:26所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:27所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:28所示的轻链可变CDR3序列(L-CDR3),
(iii)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:62所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:63所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:64所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:66所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:67所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:68所示的轻链可变CDR3序列(L-CDR3),
(iv)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:72所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:73所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:74所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:76所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:77所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:78所示的轻链可变CDR3序列(L-CDR3),
(v)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CD123抗体,所述重链可变区包含如SEQ ID NO:82所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:83所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:84所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:86所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:87所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:88所示的轻链可变CDR3序列(L-CDR3),
(vi)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CXCR5抗体,所述重链可变区包含如SEQ ID NO:92所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:93所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:94所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:96所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:97所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:98所示的轻链可变CDR3序列(L-CDR3),或(vii)代表包含重链可变区(VH)和轻链可变区(VL)的抗-CXCR5抗体,所述重链可变区包含如SEQ IDNO:102所示的重链可变CDR1序列(H-CDR1)、如SEQ ID NO:103所示的重链可变CDR2序列(H-CDR2)和如SEQ ID NO:104所示的重链可变CDR3序列(H-CDR3),且所述轻链可变区包含如SEQ ID NO:106所示的轻链可变CDR1序列(L-CDR1)、如SEQ ID NO:107所示的轻链可变CDR2序列(L-CDR2)和如SEQ ID NO:108所示的轻链可变CDR3序列(L-CDR3),
或代表这些抗体的结合抗原的片段。
15.根据实施方式1至14中一项或多项所述的结合剂-活性物质-缀合物,其中AK(AK1、AK2)
(I)代表包含如SEQ ID NO:51所示的重链可变区(VH)和如SEQ ID NO:55所示的轻链可变区(VL)的抗-B7H3抗体,
(ii)代表包含如SEQ ID NO:21所示的重链可变区(VH)和如SEQ ID NO:25所示的轻链可变区(VL)的抗-CD123抗体,
(iii)代表包含如SEQ ID NO:61所示的重链可变区(VH)和如SEQ ID NO:65所示的轻链可变区(VL)的抗-CD123抗体,
(iv)代表包含如SEQ ID NO:71所示的重链可变区(VH)和如SEQ ID NO:75所示的轻链可变区(VL)的抗-CD123抗体,
(v)代表包含如SEQ ID NO:81所示的重链可变区(VH)和如SEQ ID NO:85所示的轻链可变区(VL)的抗-CD123抗体,
(vi)代表包含如SEQ ID NO:91所示的重链可变区(VH)和如SEQ ID NO:95所示的轻链可变区(VL)的抗-CXCR5抗体,
(vii)代表包含如SEQ ID NO:101所示的重链可变区(VH)和如SEQ ID NO:105所示的轻链可变区(VL)的抗-CXCR5抗体,
或代表这些抗体的结合抗原的片段。
16.根据实施方式1至15中一项或多项所述的结合剂-活性物质-缀合物,其中AK(AK1、AK2)
(i)代表包含如SEQ ID NO:59所示的重链区和如SEQ ID NO:60所示的轻链区的抗-B7H3抗体,
(ii)代表包含如SEQ ID NO:29所示的重链区和如SEQ ID NO:30所示的轻链区的抗-CD123抗体,
(iii)代表包含如SEQ ID NO:69所示的重链区和如SEQ ID NO:70所示的轻链区的抗-CD123抗体,
(iv)代表包含如SEQ ID NO:79所示的重链区和如SEQ ID NO:80所示的轻链区的抗-CD123抗体,
(v)代表包含如SEQ ID NO:89所示的重链区和如SEQ ID NO:90所示的轻链区的抗-CD123抗体,
(vi)代表包含如SEQ ID NO:99所示的重链区和如SEQ ID NO:100所示的轻链区的抗-CXCR5抗体,或(vii)代表包含如SEQ ID NO:109所示的重链区和如SEQ ID NO:110所示的轻链区的抗-CXCR5抗体,
或代表这些抗体的结合抗原的片段。
17.根据实施方式1至16中任一项所述的结合剂-活性物质-缀合物,其中所述抗体或结合抗原的抗体片段结合至细胞外靶分子。
18.根据实施方式1至17中任一项所述的结合剂-活性物质-缀合物,其中所述抗体或结合抗原的抗体片段结合至细胞外癌症靶分子。
19.根据实施方式1至18中任一项所述的结合剂-活性物质-缀合物,其中所述抗体或结合抗原的抗体片段在结合至其在靶细胞上的细胞外靶分子之后通过结合被所述靶细胞内化。
20.药物组合物,其包含至少一种根据前述实施方式中的一项或多项所述的结合剂-活性物质-缀合物与惰性、无毒、药学上合适的助剂的组合。
21.根据前述实施方式中的一项或多项所述的结合剂-活性物质-缀合物,其用于治疗和/或预防疾病的方法中。
22.根据前述实施方式中的一项或多项所述的结合剂-活性物质-缀合物,其用于治疗过度增生和/或血管生成病症的方法中。
23.根据前述实施方式中的一项或多项所述的结合剂-活性物质-缀合物,其用于治疗癌症和肿瘤的方法中。
24.根据前述实施方式中的一项或多项所述的结合剂-活性物质-缀合物,其与一种或多种用于癌症免疫治疗的治疗配药、或与一种或多种针对癌症免疫治疗的分子靶标的活性物质组合用于治疗癌症和肿瘤的方法中。
实施例
下列实施例说明本发明。本发明不限于这些实施例。
除非另行指明,下列测试和实施例中的百分比数据为重量百分比;份数为重量份。液体/液体溶液的溶剂比、稀释比和浓度数据在每种情况下都基于体积。
合成途径:
对于实施例,在下列方案中示例性地显示产生实施例的示例性合成途径:方案1:具有豆荚蛋白可裂解接头的赖氨酸连接的ADC的合成
在上述反应方案中,X1、X2、X3、n和AK2具有式(I)中给出的含义。
a):HATU,DMF,N,N-二异丙基乙胺,室温;b)H2,10% Pd-C,甲醇1.5小时,室温;c)1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮,N,N-二异丙基乙胺,DMF,在室温下搅拌过夜;d)PBS中的AK2,在氩气下添加溶解于DMSO中的3-5当量的活性酯,在室温和氩气下搅拌60分钟,再添加溶解于DMSO中的3-5当量的活性酯,在室温和氩气下搅拌60分钟,然后通过用PBS缓冲液(pH 7.2)平衡的PD10柱(G-25,GEHealthcare)纯化,且随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)设定所需浓度。任选地,随后在体内批料的情况下还进行无菌过滤。
方案2:半胱氨酸连接的ADC的合成
在上述反应方案中,X1、X2、X3、n和AK1具有式(I)中给出的含义。
a):HATU,DMF,N,N-二异丙基乙胺,室温;b)氯化锌,三氟乙醇,50℃,EDTAc):HATU,DMF,N,N-二异丙基乙胺,室温;d)H2,10% Pd-C,甲醇1.5小时,室温;e)1-{6-[(2,5-二氧代吡咯烷-1-基)氧基]-6-氧代己基}-1H-吡咯-2,5-二酮,N,N-二异丙基乙胺,DMF,在室温下搅拌;f)AK1溶解于PBS中,在氩气下添加PBS缓冲液中的3-4当量的TCEP,并在室温下搅拌约30分钟,然后添加溶解于DMSO中的5-10当量的化合物E,在室温下搅拌约90分钟,然后通过用PBS缓冲液(pH 7.2)平衡的PD10柱(G-25,GE Healthcare)纯化,且随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)设定所需浓度]。任选地,随后在体内批料的情况下还进行无菌过滤。
在上述反应方案中,X1、X2、X3、n和AK1具有式(I)中给出的含义。
[a):HATU,DMF,N,N-二异丙基乙胺,室温;b)氯化锌,三氟乙醇,50℃,EDTAc):HATU,DMF,N,N-二异丙基乙胺,室温;d)H2,10% Pd-C,甲醇1.5小时,室温;e)1-{2-[(2,5-二氧代吡咯烷-1-基)氧基]-2-氧代乙基}-1H-吡咯-2,5-二酮,N,N-二异丙基乙胺,DMF,在室温下搅拌;f)AK1溶解于PBS,在氩气下添加PBS缓冲液中的3-4当量TCEP和在室温下搅拌约30min,然后添加溶解于DMSO中的5-10当量化合物E,在室温下搅拌约90min,然后通过用PBS缓冲剂(pH 8)平衡PD 10柱(G-25,GE Healthcare)再缓冲至pH 8,然后在室温下搅拌过夜,然后任选地通过用PBS缓冲剂(pH 7.2)平衡的PD 10柱(G-25,GE Healthcare)纯化,且随后通过超速离心浓缩并用PBS缓冲剂(pH 7.2)设定所需的浓度]。任选地,随后在体内批料的情况下还进行无菌过滤。
A.实施例
缩写和首字母缩略词:
ABCB1 ATP-结合盒亚家族B成员1(P-gp和MDR1的同义词)
abs. 纯
Ac 乙酰基
ACN 乙腈
aq. 含水,水溶液
ATP 三磷酸腺苷
BCRP 乳腺癌耐药蛋白,外排转运蛋白
BEP 2-溴-1-乙基吡啶鎓四氟硼酸盐
Boc 叔丁氧基羰基
br. 宽(在NMR中)
Bsp. 实施例
BxPC3 人肿瘤细胞系
C 浓度
ca. 大约、约
CI 化学电离(在MS中)
DAR 药物:抗体比
D 双重峰(在NMR中)
D 天
DC 薄层色谱法
DCI 直接化学电离(在MS中)
DCM 二氯甲烷
Dd 双重双峰(在NMR中)
DMAP 4-N,N-二甲基氨基吡啶
DME 1,2-二甲氧基乙烷
DMEM Dulbecco氏改良的Eagle培养基(用于细胞培养的标准化营养培养基)
DMF N,N-二甲基甲酰胺
DMSO 二甲亚砜
D/P 染料(荧光染料)/蛋白比
DPBS、D-PBS Dulbecco氏磷酸盐缓冲的盐溶液
DSMZ 德国微生物和细胞培养物保藏中心
PBS PBS=DPBS=D-PBS,pH 7.4,来自Sigma公司,编号D8537
组成:
0.2g KCl
0.2g KH2PO4(无水)
8.0g NaCl
1.15g Na2HPO4(无水)
用H2O补充至1升
Dt 双重三峰(在NMR中)
DTT DL-二硫苏糖醇
d.Th. 理论值的(在化学产率中)
EDC N'-(3-二甲基氨基丙基)-N-乙基碳二亚胺盐酸盐
EGFR Epidermal growth factor receptor=表皮生长因子受体
EI 电子碰撞电离(在MS中)
ELISA 酶联免疫吸附测定法
eq. 当量
ESI 电喷雾电离(在MS中)
ESI-MicroTofq ESI-MicroTofq(质谱仪名称,Tof=飞行时间和q=四极)
FCS 胎牛血清
Fmoc (9H-芴-9-基甲氧基)羰基
ges. 饱和
GTP 5'-三磷酸鸟苷
H 小时
HATU O-(7-氮杂苯并三唑-1-基)-N,N,N',N'-四甲基脲鎓六氟磷酸盐
HEPES 4-(2-羟乙基)哌嗪-1-乙烷磺酸
HOAc 乙酸
HOAt 1-羟基-7-氮杂苯并三唑
HOBt 1-羟基-1H-苯并三唑水合物
HOSu N-羟基琥珀酰亚胺
HPLC 高压高效液相色谱法
IC50 半最大抑制浓度
i.m. 肌肉内,施用至肌肉中
i.v. 静脉,施用至静脉中
konz. 浓缩
KPL-4 人肿瘤细胞系
KU-19-19 人肿瘤细胞系
LC-MS 液相色谱法-质谱法联用
LLC-PK1-Zellen Lewis肺癌猪肾细胞系
L-MDR 人MDR1转染的LLC-PK1细胞
LoVo 人肿瘤细胞系
M 多重峰(在NMR中)
Me 甲基
MDR1 多药耐药蛋白1
MeCN 乙腈
Min 分钟
MOLM-13 人肿瘤细胞系
MS 质谱法
MTT 溴化3-(4,5-二甲基噻唑-2-基)-2,5-二苯基-2H-四唑鎓
MV-4-11 人肿瘤细胞系
NB4 人肿瘤细胞系
NCI-H292 人肿瘤细胞系
NMM N-甲基吗啉
NMP N-甲基-2-吡咯烷酮
NMR 核磁共振谱法
NMRI 小鼠品系,源自海军医学研究所(Naval Medical ResearchInstitute)(NMRI)
NSCLC Non small cell lung cancer(非小细胞肺癌)
PBS 磷酸盐缓冲的盐溶液
Pd/C 活性炭载钯
P-gp P-糖蛋白,转运蛋白
PNGaseF 用于糖裂解的酶
quant. 定量(在产率中)
Quart 四重峰(在NMR中)
Quint 五重峰(在NMR中)
Rec-1 人肿瘤细胞系
Rf 保留指数(在DC中)
RT 室温
Rt 保留时间(在HPLC中)
S 单峰(在NMR中)
s.c. 皮下,在皮肤下施用
SCID小鼠 具有重症联合免疫缺陷(severe combined immunodeficiency)的受试小鼠
SK-HEP-1 人肿瘤细胞系
t 三重峰(在NMR中)
TBAF 四正丁基氟化铵
TCEP 三(2-羧乙基)膦
TEMPO (2,2,6,6-四甲基哌啶-1-基)氧基
Teoc 三甲基甲硅烷基乙氧基羰基
tert. 叔
TFA 三氟乙酸
THF 四氢呋喃
U251 人肿瘤细胞系
UV 紫外光谱法
v/v (溶液的)体积比
Z 苄氧基羰基。
HPLC和LC-MS方法:
方法1(LC-MS):
仪器:Waters ACQUITY SQD UPLC系统;柱:Waters Acquity UPLC HSS T3 1.8μ50×1mm;洗脱液A:1l水+0.25ml 99%甲酸,洗脱液B:1l乙腈+0.25ml 99%甲酸;梯度:0.0min90% A→1.2min 5%A→2.0min5%A;烘箱:50℃;流速:0.40mL/min;UV检测:208-400nm。
方法2(LC-MS):
MS仪器类型:Waters Synapt G2S;UPLC仪器类型:Waters Acquity I-CLASS;柱:Waters,BEH300,2.1×150mm,C18 1.7μm;洗脱液A:1l水+0.01%甲酸;洗脱液B:1l乙腈+0.01%甲酸;梯度:0.0min 2% B→1.5min 2% B→8.5min 95% B→10.0min 95% B;烘箱:50℃;流速:
0.50mL/min;UV检测:220nm。
方法3(LC-MS):
MS仪器:Waters(Micromass)QM;HPLC仪器:Agilent 1100系列;柱:AgilentZORBAX Extend-C183.0×50mm 3.5微米;洗脱液A:1l水+0.01mol碳酸铵,洗脱液B:1l乙腈;梯度:0.0min 98% A→0.2min 98%A→3.0min 5% A→4.5min 5% A;烘箱:40℃;流速:1.75mL/min;UV检测:210nm。
方法4(LC-MS):
MS仪器类型:Waters Synapt G2S;UPLC仪器类型:Waters Acquity I-CLASS;柱:Waters,HSST3,2.1×50mm,C18 1.8μm;洗脱液A:1l水+0.01%甲酸;洗脱液B:1l乙腈+0.01%甲酸;梯度:0.0min 10% B→0.3min 10% B→1.7min 95% B→2.5min 95% B;烘箱:50℃;流速:
1.20mL/min;UV检测:210nm。
方法5(LC-MS):
仪器:Waters ACQUITY SQD UPLC系统;柱:Waters Acquity UPLC HSS T3 1.8μ50×1mm;洗脱液A:1l水+0.25ml 99%甲酸;洗脱液B:1l乙腈+0.25ml 99%甲酸;梯度:0.0min95% A→6.0min 5%A→7.5min5%A烘箱:50℃;流速:0.35mL/min;UV检测:210-400nm。
方法6(LC-MS):
仪器:Micromass Quattro Premier与Waters UPLC Acquity;柱:ThermoHypersil GOLD 1.9μ50×1mm;洗脱液A:1l水+0.5ml 50%甲酸,洗脱液B:1l乙腈+0.5ml50%甲酸;梯度:0.0min 97% A→0.5min 97% A→3.2min 5% A→4.0min 5% A烘箱:50℃;流速:0.3mL/min;UV检测:210nm。
方法7(LC-MS):
仪器:Agilent MS Quad 6150;HPLC:Agilent 1290;柱:Waters Acquity UPLCHSS T3 1.8μ50×2.1mm;洗脱液A:1l水+0.25ml 99%甲酸;洗脱液B:1l乙腈+0.25ml 99%甲酸;梯度:0.0min 90% A→0.3min 90% A→1.7min 5% A→3.0min 5% A烘箱:50℃;流速:1.20mL/min;UV检测:205-305nm。
方法8(LC-MS):
MS仪器类型:Waters Synapt G2S;UPLC仪器类型:Waters Acquity I-CLASS;柱:Waters,HSST3,2.1×50mm,C18 1.8μm;洗脱液A:1l水+0.01%甲酸;洗脱液B:1l乙腈+0.01%甲酸;梯度:0.0min 2% B→2.0min 2% B→13.0min 90% B→15.0min 90% B;烘箱:50℃;流速:1.20ml/min;UV检测:210nm。
方法9:(LC-MS-制备型纯化方法)
MS仪器:Waters,HPLC仪器:Waters(柱Waters X-Bridge C18,19mm×50mm,5μm,洗脱液A:水+0.05%氨,洗脱液B:具有梯度的乙腈(ULC);流速:40ml/min;UV检测:DAD;210-400nm)。
或:
MS仪器:Waters,HPLC仪器:Waters(柱Phenomenex Luna 5μC18(2)100A,AXIATech.50×21.2mm,洗脱液A:水+0.05%甲酸,洗脱液B:具有梯度的乙腈(ULC);流速:40ml/min;UV检测:DAD;210-400nm)。
方法10:(LC-MS分析方法)
MS仪器:Waters SQD;HPLC仪器:Waters UPLC;柱:Zorbax SB-Aq(Agilent),50mm×2.1mm,1.8μm;洗脱液A:水+0.025%甲酸,洗脱液B:乙腈(ULC)+0.025%甲酸;梯度:0.0min 98%A-0.9min 25%A-1.0min 5%A-1.4min 5%A-1.41min 98%A-1.5min 98%A;烘箱:40℃;流速:0.600ml/min;UV检测:DAD;210nm。
方法11(HPLC):
仪器:HP1100系列柱:Merck Chromolith SpeedROD RP-18e,50-4.6mm,目录号1.51450.0001,预柱Chromolith Guard Cartridge Kit,RP-18e,5-4.6mm,目录号1.51470.0001;
梯度:流速5mL/Min;
注射体积5μl;
溶剂A:水中的HClO4(70%)(4mL/l),
溶剂B:乙腈
起始20% B
0.50Min 20% B
3.00Min 90% B
3.50Min 90% B
3.51Min 20% B
4.00Min 20% B
柱温度:40℃,
波长:210nm。
方法12(LC-MS):
MS仪器类型:Thermo Scientific FT-MS;UHPLC+仪器类型:Thermo ScientificUltiMate 3000;柱:Waters,HSST3,2.1×75mm,C18 1.8μm;洗脱液A:1l水+0.01%甲酸;洗脱液B:1l乙腈+0.01%甲酸;梯度:0.0min 10% B→2.5min 95% B→3.5min 95% B;烘箱:50℃;流速:0.90ml/min;UV检测:210nm/最佳积分途径210-300nm。
方法13:(LC-MS):
MS仪器:Waters(Micromass)Quattro Micro;仪器Waters UPLC Acquity;柱:Waters BEH C18 1.7μ50×2.1mm;洗脱液A:1l水+0.01mol甲酸铵,洗脱液B:1l乙腈;梯度:0.0min 95% A→0.1min 95% A→2.0min15% A→2.5min 15% A→2.51min 10% A→3.0min 10% A;烘箱:40℃;流速:0.5ml/min;UV检测:210nm。
方法14:(LC-MS)(MCW-LTQ-POROSHELL-TFA98-10min)MS仪器类型:ThermoFisherScientific LTQ-Orbitrap-XL;HPLC仪器类型:Agilent 1200SL;柱:Agilent,POROSHELL 120,3×150mm,SB-C18 2.7μm;洗脱液A:1l水+0.1%三氟乙酸;洗脱液B:1l乙腈+0.1%三氟乙酸;梯度:0.0min 2% B→0.3min 2% B→5.0min 95% B→10.0min95% B;烘箱:40℃;流速:0.75ml/min;UV检测:210nm。
下文没有明确描述其制备的所有反应物或试剂购自一般可得的来源。对于其制备同样没有描述在下文中并且不可购得或获自非一般可得的来源的所有其它反应物或试剂,参考描述了其制备的公开文献。
起始化合物和中间体:
中间体C52
(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙-1-胺
将10.00g(49.01mmol)4-溴-1H-吡咯-2-甲酸甲酯预先置入100.0mL DMF,并添加20.76g(63.72mmol)碳酸铯和9.22g(53.91mmol)苄基溴。将反应混合物在室温下搅拌过夜。将反应混合物分配于水和乙酸乙酯之间且水相用乙酸乙酯萃取。合并的有机相经硫酸镁干燥并在减压下蒸发溶剂。用90.0g 4-溴-1H-吡咯-2-甲酸甲酯重复反应。
合并的两组批料通过制备型RP-HPLC(柱:Daiso 300x100;10μ,流速:250mL/min,MeCN/水)纯化。在真空下蒸发溶剂且残余物在高真空下干燥。这得到125.15g(理论值的87%)化合物1-苄基-4-溴-1H-吡咯-2-甲酸甲酯。
LC-MS(方法1):Rt=1.18min;MS(ESIpos):m/z=295[M+H]+。
在氩气下,将4.80g(16.32mmol)1-苄基-4-溴-1H-吡咯-2-甲酸甲酯预先置入DMF,并添加3.61g(22.85mmol)(2,5-二氟苯基)硼酸、19.20mL饱和碳酸钠溶液和1.33g(1.63mmol)[1,1'-双(二苯基膦基)二茂铁]-二氯钯(II):二氯甲烷。将反应混合物在85℃下搅拌过夜。将反应混合物通过C盐过滤且滤饼用乙酸乙酯洗涤。有机相用水萃取且然后用饱和NaCl溶液洗涤。有机相经硫酸镁干燥并在真空下蒸发溶剂。残余物借助硅胶纯化(流动相:环己烷/乙酸乙酯100:3)。在真空下蒸发溶剂且残余物在高真空下干燥。这得到3.60g(理论值的67%)化合物1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-甲酸甲酯。
LC-MS(方法7):Rt=1.59min;MS(ESIpos):m/z=328[M+H]+。
将3.60g(11.00mmol)1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-甲酸甲酯预先置入90.0mL THF,并在0℃下添加1.04g(27.50mmol)氢化锂铝(2.4M,在THF中)。将反应混合物在0℃下搅拌30分钟。在0℃下,添加饱和酒石酸钾钠溶液,并向反应混合物添加乙酸乙酯。有机相用饱和酒石酸钾钠溶液萃取三次。有机相用饱和NaCl溶液洗涤一次且经硫酸镁干燥。在真空下蒸发溶剂并将残余物溶解于30.0mL二氯甲烷中。添加3.38g(32.99mmol)氧化锰(IV),并在室温下搅拌48小时。添加另外2.20g(21.47mmol)氧化锰(IV),并在室温下搅拌过夜。将反应混合物通过C盐过滤且滤饼用二氯甲烷洗涤。在真空下蒸发溶剂且残余物2.80g(1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-甲醛)未经进一步纯化即用于下一合成步骤。
LC-MS(方法7):Rt=1.48min;MS(ESIpos):m/z=298[M+H]+。
将28.21g(94.88mmol)1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-甲醛与23.00g(189.77mmol)(R)-2-甲基丙烷-2-亚磺酰胺一起预先置入403.0mL无水THF中,并添加67.42g(237.21mmol)异丙醇钛(IV)并在室温下搅拌过夜。添加500mL饱和NaCl溶液和1000.0mL乙酸乙酯,并在室温下搅拌1小时。通过硅藻土过滤且滤液用饱和NaCl溶液洗涤两次。有机相经硫酸镁干燥,在真空下蒸发溶剂且残余物使用Biotage Isolera(硅胶,柱1500+340g SNAP,流速200mL/min,乙酸乙酯/环己烷1:10)纯化。LC-MS(方法7):Rt=1.63min;MS(ESIpos):m/z=401[M+H]+。
在氩气下将25.00g(62.42mmol)(R)-N-{(E/Z)-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]亚甲基}-2-甲基丙烷-2-亚磺酰胺预先置入无水THF中并冷却至-78℃。然后在-78℃下添加12.00g(187.27mmol)叔丁基锂(戊烷中的1.7M溶液)并在该温度下搅拌3小时。在-78℃下,然后相继添加71.4mL甲醇和214.3mL饱和氯化铵溶液,并使反应混合物升温至室温并在室温下搅拌1小时。用乙酸乙酯稀释并用水洗涤。有机相经硫酸镁干燥并在真空下蒸发溶剂。残余物(R)-N-{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}-2-甲基丙烷-2-亚磺酰胺未经进一步纯化即用于下一合成步骤。
LC-MS(方法6):Rt=2.97min;MS(ESIpos):m/z=459[M+H]+。
将28.00g(61.05mmol)(R)-N-{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}-2-甲基丙烷-2-亚磺酰胺预先置入186.7mL1,4-二氧杂环己烷中,然后添加45.8mL 1,4-二氧杂环己烷溶液形式的HCl(4.0M)。将反应混合物在室温下搅拌2小时并在真空下蒸发溶剂。残余物通过制备型HPLC纯化(柱:Kinetix 100x30;流速:60mL/min,MeCN/水)。在真空下蒸发乙腈并将二氯甲烷添加至水性残余物。有机相用碳酸氢钠溶液洗涤且经硫酸镁干燥。在真空下蒸发溶剂且残余物在高真空下干燥。这得到16.2g(理论值的75%)标题化合物。
LC-MS(方法6):Rt=2.10min;MS(ESIpos):m/z=338[M-NH2]+,709[2M+H]+。
1H-NMR(400MHz,DMSO-d6):δ[ppm]=0.87(s,9H),1.53(s,2H),3.59(s,1H),5.24(d,2H),6.56(s,1H),6.94(m,1H),7.10(d,2H),7.20(m,1H),7.26(m,2H),7.34(m,2H),7.46(m,1H)。
中间体C58
(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-2-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酸
将4.3g(12.2mmol)的中间体C52溶解于525mL DCM中,并添加3.63g(17.12mmol)三乙酰氧基硼氢化钠和8.4mL乙酸。在室温下搅拌5min之后,添加溶解于175mL DCM中的8.99g(24.5mmol)中间体L57并将批料在室温下再搅拌45min。然后用300mL DCM稀释批料并用100mL碳酸氢钠溶液洗涤二次并用饱和的NaCl溶液洗涤一次。将有机相经硫酸镁干燥,在真空下蒸发溶剂并在高真空下干燥残余物。然后通过制备型RP-HPLC纯化残余物(柱:Chromatorex C18)。将相应的级分合并之后,在真空下蒸发溶剂并在高真空下干燥残余物。这得到4.6g(理论值的61%)(2S)-4-({(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}氨基)-2-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酸甲酯。
LC-MS(方法12):Rt=1.97min;MS(ESIpos):m/z=614(M+H)+。
将2.06g(3.36mmol)该中间体预先置入76mL DCM中并用0.81mL(7.17mmol)乙酸2-氯-2-氧代乙酯在2.1ml三乙胺存在的情况下酰化。在室温下搅拌20h之后,添加0.36mL乙酸2-氯-2-氧代乙酯和0.94ml三乙胺并将批料在室温下再搅拌15min。然后用500mL乙酸乙酯稀释并相继用300mL 5%柠檬酸振荡萃取二次,用300mL饱和碳酸氢钠溶液振荡萃取两次并用100mL饱和氯化钠溶液振荡萃取一次,且然后经硫酸镁干燥和浓缩。在高真空下干燥,得到2.17g(理论值的79%)经保护的中间体。
LC-MS(方法1):Rt=1.48min;MS(ESIpos):m/z=714(M+H)+。
将2.17mg(2.64mmol)的该中间体溶解于54mL THF和27mL水,并添加26mL 2摩尔浓度氢氧化锂溶液。将批料在室温下搅拌30min,然后使用1.4mL TFA将pH值调节至3至4。在真空下浓缩该批料。在基本上蒸馏除去THF后,用DCM萃取水溶液两次且然后在真空下浓缩至干燥。通过制备型HPLC纯化残余物(柱:Chromatorex C18)。将相应的级分合并之后,在真空下蒸发溶剂并将残余物从乙腈/水冻干。这得到1.1g(理论值的63%)的标题化合物。
LC-MS(方法1):Rt=1.34min;MS(ESIpos):m/z=656(M-H)-。
1H-NMR(400MHz,DMSO-d6):δ[ppm]=0.03(s,9H),0.58(m,1H),0.74-0.92(m,11H),1.40(m,1H),3.3(m,2H),3.7(m,1H),3.8-4.0(m,2H),4.15(q,2H),4.9和5.2(2d,2H),5.61(s,1H),6.94(m,2H),7.13-7.38(m,7H),7.48(s,1H),7.60(m,1H),12.35(s,1H)。
中间体C61
N-[(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-2-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酰基]-β-丙氨酸
通过将60mg(0.091mmol)的中间体C58与β-丙氨酸甲酯偶联和随后用2M氢氧化锂溶液进行酯裂解来制备标题化合物。这经2个步骤得到67mg(理论值的61%)的标题化合物。
LC-MS(方法1):Rt=1.29min;MS(ESIpos):m/z=729(M+H)+。
中间体C102
(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-2-{[(苄基氧基)羰基]氨基}丁酸
首先,类似于中间体C2,将中间体C52用(2S)-2-{[(苄基氧基)羰基]氨基}-4-氧代丁酸苄酯还原性烷基化。然后将仲氨基用乙酸2-氯-2-氧代乙酯酰化,然后用甲醇中的2M氢氧化锂溶液水解两个酯基。
LC-MS(方法1):Rt=1.31min;MS(ESIpos):m/z=646(M-H)-。
中间体C110(D)
N-{(2S)-2-氨基-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]丁酰基}-β-丙氨酰-D-谷氨酸二苄酯
通过标题化合物如下制备:在HATU和N,N-二异丙基乙胺存在的情况下将预先通过分配于乙酸乙酯和5%碳酸氢钠溶液之间从其对甲苯磺酸盐中释放的D-谷氨酸二苄酯与中间体C61偶联,且随后通过三氟乙醇中的氯化锌裂解出Teoc保护基。
LC-MS(方法1):Rt=1.08min;MS(ESIpos):m/z=894[M+H]+。
中间体C111
N-{(2S)-2-氨基-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]丁酰基}-β-丙氨酰-D-谷氨酸二叔丁酯
首先,通过常规的肽化学方法,通过在HATU存在的情况下将市售的N-[(苄基氧基)羰基]-β-丙氨酸和D-谷氨酸二叔丁酯盐酸盐(1:1)偶联和随后以氢解的方式裂解出Z保护基,制备二肽衍生物β-丙氨酰-D-谷氨酸二叔丁酯。然后标题化合物通过如下方式来制备:在HATU和N,N-二异丙基乙胺存在的情况下将该中间体与中间体C102偶联,且随后通过在室温下在标准氢气压力下在DCM/甲醇1:1中在活性炭上的10%钯上氢化1小时来裂解出Z保护基。
LC-MS(方法1):Rt=1.06min;MS(ESIpos):m/z=826[M+H]+。
中间体C117
N-{(2S)-2-(L-天冬酰胺基氨基)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]丁酰基}-β-丙氨酰-D-谷氨酸二苄酯三氟乙酸盐
将中间体C110D和N2-(叔丁氧基羰基)-L-天冬酰胺2,5-二氧代吡咯烷-1-基酯(251mg,764μmol)溶解于21ml DMF中,并添加N,N-二异丙基乙胺(363μl,2.01mmol)。将反应物在室温下搅拌,且然后直接通过制备型RP-HPLC(柱:Chromatorex C18-10)纯化。在真空下蒸发溶剂,并将残余物冻干。将获得的中间体(578mg,52μmol)溶解于20.0ml三氟乙醇中。向反应混合物添加氯化锌(426mg,3.13mmol),并在50℃下再搅拌40分钟。向该批料添加乙二胺-N,N,N',N'-四乙酸(914mg,3.13mmol),并用20ml水稀释,添加TFA(200μl)并短暂地继续搅拌。将该批料过滤并通过制备型RP-HPLC(柱:Chromatorex C18-5;125x40,流速:100ml/min,MeCN/水,0.1% TFA梯度)纯化。冻干后得到标题化合物。
中间体L57
(2S)-4-氧代-2-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酸甲酯
将500.0mg(2.72mmol)L-天冬氨酸甲酯盐酸盐和706.3mg(2.72mmol)2,5-二氧代吡咯烷-1-甲酸2-(三甲基甲硅烷基)乙酯预先置入5.0mL 1,4-二氧杂环己烷中,并添加826.8mg(8.17mmol)三乙胺。将反应混合物在室温下搅拌过夜。反应混合物直接通过制备型RP-HPLC纯化(柱:Reprosil 250x40;10μ,流速:50mL/min,MeCN/水,0.1% TFA)。然后在真空下蒸发溶剂并在高真空下干燥残余物。这得到583.9mg(理论值的74%)化合物(3S)-4-甲氧基-4-氧代-3-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酸。
LC-MS(方法1):Rt=0.89min;MS(ESIneg):m/z=290(M-H)-。
将592.9mg(3S)-4-甲氧基-4-氧代-3-({[2-(三甲基甲硅烷基)乙氧基]羰基}氨基)丁酸预先置入10.0mL 1,2-二甲氧基乙烷中,冷却至-15℃并添加205.8mg(2.04mmol)4-甲基吗啉和277.9mg(2.04mmol)氯甲酸异丁酯。15分钟后,以抽吸滤出沉淀并用每次10.0mL1,2-二甲氧基乙烷洗涤两次。将滤液冷却至-10℃,并在强烈搅拌下添加溶解于10mL水中的115.5mg(3.05mmol)硼氢化钠。分离各相并将有机相用饱和碳酸氢钠溶液和饱和NaCl溶液洗涤各一次。有机相经硫酸镁干燥,在真空下蒸发溶剂并在高真空下干燥残余物。这得到515.9mg(理论值的91%)化合物N-{[2-(三甲基甲硅烷基)乙氧基]羰基}-L-高丝氨酸甲酯。
LC-MS(方法1):Rt=0.87min;MS(ESIpos):m/z=278(M+H)+。
将554.9mg(2.00mmol)N-{[2-(三甲基甲硅烷基)乙氧基]羰基}-L-高丝氨酸甲酯预先置入30.0mL二氯甲烷中,并添加1.27g(3.0mmol)戴斯-马丁氧化剂和474.7mg(6.00mmol)吡啶。在室温下搅拌过夜。4小时后,将批料用二氯甲烷稀释并将有机相用10%Na2S2O3溶液、10%柠檬酸溶液和饱和碳酸氢钠溶液洗涤各三次。有机相经硫酸镁干燥并在真空下蒸发溶剂。这得到565.7mg(理论值的97%)标题化合物。
1H-NMR(400MHz,DMSO-d6):δ[ppm]=0.03(s,9H),0.91(m,2H),2.70-2.79(m,1H),2.88(dd,1H),3.63(s,3H),4.04(m,2H),4.55(m,1H),7.54(d,1H),9.60(t,1H)。
中间体L95
N-[(苄基氧基)羰基]-L-缬氨酰-L-丙氨酸
该中间体通过肽化学的常规方法从N-[(苄基氧基)羰基]-L-缬氨酸和L-丙氨酸叔丁酯盐酸盐开始制备。
LC-MS(方法12):Rt=1.34min;MS(ESIpos):m/z=323.16(M+H)+。
中间体L103
标题化合物通过如下方式制备:通过常规的肽化学方法,首先在HATU和N,N-二异丙基乙胺存在的情况下将4-吡啶乙酸与市售的L-丙氨酰-L-丙氨酸叔丁酯偶联,随后用三氟乙酸脱保护,与L-天冬酰胺叔丁酯偶联,且随后用三氟乙酸将羧基脱保护。
LC-MS(方法1):Rt=0.15min;MS(ESIpos):m/z=394(M+H)+。
中间体L116
N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酸
通过经典的肽化学方法从市售的N-[(苄基氧基)羰基]-L-丙氨酸开始,经由在HATU存在的情况下与N-甲基-L-丙氨酸叔丁酯盐酸盐偶联,且最后通过用TFA裂解出叔丁酯保护基,制备标题化合物。
LC-MS(方法1):Rt=0.68min;MS(ESIpos):m/z=309[M+H]+。
中间体L117
N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酰-L-天冬酰胺三氟乙酸盐
通过经典的肽化学方法从市售的L-天冬酰胺4-叔丁酯开始,经由在HATU存在的情况下与N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酸(中间体L116)偶联,且最后通过用TFA裂解出叔丁酯保护基,制备标题化合物。
LC-MS(方法1):Rt=0.57min;MS(ESIneg):m/z=421[M-H]-。
中间体L118
N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酰-L-丙氨酸
通过经典的肽化学方法从市售的L-丙氨酸叔丁酯盐酸盐开始,经由在HATU存在的情况下与N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酸(中间体L116)偶联,且最后通过用TFA裂解出叔丁酯保护基,制备标题化合物。
LC-MS(方法12):Rt=1.25min;MS(ESIneg):m/z=378[M-H]-。
中间体L121
N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酰-L-亮氨酸
通过经典的肽化学方法从市售的L-亮氨酸叔丁酯盐酸盐开始,经由在HATU存在的情况下与N-[(苄基氧基)羰基]-L-丙氨酰-N-甲基-L-丙氨酸(中间体L116)偶联,且最后通过用TFA裂解出叔丁酯保护基,制备标题化合物。
LC-MS(方法12):Rt=0.83min;MS(ESIneg):m/z=420[M-H]-。
中间体L122
(5S,8S,11S)-11-(2-氨基-2-氧代乙基)-8-[2-(苄基氧基)-2-氧代乙基]-5-甲基-3,6,9-三氧代-1-苯基-2-氧杂-4,7,10-三氮杂十二烷-12-酸
通过经典的肽化学方法从市售的1-叔丁基-L-天冬氨酸4-苄基酯盐酸盐(1:1)开始,首先经由与N-(苄基氧基)羰基]-L-丙氨酸2,5-二氧代吡咯烷-1-基酯偶联,然后用TFA裂解出叔丁酯保护基,然后随后在HATU存在的情况下与L-天冬酰胺4-叔丁酯偶联,且最后用TFA再一次裂解出叔丁酯TFA保护基,制备标题化合物。
LC-MS(方法1):Rt=0.76min;MS(ESIpos):m/z=543[M+H]+。
中间体L138
1-溴-2-氧代-6,9,12,15-四氧杂-3-氮杂十八烷-18-酸
通过在N,N-二异丙基乙胺存在的情况下将1-氨基-3,6,9,12-四氧杂十五烷-15-酸与溴乙酸酐偶联来制备标题化合物。
LC-MS(方法5):Rt=1.05min;MS(ESIpos):m/z=386和388(M+H)+。
中间体Q1
N-[(2,5-二氧代-2,5-二氢-1H-吡咯-1-基)乙酰基]-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L117偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1-{2-[(2,5-二氧代吡咯烷-1-基)氧基]-2-氧代乙基}-1H-吡咯-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法12):Rt=1.66min;MS(ESIneg):m/z=1119[M-H]-。
中间体Q2
N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L117偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.93min;MS(ESIpos):m/z=1195[M+H]+。
中间体Q3
N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-丙氨酰-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C117开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与N-(叔丁氧基羰基)-L-丙氨酰-L-丙氨酸偶联,制备标题化合物。然后将中间体置于三氟乙醇中,并且通过在50℃下在氯化锌存在的情况下搅拌,释放叔丁氧基羰基保护的胺。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有苄基保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.90min;MS(ESIneg):m/z=1181[M-H]-。
中间体Q4
N-[6-(2,5-二氧代-2,5-二氢-1H-吡咯-1-基)己酰基]-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L117偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1-{6-[(2,5-二氧代吡咯烷-1-基)氧基]-6-氧代己基}-1H-吡咯-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=3.2min;MS(ESIpos):m/z=1177[M+H]+。
中间体Q5
N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-丙氨酰-N-甲基-L-丙氨酰-N-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-丙氨酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L118偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.96min;MS(ESIpos):m/z=1152[M+H]+。
中间体Q6
N-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-2-[(N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-缬氨酰-L-丙氨酰)氨基]丁酰基}-β-丙氨酰-D-谷氨酸
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L95偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.98min;MS(ESIpos):m/z=1095[M+H]+。
中间体Q7
N-[(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-2-({N-[(2,5-二氧代-2,5-二氢-1H-吡咯-1-基)乙酰基]-L-缬氨酰-L-丙氨酰}氨基)丁酰基]-β-丙氨酰-D-谷氨酸
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L95偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1-{2-[(2,5-二氧代吡咯烷-1-基)氧基]-2-氧代乙基}-1H-吡咯-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.98min;MS(ESIpos):m/z=1021[M+H]+。
中间体Q8
N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-亮氨酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L121偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在乙醇中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在N,N-二异丙基乙胺存在的情况下与1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=1.02min;MS(ESIpos):m/z=1194[M+H]+。
中间体Q9
N-{5-[(2,5-二氧代吡咯烷-1-基)氧基]-5-氧代戊酰基}-L-丙氨酰-N-甲基-L-α-天冬氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L122偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在甲醇中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在3当量的N,N-二异丙基乙胺存在的情况下与3当量的1,1'-[(1,5-二氧代戊烷-1,5-二基)双(氧基)]二吡咯烷-2,5-二酮反应来将脱保护的中间体转化为标题化合物。
LC-MS(方法1):Rt=0.89min;MS(ESIpos):m/z=1225[M+H]+。
中间体Q10
N-(溴乙酰基)-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
从化合物C110D开始,首先通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L117偶联,制备标题化合物。在下一步骤中,通过在标准氢气压力下在室温下在DCM-甲醇1:1中在活性炭上的10%钯上氢化1小时来除去所有保护基,且然后通过在3当量的N,N-二异丙基乙胺存在的情况下与溴乙酸酐反应来将脱保护的中间体转化为标题化合物。LC-MS(方法1):Rt=0.95min;MS(ESIpos):m/z=1104和1106[M+H]+。
中间体Q11
N-(18-溴-17-氧代-4,7,10,13-四氧杂-16-氮杂十八烷-1-酰基)-L-丙氨酰-N-甲基-L-丙氨酰-N1-{(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-[(3-{[(1R)-1,3-二羧基丙基]氨基}-3-氧代丙基)氨基]-1-氧代丁-2-基}-L-天冬酰胺
首先通过在1.5当量HATU和3当量N,N-二异丙基乙胺存在的情况下将中间体C111与中间体L117在DMF中偶联来实施标题化合物的合成。随后,通过在氢气标准压力下在室温下在乙醇中在活性炭上的10%钯上氢化2小时来除去Z保护基。然后在1.5当量HATU和3当量N,N-二异丙基乙胺存在的情况下将脱保护的中间体与中间体L138在DMF中反应。在最后步骤中,通过在50℃下用三氟乙醇中的8当量氯化锌搅拌2小时来裂解出叔丁酯基团,得到标题化合物。
LC-MS(方法8):Rt=4.06min;MS(ESI-pos):m/z=1353[M+H]+。
B:抗体-活性物质-缀合物(ADC)的制备
B-1.用于生成抗体的一般方法
将所用的抗体例如TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574和TPP-9580的蛋白序列(氨基酸序列)通过本领域技术人员已知的方法转变成编码相应蛋白的DNA序列,并插入适用于瞬时哺乳动物细胞培养的表达载体中(如来自Tom等人,Methods Express的第12章:Expression Systems,由Micheal R.Dyson和Yves Durocher编辑,Scion Publishing Ltd,2007中所述)。
B-2.用于在哺乳动物细胞中表达抗体的一般方法抗体例如TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574和TPP-9580在瞬时哺乳动物细胞培养物中产生,如来自Tom等人,Methods Express的第12章:Expression Systems,由Micheal R.Dyson和Yves Durocher编辑,Scion Publishing Ltd,2007中所述。
B-3.从细胞上清液中纯化抗体的一般方法抗体例如TPP-981、TPP-1015、TPP-6013、TPP-7006、TPP-7007、TPP-8382、TPP-8987、TPP-8988、TPP-9476、TPP-9574和TPP-9580获自细胞培养上清液。该细胞上清液通过细胞离心来澄清化。该细胞上清液然后通过在MabSelect Sure(GE Healthcare)色谱柱上的亲和色谱法纯化。为此,该柱在DPBS pH 7.4(Sigma/Aldrich)中平衡,施加细胞上清液,且该柱用约10柱体积的DPBS pH 7.4+500mM氯化钠洗涤。抗体在50mM乙酸钠pH 3.5+500mM氯化钠中洗脱,然后通过在Superdex 200柱(GEHealthcare)上在DPBS pH 7.4中的凝胶渗透色谱法进一步纯化。
市售抗体通过标准色谱法(蛋白A色谱,制备型凝胶过滤色谱(SEC-大小排阻色谱))从市售产品纯化。
B-4.偶联至半胱氨酸侧链的一般方法
下列抗体用于该偶联反应中:
实施例a:TPP-981西妥昔单抗(抗-EGFR AK)
实施例c:TPP-6013(抗-CD123 AK)
TPP-8987(抗-CD123 AK)
TPP-8988(抗-CD123 AK)
TPP-9476(抗-CD123 AK)
实施例h:TPP-8382(抗-B7H3 AK)
实施例e:TPP-1015(抗-Her2 AK)
实施例k:TPP-7006(抗-TWEAKR AK)
TPP-7007(抗-TWEAKR AK)
实施例x:TPP-9574(抗-CXCR5 AK)
TPP-9580(抗-CXCR5 AK)
所述偶联反应通常在氩气下实施。
将溶解在PBS缓冲液中的2至5当量的三(2-羧乙基)膦盐酸盐(TCEP)添加至在1mg/ml至20mg/ml浓度范围内,优选约10mg/ml至15mg/ml的相应抗体在PBS缓冲液中的溶液中,并在室温下搅拌1小时。为此,各自使用的抗体的溶液可以以实施例中所述的浓度使用,或者也可任选地用PBS缓冲液稀释至所述起始浓度的约一半,以达到优选的浓度范围。随后,根据所需载量,作为在DMSO中的溶液添加2至12当量,优选约5-10当量的待偶联的马来酰亚胺前体化合物或卤化物前体化合物。在此,DMSO的量不应超过总体积的10%。将该批料在马来酰亚胺前体的情况下在室温下搅拌60-240分钟,并且在卤化物前体的情况下在室温下搅拌8-24小时,且然后置于在PBS中平衡的PD10柱(G-25,GE Healthcare)上并用PBS缓冲液洗脱。通常,除非另有说明,否则将PBS缓冲液中的5mg相应抗体用于还原和随后的偶联。在PD10柱上纯化后,因此在每种情况下得到相应ADC在3.5ml PBS缓冲液中的溶液。然后通过超速离心浓缩,并将样品任选地用PBS缓冲液稀释回去。如果需要,为了更好地分离出低分子量成分,用PBS缓冲液稀释回去后重复通过超滤的浓缩。对于生物学测试,如果需要,任选地通过稀释回去而将最终ADC样品中的浓度调节至0.5-15mg/ml。对于ADC溶液,确定实施例中各自所述的蛋白浓度。此外,使用B-6中描述的方法测定抗体载量(药物/mAb比率)。
取决于接头,实施例中显示的ADC也可以任选地或多或少程度地以水解的开链琥珀酰胺的形式与抗体连接着存在。
特别地,也可以任选地通过在偶联之后重新缓冲和根据方案28在pH 8下有针对性地搅拌到经由开链琥珀酰胺连接的ADC中约20-24小时,制备经由以下接头结构与抗体的巯基连接的KSP-I-ADC
#1代表至所述抗体的硫桥,且#2代表与经修饰的KSP抑制剂的连接点。
其中接头经由水解的开链琥珀酰胺与抗体连接着存在的此类ADC也可以任选地有针对性地通过例如此处所示的小规模和大规模偶联来制备:
将溶解在PBS缓冲液中的2至7当量的三(2-羧乙基)膦盐酸盐(TCEP)添加至在1mg/ml至20mg/ml浓度范围内,优选约5mg/ml至15mg/ml的2-5mg相应抗体在PBS缓冲液中的溶液中,并在室温下搅拌30分钟至1小时。随后,根据所需载量,作为在DMSO中的溶液添加2至20当量,优选约5-10当量的待偶联的马来酰亚胺前体化合物。为了实现更高的DAR,也可以使用15-20当量。在此,DMSO的量不应超过总体积的10%。将该批料在室温下搅拌60-240分钟。将洗脱物用PBS缓冲液pH 8稀释至1-5mg/ml的浓度且然后置于用PBS缓冲液pH 8平衡的PD-10柱(G-25,GE Healthcare)上,并用PBS缓冲液pH 8洗脱。将洗脱物在室温下在氩气下搅拌过夜。随后,溶液通过超速离心来浓缩并用PBS缓冲液(pH 7.2)稀释回去。
中等规模偶联:
在氩气下,将2-7当量,优选3当量TCEP在PBS缓冲液中的溶液(c~0.2-0.8mg/ml,优选0.5mg/ml)添加至PBS缓冲液中的20-200mg所涉抗体(c~5-15mg/ml。将该批料在室温下搅拌30分钟,然后添加溶解于DMSO中的2-20、优选5-10当量马来酰亚胺前体化合物。为了实现更高的DAR,也可以使用15-20当量。在室温下搅拌另外1.5小时-2小时后,用已预先调节至pH 8的PBS缓冲液稀释该批料。然后将该溶液置于用PBS缓冲液pH 8平衡的PD 10柱(G-25,GE Healthcare)上并用PBS缓冲液pH 8洗脱。洗脱物用PBS缓冲液pH 8稀释至2-7mg/mL的浓度。将该溶液在室温下在氩气下搅拌过夜。如果需要,然后将溶液再缓冲至pH 7.2。该ADC溶液通过超速离心浓缩,用PBS缓冲液(pH 7.2)稀释回去,然后任选地再次浓缩至约10mg/mL的浓度。
在所示结构式中,AK1在此可具有以下含义:
实施例a:TPP-981西妥昔单抗(部分还原的)-S§1
实施例c:TPP-6013(抗-CD123 AK)(部分还原的)-S§1
TPP-8987(抗-CD123 AK)(部分还原的)-S§1
TPP-8988(抗-CD123 AK)(部分还原的)-S§1
TPP-9476(抗-CD123 AK)(部分还原的)-S§1
实施例e:TPP-1015(抗-Her2 AK)(部分还原的)-S§1
实施例h:TPP-8382(抗-B7H3 AK)(部分还原的)-S§1
实施例k:TPP-7006(抗-TWEAKR)(部分还原的)-S§1
TPP-7007(抗-TWEAKR)(部分还原的)-S§1
实施例x:TPP-9574(抗-CXCR5 AK)(部分还原的)-S§1
TPP-9580(抗-CXCR5 AK)(部分还原的)-S§1
其中
§1代表与琥珀酰亚胺基团或与任选由其产生的异构水解开链琥珀酰胺或亚烷基残基的键,
且
S代表部分还原的抗体的半胱氨酸残基的硫原子。
B-5.用于偶联至赖氨酸侧链的一般方法以下抗体用于偶联反应:
实施例a:TPP-981西妥昔单抗(抗-EGFR AK)
实施例c:TPP-6013(抗-CD123 AK)
TPP-8987(抗-CD123 AK)
TPP-8988(抗-CD123 AK)
TPP-9476(抗-CD123 AK)
实施例e:TPP-1015(抗-Her2 AK)
实施例k:TPP-7006(抗-TWEAKR AK)
TPP-7007(抗-TWEAKR AK)
实施例x:TPP-9574(抗-CXCR5 AK)
TPP-9580(抗-CXCR5 AK)
所述偶联反应通常在氩气下实施。
根据所需载量,将2至8当量的待偶联的前体化合物作为DMSO中的溶液添加至在1mg/ml至20mg/ml的浓度范围,优选约10mg/ml的相应抗体在PBS缓冲液中的溶液。在室温下搅拌30分钟至6小时后,再次添加相同量的在DMSO中的前体化合物。在此,DMSO的量不应超过总体积的10%。在室温下再搅拌30分钟至6小时后,将该批料置于在PBS中平衡的PD10柱(G-25,GE Healthcare)上并用PBS缓冲液洗脱。在PD10柱上纯化后,因此在每种情况下得到相应ADC在PBS缓冲液中的溶液。然后通过超速离心浓缩,并将样品任选地用PBS缓冲液稀释回去。如果需要,为了更好地分离出低分子量成分,用PBS缓冲液稀释回去后重复通过超滤的浓缩。对于生物学测试,如果需要,任选地通过稀释回去而将最终ADC样品的浓度调节至0.5-15mg/ml。
对于ADC溶液,确定实施例中各自所述的蛋白浓度。此外,使用B-6中描述的方法测定抗体载量(药物/mAb比率)。
在所示的结构式中,AK2在此具有以下含义实施例a:TPP-981西妥昔单抗(抗-EGFRAK)-NH§2
实施例c:TPP-6013(抗-CD123 AK)-NH§2
TPP-8987(抗-CD123 AK)-NH§2
TPP-8988(抗-CD123 AK)-NH§2
TPP-9476(抗-CD123 AK)-NH§2
实施例e:TPP-1015(抗-Her2 AK)-NH§2
实施例k:TPP-7006(抗-TWEAKR AK)-NH§2
TPP-7007(抗-TWEAKR AK)-NH§2
实施例x:TPP-9574(抗-CXCR5 AK)-NH§2
TPP-9580(抗-CXCR5 AK)-NH§2
其中
§2代表与羰基的键
且
NH代表抗体的赖氨酸残基的侧链氨基。
根据本发明的缀合物的进一步纯化和表征在进行反应后,在一些情况下,例如通过超滤浓缩反应混合物,且然后通过色谱法,例如使用G-25柱脱盐和纯化。例如用磷酸盐缓冲的盐溶液(PBS)进行洗脱。然后将该溶液无菌过滤并冷冻。或者,可以将该缀合物冻干。
B-6.抗体、毒簇载量和开放半胱氨酸加合物含量的测定为了鉴定蛋白,除分子量测定外,在去糖基化和/或变性后进行胰蛋白酶消化,其在变性、还原和衍生化后通过发现的胰蛋白酶肽证实蛋白的身份。
如下测定实施例中描述的缀合物在PBS缓冲液中的所得溶液的毒簇载量(在表中表示为DAR,药物/抗体比):
通过各缀合物物类的分子量的质谱测定,进行赖氨酸连接的ADC的毒簇载量的测定。在此,该抗体缀合物预先用PNGaseF去糖基化,并将样品酸化并在HPLC分离/脱盐后使用ESI-MicroTofQ(Bruker Daltonik)通过质谱法分析。将TIC(总离子色谱图)中的信号上的所有波谱相加,并基于MaxEnt去卷积计算不同缀合物物类的分子量。在不同物类的信号积分后,然后计算DAR(=药物/抗体比)。为此,将毒簇数所加权的所有物类的积分结果的总和除以简单加权的所有物类的积分结果的总和。
通过还原和变性的ADC的反相色谱法,测定半胱氨酸连接的缀合物的毒簇载量的测定。将盐酸胍(GuHCl)(28.6mg)和DL-二硫苏糖醇(DTT)溶液(500mM,3μl)添加至ADC溶液(1mg/mL,50μl)。将该混合物在55℃下孵育1小时并通过HPLC分析。
在Agilent 1260HPLC系统上用在220nm的检测进行HPLC分析。在1mL/min的流速下以下列梯度使用Polymer Laboratories PLRP-S聚合反相柱(目录号PL1912-3802)(2.1x150 mm,8微米粒度,):0min,25%B;3min,25%B;28min,50%B。洗脱液A由水中的0.05%三氟乙酸(TFA)组成,洗脱液B由乙腈中的0.05%三氟乙酸组成。
通过与非缀合抗体的轻链(L0)和重链(H0)的保留时间比较,将检测的峰赋值。将仅在缀合样品中检测到的峰赋值给具有一个毒簇的轻链(L1)和具有一个、两个和三个毒簇的重链(H1、H2、H3)。
从通过积分确定的作为HC载量和LC载量的总和的两倍的峰面积确定具有毒簇的抗体的平均载量(所谓的DAR,药物/抗体比),其中从毒簇数所加权的所有LC峰的积分结果的总和除以简单加权的所有LC峰的积分结果的总和计算LC载量,且其中从毒簇数加权的所有HC峰的积分结果的总和除以简单加权的所有LC峰的积分结果的总和计算HC载量。在个别情况下,由于某些峰的共洗脱,可能无法精确确定毒簇载量。
在通过HPLC无法充分分离轻链和重链的情况下,通过轻链和重链处的各缀合物物类的分子量的质谱测定进行半胱氨酸连接的缀合物的毒簇载量的确定。
为此,将盐酸胍(GuHCl)(28.6mg)和DL-二硫苏糖醇(DTT)溶液(500mM,3μl)添加至ADC溶液(1mg/ml,50μl)。将该混合物在55℃下孵育1小时,并在使用ESI-MicroTofQ(BrukerDaltonik)在线脱盐后通过质谱法分析。
对于DAR(药物:抗体比)测定,将TIC(总离子色谱图)中的信号上的所有波谱相加,并基于MaxEnt去卷积计算轻链和重链处的不同缀合物物类的分子量。从通过积分确定的作HC载量和LC载量的总和的两倍的峰面积确定具有毒簇的抗体的平均载量。在此,从毒簇数加权的所有LC峰的积分结果的总和除以简单加权的所有LC峰的积分结果的总和计算LC载量,且从毒簇数加权的所有HC峰的积分结果的总和除以简单加权的所有HC峰的积分结果的总和计算HC载量。
在开放构建体的情况下,为了测定开放半胱氨酸加合物的含量,测定所有单缀合的轻链和重链变体的封闭与开放半胱氨酸加合物(分子量Δ18道尔顿)的分子量面积比。所有变体的平均值得出开放半胱氨酸加合物的含量。
B-7.验证ADC的抗原-结合
在进行偶联后检查结合剂结合至靶分子的能力。本领域技术人员已知可用于此目的的各种方法;例如,可以使用ELISA技术或表面等离子体共振分析(BIAcore测量)检查缀合物的亲和力。本领域技术人员可以使用常用方法测量缀合物浓度,例如对抗体缀合物而言通过蛋白测定法(也参见Doronina等人;Nature Biotechnol.2003;21:778-784和Polson等人,Blood 2007;1102:616-623)。
代谢物的实施例
实施例M1
N-{(2S)-2-氨基-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]丁酰基}-β-丙氨酰-D-谷氨酸
通过在氢气标准压力下在室温下在乙醇中在活性炭上的10%钯上氢化1小时来将中间体C110D转化为标题化合物。
LC-MS(方法1):Rt=1.78min;MS(ESIpos):m/z=714[M+H]+。
下面示例性显示的ADC能够释放优选的代谢物M1,其具有优选的药理学性质。
实施例ADC
经由马来酰亚胺残基偶联至抗体的半胱氨酸侧链的在实施例的结构式中所示的ADC根据接头和偶联程序而主要以在每种情况下所示的开环或闭环形式存在。然而,制剂可包含小含量的各自其它形式。偶联反应在氩气下实施。用于体内测试的所有较大批料在制备结束时进行无菌过滤。
实施例1
示例性规程A:
在氩气下,将0.029mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.5ml PBS中的5mg相应抗体(c=10mg/mL)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.26mg(0.00023mmol)中间体Q1。在室温下再搅拌90min之后,该批料用预先调节至pH 8的PBS缓冲液稀释至2.5mL体积,且然后置于用PBS缓冲液pH 8平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液pH 8洗脱。将洗脱物在室温下在氩气下搅拌过夜。随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
示例性规程B:
在氩气下,将0.172mg TCEP在0.3ml PBS缓冲液中的溶液添加至3ml PBS中的30mg相应抗体(c=10mg/mL)。将该批料在室温下搅拌30min,且然后添加溶解于300μl DMSO中的1.57mg(0.0014mmol)中间体Q1。在室温下再搅拌90min之后,将批料用预先调节至pH 8的PBS缓冲液稀释至5mL体积,且然后置于用PBS缓冲液pH 8平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液pH 8洗脱。将洗脱物用PBS缓冲液pH 8稀释至7.5ml的体积,并在室温下氩气下搅拌过夜。然后将该溶液置于用PBS缓冲液pH 7.2平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液pH 7.2洗脱。然后以超速离心浓缩,用PBS缓冲液(pH 7.2)稀释回去,并再次浓缩和无菌过滤。
下列ADC类似于这些规程制备且如下表中所示表征:
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 1a-981 | EGFR | 981 | A | 1.85 | 2.5 |
| 1c-6013 | CD123 | 6013 | A | 2.0 | 2.4 |
| 1c-9476 | CD123 | 9476 | A | 1.96 | 3.1 |
| 1e-1015 | HER2 | 1015 | A | 1.75 | 3.3 |
| 1h-8382 | B7H3 | 8382 | B | 11.01 | 3.5 |
| 1k-7006 | TWEAKR | 7006 | A | 1.8 | 2.9 |
| 1k-7007 | TWEAKR | 7007 | B | 7.84 | 3.3 |
| 1x-9574 | CXCR5 | 9574 | A | 1.26 | 2.9 |
实施例2
示例性规程A:
在氩气下,将溶解于50μl DMSO中的5当量(0.2mg)中间体Q2添加至0.5ml PBS中的5mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
示例性规程B:
在氩气下,将溶解于50μl DMSO中的4当量(1mg)中间体Q2添加至3ml PBS缓冲液(pH 7.2)中的30mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。然后将该批料用PBS缓冲液(pH 7.2)稀释至5ml,在Sephadex柱上纯化,然后通过超速离心浓缩,用PBS(pH 7.2)稀释回去并再次浓缩和无菌过滤。
示例性规程C:
在氩气下,将溶解于250μl DMSO中的2.5当量(1mg)中间体Q2添加至5ml PBS缓冲液(pH 7.2)中的50mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。然后将该批料用PBS缓冲液(pH 7.2)稀释至7.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩,用PBS(pH 7.2)稀释回去并再次浓缩和无菌过滤。
示例性规程D:
在氩气下,将溶解于7.5ml DMSO中的4.5当量(36mg)中间体Q2添加至150ml PBS缓冲液(pH 7.2)中的1000mg所涉抗体(c=6.7mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。然后将该批料通过错流过滤纯化,浓缩并无菌过滤。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 2a-981 | EGFR | 981 | A | 2.23 | 4.5 |
| 2c-6013 | CD123 | 6013 | A | 2.32 | 4.9 |
| 2c-8987 | CD123 | 8987 | B | 8.86 | 5.8 |
| 2c-8988 | CD123 | 8988 | B | 9.81 | 3.6 |
| 2c-9476B | CD123 | 9476 | B | 10.27 | 4.2 |
| 2c-9476C | CD123 | 9476 | C | 9.22 | 3.4 |
| 2c-9476D | CD123 | 9476 | D | 15.83 | 6.3 |
| 2e-1015 | HER2 | 1015 | A | 2.05 | 5.4 |
| 2k-7006 | TWEAKR | 7006 | A | 2.09 | 5.9 |
| 2k-7007 | TWEAKR | 7007 | B | 9.32 | 3.4 |
| 2x-9574 | CXCR5 | 9574 | B | 9.5 | 4.8 |
| 2x-9580 | CXCR5 | 9580 | B | 10.12 | 4.8 |
实施例3
示例性规程A:
在氩气下,将溶解于50μl DMSO中的5当量(0.2mg)中间体Q3添加至0.5ml PBS中的5mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
示例性规程B:
在氩气下,将溶解于50μl DMSO中的4当量(1mg)中间体Q3添加至3ml PBS缓冲液(pH 7.2)中的30mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。然后将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩,用PBS(pH 7.2)稀释回去并再次浓缩和无菌过滤。
实施例4
示例性规程A:
在氩气下,将0.029mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.4ml PBS缓冲液(pH 7.2)中的5mg所涉抗体(c=12.5mg/ml)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.275mg(0.00023mmol)中间体Q4。在室温下再搅拌90分钟后,将该批料用PBS缓冲液稀释至2.5ml的总体积。然后将该溶液置于用PBS缓冲液(pH 7.2)平衡的PD10柱(G-25,GE Healthcare)上,并用PBS缓冲液(pH 7.2)洗脱。随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 4c-9476 | CD123 | 9476 | A | 2.06 | 3.5 |
| 4k-7007 | TWEAKR | 7007 | A | 1.87 | 4.0 |
| 4x-9574 | CXCR5 | 9574 | A | 1.93 | 3.6 |
实施例5
示例性规程A:
在氩气下,将溶解于50μl DMSO中的5当量(0.2mg)中间体Q5添加至0.5ml PBS中的5mg所涉抗体(c=10mg/m1)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5 ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/m1] | DAR |
| 5c-9476 | CD123 | 9476 | A | 2.37 | 5.3 |
| 5e-1015 | HER2 | 1015 | A | 2.33 | 5.5 |
| 5k-7007 | TWEAKR | 7007 | A | 2.18 | 5.6 |
| 5x-9574 | CXCR5 | 9574 | A | 1.88 | 6.8 |
实施例6
示例性规程A:
在氩气下,将溶解于50μl DMSO中的5当量(0.18mg)中间体Q6添加至0.4ml PBS中的5mg所涉抗体(c=12.5mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 6a-981 | EGFR | 981 | A | 2.39 | 4.9 |
| 6c-9476 | CD123 | 9476 | A | 1.8 | 5.3 |
| 6e-1015 | HER2 | 1015 | A | 2.23 | 6.2 |
| 6k-7007 | TWEAKR | 7007 | A | 2.57 | 5.6 |
实施例7
示例性规程A:
在氩气下,将0.029mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.4ml PBS中的5mg所涉抗体(c=12.5mg/ml)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.24mg(0.00023mmol)中间体Q7。在室温下再搅拌90min之后,将该批料用预先调整至pH 8的PBS缓冲液稀释至2.5ml的体积,且然后置于用PBS缓冲液pH 8平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液pH 8洗脱。将洗脱物在室温下氩气下搅拌过夜。这随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 7a-981 | EGFR | 981 | A | 2.03 | 3.4 |
| 7c-9476 | CD123 | 9476 | A | 1.53 | 4.0 |
| 7e-1015 | HER2 | 1015 | A | 1.88 | 3.8 |
| 7k-7007 | TWEAKR | 7007 | A | 1.99 | 3.6 |
实施例8
示例性规程A:
在氩气下,将溶解于50 μl DMSO中的5当量(0.2mg)中间体Q8添加至0.5ml PBS中的5mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/m1] | DAR |
| 8a-981 | EGFR | 981 | A | 2.32 | 6.5 |
| 8c-9476 | CD123 | 9476 | A | 2.37 | 6.9 |
| 8e-1015 | HER2 | 1015 | A | 1.46 | 6.6 |
| 8k-7007 | TWEAKR | 7007 | A | 2.43 | 6.7 |
实施例9
示例性规程A:
在氩气下,将溶解于50μl DMSO中的5当量(0.2mg)中间体Q9添加至0.5ml PBS中的5mg所涉抗体(c=10mg/ml)。在室温下搅拌1小时后,再次添加相同的量,并将该批料在室温下再搅拌1小时。将该批料随后用PBS缓冲液(pH 7.2)稀释至2.5ml,在Sephadex柱上纯化,然后通过超速离心浓缩并用PBS(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 9a-981 | EGFR | 981 | A | 2.34 | 4.4 |
| 9c-9476 | CD123 | 9476 | A | 2.65 | 4.2 |
| 9e-1015 | HER2 | 1015 | A | 2.22 | 4.8 |
| 9k-7007 | TWEAKR | 7007 | A | 2.14 | 3.8 |
实施例10
示例性规程A:
在氩气下,将0.029mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.5ml PBS缓冲液(pH 7.2)中的5mg所涉抗体(c=10mg/ml)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.295mg(0.00023mmol)中间体Q10。在室温下再搅拌20h后,将该批料用PBS缓冲液稀释至2.5ml的总体积。然后将该溶液置于用PBS缓冲液(pH 7.2)平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液(pH 7.2)洗脱。随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
用于获得更高DAR的示例性规程C:
在氩气下,将0.057mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.5ml PBS缓冲液(pH 7.2)中的5mg所涉抗体(c=10mg/ml)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.59mg(0.00053mmol)中间体Q10。在室温下再搅拌20h后,将该批料用PBS缓冲液稀释至2.5ml的总体积。然后将该溶液置于用PBS缓冲液(pH 7.2)平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液(pH 7.2)洗脱。随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
实施例11
示例性规程A:
在氩气下,将0.029mg TCEP在0.05ml PBS缓冲液中的溶液添加至0.4ml PBS缓冲液(pH 7.2)中的5mg所涉抗体(c=12.5mg/ml)。将该批料在室温下搅拌30min,且然后添加溶解于50μl DMSO中的0.32mg(0.00023mmol)中间体Q11。在室温下再搅拌20h后,将该批料用PBS缓冲液稀释至2.5ml的总体积。然后将该溶液置于用PBS缓冲液(pH 7.2)平衡的PD 10柱(G-25,GE Healthcare)上,并用PBS缓冲液(pH 7.2)洗脱。随后通过超速离心浓缩并用PBS缓冲液(pH 7.2)稀释回去。
| 实施例 | 靶标 | 抗体TPP- | 规程 | C[mg/ml] | DAR |
| 11a-981 | EGFR | 981 | A | 1.88 | 1.9 |
| 11c-9476 | CD123 | 9476 | A | 1.89 | 1.6 |
| 11e-1015 | HER2 | 1015 | A | 1.69 | 2.3 |
| 11k-7007 | TWEAKR | 7007 | A | 1.17 | 1.9 |
为了比较目的,制备以下ADC:
参比实施例R1:
此类ADC公开于WO2015/096982和WO2016/096610中,其具有各种抗体,如例如西妥昔单抗和曲妥珠单抗。为了比较目的,其中公开的前体中间体F194还与TPP-6013(抗-CD123AK)反应。以下ADC用于比较目的:
| 实施例 | 靶标 | 抗体TPP- | C[mg/ml] | DAR |
| R1a | EGFR | 981 | 1.67 | 1.9 |
| R1c | CD123 | 6013 | 0.42 | 2.9 |
| R1e | HER2 | 1015 | 1.39 | 2.4 |
| R1x | CXCR5 | 9574 | 1.28 | 2.2 |
参比实施例R2:
此类ADC公开于WO2016/096610中,其具有非糖基化的抗-TWEAKR抗体。为了比较目的,其中公开的前体中间体F291还与TPP-9574(抗-CXCR5 AK)、TPP-981(抗-EGFR)和TPP-1015(抗-HER2 AK)反应。以下ADC用于比较目的:
| 实施例 | 靶标 | 抗体TPP- | C[mg/ml] | DAR | |
| R2a | EGFR | 981 | 1.46 | 3.4 | |
| R2e | HER2 | 1015 | 1.42 | 3.5 | |
| R2x | CXCR5 | 9574 | 1.41 | 3.6 |
对于参比实施例R1,WO2015/096982描述了由其形成的代谢物实施例98。对于参比实施例R2,WO2016/096610描述了相同的代谢物实施例M9,其在此列为参比实施例R3M。
参比实施例R3M:
N-(3-氨基丙基)-N-{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}-2-羟基乙酰胺
制备在WO2015/096982中描述为实施例98。
在所述申请中公开或对于新型参比化合物获得的这些参比化合物的生物学数据描述于章节C中。
C:生物学效用的评估
根据本发明的化合物的生物作用可以通过下述测定显示:
a.C-1a ADC的细胞毒性作用的测定
用多种细胞系进行ADC的细胞毒性作用的分析:
NCI-H292:人黏液表皮样肺癌细胞,ATCC-CRL-1848,标准培养基:RPMI 1640(Biochrom;#FG1215,稳定谷氨酰胺)+10% FCS(Sigma;#F2442),TWEAKR-阳性;EGFR-阳性。
BxPC3:人胰腺癌细胞,ATCC-CRL-1687,标准培养基:RPMI 1640(Biochrom;#FG1215,稳定谷氨酰胺)+10%FCS(Sigma;#F2442),TWEAKR阳性。
LoVo:人结肠直肠癌细胞,ATCC编号CCL-229,用于MTT测定的培养:标准培养基:Kaighn's+L-谷氨酰胺(Invitrogen 21127)+10%热失活的FCS(来自Gibco公司,编号10500-064)。用于CTG测定的培养:RPMI 1640(Biochrom;#FG1215,稳定谷氨酰胺)+10%FCS(Sigma#F2442)。TWEAKR-阳性。
KPL4:人乳腺癌细胞系,Bayer Pharma AG(在2012年7月19日在DSMZ身份检查和证实),标准培养基:RPMI 1640(来自Gibco公司;#21875-059,稳定的L-谷氨酰胺)+10%热失活的FBS(来自Gibco公司,编号10500-064);HER2-阳性。
SK-HEP-1:人肝癌细胞系,ATCC编号HTB-52,标准培养基:含有Earle氏盐+Glutamax I(Invitrogen 41090)+10%热失活的FCS(来自Gibco公司,编号10500-064)的MEM;EGFR-阳性,TWEAKR-阳性MOLM-13:人急性单核细胞白血病细胞(AML-M5a),DSMZ,编号ACC 554,标准培养基:RPMI 1640(来自Gibco公司;#21875-059,稳定L-谷氨酰胺)+20%热失活的FCS(来自Gibco公司,编号10500-064);CD123-阳性。
MV-4-11:获得自外周血液的人双表型B骨髓单核细胞白血病细胞,ATCC-CRL-9591,标准培养基:IMDM(ATCC:30-2005)+10%热失活的FCS(Gibco,编号10500-064);CD123-阳性。
NB4:获得自骨髓的人急性前骨髓细胞白血病细胞,DSMZ,编号ACC 207,标准培养基:RPMI 1640+GlutaMAX I(Invitrogen 61870)+10%热失活的FCS(Gibco,编号10500-064)+2.5g的葡萄糖(20%葡萄糖溶液,Gibco,编号19002)+10mM Hepes(Invitrogen15630)+1mM丙酮酸钠(Invitrogen 11360);CD123-阴性
Rec-1:人套细胞淋巴瘤细胞(B细胞非霍奇金氏淋巴瘤)ATCC CRL-3004,标准培养基:RPMI 1640+GlutaMAX I(Invitrogen 61870)+10%热失活的FCS(Gibco,编号10500-064)+10mM)CXCR5-阳性
U251:人胶质母细胞瘤细胞,标准培养基:RPMI 1640(Biochrom;#FG1215,稳定谷氨酰胺)+10% FCS(Biochrom;#S0415),B7H3阳性。HBL-1:人B细胞淋巴瘤细胞(弥漫性大B细胞淋巴瘤)ATT CRL-RRID(资源识别倡议):CVCL_4213,首先描述于Abe等人Cancer61:483-490(1988),获得自Münster大学的Lenz教授;标准培养基:RPMI 1640(Biochrom;#FG1215,稳定谷氨酰胺)+10% FCS(Biochrom;#S0415),类似于Rec-1细胞的培养;CXCR5阳性细胞通过如美国组织培养物保藏中心(American Tissue Culture Collection;ATCC)或Leibniz研究所DSMZ-德国微生物和细胞培养物保藏中心(DSMZ)针对各自细胞系所述的标准方法进行培养。
CTG测定
将细胞通过标准方法培养,其中生长培养基在C-1下所示。以如下方式实施:用胰蛋白酶(0.05%)和EDTA(0.02%)在PBS(Biochrom AG#L2143)中的溶液分离细胞、制丸、再悬浮于培养基中、计数并接种至具有白底的96孔培养板(Costar#3610)中(以75μl/孔,每孔具有以下细胞数:NCI-H292:2500个细胞/孔,BxPC3 2500个细胞/孔,LoVo 3000个细胞/孔)并在培养箱中在37℃和5%二氧化碳下孵育。将悬浮细胞计数并接种至具有白底的96孔培养板(Costar#3610)中(以75μl/孔,每孔具有以下细胞数:Rec-1:3000个细胞/孔,HBL-1:6000个细胞/孔)。24小时后,将抗体-活性物质-缀合物在25μl培养基中(浓缩4倍)置于细胞上,以在细胞上达到3x 10-7M至3x 10-11M的抗体活性物质-缀合物最终浓度(一式三份)。然后将细胞在培养箱中在37℃和5%二氧化碳下孵育。在平行板上,使用Cell Titer Glow(CTG)发光细胞活力测定法(Promega#G7573和#G7571)测定活性物质处理开始时(第0天)的细胞活力。为此,每个细胞批料添加100μl底物,然后用铝箔覆盖该板,使用板振荡器以180rpm振荡2分钟,在实验室台上静置8分钟,然后使用发光计(Victor X2,Perkin Elmer)测量。底物检测活细胞中的ATP含量,其中产生发光信号,其强度与细胞的活力直接成比例。在用抗体活性物质-缀合物孵育72小时后,现在还使用Cell Titer Glow发光细胞活力测定法如上所述测定这些细胞的活力。使用DRC(剂量反应曲线)分析电子表格并借助4参数拟合,与第0天相比着由测量的数据计算生长抑制的IC50。DRC分析电子表格是由Bayer PharmaAG和Bayer Business Services在IDBS E-WorkBook Suite平台上开发的生物书电子表格(IDBS:ID Business Solutions Ltd.,Guildford,UK)。
MTT测定
用C-1下所示的生长培养基通过标准方法培养细胞。以如下方式实施:将细胞用Accutase在PBS中的溶液(Biochrom AG#L2143)分离、造粒、再悬浮于培养基中、计数且接种至具有白底的96孔培养板(Costar公司#3610)(NCI H292:2500个细胞/孔,SK-HEP-1:1000个细胞/孔;KPL-4:1200个细胞/孔;在100μl的总体积中)中。然后将细胞在培养箱中在37℃和5%二氧化碳下孵育。48小时之后,更换培养基。然后将浓度为10-5M至10-13M的在10μl培养基中的抗体-活性物质-缀合物移液至细胞(一式三份),然后将该批料在培养箱中在37℃和5%二氧化碳下孵育。将悬浮液细胞计数并接种至具有白底的96孔培养板(Costar公司#3610)(#3610)(MOLM-13:2000个细胞/孔;NB4:7000个细胞/孔;MV-4-11:5000个细胞/孔,总体积100μl)。在37℃和5%二氧化碳下孵育6小时之后,更换培养基,并将浓度为10-5M至10- 13M的在10μl的培养基中的抗体-活性物质-缀合物或代谢物移液至90μl的细胞(一式三份)。将该批料在37℃和5%二氧化碳下在孵育箱中孵育。96小时之后,借助MTT测定(ATCC,Manassas,Virginia,USA;目录号30-1010K)检测细胞增殖。为此,将MTT试剂与细胞一起孵育4小时,然后通过添加去垢剂来将细胞裂解过夜。在570nm下检测所形成的染料(InfiniteM1000 pro,Tecan公司)。使用DRC(剂量反应曲线)由测量的数据来计算生长抑制的IC50值。未用测试物质、但在其它方面相同处理的细胞的增殖被定义为100%的值。
下表1a和1b列出来自这些测定的代表性实施例的IC50值:
表1a
表1b
下表1c列出来自这些测定的参比实施例的IC50值。
表1c
所示的活性数据基于本实验部分中所述的具有所示药物/mAB比率的实施例。所述值可能在不同的药物/mAB比率下任选地偏差。IC50值是几个独立实验的平均值或单个值。抗体-活性物质-缀合物的作用对于包含各自相应接头和毒簇的各同种型对照是选择性的。对于针对CD123的ADC,另外通过在CD123阴性细胞上测试来表明靶标特异性。
通常,与相应的参比实施例相比,根据本发明的ADC表现出显著改善的细胞毒性功效。
C-1b所选实施例对驱动蛋白纺锤体蛋白KSP/Eg5的抑制的测定在室温下,将人驱动蛋白纺锤体蛋白KSP/Eg5的马达结构域(tebu-bio/Cytoskeleton Inc公司,编号027EG01-XL)以10nM的浓度与用50μg/ml紫杉酚(Sigma公司,编号T7191-5MG)稳定化的微管(牛或猪,tebu-bio/Cytoskeleton Inc公司)一起在15mM PIPES,pH 6.8(5mM MgCl2和10mMDTT,Sigma公司)中孵育5分钟。将新鲜制备的混合物等分至384MTP(来自Corning公司)中。然后添加浓度为1.0x 10-6M至1.0x 10-13M的待检测的抑制剂以及ATP(最终浓度500μM,Sigma公司)。在室温下孵育2小时。通过使用孔雀绿(Biomol公司)检测所形成的无机磷酸盐来检测ATP酶活性。添加试剂之后,在室温下孵育50分钟,然后在620nm的波长下检测吸收。所用的阳性对照是单星素(Monastrol)(Sigma公司,M8515-1mg)和伊斯平斯(Ispinesib)(AdooQ Bioscience公司A10486)。剂量-反应曲线的各个数据是八倍测定。IC50值是两次独立实验的平均值。充当100%对照的是未用抑制剂处理的样品。
下表2概述来自所述测定和相应的细胞毒性数据(MTT测定)的代表性实施例的IC50值。
表2
所示的活性数据基于本实验部分中所述的实施例。
C-1c酶促测定
a:组织蛋白酶B测定
对于待检测的每种组织蛋白酶B-可裂解的前药,在微反应容器(0.5ml,Eppendorf公司)中配制批料。此处使用的酶获得自人肝组织。预先置入2μg组织蛋白酶B(Sigma C857125μg),并用50mM磷酸钠缓冲液,pH6.0,2mM DTT补足至200μl的总体积。然后移入50μl待检测的底物溶液。将该批料在加热块(Thermo Fisher Scientific公司)中在40℃下在300rpm的恒定搅拌下孵育。动力学控制酶促反应。为此,在不同时间点取10μl样品。向取出的样品立即添加20μl冰冷的甲醇,以终止酶促反应,然后在-20℃下冷冻。所选的用于取样的时间点是在10min、2h、4h和24h之后。通过RP-HPLC分析(反相HPLC,Agilent Technologies公司1200系列)检测样品。释放的毒簇的测定使得能够测定酶促反应的半衰期t1/2。
b:豆荚蛋白测定
豆荚蛋白测定用重组人酶进行。将rh豆荚蛋白酶溶液(目录号2199-CY,R&DSystems)在50mM乙酸钠缓冲液/100mM NaCl,pH 4.0中稀释至所需浓度,并在37℃下预孵育2h。然后将rh豆荚蛋白在50mM MES缓冲液,250mM NaCl,pH 5.0中调节至1ng/μl的最终浓度。对于待检测的每种豆荚蛋白可裂解的前药,在微反应容器(0.5ml,Eppendorf公司)中配制批料。为此,将底物溶液用50mM MES缓冲液,250mM NaCl,pH 5.0调节至所需浓度(双倍浓度)。对于酶促反应的动力学测量,首先预先置入250μl豆荚蛋白溶液,并通过添加250μl底物溶液(最终浓度单倍浓缩;3μM)开始酶反应。在各个时间点,各取50μl样品。向所述样品立即添加100μl冰冷的甲醇,以停止酶促反应,然后将样品在-20℃下冷冻。所选的用于取样的时间点是在0.5h、1h、3h和24h之后。然后随后通过RP-HPLC分析和LC-MS分析来分析样品。释放的毒簇的测定使得能够测定酶促反应的半衰期t1/2。
作为显示豆荚蛋白介导的裂解的代表性实例,在豆荚蛋白测定中制备模型化合物A和B作为底物。
参比实施例模型化合物A
N-(吡啶-4-基乙酰基)-L-丙氨酰-L-丙氨酰-N1-[(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-(甲基氨基)-1-氧代丁-2-基]-L-天冬酰胺
首先,如WO2015096982A1中所述制备三氟乙酸(2S)-2-氨基-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-N-甲基丁酰胺。随后,由该中间体通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L103在DMF中偶联来制备标题化合物。LC-MS(方法1):Rt=0.86min;MS(ESIpos):m/z=902[M+H]+。
参比实施例模型化合物B
N-(吡啶-4-基乙酰基)-L-丙氨酰-N-甲基-L-丙氨酰-N1-[(2S)-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-1-(甲基氨基)-1-氧代丁-2-基]-L-天冬酰胺
首先,如WO2015096982A1中所述制备三氟乙酸(2S)-2-氨基-4-[{(1R)-1-[1-苄基-4-(2,5-二氟苯基)-1H-吡咯-2-基]-2,2-二甲基丙基}(乙醇酰基)氨基]-N-甲基丁酰胺。随后,由该中间体通过在HATU和N,N-二异丙基乙胺存在的情况下与中间体L118在DMF中偶联来制备标题化合物。LC-MS(方法1):Rt=0.83min;MS(ESIpos):m/z=916[M+H]+。
将模型化合物A在上述条件下以0.4h的半衰期由豆荚蛋白裂解以产生目标化合物。
将模型化合物B在上述条件下以0.5h的半衰期由豆荚蛋白裂解以产生目标化合物。
C-2内化测定内化是能够经由抗体-活性物质-缀合物(ADC)在表达抗原的癌细胞中特异性且有效地提供细胞毒性有效负载的关键过程。经由特异性抗体和同种型对照抗体的荧光标记来监测该过程。为此,首先将荧光染料缀合至抗体的赖氨酸。使用两倍至10倍摩尔过量的CypHer 5E单NHS酯(批次357392,GE Healthcare)在pH 8.3下进行缀合。在进行偶联之后,反应混合物通过凝胶色谱(Zeba旋转脱盐柱,40K,Thermo Scientific公司,编号87768;洗脱缓冲液:DULBECCO氏PBS,Sigma-Aldrich公司,编号D8537)纯化,以消除过量染料和调节pH值。使用VIVASPIN 500柱(Sartorius stedim biotec公司)浓缩蛋白溶液。抗体的染料载量通过分光光度分析(NanoDrop公司)和随后计算(D/P=A染料ε蛋白:(A280-0.16A染料)ε染料)来确定。
在此检测的抗体和同种型对照的染料载量具有可比拟的数量级。在细胞结合测定中测得偶联不导致抗体亲和力的变化。
对于内化,测定使用经标记的抗体。在处理开始前,将100μl培养基中的细胞(2x104/孔)接种至96-MTP(粗,黑色,透明底部,编号4308776,Applied Biosystems公司)中。在37℃/5% CO2下孵育18小时之后,更换培养基,并以不同浓度(10、5、2.5、1、0.1μg/mL)添加经标记的抗体。对经标记的同种型对照(阴性对照)进行相同处理方案。所选的孵育时间为0小时、0.25小时、0.5小时、1小时、1.5小时、2小时、3小时、6小时和24小时。借助InCellAnalyzer 1000(GE Healthcare公司)进行荧光测量。经由测量参数颗粒计数/细胞和总颗粒强度/细胞来进行动力学评估。
在结合至受体之后,检测抗体的内化能力。为此,选择具有不同受体表达水平的细胞。用所述抗体观察到靶标介导的特异性内化,而同种型对照未显示内化。
C-2b用悬浮细胞的内化测定
如C-2中所述进行荧光染料的偶联。待检测的抗原由造血悬浮细胞表达;因此,在基于FACS的内化测定中检测内化。
检测具有不同靶标表达水平的细胞。将细胞(5x104/孔)以100μl总体积接种至96-MTP(Greiner bio-one,CELLSTAR,650 180,U型底)中。以10μg/ml的最终浓度添加靶标特异性抗体之后,将批料在37℃下孵育不同的时间段(1h、2h、6h,一式三份)。在相同的条件下处理同种型对照。平行批料恒定在4℃下处理和孵育(阴性对照)。借助Guava流式细胞仪(Millipore)进行FACS分析。通过测量荧光强度进行动力学评估,并借助guavaSoft 2.6软件(Millipore)进行评估。对于此处所述的靶标和靶标特异性抗体,在各种细胞中检测到显著和特异性内化;同种型对照未显示内化。
C-2c抗-CD123抗体的共定位测定
由于接头,抗体-活性物质-缀合物的活性代谢物通过溶酶体降解来生成。因此,细胞内运输在进行内化后是至关重要的。关于使用对溶酶体细胞器特异性的标记(例如表面分子或小GTP酶)的抗体的共定位检测使得能够选择具有所需概况的抗体。为此,将总体积为100μl的靶标阳性细胞(5x104/孔)接种至96-MTP(Greiner bio-one,CELLSTAR,650 180,U型底)。在添加经CypHer5E标记的抗-靶标抗体(最终浓度20μg/ml)后,将批料(每个时间点一式两份)在孵育箱(5% CO2)中在37℃下孵育30min、2h和6h。在所选的孵育时间结束前30min,向待检测的批料中添加溶酶体特异性标记。将溶酶体用CytoPainter LysoGreen指示剂(最终浓度1:2000;abcam,ab176826)染色。在孵育后,添加200μl冰冷的FACS缓冲液(DULBECCO氏PBS,Sigma-Aldrich,编号D8537+3%FBS热失活的FBS,Gibco,编号10500-064),并将细胞悬浮液在400x g和4℃下离心5min。将细胞丸粒再悬浮于300μl冰冷的FACS缓冲液并再次离心(4min,400x g,在4℃下)。在进行离心之后,将上清液丢弃并将细胞丸粒置于30μl冰冷的FACS缓冲液中。然后立刻将样品进行FACS/成像分析(FlowSight amnis,Millipore)。借助特定的软件(共定位软件IDEAS Application v6.1)评估共定位。表3概述来自例如用于抗-CD123抗体的测定的结果。
表3
| 实施例 | 共定位[%] |
| TPP-9476 | 29 |
| TPP-8987 | 28 |
| TPP-8988 | 41 |
| TPP-6013 | 43 |
| 7G3 | 10 |
| 同种型对照 | 0.2 |
相比于亲本鼠抗体,人源化抗体TPP-9476和TPP-8987展现显著改善的概况。
C-3用于测定细胞渗透性的体外测试
物质的细胞渗透性可借助体外测试在使用Caco-2细胞的通量测定中进行研究[M.D.Troutman和D.R.Thakker,Pharm.Res.20(8),1210-1224(2003)]。为此,将细胞在24孔过滤板上培养15-16天。为了测定渗透,将各种测试物质在HEPES缓冲液中置于细胞顶端(A)或基底(B)上并孵育2小时。0小时之后和2小时之后,从顺式和反式隔室中获取样品。通过使用反相柱的HPLC(Agilent 1200,德国)分离样品。HPLC系统经由Turbo离子喷雾界面与三重四极质谱仪API 4000(AB SCIEX Deutschland GmbH,Darmstadt,德国)联用。借助Papp值来评估渗透性,该值使用Schwab等人公开的公式计算[D.Schwab等人,J.Med.Chem.46,1716-1725(2003)]。当Papp(B-A)与Papp(A-B)的比率(流出比率)>2或<0.5时,物质被分类为主动输送。
对于细胞内释放的毒簇而言至关重要的是B至A的渗透率[Papp(B-A)]和Papp(B-A)与Papp(A-B)的比率(流出比率):该渗透率越低,物质通过Caco-2细胞单层的主动和被动输送过程越慢,以使得物质在细胞内释放后在细胞内保留更长时间。代谢物在细胞中保留更长时间增加了与生化靶标(此处:驱动蛋白纺锤体蛋白,KSP/Eg5)相互作用的可能性,这导致细胞毒性作用改善。
下表4列出来自该测定的代表性实施例的渗透率数据:
表4
| 实施例 | Papp(B-A)[nm/s] | 流出比率 |
| M1 | 2.7 | 1.6 |
| R3M | 213 | 16 |
与可以由参比实施例2的结合剂-活性物质-缀合物形成的参比代谢物R3M相比,可以由根据本发明的结合剂-活性物质-缀合物形成的代谢物M1表现出明显降低的来自细胞的输送和降低的流出比率。
C-4用于测定P-糖蛋白(P-gp)的底物性质的体外测试许多肿瘤细胞表达用于活性物质的转运蛋白,这经常伴随着针对细胞抑制剂的抗性发展。不是此类转运蛋白(例如P-糖蛋白(P-gp)或BCRP)的底物的物质因此可展现改善的作用概况。
用于P-gp的物质(ABCB1)的底物性质借助使用过表达P-gp的LLC-PK1细胞(L-MDR1细胞)的通量测定[A.H.Schinkel等人,J.Clin.Invest.96,1698-1705(1995)]来测定。为此,将LLC-PK1细胞或L-MDR1细胞在96孔过滤板上培养3-4天。为了测定渗透,将单独或在抑制剂(例如伊维菌素(Ivermectin)或维拉帕米(Verapamil))存在的情况下的各种测试物质在HEPES缓冲液中置于细胞顶端(A)或基底(B)上并孵育2小时。0小时之后和2小时之后,从顺式和反式隔室中获取样品。通过使用反相柱的HPLC分离样品。HPLC系统经由Turbo离子喷雾界面与三重四极质谱仪API 3000(Applied Biosystems Applera,Darmstadt,德国)联用。借助Papp值来评估渗透性,该值使用Schwab等人公开的公式计算[D.Schwab等人,J.Med.Chem.46,1716-1725(2003)]。当Papp(B-A)与Papp(A-B)的流出比率>2时,物质被分类为P-gp底物。
作为评估P-gp底物性质的另外标准,可相互比较L-MDR1细胞和LLC-PK1细胞中的流出比率或在抑制剂存在或不存在的情况下的流出比率。如果这些值相差大于2倍,则所涉物质为P-gp底物。
C-5药代动力学
在雄性Wistar大鼠中静脉内施用5mg/kg实施例2c-9476(DAR 6.3)和实施例2c-9476(DAR 3.4)之后,通过ELISA测量ADC的血浆浓度,并计算药代动力学参数诸如清除率(CL)、曲线下面积(AUC)和半衰期(t1/2)。
表5概述具有DAR 6.3和DAR 3.4的实施例2c-9476的药代动力学参数。
表5
| 实施例 | 2c-9476C | 2c-9476D | |
| DAR | 3.4 | 6.3 | |
| 物种 | 大鼠 | 大鼠 | |
| 品系 | Wistar | Wistar | |
| 性别 | 雄性 | 雄性 | |
| 施用 | 静脉内单次快速推注 | 静脉内单次快速推注 | |
| 施用的剂量 | [mg/kg] | 5.0 | 5.0 |
| AUC正常 | [kg*h/l] | 4897 | 4069 |
| AUC | [mg*h/l] | 24484 | 20343 |
| Cl基质 | [ml/h/kg] | 0.20 | 0.25 |
| VSS | [l/kg] | 0.063 | 0.069 |
| MRT | [h] | 306 | 281 |
| t1/2 | [h] | 229 | 219 |
在静脉内施用后的这种定向性的大鼠PK研究中,对于两个实施例观察到典型的IgG概况。在具有DAR 6.3和DAR 3.4的实施例2c-9476之间不能观察到显著差异。
所用ADC的定量的分析
使用配体结合测定(ELISA)测定ADC的抗体部分作为血浆样品和肿瘤裂解物中的总IgG浓度。此处,使用夹心ELISA形式。该ELISA已被鉴定并验证用于血浆和肿瘤样品中的测定。用山羊的抗人IgG-Fc抗体涂覆ELISA板。与样品一起孵育后,洗涤该板并与猿猴的抗人IgG(H+L)抗体和辣根过氧化物酶(HRP)的检测器缀合物一起孵育。在进一步洗涤步骤后,将HRP底物添加至OPD,并经由在490nm处的吸收监测显色。使用4-参数方程拟合具有已知IgG浓度的标准样品。在较低(LLOQ)和较高(ULOQ)定量限值内,通过内插测定未知浓度。
C5a:体外内化后的ADC代谢物的鉴定
方法描述:
进行用免疫缀合物的内化研究,以分析细胞内形成的代谢物。为此,将人肺肿瘤细胞NCI H292(3x105/孔)接种至6孔板中并孵育过夜(37℃,5%CO2)。用10μg/mL(66nM)待检测的ADC处理细胞。内化在37℃和5%CO2下进行。在各个时间点(0、4、24、48、72h)取细胞样品用于进一步分析。首先,收获上清液(约5mL),并在进行离心后(2min,RT,1000rpm HeraeusVariofuge 3.0R),在-80℃下储存。将细胞用PBS洗涤,用Accutase分离,并确定细胞数。再次洗涤后,向特定数量的细胞(2x 105)添加100mL裂解缓冲液(哺乳动物细胞裂解试剂盒(Sigma MCL1),并在连续振荡下(Thermomixer,15min,4℃,650rpm)在蛋白LoBind管(eppendorf目录号0030 108.116)中孵育。孵育后,将裂解物离心(10min,4℃,12000g,eppendorf 5415R)并收获上清液。将获得的上清液在-80℃下储存。然后如下分析所有样品。
为了对50μL培养上清液/细胞裂解物进行后处理,向其添加150μL的沉淀试剂(甲醇)并振荡10秒。沉淀试剂含有适合浓度(通常20-100μg/L)的内标(ISTD)。以1881g离心10分钟之后,将上清液转移至用300μl的与洗脱液匹配的缓冲剂填充的自动取样器小瓶中,并再次振荡并以1881g离心10分钟。
最后在AB SCIEX Deutschland GmbH公司的与HPLC联用的三重四极质谱仪API6500上测量细胞裂解物样品和上清液样品。
对于校准,添加相应浓度(0.1-1000μg/l)的空白裂解物或空白上清液。检测限值(LLOQ)为约0.2μg/L。
用于检测有效性的品质对照含有4和40μg/L。
C5b:体内的ADC代谢物的鉴定
在静脉内施用3-30mg/kg的不同ADC后,可以测量ADC以及可能存在的代谢物的血浆浓度和肿瘤浓度并计算药代动力学参数诸如清除率(CL)、曲线下面积(AUC)和半衰期(t1/2)。
可能出现的代谢物的定量的分析
血浆、肿瘤、肝和肾中的化合物的测量在通常用甲醇沉淀蛋白后通过高压液相色谱(HPLC)与三重四极质谱仪(MS)的联用进行。
为了对50μL血浆进行后处理,向其添加150μL的沉淀试剂(通常为甲醇)并振荡10秒。沉淀试剂含有相应浓度(通常20-100μg/L)的内标(ISTD)。以1881g离心10分钟后,将上清液转移至用300μL的与洗脱液匹配的缓冲剂填充的自动取样器小瓶中,并再次振荡。
在肿瘤材料或器官材料的后处理中,向各材料添加3-20倍量的提取缓冲液。该提取缓冲液含有50mL的组织蛋白提取试剂(Pierce,Rockford,IL)、两个丸粒的完全-蛋白酶-抑制剂-混合物(Roche Diagnostics GmbH,Mannheim,Germany)和最终浓度为1mM的苯基甲基磺酰氟(Sigma,St.Louis,MO)。根据组织类型(硬:肿瘤;软:肝、肾),选择Prescellys 24裂解和均质化仪器的裂解和均质化程序(Bertin Technologies)(www.prescellys.com)。让均质化的样品在4℃下静置过夜。将50μL的均质化物转移至自动取样器小瓶中,并用150μl的包括ISTD的甲醇填充,振荡10秒,然后静置5min。添加300μL的乙酸铵缓冲液(pH 6.8)并短暂振荡后,将样品以1881g离心10分钟。
为了校准,对于血浆样品而言添加浓度为0.6-1000μg/L的血浆,并且对于组织样品而言添加浓度为0.6-1000μg/L的相应的空白基质。根据样品类型或组织类型,检测限值(LOQ)为1至20μg/L。
最后在AB SCIEX Deutschland GmbH公司的与HPLC联用的三重四极柱质谱仪API4500上测量血浆和基质样品。
用于检测有效性的品质对照组含有4、40和400μg/L。
表6显示在施用5mg/kg来自实施例2c-9476的ADC(n=3)后24h在MOLM-13异种移植物小鼠模型中的肿瘤、肝脏、肾脏和血浆中测量的代谢物浓度。测量的代谢物是:代谢物M1。n.c.=未计算;LOQ:定量限值
表6:
施用具有豆荚蛋白可裂解接头的根据本发明的ADC实施例2c-9476导致与其它的健康器官/组织相比在靶组织(肿瘤)处显著选择性地富集活性的活性物质。
C-6体内的效用测试
例如使用异种移植模型,体内测试根据本发明的缀合物的效用。本领域技术人员熟悉现有技术中可用于测试根据本发明的化合物的效用的方法(参见例如WO 2005/081711;Polson等人,Cancer Res.2009年3月15日;69(6):2358-64)。为此,将表达结合剂的靶分子的肿瘤细胞系接种至啮齿动物(例如小鼠)。然后将根据本发明的缀合物、同种型抗体对照缀合物或对照抗体或等渗盐溶液施用于经接种的动物。施用发生一次或更频繁。在几天的孵育时间后,通过比较经缀合物治疗的动物和对照组来确定肿瘤的大小。经缀合物治疗的动物展现较小的肿瘤大小。
C-6a.小鼠中的实验肿瘤的生长抑制/消退将表达抗体-活性物质-缀合物的抗原的人肿瘤细胞皮下接种至免疫抑制小鼠(例如NMRi裸小鼠或SCID小鼠)的侧腹中。从细胞培养物中分离1至10百万个细胞,离心并用培养基或培养基/基质胶再悬浮。将细胞悬浮液注射到小鼠的皮肤下。
在数天内,肿瘤生长。在建立肿瘤后,大致在肿瘤大小为40mm2时开始治疗。为了检测对较大肿瘤的作用,也可以在肿瘤大小为50-100mm2时才开始治疗。
用APDC和ADC的治疗经由静脉内(i.v.)途径进入小鼠尾静脉来进行。ADC以5mL/kg的体积来施用。
治疗方案取决于抗体的药代动力学。作为标准,用根据本发明的缀合物每周一次实现治疗,持续2或3周。对于快速评估,用单次治疗的方案也可以是合适的。然而,治疗也可进一步继续,或可以在以后的时间点接着进行具有3个治疗天数的第二轮。
作为标准,每个治疗组使用8只动物。除了施用活性物质的组以外,作为对照组的一组根据相同的方案仅用缓冲剂治疗。
在实验期间,使用卡尺定期测量二维(长/宽)肿瘤面积。肿瘤面积借助长x宽来确定。治疗组与对照组的平均肿瘤面积的对比作为T/C面积给出。
如果治疗结束后所有的实验组同时停止,可取出肿瘤并称重。治疗组与对照组的平均肿瘤重量的对比作为T/C重量给出。
C-6b.根据本发明的ADC在各种肿瘤模型中的效用将肿瘤细胞(例如,NCI-H292、REC-1、MOLM-13和MV-4-11)以皮下接种至雌性NMRI-裸小鼠(Janvier)的侧腹中。在肿瘤大小为~40mm2时,用抗体-活性物质-缀合物进行静脉内治疗。治疗之后,任选地继续监测肿瘤生长。
相比于对照组和经缀合的同种型对照抗体,用根据本发明的ADC治疗导致肿瘤生长的显著和在一些情况下持久的抑制。表7给出分别在实验结束的那天(从治疗开始时计算)对于肿瘤面积所确定的T/C值。
表7:
Claims (10)
1.式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐
其中
X1代表N,
X2代表N,且
X3代表C;
或
X1代表N,
X2代表C,且
X3代表N;
或
X1代表CH或CF,
X2代表C,且
X3代表N;
或
X1表示NH,
X2代表C,且
X3代表C;
或
X1代表CH,
X2代表N,且
X3代表C,
R1代表氢或甲基,
R2代表甲基、乙基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,R3代表甲基、乙基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)2-8-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)1-8-(CH2)2-NH-C(=O)-CH2-##,
W代表以下基团
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
##代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
2.根据权利要求1所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
X1代表CH,
X2代表C,
X3代表N;
R1代表氢或甲基,
R2代表甲基、-CH2-CH(CH3)2、-CH2-C(=O)OH或异丙基,R3代表甲基、-CH2-CH(CH3)2或–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,#-C(=O)-CH(CH3)-NH-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,#-C(=O)-CH(CH3)-NH-C(=O)-CH2-W,
#-C(=O)-CH2-NH-C(=O)-CH2-CH(##)-COOH,
#-C(=O)-CH2-NH-C(=O)-CH(##)-CH2-COOH,
#-C(=O)-CH2-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-(CH2)3-C(=O)-###,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)5-W,
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)-##或
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2-CH2-O)4-(CH2)2-NH-C(=O)-CH2-##,
W代表以下基团
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
##代表连接至所述结合剂的半胱氨酸侧链的硫原子的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
3.根据权利要求1和2所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,
其中
R1代表氢或甲基,
R2代表甲基或异丙基,
R3代表甲基或–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
4.根据权利要求1至3所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至50的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
5.根据权利要求1至4所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,
AK代表结合剂或其衍生物,优选抗体或结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至所述结合剂的赖氨酸侧链的氮原子的键。
6.根据权利要求1至5所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,且
AK代表抗-CD123抗体、抗-CXCR5抗体、抗-B7H3抗体、抗-TWEAKR抗体、抗-Her2抗体或抗-EGFR抗体或代表它们的结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键。
7.根据权利要求1至6所述的式(I)的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
R1代表甲基,
R2代表甲基,
R3代表–CH2-C(=O)-NH2,
M代表以下基团
#-C(=O)-CH(CH3)-NH-C(=O)-(CH2)3-C(=O)-###,
n代表1至20的数目,且
AK代表选自TPP-9476、TPP-8988、TPP-8987和TPP-6013的抗-CD123抗体,代表选自TPP-9574和TPP-9580的抗-CXCR5抗体,代表抗-B7H3抗体TPP-8382,代表选自TPP-7006和TPP-7007的抗-TWEAKR抗体,代表抗-Her2抗体TPP-1015或代表抗-EGFR抗体TPP-981或代表它们的结合抗原的抗体片段,
#代表连接至所述化合物的键,
###代表连接至抗体(AK)或其结合抗原的抗体片段的赖氨酸侧链的氮原子的键。
9.根据权利要求8所述的结合剂-活性物质-缀合物以及其盐、溶剂化物和这些溶剂化物的盐,其中
n代表1至20。
10.药物组合物,其包含至少一种根据前述权利要求中的一项或多项所述的结合剂-活性物质-缀合物与惰性、无毒、药学上合适的助剂的组合。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16205868 | 2016-12-21 | ||
| EP16205868.9 | 2016-12-21 | ||
| PCT/EP2017/082789 WO2018114578A1 (de) | 2016-12-21 | 2017-12-14 | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| CN201780087040.6A CN110312534B (zh) | 2016-12-21 | 2017-12-14 | 具有酶促可裂解基团的抗体-药物-缀合物(adc) |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780087040.6A Division CN110312534B (zh) | 2016-12-21 | 2017-12-14 | 具有酶促可裂解基团的抗体-药物-缀合物(adc) |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116327974A true CN116327974A (zh) | 2023-06-27 |
Family
ID=57614197
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780087040.6A Active CN110312534B (zh) | 2016-12-21 | 2017-12-14 | 具有酶促可裂解基团的抗体-药物-缀合物(adc) |
| CN202310307417.1A Pending CN116327974A (zh) | 2016-12-21 | 2017-12-14 | 具有酶促可裂解基团的抗体-药物-缀合物(adc) |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780087040.6A Active CN110312534B (zh) | 2016-12-21 | 2017-12-14 | 具有酶促可裂解基团的抗体-药物-缀合物(adc) |
Country Status (14)
| Country | Link |
|---|---|
| US (3) | US11660351B2 (zh) |
| EP (1) | EP3558388A1 (zh) |
| JP (2) | JP7066714B2 (zh) |
| KR (3) | KR102556826B1 (zh) |
| CN (2) | CN110312534B (zh) |
| AR (1) | AR110418A1 (zh) |
| AU (3) | AU2017380871C1 (zh) |
| CA (1) | CA3047489A1 (zh) |
| IL (3) | IL291308B2 (zh) |
| MX (3) | MX2019007641A (zh) |
| PE (1) | PE20191235A1 (zh) |
| RU (1) | RU2761390C2 (zh) |
| TW (2) | TWI781125B (zh) |
| WO (1) | WO2018114578A1 (zh) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016207089A1 (de) | 2015-06-22 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) und binder-prodrug-konjugate (apdcs) mit enzymatisch spaltbaren gruppen |
| US10973923B2 (en) | 2015-06-23 | 2021-04-13 | Bayer Pharma Aktiengesellschaft | Site specific homogeneous with KSP inhibitors |
| CA2990398A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-cd123-antibodies |
| KR20180123047A (ko) | 2016-03-24 | 2018-11-14 | 바이엘 파마 악티엔게젤샤프트 | 효소적으로 절단가능한 기를 갖는 세포독성 활성제의 전구약물 |
| WO2017216028A1 (en) | 2016-06-15 | 2017-12-21 | Bayer Pharma Aktiengesellschaft | Specific antibody-drug-conjugates (adcs) with ksp inhibitors and anti-cd123-antibodies |
| US12059472B2 (en) | 2016-12-21 | 2024-08-13 | Bayer Aktiengesellschaft | Prodrugs of cytotoxic active agents having enzymatically cleavable groups |
| WO2018114578A1 (de) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| CA3047522A1 (en) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Specific antibody drug conjugates (adcs) having ksp inhibitors |
| EP3658172A4 (en) | 2017-07-25 | 2021-05-05 | TrueBinding, Inc. | TREATING CANCER BY BLOCKING THE INTERACTION OF TIM-3 AND HIS LIGAND |
| KR102804751B1 (ko) * | 2017-08-23 | 2025-05-13 | 막스-델부뤽-센트럼 퓌어 몰레쿨라레 메디친 인 데어 헬름홀츠-게마인샤프트 | Cxcr5에 결합하는 키메라 항원 수용체 및 car-t 세포 |
| WO2019243159A1 (de) * | 2018-06-18 | 2019-12-26 | Bayer Aktiengesellschaft | Gegen cxcr5 gerichtete binder-wirkstoff-konjugate mit enzymatisch spaltbaren linkern und verbessertem wirkungsprofil |
| CN120058944A (zh) | 2019-01-30 | 2025-05-30 | 真和制药有限公司 | 抗gal3抗体及其用途 |
| MX2022014786A (es) | 2020-05-26 | 2023-01-16 | Truebinding Inc | Metodos para tratar enfermedades inflamatorias mediante el bloqueo de galectina-3. |
| WO2022175595A1 (en) * | 2021-02-16 | 2022-08-25 | Glykos Finland Oy | Linker-payloads and conjugates thereof |
| TW202320857A (zh) | 2021-07-06 | 2023-06-01 | 美商普方生物製藥美國公司 | 連接子、藥物連接子及其結合物及其使用方法 |
| WO2024105205A1 (en) | 2022-11-17 | 2024-05-23 | Bayer Aktiengesellschaft | Antibody-drug conjugates (a2dcs) with enzymatically cleavable groups |
| WO2025027529A1 (en) | 2023-07-31 | 2025-02-06 | Advesya | Anti-il-1rap antibody drug conjugates and methods of use thereof |
| TW202530255A (zh) | 2023-12-15 | 2025-08-01 | 法商亞維西亞有限公司 | 抗il-1rap結合結構域及其抗體-藥物偶聯物 |
| WO2025149667A1 (en) | 2024-01-12 | 2025-07-17 | Pheon Therapeutics Ltd | Antibody drug conjugates and uses thereof |
Family Cites Families (152)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CU22545A1 (es) | 1994-11-18 | 1999-03-31 | Centro Inmunologia Molecular | Obtención de un anticuerpo quimérico y humanizado contra el receptor del factor de crecimiento epidérmico para uso diagnóstico y terapéutico |
| US5179017A (en) | 1980-02-25 | 1993-01-12 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4634665A (en) | 1980-02-25 | 1987-01-06 | The Trustees Of Columbia University In The City Of New York | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4399216A (en) | 1980-02-25 | 1983-08-16 | The Trustees Of Columbia University | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| US4714681A (en) | 1981-07-01 | 1987-12-22 | The Board Of Reagents, The University Of Texas System Cancer Center | Quadroma cells and trioma cells and methods for the production of same |
| US4474893A (en) | 1981-07-01 | 1984-10-02 | The University of Texas System Cancer Center | Recombinant monoclonal antibodies |
| US4510245A (en) | 1982-11-18 | 1985-04-09 | Chiron Corporation | Adenovirus promoter system |
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US5168062A (en) | 1985-01-30 | 1992-12-01 | University Of Iowa Research Foundation | Transfer vectors and microorganisms containing human cytomegalovirus immediate-early promoter-regulatory DNA sequence |
| US4968615A (en) | 1985-12-18 | 1990-11-06 | Ciba-Geigy Corporation | Deoxyribonucleic acid segment from a virus |
| DE8808645U1 (de) | 1988-07-06 | 1988-08-25 | Hofer, Daniel, 7730 Villingen-Schwenningen | Anzeigeeinrichtung für Feuerlöscher |
| US4925648A (en) | 1988-07-29 | 1990-05-15 | Immunomedics, Inc. | Detection and treatment of infectious and inflammatory lesions |
| US5601819A (en) | 1988-08-11 | 1997-02-11 | The General Hospital Corporation | Bispecific antibodies for selective immune regulation and for selective immune cell binding |
| ES2096590T3 (es) | 1989-06-29 | 1997-03-16 | Medarex Inc | Reactivos biespecificos para la terapia del sida. |
| DK0595798T3 (da) | 1989-10-20 | 1999-09-27 | Medarex Inc | Bispecifikke heteroantistoffer med dobbelte effektorfunktioner |
| US5270163A (en) | 1990-06-11 | 1993-12-14 | University Research Corporation | Methods for identifying nucleic acid ligands |
| CA2093022C (en) | 1990-10-05 | 2005-02-22 | Michael W. Fanger | Targeted immunostimulation with bispecific reagents |
| EP0557300B1 (en) | 1990-10-29 | 1997-11-19 | Chiron Corporation | Bispecific antibodies, method of production, and uses thereof |
| DE69233153T2 (de) | 1991-03-06 | 2004-05-27 | Merck Patent Gmbh | Humanisierte monoklonale antikörper |
| WO1992019973A1 (en) | 1991-04-26 | 1992-11-12 | Surface Active Limited | Novel antibodies, and methods for their use |
| ES2193143T3 (es) | 1992-03-05 | 2003-11-01 | Univ Texas | Uso de inmunoconjugados para la diagnosis y/o terapia de tumores vascularizaos. |
| ATE188874T1 (de) | 1992-08-18 | 2000-02-15 | Centro Inmunologia Molecular | Monoklonale antikörper gegen den epidermalen wachstumsfaktorrezeptor, zellen und verfahren zur ihrer herstellung und sie erhaltende zusammensetzungen |
| DE69531187T2 (de) | 1994-12-20 | 2004-04-22 | Merck Patent Gmbh | Monoklonaler Antikörper gegen das Alpha-V-Integrin |
| DK1143006T3 (da) | 1995-08-18 | 2008-07-14 | Morphosys Ip Gmbh | Vektorer/DNA-sekvenser fra humane kombinatoriske antistofbiblioteker |
| WO1997024373A1 (en) | 1995-12-29 | 1997-07-10 | Medvet Science Pty. Limited | Monoclonal antibody antagonists to haemopoietic growth factors |
| AU725583B2 (en) | 1996-03-25 | 2000-10-12 | E. R. Squibb & Sons, L.L.C. | Monoclonal antibodies specific for the extracellular domain of prostate specific membrane antigen |
| US6150508A (en) | 1996-03-25 | 2000-11-21 | Northwest Biotherapeutics, Inc. | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen |
| NZ517331A (en) | 1999-07-29 | 2004-02-27 | Medarex Inc | Human monoclonal antibodies to prostate specific membrane antigen and a transgenic mouse to produce the antibody |
| SK12232002A3 (sk) | 2000-02-25 | 2003-03-04 | The Government Of The United States, As Represented By The | Anti-ERGFRvIII scFv so zlepšenou cytotoxicitou a výťažkom, imunotoxíny a spôsoby ich použitia |
| JP2003533987A (ja) | 2000-05-19 | 2003-11-18 | イス ケミカル カンパニー リミテッド | 表皮成長因子収容体に対するヒト化抗体 |
| US6884446B1 (en) | 2000-07-27 | 2005-04-26 | Red Arrow Products Co., Llc | Article for browning and flavoring foodstuffs |
| US7288390B2 (en) | 2000-08-07 | 2007-10-30 | Centocor, Inc. | Anti-dual integrin antibodies, compositions, methods and uses |
| AUPR395801A0 (en) | 2001-03-26 | 2001-04-26 | Austin Research Institute, The | Antibodies against cancer |
| HUP0501113A3 (en) | 2001-04-26 | 2007-12-28 | Biogen Idec Inc | Cripto blocking antibodies and uses thereof |
| PT1392359E (pt) | 2001-05-11 | 2010-01-27 | Ludwig Inst For Cancer Res Ltd | Proteínas de ligação específica e suas utilizações |
| US7595378B2 (en) | 2001-06-13 | 2009-09-29 | Genmab A/S | Human monoclonal antibodies to epidermal growth factor receptor (EGFR) |
| CN100497389C (zh) | 2001-06-13 | 2009-06-10 | 根马布股份公司 | 表皮生长因子受体(egfr)的人单克隆抗体 |
| WO2003060064A2 (en) | 2001-07-12 | 2003-07-24 | Incyte Genomics, Inc. | Intracellular signaling molecules |
| SG114505A1 (en) | 2001-10-17 | 2005-09-28 | First Cube Pte Ltd | System and method for facilitating delivery and return service |
| EP2360169B1 (en) | 2001-10-23 | 2015-10-14 | Psma Development Company, L.L.C. | PSMA antibodies |
| DE60232994D1 (de) | 2001-12-06 | 2009-08-27 | Merck & Co Inc | Inhibitoren von mitotischem kinesin |
| US20080193445A1 (en) | 2002-01-18 | 2008-08-14 | Liliane Goetsch | Novel anti-IGF-IR antibodies and uses thereof |
| US7282567B2 (en) | 2002-06-14 | 2007-10-16 | Immunomedics, Inc. | Monoclonal antibody hPAM4 |
| CA2478833C (en) | 2002-03-13 | 2015-11-10 | Biogen, Inc. | Anti-.alpha.v.beta.6 antibodies |
| EP1494693B1 (en) | 2002-03-22 | 2010-12-08 | Biogen Idec MA Inc. | Cripto-specific antibodies |
| MXPA05003830A (es) | 2002-10-11 | 2005-06-23 | Cytokinetics Inc | Compuestos, composiciones y metodos. |
| US8658377B2 (en) * | 2002-11-15 | 2014-02-25 | Morehouse School Of Medicine | Detecting cancer with anti-CCL25 and anti-CCR9 antibodies |
| US8512701B2 (en) * | 2002-11-15 | 2013-08-20 | Morehouse School Of Medicine | Anti-CXCL13 and anti-CXCR5 antibodies for the prevention and treatment of cancer and cancer cell migration |
| JP2006524693A (ja) | 2003-04-11 | 2006-11-02 | メディミューン,インコーポレーテッド | EphA2および非腫瘍性過増殖性細胞障害 |
| WO2004100873A2 (en) | 2003-05-07 | 2004-11-25 | Cytokinetics, Inc. | Compounds, compositions, and methods |
| BRPI0411803A (pt) | 2003-06-27 | 2006-05-23 | Abgenix Inc | anticorpos dirigidos aos mutantes de deleção de receptor de fator de crescimento epidérmico e seus usos |
| FR2857811A1 (fr) | 2003-07-16 | 2005-01-21 | St Microelectronics Sa | Methode de chiffrage d'un flux audio ou video compresse a tolerance d'erreurs |
| WO2005009369A2 (en) | 2003-07-21 | 2005-02-03 | Immunogen, Inc. | A ca6 antigen-specific cytotoxic conjugate and methods of using the same |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| KR20060127413A (ko) | 2003-11-25 | 2006-12-12 | 카이론 코포레이션 | 항암제로서의 퀴나졸리논 화합물 |
| EP1701979A2 (en) | 2003-12-03 | 2006-09-20 | Xencor, Inc. | Optimized antibodies that target the epidermal growth factor receptor |
| US7662581B1 (en) | 2003-12-18 | 2010-02-16 | Novartis Vaccines And Diagnostics, Inc. | Eg5 co-crystals |
| US7767792B2 (en) | 2004-02-20 | 2010-08-03 | Ludwig Institute For Cancer Research Ltd. | Antibodies to EGF receptor epitope peptides |
| US7598350B2 (en) | 2004-03-19 | 2009-10-06 | Imclone Llc | Human anti-epidermal growth factor receptor antibody |
| KR101170925B1 (ko) | 2004-06-18 | 2012-08-07 | 노바티스 백신즈 앤드 다이아그노스틱스 인코포레이티드 | 암 치료용 키네신 방추 단백질 (ksp) 억제제로서의n-(1-(1-벤질-4-페닐-1h-이미다졸-2-일)-2,2-디메틸프로필)벤자미드 유도체 및 관련 화합물 |
| EP1773884B1 (en) | 2004-08-03 | 2012-03-07 | Innate Pharma | Therapeutic and diagnostic methods and compositions targeting 4ig-b7-h3 and its counterpart nk cell receptor |
| US7449486B2 (en) | 2004-10-19 | 2008-11-11 | Array Biopharma Inc. | Mitotic kinesin inhibitors and methods of use thereof |
| US20100093767A1 (en) | 2004-12-03 | 2010-04-15 | Takeda San Diego, Inc. | Mitotic Kinase Inhibitors |
| EA013323B1 (ru) | 2004-12-09 | 2010-04-30 | Сентокор, Инк. | Иммуноконъюгаты против интегрина, способы и варианты применения |
| GB0428250D0 (en) | 2004-12-23 | 2005-01-26 | Novartis Ag | Organic compounds |
| EP2230517A1 (en) | 2005-01-07 | 2010-09-22 | Diadexus, Inc. | OVR110 antibody compositions and methods of use |
| US8207303B2 (en) | 2005-02-18 | 2012-06-26 | Medarex, Inc. | Monoclonal antibodies against CD30 lacking in fucosyl residues |
| GB0505969D0 (en) | 2005-03-23 | 2005-04-27 | Novartis Ag | Organic compounds |
| CN103127523A (zh) | 2005-06-20 | 2013-06-05 | Psma开发有限公司 | Psma抗体-药物缀合物 |
| TW200800951A (en) | 2005-08-09 | 2008-01-01 | Novartis Ag | Substituted imidazole compounds as KSP inhibitors |
| CA2893252C (en) | 2005-08-24 | 2018-05-29 | Immunogen, Inc. | Process for preparing antibody maytansinoid conjugates |
| EA016186B1 (ru) | 2005-09-26 | 2012-03-30 | Медарекс, Инк. | Человеческие моноклональные антитела к cd70 и их применение |
| EP1790664A1 (en) | 2005-11-24 | 2007-05-30 | Ganymed Pharmaceuticals AG | Monoclonal antibodies against claudin-18 for treatment of cancer |
| CN101374856A (zh) * | 2005-11-29 | 2009-02-25 | 斯克里普斯研究学院 | 抑制肿瘤细胞浸润、转移和血管生成 |
| DOP2006000277A (es) | 2005-12-12 | 2007-08-31 | Bayer Pharmaceuticals Corp | Anticuerpos anti mn y métodos para su utilización |
| WO2008004834A1 (en) | 2006-07-06 | 2008-01-10 | Isu Abxis Co., Ltd | Humanized monoclonal antibody highly binding to epidermal growth factor receptor, egf receptor |
| EP2066349B1 (en) | 2006-09-08 | 2012-03-28 | MedImmune, LLC | Humanized anti-cd19 antibodies and their use in treatment of tumors, transplantation and autoimmune diseases |
| AU2007294122B2 (en) | 2006-09-10 | 2013-03-07 | Glycotope Gmbh | Use of human cells of myeloid leukaemia origin for expression of antibodies |
| EP1900750A1 (en) | 2006-09-18 | 2008-03-19 | Glycotope Gmbh | Fully human high yield production system for improved antibodies |
| EP1911766A1 (en) | 2006-10-13 | 2008-04-16 | Glycotope Gmbh | Use of human cells of myeloid leukaemia origin for expression of antibodies |
| WO2008036688A2 (en) | 2006-09-18 | 2008-03-27 | Xencor, Inc. | Optimized antibodies that target hm1.24 |
| EP1914242A1 (en) | 2006-10-19 | 2008-04-23 | Sanofi-Aventis | Novel anti-CD38 antibodies for the treatment of cancer |
| PT2099823E (pt) | 2006-12-01 | 2014-12-22 | Seattle Genetics Inc | Agentes de ligação ao alvo variantes e suas utilizações |
| WO2008140603A2 (en) | 2006-12-08 | 2008-11-20 | Macrogenics, Inc. | METHODS FOR THE TREATMENT OF DISEASE USING IMMUNOGLOBULINS HAVING FC REGIONS WITH ALTERED AFFINITIES FOR FCγR ACTIVATING AND FCγR INHIBITING |
| GEP20125415B (en) | 2007-01-05 | 2012-03-12 | Novartis Ag | Imidazole derivatives as kinesin spindle protein inhibitors (eg-5) |
| WO2008092117A2 (en) | 2007-01-25 | 2008-07-31 | Xencor, Inc. | Immunoglobulins with modifications in the fcr binding region |
| US20100143245A1 (en) | 2007-03-22 | 2010-06-10 | Sloan-Kettering Institute For Cancer Research | Uses of monoclonal antibody 8h9 |
| KR20090122403A (ko) | 2007-03-29 | 2009-11-27 | 노파르티스 아게 | 증식성 질환의 치료를 위한 3-이미다졸릴-인돌 |
| US8163279B2 (en) | 2007-04-13 | 2012-04-24 | Stemline Therapeutics, Inc. | IL3Rα antibody conjugates and uses thereof |
| NZ556142A (en) | 2007-06-25 | 2009-11-27 | Novartis Ag | Animal remedy dispensing means |
| KR20100029099A (ko) | 2007-06-28 | 2010-03-15 | 톰슨 라이센싱 | 비디오 믹서 교차점 매트릭스의 2중 사용 |
| JP5409628B2 (ja) | 2007-08-03 | 2014-02-05 | アッヴィ・バイオセラピューティクス・インコーポレイテッド | 抗tweak受容体抗体の治療上の使用 |
| JP5532486B2 (ja) | 2007-08-14 | 2014-06-25 | ルードヴィッヒ インスティテュート フォー キャンサー リサーチ | Egf受容体を標的とするモノクローナル抗体175ならびにその誘導体および用途 |
| US8865875B2 (en) | 2007-08-22 | 2014-10-21 | Medarex, L.L.C. | Site-specific attachment of drugs or other agents to engineered antibodies with C-terminal extensions |
| MX2010001975A (es) | 2007-08-29 | 2010-03-10 | Sanofi Aventis | Anticuerpos anti-cxcr5 humanizados, derivados de los mismos y su uso. |
| HRP20130649T1 (hr) | 2007-09-07 | 2013-08-31 | Agensys, Inc. | Protutijela i povezane molekule koje se vežu za 24p4c12 proteine |
| US8039597B2 (en) | 2007-09-07 | 2011-10-18 | Agensys, Inc. | Antibodies and related molecules that bind to 24P4C12 proteins |
| US9023351B2 (en) | 2007-11-26 | 2015-05-05 | Bayer Intellectual Property Gmbh | Anti-mesothelin antibodies and uses thereof |
| EA201070687A1 (ru) | 2007-12-06 | 2010-12-30 | Си Эс Эл ЛИМИТЕД | Способ ингибирования лейкозных стволовых клеток |
| US8252832B2 (en) | 2007-12-14 | 2012-08-28 | Novartis Ag | Kinesin inhibitors as cancer therapeutics |
| ES2526433T3 (es) | 2007-12-26 | 2015-01-12 | Biotest Ag | Inmunoconjugados dirigidos a CD138 y usos de los mismos |
| EP2238168B8 (en) | 2007-12-26 | 2014-07-23 | Biotest AG | Agents targeting cd138 and uses thereof |
| AU2009231991B2 (en) | 2008-04-02 | 2014-09-25 | Macrogenics, Inc. | HER2/neu-specific antibodies and methods of using same |
| CA2723973A1 (en) | 2008-05-15 | 2009-11-19 | Biogen Idec Ma Inc. | Anti-fn14 antibodies and uses thereof |
| EP2331577B1 (en) | 2008-08-29 | 2017-06-07 | Symphogen A/S | Recombinant anti-epidermal growth factor receptor antibody compositions |
| WO2010084186A1 (en) | 2009-01-26 | 2010-07-29 | Novartis Ag | Salts and polymorphs of a kinesin inhibitor compound |
| SG174963A1 (en) | 2009-03-31 | 2011-11-28 | Roche Glycart Ag | Treatment of cancer with a humanized anti-egfr igg1 antibody and irinotecan |
| AR075982A1 (es) | 2009-03-31 | 2011-05-11 | Roche Glycart Ag | Terapia de combinacion de un anticuerpo afucosilado y una o mas de las citoquinas seleccionadas de gm- csf humano, m -csf humano y/o il-3 humano y composicion |
| EP2426148B1 (en) | 2009-04-27 | 2015-08-05 | Kyowa Hakko Kirin Co., Ltd. | Anti-il-3ra antibody for use in treatment of blood tumor |
| CN101959216B (zh) | 2009-07-20 | 2014-06-18 | 电信科学技术研究院 | 一种分载波配置增强cell_fach的方法、系统和设备 |
| PL2486141T3 (pl) | 2009-10-07 | 2018-07-31 | Macrogenics, Inc. | Polipeptydy zawierające regiony fc i mające w wyniku zmian w zakresie fukozylacji ulepszoną funkcję efektorową, i sposoby zastosowania tych polipeptydów |
| WO2012010582A1 (en) * | 2010-07-21 | 2012-01-26 | Roche Glycart Ag | Anti-cxcr5 antibodies and methods of use |
| NZ604510A (en) | 2010-08-17 | 2013-10-25 | Csl Ltd | Dilutable biocidal compositions and methods of use |
| AR086363A1 (es) | 2011-04-21 | 2013-12-11 | Bayer Ip Gmbh | Conjugados de principio activo-ligante (adc) y el uso de los mismos |
| KR102087854B1 (ko) | 2011-06-10 | 2020-03-12 | 메르사나 테라퓨틱스, 인코포레이티드 | 단백질-중합체-약물 접합체 |
| US9726666B2 (en) * | 2011-06-13 | 2017-08-08 | Tla Targeted Immunotherapies Ab | Diagnosing and treating inflammatory diseases |
| AR088941A1 (es) | 2011-11-23 | 2014-07-16 | Bayer Ip Gmbh | Anticuerpos anti-fgfr2 y sus usos |
| UA112096C2 (uk) | 2011-12-12 | 2016-07-25 | Байєр Інтеллектуал Проперті Гмбх | Заміщені триазолопіридини та їх застосування як інгібіторів ttk |
| AU2013222935B2 (en) * | 2012-02-24 | 2016-03-10 | Alteogen Inc. | Modified antibody in which motif comprising cysteine residue is bound, modified antibody-drug conjugate comprising the modified antibody, and production method for same |
| PT2850106T (pt) | 2012-05-18 | 2022-07-18 | Aptevo Res & Development Llc | Imunofusão biespecífica (bif) de scfv de ligação a cd123 e cd3 |
| WO2014061277A1 (ja) | 2012-10-19 | 2014-04-24 | 第一三共株式会社 | 親水性構造を含むリンカーで結合させた抗体-薬物コンジュゲート |
| WO2014093640A1 (en) | 2012-12-12 | 2014-06-19 | Mersana Therapeutics,Inc. | Hydroxy-polmer-drug-protein conjugates |
| TW201437211A (zh) | 2013-03-01 | 2014-10-01 | Bayer Pharma AG | 經取代咪唑并嗒□ |
| US9498532B2 (en) | 2013-03-13 | 2016-11-22 | Novartis Ag | Antibody drug conjugates |
| US9498540B2 (en) | 2013-03-15 | 2016-11-22 | Novartis Ag | Cell proliferation inhibitors and conjugates thereof |
| CN105451773A (zh) * | 2013-03-15 | 2016-03-30 | 诺华股份有限公司 | 细胞增殖抑制剂及其缀合物 |
| WO2014177652A1 (en) | 2013-05-02 | 2014-11-06 | Ares Trading S.A | Monoclonal antibody directed against cxcr5 |
| CN105308070A (zh) | 2013-06-14 | 2016-02-03 | 拜耳制药股份公司 | 抗tweakr抗体及其用途 |
| KR102087850B1 (ko) | 2013-10-11 | 2020-03-12 | 메르사나 테라퓨틱스, 인코포레이티드 | 단백질-고분자-약물 접합체 |
| CA2932476A1 (en) | 2013-12-12 | 2015-06-18 | Stemcentrx, Inc. | Novel anti-dpep3 antibodies and methods of use |
| KR102329024B1 (ko) | 2013-12-23 | 2021-11-19 | 바이엘 파마 악티엔게젤샤프트 | 키네신 스핀들 단백질(ksp)과의 항체 약물 접합체 (adcs) |
| AU2015229463A1 (en) | 2014-03-12 | 2016-09-15 | Novartis Ag | Specific sites for modifying antibodies to make immunoconjugates |
| WO2015189143A1 (en) | 2014-06-12 | 2015-12-17 | Bayer Pharma Aktiengesellschaft | Aglycosyl anti-tweakr antibodies and uses thereof |
| US10786578B2 (en) | 2014-08-05 | 2020-09-29 | Novartis Ag | CKIT antibody drug conjugates |
| JP2017525710A (ja) | 2014-08-22 | 2017-09-07 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Cxcr5に結合する抗原結合タンパク質 |
| MX2017003123A (es) * | 2014-09-12 | 2017-05-12 | Genentech Inc | Anticuerpos y conjugados modificados geneticamente con cisteina. |
| JP6743015B2 (ja) | 2014-12-15 | 2020-08-19 | バイエル ファーマ アクチエンゲゼルシャフト | Ksp阻害剤の脱グリコシル化抗tweakr抗体との抗体薬物複合体(adc類) |
| TW201709932A (zh) | 2015-06-12 | 2017-03-16 | 西雅圖遺傳學公司 | Cd123抗體及其共軛物 |
| WO2016207089A1 (de) | 2015-06-22 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) und binder-prodrug-konjugate (apdcs) mit enzymatisch spaltbaren gruppen |
| US10973923B2 (en) * | 2015-06-23 | 2021-04-13 | Bayer Pharma Aktiengesellschaft | Site specific homogeneous with KSP inhibitors |
| CN108025085A (zh) | 2015-06-23 | 2018-05-11 | 拜耳制药股份公司 | Ksp抑制剂与抗b7h3抗体的抗体药物缀合物(adc) |
| JP2018525334A (ja) | 2015-06-23 | 2018-09-06 | バイエル ファーマ アクチエンゲゼルシャフト | キネシンスピンドルタンパク質(ksp)阻害剤の抗tweakr抗体との抗体薬物複合体 |
| CA2990411A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-b7h3-antibodies |
| CA2990398A1 (en) | 2015-06-23 | 2016-12-29 | Bayer Pharma Aktiengesellschaft | Antibody drug conjugates of kinesin spindel protein (ksp) inhibitors with anti-cd123-antibodies |
| KR20180123047A (ko) | 2016-03-24 | 2018-11-14 | 바이엘 파마 악티엔게젤샤프트 | 효소적으로 절단가능한 기를 갖는 세포독성 활성제의 전구약물 |
| WO2017216028A1 (en) | 2016-06-15 | 2017-12-21 | Bayer Pharma Aktiengesellschaft | Specific antibody-drug-conjugates (adcs) with ksp inhibitors and anti-cd123-antibodies |
| CA3047522A1 (en) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Specific antibody drug conjugates (adcs) having ksp inhibitors |
| WO2018114578A1 (de) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| US12059472B2 (en) | 2016-12-21 | 2024-08-13 | Bayer Aktiengesellschaft | Prodrugs of cytotoxic active agents having enzymatically cleavable groups |
| WO2019243159A1 (de) | 2018-06-18 | 2019-12-26 | Bayer Aktiengesellschaft | Gegen cxcr5 gerichtete binder-wirkstoff-konjugate mit enzymatisch spaltbaren linkern und verbessertem wirkungsprofil |
| IL282748B2 (en) | 2018-11-05 | 2025-07-01 | Bayer Pharma AG | Cytostatic conjugates with integrin ligands |
-
2017
- 2017-12-14 WO PCT/EP2017/082789 patent/WO2018114578A1/de not_active Ceased
- 2017-12-14 EP EP17837949.1A patent/EP3558388A1/de active Pending
- 2017-12-14 MX MX2019007641A patent/MX2019007641A/es unknown
- 2017-12-14 JP JP2019533395A patent/JP7066714B2/ja active Active
- 2017-12-14 IL IL291308A patent/IL291308B2/en unknown
- 2017-12-14 KR KR1020197020706A patent/KR102556826B1/ko active Active
- 2017-12-14 KR KR1020237018668A patent/KR102583006B1/ko active Active
- 2017-12-14 CN CN201780087040.6A patent/CN110312534B/zh active Active
- 2017-12-14 US US16/472,749 patent/US11660351B2/en active Active
- 2017-12-14 CN CN202310307417.1A patent/CN116327974A/zh active Pending
- 2017-12-14 PE PE2019001293A patent/PE20191235A1/es unknown
- 2017-12-14 RU RU2019122802A patent/RU2761390C2/ru active
- 2017-12-14 AU AU2017380871A patent/AU2017380871C1/en active Active
- 2017-12-14 KR KR1020237018663A patent/KR102628678B1/ko active Active
- 2017-12-14 CA CA3047489A patent/CA3047489A1/en active Pending
- 2017-12-19 TW TW106144529A patent/TWI781125B/zh active
- 2017-12-19 TW TW111134796A patent/TWI823564B/zh active
- 2017-12-21 AR ARP170103619A patent/AR110418A1/es unknown
-
2019
- 2019-06-18 IL IL267473A patent/IL267473B/en unknown
- 2019-06-21 MX MX2024008464A patent/MX2024008464A/es unknown
- 2019-06-21 MX MX2023009205A patent/MX2023009205A/es unknown
-
2021
- 2021-09-01 US US17/464,565 patent/US11478554B2/en active Active
-
2022
- 2022-04-26 JP JP2022072343A patent/JP7307231B2/ja active Active
-
2023
- 2023-03-10 US US18/182,093 patent/US20230338559A1/en active Pending
-
2024
- 2024-01-31 IL IL310558A patent/IL310558B2/en unknown
- 2024-09-27 AU AU2024220179A patent/AU2024220179A1/en active Pending
- 2024-09-27 AU AU2024220178A patent/AU2024220178A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110312534B (zh) | 具有酶促可裂解基团的抗体-药物-缀合物(adc) | |
| CN110312533B (zh) | 具有酶促可裂解的基团的细胞毒性活性剂的前药 | |
| CN112601553A (zh) | 具有可酶切的接头和改善的活性谱的针对cxcr5的结合剂-药物缀合物 | |
| CN110072556A (zh) | 具有ksp抑制剂的特异性抗体药物缀合物(adc) | |
| HK40096469A (zh) | 具有酶促可裂解基团的抗体-药物-缀合物(adc) | |
| HK40016986B (zh) | 具有酶促可裂解基团的抗体-药物-缀合物(adc) | |
| HK40016986A (zh) | 具有酶促可裂解基团的抗体-药物-缀合物(adc) | |
| BR112019012883B1 (pt) | Conjugados de anticorpo-fármaco, uso dos mesmos e composição farmacêutica |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 40096469 Country of ref document: HK |