JP2022543106A - Hdac6インヒビターおよびそれらの使用 - Google Patents
Hdac6インヒビターおよびそれらの使用 Download PDFInfo
- Publication number
- JP2022543106A JP2022543106A JP2022506695A JP2022506695A JP2022543106A JP 2022543106 A JP2022543106 A JP 2022543106A JP 2022506695 A JP2022506695 A JP 2022506695A JP 2022506695 A JP2022506695 A JP 2022506695A JP 2022543106 A JP2022543106 A JP 2022543106A
- Authority
- JP
- Japan
- Prior art keywords
- substituted
- unsubstituted
- compound
- pharmaceutically acceptable
- hydrogen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D205/00—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom
- C07D205/12—Heterocyclic compounds containing four-membered rings with one nitrogen atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D217/00—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems
- C07D217/02—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems with only hydrogen atoms or radicals containing only carbon and hydrogen atoms, directly attached to carbon atoms of the nitrogen-containing ring; Alkylene-bis-isoquinolines
- C07D217/04—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems with only hydrogen atoms or radicals containing only carbon and hydrogen atoms, directly attached to carbon atoms of the nitrogen-containing ring; Alkylene-bis-isoquinolines with hydrocarbon or substituted hydrocarbon radicals attached to the ring nitrogen atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/06—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with radicals, containing only hydrogen and carbon atoms, attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/08—Indoles; Hydrogenated indoles with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/54—Spiro-condensed
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/96—Spiro-condensed ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/20—Spiro-condensed ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/22—Bridged ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D237/00—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings
- C07D237/26—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings condensed with carbocyclic rings or ring systems
- C07D237/30—Phthalazines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D267/00—Heterocyclic compounds containing rings of more than six members having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D267/02—Seven-membered rings
- C07D267/08—Seven-membered rings having the hetero atoms in positions 1 and 4
- C07D267/10—Seven-membered rings having the hetero atoms in positions 1 and 4 not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/04—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms
- C07D295/14—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D295/145—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals with the ring nitrogen atoms and the carbon atoms with three bonds to hetero atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings
- C07D295/15—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals with the ring nitrogen atoms and the carbon atoms with three bonds to hetero atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings to an acyclic saturated chain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
- C07D451/04—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof with hetero atoms directly attached in position 3 of the 8-azabicyclo [3.2.1] octane or in position 7 of the 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring system
- C07D451/06—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/107—Spiro-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D498/18—Bridged systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
関連出願
本出願は、35 U.S.C.§119(e)の下、2019年7月30日に出願された米国仮出願第(U.S.S.N.)62/880,284号(この全内容は、参照により本明細書に組み込まれる)に対し優先権を主張するものである。
本出願は、35 U.S.C.§119(e)の下、2019年7月30日に出願された米国仮出願第(U.S.S.N.)62/880,284号(この全内容は、参照により本明細書に組み込まれる)に対し優先権を主張するものである。
背景
ヒストンデアセチラーゼ(HDAC)は、配列相同性に基づき4クラスに分けられる。クラスII HDACのHDAC6は、細胞質の微小管関連(microtubule-associated)酵素である。HDAC6は、HDACパラログのなかでもユニークな特色を有する。HDAC6は、他のHDACとは違って、2つのデアセチラーゼドメインと、タンパク質のアセチル化とユビキチン化との夫々を伴う別個の細胞シグナリング系においてHDAC6に機能できるようにさせるユビキチン結合ドメインとを含有する。重要なことには、これはヒストンを脱アセチル化しない。HDAC6は、チューブリン、タウ、Hsp90、コルタクチン、および新たに出現した(emerging)他の標的を脱アセチル化する。HDAC6デアセチラーゼの機能は、微小管をベースとしたカーゴ輸送(transport)、タンパク質分解/再生(recycling)、およびストレス誘導性のグルココルチコイド受容体シグナリングに関与する。HDAC6デアセチラーゼの機能はまた、細胞形態学、運動性および遊走、ならびに細胞の成長および生存にも関与する。デアセチラーゼ機能に加えて、HDAC6は、ユビキチン依存性の機能と連関したパートナータンパク質と複合体を形成して、アグリソーム経路を介するタンパク質の凝集(aggregation)、輸送(trafficking)、および分解に影響を及ぼす。HDAC6の発現は、アルツハイマー病の患者からの死後脳試料において上昇していたことが示された。HDAC6の異常な発現はまた、腫瘍発生とも相関し、かつがん細胞の転移とも連関する。
ヒストンデアセチラーゼ(HDAC)は、配列相同性に基づき4クラスに分けられる。クラスII HDACのHDAC6は、細胞質の微小管関連(microtubule-associated)酵素である。HDAC6は、HDACパラログのなかでもユニークな特色を有する。HDAC6は、他のHDACとは違って、2つのデアセチラーゼドメインと、タンパク質のアセチル化とユビキチン化との夫々を伴う別個の細胞シグナリング系においてHDAC6に機能できるようにさせるユビキチン結合ドメインとを含有する。重要なことには、これはヒストンを脱アセチル化しない。HDAC6は、チューブリン、タウ、Hsp90、コルタクチン、および新たに出現した(emerging)他の標的を脱アセチル化する。HDAC6デアセチラーゼの機能は、微小管をベースとしたカーゴ輸送(transport)、タンパク質分解/再生(recycling)、およびストレス誘導性のグルココルチコイド受容体シグナリングに関与する。HDAC6デアセチラーゼの機能はまた、細胞形態学、運動性および遊走、ならびに細胞の成長および生存にも関与する。デアセチラーゼ機能に加えて、HDAC6は、ユビキチン依存性の機能と連関したパートナータンパク質と複合体を形成して、アグリソーム経路を介するタンパク質の凝集(aggregation)、輸送(trafficking)、および分解に影響を及ぼす。HDAC6の発現は、アルツハイマー病の患者からの死後脳試料において上昇していたことが示された。HDAC6の異常な発現はまた、腫瘍発生とも相関し、かつがん細胞の転移とも連関する。
概要
HDAC6の細胞質内の場所、別個の基質、および構造は、HDACパラログのなかでもユニークであり、HDAC6選択的処置計画は、第1世代の汎HDACインヒビターの副作用の多くを回避する見込みがある。しかしながら、パラログ選択性を得ることは困難である。本開示は、HDACパラログのなかでもHDAC6のユニークな構造および機能は選択的HDAC6インヒビターを設計する好機を提供するという認識に端を発する。本開示はまた、HDAC6媒介経路を標的にすることが神経学的障害への改善された処置を提供し得ることも認識している。神経変性に関し、HDAC6は、(1)チューブリンを脱アセチル化することによる微小管機能を損なっており、これによって軸索輸送およびミトコンドリア輸送における欠陥へ繋がる;(2)タウを脱アセチル化することによるタウ凝集を促進し、これによって病的なタウリン酸化および神経原線維のもつれの形成へ繋がる;ならびに(3)HSP90を脱アセチル化することによるHSP90のクライアント(client)タンパク質(誤って折り畳まれた(misfolded)タウを包含する)の分解を防止し、これによってタンパク質の再折り畳み/再生に関連するシャペロン複合体が安定化される。よって、本開示は、脳透過性の選択的HDAC6インヒビターを提供する。これらの化合物は、HDAC6活性(例として、アルツハイマー病および他のタウオパチーなどの神経学的障害、筋萎縮性側索硬化症、ならびにがん)に関連する疾患の処置のための新しい組成物および方法を提供する。
HDAC6の細胞質内の場所、別個の基質、および構造は、HDACパラログのなかでもユニークであり、HDAC6選択的処置計画は、第1世代の汎HDACインヒビターの副作用の多くを回避する見込みがある。しかしながら、パラログ選択性を得ることは困難である。本開示は、HDACパラログのなかでもHDAC6のユニークな構造および機能は選択的HDAC6インヒビターを設計する好機を提供するという認識に端を発する。本開示はまた、HDAC6媒介経路を標的にすることが神経学的障害への改善された処置を提供し得ることも認識している。神経変性に関し、HDAC6は、(1)チューブリンを脱アセチル化することによる微小管機能を損なっており、これによって軸索輸送およびミトコンドリア輸送における欠陥へ繋がる;(2)タウを脱アセチル化することによるタウ凝集を促進し、これによって病的なタウリン酸化および神経原線維のもつれの形成へ繋がる;ならびに(3)HSP90を脱アセチル化することによるHSP90のクライアント(client)タンパク質(誤って折り畳まれた(misfolded)タウを包含する)の分解を防止し、これによってタンパク質の再折り畳み/再生に関連するシャペロン複合体が安定化される。よって、本開示は、脳透過性の選択的HDAC6インヒビターを提供する。これらの化合物は、HDAC6活性(例として、アルツハイマー病および他のタウオパチーなどの神経学的障害、筋萎縮性側索硬化症、ならびにがん)に関連する疾患の処置のための新しい組成物および方法を提供する。
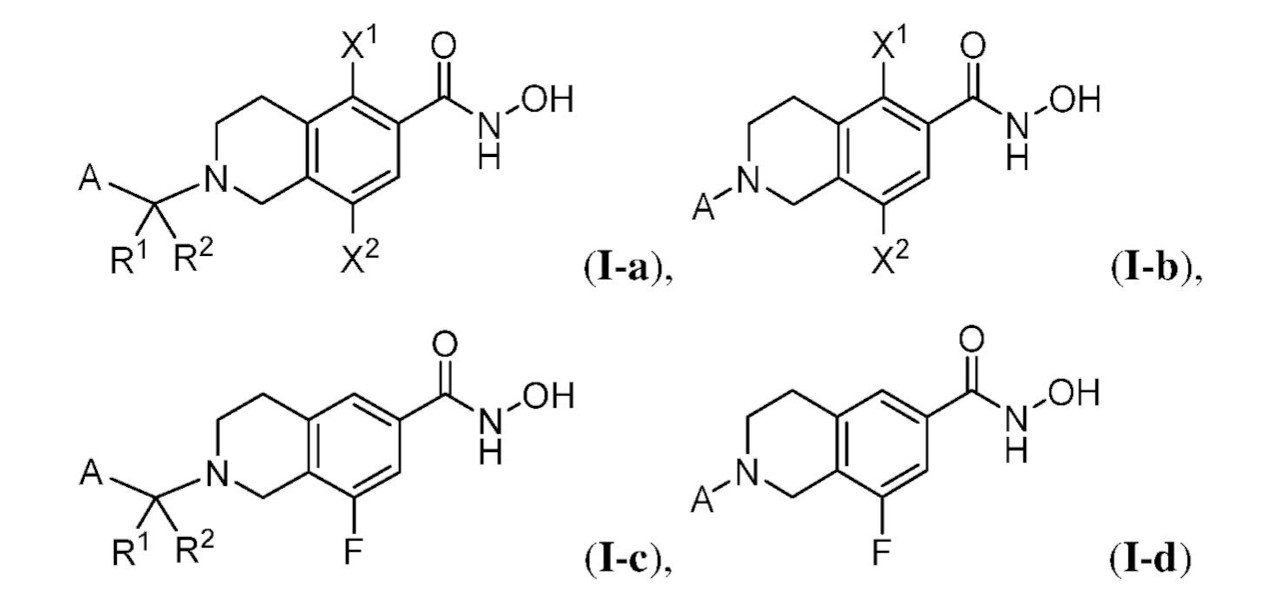
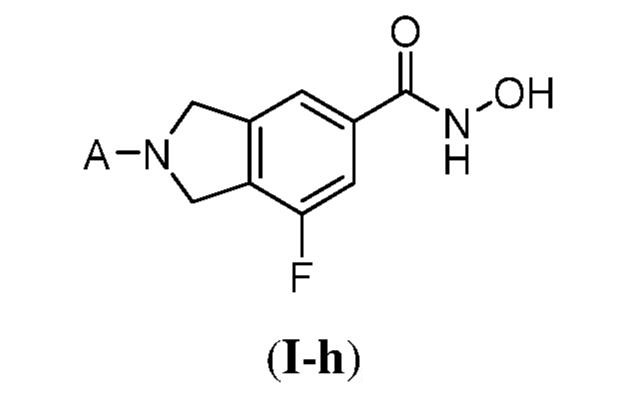
一側面において、提供されるのは、式(I):
で表される化合物、およびそれらの薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである;
Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;
mは、0または1である;および
nは、0または1である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである;
Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;
mは、0または1である;および
nは、0または1である。
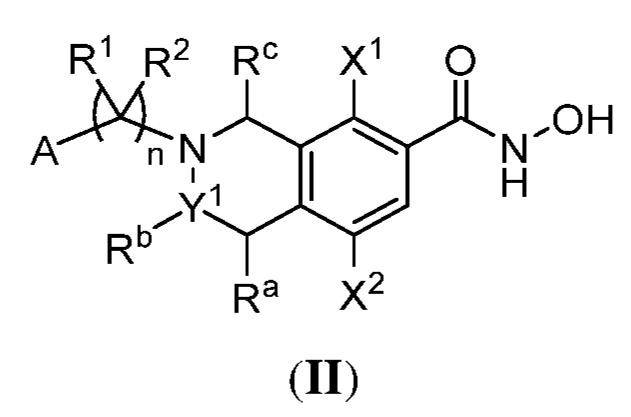
別の側面において、提供されるのは、式(II):
で表される化合物、またはその薬学的に許容し得る塩であるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
各R1は、独立して、水素、または置換もしくは非置換のアルキルである;
各R2は、独立して、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;および
各nは、独立して、0または1である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
各R1は、独立して、水素、または置換もしくは非置換のアルキルである;
各R2は、独立して、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;および
各nは、独立して、0または1である。
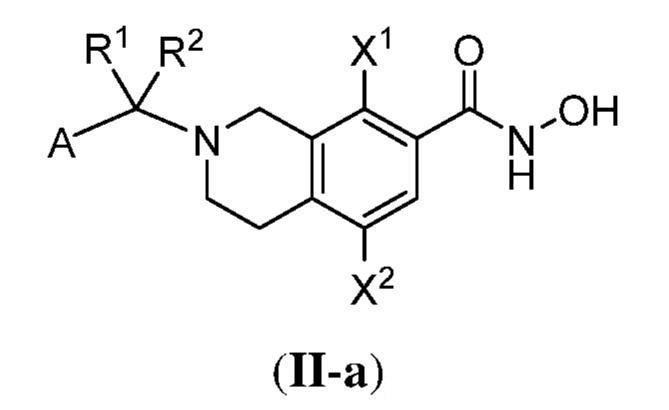
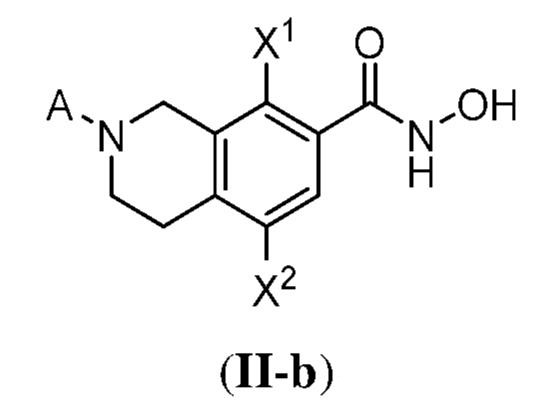
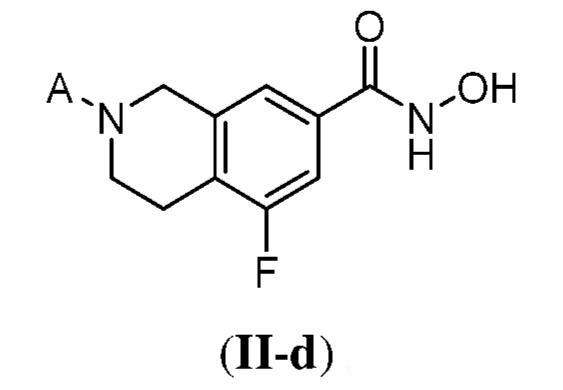
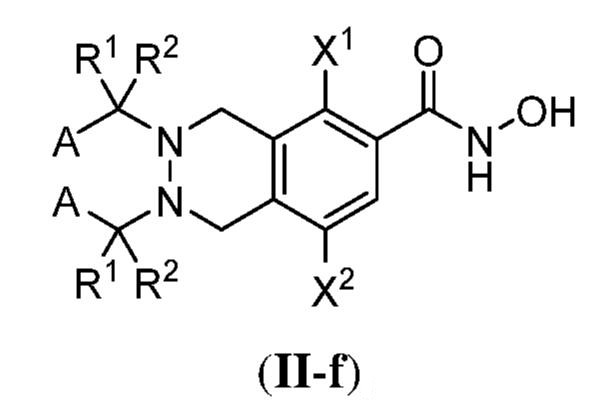
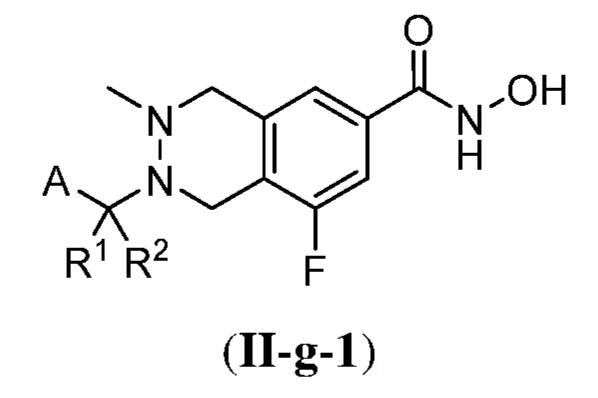
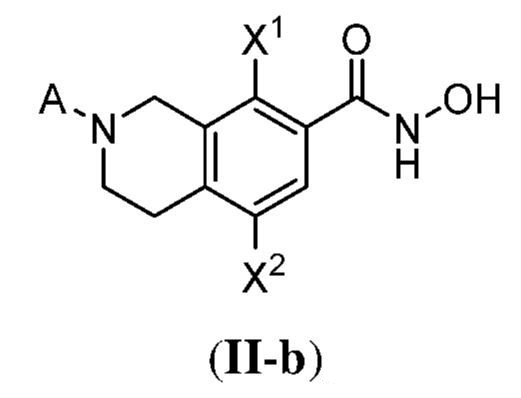
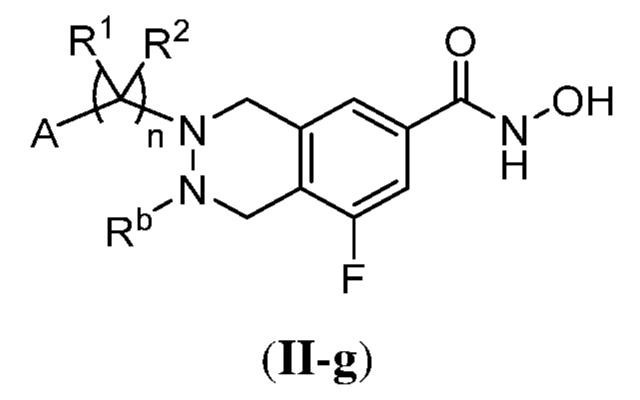
ある態様において、式(II)で表される化合物は、式(II-a)、(II-b)、(II-c)、(II-d)、(II-e)、(II-f)、(II-g)、もしくは(II-h):
で表される化合物、またはそれらの薬学的に許容し得る塩である。
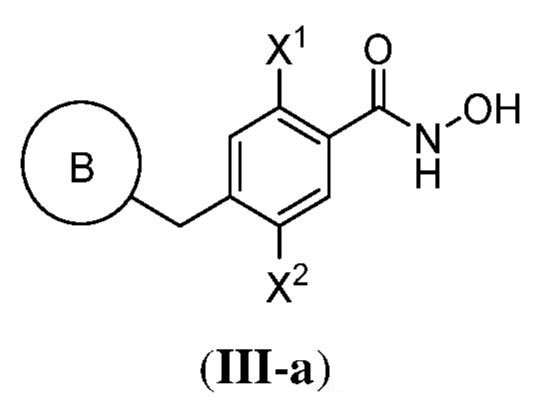
別の側面において、提供されるのは、式(III):
で表される化合物、およびそれらの薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
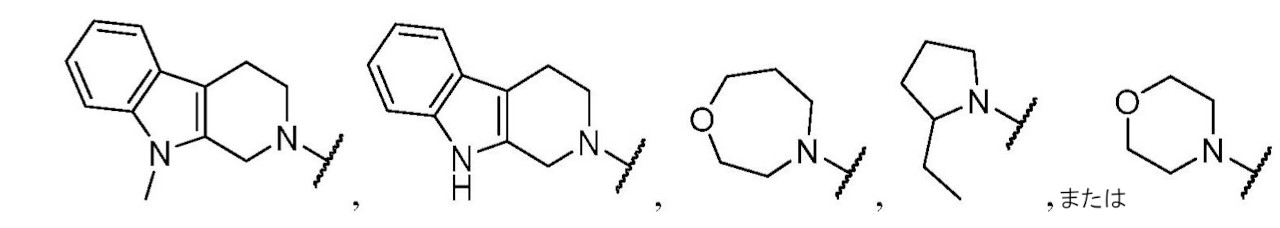
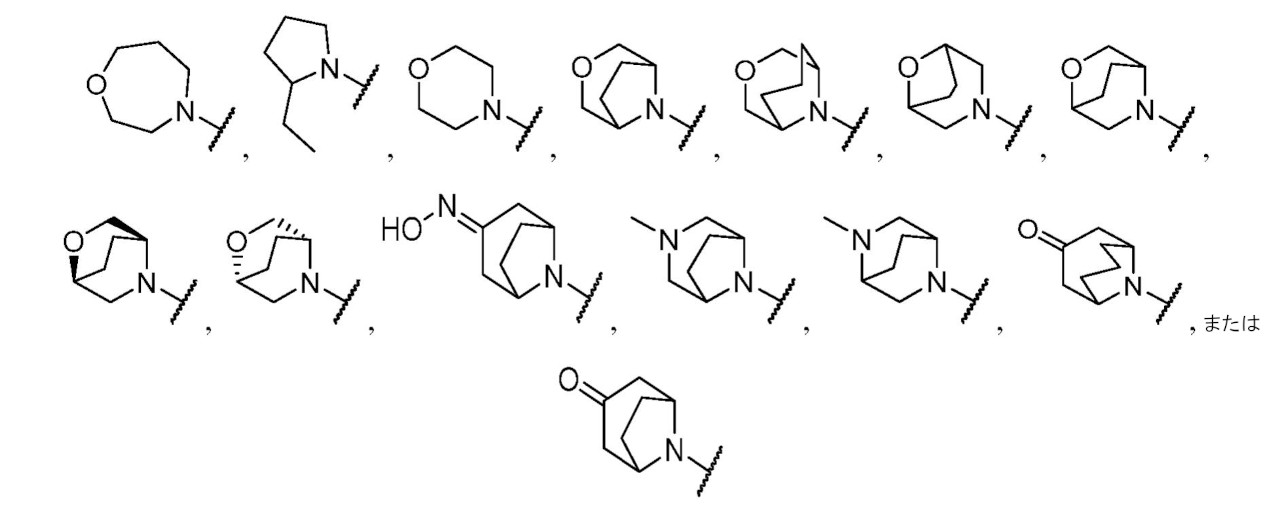
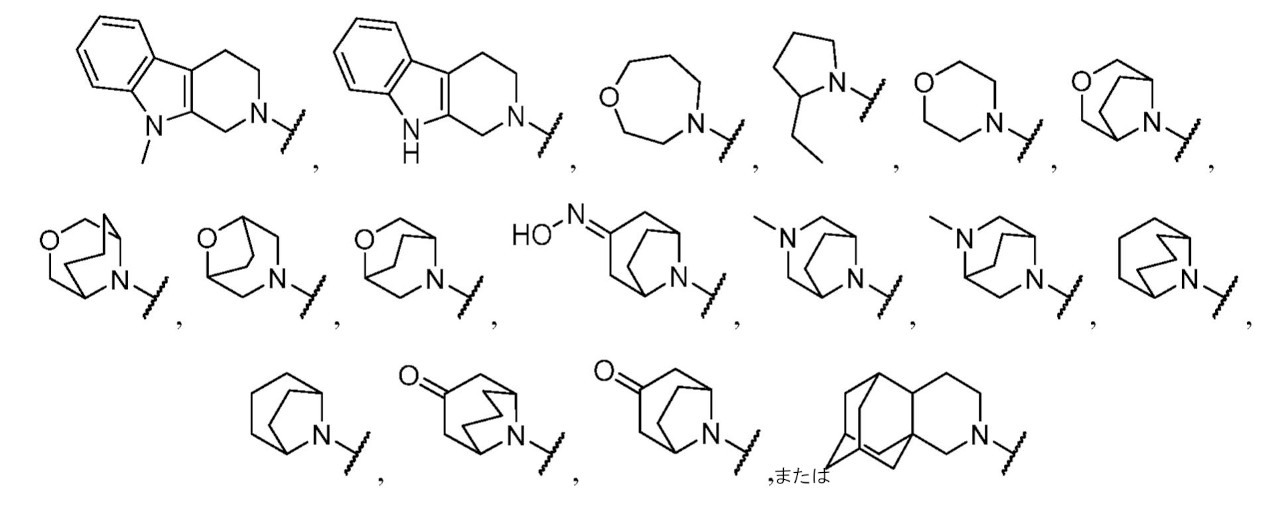
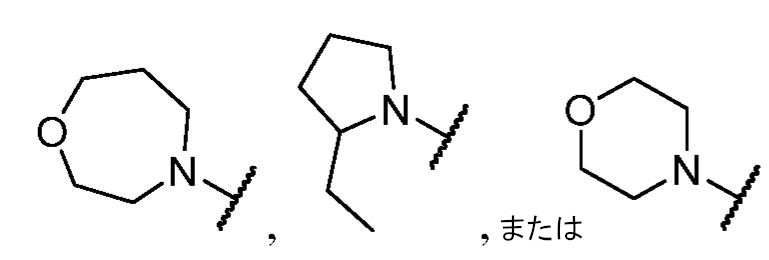
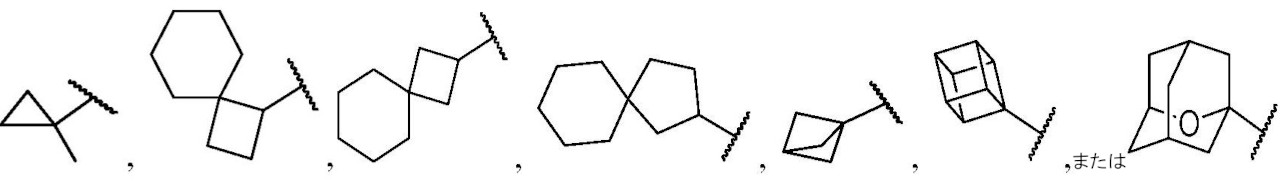
Bは、置換もしくは非置換の多環式のスピロ環系、置換もしくは非置換の架橋環系、
である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換の多環式のスピロ環系、置換もしくは非置換の架橋環系、
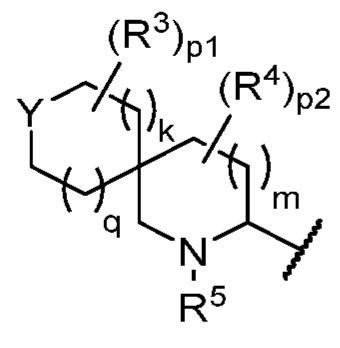
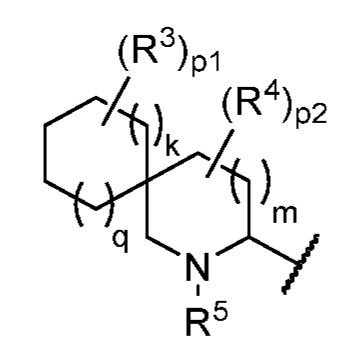
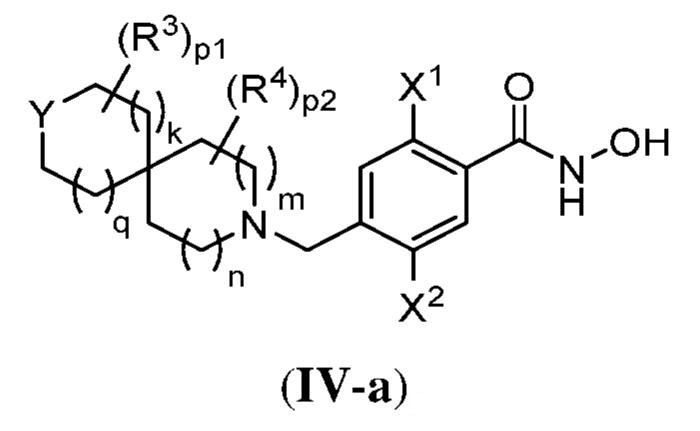
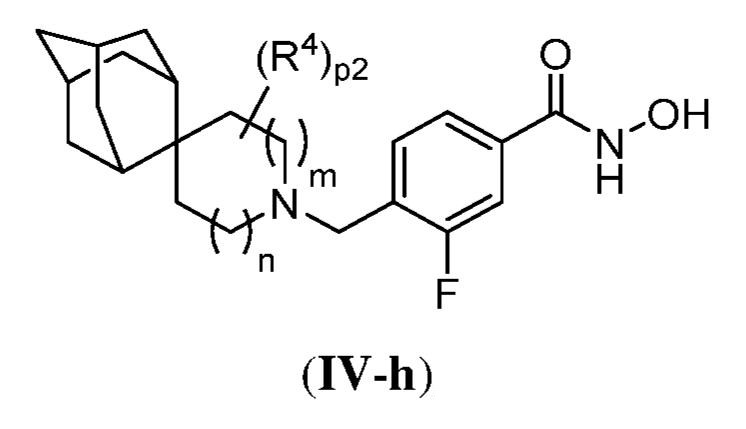
ある態様において、式(III)で表される化合物は、式(IV):
で表される化合物、およびそれらの薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
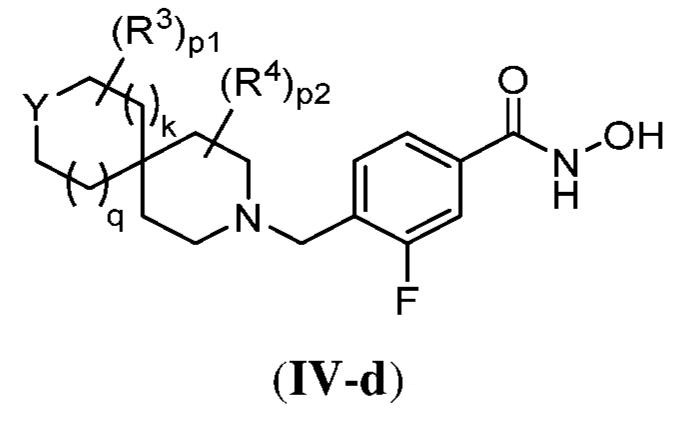
ある態様において、式(IV)で表される化合物は、式(IV-a)、(IV-b)、(IV-c)、(IV-d)、(IV-e)、(IV-f)、(IV-g)、もしくは(IV-h):
で表される化合物、またはそれらの薬学的に許容し得る塩である。
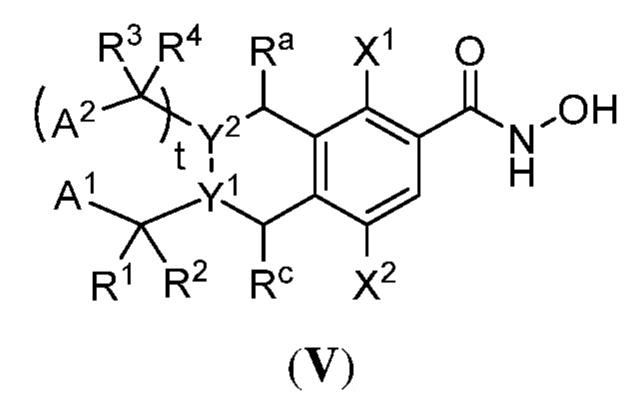
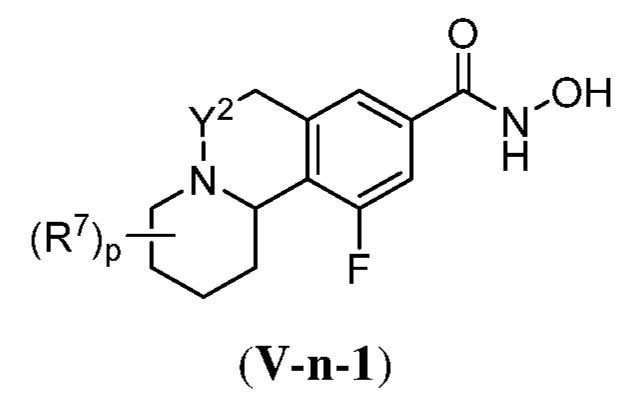
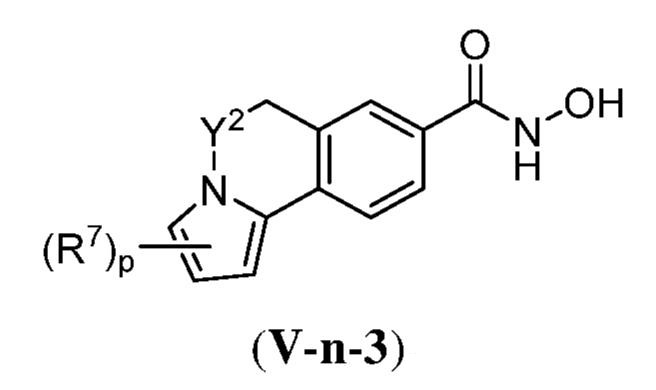
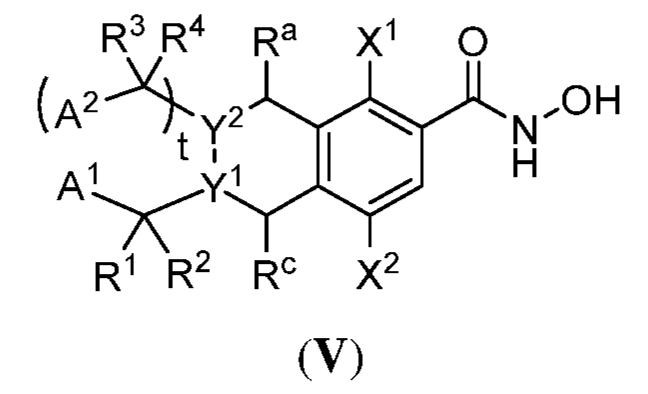
別の側面において、提供されるのは、式(V):
で表される化合物、およびそれらの薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、独立して、窒素またはCRxである;
Y2は、独立して、窒素、CRd、結合、-CH2-、または-NH-である;
A1は、A2、Ra、またはRcのうち1個と結び合わされることで、置換または非置換の環を形成している;
A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;
R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;あるいはR1およびR2は一緒に、カルボニルを形成している;
R3は、水素、または置換もしくは非置換のアルキルであるか、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;
R4は、水素、または置換もしくは非置換のアルキルであるか、あるいはR4は、R1またはR2と結び合わされることで、置換または非置換の環を形成している;あるいはR3およびR4は一緒に、カルボニルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している;および
tは、0または1である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、独立して、窒素またはCRxである;
Y2は、独立して、窒素、CRd、結合、-CH2-、または-NH-である;
A1は、A2、Ra、またはRcのうち1個と結び合わされることで、置換または非置換の環を形成している;
A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;
R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;あるいはR1およびR2は一緒に、カルボニルを形成している;
R3は、水素、または置換もしくは非置換のアルキルであるか、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;
R4は、水素、または置換もしくは非置換のアルキルであるか、あるいはR4は、R1またはR2と結び合わされることで、置換または非置換の環を形成している;あるいはR3およびR4は一緒に、カルボニルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している;および
tは、0または1である。
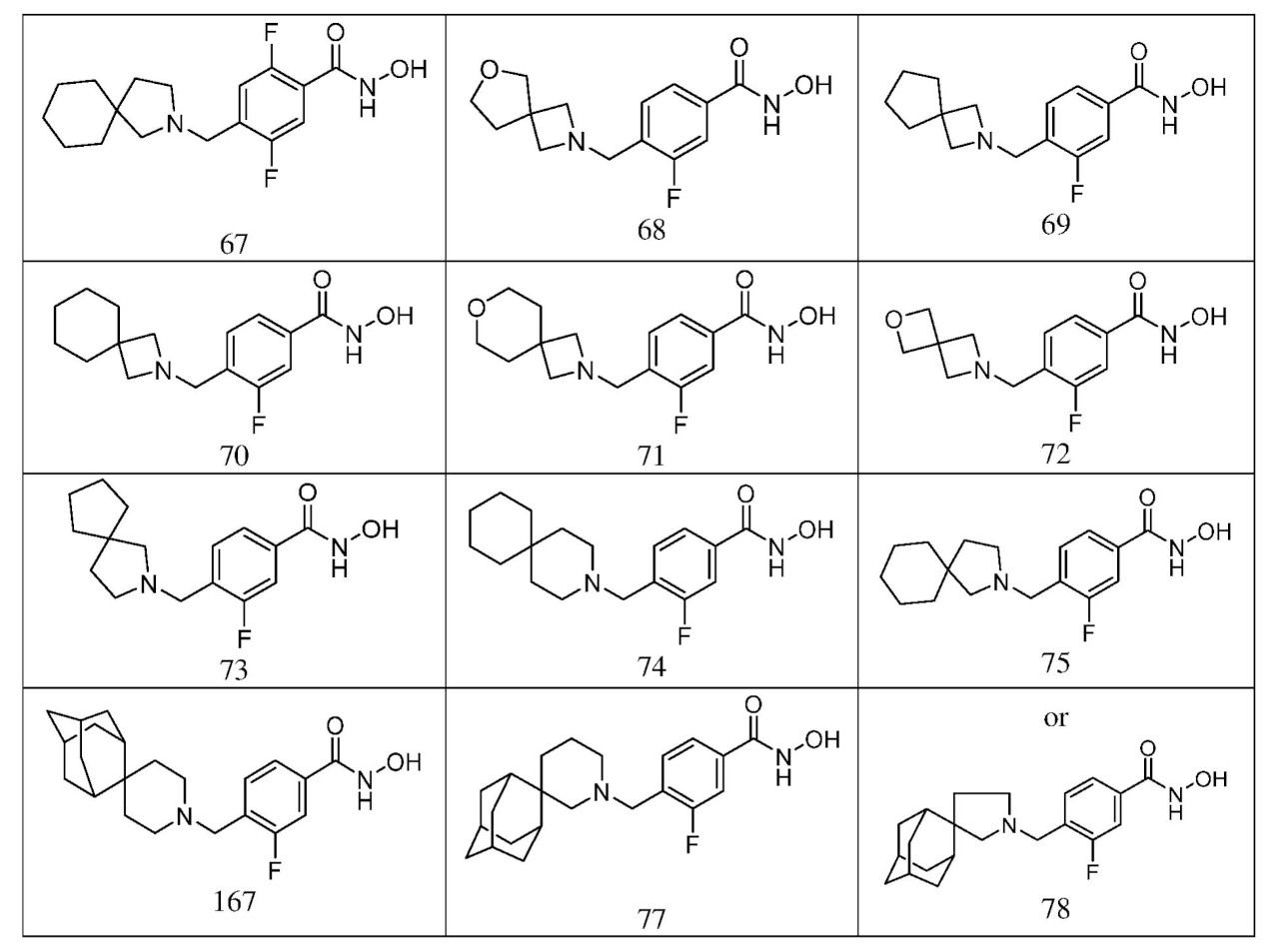
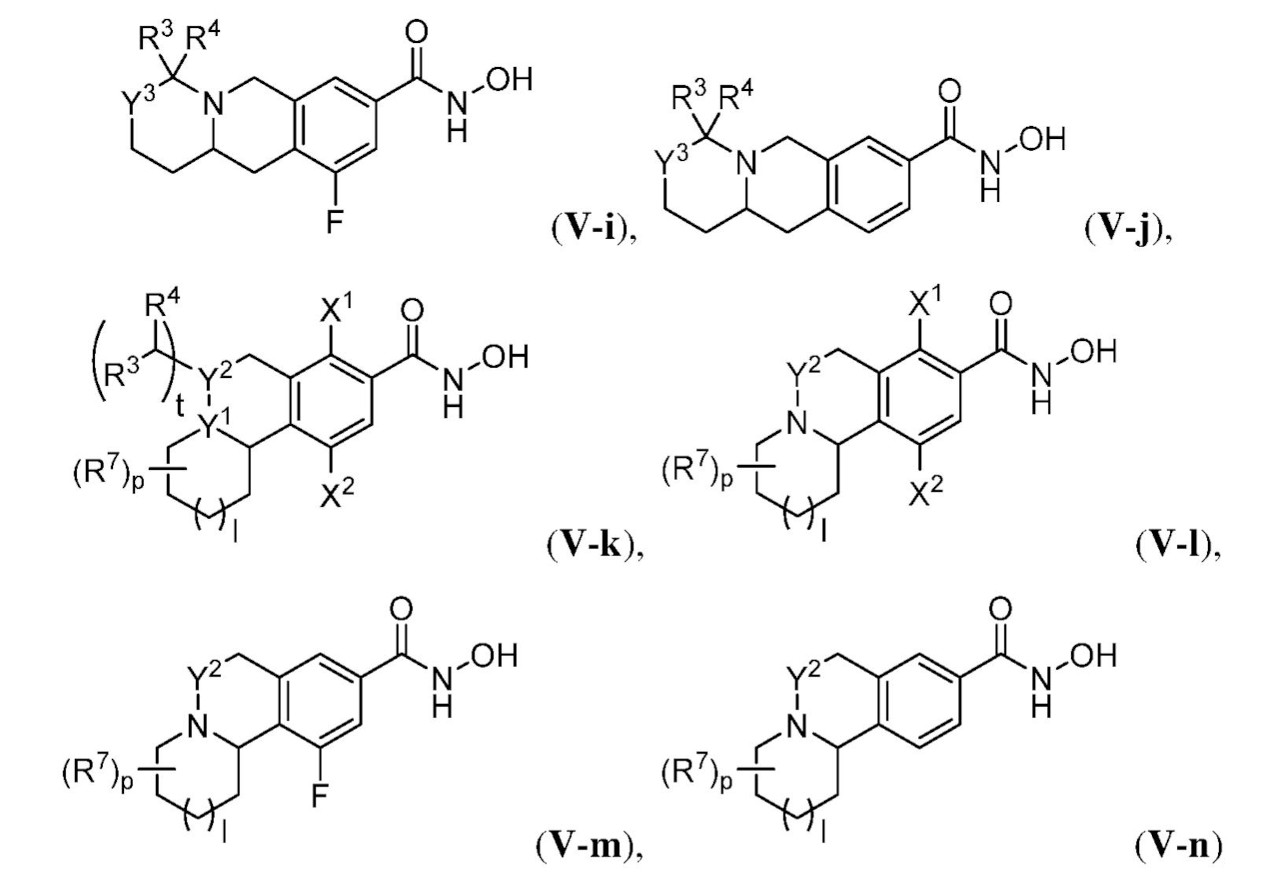
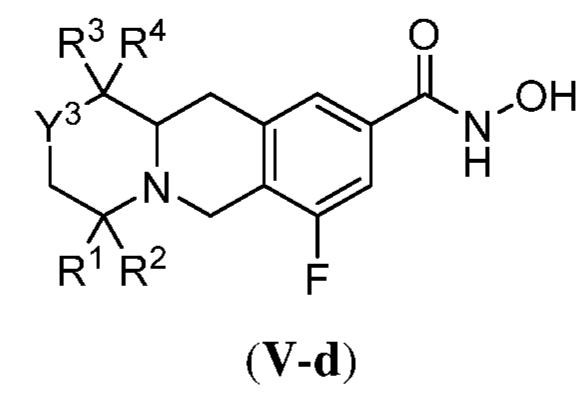
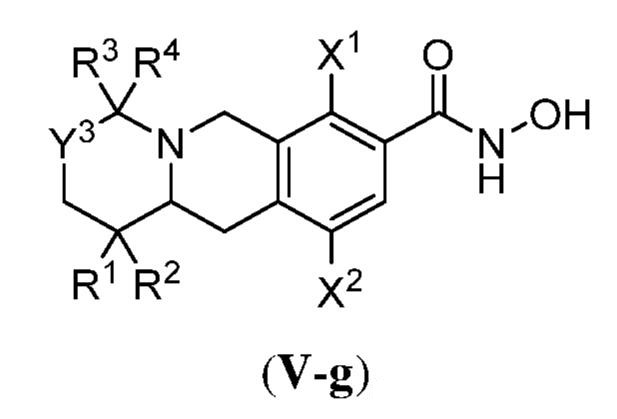
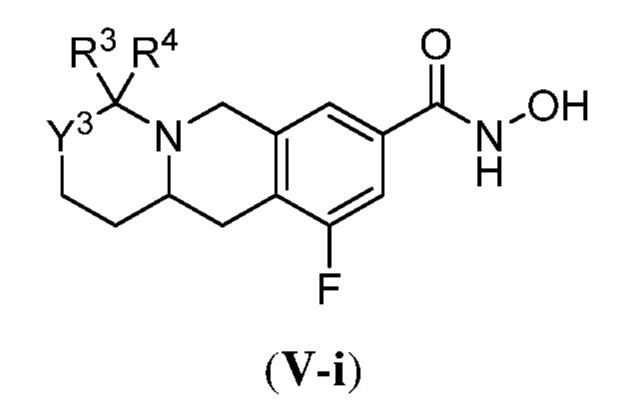
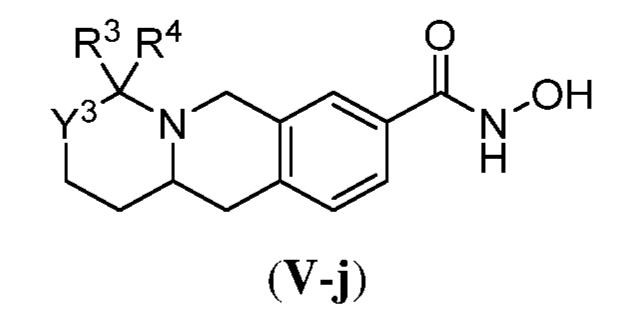
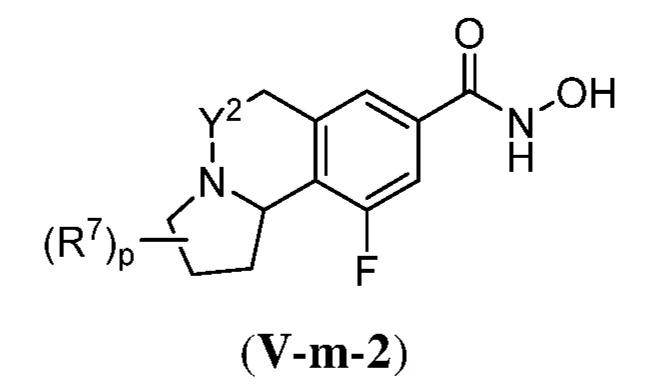
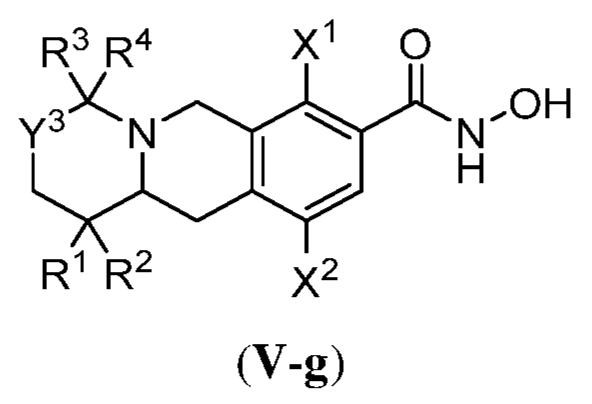
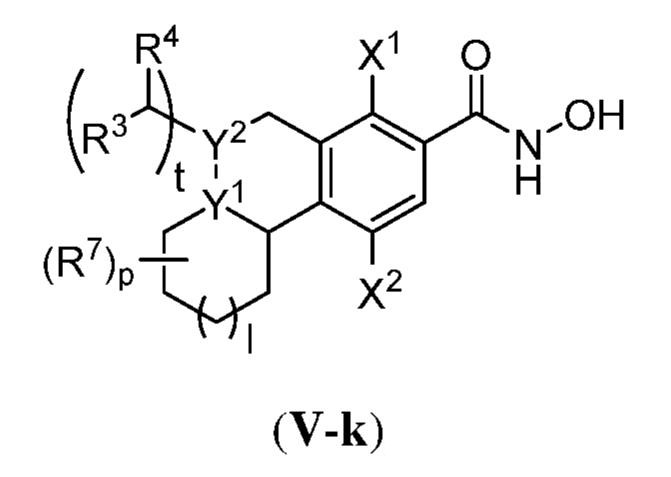
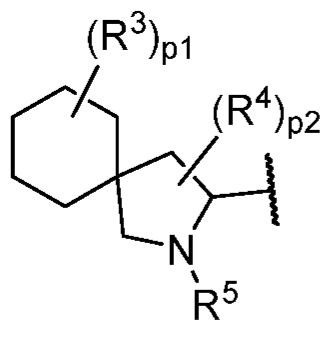
ある態様において、式(V)で表される化合物は、式(V-a)、(V-b)、(V-c)、(V-d)、(V-e)、(V-f)、(V-g)、(V-h)、(V-i)、(V-j)、(V-k)、(V-l)、(V-m)、もしくは(V-n):
で表される化合物、またはそれらの薬学的に許容し得る塩である。
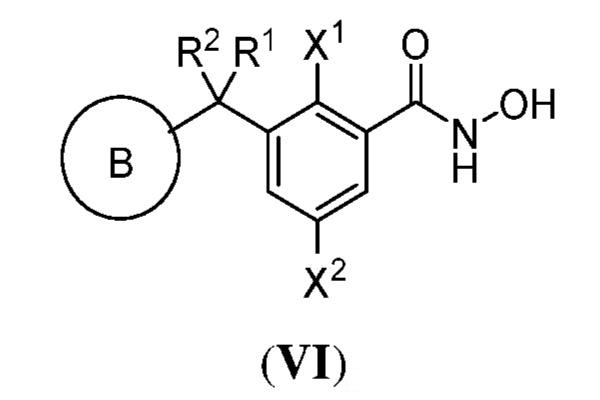
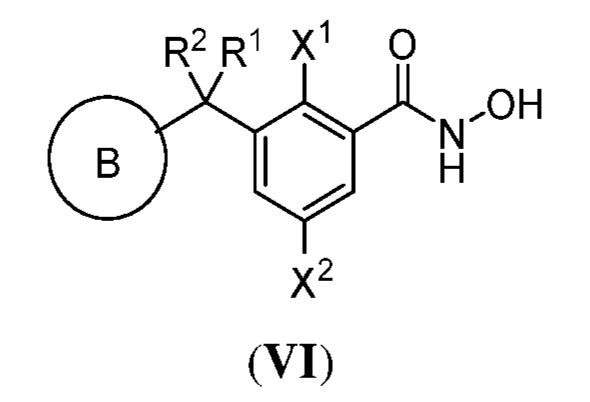
別の側面において、提供されるのは、式(VI):
で表される化合物、およびそれらの薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
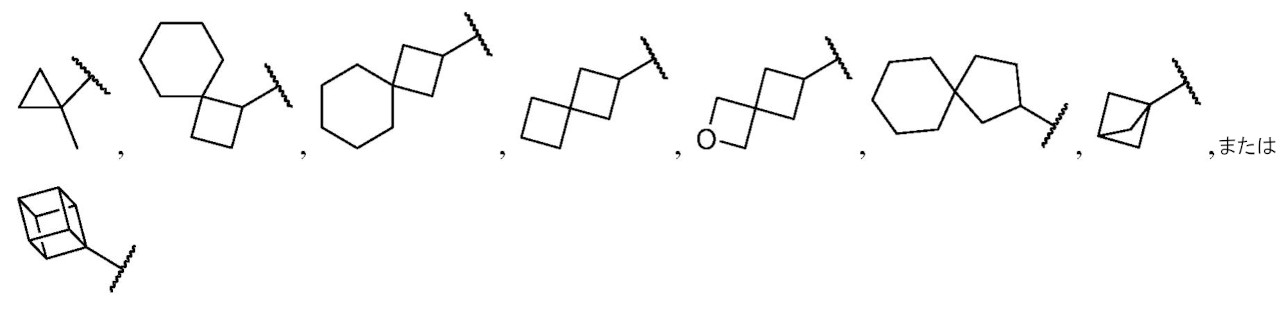
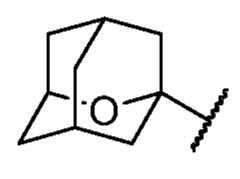
Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
別の側面において、提供されるのは、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩と、任意に、薬学的に許容し得る賦形剤とを含む、医薬組成物である。
別の側面において、提供されるのは、疾患または障害の処置を、これを必要とする対象においてする方法であるが、ここで疾患または障害は、これを必要とする対象における増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害(neurological disorder)、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害であり、方法は、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩、あるいは式(I)、(II)、(III)、(IV)、(V)、または(VI)で表される化合物を含む医薬組成物を対象へ投与することを含む。
ある態様において、本明細書に記載の化合物または組成物を使用して処置される疾患または障害は、増殖性疾患である。ある態様において、増殖性疾患は、がんである。ある態様において、がんは、血液がんである。ある態様において、がんは、白血病、T細胞リンパ腫、ホジキン病、非ホジキンリンパ腫、または多発性骨髄腫である。ある態様において、がんは、固形腫瘍を含む。ある態様において、がんは、マントル細胞リンパ腫である。ある態様において、がんは、神経膠腫、膠芽腫、非小細胞肺がん、脳腫瘍、神経芽細胞腫、骨腫瘍、軟部組織肉腫、頭頸部がん、尿生殖器がん、肺がん、乳房がん(breast cancer)、膵臓がん、黒色腫、胃がん、脳がん、肝臓がん、甲状腺がん、明細胞癌、子宮がん、または卵巣がんである。
ある態様において、本明細書に記載の化合物または組成物を使用して処置される疾患または障害は、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患(neuropathy disease)である。ある態様において、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患は、脆弱X症候群、シャルコー・マリー・トゥース病、アルツハイマー病、パーキンソン病、ハンチントン病、多発性硬化症、筋萎縮性側索硬化症、クロイツフェルト・ヤコブ病、レビー小体型認知症、血管性認知症、筋萎縮、発作(seizure)誘発性の記憶喪失、統合失調症、ルビンシュタイン・テイビ症候群、レット症候群、注意欠陥多動性障害、失読症、双極性障害、自閉症に関連する社会障害、認知障害、および学習障害、注意欠陥障害、統合失調症、大うつ病性障害、末梢神経障害、糖尿病網膜症、糖尿病性末梢神経障害、化学療法誘発性の末梢神経障害、外傷性脳損傷(TBI)、慢性外傷性脳症(CTE)、またはタウオパチーである。ある態様において、タウオパチーは、原発性年齢関連タウオパチー(PART)/神経原線維優位型老年認知症、慢性外傷性脳症、ボクサー認知症、進行性の核上性麻痺、大脳皮質基底核変性症、ピック病、17番染色体と連関した前頭側頭型認知症およびパーキンソニズム、リティコ・ボディグ(Lytico-Bodig)病、神経節膠腫、神経節細胞腫、髄膜血管腫症、脳炎後パーキンソニズム、亜急性硬化性全脳炎、鉛脳症、結節性硬化症、リポフスチン症、アルツハイマー病、または嗜銀性顆粒病である。
別の側面において、提供されるのは、HDAC6の活性を阻害する方法であって、方法は、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩をHDAC6と接触させることを含む。ある態様において、HDAC6は、細胞(例として、ヒト細胞)中にある。
別の側面において、提供されるのは、増殖性疾患、炎症性疾患、感染性疾患《感染症》、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害の処置を、これを必要とする対象においてするのに使用するための、式(I)、(II)、(III)、(IV)、(V)、または(VI)で表される化合物、およびそれらの薬学的に許容し得る塩、ならびに式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩を含む医薬組成物である。
別の側面において、提供されるのは、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩、あるいは式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩を含む医薬組成物を含むキットである。ある態様において、キットは、投与(例として、ヒト投与)への指示をさらに含む。
本発明のある態様の詳細は、下に記載されるとおり、ある態様の詳細な記載で表される。本発明の他の特色、目的、および利点は、定義、例、およびクレームから明らかであろう。
定義
化学的な定義
特定の官能基および化学用語の定義は、より詳細に下に記載される。化学元素は、Handbook of Chemistry and Physics, 75th Ed.内表紙の元素周期表CAS版に従って同定され、特定の官能基はそこに記載のとおり、一般に定義される。加えて、有機化学の一般法則、ならびに特定の官能部分および反応性は、Organic Chemistry,Thomas Sorrell,University Science Books,Sausalito,1999;Smith and March,March's Advanced Organic Chemistry,5th Edition,John Wiley & Sons,Inc.,New York,2001;Larock,Comprehensive Organic Transformations,VCH Publishers,Inc.,New York,1989;およびCarruthers,Some Modern Methods of Organic Synthesis,3rd Edition,Cambridge University Press,Cambridge,1987に記載されている。
化学的な定義
特定の官能基および化学用語の定義は、より詳細に下に記載される。化学元素は、Handbook of Chemistry and Physics, 75th Ed.内表紙の元素周期表CAS版に従って同定され、特定の官能基はそこに記載のとおり、一般に定義される。加えて、有機化学の一般法則、ならびに特定の官能部分および反応性は、Organic Chemistry,Thomas Sorrell,University Science Books,Sausalito,1999;Smith and March,March's Advanced Organic Chemistry,5th Edition,John Wiley & Sons,Inc.,New York,2001;Larock,Comprehensive Organic Transformations,VCH Publishers,Inc.,New York,1989;およびCarruthers,Some Modern Methods of Organic Synthesis,3rd Edition,Cambridge University Press,Cambridge,1987に記載されている。
本明細書に記載の化合物は、1以上の不斉中心を含み得、よって様々な立体異性体の形態、例として鏡像異性体および/またはジアステレオマーで存在し得る。例えば、本明細書に記載の化合物は、個々のエナンチオマー、ジアステレオマー、または幾何異性体の形態であり得るか、または立体異性体の混合物(ラセミ混合物、および1以上の立体異性体が富化された混合物を包含する)の形態であり得る。異性体は、当業者に知られている方法(キラル高圧液体クロマトグラフィー(HPLC)、およびキラル塩の形成および結晶化を包含する)によって混合物から単離され得る;または好ましい異性体は、不斉合成によって調製され得る。例えば、Jacques et al.,Enantiomers,Racemates and Resolutions(Wiley Interscience,New York,1981);Wilen et al.,Tetrahedron 33:2725(1977);Eliel,E.L.Stereochemistry of Carbon Compounds(McGraw-Hill,NY,1962);およびWilen,S.H.,Tables of Resolving Agents and Optical Resolutions p.268(E.L.Eliel,Ed.,Univ.of Notre Dame Press,Notre Dame,IN 1972)を参照。本発明は加えて、他の異性体が実質的にない個々の異性体としても、代わりに様々な異性体の混合物としても、本明細書に記載の化合物を網羅する。
別様に述べられない限り、ここに描かれる構造はまた、同位体が濃縮された1以上の原子の存在でしか相違しない化合物を包含することも意図する。例えば、水素の重水素もしくはトリチウムによる置き換え、19Fの18Fとの置き換え、または12Cの13Cもしくは14Cとの置き換えを除く本構造を有する化合物は、本開示の範囲内にある。かかる化合物は、例えば、生物学的アッセイにおける分析用のツールまたはプローブとして有用である。
値の範囲が列挙されるとき、その範囲内の各値および部分範囲も網羅することを意図する。例えば「C1~6アルキル」は、C1、C2、C3、C4、C5、C6、C1~6、C1~5、C1~4、C1~3、C1~2、C2~6、C2~5、C2~4、C2~3、C3~6、C3~5、C3~4、C4~6、C4~5、およびC5~6のアルキルを網羅することを意図する。
用語「脂肪族」は、アルキル基、アルケニル基、アルキニル基、および炭素環基を指す。同じく、用語「ヘテロ脂肪族」は、ヘテロアルキル基、ヘテロアルケニル基、ヘテロアルキニル基、および複素環式の基を指す。
用語「アルキル」は、1個から10個までの炭素原子を有する直鎖または分枝の飽和炭化水素基のラジカルを指す(「C1~10アルキル」)。いくつかの態様において、アルキル基は、1~9個の炭素原子を有する(「C1~9アルキル」)。いくつかの態様において、アルキル基は、1~8個の炭素原子を有する(「C1~8アルキル」)。いくつかの態様において、アルキル基は、1~7個の炭素原子を有する(「C1~7アルキル」)。いくつかの態様において、アルキル基は、1~6個の炭素原子を有する(「C1~6アルキル」)。いくつかの態様において、アルキル基は、1~5個の炭素原子を有する(「C1~5アルキル」)。いくつかの態様において、アルキル基は、1~4個の炭素原子を有する(「C1~4アルキル」)。いくつかの態様において、アルキル基は、1~3個の炭素原子を有する(「C1~3アルキル」)。いくつかの態様において、アルキル基は、1~2個の炭素原子を有する(「C1~2アルキル」)。いくつかの態様において、アルキル基は、1個の炭素原子を有する(「C1アルキル」)。いくつかの態様において、アルキル基は、2~6個の炭素原子を有する(「C2~6アルキル」)。C1~6アルキル基の例は、メチル(C1)、エチル(C2)、プロピル(C3)(例として、n-プロピル、イソプロピル)、ブチル(C4)(例として、n-ブチル、tert-ブチル、sec-ブチル、イソ-ブチル)、ペンチル(C5)(例として、n-ペンチル、3-ペンタニル、アミル、ネオペンチル、3-メチル-2-ブタニル、三級アミル)、およびヘキシル(C6)(例として、n-ヘキシル)を包含する。アルキル基の追加例は、n-へプチル(C7)、n-オクチル(C8),等を包含する。別様に特定されない限り、アルキル基の各場合は、独立して、非置換であるか(「非置換アルキル」)、または1以上の置換基(例として、Fなどのハロゲン)で置換されている(「置換アルキル」)。ある態様において、アルキル基は、非置換C1~10アルキル(非置換C1~6アルキル、例として、-CH3(Me)、非置換エチル(Et)、非置換プロピル(Pr、例として、非置換n-プロピル(n-Pr)、非置換イソプロピル(i-Pr))、非置換ブチル(Bu、例として、非置換n-ブチル(n-Bu)、非置換tert-ブチル(tert-Buまたはt-Bu)、非置換sec-ブチル(sec-Bu)、非置換イソブチル(i-Bu)など)である。ある態様において、アルキル基は、置換C1~10アルキル(置換C1~6アルキル、例として、-CF3、Bnなど)である。
用語「ハロアルキル」は、置換アルキル基、ここで水素原子の1個以上は、独立して、ハロゲン、例として、フルオロ、ブロモ、クロロ、またはヨードによって置き換えられている。いくつかの態様において、ハロアルキル部分は、1~8個の炭素原子を有する(「C1~8ハロアルキル」)。いくつかの態様において、ハロアルキル部分は、1~6個の炭素原子を有する(「C1~6ハロアルキル」)。いくつかの態様において、ハロアルキル部分は、1~4個の炭素原子を有する(「C1~4ハロアルキル」)。いくつかの態様において、ハロアルキル部分は、1~3個の炭素原子を有する(「C1~3ハロアルキル」)。いくつかの態様において、ハロアルキル部分は、1~2個の炭素原子を有する(「C1~2ハロアルキル」)。ハロアルキル基の例は、-CHF2、-CH2F、-CF3、-CH2CF3、-CF2CF3、-CF2CF2CF3、-CCl3、-CFCl2、-CF2Cl等を包含する。
用語「アルコキシ」は、親分子部分へ酸素原子を通して付け足された、本明細書に定義されるとおりのアルキル基を指す。いくつかの態様において、アルコキシ部分は、1~8個の炭素原子を有する(「C1~8アルコキシ」)。いくつかの態様において、アルコキシ部分は、1~6個の炭素原子を有する(「C1~6アルコキシ」)。いくつかの態様において、アルコキシ部分は、1~4個の炭素原子を有する(「C1~4アルコキシ」)。いくつかの態様において、アルコキシ部分は、1~3個の炭素原子を有する(「C1~3アルコキシ」)。いくつかの態様において、アルコキシ部分は、1~2個の炭素原子を有する(「C1~2アルコキシ」)。アルコキシの代表例は、これらに限定されないが、メトキシ、エトキシ、プロポキシ、2-プロポキシ、ブトキシ、およびtert-ブトキシを包含する。
用語「アルコキシアルキル」は、水素原子の1個以上が、独立して、本明細書に定義されるとおりのアルコキシ基によって置き換えられている、置換アルキル基である。いくつかの態様において、アルコキシアルキル部分は、1~8個の炭素原子を有する(「C1~8アルコキシアルキル」)。いくつかの態様において、アルコキシアルキル部分は、1~6個の炭素原子を有する(「C1~6アルコキシアルキル」)。いくつかの態様において、アルコキシアルキル部分は、1~4個の炭素原子を有する(「C1~4アルコキシアルキル」)。いくつかの態様において、アルコキシアルキル部分は、1~3個の炭素原子を有する(「C1~3アルコキシアルキル」)。いくつかの態様において、アルコキシアルキル部分は、1~2個の炭素原子を有する(「C1~2アルコキシアルキル」)。
用語「ヘテロアルキル」は、酸素、窒素、または硫黄から選択される少なくとも1個のヘテロ原子(例として、1個、2個、3個、もしくは4個のヘテロ原子)をさらに、親鎖内に(すなわち、親鎖の隣接する炭素原子間に挿入されて)および/または親鎖の1以上の末端位(単数もしくは複数)に置かれて包含するアルキル基を指す。ある態様において、ヘテロアルキル基は、1個から20個までの炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基を指す(「ヘテロC1~20アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~18個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~18アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~16個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~16アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~14個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~14アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~12個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~12アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~10個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~10アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~8個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~8アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~6個の炭素原子と1個以上のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~6アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~4個の炭素原子と1個または2個のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~4アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~3個の炭素原子と1個のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~3アルキル」)。いくつかの態様において、ヘテロアルキル基は、1~2個の炭素原子と1個のヘテロ原子とを親鎖内に有する飽和基である(「ヘテロC1~2アルキル」)。いくつかの態様において、ヘテロアルキル基は、1個の炭素原子と1個のヘテロ原子とを有する飽和基である(「ヘテロC1アルキル」)。いくつかの態様において、本明細書に定義されるヘテロアルキル基は、1個以上のヘテロ原子を親鎖内に有し、かつカルボニル基などの少なくとも1個の不飽和炭素を有する部分的に不飽和の基である。例えば、ヘテロアルキル基は、1個以上の炭素原子が不飽和カルボニル基であるように、アミドまたはエステルの機能性をその親鎖中に含んでいてもよい。別様に特定されない限り、ヘテロアルキル基の各場合は、独立して、非置換であるか(「非置換ヘテロアルキル」)、または1以上の置換基で置換されている(「置換ヘテロアルキル」)。ある態様において、ヘテロアルキル基は、非置換ヘテロC1~20アルキルである。ある態様において、ヘテロアルキル基は、非置換ヘテロC1~10アルキルである。ある態様において、ヘテロアルキル基は、置換ヘテロC1~20アルキルである。ある態様において、ヘテロアルキル基は、非置換ヘテロC1~10アルキルである。
用語「アルケニル」は、2個から10個までの炭素原子と1以上の炭素-炭素二重結合(例として、1個、2個、3個、もしくは4個の二重結合)とを有する、直鎖または分枝の炭化水素基のラジカルを指す。いくつかの態様において、アルケニル基は、2~9個の炭素原子を有する(「C2~9アルケニル」)。いくつかの態様において、アルケニル基は、2~8個の炭素原子を有する(「C2~8アルケニル」)。いくつかの態様において、アルケニル基は、2~7個の炭素原子を有する(「C2~7アルケニル」)。いくつかの態様において、アルケニル基は、2~6個の炭素原子を有する(「C2~6アルケニル」)。いくつかの態様において、アルケニル基は、2~5個の炭素原子を有する(「C2~5アルケニル」)。いくつかの態様において、アルケニル基は、2~4個の炭素原子を有する(「C2~4アルケニル」)。いくつかの態様において、アルケニル基は、2~3個の炭素原子を有する(「C2~3アルケニル」)。いくつかの態様において、アルケニル基は、2個の炭素原子を有する(「C2アルケニル」)。1以上の炭素-炭素二重結合は、内部にあるか(2-ブテニル中の二重結合など)、または末端にあり得る(1-ブテニル中の二重結合など)。C2~4アルケニル基の例は、エテニル(C2)、1-プロペニル(C3)、2-プロペニル(C3)、1-ブテニル(C4)、2-ブテニル(C4)、ブタジエニル(C4)等を包含する。C2~6アルケニル基の例は、先述のC2~4アルケニル基、ならびにペンテニル(C5)、ペンタジエニル(C5)、ヘキセニル(C6)等を包含する。アルケニルの追加例は、ヘプテニル(C7)、オクテニル(C8)、オクタトリエニル(C8)等を包含する。別様に特定されない限り、アルケニル基の各場合は、独立して、非置換であるか(「非置換アルケニル」)、または1以上の置換基で置換されている(「置換アルケニル」)。ある態様において、アルケニル基は、非置換C2~10アルケニルである。ある態様において、アルケニル基は、置換C2~10アルケニルである。アルケニル基中、立体化学が特定されていないC=C二重結合(例として、-CH=CHCH3または
は、(E)-または(Z)-二重結合であってもよい。
用語「ヘテロアルケニル」は、酸素、窒素、または硫黄から選択される少なくとも1個のヘテロ原子(例として、1個、2個、3個、もしくは4個のヘテロ原子)をさらに、親鎖内に(すなわち、親鎖の隣接する炭素原子間に挿入されて)および/または親鎖の1以上の末端位(単数もしくは複数)に置かれて包含するアルケニル基を指す。ある態様において、ヘテロアルケニル基は、2個から10個までの炭素原子、少なくとも1個の二重結合、および1個以上のヘテロ原子を親鎖内に有する基を指す(「ヘテロC2~10アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~9個の炭素原子、少なくとも1個の二重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~9アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~8個の炭素原子、少なくとも1個の二重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~8アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、を有する 2~7個の炭素原子、少なくとも1個の二重結合、および1個以上のヘテロ原子 親鎖内に(「ヘテロC2~7アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~6個の炭素原子、少なくとも1個の二重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~6アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~5個の炭素原子、少なくとも1個の二重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~5アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~4個の炭素原子、少なくとも1個の二重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~4アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~3個の炭素原子、少なくとも1個の二重結合、および1個のヘテロ原子を親鎖内に有する(「ヘテロC2~3アルケニル」)。いくつかの態様において、ヘテロアルケニル基は、2~6個の炭素原子、少なくとも1個の二重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~6アルケニル」)。別様に特定されない限り、ヘテロアルケニル基の各場合は、独立して、非置換であるか(「非置換ヘテロアルケニル」)、または1以上の置換基で置換されている(「置換ヘテロアルケニル」)。ある態様において、ヘテロアルケニル基は、非置換ヘテロC2~10アルケニルである。ある態様において、ヘテロアルケニル基は、置換ヘテロC2~10アルケニルである。
用語「アルキニル」は、2個から10個までの炭素原子と1以上の炭素-炭素三重結合(例として、1個、2個、3個、または4個の三重結合)とを有する、直鎖または分枝の炭化水素基のラジカルを指す(「C2~10アルキニル」)。いくつかの態様において、アルキニル基は、2~9個の炭素原子を有する(「C2~9アルキニル」)。いくつかの態様において、アルキニル基は、2~8個の炭素原子を有する(「C2~8アルキニル」)。いくつかの態様において、アルキニル基は、2~7個の炭素原子を有する(「C2~7アルキニル」)。いくつかの態様において、アルキニル基は、2~6個の炭素原子を有する(「C2~6アルキニル」)。いくつかの態様において、アルキニル基は、2~5個の炭素原子を有する(「C2~5アルキニル」)。いくつかの態様において、アルキニル基は、2~4個の炭素原子を有する(「C2~4アルキニル」)。いくつかの態様において、アルキニル基は、2~3個の炭素原子(を有する「C2~3アルキニル」)。いくつかの態様において、アルキニル基は、2個の炭素原子を有する(「C2アルキニル」)。1以上の炭素-炭素三重結合は、内部にあるか(2-ブチニル中の三重結合など)、または末端にあり得る(1-ブチニル中の三重結合など)。C2~4アルキニル基の例は、限定せずに、エチニル(C2)、1-プロピニル(C3)、2-プロピニル(C3)、1-ブチニル(C4)、2-ブチニル(C4)等を包含する。C2~6アルケニル基の例は、先述のC2~4アルキニル基、ならびにペンチニル(C5)、ヘキシニル(C6)等を包含する。アルキニルの追加例は、ヘプチニル(C7)、オクチニル(C8)等を包含する。別様に特定されない限り、アルキニル基の各場合は、独立して、非置換であるか(「非置換アルキニル」)、または1以上の置換基で置換されている(「置換アルキニル」)。ある態様において、アルキニル基は、非置換C2~10アルキニルである。ある態様において、アルキニル基は、置換C2~10アルキニルである。
用語「ヘテロアルキニル」は、酸素、窒素、または硫黄から選択される少なくとも1個のヘテロ原子(例として、1個、2個、3個、もしくは4個のヘテロ原子)をさらに、親鎖内に(すなわち、親鎖の隣接する炭素原子間に挿入されて)および/または親鎖の1以上の末端位(単数もしくは複数)に置かれて包含するアルキニル基を指す。ある態様において、ヘテロアルキニル基は、2個から10個までの炭素原子、少なくとも1個の三重結合、および1個以上のヘテロ原子を親鎖内に有する基を指す(「ヘテロC2~10アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~9個の炭素原子、少なくとも1個の三重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~9アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~8個の炭素原子、少なくとも1個の三重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~8アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~7個の炭素原子、少なくとも1個の三重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~7アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~6個の炭素原子、少なくとも1個の三重結合、および1個以上のヘテロ原子を親鎖内に有する(「ヘテロC2~6アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~5個の炭素原子、少なくとも1個の三重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~5アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~4個の炭素原子、少なくとも1個の三重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~4アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~3個の炭素原子、少なくとも1個の三重結合、および1個のヘテロ原子を親鎖内に有する(「ヘテロC2~3アルキニル」)。いくつかの態様において、ヘテロアルキニル基は、2~6個の炭素原子、少なくとも1個の三重結合、および1個または2個のヘテロ原子を親鎖内に有する(「ヘテロC2~6アルキニル」)。別様に特定されない限り、ヘテロアルキニル基の各場合は、独立して、非置換であるか(「非置換ヘテロアルキニル」)、または1以上の置換基で置換されている(「置換ヘテロアルキニル」)。ある態様において、ヘテロアルキニル基は、非置換ヘテロC2~10アルキニルである。ある態様において、ヘテロアルキニル基は、置換ヘテロC2~10アルキニルである。
用語「カルボシクリル」または「炭素環式」は、非芳香環系中に3個から14個までの環炭素原子(「C3~14カルボシクリル」)とゼロ個のヘテロ原子とを有する、非芳香族環式の炭化水素基のラジカルを指す。いくつかの態様において、カルボシクリル基は、3~10個の環炭素原子を有する(「C3~10カルボシクリル」)。いくつかの態様において、カルボシクリル基は、3~8個の環炭素原子を有する(「C3~8カルボシクリル」)。いくつかの態様において、カルボシクリル基は、3~7個の環炭素原子を有する(「C3~7カルボシクリル」)。いくつかの態様において、カルボシクリル基は、3~6個の環炭素原子を有する(「C3~6カルボシクリル」)。いくつかの態様において、カルボシクリル基は、4~6個の環炭素原子を有する(「C4~6カルボシクリル」)。いくつかの態様において、カルボシクリル基は、5~6個の環炭素原子を有する(「C5~6カルボシクリル」)。いくつかの態様において、カルボシクリル基は、5~10個の環炭素原子を有する(「C5~10カルボシクリル」)。例示のC3~6カルボシクリル基は、限定せずに、シクロプロピル(C3)、シクロプロペニル(C3)、シクロブチル(C4)、シクロブテニル(C4)、シクロペンチル(C5)、シクロペンテニル(C5)、シクロヘキシル(C6)、シクロヘキセニル(C6)、シクロヘキサジエニル(C6)等を包含する。例示のC3~8カルボシクリル基は、限定せずに、先述のC3~6カルボシクリル基、ならびにシクロへプチル(C7)、シクロヘプテニル(C7)、シクロへプタジエニル(C7)、シクロへプタトリエニル(C7)、シクロオクチル(C8)、シクロオクテニル(C8)、ビシクロ[2.2.1]ヘプタニル(C7)、ビシクロ[2.2.2]オクタニル(C8)等を包含する。例示のC3~10カルボシクリル基は、限定せずに、先述のC3~8カルボシクリル基、ならびにシクロノニル(C9)、シクロノネニル(C9)、シクロデシル(C10)、シクロデセニル(C10)、オクタヒドロ-1H-インデニル(C9)、デカヒドロナフタレニル(C10)、スピロ[4.5]デカニル(C10)等を包含する。上記の例に説明されるとおり、ある態様において、カルボシクリル基は、単環式(「単環式のカルボシクリル」)あるいは多環式(例として、二環系(「二環式のカルボシクリル」)もしくは三環系(「三環式のカルボシクリル」)などの、縮合環系、架橋環系、またはスピロ環系を含有する)のいずれかであって、飽和であり得るか、または1以上の炭素-炭素二重結合もしくは三重結合を含有し得る。「カルボシクリル」はまた、上に定義されるとおりのカルボシクリル環が1以上のアリール基またはヘテロアリール基と縮合された環系も包含するが、ここで付着点はカルボシクリル環上にあり、かかる場合において炭素数は炭素環式の環系中の炭素数を通して指定される。別様に特定されない限り、カルボシクリル基の各場合は、独立して、非置換であるか(「非置換カルボシクリル」)、または1以上の置換基で置換されている(「置換カルボシクリル」)。ある態様において、カルボシクリル基は、非置換C3~14カルボシクリルである。ある態様において、カルボシクリル基は、置換C3~14カルボシクリルである。
いくつかの態様において、「カルボシクリル」は、3個から14個までの環炭素原子を有する、単環式の、飽和カルボシクリル基である(「C3~14シクロアルキル」)。いくつかの態様において、シクロアルキル基は、3~10個の環炭素原子を有する(「C3~10シクロアルキル」)。いくつかの態様において、シクロアルキル基は、3~8個の環炭素原子を有する(「C3~8シクロアルキル」)。いくつかの態様において、シクロアルキル基は、3~6個の環炭素原子を有する(「C3~6シクロアルキル」)。いくつかの態様において、シクロアルキル基は、4~6個の環炭素原子を有する(「C4~6シクロアルキル」)。いくつかの態様において、シクロアルキル基は、5~6個の環炭素原子を有する(「C5~6シクロアルキル」)。いくつかの態様において、シクロアルキル基は、5~10個の環炭素原子を有する(「C5~10シクロアルキル」)。C5~6シクロアルキル基の例は、シクロペンチル(C5)およびシクロヘキシル(C5)を包含する。C3~6シクロアルキル基の例は、先述のC5~6シクロアルキル基、ならびにシクロプロピル(C3)およびシクロブチル(C4)を包含する。C3~8シクロアルキル基の例は、先述のC3~6シクロアルキル基、ならびにシクロへプチル(C7)およびシクロオクチル(C8)を包含する。別様に特定されない限り、シクロアルキル基の各場合は、独立して、非置換であるか(「非置換シクロアルキル」)、または1以上の置換基で置換されている(「置換シクロアルキル」)。ある態様において、シクロアルキル基は、非置換C3~14シクロアルキルである。ある態様において、シクロアルキル基は、置換C3~14シクロアルキルである。
用語「ヘテロシクリル」または「複素環式」は、環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する、3~14員の非芳香環系のラジカルを指す(「3~14員のヘテロシクリル」)。1個以上の窒素原子を含有するヘテロシクリル基中、付着点は、原子価が許す限り、炭素原子または窒素原子であり得る。ヘテロシクリル基は、単環式(「単環式のヘテロシクリル」)あるいは多環式(例として、二環系(「二環式のヘテロシクリル」)もしくは三環系(「三環式のヘテロシクリル」)などの、縮合環系、架橋環系、またはスピロ環系)のいずれかであり得、飽和であり得るか、または1以上の炭素-炭素二重結合もしくは三重結合を含有し得る。ヘテロシクリル多環式の環系は、一方の環中または両方の環中に、1個以上のヘテロ原子を包含し得る。「ヘテロシクリル」はまた、上に定義されるとおりのヘテロシクリル環が1以上のカルボシクリル基と縮合された環系(ここで付着点は、カルボシクリル環上またはヘテロシクリル環上のいずれかにある)、あるいは上に定義されるとおりのヘテロシクリル環が1以上のアリール基またはヘテロアリール基と縮合された環系(ここで付着点は、ヘテロシクリル環上にある)も包含し、かかる場合において、環員数は、ヘテロシクリル環系中の環員数を通して指定される。別様に特定されない限り、ヘテロシクリルの各場合は、独立して、非置換であるか(「非置換ヘテロシクリル」)、または1以上の置換基で置換されている(「置換ヘテロシクリル」)。ある態様において、ヘテロシクリル基は、非置換3~14員ヘテロシクリルである。ある態様において、ヘテロシクリル基は、置換3~14員ヘテロシクリルである。
いくつかの態様において、ヘテロシクリル基は、環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~10員の非芳香環系である(「5~10員のヘテロシクリル」)。いくつかの態様において、ヘテロシクリル基は、環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~8員の非芳香環系である(「5~8員のヘテロシクリル」)。いくつかの態様において、ヘテロシクリル基は、環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~6員の非芳香環系である(「5~6員のヘテロシクリル」)。いくつかの態様において、5~6員のヘテロシクリルは、窒素、酸素、および硫黄から選択される1~3個の環ヘテロ原子を有する。いくつかの態様において、5~6員のヘテロシクリルは、窒素、酸素、および硫黄から選択される1~2個の環ヘテロ原子を有する。いくつかの態様において、5~6員のヘテロシクリルは、窒素、酸素、および硫黄から選択される1個の環ヘテロ原子を有する。
例示の、1個のヘテロ原子を含有する3員のヘテロシクリル基は、限定せずに、アジリジニル、オキシラニル、およびチイラニルを包含する。例示の、1個のヘテロ原子を含有する4員ヘテロシクリル基は、限定せずに、アゼチジニル、オキセタニル、およびチエタニルを包含する。例示の、1個のヘテロ原子を含有する5員ヘテロシクリル基は、限定せずに、テトラヒドロフラニル、ジヒドロフラニル、テトラヒドロチオフェニル、ジヒドロチオフェニル、ピロリジニル、ジヒドロピロリル、およびピロリル-2,5-ジオンを包含する。例示の、2個のヘテロ原子を含有する5員ヘテロシクリル基は、限定せずに、ジオキソラニル、オキサチオラニルおよびジチオラニルを包含する。例示の、3個のヘテロ原子を含有する5員ヘテロシクリル基は、限定せずに、トリアゾリニル、オキサジアゾリニル、およびチアジアゾリニルを包含する。例示の、1個のヘテロ原子を含有する6員ヘテロシクリル基は、限定せずに、ピペリジニル、テトラヒドロピラニル、ジヒドロピリジニル、およびチアニルを包含する。例示の、2個のヘテロ原子を含有する6員ヘテロシクリル基は、限定せずに、ピペラジニル、モルホリニル、ジチアニル、およびジオキサニルを包含する。例示の、3個のヘテロ原子を含有する6員ヘテロシクリル基は、限定せずに、トリアジニルを包含する。例示の、1個のヘテロ原子を含有する7員ヘテロシクリル基は、限定せずに、アゼパニル、オキセパニル、およびチエパニルを包含する。例示の、1個のヘテロ原子を含有する8員ヘテロシクリル基は、限定せずに、アゾカニル、オキセカニル、およびチオカニルを包含する。例示の二環式ヘテロシクリル基は、限定せずに、インドリニル、イソインドリニル、ジヒドロベンゾフラニル、ジヒドロベンゾチエニル、テトラヒドロベンゾチエニル、テトラヒドロベンゾフラニル、テトラヒドロインドリル、テトラヒドロキノリニル、テトラヒドロイソキノリニル、デカヒドロキノリニル、デカヒドロイソキノリニル、オクタヒドロクロメニル、オクタヒドロイソクロメニル、デカヒドロナフチリジニル、デカヒドロ-1,8-ナフチリジニル、オクタヒドロピロロ[3,2-b]ピロール、インドリニル、フタルイミジル、ナフタルイミジル、クロマニル、クロメニル、1H-ベンゾ[e][1,4]ジアゼピニル、1,4,5,7-テトラヒドロピラノ[3,4-b]ピロリル、5,6-ジヒドロ-4H-フロ[3,2-b]ピロリル、6,7-ジヒドロ-5H-フロ[3,2-b]ピラニル、5,7-ジヒドロ-4H-チエノ[2,3-c]ピラニル、2,3-ジヒドロ-1H-ピロロ[2,3-b]ピリジニル、2,3-ジヒドロフロ[2,3-b]ピリジニル、4,5,6,7-テトラヒドロ-1H-ピロロ[2,3-b]ピリジニル、4,5,6,7-テトラヒドロフロ[3,2-c]ピリジニル、4,5,6,7-テトラヒドロチエノ[3,2-b]ピリジニル、1,2,3,4-テトラヒドロ-1,6-ナフチリジニル等を包含する。
用語「アリール」は、芳香環系中に提供された6~14個の環炭素原子とゼロ個のヘテロ原子とを有する、単環式または多環式(例として、二環式もしくは三環式)の4n+2芳香環系(例として、環状アレイ中に共有された6個、10個、または14個の電子を有する)のラジカルを指す(「C6~14アリール」)。いくつかの態様において、アリール基は、6個の環炭素原子を有する(「C6アリール」;例として、フェニル)。いくつかの態様において、アリール基は、10個の環炭素原子を有する(「C10アリール」;例として、1-ナフチルおよび2-ナフチルなどのナフチル)。いくつかの態様において、アリール基は、14個の環炭素原子を有する(「C14アリール」;例として、アントラシル)。「アリール」はまた、上に定義されるとおりのアリール環が1以上のカルボシクリル基またはヘテロシクリル基と縮合された環系(ここでラジカルもしくは付着点は、アリール環上にある)も包含し、かかる場合において、炭素原子数は、アリール環系中の炭素原子数を通して指定される。別様に特定されない限り、アリール基の各場合は、独立して、非置換であるか(「非置換アリール」)、または1以上の置換基で置換されている(「置換アリール」)。ある態様において、アリール基は、非置換C6~14アリールである。ある態様において、アリール基は、置換C6~14アリールである。
「アラルキル」は、「アルキル」の部分集合であって、アリール基で置換されたアルキル基を指すが、ここで付着点は、アルキル部分上にある。
用語「ヘテロアリール」は、芳香環系中に提供された環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する、5~14員の単環式または多環式(例として、二環式、三環式)の4n+2芳香環系(例として、環状アレイ中に共有された6個、10個、もしくは14個の電子を有する)のラジカルを指す(「5~14員のヘテロアリール」)。1個以上の窒素原子を含有するヘテロアリール基中、付着点は、原子価が許す限り、炭素原子または窒素原子であり得る。ヘテロアリール多環式の環系は、一方の環中または両方の環中に、1個以上のヘテロ原子を包含し得る。「ヘテロアリール」は、上に定義されるとおりのヘテロアリール環が1以上のカルボシクリル基またはヘテロシクリル基と縮合された環系(ここで付着点は、ヘテロアリール環上にある)を包含し、かかる場合において、環員数は、ヘテロアリール環系中の環員数を通して指定される。「ヘテロアリール」はまたは、上に定義されるとおりのヘテロアリール環が1以上のアリール基と縮合された環系(ここで付着点は、アリール環上またはヘテロアリール環上のいずれかにある)も包含し、かかる場合において、環員数は、縮合された多環式の(アリール/ヘテロアリール)環系中の環員数を通して指定される。1つの環がヘテロ原子を含有しない多環ヘテロアリール基(例として、インドリル、キノリニル、カルバゾリル等)において、付着点は、いずれかの環、すなわち、ヘテロ原子を担持する環(例として、2-インドリル)またはヘテロ原子を含有しない環(例として、5-インドリル)のいずれかの環上にあり得る。
いくつかの態様において、ヘテロアリール基は、芳香環系中に提供された環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~10員の芳香環系である(「5~10員のヘテロアリール」)。いくつかの態様において、ヘテロアリール基は、芳香環系中に提供された環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~8員の芳香環系である(「5~8員のヘテロアリール」)。いくつかの態様において、ヘテロアリール基は、芳香環系中に提供された環炭素原子と1~4個の環ヘテロ原子(ここで各ヘテロ原子は、独立して、窒素、酸素、および硫黄から選択される)とを有する5~6員の芳香環系である(「5~6員のヘテロアリール」)。いくつかの態様において、5~6員のヘテロアリールは、窒素、酸素、および硫黄から選択される1~3個の環ヘテロ原子を有する。いくつかの態様において、5~6員のヘテロアリールは、窒素、酸素、および硫黄から選択される1~2個の環ヘテロ原子を有する。いくつかの態様において、5~6員のヘテロアリールは、窒素、酸素、および硫黄から選択される1個の環ヘテロ原子を有する。別様に特定されない限り、ヘテロアリール基の各場合は、独立して、非置換であるか(「非置換ヘテロアリール」)、または1以上の置換基で置換されている(「置換ヘテロアリール」)。ある態様において、ヘテロアリール基は、非置換の5~14員ヘテロアリールである。ある態様において、ヘテロアリール基は、置換の5~14員ヘテロアリールである。
例示の、1個のヘテロ原子を含有する5員ヘテロアリール基は、限定せずに、ピロリル、フラニル、およびチオフェニルを包含する。例示の、2個のヘテロ原子を含有する5員ヘテロアリール基は、限定せずに、イミダゾリル、ピラゾリル、オキサゾリル、イソオキサゾリル、チアゾリル、およびイソチアゾリルを包含する。例示の、3個のヘテロ原子を含有する5員ヘテロアリール基は、限定せずに、トリアゾリル、オキサジアゾリル、およびチアジアゾリルを包含する。例示の、4個のヘテロ原子を含有する5員ヘテロアリール基は、限定せずに、テトラゾリルを包含する。例示の、1個のヘテロ原子を含有する6員のヘテロアリール基は、限定せずに、ピリジニルを包含する。例示の、2個のヘテロ原子を含有する6員ヘテロアリール基は、限定せずに、ピリダジニル、ピリミジニル、およびピラジニルを包含する。例示の、3個または4個のヘテロ原子を含有する6員ヘテロアリール基は夫々、限定せずに、トリアジニルおよびテトラジニルを包含する。例示の、1個のヘテロ原子を含有する7員のヘテロアリール基は、限定せずに、アゼピニル、オキセピニル、およびチエピニルを包含する。例示の5,6-二環式ヘテロアリール基は、限定せずに、インドリル、イソインドリル、インダゾリル、ベンゾトリアゾリル、ベンゾチオフェニル、イソベンゾチオフェニル、ベンゾフラニル、ベンゾイソフラニル、ベンズイミダゾリル、ベンズオキサゾリル、ベンズイソオキサゾリル、ベンゾオキサジアゾリル、ベンズチアゾリル、ベンズイソチアゾリル、ベンズチアジアゾリル、インドリジニル、およびプリニルを包含する。例示の6,6-二環式ヘテロアリール基は、限定せずに、ナフチリジニル、プテリジニル、キノリニル、イソキノリニル、シンノリニル、キノキサリニル、フタラジニル、およびキナゾリニルを包含する。例示の三環式ヘテロアリール基は、限定せずに、フェナントリジニル、ジベンゾフラニル、カルバゾリル、アクリジニル、フェノチアジニル、フェノキサジニル、およびフェナジニルを包含する。
「ヘテロアラルキル」は、「アルキル」の部分集合であって、置換by ヘテロアリール基によって置換されたアルキル基を指し、ここで付着点は、アルキル部分上にある。
用語「多環式のスピロ環系」は、1個の共通の原子によって連結された2以上の環を有する環系を指す。共通の原子は、スピロ原子として知られている。環系は、完全に炭素環式(すべて炭素)であっても、または複素環式(1個以上の非炭素原子を有する)であってもよい。環系は、スピロ原子またはいずれかの環中のいずれかの原子が炭素原子でない場合、複素環式と見なされる。
用語「架橋環系」は、2個の「橋頭」原子を接続させる架橋-単一の原子または原子の非分枝鎖(またはただの原子価結合でさえも)を含有する2以上の環を有する環系を指す。橋頭原子は、水素ではないいずれの原子としても定義され、3個以上の他の骨格原子へ結合した分子の骨格フレームワークの一部である。環系は、完全に炭素環式(すべて炭素)であっても、または複素環式(1個以上の非炭素原子を有する)であってもよい。環系は、いずれの原子も炭素原子ではない場合、複素環式と見なされる。
用語「不飽和結合」は、二重結合または三重結合を指す。
用語「不飽和」または「部分的に不飽和」は、少なくとも1つの二重結合または三重結合を包含する部分を指す。
用語「飽和」は、二重結合も三重結合も含有しない部分、すなわち、単結合しか含有しない部分を指す。
接尾辞「-エン」を基へ付すことは、基が二価成分である、例として、アルキレンがアルキルの二価成分である、アルケニレンがアルケニルの二価成分である、アルキニレンがアルキニルの二価成分である、ヘテロアルキレンがヘテロアルキルの二価成分である、ヘテロアルケニレンがヘテロアルケニルの二価成分である、ヘテロアルキニレンがヘテロアルキニルの二価成分である、カルボシクリレンがカルボシクリルの二価成分である、ヘテロシクリレンがヘテロシクリルの二価成分である、アリーレンがアリールの二価成分である、およびヘテロアリーレンがヘテロアリールの二価成分であることを指し示す。
基は、別様にはっきりと提供されていない限り、任意に置換されている。用語「任意に置換されている」は、置換されていること、または非置換であることを指す。ある態様において、アルキル基、アルケニル基、アルキニル基、ヘテロアルキル基、ヘテロアルケニル基、ヘテロアルキニル基、カルボシクリル基、ヘテロシクリル基、アリール基、およびヘテロアリール基は、任意に置換されている。「任意に置換されている」は、置換されていてもまたは非置換であってもよい基(例として、「置換」もしくは「非置換」のアルキル基、「置換」もしくは「非置換」のアルケニル基、「置換」もしくは「非置換」のアルキニル基、「置換」もしくは「非置換」のヘテロアルキル基、「置換」もしくは「非置換」のヘテロアルケニル基、「置換」もしくは「非置換」のヘテロアルキニル基、「置換」もしくは「非置換」のカルボシクリル基、「置換」もしくは「非置換」のヘテロシクリル基、「置換」もしくは「非置換」のアリール基、または「置換」もしくは「非置換」のヘテロアリール基)を指す。一般に、用語「置換(された/されている/の)」は、基上に存在する少なくとも1個の水素が、容認できる置換基(例として、置換された際、安定した化合物(例として、再配置、環化、脱離などによる転換も、他の反応も自発的に経ることがない化合物)をもたらす置換基)に置き換えられていることを意味する。別様に示されない限り、「置換された」基は、置換基を、基の1以上の置換可能な位置にて有し、いずれか所定の構造中1より多くの位置が置換されたとき、置換基は、各位置にて同じかまたは異なるかのいずれかである。用語「置換(された/されている/の)」は、有機化合物であるすべての容認できる置換基での置換を包含することが企図されており、かつ安定した化合物の形成をもたらす本明細書に記載の置換基のいずれも包含する。本発明は、安定した化合物に達するのに、ありとあらゆるかかる組み合わせを企図する。本発明の目的上、窒素などのヘテロ原子は、水素置換基、および/またはヘテロ原子の原子価を満たしかつ安定した部分の形成をもたらす本明細書に記載のとおりのいずれの好適な置換基を有していてもよい。本発明は、形はどうあれ、本明細書に記載の例示置換基によって限定されることは意図しない。
例示の炭素原子置換基は、これらに限定されないが、ハロゲン、-CN、-NO2、-N3、-SO2H、-SO3H、-OH、-ORaa、-ON(Rbb)2、-N(Rbb)2、-N(Rbb)3
+X-、-N(ORcc)Rbb、-SH、-SRaa、-SSRcc、-C(=O)Raa、-CO2H、-CHO、-C(ORcc)3、-CO2Raa、-OC(=O)Raa、-OCO2Raa、-C(=O)N(Rbb)2、-OC(=O)N(Rbb)2、-NRbbC(=O)Raa、-NRbbCO2Raa、-NRbbC(=O)N(Rbb)2、-C(=NRbb)Raa、-C(=NRbb)ORaa、-OC(=NRbb)Raa、-OC(=NRbb)ORaa、-C(=NRbb)N(Rbb)2、-OC(=NRbb)N(Rbb)2、-NRbbC(=NRbb)N(Rbb)2、-C(=O)NRbbSO2Raa、-NRbbSO2Raa、-SO2N(Rbb)2、-SO2Raa、-SO2ORaa、-OSO2Raa、-S(=O)Raa、-OS(=O)Raa、-Si(Raa)3、-OSi(Raa)3 -C(=S)N(Rbb)2、-C(=O)SRaa、-C(=S)SRaa、-SC(=S)SRaa、-SC(=O)SRaa、-OC(=O)SRaa、-SC(=O)ORaa、-SC(=O)Raa、-P(=O)(Raa)2、-P(=O)(ORcc)2、-OP(=O)(Raa)2、-OP(=O)(ORcc)2、-P(=O)(N(Rbb)2)2、-OP(=O)(N(Rbb)2)2、-NRbbP(=O)(Raa)2、-NRbbP(=O)(ORcc)2、-NRbbP(=O)(N(Rbb)2)2、-P(Rcc)2、-P(ORcc)2、-P(Rcc)3
+X-、-P(ORcc)3
+X-、-P(Rcc)4、-P(ORcc)4、-OP(Rcc)2、-OP(Rcc)3
+X-、-OP(ORcc)2、-OP(ORcc)3
+X-、-OP(Rcc)4、-OP(ORcc)4、-B(Raa)2、-B(ORcc)2、-BRaa(ORcc)、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールを包含するが、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;ここでX-は、対イオンである;
あるいは炭素原子上2個のジェミナル(geminal)水素は、基=O、=S、=NN(Rbb)2、=NNRbbC(=O)Raa、=NNRbbC(=O)ORaa、=NNRbbS(=O)2Raa、=NRbb、または=NORccに置き換えられている;
Raaの各場合は、独立して、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRaa基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;
Rbbの各場合は、独立して、水素、-OH、-ORaa、-N(Rcc)2、-CN、-C(=O)Raa、-C(=O)N(Rcc)2、-CO2Raa、-SO2Raa、-C(=NRcc)ORaa、-C(=NRcc)N(Rcc)2、-SO2N(Rcc)2、-SO2Rcc、-SO2ORcc、-SORaa、-C(=S)N(Rcc)2、-C(=O)SRcc、-C(=S)SRcc、-P(=O)(Raa)2、-P(=O)(ORcc)2、-P(=O)(N(Rcc)2)2、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRbb基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;ここでX-は、対イオンである;
Rccの各場合は、独立して、水素、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRcc基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;
Rddの各場合は、独立して、ハロゲン、-CN、-NO2、-N3、-SO2H、-SO3H、-OH、-ORee、-ON(Rff)2、-N(Rff)2、-N(Rff)3 +X-、-N(ORee)Rff、-SH、-SRee、-SSRee、-C(=O)Ree、-CO2H、-CO2Ree、-OC(=O)Ree、-OCO2Ree、-C(=O)N(Rff)2、-OC(=O)N(Rff)2、-NRffC(=O)Ree、-NRffCO2Ree、-NRffC(=O)N(Rff)2、-C(=NRff)ORee、-OC(=NRff)Ree、-OC(=NRff)ORee、-C(=NRff)N(Rff)2、-OC(=NRff)N(Rff)2、-NRffC(=NRff)N(Rff)2、-NRffSO2Ree、-SO2N(Rff)2、-SO2Ree、-SO2ORee、-OSO2Ree、-S(=O)Ree、-Si(Ree)3、-OSi(Ree)3、-C(=S)N(Rff)2、-C(=O)SRee、-C(=S)SRee、-SC(=S)SRee、-P(=O)(ORee)2、-P(=O)(Ree)2、-OP(=O)(Ree)2、-OP(=O)(ORee)2、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、3~10員のヘテロシクリル、C6~10アリール、5~10員のヘテロアリールから選択され、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されているか、または2個のジェミナルRdd置換基は、結び合わされることで、=Oもしくは=Sを形成し得る;ここでX-は、対イオンである;
Reeの各場合は、独立して、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、C6~10アリール、3~10員のヘテロシクリル、および3~10員のヘテロアリールから選択され、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されている;
Rffの各場合は、独立して、水素、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、3~10員のヘテロシクリル、C6~10アリールおよび5~10員のヘテロアリールから選択されるか、または2個のRff基は、結び合わされることで、3~10員のヘテロシクリルもしくは5~10員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されている;および
Rggの各場合は、独立して、ハロゲン、-CN、-NO2、-N3、-SO2H、-SO3H、-OH、-OC1~6アルキル、-ON(C1~6アルキル)2、-N(C1~6アルキル)2、-N(C1~6アルキル)3 +X-、-NH(C1~6アルキル)2 +X-、-NH2(C1~6アルキル)+X-、-NH3 +X-、-N(OC1~6アルキル)(C1~6アルキル)、-N(OH)(C1~6アルキル)、-NH(OH)、-SH、-SC1~6アルキル、-SS(C1~6アルキル)、-C(=O)(C1~6アルキル)、-CO2H、-CO2(C1~6アルキル)、-OC(=O)(C1~6アルキル)、-OCO2(C1~6アルキル)、-C(=O)NH2、-C(=O)N(C1~6アルキル)2、-OC(=O)NH(C1~6アルキル)、-NHC(=O)(C1~6アルキル)、-N(C1~6アルキル)C(=O)(C1~6アルキル)、-NHCO2(C1~6アルキル)、-NHC(=O)N(C1~6アルキル)2、-NHC(=O)NH(C1~6アルキル)、-NHC(=O)NH2、-C(=NH)O(C1~6アルキル)、-OC(=NH)(C1~6アルキル)、-OC(=NH)OC1~6アルキル、-C(=NH)N(C1~6アルキル)2、-C(=NH)NH(C1~6アルキル)、-C(=NH)NH2、-OC(=NH)N(C1~6アルキル)2、-OC(=NH)NH(C1~6アルキル)、-OC(=NH)NH2、-NHC(=NH)N(C1~6アルキル)2、-NHC(=NH)NH2、-NHSO2(C1~6アルキル)、-SO2N(C1~6アルキル)2、-SO2NH(C1~6アルキル)、-SO2NH2、-SO2(C1~6アルキル)、-SO2O(C1~6アルキル)、-OSO2(C1~6アルキル)、-SO(C1~6アルキル)、-Si(C1~6アルキル)3、-OSi(C1~6アルキル)3 -C(=S)N(C1~6アルキル)2、C(=S)NH(C1~6アルキル)、C(=S)NH2、-C(=O)S(C1~6アルキル)、-C(=S)SC1~6アルキル、-SC(=S)SC1~6アルキル、-P(=O)(OC1~6アルキル)2、-P(=O)(C1~6アルキル)2、-OP(=O)(C1~6アルキル)2、-OP(=O)(OC1~6アルキル)2、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、C6~10アリール、3~10員のヘテロシクリル、5~10員のヘテロアリールである;または2個のジェミナルRgg置換基は、結び合わされることで、=Oもしくは=Sを形成し得る;ここでX-は、対イオンである。
あるいは炭素原子上2個のジェミナル(geminal)水素は、基=O、=S、=NN(Rbb)2、=NNRbbC(=O)Raa、=NNRbbC(=O)ORaa、=NNRbbS(=O)2Raa、=NRbb、または=NORccに置き換えられている;
Raaの各場合は、独立して、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRaa基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;
Rbbの各場合は、独立して、水素、-OH、-ORaa、-N(Rcc)2、-CN、-C(=O)Raa、-C(=O)N(Rcc)2、-CO2Raa、-SO2Raa、-C(=NRcc)ORaa、-C(=NRcc)N(Rcc)2、-SO2N(Rcc)2、-SO2Rcc、-SO2ORcc、-SORaa、-C(=S)N(Rcc)2、-C(=O)SRcc、-C(=S)SRcc、-P(=O)(Raa)2、-P(=O)(ORcc)2、-P(=O)(N(Rcc)2)2、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRbb基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;ここでX-は、対イオンである;
Rccの各場合は、独立して、水素、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールから選択されるか、または2個のRcc基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されている;
Rddの各場合は、独立して、ハロゲン、-CN、-NO2、-N3、-SO2H、-SO3H、-OH、-ORee、-ON(Rff)2、-N(Rff)2、-N(Rff)3 +X-、-N(ORee)Rff、-SH、-SRee、-SSRee、-C(=O)Ree、-CO2H、-CO2Ree、-OC(=O)Ree、-OCO2Ree、-C(=O)N(Rff)2、-OC(=O)N(Rff)2、-NRffC(=O)Ree、-NRffCO2Ree、-NRffC(=O)N(Rff)2、-C(=NRff)ORee、-OC(=NRff)Ree、-OC(=NRff)ORee、-C(=NRff)N(Rff)2、-OC(=NRff)N(Rff)2、-NRffC(=NRff)N(Rff)2、-NRffSO2Ree、-SO2N(Rff)2、-SO2Ree、-SO2ORee、-OSO2Ree、-S(=O)Ree、-Si(Ree)3、-OSi(Ree)3、-C(=S)N(Rff)2、-C(=O)SRee、-C(=S)SRee、-SC(=S)SRee、-P(=O)(ORee)2、-P(=O)(Ree)2、-OP(=O)(Ree)2、-OP(=O)(ORee)2、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、3~10員のヘテロシクリル、C6~10アリール、5~10員のヘテロアリールから選択され、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されているか、または2個のジェミナルRdd置換基は、結び合わされることで、=Oもしくは=Sを形成し得る;ここでX-は、対イオンである;
Reeの各場合は、独立して、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、C6~10アリール、3~10員のヘテロシクリル、および3~10員のヘテロアリールから選択され、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されている;
Rffの各場合は、独立して、水素、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、3~10員のヘテロシクリル、C6~10アリールおよび5~10員のヘテロアリールから選択されるか、または2個のRff基は、結び合わされることで、3~10員のヘテロシクリルもしくは5~10員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRgg基で置換されている;および
Rggの各場合は、独立して、ハロゲン、-CN、-NO2、-N3、-SO2H、-SO3H、-OH、-OC1~6アルキル、-ON(C1~6アルキル)2、-N(C1~6アルキル)2、-N(C1~6アルキル)3 +X-、-NH(C1~6アルキル)2 +X-、-NH2(C1~6アルキル)+X-、-NH3 +X-、-N(OC1~6アルキル)(C1~6アルキル)、-N(OH)(C1~6アルキル)、-NH(OH)、-SH、-SC1~6アルキル、-SS(C1~6アルキル)、-C(=O)(C1~6アルキル)、-CO2H、-CO2(C1~6アルキル)、-OC(=O)(C1~6アルキル)、-OCO2(C1~6アルキル)、-C(=O)NH2、-C(=O)N(C1~6アルキル)2、-OC(=O)NH(C1~6アルキル)、-NHC(=O)(C1~6アルキル)、-N(C1~6アルキル)C(=O)(C1~6アルキル)、-NHCO2(C1~6アルキル)、-NHC(=O)N(C1~6アルキル)2、-NHC(=O)NH(C1~6アルキル)、-NHC(=O)NH2、-C(=NH)O(C1~6アルキル)、-OC(=NH)(C1~6アルキル)、-OC(=NH)OC1~6アルキル、-C(=NH)N(C1~6アルキル)2、-C(=NH)NH(C1~6アルキル)、-C(=NH)NH2、-OC(=NH)N(C1~6アルキル)2、-OC(=NH)NH(C1~6アルキル)、-OC(=NH)NH2、-NHC(=NH)N(C1~6アルキル)2、-NHC(=NH)NH2、-NHSO2(C1~6アルキル)、-SO2N(C1~6アルキル)2、-SO2NH(C1~6アルキル)、-SO2NH2、-SO2(C1~6アルキル)、-SO2O(C1~6アルキル)、-OSO2(C1~6アルキル)、-SO(C1~6アルキル)、-Si(C1~6アルキル)3、-OSi(C1~6アルキル)3 -C(=S)N(C1~6アルキル)2、C(=S)NH(C1~6アルキル)、C(=S)NH2、-C(=O)S(C1~6アルキル)、-C(=S)SC1~6アルキル、-SC(=S)SC1~6アルキル、-P(=O)(OC1~6アルキル)2、-P(=O)(C1~6アルキル)2、-OP(=O)(C1~6アルキル)2、-OP(=O)(OC1~6アルキル)2、C1~6アルキル、C1~6ペルハロアルキル、C2~6アルケニル、C2~6アルキニル、ヘテロC1~6アルキル、ヘテロC2~6アルケニル、ヘテロC2~6アルキニル、C3~10カルボシクリル、C6~10アリール、3~10員のヘテロシクリル、5~10員のヘテロアリールである;または2個のジェミナルRgg置換基は、結び合わされることで、=Oもしくは=Sを形成し得る;ここでX-は、対イオンである。
用語「ハロ」または「ハロゲン」は、フッ素(フルオロ、-F)、塩素(クロロ、-Cl)、臭素(ブロモ、-Br)、またはヨウ素(ヨード、-I)を指す。
用語「ヒドロキシル」または「ヒドロキシ」は、基-OHを指す。用語「置換ヒドロキシル」または「置換ヒドロキシルは、その延長線上で考えると、親分子へ直接付着された酸素原子が水素以外の基で置換されており、かつ-ORaa、-ON(Rbb)2、-OC(=O)SRaa、-OC(=O)Raa、-OCO2Raa、-OC(=O)N(Rbb)2、-OC(=NRbb)Raa、-OC(=NRbb)ORaa、-OC(=NRbb)N(Rbb)2、-OS(=O)Raa、-OSO2Raa、-OSi(Raa)3、-OP(Rcc)2、-OP(Rcc)3
+X-、-OP(ORcc)2、-OP(ORcc)3
+X-、-OP(=O)(Raa)2、-OP(=O)(ORcc)2、および-OP(=O)(N(Rbb)2)2から選択される基(ここでX-、Raa、Rbb、およびRccは、本明細書に定義されるとおりである)を包含するヒドロキシル基を指す。
用語「アミノ」は、基-NH2を指す。用語「置換アミノ」は、その延長線上で考えると、単置換されたアミノ、二置換されたアミノ、または三置換されたアミノを指す。ある態様において、「置換アミノ」は、単置換されたアミノまたは二置換されたアミノ基である。
用語「単置換されたアミノ」は、親分子へ直接付着された窒素原子が1個の水素と水素以外の1個の基とで置換されており、かつ-NH(Rbb)、-NHC(=O)Raa、-NHCO2Raa、-NHC(=O)N(Rbb)2、-NHC(=NRbb)N(Rbb)2、-NHSO2Raa、-NHP(=O)(ORcc)2、および-NHP(=O)(N(Rbb)2)2から選択される基(ここでRaa、RbbおよびRccは、本明細書に定義されるとおりであって、およびここで基-NH(Rbb)のRbbは、水素ではない)を包含するアミノ基を指す。
用語「二置換されたアミノ」は、親分子へ直接付着された窒素原子が水素以外の2個の基で置換されており、かつ-N(Rbb)2、-NRbbC(=O)Raa、-NRbbCO2Raa、-NRbbC(=O)N(Rbb)2、-NRbbC(=NRbb)N(Rbb)2、-NRbbSO2Raa、-NRbbP(=O)(ORcc)2、および-NRbbP(=O)(N(Rbb)2)2から選択される基(ここでRaa、Rbb、およびRccは、本明細書に定義されるとおりであるが、ただし親分子へ直接付着された窒素原子は、水素では置換されていない)を包含するアミノ基を指す。
用語「三置換されたアミノ」は、親分子へ直接付着された窒素原子が3個の基で置換されており、かつ-N(Rbb)3および-N(Rbb)3
+X-から選択される基(ここでRbbおよびX-は、本明細書に定義されるとおりである)を包含するアミノ基を指す。
用語「スルホニル」は、-SO2N(Rbb)2、-SO2Raa、および-SO2ORaaから選択される基を指すが、ここでRaaおよびRbbは、本明細書に定義されるとおりである。
用語「スルフィニル」は、基-S(=O)Raaを指すが、ここでRaaは、本明細書に定義されるとおりである。
用語「アシル」は、一般式:-C(=O)RX1、-C(=O)ORX1、-C(=O)-O-C(=O)RX1、-C(=O)SRX1、-C(=O)N(RX1)2、-C(=S)RX1、-C(=S)N(RX1)2、-C(=S)O(RX1)、-C(=S)S(RX1)、-C(=NRX1)RX1、-C(=NRX1)ORX1、-C(=NRX1)SRX1、または-C(=NRX1)N(RX1)2を有する基を指すが、ここでRX1は、水素;ハロゲン;置換もしくは非置換のヒドロキシル;置換もしくは非置換のチオール;置換もしくは非置換のアミノ;置換もしくは非置換のアシル、環状もしくは非環式の、置換または非置換の、分枝あるいは非分枝の脂肪族;環状もしくは非環式の、置換または非置換の、分枝あるいは非分枝のヘテロ脂肪族;環状もしくは非環式の、置換または非置換の、分枝あるいは非分枝のアルキルである;環状もしくは非環式の、置換または非置換の、分枝あるいは非分枝のアルケニル;置換もしくは非置換のアルキニル;置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、脂肪族オキシ、ヘテロ脂肪族オキシ、アルキルオキシ、ヘテロアルキルオキシ、アリールオキシ、ヘテロアリールオキシ、脂肪族チオキシ、ヘテロ脂肪族チオキシ、アルキルチオキシ、ヘテロアルキルチオキシ、アリールチオキシ、ヘテロアリールチオキシ、モノ-もしくはジ-脂肪族アミノ、モノ-もしくはジ-ヘテロ脂肪族アミノ、モノ-もしくはジ-アルキルアミノ、モノ-もしくはジ-ヘテロアルキルアミノ、モノ-もしくはジ-アリールアミノ、またはモノ-もしくはジ-ヘテロアリールアミノである;あるいは2個のRX1基は一緒になって、5~6員の複素環式の環を形成している。例示のアシル基は、アルデヒド(-CHO)、カルボン酸(-CO2H)、ケトン、ハロゲン化アシル、エステル、アミド、イミン、カーボネート、カルバマート、および尿素を包含する。アシル置換基は、これらに限定されないが、安定した部分の形成をもたらす本明細書に記載の置換基(例として、脂肪族、アルキル、アルケニル、アルキニル、ヘテロ脂肪族、複素環式、アリール、ヘテロアリール、アシル、オキソ、イミノ、チオオキソ、シアノ、イソシアノ、アミノ、アジド、ニトロ、ヒドロキシル、チオール、ハロ、脂肪族アミノ、ヘテロ脂肪族アミノ、アルキルアミノ、ヘテロアルキルアミノ、アリールアミノ、ヘテロアリールアミノ、アルキルアリール、アリールアルキル、脂肪族オキシ、ヘテロ脂肪族オキシ、アルキルオキシ、ヘテロアルキルオキシ、アリールオキシ、ヘテロアリールオキシ、脂肪族チオキシ、ヘテロ脂肪族チオキシ、アルキルチオキシ、ヘテロアルキルチオキシ、アリールチオキシ、ヘテロアリールチオキシ、アシルオキシ等、これらの各々はさらに置換されていてもいなくてもよい)のいずれも包含する。
用語「オキソ」は、基=Oを指し、用語「チオオキソ」は、基=Sを指す。
窒素原子は、原子価が許す限り、置換もしくは非置換であり得、一級、二級、三級、および四級の窒素原子を包含する。例示の窒素原子置換基は、これらに限定されないが、水素、-OH、-ORaa、-N(Rcc)2、-CN、-C(=O)Raa、-C(=O)N(Rcc)2、-CO2Raa、-SO2Raa、-C(=NRbb)Raa、-C(=NRcc)ORaa、-C(=NRcc)N(Rcc)2、-SO2N(Rcc)2、-SO2Rcc、-SO2ORcc、-SORaa、-C(=S)N(Rcc)2、-C(=O)SRcc、-C(=S)SRcc、-P(=O)(ORcc)2、-P(=O)(Raa)2、-P(=O)(N(Rcc)2)2、C1~10アルキル、C1~10ペルハロアルキル、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリールを包含するか、またはN原子へ付着された2個のRcc基は、結び合わされることで、3~14員のヘテロシクリルもしくは5~14員のヘテロアリール環を形成しており、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されており、およびここでRaa、Rbb、RccおよびRddは、本明細書に定義されるとおりである。
ある態様において、窒素原子上に存在する置換基は、窒素保護基である(また本明細書中、「アミノ保護基」とも称される)。窒素保護基は、これらに限定されないが、-OH、-ORaa、-N(Rcc)2、-C(=O)Raa、-C(=O)N(Rcc)2、-CO2Raa、-SO2Raa、-C(=NRcc)Raa、-C(=NRcc)ORaa、-C(=NRcc)N(Rcc)2、-SO2N(Rcc)2、-SO2Rcc、-SO2ORcc、-SORaa、-C(=S)N(Rcc)2、-C(=O)SRcc、-C(=S)SRcc、C1~10アルキル(例として、アラルキル、ヘテロアラルキル)、C2~10アルケニル、C2~10アルキニル、ヘテロC1~10アルキル、ヘテロC2~10アルケニル、ヘテロC2~10アルキニル、C3~10カルボシクリル、3~14員のヘテロシクリル、C6~14アリール、および5~14員のヘテロアリール基を包含し、ここで各アルキル、アルケニル、アルキニル、ヘテロアルキル、ヘテロアルケニル、ヘテロアルキニル、カルボシクリル、ヘテロシクリル、アラルキル、アリール、およびヘテロアリールは、独立して、0個、1個、2個、3個、4個、または5個のRdd基で置換されており、およびここでRaa、Rbb、RccおよびRddは、本明細書に定義されるとおりである。窒素保護基は、当該技術分野において周知であり、Protecting Groups in Organic Synthesis,T.W.Greene and P.G.M.Wuts,3rd edition,John Wiley & Sons,1999(参照により本明細書に組み込まれる)において詳細に記載されるものを包含する。
例えば、アミド基(例として、-C(=O)Raa)などの窒素保護基は、これらに限定されないが、ホルムアミド、アセトアミド、クロロアセトアミド、トリクロロアセトアミド、トリフルオロアセトアミド、フェニルアセトアミド、3-フェニルプロパンアミド、ピコリンアミド、3-ピリジルカルボキサミド、N-ベンゾイルフェニルアラニル誘導体、ベンズアミド、p-フェニルベンズアミド、o-ニトロフェニルアセトアミド、o-ニトロフェノキシアセトアミド、アセトアセトアミド、(N'-ジチオベンジルオキシアシルアミノ)アセトアミド、3-(p-ヒドロキシフェニル)プロパンアミド、3-(o-ニトロフェニル)プロパンアミド、2-メチル-2-(o-ニトロフェノキシ)プロパンアミド、2-メチル-2-(o-フェニルアゾフェノキシ)プロパンアミド、4-クロロブタンアミド、3-メチル-3-ニトロブタンアミド、o-ニトロシンナミド、N-アセチルメチオニン誘導体、o-ニトロベンズアミド、およびo-(ベンゾイルオキシメチル)ベンズアミドを包含する。
カルバマート基(例として、-C(=O)ORaa)などの窒素保護基は、これらに限定されないが、メチルカルバマート、エチルカルバマート、9-フルオレニルメチルカルバマート(Fmoc)、9-(2-スルホ)フルオレニルメチルカルバマート、9-(2,7-ジブロモ)フルオロエニルメチルカルバマート、2,7-ジ-t-ブチル-[9-(10,10-ジオキソ-10,10,10,10-テトラヒドロチオキサンチル)]メチルカルバマート(DBD-Tmoc)、4-メトキシフェナシル カルバマート(Phenoc)、2,2,2-トリクロロエチルカルバマート(Troc)、2-トリメチルシリルエチルカルバマート(Teoc)、2-フェニルエチルカルバマート(hZ)、1-(1-アダマンチル)-1-メチルエチルカルバマート(Adpoc)、1,1-ジメチル-2-ハロエチルカルバマート、1,1-ジメチル-2,2-ジブロモエチルカルバマート(DB-t-BOC)、1,1-ジメチル-2,2,2-トリクロロエチルカルバマート(TCBOC)、1-メチル-1-(4-ビフェニリル)エチルカルバマート(Bpoc)、1-(3,5-ジ-t-ブチルフェニル)-1-メチルエチルカルバマート(t-Bumeoc)、2-(2-および4'-ピリジル)エチルカルバマート(Pyoc)、2-(N,N-ジシクロヘキシルカルボキサミド)エチルカルバマート、t-ブチルカルバマート(BOCまたはBoc)、1-アダマンチルカルバマート(Adoc)、ビニルカルバマート(Voc)、アリルカルバマート(Alloc)、1-イソプロピルアリルカルバマート(Ipaoc)、シンナミルカルバマート(Coc)、4-ニトロシンナミルカルバマート(Noc)、8-キノリルカルバマート、N-ヒドロキシピペリジニルカルバマート、アルキルジチオカルバマート、ベンジルカルバマート(Cbz)、p-メトキシベンジルカルバマート(Moz)、p-ニトロベンジルカルバマート、p-ブロモベンジルカルバマート、p-クロロベンジルカルバマート、2,4-ジクロロベンジルカルバマート、4-メチルスルフィニルベンジルカルバマート(Msz)、9-アントリルメチルカルバマート、ジフェニルメチルカルバマート、2-メチルチオエチルカルバマート、2-メチルスルホニルエチルカルバマート、2-(p-トルエンスルホニル)エチルカルバマート、[2-(1,3-ジチアニル)]メチルカルバマート(Dmoc)、4-メチルチオフェニルカルバマート(Mtpc)、2,4-ジメチルチオフェニルカルバマート(Bmpc)、2-ホスホニオエチルカルバマート(Peoc)、2-トリフェニルホスホニオイソプロピルカルバマート(Ppoc)、1,1-ジメチル-2-シアノエチルカルバマート、m-クロロ-p-アシルオキシベンジルカルバマート、p-(ジヒドロキシボリル)ベンジルカルバマート、5-ベンズイソオキサゾリルメチルカルバマート、2-(トリフルオロメチル)-6-クロモニルメチルカルバマート(Tcroc)、m-ニトロフェニル カルバマート、3,5-ジメトキシベンジルカルバマート、o-ニトロベンジルカルバマート、3,4-ジメトキシ-6-ニトロベンジルカルバマート、フェニル(o-ニトロフェニル)メチルカルバマート、t-アミルカルバマート、S-ベンジルチオカルバマート、p-シアノベンジルカルバマート、シクロブチルカルバマート、シクロヘキシルカルバマート、シクロペンチルカルバマート、シクロプロピルメチルカルバマート、p-デシルオキシベンジルカルバマート、2,2-ジメトキシアシルビニルカルバマート、o-(N,N-ジメチルカルボキサミド)ベンジルカルバマート、1,1-ジメチル-3-(N,N-ジメチルカルボキサミド)プロピル カルバマート、1,1-ジメチルプロピニルカルバマート、ジ(2-ピリジル)メチルカルバマート、2-フラニルメチルカルバマート、2-ヨードエチルカルバマート、イソボルニルカルバマート、イソブチルカルバマート、イソニコチニルカルバマート、p-(p'-メトキシフェニルアゾ)ベンジルカルバマート、1-メチルシクロブチルカルバマート、1-メチルシクロヘキシルカルバマート、1-メチル-1-シクロプロピルメチルカルバマート、1-メチル-1-(3,5-ジメトキシフェニル)エチルカルバマート、1-メチル-1-(p-フェニルアゾフェニル)エチルカルバマート、1-メチル-1-フェニルエチルカルバマート、1-メチル-1-(4-ピリジル)エチルカルバマート、フェニルカルバマート、p-(フェニルアゾ)ベンジルカルバマート、2,4,6-トリ-t-ブチルフェニルカルバマート、4-(トリメチルアンモニウム)ベンジルカルバマート、および2,4,6-トリメチルベンジルカルバマートを包含する。
スルホンアミド基(例として、-S(=O)2Raa)などの窒素保護基は、これらに限定されないが、p-トルエンスルホンアミド(Ts)、ベンゼンスルホンアミド、2,3,6-トリメチル-4-メトキシベンゼンスルホンアミド(Mtr)、2,4,6-トリメトキシベンゼンスルホンアミド(Mtb)、2,6-ジメチル-4-メトキシベンゼンスルホンアミド(Pme)、2,3,5,6-テトラメチル-4-メトキシベンゼンスルホンアミド(Mte)、4-メトキシベンゼンスルホンアミド(Mbs)、2,4,6-トリメチルベンゼンスルホンアミド(Mts)、2,6-ジメトキシ-4-メチルベンゼンスルホンアミド(iMds)、2,2,5,7,8-ペンタメチルクロマン-6-スルホンアミド(Pmc)、メタンスルホンアミド(Ms)、β-トリメチルシリルエタンスルホンアミド(SES)、9-アントラセンスルホンアミド、4-(4',8'-ジメトキシナフチルメチル)ベンゼンスルホンアミド(DNMBS)、ベンジルスルホンアミド、トリフルオロメチルスルホンアミド、およびフェナシルスルホンアミドを包含する。
他の窒素保護基は、これらに限定されないが、フェノチアジニル-(10)-アシル誘導体、N'-p-トルエンスルホニルアミノアシル誘導体、N'-フェニルアミノチオアシル誘導体、N-ベンゾイルフェニルアラニル誘導体、N-アセチルメチオニン誘導体、4,5-ジフェニル-3--オキサゾリン2-オン、N-フタルイミド、N-ジチアスクシンイミド(Dts)、N-2,3-ジフェニルマレイミド、N-2,5-ジメチルピロール、N-1,1,4,4-テトラメチルジシリルアザシクロペンタン付加体(STABASE)、5-置換1,3-ジメチル-1,3,5-トリアザシクロヘキサン-2-オン、5-置換1,3-ジベンジル-1,3,5-トリアザシクロヘキサン-2-オン、1-置換3,5-ジニトロ-4-ピリドン、N-メチルアミン、N-アリルアミン、N-[2-(トリメチルシリル)エトキシ]メチルアミン(SEM)、N-3-アセトキシプロピルアミン、N-(1-イソプロピル-4-ニトロ-2-オキソ-3-ピロリン-3-イル)アミン、四級アンモニウム塩、N-ベンジルアミン、N-ジ(4-メトキシフェニル)メチルアミン、N-5-ジベンゾスベリルアミン、N-トリフェニルメチルアミン(Tr)、N-[(4-メトキシフェニル)ジフェニルメチル]アミン(MMTr)、N-9-フェニルフルオレニルアミン(PhF)、N-2,7-ジクロロ-9-フルオレニルメチレンアミン、N-フェロセニルメチルアミノ(Fcm)、N-2-ピコリルアミノN'-オキシド、N-1,1-ジメチルチオメチレンアミン、N-ベンジリデンアミン、N-p-メトキシベンジリデンアミン、N-ジフェニルメチレンアミン、N-[(2-ピリジル)メシチル]メチレンアミン、N-(N',N'-ジメチルアミノメチレン)アミン、N,N'-イソプロピリデンジアミン、N-p-ニトロベンジリデンアミン、N-サリチリデンアミン、N-5-クロロサリチリデンアミン、N-(5-クロロ-2-ヒドロキシフェニル)フェニルメチレンアミン、N-シクロヘキシリデンアミン、N-(5,5-ジメチル-3-オキソ-1-シクロヘキセニル)アミン、N-ボラン誘導体、N-ジフェニルボリン酸誘導体、N-[フェニル(ペンタアシルクロム-またはタングステン)アシル]アミン、N-銅キレート、N-亜鉛キレート、N-ニトロアミン、N-ニトロソアミン、アミンN-オキシド、ジフェニルホスフィンアミド(Dpp)、ジメチルチオホスフィンアミド(Mpt)、ジフェニルチオホスフィンアミド(Ppt)、ジアルキルホスホロアミダート、ジベンジルホスホロアミダート、ジフェニルホスホロアミダート、ベンゼンスルフェンアミド、o-ニトロベンゼンスルフェンアミド(Nps)、2,4-ジニトロベンゼンスルフェンアミド、ペンタクロロベンゼンスルフェンアミド、2-ニトロ-4-メトキシベンゼンスルフェンアミド、トリフェニルメチルスルフェンアミド、および3-ニトロピリジンスルフェンアミド(Npys)を包含する。ある態様において、窒素保護基は、ベンジル(Bn)、tert-ブチルオキシカルボニル(BOC)、カルボベンジルオキシ(Cbz)、9-フルオレニルメチルオキシカルボニル(Fmoc)、トリフルオロアセチル、トリフェニルメチル、アセチル(Ac)、ベンゾイル(Bz)、p-メトキシベンジル(PMB)、3,4-ジメトキシベンジル(DMPM)、p-メトキシフェニル(PMP)、2,2,2-トリクロロエチルオキシカルボニル(Troc)、トリフェニルメチル(Tr)、トシル(Ts)、ブロシル(Bs)、ノシル(Ns)、メシル(Ms)、トリフリル(Tf)、またはダンシル(Ds)である。
ある態様において、酸素原子上に存在する置換基は、酸素保護基である(また本明細書中「ヒドロキシル保護基」とも称される)。酸素保護基は、これらに限定されないが、-Raa、-N(Rbb)2、-C(=O)SRaa、-C(=O)Raa、-CO2Raa、-C(=O)N(Rbb)2、-C(=NRbb)Raa、-C(=NRbb)ORaa、-C(=NRbb)N(Rbb)2、-S(=O)Raa、-SO2Raa、-Si(Raa)3、-P(Rcc)2、-P(Rcc)3
+X-、-P(ORcc)2、-P(ORcc)3
+X-、-P(=O)(Raa)2、-P(=O)(ORcc)2、および-P(=O)(N(Rbb)2)2を包含し、ここでX-、Raa、Rbb、およびRccは、本明細書に定義されるとおりである。酸素保護基は、当該技術分野において周知であり、Protecting Groups in Organic Synthesis,T.W.Greene and P.G.M.Wuts,3rd edition,John Wiley & Sons,1999(参照により本明細書に組み込まれる)において詳細に記載されるものを包含する。
例示の酸素保護基は、これらに限定されないが、メチル、メトキシルメチル(MOM)、メチルチオメチル(MTM)、t-ブチルチオメチル、(フェニルジメチルシリル)メトキシメチル(SMOM)、ベンジルオキシメチル(BOM)、p-メトキシベンジルオキシメチル(PMBM)、(4-メトキシフェノキシ)メチル(p-AOM)、グアイアコールメチル(GUM)、t-ブトキシメチル、4-ペンテニルオキシメチル(POM)、シロキシメチル、2-メトキシエトキシメチル(MEM)、2,2,2-トリクロロエトキシメチル、ビス(2-クロロエトキシ)メチル、2-(トリメチルシリル)エトキシメチル(SEMOR)、テトラヒドロピラニル(THP)、3-ブロモテトラヒドロピラニル、テトラヒドロチオピラニル、1-メトキシシクロヘキシル、4-メトキシテトラヒドロピラニル(MTHP)、4-メトキシテトラヒドロチオピラニル、4-メトキシテトラヒドロチオピラニルS,S-ジオキシド、1-[(2-クロロ-4-メチル)フェニル]-4-メトキシピペリジン-4-イル(CTMP)、1,4-ジオキサン-2-イル、テトラヒドロフラニル、テトラヒドロチオフラニル、2,3,3a,4,5,6,7,7a-オクタヒドロ-7,8,8-トリメチル-4,7-メタノベンゾフラン-2-イル、1-エトキシエチル、1-(2-クロロエトキシ)エチル、1-メチル-1-メトキシエチル、1-メチル-1-ベンジルオキシエチル、1-メチル-1-ベンジルオキシ-2-フルオロエチル、2,2,2-トリクロロエチル、2-トリメチルシリルエチル、2-(フェニルセレニル)エチル、t-ブチル、アリル、p-クロロフェニル、p-メトキシフェニル、2,4-ジニトロフェニル、ベンジル(Bn)、p-メトキシベンジル、3,4-ジメトキシベンジル、o-ニトロベンジル、p-ニトロベンジル、p-ハロベンジル、2,6-ジクロロベンジル、p-シアノベンジル、p-フェニルベンジル、2-ピコリル、4-ピコリル、3-メチル-2-ピコリルN-オキシド、ジフェニルメチル、p,p'-ジニトロベンズヒドリル、5-ジベンゾスベリル、トリフェニルメチル、α-ナフチルジフェニルメチル、p-メトキシフェニルジフェニルメチル、ジ(p-メトキシフェニル)フェニルメチル、トリ(p-メトキシフェニル)メチル、4-(4'-ブロモフェナシルオキシフェニル)ジフェニルメチル、4,4',4''-トリス(4,5-ジクロロフタルイミドフェニル)メチル、4,4',4''-トリス(レブリノイルオキシフェニル)メチル、4,4',4''-トリス(ベンゾイルオキシフェニル)メチル、3-(イミダゾール-1-イル)ビス(4',4''-ジメトキシフェニル)メチル、1,1-ビス(4-メトキシフェニル)-1'-ピレニルメチル、9-アントリル、9-(9-フェニル)キサンテニル、9-(9-フェニル-10-オキソ)アントリル、1,3-ベンゾジチオラン-2-イル、ベンズイソチアゾリルS,S-ジオキシド、トリメチルシリル(TMS)、トリエチルシリル(TES)、トリイソプロピルシリル(TIPS)、ジメチルイソプロピルシリル(IPDMS)、ジエチルイソプロピルシリル(DEIPS)、ジメチルテキシルシリル、t-ブチルジメチルシリル(TBDMS)、t-ブチルジフェニルシリル(TBDPS)、トリベンジルシリル、トリ-p-キシリルシリル、トリフェニルシリル、ジフェニルメチルシリル(DPMS)、t-ブチルメトキシフェニルシリル(TBMPS)、ホルマート、ベンゾイルホルマート、アセタート、クロロアセタート、ジクロロアセタート、トリクロロアセタート、トリフルオロアセタート、メトキシアセタート、トリフェニルメトキシアセタート、フェノキシアセタート、p-クロロフェノキシアセタート、3-フェニルプロピオナート、4-オキソペンタノアート(レブリナート)、4,4-(エチレンジチオ)ペンタノアート(レブリノイルジチオアセタール)、ピバロアート、アダマントアート(adamantoate)、クロトナート、4-メトキシクロトナート、ベンゾアート、p-フェニルベンゾアート、2,4,6-トリメチルベンゾアート(メシトアート)、炭酸メチル、9-フルオレニルメチルカーボネート(Fmoc)、炭酸エチル、2,2,2-トリクロロエチルカーボネート(Troc)、2-(トリメチルシリル)エチルカーボネート(TMSEC)、2-(フェニルスルホニル)エチルカーボネート(Psec)、2-(トリフェニルホスホニオ)エチルカーボネート(Peoc)、イソブチルカーボネート、ビニルカーボネート、アリルカーボネート、t-ブチルカーボネート(BOCまたはBoc)、p-ニトロフェニルカーボネート、ベンジルカーボネート、p-メトキシベンジルカーボネート、3,4-ジメトキシベンジルカーボネート、o-ニトロベンジルカーボネート、p-ニトロベンジルカーボネート、S-ベンジルチオカーボネート、4-エトキシ-1-ナフトチル(napththyl)カーボネート、メチルジチオカーボネート、2-ヨードベンゾアート、4-アジドブチラート、4-ニトロ-4-メチルペンタノアート、o-(ジブロモメチル)ベンゾアート、2-ホルミルベンゼンスルホナート、2-(メチルチオメトキシ)エチル、4-(メチルチオメトキシ)ブチラート、2-(メチルチオメトキシメチル)ベンゾアート、2,6-ジクロロ-4-メチルフェノキシアセタート、2,6-ジクロロ-4-(1,1,3,3-テトラメチルブチル)フェノキシアセタート、2,4-ビス(1,1-ジメチルプロピル)フェノキシアセタート、クロロジフェニルアセタート、イソブチラート、モノスクシノアート、(E)-2-メチル-2-ブテノアート、o-(メトキシアシル)ベンゾアート、α-ナフトエアート、ニトラート、アルキルN,N,N',N'-テトラメチルホスホロジアミダート、アルキルN-フェニルカルバマート、ボラート、ジメチルホスフィノチオイル、アルキル2,4-ジニトロフェニルスルフェナート、スルファート、メタンスルホナート(メシラート)、ベンジルスルホナート、およびトシラート(Ts)を包含する。ある態様において、酸素保護基は、シリルである。ある態様において、酸素保護基は、t-ブチルジフェニルシリル(TBDPS)、t-ブチルジメチルシリル(TBDMS)、トリイソプロイルシリル(TIPS)、トリフェニルシリル(TPS)、トリエチルシリル(TES)、トリメチルシリル(TMS)、トリイソプロピルシロキシメチル(TOM)、アセチル(Ac)、ベンゾイル(Bz)、アリルカーボネート、2,2,2-トリクロロエチルカーボネート(Troc)、2-トリメチルシリルエチルカーボネート、メトキシメチル(MOM)、1-エトキシエチル(EE)、2-メチオキシ-2-プロピル(MOP)、2,2,2-トリクロロエトキシエチル、2-メトキシエトキシメチル(MEM)、2-トリメチルシリルエトキシメチル(SEM)、メチルチオメチル(MTM)、テトラヒドロピラニル(THP)、テトラヒドロフラニル(THF)、p-メトキシフェニル(PMP)、トリフェニルメチル(Tr)、メトキシトリチル(MMT)、ジメトキシトリチル(DMT)、アリル、p-メトキシベンジル(PMB)、t-ブチル、ベンジル(Bn)、アリル、またはピバロイル(Piv)である。
ある態様において、硫黄原子上に存在する置換基は、硫黄保護基である(また「チオール保護基」とも称される)。硫黄保護基は、これらに限定されないが、-Raa、-N(Rbb)2、-C(=O)SRaa、-C(=O)Raa、-CO2Raa、-C(=O)N(Rbb)2、-C(=NRbb)Raa、-C(=NRbb)ORaa、-C(=NRbb)N(Rbb)2、-S(=O)Raa、-SO2Raa、-Si(Raa)3、-P(Rcc)2、-P(Rcc)3
+X-、-P(ORcc)2、-P(ORcc)3
+X-、-P(=O)(Raa)2、-P(=O)(ORcc)2、および-P(=O)(N(Rbb)2)2を包含し、ここでRaa、Rbb、およびRccは、本明細書に定義されるとおりである。硫黄保護基は、当該技術分野において周知であり、Protecting Groups in Organic Synthesis,T.W.Greene and P.G.M.Wuts,3rd edition,John Wiley & Sons,1999(参照により本明細書に組み込まれる)において詳細に記載されるものを包含する。ある態様において、硫黄保護基は、アセトアミドメチル、t-Bu、3-ニトロ-2-ピリジンスルフェニル、2-ピリジン-スルフェニル、またはトリフェニルメチルである。
「対イオン」または「アニオン性対イオン」は、電子的中性を維持するために、正に荷電した基と結び付けられた負に荷電した基である。アニオン性対イオンは、一価であってもよい(すなわち、負の形式電荷を1個包含する)。アニオン性対イオンはまた、二価または三価などの多価であってもよい(すなわち、負の形式電荷を1個以上包含する)。例示の対イオンは、ハロゲン化物イオン(例として、F-、Cl-、Br-、I-)、NO3
-、ClO4
-、OH-、H2PO4
-、HCO3
-、HSO4
-、スルホン酸イオン(例として、メタンスルホン酸、トリフルオロメタンスルホン酸、p-トルエンスルホン酸、ベンゼンスルホン酸、10-カンファ-スルホン酸、ナフタレン-2-スルホン酸、ナフタレン-1-スルホン酸-5-スルホン酸、エタン-1-スルホン酸-2-スルホン酸等)、カルボン酸イオン(例として、酢酸、プロパン酸、安息香酸、グリセリン酸、乳酸、酒石酸、グリコール酸、グリコン酸等)、BF4
-、PF4
-、PF6
-、AsF6
-、SbF6
-、B[3,5-(CF3)2C6H3]4]-、B(C6F5)4
-、BPh4
-、Al(OC(CF3)3)4
-、およびカルボランアニオン(例として、CB11H12
-または(HCB11Me5Br6)-)を包含する。多価であってもよい例示の対イオンは、CO3
2-、HPO4
2-、PO4
3-、B4O7
2-、SO4
2-、S2O3
2-、カルボン酸アニオン(例として、酒石酸、クエン酸、フマル酸、マレイン酸、リンゴ酸、マロン酸、グリコン酸、コハク酸、グルタル酸、アジピン酸、ピメリン酸、スベリン酸、アゼライン酸、セバシン酸、サリチル酸、フタル酸、アスパラギン酸、グルタミン酸等)、およびカルボランを包含する。
これらの例示置換基および他の例示置換基は、詳細な記載、例、およびクレームにおいてより詳細に記載されている。本発明は、形はどうあれ、置換基の上の例示列挙によって限定されることは意図しない。
他の定義
以下の定義は、本出願を通してずっと使用されるより一般的な用語である。
以下の定義は、本出願を通してずっと使用されるより一般的な用語である。
本明細書に使用されるとき、用語「塩」は、ありとあらゆる塩を指し、かつ薬学的に許容し得る塩を網羅する。
用語「薬学的に許容し得る塩」は、正当な医学的見識の範囲内において、ヒトおよび/または動物の組織との接触における使用に好適であって、過度の毒性、刺激、アレルギー性応答等がなく、妥当なベネフィット/リスク比に見合った塩を指す。薬学的に許容し得る塩は、当該技術分野において周知である。例えば、Bergeらは薬学的に許容し得る塩を詳細にJ.Pharmaceutical Sciences,1977,66,1-19(参照により本明細書に組み込まれる)に記載している。本開示の化合物の薬学的に許容し得る塩は、好適な無機および有機の酸ならびに塩基に由来するものを包含する。薬学的に許容し得る無毒な酸付加塩の例は、無機酸(塩酸、臭化水素酸、リン酸、硫酸、および過塩素酸など)で、または有機酸(酢酸、シュウ酸、マレイン酸、酒石酸、クエン酸、コハク酸、またはマロン酸)で、または当該技術分野において知られている他の方法(イオン交換など)を使用することによって、形成されるアミノ基の塩である。他の薬学的に許容し得る塩は、アジピン酸塩、アルギン酸塩、アスコルビン酸塩、アスパラギン酸塩、ベンゼンスルホン酸塩、安息香酸塩、重硫酸塩、ホウ酸塩、酪酸塩、しょうのう酸塩、カンファースルホン酸塩、クエン酸塩、シクロペンタンプロピオン酸塩、二グルコン酸塩、ドデシル硫酸塩、エタンスルホン酸塩、ギ酸塩、フマル酸塩、グルコヘプトン酸塩、グリセロリン酸塩、グルコン酸塩、ヘミ硫酸塩、ヘプタン酸塩、ヘキサン酸塩、ヨウ化水素塩、2-ヒドロキシ-エタンスルホン酸塩、ラクトビオン酸塩、乳酸塩、ラウリン酸塩、ラウリル硫酸塩、リンゴ酸塩、マレイン酸塩、マロン酸塩、メタンスルホン酸塩、2-ナフタレンスルホン酸塩、ニコチン酸塩、硝酸塩、オレイン酸塩、シュウ酸塩、パルミチン酸塩、パモ酸塩、ペクチニン酸塩、過硫酸塩、3-フェニルプロピオン酸塩、リン酸塩、ピクリン酸塩、ピバル酸塩、プロピオン酸塩、ステアリン酸塩、コハク酸塩、硫酸塩、酒石酸塩、チオシアン酸塩、p-トルエンスルホン酸塩、ウンデカン酸塩、吉草酸塩等を包含する。適切な塩基に由来する塩は、アルカリ金属、アルカリ土類金属、アンモニウム、およびN+(C1~4アルキル)4
-塩を包含する。代表的なアルカリまたはアルカリ土類金属の塩は、ナトリウム、リチウム、カリウム、カルシウム、マグネシウム等を包含する。さらなる薬学的に許容し得る塩は、適切な場合、無毒のアンモニウム、四級アンモニウム、および対イオン(ハロゲン化物、水酸化物、カルボン酸、硫酸、リン酸、硝酸、低級アルキルスルホン酸、およびアリールスルホン酸など)を使用して形成されたアミンカチオンを包含する。
用語「溶媒和物」は、通常ソルボリシス反応によって、溶媒と結び付いた化合物またはその塩の形態を指す。この物理的な結び付きは、水素結合を包含してもよい。従来の溶媒は、水、メタノール、エタノール、酢酸、DMSO、THF、ジエチルエーテル等を包含する。本明細書に記載の化合物は、例として結晶形態で調製されてもよく、溶媒和されてもよい。好適な溶媒和物は、薬学的に許容し得る溶媒和物を包含し、さらに、化学量論的な溶媒和物および非化学量論的な溶媒和物の両方を包含する。ある実例において、溶媒和物は、例えば1個以上の溶媒分子が、結晶固体の結晶格子中に組み込まれるときに、単離できるであろう。「溶媒和物」は、溶液相と単離可能な溶媒和物との両方を網羅する。代表的な溶媒和物は、水和物、エタノラート、およびメタノラートを包含する。
用語「水和物」は、水分子と結び付いた化合物を指す。典型的には、化合物の水和物中に含有される水分子数が、水和物中の化合物分子数に対して一定の比である。したがって、化合物の水和物は、例えば一般的式R・xH2O(ここでRは、化合物であり、xは、0より大きい数である)によって表されてもよい。所定の化合物は、1より多いタイプの水和物を形成してもよく、例として、一水和物(xは、1である)、低級水和物(xは、0より大きくかつ1より小さい数であり、例として、ヘミ水和物(R・0.5H2O))、および多水和物(xは、1より大きい数であり、例として、二水和物(R・2H2O)および六水和物(R・6H2O))包含する。
用語「互変異性体」または「互変異性体の」は、水素原子の少なくとも1つのホルマール移動と原子価の少なくとも1つの変化(例として、単結合~二重結合、三重結合~単結合、または逆も同様)との結果として生じる、2以上の相互転換できる化合物を指す。互変異性体の厳密な比率は、温度、溶媒、およびpHを包含する数種の因子に依存する。互変異性体化(すなわち、互変異性体の対を提供する反応)は、酸または塩基によって触媒されることもある。例示の互変異性体化は、ケト~エノール、アミド~イミド、ラクタム~ラクチム、エナミン~イミン、およびエナミン~(異なるエナミン)の互変異性体化を包含する。
同じ分子式を有するが、それらの原子の結合の性質もしくは順序、または空間中のそれらの原子の配置が異なる化合物は、「異性体」と呼ばれることもまた理解されるであろう。空間中のそれらの原子の配置が異なる異性体は、「立体異性体」と呼ばれる。
相互の鏡像ではない立体異性体は、「ジアステレオマー」と呼ばれ、互いの重ね合わせ不可能な鏡像であるものは、「鏡像異性体」と呼ばれる。化合物が不斉中心を有する(例えば、それが4つの異なる基へ結合している)とき、一対のエナンチオマーが可能である。鏡像異性体は、その不斉中心の絶対立体配置によって特徴付けられ得、CahnおよびPrelogのRおよびS順位則によって、または分子が偏光面を回転させる様式によって、記載され、右旋性または左旋性として(すなわち、夫々(+)または(-)異性体として)指定される。キラル化合物は、個々の鏡像異性体またはその混合物のいずれかとして存在し得る。等しい割合の鏡像異性体を含有する混合物は、「ラセミ混合物」と呼称される。
用語「多形」は、化合物(またはその塩、水和物、もしくは溶媒和物)の結晶形態を指す。多くの化合物は、様々な異なる結晶形態(すなわち、異なる多形)を採用し得る。典型的には、かかる異なる結晶形態は、異なるX線回折パターン、赤外スペクトルを有するか、および/または、融点、密度、硬度、結晶形状、光学特性および電気特性、安定性、可溶性、ならびにバイオアベイラビリティなどの、いくつかの特性またはすべての特性の点で変動し得る。再結晶の溶媒、結晶化率、保管温度、および他の因子は、所定の調製物の中心となる1つの結晶形態をもたらすことがある。化合物の様々な多形は、異なる条件下の結晶化によって調製され得る。
用語「共結晶」は、少なくとも2つの構成要素から構成される結晶構造を指す。ある態様において、共結晶は、本開示の化合物と、これらに限定されないが、原子、イオン、分子、または溶媒分子を包含する1以上の他の構成要素(単数または複数)とを含有する。ある態様において、共結晶は、本開示の化合物および1以上の溶媒分子を含有する。ある態様において、共結晶は、本開示の化合物および1以上の酸または塩基を含有する。ある態様において、共結晶は、本開示の化合物と、該化合物に関する1以上の構成要素(これらに限定されないが、該化合物の異性体、互変異性体、塩、溶媒和物、水和物、合成前駆体、合成誘導体、フラグメント、または不純物)とを含有する。
用語「プロドラッグ」は、加溶媒分解によってかまたは生理学的条件下で除去されることで、in vivoで薬学的に活性のある本明細書に記載の化合物を提供する、切断可能な基を有する化合物を指す。かかる例は、これらに限定されないが、コリンエステル誘導体等、N-アルキルモルホリンエステル等を包含する。本明細書に記載の化合物の他の誘導体は、それらの酸および酸誘導体の両形態においては活性を有するが、酸感受性の形態においてはしばしば、哺乳類生物における可溶性、組織適合性、または遅延放出の利点を供与する(Bundgard,H.,Design of Prodrugs,pp.7-9,21-24,Elsevier,Amsterdam 1985を見よ)。プロドラッグは、親酸の好適なアルコールとの反応によって調製されるエステル、または親酸化合物の置換もしくは非置換のアミンとの反応によって調製されるアミド、または酸無水物、または混合された無水物などの、当業者に周知の酸誘導体を包含する。本明細書に記載の化合物上に吊り下げられた(pendant)酸性基に由来する、単純な脂肪族または芳香族のエステル、アミド、および無水物は、具体的なプロドラッグである。いくつかのケースにおいて、(アシルオキシ)アルキルエステルまたは((アルコキシカルボニル)オキシ)アルキルエステルなどの二重エステル型プロドラッグを調製することが所望される。本明細書に記載の化合物のC1~8アルキル、C2~8アルケニル、C2~8アルキニル、アリール、C7~12置換アリール、およびC7~12アリールアルキルエステルが、好ましいこともある。
用語「組成物」および「製剤」は、互換的に使用される。
投与が企図される「対象」は、ヒト(すなわち、いずれの年齢群の男性(male)または女性、例として、小児対象(例として、幼児、子ども、未成年)、または成人対象(例として、若年成人、中年成人、もしくは高齢成人))、あるいは非ヒト動物を指す。ある態様において、非ヒト動物は、哺乳動物(例として、霊長目の動物(例として、カニクイザルもしくは赤毛猿)、商業的に関係のある哺乳動物(例として、畜牛、ブタ、ウマ、ヒツジ、ヤギ、ネコ、もしくはイヌ)、または鳥類(例として、ニワトリ、アヒル、ガチョウ、もしくはシチメンチョウなどの、商業的に関係のある鳥類))である。ある態様において、非ヒト動物は、魚類、爬虫類、または両生類の動物である。非ヒト動物は、いずれの発生段階にもあるオスまたはメスであってもよい。非ヒト動物は、トランスジェニック動物または遺伝子学的に改変された動物であってもよい。用語「患者」は、疾患の処置を必要とするヒト対象を指す。対象はまた、植物であってもよい。ある態様において、植物は、陸生植物である。ある態様において、植物は、非維管束陸生植物である。ある態様において、植物は、維管束陸生植物である。ある態様において、植物は、種子植物である。ある態様において、植物は、栽培植物である。ある態様において、植物は、双子葉植物である。ある態様において、植物は、単子葉植物である。ある態様において、植物は、顕花植物である。いくつかの態様において、植物は、穀物用植物、例として、トウモロコシ(maize)、トウキビ(corn)、小麦、稲、燕麦、大麦、ライ麦、またはキビである。いくつかの態様において、植物は、マメ科植物、例として、豆(bean)植物、例として、大豆(soybean)植物である。いくつかの態様において、植物は、高木(tree)または低木(shrub)である。
用語「生体試料」は、組織試料(組織切片および組織の針生検など);細胞試料(例として、細胞学的塗抹標本(パップスメアもしくは血液塗抹標本(Pap or blood smears)または顕微解剖によって得られた細胞の試料など);生物全体という試料(酵母または細菌の試料など);あるいは細胞の画分、フラグメント、またはオルガネラ(細胞をライスして(lysing)その構成要素を遠心分離または別の方法によって分離することによって得られたものなど)を包含する、いずれの試料も指す。生体試料の他の例は、血液、血清、尿、精液、排泄物、脳脊髄液、間質液、粘液性の、涙液、汗、膿、生検組織(例として、外科生検または針生検によって得られたもの)、乳頭吸引物、乳、膣液、唾液、ぬぐい液(口腔内ぬぐい液など)、または第一(first)生体試料に由来する生体分子を含有するいずれの材料も包含する。
用語「投与する(施す)」、「投与すること(施すこと)」、または「投与(施し)」は、本明細書に記載の化合物もしくはその医薬組成物を、対象中または対象上に、インプラントすること、吸収させること、摂取させること、注射すること、吸入させること、あるいは別の方法で導入することを指す。
用語「処置」、「処置する」、および「処置すること」は、本明細書に記載の疾患を食い止めること、緩和すること、その発病を遅延させること、またはその進行を阻害することを指す。いくつかの態様において、処置は、疾患の1以上の兆候もしくは症状が発症した後または観察された後に、施されてもよい。他の態様において、処置は、疾患の兆候または症状の非存在下で施されてもよい。例えば、処置は、症状の発病に先立って(例として、症状の既往に照らして)、罹患しやすい(susceptible)対象に施されてもよい。処置はまた、例えば、再発(recurrence)を遅延させるかおよび/または予防するために、症状が消散した後でも継続されてもよい。
用語「疾病」、「疾患」、および「障害」は、互換的に使用される。
本明細書に記載の化合物の「有効量」は、所望される生物学的な応答を惹起するのに充分な量を指す。本明細書に記載の化合物の有効量は、所望される生物学的なエンドポイント、化合物の薬物動態、処置される疾病、投与モード、ならびに対象の齢(age)および健康状態などの因子に応じて変動してもよい。ある態様において、有効量は、治療的に有効な量である。ある態様において、有効量は、予防的な処置である。例えば、がんを処置することにおいて、有効量の本発明の組成物は、腫瘍の再成長を予防、腫瘍負荷を低減、または腫瘍の成長もしくは広がりを停止することもある。ある態様において、有効量は、単回用量における本明細書に記載の化合物の量である。ある態様において、有効量は、複数回用量における本明細書に記載の化合物の合わせた量である。
本明細書に記載の化合物の「治療的に有効な量」は、疾病の処置の点で治療ベネフィットを提供するのに、または疾病と関連する1以上の症状を遅延もしくは最小化するのに、充分な量である。化合物の治療的な有効な量は、治療剤単独での量、または他の治療と組み合わせた治療剤の量を意味し、この量は、状態の処置の点で治療ベネフィットを提供する。用語「治療的に有効な量」は、治療を全面的に改善する量、状態の症状、もしくは原因を減少または回避する量、および/または別の治療剤の治療有効性を増強する量を網羅し得る。ある態様において、治療的に有効な量は、HDAC6阻害(例として、HDAC6活性の少なくとも5%、少なくとも10%、少なくとも20%、少なくとも30%、少なくとも40%、少なくとも50%、少なくとも60%、少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、または少なくとも99%阻害)に充分な量である。ある態様において、治療的に有効な量は、疾患または障害(例として、神経学的障害、がん)を処置するのに充分な量である。ある態様において、治療的に有効な量は、HDAC6の阻害に、および疾患または障害(例として、神経学的障害、がん)を処置するのに充分な量である。
明細書に記載の化合物の「予防的に有効な量」は、疾病、もしくは疾病と関連する1以上の兆候または症状を予防するのに、あるいはその再発(recurrence)を予防するのに、充分な量である。化合物の予防的に有効な量は、治療剤単独での量、または他の剤と組み合わせた治療剤の量を意味し、この量は、疾病の予防の点で予防的ベネフィットを提供する。用語「予防的に有効な量」は、予防法を全面的に改善する量、または別の予防的な剤の予防的な有効性を増強する量を網羅し得る。ある態様において、予防的に有効な量は、HDAC6阻害に充分な量である。ある態様において、予防的に有効な量は、疾患または障害(例として、神経学的障害、がん)を処置するのに充分な量である。ある態様において、予防的に有効な量は、HDAC6の阻害に、および疾患または障害(例として、神経学的障害、がん)を処置するのに充分な量である。
本明細書に使用されるとき、用語「阻害する」または「阻害」は、酵素という文脈において、例えば、HDAC6の文脈において、酵素活性の低減を指す。いくつかの態様において、用語は、酵素活性、例として、HDAC6活性のレベルの、当初レベル(これは、例えば、酵素活性のベースラインレベルであってもよい)より統計的に有意に低いレベルへの低減を指す。いくつかの態様において、用語は、酵素活性、例として、HDAC6活性のレベルの、当初レベル(これは、例えば、酵素活性のベースラインレベルであってもよい)の75%未満、50%未満、40%未満、30%未満、25%未満、20%未満、10%未満、9%未満、8%未満、7%未満、6%未満、5%未満、4%未満、3%未満、2%未満、1%未満、0.5%未満、0.1%未満、0.01%未満、0.001%未満、または0.0001%未満であるレベルへの低減を指す。
「増殖性疾患」は、細胞の倍増による正常でない成長または伸展が原因で生起する疾患を指す(Walker,Cambridge Dictionary of Biology;Cambridge University Press:Cambridge,UK,1990)。増殖性疾患は、1)正常には静止期の細胞の、病的な増殖;2)それらの正常な所在からの細胞の病的な移動(例として、新生物性細胞の転移);3)マトリックスメタロプロテイナーゼなどのタンパク質分解酵素(例として、コラゲナーゼ、ゼラチナーゼ、およびエラスターゼ)の病的な発現;または4)増殖性網膜症および腫瘍転移に見られるような病的な血管新生、と関連し得る。例示の増殖性疾患は、がん(すなわち、「悪性新生物」)、良性新生物、血管新生または血管新生に関連する疾患、炎症性疾患、自己炎症性疾患、および自己免疫疾患を包含する。
用語「新生物」および「腫瘍」は本明細書中互換的に使用され、組織の正常でない塊を指し、ここで塊の成長は、正常な組織の成長を上回り、正常な組織の成長と調和しない。新生物または腫瘍は、以下の特徴:細胞分化の程度(モルホロジーおよび機能性を包含する)、成長の速度、局所浸潤、および転移、に依存して「良性」であってもまたは「悪性」であってもよい。「良性新生物」は、一般に十分に分化しており、特徴として悪性新生物よりも低速の成長を有し、元の部位に局在したままである。加えて、良性新生物は、浸潤、侵襲、または遠隔部位へ転移する性質を有さない。例示的な良性新生物は、これらに限定されないが、脂肪腫、軟骨腫、アデノーマ、アクロコルドン、老人性血管腫、脂漏性角化症、黒子、および脂腺増殖症を包含する。いくつかのケースにおいて、ある「良性」腫瘍は、後に、悪性新生物を生じさせ得、これは腫瘍の新生物性細胞の部分集団中の追加の遺伝子変化からもたらされ得、これらの腫瘍は「前悪性新生物」と言及される。前悪性新生物の例は、テラトーマである。対照的に「悪性新生物」は、一般に不十分に分化しており(退形成)、特徴として進行性の浸潤、侵襲、および周辺組織の破壊を伴う急速な成長を有する。しかも、悪性新生物は一般に、遠隔部位へ転移する性質を有する。
用語「転移」、「転移性(の)」、または「転移する」は、原発性のまたは元の腫瘍から別の臓器または組織へのがん性細胞の拡散または移動を指し、典型的には、二次性(転移性)腫瘍が在る臓器または組織のものではなく、原発性のまたは元の腫瘍の組織型の「二次性腫瘍」または「二次性細胞塊」の存在によって同定可能である。例えば、骨へ移動した前立腺がんは、転移性前立腺がんと言われ、骨組織中で成長するがん性前立腺がん細胞を包含する。
用語「がん」は悪性新生物を指す(Stedman's Medical Dictionary,25th ed.;Hensyl ed.;Williams & Wilkins:Philadelphia,1990)。例示のがんは、これらに限定されないが、聴神経腫;腺癌;副腎のがん;肛門がん;血管肉腫(例として、リンパ管肉腫、リンパ管内皮性肉腫、血管肉腫);虫垂がん;良性単一クローン性免疫グロブリン血症;胆管がん(例として、胆管癌);膀胱がん;乳房がん(breast cancer)(例として、乳房の腺癌、乳房の乳頭癌、乳がん(mammary cancer)、乳房の髄様癌;脳がん(例として、髄膜腫、神経膠芽腫、神経膠腫(例として、星状細胞腫、乏突起神経膠腫)、髄芽腫);気管支がん;カルチノイド腫瘍;子宮頚がん(例として、子宮頸部腺癌);絨毛癌;脊索腫;頭蓋咽頭腫;大腸がん(colorectal cancer)(例として、結腸(colon)がん、直腸(rectal)がん、結腸直腸腺癌);結合組織のがん;上皮癌;上衣腫;内皮性肉腫(例として、カポジ肉腫、多発性特発性出血性肉腫);子宮内膜がん(例として、子宮がん、子宮肉腫);食道がん(例として、食道の腺癌、バレット腺癌);ユーイング肉腫;眼がん(例として、眼内黒色腫、網膜芽細胞腫);家族性過好酸球増加症;胆嚢がん;胃部のがん(例として、胃腺癌);消化管間質腫瘍(GIST);胚細胞がん;頭頸部がん(例として、頭頸部扁平上皮癌、口腔がん(例として、口腔扁平上皮癌)、咽喉がん(例として、喉頭がん、咽頭がん、鼻咽頭がん、口腔咽頭がん));血液がん(例として、急性リンパ芽球性白血病(ALL)(例として、B細胞ALL、T細胞ALL)、急性骨髄性白血病(AML)(例として、B細胞AML、T細胞AML)、慢性骨髄性白血病(CML)(例として、B細胞CML、T細胞CML)、および慢性リンパ性白血病(CLL)(例として、B細胞CLL、T細胞CLL)などの白血病);ホジキンリンパ腫(HL)(例として、B細胞HL、T細胞HL)および非ホジキンリンパ腫(NHL)(例として、びまん性大細胞型B細胞性リンパ腫(DLBCL))、濾胞性リンパ腫、慢性リンパ球性白血病/小リンパ球性リンパ腫(CLL/SLL)、マントル細胞リンパ腫(MCL)、辺縁帯B細胞リンパ腫(例として、粘膜関連リンパ組織(MALT)リンパ腫、節性辺縁帯B細胞性リンパ腫、脾辺縁帯B細胞リンパ腫)、原発性縦隔B細胞リンパ腫、バーキットリンパ腫、リンパ形質細胞性リンパ腫(すなわち、ワルデンストレームマクログロブリン血症)、有毛細胞性白血病(HCL)、免疫芽球型大細胞性リンパ腫、前駆Bリンパ芽球性リンパ腫、および原発性中枢神経系(CNS)リンパ腫などのリンパ腫;および、前駆Tリンパ芽球性リンパ腫/白血病、末梢性T細胞リンパ腫(PTCL)(例として、皮膚T細胞リンパ腫(CTCL)(例として、菌状息肉症、セザリー症候群)、血管免疫芽球性T細胞リンパ腫、節外性ナチュラルキラーT細胞リンパ腫、腸管症型T細胞リンパ腫、皮下蜂窩織炎様T細胞リンパ腫、および未分化大細胞性リンパ腫)などのT細胞NHL;上に記載の1以上の白血病/リンパ腫の混合物;および多発性骨髄腫、重鎖病(例として、アルファ鎖病、ガンマ鎖病、ミュー鎖病);血管芽腫;下咽頭がん;炎症性筋線維芽細胞腫瘍;免疫球性アミロイドーシス;腎臓がん(例として、腎芽細胞腫、別名ウィルムス腫瘍、腎細胞癌);肝臓がん(例として、肝細胞がん(HCC)、悪性肝細胞癌);肺がん(例として、気管支癌、小細胞肺がん(SCLC)、非小細胞肺がん(NSCLC)、肺の腺癌)平滑筋肉腫(LMS);肥満細胞症(例として、全身性肥満細胞症);筋肉のがん;骨髄異形成症候群(MDS);中皮腫;骨髄増殖性疾患(MPD)(例として、真性多血症(PV)、本態性血小板増加症(ET)、特発性骨髄様化生(AMM)、別名骨髄線維症(MF)、慢性特発性骨髄線維症、慢性骨髄性白血病(CML)、慢性好中球性白血病(CNL)、好酸球増多症候群(HES));神経芽細胞腫;神経線維腫(例として、神経線維腫症(NF)1または2型、神経鞘腫症);神経内分泌癌(例として、胃腸すい管神経内分泌腫瘍(GEP-NET)、カルチノイド腫瘍);骨肉腫(例として、骨のがん);卵巣がん(例として、嚢胞腺癌、卵巣胎児性癌、卵巣腺癌);乳頭腺癌;膵臓がん(例として、膵臓腺癌、管内乳頭粘液性腫瘍(IPMN)、膵島細胞腫瘍);陰茎がん(例として、陰茎と陰嚢のパジェット病);松果体腫;原始神経外胚葉性腫瘍(PNT);形質細胞新生物;腫瘍随伴症候群;上皮内新生物;前立腺がん(例として、前立腺腺癌);直腸がん;横紋筋肉腫;唾液腺のがん;皮膚がん(例として、扁平上皮癌(SCC)、角化棘細胞腫(KA)、黒色腫、基底細胞癌(BCC));小腸がん(例として、虫垂がん);軟部組織肉腫(例として、悪性線維性組織球腫(MFH)、脂肪肉腫、悪性末梢神経鞘腫瘍(MPNST)、軟骨肉腫、線維肉腫、粘液肉腫);皮脂腺癌;小腸がん;汗腺癌;滑膜腫;精巣がん(例として、精上皮腫、精巣胚性癌腫);甲状腺がん(例として、甲状腺の乳頭癌、甲状腺乳頭癌(PTC)、甲状腺髄様がん);尿道がん;膣のがん;および外陰がん(例として、外陰部パジェット病)を包含する。
用語「免疫治療」は、免疫応答を誘導、増強、または抑制することによって疾患の処置を促進する治療剤を指す。免疫応答を惹起または増幅するよう設計された免疫療法が、活性化免疫療法として分類される一方、低減または抑制する免疫療法は、抑制免疫療法として分類される。免疫療法は、例外もあるが典型的には、生物学的治療剤(biotherapeutic agents)である。無数の免疫療法が、がんを処置するのに使用されている。これらは、これらに限定されないが、モノクローナル抗体、養子細胞移入、サイトカイン、ケモカイン、ワクチン、および小分子インヒビターを包含する。
用語「生物製剤(biologic)」、「生物学的薬物(biologic drug)」、および「生物学的製品(biological product)」は、ワクチン、血液および血液構成要素、アレルゲン(allergenics)、体細胞、遺伝子治療、組織、核酸、ならびにタンパク質などの広範な生成物を指す。生物製剤は、糖、タンパク質、もしくは核酸、またはこれら物質の複雑な組み合わせを包含していてもよく、あるいは細胞および組織などの生命体(living entities)であってもよい。生物製剤は、様々な天然の供給源(例として、ヒト、動物、微生物)から単離されたものであってもよく、生物工学的な(biotechnological)方法および他の技術によって産生されたものであってもよい。
用語「小分子」または「小分子治療薬(small molecule therapeutic)」は、天然に存在するかまたは人工的に(例として、化学合成を介して)創出されたかにかかわらず、相対的に低分子量を有する分子を指す。典型的には、小分子は、有機化合物である(すなわち、これは炭素を含有する)。小分子は、複数の炭素-炭素結合、立体中心、および他の官能基(例として、アミン、ヒドロキシル、カルボニル、および複素環式の環等々)を含有していてもよい。ある態様において、小分子の分子量は、約1,000g/mol以下、約900g/mol以下、約800g/mol以下、約700g/mol以下、約600g/mol以下、約500g/mol以下、約400g/mol以下、約300g/mol以下、約200g/mol以下、または約100g/mol以下である。ある態様において、小分子の分子量は、少なくとも約100g/mol、少なくとも約200g/mol、少なくとも約300g/mol、少なくとも約400g/mol、少なくとも約500g/mol、少なくとも約600g/mol、少なくとも約700g/mol、少なくとも約800g/mol、または少なくとも約900g/mol、または少なくとも約1,000g/molである。上の範囲の組み合わせ(例として、少なくとも約200g/molおよび約500g/mol以下)もまた、あり得る。ある態様において、小分子は、薬物(例として、連邦規則集(C.F.R.)に規定されるとおり米国食品医薬品局によって承認された分子)などの治療的に活性がある剤である。小分子はまた、1以上の金属原子および/または金属イオンとも複合体化されていてよい。この場合において、小分子はまた、「有機金属小分子」とも称される。好ましい小分子は、動物、好ましくは哺乳動物、より好ましくはヒトにおいて生物学的効果を産生するという点で、生物学的に活性がある。小分子は、これらに限定されないが、放射性核種および造影剤を包含する。ある態様において、小分子は、薬物である。好ましくは、必ずしもそうではないが、薬物は、適切な政府機関もしくは規制機関によってヒトまたは動物における使用に安全かつ有効であると既に見なされているものである。例えば、ヒトへの使用が承認された薬物は、21 C.F.R.§§330.5、331~361および440~460(参照により本明細書に組み込まれる)の下、FDAによって列挙されている;獣医学的使用のための薬物は、21 C.F.R.§§500~589(参照により本明細書に組み込まれる)の下、FDAによって列挙されている。列挙されたすべての薬物は、本発明に従う使用に許容し得るものと見なされる。
用語「治療剤」は、所望される大抵は有益な効果を産生する治療特性を有するいずれの物質も指す。例えば、治療剤は、疾患を処置、改善(ameliorate)、および/または予防し得る。治療剤は、本明細書に開示のとおり、生物製剤もしくは小分子治療薬、またはそれらの組み合わせであってもよい。
用語「化学療法剤」は、がんへの化学療法において使用されることが知られている治療剤を指す。
「血液がん」は、造血細胞または組織を侵すがんを包含する。血液がんは、異常な血液学的内容物および/または機能に関連するがんを包含する。血液がんの例は、これらに限定されないが、白血病、たとえば、急性リンパ球性白血病(ALL)(例として、B細胞ALL、T細胞ALL)、急性骨髄球性白血病(AML)(例として、B細胞AML、T細胞AML)、慢性骨髄球性白血病(CML)(例として、B細胞CML、T細胞CML)、慢性リンパ球性白血病(CLL)(例として、B細胞CLL、T細胞CLL))、リンパ腫、たとえば、ホジキンリンパ腫(HL)(例として、B細胞HL、T細胞HL)、非ホジキンリンパ腫(NHL)(例として、びまん性大細胞型B細胞リンパ腫(DLBCL))、濾胞性リンパ腫、慢性リンパ球性白血病/小リンパ球性リンパ腫(CLL/SLL)、マントル細胞リンパ腫(MCL)、辺縁帯B細胞リンパ腫(例として、粘膜内リンパ組織(MALT)リンパ腫、筋性辺縁帯B細胞リンパ腫、脾臓周辺帯B細胞リンパ腫)、原発性縦隔B細胞リンパ腫、バーキットリンパ腫、リンパ形質細胞性リンパ腫(すなわち、ワルデンストレームのマクログロブリン血症)、有毛細胞白血病(HCL)、免疫芽球性大細胞型リンパ腫、前駆体Bリンパ芽球性リンパ腫、原発性中枢神経系(CNS)リンパ腫、T細胞NHL、たとえば、前駆体Tリンパ芽球性リンパ腫/白血病、末梢T細胞リンパ腫(PTCL)(例として、皮膚T細胞性リンパ腫(CTCL)(例として、菌状息肉症、セザリー症候群)、血管免疫芽球性T細胞リンパ腫、節外性ナチュラルキラーT細胞リンパ腫、腸管症型T細胞リンパ腫、皮下脂肪識炎様T細胞リンパ腫、および未分化大細胞リンパ腫)、上に記載のとおりの1以上の白血病/リンパ腫の混合型、多発性骨髄腫、重鎖病(例として、アルファ鎖病、ガンマ鎖病、ミュー鎖病)、急性非リンパ球性白血病(ANLL)、急性前骨髄球性白血病(APL)、急性骨髄単球性白血病(AMMoL)、真性赤血球増加症、ウィルムス腫瘍、およびユーイング肉腫を包含する。
用語「異種免疫疾患」は、外来性の抗原(例として、薬物、病原体)への免疫応答が免疫病理学的な変化をもたらす状態を指す。免疫応答は、異なる種からの抗原によって引き起こされ(異種免疫)、よってこれは、免疫応答に重きが置かれ、疾患を生じさせる外来種(感染性の病原体)ではないことから、感染性疾患とは異なる。
図面の簡単な記載
図1は、未分化のSH-SY5Y細胞におけるアセチルチューブリン、チューブリン、アセチルヒストンH3K9、およびヒストンH3に対する化合物34の効果を示すウェスタン免疫ブロットである。
図2Aは、オスC57BL/6マウスへの腹腔内投与後の例示化合物16、34、58、および75の血漿中の濃度を示すグラフである。図2Bは、オスC57BL/6マウスへの腹腔内投与後の例示化合物16、34、58、および75の脳組織中の濃度を示すグラフである。
図3Aは、シスプラチンで処置された初代ラット後根神経節(DRG)におけるin vitroでの神経変性に対する例示化合物の効果を示すグラフである。図3Bは、シスプラチンで処置された初代ラットDRGにおけるin vitroでの軸索面積に対する例示化合物の効果を示すグラフである。MedChem Expressから得られるACY-1083は、HDAC6選択的インヒビターとして公開されており、ベンチマークとして使用した。盲検の(Blinded)DMSOを追加の陰性対照として使用した。初代成体ラット後根神経節を、5μMの指し示された化合物および0.5mMシスプラチンで4日間共処置した。神経変性を、ベータチューブリン染色の蛍光画像化によって視覚化されたとおり面積あたりのブレブ(blebs)によって評価した。軸索面積もまた、ベータチューブリン染色の蛍光画像化によって評価した。図3Aは、16、173、またはACY-1083(盲検のDMSOも79もない)での処置が、シスプラチン存在下のビヒクルと比較して、面積あたりのブレブを減少させることを示す。図3Bは、16および79(盲検のDMSOもACY-1083も173もない)での処置が、シスプラチン存在下のビヒクルと比較して、軸索面積を増大することを示す。P値は、シスプラチン+ビヒクルと比較した、偽陽性率(FDR)多重比較補正ありの通常の一元配置(one-way)ANOVAによって決定した;標準誤差(SEM)ありの平均値を示す。* P<0.05、** P<0.01、*** P<0.001、**** P<0.0001。
図4A~Fは、化学療法誘発性の末梢神経障害(CIPN)マウスモデルにおける例示化合物16のin vivoでの効き目のデータを要約する一連のグラフである。MedChem Expressから得られるACY-1083は、HDAC6選択的インヒビターとして公開されており、ベンチマークとして使用した。オスC57BL/6マウスを、図4Aに指し示されるとおり、シスプラチンの存在下16またはACY-1083で共処置した。健康全般を生存率および体重によって評価した。機械的アロディニアをフォン・フライ(Von Frey)試験によって評価した。神経の完全性(integrity)を表皮内神経線維(IENF)密度によって評価した。図4Bは、ACY-1083ではなく16での処置が、シスプラチン存在下のビヒクルと比較して、生存率を救済したことを示すカプラン・マイヤーグラフである。
図4Cおよび4Dは、ACY-1083ではなく16での処置が、シスプラチン存在下のビヒクルと比較して、体重を増大したことを示すグラフである。
図4Eは、ACY-1083ではなく16での処置が、シスプラチン存在下のビヒクルと比較して、第16日にて機械的アロディニアを改善したことを示すグラフである。図4Fは、ACY-1083ではなく16での処置が、シスプラチン存在下のビヒクルと比較して、IENF密度を救済したことを示すグラフである。P値は、シスプラチン+ビヒクルと比較した、FDR多重比較補正ありの通常の一元配置ANOVA(カプラン・マイヤーを除く)によって決定した;SEMありの平均値を示す。* P<0.05、** P<0.01、*** P<0.001、**** P<0.0001。
図5A~Bは、ALS患者からの人工多能性幹細胞(iPSC)由来運動ニューロンにおけるin vitroでの軸索輸送およびチューブリンアセチル化に対する例示化合物の効果を要約する一連のグラフである。MedChem Expressから得られるACY-775は、HDAC6選択的インヒビターとして公開されており、ベンチマークとして使用した。盲検のDMSOを追加の陰性対照として使用した。FUSP525L突然変異をもつ患者からのiPSCおよび同質遺伝子対照系統を運動ニューロンへ分化させた。運動ニューロンを5μMの指し示された化合物で24時間処置した。軸索輸送を、MitoTracker Redによって視覚化されたとおり、ミトコンドリア輸送の生細胞画像化を使用して評価した。チューブリンアセチル化を、ウェスタンブロッティングを使用して測定した。図5Aは、58またはACY-775での処置がミトコンドリア運動(各条件につき(per condition)n=21神経突起)を野生型レベルまで回復させたこと(左)、ACY-775での処置がチューブリンアセチル化(各条件につきn=3ライセート(lysates))を増大させたこと(右)、58が傾向レベル(trend level)を増大させたことを示す2つのグラフである。図5Bは、173および79(盲検のDMSOではない)での処置が、ミトコンドリア運動(各条件につきn=28神経突起)を野生型レベルまで回復させたこと(左)、および増大したチューブリンアセチル化(各条件につきn=3ライセート)を増大させたこと(右)を示す2つのグラフである。P値は、ALS(P525L)と比較した、FDR多重比較補正ありの通常の一元配置ANOVAによって決定した;SEMありの平均値を示す。* P<0.05、** P<0.01、*** P<0.001、**** P<0.0001。
ある態様の詳細な記載
本明細書に提供されるのは、HDACインヒビター(例として、HDAC6インヒビター)である化合物である。本明細書に記載の化合物は、HDAC6の選択的阻害および/または血液脳関門の通過能などの有利な特性を保有し、これによって化合物が治療剤として有用なものになり得る。一側面において、提供されるHDAC6インヒビターは、式(I)、(II)、(III)、(IV)、(V)、および(VI)で表される化合物、およびそれらの薬学的に許容し得る塩、溶媒和物、水和物、多形、共結晶、互変異性体、立体異性体、同位体標識された誘導体、プロドラッグ、ならびに医薬組成物である。結果的に、化合物は、HDAC6活性に関連する疾患および障害(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の処置および/または予防を、これを必要とする対象においてするのに有用である。
本明細書に記載の化合物は、HDAC6と相互作用する。本明細書に記載のとおり、治療効果は、本明細書に記載の化合物によるHDAC6の阻害、モジュレーション、結合、および/または修飾の結果であってもよい。化合物は、その薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグとしての、本明細書に記載されるいずれの組成物、キット、または方法における使用が提供されてもよい。
本明細書に提供されるのは、HDACインヒビター(例として、HDAC6インヒビター)である化合物である。本明細書に記載の化合物は、HDAC6の選択的阻害および/または血液脳関門の通過能などの有利な特性を保有し、これによって化合物が治療剤として有用なものになり得る。一側面において、提供されるHDAC6インヒビターは、式(I)、(II)、(III)、(IV)、(V)、および(VI)で表される化合物、およびそれらの薬学的に許容し得る塩、溶媒和物、水和物、多形、共結晶、互変異性体、立体異性体、同位体標識された誘導体、プロドラッグ、ならびに医薬組成物である。結果的に、化合物は、HDAC6活性に関連する疾患および障害(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の処置および/または予防を、これを必要とする対象においてするのに有用である。
本明細書に記載の化合物は、HDAC6と相互作用する。本明細書に記載のとおり、治療効果は、本明細書に記載の化合物によるHDAC6の阻害、モジュレーション、結合、および/または修飾の結果であってもよい。化合物は、その薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、またはプロドラッグとしての、本明細書に記載されるいずれの組成物、キット、または方法における使用が提供されてもよい。
式(I)で表される化合物
一側面において、開示されるのは、式(I):
で表される化合物、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フッ素である;
Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;
mは、0または1である;ならびに
nは、0または1である。
一側面において、開示されるのは、式(I):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フッ素である;
Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;
mは、0または1である;ならびに
nは、0または1である。
X1およびX2
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フッ素である。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フッ素である。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。
A
本明細書に記載のとおり、Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
本明細書に記載のとおり、Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
ある態様において、Aは、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
ある態様において、Aは、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のアリールである。
ある態様において、Aは、置換もしくは非置換のシクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~10シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10架橋シクロアルキル、置換もしくは非置換のC5~10スピロ環状シクロアルキル、または置換もしくは非置換のC3~8単環式シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10架橋シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10スピロ環状シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC8~10スピロ環状シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~8単環式シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~6単環式シクロアルキルである。
ある態様において、Aは、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。ある態様において、Aは、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。
ある態様において、Aは、置換もしくは非置換のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の4~10員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~7員のヘテロシクリル、または置換もしくは非置換の5~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~7員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~6員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~5員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の5~6員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の5~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の6~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の8~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の10員の架橋ヘテロシクリルである。
ある態様において、Aは、置換もしくは非置換のオキセタニル、置換もしくは非置換のテトラヒドロフラニル、置換もしくは非置換のピラニル、置換もしくは非置換のジヒドロピラニル、置換もしくは非置換のテトラヒドロピラニル、置換もしくは非置換のジオキサニル、置換もしくは非置換のオキセパニル、置換もしくは非置換のアゼチジニル、置換もしくは非置換のピロリジニル、置換もしくは非置換のピペリジニル、置換もしくは非置換のピペラジニル、置換もしくは非置換のアゼパニル、置換もしくは非置換のジアゼパニル、置換もしくは非置換のモルホリニル、置換もしくは非置換のオキサゼパニル、またはオキサアダマンタニルである。ある態様において、Aは、テトラヒドロフラニル、オキセタニル、または
である。
ある態様において、Aは、置換もしくは非置換のアリールである。ある態様において、Aは、置換もしくは非置換のフェニルである。ある態様において、Aは、非置換のフェニルである。ある態様において、Aは、ハロゲン、シアノ、アルキル、ハロアルキル、アルケニル、アルキニル、アルコキシ、ハロアルコキシ、またはアルコキシアルキルから選択される1~5個の置換基で置換されたフェニルである。ある態様において、Aは、2,6-ジメチルフェニルである。
ある態様において、Aは、非置換のC1~4アルキルまたはC1~4ハロアルキルである。ある態様において、Aは、非置換のC1~4アルキルである。ある態様において、Aは、メチル、エチル、n-プロピル、イソプロピル、n-ブチル、sec-ブチル、t-ブチル、またはイソブチルである。ある態様において、Aは、t-ブチルである。ある態様において、Aは、C1~4ハロアルキルである。ある態様において、Aは、-CF3、-CHF2、または-CH2Fである。ある態様において、Aは、-CF3である。ある態様において、Aは、-CF3またはt-ブチルである。
ある態様において、Aは、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のC8~10スピロ環状シクロアルキル、置換もしくは非置換のC3~6単環式シクロアルキル、置換もしくは非置換の単環式の4~7員のヘテロシクリル、置換もしくは非置換の8~10員の架橋ヘテロシクリル、または置換もしくは非置換のフェニルである。
ある態様において、Aは、-CF3、-C(CH3)3、フェニル、2,6-ジメチルフェニル、テトラヒドロフラニル、オキセタニル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。
ある態様において、Aは、-CF3、-C(CH3)3、フェニル、2,6-ジメチルフェニル、テトラヒドロフラニル、オキセタニル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。
R1およびR2
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルである;およびR2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルである;およびR2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、を非置換のC3~6シクロアルキル形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチル;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である。ある態様において、R1は、メチルまたはエチルである;およびR2は、水素である。ある態様において、R1は、メチルである;およびR2は、水素である。ある態様において、R1は、エチルである;およびR2は、水素である。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1およびR2は一緒に、置換もしくは非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロプロピルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロペンチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロヘキシルを形成している。
ある態様において、R1は、水素である;およびR2は、水素である。
Ra、Rb、Rc、m、およびn
本明細書に記載のとおり、Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している。
本明細書に記載のとおり、Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;Rbは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Raは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、Raは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の炭素環式の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の複素環式の架橋環を形成している;およびRbは、水素である。
ある態様において、Rbは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、Rbは、とRc結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の炭素環式の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の複素環式の架橋環を形成している;およびRaは、水素である。
ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または置換もしくは非置換のアルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または非置換のアルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または非置換のC1~4アルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素である。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、非置換のC1~4アルキルである。
本明細書に記載のとおり、mは、0または1である。ある態様において、mは、0である。ある態様において、mは、1である。本明細書に記載のとおり、nは、0または1である。ある態様において、nは、0である。ある態様において、nは、1である。
ある態様において、mは、0または1である;およびnは、0である。ある態様において、mは、0または1である;およびnは、1である。ある態様において、mは、0である;およびnは、0または1である。ある態様において、mは、1である;およびnは、0または1である。ある態様において、mは、0である;およびnは、1である。ある態様において、mは、0である;およびnは、0である。ある態様において、mは、1である;およびnは、0である。
ある態様
ある態様において、式(I)で表される化合物は、式(I-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-a):
ある態様において、式(I)で表される化合物は、式(I-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-d):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでAは、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-e):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-f):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-g):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、式(I-h):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでAは、本明細書に定義されるとおりである。
ある態様において、式(I)で表される化合物は、以下の化合物:
のうちの1つであるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
ある態様において、式(I)で表される化合物は、以下の化合物:
のうちの1つであるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
式(II)で表される化合物
別の側面において、開示されるのは、式(II):
で表される化合物、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
各R1は、独立して、水素、または置換もしくは非置換のアルキルである;
各R2は、独立して、水素、または置換もしくは非置換のアルキルである;またはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;および
各nは、独立して、0または1である。
別の側面において、開示されるのは、式(II):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
各R1は、独立して、水素、または置換もしくは非置換のアルキルである;
各R2は、独立して、水素、または置換もしくは非置換のアルキルである;またはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;および
各nは、独立して、0または1である。
X1およびX2
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、水素である;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、水素である;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。
Y1
本明細書に記載のとおり、Y1は、窒素またはCHである。ある態様において、Y1は、窒素である。ある態様において、Y1は、CHである。
本明細書に記載のとおり、Y1は、窒素またはCHである。ある態様において、Y1は、窒素である。ある態様において、Y1は、CHである。
A
本明細書に記載のとおり、各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。ある態様において、Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
本明細書に記載のとおり、各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。ある態様において、Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
ある態様において、Aは、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである。
ある態様において、Aは、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のアリールである。
ある態様において、Aは、置換もしくは非置換のシクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~10シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10架橋シクロアルキル、置換もしくは非置換のC5~10スピロ環状シクロアルキル、または置換もしくは非置換のC3~8単環式シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10架橋シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC5~10スピロ環状シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC8~10スピロ環状シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~8単環式シクロアルキルである。ある態様において、Aは、置換もしくは非置換のC3~6単環式シクロアルキルである。
ある態様において、Aは、置換もしくは非置換のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の4~10員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~7員のヘテロシクリル、または置換もしくは非置換の5~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~7員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~6員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の4~5員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の単環式の5~6員のヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の5~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の6~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の8~10員の架橋ヘテロシクリルである。ある態様において、Aは、置換もしくは非置換の10員の架橋ヘテロシクリルである。
ある態様において、Aは、置換もしくは非置換のオキセタニル、置換もしくは非置換のテトラヒドロフラニル、置換もしくは非置換のピラニル、置換もしくは非置換のジヒドロピラニル、置換もしくは非置換のテトラヒドロピラニル、置換もしくは非置換のジオキサニル、置換もしくは非置換のオキセパニル、置換もしくは非置換のアゼチジニル、置換もしくは非置換のピロリジニル、置換もしくは非置換のピペリジニル、置換もしくは非置換のピペラジニル、置換もしくは非置換のアゼパニル、置換もしくは非置換のジアゼパニル、置換もしくは非置換のモルホリニル、置換もしくは非置換のオキサゼパニル、またはオキサアダマンタニルである。ある態様において、Aは、テトラヒドロフラニル、オキセタニル、または
である。ある態様において、Aは、オキセタニルである。
ある態様において、Aは、置換もしくは非置換のアリールである。ある態様において、Aは、置換もしくは非置換のフェニルである。ある態様において、Aは、非置換のフェニルである。ある態様において、Aは、ハロゲン、シアノ、アルキル、ハロアルキル、アルケニル、アルキニル、アルコキシ、ハロアルコキシ、またはアルコキシアルキルから選択される1~5個の置換基で置換されたフェニルである。ある態様において、Aは、2,6-ジメチルフェニルである。
ある態様において、Aは、水素、非置換のC1~4アルキル、またはC1~4ハロアルキルである。ある態様において、Aは、水素、または非置換のC1~4アルキルである。ある態様において、Aは、非置換のC1~4アルキルまたはC1~4ハロアルキルである。ある態様において、Aは、非置換のC1~4アルキルである。ある態様において、Aは、メチル、エチル、n-プロピル、イソプロピル、n-ブチル、sec-ブチル、t-ブチル、またはイソブチルである。ある態様において、Aは、t-ブチルである。ある態様において、Aは、C1~4ハロアルキルである。ある態様において、Aは、-CF3、-CHF2、または-CH2Fである。ある態様において、Aは、-CF3である。ある態様において、Aは、-CF3またはt-ブチルである。ある態様において、Aは、メチルまたは水素である。ある態様において、Aは、メチルまたは水素であり、およびnは、0である。ある態様において、Aは、メチルである。ある態様において、Aは、メチルであり、およびnは、0である。ある態様において、Aは、水素である。ある態様において、Aは、水素であり、およびnは、0である。
ある態様において、Aは、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のC8~10スピロ環状シクロアルキル、置換もしくは非置換のC3~6単環式シクロアルキル、置換もしくは非置換の単環式の4~7員のヘテロシクリル、置換もしくは非置換の8~10員の架橋ヘテロシクリル、または置換もしくは非置換のフェニルである。
ある態様において、Aは、-CF3、-C(CH3)3、フェニル、2,6-ジメチルフェニル、テトラヒドロフラニル、オキセタニル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。
ある態様において、Aは、-CF3、-C(CH3)3、フェニル、2,6-ジメチルフェニル、テトラヒドロフラニル、オキセタニル、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、アダマンチル、
である。
R1およびR2
本明細書に記載のとおり、各R1は、独立して、水素、または置換もしくは非置換のアルキルである;および各R2は、独立して、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
本明細書に記載のとおり、各R1は、独立して、水素、または置換もしくは非置換のアルキルである;および各R2は、独立して、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である。ある態様において、R1は、メチルまたはエチルである;およびR2は、水素である。ある態様において、R1は、メチルである;およびR2は、水素である。ある態様において、R1は、エチルである;およびR2は、水素である。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1およびR2は一緒に、置換もしくは非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロプロピルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロペンチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロヘキシルを形成している。
ある態様において、R1は、水素である;およびR2は、水素である。
Ra、Rb、Rc、Rx、およびn
本明細書に記載のとおり、Rxは、水素、または置換もしくは非置換のアルキルである;Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している。
本明細書に記載のとおり、Rxは、水素、または置換もしくは非置換のアルキルである;Raは、水素であるか、またはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRcは、水素、または置換もしくは非置換のアルキルであるか、あるいは、RaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Rxは、水素である。ある態様において、Rxは、置換もしくは非置換のアルキルである。ある態様において、Rxは、置換もしくは非置換のC1~6アルキルである。ある態様において、Rxは、置換もしくは非置換のC1~4アルキルである。ある態様において、Rxは、置換もしくは非置換のC1~3アルキルである。ある態様において、Rxは、置換アルキルである。ある態様において、Rxは、置換C1~6アルキルである。ある態様において、Rxは、置換C1~4アルキルである。ある態様において、Rxは、置換C1~3アルキルである。ある態様において、Rxは、非置換のアルキルである。ある態様において、Rxは、非置換のC1~6アルキルである。ある態様において、Rxは、非置換のC1~4アルキルである。ある態様において、Rxは、非置換のC1~3アルキルである。
ある態様において、Raは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、Raは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の炭素環式の架橋環を形成している;およびRbは、水素である。ある態様において、Raは、Rcと結び合わされることで、非置換の複素環式の架橋環を形成している;およびRbは、水素である。
ある態様において、Rbは、水素である。ある態様において、Rbは、置換もしくは非置換のアルキルである。ある態様において、Rbは、非置換のアルキルである。ある態様において、Rbは、非置換のC1~4アルキルである。ある態様において、Rbは、A(CR1R2)n-であり、およびnは、1である。ある態様において、Rbは、A(CR1R2)n-であるり、およびnは、0である。ある態様において、Rbは、Rcと結び合わされることで、置換もしくは非置換の架橋環。を形成しているある態様において、Rbは、Rcと結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の炭素環式の架橋環を形成している;およびRaは、水素である。ある態様において、Rbは、Rcと結び合わされることで、非置換の複素環式の架橋環を形成している;およびRaは、水素である。
ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または置換もしくは非置換のアルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または非置換のアルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素、または非置換のC1~4アルキルである。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、水素である。ある態様において、Raは、水素である;Rbは、水素である;およびRcは、非置換のC1~4アルキルである。
ある態様において、nは、0である。ある態様において、nは、1である。
ある態様
ある態様において、式(II)で表される化合物は、式(II-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-a):
ある態様において、式(II)で表される化合物は、式(II-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-d):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでAは、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-e):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、X2、Rb、およびnは、本明細書に定義されるとおりである。
式(II-e)で表される化合物のある態様において、Rbは、水素、または非置換のアルキルである。式(II-e)で表される化合物のある態様において、Rbは、水素である。式(II-e)で表される化合物のある態様において、Rbは、メチルである。
ある態様において、式(II-e)で表される化合物は、式(II-e-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(II-e)で表される化合物は、式(II-e-2):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-f):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-g):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、R2、Rb、およびnは、本明細書に定義されるとおりである。
式(II-g)で表される化合物のある態様において、Rbは、水素、または非置換のアルキルである。式(II-g)で表される化合物のある態様において、Rbは、水素である。式(II-g)で表される化合物のある態様において、Rbは、メチルである。
ある態様において、式(II-g)で表される化合物は、式(II-g-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(II-g)で表される化合物は、式(II-g-2):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、式(II-h):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでA、R1、およびR2は、本明細書に定義されるとおりである。
ある態様において、式(II)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
ある態様において、式(II)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
式(III)で表される化合物
別の側面において、開示されるのは、式(III):
で表される化合物、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換の多環式のスピロ環系、架橋環系、
である。
別の側面において、開示されるのは、式(III):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換の多環式のスピロ環系、架橋環系、
X1およびX2
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
ある態様において、Bは、置換もしくは非置換の架橋環系である。ある態様において、Bは、置換もしくは非置換の複素環式の架橋環系である。
ある態様において、Bは、式:
で表される;式中Zは、-O-、-NCH3-、-C(=O)-、-C(=NOH)-、もしくは-CHRa6-である;Ra1は、水素であるか、またはRa3もしくはRa4と結び合わされることで、1~4個の炭素架橋を形成している;Ra2は、水素であるか、またはRa3もしくはRa4と結び合わされることで、1~4個の炭素架橋を形成している;Ra3は、水素であるか、またはRa1もしくはRa2と結び合わされることで、1~4個の炭素架橋を形成している;Ra4は、水素であるか、またはRa1もしくはRa2と結び合わされることで、1~4個の炭素架橋を形成している;Ra5は、水素であるか、またはRa6と結び合わされることで、置換もしくは非置換のシクロアルキルを形成している;およびRa6は、水素であるか、またはRa5と結び合わされることで、置換もしくは非置換のシクロアルキルを形成している。
R1およびR2
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルである;およびR2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルである;およびR2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である。ある態様において、R1は、メチルまたはエチルである;およびR2は、水素である。ある態様において、R1は、メチルである;およびR2は、水素である。ある態様において、R1は、エチルである;およびR2は、水素である。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1およびR2は一緒に、置換もしくは非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロプロピルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロペンチルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロヘキシルを形成している。
ある態様において、R1は、水素である;およびR2は、水素である。
ある態様
ある態様において、式(III)で表される化合物は、式(III-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでB、X1、およびX2は、本明細書に定義されるとおりである。
ある態様において、式(III)で表される化合物は、式(III-a):
ある態様において、式(III)で表される化合物は、式(III-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでBおよびX2は、本明細書に定義されるとおりである。
ある態様において、式(III)で表される化合物は、式(III-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでBは、本明細書に定義されるとおりである。
ある態様において、式(III)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
ある態様において、式(III)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
式(IV)で表される化合物
式(III)で表される化合物のある態様において、Bは、置換もしくは非置換の多環式のスピロ環系である。ある態様において、式(III)で表される化合物は、式(IV):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1,、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
式(III)で表される化合物のある態様において、Bは、置換もしくは非置換の多環式のスピロ環系である。ある態様において、式(III)で表される化合物は、式(IV):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1,、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
X1およびX2
ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
R1およびR2
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチル;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチル;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である。ある態様において、R1は、メチルまたはエチル;およびR2は、水素である。ある態様において、R1は、メチルである;およびR2は、水素である。ある態様において、R1は、エチルである;およびR2は、水素である。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1およびR2は一緒に、置換もしくは非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、水素である;およびR2は、水素である。
B
本明細書に記載のとおり、Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
本明細書に記載のとおり、Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;ならびにR3、R4、およびRa1は、本明細書に定義されるとおりである。ある態様において、Yは、-O-である。ある態様において、Yは、-(CR3R4)-である;ならびにR3、R4、およびRa1は、本明細書に定義されるとおりである。ある態様において、Yは、-NRa1-である;およびRa1は、本明細書に定義されるとおりである。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-または-(CR3R4)-である;およびR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-または-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-または-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-または-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CHR3)-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CHR3)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CHR3)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CHR3)-である;およびR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、mとnとの和は、0、1、または2である。ある態様において、mは、0である;およびnは、0である。ある態様において、mは、1である;およびnは、0である。ある態様において、mは、2である;およびnは、0である。ある態様において、mは、0である;およびnは、1である。ある態様において、mは、1である;およびnは、1である。ある態様において、mは、0である;およびnは、2である。
ある態様において、kとqとの和は、0、1、または2である。ある態様において、kは、0である;およびqは、0である。ある態様において、kは、1である;およびqは、0である。ある態様において、kは、2である;およびqは、0である。ある態様において、kは、0である;およびqは、1である。ある態様において、kは、1である;およびqは、1である。ある態様において、kは、0である;およびqは、2である。
ある態様
ある態様において、式(IV)で表される化合物は、式(IV-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでX1、X2、R3、R4、Y、p1、p2、m、n、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-a):
ある態様において、式(IV)で表される化合物は、式(IV-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでX2、R3、R4、Y、p1、p2、m、n、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、Y、p1、p2、m、n、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-d):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、Y、p1、p2、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-e):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、Y、p1、p2、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-f):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、Y、p1、p2、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-g):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、Y、p1、p2、k、およびqは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、式(IV-h):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR4、p2、m、およびnは、本明細書に定義されるとおりである。
ある態様において、式(IV)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
式(V)で表される化合物
別の側面において、開示されるのは、式(V):
で表される化合物、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
Y2は、窒素、CRd、結合、-CH2-、または-NH-である;
A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換または非置換の環を形成している;
A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;
R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;あるいはR1およびR2は一緒に、カルボニルを形成している;
R3は、水素、または置換もしくは非置換のアルキルであるか、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;
R4は、水素、または置換もしくは非置換のアルキルであるか、あるいはR4は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;あるいはR3およびR4は一緒に、カルボニルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rdは、水素であるか、あるいはR1もしくはR2と結び合わされることで、置換または非置換の環を形成している;および
tは、0または1である。
別の側面において、開示されるのは、式(V):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
Y2は、窒素、CRd、結合、-CH2-、または-NH-である;
A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換または非置換の環を形成している;
A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;
R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;あるいはR1およびR2は一緒に、カルボニルを形成している;
R3は、水素、または置換もしくは非置換のアルキルであるか、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;
R4は、水素、または置換もしくは非置換のアルキルであるか、あるいはR4は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;あるいはR3およびR4は一緒に、カルボニルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rdは、水素であるか、あるいはR1もしくはR2と結び合わされることで、置換または非置換の環を形成している;および
tは、0または1である。
X1およびX2
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
Y1およびY2
本明細書に記載のとおり、Y1は、窒素またはCHである。ある態様において、Y1は、窒素である。ある態様において、Y1は、CHである。
本明細書に記載のとおり、Y1は、窒素またはCHである。ある態様において、Y1は、窒素である。ある態様において、Y1は、CHである。
本明細書に記載のとおり、Y2は、窒素、CRd、結合、-CH2-、または-NH-である;およびRdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、Y2は、窒素、CH、もしくは結合である;またはY2は、tが0であるとき、-CH2-もしくは-NH-である。ある態様において、Y2は、窒素、CH、または結合である。ある態様において、Y2は、窒素またはCHである。ある態様において、Y2は、窒素または結合である。ある態様において、Y2は、CHまたは結合である。ある態様において、Y2は、窒素である。ある態様において、Y2は、窒素である;およびA2、R3、およびR4は各々、置換もしくは非置換のアルキルである。ある態様において、Y2は、窒素である;ならびにA2、R3、およびR4は各々、水素である。ある態様において、Y2は、結合である。ある態様において、Y2は、tが0であるとき、-CH2-である。ある態様において、Y2は、tが0であるとき、-NH-である。ある態様において、Y2は、CRdである;およびRdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、Y2は、CRdである;およびRdは、R3もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、Y2は、CRdである;およびRdは、R3もしくはR4と結び合わされることで、置換または非置換の架橋環を形成している。
ある態様において、Y1は、窒素である;およびY2は、窒素、CRd、結合、-CH2-、または-NH-である;およびRdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、Y1は、窒素である;およびY2は、窒素、CRd、結合、-CH2-、または-NH-である。ある態様において、Y1は、窒素である;およびY2は、窒素、CH、または結合である。ある態様において、Y1は、窒素である;およびY2は、窒素である。ある態様において、Y1は、窒素である;およびY2は、CHである。ある態様において、Y1は、窒素である;およびY2は、結合である。ある態様において、Y1は、窒素である;およびY2は、tが0であるとき、-CH2-または-NH-である。ある態様において、Y1は、窒素である;およびY2は、tが0であるとき、-CH2-である。ある態様において、Y1は、窒素である;Y2は、CRdである;およびRdは、R3もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、Y1は、窒素である;Y2は、CRdである;およびRdは、R3もしくはR4と結び合わされることで、置換または非置換の架橋環を形成している。
A1およびA2
本明細書に記載のとおり、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換または非置換の環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロアリール環、ヘテロシクリル環、あるいはシクロアルキル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環あるいはシクロアルキル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロアリール環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のシクロアルキル環を形成している。
本明細書に記載のとおり、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換または非置換の環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロアリール環、ヘテロシクリル環、あるいはシクロアルキル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環あるいはシクロアルキル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロアリール環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換もしくは非置換の5員または6員のシクロアルキル環を形成している。
ある態様において、A1は、A2と結び合わされることで、置換または非置換の環を形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換のピペリジンを形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換のモルホリンを形成している。ある態様において、A1は、A2と結び合わされることで、置換もしくは非置換のヘキサヒドロピリダジンを形成している。
ある態様において、A1は、Raと結び合わされることで、置換または非置換の環を形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、A1は、Raと結び合わされることで、置換もしくは非置換のピペリジンを形成している。
ある態様において、A1は、Rcと結び合わされることで、置換または非置換の環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環あるいはヘテロアリール環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換のピペリジンを形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員または6員のヘテロアリール環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の5員のヘテロアリール環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換の6員のヘテロアリール環を形成している。ある態様において、A1は、Rcと結び合わされることで、置換もしくは非置換のピロールを形成している。
本明細書に記載のとおり、A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している。ある態様において、A2は、水素である。ある態様において、A2は、A1と結び合わされることで、置換または非置換の環を形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換のピペリジンを形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換のモルホリンを形成している。ある態様において、A2は、A1と結び合わされることで、置換もしくは非置換のヘキサヒドロピリダジンを形成している。
R1およびR2
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、置換もしくは非置換のアルキルである。ある態様において、R1は、非置換のアルキルである。ある態様において、R1は、非置換のC1~6アルキルである。ある態様において、R1は、非置換のC1~4アルキルである。ある態様において、R1は、水素である。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
本明細書に記載のとおり、R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、置換もしくは非置換のアルキルである。ある態様において、R1は、非置換のアルキルである。ある態様において、R1は、非置換のC1~6アルキルである。ある態様において、R1は、非置換のC1~4アルキルである。ある態様において、R1は、水素である。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、Rdと結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、R3と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R1は、R4と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
本明細書に記載のとおり、R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、置換もしくは非置換のアルキルである。ある態様において、R2は、非置換のアルキルである。ある態様において、R2は、非置換のC1~6アルキルである。ある態様において、R2は、非置換のC1~4アルキルである。ある態様において、R2は、水素である。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員あるいは6員の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
ある態様において、R1およびR2は一緒に、カルボニルを形成している。ある態様において、R1は、水素である;およびR2は、水素である。
R3およびR4
本明細書に記載のとおり、R3は、水素、または置換もしくは非置換のアルキル、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、置換もしくは非置換のアルキルである。ある態様において、R3は、非置換のアルキルである。ある態様において、R3は、非置換のC1~6アルキルである。ある態様において、R3は、非置換のC1~4アルキルである。ある態様において、R3は、水素である。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の5員あるいは6員の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
本明細書に記載のとおり、R3は、水素、または置換もしくは非置換のアルキル、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、置換もしくは非置換のアルキルである。ある態様において、R3は、非置換のアルキルである。ある態様において、R3は、非置換のC1~6アルキルである。ある態様において、R3は、非置換のC1~4アルキルである。ある態様において、R3は、水素である。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の5員あるいは6員の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R3は、R1もしくはR2と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R1と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換または非置換の環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R3は、R2と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
本明細書に記載のとおり、R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、置換もしくは非置換のアルキルである。ある態様において、R2は、非置換のアルキルである。ある態様において、R2は、非置換のC1~6アルキルである。ある態様において、R2は、非置換のC1~4アルキルである。ある態様において、R2は、水素である。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員あるいは6員の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の5員の架橋環を形成している。ある態様において、R2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の6員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、Rdと結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、R3と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換または非置換の環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、R2は、R4と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
ある態様において、R3およびR4は一緒に、カルボニルを形成している。ある態様において、R3は、水素である;およびR4は、水素である。
Ra、Rc、Rd、Rx、およびt
本明細書に記載のとおり、Rxは、水素、または置換もしくは非置換のアルキルである;Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している。ある態様において、Raは、水素である。ある態様において、Raは、A1と結び合わされることで、置換または非置換の環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換のピペリジンを形成している。
本明細書に記載のとおり、Rxは、水素、または置換もしくは非置換のアルキルである;Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している。ある態様において、Raは、水素である。ある態様において、Raは、A1と結び合わされることで、置換または非置換の環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、Raは、A1と結び合わされることで、置換もしくは非置換のピペリジンを形成している。
ある態様において、Rxは、水素である。ある態様において、Rxは、置換もしくは非置換のアルキルである。ある態様において、Rxは、置換もしくは非置換のC1~6アルキルである。ある態様において、Rxは、置換もしくは非置換のC1~4アルキルである。ある態様において、Rxは、置換もしくは非置換のC1~3アルキルである。ある態様において、Rxは、置換アルキルである。ある態様において、Rxは、置換C1~6アルキルである。ある態様において、Rxは、置換C1~4アルキルである。ある態様において、Rxは、置換C1~3アルキルである。ある態様において、Rxは、非置換のアルキルである。ある態様において、Rxは、非置換のC1~6アルキルである。ある態様において、Rxは、非置換のC1~4アルキルである。ある態様において、Rxは、非置換のC1~3アルキルである。
本明細書に記載のとおり、Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している。ある態様において、Rcは、水素である。ある態様において、Rcは、A1と結び合わされることで、置換または非置換の環を形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換の5員または6員のヘテロシクリル環を形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換の5員のヘテロシクリル環を形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換の6員のヘテロシクリル環を形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換のピロリジンを形成している。ある態様において、Rcは、A1と結び合わされることで、置換もしくは非置換のピペリジンを形成している。
ある態様において、Rdは、R1と結び合わされることで、置換または非置換の環を形成している。ある態様において、Rdは、R1と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、Rdは、R1と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、Rdは、R1と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、Rdは、R1と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
ある態様において、Rdは、R2と結び合わされることで、置換または非置換の環を形成している。ある態様において、Rdは、R2と結び合わされることで、置換もしくは非置換の架橋環を形成している。ある態様において、Rdは、R2と結び合わされることで、置換もしくは非置換の5員または6員の架橋環を形成している。ある態様において、Rdは、R2と結び合わされることで、置換もしくは非置換の5員の架橋環を形成している。ある態様において、Rdは、R2と結び合わされることで、置換もしくは非置換の6員の架橋環を形成している。
本明細書に記載のとおり、tは、0または1である。ある態様において、tは、0である。ある態様において、tは、1である。
ある態様
ある態様において、式(V)で表される化合物は、式(V-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、R4、Y1、Y2、X1、およびX2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;
Reは、水素、置換もしくは非置換のアルキル、または保護基である;および
R5およびR6は、各々独立して、水素、置換もしくは非置換のアルキルであるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。
ある態様において、式(V)で表される化合物は、式(V-a):
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;
Reは、水素、置換もしくは非置換のアルキル、または保護基である;および
R5およびR6は、各々独立して、水素、置換もしくは非置換のアルキルであるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。
式(V-a)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-a)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-a)で表される化合物のある態様において、Y3は、-CH2-である。式(V-a)で表される化合物のある態様において、Y3は、-O-である。式(V-a)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
式(V-a)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である;ならびにR5およびR6は、各々独立して、水素であるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。式(V-a)で表される化合物のある態様において、Y3は、-CH2-または-O-である;ならびにR5およびR6は、各々独立して、水素であるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。式(V-a)で表される化合物のある態様において、Y3は、-CH2-である;ならびにR5およびR6は、各々独立して、水素であるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。式(V-a)で表される化合物のある態様において、Y3は、-O-である;ならびにR5およびR6は、各々独立して、水素であるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。
ある態様において、式(V-a)で表される化合物は、式(V-a-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、R4、Y1、Y2、X1、およびX2は、本明細書に定義されるとおりである;および
R5およびR6は、各々独立して、水素、置換もしくは非置換のアルキルであるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。
R5およびR6は、各々独立して、水素、置換もしくは非置換のアルキルであるか、または一緒に、置換もしくは非置換のシクロアルキルを形成している。
ある態様において、式(V)で表される化合物は、式(V-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、R4、Y1、Y2、X1、およびX2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-b)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-b)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-b)で表される化合物のある態様において、Y3は、-CH2-である。式(V-b)で表される化合物のある態様において、Y3は、-O-である。式(V-b)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
ある態様において、式(V)で表される化合物は、式(V-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、R4、X1、およびX2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-c)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-c)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-c)で表される化合物のある態様において、Y3は、-CH2-である。式(V-c)で表される化合物のある態様において、Y3は、-O-である。式(V-c)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
ある態様において、式(V)で表される化合物は、式(V-d):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、およびR4は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-d)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-d)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-d)で表される化合物のある態様において、Y3は、-CH2-である。式(V-d)で表される化合物のある態様において、Y3は、-O-である。式(V-d)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
ある態様において、式(V)で表される化合物は、式(V-e):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1およびR2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-e)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-e)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-e)で表される化合物のある態様において、Y3は、-CH2-である。式(V-e)で表される化合物のある態様において、Y3は、-O-である。式(V-e)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
ある態様において、式(V)で表される化合物は、式(V-f):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1およびR2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-f)で表される化合物のある態様において、Y3は、結合、-CH2-、または-O-である。式(V-f)で表される化合物のある態様において、Y3は、-CH2-または-O-である。式(V-f)で表される化合物のある態様において、Y3は、-CH2-である。式(V-f)で表される化合物のある態様において、Y3は、-O-である。式(V-f)で表される化合物のある態様において、Y3は、-O-である;ならびにR1およびR2は一緒に、カルボニルを形成している。
ある態様において、式(V)で表される化合物は、式(V-g):
で表されるが、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、R4、X1、およびX2は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-g)で表される化合物のある態様において、Y3は、結合または-CH2-である。式(V-g)で表される化合物のある態様において、Y3は、結合である。式(V-g)で表される化合物のある態様において、Y3は、-CH2-である。
ある態様において、式(V)で表される化合物は、式(V-h):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR1、R2、R3、およびR4は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-h)で表される化合物のある態様において、Y3は、結合または-CH2-である。式(V-h)で表される化合物のある態様において、Y3は、結合である。式(V-h)で表される化合物のある態様において、Y3は、-CH2-である。
ある態様において、式(V)で表される化合物は、式(V-i):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3およびR4は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-i)で表される化合物のある態様において、Y3は、結合または-CH2-である。式(V-i)で表される化合物のある態様において、Y3は、結合である。式(V-i)で表される化合物のある態様において、Y3は、-CH2-である。
ある態様において、式(V)で表される化合物は、式(V-j):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3およびR4は、本明細書に定義されるとおりである;
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
Y3は、結合、-CH2-、-O-、-S-、または-NRe-である;および
Reは、水素、置換もしくは非置換のアルキル、または保護基である。
式(V-j)で表される化合物のある態様において、Y3は、結合または-CH2-である。式(V-j)で表される化合物のある態様において、Y3は、結合である。式(V-j)で表される化合物のある態様において、Y3は、-CH2-である。
ある態様において、式(V)で表される化合物は、式(V-k):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでR3、R4、t、Y1、Y2、X1、およびX2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;pは、0、1、2、または3である;およびlは、0または1である。
ある態様において、式(V)で表される化合物は、式(V-l):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、X1、およびX2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;pは、0、1、2、または3である;およびlは、0または1である。
ある態様において、式(V-l)で表される化合物は、式(V-l-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、X1、およびX2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;およびpは、0、1、2、または3である。
ある態様において、式(V-l)で表される化合物は、式(V-l-2):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、X1、およびX2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;およびpは、0、1、2、または3である。
ある態様において、式(V-l)で表される化合物は、式(V-l-3):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、X1、およびX2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;およびpは、0、1、2、または3である。
式(V-l)で表される化合物のある態様において、Y2は、-NH-、-NMe-、-CH2-、または結合である。式(V-l)で表される化合物のある態様において、Y2は、-NMe-、-CH2-、または結合である。式(V-l)で表される化合物のある態様において、Y2は、-NMe-である。式(V-l)で表される化合物のある態様において、Y2は、-CH2-である。式(V-l)で表される化合物のある態様において、Y2は、結合である。
ある態様において、式(V)で表される化合物は、式(V-m):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;pは、0、1、2、または3である;およびlは、0または1である。
ある態様において、で表される化合物 式(V-m)は、式(V-m-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、R7、およびpは、本明細書に定義されるとおりである。
ある態様において、で表される化合物 式(V-m)は、式(V-m-2):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、R7、およびpは、本明細書に定義されるとおりである。
ある態様において、で表される化合物 式(V-m)は、式(V-m-3):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、R7、およびpは、本明細書に定義されるとおりである。
式(V-m)で表される化合物のある態様において、Y2は、-NH-、-NMe-、-CH2-、または結合である。式(V-m)で表される化合物のある態様において、Y2は、-NMe-、-CH2-、または結合である。式(V-m)で表される化合物のある態様において、Y2は、-NMe-である。式(V-m)で表される化合物のある態様において、Y2は、-CH2-である。式(V-m)で表される化合物のある態様において、Y2は、結合である。
ある態様において、式(V)で表される化合物は、式(V-n):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2は、本明細書に定義されるとおりである;各R7は、独立して、置換もしくは非置換のアルキル、ハロゲンであるか、あるいはR7の2個の場合は一緒に、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のヘテロシクリルを形成している;pは、0、1、2、または3である;およびlは、0または1である。
ある態様において、式(V)で表される化合物は、式(V-n-1):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2は、本明細書に定義されるとおりである。
ある態様において、式(V)で表される化合物は、式(V-n-2):
で表される、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、R7、およびpは、本明細書に定義されるとおりである。
ある態様において、式(V)で表される化合物は、式(V-n-3):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでY2、R7、およびpは、本明細書に定義されるとおりである。
式(V-n)で表される化合物のある態様において、Y2は、-NH-、-NMe-、-CH2-、または結合である。式(V-n)で表される化合物のある態様において、Y2は、-NMe-、-CH2-、または結合である。式(V-n)で表される化合物のある態様において、Y2は、-NMe-である。式(V-n)で表される化合物のある態様において、Y2は、-CH2-である。式(V-n)で表される化合物のある態様において、Y2は、結合である。
ある態様において、式(V)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
ある態様において、式(V)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
式(VI)で表される化合物
別の側面において、開示されるのは、式(VI):
で表される化合物、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグであるが、式中:
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
別の側面において、開示されるのは、式(VI):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
X1およびX2
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
本明細書に記載のとおり、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである。ある態様において、X1は、水素またはフルオロである;およびX2は、水素またはフルオロである;ただし、X1およびX2 のうち少なくとも1個は、フルオロである。ある態様において、X1は、水素である;およびX2は、フルオロである。ある態様において、X1は、フルオロである;およびX2は、水素である。ある態様において、X1は、フルオロである;およびX2は、フルオロである。ある態様において、X1は、水素である;およびX2は、水素である。
R1およびR2
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、水素である;およびR2は、メチルもしくはエチルである;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1は、メチルもしくはエチルである;およびR2は、水素である;またはR1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、非置換のC1~4アルキルである;およびR2は、水素である。ある態様において、R1は、メチルまたはエチルである;およびR2は、水素である。ある態様において、R1は、メチルである;およびR2は、水素である。ある態様において、R1は、エチルである;およびR2は、水素である。
ある態様において、R1は、水素である;およびR2は、非置換のC1~4アルキルである。ある態様において、R1は、水素である;およびR2は、メチルまたはエチルである。ある態様において、R1は、水素である;およびR2は、メチルである。ある態様において、R1は、水素である;およびR2は、エチルである。
ある態様において、R1およびR2は一緒に、置換もしくは非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のC3~6シクロアルキルを形成している。ある態様において、R1およびR2は一緒に、非置換のシクロブチルを形成している。
ある態様において、R1は、水素である;およびR2は、水素である。
B
本明細書に記載のとおり、Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
本明細書に記載のとおり、Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である。
ある態様において、Bは、置換もしくは非置換の架橋環系である。ある態様において、Bは、置換もしくは非置換の複素環式の架橋環系である。
ある態様において、Bは、式:
で表される;式中Zは、-O-、-NCH3-、-C(=O)-、-C(=NOH)-、または-CHRa6-である;Ra1は、水素であるか、またはRa3もしくはRa4と結び合わされることで、1~4個の炭素架橋を形成している;Ra2は、水素であるか、またはRa3もしくはRa4と結び合わされることで、1~4個の炭素架橋を形成している;Ra3は、水素であるか、またはRa1もしくはRa2と結び合わされることで、1~4個の炭素架橋を形成している;Ra4は、水素であるか、またはRa1もしくはRa2と結び合わされることで、1~4個の炭素架橋を形成している;Ra5は、水素であるか、またはRa6と結び合わされることで、置換もしくは非置換のシクロアルキルを形成している;およびRa6は、水素であるか、またはRa5と結び合わされることで、置換もしくは非置換のシクロアルキルを形成している。
ある態様において、Bは、式:
ある態様において、
Bは、
であるが、式中
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
R5は、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
Bは、
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
R5は、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;およびR3、R4、およびRa1は、本明細書に定義されるとおりである。ある態様において、Yは、-O-である。ある態様において、Yは、-(CR3R4)-である;およびR3、R4、およびRa1は、本明細書に定義されるとおりである。ある態様において、Yは、-NRa1-である;およびRa1は、本明細書に定義されるとおりである。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-O-、-(CR3R4)-、または-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;およびRa1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である。
ある態様において、Yは、-NRa1-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;mとnとの和は、0、1、または2である;および#kとqとの和は、0、1、または2である。
ある態様において、Yは、-O-または-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-または-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-または-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-または-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-である;およびR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-O-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-O-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CR3R4)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CR3R4)-である;R3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CHR3)-である;ならびにR3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CHR3)-である;R3およびR4の各出現は、独立して、水素、ハロゲン、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、Yは、-(CHR3)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している。
ある態様において、Yは、-(CHR3)-である;ならびにR3およびR4の各出現は、独立して、水素、または置換もしくは非置換のアルキルである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;mとnとの和は、0、1、または2である;およびkとqとの和は、0、1、または2である。
ある態様において、mとnとの和は、0、1、または2である。ある態様において、mは、0である;およびnは、0である。ある態様において、mは、1である;およびnは、0である。ある態様において、mは、2である;およびnは、0である。ある態様において、mは、0である;およびnは、1である。ある態様において、mは、1である;およびnは、1である。ある態様において、mは、0である;およびnは、2である。
ある態様において、kとqとの和は、0、1、または2である。ある態様において、kは、0である;およびqは、0である。ある態様において、kは、1である;およびqは、0である。ある態様において、kは、2である;およびqは、0である。ある態様において、kは、0である;およびqは、1である。ある態様において、kは、1である;およびqは、1である。ある態様において、kは、0である;およびqは、2である。
ある態様において、Bは、式:
ある態様
ある態様において、式(VI)で表される化合物は、式(VI-a):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでX2、R1、R2、およびBは、本明細書に定義されるとおりである。
ある態様において、式(VI)で表される化合物は、式(VI-a):
ある態様において、式(VI)で表される化合物は、式(VI-b):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでX2およびBは、本明細書に定義されるとおりである。
ある態様において、式(VI)で表される化合物は、式(VI-c):
で表されるか、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである;ここでBは、本明細書に定義されるとおりである。
ある態様において、式(VI)で表される化合物は、以下の化合物:
のうちの1つ、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグである。
ある態様において、提供される化合物(例として、式(I)、(II)、(III)、(IV)、(V)、および(VI)で表される化合物)は、HDAC6を、100,000nM未満、50,000nM未満、20,000nM未満、10,000nM未満、5,000nM未満、2,500nM未満、1,000nM未満、900nM未満、800nM未満、700nM未満、600nM未満、500nM未満、400nM未満、300nM未満、200nM未満、100nM未満、90nM未満、80nM未満、70nM未満、60nM未満、50nM未満、40nM未満、30nM未満、20nM未満、10nM未満、5nM未満、4nM未満、3nM未満、2nM未満、または1nM未満のIC50で阻害する。
ある態様において、提供される化合物(例として、式(I)、(II)、(III)、(IV)、(V)、および(VI)で表される化合物)は、HDAC1、HDAC2、HDAC3、HDAC4、HDAC5、HDAC7、HDAC8、HDAC9、HDAC10、およびHDAC11のいずれよりも選択的にHDAC6を阻害する。ある態様において、化合物は、HDAC1、HDAC2、HDAC3、HDAC4、HDAC5、HDAC7、HDAC8、HDAC9、HDAC10、およびHDAC11の各々より選択的にHDAC6を阻害する。ある態様において、化合物は、HDAC1、HDAC2、HDAC3、HDAC4、HDAC5、HDAC7、HDAC8、HDAC9、HDAC10、およびHDAC11のいずれよりも、5倍、10倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍、1,000倍、または10,000倍、より選択的なHDAC6のインヒビターである。ある態様において、化合物は、HDAC1、HDAC2、HDAC3、HDAC4、HDAC5、HDAC7、HDAC8、HDAC9、HDAC10、およびHDAC11の各々より、5倍、10倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍、1,000倍、または10,000倍、より選択的なHDAC6のインヒビターである。ある態様において、化合物は、HDAC8より、5倍、10倍、20倍、30倍、40倍、50倍、60倍、70倍、80倍、90倍、100倍、1,000倍、または10,000倍、より選択的なHDAC6のインヒビターである。
医薬組成物、キット、および投与
本開示は、開示された化合物(例として、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物)、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグ、および任意に、薬学的に許容し得る賦形剤を含む医薬組成物を提供する。ある態様において、本明細書に記載の医薬組成物は、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩、および薬学的に許容し得る賦形剤を含む。
本開示は、開示された化合物(例として、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物)、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグ、および任意に、薬学的に許容し得る賦形剤を含む医薬組成物を提供する。ある態様において、本明細書に記載の医薬組成物は、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物、またはその薬学的に許容し得る塩、および薬学的に許容し得る賦形剤を含む。
ある態様において、式(I)、(II)、(III)、(IV)、(V)、または(VI)で表される化合物は、医薬組成物中、有効量で提供されている。ある態様において、有効量は、治療的に有効な量である。ある態様において、有効量は、予防的に有効な量である。ある態様において、有効量は、増殖性疾患の処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、がんの処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、がんの予防を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、血液がんの処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、固形腫瘍を含むがんの処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、炎症性疾患の処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、炎症性疾患の予防を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、感染性疾患の処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、感染性疾患の予防を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、心血管疾患の処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、神経学的障害の処置を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、神経学的障害の予防を、これを必要とする対象においてするのに有効な量である。ある態様において、有効量は、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患の処置を、これを必要とする対象においてするのに有効な量である。
ある態様において、有効量は、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、神経学的障害、または心血管疾患)を発症するリスクの低減を、これを必要とする対象においてするのに有効な量である。
ある態様において、有効量は、対象、組織、生体試料、または細胞におけるHDAC6の活性(例として、増大した活性などの、異常な活性)を阻害するのに有効な量である。
ある態様において、本明細書に記載の化合物で処置されるか、またはこれを投与される対象は、動物である。動物は、いずれの性であってもよく、発生のいずれのステージにあってもよい。ある態様において、本明細書に記載の対象は、ヒトである。ある態様において、対象は、非ヒト動物である。ある態様において、対象は、哺乳動物である。ある態様において、対象は、非ヒト哺乳動物である。ある態様において、対象は、イヌ、ネコ、ウシ、ブタ、ウマ、ヒツジ、またはヤギなどの飼育動物(domesticated animal)である。ある態様において、対象は、イヌまたはネコなどのコンパニオン動物である。ある態様において、対象は、ウシ、ブタ、ウマ、ヒツジ、またはヤギなどの家畜動物(livestock animal)である。ある態様において、対象は、動物園の動物である。別の態様において、対象は、齧歯動物(例として、マウス、ラット)、イヌ、ブタ、または霊長目の非ヒト動物などの研究動物である。ある態様において、動物は、遺伝子操作された動物である。ある態様において、対象は、トランスジェニック動物(例として、トランスジェニックマウスおよびトランスジェニックブタ)である。ある態様において、対象は、魚類または爬虫類の動物である。
ある態様において、有効量は、HDAC6の活性を、少なくとも約10%、少なくとも約20%、少なくとも約30%、少なくとも約40%、少なくとも約50%、少なくとも約60%、少なくとも約70%、少なくとも約80%、少なくとも約90%、少なくとも約95%、少なくとも約98%、または少なくとも約99%まで阻害するのに有効な量である。ある態様において、有効量は、HDAC6の活性を、本段落に記載のあるパーセンテージと本段落に記載の別のパーセンテージとの間の範囲(両端含む)まで阻害するのに有効な量である。
本開示は、HDAC6に関する疾患または障害の処置を、これを必要とする対象においてすることにおける使用のための、HDAC6と相互作用する(例として、これを阻害する)化合物を含む医薬組成物を提供する。本開示は、HDAC6の異常な活性に関連する疾患または障害の処置を、これを必要とする対象においてすることにおける使用のための、HDAC6と相互作用する(例として、これを阻害する)化合物を含む医薬組成物を提供する。本開示は、HDAC6の増大した活性に関連する疾患または障害の処置を、これを必要とする対象においてすることにおける使用のための、HDAC6と相互作用する(例として、これを阻害する)化合物を含む医薬組成物を提供する。
ある態様において、組成物は、増殖性疾患の処置を、これを必要とする対象においてすることにおける使用のためのものである。ある態様において、組成物は、がんの処置を、これを必要とする対象においてすることにおける使用のためのものである。ある態様において、組成物は、血液がんを処置することにおける使用のためのものである。ある態様において、組成物は、白血病、T細胞リンパ腫、ホジキン病、非ホジキンリンパ腫、または多発性骨髄腫を処置することにおける使用のためのものである。ある態様において、組成物は、固形腫瘍を含むがんを処置することにおける使用のためのものである。ある態様において、組成物は、神経膠腫、膠芽腫、非小細胞肺がん、脳腫瘍、神経芽細胞腫、骨腫瘍、軟部組織肉腫、頭頸部がん、尿生殖器がん、肺がん、乳房がん、膵臓がん、黒色腫、胃がん、脳がん、肝臓がん、甲状腺がん、明細胞癌、子宮がん、または卵巣がんを処置することにおける使用のためのものである。
ある態様において、組成物は、炎症性疾患を処置することにおける使用のためのものである。ある態様において、組成物は、骨関節炎、リウマチ性関節炎、ループス、炎症性腸疾患、クローン病、潰瘍性大腸炎、貧血症、白血球増加症、喘息、慢性閉塞性肺疾患、虫垂炎、気管支炎、滑液包炎、結膜炎、皮膚炎、脳炎、脊髄炎、心筋炎、副鼻腔炎、皮膚炎、乾癬、湿疹、または座瘡を処置することにおける使用のためのものである。
ある態様において、組成物は、感染性疾患を処置することにおける使用のためのものである。ある態様において、組成物は、細菌の、真菌の、または原生動物の感染症を処置することにおける使用のためのものである。
ある態様において、組成物は、自己免疫疾患を処置することにおける使用のためのものである。ある態様において、組成物は、糖尿病、甲状腺炎、グレーブス病、ギラン・バレー症候群、アジソン病、強皮症、原発性胆汁性肝硬変、ライター症候群、乾癬、慢性疲労、または子宮内膜症を処置することにおける使用のためのものである。
ある態様において、組成物は、異種免疫疾患を処置することにおける使用のためのものである。ある態様において、組成物は、移植片対宿主病、移植、輸血、アナフィラキシー、アレルギー性結膜炎、またはアレルギー性鼻炎を処置することにおける使用のためのものである。
ある態様において、組成物は、神経学的障害を処置することにおける使用のためのものである。ある態様において、組成物は、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患を処置することにおける使用のためのものである。ある態様において、組成物は、脆弱X症候群、シャルコー・マリー・トゥース病、アルツハイマー病、パーキンソン病、ハンチントン病、多発性硬化症、筋萎縮性側索硬化症、クロイツフェルト・ヤコブ病、レビー小体型認知症、血管性認知症、筋萎縮、発作誘発性の記憶喪失、統合失調症、ルビンシュタイン・テイビ症候群、レット症候群、注意欠陥多動性障害、失読症、双極性障害、自閉症に関連する社会障害、認知障害、および学習障害、注意欠陥障害、統合失調症、大うつ病性障害、末梢神経障害、糖尿病網膜症、糖尿病性末梢神経障害、化学療法誘発性の末梢神経障害、外傷性脳損傷(TBI)、慢性外傷性脳症(CTE)、またはタウオパチーを処置することにおける使用のためのものである。ある態様において、組成物は、原発性年齢関連タウオパチー(PART)/神経原線維優位型老年認知症、慢性外傷性脳症、ボクサー認知症、進行性の核上性麻痺、大脳皮質基底核変性症、ピック病、17番染色体と連関した前頭側頭型認知症およびパーキンソニズム、リティコ・ボディグ病、神経節膠腫、神経節細胞腫、髄膜血管腫症、脳炎後パーキンソニズム、亜急性硬化性全脳炎、鉛脳症、結節性硬化症、リポフスチン症、アルツハイマー病、または嗜銀性顆粒病を処置することにおける使用のためのものである。
ある態様において、組成物は、T細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害を処置することにおける使用のためのものである。ある態様において、組成物は、関節炎、大腸炎、同種移植片拒絶、ループス、喘息、乾癬、炎症、アレルギー、アレルギー性脳脊髄炎、自己免疫リンパ増殖性障害、多腺性自己免疫症候群II型、I型糖尿病、リンパ腫、ウィスコット・アルドリッチ症候群、または重症筋無力症を処置することにおける使用のためのものである。
化合物または組成物は、本明細書に記載のとおり、1以上の追加の医薬品(例として、治療的におよび/または予防的に活性のある剤)と組み合わせて投与され得る。化合物または組成物は、それらの活性(例として、疾患の処置をこれを必要とする対象においてすることにおける、疾患の予防をこれを必要とする対象においてすることにおける、および/または疾患が発症するリスクの低減をこれを必要とする対象においてすることにおける、活性(例として、効能および/または効き目))を改善するか、バイオアベイラビリティを改善するか、安全性を改善するか、薬物耐性を低減するか、代謝を低減および/または修飾するか、排出を阻害するか、および/または対象もしくは細胞における分布を変更する、追加の医薬品と組み合わせて投与され得る。採用される治療が、同障害に対して所望される効果を達成し得るか、および/またはこれが異なる効果を達成し得ることもまた、解されるであろう。ある態様において、本明細書に記載の化合物および追加の医薬品を包含する本明細書に記載の医薬組成物は、化合物と追加の医薬品とのうち一方を包含するが両方は包含しない医薬組成物には存在しない相乗効果を呈する。
化合物もしくは組成物は、1以上の追加の医薬品と同時、これに先立ち、またはこれに続いて、投与され得るが、これは、例として併用療法として、有用なこともある。医薬品は、治療的に活性のある剤を包含する。医薬品はまた、予防的に活性のある剤も包含する。医薬品は、薬物化合物(例として、連邦規則集(CFR)に規定されるとおりヒトへの使用または獣医学の使用について米国食品医薬品局によって承認された化合物)、ペプチド、タンパク質、炭水化物、単糖類、オリゴ糖類、多糖類、核タンパク質、ムコタンパク質、リポタンパク質、合成ポリペプチドまたは合成タンパク質、タンパク質、糖タンパク質、ステロイド、核酸、DNA、RNA、ヌクレオチド、ヌクレオシド、オリゴヌクレオチド、アンチセンスオリゴヌクレオチド、脂質、ホルモン、ビタミン、および細胞へ連結された小分子などの有機小分子を包含する。ある態様において、追加の医薬品は、疾患(例として、増殖性疾患、血液がん、化学療法誘発性の(chemo-induced)神経障害、神経学的障害、自己免疫疾患、および/または炎症性疾患)を処置および/または予防するのに有用な医薬品である。追加の各医薬品は、その医薬品について決定されている用量にて、および/またはタイムスケジュールどおりに投与されてもよい。追加の医薬品はまた、互いとおよび/または本明細書に記載の化合物もしくは組成物と一緒に単回用量で投与されても、あるいは個別に異なる用量で投与されてもよい。レジメンに採用される具体的な組み合わせは、本明細書に記載の化合物の、追加の医薬品(単数もしくは複数)との適合性、および/または達成されるべき所望の治療効果および/または予防効果を考慮するであろう。一般に、組み合わせにおける追加の医薬品(単数または複数)は、それらが個々に利用されるレベルを超えないレベルにて利用されることが期待される。いくつかの態様において、組み合わせにおいて利用されるレベルは、個々に利用されるレベルより低いであろう。
追加の医薬品は、これらに限定されないが、抗増殖剤、抗がん剤、抗血管新生剤、抗炎症剤、および免疫抑制薬を包含する。ある態様において、追加の医薬品は、抗炎症剤である。ある態様において、追加の医薬品は、免疫治療薬である。ある態様において、追加の医薬品は、抗増殖剤である。ある態様において、追加の医薬品は、抗がん剤である。ある態様において、抗がん剤は、これらに限定されないが、後成的または転写のモジュレーター(例として、DNAメチルトランスフェラーゼインヒビター、HDACインヒビター、リシンメチルトランスフェラーゼインヒビター)、抗有糸分裂薬(例として、タキサンおよびビンカアルカロイド)、細胞シグナリング経路インヒビター(例として、チロシンタンパク質キナーゼインヒビター)、タンパク質安定性のモジュレーター(例として、プロテアソームインヒビター)、Hsp90インヒビター、グルココルチコイド、オールトランス型レチノイン酸、抗エストロゲン(例として、タモキシフェン、ラロキシフェン、およびメゲストロール)、LHRHアゴニスト(例として、ゴセレリンおよびリュープロリド)、抗アンドロゲン薬(例として、フルタミドおよびビカルタミド)、光線力学的治療薬(例として、ベルテポルフィン(BPD-MA)、フタロシアニン、光増感剤Pc4、およびデメトキシ-ヒポクレリンA(2BA-2-DMHA))、ナイトロジェンマスタード(例として、シクロホスファミド、イホスファミド、トロホスファミド、クロラムブシル、エストラムスチン、およびメルファラン)、ニトロソ尿素(例として、カルムスチン(BCNU)およびロムスチン(CCNU))、スルホン酸アルキル(例として、ブスルファンおよびトレオスルファン)、トリアゼン(例として、ダカルバジン、テモゾロミド)、白金含有化合物(例として、シスプラチン、カルボプラチン、オキサリプラチン)、ビンカアルカロイド(例として、ビンクリスチン、ビンブラスチン、ビンデシン、およびビノレルビン)、タキソイド(例として、パクリタキセル、またはナノ粒子アルブミン結合パクリタキセル(ABRAXANE)、ドコサキサエン酸結合パクリタキセル(DHA-パクリタキセル、タキソプレキシン)、ポリグルタマート結合パクリタキセル(PG-パクリタキセル、パクリタキセル・ポリグルメックス、CT-2103、XYOTAXなどのパクリタキセル等価物)、腫瘍活性化プロドラッグ(TAP)ANG1005(3分子のパクリタキセルへ結合したAngiopep-2)、パクリタキセル-EC-1(erbB2認識ペプチドEC-1へ結合したパクリタキセル)、およびグルコース抱合パクリタキセル、例として、2'-パクリタキセルメチル2-グルコピラノシルスクシナート;ドセタキセル、タキソール)、エピポドフィリン(epipodophyllins)(例として、エトポシド、リン酸エトポシド、テニポシド、トポテカン、9-アミノカンプトテシン、カンプトイリノテカン(camptoirinotecan)、イリノテカン、クリスナトール、マイトマイシンC)、代謝拮抗薬、DHFRインヒビター(例として、メトトレキサート、ジクロロメトトレキサート、トリメトレキサート、エダトレキサート)、IMPデヒドロゲナーゼインヒビター(例として、ミコフェノール酸、チアゾフリン、リバビリン、およびEICAR)、リボヌクレオチドレダクターゼインヒビター(例として、ヒドロキシ尿素およびデフェロキサミン)、ウラシル類似体(例として、5-フルオロウラシル(5-FU)、フロクスウリジン、ドキシフルリジン、ラルチトレキセド、テガフール-ウラシル、カペシタビン)、シトシン類似体(例として、シタラビン(ara C)、シトシンアラビノシド、およびフルダラビン)、プリン類似体(例として、メルカプトプリンおよびチオグアニン)、ビタミンD3類似体(例として、EB 1089、CB 1093、およびKH 1060)、イソプレニル化インヒビター(例として、ロバスタチン)、ドーパミン作動性神経毒(例として、1-メチル-4-フェニルピリジニウムイオン)、細胞周期インヒビター(例として、スタウロスポリン)、アクチノマイシン(例として、アクチノマイシンD、ダクチノマイシン)、ブレオマイシン(例として、ブレオマイシンA2、ブレオマイシンB2、ペプロマイシン)、アントラサイクリン(例として、ダウノルビシン、ドキソルビシン、ペグ化リポソームドキソルビシン、イダルビシン、エピルビシン、ピラルビシン、ゾルビシン、ミトキサントロン)、MDRインヒビター(例として、ベラパミル)、Ca2+ ATPアーゼインヒビター(例として、タプシガルジン)、サリドマイド、レナリドマイド、ポマリドミド、チロシンキナーゼインヒビター(例として、アキシチニブ、ボスチニブ、セジラニブ(RECENTINTM)、ダサチニブ(SPRYCEL(登録商標))、エルロチニブ(TARCEVA(登録商標))、ゲフィチニブ(IRESSA(登録商標))、イマニチブ(Gleevec(登録商標))、ラパチニブ(TYKERB(登録商標)、TYVERB(登録商標))、レスタウルチニブ、ネラチニブ、ニロチニブ(TASIGNA(登録商標))、セマクサニブ、スニチニブ(SUTENT(登録商標))、トセラニブ(PALLADIA(登録商標))、バンデタニブ(ZACTIMA(登録商標)、ZD6474)、バタラニブ(PTK787)、ニロチニブ(TASIGNA(登録商標))、ソラフェニブ(NEXAVAR(登録商標))、エベロリムス(AFINITOR(登録商標))、ゲムツズマブ・オゾガマイシン(MYLOTARG(登録商標))、テムシロリムス(TORISEL(登録商標))、ENMD-2076、PCI-32765、AC220、乳酸ドビチニブ(TKI258、CHIR-258)、BIBW 2992(TOVOKTM)、SGX523、PF-04217903、PF-02341066、PF-299804、BMS-777607、ABT-869、MP470、BIBF 1120(VARGATEF(登録商標))、AP24534、JNJ-26483327、MGCD265、DCC-2036、BMS-690154、CEP-11981、チボザニブ(AV-951)、OSI-930、MM-121、XL-184、XL-647、および/またはXL228)、プロテアソームインヒビター(例として、ボルテゾミブ(VELCADE))、mTORインヒビター(例として、ラパマイシン、テムシロリムス(CCI-779)、エベロリムス(RAD-001)、リダフォロリムス、AP23573(Ariad)、AZD8055(AstraZeneca)、BEZ235(Novartis)、BGT226(Norvartis)、XL765(Sanofi Aventis)、PF-4691502(Pfizer)、GDC0980(Genetech)、SF1126(Semafoe)、およびOSI-027(OSI))、オブリメルセン、ゲムシタビン、カルミノマイシン、ロイコボリン、ペメトレキセド、シクロホスファミド、ダカルバジン、プロカルバジン、プレドニゾロン、デキサメタゾン、カンプトテシン、プリカマイシン、アスパラギナーゼ、アミノプテリン、メトプテリン、ポルフィロマイシン、メルファラン、ロイロシジン、ロイロシン、クロラムブシル、トラベクテジン、プロカルバジン、ディスコデルモリド、カルミノマイシン、アミノプテリン、およびヘキサメチルメラミンを包含する。ある態様において、追加の医薬品は、シスプラチンである。ある態様において、追加の医薬品は、パクリタキセルである。ある態様において、追加の医薬品は、ビンクリスチンである。
ある態様において、追加の医薬品は、免疫治療薬である。ある態様において、免疫治療薬は、がんの処置に有用である。例示の免疫治療薬は、これらに限定されないが、T細胞治療薬、インターフェロン、サイトカイン(例として、腫瘍壊死因子、インターフェロンα、インターフェロンγ)、ワクチン、造血成長因子、モノクローナル血清療法薬、免疫刺激薬、および/または免疫調節剤(例として、IL-1、2、4、6、または12)、免疫細胞成長因子(例として、GM-CSF)、および抗体を包含する。ある態様において、免疫治療薬は、T細胞治療薬である。ある態様において、T細胞治療薬は、キメラ抗原受容体T細胞(CAR-T)である。ある態様において、免疫治療薬は、抗体である。ある態様において、抗体は、抗PD-1抗体、抗PD-L1抗体、抗CTLA-4抗体、抗TIM3抗体、抗OX40抗体、抗GITR抗体、抗LAG-3抗体、抗CD137抗体、抗CD27抗体、抗CD28抗体、抗CD28H抗体、抗CD30抗体、抗CD39抗体、抗CD40抗体、抗CD47抗体、抗CD48抗体、抗CD70抗体、抗CD73抗体、抗CD96抗体、抗CD160抗体、抗CD200抗体、抗CD244抗体、抗ICOS抗体、抗TNFRSF25抗体、抗TMIGD2抗体、抗DNAM1抗体、抗BTLA抗体、抗LIGHT抗体、抗TIGIT抗体、抗VISTA抗体、抗HVEM抗体、抗Siglec抗体、抗GAL1抗体、抗GAL3抗体、抗GAL9抗体、抗BTNL2(ブトロフィリン(butrophylins))抗体、抗B7-H3抗体、抗B7-H4抗体、抗B7-H5抗体、抗B7-H6抗体、抗KIR抗体、抗LIR抗体、抗ILT抗体、抗MICA抗体、抗MICB抗体、抗NKG2D抗体、抗NKG2A抗体、抗TGFβ抗体、抗TGFβR抗体、抗CXCR4抗体、抗CXCL12抗体、抗CCL2抗体、抗IL-10抗体、抗IL-13抗体、抗IL-23抗体、抗ホスファチジルセリン抗体、抗ニューロピリン抗体、抗GalCer抗体、抗HER2抗体、抗VEGFA抗体、抗VEGFR抗体、抗EGFR抗体、または抗Tie2抗体である。ある態様において、抗体は、ペンブロリズマブ、ニボルマブ、ピディリズマブ、イピリムマブ、トレメリムマブ、デュルバルマブ、アテゾリズマブ、アベルマブ、PF-06801591、ウトミルマブ、PDR001、PBF-509、MGB453、LAG525、AMP-224、INCSHR1210、INCAGN1876、INCAGN1949、サマリズマブ、PF-05082566、ウレルマブ、リリルマブ、ルリズマブ、BMS-936559、BMS-936561、BMS-986004、BMS-986012、BMS-986016、BMS-986178、IMP321、IPH2101、IPH2201、バリルマブ、ウロクプルマブ、モナリズマブ、MEDI0562、MEDI0680、MEDI1873、MEDI6383、MEDI6469、MEDI9447、AMG228、AMG820、CC-90002、CDX-1127、CGEN15001T、CGEN15022、CGEN15029、CGEN15049、CGEN15027、CGEN15052、CGEN15092、CX-072、CX-2009、CP-870893、ルカツムマブ、ダセツズマブ、Chi Lob 7/4、RG6058、RG7686、RG7876、RG7888、TRX518、MK-4166、MGA271、IMC-CS4、エマクツヅマブ、ペルツズマブ、オビヌツズマブ、カビラリズマブ、マルゲツキシマブ、エノブリツズマブ、モガムリズマブ、カルルマブ、ベバシズマブ、トラスツズマブ(ハーセプチン(登録商標))、ベバシズマブ(AVASTIN(登録商標))、リツキシマブ(リツキサン(登録商標))、セツキシマブ(アービタックス(登録商標))、パニツムマブ(ベクチビックス(登録商標))、アレムツズマブ(CAMPATH(登録商標))、またはラニビズマブ(Lucentis(登録商標))である。
ある態様において、追加の医薬品は、コリンエステラーゼインヒビター(例として、ARICEPT(登録商標)、EXELON(登録商標)、RAZADYNE(登録商標)、ドネペジル、リバスチグミン、およびガランタミン)、ならびにグルタマート調節因子(例として、NAMENDA(登録商標)、メマンチン)などの対症的薬物(symptomatic drug)である。ある態様において、追加の医薬品は、リルゾールである。ある態様において、追加の医薬品は、エダラボンである。ある態様において、追加の医薬品は、抗アミロイド抗体または抗タウ抗体である。ある態様において、追加の医薬品は、アルツハイマー病の処置に有用ないずれの剤(例として、小分子、抗体、ポリペプチド、アンチセンスオリゴ、RNA)でもある。
ある態様において、本明細書に記載の化合物または医薬組成物は、これらに限定されないが、外科手術、放射線治療、および移植(例として、幹細胞移植、骨髄移植)を包含する抗がん治療と組み合わせて施され得る。
ある態様において、化合物または医薬組成物は、固体である。ある態様において、化合物または医薬組成物は、粉末である。ある態様において、化合物または医薬組成物は、溶液を作製するために液体に溶解され得る。ある態様において、化合物または医薬組成物は、水溶液を作製するために水に溶解される。ある態様において、医薬組成物は、非経口注射のための液体である。ある態様において、医薬組成物は、経口投与(例として、摂取)のための液体である。ある態様において、医薬組成物は、静脈内注射のための液体(例として、水溶液)である。ある態様において、医薬組成物は、皮下注射のための液体(例として、水溶液)である。
適切な薬学的に許容し得る賦形剤とともに所望される投薬量で製剤化された後、本開示の医薬組成物は、ヒトおよび他の動物へ、処置される疾患または疾病に応じて、経口的に、非経口的に、大槽内に(intracisternally)、腹腔内に、局所的に、口腔内に等々、投与され得る。
ある態様において、式(I)、(II)、(III)、(IV)、(V)、または(VI)で表される化合物を含む医薬組成物は、経口的にまたは非経口的に、1日または数日間1回以上の用量投与(投与モードに依存)における各医薬組成物の約0.001mg/kgから約200mg/kgまでを送達するのに充分な投薬量レベルにて投与される。ある態様において、用量あたりの有効量は、所望される治療効果および/または予防効果を得るため、1日1回以上、1日あたり対象体重の約0.001mg/kgから約200mg/kgまで、約0.001mg/kgから約100mg/kgまで、約0.01mg/kgから約100mg/kgまで、約0.01mg/kgから約50mg/kgまで、好ましくは約0.1mg/kgから約40mg/kgまで、好ましくは約0.5mg/kgから約30mg/kgまで、約0.01mg/kgから約10mg/kgまで、約0.1mg/kgから約10mg/kgまで変動する。ある態様において、本明細書に記載の化合物は、所望される治療効果および/または予防効果を得るため、1日1回以上、1日あたり対象体重の約0.001mg/kgから約200mg/kgまで、約0.001mg/kgから約100mg/kgまで、約0.01mg/kgから約100mg/kgまで、約0.01mg/kgから約50mg/kgまで、好ましくは約0.1mg/kgから約40mg/kgまで、好ましくは約0.5mg/kgから約30mg/kgまで、約0.01mg/kgから約10mg/kgまで、約0.1mg/kgから約10mg/kgまで、より好ましくは約1mg/kgから約25mg/kgまで送達するのに充分な投薬量レベルにあってもよい。所望される投薬量は、1日3回、1日2回、1日に、隔日に、3日毎に、1週毎に、2週毎に、3週毎に、または4週毎に1度、送達されてもよい。ある態様において、所望される投薬量は、複数回投与(例として、2回、3回、4回、5回、6回、7回、8回、9回、10回、11回、12回、13回、14回、またはこれより多い投与)を使用して送達されてもよい。ある態様において、本明細書に記載の組成物は、剤が非特異的な効果を生じさせる用量を下回る用量にて投与される。
ある態様において、医薬組成物は、単位用量あたり約0.001mg~約1000mgの用量にて投与される。ある態様において、医薬組成物は、単位用量あたり約0.01mg~約200mgの用量にて投与される。ある態様において、医薬組成物は、単位用量あたり約0.01mg~約100mgの用量にて投与される。ある態様において、医薬組成物は、単位用量あたり約0.01mg~約50mgの用量にて投与される。ある態様において、医薬組成物は、単位用量あたり約0.01mg~約10mgの用量にて投与される。ある態様において、医薬組成物は、単位用量あたり約0.1mg~約10mgの用量にて投与される。
本明細書に記載の医薬組成物は、薬理学の分野において知られているいずれの方法によっても調製され得る。一般に、かかる調製方法は、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物を含む組成物を、担体および/または1以上の他の補助成分と結び付けさせるステップ、次いで、必要ならばおよび/または所望ならば、生成物を所望の単回用量もしくは複数回用量の単位に成形および/またはパッケージングするステップを包含する。
医薬組成物は、バルクで、単回単位用量として、および/または複数の単回単位用量として、調製され、パッケージングされ、および/または販売され得る。本明細書に使用されるとき、「単位用量」は、活性成分の所定量を含む医薬組成物の個別の量である。活性成分の量は一般に、対象に投与されるであろう活性成分の投薬量、および/または、例えば、かかる投薬量の2分の1または3分の1など、かかる投薬量の好都合な画分に等しい。
本発明の医薬組成物中の活性成分、薬学的に許容し得る賦形剤、および/またはいずれの追加の成分の相対量は、処置される対象の固有性(identity)、サイズ、および/または状態に応じて、およびさらに、組成物が投与されるべき経路に応じて、変動し得る。一例として、組成物は、0.1%と100%(w/w)との間で活性成分を含んでいてもよい。
提供される医薬組成物の製造に使用される薬学的に許容し得る賦形剤は、不活性希釈剤、分散剤および/または造粒剤、界面活性剤および/または乳化剤、崩壊剤、結合剤、保存剤、緩衝剤、潤滑剤、および/または油を包含する。ココアバターおよび坐剤ワックスなどの賦形剤、着色剤、コーティング剤、甘味料、香味料(flavoring)、および香料(perfuming agents)もまた、組成物中に存在していてもよい。
例示の希釈剤は、炭酸カルシウム、炭酸ナトリウム、リン酸カルシウム、リン酸二カルシウム、硫酸カルシウム、リン酸水素カルシウム、リン酸ナトリウム、ラクトース、スクロース、セルロース、微結晶性セルロース、カオリン、マンニトール、ソルビトール、イノシトール、塩化ナトリウム、乾燥デンプン、コーンスターチ、粉砂糖、およびこれらの混合物を包含する。
例示の造粒剤および/または分散剤は、ジャガイモデンプン、トウモロコシデンプン、タピオカデンプン、デンプングリコール酸ナトリウム、クレー、アルギン酸、グアーガム、シトラスパルプ、寒天(agar)、ベントナイト、セルロース、および木製品、天然スポンジ、カチオン交換樹脂、炭酸カルシウム、ケイ酸塩、炭酸ナトリウム、架橋ポリ(ビニル-ピロリドン)(クロスポビドン)、カルボキシメチルスターチナトリウム(デンプングリコール酸ナトリウム)、カルボキシメチルセルロース、架橋カルボキシメチルセルロースナトリウム(クロスカルメロース)、メチルセルロース、アルファ化デンプン(starch 1500)、微晶質デンプン、水不溶性デンプン、カルボキシメチルセルロースカルシウム、ケイ酸アルミニウムマグネシウム(Veegum)、ラウリル硫酸ナトリウム、四級アンモニウム化合物、およびこれらの混合物を包含する。
例示の界面活性剤および/または乳化剤は、天然の乳化剤(例として、アカシア、寒天、アルギン酸、アルギン酸ナトリウム、トラガカント、コンドラックス(chondrux)、コレステロール、キサンタン、ペクチン、ゼラチン、卵黄、カゼイン、羊毛脂、コレステロール、ワックス、およびレシチン)、コロイドクレー(例として、ベントナイト(ケイ酸アルミニウム)およびVeegum(ケイ酸アルミニウムマグネシウム))、長鎖アミノ酸誘導体、高分子量アルコール(例として、ステアリルアルコール、セチルアルコール、オレイルアルコール、トリアセチンモノステアラート、エチレングリコールジステアラート、グリセリルモノステアラート、およびプロピレングリコールモノステアラート、ポリビニルアルコール)、カルボマー(例として、カルボキシポリメチレン、ポリアクリル酸、アクリル酸ポリマー、およびカルボキシビニルポリマー)、カラギーナン、セルロース誘導体(例として、カルボキシメチルセルロースナトリウム、粉末セルロース、ヒドロキシメチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース)、ソルビタン脂肪酸エステル類(例として、ポリオキシエチレンソルビタンモノラウラート(Tween 20)、ポリオキシエチレンソルビタン(Tween 60)、ポリオキシエチレンソルビタンモノオレアート(Tween 80)、ソルビタンモノパルミタート(Span 40)、ソルビタンモノステアラート(Span 60)、ソルビタントリステアラート(Span 65)、グリセリルモノオレアート、ソルビタンモノオレアート(Span 80))、ポリオキシエチレンエステル(例として、ポリオキシエチレンモノステアラート(Myrj 45)、ポリオキシエチレン硬化ヒマシ油、ポリエトキシル化ヒマシ油、ポリオキシメチレンステアラート、およびSolutol)、ショ糖脂肪酸エステル、ポリエチレングリコール脂肪酸エステル(例として、Cremophor(商標))、ポリオキシエチレンエーテル(例えば、ポリオキシエチレンラウリルエーテル(Brij 30))、ポリ(ビニルピロリドン)、ジエチレングリコールモノラウラート、トリエタノールアミンオレアート、オレイン酸ナトリウム、オレイン酸カリウム、オレイン酸エチル、オレイン酸、ラウリン酸エチル、ラウリル硫酸ナトリウム、Pluronic F-68、Poloxamer-188、臭化セトリモニウム、塩化セチルピリジニウム、塩化ベンザルコニウム、ドクサート・ナトリウム、および/またはこれらの混合物を包含する。
例示の結合剤は、デンプン(例として、コーンスターチおよびデンプン糊)、ゼラチン、糖(例として、スクロース、グルコース、デキストロース、デキストリン、糖蜜、ラクトース、ラクチトール、マンニトールなど)、天然および合成ゴム(例として、アカシア、アルギン酸ナトリウム、アイリッシュモスの抽出物、パンワルゴム(panwar gum)、ガッチゴム(ghatti gum)、イサポール殻(isapol husk)の粘液、カルボキシメチルセルロース、メチルセルロース、エチルセルロース、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、微結晶性セルロース、酢酸セルロース、ポリ(ビニルピロリドン)、ケイ酸アルミニウムマグネシウム(Veegum)、および落葉松アラボガラクタン)、アルギナート、ポリエチレンオキシド、ポリエチレングリコール、無機カルシウム塩、ケイ酸、ポリメタクリラート、ワックス、水、アルコール、および/またはこれらの混合物を包含する。
例示の保存剤は、抗酸化剤、キレート剤、抗菌性保存剤、抗真菌性保存剤、アルコール保存剤、酸性保存剤、および他の保存剤を包含する。ある態様において、保存剤は、抗酸化剤である。他の態様において、保存剤は、キレート剤である。
例示の酸化防止剤は、アルファトコフェロール、アスコルビン酸、パルミチン酸アスコルビル、ブチル化ヒドロキシアニソール、ブチル化ヒドロキシトルエン、モノチオグリセロール、メタ重亜硫酸カリウム、プロピオン酸、没食子酸プロピル、アスコルビン酸ナトリウム、亜硫酸水素ナトリウム、メタ重亜硫酸ナトリウム、および亜硫酸ナトリウムを包含する。
例示のキレート剤は、エチレンジアミン四酢酸(EDTA)およびその塩および水和物(例として、エデト酸ナトリウム、エデト酸二ナトリウム、エデト酸三ナトリウム、エデト酸カルシウム二ナトリウム、エデト酸二カリウム等)、クエン酸およびその塩および水和物(例として、クエン酸一水和物)、フマル酸およびその塩および水和物、リンゴ酸塩およびその塩および水和物、リン酸およびその塩および水和物、ならびに酒石酸およびその塩および水和物を包含する。例示的な抗菌性保存剤は、塩化ベンザルコニウム、塩化ベンゼトニウム、ベンジルアルコール、ブロノポール、セトリミド、塩化セチルピリジニウム、クロルヘキシジン、クロロブタノール、クロロクレゾール、クロロキシレノール、クレゾール、エチルアルコール、グリセリン、ヘキセチジン、イミド尿素、フェノール、フェノキシエタノール、フェニルエチルアルコール、硝酸フェニル水銀、プロピレングリコール、およびチメロサールを包含する。
例示の抗真菌性保存剤は、ブチルパラベン、メチルパラベン、エチルパラベン、プロピルパラベン、安息香酸、ヒドロキシ安息香酸、安息香酸カリウム、ソルビン酸カリウム、安息香酸ナトリウム、プロピオン酸ナトリウム、およびソルビン酸を包含する。
例示のアルコール保存剤は、エタノール、ポリエチレングリコール、フェノール、フェノール化合物、ビスフェノール、クロロブタノール、ヒドロキシベンゾアート、およびフェニルエチルアルコールを包含する。
例示の酸性保存剤は、ビタミンA、ビタミンC、ビタミンE、ベータカロチン、クエン酸、酢酸、デヒドロ酢酸、アスコルビン酸、ソルビン酸、およびフィチン酸を包含する。
他の保存剤は、トコフェロール、酢酸トコフェロール、メシル酸デテロキシム(deteroxime mesylate)、セトリミド、ブチル化ヒドロキシアニソール(BHA)、ブチル化ヒドロキシトルエン(BHT)、エチレンジアミン、ラウリル硫酸ナトリウム(SLS)、ラウリルエーテル硫酸ナトリウム(SLES)、亜硫酸水素ナトリウム、メタ重亜硫酸ナトリウム、亜硫酸カリウム、メタ重亜硫酸カリウム、Glydant Plus、Phenonip、メチルパラベン、Germall 115、Germaben II、Neolone、Kathon、およびEuxylを包含する。
例示の緩衝剤は、クエン酸緩衝液、酢酸緩衝液、リン酸緩衝液、塩化アンモニウム、炭酸カルシウム、塩化カルシウム、クエン酸カルシウム、グルビオン酸カルシウム、グルセプト酸カルシウム、グルコン酸カルシウム、D-グルコン酸、グリセロリン酸カルシウム、乳酸カルシウム、プロパン酸、レブリン酸カルシウム、ペンタン酸、二塩基性リン酸カルシウム、リン酸、三塩基性リン酸カルシウム、リン酸カルシウムヒドロキシド(calcium hydroxide phosphate)、酢酸カリウム、塩化カリウム、グルコン酸カリウム、カリウム混合物、二塩基性リン酸カリウム、一塩基性リン酸カリウム、リン酸カリウム混合物、酢酸ナトリウム、重炭酸ナトリウム、塩化ナトリウム、クエン酸ナトリウム、乳酸ナトリウム、二塩基性リン酸ナトリウム、一塩基性リン酸ナトリウム、リン酸ナトリウム混合物、トロメタミン、水酸化マグネシウム、水酸化アルミニウム、アルギン酸、発熱物質非含有水、等張食塩水、リンゲル液、エチルアルコール、およびこれらの混合物を包含する。
例示の潤滑剤は、ステアリン酸マグネシウム、ステアリン酸カルシウム、ステアリン酸、シリカ、タルク、麦芽、ベヘン酸グリセリル、水素化植物油、ポリエチレングリコール、安息香酸ナトリウム、酢酸ナトリウム、塩化ナトリウム、ロイシン、ラウリル硫酸マグネシウム、ラウリル硫酸ナトリウム、およびこれらの混合物を包含する。
例示の天然オイルは、アーモンド、杏仁、アボカド、ババス、ベルガモット、ブラックカレント種子、ルリジサ、カデ、カモミール、キャノーラ、キャラウェイ、カルナバ、ヒマシ油、シナモン、ココアバター、ココナッツ、タラ肝臓、コーヒー、トウモロコシ、綿実、エミュー、ユーカリ、月見草、魚、アマニ、ゲラニオール、ヘチマ、ブドウ種子、ヘーゼルナッツ、ヒソップ、ミリスチン酸イソプロピル、ホホバ、ククイナッツ、ラバンジン、ラベンダー、レモン、リツェアクベバ、マカデミアナッツ、ゼニアオイ、マンゴー種子、メドウフォームシード、ミンク、ナツメグ、オリーブ、オレンジ、オレンジラフィー、パーム、パーム核、桃仁、ピーナッツ、ケシの実、カボチャの種、菜種、米ぬか、ローズマリー、ベニバナ、サンダルウッド、サザンカ、セイボリー、シーバックソーン、ゴマ、シアバター、シリコーン、大豆、ヒマワリ、ティーツリー、アザミ、ツバキ、ベチベル、クルミ、および小麦胚芽を包含する。例示の合成油は、これらに限定はされないが、ステアリン酸ブチル、カプリル酸トリグリセリド、カプリン酸トリグリセリド、シクロメチコン、セバシン酸ジエチル、ジメチコーン360、ミリスチン酸イソプロピル、鉱油、オクチルドデカノール、オレイルアルコール、シリコーン油、およびこれらの混合物を包含する。
経口投与および非経口投与のための液体剤形は、これらに限定されないが、薬学的に許容し得るエマルション、マイクロエマルション、溶液、懸濁液、シロップ、およびエリキシル剤を包含する。活性剤に加えて、液体剤形は、例えば、水または他の溶媒などの、当該技術分野において一般的に使用される不活性希釈剤、エチルアルコール、イソプロピルアルコール、炭酸酢酸エチルエチル、ベンジルアルコール、安息香酸ベンジル、プロピレングリコール、1,3-ブチレングリコール、ジメチルホルムアミド、油(とりわけ、綿実油、ラッカセイ油、トウモロコシ油、胚芽油、オリーブ油、ヒマシ油、およびゴマ油)、グリセロール、テトラヒドロフルフリルアルコール、ポリエチレングリコールおよびソルビタンの脂肪酸エステルなどの、可溶化剤および乳化剤、およびこれらの混合物を含有していてもよい。不活性希釈剤の他に、経口組成物はまた、湿潤剤、乳化剤および懸濁剤などのアジュバント、甘味料、香味料、および香料も包含し得る。非経口投与のためのある態様において、本発明の剤は、CREMOPHOR EL(登録商標)(ポリエトキシル化ヒマシ油)、アルコール、油、変性油、グリコール、ポリソルベート、シクロデキストリン、ポリマー、およびそれらの組み合わせなどの可溶化剤と混合されている。
注射用調製物において、例えば、無菌の注射用水性または油性の懸濁液は、好適な分散または湿潤剤および懸濁剤を使用して、知られている技術に従って製剤化されていてもよい。無菌注射用調製物はまた、非毒性の非経口的に許容し得る希釈剤または溶媒中の無菌の注射用溶液、懸濁液、またはエマルション、例えば、1,3-ブタンジオール中の溶液であってもよい。許容し得るビヒクルおよび溶媒のうち採用されてもよいのは、水、Ringer溶液(U.S.P.)、および等張塩化ナトリウム溶液である。加えて、無菌の固定油は従来、溶媒または懸濁媒体として採用されている。この目的において、合成モノ-またはジグリセリドを包含するいずれの無刺激性の固定油も採用され得る。加えて、オレイン酸などの脂肪酸が、注射用の調製物に使用される。
注射用製剤は、例えば、細菌保持フィルターに通す濾過によって、または使用に先立ち、滅菌水もしくは他の滅菌注射用媒体に溶解または分散され得る滅菌固体組成物の形態で滅菌剤を組み込むことによって、滅菌され得る。
経口投与のための固体剤形は、カプセル剤、錠剤、丸剤、粉末剤、および顆粒剤を含む。かかる固体剤形において、活性剤は、クエン酸ナトリウムまたはリン酸二カルシウムなどの少なくとも1つの不活性な、薬学的に許容し得る賦形剤もしくは担体、および/またはa)デンプン、ラクトース、スクロース、グルコース、マンニトール、およびケイ酸などの充填剤または増量剤、b)例えば、カルボキシメチルセルロース、アルギナート、ゼラチン、ポリビニルピロリジノン、スクロース、およびアカシアなどのバインダー、c)グリセロールなどの湿潤剤(humectant)、d)寒天(agar-agar)、炭酸カルシウム、ジャガイモまたはタピオカデンプン、アルギン酸、あるシリカート、および炭酸ナトリウムなどの崩壊剤、e)パラフィンなどの溶解遅延剤(solution retarding agent)、f)四級アンモニウム化合物などの吸収促進剤、g)例えば、セチルアルコールおよびグリセロールモノステアラートなどの湿潤剤(wetting agent)、h)カオリンおよびベントナイトクレーなどの吸収剤、ならびにi)タルク、ステアリン酸カルシウム、ステアリン酸マグネシウム、固体ポリエチレングリコール、ラウリル硫酸ナトリウムなどの潤滑剤、およびこれらの混合物と混合される。カプセル剤、錠剤、および丸剤のケースにおいて、剤形はまた、緩衝剤を包含していてもよい。
類似タイプの固体組成物はまた、ラクトースまたは乳糖ならびに高分子量ポリエチレングリコール等のような賦形剤を使用する、軟質および硬質の充填ゼラチンカプセル中の充填剤として採用されてもよい。錠剤、糖衣錠、カプセル、丸薬、および顆粒の固体剤形は、腸溶コーティングおよび医薬製剤の技術分野において知られている他のコーティングなどのコーティングおよび外郭(shells)で調製され得る。それらは任意に不透明化剤を含んでいてもよく、それらはまた、活性成分(単数もしくは複数)のみを、またはこれを優先的に、腸管のある部分において、任意に遅延様式で、放出するという組成物からも成り得る。使用され得る包埋化組成物の例は、ポリマー物質およびワックスを包含する。類似タイプの固体組成物はまた、ラクトースまたは乳糖ならびに高分子量ポリエチレングリコール等のような賦形剤を使用する、軟質および硬質の充填ゼラチンカプセル中の充填剤として採用されてもよい。
活性剤はまた、上に述べたとおりの1以上の賦形剤をもつマイクロカプセル化形態でもあり得る。錠剤、糖衣錠、カプセル剤、丸剤、および顆粒剤の固体剤形は、腸溶コーティング、放出制御コーティング、および医薬製剤分野(pharmaceutical formulating art)において知られている他のコーティングなどの、コーティングおよび外郭で調製され得る。かかる固体剤形において、活性剤は、スクロース、ラクトース、またはデンプンなどの少なくとも1個の不活性希釈剤と混和されていてもよい。かかる固体剤形はまた、通常の実践の場合、不活性な希釈剤以外に追加の物質、例として、錠剤化潤滑剤および他の錠剤化補助剤(ステアリン酸マグネシウムおよび微結晶性セルロースなど)を含んでいてもよい。カプセル剤、錠剤、および丸剤のケースにおいて、剤形はまた、緩衝剤を含んでいてもよい。それらは任意に不透明化剤を含有していてもよく、それらはまた、活性成分(単数もしくは複数)のみを、またはこれを優先的に、腸管のある部分において、任意に遅延様式で、放出するという組成物からも成り得る。使用され得る包埋化組成物の例は、ポリマー物質およびワックスを包含する。
局所投与に好適な製剤は、リニメント、ローション、ゲル、外用薬(applications)などの液体調製物または半液体調製物、クリーム、軟膏、もしくはペーストなどの水中油型または油中水型エマルション;あるいは点滴薬などの溶液または懸濁液を包含する。皮膚表面への局所投与のための製剤は、薬物を、ローション、クリーム、軟膏、または石けんなどの皮膚科学的に許容し得る担体とともに分散させることによって調製され得る。有用な担体は、適用を局在化しかつ除去を阻害するためのフィルムまたは層を皮膚上に形成することが可能である。内部組織表面への局所投与について、剤は、液体組織接着剤または組織表面への吸着を増強することが知られている他の物質に分散させ得る。例えば、ヒドロキシプロピルセルロースまたはフィブリノゲン/トロンビンの溶液は、促進するために使用され得る。代替的に、ペクチン含有製剤などの組織コーティング溶液も使用され得る。点眼用製剤、点耳薬、および点眼薬もまた、本発明の範囲内のものとして企図される。加えて、本開示は経皮パッチの使用も企図し、これは剤の身体への制御送達を提供するという追加の利点を有する。かかる剤形は、剤を適正な媒体に溶解および/または分配することによって作製され得る。吸収増強剤はまた、剤の皮膚を越える流動を増大するのにも使用され得る。速度は、速度制御膜を提供すること、または剤をポリマーマトリックスもしくはゲルに分散させることのいずれかによって、制御され得る。
加えて、局所製剤のための担体は、水アルコール系(例として、液体およびゲル)、無水油もしくはシリコーンベースの系、またはエマルション系(これらに限定されないが、水中油型、油中水型、水中油中水型、およびシリコーン中水中油型のエマルションを包含する)の形態であり得る。エマルションは、薄いローション(これはまた、スプレー送達もしくはエアロゾル送達にも好適であり得る)、クリーム状の(creamy)ローション、ライトクリーム、ヘビークリーム等を包含する、広範囲の粘度(consistencies)に及び得る。エマルションはまた、マイクロエマルション系を包含し得る。他の好適な局所担体は、無水固体および半固体(ゲルおよびスティック(sticks)など);および水ベースのムース系を包含する。
本開示によって網羅されるのにはまた、キット(例として、医薬パック(pharmaceutical packs))もある。提供されるキットは、本明細書に記載の医薬組成物または化合物および容器(例として、バイアル、アンプル、瓶、シリンジ、および/またはディスペンサーパッケージ(dispenser package)、または他の好適な容器)を含んでもよい。いくつかの態様において、提供されるキットは任意にさらに、本明細書に記載の医薬組成物もしくは化合物の希釈または懸濁のための医薬賦形剤を含む第2容器を包含する。いくつかの態様において、第1容器および第2容器において提供される本明細書に記載の医薬組成物または化合物は、組み合わされて、1単位の剤形を形成する。
よって、一側面において、提供されるのは、本明細書に記載の化合物または医薬組成物を含む第1容器を包含するキットである。ある態様において、キットは、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の処置を、これを必要とする対象においてするのに有用である。ある態様において、キットは、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の予防を、これを必要とする対象においてするのに有用である。ある態様において、キットは、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の発症するリスクの低減を、これを必要とする対象においてするのに有用である。ある態様において、キットは、対象または細胞におけるHDAC6の活性(例として、増大した活性などの、異常な活性)を阻害するのに有用である。
ある態様において、本明細書に記載のキットはさらに、キットを使用するための指示を包含する。本明細書に記載のキットはまた、必要に応じ、米国食品医薬品局(FDA)などの規制当局による情報を包含していてもよい。ある態様において、キットに包含される情報は、処方情報である。ある態様において、キットおよび指示は、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の処置を、これを必要とする対象においてすることを提供する。ある態様において、キットおよび指示は、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の予防を、これを必要とする対象においてすることを提供する。ある態様において、キットおよび指示は、疾患(例として、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、またはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害)の発症するリスクの低減を、これを必要とする対象においてすることを提供する。ある態様において、キットおよび指示は、対象または細胞におけるHDAC6の活性(例として、増大した活性などの、異常な活性)を阻害することを提供する。本明細書に記載のキットは、本明細書に記載の1以上の追加の医薬品を別々の組成物として包含していてもよい。
処置の方法
HDAC6は、すべてのHDACパラログのなかでも構造および機能の点でユニークである。とりわけ、これは、2つの触媒(デアセチラーゼ)ドメインおよび亜鉛フィンガーユビキチン結合ドメインを保有する。HDAC6はヒストンを脱アセチル化しないものの、微小管安定性、軸索輸送およびミトコンドリア輸送、タンパク質凝集、ならびにオートファジーを包含する疾患に関係のある経路に影響を及ぼす複数の基質と相互作用する。例えば、HDAC6の直接的な基質(例として、タウ、チューブリン、およびHSP90)は、アルツハイマー病において鍵となる機序に関与している。そのユニークな構造および機能の結果として、HDAC6活性を選択的に標的にして阻害することは、複数のHDACパラログの広い阻害および/またはHDAC1および/または2の阻害に起因する臨床毒性(これは、ほとんどのFDA承認汎HDACインヒビターの用量制限毒性である、血小板減少症を引き起こすことが知られている)をもたらす現行のFDA承認HDACインヒビターに典型的な副作用を回避することもある。よって、HDAC6選択的インヒビターでのHDAC6に関する疾患の処置は、具体的に有効なこともある。
HDAC6は、すべてのHDACパラログのなかでも構造および機能の点でユニークである。とりわけ、これは、2つの触媒(デアセチラーゼ)ドメインおよび亜鉛フィンガーユビキチン結合ドメインを保有する。HDAC6はヒストンを脱アセチル化しないものの、微小管安定性、軸索輸送およびミトコンドリア輸送、タンパク質凝集、ならびにオートファジーを包含する疾患に関係のある経路に影響を及ぼす複数の基質と相互作用する。例えば、HDAC6の直接的な基質(例として、タウ、チューブリン、およびHSP90)は、アルツハイマー病において鍵となる機序に関与している。そのユニークな構造および機能の結果として、HDAC6活性を選択的に標的にして阻害することは、複数のHDACパラログの広い阻害および/またはHDAC1および/または2の阻害に起因する臨床毒性(これは、ほとんどのFDA承認汎HDACインヒビターの用量制限毒性である、血小板減少症を引き起こすことが知られている)をもたらす現行のFDA承認HDACインヒビターに典型的な副作用を回避することもある。よって、HDAC6選択的インヒビターでのHDAC6に関する疾患の処置は、具体的に有効なこともある。
本開示は、HDAC6に関する疾患および障害を処置するための方法を提供する。ある態様において、本出願は、増殖性疾患を処置する方法を提供する。ある態様において、本出願は、がんを処置する方法を提供する。ある態様において、本出願は、血液がんを処置する方法を提供する。ある態様において、本出願は、白血病、T細胞リンパ腫、ホジキン病、非ホジキンリンパ腫、または多発性骨髄腫を処置する方法を提供する。ある態様において、本出願は、固形腫瘍を含むがんを処置する方法を提供する。ある態様において、本出願は、神経膠腫、膠芽腫、非小細胞肺がん、脳腫瘍、神経芽細胞腫、骨腫瘍、軟部組織肉腫、頭頸部がん、尿生殖器がん、肺がん、乳房がん、膵臓がん、黒色腫、胃がん、脳がん、肝臓がん、甲状腺がん、明細胞癌、子宮がん、または卵巣がんを処置する方法を提供する。
ある態様において、本出願は、炎症性疾患を処置する方法を提供する。ある態様において、本出願は、骨関節炎、リウマチ性関節炎、ループス、炎症性腸疾患、クローン病、潰瘍性大腸炎、貧血症、白血球増加症、喘息、慢性閉塞性肺疾患、虫垂炎、気管支炎、滑液包炎、結膜炎、皮膚炎、脳炎、脊髄炎、心筋炎、副鼻腔炎、皮膚炎、乾癬、湿疹、または座瘡を処置する方法を提供する。
ある態様において、本出願は、感染性疾患を処置する方法を提供する。ある態様において、本出願は、細菌の、真菌の、または原生動物の感染症を処置する方法を提供する。
ある態様において、本出願は、自己免疫疾患を処置する方法を提供する。ある態様において、本出願は、糖尿病、甲状腺炎、グレーブス病、ギラン・バレー症候群、アジソン病、強皮症、原発性胆汁性肝硬変、ライター症候群、乾癬、慢性疲労、または子宮内膜症を処置する方法を提供する。
ある態様において、本出願は、異種免疫疾患を処置する方法を提供する。ある態様において、本出願は、移植片対宿主病、移植、輸血、アナフィラキシー、アレルギー性結膜炎、またはアレルギー性鼻炎を処置する方法を提供する。
ある態様において、本出願は、神経学的障害を処置する方法を提供する。ある態様において、本出願は、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患を処置する方法を提供する。ある態様において、本出願は、脆弱X症候群、シャルコー・マリー・トゥース病、アルツハイマー病、パーキンソン病、ハンチントン病、多発性硬化症、筋萎縮性側索硬化症、クロイツフェルト・ヤコブ病、レビー小体型認知症、血管性認知症、筋萎縮、発作誘発性の記憶喪失、統合失調症、ルビンシュタイン・テイビ症候群、レット症候群、注意欠陥多動性障害、失読症、双極性障害、自閉症に関連する社会障害、認知障害、および学習障害、注意欠陥障害、統合失調症、大うつ病性障害、末梢神経障害、糖尿病網膜症、糖尿病性末梢神経障害、化学療法誘発性の末梢神経障害、外傷性脳損傷(TBI)、慢性外傷性脳症(CTE)、またはタウオパチーを処置する方法を提供する。ある態様において、本出願は、原発性年齢関連タウオパチー(PART)/神経原線維優位型老年認知症、慢性外傷性脳症、ボクサー認知症、進行性の核上性麻痺、大脳皮質基底核変性症、ピック病、17番染色体に連関した前頭側頭型認知症およびパーキンソニズム、リティコ・ボディグ病、神経節膠腫、神経節細胞腫、髄膜血管腫症、脳炎後パーキンソニズム、亜急性硬化性全脳炎、鉛脳症、結節性硬化症、リポフスチン症、アルツハイマー病、または嗜銀性顆粒病を処置する方法を提供する。ある態様において、本出願は、アルツハイマー病を処置する方法を提供する。
ある態様において、本出願は、嚢胞性線維症を処置する方法を提供する。ある態様において、本出願は、多発性嚢胞腎疾患を処置する方法を提供する。ある態様において、本出願は、肺高血圧症を処置する方法を提供する。ある態様において、本出願は、心機能障害を処置する方法を提供する。
本開示は、HDACの活性を阻害する方法を提供する。ある態様において、本出願は、HDAC6の活性を阻害する方法を提供する。ある態様において、本出願は、HDAC6の活性をin vitroで阻害する方法を提供する。ある態様において、本出願は、HDAC6の活性をin vivoで阻害する方法を提供する。ある態様において、本出願は、細胞中のHDAC6の活性を阻害する方法を提供する。ある態様において、本出願は、ヒト細胞中のHDAC6の活性を阻害する方法を提供する。
ある態様において、方法は、HDAC6と相互作用する化合物、例えば、HDAC6のインヒビター、HDAC6のモジュレーター、HDAC6の結合剤である化合物、またはHDAC6を修飾する化合物を、これを必要とする対象(例として、神経学的障害の対象)へ投与することを含む。ある態様において、方法は、本開示の化合物(例として、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物)、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグ、あるいは組成物を、これを必要とする対象へ投与することを含む。いくつかの態様において、方法は、本開示の化合物(例として、式(I)、(II)、(III)、(IV)、(V)、もしくは(VI)で表される化合物)、またはその薬学的に許容し得る塩、共結晶、互変異性体、立体異性体、溶媒和物、水和物、多形、同位体が濃縮された誘導体、もしくはプロドラッグ、あるいは組成物を含む医薬組成物を、これを必要とする対象へ投与することを含む。
例
本明細書に記載の本発明がより完全に理解され得るために、以下の例を記す。本出願に記載の例は本明細書に提供される化合物、医薬組成物、および方法を説明するために供与されるが、いずれにしてもそれらの範囲を限定するものとして解釈されるべきではない。
本明細書に記載の本発明がより完全に理解され得るために、以下の例を記す。本出願に記載の例は本明細書に提供される化合物、医薬組成物、および方法を説明するために供与されるが、いずれにしてもそれらの範囲を限定するものとして解釈されるべきではない。
合成方法
一般的な詳細。
すべての酸素反応および/または感湿反応を、真空下(およそ0.5mmHg)で火力乾燥させて使用に先立ちN2でパージしたガラス製品中、窒素(N2)雰囲気下で実行した。すべての試薬および溶媒は、供給商業者(commercial vendors)から購入し、受け取った状態のまま使用するか、または既に報告された方法に従う合成に使用した。NMRスペクトルを、Bruker 300(300MHz 1H、75MHz 13C)分光計またはVariann UNITY INOVA 500(500MHz 1H、125MHz 13C)分光計上で記録した。プロトンおよび炭素の化学シフトは、NMR溶媒を参照しppm(δ)で報告する。データは、以下:化学シフト、多重度(br=ブロード、s=一重項、d=二重項、t=三重項、q=四重項、m=多重項;Hz単位のカップリング定数(単数または複数))のとおりに報告する。別様に指し示されていない限り、NMRデータは25℃にて収集した。フラッシュクロマトグラフィーは、Teledyne Isco Combiflash Rf上、40~60μmシリカゲル(60Aメッシュ)を使用して実施した。タンデム型液体クロマトグラフィー/質量分析(LC/MS)は、Waters 2795分離モジュールおよび3100質量検出器上で実施した。分析薄層クロマトグラフィー(TLC)は、EM Reagent 0.25mmシリカゲル60-Fプレート上で実施した。
一般的な詳細。
すべての酸素反応および/または感湿反応を、真空下(およそ0.5mmHg)で火力乾燥させて使用に先立ちN2でパージしたガラス製品中、窒素(N2)雰囲気下で実行した。すべての試薬および溶媒は、供給商業者(commercial vendors)から購入し、受け取った状態のまま使用するか、または既に報告された方法に従う合成に使用した。NMRスペクトルを、Bruker 300(300MHz 1H、75MHz 13C)分光計またはVariann UNITY INOVA 500(500MHz 1H、125MHz 13C)分光計上で記録した。プロトンおよび炭素の化学シフトは、NMR溶媒を参照しppm(δ)で報告する。データは、以下:化学シフト、多重度(br=ブロード、s=一重項、d=二重項、t=三重項、q=四重項、m=多重項;Hz単位のカップリング定数(単数または複数))のとおりに報告する。別様に指し示されていない限り、NMRデータは25℃にて収集した。フラッシュクロマトグラフィーは、Teledyne Isco Combiflash Rf上、40~60μmシリカゲル(60Aメッシュ)を使用して実施した。タンデム型液体クロマトグラフィー/質量分析(LC/MS)は、Waters 2795分離モジュールおよび3100質量検出器上で実施した。分析薄層クロマトグラフィー(TLC)は、EM Reagent 0.25mmシリカゲル60-Fプレート上で実施した。
式(I)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
8-フルオロ-N-ヒドロキシ-2-((1-メチルシクロプロピル)メチル)-1,2,3,4-テトラヒドロイソキノリン-6-カルボキサミド(1)
8-フルオロ-N-ヒドロキシ-2-((1-メチルシクロプロピル)メチル)-1,2,3,4-テトラヒドロイソキノリン-6-カルボキサミド(1)
MeOH中のメチル8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(A、150mg、0.717mmol、1当量)の溶液へ、1-メチルシクロプロパン-1-カルバルデヒド(B、66.3mg、0.7894mmol、1.1当量)を加えて15分間撹拌し、NaCNBH3(90.11mg、1.434mmol、2当量)を加えた。その結果得られた反応混合物を室温にて1時間撹拌した。反応完了後、揮発性物質を蒸発させた。粗材料をジクロロメタン(25ml)で希釈し、水で洗浄した。有機層を硫酸ナトリウム上で乾燥させ、濾過し濃縮した。粗産物をカラムクロマトグラフィーによって精製することで、メチル8-フルオロ-2-((1-メチルシクロプロピル)メチル)-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(C、98.3mg、0.3548mmol、50%)が粘着性固体として生産された。
メタノール(2mL)中のメチル8-フルオロ-2-((1-メチルシクロプロピル)メチル)-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(C、90mg、0.325mmol、1当量)の撹拌溶液へ、50%aq.NH2OH(214.4mg、6.498mmol、20当量;H2O中の50% aq溶液)およびKOH(35.6mg、0.648mmol、2当量)を0℃にて加えた。反応物を0℃~室温にて10分間撹拌し、次いでNaHCO3の飽和溶液でクエンチし、濾過してn-ヘキサンで洗浄することで、化合物1(0.010g、0.0359mmol、11%)が得られた。1H NMR(400MHz,DMSO-d6)δ11.23(bs,1H),9.09(bs,1H),7.40(s,1H),7.31(d,J=10.4Hz,1H),3.57(s,2H),2.88-2.84(m,2H),2.70(t,J=5.9Hz,2H),2.33(s,2H),1.05(s,3H),0.33(d,J=10.2Hz,4H)。MS(ESI):279[M+H]+.
以下の化合物を、化合物1を調製するのに使用したのと類似のやり方で調製した。化合物対8/9、30/31、107/108、および109/110は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
式(III)および(IV)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
4-((2-アザスピロ[4.5]デカン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(75)
4-((2-アザスピロ[4.5]デカン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(75)
アセトニトリル(5mL)中のメチル4-(ブロモメチル)-3-フルオロベンゾアート(D、150mg、0.6098mmol、1当量)の撹拌溶液へ、Cs2CO3(397mg、1.2196mmol、2.0当量)および2-アザスピロ[4.5]デカン(84mg、0.6098mmol、1当量)を室温にて加えた。反応物を室温にて2h撹拌し、次いで水(10mL)でクエンチして酢酸エチル(10mL×3)で抽出した。合わせた有機相をブライン(10mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、濾過してin vacuoで濃縮した。残渣をフラッシュシリカゲルカラムクロマトグラフィーによって精製した。産物をヘキサン中5%EtOAcにて溶離することで、4-((2-アザスピロ[4.5]デカン-2-イル)メチル)-3-フルオロベンゾアート(E)が無色油(110mg、0.3604mmol、59%)として与えられた。1H NMR(400MHz,CDCl3)δ7.81(dd,J=8.0,1.7Hz,1H),7.69(dd,J=10.4,1.7Hz,1H),7.55(s,1H),3.93(s,3H),3.71(s,2H),2.62(s,2H),2.39(s,2H),1.41(d,J=18.8Hz,12H),1.27(t,J=3.5Hz,1H)。MS(ESI):305[M+H]+
メタノール(1mL)中のメチル4-((2-アザスピロ[4.5]デカン-2-イル)メチル)-3-フルオロベンゾアート(E、110mg、0.3604mmol、1.0当量)の撹拌溶液へ、NH2OH(50%aq.)(0.4mL、7.2mmol、20.0当量)およびKOH(40mg、0.72mmol、2.0当量)を0℃にて加えた。反応物を0℃にて10分間撹拌し、次いでNaHCO3(2mL)の飽和溶液でクエンチした。白色化合物を沈殿させて濾過し、n-ヘキサンで洗浄することで、標題化合物(75)が灰白色固体(55mg、0.1795mmol、50%)として得られた。1H NMR(400MHz,DMSO-d6)δ11.17(s,1H),9.17(s,1H),7.56(d,J=7.8Hz,1H),7.52-7.39(m,2H),3.59(s,2H),2.30(s,2H),1.50(t,J=6.8Hz,2H),1.34(d,J=13.5Hz,10H)。MS(ESI):306.38[M+H]+
以下の化合物を、化合物75を調製するのに使用したのと類似のやり方で調製した。化合物対48/49および172/173は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
式(V)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
(S)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(79)、および
(R)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(80)
(S)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(79)、および
(R)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(80)
メチル2-アリル-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(G):
DCM(40mL)中のメチル8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(F、2.0g、9.556mmol、1.0当量)の溶液へ、DIPEA(2.46g、19.11mmol、2.0当量)および臭化アリル(1.26g、10.472mmol、1.1当量)を0℃にて加えた。反応混合物をrtにて2h撹拌した。反応をTLCおよび質量分析(mass)によって監視した。反応完了後、反応混合物を水に注ぎ、DCM(3×50mL)で抽出した。合わせた有機層をNa2SO4上で乾燥させ、減圧下で濃縮した。粗材料をフラッシュクロマトグラフィーによって精製した。所望の化合物を5%(エチルアセタート/ヘキサン)中で溶離することで、メチル2-アリル-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(G、1.6g、6.418mmol、67%)が、薄黄色がかった固体として供与された。MS(ESI):250[M+H]+
DCM(40mL)中のメチル8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(F、2.0g、9.556mmol、1.0当量)の溶液へ、DIPEA(2.46g、19.11mmol、2.0当量)および臭化アリル(1.26g、10.472mmol、1.1当量)を0℃にて加えた。反応混合物をrtにて2h撹拌した。反応をTLCおよび質量分析(mass)によって監視した。反応完了後、反応混合物を水に注ぎ、DCM(3×50mL)で抽出した。合わせた有機層をNa2SO4上で乾燥させ、減圧下で濃縮した。粗材料をフラッシュクロマトグラフィーによって精製した。所望の化合物を5%(エチルアセタート/ヘキサン)中で溶離することで、メチル2-アリル-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(G、1.6g、6.418mmol、67%)が、薄黄色がかった固体として供与された。MS(ESI):250[M+H]+
メチル10-フルオロ-5,6-ジヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(H):
トルエン(20mL)中のメチル2-アリル-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(G、1.6g、6.418mmol、1.0当量)の溶液へ、Ag2CO3(17.69g、64.18mmol、10.0当量)を室温にて加えた。反応混合物を110℃にて72h撹拌した。反応完了後、反応混合物を水(20ml)に注ぎ、酢酸エチル(3×50mL)で抽出した。合わせた有機層をNa2SO4上で乾燥させて減圧下で濃縮することで、メチル10-フルオロ-5,6ジヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(H、400mg、1.630mmol、25%)が帯黄色油として与えられた。MS(ESI):246[M+H]+
トルエン(20mL)中のメチル2-アリル-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-6-カルボキシラート(G、1.6g、6.418mmol、1.0当量)の溶液へ、Ag2CO3(17.69g、64.18mmol、10.0当量)を室温にて加えた。反応混合物を110℃にて72h撹拌した。反応完了後、反応混合物を水(20ml)に注ぎ、酢酸エチル(3×50mL)で抽出した。合わせた有機層をNa2SO4上で乾燥させて減圧下で濃縮することで、メチル10-フルオロ-5,6ジヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(H、400mg、1.630mmol、25%)が帯黄色油として与えられた。MS(ESI):246[M+H]+
メチル10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(I):
THF(5mL)中のメチル10-フルオロ-5,6-ジヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(H、400mg、1.630mmol、1当量)の撹拌溶液へ、(200psi)でのH2雰囲気下で撹拌しながら1N HCl(cat.)およびPtO2(200mg)を加え、混合物を室温で8h撹拌した。反応完了後、触媒を、THFの洗浄によるセライトで濾別した。残渣をフラッシュクロマトグラフィーによって精製し、所望の化合物を10%(MeOH/DCM)中で溶離することで、メチル10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラートが黄色油(I、190mg、0.762mmol、47%)として与えられた。100mgのラセミ化合物をWaters SFC 200およびUV検出器上で精製した。カラムとしてChiralpak IG(250*21.0)mm、5ミクロンを使用し、カラムフローは80.0ml/minであり、ABPRは100barであった。移動相として(A)液体二酸化炭素(Liq.CO2)および(B)メタノール:アセトニトリル(50:50)中0.1%DEAを使用した。(Fr-1(Ia):20mg LCMS-100%、Fr-2(Ib):32mg LCMS-100%)。MS(ESI):250[M+H]+
THF(5mL)中のメチル10-フルオロ-5,6-ジヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(H、400mg、1.630mmol、1当量)の撹拌溶液へ、(200psi)でのH2雰囲気下で撹拌しながら1N HCl(cat.)およびPtO2(200mg)を加え、混合物を室温で8h撹拌した。反応完了後、触媒を、THFの洗浄によるセライトで濾別した。残渣をフラッシュクロマトグラフィーによって精製し、所望の化合物を10%(MeOH/DCM)中で溶離することで、メチル10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラートが黄色油(I、190mg、0.762mmol、47%)として与えられた。100mgのラセミ化合物をWaters SFC 200およびUV検出器上で精製した。カラムとしてChiralpak IG(250*21.0)mm、5ミクロンを使用し、カラムフローは80.0ml/minであり、ABPRは100barであった。移動相として(A)液体二酸化炭素(Liq.CO2)および(B)メタノール:アセトニトリル(50:50)中0.1%DEAを使用した。(Fr-1(Ia):20mg LCMS-100%、Fr-2(Ib):32mg LCMS-100%)。MS(ESI):250[M+H]+
(S)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(79):
MeOH(1mL)中のメチル(S)-10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(Ia、20mg、0.080mmol、1.0当量)の溶液へ、NH2OH(0.1mL、1.606mmol、50%水溶液、20.0当量)およびKOH(14mg、0.240mmol、3.0当量)を0℃~室温にて加え、反応物を10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視し、反応をNaHCO3の飽和溶液でクエンチして10分間撹拌した。形成された沈殿物を濾過し、水およびn-ヘキサンで洗浄することで、粗産物が白色残渣として得られた。粗化合物を、水中5mM ABC+0.1%NH3およびCH3CNを移動相として使用する分取HPLC法によって精製することで、(S)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド、(79、7.884mg、0.031mmol、39%収率)が黄色油として与えられた。1H NMR(400MHz,DMSO-d6)δ7.40(s,1H),7.29(d,J=11.0Hz,1H),3.67(t,J=8.3Hz,1H),2.99-2.87(m,2H),2.80-2.58(m,4H),2.38-2.30(m,1H),1.86-1.70(m,2H),1.62-1.51(m,1H)。MS(ESI):251[M+H]+
MeOH(1mL)中のメチル(S)-10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(Ia、20mg、0.080mmol、1.0当量)の溶液へ、NH2OH(0.1mL、1.606mmol、50%水溶液、20.0当量)およびKOH(14mg、0.240mmol、3.0当量)を0℃~室温にて加え、反応物を10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視し、反応をNaHCO3の飽和溶液でクエンチして10分間撹拌した。形成された沈殿物を濾過し、水およびn-ヘキサンで洗浄することで、粗産物が白色残渣として得られた。粗化合物を、水中5mM ABC+0.1%NH3およびCH3CNを移動相として使用する分取HPLC法によって精製することで、(S)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド、(79、7.884mg、0.031mmol、39%収率)が黄色油として与えられた。1H NMR(400MHz,DMSO-d6)δ7.40(s,1H),7.29(d,J=11.0Hz,1H),3.67(t,J=8.3Hz,1H),2.99-2.87(m,2H),2.80-2.58(m,4H),2.38-2.30(m,1H),1.86-1.70(m,2H),1.62-1.51(m,1H)。MS(ESI):251[M+H]+
(R)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10bヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(80):
MeOH(1mL)中のメチル(R)-10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(Ib、32mg、0.128mmol、1.0当量)の溶液へ、NH2OH(0.2mL、2.567mmol、50%水溶液、20.0当量)およびKOH(21.56mg、0.385mmol、3.0当量)を0℃~室温にて加え、反応物を10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視し、反応をNaHCO3の飽和溶液でクエンチして10分間撹拌した。形成された沈殿物を濾過し、水およびn-ヘキサンで洗浄することで、粗産物が白色残渣として得られた。粗化合物を、水中5mM ABC+0.1%NH3およびCH3CNを移動相として使用する分取HPLC法によって精製することで、(R)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10bヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(80、6.924mg、0.027mmol、21%収率)が与えられた。1H NMR(400MHz,DMSO-d6)δ7.38(s,1H),7.29(d,J=11.0Hz,1H),3.67(t,J=8.3Hz,1H),2.99-2.87(m,2H),2.80-2.58(m,4H),2.38-2.30(m,1H),1.86-1.70(m,2H),1.62-1.51(m,1H)。MS(ESI):251[M+H]+
MeOH(1mL)中のメチル(R)-10-フルオロ-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキシラート(Ib、32mg、0.128mmol、1.0当量)の溶液へ、NH2OH(0.2mL、2.567mmol、50%水溶液、20.0当量)およびKOH(21.56mg、0.385mmol、3.0当量)を0℃~室温にて加え、反応物を10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視し、反応をNaHCO3の飽和溶液でクエンチして10分間撹拌した。形成された沈殿物を濾過し、水およびn-ヘキサンで洗浄することで、粗産物が白色残渣として得られた。粗化合物を、水中5mM ABC+0.1%NH3およびCH3CNを移動相として使用する分取HPLC法によって精製することで、(R)-10-フルオロ-N-ヒドロキシ-1,2,3,5,6,10bヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(80、6.924mg、0.027mmol、21%収率)が与えられた。1H NMR(400MHz,DMSO-d6)δ7.38(s,1H),7.29(d,J=11.0Hz,1H),3.67(t,J=8.3Hz,1H),2.99-2.87(m,2H),2.80-2.58(m,4H),2.38-2.30(m,1H),1.86-1.70(m,2H),1.62-1.51(m,1H)。MS(ESI):251[M+H]+
化合物79および80は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(S)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(89)および(R)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(90)
(S)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(89)および(R)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(90)
1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-オール(K):
ジクロロメタン(15mL)中の9-メトキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン(J、1.2g、5.52mmol、1.0当量)の溶液へ、DCM(14ml、13.81mmol、2.0当量)中1M BBr3を0℃にて加え、室温にて3hrs撹拌した。反応完了後、冷水(10ml)を反応混合物へ加え、形成された沈殿物をブフナー漏斗に通して濾過し、氷冷DCM(15mL)で洗浄した。固体をDCM(150mL)中5%メタノールに吸収され、gave wash of重炭酸塩の飽和溶液(100mL)の洗浄をした。有機層を分離し、Na2SO4上で乾燥させて蒸発乾固させることで、1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-オール(K、1.0g、4.92mmol、89%収率)が与えられた。MS(ESI):204[M+H]+
ジクロロメタン(15mL)中の9-メトキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン(J、1.2g、5.52mmol、1.0当量)の溶液へ、DCM(14ml、13.81mmol、2.0当量)中1M BBr3を0℃にて加え、室温にて3hrs撹拌した。反応完了後、冷水(10ml)を反応混合物へ加え、形成された沈殿物をブフナー漏斗に通して濾過し、氷冷DCM(15mL)で洗浄した。固体をDCM(150mL)中5%メタノールに吸収され、gave wash of重炭酸塩の飽和溶液(100mL)の洗浄をした。有機層を分離し、Na2SO4上で乾燥させて蒸発乾固させることで、1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-オール(K、1.0g、4.92mmol、89%収率)が与えられた。MS(ESI):204[M+H]+
1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-イルトリフルオロメタンスルホナート(L):
乾燥DCM(15mL)中の1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-オール(K、1.0g、4.92mmol、1.0当量)の撹拌溶液へ、トリエチルアミン(1.6ml、12.31mmol、2.5当量)および4-ジメチルアミノ)ピリジン(60mg、0.49mmol、0.1当量)を加えた。約20分後、N-フェニルビス(トリフルオロメタンスルホンイミド)(2.63g、7.38mmol、1.5当量)を分けて(in portions)加えた。添加が完了したら反応混合物を室温にて8h撹拌し、TLCおよびLC-MSで監視した。反応完了後、溶媒を減圧下で除去し、こうして得られた産物を、ヘキサン中70%EtOAcを使用するシリカゲルクロマトグラフィーで精製することで、1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-イルトリフルオロメタンスルホナート(L、1.35g、4.0mmol、82%収率)が茶色油として供与された。MS(ESI):336[M+H]+
乾燥DCM(15mL)中の1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-オール(K、1.0g、4.92mmol、1.0当量)の撹拌溶液へ、トリエチルアミン(1.6ml、12.31mmol、2.5当量)および4-ジメチルアミノ)ピリジン(60mg、0.49mmol、0.1当量)を加えた。約20分後、N-フェニルビス(トリフルオロメタンスルホンイミド)(2.63g、7.38mmol、1.5当量)を分けて(in portions)加えた。添加が完了したら反応混合物を室温にて8h撹拌し、TLCおよびLC-MSで監視した。反応完了後、溶媒を減圧下で除去し、こうして得られた産物を、ヘキサン中70%EtOAcを使用するシリカゲルクロマトグラフィーで精製することで、1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-イルトリフルオロメタンスルホナート(L、1.35g、4.0mmol、82%収率)が茶色油として供与された。MS(ESI):336[M+H]+
メチル1,3,4,6,7,11b-ヘキサヒドロ-2Hピリド[2,1-a]イソキノリン-9-カルボキシラート(M):
乾燥メタノール(20mL)中の1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-イルトリフルオロメタンスルホナート(3、0.9g、2.68mmol、1.0当量)の撹拌溶液へ、DMF(2ml)をN2ガスで10分間脱気した。酢酸パラジウム(9mg、0.040mmol、0.15当量)、1,3-ビス(ジフェニルホスフィノ)プロパン(0.221g、0.53mmol、0.2当量)、TEA(1.12mL、8.05mmol、3当量)を上の反応混合物へ加えた。反応混合物をCO(250psi)の雰囲気下120℃にて1h撹拌した。混合物を室温まで冷却し、固体を濾過によって除去した。濾過物を減圧下で濃縮し、残渣を、シリカゲルフラッシュクロマトグラフィー(70%EtOAc/ヘキサン)によって精製することで、メチル1,3,4,6,7,11b-ヘキサヒドロ-2Hピリド[2,1-a]イソキノリン-9-カルボキシラート(M、0.38g、1.55mmol、58%収率)が提供された。Mの鏡像異性体を、120mgスケールのWaters SFC 200およびUV検出器で分離した。カラムとしてChiralpak IG(250*21.0)mm、5ミクロンを使用し、カラムフローは80.0ml /minであり、ABPRは100barであった。移動相として(A)液体二酸化炭素(Liq.CO2)および(B)メタノール中0.1%DEAを使用した。UVスペクトルを236nm Lambdamaxにて記録した。(Fr-1(Ma):40mg LCMS-100%、Fr-2(Mb):57mg LCMS-100%)。MS(ESI):246[M+H]+
乾燥メタノール(20mL)中の1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-イルトリフルオロメタンスルホナート(3、0.9g、2.68mmol、1.0当量)の撹拌溶液へ、DMF(2ml)をN2ガスで10分間脱気した。酢酸パラジウム(9mg、0.040mmol、0.15当量)、1,3-ビス(ジフェニルホスフィノ)プロパン(0.221g、0.53mmol、0.2当量)、TEA(1.12mL、8.05mmol、3当量)を上の反応混合物へ加えた。反応混合物をCO(250psi)の雰囲気下120℃にて1h撹拌した。混合物を室温まで冷却し、固体を濾過によって除去した。濾過物を減圧下で濃縮し、残渣を、シリカゲルフラッシュクロマトグラフィー(70%EtOAc/ヘキサン)によって精製することで、メチル1,3,4,6,7,11b-ヘキサヒドロ-2Hピリド[2,1-a]イソキノリン-9-カルボキシラート(M、0.38g、1.55mmol、58%収率)が提供された。Mの鏡像異性体を、120mgスケールのWaters SFC 200およびUV検出器で分離した。カラムとしてChiralpak IG(250*21.0)mm、5ミクロンを使用し、カラムフローは80.0ml /minであり、ABPRは100barであった。移動相として(A)液体二酸化炭素(Liq.CO2)および(B)メタノール中0.1%DEAを使用した。UVスペクトルを236nm Lambdamaxにて記録した。(Fr-1(Ma):40mg LCMS-100%、Fr-2(Mb):57mg LCMS-100%)。MS(ESI):246[M+H]+
(S)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(89):
メタノール(1.5mL)中のメチル(R)-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキシラート(Ma、40mg、0.163mmol、1.0当量)の溶液へ、NH2OH(0.215mL、3.26mmol、50%水溶液、20.0当量)およびKOH(27.46mg、0.489mmol、3.0当量)を0℃にて加え、室温にて1h撹拌した。反応の完了をTLCによって確認した。反応混合物を蒸発乾固させた;粗材料を、(A)水中5mM重炭酸アンモニウム+0.1%アンモニア、(2)100%アセトニトリルを使用する分取HPLC精製によって精製した。溶媒を凍結乾燥させることで、(S)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(89、9mg、0.036mmol、22%収率)が与えられた。1H NMR(400MHz,DMSO-d6)δ11.06(s,1H),8.96(s,1H),7.58-7.38(m,2H),7.30(d,J=8.1Hz,1H),3.14-2.84(m,4H),2.67(d,J=15.0Hz,1H),2.35-2.18(m,3H),1.83(d,J=12.2Hz,1H),1.64-1.39(m,3H),1.29-1.17(m,1H)。MS(ESI):245[M-H]-
メタノール(1.5mL)中のメチル(R)-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキシラート(Ma、40mg、0.163mmol、1.0当量)の溶液へ、NH2OH(0.215mL、3.26mmol、50%水溶液、20.0当量)およびKOH(27.46mg、0.489mmol、3.0当量)を0℃にて加え、室温にて1h撹拌した。反応の完了をTLCによって確認した。反応混合物を蒸発乾固させた;粗材料を、(A)水中5mM重炭酸アンモニウム+0.1%アンモニア、(2)100%アセトニトリルを使用する分取HPLC精製によって精製した。溶媒を凍結乾燥させることで、(S)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(89、9mg、0.036mmol、22%収率)が与えられた。1H NMR(400MHz,DMSO-d6)δ11.06(s,1H),8.96(s,1H),7.58-7.38(m,2H),7.30(d,J=8.1Hz,1H),3.14-2.84(m,4H),2.67(d,J=15.0Hz,1H),2.35-2.18(m,3H),1.83(d,J=12.2Hz,1H),1.64-1.39(m,3H),1.29-1.17(m,1H)。MS(ESI):245[M-H]-
(R)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(90):
メタノール(1.5mL)中のメチル(S)-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキシラート(Mb、57mg、0.23mmol、1.0当量)の溶液へ、NH2OH(0.307mL、4.65mmol、50.00%水溶液、20.0当量)およびKOH(39.16mg、0.69mmol、3.0当量)を0℃にて加え、室温にて1hr撹拌した。反応の完了をTLCによって確認した。反応混合物を蒸発乾固させた;粗材料を、(A)水中5mM重炭酸アンモニウム塩+0.1%アンモニア、(2)100%アセトニトリルを使用する分取HPLC精製によって精製した。溶媒を凍結乾燥させることで、(R)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(90、16.8mg、0.068mmol、29%)が与えられた。1H NMR(400MHz,DMSO-d6)δ10.83(s,1H),8.96(s,1H),7.64-7.38(m,2H),7.30(d,J=8.1Hz,1H),3.09-2.88(m,4H),2.68(m,1H),2.33-2.23(m,3H),1.83(d,J=12.4Hz,1H),1.62-1.39(m,3H),1.24-1.18(m,1H)。MS(ESI):245[M-H]-
メタノール(1.5mL)中のメチル(S)-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキシラート(Mb、57mg、0.23mmol、1.0当量)の溶液へ、NH2OH(0.307mL、4.65mmol、50.00%水溶液、20.0当量)およびKOH(39.16mg、0.69mmol、3.0当量)を0℃にて加え、室温にて1hr撹拌した。反応の完了をTLCによって確認した。反応混合物を蒸発乾固させた;粗材料を、(A)水中5mM重炭酸アンモニウム塩+0.1%アンモニア、(2)100%アセトニトリルを使用する分取HPLC精製によって精製した。溶媒を凍結乾燥させることで、(R)-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(90、16.8mg、0.068mmol、29%)が与えられた。1H NMR(400MHz,DMSO-d6)δ10.83(s,1H),8.96(s,1H),7.64-7.38(m,2H),7.30(d,J=8.1Hz,1H),3.09-2.88(m,4H),2.68(m,1H),2.33-2.23(m,3H),1.83(d,J=12.4Hz,1H),1.62-1.39(m,3H),1.24-1.18(m,1H)。MS(ESI):245[M-H]-
化合物89および90は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(93)、および
(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(94)
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(93)、および
(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(94)
2-(3-フルオロ-5-メトキシベンジル)ピリジン(P):
乾燥THF(10mL)中の1-(ブロモメチル)-3-フルオロ-5-メトキシベンゼン、(O、5.3g、24.2mmol、1当量)の溶液を窒素下、乾燥THF(40mL)中の亜鉛末(7.86g、121.0mmol)(aq.HClで洗浄することによって活性化した)の懸濁液へ滴加した。フラスコが室温に達したらすぐに、その結果得られた溶液を、乾燥THF(40mL)中の2-ブロモピリジン(N、3.82g、24.2mmol、1当量)とPd(PPh3)4(0.2796g、0.242mmol、1mol%)との撹拌した混合物へ加えた。混合物を終夜撹拌した。溶媒を蒸発させて残渣を、AcOEt-ヘキサンを溶離液として使用するカラムクロマトグラフィーによって精製することで、2-(3-フルオロ-5-メトキシベンジル)ピリジン(P、4.1g、78.1%)が無色油として与えられた。MS(ESI):218[M+H]+
乾燥THF(10mL)中の1-(ブロモメチル)-3-フルオロ-5-メトキシベンゼン、(O、5.3g、24.2mmol、1当量)の溶液を窒素下、乾燥THF(40mL)中の亜鉛末(7.86g、121.0mmol)(aq.HClで洗浄することによって活性化した)の懸濁液へ滴加した。フラスコが室温に達したらすぐに、その結果得られた溶液を、乾燥THF(40mL)中の2-ブロモピリジン(N、3.82g、24.2mmol、1当量)とPd(PPh3)4(0.2796g、0.242mmol、1mol%)との撹拌した混合物へ加えた。混合物を終夜撹拌した。溶媒を蒸発させて残渣を、AcOEt-ヘキサンを溶離液として使用するカラムクロマトグラフィーによって精製することで、2-(3-フルオロ-5-メトキシベンジル)ピリジン(P、4.1g、78.1%)が無色油として与えられた。MS(ESI):218[M+H]+
2-(3-フルオロ-5-メトキシベンジル)ピペリジン(Q):
THF(15mL)中の2-(3-フルオロ-5-メトキシベンジル)ピリジン(P、4.0g、18.430mmol、1当量)の撹拌溶液へ、1N HCl(0.5mL)およびPtO2(100mg)を撹拌しながら加えた。反応混合物をH2雰囲気下(200psi)室温にて4h撹拌し、触媒をセライトで濾別してTHFで洗浄した。溶媒を減圧下で蒸発させることで、2-(3-フルオロ-5-メトキシベンジル)ピペリジンが白色固体(Q、2.3g、10.31mmol、56%)として与えられ、これをさらなる精製はせずに次の反応へ使用した。MS(ESI):224[M+H]+
THF(15mL)中の2-(3-フルオロ-5-メトキシベンジル)ピリジン(P、4.0g、18.430mmol、1当量)の撹拌溶液へ、1N HCl(0.5mL)およびPtO2(100mg)を撹拌しながら加えた。反応混合物をH2雰囲気下(200psi)室温にて4h撹拌し、触媒をセライトで濾別してTHFで洗浄した。溶媒を減圧下で蒸発させることで、2-(3-フルオロ-5-メトキシベンジル)ピペリジンが白色固体(Q、2.3g、10.31mmol、56%)として与えられ、これをさらなる精製はせずに次の反応へ使用した。MS(ESI):224[M+H]+
7-フルオロ-9-メトキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン(Ra)、および
9-フルオロ-7-メトキシ1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン(Rb):
酢酸/トリフルオロ酢酸(4:1)(10mL)中の2-(3-フルオロ-5-メトキシベンジル)ピペリジン(Q、2.3g、10.31mmol、1当量)の撹拌溶液へ、シールド管中ヘキサメチレンテトラミン(2.908g、20.62mmol、2当量)を加えた。反応混合物を100℃にて4時間撹拌し、TLC分析によって監視した。反応完了後、混合物を水性重炭酸ナトリウム(20mL)の添加によって慎重にクエンチし、酢酸エチル(2×20mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を減圧下で濃縮し、カラムクロマトグラフィーによって精製することで、7-フルオロ-9-メトキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン(Ra)と9-フルオロ-7-メトキシ1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリンとの混合物が白色固体(Rb)(1.5g、6.383mmols、62%)として生産された。RaとRbとの混合物を、さらなる精製はせずに次のステップへ使用した。ほんのわずかのRaを精製し、1H NMRによって特徴付けた。1H NMR(400MHz,クロロホルム-d)δ6.44(d,J=12.4Hz,1H),4.03(d,J=15.5Hz,1H),3.77(s,2H),3.25-3.07(m,1H),2.75(q,J=10.0,8.1Hz,1H),2.34-2.12(m,1H),1.38(s,2H),1.31-1.18(m,1H)。MS(ESI):236[M+H]+
9-フルオロ-7-メトキシ1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン(Rb):
酢酸/トリフルオロ酢酸(4:1)(10mL)中の2-(3-フルオロ-5-メトキシベンジル)ピペリジン(Q、2.3g、10.31mmol、1当量)の撹拌溶液へ、シールド管中ヘキサメチレンテトラミン(2.908g、20.62mmol、2当量)を加えた。反応混合物を100℃にて4時間撹拌し、TLC分析によって監視した。反応完了後、混合物を水性重炭酸ナトリウム(20mL)の添加によって慎重にクエンチし、酢酸エチル(2×20mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を減圧下で濃縮し、カラムクロマトグラフィーによって精製することで、7-フルオロ-9-メトキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン(Ra)と9-フルオロ-7-メトキシ1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリンとの混合物が白色固体(Rb)(1.5g、6.383mmols、62%)として生産された。RaとRbとの混合物を、さらなる精製はせずに次のステップへ使用した。ほんのわずかのRaを精製し、1H NMRによって特徴付けた。1H NMR(400MHz,クロロホルム-d)δ6.44(d,J=12.4Hz,1H),4.03(d,J=15.5Hz,1H),3.77(s,2H),3.25-3.07(m,1H),2.75(q,J=10.0,8.1Hz,1H),2.34-2.12(m,1H),1.38(s,2H),1.31-1.18(m,1H)。MS(ESI):236[M+H]+
7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-オール(Sa)、および
9-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-7-オール(Sb):
DCM(25mL)中のSaおよびSb(1.2g、5.106mmol、1当量)の撹拌溶液へ、BBr3溶液(3.19g、12.76mmol、2.5当量)を加えた。反応混合物をrtまで加温させ、TLC分析で監視した。反応完了後、反応混合物を水性重炭酸ナトリウム(25mL)の添加によって慎重にクエンチし、酢酸エチル(5×25mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を濃縮することで、混合物 of 7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-オール(Sa)と9-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-7-オール(Sb)との混合物が茶色固体(890mg、4.022mmol、79%)として生産された。SaとSbとの混合物を、さらなる精製はせずに次のステップに使用した。MS(ESI):222[M+H]+
9-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-7-オール(Sb):
DCM(25mL)中のSaおよびSb(1.2g、5.106mmol、1当量)の撹拌溶液へ、BBr3溶液(3.19g、12.76mmol、2.5当量)を加えた。反応混合物をrtまで加温させ、TLC分析で監視した。反応完了後、反応混合物を水性重炭酸ナトリウム(25mL)の添加によって慎重にクエンチし、酢酸エチル(5×25mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を濃縮することで、混合物 of 7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-オール(Sa)と9-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-7-オール(Sb)との混合物が茶色固体(890mg、4.022mmol、79%)として生産された。SaとSbとの混合物を、さらなる精製はせずに次のステップに使用した。MS(ESI):222[M+H]+
7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-イルトリフルオロメタンスルホナート(Ta)、および
8-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-10-イルトリフルオロメタンスルホナート(Tb):
ピリジン(5mL)中のSaおよびSb(450g、2.036mmol、1当量)の撹拌溶液へ、Tf2O(851.7mg、3.108mmol、1.5当量)を加えた。反応混合物をrtまで加温させてTLC分析で監視した。反応完了後、反応混合物を水の添加によって慎重にクエンチし、酢酸エチル(3×25mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を濃縮することで、TaとTbとの混合物が粘着性固体(710mg、2.011mmols、99%)として生産された。TaとTbとの混合物をさらなる精製はせずに次のステップに使用した。MS(ESI):354[M+H]+
8-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-10-イルトリフルオロメタンスルホナート(Tb):
ピリジン(5mL)中のSaおよびSb(450g、2.036mmol、1当量)の撹拌溶液へ、Tf2O(851.7mg、3.108mmol、1.5当量)を加えた。反応混合物をrtまで加温させてTLC分析で監視した。反応完了後、反応混合物を水の添加によって慎重にクエンチし、酢酸エチル(3×25mL)で抽出して硫酸ナトリウム上で乾燥させた。有機層を濃縮することで、TaとTbとの混合物が粘着性固体(710mg、2.011mmols、99%)として生産された。TaとTbとの混合物をさらなる精製はせずに次のステップに使用した。MS(ESI):354[M+H]+
メチル7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキシラート(Ua):
MeOH(25mL)中のTaおよびTb(700mg、1.9830mmol、1当量)の溶液へ、Pd(OAc)2(64mg、0.285mmol、0.15当量)、トリエチルアミン(0.9595mg、9.5mmol、5当量)、およびDPPP(156.5mg、0.38mmol、0.2当量)を加えた。その結果得られた混合物を、窒素ガスを使用して脱気した。反応混合物を一酸化炭素圧力(350psi)下110℃にて24h撹拌した。反応混合物をセライトパッドに通して濾過し、濾過物を減圧下で濃縮した。粗反応混合物をカラムクロマトグラフィーによって精製することで、U(175mg、0.6653mmol、34%収率)が生産された。100mgのUを分取HPLC(Shimadzu LC-20APおよびUV検出器)によって精製した。カラムとしてCHIRALPAK IG(250*21.0)mm、5ミクロンを使用した;カラムフローは12.0ml/minであった。個々の鏡像異性体を提供する移動相:(A)ヘキサン中0.1%DEA、(B)IPA:MEOH(50:50)中0.1%DEA。(Fr-1(Ua):42mg LCMS-100%、Fr-2(Ub):32mg LCMS-100%)。Ua:1H NMR(400MHz,クロロホルム-d)δ7.60(s,1H),7.51(d,J=10.0Hz,1H),4.17(d,J=17.0Hz,1H),3.92(s,3H),3.33(s,1H),3.20(s,1H),2.86(s,2H),2.27(s,2H),1.91(s,2H),1.79(s,2H),1.28(s,1H)。MS(ESI):264[M+H]+
MeOH(25mL)中のTaおよびTb(700mg、1.9830mmol、1当量)の溶液へ、Pd(OAc)2(64mg、0.285mmol、0.15当量)、トリエチルアミン(0.9595mg、9.5mmol、5当量)、およびDPPP(156.5mg、0.38mmol、0.2当量)を加えた。その結果得られた混合物を、窒素ガスを使用して脱気した。反応混合物を一酸化炭素圧力(350psi)下110℃にて24h撹拌した。反応混合物をセライトパッドに通して濾過し、濾過物を減圧下で濃縮した。粗反応混合物をカラムクロマトグラフィーによって精製することで、U(175mg、0.6653mmol、34%収率)が生産された。100mgのUを分取HPLC(Shimadzu LC-20APおよびUV検出器)によって精製した。カラムとしてCHIRALPAK IG(250*21.0)mm、5ミクロンを使用した;カラムフローは12.0ml/minであった。個々の鏡像異性体を提供する移動相:(A)ヘキサン中0.1%DEA、(B)IPA:MEOH(50:50)中0.1%DEA。(Fr-1(Ua):42mg LCMS-100%、Fr-2(Ub):32mg LCMS-100%)。Ua:1H NMR(400MHz,クロロホルム-d)δ7.60(s,1H),7.51(d,J=10.0Hz,1H),4.17(d,J=17.0Hz,1H),3.92(s,3H),3.33(s,1H),3.20(s,1H),2.86(s,2H),2.27(s,2H),1.91(s,2H),1.79(s,2H),1.28(s,1H)。MS(ESI):264[M+H]+
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(93):
メタノール(2mL)中のメチル(S)-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキシラート(Ua、42mg、0.1597mmol、1当量)の撹拌溶液へ、50%aq.H2OH(0.0210mL、3.194mmol、20当量;H2O中の50%aq溶液)およびKOH(17.88mg、0.3194mmol、2当量)を0℃にて加えた。反応物を0℃~rtにて10分間撹拌し、次いでNaHCO3の飽和溶液でクエンチし、n-ヘキサンで洗浄することで白色残渣が得られたが、移動相としてACNおよび水を使用する分取HPLC精製によって精製することで、純粋な(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(93、18.2mg、0.0688mmol、43%)が入手された。1H NMR(400MHz,DMSO-d6)δ11.20(s,1H),9.10(s,1H),7.36(s,1H),7.30(d,J=10.0Hz,1H),3.93(d,J=16.4Hz,1H),3.12(d,J=16.5Hz,1H),3.01(d,J=11.5Hz,1H),2.80(dd,J=17.1,3.7Hz,1H),2.16(t,J=6.6Hz,1H),2.05(td,J=11.8,2.8Hz,1H),1.80(d,J=11.4Hz,1H),1.76-1.59(m,2H),1.51(d,J=13.1Hz,1H),1.25(q,J=13.6Hz,2H)。MS(ESI):265[M+H]+
メタノール(2mL)中のメチル(S)-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキシラート(Ua、42mg、0.1597mmol、1当量)の撹拌溶液へ、50%aq.H2OH(0.0210mL、3.194mmol、20当量;H2O中の50%aq溶液)およびKOH(17.88mg、0.3194mmol、2当量)を0℃にて加えた。反応物を0℃~rtにて10分間撹拌し、次いでNaHCO3の飽和溶液でクエンチし、n-ヘキサンで洗浄することで白色残渣が得られたが、移動相としてACNおよび水を使用する分取HPLC精製によって精製することで、純粋な(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(93、18.2mg、0.0688mmol、43%)が入手された。1H NMR(400MHz,DMSO-d6)δ11.20(s,1H),9.10(s,1H),7.36(s,1H),7.30(d,J=10.0Hz,1H),3.93(d,J=16.4Hz,1H),3.12(d,J=16.5Hz,1H),3.01(d,J=11.5Hz,1H),2.80(dd,J=17.1,3.7Hz,1H),2.16(t,J=6.6Hz,1H),2.05(td,J=11.8,2.8Hz,1H),1.80(d,J=11.4Hz,1H),1.76-1.59(m,2H),1.51(d,J=13.1Hz,1H),1.25(q,J=13.6Hz,2H)。MS(ESI):265[M+H]+
(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(94):
メタノール(2mL)中のメチル(R)-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキシラート(Ub、38mg、0.1444mmol、1当量)の撹拌溶液へ、50%aq.NH2OH(0.0190mL、2.889mmol、20当量;H2O中の50%aq溶液)およびKOH(16.19mg、0.2889mmol、2当量)を0℃にて加えた。反応物を0℃~rtにて10分間撹拌し、次いでNaHCO3の飽和溶液でクエンチし、濾過してn-ヘキサンで洗浄することで白色残渣が得られたが、移動相としてACNおよび水を使用する分取HPLC精製によって精製することで、純粋な(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(94、19.482mg、0.07407mmol、51%)が入手された。1H NMR(400MHz,DMSO-d6)δ11.22(s,1H),9.10(s,1H),7.35(s,1H),7.30(d,J=10.0Hz,1H),3.93(d,J=16.8Hz,1H),3.12(d,J=16.6Hz,1H),3.01(d,J=11.2Hz,1H),2.80(d,J=17.1Hz,1H),2.16(s,1H),2.05(t,J=11.7Hz,1H),1.80(d,J=11.1Hz,1H),1.76-1.59(m,2H),1.51(m,1H),1.25(m,2H)。MS(ESI):265[M+H]+.
メタノール(2mL)中のメチル(R)-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキシラート(Ub、38mg、0.1444mmol、1当量)の撹拌溶液へ、50%aq.NH2OH(0.0190mL、2.889mmol、20当量;H2O中の50%aq溶液)およびKOH(16.19mg、0.2889mmol、2当量)を0℃にて加えた。反応物を0℃~rtにて10分間撹拌し、次いでNaHCO3の飽和溶液でクエンチし、濾過してn-ヘキサンで洗浄することで白色残渣が得られたが、移動相としてACNおよび水を使用する分取HPLC精製によって精製することで、純粋な(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-2H-ピリド[1,2-b]イソキノリン-9-カルボキサミド(94、19.482mg、0.07407mmol、51%)が入手された。1H NMR(400MHz,DMSO-d6)δ11.22(s,1H),9.10(s,1H),7.35(s,1H),7.30(d,J=10.0Hz,1H),3.93(d,J=16.8Hz,1H),3.12(d,J=16.6Hz,1H),3.01(d,J=11.2Hz,1H),2.80(d,J=17.1Hz,1H),2.16(s,1H),2.05(t,J=11.7Hz,1H),1.80(d,J=11.1Hz,1H),1.76-1.59(m,2H),1.51(m,1H),1.25(m,2H)。MS(ESI):265[M+H]+.
化合物93および94は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
メチル1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキシラート(X):
アセトニトリル(ACN)(5mL)中のヘキサヒドロピリダジン塩化水素(V、98mg、0.616mmol、1.0当量)の溶液へ、メチル3,4-ビス(ブロモメチル)ベンゾアート(W、198.4mg、0.616mmol、1.0当量)およびCs2CO3(803mg、2.46mmol、4.0当量)を加えた。反応混合物を室温にて2h撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応混合物を濾過して濃縮した。粗メチル1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキシラート(X、150mg、0.608mmol、99%)をそのまま次のステップへ使用した。MS(ESI):247[M+H]+
アセトニトリル(ACN)(5mL)中のヘキサヒドロピリダジン塩化水素(V、98mg、0.616mmol、1.0当量)の溶液へ、メチル3,4-ビス(ブロモメチル)ベンゾアート(W、198.4mg、0.616mmol、1.0当量)およびCs2CO3(803mg、2.46mmol、4.0当量)を加えた。反応混合物を室温にて2h撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応混合物を濾過して濃縮した。粗メチル1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキシラート(X、150mg、0.608mmol、99%)をそのまま次のステップへ使用した。MS(ESI):247[M+H]+
N-ヒドロキシ-1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキサミド(106):
MeOH(3mL)中のメチル1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキシラート(X、150mg、0.608mmol、1.0当量)の溶液へNH2OH(0.8mL、12.16mmol、50%水溶液、20.0当量)およびKOH(102.1mg、1.824mmol、3.0当量)を0℃にて加えた。反応物をrtにて10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視した。反応混合物を濃縮し、分取HPLC(移動相(A:水中5mM AA+0.1%NH3、B:100%ACN))によって精製することで、N-ヒドロキシ-1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキサミド(106、19.9mg、0.065mmol、11%収率)が供与された。1H NMR(400MHz,DMSO-d6)δ7.77-7.74(m,2H),7.42(d,J=7.8Hz,1H),5.13-5.01(m,4H),3.72-3.70(m,2H),3.12(s,2H),1.96(s,2H),1.74(s,3H),1.61(s,2H)。MS(ESI):248[M+H]+
MeOH(3mL)中のメチル1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキシラート(X、150mg、0.608mmol、1.0当量)の溶液へNH2OH(0.8mL、12.16mmol、50%水溶液、20.0当量)およびKOH(102.1mg、1.824mmol、3.0当量)を0℃にて加えた。反応物をrtにて10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視した。反応混合物を濃縮し、分取HPLC(移動相(A:水中5mM AA+0.1%NH3、B:100%ACN))によって精製することで、N-ヒドロキシ-1,2,3,4,6,11-ヘキサヒドロピリダジノ[1,2-b]フタラジン-8-カルボキサミド(106、19.9mg、0.065mmol、11%収率)が供与された。1H NMR(400MHz,DMSO-d6)δ7.77-7.74(m,2H),7.42(d,J=7.8Hz,1H),5.13-5.01(m,4H),3.72-3.70(m,2H),3.12(s,2H),1.96(s,2H),1.74(s,3H),1.61(s,2H)。MS(ESI):248[M+H]+
式(II)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-N-ヒドロキシ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキサミド(113)
2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-N-ヒドロキシ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキサミド(113)
(E)-1-(3-ブロモ-5-フルオロフェニル)-N-(2,2-ジメトキシエチル)メタンイミン(AA):
トルエン(50mL)中の3-ブロモ-5-フルオロベンズアルデヒド(Y、5.0g、24.293mmol、1.0当量)および2,2-ジメトキシエタン-1-アミン(Z、3.103g、29.555mmol、1.2当量)の撹拌溶液を、ディーン・スターク装置を使用し120℃にて6h還流した。反応の完了をTLCによって監視した。次いで反応混合物を真空下で濃縮した。固体残渣をペンタンとともに粉砕することで、(E)-1-(3-ブロモ-5-フルオロフェニル)-N-(2,2-ジメトキシエチル)メタンイミン(AA、7.5g、25.850mmol、91%)が与えられ、これをそのまま次のステップに使用した。MS(ESI):290[M+H]+.
トルエン(50mL)中の3-ブロモ-5-フルオロベンズアルデヒド(Y、5.0g、24.293mmol、1.0当量)および2,2-ジメトキシエタン-1-アミン(Z、3.103g、29.555mmol、1.2当量)の撹拌溶液を、ディーン・スターク装置を使用し120℃にて6h還流した。反応の完了をTLCによって監視した。次いで反応混合物を真空下で濃縮した。固体残渣をペンタンとともに粉砕することで、(E)-1-(3-ブロモ-5-フルオロフェニル)-N-(2,2-ジメトキシエチル)メタンイミン(AA、7.5g、25.850mmol、91%)が与えられ、これをそのまま次のステップに使用した。MS(ESI):290[M+H]+.
7-ブロモ-5-フルオロイソキノリンメタンイミン(AB):
五酸化リン(10.0g)および濃硫酸(3mL)を混合し、濃茶色の粘性物質を形成するまで撹拌した。次に(E)-1-(3-ブロモ-5-フルオロフェニル)-N-(2,2-ジメトキシエチル)メタンイミン(AA、7.5g、25.85mmol)を冷(5℃)濃硫酸(30mL)に溶解し、上で調製された五酸化リンと濃硫酸との混合物へゆっくり加えた。その結果得られた暗色の反応混合物を激しく撹拌し、160℃にて30分間加熱した。室温まで冷却した後、暗褐色の粘性反応混合物を激しく撹拌しながら慎重に氷水(500mL)中へ注いだ。pHを1N NaOHを使用して7へ調整し、黒色タール状沈殿物を濾過した。次いで1N NaOHを使用しpHを9までさらに増加させた。この塩基性の水相をEtOAc(3×500mL)で抽出した。合わせた有機層をブラインで洗浄し、MgSO4上で乾燥させ蒸発させることで、7gの茶色油が供与された。粗産物を分取HPLCによって精製することで、7-ブロモ-5-フルオロイソキノリン(AB、1.5g、6.6371mmol、38%)が供与された。MS(ESI):227[M+H]+.
五酸化リン(10.0g)および濃硫酸(3mL)を混合し、濃茶色の粘性物質を形成するまで撹拌した。次に(E)-1-(3-ブロモ-5-フルオロフェニル)-N-(2,2-ジメトキシエチル)メタンイミン(AA、7.5g、25.85mmol)を冷(5℃)濃硫酸(30mL)に溶解し、上で調製された五酸化リンと濃硫酸との混合物へゆっくり加えた。その結果得られた暗色の反応混合物を激しく撹拌し、160℃にて30分間加熱した。室温まで冷却した後、暗褐色の粘性反応混合物を激しく撹拌しながら慎重に氷水(500mL)中へ注いだ。pHを1N NaOHを使用して7へ調整し、黒色タール状沈殿物を濾過した。次いで1N NaOHを使用しpHを9までさらに増加させた。この塩基性の水相をEtOAc(3×500mL)で抽出した。合わせた有機層をブラインで洗浄し、MgSO4上で乾燥させ蒸発させることで、7gの茶色油が供与された。粗産物を分取HPLCによって精製することで、7-ブロモ-5-フルオロイソキノリン(AB、1.5g、6.6371mmol、38%)が供与された。MS(ESI):227[M+H]+.
メチル5-フルオロイソキノリン-7-カルボキシラート(AC):
メタノール(20mL)中の7-ブロモ-5-フルオロイソキノリン(AB、1.1g、4.8672mmol、1当量)の撹拌溶液へ、TEA(3.3mL、24.336mmol、5当量)およびPdCl2(dppf)(177mg、0.2433mmol、0.05当量)を窒素下で加えた。反応混合物を一酸化炭素(400psi)下100℃まで4h加熱した。反応をTLCによって監視した。反応混合物をセライトに通して濾過してメタノール(50mL)で洗浄し、合わせた濾過物を真空下で濃縮し、その結果得られた残渣を、42%EtOAc:ヘキサンで溶離するコンビ(combi)フラッシュクロマトグラフィーによって精製することで、メチル7-フルオロイソキノリン-5-カルボキシラート(AC、770mg、3.7551mmol、73%)が固体として供与された。MS(ESI):206[M+H]+.
メタノール(20mL)中の7-ブロモ-5-フルオロイソキノリン(AB、1.1g、4.8672mmol、1当量)の撹拌溶液へ、TEA(3.3mL、24.336mmol、5当量)およびPdCl2(dppf)(177mg、0.2433mmol、0.05当量)を窒素下で加えた。反応混合物を一酸化炭素(400psi)下100℃まで4h加熱した。反応をTLCによって監視した。反応混合物をセライトに通して濾過してメタノール(50mL)で洗浄し、合わせた濾過物を真空下で濃縮し、その結果得られた残渣を、42%EtOAc:ヘキサンで溶離するコンビ(combi)フラッシュクロマトグラフィーによって精製することで、メチル7-フルオロイソキノリン-5-カルボキシラート(AC、770mg、3.7551mmol、73%)が固体として供与された。MS(ESI):206[M+H]+.
メチル5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AD):
THF(15mL)中のメチル7-フルオロイソキノリン-5-カルボキシラート(AC、770mg、3.75mmol)の撹拌溶液へ、1N HCl(2.0mL)およびPtO2(300mg)を室温にて加えた。その結果得られた混合物を室温にてH2ガス(200psi)下4h撹拌した。反応をTLCによって監視した。次いで反応混合物をセライトに通して濾過してTHF(30mL)で洗浄し、合わせた濾過物を濃縮することで、メチル5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AD、581mg、2.78mmol、74%)が茶色固体として供与された。MS(ESI):210[M+H]+.
THF(15mL)中のメチル7-フルオロイソキノリン-5-カルボキシラート(AC、770mg、3.75mmol)の撹拌溶液へ、1N HCl(2.0mL)およびPtO2(300mg)を室温にて加えた。その結果得られた混合物を室温にてH2ガス(200psi)下4h撹拌した。反応をTLCによって監視した。次いで反応混合物をセライトに通して濾過してTHF(30mL)で洗浄し、合わせた濾過物を濃縮することで、メチル5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AD、581mg、2.78mmol、74%)が茶色固体として供与された。MS(ESI):210[M+H]+.
メチル2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-1,2,3,4テトラヒドロイソキノリン-7-カルボキシラート(AF):
メタノール(10mL)中のメチル5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AD、200mg、0.9559mmol、1.0当量)の撹拌溶液へ、酢酸(cat.)、アダマンタン-1-カルバルデヒド(AE、313mg、1.9118mmol、2.0当量)、およびNaCNBH3(118mg、1.9118mmol、2.0当量)を0℃にて加えた。反応混合物を60℃にて16h撹拌した。反応をTLCによって監視した。反応を重炭酸ナトリウム溶液(50mL)でクエンチし、EtOAc(3×50mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、減圧下で濃縮することで、粗材料が得られた。これをシリカゲルカラムによって精製した。化合物をヘキサン中3.4%EtOAcにて溶離することで、メチル2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AF、45mg、0.1256mmol、13%)が供与された。MS(ESI):358[M+H]+.
メタノール(10mL)中のメチル5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AD、200mg、0.9559mmol、1.0当量)の撹拌溶液へ、酢酸(cat.)、アダマンタン-1-カルバルデヒド(AE、313mg、1.9118mmol、2.0当量)、およびNaCNBH3(118mg、1.9118mmol、2.0当量)を0℃にて加えた。反応混合物を60℃にて16h撹拌した。反応をTLCによって監視した。反応を重炭酸ナトリウム溶液(50mL)でクエンチし、EtOAc(3×50mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、減圧下で濃縮することで、粗材料が得られた。これをシリカゲルカラムによって精製した。化合物をヘキサン中3.4%EtOAcにて溶離することで、メチル2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AF、45mg、0.1256mmol、13%)が供与された。MS(ESI):358[M+H]+.
2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-N-ヒドロキシ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキサミド(113):
MeOH(1mL)中のメチル2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AF、40mg、0.1120mmol、1.0当量)の溶液へ、NH2OH(0.1mL、1.6806mmol、50% 水性溶液、15.0当量)およびKOH(18mg、0.336mmol、3.0当量)を0℃にて加えた。反応物を室温にて10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視した。反応混合物を分取HPLC(移動相(A:水中5mM酢酸アンモニウム+0.1%NH3、B:100%ACN))によって濃縮し精製することで、2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-N-ヒドロキシ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキサミド(113、4.1mg、0.011mmol、10.22%収率)が供与された。1H NMR(400MHz,メタノール-d4)δ7.27-7.25(m,2H),3.70(s,2H),2.81(dt,J=9.3,4.6Hz,4H),2.17(s,2H),1.95(s,3H),1.75(d,J=12.3Hz,3H),1.68(d,J=12.4Hz,3H),1.59(d,J=2.8Hz,6H)。MS(ESI):359[M+H]+.
MeOH(1mL)中のメチル2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキシラート(AF、40mg、0.1120mmol、1.0当量)の溶液へ、NH2OH(0.1mL、1.6806mmol、50% 水性溶液、15.0当量)およびKOH(18mg、0.336mmol、3.0当量)を0℃にて加えた。反応物を室温にて10分間撹拌した。反応の完了をTLCおよびLCMS分析によって監視した。反応混合物を分取HPLC(移動相(A:水中5mM酢酸アンモニウム+0.1%NH3、B:100%ACN))によって濃縮し精製することで、2-(((3r,5r,7r)-アダマンタン-1-イル)メチル)-5-フルオロ-N-ヒドロキシ-1,2,3,4-テトラヒドロイソキノリン-7-カルボキサミド(113、4.1mg、0.011mmol、10.22%収率)が供与された。1H NMR(400MHz,メタノール-d4)δ7.27-7.25(m,2H),3.70(s,2H),2.81(dt,J=9.3,4.6Hz,4H),2.17(s,2H),1.95(s,3H),1.75(d,J=12.3Hz,3H),1.68(d,J=12.4Hz,3H),1.59(d,J=2.8Hz,6H)。MS(ESI):359[M+H]+.
以下の化合物を、化合物113を調製するのに使用したのと類似のやり方で調製した。
3-ベンジル-N-ヒドロキシ-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキサミド(117)、および
2-ベンジル-N-ヒドロキシ-3-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキサミド(118)
2-ベンジル-N-ヒドロキシ-3-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキサミド(118)
メチルフタラジン-6-カルボキシラート(AH):
メタノール中の6-ブロモフタラジン(AG、800mg、3.8277mmol、1当量)の撹拌溶液へ、TEA(2.66mL、19.1385mmol、5.0当量)およびPdCl2(dppf)(139.90mg、0.1913mmol、0.05当量)を窒素雰囲気下室温にて加えた。混合物を一酸化炭素(400psi)下100℃まで3h加熱した。反応をTLCによって監視した。反応混合物をセライトに通して濾過し、メタノールで洗浄した。濾過物を真空濃縮し、50%EtOAc:ヘキサンで溶離するコンビフラッシュクロマトグラフィーによって精製することで、メチルフタラジン-6-カルボキシラート(AH、250mg、1.3297mmol、35%)が白色固体として供与された。MS(ESI):189[M+H]+.
メタノール中の6-ブロモフタラジン(AG、800mg、3.8277mmol、1当量)の撹拌溶液へ、TEA(2.66mL、19.1385mmol、5.0当量)およびPdCl2(dppf)(139.90mg、0.1913mmol、0.05当量)を窒素雰囲気下室温にて加えた。混合物を一酸化炭素(400psi)下100℃まで3h加熱した。反応をTLCによって監視した。反応混合物をセライトに通して濾過し、メタノールで洗浄した。濾過物を真空濃縮し、50%EtOAc:ヘキサンで溶離するコンビフラッシュクロマトグラフィーによって精製することで、メチルフタラジン-6-カルボキシラート(AH、250mg、1.3297mmol、35%)が白色固体として供与された。MS(ESI):189[M+H]+.
メチル2-ベンジル-1,2-ジヒドロフタラジン-6-カルボキシラート(AIa)、および
メチル-3-ベンジル-3,4-ジヒドロフタラジン-6-カルボキシラート(AIb):
MeOH(10mL)中のメチルフタラジン-6-カルボキシラート(AH、250mg、1.3297mmol、1.0当量)の撹拌溶液へ、臭化ベンジル(2.3mL,1.5937mmol、1.5当量)およびNaBH3CN(329mg、5.3191mmol、4.0当量)を加えた。溶液を室温にて6h撹拌した。反応をTLCで監視した。反応を水(10mL)でクエンチし、EtOAc(3×10mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、減圧下濃縮することで、粗AIa+AIb(300mg)が得られたが、これを次のステップに即時使用した。MS(ESI):281[M+H]+.
メチル-3-ベンジル-3,4-ジヒドロフタラジン-6-カルボキシラート(AIb):
MeOH(10mL)中のメチルフタラジン-6-カルボキシラート(AH、250mg、1.3297mmol、1.0当量)の撹拌溶液へ、臭化ベンジル(2.3mL,1.5937mmol、1.5当量)およびNaBH3CN(329mg、5.3191mmol、4.0当量)を加えた。溶液を室温にて6h撹拌した。反応をTLCで監視した。反応を水(10mL)でクエンチし、EtOAc(3×10mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、減圧下濃縮することで、粗AIa+AIb(300mg)が得られたが、これを次のステップに即時使用した。MS(ESI):281[M+H]+.
メチル2-ベンジル-3-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキシラート(AJa)、および
メチル3-ベンジル-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキシラート(AJb):
MeOH(15mL)中のメチル2-ベンジル-1,2-ジヒドロフタラジン-6-カルボキシラートおよびメチル3-ベンジル-3,4-ジヒドロフタラジン-6-カルボキシラート(AIa+AIb、300mg、1.0714mmol、1.0当量)の撹拌溶液へ、NaBH3CN(66.42mg、2.1428mmol、2.0当量)を加えて濃HCl(0.05mL)を加えた。溶液を室温にて1h撹拌し、TLCで監視した。1時間後、さらにNaBH3CN(66.42mg、2.1428mmol、2.0当量)およびホルムアルデヒド溶液(10mL)を加えた。反応混合物を室温にて2h撹拌した。反応を次いで水(100mL)でクエンチし、EtOAc(3×100mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、有機層を減圧下で濃縮することで粗材料が得られた。これを50%EtOAc:ヘキサンで溶離するコンビフラッシュクロマトグラフィーによって精製することで、位置異性体の混合物(88mg)が入手された。位置異性体をさらに、CHIRAL pack AD-H(250×4.6mm)5μカラム)上、MeOH中0.1%DEAを使用するキラル分取HPLCを使用して分離することで、個々の異性体が提供された。(Fr-1(AJb):32mg、Fr-2(AJa):25mg。MS(ESI):297[M+H]+。AJaおよびAJbを純粋なものとして単離し、NOE実験によって確認した。画分-2は(AJa)であることが見出された。
メチル3-ベンジル-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキシラート(AJb):
MeOH(15mL)中のメチル2-ベンジル-1,2-ジヒドロフタラジン-6-カルボキシラートおよびメチル3-ベンジル-3,4-ジヒドロフタラジン-6-カルボキシラート(AIa+AIb、300mg、1.0714mmol、1.0当量)の撹拌溶液へ、NaBH3CN(66.42mg、2.1428mmol、2.0当量)を加えて濃HCl(0.05mL)を加えた。溶液を室温にて1h撹拌し、TLCで監視した。1時間後、さらにNaBH3CN(66.42mg、2.1428mmol、2.0当量)およびホルムアルデヒド溶液(10mL)を加えた。反応混合物を室温にて2h撹拌した。反応を次いで水(100mL)でクエンチし、EtOAc(3×100mL)で抽出した。合わせた有機層を無水Na2SO4上で乾燥させ、有機層を減圧下で濃縮することで粗材料が得られた。これを50%EtOAc:ヘキサンで溶離するコンビフラッシュクロマトグラフィーによって精製することで、位置異性体の混合物(88mg)が入手された。位置異性体をさらに、CHIRAL pack AD-H(250×4.6mm)5μカラム)上、MeOH中0.1%DEAを使用するキラル分取HPLCを使用して分離することで、個々の異性体が提供された。(Fr-1(AJb):32mg、Fr-2(AJa):25mg。MS(ESI):297[M+H]+。AJaおよびAJbを純粋なものとして単離し、NOE実験によって確認した。画分-2は(AJa)であることが見出された。
3-ベンジル-N-ヒドロキシ-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキサミド(117):
MeOH(2mL)中のメチル3-ベンジル-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキシラート(AJa、25mg、0.08446mmol、1.0当量)の撹拌溶液へ、NH2OH(0.1mL、1.26689mmol、50%水溶液、15.0当量)およびKOH(23mg、0.4223mmol、5.0当量)を0℃にて加えた。反応混合物を室温にて10分間撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応をNaHCO3飽和溶液でクエンチし、10分間撹拌した。沈殿物を濾過し、水およびn-ヘキサンで洗浄した。白色残渣を分取HPLC(移動相(A:水中0.1%ギ酸、B:100%ACN))によって精製することで、3-ベンジル-N-ヒドロキシ-2-メチル-1,2,3,4-テトラヒドロフタラジン-カルボキサミドが供与された(117、4.094mg、0.01378mmol、13%)。MS(ESI):298[M+H]+.
MeOH(2mL)中のメチル3-ベンジル-2-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキシラート(AJa、25mg、0.08446mmol、1.0当量)の撹拌溶液へ、NH2OH(0.1mL、1.26689mmol、50%水溶液、15.0当量)およびKOH(23mg、0.4223mmol、5.0当量)を0℃にて加えた。反応混合物を室温にて10分間撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応をNaHCO3飽和溶液でクエンチし、10分間撹拌した。沈殿物を濾過し、水およびn-ヘキサンで洗浄した。白色残渣を分取HPLC(移動相(A:水中0.1%ギ酸、B:100%ACN))によって精製することで、3-ベンジル-N-ヒドロキシ-2-メチル-1,2,3,4-テトラヒドロフタラジン-カルボキサミドが供与された(117、4.094mg、0.01378mmol、13%)。MS(ESI):298[M+H]+.
2-ベンジル-N-ヒドロキシ-3-メチル-1,2,3,4-テトラヒドロフタラジン-6-カルボキサミド(118):
この化合物を、113に使用したのと類似のやり方でAJbから調製した。
1H NMR(400MHz,DMSO-d6)δ11.14(bs,1H),9.01(bs,1H),7.55-7.50(m,2H),7.30(d,J=4.3Hz,4H),7.23(dt,J=8.7,4.3Hz,1H),7.13(d,J=8.0Hz,1H),3.89(s,2H),3.72(d,J=8.7Hz,4H),2.40(s,3H)。MS(ESI):298[M+H]+.
この化合物を、113に使用したのと類似のやり方でAJbから調製した。
1H NMR(400MHz,DMSO-d6)δ11.14(bs,1H),9.01(bs,1H),7.55-7.50(m,2H),7.30(d,J=4.3Hz,4H),7.23(dt,J=8.7,4.3Hz,1H),7.13(d,J=8.0Hz,1H),3.89(s,2H),3.72(d,J=8.7Hz,4H),2.40(s,3H)。MS(ESI):298[M+H]+.
式(V)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
(S)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(119)、および
(R)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(120)
(S)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(119)、および
(R)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(120)
tert-ブチル2-(3-フルオロ-5-メトキシベンジル)ピロリジン-1-カルボキシラート(AM):
トルエン(15mL)中のtert-ブチルペンタ-4-エン-1-イルカルバマート(AK、0.99g、5.39mmol、1.1当量)および1-ブロモ-3-フルオロ-5-メトキシベンゼン(AL、1.0g、4.90mmol、1.0当量)の撹拌溶液を、窒素を使用して15分間脱気し、この後にDPE-Phos(52mg、0.098mmol、0.02当量)、NaOtBu(0.706g、7.35mmol、1.5当量)、およびPd2(dba)3(44mg、0.049mmol、0.01当量)を加えた。反応混合物を18h還流し、TLCによって監視した。反応混合物を水(100mL)上に注ぎ、酢酸エチル(2×100mL)で抽出した。合せた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られた。粗材料を、酢酸エチル/ヘキサン(2:8)を使用するカラムクロマトグラフィーによって精製することで、tert-ブチル2-(3-フルオロ-5-メトキシベンジル)ピロリジン-1-カルボキシラート(AM、1.2g、3.88mmol、79%)が黄色油として入手された。MS(ESI): 310[M+H]+
トルエン(15mL)中のtert-ブチルペンタ-4-エン-1-イルカルバマート(AK、0.99g、5.39mmol、1.1当量)および1-ブロモ-3-フルオロ-5-メトキシベンゼン(AL、1.0g、4.90mmol、1.0当量)の撹拌溶液を、窒素を使用して15分間脱気し、この後にDPE-Phos(52mg、0.098mmol、0.02当量)、NaOtBu(0.706g、7.35mmol、1.5当量)、およびPd2(dba)3(44mg、0.049mmol、0.01当量)を加えた。反応混合物を18h還流し、TLCによって監視した。反応混合物を水(100mL)上に注ぎ、酢酸エチル(2×100mL)で抽出した。合せた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られた。粗材料を、酢酸エチル/ヘキサン(2:8)を使用するカラムクロマトグラフィーによって精製することで、tert-ブチル2-(3-フルオロ-5-メトキシベンジル)ピロリジン-1-カルボキシラート(AM、1.2g、3.88mmol、79%)が黄色油として入手された。MS(ESI): 310[M+H]+
119および120の調製のためのこれに続くステップを、化合物93および94の調製に使用したのと類似のやり方で実施した。
(S)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(119)
1H NMR(400MHz,DMSO-d6)δ11.22(s,1H),9.08(s,1H),7.41-7.31(m,2H),4.19(d,J=16.0Hz,1H),3.42(m,1H),3.03(d,J=15.6Hz,2H),2.22(m,1H),2.62(m,2H),2.04(m,1H),1.77(m,2H),1.45(m,1H)。MS(ESI):251[M+H]+
1H NMR(400MHz,DMSO-d6)δ11.22(s,1H),9.08(s,1H),7.41-7.31(m,2H),4.19(d,J=16.0Hz,1H),3.42(m,1H),3.03(d,J=15.6Hz,2H),2.22(m,1H),2.62(m,2H),2.04(m,1H),1.77(m,2H),1.45(m,1H)。MS(ESI):251[M+H]+
(R)-6-フルオロ-N-ヒドロキシ-1,2,3,5,10,10a-ヘキサヒドロピロロ[1,2-b]イソキノリン-8-カルボキサミド(120)
1H NMR(400MHz,DMSO-d6)δ11.21(s,1H),9.19(s,1H),7.40(s,1H),7.32(d,J=10.4Hz,1H),4.16(d,J=16.0Hz,1H),3.17(d,J=6.8Hz,2H),2.99(dd,J=16.0,3.2Hz,1H),2.62-2.56(m,1H),2.27-2.19(m,2H),2.05-2.00(m,1H),1.81-1.77(m,2H),1.49-1.42(m,1H)。MS(ESI):251.2[M+H]+
1H NMR(400MHz,DMSO-d6)δ11.21(s,1H),9.19(s,1H),7.40(s,1H),7.32(d,J=10.4Hz,1H),4.16(d,J=16.0Hz,1H),3.17(d,J=6.8Hz,2H),2.99(dd,J=16.0,3.2Hz,1H),2.62-2.56(m,1H),2.27-2.19(m,2H),2.05-2.00(m,1H),1.81-1.77(m,2H),1.49-1.42(m,1H)。MS(ESI):251.2[M+H]+
化合物119および120は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
以下の化合物を、化合物119および120を調製するのに使用したのと類似のやり方で調製した。化合物対121/122、123/124、125/126、および127/128は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキサミド(129)、および
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキサミド(130)
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキサミド(130)
(Z)-2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)アクリル酸(AV):
無水酢酸(24mL)中の3-ブロモ-5-フルオロベンズアルデヒド(AT、15g、73.892mmol、1.0当量)の溶液へ、N-アセチルグリシン(AU、8.6g、73.892mmol、1.0当量)およびNaOAc(6g、73.892mmol、1.0当量)を加えた。反応混合物を120℃にて5h撹拌した。反応の完了をTLCおよびLCMSによって監視した。その結果得られた溶液は室温まで冷却したら固化し、これを氷冷水でクエンチして濾過した。固体を水(50mL)で洗浄し、減圧下で乾燥させることで、産物(Z)-2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)アクリル酸(AV、9.0g、29.903mmol、40%)が茶色固体として入手された。MS(ESI):302[M+H]+
無水酢酸(24mL)中の3-ブロモ-5-フルオロベンズアルデヒド(AT、15g、73.892mmol、1.0当量)の溶液へ、N-アセチルグリシン(AU、8.6g、73.892mmol、1.0当量)およびNaOAc(6g、73.892mmol、1.0当量)を加えた。反応混合物を120℃にて5h撹拌した。反応の完了をTLCおよびLCMSによって監視した。その結果得られた溶液は室温まで冷却したら固化し、これを氷冷水でクエンチして濾過した。固体を水(50mL)で洗浄し、減圧下で乾燥させることで、産物(Z)-2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)アクリル酸(AV、9.0g、29.903mmol、40%)が茶色固体として入手された。MS(ESI):302[M+H]+
2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AW):
MeOH(70mL)中の(Z)-2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)アクリル酸(AV、7g、23.258mmol、1.0当量)の溶液へPtO2(2g)を加え、混合物を水素化装置中200psi H2(g)の下、室温にて16h撹拌し、TLCを使用して監視した。反応混合物をセライトに通して濾過し、濾過物を減圧下で濃縮することで、2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AW、7.0g、23.02mmol、99%)が粘着性茶色固体として得られた。MS(ESI):304[M+H]+
MeOH(70mL)中の(Z)-2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)アクリル酸(AV、7g、23.258mmol、1.0当量)の溶液へPtO2(2g)を加え、混合物を水素化装置中200psi H2(g)の下、室温にて16h撹拌し、TLCを使用して監視した。反応混合物をセライトに通して濾過し、濾過物を減圧下で濃縮することで、2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AW、7.0g、23.02mmol、99%)が粘着性茶色固体として得られた。MS(ESI):304[M+H]+
2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AX):
2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AW、7g、23.02mmol、1.0当量)を含有する丸底フラスコへ、25%HCl溶液(100mL)を加えた。反応混合物を100℃にて16h還流し、LCMSによって監視した。反応が完了したら、これを減圧下で濃縮し、酢酸エチルを加えることで白色固体が得られた。これを濾過し、減圧下で乾燥させることで、2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AX、6.0g、22.99mmol、99%)が入手された。MS(ESI):263[M+H]+
2-アセトアミド-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AW、7g、23.02mmol、1.0当量)を含有する丸底フラスコへ、25%HCl溶液(100mL)を加えた。反応混合物を100℃にて16h還流し、LCMSによって監視した。反応が完了したら、これを減圧下で濃縮し、酢酸エチルを加えることで白色固体が得られた。これを濾過し、減圧下で乾燥させることで、2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AX、6.0g、22.99mmol、99%)が入手された。MS(ESI):263[M+H]+
メチル2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパノアート(AY):
MeOH(140mL)中の2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AX、6.0g、22.99mmol、1.0当量)の撹拌溶液へ塩化チオニル(2.0mL、27.58mmol、1.2当量)を-10℃にて加えた。次いで溶液を90℃にて2h還流し、TLCおよびLCMSによって監視した。反応が完了したらこれを減圧下で濃縮し、ジエチルエーテルとともに粉砕することで、メチル2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパノアート(AY、5.0g、18.11mmol、79%)が白色固体として得られた。MS(ESI):277[M+H]+
MeOH(140mL)中の2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパン酸(AX、6.0g、22.99mmol、1.0当量)の撹拌溶液へ塩化チオニル(2.0mL、27.58mmol、1.2当量)を-10℃にて加えた。次いで溶液を90℃にて2h還流し、TLCおよびLCMSによって監視した。反応が完了したらこれを減圧下で濃縮し、ジエチルエーテルとともに粉砕することで、メチル2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパノアート(AY、5.0g、18.11mmol、79%)が白色固体として得られた。MS(ESI):277[M+H]+
メチル3-(3-ブロモ-5-フルオロフェニル)-2-((メトキシカルボニル)アミノ)プロパノアート(AZ):
NaHCO3飽和溶液(100mL)中のメチル2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパノアート(AY、5.0g、18.11mmol、1.0当量)の撹拌溶液へ、メチルクロロホルマート(2.79mL、36.23mmol、2.0当量)を室温にて加え、反応混合物を室温にて1h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水(100mL)上へ注ぎ、酢酸エチル(3×100mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、メチル3-(3-ブロモ-5-フルオロフェニル)-2-((メトキシカルボニル)アミノ)プロパノアート(AZ、4.8g、14.36mmol、79%)が入手された。MS(ESI):335[M+H]+
NaHCO3飽和溶液(100mL)中のメチル2-アミノ-3-(3-ブロモ-5-フルオロフェニル)プロパノアート(AY、5.0g、18.11mmol、1.0当量)の撹拌溶液へ、メチルクロロホルマート(2.79mL、36.23mmol、2.0当量)を室温にて加え、反応混合物を室温にて1h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水(100mL)上へ注ぎ、酢酸エチル(3×100mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、メチル3-(3-ブロモ-5-フルオロフェニル)-2-((メトキシカルボニル)アミノ)プロパノアート(AZ、4.8g、14.36mmol、79%)が入手された。MS(ESI):335[M+H]+
ジメチル6-ブロモ-8-フルオロ-3,4-ジヒドロイソキノリン-2,3(1H)-ジカルボキシラート(BA):
AcOH:濃H2SO4(14.4mL:4.8mL)中のメチル3-(3-ブロモ-5-フルオロフェニル)-2-((メトキシカルボニル)アミノ)プロピオナート(AZ、4.8g、14.36mmol、1.0当量)の撹拌溶液へ、パラホルムアルデヒド(2.1g、71.83mmol、5.0当量)を室温にて加えた。反応混合物を室温にて5h撹拌し、TLCおよびLCMSによって監視した。完了したら反応混合物を氷水(50mL)中へ注ぎ、酢酸エチル(3×50mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗化合物が入手されたが、これを、DCM:MeOH(9.5:5)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、ジメチル6-ブロモ-8-フルオロ-3,4-ジヒドロイソキノリン-2,3-(1H)-ジカルボキシラート(BA、3.0g、8.67mmol、60%)が入手された。MS(ESI):346[M+H]+
AcOH:濃H2SO4(14.4mL:4.8mL)中のメチル3-(3-ブロモ-5-フルオロフェニル)-2-((メトキシカルボニル)アミノ)プロピオナート(AZ、4.8g、14.36mmol、1.0当量)の撹拌溶液へ、パラホルムアルデヒド(2.1g、71.83mmol、5.0当量)を室温にて加えた。反応混合物を室温にて5h撹拌し、TLCおよびLCMSによって監視した。完了したら反応混合物を氷水(50mL)中へ注ぎ、酢酸エチル(3×50mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗化合物が入手されたが、これを、DCM:MeOH(9.5:5)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、ジメチル6-ブロモ-8-フルオロ-3,4-ジヒドロイソキノリン-2,3-(1H)-ジカルボキシラート(BA、3.0g、8.67mmol、60%)が入手された。MS(ESI):346[M+H]+
メチル-6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-カルボキシラート(BB):
THF(10mL)中のジメチル6-ブロモ-8-フルオロ-3,4-ジヒドロイソキノリン-2,3(1H)-ジカルボキシラート(BA、850mg、2.46mmol、1.0当量)の撹拌溶液へ、LiBH4(64mg、2.95mmol、1.2当量)を加えた。反応混合物を室温にて16h撹拌し、反応の完了をTLCおよびLCMSによって監視した。完了したら反応混合物を水(10mL)上へ注ぎ、酢酸エチル(3×12mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗化合物が入手されたが、これを、DCM:MeOH(9:1)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル-6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-カルボキシラート(BB、500mg、1.57mmol、64%)が入手された。MS(ESI):319[M+H]+
THF(10mL)中のジメチル6-ブロモ-8-フルオロ-3,4-ジヒドロイソキノリン-2,3(1H)-ジカルボキシラート(BA、850mg、2.46mmol、1.0当量)の撹拌溶液へ、LiBH4(64mg、2.95mmol、1.2当量)を加えた。反応混合物を室温にて16h撹拌し、反応の完了をTLCおよびLCMSによって監視した。完了したら反応混合物を水(10mL)上へ注ぎ、酢酸エチル(3×12mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗化合物が入手されたが、これを、DCM:MeOH(9:1)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル-6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-カルボキシラート(BB、500mg、1.57mmol、64%)が入手された。MS(ESI):319[M+H]+
(6-ブロモ-8-フルオロ-1,2,3,4-テトラヒドロイソキノリン-3-イル)メタノール(BC):
MeOH:THF:2M LiOH溶液(1:1:1)(20mL)中のメチル6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-カルボキシラート(BB、2g、6.29mmol、1.0当量)の撹拌溶液を室温にて調製した。その結果得られた混合物をマイクロ波中120℃にて10分間加熱した。反応の完了をTLCによって監視し、反応の完了後酢酸エチル(20mL)を加えて濾過し、濾過物を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで(6-ブロモ-8フルオロ-1,2,3,4-テトラヒドロイソキノリン-3-イル)メタノール(BC、1.5g、5.77mmol、92%)が入手された。MS(ESI):261[M+H]+
MeOH:THF:2M LiOH溶液(1:1:1)(20mL)中のメチル6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-カルボキシラート(BB、2g、6.29mmol、1.0当量)の撹拌溶液を室温にて調製した。その結果得られた混合物をマイクロ波中120℃にて10分間加熱した。反応の完了をTLCによって監視し、反応の完了後酢酸エチル(20mL)を加えて濾過し、濾過物を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで(6-ブロモ-8フルオロ-1,2,3,4-テトラヒドロイソキノリン-3-イル)メタノール(BC、1.5g、5.77mmol、92%)が入手された。MS(ESI):261[M+H]+
1-(6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-イル)-2-クロロエタン-1-オン(BD):
DCM(75mL)中の(6-ブロモ-1,2,3,4-テトラヒドロイソキノリン-3-イル) メタノール(BC、1.5g、5.77mmol、1.0当量)の撹拌溶液へ、TEA(0.8mL、5.77mmol、1.0当量)を加えた。次いでこれを0℃まで冷却し、クロロ塩化アセチル(0.45mL、5.77mmol、1.0当量)を滴加した。反応混合物を室温にて2h撹拌した。反応が完了したら、反応混合物を希HCl(80mL)および水(100mL)で洗浄した。有機層を無水硫酸ナトリウム上で乾燥させて濾過し、減圧下で濃縮することで粗化合物が入手されたが、これをDCM:MeOH(9.5:5)を使用するカラムクロマトグラフィーによって精製することで、1-(6-ブロモ-8-フルオロ3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-イル)-2-クロロエタン-1-オン(BD、1.2g、3.57mmol、62%)が無色半固体として入手された。MS(ESI):337[M+H]+.
DCM(75mL)中の(6-ブロモ-1,2,3,4-テトラヒドロイソキノリン-3-イル) メタノール(BC、1.5g、5.77mmol、1.0当量)の撹拌溶液へ、TEA(0.8mL、5.77mmol、1.0当量)を加えた。次いでこれを0℃まで冷却し、クロロ塩化アセチル(0.45mL、5.77mmol、1.0当量)を滴加した。反応混合物を室温にて2h撹拌した。反応が完了したら、反応混合物を希HCl(80mL)および水(100mL)で洗浄した。有機層を無水硫酸ナトリウム上で乾燥させて濾過し、減圧下で濃縮することで粗化合物が入手されたが、これをDCM:MeOH(9.5:5)を使用するカラムクロマトグラフィーによって精製することで、1-(6-ブロモ-8-フルオロ3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-イル)-2-クロロエタン-1-オン(BD、1.2g、3.57mmol、62%)が無色半固体として入手された。MS(ESI):337[M+H]+.
9-ブロモ-7-フルオロ-1,6,11,11a-テトラヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-4(3H)-オン(BE):
THF(60mL)中の1-(6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-イル)-2-クロロエタン-1-オン(BD、1.2g、3.57mmol、1.0当量)の撹拌溶液へ、水素化ナトリウム(55%)(0.47g、10.71mmol、3.0当量)を0℃にて加えた。反応混合物を室温にさせて2h撹拌した。過剰の試薬を水の添加によって分解し、pHを3N 水性の塩酸で5~6へ調整した。溶液を酢酸エチル(3×70mL)で抽出した。有機層をブライン溶液(100mL)で洗浄し、硫酸ナトリウム上で乾燥させた。これを減圧下で濃縮することで粗化合物が入手されたが、これをn-ヘキサン:酢酸エチル(7:3)を使用するカラムクロマトグラフィーによって精製することで、9-ブロモ-7-フルオロ-1,6,11,11a-テトラヒドロ-[1,4]-オキサジノ-[4,3-b]イソキノリン-4(3H)-オン(BE、0.8g、2.67mmol、75%)が灰白色固体として入手された。MS(ESI):301[M+H]+.
THF(60mL)中の1-(6-ブロモ-8-フルオロ-3-(ヒドロキシメチル)-3,4-ジヒドロイソキノリン-2(1H)-イル)-2-クロロエタン-1-オン(BD、1.2g、3.57mmol、1.0当量)の撹拌溶液へ、水素化ナトリウム(55%)(0.47g、10.71mmol、3.0当量)を0℃にて加えた。反応混合物を室温にさせて2h撹拌した。過剰の試薬を水の添加によって分解し、pHを3N 水性の塩酸で5~6へ調整した。溶液を酢酸エチル(3×70mL)で抽出した。有機層をブライン溶液(100mL)で洗浄し、硫酸ナトリウム上で乾燥させた。これを減圧下で濃縮することで粗化合物が入手されたが、これをn-ヘキサン:酢酸エチル(7:3)を使用するカラムクロマトグラフィーによって精製することで、9-ブロモ-7-フルオロ-1,6,11,11a-テトラヒドロ-[1,4]-オキサジノ-[4,3-b]イソキノリン-4(3H)-オン(BE、0.8g、2.67mmol、75%)が灰白色固体として入手された。MS(ESI):301[M+H]+.
9-ブロモ-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン(BF):
THF(5.0mL)中の9-ブロモ-7-フルオロ-1,6,11,11a-テトラヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-4(3H)-オン(BE、800mg、2.67mmol、1当量)の撹拌溶液へ、BH3-DMS(0.7mL、7.99mmol、3.0当量)を0℃にて加えた。次いで反応混合物を80℃にて16h撹拌し、反応の完了をTLCによって監視した。反応が完了したらメタノール(8mL)を、これに続き6N HCl溶液(3mL)を0℃にてゆっくり加えた。その結果得られた混合物を80℃にて16h還流した。反応混合物を減圧下で濃縮し、ジエチルエーテルとともに粉砕することで、9-ブロモ-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン(BF、800mg、2.79mmol、96%)が入手された。MS(ESI):286[M+H]+.
THF(5.0mL)中の9-ブロモ-7-フルオロ-1,6,11,11a-テトラヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-4(3H)-オン(BE、800mg、2.67mmol、1当量)の撹拌溶液へ、BH3-DMS(0.7mL、7.99mmol、3.0当量)を0℃にて加えた。次いで反応混合物を80℃にて16h撹拌し、反応の完了をTLCによって監視した。反応が完了したらメタノール(8mL)を、これに続き6N HCl溶液(3mL)を0℃にてゆっくり加えた。その結果得られた混合物を80℃にて16h還流した。反応混合物を減圧下で濃縮し、ジエチルエーテルとともに粉砕することで、9-ブロモ-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン(BF、800mg、2.79mmol、96%)が入手された。MS(ESI):286[M+H]+.
メチル7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキシラート(BG):
マグネチックスターラーバー、9-ブロモ-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン(BE、600mg、2.097mmol、1.0当量)を含有するオートクレーブへ、メタノール(15mL)およびKOAc(617mg、6.29mmol、3.0当量)を加えた。溶液をN2(g)で30分間脱気した。次いでPd(OAc)2(94mg、0.4193mmol、0.2当量)およびDPPP(303mg、0.7338mmol、0.35当量)を加えた。反応混合物を次いで一酸化炭素圧力(350psi)下110℃にて48h加熱し、TLCおよびLCMSによって監視した。反応完了後、反応混合物をセライトに通して濾過し、メタノール(25mL)で洗浄した。合わせた濾過物を減圧下で濃縮し、残渣を、n-ヘキサン:酢酸エチル(7:3)を使用するカラムクロマトグラフィーによって精製することでラセミのメチル7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキシラート(BG)が入手されたが、これをキラル分取HPLCによって分離した。
マグネチックスターラーバー、9-ブロモ-7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン(BE、600mg、2.097mmol、1.0当量)を含有するオートクレーブへ、メタノール(15mL)およびKOAc(617mg、6.29mmol、3.0当量)を加えた。溶液をN2(g)で30分間脱気した。次いでPd(OAc)2(94mg、0.4193mmol、0.2当量)およびDPPP(303mg、0.7338mmol、0.35当量)を加えた。反応混合物を次いで一酸化炭素圧力(350psi)下110℃にて48h加熱し、TLCおよびLCMSによって監視した。反応完了後、反応混合物をセライトに通して濾過し、メタノール(25mL)で洗浄した。合わせた濾過物を減圧下で濃縮し、残渣を、n-ヘキサン:酢酸エチル(7:3)を使用するカラムクロマトグラフィーによって精製することでラセミのメチル7-フルオロ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキシラート(BG)が入手されたが、これをキラル分取HPLCによって分離した。
129および130の調製のためのこれに続くステップを、化合物93および94の調製に使用されたのと類似のやり方で実施した。
(R)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキサミド.TFA(129)。MS(ESI):267[M+H]+
(S)-7-フルオロ-N-ヒドロキシ-1,3,4,6,11,11a-ヘキサヒドロ-[1,4]オキサジノ[4,3-b]イソキノリン-9-カルボキサミド.TFA(130) HPLC純度:100%、MS(ESI):267[M+H]+
化合物129および130は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
以下の化合物を、化合物129および130を調製するのに使用したのと類似のやり方で調製した。化合物対131/132および133/134は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(R)-6'-フルオロ-N-ヒドロキシ-1',5',10',10a'-テトラヒドロ-3'H-スピロ[シクロヘキサン-1,2'-ピロロ[1,2-b]イソキノリン]-8'-カルボキサミド(135)、および
(S)-6'-フルオロ-N-ヒドロキシ-1',5',10',10a'-テトラヒドロ-3'H-スピロ[シクロヘキサン-1,2'-ピロロ[1,2-b]イソキノリン]-8'-カルボキサミド(136)
(S)-6'-フルオロ-N-ヒドロキシ-1',5',10',10a'-テトラヒドロ-3'H-スピロ[シクロヘキサン-1,2'-ピロロ[1,2-b]イソキノリン]-8'-カルボキサミド(136)
1-アリルシクロヘキサン-1-カルボニトリル(BJ):
THF(30mL)中のシクロヘキサンカルボニトリル(BH、3.0g、27.50mmol、1.0当量)の撹拌溶液へ-78℃にて、ヘキサン(30.25mL、30.25mmol、1.1当量)中の1M LiHMDSを滴加した。その結果得られた反応混合物を同じ温度にて30分間撹拌した。この反応混合物へ臭化アリル(BI、8.32g、68.75mmol、2.5当量)を滴加した。反応混合物を室温にて18h撹拌した。反応完了後これを氷冷水(100mL)の添加によってクエンチし、DCM(2×100mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、濃縮することで1-アリルシクロヘキサン-1-カルボニトリル(BJ、3.0g、20.10mmol、73%)が与えられた。1H NMR(400MHz,クロロホルム-d)δ5.93(ddt,J=17.3,10.3,7.4Hz,1H),5.33-5.13(m,2H),2.32(d,J=7.3Hz,2H),2.06-1.92(m,2H),1.78(ddt,J=11.2,7.3,3.4Hz,2H),1.70-1.59(m,2H),1.36-1.14(m,2H).
THF(30mL)中のシクロヘキサンカルボニトリル(BH、3.0g、27.50mmol、1.0当量)の撹拌溶液へ-78℃にて、ヘキサン(30.25mL、30.25mmol、1.1当量)中の1M LiHMDSを滴加した。その結果得られた反応混合物を同じ温度にて30分間撹拌した。この反応混合物へ臭化アリル(BI、8.32g、68.75mmol、2.5当量)を滴加した。反応混合物を室温にて18h撹拌した。反応完了後これを氷冷水(100mL)の添加によってクエンチし、DCM(2×100mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ、濃縮することで1-アリルシクロヘキサン-1-カルボニトリル(BJ、3.0g、20.10mmol、73%)が与えられた。1H NMR(400MHz,クロロホルム-d)δ5.93(ddt,J=17.3,10.3,7.4Hz,1H),5.33-5.13(m,2H),2.32(d,J=7.3Hz,2H),2.06-1.92(m,2H),1.78(ddt,J=11.2,7.3,3.4Hz,2H),1.70-1.59(m,2H),1.36-1.14(m,2H).
(1-アリルシクロヘキシル)メタンアミン(BK):
THF(30mL)中の1-アリルシクロヘキサン-1-カルボニトリル(BJ、3.0g、20.10mmol、1.0当量)の撹拌溶液へ0℃にて、THF(22.11mL、22.11mmol、1.1当量)中の1M LiAlH4を滴加した。その結果得られた反応混合物を室温にて3時間撹拌した。反応完了後反応混合物を酢酸エチル(50mL)および水(10mL)の慎重な添加によってクエンチした。その結果得られた懸濁液をセライトベッドに通して濾過し、エチルアセタート(50mL)で洗浄し、減圧下で濃縮することで、(1-アリルシクロヘキシル)メタンアミン(BK、1.7g、11.10mmol、55%)が与えられた。1H NMR(400MHz,クロロホルム-d)δ5.86(tt,J=17.0,9.5Hz,1H),5.25-4.90(m,2H),2.56(s,2H),2.24-2.01(m,2H),1.44-1.11(m,10H).
THF(30mL)中の1-アリルシクロヘキサン-1-カルボニトリル(BJ、3.0g、20.10mmol、1.0当量)の撹拌溶液へ0℃にて、THF(22.11mL、22.11mmol、1.1当量)中の1M LiAlH4を滴加した。その結果得られた反応混合物を室温にて3時間撹拌した。反応完了後反応混合物を酢酸エチル(50mL)および水(10mL)の慎重な添加によってクエンチした。その結果得られた懸濁液をセライトベッドに通して濾過し、エチルアセタート(50mL)で洗浄し、減圧下で濃縮することで、(1-アリルシクロヘキシル)メタンアミン(BK、1.7g、11.10mmol、55%)が与えられた。1H NMR(400MHz,クロロホルム-d)δ5.86(tt,J=17.0,9.5Hz,1H),5.25-4.90(m,2H),2.56(s,2H),2.24-2.01(m,2H),1.44-1.11(m,10H).
tert-ブチル((1-アリルシクロヘキシル)メチル)カルバマート(BL):
DCM(17mL)中の(1-アリルシクロヘキシル)メタンアミン(BK、1.7g、11.10mmol、1.0当量)の溶液へ、TEA(4.64mL、33.30mmol、3.0当量)、DMAP(0.135g、1.11mmol、0.1当量)、およびジ-tert-ブチルジカーボネート(3.35g、27.75mmol、2.5当量)を加えた。その結果得られた反応混合物を室温にて2h撹拌した。反応完了後反応混合物をDCM(100mL)で希釈し、水(100mL)で洗浄した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。残渣を、ヘキサン中10%酢酸エチル中産物を溶離するカラムクロマトグラフィーによって精製することで、tert-ブチル((1-アリルシクロヘキシル)メチル)カルバマート(BL、1.6g、6.31mmol、57%)が粘着性液体として生産された。1H NMR(400MHz,クロロホルム-d)δ5.95-5.82(m,1H),5.15-5.01(m,2H),4.56(s,1H),3.08(d,J=6.5Hz,2H),2.08(d,J=7.4Hz,2H),1.48(s,9H),1.38-1.18(m,10H).
DCM(17mL)中の(1-アリルシクロヘキシル)メタンアミン(BK、1.7g、11.10mmol、1.0当量)の溶液へ、TEA(4.64mL、33.30mmol、3.0当量)、DMAP(0.135g、1.11mmol、0.1当量)、およびジ-tert-ブチルジカーボネート(3.35g、27.75mmol、2.5当量)を加えた。その結果得られた反応混合物を室温にて2h撹拌した。反応完了後反応混合物をDCM(100mL)で希釈し、水(100mL)で洗浄した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮した。残渣を、ヘキサン中10%酢酸エチル中産物を溶離するカラムクロマトグラフィーによって精製することで、tert-ブチル((1-アリルシクロヘキシル)メチル)カルバマート(BL、1.6g、6.31mmol、57%)が粘着性液体として生産された。1H NMR(400MHz,クロロホルム-d)δ5.95-5.82(m,1H),5.15-5.01(m,2H),4.56(s,1H),3.08(d,J=6.5Hz,2H),2.08(d,J=7.4Hz,2H),1.48(s,9H),1.38-1.18(m,10H).
135および136の調製のためのこれに続くステップを、化合物119および120の調製に使用されたのと類似のやり方で実施した。化合物135および136は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
以下の化合物を、化合物135を調製するのに使用したのと類似のやり方で調製した。化合物137および138は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(S)-11-フルオロ-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(139)、および
(R)-11-フルオロ-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(140)。
(R)-11-フルオロ-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(140)。
2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT):
メタノール(150mL)中の2-(3-フルオロ-5-メトキシフェニル)アセトニトリル(BS、8.0g、48.46mmol、1.0当量)の溶液へ、NiCl2.6H2O(5.76g、24.23mmol、0.5当量)、Boc無水物(31.69g、0.145mmol、3.0当量)、および水素化ホウ素ナトリウム(小分けで(portion wise))(5.50g、0.145mmol、3.0当量)を0℃にて加えた。その結果得られた混合物を室温にて1h撹拌した。反応をTLCによって監視した。反応混合物をセライトに通して濾過し、メタノール(100mL)で洗浄した。合わせた濾過物を蒸発させ、残渣を酢酸エチル(250mL)に溶解し、不溶性粒子をセライトに通して濾過し、酢酸エチル(100mL)で洗浄した。合わせた濾過物を蒸発乾固させた。残渣を、ヘキサン中10%酢酸エチルを溶離液として使用するコンビフラッシュによって精製した。純粋な画分を蒸発させることで、tert-ブチル(3-フルオロ-5-メトキシフェネチル)カルバマート(10.5g、39.02mmol、80%)が与えられた。MS(ESI):270[M+H]+。DCM(80mL)中のtert-ブチル(3-フルオロ-5-メトキシフェネチル)カルバマート(10.5g、39.02mmol、1.0当量)の溶液へ、TFA(390.20mmol、29.65mL、10当量)を0℃にて加えた。その結果得られた混合物を室温にて16h撹拌した。反応混合物を次いで重炭酸塩飽和溶液(100mL)に注ぎ、DCM(3×100mL)で抽出した。合わせた有機物を硫酸ナトリウム上で乾燥させて蒸発させることで、2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、4.5g、26.21mmol、67%)が与えられた。MS(ESI):170[M+H]+.
メタノール(150mL)中の2-(3-フルオロ-5-メトキシフェニル)アセトニトリル(BS、8.0g、48.46mmol、1.0当量)の溶液へ、NiCl2.6H2O(5.76g、24.23mmol、0.5当量)、Boc無水物(31.69g、0.145mmol、3.0当量)、および水素化ホウ素ナトリウム(小分けで(portion wise))(5.50g、0.145mmol、3.0当量)を0℃にて加えた。その結果得られた混合物を室温にて1h撹拌した。反応をTLCによって監視した。反応混合物をセライトに通して濾過し、メタノール(100mL)で洗浄した。合わせた濾過物を蒸発させ、残渣を酢酸エチル(250mL)に溶解し、不溶性粒子をセライトに通して濾過し、酢酸エチル(100mL)で洗浄した。合わせた濾過物を蒸発乾固させた。残渣を、ヘキサン中10%酢酸エチルを溶離液として使用するコンビフラッシュによって精製した。純粋な画分を蒸発させることで、tert-ブチル(3-フルオロ-5-メトキシフェネチル)カルバマート(10.5g、39.02mmol、80%)が与えられた。MS(ESI):270[M+H]+。DCM(80mL)中のtert-ブチル(3-フルオロ-5-メトキシフェネチル)カルバマート(10.5g、39.02mmol、1.0当量)の溶液へ、TFA(390.20mmol、29.65mL、10当量)を0℃にて加えた。その結果得られた混合物を室温にて16h撹拌した。反応混合物を次いで重炭酸塩飽和溶液(100mL)に注ぎ、DCM(3×100mL)で抽出した。合わせた有機物を硫酸ナトリウム上で乾燥させて蒸発させることで、2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、4.5g、26.21mmol、67%)が与えられた。MS(ESI):170[M+H]+.
1-(3-フルオロ-5-メトキシフェネチル)ピペリジン-2,6-ジオン(BV):
乾燥酢酸エチル(20mL)中の2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、2.2g、13.01mmol、1.0当量)および グルタル酸無水物(BU、1.78mmol、1.2当量)の溶液を室温にて30分間撹拌した。酢酸エチルを減圧下で除去し、その結果得られた残渣をトルエン(20mL)に溶解した。この反応混合物へ塩化アセチル(5.1g、65.05mmol、5当量)を加え、1h還流した。反応混合物を水性Na2CO3で洗浄し、無水Na2SO4上で乾燥させた。有機層を減圧下で濃縮し、これに続きヘキサン中30%酢酸エチルを溶離液として使用するシリカゲルカラム精製を行うことで、1-(3-フルオロ-5-メトキシフェネチル)ピペリジン-2,6-ジオン(BV、2.7g、10.18mmol、78%)が無色液体として供与された。1H NMR(400MHz,クロロホルム-d)δ6.74-6.39(m,3H),4.09-3.90(m,2H),3.81(s,3H),2.78(t,J=7.9Hz,2H),2.66(t,J=6.4Hz,4 H),1.95(h,J=7.4,6.6Hz,2H).
乾燥酢酸エチル(20mL)中の2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、2.2g、13.01mmol、1.0当量)および グルタル酸無水物(BU、1.78mmol、1.2当量)の溶液を室温にて30分間撹拌した。酢酸エチルを減圧下で除去し、その結果得られた残渣をトルエン(20mL)に溶解した。この反応混合物へ塩化アセチル(5.1g、65.05mmol、5当量)を加え、1h還流した。反応混合物を水性Na2CO3で洗浄し、無水Na2SO4上で乾燥させた。有機層を減圧下で濃縮し、これに続きヘキサン中30%酢酸エチルを溶離液として使用するシリカゲルカラム精製を行うことで、1-(3-フルオロ-5-メトキシフェネチル)ピペリジン-2,6-ジオン(BV、2.7g、10.18mmol、78%)が無色液体として供与された。1H NMR(400MHz,クロロホルム-d)δ6.74-6.39(m,3H),4.09-3.90(m,2H),3.81(s,3H),2.78(t,J=7.9Hz,2H),2.66(t,J=6.4Hz,4 H),1.95(h,J=7.4,6.6Hz,2H).
11-フルオロ-9-メトキシ-1,2,3,6,7,11b-ヘキサヒドロ-4H-ピリド[2,1-a]イソキノリン-4-オン(BW):
乾燥ジクロロメタン(30mL)中の1-(3-フルオロ-5-メトキシフェネチル)ピペリジン-2,6-ジオン(BV、2.7g、10.18mmol、1.0当量)の溶液を0℃まで冷却した。この溶液へ、撹拌しながらTfOH(6.11g、40.73mmol、4.0当量)を加えた。45分後、内容物を室温まで加温し、NaBH4(1.54g、40.73mmol、4.0当量)を、これに続きTFA(3.11mL、40.73mmol、4.0当量)を加えた。その結果得られた溶液を色が消失するまで撹拌した。(色が長時間残るか、NaBH4およびTFAを追加で使用した)。反応混合物を減圧下で蒸発乾固させた。固体残渣をジクロロメタン(180mL)に溶解し、不溶性の材料を濾過によって除去した。濾過物をNaHCO3飽和溶液(250mL)で洗浄した。有機層を無水Na2SO4上で乾燥させて濾過した。溶媒を真空下で蒸発させることで、11-フルオロ-9-メトキシ-1,2,3,6,7,11b-ヘキサヒドロ-4H-ピリド[2,1-a]イソキノリン-4-オン(BW、2.54g、10.18mmol、100%)が与えられた。MS(ESI):250.4[M+H]+.
乾燥ジクロロメタン(30mL)中の1-(3-フルオロ-5-メトキシフェネチル)ピペリジン-2,6-ジオン(BV、2.7g、10.18mmol、1.0当量)の溶液を0℃まで冷却した。この溶液へ、撹拌しながらTfOH(6.11g、40.73mmol、4.0当量)を加えた。45分後、内容物を室温まで加温し、NaBH4(1.54g、40.73mmol、4.0当量)を、これに続きTFA(3.11mL、40.73mmol、4.0当量)を加えた。その結果得られた溶液を色が消失するまで撹拌した。(色が長時間残るか、NaBH4およびTFAを追加で使用した)。反応混合物を減圧下で蒸発乾固させた。固体残渣をジクロロメタン(180mL)に溶解し、不溶性の材料を濾過によって除去した。濾過物をNaHCO3飽和溶液(250mL)で洗浄した。有機層を無水Na2SO4上で乾燥させて濾過した。溶媒を真空下で蒸発させることで、11-フルオロ-9-メトキシ-1,2,3,6,7,11b-ヘキサヒドロ-4H-ピリド[2,1-a]イソキノリン-4-オン(BW、2.54g、10.18mmol、100%)が与えられた。MS(ESI):250.4[M+H]+.
11-フルオロ-9-メトキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン(BX):
乾燥THF(25mL)中の11-フルオロ-9-メトキシ-1,2,3,6,7,11b-ヘキサヒドロ-4H-ピリド[2,1-a]イソキノリン-4-オン(BW、2.54g、10.18mmol、1.0当量)の溶液へ、水素化ホウ素ナトリウム(0.963g、25.45mmol、2.5当量)を0℃にて加えた。乾燥THF中のヨウ素(0.661g、5.21mmol、0.51当量)の溶液を、シリンジを介して滴加し、同じ温度にて2h撹拌した。混合物を次いで24h還流した。反応物を室温までもっていき、メタノール(30mL)でクエンチし、その後溶媒を蒸発させた。得られた残渣を5M KOH(50mL)で18h還流し、反応混合物をDCM(2×150mL)で抽出した。有機層を無水Na2SO4上で乾燥させ、蒸発させることで(BX、1.2g、5.10mmol、50%)が与えられた。MS(ESI):222[M+H]+.
乾燥THF(25mL)中の11-フルオロ-9-メトキシ-1,2,3,6,7,11b-ヘキサヒドロ-4H-ピリド[2,1-a]イソキノリン-4-オン(BW、2.54g、10.18mmol、1.0当量)の溶液へ、水素化ホウ素ナトリウム(0.963g、25.45mmol、2.5当量)を0℃にて加えた。乾燥THF中のヨウ素(0.661g、5.21mmol、0.51当量)の溶液を、シリンジを介して滴加し、同じ温度にて2h撹拌した。混合物を次いで24h還流した。反応物を室温までもっていき、メタノール(30mL)でクエンチし、その後溶媒を蒸発させた。得られた残渣を5M KOH(50mL)で18h還流し、反応混合物をDCM(2×150mL)で抽出した。有機層を無水Na2SO4上で乾燥させ、蒸発させることで(BX、1.2g、5.10mmol、50%)が与えられた。MS(ESI):222[M+H]+.
139および140の調製のためのこれに続くステップを、化合物119および120の調製に使用されたのと類似のやり方で実施した。
(S)-11-フルオロ-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(139)。1H NMR(400MHz,DMSO-d6)δ11.19(s,1H),9.11(s,1H),7.37(s,1H),7.29(d,J=11.9Hz,1H),3.55(d,J=10.9Hz,1H),3.29-3.11(m,1H),3.03-2.75(m,3H),2.73-2.60(m,2H),2.11(d,J=12.6Hz,1H),1.80(d,J=11.4Hz,1H),1.49-1.33(m,4H)。MS(ESI):265[M+H]+.
(R)-11-フルオロ-N-ヒドロキシ-1,3,4,6,7,11b-ヘキサヒドロ-2H-ピリド[2,1-a]イソキノリン-9-カルボキサミド(140)。1H NMR(400MHz,DMSO-d6)δ11.17(s,1H),9.10(s,1H),7.37(s,1H),7.29(d,J=12.2Hz,1H),3.28-3.317(m,1H),3.55(d,J=10.4Hz,1H),3.03-2.86(m,3H),2.73-2.55(m,2H),2.12(d,J=12.5Hz,1H),1.81(d,J=11.5Hz,1H),1.61-1.34(m,4H)。MS(ESI):265[M+H]+
化合物139および140は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
以下の化合物を、化合物93を調製するのに使用したのと類似のやり方で調製した。化合物対143/144および145/146は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
以下の化合物を、化合物79および80を調製するのに使用したのと類似のやり方で調製した。化合物対148/149、151/152、および153/154は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(3R,10bR)-10-フルオロ-N-ヒドロキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(156)、および
(3S,10bS)-10-フルオロ-N-ヒドロキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(157)
(3S,10bS)-10-フルオロ-N-ヒドロキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン-8-カルボキサミド(157)
1-(3-フルオロ-5-メトキシフェネチル)-5-メチルピロリジン-2-オン(CC):
2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、7.0g、41.38mmol、1.5当量)およびレブリン酸(CB、3.2g、27.58mmol、1.0当量)を圧力管中に入れた。混合物へDMSO(78mL)、ギ酸(5.2mL、137.93mmol、5.0当量)、およびNEt3(3.84mL、27.58mmol、1.0当量)を注入した。混合物をアルゴンで15分間通気し、次いで100℃にて5h撹拌した。室温まで冷却後、反応をNaOH飽和溶液(150mL)で塩基性化し、DCM(3×100mL)で抽出した。有機層をブライン(100mL)で洗浄し、Na2SO4上で乾燥させた。有機溶媒を減圧下で除去し、産物を、30%酢酸エチルを0.1%トリエチルアミンとともに溶離液として使用するフラッシュクロマトグラフィーによって精製した。純粋な画分を蒸発させることで1-(3-フルオロ-5-メトキシフェネチル)-5-メチルピロリジン-2-オン(CC、6.0g、23.89mmol、87%)が与えられた。MS(ESI):252[M+H]+
2-(3-フルオロ-5-メトキシフェニル)エタン-1-アミン(BT、7.0g、41.38mmol、1.5当量)およびレブリン酸(CB、3.2g、27.58mmol、1.0当量)を圧力管中に入れた。混合物へDMSO(78mL)、ギ酸(5.2mL、137.93mmol、5.0当量)、およびNEt3(3.84mL、27.58mmol、1.0当量)を注入した。混合物をアルゴンで15分間通気し、次いで100℃にて5h撹拌した。室温まで冷却後、反応をNaOH飽和溶液(150mL)で塩基性化し、DCM(3×100mL)で抽出した。有機層をブライン(100mL)で洗浄し、Na2SO4上で乾燥させた。有機溶媒を減圧下で除去し、産物を、30%酢酸エチルを0.1%トリエチルアミンとともに溶離液として使用するフラッシュクロマトグラフィーによって精製した。純粋な画分を蒸発させることで1-(3-フルオロ-5-メトキシフェネチル)-5-メチルピロリジン-2-オン(CC、6.0g、23.89mmol、87%)が与えられた。MS(ESI):252[M+H]+
10-フルオロ-8-メトキシ-3-メチル-2,3,5,6-テトラヒドロ-1H-ピロロ[2,1-a]イソキノリン-4-ium(CD):
アセトニトリル(240mL)中の1-(3-フルオロ-5-メトキシフェネチル)-5-メチルピロリジン-2-オン(CC、6.0g、23.89mmol、1.0当量)の溶液へ、オキシ塩化リン(11.16mL、119.46mmol、5.0当量)を0℃にて加えた。合わせた反応混合物を120℃にて3h還流加熱した。反応の完了をTLCおよびLCMSによって確認した。反応物を室温まで冷却した。溶媒を蒸発乾固させた。残渣をジエチルエーテル(50mL)で洗浄することで、10-フルオロ-8-メトキシ-3-メチル-2,3,5,6-テトラヒドロ-1H-ピロロ[2,1-a]イソキノリン-4-ium(CD、6.0g、25.62mmol)が与えられた。MS(ESI):234[M]+.
アセトニトリル(240mL)中の1-(3-フルオロ-5-メトキシフェネチル)-5-メチルピロリジン-2-オン(CC、6.0g、23.89mmol、1.0当量)の溶液へ、オキシ塩化リン(11.16mL、119.46mmol、5.0当量)を0℃にて加えた。合わせた反応混合物を120℃にて3h還流加熱した。反応の完了をTLCおよびLCMSによって確認した。反応物を室温まで冷却した。溶媒を蒸発乾固させた。残渣をジエチルエーテル(50mL)で洗浄することで、10-フルオロ-8-メトキシ-3-メチル-2,3,5,6-テトラヒドロ-1H-ピロロ[2,1-a]イソキノリン-4-ium(CD、6.0g、25.62mmol)が与えられた。MS(ESI):234[M]+.
10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE1)、および
10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE2):
メタノール(240mL)中の10-フルオロ-8-メトキシ-3-メチル-2,3,5,6-テトラヒドロ-1H-ピロロ[2,1-a]イソキノリン-4-ium(CD、6.0g、25.62mmol、1当量)の溶液へ、NaBH4(2.42g、64.10mmol、2.5当量)を0℃にて加えた。反応混合物を室温にて3h撹拌した。反応の完了をTLCによって確認した。メタノールを蒸発乾固させ、水(100mL)を加えた。その結果得られたエマルションを酢酸エチル(2×100mL)で抽出した。有機層を分離し、Na2SO4上で乾燥させて蒸発させた。残渣をコンビフラッシュによって精製した。産物をヘキサン中の10%酢酸エチルと0.1%TEAにて溶離した。ジアステレオマーを分取HPLCによってさらに分離することで、10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE1、0.65g、2.76mmol、12%)が油として供与された。1H NMR(400MHz,クロロホルム-d)δ6.57-6.33(m,2H),3.75(d,J=4.1Hz,3H),3.36-2.97(m,3H),2.84(d,J=16.6Hz,1H),2.53-2.35(m,2H),2.29(q,J=6.8Hz,1H),2.04(d,J=8.0Hz,2H),1.80-1.68(m,1H),1.50(tdd,J=12.2,8.6,3.7Hz,1H),1.20(d,J=6.1Hz,4H),MS(ESI):236[M+H]+。および10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE2,0.2g,0.85mmol,4%)。1H NMR(400MHz,DMSO-d6)δ6.64(dd,J=12.2,2.5Hz,1H),6.57(d,J=2.5Hz,1H),4.35(t,J=7.7Hz,1H),3.73(s,3H),3.05(q,J=10.1,9.2Hz,2H),2.88-2.72(m,2H),2.43-2.34(m,1H),1.94(dt,J=9.9,7.1Hz,1H),1.53(q,J=11.2,10.2Hz,1H),1.38(p,J=8.8Hz,1H),1.10(d,J=6.1Hz,3H),MS(ESI):236[M+H]+。CE1の立体化学をNOE実験によって確認した。
10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE2):
メタノール(240mL)中の10-フルオロ-8-メトキシ-3-メチル-2,3,5,6-テトラヒドロ-1H-ピロロ[2,1-a]イソキノリン-4-ium(CD、6.0g、25.62mmol、1当量)の溶液へ、NaBH4(2.42g、64.10mmol、2.5当量)を0℃にて加えた。反応混合物を室温にて3h撹拌した。反応の完了をTLCによって確認した。メタノールを蒸発乾固させ、水(100mL)を加えた。その結果得られたエマルションを酢酸エチル(2×100mL)で抽出した。有機層を分離し、Na2SO4上で乾燥させて蒸発させた。残渣をコンビフラッシュによって精製した。産物をヘキサン中の10%酢酸エチルと0.1%TEAにて溶離した。ジアステレオマーを分取HPLCによってさらに分離することで、10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE1、0.65g、2.76mmol、12%)が油として供与された。1H NMR(400MHz,クロロホルム-d)δ6.57-6.33(m,2H),3.75(d,J=4.1Hz,3H),3.36-2.97(m,3H),2.84(d,J=16.6Hz,1H),2.53-2.35(m,2H),2.29(q,J=6.8Hz,1H),2.04(d,J=8.0Hz,2H),1.80-1.68(m,1H),1.50(tdd,J=12.2,8.6,3.7Hz,1H),1.20(d,J=6.1Hz,4H),MS(ESI):236[M+H]+。および10-フルオロ-8-メトキシ-3-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]イソキノリン(CE2,0.2g,0.85mmol,4%)。1H NMR(400MHz,DMSO-d6)δ6.64(dd,J=12.2,2.5Hz,1H),6.57(d,J=2.5Hz,1H),4.35(t,J=7.7Hz,1H),3.73(s,3H),3.05(q,J=10.1,9.2Hz,2H),2.88-2.72(m,2H),2.43-2.34(m,1H),1.94(dt,J=9.9,7.1Hz,1H),1.53(q,J=11.2,10.2Hz,1H),1.38(p,J=8.8Hz,1H),1.10(d,J=6.1Hz,3H),MS(ESI):236[M+H]+。CE1の立体化学をNOE実験によって確認した。
156、157、158および159の調製のためのこれに続くステップを、化合物119および120の調製に使用されたのと類似のやり方で実施した。化合物対156/157および158/159は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(S)-N-ヒドロキシ-5-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]フタラジン-8-カルボキサミド(160)、および
(R)-N-ヒドロキシ-5-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]フタラジン-8-カルボキサミド(161)
(R)-N-ヒドロキシ-5-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]フタラジン-8-カルボキサミド(161)
メチル4-ブロモ-3-(ブロモメチル)ベンゾアート(CK):
25%NaHCO3溶液(5mL)中の1H-ピロール-1-アミン(CI、3g、36.54mmol、1.0当量)の撹拌溶液へ、エチルクロロホルマート(CJ、6.96mL、73.074mmol、2.0当量)を室温にて加えた。反応混合物を室温にて10分間撹拌し、TLCによって監視した。反応を水(20mL)で希釈し、EtOAc(3×25mL)で抽出した。合わせた有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、粗材料エチル(1H-ピロール-1-イル)カルバマート(CK、3.2g、20.756mmol、85%)が得られた。MS(ESI):155[M+H]+.
25%NaHCO3溶液(5mL)中の1H-ピロール-1-アミン(CI、3g、36.54mmol、1.0当量)の撹拌溶液へ、エチルクロロホルマート(CJ、6.96mL、73.074mmol、2.0当量)を室温にて加えた。反応混合物を室温にて10分間撹拌し、TLCによって監視した。反応を水(20mL)で希釈し、EtOAc(3×25mL)で抽出した。合わせた有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、粗材料エチル(1H-ピロール-1-イル)カルバマート(CK、3.2g、20.756mmol、85%)が得られた。MS(ESI):155[M+H]+.
メチル4-ブロモ-3-(((エトキシカルボニル)(1H-ピロール-1-イル)アミノ)メチル)ベンゾアート(CM):
THF(25mL)中の(CK、0.5g、3.24mmol、1.0当量)の溶液へ、KOtBu(0.40g、3.5674mmol,1.1当量)を加え、混合物を5℃にて1時間撹拌した。これに続きCL(0.99g、3.2431mmol、1.0当量)を加え、5℃にて1hおよび室温にて7h撹拌した。混合物を氷冷水(25mL)上へ注ぎ、5分間撹拌し、酢酸エチル(2×25mL)で抽出した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮し、EtOAc:ヘキサン(3:7)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル4-ブロモ-3-(((エトキシカルボニル)(1H-ピロール-1-イル)アミノ)メチル)ベンゾアート(CM、1.1g、2.885mmol、89%)が得られた。MS(ESI):382[M+H]+.
THF(25mL)中の(CK、0.5g、3.24mmol、1.0当量)の溶液へ、KOtBu(0.40g、3.5674mmol,1.1当量)を加え、混合物を5℃にて1時間撹拌した。これに続きCL(0.99g、3.2431mmol、1.0当量)を加え、5℃にて1hおよび室温にて7h撹拌した。混合物を氷冷水(25mL)上へ注ぎ、5分間撹拌し、酢酸エチル(2×25mL)で抽出した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮し、EtOAc:ヘキサン(3:7)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル4-ブロモ-3-(((エトキシカルボニル)(1H-ピロール-1-イル)アミノ)メチル)ベンゾアート(CM、1.1g、2.885mmol、89%)が得られた。MS(ESI):382[M+H]+.
5-エチル8-メチルピロロ[2,1-a]フタラジン-5,8(6H)-ジカルボキシラート(CN):
DMA(10mL)中のメチル4-ブロモ-3-(((エトキシカルボニル)(1H-ピロール-1-イル)アミノ)メチル)ベンゾアート(CM、1.1g、2.88mmol、1.0当量)の溶液へ、トリフェニルホスフィン(0.151g、0.5774mmol、0.2当量)、Pd(OAc)2(0.064g、0.2887mmol、0.1当量)、および酢酸カリウム(0.566g、5.7742mmol、2当量)を窒素下室温にて加えた。反応物を150℃にて7h撹拌し、次いで水(30mL)でクエンチし、酢酸エチル(3×20mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、濾過してin vacuoで濃縮した。残渣をフラッシュシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン(5:5))によって精製することで、5-エチル8-メチルピロロ[2,1-a]フタラジン-5,8(6H)-ジカルボキシラートが灰白色固体(CN、0.812g、2.71mmol、93%)として与えられた。MS(ESI):301[M+H]+.
DMA(10mL)中のメチル4-ブロモ-3-(((エトキシカルボニル)(1H-ピロール-1-イル)アミノ)メチル)ベンゾアート(CM、1.1g、2.88mmol、1.0当量)の溶液へ、トリフェニルホスフィン(0.151g、0.5774mmol、0.2当量)、Pd(OAc)2(0.064g、0.2887mmol、0.1当量)、および酢酸カリウム(0.566g、5.7742mmol、2当量)を窒素下室温にて加えた。反応物を150℃にて7h撹拌し、次いで水(30mL)でクエンチし、酢酸エチル(3×20mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、濾過してin vacuoで濃縮した。残渣をフラッシュシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン(5:5))によって精製することで、5-エチル8-メチルピロロ[2,1-a]フタラジン-5,8(6H)-ジカルボキシラートが灰白色固体(CN、0.812g、2.71mmol、93%)として与えられた。MS(ESI):301[M+H]+.
5,6-ジヒドロピロロ[2,1-a]フタラジン-8-カルボン酸(CO1)、および
ピロロ[2,1-a]フタラジン-8-カルボン酸(CO2):
THFおよび水(3mL)中の5-エチル8-メチルピロロ[2,1-a]フタラジン-5,8(6H)-ジカルボキシラート(CN,0.812g、2.70mmol、1.0当量)の撹拌溶液へ、水酸化ナトリウム(0.270g、6.76mmol、2.5当量)を室温にて加えた。反応混合物を90℃まで加熱し、反応をTLCによって監視した。反応完了後これを、希HClを使用して酸性化することで、産物CO1、CO2が沈殿物として得られたが、これを真空下で乾燥させた。産物の形成をLCMSによって確認し、化合物の混合物をさらなる精製はせずに次のステップにそのまま使用した。CO2:MS(ESI):213[M+H]+、CO1:MS(ESI):215[M+H]+
ピロロ[2,1-a]フタラジン-8-カルボン酸(CO2):
THFおよび水(3mL)中の5-エチル8-メチルピロロ[2,1-a]フタラジン-5,8(6H)-ジカルボキシラート(CN,0.812g、2.70mmol、1.0当量)の撹拌溶液へ、水酸化ナトリウム(0.270g、6.76mmol、2.5当量)を室温にて加えた。反応混合物を90℃まで加熱し、反応をTLCによって監視した。反応完了後これを、希HClを使用して酸性化することで、産物CO1、CO2が沈殿物として得られたが、これを真空下で乾燥させた。産物の形成をLCMSによって確認し、化合物の混合物をさらなる精製はせずに次のステップにそのまま使用した。CO2:MS(ESI):213[M+H]+、CO1:MS(ESI):215[M+H]+
メチル5,6-ジヒドロピロロ[2,1-a]フタラジン-8-カルボキシラート(CP1):
ACN(2mL)中の混合物(CO1&CO2、200mg、0.93mmol、1当量)の撹拌溶液へ、K2CO3(0.516g、3.74mmol、4.0当量)およびMeI(0.397mg、2.7969mmol、3当量)を窒素下室温にて滴加した。反応物を室温にて2h撹拌し、TLCを使用して監視した。反応が完了したら、これを水(30mL)で希釈し、酢酸エチル(3×20mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させて濾過し、真空中で濃縮した。残渣をフラッシュシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン(2.5:7.5))によって精製することで、CP1(32mg、0.1322mmol、14%)、CP2(43mg、0.1842mmol、20%)、CP3(39mg、0.1725mmol、18%)が与えられた。CP1:MS(ESI):243[M+H]+、CP2:MS(ESI):229[M+H]+、CP3:MS(ESI):227[M+H]+
ACN(2mL)中の混合物(CO1&CO2、200mg、0.93mmol、1当量)の撹拌溶液へ、K2CO3(0.516g、3.74mmol、4.0当量)およびMeI(0.397mg、2.7969mmol、3当量)を窒素下室温にて滴加した。反応物を室温にて2h撹拌し、TLCを使用して監視した。反応が完了したら、これを水(30mL)で希釈し、酢酸エチル(3×20mL)で抽出した。合わせた有機相をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させて濾過し、真空中で濃縮した。残渣をフラッシュシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン(2.5:7.5))によって精製することで、CP1(32mg、0.1322mmol、14%)、CP2(43mg、0.1842mmol、20%)、CP3(39mg、0.1725mmol、18%)が与えられた。CP1:MS(ESI):243[M+H]+、CP2:MS(ESI):229[M+H]+、CP3:MS(ESI):227[M+H]+
メチル5-メチル-1,2,3,5,6,10b-ヘキサヒドロピロロ[2,1-a]フタラジン-8-カルボキシラート(CQ):
炉乾燥オートクレーブへ、メチル5-メチル-5,6-ジヒドロピロロ[2,1-a]フタラジン-8-カルボキシラート(CP1、0.054g、0.222mmol、1当量)、AcOH(3mL)、およびPd/C(0.05g)を加えた。オートクレーブをH2(g)(100psi)で加圧し、室温にて48h撹拌し、TLCによって監視した。反応完了後、反応混合物をセライトに通して濾過し、THF(20mL)で洗浄した。得られた濾過物を減圧下で濃縮し、分取HPLCによって精製することで、緑色がかった油(CQ、32mg、58%)が得られた。MS(ESI):247[M+H]+
炉乾燥オートクレーブへ、メチル5-メチル-5,6-ジヒドロピロロ[2,1-a]フタラジン-8-カルボキシラート(CP1、0.054g、0.222mmol、1当量)、AcOH(3mL)、およびPd/C(0.05g)を加えた。オートクレーブをH2(g)(100psi)で加圧し、室温にて48h撹拌し、TLCによって監視した。反応完了後、反応混合物をセライトに通して濾過し、THF(20mL)で洗浄した。得られた濾過物を減圧下で濃縮し、分取HPLCによって精製することで、緑色がかった油(CQ、32mg、58%)が得られた。MS(ESI):247[M+H]+
160、161、162および163の調製のためのこれに続くステップを、化合物79の調製に使用されたのと類似のやり方で実施した。化合物160および161は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(R)-N-ヒドロキシ-2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキサミド(164)、および
(S)-N-ヒドロキシ-2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキサミド(165)
(S)-N-ヒドロキシ-2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキサミド(165)
3-((1H-ピロール-1-イル)メチル)-4-ブロモ安息香酸(CT):
DMF(20mL)中のメチル4-ブロモ-3-(ブロモメチル)ベンゾアート(CS、2.0g、6.4935mmol、1.0当量)の撹拌溶液へ、水素化ナトリウム(55%)(611mg、12.987mmol、2.0当量)を、続いてピロール(CR、522mg、7.7922mmol、1.2当量)を0℃にて加え、反応混合物を110℃にて16h撹拌した。反応の完了をTLCおよびLCMSによって監視した。過剰の試薬を水の添加によって分解し、pHを1N 水性塩酸で5~6へ調整した。これを次いで酢酸エチル(3×70mL)で抽出し、有機層をブライン溶液(100mL)で洗浄して硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、3-((1H-ピロール-1-イル)メチル)-4-ブロモ安息香酸(CT、1.5g、5.38mmol、82%)が粗化合物として入手されたが、これを精製せずにさらなる次のステップに使用した。MS(ESI):280[M+H]+.
DMF(20mL)中のメチル4-ブロモ-3-(ブロモメチル)ベンゾアート(CS、2.0g、6.4935mmol、1.0当量)の撹拌溶液へ、水素化ナトリウム(55%)(611mg、12.987mmol、2.0当量)を、続いてピロール(CR、522mg、7.7922mmol、1.2当量)を0℃にて加え、反応混合物を110℃にて16h撹拌した。反応の完了をTLCおよびLCMSによって監視した。過剰の試薬を水の添加によって分解し、pHを1N 水性塩酸で5~6へ調整した。これを次いで酢酸エチル(3×70mL)で抽出し、有機層をブライン溶液(100mL)で洗浄して硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、3-((1H-ピロール-1-イル)メチル)-4-ブロモ安息香酸(CT、1.5g、5.38mmol、82%)が粗化合物として入手されたが、これを精製せずにさらなる次のステップに使用した。MS(ESI):280[M+H]+.
メチル3-((1H-ピロール-1-イル)メチル)-4-ブロモベンゾアート(CU):
アセトニトリル(20mL)中の3-((1H-ピロール-1-イル)メチル)-4-ブロモ安息香酸(CT、1.5g、5.35mmol、1.0当量)の撹拌溶液へ、炭酸カリウム(2.2g、16.0mmol、3当量)およびヨウ化メチル(1.1g、8.03mmol、1.5当量)を室温にて加えた。反応混合物を室温にて16h撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応が完了したら、これを水(20mL)で希釈し、酢酸エチル(40mL)で抽出して有機層をブライン溶液(20mL)で洗浄し、硫酸ナトリウム上で乾燥させて減圧下で濃縮することで、粗混合物が入手された。これを次いでEtOAc:ヘキサン(5%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、CU、メチル3-((1H-ピロール-1-イル)メチル)-4-ブロモベンゾアート(1.3g、4.28mmol、82%)が白色固体として得られた。MS(ESI):294[M+H]+
アセトニトリル(20mL)中の3-((1H-ピロール-1-イル)メチル)-4-ブロモ安息香酸(CT、1.5g、5.35mmol、1.0当量)の撹拌溶液へ、炭酸カリウム(2.2g、16.0mmol、3当量)およびヨウ化メチル(1.1g、8.03mmol、1.5当量)を室温にて加えた。反応混合物を室温にて16h撹拌した。反応の完了をTLCおよびLCMSによって監視した。反応が完了したら、これを水(20mL)で希釈し、酢酸エチル(40mL)で抽出して有機層をブライン溶液(20mL)で洗浄し、硫酸ナトリウム上で乾燥させて減圧下で濃縮することで、粗混合物が入手された。これを次いでEtOAc:ヘキサン(5%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、CU、メチル3-((1H-ピロール-1-イル)メチル)-4-ブロモベンゾアート(1.3g、4.28mmol、82%)が白色固体として得られた。MS(ESI):294[M+H]+
メチル5H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CV):
メチル3-((1H-ピロール-1-イル)メチル)-4-ブロモベンゾアート(CU、1.3g、4.436mmol、1.0当量)、酢酸カリウム(879mg、8.872mmol、2.0当量)を含有するシュレンク管へ、DMF(10mL)をN2(g)雰囲気下で加えた。その結果得られた溶液をN2(g)で20分間脱気し、次いでパラジウムアセタート(0.099g、0.44mmol、0.1当量)およびトリフェニルホスフィン(0.23g、0.88mmol、0.2当量)を加えた。反応混合物を150℃にて3h加熱し、TLCおよびLCMSによって監視した。反応が完了したら、これを室温まで冷却し、氷冷水(20mL)で希釈し、酢酸エチル(40mL)で抽出した。有機層をブライン溶液(20mL)で洗浄し、硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が入手された。これを次いでEtOAc:ヘキサン(6%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル5H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CV、0.49g、2.1596mmol、52%)が固体として得られた。MS(ESI):214[M+H]+
メチル3-((1H-ピロール-1-イル)メチル)-4-ブロモベンゾアート(CU、1.3g、4.436mmol、1.0当量)、酢酸カリウム(879mg、8.872mmol、2.0当量)を含有するシュレンク管へ、DMF(10mL)をN2(g)雰囲気下で加えた。その結果得られた溶液をN2(g)で20分間脱気し、次いでパラジウムアセタート(0.099g、0.44mmol、0.1当量)およびトリフェニルホスフィン(0.23g、0.88mmol、0.2当量)を加えた。反応混合物を150℃にて3h加熱し、TLCおよびLCMSによって監視した。反応が完了したら、これを室温まで冷却し、氷冷水(20mL)で希釈し、酢酸エチル(40mL)で抽出した。有機層をブライン溶液(20mL)で洗浄し、硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が入手された。これを次いでEtOAc:ヘキサン(6%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル5H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CV、0.49g、2.1596mmol、52%)が固体として得られた。MS(ESI):214[M+H]+
メチル2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CW):
酢酸(1mL)中のメチル5H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CV、0.3g、1.38mmol、1.0当量)の撹拌溶液へ、炭素上パラジウム(50%)(0.30g)を加えた。反応混合物を室温にて絶えずH2(g)で4hパージし、TLCおよびLCMSによって監視した。反応が完了したら、これをセライトに通して濾過し、減圧下で濃縮することで、粗混合物が入手された。これを次いでEtOAc:ヘキサン(60%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CW、0.096 g,0.442mmol、47%)が固体として得られた。MS(ESI):216[M-H]-
酢酸(1mL)中のメチル5H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CV、0.3g、1.38mmol、1.0当量)の撹拌溶液へ、炭素上パラジウム(50%)(0.30g)を加えた。反応混合物を室温にて絶えずH2(g)で4hパージし、TLCおよびLCMSによって監視した。反応が完了したら、これをセライトに通して濾過し、減圧下で濃縮することで、粗混合物が入手された。これを次いでEtOAc:ヘキサン(60%)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、メチル2,3,5,9b-テトラヒドロ-1H-ピロロ[2,1-a]イソインドール-7-カルボキシラート(CW、0.096 g,0.442mmol、47%)が固体として得られた。MS(ESI):216[M-H]-
164、165および166の調製のためのこれに続くステップを、化合物94の調製に使用されたのと類似のやり方で実施した。化合物164および165は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
式(III)で表される化合物を、下に詳細に記載される合成スキームおよび手順に倣い調製した。
3-フルオロ-N-ヒドロキシ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンズアミド(167)
3-フルオロ-N-ヒドロキシ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンズアミド(167)
メチル(1r,3r,5r,7r)-アダマンタン-2-カルボキシラート(CZ):
トルエン(150mL)中の(1r,3r,5r,7r)-アダマンタン-2-カルボン酸(CY、24g、133.48mmol、1.0当量)の撹拌溶液へ、塩化チオニル(150mL、2135.6mmol、16当量)を0℃にて加えた。反応混合物を45℃にて45分間撹拌し、TLCによって監視した。出発材料が消費されたら、反応混合物を減圧下で濃縮することで、粗混合物が得られた。粗材料にメタノールを0℃にてゆっくり滴加し、次いで反応混合物を20℃にて24h撹拌した。反応をTLCによって監視し、反応が完了したら;反応混合物を減圧下で濃縮することで、粗混合物が得られた。粗材料を、酢酸エチル/ヘキサン(5:5)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、メチル(1r,3r,5r,7r)-アダマンタン-2-カルボキシラート(CZ、23g、118.39mmol、89%)が供与された。1H NMR(400MHz,クロロホルム-d)δ3.69(s,3H),2.59-2.61(m,1H),2.32(d,J=3.9Hz,2H),1.83-1.90(m,6H),1.72-1.76(m,4H),1.60-1.64(m,3H).
トルエン(150mL)中の(1r,3r,5r,7r)-アダマンタン-2-カルボン酸(CY、24g、133.48mmol、1.0当量)の撹拌溶液へ、塩化チオニル(150mL、2135.6mmol、16当量)を0℃にて加えた。反応混合物を45℃にて45分間撹拌し、TLCによって監視した。出発材料が消費されたら、反応混合物を減圧下で濃縮することで、粗混合物が得られた。粗材料にメタノールを0℃にてゆっくり滴加し、次いで反応混合物を20℃にて24h撹拌した。反応をTLCによって監視し、反応が完了したら;反応混合物を減圧下で濃縮することで、粗混合物が得られた。粗材料を、酢酸エチル/ヘキサン(5:5)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、メチル(1r,3r,5r,7r)-アダマンタン-2-カルボキシラート(CZ、23g、118.39mmol、89%)が供与された。1H NMR(400MHz,クロロホルム-d)δ3.69(s,3H),2.59-2.61(m,1H),2.32(d,J=3.9Hz,2H),1.83-1.90(m,6H),1.72-1.76(m,4H),1.60-1.64(m,3H).
(1r,3r,5r,7r)-2-(メトキシカルボニル)アダマンタン-2-カルボン酸(DA):
THF(230mL)中のメチル(1r,3r,5r,7r)-アダマンタン-2-カルボキシラート(CZ、23g、118.39mmol、1.0当量)の撹拌溶液へ、LDA(177mL、177.58mmol、1.5当量)をN2(g)雰囲気にて-78℃にて加えた。反応混合物を-78℃~-40℃にて1h撹拌し、次いでCO2(g)を反応混合物中-78℃~-40℃にて1hパージした。反応混合物を20℃にて24hさらに撹拌した。TLCによって監視したとおり反応が完了したら、反応混合物を水(150mL)に注ぎ、酢酸エチル(3×200mL)で抽出した。水層を、1N HClを使用して酸性化することで、白色沈殿物が得られたが、これを濾過し、真空下で乾燥させることで、(1r,3r,5r,7r)-2-(メトキシカルボニル)アダマンタン-2-カルボン酸(DA、25g、104.91mmol、89%)が白色固体として与えられた。1H NMR(400MHz,DMSO-d6)δ12.90(s,1H),3.64(s,3H),2.55(s,2H),1.83(d,J=13.0Hz,2H),1.74(d,J=11.3Hz,4H),1.65(d,J=12.9Hz,6H).
THF(230mL)中のメチル(1r,3r,5r,7r)-アダマンタン-2-カルボキシラート(CZ、23g、118.39mmol、1.0当量)の撹拌溶液へ、LDA(177mL、177.58mmol、1.5当量)をN2(g)雰囲気にて-78℃にて加えた。反応混合物を-78℃~-40℃にて1h撹拌し、次いでCO2(g)を反応混合物中-78℃~-40℃にて1hパージした。反応混合物を20℃にて24hさらに撹拌した。TLCによって監視したとおり反応が完了したら、反応混合物を水(150mL)に注ぎ、酢酸エチル(3×200mL)で抽出した。水層を、1N HClを使用して酸性化することで、白色沈殿物が得られたが、これを濾過し、真空下で乾燥させることで、(1r,3r,5r,7r)-2-(メトキシカルボニル)アダマンタン-2-カルボン酸(DA、25g、104.91mmol、89%)が白色固体として与えられた。1H NMR(400MHz,DMSO-d6)δ12.90(s,1H),3.64(s,3H),2.55(s,2H),1.83(d,J=13.0Hz,2H),1.74(d,J=11.3Hz,4H),1.65(d,J=12.9Hz,6H).
ジメチル(1r,3r,5r,7r)-アダマンタン-2,2-ジカルボキシラート(DB):
DMF(250mL)中の(1r,3r,5r,7r)-2-(メトキシカルボニル)アダマンタン-2-カルボン酸(DA、25g、104.91mmol、1.0当量)の撹拌溶液へ、K2CO3(28.9g、209.83mmol、2.0当量)およびヨウ化メチル(74.4g、524.59mmol、5.0当量)を室温にて加えた。反応混合物を室温にて2h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を氷冷水(500mL)上に注ぐことで、白色沈殿物が得られたが、これを濾過して真空下で乾燥させることで、ジメチル(1r,3r,5r,7r)-アダマンタン-2,2-ジカルボキシラート(DB、23g、91.157mmol、87%)が白色固体として与えられた。1H NMR(400MHz,クロロホルム-d)δ3.72(s,6H),2.72(m,2H),1.87-1.83(m,6H),1.74-1.70(m,6H).
DMF(250mL)中の(1r,3r,5r,7r)-2-(メトキシカルボニル)アダマンタン-2-カルボン酸(DA、25g、104.91mmol、1.0当量)の撹拌溶液へ、K2CO3(28.9g、209.83mmol、2.0当量)およびヨウ化メチル(74.4g、524.59mmol、5.0当量)を室温にて加えた。反応混合物を室温にて2h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を氷冷水(500mL)上に注ぐことで、白色沈殿物が得られたが、これを濾過して真空下で乾燥させることで、ジメチル(1r,3r,5r,7r)-アダマンタン-2,2-ジカルボキシラート(DB、23g、91.157mmol、87%)が白色固体として与えられた。1H NMR(400MHz,クロロホルム-d)δ3.72(s,6H),2.72(m,2H),1.87-1.83(m,6H),1.74-1.70(m,6H).
((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジメタノール(DC):
THF(10mL)中のジメチル(1r,3r,5r,7r)-アダマンタン-2,2-ジカルボキシラート(DB、1.0g、3.978mmol、1.0当量)の撹拌溶液へ、水素化アルミニウムリチウム(THF中1.0M)(20mL)を0℃にて加えた。混合物を25h還流した。反応をTLCおよびLCMSによって監視した。反応が完了したら、反応混合物を氷冷水(20mL)上に注ぎ、酢酸エチル(100mL)で抽出した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジメタノール(DC、700mg、3.566mmol、90%)が白色固体として供与された。1H NMR(400MHz,DMSO-d6)δ4.20(t,J=5.2Hz,2H),3.61(d,J=5.2Hz,4H),1.98(d,J=12.7Hz,4H),1.82-1.80(m,2H),1.62(dt,J= 5.8,3.1Hz,4H),1.48-1.42(m,4H).
THF(10mL)中のジメチル(1r,3r,5r,7r)-アダマンタン-2,2-ジカルボキシラート(DB、1.0g、3.978mmol、1.0当量)の撹拌溶液へ、水素化アルミニウムリチウム(THF中1.0M)(20mL)を0℃にて加えた。混合物を25h還流した。反応をTLCおよびLCMSによって監視した。反応が完了したら、反応混合物を氷冷水(20mL)上に注ぎ、酢酸エチル(100mL)で抽出した。有機層を硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで、((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジメタノール(DC、700mg、3.566mmol、90%)が白色固体として供与された。1H NMR(400MHz,DMSO-d6)δ4.20(t,J=5.2Hz,2H),3.61(d,J=5.2Hz,4H),1.98(d,J=12.7Hz,4H),1.82-1.80(m,2H),1.62(dt,J= 5.8,3.1Hz,4H),1.48-1.42(m,4H).
((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ビス(メチレン)ジメタンスルホナート(DD):
DCM(5mL)中の((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジメタノール(DC、370mg、1.887mmol、1.0当量)の撹拌溶液へ、メタン塩化スルホニル(324.3mg、2.831mmol、1.5当量)、N,N-ジメチルアミノピリジン(46.12mg、0.3775mmol、0.2当量)、およびピリジン(299mg、3.775mmol、2.0当量)を加えた。反応混合物を室温にて16h撹拌し、TLCおよびLCMSによって監視した。反応が完了したら、反応混合物を水上に注ぎ、酢酸エチル(3×50mL)で抽出し、合わせた有機層を減圧下で濃縮することで、粗混合物が得られた。粗混合物を、15%(酢酸エチル/ヘキサン)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ビス(メチレン)ジメタンスルホナート(DD、250mg、0.709mmol、37%)が白色固体として供与された。1H NMR(400MHz,DMSO-d6)δ4.36(s,4H),3.22(s,6H),1.99(d,J=13.2Hz,4H),1.87(s,2H),1.69(d,J=8.6Hz,4H),1.60(d,J=13.2Hz,4H).
DCM(5mL)中の((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジメタノール(DC、370mg、1.887mmol、1.0当量)の撹拌溶液へ、メタン塩化スルホニル(324.3mg、2.831mmol、1.5当量)、N,N-ジメチルアミノピリジン(46.12mg、0.3775mmol、0.2当量)、およびピリジン(299mg、3.775mmol、2.0当量)を加えた。反応混合物を室温にて16h撹拌し、TLCおよびLCMSによって監視した。反応が完了したら、反応混合物を水上に注ぎ、酢酸エチル(3×50mL)で抽出し、合わせた有機層を減圧下で濃縮することで、粗混合物が得られた。粗混合物を、15%(酢酸エチル/ヘキサン)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ビス(メチレン)ジメタンスルホナート(DD、250mg、0.709mmol、37%)が白色固体として供与された。1H NMR(400MHz,DMSO-d6)δ4.36(s,4H),3.22(s,6H),1.99(d,J=13.2Hz,4H),1.87(s,2H),1.69(d,J=8.6Hz,4H),1.60(d,J=13.2Hz,4H).
((1r,3r,5r,7r)-2-(シアノメチル)アダマンタン-2-イル)メチルメタンスルホナート(DE):
DMF(3mL)中の((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ビス(メチレン)ジメタンスルホナート(DD、250mg、0.709mmol、1.0当量)の撹拌溶液へ、テトラブチルアンモニウムシアニド(952mg、3.546mmol、5.0当量)を加えた。反応混合物を105℃にて24h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を水(10mL)上に注ぎ、酢酸エチル(3×30mL)で抽出し、合わせた有機層を減圧下で濃縮することで、((1r,3r,5r,7r)-2-(シアノメチル)アダマンタン-2-イル)メチルメタンスルホナート(DE、250mg、0.882mmol)が黄色油として与えられた。1H NMR(400MHz,DMSO-d6)δ4.37(s,2H),3.26(s,3H),2.88(s,1H),2.69(s,1H),2.04-1.91(m,4H),1.89-1.83(d,J=8.2Hz,2H),1.72-1.54(m,8H).
DMF(3mL)中の((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ビス(メチレン)ジメタンスルホナート(DD、250mg、0.709mmol、1.0当量)の撹拌溶液へ、テトラブチルアンモニウムシアニド(952mg、3.546mmol、5.0当量)を加えた。反応混合物を105℃にて24h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を水(10mL)上に注ぎ、酢酸エチル(3×30mL)で抽出し、合わせた有機層を減圧下で濃縮することで、((1r,3r,5r,7r)-2-(シアノメチル)アダマンタン-2-イル)メチルメタンスルホナート(DE、250mg、0.882mmol)が黄色油として与えられた。1H NMR(400MHz,DMSO-d6)δ4.37(s,2H),3.26(s,3H),2.88(s,1H),2.69(s,1H),2.04-1.91(m,4H),1.89-1.83(d,J=8.2Hz,2H),1.72-1.54(m,8H).
2,2'-((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジアセトニトリル(DF):
DMF(3mL)中の((1r,3r,5r,7r)-2-(シアノメチル)アダマンタン-2-イル)メチルメタンスルホナート(DE、250mg、0.882mmol、1.0当量)の撹拌溶液へ、テトラブチルアンモニウムシアニド(1.19g、4.410mmol、5.0当量)を加えた。反応混合物を105℃にて24h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を水(10mL)上に注ぎ、酢酸エチル(3×30mL)で抽出し、合わせた有機層を減圧下で濃縮することで、粗混合物が与えられた。粗混合物を、5%(酢酸エチル/ヘキサン)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、2,2'-((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジアセトニトリル(DF、120mg、0.559mmol、64%)が灰白色固体として与えられた。1H NMR(400MHz,DMSO-d6)δ2.94(s,4H),1.97(d,J=13.1Hz,4H),1.81(s,2H),1.65-1.59(m,8H).
DMF(3mL)中の((1r,3r,5r,7r)-2-(シアノメチル)アダマンタン-2-イル)メチルメタンスルホナート(DE、250mg、0.882mmol、1.0当量)の撹拌溶液へ、テトラブチルアンモニウムシアニド(1.19g、4.410mmol、5.0当量)を加えた。反応混合物を105℃にて24h撹拌し、TLCによって監視した。反応が完了したら、反応混合物を水(10mL)上に注ぎ、酢酸エチル(3×30mL)で抽出し、合わせた有機層を減圧下で濃縮することで、粗混合物が与えられた。粗混合物を、5%(酢酸エチル/ヘキサン)を使用するシリカゲルフラッシュクロマトグラフィーによって精製することで、2,2'-((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)ジアセトニトリル(DF、120mg、0.559mmol、64%)が灰白色固体として与えられた。1H NMR(400MHz,DMSO-d6)δ2.94(s,4H),1.97(d,J=13.1Hz,4H),1.81(s,2H),1.65-1.59(m,8H).
2-((1r,3r,5r,7r)-2-(2-アミノ-2-オキソエチル)アダマンタン-2-イル)酢酸(DG):
MeOH(1mL)中の2,2'-((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)diアセトニトリル(DF、100mg、0.466mmol、1.0当量)の撹拌溶液へ、KOH(水中35%溶液、7.5mL)を加えた。反応混合物を70℃にて24h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水(5mL)上に注ぐことで白色沈殿物が入手された。沈殿物を濾過し、真空下で乾燥させることで、2-((1r,3r,5r,7r)-2-(2-アミノ-2-オキソエチル)アダマンタン-2-イル)酢酸(DG、70mg、0.278mmol、60%)が白色固体として与えられた。MS(ESI):252[M+H]+、1H NMR(400MHz,DMSO-d6)δ12.34(s,1H),7.35(s,1H),6.97(s,1H),2.79(s,2H),2.56(d,J=8.8Hz,2H),2.08(t,J=17.0Hz,4H),1.79-1.64(m,6H),1.51(d,J=13.0Hz,4H).
MeOH(1mL)中の2,2'-((1r,3r,5r,7r)-アダマンタン-2,2-ジイル)diアセトニトリル(DF、100mg、0.466mmol、1.0当量)の撹拌溶液へ、KOH(水中35%溶液、7.5mL)を加えた。反応混合物を70℃にて24h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水(5mL)上に注ぐことで白色沈殿物が入手された。沈殿物を濾過し、真空下で乾燥させることで、2-((1r,3r,5r,7r)-2-(2-アミノ-2-オキソエチル)アダマンタン-2-イル)酢酸(DG、70mg、0.278mmol、60%)が白色固体として与えられた。MS(ESI):252[M+H]+、1H NMR(400MHz,DMSO-d6)δ12.34(s,1H),7.35(s,1H),6.97(s,1H),2.79(s,2H),2.56(d,J=8.8Hz,2H),2.08(t,J=17.0Hz,4H),1.79-1.64(m,6H),1.51(d,J=13.0Hz,4H).
(1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン](DH):
THF(1mL)中の2-((1r,3r,5r,7r)-2-(2-アミノ-2-オキソエチル)アダマンタン-2-イル)酢酸(DG、70mg、0.278mmol、1.0当量)の撹拌溶液へ、水素化アルミニウムリチウム(THF中1.0M)(1.39mL)を0℃にて加えた。混合物を25h還流し、TLCおよびLCMSによって監視した。反応が完了したら、反応混合物を0℃まで冷却し、水(1mL)、15%水酸化ナトリウム溶液(1mL)で希釈し、濾別した。濾過物を減圧下で濃縮することで、(1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン](DH、70mg、0.34mmol、100%)が入手されたが、これを次のステップに直接使用した。MS(ESI):206[M+H]+
THF(1mL)中の2-((1r,3r,5r,7r)-2-(2-アミノ-2-オキソエチル)アダマンタン-2-イル)酢酸(DG、70mg、0.278mmol、1.0当量)の撹拌溶液へ、水素化アルミニウムリチウム(THF中1.0M)(1.39mL)を0℃にて加えた。混合物を25h還流し、TLCおよびLCMSによって監視した。反応が完了したら、反応混合物を0℃まで冷却し、水(1mL)、15%水酸化ナトリウム溶液(1mL)で希釈し、濾別した。濾過物を減圧下で濃縮することで、(1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン](DH、70mg、0.34mmol、100%)が入手されたが、これを次のステップに直接使用した。MS(ESI):206[M+H]+
メチル3-フルオロ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンゾアート(DJ):
ACN(1mL)中の(1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン](DH、70mg、0.340mmol、1.0当量)の撹拌溶液へ、メチル4-(ブロモメチル)-3-フルオロベンゾアート(84.2mg、0.340mmol、1.0当量)およびCs2CO3(333mg、1.022mmol、3.0当量)を加えた。反応混合物を室温にて2h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水上に注ぐことで白色沈殿物が入手されたが、これを濾過し真空下で乾燥させることで、メチル3-フルオロ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンゾアート(DJ、40mg、0.107mmol、32%)が白色固体として供与された。MS(ESI):372[M+H]+
ACN(1mL)中の(1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン](DH、70mg、0.340mmol、1.0当量)の撹拌溶液へ、メチル4-(ブロモメチル)-3-フルオロベンゾアート(84.2mg、0.340mmol、1.0当量)およびCs2CO3(333mg、1.022mmol、3.0当量)を加えた。反応混合物を室温にて2h撹拌し、TLCおよびLCMSによって監視した。反応混合物を水上に注ぐことで白色沈殿物が入手されたが、これを濾過し真空下で乾燥させることで、メチル3-フルオロ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンゾアート(DJ、40mg、0.107mmol、32%)が白色固体として供与された。MS(ESI):372[M+H]+
3-フルオロ-N-ヒドロキシ-4-(((1r,3r,5r,7r)-スピロ[アダマンタン-2,4'-ピペリジン]-1'-イル)メチル)ベンズアミド(167)。167の調製のためのこのステップを、化合物75の調製に使用したのと類似のやり方で実施した。1H NMR(400MHz,DMSO-d6)δ11.26(s,1H),9.14(s,1H),7.56(d,J=8.2Hz,1H),7.49(m,2H),3.50(s,2H),2.33(s,4H),1.97(d,J=12.6Hz,4H),1.79(m,2H),1.63(m,6H),1.55(m,2H),1.47(d,J=12.6Hz,4H)。MS(ESI):373[M+H]+
(S)-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(168)、および
(R)-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(169):
(S)-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(168)、および
(R)-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロ-N-ヒドロキシベンズアミド(169):
(R,Z)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミド(DM):
無水THF(10mL)中のプロピオンアルデヒド(DK、1.5g、25.83mmol、1.0当量)の撹拌溶液へN2(g)下室温にて、Ti(OEt)4(1.09mL、38.74mmol、1.5当量)を、これに続き(R)tert-ブチルスルフィンアミド(DL、3.44g、28.41mmol、1.1当量)を滴加した。その結果得られた混合物を60℃にて2.5h加熱した。2.5h後、反応物を室温まで冷却し、ブライン溶液(60mL)上へ注ぎ、酢酸エチル(3×30mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ減圧下で濃縮することで(R)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミドが黄色油として入手されたが、これをシリカゲルクロマトグラフィー(EtOAc/ヘキサン、1:4)によって精製することで、(R,Z)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミド(DM、3.5g、21.70mmol、84%)が透明油として供与された。MS(ESI):162[M+H]+
無水THF(10mL)中のプロピオンアルデヒド(DK、1.5g、25.83mmol、1.0当量)の撹拌溶液へN2(g)下室温にて、Ti(OEt)4(1.09mL、38.74mmol、1.5当量)を、これに続き(R)tert-ブチルスルフィンアミド(DL、3.44g、28.41mmol、1.1当量)を滴加した。その結果得られた混合物を60℃にて2.5h加熱した。2.5h後、反応物を室温まで冷却し、ブライン溶液(60mL)上へ注ぎ、酢酸エチル(3×30mL)で抽出した。合わせた有機層を硫酸ナトリウム上で乾燥させ減圧下で濃縮することで(R)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミドが黄色油として入手されたが、これをシリカゲルクロマトグラフィー(EtOAc/ヘキサン、1:4)によって精製することで、(R,Z)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミド(DM、3.5g、21.70mmol、84%)が透明油として供与された。MS(ESI):162[M+H]+
メチル1-(1-(((R)-tert-ブチルスルフィニル)アミノ)プロピル)シクロペンタン-1-カルボキシラート(DO):
無水THF(17mL)中の(R)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミド(DM、1.7g、10.54mmol、1当量)およびメチルシクロペンタンカルボキシラート(DN、6.76g、52.71mmol、5当量)の撹拌溶液へN2(g)雰囲気下-78℃にて、LiHMDS(53mL、THF中1M溶液、52.71mmol、5当量)を滴加した。反応物を-78℃にて3h、次いで室温にて12h撹拌した。反応完了後これを水(10mL)でクエンチした。反応混合物をEtOAc(3×30mL)で抽出し、合わせた有機層を無水硫酸ナトリウム上で乾燥させた。溶媒を減圧下で濃縮することで粗産物が得られたが、これをシリカゲルカラムクロマトグラフィー(1:3、EtOAc/ヘキサン)によって精製することで、メチル1-(1-(((R)-tert-ブチルスルフィニル)アミノ)プロピル)シクロペンタン-1-カルボキシラート(DO、2.0g、6.91mmol、65%)としての純粋な産物が粘着性油として得られた。1H NMR(400MHz,クロロホルム-d)δ4.61(d,J=7.8Hz,1H),3.72(s,3H),2.99(t,J=8.5Hz,1H),2.34(dd,J=12.9,6.3Hz,1H),2.06-1.98(m,2H),1.71-1.70(m,3H),1.29-1.23(m,13H),0.94(t,J=7.3Hz,3H).
無水THF(17mL)中の(R)-2-メチル-N-プロピリデンプロパン-2-スルフィンアミド(DM、1.7g、10.54mmol、1当量)およびメチルシクロペンタンカルボキシラート(DN、6.76g、52.71mmol、5当量)の撹拌溶液へN2(g)雰囲気下-78℃にて、LiHMDS(53mL、THF中1M溶液、52.71mmol、5当量)を滴加した。反応物を-78℃にて3h、次いで室温にて12h撹拌した。反応完了後これを水(10mL)でクエンチした。反応混合物をEtOAc(3×30mL)で抽出し、合わせた有機層を無水硫酸ナトリウム上で乾燥させた。溶媒を減圧下で濃縮することで粗産物が得られたが、これをシリカゲルカラムクロマトグラフィー(1:3、EtOAc/ヘキサン)によって精製することで、メチル1-(1-(((R)-tert-ブチルスルフィニル)アミノ)プロピル)シクロペンタン-1-カルボキシラート(DO、2.0g、6.91mmol、65%)としての純粋な産物が粘着性油として得られた。1H NMR(400MHz,クロロホルム-d)δ4.61(d,J=7.8Hz,1H),3.72(s,3H),2.99(t,J=8.5Hz,1H),2.34(dd,J=12.9,6.3Hz,1H),2.06-1.98(m,2H),1.71-1.70(m,3H),1.29-1.23(m,13H),0.94(t,J=7.3Hz,3H).
(R)-N-(1-(1-(ヒドロキシメチル)シクロペンチル)プロピル)-2-メチルプロパン-2-スルフィンアミド(DP):
無水THF(20mL)中のメチル1-(1-(((R)-tert-ブチルスルフィニル)アミノ)プロピル)シクロペンタン-1-カルボキシラート(DO、2.0g、6.91mmol、1.0当量)の溶液へ、水素化アルミニウムリチウム(THF中1.0M、13.84mL、13.84mmol、2当量)をゆっくり0℃にて加え、N2(g)雰囲気下2h撹拌した。反応完了後これを水(10mL)でクエンチし、EtOAc(3×30mL)で抽出した。合わせた有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られた。粗混合物をシリカゲルカラムクロマトグラフィーによって精製することで、(R)-N-(1-(1-(ヒドロキシメチル)シクロペンチル)プロピル)-2-メチルプロパン-2-スルフィンアミド(DP、1.1g、4.20mmol、61%)が無色液体として生産された。1H NMR(400MHz,クロロホルム-d)δ4.01(d,J=7.2Hz,1H),3.80(d,J=6.6Hz,1H),3.60-3.56(m,1H),3.41-3.37(m,1H),3.10-2.94(m,1H),1.50-1.20(m,19H),0.97(dt,J=12.0,7.3Hz,3H).
無水THF(20mL)中のメチル1-(1-(((R)-tert-ブチルスルフィニル)アミノ)プロピル)シクロペンタン-1-カルボキシラート(DO、2.0g、6.91mmol、1.0当量)の溶液へ、水素化アルミニウムリチウム(THF中1.0M、13.84mL、13.84mmol、2当量)をゆっくり0℃にて加え、N2(g)雰囲気下2h撹拌した。反応完了後これを水(10mL)でクエンチし、EtOAc(3×30mL)で抽出した。合わせた有機層を無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られた。粗混合物をシリカゲルカラムクロマトグラフィーによって精製することで、(R)-N-(1-(1-(ヒドロキシメチル)シクロペンチル)プロピル)-2-メチルプロパン-2-スルフィンアミド(DP、1.1g、4.20mmol、61%)が無色液体として生産された。1H NMR(400MHz,クロロホルム-d)δ4.01(d,J=7.2Hz,1H),3.80(d,J=6.6Hz,1H),3.60-3.56(m,1H),3.41-3.37(m,1H),3.10-2.94(m,1H),1.50-1.20(m,19H),0.97(dt,J=12.0,7.3Hz,3H).
2-((R)-tert-ブチルスルフィニル)-1-エチル-2-アザスピロ[3.4]オクタン(DQ):
無水THF(10mL)中の(R)-N-(1-(1-(ヒドロキシメチル)シクロペンチル)プロピル)-2-メチルプロパン-2-スルフィンアミド(DP、1.0g、3.83mmol、1.0当量)の撹拌溶液へ0℃にて、塩化トシル(1.09g、5.74mmol、1.5当量)を加え、60%NaH(0.459g、11.48mmol、3.0当量)の添加をこれに続けた。その結果得られた混合物をN2(g)雰囲気下室温にて12h撹拌した。反応完了後これを水(10mL)でクエンチし、EtOAc(3×30mL)で抽出した。合わせた有機層を減圧下で濃縮することで粗混合物が得られたが、これをシリカゲルカラムクロマトグラフィー(1:3、EtOAc/ヘキサン)によって精製することで、2-((R)-tert-ブチルスルフィニル)-1-エチル-2-アザスピロ[3.4]オクタン(DQ、0.600g、2.46mmol、64%)が無色液体として得られた。1H NMR(400MHz,クロロホルム-d)δ3.99(d,J=7.5Hz,1H),3.83(t,J=7.1Hz,1H),2.92(d,J=7.5Hz,1H),1.81-1.69(m,3H),1.63-1.50(m,4H),1.15(s,10H),0.88(t,J=7.5Hz,3H).
無水THF(10mL)中の(R)-N-(1-(1-(ヒドロキシメチル)シクロペンチル)プロピル)-2-メチルプロパン-2-スルフィンアミド(DP、1.0g、3.83mmol、1.0当量)の撹拌溶液へ0℃にて、塩化トシル(1.09g、5.74mmol、1.5当量)を加え、60%NaH(0.459g、11.48mmol、3.0当量)の添加をこれに続けた。その結果得られた混合物をN2(g)雰囲気下室温にて12h撹拌した。反応完了後これを水(10mL)でクエンチし、EtOAc(3×30mL)で抽出した。合わせた有機層を減圧下で濃縮することで粗混合物が得られたが、これをシリカゲルカラムクロマトグラフィー(1:3、EtOAc/ヘキサン)によって精製することで、2-((R)-tert-ブチルスルフィニル)-1-エチル-2-アザスピロ[3.4]オクタン(DQ、0.600g、2.46mmol、64%)が無色液体として得られた。1H NMR(400MHz,クロロホルム-d)δ3.99(d,J=7.5Hz,1H),3.83(t,J=7.1Hz,1H),2.92(d,J=7.5Hz,1H),1.81-1.69(m,3H),1.63-1.50(m,4H),1.15(s,10H),0.88(t,J=7.5Hz,3H).
1-エチル-2-アザスピロ[3.4]オクタン(DR):
ジエチルエーテル(1mL)中の2-((R)-tert-ブチルスルフィニル)-1-エチル-2-アザスピロ[3.4]オクタン(DQ、0.6g、2.46mmol、1当量)の撹拌溶液へ、HCl(1,4-ジオキサン中2.0M溶液、5.0mmol)を室温にて加え、1h撹拌した。反応完了後、これを乾燥するまで真空下で濃縮することで1-エチル-2-アザスピロ[3.4]オクタン(DR、0.225g、1.28mmol、52%)が粗産物として得られたが、これをさらなる精製はせずにそのまま使用した。
ジエチルエーテル(1mL)中の2-((R)-tert-ブチルスルフィニル)-1-エチル-2-アザスピロ[3.4]オクタン(DQ、0.6g、2.46mmol、1当量)の撹拌溶液へ、HCl(1,4-ジオキサン中2.0M溶液、5.0mmol)を室温にて加え、1h撹拌した。反応完了後、これを乾燥するまで真空下で濃縮することで1-エチル-2-アザスピロ[3.4]オクタン(DR、0.225g、1.28mmol、52%)が粗産物として得られたが、これをさらなる精製はせずにそのまま使用した。
メチル-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロベンゾアート(DT):
ACN(15mL)中のメチル4-(ブロモメチル)-3-フルオロベンゾアート(DR、0.317g、1.28mmol、1当量)の撹拌溶液へ、Cs2CO3(0.834g、2.56mmol、2.0当量)および(S)-1-エチル-2-アザスピロ[3.4]オクタン塩酸塩(DS、0.225g、1.28mmol、1当量)を室温にて加えた。反応物を室温にて2h撹拌し、次いで水(30mL)でクエンチし、酢酸エチル(3×20mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られたが、これをフラッシュシリカゲルカラムクロマトグラフィー(5%EtOAc:ヘキサン)によって精製することで、メチル-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロベンゾアート(DT、0.220g、0.7203mmol、56%)が粘着性液体として得られた。Mass(ESI):306 [M+H]+;1H NMR(400MHz,クロロホルム-d)δ7.79(dd,J=7.9,1.7Hz,1H),7.68(dd,J=10.3,1.7Hz,1H),7.50(s,1H),3.93(m,4H),3.61(d,J=14.0Hz,1H),3.25(s,1H),3.04(s,1H),2.67(s,1H),1.76(d,J=7.6Hz,3H),1.65-1.42(m,10H),1.27(s,2H),0.85(t,J=7.5Hz,3H).
ACN(15mL)中のメチル4-(ブロモメチル)-3-フルオロベンゾアート(DR、0.317g、1.28mmol、1当量)の撹拌溶液へ、Cs2CO3(0.834g、2.56mmol、2.0当量)および(S)-1-エチル-2-アザスピロ[3.4]オクタン塩酸塩(DS、0.225g、1.28mmol、1当量)を室温にて加えた。反応物を室温にて2h撹拌し、次いで水(30mL)でクエンチし、酢酸エチル(3×20mL)で抽出した。合わせた有機層をブライン(20mL)で洗浄し、無水硫酸ナトリウム上で乾燥させ、減圧下で濃縮することで粗混合物が得られたが、これをフラッシュシリカゲルカラムクロマトグラフィー(5%EtOAc:ヘキサン)によって精製することで、メチル-4-((1-エチル-2-アザスピロ[3.4]オクタン-2-イル)メチル)-3-フルオロベンゾアート(DT、0.220g、0.7203mmol、56%)が粘着性液体として得られた。Mass(ESI):306 [M+H]+;1H NMR(400MHz,クロロホルム-d)δ7.79(dd,J=7.9,1.7Hz,1H),7.68(dd,J=10.3,1.7Hz,1H),7.50(s,1H),3.93(m,4H),3.61(d,J=14.0Hz,1H),3.25(s,1H),3.04(s,1H),2.67(s,1H),1.76(d,J=7.6Hz,3H),1.65-1.42(m,10H),1.27(s,2H),0.85(t,J=7.5Hz,3H).
168および169の調製のためのこれに続くステップを、化合物75の調製に使用されたのと類似のやり方で実施した。化合物168および169は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
(R)-3-フルオロ-N-ヒドロキシ-5-((2-メチル-2-アザスピロ[5.5]ウンデカン-3-イル)メチル)ベンズアミド(170)、および
(S)-3-フルオロ-N-ヒドロキシ-5-((2-メチル-2-アザスピロ[5.5]ウンデカン-3-イル)メチル)ベンズアミド(171)
(S)-3-フルオロ-N-ヒドロキシ-5-((2-メチル-2-アザスピロ[5.5]ウンデカン-3-イル)メチル)ベンズアミド(171)
tert-ブチル3-(3-フルオロ-5-メトキシベンジル)-2-アザスピロ[5.5]ウンデカン-2-カルボキシラート(DU)。この化合物を、化合物135における中間体BNの調製に使用したのと類似のやり方で調製した。MS(ESI):392[M+H]+
3-(3-フルオロ-5-メトキシベンジル)-2-メチル-2-アザスピロ[5.5]ウンデカン(DV):
DCM(15mL)中のtert-ブチル3-(3-フルオロ-5-メトキシベンジル)-2-アザスピロ[5.5]ウンデカン-2-カルボキシラート(DU、1.3g、3.325mmol、1.0当量)の撹拌溶液へ、TFA(1.4mL、13.299mmol、4.0当量)を0℃にて加えた。反応混合物を0℃にて16h撹拌し、TLCおよびLCMSによって監視した。反応が完了したら、これを減圧下で濃縮することで粗混合物が入手された。これをメタノール(15mL)に溶解し、これへp-ホルムアルデヒド(1.4g、44.61mmol、10当量)を0℃にて加えた。反応混合物を0℃にて30分間撹拌し、これに続けてシアノ水素化ホウ素ナトリウム(596mg、9.6218mmol、2.0当量)を加えた。反応混合物を室温にて6h撹拌した。反応が完了したら減圧下で濃縮することで粗混合物が入手されたが、これを次いで、EtOAc:ヘキサン(1:9)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、3-(3-フルオロ-5-メトキシベンジル)-2-メチル-2-アザスピロ[5.5]ウンデカン(DV、(670mg、2.1967mmol、66%)が固体として得られた。MS(ESI):306[M+H]+
DCM(15mL)中のtert-ブチル3-(3-フルオロ-5-メトキシベンジル)-2-アザスピロ[5.5]ウンデカン-2-カルボキシラート(DU、1.3g、3.325mmol、1.0当量)の撹拌溶液へ、TFA(1.4mL、13.299mmol、4.0当量)を0℃にて加えた。反応混合物を0℃にて16h撹拌し、TLCおよびLCMSによって監視した。反応が完了したら、これを減圧下で濃縮することで粗混合物が入手された。これをメタノール(15mL)に溶解し、これへp-ホルムアルデヒド(1.4g、44.61mmol、10当量)を0℃にて加えた。反応混合物を0℃にて30分間撹拌し、これに続けてシアノ水素化ホウ素ナトリウム(596mg、9.6218mmol、2.0当量)を加えた。反応混合物を室温にて6h撹拌した。反応が完了したら減圧下で濃縮することで粗混合物が入手されたが、これを次いで、EtOAc:ヘキサン(1:9)を使用するシリカゲルカラムクロマトグラフィーによって精製することで、3-(3-フルオロ-5-メトキシベンジル)-2-メチル-2-アザスピロ[5.5]ウンデカン(DV、(670mg、2.1967mmol、66%)が固体として得られた。MS(ESI):306[M+H]+
170および171の調製のためのこれに続くステップを、化合物94の調製に使用されたのと類似のやり方で実施した。化合物170および171は(S)および(R)の鏡像異性体として指定されているが、各鏡像異性体を調製し単離したため、各々の絶対立体化学は不明である。
生物学的アッセイのデータおよび手順
HDAC酵素活性のためのキャリパー(Caliper)エンドポイントアッセイ
HDAC反応物を以下のとおり、20μLの総体積で384ウェルプレート(Greiner)に集めた:HDACタンパク質(および該当する場合、それらの調節サブユニット)を、100mM HEPES(pH7.5)、0.1%BSA、0.01%Triton X-100、25mM KClを含むアッセイ緩衝剤に予め希釈し、384ウェルプレート(1ウェルあたり10μL)中へ分注した。各アッセイにおいて使用された酵素濃度の例を下の表中に挙げる。
HDAC酵素活性のためのキャリパー(Caliper)エンドポイントアッセイ
HDAC反応物を以下のとおり、20μLの総体積で384ウェルプレート(Greiner)に集めた:HDACタンパク質(および該当する場合、それらの調節サブユニット)を、100mM HEPES(pH7.5)、0.1%BSA、0.01%Triton X-100、25mM KClを含むアッセイ緩衝剤に予め希釈し、384ウェルプレート(1ウェルあたり10μL)中へ分注した。各アッセイにおいて使用された酵素濃度の例を下の表中に挙げる。
試験化合物を予め、3倍希釈ステップを使用して100%DMSOに段階希釈し、アコースティック分注(Labcyte Echo)によってタンパク質試料へ加えた。DMSOの濃度をすべての試料において一様に1%とした。アッセイの最終化合物濃度は典型的には、12点濃度-応答方式について100μMから0.00056μMまで及んだ。TSA(トリコスタチンA)およびMS-275などの参照化合物も、同一のやり方で試験した。
4つの反復測定(replicates)(各キャリパーシッパーにつき)において、対照試料(インヒビター不在下、DMSOのみの0%-阻害)および100%-阻害(酵素の不在下)を集め、化合物存在下の%-阻害を算出するのに使用した。このステップにて、化合物を予め酵素とともに室温にて(20~23℃)30分間インキュベートした。反応を、同じアッセイ緩衝剤に予め希釈された10μLのFAM標識基質ペプチド(上の表を見よ)の添加によって始めた。基質ペプチドの最終濃度は1μM(HDAC1~10)および2μM(HDAC11)であった。反応を室温にて(20~23℃)進めた。各HDACに係る典型的なインキュベーション時間は、既定の酵素プログレス曲線に基づき変動させるが、これを上の表中に挙げる。
インキュベーションに続き、反応を50μLの終止緩衝剤(100mM HEPES(pH7.5)、0.01%Triton X-100、0.05%SDS)の添加によってクエンチした。終止されたプレートを、アセチル化基質から脱アセチル化産物の電気泳動分離を可能にさせる微少流体電気泳動器械(Caliper LabChip(登録商標)3000、Caliper Life Sciences/Perkin Elmer)上で分析した。ペプチド基質と産物との相対強度の変化は、測定されるパラメータである。各試験試料の活性を、総和に対する産物の比率(PSR):P/(S+P)として決定したが、ここでPは産物のピーク高さであり、Sは基質のピーク高さである。パーセント阻害(P阻)は以下の方程式:P阻=(PSR0%阻-PSR化合物)/(PSR0%阻-PSR100%阻)*100を使用して決定し、式中:PSR化合物は、化合物存在下の産物/総和の比率であり、PSR0%阻は、化合物不在下の産物/総和の比率であり、PSR100%阻は、酵素不在下の産物/総和の比率である。化合物(50%-阻害)のIC50を決定するため、%-阻データ(P阻 対 化合物濃度)を、XLfitソフトウェア(IDBS)を使用し4パラメータシグモイド用量-応答モデルによってフィッティングさせた。
例示化合物をHDACパラログ一団の阻害活性について評価した。表1~4中の結果は、本開示の化合物がHDAC6に対して強力な活性を有し、多くの化合物がHDAC8より選択的にHDAC6を阻害することを実証する。IC50の範囲:A:0.001~0.1μM;B:>0.1~1μM;C:>1~10μM;D:>10~100μM;E:>100μM。選択性の範囲(HDAC8 IC50/HDAC6 IC50の比率):I:0.1~1;II:>1~10;III:>10~100;IV:>100~1000;V:>1000
表1.例示化合物に係るIn vitroでの酵素IC50値
表2.例示化合物に係るIn vitroでの酵素IC50値
表1.例示化合物に係るIn vitroでの酵素IC50値
熱力学的水溶解度
10mM貯蔵溶液(DMSO中)を試験試料に対し調製した。10mM貯蔵溶液から、2μMの作業液(working solution)を、試験試料を移動相溶液(典型的には、好適な内部標準-カルバマゼピン/ジクロフェナクを含有するメタノール:2mM酢酸アンモニウム)に希釈することによって調製した。さらに、作業液を移動相溶液に最大4~5線形点(linearity point)まで段階希釈することで、較正曲線をプロットするための標準溶液を調製した。各標準試料に係る面積を、LCMS/MSを使用して分析した。正規化面積値を濃度に対しプロットして較正方程式を取得する。試験化合物の熱力学的(TD)水溶解度を突き止めるため、1mg粉末形態の化合物を1mLのダルベッコのリン酸緩衝生理食塩水(DPBS、pH@7.4)へ加えることで、1mg/mLと等価な理論濃度を取得した。試験化合物(一重項)を、ボルテックスミキサーを使用して緩衝溶液に分散した。
10mM貯蔵溶液(DMSO中)を試験試料に対し調製した。10mM貯蔵溶液から、2μMの作業液(working solution)を、試験試料を移動相溶液(典型的には、好適な内部標準-カルバマゼピン/ジクロフェナクを含有するメタノール:2mM酢酸アンモニウム)に希釈することによって調製した。さらに、作業液を移動相溶液に最大4~5線形点(linearity point)まで段階希釈することで、較正曲線をプロットするための標準溶液を調製した。各標準試料に係る面積を、LCMS/MSを使用して分析した。正規化面積値を濃度に対しプロットして較正方程式を取得する。試験化合物の熱力学的(TD)水溶解度を突き止めるため、1mg粉末形態の化合物を1mLのダルベッコのリン酸緩衝生理食塩水(DPBS、pH@7.4)へ加えることで、1mg/mLと等価な理論濃度を取得した。試験化合物(一重項)を、ボルテックスミキサーを使用して緩衝溶液に分散した。
その結果得られた溶液を次いで、室温にて(25℃)24時間50rpmにてRotoSpin(シェーカー)上に保った。インキュベーション時間後、内容物を0.45μm PVDF親水性シリンジフィルターに通して濾過し、濾過物をLCMS/MSによって定量した。濾過物を移動相に希釈し、続いてAUCを希薄された試料についてLCMS/MSを使用して突き止めた。試験試料のAUCから、対応する濃度を、4~5点線形/較正曲線を使用して算出した。結果は、独立した3実験の平均である。
肝臓ミクロソームの代謝安定性
10mM貯蔵溶液(DMSO中)を化合物に対し調製した。貯蔵溶液から、150μMの作業液を、化合物をDMSOに希釈することによって調製した。(この作業液の濃度は、最終濃度1μMを考慮して調製されたことに留意)。
10mM貯蔵溶液(DMSO中)を化合物に対し調製した。貯蔵溶液から、150μMの作業液を、化合物をDMSOに希釈することによって調製した。(この作業液の濃度は、最終濃度1μMを考慮して調製されたことに留意)。
これに続き、所望の種(いずれかの株)からの肝臓ミクロソームのマスターミックス(master mix)(最終タンパク質濃度0.3mg/mL)および0.1Mリン酸カリウム緩衝剤を、要される反応数に対し調製した。このマスターミックスへ、試験化合物を1μM(0.5%DMSO)の濃度にて混ぜた(spiked)。先述の試料を37℃にて5分間予めインキュベートした。これに続き、試料を陽性および陰性の対照反応のために等分した。続いて、反応あたり10mM NADPH(補因子として;0.1Mリン酸カリウム緩衝剤に調製した)を加えることで陽性対照反応(最終濃度1mM)を始めさせ、0.1Mリン酸緩衝液(NADPHなし)を加えることで陰性対照反応を始めさせた。試料を次いで、400rpmの振盪条件で37℃にて所望される時点までの間(for desired time points)インキュベートした。
各時点(0、15、30、60および120分)にて試料を取り出し、反応を、冷蔵アセトニトリル/メタノール:2mM酢酸アンモニウム(80:20)および好適な内部標準(カルバマゼピン-60ng/mL)を使用して終止させた。試料を4000pm、4℃にて30分間遠心分離し、上清をLC-MS/MSによって二通りに分析した。各時点にて残存する化合物パーセントを0分試料のそれを基準として算出した。次いでデータを分析して半減期および固有クリアランス(CL固)を算出した。陰性対照試料は最初および最終の時点のみNADPHで行い、DMSOを使用してブランク試料を調製した(試験化合物なし)ことに留意。
表3.例示化合物に係る溶解度および肝臓ミクロソーム安定性
表3.例示化合物に係る溶解度および肝臓ミクロソーム安定性
血漿タンパク質結合アッセイ
血漿タンパク質結合アッセイを、Thermo scientificからのREDデバイスインサート(Cat#89810)を使用する迅速平衡透析(RED)方法を使用して実施した。
血漿タンパク質結合アッセイを、Thermo scientificからのREDデバイスインサート(Cat#89810)を使用する迅速平衡透析(RED)方法を使用して実施した。
化合物の10mM貯蔵をDMSOで調製した。貯蔵溶液から化合物の2.5mM作業液をDMSOで調製し、正味の(neat)血漿(所望の種からの)に混ぜることで、インキュベーション混合物中最終濃度10μMを取得した。続いてこの混合物から50μLの試料を50μLのDPBS中へ加え、内部標準-カルバマゼピン(60ng/mL)を含有する400μLの沈殿緩衝剤(0.1%ギ酸ありの冷90/10メタノール/アセトニトリル)とともに即時ボルテックスした。もたらされたこの試料(T=0分)を氷上30分間インキュベートし、次いで4000rpmおよび4℃にて30分間遠心分離した。
REDデバイスをベースプレート上へ設置し、これに続き200μLのインキュベーション混合物を、赤色環によって取り囲まれたREDデバイスのチャンバーに加えた。他のチャンバーに350μLの緩衝剤(DPBS、pH7.4)を加え、チャンバーから試料のいずれの蒸発または流出も回避するため密封した(シーラーで)。ベースプレートを次いでオービタルシェーカー上37℃にて5時間300rpmにて置いた。このインキュベーション時間後ベースプレートを外し、続いて両チャンバーからの50μLの透析後試料を96ウェルのディープウェルプレートの別々のウェルに収集した。
これに続き、50μLの適正な(pertinent)血漿を収集された緩衝剤試料へ加え、50μLの緩衝剤を収集された血漿試料へ加えた。内部標準-カルバマゼピン(60ng/mL)を含有する沈殿緩衝剤(400μL;0.1%ギ酸ありの冷90/10メタノール/アセトニトリル)を、タンパク質を沈殿させて化合物を放出するために加えた。試料をボルテックスし、氷上30分間インキュベートした。インキュベーションに続き、試料を4000rpmおよび4℃にて30分間遠心分離した。すべての試料からの上清をLCMSバイアルに収集し、LCMS/MSを使用して二通りに分析した。試験化合物の濃度を、血漿チャンバーおよび緩衝剤において、得られたピーク面積から決定した(LCMS/MS分析)。
結合した試験化合物のパーセンテージおよび%回収を以下の式に基づき算出した:
%遊離=(緩衝剤チャンバーの濃度/血漿チャンバーの濃度)×100%
%結合=100%-%遊離
%回収={(V透析物×C遊離+V血漿×C合計)/(V血漿×Cゼロ)}×100%
式中、V透析物=緩衝剤チャンバーの体積、C遊離=透析後の緩衝剤チャンバーの濃度、V血漿=血漿チャンバーの体積、C合計=透析後の血漿チャンバーの濃度、Cゼロ= T=0分での初濃度
%遊離=(緩衝剤チャンバーの濃度/血漿チャンバーの濃度)×100%
%結合=100%-%遊離
%回収={(V透析物×C遊離+V血漿×C合計)/(V血漿×Cゼロ)}×100%
式中、V透析物=緩衝剤チャンバーの体積、C遊離=透析後の緩衝剤チャンバーの濃度、V血漿=血漿チャンバーの体積、C合計=透析後の血漿チャンバーの濃度、Cゼロ= T=0分での初濃度
血漿安定性アッセイ
10mM貯蔵溶液(DMSO中)を試験化合物用に調製した。貯蔵溶液から2.5mMの作業液を、化合物をDMSOに希釈することによって調製した。これに続き正味の血漿(所望の種からの)を等分し、37℃にて5分間予めインキュベートした。この血漿へ試験化合物を10μM(0.4%DMSO)の濃度にて混ぜることで反応を始めさせた。試料を次いで37℃にて所望される時点までの間インキュベートした。
10mM貯蔵溶液(DMSO中)を試験化合物用に調製した。貯蔵溶液から2.5mMの作業液を、化合物をDMSOに希釈することによって調製した。これに続き正味の血漿(所望の種からの)を等分し、37℃にて5分間予めインキュベートした。この血漿へ試験化合物を10μM(0.4%DMSO)の濃度にて混ぜることで反応を始めさせた。試料を次いで37℃にて所望される時点までの間インキュベートした。
各時点(0、60、120、240および300分)にて試料を取り出し、反応を、内部標準-カルバマゼピンを含有する沈殿緩衝剤(0.1%ギ酸ありの冷90/10メタノール/アセトニトリル)を使用して停止させた。試料を4000rpm;4℃にて30分間遠心分離し、上清をLC-MS/MSによって二通りに分析した。各時点にて残存する化合物パーセントを、0分試料のそれを基準として算出した。DMSOを使用してブランク試料を調製したこと(試験化合物なし)に留意。
表4.例示化合物に係る血漿タンパク質結合および血漿安定性
表4.例示化合物に係る血漿タンパク質結合および血漿安定性
細胞中チューブリン-およびヒストンH3アセチル化への化合物EC 50 決定
未分化SH-SY5Y細胞中の標的タンパク質アセチル化を変更させる例示化合物に係るEC50の概算を、標準的なウェスタン免疫ブロッティング方法を使用して実施した。化合物34に係る代表的な例を図1に示す。SH-SY5Y細胞を滅菌細胞成長プレート上90%密集度(confluency)まで成長させた。10mM化合物貯蔵をDMSOで調製して2倍段階希釈をその貯蔵から調製し、細胞へ適用することで10μMの上限からDMSO[ゼロ化合物]の下限までの細胞培地中12点濃度範囲を取得した。
未分化SH-SY5Y細胞中の標的タンパク質アセチル化を変更させる例示化合物に係るEC50の概算を、標準的なウェスタン免疫ブロッティング方法を使用して実施した。化合物34に係る代表的な例を図1に示す。SH-SY5Y細胞を滅菌細胞成長プレート上90%密集度(confluency)まで成長させた。10mM化合物貯蔵をDMSOで調製して2倍段階希釈をその貯蔵から調製し、細胞へ適用することで10μMの上限からDMSO[ゼロ化合物]の下限までの細胞培地中12点濃度範囲を取得した。
細胞を正常な成長条件(37℃、5%CO2)下、化合物の存在下で4時間インキュベートし、次いで培地を吸引し、細胞を37℃まで加温したカルシウムおよびマグネシウムありの1×DPBSで2回濯いだ。細胞をドライアイスのベッド上5分間プレート上で直接凍結させ、次いでタンパク質抽出まで-80℃にて保管した。
表5.細胞をベースとしたアッセイにおけるチューブリンおよびヒストンH3アセチル化に係るEC50値
表5.細胞をベースとしたアッセイにおけるチューブリンおよびヒストンH3アセチル化に係るEC50値
タンパク質抽出を、Pierce protease inhibitor mini tables(Thermofisher cat#A32953)で補充されたRIPA緩衝剤(50mM Tris-HCL(pH8.0)、150mM NaCl、0.5%デオキシコール酸ナトリウム、0.1%ドデシル硫酸ナトリウム、1%NP-40)において、製造業者によって記載されるとおり厳密に実施した。ウェットアイス(wet ice)のベッド上でプレートを10分間解凍後、リシス(lysis)緩衝剤を各ウェル(例として、24ウェルプレートの1ウェルあたり100μL)へ加え、細胞を各ウェルの底部からかき集めた。次いでライセートを氷上で超音波処理し(40%出力、1秒間の30パルスをオン、2秒間オフ)、4℃にて10分間16,000gにて遠心分離し、澄んだ上清を確保した。タンパク質濃度をBCAアッセイによって決定し、ライセート上清アリコートを1/3総体積の3×ゲルローディング緩衝剤(DTT(NEB Cat.#B7703S)を含有)と合せることによって1レーンあたり少なくとも3μgを調製し、95℃にて5分間加熱して簡単に遠心分離し、次いでSDS-PAGEゲル上にロードした。
タンパク質を4~20%Tris-グリシンゲル上で分解し、iBlot2ドライ転写(dry transfer)系を使用してPVDF膜へ転写した。膜を次いで5%ミルクまたは5%ウシ血清アルブミンを含有するTBST中、室温にて少なくとも30分間ブロッキングし、次いで以下の表からの単一の一次抗体とともに4℃にて終夜インキュベートした:
一次抗体インキュベーションに続き、膜を洗浄し、二次抗体においてインキュベートして洗浄し、膜を露出させながらECLプライムウェスタンブロッティング検出試薬(Amersham #RPN223)においてインキュベートし、LI-COR Odyssey Imaging系においてECLシグナル捕捉をした。例の画像(右)には、記載されるとおりの希釈の範囲を越える10μMの上限濃度からの化合物34で処置された細胞が包含される。これに続き免疫反応性のバンドの濃度測定を、以下の比率:アセチルチューブリン/チューブリンおよびアセチルヒストンH3K9/ヒストンH3をもたらすImageStudioソフトウェアおよびMicrosoft Excelを使用して実施した。未加工の比率を、GraphPad Prism v7.0へ、対数変換データ[log(アゴニスト) vs Prismにおける応答]につき可変勾配(variable slope)方程式を使用してモデル化されたEC50値とともにアップロードした。
ミクロソームのおよび脳のタンパク質の結合
ミクロソームのタンパク質結合アッセイ、Thermo scientificからのREDデバイスインサート(Cat#89810)を使用する迅速平衡透析(RED)方法を使用して実施した。化合物の10mM貯蔵をDMSOで調製した。貯蔵溶液から1mMの作業液をDMSOで調製し、化合物をアセトニトリル:水(50:50)に希釈することによってさらに250μMまでにした。肝臓ミクロソーム(所望の種から)を0.1Mリン酸緩衝液中0.3mg/mlにて調製した。化合物を調製ミクロソーム(夫々の代謝安定性インキュベーションに使用されたタンパク質濃度にて)にて混ぜることで所望される1μMの最終濃度を取得した。ミクロソーム-化合物の混合物を混合し、続いてこの混合物からの50μLアリコートをT=0時間反応のため、50μLの0.1Mリン酸緩衝液に加えた。この反応を、内部標準(カルバマゼピン)を含有する600μLのアセトニトリル:水(90:10)で即時に終止し、試料を4Cにて16時間保管した。
ミクロソームのタンパク質結合アッセイ、Thermo scientificからのREDデバイスインサート(Cat#89810)を使用する迅速平衡透析(RED)方法を使用して実施した。化合物の10mM貯蔵をDMSOで調製した。貯蔵溶液から1mMの作業液をDMSOで調製し、化合物をアセトニトリル:水(50:50)に希釈することによってさらに250μMまでにした。肝臓ミクロソーム(所望の種から)を0.1Mリン酸緩衝液中0.3mg/mlにて調製した。化合物を調製ミクロソーム(夫々の代謝安定性インキュベーションに使用されたタンパク質濃度にて)にて混ぜることで所望される1μMの最終濃度を取得した。ミクロソーム-化合物の混合物を混合し、続いてこの混合物からの50μLアリコートをT=0時間反応のため、50μLの0.1Mリン酸緩衝液に加えた。この反応を、内部標準(カルバマゼピン)を含有する600μLのアセトニトリル:水(90:10)で即時に終止し、試料を4Cにて16時間保管した。
反応を始めるため、REDデバイスをベースプレート上へ設置し、これに続き200μLのミクロソーム-化合物混合物を、赤色環によって取り囲まれたREDデバイスのチャンバー(赤色チャンバー)に加えた。他のチャンバー(白色チャンバー)に350μLの緩衝剤(0.1Mリン酸緩衝液、pH7.4)を加え、チャンバーから試料のいずれの蒸発または流出も回避するため密封した(シーラーで)。ベースプレートを次いでオービタルシェーカー上37℃にて16時間400rpmにて置いた。このインキュベーション時間後ベースプレートを外し、続いて両チャンバーからの50μLの透析後試料をディープウェルプレートに収集した。これに続き、50μLの適正なマウス肝臓ミクロソーム溶液を、白色チャンバーから収集された緩衝剤試料へ加え、50μLの緩衝剤を、赤色チャンバーから収集されたマウス肝臓ミクロソーム試料漿試料へ加えた。タンパク質を沈殿させて化合物を放出するために、内部標準(カルバマゼピン)を含有する600μLのアセトニトリル:水(90:10)で反応を終止した。その結果得られたT=0時間ならびにT=16時間からの試料を混合し、13,000rpmにて10分間遠心分離した。すべての試料からの上清をバイアルに収集し、LCMS/MSを使用して二通りに分析した。試験化合物の濃度を、緩衝剤およびミクロソームのチャンバーにおいて、得られたピーク面積から決定した(LCMS/MS分析)。
結合しなかった試験化合物画分のパーセンテージを以下の式に基づき算出した:%Fu(結合しなかった画分(Fraction unbound))=1-(タンパク質含有チャンバーの濃度-緩衝剤チャンバーの濃度/タンパク質含有チャンバーの濃度)。
脳タンパク質結合アッセイを、Thermo scientificからのREDデバイスインサート(Cat#89810)を使用する迅速平衡透析(RED)方法を使用して実施した。脳組織ホモジネート試料を、1体積の全脳組織(所望の種)を、3体積の透析緩衝剤(リン酸緩衝生理食塩水(pH7.4)-0.1Mリン酸ナトリウムおよび0.15M塩化ナトリウム)で希釈することによって調製し、4倍希釈ホモジネートが生産された。試験化合物の1mM貯蔵溶液をDMSOで調製し、脳ホモジネートに200倍希釈することで5μMの濃度を生産した。最終DMSO濃度は0.5%であった。迅速平衡透析を、分子量カットオフが8,000ダルトンの透析膜を含有する迅速平衡透析(RED)デバイスで実施した。各透析インサートは2種のチャンバーを含有する。赤色チャンバーは脳ホモジネートであり、一方白色チャンバーは緩衝剤であった。
脳ホモジネート中200μLアリコートの試験化合物および陽性対照(三通り)を透析インサートの赤色チャンバーへ加えた。350μLアリコートの透析緩衝剤をインサートの緩衝剤チャンバーへ加えた。REDデバイスを粘着フィルムで密封した後、100RPMにて4時間振盪させながら37℃にて透析をした。50μLアリコートの試験化合物および陽性対照を個別に0.5mL微小遠心管へ加えた。2種のアリコートを即時に凍結した(0分試料)。2種の他のアリコートをREDデバイスと併せて37℃にて4時間インキュベートした。透析に続き、アリコートの50μLを各ウェル(脳ホモジネートおよび緩衝剤)から除去し、等体積の逆のマトリックスで希釈することでマトリックス効果を無効にした。同様に緩衝剤を回収試料および安定性試料へ加えた。アリコートの100μLをLC-MS/MS分析用に提出した。25μLアリコートの陽性対照および試験化合物を、内部標準(グリピジド)を含有する100μLのアセトニトリルでクラッシュさせ(crashed)、5分間ボルテックスした。試料を4℃にて10分4000RPMにて間遠心分離し、100μLの上清をLC-MS/MS分析用に提出した。試料を、LC-MS/MSを使用するMRMモードにおいて親化合物につき監視した。
表6.例示化合物に係るマウス脳タンパク質および肝臓ミクロソームの結合
脳ホモジネート中200μLアリコートの試験化合物および陽性対照(三通り)を透析インサートの赤色チャンバーへ加えた。350μLアリコートの透析緩衝剤をインサートの緩衝剤チャンバーへ加えた。REDデバイスを粘着フィルムで密封した後、100RPMにて4時間振盪させながら37℃にて透析をした。50μLアリコートの試験化合物および陽性対照を個別に0.5mL微小遠心管へ加えた。2種のアリコートを即時に凍結した(0分試料)。2種の他のアリコートをREDデバイスと併せて37℃にて4時間インキュベートした。透析に続き、アリコートの50μLを各ウェル(脳ホモジネートおよび緩衝剤)から除去し、等体積の逆のマトリックスで希釈することでマトリックス効果を無効にした。同様に緩衝剤を回収試料および安定性試料へ加えた。アリコートの100μLをLC-MS/MS分析用に提出した。25μLアリコートの陽性対照および試験化合物を、内部標準(グリピジド)を含有する100μLのアセトニトリルでクラッシュさせ(crashed)、5分間ボルテックスした。試料を4℃にて10分4000RPMにて間遠心分離し、100μLの上清をLC-MS/MS分析用に提出した。試料を、LC-MS/MSを使用するMRMモードにおいて親化合物につき監視した。
表6.例示化合物に係るマウス脳タンパク質および肝臓ミクロソームの結合
マウスにおける脳透過性のIn vivo査定
マウスにおける脳透過性の予備的評価を、選択した例示化合物について実施し、結果を表8に示す。合計4マウスを各研究につき使用し、すべての動物に化合物を、溶液製剤(典型的には5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液(normal saline)中)を用い1mg/kg(at 5mL/kg用量体積)にて静脈内投与した。血液試料(およそ60μL)を光(light)イソフルレン麻酔下で2マウスから0.25hrおよび1hrにて収集した。血漿を血液の遠心分離によって調達し、分析まで-70±10℃にて保管した。血液収集後に脳を灌流し、0.25hrおよび1hrにて単離した。脳を氷冷リン酸緩衝生理食塩水中に3回浸し、拭き取って乾燥させ、重さを量った。脳試料を2倍体積の脳重量を用いて、氷冷リン酸緩衝生理食塩水を使用しホモジナイズすることで、合計ホモジネート3体積を作製し、-70±10℃を下回る温度にて分析まで保管した。
マウスにおける脳透過性の予備的評価を、選択した例示化合物について実施し、結果を表8に示す。合計4マウスを各研究につき使用し、すべての動物に化合物を、溶液製剤(典型的には5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液(normal saline)中)を用い1mg/kg(at 5mL/kg用量体積)にて静脈内投与した。血液試料(およそ60μL)を光(light)イソフルレン麻酔下で2マウスから0.25hrおよび1hrにて収集した。血漿を血液の遠心分離によって調達し、分析まで-70±10℃にて保管した。血液収集後に脳を灌流し、0.25hrおよび1hrにて単離した。脳を氷冷リン酸緩衝生理食塩水中に3回浸し、拭き取って乾燥させ、重さを量った。脳試料を2倍体積の脳重量を用いて、氷冷リン酸緩衝生理食塩水を使用しホモジナイズすることで、合計ホモジネート3体積を作製し、-70±10℃を下回る温度にて分析まで保管した。
血漿および脳試料を、目的にかなったLC-MS/MS方法によって定量した。血漿/脳試料のためのと、混ぜられた血漿/脳の較正標準との抽出手順は同一であった:25μLの研究試料または混ぜられた血漿/脳の較正標準を、予め標識された個々の微小遠心管へ加え、これに続きアセトニトリル(グリピジド、500ng/mL)で調製された100μLの内部標準を、100μLのアセトニトリルが加えられたブランクを除いて、加えた。試料を5分間ボルテックスした。試料を4℃にて5分間4000rpmのスピードにて遠心分離した。遠心分離に続き、100μLの透明な上清を96ウェルプレートに移し、以下を伴う標準的なLC-MS/MS方法を使用するLC-MS/MSを使用して分析した:
カラム:Phenomenex、Kinetex EVO、5μm、C18、100A、100×4.6mm
注射体積:5μl
カラム温度:45℃
流速:0.8mL/min
移動相A:アセトニトリル中0.1%ギ酸
移動相B:水中0.1%ギ酸
勾配:
表7.予備的in vivo曝露:1mg/kg用量のIV投与後のBL/6マウスにおける血漿および脳レベル
製剤:5%NMP、5%Solutol HS-15、90%生理食塩水、ただし*=アセタート緩衝剤50mM(pH-4.5)を除く
カラム:Phenomenex、Kinetex EVO、5μm、C18、100A、100×4.6mm
注射体積:5μl
カラム温度:45℃
流速:0.8mL/min
移動相A:アセトニトリル中0.1%ギ酸
移動相B:水中0.1%ギ酸
勾配:
細胞生存率
化合物への4~48時間曝露後の細胞生存率を2種のヒト細胞株;ヒト神経芽細胞腫(ATCC#CRL-2266)であるSH-SY5Yと、ヒト胚腎臓(ATCC#CRL-1573)であるHEK293とにおいて、CellTiter Gloアッセイ(Promega#G7570)を使用し評価した。生存率アッセイを実施するため、SH-SY5Y細胞およびHEK293細胞を、96ウェル白色透明底組織培養プレート上5000細胞/50μl成長培地/ウェルにて播種した。細胞を37℃および5%CO2にて終夜インキュベートすることで、回復させて再接着させた。翌日、細胞を試験化合物で、4時間および24時間(SH-SY5Y)または24時間および48時間(HEK293)処置した。試験化合物の最終濃度は30μMであり、DMSOの最終濃度は0.3%であった。細胞毒素シスプラチン(100μM最終濃度)を細胞死用の陽性対照として使用した。処置後、細胞生存率をCellTiter-Glo(登録商標)Luminescent Cell Viability Assayによって測定した。CellTiter-Gloアッセイを実施するため、100μlのCellTiter Glo試薬を各ウェルへ加え、プレートを室温にてさらに10~20分間インキュベートした。
発光を、ルミノメーター(BioTek SynergyTM2マイクロプレートリーダー)を使用して測定した。
化合物への4~48時間曝露後の細胞生存率を2種のヒト細胞株;ヒト神経芽細胞腫(ATCC#CRL-2266)であるSH-SY5Yと、ヒト胚腎臓(ATCC#CRL-1573)であるHEK293とにおいて、CellTiter Gloアッセイ(Promega#G7570)を使用し評価した。生存率アッセイを実施するため、SH-SY5Y細胞およびHEK293細胞を、96ウェル白色透明底組織培養プレート上5000細胞/50μl成長培地/ウェルにて播種した。細胞を37℃および5%CO2にて終夜インキュベートすることで、回復させて再接着させた。翌日、細胞を試験化合物で、4時間および24時間(SH-SY5Y)または24時間および48時間(HEK293)処置した。試験化合物の最終濃度は30μMであり、DMSOの最終濃度は0.3%であった。細胞毒素シスプラチン(100μM最終濃度)を細胞死用の陽性対照として使用した。処置後、細胞生存率をCellTiter-Glo(登録商標)Luminescent Cell Viability Assayによって測定した。CellTiter-Gloアッセイを実施するため、100μlのCellTiter Glo試薬を各ウェルへ加え、プレートを室温にてさらに10~20分間インキュベートした。
発光を、ルミノメーター(BioTek SynergyTM2マイクロプレートリーダー)を使用して測定した。
アッセイを各濃度にて三通りに実施した。化合物の不在下(しかしDMSO 0.3%の存在下)での各データ一式の発光強度(Lt)を100%として定義した。細胞の不在下での各データ一式の発光強度(Lt)を0%として定義した。各化合物の存在下でのパーセント発光を以下の方程式に従い算出した:%発光=(L-Lb)/(Lt-Lb)、ここでL=化合物存在下の発光強度、Lb=細胞不在下の発光強度、およびLt=化合物不在下の発光強度。パーセント発光は、このアッセイにおけるパーセント生存率を指し示し、±標準偏差で一覧にする。
表8.例示化合物への曝露後の分裂細胞の細胞生存率
表8.例示化合物への曝露後の分裂細胞の細胞生存率
初代ラット後根神経節(DRG)の細胞生存率
選択した例示化合物を、処置から3時間後または72時間後に初代ラット後根神経節(DRG)細胞の細胞生存率について評価した。選択化合物のデータを下の表9に示す。化合物を100%DMSOに溶解して50ミリモル濃度(mM)貯蔵溶液を作製した。貯蔵溶液を、段階希釈を使用してDMSOおよび細胞培地に希釈することで、最高化合物濃度が100μMのもの、9つのハーフログ(half-log)希釈、およびDMSO(0μM)用量の11用量を創作した。
選択した例示化合物を、処置から3時間後または72時間後に初代ラット後根神経節(DRG)細胞の細胞生存率について評価した。選択化合物のデータを下の表9に示す。化合物を100%DMSOに溶解して50ミリモル濃度(mM)貯蔵溶液を作製した。貯蔵溶液を、段階希釈を使用してDMSOおよび細胞培地に希釈することで、最高化合物濃度が100μMのもの、9つのハーフログ(half-log)希釈、およびDMSO(0μM)用量の11用量を創作した。
ラットDRG細胞を適切な培養培地(90%DMEM、10%FBS、1%ペニシリン-ストレプトマイシン、1%グルタミン)中37C度にてCO2雰囲気で培養した。培養培地を除去し、細胞をPBSで2度穏やかに洗浄してPBSをウェルから除去した。細胞を3mL 0.25%トリプシンで消化され、消化を10mL培養培地で終わらせた。DRG細胞(80μL)を培養培地中、不透明壁の96ウェルプレートに播き、24時間インキュベートした。化合物用量(5×、20μL)を三通りにDRG細胞へ、3時間または72時間適用した。細胞がない培地含有ウェルを、背景発光に係る値を得るため調製した。プレートを室温にておよそ30分間平衡化した。化学毒物(chemotoxic agent)のシスプラチンは細胞死用の陽性対照として働いた。ボリノスタット(SAHA)は、公開された非選択的HDACインヒビターであって、がん処置用にFDA承認されている。リコリノスタット(ACY-1215)は、末梢の適応症のための、Acetylon/Celgene/Regenacyの臨床開発候補である。
細胞生存率を、CellTiter-Glo(登録商標)Luminescent Cell Viability Assay(Promega,G7573)を使用して決定した。CellTiter-Glo(登録商標)Reagent(100μL)を各ウェルへ加えた。内容物をオービタルシェーカー上2分間混合することで、細胞のリシスを誘導した。発光シグナルを安定化させるため、プレートを室温にて10分間インキュベートした。発光を記録した。発光シグナルは細胞生存率のレベルを反映する。CC50は、細胞生存率が50%であるときの化合物の濃度であり、以下のとおり算出した:
細胞生存率(%)=(LumCPD-LumMC)/(LumCC-LumMC)*100%
Lum:発光シグナル
CC:DMSO群
MC:培地対照
CPD:化合物群
3時間時点でのCC50値は、細胞生存率の喪失が観察されなかったところ、算出不能(nc)であった。
表9.処置から3時間後または72時間後の初代ラットDRGにおける細胞生存率データの概要
nc=算出不能
細胞生存率(%)=(LumCPD-LumMC)/(LumCC-LumMC)*100%
Lum:発光シグナル
CC:DMSO群
MC:培地対照
CPD:化合物群
3時間時点でのCC50値は、細胞生存率の喪失が観察されなかったところ、算出不能(nc)であった。
表9.処置から3時間後または72時間後の初代ラットDRGにおける細胞生存率データの概要
薬物動態
選択した例示化合物を、5mg/kgでの単回腹腔内投与後のオスC57BL/6マウスにおける血漿薬物動態および脳分布について評価した。選択化合物に係るデータを図2Aおよび図2Bに示し、下の表10にまとめる。各化合物について、14匹のオスマウス一群に、5mg/kgにて5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液(または50mg/kg用量にて、7.5%NMP、5%Solutol HS-15、30%PEG-400、および57.5%クエン酸(10mM))中調製された化合物を腹腔内投与した。血液試料を、光イソフルレン麻酔下0.25、0.5、1、2、4、8および24hr(IP)にて、抗凝固薬としてK2EDTAを含有する標識された微小遠心管中に収集した。血液収集後即時に血漿を遠心分離によって調達し、分析まで-70±10℃にて保管した。血液収集に続き、動物をCO2窒息によって安楽死させ、脳試料を各時点にて収集した。収集された脳試料を氷冷リン酸緩衝生理食塩水に3度浸し、拭き取って乾燥させた。脳試料を2倍体積の脳重量を用いて、氷冷リン酸緩衝生理食塩水を使用しホモジナイズすることで、合計ホモジネート3体積を作製し、-70±10℃を下回る温度にて分析まで保管した。
選択した例示化合物を、5mg/kgでの単回腹腔内投与後のオスC57BL/6マウスにおける血漿薬物動態および脳分布について評価した。選択化合物に係るデータを図2Aおよび図2Bに示し、下の表10にまとめる。各化合物について、14匹のオスマウス一群に、5mg/kgにて5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液(または50mg/kg用量にて、7.5%NMP、5%Solutol HS-15、30%PEG-400、および57.5%クエン酸(10mM))中調製された化合物を腹腔内投与した。血液試料を、光イソフルレン麻酔下0.25、0.5、1、2、4、8および24hr(IP)にて、抗凝固薬としてK2EDTAを含有する標識された微小遠心管中に収集した。血液収集後即時に血漿を遠心分離によって調達し、分析まで-70±10℃にて保管した。血液収集に続き、動物をCO2窒息によって安楽死させ、脳試料を各時点にて収集した。収集された脳試料を氷冷リン酸緩衝生理食塩水に3度浸し、拭き取って乾燥させた。脳試料を2倍体積の脳重量を用いて、氷冷リン酸緩衝生理食塩水を使用しホモジナイズすることで、合計ホモジネート3体積を作製し、-70±10℃を下回る温度にて分析まで保管した。
下の表11は、1mg/kgまたは2mg/kgでの単回静脈内投与後に同様に評価された、選択した例示化合物に係るデータをまとめる。各化合物について、21匹のオスマウス一群に、5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液中1mg/kgまたは2mg/kgにて調製された化合物製剤を静脈内投与した。血液および脳組織試料を収集し、上に詳述されたとおり0.083、0.25、0.5、1、2、4および8hr、または0.25、0.5、1、2、4、8および12hr(IV)にて処理した。
上の表12は、5%NMP、5%Solutol HS-15、および90%通常生理食塩溶液(10mg/kg用量)で、または7.5%NMP、5%Solutol HS-15、30%PEG-400、および57.5%クエン酸(10mM)(30mg/kg用量)で調製された化合物製剤の単回経口投与後に同様に評価された、選択した例示化合物に係るデータをまとめる。血液および脳組織試料を収集し、上に詳述されたとおり0.25、0.5、1、2、4、8および12hr(PO)にて処理した。
すべての試料を、アセトニトリルを使用するタンパク質沈殿によって分析用に処理し、目的にかなったLC-MS/MS方法で、上に記載のとおりに分析した。薬物動態パラメータを、Phoenix WinNonlin(登録商標)(Version 7.0)というノンコンパートメント(non-compartmental)分析ツールを使用して算出した。
表10.IP投与後のC57BL/6マウスにおける薬物動態特性の概要
ACY-775は、MedChem Expressから得られ、公開されたHDAC6選択的インヒビターであって、ベンチマークとして使用した。化合物75を除くすべての化合物の用量は5mg/kgであった。示される化合物75の値は50mg/kgのものである;5mg/kg値は、迅速なクリアランスに起因し算出不能(nc)であった。173および79の値も迅速なクリアランスに起因し算出不能(nc)であった。
表11.IV投与後のC57BL/6マウスにおける薬物動態特性の概要
脳中の79の値は算出不能(nc)であった
表12.PO投与後のC57BL/6マウスにおける薬物動態特性の概要
脳中の75および173の値は算出不能(nc)であった
表10.IP投与後のC57BL/6マウスにおける薬物動態特性の概要
表11.IV投与後のC57BL/6マウスにおける薬物動態特性の概要
表12.PO投与後のC57BL/6マウスにおける薬物動態特性の概要
シスプラチンで処置されたラットDRGにおけるIn vitroでの化学療法誘発性末梢神経障害
選択した例示化合物を、成体初代ラット後根神経節(DRG)を使用し、in vitroでの化学療法誘発性神経障害モデルにおける神経変性の予防について評価した。化合物は処置および分析について盲検し(blinded)、DMSOをビヒクル対照として使用した。16、173、79、ACY-1083(ベンチマーク)、およびDMSO(盲検の陰性対照)を、処置にあたり2個のカバースリップを使用して査定した。化合物を、0.5mMシスプラチンの存在下5μMにて4日間DRG上でインキュベーション後に試験し、ビヒクルで処置された0.5mMシスプラチンと比較した。ブレブ(フラグメント)は神経変性プロセスの始まりの表れである。総軸索面積は、ニューロンの生存に関し、神経保護のより一般的な評価基準(measure)である。選択化合物に係るデータを図3Aおよび3Bに示す。
選択した例示化合物を、成体初代ラット後根神経節(DRG)を使用し、in vitroでの化学療法誘発性神経障害モデルにおける神経変性の予防について評価した。化合物は処置および分析について盲検し(blinded)、DMSOをビヒクル対照として使用した。16、173、79、ACY-1083(ベンチマーク)、およびDMSO(盲検の陰性対照)を、処置にあたり2個のカバースリップを使用して査定した。化合物を、0.5mMシスプラチンの存在下5μMにて4日間DRG上でインキュベーション後に試験し、ビヒクルで処置された0.5mMシスプラチンと比較した。ブレブ(フラグメント)は神経変性プロセスの始まりの表れである。総軸索面積は、ニューロンの生存に関し、神経保護のより一般的な評価基準(measure)である。選択化合物に係るデータを図3Aおよび3Bに示す。
研究第1日に解離溶液(2mLのHEPES(1M、pH7.25)ありの100mLのHBSS)を調製し、予め4℃まで冷却した。24ウェル細胞培養プレートをECLでコーティングした。各ウェルを0.3mLのECL溶液(滅菌PBS中1:25)でコーティングし、37℃にて終夜インキュベートした。研究第2日にECL溶液を吸引し、ウェルプレートを神経細胞用基礎(neurobasal)培地で濯いだ。次いでプレートを1ウェルあたり0.5mLのDRGニューロン培養培地(Neurobasal(登録商標)-A培地中2mLのB-27(登録商標) Supplement 50× プラス 5mL FBS プラス 3μLゲンタマイシン(Neurobasal(登録商標)中1ug/mL)、100mLに仕上げた)で予めインキュベートし、インキュベーター中へ設置した。
ハサミおよび鉗子を70%エタノール中30分間消毒し、これに続いて風乾した。Sprague Dawleyラット(オス)を、頸椎脱臼を介して死なせ(terminated)、脊髄を一般的な(standard)ハサミ1丁で迅速に解剖した。脊髄を調製し、皮膚を腹側の正中線にて一般的なハサミで切開した。臓器を胸腔および腹腔から除去した。一般的なハサミを使用し、脊柱に対して左右近接して2本の長い切れ目を入れた。実体顕微鏡を使用し、すべての脊髄レベルからDRGを慎重に除去し、3mLのHBSS中、氷上に設置した35mm解剖皿に収集した。学生バネハサミ(student spring scissors)の一方の刃を腹側から脊柱管中へ挿入した。ハサミの他方の刃を脊柱の外側であってその腹側に置いた。脊椎に沿って2箇所切開し、1つは腹側の正中(midline)の左およびもう1つは右であった。DRGは、白色の神経線維束とは異なる丸い形状およびガラス質の外観によって特徴付けられる。学生バネハサミ、Dumont#7bおよび#4鉗子を使用して、脊髄の3つの断片の各々につき、露出した神経節を慎重に単離した。単離されたDRGを、5mLのDRG調製培地で満たされた35mmペトリ皿に収集した。皿を氷上に置いた。およそ20~40の神経節が得られた。
神経節を取り囲む神経上膜の結合組織の薄層を、バネハサミ1丁およびDumont鉗子を用いて除去した。次いでDRGを、DRG調製培地で満たされた氷上の第2の35mm皿へ移した。コラゲナーゼII溶液(1mLの解離溶液中10mgのコラゲナーゼII)を調製し、37℃まで10分間予熱した。単離されたDRGを層流型作業台の下、15mL遠心分離管中へ移した。DRGを管の底まで沈ませた後、上清を除去し捨てた。DRGを、予め冷却しかつ滅菌した5mLの解離溶液で濯いだ。再度上清を除去した。DRGを合計3回、各々5mLの解離溶液で洗浄した。最後の洗浄ステップの後2mLの解離溶液を残し、1mLのコラゲナーゼII溶液を加えた。DRGを、10分毎にFalconsを穏やかに振盪しながら、37℃にて1時間インキュベートした。2%トリプシン貯蔵溶液(5mLのHBSS中100mgのトリプシン)のアリコートを解凍し(defrosted)、37℃まで20分間予熱した。150μLの活性化トリプシンを加えた。DRGを、3分毎にFalconを穏やかに振盪しながら、37℃にてさらに9分間インキュベートした。上清を慎重に除去し、5mLの解離溶液で洗浄した。最後の洗浄ステップの後、1.5mLの解離溶液を残した。
単細胞を得るため、DRGをガラスのパスツールピペットで解離させた。2本のガラスのパスツールピペットを火仕上げすることで、より小さい開口を得た。本来の開口直径が1.1~1.3mmのガラスピペットを使用し、溶液が均一に見えるまでDRGを、およそ10回上下にピペッティングした。次いでより小さい直径の(火仕上げされた)パスツールピペットを使用し、溶液を8回摩砕した(triturated)。最後に、極めて小さい直径(火仕上げされた)パスツールピペットを3回使用した。単細胞懸濁液を160×gにて5分間遠心分離した。上清を細胞ペレットから除去した。DRGニューロン培養培地を細胞ペレットへ加えた;細胞を再懸濁し、200RPMにて5分間遠心分離した。上清を慎重に除去し、細胞を1,000μLピペットでDRGニューロン培養培地に再懸濁した。細胞を14ウェルに播種し、5%CO2雰囲気下37Cにて設置した。
化合物を、化学療法剤と併せて培養している培地へ加えた。メタノールを使用して細胞をカバースリップ上で固定し、4日後に神経突起の画像化のためベータ-チューブリンIIIに対する抗体で染色した。免疫細胞化学のため、カバースリップを100%氷冷メタノールで固定し、0.02%Triton X-100で透過処理した(permeabilized)。次いでニューロンをBSA中、室温にて1時間インキュベートし、これに続き夫々の抗体:ベータ-チューブリンIII(Merck,cat#T2200)と、後で、Alexa Fluor 594が抱合された二次抗ウサギAbとともにインキュベーションした。蛍光マウンティング培地(Gbi,cat#E19-s)を使用し、カバースリップをスライド上にマウントした(mounted)。1処置群あたり2カバースリップ分の面積を取った。Olympusによる標準の「CellSens」ソフトウェアによって駆動されるBX43 Olympus顕微鏡を使用して画像化した。画像を、DP74カメラ(Olympus)を使用し60×水浸対物レンズ下で撮った。軸索の変性を推定するため、ImageJプラグイン-「Neurophysiology」を使用した。閾値の設定を適用した後、「分析粒子」機能を、すべての粒子を包含するよう0~∞の画素サイズ(画素2)設定および0~1.0の円形設定で使用した。データ出力には、検出された物体の総面積(総画素2)、および「find maxima」機能で検出されたブレブ数が包含された。画像あたりの神経突起面積およびブレブ数を算出し、それらの比率の値をシスプラチン+ビヒクル群と比較した。読み出された情報(Readouts)は、面積あたりのブレブおよび軸索の総面積であった。
シスプラチンで処置されたマウスにおけるIn vivoでの化学療法誘発性末梢神経障害
選択した例示化合物を、シスプラチンを使用して、in vivoでの化学療法誘発性末梢神経障害(CIPN)マウスモデルにおける効き目について評価した。16(30mg/kg PO)、ACY-1083(ベンチマーク、10mg/kg IP)、およびビヒクル(IP)を、下に概要したとおり1群あたりn=15動物で共処置の範例(paradigm)を使用し、シスプラチン(2.3mg/kg IP)の存在下で査定した。健康全般を体重および生存によって監視した。機械的アロディニアをフォン・フライ試験によって査定した。神経の完全性を表皮内神経線維(IENF)密度によって測定した。選択化合物に係るデータを図4に示す。
選択した例示化合物を、シスプラチンを使用して、in vivoでの化学療法誘発性末梢神経障害(CIPN)マウスモデルにおける効き目について評価した。16(30mg/kg PO)、ACY-1083(ベンチマーク、10mg/kg IP)、およびビヒクル(IP)を、下に概要したとおり1群あたりn=15動物で共処置の範例(paradigm)を使用し、シスプラチン(2.3mg/kg IP)の存在下で査定した。健康全般を体重および生存によって監視した。機械的アロディニアをフォン・フライ試験によって査定した。神経の完全性を表皮内神経線維(IENF)密度によって測定した。選択化合物に係るデータを図4に示す。
すべての製剤を各投薬前に新たに調製し、所要の時点にてIPルートまたはPOルートによって投与した。2.3mg/kgシスプラチンを使用し、CIPNモデルを誘発させた。シスプラチンを0.46mg/mLの濃度にて滅菌生理食塩水に溶解した。ACY-1083を、10mL/kg体積のIP注射を介する10mg/kg用量にて与えた。ACY-1083粉末を水中の20% 2-ヒドロキシプロピル-B-シクロデキストリン+0.5%ヒドロキシプロピルメチルセルロースに溶解し、1mg/mLの溶液強度を達成した。16を、体積10mL/kgの経口強制飼養を介する30mg/kg用量にて与えた。16を、3mg/mLの溶液強度にて、7.5%NMP;5%Solutol HS-15;30%PEG-400;57.5%10mMクエン酸に溶解した。ACY-1083(水中20%2-ヒドロキシプロピル-B-シクロデキストリン+0.5%ヒドロキシプロピルメチルセルロース;10mL/kg、IPルート)用のビヒクルをビヒクル対照と見なした。7日間の順応のためオスC57BL/6マウスをケージあたり4匹の群において飼育した。これらは実験開始時18~22gの重さがあった。温度および湿度を制御した(夫々、23±2℃および50±5%を目標とした)。動植物飼養場(vivarium)を12時間の明/暗サイクル(光は07:00時間にてオフ)で維持した。食料および水は適宜入手可能であった。
生理食塩水またはシスプラチンを第1日~5日および第11日~15日にQD投与した。ビヒクル(IP)、ACY-1083(IP)、または16(経口強制飼養)を第1日~17日にQD投与した。第1日~5日および第11日~15日に、投与をシスプラチン処置の1時間前にした。すべてのマウスの体重を毎日監視した。臨床観察を毎日した。
試験を3時点(ベースライン、第7日、および第16日)にて実施した。第7日および1フォン・フライ6日に、試験をビヒクル/ACY-1083/16投薬から2時間後に実施した。マウスを機械的アロディニア試験のベースラインデータに基づき無作為にグループ化した。マウスを3日間、アロディニア測定前の15分間試験環境に慣れさせた。マウスの左足を、硬さが対数的に増加する一連の8種のフォン・フライの毛(0.02g、0.04g、0.07g、0.16g、0.4g、0.6g、1.0g、および1.4g)(S.R.Chaplan,F.W.Bacha.1994)のうち1つに触れさせた。フォン・フライの毛を、足に対してわずかな座屈を引き起こすのに充分な力で足底面に対し垂直に提示し、およそ6~8秒間保持した。刺激を数秒の間隔にて提示し、先の刺激に対するいずれの行動反応も見掛け上解消させるようにさせた。
足を敏速に引っ込めたら、正反応と書き留めた。毛を除去した際即時に尻込みすることもまた、正反応と見なした。歩行は曖昧な反応と見なし、かかるケースにおいては刺激を繰り返した。50%の引っ込め閾値を決定するため、試験を0.16gファイバーで始めた。ファイバーを、上げていくか(初めに選択したファイバーに対して足を引っ込める反応がなかったら、次に最高ファイバーを提示した)または下げていくか(足を引っ込めた事象において、次により弱いファイバーを提示した)にかかわらず、連続して(in a consecutive fashion)提示した。次いで所見(引っ込めた(x)/引っ込めなかった(o))を、自動的に閾値(グラム)を算出するテンプレート中へ入力した。機械的アロディニアを、式:
50%反応閾値(g)=(10(Xf+kδ))/10,000
Xf=最終的に使用されたフォン・フライの繊維の値(ログ単位)
k=正/負の反応パターンに係る表形式の値(Chaplan et al.1994,appendix 1,page 62)
δ=刺激同士間の平均差(ログ単位)
を使用して算出し、表した。
足を敏速に引っ込めたら、正反応と書き留めた。毛を除去した際即時に尻込みすることもまた、正反応と見なした。歩行は曖昧な反応と見なし、かかるケースにおいては刺激を繰り返した。50%の引っ込め閾値を決定するため、試験を0.16gファイバーで始めた。ファイバーを、上げていくか(初めに選択したファイバーに対して足を引っ込める反応がなかったら、次に最高ファイバーを提示した)または下げていくか(足を引っ込めた事象において、次により弱いファイバーを提示した)にかかわらず、連続して(in a consecutive fashion)提示した。次いで所見(引っ込めた(x)/引っ込めなかった(o))を、自動的に閾値(グラム)を算出するテンプレート中へ入力した。機械的アロディニアを、式:
50%反応閾値(g)=(10(Xf+kδ))/10,000
Xf=最終的に使用されたフォン・フライの繊維の値(ログ単位)
k=正/負の反応パターンに係る表形式の値(Chaplan et al.1994,appendix 1,page 62)
δ=刺激同士間の平均差(ログ単位)
を使用して算出し、表した。
第17日に、最終治療介入の投薬から2時間後すべての動物をCO2吸入によってサクリファイスした。血漿および神経を、バイオ質量分析(mass-spec bioanalysis)用に送り、化合物の存在を確認して、結合しなかった画分を決定した。後足からの皮膚(1群あたり12マウスのうち6匹)をIENF測定用に調製した。後足蹠の皮膚を慎重に解剖し、4%パラホルムアルデヒド(リン酸緩衝生理食塩水(PBS)中、pH7.2)へ室温(RT)にて24時間移した。組織を脱水する目的で20%スクロース(PBS中)溶液中におよそ48時間浸けた。皮膚を凍結緩衝剤(O.C.T./20%スクロース(1:1))中に包埋し、これに続きドライアイス上で瞬間凍結した。皮膚の近位端をプラスチック包埋箱の側壁へ付着させたことに留意(これを最初に切開することになっている)。凍結組織塊をクライオトーム(cryotome)クリオスタット(チャンバー温度を-20℃にて、標本の先頭は-19℃にて設定した)へ移した。最初の0.4mm組織は捨てた。次いで皮膚の薄片を10μmにて切って収集した。薄片をPBSで2回、各回5分間洗浄した。10%ヤギ血清(PBS中)をrtにて1~2時間加えた。一次抗体(抗PGP9.5、ウサギ由来、抗体希釈剤中1:500)を、密封された湿潤容器中、4℃にて終夜インキュベートした。スライドをPBSで3回、各回10分間洗浄した。二次抗体(蛍光色素がカップリングされたヤギ抗ウサギ、抗体希釈剤中1:400)をrtにて1時間インキュベートした。120μLのDAPI含有マウンティング培地を適用し、カバースリップでマウントした。スライドを4℃にて終夜乾燥させた。組織切片の全情報が得られるため、Leica蛍光スキャナーを使用して画像化を実施した。
表皮の基底膜(BM)を細胞形態学に従って引き出した。IENFをBMに沿って引き出した。計数規則を下に列挙する(2017年に公開されたMangus et al.の総括に倣う)。
(1)BMを貫通する神経線維を計数する。
(2)BMを横断しかつ表皮にて分岐する神経を、1IENFとして計数する。
(3)真皮にて分かれ、次いでBMを貫通する神経を、別々の単位として計数する。
IENF密度(IENF/mm)は、表皮の長さ(mm)によって分類されたIENF数に等しい。
(1)BMを貫通する神経線維を計数する。
(2)BMを横断しかつ表皮にて分岐する神経を、1IENFとして計数する。
(3)真皮にて分かれ、次いでBMを貫通する神経を、別々の単位として計数する。
IENF密度(IENF/mm)は、表皮の長さ(mm)によって分類されたIENF数に等しい。
iPSC由来ALS運動ニューロンにおける軸索輸送
選択した例示化合物を、筋萎縮性側索硬化症(ALS)の患者からのヒト人工多能性幹細胞(iPSC)由来運動ニューロン(MN)におけるチューブリンアセチル化の軸索輸送および応答の救済について評価した。選択化合物に係るデータを図5に示す。DMSOをビヒクル対照として使用し、すべての化合物をFUS患者系統P525LのiPSC由来MNにおいて試験した。同質遺伝子P525P iPSC対照系統からのMNもまたDMSOで処置し、P525L系統における軸索の輸送欠陥および試験された化合物の潜在的な救済効果を確認した。化合物は処置および分析について盲検とし、58およびACY-775(ベンチマーク)は1つの分化において査定し、173、79およびDMSO(盲検の陰性対照)は別々の分化において査定した。ミトコンドリアの軸索輸送のため、分化第30日および31日にて化合物を終夜インキュベーション後5μMにて試験し、チューブリンアセチル化のウェスタンブロット(WB)分析用試料を第32日にて収集した。
選択した例示化合物を、筋萎縮性側索硬化症(ALS)の患者からのヒト人工多能性幹細胞(iPSC)由来運動ニューロン(MN)におけるチューブリンアセチル化の軸索輸送および応答の救済について評価した。選択化合物に係るデータを図5に示す。DMSOをビヒクル対照として使用し、すべての化合物をFUS患者系統P525LのiPSC由来MNにおいて試験した。同質遺伝子P525P iPSC対照系統からのMNもまたDMSOで処置し、P525L系統における軸索の輸送欠陥および試験された化合物の潜在的な救済効果を確認した。化合物は処置および分析について盲検とし、58およびACY-775(ベンチマーク)は1つの分化において査定し、173、79およびDMSO(盲検の陰性対照)は別々の分化において査定した。ミトコンドリアの軸索輸送のため、分化第30日および31日にて化合物を終夜インキュベーション後5μMにて試験し、チューブリンアセチル化のウェスタンブロット(WB)分析用試料を第32日にて収集した。
ヒトiPSCsを、ペニシリン-ストレプトマイシンで補充されたEssential8培地(A1517001,Gibco)中、GeltrexR(A1413302,Gibco)上で維持した。コロニーを、ダルベッコのリン酸緩衝生理食塩水(DPBS)中0.5mM EDTA(15575-020,Invitrogen)で定型的に継代した。培養物をPCRによってマイコプラズマ汚染について定型的に分析した。MNを、前に記載のとおり(Guo et al.Nat Commun 2017)、iPSCsから分化させた。手短に言えば、iPSCクローンを懸濁し、コラゲナーゼI型V消化を使用して6ウェルプレートから、神経細胞用基礎(neuronal basic)培地(Neurobasal培地とDMEM/F12培地との1:1混合物、N2およびB27あり、ビタミンAなし)のあるT-25低付着フラスコ中へ移し、胚様体を形成させた。5μM ROCKインヒビター(Y-27632,Merck Millipore)、40μM TGF-βインヒビター(SB 431524,SB,Tocris Bioscience)、0.2μM 骨形成タンパク質インヒビター(LDN-193189,LDN,Stemgent)、および3μM GSK-3インヒビター(CHIR99021,CHIR,Tocris Bioscience)とともに2日間インキュベーションした後、懸濁した胚様体を、0.1μMレチノイン酸(RA,Sigma)および500nM Smoothened Agonist(SAG,Merck Millipore)を含有する神経細胞用基礎培地とともに4日間インキュベートした。細胞を続いて、RA、SAG、10ng/mL脳由来神経栄養因子(BDNF,Peprotech)、および10ng/mLグリア細胞由来神経栄養因子(GDNF,Peprotech)を含有する神経細胞用基礎培地中2日間インキュベートした。分化第9日にて、細胞スフェア(spheres)を、0.05%トリプシン(Gibco)を37℃にて20分間使用して解離させ、単一細胞にした。細胞を計数後、規定数の細胞を、ポリ-L-オルニチン(100μg/mL)とラミニン(20μg/mL)とでコーティングされたプレートに播き、RA、SAG、BDNF、GDNF、および10μM γ-セクレターゼのインヒビター(DAPT,Tocris Bioscienceから)を含有する神経細胞用基礎培地中5日間インキュベートし、次いでBDNF、GDNF、および20μM DAPTを含有する神経細胞用基礎培地中2日間インキュベートした。MN成熟のため、細胞を、BDNF、GDNF、および毛様体神経栄養因子(CNTF;各10ng/ml,Peprotech)で補充された神経細胞用培地中で保った。培地の半分を置き換えることによって培地を隔日毎に代えた。すべての実験を分化の第5週までの間に実施した。MN分化効率を2回目の分化においてチェックしたところ、80%超の細胞がMN特異的マーカーChat、Isl、SMI32に対して陽性染色され、いずれの系統間にも差がなかったことが示された。
透明底部24ウェルプレート(PerkinElmer,1450-602)中に播かれた運動ニューロンを、HEPES緩衝塩溶液(pH7.4、150mM NaCl、5mM KCl、1mM MgCl2、2mM CaCl2、10mMグルコース、10mM HEPES)中50nM MitoTracker-Green(Thermofisher,M7514)とともに20分間ロードした。次いで過剰のMitoTracker-GreenをHEPES緩衝塩溶液で洗浄し、37℃にて維持されたMNにおいて、InCell Analyzer 2000顕微鏡上60×対物レンズを使用して画像化した(GE Healthcare Life Sciences)。各視野を手動で選択し、1秒の低速度撮影画像を200秒間撮った。FiJiを使用しすべての画像分析を実施した。各神経突起を手動で選択し、Resliceツールを使用してキモグラムを生成したが、ここで軸索の長さが得られ、移動しているミトコンドリアを手動で計数した。神経突起あたりのミトコンドリアの総数を入手するために、TrackMate PlugInのセグメンテーションツールを各低速度撮影シリーズの最初の画像において使用した。いくつかのケースにおいて大量の画像を並べるためにLinear Stack AlignmentをSIFT PlugInとともに使用した。
MNを収集して、PhosStop(Roche,4906845001)とcOmplete(Roche,05892970001)とを含有する商業用RIPA緩衝剤(Sigma,R0278)中、氷上で30分間ライスし、4℃にて10分間16.000gにて遠心分離して上清を収集した。タンパク質濃度を、標準的なBCAキット(Thermofisher,23225)を使用して決定し、1ウェルあたり0.5ugのタンパク質をタンパク質電気泳動のため商業用アクリルアミドゲル(Bio-Rad,456-8096)にロードした。次いでタンパク質をニトロセルロース膜(GE Healthcare,10600001)へ転写して5%BSAで1時間ブロッキングし、以下の一次抗体:抗アセチル化チューブリン(Sigma,T673;1:5000希釈、室温にて2時間)、抗α-チューブリン(Sigma,T6199、1:5000希釈、4℃にて終夜)、および抗カルネキシン(Enzo Life Sciences,ADISPA-860;1:5000希釈、4℃にて終夜)とともにブロットした(blotted)。TBSTで洗浄した後、膜を二次抗体(Dako,P0447およびP0448、1:500希釈)とともに室温にて1時間インキュベートしてTBSTおよびTBSで洗浄し、ECLおよびSuperSignal(ThermoFisher,32106)ならびにImageQuant LAS 4000撮像装置(GE Healthcare)を使用して撮像した。
アカゲザル脳におけるIn vivoでの標的占有率測定
選択した例示化合物をオス赤毛猿(Macaca mulatta)の脳におけるin vivoでの標的占有率について評価した。選択化合物に係るデータを下の表13に示す。実験を、現地のUniversity Ethics Committee for Animalsから承認された後Belgian code of practice for care and use of animalsに従って行った。脳の標的占有率は、ベースラインおよび異種-ブロッキング陽電子放射断層撮影(PET)神経画像研究を介して確立された。占有率を、0.1mg/kgおよび2mg/kgの16ならびにACY-775でIV前処置した後の1匹のサルにおいて決定した。0.4mL/kg体積の[18F]Bavarostat注射の5分前にIV前処置研究を実施した。占有率を、2mg/kgの173でのIV前処置後および2mg/kgの16でのPO前処置後に異なるサルにおいて決定した。IV前処置研究を0.4mL/kg体積の[18F]Bavarostat注射の5分前に実施し、PO前処置研究を~45mLの飲用溶液中の[18F]Bavarostat注射の2時間前に実施した。16、173、およびACY-775でのIVブロッキングスキャン用に、7.5%NMP、5%Solutol HS-15、30%PEG-400、および57.5%10mMクエン酸を使用して製剤化を実施した。16でのPOブロッキングスキャン用に、蜂蜜と水との1:1(v/v)混合物中の2mg/kg化合物の懸濁液を使用して製剤化を実施した。
選択した例示化合物をオス赤毛猿(Macaca mulatta)の脳におけるin vivoでの標的占有率について評価した。選択化合物に係るデータを下の表13に示す。実験を、現地のUniversity Ethics Committee for Animalsから承認された後Belgian code of practice for care and use of animalsに従って行った。脳の標的占有率は、ベースラインおよび異種-ブロッキング陽電子放射断層撮影(PET)神経画像研究を介して確立された。占有率を、0.1mg/kgおよび2mg/kgの16ならびにACY-775でIV前処置した後の1匹のサルにおいて決定した。0.4mL/kg体積の[18F]Bavarostat注射の5分前にIV前処置研究を実施した。占有率を、2mg/kgの173でのIV前処置後および2mg/kgの16でのPO前処置後に異なるサルにおいて決定した。IV前処置研究を0.4mL/kg体積の[18F]Bavarostat注射の5分前に実施し、PO前処置研究を~45mLの飲用溶液中の[18F]Bavarostat注射の2時間前に実施した。16、173、およびACY-775でのIVブロッキングスキャン用に、7.5%NMP、5%Solutol HS-15、30%PEG-400、および57.5%10mMクエン酸を使用して製剤化を実施した。16でのPOブロッキングスキャン用に、蜂蜜と水との1:1(v/v)混合物中の2mg/kg化合物の懸濁液を使用して製剤化を実施した。
サルを、0.3mL Rompun(キシラジン2%溶液)と0.35mL Nimatek(ケタミン100mg/mL)との組み合わせの筋肉内注射によって落ち着かせた(トレーサー注射の~75分前)。最初の注射から約60分後、サルにIV注射を介して0.15mL Rompunおよび0.175mL Nimatekの追加用量を受けさせた。血中O2およびCO2の飽和と心拍数とをスキャニングの間中絶えず監視し、電子的に制御された温熱パッドを介して体温を維持した。
静脈ラインを、放射性トレーサーおよびブロッキング化合物(PO用量を除く)の一方の肢における投与のために挿入した。カテーテルを、動脈血液試料採取のため他方の肢において大腿骨の動脈中に設置した。前処置/ビヒクル注射に先立ち、動脈血液試料を血漿フリー画分決定のため採取した。
脳のスキャンを、Focus(商標)220マイクロPETスキャナー(Concorde Microsystems,Knoxville,TN,USA)を使用して取得した。放射性トレーサー注射の前、57Co線源を使用する10分間の透過スキャンを得ることで、位置決めと、これに続く減衰補正とを査定した。[18F]Bavarostat(185MBq、30秒にわたる手動ボーラス、伏在静脈(vena saphena))の注射と同時に、120分間の動的PETスキャンをリストモード(list mode)で取得した。データを4×15s、4×60s、5×180s、8×300s、および6×600sの時間枠の中でヒストグラム化し(histogrammed)、256×256×95画素へ減衰補正するMAPアルゴリズム(18反復、分解能1.5mm)を使用して再構築した。散乱補正は適用しなかった。
各動物の3次元のT1加重(-weighted)MR脳スキャンを、共同登録(co-registration)する目的から、以下のパラメータ:繰り返し時間2700ms、エコー時間3.8ms、反転時間850ms、フリップ角9°、256×208×144マトリックス、0.6mmボクセルサイズで、磁化準備型高速グラディエントエコー(MPRAGE)配列(*tfl3d1_16)を使用する3.0 Tesla全身スキャナー(Tim Trio Scanner,Siemens)上で得た。
動脈血液を、最初の[18F]Bavarostat注射から4分後に、Twiliteインライン(in-line)血液監視装置(Swisstrace,Switzerland)を使用して測定した。初めのスキャン時間後、SwisstraceポンプのスイッチをオフにしてTwilite電波探知器中の動脈血液をEDTA管中に回収し、予め選択した時点(トレーサー注射から5、10、20、40、60、100分後)にて動脈血液試料採取を手動で(三方弁を介し)続けた。収集されたすべての血液試料を即時に氷上で保管して代謝を停止させた。遠心分離(2330×g、5分間)後、全血試料(50μL)および血漿試料(50μL)を分離して重さを量った。収集された6試料の血漿の残りを処理し、HPLCを使用して分析することで種々の時点での完全なままの(intact tracer)トレーサー画分を定量した。約0.3mLの血漿へ等量のCH3CNを加え、その結果得られた懸濁液を遠心分離(2330×g、5分間)することで沈殿タンパク質を上清から分離した。次に、0.5mLの上清をシリンジフィルター(0.22μm;Millipore)に通して濾過し、水(1/2の体積)で希釈して10μgの真正(authentic)Bavarostatを混ぜた。0.5mL体積の抽出物を、分析用XTerraカラム(C18;5μm、4.6mm×250mm、Waters)からなるHPLC系上へ注入し、0.05M酢酸ナトリウム(pH5.5+0.005M EDTA)とCH3CN(55:45v/v)との混合物で流速1mL/minにて溶離した。当初の研究用に、電波探知器およびUV検出器(280nm)を通過させた後、自動画分収集器(automated fraction collector)を使用してHPLC溶離液を1mL画分として収集した。後に放射性代謝体プロファイルが分かったとき、HPLC溶離液を2つの画分(極性の放射性代謝体(単数または複数)を含有する画分n°1、および完全なままのトレーサーからなる画分n°2)において収集した。濾過された血漿(HPLCに先立つ)、フィルター、およびHPLC溶離液画分の放射能はすべて、マルチチャネル分析装置(Wallac 1480 Wizard,Wallac,Turku,Finland)へカップリングされた3インチ(3-in)NaI(Tl)ウェル結晶(well crystal)を備えた相互較正(cross-calibrated)ウェル型ガンマ計数器で計数した。結果を、背景放射線、検出器不感時間、および計数中の物理的減衰について補正した。実験日に用量較正器、PETカメラ、ガンマ計数器、およびTwiliteデバイスを[18F]FDGの溶液で相互較正した。
各動物からのMRIデータを、PFUSIT 4.0(PMOD,Switzerland)を使用しマカク脳地図に対して正規化した。動的なペットデータを平均して個々のMRIスキャンへ共同登録した後、公的に入手可能な脳地図からの関心のある体積をPET空間(space)へ転換することで速度論的分析用の時間放射能(activity)曲線が生成された。2組織コンパートメントモデリングおよびLoganグラフ分析用の入力関数として使用された、代謝体で補正された血漿放射能(activity)曲線を用いて、速度論的な分析をPKIN(PMOD,Switzerland)においてした。後者について、時間を40分に設定したのは、データがこの点にて目に見えて線形であるからである。化合物占有率レベルを、局所脳体積の分布(VT)値を使用するLassenプロットを介して算出した。2組織コンパートメントモデリングおよびLoganグラフ分析に由来するVT推定値は、酷似する結果を産生した。標的占有率を、Loganグラフ分析から生成されたVT推定値を使用する下の表に報告する。このデータの一部は公開されている;Celen et al.ACS Chemical Neuroscience 2020を見よ。
表13.Loganグラフ分析から生成された局所分布体積(VT)推定値を使用するLassenプロットによって決定されたとおりの、IV処置またはPO処置、これに続く[18F]Bavarostat PETの後の、アカゲザル脳におけるin vivoでの標的占有率データの概要
表13.Loganグラフ分析から生成された局所分布体積(VT)推定値を使用するLassenプロットによって決定されたとおりの、IV処置またはPO処置、これに続く[18F]Bavarostat PETの後の、アカゲザル脳におけるin vivoでの標的占有率データの概要
均等物および範囲
クレームにおいて、「a」、「an」、および「the」などの冠詞は、1または1より多いことを意味してもよいが、それと反する指示がないか、またはそれとは別に、文脈から明らかでない場合に限る。ある群の1以上のメンバー間に「または」を包含するクレームまたは記載は、その群のメンバーのうち、1つ、1つより多いか、または、すべてが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係があるか、を満たすと考えるが、それと反する指示がないか、またはそれとは別に、文脈から明らかでない場合に限る。本発明は、その群のうち、正確に1つのメンバーが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係がある態様を包含する。本発明は、その群のメンバーのうち、1つより多いかまたはすべてが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係がある態様を包含する。
クレームにおいて、「a」、「an」、および「the」などの冠詞は、1または1より多いことを意味してもよいが、それと反する指示がないか、またはそれとは別に、文脈から明らかでない場合に限る。ある群の1以上のメンバー間に「または」を包含するクレームまたは記載は、その群のメンバーのうち、1つ、1つより多いか、または、すべてが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係があるか、を満たすと考えるが、それと反する指示がないか、またはそれとは別に、文脈から明らかでない場合に限る。本発明は、その群のうち、正確に1つのメンバーが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係がある態様を包含する。本発明は、その群のメンバーのうち、1つより多いかまたはすべてが、所定の生成物またはプロセスに存在するか、それに採用されるか、またはそれとは別に、それに関係がある態様を包含する。
しかも、本発明は、列挙されたクレームの1以上からの1以上の限定、要素、節、および記述用語(descriptive terms)が、別のクレーム中へ導入される、すべての変動、組み合わせ、および順列を網羅する。例えば、別のクレームに従属するいずれのクレームも、同じ基本クレームに従属するいずれか他のクレーム中に見出される1以上の限定を包含するように修飾され得る。要素が、例として、マーカッシュ群形式において列挙されたものとして提示されている場合、要素の各下位群もまた開示されており、いずれの要素(単数または複数)も群から除去され得る。一般に、本発明、または本発明の側面が、特定の要素および/または特長を含むとして見なされる場合、本発明のある態様または本発明のある側面は、かかる要素および/または特長からなるか、または実質的にそれからなると理解されるべきである。簡潔さを目的として、それらの態様は、本明細書中、in haec verbaで具体的に表明されていない。用語「含むこと(comprising)」および「含有すること(containing)」が、オープンであることを意図し、追加の要素またはステップの包含を容認することにもまた留意する。範囲が与えられるとき、エンドポイントも包含される。しかも、別段の指示がないか、またはそれとは別に、文脈および当業者の理解から明らかでない場合に限り、範囲として表現された値は、いずれか具体的な値、または本発明の異なる態様において述べられた範囲内の部分範囲を、文脈が明確に別段の指図をしない限り範囲の下限の単位の10倍まで、想定し得る。
本出願は、種々の発行済み特許、公開特許出願、雑誌記事、および他の公刊物を参照し、これらのすべては参照によって本明細書に組み込まれる。組み込まれる参照のいずれかと本明細書との間に矛盾がある場合、本明細書がコントロールする(control)ものとする。加えて、先行技術に属する本発明のいずれか特定の態様は、クレームのいずれかの1以上からはっきりと除外され得る。かかる態様は当業者に知られていると思われるので、それらは、除外が本明細書においてはっきりと表明されていない場合であっても、除外され得る。本発明のいずれか特定の態様は、先行技術の存在に関するか否かにかかわらず、いずれかのクレームから、いずれかの理由で除外され得る。
当業者は、本明細書に記載の具体的な態様の多くの均等物を認識するか、またはせいぜいルーチンな実験法を使用して確かめる能力があるであろう。本明細書に記載の本態様の範囲は、上の記載に限定されることを意図せず、むしろ添付のクレームに表明されているとおりである。当業者は、以下のクレームにおいて定義されるとおり、本発明の精神または範囲から逸脱せずに、この記載への種々の変化および修飾がなされてもよいことを解するであろう。
Claims (136)
- 式(I):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;ただし、X1およびX2のうち少なくとも1個は、フルオロである;
Aは、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Raは、水素であるか、またはRcと結び合わされることで置換もしくは非置換の架橋環を形成している;
Rbは、水素であるか、またはRcと結び合わされることで置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで置換もしくは非置換の架橋環を形成している;
mは、0または1である;および
nは、0または1である、前記化合物またはその薬学的に許容し得る塩。 - 式中:X1が、水素である;およびX2が、フルオロである、請求項1に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、フルオロである;およびX2が、水素である、請求項1に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Aが、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである、
請求項1~3のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:Aが、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のアリールである、
請求項1~4のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:R1が、水素である;およびR2が、非置換のC1~4アルキルである;または
R1およびR2が一緒に、非置換のシクロアルキルを形成している、
請求項1~7のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:R1が、水素である;およびR2が、水素である、請求項1~8のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Ra、Rb、およびRcが各々、水素である、請求項1~9のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:mが、0である、請求項1~10のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:mが、1である、請求項1~10のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:nが、0である、請求項1~12のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:nが、1である、請求項1~12のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式(II):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
各Aは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである;
各R1は、独立して、水素、または置換もしくは非置換のアルキルである;
各R2は、独立して、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはRcと結び合わされることで置換もしくは非置換の架橋環を形成している;
Rbは、水素、置換もしくは非置換のアルキル、またはA(CR1R2)n-であるか、あるいはRcと結び合わされることで、置換もしくは非置換の架橋環を形成している;
Rcは、水素、または置換もしくは非置換のアルキルであるか、あるいはRaおよびRbのうち少なくとも1個と結び合わされることで、置換もしくは非置換の架橋環を形成している;および
各nは、独立して、0または1である、
前記化合物、またはその薬学的に許容し得る塩。 - 式中:X1およびX2のうち少なくとも1個が、フルオロである、請求項20に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、水素である;およびX2が、フルオロである、請求項20または21に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、フルオロである;およびX2が、水素である、請求項20または21に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Y1が、窒素である、請求項20~23のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Y1が、CHである、請求項20~23のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:各Aが、独立して、水素、非置換のC1~4アルキル、C1~4ハロアルキル、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のアリールである、
請求項20~25のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:Aが、置換もしくは非置換のシクロアルキル、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のアリールである、
請求項20~26のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:R1が、水素である;およびR2が、非置換のC1~4アルキルである;または
R1およびR2が一緒に、非置換のシクロアルキルを形成している、
請求項20~29のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:R1が、水素である;およびR2が、水素である、請求項20~30のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Rbが、水素、非置換のアルキル、またはA(CR1R2)n-である、請求項20~31のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Ra、Rb、およびRcが各々、水素である、請求項20~32のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:nが、0である、請求項1~33のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:nが、1である、請求項1~33のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1およびX2のうち少なくとも1個が、フルオロである、請求項45に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、水素である;およびX2が、フルオロである、請求項45または46に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、非置換のC1~4アルキルである、請求項45~47のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、水素である、請求項45~47のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 化合物が、式(IV):
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;ここで2個または3個のR4基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、n、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である、
請求項45に記載の化合物、またはその薬学的に許容し得る塩。 - 式中:X1が、水素である;およびX2が、フルオロである、請求項55に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、非置換のC1~4アルキルである、請求項55または56に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、水素である、請求項55~57のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Yが、-O-、-(CR3R4)-、または-NRa1-である、請求項55~58のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Yが、-(CR3R4)-である、請求項55~59のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R3およびR4の各出現が、独立して、水素、ハロゲン、置換もしくは非置換のアルキルである;式中2個または3個のR3基は、任意に結び合わされることで、置換もしくは非置換の架橋環を形成している、請求項55~60のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:mおよびnの和が、0、1、または2である、請求項55~61のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:kおよびqの和が、0、1、または2である、請求項55~62のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式(V):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
Y1は、窒素またはCRxである;
Y2は、窒素、CRd、結合、-CH2-、または-NH-である;
A1は、A2、Ra、およびRcのうち1個と結び合わされることで、置換または非置換の環を形成している;
A2は、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
R1は、水素、または置換もしくは非置換のアルキルであるか、あるいはR1は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;
R2は、水素、または置換もしくは非置換のアルキルであるか、あるいはR2は、Rd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している;あるいはR1およびR2は一緒に、カルボニルを形成している;
R3は、水素、または置換もしくは非置換のアルキルであるか、あるいはR3は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;
R4は、水素、または置換もしくは非置換のアルキルであるか、あるいはR4は、R1もしくはR2と結び合わされることで、置換または非置換の環を形成している;あるいはR3およびR4は一緒に、カルボニルを形成している;
Rxは、水素、または置換もしくは非置換のアルキルである;
Raは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rcは、水素であるか、またはA1と結び合わされることで、置換もしくは非置換の環を形成している;
Rdは、水素であるか、あるいはR3もしくはR4と結び合わされることで、置換または非置換の環を形成している;および
tは、0または1である、
前記化合物、またはその薬学的に許容し得る塩。 - 式中:X1およびX2のうち少なくとも1個が、フルオロである、請求項73に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、水素である;およびX2が、フルオロである、請求項73または74に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Y1が、窒素である、請求項73~75のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Y2が、窒素である、請求項73~76のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Y1が、窒素である;およびY2が、CRd、結合、または-CH2-である、請求項73~76のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:A1が、A2と結び合わされることで、置換もしくは非置換の5員または6員の環を形成している、請求項73~78のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:A1は、Raと結び合わされることで、置換もしくは非置換の5員または6員の環を形成している、請求項73~78のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:A1は、Rcと結び合わされることで、置換もしくは非置換の5員または6員の環である、請求項73~78のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素であるか、あるいはRd、R3、もしくはR4と結び合わされることで、置換または非置換の環を形成している、請求項73~79のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、水素である、請求項73~82のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R3が、水素であるか、あるいはR1もしくはR2と結び合わされることで、置換または非置換の環を形成している、請求項73~82のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R3が、水素である;およびR4が、水素である、請求項73~84のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:RaおよびRcが各々、水素である、請求項73~79または82~85のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:tが、1である、請求項73~86のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:tが、0である、請求項73~78または80~86のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式(VI):
X1は、水素またはフルオロである;
X2は、水素またはフルオロである;
R1は、水素、または置換もしくは非置換のアルキルである;
R2は、水素、または置換もしくは非置換のアルキルである;あるいはR1およびR2は一緒に、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換のシクロアルキルを形成している;および
Bは、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のカルボシクリル、置換もしくは非置換の多環式のスピロ環系、または置換もしくは非置換の架橋環系である、
前記化合物、またはその薬学的に許容し得る塩。 - 式中:X1およびX2のうち少なくとも1個が、フルオロである、請求項99に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:X1が、水素である;およびX2が、フルオロである、請求項99または100に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、非置換のC1~4アルキルである、請求項99~101のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:R1が、水素である;およびR2が、水素である、請求項99~101のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Bが、置換もしくは非置換のヘテロシクリル、または置換もしくは非置換の多環式のスピロ環系である、請求項99~103のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Bが、置換もしくは非置換の多環式のスピロ環系である、請求項99~104のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。
- 式中:Bが、
Yは、-O-、-S-、-NRa1-、または-(CR3R4)-である;
R3およびR4の各出現は、独立して、水素、ハロゲン、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、置換もしくは非置換のヘテロアルキル、-N(Ra1)2、-ORb1、-SRc1、または-CNである;ここで2個もしくは3個のR3基は、任意に結び合わされることで、置換または非置換の架橋環を形成している;ここで2個もしくは3個のR4基は、任意に結び合わされることで、置換または非置換の架橋環を形成している;
R5は、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、または窒素保護基である;
Ra1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または窒素保護基であるか、あるいは2個のRa1基は、結び合わされることで、置換もしくは非置換の複素環式の環を形成している;
Rb1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または酸素保護基である;
Rc1の各出現は、独立して、水素、置換もしくは非置換のアシル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のカルボシクリル、置換もしくは非置換のヘテロシクリル、または硫黄保護基である;
m、k、およびqは、各々独立して、0、1、または2である;および
p1およびp2は、各々独立して、0、1、2、3、または4である、
請求項99~105のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩。 - 請求項1~115のいずれか一項に記載の化合物、またはその薬学的に許容し得る塩と、薬学的に許容し得る賦形剤とを含む、医薬組成物。
- 疾患または障害の処置を、これを必要とする対象においてする方法であって、
疾患または障害が、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、あるいはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害であり、
方法が、請求項1~115のいずれか一項に記載の化合物、もしくはその薬学的に許容し得る塩、または請求項116に記載の医薬組成物を対象へ投与することを含む、前記方法。 - 疾患または障害が、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患である、請求項117に記載の方法。
- 神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患が、脆弱X症候群、シャルコー・マリー・トゥース病、アルツハイマー病、パーキンソン病、ハンチントン病、多発性硬化症、筋萎縮性側索硬化症、クロイツフェルト・ヤコブ病、レビー小体型認知症、血管性認知症、筋萎縮、発作誘発性の記憶喪失、統合失調症、ルビンシュタイン・テイビ症候群、レット症候群、注意欠陥多動性障害、失読症、双極性障害、自閉症に関連する社会障害、認知障害、および学習障害、注意欠陥障害、統合失調症、大うつ病性障害、末梢神経障害、糖尿病網膜症、糖尿病性末梢神経障害、化学療法誘発性の末梢神経障害、外傷性脳損傷(TBI)、慢性外傷性脳症(CTE)、またはタウオパチーである、請求項118に記載の方法。
- タウオパチーが、原発性年齢関連タウオパチー(PART)/神経原線維優位型老年認知症、慢性外傷性脳症、ボクサー認知症、進行性核上性麻痺、大脳皮質基底核変性症、ピック病、17番染色体と連関した前頭側頭型認知症およびパーキンソニズム、リティコ・ボディグ病、神経節膠腫、神経節細胞腫、髄膜血管腫症、脳炎後パーキンソニズム、亜急性硬化性全脳炎、鉛脳症、結節性硬化症、リポフスチン症、アルツハイマー病、または嗜銀性顆粒病である、請求項119に記載の方法。
- 疾患または障害が、がんである、請求項117に記載の方法。
- がんが、血液がんである、請求項121に記載の方法。
- がんが、白血病、T細胞リンパ腫、ホジキン病、非ホジキンリンパ腫、または多発性骨髄腫である、請求項122に記載の方法。
- がんが、固形腫瘍を含む、請求項123に記載の方法。
- がんが、神経膠腫、膠芽腫、非小細胞肺がん、脳腫瘍、神経芽細胞腫、骨腫瘍、軟部組織肉腫、頭頸部がん、尿生殖器がん、肺がん、乳房がん、膵臓がん、黒色腫、胃がん、脳がん、肝臓がん、甲状腺がん、明細胞癌、子宮がん、または卵巣がんである、請求項124に記載の方法。
- 追加の治療剤を投与することをさらに含む、請求項117~125のいずれか一項に記載の方法。
- 疾患または障害の処置を、これを必要とする対象において使用するための、請求項1~115のいずれか一項に記載の化合物であって、疾患または障害が、増殖性疾患、炎症性疾患、感染性疾患、自己免疫疾患、異種免疫疾患、神経学的障害、代謝疾患、嚢胞性線維症、多発性嚢胞腎疾患、肺高血圧症、心機能障害、あるいはT細胞の調節異常によって媒介されるかもしくはこれと連関した疾患または障害である、前記化合物。
- 疾患または障害が、神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患である、請求項127に記載の化合物。
- 神経変性疾患、神経発達疾患、神経精神疾患、または神経障害疾患が、脆弱X症候群、シャルコー・マリー・トゥース病、アルツハイマー病、パーキンソン病、ハンチントン病、多発性硬化症、筋萎縮性側索硬化症、クロイツフェルト・ヤコブ病、レビー小体型認知症、血管性認知症、筋萎縮、発作誘発性の記憶喪失、統合失調症、ルビンシュタイン・テイビ症候群、レット症候群、注意欠陥多動性障害、失読症、双極性障害、自閉症に関連する社会障害、認知障害、および学習障害、注意欠陥障害、統合失調症、大うつ病性障害、末梢神経障害、糖尿病網膜症、糖尿病性末梢神経障害、化学療法誘発性の末梢神経障害、外傷性脳損傷(TBI)、慢性外傷性脳症(CTE)、またはタウオパチーである、請求項128に記載の化合物。
- タウオパチーが、原発性年齢関連タウオパチー(PART)/神経原線維優位型老年認知症、慢性外傷性脳症、ボクサー認知症、進行性核上性麻痺、大脳皮質基底核変性症、ピック病、17番染色体と連関した前頭側頭型認知症およびパーキンソニズム、リティコ・ボディグ病、神経節膠腫、神経節細胞腫、髄膜血管腫症、脳炎後パーキンソニズム、亜急性硬化性全脳炎、鉛脳症、結節性硬化症、リポフスチン症、アルツハイマー病、または嗜銀性顆粒病である、請求項129に記載の化合物。
- 疾患または障害は、がんである、請求項127に記載の化合物。
- がんが、血液がんである、請求項131に記載の化合物。
- がんが、白血病、T細胞リンパ腫、ホジキン病、非ホジキンリンパ腫、または多発性骨髄腫である、請求項132に記載の化合物。
- がんが、固形腫瘍を含む、請求項131に記載の化合物。
- がんが、神経膠腫、膠芽腫、非小細胞肺がん、脳腫瘍、神経芽細胞腫、骨腫瘍、軟部組織肉腫、頭頸部がん、尿生殖器がん、肺がん、乳房がん、膵臓がん、黒色腫、胃がん、脳がん、肝臓がん、甲状腺がん、明細胞癌、子宮がん、または卵巣がんである、請求項134に記載の化合物。
- 請求項1~115のいずれか一項に記載の化合物、もしくはその薬学的に許容し得る塩、または請求項116に記載の医薬組成物;および化合物、その薬学的に許容し得る塩、または医薬組成物を対象へ投与するための指示を含む、キット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962880284P | 2019-07-30 | 2019-07-30 | |
| US62/880,284 | 2019-07-30 | ||
| PCT/US2020/044148 WO2021021979A2 (en) | 2019-07-30 | 2020-07-30 | Hdac6 inhibitors and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2022543106A true JP2022543106A (ja) | 2022-10-07 |
Family
ID=74229821
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022506695A Pending JP2022543106A (ja) | 2019-07-30 | 2020-07-30 | Hdac6インヒビターおよびそれらの使用 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US12528767B2 (ja) |
| EP (1) | EP4003319A4 (ja) |
| JP (1) | JP2022543106A (ja) |
| CN (1) | CN114727974A (ja) |
| AU (2) | AU2020321955A1 (ja) |
| CA (1) | CA3149096A1 (ja) |
| WO (1) | WO2021021979A2 (ja) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2536650A (en) | 2015-03-24 | 2016-09-28 | Augmedics Ltd | Method and system for combining video-based and optic-based augmented reality in a near eye display |
| US10357493B2 (en) | 2017-03-10 | 2019-07-23 | Selenity Therapeutics (Bermuda), Ltd. | Metalloenzyme inhibitor compounds |
| US12458411B2 (en) | 2017-12-07 | 2025-11-04 | Augmedics Ltd. | Spinous process clamp |
| US12521201B2 (en) | 2017-12-07 | 2026-01-13 | Augmedics Ltd. | Spinous process clamp |
| US11980507B2 (en) | 2018-05-02 | 2024-05-14 | Augmedics Ltd. | Registration of a fiducial marker for an augmented reality system |
| US11766296B2 (en) | 2018-11-26 | 2023-09-26 | Augmedics Ltd. | Tracking system for image-guided surgery |
| US11980506B2 (en) | 2019-07-29 | 2024-05-14 | Augmedics Ltd. | Fiducial marker |
| US12178666B2 (en) | 2019-07-29 | 2024-12-31 | Augmedics Ltd. | Fiducial marker |
| JP2022543106A (ja) | 2019-07-30 | 2022-10-07 | エイコニゾ セラピューティクス,インコーポレーテッド | Hdac6インヒビターおよびそれらの使用 |
| US11382712B2 (en) | 2019-12-22 | 2022-07-12 | Augmedics Ltd. | Mirroring in image guided surgery |
| US11389252B2 (en) | 2020-06-15 | 2022-07-19 | Augmedics Ltd. | Rotating marker for image guided surgery |
| US12502163B2 (en) | 2020-09-09 | 2025-12-23 | Augmedics Ltd. | Universal tool adapter for image-guided surgery |
| US12239385B2 (en) | 2020-09-09 | 2025-03-04 | Augmedics Ltd. | Universal tool adapter |
| WO2022169985A1 (en) * | 2021-02-03 | 2022-08-11 | Eikonizo Therapeutics, Inc. | Hdac6 inhibitors and uses thereof |
| US11896445B2 (en) | 2021-07-07 | 2024-02-13 | Augmedics Ltd. | Iliac pin and adapter |
| US12150821B2 (en) | 2021-07-29 | 2024-11-26 | Augmedics Ltd. | Rotating marker and adapter for image-guided surgery |
| WO2023021451A1 (en) | 2021-08-18 | 2023-02-23 | Augmedics Ltd. | Augmented reality assistance for osteotomy and discectomy |
| WO2023150203A1 (en) * | 2022-02-03 | 2023-08-10 | Eikonizo Therapeutics, Inc. | Hdac6 inhibitors and uses thereof |
| EP4511809A1 (en) | 2022-04-21 | 2025-02-26 | Augmedics Ltd. | Systems and methods for medical image visualization |
| WO2024057210A1 (en) | 2022-09-13 | 2024-03-21 | Augmedics Ltd. | Augmented reality eyewear for image-guided medical intervention |
| CN117169379A (zh) * | 2023-09-06 | 2023-12-05 | 河南逸祥卫生科技有限公司 | 一种湿巾中西吡氯铵含量检测方法 |
| CN118027033A (zh) * | 2024-01-26 | 2024-05-14 | 四川大学 | 一种hdac6抑制剂及其制备方法和在抗炎和溃疡性结肠炎中的用途 |
| CN118806740B (zh) * | 2024-07-16 | 2025-06-06 | 徐州医科大学 | 小分子化合物在制备治疗肿瘤的药物中的应用 |
Family Cites Families (330)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4205085A (en) | 1978-03-09 | 1980-05-27 | American Cyanamid Company | Hypolipidemic and antiatherosclerotic 4-(polyfluoroalkylamino)phenyl compounds |
| EP0093488A3 (en) | 1982-03-18 | 1984-05-23 | Beecham Group Plc | Nortropyl benzopyrrolinone compounds, process for their preparation and pharmaceutical compositions containing them |
| DE3929233A1 (de) | 1989-09-02 | 1991-03-07 | Bayer Ag | 5-heterocyclyl-pyridin-3-carbon-benzylamide und -anilide |
| DE4029466A1 (de) | 1989-09-18 | 1991-03-28 | Ciba Geigy Ag | Neue unkrautbekaempfungsmittel |
| DE4025891A1 (de) | 1990-08-16 | 1992-02-20 | Bayer Ag | Pyrimidyl-substituierte acrylsaeureester |
| JPH04272989A (ja) | 1991-02-27 | 1992-09-29 | Canon Inc | 液晶組成物、それを有する液晶素子、それ等を用いた表示方法及び表示装置 |
| US5272158A (en) | 1991-10-29 | 1993-12-21 | Merck & Co., Inc. | Fibrinogen receptor antagonists |
| CH683522A5 (de) | 1992-03-13 | 1994-03-31 | Hoffmann La Roche | Verfahren zur Herstellung von Diarylen. |
| JP3187611B2 (ja) | 1993-05-17 | 2001-07-11 | キヤノン株式会社 | 液晶性化合物、これを含む液晶組成物、それを有する液晶素子、それらを用いた表示方法および表示装置 |
| CN1076345C (zh) | 1993-10-19 | 2001-12-19 | 住友制药株式会社 | 2,3-二氨基丙酸衍生物 |
| JPH07206829A (ja) | 1994-01-12 | 1995-08-08 | Nippon Soda Co Ltd | イミダゾリン化合物および除草剤 |
| JPH07278545A (ja) | 1994-04-14 | 1995-10-24 | Chisso Corp | ネマテック液晶組成物 |
| US5728844A (en) | 1995-08-29 | 1998-03-17 | Celgene Corporation | Immunotherapeutic agents |
| US5728845A (en) | 1995-08-29 | 1998-03-17 | Celgene Corporation | Immunotherapeutic nitriles |
| WO1997040017A2 (en) | 1996-04-19 | 1997-10-30 | Novo Nordisk A/S | Modulators of molecules with phosphotyrosine recognition units |
| JPH10251255A (ja) | 1997-03-14 | 1998-09-22 | Nissan Chem Ind Ltd | アジン誘導体 |
| NZ337698A (en) | 1997-04-04 | 2001-07-27 | Pfizer Prod Inc | Nicotinamide derivatives for selective inhibition of phosphodiesterase type 4 (PDE4) and the production of tumour necrosis factor (TNF) useful for the treatment of respiratory, rheumatoid and allergic diseases |
| DE19744792A1 (de) | 1997-10-10 | 1999-04-15 | Hoechst Ag | Triptycenderivate und ihre Verwendung für optoelektronische Anwendungen, insbesondere als Elektrolumineszenzmaterialien |
| JP2002524562A (ja) | 1998-09-16 | 2002-08-06 | ダウ・アグロサイエンス・エル・エル・シー | 殺菌・殺カビ剤としての、ピリジン環上に5員複素環式環を有する2−メトキシイミノ−2−(ピリジニルオキシメチル)フェニルアセトアミド |
| AU4589800A (en) | 1999-05-05 | 2000-11-21 | Darwin Discovery Limited | 9-(1,2,3,4-tetrahydronaphthalen-1-yl)-1,9-dihydropurin-6-one derivatives as pde7inhibitors |
| AU2001249399A1 (en) | 2000-03-24 | 2001-10-08 | Cor Therapeutics, Inc. | Isoquinolone inhibitors of factor xa |
| WO2001085695A1 (en) | 2000-05-11 | 2001-11-15 | Bristol-Myers Squibb Co. | Tetrahydroisoquinoline analogs useful as growth hormone secretagogues |
| CA2414976A1 (en) | 2000-07-04 | 2002-01-10 | Takeda Chemical Industries, Ltd. | Gpr14 antagonistic agent |
| AU2001290131B2 (en) | 2000-09-29 | 2007-11-15 | Topotarget Uk Limited | Carbamic acid compounds comprising a sulfonamide linkage as HDAC inhibitors |
| GB0023983D0 (en) | 2000-09-29 | 2000-11-15 | Prolifix Ltd | Therapeutic compounds |
| EP1598067B1 (en) | 2000-09-29 | 2009-05-06 | TopoTarget UK Limited | Carbamic acid compounds comprising an amide linkage for the treatment of malaria |
| JP2002305083A (ja) | 2001-04-04 | 2002-10-18 | Mitsubishi Chemicals Corp | 有機電界発光素子 |
| ES2296926T3 (es) | 2001-06-06 | 2008-05-01 | Aventis Pharma Limited | Tetrahidroisoquinolinas sustituidas para usar en el tratamiento de enfermedades inflamatorias. |
| US6897220B2 (en) | 2001-09-14 | 2005-05-24 | Methylgene, Inc. | Inhibitors of histone deacetylase |
| KR20100107509A (ko) | 2001-09-14 | 2010-10-05 | 9222-9129 퀘벡 인코포레이티드 | 히스톤 데아세틸라아제의 억제제 |
| AU2002357692A1 (en) | 2001-11-09 | 2003-05-26 | Bristol-Myers Squibb Company | Tetrahydroisoquinoline analogs as modulators of chemokine receptor activity |
| US7619012B2 (en) | 2006-07-18 | 2009-11-17 | The Regents Of The University Of California | Method and apparatus for steam hydro-gasification in a fluidized bed reactor |
| US7928121B2 (en) | 2002-02-19 | 2011-04-19 | Laboratorios Del Dr. Esteve, S.A. | 5-HT7 receptor antagonists |
| EP1676844A1 (en) | 2004-12-28 | 2006-07-05 | Laboratorios Del Dr. Esteve, S.A. | 5-HT7 receptor antagonists |
| AU2003217810C9 (en) | 2002-02-28 | 2008-06-12 | Icagen, Inc. | Methods for treating diseases related to intraocular pressure |
| MXPA04009490A (es) | 2002-04-03 | 2005-06-08 | Topo Target Uk Ltd | Compuesto de acido carbamico que comprenden un enlace de piperazina como inhibidores de histona desacetilasa. |
| EP1676840A1 (en) | 2004-12-28 | 2006-07-05 | Laboratorios Del Dr. Esteve, S.A. | 5-HT7 Receptor antagonists |
| US7553965B2 (en) | 2002-11-07 | 2009-06-30 | Laboratories Del Dr. Esteve, S.A. | 5-HT7 receptor antagonists |
| AU2004205372B2 (en) | 2003-01-17 | 2011-02-24 | Topotarget Uk Limited | Hydroxamic acid compounds comprising an ester or ketone linkage as HDAC inhibitors |
| AU2004215624B2 (en) | 2003-02-25 | 2011-06-02 | Topotarget Uk Limited | Hydroxamic acid compounds comprising a bicyclic heteroaryl group as HDAC inhibitors |
| US7169801B2 (en) | 2003-03-17 | 2007-01-30 | Takeda San Diego, Inc. | Histone deacetylase inhibitors |
| DE10312963A1 (de) | 2003-03-24 | 2004-10-07 | Aventis Pharma Deutschland Gmbh | Substituierte 4-Phenyltetrahydroisochinoline, Verfahren zu ihrer Herstellung, ihre Verwendung als Medikament, sowie sie enthaltendes Medikament |
| GB0310865D0 (en) | 2003-05-12 | 2003-06-18 | Black James Foundation | Gastrin and cholecystokinin receptor ligands |
| GB0315111D0 (en) | 2003-06-27 | 2003-07-30 | Cancer Rec Tech Ltd | Substituted 5-membered ring compounds and their use |
| AU2004268621C1 (en) | 2003-08-29 | 2011-08-18 | Exelixis, Inc. | c-Kit modulators and methods of use |
| EP2251327B1 (en) | 2003-11-19 | 2014-02-12 | Array Biopharma, Inc. | Heterocyclic inhibitors of mek |
| WO2005066151A2 (en) | 2003-12-19 | 2005-07-21 | Takeda San Diego, Inc. | Histone deacetylase inhibitors |
| US20050159470A1 (en) | 2003-12-19 | 2005-07-21 | Syrrx, Inc. | Histone deacetylase inhibitors |
| US20050165015A1 (en) | 2004-01-23 | 2005-07-28 | Ncube Mghele V. | Vanilloid receptor ligands and their use in treatments |
| KR101258504B1 (ko) | 2004-03-26 | 2013-04-26 | 메틸진 인코포레이티드 | 히스톤 데아세틸라제의 억제제 |
| EP1776357A1 (en) | 2004-08-09 | 2007-04-25 | Astellas Pharma Inc. | Hydroxyamide compounds having activity as inhibitors of histone deacetylase (hdac) |
| EP1630158A1 (en) | 2004-08-18 | 2006-03-01 | Laboratorios Del Dr. Esteve, S.A. | 5-HT7 receptor antagonists |
| EP1630159A1 (en) | 2004-08-18 | 2006-03-01 | Laboratorios Del Dr. Esteve, S.A. | 5-HT7 receptor antagonists |
| GB0519957D0 (en) | 2005-09-30 | 2005-11-09 | Sb Pharmco Inc | Chemical compound |
| WO2006065842A2 (en) | 2004-12-13 | 2006-06-22 | Synta Pharmaceuticals Corp. | 5,6,7,8-tetrahydroquinolines and related compounds and uses thereof |
| WO2006066133A2 (en) | 2004-12-16 | 2006-06-22 | Takeda San Diego, Inc. | Histone deacetylase inhibitors |
| SG159528A1 (en) | 2005-02-04 | 2010-03-30 | Senomyx Inc | Compounds comprising linked hetero aryl moieties and their use as novel umami flavor modifiers, tastants and taste enhancers for comestible compositions |
| CA2596522A1 (en) | 2005-02-15 | 2006-08-24 | Novo Nordisk A/S | 3,4-dihydro-1h-isoquinoline-2-carboxylic acid 5-aminopyridin-2-yl esters |
| CN103110635A (zh) | 2005-07-04 | 2013-05-22 | 海波因特制药有限责任公司 | 组胺h3受体拮抗剂 |
| WO2007011626A2 (en) | 2005-07-14 | 2007-01-25 | Takeda San Diego, Inc. | Histone deacetylase inhibitors |
| GB0518237D0 (en) | 2005-09-07 | 2005-10-19 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| AU2006311433B2 (en) | 2005-11-08 | 2012-06-28 | Choongwae Pharma Corporation | Alpha-helix mimetics and method relating to the treatment of cancer stem cells |
| JP2009525955A (ja) | 2006-01-13 | 2009-07-16 | タケダ サン ディエゴ インコーポレイテッド | ヒストンデアセチラーゼ阻害剤 |
| AR059037A1 (es) | 2006-01-17 | 2008-03-12 | Schering Corp | Compuestos para el tratamiento de trastornos inflamatorios |
| GB0603041D0 (en) | 2006-02-15 | 2006-03-29 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| US8232399B2 (en) | 2006-03-02 | 2012-07-31 | Chao-Jun Li | Chiral ligands, their preparation and uses thereof in asymmetric reactions |
| US20080004282A1 (en) | 2006-04-10 | 2008-01-03 | Painceptor Pharma Corporation | Compositions and methods for modulating gated ion channels |
| WO2008016123A1 (en) | 2006-08-03 | 2008-02-07 | Takeda Pharmaceutical Company Limited | GSK-3β INHIBITOR |
| US7820711B2 (en) | 2006-11-14 | 2010-10-26 | Pharmacyclics Inc. | Uses of selective inhibitors of HDAC8 for treatment of T-cell proliferative disorders |
| WO2008063888A2 (en) | 2006-11-22 | 2008-05-29 | Plexxikon, Inc. | Compounds modulating c-fms and/or c-kit activity and uses therefor |
| CN101610996A (zh) | 2006-12-19 | 2009-12-23 | 梅特希尔基因公司 | 组蛋白脱乙酰酶抑制剂及其前体药物 |
| US20080186971A1 (en) | 2007-02-02 | 2008-08-07 | Tarari, Inc. | Systems and methods for processing access control lists (acls) in network switches using regular expression matching logic |
| EP2148878A4 (en) | 2007-04-20 | 2011-08-10 | Merck Canada Inc | NEW HETEROAROMATIC COMPOUNDS AS INHIBITORS OF STEAROYL-COENZYME-A-DELTA-9-DESATURASE |
| TW200920372A (en) | 2007-07-13 | 2009-05-16 | Genelabs Tech Inc | Anti-viral compounds, compositions, and methods of use |
| US20090197880A1 (en) | 2007-07-13 | 2009-08-06 | Genelabs Technologies, Inc. | Anti-viral compounds, compositions, and methods of use |
| EP2195029A2 (en) | 2007-08-24 | 2010-06-16 | Oryzon Genomics SA | Treatment and prevention of neurodegenerative diseases |
| US8183378B2 (en) | 2007-11-07 | 2012-05-22 | Chao-Jun Li | Ligands, their preparation and uses thereof in asymmetric reactions |
| CA2709883A1 (en) | 2007-12-19 | 2009-06-25 | The Scripps Research Institute | Benzimidazoles and analogs as rho kinase inhibitors |
| EP2100879A1 (en) * | 2008-03-13 | 2009-09-16 | 4Sc Ag | Novel N-substituted tetrahydroisoquinoline/isoindoline hydroxamic acid compounds |
| WO2009129036A1 (en) | 2008-04-14 | 2009-10-22 | Merck & Co., Inc. | Substituted cyclopropyl compounds, compositions containing such compounds and methods of treatment |
| CA2721218C (en) | 2008-04-15 | 2015-03-24 | Pharmacyclics, Inc. | Selective inhibitors of histone deacetylase |
| ES2620027T3 (es) | 2008-09-03 | 2017-06-27 | Biomarin Pharmaceutical Inc. | Composiciones que incluyen derivados del ácido 6-aminohexanoico como inhibidores de HDAC |
| WO2010033906A2 (en) | 2008-09-19 | 2010-03-25 | President And Fellows Of Harvard College | Efficient induction of pluripotent stem cells using small molecule compounds |
| US20110212943A1 (en) | 2008-10-15 | 2011-09-01 | Orchid Research Laboratories Limited | Novel bridged cyclic compounds as histone deacetylase inhibitors |
| US8759362B2 (en) | 2008-10-24 | 2014-06-24 | Purdue Pharma L.P. | Bicycloheteroaryl compounds and their use as TRPV1 ligands |
| WO2010054278A2 (en) | 2008-11-10 | 2010-05-14 | Schering Corporation | Compounds for the treatment of inflammatory disorders |
| WO2010075551A1 (en) | 2008-12-24 | 2010-07-01 | Massachusetts Institute Of Technology | Compositions of modulators of the wnt/beta-catenin pathway and benzamide and/or hydroxamic acid derivatives to treat bipolar disorder |
| EP3351248B1 (en) | 2008-12-31 | 2021-06-09 | Ardelyx, Inc. | Compounds and methods for inhibiting nhe-mediated antiport in the treatment of disorders associated with fluid retention or salt overload and gastrointestinal tract disorders |
| TW201030002A (en) | 2009-01-16 | 2010-08-16 | Bristol Myers Squibb Co | Bicyclic compounds for the reduction of beta-amyloid production |
| WO2010086311A1 (en) | 2009-01-28 | 2010-08-05 | Bayer Cropscience Ag | Fungicide n-cycloalkyl-n-bicyclicmethylene-carboxamide derivatives |
| WO2010088408A2 (en) | 2009-01-28 | 2010-08-05 | Emory University | Subunit selective nmda receptor antagonists for the treatment of neurological conditions |
| GB0904287D0 (en) | 2009-03-12 | 2009-04-22 | Prosidion Ltd | Compounds for the treatment of metabolic disorders |
| EA201171293A1 (ru) | 2009-04-24 | 2012-05-30 | Глэксо Груп Лимитед | 3-азабицикло[4.1.0]гептаны, применяемые в качестве антагонистов орексина |
| JP2011008205A (ja) | 2009-05-27 | 2011-01-13 | Fujifilm Corp | 二軸性光学異方性膜を作製するための組成物 |
| EP2438052A1 (en) | 2009-06-05 | 2012-04-11 | Oslo University Hospital HF | Azole derivatives as wtn pathway inhibitors |
| US9096518B2 (en) | 2009-06-22 | 2015-08-04 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| WO2011002520A2 (en) | 2009-07-02 | 2011-01-06 | Angion Biomedica Corp. | Small molecule inhibitors of parp activity |
| CN103492391A (zh) | 2009-09-25 | 2014-01-01 | 沃泰克斯药物股份有限公司 | 用于制备用作蛋白激酶抑制剂的嘧啶衍生物的方法 |
| WO2011058582A1 (en) | 2009-11-16 | 2011-05-19 | Orchid Research Laboratories Ltd. | Histone deacetylase inhibitors for the treatment of fungal infections |
| JP2013517279A (ja) | 2010-01-13 | 2013-05-16 | テンペロ、ファーマシューティカルズ、インコーポレイテッド | 化合物及び方法 |
| JP2013517281A (ja) | 2010-01-13 | 2013-05-16 | テンペロ、ファーマシューティカルズ、インコーポレイテッド | 化合物及び方法 |
| EP2533783B8 (en) | 2010-01-13 | 2015-12-16 | Tempero Pharmaceuticals, Inc. | COMPOUNDS AND METHODS for the inhibition of HDAC |
| JP2011148714A (ja) | 2010-01-19 | 2011-08-04 | Nippon Soda Co Ltd | 病害防除方法 |
| US20110212969A1 (en) | 2010-02-26 | 2011-09-01 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| WO2011130163A1 (en) | 2010-04-12 | 2011-10-20 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| AR081331A1 (es) | 2010-04-23 | 2012-08-08 | Cytokinetics Inc | Amino- pirimidinas composiciones de las mismas y metodos para el uso de los mismos |
| US9133123B2 (en) | 2010-04-23 | 2015-09-15 | Cytokinetics, Inc. | Certain amino-pyridines and amino-triazines, compositions thereof, and methods for their use |
| US9518032B2 (en) | 2010-04-30 | 2016-12-13 | Dana-Farber Cancer Institute, Inc. | Small molecule inhibitors of USP1 deubiquitinating enzyme activity |
| US8513421B2 (en) | 2010-05-19 | 2013-08-20 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| MX2012014382A (es) | 2010-06-09 | 2013-01-29 | Janssen Pharmaceutica Nv | Derivados de 5-amino-3, 6-dihidro-1h-pirazin-2-ona utiles como inhibidores de beta-secretasa (bace). |
| CN102933564B (zh) | 2010-06-09 | 2015-07-22 | 詹森药业有限公司 | 用作β-分泌酶(BACE)抑制剂的5,6-二氢-2H-[1,4]噁嗪-3-基-胺衍生物 |
| US20120015942A1 (en) | 2010-07-19 | 2012-01-19 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| WO2012027564A1 (en) | 2010-08-26 | 2012-03-01 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| MY160138A (en) | 2010-09-22 | 2017-02-28 | Janssen Pharmaceutica Nv | 4,7-dihydro-pyrazolo[1,5-a]pyrazin-6-ylamine derivatives useful as inhibitors of beta-secretase (bace) |
| JP2013540767A (ja) | 2010-10-07 | 2013-11-07 | ザ ジェイ. デヴィッド グラッドストーン インスティテューツ | 免疫不全ウイルス転写を調節するための組成物および方法 |
| EP2624832B1 (en) | 2010-10-08 | 2017-09-27 | Vib Vzw | Hdac inhibitors to treat charcot-marie-tooth disease |
| WO2012054332A1 (en) | 2010-10-18 | 2012-04-26 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| CN103429574B (zh) | 2010-11-16 | 2016-11-16 | 阿塞蒂隆制药公司 | 作为蛋白质去乙酰化酶抑制剂的嘧啶羟基酰胺化合物和其使用方法 |
| JP2013544874A (ja) | 2010-12-08 | 2013-12-19 | オスロ ユニヴァーシティー ホスピタル エイチエフ | Wntシグナル伝達経路阻害薬としてのトリアゾール誘導体 |
| ES2648143T3 (es) | 2010-12-22 | 2017-12-28 | Janssen Pharmaceutica Nv | Derivados de 5,6-dihidro-imidazo[1,2-a]pirazin-8-ilamina útiles como inhibidores de la beta-secretasa (BACE) |
| WO2012088015A2 (en) | 2010-12-22 | 2012-06-28 | Millennium Pharmaceuticals, Inc. | Substituted hydroxamic acids and uses thereof |
| TW201245115A (en) | 2011-01-24 | 2012-11-16 | Chdi Foundation Inc | Histone deacetylase inhibitors and compositions and methods of use thereof |
| ES2597972T3 (es) | 2011-02-08 | 2017-01-24 | Pfizer Inc | Modulador del receptor de glucagón |
| CA2824360C (en) | 2011-03-01 | 2020-01-14 | Janssen Pharmaceutica Nv | 6,7-dihydro-pyrazolo[1,5-a]pyrazin-4-ylamine derivatives useful as inhibitors of beta-secretase (bace) |
| BR112013022917A2 (pt) | 2011-03-09 | 2016-12-06 | Janssen Pharmaceutica Nv | derivados 3,4-dihidro-pirrolo[1,2-a]pirazino-1-ilamina úteis como inibidores de beta-secretase (bace) |
| CN103597039B (zh) | 2011-03-15 | 2017-05-03 | 雷蒙特亚特特拉维夫大学有限公司 | 可活化的发荧光的化合物及其作为近红外探针的用途 |
| WO2012136111A1 (zh) | 2011-04-02 | 2012-10-11 | 中国人民解放军军事医学科学院毒物药物研究所 | 苯丙酸化合物、其制备方法及其医药用途 |
| JP6113151B2 (ja) | 2011-05-17 | 2017-04-12 | プレキシコン インコーポレーテッドPlexxikon Inc. | キナーゼ調節およびその適応症 |
| KR101348900B1 (ko) | 2011-05-19 | 2014-01-07 | 광주과학기술원 | 신규한 헤테로방향족 화합물 및 이의 용도 |
| ES2602813T3 (es) | 2011-06-09 | 2017-02-22 | Rhizen Pharmaceuticals S.A. | Nuevos compuestos como moduladores de GPR-119 |
| EP2723338A2 (en) | 2011-06-24 | 2014-04-30 | The Trustees of Stevens Institute of Technology | Selective inhibitors of histone deacetylase isoform 6 and methods thereof |
| WO2013006408A1 (en) | 2011-07-01 | 2013-01-10 | Tempero Pharmaceuticals, Inc. | Compounds and methods |
| MX2014000341A (es) | 2011-07-08 | 2014-05-01 | Novartis Ag | Novedosos derivados de trifluoro-metil-oxadiazol y su uso en el tratamiento de enfermedades. |
| WO2013009827A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013009810A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013009830A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013009812A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc | Methods of treatment |
| WO2013059582A2 (en) | 2011-10-20 | 2013-04-25 | Nupotential, Inc. | Small molecule inhibitors of histone deacteylases |
| WO2013063549A1 (en) | 2011-10-28 | 2013-05-02 | Vanderbilt University | Substituted 2-(4-heterocyclylbenzyl)isoindolin-1-one analogs as positive allosteric modulators of the muscarinic acetylcholine receptor m1 |
| CA2846066A1 (en) | 2011-10-28 | 2013-05-02 | Chong Kun Dang Pharmaceutical Corp. | Hydroxamate derivatives for hdac inhibitor, and the pharmaceutical composition comprising thereof |
| WO2013066833A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods to inhibit histone deacetylase (hdac) enzymes |
| WO2013066836A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066832A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066834A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066839A2 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066835A2 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066838A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066831A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| CN103102322B (zh) | 2011-11-14 | 2016-02-24 | 上海交通大学 | 噁唑类化合物及其制备方法、药物组合物及其用途 |
| JP5966014B2 (ja) | 2011-11-28 | 2016-08-10 | ノバルティス アーゲー | 新規トリフルオロメチル−オキサジアゾール誘導体および疾患の処置におけるその使用 |
| WO2013085890A1 (en) | 2011-12-06 | 2013-06-13 | Glaxo Group Limited | Therapeutic methods |
| CA2862259A1 (en) | 2011-12-29 | 2013-07-04 | Pharmacyclics, Inc. | Cinnamic acid hydroxyamides as inhibitors of histone deacetylase 8 |
| JP6352244B2 (ja) | 2012-04-11 | 2018-07-04 | サイトキネティックス, インコーポレイテッド | 骨格筋疲労に対する耐性を向上させるための方法 |
| US9227972B2 (en) | 2012-05-09 | 2016-01-05 | Merck Sharp & Dohme Corp. | Aliphatic spirolactam CGRP receptor antagonists |
| WO2013185353A1 (en) | 2012-06-15 | 2013-12-19 | Curegenix Inc. | Compound as wnt signaling inhibitor, composition, and use thereof |
| AR091773A1 (es) | 2012-07-16 | 2015-02-25 | Chdi Foundation Inc | Inhibidores de la histona desacetilasa y composiciones y sus metodos de uso |
| FR3000491B1 (fr) | 2012-09-27 | 2015-08-28 | Univ Lille Ii Droit & Sante | Composes utilisables dans le traitement des infections mycobacteriennes |
| WO2014059306A1 (en) | 2012-10-12 | 2014-04-17 | The Trustees Of The University Of Pennsylvania | Pyrimidine hydroxy amide compounds as protein deacetylase inhibitors and methods of use thereof |
| US9914717B2 (en) | 2012-12-20 | 2018-03-13 | The Broad Institute, Inc. | Cycloalkenyl hydroxamic acid derivatives and their use as histone deacetylase inhibitors |
| US20160031863A1 (en) | 2013-03-14 | 2016-02-04 | Chdi Foundation, Inc. | Histone deacetylase inhibitors and compositions and methods of use thereof |
| EP2968233A4 (en) | 2013-03-14 | 2016-08-03 | Chdi Foundation Inc | HISTON DEACETYLASE HEMMER AND COMPOSITIONS AND METHOD FOR USE THEREOF |
| US9617259B2 (en) | 2013-03-14 | 2017-04-11 | Chdi Foundation, Inc. | Histone deacetylase inhibitors and compositions and methods of use thereof |
| EP2968232B1 (en) | 2013-03-14 | 2018-12-05 | CHDI Foundation, Inc. | Histone deacetylase inhibitors and compositions and methods of use thereof |
| CN105263920B (zh) | 2013-04-15 | 2017-09-26 | 杜邦公司 | 杀真菌酰胺 |
| NZ712696A (en) | 2013-04-29 | 2016-07-29 | Chong Kun Dang Pharm Corp | Novel compounds for selective histone deacetylase inhibitors, and pharmaceutical composition comprising the same |
| EP2801569A1 (en) | 2013-05-09 | 2014-11-12 | Ikerchem, S.L. | Histone deacetylase inhibitors based on derivatives of tricyclic polyhydroacridine and analogs possessing fused saturated five- and seven-membered rings |
| WO2014181137A1 (en) | 2013-05-10 | 2014-11-13 | Karus Therapeutics Ltd | Novel histone deacetylase inhibitors |
| US9918983B2 (en) | 2013-05-30 | 2018-03-20 | The Board Of Regents Of The Nevada System Of Higher Education On Behalf Of The University Of Nevada, Las Vegas | Suicidal LSD1 inhibitors targeting SOX2-expressing cancer cells |
| TW201534586A (zh) | 2013-06-11 | 2015-09-16 | Orion Corp | 新穎cyp17抑制劑/抗雄激素劑 |
| US20160067241A1 (en) | 2013-06-13 | 2016-03-10 | Dennis M. Brown | Compositions and methods to improve the therapeutic benefit of suboptimally administered chemical compounds including substituted naphthalimides such as amonafide for the treatment of immunological, metabolic, infectious, and benign or neoplastic hyperproliferative disease conditions |
| WO2015017546A1 (en) | 2013-07-30 | 2015-02-05 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Selective histone deactylase 6 inhibitors |
| BR112016007589A2 (pt) | 2013-10-08 | 2017-09-12 | Bayer Cropscience Ag | n-hetaril(tio)carbonil-2-(benzocicloalquen-1-il)ciclaminas e seu uso como fungicidas |
| WO2015058106A1 (en) | 2013-10-18 | 2015-04-23 | The General Hospital Corporation | Imaging histone deacetylases with a radiotracer using positron emission tomography |
| US9650379B2 (en) | 2013-12-12 | 2017-05-16 | Chong Kun Dang Pharmaceutical Corp. | Azaindole derivatives as selective histone deacetylase (HDAC) inhibitors and pharmaceutical compositions comprising the same |
| KR101685639B1 (ko) | 2014-01-03 | 2016-12-12 | 주식회사 종근당 | 신규한 인돌 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| CN106232584B (zh) | 2014-03-12 | 2019-06-28 | 株式会社钟根堂 | 作为组蛋白脱乙酰酶6抑制剂的新型化合物和包含其的药物组合物 |
| CA2946538A1 (en) | 2014-04-04 | 2015-10-08 | Del Mar Pharmaceuticals | Use of dianhydrogalactitol and analogs or derivatives thereof to treat non-small-cell carcinoma of the lung and ovarian cancer |
| WO2015165960A1 (en) | 2014-04-30 | 2015-11-05 | Basf Se | N-acylamidine compounds |
| WO2015187542A1 (en) | 2014-06-02 | 2015-12-10 | Chdi Foundation Inc. | Histone deacetylase inhibitors and compositions and methods of use thereof |
| US20150359794A1 (en) | 2014-06-13 | 2015-12-17 | Buck Institute For Research On Aging | Impairment of the large ribosomal subunit protein rpl24 by depletion or acetylation |
| UY36196A (es) | 2014-07-25 | 2016-02-29 | Bayer Animal Health Gmbh | Compuestos para usar en el tratamiento antihelmíntico |
| WO2016018795A1 (en) | 2014-07-28 | 2016-02-04 | The General Hospital Corporation | Histone deacetylase inhibitors |
| US10081624B2 (en) | 2014-08-26 | 2018-09-25 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| EP3191445B1 (en) | 2014-09-09 | 2019-06-12 | Bristol-Myers Squibb Company | Cyclobutane containing carboxylic acid gpr120 modulators |
| WO2016055786A1 (en) | 2014-10-08 | 2016-04-14 | Redx Pharma Plc | N-pyridinyl acetamide derivatives as inhibitors of the wnt signalling pathway |
| GB201419264D0 (en) | 2014-10-29 | 2014-12-10 | Karus Therapeutics Ltd | Compounds |
| CN107001352B (zh) | 2014-12-01 | 2021-06-04 | 先正达参股股份有限公司 | 具有含硫取代基的杀有害生物活性酰胺杂环衍生物 |
| WO2016087257A1 (en) | 2014-12-01 | 2016-06-09 | Syngenta Participations Ag | Pesticidally active amide heterocyclic derivatives with sulphur containing substituents |
| US20190125745A1 (en) | 2014-12-17 | 2019-05-02 | Rgenix, Inc. | Treatment and diagnosis of cancer |
| JP6815318B2 (ja) | 2014-12-23 | 2021-01-20 | ダナ−ファーバー キャンサー インスティテュート,インコーポレイテッド | 二官能性分子によって標的化タンパク質分解を誘導する方法 |
| WO2016120182A1 (en) | 2015-01-30 | 2016-08-04 | Syngenta Participations Ag | Pesticidally active amide heterocyclic derivatives with sulphur containing substituents |
| US10183934B2 (en) | 2015-02-02 | 2019-01-22 | Forma Therapeutics, Inc. | Bicyclic [4,6,0] hydroxamic acids as HDAC inhibitors |
| MA42032A (fr) | 2015-02-02 | 2018-03-14 | Forma Therapeutics Inc | Acides 3-aryl-4-amido-bicyclo [4,5,0]hydroxamiques en tant qu'inhibiteurs de hdac |
| WO2016128541A1 (en) | 2015-02-13 | 2016-08-18 | Azienda Ospedaliera Universitaria Senese | Human helicase ddx3 inhibitors as therapeutic agents |
| WO2016168598A1 (en) | 2015-04-17 | 2016-10-20 | Forma Therapeutics, Inc. | 3-spirocyclic-6-hydroxamic acid tetralins as hdac inhibitors |
| JP6782255B2 (ja) | 2015-05-07 | 2020-11-11 | シーエイチディーアイ ファウンデーション,インコーポレーテッド | ヒストンデアセチラーゼ阻害薬及び組成物並びにそれらの使用の方法 |
| KR20180002729A (ko) | 2015-05-07 | 2018-01-08 | 씨에이치디아이 파운데이션, 인코포레이티드 | 히스톤 탈아세틸효소 억제제 및 그것의 조성물 및 사용 방법 |
| WO2016190630A1 (en) | 2015-05-22 | 2016-12-01 | Chong Kun Dang Pharmaceutical Corp. | Heterocyclicalkyl derivative compounds as selective histone deacetylase inhibitors and pharmaceutical compositions comprising the same |
| PE20180506A1 (es) | 2015-06-03 | 2018-03-09 | Bristol Myers Squibb Co | Agonistas de receptor de apelina (apj) de 4-hidroxi-3-(heteroaril) piridin-2-ona como para uso en el tratamiento de trastornos cardiovasculares |
| EP3319938B1 (en) | 2015-07-10 | 2022-04-06 | University of Maryland, Baltimore | Small molecule inhibitors of the mcl-1 oncoprotein and uses thereof |
| WO2017014321A1 (en) | 2015-07-17 | 2017-01-26 | Takeda Pharmaceutical Company Limited | Oxadiazole derivatives useful as hdac inhibitors |
| KR101799005B1 (ko) | 2015-07-27 | 2017-11-17 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 설프아마이드 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| US10538498B2 (en) | 2015-07-27 | 2020-01-21 | Chong Kun Dang Pharmaceutical Corp. | 1,3,4-oxadiazole sulfonamide derivative compounds as histone deacetylase 6 inhibitor, and the pharmaceutical composition comprising the same |
| HUE051537T2 (hu) | 2015-07-27 | 2021-03-01 | Chong Kun Dang Pharmaceutical Corp | 1,3,4-oxadiazolamid-származék vegyület mint hiszton deacetiláz 6 inhibitor és ezt tartalmazó gyógyszerkészítmény |
| JP6615983B2 (ja) | 2015-08-03 | 2019-12-04 | クワドリガ バイオサイエンシーズ, インコーポレイテッド | 化学療法剤としてのβ置換βアミノ酸および類似体ならびにそれらの使用 |
| CA2994688C (en) | 2015-08-04 | 2020-11-03 | Chong Kun Dang Pharmaceutical Corp. | 1,3,4-oxadiazole derivative compounds as histone deacetylase 6 inhibitor, and the pharmaceutical composition comprising the same |
| GB201514756D0 (en) | 2015-08-19 | 2015-09-30 | Karus Therapeutics Ltd | Compound and method of use |
| US10406146B2 (en) | 2015-08-25 | 2019-09-10 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| GB201515350D0 (en) | 2015-08-28 | 2015-10-14 | Econic Technologies Ltd | Method for preparing polyols |
| EP3359532A1 (en) | 2015-10-06 | 2018-08-15 | GlaxoSmithKline Intellectual Property Development Limited | Biaryl pyrazoles as nrf2 regulators |
| AU2016338118B2 (en) | 2015-10-12 | 2019-03-14 | Chong Kun Dang Pharmaceutical Corp. | Oxadiazole amine derivative compounds as histone deacetylase 6 inhibitor, and the pharmaceutical composition comprising the same |
| EP3371177A1 (en) | 2015-11-02 | 2018-09-12 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| TW201737944A (zh) | 2015-11-12 | 2017-11-01 | 輝瑞大藥廠 | 使用crispr-cas9之組織特異性基因組工程 |
| WO2017081310A1 (en) | 2015-11-13 | 2017-05-18 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AR106679A1 (es) | 2015-11-13 | 2018-02-07 | Basf Se | Oxadiazoles sustituidos para combatir hongos fitopatógenos |
| CN105884767B (zh) | 2015-11-24 | 2018-01-19 | 西华大学 | 9‑位取代的吡啶并[3,4‑b]吲哚衍生物及其制备方法和作为SIRT蛋白抑制剂的用途 |
| CA3043549C (en) * | 2015-11-30 | 2023-11-21 | Children's Medical Center Corporation | Compounds for treating proliferative diseases |
| CN108366564A (zh) | 2015-12-03 | 2018-08-03 | 巴斯夫欧洲公司 | 用于防治植物病原性真菌的取代噁二唑类 |
| CN108430980B (zh) | 2015-12-22 | 2022-09-02 | 先正达参股股份有限公司 | 杀微生物的噁二唑衍生物 |
| WO2017110862A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物及びその用途 |
| WO2017111152A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物及びその用途 |
| WO2017110861A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物を含有する植物病害防除剤 |
| CN108698997A (zh) | 2015-12-28 | 2018-10-23 | 赛尔基因昆蒂赛尔研究公司 | 组蛋白脱甲基酶抑制剂 |
| WO2017123568A2 (en) | 2016-01-11 | 2017-07-20 | The Rockefeller University | Methods for the treatment of myeloid derived suppressor cells related disorders |
| US10456394B2 (en) * | 2016-02-16 | 2019-10-29 | The Board Of Trustees Of The University Of Illinois | Tetrahydroquinoline substituted hydroxamic acids as selective histone deacetylase 6 inhibitors |
| WO2017156350A1 (en) | 2016-03-09 | 2017-09-14 | K-Gen, Inc. | Methods of cancer treatment |
| PT3433234T (pt) | 2016-03-22 | 2021-12-22 | Merck Sharp & Dohme | Moduladores alostéricos de recetores de acetilcolina nicotínica |
| ITUA20161994A1 (it) | 2016-03-24 | 2017-09-24 | Azienda Ospedaliera Univ Senese | Uso degli inibitori ddx3 come agenti anti-iperproliferativi |
| JP2017190296A (ja) | 2016-04-13 | 2017-10-19 | 住友化学株式会社 | 有害生物防除組成物およびその用途 |
| EP3448520A4 (en) | 2016-04-29 | 2020-07-29 | Board Of Regents, The University Of Texas System | SIGMA RECEIVER BINDERS |
| TW201808914A (zh) | 2016-05-05 | 2018-03-16 | 嘉來克生命科學有限責任公司 | 整合應激途徑之調節劑 |
| EP3455218A4 (en) | 2016-05-10 | 2019-12-18 | C4 Therapeutics, Inc. | C3 CARBON-BASED GLUTARIMIDE DEGRONIMERS FOR TARGET PROTEIN REDUCTION |
| GB201609786D0 (en) | 2016-06-03 | 2016-07-20 | Karus Therapeutics Ltd | Compounds and method of use |
| WO2017213252A1 (en) | 2016-06-10 | 2017-12-14 | Sumitomo Chemical Company, Limited | Oxadiazole compound and use as pesticide |
| WO2017222950A1 (en) | 2016-06-23 | 2017-12-28 | Merck Sharp & Dohme Corp. | 3-heterocyclyl substituted 5-trifluoromethyl oxadiazoles as histone deacetylase 6 (hdac6) inhibitors |
| WO2017222951A1 (en) | 2016-06-23 | 2017-12-28 | Merck Sharp & Dohme Corp. | 3-aryl and heteroaryl substituted 5-trifluoromethyl oxadiazoles as histone deacetylase 6 (hdac6) inhibitors |
| WO2017222952A1 (en) | 2016-06-23 | 2017-12-28 | Merck Sharp & Dohme Corp. | 3- heteroaryl substituted 5-trifluoromethyl oxadiazoles as histone deacetylase 6 (hdac6) inhibitors |
| TWI771303B (zh) | 2016-06-30 | 2022-07-21 | 美商艾克奎斯特有限責任公司 | 化合物及其於降低尿酸位準之用途(一) |
| EP3512602B1 (en) | 2016-09-16 | 2024-03-27 | HSF Pharmaceuticals | Inhibitors of heat shock factors (hsf) and uses thereof |
| CN109923112A (zh) | 2016-09-23 | 2019-06-21 | 先正达参股股份有限公司 | 杀微生物的噁二唑衍生物 |
| US20180127386A1 (en) | 2016-10-20 | 2018-05-10 | Forma Therapeutics, Inc. | Methods using hdac11 inhibitors |
| US11026958B2 (en) | 2016-11-01 | 2021-06-08 | Merck Sharp & Dohme Corp. | Substituted 6-membered aryl or heteroaryl allosteric modulators of nicotinic acetylcholine receptors |
| EP4046989A1 (en) | 2017-01-09 | 2022-08-24 | Shuttle Pharmaceuticals, Inc. | Selective histone deacetylase inhibitors for the treatment of human disease |
| WO2018154466A1 (en) | 2017-02-21 | 2018-08-30 | Glaxosmithkline Intellectual Property Development Limited | Dihydroquinolizinones as antivirals |
| US10357493B2 (en) | 2017-03-10 | 2019-07-23 | Selenity Therapeutics (Bermuda), Ltd. | Metalloenzyme inhibitor compounds |
| TWI886480B (zh) | 2017-04-06 | 2025-06-11 | 美商富曼西公司 | 殺真菌之噁二唑 |
| WO2018188962A1 (en) | 2017-04-11 | 2018-10-18 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AU2018250599B2 (en) | 2017-04-11 | 2022-05-26 | The General Hospital Corporation | HDAC6 inhibitors and imaging agents |
| IT201700041723A1 (it) | 2017-04-14 | 2018-10-14 | Italfarmaco Spa | Nuovi inibitori selettivi di HDAC6 |
| WO2018202491A1 (en) | 2017-05-04 | 2018-11-08 | Basf Se | Substituted trifluoromethyloxadiazoles for combating phytopathogenic fungi |
| WO2018213364A1 (en) | 2017-05-16 | 2018-11-22 | Annji Pharmaceutical Co., Ltd. | Histone deacetylases (hdacs) inhibitors |
| CN108976223B (zh) | 2017-06-01 | 2020-08-07 | 广东东阳光药业有限公司 | 稠合三环类化合物及其在药物中的应用 |
| CN110066278B (zh) | 2017-06-01 | 2021-06-08 | 广东东阳光药业有限公司 | 稠合三环类化合物及其在药物中的应用 |
| JP7135007B2 (ja) | 2017-07-31 | 2022-09-12 | 武田薬品工業株式会社 | 複素環化合物 |
| US10597378B2 (en) | 2017-09-08 | 2020-03-24 | National Health Research Institutes | Tetrahydroisoquinolines for use as MOR/NOP dual agonists |
| CA3073212A1 (en) | 2017-09-19 | 2019-03-28 | Merck Sharp & Dohme Corp. | Heteroaryl allosteric modulators of nicotinic acetylcholine receptors |
| CN109651357A (zh) | 2017-10-11 | 2019-04-19 | 中国科学院上海有机化学研究所 | 6,7-二氢-5h-喹啉-8-腙类衍生物铁螯合剂及其制备抗肿瘤药物的用途 |
| EP3694856B1 (en) | 2017-11-22 | 2023-10-25 | Sunshine Lake Pharma Co., Ltd. | Fused tricyclic compounds and uses thereof in medicine |
| EP3713934B1 (en) | 2017-11-23 | 2022-04-13 | Universita' degli Studi di Palermo | Oxadiazole derivatives for the treatment of genetic diseases due to nonsense mutations |
| SG11202003664TA (en) | 2017-11-30 | 2020-05-28 | Arrakis Therapeutics Inc | Nucleic acid-binding photoprobes and uses thereof |
| BR112020010534A2 (pt) | 2017-12-05 | 2020-10-20 | Oryzon Genomics, S.A. | derivados de 1,2,4-oxadiazol como inibidores de histona desacetilase 6 |
| MX2020006595A (es) | 2017-12-22 | 2020-09-10 | Bayer Ag | Oxadiazoles fungicidas. |
| US11407723B2 (en) | 2018-01-09 | 2022-08-09 | Shuttle Pharmaceuticals, Inc. | Selective histone deacetylase inhibitors for the treatment of human disease |
| KR20190099952A (ko) | 2018-02-20 | 2019-08-28 | 주식회사 종근당 | 포도막염의 예방 또는 치료를 위한 조성물 |
| GB201803361D0 (en) | 2018-03-01 | 2018-04-18 | Karus Therapeutics Ltd | Histone deacetylase inhibitors |
| EP3762367A1 (en) | 2018-03-09 | 2021-01-13 | PI Industries Ltd. | Heterocyclic compounds as fungicides |
| WO2019200238A1 (en) | 2018-04-14 | 2019-10-17 | Dynavax Technologies Corporation | Combinations including a cpg-c type oligonucleotide and a histone deacetylase inhibitor for treating cancer |
| US11535607B2 (en) | 2018-04-20 | 2022-12-27 | Valo Health, Inc. | Isoindolines as HDAC inhibitors |
| JP2021522324A (ja) | 2018-04-20 | 2021-08-30 | ヴァロ アーリー ディスカバリー, インコーポレイテッド | Hdac阻害剤としてのイソインドリン |
| DK3788043T3 (da) | 2018-05-01 | 2024-12-16 | Merck Sharp & Dohme Llc | Spiropiperidin som allosteriske modulatorer af nicotinacetylcholinreceptorer |
| CN110054596B (zh) | 2018-05-29 | 2023-03-31 | 沈阳化工大学 | 一种取代噁二唑类化合物及其应用 |
| EP3594205A1 (en) | 2018-07-09 | 2020-01-15 | Abivax | Phenyl-n-aryl derivatives for treating a rna virus infection |
| KR102316234B1 (ko) | 2018-07-26 | 2021-10-22 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| WO2020028150A1 (en) | 2018-08-01 | 2020-02-06 | Merck Sharp & Dohme Corp. | Inhibitors of histone deacetylase useful for the treatment or prevention of hiv infection |
| WO2020029908A1 (zh) | 2018-08-08 | 2020-02-13 | 广州市恒诺康医药科技有限公司 | 螺桥环化合物、其药物组合物及其用途 |
| WO2020039028A1 (en) | 2018-08-22 | 2020-02-27 | Asceneuron S. A. | Tetrahydro-benzoazepine glycosidase inhibitors |
| WO2020061118A1 (en) | 2018-09-18 | 2020-03-26 | Metacrine, Inc. | Farnesoid x receptor agonists and uses thereof |
| JP2022500391A (ja) | 2018-09-18 | 2022-01-04 | メタクリン,インク. | ファルネソイドx受容体アゴニストおよびその使用 |
| CN112739349B (zh) | 2018-09-18 | 2024-03-01 | 圣诺康生命科学公司 | 用于治疗血癌的组合疗法 |
| CN110950860B (zh) | 2018-09-26 | 2023-03-31 | 广东东阳光药业有限公司 | 稠合三环类化合物及其在药物中的应用 |
| KR20210098949A (ko) | 2018-10-01 | 2021-08-11 | 피아이 인더스트리스 엘티디. | 새로운 옥사디아졸 |
| EP3876928B1 (en) | 2018-11-08 | 2024-10-23 | Merck Sharp & Dohme LLC | Inhibitors of histone deacetylase useful for the treatment or prevention of hiv infection |
| CN113164470A (zh) | 2018-11-23 | 2021-07-23 | 株式会社钟根堂 | 包含组蛋白脱乙酰酶6抑制剂的药物组合物 |
| CN113453679B (zh) | 2018-12-20 | 2025-07-08 | C4医药公司 | 靶向蛋白降解 |
| EP3897154A1 (en) | 2018-12-21 | 2021-10-27 | Bayer Aktiengesellschaft | 1,3,4-oxadiazoles and their derivatives as new antifungal agents |
| WO2020158762A1 (ja) | 2019-01-30 | 2020-08-06 | 武田薬品工業株式会社 | 複素環化合物 |
| WO2020194272A1 (en) | 2019-03-27 | 2020-10-01 | 2681603 Ontario Inc. | Halogenated phenylsulfonamide hydroxamic acid compounds, compositions and uses thereof as selective hdac6 inhibitors |
| EP3946618A1 (en) | 2019-04-05 | 2022-02-09 | Storm Therapeutics Ltd | Mettl3 inhibitory compounds |
| JP7707073B2 (ja) | 2019-04-09 | 2025-07-14 | エフ. ホフマン-ラ ロシュ アーゲー | モノアシルグリセロールリパーゼ(magl)の阻害剤としての複素環式化合物 |
| DK3956324T3 (da) | 2019-04-17 | 2024-05-13 | Quimatryx S L | 1,3,4-oxadiazol-derivater som histondeacetylase-inhibitorer |
| EP3958861A4 (en) | 2019-04-23 | 2023-05-03 | Dana-Farber Cancer Institute, Inc. | DEGRADERS OF CYCLIN DEPENDENT KINASE 12 (CDK12) AND USES THEREOF |
| EP3962483A4 (en) | 2019-05-02 | 2023-01-25 | Merck Sharp & Dohme LLC | ALLOSTERIC SPIROPIPERIDINE MODULATORS OF NICOTINE ACETYLCHOLINE RECEPTORS |
| MX2021014315A (es) | 2019-05-31 | 2022-01-04 | Chong Kun Dang Pharmaceutical Corp | Compuestos derivados de 1,3,4-oxadiazol homoftalimida como inhibidores de histona desacetilasa 6, y la composicion farmaceutica que comprende los mismos. |
| KR102476818B1 (ko) | 2019-05-31 | 2022-12-13 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| JP7523146B2 (ja) | 2019-06-06 | 2024-07-26 | オリゾン・ゲノミクス・ソシエダッド・アノニマ | Hdac6阻害薬としての3-(2-(ヘテロアリール)-ピリジン-4-イル)-5-(トリフルオロメチル)-1,2,4-オキサジアゾール誘導体 |
| WO2020254494A1 (en) | 2019-06-21 | 2020-12-24 | Bayer Aktiengesellschaft | Fungicidal oxadiazoles |
| EP3990618A4 (en) | 2019-06-27 | 2023-08-09 | The George Washington University, A Congressionally Chartered Not-For-Profit Corporation | HDAC6-ACTIVATED MACROPHAGES, COMPOSITIONS AND ASSOCIATED USES |
| US20220251043A1 (en) | 2019-07-23 | 2022-08-11 | Taipei Medical University | Histone deacetylase 6 inhibitors and method for treating neuropathic pain |
| JP2022543106A (ja) | 2019-07-30 | 2022-10-07 | エイコニゾ セラピューティクス,インコーポレーテッド | Hdac6インヒビターおよびそれらの使用 |
| US20220251097A1 (en) | 2019-08-01 | 2022-08-11 | St. Jude Childrens's Research Hospital | Molecules and methods related to treatment of uncontrolled cellular proliferation |
| AU2020341464A1 (en) | 2019-09-05 | 2022-04-21 | Trevena, Inc. | Methods of treating epilepsy using the same |
| CA3151516A1 (en) | 2019-09-12 | 2021-03-18 | F. Hoffmann-La Roche Ag | 4,4a,5,7,8,8a-hexapyrido[4,3-b][1,4]oxazin-3-one compounds as magl inhibitors |
| CN112552293A (zh) | 2019-09-25 | 2021-03-26 | 珠海宇繁生物科技有限责任公司 | 一种protac小分子化合物及其应用 |
| BR112022005595A2 (pt) | 2019-09-27 | 2022-07-19 | Takeda Pharmaceuticals Co | Composto, medicamento, métodos para inibir histona deacetilase 6 e para profilaxia ou tratamento de doença de alzheimer ou paralisia supranuclear progressiva em um mamífero, e, uso de composto |
| WO2021067859A1 (en) | 2019-10-03 | 2021-04-08 | Tenaya Therapeutics, Inc. | 5-fluoronicotinamide derivatives and uses thereof |
| CA3152306A1 (en) | 2019-11-06 | 2021-05-14 | Eric S. FISCHER | Selective hdac6 degraders and methods of use thereof |
| CA3152582A1 (en) | 2019-11-06 | 2021-05-14 | Dana-Farber Cancer Institute, Inc. | Selective histone deacetylase (hdac) degraders and methods of use thereof |
| US20220387604A1 (en) | 2019-11-06 | 2022-12-08 | Dana-Farber Cancer Institute, Inc. | Selective dual histone deacetylase 6/8 (hdac6/8) degraders and methods of use thereof |
| KR20220119653A (ko) | 2019-12-20 | 2022-08-30 | 테나야 테라퓨틱스, 인코포레이티드 | 플루오로알킬-옥사디아졸 및 이의 용도 |
| US11339150B2 (en) | 2019-12-27 | 2022-05-24 | Onkure, Inc. | Benzimidazole compounds as HDAC6 inhibitors |
| KR102537615B1 (ko) | 2020-02-25 | 2023-05-30 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| KR102537616B1 (ko) | 2020-02-25 | 2023-05-26 | 주식회사 종근당 | 히스톤 탈아세틸화 효소 6 억제제로서의 1,3,4-옥사다이아졸 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| KR102576148B1 (ko) | 2020-04-13 | 2023-09-07 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 유도체 화합물 및 이를 포함하는 약제학적 조성물 |
| CN113527206B (zh) | 2020-04-17 | 2022-12-30 | 上海中泽医药科技有限公司 | 一种苯并氮杂环类化合物、其制备方法及用途 |
| EP4153160A4 (en) | 2020-05-19 | 2024-12-04 | University of Florida Research Foundation, Inc. | BENZOYLHYDRAZIDE-DERIVED HDAC DEGRADING AGENTS AS THERAPEUTIC AGENTS FOR THE TREATMENT OF CANCER AND OTHER HUMAN DISEASES |
| CN116437948A (zh) | 2020-06-26 | 2023-07-14 | 伊利诺伊大学董事会 | 选择性组蛋白脱乙酰酶6抑制剂 |
| EP4185586A4 (en) | 2020-07-14 | 2024-07-24 | Chong Kun Dang Pharmaceutical Corp. | Novel compounds as histone deacetylase 6 inhibitor, and pharmaceutical composition comprising the same |
| US20230286970A1 (en) | 2020-08-07 | 2023-09-14 | Italfarmaco S.P.A. | Novel oxadiazole-based selective hdac6 inhibitors |
| KR102685058B1 (ko) | 2020-09-02 | 2024-07-15 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 새로운 구조의 화합물 및 이를 포함하는 약제학적 조성물 |
| CN116723839A (zh) | 2020-10-14 | 2023-09-08 | C4医药公司 | 用于降解靶蛋白质的三环杂双官能化合物 |
| EP4267539A4 (en) | 2020-12-23 | 2025-03-19 | The University of Queensland | Histone deacetylase inhibitors |
| WO2022169985A1 (en) | 2021-02-03 | 2022-08-11 | Eikonizo Therapeutics, Inc. | Hdac6 inhibitors and uses thereof |
| WO2022174193A1 (en) | 2021-02-15 | 2022-08-18 | The Research Foundation For The State University Of New York | Radiolabeled compositions and methods of use thereof |
| WO2022187690A1 (en) | 2021-03-05 | 2022-09-09 | Umbra Therapeutics Inc. | Covalent binding compounds for the treatment of disease |
| EP4308097A4 (en) | 2021-03-15 | 2025-08-20 | Univ Michigan Regents | NON-HYDROXAMATE HDAC6 INHIBITORS AND METHODS OF USE THEREOF |
| CN112794860B (zh) | 2021-03-24 | 2021-06-29 | 上海肇钰医药科技有限公司 | 噁唑嘧啶酮酰胺类化合物或其可药用盐,制备方法及用途 |
| AU2022254646A1 (en) | 2021-04-05 | 2023-09-28 | Dana-Farber Cancer Institute, Inc. | Bioorthogonal reaction suitable for click/unclick applications |
| KR102905373B1 (ko) | 2021-04-08 | 2025-12-29 | 주식회사 종근당 | 히스톤 탈아세틸화효소 6 억제제로서의 1,3,4-옥사다이아졸 싸이오카보닐 화합물 및 이를 포함하는 약제학적 조성물 |
| EP4452265A2 (en) | 2021-12-22 | 2024-10-30 | Augustine Therapeutics | Compounds and use thereof as hdac6 inhibitors |
| WO2023150203A1 (en) | 2022-02-03 | 2023-08-10 | Eikonizo Therapeutics, Inc. | Hdac6 inhibitors and uses thereof |
-
2020
- 2020-07-30 JP JP2022506695A patent/JP2022543106A/ja active Pending
- 2020-07-30 US US17/631,422 patent/US12528767B2/en active Active
- 2020-07-30 EP EP20847655.6A patent/EP4003319A4/en active Pending
- 2020-07-30 AU AU2020321955A patent/AU2020321955A1/en active Pending
- 2020-07-30 CN CN202080055409.7A patent/CN114727974A/zh active Pending
- 2020-07-30 WO PCT/US2020/044148 patent/WO2021021979A2/en not_active Ceased
- 2020-07-30 CA CA3149096A patent/CA3149096A1/en active Pending
-
2025
- 2025-09-09 AU AU2025230659A patent/AU2025230659A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US12528767B2 (en) | 2026-01-20 |
| EP4003319A2 (en) | 2022-06-01 |
| AU2025230659A1 (en) | 2025-10-02 |
| WO2021021979A2 (en) | 2021-02-04 |
| WO2021021979A3 (en) | 2021-04-08 |
| EP4003319A4 (en) | 2023-11-08 |
| AU2020321955A1 (en) | 2022-03-17 |
| US20220281814A1 (en) | 2022-09-08 |
| CN114727974A (zh) | 2022-07-08 |
| CA3149096A1 (en) | 2021-02-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2022543106A (ja) | Hdac6インヒビターおよびそれらの使用 | |
| JP7308146B2 (ja) | インターロイキン1受容体関連キナーゼの阻害剤およびその使用 | |
| JP7590185B2 (ja) | Taireファミリーキナーゼインヒビターおよびそれらの使用 | |
| JP2019537599A (ja) | Malt1分解のための化合物 | |
| JP7142022B2 (ja) | Malt1の阻害剤およびそれらの使用 | |
| JP2016512846A (ja) | Ras阻害剤およびその使用 | |
| JP7675070B2 (ja) | 治療、特にmyd88変異疾患における使用のためのhck阻害剤としてのピラゾロピリミジン誘導体 | |
| JP2024099510A (ja) | がんの処置のための選択的ヒストンデアセチラーゼ3(hdac3)インヒビターと免疫治療剤との組み合わせ | |
| CN111566113B (zh) | 大环化合物及其用途 | |
| KR20250099692A (ko) | 세레블론 동원 bcl-xl/bcl-2 이중 분해제 | |
| AU2021203883A1 (en) | Phenylsulfonamido-benzofuran derivatives and uses thereof in the treatment of proliferative diseases | |
| WO2022169985A1 (en) | Hdac6 inhibitors and uses thereof | |
| JP2024518089A (ja) | Nampt阻害剤とその使用 | |
| WO2016077581A1 (en) | Isosteviol triazoles and uses thereof | |
| WO2023150203A1 (en) | Hdac6 inhibitors and uses thereof | |
| JP2018538364A (ja) | ポリアミンスルホンアミドおよびこれらの使用 | |
| WO2017218874A1 (en) | Hedgehog acyltransferase inhibitors and uses thereof |