CN102659511A - 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 - Google Patents
在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 Download PDFInfo
- Publication number
- CN102659511A CN102659511A CN2012100221382A CN201210022138A CN102659511A CN 102659511 A CN102659511 A CN 102659511A CN 2012100221382 A CN2012100221382 A CN 2012100221382A CN 201210022138 A CN201210022138 A CN 201210022138A CN 102659511 A CN102659511 A CN 102659511A
- Authority
- CN
- China
- Prior art keywords
- aliphatic hydrocarbons
- polyhydroxylated aliphatic
- water
- chloro
- hydrin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 191
- 150000002148 esters Chemical class 0.000 title claims abstract description 78
- 150000003839 salts Chemical class 0.000 title abstract description 18
- 229910052751 metal Inorganic materials 0.000 title abstract description 11
- 239000002184 metal Substances 0.000 title abstract description 11
- 150000002430 hydrocarbons Chemical class 0.000 title description 7
- 239000004215 Carbon black (E152) Substances 0.000 title description 6
- 229930195733 hydrocarbon Natural products 0.000 title description 6
- SSZWWUDQMAHNAQ-UHFFFAOYSA-N 3-chloropropane-1,2-diol Chemical compound OCC(O)CCl SSZWWUDQMAHNAQ-UHFFFAOYSA-N 0.000 title 1
- XENVCRGQTABGKY-ZHACJKMWSA-N chlorohydrin Chemical compound CC#CC#CC#CC#C\C=C\C(Cl)CO XENVCRGQTABGKY-ZHACJKMWSA-N 0.000 claims abstract description 134
- 239000000203 mixture Substances 0.000 claims abstract description 88
- 238000006243 chemical reaction Methods 0.000 claims abstract description 35
- 239000007787 solid Substances 0.000 claims abstract description 28
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 claims description 188
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 99
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 67
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical group Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 54
- 238000004821 distillation Methods 0.000 claims description 47
- 239000003795 chemical substances by application Substances 0.000 claims description 46
- 239000007788 liquid Substances 0.000 claims description 41
- 239000012429 reaction media Substances 0.000 claims description 37
- 239000011541 reaction mixture Substances 0.000 claims description 36
- 235000011187 glycerol Nutrition 0.000 claims description 32
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 claims description 31
- 229910000041 hydrogen chloride Inorganic materials 0.000 claims description 31
- 239000007789 gas Substances 0.000 claims description 27
- 239000003921 oil Substances 0.000 claims description 26
- 235000019198 oils Nutrition 0.000 claims description 25
- 238000001914 filtration Methods 0.000 claims description 22
- 238000004519 manufacturing process Methods 0.000 claims description 21
- 239000002253 acid Substances 0.000 claims description 20
- 238000005660 chlorination reaction Methods 0.000 claims description 20
- 238000012545 processing Methods 0.000 claims description 20
- 238000007033 dehydrochlorination reaction Methods 0.000 claims description 12
- 238000001704 evaporation Methods 0.000 claims description 12
- 230000008020 evaporation Effects 0.000 claims description 12
- 239000002994 raw material Substances 0.000 claims description 12
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims description 7
- 241000282326 Felis catus Species 0.000 claims description 6
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 claims description 6
- 238000006460 hydrolysis reaction Methods 0.000 claims description 6
- 238000005809 transesterification reaction Methods 0.000 claims description 6
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 claims description 5
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 claims description 5
- DPDMMXDBJGCCQC-UHFFFAOYSA-N [Na].[Cl] Chemical group [Na].[Cl] DPDMMXDBJGCCQC-UHFFFAOYSA-N 0.000 claims description 5
- 239000001257 hydrogen Substances 0.000 claims description 5
- 229910052739 hydrogen Inorganic materials 0.000 claims description 5
- 239000003456 ion exchange resin Substances 0.000 claims description 5
- 229920003303 ion-exchange polymer Polymers 0.000 claims description 5
- 238000010992 reflux Methods 0.000 claims description 5
- 208000006558 Dental Calculus Diseases 0.000 claims description 4
- 241000196324 Embryophyta Species 0.000 claims description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 4
- 238000010521 absorption reaction Methods 0.000 claims description 4
- 239000002551 biofuel Substances 0.000 claims description 4
- 238000009835 boiling Methods 0.000 claims description 4
- 235000019197 fats Nutrition 0.000 claims description 4
- 229910052938 sodium sulfate Inorganic materials 0.000 claims description 4
- 235000011152 sodium sulphate Nutrition 0.000 claims description 4
- 244000020551 Helianthus annuus Species 0.000 claims description 3
- 235000003222 Helianthus annuus Nutrition 0.000 claims description 3
- 235000019484 Rapeseed oil Nutrition 0.000 claims description 3
- 238000009833 condensation Methods 0.000 claims description 3
- 230000005494 condensation Effects 0.000 claims description 3
- 238000007127 saponification reaction Methods 0.000 claims description 3
- 210000000582 semen Anatomy 0.000 claims description 3
- 235000020238 sunflower seed Nutrition 0.000 claims description 3
- ZEMPKEQAKRGZGQ-AAKVHIHISA-N 2,3-bis[[(z)-12-hydroxyoctadec-9-enoyl]oxy]propyl (z)-12-hydroxyoctadec-9-enoate Chemical compound CCCCCCC(O)C\C=C/CCCCCCCC(=O)OCC(OC(=O)CCCCCCC\C=C/CC(O)CCCCCC)COC(=O)CCCCCCC\C=C/CC(O)CCCCCC ZEMPKEQAKRGZGQ-AAKVHIHISA-N 0.000 claims description 2
- 235000006008 Brassica napus var napus Nutrition 0.000 claims description 2
- 235000001169 Brassica oleracea var oleracea Nutrition 0.000 claims description 2
- 241001674939 Caulanthus Species 0.000 claims description 2
- 244000174788 Crambe maritima Species 0.000 claims description 2
- 235000005664 Crambe maritima Nutrition 0.000 claims description 2
- 235000019483 Peanut oil Nutrition 0.000 claims description 2
- 239000010480 babassu oil Substances 0.000 claims description 2
- 235000014121 butter Nutrition 0.000 claims description 2
- 239000003822 epoxy resin Substances 0.000 claims description 2
- 235000021323 fish oil Nutrition 0.000 claims description 2
- 238000012239 gene modification Methods 0.000 claims description 2
- 230000005017 genetic modification Effects 0.000 claims description 2
- 235000013617 genetically modified food Nutrition 0.000 claims description 2
- 238000009396 hybridization Methods 0.000 claims description 2
- 235000021388 linseed oil Nutrition 0.000 claims description 2
- 239000000944 linseed oil Substances 0.000 claims description 2
- 239000000312 peanut oil Substances 0.000 claims description 2
- 229920000647 polyepoxide Polymers 0.000 claims description 2
- 239000008400 supply water Substances 0.000 claims description 2
- 235000013311 vegetables Nutrition 0.000 claims description 2
- 241000218922 Magnoliophyta Species 0.000 claims 1
- 239000000479 mixture part Substances 0.000 claims 1
- 238000000926 separation method Methods 0.000 abstract description 5
- 239000012320 chlorinating reagent Substances 0.000 abstract description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 37
- 150000001875 compounds Chemical class 0.000 description 22
- 229910052801 chlorine Inorganic materials 0.000 description 20
- 239000000047 product Substances 0.000 description 19
- 239000000460 chlorine Substances 0.000 description 18
- 239000012535 impurity Substances 0.000 description 18
- 150000002924 oxiranes Chemical class 0.000 description 18
- 239000006227 byproduct Substances 0.000 description 17
- 239000012043 crude product Substances 0.000 description 17
- 238000004140 cleaning Methods 0.000 description 16
- 239000002904 solvent Substances 0.000 description 16
- 150000003945 chlorohydrins Chemical class 0.000 description 15
- 239000012071 phase Substances 0.000 description 14
- SZIFAVKTNFCBPC-UHFFFAOYSA-N 2-chloroethanol Chemical compound OCCCl SZIFAVKTNFCBPC-UHFFFAOYSA-N 0.000 description 13
- 239000007791 liquid phase Substances 0.000 description 13
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical group [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 11
- 229910052799 carbon Inorganic materials 0.000 description 11
- 239000000376 reactant Substances 0.000 description 11
- 239000007864 aqueous solution Substances 0.000 description 10
- 150000002632 lipids Chemical class 0.000 description 10
- -1 metals salt Chemical class 0.000 description 10
- 239000013505 freshwater Substances 0.000 description 9
- 239000000463 material Substances 0.000 description 9
- 239000000126 substance Substances 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 238000010828 elution Methods 0.000 description 8
- 150000002576 ketones Chemical class 0.000 description 8
- VZIQXGLTRZLBEX-UHFFFAOYSA-N 2-chloro-1-propanol Chemical compound CC(Cl)CO VZIQXGLTRZLBEX-UHFFFAOYSA-N 0.000 description 7
- 239000007806 chemical reaction intermediate Substances 0.000 description 7
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- 150000001721 carbon Chemical group 0.000 description 6
- 239000007795 chemical reaction product Substances 0.000 description 6
- 150000007524 organic acids Chemical class 0.000 description 6
- 230000001376 precipitating effect Effects 0.000 description 6
- 238000004064 recycling Methods 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 125000001309 chloro group Chemical group Cl* 0.000 description 5
- 230000002194 synthesizing effect Effects 0.000 description 5
- DEWLEGDTCGBNGU-UHFFFAOYSA-N 1,3-dichloropropan-2-ol Chemical compound ClCC(O)CCl DEWLEGDTCGBNGU-UHFFFAOYSA-N 0.000 description 4
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 4
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 4
- 238000009825 accumulation Methods 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 229910052728 basic metal Inorganic materials 0.000 description 4
- 150000003818 basic metals Chemical group 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 238000007600 charging Methods 0.000 description 4
- NEHMKBQYUWJMIP-UHFFFAOYSA-N chloromethane Chemical compound ClC NEHMKBQYUWJMIP-UHFFFAOYSA-N 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical class 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 230000003647 oxidation Effects 0.000 description 4
- 238000007254 oxidation reaction Methods 0.000 description 4
- 229920000728 polyester Polymers 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 238000011282 treatment Methods 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- 229910052725 zinc Inorganic materials 0.000 description 4
- 239000011701 zinc Substances 0.000 description 4
- UXFQFBNBSPQBJW-UHFFFAOYSA-N 2-amino-2-methylpropane-1,3-diol Chemical compound OCC(N)(C)CO UXFQFBNBSPQBJW-UHFFFAOYSA-N 0.000 description 3
- OSDWBNJEKMUWAV-UHFFFAOYSA-N Allyl chloride Chemical group ClCC=C OSDWBNJEKMUWAV-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 3
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 3
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 3
- 229910052783 alkali metal Inorganic materials 0.000 description 3
- 150000001340 alkali metals Chemical class 0.000 description 3
- 239000004411 aluminium Substances 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000003651 drinking water Substances 0.000 description 3
- 235000020188 drinking water Nutrition 0.000 description 3
- 230000032050 esterification Effects 0.000 description 3
- 238000005886 esterification reaction Methods 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 239000002638 heterogeneous catalyst Substances 0.000 description 3
- 230000007062 hydrolysis Effects 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 230000008929 regeneration Effects 0.000 description 3
- 238000011069 regeneration method Methods 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000010936 titanium Substances 0.000 description 3
- 229910052719 titanium Inorganic materials 0.000 description 3
- 239000006200 vaporizer Substances 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 2
- CTKINSOISVBQLD-UHFFFAOYSA-N Glycidol Chemical compound OCC1CO1 CTKINSOISVBQLD-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- 229910000831 Steel Inorganic materials 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical compound ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 description 2
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical group ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 2
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 2
- SRBFZHDQGSBBOR-LECHCGJUSA-N alpha-D-xylose Chemical compound O[C@@H]1CO[C@H](O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-LECHCGJUSA-N 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 2
- 229910052797 bismuth Inorganic materials 0.000 description 2
- JCXGWMGPZLAOME-UHFFFAOYSA-N bismuth atom Chemical compound [Bi] JCXGWMGPZLAOME-UHFFFAOYSA-N 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- BULLHNJGPPOUOX-UHFFFAOYSA-N chloroacetone Chemical compound CC(=O)CCl BULLHNJGPPOUOX-UHFFFAOYSA-N 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 150000002194 fatty esters Chemical class 0.000 description 2
- 239000010408 film Substances 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 239000010439 graphite Substances 0.000 description 2
- 229910002804 graphite Inorganic materials 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 229920001903 high density polyethylene Polymers 0.000 description 2
- 239000004700 high-density polyethylene Substances 0.000 description 2
- 238000007327 hydrogenolysis reaction Methods 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 229910017053 inorganic salt Inorganic materials 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 229910001510 metal chloride Inorganic materials 0.000 description 2
- 239000007769 metal material Substances 0.000 description 2
- 229940050176 methyl chloride Drugs 0.000 description 2
- 150000004831 organic oxygen compounds Chemical class 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920001021 polysulfide Polymers 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 239000010959 steel Substances 0.000 description 2
- 238000010408 sweeping Methods 0.000 description 2
- 229910052715 tantalum Inorganic materials 0.000 description 2
- GUVRBAGPIYLISA-UHFFFAOYSA-N tantalum atom Chemical compound [Ta] GUVRBAGPIYLISA-UHFFFAOYSA-N 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical compound CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 2
- 229960003487 xylose Drugs 0.000 description 2
- MEIRRNXMZYDVDW-MQQKCMAXSA-N (2E,4E)-2,4-hexadien-1-ol Chemical compound C\C=C\C=C\CO MEIRRNXMZYDVDW-MQQKCMAXSA-N 0.000 description 1
- AOFUBOWZWQFQJU-SNOJBQEQSA-N (2r,3s,4s,5r)-2,5-bis(hydroxymethyl)oxolane-2,3,4-triol;(2s,3r,4s,5s,6r)-6-(hydroxymethyl)oxane-2,3,4,5-tetrol Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O.OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@@H]1O AOFUBOWZWQFQJU-SNOJBQEQSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- OWXJKYNZGFSVRC-NSCUHMNNSA-N (e)-1-chloroprop-1-ene Chemical compound C\C=C\Cl OWXJKYNZGFSVRC-NSCUHMNNSA-N 0.000 description 1
- XEPXTKKIWBPAEG-UHFFFAOYSA-N 1,1-dichloropropan-1-ol Chemical compound CCC(O)(Cl)Cl XEPXTKKIWBPAEG-UHFFFAOYSA-N 0.000 description 1
- BZPCMSSQHRAJCC-UHFFFAOYSA-N 1,2,3,3,4,4,5,5,5-nonafluoro-1-(1,2,3,3,4,4,5,5,5-nonafluoropent-1-enoxy)pent-1-ene Chemical compound FC(F)(F)C(F)(F)C(F)(F)C(F)=C(F)OC(F)=C(F)C(F)(F)C(F)(F)C(F)(F)F BZPCMSSQHRAJCC-UHFFFAOYSA-N 0.000 description 1
- KNKRKFALVUDBJE-UHFFFAOYSA-N 1,2-dichloropropane Chemical compound CC(Cl)CCl KNKRKFALVUDBJE-UHFFFAOYSA-N 0.000 description 1
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical compound CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- KMZHZAAOEWVPSE-UHFFFAOYSA-N 2,3-dihydroxypropyl acetate Chemical compound CC(=O)OCC(O)CO KMZHZAAOEWVPSE-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- HXDLWJWIAHWIKI-UHFFFAOYSA-N 2-hydroxyethyl acetate Chemical compound CC(=O)OCCO HXDLWJWIAHWIKI-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 235000019737 Animal fat Nutrition 0.000 description 1
- 239000002028 Biomass Substances 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- UXDDRFCJKNROTO-UHFFFAOYSA-N Glycerol 1,2-diacetate Chemical compound CC(=O)OCC(CO)OC(C)=O UXDDRFCJKNROTO-UHFFFAOYSA-N 0.000 description 1
- 239000004348 Glyceryl diacetate Substances 0.000 description 1
- 239000004347 Glyceryl monoacetate Substances 0.000 description 1
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- CYTYCFOTNPOANT-UHFFFAOYSA-N Perchloroethylene Chemical group ClC(Cl)=C(Cl)Cl CYTYCFOTNPOANT-UHFFFAOYSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 239000005864 Sulphur Substances 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 229920002494 Zein Polymers 0.000 description 1
- XDODWINGEHBYRT-UHFFFAOYSA-N [2-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCCCC1CO XDODWINGEHBYRT-UHFFFAOYSA-N 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 239000010775 animal oil Substances 0.000 description 1
- 229910052787 antimony Inorganic materials 0.000 description 1
- WATWJIUSRGPENY-UHFFFAOYSA-N antimony atom Chemical compound [Sb] WATWJIUSRGPENY-UHFFFAOYSA-N 0.000 description 1
- 229910052785 arsenic Inorganic materials 0.000 description 1
- RQNWIZPPADIBDY-UHFFFAOYSA-N arsenic atom Chemical compound [As] RQNWIZPPADIBDY-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- BMRWNKZVCUKKSR-UHFFFAOYSA-N butane-1,2-diol Chemical compound CCC(O)CO BMRWNKZVCUKKSR-UHFFFAOYSA-N 0.000 description 1
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 1
- 229910052793 cadmium Inorganic materials 0.000 description 1
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 150000001728 carbonyl compounds Chemical class 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- NEHMKBQYUWJMIP-NJFSPNSNSA-N chloro(114C)methane Chemical compound [14CH3]Cl NEHMKBQYUWJMIP-NJFSPNSNSA-N 0.000 description 1
- HRYZWHHZPQKTII-UHFFFAOYSA-N chloroethane Chemical compound CCCl HRYZWHHZPQKTII-UHFFFAOYSA-N 0.000 description 1
- YACLQRRMGMJLJV-UHFFFAOYSA-N chloroprene Chemical compound ClC(=C)C=C YACLQRRMGMJLJV-UHFFFAOYSA-N 0.000 description 1
- 239000003245 coal Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 238000010924 continuous production Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 208000012839 conversion disease Diseases 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 125000000853 cresyl group Chemical class C1(=CC=C(C=C1)C)* 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- PDXRQENMIVHKPI-UHFFFAOYSA-N cyclohexane-1,1-diol Chemical compound OC1(O)CCCCC1 PDXRQENMIVHKPI-UHFFFAOYSA-N 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- RCJVRSBWZCNNQT-UHFFFAOYSA-N dichloridooxygen Chemical compound ClOCl RCJVRSBWZCNNQT-UHFFFAOYSA-N 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000010981 drying operation Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000002573 ethenylidene group Chemical group [*]=C=C([H])[H] 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- UHCBBWUQDAVSMS-UHFFFAOYSA-N fluoroethane Chemical compound CCF UHCBBWUQDAVSMS-UHFFFAOYSA-N 0.000 description 1
- XUCNUKMRBVNAPB-UHFFFAOYSA-N fluoroethene Chemical compound FC=C XUCNUKMRBVNAPB-UHFFFAOYSA-N 0.000 description 1
- 239000000446 fuel Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 150000002314 glycerols Chemical class 0.000 description 1
- 235000019443 glyceryl diacetate Nutrition 0.000 description 1
- 235000019442 glyceryl monoacetate Nutrition 0.000 description 1
- 150000002334 glycols Chemical group 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 1
- 238000011221 initial treatment Methods 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 239000011133 lead Substances 0.000 description 1
- 235000020778 linoleic acid Nutrition 0.000 description 1
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- KQQKGWQCNNTQJW-UHFFFAOYSA-N linolenic acid Natural products CC=CCCC=CCC=CCCCCCCCC(O)=O KQQKGWQCNNTQJW-UHFFFAOYSA-N 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 238000005360 mashing Methods 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 150000004702 methyl esters Chemical group 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- SNMVRZFUUCLYTO-UHFFFAOYSA-N n-propyl chloride Chemical compound CCCCl SNMVRZFUUCLYTO-UHFFFAOYSA-N 0.000 description 1
- 239000003345 natural gas Substances 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 150000002896 organic halogen compounds Chemical class 0.000 description 1
- 235000020030 perry Nutrition 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 239000005077 polysulfide Substances 0.000 description 1
- 150000008117 polysulfides Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- MWWATHDPGQKSAR-UHFFFAOYSA-N propyne Chemical group CC#C MWWATHDPGQKSAR-UHFFFAOYSA-N 0.000 description 1
- 238000010926 purge Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- 238000000197 pyrolysis Methods 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 235000003441 saturated fatty acids Nutrition 0.000 description 1
- 150000004671 saturated fatty acids Chemical class 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 238000010517 secondary reaction Methods 0.000 description 1
- 239000011669 selenium Substances 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000003760 tallow Substances 0.000 description 1
- 229950011008 tetrachloroethylene Drugs 0.000 description 1
- BFKJFAAPBSQJPD-UHFFFAOYSA-N tetrafluoroethene Chemical group FC(F)=C(F)F BFKJFAAPBSQJPD-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 238000010977 unit operation Methods 0.000 description 1
- 238000004148 unit process Methods 0.000 description 1
- 235000021122 unsaturated fatty acids Nutrition 0.000 description 1
- 150000004670 unsaturated fatty acids Chemical class 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 238000004457 water analysis Methods 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 239000005019 zein Substances 0.000 description 1
- 229940093612 zein Drugs 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/14—Fractional distillation or use of a fractionation or rectification column
- B01D3/143—Fractional distillation or use of a fractionation or rectification column by two or more of a fractionation, separation or rectification step
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/62—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by introduction of halogen; by substitution of halogen atoms by other halogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/74—Separation; Purification; Use of additives, e.g. for stabilisation
- C07C29/76—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment
- C07C29/80—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment by distillation
- C07C29/82—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment by distillation by azeotropic distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C31/00—Saturated compounds having hydroxy or O-metal groups bound to acyclic carbon atoms
- C07C31/34—Halogenated alcohols
- C07C31/36—Halogenated alcohols the halogen not being fluorine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C31/00—Saturated compounds having hydroxy or O-metal groups bound to acyclic carbon atoms
- C07C31/34—Halogenated alcohols
- C07C31/42—Polyhydroxylic acyclic alcohols
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D301/00—Preparation of oxiranes
- C07D301/02—Synthesis of the oxirane ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D301/00—Preparation of oxiranes
- C07D301/02—Synthesis of the oxirane ring
- C07D301/03—Synthesis of the oxirane ring by oxidation of unsaturated compounds, or of mixtures of unsaturated and saturated compounds
- C07D301/04—Synthesis of the oxirane ring by oxidation of unsaturated compounds, or of mixtures of unsaturated and saturated compounds with air or molecular oxygen
- C07D301/06—Synthesis of the oxirane ring by oxidation of unsaturated compounds, or of mixtures of unsaturated and saturated compounds with air or molecular oxygen in the liquid phase
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D301/00—Preparation of oxiranes
- C07D301/02—Synthesis of the oxirane ring
- C07D301/24—Synthesis of the oxirane ring by splitting off HAL—Y from compounds containing the radical HAL—C—C—OY
- C07D301/26—Y being hydrogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D303/00—Compounds containing three-membered rings having one oxygen atom as the only ring hetero atom
- C07D303/02—Compounds containing oxirane rings
- C07D303/08—Compounds containing oxirane rings with hydrocarbon radicals, substituted by halogen atoms, nitro radicals or nitroso radicals
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Epoxy Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Paints Or Removers (AREA)
- Epoxy Resins (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Catalysts (AREA)
Abstract
本申请披露了通过多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间的反应用于生产氯代醇的方法,根据所述方法所使用的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有至少一种固体或溶解的金属盐,该方法包括一分离操作以除去至少部分的金属盐。
Description
本申请是申请日为2006年5月19日,申请号为200680000566.8,发明名称为“在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法”的发明专利申请的分案申请。
本专利申请要求享有于2005年5月20日提交的专利申请FR05.05120和专利申请EP 05104321.4,以及于2005年11月8日提交的美国临时专利申请60/734659、60/734627、60/734657、60/734658、60/734635、60/734634、60/734637和60/734636的优先权,并将上述专利申请的内容合并于此作为参考。
本发明涉及一种用于生产一种有机物的方法,更具体而言涉及一种用于生产氯代醇的方法。
已知可以从地球上获得的天然石化资源例如油和天然气是有限的。目前这些资源被用于生产燃料以及作为起始产物用于生产大量有用的有机化合物,如用于生产塑料的单体或反应物,例如环氧乙烷、氯乙醇(参见,例如K.Weissermel and H.-J.Arpe in Industrial Organic Chemistry,Third Completely Revised Edition,VCH Editor,1997,page 149),环氧丙烷和一氯丙醇(参见,例如K.Weissermel and H.-J.Arpe in Industrial Organic Chemistry,Third Completely Revised Edition,VCH Editor,1997,page 275),表氯醇或二氯丙烷(参见,例如Ullmann’s Encyclopedia of Industrial Chemistry,5.ed.,Vol.A9,p.539-540)。文献Documents Chemistry and Industry,November 20,1931,Part III,pages 949 to 954,and November 27,1931,Part III, pages 970to 975描述了一种由甘油和盐酸在作为催化剂的乙酸存在下用于合成二氯丙醇的方法。
根据已知的用于生产氯代醇的方法,产物通常以具有5到15重量%的滴定度的高度稀释的水溶液形式得到。接着对它的纯化是非常昂贵的。而且,根据这样的方法得到的主要异构体是2,3-二氯丙-1-醇。
希望找到能够使得降低天然石化资源的消耗成为可能的用途和方法,尤其是上面提到的用途。
还希望找到用于再利用其它生产过程的副产物的方法,使得必须消除或破坏掉的副产物的总量最小。
还希望找到用于使与高度稀释的水溶液相联系的分离操作的费用最小化的方法。
因此,本发明涉及一种通过多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间的反应用于生产氯代醇的方法,根据该方法所使用的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有至少一种固体或溶解的金属盐,该方法包括一分离操作以除去至少部分金属盐。
术语“多羟基脂肪烃”是指一种含有至少两个连接到两个不同的饱和碳原子上的羟基基团的烃。该多羟基脂肪烃可以含有但不限于2到60个碳原子。
每个带有羟基官能团(OH)的多羟基脂肪烃的碳原子不能具有多于1个的OH基团,并且必须具有sp3杂化。带有OH基团的碳原子可以是伯碳、仲碳或叔碳。在本发明中使用的多羟基脂肪烃必须含有至少两个sp3杂化的各带有一个OH基团的碳原子。该多 羟基脂肪烃包括含有连二醇(1,2-二醇)或连三醇(1,2,3-三醇)的任何烃,包括这些重复单元的相连或相邻的更高级的排序。该多羟基脂肪烃的定义还包括例如一个或多个1,3-、1,4-、1,5-和1,6-二醇官能团。该多羟基脂肪烃也可以是聚合物如聚乙烯醇。例如偕二醇是排除在这类多羟基脂肪烃之外的。
应该理解该多羟基脂肪烃可以含有芳香部分或杂原子,包括例如卤素、硫、磷、氮、氧、硅和硼这些杂原子,以及它们的混合物。
可以在本发明中使用的多羟基脂肪烃包括:如1,2-乙二醇(乙二醇)、1,2-丙二醇(丙二醇)、1,3-丙二醇、1-氯-2,3-丙二醇(氯丙二醇)、2-氯-1,3-丙二醇(氯丙二醇)、1,4-丁二醇、1,5-戊二醇、环己二醇、1,2-丁二醇、1,2-环己烷二甲醇、1,2,3-丙三醇(也称为“甘油”或“丙三醇”),以及它们的混合物。用于本发明的优选的多羟基脂肪烃包括:例如1,2-乙二醇、1,2-丙二醇、1,3-丙二醇、1,2,3-丙三醇,以及它们的混合物。更优选地,用于本发明的多羟基脂肪烃包括:例如1,2-乙二醇、1,2-丙二醇、氯丙二醇和1,2,3-丙三醇,以及它们的任意混合物。最优选的是1,2,3-丙三醇。
多羟基脂肪烃的酯可以存在于多羟基脂肪烃中,和/或可以在根据本发明的生产氯代醇的过程中生成,和/或可以在生产氯代醇的过程之前生产。多羟基脂肪烃的酯的例子包括:乙二醇单乙酸酯、丙二醇单乙酸酯、甘油单乙酸酯、甘油单硬脂酸酯、甘油二乙酸酯以及它们的混合物。
术语“氯代醇”是指一种含有连接到不同饱和碳原子上的至少一个羟基基团和至少一个氯原子的化合物。含有至少两个羟基的氯代醇也是一种多羟基脂肪烃。相应地,本发明的起始物质和产物可以分别是氯代醇。在这种情况下,产物氯代醇比起始的氯代醇是更深度氯化的,换言之,产物氯代醇比起始的氯代醇具有更多的氯原 子和更少的羟基基团。优选的氯代醇是例如氯乙醇、氯丙醇、氯丙二醇以及二氯丙醇,而最优选的是二氯丙醇。特别优选的氯代醇是2-氯乙醇、1-氯丙-2-醇、2-氯丙-1-醇、1-氯丙-2,3-二醇、2-氯丙-1,3-二醇、1,3-二氯丙-2-醇、2,3-二氯丙-1-醇以及它们的混合物。
该多羟基脂肪烃可以是合成的多羟基脂肪烃、由可再生原料得到的多羟基脂肪烃、或它们的混合物。优选地,在根据本发明的方法中使用的多羟基脂肪烃至少部分是由可再生原料生产的。将相同的提法(或考虑因素)应用于多羟基脂肪烃的酯、或多羟基脂肪烃的酯与多羟基脂肪烃的混合物。
表述“合成”是指该多羟基脂肪烃是由化石原料得到的。其中化石原料,其是指由例如石油、天然气和煤这样的天然石化原料得到的材料。在这些材料中优选的是含有二和三个碳原子的有机化合物。当该氯代醇是二氯丙醇或氯丙二醇时,烯丙基氯、烯丙醇以及“合成”甘油是更优选的。其中“合成”甘油,其是指由石化原料得到的甘油。当该氯代醇是氯乙醇时,乙烯和“合成”乙二醇是更优选的。其中“合成”乙二醇,其是指由石化原料得到的乙二醇。当该氯代醇是氯丙醇时,丙烯和“合成”丙二醇是更优选的。其中“合成”丙二醇,其是指石化原料得到的丙二醇。将相同的提法(或考虑因素)应用于多羟基脂肪烃的酯、或多羟基脂肪烃的酯与多羟基脂肪烃的混合物。
其中可再生原料,其是指由加工可再生原料得到的材料。在这些材料中优选的是天然乙二醇、天然丙二醇和天然甘油。“天然”乙二醇、丙二醇和甘油可以由例如通过热化学方法转化糖得到的,这些糖可以由生物质加工得到,如在“Industrial Bioproducts:Today and Tomorrow,Energetics,Incorporated for the U.S.Department of Energy,Office of Energy Efficiency and Renewable Energy,Office of the Biomass Program,July 2003,pages 49,52 to 56中加以描述的。这 些方法其中之一是例如,催化氢解通过热化学转化葡萄糖得到的山梨醇。另外一个方法是例如,催化氢解通过木糖加氢得到的木糖醇。该木糖可以通过例如水解存在于玉米纤维中的半纤维素得到。
表述“由可再生原料得到的甘油”或“天然甘油”尤其是指在生产生物柴油过程中得到的甘油,或者在通常如皂化、酯基转移(或酯交换)作用或水解反应转化植物或动物脂肪或油时得到的甘油。
在本申请可以用的油中,其可以提及所有现存的油,如玉米油、葵花(籽)油、陈旧的或新的菜籽油、巴巴苏油、椰子油、甘蓝树油、棕榈油、蓖麻油和棉(籽)油、花生油、大豆油、亚麻油和海甘蓝油,以及所有由通过基因修饰或杂交得到的向日葵作物或菜籽作物而得到的油。甚至可以使用煎炸过的陈油,各种动物油,如鱼油、牛油、猪油、甚至肢解的脂肪。在使用的油中,还可以指例如通过多聚或低聚而部分改性的油,例如“亚麻籽油定油”、葵花籽油和吹制植物油。
在转化动物脂肪时可以得到一种特别合适的甘油。另外一种特别合适的甘油可以在生产生物柴油时得到。又一种特别合适的甘油可以在多相催化剂存在下通过酯基转移(或酯交换)作用转化植物或动物的脂肪或油时得到,如在申请文件FR 2752242、FR 2869612和FR 2869613中所描述的。更具体而言,该多相催化剂选自铝和锌的混合氧化物,锌和钛的混合氧化物,锌、钛和铝的混合氧化物,以及铋和铝的混合氧化物,并且该多相催化剂是以固定床的形式使用的。在根据本发明的方法中,甘油可以是如在与本申请同日以SOLVAY SA名义提交的名称为“Process for preparing a chlorohydrin by chlorinating a polyhydroxylated aliphatic hydrocarbon”的申请中所描述的,并将上述申请的内容合并于此作为参考。
尤其提及一种用于生产氯代醇的方法,其中以元素形式表示的总金属含量大于或等于0.1μg/kg且小于或等于1000mg/kg的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂进行反应。
与之相反,“合成的多羟基脂肪烃”通常由石化产品资源获得。将相同的提法(或考虑因素)应用于多羟基脂肪烃的酯、或多羟基脂肪烃的酯与多羟基脂肪烃的混合物。
在根据本发明制备环氧化物的方法中,使用的多羟基脂肪烃可以是多羟基脂肪烃的粗产物或多羟基脂肪烃的纯化产物。多羟基脂肪烃的“粗”产物是在其生产之后未进行过任何处理。多羟基脂肪烃的“纯化”产物是在其生产之后进行过至少一次处理。当多羟基脂肪烃是由可再生原料获得的粗产物时,它可以含有例如除金属盐之外的水。该金属盐尤其是金属氯化物,其优先选自NaCl和KCl。该金属盐还可以选自金属硫酸盐,如硫酸钠和硫酸钾。在根据本发明方法中使用的多羟基脂肪烃含有至少一种固体或溶解的金属盐,其优先选自氯化钠、氯化钾、硫酸钠和硫酸钾。在根据本发明方法中使用的多羟基脂肪烃通常含有至少0.5重量%的金属盐含量,优选大于或等于大约1重量%,更优选大于或等于大约2重量%,最优选大于或等于大约3重量%。该金属盐含量通常至多为15重量%,优选小于或等于大约10重量%,更优选小于或等于大约7.5重量%,最优选小于或等于大约5重量%。将相同的提法(或考虑因素)应用于多羟基脂肪烃的酯、或多羟基脂肪烃的酯与多羟基脂肪烃的混合物。
在根据本发明的方法中,多羟基脂肪烃的粗产物可以含有有机杂质如羰基化合物,尤其是醛、脂肪酸、脂肪酸的盐或脂肪酸的酯,如尤其是多羟基脂肪烃与脂肪酸可选在与水的组合物中的单酯或多元酯。当多羟基脂肪烃是甘油时,优选的脂肪酸是含有多于12个碳院子的饱和和不饱和脂肪酸,例如油酸、亚油酸和亚麻酸。这 些酸是例如通过皂化、酯基转移(酯交换)或水解反应转化菜籽油的过程中产生的。优选的脂肪酸酯是甲基酯。
在根据本发明的方法中,该粗产物通常含有至多10重量%的有机杂质,经常为8%的有机杂质。经常地,该粗产物含有至多6重量%的有机杂质。优选地,它含有至多2重量%的有机杂质。最优选地,它含有至多1重量%的有机杂质。典型地,该有机杂质基本上由脂肪酸和其衍生物组成。
此外,本申请还涉及一种用于生产氯代醇的方法,根据该方法使含有至多8重量%的有机杂质的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂进行反应。
令人惊奇地,研究发现使用具有高含量的有机杂质的粗产物对于进行本发明方法的反应基本上没有影响。来自该有机杂质的可选的副产物可以很容易地从反应混合物中除去,例如(如果可适用的话)如在以SOLVAY SA名义提交的专利申请WO 2005/054167第17页第33行到第18页第33行、第24页第8行到第25页第10行中所描述的通过控制清洗物的比率来实现,将上述申请的内容合并于此作为参考。
在根据本发明的方法中,该多羟基脂肪烃的粗产物通常含有至少40重量%的多羟基脂肪烃。经常地,该粗产物含有至少50重量%的多羟基脂肪烃。优选地,它含有至少70重量%的多羟基脂肪烃。经常地,该粗产物含有至多99重量%的多羟基脂肪烃。典型地,它含有至多95重量%的多羟基脂肪烃。
在根据本发明的方法中,该多羟基脂肪烃的粗产物通常含有至少5重量%的水,或者在不存在不是水和多羟基脂肪烃的其它化合物时含有至少1重量%的水。在根据本发明的方法中,该多羟基脂 肪烃的粗产物通常含有至多50重量%的水,或者在不存在不是水和多羟基脂肪烃的其它化合物时含有至多60重量%的水。经常地,该多羟基脂肪烃的粗产物含有至多30重量%的水,优选为至多21重量%的水。
在另一实施例中,该多羟基脂肪烃的粗产物含有至多89重量%的多羟基脂肪烃。在该实施例中,多羟基脂肪烃的粗产物含有至多85重量%的多羟基脂肪烃。在该实施例中,多羟基脂肪烃的粗产物通常含有至少10重量%的水,而经常含有至少14%的水。
该多羟基脂肪烃的粗产物具有至少0.5重量%的金属盐含量,优选为大于或等于大约1%,而更优选为大于或等于大约1.5%。该多羟基脂肪烃的粗产物具有至多15重量%的金属盐含量,优选为小于或等于12%,而更优选为小于或等于大约7.5%。
根据本发明的分离操作尤其优选应用于由多羟基脂肪烃起始的氯代化合物的生产中,尤其是应用于氯代醇和环氧化物的生产中。令人惊奇地,本发明的分离操作使得由可再生原料经济地获得这些化合物成为可能。
术语“环氧化物”是用来描述一种含有至少一个桥接在碳-碳键上的氧的化合物。通常而言,该碳-碳键的碳原子是相邻的,并且该化合物可以含有除碳原子和氧原子以外的原子,例如氢原子和卤素。优选的环氧化物是环氧乙烷、环氧丙烷、缩水甘油和表氯醇。
因此,本发明还尤其涉及一种用于生产氯代有机化合物的方法,根据该方法使用由可再生原料获得的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物,而所使用的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有至少一种固体或溶解的金属盐,并且该方法包括一分离操作以除去至少部分的金属盐。
应该理解,本文中所描述的生产方法还可以利用普通的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物来实施,而不局限于优选使用的由可再生原料获得的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物。
在下面,表述“氯代化合物”应该理解为“氯代醇”。优选的氯代醇是例如氯乙醇、氯丙醇、氯丙二醇和二氯丙醇,而二氯丙醇是最优选的。
术语“氯乙醇”是用来表示包括2-氯乙醇的混合物。
术语“氯丙醇”是用来表示包括1-氯丙-2-醇和2-氯丙-1-醇的混合物。
术语“氯丙二醇”是用来表示包括1-氯丙-2,3-二醇和2,3-二氯丙-1-醇的混合物。
在根据本发明生产氯代醇的方法中,该氯化剂可以是如在SOLVAY SA的专利申请WO 2005/054167的第4页第30行到第6页第2行中所描述的氯化氢和/或盐酸。尤其提及的氯化剂可以是气体氯化氢、盐酸水溶液或二者的组合。氯化氢可以从热解有机氯化物的过程例如从氯乙烯生产过程中得到,从生产4,4-亚甲基二丙基二异氰酸酯(MDI)或甲苯基二异氰酸酯(TDI)过程中,从金属清洗过程中,或从如硫酸或磷酸这样的无机酸与如氯化钠、氯化钾或氯化钙这样的金属氯化物反应中得到。
在根据本发明生产氯代醇的方法中,该氯化剂可以是氯化氢水溶液或优选的无水氯化氢,来源于用于生产烯丙基氯的装置和/或用于生产氯甲烷的装置和/或氯解装置和/或高温氧化装置,如在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin by reaction between a multi-hydroxylated aliphatic hydrocarbon and a chlorinating agent”的申请中加以披露,并将上述申请内容合并于此作为参考。
特别提及一种由多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物和氯化剂制备氯代醇的方法,该试剂含有至少一种如下的化合物:氮(气)、氧(气)、氢(气)、氯(气)、碳氢化合物(或烃)、有机卤化物、有机氧化物以及金属。
特别提及一种选自芳香烃、饱和及不饱和脂肪烃或它们的混合物的碳氢化合物。
特别提及一种选自乙炔、乙烯、丙烯、丁烯、丙二烯、甲基乙炔以及它们的混合物的不饱和脂肪烃,选自甲烷、乙烷、丙烷、丁烷以及它们的混合物的饱和脂肪烃以及芳香烃苯。
特别提及一种选自氯甲烷、氯乙烷、氯丙烷、氯丁烷、氯乙烯、偏氯乙烯、一氯丙烯、全氯乙烯、三氯乙烯、氯丁二烯、氯苯以及它们的混合物的有机氯化物的有机卤代物。
特别提及一种选自氟代甲烷、氟代乙烷、氟乙烯、偏氟乙烯以及它们的混合物的有机氟化物的有机卤代物。
特别提及一种选自醇、氯醇、含氯醚以及它们的混合物的有机氧化物。
特别提及选自碱金属、碱土金属、铁、镍、铜、铅、砷、钴、钛、镉、锑、汞、锌、硒、铝、铋以及它们的混合物的金属。
更特别提及一种方法,其中该氯化剂至少一部分是从生产烯丙基氯的过程中和/或从生产氯甲烷的过程中和/或从氯解的过程和/或从在温度高于或等于800℃时氧化氯化物的过程中得到的。
在一更优选的实施例中,该氯化剂不含有气体氯化氢。
根据本发明的用于生产氯代醇的方法可以在如SOLVAY SA的申请WO 2005/054167的第6页第3行到第23行所具体披露的反应器中进行。
特别提及一种由在反应条件下耐氯化剂尤其是氯化氢的材料制造或涂覆的装置。更特别提及一种由搪瓷钢或钽制造的装置。根据本发明的用于生产氯代醇的方法可以在由耐氯化剂的材料制造或涂覆的装置中进行,如在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin in equipments resisting to corrosion”的专利申请中所描述的,并将上述专利申请的内容合并于此作为参考。
特别提及一种用于生产氯代醇的方法,该方法包括一个多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与含有氯化氢的氯化剂进行反应的步骤,以及至少另一个是在由在这些步骤的条件下耐氯化剂的材料制造或涂覆(或覆盖)的设备中进行反应的步骤。更特别提及的是金属材料如搪瓷钢、金和钽,以及非金属材料如高密度聚乙烯、聚丙烯、聚偏氟乙烯、聚四氟乙烯、全氟烷氧基烷烃和聚全氟丙基乙烯基醚、聚砜和多硫化物(或聚硫化物)、石墨以及浸渍的石墨。
根据本发明的用于生产氯代醇的方法可以在如与本申请同日以SOLVAY SA名义提交的名称为“Continuous process for the manufacture of chlorohydrins”的申请中所描述的反应介质中进行,并将上述申请的内容合并于此作为参考。
特别提及一种用于生产氯代醇的连续方法,其中多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物在液体反应介质中与氯化剂 和有机酸进行反应,该介质的稳态组成(或稳定态组成)包括多羟基脂肪烃和多羟基脂肪烃的酯,以多羟基脂肪烃的摩尔数表示的多羟基脂肪烃和多羟基脂肪烃的酯的总含量大于1.1mol%且小于或等于30mol%,该百分比是以相对于该液体反应介质的有机部分表示的。
该液体介质的有机部分被定义为该液体介质的有机化合物的总和,也就是说,所述化合物分子含有至少一个碳原子。
在根据本发明生产氯代醇的方法中,该多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂的反应可以在如SOLVAY SA的专利申请WO 2005/054167的第6页第28行到第8页第5行中所具体披露的催化剂存在下进行。特别提及一种基于常压沸点高于或等于200℃的羧酸或羧酸衍生物的催化剂,尤其是己二酸和己二酸的衍生物的催化剂。
在根据本发明生产氯代醇的方法中,该多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂的反应可以在如SOLVAY SA的专利申请WO 2005/054167的第8页第6行到第10页第10行中所具体披露的温度、压力和滞留时间下进行。
特别提及的是温度为至少20℃至多160℃,压力为至少0.3巴至多100巴,而滞留时间为至少1h至多50h。
在根据本发明生产氯代醇的方法中,该多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂的反应可以在如SOLVAY SA的专利申请WO 2005/054167的第11页第12行到第36行中所具体披露的溶剂存在下进行。
特别提及的是如氯化有机溶剂,醇,酮,酯或醚,如氯乙醇、氯丙醇、氯丙二醇、二氯丙醇、二氧杂环己烷、苯酚、甲酚以及氯 丙二醇和二氯丙醇的混合物这样的与该多羟基脂肪烃不混溶的无水溶剂,或者如该多羟基脂肪烃的至少部分氯化和/或酯化的低聚物这样的重反应产物的有机溶剂。
在根据本发明生产氯代醇的方法中,该多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间的反应可以在如与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin in a liquid phase”的专利申请中所描述的含有重化合物的液相存在下进行,并将上述申请的内容合并于此作为参考。
特别提及一种生产氯代醇的方法,其中多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物在含有重化合物的液相存在下与氯化剂进行反应,而该液相在绝对压力1巴下的沸点温度至少比在绝对压力1巴下该氯代醇的沸点温度高15℃。
根据本发明用于生产氯代醇的方法可以以间歇方式或连续方式进行。尤其优选的是连续方式。
在根据本发明生产氯代醇的方法中,该多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间的反应优选在液体反应介质中进行。该液体反应介质可以是单相介质或多相介质。
该液体反应介质是由在反应温度下所有的溶解或分散的固体化合物、溶解或分散的气体以及溶解或分散的液体组成的。
该反应介质包括反应物,催化剂,溶剂,在反应物中、催化剂中和溶剂中存在的杂质,反应中间体,反应产物以及反应副产物。
其中反应物,其是指该多羟基脂肪烃、多羟基脂肪烃的酯和氯化剂。
在多羟基脂肪烃中存在的杂质中可以提及羧酸,羧酸盐,脂肪酸与多羟基脂肪烃的酯,脂肪酸与用于酯基转移过程中的醇形成的酯,以及如碱金属或碱土金属的氯化物(或盐酸盐)和硫酸盐这样的无机盐。
当该多羟基脂肪烃是甘油时,在甘油中的杂质可以提及羧酸,羧酸盐,如单酸甘油酯、二酸甘油酯和三酸甘油酯的脂肪酸酯,脂肪酸与用于酯基转移过程中的醇的形成的酯,以及如碱金属或碱土金属的氯化物和硫酸盐这样的无机盐。
在反应中间体中,其可以提及该多羟基脂肪烃的一氯代醇和它们的酯和/或聚酯,该多羟基脂肪烃的酯和/或聚酯以及该多氯代醇的酯。
当该氯代醇是二氯丙醇时,其在反应中间体中可以提及甘油的一氯代醇和它的酯和/或聚酯,甘油的酯和/或聚酯以及二氯丙醇的酯。
因而,该多羟基脂肪烃的酯可以是反应物、该多羟基脂肪烃的杂质或反应中间体。
其中反应产物,其用来指氯代醇和水。水可以是在氯代反应中形成的水和/或引入到该方法中的水。
在副产物中,其可以提及例如该多羟基脂肪烃的部分氯化和/或酯化的低聚物。
当该多羟基脂肪烃是甘油时,在副产物中可以提及甘油部分氯化和/或酯化的低聚物。
在该方法的不同步骤中可以形成该反应中间体和副产物,例如在该氯代醇的生产过程中或者在该氯代醇的分离步骤中。
因而,该液体反应介质可以含有该多羟基脂肪烃,溶解或以气泡形式分散的氯化剂,催化剂,溶剂,在反应物中、催化剂中和溶剂中存在的杂质,如溶解的或固体的盐,例如反应中间体、反应产物以及反应副产物。
在根据本发明的方法中,从反应介质中分离氯代醇以及其它化合物可以采用与在SOLVAY SA的专利申请WO 2005/054167的第12页第1行到第16页第35行和第18页第6行到第13行中所披露的方法进行。这些其它化合物是那些在上面已经提及的,并且包括未消耗的反应物,在反应物、催化剂和溶剂中存在的杂质,催化剂,溶剂,反应中间体,水以及反应的副产物。
在根据本发明的方法中,分离和处理反应介质中的其它化合物可以如在SOLVAY SA的专利申请WO 2005/054167的第18页第6行到第13行中所披露的方法进行。
特别提及的是水/氯代醇/氯化剂的混合物在氯化剂损失最小的条件下通过共沸蒸馏的分离,该氯代醇分离后接着进行沉析(或倾析)。
在根据本发明生产氯代醇的方法中,从反应介质中将氯代醇与其它化合物分离开可以如在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin”的专利申请中披露的相同的方法进行,并将上述申请的内容合并于此作为参考。
特别提及一种用于制备氯代醇的方法,其中包括如下步骤:(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂和有机酸反应从而得到含有该氯代醇和该氯代醇的酯的混合物, (b)将在步骤(a)中得到的至少部分混合物在步骤(a)之后的步骤中进行一次或多次处理,以及(c)在步骤(a)之后的至少一个步骤中加入该多羟基脂肪烃,使得在温度为至少20℃时与氯代醇酯反应,以便至少部分形成多羟基脂肪烃的酯。更特别提及一种方法,其中该多羟基脂肪烃是甘油,而该氯代醇是二氯丙醇。
在根据本发明生产氯代醇的方法中,从反应介质中分离氯代醇和其它化合物可以采用在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin from a multi-hydroxylated aliphatic hydrocarbon”的申请中所描述的相同的方法进行,并将上述申请的内容合并于此作为参考。
特别提及一种通过多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间在带有一个或多个液流进料的反应器中的反应用于生产氯代醇的方法,相对于引入该反应器中的全部液流的总重量而言,该液流含有小于50重量%的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物。更特别提及一种方法,包括如下步骤:(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂反应从而得到含有氯代醇、水和氯化剂的至少一种介质,(b)取出在反应步骤(a)中得到的至少一部分混合物,以及(c)将在步骤(b)中取出的部分(或馏分)进行蒸馏和/或汽提操作,其中加入该多羟基脂肪烃以便从在步骤(b)中取出的部分(或馏分)中分离出含有水和氯代醇的混合物,并且其与在步骤(b)中取出的馏分相比表现出降低的氯化剂含量。
在根据本发明生产氯代醇的方法中,从反应介质中分离氯代醇和其它化合物可以采用在与本申请同日以SOLVAY SA名义提交的名称为“Process for converting multi-hydroxylated aliphatic hydrocarbons into chlrohydrins”的专利申请中所描述的相同的方法进行,并将上述申请的内容合并于此作为参考。
特别提及一种包括如下步骤用于生产氯代醇的方法:包括以下步骤:(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂反应,从而得到含有氯代醇、氯代醇的酯和水的混合物;(b)将至少一部分(或馏分)在步骤(a)中得到的混合物进行蒸馏和/或汽提处理,从而得到富集(或浓缩)有水、氯代醇和氯代醇的酯的部分;以及(c)将至少一部分在步骤(b)中得到的部分(或馏分)在存在至少一种添加剂的条件下进行分离操作,从而得到富集(或浓缩)有氯代醇和氯代醇酯且含有小于40重量%水的部分。该分离操作更特别的是沉析(或倾析)。
在根据本发明的方法中,从反应介质中分离和处理其它化合物可以采用在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing a chlorohydrin by chlorination of a multi-hydroxylated aliphatic hydrocarbon”的专利申请中所描述的相同的方法进行。优选的处理方法可以包括将一部分的其它产物进行高温氧化。
特别提及一种包括如下步骤的用于生产氯代醇的方法:(a)使碱金属和/或碱土金属含量小于或等于5g/kg的多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂和有机酸进行反应,从而得到至少含有氯代醇和℃副产物的混合物,(b)将至少一部分在步骤(a)中得到的混合物在步骤(a)后的步骤中进行一次或多次处理,以及(c)步骤(a)后的至少一个步骤是在温度高于或等于800℃时的氧化作用。更特别提及一种方法,其中在随后的步骤中取出在步骤(a)中得到的一部分混合物,并将该部分在取出过程中在温度高于或等于800℃时进行氧化。还特别提及一种方法,其中步骤(b)的处理是选自沉析(相分离)、过滤、离心、提取、洗涤、蒸发、汽提、蒸馏和吸附操作,或至少两种这些操作的组合的分离操作。
在根据本发明用于生产氯代醇的方法中,可以进行反应介质的蒸汽汽提,尤其是水蒸气汽提(或水蒸气蒸馏)。反应介质如上定义。该介质优选是如上定义的液体反应介质(液相)。当反应介质是液相时,表述“反应介质”还包括与液相平衡的气相。因而在下面,表述“反应介质”将用来不明确地指在其中多羟基脂肪烃与氯化剂之间发生反应的液相以及与该液相平衡的气相。当进行反应介质的蒸汽汽提时,可以获得含有1到5、有时为2到3、而优选为1.5到2.5mol/l的氯代有机化合物(尤其为氯代醇)的汽提馏分。该汽提馏分主要由水和氯代醇组成。
在根据本发明用于生产氯代醇的方法中,当氯代醇通过取出馏分(或部分)而没有完全从反应混合物中移出时,可以至少移出含有氯代醇的反应介质的另一馏分。
在根据本发明用于生产氯代醇的方法的这个方面,通常回收含有50到96重量%的氯代醇和至多50重量%的水的至少一种馏分。优选地,该馏分含有75到99.9重量%的氯代醇和0.01到25重量%的水,经常为75到99重量%的氯代醇和1到25重量%的水。
回收优选通过蒸馏或蒸发进行。在该步骤过程中获得的含有例如中间体、可选的多羟基脂肪烃和催化剂的其它馏分可以被再循环以与氯化剂反应。如在SOLVAY SA的专利申请WO 2005/054167第1页第32行到第11页第34行中所描述的,还可以分离含有反应重副产物的至少一种馏分,尤其是氯代的多羟基脂肪烃的聚合物,其可以被破坏或者可以可选地,例如通过脱氯化氢作用,用于生产多羟基脂肪烃的聚合物的过程中。
蒸馏或蒸发通常是在至少20℃的温度下进行的。该温度经常为至少60℃。其优选为至少70℃。蒸馏或蒸发通常是在至多180℃的温度下进行的。该温度经常为至多140℃。
蒸馏或蒸发通常在大于0.001巴的压力下进行。该压力优选大于或等于约0.003巴。蒸馏或蒸发通常在最大为15巴的压力下进行。该压力经常是最大为10巴。优选最大为7巴,更优选最大为1巴,更甚优选为最大1巴,而最优选为最大0.1巴。
蒸馏或蒸发操作可以利用蒸馏塔或利用蒸发器、膜蒸发器或作为替代方案的扫壁式薄膜蒸发器进行。
残留物的可回收馏分可以通过配有内部或外部冷凝器的扫壁式薄膜蒸发器从中有利地分离。化学操作的一个实例是残留物的水解用以回收例如催化剂。
在本发明的方法的一具体变化方案中,当氯代醇是二氯代醇时,该二氯代醇根据包括下列步骤的方法生产:
(a)第一反应步骤,其中使多羟基脂肪烃与氯化剂进行接触,从而获得至少包含一氯代醇的一部分产物(或产物的一种馏分);
(b)可选将至少部分的产物馏分(或部分产物)进行干燥操作;
(c)将至少部分的可选干燥的产物馏分(或部分产物)引入到第二反应步骤中,其中至少部分的一氯代醇与氯化剂反应。
该变化方案中的步骤(a)和(c)优选在一定条件下,并以如上所描述的根据本发明用于生产氯代醇的方法的优选值进行。然而,优选的是在水的存在下实施步骤(a)的反应,其中水的含量优选为反应介质总重量的3~40重量%。
例如,可以在步骤(a)或(c)的至少一个反应器中通过汽提操作或利用置于反应器外部的再循环管上的蒸发器或者通过蒸馏进行步骤(b)。根据另一优选的变化方案,通过膜技术除去水。
根据本发明生产氯代醇的方法可以例如在级联反应器、在至少一个板式塔或在至少一个泡罩塔、或者这些反应器的组合装置中进行。
反应器可以有效地是通过内部搅拌或通过在反应器外部的再循环管搅拌的类型。
当在根据本发明的方法中加热反应介质时,可以例如通过夹套或通过内部热交换器进行加热。也可以通过在反应器外部再循环管上的热交换器进行加热。可选地,通过组合使用夹套和在反应器外部再循环管上的热交换器进行加热。
尤其是当根据本发明的方法以连续或间歇进料模式操作时,次级反应可以导致反应器中低挥发性副产物的积累,其中或多或少的是多羟基脂肪烃的氯化低聚物。这种积累会导致反应介质体积的递增,导致生产能力损失的递增,从而需要连续或不连续地清洗反应器,以将体积保持在足够的水平。其中表述“清洗”,其是用来指取出反应介质的馏分(或部分)。
如果合适的话,这种清洗操作过程中除去的催化剂的量可以通过引入等量的纯的或纯化的催化剂来补偿。
来自反应混合物的清洗物中包含的催化剂可以经济地在纯化处理之后在反应器中再循环。例如,在水中具有低溶解度的催化剂可以进行水解处理,优选在高于30℃、优选至少50℃的温度下进行,接着是例如通过倾析(或相分离)、过滤或提取(或萃取)的 分离步骤。已经发现在己二酸的情况下,清洗物的水解导致在冷却和过滤之后以良好产率回收高纯度的结晶己二酸。
尤其是当根据本发明的方法以连续或间歇进料模式操作时,金属盐,尤其是NaCl(其可选存在于原材料,例如多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物中,来自于如上所述的可再生资源)可以在反应器中富集,在该反应器中进行多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂之间的反应。金属盐含量的增加导致不溶性物质的结晶的积累并导致与固体物质相关的各种问题,如在反应器壁上、搅拌器上和进料管线和清洗物管线上以及阀门上的沉积物形成,该不溶性物质导致反应混合物体积的增加。在反应器壁上的沉积物形成可以降低传热效率并需要增加量的能量以维持反应温度。在管线和阀门上的沉积物形成会导致堵塞问题。在反应混合物中的增加量的固体可以降低搅拌效率并且需要更大量的能量以实现适当的搅动。而金属盐含量的增加需要更高的连续或不连续的清洗频率,从而导致更高的产物损失。
然而令人惊奇的是在根据本发明的方法中存在金属盐是可接受的,因此希望可以从例如反应系统中除去至少一部分的金属盐,尤其是NaCl,从而防止金属盐在反应混合物中的任意积累。这样的除去可以适宜地通过使含有固体或溶解的金属盐的反应混合物的至少一部分(或一种馏分)进行处理(其包括至少一种分离操作)来实施用以从所述部分(或馏分)中除去至少一部分金属盐。
该分离操作可以选自液/固、液/液、液/气和固/气分离。
该液/固分离操作可以选自倾析(沉析或相分离)、离心、过滤、吸附以及用离子交换树脂处理。该液/液分离操作可以选自倾析和离心。该液/气分离操作可以选自汽提、蒸发和蒸馏。
液/固分离操作是优选的,过滤是更优选的,而过滤除去其中作为固体的金属盐是最优选的。
在根据本发明的方法中,反应优选是在反应混合物中进行的,而分离操作是在反应混合物的至少一部分中进行的。该部分反应混合物可以在该分离操作之前进行处理以除去至少一种不是金属盐的成分。该处理可以是汽提或蒸馏操作。
要进行分离操作的反应混合物的部分(或馏分)可以直接取自反应混合物中,特别是当反应是在液相中进行时。要进行分离操作的反应混合物的部分(或馏分)还可以取自反应混合物中并在除去金属盐之前进行另外的处理。适宜的处理的实例是对反应混合物的液体部分进行浓缩操作,其中挥发性化合物如起始原料和反应产物,其可以可选地进行回收和/或再循环至反应混合物中,例如通过汽提、蒸馏或蒸发来分离,从而获得具有增加含量的固体或溶解的金属盐的浓缩馏分(或部分)并进行处理以便分离金属盐。
因而,该分离步骤可以如在SOLVAY SA的专利申请WO 2005/054167第12页第1行至第18页第13行中所描述的用于生产氯代醇的方法的任何步骤中进行,例如在氯化反应之后、在从反应混合物中移出氯代醇和水的混合物的步骤之后、在通过蒸馏后蒸发移出氯代醇之后、在反应副产物的清洗之后或在用于从清洗物中回收催化剂的处理之后进行。
在一优选实施例中,该含有金属盐的反应混合物的部分是从反应在其中发生的反应器的清洗物中得到的,并被送入到至少一个分离单元中,在该分离单元中例如通过吸附、蒸馏、提取、沉析、离心、过滤以及用离子交换树脂处理来进行金属盐的分离。液/固分离操作是优选的,而过滤是更优选的。经分离的液体优选再循环回到反应器中而金属盐留在过滤器中。
过滤步骤可以在通常大于或等于4℃的温度下,优选大于或等于20℃,更优选大于或等于30℃,再优选大于或等于50℃,最优选大于或等于80℃的温度下进行。该温度通常低于或等于150℃,优选低于或等于140℃。
过滤系统的种类是非临界的并且对于知晓本发明的技术人员是显而易见的。对于适宜的过滤系统的描述可以在“Perry’s Chemical Engineers’Handbook,Sixth Edition,1984,Sections 19-65 to19-103”中找到。
对于金属盐在过滤系统中的积聚,通常推荐通过移出过滤出的盐而周期性地再生过滤单元。再生可以通过任何方式,例如通过移出尤其是通过机械方式移出固体或通过溶解盐来完成再生。可选地,可以将固体洗脱(或洗提)处理合并入再生程序中。
在根据本发明的一个实施例中,从过滤系统作为固体移出金属盐而无需任何预处理。
在第一变化方案中,以适宜的方式除去盐而无需进一步的处理。
在第二变化方案中,盐被储存在分离釜用于进一步的处理。进一步的处理可以包括用溶剂洗脱固体以及用溶剂溶解固体。这样的处理在下文中的优选具体实施例中加以描述。
在根据本发明的优选实施例中,在从过滤系统中移出金属盐之前,对该金属盐进行处理。
可选地,吸附的产物和反应物尤其是如催化剂和氯代醇及其酯可以从金属盐尤其是从NaCl中用适宜的洗脱溶剂如水和氯代醇的混合物通过洗脱来除去。水和氯代醇之间的任何比率都是适宜的。 优选使用在室温下饱和有水的氯代醇。特别优选使用由氯代醇和水之间的相分离而得到的一相。用作洗脱溶剂的氯代醇的水含量通常小于或等于20重量%,优选小于或等于15重量%,而最优选小于或等于约12重量%。在水和氯代醇的混合物中的水含量通常大于或等于1重量%。
在另一实施例中,洗脱溶剂基本上是由氯代醇组成的。在该实施例中,水含量通常小于1重量%,优选小于或等于0.5%中重量。
在又一实施例中,洗脱溶剂是水,例如如上定义的新鲜的水。
洗脱步骤可以在通常为大于或等于20℃的温度下进行,优选在大于或等于50℃,最优选在大于或等于80℃的温度下进行。该温度通常小于或等于150℃,而优选小于或等于140℃。
在洗脱后,用于洗脱金属盐的溶剂可以再循环至氯化反应器中。
可以实施若干个洗脱步骤。
尤其是,在用氯代醇洗脱之后,金属盐可以接着可选地用水溶液进一步洗脱。该水溶液可以来自于该方法的任何步骤。优选使用如上定义的新鲜的水。
洗脱步骤可以在通常为大于或等于20℃的温度下进行,优选在大于或等于50℃,最优选在大于或等于80℃的温度下进行。该温度通常小于或等于150℃,而优选小于或等于140℃。
在洗脱后,用于洗脱金属盐的水溶液可以被送入到氯化反应器中、脱氯化氢单元中、生物处理单元中或氧化处理单元中。
在第一变化方案中,在用氯代醇和水洗脱之后,盐作为固体以适宜的方式被移出而无需进一步的处理。该盐接着以适宜的方式被处置。
在第二变化方案中,在用氯代醇和水洗脱之后,盐被用水溶液溶解了。
该水溶液可以来自于该方法的任何步骤。优选使用如上定义的新鲜的水。
溶解步骤可以在通常为大于或等于20℃的温度下进行,优选在大于或等于50℃,最优选在大于或等于80℃的温度下进行。该温度通常小于或等于150℃,而优选小于或等于140℃。
含有溶解的金属盐的水溶液可以被处置。优选地,它可以被送入到脱氯化氢单元中、生物处理单元中或氧化处理单元中。
在上述的变化方案中,用水洗脱金属盐和用水溶解金属盐可以是单个单元操作的一部分。
当金属盐是氯化钠或氯化钾或硫酸钠或硫酸钾或它们的任意混合物时,上述操作是尤其适宜的,更尤其适用于氯化钠。
当清洗是以不连续方式进行时,一个过滤单元通常是足够的,因为过滤系统可以在清洗停车过程中进行再生。当清洗是以连续方式进行时,优选具有至少两个过滤单元交替工作,一个处于过滤模式而另一个处于再生模式。
过滤操作可以以间歇方式或连续方式进行。
当使用无水HCl作为氯化剂时,优选逆着HCl物流的流动引导含多羟基脂肪烃的液体流。当该过程在几个反应器中进行时,HCl有利地在两个反应器之间干燥,例如通过用合适的固体如分子筛吸附,或通过合适的膜进行反渗透。
根据本发明方法的该具体实施例使得可以特别经济地获得浓缩的氯代醇,其中氯代醇的含量经常是大于或等于氯代醇总重量的90重量%。当氯代醇是二氯丙醇时,通过该方法,可以获得1,3-二氯丙-2-醇作为主要异构体,而该异构体纯度大于80%。
在根据本发明的方法中,混合物可以含有以1,3-二氯丙-2-醇:2,3-二氯丙-1醇的质量比表示的1,3-二氯丙-2-醇和2,3-二氯丙-1醇的异构体通常大于或等于0.5,经常大于或等于3,常常大于或等于7,尤其大于或等于20.0。
本发明还涉及一种用于生产氯代醇的方法,根据该方法:
(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物在反应介质中与氯化剂进行反应,
(b)连续或周期性地取出至少含有水和氯代醇的一部分反应介质,
(c)将在步骤(b)中得到的反应介质(或馏分)的至少一部分引入到蒸馏步骤中,
(d)通过将水供给到所述蒸馏步骤而控制该蒸馏步骤的回流比。
反应介质是如上定义的。
在步骤(b)中的取出部分(或馏分)的水含量优选相对于取出部分的总重量大于或等于12重量%。
在步骤(b)中的取出部分(或馏分)还可以含有氯化氢。优选地,该部分是以其组分形式被连续取出的。得到的该部分可以在蒸馏步骤之后随后进行沉析(或相分离)操作。
步骤(a)的反应介质可以供给水,尤其是水蒸气。该进料可以用来源于适当的管线的外来水或者可选地用从其它单元反应或操作回收的残留水来实现。
该进料通常以这样的方式实施,以便将反应介质中的水含量维持在如在以SOLVAY SA名义的专利申请WO 2005/054167第10页第31行到第11页第11行中所描述的范围内。
连续或周期性取出可以通过向蒸馏步骤中引入气相来实现,具体而言是取出与液相处于平衡状态的气相并将该气相引入到蒸馏步骤中。在根据本发明的方法的具体实施例中,步骤(a)到(d)是在顶部装有合适蒸馏塔的反应器中进行的。步骤(a)是在该反应器中进行的。该实施例当盐酸水溶液用作氯化剂时是特别合适的。当氯化剂不含有气体氯化氢时它是最合适的。在根据本发明的方法的另一实施例中,还可以将蒸馏塔和反应器分开布置,反应器的底部液体可以被送回到反应介质中。该实施例在氯化氢例如气态或基本无水的氯化氢用作氯化剂时特别合适。无水的氯化氢通常具有小于或等于40重量%的水含量,优选小于或等于30重量%,而最优选小于或等于25重量%。无水的氯化氢的水含量通常大于或等于1ppm重量。
在一个方面,将要引入到与反应器分开的蒸馏塔中的部分(或馏分)连续或周期性地、优选连续地从液体反应混合物中取出,并 将至少水和氯代醇分离。此外,含有机产物如重副产物的一个或多个部分(或馏分),具体是催化剂和/或氯化氢也可以在该蒸馏步骤中分离,并通常再循环至反应混合物中。通过选择合适的回流比,可以在这一方面分离至少含有水、基本不含氯化氢的馏分。
回流比可以通过供给水而适当地加以调整,该水优选基本不含氯化氢并进入蒸馏塔中。在该实施例中,优选将水供给到蒸馏塔顶。可以例如通过将至少一部分在蒸馏操作中分离的水再循环至蒸馏塔顶而供给水。还可以通过将新鲜的水加入至蒸馏塔顶而供给水。这两种供给水的方式可以结合使用。加入新鲜的水得到尤其好的结果。
“基本不含氯化氢”具体理解为含水馏分(或部分)中的氯化氢含量等于或小于含水馏分总重量的10重量%。经常是该含量等于或小于5重量%,优选等于或小于1重量%,更优选等于或小于0.3重量%。如果在馏分中存在的氯化氢是“基本不含氯化氢”,它的含量相对于含水馏分的总重量通常等于或大于1mg/kg,经常为等于或大于10mg/kg。
“新鲜的”水应理解为水具有的不是水的其它有机或无机组分的含量相对于水和其它组分的总重量小于或等于12重量%,优选小于或等于10重量%,最优选小于或等于1重量%。通常,“新鲜的”水具体理解为水具有的非水其它有机或无机组分的含量相对于水和其它组分的总重量大于或等于0.001mg/kg,经常大于或等于1mg/kg,常常大于或等于10mg/kg。新鲜水的可能来源可以是例如在下文中描述的用于洗脱金属盐的水:通过离子交换树脂得到的软化水、蒸馏水或来自水蒸气冷凝的水。
其中不是水的组分,其更具体是指氯代醇。
已经发现,利用水-氯化氢-氯代醇三元组成的液体-蒸汽平衡(气液平衡)特征使得可以从生产反应中取出具体包含氯代醇和水的反应产物,同时使得大部分催化剂和反应物(包括氯化氢)再循环至反应器中,尤其是当氯代醇是二氯丙醇时。
本发明还涉及一种用于生产氯代醇的方法,根据该方法:
(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物在反应混合物中与氯化氢进行反应,
(b)连续或周期性地取出至少含有水、氯代醇和氯化氢的一部分反应混合物,
(c)将在步骤(b)中得到的部分(或馏分)的至少一部分引入到蒸馏步骤中,
其中进入该蒸馏步骤的馏分中的氯化氢浓度/水浓度的比率小于在蒸馏温度和压力下,氯化氢/水二元共沸组成中的氯化氢/水的浓度比。
该方法优选是连续进行的。
在根据本发明的方法中,优选对多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯代醇在其中进行反应的反应器的操作条件,如反应物(具体是氯化氢和多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物)的进料速率、催化剂进料速率、温度、反应器体积和压力进行调节,使得引入到蒸馏步骤中的混合物的氯化氢浓度在蒸馏温度和压力下低于氯化氢/水的二元共沸组成中的氯化氢浓度。调节该浓度的有效方法是控制氯化氢向液体反应介质中的供应。
例如可以通过加入水来控制步骤(b)中的氯化氢含量。这种加入可以例如通过将蒸汽注入到蒸馏步骤中所使用的蒸馏塔锅炉中来进行,或通过向蒸馏步骤再循环水相来进行,所述水相可以例如通过倾析(或相分离)从蒸馏塔顶部取出的馏分而获得的,或者通过将新鲜的水加入到蒸馏塔的顶部来进行,或通过加入再循环的水和新鲜的水的混合物来进行。
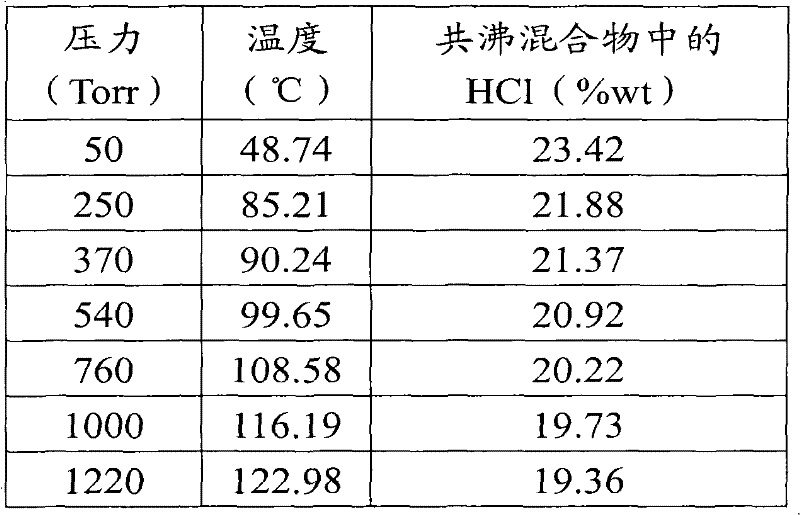
最大的适宜氯化氢浓度在操作压力较高时略有下降,其与由Bonner和Titus公布的共沸氯化氢的液-汽平衡(或气液平衡)数据(J.Amer.Chem.Soc.52,633(1930))相一致,将其部分数据复制在下表中:
在这样的条件下,如上定义的包含水、基本上不含氯化氢的馏分可以通过蒸馏而从反应混合物中或从在液体反应混合物上方的气相中回收,例如通过蒸馏取自所述气相的物质以及优选在蒸馏塔顶部获得的包含水的馏分。
例如,在大气压(101.3kPa)下,如果与反应介质接触的气相中的氯化氢含量相对于总的氯化氢和水含量低于约20.22重量%,则可以通过蒸馏反应器气相而获得水和二氯丙醇的二元共沸混合物,其含有23重量%的二氯丙醇。
在根据本发明生产氯代醇的方法中,氯代醇可以包括含量增高的卤化酮,特别是氯丙酮,如在于2005年5月20日以SOLVAY SA名义提交的专利申请FR 05.05120中所描述的,并将上述专利申请的内容合并于此作为参考。在根据本发明生产氯代醇的方法中,氯代醇中的卤代酮含量可以通过在水存在下进行共沸蒸馏或对该氯代醇进行脱氯化氢处理来减少,如在于2005年5月20日提交的SOLVAY SA的专利申请FR 05.05120中所描述的。特别提及一种用于生产环氧化物的方法,其中卤代酮是作为副产物形成的,并且该方法包括至少一步用于除去至少一部分所形成的卤代酮的处理。更特别提及一种通过氯代醇脱氯化氢作用用于生产环氧化物的方法,其中至少一部分氯代醇是通过氯化多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物来生产的,通过脱氯化氢处理和通过共沸蒸馏处理水-卤代酮混合物用于除去至少一部分形成的卤代酮来生产的,以及一种用于生产表氯醇的工艺(或方法),其中卤代酮是氯丙酮。
在根据本发明生产氯代醇的方法中,当氯代醇是二氯丙醇时,令人惊奇地得到了对于1,3-二氯丙-2-醇的高选择性,1,3-二氯丙-2-醇尤其适宜作为起始产物用于脱氯化氢以用于生产表氯醇。
在根据本发明的方法中,氯代醇可以进行脱氯化氢反应以生产环氧化物,如在以SOLVAY SA名义的专利申请WO 2005/054167和FR 05.05120中所描述的。
在根据本发明的方法中,氯代醇可以进行脱氯化氢反应,如在与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing an epoxide from a multi-hydroxylated aliphatic hydrocarbon and a chlorinating agent”的专利申请中所描述的,将其内容合并于此作为参考。
特别提及一种用于生产环氧化物的方法,其中从多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂反应中得到反应混合物,该反应混合物含有至少10g的氯代醇/kg反应混合物,其进行另外的化学反应而无需中间处理。
尤其提及一种用于生产环氧化物的方法,包括如下步骤:(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂和有机酸进行反应,从而在含有多羟基脂肪烃、多羟基脂肪烃的酯,水,该氯化剂和有机酸的反应混合物中形成氯代醇和氯代醇的酯,该反应混合物在每kg的反应混合物中含有至少10g氯代醇;(b)将在步骤(a)中得到的至少一部分反应混合物(该部分混合物与在步骤(a)中得到的反应混合物具有同样的组成)在步骤(a)之后的步骤中进行一次或多次处理;以及(c)在步骤(a)之后的至少一个步骤中加入碱性化合物,以便至少部分与氯代醇、氯代醇的酯,氯化剂和有机酸反应从而形成一种环氧化物和盐。
根据本发明用于生产氯代醇的方法可以被整合在如与本申请同日以SOLVAY SA名义提交的名称为“Process for manufacturing an epoxide from a chlorohydrin”的专利申请中所描述的整个设计之中,并且将上述专利申请的内容合并于此作为参考。
特别提及一种用于生产环氧化物的方法,包括至少一个纯化生成的环氧化物的步骤,该环氧化物至少部分是通过氯代醇脱氯化氢的方法生成的,该氯代醇至少部分是通过氯化多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物的方法生产的。
当该氯代醇是二氯丙醇时,本发明的方法可以接着通过将二氯丙醇脱氯化氢来生产表氯醇,并且当该环氧化物是表氯醇时,该表氯醇通常可以用于生产环氧树脂。
图1示出了可以用于实施根据本发明生产氯代醇的尤其优选的设备流程图。其以连续或间歇方式,通过管线(1)向反应器(4)供应多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物,通过管线(2)供应催化剂,氯化剂的进料是通过管线(3)连续或以间歇方式进行的,蒸馏塔(6)通过管线(5)供应由反应器(4)产生的蒸汽,通过管线(7)从塔(6)中取出一股流体并送入到冷凝器(8),来自冷凝器(8)的一股流体通过管线(9)送入到倾析器(或相分离器)(10)中,在倾析器中水相和有机相被分离。分离后的水相的一部分可选通过管线(11)再循环至塔顶用于维持回流(比)。新鲜的水可以通过管线(12)加入到塔顶用于维持回流(比)。生成的氯代醇在通过管线(14)取出的有机相与通过管线(13)取出的水相之间进行分配。来自塔(6)的残留物可以通过管线(15)再循环至反应器。重副产物可以可选地借助位于反应器底部液体中的清洗物(16)从反应器中移出。从清洗物(16)中取出一股液流并通过管线(17)送入到蒸发器(18)内,在那里进行部分蒸发操作,例如通过加热或通过用氮气或水蒸气吹扫,来自液流(17)包含大部分氯化剂的气相通过管线(19)再循环至塔(6)或通过管线(20)再循环至反应器(4)中,蒸馏塔或汽提塔(22)通过管线(21)供应来自蒸发器(18)的液相,氯代醇的主要馏分经过管线(23)采集自塔(22)的顶部并且塔的残留物通过管线(24)供给到过滤单元(25),在那里固体和液相被分离开,液相通过管线(26)被再循环至反应器(4)。固体可以通过管线(27)作为固体或作为溶液从过滤单元(25)中取出。溶剂可以通过管线(28)和(29)加入到过滤单元(25)中用于洗涤和/或固体溶解并从管线(27)中取出。可选地,从清洗物(16)中取出一股液流并通过管线(30)供给到过滤单元(25)内。汽提塔(18)和蒸馏塔(22)接着被旁路。
根据这个最后(汽提塔(18)和(蒸馏)塔(22)被旁路的)流程图得到的结果被详细记录在实施例中。
当该多羟基脂肪烃是乙二醇、丙二醇和甘油,氯代醇是氯乙醇、氯丙醇、氯丙二醇和二氯丙醇,环氧化物是环氧乙烷、环氧丙烷、缩水甘油和表氯醇以及氯化剂是无水氯化氢或氯化氢水溶液时,上面描述的方法是非常适宜的。当多羟基脂肪烃是甘油、氯代醇是二氯丙醇而环氧化物是表氯醇时,该方法是尤其方便的。
当多羟基脂肪烃是甘油时,该方法的这个变化方案允许通过共沸性在(塔)顶移出几乎全部来自反应的、来自起始原料的和/或可能在反应器或塔底部供给的水,从而得到极高纯度的二氯丙醇的混合物,对于两种异构体的总和为超过99.5重量%(其相对于烃链和氯化氢具有高于99重量%的选择性),并移出当在反应器中使用粗制甘油时可以积聚在反应器中的金属盐。
下面的实施例是用来说明本发明而不是用来限制本发明的。
实施例1
括号中的数字参照图1。在图1流程中具有汽提塔(18)和(蒸馏)塔(22)的附加设备在这个实例中没有使用。
反应器(4)以相对流量质量比为2.06已经被连续供给粗制甘油和33重量%的盐酸水溶液。该粗制甘油是生产生物柴油的副产物,并含有85%的甘油、6%的NaCl和0.5%的有机杂质(脂肪酸及衍生物)。停留时间是16h,在反应介质中的己二酸的浓度为2.5mol酸官能团/kg。反应器在大气压和115℃下操作。反应混合物已经用氮气汽提并且产生的蒸汽相通过管线(5)已经在蒸馏塔(6)中被处理(图1)。从塔(6)中移出的气相已经在25℃被冷凝(8)并在倾析器(10)中倾析(或相分离)。调节回流比用以通过再循环 来自倾析器的合适量的水相而在塔顶部取出所生产的全部二氯丙醇。在倾析器的出口处回收含15.0%二氯丙醇的水相(13)以及含88%二氯丙醇的有机相(14)。在这两相中的有机杂质测量结果没有显示出与在本方法中使用纯的甘油有不同。
已经将来自反应器的浆料泵送到在过滤塔(25)中的115微米的PTFE膜过滤器上。在过滤器中的盐饼已经在20℃下用饱和有水的二氯丙醇洗涤。在移出液相并排出固体,将盐溶于水并弃去盐水相。洗涤和盐溶解的持续时间为约2小时。接着来自反应器的浆料进行了新的过滤循环。通过连续进料已经将二氯丙醇洗涤液再循环回反应器中。带有盐的水相分析表明二氯丙醇:NaCl的质量比为1.44以及少量的催化剂(小于10g/kg)。在盐水中的二氯丙醇的量表现为二氯丙醇总产品的1.6%。
以二氯丙醇(表示)的总产率为93%。
Claims (28)
1.用于生产氯代醇的方法,根据所述方法
(a)使多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物与氯化剂在反应介质中进行反应;
(b)连续或间歇地从所述反应介质中取出至少含有水和所述氯代醇的部分;
(c)将至少部分在步骤(b)中得到的所述部分引入到蒸馏步骤中;以及
(d)通过向所述蒸馏步骤供给水来控制所述蒸馏步骤的回流比。
2.根据权利要求1所述的方法,其中在步骤(b)中的所述取出部分相对于所述取出部分的总重量具有大于或等于21重量%的水含量。
3.根据权利要求1所述的方法,其中所述氯化剂是氯化氢,其中将至少部分在步骤(b)中获得的所述部分供给到蒸馏塔,并且其中供给到蒸馏塔的水中的氯化氢含量等于或小于10重量%,且等于或大于1mg/kg。
4.根据权利要求1所述的方法,其中将至少部分在步骤(b)中获得的所述部分供给到蒸馏塔,并且其中供给到蒸馏塔的水中的不是水的其他组分的含量为相对于水和其他组分的总重量小于或等于12%,且大于或等于1mg/kg。
5.根据权利要求4所述的方法,其中不是水的其他组分是氯代醇。
6.根据权利要求4所述的方法,其中所述水选自通过离子交换树脂得到的软化水、蒸馏水和来自水蒸气冷凝的水。
7.根据权利要求3或4所述的方法,其中将水供给到蒸馏塔顶。
8.根据权利要求1所述的方法,其中所述多羟基脂肪烃是甘油,而所述氯代醇是二氯丙醇。
9.根据权利要求8所述的方法,随后通过二氯丙醇脱氯化氢作用生产表氯醇。
10.根据权利要求9所述的方法,其中所述表氯醇用于生产环氧树脂。
11.根据权利要求1所述的方法,根据所述方法使用的所述多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有至少一种固体或溶解的金属盐,所述方法包括一分离操作以除去至少部分所述金属盐。
12.根据权利要求1所述的方法,其中使用的所述多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物至少部分是由可再生原料获得的。
13.根据权利要求11所述的方法,其中所述金属盐选自氯化钠、氯化钾、硫酸钠和硫酸钾。
14.根据权利要求11中任一项所述的方法,其中所述多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有0.5至15重量%的金属盐。
15.根据权利要求1所述的方法,其中所述氯化剂是气体氯化氢。
16.根据权利要求1所述的方法,其中所述反应是在催化剂存在下进行的。
17.根据权利要求16所述的方法,其中所述催化剂是羧酸或羧酸衍生物。
18.根据权利要求17所述的方法,其中所述羧酸具有高于或等于200℃的常压沸点,优选是己二酸或己二酸的衍生物。
19.根据权利要求11所述的方法,其中所述分离操作选自液/固、液/液、液/气和固/气分离。
20.根据权利要求19所述的方法,其中所述液/固分离操作选自倾析、离心、过滤、吸附以及用离子交换树脂处理,所述液/液分离操作选自倾析和离心,所述液/气分离操作选自汽提、蒸发和蒸馏。
21.根据权利要求20所述的方法,其中所述液/固分离操作是过滤,并且其中所述金属盐是作为固体除去的。
22.根据权利要求11中任一项所述的方法,其中所述反应是在反应混合物中进行的,并且所述分离操作是在所述反应混合物的至少一部分中进行的。
23.根据权利要求22所述的方法,其中对所述反应混合物的一部分进行处理以在所述分离操作之前除去不是所述金属盐的至少一种成分。
24.根据权利要求23所述的方法,其中所述处理是汽提或蒸馏操作。
25.根据权利要求1所述的方法,所述方法是以连续方式进行的。
26.根据权利要求1所述的方法,根据所述方法多羟基脂肪烃、多羟基脂肪烃的酯或它们的混合物含有至多10重量%有机杂质。
27.根据权利要求8所述的方法,其中使用的所述甘油一部分是在生产生物柴油的过程中得到的,或者是在植物或动物来源的脂肪或油的转化过程中得到的,所述转化选自皂化、酯基转移或水解反应。
28.根据权利要求27所述的方法,其中所述油或脂肪选自玉米油、葵花籽油、陈旧的或新的菜籽油、巴巴苏油、椰子油、甘蓝树油、棕榈油、蓖麻油和棉籽油、花生油、大豆油、亚麻油和海甘蓝油、由通过基因修饰或杂交得到的向日葵作物或菜籽作物而得到的油、煎炸过的陈油、鱼油、牛油、猪油、肢解的脂肪、“亚麻籽油定油”、部分多聚或低聚的葵花籽油和开花植物油。
Applications Claiming Priority (20)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP05104321.4 | 2005-05-20 | ||
| EP05104321A EP1762556A1 (en) | 2005-05-20 | 2005-05-20 | Process for producing dichloropropanol from glycerol |
| FR0505120A FR2885903B1 (fr) | 2005-05-20 | 2005-05-20 | Procede de fabrication d'epichlorhydrine |
| FR0505120 | 2005-05-20 | ||
| US73465905P | 2005-11-08 | 2005-11-08 | |
| US73465805P | 2005-11-08 | 2005-11-08 | |
| US73463605P | 2005-11-08 | 2005-11-08 | |
| US73465705P | 2005-11-08 | 2005-11-08 | |
| US73463705P | 2005-11-08 | 2005-11-08 | |
| US73462705P | 2005-11-08 | 2005-11-08 | |
| US73463505P | 2005-11-08 | 2005-11-08 | |
| US73463405P | 2005-11-08 | 2005-11-08 | |
| US60/734,634 | 2005-11-08 | ||
| US60/734,627 | 2005-11-08 | ||
| US60/734,635 | 2005-11-08 | ||
| US60/734,637 | 2005-11-08 | ||
| US60/734,658 | 2005-11-08 | ||
| US60/734,636 | 2005-11-08 | ||
| US60/734,657 | 2005-11-08 | ||
| US60/734,659 | 2005-11-08 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2006800005668A Division CN1993308B (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102659511A true CN102659511A (zh) | 2012-09-12 |
Family
ID=39543862
Family Applications (13)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2006800006054A Expired - Fee Related CN101006037B (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯代醇的方法 |
| CN2006800005348A Expired - Fee Related CN101031532B (zh) | 2005-05-20 | 2006-05-19 | 将多羟基脂肪烃转化为氯醇的方法 |
| CN2012100221289A Pending CN102603474A (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
| CN2006800005530A Expired - Fee Related CN101052606B (zh) | 2005-05-20 | 2006-05-19 | 从多羟基脂肪烃开始制备氯醇的方法 |
| CN2006800005352A Expired - Fee Related CN1993307B (zh) | 2005-05-20 | 2006-05-19 | 通过多羟基脂肪烃与氯化剂反应制备氯醇的方法 |
| CN2006800005507A Expired - Fee Related CN101107208B (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯醇的连续方法 |
| CN2012100221382A Pending CN102659511A (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
| CN2006800006073A Ceased CN101006068B (zh) | 2005-05-20 | 2006-05-19 | 用于制备环氧化物的方法 |
| CN200680000523XA Expired - Fee Related CN1993306B (zh) | 2005-05-20 | 2006-05-19 | 通过将多羟基脂肪烃氯化制备氯醇的方法 |
| CN2006800005511A Expired - Fee Related CN101098843B (zh) | 2005-05-20 | 2006-05-19 | 在存在重质化合物的液相中制备氯醇的方法 |
| CN2012100221306A Pending CN102603475A (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
| CN201110379336XA Pending CN102531841A (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯醇的连续方法 |
| CN2012101645245A Pending CN102690168A (zh) | 2005-05-20 | 2006-05-19 | 通过将多羟基脂肪烃氯化制备氯醇的方法 |
Family Applications Before (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2006800006054A Expired - Fee Related CN101006037B (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯代醇的方法 |
| CN2006800005348A Expired - Fee Related CN101031532B (zh) | 2005-05-20 | 2006-05-19 | 将多羟基脂肪烃转化为氯醇的方法 |
| CN2012100221289A Pending CN102603474A (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
| CN2006800005530A Expired - Fee Related CN101052606B (zh) | 2005-05-20 | 2006-05-19 | 从多羟基脂肪烃开始制备氯醇的方法 |
| CN2006800005352A Expired - Fee Related CN1993307B (zh) | 2005-05-20 | 2006-05-19 | 通过多羟基脂肪烃与氯化剂反应制备氯醇的方法 |
| CN2006800005507A Expired - Fee Related CN101107208B (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯醇的连续方法 |
Family Applications After (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2006800006073A Ceased CN101006068B (zh) | 2005-05-20 | 2006-05-19 | 用于制备环氧化物的方法 |
| CN200680000523XA Expired - Fee Related CN1993306B (zh) | 2005-05-20 | 2006-05-19 | 通过将多羟基脂肪烃氯化制备氯醇的方法 |
| CN2006800005511A Expired - Fee Related CN101098843B (zh) | 2005-05-20 | 2006-05-19 | 在存在重质化合物的液相中制备氯醇的方法 |
| CN2012100221306A Pending CN102603475A (zh) | 2005-05-20 | 2006-05-19 | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 |
| CN201110379336XA Pending CN102531841A (zh) | 2005-05-20 | 2006-05-19 | 用于制备氯醇的连续方法 |
| CN2012101645245A Pending CN102690168A (zh) | 2005-05-20 | 2006-05-19 | 通过将多羟基脂肪烃氯化制备氯醇的方法 |
Country Status (12)
| Country | Link |
|---|---|
| US (12) | US20080194850A1 (zh) |
| EP (16) | EP1885675A1 (zh) |
| JP (13) | JP5405821B2 (zh) |
| KR (7) | KR101337048B1 (zh) |
| CN (13) | CN101006037B (zh) |
| BR (8) | BRPI0610745A2 (zh) |
| CA (13) | CA2608961C (zh) |
| EA (14) | EA014241B1 (zh) |
| MX (7) | MX2007014525A (zh) |
| MY (4) | MY148345A (zh) |
| TW (16) | TWI333945B (zh) |
| WO (13) | WO2006106155A2 (zh) |
Families Citing this family (95)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7838708B2 (en) | 2001-06-20 | 2010-11-23 | Grt, Inc. | Hydrocarbon conversion process improvements |
| US20050171393A1 (en) | 2003-07-15 | 2005-08-04 | Lorkovic Ivan M. | Hydrocarbon synthesis |
| JP2007525477A (ja) | 2003-07-15 | 2007-09-06 | ジーアールティー インコーポレイテッド | 炭化水素の合成 |
| EP2053034B1 (en) | 2003-11-20 | 2018-01-24 | Solvay Sa | Process for producing a chlorohydrin |
| US7674941B2 (en) | 2004-04-16 | 2010-03-09 | Marathon Gtf Technology, Ltd. | Processes for converting gaseous alkanes to liquid hydrocarbons |
| US20080275284A1 (en) | 2004-04-16 | 2008-11-06 | Marathon Oil Company | Process for converting gaseous alkanes to liquid hydrocarbons |
| US8642822B2 (en) | 2004-04-16 | 2014-02-04 | Marathon Gtf Technology, Ltd. | Processes for converting gaseous alkanes to liquid hydrocarbons using microchannel reactor |
| US7244867B2 (en) | 2004-04-16 | 2007-07-17 | Marathon Oil Company | Process for converting gaseous alkanes to liquid hydrocarbons |
| US8173851B2 (en) | 2004-04-16 | 2012-05-08 | Marathon Gtf Technology, Ltd. | Processes for converting gaseous alkanes to liquid hydrocarbons |
| US20060100469A1 (en) | 2004-04-16 | 2006-05-11 | Waycuilis John J | Process for converting gaseous alkanes to olefins and liquid hydrocarbons |
| US20080005956A1 (en) * | 2004-05-14 | 2008-01-10 | Tran Bo L | Methods and compositions for controlling bulk density of coking coal |
| US7906690B2 (en) * | 2004-07-21 | 2011-03-15 | Dow Global Technologies Inc. | Batch, semi-continuous or continuous hydrochlorination of glycerin with reduced volatile chlorinated hydrocarbon by-products and chloracetone levels |
| US7910781B2 (en) * | 2004-07-21 | 2011-03-22 | Dow Global Technologies Llc | Process for the conversion of a crude glycerol, crude mixtures of naturally derived multihydroxylated aliphatic hydrocarbons or esters thereof to a chlorohydrin |
| KR20080037615A (ko) * | 2005-05-20 | 2008-04-30 | 솔베이(소시에떼아노님) | 클로로히드린의 제조 방법 |
| TWI333945B (en) * | 2005-05-20 | 2010-12-01 | Solvay | Process for preparing a chlorohydrin by converting polyhydroxylated aliphatic hydrocarbons |
| BRPI0618325A2 (pt) | 2005-11-08 | 2011-08-23 | Solvay | processo parar a produção de dicloropropanol |
| AU2007215476B2 (en) | 2006-02-03 | 2011-11-10 | Grt, Inc. | Continuous process for converting natural gas to liquid hydrocarbons |
| EP1993951B1 (en) | 2006-02-03 | 2014-07-30 | GRT, Inc. | Separation of light gases from bromine |
| BRPI0712775A2 (pt) | 2006-06-14 | 2012-09-04 | Solvay | Produto com base em glicerol bruto, e, processos para a purificação do produto com base em glicerol bruto, para a fabricação de dicloropropanol partindo de glicerol, para a fabricação de epocloroidrina, para a fabricação de resinas de epóxi, e, para a fabricação de dicloropropanol |
| US7930651B2 (en) | 2007-01-18 | 2011-04-19 | Research In Motion Limited | Agenda display in an electronic device |
| US20100032617A1 (en) * | 2007-02-20 | 2010-02-11 | Solvay (Societe Anonyme) | Process for manufacturing epichlorohydrin |
| FR2913421B1 (fr) | 2007-03-07 | 2009-05-15 | Solvay | Procede de fabrication de dichloropropanol. |
| FR2913684B1 (fr) * | 2007-03-14 | 2012-09-14 | Solvay | Procede de fabrication de dichloropropanol |
| US20080239428A1 (en) * | 2007-04-02 | 2008-10-02 | Inphase Technologies, Inc. | Non-ft plane angular filters |
| WO2008128013A1 (en) * | 2007-04-12 | 2008-10-23 | Dow Global Technologies Inc. | Process and apparatus for azeotropic recovery of dichlorohydrins |
| TWI432407B (zh) * | 2007-04-12 | 2014-04-01 | Dow Global Technologies Llc | 回收二氯丙醇之多階方法和裝置 |
| KR20100016464A (ko) * | 2007-04-12 | 2010-02-12 | 다우 글로벌 테크놀로지스 인크. | 다중하이드록실화된-지방족 탄화수소 또는 이의 에스터의 클로로하이드린으로의 전환 |
| US20110152580A1 (en) * | 2007-04-12 | 2011-06-23 | Hook Bruce D | Process and apparatus for vapor phase purification during hydrochlorination of multi-hydroxylated aliphatic hydrocarbon compounds |
| US8420870B2 (en) * | 2007-04-12 | 2013-04-16 | Dow Global Technologies Llc | Process and apparatus for recovery of dichlorohydrins via codistillation |
| AU2008256606A1 (en) | 2007-05-24 | 2008-12-04 | Grt, Inc. | Zone reactor incorporating reversible hydrogen halide capture and release |
| TW200911740A (en) | 2007-06-01 | 2009-03-16 | Solvay | Process for manufacturing a chlorohydrin |
| TW200911693A (en) | 2007-06-12 | 2009-03-16 | Solvay | Aqueous composition containing a salt, manufacturing process and use |
| TWI500609B (zh) * | 2007-06-12 | 2015-09-21 | Solvay | 含有環氧氯丙烷的產品,其製備及其不同應用中的用途 |
| FR2918058A1 (fr) * | 2007-06-28 | 2009-01-02 | Solvay | Produit a base de glycerol, procede pour sa purification et son utilisation dans la fabrication de dichloropropanol |
| FR2919609A1 (fr) * | 2007-07-30 | 2009-02-06 | Solvay | Procede de fabrication de glycidol |
| JP2010536561A (ja) | 2007-08-23 | 2010-12-02 | ダウ グローバル テクノロジーズ インコーポレイティド | 工業用ブラインの精製のための方法、適合化微生物、組成物及び装置 |
| KR20100068246A (ko) | 2007-08-23 | 2010-06-22 | 다우 글로벌 테크놀로지스 인크. | 염수 정제법 |
| KR20100051104A (ko) | 2007-08-23 | 2010-05-14 | 다우 글로벌 테크놀로지스 인크. | 산업적 염수의 정제 방법 및 장치 |
| KR101410019B1 (ko) * | 2007-09-28 | 2014-06-26 | 한화케미칼 주식회사 | 다가알코올과 염화수소의 반응에 의한 클로로히드린화합물의 제조방법 |
| KR20100089835A (ko) * | 2007-10-02 | 2010-08-12 | 솔베이(소시에떼아노님) | 용기의 내부식성 향상을 위한 실리콘-함유 조성물의 용도 |
| FR2925045B1 (fr) * | 2007-12-17 | 2012-02-24 | Solvay | Produit a base de glycerol, procede pour son obtention et son utilisation dans la fabrication de dichloropropanol |
| RU2358964C1 (ru) * | 2007-12-27 | 2009-06-20 | Общество с ограниченной ответственностью "Синтез-2" | Способ получения дихлорпропанолов |
| TWI478875B (zh) | 2008-01-31 | 2015-04-01 | Solvay | 使水性組成物中之有機物質降解之方法 |
| EA201071157A1 (ru) * | 2008-04-03 | 2011-04-29 | Солвей (Сосьете Аноним) | Композиция, содержащая глицерин, способ ее получения и применение в производстве дихлорпропанола |
| BRPI0906911A2 (pt) * | 2008-04-09 | 2015-07-21 | Dow Global Technologies Inc | Processo e aparelhagem para recuperar dicloridrinas a partir de uma mistura compreendendo dicloridrinas. |
| JP2011518160A (ja) * | 2008-04-16 | 2011-06-23 | ダウ グローバル テクノロジーズ リミティド ライアビリティ カンパニー | 多ヒドロキシル化脂肪族炭化水素またはそのエステルのクロロヒドリンへの変換 |
| US8282810B2 (en) | 2008-06-13 | 2012-10-09 | Marathon Gtf Technology, Ltd. | Bromine-based method and system for converting gaseous alkanes to liquid hydrocarbons using electrolysis for bromine recovery |
| NZ591207A (en) | 2008-07-18 | 2013-03-28 | Grt Inc | Continuous process for converting natural gas to liquid hydrocarbons |
| AT507260B1 (de) † | 2008-08-25 | 2010-10-15 | Kanzler Walter | Verfahren zur herstellung von epichlorhydrin aus glyzerin |
| ITMI20081535A1 (it) * | 2008-08-26 | 2010-02-26 | Biocompany Srl | Processo per la preparazione di 1,3-dicloro-2-propanolo |
| FR2935699A1 (fr) * | 2008-09-10 | 2010-03-12 | Solvay | Procede de fabrication d'un produit chimique |
| FR2935968B1 (fr) * | 2008-09-12 | 2010-09-10 | Solvay | Procede pour la purification de chlorure d'hydrogene |
| FR2939434B1 (fr) * | 2008-12-08 | 2012-05-18 | Solvay | Procede de traitement de glycerol. |
| EP2496625A1 (en) | 2009-11-04 | 2012-09-12 | Solvay Sa | Process for manufacturing an epoxy resin |
| FR2952060B1 (fr) | 2009-11-04 | 2011-11-18 | Solvay | Procede de fabrication d'un produit derive de l'epichlorhydrine |
| US8367884B2 (en) | 2010-03-02 | 2013-02-05 | Marathon Gtf Technology, Ltd. | Processes and systems for the staged synthesis of alkyl bromides |
| US8198495B2 (en) | 2010-03-02 | 2012-06-12 | Marathon Gtf Technology, Ltd. | Processes and systems for the staged synthesis of alkyl bromides |
| WO2011112426A1 (en) * | 2010-03-10 | 2011-09-15 | Dow Global Technologies Llc | Process for preparing divinylarene dioxides |
| KR101705208B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류 조성물의 제조방법 및 그 방법에 의해 제조된 클로로히드린류 조성물을 사용하는 에피클로로히드린의 제조방법 |
| KR101705209B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류 조성물의 제조방법 및 그 방법에 의해 제조된 클로로히드린류 조성물을 사용하는 에피클로로히드린의 제조방법 |
| KR101705206B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류의 제조방법 및 그 방법에 의해 제조된 클로로히드린류를 사용하는 에피클로로히드린의 제조방법 |
| KR101705207B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류의 제조방법 및 그 방법에 의해 제조된 클로로히드린류를 사용하는 에피클로로히드린의 제조방법 |
| KR101705210B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류 조성물의 제조방법 및 그 방법에 의해 제조된 클로로히드린류 조성물을 사용하는 에피클로로히드린의 제조방법 |
| KR101705205B1 (ko) * | 2010-06-30 | 2017-02-09 | 롯데정밀화학 주식회사 | 클로로히드린류의 제조방법 및 그 방법에 의해 제조된 클로로히드린류를 사용하는 에피클로로히드린의 제조방법 |
| EP2598665B1 (en) | 2010-07-28 | 2015-12-30 | Dow Global Technologies LLC | Chlorohydrin processing equipment comprising stainless steel |
| FR2963338B1 (fr) * | 2010-08-02 | 2014-10-24 | Solvay | Procede d'electrolyse |
| FR2964096A1 (fr) | 2010-08-27 | 2012-03-02 | Solvay | Procede d'epuration d'une saumure |
| EP2621911A1 (en) | 2010-09-30 | 2013-08-07 | Solvay Sa | Derivative of epichlorohydrin of natural origin |
| FR2966825B1 (fr) | 2010-10-29 | 2014-05-16 | Solvay | Procede de fabrication d'epichlorhydrine |
| JP2012116920A (ja) * | 2010-11-30 | 2012-06-21 | Polyplastics Co | ポリオキシメチレン樹脂の製造方法 |
| PL215730B1 (pl) | 2011-01-10 | 2014-01-31 | Inst Ciezkiej Syntezy Orga | Sposób wytwarzania dichloropropanoli z gliceryny |
| US8815050B2 (en) | 2011-03-22 | 2014-08-26 | Marathon Gtf Technology, Ltd. | Processes and systems for drying liquid bromine |
| PL218074B1 (pl) | 2011-04-11 | 2014-10-31 | Inst Ciężkiej Syntezy Organicznej Blachownia | Sposób suchego chlorowodorowania masy z chlorowodorowania gliceryny kwasem solnym i urządzenie do suchego chlorowodorowania masy z chlorowodorowania gliceryny kwasem solnym |
| US8436220B2 (en) | 2011-06-10 | 2013-05-07 | Marathon Gtf Technology, Ltd. | Processes and systems for demethanization of brominated hydrocarbons |
| US8829256B2 (en) | 2011-06-30 | 2014-09-09 | Gtc Technology Us, Llc | Processes and systems for fractionation of brominated hydrocarbons in the conversion of natural gas to liquid hydrocarbons |
| US8802908B2 (en) | 2011-10-21 | 2014-08-12 | Marathon Gtf Technology, Ltd. | Processes and systems for separate, parallel methane and higher alkanes' bromination |
| US9193641B2 (en) | 2011-12-16 | 2015-11-24 | Gtc Technology Us, Llc | Processes and systems for conversion of alkyl bromides to higher molecular weight hydrocarbons in circulating catalyst reactor-regenerator systems |
| CN104080737A (zh) | 2011-12-19 | 2014-10-01 | 索尔维公司 | 用于减少水性组合物的总有机碳的方法 |
| EP2669307A1 (en) | 2012-06-01 | 2013-12-04 | Solvay Sa | Process for manufacturing an epoxide |
| EP2669247A1 (en) | 2012-06-01 | 2013-12-04 | Solvay Sa | Process for manufacturing dichloropropanol |
| EP2669308A1 (en) | 2012-06-01 | 2013-12-04 | Solvay Sa | Process for manufacturing an epoxy resin |
| EP2669305A1 (en) | 2012-06-01 | 2013-12-04 | Solvay Sa | Process for manufacturing an epoxy resin |
| EP2669306B1 (en) | 2012-06-01 | 2015-08-12 | Solvay Sa | Process for manufacturing an epoxy resin |
| CN104341271B (zh) * | 2013-08-02 | 2016-05-18 | 中国石油化工股份有限公司 | 一种盐酸和甘油连续制备二氯丙醇的方法 |
| WO2015074684A1 (en) | 2013-11-20 | 2015-05-28 | Solvay Sa | Process for manufacturing an epoxy resin |
| CN106630083B (zh) * | 2015-10-29 | 2021-05-14 | 中国石油化工股份有限公司 | 一种环氧化废水的无害化处理方法 |
| TWI547470B (zh) | 2015-12-18 | 2016-09-01 | 長春人造樹脂廠股份有限公司 | 製造二氯丙醇之方法 |
| TWI592392B (zh) * | 2016-05-31 | 2017-07-21 | 國立清華大學 | 改善二氯丙醇的產率的製造裝置及其製造方法 |
| KR102058483B1 (ko) | 2017-02-27 | 2019-12-23 | 중앙대학교 산학협력단 | 높은 단맛을 가지는 신규한 브라제인 다중 변이체 및 이의 제조방법 |
| CN118978535A (zh) | 2018-05-01 | 2024-11-19 | 锐新医药公司 | 作为mTOR抑制剂的C40-、C28-及C-32连接的雷帕霉素类似物 |
| MX2020011564A (es) | 2018-05-01 | 2021-01-29 | Revolution Medicines Inc | Analogos de rapamicina unidos a c26 como inhibidores de mtor. |
| FR3081721B1 (fr) * | 2018-06-01 | 2022-04-15 | Arkema France | Procede de preparation d'un sel de lithium de bis(fluorosulfonyl)imide |
| CN111875477A (zh) * | 2020-08-03 | 2020-11-03 | 岳阳隆兴实业公司 | 一种邻氯醇共沸提纯方法 |
| CA3256390A1 (en) | 2022-05-25 | 2023-11-30 | Revolution Medicines, Inc. | CANCER TREATMENT METHODS USING AN MTOR INHIBITOR |
| CN115583869B (zh) * | 2022-09-13 | 2024-04-23 | 安徽海华科技集团有限公司 | 一种酚类化合物选择性氧化氯化方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2144612A (en) * | 1936-09-10 | 1939-01-24 | Dow Chemical Co | Preparation of glycerol dichlorohydrin |
| WO2005021476A1 (en) * | 2003-09-01 | 2005-03-10 | Spolek Pro Chemickou A Hutni Vyrobu, Akciova Spolecnost | Method of preparing dichloropropanols from glycerine |
Family Cites Families (270)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US449255A (en) * | 1891-03-31 | Watch-bow fastener | ||
| US280893A (en) * | 1883-07-10 | Treating waters containing glycerine obtained by the decomposition of fatty matters | ||
| DE197309C (zh) | ||||
| DE197308C (zh) * | ||||
| DE180668C (zh) | ||||
| US3061615A (en) | 1962-10-30 | Process for the production of alpha-epichlorhydrin | ||
| DE238341C (zh) | ||||
| DE58396C (de) | Dr. P. FRITSCH in Rostock i. M., Augustenstr. 40 | Verfahren zur Darstellung von Glyceriden aromatischer Säuren | ||
| DE216471C (zh) | ||||
| DE1075103B (de) | 1960-02-11 | VEB Leuna-Werke "Walter Ulbricht", Leuna (Kr. Merseburg) | Verfahren zur kontinuierlichen Herstellung von Epichlorhydrin aus Glyzerin | |
| US865727A (en) | 1907-08-09 | 1907-09-10 | Augustin L J Queneau | Method of making and utilizing gas. |
| GB191314767A (en) * | 1913-06-26 | 1914-01-08 | Henry Fairbrother | Process for Directly Producing Glycerol-halogen-hydrins and Poly-oxy Fatty Acid Esters. |
| GB405345A (en) | 1931-05-08 | 1934-01-29 | Boston Blacking Company Ltd | Improvements in or relating to the compounding of latex and to compounded latex |
| GB406345A (en) | 1931-08-24 | 1934-02-26 | Du Pont | Improvements in or relating to the production of formic acid |
| GB404938A (en) | 1932-07-15 | 1934-01-15 | Henry Dreyfus | Manufacture of chlorhydrins and ethers thereof |
| US2063891A (en) * | 1932-07-15 | 1936-12-15 | Dreyfus Henry | Manufacture of chlorhydrins and their ethers |
| US2060715A (en) | 1933-01-13 | 1936-11-10 | Du Pont | Synthetic resins |
| GB467481A (en) | 1935-09-12 | 1937-06-14 | Eastman Kodak Co | Processes of removing water from aqueous aliphatic acids |
| US2198600A (en) | 1936-09-10 | 1940-04-30 | Dow Chemical Co | Glycerol dichlorohydrin |
| BE422877A (zh) | 1937-07-28 | 1937-08-31 | ||
| US2319876A (en) | 1937-12-04 | 1943-05-25 | Celanese Corp | Preparation of aromatic sulphonamide-phenol-dihalide reaction products |
| GB541357A (en) | 1939-02-24 | 1941-11-24 | Du Pont | Improvements in or relating to the production of glycerol |
| US2248635A (en) | 1939-06-20 | 1941-07-08 | Shell Dev | Treatment of halogenated polyhydric alcohols |
| NL59974C (zh) * | 1943-06-16 | |||
| DE869193C (de) | 1944-08-22 | 1953-03-05 | Chloberag Chlor Betr Rheinfeld | Verfahren zum Reinigen von Chlorwasserstoff |
| GB679536A (en) | 1947-06-11 | 1952-09-17 | Devoe & Raynolds Co | Improvements in epoxide preparation |
| US2505735A (en) * | 1948-05-22 | 1950-04-25 | Harshaw Chem Corp | Purufication of crude glycerine |
| DE848799C (de) * | 1948-12-23 | 1956-08-02 | Elektrochemische Werke Rheinfe | Vorrichtung zur Absorption von Gasen durch Fluessigkeiten, insbesondere zur Erzeugung von Salzsaeure |
| GB702143A (en) | 1949-10-25 | 1954-01-13 | Hoechst Ag | Cold-hardening compositions containing phenol-formaldehyde condensation products, and a process for making such compositions |
| US2735829A (en) | 1952-07-05 | 1956-02-21 | Compositions containing a mixture of | |
| DE1041488B (de) | 1954-03-19 | 1958-10-23 | Huels Chemische Werke Ag | Verfahren zur Herstellung von Oxidoalkoholen |
| US2875217A (en) | 1954-07-14 | 1959-02-24 | Upjohn Co | Producing 17-hydroxy 20-keto steroids by the use of osmium tetroxide and an organicpolyvalent iodo oxide |
| US2811227A (en) | 1955-01-20 | 1957-10-29 | Houdaille Industries Inc | Flutter damper |
| US2860146A (en) * | 1955-04-14 | 1958-11-11 | Shell Dev | Manufacture of epihalohydrins |
| US2829124A (en) | 1955-12-23 | 1958-04-01 | Borden Co | Epoxide resin |
| GB799567A (en) | 1956-04-30 | 1958-08-13 | Solvay | Process for the production of alpha-epichlorhydrin |
| US2945004A (en) | 1956-05-29 | 1960-07-12 | Devoe & Raynolds Co | Epoxide resins reacted with polyhydric phenols |
| US2876217A (en) * | 1956-12-31 | 1959-03-03 | Corn Products Co | Starch ethers containing nitrogen and process for making the same |
| US2960447A (en) | 1957-07-15 | 1960-11-15 | Shell Oil Co | Purification of synthetic glycerol |
| US3135705A (en) | 1959-05-11 | 1964-06-02 | Hercules Powder Co Ltd | Polymeric epoxides |
| US3026270A (en) * | 1958-05-29 | 1962-03-20 | Hercules Powder Co Ltd | Cross-linking of polymeric epoxides |
| SU123153A3 (ru) | 1958-11-18 | 1958-11-30 | Словак Гельмут | Способ непрерывного получени эпихлоргидрина |
| US3052612A (en) * | 1959-02-16 | 1962-09-04 | Olin Mathieson | Recovery of chlorine from electrol ysis of brine |
| US3158580A (en) * | 1960-03-11 | 1964-11-24 | Hercules Powder Co Ltd | Poly (epihalohydrin) s |
| GB984446A (en) | 1960-07-05 | 1965-02-24 | Pfaudler Permutit Inc | Improvements relating to semicrystalline glass and to the coating of metal therewith |
| US3158581A (en) * | 1960-07-27 | 1964-11-24 | Hercules Powder Co Ltd | Polymeric epoxides |
| NL270270A (zh) * | 1960-10-17 | |||
| FR1306231A (fr) | 1960-10-17 | 1962-10-13 | Shell Int Research | Procédé de préparation de polyéthers glycidiques |
| FR1279331A (fr) | 1960-11-07 | 1961-12-22 | Electrochimie Soc | Procédé et fabrication de résines époxy et produits obtenus |
| US3247227A (en) * | 1962-04-24 | 1966-04-19 | Ott Chemical Company | Epoxidation of organic halohydrins |
| US3260259A (en) | 1962-10-08 | 1966-07-12 | S H Camp & Company | Abduction splint |
| US3328331A (en) | 1963-01-22 | 1967-06-27 | Hoechst Ag | Epoxy resin masses and process for preparing them |
| US3341491A (en) | 1963-09-10 | 1967-09-12 | Hercules Inc | Vulcanized epihalohydrin polymers |
| NL129282C (zh) | 1963-10-21 | |||
| FR1417388A (fr) | 1963-10-21 | 1965-11-12 | Hooker Chemical Corp | Purification de l'acide chlorhydrique |
| CH460734A (de) | 1963-11-19 | 1968-08-15 | Shell Int Research | Herstellung von neuen Epoxyäthern |
| JPS3927230Y1 (zh) | 1963-12-30 | 1964-09-15 | ||
| DE1226554B (de) | 1964-06-06 | 1966-10-13 | Henkel & Cie Gmbh | Verfahren zur Herstellung von Glycid aus Glycerinmonochlorhydrin |
| FR1417386A (fr) | 1964-10-21 | 1965-11-12 | Radyne Ltd | Perfectionnement à la spectrométrie |
| US3355511A (en) * | 1965-04-09 | 1967-11-28 | Shell Oil Co | Flame retardant epoxy compositions containing polyglycidyl ethers of hexahalo bicycloheptadiene bisphenols |
| FR1476073A (fr) | 1965-04-09 | 1967-04-07 | Shell Int Research | Résine époxyde retardant la propagation des flammes |
| US3445197A (en) | 1966-05-27 | 1969-05-20 | Continental Oil Co | Removing benzene from aqueous muriatic acid using a liquid paraffin |
| US3457282A (en) * | 1966-06-01 | 1969-07-22 | Olin Mathieson | Glycidol recovery process |
| US3455197A (en) * | 1966-11-21 | 1969-07-15 | Ppg Industries Inc | Adjustable guillotine and table for severing sheet plastic |
| DE1643497C3 (de) | 1967-09-02 | 1979-06-21 | Hoechst Ag, 6000 Frankfurt | Verfahren zur Herstellung von Glycidyläthern ein- und mehrwertiger Phenole |
| US3968178A (en) * | 1967-11-08 | 1976-07-06 | Stauffer Chemical Company | Chlorination of hydrocarbons |
| DE2007867B2 (de) * | 1970-02-20 | 1978-11-02 | Hoechst Ag, 6000 Frankfurt | Verfahren zur kontinuierlichen Herstellung von Dichlorpropanolen |
| DE1809607C3 (de) | 1968-11-19 | 1974-01-10 | Deutsche Gold- Und Silber-Scheideanstalt Vormals Roessler, 6000 Frankfurt | Verfahren zur absorptiven Trennung von bei der Gasphasenreaktion von Chlor und Cyanwasserstoff anfallenden Gemischen aus Chlorcyan und Chlorwasserstoff |
| BE744659A (fr) | 1969-01-27 | 1970-07-01 | Haveg Industries Inc | Article metallique revetu et procede pour le fabriquer |
| US3867166A (en) | 1969-01-27 | 1975-02-18 | Tycon Spa | Coated metal article and method of making the same |
| CH544801A (de) * | 1970-03-16 | 1973-11-30 | Reichhold Albert Chemie Ag | Verfahren zum Herstellen von Glycidyläthern |
| US3711388A (en) * | 1970-12-11 | 1973-01-16 | Dow Chemical Co | Oxidation step in electrolysis of aqueous hci |
| CH545778A (zh) | 1971-03-26 | 1974-02-15 | ||
| US3839169A (en) | 1971-08-11 | 1974-10-01 | Dow Chemical Co | Photooxidizing organic contaminants in aqueous brine solutions |
| BE792326A (fr) | 1971-12-07 | 1973-03-30 | Degussa | Procede pour la preparation d'halogenohydrines |
| DE2163096B2 (de) | 1971-12-18 | 1974-02-14 | Gutehoffnungshuette Sterkrade Ag, 4200 Oberhausen | Verfahren zur Wiederaufwärmung eines verdichteten Gasstromes über dem Taupunkt |
| LU67005A1 (zh) | 1973-02-12 | 1974-10-01 | ||
| US4173710A (en) * | 1972-05-15 | 1979-11-06 | Solvay & Cie | Halogenated polyether polyols and polyurethane foams produced therefrom |
| DE2241393A1 (de) | 1972-08-23 | 1974-02-28 | Bayer Ag | Glycidylaether mehrwertiger phenole |
| CH575405A5 (zh) | 1973-02-15 | 1976-05-14 | Inventa Ag | |
| US3865886A (en) * | 1973-06-20 | 1975-02-11 | Lummus Co | Production of allyl chloride |
| JPS5037714A (zh) * | 1973-08-15 | 1975-04-08 | ||
| CH593272A5 (zh) | 1974-05-24 | 1977-11-30 | Inventa Ag | |
| LU70739A1 (zh) * | 1974-08-14 | 1976-08-19 | ||
| US4011251A (en) * | 1975-03-13 | 1977-03-08 | Boris Konstantinovich Tjurin | Method of preparing esters of glycerol and polyglycerols and C5-C9 monocarboxylic fatty acids |
| US4024301A (en) | 1975-05-02 | 1977-05-17 | The B. F. Goodrich Company | Internally coated reaction vessel for use in olefinic polymerization |
| DE2522286C3 (de) * | 1975-05-20 | 1978-05-18 | Hoechst Ag, 6000 Frankfurt | Verfahren zur Reinigung von Rohchlorwasserstoff |
| US3954581A (en) * | 1975-07-22 | 1976-05-04 | Ppg Industries, Inc. | Method of electrolysis of brine |
| FR2321455A1 (fr) | 1975-08-22 | 1977-03-18 | Ugine Kuhlmann | Nouveau procede d'epuration oxydante des eaux |
| US4255470A (en) | 1977-07-15 | 1981-03-10 | The B. F. Goodrich Company | Process for preventing polymer buildup in a polymerization reactor |
| US4127594A (en) | 1978-02-21 | 1978-11-28 | Shell Oil Company | Selective hydrogenation of olefinic impurities in epichlorohydrin |
| FR2455580A1 (fr) | 1979-05-04 | 1980-11-28 | Propylox Sa | Procede pour l'epuration de solutions organiques de peracides carboxyliques |
| JPS55157607A (en) * | 1979-05-25 | 1980-12-08 | Ryonichi Kk | Suspension polymerization of vinyl chloride |
| US4415460A (en) | 1979-07-30 | 1983-11-15 | The Lummus Company | Oxidation of organics in aqueous salt solutions |
| US4240885A (en) * | 1979-07-30 | 1980-12-23 | The Lummus Company | Oxidation of organics in aqueous salt solutions |
| JPS5699432A (zh) | 1979-12-28 | 1981-08-10 | Sorutan Ogurii Shiyarif Gabiru | |
| CA1119320A (en) | 1980-01-15 | 1982-03-02 | James P. Mcmullan | Bassinet |
| DE3003819A1 (de) | 1980-02-02 | 1981-08-13 | Basf Ag, 6700 Ludwigshafen | Elektroden |
| US4309394A (en) | 1980-04-09 | 1982-01-05 | Monsanto Company | Method of preparing ultraphosphoric acid |
| US4609751A (en) * | 1981-12-14 | 1986-09-02 | General Electric Company | Method of hydrolyzing chlorosilanes |
| US4390680A (en) * | 1982-03-29 | 1983-06-28 | The Dow Chemical Company | Phenolic hydroxyl-containing compositions and epoxy resins prepared therefrom |
| US4405465A (en) * | 1982-06-30 | 1983-09-20 | Olin Corporation | Process for the removal of chlorate and hypochlorite from spent alkali metal chloride brines |
| US4499255B1 (en) * | 1982-09-13 | 2000-01-11 | Dow Chemical Co | Preparation of epoxy resins |
| SU1125226A1 (ru) | 1982-10-15 | 1984-11-23 | Башкирский государственный научно-исследовательский и проектный институт нефтяной промышленности | Способ обработки глинистых буровых и цементных растворов |
| DE3243617A1 (de) | 1982-11-25 | 1984-05-30 | Hermetic-Pumpen Gmbh, 7803 Gundelfingen | Pumpe zum foerdern hochkorrosiver medien |
| US4595469A (en) * | 1983-05-31 | 1986-06-17 | Chevron Research Company | Electrolytic process for production of gaseous hydrogen chloride and aqueous alkali metal hydroxide |
| DD216471A1 (de) | 1983-06-30 | 1984-12-12 | Leuna Werke Veb | Verfahren zur aufarbeitung von epoxidharzhaltigen reaktionsgemischen |
| SU1159716A1 (ru) | 1983-07-13 | 1985-06-07 | Чувашский государственный университет им.И.Н.Ульянова | Св зующее дл изготовлени литейных форм и стержней теплового отверждени |
| DE3339051A1 (de) | 1983-10-28 | 1985-05-09 | Henkel KGaA, 4000 Düsseldorf | Verfahren zur verbesserten destillativen aufarbeitung von glycerin |
| JPS60258171A (ja) * | 1984-06-04 | 1985-12-20 | Showa Denko Kk | エピクロルヒドリンの製造方法 |
| US4599178A (en) | 1984-07-16 | 1986-07-08 | Shell Oil Company | Recovery of glycerine from saline waters |
| DE3471768D1 (en) | 1984-11-09 | 1988-07-07 | Agfa Gevaert Nv | Photographic elements comprising protective layers containing antistats |
| US4560812A (en) | 1984-12-10 | 1985-12-24 | Shell Oil Company | Recovery of glycerine from saline waters |
| GB2173496B (en) | 1985-04-04 | 1989-01-05 | Inst Ciezkiej Syntezy Orga | Method for producing epichlorohydrin |
| DD238341B1 (de) | 1985-06-20 | 1988-06-22 | Thaelmann Schwermaschbau Veb | Verfahren zur regenerierung von altsanden |
| JPS62242638A (ja) | 1986-04-14 | 1987-10-23 | Nisso Yuka Kogyo Kk | 塩素化エ−テル化合物の製造方法 |
| CN1025432C (zh) * | 1987-05-29 | 1994-07-13 | 三井石油化学工业株式会社 | 一种制备环氧化合物的方法 |
| DE3721003C1 (en) | 1987-06-25 | 1988-12-01 | Solvay Werke Gmbh | Process for the preparation of polyglycerols |
| DE3811826A1 (de) | 1987-06-25 | 1989-10-19 | Solvay Werke Gmbh | Verfahren zur herstellung von polyglycerinen |
| DE3809882A1 (de) * | 1988-03-24 | 1989-10-05 | Solvay Werke Gmbh | Verfahren zur herstellung von polyglycerinen |
| DE3811524A1 (de) * | 1988-04-06 | 1989-10-19 | Solvay Werke Gmbh | Verfahren und vorrichtung zur herstellung von reinst-epichlorhydrin |
| DE3816783A1 (de) * | 1988-05-17 | 1989-11-30 | Wacker Chemie Gmbh | Verfahren zur reinigung von rohem, gasfoermigem chlorwasserstoff |
| US4882098A (en) | 1988-06-20 | 1989-11-21 | General Signal Corporation | Mass transfer mixing system especially for gas dispersion in liquids or liquid suspensions |
| KR900006513Y1 (ko) | 1988-07-06 | 1990-07-26 | 주식회사 불티나종합상사 | 라이터의 잠금장치 |
| CA1329782C (en) | 1988-08-09 | 1994-05-24 | Thomas Buenemann | Process for purifying crude glycerol |
| DE3842692A1 (de) * | 1988-12-19 | 1990-06-21 | Solvay Werke Gmbh | Verfahren zur herstellung von polyglycerinen |
| JPH0798763B2 (ja) | 1989-06-09 | 1995-10-25 | 鐘淵化学工業株式会社 | 1,2―ジクロルエタンの熱分解方法 |
| SU1685969A1 (ru) | 1989-07-26 | 1991-10-23 | Всесоюзный научно-исследовательский и проектный институт галургии | Способ пылеподавлени водорастворимых солей |
| KR910007854A (ko) | 1989-10-04 | 1991-05-30 | 리챠드 지. 워터만 | 모노에폭사이드의 제조방법 |
| WO1991009924A1 (en) | 1989-12-29 | 1991-07-11 | The Procter & Gamble Company | Ultra mild surfactant with good lather |
| DE4000104A1 (de) | 1990-01-04 | 1991-07-11 | Dallmer Gmbh & Co | Ablaufarmatur fuer eine brausewanne |
| JPH0625196B2 (ja) * | 1990-01-29 | 1994-04-06 | ダイソー株式会社 | エピクロルヒドリンの製造方法 |
| US5146011A (en) * | 1990-03-05 | 1992-09-08 | Olin Corporation | Preparation of chlorohydrins |
| US5278260A (en) | 1990-04-12 | 1994-01-11 | Ciba-Geigy Corporation | Process for the preparation of epoxy resins with concurrent addition of glycidol and epihalohydrin |
| KR0168057B1 (ko) | 1990-04-12 | 1999-03-20 | 베르너 발데크 | 에폭시 수지의 제조방법 |
| JPH085821B2 (ja) * | 1990-08-01 | 1996-01-24 | 昭和電工株式会社 | 塩素化反応器 |
| DE4039750A1 (de) | 1990-12-13 | 1992-06-17 | Basf Ag | Verfahren zur entfernung von phosgen aus abgasen |
| FR2677643B1 (fr) | 1991-06-12 | 1993-10-15 | Onidol | Procede pour l'obtention de polyglycerols et d'esters de polyglycerols. |
| IT1248564B (it) | 1991-06-27 | 1995-01-19 | Permelec Spa Nora | Processo di decomposizione elettrochimica di sali neutri senza co-produzione di alogeni o di acido e cella di elettrolisi adatta per la sua realizzazione. |
| DE4131938A1 (de) * | 1991-09-25 | 1993-04-01 | Krupp Koppers Gmbh | Verfahren zur aufarbeitung des sumpfproduktes einer extraktivdestillation zur gewinnung reiner kohlenwasserstoffe |
| US5139622A (en) | 1991-10-03 | 1992-08-18 | Texaco Chemical Company | Purification of propylene oxide by extractive distillation |
| BE1005719A3 (fr) * | 1992-03-17 | 1993-12-28 | Solvay | Procede de production d'epichlorhydrine. |
| DE4210997C1 (zh) | 1992-04-02 | 1993-01-14 | Krupp Vdm Gmbh, 5980 Werdohl, De | |
| US5393724A (en) | 1992-04-30 | 1995-02-28 | Tosoh Corporation | Process for removing oxidizable substance or reducible substance, composite containing metal oxide or hydroxide, and process for production thereof |
| DE4225870A1 (de) * | 1992-08-05 | 1994-02-10 | Basf Ag | Verfahren zur Herstellung von Glycerincarbonat |
| EP0586998B1 (de) | 1992-09-06 | 1998-01-07 | Solvay Deutschland GmbH | Verfahren zur Behandlung von organischen Stoffen, insbesondere chlororganische Verbindungen enthaltenden Abwässern aus der Epichlorhydrinherstellung |
| US5286354A (en) * | 1992-11-30 | 1994-02-15 | Sachem, Inc. | Method for preparing organic and inorganic hydroxides and alkoxides by electrolysis |
| JP3041443B2 (ja) | 1992-12-15 | 2000-05-15 | 花王株式会社 | グリセリンの製造方法 |
| DE4244482A1 (de) * | 1992-12-30 | 1994-07-07 | Solvay Deutschland | Verfahren zur Abwasserbehandlung |
| DE4302306A1 (de) | 1993-01-28 | 1994-08-04 | Erdoelchemie Gmbh | Verfahren zur Verminderung des AOX-Gehaltes von AOX-haltigen Abwässern |
| DE4309741A1 (de) | 1993-03-25 | 1994-09-29 | Henkel Kgaa | Verfahren zum Herstellen von Diglycerin |
| EP0618170B1 (en) | 1993-03-31 | 1996-09-04 | Basf Corporation | Process for producing reagent grade hydrochloric acid from the manufacture of organic isocyanates |
| DE4314108A1 (de) | 1993-04-29 | 1994-11-03 | Solvay Deutschland | Verfahren zur Behandlung von organische und anorganische Verbindungen enthaltenden Abwässern, vorzugsweise aus der Epichlorhydrin-Herstellung |
| JP3268890B2 (ja) | 1993-05-17 | 2002-03-25 | 東和化成工業株式会社 | 1,3−シクロヘキサンジカルボン酸の製造方法 |
| DE4335311A1 (de) | 1993-10-16 | 1995-04-20 | Chema Balcke Duerr Verfahrenst | Begasungsrührsystem |
| US5532389A (en) * | 1993-11-23 | 1996-07-02 | The Dow Chemical Company | Process for preparing alkylene oxides |
| DE4401635A1 (de) | 1994-01-21 | 1995-07-27 | Bayer Ag | Substituierte 1,2,3,4-Tetrahydro-5-nitro-pyrimidine |
| JPH083087A (ja) * | 1994-06-22 | 1996-01-09 | Mitsubishi Chem Corp | α−位にトリフルオロメチル基を有するアルコールの製造方法 |
| FR2723585B1 (fr) | 1994-08-12 | 1996-09-27 | Rhone Poulenc Chimie | Procede de preparation de composes du type polyisocyanates aromatiques en phase gazeuse. |
| ATE174009T1 (de) * | 1994-09-08 | 1998-12-15 | Solvay Umweltchemie Gmbh | Verfahren zur entfernung von chlorat- und bromatverbindungen aus wasser durch katalytische reduktion |
| US5486627A (en) | 1994-12-02 | 1996-01-23 | The Dow Chemical Company | Method for producing epoxides |
| US5578740A (en) | 1994-12-23 | 1996-11-26 | The Dow Chemical Company | Process for preparation of epoxy compounds essentially free of organic halides |
| US5731476A (en) | 1995-01-13 | 1998-03-24 | Arco Chemical Technology, L.P. | Poly ether preparation |
| US6177599B1 (en) | 1995-11-17 | 2001-01-23 | Oxy Vinyls, L.P. | Method for reducing formation of polychlorinated aromatic compounds during oxychlorination of C1-C3 hydrocarbons |
| JP3827358B2 (ja) | 1996-03-18 | 2006-09-27 | 株式会社トクヤマ | 塩酸水溶液の製造方法 |
| US5763630A (en) * | 1996-03-18 | 1998-06-09 | Arco Chemical Technology, L.P. | Propylene oxide process using alkaline earth metal compound-supported silver catalysts |
| US5744655A (en) * | 1996-06-19 | 1998-04-28 | The Dow Chemical Company | Process to make 2,3-dihalopropanols |
| FR2752242B1 (fr) | 1996-08-08 | 1998-10-16 | Inst Francais Du Petrole | Procede de fabrication d'esters a partir d'huiles vegetales ou animales et d'alcools |
| JP3228156B2 (ja) | 1996-11-14 | 2001-11-12 | 東亞合成株式会社 | 1,1−ビス(クロロメチル)−1−ヒドロキシメチルプロパンおよび1−モノ(クロロメチル)−1,1−ビス(ヒドロキシメチル)プロパンの製造方法 |
| JP4392862B2 (ja) * | 1997-02-20 | 2010-01-06 | ゾルファイ ドイチュラント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 溶液から塩素酸イオンを除去するための方法 |
| BE1011456A3 (fr) | 1997-09-18 | 1999-09-07 | Solvay | Procede de fabrication d'un oxiranne. |
| EP0916624B1 (en) | 1997-11-11 | 2001-07-25 | Kawasaki Steel Corporation | Porcelain-enameled steel sheets and frits for enameling |
| BE1011576A3 (fr) * | 1997-11-27 | 1999-11-09 | Solvay | Produit a base d'epichlorhydrine et procede de fabrication de ce produit. |
| EP1042219A1 (en) * | 1997-12-22 | 2000-10-11 | The Dow Chemical Company | Production of one or more useful products from lesser value halogenated materials |
| JP3223267B2 (ja) | 1997-12-25 | 2001-10-29 | 独立行政法人物質・材料研究機構 | 蛍石型またはその派生構造の酸化物焼結体とその製造方法 |
| AU749910B2 (en) * | 1998-03-19 | 2002-07-04 | Mitsubishi Chemical Corporation | Method for producing monoethylene glycol |
| JP4122603B2 (ja) * | 1998-03-31 | 2008-07-23 | 昭和電工株式会社 | ジクロロアセトキシプロパン及びその誘導体の製造方法 |
| DE19817656B4 (de) | 1998-04-21 | 2007-08-02 | Scintilla Ag | Handwerkzeugmaschine, insbesondere Stichsäge |
| BE1011880A4 (fr) | 1998-04-21 | 2000-02-01 | Solvay | Procede d'epuration de saumures. |
| US6103092A (en) | 1998-10-23 | 2000-08-15 | General Electric Company | Method for reducing metal ion concentration in brine solution |
| US6142458A (en) * | 1998-10-29 | 2000-11-07 | General Signal Corporation | Mixing system for dispersion of gas into liquid media |
| KR100715882B1 (ko) * | 1998-12-18 | 2007-05-09 | 다우 글로벌 테크놀로지스 인크. | 2,3-디할로프로판올의 제조방법 |
| DE60014831T2 (de) | 1999-05-17 | 2005-10-13 | Mitsubishi Heavy Industries, Ltd. | Verfahren zur behandlung der abwässer einer abgasenentschwefelungsanlage |
| US6111153A (en) | 1999-06-01 | 2000-08-29 | Dow Corning Corporation | Process for manufacturing methyl chloride |
| EP1059278B1 (en) | 1999-06-08 | 2004-12-01 | Showa Denko Kabushiki Kaisha | Process for producing epichlorohydrin and intermediate thereof |
| US6333420B1 (en) * | 1999-06-08 | 2001-12-25 | Showa Denko K.K. | Process for producing epichlorohydrin and intermediate thereof |
| JP2001037469A (ja) | 1999-07-27 | 2001-02-13 | Nissan Chem Ind Ltd | エピクロロヒドリンの微生物分解 |
| CN1119320C (zh) | 1999-11-10 | 2003-08-27 | 中国石化集团齐鲁石油化工公司 | 3-氯-2-羟丙基三甲基氯化铵有机副产物的分离方法 |
| US6713035B1 (en) | 2000-01-19 | 2004-03-30 | Sumitomo Chemical Company, Limited | Process for producing chlorine |
| JP3712903B2 (ja) * | 2000-01-28 | 2005-11-02 | 花王株式会社 | グリセリンの製造方法 |
| JP4389327B2 (ja) | 2000-03-16 | 2009-12-24 | 東亞合成株式会社 | 塩酸の回収方法 |
| JP2001276572A (ja) | 2000-04-04 | 2001-10-09 | Nkk Corp | 有害ポリハロゲン化化合物の分解方法及び装置 |
| US6613127B1 (en) | 2000-05-05 | 2003-09-02 | Dow Global Technologies Inc. | Quench apparatus and method for the reformation of organic materials |
| CN1427879A (zh) | 2000-05-05 | 2003-07-02 | 陶氏环球技术公司 | 耐火压力容器 |
| JP5407100B2 (ja) | 2000-05-08 | 2014-02-05 | 東ソー株式会社 | 有機物含有無機塩の精製方法及び食塩電解用精製塩 |
| US6740633B2 (en) * | 2000-05-09 | 2004-05-25 | Basf Aktiengesellschaft | Polyelectrolyte complexes and a method for production thereof |
| JP3825959B2 (ja) | 2000-06-16 | 2006-09-27 | キヤノン株式会社 | 汚染物質分解方法及び装置 |
| JP4200640B2 (ja) | 2000-06-20 | 2008-12-24 | マックス株式会社 | プリンタ |
| JP2002020333A (ja) * | 2000-07-06 | 2002-01-23 | Toagosei Co Ltd | 水酸基の塩素化方法 |
| JP2002038195A (ja) | 2000-07-27 | 2002-02-06 | Closs Co Ltd | 洗浄剤、この洗浄剤の製造方法、この洗浄剤の製造装置、及び、この洗浄剤を用いた洗浄方法 |
| BR0115908B1 (pt) * | 2000-12-04 | 2011-10-04 | processo para a produção de ésteres de ácido graxo. | |
| JP2003089680A (ja) | 2001-02-02 | 2003-03-28 | Nippon Shokubai Co Ltd | 芳香族化合物の製造方法 |
| EP1231189B2 (de) | 2001-02-08 | 2018-03-07 | Pfaudler GmbH | Hochkorrosionsbeständige schwermetallfreie Emailzusammensetzung sowie Verfahren zu deren Herstellung und Verwendung, und beschichtete Körper |
| JP2002265985A (ja) | 2001-03-06 | 2002-09-18 | Kanegafuchi Chem Ind Co Ltd | アポリポ蛋白質b分泌抑制性脂質組成物 |
| JP2002265986A (ja) * | 2001-03-15 | 2002-09-18 | Akio Kobayashi | 脂肪酸アルキルエステル及びグリセリンの製造方法 |
| US6588287B2 (en) * | 2001-04-02 | 2003-07-08 | Daimlerchrysler | Multiple stage system for aerodynamic testing of a vehicle on a static surface and related method |
| JP4219608B2 (ja) | 2001-04-05 | 2009-02-04 | 日本曹達株式会社 | ジフェニルスルホン化合物の製造方法 |
| DE10124386A1 (de) | 2001-05-18 | 2002-11-28 | Basf Ag | Verfahren zur Destillation oder Reaktivdestillation eines Gemisches, das mindestens eine toxische Komponente enthält |
| JP2003081891A (ja) | 2001-06-28 | 2003-03-19 | Sumitomo Chem Co Ltd | 1,2―ジクロロエタンの製造方法 |
| EP1411027A4 (en) | 2001-06-28 | 2009-07-29 | Sumitomo Chemical Co | PROCESS FOR CLEANING CHLORINE AND METHOD FOR PRODUCING 1,2-DICHLORETHANE |
| JP2003026791A (ja) * | 2001-07-11 | 2003-01-29 | Mitsubishi Gas Chem Co Inc | 芳香族ポリカーボネート樹脂の製造方法 |
| US6794478B2 (en) | 2001-09-28 | 2004-09-21 | Dainippon Ink And Chemicals, Inc. | Preparing epoxy resin by distilling two fractions to recover and reuse epihalohydrin without glycidol |
| US7517445B2 (en) | 2001-10-09 | 2009-04-14 | Scimist, Inc. | Mediated electrochemical oxidation of food waste materials |
| US6806396B2 (en) | 2001-12-18 | 2004-10-19 | E. I. Du Pont De Nemours And Company | Disposal of fluoroform (HFC-23) |
| JP3981556B2 (ja) | 2001-12-20 | 2007-09-26 | 株式会社トクヤマ | 塩化メチルの製造方法 |
| JP2003206473A (ja) | 2002-01-15 | 2003-07-22 | Mitsubishi Heavy Ind Ltd | シール材ならびに該シール材を適用した有機ハロゲン化合物の分解装置 |
| DE10203914C1 (de) | 2002-01-31 | 2003-10-02 | Degussa | Verfahren zur Reinigung eines HCI-haltigen Abgases aus der Organosilanesterherstellung und dessen Verwendung |
| DE10207442A1 (de) * | 2002-02-22 | 2003-09-11 | Bayer Ag | Aufbereitung von Kochsalz enthaltenden Abwässern zum Einsatz in der Chlor-Alkali-Elektrolyse |
| US6719957B2 (en) * | 2002-04-17 | 2004-04-13 | Bayer Corporation | Process for purification of anhydrous hydrogen chloride gas |
| US6802976B2 (en) | 2002-05-13 | 2004-10-12 | E. I. Du Pont De Nemours And Company | Organic sulfur reduction in wastewater |
| US6745726B2 (en) * | 2002-07-29 | 2004-06-08 | Visteon Global Technologies, Inc. | Engine thermal management for internal combustion engine |
| DE10235476A1 (de) * | 2002-08-02 | 2004-02-12 | Basf Ag | Integriertes Verfahren zur Herstellung von Isocyanaten |
| US7037481B2 (en) * | 2002-09-09 | 2006-05-02 | United Brine Services Company, Llc | Production of ultra pure salt |
| DE10254709A1 (de) | 2002-11-23 | 2004-06-09 | Reinhold Denz | Elektrolyse-Vorrichtung |
| DE10260084A1 (de) | 2002-12-19 | 2004-07-01 | Basf Ag | Auftrennung eines Stoffgemisches aus Clorwasserstoff und Phosgen |
| JP2004216246A (ja) | 2003-01-14 | 2004-08-05 | Toshiba Corp | 高周波プラズマ処理装置及び高周波プラズマ処理方法 |
| KR200329740Y1 (ko) | 2003-04-21 | 2003-10-10 | 심구일 | 건축용 외장 복합판넬 |
| KR100514819B1 (ko) | 2003-05-12 | 2005-09-14 | 주식회사 알에스텍 | 키랄 글리시딜 유도체의 제조방법 |
| JP2005007841A (ja) * | 2003-06-18 | 2005-01-13 | Nittetu Chemical Engineering Ltd | 耐食性の良好なフッ素樹脂ライニング方法 |
| JP2005097177A (ja) | 2003-09-25 | 2005-04-14 | Sumitomo Chemical Co Ltd | プロピレンオキサイドの精製方法 |
| ES2367572T3 (es) | 2003-11-20 | 2011-11-04 | Solvay (Société Anonyme) | Proceso para producción de dicloropropanol a partir de glicerol y un agente clorado y en presencia de un catalizador seleccionado de ácido adípico y ácido glutárico. |
| FR2868419B1 (fr) | 2004-04-05 | 2008-08-08 | Solvay Sa Sa Belge | Procede de fabrication de dichloropropanol |
| FR2862644B1 (fr) | 2003-11-20 | 2007-01-12 | Solvay | Utilisation de ressources renouvelables |
| EP2053034B1 (en) | 2003-11-20 | 2018-01-24 | Solvay Sa | Process for producing a chlorohydrin |
| FR2865903A1 (fr) | 2004-02-05 | 2005-08-12 | Michel Jean Robert Larose | Produit alimentaire fourre pour la restauration rapide. |
| EP1593732A1 (fr) * | 2004-05-03 | 2005-11-09 | Institut Français du Pétrole | Procede de transesterification d'huiles vegezales ou animales au moyen de catalyseurs heterogenes a base de zinc ou de bismuth de titane et d'aluminium |
| FR2869612B1 (fr) | 2004-05-03 | 2008-02-01 | Inst Francais Du Petrole | Procede de transesterification d'huiles vegetales ou animales au moyen de catalyseurs heterogenes a base de zinc, de titane et d'aluminium |
| FR2869613B1 (fr) | 2004-05-03 | 2008-08-29 | Inst Francais Du Petrole | Procede de transesterification d'huiles vegetales ou animales au moyen de catalyseurs heterogenes a base de bismuth, de titane et d'aluminium |
| US20060228692A1 (en) | 2004-06-30 | 2006-10-12 | Panda Computer Services, Inc. | Method and apparatus for effectively capturing a traditionally delivered classroom or a presentation and making it available for review over the Internet using remote production control |
| FR2872504B1 (fr) | 2004-06-30 | 2006-09-22 | Arkema Sa | Purification de l'acide chlorhydrique sous-produit de la synthese de l'acide methane sulfonique |
| CN102516205B (zh) * | 2004-07-21 | 2016-05-04 | 兰科知识产权有限责任公司 | 多羟基化脂族烃或其酯向氯醇的转化 |
| US7910781B2 (en) * | 2004-07-21 | 2011-03-22 | Dow Global Technologies Llc | Process for the conversion of a crude glycerol, crude mixtures of naturally derived multihydroxylated aliphatic hydrocarbons or esters thereof to a chlorohydrin |
| EP1632558A1 (en) | 2004-09-06 | 2006-03-08 | The Procter & Gamble | A composition comprising a surface deposition enhancing cationic polymer |
| DE102004044592A1 (de) | 2004-09-13 | 2006-03-30 | Basf Ag | Verfahren zur Trennung von Chlorwasserstoff und Phosgen |
| JP2008516048A (ja) * | 2004-10-08 | 2008-05-15 | ザ プロクター アンド ギャンブル カンパニー | オリゴマーアルキルグリセリルスルホネート及び/又はサルフェート界面活性剤混合物、並びにそれを含む洗剤組成物 |
| FR2881732B1 (fr) * | 2005-02-08 | 2007-11-02 | Solvay | Procede pour la purification de chlorure d'hydrogene |
| TW200630385A (en) | 2005-02-09 | 2006-09-01 | Vinnolit Gmbh & Co Kg | Process for the polymerisation of vinyl-containing monomers |
| TWI333945B (en) | 2005-05-20 | 2010-12-01 | Solvay | Process for preparing a chlorohydrin by converting polyhydroxylated aliphatic hydrocarbons |
| EP1762556A1 (en) | 2005-05-20 | 2007-03-14 | SOLVAY (Société Anonyme) | Process for producing dichloropropanol from glycerol |
| FR2885903B1 (fr) | 2005-05-20 | 2015-06-26 | Solvay | Procede de fabrication d'epichlorhydrine |
| JP4904730B2 (ja) | 2005-07-04 | 2012-03-28 | 住友化学株式会社 | 芳香族化合物と塩化水素の分離回収方法 |
| BRPI0618325A2 (pt) | 2005-11-08 | 2011-08-23 | Solvay | processo parar a produção de dicloropropanol |
| US7126032B1 (en) * | 2006-03-23 | 2006-10-24 | Sunoco, Inc. (R&M) | Purification of glycerin |
| BRPI0712775A2 (pt) | 2006-06-14 | 2012-09-04 | Solvay | Produto com base em glicerol bruto, e, processos para a purificação do produto com base em glicerol bruto, para a fabricação de dicloropropanol partindo de glicerol, para a fabricação de epocloroidrina, para a fabricação de resinas de epóxi, e, para a fabricação de dicloropropanol |
| FR2913683A1 (fr) | 2007-03-15 | 2008-09-19 | Solvay | Produit brut a base de glycerol, procede pour sa purification et son utilisation dans la fabrication de dichloropropanol |
| DE102006041465A1 (de) * | 2006-09-02 | 2008-03-06 | Bayer Materialscience Ag | Verfahren zur Herstellung von Diarylcarbonat |
| FR2912743B1 (fr) | 2007-02-20 | 2009-04-24 | Solvay | Procede de fabrication d'epichlorhydrine |
| CN101041421A (zh) | 2007-03-22 | 2007-09-26 | 广东富远稀土新材料股份有限公司 | 萃取提纯工业盐酸的方法 |
| FR2917411B1 (fr) | 2007-06-12 | 2012-08-03 | Solvay | Epichlorhydrine, procede de fabrication et utilisation |
| FR2918058A1 (fr) | 2007-06-28 | 2009-01-02 | Solvay | Produit a base de glycerol, procede pour sa purification et son utilisation dans la fabrication de dichloropropanol |
| DE102007058701A1 (de) * | 2007-12-06 | 2009-06-10 | Bayer Materialscience Ag | Verfahren zur Herstellung von Diarylcarbonat |
| FR2925046A1 (fr) | 2007-12-14 | 2009-06-19 | Rhodia Poliamida E Especialidades Ltda | Procede d'obtention d'alcool a partir d'un aldehyde |
| FR2925045B1 (fr) | 2007-12-17 | 2012-02-24 | Solvay | Produit a base de glycerol, procede pour son obtention et son utilisation dans la fabrication de dichloropropanol |
| EP2085364A1 (en) | 2008-01-31 | 2009-08-05 | SOLVAY (Société Anonyme) | Process for degrading organic substances in an aqueous composition |
| US20090196041A1 (en) * | 2008-02-05 | 2009-08-06 | Joseph Peter D | Energy efficient light |
| JP2009263338A (ja) | 2008-03-12 | 2009-11-12 | Daiso Co Ltd | エピクロロヒドリンの新規な製造方法 |
| FR2929611B3 (fr) | 2008-04-03 | 2010-09-03 | Solvay | Composition comprenant du glycerol, procede pour son obtention et son utilisation dans la fabrication de dichloropropanol |
| TWI368616B (en) * | 2008-08-01 | 2012-07-21 | Dow Global Technologies Llc | Process for producing epoxides |
| FR2935699A1 (fr) | 2008-09-10 | 2010-03-12 | Solvay | Procede de fabrication d'un produit chimique |
| FR2935968B1 (fr) | 2008-09-12 | 2010-09-10 | Solvay | Procede pour la purification de chlorure d'hydrogene |
-
2006
- 2006-05-19 TW TW095117942A patent/TWI333945B/zh not_active IP Right Cessation
- 2006-05-19 WO PCT/EP2006/062466 patent/WO2006106155A2/fr not_active Ceased
- 2006-05-19 WO PCT/EP2006/062437 patent/WO2006100311A2/fr not_active Ceased
- 2006-05-19 CN CN2006800006054A patent/CN101006037B/zh not_active Expired - Fee Related
- 2006-05-19 MX MX2007014525A patent/MX2007014525A/es active IP Right Grant
- 2006-05-19 CN CN2006800005348A patent/CN101031532B/zh not_active Expired - Fee Related
- 2006-05-19 EA EA200702564A patent/EA014241B1/ru not_active IP Right Cessation
- 2006-05-19 CA CA2608961A patent/CA2608961C/en not_active Expired - Fee Related
- 2006-05-19 TW TW095117952A patent/TW200700401A/zh unknown
- 2006-05-19 KR KR1020077029670A patent/KR101337048B1/ko not_active Expired - Fee Related
- 2006-05-19 CN CN2012100221289A patent/CN102603474A/zh active Pending
- 2006-05-19 KR KR1020077029659A patent/KR100982618B1/ko not_active Expired - Fee Related
- 2006-05-19 BR BRPI0610745-1A patent/BRPI0610745A2/pt not_active Application Discontinuation
- 2006-05-19 EP EP06755272A patent/EP1885675A1/fr not_active Withdrawn
- 2006-05-19 EP EP10182309A patent/EP2275417A3/en not_active Withdrawn
- 2006-05-19 CA CA2608946A patent/CA2608946C/en not_active Expired - Fee Related
- 2006-05-19 CA CA002608937A patent/CA2608937A1/en not_active Abandoned
- 2006-05-19 CN CN2006800005530A patent/CN101052606B/zh not_active Expired - Fee Related
- 2006-05-19 WO PCT/EP2006/062442 patent/WO2006100314A1/fr not_active Ceased
- 2006-05-19 US US11/915,046 patent/US20080194850A1/en not_active Abandoned
- 2006-05-19 EA EA200702546A patent/EA200702546A1/ru unknown
- 2006-05-19 TW TW098117312A patent/TWI332942B/zh not_active IP Right Cessation
- 2006-05-19 US US11/915,067 patent/US20080200701A1/en not_active Abandoned
- 2006-05-19 WO PCT/EP2006/062444 patent/WO2006100315A2/fr not_active Ceased
- 2006-05-19 TW TW095117957A patent/TWI332940B/zh not_active IP Right Cessation
- 2006-05-19 EA EA200702561A patent/EA200702561A1/ru unknown
- 2006-05-19 CA CA002608719A patent/CA2608719A1/en not_active Abandoned
- 2006-05-19 WO PCT/EP2006/062448 patent/WO2006106153A2/fr not_active Ceased
- 2006-05-19 BR BRPI0610789-3A patent/BRPI0610789A2/pt not_active Application Discontinuation
- 2006-05-19 MX MX2007014514A patent/MX2007014514A/es active IP Right Grant
- 2006-05-19 US US11/914,836 patent/US7893193B2/en active Active
- 2006-05-19 EP EP06763198A patent/EP1885678A1/fr not_active Withdrawn
- 2006-05-19 CA CA002608723A patent/CA2608723A1/en not_active Abandoned
- 2006-05-19 EP EP06755271A patent/EP1885706A2/fr not_active Withdrawn
- 2006-05-19 WO PCT/EP2006/062461 patent/WO2006100319A1/fr not_active Ceased
- 2006-05-19 CA CA002608953A patent/CA2608953A1/en not_active Abandoned
- 2006-05-19 JP JP2008511726A patent/JP5405821B2/ja not_active Expired - Fee Related
- 2006-05-19 EP EP06755273A patent/EP1885676A2/fr not_active Withdrawn
- 2006-05-19 BR BRPI0610799-0A patent/BRPI0610799A2/pt not_active IP Right Cessation
- 2006-05-19 US US11/914,862 patent/US7615670B2/en not_active Expired - Fee Related
- 2006-05-19 TW TW095117970A patent/TW200700403A/zh unknown
- 2006-05-19 MX MX2007014532A patent/MX2007014532A/es not_active Application Discontinuation
- 2006-05-19 BR BRPI0610748-6A patent/BRPI0610748A2/pt not_active IP Right Cessation
- 2006-05-19 EA EA200702553A patent/EA200702553A1/ru unknown
- 2006-05-19 TW TW095117967A patent/TWI322142B/zh active
- 2006-05-19 KR KR1020077029669A patent/KR101331367B1/ko not_active Expired - Fee Related
- 2006-05-19 BR BRPI0610791-5A patent/BRPI0610791A2/pt active Search and Examination
- 2006-05-19 EA EA200702555A patent/EA200702555A1/ru unknown
- 2006-05-19 CN CN2006800005352A patent/CN1993307B/zh not_active Expired - Fee Related
- 2006-05-19 TW TW095117955A patent/TWI335323B/zh not_active IP Right Cessation
- 2006-05-19 CA CA002608722A patent/CA2608722A1/en not_active Abandoned
- 2006-05-19 CN CN2006800005507A patent/CN101107208B/zh not_active Expired - Fee Related
- 2006-05-19 KR KR1020077029658A patent/KR100982605B1/ko active Active
- 2006-05-19 TW TW095117962A patent/TWI332493B/zh not_active IP Right Cessation
- 2006-05-19 EP EP06755270A patent/EP1885674A1/fr not_active Withdrawn
- 2006-05-19 CN CN2012100221382A patent/CN102659511A/zh active Pending
- 2006-05-19 EA EA200702551A patent/EA200702551A1/ru unknown
- 2006-05-19 CA CA002608732A patent/CA2608732A1/en not_active Abandoned
- 2006-05-19 TW TW098117310A patent/TWI332941B/zh not_active IP Right Cessation
- 2006-05-19 EP EP06763189A patent/EP1885677A2/fr not_active Withdrawn
- 2006-05-19 KR KR1020077029655A patent/KR100978436B1/ko active Active
- 2006-05-19 JP JP2008511713A patent/JP5777268B2/ja active Active
- 2006-05-19 MX MX2007014530A patent/MX2007014530A/es not_active Application Discontinuation
- 2006-05-19 WO PCT/EP2006/062459 patent/WO2006100318A2/fr not_active Ceased
- 2006-05-19 JP JP2008511730A patent/JP2008540617A/ja active Pending
- 2006-05-19 EA EA200702565A patent/EA200702565A1/ru unknown
- 2006-05-19 BR BRPI0610744-3A patent/BRPI0610744A2/pt not_active Application Discontinuation
- 2006-05-19 KR KR1020077029628A patent/KR100979371B1/ko active Active
- 2006-05-19 WO PCT/EP2006/062438 patent/WO2006100312A2/en not_active Ceased
- 2006-05-19 EA EA201300253A patent/EA201300253A1/ru unknown
- 2006-05-19 EP EP06755262.0A patent/EP1885705B1/fr active Active
- 2006-05-19 US US11/915,056 patent/US7557253B2/en not_active Expired - Fee Related
- 2006-05-19 EA EA200702562A patent/EA013681B1/ru not_active IP Right Cessation
- 2006-05-19 MX MX2007014523A patent/MX2007014523A/es active IP Right Grant
- 2006-05-19 TW TW095117946A patent/TWI313261B/zh not_active IP Right Cessation
- 2006-05-19 CN CN2006800006073A patent/CN101006068B/zh not_active Ceased
- 2006-05-19 KR KR1020077029668A patent/KR101345965B1/ko active Active
- 2006-05-19 MY MYPI20062332A patent/MY148345A/en unknown
- 2006-05-19 TW TW098117309A patent/TWI349657B/zh not_active IP Right Cessation
- 2006-05-19 JP JP2008511725A patent/JP2008540613A/ja active Pending
- 2006-05-19 JP JP2008511721A patent/JP2008545643A/ja active Pending
- 2006-05-19 US US11/914,874 patent/US7906692B2/en not_active Expired - Fee Related
- 2006-05-19 CN CN200680000523XA patent/CN1993306B/zh not_active Expired - Fee Related
- 2006-05-19 BR BRPI0610746-0A patent/BRPI0610746A2/pt not_active IP Right Cessation
- 2006-05-19 JP JP2008511714A patent/JP2008545640A/ja active Pending
- 2006-05-19 EP EP10182403A patent/EP2284163A3/en not_active Withdrawn
- 2006-05-19 EP EP10182191.6A patent/EP2284162B1/en active Active
- 2006-05-19 US US11/914,879 patent/US8173823B2/en active Active
- 2006-05-19 BR BRPI0610751-6A patent/BRPI0610751A2/pt not_active Application Discontinuation
- 2006-05-19 TW TW095117968A patent/TWI388542B/zh not_active IP Right Cessation
- 2006-05-19 WO PCT/EP2006/062462 patent/WO2006100320A2/fr not_active Ceased
- 2006-05-19 CA CA002608725A patent/CA2608725A1/en not_active Abandoned
- 2006-05-19 MY MYPI20062328A patent/MY158842A/en unknown
- 2006-05-19 JP JP2008511717A patent/JP5259390B2/ja not_active Expired - Fee Related
- 2006-05-19 MY MYPI20062334A patent/MY148378A/en unknown
- 2006-05-19 EA EA200702552A patent/EA017149B1/ru not_active IP Right Cessation
- 2006-05-19 CA CA002608816A patent/CA2608816A1/en not_active Abandoned
- 2006-05-19 CA CA002608715A patent/CA2608715A1/en not_active Abandoned
- 2006-05-19 US US11/915,088 patent/US20080214848A1/en not_active Abandoned
- 2006-05-19 US US11/914,868 patent/US8344185B2/en not_active Expired - Fee Related
- 2006-05-19 TW TW095117963A patent/TWI320037B/zh not_active IP Right Cessation
- 2006-05-19 EA EA200702554A patent/EA200702554A1/ru unknown
- 2006-05-19 JP JP2008511727A patent/JP5551359B2/ja not_active Expired - Fee Related
- 2006-05-19 CN CN2006800005511A patent/CN101098843B/zh not_active Expired - Fee Related
- 2006-05-19 WO PCT/EP2006/062447 patent/WO2006100317A1/fr not_active Ceased
- 2006-05-19 MX MX2007014516A patent/MX2007014516A/es not_active Application Discontinuation
- 2006-05-19 JP JP2008511718A patent/JP5179351B2/ja not_active Expired - Fee Related
- 2006-05-19 EA EA200702549A patent/EA018478B1/ru not_active IP Right Cessation
- 2006-05-19 EP EP06755268A patent/EP1885672A2/fr not_active Withdrawn
- 2006-05-19 JP JP2008511720A patent/JP5419446B2/ja active Active
- 2006-05-19 EP EP06755267A patent/EP1885671A1/fr not_active Withdrawn
- 2006-05-19 TW TW095117959A patent/TWI321129B/zh not_active IP Right Cessation
- 2006-05-19 CA CA002608956A patent/CA2608956A1/en not_active Abandoned
- 2006-05-19 MX MX2007014527A patent/MX2007014527A/es active IP Right Grant
- 2006-05-19 TW TW095117961A patent/TWI320036B/zh not_active IP Right Cessation
- 2006-05-19 EA EA200702550A patent/EA018479B1/ru not_active IP Right Cessation
- 2006-05-19 EP EP06755264A patent/EP1890988A2/fr not_active Withdrawn
- 2006-05-19 CN CN2012100221306A patent/CN102603475A/zh active Pending
- 2006-05-19 JP JP2008511716A patent/JP2008540609A/ja active Pending
- 2006-05-19 US US11/914,891 patent/US8106245B2/en not_active Expired - Fee Related
- 2006-05-19 JP JP2008511715A patent/JP2008545641A/ja active Pending
- 2006-05-19 CN CN201110379336XA patent/CN102531841A/zh active Pending
- 2006-05-19 EP EP06755269.5A patent/EP1885673B1/fr not_active Not-in-force
- 2006-05-19 WO PCT/EP2006/062445 patent/WO2006100316A1/fr not_active Ceased
- 2006-05-19 JP JP2008511728A patent/JP5280842B2/ja not_active Expired - Fee Related
- 2006-05-19 MY MYPI20062337A patent/MY148295A/en unknown
- 2006-05-19 TW TW095117948A patent/TWI323249B/zh not_active IP Right Cessation
- 2006-05-19 US US11/914,856 patent/US7906691B2/en active Active
- 2006-05-19 CN CN2012101645245A patent/CN102690168A/zh active Pending
- 2006-05-19 US US11/915,053 patent/US8389777B2/en not_active Expired - Fee Related
- 2006-05-19 EP EP06755263A patent/EP1904427A2/en not_active Withdrawn
- 2006-05-19 CA CA002608720A patent/CA2608720A1/en not_active Abandoned
- 2006-05-19 WO PCT/EP2006/062463 patent/WO2006106154A1/fr not_active Ceased
- 2006-05-19 EP EP06763200A patent/EP1891032A2/fr not_active Withdrawn
- 2006-05-19 WO PCT/EP2006/062439 patent/WO2006100313A2/fr not_active Ceased
- 2006-05-19 EA EA200702548A patent/EA200702548A1/ru unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2144612A (en) * | 1936-09-10 | 1939-01-24 | Dow Chemical Co | Preparation of glycerol dichlorohydrin |
| WO2005021476A1 (en) * | 2003-09-01 | 2005-03-10 | Spolek Pro Chemickou A Hutni Vyrobu, Akciova Spolecnost | Method of preparing dichloropropanols from glycerine |
Non-Patent Citations (1)
| Title |
|---|
| G.P.GIBSON: "The Preparation,Properties And Uses Of Glycerol Derivatives.Part III.The Chlorohydrins", 《CHEMISTRY AND INDUSTRY》 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102659511A (zh) | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 | |
| CN1993308B (zh) | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 | |
| CN101921175B (zh) | 用于生产有机化合物的方法 | |
| CN100577622C (zh) | 从甘油生产二氯丙醇的方法,甘油最终来自生物柴油生产中动物脂肪的转化 | |
| US8420871B2 (en) | Process for producing an organic compound | |
| CN101090878B (zh) | 通过转化多羟基脂肪烃制备氯代醇的方法 | |
| HK1153460A (zh) | 用於生产二氯丙醇的方法 | |
| HK1153461A (zh) | 用於生产二氯丙醇的方法 | |
| HK1105951A (zh) | 含有二氯丙醇的假共沸组合物以及用於生产该组合物的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20120912 |