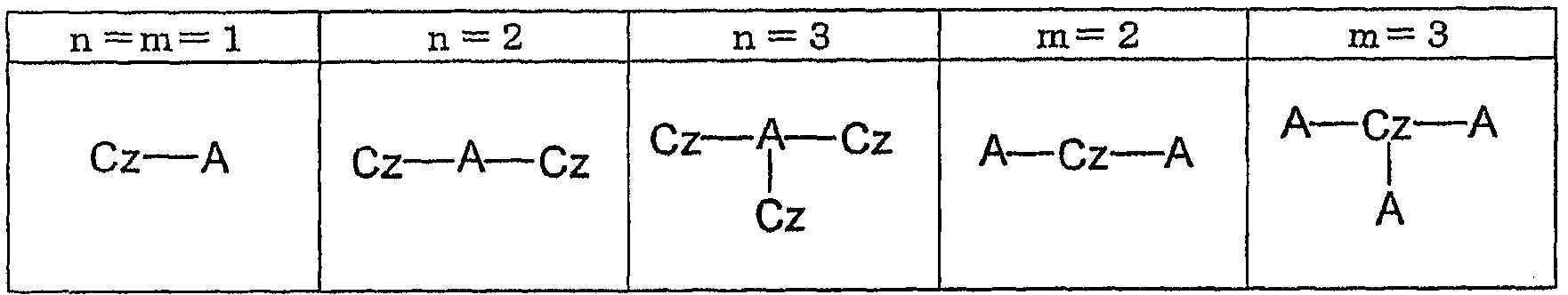KR100948700B1 - 유기 전기 발광 소자용 재료 및 이를 이용한 유기 전기발광 소자 - Google Patents
유기 전기 발광 소자용 재료 및 이를 이용한 유기 전기발광 소자 Download PDFInfo
- Publication number
- KR100948700B1 KR100948700B1 KR1020047014947A KR20047014947A KR100948700B1 KR 100948700 B1 KR100948700 B1 KR 100948700B1 KR 1020047014947 A KR1020047014947 A KR 1020047014947A KR 20047014947 A KR20047014947 A KR 20047014947A KR 100948700 B1 KR100948700 B1 KR 100948700B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- formula
- substituted
- organic electroluminescent
- electroluminescent device
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 239000000463 material Substances 0.000 title claims abstract description 78
- 150000001875 compounds Chemical class 0.000 claims abstract description 109
- 239000010409 thin film Substances 0.000 claims abstract description 21
- -1 azaindolidine Chemical compound 0.000 claims description 140
- 125000004432 carbon atom Chemical group C* 0.000 claims description 45
- 238000000034 method Methods 0.000 claims description 21
- 125000003118 aryl group Chemical group 0.000 claims description 19
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 claims description 18
- 125000000732 arylene group Chemical group 0.000 claims description 13
- 125000001072 heteroaryl group Chemical group 0.000 claims description 12
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 claims description 10
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 claims description 10
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 claims description 10
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 8
- AIFRHYZBTHREPW-UHFFFAOYSA-N β-carboline Chemical compound N1=CC=C2C3=CC=CC=C3NC2=C1 AIFRHYZBTHREPW-UHFFFAOYSA-N 0.000 claims description 8
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 claims description 7
- 230000005284 excitation Effects 0.000 claims description 7
- 125000006267 biphenyl group Chemical group 0.000 claims description 6
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims description 6
- 125000002993 cycloalkylene group Chemical group 0.000 claims description 6
- 125000001624 naphthyl group Chemical group 0.000 claims description 6
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 claims description 5
- 230000005525 hole transport Effects 0.000 claims description 5
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 claims description 5
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 claims description 5
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 claims description 4
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 claims description 4
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 claims description 4
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 claims description 4
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical compound N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 claims description 4
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 claims description 4
- 150000002484 inorganic compounds Chemical class 0.000 claims description 4
- 229910010272 inorganic material Inorganic materials 0.000 claims description 4
- JFJNVIPVOCESGZ-UHFFFAOYSA-N 2,3-dipyridin-2-ylpyridine Chemical compound N1=CC=CC=C1C1=CC=CN=C1C1=CC=CC=N1 JFJNVIPVOCESGZ-UHFFFAOYSA-N 0.000 claims description 3
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 claims description 3
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 3
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 3
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 claims description 2
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 claims description 2
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 claims description 2
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 claims description 2
- 125000004957 naphthylene group Chemical group 0.000 claims description 2
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 claims 3
- UTCSSFWDNNEEBH-UHFFFAOYSA-N imidazo[1,2-a]pyridine Chemical compound C1=CC=CC2=NC=CN21 UTCSSFWDNNEEBH-UHFFFAOYSA-N 0.000 claims 3
- IAGGQPCKLSLSEC-UHFFFAOYSA-N 1h-azepine-2,3-dicarbonitrile Chemical compound N#CC1=C(C#N)C=CC=CN1 IAGGQPCKLSLSEC-UHFFFAOYSA-N 0.000 claims 1
- 125000000623 heterocyclic group Chemical group 0.000 abstract description 6
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 abstract description 6
- 239000010410 layer Substances 0.000 description 106
- 230000015572 biosynthetic process Effects 0.000 description 81
- 238000003786 synthesis reaction Methods 0.000 description 79
- 238000000434 field desorption mass spectrometry Methods 0.000 description 49
- 239000010408 film Substances 0.000 description 42
- 238000002347 injection Methods 0.000 description 37
- 239000007924 injection Substances 0.000 description 37
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 33
- 239000013078 crystal Substances 0.000 description 29
- 239000007787 solid Substances 0.000 description 25
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 238000005259 measurement Methods 0.000 description 21
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 20
- 229910052757 nitrogen Inorganic materials 0.000 description 20
- 239000000243 solution Substances 0.000 description 20
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 18
- 238000006243 chemical reaction Methods 0.000 description 18
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 18
- 238000005160 1H NMR spectroscopy Methods 0.000 description 14
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 12
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 12
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- 238000010992 reflux Methods 0.000 description 12
- 239000000758 substrate Substances 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 10
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 10
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 9
- 239000011347 resin Substances 0.000 description 9
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 8
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 8
- 229910052751 metal Inorganic materials 0.000 description 8
- 239000002184 metal Substances 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 229920005989 resin Polymers 0.000 description 8
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 7
- 229910052782 aluminium Inorganic materials 0.000 description 7
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 7
- 230000000052 comparative effect Effects 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 239000003960 organic solvent Substances 0.000 description 7
- 239000002904 solvent Substances 0.000 description 7
- 230000032258 transport Effects 0.000 description 7
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 6
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 6
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 6
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000012300 argon atmosphere Substances 0.000 description 6
- GBRBMTNGQBKBQE-UHFFFAOYSA-L copper;diiodide Chemical compound I[Cu]I GBRBMTNGQBKBQE-UHFFFAOYSA-L 0.000 description 6
- 125000002524 organometallic group Chemical group 0.000 description 6
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 6
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical class N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 229910052763 palladium Inorganic materials 0.000 description 5
- 229910000027 potassium carbonate Inorganic materials 0.000 description 5
- 229910000160 potassium phosphate Inorganic materials 0.000 description 5
- 235000011009 potassium phosphates Nutrition 0.000 description 5
- 229920002545 silicone oil Polymers 0.000 description 5
- SSJXIUAHEKJCMH-PHDIDXHHSA-N (1r,2r)-cyclohexane-1,2-diamine Chemical compound N[C@@H]1CCCC[C@H]1N SSJXIUAHEKJCMH-PHDIDXHHSA-N 0.000 description 4
- XEZNGIUYQVAUSS-UHFFFAOYSA-N 18-crown-6 Chemical compound C1COCCOCCOCCOCCOCCO1 XEZNGIUYQVAUSS-UHFFFAOYSA-N 0.000 description 4
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 4
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 239000000956 alloy Substances 0.000 description 4
- 229910045601 alloy Inorganic materials 0.000 description 4
- 239000012298 atmosphere Substances 0.000 description 4
- 0 c(cc1)ccc1-c(nc1)cc(c2ccccc22)c1[n]2-c1ccc(*2c(cccc3)c3-c3c2cccc3)cc1 Chemical compound c(cc1)ccc1-c(nc1)cc(c2ccccc22)c1[n]2-c1ccc(*2c(cccc3)c3-c3c2cccc3)cc1 0.000 description 4
- 238000004140 cleaning Methods 0.000 description 4
- XCJYREBRNVKWGJ-UHFFFAOYSA-N copper(II) phthalocyanine Chemical compound [Cu+2].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 XCJYREBRNVKWGJ-UHFFFAOYSA-N 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 238000004020 luminiscence type Methods 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 4
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 4
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 4
- 125000004076 pyridyl group Chemical group 0.000 description 4
- 229910052709 silver Inorganic materials 0.000 description 4
- 239000004332 silver Substances 0.000 description 4
- 229910000029 sodium carbonate Inorganic materials 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 4
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 4
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 3
- AJKVQEKCUACUMD-UHFFFAOYSA-N 2-Acetylpyridine Chemical compound CC(=O)C1=CC=CC=N1 AJKVQEKCUACUMD-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 3
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 239000004020 conductor Substances 0.000 description 3
- 229920001577 copolymer Polymers 0.000 description 3
- 125000004093 cyano group Chemical group *C#N 0.000 description 3
- 229910052731 fluorine Inorganic materials 0.000 description 3
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 3
- 229910052737 gold Inorganic materials 0.000 description 3
- 239000010931 gold Substances 0.000 description 3
- 229910052749 magnesium Inorganic materials 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical group C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 3
- 125000005561 phenanthryl group Chemical group 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 238000010791 quenching Methods 0.000 description 3
- 125000005493 quinolyl group Chemical group 0.000 description 3
- 229910052707 ruthenium Inorganic materials 0.000 description 3
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical group C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 238000001771 vacuum deposition Methods 0.000 description 3
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 2
- KLCLIOISYBHYDZ-UHFFFAOYSA-N 1,4,4-triphenylbuta-1,3-dienylbenzene Chemical class C=1C=CC=CC=1C(C=1C=CC=CC=1)=CC=C(C=1C=CC=CC=1)C1=CC=CC=C1 KLCLIOISYBHYDZ-UHFFFAOYSA-N 0.000 description 2
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical group CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 2
- BRSRUYVJULRMRQ-UHFFFAOYSA-N 1-phenylanthracene Chemical class C1=CC=CC=C1C1=CC=CC2=CC3=CC=CC=C3C=C12 BRSRUYVJULRMRQ-UHFFFAOYSA-N 0.000 description 2
- ICSNLGPSRYBMBD-UHFFFAOYSA-N 2-aminopyridine Chemical compound NC1=CC=CC=N1 ICSNLGPSRYBMBD-UHFFFAOYSA-N 0.000 description 2
- JBWRZTKHMKVFMQ-UHFFFAOYSA-N 3,6-dibromo-9-phenylcarbazole Chemical compound C12=CC=C(Br)C=C2C2=CC(Br)=CC=C2N1C1=CC=CC=C1 JBWRZTKHMKVFMQ-UHFFFAOYSA-N 0.000 description 2
- PCMKGEAHIZDRFL-UHFFFAOYSA-N 3,6-diphenyl-9h-carbazole Chemical compound C1=CC=CC=C1C1=CC=C(NC=2C3=CC(=CC=2)C=2C=CC=CC=2)C3=C1 PCMKGEAHIZDRFL-UHFFFAOYSA-N 0.000 description 2
- GAMYYCRTACQSBR-UHFFFAOYSA-N 4-azabenzimidazole Chemical compound C1=CC=C2NC=NC2=N1 GAMYYCRTACQSBR-UHFFFAOYSA-N 0.000 description 2
- ZRYZBQLXDKPBDU-UHFFFAOYSA-N 4-bromobenzaldehyde Chemical compound BrC1=CC=C(C=O)C=C1 ZRYZBQLXDKPBDU-UHFFFAOYSA-N 0.000 description 2
- 229910017109 AlON Inorganic materials 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 2
- 238000004566 IR spectroscopy Methods 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 229910001508 alkali metal halide Inorganic materials 0.000 description 2
- 150000008045 alkali metal halides Chemical class 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000003545 alkoxy group Chemical group 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 2
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 2
- 125000003710 aryl alkyl group Chemical group 0.000 description 2
- 125000004104 aryloxy group Chemical group 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- WZJYKHNJTSNBHV-UHFFFAOYSA-N benzoquinoline Natural products C1=CN=C2C3=CC=CC=C3C=CC2=C1 WZJYKHNJTSNBHV-UHFFFAOYSA-N 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 150000004696 coordination complex Chemical class 0.000 description 2
- VPUGDVKSAQVFFS-UHFFFAOYSA-N coronene Chemical compound C1=C(C2=C34)C=CC3=CC=C(C=C3)C4=C4C3=CC=C(C=C3)C4=C2C3=C1 VPUGDVKSAQVFFS-UHFFFAOYSA-N 0.000 description 2
- 125000004956 cyclohexylene group Chemical group 0.000 description 2
- ZSWFCLXCOIISFI-UHFFFAOYSA-N cyclopentadiene Chemical compound C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- 230000005684 electric field Effects 0.000 description 2
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 2
- 230000005281 excited state Effects 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 229910052733 gallium Inorganic materials 0.000 description 2
- PVADDRMAFCOOPC-UHFFFAOYSA-N germanium monoxide Inorganic materials [Ge]=O PVADDRMAFCOOPC-UHFFFAOYSA-N 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000004857 imidazopyridinyl group Chemical group N1C(=NC2=C1C=CC=N2)* 0.000 description 2
- 229910052741 iridium Inorganic materials 0.000 description 2
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 2
- QWTDNUCVQCZILF-UHFFFAOYSA-N isopentane Chemical compound CCC(C)C QWTDNUCVQCZILF-UHFFFAOYSA-N 0.000 description 2
- 125000005956 isoquinolyl group Chemical group 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- LKKPNUDVOYAOBB-UHFFFAOYSA-N naphthalocyanine Chemical class N1C(N=C2C3=CC4=CC=CC=C4C=C3C(N=C3C4=CC5=CC=CC=C5C=C4C(=N4)N3)=N2)=C(C=C2C(C=CC=C2)=C2)C2=C1N=C1C2=CC3=CC=CC=C3C=C2C4=N1 LKKPNUDVOYAOBB-UHFFFAOYSA-N 0.000 description 2
- 229910052762 osmium Inorganic materials 0.000 description 2
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 2
- 150000004866 oxadiazoles Chemical class 0.000 description 2
- 230000000737 periodic effect Effects 0.000 description 2
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 2
- 238000001296 phosphorescence spectrum Methods 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920000548 poly(silane) polymer Polymers 0.000 description 2
- 229920002492 poly(sulfone) Polymers 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920000128 polypyrrole Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 229920000123 polythiophene Polymers 0.000 description 2
- 229920002635 polyurethane Polymers 0.000 description 2
- 239000004814 polyurethane Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 125000003373 pyrazinyl group Chemical group 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 125000001725 pyrenyl group Chemical group 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- CYIDZMCFTVVTJO-UHFFFAOYSA-N pyromellitic acid Chemical compound OC(=O)C1=CC(C(O)=O)=C(C(O)=O)C=C1C(O)=O CYIDZMCFTVVTJO-UHFFFAOYSA-N 0.000 description 2
- 230000000171 quenching effect Effects 0.000 description 2
- 229910052702 rhenium Inorganic materials 0.000 description 2
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 2
- 229910052703 rhodium Inorganic materials 0.000 description 2
- 239000010948 rhodium Substances 0.000 description 2
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 2
- 230000000630 rising effect Effects 0.000 description 2
- 229910052814 silicon oxide Inorganic materials 0.000 description 2
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 2
- 238000004544 sputter deposition Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 125000006836 terphenylene group Chemical group 0.000 description 2
- IBBLKSWSCDAPIF-UHFFFAOYSA-N thiopyran Chemical compound S1C=CC=C=C1 IBBLKSWSCDAPIF-UHFFFAOYSA-N 0.000 description 2
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical class [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 2
- 150000003852 triazoles Chemical class 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- 238000004506 ultrasonic cleaning Methods 0.000 description 2
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- UWRZIZXBOLBCON-VOTSOKGWSA-N (e)-2-phenylethenamine Chemical compound N\C=C\C1=CC=CC=C1 UWRZIZXBOLBCON-VOTSOKGWSA-N 0.000 description 1
- POILWHVDKZOXJZ-ARJAWSKDSA-M (z)-4-oxopent-2-en-2-olate Chemical compound C\C([O-])=C\C(C)=O POILWHVDKZOXJZ-ARJAWSKDSA-M 0.000 description 1
- MHCVCKDNQYMGEX-UHFFFAOYSA-N 1,1'-biphenyl;phenoxybenzene Chemical group C1=CC=CC=C1C1=CC=CC=C1.C=1C=CC=CC=1OC1=CC=CC=C1 MHCVCKDNQYMGEX-UHFFFAOYSA-N 0.000 description 1
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N 1,1-dimethoxyethane Chemical compound COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 1
- YWDUZLFWHVQCHY-UHFFFAOYSA-N 1,3,5-tribromobenzene Chemical compound BrC1=CC(Br)=CC(Br)=C1 YWDUZLFWHVQCHY-UHFFFAOYSA-N 0.000 description 1
- 125000000355 1,3-benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 1
- MKZHJJQCUIZEDE-UHFFFAOYSA-N 1-[(2-hydroxy-3-naphthalen-1-yloxypropyl)-propan-2-ylamino]-3-naphthalen-1-yloxypropan-2-ol Chemical compound C1=CC=C2C(OCC(O)CN(CC(O)COC=3C4=CC=CC=C4C=CC=3)C(C)C)=CC=CC2=C1 MKZHJJQCUIZEDE-UHFFFAOYSA-N 0.000 description 1
- UVHXEHGUEKARKZ-UHFFFAOYSA-N 1-ethenylanthracene Chemical compound C1=CC=C2C=C3C(C=C)=CC=CC3=CC2=C1 UVHXEHGUEKARKZ-UHFFFAOYSA-N 0.000 description 1
- GUPMCMZMDAGSPF-UHFFFAOYSA-N 1-phenylbuta-1,3-dienylbenzene Chemical compound C=1C=CC=CC=1[C](C=C[CH2])C1=CC=CC=C1 GUPMCMZMDAGSPF-UHFFFAOYSA-N 0.000 description 1
- 125000001462 1-pyrrolyl group Chemical group [*]N1C([H])=C([H])C([H])=C1[H] 0.000 description 1
- NLXDFCLCNCWKND-UHFFFAOYSA-N 10-n-(4-butylphenyl)phenanthrene-9,10-diamine Chemical compound C1=CC(CCCC)=CC=C1NC1=C(N)C2=CC=CC=C2C2=CC=CC=C12 NLXDFCLCNCWKND-UHFFFAOYSA-N 0.000 description 1
- YTQQIHUQLOZOJI-UHFFFAOYSA-N 2,3-dihydro-1,2-thiazole Chemical compound C1NSC=C1 YTQQIHUQLOZOJI-UHFFFAOYSA-N 0.000 description 1
- MUNFOTHAFHGRIM-UHFFFAOYSA-N 2,5-dinaphthalen-1-yl-1,3,4-oxadiazole Chemical compound C1=CC=C2C(C3=NN=C(O3)C=3C4=CC=CC=C4C=CC=3)=CC=CC2=C1 MUNFOTHAFHGRIM-UHFFFAOYSA-N 0.000 description 1
- PQYIVUDIIIJJDM-UHFFFAOYSA-N 2,5-dinaphthalen-1-yl-1,3,4-thiadiazole Chemical compound C1=CC=C2C(C3=NN=C(S3)C=3C4=CC=CC=C4C=CC=3)=CC=CC2=C1 PQYIVUDIIIJJDM-UHFFFAOYSA-N 0.000 description 1
- KIPSWFPQUFQEAS-UHFFFAOYSA-N 2-(4-bromophenyl)-6H-1,4-diazepine Chemical compound BrC1=CC=C(C=C1)C=1N=CCC=NC=1 KIPSWFPQUFQEAS-UHFFFAOYSA-N 0.000 description 1
- GRZUOGFRIHABDK-UHFFFAOYSA-N 2-(4-bromophenyl)imidazo[1,2-a]pyridine Chemical compound C1=CC(Br)=CC=C1C1=CN(C=CC=C2)C2=N1 GRZUOGFRIHABDK-UHFFFAOYSA-N 0.000 description 1
- FKJSFKCZZIXQIP-UHFFFAOYSA-N 2-bromo-1-(4-bromophenyl)ethanone Chemical compound BrCC(=O)C1=CC=C(Br)C=C1 FKJSFKCZZIXQIP-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- KXJIIWGGVZEGBD-UHFFFAOYSA-N 2-methyl-n,n-bis(2-methylphenyl)aniline Chemical compound CC1=CC=CC=C1N(C=1C(=CC=CC=1)C)C1=CC=CC=C1C KXJIIWGGVZEGBD-UHFFFAOYSA-N 0.000 description 1
- 125000000389 2-pyrrolyl group Chemical group [H]N1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 1
- ZLDMZIXUGCGKMB-UHFFFAOYSA-N 3,5-dibromobenzaldehyde Chemical compound BrC1=CC(Br)=CC(C=O)=C1 ZLDMZIXUGCGKMB-UHFFFAOYSA-N 0.000 description 1
- MWKLOMOIKCPLOY-UHFFFAOYSA-N 3,5-dinaphthalen-1-yl-1h-1,2,4-triazole Chemical compound C1=CC=C2C(C3=NN=C(N3)C=3C4=CC=CC=C4C=CC=3)=CC=CC2=C1 MWKLOMOIKCPLOY-UHFFFAOYSA-N 0.000 description 1
- JXHKUYQCEJILEI-UHFFFAOYSA-N 3,5-diphenyl-1h-pyrazole Chemical compound C=1C(C=2C=CC=CC=2)=NNC=1C1=CC=CC=C1 JXHKUYQCEJILEI-UHFFFAOYSA-N 0.000 description 1
- JHUUPUMBZGWODW-UHFFFAOYSA-N 3,6-dihydro-1,2-dioxine Chemical compound C1OOCC=C1 JHUUPUMBZGWODW-UHFFFAOYSA-N 0.000 description 1
- GOLORTLGFDVFDW-UHFFFAOYSA-N 3-(1h-benzimidazol-2-yl)-7-(diethylamino)chromen-2-one Chemical compound C1=CC=C2NC(C3=CC4=CC=C(C=C4OC3=O)N(CC)CC)=NC2=C1 GOLORTLGFDVFDW-UHFFFAOYSA-N 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- OAIASDHEWOTKFL-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(4-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=C(C)C=CC=1)C1=CC=CC=C1 OAIASDHEWOTKFL-UHFFFAOYSA-N 0.000 description 1
- 125000001397 3-pyrrolyl group Chemical group [H]N1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- UAPNUNDZDVNTDQ-UHFFFAOYSA-N 4,5-diphenyl-1,2,3-triazole Chemical compound C1=CC=CC=C1C1=NNN=C1C1=CC=CC=C1 UAPNUNDZDVNTDQ-UHFFFAOYSA-N 0.000 description 1
- YOPJQOLALJLPBS-UHFFFAOYSA-N 4,5-diphenyloxadiazole Chemical compound C1=CC=CC=C1C1=C(C=2C=CC=CC=2)ON=N1 YOPJQOLALJLPBS-UHFFFAOYSA-N 0.000 description 1
- QVGVWLHVMVQIQI-UHFFFAOYSA-N 4,5-diphenylthiadiazole Chemical compound C1=CC=CC=C1C1=C(C=2C=CC=CC=2)SN=N1 QVGVWLHVMVQIQI-UHFFFAOYSA-N 0.000 description 1
- CMSGUKVDXXTJDQ-UHFFFAOYSA-N 4-(2-naphthalen-1-ylethylamino)-4-oxobutanoic acid Chemical compound C1=CC=C2C(CCNC(=O)CCC(=O)O)=CC=CC2=C1 CMSGUKVDXXTJDQ-UHFFFAOYSA-N 0.000 description 1
- DDTHMESPCBONDT-UHFFFAOYSA-N 4-(4-oxocyclohexa-2,5-dien-1-ylidene)cyclohexa-2,5-dien-1-one Chemical compound C1=CC(=O)C=CC1=C1C=CC(=O)C=C1 DDTHMESPCBONDT-UHFFFAOYSA-N 0.000 description 1
- MZWDAEVXPZRJTQ-WUXMJOGZSA-N 4-[(e)-(4-fluorophenyl)methylideneamino]-3-methyl-1h-1,2,4-triazole-5-thione Chemical compound CC1=NNC(=S)N1\N=C\C1=CC=C(F)C=C1 MZWDAEVXPZRJTQ-WUXMJOGZSA-N 0.000 description 1
- ZYASLTYCYTYKFC-UHFFFAOYSA-N 9-methylidenefluorene Chemical compound C1=CC=C2C(=C)C3=CC=CC=C3C2=C1 ZYASLTYCYTYKFC-UHFFFAOYSA-N 0.000 description 1
- VESMRDNBVZOIEN-UHFFFAOYSA-N 9h-carbazole-1,2-diamine Chemical compound C1=CC=C2C3=CC=C(N)C(N)=C3NC2=C1 VESMRDNBVZOIEN-UHFFFAOYSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- PXURFDUOJHBBBV-UHFFFAOYSA-N C(C(C=C1)[n](c2ccccc2c2c3)c2c(-c2ccccc2)nc3-c2ccccc2)C=C1[n]1c(cccc2)c2c2c1cccc2 Chemical compound C(C(C=C1)[n](c2ccccc2c2c3)c2c(-c2ccccc2)nc3-c2ccccc2)C=C1[n]1c(cccc2)c2c2c1cccc2 PXURFDUOJHBBBV-UHFFFAOYSA-N 0.000 description 1
- DYXUPWNLSWKZMA-UHFFFAOYSA-N C(CC1)CCC1(c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2)c1cc(-c2ccccn2)nc(-c2ncccc2)c1 Chemical compound C(CC1)CCC1(c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2)c1cc(-c2ccccn2)nc(-c2ncccc2)c1 DYXUPWNLSWKZMA-UHFFFAOYSA-N 0.000 description 1
- XEUAUVQUBVFROH-UHFFFAOYSA-N C1=CC=CC=C1C1=CC=CC=C1.C1=CC(Br)=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 Chemical compound C1=CC=CC=C1C1=CC=CC=C1.C1=CC(Br)=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 XEUAUVQUBVFROH-UHFFFAOYSA-N 0.000 description 1
- 229910004261 CaF 2 Inorganic materials 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- 229920000219 Ethylene vinyl alcohol Polymers 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WZELXJBMMZFDDU-UHFFFAOYSA-N Imidazol-2-one Chemical class O=C1N=CC=N1 WZELXJBMMZFDDU-UHFFFAOYSA-N 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical compound C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- VQTUBCCKSQIDNK-UHFFFAOYSA-N Isobutene Chemical group CC(C)=C VQTUBCCKSQIDNK-UHFFFAOYSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- YXLXNENXOJSQEI-UHFFFAOYSA-L Oxine-copper Chemical compound [Cu+2].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 YXLXNENXOJSQEI-UHFFFAOYSA-L 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 241000282320 Panthera leo Species 0.000 description 1
- 239000004696 Poly ether ether ketone Substances 0.000 description 1
- 229920002319 Poly(methyl acrylate) Polymers 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004697 Polyetherimide Substances 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- NRCMAYZCPIVABH-UHFFFAOYSA-N Quinacridone Chemical compound N1C2=CC=CC=C2C(=O)C2=C1C=C1C(=O)C3=CC=CC=C3NC1=C2 NRCMAYZCPIVABH-UHFFFAOYSA-N 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- 229910003071 TaON Inorganic materials 0.000 description 1
- XBDYBAVJXHJMNQ-UHFFFAOYSA-N Tetrahydroanthracene Natural products C1=CC=C2C=C(CCCC3)C3=CC2=C1 XBDYBAVJXHJMNQ-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 229910010282 TiON Inorganic materials 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000000862 absorption spectrum Methods 0.000 description 1
- LBGCRGLFTKVXDZ-UHFFFAOYSA-M ac1mc2aw Chemical compound [Al+3].[Cl-].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 LBGCRGLFTKVXDZ-UHFFFAOYSA-M 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 229910000272 alkali metal oxide Inorganic materials 0.000 description 1
- 229910001615 alkaline earth metal halide Inorganic materials 0.000 description 1
- 229910000287 alkaline earth metal oxide Inorganic materials 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 125000006295 amino methylene group Chemical group [H]N(*)C([H])([H])* 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- SMWDFEZZVXVKRB-UHFFFAOYSA-N anhydrous quinoline Natural products N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 1
- NDMVXIYCFFFPLE-UHFFFAOYSA-N anthracene-9,10-diamine Chemical compound C1=CC=C2C(N)=C(C=CC=C3)C3=C(N)C2=C1 NDMVXIYCFFFPLE-UHFFFAOYSA-N 0.000 description 1
- HAQFCILFQVZOJC-UHFFFAOYSA-N anthracene-9,10-dione;methane Chemical compound C.C.C1=CC=C2C(=O)C3=CC=CC=C3C(=O)C2=C1 HAQFCILFQVZOJC-UHFFFAOYSA-N 0.000 description 1
- 125000005427 anthranyl group Chemical group 0.000 description 1
- RJGDLRCDCYRQOQ-UHFFFAOYSA-N anthrone Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3CC2=C1 RJGDLRCDCYRQOQ-UHFFFAOYSA-N 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- LZCZIHQBSCVGRD-UHFFFAOYSA-N benzenecarboximidamide;hydron;chloride Chemical compound [Cl-].NC(=[NH2+])C1=CC=CC=C1 LZCZIHQBSCVGRD-UHFFFAOYSA-N 0.000 description 1
- HFACYLZERDEVSX-UHFFFAOYSA-N benzidine Chemical compound C1=CC(N)=CC=C1C1=CC=C(N)C=C1 HFACYLZERDEVSX-UHFFFAOYSA-N 0.000 description 1
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 1
- GQVWHWAWLPCBHB-UHFFFAOYSA-L beryllium;benzo[h]quinolin-10-olate Chemical compound [Be+2].C1=CC=NC2=C3C([O-])=CC=CC3=CC=C21.C1=CC=NC2=C3C([O-])=CC=CC3=CC=C21 GQVWHWAWLPCBHB-UHFFFAOYSA-L 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- SAFSBZNYWAEVOQ-UHFFFAOYSA-N c(cc1)ccc1-c(cc1c2ccccc22)nc(-c3ccccc3)c1[n]2-c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2 Chemical compound c(cc1)ccc1-c(cc1c2ccccc22)nc(-c3ccccc3)c1[n]2-c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2 SAFSBZNYWAEVOQ-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- XOYLJNJLGBYDTH-UHFFFAOYSA-M chlorogallium Chemical compound [Ga]Cl XOYLJNJLGBYDTH-UHFFFAOYSA-M 0.000 description 1
- 125000002676 chrysenyl group Chemical group C1(=CC=CC=2C3=CC=C4C=CC=CC4=C3C=CC12)* 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 150000004775 coumarins Chemical class 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004977 cycloheptylene group Chemical group 0.000 description 1
- 125000004979 cyclopentylene group Chemical group 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 150000004985 diamines Chemical class 0.000 description 1
- 229940117389 dichlorobenzene Drugs 0.000 description 1
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- AFABGHUZZDYHJO-UHFFFAOYSA-N dimethyl butane Natural products CCCC(C)C AFABGHUZZDYHJO-UHFFFAOYSA-N 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 239000002019 doping agent Substances 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 229920000840 ethylene tetrafluoroethylene copolymer Polymers 0.000 description 1
- 239000005038 ethylene vinyl acetate Substances 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 150000007857 hydrazones Chemical class 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- NBGMRMDAEWWFIR-UHFFFAOYSA-N imidazole-2-thione Chemical class S=C1N=CC=N1 NBGMRMDAEWWFIR-UHFFFAOYSA-N 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 150000002466 imines Chemical class 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910003437 indium oxide Inorganic materials 0.000 description 1
- PJXISJQVUVHSOJ-UHFFFAOYSA-N indium(iii) oxide Chemical compound [O-2].[O-2].[O-2].[In+3].[In+3] PJXISJQVUVHSOJ-UHFFFAOYSA-N 0.000 description 1
- 238000007733 ion plating Methods 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 239000011133 lead Substances 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- XNUVVHVFAAQPQY-UHFFFAOYSA-L manganese(2+) quinolin-8-olate Chemical compound N1=CC=CC2=CC=CC(=C12)[O-].[Mn+2].N1=CC=CC2=CC=CC(=C12)[O-] XNUVVHVFAAQPQY-UHFFFAOYSA-L 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- YERRTOUSFSZICJ-UHFFFAOYSA-N methyl 2-amino-2-(4-bromophenyl)acetate Chemical compound COC(=O)C(N)C1=CC=C(Br)C=C1 YERRTOUSFSZICJ-UHFFFAOYSA-N 0.000 description 1
- YQVDNJJYNQAOER-UHFFFAOYSA-N n-[4-(4-aminophenyl)phenyl]-4-methylaniline Chemical compound C1=CC(C)=CC=C1NC1=CC=C(C=2C=CC(N)=CC=2)C=C1 YQVDNJJYNQAOER-UHFFFAOYSA-N 0.000 description 1
- KKFHAJHLJHVUDM-UHFFFAOYSA-N n-vinylcarbazole Chemical compound C1=CC=C2N(C=C)C3=CC=CC=C3C2=C1 KKFHAJHLJHVUDM-UHFFFAOYSA-N 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 150000002916 oxazoles Chemical class 0.000 description 1
- YRZZLAGRKZIJJI-UHFFFAOYSA-N oxyvanadium phthalocyanine Chemical compound [V+2]=O.C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 YRZZLAGRKZIJJI-UHFFFAOYSA-N 0.000 description 1
- NRNFFDZCBYOZJY-UHFFFAOYSA-N p-quinodimethane Chemical compound C=C1C=CC(=C)C=C1 NRNFFDZCBYOZJY-UHFFFAOYSA-N 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- UQPUONNXJVWHRM-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 UQPUONNXJVWHRM-UHFFFAOYSA-N 0.000 description 1
- DGBWPZSGHAXYGK-UHFFFAOYSA-N perinone Chemical compound C12=NC3=CC=CC=C3N2C(=O)C2=CC=C3C4=C2C1=CC=C4C(=O)N1C2=CC=CC=C2N=C13 DGBWPZSGHAXYGK-UHFFFAOYSA-N 0.000 description 1
- FVDOBFPYBSDRKH-UHFFFAOYSA-N perylene-3,4,9,10-tetracarboxylic acid Chemical compound C=12C3=CC=C(C(O)=O)C2=C(C(O)=O)C=CC=1C1=CC=C(C(O)=O)C2=C1C3=CC=C2C(=O)O FVDOBFPYBSDRKH-UHFFFAOYSA-N 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- RDOWQLZANAYVLL-UHFFFAOYSA-N phenanthridine Chemical group C1=CC=C2C3=CC=CC=C3C=NC2=C1 RDOWQLZANAYVLL-UHFFFAOYSA-N 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- SIOXPEMLGUPBBT-UHFFFAOYSA-M picolinate Chemical compound [O-]C(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-M 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 1
- 229920002493 poly(chlorotrifluoroethylene) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920001230 polyarylate Polymers 0.000 description 1
- 239000005023 polychlorotrifluoroethylene (PCTFE) polymer Substances 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920002530 polyetherether ketone Polymers 0.000 description 1
- 229920001601 polyetherimide Polymers 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 229920002620 polyvinyl fluoride Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 150000004033 porphyrin derivatives Chemical class 0.000 description 1
- 239000011241 protective layer Substances 0.000 description 1
- JEXVQSWXXUJEMA-UHFFFAOYSA-N pyrazol-3-one Chemical compound O=C1C=CN=N1 JEXVQSWXXUJEMA-UHFFFAOYSA-N 0.000 description 1
- DNXIASIHZYFFRO-UHFFFAOYSA-N pyrazoline Chemical compound C1CN=NC1 DNXIASIHZYFFRO-UHFFFAOYSA-N 0.000 description 1
- 125000005412 pyrazyl group Chemical group 0.000 description 1
- 125000005548 pyrenylene group Chemical group 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 229910001404 rare earth metal oxide Inorganic materials 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- YYMBJDOZVAITBP-UHFFFAOYSA-N rubrene Chemical compound C1=CC=CC=C1C(C1=C(C=2C=CC=CC=2)C2=CC=CC=C2C(C=2C=CC=CC=2)=C11)=C(C=CC=C2)C2=C1C1=CC=CC=C1 YYMBJDOZVAITBP-UHFFFAOYSA-N 0.000 description 1
- 238000001275 scanning Auger electron spectroscopy Methods 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229920002050 silicone resin Polymers 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- SUBJHSREKVAVAR-UHFFFAOYSA-N sodium;methanol;methanolate Chemical compound [Na+].OC.[O-]C SUBJHSREKVAVAR-UHFFFAOYSA-N 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- 125000001935 tetracenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C12)* 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- VLLMWSRANPNYQX-UHFFFAOYSA-N thiadiazole Chemical compound C1=CSN=N1.C1=CSN=N1 VLLMWSRANPNYQX-UHFFFAOYSA-N 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- NZFNXWQNBYZDAQ-UHFFFAOYSA-N thioridazine hydrochloride Chemical compound Cl.C12=CC(SC)=CC=C2SC2=CC=CC=C2N1CCC1CCCCN1C NZFNXWQNBYZDAQ-UHFFFAOYSA-N 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 1
- 229910001887 tin oxide Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- KWQNQSDKCINQQP-UHFFFAOYSA-K tri(quinolin-8-yloxy)gallane Chemical compound C1=CN=C2C(O[Ga](OC=3C4=NC=CC=C4C=CC=3)OC=3C4=NC=CC=C4C=CC=3)=CC=CC2=C1 KWQNQSDKCINQQP-UHFFFAOYSA-K 0.000 description 1
- NHDIQVFFNDKAQU-UHFFFAOYSA-N tripropan-2-yl borate Chemical compound CC(C)OB(OC(C)C)OC(C)C NHDIQVFFNDKAQU-UHFFFAOYSA-N 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- VWQVUPCCIRVNHF-UHFFFAOYSA-N yttrium atom Chemical compound [Y] VWQVUPCCIRVNHF-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- HTPBWAPZAJWXKY-UHFFFAOYSA-L zinc;quinolin-8-olate Chemical compound [Zn+2].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 HTPBWAPZAJWXKY-UHFFFAOYSA-L 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0046—Ruthenium compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
- H10K2102/10—Transparent electrodes, e.g. using graphene
- H10K2102/101—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO]
- H10K2102/103—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO] comprising indium oxides, e.g. ITO
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/321—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3]
- H10K85/324—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3] comprising aluminium, e.g. Alq3
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
Claims (21)
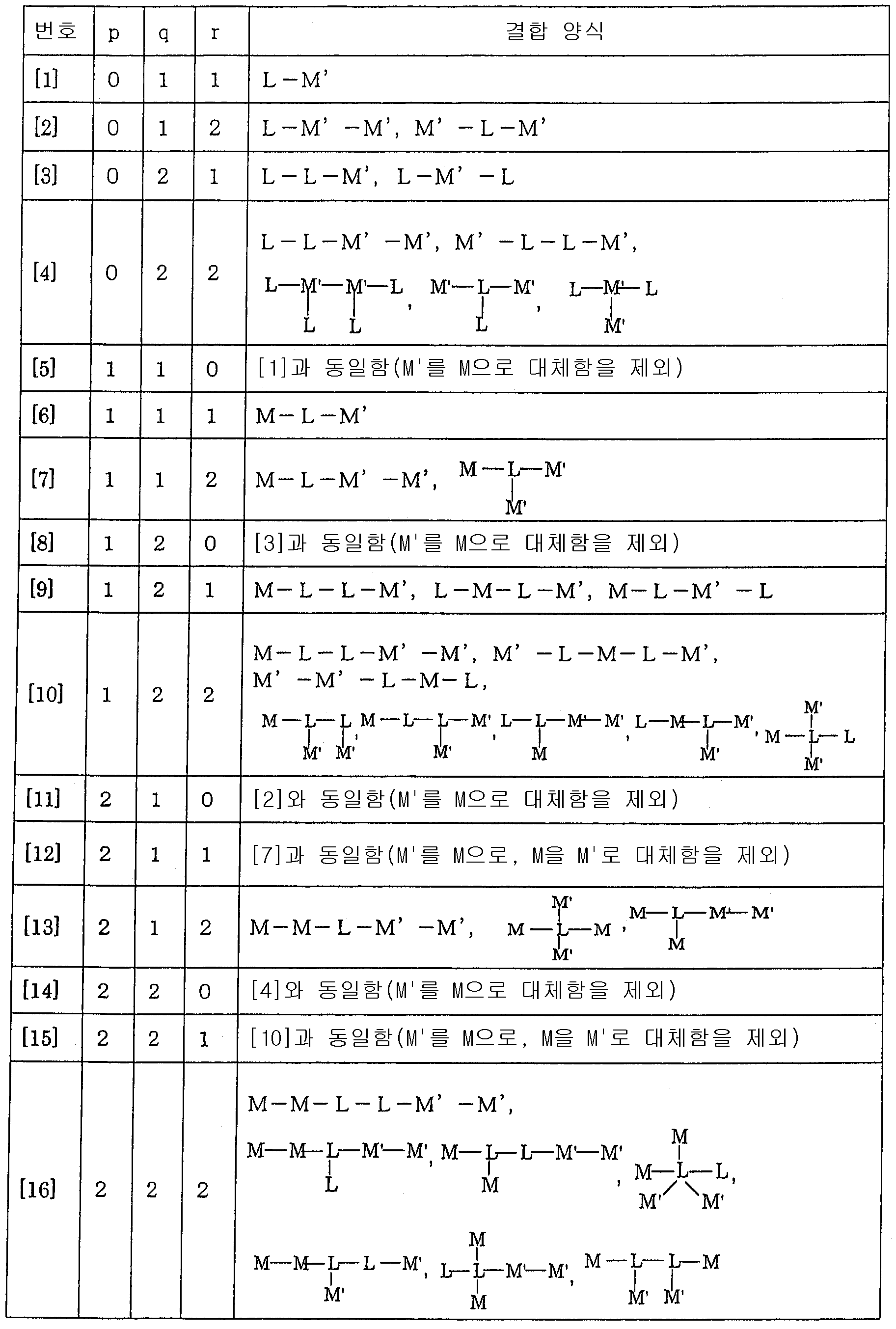
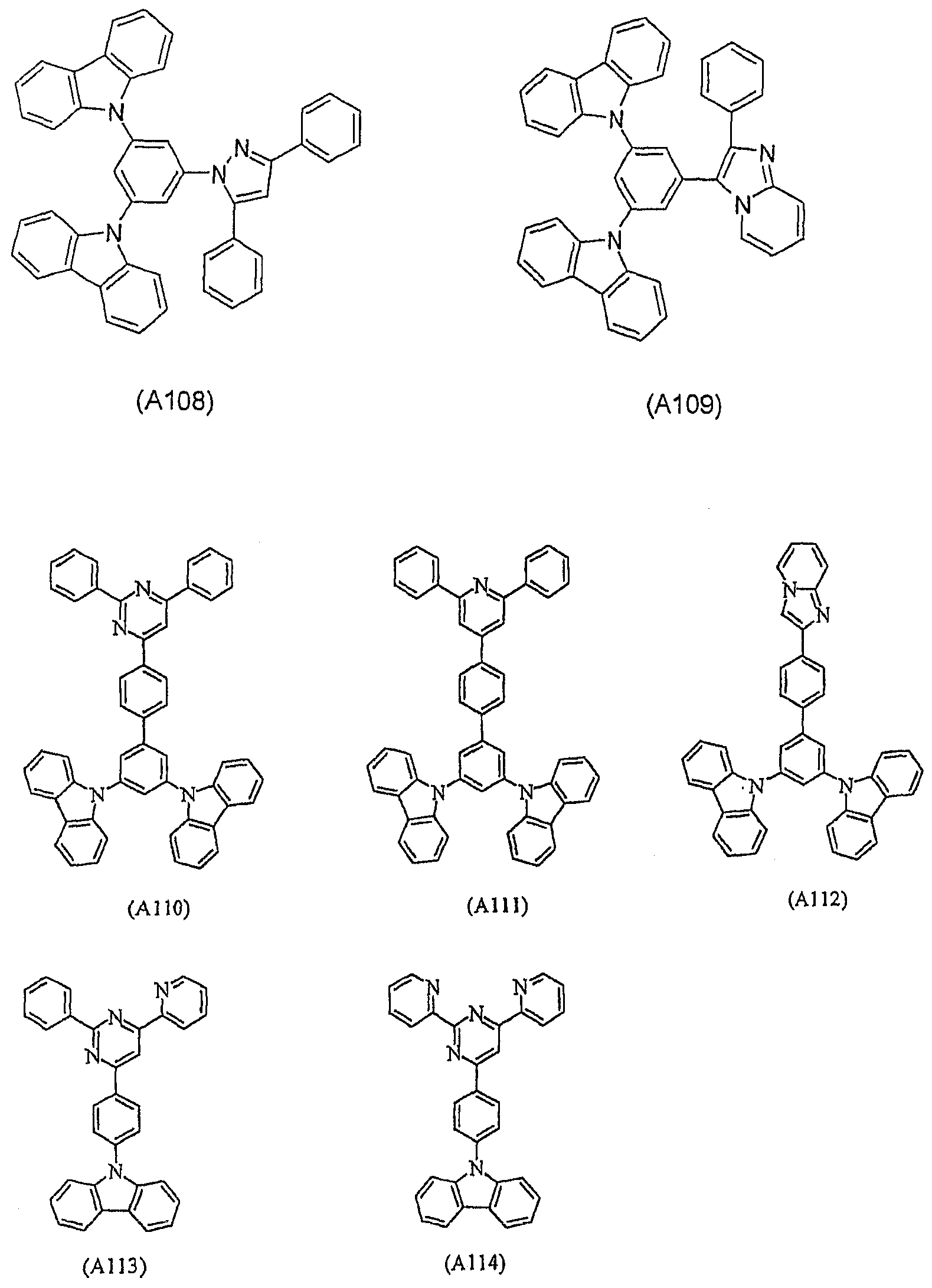
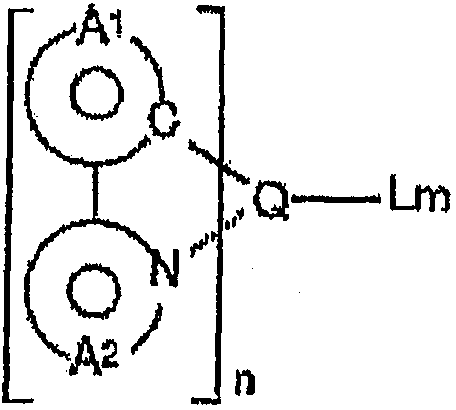
- 하기 화학식 1 또는 2로 표시되는 화합물로 이루어진 유기 전기 발광 소자용 재료:화학식 1화학식 2상기 식들에서,Cz는 치환되거나 비치환된 아릴카바졸릴기이며, 아릴 배위 또는 카바졸릴 배위를 통해서 A에 결합되고,A는 하기 화학식 A로 표시되는 기이고,n 및 m은 각각 1 내지 3의 정수이다.화학식 A[상기 화학식 A에서,M 및 M'는 각각 독립적으로 치환되거나 비치환된 질소 함유 헤테로 방향족환으로, 동일하거나 상이할 수 있고, 상기 질소 함유 헤테로 방향족환은 피리미딘, 피라진, 트라이아진, 아지리딘, 아자인돌리딘, 인돌리딘, 이미다졸, 인돌, 아이소인돌, 인다졸, 푸린, 푸테리딘, β-카볼린, 나프틸리딘, 퀴녹살린, 터피리딘, 바이피리딘, 아크리딘, 페난트롤린, 페나진, 이미다조[1,2-a]피리딘, 파이로피리딘, 다이사이아노아제핀 및 피라졸로부터 선택되고,L은 단일 결합, 치환되거나 비치환된 탄소수 6 내지 30의 아릴기 또는 아릴렌기, 또는 치환되거나 비치환된 탄소수 5 내지 30의 사이클로알킬렌기이고,Cz는 M, L, M' 중 어느 하나에 결합될 수 있고,p는 0 내지 2, q는 1 내지 2, r은 0 내지 2의 정수이되, 단 p+r은 1 이상이다.]
- 제 1 항에 있어서,상기 화학식 1에서 n=1이고, 상기 화학식 A에서 p=1, r=0이고,화학식 1에서 Cz가 치환되거나 비치환된 아릴카바졸릴기이고,화학식 A에서 M이 치환되거나 비치환된 피리미딘, 피라진, 다이사이아노아제핀, 이미다졸, 피라졸, 인돌리딘, 인돌, 아이소인돌, β-카볼린, 나프틸리딘, 퀴녹살린, 바이피리딘 및 이미다조[1,2-a]피리딘으로부터 선택되는 질소 함유 헤테로 방향족환이고,L이 치환되거나 비치환된 탄소수 6 내지 30의 아릴기 또는 아릴렌기, 또는 치환되거나 비치환된 탄소수 2 내지 30의 헤테로 방향족환인 유기 전기 발광 소자용 재료.
- 제 1 항에 있어서,상기 화학식 1에서 n=2이고, 상기 화학식 A에서 p=1, r=0이고,화학식 1에서 Cz가 치환되거나 비치환된 아릴카바졸릴기이고,화학식 A에서 M이 치환되거나 비치환된 피리미딘, 피라진, 다이사이아노아제핀, 이미다졸, 피라졸, 인돌리딘, 인돌, 아이소인돌, β-카볼린, 나프틸리딘, 퀴녹살린, 바이피리딘 및 이미다조[1,2-a]피리딘으로부터 선택되는 질소 함유 헤테로 방향족환이고,L이 치환되거나 비치환된 탄소수 6 내지 30의 아릴기 또는 아릴렌기, 또는 치환되거나 비치환된 탄소수 2 내지 30의 헤테로 방향족환인 유기 전기 발광 소자용 재료.
- 제 1 항에 있어서,상기 화학식 1에서 n=1이고, 상기 화학식 A에서 p=2, r=0이고,화학식 1에서 Cz가 치환되거나 비치환된 아릴카바졸릴기이고,L이 치환되거나 비치환된 탄소수 6 내지 30의 아릴기 또는 아릴렌기, 또는 치환되거나 비치환된 탄소수 2 내지 30의 헤테로 방향족환인 유기 전기 발광 소자용 재료.
- 제 1 항에 있어서,상기 화학식 2에서 m=2이고, 상기 화학식 A에서 p=q=1이고,화학식 2에서 Cz가 치환되거나 비치환된 아릴카바졸릴기이고,L이 치환되거나 비치환된 탄소수 6 내지 30의 아릴기 또는 아릴렌기, 치환되거나 비치환된 탄소수 5 내지 30의 사이클로알킬렌기, 또는 치환되거나 비치환된 탄소수 2 내지 30의 헤테로 방향족환인 유기 전기 발광 소자용 재료.
- 삭제
- 제 1 항에 있어서,Cz가 치환되거나 비치환된 페닐카바졸릴기인 유기 전기 발광 소자용 재료.
- 제 1 항에 있어서,아릴카바졸릴기의 아릴 부위가 카바졸릴기로 치환되어 있는 유기 전기 발광 소자용 재료.
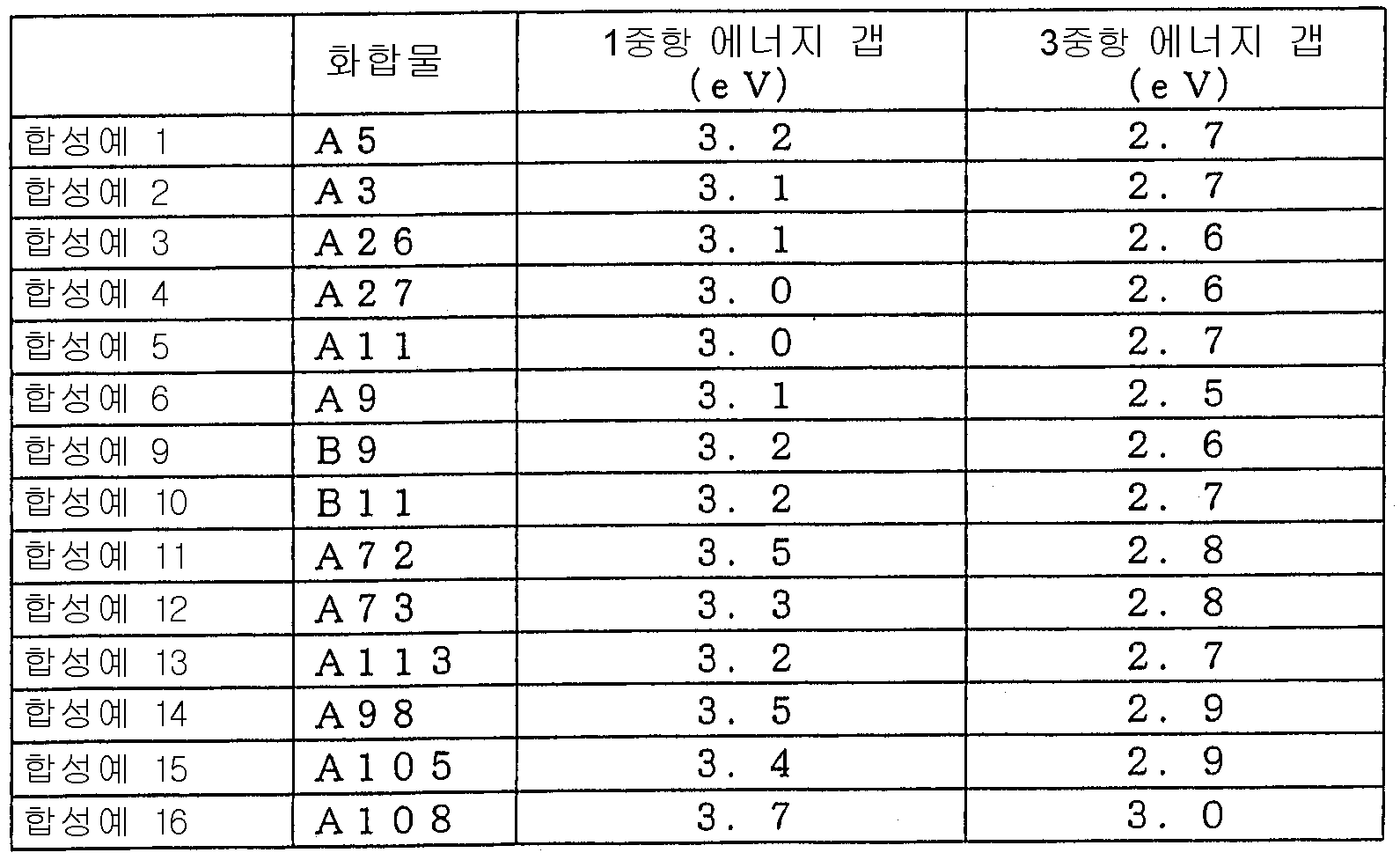
- 제 1 항에 있어서,상기 화학식 1 또는 2로 표시되는 화합물의 3중항 에너지 갭이 2.5 내지 3.3eV인 유기 전기 발광 소자용 재료.
- 제 1 항에 있어서,상기 화학식 1 또는 2로 표시되는 화합물의 1중항 에너지 갭이 2.8 내지 3.8eV인 유기 전기 발광 소자용 재료.
- 음극과 양극 사이에 한 층 또는 복수층으로 이루어진 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서, 당해 유기 박막층의 적어도 한 층이 제 1 항에 따른 유기 전기 발광 소자용 재료를 함유하는 유기 전기 발광 소자.
- 음극과 양극 사이에 한 층 또는 복수층으로 이루어진 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서, 발광층이 제 1 항에 따른 유기 전기 발광 소자용 재료를 함유하는 유기 전기 발광 소자.
- 음극과 양극 사이에 한 층 또는 복수층으로 이루어진 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서, 전자 수송층이 제 1 항에 따른 유기 전기 발광 소자용 재료를 함유하는 유기 전기 발광 소자.
- 음극과 양극 사이에 한 층 또는 복수층으로 이루어진 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서, 정공 수송층이 제 1 항에 따른 유기 전기 발광 소자용 재료를 함유하는 유기 전기 발광 소자.
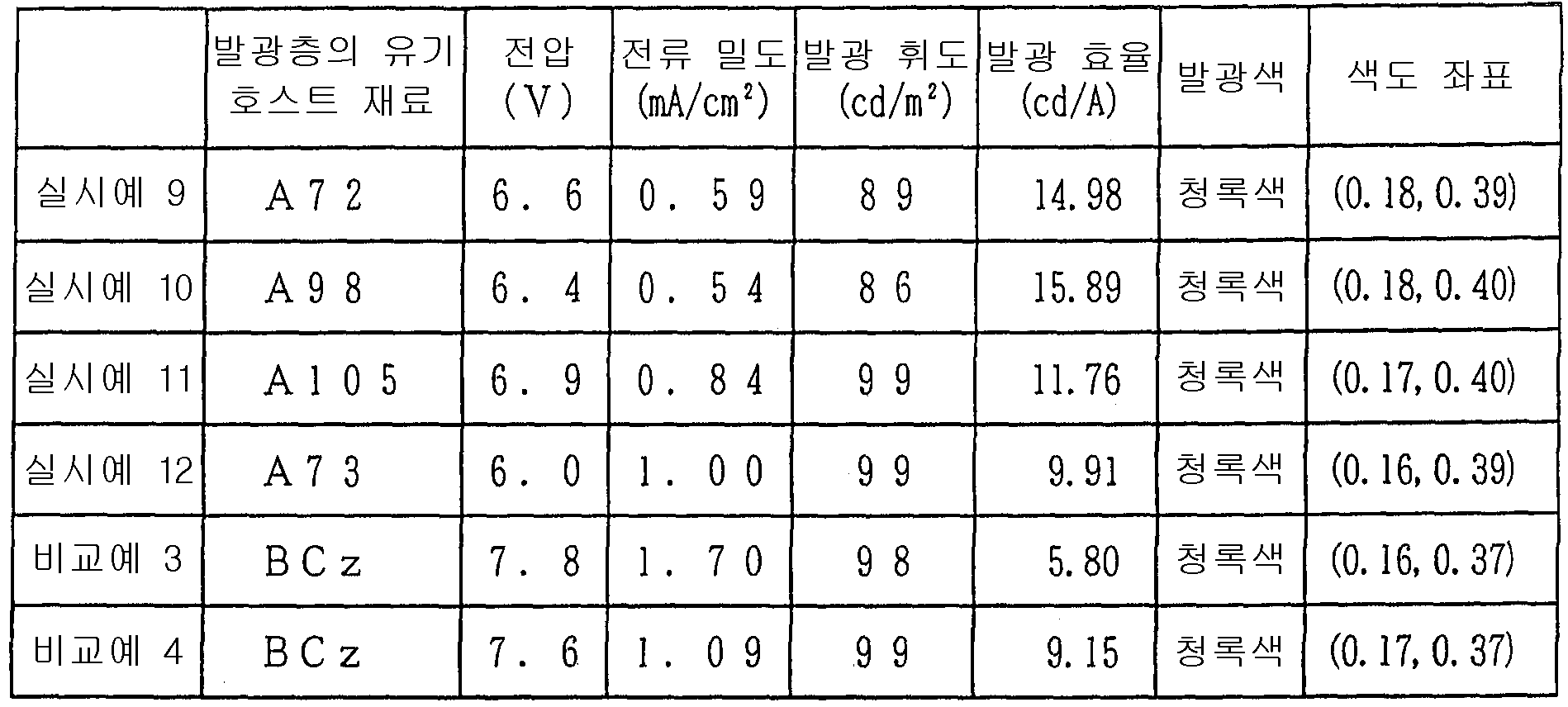
- 제 11 항에 있어서,상기 유기 전기 발광 소자용 재료가 유기 호스트 재료인 유기 전기 발광 소자.
- 제 11 항에 있어서,적어도 한쪽의 전극과 상기 유기 박막층 사이에 무기 화합물층을 갖는 유기 전기 발광 소자.
- 제 11 항에 있어서,3중항 여기 또는 그 이상의 다중항 여기에 의해 발광하는 유기 전기 발광 소자.
- 제 11 항에 있어서,청색계로 발광하는 유기 전기 발광 소자.
- 제 1 항에 있어서,상기 화학식 A가 L-M, L-L-M 또는 L-M-L인 유기 전기 발광 소자용 재료.
- 제 19 항에 있어서,상기 L이 단일 결합, 페닐기, 바이페닐기, 나프틸기, 페닐렌기, 바이페닐렌기 또는 나프틸렌기인 유기 전기 발광 소자용 재료.
- 제 19 항에 있어서,상기 M이 피리미딘인 유기 전기 발광 소자용 재료.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002081234 | 2002-03-22 | ||
| JPJP-P-2002-00081234 | 2002-03-22 | ||
| JP2002299810 | 2002-10-15 | ||
| JPJP-P-2002-00299810 | 2002-10-15 | ||
| PCT/JP2003/003329 WO2003080760A1 (en) | 2002-03-22 | 2003-03-19 | Material for organic electroluminescent devices and organic electroluminescent devices made by using the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20040094842A KR20040094842A (ko) | 2004-11-10 |
| KR100948700B1 true KR100948700B1 (ko) | 2010-03-22 |
Family
ID=28456229
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020047014947A Ceased KR100948700B1 (ko) | 2002-03-22 | 2003-03-19 | 유기 전기 발광 소자용 재료 및 이를 이용한 유기 전기발광 소자 |
Country Status (6)
| Country | Link |
|---|---|
| US (4) | US20040086745A1 (ko) |
| EP (2) | EP1489155A4 (ko) |
| JP (3) | JP4316387B2 (ko) |
| KR (1) | KR100948700B1 (ko) |
| TW (2) | TWI306890B (ko) |
| WO (1) | WO2003080760A1 (ko) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20130011446A (ko) | 2011-07-21 | 2013-01-30 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| KR20140034183A (ko) * | 2011-05-13 | 2014-03-19 | 이데미쓰 고산 가부시키가이샤 | 유기 el 다색 발광 장치 |
| KR20150064878A (ko) | 2013-12-04 | 2015-06-12 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20150124886A (ko) | 2014-04-29 | 2015-11-06 | 롬엔드하스전자재료코리아유한회사 | 전자전달재료 및 이를 포함하는 유기 전계 발광 소자 |
| US11926603B2 (en) | 2018-01-24 | 2024-03-12 | Samsung Sdi Co., Ltd. | Compound, composition, organic optoelectronic diode, and display device |
| US12010913B2 (en) | 2019-10-02 | 2024-06-11 | Samsung Sdi Co., Ltd. | Compound for organic optoelectronic device, organic optoelectronic device and display device |
Families Citing this family (222)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100957288B1 (ko) * | 2002-03-15 | 2010-05-12 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 이를 이용한 유기 전기발광소자 |
| EP1489155A4 (en) | 2002-03-22 | 2006-02-01 | Idemitsu Kosan Co | MATERIAL FOR ORGANIC ELECTROLUMINESCENT DEVICES AND THE EQUIVALENT DEVICES |
| JP4036041B2 (ja) * | 2002-06-24 | 2008-01-23 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP2004123595A (ja) * | 2002-10-01 | 2004-04-22 | Daicel Chem Ind Ltd | アゼピン化合物 |
| JPWO2004034751A1 (ja) * | 2002-10-09 | 2006-02-09 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JP4427947B2 (ja) * | 2002-11-18 | 2010-03-10 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子及び表示装置 |
| EP2248870B1 (en) * | 2002-11-26 | 2018-12-26 | Konica Minolta Holdings, Inc. | Organic electroluminscent element and display and illuminator |
| JP4707082B2 (ja) * | 2002-11-26 | 2011-06-22 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子および表示装置 |
| JPWO2004074399A1 (ja) * | 2003-02-20 | 2006-06-01 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP2236579B1 (en) * | 2003-04-23 | 2014-04-09 | Konica Minolta Holdings, Inc. | Organic electroluminescent element and display |
| JP4762514B2 (ja) * | 2003-09-05 | 2011-08-31 | 株式会社リコー | 3,6−ジフェニルカルバゾール誘導体 |
| JP4886975B2 (ja) * | 2003-10-31 | 2012-02-29 | 株式会社リコー | 電界発光素子 |
| US7795801B2 (en) * | 2003-09-30 | 2010-09-14 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| KR100553752B1 (ko) * | 2003-10-13 | 2006-02-20 | 삼성에스디아이 주식회사 | 이미다졸 고리 함유 화합물 및 이를 이용한 유기 전계발광 소자 |
| JP4630637B2 (ja) * | 2003-11-21 | 2011-02-09 | キヤノン株式会社 | 有機発光素子及び有機化合物 |
| EP1708547A1 (en) * | 2004-01-21 | 2006-10-04 | Idemitsu Kosan Co., Ltd. | Host material for organic electroluminescent element and organic electroluminescent element |
| TW200531590A (en) * | 2004-02-06 | 2005-09-16 | Idemitsu Kosan Co | Organic electroluminescent device |
| TWI428053B (zh) | 2004-02-09 | 2014-02-21 | Idemitsu Kosan Co | Organic electroluminescent element |
| US7011871B2 (en) | 2004-02-20 | 2006-03-14 | E. I. Du Pont De Nemours And Company | Charge transport compounds and electronic devices made with such compounds |
| JP4952247B2 (ja) * | 2004-02-26 | 2012-06-13 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| EP1722603B2 (en) * | 2004-03-02 | 2021-02-17 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| JP4351935B2 (ja) * | 2004-03-10 | 2009-10-28 | 富士フイルム株式会社 | 有機電界発光素子 |
| EP1750487A4 (en) * | 2004-05-14 | 2008-12-17 | Idemitsu Kosan Co | ORGANIC ELECTROLUMINESCENCE ELEMENT |
| EP2178348B1 (en) * | 2004-07-23 | 2012-11-21 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, display and illuminator |
| JP4626613B2 (ja) * | 2004-08-04 | 2011-02-09 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| JP5055689B2 (ja) * | 2004-08-26 | 2012-10-24 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、照明装置および表示装置 |
| KR100670778B1 (ko) * | 2004-10-11 | 2007-01-17 | 한국전자통신연구원 | 트리아진 그룹을 갖는 유기 반도체 소자용 화합물과, 이를포함하는 유기 반도체 박막 및 유기 반도체 소자와,이들의 제조 방법 |
| JP2006131519A (ja) * | 2004-11-04 | 2006-05-25 | Idemitsu Kosan Co Ltd | 縮合環含有化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR100787423B1 (ko) * | 2004-11-05 | 2007-12-26 | 삼성에스디아이 주식회사 | 유기 전계 발광 소자 |
| JP4810669B2 (ja) * | 2004-11-25 | 2011-11-09 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2006151866A (ja) * | 2004-11-29 | 2006-06-15 | Canon Inc | フェナントロリン化合物及び発光素子 |
| KR101388472B1 (ko) | 2004-12-10 | 2014-04-23 | 미쓰비시 가가꾸 가부시키가이샤 | 유기 화합물, 전하 수송 재료 및 유기 전계 발광 소자 |
| KR20120082938A (ko) | 2004-12-24 | 2012-07-24 | 미쓰비시 가가꾸 가부시키가이샤 | 유기 화합물, 전하 수송 물질 및 유기 전계발광 소자 |
| JP4797470B2 (ja) * | 2004-12-24 | 2011-10-19 | 三菱化学株式会社 | キノリン誘導体及びこれを含有する有機el素子 |
| JP5098177B2 (ja) * | 2005-01-25 | 2012-12-12 | パイオニア株式会社 | 有機化合物、電荷輸送材料及び有機電界発光素子 |
| US8168307B2 (en) | 2005-01-25 | 2012-05-01 | Pioneer Corporation | Organic compound, charge transport material and organic electroluminescent device |
| EP1844119A2 (de) * | 2005-01-28 | 2007-10-17 | Basf Aktiengesellschaft | Copolymer umfassend derivate monoethylenisch ungesättigter dicarbonsäuren |
| JP4311360B2 (ja) * | 2005-02-25 | 2009-08-12 | セイコーエプソン株式会社 | 発光素子、発光装置および電子機器 |
| CN101184732B (zh) * | 2005-03-28 | 2012-05-16 | 株式会社半导体能源研究所 | 蒽衍生物、发光元件用材料、发光元件、发光装置和电子器件 |
| WO2006119800A1 (en) * | 2005-05-09 | 2006-11-16 | Technische Universität Braunschweig | Light emitting compound for electroluminescent applications |
| JP5261887B2 (ja) | 2005-05-17 | 2013-08-14 | 三菱化学株式会社 | モノアミン化合物、電荷輸送材料および有機電界発光素子 |
| EP1887640A4 (en) | 2005-05-24 | 2012-04-04 | Pioneer Corp | ORGANIC ELECTROLUMINESCENCE ELEMENT |
| WO2006132012A1 (ja) * | 2005-06-09 | 2006-12-14 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| KR20080025393A (ko) * | 2005-07-06 | 2008-03-20 | 이데미쓰 고산 가부시키가이샤 | 유기 전계 발광 소자 |
| JP5167607B2 (ja) * | 2005-08-23 | 2013-03-21 | 三菱化学株式会社 | 電荷輸送材料、電荷輸送材料組成物及び有機電界発光素子 |
| WO2007026626A1 (en) * | 2005-08-31 | 2007-03-08 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative, material for light emitting element, light emitting element, light emitting device, and electronic device |
| JP2007169268A (ja) * | 2005-11-22 | 2007-07-05 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、電荷輸送材料組成物および有機電界発光素子 |
| US7651791B2 (en) | 2005-12-15 | 2010-01-26 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and electroluminescence device employing the same |
| US9012035B2 (en) * | 2005-12-16 | 2015-04-21 | Pioneer Corporation | Organic electroluminescence device |
| JP5017858B2 (ja) * | 2005-12-27 | 2012-09-05 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| US7731377B2 (en) * | 2006-03-21 | 2010-06-08 | Semiconductor Energy Laboratory Co., Ltd. | Backlight device and display device |
| JPWO2007111263A1 (ja) * | 2006-03-27 | 2009-08-13 | 出光興産株式会社 | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP5555972B2 (ja) * | 2006-05-17 | 2014-07-23 | 三菱化学株式会社 | 有機電界発光素子 |
| JP2014197696A (ja) * | 2006-05-17 | 2014-10-16 | 三菱化学株式会社 | 有機電界発光素子用組成物 |
| JP5233081B2 (ja) * | 2006-05-17 | 2013-07-10 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2008024698A (ja) * | 2006-06-21 | 2008-02-07 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、電荷輸送材料組成物及び有機電界発光素子 |
| WO2008026614A1 (en) * | 2006-08-30 | 2008-03-06 | Semiconductor Energy Laboratory Co., Ltd. | Method for synthesizing anthracene derivative and anthracene derivative, light emitting element, light emitting device, electronic device |
| JP4939207B2 (ja) * | 2006-12-27 | 2012-05-23 | キヤノン株式会社 | カルバゾール化合物及びそれを用いた有機発光素子 |
| JP5446096B2 (ja) * | 2007-02-06 | 2014-03-19 | 住友化学株式会社 | 組成物及び該組成物を用いてなる発光素子 |
| US7723722B2 (en) | 2007-03-23 | 2010-05-25 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, anthracene derivative, and light-emitting element, light-emitting device, and electronic device using anthracene derivative |
| JP5430073B2 (ja) * | 2007-03-30 | 2014-02-26 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| CN101657517B (zh) * | 2007-04-13 | 2013-03-27 | 第一毛织株式会社 | 包括电子传输单元和空穴传输单元的有机光电装置材料及有机光电装置 |
| CN104370834B (zh) | 2007-05-17 | 2017-04-19 | 株式会社半导体能源研究所 | 三唑衍生物 |
| US20080286445A1 (en) * | 2007-05-17 | 2008-11-20 | Semiconductor Energy Laboratory Co., Ltd. | Composition, and method of fabricating light-emitting element |
| JP5325402B2 (ja) * | 2007-08-03 | 2013-10-23 | ケミプロ化成株式会社 | 新規なビカルバゾール誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
| KR20090024998A (ko) | 2007-09-05 | 2009-03-10 | 제일모직주식회사 | 분자 내에 정공수송기와 전자수송기를 동시에 가지는바이폴라 유기화합물을 포함하는 유기광전소자용 재료 및이를 이용한 유기광전소자 |
| KR100957620B1 (ko) * | 2007-11-01 | 2010-05-13 | 제일모직주식회사 | 유기광전소자용 재료, 및 이를 이용한 유기광전소자 |
| KR20090048299A (ko) * | 2007-11-08 | 2009-05-13 | 주식회사 엘지화학 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자 |
| EP2239255A4 (en) * | 2007-12-27 | 2011-09-14 | Nippon Steel Chemical Co | COMPOUND FOR ORGANIC ELECTROLUMINESCENCE DEVICE AND ORGANIC ELECTROLUMINESCENCE DEVICE USING THE SAME |
| CN102317328B (zh) * | 2008-02-22 | 2014-05-14 | 昭和电工株式会社 | 高分子化合物和使用该高分子化合物的有机电致发光元件 |
| JP4830126B2 (ja) * | 2008-03-22 | 2011-12-07 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP4830127B2 (ja) * | 2008-03-22 | 2011-12-07 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子及び表示装置 |
| KR101058103B1 (ko) | 2008-04-15 | 2011-08-24 | 삼성모바일디스플레이주식회사 | 바이피리딘계 화합물 및 이를 포함한 유기막을 구비한 유기발광 소자 |
| JP5604804B2 (ja) * | 2008-04-25 | 2014-10-15 | 住友化学株式会社 | 含窒素複素環式化合物を含む組成物 |
| EP2479234B1 (en) | 2008-05-13 | 2017-06-21 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, display device and lighting device |
| JP2010013421A (ja) * | 2008-07-07 | 2010-01-21 | Chemiprokasei Kaisha Ltd | 新規なビス(ジカルバゾリルフェニル)誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
| WO2010005066A1 (en) * | 2008-07-08 | 2010-01-14 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative, light-emitting element material, light-emitting element, and light-emitting device |
| JP5371312B2 (ja) * | 2008-07-28 | 2013-12-18 | ケミプロ化成株式会社 | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 |
| JP5338184B2 (ja) * | 2008-08-06 | 2013-11-13 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、表示装置、照明装置 |
| EP2332907B1 (en) * | 2008-08-13 | 2015-07-01 | Ube Industries, Ltd. | Organic sulfur compound, process for production of the same, and organic electroluminescence element utilizing the same |
| KR101174090B1 (ko) * | 2008-08-25 | 2012-08-14 | 제일모직주식회사 | 유기광전소자용 재료 및 이를 포함하는 유기광전소자 |
| EP2166001B1 (en) * | 2008-09-19 | 2011-07-20 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole Derivative and Method for Producing the Same |
| JP5481057B2 (ja) * | 2008-11-19 | 2014-04-23 | 株式会社東芝 | 有機電界発光素子 |
| KR101233375B1 (ko) | 2008-12-24 | 2013-02-15 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| JP5624784B2 (ja) * | 2009-03-31 | 2014-11-12 | 株式会社半導体エネルギー研究所 | ヘテロ芳香環を有する誘導体、ヘテロ芳香環を有する誘導体を用いた発光素子、発光装置、照明装置、電子機器 |
| KR101172052B1 (ko) * | 2009-05-08 | 2012-08-07 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| JP4523992B1 (ja) * | 2009-07-31 | 2010-08-11 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4474493B1 (ja) * | 2009-07-31 | 2010-06-02 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4590020B1 (ja) * | 2009-07-31 | 2010-12-01 | 富士フイルム株式会社 | 電荷輸送材料及び有機電界発光素子 |
| EP3389110B1 (en) | 2009-07-31 | 2023-12-27 | UDC Ireland Limited | Organic electroluminescent element |
| KR101810591B1 (ko) | 2009-09-16 | 2017-12-20 | 닛토덴코 가부시키가이샤 | 유기 발광 다이오드 발광층을 위한 화합물 |
| JPWO2011046182A1 (ja) | 2009-10-16 | 2013-03-07 | 出光興産株式会社 | 含フルオレン芳香族化合物、有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102009053382A1 (de) * | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| US8617720B2 (en) | 2009-12-21 | 2013-12-31 | E I Du Pont De Nemours And Company | Electroactive composition and electronic device made with the composition |
| JP4637271B1 (ja) | 2010-01-15 | 2011-02-23 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4691611B1 (ja) | 2010-01-15 | 2011-06-01 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP5650932B2 (ja) | 2010-01-28 | 2015-01-07 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子及び電荷輸送材料 |
| JP5620125B2 (ja) | 2010-01-28 | 2014-11-05 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| US8785003B2 (en) | 2010-03-05 | 2014-07-22 | Idemtisu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device using the same |
| KR20120057561A (ko) | 2010-04-20 | 2012-06-05 | 이데미쓰 고산 가부시키가이샤 | 비스카르바졸 유도체, 유기 일렉트로루미네선스 소자용 재료 및 그것을 사용한 유기 일렉트로루미네선스 소자 |
| KR20110122051A (ko) * | 2010-05-03 | 2011-11-09 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| JP5783173B2 (ja) | 2010-06-02 | 2015-09-24 | Jnc株式会社 | 電子受容性窒素含有へテロアリールを含む置換基を有するカルバゾール化合物および有機電界発光素子 |
| JP4729642B1 (ja) * | 2010-07-09 | 2011-07-20 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4680322B1 (ja) * | 2010-07-09 | 2011-05-11 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4751955B1 (ja) * | 2010-07-09 | 2011-08-17 | 富士フイルム株式会社 | 有機電界発光素子 |
| TW201300501A (zh) * | 2010-07-30 | 2013-01-01 | 羅門哈斯電子材料韓國公司 | 使用電場發光化合物作為發光材料之電場發光裝置 |
| JP5760779B2 (ja) * | 2010-08-06 | 2015-08-12 | 株式会社リコー | 発光素子及び表示装置 |
| JP2012056880A (ja) * | 2010-09-08 | 2012-03-22 | Idemitsu Kosan Co Ltd | インドロカルバゾール化合物、有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102010046412B4 (de) | 2010-09-23 | 2022-01-13 | Merck Patent Gmbh | Metall-Ligand Koordinationsverbindungen |
| DE102011123058B3 (de) * | 2010-10-28 | 2020-12-03 | Lg Display Co., Ltd. | Phosphoreszierende Verbindung und diese verwendende organische elektrolumineszente Vorrichtung |
| US8883323B2 (en) | 2010-11-22 | 2014-11-11 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| US9324950B2 (en) * | 2010-11-22 | 2016-04-26 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| CN103228647B (zh) * | 2010-11-24 | 2017-02-15 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| DE102010062877A1 (de) * | 2010-12-13 | 2012-06-21 | Osram Opto Semiconductors Gmbh | Organisches Lichtemittierendes Bauelement und Verwendung eines Kupferkomplexes in einer Ladungstransportschicht |
| DE102010054525A1 (de) | 2010-12-15 | 2012-04-26 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| KR102158326B1 (ko) * | 2010-12-20 | 2020-09-21 | 주식회사 엘지화학 | 전자적 응용을 위한 전기활성 조성물 |
| EP2662368A4 (en) | 2010-12-20 | 2014-06-25 | Idemitsu Kosan Co | AROMATIC HETEROCYCLIC DERIVATIVE AND ORGANIC ELECTROLUMINESCENT ELEMENT THEREWITH |
| DE102010055901A1 (de) | 2010-12-23 | 2012-06-28 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102010055902A1 (de) | 2010-12-23 | 2012-06-28 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| JP5955228B2 (ja) * | 2011-01-18 | 2016-07-20 | 保土谷化学工業株式会社 | 置換されたビピリジル基とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| KR101831015B1 (ko) | 2011-01-20 | 2018-02-21 | 이데미쓰 고산 가부시키가이샤 | 유기 일렉트로 루미네선스 소자 |
| KR20140009263A (ko) * | 2011-02-11 | 2014-01-22 | 유니버셜 디스플레이 코포레이션 | 유기 발광 디바이스 및 이것에 사용되는 재료 |
| CN105762279B (zh) | 2011-03-25 | 2018-04-17 | 出光兴产株式会社 | 有机电致发光器件 |
| JP4935937B2 (ja) * | 2011-04-01 | 2012-05-23 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| KR101311767B1 (ko) * | 2011-04-27 | 2013-09-26 | 한국화학연구원 | 터피리딘 또는 페난쓰롤린 기능기를 함유하는 새로운 구조의 디아민의 제조와 이의 응용 |
| KR101993015B1 (ko) * | 2011-06-24 | 2019-06-25 | 이데미쓰 고산 가부시키가이샤 | 유기 일렉트로루미네선스 소자 |
| JP2013093541A (ja) | 2011-10-06 | 2013-05-16 | Udc Ireland Ltd | 有機電界発光素子とそれに用いることができる化合物および有機電界発光素子用材料、並びに該素子を用いた発光装置、表示装置及び照明装置 |
| JP2013084732A (ja) | 2011-10-07 | 2013-05-09 | Udc Ireland Ltd | 有機電界発光素子及び該素子用発光材料並びに発光装置、表示装置及び照明装置 |
| WO2013062075A1 (ja) | 2011-10-26 | 2013-05-02 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および有機エレクトロルミネッセンス素子用材料 |
| JP2013118349A (ja) | 2011-11-02 | 2013-06-13 | Udc Ireland Ltd | 有機電界発光素子、有機電界発光素子用材料並びに該有機電界発光素子を用いた発光装置、表示装置及び照明装置 |
| JP2013103918A (ja) | 2011-11-15 | 2013-05-30 | Udc Ireland Ltd | 電荷輸送材料、有機電界発光素子及び該素子を用いたことを特徴とする発光装置、表示装置または照明装置 |
| CN103380508B (zh) | 2011-11-22 | 2017-09-08 | 出光兴产株式会社 | 芳香族杂环衍生物、有机电致发光元件用材料以及有机电致发光元件 |
| KR102261235B1 (ko) | 2011-11-22 | 2021-06-04 | 이데미쓰 고산 가부시키가이샤 | 방향족 복소 고리 유도체, 유기 일렉트로루미네선스 소자용 재료 및 유기 일렉트로루미네선스 소자 |
| US9530969B2 (en) | 2011-12-05 | 2016-12-27 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device |
| CN103959503B (zh) * | 2011-12-05 | 2016-08-24 | 出光兴产株式会社 | 有机电致发光元件用材料以及有机电致发光元件 |
| JP6118034B2 (ja) | 2012-02-06 | 2017-04-19 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子とそれに用いることができる化合物および有機電界発光素子用材料、並びに該素子を用いた発光装置、表示装置及び照明装置 |
| US9130174B2 (en) * | 2012-02-29 | 2015-09-08 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device |
| JP2015135836A (ja) | 2012-03-29 | 2015-07-27 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および有機エレクトロルミネッセンス素子用材料 |
| WO2013175789A1 (ja) | 2012-05-24 | 2013-11-28 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2013180241A1 (ja) | 2012-06-01 | 2013-12-05 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および有機エレクトロルミネッセンス素子用材料 |
| CN104507927A (zh) | 2012-06-18 | 2015-04-08 | 东曹株式会社 | 环状吖嗪化合物、其制造方法、及含有其的有机电致发光元件 |
| JP6122112B2 (ja) | 2012-07-13 | 2017-04-26 | エルジー・ケム・リミテッド | ヘテロ環化合物およびこれを用いた有機電子素子 |
| JP5959970B2 (ja) * | 2012-07-20 | 2016-08-02 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| KR101536163B1 (ko) * | 2012-08-29 | 2015-07-14 | 주식회사 엠비케이 | 신규한 유기발광화합물 및 이를 포함하는 유기전기발광소자 |
| US20150097162A1 (en) | 2012-09-11 | 2015-04-09 | Jnc Corporation | Material for organic electroluminescent elements, organic electroluminescent element, display device, and lighting device |
| KR101571589B1 (ko) * | 2012-09-19 | 2015-11-25 | 주식회사 두산 | 인돌로인돌계 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP2014075556A (ja) * | 2012-10-05 | 2014-04-24 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2014103243A (ja) | 2012-11-20 | 2014-06-05 | Samsung Display Co Ltd | カルバゾリル基を有するアザカルバゾール誘導体を含む有機el材料及びそれを用いた有機el素子 |
| US9502667B2 (en) | 2013-01-24 | 2016-11-22 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence |
| JP6317544B2 (ja) * | 2013-02-15 | 2018-04-25 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および電子機器 |
| JP6376727B2 (ja) * | 2013-04-26 | 2018-08-22 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および電子機器 |
| WO2014188947A1 (ja) * | 2013-05-20 | 2014-11-27 | 保土谷化学工業株式会社 | 新規なピリミジン誘導体および有機エレクトロルミネッセンス素子 |
| US9673401B2 (en) * | 2013-06-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR20150052449A (ko) | 2013-11-05 | 2015-05-14 | 삼성디스플레이 주식회사 | 유기 발광 장치 |
| CN105473569B (zh) | 2013-11-13 | 2021-01-01 | 出光兴产株式会社 | 化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 |
| WO2015097841A1 (ja) * | 2013-12-27 | 2015-07-02 | 株式会社日立製作所 | 有機発光材料、有機発光素子およびそれを用いた光源 |
| KR102280686B1 (ko) | 2014-02-11 | 2021-07-22 | 삼성전자주식회사 | 카바졸계 화합물 및 이를 포함한 유기 발광 소자 |
| US10403825B2 (en) | 2014-02-27 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR101754715B1 (ko) | 2014-04-08 | 2017-07-10 | 롬엔드하스전자재료코리아유한회사 | 복수종의 호스트 재료와 이를 포함하는 유기 전계 발광 소자 |
| JP6378106B2 (ja) | 2014-04-16 | 2018-08-22 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子および電子機器 |
| JP2017212024A (ja) | 2014-08-28 | 2017-11-30 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および電子機器 |
| EP3189551B1 (de) | 2014-09-05 | 2021-01-27 | Merck Patent GmbH | Formulierungen und verfahren zur herstellung einer organischen elektrolumineszenzvorrichtung |
| KR102304719B1 (ko) * | 2014-10-01 | 2021-09-27 | 삼성디스플레이 주식회사 | 카바졸계 화합물 및 이를 포함한 유기 발광 소자 |
| KR101560102B1 (ko) * | 2014-11-20 | 2015-10-13 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2016084962A1 (ja) | 2014-11-28 | 2016-06-02 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子および電子機器 |
| WO2016107663A1 (de) | 2014-12-30 | 2016-07-07 | Merck Patent Gmbh | Formulierungen und elektronische vorrichtungen |
| DE102015108016A1 (de) * | 2015-01-20 | 2016-07-21 | Cynora Gmbh | Organische Moleküle, insbesondere zur Verwendung in optoelektronischen Bauelementen |
| US10566543B2 (en) * | 2015-01-20 | 2020-02-18 | Hodogaya Chemical Co., Ltd. | Pyrimidine derivative and organic electroluminescent devices |
| WO2016155866A1 (en) | 2015-03-30 | 2016-10-06 | Merck Patent Gmbh | Formulation of an organic functional material comprising a siloxane solvent |
| KR102654992B1 (ko) | 2015-06-12 | 2024-04-04 | 메르크 파텐트 게엠베하 | Oled 제제에 대한 용매로서 비-방향족 사이클을 함유하는 에스테르 |
| CN106328816B (zh) | 2015-06-16 | 2018-11-13 | 昆山国显光电有限公司 | 一种有机电致发光器件及其制备方法 |
| EP3341981B1 (en) | 2015-08-28 | 2020-08-19 | Merck Patent GmbH | Formulation of an organic functional material comprising an epoxy group containing solvent |
| CN108368361A (zh) | 2015-12-10 | 2018-08-03 | 默克专利有限公司 | 含有包含非芳族环的酮的制剂 |
| JP7051684B2 (ja) | 2015-12-15 | 2022-04-11 | メルク パテント ゲーエムベーハー | 有機電子調合物のための溶媒として芳香族基を含むエステル |
| KR20180095028A (ko) | 2015-12-16 | 2018-08-24 | 메르크 파텐트 게엠베하 | 둘 이상의 상이한 용매의 혼합물을 함유하는 제형 |
| EP3390549B1 (en) | 2015-12-16 | 2022-06-29 | Merck Patent GmbH | Formulations containing a solid solvent |
| JP6716138B2 (ja) * | 2016-01-29 | 2020-07-01 | 国立大学法人山形大学 | ターピリジン誘導体、それよりなる発光材料及びそれを用いた有機el素子 |
| US10840448B2 (en) | 2016-02-17 | 2020-11-17 | Merck Patent Gmbh | Formulation of an organic functional material |
| KR102844041B1 (ko) | 2016-02-26 | 2025-08-11 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 유기 화합물, 발광 소자, 발광 장치, 전자 기기, 및 조명 장치 |
| DE102016003104A1 (de) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Behälter umfassend eine Formulierung enthaltend mindestens einen organischen Halbleiter |
| CN109153871A (zh) | 2016-06-16 | 2019-01-04 | 默克专利有限公司 | 有机功能材料的制剂 |
| JP2019523998A (ja) | 2016-06-17 | 2019-08-29 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| TW201815998A (zh) | 2016-06-28 | 2018-05-01 | 德商麥克專利有限公司 | 有機功能材料之調配物 |
| WO2018024719A1 (en) | 2016-08-04 | 2018-02-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| EP3287451B1 (de) * | 2016-08-24 | 2019-12-11 | Cynora Gmbh | Organische moleküle, insbesondere zur verwendung in organischen optoelektronischen vorrichtungen |
| JP7013459B2 (ja) | 2016-10-31 | 2022-01-31 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| CN109863223B (zh) | 2016-10-31 | 2023-06-20 | 默克专利有限公司 | 有机功能材料的制剂 |
| KR102472751B1 (ko) | 2016-12-06 | 2022-11-30 | 메르크 파텐트 게엠베하 | 전자 디바이스의 제조 방법 |
| CN110168047B (zh) | 2016-12-13 | 2023-08-08 | 默克专利有限公司 | 有机功能材料的制剂 |
| KR102504432B1 (ko) | 2016-12-22 | 2023-02-27 | 메르크 파텐트 게엠베하 | 적어도 2종의 유기-기능성 화합물을 포함하는 혼합물 |
| KR102109545B1 (ko) * | 2016-12-22 | 2020-05-12 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| TWI763772B (zh) | 2017-01-30 | 2022-05-11 | 德商麥克專利有限公司 | 電子裝置之有機元件的形成方法 |
| TWI791481B (zh) | 2017-01-30 | 2023-02-11 | 德商麥克專利有限公司 | 形成有機電致發光(el)元件之方法 |
| JP6317499B2 (ja) * | 2017-03-22 | 2018-04-25 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JP7123967B2 (ja) | 2017-03-31 | 2022-08-23 | メルク パテント ゲーエムベーハー | 有機発光ダイオード(oled)のための印刷方法 |
| CN110494514A (zh) | 2017-04-10 | 2019-11-22 | 默克专利有限公司 | 有机功能材料的制剂 |
| JP7330898B2 (ja) | 2017-05-03 | 2023-08-22 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| EP3428164A1 (en) * | 2017-07-14 | 2019-01-16 | Cynora Gmbh | Organic molecules, in particular for use in optoelectronic devices |
| EP3530659B1 (en) * | 2017-07-14 | 2023-04-19 | Samsung Display Co., Ltd. | Organic molecules, in particular for use in optoelectronic devices |
| WO2019016184A1 (en) | 2017-07-18 | 2019-01-24 | Merck Patent Gmbh | FORMULATION OF AN ORGANIC FUNCTIONAL MATERIAL |
| CA3073931A1 (en) * | 2017-09-01 | 2019-03-07 | Kadmon Corporation, Llc | Inhibitors of rho associated coiled-coil containing protein kinase |
| CN111418081B (zh) | 2017-12-15 | 2024-09-13 | 默克专利有限公司 | 有机功能材料的制剂 |
| JP7247231B2 (ja) | 2018-02-26 | 2023-03-28 | メルク パテント ゲーエムベーハー | 有機機能材料の調合物 |
| EP3807367B1 (en) | 2018-06-15 | 2023-07-19 | Merck Patent GmbH | Formulation of an organic functional material |
| US20200144512A1 (en) * | 2018-07-13 | 2020-05-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR102529109B1 (ko) | 2018-08-07 | 2023-05-03 | 엘지디스플레이 주식회사 | 발광다이오드 및 전계발광 표시장치 |
| KR20210056432A (ko) | 2018-09-24 | 2021-05-18 | 메르크 파텐트 게엠베하 | 과립형 재료의 제조 방법 |
| WO2020094538A1 (en) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| KR102213664B1 (ko) | 2018-11-28 | 2021-02-05 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시 장치 |
| CN111320626B (zh) | 2018-12-17 | 2022-09-02 | 广东阿格蕾雅光电材料有限公司 | 有机电致发光材料、其制备方法及有机电致发光器件 |
| KR102667691B1 (ko) * | 2018-12-28 | 2024-05-20 | 엘지디스플레이 주식회사 | 유기발광다이오드 및 유기발광장치 |
| KR102471152B1 (ko) | 2019-01-10 | 2022-11-24 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시 장치 |
| KR102541446B1 (ko) * | 2019-01-22 | 2023-06-09 | 삼성디스플레이 주식회사 | 유기 발광 소자 및 이를 포함하는 표시 장치 |
| WO2021213918A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Formulation of an organic functional material |
| US20220109112A1 (en) * | 2020-05-29 | 2022-04-07 | Lg Display Co., Ltd. | Organic light emitting device |
| WO2021259824A1 (de) | 2020-06-23 | 2021-12-30 | Merck Patent Gmbh | Verfahren zur herstellung einer mischung |
| WO2022122607A1 (en) | 2020-12-08 | 2022-06-16 | Merck Patent Gmbh | An ink system and a method for inkjet printing |
| WO2022223675A1 (en) | 2021-04-23 | 2022-10-27 | Merck Patent Gmbh | Formulation of an organic functional material |
| CN117355364A (zh) | 2021-05-21 | 2024-01-05 | 默克专利有限公司 | 用于连续纯化至少一种功能材料的方法和用于连续纯化至少一种功能材料的装置 |
| TW202349760A (zh) | 2021-10-05 | 2023-12-16 | 德商麥克專利有限公司 | 電子裝置之有機元件的形成方法 |
| TW202440819A (zh) | 2022-12-16 | 2024-10-16 | 德商麥克專利有限公司 | 有機功能性材料之調配物 |
| WO2025032039A1 (en) | 2023-08-07 | 2025-02-13 | Merck Patent Gmbh | Process for the preparation of an electronic device |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000068059A (ja) * | 1998-08-24 | 2000-03-03 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| JP2000169448A (ja) * | 1998-12-07 | 2000-06-20 | Minolta Co Ltd | 新規アミノ化合物とその製造方法、および用途 |
| JP2001247858A (ja) * | 2000-03-07 | 2001-09-14 | Fuji Photo Film Co Ltd | ベンズイミダゾール誘導体、発光素子材料及び発光素子 |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1119824A (en) | 1964-07-30 | 1968-07-17 | Nat Res Dev | Derivatives of s-triazine |
| JP2897138B2 (ja) | 1989-06-30 | 1999-05-31 | 株式会社リコー | 電界発光素子 |
| JPH04316387A (ja) | 1991-04-15 | 1992-11-06 | Nippon Telegr & Teleph Corp <Ntt> | 面発光レーザ |
| JP3200889B2 (ja) | 1991-10-23 | 2001-08-20 | ソニー株式会社 | 画像の振動補正装置 |
| JPH07138561A (ja) | 1993-11-17 | 1995-05-30 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP3816969B2 (ja) | 1994-04-26 | 2006-08-30 | Tdk株式会社 | 有機el素子 |
| JP3724833B2 (ja) | 1995-03-06 | 2005-12-07 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| US6242115B1 (en) * | 1997-09-08 | 2001-06-05 | The University Of Southern California | OLEDs containing thermally stable asymmetric charge carrier materials |
| JP3633236B2 (ja) * | 1997-10-06 | 2005-03-30 | 東洋インキ製造株式会社 | 有機エレクトロルミネッセンス素子材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| JP3965800B2 (ja) * | 1997-12-01 | 2007-08-29 | チッソ株式会社 | トリアリールアミン誘導体を用いた有機電界発光素子 |
| JP3945032B2 (ja) * | 1998-08-10 | 2007-07-18 | 東洋インキ製造株式会社 | 有機エレクトロルミネッセンス素子用発光材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| JP4686011B2 (ja) | 1999-07-22 | 2011-05-18 | 富士フイルム株式会社 | 新規ヘテロ環化合物、発光素子材料およびそれを使用した発光素子 |
| JP2001064640A (ja) * | 1999-08-30 | 2001-03-13 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子用材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| TWI263636B (en) * | 1999-09-16 | 2006-10-11 | Ciba Sc Holding Ag | Fluorescent maleimides and use thereof |
| JP4116225B2 (ja) * | 1999-10-27 | 2008-07-09 | 富士フイルム株式会社 | 新規縮合へテロ環化合物、発光素子材料およびそれを使用した発光素子 |
| JP2001160489A (ja) | 1999-12-01 | 2001-06-12 | Toyota Central Res & Dev Lab Inc | 有機電界発光素子 |
| JP2001207167A (ja) * | 2000-01-24 | 2001-07-31 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子用発光材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| US6660410B2 (en) * | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| JP4211191B2 (ja) | 2000-04-03 | 2009-01-21 | 東洋インキ製造株式会社 | 有機エレクトロルミネッセンス素子用材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| JP2002008860A (ja) * | 2000-04-18 | 2002-01-11 | Mitsubishi Chemicals Corp | 有機電界発光素子 |
| DE60143106D1 (de) | 2000-07-17 | 2010-11-04 | Fujifilm Corp | Lichtemittierendes Element und Azolverbindung |
| JP4344494B2 (ja) * | 2000-08-24 | 2009-10-14 | 富士フイルム株式会社 | 発光素子及び新規重合体子 |
| JP2002081234A (ja) | 2000-09-08 | 2002-03-22 | Iseki & Co Ltd | 作業車両のドアロック装置 |
| US6893743B2 (en) * | 2000-10-04 | 2005-05-17 | Mitsubishi Chemical Corporation | Organic electroluminescent device |
| EP1202608B2 (en) | 2000-10-30 | 2012-02-08 | Kabushiki Kaisha Toyota Chuo Kenkyusho | Organic light-emitting devices |
| JP4092901B2 (ja) * | 2000-10-30 | 2008-05-28 | 株式会社豊田中央研究所 | 有機電界発光素子 |
| JP4040249B2 (ja) * | 2000-11-16 | 2008-01-30 | 富士フイルム株式会社 | 発光素子 |
| JP4404473B2 (ja) | 2000-12-25 | 2010-01-27 | 富士フイルム株式会社 | 新規含窒素へテロ環化合物、発光素子材料およびそれらを使用した発光素子 |
| JP2002299810A (ja) | 2001-04-02 | 2002-10-11 | Matsushita Electric Ind Co Ltd | 電子部品の実装方法 |
| JP2003022893A (ja) * | 2001-07-06 | 2003-01-24 | Fuji Photo Film Co Ltd | 発光素子 |
| JP2003031371A (ja) * | 2001-07-17 | 2003-01-31 | Mitsubishi Chemicals Corp | 有機電界発光素子及び青色発光素子 |
| JP4140323B2 (ja) * | 2001-09-19 | 2008-08-27 | 富士ゼロックス株式会社 | 有機電界発光素子 |
| JP4220767B2 (ja) * | 2001-12-04 | 2009-02-04 | 日本放送協会 | 有機化合物、有機el素子およびディスプレイ |
| KR100957288B1 (ko) * | 2002-03-15 | 2010-05-12 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 이를 이용한 유기 전기발광소자 |
| US7641986B2 (en) * | 2002-03-18 | 2010-01-05 | Isis Innovation Limited | Phosphorescent dendrimers for use in light-emitting devices |
| EP1489155A4 (en) | 2002-03-22 | 2006-02-01 | Idemitsu Kosan Co | MATERIAL FOR ORGANIC ELECTROLUMINESCENT DEVICES AND THE EQUIVALENT DEVICES |
| ITPD20030058A1 (it) | 2003-03-20 | 2004-09-21 | Orv Spa | Prodotto stratiforme impregnato impiegabile come |
| EP1708547A1 (en) | 2004-01-21 | 2006-10-04 | Idemitsu Kosan Co., Ltd. | Host material for organic electroluminescent element and organic electroluminescent element |
-
2003
- 2003-03-19 EP EP03712758A patent/EP1489155A4/en not_active Withdrawn
- 2003-03-19 WO PCT/JP2003/003329 patent/WO2003080760A1/ja not_active Ceased
- 2003-03-19 JP JP2003578493A patent/JP4316387B2/ja not_active Expired - Lifetime
- 2003-03-19 KR KR1020047014947A patent/KR100948700B1/ko not_active Ceased
- 2003-03-19 EP EP08156371.0A patent/EP2169028B1/en not_active Expired - Lifetime
- 2003-03-21 TW TW092106356A patent/TWI306890B/zh not_active IP Right Cessation
- 2003-03-21 TW TW097115521A patent/TW200904942A/zh not_active IP Right Cessation
- 2003-03-24 US US10/393,988 patent/US20040086745A1/en not_active Abandoned
-
2005
- 2005-06-13 US US11/150,342 patent/US8580391B2/en not_active Expired - Fee Related
-
2008
- 2008-11-07 JP JP2008286590A patent/JP5584406B2/ja not_active Expired - Lifetime
-
2012
- 2012-05-31 US US13/485,111 patent/US20120298975A1/en not_active Abandoned
- 2012-08-31 US US13/601,300 patent/US8741450B2/en not_active Expired - Lifetime
-
2013
- 2013-04-18 JP JP2013087646A patent/JP5771644B2/ja not_active Expired - Lifetime
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000068059A (ja) * | 1998-08-24 | 2000-03-03 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| JP2000169448A (ja) * | 1998-12-07 | 2000-06-20 | Minolta Co Ltd | 新規アミノ化合物とその製造方法、および用途 |
| JP2001247858A (ja) * | 2000-03-07 | 2001-09-14 | Fuji Photo Film Co Ltd | ベンズイミダゾール誘導体、発光素子材料及び発光素子 |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20140034183A (ko) * | 2011-05-13 | 2014-03-19 | 이데미쓰 고산 가부시키가이샤 | 유기 el 다색 발광 장치 |
| US10276637B2 (en) | 2011-05-13 | 2019-04-30 | Idemitsu Kosan Co., Ltd. | Organic EL multi-color light-emitting device |
| KR102029108B1 (ko) * | 2011-05-13 | 2019-10-07 | 이데미쓰 고산 가부시키가이샤 | 유기 el 다색 발광 장치 |
| KR20130011446A (ko) | 2011-07-21 | 2013-01-30 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| KR20150064878A (ko) | 2013-12-04 | 2015-06-12 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20150124886A (ko) | 2014-04-29 | 2015-11-06 | 롬엔드하스전자재료코리아유한회사 | 전자전달재료 및 이를 포함하는 유기 전계 발광 소자 |
| US10818846B2 (en) | 2014-04-29 | 2020-10-27 | Rohm And Haas Electronic Materials Korea Ltd. | Electron transport material and organic electroluminescent device comprising the same |
| US11926603B2 (en) | 2018-01-24 | 2024-03-12 | Samsung Sdi Co., Ltd. | Compound, composition, organic optoelectronic diode, and display device |
| US12010913B2 (en) | 2019-10-02 | 2024-06-11 | Samsung Sdi Co., Ltd. | Compound for organic optoelectronic device, organic optoelectronic device and display device |
Also Published As
| Publication number | Publication date |
|---|---|
| TW200304937A (en) | 2003-10-16 |
| EP2169028A3 (en) | 2011-02-09 |
| US20040086745A1 (en) | 2004-05-06 |
| WO2003080760A1 (en) | 2003-10-02 |
| US8741450B2 (en) | 2014-06-03 |
| US8580391B2 (en) | 2013-11-12 |
| EP1489155A4 (en) | 2006-02-01 |
| TW200904942A (en) | 2009-02-01 |
| JP5584406B2 (ja) | 2014-09-03 |
| JP4316387B2 (ja) | 2009-08-19 |
| JP2009088538A (ja) | 2009-04-23 |
| EP2169028B1 (en) | 2018-11-21 |
| US20050249976A1 (en) | 2005-11-10 |
| US20120298975A1 (en) | 2012-11-29 |
| EP2169028A2 (en) | 2010-03-31 |
| TWI370839B (ko) | 2012-08-21 |
| US20120319099A1 (en) | 2012-12-20 |
| JP5771644B2 (ja) | 2015-09-02 |
| KR20040094842A (ko) | 2004-11-10 |
| TWI306890B (en) | 2009-03-01 |
| EP1489155A1 (en) | 2004-12-22 |
| JPWO2003080760A1 (ja) | 2005-07-21 |
| JP2013175763A (ja) | 2013-09-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100948700B1 (ko) | 유기 전기 발광 소자용 재료 및 이를 이용한 유기 전기발광 소자 | |
| KR100957288B1 (ko) | 유기 전기발광 소자용 재료 및 이를 이용한 유기 전기발광소자 | |
| KR100831510B1 (ko) | 신규 아릴아민 화합물 및 유기 전기발광 소자 | |
| KR20040094866A (ko) | 유기 전자발광 소자용 재료 및 이를 이용한 유기 전자발광소자 | |
| CN102292327A (zh) | 具有连接有吡啶基的三唑环结构的化合物以及有机电致发光器件 | |
| JP4030093B2 (ja) | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 | |
| CN103201273A (zh) | 用于有机电子材料的新化合物以及使用该化合物的有机电致发光器件 | |
| JP4028996B2 (ja) | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 | |
| JP2007266620A (ja) | 有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20040921 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20071113 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20090424 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20091221 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20100312 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20100312 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| PR1001 | Payment of annual fee |
Payment date: 20130227 Start annual number: 4 End annual number: 4 |
|
| J204 | Request for invalidation trial [patent] | ||
| PJ0204 | Invalidation trial for patent |
Patent event date: 20131121 Comment text: Request for Trial Patent event code: PJ02042R01D Patent event date: 20100312 Comment text: Registration of Establishment Patent event code: PJ02041E01I Appeal kind category: Invalidation Request date: 20131121 Decision date: 20140502 Appeal identifier: 2013100003068 |
|
| FPAY | Annual fee payment |
Payment date: 20140220 Year of fee payment: 5 |
|
| PR1001 | Payment of annual fee |
Payment date: 20140220 Start annual number: 5 End annual number: 5 |
|
| J301 | Trial decision |
Free format text: TRIAL DECISION FOR INVALIDATION REQUESTED 20131121 Effective date: 20140502 |
|
| PJ1301 | Trial decision |
Patent event code: PJ13011S05D Patent event date: 20140502 Comment text: Trial Decision on Invalidation (Patent, Utility Model, Industrial Design) Appeal kind category: Invalidation Request date: 20131121 Decision date: 20140502 Appeal identifier: 2013100003068 |
|
| PC2102 | Extinguishment |
Termination category: Others Termination date: 20140813 |
|
| PG1701 | Publication of correction |
Publication date: 20150320 |