CN111068061A - 用于降低不期望体液免疫应答的给药组合 - Google Patents
用于降低不期望体液免疫应答的给药组合 Download PDFInfo
- Publication number
- CN111068061A CN111068061A CN201911306104.4A CN201911306104A CN111068061A CN 111068061 A CN111068061 A CN 111068061A CN 201911306104 A CN201911306104 A CN 201911306104A CN 111068061 A CN111068061 A CN 111068061A
- Authority
- CN
- China
- Prior art keywords
- administration
- synthetic nanocarriers
- therapeutic
- nanocarriers
- immune response
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
- A61K38/13—Cyclosporins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- A61K38/1761—Apoptosis related proteins, e.g. Apoptotic protease-activating factor-1 (APAF-1), Bax, Bax-inhibitory protein(s)(BI; bax-I), Myeloid cell leukemia associated protein (MCL-1), Inhibitor of apoptosis [IAP] or Bcl-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1767—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from invertebrates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/195—Chemokines, e.g. RANTES
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/21—Interferons [IFN]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/36—Blood coagulation or fibrinolysis factors
- A61K38/37—Factors VIII
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/38—Albumins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/47—Hydrolases (3) acting on glycosyl compounds (3.2), e.g. cellulases, lactases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/48—Hydrolases (3) acting on peptide bonds (3.4)
- A61K38/482—Serine endopeptidases (3.4.21)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/50—Hydrolases (3) acting on carbon-nitrogen bonds, other than peptide bonds (3.5), e.g. asparaginase
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0003—Invertebrate antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/593—Polyesters, e.g. PLGA or polylactide-co-glycolide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6923—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being an inorganic particle, e.g. ceramic particles, silica particles, ferrite or synsorb
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
- A61K47/6931—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer
- A61K47/6935—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer the polymer being obtained otherwise than by reactions involving carbon to carbon unsaturated bonds, e.g. polyesters, polyamides or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
- A61K47/6931—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer
- A61K47/6935—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer the polymer being obtained otherwise than by reactions involving carbon to carbon unsaturated bonds, e.g. polyesters, polyamides or polyglycerol
- A61K47/6937—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle the material constituting the nanoparticle being a polymer the polymer being obtained otherwise than by reactions involving carbon to carbon unsaturated bonds, e.g. polyesters, polyamides or polyglycerol the polymer being PLGA, PLA or polyglycolic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Synthetic bilayered vehicles, e.g. liposomes or liposomes with cholesterol as the only non-phosphatidyl surfactant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5115—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/513—Organic macromolecular compounds; Dendrimers
- A61K9/5146—Organic macromolecular compounds; Dendrimers obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyamines, polyanhydrides
- A61K9/5153—Polyesters, e.g. poly(lactide-co-glycolide)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5192—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/575—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 humoral response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/577—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 tolerising response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
- A61K2039/622—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier non-covalent binding
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y305/00—Hydrolases acting on carbon-nitrogen bonds, other than peptide bonds (3.5)
- C12Y305/01—Hydrolases acting on carbon-nitrogen bonds, other than peptide bonds (3.5) in linear amides (3.5.1)
- C12Y305/01001—Asparaginase (3.5.1.1)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Nanotechnology (AREA)
- Zoology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Optics & Photonics (AREA)
- Biomedical Technology (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Inorganic Chemistry (AREA)
- Biophysics (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Hematology (AREA)
- Ceramic Engineering (AREA)
- Endocrinology (AREA)
- Dermatology (AREA)
- Dispersion Chemistry (AREA)
- Rheumatology (AREA)
- Transplantation (AREA)
- Physical Education & Sports Medicine (AREA)
- Obesity (AREA)
Abstract
本申请涉及用于降低不期望体液免疫应答的给药组合。公开了与无合成纳米载体之治疗性大分子的给药相组合的治疗性大分子和免疫抑制剂(在一些实施方案中,与合成纳米载体连接)的给药,以及提供降低的体液免疫应答的相关方法。
Description
本申请是申请日为2014年5月2日、申请号为“201480031937.3”、发明名称为“用于降低不期望体液免疫应答的给药组合”的中国专利申请的分案申请,原申请是国际申请PCT/US2014/036698的中国国家阶段申请。
相关申请
本申请依据35U.S.C.§119要求于2013年5月3日提交的美国临时申请61/819517、于2013年9月24日提交的美国临时申请61/881851、于2013年9月24日提交的美国临时申请61/881913、于2013年9月24日提交的美国临时申请61/881921、于2013年11月21日提交的美国临时申请61/907177、于2014年3月5日提交的美国临时申请61/948313、以及于2014年3月5日提交的美国临时申请61/948384的权益,其每一个的全部内容均通过引用并入本文。
技术领域
本发明涉及与免疫抑制剂(例如与合成纳米载体连接的那些)伴随施用之治疗性大分子的剂量与单独治疗性大分子的剂量的组合,及相关方法。所述组合物和方法允许有效地降低不期望的体液免疫应答。此类不期望免疫应答可中和治疗性治疗的效力或引起针对该治疗剂的超敏反应。因此,所提供的组合物和方法可用于其中施用导致不期望体液免疫应答之治疗性大分子的对象。
背景技术
治疗性治疗(例如蛋白质或酶替代治疗)通常导致针对特定治疗剂的不期望免疫应答。在这样的情况下,免疫系统中的细胞将该治疗剂识别为外来的并试图将其中和或破坏,正如它们试图破坏感染性微生物,例如细菌和病毒。可通过使用免疫抑制药物来降低此类不期望免疫应答。然而,常规的免疫抑制药物作用广泛,并且作用广泛的免疫抑制剂的使用与严重副作用的风险相关,所述副作用例如肿瘤、感染、肾毒性和代谢紊乱。因此,新的治疗将是有益的。
发明内容
在一个方面,提供了一种方法,其包括:(1)第一给药(first dosing),其包括伴随施用(a)未与任何合成纳米载体连接的治疗性大分子,和(b)免疫抑制剂,例如与合成纳米载体连接并且不包含治疗性大分子的治疗性大分子抗原呈递细胞(antigen-presentingcell,APC)可呈递抗原的那些;(2)第二给药,其包括(c)施用未与任何合成纳米载体连接的治疗性大分子,并且不施用任何合成纳米载体;以及(3)根据降低针对治疗性大分子的不期望体液免疫应答的施用方案向对象施用第一和第二给药。
在本文中提供的任一种方法的一个实施方案中,所述方法还包括(4)确定降低针对治疗性大分子的不期望体液免疫应答的用于第一和第二给药的施用方案。在本文中提供的任一种方法的另一个实施方案中,针对治疗性大分子的不期望体液免疫应答由无第一给药的第二给药引起。在本文中提供的任一种方法的另一个实施方案中,所述第一给药包括向对象施用(a)和(b)一次或更多次。在本文中提供的任一种方法的另一个实施方案中,施用(a)和(b)至少1、2、3、4或5次。在本文中提供的任一种方法的另一个实施方案中,在第一给药之后至少1、2、3、4、5、6、7或8周,向所述对象施所述第二给药。在本文中提供的任一种方法的另一个实施方案中,所述方法还包括在施用第一给药和第二给药之前和/或之后评估对象中的不期望体液免疫应答。在本文中提供的任一种方法的另一个实施方案中,第一给药和/或第二给药的施用通过静脉内、腹膜内或皮下施用进行。在本文中提供的任一种方法的另一个实施方案中,所述方法还包括鉴定对象为具有针对治疗性大分子的不期望体液免疫应答或者处于其风险之中。在一些实施方案中,预期或怀疑对象具有针对治疗性大分子的不期望体液免疫应答。
在另一个方面,提供了一种组合物,其包含:(1)一个或更多个第一剂量,其各自包含(a)未与任何合成纳米载体连接的治疗性大分子,和(b)免疫抑制剂,例如与合成纳米载体群连接并且不包含治疗性大分子的治疗性大分子APC可呈递抗原的那些;和(2)一个或更多个第二剂量,其包含未与任何合成纳米载体连接的治疗性大分子。在本文中提供的任一种组合物的一个实施方案中,所述组合物用于降低针对治疗性大分子的不期望体液免疫应答的方法。在本文中提供的任一种方法的另一个实施方案中,所述方法包括根据施用方案向对象施用第一和第二剂量。在另一个实施方案中,所述方法还包括确定降低针对治疗性大分子的不期望体液免疫应答的用于第一和第二剂量的施用方案。在另一个实施方案中,所述方法为本文中提供的任一种方法。
在本文中提供的任一种组合物的另一个实施方案中,所述第二剂量不包含任何合成纳米载体。在本文中提供的任一种组合物的另一个实施方案中,所述组合物为药盒(kit)并且一个或更多个第一剂量和一个或更多个第二剂量各自容纳在药盒中的容器中。在本文中提供的任一种组合物的另一个实施方案中,所述组合物还包含可药用载体。
在本文中提供的任一种方法或组合物的一个实施方案中,所述免疫抑制剂包含他汀类、mTOR抑制剂、TGF-β信号传导剂(TGF-β signaling agent)、皮质类固醇、线粒体功能的抑制剂、P38抑制剂、NF-κB抑制剂、腺苷受体激动剂、前列腺素E2激动剂、磷酸二酯酶4抑制剂、HDAC抑制剂或蛋白酶体抑制剂。在本文中提供的任一种方法或组合物的另一个实施方案中,mTOR抑制剂是雷帕霉素。
在本文中提供的任一种方法或组合物的另一个实施方案中,所述治疗性大分子是治疗性蛋白质。在本文中提供的任一种方法或组合物的另一个实施方案中,所述治疗性大分子是治疗性多核苷酸。在本文中提供的任一种方法或组合物的另一个实施方案中,所述治疗性大分子用于蛋白质替代或蛋白质补充治疗。在本文中提供的任一种方法或组合物的另一个实施方案中,所述治疗性大分子包含可输注或可注射的治疗性蛋白质、酶、酶辅因子、激素、血液因子或凝血因子、细胞因子、干扰素、生长因子、单克隆抗体、多克隆抗体或与庞皮病(Pompe’s disease)相关的蛋白质。在本文中提供的任一种方法或组合物的另一个实施方案中,所述可输注或可注射的治疗性蛋白质包含托珠单抗(Tocilizumab)、α-1抗胰蛋白酶、Hematide、白蛋白干扰素α-2b(albinterferon alfa-2b)、Rhucin、替莫瑞林、奥瑞珠单抗、贝利木单抗、聚乙二醇化重组尿酸酶(pegloticase)、聚乙二醇化重组假丝酵母尿酸酶(pegsticase)、他利苷酶α(taliglucerase alfa)、阿加糖酶α(agalsidase alfa)或葡糖脑苷脂酶α(velaglucerase alfa)。在本文中提供的任一种方法或组合物的另一个实施方案中,所述酶包含氧化还原酶、转移酶、水解酶、裂合酶、异构酶或连接酶。在本文中提供的任一种方法或组合物的另一个实施方案中,所述酶包含用于对溶酶体贮积症进行酶替代治疗的酶。在本文中提供的任一种方法或组合物的另一个实施方案中,所述用于对溶酶体贮积症进行酶替代治疗的酶包含伊米苷酶、a-半乳糖苷酶A(a-gal A)、阿加糖酶β(agalsidase beta)、酸性a-葡糖苷酶(GAA)、阿葡糖苷酶α(alglucosidase alfa)、LUMIZYME、MYOZYME、芳基硫酸酯酶B、拉罗尼酶(laronidase)、ALDURAZYME、艾杜硫酶(idursulfase)、ELAPRASE、芳基硫酸酯酶B或NAGLAZYME。在本文中提供的任一种方法或组合物的另一个实施方案中,所述酶包含KRYSTEXXA(聚乙二醇化重组尿酸酶)或聚乙二醇化重组假丝酵母尿酸酶。在本文中提供的任一种方法或组合物的另一个实施方案中,所述单克隆抗体包含HUMIRA(阿达木单抗)。在本文中提供的任一种方法或组合物的另一个实施方案中,所述细胞因子包含淋巴因子、白介素、趋化因子、1型细胞因子或2型细胞因子。在本文中提供的任一种方法或组合物的另一个实施方案中,所述血液因子或凝血因子包含因子I、因子II、组织因子、因子V、因子VII、因子VIII、因子Ⅸ、因子X、因子Xa、因子XII、因子XIII、冯·维勒布兰德因子(von Willebrand factor)、前激肽释放酶、高分子量激肽原、纤连蛋白、抗凝血酶III、肝素辅因子II、蛋白C(protein C)、蛋白S(protein S)、蛋白Z(proteinZ)、蛋白Z相关蛋白酶抑制剂(protein Z-related protease inhibitor,ZPI)、纤溶酶原、α2-抗纤溶酶、组织纤溶酶原激活物(tissue plasminogen activator,tPA)、尿激酶、纤溶酶原激活物抑制剂-1(plasminogen activator inhibitor-1,PAI1)、纤溶酶原激活物抑制剂-2(plasminogen activator inhibitor-2,PAI2)、癌促凝物质(cancer procoagulant)或阿法依伯汀(epoetin alfa)。在本文中提供的任一种方法或组合物的另一个实施方案中,所述血液因子或凝血因子包含因子VIII。
在本文中提供的任一种方法或组合物的另一个实施方案中,基于整个合成纳米载体群的平均值,免疫抑制剂的载量为0.1%至50%。在本文中提供的任一种方法或组合物的另一个实施方案中,基于整个合成纳米载体群的平均值,免疫抑制剂的载量为0.1%至20%。
在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体包含脂质纳米颗粒、聚合物纳米颗粒、金属纳米颗粒、基于表面活性剂的乳剂、树状聚体、巴基球(buckyball)、纳米线(nanowire)、病毒样颗粒或者肽或蛋白质颗粒。在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体包含脂质纳米颗粒。在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体包含脂质体。在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体包含金属纳米颗粒。在本文中提供的任一种方法或组合物的另一个实施方案中,所述金属纳米颗粒包含金纳米颗粒。在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体包含聚合物纳米颗粒。在本文中提供的任一种方法或组合物的另一个实施方案中,所述合成聚合物纳米颗粒包含聚合物,所述聚合物为非甲氧基封端(non-methoxy-terminated)的普朗尼克聚合物(pluronic polymer)。在本文中提供的任一种方法或组合物的另一个实施方案中,所述聚合物纳米颗粒包含聚酯、与聚醚偶联的聚酯、聚氨基酸、聚碳酸酯、聚缩醛、聚缩酮、多糖、聚乙基唑啉或聚乙烯亚胺。在本文中提供的任一种方法或组合物的另一个实施方案中,所述聚酯包含聚(乳酸)、聚(乙醇酸)、聚乳酸-乙醇酸共聚物或聚己内酯。在本文中提供的任一种方法或组合物的另一个实施方案中,所述聚合物纳米颗粒包含聚酯和与聚醚偶联的聚酯。在本文中提供的任一种方法或组合物的另一个实施方案中,所述聚醚包含聚乙二醇或聚丙二醇。
在本文中提供的任一种方法或组合物的另一个实施方案中,使用所述群中之合成纳米载体的动态光散射获得的颗粒大小分布的平均值为大于100nm的直径。在本文中提供的任一种方法或组合物的另一个实施方案中,所述直径大于150nm。在本文中提供的任一种方法或组合物的另一个实施方案中,所述直径大于200nm。在本文中提供的任一种方法或组合物的另一个实施方案中,所述直径大于250nm。在本文中提供的任一种方法或组合物的另一个实施方案中,所述直径大于300nm。
在本文中提供的任一种方法或组合物的另一个实施方案中,所述群中的合成纳米载体的纵横比(aspect ratio)大于1∶1、1∶1.2、1∶1.5、1∶2、1∶3、1∶5、1∶7或1∶10。
在另一个方面,提供了制备本文中提供的任一种组合物或药盒的方法。在一个实施方案中,制备方法包括产生治疗性大分子的一种或更多种剂量或剂型并且产生免疫抑制剂的一种或更多种剂量或剂型。在所提供之任一种制备方法的另一个实施方案中,产生免疫抑制剂的一种或更多种剂量或剂型的步骤包括使免疫抑制剂与合成纳米载体连接。在所提供之任一种制备方法的另一个实施方案中,所述方法还包括将免疫抑制剂的一种或更多种剂量或剂型与治疗性大分子的一种或更多种剂量或剂型在药盒中组合。
在另一个方面,提供了本文中提供的任一种组合物或药盒用于制备用于在对象中降低针对治疗性大分子的不期望免疫应答的药物的用途。在一个实施方案中,所述组合物或药盒包含含有免疫抑制剂的一种或更多种剂量或剂型和含有治疗性大分子的一种或更多种剂量或剂型,其中根据本文中提供的任一种方法施用免疫抑制剂和治疗性大分子。在本文中提供的任一种用途的另一个实施方案中,免疫抑制剂与合成纳米载体连接。在本文中提供的任一种用途的一些实施方案中,免疫抑制剂不包含治疗性大分子的治疗性大分子抗原呈递细胞(APC)可呈递抗原。在本文中提供的任一种用途的一些实施方案中,所述组合物或药盒还包含用作一次或更多次第二给药的含有治疗性大分子的一种或更多种剂量或剂型。
在另一个方面,提供了本文中提供的任一种组合物或药盒以用于包含免疫抑制剂的一种或更多种剂量或剂型和包含治疗性大分子的一种或更多种剂量或剂型中的任一种。在另一个实施方案中,所述组合物或药盒还包含用作一次或更多次第二给药的含有治疗性大分子的一种或更多种剂量或剂型。在另一个实施方案中,免疫抑制剂与合成纳米载体连接。在另一个实施方案中,免疫抑制剂不包含治疗性大分子的治疗性大分子抗原呈递细胞(APC)可呈递抗原。
附图说明
图1A和1B示出了血友病A小鼠中纳米载体和FVIII给药的效力。
图2示出了在最后的纳米载体和FVIII给药后1个月,针对FVIII的抗体回忆应答。
图3A和3B示出了在有或无与雷帕霉素连接之纳米载体的情况下,经HUMIRA/阿达木单抗处理的小鼠中针对HUMIRA的免疫应答。
图4示出了在有或无与雷帕霉素连接之纳米载体的情况下,经钥孔林普贝血蓝蛋白(Keyhole Limpet Hemocyanin,KLH)处理的小鼠中的抗KLH抗体效价。
图5示出了在有或无与雷帕霉素连接之纳米载体的情况下,经卵清蛋白(ovalbumin,OVA)处理的小鼠中的抗OVA抗体效价。
图6示出了在有或无与雷帕霉素连接之纳米载体的情况下,经KRYSTEXXA处理的小鼠中的抗KRYSTEXXA抗体效价。
图7示出了在存在或不存在与雷帕霉素连接之纳米载体的情况下,经OVA和KLH处理的小鼠中的抗体效价。
图8A和8B示出了在有或无与雷帕霉素连接之纳米载体的情况下,经KLH处理的小鼠中针对KLH的免疫应答。
图9A和9B示出了在有或无与雷帕霉素连接之纳米载体的情况下,经HUMIRA/阿达木单抗处理的小鼠中针对HUMIRA/阿达木单抗的免疫应答。
图10示出了经或未经与雷帕霉素连接的纳米载体处理的小鼠中针对PEG-KLH的免疫应答。
图11示出了在有或无与雷帕霉素连接之纳米载体的情况下,HUMIRA的免疫应答和治疗应答。
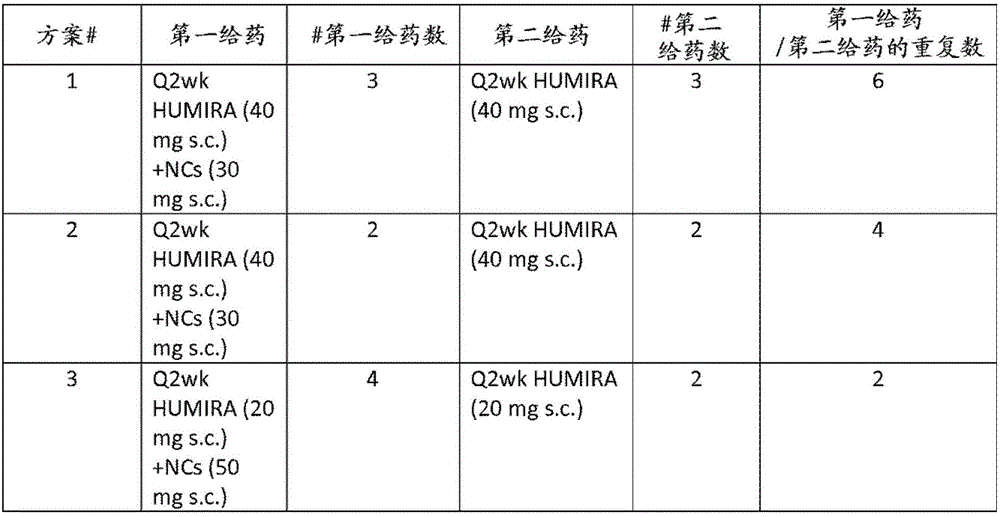
图12示出了施用方案。
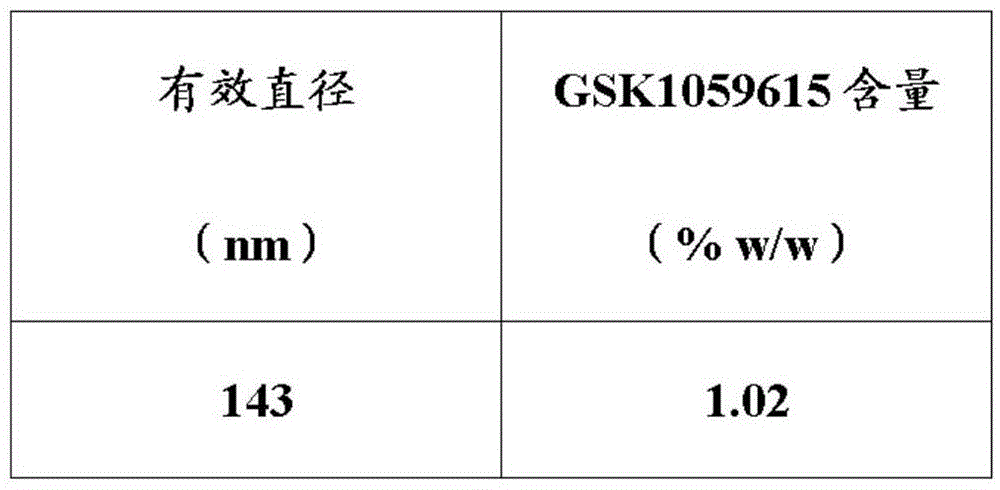
图13证明与经包封蛋白质伴随施用之与雷帕霉素连接的合成纳米载体或与GSK1059615连接的纳米载体的效应。
具体实施方式
在对本发明进行详细描述之前,应当理解,本发明不限于具体举例说明的材料或工艺参数,因为它们当然可以变化。还应理解的是,本文中使用的术语仅是为了描述本发明的一些具体实施方案,并非旨在对描述本发明的替代术语的用途进行限制。
出于所有目的,本文中引用的所有出版物、专利和专利申请(无论上文或下文)均在此通过引用整体并入。
除非所述内容另有明确指出,否则本说明书及所附权利要求书中使用的没有数量词修饰的名词表示一个/种或更多个/种。例如,提及的“聚合物”包含两种或更多种此类分子的混合物或不同分子量的单一聚合物种类的混合物,提及的“合成纳米载体”包含两种或更多种此类合成纳米载体的混合物或多种这样的合成纳米载体,提及的“RNA分子”包含两种或更多种此类RNA分子的混合物或多种这样的RNA分子,提及的“免疫抑制剂”包含两种或更多种此类材料的混合物或多种这样的免疫抑制剂分子等。
本文中使用的术语“包含/包括”或其变化形式应理解为指包括引用的任何整体(例如特点、要素、特征、特性、方法/处理步骤或限制)或整体(例如特点、要素、特征、特性、方法/处理步骤或限制)的组,但不排除任何其他整体或整体的组。因此,本文中使用的术语“包含/包括”是包括性的并且不排除另外的未引用整体或方法/处理步骤。
在本文中提供任一种组合物和方法的一些实施方案中,可用“基本由...组成”或“由...组成”来替代“包含/包括”。本文中使用的短语“基本由...组成”要求指定的整体或步骤以及不实质地影响所要求保护之发明的特征或功能的那些。本文中使用的术语“由...组成”仅用于指所引用的整体(例如特点、要素、特征、特性、方法/处理步骤或限制)或整体(例如特点、要素、特征、特性、方法/处理步骤或限制)的组的存在。
A.引言
已令人惊讶地发现,伴随递送免疫抑制剂(例如当与合成纳米载体连接时)和治疗性大分子并组合递送不与合成纳米载体一起施用的治疗性大分子可有效地降低抗治疗性大分子特异性抗体的产生。由于在用治疗性大分子进行治疗性治疗期间降低可以是有益的,本发明可用于需要用产生或预期产生针对它的不期望体液免疫应答的治疗性大分子进行治疗的对象。在一些实施方案中,本发明预防或抑制可中和某些治疗性大分子治疗的有益作用的不期望体液免疫应答。
本发明人已出乎意料且令人惊讶地发现,上述问题和限制可通过实施本文中公开的发明来克服。特别地,本发明人已出乎意料地发现,可以以降低治疗性大分子特异性的不期望体液免疫应答的某些组合提供免疫抑制剂和治疗性大分子给药,特别是在其中在伴随施用免疫抑制剂组合物和治疗性大分子之后施用治疗性大分子而无合成纳米载体的一些实施方案中。
现在,将在下文对本发明进行更详细的描述。
B.定义
“施用”及其变化形式意指以在药理学上可用的方式向对象提供物质。在一些实施方案中,该术语旨在包括“引起施用”。“引起施用”意指直接或间接地引起、促使、鼓励、帮助、诱导或指导另一方施用物质。
“施用方案”指根据预定方案施用第一给药和第二给药。所述方案可包括第一给药和第二给药的数量以及这些给药的频率或给药之间的间隔时间。这样的施用方案可包括多个参数,这些参数可有所不同以达到特定目的,优选是降低针对治疗性大分子的不期望体液免疫应答。在一些实施方案中,施用方案为下文的实施例中提供的任一种实施方案。在一些实施方案中,根据本发明的施用方案可用于向一个或更多个测试对象施用第一和第二给药。然后,可评估这些测试对象中的免疫应答以确定该方案是否有效地降低不期望的体液免疫应答。可使用本文中提供的或本领域中另外已知的任一种方法来确定该方案是否具有期望效果。例如,样品可获自已根据特定施用方案向其施用本文中提供的给药的对象以确定特定免疫细胞、细胞因子、抗体等是否得以降低、产生、活化等。可用于检测免疫细胞的存在和/或数量的方法包括但不限于:流式细胞术法(例如,FACS)、ELISpot、增殖应答、细胞因子产生和免疫组织化学法。可用于确定抗体产生水平的方法在本领域中是公知的并且包括本文中提供的测定。这样的测定包括ELISA测定。
在用于向对象施用之组合物或剂型的情况下,“有效量”指该组合物或剂型在对象中产生一种或更多种期望免疫应答(例如不期望体液免疫应答的降低)的量。因此,在一些实施方案中,有效量为本文中提供的组合物或剂型之降低不期望体液免疫应答的任意量。有效量可用于体外或体内目的。对于体内目的,该量可以是临床医生认为可对本文中提供的对象具有临床益处的量,所述对象例如需要治疗性大分子施用和/或针对它的抗原特异性免疫耐受的对象。
有效量可涉及降低不期望免疫应答的水平,但是在一些实施方案中,其涉及完全阻止不期望的免疫应答。有效量还可涉及延迟不期望免疫应答的发生。有效量还可以是产生期望治疗终点或期望治疗结果的量。优选地,有效量导致对象中治疗性大分子特异性的不期望体液免疫应答降低。有效量还可在对象中产生针对抗原(例如治疗性大分子)的致耐受性免疫应答。在另一些实施方案中,有效量可涉及增强期望免疫应答(例如治疗终点或结果)的水平。可通过常规方法来监测上述任一项的实现。
在所提供之任一种组合物或方法的一些实施方案中,有效量为其中期望的免疫应答在对象中持续至少1周、至少2周、至少1个月、至少2个月、至少3个月、至少4个月、至少5个月或更久的量。在所提供之任一种组合物或方法的另一些实施方案中,有效量为在至少1周、至少2周、至少1个月、至少2个月、至少3个月、至少4个月、至少5个月或更久内产生可测量的期望免疫应答(例如体液免疫应答(例如,针对特定抗原的免疫应答)的可测量降低)的量。
当然,有效量将取决于所治疗的具体对象;病症、疾病或紊乱的严重程度;个体患者的参数,包括年龄、身体状况、身材和体重;治疗的持续时间;同时治疗(如果有的话)的性质;具体的施用途径以及在健康从业者的知识和经验范围内的类似因素。这些因素是本领域普通技术人员所众所周知的并且可仅用常规试验就可解决。一般优选使用最大剂量,即根据合理医疗判断的最高安全剂量。然而,本领域普通技术人员将理解,患者可由于医学原因、心理原因或实际上任何其他原因而坚持使用较低剂量或可耐受剂量。
一般来说,本发明组合物中免疫抑制剂和/或治疗性大分子的剂量指免疫抑制剂和/或治疗性大分子的量。或者,可基于提供期望量的免疫抑制剂的合成纳米载体的数量来施用所述剂量。
“抗原”意指B细胞抗原或T细胞抗原。“抗原的类型”意指共有相同或基本相同的抗原性特征的分子。在一些实施方案中,抗原可以是蛋白质、多肽、肽、脂蛋白、糖脂、多核苷酸、多糖或者包含在细胞中或在细胞内表达。在一些实施方案中,例如当抗原未经充分定义或表征的时,抗原可包含在细胞或组织制备物、细胞碎片、细胞外来体、条件化培养基等中。
“抗原特异性的”指由于该抗原或其部分的存在而产生的任何免疫应答或产生特异性地识别或结合该抗原之分子的任何免疫应答。在一些实施方案中,当抗原包含治疗性大分子时,抗原特异性可意指治疗性大分子特异性的。例如,当免疫应答是抗原特异性抗体产生(例如治疗性大分子特异性抗体产生)时,产生特异性地与该抗原(例如治疗性大分子)结合的抗体。作为另一个实例,当免疫应答是抗原特异性B细胞或CD4+ T细胞增殖和/或活性时,增殖和/或活性由识别单独或在与MHC分子、B细胞等复合的抗原或其部分引起。
“评估免疫应答”指对体外或体内免疫应答的水平、存在或不存在、降低、提高等的任何测量或确定。可对从对象获得的一份或更多份样品进行这样的测量或确定。这样的评估可用本文中提供的或本领域中另外已知的任何方法来进行。
“连接”或“连接的”或者“偶联”或“偶联的”(等)意指使一个实体(例如一个部分)与另一个在化学上缔合。在一些实施方案中,连接是共价的,意指连接发生在两个实体之间存在共价键的情况下。在非共价实施方案中,非共价连接由非共价相互作用介导,所述非共价相互作用包括但不限于:电荷相互作用、亲和性相互作用、金属配位、物理吸附、主体-客体相互作用、疏水性相互作用、TT堆积相互作用、氢键合相互作用、范德华相互作用、磁性相互作用、静电相互作用、偶极-偶极相互作用和/或其组合。在一些实施方案中,包封是连接的一种形式。在一些实施方案中,治疗性大分子和免疫抑制剂彼此未连接,意指治疗性大分子和免疫抑制剂未经历特异性地意图使彼此化学缔合的过程。在一些实施方案中,治疗性大分子和/或免疫抑制剂未与合成纳米载体连接,意指治疗性大分子(和/或免疫抑制剂)和合成纳米载体未经历特异性地旨在使彼此化学缔合的过程
“处于风险之中”的对象为保健人员认为其中具有患疾病、紊乱或病症的可能的对象或者为保健人员认为具有经历本文中提供的不期望体液免疫应答的可能并且将受益于所提供的组合物和方法的对象。在一些实施方案中,所述对象为预期具有针对治疗性大分子的不期望体液免疫应答的那些。
除非另有指出,否则本文中使用的术语“平均值”指算术平均值。
当应用于两种或更多种材料和/或药剂(在本文中也称为组分)时,“组合”旨在对其中两种或更多种材料/药剂相缔合的材料进行定义。可将组分单独标识,例如第一组分、第二组分、第三组分等。在该情况下的术语“组合的”和“组合”可作相应解释。
两种或更多种材料/药剂以组合相缔合可以是物理的或非物理的。物理缔合的组合材料/药剂的实例包括:
·包含混合的两种或更多种材料/药剂(例如在同一单位剂量内)的组合物(例如单一制剂);
·包含其中两种或更多种材料/药剂经化学/物理化学连接(例如通过交联、分子聚集或与常见的载剂部分结合)的材料的组合物;
·包含其中两种或更多种材料/药剂经化学/物理化学共包装(例如,布置在脂囊泡、颗粒(例如微米颗粒或纳米颗粒)或乳剂微滴之上或之中)的材料的组合物;
·其中两种或更多种材料/药剂经共包装或共存在(例如作为一组单位剂量的一部分)的药盒、药物包装或患者包装;
经非物理缔合的组合材料/药剂的实例包括:
·包含两种或更多种材料/药剂中的至少一种的材料(例如非单一制剂),附带有用于使该至少一种化合物/药剂临时缔合以形成这两种或更多种材料/药剂的物理缔合的说明书;
·包含两种或更多种材料/药剂中的至少一种的材料(例如非单一制剂),附带有用于使用这两种或更多种材料/药剂进行联合治疗的说明书;
·包含两种或更多种材料/药剂中的至少一种的材料,附带有用于向已施用(或正在施用)该两种或更多种材料/药剂中的其他材料/药剂的患者群施用的说明书;
·以特异性地适合与两种或更多种材料/药剂中的其他材料/药剂组合使用的量或形式包含这两种或更多种材料/药剂中的至少一种的材料。
本文中使用的术语“联合治疗”旨在对治疗进行定义,其包括使用两种或更多种材料/药剂的组合(如下文所定义的)。因此,本申请中提及的材料/药剂的“联合治疗”、“组合”和“组合使用”可指作为同一总治疗方案的一部分施用的材料/药剂。因此,两种或更多种材料/药剂各自的剂量学可有所不同:每一种可在相同时间或不同时间施用。因此,应当理解,可依次(例如之前或之后)或同时(在同一药物制剂(即一起)中或者在不同药物制剂(即独立地)中)施用组合中的材料/药剂。在同一制剂中时,同时是作为单一制剂;而在不同药物制剂中时,同时为非单一的。两种或更多种材料/药剂各自在联合治疗中的剂量学在施用途径方面也可有所不同。
“伴随”意指将两种或更多种材料/药剂以时间上相关、优选时间上足够相关以提供对免疫应答或生理学应答之调节的方式施用于对象,并且甚至更优选地将两种或更多种材料/药剂组合施用。在一些实施方案中,伴随施用可包括在指定时间内,优选在1个月内,更优选在1周内,仍更优选在1天内并且甚至更优选在1小时内施用两种或更多种材料/药剂。在一些实施方案中,可重复地伴随施用所述材料/药剂;即不止一次进行伴随施用,如实施例中可提供的。
“确定”意指确知实际关系。确定可以以多种方式实现,包括但不限于进行实验或者作出预测。例如,可如下确定免疫抑制剂或治疗性大分子的剂量:以测试剂量开始并使用已知的缩放(scaling)技术(例如异速缩放或等速缩放)来确定施用剂量。这还可用于确定如本文中提供的方案或施用方案。在另一个实施方案中,可通过在对象中测试多种剂量来确定所述剂量,即通过基于经验和指导数据进行直接试验。在一些实施方案中,“确定”包括“引起确定”。“引起确定”意指引起、促使、鼓励、帮助、诱导或指导实体确知实际关系或者与实体协同作用以使其确知实际关系;包括直接或间接地,或者明确或隐含地。
“给药”意指向对象施用药理学和/或免疫学活性材料或药理学和/或免疫学活性材料的组合。
“剂量”指在给定时间内向对象施用的药理学和/或免疫学活性材料的具体量。
“包封”意指将至少一部分物质封装在合成纳米载体内。在一些实施方案中,将物质全部封装在合成纳米载体内。在另一些实施方案中,大部分或全部的经包封物质不暴露于合成载体外部的局部环境。在另一些实施方案中,不超过50%、40%、30%、20%、10%或5%(重量/重量)暴露于局部环境。包封与吸附不同,吸附将大部分或全部的物质置于合成载体的表面上并使物质暴露于合成载体外部的局部环境。
“产生”意指自身直接或间接地引起作用例如发生免疫应答或生理学应答(例如,致耐受性免疫应答)。
“鉴定对象”为这样的任何活动或活动集合,其允许临床医生将对象识别为可受益于本文中提供的方法、组合物或药盒的对象。优选地,经鉴定的对象为需要来自如本文中提供的治疗性大分子的治疗益处和预期在其中发生不期望的体液免疫应答的对象。所述活动或活动集合可以是本身直接的或间接的。在本文中提供之任一种方法的一个实施方案中,所述方法还包括鉴定需要本文中提供的方法、组合物或药盒的对象。
“免疫抑制剂”意指这样的化合物,其导致APC具有免疫抑制作用(例如,致耐受性作用)或者T细胞或B细胞被抑制。免疫抑制作用一般指APC产生或表达降低、抑制或预防不期望的免疫应答或促进期望免疫应答(例如,调节性免疫应答)的细胞因子或其他因子。当APC在识别由该APC呈递之抗原的免疫细胞上获取免疫抑制功能(属于免疫抑制作用)时,认为该免疫抑制作用对所呈递的抗原具有特异性。不受任何特定理论的限制,认为:免疫抑制作用是免疫抑制剂被递送至APC的结果,优选在抗原存在下。在一个实施方案中,免疫抑制剂致使APC促进一个或更多个免疫效应细胞中的调节性表型。例如,调节性表型的特征可在于:抑制抗原特异性CD4+ T细胞或B细胞的产生、诱导、刺激或募集,抑制抗原特异性抗体的产生,Treg细胞(例如CD4+CD25高FoxP3+ Treg细胞)的产生、诱导、刺激或募集等。这可以是CD4+ T细胞或B细胞转化成调节性表型的结果。这也可以是其他免疫细胞(CD8+ T细胞、巨噬细胞和iNKT细胞)中诱导FoxP3的结果。在一个实施方案中,免疫抑制剂在其对抗原进行加工之后影响APC的应答。在另一个实施方案中,免疫抑制剂不干涉对抗原的加工。在另一个实施方案中,免疫抑制剂不是细胞凋亡信号传导分子。在另一个实施方案中,免疫抑制剂不是磷脂。
免疫抑制剂包括但不限于:他汀类;mTOR抑制剂,例如雷帕霉素或雷帕霉素类似物;TGF-β信号传导剂;TGF-β受体激动剂;组蛋白去乙酰化酶抑制剂,例如曲古抑菌素A;皮质类固醇;线粒体功能的抑制剂,例如鱼藤酮;P38抑制剂;NF-κB抑制剂,例如6Bio、地塞米松、TCPA-1、IKK VII;腺苷受体激动剂;前列腺素E2激动剂(prostaglandin E2 agonist,PGE2),例如米索前列醇;磷酸二酯酶抑制剂,例如磷酸二酯酶4抑制剂(phosphodiesterase4 inhibitor,PDE4),例如咯利普兰;蛋白酶体抑制剂;激酶抑制剂;G蛋白偶联受体激动剂;G蛋白偶联受体拮抗剂;糖皮质激素;类视黄醇;细胞因子抑制剂;细胞因子受体抑制剂;细胞因子受体激活剂;过氧化物酶体增殖物激活受体拮抗剂;过氧化物酶体增殖物激活受体激动剂;组蛋白去乙酰化酶抑制剂;钙调神经磷酸酶抑制剂;磷酸酶抑制剂;PI3KB抑制剂,例如TGX-221;自噬抑制剂,例如3-甲基腺嘌呤;芳基烃受体抑制剂;蛋白酶体抑制剂I(proteasome inhibitor I,PSI);以及氧化的ATP,例如P2X受体阻断剂。免疫抑制剂还包括:IDO、维生素D3、环孢素(例如环孢素A)、芳基烃受体抑制剂、白藜芦醇、硫唑嘌呤(azathiopurine,Aza)、6-巯基嘌呤(6-mercaptopurine,6-MP)、6-硫鸟嘌呤(6-thioguanine,6-TG)、FK506、萨菲菌素A(sanglifehrin A)、沙美特罗、麦考酚酸吗乙酯(mycophenolate mofetil,MMF)、阿司匹林以及其他COX抑制剂、尼氟灭酸、雌三醇、甲氨喋呤和雷公藤内酯(triptolide)。在一些实施方案中,免疫抑制剂可包括本文中提供的药剂中的任一种。
免疫抑制剂可以是直接提供对APC的免疫抑制作用或者其可以是间接提供免疫抑制作用的化合物(即,在施用后以某种方式进行加工)。因此,免疫抑制剂包括本文中提供的任何化合物的前药形式。
在本文中提供之任一种方法、组合物或药盒的一些实施方案中,本文中提供的免疫抑制剂与合成纳米载体连接。在一些优选实施方案中,免疫抑制剂是除构成合成纳米载体之结构的材料之外的组分。例如,在一个实施方案中,当合成纳米载体由一种或更多种聚合物构成时,免疫抑制剂为除所述一种或更多种聚合物之外并与其连接的化合物。作为另一个实例,在一个实施方案中,当合成纳米载体由一种或更多种脂质构成时,免疫抑制剂仍为除所述一种或更多种脂质之外并与其连接。在一些实施方案中,例如当合成纳米载体的材料也引起免疫抑制作用时,免疫抑制剂为除合成纳米载体的材料之外存在的引起免疫抑制作用的组分。
其他示例性的免疫抑制剂包括但不限于:小分子药物、天然产物、抗体(例如针对CD20、CD3、CD4的抗体)、基于生物制品的药物、基于碳水化合物的药物、纳米颗粒、脂质体、RNAi、反义核酸、适配体、甲氨蝶呤、NSAID;芬戈莫德;那他珠单抗;阿仑单抗;抗-CD3;他克莫司(FK506);细胞因子和生长因子,例如TGF-β和IL-10;等。另一些免疫抑制剂是本领域技术人员已知的并且本发明在此方面不受限制。
在本文中提供之任一种方法、组合物或药盒的一些实施方案中,免疫抑制剂是如纳米结晶形式的形式,由此免疫抑制剂的形式本身是颗粒或颗粒样。在一些实施方案中,这样的形式模拟病毒或其他外来病原体。很多药物是已被纳米化的并且本领域普通技术人员知晓用于产生这样的药物形式的合适方法。药物纳米晶体(例如纳米结晶雷帕霉素)是本领域普通技术人员已知的(Katteboinaa,等2009,International Journal of PharmTechResesarch;第1卷,第3期;第682-694页)。本文中使用的“药物纳米晶体”指不包含载体或基质材料的药物(例如,免疫抑制剂)的形式。在一些实施方案中,药物纳米晶体包含90%、95%、98%或99%或更多药物。用于产生药物纳米晶体的方法包括但不限于:研磨、高压均质化、沉淀、喷雾干燥、超临界溶液的迅速膨胀(rapid expansion of supercriticalsolution,RESS)、技术(Baxter Healthcare)和Nanocrystal TechnologyTM(Elan Corporation)。在一些实施方案中,表面活性剂或稳定剂可用于药物纳米晶体的空间或静电稳定性。在一些实施方案中,免疫抑制剂的纳米晶体或纳米结晶形式可用于提高免疫抑制剂(特别是不溶性或不稳定的免疫抑制剂)的溶解度、稳定性和/或生物利用度。在一些实施方案中,施用包含治疗性大分子和纳米结晶形式的免疫抑制剂的第一给药,并随后施用治疗性大分子的第二给药导致不期望的治疗性大分子特异性体液免疫应答的降低。
当与合成纳米载体连接时,免疫抑制剂的“载量”为基于整个合成纳米载体中材料的总干配方重量之与合成纳米载体连接的免疫抑制剂的量(重量/重量)。一般来说,将这样的载量计算为整个合成纳米载体群的平均值。在一个实施方案中,基于所有合成纳米载体的平均值,免疫抑制剂的载量为0.1%至99%。在另一个实施方案中,所述载量为0.1%至50%。在又一个实施方案中,免疫抑制剂的载量为0.1%至20%。在另一个实施方案中,免疫抑制剂的载量为0.1%至10%。在又一个实施方案中,免疫抑制剂的载量为1%至10%。在又一个实施方案中,免疫抑制剂的载量为7%至20%。在又一个实施方案中,基于整个合成纳米载体群的平均值,免疫抑制剂的载量为至少0.1%、至少0.2%、至少0.3%、至少0.4%、至少0.5%、至少0.6%、至少0.7%、至少0.8%、至少0.9%、至少1%、至少2%、至少3%、至少4%、至少5%、至少6%、至少至少7%、至少8%、至少9%、至少10%、至少11%、至少12%、至少13%、至少14%、至少15%、至少16%、至少17%、至少18%、至少19%或至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少95%、至少96%、至少97%、至少98%或至少99%。在又一个实施方案中,基于整个合成纳米载体群的平均值,免疫抑制剂的载量为0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%或20%。在上述实施方案的一些实施方案中,基于整个合成纳米载体群的平均值,免疫抑制剂的载量为不超过25%。在一些实施方案中,可如实施例中所述或者如本领域中另外已知的计算载量。
在一些实施方案中,当免疫抑制剂的形式本身是颗粒或颗粒样(例如纳米结晶免疫抑制剂)时,免疫抑制剂的载量为颗粒等中免疫抑制剂的量(重量/重量)。在这样的一些实施方案中,载量可接近97%、98%、99%或更多。
“合成纳米载体的最大尺寸”意指沿合成纳米载体之任意轴测量的该纳米载体的最大尺寸。“合成纳米载体的最小尺寸”意指沿合成纳米载体之任意轴测量的该合成纳米载体的最小尺寸。例如,对于球形合成纳米载体,合成纳米载体的最大尺寸和最小尺寸基本相同并且是其直径的尺寸。类似地,对于立方形合成纳米载体,合成纳米载体的最小尺寸是其高度、宽度或长度中的最小者,而合成纳米载体的最大尺寸是其高度、宽度或长度中的最大者。在一个实施方案中,基于样品中合成纳米载体的总数,该样品中至少75%,优选至少80%,更优选至少90%的合成纳米载体的最小尺寸等于或大于100nm。在一个实施方案中,基于样品中合成纳米载体的总数,该样品中至少75%,优选至少80%,更优选至少90%的合成纳米载体的最大尺寸等于或小于5μm。优选地,基于样品中合成纳米载体的总数,该样品中至少75%,优选至少80%,更优选至少90%的合成纳米载体的最小尺寸大于110nm,更优选大于120nm,更优选大于130nm,并且更优选还大于150nm。合成纳米载体的最大尺寸和最小尺寸的纵横比可根据实施方案而不同。例如,合成纳米载体的最大尺寸∶最小尺寸的纵横比可以是1∶1至1,000,000∶1,优选1∶1至100,000∶1,更优选1∶1至10,000∶1,更优选1∶1至1000∶1,仍更优选1∶1至100∶1并且还更优选1∶1至10∶1。优选地,基于样品中合成纳米载体的总数,该样品中至少75%,优选至少80%,更优选至少90%的合成纳米载体的最大尺寸等于或小于3μm,更优选等于或小于2μm,更优选等于或小于1μm,更优选等于或小于800nm,更优选等于或小于600nm,并且更优选还等于或小于500nm。在一些优选实施方案中,基于样品中合成纳米载体的总数,该样品中至少75%,优选至少80%,更优选至少90%的合成纳米载体的最小尺寸等于或大于100nm,更优选地等于或大于120nm,更优选等于或大于130nm,更优选等于或大于140nm,并且更优选还等于或大于150nm。在一些实施方案中,可如下获得合成纳米载体尺寸(例如,有效直径)的测量:使合成纳米载体混悬于液体介质(通常为水性介质)中并使用动态光散射(dynamic light scattering,DLS)(例如使用BrookhavenZetaPALS仪器)。例如,可将合成纳米载体的混悬液从水性缓冲液稀释到纯水中以获得约0.01mg/mL至0.1mg/mL的最终合成纳米载体混悬液浓度。可在用于DLS分析的合适比色皿内直接制备经稀释的混悬液或者可将经稀释的混悬液转移至用于DLS分析的合适比色皿。然后,可将比色皿放置在DLS中,允许平衡至受控温度,随后基于针对介质之黏度和样品之折射指数的合适输入,扫描足够的时间以获取稳定且可重现的分布。然后,报道有效直径或分布的平均值。确定高纵横比或非球形合成纳米载体的有效尺寸可需要放大技术(例如电子显微术)以获得更准确的测量。合成纳米载体的“尺寸”或“大小”或“直径”意指例如使用动态光散射获得的颗粒大小分布的平均值。
“非甲氧基封端的聚合物”意指至少一个末端以不同于甲氧基的部分结尾的聚合物。在一些实施方案中,所述聚合物具有至少两个以不同于甲氧基的部分结尾的末端。在另一些实施方案中,所述聚合物没有以甲氧基结尾的末端。“非甲氧基封端的普朗尼克聚合物”意指不同于两端都具有甲氧基的线性普朗尼克聚合物的聚合物。本文中提供的聚合物纳米颗粒可包含非甲氧基封端的聚合物或非甲氧基封端的普朗尼克聚合物。
“可药用赋形剂”或“可药用载体”意指与药理学活性材料一起使用以配制组合物的药理学惰性材料。可药用赋形剂包括本领域中已知的多种材料,包括但不限于糖类(例如葡萄糖、乳糖等)、防腐剂(例如抗微生物剂)、重构助剂(reconstitution aid)、着色剂、盐水(例如磷酸缓冲盐水)和缓冲剂。
“提供”意指个体进行的供给用于实施本发明的所需项目或项目组或方法的活动或活动集合。所述活动或活动集合可本身直接采取或者间接采取。
“提供对象”为这样的任何活动或活动集合,其促使临床医生与对象接触并向其施用本文中提供的组合物或者对其进行本文中提供的方法。优选地,所述对象是需要治疗性大分子施用和针对它的抗原特异性免疫耐受的对象。所述活动或活动集合可本身直接采取或者间接采取。本文中提供的任一种方法的一个实施方案中,所述方法还包括提供对象。
“对象”意指动物,包括温血哺乳动物,例如人和灵长类动物;禽类;驯养的家养或农场动物,例如猫、狗、绵羊、山羊、牛、马和猪;实验室动物,例如小鼠、大鼠和豚鼠;鱼;爬行动物;动物园动物和野生动物;等。
“合成纳米载体”意指不存在于自然界中并且至少一个维度的尺寸小于或等于5微米的离散物体。白蛋白纳米颗粒一般作为合成纳米载体包括在内,然而在某些实施方案中,合成纳米载体不包括白蛋白纳米颗粒。在一些实施方案中,合成纳米载体不包含壳聚糖。在另一些实施方案中,合成纳米载体不是基于脂质的纳米颗粒。在另一些实施方案中,合成纳米载体不包含磷脂。
合成纳米载体可以是,但不限于以下中的一种或多种:基于脂质的纳米颗粒(在本文中也称为脂质纳米颗粒,即构成其结构的大部分材料为脂质的纳米颗粒)、聚合物纳米颗粒、金属纳米颗粒、基于表面活性剂的乳剂、树状聚体、巴基球、纳米线、病毒样颗粒(即,主要由非感染性或具有低感染性的病毒结构蛋白构成的颗粒)、基于肽或蛋白质的颗粒(在本文中也称为蛋白质颗粒,即,构成其结构的大部分材料是肽或蛋白质的颗粒)(例如白蛋白纳米颗粒)和/或使用纳米材料之组合开发的纳米颗粒(例如脂质-聚合物纳米颗粒)。合成纳米载体可以是多种不同的形状,包括但不限于球形、立方形、棱锥形、长方形、圆柱形、环形等。根据本发明的合成纳米载体包括一个或更多个表面。适用于实施本发明的示例性合成纳米载体包括:(1)Gref等的美国专利5,543,158中公开的生物可降解纳米颗粒,(2)Saltzman等的公开的美国专利申请20060002852中的聚合物纳米颗粒,(3)DeSimone等的公开的美国专利申请20090028910中以平版印刷方式构建的纳米颗粒,(4)von Andrian等的WO 2009/051837的公开内容,(5)Penades等的公开的美国专利申请2008/0145441中公开的纳米颗粒,(6)de los Rios等的公开的美国专利申请20090226525中公开的蛋白质纳米颗粒,(7)Sebbel等的公开的美国专利申请20060222652中公开的病毒样颗粒,(8)Bachmann等的公开的美国专利申请20060251677中公开的核酸连接的病毒样颗粒,(9)WO2010047839A1或WO2009106999A2中公开的病毒样颗粒,(10)P.Paolicelli等,“Surface-modified PLGA-based Nanoparticles that can Efficiently Associate and Deliver Virus-likeParticles”Nanomedicine.5(6):843-853(2010)中公开的经纳米沉淀的纳米颗粒,(11)美国公开2002/0086049中公开的凋亡细胞、凋亡体或者合成或半合成模拟物,或者(12)Look等,Nanogel-based delivery of mycophenolic acid ameliorates systemic lupuserythematosus in mice”J.Clinical Investigation 123(4):1741-1749(2013)中的那些。在一些实施方案中,合成纳米载体的纵横比可大于1∶1、1∶1.2、1∶1.5、1∶2、1∶3、1∶5、1∶7,或大于1∶10。
最小尺寸等于或小于约100nm、优选等于或小于100nm之根据本发明的合成纳米载体不包含具有激活补体的羟基的表面,或者作为替代地包含基本由不是激活补体之羟基的部分组成的表面。在一个优选实施方案中,最小尺寸等于或小于约100nm、优选等于或小于100nm之根据本发明的合成纳米载体不包含显著激活补体的表面,或者作为替代地包含基本由不显著激活补体的部分组成的表面。在一个更优选的实施方案中,最小尺寸等于或小于约100nm、优选等于或小于100nm之根据本发明的合成纳米载体不包含激活补体的表面,或者作为替代地包含基本由不激活补体的部分组成的表面。在一些实施方案中,合成纳米载体不包括病毒样颗粒。在一些实施方案中,合成纳米载体的纵横比可大于1∶1、1∶1.2、1∶1.5、1∶2、1∶3、1∶5、1∶7,或大于1∶10。
“治疗性大分子”指可向对象施用并且具有治疗效果的任何蛋白质、碳水化合物、脂质或核酸。在一些实施方案中,向对象施用治疗性大分子可引起不期望的体液免疫应答,包括抗治疗性大分子特异性抗体的产生。如本文中所述,施用如本文中提供的治疗性大分子与免疫抑制剂可降低不期望的体液免疫应答和/或增强该治疗性大分子的治疗有效性。在一些实施方案中,治疗性大分子可以是治疗性多核苷酸或治疗性蛋白质。
“治疗性多核苷酸”意指可向对象施用并且具有治疗效果的任何多核苷酸或基于多核苷酸的治疗。这样的治疗包括基因沉默。这样的治疗的实例在本领域中是已知的并且包括但不限于裸RNA(包括信使RNA、经修饰的信使RNA以及RNAi的形式)。本文中的其他部分还提供了其他治疗性多核苷酸的实例。治疗性多核苷酸可在细胞中产生、在细胞上产生或者由细胞产生,并且还可使用无细胞体外方法获得或者由完全体外合成方法获得。因此,对象包括需要前述任何治疗性多核苷酸进行治疗的任何对象。这样的对象包括将接受前述任何治疗性多核苷酸的那些。
“治疗性蛋白质”意指可向对象施用并且具有治疗效果的任何蛋白质或基于蛋白质的治疗。这样的治疗包括蛋白质替代治疗或蛋白质补充治疗。这样的治疗还包括施用外源或外来蛋白质、抗体治疗和细胞治疗或基于细胞的治疗。治疗性蛋白质包括但不限于酶、酶辅因子、激素、凝血因子、细胞因子、生长因子、单克隆抗体、抗体-药物缀合物和多克隆抗体。本文中的其他部分还提供了其他治疗性蛋白质的实例。治疗性蛋白质可在细胞中产生、在细胞上产生或者由细胞产生,并且可从这样的细胞获得或者以这样的细胞的形式施用。在一些实施方案中,治疗性蛋白质在哺乳动物细胞、昆虫细胞、酵母细胞、细菌细胞、植物细胞、转基因动物细胞、转基因植物细胞等中产生、在其上产生或者由其产生。治疗性蛋白质可在这样的细胞中重组产生。治疗性蛋白质可在经病毒转化的细胞中产生、在其上产生或者由其产生。因此,对象可包括需要前述任何治疗性蛋白质进行治疗的任何对象。这样的对象包括将接受前述任何治疗性蛋白质的那些。
“治疗性大分子APC可呈递抗原”意指与治疗性大分子相关的抗原(即,治疗性大分子或其可产生针对该治疗性大分子的免疫应答(例如,抗治疗性大分子特异性抗体的产生)的片段)。一般来说,治疗性大分子抗原呈递细胞(APC)可呈递抗原可被呈递为被免疫系统(例如,免疫系统中的细胞,例如通过抗原呈递细胞呈递的细胞,包括但不限于树突细胞、B细胞或巨噬细胞)识别。治疗性大分子APC可呈递抗原可被呈递为被例如T细胞识别。这样的抗原可通过呈递与I类或II类主要组织相容性复合物分子(maior histocompatabilitycomplex molecule,MHC)结合之抗原的表位而被T细胞识别并触发T细胞中的免疫应答。治疗性大分子APC可呈递抗原一般包括蛋白质、多肽、肽、多核苷酸、脂蛋白或者包含在细胞中或者在细胞内表达、细胞上表达或由细胞表达。在一些实施方案中,治疗性大分子抗原包含MHC I类限制性表位和/或MHC II类限制性表位和/或B细胞表位。优选地,用本文中提供的方法、组合物或药盒引起治疗性大分子特异性的一种或更多种致耐受性免疫应答。在一些实施方案中,合成纳米载体群不包含添加的治疗性大分子APC可呈递抗原,意指在合成纳米载体制备期间未有意地向其中添加显著量的治疗性大分子APC可呈递抗原。
“不期望的体液免疫应答”指这样的任何不期望体液免疫应答,其是由暴露于抗原引起的、促进或加重本文中提供疾病、紊乱或病症(或其症状),或者其为本文中提供的疾病、紊乱或病症的症状。这样的免疫应答一般对对象的健康具有不良影响或者为对对象之健康的不良影响的症状。不期望的体液免疫应答包括抗原特异性抗体产生、抗原特异性B细胞增殖和/或活性或抗原特异性CD4+ T细胞增殖和/或活性。一般来说,这些不期望的免疫应答是治疗性大分子特异性的并且抵消施用所述治疗性大分子所期望的有益效果。
C.可用于实施所述方法的组合物
本文中提供了组合可降低不期望的体液免疫应答的第一和第二给药。一般来说,这样的第一和第二给药还可导致治疗性大分子的效力提高。因此,本文中提供的方法及相关组合物可用于需要用治疗性大分子进行治疗的对象。特别地,第一给药包含免疫抑制剂(在一些实施方案中,与合成纳米载体连接)与未与合成纳米载体连接之治疗性大分子的组合,并且第二给药包含也未与合成纳米载体连接的治疗性大分子。
多种合成纳米载体可用于与第一给药中的免疫抑制剂连接。在一些实施方案中,合成纳米载体为球体或球状体。在一些实施方案中,合成纳米载体是平的或板状的。在一些实施方案中,合成纳米载体为立方体物或者是立方体的。在一些实施方案中,合成纳米载体为卵形或椭圆形。在一些实施方案中,合成纳米载体为圆柱体、圆锥体或棱锥体。
在一些实施方案中,期望使用在尺寸或形状方面相对均一的合成纳米载体群使得每个合成纳米载体具有类似的特性。例如,基于合成纳米载体的总数,至少80%、至少90%或至少95%的合成纳米载体的最小尺寸或最大尺寸可落入合成纳米载体之平均直径或平均尺寸的5%、10%或20%内。
合成纳米载体可以是实心的或中空的并且可包含一个或更多个层。在一些实施方案中,相对于其他层,每个层均具有独特的组成和独特的特性。仅为了给出一个实例,合成纳米载体可具有芯/壳结构,其中芯为一个层(例如聚合物芯)而壳为第二层(例如脂质双层或单层)。合成纳米载体可包括多个不同的层。
在一些实施方案中,合成纳米载体可任选地包含一种或更多种脂质。在一些实施方案中,合成纳米载体可包含脂质体。在一些实施方案中,合成纳米载体可包含脂质双层。在一些实施方案中,合成纳米载体可包含脂质单层。在一些实施方案中,合成纳米载体可包括胶束。在一些实施方案中,合成纳米载体可包含由脂质层(例如,脂质双层、脂质单层等)包围的包含聚合物基质的芯。在一些实施方案中,合成纳米载体可包含由脂质层(例如,脂质双层、脂质单层等)包围的非聚合物芯(例如,金属颗粒、量子点、陶瓷颗粒、骨颗粒、病毒颗粒、蛋白质、核酸、碳水化合物等)。
在另一些实施方案中,合成纳米载体可包含金属颗粒、量子点、陶瓷颗粒等。在一些实施方案中,非聚合物合成纳米载体是非聚合物组分的聚集体,例如金属原子(例如,金原子)的聚集体。
在一些实施方案中,合成纳米载体可任选地包含一种或更多种两亲性实体。在一些实施方案中,两亲性实体可促进产生稳定性提高、均匀性提高或黏度提高的合成纳米载体。在一些实施方案中,两亲性实体可与脂质膜(例如,脂质双层、脂质单层等)的内表面相缔合。本领域中已知的很多两亲性实体均适用于制备根据本发明的合成纳米载体。这样的两亲性实体包括但不限于:磷酸甘油酯;磷脂酰胆碱;二棕榈酰磷脂酰胆碱(DPPC);二油烯基磷脂酰乙醇胺(DOPE);二油烯氧基丙基三乙铵(DOTMA);二油酰磷脂酰胆碱;胆固醇;胆固醇酯;二酰甘油;琥珀酸二酰甘油酯;二磷脂酰甘油(DPPG);十六烷醇(hexanedecanol);脂肪醇,例如聚乙二醇(PEG);聚氧乙烯-9-月桂基醚;表面活性脂肪酸,例如棕榈酸或油酸;脂肪酸;脂肪酸单甘油酯;脂肪酸二甘油酯;脂肪酸酰胺;去水山梨糖醇三油酸酯甘氨胆酸盐;去水山梨糖醇单月桂酸酯聚山梨醇酯20聚山梨醇酯60聚山梨醇酯65聚山梨醇酯80聚山梨醇酯85聚氧乙烯单硬脂酸酯;表面活性素;泊洛沙姆;去水山梨糖醇脂肪酸酯,例如去水山梨糖醇三油酸酯;卵磷脂;溶血卵磷脂;磷脂酰丝氨酸;磷脂酰肌醇;鞘磷脂;磷脂酰乙醇胺(脑磷脂);心磷脂;磷脂酸;脑苷脂;磷酸二鲸蜡酯;二棕榈酰磷脂酰甘油;硬脂酰胺;十二烷胺;十六烷胺;乙酰棕榈酸酯;蓖麻醇酸甘油酯;硬脂酸十六烷酯;肉豆蔻酸异丙酯;泰洛沙泊;聚(乙二醇)5000-磷脂酰乙醇胺;聚(乙二醇)400-单硬脂酸酯;磷脂;具有高表面活性剂特性的合成和/或天然洗涤剂;脱氧胆酸盐;环糊精;离液盐;离子配对剂;及其组合。两亲性实体组分可以是不同两亲性实体的混合物。本领域技术人员将认识到:这是具有表面活性剂活性之物质的示例性的非全面性列表。任何两亲性实体均可用于产生根据本发明使用的合成纳米载体。
在一些实施方案中,合成纳米载体可任选地包含一种或更多种碳水化合物。碳水化合物可以是天然的或合成的。碳水化合物可以是衍生化的天然碳水化合物。在某些实施方案中,碳水化合物包含单糖或二糖,包括但不限于:葡萄糖、果糖、半乳糖、核糖、乳糖、蔗糖、麦芽糖、海藻糖、纤维二糖、甘露糖、木糖、阿拉伯糖、葡萄糖醛酸、半乳糖醛酸、甘露糖醛酸、葡糖胺、半乳糖胺和神经氨酸。在某些实施方案中,碳水化合物为多糖,包括但不限于:普鲁兰多糖、纤维素、微晶纤维素、羟丙基甲基纤维素(HPMC)、羟基纤维素(HC)、甲基纤维素(MC)、葡聚糖、环葡聚糖、糖原、羟乙基淀粉、角叉菜胶、糖苷配糖基(glycon)、直链淀粉、壳聚糖、N,O-羧甲基壳聚糖、藻胶和藻酸、淀粉、甲壳质、菊粉、魔芋、葡甘露聚糖、石耳素(pustulan)、肝素、透明质酸、凝胶多糖(curdlan)和黄原胶。在一些实施方案中,合成纳米载体不包含(或者特别排除)碳水化合物,例如多糖。在某些实施方案中,碳水化合物可包含碳水化合物衍生物,例如糖醇,包括但不限于甘露糖醇、山梨糖醇、木糖醇、赤藓糖醇、麦芽糖醇和乳糖醇。
在一些实施方案中,合成纳米载体可包含一种或更多种聚合物。在一些实施方案中,合成纳米载体可包含一种或更多种这样的聚合物,其为非甲氧基封端的普朗尼克聚合物。在一些实施方案中,构成合成纳米载体的至少1%、2%、3%、4%、5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%或99%(重量/重量)聚合物为非甲氧基封端的普朗尼克聚合物。在一些实施方案中,构成合成纳米载体的所有聚合物均为非甲氧基封端的普朗尼克聚合物。在一些实施方案中,合成纳米载体包含一种或更多种这样的聚合物,其为非甲氧基封端的聚合物。在一些实施方案中,构成合成纳米载体的至少1%、2%、3%、4%、5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%或99%(重量/重量)聚合物为非甲氧基封端的聚合物。在一些实施方案中,构成合成纳米载体的所有聚合物均为非甲氧基封端的聚合物。在一些实施方案中,合成纳米载体包含一种或更多种不含普朗尼克聚合物的聚合物。在一些实施方案中,构成合成纳米载体的至少1%、2%、3%、4%、5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%或99%(重量/重量)聚合物不包含普朗尼克聚合物。在一些实施方案中,构成合成纳米载体的所有聚合物均不包含普朗尼克聚合物。在一些实施方案中,这样的聚合物可由包被层(例如,脂质体、脂质单层、胶束等)包围。在一些实施方案中,合成纳米载体中的多种组分可与聚合物连接。
可通过多种方法中的任一种来使免疫抑制剂与合成纳米载体连接。一般来说,连接可以是免疫抑制剂与合成纳米载体之间键合的结果。这种键合可导致免疫抑制剂与合成纳米载体的表面连接和/或包含(包封)在合成纳米载体中。然而,在一些实施方案中,由于合成纳米载体的结构的原因,免疫抑制剂被合成纳米载体包封而不是与合成纳米载体键合。在一些优选实施方案中,合成纳米载体包含本文中提供的聚合物,并且免疫抑制剂与聚合物连接。
当由于免疫抑制剂与合成纳米载体之间的键合而发生连接时,所述连接可经由偶联部分发生。偶联部分可以是免疫抑制剂通过它与合成纳米载体键合的任何部分。这样的部分包括共价键(例如酰胺键或酯键)以及使免疫抑制剂与合成纳米载体(共价或非共价)键合的独立分子。这样的分子包含接头或聚合物或其单元。例如,偶联部分可包含与免疫抑制剂静电结合的带电聚合物。作为另一个实例,偶联部分可包含与免疫抑制剂共价键合的聚合物或其单元。
在一些优选实施方案中,合成纳米载体包含本文中提供的聚合物。这些合成纳米载体可以是完全聚合物的或者其可以是聚合物与其他材料的混合物。
在一些实施方案中,合成纳米载体中的聚合物缔合以形成聚合物基质。在这些实施方案中的一些中,组分如免疫抑制剂可与聚合物基质中的一种或更多种聚合物共价缔合。在一些实施方案中,共价缔合由接头介导。在一些实施方案中,组分可与聚合物基质中的一种或更多种聚合物非共价缔合。例如,在一些实施方案中,组分可包封在聚合物基质内、被聚合物基质包围和/或分散在聚合物基质中。作为替代或补充,组分与聚合物基质中的一种或更多种聚合物可通过疏水性相互作用、电荷相互作用、范德华力等缔合。多种聚合物以及用于由其形成聚合物基质的方法均是常规已知的。
聚合物可以是天然聚合物或非天然(合成)聚合物。聚合物可以是含有两个或更多个单体的均聚物或共聚物。就序列而言,共聚物可以是随机的、嵌段的,或者包含随机序列和嵌段序列的组合。通常来说,根据本发明的聚合物是有机聚合物。
在一些实施方案中,聚合物包含聚酯、聚碳酸酯、聚酰胺或聚醚或其单元。在另一些实施方案中,聚合物包含聚(乙二醇)(PEG)、聚丙二醇、聚(乳酸)、聚(乙醇酸)、聚乳酸-乙醇酸共聚物或聚己内酯或其单元。在一些实施方案中,优选地,聚合物是生物可降解的。因此,在这些实施方案中,优选地,如果聚合物包含聚醚(例如聚(乙二醇)、聚丙二醇或其单元),则该聚合物包含聚醚和生物可降解聚合物的嵌段共聚物,使得该聚合物是生物可降解的。在另一些实施方案中,聚合物不仅包含聚醚或其单元,例如聚(乙二醇)或聚丙二醇或其单元。
适用于本发明中的聚合物的其他实例包括但不限于:聚乙烯、聚碳酸酯(例如聚(1,3-二烷-2酮))、聚酐(例如聚(癸二酐))、聚丙基富马酸酯、聚酰胺(例如聚己内酰胺)、聚缩醛、聚醚、聚酯(例如,聚丙交酯、聚乙交酯、聚丙交酯-乙交酯共聚物、聚己内酯、聚羟基酸(例如聚(β-羟基烷酸酯)))、聚(原酸酯)、聚氰基丙烯酸酯、聚乙烯醇、聚氨酯、聚磷腈、聚丙烯酸酯、聚甲基丙烯酸酯、聚脲、聚苯乙烯以及聚胺、聚赖氨酸、聚赖氨酸-PEG共聚物和聚(乙烯亚胺)、聚(乙烯亚胺)-PEG共聚物。
在一些实施方案中,根据本发明的聚合物包括已由美国食品药品管理局(U.S.Food and Drug Administration,FDA)根据21C.ER.§177.2600批准用于人的聚合物,包括但不限于:聚酯(例如,聚乳酸、聚乳酸-乙醇酸共聚物、聚己内酯、聚戊内酯、聚(1,3-二烷-2酮));聚酐(例如,聚(癸二酐));聚醚(例如,聚乙二醇);聚氨酯;聚甲基丙烯酸酯;聚丙烯酸酯;和聚氰基丙烯酸酯。
在一些实施方案中,聚合物可以是亲水性的。例如,聚合物可包含阴离子基团(例如,磷酸根基团、硫酸根基团、羧酸根基团);阳离子基团(例如,季胺基团);或极性基团(例如,羟基、巯基、胺基)。在一些实施方案中,包含亲水性聚合物基质的合成纳米载体在合成纳米载体内产生亲水性环境。在一些实施方案中,聚合物可以是疏水性的。在一些实施方案中,包含疏水性聚合物基质的合成纳米载体在合成纳米载体内产生疏水性环境。对聚合物之亲水性或疏水性的选择可影响合成纳米载体中掺入(例如连接)的材料的性质。
在一些实施方案中,可用一个或更多个部分和/或官能团对聚合物进行修饰。根据本发明可使用多种部分或官能团。在一些实施方案中,可用聚乙二醇(PEG)、碳水化合物和/或由多糖衍生的无环聚缩醛(Papisov,2001,ACS Symposium Series,786:301)对聚合物进行修饰。某些实施方案可使用Gref等的美国专利No.5543158或Von Andrian等的WO公开WO2009/051837的一般性教导来进行。
在一些实施方案中,可用脂质或脂肪酸基团来对聚合物进行修饰。在一些实施方案中,脂肪酸基团可以是以下中的一种或更多种:丁酸、己酸、辛酸、癸酸、月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、花生酸、山嵛酸或二十四烷酸。在一些实施方案中,脂肪酸基团可以是以下中的一种或更多种:棕榈油酸、油酸、异油酸、亚油酸、α-亚油酸、γ-亚油酸、花生四烯酸、鳕油酸、花生四烯酸、二十碳五烯酸、二十二碳六烯酸或芥酸。
在一些实施方案中,聚合物可以是聚酯,包括含有乳酸和乙醇酸单元的共聚物,例如聚乳酸-乙醇酸共聚物和聚丙交酯-乙交酯共聚物,在本文中将其统称为“PLGA”;以及含有乙醇酸单元的均聚物(在本文中称为“PGA”)和含有乳酸单元的均聚物,例如聚-L-乳酸、聚-D-乳酸、聚-D,L-乳酸、聚-L-丙交酯、聚-D-丙交酯和聚-D,L-丙交酯(在本文中统称为“PLA”)。在一些实施方案中,示例性的聚酯包括例如:聚羟基酸;PEG共聚物及丙交酯和乙交酯的共聚物(例如,PLA-PEG共聚物、PGA-PEG共聚物、PLGA-PEG共聚物,及其衍生物。在一些实施方案中,聚酯包括例如聚(己内酯)、聚(己内酯)-PEG共聚物、聚L-丙交酯-L-赖氨酸共聚物、聚(丝氨酸酯)、聚(4-羟基-L-脯氨酸酯)、聚[α-(4-氨基丁基)-L-乙醇酸],及其衍生物。
在一些实施方案中,聚合物可以是PLGA。PLGA是乳酸和乙醇酸的生物相容性的生物可降解共聚物,并且多种PLGA形式通过乳酸∶乙醇酸之比来表征。乳酸可以是L-乳酸、D-乳酸或D,L-乳酸。可通过改变乳酸∶乙醇酸之比来调节PLGA的降解速率。在一些实施方案中,根据本发明使用的PLGA的特征在于:乳酸∶乙醇酸之比为约85∶15、约75∶25、约60∶40、约50∶50、约40∶60、约25∶75或约15∶85。
在一些实施方案中,聚合物可以是一种或更多种丙烯酸类聚合物。在某些实施方案中,丙烯酸类聚合物包括例如:丙烯酸和甲基丙烯酸共聚物、甲基丙烯酸甲酯共聚物、甲基丙烯酸乙氧基乙酯、甲基丙烯酸氰基乙酯、甲基丙烯酸氨基烷酯共聚物、聚(丙烯酸)、聚(甲基丙烯酸)、甲基丙烯酸烷基酰胺共聚物、聚(甲基丙烯酸甲酯)、聚(甲基丙烯酸酐)、甲基丙烯酸甲酯、聚甲基丙烯酸酯、聚(甲基丙烯酸甲酯)共聚物、聚丙烯酰胺、甲基丙烯酸氨基烷酯共聚物、甲基丙烯酸缩水甘油酯共聚物、聚氰基丙烯酸酯以及包含前述聚合物中一种或更多种的组合。丙烯酸类聚合物可包括丙烯酸酯和甲基丙烯酸酯的具有低含量季铵基团的完全聚合的共聚物。
在一些实施方案中,聚合物可以是阳离子聚合物。一般来说,阳离子聚合物能够缩合和/或保护核酸的带负电链。含胺聚合物例如聚(赖氨酸)(Zauner等,1998,Adv.DrugDel.Rev.,30:97;和Kabanov等,1995,Bioconjugate Chem.,6:7)、聚(乙烯亚胺)(PEI;Boussif等,1995,Proc.Natl.Acad.Sci.,USA,1995,92:7297)和聚(酰胺胺)树状聚体(Kukowska-Latallo等,1996,Proc.Natl.Acad.Sci.,USA,93:4897;Tang等,1996,Bioconjugate Chem.,7:703;和Haensler等,1993,Bioconjugate Chem.,4:372)在生理pH下带正电并且与核酸形成离子对。在一些实施方案中,合成纳米载体可不包含(或者可排除)阳离子聚合物。
在一些实施方案中,聚合物可以是携带阳离子侧链的可降解聚酯(Putnam等,1999,Macromolecules,32:3658;Barrera等,1993,J.Am.Chem.Soc.,115:11010;Kwon等,1989,Macromolecules,22:3250;Lim等,1999,J.Am.Chem.Soc.,121:5633;和Zhou等,1990,Macromolecules,23:3399)。这些聚酯的实例包括聚L-丙交酯-L-赖氨酸共聚物(Barrera等,1993,J.Am.Chem.Soc.,115:11010)、聚(丝氨酸酯)(Zhou等,1990,Macromolecules,23:3399)、聚(4-羟基-L-脯氨酸酯)(Putnam等,1999,Macromolecules,32:3658;和Lim等,1999,J.Am.Chem.Soc.,121:5633)和聚(4-羟基-L-脯氨酸酯)(Putnam等,1999,Macromolecules,32:3658;和Lim等,1999,J.Am.Chem.Soc.,121:5633)。
这些和其他聚合物的特性及其制备方法在本领域中是公知的(参见,例如,美国专利6,123,727;5,804,178;5,770,417;5,736,372;5,716,404;6,095,148;5,837,752;5,902,599;5,696,175;5,514,378;5,512,600;5,399,665;5,019,379;5,010,167;4,806,621;4,638,045;和4,946,929;Wang等,2001,J.Am.Chem.Soc.,123:9480;Lim等.,2001,J.Am.Chem.Soc.,123:2460;Langer,2000,Acc.Chem.Res.,33:94;Langer,1999,J.Control.Release,62:7;和Uhrich等,1999,Chem.Rev.,99:3181)。更一般地,用于合成某些合适聚合物的多种方法在以下中进行了描述:Concise Encyclopedia of PolymerScience and Polymeric Amines and Ammonium Salts,由Goethals编辑,PergamonPress,1980;Principles of Polymerization,Odian,John Wiley&Sons,第四版,2004;Contemporary Polymer Chemistry,Allcock等,Prentice-Hall,1981;Deming等,1997,Nature,390:386;以及美国专利6,506,577、6,632,922、6,686,446和6,818,732。
在一些实施方案中,聚合物可以是直链聚合物或支链聚合物。在一些实施方案中,聚合物可以是树状聚体。在一些实施方案中,聚合物可彼此基本交联。在一些实施方案中,聚合物可基本无交联。在一些实施方案中,可根据本发明在不经历交联步骤的情况下使用聚合物。还应当理解的是,合成纳米载体可包含前述及其他聚合物的嵌段共聚物、接枝共聚物、共混物、混合物和/或加合物。本领域技术人员将认识到,本文中所列举的聚合物代表可根据本发明使用之聚合物的示例性的非全面性列表。
在一些实施方案中,合成纳米载体不包含聚合物组分。在一些实施方案中,合成纳米载体可包含金属颗粒、量子点、陶瓷颗粒等。在一些实施方案中,非聚合物合成纳米载体为非聚合物组分的聚集体,例如金属原子(例如,金原子)的聚集体。
根据本发明的第一和/或第二给药可包含可药用赋形剂,例如防腐剂、缓冲剂、盐水和磷酸缓冲盐水。所述组合物可使用常规的药物制备和配合技术制成以实现可用的剂型。在一些实施方案中,将给药的组合物与防腐剂一起混悬于无菌盐水溶液中以用于注射。在一些实施方案中,将合成纳米载体与防腐剂一起混悬于无菌盐水溶液中以用于注射。
在一些实施方案中,当制备用于与免疫抑制剂一起使用的合成纳米载体时,用于使组分与合成纳米载体连接方法是可用的。如果组分是小分子,有利地可在组装合成纳米载体之前使该组分与聚合物连接。在一些实施方案中,还有利的是,可制备具有表面基团的合成纳米载体,其可用于通过使用这些表面基团来使组分与合成纳米载体连接,而非使组分与聚合物连接并然后在构建合成纳米载体中使用该聚合物缀合物。
在某些实施方案中,连接可以是共价接头。在一些实施方案中,根据本发明的组分可与外表面经由1,2,3-三唑接头共价连接,所述接头通过纳米载体之表面上的叠氮基与含有炔基之组分的1,3-偶极环加成反应形成或者通过纳米载体之表面上的炔与含有叠氮基之组分的1,3-偶极环加成反应形成。优选在Cu(I)催化剂以及合适Cu(I)配体和还原剂存在下进行这样的环加成反应以将Cu(II)化合物还原成催化活性的Cu(I)化合物。还可将这种Cu(I)催化的叠氮化物-炔环加成(CuAAC)称为点击反应。
另外,共价连接可包含共价接头,其包括酰胺接头、二硫接头、硫醚接头、腙接头、酰肼接头、亚胺或肟接头、脲或硫脲接头、脒接头、胺接头和磺酰胺接头。
酰胺接头通过一种组分(例如免疫抑制剂)上的胺与第二组分(例如纳米载体)的羧酸基团之间的酰胺键形成。接头中的酰胺键可使用经适当保护的氨基酸和活化羧酸(例如N-羟基琥珀酰亚胺活化的酯)利用任何常规的酰胺键形成反应形成。
二硫接头通过在形式为例如RI-S-S-R2的两个硫原子之间形成二硫(S-S)键构成。二硫键可通过使含有巯基/硫醇基(-SH)的组分与聚合物或纳米载体上的另一个活化巯基进行巯基交换形成,或者通过使含有巯基/硫醇基的纳米载体与含有活化巯基的组分进行巯基交换形成。
三唑接头,特别是其中R1和R2可以是任何化学实体之形式的1,2,3-三唑,通过与第一组分(例如纳米载体)连接之叠氮化物和与第二组分(例如免疫抑制剂)连接之末端炔的1,3-偶极环加成反应形成。在存在或无催化剂,优选Cu(I)催化剂的情况下进行1,3-偶极环加成反应,其通过1,2,3-三唑功能将两种组分连接。Sharpless等,Angew.Chem.Int.第41(14)版,2596,(2002)和Meldal,等,Chem.Rev.,2008,108(8),2952-3015对这一化学进行了详细描述,并且通常将其称为“点击”反应或CuAAC。
在一些实施方案中,制备聚合物链末端包含叠氮化合物或炔基团的聚合物。然后,使用这种聚合物以使得多个炔或叠氮化物基团位于合成纳米载体之表面的方式制备合成纳米载体。或者,可通过另一途径制备合成纳米载体并随后用炔或叠氮化物进行官能化。在炔(如果聚合物包含叠氮化物)基团或叠氮化物(如果聚合物包含炔)基团存在下制备该组分。然后,在催化剂存在或不存在下使该组分与纳米载体经由1,3-偶极环加成反应而反应,所述催化剂使该组分与颗粒通过1,4-二取代的1,2,3-三唑接头连接。
硫醚接头通过以例如RI-S-R2的形式形成硫-碳(硫醚)键构成。硫醚可通过一种组分上的巯基/硫醇基(-SH)与第二组分上的烷基化基团(例如卤化物或环氧化物)的烷基化形成。硫醚接头还可通过将一种组分上的巯基/硫醇基Michael加成到含有马来酰亚胺基团或乙烯砜基团作为Michael接受体之第二组分上的缺电子烯基团形成。在另一种方式中,硫醚接头可通过一种组分上的巯基/硫醇基与第二组分上的烯基团的自由基巯基-烯反应制备。
腙接头通过使一种组分上的酰肼基团与第二组分上的醛/酮基团反应形成。
酰肼接头通过使一种组分上的肼基团与第二组分上的羧酸基团反应形成。这样的反应一般使用与其中羧酸经活化试剂激活的酰胺键形成类似的化学来进行。
亚胺接头或肟接头通过使一种组分上的胺或N-烷氧基胺(或氨基氧基)基团与第二组分上的醛或酮基团反应形成。
脲或硫脲接头通过使一种组分上的胺基团与第二组分上的异腈酸酯或硫代异腈酸酯基团反应制备。
脒接头通过使一种组分上的胺基团与第二组分上的亚氨酸酯基团反应制备。
胺接头通过一种组分上的胺基团与第二组分上的烷基化基团(例如卤化物、环氧化物或磺酸酯基团)的烷基化反应形成。或者,胺接头还可通过使一种组分上的胺基团与第二组分上的醛或酮基团在合适还原剂(例如氰基硼氢化钠或三乙酰氧基硼氢化钠)存在下进行还原胺化形成。
磺酰胺接头通过使一种组分上的胺基团与第二组分上的磺酰卤(例如磺酰氯)基团反应形成。
砜接头通过将亲核体Michael加成到乙烯砜形成。乙烯砜或亲核体可以在纳米载体的表面上或者与组分连接。
组分(优选为免疫抑制剂)还可通过非共价缀合方法与纳米载体缀合。例如,带负电的免疫抑制剂可与带正电的纳米载体通过静电吸附缀合。含有金属配体的组分也可与含有金属复合物的纳米载体经由金属-配体复合物缀合。
在一些实施方案中,可在组装合成纳米载体之前使组分与聚合物(例如聚乳酸-乙二醇嵌段共聚物)连接,或者合成纳米载体可形成为在其表面上具有反应性或可活化基团。在后一种情况下,组分可使用与通过合成纳米载体之表面呈现的连接化学相容的基团制备。在另一些实施方案中,可使用合适的接头使肽组分与VLP或脂质体连接。接头为能够将两个分子连接在一起的化合物或试剂。在一个实施方案中,接头可以是Hermanson 2008中所述的同双功能试剂或异双功能试剂。例如,可在EDC存在下用同双功能接头己二酸二酰肼(adipic dihydrazide,ADH)处理表面上包含羧基的VLP或脂质体合成纳米载体以形成具有ADH接头的相应合成纳米载体。然后,使所得ADH连接的合成纳米载体经由该纳米载体上ADH接头的另一端与含有酸基团的肽组分缀合以产生相应的VLP或脂质体肽缀合物。
有关可用缀合方法的详细描述,参见Hermanson G T“BioconjugateTechniques”,第2版,由Academic Press出版,Inc.,2008。除共价连接之外,组分可与预先形成的合成纳米载体通过吸附连接或者其可在形成合成纳米载体期间通过包封连接。
可使用本文中提供的任何免疫抑制剂,并且在一些实施方案中,与合成纳米载体连接。免疫抑制剂包括但不限于:他汀类;mTOR抑制剂,例如雷帕霉素或雷帕霉素类似物;TGF-β信号传导剂;TGF-β受体激动剂;组蛋白去乙酰化酶(HDAC)抑制剂;皮质类固醇;线粒体功能的抑制剂,例如鱼藤酮;P38抑制剂;NF-κB抑制剂;腺苷受体激动剂;前列腺素E2激动剂;磷酸二酯酶抑制剂,例如磷酸二酯酶4抑制剂;蛋白酶体抑制剂;激酶抑制剂;G蛋白偶联受体激动剂;G蛋白偶联受体拮抗剂;糖皮质激素;类视黄醇;细胞因子抑制剂;细胞因子受体抑制剂;细胞因子受体激活剂;过氧化物酶体增殖物激活受体拮抗剂;过氧化物酶体增殖物激活受体激动剂;组蛋白去乙酰化酶抑制剂;钙调神经磷酸酶(calcineurin)抑制剂;磷酸酶抑制剂和氧化的ATP。免疫抑制剂还包括1DO、维生素D3、环孢素A、芳基烃受体抑制剂、白藜芦醇、硫唑嘌呤、6-巯基嘌呤、阿司匹林、尼氟灭酸、雌三醇、雷公藤内酯、白介素(例如,IL-1、IL-10)、环孢素A、靶向细胞因子或细胞因子受体的siRNA等。
mTOR抑制剂的实例包括雷帕霉素及其类似物(例如,CCL-779、RAD001、AP23573、C20-甲基烯丙基雷帕霉素(C20-Marap)、C16-(S)-丁基磺酰氨基雷帕霉素(C16-Bsrap)、C16-(S)-3-甲基吲哚雷帕霉素(C16-iRap)(Bayle等Chemistry&Biology 2006,13:99-107))、AZD8055、BEZ235(NVP-BEZ235)、大黄根酸(大黄酚)、地磷莫司(deforolimus,MK-8669)、依维莫司(RAD0001)、KU-0063794、PI-103、PP242、坦罗莫司和WYE-354(可获自Selleck,Houston,TX,USA)。
TGF-β信号传导剂的实例包括TGF-β配体(例如,活化素A、GDF1、GDF11、骨形态生成蛋白、nodal、TGF-β)及其受体(例如,ACVR1B、ACVR1C、ACVR2A、ACVR2B、BMPR2、BMPR1A、BMPR1B、TGFβRI、TGFβRII)、R-SMADS/co-SMADS(例如,SMAD1、SMAD2、SMAD3、SMAD4、SMAD5、SMAD8)和配体抑制剂(例如,卵泡抑素、头蛋白(noggin)、脊索蛋白(chordin)、DAN、lefty、LTBP1、THBS1、Decorin)。
线粒体功能的抑制剂的实例包括苍术苷(二钾盐)、米醇菌酸(三铵盐)、羰基氰化物间氯苯腙、羧基苍术苷(例如,来自欧苍术(Atractylis gummifera))、CGP-37157、(-)-鱼藤素(例如,来自绢毛萌豆(Mundulea sericea))、F16、己糖激酶II VDAC结合结构域肽、寡霉素、鱼藤酮、Ru360、SFK1和缬氨霉素(例如,来自极暗黄链霉菌(Streptomycesfulvissimus)(EMD4Biosciences,USA)。
P38抑制剂的实例包括SB-203580(4-(4-氟苯基)-2-(4-甲基亚磺酰基苯基)-5-(4-吡啶基)1H-咪唑)、SB-239063(反式-1-(4羟基环己基)-4-(氟苯基)-5-(2-甲氧基-嘧啶-4-基)咪唑)、SB-220025(5-(2氨基-4-嘧啶基)-4-(4-氟苯基)-1-(4-哌啶基)咪唑))和ARRY-797。
NF(例如,NK-κB)抑制剂的实例包括IFRD1、2-(1,8-萘啶-2-基)苯酚、5-氨基水杨酸、BAY 11-7082、BAY 11-7085、CAPE(咖啡酸苯乙酯)、马来酸二乙酯、IKK-2抑制剂IV、IMD0354、乳胞素、MG-132[Z-Leu-Leu-Leu-CHO]、NFκB激活抑制剂III、NF-κB激活抑制剂II、JSH-23、小白菊内酯、氧化苯胂(PAO)、PPM-18、吡咯烷二硫代氨基甲酸铵盐、QNZ、RO 106-9920、楝酰胺、楝酰胺AL、楝酰胺C、楝酰胺I、楝酰胺J、洛克米兰醇(rocaglaol)、(R)-MG-132、水杨酸钠、雷公藤内酯(PG490)和蟛蜞菊内酯(wedelolactone)。
腺苷受体激动剂的实例包括CGS-21680和ATL-146e。
前列腺素E2激动剂的实例包括E-Prostanoid 2和E-Prostanoid 4。
磷酸二酯酶抑制剂(非选择性和选择性抑制剂)的实例包括咖啡因、氨茶碱、IBMX(3-异丁基-1-甲基黄嘌呤)、副黄嘌呤、己酮可可碱、可可碱、茶碱、甲基化黄嘌呤、长春西汀、EHNA(赤型-9-(2-羟基-3-壬基)腺嘌呤)、阿那格雷、依诺昔酮(PERFANTM)、米立农、左西孟旦、日中花碱(mesembrine)、异丁司特、吡拉米司特、木犀草素、屈他维林、罗氟司特(DAXASTM、DALIRESPTM)、西地那非 他达拉非伐地那非 乌地那非、阿伐那非、淫羊藿苷(icariin)、4-甲基哌嗪和吡唑并嘧啶-7-1。
蛋白酶体抑制剂的实例包括硼替佐米、双硫仑、表没食子儿茶素-3-没食子酸酯和salinosporamide A。
激酶抑制剂的实例包括贝伐单抗、BIBW 2992、西妥昔单抗伊马替尼曲妥珠单抗吉非替尼雷珠单抗哌加他尼、索拉非尼、达沙替尼、舒尼替尼、埃罗替尼、尼洛替尼、拉帕替尼、帕尼单抗、凡德他尼、E7080、帕唑帕尼(pazopanib)和木利替尼(mubritinib)。
糖皮质激素的实例包括氢化可的松(皮质醇)、醋酸可的松、泼尼松、泼尼松龙、甲泼尼龙、地塞米松、倍他米松、曲安西龙、倍氯米松、醋酸氟氢可的松、醋酸脱氧皮质酮(DOCA)和醛固酮。
过氧化物酶体增殖物激活受体拮抗剂的实例包括GW9662、PPARγ拮抗剂III、G335和T0070907(EMD4Biosciences,USA)。
过氧化物酶体增殖物激活受体激动剂的实例包括吡格列酮、环格列酮、氯贝丁酯、GW1929、GW7647、L-165,041、LY 171883、PPARγ激活剂、Fmoc-Leu、曲格列酮和WY-14643(EMD4Biosciences,USA)。
组蛋白去乙酰化酶抑制剂的实例包括异羟肟酸(或氧肟酸盐)例如曲古抑菌素A、环四肽(例如trapoxin B)和缩酚酸肽、苯甲酰胺、亲电性酮类、脂族酸化合物(例如苯丁酸和丙戊酸)、异羟肟酸(例如伏立诺他(SAHA)、贝利司他(PXD101)、LAQ824和帕比司他(LBH589))、苯甲酰胺(例如恩替诺特(MS-275)、CI994和mocetinostat(MGCD0103))、烟酰胺、NAD衍生物、二氢香豆素类、萘并吡喃酮类、以及2-羟基萘醛。
钙调神经磷酸酶抑制剂的实例包括环孢素、吡美莫司、伏环孢素(voclosporin)和他克莫司。
磷酸酶抑制剂的实例包括BN82002盐酸盐、CP-91149、花萼海绵诱癌素A(calyculin A)、斑蝥酸、斑蝥素、氯氰菊酯、乙基-3,4-迪磷他汀、福司曲星钠盐、MAZ51、甲基-3,4-迪磷他汀、NSC 95397、去甲斑蝥酸、来自凹形原甲藻(prorocentrum concavum)的冈田酸铵盐、冈田酸、冈田酸钾盐、冈田酸钠盐、氧化苯胂、多种磷酸酶抑制剂混合物、蛋白质磷酸酶1C、蛋白质磷酸酶2A抑制剂蛋白、蛋白质磷酸酶2A1、蛋白质磷酸酶2A2和正钒酸钠。
治疗性大分子可以以治疗性大分子自身的形式递送或者以其片段或衍生物的形式递送。治疗性大分子可包括治疗性蛋白质或治疗性多核苷酸。治疗性蛋白质包括但不限于:可输注的治疗性蛋白质、酶、酶辅因子、激素、凝血因子、细胞因子和干扰素、生长因子、单克隆抗体和多克隆抗体(其例如作为替代治疗施用于对象)以及与庞皮病相关的蛋白质(例如,酸性葡糖苷酶α,rhGAA)(例如,Myozyme和Lumizyme(Genzyme))。治疗性蛋白质还包括参与凝血级联的蛋白质。治疗性蛋白质包括但不限于:因子VIII、因子VII、因子IX、因子V、冯·维勒布兰德因子、von Heldebrant因子、组织纤溶酶原激活物、胰岛素、生长激素、红细胞生成素α、VEGF、血小板生成素、溶菌酶、抗凝血酶等。治疗性蛋白质还包括脂肪素(adipokine),例如瘦素和脂联素。治疗性蛋白质的其他实例如下文及本文中的其他部分所述。
用于患有溶酶体贮积症之对象的酶替代治疗中的治疗性蛋白质的实例包括但不限于:用于治疗戈谢病(Gaucher’s disease)的伊米苷酶(例如,CEREZYMETM),用于治疗法布里病(Fabry disease)的a-半乳糖苷酶A(a-gal A)(例如,阿加糖酶β、FABRYZYMETM),用于治疗庞皮病的酸性α-葡糖苷酶(GAA(例如,酸性葡糖苷酶α、LUMIZYMETM、MYOZYMETM),用于治疗黏多醣贮积症(Mucopolysaccharidose)的芳基硫酸酯酶B(例如,拉罗尼酶、ALDURAZYMETM、艾杜硫酶、ELAPRASETM、芳基硫酸酯酶B、NAGLAZYMETM),聚乙二醇化重组尿酸酶(KRYSTEXXA)和聚乙二醇化重组假丝酵母尿酸酶。
酶的实例包括:氧化还原酶、转移酶、水解酶、裂合酶、异构酶、天冬酰胺酶、尿酸酶、糖苷酶、天冬酰胺酶、尿酸酶、蛋白酶、核酸酶、胶原酶、透明质酸酶、肝素酶、类肝素酶、细胞溶素(lysin)和连接酶。
治疗性蛋白质还可包括分离自或来源于细菌、真菌或病毒来源的任何酶、毒素或其他蛋白质或肽。
激素的实例包括:褪黑激素(N-乙酰基-5-甲氧基色胺)、血清素、甲状腺素(或四碘甲腺原氨酸)(甲状腺激素)、三碘甲腺氨酸(甲状腺激素)、肾上腺素(或肾上腺激素)、去甲肾上腺素(或去甲肾上腺激素)、多巴胺(或催乳素抑制激素)、抗米勒管激素(或米勒管抑制因子或激素)、脂连蛋白、促肾上腺皮质激素(或促皮质素)、血管紧张素原和血管紧张素、抗利尿激素(或加压素、精氨酸加压素)、心房钠尿肽(或心钠素)、降钙素、胆囊收缩素、促皮质素释放激素、红细胞生成素、促卵泡激素、胃泌素、生长素释放肽、胰高血糖素、胰高血糖素样肽(GLP-1)、GIP、促性腺素释放激素、生长激素释放激素、人绒毛膜促性腺素、人胎盘催乳素、生长激素、抑制素、胰岛素、胰岛素样生长因子(或生长调节素)、瘦素、黄体化激素、黑素细胞刺激激素、食欲素、催产素、甲状旁腺激素、催乳素、松弛素、分泌素、生长激素抑制素、血小板生成素、甲状腺刺激激素(或促甲状腺素)、促甲状腺素释放激素、皮质醇、醛固酮、睾酮、去氢表雄酮、雄烯二酮、二氢睾酮、雌二醇、雌酮、雌三醇、黄体酮、骨化三醇(1,25-二羟基维生素D3)、骨化二醇(25-羟基维生素D3)、前列腺素类、白三烯类、前列环素、血栓烷类、催乳素释放激素、促脂解素、脑钠尿肽、神经肽Y、组胺、内皮素、胰多肽、肾素和脑啡肽。
血液因子或凝血因子的实例包括因子I(纤维蛋白原)、因子II(凝血酶原)、组织因子、因子V(前加速素,不稳定因子)、因子VII(稳定因子、前转化素)、因子VIII(抗血友病球蛋白)、因子Ⅸ(克雷司马斯因子(Christmas factor)或血浆促凝血酶原激酶组分)、因子X(斯图尔特因子(Stuart-Prower factor))、因子Xa、因子XI、因子XII(哈格曼因子(Hagemanfactor))、因子XIII(纤维蛋白稳定因子)、冯·维勒布兰德因子、前激肽释放酶(弗莱彻因子(Fletcher factor))、高分子量激肽原(HMWK)(菲兹杰拉尔德因子(Fitzgeraldfactor))、纤连蛋白、纤维蛋白、凝血酶、抗凝血酶III、肝素辅因子II、蛋白C、蛋白S、蛋白Z、蛋白Z相关蛋白酶抑制剂(ZPI)、纤溶酶原、α2-抗纤溶酶、组织纤溶酶原激活物(tPA)、尿激酶、纤溶酶原激活物抑制剂-1(PAI1)、纤溶酶原激活物抑制剂-2(PAI2)、癌促凝物质或阿法依伯汀(Epogen,Procrit)。
细胞因子的实例包括淋巴因子、白介素、以及趋化因子、1型细胞因子(例如IFN-γ、TGF-β)和2型细胞因子(例如IL-4、IL-10和IL-13)。
生长因子的实例包括肾上腺髓质素(AM)、血管生成素(Ang)、自分泌运动因子、骨形态生成蛋白(Bone morphogenetic protein,BMP)、脑源性神经营养因子(Brain-derivedneurotrophic factor,BDNF)、表皮生长因子(Epidermal growth factor,EGF)、红细胞生成素(EPO)、成纤维细胞生长因子(Fibroblast growth factor,FGF)、神经胶质细胞系源性神经营养因子(Glial cell line-derived neurotrophic factor,GDNF)、粒细胞集落刺激因子(Granulocyte colony-stimulating factor,G-CSF)、粒细胞-巨噬细胞集落刺激因子(Granulocyte macrophage colony-stimulating factor,GM-CSF)、生长分化因子-9(Growth differentiation factor-9,GDF9)、肝细胞生长因子(Hepatocyte growthfactor,HGF)、肝癌源性生长因子(Hepatoma-derived growth factor,HDGF)、胰岛素样生长因子(Insulin-like growth factor,IGF)、促移行因子、肌生长抑制素(GDF-8)、神经生长因子(Nerve growth factor,NGF)及其他神经营养因子、血小板源性生长因子(Platelet-derived growth factor,PDGF)、血小板生成素(TPO)、转化生长因子α(Transforming growth factor alpha,TGF-α)、转化生长因子β(Transforming growthfactor beta,TGF-β)、肿瘤坏死因子α(Tumour_necrosis_factor-alpha,TNF-α)、血管内皮生长因子(Vascular endothelial growth factor,VEGF)、Wnt信号传导途径、胎盘生长因子(placental growth factor,P1GF)、(胎牛促生长素,Foetal Bovine Somatotrophin)(FBS)、IL-1、IL-2、IL-3、IL-4、IL-5、IL-6和IL-7。
单克隆抗体的实例包括阿巴伏单抗、阿昔单抗、阿达木单抗、阿德木单抗、阿非莫单抗、阿夫土珠单抗(Afutuzumab)、培化阿珠单抗、ALD、阿仑单抗、阿妥莫单抗喷替酸盐、麻安莫单抗、安芦珠单抗、抗胸腺细胞珠蛋白、阿泊珠单抗、阿西莫单抗、阿塞珠单抗、Atlizumab(托珠单抗)、阿托木单抗、Bapineuzumab、巴利昔单抗、巴维昔单抗、贝妥莫单抗、贝利木单抗、Benralizumab、柏替木单抗、贝索单抗、贝伐单抗、比西单抗、莫比伐珠单抗、Blinatumomab、Brentuximab vedotin、Briakinumab、卡那单抗、莫坎妥珠单抗、卡罗单抗喷地肽、卡妥索单抗、西利珠单抗、赛妥珠单抗、西妥昔单抗、泊西他珠单抗、Cixutumumab、克立昔单抗、Clivatuzumab tetraxetan、Conatumumab、Dacetuzumab、达珠单抗、Daratumumab、狄迪诺塞麦、地莫单抗、阿托度单抗、Dorlixizumab、依美昔单抗、依库珠单抗、埃巴单抗、依决可单抗、依法利珠单抗、依芬古单抗、埃罗妥珠单抗、艾西莫单抗、培戈赖莫单抗、西依匹莫单抗、依帕珠单抗、Erlizumab、厄妥索单抗、Etaracizumab、艾韦单抗、Fanolesomab、法拉莫单抗、Farletuzumab、非维珠单抗、非扎奴单抗、Figitumumab、芳妥珠单抗、Foravirumab、Fresolimumab、Galiximab、Gantenerumab、加维莫单抗、吉妥单抗、GC1008、Girentuximab、Glembatumumab vedotin、戈利木单抗、Gomiliximab、Ibalizumab、替伊莫单抗、伊戈伏单抗、英西单抗、英夫利昔单抗、Intetumumab、伊诺莫单抗、奥英妥珠单抗、依匹木单抗、Iratumumab、凯利昔单抗、拉贝珠单抗、Lebrikizumab、来马索单抗、乐地单抗、来沙木单抗、利韦单抗、林妥珠单抗、Lorvotuzumab mertansine、Lucatumumab、鲁昔单抗、马帕木单抗、马司莫单抗、马妥珠单抗、美泊利单抗、美替木单抗、Milatuzumab、明瑞莫单抗、米妥莫单抗、莫罗木单抗、Motavizumab、鼠单克隆抗体-CD3、他那可单抗、Naptumomabestafenatox、那他珠单抗、奈巴库单抗、Necitumumab、奈瑞莫单抗、尼妥珠单抗、巯诺莫单抗、Ocrelizumab、奥度莫单抗、奥法木单抗、Olaratumab、奥马珠单抗、莫奥珠单抗、奥戈伏单抗、Otelixizumab、Pagibaximab、帕利珠单抗、帕尼单抗、Panobacumab、帕考珠单抗、Pemtumomab、帕妥珠单抗、Pexelizumab、平妥莫单抗、普立昔单抗、Pritumumab、雷韦单抗、雷莫芦单抗、雷珠单抗、Raxibacumab、瑞加韦单抗、瑞利珠单抗、Rilotumumab、利妥昔单抗、Robatumumab、Rontalizumab、罗维珠单抗、鲁利单抗、沙妥莫单抗喷地肽、司韦单抗、西罗珠单抗、西法木单抗、Siltuximab、西利珠单抗、Solanezumab、Sonepcizumab、Sontuzumab、Stamulumab、硫索单抗、Tacatuzumab tetraxetan、他度珠单抗、Talizumab、尼珠单抗、帕他普莫单抗、替非珠单抗、阿替莫单抗、Tenatumomab、替奈昔单抗、Teplizumab、Ticilimumab(替西木单抗)、替加珠单抗、托珠单抗(atlizumab)、托利珠单抗、托西莫单抗、曲妥珠单抗、替西木单抗、Tucotuzumab celmoleukin、妥韦单抗、乌珠单抗、Ustekinumab、伐利昔单抗、维多珠单抗、维妥珠单抗、维帕莫单抗、Visilizumab、伏洛昔单抗、伏妥莫单抗、Zalutumumab、扎木单抗、齐拉木单抗和阿佐莫单抗。单克隆抗体还包括抗-TNFα抗体。
输注治疗或可注射的治疗性蛋白质的实例包括例如:托珠单抗(Roche/)、α-1抗胰蛋白酶(Kamada/AAT)、(Affymax和Takeda,合成肽)、白蛋白干扰素α-2b(albinterferon alfa-2b)(Novartis/ZalbinTM)、(Pharming Group,C1抑制剂替代治疗)、替莫瑞林(Theratechnologies/Egrifta,合成生长激素释放因子)、奥瑞珠单抗(Genentech、Roche和Biogen)、贝利木单抗(GlaxoSmithKline/)、聚乙二醇化重组尿酸酶(Savient Pharmaceuticals/KrystexxaTM)、聚乙二醇化重组假丝酵母尿酸酶、他利苷酶α(Protalix/Uplyso)、阿加糖酶α(Shire/)、葡糖脑苷脂酶α(Shire)和钥孔林普贝血蓝蛋白(KLH)。
另外的治疗性蛋白质包括例如:工程化蛋白质,例如Fc融合蛋白、双特异性抗体、多特异性抗体、纳米体、抗原结合蛋白、抗体片段和蛋白质缀合物,例如抗体药物缀合物。
治疗性多核苷酸包括但不限于:核酸适配体例如哌加他尼(Macugen,一种聚乙二醇化抗VEGF适配体)、反义治疗性多核苷酸例如反义多核苷酸或反义寡核苷酸(例如,抗病毒药福米韦生,或米泊美生,靶向载脂蛋白B的信使RNA以降低胆固醇水平的反义治疗剂);小干扰RNA(siRNA)(例如,dicer底物siRNA分子(DsiRNA),其为以极高效力介导RNAi的25-30个碱基对的不对称双链RNA);或经修饰的信使RNA(mmRNA)例如Fougerolles等的美国专利申请2013/0115272和Schrum等的公开的美国专利申请2012/0251618中所述的那些。
可根据本发明的一些方面使用的其他治疗性大分子对本领域技术人员是显而易见的,并且本发明在此方面不受限制。
在一些实施方案中,组分(例如治疗性大分子或免疫抑制剂)可以是经分离的。“经分离的”指组分与其天然环境分离并且以足够量存在以允许其鉴定或使用。这意味着,例如,组分可(i)通过表达克隆选择性地产生或者(ii)通过色谱或电泳进行纯化。经分离的组分可以但不需要是基本纯的。由于可将经分离的组分与可药用赋形剂一起混合在药物制剂中,所述组分可仅占制剂的小重量百分比。组分仍是经分离的,只要其已与在活系统中与其相关的物质分离,即与其他脂质或蛋白质分离。本文中提供的任一种组分均可以是经分离的并且以经分离形式包含在组合物中或者用于方法中。
D.制备和使用所述组合物的方法及相关方法
可如下确定施用方案:改变第一给药和第二给药的数量和/或改变第一给药和第二给药之间的时间长度并评估针对治疗性大分子的不期望体液免疫应答。例如,在施用第一给药和第二给药之后,可测量针对治疗性大分子的不期望体液免疫应答。将该不期望体液免疫应答与在无第一和第二给药时发生的相同类型的免疫应答进行比较,例如当在没有与免疫抑制剂(例如当与合成纳米载体连接时)伴随施用时仅已发生治疗性大分子的一次或更多次给药时。一般来说,如果发现在第一和第二给药之后不期望免疫应答的水平降低,则施用方案对需要用治疗性大分子进行治疗的对象有益并且可与本文中提供的本发明的方法和组合物一起使用。可如下确定施用方案:以第一给药和第二给药的测试方案开始并在适当时使用已知的缩放技术(例如异速缩放或等速缩放)。在另一个实施方案中,可如下确定施用方案:基于经验和指导数据,借助例如直接实验在对象中对多种方案进行测试。
可使用本领域中已知的多种方法来制备合成纳米载体。例如,可通过以下方法及本领域普通技术人员公知的其他方法来形成合成纳米载体:例如,纳米沉淀、使用流体通道的流体聚焦、喷雾干燥、单乳化溶剂蒸发和双乳化溶剂蒸发、溶剂萃取、相分离、研磨、微乳化法、微制造、纳米制造、牺牲层、简单凝聚和复合凝聚。作为替代或补充,用于单分散半导体纳米材料、电导性纳米材料、磁性纳米材料、有机纳米材料及其他纳米材料的水性溶剂和有机溶剂合成已有描述(Pellegrino等,2005,Small,1:48;Murray等,2000,Ann.Rev.Mat.Sci.,30:545;和Trindade等,2001,Chem.Mat.,13:3843)。另外的方法已在以下文献中进行了描述(参见,例如,Doubrow,编辑,“Microcapsules and Nanoparticles inMedicine and Pharmacy,”CRC Press,Boca Raton,1992;Mathiowitz等,1987,J.Control.Release,5:13;Mathiowitz等,1987,Reactive Polymers,6:275;和Mathiowitz等,1988,J.Appl.Polymer Sci.,35:755;美国专利5578325和6007845;P.Paolicelli等,“Surface-modified PLGA-based Nanoparticles that can Efficiently Associate andDeliver Virus-like Particles”Nanomedicine.5(6):843-853(2010))。
如果期望的话,可使用多种方法将多种材料包封在合成纳米载体内,所述方法包括但不限于C.Astete等,“Synthesis and characterization of PLGA nanoparticles”J.Biomater.Sci.Polymer Edn,第17卷,第3期,第247-289页(2006);K.Avgoustakis“Pegylated Poly(Lactide)and Poly(Lactide-Co-Glycolide)Nanoparticles:Preparation,Properties and Possible Applications in Drug Delivery”CurrentDrug Delivery 1:321-333(2004);C.Reis等,“Nanoencapsulation I.Methods forpreparation of drug-loaded polymeric nanoparticles”Nanomedicine 2:8-21(2006);P.Paolicelli等,“Surface-modified PLGA-based Nanoparticles that canEfficiently Associate and Deliver Virus-like Particles”Nanomedicine.5(6):843-853(2010)。也可使用适合将材料包封在合成纳米载体内的其他方法,包括但不限于于2003年10月14日授权的Unger的美国专利6,632,671中所公开的方法。
在某些实施方案中,通过纳米沉淀法或喷雾干燥来制备合成纳米载体。可对用于制备合成纳米载体的条件进行改变以产生具有期望尺寸或特性(例如,疏水性、亲水性、外部形态、“黏性”、形状等)的颗粒。制备合成纳米载体的方法及所使用的条件(例如,溶剂、温度、浓度、空气流速等)可取决于待与合成纳米载体连接的材料和/或聚合物基质的组成。
如果通过上述任一种方法制备的合成纳米载体的尺寸范围在期望范围之外,则可例如使用筛对此类合成纳米载体进行尺寸选择。
合成纳米载体的成分(即,组分)可与整个合成纳米载体例如通过一个或更多个共价键连接,或者可借助一个或更多个接头连接。官能化合成纳米载体的另外方法可改编自Saltzman等的公开的美国专利申请2006/0002852、DeSimone等的公开的美国专利申请2009/0028910或Murthy等的公开的国际专利申请WO/2008/127532 A1。
作为替代或补充,合成纳米载体与组分可直接地或间接地经由非共价相互作用连接。在非共价实施方案中,非共价偶联由非共价相互作用介导,所述非共价相互作用包括但不限于:电荷相互作用、亲和性相互作用、金属配位、物理吸附、主体-客体相互作用、疏水性相互作用、TT堆积相互作用、氢键合相互作用、范德华相互作用、磁性相互作用、静电相互作用、偶极-偶极相互作用和/或其组合。这样的偶联可布置成在合成纳米载体的外表面或内表面上。在一些实施方案中,包封和/或吸附是偶联的形式。在一些实施方案中,可将合成纳米载体与治疗性大分子或其他组成通过混合在同一载剂或递送系统中而组合。
本文中提供的组合物可包含无机或有机缓冲剂(例如,磷酸、碳酸、醋酸或柠檬酸的钠盐或钾盐)和pH调节剂(例如,盐酸、氢氧化钠或氢氧化钾、柠檬酸或醋酸的盐、氨基酸及其盐)、抗氧化剂(例如,抗坏血酸、α-生育酚)、表面活性剂(例如,聚山梨醇酯20、聚山梨醇酯80、聚氧乙烯9-10壬基苯酚、去氧胆酸钠)、溶液剂和/或冷冻/冻干稳定剂(例如,蔗糖、乳糖、甘露醇、海藻糖)、渗透调节剂(例如,盐或糖)、抗菌剂(例如,苯甲酸、苯酚、庆大霉素)、消泡剂(例如,聚二甲基硅氧烷)、防腐剂(例如,硫柳汞、2-苯氧基乙醇、EDTA)、聚合物稳定剂和黏度调节剂(例如,聚乙烯吡咯烷酮、泊洛沙姆488、羧甲基纤维素)和潜溶剂(例如甘油、聚乙二醇、乙醇)。
根据本发明的组合物可包含可药用赋形剂。所述组合物可使用常规的药物制备和配合技术制成以实现可用的剂型。适用于实施本发明的技术可见于Handbook ofIndustrial Mixing:Science and Practice,由Edward L.Paul,Victor A.Atiemo-Obeng和Suzanne M.Kresta编辑,2004John Wiley&SoHs,Inc.;和Pharmaceutics:The Scienceof Dosage Form Design,第2版.由M.E.Auten编辑,2001,Churchill Livingstone中。在一个实施方案中,组合物与防腐剂一起存在于无菌盐水溶液中以用于注射。
应当理解,本发明的组合物可以以任何合适的方式制备,并且本发明不以任何方式局限于可使用本文中所述的方法制备的组合物。对合适制备方法的选择可需要注意所缔合的具体部分的特性。
在一些实施方案中,组合物是在无菌条件下制备的,或者是经最终灭菌的。这可确保,所得组合物是无菌的和非感染性的,从而当与非无菌组合物相比时,安全性提高。这提供了有价值的安全措施,尤其是当接受组合物的对象具有免疫缺陷、患有感染和/或易受感染时。在一些实施方案中,可将组合物冷冻干燥并悬浮储存或者作为冻干粉末储存,这取决于不丧失活性的长期配制策略。
根据本发明的施用可通过多种途径,包括但不限于:皮下、静脉内、腹膜内、肌内、经粘膜、经皮、经皮肤或皮内途径。在一个优选实施方案中,施用经由皮下施用途径。可使用常规方法将本文中提及的组合物配制和制备成用于施用,优选用于伴随施用。
可以以有效量(例如本文中其他部分所述的有效量)施用本发明的组合物。根据本发明,剂型的剂量可包含不同量的免疫抑制剂。根据本发明,剂型的剂量可包含不同量的治疗性大分子。剂型中存在的各种组分的量可根据以下方面而不同:组分的性质、需达到的治疗益处及其他这样的参数。在一些实施方案中,可进行剂量范围研究以建立剂型中存在的组分的最佳治疗量。在一些实施方案中,组分以在施用于对象时有效降低针对治疗性大分子的不期望体液免疫应答的量存在于剂型中。可使用常规的剂量范围研究和技术来确定在对象中有效降低不期望的体液免疫应答的组分的量。剂型可以以多种频率施用(即,根据施用方案)。在一个优选实施方案中,剂型的至少一次施用足以产生药理学上相关的应答。在一些更优选的实施方案中,利用至少两次施用或至少三次施用以确保药理学上相关的应答。
本公开内容的另一个方面涉及药盒。在一些实施方案中,所述药盒包含本文中提供的一个或更多个第一剂量和/或一个或更多个第二剂量。药盒中的每种剂量可包含在药盒中的独立容器中或者包含在药盒中的同一容器中。在一些实施方案中,所述容器为小瓶或安瓿。在一些实施方案中,每个剂量包含在与容器分开的溶液中,使得可随后将所述剂量添加至容器。在一些实施方案中,剂量以冻干形式各自存在于独立容器中或同一容器中,使得它们可随后重构。在一些实施方案中,所述药盒还包含用于重构、混合、施用等的说明书。在一些实施方案中,所述说明书包含对本文中所述的方法的说明。说明书可以是任何合适的形式,例如,作为印刷插入物或标签。在一些实施方案中,所述药盒还包含一个或更多个注射器。
实施例
实施例1:用于制备与雷帕霉素连接的纳米载体的方法
材料
雷帕霉素购自TSZ CHEM(185Wilson Street,Framingham,MA01702;产品代码R1017)。丙交酯∶乙交酯之比为3∶1并且特性黏度为0.75dL/g的PLGA购自SurModicsPharmaceuticals(756Tom Martin Drive,Birmingham,AL 35211;产品代码7525DLG 7A)。甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.5DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biochemicals(756Tom Martin Drive,Birmingham,AL 35211;产品代码100DL mPEG 50005CE)。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa·s至4.6mPa·s)购自EMD Chemicals Inc.(480South Democrat Road Gibbstown,NJ 08027.产品代码1.41350)。
方法
如下制备溶液:
溶液1:二氯甲烷中的75mg/mL PLGA、25mg/mL PLA-PEG-OMe和12.5mg/mL的雷帕霉素。该溶液通过将PLGA、PLA-PEG-OMe和雷帕霉素溶解于纯二氯甲烷中制备。
溶液2:100mM pH 8磷酸盐缓冲液中的50mg/mL聚乙烯醇。
使用水包油型(O/W)乳剂制备纳米载体。如下制备O/W乳剂:将溶液1(1.0mL)和溶液2(3.0mL)合并在小压力管中并使用Branson Digital Sonifier 250以30%振幅进行超声处理60秒。将O/W乳剂添加至含有70mM pH 8磷酸盐缓冲溶液的烧杯并在室温下搅拌2小时以使二氯甲烷蒸发并形成纳米载体。将一部分的纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600×g和4℃下离心50分钟,除去上清液并将沉淀物重悬于磷酸缓冲盐水中。重复洗涤操作并将沉淀物重悬于磷酸缓冲盐水中以获得约10mg/mL的最终纳米载体分散体。
通过动态光散射确定纳米载体的尺寸。通过HPLC分析确定纳米载体中雷帕霉素的量。通过重量法确定总干纳米载体质量/mL混悬液。
与雷帕霉素连接的纳米载体的有效直径和雷帕霉素含量
材料
雷帕霉素购自TSZ CHEM(185Wilson Street,Framingham,MA01702;产品代码R1017)。丙交酯∶乙交酯比为1∶1并且特性黏度为0.24dL/g的PLGA购自SurModicsPharmaceuticals(756Tom Martin Drive,Birmingham,AL 35211;产品代码5050DLG2.5A)。甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.5DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biochemicals(756Tom Martin Drive,Birmingham,AL 35211;产品代码100DL mPEG 50005CE)。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa·s至4.6mPa·s)购自EMD Chemicals Inc.(480South Democrat RoadGibbstown,NJ 08027.产品代码1.41350)。
方法
如下制备溶液:
溶液1:二氯甲烷中的75mg/mL PLGA、25mg/mL PLA-PEG-OMe和12.5mg/mL的雷帕霉素。该溶液通过将PLGA、PLA-PEG-OMe和雷帕霉素溶解于纯二氯甲烷中制备。
溶液2:100mM pH 8磷酸盐缓冲液中的50mg/mL聚乙烯醇。
溶液3:70mM磷酸盐缓冲液,DH 8。
如下制备水包油型乳剂:将溶液1(1.0mL)和溶液2(3.0mL)混合在小压力管中并使用Branson Digital Sonifier 250以30%振幅进行超声处理60秒。将乳剂添加至含有溶液3(30mL)的50mL敞开烧杯并在室温下搅拌2小时以使二氯甲烷蒸发并在混悬液中形成纳米载体。然后,将一部分的混悬纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600rcf旋转40分钟,除去上清液并将沉淀物重悬于磷酸缓冲盐水中。重复洗涤操作并随后将沉淀物重悬于PBS 1X中以获得基于聚合物的标称浓度为10mg/mL的纳米载体混悬液。将混悬液冷冻储存在-20℃下直至使用。
通过动态光散射确定纳米载体的尺寸。通过HPLC分析确定纳米载体中的雷帕霉素量。通过重量法确定总干纳米载体质量/mL混悬液。
与雷帕霉素连接的纳米载体的有效直径和雷帕霉素含量
材料
丙交酯∶乙交酯比为1∶1并且特性黏度为0.24dL/g的PLGA购自SurModicsPharmaceuticals(756Tom Martin Drive,Birmingham,AL35211;产品代码5050DLG2.5A)。甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.5DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biochemicals(756Tom Martin Drive,Birmingham,AL 35211;产品代码100DL mPEG 50005CE)。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa·s至4.6mPa·s)购自EMD Chemicals Inc.(480South Democrat Road Gibbstown,NJ 08027.产品代码1.41350)。
方法
如下制备溶液:
溶液1:二氯甲烷中的75mg/mL PLGA和25mg/mL PLA-PEG-OMe。该溶液通过将PLGA和PLA-PEG-OMe溶解于纯二氯甲烷中制备。
溶液2:100mM pH8磷酸盐缓冲液中的50mg/mL聚乙烯醇。
溶液3:70mM磷酸盐缓冲液,pH8。
如下制备水包油型乳剂:将溶液1(1.0mL)和溶液2(3.0mL)混合在小压力管中并使用Branson Digital Sonifier 250以30%振幅进行超声处理60秒。将乳剂添加至含有溶液3(30mL)的50mL敞开烧杯并在室温下搅拌2小时以使二氯甲烷蒸发并在混悬液中形成纳米载体。然后,将一部分的混悬纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600rcf旋转40分钟,除去上清液并将沉淀物重悬于磷酸缓冲盐水中。重复洗涤操作并随后将沉淀物重悬于PBS 1X中以获得基于聚合物的标称浓度为10mg/mL的纳米载体混悬液。将混悬液冷冻储存在-20℃下直至使用。
通过动态光散射确定纳米载体的尺寸。通过重量法确定总干纳米载体质量/mL混悬液。
实施例2:评价针对FVIII的不期望体液免疫应答
如图1A中示意性地所示,使血友病A小鼠(E16小鼠)(第0天n=8)每周接受以下第一给药:静脉内(i.v.)伴随注射凝血蛋白(因子VIII(FVIII))和与雷帕霉素连接的合成纳米载体(纳米载体ID 4),或者空纳米载体(NP)(纳米载体ID 5)和FVIII或者IVIG(静脉内免疫球蛋白)和FVIII,持续连续5周。分别在第57、81、125、143和187天,在不存在进一步处理的情况下用FVIII(i.v.或腹膜内(i.p.))的第二给药攻击小鼠。通过ELISA确定抗FVIII抗体的水平。将每个时间点的数据表示为平均值±SEM(图1B)。对于统计学分析,使用具有双尾分布的t-检验(student t-test)将与雷帕霉素连接之合成纳米载体的组与空纳米颗粒(NP)对照组进行比较。*p<0.05和**p<0.01。FVIII的所有注射均为1μg/注射。纳米载体ID 4的所有注射均为100μg/注射。
为了评价在FVIII和与雷帕霉素连接之合成纳米载体的最后给药后1个月针对FVIII的抗体回忆应答,使用显色FVIII活性测定试剂盒(Coatest SP4 FVIII)通过Bethesda测定确定抑制剂效价,如图2中所示。
数据表明与合成纳米载体连接之免疫抑制剂和FVIII的第一给药降低了抗因子FVIII抗体应答。数据还表明这样的施用可导致因子VIII的活性提高。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答并提高效力。数据还证明了降低针对因子VIII的不期望体液应答的施用方案。
实施例3:评价针对HUMIRA/阿达木单抗的不期望体液免疫应答
一周一次地,在前肢内向对照年龄匹配的(5周至6周)雌性C57BL/6皮下(s.c.)注射60μg HUMIRA,直至第29天(d0、7、14、22、29,在所有组和条件下)。使另一组接受类似的注射,但在开始第0天,将0.9mg与雷帕霉素连接的合成纳米载体(纳米载体ID 1、2或3)与HUMIRA的溶液混合(第一给药)。图3A中所示的结果示出了在第21天所有动物的血液中的抗体效价。对照动物发生针对HUMIRA的稳健的抗体应答,而经处理的动物甚至在20天和在无处理情况下进行两次HUMIRA注射(第二给药)后保持完全阴性。在第29天,在一个后肢内使动物接受再一次攻击(又一次第二给药),而使另一后肢接受盐水以测试局部抗体介导的I型超敏反应。为此,注射后1小时借助卡尺测量后肢的厚度。两个肢体间的厚度差异示于图3B中。与抗体结果类似,合成纳米载体处理消除了通过局部施用HUMIRA引起的炎性应答。
这些结果表明,施用第一和第二给药可降低不期望的抗HUMIRA抗体应答以及消除可由施用HUMIRA引起的不期望炎性应答。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对HumiraTM的不期望体液应答的施用方案。
实施例4:评价针对钥孔林普贝血蓝蛋白(KLH)的不期望体液免疫应答
从第0天或第21天开始,一周一次地在尾静脉内向对照年龄匹配的(5周至6周)雌性C57BL/6静脉内(i.v.)注射200μg钥孔林普贝血蓝蛋白(KLH),直至第34天(d0、7、14、21、28、34)。在第0天至第34天,使另一组接受类似的注射,但在第0、14和21天,将0.47mg与雷帕霉素连接的合成纳米载体(纳米载体ID1、2或3)与KLH的溶液混合(第一给药),之后在第21天至第34天每周进行单独KLH注射(第二给药)(d21、28、34)。图4中所示的结果示出了在指定时间点动物的血液中的KLH抗体效价。在使用相同量的KLH进行三次注射后(分别在第26天和第40天),在第0天或第21天开始免疫的对照动物发生非常类似的应答(EC50=3×103至5×103)。相比之下,在进行三次单独KLH的注射后,接受三次与雷帕霉素连接之合成纳米载体的注射的动物保持完全阴性。
这些结果表明,施用第一和第二给药可降低由施用KLH引起的不期望抗KLH抗体应答。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对KLH的不期望体液应答的施用方案。
实施例5:评价针对卵清蛋白的不期望体液免疫应答
在第-21天和第-13天,在尾静脉内对年龄匹配的(5周至6周)雌性C57BL/6静脉内注射1.2mg未偶联纳米颗粒(NP[空])(纳米载体ID 5),游离雷帕霉素(fRapa)(100μg),22μg游离鸡卵清蛋白(fOVA),fRapa和fOVA的组合,单独或与22μg fOVA组合之1.2mg与雷帕霉素连接的合成纳米载体(NP[Rapa],100μg雷帕霉素内容物)(纳米载体ID 1、2或3)。在第0天,在后肢内,对所有动物皮下注射与2μg CpG混合的2.5μg颗粒OVA(pOVA),之后在第7天和第14天注射2.5μg pOVA。在不存在任何处理的情况下(NP[空]),动物发生针对OVA的稳健免疫应答,这可通过抗OVA IgG抗体效价测量。图5中所示的第22天抗体效价证明在相同溶液(fOVA+NP[Rapa])中与OVA伴随施用之与雷帕霉素连接的合成纳米载体的两个剂量(第一给药)甚至在1次OVA+CpG注射和2次单独OVA注射(第二给药)之后有效地预防针对OVA的抗体形成。
这些结果表明,施用第一和第二给药可降低不期望的抗OVA抗体应答,并且甚至在将OVA与强佐剂组合施用后仍可保持这样的降低。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对OVA的不期望体液应答的施用方案。
实施例6:评价针对KRYSTEXXA的不期望体液免疫应答
在第-21天和第-14天,在尾静脉内,向对照组年龄匹配的(5周至6周)雌性C57BL/6静脉内注射PBS,而向处理组注射0.9mg与雷帕霉素连接的合成纳米载体(纳米载体ID 1、2或3)和40μg KRYSTEXXA的组合。在第0天至第28天,在后肢内使所有动物每周接受与20μgCpG s.c.之组合100μg KRYSTEXXA的注射(d0、7、12、28)。对照动物发生针对KRYSTEXXA的免疫应答,这可通过抗KRYSTEXXA IgM抗体效价测量。图6中的结果表明,在同一溶液中用和KRYSTEXXA伴随施用之与雷帕霉素连接的合成纳米载体(第一给药)处理动物有效地在长时间内预防针对KRYSTEXXA的抗体形成。经处理的动物甚至在无合成纳米载体的情况下进行5次KRYSTEXXA+CpG注射(第二给药)后未发生抗KRYSTEXXA应答。
这些结果表明,施用第一和第二给药可降低不期望的抗KRYSTEXXA抗体应答,并且甚至在将KRYSTEXXA与强佐剂组合施用后仍可保持这样的降低。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对KrystexxaTM的不期望体液应答的施用方案。
实施例7:评价针对卵清蛋白和KLH的不期望体液免疫应答
一周一次地,在尾静脉内向对照组年龄匹配的(5周至6周)雌性C57BL/6静脉内注射2.5μg颗粒卵清蛋白(pOVA)的免疫原性形式并在后肢内皮下注射2μg钥孔林普贝血蓝蛋白(KLH),持续49天(d0、7、14、20、28、35、42、49)。以相同的途径和量使其他动物组接受pOVA和KLH,但在第0、7和14天将pOVA和KLH与0.2mg连接有雷帕霉素的合成纳米载体(纳米载体ID 1、2或3)混合,之后在第20天至第42天进行pOVA注射(与之前相同的量)。对照动物发生针对OVA和KLH的稳健的免疫应答,这可通过抗OVA或抗KLH IgG抗体效价测量。图7中所示的第54天抗体效价证明,在同一溶液中和pOVA伴随施用之与雷帕霉素连接的合成纳米载体的3个剂量(第一给药)有效地在长时间内降低和预防针对OVA的抗体形成,而KLH则并不然(注射在另一位置s.c.)。经处理的动物甚至在5次单独pOVA的注射(第二给药)后未发生抗OVA应答。
这些结果表明,施用第一和第二给药可降低不期望的抗OVA抗体应答,并且甚至在施用OVA后仍可保持这样的降低。然而,该应答对在同一位置施用的蛋白质具有特异性。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低不期望体液免疫应答的本文中提供的施用方案。
实施例8:评价针对KLH的不期望体液免疫应答
一周一次地,在尾静脉内向对照年龄匹配的(5周至6周)雌性C57BL/6静脉内(i.v.)注射200μg钥孔林普贝血蓝蛋白(KLH),持续63天(d0、7、14、21、28、35、42、49、56、63)。使另一组接受类似的注射但在第0、7、14和21天,将0.9mg与雷帕霉素连接的合成纳米载体(ID 1、2或3)与KLH的溶液混合,之后在第28天至第63天进行6次KLH注射(相同量)。对照动物发生针对KLH的稳健应答,这可通过抗KLH IgG抗体效价以及由注射引起的过敏反应测量。由三个独立的观察者确定过敏反应评分,如下:0=无症状,1=嗜睡,2=嗜睡和不能直立,3=垂死。图8A中的结果示出了在指定时间点所有动物的血液中的抗体效价,并且由注射抗原导致的过敏反应评分示于图8B中。和KLH伴随施用之与雷帕霉素连接的合成纳米载体的4个剂量(第一给药)有效地在长时间内降低和预防抗体形成和过敏反应。事实上,经处理的动物未发生抗KLH应答,甚至在4次单独KLH的注射(第二给药)后,在对照动物中,4次单独KLH的注射在很大程度上足以产生应答(第26天)。
这些结果表明,施用第一和第二给药可降低不期望的抗KLH抗体应答,并且消除不期望的过敏反应。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对KLH的不期望体液应答的施用方案。
实施例9:评价关节炎动物中的抗HUMIRA免疫应答
过表达人肿瘤坏死因子α的转基因动物(transgenic animals overexpressinghuman tumor necrosis factor alpha,huTNFaTg)在出生后20周内发生进行性类风湿性关节炎。这一过程可通过使用全人抗人TNFα抗体HUMIRA/阿达木单抗来预防。然而,重复施用初始治疗剂量的HUMIRA(60μg)导致中和治疗益处的抗药物抗体形成(anti-drug antibodyformation,ADA)。再者,只有非常高的剂量才可维持治疗益处和克服中和性免疫应答。例如,认为,在这样的小鼠模型的一个实例中产生炎症的最大抑制需要约200μg(Binder等,Arthritis&Rheumatism,第65卷(第3期),2013年3月,第608-617页)。
对于前7次注射,在肩胛下区域内,向年龄匹配的huTNFaTg5周龄雌性动物皮下注射盐水(PBS)或60μgHUMIRA(每周),或者HUMIRA和0.87mg与雷帕霉素连接的合成纳米载体(ID1、2或3)的混合物(第0、7、14、21、28、35、42天,5周至12周龄)(第一给药),之后进行3次单独HUMIRA的注射(相同量)(第49天至第63天,13周至15周龄)(第二给药)。图9A中的结果示出了在第21天所有动物的血液中的抗体效价。如所预期的,未接受HUMIRA的对照动物无抗HUMIRA效价;而在仅接受HUMIRA的对照动物中可观察到稳健的抗体应答。相比之下,经合成纳米载体处理的动物甚至在无处理的情况下进行三次HUMIRA注射后保持完全阴性。对这些动物之肢体的监测揭示了在对照动物中在10周龄就已显现的进行性疾病。经单独HUMIRA处理的动物显著阻断疾病进程,而向该方案添加合成纳米载体极大地阻断关节炎症状的出现。图9B中所示的评分为4个独立评分员的总分,如下:1)表示滑膜炎、关节积液和软组织肿胀,2)包括增殖性发炎滑液组织,其生长进入关节腔并破坏软骨,3)表示软骨的广泛损失、关节边缘的腐蚀和畸形,4)几乎为具有关节的纤维性或骨性硬化的疾病的末期,其结束其功能寿命。
这些结果表明,施用第一和第二给药可降低不期望的抗HUMIRA抗体应答以及提高治疗性蛋白质的治疗效力。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。数据还证明了降低针对HumiraTM的不期望体液应答的施用方案。
实施例10:具有连接的布洛芬的介孔二氧化硅纳米颗粒(预示性的)
通过溶胶-凝胶法制备介孔SiO2纳米颗粒芯。将十六烷基三甲基溴化铵(Hexadecyltrimethyl-ammonium bromide,CTAB)(0.5g)溶解于去离子水(500mL)中,然后向CTAB溶液添加2M NaOH水溶液(3.5mL)。将溶液搅拌30分钟,然后向溶液添加四乙氧基硅烷(Tetraethoxysilane,TEOS)(2.5mL)。将所得凝胶在80℃的温度下搅拌3小时。通过过滤捕获形成的白色沉淀物,之后用去离子水洗涤并在室温下干燥。然后,将剩余的表面活性剂通过混悬于HCl的乙醇溶液中过夜来从颗粒中萃取。将颗粒用乙醇洗涤,离心并在超声处理下重分散。再重复该洗涤操作两次。
然后,使用(3-氨基丙基)-三乙氧基硅烷((3-aminopropyl)-triethoxysilane,APTMS)用氨基官能化SiO2纳米颗粒。为了实现这一点,将颗粒混悬于乙醇(30mL)中,并向混悬液添加APTMS(50μL)。使混悬液在室温下静置2小时,然后煮沸4小时,通过定期添加乙醇使体积保持不变。如下除去剩余的反应物:通过离心进行5个循环的洗涤并重分散于纯乙醇中。
在独立反应中,制备直径为1nm至4nm的金籽晶(gold seed)。首先,对该反应中使用的所有水进行去离子并随后从玻璃蒸馏。向100mL的圆底瓶添加水(45.5mL)。在搅拌的同时,添加0.2M NaOH水溶液(1.5mL),之后添加四(羟甲基)氯化(tetrakis(hydroxymethyl)phosphonium chloride,THPC)的1%水溶液(1.0mL)。在添加THPC溶液后2分钟,添加已陈化至少15分钟的氯金酸的10mg/mL水溶液(2mL)。通过用水透析纯化金籽晶。
为了形成芯-壳纳米载体,首先,将上述形成的氨基官能化SiO2纳米颗粒与金籽晶在室温下混合2小时。通过离心收集经金装饰的SiO2颗粒并将其与氯金酸和碳酸氢钾的水溶液混合以形成金壳。然后,通过离心并重分散于水中对颗粒进行洗涤。通过将颗粒混悬于布洛芬钠的溶液(1mg/L)中72小时装载布洛芬。然后,通过离心并重分散于水中从颗粒中洗去游离的布洛芬。
实施例11:包含环孢素A的脂质体(预示性的)
使用薄膜水合形成脂质体。将1,2-二棕榈酰基-sn-甘油基-3-磷酸胆碱(1,2-Dipalmitoyl-sn-glycero-3-phosphocholine,DPPC)(32μmol)、胆固醇(32μmol)和环孢素A(6.4μmol)溶解于纯氯仿(3mL)中。将该脂质溶液添加至50mL的圆底瓶,并在60℃的温度下在旋转蒸发器上使溶剂蒸发。然后,用氮气吹洗该瓶以除去剩余的溶剂。向该瓶添加磷酸缓冲盐水(2mL)和5个玻璃珠,通过在60℃下摇动1小时以形成混悬液来对脂质膜进行水合。将混悬液转移至小压力管并在60℃下超声处理4个30秒脉冲的循环,其中每个脉冲之间具有30秒延迟。然后,使混悬液在室温下静置2小时以允许完全水合。通过离心并随后重悬于新鲜的磷酸缓冲盐水中对脂质体进行洗涤。
实施例12:制备包含雷帕霉素的金纳米载体(AuNC)(预示性的)
制备HS-PEG-雷帕霉素:
将PEG酸二硫化物(1.0当量)、雷帕霉素(2.0当量至2.5当量)、DCC(2.5当量)和DMAP(3.0当量)在无水DMF中的溶液在室温下搅拌过夜。通过过滤除去不溶性二环己基脲并将滤液添加至异丙醇(IPA)以沉淀出PEG-二硫化物-二-雷帕霉素酯,用IPA洗涤并干燥。然后,用DMF中的三(2-羧基乙基)膦盐酸盐处理聚合物以将PEG二硫化物还原成巯基PEG雷帕霉素酯(HS-PEG-雷帕霉素)。通过从IPA中沉淀出回收所得聚合物,如前所述进行干燥并通过H NMR和GPC分析。
金NC(AuNC)的形成:
在剧烈搅拌下,将500mL 1mM HAuCl4的水溶液在装备有冷凝器的1L圆底瓶中加热回流10分钟。然后,向搅拌中的溶液迅速添加50mL40mM柠檬酸三钠的溶液。将所得的深酒红色溶液在回流下保持25分钟至30分钟并输出热量,将溶液冷却至室温。然后,通过0.8μm膜过滤器过滤溶液以得到AuNC溶液。使用可见光谱和透射电子显微术对AuNC进行表征。经柠檬酸盐包被的AuNC的直径为约20nm,并且在520nm下具有峰吸收。
具有HS-PEG-雷帕霉素的AuNC缀合物:
向1mL直径为20nm的经柠檬酸盐包被金纳米载体(1.16nM)添加150μl HS-PEG-雷帕霉素(10mM pH 9.0碳酸盐缓冲液中10μM)的溶液以产生巯基∶金为2500∶1的摩尔比。将混合物在氩气下在室温下搅拌1小时以使巯基与金纳米载体上的柠檬酸盐完全交换。然后,通过在12,000g下离心30分钟纯化表面上具有PEG-雷帕霉素的AuNC。将上清液倒出并随后用1×PBS缓冲液洗涤含有AuNC-S-PEG-雷帕霉素的沉淀物。然后,将经纯化的金-PEG-雷帕霉素纳米载体重悬于合适的缓冲液中以进行进一步的分析和生物测定。
实施例13.评价抗-PEG免疫应答
材料
雷帕霉素购自TSZ CHEM(185Wilson Street,Framingham,MA01702;产品代码R1017)。丙交酯∶乙交酯比为3∶1并且特性黏度为0.75dL/g的PLGA购自SurModicsPharmaceuticals(756Tom Martin Drive,Birmingham,AL 35211;产品代码7525DLG 7A)。甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.5DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biochemicals(756Tom Martin Drive,Birmingham,AL 35211;产品代码100DL mPEG 5000 5CE)。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa·s至4.6mPa·s)购自EMD Chemicals Inc.(480South Democrat Road Gibbstown,NJ 08027.产品代码1.41350)。
方法
如下制备溶液:
溶液1:二氯甲烷中的75mg/mL PLGA、25mg/mL PLA-PEG-OMe和12.5mg/mL的雷帕霉素。该溶液通过将PLGA、PLA-PEG-OMe和雷帕霉素溶解于纯二氯甲烷中制备。溶液2:100mMpH 8磷酸盐缓冲液中的50mg/mL聚乙烯醇。
使用水包油型乳剂制备纳米载体。如下制备O/W乳剂:将溶液1(1.0mL)和溶液2(3.0mL)合并在小压力管中并使用Branson Digital Sonifier250以30%振幅进行超声处理60秒。将O/W乳剂添加至含有70mM pH8磷酸盐缓冲溶液的烧杯并在室温下搅拌2小时以使二氯甲烷蒸发并形成纳米载体。将一部分的纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600×g和4℃下离心50分钟,除去上清液并将沉淀物重悬于磷酸缓冲盐水中。重复洗涤操作并将沉淀物重悬于磷酸缓冲盐水中以获得约10mg/mL的最终纳米载体分散体。
通过动态光散射确定纳米载体的尺寸。通过HPLC分析确定纳米载体中雷帕霉素的量。通过重量法确定总干纳米载体质量/mL混悬液。
对于前5次注射,在存在(第一给药)(第0、7、14、21、28天)或不存在0.47mg含雷帕霉素之纳米载体(NP[Rapa],50μg雷帕霉素内容物)的情况下,在尾静脉内对年龄匹配的(5周至6周)雌性C57BL/6每周(第0、7、14、21、28、35、42、49天)静脉内注射250μg钥孔林普贝血蓝蛋白和聚乙二醇的缀合物(KLH-PEG)。接下来的3次注射由相同量的单独KLH-PEG(第二给药)组成。每周(第12、20、34、40、47、54天)对这些动物的血液中针对PEG的IgM抗体应答进行监测。
如图10中所示,在相同溶液i.v.中与KLH-PEG伴随施用之合成纳米载体的5个剂量有效地预防针对PEG的抗体形成。这些结果表明,与聚乙二醇化蛋白质伴随施用之含雷帕霉素的纳米载体可降低或预防针对PEG的抗体形成。因此,施用第一和第二给药可用于降低针对聚乙二醇化治疗性蛋白质的不期望免疫应答。这些数据还证明了用于实现这样的效果的施用方案。
实施例14.评价抗HUMIRA免疫应答
使用上文实施例13中所述的材料和方法产生含雷帕霉素的纳米载体。
通过动态光散射确定纳米载体的尺寸。通过HPLC分析确定纳米载体中雷帕霉素的量。通过重量法确定总干纳米载体质量/mL混悬液。
对关节炎动物中的抗HUMIRA免疫应答和中和应答进行评价。过表达人肿瘤坏死因子α的转基因动物(huTNFaTg)在出生后20周内发生进行性类风湿性关节炎。这一过程可通过使用全人抗人TNFα抗体阿达木单抗或HUMIRA来预防。然而,重复施用初始治疗剂量的HUMIRA(60μg)导致中和治疗益处的抗药物抗体形成(ADA)。考虑到Humira的治疗效果,可注射较高量的Humira(200μg)以克服该对抗性免疫应答。
对于前3次注射(第5周至7周龄),在肩胛下区域内,向年龄匹配的huTNFaTg 5周龄雌性动物皮下注射盐水(PBS)或者60μg或200μg HUMIRA(每周)(第5周至第10周),或者60μgHUMIRA和0.87mg与致耐受性纳米颗粒的混合物(第一给药),之后按周进行3次单独HUMIRA的注射(相同量)(第二给药)(第8周至第10周龄)。图11(左图)中的结果示出了在不同时间点所有动物的血液中的抗体效价。如所预期的,经对照模拟物处理的动物无效价;而在仅接受HUMIRA的动物中可观察到稳健的抗HUMIRA抗体应答。在第5周至7周龄,用纳米载体进行处理导致完全抵抗发生抗HUMIRA效价,甚至在无处理的情况下进行3次HUMIRA注射(第8周至第10周)后。值得注意的是,三次HUMIRA注射导致对照动物具有非常高的效价(第7周效价),而经纳米载体处理动物中的三次类似注射(总共6次注射)则完全抵抗发生效价(第10周)。图12示出了给药方案。
对这些动物之肢体的监测揭示了在6周龄就已显现的进行性疾病。单独HUMIRA显著阻断疾病进程,而向该方案添加纳米载体极大地阻断关节炎症状的出现。评分(图11(右图))为4个独立评分员的平均总分,如下:1)表示滑膜炎、关节积液和软组织肿胀,2)包括增殖性发炎滑液组织,其生长进入关节腔并破坏软骨,3)表示软骨的广泛损失、关节边缘的腐蚀和畸形,以及4)几乎为具有关节的纤维性或骨性硬化的疾病的末期,其结束其功能寿命。
这些结果表明,本文中提供的方法和组合物可降低或预防针对治疗性蛋白质的抗体形成,并且提高其效力和治疗窗。特别地,这些结果表明,施用第一和第二给药可降低不期望的抗HUMIRA抗体应答,以及提高治疗性蛋白质的治疗效力。这证明,本文中提供的第一和第二给药降低针对蛋白质的不期望体液免疫应答。还提供了降低针对HumiraTM的不期望体液应答的施用方案。
实施例15:针对具有经包封雷帕霉素的鸡卵清蛋白的抗体特异性致耐受性应答
NP[Rapa]材料和方法
材料
雷帕霉素购自TSZ CHEM(185Wilson Street,Framingham,MA01702),产品代码R1017。丙交酯∶乙交酯之比为1∶1并且特性黏度为0.24dL/g的PLGA购自LakeshoreBiomaterials(756Tom Martin Drive,Birmingham,AL 35211),产品代码5050 DLG 2.5A。甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.50DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biomaterials(756Tom Martin Drive,Birmingham,AL 35211),产品代码100DL mPEG 5000 5CE。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa·s至4.6mPa·s)购自EMD Chemicals Inc.(480 South Democrat RoadGibbstown,NJ 08027),产品代码1.41350。Cellgro磷酸缓冲盐水1×(PBS1×)购自Corning(9345 Discovery Blvd.Manassas,VA 20109),产品代码21-040-CV。
方法
如下制备溶液:
溶液1:聚合物和雷帕霉素混合物通过将75mg/mL PLGA、25mg/mL PLA-PEG-OMe和12.5mg/mL雷帕霉素溶解于二氯甲烷中制备。溶液2:在100mM pH 8磷酸盐缓冲液中以50mg/mL制备聚乙烯醇。
如下制备O/W乳剂:将溶液1(1.0mL)和溶液2(3.0mL)合并在小压力管中并使用Branson Digital Sonifier 250以30%振幅进行超声处理60秒。将O/W乳剂添加至含有70mM pH 8磷酸盐缓冲溶液(60mL)的敞开烧杯。制备另外三份相同的O/W乳剂,并添加至与第一乳剂相同的烧杯。然后,将这些乳剂在室温下搅拌2小时以使二氯甲烷蒸发并形成纳米载体。将一部分的纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600×g和4℃下离心35分钟,除去上清液并将沉淀物重悬于PBS 1X中。重复洗涤操作并将沉淀物重悬于PBS 1X中以获得基于聚合物的标称浓度为10mg/mL的纳米载体混悬液。如上所述在独立烧杯中制备相同的配制物并在洗涤步骤之后与第一配制物合并。使用来自Pall型号4656的1.2μm PES膜注射式过滤器过滤经混合的纳米载体溶液并将其储存在-20℃下。
通过动态光散射确定纳米载体的尺寸。通过HPLC分析确定纳米载体中雷帕霉素的量。通过重量法确定总干纳米载体质量/mL混悬液。
NP[OVA]材料和方法
材料
卵清蛋白购自Worthington Biochemical Corporation(730Vassar Avenue,Lakewood,NJ 08701),产品代码LS003054)。具有54%丙交酯和46%乙交酯含量并且特性黏度为0.24dL/g的PLGA购自Lakeshore Biomaterials(756Tom Martin Drive,Birmingham,AL 35211),产品代码5050 DLG 2.5A)。甲基醚封端的PEG嵌段为约5,000Da并且Mw为28,000Da,特性黏度为0.38dL/g的PLA-PEG嵌段共聚物购自Lakeshore Biomaterials(756 TomMartin Drive,Birmingham,AL 35211),产品代码100DL mPEG 5000 4CE。聚乙烯醇4-88,USP(85%至89%水解的,黏度为3.4mPa.s至4.6mPa.s)购自EMD ChemicalsInc.(480South Democrat Road Gibbstown,NJ 08027),产品代码1.41350.1001。Cellgro磷酸缓冲盐水1X(PBS 1X)购自Corning(9345Discovery Blvd.Manassas,VA 20109),产品代码21-040-CV。
方法
如下制备溶液:
溶液1:在具有10重量%蔗糖的10mM磷酸盐缓冲液pH 8中制备50mg/mL卵清蛋白。溶液2:PLGA通过在化学通风橱中以100mg/mL二氯甲烷溶解PLGA制备。溶液3:PLA-PEG-OMe通过在化学通风橱中以100mg/mL二氯甲烷溶解PLA-PEG-OMe制备。溶液4∶100mM磷酸盐缓冲液,pH 8中的65mg/mL聚乙烯醇。
首先,通过将溶液1至溶液3混合制备初级(W1/O)乳剂。将溶液1(0.2mL)、溶液2(0.75mL)和溶液3(0.25mL)合并在经在冰水浴中预冷却>4分钟的小玻璃压力管中并使用Branson Digital Sonifier 250在冰浴上以50%振幅进行超声处理40秒。然后,如下形成次级(W1/O/W2)乳剂:向初级乳剂添加溶液4(3mL),涡旋混合以产生乳状分散体并随后使用Branson Digital Sonifier 250在冰浴上以30%振幅进行超声处理60秒。将次级乳剂添加至含有PBS 1X(30mL)的敞开50mL烧杯。如上所述制备第二相同的双乳剂配制物并添加至与第一乳剂配制物相同的50mL烧杯。将两份制备物在室温下搅拌2小时以使二氯甲烷蒸发并在混悬液中形成纳米载体。将一部分的混悬的纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600rcf下离心50分钟,除去上清液并将沉淀物重悬于PBS 1X中。重复洗涤操作并将沉淀物重悬于PBS 1X中以获得基于聚合物的标称浓度为10mg/mL的纳米载体混悬液。将混悬液冷冻储存在-20℃下直至使用。
NP[GSK1059615]材料和方法
材料
GSK1059615购自MedChem Express(11Deer Park Drive,Suite102D MonmouthJunction,NJ 08852),产品代码HY-12036。丙交酯∶乙交酯之比为1∶1并且特性黏度为0.24dL/g的PLGA购自Lakeshore Biomaterials(756Tom Martin Drive,Birmingham,AL35211),产品代码5050 DLG 2.5A。具有甲基醚封端的PEG嵌段为约5,000Da并且整体特性黏度为0.26DL/g的PLA-PEG-OMe嵌段共聚物购自Lakeshore Biomaterials(756Tom Martin Drive,Birmingham,AL 35211;产品代码100DL mPEG 5000 5K-E)。Cellgro磷酸缓冲盐水1X pH7.4(PBS 1X)购自Corning(9345Discovery Blvd.Manassas,VA 20109),产品代码21-040-CV。
方法
如下制备溶液
溶液1:将PLGA(125mg)和PLA-PEG-OMe(125mg)溶解于10mL丙酮中。溶液2:以1mLN-甲基-2-吡咯烷酮(NMP)中10mg制备GSK1059615。
如下制备纳米载体:将溶液1(4mL)和溶液2(0.25mL)合并在小玻璃压力管中并在搅拌下将混合物逐滴添加至含有20mL超纯水的250mL圆底瓶。将该瓶安装在旋转式蒸发装置上,并在减压下除去丙酮。将一部分的纳米载体经如下洗涤:将纳米载体混悬液转移至离心管并在75,600rcf和4℃下离心50分钟,除去上清液并将沉淀物重悬于PBS 1X中。重复洗涤操作并将沉淀物重悬于PBS 1X中以获得基于聚合物的标称浓度为10mg/mL的纳米载体混悬液。然后,使用来自Pall,型号4656的1.2μm PES膜注射式过滤器过滤经洗涤的纳米载体溶液。如上所述制备相同的纳米载体溶液并在过滤步骤之后与第一纳米载体溶液合并。将均质混悬液冷冻储存在-20℃下。
通过动态光散射确定纳米载体的尺寸。通过351nm下的UV吸收确纳米载体中GSK1059615的量。通过重量法确定总干纳米载体质量/mL混暴液。
在第-21天和第-14天,在尾静脉内对年龄匹配的(5周至6周)雌性C57BL/6小鼠静脉内注射盐水(未处理),与1.2mg含雷帕霉素之纳米载体(NP[Rapa])(第一给药)或8mg装载GSK1059615之纳米载体(NP[GSK1059615])组合的1.1mg装载全卵清蛋白的纳米载体(NP[OVA])。
在第0天,在后肢内对所有动物皮下注射与2μg CpG混合的25μg颗粒OVA(pOVA),随后在第7天和第14天仅注射25μg pOVA(第二给药)。在第21天,测量抗体效价。在不存在任何处理的情况下,动物发生针对OVA的稳健免疫应答,其可通过抗OVA IgG抗体效价进行测量。图13中所示之第21天的抗体效价证明:在相同溶液(NP[OVA]+NP[Rapa]或NP[GSK1059615])中与经包封OVA伴随施用的两种合成致耐受性纳米载体剂量甚至在单独注射1次OVA+CpG1次和注射2次OVA后有效地降低针对OVA的抗体形成。
这些结果表明:经包封的免疫抑制剂(例如,雷帕霉素和GSK1059615)当与蛋白质伴随递送时可在多次攻击和多个时间段内预防针对该蛋白质的抗体形成。另外,该实施例提供了用于降低不期望体液免疫应答的第一和第二给药的有效方案。
实施例16.使用合成纳米载体和HUMIRA/阿达木单抗的本发明给药(预示性的)
制备实施例11的合成纳米载体和HUMIRA以用于处于发生针对HUMIRA之抗药物抗体应答的风险之中的人对象中的第一给药。第一给药包括HUMIRA(40mg)和实施例11的合成纳米载体(50mg)的3个伴随q2周施用。第二给药包括单独HUMIRA(无合成纳米载体)的3个q2周施用。产生施用方案,其中在第一给药之后进行第二给药。在第一给药之前和第二给药之后,评价人对象的抗HUMIRA抗体(使用标准ELISA技术)。注意两个抗HUMIRA抗体读出之间的任何差异。
实施例17.使用合成纳米载体和HUMIRA/阿达木单抗的本发明给药(预示性的)
制备实施例1的合成纳米载体,纳米载体ID 1。将其与HUMIRA组合并以根据以下方案伴随施用的第一给药和第二给药进行施用,如表1中所示。
表1:
实施例18.使用合成纳米载体和mmRNA的本发明给药(预示性的)
制备实施例11的合成纳米载体和编码天冬酰胺酶的mmRNA(一般根据deFougerolles等的美国专利申请2013/0115272制备,(“mmRNA”))以用于处于发生针对mmRNA之抗药物抗体应答的风险之中的人对象中的第一给药。第一给药包括mmRNA(100ng)和实施例11的合成纳米载体(50mg)的3个伴随q2周施用。第二给药包括单独mmRNA的3个q2周施用(无合成纳米载体)。产生施用方案,其中在第一给药之后进行第二给药。在第一给药之前和第二给药之后,评价对人对象的抗mmRNA抗体(使用标准ELISA技术)。注意两个抗mmRNA抗体读出之间的任何差异。
实施例19.针对具有纳米结晶雷帕霉素的鸡卵清蛋白的抗原特异性致耐受性应答
(预示性的)
在第-21天和第-14天,在尾静脉内向年龄匹配的(5周至6周)雌性C57BL/6小鼠静脉内注射盐水(未处理),或者1.1mg全卵清蛋白和1.2mg纳米结晶雷帕霉素(第一给药)。
在第0天,在后肢内向所有动物皮下注射与2μg CpG混合之25μg颗粒OVA(pOVA)的第一给药,随后在第7天和第14天仅注射25μg pOVA(第二给药)。在第21天,测量抗体效价。在不存在任何处理的情况下,动物发生针对OVA的稳健免疫应答,其可通过抗OVA IgG抗体效价进行测量。
在接受OVA与纳米结晶雷帕霉素之组合的动物中OVA特异性IgG抗体降低表明:纳米结晶形式的免疫抑制剂当与蛋白质伴随递送时可在多次攻击和多个时间段内预防针对该蛋白质的抗体形成。
实施例20.使用纳米结晶免疫抑制剂和HUMIRA/阿达木单抗的本发明给药(预示性
的)
购买纳米结晶雷帕霉素。将纳米结晶雷帕霉素与HUMIRA组合并以根据如表1中所示的以下方案伴随施用的第一给药和第二给药进行施用。
实施例21.使用纳米结晶免疫抑制剂和mmRNA的本发明给药(预示性的)
购买纳米结晶雷帕霉素并制备编码天冬酰胺酶的mmRNA(一般根据deFougerolles等的美国专利申请2013/0115272制备,(“mmRNA”))以用于处于发生针对mmRNA之抗药物抗体应答的风险之中的人对象中的第一给药。第一给药包括mmRNA(100ng)和纳米结晶雷帕霉素(50mg)的3个伴随q2周施用。第二给药包括单独mmRNA的3个q2周施用(无纳米结晶雷帕霉素)。产生施用方案,其中在第一给药之后进行第二给药。在第一给药之前和第二给药之后,评价对人对象的抗mmRNA抗体(使用标准ELISA技术)。注意两个抗mmRNA抗体读出之间的任何差异。
本发明还涉及以下实施方案:
1.一种方法,其包括:
(1)第一给药,其包括伴随施用
(a)未与任何合成纳米载体连接的治疗性大分子,和
(b)合成纳米载体群,其与免疫抑制剂连接,并且不包含所述治疗性大分子的治疗性大分子抗原呈递细胞(APC)可呈递抗原;
(2)第二给药,其包括
(c)施用所述未与任何合成纳米载体连接的治疗性大分子,并且不施用任何合成纳米载体;以及
(3)根据降低针对所述治疗性大分子的不期望体液免疫应答的施用方案向对象施用所述第一和第二给药。
2.实施方案1所述的方法,其还包括(4)确定降低针对所述治疗性大分子的不期望体液免疫应答的用于所述第一和第二给药的施用方案。
3.实施方案1或2所述的方法,其中所述针对所述治疗性大分子的不期望体液免疫应答由无所述第一给药的所述第二给药引起。
4.实施方案1至3中任一项所述的方法,其中所述第一给药包括向所述对象施用(a)和(b)一次或更多次。
5.实施方案4所述的方法,其中(a)和(b)施用至少1、2、3、4或5次。
6.实施方案1至5中任一项所述的方法,其中在所述第一给药之后至少1、2、3、4、5、6、7或8周,向所述对象施用所述第二给药。
7.实施方案1至6中任一项所述的方法,其中所述方法还包括在施用所述第一给药和第二给药之前和/或之后在所述对象中评估所述不期望体液免疫应答。
8.实施方案1至7中任一项所述的方法,其中所述第一给药和/或第二给药的施用通过静脉内、腹膜内或皮下施用进行。
9.实施方案1至8中任一项所述的方法,其中所述方法还包括鉴定所述对象为具有针对所述治疗性大分子的不期望体液免疫应答或者处于其风险之中。
10.一种组合物,其包含:
(1)一个或更多个第一剂量,其各自包含
(a)未与任何合成纳米载体连接的治疗性大分子,和
(b)合成纳米载体群,其与免疫抑制剂连接,并且不包含所述治疗性大分子的治疗性大分子APC可呈递抗原;以及
(2)包含未与任何合成纳米载体连接的治疗性大分子的一个或更多个第二剂量,所述组合物用于降低针对所述治疗性大分子的不期望体液免疫应答的方法,其中所述方法包括根据施用方案向对象施用所述第一和第二剂量。
11.实施方案10所述的组合物,其中所述第二剂量不包含任何合成纳米载体。
12.实施方案10或11所述的组合物,其中所述方法还包括确定降低针对所述治疗性大分子的不期望体液免疫应答的用于所述第一和第二剂量的施用方案。
13.实施方案10至12中任一项所述的组合物,其中所述方法为本文中所提供的任意方法。
14.实施方案10至13中任一项所述的组合物,其中所述组合物为药盒并且所述第一剂量和所述第二剂量的一个或更多个各自容纳在所述药盒中的容器中。
15.实施方案10至13中任一项所述的组合物,其中所述组合物还包含可药用载体。
16.前述实施方案中任一项所述的方法或组合物,其中所述免疫抑制剂包含:他汀类、mTOR抑制剂、TGF-β信号传导剂、皮质类固醇、线粒体功能的抑制剂、P38抑制剂、NF-κB抑制剂、腺苷受体激动剂、前列腺素E2激动剂、磷酸二酯酶4抑制剂、HDAC抑制剂或蛋白酶体抑制剂。
17.实施方案16所述的方法或组合物,其中所述mTOR抑制剂是雷帕霉素。
18.前述实施方案中任一项所述的方法或组合物,其中所述治疗性大分子是治疗性蛋白质。
19.实施方案18所述的方法或组合物,其中所述治疗性蛋白质用于蛋白质替代或蛋白质补充治疗。
20.前述实施方案中任一项所述的方法或组合物,其中所述治疗性大分子包含:可输注或可注射的治疗性蛋白质、酶、酶辅因子、激素、血液因子或凝血因子、细胞因子、干扰素、生长因子、单克隆抗体、多克隆抗体或与庞皮病相关的蛋白质。
21.实施方案20所述的方法或组合物,其中所述可输注或可注射的治疗性蛋白质包含:托珠单抗、α-1抗胰蛋白酶、Hematide、白蛋白干扰素α-2b、Rhucin、替莫瑞林、奥瑞珠单抗、贝利木单抗、聚乙二醇化重组尿酸酶、他利苷酶α、阿加糖酶α或葡糖脑苷脂酶α。
22.实施方案20所述的方法或组合物,其中所述酶包含氧化还原酶、转移酶、水解酶、裂合酶、异构酶或连接酶。
23.实施方案20所述的方法或组合物,其中所述酶包含用于对溶酶体贮积症进行酶替代治疗的酶。
24.实施方案23所述的方法或组合物,其中所述用于对溶酶体贮积症进行酶替代治疗的酶包含:伊米苷酶、a-半乳糖苷酶A(a-gal A)、阿加糖酶β、酸性α-葡糖苷酶(GAA)、阿葡糖苷酶α、LUMIZYME、MYOZYME、芳基硫酸酯酶B、拉罗尼酶、ALDURAZYME、艾杜硫酶、ELAPRASE、芳基硫酸酯酶B或NAGLAZYME。
25.实施方案20所述的方法或组合物,其中所述酶包含KRYSTEXXA(聚乙二醇化重组尿酸酶)或聚乙二醇化重组假丝酵母尿酸酶。
26.实施方案20所述的方法或组合物,其中所述单克隆抗体包含HUMIRA(阿达木单抗)。
27.实施方案20所述的方法或组合物,其中所述细胞因子包含:淋巴因子、白介素、趋化因子、1型细胞因子或2型细胞因子。
28.实施方案20所述的方法或组合物,其中所述血液因子或凝血因子包含:因子I、因子II、组织因子、因子V、因子VII、因子VIII、因子IX、因子X、因子Xa、因子XII、因子XIII、冯·维勒布兰德因子、前激肽释放酶、高分子量激肽原、纤连蛋白、抗凝血酶III、肝素辅因子II、蛋白C、蛋白S、蛋白Z、蛋白Z相关蛋白酶抑制剂(ZPI)、纤溶酶原、α2-抗纤溶酶、组织纤溶酶原激活物(tPA)、尿激酶、纤溶酶原激活物抑制剂-1(PAI1)、纤溶酶原激活物抑制剂-2(PAI2)、癌促凝物质或阿法依伯汀。
29.实施方案29所述的方法或组合物,其中所述血液因子或凝血因子包含因子VIII。
30.前述实施方案中任一项所述的方法或组合物,其中基于整个所述合成纳米载体群的平均值,所述免疫抑制剂的载量为0.1%至50%。
31.实施方案30所述的方法或组合物,其中基于整个所述合成纳米载体群的平均值,所述免疫抑制剂的载量为0.1%至20%。
32.前述实施方案中任一项所述的方法或组合物,其中所述群中的合成纳米载体包含:脂质纳米颗粒、聚合物纳米颗粒、金属纳米颗粒、基于表面活性剂的乳剂、树状聚体、巴基球、纳米线、病毒样颗粒或者肽或蛋白质颗粒。
33.实施方案32所述的方法或组合物,其中所述群中的合成纳米载体包含脂质纳米颗粒。
34.实施方案32所述的方法或组合物,其中所述群中的合成纳米载体包含脂质体。
35.实施方案32所述的方法或组合物,其中所述群中的合成纳米载体包含金属纳米颗粒。
36.实施方案35所述的方法或组合物,其中所述金属纳米颗粒包含金纳米颗粒。
37.实施方案32所述的方法或组合物,其中所述群中的合成纳米载体包含聚合物纳米颗粒。
38.实施方案37所述的方法或组合物,其中所述聚合物纳米颗粒包含聚合物,所述聚合物为非甲氧基封端的普朗尼克聚合物。
40.实施方案39所述的方法或组合物,其中所述聚酯包含聚(乳酸)、聚(乙醇酸)、聚乳酸-乙醇酸共聚物或聚己内酯。
41.实施方案39或40所述的方法或组合物,其中所述聚合物纳米颗粒包含聚酯和与聚醚偶联的聚酯。
42.实施方案39至41中任一项所述的方法或组合物,其中所述聚醚包含聚乙二醇或聚丙二醇。
43.前述实施方案中任一项所述的方法或组合物,其中使用所述群中的合成纳米载体的动态光散射获得的颗粒大小分布的平均值为大于100nm的直径。
44.实施方案43所述的方法或组合物,其中所述直径大于150nm。
45.实施方案44所述的方法或组合物,其中所述直径大于200nm。
46.实施方案45所述的方法或组合物,其中所述直径大于250nm。
47.实施方案46所述的方法或组合物,其中所述直径大于300nm。
48.前述实施方案中任一项所述的方法或组合物,其中所述群中的所述合成纳米载体的纵横比大于1∶1、1∶1.2、1∶1.5、1∶2、1∶3、1∶5、1∶7或1∶10。
Claims (10)
1.一种方法,其包括:
(1)第一给药,其包括伴随施用
(a)未与任何合成纳米载体连接的治疗性大分子,和
(b)合成纳米载体群,其与免疫抑制剂连接,并且不包含所述治疗性大分子的治疗性大分子抗原呈递细胞(APC)可呈递抗原;
(2)第二给药,其包括
(c)施用所述未与任何合成纳米载体连接的治疗性大分子,并且不施用任何合成纳米载体;以及
(3)根据降低针对所述治疗性大分子的不期望体液免疫应答的施用方案向对象施用所述第一和第二给药。
2.权利要求1所述的方法,其还包括(4)确定降低针对所述治疗性大分子的不期望体液免疫应答的用于所述第一和第二给药的施用方案。
3.权利要求1或2所述的方法,其中所述针对所述治疗性大分子的不期望体液免疫应答由无所述第一给药的所述第二给药引起。
4.权利要求1至3中任一项所述的方法,其中所述第一给药包括向所述对象施用(a)和(b)一次或更多次。
5.权利要求4所述的方法,其中(a)和(b)施用至少1、2、3、4或5次。
6.权利要求1至5中任一项所述的方法,其中在所述第一给药之后至少1、2、3、4、5、6、7或8周,向所述对象施用所述第二给药。
7.权利要求1至6中任一项所述的方法,其中所述方法还包括在施用所述第一给药和第二给药之前和/或之后在所述对象中评估所述不期望体液免疫应答。
8.权利要求1至7中任一项所述的方法,其中所述第一给药和/或第二给药的施用通过静脉内、腹膜内或皮下施用进行。
9.权利要求1至8中任一项所述的方法,其中所述方法还包括鉴定所述对象为具有针对所述治疗性大分子的不期望体液免疫应答或者处于其风险之中。
10.一种组合物,其包含:
(1)一个或更多个第一剂量,其各自包含
(a)未与任何合成纳米载体连接的治疗性大分子,和
(b)合成纳米载体群,其与免疫抑制剂连接,并且不包含所述治疗性大分子的治疗性大分子APC可呈递抗原;以及
(2)包含未与任何合成纳米载体连接的治疗性大分子的一个或更多个第二剂量,所述组合物用于降低针对所述治疗性大分子的不期望体液免疫应答的方法,其中所述方法包括根据施用方案向对象施用所述第一和第二剂量。
Applications Claiming Priority (15)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361819517P | 2013-05-03 | 2013-05-03 | |
| US61/819,517 | 2013-05-03 | ||
| US201361881921P | 2013-09-24 | 2013-09-24 | |
| US201361881851P | 2013-09-24 | 2013-09-24 | |
| US201361881913P | 2013-09-24 | 2013-09-24 | |
| US61/881,851 | 2013-09-24 | ||
| US61/881,921 | 2013-09-24 | ||
| US61/881,913 | 2013-09-24 | ||
| US201361907177P | 2013-11-21 | 2013-11-21 | |
| US61/907,177 | 2013-11-21 | ||
| US201461948313P | 2014-03-05 | 2014-03-05 | |
| US201461948384P | 2014-03-05 | 2014-03-05 | |
| US61/948,384 | 2014-03-05 | ||
| US61/948,313 | 2014-03-05 | ||
| CN201480031937.3A CN105307641A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201480031937.3A Division CN105307641A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN111068061A true CN111068061A (zh) | 2020-04-28 |
Family
ID=51841530
Family Applications (18)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201911069459.6A Pending CN110841066A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480037123.0A Pending CN105339012A (zh) | 2013-05-03 | 2014-05-02 | 降低i型和iv型超敏反应的致耐受性合成纳米载体的局部伴随施用 |
| CN201911069542.3A Pending CN110841067A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480032251.6A Pending CN105283175A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN202010594335.6A Pending CN111760025A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
| CN201480034670.3A Pending CN105338968A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN201911307714.6A Pending CN111053908A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
| CN201910874364.5A Pending CN110694077A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN201910552107.XA Pending CN110251676A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN201910552053.7A Pending CN110251675A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN202010594054.0A Pending CN111686255A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
| CN201911306104.4A Pending CN111068061A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
| CN201910874452.5A Pending CN110639024A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN202410981673.3A Pending CN118987263A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN202410347642.2A Pending CN118370823A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480032224.9A Pending CN105263478A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
| CN201480031937.3A Pending CN105307641A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
| CN201480037076.XA Pending CN105338979A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
Family Applications Before (11)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201911069459.6A Pending CN110841066A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480037123.0A Pending CN105339012A (zh) | 2013-05-03 | 2014-05-02 | 降低i型和iv型超敏反应的致耐受性合成纳米载体的局部伴随施用 |
| CN201911069542.3A Pending CN110841067A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480032251.6A Pending CN105283175A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN202010594335.6A Pending CN111760025A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
| CN201480034670.3A Pending CN105338968A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN201911307714.6A Pending CN111053908A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
| CN201910874364.5A Pending CN110694077A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN201910552107.XA Pending CN110251676A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN201910552053.7A Pending CN110251675A (zh) | 2013-05-03 | 2014-05-02 | 降低或预防响应于非变应原性抗原的过敏反应的致耐受性合成纳米载体 |
| CN202010594054.0A Pending CN111686255A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
Family Applications After (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201910874452.5A Pending CN110639024A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN202410981673.3A Pending CN118987263A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
| CN202410347642.2A Pending CN118370823A (zh) | 2013-05-03 | 2014-05-02 | 用于降低的或增强的药效学作用的致耐受性合成纳米载体和治疗性大分子 |
| CN201480032224.9A Pending CN105263478A (zh) | 2013-05-03 | 2014-05-02 | 用于诱导免疫耐受的具有特定药效学有效持续期之免疫抑制剂与抗原的递送 |
| CN201480031937.3A Pending CN105307641A (zh) | 2013-05-03 | 2014-05-02 | 用于降低不期望体液免疫应答的给药组合 |
| CN201480037076.XA Pending CN105338979A (zh) | 2013-05-03 | 2014-05-02 | 用于增强cd4+调节性t细胞的方法和组合物 |
Country Status (15)
| Country | Link |
|---|---|
| US (15) | US10357483B2 (zh) |
| EP (7) | EP3763359A1 (zh) |
| JP (19) | JP2016520051A (zh) |
| KR (18) | KR20240119155A (zh) |
| CN (18) | CN110841066A (zh) |
| AU (16) | AU2014262165B2 (zh) |
| BR (6) | BR112015027279A8 (zh) |
| CA (5) | CA2910584A1 (zh) |
| DK (1) | DK2991646T3 (zh) |
| EA (6) | EA201592103A3 (zh) |
| ES (1) | ES2842206T3 (zh) |
| HU (1) | HUE052599T2 (zh) |
| IL (14) | IL284732B2 (zh) |
| MX (12) | MX382604B (zh) |
| WO (5) | WO2014179772A2 (zh) |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MX357630B (es) | 2009-05-27 | 2018-07-17 | Selecta Biosciences Inc | Nanoportadores sintéticos objetivo con liberación sensible al ph de agentes inmunomoduladores. |
| EA030813B1 (ru) | 2010-05-26 | 2018-10-31 | Селекта Байосайенсиз, Инк | Способы генерации антительного иммунного ответа и увеличения местной индукции иммунных цитокинов при использовании синтетических наноносителей, соединенных с адъювантами |
| US9994443B2 (en) | 2010-11-05 | 2018-06-12 | Selecta Biosciences, Inc. | Modified nicotinic compounds and related methods |
| MX2013012596A (es) | 2011-04-29 | 2014-08-21 | Selecta Biosciences Inc | Nanoportadores sintéticos tolerogénicos para generar linfocitos t reguladores cd8+. |
| WO2013019648A1 (en) | 2011-07-29 | 2013-02-07 | Selecta Biosciences, Inc. | Control of antibody responses to synthetic nanocarriers |
| BR112015027279A8 (pt) | 2013-05-03 | 2018-01-30 | Selecta Biosciences Inc | métodos e composições para acentuar células t reguladoras cd4+ |
| US20160074532A1 (en) | 2014-09-07 | 2016-03-17 | Selecta Biosciences, Inc. | Methods and compositions for attenuating gene editing anti-viral transfer vector immune responses |
| WO2017025889A1 (en) * | 2015-08-13 | 2017-02-16 | Pfizer Inc. | Polymeric nanoparticles with dec-205 ligand and co-encapsulating an antigen subject to an autoimmune response and a glucocorticoid receptor agonist |
| US10744209B2 (en) | 2015-11-12 | 2020-08-18 | New York University | Biodegradable polymeric nanoparticle conjugates and use thereof |
| DK3426285T3 (da) * | 2016-03-11 | 2024-08-26 | Cartesian Therapeutics Inc | Formuleringer og doser af pegyleret uricase |
| US11458106B2 (en) | 2016-05-09 | 2022-10-04 | Astrazeneca Ab | Lipid nanoparticles comprising lipophilic anti-inflammatory agents and methods of use thereof |
| EP3494208A1 (en) * | 2016-08-05 | 2019-06-12 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Ex vivo generation of gamma delta foxp3+ regulatory t cells and therapeutic uses thereof |
| EP3494209A1 (en) * | 2016-08-05 | 2019-06-12 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Ex vivo generation of mhcii restricted cd4+foxp3+ regulatory t cells and therapeutic uses thereof |
| JP2020506890A (ja) * | 2017-01-07 | 2020-03-05 | セレクタ バイオサイエンシーズ インコーポレーテッドSelecta Biosciences,Inc. | 合成ナノキャリアにカップリングした免疫抑制剤のパターン化された投与 |
| EP3592389B1 (en) | 2017-03-11 | 2025-05-07 | Cartesian Therapeutics, Inc. | Methods and compositions related to combined treatment with anti-inflammatories and synthetic nanocarriers comprising an immunosuppressant |
| KR20200086670A (ko) * | 2017-10-13 | 2020-07-17 | 셀렉타 바이오사이언시즈, 인크. | 항바이러스 전달 벡터 IgM 반응을 약화시키기 위한 방법 및 조성물 |
| US20200400685A1 (en) * | 2017-12-27 | 2020-12-24 | Vito Nv | Biomarkers for Typing Allograft Recipients |
| CN108295303A (zh) * | 2018-02-08 | 2018-07-20 | 中山大学附属第三医院(中山大学肝脏病医院) | 一种钛金属植入物及其制备方法和用途 |
| WO2019184993A1 (zh) * | 2018-03-29 | 2019-10-03 | 天津键凯科技有限公司 | 聚乙二醇与雷帕霉素的结合物及其用途 |
| CN109045304B (zh) * | 2018-04-13 | 2022-04-05 | 中山大学 | 一种携带Polymerase I抑制剂的核仁靶向纳米载体及其制备方法和应用 |
| WO2021016293A1 (en) * | 2019-07-22 | 2021-01-28 | University Of Louisville Research Foundation, Inc. | Immunomodulatory compositions and methods of using |
| WO2021096972A1 (en) * | 2019-11-11 | 2021-05-20 | The Regents Of The University Of California | Polymeric nanoparticles that target liver sinusoidal endothelial cells to induce antigen-specific immune tolerance |
| CN110747276B (zh) * | 2019-11-22 | 2020-06-30 | 山东大学齐鲁医院 | Bace2作为胶质瘤预后/诊断/治疗标志物的应用 |
| CA3173734A1 (en) * | 2020-02-26 | 2021-09-02 | Selecta Biosciences, Inc. | Methods and compositions using synthetic nanocarriers comprising immunosuppressant |
| EP4135693A1 (en) * | 2020-04-14 | 2023-02-22 | Selecta Biosciences, Inc. | Methods and compositions for inducing autophagy |
| CN113825832B (zh) * | 2020-07-28 | 2024-12-13 | 浙江大学 | 一种体外诱导CD4+Foxp3+CD69+Treg的扩增方法及其用途 |
| WO2022022599A1 (zh) * | 2020-07-28 | 2022-02-03 | 浙江大学 | 一种体外诱导CD4 +Foxp3 +CD69 +Treg的扩增方法及其用途 |
| JP7544541B2 (ja) | 2020-09-14 | 2024-09-03 | 聡 安斎 | 地盤掘削装置 |
| CN112480244A (zh) * | 2020-11-24 | 2021-03-12 | 华科同济干细胞基因工程有限公司 | 一种抗过敏性纳米抗体组合物、抗体测定方法及喷雾剂 |
| CN112961831B (zh) * | 2021-02-26 | 2022-10-11 | 仲恺农业工程学院 | 一种肠源外泌体的制备方法 |
| EP4323015A4 (en) | 2021-04-16 | 2025-10-22 | Askbio Inc | RATIONALLY POLYPLOID AAV VIRIONS CROSS THE BLOOD-BRAIN BARRIER AND TRIGGER A REDUCED HUMORAL RESPONSE |
| WO2023086615A1 (en) * | 2021-11-14 | 2023-05-19 | Selecta Biosciences, Inc. | Multiple dosing with viral vectors |
| JP2025541237A (ja) * | 2022-12-13 | 2025-12-18 | デイナ ファーバー キャンサー インスティチュート,インコーポレイテッド | 免疫療法を強化するためのチェックポイントモジュレーター |
| WO2024181580A1 (ja) | 2023-03-02 | 2024-09-06 | 国立研究開発法人科学技術振興機構 | 脂質ナノ粒子、医薬組成物、および脂質ナノ粒子の製造方法 |
| WO2024190532A1 (ja) | 2023-03-14 | 2024-09-19 | 株式会社フジミインコーポレーテッド | 研磨用組成物、研磨用組成物の濃縮液および研磨方法 |
| WO2025256977A1 (en) | 2024-06-13 | 2025-12-18 | Bayer Aktiengesellschaft | Novel igm and igg cleaving enzymes |
| WO2025256978A1 (en) | 2024-06-13 | 2025-12-18 | Bayer Aktiengesellschaft | Variants of igm and igg cleaving enzymes |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1795185A2 (en) * | 2005-12-07 | 2007-06-13 | Cordis Corporation | Nano- and/or micro-particulate formulations for local injection-based treatment of vascular diseases |
| CN1979166A (zh) * | 2005-11-30 | 2007-06-13 | 北京有色金属研究总院 | 一种制备免疫检测用纳米胶体金的工艺方法及其反应装置 |
| CN101437491A (zh) * | 2006-02-21 | 2009-05-20 | 洛桑聚合联合学院 | 用于免疫疗法的纳米颗粒 |
| WO2012149255A2 (en) * | 2011-04-29 | 2012-11-01 | Selecta Biosciences, Inc. | Tolerogenic synthetic nanocarriers to reduce immune responses to therapeutic proteins |
| CN102871966A (zh) * | 2012-10-19 | 2013-01-16 | 东南大学 | 用于改善雷帕霉素生物利用度的纳米载药颗粒及其制备方法 |
Family Cites Families (289)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1995A (en) | 1841-03-03 | Latch of door and other locks | ||
| US4946929A (en) | 1983-03-22 | 1990-08-07 | Massachusetts Institute Of Technology | Bioerodible articles useful as implants and prostheses having predictable degradation rates |
| US4638045A (en) | 1985-02-19 | 1987-01-20 | Massachusetts Institute Of Technology | Non-peptide polyamino acid bioerodible polymers |
| US4806621A (en) | 1986-01-21 | 1989-02-21 | Massachusetts Institute Of Technology | Biocompatible, bioerodible, hydrophobic, implantable polyimino carbonate article |
| CA1340581C (en) | 1986-11-20 | 1999-06-08 | Joseph P. Vacanti | Chimeric neomorphogenesis of organs by controlled cellular implantation using artificial matrices |
| US5736372A (en) | 1986-11-20 | 1998-04-07 | Massachusetts Institute Of Technology | Biodegradable synthetic polymeric fibrous matrix containing chondrocyte for in vivo production of a cartilaginous structure |
| US5804178A (en) | 1986-11-20 | 1998-09-08 | Massachusetts Institute Of Technology | Implantation of cell-matrix structure adjacent mesentery, omentum or peritoneum tissue |
| DE3875306T2 (de) * | 1987-02-24 | 1993-04-01 | Xoma Corp | Immunosuppression bei der auf immunotoxin basierten behandlung von menschen. |
| US5912017A (en) | 1987-05-01 | 1999-06-15 | Massachusetts Institute Of Technology | Multiwall polymeric microspheres |
| US5019379A (en) | 1987-07-31 | 1991-05-28 | Massachusetts Institute Of Technology | Unsaturated polyanhydrides |
| JP2670680B2 (ja) | 1988-02-24 | 1997-10-29 | 株式会社ビーエムジー | 生理活性物質含有ポリ乳酸系微小球およびその製造法 |
| US5010167A (en) | 1989-03-31 | 1991-04-23 | Massachusetts Institute Of Technology | Poly(amide-and imide-co-anhydride) for biological application |
| US5268455A (en) | 1989-05-25 | 1993-12-07 | Genentech, Inc. | Process for making biologically active polypeptides based on transforming growth factor-βsequences |
| US5399665A (en) | 1992-11-05 | 1995-03-21 | Massachusetts Institute Of Technology | Biodegradable polymers for cell transplantation |
| US5843452A (en) | 1992-11-09 | 1998-12-01 | Pharmagenesis, Inc. | Immunotherapy composition and method |
| US5679347A (en) | 1992-12-10 | 1997-10-21 | Brigham And Women's Hospital | Methods of isolating CD1-presented antigens, vaccines comprising CD1-presented antigens, and cell lines for use in said methods |
| EP0678034B1 (en) | 1993-01-11 | 1999-05-26 | Dana Farber Cancer Institute | Inducing cytotoxic t lymphocyte responses |
| US5512600A (en) | 1993-01-15 | 1996-04-30 | Massachusetts Institute Of Technology | Preparation of bonded fiber structures for cell implantation |
| US5514378A (en) | 1993-02-01 | 1996-05-07 | Massachusetts Institute Of Technology | Biocompatible polymer membranes and methods of preparation of three dimensional membrane structures |
| US5543158A (en) | 1993-07-23 | 1996-08-06 | Massachusetts Institute Of Technology | Biodegradable injectable nanoparticles |
| WO1995003035A1 (en) | 1993-07-23 | 1995-02-02 | Massachusetts Institute Of Technology | Polymerized liposomes with enhanced stability for oral delivery |
| US5565215A (en) | 1993-07-23 | 1996-10-15 | Massachusettes Institute Of Technology | Biodegradable injectable particles for imaging |
| US5468729A (en) | 1993-10-26 | 1995-11-21 | Alpha 1 Biomedicals | Method for treatment of autoimmune hepatitis |
| DE69518838T2 (de) | 1994-05-18 | 2001-05-03 | The Protein Engineering Network Of Centres Of Excellence (Pence), Inc. | Heterodimere trägerzusammensetzung von immunogenen polypeptiden und verfahren zu deren verwendung |
| US6007845A (en) | 1994-07-22 | 1999-12-28 | Massachusetts Institute Of Technology | Nanoparticles and microparticles of non-linear hydrophilic-hydrophobic multiblock copolymers |
| US5814617A (en) * | 1994-10-07 | 1998-09-29 | The United States Of America As Represented By The Secretary Of The Navy | Protective 17 KDA malaria hepatic and erythrocytic stage immunogen and gene |
| CA2200869A1 (en) | 1994-10-19 | 1996-05-02 | Bruce C. Trapnell | Gene therapy involving concurrent and repeated administration of adenoviruses and immunosuppressive agents |
| US5716404A (en) | 1994-12-16 | 1998-02-10 | Massachusetts Institute Of Technology | Breast tissue engineering |
| DE69630514D1 (de) | 1995-01-05 | 2003-12-04 | Univ Michigan | Oberflächen-modifizierte nanopartikel und verfahren für ihre herstellung und verwendung |
| US6251957B1 (en) | 1995-02-24 | 2001-06-26 | Trustees Of The University Of Pennsylvania | Method of reducing an immune response to a recombinant virus |
| US6123727A (en) | 1995-05-01 | 2000-09-26 | Massachusetts Institute Of Technology | Tissue engineered tendons and ligaments |
| JP3462313B2 (ja) | 1995-08-24 | 2003-11-05 | キッコーマン株式会社 | 変異型ウリカーゼ、変異型ウリカーゼ遺伝子、新規な組み換え体dna及び変異型ウリカーゼの製造法 |
| US6095148A (en) | 1995-11-03 | 2000-08-01 | Children's Medical Center Corporation | Neuronal stimulation using electrically conducting polymers |
| DE19545257A1 (de) | 1995-11-24 | 1997-06-19 | Schering Ag | Verfahren zur Herstellung von morphologisch einheitlichen Mikrokapseln sowie nach diesem Verfahren hergestellte Mikrokapseln |
| US5902599A (en) | 1996-02-20 | 1999-05-11 | Massachusetts Institute Of Technology | Biodegradable polymer networks for use in orthopedic and dental applications |
| EP0937082A2 (en) | 1996-07-12 | 1999-08-25 | Ariad Pharmaceuticals, Inc. | Materials and method for treating or preventing pathogenic fungal infection |
| WO1998010056A1 (en) | 1996-09-03 | 1998-03-12 | Health Research Inc. | Treatment of antigen presenting cells to modulate antigen presenting cell function |
| US6060082A (en) | 1997-04-18 | 2000-05-09 | Massachusetts Institute Of Technology | Polymerized liposomes targeted to M cells and useful for oral or mucosal drug delivery |
| US5837752A (en) | 1997-07-17 | 1998-11-17 | Massachusetts Institute Of Technology | Semi-interpenetrating polymer networks |
| ATE423789T1 (de) | 1997-09-16 | 2009-03-15 | Univ Oregon Health & Science | Rekombinante mhc-moleküle welche nützlich sind für die manipulation von antigen-spezifischen t- zellen |
| EP2042192A3 (en) | 1997-10-30 | 2009-05-27 | Laboratorios LETI, S.L. | Tolerogenic fragments of natural allergens |
| US6018817A (en) | 1997-12-03 | 2000-01-25 | International Business Machines Corporation | Error correcting code retrofit method and apparatus for multiple memory configurations |
| US6197229B1 (en) | 1997-12-12 | 2001-03-06 | Massachusetts Institute Of Technology | Method for high supercoiled DNA content microspheres |
| NZ505325A (en) | 1997-12-23 | 2003-07-25 | Crucell Holland B | Adeno-associated virus and adenovirus chimeric recombinant viruses useful for the integration of foreign genetic information into the chromosomal dna of target cells |
| WO1999034826A1 (en) | 1998-01-09 | 1999-07-15 | Circassia Limited | Methods and compositions for desensitisation |
| FR2775435B1 (fr) | 1998-02-27 | 2000-05-26 | Bioalliance Pharma | Nanoparticules comprenant au moins un polymere et au moins un compose apte a complexer un ou plusieurs principes actifs |
| US6632922B1 (en) | 1998-03-19 | 2003-10-14 | The Regents Of The University Of California | Methods and compositions for controlled polypeptide synthesis |
| US6506577B1 (en) | 1998-03-19 | 2003-01-14 | The Regents Of The University Of California | Synthesis and crosslinking of catechol containing copolypeptides |
| US6686446B2 (en) | 1998-03-19 | 2004-02-03 | The Regents Of The University Of California | Methods and compositions for controlled polypeptide synthesis |
| SE9801288D0 (sv) | 1998-04-14 | 1998-04-14 | Astra Ab | Vaccine delivery system and metod of production |
| US6436392B1 (en) | 1998-05-20 | 2002-08-20 | University Of Iowa Research Foundation | Adeno-associated virus vectors |
| PL202799B1 (pl) | 1998-08-06 | 2009-07-31 | Mountain View Pharmaceuticals | Sposób izolowania urykazy w postaci tetramerycznej oraz wyizolowana tetrameryczna urykaza |
| ES2222728T3 (es) | 1998-10-05 | 2005-02-01 | Pharmexa A/S | Procedimiento de vacunacion terapeutica. |
| US6306640B1 (en) | 1998-10-05 | 2001-10-23 | Genzyme Corporation | Melanoma antigenic peptides |
| DK2319928T3 (da) | 1998-10-23 | 2013-06-24 | Kirin Amgen Inc | Dimere trombopoietiske peptidomimetika, der binder til MPL-receptor og har trombopoietisk aktivitet |
| US6759237B1 (en) | 1998-11-05 | 2004-07-06 | The Trustees Of The University Of Pennsylvania | Adeno-associated virus serotype 1 nucleic acid sequences, vectors and host cells containing same |
| US20040009535A1 (en) | 1998-11-27 | 2004-01-15 | Celltech R&D, Inc. | Compositions and methods for increasing bone mineralization |
| ES2639020T3 (es) | 1998-11-27 | 2017-10-25 | Ucb Pharma S.A. | Composiciones y métodos para incrementar la mineralización de la substancia ósea |
| US6153217A (en) * | 1999-01-22 | 2000-11-28 | Biodelivery Sciences, Inc. | Nanocochleate formulations, process of preparation and method of delivery of pharmaceutical agents |
| US6800296B1 (en) | 1999-05-19 | 2004-10-05 | Massachusetts Institute Of Technology | Modification of surfaces using biological recognition events |
| WO2000074688A1 (en) | 1999-06-08 | 2000-12-14 | The Children's Hospital Of Philadelphia | Methods for preventing formation of inhibitory antibodies in the setting of gene therapy |
| DE19951970A1 (de) | 1999-10-28 | 2001-05-03 | Bionetworks Gmbh | Arzneimittel für die Toleranzinduktion |
| EP1267946A4 (en) | 2000-02-28 | 2008-07-02 | Genesegues Inc | SYSTEM AND METHOD FOR ENCAPSULATING NANOCAPSULES |
| AU2001249182A1 (en) | 2000-03-14 | 2001-09-24 | Genetics Institute Inc. | Use of rapamycin and agents that inhibit b7 activity in immunomodulation |
| WO2001085208A2 (en) | 2000-05-05 | 2001-11-15 | Cytos Biotechnology Ag | Molecular antigen arrays and vaccines |
| WO2001091802A1 (en) | 2000-05-30 | 2001-12-06 | Baylor College Of Medicine | Chimeric viral vectors for gene therapy |
| WO2001092551A2 (en) | 2000-06-01 | 2001-12-06 | University Of North Carolina At Chapel Hill | Duplexed parvovirus vectors |
| AU2001269923A1 (en) | 2000-06-19 | 2002-01-02 | Genzyme Corporation | Combination enzyme replacement, gene therapy and small molecule therapy for lysosomal storage diseases |
| US20040204379A1 (en) | 2000-06-19 | 2004-10-14 | Cheng Seng H. | Combination enzyme replacement, gene therapy and small molecule therapy for lysosomal storage diseases |
| US20020014242A1 (en) | 2000-07-31 | 2002-02-07 | Abraham Scaria | Use of rapamycin to inhibit immune response and induce tolerance to gene therapy vector and encoded transgene products |
| MY138883A (en) * | 2000-08-29 | 2009-08-28 | Government Of Malaysia As Represented By The Ministry Of Science Tehnology And Innovation Malaysia | Use of asiatic acid for treatment of cencer |
| CA2319928A1 (en) | 2000-09-18 | 2002-03-18 | Vasogen Ireland Limited | Apoptosis-mimicking synthetic entities and use thereof in medical treatments |
| GB0025414D0 (en) | 2000-10-16 | 2000-11-29 | Consejo Superior Investigacion | Nanoparticles |
| WO2002088304A2 (en) | 2001-04-11 | 2002-11-07 | Trustees Of The University Of Pennsylvania | Compositions and methods for suppressing immune responses |
| US6913915B2 (en) | 2001-08-02 | 2005-07-05 | Phoenix Pharmacologics, Inc. | PEG-modified uricase |
| US6818732B2 (en) | 2001-08-30 | 2004-11-16 | The Regents Of The University Of California | Transition metal initiators for controlled poly (beta-peptide) synthesis from beta-lactam monomers |
| CN1294268C (zh) | 2001-09-03 | 2007-01-10 | 上海三维生物技术有限公司 | 可在肿瘤细胞内特异性复制并扩散的重组腺病毒载体 |
| ES2266564T3 (es) | 2001-10-19 | 2007-03-01 | Isotechnika Inc. | Sintesis de analogos de cicloporinas. |
| WO2003052051A2 (en) | 2001-12-17 | 2003-06-26 | The Trustees Of The University Of Pennsylvania | Adeno-associated virus (aav) serotype 8 sequences |
| GB0207440D0 (en) | 2002-03-28 | 2002-05-08 | Ppl Therapeutics Scotland Ltd | Tolerogenic antigen-presenting cells |
| US20040038303A1 (en) | 2002-04-08 | 2004-02-26 | Unger Gretchen M. | Biologic modulations with nanoparticles |
| US7485314B2 (en) | 2002-05-06 | 2009-02-03 | Los Angeles Biomedical Research Institute At Harbor-Ucla Medical Center | Induction of antigen specific immunologic tolerance |
| AU2003228768B2 (en) | 2002-05-22 | 2009-02-05 | The Cleveland Clinic Foundation | Induction and maintenance of tolerance to composite tissue allografts |
| WO2003102162A2 (en) | 2002-06-04 | 2003-12-11 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Novel tolerogenic dendritic cells and therapeutic uses therefor |
| AU2003247880B2 (en) | 2002-07-03 | 2010-09-02 | Coley Pharmaceutical Group, Inc. | Nucleic acid compositions for stimulating immune responses |
| US9809654B2 (en) | 2002-09-27 | 2017-11-07 | Vaccinex, Inc. | Targeted CD1d molecules |
| EP1565183B1 (en) | 2002-11-29 | 2008-08-13 | Maria Grazia Roncarolo | Rapamycin and il-10 for the treatment of autoimmune diseases |
| US8575110B2 (en) | 2003-02-17 | 2013-11-05 | Alpha-O Peptides G | Peptidic nanoparticles as drug delivery and antigen display systems |
| WO2004075861A2 (en) | 2003-02-26 | 2004-09-10 | Children's Hospital, Inc. | Recombinant adeno-associated virus production |
| CN102040662A (zh) | 2003-03-14 | 2011-05-04 | 惠氏有限责任公司 | 抗人il-21受体的抗体及其应用 |
| AU2004224762B2 (en) | 2003-03-26 | 2009-12-24 | Kuros Us Llc | Packaging of immunostimulatory oligonucleotides into virus-like particles: method of preparation and use |
| US7186699B2 (en) | 2003-06-03 | 2007-03-06 | Cell Genesys, Inc. | Method for treating cancer by vector-mediated delivery of one or more anti-angiogenic or pro-apoptotic genes |
| US7727969B2 (en) | 2003-06-06 | 2010-06-01 | Massachusetts Institute Of Technology | Controlled release nanoparticle having bound oligonucleotide for targeted delivery |
| EP1486567A1 (en) | 2003-06-11 | 2004-12-15 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Improved adeno-associated virus (AAV) vector for gene therapy |
| WO2005014650A2 (en) | 2003-06-16 | 2005-02-17 | Celltech R & D, Inc. | Antibodies specific for sclerostin and methods for increasing bone mineralization |
| US20060251711A1 (en) | 2003-08-28 | 2006-11-09 | Vgsk Technologies, Inc. | Sterically stabilized carrier for aerosol therapeutics, compositions and methods for treating diseases of the respiratory tract of a mammal |
| US20080160089A1 (en) | 2003-10-14 | 2008-07-03 | Medivas, Llc | Vaccine delivery compositions and methods of use |
| DE10347710B4 (de) | 2003-10-14 | 2006-03-30 | Johannes-Gutenberg-Universität Mainz | Rekombinante Impfstoffe und deren Verwendung |
| JP2008504216A (ja) | 2003-12-02 | 2008-02-14 | サイトイミューン サイエンシズ インコーポレイテッド | モノクローナル抗体の生成のための方法および組成物 |
| KR101376715B1 (ko) | 2003-12-19 | 2014-03-27 | 더 유니버시티 오브 노쓰 캐롤라이나 엣 채플 힐 | 소프트 또는 임프린트 리소그래피를 이용하여 분리된 마이크로- 및 나노- 구조를 제작하는 방법 |
| CN1960726A (zh) | 2004-04-08 | 2007-05-09 | 应用研究系统Ars股份公司 | 包含jnk抑制剂和环孢菌素的组合物 |
| EP1756147A2 (en) | 2004-06-01 | 2007-02-28 | Innogenetics N.V. | Peptides for inducing a ctl and/or htl response to hepatitis c virus |
| JP2008512350A (ja) * | 2004-07-01 | 2008-04-24 | イェール ユニバーシティ | 標的化され、そして高密度で薬物が負荷されるポリマー性物質 |
| US20080206270A1 (en) | 2004-07-08 | 2008-08-28 | Minev Boris R | Enhancing Class I Antigen Presentation With Synthetic Sequences |
| FR2874384B1 (fr) | 2004-08-17 | 2010-07-30 | Genethon | Vecteur viral adeno-associe pour realiser du saut d'exons dans un gene codant une proteine a domaines dispensables |
| US20090017016A1 (en) | 2004-10-05 | 2009-01-15 | Tanox Inc. | Treatment and prevention of hypersensitivity and/or anaphylaxis with anti-ige antibodies in patients receiving replacement therapy |
| US9492400B2 (en) | 2004-11-04 | 2016-11-15 | Massachusetts Institute Of Technology | Coated controlled release polymer particles as efficient oral delivery vehicles for biopharmaceuticals |
| US20060159766A1 (en) | 2004-12-15 | 2006-07-20 | Elan Pharma International Limited | Nanoparticulate tacrolimus formulations |
| CA2593862C (en) | 2004-12-31 | 2014-10-21 | Iceutica Pty Ltd | Nanoparticle composition and methods for synthesis thereof |
| GB0504206D0 (en) | 2005-03-01 | 2005-04-06 | Glaxo Group Ltd | Combination therapy |
| CN101137365A (zh) | 2005-03-08 | 2008-03-05 | 生命周期药物公司 | 包含西罗莫司和/或其类似物的药物组合物 |
| MX2007011494A (es) * | 2005-03-17 | 2007-12-06 | Elan Pharma Int Ltd | Composiciones inyectables de compuestos inmunosupresores nanoparticulados. |
| US7884109B2 (en) | 2005-04-05 | 2011-02-08 | Wyeth Llc | Purine and imidazopyridine derivatives for immunosuppression |
| EP1871343A2 (en) | 2005-04-12 | 2008-01-02 | Wisconsin Alumni Research Foundation | Micelle composition of polymer and passenger drug |
| WO2006122223A2 (en) | 2005-05-10 | 2006-11-16 | Emory University | Strategies for delivery of active agents using micelles and particles |
| TW200711649A (en) | 2005-06-17 | 2007-04-01 | Combinatorx Inc | Combination therapy for the treatment of immunoinflammatory disorders |
| CN102016814B (zh) | 2005-06-17 | 2013-10-23 | 北卡罗来纳大学查珀尔希尔分校 | 纳米粒子制备方法、系统及材料 |
| EP1932538A4 (en) | 2005-08-25 | 2009-10-21 | Taiho Pharmaceutical Co Ltd | BIODEGRADABLE NANOPARTICLE HAVING RECYCLABLE IMMUNIZED T-EPITOPE PEPTIDE IMMOBILIZED ON OR ENCAPSULATED THEREIN |
| ATE552837T1 (de) | 2005-12-02 | 2012-04-15 | Univ Johns Hopkins | Verwendung von hochdosierten oxazaphosphorin- arzneimitteln zur behandlung von immunstörungen |
| MX2008007287A (es) | 2005-12-08 | 2008-10-27 | Univ Louisville Res Found | Metodos y composiciones para expandir celulas reguladoras t. |
| US9267937B2 (en) | 2005-12-15 | 2016-02-23 | Massachusetts Institute Of Technology | System for screening particles |
| WO2007087341A2 (en) | 2006-01-25 | 2007-08-02 | The Board Of Trustees Of The University Of Illinois | Tolerogenic biodegradable artificial antigen presenting system |
| AU2007215328A1 (en) | 2006-02-13 | 2007-08-23 | Oncolytics Biotech Inc. | Use of local immune suppression to enhance oncolytic viral therapy |
| US8568487B2 (en) | 2006-02-27 | 2013-10-29 | Biomet Manufacturing, Llc | Patient-specific hip joint devices |
| EP2004666B1 (en) | 2006-03-27 | 2014-09-03 | Globeimmune, Inc. | Ras mutation and compositions and methods related thereto |
| US20070254897A1 (en) * | 2006-04-28 | 2007-11-01 | Resolvyx Pharmaceuticals, Inc. | Compositions and methods for the treatment of cardiovascular disease |
| US8367113B2 (en) | 2006-05-15 | 2013-02-05 | Massachusetts Institute Of Technology | Polymers for functional particles |
| US20110052697A1 (en) | 2006-05-17 | 2011-03-03 | Gwangju Institute Of Science & Technology | Aptamer-Directed Drug Delivery |
| EP1880729A1 (en) | 2006-07-20 | 2008-01-23 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Use of soluble CD160 to suppress immunity |
| DK2051987T3 (en) * | 2006-08-18 | 2015-01-05 | Argos Therapeutics Inc | USE OF CD83 IN COMBINATION THERAPY |
| US20120269774A1 (en) | 2006-09-21 | 2012-10-25 | Medistem Laboratories, Inc | Allogeneic stem cell transplants in non-conditioned recipients |
| CN101583379B (zh) * | 2006-10-05 | 2013-04-03 | 约翰斯霍普金斯大学 | 使用优良聚合物纳米粒子的水溶性差药物的水可分散性口服,肠胃外和局部制剂 |
| CA2702340C (en) | 2006-10-12 | 2014-12-16 | The University Of Queensland | Compositions and methods for modulating immune responses |
| CN101646418B (zh) | 2006-10-12 | 2013-07-17 | 昆士兰大学 | 调节免疫应答的组合物和方法 |
| US20100112077A1 (en) * | 2006-11-06 | 2010-05-06 | Abraxis Bioscience, Llc | Nanoparticles of paclitaxel and albumin in combination with bevacizumab against cancer |
| US20100172994A1 (en) | 2006-11-22 | 2010-07-08 | University Of Florida Research Foundation, Inc. | Nanoparticles for Protection of Cells from Oxidative Stress |
| WO2008069942A2 (en) | 2006-12-05 | 2008-06-12 | Biogen Idec Ma Inc. | Novel methods of enhancing delivery of a gene therapy vector using steroids |
| PL2118309T3 (pl) | 2006-12-29 | 2015-07-31 | Univ Colorado Regents | Cel diagnostyczny i terapeutyczny dla chorób autoimmunologicznych i jego zastosowania |
| CA2678618C (en) | 2007-02-21 | 2019-03-12 | Vaccinex, Inc. | Modulation of nkt cell activity with antigen-loaded cd1d molecules |
| KR20080078204A (ko) | 2007-02-22 | 2008-08-27 | 크레아젠 주식회사 | 면역억제능이 증가된 간엽줄기세포-매개 자가유래수지상세포 |
| SI2131821T1 (sl) * | 2007-03-07 | 2018-11-30 | Abraxis Bioscience, Llc | Nanodelci, ki zajemajo rapamicin in albumin kot sredstvo proti raku |
| ES2525801T3 (es) | 2007-03-07 | 2014-12-30 | Uti Limited Partnership | Composiciones y métodos para la prevención y el tratamiento de enfermedades autoinmunes |
| CN101730526A (zh) * | 2007-03-07 | 2010-06-09 | 阿布拉科斯生物科学有限公司 | 作为抗癌剂的包含雷帕霉素和白蛋白的纳米颗粒 |
| WO2008124639A2 (en) | 2007-04-04 | 2008-10-16 | Massachusetts Institute Of Technology | Poly (amino acid) targeting moieties |
| CA2683415C (en) | 2007-04-04 | 2020-12-08 | Sigmoid Pharma Limited | An oral pharmaceutical composition |
| US20090226525A1 (en) | 2007-04-09 | 2009-09-10 | Chimeros Inc. | Self-assembling nanoparticle drug delivery system |
| AU2008239795A1 (en) | 2007-04-12 | 2008-10-23 | Emory University | Novel strategies for delivery of active agents using micelles and particles |
| WO2008150868A1 (en) | 2007-05-29 | 2008-12-11 | The Board Of Trustees Of The University Of Illinois | Methods for inducing therapeutic t cells for immune diseases |
| US20080311140A1 (en) | 2007-05-29 | 2008-12-18 | Baylor College Of Medicine | Antigen specific immunosuppression by dendritic cell therapy |
| JP6035503B2 (ja) | 2007-05-31 | 2016-11-30 | アカデミシュ ジーケンハウス ライデン ハー.オー.デー.エン. ルムク | ワクチンで使用するための、子宮頸部悪性腫瘍に浸潤するt細胞によって標的とされるhpvエピトープ |
| WO2008148761A1 (en) | 2007-06-05 | 2008-12-11 | Novartis Ag | Induction of tolerogenic phenotype in mature dendritic cells |
| US20090004259A1 (en) | 2007-06-14 | 2009-01-01 | Consejo Nacional De Investigaciones Cientificas Y Tecnicas (Conicet) | Methods of preparing a therapeutic formulation comprising galectin-induced tolerogenic dendritic cells |
| US8138183B2 (en) | 2007-07-09 | 2012-03-20 | Astrazeneca Ab | Morpholino pyrimidine derivatives used in diseases linked to mTOR kinase and/or PI3K |
| GB0714963D0 (en) | 2007-08-01 | 2007-09-12 | Novartis Ag | Compositions comprising antigens |
| MX2010001779A (es) | 2007-08-15 | 2010-07-06 | Circassia Ltd | Peptidos para vacunas. |
| CA2700378A1 (en) | 2007-09-21 | 2009-03-29 | Cytimmune Sciences, Inc. | Nanotherapeutic colloidal metal compositions and methods |
| AU2008314647B2 (en) * | 2007-10-12 | 2013-03-21 | Massachusetts Institute Of Technology | Vaccine nanotechnology |
| WO2009062502A1 (en) | 2007-11-13 | 2009-05-22 | Dandrit Biotech A/S | Method for generating tolerogenic dendritic cells employing decreased temperature |
| US20090142318A1 (en) * | 2007-11-30 | 2009-06-04 | Therakos, Inc. | METHOD TO EXPAND nTREG CELLS USING p70 S6 KINASE ANTAGONIST |
| AU2008346801A1 (en) | 2007-12-31 | 2009-07-16 | Nanocor Therapeutics, Inc. | RNA interference for the treatment of heart failure |
| EP2249900A4 (en) | 2008-02-08 | 2013-11-06 | Terumo Corp | DEVICE FOR LOCAL INTRALUMINAL TRANSPORT OF A BIOLOGICALLY AND PHYSIOLOGICALLY ACTIVE AGENCY |
| EP2262489A2 (en) | 2008-02-28 | 2010-12-22 | Deutsches Krebsforschungszentrum, Stiftung des öffentlichen Rechts | Hollow nanoparticles and uses thereof |
| US9669057B2 (en) | 2008-04-25 | 2017-06-06 | Duke University | Regulatory B cells and their uses |
| EP2300102B1 (en) | 2008-05-15 | 2014-01-08 | Dynavax Technologies Corporation | Immunostimulatory sequences containing CpG for use in the treatment of allergic rhinitis |
| JP5549014B2 (ja) | 2008-05-27 | 2014-07-16 | 国立大学法人名古屋大学 | 免疫調節剤及びその利用 |
| US20090297621A1 (en) | 2008-06-03 | 2009-12-03 | Abbott Cardiovascular Systems Inc. | Microparticles For The Treatment Of Disease |
| US8613951B2 (en) | 2008-06-16 | 2013-12-24 | Bind Therapeutics, Inc. | Therapeutic polymeric nanoparticles with mTor inhibitors and methods of making and using same |
| ES2765240T3 (es) | 2008-06-16 | 2020-06-08 | Pfizer | Nanopartículas poliméricas cargadas de fármaco y procedimientos de fabricación y uso de las mismas |
| US20120034156A1 (en) | 2010-08-03 | 2012-02-09 | Searete Llc, A Limited Liability Corporation Of The State Of Delaware | Artificial cells |
| WO2010018384A1 (en) | 2008-08-15 | 2010-02-18 | Circassia Limited | T-cell antigen peptide from allergen for stimulation of il-10 production |
| US8323696B2 (en) | 2008-08-29 | 2012-12-04 | Ecole Polytechnique Federale De Lausanne | Nanoparticles for immunotherapy |
| EP2341953B1 (en) | 2008-09-04 | 2018-11-21 | The General Hospital Corporation | Hydrogels for vocal cord and soft tissue augmentation and repair |
| CN101676291B (zh) | 2008-09-18 | 2012-05-09 | 上海海和药物研究开发有限公司 | 一类雷帕霉素碳酸酯类似物、其药物组合物及其制备方法和用途 |
| US8889124B2 (en) | 2008-09-25 | 2014-11-18 | The Board Of Trustees Of The Leland Stanford Junior University | Tolerogenic populations of dendritic cells |
| US10369204B2 (en) | 2008-10-02 | 2019-08-06 | Dako Denmark A/S | Molecular vaccines for infectious disease |
| US8277812B2 (en) | 2008-10-12 | 2012-10-02 | Massachusetts Institute Of Technology | Immunonanotherapeutics that provide IgG humoral response without T-cell antigen |
| US8343498B2 (en) * | 2008-10-12 | 2013-01-01 | Massachusetts Institute Of Technology | Adjuvant incorporation in immunonanotherapeutics |
| US8591905B2 (en) | 2008-10-12 | 2013-11-26 | The Brigham And Women's Hospital, Inc. | Nicotine immunonanotherapeutics |
| US8343497B2 (en) | 2008-10-12 | 2013-01-01 | The Brigham And Women's Hospital, Inc. | Targeting of antigen presenting cells with immunonanotherapeutics |
| JP5552630B2 (ja) | 2008-10-24 | 2014-07-16 | 学校法人 聖マリアンナ医科大学 | Htlv−i関連脊髄症を治療または予防するための医薬、およびhtlv−i関連脊髄症の患者に対する抗体療法の効果を試験する方法 |
| WO2010047839A1 (en) | 2008-10-25 | 2010-04-29 | Aura Biosciences | Modified plant virus particles and uses therefor |
| WO2010056143A1 (en) | 2008-11-13 | 2010-05-20 | Instituto De Medicina Molecular | The use of adjuvant to facilitate the induction of immune tolerance |
| US20100216804A1 (en) | 2008-12-15 | 2010-08-26 | Zale Stephen E | Long Circulating Nanoparticles for Sustained Release of Therapeutic Agents |
| CA2750098A1 (en) | 2009-01-20 | 2010-07-29 | Myelin Repair Foundation, Inc. | Compositions and methods for induction of antigen-specific tolerance |
| EP2218784A1 (en) | 2009-02-04 | 2010-08-18 | Universität Leipzig | Vector(s) containing an inducible gene encoding a CDK4/CD6 inhibitor useful for treating neurodegenerative disorders |
| EP2891662A1 (en) | 2009-02-05 | 2015-07-08 | Circassia Limited | Grass peptides for vaccine |
| KR20100099849A (ko) | 2009-03-04 | 2010-09-15 | 동국대학교 산학협력단 | 면역억제제와 트랜스글루타미나제 2의 억제제를 함유한 아토피 피부염 치료용 조성물 |
| WO2010114948A2 (en) | 2009-04-02 | 2010-10-07 | University Of Florida Research Foundation, Inc. | An inducible system for highly efficient production of recombinant adeno-associated virus (raav) vectors |
| GB0906159D0 (en) | 2009-04-09 | 2009-05-20 | Summit Corp Plc | Drug combination for the treatment of proteostatic diseases |
| KR20120022984A (ko) * | 2009-04-21 | 2012-03-12 | 셀렉타 바이오사이언시즈, 인크. | Th1 편향 반응을 제공하는 면역나노치료법 |
| WO2010123501A1 (en) | 2009-04-22 | 2010-10-28 | Massachusetts Institute Of Technology | Innate immune suppression enables repeated delivery of long rna molecules |
| JP5740390B2 (ja) | 2009-04-27 | 2015-06-24 | イミューロン リミテッドImmuron Limited | 病的障害の治療および/または予防において使用するための抗lps強化免疫グロブリン製剤 |
| MX357630B (es) | 2009-05-27 | 2018-07-17 | Selecta Biosciences Inc | Nanoportadores sintéticos objetivo con liberación sensible al ph de agentes inmunomoduladores. |
| PL398781A1 (pl) | 2009-06-25 | 2012-11-19 | Savient Pharmaceuticals, Inc. | Sposoby i zestawy do prognozowania ryzyka wystapienia reakcji na wlew oraz zaniku odpowiedzi której posrednicza przeciwciala poprzez monitorowanie kwasu moczowego w surowicy podczas terapii z zastosowaniem pegylowanej urykazy |
| AU2010293059B2 (en) | 2009-08-26 | 2017-03-16 | Selecta Biosciences, Inc. | Compositions that induce T cell help |
| AR078161A1 (es) | 2009-09-11 | 2011-10-19 | Hoffmann La Roche | Formulaciones farmaceuticas muy concentradas de un anticuerpo anti cd20. uso de la formulacion. metodo de tratamiento. |
| EP2305277A1 (en) | 2009-09-18 | 2011-04-06 | Forskarpatent I Syd AB | Use of tolerogenic dendritic cells in treatment and prevention of atherosclerosis |
| CN101703781A (zh) | 2009-10-28 | 2010-05-12 | 陕西北美基因股份有限公司 | 一种免疫抑制剂的磁性载药方法 |
| KR101267813B1 (ko) | 2009-12-30 | 2013-06-04 | 주식회사 삼양바이오팜 | 향상된 수용해도를 갖는 라파마이신 함유 고분자나노입자 주사제형 조성물 및 그 제조방법, 및 방사선 요법과 병용하기 위한 항암 조성물 |
| WO2011085231A2 (en) | 2010-01-08 | 2011-07-14 | Selecta Biosciences, Inc. | Synthetic virus-like particles conjugated to human papillomavirus capsid peptides for use as vaccines |
| US9228171B2 (en) | 2010-02-05 | 2016-01-05 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Regulatory B cells (tBREGS) and their use |
| WO2011109833A2 (en) | 2010-03-05 | 2011-09-09 | President And Fellows Of Harvard College | Induced dendritic cell compositions and uses thereof |
| US20110262491A1 (en) | 2010-04-12 | 2011-10-27 | Selecta Biosciences, Inc. | Emulsions and methods of making nanocarriers |
| US20110272836A1 (en) | 2010-04-12 | 2011-11-10 | Selecta Biosciences, Inc. | Eccentric vessels |
| US8927514B2 (en) | 2010-04-30 | 2015-01-06 | City Of Hope | Recombinant adeno-associated vectors for targeted treatment |
| PH12012502143A1 (en) | 2010-05-07 | 2019-07-03 | Xoma Us Llc | Methods for the treatment of il-1beta related conditions |
| EA030813B1 (ru) | 2010-05-26 | 2018-10-31 | Селекта Байосайенсиз, Инк | Способы генерации антительного иммунного ответа и увеличения местной индукции иммунных цитокинов при использовании синтетических наноносителей, соединенных с адъювантами |
| PH12012502399A1 (en) | 2010-06-07 | 2013-02-11 | Abraxis Bioscience Llc | Combination therapy methods for treating proliferative diseases |
| WO2012019041A2 (en) | 2010-08-04 | 2012-02-09 | Duke University | Regulatory b cells and their uses |
| EP2603520A4 (en) | 2010-08-10 | 2014-02-19 | Ecole Polytech | ERYTHROCYTE BINDING THERAPEUTICS |
| WO2012024629A1 (en) | 2010-08-20 | 2012-02-23 | Selecta Biosciences, Inc. | Synthetic nanocarrier vaccines comprising proteins obtained or derived from human influenza a virus hemagglutinin |
| AU2011293508A1 (en) * | 2010-08-23 | 2013-01-24 | Selecta Biosciences, Inc. | Targeted multi-epitope dosage forms for induction of an immune response to antigens |
| CA2810842C (en) | 2010-09-09 | 2018-06-26 | Micell Technologies, Inc. | Macrolide dosage forms |
| US10016371B2 (en) | 2010-10-22 | 2018-07-10 | University Of Florida Research Foundation | Antigen-specific, tolerance-inducing microparticles and uses thereof |
| US9994443B2 (en) | 2010-11-05 | 2018-06-12 | Selecta Biosciences, Inc. | Modified nicotinic compounds and related methods |
| US20120171229A1 (en) | 2010-12-30 | 2012-07-05 | Selecta Biosciences, Inc. | Synthetic nanocarriers with reactive groups that release biologically active agents |
| MX2013009191A (es) | 2011-02-08 | 2013-11-04 | Charlotte Mecklenburg Hospital | Oligonucleotidos antisentido. |
| WO2012112578A2 (en) | 2011-02-14 | 2012-08-23 | The Children's Hospital Of Philadelphia | Improved aav8 vector with enhanced functional activity and methods of use thereof |
| US8654487B2 (en) | 2011-03-11 | 2014-02-18 | Siemens Industry, Inc. | Methods, systems, and apparatus and for detecting parallel electrical arc faults |
| JP6320912B2 (ja) | 2011-03-25 | 2018-05-09 | セレクタ バイオサイエンシーズ インコーポレーテッドSelecta Biosciences,Inc. | 浸透圧媒介性放出合成ナノ担体 |
| US8710200B2 (en) | 2011-03-31 | 2014-04-29 | Moderna Therapeutics, Inc. | Engineered nucleic acids encoding a modified erythropoietin and their expression |
| US20140155469A1 (en) | 2011-04-19 | 2014-06-05 | The Research Foundation Of State University Of New York | Adeno-associated-virus rep sequences, vectors and viruses |
| EP2699688A1 (en) | 2011-04-20 | 2014-02-26 | The Trustees Of The University Of Pennsylvania | Regimens and compositions for aav-mediated passive immunization of airborne pathogens |
| CN103648501A (zh) | 2011-05-16 | 2014-03-19 | 建新公司 | 使用甲氨蝶呤诱导免疫耐受性 |
| WO2013019648A1 (en) | 2011-07-29 | 2013-02-07 | Selecta Biosciences, Inc. | Control of antibody responses to synthetic nanocarriers |
| US20130058976A1 (en) | 2011-09-06 | 2013-03-07 | Selecta Biosciences, Inc. | Allergen-specific induced tolerogenic dendritic cells for allergy therapy |
| AU2012304313A1 (en) | 2011-09-08 | 2014-03-06 | University Of Florida Research Foundation, Inc. | Materials and methods for modulating immune responses |
| US8865487B2 (en) * | 2011-09-20 | 2014-10-21 | General Electric Company | Large area hermetic encapsulation of an optoelectronic device using vacuum lamination |
| BR112014007852B1 (pt) | 2011-10-03 | 2021-11-03 | Moderna Therapeutics, Inc | Polinucleotídeo isolado modificado e composição farmacêutica |
| WO2013058812A1 (en) | 2011-10-19 | 2013-04-25 | President And Fellows Of Harvard College | Targeted delivery to pancreatic islet endothelial cells |
| EP2591801A1 (en) | 2011-11-14 | 2013-05-15 | Universitätsklinikum Hamburg-Eppendorf | Nanoparticle compositions for generation of regulatory T cells and treatment of autoimmune diseases and other chronic inflammatory conditions |
| US10640785B2 (en) | 2011-11-22 | 2020-05-05 | The Children's Hospital Of Philadelphia | Virus vectors for highly efficient transgene delivery |
| US20150111955A1 (en) | 2012-02-17 | 2015-04-23 | The Children's Hospital Of Philadelphia | Aav vector compositions and methods for gene transfer to cells, organs and tissues |
| HUE054087T2 (hu) | 2012-04-18 | 2021-09-28 | Childrens Hospital Philadelphia | Készítmények és eljárások nagy hatékonyságú géntranszferre AAV kapszidvariánsok alkalmazásával |
| CA2871786C (en) | 2012-04-24 | 2021-11-16 | Ohio State Innovation Foundation | Compositions and methods for treating and preventing porcine reproductive and respiratory syndrome |
| MX363147B (es) | 2012-09-17 | 2019-03-11 | Pfizer Inc Star | Nanoparticulas terapeuticas que comprenden un agente terapeutico y metodos para realizarlas y usarlas. |
| EP2968499A4 (en) | 2013-03-15 | 2016-11-30 | Haplomics Inc | COMPOSITIONS AND METHODS FOR THE IMMUNO-TOLERANCE INDUCTION FOR FACTOR VIII SPATIAL THERAPIES IN PERSONS WITH HEMOPHILIA A |
| US9944918B2 (en) | 2013-03-15 | 2018-04-17 | The United States Of America, As Represented By The Secretary, Dept. Of Health & Human Services | Synthetic methylmalonyl-CoA mutase transgene for the treatment of MUT class methylmalonic acidemia (MMA) |
| CA2909085C (en) | 2013-04-08 | 2023-08-29 | University Of Iowa Research Foundation | Chimeric adeno-associated virus/ bocavirus parvovirus vector |
| TWI679019B (zh) | 2013-04-29 | 2019-12-11 | 法商賽諾菲公司 | 抗il-4/抗il-13之雙特異性抗體調配物 |
| BR112015027279A8 (pt) | 2013-05-03 | 2018-01-30 | Selecta Biosciences Inc | métodos e composições para acentuar células t reguladoras cd4+ |
| AU2014262164B2 (en) | 2013-05-03 | 2020-02-27 | Selecta Biosciences, Inc. | Dosing combinations for reducing undesired humoral immune responses |
| AU2014274894A1 (en) | 2013-06-04 | 2015-11-26 | Selecta Biosciences, Inc. | Repeated administration of non-immunosupressive antigen specific immunotherapeutics |
| RU2687143C2 (ru) | 2013-10-06 | 2019-05-07 | Дзе Юнайтед Стейтс Оф Америка, Эз Репрезентед Бай Дзе Секретари, Департмент Оф Хелс Энд Хьюман Сёрвисез | Модифицированный экзотоксин а псевдомонад |
| US9276815B2 (en) * | 2013-12-27 | 2016-03-01 | Dell Products L.P. | N-node virtual link trunking (VLT) systems management plane |
| EP2916319A1 (en) | 2014-03-07 | 2015-09-09 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Concept for encoding of information |
| PL3116900T3 (pl) | 2014-03-09 | 2021-03-08 | The Trustees Of The University Of Pennsylvania | Kompozycje użyteczne w leczeniu niedoboru transkarbamylazy ornitynowej (otc) |
| GB201407322D0 (en) | 2014-04-25 | 2014-06-11 | Ospedale San Raffaele | Gene therapy |
| US20150358333A1 (en) * | 2014-06-04 | 2015-12-10 | Grandios Technologies, Llc | Geo-location and biometric presence security |
| US20150359865A1 (en) | 2014-06-17 | 2015-12-17 | Selecta Biosciences, Inc. | Tolerogenic synthetic nanocarriers for t-cell-mediated autoimmune disease |
| US20160220501A1 (en) | 2015-02-03 | 2016-08-04 | Selecta Biosciences, Inc. | Tolerogenic synthetic nanocarriers to reduce immune responses to therapeutic proteins |
| WO2015200728A1 (en) | 2014-06-25 | 2015-12-30 | Selecta Biosciences, Inc. | Methods and compositions for treatment with synthetic nanocarriers and immune checkpoint inhibitors |
| US20160074532A1 (en) | 2014-09-07 | 2016-03-17 | Selecta Biosciences, Inc. | Methods and compositions for attenuating gene editing anti-viral transfer vector immune responses |
| WO2016055437A1 (en) | 2014-10-06 | 2016-04-14 | Arthrogen B.V. | Aav-based gene therapy |
| CN107072964A (zh) | 2014-11-05 | 2017-08-18 | 西莱克塔生物科技公司 | 与低hlb表面活性剂在生产包含rapalog的合成纳米颗粒中之用途相关的方法和组合物 |
| TWI726897B (zh) | 2015-07-15 | 2021-05-11 | 日商協和麒麟股份有限公司 | 與人類crth2特異性結合之抗體 |
| WO2017139212A1 (en) | 2016-02-08 | 2017-08-17 | Cyta Therapeutics, Inc. | Particle delivery of rapamycin to the liver |
| AU2016392719A1 (en) | 2016-02-10 | 2018-08-02 | Pfizer Inc. | Therapeutic nanoparticles having EGFR ligands and methods of making and using same |
| DK3426285T3 (da) | 2016-03-11 | 2024-08-26 | Cartesian Therapeutics Inc | Formuleringer og doser af pegyleret uricase |
| GB201608323D0 (en) | 2016-05-12 | 2016-06-29 | Ucb Biopharma Sprl | Pharmaceutical compositions |
| US10545815B2 (en) | 2016-08-03 | 2020-01-28 | Futurewei Technologies, Inc. | System and method for data redistribution in a database |
| US20180071394A1 (en) | 2016-08-25 | 2018-03-15 | Selecta Biosciences, Inc. | Polyester polymer matrices for the delivery of allergens |
| WO2018064215A1 (en) | 2016-09-27 | 2018-04-05 | Selecta Biosciences, Inc. | Recombinant immunotoxins for use in the treatment of cancer |
| US11583504B2 (en) | 2016-11-08 | 2023-02-21 | Modernatx, Inc. | Stabilized formulations of lipid nanoparticles |
| WO2018093868A1 (en) | 2016-11-16 | 2018-05-24 | University Of Florida Research Foundation, Inc. | Immunoglobulin proteases, compositions, and uses thereof |
| US11104887B2 (en) | 2017-01-03 | 2021-08-31 | Ethris Gmbh | Ornithine transcarbamylase coding polyribonucleotides and formulations thereof |
| JP2020506890A (ja) | 2017-01-07 | 2020-03-05 | セレクタ バイオサイエンシーズ インコーポレーテッドSelecta Biosciences,Inc. | 合成ナノキャリアにカップリングした免疫抑制剤のパターン化された投与 |
| EP3592389B1 (en) | 2017-03-11 | 2025-05-07 | Cartesian Therapeutics, Inc. | Methods and compositions related to combined treatment with anti-inflammatories and synthetic nanocarriers comprising an immunosuppressant |
| KR20200086670A (ko) | 2017-10-13 | 2020-07-17 | 셀렉타 바이오사이언시즈, 인크. | 항바이러스 전달 벡터 IgM 반응을 약화시키기 위한 방법 및 조성물 |
| US20210128534A1 (en) | 2018-02-26 | 2021-05-06 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Drug delivery systems |
| CA3103661A1 (en) | 2018-05-09 | 2019-11-14 | Yale University | Particles for spatiotemporal release of agents |
| CN112771070A (zh) | 2018-07-16 | 2021-05-07 | 西莱克塔生物科技公司 | Otc构建体和载体的方法和组合物 |
| MX2021000638A (es) | 2018-07-16 | 2021-06-23 | Selecta Biosciences Inc | Métodos y composiciones de construcciones y vectores de acidemia metilmalónica. |
| JP2022531201A (ja) | 2019-04-28 | 2022-07-06 | セレクタ バイオサイエンシーズ インコーポレーテッド | ウイルス導入ベクターに対する既存の免疫を伴う対象の処置のための方法 |
| CN114206396A (zh) | 2019-05-28 | 2022-03-18 | 西莱克塔生物科技公司 | 用于减弱抗病毒转移载体免疫应答的方法和组合物 |
| EP3980784A1 (en) | 2019-06-04 | 2022-04-13 | Selecta Biosciences, Inc. | Formulations and doses of pegylated uricase |
| EP4048269A1 (en) | 2019-10-21 | 2022-08-31 | Selecta Biosciences, Inc. | Methods and compositions for treating liver diseases and disorders |
| CN118384281A (zh) | 2019-11-08 | 2024-07-26 | 西莱克塔生物科技公司 | 聚乙二醇化尿酸酶的制剂和剂量 |
| CA3173734A1 (en) | 2020-02-26 | 2021-09-02 | Selecta Biosciences, Inc. | Methods and compositions using synthetic nanocarriers comprising immunosuppressant |
| EP4117631A1 (en) | 2020-03-11 | 2023-01-18 | Selecta Biosciences, Inc. | Methods and compositions related to synthetic nanocarriers |
| WO2022057942A1 (zh) | 2020-09-21 | 2022-03-24 | 上海宝济药业有限公司 | 一种药物组合及其应用 |
| WO2022098901A1 (en) | 2020-11-04 | 2022-05-12 | Selecta Biosciences, Inc. | Compositions for reducing immune responses against immunoglobulin proteases |
| WO2022150335A1 (en) | 2021-01-05 | 2022-07-14 | Selecta Biosciences, Inc. | Viral vector dosing protocols |
| BR112023020597A2 (pt) | 2021-04-09 | 2023-12-12 | Selecta Biosciences Inc | Nanocarreadores sintéticos que compreendem um imunossupressante em combinação com agonistas do receptor de il-2 de alta afinidade para aumentar a tolerância imune |
| EP4079848A1 (en) | 2021-04-22 | 2022-10-26 | Genovis Ab | Immunoglobulin cleaving enzyme |
| WO2023064350A1 (en) | 2021-10-12 | 2023-04-20 | Selecta Biosciences, Inc. | Viral vector dosing protocols |
| WO2023064367A1 (en) | 2021-10-12 | 2023-04-20 | Selecta Biosciences, Inc. | Methods and compositions for attenuating anti-viral transfer vector igm responses |
| US20230357437A1 (en) | 2022-03-09 | 2023-11-09 | Selecta Biosciences, Inc. | Immunosuppressants in combination with anti-igm agents and related dosing |
| CA3264659A1 (en) | 2022-08-11 | 2024-02-15 | Cartesian Therapeutics, Inc. | COMPOSITIONS AND PROCESSES ASSOCIATED WITH IMMUNOGLOBULIN PROTEASES AND FUSION THEREOF |
-
2014
- 2014-05-02 BR BR112015027279A patent/BR112015027279A8/pt not_active Application Discontinuation
- 2014-05-02 WO PCT/US2014/036699 patent/WO2014179772A2/en not_active Ceased
- 2014-05-02 EP EP20167362.1A patent/EP3763359A1/en not_active Withdrawn
- 2014-05-02 US US14/269,056 patent/US10357483B2/en active Active
- 2014-05-02 CN CN201911069459.6A patent/CN110841066A/zh active Pending
- 2014-05-02 KR KR1020247024661A patent/KR20240119155A/ko not_active Ceased
- 2014-05-02 KR KR1020247024763A patent/KR20240119160A/ko not_active Ceased
- 2014-05-02 KR KR1020227004759A patent/KR20220025908A/ko not_active Ceased
- 2014-05-02 CN CN201480037123.0A patent/CN105339012A/zh active Pending
- 2014-05-02 KR KR1020157034133A patent/KR20160003217A/ko not_active Ceased
- 2014-05-02 CN CN201911069542.3A patent/CN110841067A/zh active Pending
- 2014-05-02 CN CN201480032251.6A patent/CN105283175A/zh active Pending
- 2014-05-02 KR KR1020227004758A patent/KR20220025907A/ko not_active Ceased
- 2014-05-02 CN CN202010594335.6A patent/CN111760025A/zh active Pending
- 2014-05-02 CN CN201480034670.3A patent/CN105338968A/zh active Pending
- 2014-05-02 CN CN201911307714.6A patent/CN111053908A/zh active Pending
- 2014-05-02 US US14/269,042 patent/US20140335186A1/en active Pending
- 2014-05-02 CN CN201910874364.5A patent/CN110694077A/zh active Pending
- 2014-05-02 IL IL284732A patent/IL284732B2/en unknown
- 2014-05-02 CN CN201910552107.XA patent/CN110251676A/zh active Pending
- 2014-05-02 CA CA2910584A patent/CA2910584A1/en active Pending
- 2014-05-02 CN CN201910552053.7A patent/CN110251675A/zh active Pending
- 2014-05-02 AU AU2014262165A patent/AU2014262165B2/en active Active
- 2014-05-02 KR KR1020247024665A patent/KR20240119157A/ko active Pending
- 2014-05-02 AU AU2014262162A patent/AU2014262162B2/en active Active
- 2014-05-02 KR KR1020157034104A patent/KR20160003830A/ko not_active Ceased
- 2014-05-02 EP EP14791089.7A patent/EP2991628A4/en active Pending
- 2014-05-02 IL IL284924A patent/IL284924B2/en unknown
- 2014-05-02 BR BR122020023215-3A patent/BR122020023215B1/pt active IP Right Grant
- 2014-05-02 JP JP2016512090A patent/JP2016520051A/ja active Pending
- 2014-05-02 KR KR1020157034121A patent/KR20160003215A/ko not_active Ceased
- 2014-05-02 JP JP2016512086A patent/JP2016517889A/ja active Pending
- 2014-05-02 JP JP2016512091A patent/JP7028556B2/ja active Active
- 2014-05-02 CN CN202010594054.0A patent/CN111686255A/zh active Pending
- 2014-05-02 CN CN201911306104.4A patent/CN111068061A/zh active Pending
- 2014-05-02 WO PCT/US2014/036700 patent/WO2014179773A2/en not_active Ceased
- 2014-05-02 BR BR112015027297-5A patent/BR112015027297B1/pt active IP Right Grant
- 2014-05-02 CN CN201910874452.5A patent/CN110639024A/zh active Pending
- 2014-05-02 IL IL292190A patent/IL292190A/en unknown
- 2014-05-02 EP EP14791119.2A patent/EP2991629A4/en active Pending
- 2014-05-02 AU AU2014262163A patent/AU2014262163A1/en not_active Abandoned
- 2014-05-02 KR KR1020227004760A patent/KR20220025909A/ko not_active Ceased
- 2014-05-02 KR KR1020227004761A patent/KR20220025910A/ko not_active Ceased
- 2014-05-02 US US14/269,058 patent/US10335395B2/en active Active
- 2014-05-02 KR KR1020157034143A patent/KR20160003219A/ko not_active Ceased
- 2014-05-02 MX MX2015015225A patent/MX382604B/es unknown
- 2014-05-02 MX MX2015015231A patent/MX2015015231A/es unknown
- 2014-05-02 MX MX2021005697A patent/MX2021005697A/es unknown
- 2014-05-02 CN CN202410981673.3A patent/CN118987263A/zh active Pending
- 2014-05-02 WO PCT/US2014/036697 patent/WO2014179770A1/en not_active Ceased
- 2014-05-02 JP JP2016512093A patent/JP6818549B2/ja active Active
- 2014-05-02 AU AU2014262155A patent/AU2014262155A1/en not_active Abandoned
- 2014-05-02 CA CA2910583A patent/CA2910583C/en active Active
- 2014-05-02 EP EP14791567.2A patent/EP2991630A4/en active Pending
- 2014-05-02 KR KR1020157034120A patent/KR20160003214A/ko not_active Ceased
- 2014-05-02 CA CA2910417A patent/CA2910417C/en active Active
- 2014-05-02 JP JP2016512094A patent/JP6580558B2/ja active Active
- 2014-05-02 KR KR1020247024767A patent/KR20240116963A/ko active Pending
- 2014-05-02 US US14/269,054 patent/US10357482B2/en active Active
- 2014-05-02 BR BR112015027291A patent/BR112015027291A8/pt not_active Application Discontinuation
- 2014-05-02 KR KR1020227004756A patent/KR20220025906A/ko not_active Ceased
- 2014-05-02 EP EP14791496.4A patent/EP2991646B1/en active Active
- 2014-05-02 WO PCT/US2014/036696 patent/WO2014179769A2/en not_active Ceased
- 2014-05-02 CN CN202410347642.2A patent/CN118370823A/zh active Pending
- 2014-05-02 EA EA201592103A patent/EA201592103A3/ru unknown
- 2014-05-02 EA EA201592104A patent/EA201592104A3/ru unknown
- 2014-05-02 DK DK14791496.4T patent/DK2991646T3/da active
- 2014-05-02 WO PCT/US2014/036687 patent/WO2014179762A1/en not_active Ceased
- 2014-05-02 JP JP2016512092A patent/JP6760838B2/ja active Active
- 2014-05-02 MX MX2015015230A patent/MX386917B/es unknown
- 2014-05-02 BR BR112015027281-9A patent/BR112015027281B1/pt active IP Right Grant
- 2014-05-02 EP EP14791147.3A patent/EP2991685A4/en active Pending
- 2014-05-02 BR BR112015027288-6A patent/BR112015027288B1/pt active IP Right Grant
- 2014-05-02 ES ES14791496T patent/ES2842206T3/es active Active
- 2014-05-02 CN CN201480032224.9A patent/CN105263478A/zh active Pending
- 2014-05-02 CN CN201480031937.3A patent/CN105307641A/zh active Pending
- 2014-05-02 CN CN201480037076.XA patent/CN105338979A/zh active Pending
- 2014-05-02 US US14/269,047 patent/US10434088B2/en active Active
- 2014-05-02 KR KR1020247024766A patent/KR20240119161A/ko active Pending
- 2014-05-02 CA CA2910578A patent/CA2910578C/en active Active
- 2014-05-02 AU AU2014262166A patent/AU2014262166B2/en active Active
- 2014-05-02 KR KR1020227004763A patent/KR20220025911A/ko not_active Ceased
- 2014-05-02 KR KR1020247024664A patent/KR20240119156A/ko not_active Ceased
- 2014-05-02 EA EA201592106A patent/EA201592106A3/ru unknown
- 2014-05-02 EA EA201592105A patent/EA201592105A1/ru unknown
- 2014-05-02 CA CA2910575A patent/CA2910575C/en active Active
- 2014-05-02 HU HUE14791496A patent/HUE052599T2/hu unknown
- 2014-05-02 EA EA201592107A patent/EA201592107A1/ru unknown
- 2014-05-02 EP EP14792080.5A patent/EP2991631A4/en active Pending
- 2014-05-02 MX MX2015015229A patent/MX2015015229A/es unknown
- 2014-05-02 KR KR1020157034102A patent/KR20160003212A/ko not_active Ceased
- 2014-05-02 EA EA201592102A patent/EA201592102A1/ru unknown
- 2014-05-02 MX MX2015015223A patent/MX380164B/es unknown
- 2014-05-02 MX MX2015015221A patent/MX394497B/es unknown
- 2014-05-02 US US14/269,048 patent/US10668053B2/en active Active
-
2015
- 2015-10-22 IL IL24221615A patent/IL242216B/en active IP Right Grant
- 2015-10-26 IL IL242272A patent/IL242272B/en active IP Right Grant
- 2015-10-26 IL IL242273A patent/IL242273B/en active IP Right Grant
- 2015-10-26 IL IL24227015A patent/IL242270B/en active IP Right Grant
- 2015-10-26 IL IL242271A patent/IL242271B/en active IP Right Grant
- 2015-10-30 MX MX2022009538A patent/MX2022009538A/es unknown
- 2015-10-30 MX MX2021001878A patent/MX2021001878A/es unknown
- 2015-10-30 MX MX2021001879A patent/MX2021001879A/es unknown
- 2015-10-30 MX MX2021001982A patent/MX2021001982A/es unknown
- 2015-10-30 MX MX2021012348A patent/MX2021012348A/es unknown
-
2018
- 2018-12-10 JP JP2018231206A patent/JP6983144B2/ja active Active
-
2019
- 2019-01-15 JP JP2019004287A patent/JP7134885B2/ja active Active
- 2019-05-13 US US16/410,876 patent/US20200069659A1/en not_active Abandoned
- 2019-06-06 US US16/433,622 patent/US20200069660A1/en not_active Abandoned
- 2019-06-11 US US16/438,147 patent/US11298342B2/en active Active
- 2019-08-26 US US16/550,725 patent/US20200113874A1/en not_active Abandoned
- 2019-08-28 JP JP2019155456A patent/JP2020015741A/ja active Pending
- 2019-10-15 AU AU2019250117A patent/AU2019250117B2/en active Active
- 2019-10-24 IL IL270133A patent/IL270133B/en unknown
- 2019-10-24 IL IL270135A patent/IL270135B/en unknown
- 2019-10-28 JP JP2019195263A patent/JP7427419B2/ja active Active
- 2019-12-02 JP JP2019217946A patent/JP2020073488A/ja active Pending
-
2020
- 2020-01-04 AU AU2020200065A patent/AU2020200065B2/en active Active
- 2020-01-24 AU AU2020200565A patent/AU2020200565A1/en not_active Abandoned
- 2020-02-05 AU AU2020200824A patent/AU2020200824A1/en not_active Abandoned
- 2020-04-24 US US16/858,349 patent/US12508249B2/en active Active
- 2020-05-21 IL IL274852A patent/IL274852B/en unknown
- 2020-05-21 AU AU2020203308A patent/AU2020203308A1/en not_active Abandoned
- 2020-07-21 IL IL276205A patent/IL276205B/en active IP Right Grant
-
2021
- 2021-01-04 JP JP2021000191A patent/JP2021073198A/ja active Pending
- 2021-03-24 US US17/211,459 patent/US20220071968A1/en not_active Abandoned
- 2021-04-04 IL IL282045A patent/IL282045B/en unknown
- 2021-09-30 JP JP2021162235A patent/JP7489362B2/ja active Active
- 2021-11-29 JP JP2021193530A patent/JP2022043071A/ja active Pending
-
2022
- 2022-01-12 AU AU2022200157A patent/AU2022200157A1/en not_active Abandoned
- 2022-03-09 US US17/690,437 patent/US12472167B2/en active Active
- 2022-03-09 AU AU2022201641A patent/AU2022201641B2/en active Active
- 2022-03-15 IL IL291394A patent/IL291394A/en unknown
- 2022-05-06 JP JP2022076787A patent/JP7440833B2/ja active Active
- 2022-05-06 JP JP2022076702A patent/JP2022122871A/ja active Pending
- 2022-05-11 AU AU2022203142A patent/AU2022203142B2/en active Active
- 2022-05-25 AU AU2022203540A patent/AU2022203540A1/en not_active Abandoned
- 2022-12-09 JP JP2022197386A patent/JP2023039981A/ja active Pending
-
2023
- 2023-05-11 AU AU2023202955A patent/AU2023202955A1/en not_active Abandoned
- 2023-12-01 US US18/527,060 patent/US20240350462A1/en active Pending
-
2024
- 2024-05-13 JP JP2024077998A patent/JP2024116128A/ja active Pending
- 2024-06-28 US US18/757,781 patent/US20250177360A1/en active Pending
- 2024-08-21 AU AU2024213104A patent/AU2024213104A1/en not_active Abandoned
- 2024-09-13 JP JP2024159048A patent/JP2025003994A/ja not_active Withdrawn
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1979166A (zh) * | 2005-11-30 | 2007-06-13 | 北京有色金属研究总院 | 一种制备免疫检测用纳米胶体金的工艺方法及其反应装置 |
| EP1795185A2 (en) * | 2005-12-07 | 2007-06-13 | Cordis Corporation | Nano- and/or micro-particulate formulations for local injection-based treatment of vascular diseases |
| CN101437491A (zh) * | 2006-02-21 | 2009-05-20 | 洛桑聚合联合学院 | 用于免疫疗法的纳米颗粒 |
| WO2012149255A2 (en) * | 2011-04-29 | 2012-11-01 | Selecta Biosciences, Inc. | Tolerogenic synthetic nanocarriers to reduce immune responses to therapeutic proteins |
| CN102871966A (zh) * | 2012-10-19 | 2013-01-16 | 东南大学 | 用于改善雷帕霉素生物利用度的纳米载药颗粒及其制备方法 |
Non-Patent Citations (3)
| Title |
|---|
| 刘国琴等: "《生物化学》", 30 June 2011, 中国农业大学出版社 * |
| 杨廷彬: "《免疫学及免疫学检验》", 31 May 1998, 人民卫生出版社 * |
| 陈万涛: "《口腔临床免疫学》", 31 January 2010, 上海交通大学出版社 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6983144B2 (ja) | 薬力学的効果の低減または向上のための寛容原性合成ナノ担体および治療用高分子 | |
| CN112933234A (zh) | 非免疫抑制性抗原特异性免疫治疗剂的重复施用 | |
| CN116568329A (zh) | 用于降低针对免疫球蛋白蛋白酶的免疫应答的组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |