RU2687143C2 - Модифицированный экзотоксин а псевдомонад - Google Patents
Модифицированный экзотоксин а псевдомонад Download PDFInfo
- Publication number
- RU2687143C2 RU2687143C2 RU2016114406A RU2016114406A RU2687143C2 RU 2687143 C2 RU2687143 C2 RU 2687143C2 RU 2016114406 A RU2016114406 A RU 2016114406A RU 2016114406 A RU2016114406 A RU 2016114406A RU 2687143 C2 RU2687143 C2 RU 2687143C2
- Authority
- RU
- Russia
- Prior art keywords
- seq
- amino acid
- acid residue
- alanine
- replacement
- Prior art date
Links
- OTLLEIBWKHEHGU-UHFFFAOYSA-N 2-[5-[[5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methoxy]-3,4-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3,5-dihydroxy-4-phosphonooxyhexanedioic acid Chemical class C1=NC=2C(N)=NC=NC=2N1C(C(C1O)O)OC1COC1C(CO)OC(OC(C(O)C(OP(O)(O)=O)C(O)C(O)=O)C(O)=O)C(O)C1O OTLLEIBWKHEHGU-UHFFFAOYSA-N 0.000 title description 5
- 125000000539 amino acid group Chemical group 0.000 claims abstract description 345
- 235000004279 alanine Nutrition 0.000 claims abstract description 208
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 claims abstract description 30
- 235000014304 histidine Nutrition 0.000 claims abstract description 30
- 230000002829 reductive effect Effects 0.000 claims abstract description 28
- 230000005847 immunogenicity Effects 0.000 claims abstract description 26
- 101710082714 Exotoxin A Proteins 0.000 claims abstract description 23
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims abstract description 19
- 235000013922 glutamic acid Nutrition 0.000 claims abstract description 18
- 239000004220 glutamic acid Substances 0.000 claims abstract description 18
- 229960001230 asparagine Drugs 0.000 claims abstract description 16
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Chemical group OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 claims abstract description 15
- 235000009582 asparagine Nutrition 0.000 claims abstract description 15
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 15
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 claims abstract description 12
- 238000004519 manufacturing process Methods 0.000 claims abstract description 11
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical group OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 claims abstract description 10
- 241000589516 Pseudomonas Species 0.000 claims abstract description 10
- 239000003814 drug Substances 0.000 claims abstract description 9
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 claims abstract description 5
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 claims abstract description 5
- 239000000427 antigen Substances 0.000 claims description 224
- 102000036639 antigens Human genes 0.000 claims description 223
- 108091007433 antigens Proteins 0.000 claims description 223
- 210000004027 cell Anatomy 0.000 claims description 215
- 230000027455 binding Effects 0.000 claims description 200
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 claims description 169
- 108090000623 proteins and genes Proteins 0.000 claims description 137
- 238000006467 substitution reaction Methods 0.000 claims description 130
- 102000004169 proteins and genes Human genes 0.000 claims description 99
- 206010028980 Neoplasm Diseases 0.000 claims description 95
- 235000001014 amino acid Nutrition 0.000 claims description 93
- 235000018102 proteins Nutrition 0.000 claims description 88
- 150000001413 amino acids Chemical group 0.000 claims description 84
- 229940024606 amino acid Drugs 0.000 claims description 80
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 64
- 201000011510 cancer Diseases 0.000 claims description 64
- 238000000034 method Methods 0.000 claims description 61
- 239000013604 expression vector Substances 0.000 claims description 47
- 230000001472 cytotoxic effect Effects 0.000 claims description 46
- 238000003259 recombinant expression Methods 0.000 claims description 46
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 44
- 241000282414 Homo sapiens Species 0.000 claims description 43
- 150000007523 nucleic acids Chemical class 0.000 claims description 38
- 108020004707 nucleic acids Proteins 0.000 claims description 37
- 102000039446 nucleic acids Human genes 0.000 claims description 37
- 102000004961 Furin Human genes 0.000 claims description 31
- 108090001126 Furin Proteins 0.000 claims description 31
- 102000003735 Mesothelin Human genes 0.000 claims description 28
- 108090000015 Mesothelin Proteins 0.000 claims description 28
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 claims description 25
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 25
- -1 CD79b Proteins 0.000 claims description 23
- 241000124008 Mammalia Species 0.000 claims description 22
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 21
- 102000010956 Glypican Human genes 0.000 claims description 21
- 108050001154 Glypican Proteins 0.000 claims description 21
- 108050007237 Glypican-3 Proteins 0.000 claims description 21
- 239000001132 aluminium potassium sulphate Substances 0.000 claims description 20
- 239000008194 pharmaceutical composition Substances 0.000 claims description 19
- 239000004475 Arginine Substances 0.000 claims description 18
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 claims description 18
- 235000009697 arginine Nutrition 0.000 claims description 18
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 18
- 239000001194 polyoxyethylene (40) stearate Substances 0.000 claims description 17
- 235000011185 polyoxyethylene (40) stearate Nutrition 0.000 claims description 17
- 239000002458 cell surface marker Substances 0.000 claims description 16
- 238000000746 purification Methods 0.000 claims description 15
- 102000005962 receptors Human genes 0.000 claims description 14
- 108020003175 receptors Proteins 0.000 claims description 14
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 claims description 13
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 13
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 claims description 13
- 238000003776 cleavage reaction Methods 0.000 claims description 13
- 230000012010 growth Effects 0.000 claims description 13
- 230000007017 scission Effects 0.000 claims description 13
- 238000012217 deletion Methods 0.000 claims description 12
- 230000037430 deletion Effects 0.000 claims description 12
- 102100033579 Trophoblast glycoprotein Human genes 0.000 claims description 11
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 claims description 11
- 230000002401 inhibitory effect Effects 0.000 claims description 11
- 102000001301 EGF receptor Human genes 0.000 claims description 10
- 239000004471 Glycine Substances 0.000 claims description 10
- 206010025323 Lymphomas Diseases 0.000 claims description 10
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 10
- 230000008685 targeting Effects 0.000 claims description 10
- 102100038080 B-cell receptor CD22 Human genes 0.000 claims description 9
- 102100024423 Carbonic anhydrase 9 Human genes 0.000 claims description 9
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 claims description 9
- 102100025243 Myeloid cell surface antigen CD33 Human genes 0.000 claims description 9
- 239000004330 calcium propionate Substances 0.000 claims description 9
- 102100041003 Glutamate carboxypeptidase 2 Human genes 0.000 claims description 8
- 101000892862 Homo sapiens Glutamate carboxypeptidase 2 Proteins 0.000 claims description 8
- 101000801433 Homo sapiens Trophoblast glycoprotein Proteins 0.000 claims description 8
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 claims description 8
- 239000001527 calcium lactate Substances 0.000 claims description 8
- 239000004328 sodium tetraborate Substances 0.000 claims description 8
- 101000934338 Homo sapiens Myeloid cell surface antigen CD33 Proteins 0.000 claims description 7
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 7
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 7
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 claims description 7
- 239000004472 Lysine Substances 0.000 claims description 7
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 7
- 239000003937 drug carrier Substances 0.000 claims description 7
- 239000001509 sodium citrate Substances 0.000 claims description 7
- 108700012439 CA9 Proteins 0.000 claims description 6
- 108060006698 EGF receptor Proteins 0.000 claims description 6
- 102100040892 Growth/differentiation factor 2 Human genes 0.000 claims description 6
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 claims description 6
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 claims description 6
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 claims description 6
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 claims description 6
- 108010033576 Transferrin Receptors Proteins 0.000 claims description 6
- 102100026144 Transferrin receptor protein 1 Human genes 0.000 claims description 6
- 125000000613 asparagine group Chemical group N[C@@H](CC(N)=O)C(=O)* 0.000 claims description 6
- 235000018977 lysine Nutrition 0.000 claims description 6
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 claims description 6
- 101800003838 Epidermal growth factor Proteins 0.000 claims description 5
- 230000004913 activation Effects 0.000 claims description 5
- 229940116977 epidermal growth factor Drugs 0.000 claims description 5
- 239000004474 valine Substances 0.000 claims description 5
- 235000014393 valine Nutrition 0.000 claims description 5
- 101100067974 Arabidopsis thaliana POP2 gene Proteins 0.000 claims description 4
- 102000000905 Cadherin Human genes 0.000 claims description 4
- 108050007957 Cadherin Proteins 0.000 claims description 4
- 102100032768 Complement receptor type 2 Human genes 0.000 claims description 4
- 101000941929 Homo sapiens Complement receptor type 2 Proteins 0.000 claims description 4
- 101100118549 Homo sapiens EGFR gene Proteins 0.000 claims description 4
- 101000851376 Homo sapiens Tumor necrosis factor receptor superfamily member 8 Proteins 0.000 claims description 4
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 claims description 4
- 102100034256 Mucin-1 Human genes 0.000 claims description 4
- 101100123851 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) HER1 gene Proteins 0.000 claims description 4
- 102100036857 Tumor necrosis factor receptor superfamily member 8 Human genes 0.000 claims description 4
- 239000003102 growth factor Substances 0.000 claims description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 4
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 claims description 3
- 102100038083 Endosialin Human genes 0.000 claims description 3
- 101710144543 Endosialin Proteins 0.000 claims description 3
- 108010090290 Growth Differentiation Factor 2 Proteins 0.000 claims description 3
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 claims description 3
- 101000893585 Homo sapiens Growth/differentiation factor 2 Proteins 0.000 claims description 3
- 101001103039 Homo sapiens Inactive tyrosine-protein kinase transmembrane receptor ROR1 Proteins 0.000 claims description 3
- 101001133056 Homo sapiens Mucin-1 Proteins 0.000 claims description 3
- 101001103036 Homo sapiens Nuclear receptor ROR-alpha Proteins 0.000 claims description 3
- 102100039615 Inactive tyrosine-protein kinase transmembrane receptor ROR1 Human genes 0.000 claims description 3
- 108010002386 Interleukin-3 Proteins 0.000 claims description 3
- 102000000646 Interleukin-3 Human genes 0.000 claims description 3
- 108010063954 Mucins Proteins 0.000 claims description 3
- 101100490437 Mus musculus Acvrl1 gene Proteins 0.000 claims description 3
- 101710160107 Outer membrane protein A Proteins 0.000 claims description 3
- 108091000080 Phosphotransferase Proteins 0.000 claims description 3
- 102100023832 Prolyl endopeptidase FAP Human genes 0.000 claims description 3
- 102100029986 Receptor tyrosine-protein kinase erbB-3 Human genes 0.000 claims description 3
- 101710100969 Receptor tyrosine-protein kinase erbB-3 Proteins 0.000 claims description 3
- 101710190034 Trophoblast glycoprotein Proteins 0.000 claims description 3
- 229950001537 amatuximab Drugs 0.000 claims description 3
- 210000002950 fibroblast Anatomy 0.000 claims description 3
- 229940076264 interleukin-3 Drugs 0.000 claims description 3
- 210000000066 myeloid cell Anatomy 0.000 claims description 3
- 102000020233 phosphotransferase Human genes 0.000 claims description 3
- 108010067225 Cell Adhesion Molecules Proteins 0.000 claims description 2
- 102000016289 Cell Adhesion Molecules Human genes 0.000 claims description 2
- 102000003886 Glycoproteins Human genes 0.000 claims description 2
- 108090000288 Glycoproteins Proteins 0.000 claims description 2
- 101000762949 Pseudomonas aeruginosa (strain ATCC 15692 / DSM 22644 / CIP 104116 / JCM 14847 / LMG 12228 / 1C / PRS 101 / PAO1) Exotoxin A Proteins 0.000 claims description 2
- 108010029180 Sialic Acid Binding Ig-like Lectin 3 Proteins 0.000 claims description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims description 2
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 claims description 2
- 210000002569 neuron Anatomy 0.000 claims description 2
- 210000002308 embryonic cell Anatomy 0.000 claims 5
- 102100026094 C-type lectin domain family 12 member A Human genes 0.000 claims 4
- 101000912622 Homo sapiens C-type lectin domain family 12 member A Proteins 0.000 claims 4
- 102100033237 Pro-epidermal growth factor Human genes 0.000 claims 3
- 102000003846 Carbonic anhydrases Human genes 0.000 claims 1
- 108090000209 Carbonic anhydrases Proteins 0.000 claims 1
- 101710197063 Lectin-3 Proteins 0.000 claims 1
- SQVRNKJHWKZAKO-UHFFFAOYSA-N beta-N-Acetyl-D-neuraminic acid Natural products CC(=O)NC1C(O)CC(O)(C(O)=O)OC1C(O)C(O)CO SQVRNKJHWKZAKO-UHFFFAOYSA-N 0.000 claims 1
- 230000005907 cancer growth Effects 0.000 claims 1
- 108010072257 fibroblast activation protein alpha Proteins 0.000 claims 1
- 210000002751 lymph Anatomy 0.000 claims 1
- 210000005036 nerve Anatomy 0.000 claims 1
- SQVRNKJHWKZAKO-OQPLDHBCSA-N sialic acid Chemical compound CC(=O)N[C@@H]1[C@@H](O)C[C@@](O)(C(O)=O)OC1[C@H](O)[C@H](O)CO SQVRNKJHWKZAKO-OQPLDHBCSA-N 0.000 claims 1
- 210000002993 trophoblast Anatomy 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 53
- 230000003013 cytotoxicity Effects 0.000 abstract description 16
- 231100000135 cytotoxicity Toxicity 0.000 abstract description 16
- 239000000126 substance Substances 0.000 abstract description 11
- 239000002095 exotoxin Substances 0.000 abstract description 9
- 231100000776 exotoxin Toxicity 0.000 abstract description 9
- 238000011319 anticancer therapy Methods 0.000 abstract 1
- 229960003767 alanine Drugs 0.000 description 164
- 125000005647 linker group Chemical group 0.000 description 119
- 125000003275 alpha amino acid group Chemical group 0.000 description 97
- 108090000765 processed proteins & peptides Proteins 0.000 description 88
- 230000004044 response Effects 0.000 description 82
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 70
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 70
- 230000035772 mutation Effects 0.000 description 55
- 230000014509 gene expression Effects 0.000 description 43
- 102000004196 processed proteins & peptides Human genes 0.000 description 43
- 239000000243 solution Substances 0.000 description 41
- 239000012634 fragment Substances 0.000 description 40
- 241000588724 Escherichia coli Species 0.000 description 36
- 125000003729 nucleotide group Chemical group 0.000 description 34
- 239000000463 material Substances 0.000 description 32
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 31
- 239000013598 vector Substances 0.000 description 31
- 239000002773 nucleotide Substances 0.000 description 30
- 229940051173 recombinant immunotoxin Drugs 0.000 description 29
- 239000013612 plasmid Substances 0.000 description 27
- 229960002885 histidine Drugs 0.000 description 26
- 239000000203 mixture Substances 0.000 description 26
- 239000000872 buffer Substances 0.000 description 25
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 23
- 201000009277 hairy cell leukemia Diseases 0.000 description 23
- 229920001481 poly(stearyl methacrylate) Polymers 0.000 description 22
- 239000004698 Polyethylene Substances 0.000 description 21
- 239000000523 sample Substances 0.000 description 21
- 238000000855 fermentation Methods 0.000 description 20
- 230000004151 fermentation Effects 0.000 description 20
- 230000000638 stimulation Effects 0.000 description 20
- 238000004458 analytical method Methods 0.000 description 19
- 230000001965 increasing effect Effects 0.000 description 19
- 230000010076 replication Effects 0.000 description 19
- 101150030083 PE38 gene Proteins 0.000 description 18
- 239000011780 sodium chloride Substances 0.000 description 17
- 241000699670 Mus sp. Species 0.000 description 16
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 15
- 230000003287 optical effect Effects 0.000 description 15
- 239000007983 Tris buffer Substances 0.000 description 14
- 210000003000 inclusion body Anatomy 0.000 description 14
- 210000002966 serum Anatomy 0.000 description 14
- 238000001542 size-exclusion chromatography Methods 0.000 description 14
- 239000000725 suspension Substances 0.000 description 14
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 14
- 230000037396 body weight Effects 0.000 description 13
- 238000002360 preparation method Methods 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 12
- 241001465754 Metazoa Species 0.000 description 12
- 238000009472 formulation Methods 0.000 description 12
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 11
- 206010027406 Mesothelioma Diseases 0.000 description 11
- 108010076504 Protein Sorting Signals Proteins 0.000 description 11
- 230000002776 aggregation Effects 0.000 description 11
- 238000004220 aggregation Methods 0.000 description 11
- 239000008103 glucose Substances 0.000 description 11
- 229940051026 immunotoxin Drugs 0.000 description 11
- 230000002637 immunotoxin Effects 0.000 description 11
- 239000002596 immunotoxin Substances 0.000 description 11
- 231100000608 immunotoxin Toxicity 0.000 description 11
- 238000011534 incubation Methods 0.000 description 11
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 11
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 10
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 10
- 231100000433 cytotoxic Toxicity 0.000 description 10
- 238000002296 dynamic light scattering Methods 0.000 description 10
- 239000000499 gel Substances 0.000 description 10
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 9
- 101000576802 Homo sapiens Mesothelin Proteins 0.000 description 9
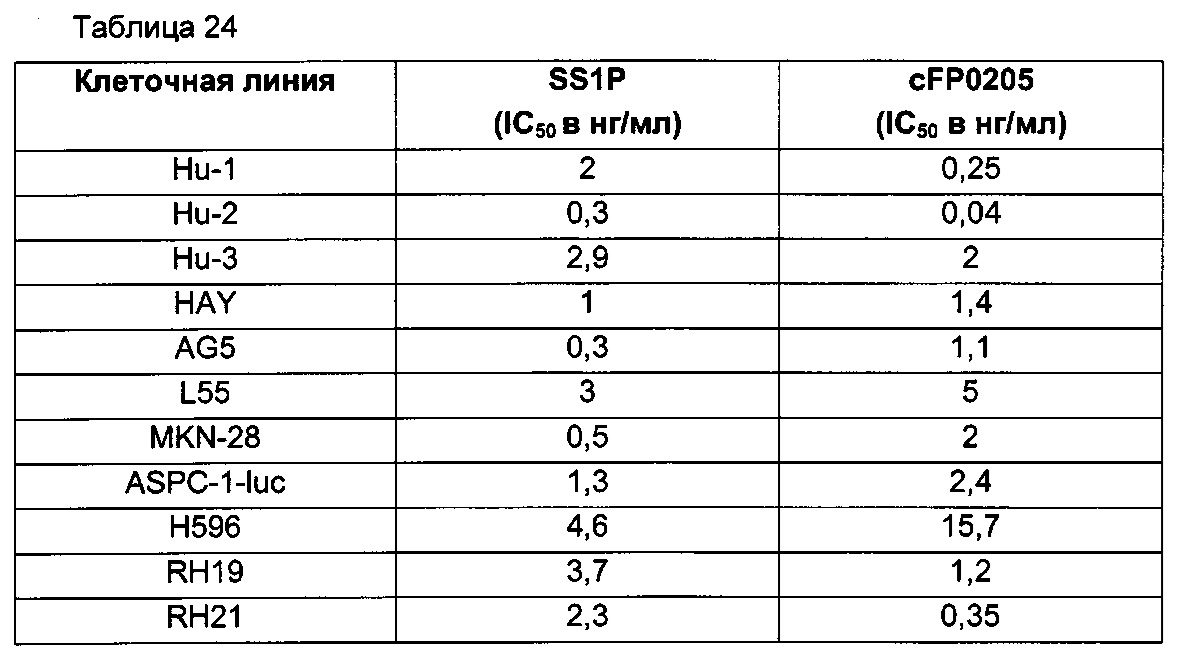
- 229940127180 SS1P Drugs 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 238000005119 centrifugation Methods 0.000 description 9
- 238000010276 construction Methods 0.000 description 9
- 239000010432 diamond Substances 0.000 description 9
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 9
- 230000002163 immunogen Effects 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 229960001153 serine Drugs 0.000 description 9
- 239000006228 supernatant Substances 0.000 description 9
- 238000013518 transcription Methods 0.000 description 9
- 210000004881 tumor cell Anatomy 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 8
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 230000004071 biological effect Effects 0.000 description 8
- 235000014113 dietary fatty acids Nutrition 0.000 description 8
- 239000013613 expression plasmid Substances 0.000 description 8
- 239000000194 fatty acid Substances 0.000 description 8
- 229930195729 fatty acid Natural products 0.000 description 8
- 239000007924 injection Substances 0.000 description 8
- 238000002347 injection Methods 0.000 description 8
- 235000015097 nutrients Nutrition 0.000 description 8
- 239000011573 trace mineral Substances 0.000 description 8
- 235000013619 trace mineral Nutrition 0.000 description 8
- 230000035897 transcription Effects 0.000 description 8
- 238000011282 treatment Methods 0.000 description 8
- 108020004414 DNA Proteins 0.000 description 7
- 102100031334 Elongation factor 2 Human genes 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 229930012538 Paclitaxel Natural products 0.000 description 7
- 108010077519 Peptide Elongation Factor 2 Proteins 0.000 description 7
- 238000010367 cloning Methods 0.000 description 7
- PJJJBBJSCAKJQF-UHFFFAOYSA-N guanidinium chloride Chemical compound [Cl-].NC(N)=[NH2+] PJJJBBJSCAKJQF-UHFFFAOYSA-N 0.000 description 7
- 239000003550 marker Substances 0.000 description 7
- 229960001592 paclitaxel Drugs 0.000 description 7
- 239000002244 precipitate Substances 0.000 description 7
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Substances [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 7
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 7
- 230000001225 therapeutic effect Effects 0.000 description 7
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 6
- 238000002965 ELISA Methods 0.000 description 6
- FFEARJCKVFRZRR-UHFFFAOYSA-N L-Methionine Natural products CSCCC(N)C(O)=O FFEARJCKVFRZRR-UHFFFAOYSA-N 0.000 description 6
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 6
- 229930195722 L-methionine Natural products 0.000 description 6
- 102100025096 Mesothelin Human genes 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 238000000692 Student's t-test Methods 0.000 description 6
- 230000002378 acidificating effect Effects 0.000 description 6
- 208000009956 adenocarcinoma Diseases 0.000 description 6
- 238000005273 aeration Methods 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 6
- 239000003599 detergent Substances 0.000 description 6
- 230000028993 immune response Effects 0.000 description 6
- 238000000338 in vitro Methods 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- 229960004452 methionine Drugs 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 238000012545 processing Methods 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 108010049777 Ankyrins Proteins 0.000 description 5
- 102000008102 Ankyrins Human genes 0.000 description 5
- 241000894006 Bacteria Species 0.000 description 5
- 239000002028 Biomass Substances 0.000 description 5
- 102100027207 CD27 antigen Human genes 0.000 description 5
- 201000009030 Carcinoma Diseases 0.000 description 5
- 102000004127 Cytokines Human genes 0.000 description 5
- 108090000695 Cytokines Proteins 0.000 description 5
- 101001002317 Homo sapiens Gastrin Proteins 0.000 description 5
- MXKCYTKUIDTFLY-ZNNSSXPHSA-N alpha-L-Fucp-(1->2)-beta-D-Galp-(1->4)-[alpha-L-Fucp-(1->3)]-beta-D-GlcpNAc-(1->3)-D-Galp Chemical compound O[C@H]1[C@H](O)[C@H](O)[C@H](C)O[C@H]1O[C@H]1[C@H](O[C@H]2[C@@H]([C@@H](NC(C)=O)[C@H](O[C@H]3[C@H]([C@@H](CO)OC(O)[C@@H]3O)O)O[C@@H]2CO)O[C@H]2[C@H]([C@H](O)[C@H](O)[C@H](C)O2)O)O[C@H](CO)[C@H](O)[C@@H]1O MXKCYTKUIDTFLY-ZNNSSXPHSA-N 0.000 description 5
- 150000001412 amines Chemical class 0.000 description 5
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 5
- 108010006025 bovine growth hormone Proteins 0.000 description 5
- 230000003833 cell viability Effects 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 230000001684 chronic effect Effects 0.000 description 5
- 238000013461 design Methods 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 230000018109 developmental process Effects 0.000 description 5
- 239000003085 diluting agent Substances 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 150000004665 fatty acids Chemical class 0.000 description 5
- 229960002449 glycine Drugs 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 210000004698 lymphocyte Anatomy 0.000 description 5
- 239000000594 mannitol Substances 0.000 description 5
- 235000010355 mannitol Nutrition 0.000 description 5
- 238000004949 mass spectrometry Methods 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 239000001301 oxygen Substances 0.000 description 5
- 229910052760 oxygen Inorganic materials 0.000 description 5
- 239000012071 phase Substances 0.000 description 5
- 238000011321 prophylaxis Methods 0.000 description 5
- 230000008929 regeneration Effects 0.000 description 5
- 238000011069 regeneration method Methods 0.000 description 5
- 238000004153 renaturation Methods 0.000 description 5
- 230000002441 reversible effect Effects 0.000 description 5
- 238000012216 screening Methods 0.000 description 5
- 206010041823 squamous cell carcinoma Diseases 0.000 description 5
- 238000010561 standard procedure Methods 0.000 description 5
- 239000004094 surface-active agent Substances 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 229940035893 uracil Drugs 0.000 description 5
- 229960004295 valine Drugs 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- RFLVMTUMFYRZCB-UHFFFAOYSA-N 1-methylguanine Chemical compound O=C1N(C)C(N)=NC2=C1N=CN2 RFLVMTUMFYRZCB-UHFFFAOYSA-N 0.000 description 4
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 4
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 4
- 206010009944 Colon cancer Diseases 0.000 description 4
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 description 4
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 4
- 206010024612 Lipoma Diseases 0.000 description 4
- 108060001084 Luciferase Proteins 0.000 description 4
- 206010033128 Ovarian cancer Diseases 0.000 description 4
- 101150112800 PE35 gene Proteins 0.000 description 4
- 229910019142 PO4 Inorganic materials 0.000 description 4
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- 208000033766 Prolymphocytic Leukemia Diseases 0.000 description 4
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 4
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 4
- 108010034546 Serratia marcescens nuclease Proteins 0.000 description 4
- 229930006000 Sucrose Natural products 0.000 description 4
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 4
- 230000006044 T cell activation Effects 0.000 description 4
- 230000005867 T cell response Effects 0.000 description 4
- JZRWCGZRTZMZEH-UHFFFAOYSA-N Thiamine Natural products CC1=C(CCO)SC=[N+]1CC1=CN=C(C)N=C1N JZRWCGZRTZMZEH-UHFFFAOYSA-N 0.000 description 4
- 102000004338 Transferrin Human genes 0.000 description 4
- 108090000901 Transferrin Proteins 0.000 description 4
- 101150050575 URA3 gene Proteins 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 230000001154 acute effect Effects 0.000 description 4
- 239000000443 aerosol Substances 0.000 description 4
- 229960000723 ampicillin Drugs 0.000 description 4
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 4
- 102000025171 antigen binding proteins Human genes 0.000 description 4
- 108091000831 antigen binding proteins Proteins 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- 230000000295 complement effect Effects 0.000 description 4
- 230000001461 cytolytic effect Effects 0.000 description 4
- 238000000502 dialysis Methods 0.000 description 4
- 238000001962 electrophoresis Methods 0.000 description 4
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 4
- 230000007717 exclusion Effects 0.000 description 4
- 206010016629 fibroma Diseases 0.000 description 4
- 108020001507 fusion proteins Proteins 0.000 description 4
- 102000037865 fusion proteins Human genes 0.000 description 4
- 206010017758 gastric cancer Diseases 0.000 description 4
- 229960002743 glutamine Drugs 0.000 description 4
- 235000011187 glycerol Nutrition 0.000 description 4
- 229960004198 guanidine Drugs 0.000 description 4
- 238000000126 in silico method Methods 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- 239000002054 inoculum Substances 0.000 description 4
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 4
- 208000032839 leukemia Diseases 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 4
- 201000002528 pancreatic cancer Diseases 0.000 description 4
- 208000008443 pancreatic carcinoma Diseases 0.000 description 4
- 238000007911 parenteral administration Methods 0.000 description 4
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 4
- 239000010452 phosphate Substances 0.000 description 4
- 229920002401 polyacrylamide Polymers 0.000 description 4
- 108091033319 polynucleotide Proteins 0.000 description 4
- 102000040430 polynucleotide Human genes 0.000 description 4
- 239000002157 polynucleotide Substances 0.000 description 4
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 230000002265 prevention Effects 0.000 description 4
- 101150116440 pyrF gene Proteins 0.000 description 4
- 238000011084 recovery Methods 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 239000012723 sample buffer Substances 0.000 description 4
- 239000005720 sucrose Substances 0.000 description 4
- KYMBYSLLVAOCFI-UHFFFAOYSA-N thiamine Chemical compound CC1=C(CCO)SCN1CC1=CN=C(C)N=C1N KYMBYSLLVAOCFI-UHFFFAOYSA-N 0.000 description 4
- 235000019157 thiamine Nutrition 0.000 description 4
- 229960003495 thiamine Drugs 0.000 description 4
- 239000011721 thiamine Substances 0.000 description 4
- 239000012581 transferrin Substances 0.000 description 4
- 241001515965 unidentified phage Species 0.000 description 4
- 239000011534 wash buffer Substances 0.000 description 4
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 3
- 108700028369 Alleles Proteins 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 206010006187 Breast cancer Diseases 0.000 description 3
- 208000026310 Breast neoplasm Diseases 0.000 description 3
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 3
- 229920002785 Croscarmellose sodium Polymers 0.000 description 3
- 241000701022 Cytomegalovirus Species 0.000 description 3
- 238000001712 DNA sequencing Methods 0.000 description 3
- 241000196324 Embryophyta Species 0.000 description 3
- 102000009024 Epidermal Growth Factor Human genes 0.000 description 3
- 102100037362 Fibronectin Human genes 0.000 description 3
- 108010067306 Fibronectins Proteins 0.000 description 3
- 201000008808 Fibrosarcoma Diseases 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 3
- 108010002350 Interleukin-2 Proteins 0.000 description 3
- 102000000588 Interleukin-2 Human genes 0.000 description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 3
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 3
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 3
- 102000019298 Lipocalin Human genes 0.000 description 3
- 108050006654 Lipocalin Proteins 0.000 description 3
- 239000005089 Luciferase Substances 0.000 description 3
- 102000000440 Melanoma-associated antigen Human genes 0.000 description 3
- 108050008953 Melanoma-associated antigen Proteins 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 101100029145 Mycobacterium tuberculosis (strain ATCC 25618 / H37Rv) PE25 gene Proteins 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 206010061535 Ovarian neoplasm Diseases 0.000 description 3
- 108010072866 Prostate-Specific Antigen Proteins 0.000 description 3
- 102100038358 Prostate-specific antigen Human genes 0.000 description 3
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 3
- 206010039491 Sarcoma Diseases 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 3
- 208000005718 Stomach Neoplasms Diseases 0.000 description 3
- 206010043276 Teratoma Diseases 0.000 description 3
- 102100024598 Tumor necrosis factor ligand superfamily member 10 Human genes 0.000 description 3
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 3
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 239000002518 antifoaming agent Substances 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- 230000003115 biocidal effect Effects 0.000 description 3
- 239000012472 biological sample Substances 0.000 description 3
- OHJMTUPIZMNBFR-UHFFFAOYSA-N biuret Chemical compound NC(=O)NC(N)=O OHJMTUPIZMNBFR-UHFFFAOYSA-N 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 239000001569 carbon dioxide Substances 0.000 description 3
- 229910002092 carbon dioxide Inorganic materials 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 3
- 208000029742 colonic neoplasm Diseases 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 229960001681 croscarmellose sodium Drugs 0.000 description 3
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 3
- 210000000805 cytoplasm Anatomy 0.000 description 3
- 238000002784 cytotoxicity assay Methods 0.000 description 3
- 231100000263 cytotoxicity test Toxicity 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 239000008367 deionised water Substances 0.000 description 3
- 229910021641 deionized water Inorganic materials 0.000 description 3
- 238000000113 differential scanning calorimetry Methods 0.000 description 3
- 230000004069 differentiation Effects 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 210000003527 eukaryotic cell Anatomy 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 229940014259 gelatin Drugs 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 229960000789 guanidine hydrochloride Drugs 0.000 description 3
- 208000014829 head and neck neoplasm Diseases 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 238000009396 hybridization Methods 0.000 description 3
- 230000001976 improved effect Effects 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 238000011081 inoculation Methods 0.000 description 3
- 239000007937 lozenge Substances 0.000 description 3
- 108020004999 messenger RNA Proteins 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 238000010369 molecular cloning Methods 0.000 description 3
- 208000025113 myeloid leukemia Diseases 0.000 description 3
- 230000003472 neutralizing effect Effects 0.000 description 3
- 230000000737 periodic effect Effects 0.000 description 3
- 230000008488 polyadenylation Effects 0.000 description 3
- 239000011148 porous material Substances 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 238000001243 protein synthesis Methods 0.000 description 3
- 230000009257 reactivity Effects 0.000 description 3
- 210000000130 stem cell Anatomy 0.000 description 3
- 201000011549 stomach cancer Diseases 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 239000000454 talc Substances 0.000 description 3
- 235000012222 talc Nutrition 0.000 description 3
- 229910052623 talc Inorganic materials 0.000 description 3
- 239000003053 toxin Substances 0.000 description 3
- 231100000765 toxin Toxicity 0.000 description 3
- 108700012359 toxins Proteins 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 230000007704 transition Effects 0.000 description 3
- 230000014616 translation Effects 0.000 description 3
- 229960004441 tyrosine Drugs 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- WOXWUZCRWJWTRT-UHFFFAOYSA-N 1-amino-1-cyclohexanecarboxylic acid Chemical compound OC(=O)C1(N)CCCCC1 WOXWUZCRWJWTRT-UHFFFAOYSA-N 0.000 description 2
- WJNGQIYEQLPJMN-IOSLPCCCSA-N 1-methylinosine Chemical compound C1=NC=2C(=O)N(C)C=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O WJNGQIYEQLPJMN-IOSLPCCCSA-N 0.000 description 2
- XDOFQFKRPWOURC-UHFFFAOYSA-N 16-methylheptadecanoic acid Chemical compound CC(C)CCCCCCCCCCCCCCC(O)=O XDOFQFKRPWOURC-UHFFFAOYSA-N 0.000 description 2
- OGNSCSPNOLGXSM-UHFFFAOYSA-N 2,4-diaminobutyric acid Chemical compound NCCC(N)C(O)=O OGNSCSPNOLGXSM-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- XMSMHKMPBNTBOD-UHFFFAOYSA-N 2-dimethylamino-6-hydroxypurine Chemical compound N1C(N(C)C)=NC(=O)C2=C1N=CN2 XMSMHKMPBNTBOD-UHFFFAOYSA-N 0.000 description 2
- AZKSAVLVSZKNRD-UHFFFAOYSA-M 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide Chemical compound [Br-].S1C(C)=C(C)N=C1[N+]1=NC(C=2C=CC=CC=2)=NN1C1=CC=CC=C1 AZKSAVLVSZKNRD-UHFFFAOYSA-M 0.000 description 2
- PECYZEOJVXMISF-UHFFFAOYSA-N 3-aminoalanine Chemical compound [NH3+]CC(N)C([O-])=O PECYZEOJVXMISF-UHFFFAOYSA-N 0.000 description 2
- OVONXEQGWXGFJD-UHFFFAOYSA-N 4-sulfanylidene-1h-pyrimidin-2-one Chemical compound SC=1C=CNC(=O)N=1 OVONXEQGWXGFJD-UHFFFAOYSA-N 0.000 description 2
- LRFVTYWOQMYALW-UHFFFAOYSA-N 9H-xanthine Chemical compound O=C1NC(=O)NC2=C1NC=N2 LRFVTYWOQMYALW-UHFFFAOYSA-N 0.000 description 2
- 230000005730 ADP ribosylation Effects 0.000 description 2
- 244000215068 Acacia senegal Species 0.000 description 2
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- QNAYBMKLOCPYGJ-UHFFFAOYSA-N Alanine Chemical compound CC([NH3+])C([O-])=O QNAYBMKLOCPYGJ-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- 206010061424 Anal cancer Diseases 0.000 description 2
- 101100321445 Arabidopsis thaliana ZHD3 gene Proteins 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 231100000699 Bacterial toxin Toxicity 0.000 description 2
- 206010005003 Bladder cancer Diseases 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 108090000342 C-Type Lectins Proteins 0.000 description 2
- 102000003930 C-Type Lectins Human genes 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- 108010022366 Carcinoembryonic Antigen Proteins 0.000 description 2
- 102100025475 Carcinoembryonic antigen-related cell adhesion molecule 5 Human genes 0.000 description 2
- 206010008342 Cervix carcinoma Diseases 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- 241000186031 Corynebacteriaceae Species 0.000 description 2
- 241000699800 Cricetinae Species 0.000 description 2
- 108700022150 Designed Ankyrin Repeat Proteins Proteins 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 102100024746 Dihydrofolate reductase Human genes 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 108090000204 Dipeptidase 1 Proteins 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- 241001646716 Escherichia coli K-12 Species 0.000 description 2
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 201000001342 Fallopian tube cancer Diseases 0.000 description 2
- 208000013452 Fallopian tube neoplasm Diseases 0.000 description 2
- 102000002090 Fibronectin type III Human genes 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 241000233866 Fungi Species 0.000 description 2
- 102100025477 GTP-binding protein Rit1 Human genes 0.000 description 2
- 101710088083 Glomulin Proteins 0.000 description 2
- 108010053070 Glutathione Disulfide Proteins 0.000 description 2
- 102000001398 Granzyme Human genes 0.000 description 2
- 108060005986 Granzyme Proteins 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 208000017604 Hodgkin disease Diseases 0.000 description 2
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 2
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 2
- 101000574654 Homo sapiens GTP-binding protein Rit1 Proteins 0.000 description 2
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 2
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 2
- 102100037850 Interferon gamma Human genes 0.000 description 2
- 108010074328 Interferon-gamma Proteins 0.000 description 2
- 108091092195 Intron Proteins 0.000 description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 description 2
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 2
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 2
- 229930182816 L-glutamine Natural products 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 2
- 208000028018 Lymphocytic leukaemia Diseases 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- 102000016943 Muramidase Human genes 0.000 description 2
- 108010014251 Muramidase Proteins 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 2
- 208000033833 Myelomonocytic Chronic Leukemia Diseases 0.000 description 2
- 208000014767 Myeloproliferative disease Diseases 0.000 description 2
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 2
- 102000019009 Neural Cell Adhesion Molecule L1 Human genes 0.000 description 2
- 108010012255 Neural Cell Adhesion Molecule L1 Proteins 0.000 description 2
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 2
- 102000000470 PDZ domains Human genes 0.000 description 2
- 108050008994 PDZ domains Proteins 0.000 description 2
- 108010079855 Peptide Aptamers Proteins 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- 206010060862 Prostate cancer Diseases 0.000 description 2
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 2
- 108700033844 Pseudomonas aeruginosa toxA Proteins 0.000 description 2
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 239000012722 SDS sample buffer Substances 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 108010090804 Streptavidin Proteins 0.000 description 2
- 239000012505 Superdex™ Substances 0.000 description 2
- 230000006052 T cell proliferation Effects 0.000 description 2
- PZBFGYYEXUXCOF-UHFFFAOYSA-N TCEP Chemical compound OC(=O)CCP(CCC(O)=O)CCC(O)=O PZBFGYYEXUXCOF-UHFFFAOYSA-N 0.000 description 2
- 102100024554 Tetranectin Human genes 0.000 description 2
- 108010009583 Transforming Growth Factors Proteins 0.000 description 2
- 102000009618 Transforming Growth Factors Human genes 0.000 description 2
- 101710097160 Tumor necrosis factor ligand superfamily member 10 Proteins 0.000 description 2
- 102000003425 Tyrosinase Human genes 0.000 description 2
- 108060008724 Tyrosinase Proteins 0.000 description 2
- 108090000848 Ubiquitin Proteins 0.000 description 2
- 102000044159 Ubiquitin Human genes 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 2
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 2
- 208000002495 Uterine Neoplasms Diseases 0.000 description 2
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 208000008383 Wilms tumor Diseases 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 238000001042 affinity chromatography Methods 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 238000012867 alanine scanning Methods 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 239000012670 alkaline solution Substances 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 239000001144 aluminium sodium sulphate Substances 0.000 description 2
- 239000003708 ampul Substances 0.000 description 2
- 238000005349 anion exchange Methods 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 239000000688 bacterial toxin Substances 0.000 description 2
- 239000013602 bacteriophage vector Substances 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 239000006227 byproduct Substances 0.000 description 2
- 229940041514 candida albicans extract Drugs 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 208000002458 carcinoid tumor Diseases 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 201000010881 cervical cancer Diseases 0.000 description 2
- 238000007385 chemical modification Methods 0.000 description 2
- 201000010902 chronic myelomonocytic leukemia Diseases 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 230000016396 cytokine production Effects 0.000 description 2
- 210000000172 cytosol Anatomy 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 238000001212 derivatisation Methods 0.000 description 2
- UQLDLKMNUJERMK-UHFFFAOYSA-L di(octadecanoyloxy)lead Chemical compound [Pb+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O UQLDLKMNUJERMK-UHFFFAOYSA-L 0.000 description 2
- 108020001096 dihydrofolate reductase Proteins 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- 230000005593 dissociations Effects 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 201000003914 endometrial carcinoma Diseases 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 239000006167 equilibration buffer Substances 0.000 description 2
- 201000004101 esophageal cancer Diseases 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- YPZRWBKMTBYPTK-BJDJZHNGSA-N glutathione disulfide Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@H](C(=O)NCC(O)=O)CSSC[C@@H](C(=O)NCC(O)=O)NC(=O)CC[C@H](N)C(O)=O YPZRWBKMTBYPTK-BJDJZHNGSA-N 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 210000004408 hybridoma Anatomy 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000009851 immunogenic response Effects 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 230000000415 inactivating effect Effects 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 229960003136 leucine Drugs 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 201000005249 lung adenocarcinoma Diseases 0.000 description 2
- 208000003747 lymphoid leukemia Diseases 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 239000004325 lysozyme Substances 0.000 description 2
- 229960000274 lysozyme Drugs 0.000 description 2
- 235000010335 lysozyme Nutrition 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 2
- 201000008968 osteosarcoma Diseases 0.000 description 2
- 238000010979 pH adjustment Methods 0.000 description 2
- 238000005192 partition Methods 0.000 description 2
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 2
- 238000002823 phage display Methods 0.000 description 2
- 239000008180 pharmaceutical surfactant Substances 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 229920001983 poloxamer Polymers 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000008057 potassium phosphate buffer Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 210000001236 prokaryotic cell Anatomy 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 230000002797 proteolythic effect Effects 0.000 description 2
- 238000003127 radioimmunoassay Methods 0.000 description 2
- 238000010188 recombinant method Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 238000003998 size exclusion chromatography high performance liquid chromatography Methods 0.000 description 2
- 238000011172 small scale experimental method Methods 0.000 description 2
- 239000000344 soap Substances 0.000 description 2
- VSIVTUIKYVGDCX-UHFFFAOYSA-M sodium;4-[2-(2-methoxy-4-nitrophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].COC1=CC([N+]([O-])=O)=CC=C1[N+]1=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=NN1C1=CC=C([N+]([O-])=O)C=C1 VSIVTUIKYVGDCX-UHFFFAOYSA-M 0.000 description 2
- 238000000527 sonication Methods 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 210000000952 spleen Anatomy 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 229940033134 talc Drugs 0.000 description 2
- 108010013645 tetranectin Proteins 0.000 description 2
- 231100001274 therapeutic index Toxicity 0.000 description 2
- 230000008646 thermal stress Effects 0.000 description 2
- 230000010512 thermal transition Effects 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 230000005945 translocation Effects 0.000 description 2
- 229960004799 tryptophan Drugs 0.000 description 2
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 2
- 201000005112 urinary bladder cancer Diseases 0.000 description 2
- 206010046766 uterine cancer Diseases 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- 239000012138 yeast extract Substances 0.000 description 2
- OCLLVJCYGMCLJG-CYBMUJFWSA-N (2r)-2-azaniumyl-2-naphthalen-1-ylpropanoate Chemical compound C1=CC=C2C([C@@](N)(C(O)=O)C)=CC=CC2=C1 OCLLVJCYGMCLJG-CYBMUJFWSA-N 0.000 description 1
- QFQYGJMNIDGZSG-YFKPBYRVSA-N (2r)-3-(acetamidomethylsulfanyl)-2-azaniumylpropanoate Chemical compound CC(=O)NCSC[C@H]([NH3+])C([O-])=O QFQYGJMNIDGZSG-YFKPBYRVSA-N 0.000 description 1
- BFNDLDRNJFLIKE-ROLXFIACSA-N (2s)-2,6-diamino-6-hydroxyhexanoic acid Chemical compound NC(O)CCC[C@H](N)C(O)=O BFNDLDRNJFLIKE-ROLXFIACSA-N 0.000 description 1
- BVAUMRCGVHUWOZ-ZETCQYMHSA-N (2s)-2-(cyclohexylazaniumyl)propanoate Chemical compound OC(=O)[C@H](C)NC1CCCCC1 BVAUMRCGVHUWOZ-ZETCQYMHSA-N 0.000 description 1
- JBFQOLHAGBKPTP-NZATWWQASA-N (2s)-2-[[(2s)-4-carboxy-2-[[3-carboxy-2-[[(2s)-2,6-diaminohexanoyl]amino]propanoyl]amino]butanoyl]amino]-4-methylpentanoic acid Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)C(CC(O)=O)NC(=O)[C@@H](N)CCCCN JBFQOLHAGBKPTP-NZATWWQASA-N 0.000 description 1
- WAMWSIDTKSNDCU-ZETCQYMHSA-N (2s)-2-azaniumyl-2-cyclohexylacetate Chemical compound OC(=O)[C@@H](N)C1CCCCC1 WAMWSIDTKSNDCU-ZETCQYMHSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- BWKMGYQJPOAASG-UHFFFAOYSA-N 1,2,3,4-tetrahydroisoquinoline-3-carboxylic acid Chemical compound C1=CC=C2CNC(C(=O)O)CC2=C1 BWKMGYQJPOAASG-UHFFFAOYSA-N 0.000 description 1
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 description 1
- 102100024341 10 kDa heat shock protein, mitochondrial Human genes 0.000 description 1
- HLYBTPMYFWWNJN-UHFFFAOYSA-N 2-(2,4-dioxo-1h-pyrimidin-5-yl)-2-hydroxyacetic acid Chemical compound OC(=O)C(O)C1=CNC(=O)NC1=O HLYBTPMYFWWNJN-UHFFFAOYSA-N 0.000 description 1
- MPUVBVXDFRDIPT-UHFFFAOYSA-N 2-Amino-2-norbornanecarboxylic acid Chemical compound C1CC2C(N)(C(O)=O)CC1C2 MPUVBVXDFRDIPT-UHFFFAOYSA-N 0.000 description 1
- SGAKLDIYNFXTCK-UHFFFAOYSA-N 2-[(2,4-dioxo-1h-pyrimidin-5-yl)methylamino]acetic acid Chemical compound OC(=O)CNCC1=CNC(=O)NC1=O SGAKLDIYNFXTCK-UHFFFAOYSA-N 0.000 description 1
- YSAJFXWTVFGPAX-UHFFFAOYSA-N 2-[(2,4-dioxo-1h-pyrimidin-5-yl)oxy]acetic acid Chemical compound OC(=O)COC1=CNC(=O)NC1=O YSAJFXWTVFGPAX-UHFFFAOYSA-N 0.000 description 1
- IVLXQGJVBGMLRR-UHFFFAOYSA-N 2-aminoacetic acid;hydron;chloride Chemical compound Cl.NCC(O)=O IVLXQGJVBGMLRR-UHFFFAOYSA-N 0.000 description 1
- JINGUCXQUOKWKH-UHFFFAOYSA-N 2-aminodecanoic acid Chemical compound CCCCCCCCC(N)C(O)=O JINGUCXQUOKWKH-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- LKKMLIBUAXYLOY-UHFFFAOYSA-N 3-Amino-1-methyl-5H-pyrido[4,3-b]indole Chemical compound N1C2=CC=CC=C2C2=C1C=C(N)N=C2C LKKMLIBUAXYLOY-UHFFFAOYSA-N 0.000 description 1
- KOLPWZCZXAMXKS-UHFFFAOYSA-N 3-methylcytosine Chemical compound CN1C(N)=CC=NC1=O KOLPWZCZXAMXKS-UHFFFAOYSA-N 0.000 description 1
- YXDGRBPZVQPESQ-QMMMGPOBSA-N 4-[(2s)-2-amino-2-carboxyethyl]benzoic acid Chemical compound OC(=O)[C@@H](N)CC1=CC=C(C(O)=O)C=C1 YXDGRBPZVQPESQ-QMMMGPOBSA-N 0.000 description 1
- GJAKJCICANKRFD-UHFFFAOYSA-N 4-acetyl-4-amino-1,3-dihydropyrimidin-2-one Chemical compound CC(=O)C1(N)NC(=O)NC=C1 GJAKJCICANKRFD-UHFFFAOYSA-N 0.000 description 1
- CMUHFUGDYMFHEI-QMMMGPOBSA-N 4-amino-L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N)C=C1 CMUHFUGDYMFHEI-QMMMGPOBSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- GTVVZTAFGPQSPC-UHFFFAOYSA-N 4-nitrophenylalanine Chemical compound OC(=O)C(N)CC1=CC=C([N+]([O-])=O)C=C1 GTVVZTAFGPQSPC-UHFFFAOYSA-N 0.000 description 1
- LQLQRFGHAALLLE-UHFFFAOYSA-N 5-bromouracil Chemical compound BrC1=CNC(=O)NC1=O LQLQRFGHAALLLE-UHFFFAOYSA-N 0.000 description 1
- VKLFQTYNHLDMDP-PNHWDRBUSA-N 5-carboxymethylaminomethyl-2-thiouridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=S)NC(=O)C(CNCC(O)=O)=C1 VKLFQTYNHLDMDP-PNHWDRBUSA-N 0.000 description 1
- ZFTBZKVVGZNMJR-UHFFFAOYSA-N 5-chlorouracil Chemical compound ClC1=CNC(=O)NC1=O ZFTBZKVVGZNMJR-UHFFFAOYSA-N 0.000 description 1
- KSNXJLQDQOIRIP-UHFFFAOYSA-N 5-iodouracil Chemical compound IC1=CNC(=O)NC1=O KSNXJLQDQOIRIP-UHFFFAOYSA-N 0.000 description 1
- ZLAQATDNGLKIEV-UHFFFAOYSA-N 5-methyl-2-sulfanylidene-1h-pyrimidin-4-one Chemical compound CC1=CNC(=S)NC1=O ZLAQATDNGLKIEV-UHFFFAOYSA-N 0.000 description 1
- LRSASMSXMSNRBT-UHFFFAOYSA-N 5-methylcytosine Chemical compound CC1=CNC(=O)N=C1N LRSASMSXMSNRBT-UHFFFAOYSA-N 0.000 description 1
- DCPSTSVLRXOYGS-UHFFFAOYSA-N 6-amino-1h-pyrimidine-2-thione Chemical compound NC1=CC=NC(S)=N1 DCPSTSVLRXOYGS-UHFFFAOYSA-N 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- MSSXOMSJDRHRMC-UHFFFAOYSA-N 9H-purine-2,6-diamine Chemical compound NC1=NC(N)=C2NC=NC2=N1 MSSXOMSJDRHRMC-UHFFFAOYSA-N 0.000 description 1
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 1
- 201000007490 Adenocarcinoma in Situ Diseases 0.000 description 1
- 208000010507 Adenocarcinoma of Lung Diseases 0.000 description 1
- 206010001233 Adenoma benign Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical class [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 201000003076 Angiosarcoma Diseases 0.000 description 1
- 102100034282 Ankyrin repeat domain-containing protein 23 Human genes 0.000 description 1
- 208000007860 Anus Neoplasms Diseases 0.000 description 1
- 101000878595 Arabidopsis thaliana Squalene synthase 1 Proteins 0.000 description 1
- 235000017060 Arachis glabrata Nutrition 0.000 description 1
- 244000105624 Arachis hypogaea Species 0.000 description 1
- 235000010777 Arachis hypogaea Nutrition 0.000 description 1
- 235000018262 Arachis monticola Nutrition 0.000 description 1
- 108010024976 Asparaginase Proteins 0.000 description 1
- 102000015790 Asparaginase Human genes 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 206010004146 Basal cell carcinoma Diseases 0.000 description 1
- 102100023995 Beta-nerve growth factor Human genes 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 241000701822 Bovine papillomavirus Species 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 102100025570 Cancer/testis antigen 1 Human genes 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 208000009458 Carcinoma in Situ Diseases 0.000 description 1
- 241001466804 Carnivora Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108010059013 Chaperonin 10 Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 208000005243 Chondrosarcoma Diseases 0.000 description 1
- 208000006332 Choriocarcinoma Diseases 0.000 description 1
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 241000195493 Cryptophyta Species 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- 208000007033 Dysgerminoma Diseases 0.000 description 1
- 206010058314 Dysplasia Diseases 0.000 description 1
- 208000000471 Dysplastic Nevus Syndrome Diseases 0.000 description 1
- 238000012286 ELISA Assay Methods 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 238000011510 Elispot assay Methods 0.000 description 1
- 206010014733 Endometrial cancer Diseases 0.000 description 1
- 206010014759 Endometrial neoplasm Diseases 0.000 description 1
- 208000005431 Endometrioid Carcinoma Diseases 0.000 description 1
- 101710181478 Envelope glycoprotein GP350 Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- YQYJSBFKSSDGFO-UHFFFAOYSA-N Epihygromycin Natural products OC1C(O)C(C(=O)C)OC1OC(C(=C1)O)=CC=C1C=C(C)C(=O)NC1C(O)C(O)C2OCOC2C1O YQYJSBFKSSDGFO-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 208000006168 Ewing Sarcoma Diseases 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 108050001049 Extracellular proteins Proteins 0.000 description 1
- 241000282324 Felis Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- NIGWMJHCCYYCSF-UHFFFAOYSA-N Fenclonine Chemical compound OC(=O)C(N)CC1=CC=C(Cl)C=C1 NIGWMJHCCYYCSF-UHFFFAOYSA-N 0.000 description 1
- 208000007659 Fibroadenoma Diseases 0.000 description 1
- 108050009401 Fibronectin type III Proteins 0.000 description 1
- 102100037880 GTP-binding protein REM 1 Human genes 0.000 description 1
- 208000022072 Gallbladder Neoplasms Diseases 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 101001070329 Geobacillus stearothermophilus 50S ribosomal protein L18 Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- 206010018404 Glucagonoma Diseases 0.000 description 1
- YWAQATDNEKZFFK-BYPYZUCNSA-N Gly-Gly-Ser Chemical compound NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O YWAQATDNEKZFFK-BYPYZUCNSA-N 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 241000219146 Gossypium Species 0.000 description 1
- 102000016355 Granulocyte-Macrophage Colony-Stimulating Factor Receptors Human genes 0.000 description 1
- 108010092372 Granulocyte-Macrophage Colony-Stimulating Factor Receptors Proteins 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- HSRJKNPTNIJEKV-UHFFFAOYSA-N Guaifenesin Chemical compound COC1=CC=CC=C1OCC(O)CO HSRJKNPTNIJEKV-UHFFFAOYSA-N 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- 108010039343 HLA-DRB1 Chains Proteins 0.000 description 1
- 208000002927 Hamartoma Diseases 0.000 description 1
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 1
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 1
- 208000001258 Hemangiosarcoma Diseases 0.000 description 1
- 206010019851 Hepatotoxicity Diseases 0.000 description 1
- 241000282418 Hominidae Species 0.000 description 1
- 101000780120 Homo sapiens Ankyrin repeat domain-containing protein 23 Proteins 0.000 description 1
- 101000856237 Homo sapiens Cancer/testis antigen 1 Proteins 0.000 description 1
- 101000721661 Homo sapiens Cellular tumor antigen p53 Proteins 0.000 description 1
- 101001027128 Homo sapiens Fibronectin Proteins 0.000 description 1
- 101001095995 Homo sapiens GTP-binding protein REM 1 Proteins 0.000 description 1
- 101001095088 Homo sapiens Melanoma antigen preferentially expressed in tumors Proteins 0.000 description 1
- 101000581981 Homo sapiens Neural cell adhesion molecule 1 Proteins 0.000 description 1
- 101001051709 Homo sapiens Ribosomal protein S6 kinase-related protein Proteins 0.000 description 1
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 229930010555 Inosine Natural products 0.000 description 1
- UGQMRVRMYYASKQ-KQYNXXCUSA-N Inosine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C2=NC=NC(O)=C2N=C1 UGQMRVRMYYASKQ-KQYNXXCUSA-N 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 208000005016 Intestinal Neoplasms Diseases 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-UWTATZPHSA-N L-Alanine Natural products C[C@@H](N)C(O)=O QNAYBMKLOCPYGJ-UWTATZPHSA-N 0.000 description 1
- ZQISRDCJNBUVMM-UHFFFAOYSA-N L-Histidinol Natural products OCC(N)CC1=CN=CN1 ZQISRDCJNBUVMM-UHFFFAOYSA-N 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- ZGUNAGUHMKGQNY-ZETCQYMHSA-N L-alpha-phenylglycine zwitterion Chemical compound OC(=O)[C@@H](N)C1=CC=CC=C1 ZGUNAGUHMKGQNY-ZETCQYMHSA-N 0.000 description 1
- 229930064664 L-arginine Natural products 0.000 description 1
- 235000014852 L-arginine Nutrition 0.000 description 1
- 239000004201 L-cysteine Substances 0.000 description 1
- 235000013878 L-cysteine Nutrition 0.000 description 1
- ZQISRDCJNBUVMM-YFKPBYRVSA-N L-histidinol Chemical compound OC[C@@H](N)CC1=CNC=N1 ZQISRDCJNBUVMM-YFKPBYRVSA-N 0.000 description 1
- JTTHKOPSMAVJFE-VIFPVBQESA-N L-homophenylalanine Chemical compound OC(=O)[C@@H](N)CCC1=CC=CC=C1 JTTHKOPSMAVJFE-VIFPVBQESA-N 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- 239000004395 L-leucine Substances 0.000 description 1
- 235000019454 L-leucine Nutrition 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 1
- 229930182821 L-proline Natural products 0.000 description 1
- 125000000174 L-prolyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])([H])[C@@]1([H])C(*)=O 0.000 description 1
- VHVGNTVUSQUXPS-YUMQZZPRSA-N L-threo-3-phenylserine Chemical compound [O-]C(=O)[C@@H]([NH3+])[C@@H](O)C1=CC=CC=C1 VHVGNTVUSQUXPS-YUMQZZPRSA-N 0.000 description 1
- 125000000510 L-tryptophano group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[C@@]([H])(C(O[H])=O)N([H])[*])C2=C1[H] 0.000 description 1
- 229940127171 LMB-2 Drugs 0.000 description 1
- 208000018142 Leiomyosarcoma Diseases 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 201000004462 Leydig Cell Tumor Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 239000012515 MabSelect SuRe Substances 0.000 description 1
- 241000282553 Macaca Species 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 208000006644 Malignant Fibrous Histiocytoma Diseases 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 102100037020 Melanoma antigen preferentially expressed in tumors Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 108010008707 Mucin-1 Proteins 0.000 description 1
- 102000015728 Mucins Human genes 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 101000966481 Mus musculus Dihydrofolate reductase Proteins 0.000 description 1
- 101000576803 Mus musculus Mesothelin Proteins 0.000 description 1
- HYVABZIGRDEKCD-UHFFFAOYSA-N N(6)-dimethylallyladenine Chemical compound CC(C)=CCNC1=NC=NC2=C1N=CN2 HYVABZIGRDEKCD-UHFFFAOYSA-N 0.000 description 1
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 description 1
- 206010028729 Nasal cavity cancer Diseases 0.000 description 1
- 208000001894 Nasopharyngeal Neoplasms Diseases 0.000 description 1
- 206010061306 Nasopharyngeal cancer Diseases 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 102100027347 Neural cell adhesion molecule 1 Human genes 0.000 description 1
- 201000004404 Neurofibroma Diseases 0.000 description 1
- 208000007256 Nevus Diseases 0.000 description 1
- 208000010505 Nose Neoplasms Diseases 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 201000010133 Oligodendroglioma Diseases 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 239000008118 PEG 6000 Substances 0.000 description 1
- 108060006580 PRAME Proteins 0.000 description 1
- 102000036673 PRAME Human genes 0.000 description 1
- 239000005662 Paraffin oil Substances 0.000 description 1
- 108010067902 Peptide Library Proteins 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 208000009565 Pharyngeal Neoplasms Diseases 0.000 description 1
- 229920002584 Polyethylene Glycol 6000 Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- WDVSHHCDHLJJJR-UHFFFAOYSA-N Proflavine Chemical compound C1=CC(N)=CC2=NC3=CC(N)=CC=C3C=C21 WDVSHHCDHLJJJR-UHFFFAOYSA-N 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 201000000582 Retinoblastoma Diseases 0.000 description 1
- 208000005678 Rhabdomyoma Diseases 0.000 description 1
- 102100024914 Ribosomal protein S6 kinase-related protein Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000239226 Scorpiones Species 0.000 description 1
- 201000010208 Seminoma Diseases 0.000 description 1
- 208000000097 Sertoli-Leydig cell tumor Diseases 0.000 description 1
- 244000000231 Sesamum indicum Species 0.000 description 1
- 235000003434 Sesamum indicum Nutrition 0.000 description 1
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 208000032383 Soft tissue cancer Diseases 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 101000582398 Staphylococcus aureus Replication initiation protein Proteins 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 241001493546 Suina Species 0.000 description 1
- ULUAUXLGCMPNKK-UHFFFAOYSA-N Sulfobutanedioic acid Chemical class OC(=O)CC(C(O)=O)S(O)(=O)=O ULUAUXLGCMPNKK-UHFFFAOYSA-N 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 1
- 108010017842 Telomerase Proteins 0.000 description 1
- 108020005038 Terminator Codon Proteins 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 1
- 102100036407 Thioredoxin Human genes 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 108010022394 Threonine synthase Proteins 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 208000015778 Undifferentiated pleomorphic sarcoma Diseases 0.000 description 1
- 208000023915 Ureteral Neoplasms Diseases 0.000 description 1
- 206010046392 Ureteric cancer Diseases 0.000 description 1
- 206010046799 Uterine leiomyosarcoma Diseases 0.000 description 1
- 208000009311 VIPoma Diseases 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 206010047741 Vulval cancer Diseases 0.000 description 1
- 208000004354 Vulvar Neoplasms Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 208000002718 adenomatoid tumor Diseases 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 208000024447 adrenal gland neoplasm Diseases 0.000 description 1
- 230000009824 affinity maturation Effects 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- JINBYESILADKFW-UHFFFAOYSA-N aminomalonic acid Chemical compound OC(=O)C(N)C(O)=O JINBYESILADKFW-UHFFFAOYSA-N 0.000 description 1
- 238000012870 ammonium sulfate precipitation Methods 0.000 description 1
- 210000002255 anal canal Anatomy 0.000 description 1
- 201000007696 anal canal cancer Diseases 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 201000011165 anus cancer Diseases 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960003272 asparaginase Drugs 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 1
- 238000002820 assay format Methods 0.000 description 1
- 238000011888 autopsy Methods 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- 230000003385 bacteriostatic effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 201000003149 breast fibroadenoma Diseases 0.000 description 1
- 201000002143 bronchus adenoma Diseases 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 229960002092 busulfan Drugs 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 238000004422 calculation algorithm Methods 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 238000013368 capillary electrophoresis sodium dodecyl sulfate analysis Methods 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 208000025188 carcinoma of pharynx Diseases 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000002771 cell marker Substances 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 208000019065 cervical carcinoma Diseases 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 208000009060 clear cell adenocarcinoma Diseases 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 230000006957 competitive inhibition Effects 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 108050003126 conotoxin Proteins 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 230000037029 cross reaction Effects 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 102000004419 dihydrofolate reductase Human genes 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 210000000959 ear middle Anatomy 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 208000028730 endometrioid adenocarcinoma Diseases 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 238000003114 enzyme-linked immunosorbent spot assay Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 238000002270 exclusion chromatography Methods 0.000 description 1
- 208000024519 eye neoplasm Diseases 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 210000000232 gallbladder Anatomy 0.000 description 1
- 201000007487 gallbladder carcinoma Diseases 0.000 description 1
- 102000013069 gamma-Crystallins Human genes 0.000 description 1
- 108010079934 gamma-Crystallins Proteins 0.000 description 1
- 208000010749 gastric carcinoma Diseases 0.000 description 1
- 208000015419 gastrin-producing neuroendocrine tumor Diseases 0.000 description 1
- 201000000052 gastrinoma Diseases 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- 230000012447 hatching Effects 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- 231100000304 hepatotoxicity Toxicity 0.000 description 1
- 230000007686 hepatotoxicity Effects 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 229940127121 immunoconjugate Drugs 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 238000001114 immunoprecipitation Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 201000004933 in situ carcinoma Diseases 0.000 description 1
- QNRXNRGSOJZINA-UHFFFAOYSA-N indoline-2-carboxylic acid Chemical compound C1=CC=C2NC(C(=O)O)CC2=C1 QNRXNRGSOJZINA-UHFFFAOYSA-N 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229960003786 inosine Drugs 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 206010022498 insulinoma Diseases 0.000 description 1
- 201000002313 intestinal cancer Diseases 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 208000014899 intrahepatic bile duct cancer Diseases 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 229940065638 intron a Drugs 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 208000022013 kidney Wilms tumor Diseases 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 210000000867 larynx Anatomy 0.000 description 1
- 201000010260 leiomyoma Diseases 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 230000021633 leukocyte mediated immunity Effects 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 206010024627 liposarcoma Diseases 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 230000006674 lysosomal degradation Effects 0.000 description 1
- 108010089256 lysyl-aspartyl-glutamyl-leucine Proteins 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 235000001055 magnesium Nutrition 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 229940091250 magnesium supplement Drugs 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 201000000289 malignant teratoma Diseases 0.000 description 1
- 208000026037 malignant tumor of neck Diseases 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 210000003071 memory t lymphocyte Anatomy 0.000 description 1
- 210000000713 mesentery Anatomy 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 238000012737 microarray-based gene expression Methods 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 201000003956 middle ear cancer Diseases 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 230000003020 moisturizing effect Effects 0.000 description 1
- LPUQAYUQRXPFSQ-DFWYDOINSA-M monosodium L-glutamate Chemical compound [Na+].[O-]C(=O)[C@@H](N)CCC(O)=O LPUQAYUQRXPFSQ-DFWYDOINSA-M 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- 229950000720 moxetumomab pasudotox Drugs 0.000 description 1
- 208000010492 mucinous cystadenocarcinoma Diseases 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 108091005763 multidomain proteins Proteins 0.000 description 1
- 238000012243 multiplex automated genomic engineering Methods 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 208000009091 myxoma Diseases 0.000 description 1
- 210000004296 naive t lymphocyte Anatomy 0.000 description 1
- 210000003928 nasal cavity Anatomy 0.000 description 1
- 201000007425 nasal cavity carcinoma Diseases 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000017066 negative regulation of growth Effects 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 208000025440 neoplasm of neck Diseases 0.000 description 1
- 201000008026 nephroblastoma Diseases 0.000 description 1
- 229940053128 nerve growth factor Drugs 0.000 description 1
- 208000007538 neurilemmoma Diseases 0.000 description 1
- 208000004649 neutrophil actin dysfunction Diseases 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 238000011580 nude mouse model Methods 0.000 description 1
- ZBNJXSZNWZUYCI-UHFFFAOYSA-N octadecyl 2-(trimethylazaniumyl)ethyl phosphate Chemical compound CCCCCCCCCCCCCCCCCCOP([O-])(=O)OCC[N+](C)(C)C ZBNJXSZNWZUYCI-UHFFFAOYSA-N 0.000 description 1
- 201000008106 ocular cancer Diseases 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 210000002747 omentum Anatomy 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 235000015205 orange juice Nutrition 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 125000006353 oxyethylene group Chemical group 0.000 description 1
- 208000021255 pancreatic insulinoma Diseases 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000013610 patient sample Substances 0.000 description 1
- 235000020232 peanut Nutrition 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 201000002628 peritoneum cancer Diseases 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 229960005190 phenylalanine Drugs 0.000 description 1
- 150000004713 phosphodiesters Chemical class 0.000 description 1
- 150000008298 phosphoramidates Chemical class 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 210000004180 plasmocyte Anatomy 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 210000004224 pleura Anatomy 0.000 description 1
- 201000003437 pleural cancer Diseases 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229940068918 polyethylene glycol 400 Drugs 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- ZNNZYHKDIALBAK-UHFFFAOYSA-M potassium thiocyanate Chemical compound [K+].[S-]C#N ZNNZYHKDIALBAK-UHFFFAOYSA-M 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 229960002429 proline Drugs 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 108020001580 protein domains Proteins 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-N pyridine Substances C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- 102000016914 ras Proteins Human genes 0.000 description 1
- 108010014186 ras Proteins Proteins 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 208000029922 reticulum cell sarcoma Diseases 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 229920002477 rna polymer Polymers 0.000 description 1
- 238000003118 sandwich ELISA Methods 0.000 description 1
- 239000002795 scorpion venom Substances 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 208000004548 serous cystadenocarcinoma Diseases 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 231100000161 signs of toxicity Toxicity 0.000 description 1
- 201000000849 skin cancer Diseases 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- RNVYQYLELCKWAN-UHFFFAOYSA-N solketal Chemical compound CC1(C)OCC(CO)O1 RNVYQYLELCKWAN-UHFFFAOYSA-N 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000010473 stable expression Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 201000000498 stomach carcinoma Diseases 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 206010042863 synovial sarcoma Diseases 0.000 description 1
- 239000007916 tablet composition Substances 0.000 description 1
- 208000001608 teratocarcinoma Diseases 0.000 description 1
- NPDBDJFLKKQMCM-UHFFFAOYSA-N tert-butylglycine Chemical compound CC(C)(C)C(N)C(O)=O NPDBDJFLKKQMCM-UHFFFAOYSA-N 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- 108060008226 thioredoxin Proteins 0.000 description 1
- 229940094937 thioredoxin Drugs 0.000 description 1
- 229960002898 threonine Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- BJBUEDPLEOHJGE-IMJSIDKUSA-N trans-3-hydroxy-L-proline Chemical compound O[C@H]1CC[NH2+][C@@H]1C([O-])=O BJBUEDPLEOHJGE-IMJSIDKUSA-N 0.000 description 1
- PMMYEEVYMWASQN-IMJSIDKUSA-N trans-4-Hydroxy-L-proline Natural products O[C@@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-IMJSIDKUSA-N 0.000 description 1
- 230000005026 transcription initiation Effects 0.000 description 1
- 239000012096 transfection reagent Substances 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 230000010474 transient expression Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 206010044412 transitional cell carcinoma Diseases 0.000 description 1
- 230000014621 translational initiation Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 101150079396 trpC2 gene Proteins 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 201000005102 vulva cancer Diseases 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 229940075420 xanthine Drugs 0.000 description 1
- 238000012447 xenograft mouse model Methods 0.000 description 1
- XOOUIPVCVHRTMJ-UHFFFAOYSA-L zinc stearate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O XOOUIPVCVHRTMJ-UHFFFAOYSA-L 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6817—Toxins
- A61K47/6829—Bacterial toxins, e.g. diphteria toxins or Pseudomonas exotoxin A
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6859—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from liver or pancreas cancer cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6871—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting an enzyme
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/21—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Pseudomonadaceae (F)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1203—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria from Gram-negative bacteria
- C07K16/1214—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from bacteria from Gram-negative bacteria from Pseudomonadaceae (F)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/303—Liver or Pancreas
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/624—Disulfide-stabilized antibody (dsFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/33—Fusion polypeptide fusions for targeting to specific cell types, e.g. tissue specific targeting, targeting of a bacterial subspecies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/50—Fusion polypeptide containing protease site
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/55—Fusion polypeptide containing a fusion with a toxin, e.g. diphteria toxin
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Oncology (AREA)
- Mycology (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Изобретение относится к биотехнологии, конкретно к получению модифицированных экзотоксинов Pseudomonas, и может быть использовано в медицине для противоопухолевой терапии. Получен экзотоксин A Pseudomonas (РЕ), в котором аминокислотный остаток R456 замещен на аланин, один или в сочетании с F443, замещенным на аланин, L477, замещенным на гистидин, R494, замещенным на аланин, и/или L552, замещенным на глутаминовую кислоту или аспарагин. На основе модифицированного РЕ получены химерные молекулы, содержащие нацеливающий на раковую клетку-мишень агент, слитый с РЕ или конъюгированный с РЕ. Изобретение обеспечивает получение экзотоксина A Pseudomonas с уменьшенной иммуногенностью при сохранении цитотоксичности. 17 н. и 25 з.п. ф-лы, 27 ил., 31 табл., 28 пр.
Description
Перекрестная ссылка на родственные заявки
[0001] Эта заявка на патент испрашивает приоритет предварительных заявок США на патенты №№61/887418, поданной 6 октября 2013 г.; 61/908464, поданной 25 ноября 2013 г.; 61/982051, поданной 21 апреля 2014 г.; и 62/052665, поданной 19 сентября 2014 г., каждая из которых включена в данный документ посредством ссылки во всей ее полноте.
Настоящее изобретение было создано при поддержке Правительства с № проекта ВС008753 Национальным институтом здоровья, Национальным институтом онкологии. Правительство имеет определенные права на изобретение.
Включение посредством ссылки материала, представленного в электронном виде
[0002] В данный документ включен посредством ссылки во всей его полноте список машинно-читаемых нуклеотидных/аминокислотных последовательностей, представленный одновременно с данной заявкой и определенный следующим образом: один файл ASCII (текст) объемом 144505 байт под названием "718581_ST25.txt" от 1 октября 2014 года.
Уровень техники
[0003] Экзотоксин А псевдомонад (от англ. Pseudomonas exotoxin - РЕ) является бактериальным токсином с цитотоксической активностью, которая может эффективно разрушать или ингибировать рост нежелательных клеток, например, раковых клеток. Соответственно, РЕ может быть использован для лечения или профилактики заболеваний, таких как, например, рак. Тем не менее, РЕ может быть высоко иммуногенным. Соответственно, введение РЕ может стимулировать иммунный ответ против РЕ, в том числе, например, продукцию анти-РЕ-антител и/или Т-клеток, что нежелательно нейтрализует цитотоксическую активность РЕ. Такая иммуногенность может уменьшить количество РЕ, который может быть введен пациенту, что, в свою очередь, может снижать эффективность РЕ в лечении заболевания, например, рака. Таким образом, существует потребность в улучшенном РЕ.
[0004] В данной области известно несколько деиммунизированных экзотоксинов псевдомонад (РЕ). Варианты с делецией домена II (например, РЕ24) могут быть менее иммуногенными и могут вызывать меньше побочных эффектов (таких как, например, синдром капиллярной утечки и гепатотоксичность) по сравнению с РЕ38, который содержит домен II. Не привязываясь к определенной теории, полагают, что снижение иммуногенности и меньшее число побочных эффектов РЕ24 может быть объяснено, по меньшей мере частично, уменьшенным размером РЕ24, что неблагоприятно приводит к снижению периода его полужизни в сыворотке. В вариантах РЕ24 могут быть использованы различные фурин-расщепляемые линкеры. РЕ-иммуноконъюгаты в основном используют dsFv-фрагменты в качестве как специфических группировок. Такие деиммунизированные экзотоксины псевдомонад (РЕ) описаны, например, в публикациях международных патентных заявок WO 2005052006, WO 2007016150, WO 2007014743, WO 2007031741, WO 200932954, WO 201132022, WO 2012/154530 и WO 2012/170617.
[0005] Предыдущие иммунотоксины имеют много недостатков. Например, деиммунизация предыдущих иммунотоксинов была неполной в отношении В-клеточных эпитопов человека, так как иммуногенные реакции до сих пор происходят. Кроме того, деиммунизация предыдущих иммунотоксинов сопровождалась снижением цитотоксической активности. Например, деиммунизированный вариант PE LO10, описанный в публикации WO 2012/170617, имеет потерю активности по меньшей мере на 40% по сравнению с РЕ дикого типа (wild type, WT) и другими вариантами РЕ. В публикации международной патентной заявки WO 2013/040141 были описаны экзотоксины псевдомонад с менее иммуногенными В-клеточными эпитопами. В варианте PE LRO10 все В-клеточные эпитопы были удалены. Тем не менее, это также привело к уменьшению цитотоксичности по отношению к опухолевым клеткам.
[0006] Кроме того, гибрид dsFv с домен II-делетированными вариантами РЕ (РЕ24) имеет более короткий период полужизни в сыворотке из-за снижения его общего размера по сравнению с гибридами dsFv с РЕ38. Линкеры предыдущих иммунотоксинов также содержали Т-клеточные эпитопы и слабую перспективность, например, плохую стабильность при 37°C. Кроме того, предыдущие иммунотоксины против мезотелина (MSLN) использовали только dsFv-фрагменты мышиного происхождения, слитые с РЕ, что может дополнительно способствовать иммуногенности. Международная патентная заявка WO 2012/154530 относится к вариантным химерным молекулам экзотоксина псевдомонад с короткими гибкими линкерами, которые имеют улучшенную цитотоксичность в отношении опухолевых клеток.
Краткое изложение сущности изобретения
[0007] Данное изобретение относится к деиммунизированным экзотоксинам псевдомонад и их Fab-гибридам (например, гуманизированным анти-MSLN), к способам лечения рака, стабилизированным фармацевтическим составам, способам уменьшения побочных эффектов и способам повышения периода полужизни в сыворотке и оптимизации схемы лечения.
[0008] Одно из воплощений согласно изобретению относится к экзотоксину А псевдомонад (РЕ), содержащему аминокислотную последовательность РЕ, где один или более чем один из аминокислотных остатков F443, R456, L477, R494 и L552, определенных относительно SEQ ID NO 1, является замещенным независимо от других, где РЕ, возможно, имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе, и эта дополнительная аминокислотная замена в одном или более чем одном В-клеточном эпитопе представляет собой, независимо от других, замену одного или более чем одного аминокислотного остатка D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, Q592 и L597, определенного относительно SEQ ID NO 1,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном эпитопе,
(iii) делецию одного или более чем одного из смежных аминокислотных остатков среди остатков 1-273 и 285-394, определенных согласно SEQ ID NO 1, или
(iv) сочетание любого одного, двух или трех пунктов из (i)-(iii).
[0009] Еще одно воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен РЕ III
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS (от англ. furin cleavage sequence) представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более чем один из смежных остатков с 365 по 394 последовательности SEQ ID 1; а также,
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где один или более чем один из аминокислотных остатков F443, R456, L477, R494 и L552, определенных относительно SEQ ID NO 1, независимо от других является замещенным, где РЕ, возможно, имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе, и эта дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой, независимо от других, замену одного или более чем одного аминокислотного остатка D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, Q592 и L597, определенного относительно SEQ ID NO 1,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном эпитопе, или
(iii) вместе (i) и (ii)
[0010] Другое воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен РЕ III
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также,
Функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где РЕ включает аргинин в позиции 458, определенной относительно SEQ ID NO 1, и
где РЕ имеет:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538.
[0011] Дополнительные воплощения данного изобретения относятся к родственным химерным молекулам, а также родственным нуклеиновым кислотам, рекомбинантным экспрессионным векторам, клеткам-хозяевам, популяциям клеток и фармацевтическим композициям.
[0012] Еще одно воплощение данного изобретения относится к способу лечения или профилактики рака у млекопитающего, включающему введение млекопитающему РЕ, химерной молекулы, нуклеиновой кислоты, рекомбинантного экспрессионного вектора, клетки-хозяина, популяции клеток или фармацевтической композиции согласно изобретению в количестве, эффективном для лечения или профилактики рака у млекопитающего.
[0013] Еще одно воплощение данного изобретения относится к способу ингибирования роста клетки-мишени, включающему контактирование клетки с РЕ, химерной молекулой, нуклеиновой кислотой, рекомбинантным экспрессионным вектором, клеткой-хозяином, популяцией клеток или фармацевтической композицией согласно изобретению в количестве, эффективном для ингибирования роста клетки-мишени.
[0014] Дополнительные воплощения согласно данному изобретению относятся к способам получения РЕ согласно изобретению и способам получения химерной молекулы согласно изобретению.
Краткое описание графических материалов
[0015] На фиг. 1А и 1В представлены тепловые карты Т-клеточных эпитопов, показывающие наиболее сильные (более20%, черные квадраты), средней силы (от 10 до 20%, темно-серые квадраты), слабые (от 3% до 10%, светло-серые квадраты) и отрицательные (отсутствие реакции; менее 3%, белые квадраты) ответы наивных доноров (n равно 50) (А) и ранее лечившихся пациентов (n равно 16) (В). Ответы представлены в процентах реагирующих пятен для каждого донора. Ответы были сгруппированы путем автоматической сортировки на основе способности реагировать на пулы.
[0016] На фиг. 2A-2D изображены графики, показывающие реакцию трех донорских образцов (А-С) и одного образца от пациента с HCL (D) (от англ. Hairy Cell Leukaemia - волосатоклеточный лейкоз) на один из 22 пептидных пулов, контрольный пул (CEFT) или на отсутствие пептида после стимуляции НА22 (заштрихованные столбцы) или LR-R494A (незаштрихованные столбцы), измеренную в образующих пятна клетках (spot-forming cell, SFC) на 10×106 клеток. * указывает на статистическую значимость между НА22 и LR-R494A (рменее0,01).
[0017] На фиг. 3А-3С представлены графики, показывающие реакцию двух донорских образцов (А-В) и одного образца от пациента с HCL (С) на один из 22 пептидных пулов, CEFT или на отсутствие пептида после стимуляции НА22 (заштрихованные столбцы) или LR-R505A (незаштрихованные столбцы), измеренную в SFC на 10×106 клеток. * указывает на статистическую значимость (p менее0,01).
[0018] На фиг. 4А-4В представлены графики, показывающие реакцию двух донорских образцов (А-В) на один из 22 пептидных пулов, CEFT или на отсутствие пептида после стимуляции НА22 (заштрихованные столбцы) или LR-R551A (незаштрихованные столбцы), измеренную в SFC на 10×106 клеток. * указывает на статистическую значимость в t-тесте Стьюдента (рменее0,01).
[0019] На фиг. 5A-5D представлены графики, показывающие реакцию двух донорских образцов (C-D) и двух образцов от пациентов с мезотелиомой (А-В) после стимуляции рекомбинантным иммунотоксином (RIT) и повторной стимуляции пептидом 93 или 94 с аминокислотной последовательностью дикого типа (WT) (черные столбцы), L552N (темно-серые столбцы) или L552E (незаштрихованные столбцы) или обработки без пептидов (светло-серые столбцы). * указывает на статистическую значимость в t-тесте Стьюдента (рменее0,05).
[0020] На фиг. 6А-6С представлены графики, показывающие реакцию трех донорских образцов на 22 пептидных пула после стимуляции либо HA22-LR (WT) (заштрихованные столбцы), либо LR-R427A (незаштрихованные столбцы) и повторной стимуляции соответствующими пептидами, измеренную в SFC на 10×106 клеток. * указывает на статистическую значимость (рменее0,05).
[0021] На фиг. 7А-7С представлены графики, показывающие реакцию двух образцов от пациентов (А-В) и одного донорского (С) на один из пулов с 8 по 22 после стимуляции либо HA22-LR (WT) (заштрихованные столбцы), либо LR-F443A (незаштрихованные столбцы) и повторной стимуляции соответствующими пептидами, измеренную в SFC на 10×106 клеток. * указывает на статистическую значимость (рменее0,01).
[0022] На фиг. 8 представлен график, показывающий кратное изменение ЕС50 при HA22-LR-GGS (круги), НА22 (вертикальная штриховка) или HA22-LR-T18 (треугольники) при различных температурах.
[0023] На фиг. 9A-9D представлены графики, показывающие реакцию четырех донорских образцов после стимуляции RIT и повторной стимуляции в отсутствие пептида, пептида WT 67 или пептида 67 с валином или аланином в позиции 471, измеренную в SFC на 10×106 клеток.
[0024] На фиг. 10А-10Е представлены графики, показывающие реакцию трех донорских образцов (А-С), образца от пациента с HCL (D) и образца от пациента с мезотелиомой (Е) после стимуляции пептидом 67 или 68, который содержит мутацию аланина (белые столбцы) или мутацию гистидина (серые столбцы) в позиции 477, или без мутации (WT) (черные столбцы).
[0025] На фиг. 11А и 11В представлены графики, демонстрирующие реакцию образцов от пациента с мезотелиомой (А) и пациента с волосатоклеточной лейкемией (hairy cell leukemia, HCL) (В) после стимуляции RIT и повторной стимуляции в отсутствие пептида, с пептидом 93, 94 или 95 либо с аминокислотной последовательностью WT (заштрихованные столбцы), либо с L556V (незаштрихованные столбцы).
[0026] На фиг. 12 представлен график, показывающий агрегацию (% площади) HMW cFP-0170 (Fab-LO10R-456A-короткий линкер, столбцы, заштрихованные по диагонали) или HMW cFP-0171 (Fab-LO10R-456А-удлиненный линкер; столбцы, заштрихованные горизонтально), измеренную путем эксклюзионной хроматографии (size exclusion chromatograph, SEC), после инкубации при 33°С.
[0027] На фиг. 13 представлен график, показывающий агрегацию (% площади) HMW cFP-0170 (Fab-LO10R-456A-короткий линкер, ромбы) или HMW cFP-0171 (Fab-LO10R-456А-удлиненный линкер; квадраты), измеренную путем эксклюзионной хроматографии (SEC), после инкубации при 33°С.
[0028] На фиг. 14 представлен график, показывающий агрегацию (радиус в нм) cFP-0166 (Fab-LO10R-короткий линкер, ромбы) или cFP-0174 (Fab-LO10R-удиненный линкер; круги), измеренную с помощью динамического рассеяния света (dynamic light scattering, DLS) при различных температурах в диапазоне от 25°С до 50°С.
[0029] На фиг. 15 представлен график, показывающий агрегацию (радиус в нм) cFP-0170 (Fab-LO10R-короткий линкер, ромбы) или cFP-0171 (Fab-LO10R-456A-удлиненный линкер; круги), измеренную с помощью DLS при различных температурах в диапазоне от 25°С до 50°С.
[0030] На фиг. 16 представлен график, показывающий агрегацию (радиус в нм) cFP-0172 (Fab-LO10R-456A-551A-короткий линкер, ромбы) или cFP-0173 (Fab-LO10R-456A-551A-удиненный линкер; круги), измеренную с помощью DLS при различных температурах в диапазоне от 25°С до 50°С.
[0031] На фиг. 17 представлен график, показывающий реакцию сывороток пациентов клона 9НЗ на (107) или (108) фагов/лунку или (107) или (108) фагов/лунку с предварительной инкубацией с антигеном, где сыворотки инкубировали с huSS1Fab-PE24LRO10 (с мутацией 458А) (заштрихованные диагональю влево столбцы), huSS1Fab-PE24LRO10R (с обратной мутацией 458R) (заштрихованные горизонтально столбцы) или huSS1Fab-PE24LRO10R-456A (с обратной мутацией 458R и мутацией 456А) (заштрихованные диагональю вправо столбцы), измеренную по оптической плотности при 450 нм.
[0032] На фиг. 18А и 18В представлены графики, показывающие антигенность химерных молекул SS1P (Т1), SS1-dsFv-LR-LO10R (Т2), SS1-dsFv-LR-LO10R456A (Т3), SS1-FABLO10R (Roche 116, Т4), SS1-FABLO10R456A-длинный линкер (Roche 171, Т5) и SS1-FABLO10R-длинный линкер (Roche 174, Т6) в отношении 20 сывороток от пациентов. Показано два репрезентативных примера (А и В). Ось Y представляет относительную IC50 (%).
[0033] На фиг. 19 представлен график, показывающий плазменную концентрацию (нг/мл) химерных молекул SS1P38 (0,4 мг/кг (ромбы)), SS1P38 (0,2 мг/кг (квадраты)), Fab-PE24 (0,231 мг/кг (треугольники)), (dsFv-PE24 (0,16 мг/кг (х)), вводимых мышам в течение определенного периода времени (в часах (ч)).
[0034] На фиг. 20 представлен график, показывающий период полужизни в сыворотке cFP (нг/мл) в дозе 0,3 мг/кг cFP_0205 (квадраты), 0,3 мг/кг SS1P (круги) или 0,3 мг/кг cFP_0205 (пунктирные линии) в течение определенного времени (часы) у яванских макак.
[0035] На фиг. 21 представлен график, показывающий изменение массы тела мышей, получавших контроль (носитель; круги); cFP 0205 3 мг/кг в/в 3q7d (квадраты на сплошной линии); cFP 0205 2 мг/кг в/в 3q7d (квадраты на линии с широким пунктиром); cFP 0205 1 мг/кг в/в 3q7d (квадраты на линии с коротким пунктиром); cFP0205 0,5 мг/кг в/в 3q7d (квадраты на линии с точечным пунктиром) с течением времени (дни после инокуляции клеток).
[0036] На фиг. 22A-F представлены флуоресцентные изображения срезов легких (А-В), селезенки (C-D) или печени (E-F) мышей, получавших меченый cFP0205, в 10× (А, С, Е) или 40× (В, D, F) увеличении.
[0037] На фиг. 22G-L представлены флуоресцентные изображения срезов легких (G-H), селезенки (I-J) или печени (K-L) мышей, получавших меченый SS1P, в 10× (G, I, K) или 40× (Н, J, L) увеличении.
[0038] На фиг. 23 представлен график, показывающий размер опухоли у мышей, не подвергавшихся лечению (незаштрихованные ромбы) или получавших только паклитаксел (серые ромбы), только RG7787 (также называемый R205 или cFP 0205) (черные ромбы) или комбинацию RG7787 и паклитаксела (черно-белые ромбы) с течением времени, измеряемого в днях.
[0039] На фиг. 24 представлен график, показывающий размер опухоли у мышей, не подвергавшихся лечению (носитель) (круги) или получавших RG7787 (квадраты), с течением времени, измеряемого в днях. Каждая точка данных представляет собой среднее значение среднего объема опухоли для n равному 9 животных, получавших RG7787, и n равному 8 контрольных животных. Столбцы погрешности показывают стандартные отклонения.
[0040] На фиг. 25 представлен график, показывающий размер опухоли у мышей, получавших носитель (контроль) (круги), только RG7787 (квадраты), только паклитаксель (треугольники), либо комбинацию RG7787 и паклитаксела (ромбы), с течением времени, измеряемого в днях. Столбцы погрешности показывают стандартные отклонения.
[0041] На фиг. 26 представлен график, показывающий размер опухоли у мышей, не получавших лечение (untreated, UT) (x), или мышей, получавших только R205 (ромбы), комбинацию R205 и таксола (квадраты), либо только таксол (треугольники) с течением времени, измеряемого в днях.
[0042] На фиг. 27А представлен график, показывающий жизнеспособность (%) CD22-экспрессирующих клеточных линий, обработанных различными концентрациями Т18 или MP RIT (нг/мл).
[0043] На фиг. 27В представлен график, показывающий относительную цитотоксическую активность (%) Т18 или MP RIT, которые нагревали до одной из различных температур (°C).
[0044] На фиг. 27C-D представлены графики, показывающие цитотоксическую активность (IC50 (нг/мл)) для MP или Т18 RIT на клетках пациентов с волосатоклеточной лейкемией (HCL) (С) или хронической лимфоцитарной лейкемией (chronic lymphocytic leukemia, CLL) (D).
[0045] На фиг. 27E представлен график, показывающий влияние LMB-T18 на размер опухоли в мышиной модели с ксенотрансплантатом после четырех инъекций 5 мг/кг (квадраты) LMB-T18, трех инъекций 7,5 мг/кг (треугольники) LMB-T18 или 0,2% человеческого сывороточного альбумина в PBS (круги). Стрелки обозначают дни инъекции для всех групп. Прерывистая стрелка указывает на группу с дополнительной инъекцией 5 мг/мл. (*) Рболее0,01 в одностороннем анализе ANOVA. Столбцы погрешности показывают SD.
[0046] На фиг. 27F представлен график, показывающий % связывания MP, HA22-LR и LMB-T18 с сывороткой пациентов с нейтрализующими антителами к MP.
Подробное описание изобретения
[0047] Экзотоксин А псевдомонад ("РЕ") представляет собой бактериальный токсин (с молекулярной массой 66 кДа), секретируемый синегнойной палочкой Pseudomonas aeruginosa. Нативная последовательность РЕ дикого типа (SEQ ID NO 1) приведена в патенте США 5602095, который включен в данный документ посредством ссылки. Нативный РЕ дикого типа включает три структурных домена, которые способствуют цитотоксичности. Домен Ia (аминокислоты с 1 по 252) опосредует клеточное связывание, домен II (аминокислоты с 253 по 364) опосредует транслокацию в цитозоль, а домен III (аминокислоты с 400 по 613) опосредует АДФ-рибозилирование фактора элонгации 2. Хотя считается, что структурная граница домена III РЕ начинается с остатка 400, предполагается, что домену III может потребоваться сегмент домена Ib для сохранения АДФ-рибозилирующей активности. Соответственно, функциональный домен III определяется как остатки РЕ с 395 по 613. Функция домена Ib (аминокислоты с 365 по 399) остается неопределенной. Не связываясь с конкретной теорией или механизмом, полагают, что цитотоксическая активность РЕ происходит через ингибирование синтеза белка в эукариотических клетках, например, путем инактивации АДФ-рибозилирования фактора элонгации 2 (elongation factor 2, EF-2).
[0048] Замены в РЕ определяются в данном документе относительно аминокислотной последовательности РЕ. Таким образом, замены в РЕ описаны в данном документе относительно аминокислотного остатка, присутствующего в определенной позиции, с идущей далее аминокислотой, на которую был заменен остаток в конкретной обсуждаемой замене. В связи с этим позиции в аминокислотной последовательности в конкретном воплощении РЕ упоминаются в данном документе как позиции в аминокислотной последовательности согласно конкретному воплощению или как позиции, определенные относительно SEQ ID NO 1. Когда позиции являются такими, как определено в SEQ ID NO 1, фактические позиции аминокислотной последовательности согласно конкретному воплощению РЕ определяются относительно соответствующих позиций в SEQ ID NO 1 и могут представлять номера позиций остатков, отличающиеся от номеров позиций остатков в SEQ ID NO 1. Так, например, замены относятся к замене аминокислотного остатка в аминокислотной последовательности согласно конкретному воплощению РЕ, соответствующего указанной позиции в 613-аминокислотной последовательности SEQ ID NO 1, с пониманием того, что фактические позиция в соответствующих аминокислотных последовательностях могут отличаться. Например, когда позиции определены согласно SEQ ID NO 1, термин "R490" относится к аргинину, обычно присутствующему в позиции 490 SEQ ID NO 1, "R490A" указывает на то, что аргинин, обычно присутствующий в позиции 490 SEQ ID NO 1, заменен аланином, в то время как "K590Q" указывает на то, что лизин, обычно присутствующий в позиции 590 в SEQ ID NO 1, заменен глутамином. В случае многократных замен в двух или более позициях два или более заместителя могут быть одинаковыми или различными, т.е. каждый аминокислотный остаток из двух или более замещенных аминокислотных остатков может быть замещен таким же или другим аминокислотным остатком, если явно не указано иное.
[0049] Термины "экзотоксин псевдомонад" и "РЕ", используемые в данном изобретении, включают РЕ, который был модифицирован по сравнению с нативным белком для уменьшения или устранения иммуногенности. Такие модификации могут включать, но не ограничиваясь ими, удаление домена Ia, различные аминокислотные делеции в доменах Ib, II и III, одиночные аминокислотные замены и добавление одной или более чем одной последовательности на карбоксильном конце, например DEL и REDL (SEQ ID NO 7). См. Siegall et al. J. Biol. Chem., 264: 14256-14261 (1989). Такие модифицированные РЕ могут быть дополнительно модифицированы так, чтобы они включали любую из замен согласно изобретению в одном или более чем одном аминокислотном остатке в одном или более чем одном Т-клеточном и/или В-клеточном эпитопе, описанном в данном документе. В одном воплощении модифицированный РЕ может быть цитотоксическим фрагментом нативного РЕ дикого типа. Цитотоксические фрагменты РЕ могут включать те, которые являются цитотоксическими, с последующим протеолитическим или другим процессингом в клетке-мишени (например, в виде белка или пребелка) или без него. В предпочтительном воплощении цитотоксический фрагмент РЕ сохраняет по меньшей мере примерно 20%, предпочтительно по меньшей мере примерно 40%, более предпочтительно по меньшей мере примерно 50%, еще более предпочтительно по меньшей мере примерно 75%, более предпочтительно по меньшей мере примерно 90%, и еще более предпочтительно по меньшей мере примерно 95% цитотоксичности нативного РЕ. В особенно предпочтительных воплощениях цитотоксический фрагмент имеет по меньшей мере цитотоксичность нативного РЕ, а предпочтительно имеет повышенную цитотоксичность по сравнению с нативным РЕ.
[0050] Модифицированный РЕ, который уменьшает или устраняет иммуногенность, включает, например, РЕ4Е, РЕ40, РЕ38, РЕ25, PE38QQR, PE38KDEL и РЕ35. В одном из воплощений РЕ может быть любым из РЕ4Е, РЕ40, РЕ38, РЕ25, PE38QQR (в котором РЕ38 имеет последовательность QQR, добавленную на С-конце), PE38KDEL (в котором РЕ38 имеет последовательность KDEL (SEQ ID NO 5), добавленную на С-конце), PE-LR (устойчивость к лизосомальной деградации) (также упоминается как РЕ24), PE24-LO10 и РЕ35.
[0051] В одном воплощении РЕ модифицировали таким образом, чтобы уменьшить иммуногенность путем удаления домена Ia, как описано в патенте США N0 4892827, который включен в данный документ посредством ссылки. РЕ также может быть модифицирован путем замены определенных остатков домена Ia. В одном из воплощений РЕ может представлять собой РЕ4Е, который является замещенным РЕ, в котором присутствует домен Ia, но в котором основные остатки домена Ia в позициях 57, 246, 247 и 249 заменены кислотными остатками (например, глутаминовой кислотой), как описано в патенте США NO 5512658, который включен в данный документ посредством ссылки.
[0052] РЕ40 представляет собой усеченное производное PE (Pai et al., Proc. Nat 'I Acad. Sci. USA, 88: 3358-62 (1991) и Kondo et al., Biol. Chem., 263: 9470-9475 (1988)). PE35 представляет собой концевой карбоксильный фрагмент РЕ размером 35 кДа, в котором аминокислотные остатки 1-279 были удалены, а молекула начинается с Met в позиции 280, за которым следуют аминокислоты 281-364 и 381-613 нативного PE. РЕ35 и РЕ40 раскрыты, например, в патентах США NONO 5602095 и 4892827, каждый из которых включен в данный документ посредством ссылки. РЕ25 содержит фрагменты из 11 остатков из домена II и весь домен III. В некоторых воплощениях РЕ содержит только домен III.
[0053] В предпочтительном воплощении РЕ представляет собой РЕ38. РЕ38 содержит транслоцирующие и АДФ-рибозилирующие домены РЕ, но не часть, связывающуюся с клеткой (Hwang J. et al., Cell, 48: 129-136 (1987)). PE38 представляет собой усеченный пробелок РЕ, состоящий из аминокислот 253-364 и 381-613, который активируется в его цитотоксическую форму при процессинге внутри клетки (см., например, патент США N0 5608039, который включен в данный документ посредством ссылки, а также Pastan et al., Biochim. Biophys. Acta, 1333: C1-C6(1997)).
[0054] В другом предпочтительном воплощении изобретения РЕ представляет собой PE-LR. PE-LR содержит делецию домена II за исключением последовательности расщепления фурином (FCS), соответствующей аминокислотным остаткам с 274 по 284 в последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и делецию аминокислотных остатков с 365 по 394 домена Ib. Таким образом, PE-LR содержит аминокислотные остатки с 274 по 284 и с 395 по 613 последовательности SEQ ID NO 1. PE-LR описан в публикации международной патентной заявки WO 2009/032954, которая включена в данный документ посредством ссылки. PE-LR, возможно, может также содержать линкерный пептид GGS (SEQ ID NO 283) между FCS и аминокислотными остатками с 395 по 613 последовательности SEQ ID N0 1.
[0055] Как было отмечено выше, альтернативно или дополнительно часть или весь домен Ib может быть удален, а остальные части соединены мостиком или непосредственно пептидной связью. Альтернативно или дополнительно некторая часть амино-части домена II может быть удалена. Альтернативно или дополнительно С-конец может содержать нативную последовательность остатков с 609 по 613 (REDLK) (SEQ ID NO 6) или может содержать изменение, которая может поддерживать способность РЕ к транслокации в цитозоль, такое как KDEL (SEQ ID NO 5) или REDL (SEQ ID NO 7) и повторы этих последовательностей. См., например, патенты США 5854044; 5821238; и 5602095 и публикацию международной патентной заявки WO 1999/051643, которые включены в данный документ посредством ссылки. Любая форма РЕ, иммуногенность которой была устранена или уменьшена, может быть использована в сочетании с любой из замен согласно изобретению одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном и/или В-клеточном эпитопе, описанных в данном документе, до тех пор пока она сохраняет цитотоксичность по отношению к клеткам-мишеням, например, за счет транслокации и рибозилирования EF-2 в клетке-мишени.
[0056] Воплощение данного изобретения относится к экзотоксину А псевдомонад (РЕ), содержащему аминокислотную последовательность РЕ, в которой один или более чем один из аминокислотных остатков F443, R456, L477, R494 и L552, которые определены относительно SEQ ID NO 1, независимо от других является замещенным, где РЕ, возможно, имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе, и эта дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой замену, независимо от других, одного или более чем одного из аминокислотных остатков D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, Q592 и L597, определенных относительно SEQ ID NO 1,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном эпитопе,
(iii) делецию одного или более чем одного из смежных аминокислотных остатков среди остатков с 1 по 273 и с 285 по 394, определенных относительно SEQ ID NO 1, или
(iv) сочетание любого одного, двух или трех из (i)-(iii).
[0057] Было обнаружено, что аминокислотные остатки F443, L477, R494 и L552 расположены в пределах одного или более чем одного Т-клеточного эпитопа РЕ. Таким образом, замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 может преимущественно удалить один или более чем один Т-клеточный эпитоп(ы). Соответственно, РЕ согласно изобретению может преимущественно быть менее иммуногенным, чем незамещенный РЕ (например, дикого типа).
[0058] Предпочтительное воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональныый домен РЕ III
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также,
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1,
где один или более чем один из аминокислотных остатков F443, L477, R494 и L552, определенных относительно SEQ ID NO 1, независимо от других является замещенным,
а РЕ, возможно, дополнительно включает еще одну замену аминокислоты в одном или более чем одном В-клеточном эпитопе.
[0059] Замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 может представлять собой замену любого аминокислотного остатка одним или более чем одним из аминокислотных остатков F443, L477, R494 и L552. В одном из воплощений согласно изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену, независимо от других, аланином, глутаминовой кислотой, гистидином или аспарагином одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552. В одном из воплощений согласно изобретению замена L552 представляет собой замену L552 глутаминовой кислотой или аспарагином, а замена L477 представляет собой замену L477 гистидином.
[0060] В одном из воплощений согласно изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой или аспарагином аминокислотного остатка L552.
[0061] В дополнение к замене (заменам) одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном эпитопе РЕ, описанном в данном документе, РЕ согласно изобретению, возможно, также может включать дополнительную замену(ы) одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1. В связи с этим в одном из воплощений согласно изобретению РЕ имеет замену одной или более чем одной аминокислоты в одном или более чем одном В-клеточном эпитопе SEQ ID NO: 1. В предпочтительном воплощении согласно данному изобретению замена одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1 включает замену аланином, глицином, серином или глутамином одной или более чем одной аминокислоты в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1. Замена(ы) в пределах одного или более чем одного В-клеточного эпитопа может, преимущественно, дополнительно уменьшать иммуногенность за счет удаления одного или более чем одного В-клеточного эпитопа. Замена(ы) может быть расположена в пределах любого подходящего В-клеточного эпитопа РЕ. Примеры В-клеточных эпитопов описаны, например, в публикациях международных патентных заявок WO 2007/016150, WO 2009/032954 и WO 2011/032022, каждая из которых включена в данный документ посредством ссылки. В предпочтительном воплощении замена одной или более чем одной аминокислоты в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1 представляет собой замену аланином, глицином, серином или глутамином, независимо от других, одного или более чем одного из аминокислотных остатков Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, D463, R467, Y481, R490, R505, R513, L516, Е522, R538, Е548, R551, R576, K590, Q592 и L597, где аминокислотные остатки Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, D463, R467, Y481, R490, R505, R513, L516, Е522, R538, Е548, R551, R576, K590, Q592 и L597, определенных относительно SEQ ID NO 1.
[0062] В одном из воплощений согласно изобретению дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой замену, независимо от других, аланином, глицином, серином или глутамином одного или более чем одного из аминокислотных остатков Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, K590, Q592, и L597, определенных относительно SEQ ID NO 1. Предпочтительно дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой замену, независимо от других, аланином, глицином или серином одного или более чем одного из аминокислотных остатков R427, R505 и R551. В особенно предпочтительном воплощении замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443, замену гистидином L477, замену аланином R494 и замену глутаминовой кислотой L552, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; и (b) замену аланином аминокислотного остатка R505, определенного относительно SEQ ID NO 1.
[0063] В одном из воплощений согласно изобретению любой из РЕ, описанных в данном документе, может иметь аргинин в позиции 458 относительно SEQ ID NO 1. Не связываясь с конкретной теорией или механизмом, полагают, что аргинин в позиции 458 связан с повышенной цитотоксичностью.
[0064] В одном из воплощений согласно изобретению РЕ имеет остаток аргинина в позиции 458, определенной относительно SEQ ID NO 1. В предпочтительном воплощении замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка R456, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1.
[0065] В одном из воплощений согласно изобретению замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену аланином аминокислотного остатка R456; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1.
[0066] В одном из воплощений согласно изобретению замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка R456, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1.
[0067] В другом воплощении согласно данному изобретению замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену аланином аминокислотного остатка R456; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1.
[0068] В предпочтительном воплощении согласно данному изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R456; (с) замену аланином аминокислотного остатка R463; (d) замену аланином аминокислотного остатка R467; (е) замену аланином аминокислотного остатка R490; (f) замену аланином аминокислотного остатка R505; и (g) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1. Предпочтительное воплощение представляет собой РЕ, который содержит SEQ ID NO 285 (T14-L010R+456A).
[0069] В предпочтительном воплощении согласно данному изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R456; (с) замену аланином аминокислотного остатка R463; (d) замену аланином аминокислотного остатка R467; (е) замену аланином аминокислотного остатка R490; (f) замену аланином аминокислотного остатка R505; и (g) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1. Предпочтительное воплощение представляет собой РЕ, который содержит SEQ ID NO 286 (T15-L010R+456A).
[0070] В предпочтительном воплощении согласно данному изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1. Предпочтительное воплощение представляет собой РЕ, который содержит SEQ ID NO 287 (T14-L010R).
[0071] В предпочтительном воплощении согласно данному изобретению замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, и дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; которые определены относительно SEQ ID NO 1. Предпочтительное воплощение представляет собой РЕ, который содержит SEQ ID NO 288 (T15-L010R).
[0072] В предпочтительном воплощении FCS представляет собой фурин-расщепляемую последовательность (furin cleavage sequence, FCS), соответствующую аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)).
[0073] В предпочтительном воплощении
n равно 1 для R1 и R2,
R1 представляет собой линкер аминокислотной последовательности SEQ ID NO 282 (DKTHKASGG),
R2 представляет собой линкер аминокислотной последовательности SEQ ID NO 284 (GGGGGS), и
FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)). В особенно предпочтительном воплощении n равен 0 для R3.
[0074] В одном из воплощений согласно изобретению РЕ имеет дополнительную замену аминокислоты в одном или более чем одном Т-клеточном эпитопе. В связи с этим РЕ может содержать аминокислотную последовательность, имеющую дополнительную замену любой аминокислотой одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенных относительно SEQ ID NO 1. В одном из воплощений согласно изобретению дополнительная замена любой аминокислотой одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 представляет собой замену одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, i450, Y470, I471, А472, Р475, А476, L477, I493, R494, N495, L498, L499, R500, V501, Y502, V503, R505, L508, Р509, R551, L552, Т554, I555, L556 и W558.
[0075] Замена одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 SEQ ID NO 1 может представлять собой замену любым аминокислотным остатком аминокислотного остатка в одной или более чем одной из позиций R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 SEQ ID NO 1. Замена одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 SEQ ID NO 1 может включать, например, замену аланином, глицином, серином или глутамином одного или более чем одного из аминокислотных остатков в позициях 421, 422, 423, 425, 427, 429, 439, 440, 443, 444, 446, 447, 450, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 481, 482, 483, 484, 485, 486, 487, 488, 489, 490, 491, 492, 493, 494, 495, 496, 497, 498, 499, 500, 501, 502, 503, 504, 505, 506, 507, 508, 509, 510, 511, 512, 513, 514, 515, 516, 517, 518, 519, 551, 552, 554, 555, 556 и 558 в SEQ ID NO 1. В предпочтительном воплощении замена одного или более чем одного из аминокислотных остатков в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 SEQ ID NO 1 представляет собой замену аланином, глицином, серином или глутамином одного или более чем одного из аминокислотных остатков R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, Y470, I471, А472, Р475, А476, L477, I493, R494, N495, L498, L499, R500, V501, Y502, V503, R505, L508, Р509, R551, L552, Т554, I555, L556 и W558. Одна или более чем одна замена в одном или более чем одном Т-клеточном эпитопе, находящаяся в позициях R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558 РЕ, определенных относительно SEQ ID NO 1, может дополнительно снижать иммуногенность РЕ. В одном из воплощений аминокислотная последовательность не имеет замен одного или более чем одного из аминокислотных остатков в позициях 427, 467, 485, 490, 505, 513, 516 и 551.
[0076] Предпочтительно РЕ содержит одну или более чем одну замену, которая повышает цитотоксичность, как описано, например, в публикации международной патентной заявки WO 2007/016150, которая включена в данный документ посредством ссылки. В связи с этим воплощение данного изобретения относится к РЕ с заменой одной аминокислоты в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1, и данная замена аминокислоты в одном или более чем одном В-клеточном эпитопе SEQ ID NO 1 представляет собой замену валином, лейцином или изолейцином аминокислотного остатка R490, где аминокислотный остаток R490 определен относительно SEQ ID NO 1. В одном из воплощений согласно изобретению замена аланином или глутамином одного или более чем одного из аминокислотных остатков в позициях 313, 327, 331, 332, 431, 432, 505, 516, 538 и 590, определенных относительно SEQ ID NO 1, может дать РЕ с увеличенной цитотоксичностью, как описано, например, в публикации международной патентной заявки WO 2007/016150, которая включена в данный документ посредством ссылки. Повышение цитотоксической активности и снижение иммуногенности могут происходить одновременно и не являются взаимоисключающими. Замены, которые одновременно повышают цитотоксическую активность и снижают иммуногенность, такие как замена R490 глицином или, более предпочтительно, аланином, являются особенно предпочтительными.
[0077] В одном из воплощений согласно изобретению другое воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен РЕ III
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также,
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где один или более чем один из аминокислотных остатков F443, R456, L477, R494 и L552, определенных относительно SEQ ID NO 1, независимо от других является замещенным, где РЕ, возможно, имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном В-клеточном эпитопе, и эта дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой, независимо от других, замену одного или более чем одного из аминокислотных остатков D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, Q592 и L597, определенных относительно SEQ ID NO 1,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном Т-клеточном эпитопе, или
(iii) вместе (i) и (ii).
[0078] Другое воплощение согласно изобретению относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен РЕ III
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также,
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где РЕ включает остаток аргинина в позиции 458, определенной относительно SEQ ID NO 1, и
где РЕ имеет:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538.
[0079] В одном из воплощений согласно изобретению n равен 0 для R1 и R2 формулы I. В другом воплощении согласно данному изобретению n равен 1 для R1 и R2. В одном из воплощений согласно изобретению, когда n равен 0 для R1 и R2, РЕ формулы I может дополнительно содержать линкерный пептид GGS (SEQ ID NO 283) между последовательностью расщепления фурином (FCS) и функциональным доменом III РЕ.
[0080] Не связываясь с конкретной теорией или механизмом, полагают, что РЕ, содержащие FCS, подвергаются протеолитическому процессингу внутри клетки-мишени, таким образом, активируя цитотоксическую активность токсина. FCS РЕ согласно изобретению могут содержать любую подходящую фурин-расщепляемую последовательность аминокислотных остатков, где указанная последовательность может быть расщеплена фурином. Примеры фурин-расщепляемых последовательностей описаны в Duckert et al., Protein Engineering, Design & Selection, 17(1):107-112 (2004) и в публикации международной патентной заявки WO 2009/032954, оба документа включены в данный документ посредством ссылки. В одном из воплощений согласно изобретению FCS содержит остатки с 274 по 284 последовательности SEQ ID NO 1 (т.е. RHRQPRGWEQL (SEQ ID NO 8)), где замена аминокислоты в одном или более чем одном из В-клеточных эпитопов SEQ ID NO 1 представляет собой замену аланином, глицином, серином или глутамином аминокислотного остатка Е282 SEQ ID NO 1. Другие подходящие аминокислотные последовательности FCS включают, но не ограничиваясь ими: R-X1-X2-R, где X1 представляет собой любую природную аминокислоту, и Х2 представляет собой любую природную аминокислоту (SEQ ID NO 9), RKKR (SEQ ID NO 10), RRRR (SEQ ID NO 11), RKAR (SEQ ID NO 12), SRVARS (SEQ ID NO 13), TSSRKRRFW (SEQ ID NO 14), ASRRKARSW (SEQ ID NO 15), RRVKKRFW (SEQ ID NO 16), RNVVRRDW (SEQ ID NO 17), TRAVRRRSW (SEQ ID NO 18), RQPR (SEQ ID NO 19), RHRQPRGW (SEQ ID NO 20), RHRQPRGWE (SEQ ID NO 21), HRQPRGWEQ (SEQ ID NO 22), RQPRGWE (SEQ ID NO 23), RHRSKRGWEQL (SEQ ID NO 24), RSKR (SEQ ID NO 25), RHRSKRGW (SEQ ID NO 26), HRSKRGWE (SEQ ID NO 27), RSKRGWEQL (SEQ ID NO 28), HRSKRGWEQL (SEQ ID NO 29), RHRSKR (SEQ ID NO 30), и R-X1-X2-R, где X1 представляет собой любую природную аминокислоту, а Х2 представляет собой аргинин или лизин (SEQ ID NO 4).
[0081] В еще одном воплощении согласно данному изобретению функциональный домен III РЕ содержит остатки с 395 по 613 последовательности SEQ ID NO 1, где один или более чем один из аминокислотных остатков F443, R456, L477, R494 и L552, определенных относительно SEQ ID NO 1, независимо от других является замещенным. Аминокислотные остатки F443, R456, L477, R494 и L552 могут быть замещены, как описано в данном документе в отношении других аспектов изобретения.
[0082] В одном из воплощений согласно изобретению FCS представлен формулой Р4-Р3-Р2-Р1, в которой Р4 представляет собой аминокислотный остаток на амино-конце, Р1 представляет собой аминокислотный остаток на карбоксильном конце, Р1 представляет собой остаток аргинина или лизина, и последовательность может расщепляться на карбоксильном конце Р1 фурином.
[0083] В другом воплощении согласно данному изобретению FCS (i) также содержит аминокислотные остатки, представленные Р6-Р5, на амино-конце, (ii) также содержит аминокислотные остатки, представленные Р1'-Р2', на карбоксильном конце, (iii) где если Р1 представляет собой остаток аргинина или лизина, то Р2' представляет собой триптофан, а Р4 представляет собой аргинин, валин или лизин, при условии, что если Р4 не является аргинином, то Р6 и Р2 являются основными остатками, и (iv) последовательность может расщепляться на карбоксильном конце Р1 фурином.
[0084] В еще одном воплощении изобретения функциональный домен III РЕ состоит из последовательности остатков с 395 по 613 последовательности SEQ ID NO 1.
[0085] В еще одном воплощении согласно данному изобретению мутантный РЕ содержит между FCS и доменом III РЕ один или более чем один из смежных остатков с 365 по 394 последовательности SEQ ID NO 1.
[0086] Аспекты для разработки химерных молекул экзотоксина псевдомонад в качестве противораковых агентов включают их цитотоксичность в отношении опухолевых клеток, их иммуногенность в отношении человеческих В-клеток и человеческих Т-клеток, а также их термостабильность. Термостабильность может быть полезна для разработки фармацевтических составов или композиций.
[0087] Таким образом, в одном аспекте согласно данному изобретению было обнаружено, что путем введения мутации R456A вместо R458A можно удалить все В-клеточные эпитопы из РЕ без существенного снижения его цитотоксичности в отношении опухолевых клеток (в случае, если другие Т-клеточные эпитопы не удаляются последующими заменами). Таким образом, впервые предложен РЕ, в котором все В-клеточные эпитопы полностью удалены, и который сохраняет свою цитотоксическую активность.
[0088] Воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен III РЕ
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемая последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также
функциональный домен III РЕ представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, и где РЕ имеет:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505
(f) замену аланином аминокислотного остатка R538; и
(g) замену аланином аминокислотного остатка R456.
[0089] В предпочтительном воплощении FCS представляет собой фурин-расщепляемую последовательность, соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)).
[0090] В предпочтительном воплощении
n равно 1 для R1 и R2,
R1 представляет собой линкер аминокислотной последовательности SEQ ID NO 282 (DKTHKASGG),
R2 представляет собой линкер аминокислотной последовательности SEQ ID NO 284 (GGGGGS), и
FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)). В особенно предпочтительном воплощении n равен 0 для R3.
[0091] В предпочтительном воплощении функциональный домен III РЕ включает аминокислотную последовательность SEQ ID NO 37.
[0092] Воплощение данного изобретения относится к выделенному мутантному экзотоксину А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен III РЕ
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; а также
функциональный домен III РЕ представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где РЕ включает аргинин в позиции 458, определенной относительно SEQ ID NO 1.
[0093] РЕ согласно изобретению может быть менее иммуногенным, чем незамещенный РЕ в соответствии с данным изобретением, если иммунный ответ на РЕ согласно изобретению количественно или качественно уменьшается по сравнению с иммунным ответом на незамещенный РЕ. Количественное снижение иммуногенности включает уменьшение величины или степени иммунного ответа. Величина или степень иммуногенности могут быть измерены на основании любого числа известных параметров, таких как снижение уровня продукции цитокина (например, антигенспецифического цитокина) (концентрации цитокина), уменьшение числа активированных лимфоцитов (например, пролиферации лимфоцитов (например, антигенспецифических лимфоцитов)) или привлеченных лимфоцитов и/или снижение продукции антител (антигенспецифических антител) и т.д. Качественное снижение иммуногенности охватывает любое изменение в отношении природы иммунного ответа, которое приводит к иммунному ответу, менее эффективному в опосредовании снижения цитотоксической активности РЕ. Способы измерения иммуногенности известны в данной области. Например, измеряя типы и уровни продуцируемых цитокинов, может измерять иммуногенность. Альтернативно или дополнительно, измеряя связывание РЕ с антителами (например, антителами, ранее подвергшимися воздействию РЕ) и/или измеряя способность РЕ индуцировать антитела при введении млекопитающему (например, людям, мышам и/или мышам, у которых мышиная иммунная система заменена человеческой иммунной системой), можно измерять иммуногенность. Менее иммуногенный РЕ может быть охарактеризован снижением продукции цитокинов, таких как любой один или более чем один из IFN-γ, TNF-a и гранзим В, и/или сниженной стимуляцией клеточно-опосредованного иммунного ответа, например, снижением пролиферации и активации Т-клеток и/или макрофагов, специфических для РЕ, по сравнению с результатами, полученными с незамещенным РЕ. Альтернативно или дополнительно, менее иммуногенный РЕ может характеризоваться увеличением продукции TGF-β и/или IL-10 по сравнению с результатами, полученными с незамещенным РЕ. В предпочтительном воплощении снижение иммуногенности характеризуется одним или более чем одним эффектом среди уменьшения стимуляции Т-клеток, уменьшения пролиферации Т-клеток, а также уменьшения Т-клеточной секреции IFN-γ и/или гранзима В. Альтернативно или дополнительно, менее иммуногенный РЕ может характеризоваться уменьшением стимуляции и/или активации В-клеток, специфичных для РЕ, по сравнению результатами, полученными с незамещенным РЕ. Например, менее иммуногенный РЕ может характеризоваться снижением дифференцировки В-клеток в плазматические клетки, секретирующие антитела, и/или в клетки памяти по сравнению с результатами, полученными с незамещенным РЕ. Снижение иммуногенности может быть охарактеризовано любым одним или более чем одним явлением среди уменьшения стимуляции В-клеток, уменьшения пролиферации В-клеток, а также уменьшения секреции анти-РЕ-антител. Качественное и количественное уменьшение иммуногенности могут происходить одновременно и не являются взаимоисключающими.
[0094] Специалисты в данной области легко поймут, что РЕ согласно изобретению могут быть модифицированы любым числом способов таким образом, чтобы терапевтическая или профилактическая эффективность РЕ согласно изобретению увеличивалась за счет модификации. Например, РЕ согласно изобретению могут быть конъюгированы или слиты либо непосредственно, либо опосредованно через линкер со специфической группировкой (нацеливающим агентом). В связи с этим воплощение данного изобретения относится к химерной молекуле, содержащей (а) специфическую группировку, конъюгированную или слитую с (b) любым из РЕ согласно изобретению, описанных в данном документе. Практика конъюгированных соединений, например, РЕ согласно изобретению, с специфическими группировками известна в данной области. См, например, Wadwa et al., J. Drug Targeting, 3: 111 (1995) и патент США NO 5087616. В одном воплощении любой из РЕ согласно изобретению, описанных в данном документе, может не иметь специфической группировки. В одном воплощении любой из РЕ согласно изобретению, описанных в данном документе, может иметь любую из специфических группировок, имеющих любую из последовательностей, описанных в данном документе.
[0095] Термин "специфическая группировка" ("нацеливающий агент"), используемый в данном документе, относится к любой молекуле или агенту, который специфически распознает и связывает маркер клеточной поверхности таким образом, что специфическая группировка направляет доставку РЕ согласно изобретению в популяцию клеток, на поверхности которых экспрессируется рецептор. Специфические группировки включают, но не ограничиваясь ими, антитела (например, моноклональные антитела) или их фрагменты, пептиды, гормоны, факторы роста, цитокины, а также любые другие природные или неприродные лиганды, такие как, например, платформенные антигенсвязывающие белки.
[0096] Платформенные антигенсвязывающие белки известны в данной области. Например, фибронектин и сконструированные белки с анкириновыми повторами (DARPin) были использованы в качестве альтернативных платформ для антигенсвязывающих доменов, см., например, Gebauer and Skerra, Curr. Opin. Chem. Biol., 13:245-255 (2009) и Stumpp et al., Drug Discov. Today, 13:695-701 (2008), обе публикации включены в данный документ посредством ссылки во всей их полноте.
[0097] В одном воплощении платформенный антигенсвязывающий белок выбран из группы, включающей CTLA-4 (фирма Evibody), липокалин, молекулы-производные белка А, например, Z-домен белка А (фирма Affibody, SpA), А-домен (фирма Avimer, Maxibody), белки теплового шока, например, GroE1 и GroES, трансферрин (трансантитело), белок с анкириновыми повторами (DARPin), пептидный аптамер, домен лектина С-типа (тетранектин), человеческий у-кристаллин и человеческий убиквитин (аффилины); домены PDZ; токсин скорпиона; домены типа kunitz ингибиторов протеазы человека; и фибронектин (аднектин), который подвергли белковой инженерии для получения связывания с лигандом, отличным от природного лиганда.
[0098] CTLA-4 (цитотоксический Т-лимфоцит-ассоциированный антиген 4) представляет собой рецептор семейства CD28, экспрессируемый в основном CD4+ Т-клетками. Его внеклеточный домен имеет складку типа вариабельного домена Ig. Петли, соответствующие участкам CDR (гипервариабельный участок, от англ. complementarity determining regions) антител, могут быть замещены гетерологичной последовательностью для придания различных связывающих свойств. Молекулы CTLA-4, сконструированные так, чтобы они имели различную специфичность связывания, также известны как Evibodies. Для получения более подробной информации см. J. Immunol. Methods, 248(1-2): 31-45 (2001).
[0099] Липокалины представляют собой семейство внеклеточных белков, которые переносят небольшие гидрофобные молекулы, такие как стероиды, билины, ретиноиды и липиды. Они имеют жесткую вторичную структуру бета-листа с некоторым количеством петель на открытом конце конической структуры, которую можно сконструировать таким образом, чтобы она связывала различные антигены-мишени. Антикалины содержат от 160 до 180 аминокислот и являются производными липокалинов. Для получения более подробной информации см. Biochim. Biophys. Acta., 1482: 337-350 (2000), US 7250297 B1 и US 20070224633.
[0100] Белок-миметик антитела (affibody, "аффитело") представляет собой платформу, полученную из белка A Staphylococcus aureus, которая может быть сконструирована для связывания с антигеном. Домен включает трехспиральный пучок длиной приблизительно 58 аминокислот. Библиотеки были получены путем рандомизации поверхностных остатков. Для получения более подробной информации см. Protein Eng. Des. Sel., 17: 455-462 (2004) и EP 1641818A1. Авимеры (avimer) представляют собой полидоменные белки, полученные из платформы семейства А-доменов. Нативные домены длиной приблизительно 35 аминокислот принимают определенную структуру, связанную дисульфидными мостиками. Разнообразие образуется за счет перетасовки природных вариантов, демонстрируемых семейством А-доменов. Для получения более подробной информации см. Nature Biotechnology, 23(12): 1556-1561 (2005) и Expert Opinion on Investigational Drugs, 16(6): 909-917(2007).
[0101] Трансферрин представляет собой мономерный сывороточный транспортный гликопротеин. Трансферрины можно сконструировать таким образом, чтобы они связывались с различными антигенами-мишенями, за счет введения пептидных последовательностей в наружные петли, доступные для встраивания. Примеры сконструированных трансферриновых платформ включают трансантитело. Для получения более подробной информации см. J. Biol. Chem., 274: 24066-24073(1999).
[0102] Сконструированные белки с анкириновыми повторами (белки DARP) являются производными анкиринов, которые представляют собой семейство белков, которые опосредуют прикрепление интегральных мембранных белков к цитоскелету. Один анкириновый повтор представляет собой мотив длиной 33 остатка, состоящий из двух альфа-спиралей и бета-изгиба. Их можно сконструировать таким образом, чтобы они связывались с различными антигенами-мишенями, за счет рандомизации остатков в первой альфа-спирали и бета-изгибе каждого повтора. Поверхность их связывания может быть увеличена за счет увеличения числа модулей (способ созревания аффинности). Для получения более подробной информации см. J. Mol. Biol., 332: 489-503 (2003); PNAS, 100(4): 1700-1705 (2003); J. Mol. Biol., 369, 1015-1028 (2007); и публикацию заявки на патент США 20040132028 А1.
[0103] Фибронектин представляет собой платформу, которую можно сконструировать таким образом, чтобы она связывалась с антигеном. Аднектины содержат остов из природной аминокислотной последовательности 10-го домена, состоящей из 15 повторяющихся единиц человеческого фибронектина типа III (FN3). Три петли на одном конце бета-сэндвича можно сконструировать таким образом, чтобы дать возможность аднектину специфически распознавать терапевтическую мишень, представляющую интерес. Для получения более подробной информации см. Protein Eng. Des. Sel., 18: 435- 444 (2005), публикацию заявки на патент США 20080139791, публикацию заявки на международный патент WO 2005056764 и патент США 6818418 В1.
[0104] Пептидные аптамеры представляет собой комбинаторные распознающие молекулы, которые включают постоянный платформенный белок, как правило, тиоредоксин (TrxA), который содержит вариабельную пептидную петлю с ограниченной конформационной свободой, вставленную на активном участке. Для получения более подробной информации см. Expert Opin. Biol. Ther., 5: 783-797 (2005).
[0105] Микроантитела являются производными природных микробелков длиной от 25 до 50 аминокислот, которые содержат от 3 до 4 цистеиновых мостика. Примеры микробелков включают KalataBI, конотоксин и кноттины. В микробелках есть петля, которую можно сконструировать таким образом, чтобы она включала до 25 аминокислот, не влияя на общее сворачивание микробелка. Для получения более подробной информации см. публикацию заявки на международный патент WO 2008098796.
[0106] Другие антигенсвязывающие белки включают белки, которые были использованы в качестве платформы для конструирования антигенсвязывающих свойств в отношении различных антигенов, включая человеческий гамма-кристаллин и человеческий убиквитин (аффилины), домены типа kunitz ингибиторов протеазы человека, домены PDZ Ras-связывающего белка AF-6, токсины скорпиона (чарибдотоксин) и домен лектина С-типа (тетранектин). См. главу 7 "Non-Antibody Scaffolds" в Handbook of Therapeutic Antibodies (2007, под редакцией Stefan Dubel) и Protein Science, 15:14-27 (2006). Эпитопсвязывающие домены согласно данному изобретению могут быть получены из любого из этих альтернативных белковых доменов.
[0107] Термин "антитело", используемый в данном документе, относится к целым (также известным как "интактные") антителам или их антигенсвязывающим частям, которые сохраняют способность распознавать и связывать антиген. Антитело или его антигенсвязывающие части могут представлять собой антитело или его антигенсвязывающую часть природного происхождения, например, антитело или его антигенсвязывающую часть, выделенную и/или очищенную из млекопитающего, например, мыши, кролика, козы, лошади, курицы, хомяка, человека и т.д. Антитело или его антигенсвязывающая часть может находиться в мономерной или полимерной форме. Кроме того, антитело или его антигенсвязывающая часть может иметь любой уровень аффинности или авидности в отношении маркера клеточной поверхности. При желании антитело или его антигенсвязывающая часть могут быть специфичными к маркеру клеточной поверхности, так что перекрестная реакция с другими пептидами или белками минимальна.
[0108] Антитело может быть моноклональным или поликлональным и может относиться к любому изотипу, например, IgM, IgG (например, IgG, IgG2, IgG3 или IgG4), IgD, IgA или IgE. Определяющие комплементарность области (complementarity determining region, CDR) антитела или одноцепочечные вариабельные фрагменты (Fv) антитела против поверхностного маркера клетки-мишени могут быть привиты или введены генно-инженерным способом в антитело выбора для придания этому антителу специфичности к поверхностному маркеру клетки-мишени. Например, CDR антитела против поверхностного маркера клетки-мишени могут быть привиты в каркасный участок человеческого антитела известной трехмерной структуры (см., например, публикации международных патентных заявок WO 1998/045322 и WO 1987/002671, патенты США 5859205; 5585089; и 4816567; публикацию европейской патентной заявки 0173494; Jones et al., Nature, 321:522 (1986); Verhoeyen et al., Science, 239: 1534 (1988), Riechmann et al., Nature, 332:323 (1988); и Winter & Milstein, Nature, 349: 293 (1991)) с образованием антител, которые могут почти не повышать или не вызывать иммуногенную реакцию при введении человеку. В предпочтительном воплощении специфическая группировка представляет собой моноклональное антитело или антигенсвязывающую часть моноклонального антитела.
[0109] Антигенсвязывающая часть может быть любой частью, которая имеет по меньшей мере один антигенсвязывающий сайт, такой как, например, вариабельные области или CDR интактного антитела. Примеры антигенсвязывающих частей антител включают, но не ограничиваясь ими, тяжелую цепь, легкую цепь, вариабельную или константную область тяжелой или легкой цепи, одноцепочечный вариабельный фрагмент (scFv) или Fc-, Fab-, Fab'-, Fv- или F(ab)2'-фрагмент; однодоменные антитела (см., например, Wesolowski, Med Microbiol Immunol., 198(3): 157-74 (2009); Saerens et al., Curr. Opin. Pharmacol., 8(5):600-8 (2008); Harmsen and de Haard, Appl. Microbiol. Biotechnol., 77(1): 13-22 (2007), спирально-стабилизированные антитела (см., например, Arndt et al., J. Mol. Biol., 312: 221-228 (2001); тримерные антитела; димерные антитела (публикация заявки на европейский патент 0404097; публикация заявки на международный патент WO 1993/011161; и Hollinger et al., Proc. Natl. Acad. Sci. USA, 90: 6444-6448 (1993)); молекулы одноцепочечных антител ("scFv", см., например, патент США 5888773); антитела, стабилизированные дисульфидными мостиками ("dsFv", см., например, патент США 5747654 и 6558672) и доменные антитела ("dAb", см., например, Holt et al., Trends Biotech, 21(11):484-490 (2003), Ghahroudi et al., FEBS Lett., 414:521 -526 (1997), Lauwereys et al., EMBO J 17:3512- 3520 (1998), Reiter et al., J. Mol. Biol. 290:685-698 (1999); и Davies и Riechmann, Biotechnology, 13:475-479 (2001)).
[0110] Способы тестирования антител или их антигенсвязывающих частей на способность связывать какой-либо маркер клеточной поверхности известны в данной области и включают любой анализ связывания типа "антитело - антиген", такой как, например, радиоиммуноанализ (RIA), ИФА (ELISA), вестерн-блот, иммунопреципитация и анализы конкурентного ингибирования (см., например, Janeway et al., см. выше, и публикацию заявки на патент США 2002/0197266 А1).
[0111] Подходящие способы изготовления антител известны в данной области. Например, стандартные гибридомные способы описаны в and Milstein, Eur. J. Immunol., 5, 511-519 (1976), Harlow and Lane (eds.), Antibodies: A Laboratory Manual, CSH Press (1988), и в C.A. Janeway et al. (eds.), Immunobiology, 5th Ed., Garland Publishing, New York, NY (2001)). Альтернативно, в данной области известны другие способы, такие как EBV-гибридомные способы (Haskard and Archer, J. Immunol. Methods, 74(2), 361-67 (1984), и Roder et al., Methods Enzymol., 121, 140-67 (1986)) и системы экспрессии бактериофаговых векторов (см., например, Huse et al., Science, 246, 1275-81 (1989)). Кроме того, способы получения антител на животных описаны, например, в патентах США 5545806, 5569825 и 5714352 и в публикации заявки на патент США 2002/0197266 А1.
[0112] Фаговый дисплей также может быть использован для создания антитела, которое может быть использовано в химерных молекулах согласно изобретению. В связи с этим фаговые библиотеки, кодирующие антигенсвязывающие вариабельные (V) домены антител, могут быть получены с использованием стандартной молекулярной биологии и методик рекомбинантной ДНК (см., например, Sambrook et al. (eds.), Molecular Cloning, A Laboratory Manual, 3rd Edition, Cold Spring Harbor Laboratory Press, New York (2001)). Фаг, кодирующий вариабельную область с нужной специфичностью, выбирают по специфическому связыванию с нужным антигеном и восстанавливают полное или частичное антитело, содержащее выбранный вариабельный домен. Нуклеиновокислотные последовательности, кодирующие восстановленное антитело, вводят в подходящую линию клеток, такую как клетки миеломы, используемые для получения гибридом, так что клетка секретирует антитела с характеристиками моноклональных антител (см., например, Janeway et al., см. выше, Huse et al., и патент США 6265150).
[0113] Альтернативно, антитела могут быть получены с помощью трансгенных мышей, которые являются трансгенными по специфическим генам тяжелой и легкой цепи иммуноглобулина. Такие способы известны в данной области и описаны, например, в патентах США 5545806 и 5569825, а также в Janeway et al., см. выше.
[0114] Альтернативно, антитело может быть генно-инженерным антителом, например, гуманизированным антителом или химерным антителом. Гуманизированные антитела преимущественно обеспечивают более низкий риск побочных эффектов и могут дольше оставаться в кровотоке. Способы получения гуманизированных антител известны в данной области и описаны подробно, например, в Janeway et al., см. выше, в патентах США 5225539, 5585089 и 5693761, европейском патенте 0239400 В1 и патенте Великобритании 2188638. Гуманизированные антитела также могут быть созданы с использованием методики перекладки антитела, описанной, например, в патенте США 5639641 и в Pedersen et al., J. Mol., Biol., 235, 959-973 (1994).
[0115] Специфическая группировка может специфически связываться с любым подходящим маркером клеточной поверхности. Выбор конкретной специфической группировки и/или маркера клеточной поверхности может быть сделан в зависимости от конкретной клеточной популяции, которая будет целевой. Маркеры клеточной поверхности известны в данной области (см., например, Mufson et al., Front. Biosci., 11:337-43 (2006); Frankel et al., Clin. Cancer Res., 6:326-334 (2000); и Kreitman et al., AAPS Journal, 8(3): E532-E551 (2006)) и могут представлять собой, например, белки или углеводы. В одном из воплощений согласно изобретению специфическая группировка представляет собой лиганд, который специфически связывается с рецептором на клеточной поверхности. Примеры лигандов включают, но не ограничиваясь ими, сосудистый эндотелиальный фактор роста (vascular endothelial growth factor, VEGF), Fas, TNF-связанный апоптозиндуцирующий лиганд (TNF-related apoptosis-inducing ligand, TRAIL), цитокин (например, IL-2, IL-15, IL-4, IL-13), лимфокин, гормон и фактор роста (например, трансформирующий фактор роста (TGFa), фактор роста нервов, эпидермальный фактор роста).
[0116] Маркер клеточной поверхности может быть, например, раковым антигеном. Термин "раковый антиген", используемый в данном документе, относится к любой молекуле (например, белку, пептиду, липиду, углеводу и т.д.) которая исключительно или преимущественно экспрессируется или сверхэкспрессируется на опухолевых клетках или раковых клетках, так что данный антиген ассоциирован с опухолью или раком. Раковый антиген дополнительно может экспрессироваться нормальными, неопухолевыми или незлокачественными клетками. Тем не менее, в таких случаях экспрессия ракового антигена нормальными, неопухолевыми или незлокачественными клетками не является столь мощной, как экспрессия опухолевыми или раковыми клетками. В связи с этим опухолевые или раковые клетки могут сверхэкспрессировать антиген или экспрессировать антиген на значительно более высоком уровне по сравнению с экспрессией антигена нормальными, неопухолевыми или незлокачественными. Кроме того, раковый антиген дополнительно может быть экспрессирован клетками различного состояния развития или созревания. Например, раковый антиген может дополнительно экспрессироваться клетками, находящимися на различных эмбриональных или фетальных стадиях, которые в норме не встречаются у взрослого хозяина. Альтернативно, раковый антиген может дополнительно экспрессироваться стволовыми клетками или клетками-предшественниками, которые в норме не встречаются у взрослого хозяина.
[0117] Раковый антиген может представлять собой антиген, экспрессированный любой клеткой любого рака или опухоли, включая раки и опухоли, описанные в данном документе. Раковый антиген может быть раковым антигеном только одного типа рака или опухоли, так что данный раковый антиген ассоциирован или характерен только для одного типа рака или опухоли. Альтернативно, раковый антиген может быть раковым антигеном (например, может быть характерен для) более чем одного типа рака или опухоли. Например, раковый антиген может экспрессироваться как клетками рака молочной железы, так и клетками рака предстательной железы, и совсем не экспрессироваться нормальными, неопухолевыми или нераковыми клетками.
[0118] Примеры раковых антигенов, с которыми может специфически связываться специфическая группировка, включают, но не ограничиваясь ими, муцин 1 (MUC1, опухоль-ассоциированный эпителиальный муцин), ассоциированный с меланомой антиген (melanoma associated antigen, MAGE), преимущественно экспрессируемый меланомой антиген (preferentially expressed antigen of melanoma, PRAME), карциноэмбриональный антиген (carcinoembryonic antigen, CEA), простатический специфический антиген (prostate-specific antigen, PSA), простатический специфический мембранный антиген (prostate specific membrane antigen, PSMA), рецептор гранулоцитарно-макрофагального колониестимулирующего фактора (granulocyte-macrophage colony-stimulating factor receptor, GM-CSFR), CD56, человеческий рецептор эпидермального фактора роста 2 (HER2/neu) (также известный как erbB-2), CD5, CD7, опухолевый антиген тирозиназа, тирозиназа-связанный белок (tyrosinase related protein, TRP)1, Trp2, NY-ESO-1, теломераза и p53. В предпочтительном воплощении маркер клеточной поверхности, с которым специфически связывается специфическая группировка, выбран из группы, включающей кластер дифференцировки (cluster of differentiation, CD) 19, CD21, CD22, CD25, CD30, CD33 (связывающий сиаловые кислоты Ig-подобный лектин 3, миелоидный антиген клеточной поверхности), CD79b, CD123 (рецептор альфа интерлейкина 3), рецептор трансферрина, рецептор EGF (от англ. epidermal growth factor), мезотелин, кадгерин, антиген Льюиса Y, глипикан-3, FAP (от англ. fibroblast activation protein alpha - белок активации фибробластов альфа), PSMA (простатический специфический мембранный антиген), СА9 или CAIX (карбоангидраза IX), L1CAM (от англ. cell adhesion molecule - молекула адгезии нервных клеток L1), эндосиалин, HER3 (активированная конформация члена 3 семейства рецепторов эпидермального фактора роста), комплекс Alk1/BMP9 (киназа 1 анапластической лимфомы/костный морфогенетический белок 9), TPBG или 5Т4 (от англ. trophoblast glycoprotein - гликопротеин трофобласта), ROR1 (рецепторный тирозинкиназоподобный поверхностный антиген), HER1 (активированная конформация рецептора эпидермального фактора роста) и CLL1 (семейство лектиновых доменов С-типа 12, член А). Мезотелин экспрессируется, например, на клетках рака яичника, мезотелиомы, немелкоклеточного рака легкого, аденокарциномы легкого, рака фаллопиевых труб, рака головы и шеи, рака шейки матки, рака поджелудочной железы. CD22 экспрессируется, например, на клетках волосатоклеточной лейкемии, хронического лимфоцитарного лейкоза (chronic lymphocytic leukemia, CLL), пролимфоцитарного лейкоза (prolymphocyte leukemia, PLL), неходжкинской лимфомы, мелкоклеточной лимфоцитарной лимфомы (small lymphocytic lymphoma, SLL) и острого лимфолейкоза (acute lymphatic leukemia, ALL). CD25 экспрессируется, например, на клетках лейкемии и лимфомы, включая волосатоклеточную лейкемию и лимфому Ходжкина. Антиген Льюиса Y экспрессируется, например, на клетках рака мочевого пузыря, рака молочной железы, рака яичников, рака толстой кишки, рака пищевода, рака желудка, рака легкого, рака поджелудочной железы. CD33 экспрессируется, например, на клетках острого миелоидного лейкоза (acute myeloid leukemia, AML), хронического миеломоноцитарного лейкоза (chronic myelomonocytic leukemia, ML) и миелопролиферативных нарушений.
[0119] В одном из воплощений согласно изобретению специфическая группировка представляет собой антитело, которое специфически связывается с раковым антигеном. Примеры антител, которые специфически связываются с раковым антигеном, включают, но не ограничиваясь ими, антитела против рецептора трансферрина (например, НВ21 и его варианты), антитела против CD22 (например, RFB4 и его варианты), антитела против CD25 (например, анти-Тас и его варианты), антитела против мезотелина (например, SS1, MORAb-009, SS, HN1, HN2, MN, MB и их варианты) и антитела против антигена Льюиса Y (например, В3 и его варианты). В связи с этим специфическая группировка может представлять собой антитело, выбранное из группы, состоящей из В3, RFB4, SS, SS1, MN, MB, HN1, HN2, НВ21 и MORAb-009, и его антигенсвязывающие части. Другие примеры специфических группировок, пригодных для использования в химерных молекулах согласно изобретению, раскрыты, например, в патентах США 5242824 (против рецептора трансферрина); 5846535 (анти-CD25); 5889157 (против антигена Льюиса Y); 5981726 (против антигена Льюиса Y); 5990296 (против антигена Льюиса Y); 7081518 (против мезотелина); 7355012 (анти-CD22 и анти-CD25); 7368110 (против мезотелина); 7470775 (анти-CD30); 7521054 (анти-CD25); и 7541034 (анти-CD22); в публикации заявки на патент США 2007/0189962 (анти-CD22); Frankel et al., Clin. Cancer Res., 6: 326-334 (2000), и Kreitman et al., AAPS Journal, 8(3): E532-E551 (2006), каждый из которых включен в данный документ посредством ссылки. В другом воплощении специфическая группировка может включать специфическую группировку иммунотоксинов, известных в данной области. Примеры иммунотоксинов включают, но не ограничиваясь ими, LMB-2 (Anti-Tac(Fv)-PE38), BL22 и НА22 (RFB4(dsFv)-PE38), SS1P (SS 1 (dsFv)-PE38), НВ21-РЕ40 и их варианты. В предпочтительном воплощении специфическая группировка представляет собой антигенсвязывающую часть НА22. НА22 содержит Fv-фрагмент анти-CD22-антитела, связанный дисульфидными мостиками, который конъюгирован с РЕ38. НА22 и его варианты описаны в публикациях международных патентных заявок WO 2003/027135 и WO 2009/032954, которые включены в данный документ посредством ссылки.
[0120] Антигенсвязывающая часть специфической группировки может содержать вариабельную область легкой цепи и/или вариабельную область тяжелой цепи. В одном воплощении согласно данному изобретению вариабельная область тяжелой цепи содержит CDR1-область тяжелой цепи, CDR2-область тяжелой цепи и CDRS-область тяжелой цепи. В связи с этим антигенсвязывающий домен может содержать одну или более чем одну из CDR1-областей тяжелой цепи, содержащих SEQ ID NO 49, 65, 81, 97, 113, 129, 145, 161 или 177; CDR2-областей тяжелой цепи, содержащих SEQ ID NO 53, 69, 85, 101, 117, 133, 149, 165 или 181; и CDR3-областей тяжелой цепи, содержащих SEQ ID NO 57, 73, 89, 105, 121, 137, 153, 169 или 185. Предпочтительно, тяжелая цепь содержит все следующие (a) SEQ ID NONO 49, 53 и 57 (CDR1-CDR3 тяжелой цепи против мезотелина, соответственно); (b) SEQ ID NONO 65, 69 и 73 (CDR1-CDR3 тяжелой цепи gc33 против глипикана 3, соответственно); (с) SEQ ID NONO 81, 85 и 89 (CDR1-CDR3 кислой тяжелой цепи антитела против глипикана 3, соответственно); (d) SEQ ID NONO 97, 101 и 105 (CDR1-CDR3 тяжелой цепи анти-FAP, соответственно); (е) SEQ ID NONO 113, 117, 121 (CDR1-CDR3 тяжелой цепи анти-PSMA, соответственно); (f) SEQ ID NONO 129, 133 и 137 (CDR1-CDR3 тяжелой цепи анти-CAIX, соответственно); (g) SEQ ID NONO 145, 149 и 153 (CDR1-CDR3 тяжелой цепи анти-L1CAM-(1), соответственно); (h) SEQ ID NONO 161, 165, 169 (CDR1-CDR3 тяжелой цепи анти-L1CAM (2), соответственно); или (i) SEQ ID NONO 177, 181 и 185 (анти-L1CAM(3) CDR1-CDR3 тяжелой цепи, соответственно).
[0121] В одном воплощении согласно данному изобретению вариабельная область легкой цепи может содержать CDR1-область легкой цепи, CDR2-область легкой цепи и CDR3-область легкой цепи. В связи с этим антигенсвязывающий домен может содержать одну или более чем одну CDR1-область легкой Цепи, содержащую SEQ ID NO 50, 66, 82, 98, 114, 130, 146, 162 или 178; CDR2-область легкой цепи, содержащую SEQ ID NO 54, 70, 86, 102, 118, 134, 150, 166 или 182; и CDR3-область легкой цепи, содержащую SEQ ID NO 58, 74, 90, 106, 122, 138, 154, 170 или 186. Предпочтительно, легкая цепь содержит все следующие (a) SEQ ID NONO 50, 54 и 58 (CDR1-CDR3 легкой цепи против мезотелина, соответственно); (b) SEQ ID NONO 66, 70 и 74 (CDR1-CDR3 легкой цепи gc33 против глипикана 3, соответственно); (с) SEQ ID NONO 82, 86 и 90 (CDR1-CDR3 кислой легкой цепи антитела против глипикана 3, соответственно); (d) SEQ ID NONO 98, 102 и 106 (CDR1-CDR3 легкой цепи анти-FAP, соответственно); (е) SEQ ID NONO 114, 118 и 122 (CDR1-CDR3 легкой цепи анти-PSMA, соответственно); (f) SEQ ID NONO 130, 134 и 138 (CDR1-CDR3 легкой цепи анти-CAIX, соответственно); (g) SEQ ID NONO 146, 150 и 154 (CDR1-CDR3 легкой цепи анти-L1CAM-(1), соответственно); (h) SEQ ID NONO 162, 166 и 170 (CDR1-CDR3 легкой цепи анти- L1CAM-(2), соответственно); или (i) SEQ ID NONO 178, 182 и 186 (CDR1-CDR3 легкой цепи анти-L1CAM-(3), соответственно).
[0122] В особенно предпочтительном воплощении антигенсвязывающая часть содержит CDR1-, CDR2-, CDR3-области легкой цепи и CDR1-, CDR2-, CDR3-области тяжелой цепи. В связи с этим антигенсвязывающая часть содержит (a) SEQ ID NONO 49, 50, 53, 54, 57 и 58; (b) SEQ ID NONO 65, 66, 69, 70, 73 и 74; (с) SEQ ID NONO 81, 82, 85, 86, 89 и 90; (d) SEQ ID NONO 97, 98, 101, 102, 105 и 106; (e) SEQ ID NONO 113, 114, 117, 118, 121 и 122; (f) SEQ ID NONO 129, 130, 133, 134, 137 и 138; (g) SEQ ID NONO 145, 146, 149, 150, 153 и 154; (h) SEQ ID NONO 161, 162, 165, 166, 169 и 170; или (i) SEQ ID NONO 177, 178, 181, 182, 185 и 186.
[0123] В одном воплощении антигенсвязывающая часть содержит каркасные области FR1, FR2, FR3, FR4 тяжелой цепи и FR1, FR2, FR3, FR4 легкой цепи в дополнение к CDR-областям, описанным выше. В связи с этим антигенсвязывающая часть может содержать FR1-область тяжелой цепи, содержащую SEQ ID NO 47, 63, 79, 95, 111, 127, 143, 159 или 175; FR2-область тяжелой цепи, содержащую SEQ ID NO 51, 67, 83, 99, 115, 131, 147, 163 или 179; FR3-область тяжелой цепи, содержащую SEQ ID NO 55, 71, 87, 103, 119, 135, 151, 167, 183; и FR4-область тяжелой цепи, содержащую SEQ ID NO 59, 75, 91, 107, 123, 139, 155, 171 или 187. Антигенсвязывающая часть может содержать FR1-область легкой цепи, содержащую SEQ ID NO 48, 64, 80, 96, 112, 128, 144, 160, 176; FR2-область легкой цепи, содержащую SEQ ID NO 52, 68, 84, 100, 116, 132, 148, 164 или 180; FR3-область легкой цепи, содержащую SEQ ID NO 56, 72, 88, 104, 120, 136, 152, 168 или 184; и FR4-область легкой цепи, содержащую SEQ ID NO 60, 76, 92, 108, 124, 140, 156, 172 или 188. Предпочтительно, антигенсвязывающая часть содержит FR1-, FR2-, FR3-, F4-, CDR1-, CDR2- и CDR3-области легкой цепи и FR1-, FR2-, FR3-, F4-, CDR1-, CDR2- и CDR3-области тяжелой цепи. В связи с этим антигенсвязывающая часть содержит (a) SEQ ID NONO с 47 по 60 (анти-мезотелин); (b) SEQ ID NONO с 63 по 76 (антитело gc33 против глипикана 3); (с) SEQ ID NONO с 79 по 92 (кислое антитело против глипикана 3); (d) SEQ ID NONO с 95 по 108 (анти-FAP); (е) SEQ ID NONO с 111 по 124 (анти-PSMA); (f) SEQ ID NONO с 127 по 140 (анти-CAIX); (g) SEQ ID NONO с 143 по 156 (анти- L1CAM(1)); (h) SEQ ID NONO с 159 по 172 (анти-L1CAM(2)); или (i) SEQ ID NONO с 175 по 188 (анти-LI CAM(3)).
[0124] В одном воплощении вариабельная область легкой цепи антигенсвязывающего домена может содержать SEQ ID NO 46, 62, 78, 94, 110, 126, 142, 158 или 174. В одном воплощении вариабельная область тяжелой цепи антигенсвязывающего домена может содержать SEQ ID NO 45, 61, 77, 93, 109, 125, 141, 157 или 173. В предпочтительном воплощении антигенсвязывающий домен содержит обе (a) SEQ ID NONO 45 и 46 (анти-мезотелин); (b) SEQ ID NONO 61 и 62 (антитела gc33 против глипикана 3); (с) SEQ ID NONO 77 и 78 (анти-gc33 кислый); (d) SEQ ID NONO 93 и 94 (анти-FAP); (e) SEQ ID NONO 109 и 110 (анти-PSMA); (f) SEQ ID NONO 125 и 126 (анти-CAIX); (g) SEQ ID NONO 141 и 142 (анти-L1CAM(1)); (h) SEQ ID NONO 157 и 158 (анти-L1CAM(2)); (i) SEQ ID NONO 173 и 174 (анти-L1CAM(3)); или (j) SEQ ID NONO 93 и 290 (анти-FAP).
[0125] Другой аспект согласно данному изобретению представляет собой гуманизированное анти-мезотелин-антитело, содержащее вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46. Гуманизированное антитело создается путем использования мышиного анти-мезотелин-антитела SS1 в качестве исходного материала и образования специфических комбинаций определенных каркасных областей с CDR-областями мышиного антитела SS1. Гуманизированное антитело преимущественно связано с хорошими связывающими свойствами, стабильностью и перспективностью использования.
[0126] В одном из воплощений согласно изобретению специфическая группировка может быть гуманизированной. В одном из воплощений согласно изобретению специфическая группировка представляет собой гуманизированное SS1 или антигенсвязывающую часть гуманизированного SS1. В связи с этим специфическая группировка может содержать легкую цепь, содержащую SEQ ID NO 33 (cFP-0199), и тяжелую цепь, содержащую SEQ ID NO 38 (cFP-0200). В другом воплощении специфическая группировка может содержать легкую цепь, содержащую SEQ ID NO 31 (cFP-0199 гуманизированный вариабельный домен легкой цепи VL) и SEQ ID NO 32 (cFP-0199 константный домен легкой цепи каппа). В одном воплощении специфическая группировка может содержать тяжелую цепь, содержащую SEQ ID NO 34 (cFP-0200 гуманизированный вариабельный домен тяжелой цепи VH) и SEQ ID NO 35 (cFP-0200 константный домен тяжелой цепи СН1). В одном воплощении специфическая группировка содержит все последовательности SEQ ID NO 31, 32, 34 и 35.
[0127] В одном из воплощений согласно изобретению химерная молекула содержит линкер. Термин "линкер", используемый в данном документе, относится к любому агенту или молекуле, которая соединяет РЕ согласно изобретению с специфической группировкой. Специалисту в данной области будет понятно, что сайты на РЕ согласно изобретению, которые не являются необходимыми для функционирования РЕ согласно изобретению, представляют собой идеальное место для прикрепления линкера и/или специфической группировки, при условии, что линкер и/или специфическая группировка, после того как они прикреплены к РЕ согласно изобретению, не мешают функциям РЕ согласно изобретению, т.е. его цитотоксической активности, ингибированию роста клетки-мишени или лечения или профилактики рака. Линкер может быть способен к формированию ковалентных связей с как РЕ, так и с специфической группировкой. Подходящие линкеры известны в данной области и включают, но не ограничиваясь ими, углеродные линкеры с прямой или разветвленной цепью, гетероциклические углеродные линкеры и пептидные линкеры. Если РЕ и специфическая группировка представляют собой полипептиды, то линкер может быть присоединен к аминокислотам через боковые группы (например, посредством дисульфидной связи с цистеином). Предпочтительно, линкеры будут присоединены к альфа-углероду амино- и карбоксильных групп концевых аминокислот.
[0128] В другом аспекте данного изобретения было обнаружено, что путем введения специфических аминокислот на обеих сторонах последовательности расщепления фурином (FCS) можно получить более стабильную химерную молекулу экзотоксина псевдомонад с специфической группировкой. Кроме того, также были удалены потенциальные Т-клеточные эпитопы в линкерной области, что может быть особенно полезным при использовании Fab-фрагментов антитела в качестве специфической группировки. Эти химерные молекулы имеют повышенную термодинамическую стабильность по сравнению с химерными молекулами без таких удлиненных линкеров и сохраняют свою цитотоксичность по отношению к опухолевым клеткам. Соответственно, в одном из воплощений согласно изобретению линкер представляет собой удлиненный линкер. Удлиненный линкер может содержать последовательность SEQ ID NO 36.
[0129] В предпочтительном воплощении R1 n-FCS-R2 n представляет собой линкер с аминокислотной последовательностью SEQ ID NO 36. Сайт расщепления фурином находится между аминокислотными остатками 15 и 16 в SEQ ID NO 36.
[0130] Воплощение согласно данному изобретению относится к химерной молекуле, содержащей (а) специфическую группировку, конъюгированную или слитую с (b) любым из РЕ, описанных в данном документе.
[0131] Воплощение согласно данному изобретению относится к выделенной химерной молекуле, содержащей (а) специфическую группировку, конъюгированную или слитую с (b) мутантным экзотоксином А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен РЕ III,
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемая последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; и
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где РЕ содержит аргинин в позиции 458, определенной относительно SEQ ID NO 1, и где РЕ имеет:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505;
(f) замену аланином аминокислотного остатка R538; и
(g) замену аланином аминокислотного остатка R456.
[0132] В предпочтительном воплощении химерной молекулы FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)).
[0133] В предпочтительном воплощении химерной молекулы
n равно 1 для R1 и R2,
R1 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 282 (DKTHKASGG),
R2 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 284 (GGGGGS), и
FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)). В особенно предпочтительном воплощении n равен 0 для R3.
[0134] В предпочтительном воплощении химерной молекулы R1n-FCS-R2n представляет собой линкер с аминокислотной последовательностью SEQ ID NO 36, а специфическая группировка содержит Fab-фрагмент антитела.
[0135] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против мезотелина, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (LO10R-456A). В одном предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против мезотелина, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46. В связи с этим химерная молекула может содержать (a) SEQ ID NONO 39 и 40; (b) SEQ ID NONO 41 и 42; или (с) SEQ ID NONO 43 и 44.
[0136] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62.
[0137] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
[0138] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, FCS, соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106, соответственно). В одном предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи VL SEQ ID NO 290. В связи с этим химерная молекула может содержать (a) SEQ ID NONO 291 и 293; (b) SEQ ID NONO 291 и 294; или (с) SEQ ID NONO 292 и 294.
[0139] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, FCS, соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0140] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, FCS, соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и PE, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 126 (SEQ ID NONO 130, 134 и 138, соответственно). В связи с этим химерная молекула может содержать (a) SEQ ID NONO 295 и 297 или (b) SEQ ID NONO 296 и 297.
[0141] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, FCS, соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37 (L010R-456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174.
[0142] В предпочтительном воплощении изобретение относится к выделенной химерной молекуле, содержащей (а) специфическую группировку, конъюгированную или слитую с (b) мутантным экзотоксином А псевдомонад (РЕ), который содержит последовательность следующей формулы:
R1 n-FCS-R2 n-R3 n-функциональный домен PE III,
в которой:
n равно 0 или 1 независимо для каждого из R1, R2 и R3,
R1 представляет собой от 1 до 10 аминокислотных остатков
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет амино-конец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; и
функциональный домен PE III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1.
где один или более чем один из аминокислотных остатков F443, L477, R494 и L552, определенных относительно SEQ ID NO 1, независимо от других является замещенным;
а РЕ, возможно, содержит дополнительную замену аминокислоты в одном или более чем одном В-клеточном эпитопе.
[0143] Было обнаружено, что замена гистидином аминокислотного остатка L477 ведет в сильному уменьшению Т-клеточных ответов по сравнению с заменами другими аминокислотами (см., например, пример 4) и в то же время повышает цитотоксическую эффективность РЕ по сравнению с заменами другими аминокислотами (см., например, примеры 3, 5 и 6). Таким образом, в предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену гистидином аминокислотного остатка L477. Замена глутаминовой кислотой или аспарагином аминокислотного остатка L552 также приводит к дальнейшему увеличению токсичности, уменьшая при этом Т-клеточные ответы. В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену гистидином аминокислотного остатка L477 и замену глутаминовой кислотой или аспарагином аминокислотного остатка L552. В одном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой или аспарагином аминокислотного остатка L552.
[0144] В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а другая замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427 и (b) замену аланином аминокислотного остатка R505, определенного относительно SEQ ID NO 1. В предпочтительном воплощении данного изобретения РЕ химерной молекулы содержит аминокислотную последовательность SEQ ID NO 289 (Т18/Т20).
[0145] В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а другая замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R456; (с) замену аланином аминокислотного остатка R463; (d) замену аланином аминокислотного остатка R467; (е) замену аланином аминокислотного остатка R490; (f) замену аланином аминокислотного остатка R505; и (g) замену аланином аминокислотного остатка R538; определенных относительно SEQ ID NO 1. В предпочтительном воплощении РЕ химерной молекулы содержит аминокислотную последовательность SEQ ID NO 285 (Т14-L010R+456A).
[0146] В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а другая замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R456; (с) замену аланином аминокислотного остатка R463; (d) замену аланином аминокислотного остатка R467; (е) замену аланином аминокислотного остатка R490; (f) замену аланином аминокислотного остатка R505; и (g) замену аланином аминокислотного остатка R538; определенных относительно SEQ ID NO 1. В предпочтительном воплощении РЕ химерной молекулы содержит аминокислотную последовательность SEQ ID NO 286 (Т15-L010R+456A).
[0147] В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а другая замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; определенных относительно SEQ ID NO 1. В предпочтительном воплощении РЕ химерной молекулы содержит аминокислотную последовательность SEQ ID NO 287 (T14-L010R).
[0148] В предпочтительном воплощении данного изобретения относительно химерной молекулы замена одного или более чем одного из аминокислотных остатков F443, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а другая замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой: (а) замену аланином аминокислотного остатка R427; (b) замену аланином аминокислотного остатка R463; (с) замену аланином аминокислотного остатка R467; (d) замену аланином аминокислотного остатка R490; (е) замену аланином аминокислотного остатка R505; и (f) замену аланином аминокислотного остатка R538; определенных относительно SEQ ID NO 1. В предпочтительном воплощении РЕ химерной молекулы содержит аминокислотную последовательность SEQ ID NO 288 (T15-L010R).
[0149] В предпочтительном воплощении относительно химерной молекулы FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)).
[0150] В предпочтительном воплощении относительно химерной молекулы
n равно 1 для R1 и R2,
R1 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 282 (DKTHKASGG),
R2 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 284 (GGGGGS), и
FCS представляет собой фурин-расщепляемую последовательность (FCS), соответствующая аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)). В особенно предпочтительном воплощении n составляет 0 для R3.
[0151] В предпочтительном воплощении относительно химерной молекулы R1 n-FCS-R2 n представляет собой линкер с аминокислотной последовательностью SEQ ID NO 36, а специфическая группировка содержит Fab-фрагмент антитела.
[0152] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против мезотелина, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против мезотелина, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46.
[0153] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против мезотелина, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против мезотелина, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46.
[0154] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против мезотелина, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против мезотелина, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46.
[0155] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против мезотелина, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против мезотелина, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 45 и вариабельный домен легкой цепи SEQ ID NO 46.
[0156] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 289 (Т18/T20). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 289 (Т18/T20). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 61 (SEQ ID NONO 65, 69 и 73, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 62 (SEQ ID NONO 66, 70 и 74, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 77 (SEQ ID NO 81, 85 и 89, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 78 (SEQ ID NONO 82, 86 и 90, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
[0157] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 285 (T14-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-LO10R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 61 (SEQ ID NO 65, 69 и 73, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 62 (SEQ ID NONO 66, 70 и 74, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 77 (SEQ ID NONO 81, 85 и 89, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 78 (SEQ ID NONO 82, 86 и 90, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
[0158] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 286 (T15-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 61 (SEQ ID NO 65, 69 и 73, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 62 (SEQ ID NONO 66, 70 и 74, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 77 (SEQ ID NONO 81, 85 и 89, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 78 (SEQ ID NONO 82, 86 и 90, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
[0159] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 287 (T14-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-LO-10R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 61 (SEQ ID NONO 65, 69 и 73, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 62 (SEQ ID NONO 66, 70 и 74, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 77 (SEQ ID NONO 81, 85 и 89, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 78 (SEQ ID NONO 82, 86 и 90, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
[0160] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 288 (T15-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть антитела против глипикана 3, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 61 (SEQ ID NONO 65, 69 и 73, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 62 (SEQ ID NONO 66, 70 и 74, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 77 (SEQ ID NONO 81, 85 и 89, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 78 (SEQ ID NONO 82, 86 и 90, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент антитела против глипикана 3, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78.
В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 289 (T18/T20). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 289 (Т18/T20). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290.
[0161] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 285 (T14-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290.
[0162] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам 274-284 SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и PE, содержащий SEQ ID NO 286 (T15-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290.
[0163] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 287 (T14-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290.
[0164] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 288 (T15-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-FAP-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 93 (SEQ ID NONO 97, 101 и 105, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 94 (SEQ ID NONO 98, 102 и 106, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94. В другом предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-FAP-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290. В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 289 (T18/T20). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 289 (Т18/Т20). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0165] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 285 (TI4-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0166] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 286 (T15-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0167] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 287 (T14-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0168] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 288 (T15-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-PSMA-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-PSMA-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 109 (SEQ ID NONO 113, 117 и 121, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 110 (SEQ ID NONO 114, 118 и 122, соответственно).
[0169] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 289 (T18/T20). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 289 (Т18/Т20). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 126 (SEQ ID NONO 130, 134 и 138).
[0170] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 285 (TI4-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID N0 126 (SEQ ID NONO 130, 134 и 138, соответственно).
[0171] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 286 (T15-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 126 (SEQ ID NONO 130, 134 и 138, соответственно).
[0172] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 287 (T14-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 126 (SEQ ID NONO 130, 134 и 138, соответственно).
[0173] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 288 (T15-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-CAIX-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-CAIX-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 125 (SEQ ID NONO 129, 133 и 137, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 126 (SEQ ID NONO 130, 134 и 138, соответственно). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 289 (T18/T20). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174.
[0174] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 285 (TI4-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 285 (T14-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174.
[0175] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 286 (T15-LO10R+456A). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 286 (T15-L010R+456A). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти- L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174.
[0176] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 287 (T14-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 287 (T14-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174.
[0177] В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, фурин-расщепляемую последовательность (FCS), соответствующую аминокислотным остаткам с 274 по 284 последовательности SEQ ID NO 1 (RHRQPRGWEQL (SEQ ID NO 8)), и РЕ, содержащий SEQ ID NO 288 (T15-LO10R). В предпочтительном воплощении химерная молекула содержит антигенсвязывающую часть анти-L1CAM-антитела, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 288 (T15-L010R). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий CDR1, CDR2 и CDR3 вариабельного домена тяжелой цепи VH SEQ ID NO 141 (SEQ ID NONO 145, 149 и 153, соответственно) и CDR1, CDR2 и CDR3 вариабельного домена легкой цепи SEQ ID NO 142 (SEQ ID NONO 146, 150 и 154, соответственно). В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 157 и вариабельный домен легкой цепи SEQ ID NO 158. В предпочтительном воплощении антигенсвязывающая часть представляет собой Fab-фрагмент анти-L1CAM-антитела, содержащий вариабельный домен тяжелой цепи VH SEQ ID NO 173 и вариабельный домен легкой цепи SEQ ID NO 174. В объем данного изобретения включены функциональные части РЕ согласно изобретению и химерные молекулы, описанные в данном документе. Термин "функциональная часть" при использовании в отношении РЕ или химерной молекулы относится к какой-либо части или фрагменту РЕ или химерной молекулы согласно изобретению, где указанная часть или фрагмент сохраняет биологическую активность РЕ или химерной молекулы, частью которой он является (родительского РЕ или химерной молекулы). Функциональные части включают, например, те части РЕ или химерной молекулы, которые сохраняют способность специфически связываться и разрушать или ингибировать рост клеток-мишеней или лечить или предотвращать рак в похожей степени, в той же степени или в более высокой степени, чем родительский РЕ или химерная молекула. В отношении родительского РЕ или химерной молекулы функциональная часть может включать, например, примерно 10% или более, примерно 25% или более, примерно 30% или более, примерно 50% или более, примерно 68% или более, примерно 80% или более, примерно 90% или более, или примерно 95% или более родительского РЕ или химерной молекулы.
[0178] Функциональная часть может включать дополнительные аминокислоты на амино- или карбоксильном конце части или на обоих концах, при этом указанных дополнительных аминокислот нет в аминокислотной последовательности родительского РЕ или химерной молекулы. Желательно, чтобы дополнительные аминокислоты не мешали биологической функции функциональной части, т.е. специфическому связыванию и разрушению или ингибированию роста клеток-мишеней, наличию возможности лечения или профилактики рака и т.д. Более желательно, чтобы дополнительные аминокислоты повышали биологическую активность по сравнению с биологической активностью родительского РЕ или химерной молекулы.
[0179] В объем данного изобретения включены функциональные варианты РЕ согласно изобретению и химерные молекулы, описанные в данном документе. Термин "функциональный вариант", используемый в данном документе, относится к РЕ или химерной молекуле, имеющей существенную или значительную идентичность или сходство последовательности с родительским РЕ или химерной молекулой, где указанный функциональный вариант сохраняет биологическую активность РЕ или химерной молекулы, вариантом которых он является. Функциональные варианты включают, например, те варианты РЕ или химерной молекулы, описанные в данном документе (родительского РЕ или химерной молекулы), которые сохраняют способность специфически связываться и разрушать или ингибировать рост клеток-мишеней в похожей степени, в той же степени или в более высокой степени, чем родительский РЕ или химерная молекула. В отношении родительского РЕ или химерной молекулы функциональный вариант может, например, иметь примерно 30% или более, примерно 50% или более, примерно 75% или более, примерно 80% или более, примерно 90% или более, примерно 95% или более, примерно 96% или более, примерно 97% или более, примерно 98% или более, или примерно 99% или более идентичности с аминокислотной последовательностью родительского РЕ или химерной молекулы.
[0180] Функциональный вариант может, например, включать аминокислотную последовательность родительского РЕ или химерной молекулы по меньшей мере с одной консервативной аминокислотной заменой. Консервативные аминокислотные замены известны в данной области и включают аминокислотные замены, в которых одна аминокислота, имеющая определенные химические и/или физические свойства, заменяет другую аминокислоту с такими же химическими или физическими свойствами. Например, консервативная аминокислотная замена может представлять собой кислую аминокислоту, замененную другой кислой аминокислотой (например, Asp или Glu), аминокислоту с неполярной боковой цепью, замененную другой аминокислотой с неполярной боковой цепью (например, Ala, Gly, Val, Ile, Leu, Met, Phe, Pro, Trp, Val и т.д.), основную аминокислоту, замененную другой основной аминокислотой (Lys, Arg и т.д.), аминокислоту с полярной боковой цепи, замененную другой аминокислотой с полярной боковой цепью (Asn, Cys, Gin, Ser, Thr, Tyr и т.п.) и т.д.
[0181] Альтернативно или дополнительно функциональные варианты могут содержать аминокислотную последовательность родительского РЕ или химерной молекулы по меньшей мере с одной неконсервативной аминокислотной заменой. В этом случае предпочтительно, чтобы неконсервативная аминокислотная замена не мешала или не ингибировала биологическую активность функционального варианта. Предпочтительно, чтобы неконсервативная аминокислотная замена повышала биологическую активность функционального варианта, чтобы биологическая активность функционального варианта увеличивалась по сравнению с родительским РЕ или химерной молекулой.
[0182] РЕ или химерная молекула согласно изобретению может состоять по существу из указанной аминокислотной последовательности или последовательностей, описанных в данном документе, так, чтобы другие компоненты функционального варианта, например, другие аминокислоты, не приводили к существенному изменению биологической активности функционального варианта.
[0183] РЕ или химерная молекула согласно изобретению (в том числе функциональные части и функциональные варианты) согласно данному изобретению могут содержать синтетические аминокислоты вместо одной или более чем одной природной аминокислоты. Такие синтетические аминокислоты известны в данной области и включают, например, аминоциклогексанкарбоновую кислоту, норлейцин, α-амино-н-декановую кислоту, гомосерин, S-ацетиламинометилцистеин, транс-3- и транс-4-гидроксипролин, 4-аминофенилаланин, 4-нитрофенилаланин, 4-хлорофенилаланин, 4-карбоксифенилаланин, β-фенилсерин, β-гидроксифенилаланин, фенилглицин, α-нафтилаланин, циклогексилаланин, циклогексилглицин, индолин-2-карбоновую кислоту, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, аминомалоновую кислоту, моноамид аминомалоновой кислоты, N'-бензил-N'-метиллизин, N',N'-дибензиллизин, 6-гидроксилизин, орнитин, α-аминоциклопентанкарбоновую кислоту, α-аминоциклогексанкарбоновую кислоту, α-аминоциклогептанкарбоновую кислоту, α-(2-амино-2-норборнан)карбоновую кислоту, α,γ-диаминомасляную кислоту, α,β-диаминопропионовую кислоту, гомофенилаланин и α-трет-бутилглицин.
[0184] РЕ или химерная молекула согласно изобретению (в том числе функциональные части и функциональные варианты) могут быть гликозилированы, амидированы, карбоксилированы, фосфорилированы, этерифицированы, N-ацилированы, циклизованы, например, через дисульфидный мостик, или превращены в соль присоединения кислоты и/или, возможно, димеризованы или полимеризованы или конъюгированы.
[0185] Воплощение данного изобретения относится к способу получения РЕ согласно изобретению, включающему (а) рекомбинантную экспрессию РЕ и (b) очистку РЕ. РЕ и химерные молекулы согласно изобретению (в том числе функциональные части и функциональные варианты) могут быть получены с помощью способов получения белков и полипептидов, известных в данной области. Подходящие способы синтеза полипептидов и белков de novo описаны в таких документах как Chan et al., Fmoc Solid Phase Peptide Synthesis, Oxford University Press, Oxford, United Kingdom, 2005; Peptide and Protein Drug Analysis, ed. Reid, R., Marcel Dekker, Inc., 2000; Epitope Mapping, ed. Westwood et al., Oxford University Press, Oxford, United Kingdom, 2000; и патент США 5449752. Кроме того, РЕ и химерные молекулы согласно изобретению могут быть рекомбинантно экспрессированы с помощью нуклеиновых кислот, описанных в данном документе, с использованием стандартных рекомбинантных способов. См, например, Sambrook et al., Molecular Cloning: A Laboratory Manual, 3rd ed., Cold Spring Harbor Press, Cold Spring Harbor, NY 2001; и Ausubel et al., Current Protocols in Molecular Biology, Greene Publishing Associates and John Wiley & Sons, NY, 1994.
[0186] Данный способ также содержит очистку РЕ. После экспрессии РЕ согласно изобретению могут быть очищены в соответствии с методиками очистки, известными в данной области. Примеры способов очистки включают, но не ограничиваясь ими, осаждение сульфатом аммония, аффинные колонки и колоночную хроматографию или процедуры, описанные, например, в R. Scopes, Protein Purification, Springer-Verlag, NY (1982).
[0187] Другое воплощение данного изобретения относится к способу получения химерной молекулы согласно изобретению, включающему (а) рекомбинантную экспрессию химерной молекулы и (b) очистку химерной молекулы. Химерная молекула может быть рекомбинантно экспрессирована и очищена, как описано в данном документе в отношении других аспектов изобретения. В одном из воплощений согласно изобретению рекомбинантная экспрессия химерной молекулы включает вставление нуклеотидной последовательности, кодирующей специфическую группировку, и нуклеотидной последовательности, кодирующей РЕ, в вектор. Способ может включать вставление нуклеотидной последовательности, кодирующей специфическую группировку, и нуклеотидной последовательности, кодирующей РЕ, в рамку таким образом, что она кодирует один непрерывный полипептид, включающий функциональную область специфической группировки и функциональную область РЕ. В одном из воплощений согласно изобретению способ включает лигирование нуклеотидной последовательности, кодирующей РЕ, с нуклеотидной последовательностью, кодирующей специфическую группировку, таким образом, что при экспрессии РЕ находится на карбоксильном конце специфической группировки. В альтернативном воплощении способ включает лигирование нуклеотидной последовательности, кодирующей РЕ, с нуклеотидной последовательностью, кодирующей специфическую группировку, таким образом, что при экспрессии РЕ находится на амино-конце специфической группировки.
[0188] Еще одно воплощение данного изобретения относится к способу получения химерной молекулы согласно изобретению, включающему (а) рекомбинантную экспрессию РЕ согласно изобретению, (b) очистку РЕ и (с) ковалентное связывание специфической группировки с очищенным РЕ. РЕ согласно изобретению может быть рекомбинантно экспрессирован, как описано в данном документе в отношении других аспектов изобретения. Способ также включает ковалентное связывание специфической группировки с очищенным РЕ. Способ присоединения РЕ к специфической группировке может варьировать в зависимости от химической структуры специфической группировки. Например, способ может включать взаимодействие любой одной или более чем одной из множества функциональных групп, например, карбоксильной (СООН), аминной (-NH2) или сульфгидрильной (-SH) группы, присутствующей на РЕ, с подходящей функциональной группой специфической группировки, и, тем самым, формирование ковалентной связи между РЕ и специфической группировкой. Альтернативно или дополнительно в способ можно включить дериватизацию специфической группировки или РЕ, чтобы экспонировать или прикрепить дополнительные реакционноспособные функциональные группы. Дериватизация может также включать присоединение одного или более чем одного линкера к специфической группировке или РЕ.
[0189] В другом воплощении данного изобретения РЕ и химерные молекулы согласно изобретению могут быть получены с использованием нерекомбинантных способов. Например, РЕ согласно изобретению и химерные молекулы, описанные в данном документе (включая функциональные части и функциональные варианты), могут быть коммерчески синтезированы компаниями, такими как Synpep (Дублин, Калифорния), Peptide Technologies Corp. (Гейтерсберг, Мэриленд) и Multiple Peptide Systems (Сан-Диего, Калифорния). В связи с этим РЕ и химерные молекулы согласно изобретению могут быть синтетическими, рекомбинантными, выделенными и/или очищенными.
[0190] В некоторых обстоятельствах может быть желательным освобождение РЕ от специфической группировки, когда химерная молекула достигает одной или более чем одной клетки-мишени. В связи с этим химерные молекулы согласно изобретению могут содержать расщепляемый линкер. Линкер может расщепляться с помощью любых подходящих средств, например, ферментативно. Например, когда клетка-мишень представляет собой раковую (например, опухолевую) клетку, химерная молекула может включать линкер, расщепляемый в условиях, присутствующих в месте опухоли (например, при воздействии ассоциированных с опухолью ферментов или кислого pH).
[0191] Воплощение данного изобретения относится к нуклеиновой кислоте, содержащей нуклеотидную последовательность, кодирующую любой из РЕ согласно изобретению или химерных молекул, описанных в данном документе. Термин "нуклеиновая кислота", используемый в данном документе, включает "полинуклеотид", "олигонуклеотид" и "нуклеиновокислотную молекулу" и, как правило, означает полимер ДНК или РНК, который может быть одноцепочечным или двухцепочечным, который может быть синтезированным или полученным (например, выделенным и/или очищенным) из природных источников, который может содержать природные, неприродные или измененные нуклеотиды, и который может содержать природные, неприродные или измененные межнуклеотидные связи, такие как фосфорамидатные связи или фосфоротиоатные связи вместо фосфодиэфирных, находящихся между нуклеотидами в немодифицированном олигонуклеотиде. В общем случае предпочтительно, чтобы нуклеиновая кислота не содержала никаких вставок, делеций, инверсий и/или замен. Тем не менее, в некоторых случаях может быть пригодным, как описано в данном документе, чтобы нуклеиновая кислота содержала одну или более чем одну вставку, делецию, инверсию и/или замену.
[0192] Предпочтительно, нуклеиновые кислоты согласно данному изобретению являются рекомбинантными. Используемый в данном документе термин "рекомбинантный" относится к (i) молекулам, которые сконструированы вне живых клеток путем соединения природных или синтетических нуклеиновокислотных сегментов, или (ii) молекулам, которые являются результатом репликации описанных выше в (i). Для целей согласно данному изобретению репликация может представлять собой репликацию in vitro или репликацию in vivo.
[0193] Нуклеиновые кислоты могут быть сконструированы на основе химического синтеза и/или ферментативных реакций лигирования с использованием процедур, известных в данной области. См., например, Sambrook et al., см. выше, и Ausubel et al., см. выше. Например, нуклеиновая кислота может быть химически синтезирована с использованием природных нуклеотидов или различным образом модифицированных нуклеотидов, предназначенных для повышения биологической стабильности молекул или для увеличения физической стабильности дуплекса, формирующегося при гибридизации (например, фосфоротиоатные производные и акридин-замещенные нуклеотиды). Примеры модифицированных нуклеотидов, которые могут быть использованы для создания нуклеиновых кислот, включают, но не ограничиваясь ими, 5-фторурацил, 5-бромурацил, 5-хлорурацил, 5-йодурацил, гипоксантин, ксантин, 4-ацетилцитозин, 5-(карбоксигидроксиметил)урацил, 5-карбоксиметиламинометил-2-тиоуридин, 5-карбоксиметиламинометилурацил, дигидроурацил, бета-D-галактозилквеуозин, инозин, N6-изопентениладенин, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-замещенный аденин, 7-метилгуанин, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, бета-D-маннозилквеуозин, 5'-метоксикарбоксиметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусную кислоту (v), вибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, сложный метиловый эфир урацил-5-оксиуксусной кислоты, 3-(3-амино-3-N-2-карбоксипропил)урацил и 2,6-диаминопурин. Альтернативно, одна или более чем одна из нуклеиновых кислот согласно изобретению может быть приобретена у таких компаний как Macromolecular Resources (Форт-Коллинс, Колорадо) и Synthegen (Хьюстон, Техас).
[0194] Данное изобретение также относится к нуклеиновой кислоте, содержащей нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности любой из нуклеиновых кислот, описанных в данном документе, или нуклеотидную последовательность, которая гибридизуется в жестких условиях с нуклеотидной последовательностью любой из нуклеиновых кислот, описанных в данном документе.
[0195] Нуклеотидная последовательность, которая гибридизуется в жестких условиях, предпочтительно гибридизуется в условиях высокой жесткости. Под "условиями высокой жесткости" подразумевается, что нуклеотидная последовательность специфически гибридизуется с последовательностью-мишенью (нуклеотидной последовательностью любой из нуклеиновых кислот, описанных в данном документе) в количестве, которое проявляется сильнее, чем неспецифическая гибридизация. Условия высокой жесткости включают условия, которые отличают полинуклеотид с точной комплементарной последовательностью или полинуклеотид, содержащий лишь несколько разрозненных несовпадений, от случайной последовательности, которая имеет лишь несколько коротких областей (например, 3-10 оснований), которые совпадают с нуклеотидной последовательностью. Такие небольшие области комплементарности более легко плавятся, чем полноразмерный комплемент из 14-17 или более оснований, а гибридизация в условиях высокой жесткости позволяет их легко отличить. Условия относительно высокой жесткости будут включать, например, низкое содержание солей и/или высокую температуру, например, примерно 0,02-0,1 М NaCl или эквивалент этого, при температуре примерно от 50 до 70°C. Такие условия высокой жесткости слабо переносят несоответствия, если таковые имеются, между нуклеотидной последовательностью и матрицей или нитью-мишенью, и особенно пригодны для определения экспрессии любого из РЕ или химерных молекул согласно изобретению. Как правило, можно учитывать, что условия можно сделать более жесткими путем добавления возрастающих количеств формамида.
[0196] Данное изобретение также относится к нуклеиновой кислоте, содержащей нуклеотидную последовательность, которая имеет примерно 70% или более, например, примерно 80% или более, примерно 90% или более, примерно 91% или более, примерно 92% или более, примерно 93% или более, примерно 94% или более, примерно 95% или более, примерно 96% или более, примерно 97% или более, примерно 98% или более, или примерно 99% или более идентичности с любой из нуклеиновых кислот, описанных в данном документе.
[0197] Нуклеиновые кислоты согласно изобретению могут быть вставлены в рекомбинантный экспрессионный вектор. В связи с этим данное изобретение относится к рекомбинантным экспрессионным векторам, содержащим любую из нуклеиновых кислот согласно изобретению. В данном описании термин "рекомбинантный экспрессионный вектор" означает генетически модифицированную олигонуклеотидную или полинуклеотидную конструкцию, которая позволяет экспрессировать мРНК, белок, полипептид или пептид клеткой-хозяином, когда конструкция содержит нуклеотидную последовательность, кодирующую мРНК, белок, полипептид или пептид, и вектор вводят в контакт с клеткой в условиях, достаточных для того, чтобы мРНК, белок, полипептид или пептид экспрессировались в клетке. Векторы согласно изобретению не встречаются в природе целиком. Тем не менее, некоторые части векторов могут иметь природное происхождение. Рекомбинантные экспрессионные векторы согласно изобретению могут содержать любой тип нуклеотидов, в том числе, но не ограничиваясь ими, ДНК и РНК, которые могут быть одноцепочечными или двухцепочечными, которые могут быть синтезированными или полученными из природных источников, и которые могут содержать природные, неприродные или измененные нуклеотиды. Рекомбинантные экспрессионные векторы могут включать природные, неприродные межнуклеотидные связи или оба типа связей. Предпочтительно, неприродные или измененные нуклеотиды или межнуклеотидные связи не препятствуют транскрипции или репликации вектора.
[0198] Рекомбинантный экспрессионный вектор согласно изобретению может представлять собой любой подходящий рекомбинантный экспрессионный вектор и может быть использован для трансформации или трансфекции любой подходящей клетки-хозяина. Подходящие векторы включают те, которые предназначены для экспансии и размножения или для экспрессии плазмид и вирусов, или для того и другого. Вектор может быть выбран из группы, состоящей из серии pUC (Fermentas Life Sciences), серии pBluescript (Stratagene, Ла-Холья, Калифорния), серии pET (Novagen, Мэдисон, Висконсин), серия pGEX (Pharmacia Biotech, Уппсала, Швеция) и серии рЕХ (Clontech, Пало-Альто, Калифорния). Также могут быть использованы бактериофаговые векторы, такие как λGT10, λGT11, λZapll (Stratagene), λEMBL4 и λNM1149. Примеры векторов для экспрессии в растениях включают pBI01, pBI101.2, pBI101.3, pBI121 и pBIN19 (Clontech). Примеры векторов для экспрессии в животных включают pEUK-Cl, pMAM и pMAMneo (Clontech). Предпочтительно, рекомбинантный экспрессионный вектор представляет собой вирусный вектор, например, ретровирусный вектор.
[0199] Рекомбинантные экспрессионные векторы согласно изобретению могут быть получены с использованием стандартных методик рекомбинантной ДНК, описанных, например, в Sambrook et al., см. выше, и Ausubel et al., см. выше. Конструкции экспрессионных векторов, которые являются кольцевыми или линейными, могут быть сделаны таким образом, чтобы содержать систему репликации, функционирующую в прокариотической или эукариотической клетке-хозяине. Системы репликации могут быть получены, например, из ColEl, плазмиды 2 μ, λ, SV40, вируса бычьей папилломы и т.п.
[0200] Желательно, чтобы рекомбинантный экспрессионный вектор содержал регуляторные последовательности, такие как кодоны инициации и терминации транскрипции и трансляции, которые являются специфическими для типа хозяина (например, бактерии, грибы, растения или животные), в которого должен быть введен вектор, в зависимости от обстоятельств и с учетом того, имеет ли вектор ДНК- или РНК-основу.
[0201] Рекомбинантный экспрессионный вектор может включать один или более чем один маркерный ген, который позволяет выбирать трансформированных или трансфицированных хозяев. Маркерные гены включают устойчивость к биоцидам, например, устойчивость к антибиотикам, тяжелым металлам и т.д., комплементацию в ауксотрофном хозяине для получения прототрофии и т.п. Подходящие гены-маркеры для экспрессионных векторов согласно изобретению включают, например, гены устойчивости к неомицину/G418, гены устойчивости к гигромицину, гены устойчивости к гистидинолу, гены устойчивости к тетрациклину, а также гены устойчивости к ампициллину.
[0202] Рекомбинантный экспрессионный вектор может содержать нативный или ненативнный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей РЕ или химерную молекулу согласно изобретению (в том числе функциональные части и функциональные варианты), или с нуклеотидной последовательностью, которая комплементарна или которая гибридизуется с нуклеотидной последовательностью, кодирующей РЕ или химерную молекулу. Специалист в данной области способен выбрать промотор, например, сильный, слабый, индуцируемый, тканеспецифический и специфический к стадии развития. Аналогичным образом, объединение нуклеотидной последовательности с промотором также находится в пределах квалификации специалиста в данной области. Промотор может быть невирусным промотором или вирусным промотором, например, цитомегаловирусным (CMV) промотором, промотором SV40, промотором RSV или промотором, находящимся в длинном концевом повторе вируса мышиных стволовых клеток.
[0203] Рекомбинантные экспрессионные векторы согласно изобретению могут быть сконструированы либо для временной экспрессии, для стабильной экспрессии, либо для обоих вариантов экспрессии. Кроме того, рекомбинантные экспрессионные векторы могут быть сделаны для конститутивной экспрессии или для индуцируемой экспрессии.
[0204] Еще одно воплощение данного изобретения также относится к клетке-хозяину, содержащей любой из рекомбинантных экспрессионных векторов, описанных в данном документе. Используемый в данном документе термин "клетка-хозяин" относится к любому типу клеток, который может содержать рекомбинантный экспрессионный вектор согласно изобретению. Клетка-хозяин может быть эукариотической клеткой, например, клеткой растения, животного, гриба или водоросли, или может быть прокариотической клеткой, например, бактерией или простейшим. Клетка-хозяин может быть культивируемой клеткой, прикрепленной клеткой или суспендированной клеткой, т.е. клеткой, которая растет в суспензии. Для получения рекомбинантного РЕ или химерной молекулы согласно изобретению клетка-хозяин предпочтительно является прокариотической клеткой, например, клеткой Е. coli.
[0205] Данное изобретение также относится к популяции клеток, содержащей по меньшей мере одну клетку-хозяина, описанную в данном документе. Популяция клеток может быть гетерогенной популяцией, содержащей клетку-хозяина с любым из описанных рекомбинантных экспрессионных векторов в дополнение по меньшей мере к одной другой клетке, например, клетке-хозяину, которая не содержит никаких рекомбинантных экспрессионных векторов. Альтернативно, популяция клеток может быть по существу гомогенной популяцией, где указанная популяция содержит в основном (например, по существу состоит из) клетки-хозяева, содержащие рекомбинантный экспрессионный вектор. Популяция также может быть клональной популяцией клеток, когда все клетки популяции являются клонами одной клетки-хозяина, содержащей рекомбинантный экспрессионный вектор, так что все клетки популяции содержат рекомбинантный экспрессионный вектор. В одном из воплощений согласно изобретению популяция клеток является клональной популяцией клетки-хозяина, содержащей рекомбинантный экспрессионный вектор, описанный в данном документе.
[0206] РЕ, химерные молекулы (в том числе функциональные части и функциональные варианты), нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева (в том числе их популяции) и популяции клеток согласно изобретению могут быть выделены и/или очищены. Термин "выделенный", используемый в данном документе, означает "извлеченный из природной среды". Термин "очищенный", используемый в данном документе, означает повышенную чистоту, где "чистота" является относительным термином и не должна быть обязательно истолкована как абсолютная чистота. Например, чистота может составлять примерно 50% или более, примерно 60% или более, примерно 70% или более, примерно 80% или более, примерно 90% или более, или примерно 100%. Чистота предпочтительно составляет примерно 90% или более (например, от примерно 90% до примерно 95%), а более предпочтительно примерно 98% или более (например, от примерно 98% до примерно 99%).
[0207] РЕ, химерные молекулы (в том числе функциональные части и функциональные варианты), нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева (в том числе их популяции) и популяции клеток согласно изобретению, которые далее все вместе называются "РЕ-материалами согласно изобретению", могут быть включены в состав композиции, такой как фармацевтическая композиция. В связи с этим данное изобретение относится к фармацевтической композиции, содержащей любой из РЕ, химерных молекул (включая функциональные части и функциональные варианты), нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев (включая их популяции) и популяций клеток и фармацевтически приемлемый носитель. Фармацевтическая композиция согласно изобретению, содержащая любой из предлагаемых в изобретении РЕ-материалов, может содержать более чем один РЕ-материал согласно изобретению, например, полипептид и нуклеиновую кислоту, или два или более двух различных РЕ. Альтернативно, фармацевтическая композиция может включать РЕ-материал согласно изобретению в комбинации с одним или более чем одним другим фармацевтически активным агентом или препаратом, таким как химиотерапевтический агент, например, аспарагиназа, бусульфан, карбоплатин, цисплатин, даунорубицин, доксорубицин, фторурацил, гемцитабин, гидроксимочевина, метотрексат, паклитаксел, ритуксимаб, винбластин, винкристин и т.п.
[0208] Предпочтительно, носитель представляет собой фармацевтически приемлемый носитель. Что касается фармацевтических композиций, носитель может быть любым из обычно используемых носителей и ограничен только физико-химическими соображениями, такими как растворимость и отсутствие реакционной способности в отношении активного соединения (соединений), а также путем введения. Фармацевтически приемлемые носители, описанные в данном документе, например, носители, адъюванты, эксципиенты и разбавители, хорошо известны специалистам в данной области и легко доступны. Предпочтительно, фармацевтически приемлемый носитель является таким, который химически инертен по отношению к активному агенту (агентам), и таким, который не имеет вредных побочных эффектов или токсичности в условиях применения.
[0209] Выбор носителя частично будет определяться конкретным РЕ-материалом согласно изобретению, а также конкретным способом, используемым для введения РЕ-материала согласно изобретению. Соответственно, существует множество подходящих составов фармацевтической композиции согласно данному изобретению. Следующие препараты для парентерального (например, подкожного, внутривенного, внутриартериального, внутримышечного, внутрикожного, внутрибрюшинного и интратекального), перорального и аэрозольного введения являются иллюстративными и никоим образом не ограничивающими. Для введения РЕ-материалов согласно изобретению может быть использован более чем один путь, а в некоторых случаях конкретный путь может обеспечить более быстрый и более эффективный ответ, чем другой путь.
[0210] Составы для местного применения хорошо известны специалистам в данной области. Такие составы особенно пригодны в контексте данного изобретения для нанесения на кожу.
[0211] Составы, пригодные для перорального введения, могут включать (а) жидкие растворы, такие как эффективное количество РЕ-материала согласно изобретению, растворенное в разбавителе, таком как вода, физиологический раствор или апельсиновый сок; (b) капсулы, саше, таблетки, леденцы и пастилки, каждая из которых содержит определенное количество активного ингредиента в виде твердого вещества или гранул; (с) порошки; (g) суспензии в подходящей жидкости; и (е) подходящие эмульсии. Жидкие составы могут включать разбавители, такие как воду и спирты, например, этанол, бензиловый спирт и полиэтиленовые спирты, с добавлением или без добавления фармацевтически приемлемого поверхностно-активного вещества. Капсульные формы могут быть обычными капсулами в твердой или мягкой желатиновой оболочке, содержащими, например, поверхностно-активные вещества, смазывающие вещества и инертные наполнители, такие как лактоза, сахароза, фосфат кальция и кукурузный крахмал. Таблетированные формы могут включать одно или более чем одно вещество из лактозы, сахарозы, маннита, кукурузного крахмала, картофельного крахмала, альгиновой кислоты, микрокристаллической целлюлозы, аравийской камеди, желатина, гуаровой камеди, коллоидного диоксида кремния, кроскармеллозы натрия, талька, стеарата магния, стеарата кальция, стеарата цинка, стеариновой кислоты и других эксципиентов, красителей, разбавителей, буферных агентов, дезинтегрирующих агентов, увлажняющих агентов, консервантов, ароматизаторов и других фармакологически приемлемых эксципиентов. Леденцовые формы могут включать РЕ-материал согласно изобретению во вкусовом агенте, как правило, в сахарозе и аравийской камеди или трагаканте, как и пастилки, содержащие РЕ-материал согласно изобретению в инертной основе, такой как желатин и глицерин или сахароза и гуммиарабик, эмульсии, гели и т.п., дополнительно содержащие такие эксципиенты, которые хорошо известны в данной области.
[0212] РЕ-материал согласно изобретению, используемый в одиночку или в комбинации с другими подходящими компонентами, может быть превращен в аэрозольные составы для введения посредством ингаляции. Эти аэрозольные составы могут быть помещены в находящиеся под давлением подходящие пропелленты, такие как дихлордифторметан, пропан, азот и т.п. Аэрозольные составы также могут быть приготовлены в виде фармацевтических препаратов для введения не под давлением, например, с помощью небулайзера или атомайзера. Такие составы-спреи также могут быть использованы для распыления на слизистую оболочку.
[0213] Составы, пригодные для парентерального введения, включают водные и неводные изотонические стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатические факторы и растворенные вещества, которые делают состав изотоничным крови предполагаемого реципиента, а также водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты, солюбилизаторы, загустители, стабилизаторы и консерванты. РЕ-материал согласно изобретению может быть введен в физиологически приемлемом разбавителе в фармацевтическом носителе, таком как стерильная жидкость или смесь жидкостей, включая воду, физиологический раствор, водные растворы декстрозы и родственных сахаров, спирт, такой как этанол или гексадециловый спирт, гликоль, такой как пропиленгликоль или полиэтиленгликоль, диметилсульфоксид, глицерин, кеталь, такой как 2,2-диметил-1,3-диоксолан-4-метанол, простые эфиры, полиэтиленгликоль 400, масла, жирные кислоты, сложные эфиры или глицериды жирных кислот или ацетилированные глицериды жирных кислот с добавлением или без добавления фармацевтически приемлемого поверхностно-активного вещества, такого как мыло или детергент, суспендирующий агент, такой как пектин, карбомеры, метилцеллюлозу, гидроксипропилметилцеллюлозу или карбоксиметилцеллюлозу, или эмульгирующие агенты и другие фармацевтические адъюванты.
[0214] Масла, которые могут быть использованы в композициях для парентерального введения, включают минеральные масла, масла животного и растительного происхождения или синтетические масла. Конкретные примеры масел включают арахисовое, соевое, кунжутное, хлопковое, кукурузное, оливковое, вазелиновое и минеральное. Подходящие жирные кислоты для применения в составах для парентерального введения включают олеиновую кислоту, стеариновую кислоту и изостеариновую кислоту. Этилолеат и изопропилмиристат являются примерами подходящих сложных эфиров жирных кислот.
[0215] Подходящие мыла для применения в составах для парентерального введения включают жирнокислотные соли щелочных металлов, аммония и триэтаноламина, а подходящие детергенты включают (а) катионные детергенты, такие как, например, диметилдиалкиламмония галогениды и алкилпиридина галогениды, (b) анионные детергенты, такие как, например, алкил-, арил- и олефинсульфонаты, алкил-, олефин-, эфир- и моноглицеридсульфаты и сульфосукцинаты, (с) неионные детергенты, такие как, например, оксиды жирных аминов, алканоламиды жирных кислот и сополимеры полиоксиэтиленполипропилена, (d) амфотерные детергенты, такие как, например, алкил-β-аминопропионаты и 2-алкилимидазолина четвертичные аммониевые соли, и (d) их смеси.
[0216] Составы для парентерального введения, как правило, будут содержат от примерно 0,5% до примерно 25% по массе РЕ-материала согласно изобретению в растворе. Могут быть использованы консерванты и буферы. Для того чтобы свести к минимуму или устранить раздражение в месте инъекции, такие композиции могут содержать одно или более чем одно неионогенное поверхностно-активное вещество, имеющее гидрофильно-липофильный баланс (hydrophile-lipophile balance, HLB) от примерно 12 до примерно 17. Количество поверхностно-активного вещества в таких составах, как правило, находится в диапазоне от примерно 5% до примерно 15% по весу. Подходящие поверхностно-активные вещества включают полиэтиленгликолевые эфиры сорбита и жирной кислоты, такие как сорбитан моноолеат и высокомолекулярный продукт присоединения этиленоксида с гидрофобным основанием, образованный путем конденсации пропиленоксида с пропиленгликолем. Составы для парентерального введения могут быть представлены в единичной дозе или в многодозовых герметичных контейнерах, таких как ампулы и пузырьки, и могут храниться в лиофилизированном (высушенном замораживанием) состоянии, требующем только добавления стерильного жидкого эксципиента, например, воды для инъекций, непосредственно перед применением. Растворы и суспензии для инъекций, которые готовят непосредственно перед применением, могут быть приготовлены из стерильных порошков, гранул и таблеток типа таких, которые описаны ранее. Требования, предъявляемые к эффективным фармацевтическим носителям для парентеральных композиций, хорошо известны специалистам в данной области (см., например, Pharmaceutics and Pharmacy Practice, J.B. Lippincott Company, Philadelphia, PA, Banker and Chalmers, eds., страницы 238-250 (1982), и ASHP Handbook on Injectable Drugs, Toissel, 4th ed., страницы 622-630 (1986)).
[0217] Специалистам в данной области будет понятно, что в дополнение к описанным выше фармацевтическим композициям РЕ-материал согласно данному изобретению может быть приготовлен в виде комплексов включения, таких как комплексы включения циклодекстринов, или липосом.
[0218] Для целей данного изобретения количество или доза вводимого РЕ-материала согласно изобретению должны быть достаточными для осуществления у млекопитающего желаемого ответа, например, терапевтического или профилактического ответа, в течение разумного периода времени. Например, доза РЕ-материала согласно изобретению должна быть достаточной для ингибирования роста клетки-мишени или лечения или профилактики рака в течение периода примерно от 2 часов или дольше, например, от 12 до 24 и более часов с момента введения. В некоторых воплощениях период времени может быть даже больше. Доза будет определяться эффективностью конкретного РЕ-материала согласно изобретению и состоянием млекопитающего (например, человека), а также массой тела млекопитающего (например, человека), подлежащего лечению.
[0219] В данной области известно много анализов для определения вводимой дозы. Вводимая доза может быть определена in vitro (например, на клеточных культурах) или in vivo (например, исследования на животных). Например, вводимая доза может быть определена путем определения IC50 (дозы, которая позволяет достичь половины максимального ингибирования симптомов), LD50 (дозы, летальной для 50% популяции), ED50 (дозы, терапевтически эффективной для 50% популяции), а также терапевтического индекса в культуре клеток и/или в исследованиях на животных. Терапевтический индекс представляет собой отношение LD50 к ED50 (т.е. LD50/ED50).
[0220] Доза РЕ-материала согласно изобретению также будет определяться наличием, природой и степенью каких-либо неблагоприятных побочных эффектов, которые могут сопровождать введение конкретного РЕ-материала согласно изобретению. Как правило, лечащий врач будет определять дозировку РЕ-материала согласно изобретению, которым он будет лечить каждого отдельного пациента, принимая во внимание различные факторы, такие как возраст, масса тела, общее состояние здоровья, диета, пол, РЕ-материал для введения согласно изобретению, путь введения, а также тяжесть состояния, подлежащего лечению. В качестве примера и без намерения ограничить изобретение, доза РЕ-материала согласно изобретению может составлять от примерно 0,001 до примерно 1000 мг/кг массы тела субъекта, подлежащего лечению, в день, от примерно 0,01 до примерно 10 мг/кг массы тела/день, от примерно 0,01 мг до примерно 1 мг/кг массы тела/день, от примерно 1 до примерно 1000 мг/кг массы тела/день, от примерно 5 до примерно 500 мг/кг массы тела/день, от примерно 10 до примерно 250 мг/кг массы тела/день, от примерно 25 до примерно 150 мг/кг массы тела/день, или примерно 10 мг/кг массы тела/день.
[0221] Альтернативно РЕ-материалы согласно изобретению могут быть переведены в депо-форму, так что способ, в котором РЕ-материал согласно изобретению выпускается в организм, в который его вводят, контролируется временем и расположением в пределах организма (см., например, патент США 4450150). Депо-формы РЕ-материалов согласно изобретению могут представлять собой, например, имплантируемую композицию, содержащую РЕ-материалы согласно изобретению и пористый или непористый материал, такой как полимер, где РЕ-материал согласно изобретению инкапсулирован или рассеян по всему материалу и/или возникает при деградации непористого материала. Затем депо имплантируют в нужное место в организме и РЕ-материалы согласно изобретению высвобождаются из имплантата с заданной скоростью.
[0222] РЕ-материалы согласно изобретению могут быть исследованы на цитотоксичность с помощью анализов, известных в данной области. Примеры анализов цитотоксичности включают WST-анализ, который измеряет пролиферацию клеток с использованием тетразолиевой соли WST-1 (реагенты и наборы, доступные от Roche Applied Sciences), как описано в публикации международной патентной заявки WO 2011/032022.
[0223] Предполагается, что фармацевтические композиции, РЕ, химерные молекулы, нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева или популяции клеток согласно изобретению могут быть использованы в способах лечения или профилактики рака. Не связываясь с конкретной теорией или механизмом, полагают, что РЕ согласно изобретению разрушают или ингибируют рост клеток посредством ингибирования синтеза белка в эукариотических клетках, например, путем инактивации АДФ-рибозилирования фактора элонгации 2 (EF-2). Без связи с конкретной теорией или механизмом, химерные молекулы согласно изобретению распознают и специфически связываются с маркерами клеточной поверхности, тем самым доставляя цитотоксический РЕ к популяции клеток, экспрессирующих маркер клеточной поверхности, с минимальной перекрестной реактивностью или вообще без нее в отношении клеток, которые не экспрессируют маркер клеточной поверхности. Таким образом, цитотоксичность РЕ может быть направлена на уничтожение или ингибирование роста определенной популяции клеток, например, раковых клеток. В связи с этим данное изобретение относится к способу лечения или профилактики рака у млекопитающего, включающему введение млекопитающему любого из РЕ, химерных молекул, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций, описанных в данном документе, в количестве, эффективном для лечения или профилактики рака у млекопитающего.
[0224] Термины "лечить" и "предотвращать", а также их слова-производные, используемые в данном документе, не обязательно означают 100% или полное лечение или предотвращение (профилактику). Скорее, существуют различные степени лечения или профилактики, которые специалисты в данной области смогут распознать как имеющие потенциальное преимущество или терапевтический эффект. В этой связи способы согласно изобретению могут обеспечить некоторый уровень лечения или профилактики рака у млекопитающего. Кроме того, лечение или профилактика способом согласно изобретению могут включать лечение или профилактику одного или более чем одного из состояний или симптомов заболевания, например, рака, который лечат или предотвращают. Кроме того, для целей согласно данному изобретению термин "профилактика" может включать отсрочку начала заболевания или симптома или состояния.
[0225] В способах согласно данному изобретению, в которых вводят клетки-хозяева или популяции клеток, клетки могут быть аллогенны или аутологичны хозяину. Предпочтительно клетки являются аутологичными хозяину.
[0226] Что касается способов согласно изобретению, рак может представлять собой любой рак, включая любой из перечисленных: рак надпочечников, саркомы (например, синовиальная саркома, остеогенная саркома, лейомиосаркома матки, ангиосаркома, фибросаркома, рабдомиосаркома, липосаркома, миксома, рабдомиома, фиброма, липома и тератома), лимфомы (например, мелкоклеточная лимфоцитраная лимфома, лимфома Ходжкина и неходжкинская лимфома), гепатоцеллюлярная карцинома, глиома, злокачественные опухоли головы (например, плоскоклеточная карцинома), злокачественные опухоли шеи (например, плоскоклеточная карцинома), острый лимфоцитарный рак, лейкемии (например, волосатоклеточная лейкемия, миелоидная лейкемия (острая и хроническая), лимфолейкоз (острый и хронический), пролимфоцитарный лейкоз (prolymphocytic leukemia, PLL), миеломоноцитарный лейкоз (острый и хронический) и лимфоцитарный лейкоз (острый и хронический), рак кости (остеогенная саркома, фибросаркома, злокачественная фиброзная гистиоцитома, хондросаркома, саркома Юинга, злокачественная лимфома (ретикулярноклеточная саркома), множественная миелома, злокачественная гигантоклеточная опухоль, хордома, остеохондрома (костно-хрящевые экзостозы), доброкачественная хондрома, хондробластома, хондромиксоидная фиброма, остеоидная остеома и гигантоклеточная опухоль), рак головного мозга (астроцитома, медуллобластома, глиома, эпендимома, герминома (пинеалома), мультиформная глиобластома, олигодендроглиома, шваннома и ретинобластома), рак фаллопиевой трубы, рак молочной железы, рак заднего прохода, рак анального канала или рак прямой кишки, рак глаза, рак внутрипеченочных желчных протоков, рак суставов, рак шеи, желчного пузыря или плевры, рак носа, носовой полости или среднего уха, рак полости рта, рак вульвы (например, плоскоклеточная карцинома, интраэпителиальная карцинома, аденокарцинома и фибросаркома), миелопролиферативные нарушения (например, хронический миелоидный рак), рак толстой кишки (например, карцинома толстой кишки), рак пищевода (например, плоскоклеточная карцинома, аденокарцинома, леймиосаркома и лимфома), рак шейки матки (карцинома шейки матки и преинвазивная дисплазия шейки матки), рак желудка, желудочно-кишечная карциноидная опухоль, рак гортаноглотки, рак гортани, рак печени (например, гепатоцеллюлярная карцинома, холангиокарцинома, гепатобластома, ангиосаркома, гепатоцеллюлярная аденома и гемангиома), рак легких (например, бронхогенная карцинома (плоскоклеточная, недифференцированная мелкоклеточная, недифференцированная крупноклеточная и аденокарцинома), альвеолярная (бронхиолярная) карцинома, бронхиальная аденома, хондроматозная гамартома, мелкоклеточный рак легкого, немелкоклеточный рак легкого и аденокарцинома легкого), мезотелиома, рак кожи (например, меланома, базально-клеточная карцинома, плоскоклеточная карцинома, саркома Капоши, невусы, диспластические невусы, липома, ангиома, фиброма кожи и келоиды), множественная миелома, рак носоглотки, рак яичников (например, карцинома яичников (серозная цистаденокарцинома, муцинозная цистаденокарцинома, эндометриоидная карцинома и светлоклеточная аденокарцинома), гранулезотекаклеточные опухоли, опухоли из клеток Сертоли-Лейдига, дисгерминома и злокачественная тератома), рак поджелудочной железы (например, протоковая аденокарцинома, инсулинома, глюкагонома, гастринома, карциноидные опухоли и ВИПома), рак брюшины, сальника, брыжейки, рак глотки, рак предстательной железы (например, аденокарцинома и саркома), рак прямой кишки, рак почки (например, аденокарцинома, опухоль Вильмса (нефробластома) и почечно-клеточная карцинома), рак тонкого кишечника (аденокарцинома, лимфома, карциноидные опухоли, саркома Капоши, лейомиома, гемангиома, липома, нейрофиброма и фиброма), рак мягких тканей, рак желудка (например, карцинома, лимфома и леймиосаркома), рак яичка (например, семинома, тератома, эмбриональная карцинома, тератокарцинома, хориокарцинома, саркома, опухоль из клеток Лейдига, фиброма, фиброаденома, аденоматоидные опухоли и липома), рак матки (например, карцинома эндометрия), рак щитовидной железы и уротелиальные злокачественные опухоли (например, плоскоклеточная карцинома, переходно-клеточная карцинома, аденокарцинома, рак мочеточника и рак мочевого пузыря).
[0227] Используемый в данном документе термин "млекопитающее" относится к любому млекопитающему, включая, но не ограничиваясь ими, млекопитающих отряда Rodentia, таких как мыши и хомяки, и млекопитающих отряда Logomorpha, таких как кролики. Предпочтительно, чтобы млекопитающие были из отряда Carnivora, включая Felines (кошки) и Canines (собаки). Более предпочтительно, чтобы млекопитающие были из отряда Artiodactyla, включая Bovines (коровы) и Swines (свиньи), или из отряда Perssodactyla, включая Equines (лошади). Наиболее предпочтительно, чтобы млекопитающие были из отряда Primates, Ceboids или Simoids (обезьяны) или отряда Anthropoids (люди и человекообразные обезьяны). Особенно предпочтительным млекопитающим является человек.
[0228] Данное изобретение также относится к способу ингибирования роста клетки-мишени, включающему контактирование клетки с РЕ, выбранным среди любых РЕ, химерных молекул, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций, описанных в данном документе, в количестве, эффективном для ингибирования роста клетки-мишени. Рост клетки-мишени может быть подавлен на любое значение, например, примерно на 10% или более, примерно на 15% или более, примерно на 20% или более, примерно на 25% или более, примерно на 30% или более, примерно на 35% или более того, примерно на 40% или более, примерно на 45% или более, примерно на 50% или более, примерно на 55% или более, примерно на 60% или более, примерно на 65% или более, примерно на 70% или более, примерно на 75% или более, примерно на 80% или более, примерно на 85% или более, примерно на 90% или более, примерно на 95% или более, или примерно на 100%. Клетка-мишень может находиться в биологическом образце. Биологический образец может быть получен из млекопитающего любым подходящим способом и из любого подходящего источника. Биологический образец, например, может быть получен путем сбора крови, лейкафереза и/или биопсии опухоли или аутопсии. Контактирование может происходить in vitro или in vivo относительно млекопитающего. Предпочтительно, чтобы контактирование происходило in vitro.
[0229] В одном из воплощений согласно изобретению клетка-мишень представляет собой раковую клетку. Клетка-мишень может представлять собой раковую клетку любого из видов рака, описанных в данном документе. В одном из воплощений согласно изобретению мишень может экспрессировать маркер клеточной поверхности. Маркер клеточной поверхности может быть любым маркером клеточной поверхности, описанным в данном документе в отношении других аспектов изобретения. Маркер клеточной поверхности может быть, например, выбран из группы, состоящей из CD19, CD21, CD22, CD25, CD30, CD33, CD79b, рецептора трансферрина, EGF-рецептор, мезотелина, кадгерина и антигена Льюиса Y.
[0230] Следующие примеры дополнительно иллюстрируют изобретение, но, разумеется, их не следует рассматривать как каким-либо образом ограничивающие его объем.
Пример 1
[0231] В этом примере показана идентификация Т-клеточных эпитопов в домене III РЕ38.
[0232] Для идентификации Т-клеточных эпитопов в РЕ38 мононуклеарные клетки периферической крови (peripheral blood mononuclear cells, PBMC) сначала инкубировали с рекомбинантным иммунотоксином (от англ. recombinant immunotoxin - RIT) в течение 14 дней, чтобы RIT процессировался донорскими АРС до релевантных пептидов, которые будут представлены Т-клеткам. Затем обогащенные PBMC подвергали воздействию пептидной библиотеки, состоящей из 111 частично перекрывающихся пептидов, охватывающих последовательность РЕ38, и измеряли активацию Т-клеток с помощью анализа ELISpot для интерлейкина-2 (IL-2).
[0233] Анализировали образцы от 50 здоровых доноров без зарегистрированного предыдущего воздействия РЕ38 и с широким распределением аллелей человеческого лейкоцитарного антигена (human leukocyte antigen, HLA). Клетки этой популяции содержали наивный Т-клеточный эпитоп. Также были проанализированы образцы от девяти пациентов с мезотелиомой и от семи пациентов с волосатоклеточным лейкозом (HCL), которые ранее получали RIT на основе РЕ, и у которых развивались высокие уровни нейтрализующих антител. Клетки этой популяции содержали эпитопы Т-клеток памяти. Ответы наивных доноров и ранее лечившихся пациентов приведены в формате тепловой карты на фиг. 1А-1В.
[0234] Фиг. 1А представляет положительные и отрицательные ответы 50 наивных доноров. Ответы представлены в процентах реагирующих пятен для каждого донора. Самый сильный положительный ответ показан как более20%, ответы средней силы показаны как от 10% до 20%, слабые ответы показаны как от 3% до 10%, а отсутствие ответа (отрицательный ответ) показано как менее 3%. Результаты включали в общей сложности 258 положительных ответов, и 201 из них были слабыми (от 3 до 10%), 44 были средней силы (от 10 до 20%), и 13 были сильными (более20%), остальные 5292 ответа были отрицательными (менее 3%). Было получено 122 ответа на домен II (пептиды 1-38), включая 11 сильных, 24 ответа средней силы и 87 слабых ответов. Было получено 136 ответов на домен III (пептиды с 39 по 111), включая 2 сильных, 20 средних и 114 слабых ответов.
[0235] Пептиды 15 и 14 (в пуле 3) давали самые сильные и наиболее частые ответы в исследовании с 21 и 18 положительными ответами, соответственно. В общей сложности 36 пептидов не вызывали никакого ответа. 16 из 50 наивных доноров имели единственный эпитоп, дающий ответ, что показано одним, двумя или тремя ответами в перекрывающихся последовательных пептидах. Пятнадцать доноров имели два отдельных эпитопа, 14 имели три эпитопа, а пятеро имели четыре эпитопа. В 22 случаях скрининг положительного пула не дал специфического ответа на пептиды или не был сделан, что дало пять последовательных положительных ответов на тепловой карте.
[0236] Фиг. 1В представляет положительные и отрицательные ответы от девяти пациентов с мезотелиомой и от семи пациентов с HCL. У пациентов с мезотелиомой было установлено 919 отрицательных ответов и 80 ответов, включающих два сильных ответа (более20%), четыре ответа средней силы (от 10 до 20%) и 74 слабых ответа (от 3 до 10%). Два сильных ответа были вызваны пептидами 13 и 14, а ответы средней силы были вызваны пептидами 15, 35, 57 и 74. Тридцать пять из этих ответов были в домене II (пептиды с 1 по 38), а 45 - в домене III (пептиды с 38 по 111). Паттерн теплового пятна, созданный в карте, был похож на паттерн теплового пятна в карте наивных доноров. Способность отвечать (которая означает, сколько эпитопов было найдено для каждого пациента) была выше, чем паттерн доноров, при этом у одного пациента было два эпитопа, у четырех пациентов было три эпитопа, у двух пациентов было четыре эпитопа, и еще двух пациентов было пять эпитопов.
[0237] Кроме того, у семи пациентов с HCL было обнаружено три сильных ответа (более20%), девять ответов средней силы (от 10 до 20%), 37 слабых ответов (от 3 до 10%) и 728 отрицательных ответов (менее 3%). Все сильные ответы были в последовательных пептидах 75, 76 и 77. 22 ответа были в домене II, и 37 ответов были в домене III. Интересно отметить, что иммунодоминантный эпитоп в пептидах 14 и 15, который был идентифицирован более чем у 40% наивных доноров и 55% пациентов с мезотелиомой (пять из девяти образцов), не был обнаружен ни у одного из пациентов с HCL. Один пациент ответил на пептиды 12 и 13, которые имеют общие аминокислоты с пептидами 14 и 15. Тем не менее, непосредственно к пептидам 14 и 15 не было обнаружено никакой реакции. Это может быть связано со смещенным распределением HLA в образцах этих пациентов или с природой заболевания.
[0238] В целом, в РЕ38 было идентифицировано восемь основных эпитопов, на которые приходилось 93% ответов. Поскольку все Т-клеточные эпитопы в домене II могут быть устранены путем удаления LR, пять эпитопов, оставшихся в домене III, оказались в центре внимания при последующем изучении. В таблице 1А приведено расположение эпитопов, последовательности, скорости ответов и мутации, которые вызывают минимальное нарушение цитотоксической активности. Рейтинг эпитопов был составлен из целого ряда факторов, включая число наивных доноров, отвечающих на эпитоп, относительную силу ответа, число отвечающих пациентов с мезотелиомой и, в меньшей степени, отвечающих пациентов с HCL. Эпитопы от пациентов с HCL в данном анализе были оценены в меньшей степени из-за смещения HLA в когорте пациентов и в популяции пациентов с HCL, где пациенты с HCL имели обогащение BRB1_11 (Annino et al., Leuk. Lymphoma, 14 (Suppl.) 1:63-5 (1994)). Эпитоп 2 охватывает пять пептидов. Для упрощения анализа он был разделен на два субэпитопа: пептиды 77-78 (2А) и пептиды 75-76 (2В). Некоторые доноры ответили на оба эпитопа, 2А и 2В, в то время как другие ответили только на один. Эпитоп 6 (пептиды с 93 по 96) и эпитоп 8 (пептиды с 56 по 59) также были разделены на два субэпитопа.
[0239] Для сравнения результатов от наивных доноров и пациентов, получавших иммунотоксин, были изучены две когорты пациентов, у которых развивались нейтрализующие антитела против RIT. Пациенты с аллелью HLA DRB1 приведены в таблице 1В. Такие же эпитопы, которые были идентифицированы в когорте доноров, присутствовали также в когортах пациентов. Одна когорта была от пациентов с мезотелиомой, получавших SS1P (анти-мезотелин-Fv, слитый с P38) (Chowdhury et al., Nat. Biotechnol., 17: 568-572 (1999)); другая от пациентов с лейкемией, получавших моксетумомаб пасудотокс (moxetumomab pasudotox, MP), RIT, включающий PE38, слитый с анти-CD22-Fv (Kreitman et al., Clin. Cancer Res., 17: 6398-6405 (2011)). Ответы на эпитопы у наивных доноров варьировали в пределах от 1 до 4 эпитопа на одного донора, в среднем 2,1, а ответы у пациентов варьировали в пределах от 1 до 7 на одного пациента с более высоким средним числом 3,4 (рменее0,001 в t-тесте Стьюдента). Это говорит о том, что некоторые ответы в наивной популяции были слишком слабы, чтобы быть обнаруженными с помощью этого способа, и усиливались после воздействия иммунотоксина. В образцах пациентов не было выявлено каких-либо главных эпитопов, которые не были бы выявлены в когорте доноров.
Пример 2
[0240] В этом примере показано устранение Т-клеточных эпитопов в домене III.
[0241] Для каждого из эпитопов в домене III, которые описаны в таблице 1, был выполнен аланин-сканирующий мутагенез. Аланиновый мутант был встроен в RIT в соответствии со следующими 11 этапами: (1) составляли список всех аланиновых пептидных вариантов для каждого эпитопа; (2) проводили прогнозирование in silico, чтобы исключить аланиновые варианты, которые увеличивают связывание по меньшей мере с шестью аллелями HLA, с использованием алгоритма связывания HLA (Immune Epitope Database, IEDB) (Wang et al., PLoS Comput. Biol., 4:e1000048 (2008)), который измерял их способность связываться с 13 основными группами HLA; (3) аланиновые варианты анализировали с использованием от 8 до 15 образцов от доноров и пациентов с экспансией in vitro и ELIspot; (4) идентифицировали аланиновую мутацию, вызывающую пониженную активацию Т-клеток; (5) клонировали аланиновую мутацию в плазмиду HA22-LR и строили RIT с одной точечной мутацией; (6) изучали активность с помощью анализа WST8.
[0242] Если белок агрегировал или обладал низкой цитотоксической активностью, использовали прогнозирование in silico (7) и кристаллическую структуру для определения альтернативных аминокислот для аланина, и (8) в плазмиду HA22-LR клонировали новую мутацию, конструировали RIT с одной точечной мутацией и изучали активность. Если белок агрегировал или обладал низкой цитотоксической активностью, то идентифицировали следующий лучший аланиновый мутант, как это было проведено на этапе 4 и 5. Если белок был активным, проводили этап 10.
[0243] Если белок был активным, (10) проводили валидацию с целью определить, что эпитоп уменьшился, и что никакие новые эпитопы не появились из-за мутации; и (11) успешные точечные мутации объединяли в один RIT.
[0244] Результаты для всех эпитопов приведены в таблицах с 2 по 7. В таблицах 2-7 подчеркнутые значения представляют менее10%, D - донор, Pt - пациент, "Meso" - мезотелиома, позиция, в которой аминокислота заменена аланином, подчеркнута, а средние значения выделены жирным шрифтом. Аланиновые варианты были проанализированы с помощью от 8 до 15 образцов от доноров и пациентов с экспансией in vitro и ELIspot.
[0245] Эпитопы 2А и 2В сканировали по отдельности, чтобы охватить 9-мерное ядро всех пяти пептидов, которые дали ответы. Y502A уменьшала ответы обоих эпитопов (таблицы 2 и 3). Для эпитопов 5 и 7 аланиновые мутанты сравнивали с пептидом 67 и 51, соответственно, и I471A и L423A имели самый низкий Т-клеточный ответ (таблицы 4 и 6). Чтобы охватить все 9-мерные ядра в эпитопах 6 и 8, которые содержали четыре положительных пептида, был синтезирован 18-мерный WT и аланиновые варианты. Было установлено, что L552A является наиболее эффективной в снижении ответа в отношении эпитопа 6 (таблица 5), a F443A был лучшим в отношении эпитопа 8 (таблица 7).
Пример 3
[0246] Этот пример демонстрирует цитотоксическую активность белков с точечной мутацией в HA22-LR.
[0247] Проводили этап 4 из примера 2. Лучшие варианты, определенные при аланиновом сканировании или с использованием дополнительного предсказания in silico, описаны в таблице 1А.
[0248] Были сконструированы 40 мутантных RIT. Цитотоксическую активность белков с точечной мутацией в HA22-LR оценивали в отношении клеток СА46, Raji и Daudi. Выход очищенного белка, рассчитанные доступные площади поверхности (Lee et al., J. Mol. Biol., 55:379-400 (1971); Roscoe et al., Infect. Immunity, 62:5055-5065 (1994)) аминокислотных остатков WT и цитотоксическая активность каждого RIT приведены в таблице 8.
Пример 4
[0249] Этот пример демонстрирует, что замены в домене III РЕ уменьшают эпитоп и не создают новых эпитопов вследствие мутации.
[0250] Измеряли ответ трех донорских образцов и одного образца от пациента на 22 пептидных пула после стимуляции либо НА22 (wt), либо LR-R494A. "LR" означает удаление всего домена II за исключением последовательности расщепления фурином. Результаты показаны на фиг. 2A-2D. Как показано на фиг. 2A-2D, эпитоп в пептиде 76 уменьшался за счет мутации R494A.
[0251] Измеряли ответ двух донорских образцов и одного образца от пациента на 22 пептидных пула после стимуляции либо НА22 (wt), либо LR-R505A. Результаты показаны на фиг. 3А-3С. Как показано на фиг. 3А-3С, эпитоп в пептиде 77 уменьшался за счет мутации R505A.
[0252] Измеряли ответ двух донорских образцов на 22 пептидных пула после стимуляции либо HA22-LR (WT), либо LR-R551A и рестимуляции соответствующими пептидами. Результаты показаны на фиг. 4А-4В. Как показано на фиг. 4А-4В, мутация R551A уменьшила эпитоп в пептиде 93.
[0253] Измеряли ответ клеток от двух доноров и от двух пациентов после стимуляции RIT и рестимуляции пептидами 93, 94 с аминокислотной последовательностью WT, L552E или L552N. Результаты показаны на фиг. 5A-5D. Как показано на фиг. 5A-5D, эпитоп в пептидах 93 и 94 уменьшался за счет мутаций L552N и L552E.
[0254] Также измеряли ответ трех донорских образцов на 22 пептидных пула после стимуляции либо HA22-LR (WT), либо LR-R427A и рестимуляции соответствующими пептидами. Результаты показаны на фиг. 6А-6С. Как показано на фиг. 6А-6С, мутация R427A уменьшила эпитоп в пептиде 51.
[0255] Измеряли ответ двух образцов от пациентов и одного донорского образца на пулы 8-22 после стимуляции либо HA22-LR (WT), либо LR-F443A и рестимуляции соответствующими пептидами. Результаты показаны на фиг. 7А-7С. Как показано на фиг. 7А-7С, мутация F443A уменьшила эпитоп в пулах 11 и 12.
[0256] Четыре донорских образца стимулировали RIT и рестимулировали пептидом 67, содержащим валин или аланин в позиции I471. Ответ показан на фиг. 9A-9D в клетках, формирующих пятно (spot forming cells, SFC)/106 клеток. Как показано на фиг. 9A-9D, мутация 1471V не уменьшила эпитоп в пептиде 67.
[0257] Также измеряли Т-клеточную активацию в ответ на стимуляцию пептидами 67 или 68, которые содержат аланиновую или гистидиновую мутацию в позиции L477 или не содержат мутаций (WT). Результаты (SFC/106 клеток) приведены в таблице 9 и на фиг. 10A-10D. Как показано на фиг. 10A-10D и в таблице 9, мутация L477H уменьшила эпитоп в пептиде 67 и 68.
[0258] Клетки от двух пациентов стимулировали RIT и рестимулировали пептидом 93, 94 или 95 с аминокислотной последовательностью WT или L556V. Результаты показаны на фиг. 11А и В. Мутация L477V не уменьшала эпитоп в пептиде 94.
Пример 5
[0259] Этот пример демонстрирует активность комбинаций мутаций в НА22-LR.
[0260] Чтобы объединить точечные мутации, которые были эффективны в уменьшении Т-клеточных эпитопов, и поддержать хорошую цитотоксическую активность, были разработаны гены, которые содержат различные комбинации точечных мутаций. Эти гены были клонированы в плазмиду HA22-LR RIT. В таблице 10 показаны семь RIT, которые были сконструированы, а также HA22-LR WT. В таблице 10 также показана цитотоксическая активность на двух клеточных линиях и вычисленный остаточный Т-клеточный ответ. Вычисленный остаточный ответ является суммой ответов, показанных на тепловой карте эпитопов для каждого из эпитопов, при условии, что мутация будет устранять ответы в эпитопе полностью. Этот расчет не принимает во внимание силу ответа.
[0261] Как показано в таблице 10, из 258 ответов, определенных в донорском скрининге РЕ38, 136 ответов были в домене III и присутствовали в HA22-LR. Устранение эпитопов в пептиде (с 77 по 78), (с 51 по 52) и (с 57 по 58) с помощью мутаций R505A, R427A и F443A (HA22-LR-T2) уменьшало рассчитанные ответы до 82 ответов и поддерживало очень активный белок с относительной активностью 280% и 135% на клетках СА46 и Raji, соответственно, по сравнению с WT. HA22-LR-Т3 содержит четыре мутации: R505A, R427A, F443A и R494A и сниженную активность 55% и 50%. HA22-LR-T7 также имеет четыре мутации (R505A, R427A, R551A и F443A) и хорошую цитотоксическую активность с относительной активностью 113% и 100% на клетках СА46 и Raji. Для конструирования HA22-LR-T5 было вставлено пять мутаций, R505A, R494A, R551A, L427A и F443A, которые уменьшали вычисленный остаточный ответ до 39 ответов. Тем не менее, цитотоксическая активность белка значительно снижалась до относительной активности 24% и 19% с ЕС50 более1 нг/мл. HA22-LR-T9 также имела пять точечных мутаций (R505A, R427A, F443A, R494A и L477A). Т9 имел 46 рассчитанных остаточных ответов; все 46 остаточных ответов были слабыми или средней силы). Он поддерживал цитотоксическую активность с ЕС50 менее1 нг/мл с относительной активностью 36% и 26% в клетках CA46 и Raji, соответственно. HA22-LR-T11 замещает L477A в Т9 на L477H, что позволяет улучшить эту активность до 0,2 нг/мл при относительной активности 85% на СА46. Наконец, Т18 (также упоминается как "LMB-T18") был первым RIT, который содержал шесть мутаций и уменьшал все главные эпитопы, которые были идентифицированы. Он имел хорошую относительную активность с IC50 менее 0,3 нг/мл и относительную активность 63% и 104% по сравнению с HA22-LR на клетках СА46 и Raji. Для повышения цитотоксической активности после сайта расщепления фурином был вставлен пептидный линкер Gly-Gly-Ser.
[0262] Чтобы охарактеризовать свойства цитотоксической активности Т3 и Т18, проводили анализы WST-8 на четырех клеточных линиях, которые экспрессируют CD22: са46, Raji, Daudi и HAL-01. Каждый анализ проводили трижды. В таблице 11А показаны средние значения ЕС50 для каждой клеточной линии. Как HA22-LR-T3, так и HA22-LR-T18 были очень цитотоксическими, хотя и несколько меньше, чем исходная молекула HA22-LR-GGS. По сравнению с HA22-LR-GGS HA22-LR-T18 показала относительную активность, которая колебалась от 28% до 55% с IC50 менее1 нг/мл в четырех клеточных линиях. HA22-LR-T3 также был очень активен, однако менее активен, чем Т18.
[0263] Анализы цитотоксичности LMB-T18 проводили на четырех клеточных линиях, экспрессирующих CD22, и сравнивали с цитотоксической активностью MP (фиг. 27А, таблица 11В). LMB-T18 был очень мощным с ЕС50 менее 10 пМ на всех клеточных линиях. По сравнению с MP наблюдалось небольшое увеличение активности LMB-T18: на 53% на клетках СА46, на 54% на клетках Daudi и более чем на 200% на клетках HAL-01 (р равно 0,2, 0,06 и 0,01, соответственно, в t-тесте Стьюдента); тем не менее, на клетках Raji наблюдалось снижение активности LMB-Т18 на 52% (р равно 0,3 в t-тесте Стьюдента). Не связываясь с конкретной теорией или механизмом, полагают, что снижение активности на клетках Raji, вероятно, вызвано делецией домена II (Weldon et al., Blood, 113: 3792-3800 (2009)). Стабильность LMB-T18 сравнивали с MP путем нагрева образцов в течение 15 мин при различных температурах и, после охлаждения, измерения остаточного цитотоксического действия (фиг. 27В) на клетках Raji. MP потерял 50% своей активности после 15-минутной инкубации при 56°С. Неожиданно было обнаружено, что LMB-T18 был более термостабильным (р менее0,05 в t-тесте Стьюдента); он потерял только 50% своей активности после 15-минутной инкубации при 70°С. Клетки от семи пациентов с HCL и шести пациентов с хроническим лимфолейкозом (CLL) использовали для определения активности на клетках пациента. Фигуры 27С-D показывают, что LMB-T18 более активен, чем MP на CLL-клетках, хотя эта разница не видна на клетках HCL.
Пример 6
[0264] Этот пример демонстрирует относительную активность RIT с модифицированным В- и Т-клеточным эпитопом.
[0265] В-клеточные эпитопы в РЕ38 предварительно идентифицировали и объемные поверхностные остатки подвергали мутированию аланином или серином для снижения антигенности (Liu et al., Protein Eng. Dec. Sel., (25)(1): 1-6 (2012)). Ранее идентифицированный мутантный RIT с низкой антигенностью был назван SS1LO10R, и он содержал следующие мутации: R505A, R427A, R490A, R463A, R467A, R538A.
[0266] Чтобы минимизировать иммуногенность RIT, нацеленного на мезотелин, в SS1P встраивали модификации LO10, а затем одну за другой включали точечные мутации Т-клеточного эпитопа. Цитотоксическую активность анализировали для каждого из вариантов с использованием клеточных линий, экспрессирующих мезотелин (А9/431 и HAY). Было обнаружено, что две мутации, R505A и R427A, являются эффективными в уменьшении как В-, так и Т-клеточных эпитопов.
[0267] В таблице 12 приведена цитотоксическая активность мутантного РЕ в отношении двух клеточных линий и вычисленный остаточный ответ комбинированного RIT, который был сконструирован. Сочетание SS1-LO10 с одной точечной мутации F443A (SS1-LO10-T2) имело высокую (от 100 до 115%) относительную активность, которая соответствует активности этих точечных мутаций в HA22-LR. Сочетание R494A и R551A в SS1-LO10-T1 давало очень низкую активность, что показывает, что сочетание R551A и R494A снижает активность белка как в НА22, так и в SS1-LO10.
[0268] SS1 LO10R-T11, который содержал R505A, R427A, R494A, F443A и L477H, имел 71% активности на клетках Н9, но только 7% на клетках HAY (анализ в HAY был сделан один раз). Т14 и Т15, которые содержали R505A, R427A, R494A, F443A и L477H, с дополнительной мутацией (L552E и L552N, соответственно) имели более100% относительной активности на клетках Н9 и IC50 более 1 нг/мл. Эти два мутанта представляют максимальную деиммунизацию Т-клеток, полученную в этом проекте до сих пор.
[0269] Мутант Т14 был выбран как лучший кандидат для этапа клинической разработки, так как она включает удаление В-клеточных и многих Т-клеточных эпитопов, но обеспечивает хорошую цитотоксическую активность в отношении клеточных линий, экспрессирующих мезотелин.
Пример 7
[0270] Этот пример демонстрирует противоопухолевую активность Т14.
[0271] Противоопухолевые эксперименты проводили путем введения физиологического раствора (контроль) или Т14 голым мышам с ксенотрансплантатами А431/Н9. Размер опухоли измеряли каждый день и отмечали в мм. В это же время взвешивали животных, и вес представляли в граммах. Результаты приведены ниже в таблице 13. В таблице 13 стрелки показывают день введения иммунотоксина. Как показано в таблице 13, дозы до 7 мг/г × 3 хорошо переносились без каких-либо признаков токсичности у мышей. Кроме того, на всех дозах Т14 была отмечена сильная регрессия опухоли.
Пример 8
[0272] Этот пример демонстрирует термическую стабильность Т18.
[0273] Стабильность Т18 исследовали путем нагревания RIT в течение 15 мин при различных температурах. Затем выполняли анализы цитотоксичности. Рассчитывали ЕС50 по-разному нагреваемых белков. Результаты показаны на фиг. 8. Показано кратное увеличение ЕС50. Как показано на фиг. 8, было установлено, что Т18 сохранял цитотоксическую активность при 60°С и терял 50% своей активности при 68°С. Leaver et al., Methods in Enzymology, 487: 545-74 (2011).
Пример 9.1
[0274] В этом примере показано конструирование, экспрессия и очистка деиммунизированных РЕ-химерных молекул против мезотелина с удлиненным линкером между тяжелой цепью анти-мезотелин-Fab-фрагмента и доменом РЕ 24 и удаление предсказанных Т-клеточных эпитопов в линкере.
[0275] Последовательность линкера, использованную в WO 2012/154530 и Weldon et al., Mol. Cancer Ther., 12: 48-57 (2013) для слияния dsFv-фрагмента (через С-конец домена VH) с деиммунизированым РЕ, также использовали для слияния Fab-фрагмента (через С-конец домена СН1) с деиммунизированным РЕ. Полученную область пептида, включающую части домена СН1, линкер и часть деиммунизированного РЕ (SEQ ID NO 273), исследовали с помощью анализа TEPITOPE (Bian et al., Methods, 34: 468-475 (2004)). Потенциальные Т-клеточные эпитопы, релевантные для населения Европы (ЕС) и Соединенных Штатов Америки, были выявлены в области между доменом СН1 и линкером и в области между линкером и доменом РЕ24. Потенциальные Т-клеточные эпитопы характеризовались доверительным числом 3 или ниже. Результаты приведены в таблице 14. Как показано в таблице 14, линкерная область без специфических удлинений (SEQ ID NO 273) показала семь потенциальных Т-клеточных эпитопов. Один из потенциальных Т-клеточных эпитопов расположен в переходной области WEQLGGSPT (SEQ ID NO 274), а остальные шесть Т-клеточных эпитопов расположены в переходной области VEPKSCKAS (SEQ ID NO 275). Обе эти области релевантны в основном для населения Европы (ЕС) и Азии.
[0276] Потенциальные Т-клеточные эпитопы разрушали за счет встраивания аминокислотной последовательности (вставки) в каждую из переходных областей, тем самым получая вставку на каждой из обеих сторон сайта расщепления фурином. Последовательность DKTH (SEQ ID NO 276) вставляли в линкер в месте, которое непосредственно не примыкает к последовательности расщепления фурином (FCS), а последовательность GGG (SEQ ID NO 277) вставляли в линкер в месте, которое непосредственно прилегает к FCS без потенциальных Т-клеточных эпитопов. Полученная удлиненная пептидная область, включающая а) части домена СН1, b) линкер, удлиненный в области Fab-слияния и удлиненный в области РЕ-слияния, и с) часть деиммунизированного РЕ, содержала аминокислотной SEQ ID NO: 278. Удлиненную пептидную область изучали с помощью анализа TEPITOPE, полученные результаты приведены в таблице 15А. Как показано в таблице 15А, удлиненный линкер не давал сигнала в анализе TEPITOPE (доверительные значения 6 или выше) и, в то же время, давал улучшенную стабильность (см. пример 9.2 ниже).
Пример 9.2
[0277] Этот пример демонстрирует стабильность деиммунизированных РЕ-гибридных белков и конъюгатов, имеющих удлиненный линкер с последовательностью SEQ ID NO 36.
[0278] Шесть вариантов Fab-линкер-РЕ24 получали и сравнивали с учетом их термической стабильности и склонности к агрегации. Все шесть вариантов содержали один и тот же гуманизированный Fab-вариант H1/L1 антитела SS1, но отличались в отношении линкера и мутанта РЕ24. Что касается линкера, был использован либо линкер, описанный в публикации международной патентной заявки WO 2012/154530 (kasggrhrqprgweqlggs (SEQ ID NO 281)), либо удлиненный линкер с дополнительными аминокислотами ("длинный линкер"; SEQ ID NO 36 (dkthkasggrhrqprgweqlgggggs))). В качестве вариантов РЕ24 в конструкциях были использованы LRO10R, LRO10R-456A (SEQ ID NO 37) или LRO10R-456A-551A.
[0279] На фиг. 12-13 показан уровень агрегации двух конструкций с вариантом РЕ24 LRO10R-456A, который измеряли как площадь под пиком агрегата при эксклюзионной хроматографии (SEC) после инкубации при 33°C. Эти две конструкции на фиг. 12-13 отличались только в отношении используемого линкера. Короткий линкер SEQ ID NO 281 был использован в конструкции cFP-0170, а удлиненный линкер SEQ ID NO 36 был использован в конструкции cFP-0171.
[0280] На фиг. 14-16 показана термическая стабильность конструкций, измеренная с помощью динамического рассеяния света (dynamic light scattering, DLS). Для динамического рассеяния света образцы готовили в концентрации 1 мг/мл в растворе 20 мМ гистидина/хлорида гистидина, 140 мМ NaCl, pH 6,0, переносили в оптический 384-луночный планшет путем центрифугирования через фильтровальный планшет с диаметром пор 0,4 мкм и покрывали парафиновым маслом. Гидродинамический радиус измеряли в планшетном ридере WYATT DYNAPRO II повторно путем динамического рассеяния света, в то время как образцы нагревали со скоростью 0,05°C/мин от 25°C до 80°C. Температуру начала агрегации определяли как температуру, при которой начинает возрастать гидродинамический радиус. Результаты показаны на фиг. с 14 по 16. Кривые DLS для шести конструкций показали более высокие температуры агрегации при удлиненном линкере по сравнению с коротким опубликованным линкером, с сильным сдвигом к более высокой температуре агрегации для варианта LRO10R (фиг. с 14 по 16).
[0281] В таблице 15В показана термическая стабильность конструкций cFP-0170 и cFP-0171, измеренная с помощью дифференциальной сканирующей калориметрии (differential scanning calorimetry, DSC). Дифференциальную сканирующую калориметрию выполняли с использованием системы MicroCal DSC (GE Healthcare). Образцы доводили до концентрации белка примерно 1 мг/мл в растворе 20 мМ гистидина/HCl, 140 мМ хлорида натрия, pH 6,0. Референсную ячейку заполняли буфером, который соответствовал буферу для образцов. Образцы помещали в ячейку для образца и нагревали от 4°C до 110°C со скоростью нагрева 60°C/ч. Предварительное сканирование составляло 15 минут, период фильтрации составлял 10 секунд, а режим обратной связи/усиления был установлен на пассивный. Срединную точку температуры теплового перехода (Tm, thermal transition temperature) получали на основе анализа данных с помощью программного обеспечения для анализа MicroCal DSC.
[0282] Как показано на фиг. с 12 по 16 и в таблице 15В, все химерные Fab-РЕ-молекулы с удлиненным линкер имели сниженную склонность к агрегации и более высокую температуру агрегации по сравнению с химерными Fab-PE-молекулами с коротким линкером, который не был удлинен.
Пример 10
[0283] Этот пример демонстрирует способность деиммунизированных РЕ-гибридных белков с удлиненным линкером уничтожать опухолевые клетки и ингибировать синтез клеточных белков. Этот пример также демонстрирует антигенность деиммунизированных РЕ-гибридных белков с удлиненным линкером.
[0284] Сравнивали активность различных Fab-РЕ24-вариантов в отношении их способности ингибировать синтез белка. Использовали клон клеточной линии рака поджелудочной линии ASPC-1 (ASPC-1 Luc), которая была стабильно трансфицирована люциферазой. Белок люцифераза в этих клетках подвергается высокому обмену, так что измеряемая активность заметно падает в течение 24 часов ингибирования его ресинтеза. Вкратце, клетки высевали в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP-вариантов и клетки инкубировали еще в течение 72 часов. В конце периода инкубации клетки лизировали, а активность люциферазы определяли с помощью анализа STEADY-GLOW в соответствии с инструкциями изготовителя. В типичном эксперименте наблюдалось снижение активности люциферазы на 80-90% в лизатах обработанных клеток по сравнению с лизатами необработанных контрольных клеток. Значения ЕС50, т.е. концентрации, которые дают половину максимального эффекта, определяли на основе свободной четырехпараметрической подгонки. В таблице 16 сравнены относительные активности в репрезентативном эксперименте с установкой значения IC50 huFabLRO10R равным 1.
[0285] Нецелевой РЕ24 (вариант LR8M) ингибировался при концентрации более 3,5 мкг/мл, в то время как ранее описанный вариант LRO10, слитый с гуманизированным Fab-фрагментом SS1, был примерно в 500 раз более активным в расчете на моли. Обратная мутация LRO10R повышала активность от 10 до 20 раз (значения ЕС50 1-2 нг/мл против 18 нг/мл). Мутация 456А не имела отрицательного влияния на активность, в то время как мутация 551А снижала активность до уровня LRO10 (EC50 от 10 до 23 нг/мл). Новый удлиненный линкер также не оказал отрицательного влияния на клеточную активность молекул при сравнении любой из трех пар конструктов с удлиненным линкером против ранее описанных с более коротким линкером.
[0286] Используя жизнеспособность клеток, оцениваемую с помощью анализов CELLTITERGLOW, сравнивали цитотоксическую активность различных Fab-РЕ24-вариантов с использованием одного и того же гуманизированного SS1 специфическего варианта на двух различных линиях опухолевых клеток (А431 Н9 и Н596). Вкратце, клетки высевали в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP, и клетки инкубировали в течение 72 часов. В конце периода инкубации жизнеспособность клеток определяли с помощью анализа CELLTITERGLOW. В таблице 16 сравнены относительные активности с установкой значения IC50 huFabLRO10R равным 1.
[0287] Результаты, аналогичные приведенным в таблице 16, также были получены с использованием анализа жизнеспособности клеток со считыванием на основе 3-[4,5-диметилтиазол-2-ил]-2,5-дифенилтетразолия бромида (МТТ) на разных клеточных линиях (таблица 17).
Пример 11
[0288] В этом примере показано удаление В-клеточных эпитопов с помощью мутаций 456А в РЕ.
[0289] Фагмиду, содержащую scFv 9Н3 в векторе pCANTAB, описанном в Liu et al., PNAS, 109: 11782-11787 (2012), получали с помощью стандартных способов, описанных в Sambrook, J. et al., Molecular cloning: A laboratory manual; Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 1989. Молекулярно-биологические реагенты использовали в соответствии с инструкциями изготовителя. Фагмидой трансформировали электрокомпетентные клетки TG1. Из отдельных колоний в течение ночи выращивали предварительные культуры и использовали для инокуляции 4 мл культуры 2×YT/1% глюкозы, дополненной соответствующим селективным антибиотиком ампициллином. При OD600 0,3-0,8 добавляли 1010 KOE фага-помощника VCSM 13 и IPTG до конечной концентрации 1 мМ. После инкубации в течение 15 минут при 37°C культуру выращивали при 37°C в течение ночи. Через два часа после добавления фага-помощника добавляли канамицин до конечной концентрации 30 мкг/мл. Содержащий фаги супернатант собирали из ночной культуры центрифугированием, а фаг, представляющий scFv, осаждали из супернатанта путем добавления 1/5 по объему 20% PEG-6000/2.5M NaCl и выделяли центрифугированием. Осадок с фагом растворяли в 0,5 мл PBS/1% BSA, и раствор фага осветляли путем центрифугирования и стерильной фильтрации. Титр фага в растворе определяли с помощью стандартных способов, описанных в Barbas, С. et al., Phage Display - A laboratory manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 2001.
[0290] 96-луночные микротитровальные планшеты MaxiSorp покрывали 100 мкг/мл Fab-РЕ24-вариантов. После блокирования PBS-буфером с добавлением 2% BSA на планшете проводили захват 107 и 108 scFv-представляющих фагов в течение одного часа. В качестве специфических отрицательных контролей scFv-представляющие фаги предварительно инкубировали с 50 мкг/м Fab-PE24-вариантов в течение 1 ч при комнатной температуре (RT) перед захватом их на планшет. Планшеты промывали PBST-буфером (PBS плюс 0,5% Tween 20). Связывание scFv-представляющего фага обнаруживали с помощью POD-конъюгированного анти-m13-антитела (Progen). После последней промывки планшеты инкубировали с субстратом POD. Абсорбцию измеряли при 405 нм. Результаты показаны на фиг. 17, где можно видеть, что В-клеточный эпитоп, содержащийся в фагмиде, содержащей scFv 9Н3, не был удален в LRO10R (с обратной мутацией 458R), в то время как он устранялся обеими мутациями 458А и 456А с немного более сильным эффектом при мутации 456А.
[0291] Тестирование антигенности проводили так, как описано в Weldon et al., Mol. Cancer Ther., 12: 48-57 (2013). Как показано на фиг. 18, по сравнению с SS1P (Т1) деиммунизированный вариант LRO10R (Т2) имел от 100 до 10000-кратное снижение реактивности с большинством сывороток от пациентов, которые ранее подвергались воздействию терапевтического гибридного белка на основе РЕ, как с форматом гибрида мышиного dsFv, так и с форматом гибрида гуманизированного Fab. Также введение мутации 456А (Т3 и Т5) или нового удлиненного линкера (Т5 и Т6) показало от 100 до 10000-кратное снижение реактивности с большинством сывороток от пациентов, которые ранее подвергались воздействию терапевтического гибридного белка на основе РЕ.
Пример 12
[0292] Этот пример демонстрирует конструирование, экспрессию и очистку деиммунизированных РЕ-вариантов и их Fab-гибридов, а также dsFv-гибридов для сравнения.
Пример 12.1: Клонирование деиммунизированных РЕ-химерных молекул против мезотелина cFP-0077 (SEQ ID NO 41 и 42) и cFP-0078 (SEQ ID NO 43 и 44).
[0293] Для экспрессии cFP-0077 и cFP-0078 использовали систему вектор/хозяин E. coli, которая делает возможной селекцию плазмиды без антибиотика с помощью комплементации ауксотрофии Е. coli (PyrF) (публикация Европейской патентной заявки 0972838 и патент США 6291245). Для манипуляций с ДНК были использованы стандартные способы, описанные в Sambrook, J. et al., см. выше. Молекулярно-биологические реагенты использовали в соответствии с инструкциями изготовителя. Нужные генные сегменты получали коммерческим путем методом генного синтеза. Синтезированные фрагменты генов клонировали в указанный экспрессионный вектор. ДНК-последовательности субклонированных фрагментов генов подтверждали секвенированием ДНК.
[0294] Экспрессионные плазмиды для продукции легкой цепи и тяжелой цепи, соответственно, были получены следующим образом: плазмиды с легкой цепью (LC) 15478 (на основе аминокислотных последовательностей cFP-0077 и кодирующей SEQ ID NO 41) и 15479 (на основе аминокислотных последовательностей cFP-0078 и кодирующей SEQ ID NO 43) являются экспрессионными плазмидами для экспрессии фрагментов легкой цепи антитела в Е. coli. Они были получены путем лигирования фрагмента VL-домена антитела в вектор с использованием сайтов рестрикции Xhol/BsiWI для 15478 и Xhol/Blpl для 15479.
[0295] Плазмиды для экспрессии легкой цепи в Е. coli содержат следующие элементы:
- сайт начала репликации из вектора pBR322 для репликации в Е. coli (соответствующий позициям 2517-3160 в соответствии с Sutcliffe et al., Quant. Biol., 43: 77-90(1979),
- ген URA3 от Saccharomyces cerevisiae, кодирующий оротидин-5'-фосфатдекарбоксилазу (Rose et al., Gene, 29: 113-124 (1984), которая позволяет выбирать плазмиды с помощью комплементации мутантных штаммов Е. coli pyrF (урацил-ауксотрофия),
- экспрессионную кассету легкой цепи антитела, содержащую:
- гибридный промотор Т5 (гибридный промотор T5-PN25/03/04 в соответствии с Bujard et al., Methods. Enzymol., 155: 416-433 (1987) и Stueber, et al., Immunol. Methods IV, 121-152 (1990), включающий синтетический сайт посадки рибосомы в соответствии с Stueber et al. (см. выше),
- вариабельный домен легкой цепи антитела, включающий CDR из SS1,
и
- человеческий Ск-домен для 15478, но не для 15479,
- два терминатора транскрипции бактериофагального происхождения, терминатор λ-Т0 (Schwarz et al., Nature, 272: 410-414 (1978)) и fd-терминатор (Beck et al., Gene, 1-3: 35-58(1981)), и
- ген-репрессор lad из E. coli (Farabaugh, Nature, 274: 765-769 (1978).
[0296] Плазмиды тяжелой цепи (НС) 15476 (на основе аминокислотных последовательностей cFP-0077 и кодирующей SEQ ID NO 42) и 15477 (на основе аминокислотных последовательностей cFP-0078 и кодирующей SEQ ID NO 44) являются экспрессионными плазмидами для экспрессии гибридного белка, включающего фрагмент тяжелой цепи антитела, линкер с сайтом расщепления фурином и мутантный домен III из экзотоксина A Pseudomonas aeruginosa (РЕ), в Е. coli. Они были получены путем лигирования фрагмента VH-домена в вектор с использованием сайтов рестрикции Xhol/BsrGl для 15476 и Xhol/HindIII для 15477.
[0297] Плазмиды для экспрессии тяжелой цепи цитолитического гибридного белка в Е. coli содержат следующие элементы:
- сайт начала репликации из вектора pBR322 для репликации в Е. coli (соответствующий позициям 2517-3160 в соответствии с Sutcliffe et al., Quant. Biol., 43: 77-90(1979),
- ген URA3 от Saccharomyces cerevisiae, кодирующий оротидин-5'-фосфатдекарбоксилазу (Rose et al., Gene, 29: 113-124 (1984), которая позволяет выбирать плазмиды с помощью комплементации мутантных штаммов Е. coli pyrF (урацил-ауксотрофия),
- экспрессионную кассету гибридного белка "тяжелая цепь - домен РЕ III", содержащую:
- гибридный промотор Т5 (гибридный промотор T5-PN25/03/04 в соответствии с Bujard et al., Methods. Enzymol., 155: 416-433 (1987) и Stueber, et al., Immunol. Methods IV, 121-152 (1990), включающий синтетический сайт посадки рибосомы в соответствии с Stueber et al. (см. выше),
- вариабельный домен тяжелой цепи антитела, включающий CDR из SS1,
- человеческий СН1-домен для 15476, но не для 15477,
- линкер, содержащий сайт расщепления фурином,
- мутантный вариант домена III из экзотоксина A Pseudomonas aeruginosa,
- два терминатора транскрипции бактериофагального происхождения: терминатор λ-Т0 (Schwarz et al., Nature, 272: 410-414 (1978)) и fd-терминатор (Beck et al., Gene, 1-3: 35-58(1981)), и
- ген-репрессор lad из E. coli (Farabaugh, Nature, 274: 765-769 (1978).
Пример 12.2: Экспрессия деиммунизированных РЕ-химерных молекул против мезотелина cFP-0077 и cFP-0078 в Е. coli.
[0298] Все полипептидные цепи экспрессировали по отдельности в штамме Е. coli CSPZ-6.
[0299] Штамм Е. coli К12 CSPZ-6 (thi-1, ΔpyrF) трансформировали путем электропорации экспрессионными плазмидами 15476, 15477, 15478 и 15479, соответственно, получая 4 штамма: cFP-0019 (на основании плазмиды 15476), cFP-0020 (на основании плазмиды 15477), cFP-0040 (на основании плазмиды 15478) и cFP-0041 (на основании плазмиды 15479). Для каждого из четырех штаммов трансформированные клетки Е. coli сначала выращивали при 37°C на чашках с агаром. Колонии, собранные с этой чашки, переносили в перемешиваемую культуру объемом 3 мл и выращивали при 37°C до оптической плотности составляющей от 1 до 2 (измеренной при 578 нм). Затем 1000 мкл культуры смешивали с 1000 мкл стерильного 86% глицерина и немедленно замораживали при -80°C для длительного хранения. Правильный продукт экспрессии этого клона вначале проверяли в мелкомасштабных экспериментах со встряхиваемыми колбами и анализировали с помощью SDS-PAGE до передачи в ферментер объемом 10 л.
Предварительное культивирование:
[0300] Для предварительной ферментации использовали среду с определенным химическим составом (CD-PCMv2.20): NH4Cl 1,0 г/л, K2HPO4 *3H2O 18,3 г/л, цитрат 1,6 г/л, глицин 0,78 г/л, L-аланин 0,29 г/л, L-аргинин 0,41 г/л, L-аспарагин*H2O 0,37 г/л, L-аспартат 0,05 г/л, L-цистеин*HCl*H2O 0,05 г/л, L-гистидин 0,05 г/л, L-изодейцин 0,31 г/л, L-лейцин 0,38 г/л, L-лизин*HCl 0,40 г/л, L-метионин 0,27 г/л, L-фенилаланин 0,43 г/л, L-пролин 0,36 г/л, L-серин 0,15 г/л, L-треонин 0,40 г/л, L-триптофан 0,07 г/л, L-валин 0,33 г/л, L-тирозин 0,51 г/л, L-глутамин 0,12 г/л, Na-L-глутамат*H2O 0,82 г/л, глюкоза*H2O 6,0 г/л, раствор микроэлементов 0,5 мл/л, MgSO4 *7H2O 0,86 г/л и тиамин*HCl 17,5 м г/л. Раствор микроэлементов содержал FeSO4 *7H2O 10,0 г/л, ZnSO4 *7H2O 2,25 г/л, MnSO4 *H2O 2,13 г/л, H3BO3 0,50 г/л, (NH4)6Mo7O24 *4H2O 0,3 г/л, CoCl2 *6H2O 0,42 г/л и CuSO4 *5H2O 1,0 г/л, растворенные в 0,5М HCl.
[0301] Для предварительной ферментации в 220 мл среды CD-PCMv2.20 в колбе Эрленмейера с четырьмя перегородками объемом 1000 мл засевали 1,0 мл из ампулы с банком исследования. Культивирование проводили на ротационном шейкере в течение 8 часов при 32°C и скорости 170 оборотов в минуту до получения оптической плотности (578 нм) 2,9. 100 мл предварительного культивирования использовали для инокуляции в партию среды для биореактора объемом 10 л.
Ферментация cFP-0019 и cFP-0020:
[0302] Для ферментации в ферментере BioStat С, DCU3 объемом 10 л (Sartorius, Мельзунген, Германия) использовали следующую партию среду с определенным химическим составом: KH2PO4 1,59 г/л, (NH4)2HPO4 7,45 г/л, K2HPO4 *3H2O 13,32 г/л, цитрат 2,07 г/л, L-метионин 1,22 г/л, NaHCO3 0,82 г/л, раствор микроэлементов 7,3 мл/л, MgSO4 *7H2O 0,99 г/л, тиамин*HCl 20,9 м г/л, глюкоза*H2O 29,3 г/л, биотин 0,2 м г/л и 1,2 мл/л 10% противопенного агента Synperonic. Раствор микроэлементов содержал FeSO4 *7H2O 10 г/л, ZnSO4 *7H2O 2,25 г/л, MnSO4 *H2O 2,13 г/л, CuSO4 *5H2O 1,0 г/л, CoCl2 *6H2O 0,42 г/л, (NH4)6Mo7O24 *4H2O 0,3 г/л, и H3BO3 0,50 г/л, солюбилизированные в 0,5М растворе HCl.
[0303] Питательный раствор 1 содержал 700 г/л глюкозы*H2O, 7,4 г/л MgSO4 *7H2O и 0,1 г/л FeSO4 *7H2O. Питательный раствор 2 содержал KH2PO4 52,7 г/л, K2HPO4 *3H2O 139,9 г/л и (NH4)2HPO4 66,0 г/л. Все компоненты были растворены в деионизированной воде. Щелочной раствор для регулирования pH представлял собой водный 12,5% (вес/объем) раствор NH3, дополненный 11,25 г/л L-метионина.
[0304] Начиная с 4,2 л стерильной партии среды плюс 100 мл инокулята из предварительного культивирования, периодическую ферментацию проводили при 31°C, pH 6,9±0,2, противодавлении 800 мбар и начальной скорости аэрации 10 л/мин. Относительное значение растворенного кислорода (рО2) поддерживали на уровне 50% в ходе ферментации за счет увеличения скорости мешалки до 1500 оборотов в минуту. После того, как первоначально введенная глюкоза истощалась, что обозначалось резким повышением значений растворенного кислорода, температуру сдвигали на 25°C, и через 15 минут ферментацию вводили в режим подпитки с началом введения обоих питательных растворов (60 и 14 г/ч соответственно). Скорость подачи раствора 2 поддерживали постоянной, в то время как скорость подачи раствора 1 увеличивали ступенчато с заранее определенным профилем подачи от 60 до 160 г/ч в течение 7 часов. Когда концентрация выделяемого газообразного диоксида углерода устанавливалась выше 2%, скорость аэрации постоянно увеличили с 10 до 20 л/мин в течение 5 часов. Экспрессию рекомбинантного белка индуцировали добавлением 2,4 г IPTG при оптической плотности примерно 120. Целевой белок экспрессировался в виде телец включения в цитоплазме.
[0305] После 24 часов культивирования была достигнута оптическая плотность 209, и весь бульон охлаждали до 4-8°C. Бактерии собирали центрифугированием с помощью проточной центрифуги (13000 оборотов в минуту, 13 л/ч), и полученную биомассу хранили при -20°C до дальнейшей обработки (разрушения клеток).
Ферментация cFP-0040 и cFP-0041:
[0306] Для ферментации в ферментере Biostat С, DCU3 объемом 10 л (Sartorius, Мельзунген, Германия) использовали следующую комплексную партию среды: бактотриптон 20 г/л, дрожжевой экстракт 15 г/л, KH2PO4 1,5 г/л, K2HPO4 *3H2O 6,6 г/л, NaCl 1,0 г/л, MgSO4 *7H2O 0,74 г/л, глюкоза*H2O 3,0 г/л, и 0,2 мл/л противопенного агента.
[0307] Питательный раствор 1 содержал бактотриптон 250 г/л и дрожжевой экстракт 175 г/л. pH регулировали с помощью 75% раствора глюкозы*H2O. Все компоненты были растворены в деионизированной воде.
[0308] Начиная с 7,6 л стерильной партии среды плюс 100 мл инокулята из предварительно культивирования, периодическую ферментацию проводили при температуре 37°C, pH 7,0±0,3, противодавлении 500 мбар и начальной скорости аэрации 10 л/мин. Относительное значение растворенного кислорода (рО2) поддерживали на уровне 50% в ходе ферментации путем увеличения скорости мешалки до 1500 оборотов в минуту. Подачу питательного раствора 1 начинали после того, как культура достигала оптической плотности 15. Когда концентрация выделяемого газообразного диоксида углерода устанавливалась выше 2%, скорость аэрации постоянно увеличивали с 10 до 20 л/мин в течение 5 часов. Экспрессию рекомбинантного белка индуцировали добавлением 2,4 г IPTG при оптической плотности примерно 20. Целевой белок экспрессировался в виде телец включения в цитоплазме.
[0309] После 13 часов культивирования была достигнута оптическая плотность 100-115, и весь бульон охлаждали до температуры от 4 до 8°C. Бактерии собирали центрифугированием с помощью проточной центрифуги (13000 оборотов в минуту, 13 л/ч), и полученную биомассу хранили при -20°C до дальнейшей обработки (разрушения клеток и получения телец включения).
Анализ формирования продукта (для cFP-0019, -0020 -0040 и -0041):
[0310] Образцы забирали из ферментера, один перед индукцией, а остальные в определенные временные точки после индукции экспрессии белка, и анализировали с помощью электрофореза в SDS-полиакриламидном геле. Из каждого образца одинаковое количество клеток (ODцелевое равно 10) суспендировали в 5 мл PBS-буфера и разрушали путем обработки ультразвуком на льду. Затем 100 мкл каждой суспензии центрифугировали (15000 оборотов в минуту, 5 минут), и каждый супернатант отбирали и переносили в отдельную пробирку. Это делали для различения растворимого и нерастворимого экспрессированного белка-мишени. К каждому супернатанту (растворимой фракции белка) добавляли 100 мкл, а к каждому осадку (нерастворимой фракции белка) 200 мкл SDS-буфера для образцов (Laemmli, Nature, 227: 680-685 (1970). Образцы нагревали в течение 15 мин при температуре 95°C в условиях интенсивного смешивания для солюбилизации и восстановления всех белков в образцах. После охлаждения до комнатной температуры 5 мкл каждого образца переносили на 4-20% полиакриламидный гель TGX Criterion Stain Free (Bio-Rad). Кроме того, наносили 5 мкл стандарта молекулярной массы (Precision Plus Protein Standard, Bio-Rad).
[0311] Электрофорез проводили в течение 60 мин при 200 В, а после этого гель переносили на GELDOC EZ Imager (Bio-Rad) и обрабатывали в течение 5 мин УФ-излучением. Изображения геля анализировали с помощью программного обеспечения для анализа изображений IMAGE LAB (Bio-Rad). Относительную количественную оценку экспрессии белка проводили путем сравнения объема полос продукта с объемом полосы стандарта молекулярной массы 25 кДа.
Подготовка препаратов телец включения:
[0312] Получение препаратов телец включения (inclusion body preparation, IBP) из ферментеров объемом 10 л начинали сразу после сбора бактерий, ресуспендируя собранные бактериальные клетки в буфере 1 (12,1 г/л Tris, 0,246 г/л MgSO4*7H2O, 12 мл/л 25% HCl). Объем буфера рассчитывали в зависимости от содержания сухого вещества в биомассе. Добавляли лизоцим (100 кЕд/мг, 0,12 мг/г сухой вес) и небольшое количество бензоназы (5 Ед/г сухой вес). Затем суспензию гомогенизировали при 900 бар (APV Rannie 5, 1 проход) для разрушения бактериальных клеток, добавляли дополнительную бензоназу (30 Ед/г сухой вес) и инкубировали в течение 30 мин при температуре от 30 до 37°C. Затем добавляли первый промывочный буфер (60 г/л Brij, 87,6 г/л NaCl, 22,5 г/л EDTA, 6 мл/л 10н NaOH) и снова инкубировали суспензию в течение 30 минут. Следующий этап центрифугирования (ВР12, Sorvall) приводил к получению взвеси телец включения, которую ресуспендировали во втором промывочном буфере (12,1 г/л Tris, 7,4 г/л EDTA, 11 мл/л 25% HCl) и инкубировали в течение 20 минут. После еще одного этапа разделения получали тельца включения, которые хранили замороженными при -20°C или немедленно солюбилизировали для рефолдинга и очистки.
Пример 12.3: Рефолдинг и очистка деиммунизированных РЕ-химерных молекул против мезотелина cFP-0077 и cFP-0078.
[0313] cFP-0077 и cFP-0078 были получены путем рефолдинга и очистки.
[0314] Ренатурация и очистка Fab-PE24 (cFP-0077): тельца включения НС-РЕ24 и LC солюбилизировали по отдельности в растворе, содержащем 8 М гуанидина гидрохлорид, 100 мМ Tris/HCl, 1 мМ EDTA, pH 8,0 плюс 100 мМ дитиотреитол (DTT), в течение ночи при комнатной температуре (1 г IB в 5 мл). Солюбилизаты доводили до pH 3 и центрифугировали, и осадок отбрасывали. После экстенсивного диализа против 8 М гуанидин-HCl, 10 мМ EDTA, pH 3,0, чтобы удалить DTT, определяли общую концентрацию белка биуретовым способом. Чистоту содержания НС и LC оценивали с помощью SDS-PAGE.
[0315] Солюбилизаты разводили в молярном соотношении 1:1 в буфере для ренатурации, содержащем 0,5 М аргинина, 2 мМ EDTA, pH 10 плюс 0,9 мМ GSH/GSSG, соответственно, при температуре 2-10°C. Концентрацию белка-мишени увеличивали на двух этапах до 0,22 г/л, при этом время инкубации между двумя дозами составляло 4 ч. После этого раствор ренатурата хранили при 2-10°C в течение ночи.
[0316] Ренатурат разбавляли H2O до менее 3 мСм/см и закачивали на анионообменную колонку (AIEX), уравновешенную 20 мМ Tris/HCl, pH 7,4. После промывания колонки уравновешивающим буфером белок элюировали градиентом до 20 мМ Tris/HCl, 400 мМ NaCl, рН 7,4. Пиковые фракции, содержащие Fab-PE24, объединяли, концентрировали и наносили на препаративную эксклюзионную колонку (SEC) в 20 мМ Tris, 150 мМ NaCl, рН 7?4, для удаления агрегатов, фрагментов и белков Е. coli. Конечный пул белка доводили до требуемой концентрации белка и анализировали с помощью SDS-PAGE, аналитической SEC и UV280, а идентичность подтверждали методом масс-спектрометрии.
[0317] Ренатурация и очистка dsFv-PE24 (cFP-0078): тельца включения НС-РЕ24 и LC солюбилизировали по отдельности в растворе, содержащем 8 М гуанидина гидрохлорид, 100 мМ Tris/HCl, 1 мМ EDTA, pH 8,0 плюс 100 мМ дитиотреитол (DTT), в течение ночи при комнатной температуре (1 г IB в 5 мл). Солюбилизаты доводили до pH 3 и центрифугировали, и осадок отбрасывали. После экстенсивного диализа против 7,2 М гуанидин-HCl, 10 мМ EDTA, pH 3,0, чтобы удалить DTT, определяли общую концентрацию белка биуретовым способом, а чистоту содержания НС и LC оценивали с помощью SDS-PAGE.
[0318] Солюбилизаты разводили 1:100 в буфере для ренатурации, содержащем 0,5 М аргинина, 2 мМ EDTA, pH 10 плюс 0,9 мМ GSH/GSSG, соответственно, в молярном соотношении 1:1, и хранили в течение ночи при температуре от 2 до 10°C.
[0319] Ренатурат разводили H2O до менее 3 мСм/см и закачивали на анионообменную колонку (AIEX), уравновешенную 20 мМ Tris/HCl, 1 мМ EDTA, pH 7,4. После промывания колонки уравновешивающим буфером белок элюировали градиентом до 20 мМ Tris/HCl, 1 мМ EDTA, 400 мМ NaCl, pH 7,4. Пиковые фракции, содержащие dsFv-PE24, объединяли, концентрировали и наносили на препаративную эксклюзионную колонку (size exclusion column, SEC) в 20 мМ Tris, 150 мМ NaCl, рН 7,4, для удаления агрегатов, фрагментов и белков Е. coli. Конечный пул белка доводили до требуемой концентрации белка и анализировали с помощью CE-SDS, аналитической SEC и UV280. Идентичность подтверждали путем масс-спектрометрии.
Пример 12.4: Белковый анализ cFP-0077 и cFP-0078.
[0320] Образцы анализировали по OD при 280 нм с помощью УФ-спектрофотометра для определения концентрации белка в растворе. Коэффициент экстинкции, необходимый для этого, рассчитывали из аминокислотной последовательности в соответствии с Pace et al., Protein Science, 4: 2411-2423 (1995). Эксклюзионную хроматографию (size-exclusion chromatography, SE-HPLC) проводили на колонках TSK-Gel300SWXL или Superdex 200 с 0,2 М калий-фосфатным буфером, включающим 0,25 М KCl, pH 7,0, в качестве подвижной фазы, чтобы определить содержание мономерных, агрегированных и деградированных форм в образцах. Электрофорез в полиакриламидном геле с додецилсульфатом натрия (sodium dodecyl sulfate, SDS) (в восстанавливающих и невосстанавливающих условиях) проводили для анализа чистоты комплексных препаратов в отношении продуктов распада, связанных с целевым продуктом, и примесей, не связанных с целевым продуктом (подробнее см. ниже) Масс-спектрометрию с ионизацией электрораспылением (electrospray ionisation mass spectrometry, ESI-MC) проводили с восстановленными (TCEP) образцами, чтобы подтвердить правильную массу/идентичность каждой цепи и выявить химические модификации. ESI-MC невосстановленных образцов проводили для анализа природы и качества полностью собранного белка и для обнаружения потенциальных побочных продуктов, связанных с целевым продуктом.
Способ SDS-PAGE и окрашивание Кумасси
[0321] Образец доводили буфером до концентрации белка 1 мг/мл. Для восстановления образца проводили следующую процедуру: готовили буфер для восстановления, содержащий 4 мл буфера для образцов (2×) и 1 мл восстанавливающего буфера (10×). Образец разводили 1:1 буфером для восстановления и инкубировали в течение 5 минут при 70°C.
[0322] Гель-электрофорез проводили при 125 В в течение 90 минут. Гели окрашивали SIMPLY BLUE Safe Stain (Invitrogen, кат. NO LC6065).
Пример 12.5: Сравнение цитотоксических свойств Fab- и dsFv-гибридных белков
[0323] Цитотоксическую активность гибридного белка формата dsFv-PE24 и формата Fab-PE24 сравнивали с использованием одной и той же гуманизированной SS1 специфической группировки на трех различных опухолевых клеточных линиях (MKN45, Н596 и А431Н9). Вкратце, клетки высевали в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP и клетки инкубировали в течение 72 часов. В конце периода инкубации жизнеспособность клеток определяли с использованием анализа CELLTITERGLOW.
[0324] В каждом случае кривые "доза - ответ" и значения IC50 для ингибирования жизнеспособности клеток были похожими для форматов dsFv-PE24 и Fab-PE24. Молярное соотношение значений IC50 приведено в таблице 18. В зависимости от анализируемой клеточной линии нацеленные РЕ24-гибридные белки были от нескольких сотен до одной тысячи раз более активными, чем ненацеленные РЕ24.
Пример 12.6: Сравнение сывороточной кинетики Fab- и dsFv-гибридных белков
[0325] Сывороточную кинетику следующих трех иммунотоксинов против мезотелина на основе экзотоксина А псевдомонад (РЕ) сравнивали на мышах SCID beige: SS1dsFv-PE38 (MW: 62,5 кДа), SS1dsFv-PE24 (MW: 49,9 кДа) и SS1Fab-PE24 (MW: 72,2 кДа). Группировку мышиного SS1-антитела использовали для всех конструкций. Кинетику сравнивали в дозах, эквимолярных 0,2 мг/кг (3,2 нмоль/кг) SS1P, что соответствует 0,231 мг/кг для SS1Fab-PE24 и 0,160 мг/кг для SS1dsFv-РЕ24.
[0326] Конструкции вводили в виде однократной внутривенной дозы и анализировали их уровни в сыворотке через 0,08, 0,5, 1, 1,5, 2, 3, 4, 5 и 7 часов после введения дозы. Девяти мышам в группе вводили исследуемый препарат и собирали кровь в шахматном порядке по три раза у каждого животного путем ретроорбитальной пункции, получая девять временных точек с n равно 3 образцов. Образцы сыворотки анализировали с помощью анализа ELISA, который выявляет только интактные тестируемые соединения, имеющие фрагмент антитела плюс РЕ-часть. В этом формате анализа cFP захватывается MSLN-покрытой поверхностью, и РЕ-группировка детектируется с помощью кроличьего поликлонального анти-РЕ-антитела и биотинилированного противокроличьего вторичного антитела.
[0327] Для каждой временной точки на графике откладывали средние сывороточные значения от трех животных для анализируемых групп вместе с архивными данными от мышей CD2F1. Конструкция SS1dsFv-PE24 очень быстро выводилась из сыворотки, имея период полужизни всего примерно 12 минут. В соответствии с архивными данными клиренс SS1P был гораздо более медленным, давая период полужизни в сыворотке от 35 до 44 минут (значения, полученные на основе измеренных и архивными данных, соответственно). Фармакокинетические свойства конструкции SS1Fab-PE24 были очень похожи на SS1dsFv-PE38 с периодом полужизни в сыворотке 43 минуты, и близкие значения были получены и для скорости клиренса, объема распределения, cmax и площади под кривой (таблица 19 и фиг. 19).
Пример 13
[0328] Этот пример демонстрирует гуманизацию антитела SS1 против мезотелина.
Пример 13.1: Разработка гуманизированных вариабельной областей тяжелой и легкой цепи.
[0329] Структуры VH- и VL-домена антитела SS1 были смоделированы in silico, и модель сравнивали со структурной базой данных человеческих доменов VH и VL. Панель наиболее структурно подобных V-доменов была выбрана для прививки CDR из SS1 в человеческие домены VH и VL. Кроме того, чтобы сузить выбор человеческих V-доменов, было принято во внимание сходство первичной последовательности при выравнивании первичной последовательности VH- и VL-домена из SS1 с репертуаром человеческих V-доменов. В некоторых вариантах гуманизации в человеческие каркасные области были введены обратные мутации на мышиные родительские остатки. Аналогичным образом, в некоторых вариантах были введены мутации в CDR, когда это было целесообразно, для потенциального повышения аффинности к антигену или для поддержания третичной структуры CDR.
[0330] Разработанные варианты V-доменов клонировали в векторы 6318 и 6319 с тяжелой цепью и легкой цепью с помощью уникальных сайтов клонирования для создания легких и тяжелых цепей человеческого IgG. Векторами с тяжелой цепью и легкой цепью котрансфицировали суспензионные клетки НЕК293 в микротитровальных планшетах для культивирования в матричной форме, чтобы получить культуры клеток, экспрессирующие полноразмерные IgG, имеющие все возможные комбинации тяжелой/легкой цепей. Через 5 дней культивирования при 37°C супернатант собирали и очищали с помощью аффинной хроматографии на белке А в микротитровальной шкале.
Пример 13.2: Клонирование гуманизированных вариабельных областей тяжелой и легкой цепи
[0331] Для манипулирования ДНК использовали стандартные способы, описанные в Sambrook, J. et al., см. выше. Молекулярно-биологические реагенты использовали в соответствии с инструкциями изготовителя. Нужные генные сегменты получали коммерческим путем методом генного синтеза. Синтезированные фрагменты генов клонировали в указанный экспрессионный вектор. ДНК-последовательности субклонированных фрагментов генов подтверждали секвенированием ДНК.
[0332] Векторы для экспрессии тяжелых цепей антитела: генные сегменты разработанных гуманизированных вариабельных доменов тяжелой цепи антитела клонировали в указанный экспрессионный вектор с помощью уникальных сайтов рестрикции HindIII и Xhol. Экспрессионный вектор разрабатывали для экспрессии вариабельного домена тяжелой цепи антитела, слитого с СН1-, шарнирным, СН2- и СН3-доменами человеческого антитела, в клетках HEK293, получая обычную тяжелую цепь антитела. Все домены были отделены нитронами. Помимо экспрессионной кассеты для тяжелой цепи антитела вектор содержал:
- сайт начала репликации из вектора pUC18 для репликации этой плазмиды в Е. coli,
- ген бета-лактамазы, который придает устойчивость к ампициллину в Е. coli,
- промотор SV40 и сайт начала экспрессии маркера селекции DHFR,
- ген мышиной дигидрофолатредуктазы (dihydrofolate reductase, DHFR) в качестве селективного маркера для экспрессии антитела, и
- раннюю сигнальную последовательность полиаденилирования SV40' ("ранний поли-А").
[0333] Транскрипционный блок тяжелой цепи антитела состоит из следующих элементов:
- немедленный ранний энхансер и промотор цитомегаловируса человека,
- 5'-нетранслируемая область зародышевого гена антитела человека,
- сигнальная последовательность тяжелой цепи мышиного иммуноглобулина, включающая интрон сигнальной последовательности (сигнальная последовательность 1, интрон, сигнальная последовательность 2 [L1- интрон-L2]),
- последовательность VH, за которой следует интрон,
- человеческие СН1-, шарнирный, СН2-, СН3-домены, разделенные интронами,
- сигнальная последовательность полиаденилирования бычьего гормона роста (bovine growth hormone, bGH) ("поли А"), и
- терминатор транскрипции человеческого гастрина (human gastrin transcription, HGT).
[0334] Векторы для экспрессии легких цепей антитела: генные сегменты разработанных гуманизированных вариабельных доменов легкой цепи антитела клонировали в указанный экспрессионный вектор с помощью уникальных сайтов рестрикции BsmI и Cell. Экспрессионный вектор разрабатывали для размещения вариабельного домена легкой цепи антитела в гибриде с доменом Ck человеческого антитела в клетках HEK293. Оба домена были разделены интронами. Помимо экспрессионной кассеты для легкой цепи антитела вектор содержал:
- сайт начала репликации из вектора pUC18 для репликации этой плазмиды в Е. coli,
- ген бета-лактамазы, который придает устойчивость к ампициллину в Е. coli.
[0335] Транскрипционный блок легкой цепи антитела состоит из следующих элементов:
- немедленный ранний энхансер и промотор цитомегаловируса человека,
- 5'-нетранслируемая область цитомегаловируса человека,
- последовательность интрона А цитомегаловируса человека,
- 5'-нетранслируемая область зародышевого гена антитела человека
- сигнальная последовательность тяжелой цепи мышиного иммуноглобулина, включающая интрон сигнальной последовательности (сигнальная последовательность 1, интрон, сигнальная последовательность 2 [L1-интрон-L2]) и уникальный сайт рестрикции BsmI на 3'-конце L2,
- домен VL с последующим интроном,
- человеческий Ск-домен,
- сигнальная последовательность полиаденилирования бычьего гормона роста (bGH) ("поли А"), и
- терминатор транскрипции человеческого гастрина (HGT).
Пример 13.3: Экспрессия гуманизированных антител
[0336] Временная трансфекция гуманизированных легких и тяжелых цепей антитела: Рекомбинантные варианты гуманизированного антитела получали путем временной трансфекции клеток HEK293-Freestyle (линии клеток человеческой эмбриональной почки 293, Invitrogen), выращенных в суспензии. Трансфицированные клетки культивировали в среде F17 (Gibco) или в среде Freestyle 293 (Invitrogen), либо в среде с добавлением 6 мМ глутамина, ультраглутамина (Biowhittake/Lonza) или L-глутамина (Sigma), с 8% CO2 при 37°C во встряхиваемых колбах в масштабе от 2 мл среды в планшетах с 48 глубокими лунками до 1 л среды в колбах. Реагент для трансфекции 293-Free (Novagen/Merck) использовали в соотношении количества реагента (мкл) к ДНК (мкг) как 4:3. Легкие и тяжелые цепи экспрессировали из двух различных плазмид, используя молярное отношение плазмид, кодирующих легкую цепь и тяжелую цепь, в пределах от 1:2 до 2:1, соответственно. Клеточные культуральные супернатанты, содержащие гуманизированное антитело, собирали через 6-8 суток после трансфекции. Общая информация касательно рекомбинантной экспрессии человеческих иммуноглобулинов, например, в клетках НЕК293, дана в: Meissner et al., Biotechnol. Bioeng., 75: 197-203 (2001). Супернатанты очищали с помощью аффинной хроматографии на колонке MabSelect Sure (GE, Protein А), уравновешенной PBS. После нанесения профильтрованных супернатантов антитела элюировали с использованием 50 мМ ацетата натрия, pH 3,2. Значение pH элюата немедленно доводили до pH более 6 с помощью 2 М Tris/HCl, pH 9,0, с последующим диализом в растворе 20 мМ гистидина, 140 мМ NaCl, pH 6,0. Антитела анализировали по UV280, SDS-PAGE и аналитической SEC. Последовательность подтверждали путем масс-спектрометрии.
Пример 13.4: Характеризация гуманизированных вариантов SS1.
[0337] ELISA-скрининг гуманизированных вариантов SS1: все варианты гуманизации SS1 в формате IgG подвергали скринингу на аффинность путем ELISA. 384-луночные микротитровальные планшеты MaxiSorp покрывали 0,5 мкг/мл анти-His-антитела (Novagen). После блокировки PBS-буфером с добавлением 2% BSA, 0,1% Tween 20 и 0,2 мкг/мл человеческого/собачьего/мышиного мезотелина (собственный/R&D Systems) проводили захват всех белков с His-меткой на планшете в течение одного часа. Планшеты промывали PBST-буфером (PBS плюс 0,1% Tween 20) и инкубировали с разведениями гуманизированных антител против мезотелина в PBS в течение 1 ч при комнатной температуре. Связывание антител определяли с помощью HRP-конъюгированного антитела против человеческого Fc (GE Healthcare). После последней промывки планшеты инкубировали с субстратом HRP. Абсорбцию измеряли при длине волны 370 нм на планшетном ридере ENVISION. Анализ подгонки кривой ЕС50 проводили с использованием плагина для анализа XLfit4 для программного обеспечения EXCEL (модель 205).
[0338] Для того чтобы нормировать полученные значения для титра IgG, определяли количество человеческого IgG путем сэндвич-ELISA с использованием планшетов, покрытых стрептавидином. Покрытые стрептавидином 384-луночные микротитровальые планшеты (Microcoat) инкубировали со смесью 0,25 мкг/мл биотинилированного антитела против человеческого IgG (Jackson Imm. Res.), 0,05 мкг/мл конъюгата противочеловеческого IgG с HRP (Jackson Imm. Res.) и разведениями гуманизированных против антител мезотелина. Через 1,5 часа инкубации при комнатной температуре (RT) планшеты промывали PBS-буфером с добавлением 0,1% Tween 20. Дабвляли субстрат HRP и измеряли абсорбцию при длине волны 370 нм на планшетном ридере ENVISION. Расчет данных проводили с использованием человеческого референсного IgG (собственный) в качестве стандарта для калибровки и с помощью плагина для анализа XLfit4 для программного обеспечения EXCEL (модель 205) для анализа путем подбора кривой.
[0339] В таблицах 20-21 ниже показаны данные ELISA для всех вариантов гуманизации. Измеряли ELISA/BIACORE-связывание с huMesothelin (ЕС50 нг/мл), результаты приведены в таблице 20 (собственный) и в таблице 21 (R&D). Нормированный по титру IgG, этот первичный скрининг выявил вариант VL001/VH001 в качестве одной из комбинаций с лучшим значением ЕС50.
[0340] BIAcore-скрининг гуманизированных вариантов SS1: лучшие варианты, содержащие CDR, наиболее близкие к SS1, были выбраны для кинетического анализа с помощью поверхностного плазмонного резонанса (SPR). Анализ на основе SPR использовали для определения кинетических параметров связывания между несколькими вариантами гуманизации MSLN PE cFP и человеческим мезотелином. Так, белок А иммобилизировали путем аминного сочетания с поверхностью биосенсорного чипа СМ5. Затем проводили захват образцов и вводили человеческий мезотелин. Поверхность сенсорного чипа подвергали регенерации между всеми циклами анализа. Наконец, получали константу равновесия KD, а также константы скорости kd и ka, путем подгонки данных по модели взаимодействия Ленгмюра 1:1. Примерно 175 единиц ответа (RU) белка А (10 мкг/мл) связывали с сенсорным чипом СМ5 при pH 4,0 с помощью набора для аминного сочетания, поставляемого компанией GE Healthcare (активация 10 минут). В качестве буфера для образцов и системного буфера выступал HBS-P + (0,01 М HEPES, 0,15 М NaCl, 0,005% поверхностно-активного вещества Р20, стерильно профильтрован, pH 7,4). Температуру проточной ячейки устанавливали на 25°C, а температуру отсека для образцов устанавливали на 12°C. Систему промывали рабочим буфером. Сайты связывания белка А насыщали IgG (примерно 0,03 мкг/мл), получая одинаковые уровни захвата для каждого образца, вводя его в течение 40 секунд со скоростью потока 10 мкл/мин. После этого один раствор человеческого мезотелина с концентрацией 50 нМ вводили в течение 120 секунд со скоростью потока 30 мкл/мин с последующей фазой диссоциации 180 секунд. Тем самым определение относительной KD позволяло ранжировать различные молекулы, связывающие MSLN. Каждый цикл подвергали регенерации двумя инъекциями глицин-HCl с pH 1,5 (30 секунд, 30 мкл/мин).
[0341] В таблице 22 ниже приведены данные BIAcore от 12 отобранных вариантов гуманизации. Окончательный вариант гуманизации VL01/VH01 показал одно из самых низких значений Kd среди всех вариантов гуманизации. В таблице 22 представлены результаты BIAcore для cFP. 15438-15457 и cFP. 15438-15459, все они содержат гуманизированный VH1. cFP.15438, который включает аминокислотную последовательность SEQ ID NO 45, демонстрирует самую высокую аффинность гуманизированных вариантов антитела SS1. Таким образом, VH в cFP.15438 обеспечивает выгодные связывающие свойства.
[0342] Пять лучших вариантов клонировали в формате Fab-линкер-РЕ, содержащем опубликованный линкер и LRO10 в качестве варианта РЕ24, экспрессировали, подвергали рефолдингу и очищали. Клонирование, экспрессию, рефолдинг и очистку проводили, как описано ниже для cFP-0205. Пять вариантов гуманизации в цитолитическом гибридном формате анализировали на стабильность при 37°C в течение 7 дней путем динамического рассеяния света, описанного в примере 9.2, эксклюзионной хроматографии, SDS-PAGE и масс-спектрометрии в различных временных точках.
[0343] Эксклюзионную хроматографию (SE-HPLC) проводили на колонках TSK-Gel300SWXL или Superdex 200 с 0,2 М калий-фосфатным буфером, содержащим 0,25 М KCl (pH 7,0), в качестве подвижной фазы, чтобы определить содержание мономерных, агрегированных и деградированных форм в образцах. Электрофорез в полиакриламидном геле с додецилсульфатом натрия (SDS) (в восстанавливающих и невосстанавливающих условиях) проводили для анализа чистоты комплексных препаратов в отношении продуктов распада, связанных с целевым продуктом, и примесей, не связанных с целевым продуктом (подробнее см. ниже) Масс-спектрометрию с ионизацией электрораспылением (ESI-MC) проводили с восстановленными (ТСЕР) образцами, чтобы подтвердить правильную массу/идентичность каждой цепи и выявить химические модификации. ESI-MC невосстановленных образцов проводили для анализа природы и качества полностью собранного белка и для обнаружения потенциальных побочных продуктов, связанных с целевым продуктом.
[0344] С помощью поверхностного плазмонного резонанса (SPR) контролировали активную концентрацию Fab-фрагментов в цитолитическом гибридном формате после температурного стресса при 37°C в течение 7 дней. Мезотелин иммобилизовали на поверхности SPR-биосенсора. При введении образца в проточные ячейки SPR-спектрометра он формировал комплекс с иммобилизованным мезотелином, что приводило к повышению массы, на поверхности сенсорного чипа и, следовательно, к более высокому ответу (такому как 1 RU, что определяется как 1 пг/мм2). После этого сенсорный чип подвергали регенерации, растворяя комплекс "образец - мезотелин". Затем полученный ответ оценивали относительно ответа, получаемого с референсным стандартом (активность которого принимается за 100%). Вначале примерно 50 единиц ответа (RU) человеческого MSLN (0,75 мкг/мл) связывали с сенсорным чипом С1 (GE Healthcare) при pH 4,5 с помощью набора для аминного сочетания от GE Healthcare. В качестве буфера для образцов и системного буфера выступал HBS-P+ (0,01 М HEPES, 0,15 М NaCl, 0,005% поверхностно-активного вещества Р20, стерильно профильтрован, pH 7,4). Температуру проточной ячейки устанавливали на 25°C, а температуру отсека для образцов устанавливали на 12°C. Систему промывали рабочим буфером. Затем вводили 5 нМ раствор конструкции MSLN РЕ cFP в течение 60 секунд со скоростью потока 30 мкл/мин с последующей фазой диссоциации 60 секунд. Затем поверхность сенсорного чипа подвергали регенерации двумя 20-секундными введениями раствора для регенерации (00,31 М KSCN, 1.22М MgCl2, 0,61 М мочевина, 1,22М гуанидин-HCl, 6,7 мМ EDTA) со скоростью потока 30 мкл/мин, после чего следовал дополнительный этап промывки буфером и 5-секундный период стабилизации.
[0345] Данные по стабильности получали путем инкубации 5 лучших гуманизированных вариантов в формате Fab-линкер-PE24LRO10 при 37°C в течение 7 дней. Результаты представлены в таблице 23. Как показано в таблице 23, вариант VH01/VL01 был единственным вариантом, который не показал никакой фрагментации после температурного стресса. При усиленном восстановлении VL01, как и всех комбинаций VL01, после температурного стресса образовывались только агрегаты, но осадок не выпадал. Отрицательные результаты измерений аффинности после температурного стресса возникали из-за этих агрегатов. Соответственно, вариант гуманизации VH1/VL1 (SEQ ID NO 45)/(SEQ ID NO 46) был выбран для дальнейшей разработки. VH1 (SEQ ID NO 45) обеспечивал благоприятные функциональные возможности и связывающие свойства. Сочетание VH1 (SEQ ID NO 45)/VL1 (SEQ ID NO 46) обеспечивало хорошую перспективность.
Пример 14
[0346] Этот пример показывает клонирование, экспрессию, рефолдинг и очистку химерного деиммунизированного PE LOR10-456A в виде Fab-гибрида с гуманизированным SS1 против мезотелина (cFP-0205).
[0347] Химерная РЕ-молекула против мезотелина cFP-0205 была получена после клонирования, экспрессии, рефолдинга и очистки. cFP-0205 (также называемый R205 или RG7787) включает аминокислотные последовательности SEQ ID NO 39 и 40.
[0348] Клонирование cFP-0205: для экспрессии cFP-0205 использовали систему вектор/хозяин Е. coli, которая делает возможной селекцию плазмиды без антибиотика с помощью комплементации ауксотрофии E. coli (PyrF) (ЕР 0972838 и US 6291245). Для манипуляций с ДНК были использованы стандартные способы, описанные в Sambrook, J. et al., см. выше. Молекулярно-биологические реагенты использовали в соответствии с инструкциями изготовителя. Нужные генные сегменты получали коммерческим путем методом генного синтеза. Синтезированные фрагменты генов клонировали в указанный экспрессионный вектор. ДНК-последовательности субклонированных фрагментов генов подтверждали секвенированием ДНК.
[0349] Экспрессионные плазмиды для продукции легкой цепи (LC) и тяжелой цепи (НС), соответственно, были получены следующим образом: плазмида LC 15496 является экспрессионной плазмидой для экспрессии легкой цепи антитела в Е. coli. Она была получена путем лигирования фрагмента VL-домена антитела в вектор с использованием сайтов рестрикции Ndel/BsiWI.
[0350] Плазмида для экспрессии легкой цепи в Е. coli содержит следующие элементы:
- сайт начала репликации из вектора pBR322 для репликации в Е. coli (соответствующий позициям 2517-3160 в соответствии с Sutcliffe et al., Quant. Biol., 43: 77-90(1979),
- ген URA3 от Saccharomyces cerevisiae, кодирующий оротидин-5'-фосфатдекарбоксилазу (Rose et al., Gene, 29: 113-124 (1984), которая позволяет выбирать плазмиды с помощью комплементации мутантных штаммов Е. coli pyrF (урацил-ауксотрофия),
- экспрессионную кассету легкой цепи антитела, содержащую:
- гибридный промотор Т5 (гибридный промотор T5-PN25/03/04 в соответствии с Bujard et al., Methods. Enzymol., 155: 416-433 (1987) и Stueber, et al., Immunol. Methods IV, 121-152 (1990), включающий синтетический сайт посадки рибосомы в соответствии с Stueber et al. (см. выше),
- вариабельный домен легкой цепи антитела, включающий CDR из SS1,
- человеческий Ск-домен,
- два терминатора транскрипции бактериофагального происхождения: терминатор λ-Т0 (Schwarz et al., Nature, 272: 410-414 (1978)) и fd-терминатор (Beck et al., Gene, 1-3: 35-58(1981)), и
- ген-репрессор lad из E.coli (Farabaugh, Nature, 274: 765-769 (1978).
[0351] Плазмида НС 18023 является экспрессионной плазмидой для экспрессии гибридного белка, включающего тяжелую цепь антитела, линкер с сайтом расщепления фурином и мутантный домен III из экзотоксина А псевдомонад (РЕ), в Е. coli. Она была получена путем лигирования фрагмента VH-домена в вектор с использованием сайтов рестрикции NdeI/BsrGI.
[0352] Плазмида для экспрессии цитолитического гибридного белка тяжелой цепи в Е. coli содержит следующие элементы:
- сайт начала репликации из вектора pBR322 для репликации в Е. coli (соответствующий позициям 2517-3160 в соответствии с Sutcliffe et al., Quant. Biol., 43: 77-90(1979),
- ген URA3 от Saccharomyces cerevisiae, кодирующий оротидин-5'-фосфатдекарбоксилазу (Rose et al., Gene, 29: 113-124 (1984), которая позволяет выбирать плазмиды с помощью комплементации мутантных штаммов Е. coli pyrF (урацил-ауксотрофия),
- экспрессионная кассета гибридного белка "тяжелая цепь - РЕ домен IIIʺ, содержащая:
- гибридный промотор Т5 (гибридный промотор T5-PN25/03/04 в соответствии с Bujard et al., Methods. Enzymol, 155: 416-433 (1987) и Stueber, et al., Immunol. Methods IV, 121-152 (1990), включающий синтетический сайт посадки рибосомы в соответствии с Stueber et al. (см. выше),
- вариабельный домен тяжелой цепи антитела, включающий CDR из SS1,
- человеческий СН1-домен,
- линкер, содержащий сайт расщепления фурином,
- мутантный вариант домена III из экзотоксина А псевдомонад
- два терминатора транскрипции бактериофагального происхождения: терминатор λ-T0 (Schwarz et al., Nature, 272: 410-414 (1978)) и fd-терминатор (Beck et al., Gene, 1-3: 35-58(1981)), и
- ген-репрессор lad из Е. coli (Farabaugh, Nature, 274: 765-769 (1978).
[0353] Экспрессия cFP-0205 в E. coli: штаммы E. coli K12 CSPZ-6 (thi-1, ΔpyrF) и CSPZ-13 (thi-1, ΔompT, ΔpyrF) трансформировали путем электропорации экспрессионными плазмидами NONO 15496 и 18023. Трансформированные клетки Е. coli сначала выращивали при 37°C на чашках с агаром. Для каждой трансформации колонии, собранные с этой чашки, переносили в перемешиваемую культуру объемом 3 мл и выращивали при 37°C до оптической плотности составляющей от 1 до 2 (измеренной при 578 нм). Затем 1000 мкл культуры смешивали с 1000 мкл стерильного 86% глицерина и немедленно замораживали при -80°C для длительного хранения. Правильный продукт экспрессии этого клона вначале проверяли в мелкомасштабных экспериментах со встряхиваемыми колбами и анализировали с помощью SDS-PAGE до передачи в ферментер объемом 10 л.
Предварительное культивирование:
[0354] Для предварительной ферментации использовали среду с определенным химическим составом (CD-PCMv2.60): NH4Cl 1,25 г/л, K2HPO4 *3H2O 18,3 г/л, цитрат 1,6 г/л, L-метионин 0,20 г/л, глюкоза*H2O 8,0 г/л, раствор микроэлементов 0,5 мл/л, MgSO4 *7H2O 0,86 г/л и тиамин*HCl 17,5 м г/л. Раствор микроэлементов содержал FeSO4 *7H2O 10,0 г/л, ZnSO4 *7H2O 2,25 г/л, MnSO4 *H2O 2,13 г/л, H3BO3 0,50 г/л, (NH4)6Mo7O24 *4H2O 0,3 г/л, CoCl2 *6H2O 0,42 г/л, CuSO4 *5H2O 1,0 г/л, растворенные в 0,5М HCl
[0355] Для предварительной ферментации в пяти встряхиваемых колбах объемом 1000 мл с четырьмя перегородками в 220 мл среды засевали 1,0 мл из ампулы с банком исследования. Культивирование проводили на ротационном шейкере в течение 11-12 часов при 37°C и скорости 170 оборотов в минуту до получения оптической плотности (578 нм) от 7 до 9. Встряхиваемые колбы объединяли и определяли оптическую плотность. Объем инокулята рассчитывали по формуле Vинок. равно 1000 мл*5/ODPC, и он зависел от оптической плотности предварительной культуры, которую использовали для инокуляции в партию среды для биореактора объемом 100 л с равным числом клеток.
Ферментация объемом 100 л:
[0356] Для ферментации в ферментере объемом 100 л (Sartorius, Мельзунген, Германия) использовали следующую партию с определенным химическим составом: KH2PO4 1.59 г/л, (NH4)2HPO4 7,45 г/л, K2HPO4 *3H2O 13,32 г/л, цитрат 2,07 г/л, L-метионин 1,22 г/л, NaHCO3 0,82 г/л, раствор микроэлементов 7,3 мл/л, MgSO4 *7H2O 0,99 г/л, тиамин*HCl 20,9 м г/л, глюкоза*H2O 29,3 г/л, биотин 0,2 мг/л и 1,2 мл/л 10% противопенного агента Synperonic. Раствор микроэлементов содержал FeSO4 *7H2O 10 г/л, ZnSO4 *7H2O 2,25 г/л, MnSO4 *H2O 2,13 г/л, CuSO4 *5H2O 1,0 г/л, CoCl2 *6H2O 0,42 г/л, (NH4)6Mo7O24 *4H2O 0,3 г/л и H3BO3 0,50 г/л, солюбилизированные в 0,5М растворе HCl.
[0357] Питательный раствор 1 содержал 700 г/л глюкозы*H2O, 7,4 г/л MgSO4 *7H2O и 0,1 г/л FeSO4 *7H2O. Питательный раствор 2 содержал KH2PO4 52,7 г/л, K2HPO4 *3H2O 139,9 г/л и (NH4)2HPO4 66,0 г/л. Все компоненты были растворены в деионизированной воде. Щелочной раствор для регулирования pH представлял собой водный 12,5% (вес/объем) раствор NH3, дополненный 11,25 г/л L-метионина.
[0358] Начиная с 42 л стерильной партии среды плюс рассчитанное количество инокулята из предварительного культивирования, периодическую ферментацию проводили при 31°C, pH 6,9±0,2, противодавлении 800 мбар и начальной скорости аэрации 50 л/мин. Относительное значение растворенного кислорода (рО2) поддерживали на уровне 50% в ходе ферментации за счет увеличения скорости мешалки до 1000 оборотов в минуту. После того, как первоначально введенная глюкоза истощалась, что обозначалось резким повышением значений растворенного кислорода, температуру сдвигали на 37°C, когда получали легкую цепь, или сохраняли постоянной, когда получали конструкцию тяжелой цепи, и через 15 минут ферментацию переводили в режим подпитки с началом введения обоих питательных растворов (600 и 140 г/ч соответственно). Скорость подачи раствора 2 поддерживали постоянной, в то время как скорость подачи раствора 1 увеличивали ступенчато с заранее определенным профилем подачи от 600 до 1400 г/ч, когда получали легкую цепь, или до 1600 г/ч, когда получали конструкцию тяжелой цепи, в течение 6-7 часов. Когда концентрация выделяемого газообразного диоксида углерода устанавливалась выше 2%, скорость аэрации ступенчато увеличивали на 10 л/мин с 50 до 100 л/мин в течение 5 часов. Экспрессию рекомбинантных целевых белков в виде телец включения, расположенных в цитоплазме, индуцировали добавлением 24 г IPTG при оптической плотности примерно 40 для вариабельной легкой Fab-цепи и 120 для вариабельной тяжелой Fab-цепи.
[0359] После 24 часов культивирования весь бульон охлаждали до температуры от 4 до 8°C и оставляли в течение ночи в сосуде ферментера. Бактерии собирали центрифугированием с помощью проточной центрифуги (13000 оборотов в минуту, 13 л/ч) и полученную биомассу хранили при -20°C до дальнейшей обработки (разрушения клеток) или немедленно обрабатывали для выделения телец включения.
Анализ образования продуктов:
[0360] Образцы забирали из ферментера, один перед индукцией, а остальные в определенные временные точки после индукции экспрессии белка. Образцы анализировали с помощью электрофореза в SDS-полиакриламидном геле. Из каждого образца одинаковое количество клеток (ODцелевое равно 10) суспендировали в 5 мл PBS-буфера и разрушали путем обработки ультразвуком на льду. Затем 100 мкл каждой суспензии центрифугировали (15000 оборотов в минуту, 5 минут), и каждый супернатант отбирали и переносили в отдельную пробирку. Это делали для различения растворимого и нерастворимого экспрессированного белка-мишени. К каждому супернатанту (растворимой фракции белка) добавляли 100 мкл, а к каждому осадку (нерастворимой фракции белка) 200 мкл SDS-буфера для образцов (Laemmli, Nature, 227: 680-685 (1970). Образцы нагревали в течение 15 мин при температуре 95°C в условиях интенсивного смешивания для солюбилизации и восстановления всех белков в образцах. После охлаждения до комнатной температуры 5 мкл каждого образца наносили на от 4 до 20% полиакриламидный гель TGX Criterion Stain Free (Bio-Rad). Кроме того, наносили 5 мкл стандарта молекулярных весов (Precision Plus Protein Standard, Bio-Rad) и 3 различных количества (0,3 мкл, 0,6 мкл и 0,9 мкл) количественного стандарта с известной концентрацией целевого белка (0,1 мкг/мкл).
[0361] Электрофорез проводили в течение 60 мин при 200 В, а после этого гель переносили на GelDoc EZ Imager (Bio-Rad) и обрабатывали в течение 5 мин УФ-излучением. Изображения геля анализировали с помощью программного обеспечения для анализа изображений IMAGE LAB (Bio-Rad). С помощью трех стандартов рассчитывали кривую линейной регрессии с коэффициентом более0,99 и рассчитывали концентрацию белка-мишени в исходном образце. Выход составлял до от 3 до 4 г/л Fab-легкой цепи и от 10 до 12 г/л гибрида PE-Fab-тяжелой цепи.
Подготовка препаратов телец включения:
[0362] Получение препаратов телец включения (IBP) из ферментеров объемом 100 л начинали сразу после сбора бактерий, ресуспендируя собранные бактериальные клетки в буфере 1 (12,1 г/л Tris, 0,246 г/л MgSO4 *7H2O, 12 мл/л 25% HCl). Объем буфера рассчитывали в зависимости от содержания сухого вещества в биомассе. Добавляли лизоцим (100 кЕд/мг, 0,12 мг/г сухой вес) и небольшое количество бензоназы (5 Ед/г сухой вес). Затем суспензию гомогенизировали при 900 бар (APV Rannie 5, 1 проход) для разрушения бактериальных клеток, добавляли дополнительную бензоназу (30 Ед/г сухой вес) и инкубировали в течение 30 мин при температуре 30-37°C. Затем добавляли первый промывочный буфер (60 г/л Brij, 87,6 г/л NaCl, 22,5 г/л EDTA, 6 мл/л 10н NaOH) и снова инкубировали суспензию в течение 30 минут. Следующий этап центрифугирования (CSC6, Westfalia) приводил к получению взвеси телец включения, которую ресуспендировали во втором промывочном буфере (12,1 г/л Tris, 7,4 г/л EDTA, 11 мл/л 25% HCl) и инкубировали в течение 20 минут. Еще один этап разделения давал тельца включения в одном стерильном пластиковом пакете, который немедленно перемещали в DSP-отдел.
Результаты:
[0363] Ферментация легкой цепи давала оптическую плотность от 170 до 190, измеренную при 578 нм, и конечный выход продукта от 10 до 12 г/л. Ферментация гибрида тяжелой цепи и токсина давала оптическую плотность от 210 до 230, измеренную при 578 нм, и конечный выход продукта от 3 до 4,5 г/л.
[0364] Рефолдинг и очистка cFP-0205: тельца включения НС-РЕ24 и LC солюбилизировали по отдельности в растворе, содержащем 8 М гуанидина гидрохлорид, 100 мМ Tris/HCl, 1 мМ EDTA, pH 8,0 плюс 100 мМ дитиотреитол (DTT), в течение ночи при комнатной температуре (1 г IB в 5 мл). Солюбилизаты доводили до pH 3 и центрифугировали, а осадок отбрасывали. После экстенсивного диализа против 8 М гуанидина-HCl, 10 мМ EDTA, pH 3,0, чтобы удалить DTT, определяли общую концентрацию белка биуретовым способом. Чистоту содержания НС и LC оценивали с помощью SDS-PAGE.
[0365] Солюбилизаты разводили в молярном соотношении 1:1 в буфере для ренатурации, содержащем 0,5 М аргинин, 2 мМ EDTA, pH 10 плюс 0,9 мМ GSH/GSSG, соответственно, при температуре 2-10°C. Концентрацию белка-мишени увеличивали поэтапно от 0,1 до 0,5 г/л, при этом время инкубации между двумя дозами составляло 2 ч. После 5 повышений раствор ренатурата хранили при температуре от 2 до 10°C в течение ночи.
[0316] Ренатурат разбавляли H2O до менее 3 мСм/см и закачивали на анионообменную колонку (AIEX), уравновешенную 20 мМ Tris/HCl, pH 7,4. После промывания колонки уравновешивающим буфером белок элюировали градиентом до 20 мМ Tris/HCl, 400 мМ NaCl, pH 7,4. Пиковые фракции, содержащие Fab-PE24, объединяли, концентрировали и наносили на препаративную эксклюзионную колонку (SEC) в 20 мМ Tris, 140 мМ NaCl, pH 5,5 или 6,0, для удаления агрегатов, фрагментов и белков Е. coli. Конечный пул белка доводили до требуемой концентрации белка и анализировали с помощью SDS-PAGE, аналитической SEC и UV280. Идентичность подтверждали методом масс-спектрометрии.
[0367] Анализ белка cFP-0205: Анализ образцов проводили так, как описано выше.
Характеризация конечного деиммунизированного РЕ-варианта в форме Fab-гибрида с гуманизированным SS1 против мезотелина (cFP0205).
[0368] Цитотоксичность и уничтожение опухолевых клеток in vitro: цитотоксическую активность CFP0205 сравнивали с таковой у SS1P в анализах клеточной жизнеспособности на различных раковых клеточных линиях и клетках первичной мезотелиомы. Результаты представлены в таблице 24. Как показано в таблице 24 для многих раковых клеточных линий, SS1P и cFP0205 имели сопоставимую активность (разница в значениях IC50 меньше или равна 3). Тем не менее, некоторые клеточные линии (например, Hu-1 и Hu-2), а также клетки первичной мезотелиомы (RH19, RH21) были значительно более чувствительными к cFP0205, чем к SS1P (значения IC50 в 6-10 раз ниже).
Характеризация конечного деиммунизированного РЕ-варианта в форме Fab-гибрида с гуманизированным SS1 против мезотелина (cFP0205).
[0369] Период полужизни в сыворотке: пилотное исследование проводили на яванских макаках (1 самец и 1 самка) с cFP0205 для оценки фармакокинетики отднократных доз. Животным внутривенно вводили 0,3 мг/кг cFP0205. Для фармакокинетического анализа брали образцы крови до введения дозы, через 0,083 (5 минут, в конце инфузии), 1, 2, 3, 5, 8, 24, 48 и 168 часов после введения дозы. Уровни свободного лекарственного препарата (пунктирная линия), а также общего препарата (черные квадраты и сплошная линия) определяли с помощью различных форматов ELISA (фиг. 20). Для определения общего уровня лекарственного препарата проводили одностадийную кислотную диссоциацию перед этапом захвата на планшете, покрытом мезотелином. Уровни свободного и общего лекарственного препарата откладывали на графике в зависимости от времени. Для сравнения архивные данные с SS1P также вставили в фиг.20 (черные круги и сплошная линия). Эти архивные данные были получены с помощью анализа цитотоксической активности в виде показаний для сывороточных уровней SS1P. Анализ цитотоксичности обнаруживает свободный лекарственный препарат, но также обнаруживает, по меньшей мере частично, лекарственный препарат, связанный с растворимым мезотелином, который может вносить вклад в наблюдаемую активность. Измеренные уровни свободного лекарственного препарата для cFP0205 были аналогичны первой фазе архивных данных с SS1P. Измеренные уровни общего лекарственного препарата для cFP0205 были сопоставимы со второй фазой кинетики, наблюдаемой для SS1P. Таким образом, не только у мышей, но также и у яванских макак кинетика сывороточного уровня SS1P и cFP0205 была очень сопоставимой.
Характеризация конечного деиммунизированного РЕ-варианта в форме Fab-гибрида с гуманизированным SS1 против мезотелина (cFP0205)
[0370] Сниженная нецелевая токсичность: мышам SCID beige с небольшими подкожными опухолями из клеток рака легкого Н596 (средний объем опухоли 100 мм3) вводили дозы 0,5, 1, 2 и 3 мг/кг cFP0205 3 раза в неделю через день (QOD) и контролировали потерю массы тела в течение одного месяца. Результаты показаны на фиг. 21.
[0371] Как показано на фиг. 21, максимально переносимая доза SS1P у мышей при внутривенном введении 3 раза в неделю QOD составляла 0,4 мг/кг.CFP0205, вводимый в таком же режиме, переносился мышами SCID beige в дозах до 3 мг/кг. Некоторая потеря массы тела наблюдалась во всех группах. Тем не менее, эффект дозы 0,5 мг/кг cFP0205 был неотличим от контроля с носителем. Дозозависимо возрастающая потеря массы тела имела место с 1, 2 и 3 мг/кг. В группе 3 мг/кг максимальная потеря веса составила 15%, и это было отмечено через 4 дня после последнего применения cFP0205. В группах 2 и 3 мг/кг после последнего введения не наблюдалось дополнительного снижения массы тела. Все животные начали восстанавливать массу тела с 5-го день после последнего введения и далее. Начальное восстановление массы тела было наиболее выраженным в группе 3 мг/кг. Таким образом, несмотря на схожие фармакокинетические свойства обеих молекул у мышей, cFP0205 переносился в дозе, почти в 10 раз превышающей дозу SS1P.
[0372] Токсикологическое исследование однократной внутривенной дозы (короткой инфузии) проводили на 8-недельных самках крыс Wistar Furth (масса тела 150-175 г) для того, чтобы оценить и сравнить нецелевую токсичность SS1P и cFP0205. В частности, исследовали риск индуцирования сосудистой утечки (отека) в легких, вызванной анализируемым продуктом. Три животных в каждой группе получали активное вещество или носитель путем внутривенной короткой инфузии со скоростью инфузии 0,3 мл/мин. Животных вскрывали через 24 часа после введения дозы. Легкие с главными бронхами и печень оценивали макроскопически, оценивали сбор жидкости в легких и проводили биохимический анализ образцов крови. Результаты приведены в таблице 25.
Ожидается, что период полужизни SS1P и cFP0205 в сыворотке у крыс будет очень похожим на тот, который показан у мышей.
[0373] Как показано в Таблице 25, у двух из трех крыс, которым внутривенно вводили 2 мг/кг SS1P, наблюдалось накопление жидкости в легких. Все животные в этой группе показали четкие клинические признаки токсичности, и у всех животных биохимические показатели свидетельствовали о серьезных повреждениях печени. Напротив, у всех трех животных, которым вводили 10 мг/кг cFP0205, не наблюдалось никаких признаков токсичности. Только у одного животного было незначительно повышено значение одного из ферментов печени. Эти результаты показывают, что молекула cFP0205 вызывает значительно меньшую гепатотоксичность и синдром утечки, чем классический формат иммунотоксина SS1P.
[0374] Пилотное токсикологическое исследование проводили на яванских макаках (1 самец и 1 самка) с cFP0205 для определения переносимости повторных ежедневных доз анализируемого продукта при внутривенном введении и для проверки на предмет возможного позднего начала токсичности (до 72 ч после последнего введения дозы). Наблюдения за животными после введения доз проводили сразу же, через 0,25, 0,5, 1, 2 и 4 часа после окончания введения дозы. Во время фазы введения дозы два раза в день наблюдали за общим поведением и внешним видом животных, а массу тела, потребление пищи и фекалии анализировали ежедневно.
[0375] Введение cFP0205 в дозе 1 мг/кг ежедневно в течение 5 дней подряд хорошо переносилось обоими животными. Не было отмечено ни одного кровоизлияния, острого воспаления или изъязвления в месте инъекции. Тот факт, что животные не показали никаких клинических признаков токсичности или непереносимости, позволил твердо установить 1 мг/кг/день ×5 как не сильно токсичную дозу, в то время как классический формат иммунотоксина, представленный SS1P, ранее был показан как непереносимый в дозе 0,3 мг/кг/день ×5 у животных, вызывая стойкие клинические признаки токсичности, такие как сгорбленная поза с тремором, пониженная активность и плохой аппетит. Таким образом, cFP0205 гораздо лучше переносится, чем SS1P, не только у мышей, но и у яванских макак, полностью перекрестно реактивных видов для целевых группировок этих иммуноконъюгатов.
Характеризация конечного деиммунизированного РЕ-варианта в форме Fab-гибрида с гуманизированным SS1 (cFP0205)
[0376] cFP0205 и SS1P метили Су5 на свободных аминогруппах. Мышам линии SCID beige с подкожными опухолями Н596 внутривенно вводили (4 мыши/группа) две флуоресцентно меченные молекулы в дозе 2 мг/кг. Через 6 часов животных умерщвляли. Легкие, печень и селезенку фиксировали формалином, заливали в воск и нарезали. Флуоресцентные изображения репрезентативных срезов этих органов снимали при разном увеличении. Результаты показаны на фиг.22A-22L.
[0377] Как показано на фиг. 22A-22L, введение SS1P привело к выраженному флуоресцентному окрашиванию ткани легких и селезенки и к массивному окрашиванию, по-видимому, ретикулоэндотелиальной системы в печени. Напротив, при использовании cFP0205 окрашивание легочной ткани не наблюдалось. Кроме того, окрашивание селезенки было значительно более слабым, и характер окрашивания отличался от животных, получавших SS1P. Кроме того, окрашивание cFP0205 в печени было резко снижено по сравнению с SS1P. Только выделенные одиночные клетки, которые, по-видимому, являются клетками Купфера, были флуоресцентно окрашены. Это говорит о том, что более низкая нецелевая токсичность Fab-PE24 по сравнению с dsFv-PE38 связана с различиями в распределении в нормальной ткани.
Пример 15
[0378] В этом примере показано получение 3-РЕ-вариантных химерных молекул против глипикана.
[0379] 3-РЕ-вариантную химерную молекулу против глипикана, содержащую линкер с аминокислотной последовательностью SEQ ID NO 36, РЕ с SEQ ID NO 37 (L010R-456A), вариабельный домен тяжелой цепи VH SEQ ID NO 61 и вариабельный домен легкой цепи SEQ ID NO 62 (GPC3-PE24-LR-LO10R-456A-длинный линкер), получали способом, аналогичным способу получения РЕ-вариантной химерной молекулы против мезотелина cFP-077, описанному в примере 12 (от клонирования до очистки).
[0380] 3-РЕ-вариантную химерную молекулу против глипикана, содержащую линкер с аминокислотной последовательностью SEQ ID NO 36, РЕ с SEQ ID NO 37 (L010R-456A), вариабельный домен тяжелой цепи VH SEQ ID NO 77 и вариабельный домен легкой цепи SEQ ID NO 78, также получали способом, аналогичным способу получения РЕ-вариантной химерной молекулы против мезотелина cFP-077, описанному в примере 12 (от клонирования до очистки).
Пример 16
[0381] Этот пример демонстрирует цитотоксические свойства 3-РЕ-вариантной химерной молекулы против глипикана GPC3-PE24-LR-LO10R-456A-длинный линкер по сравнению с GPC3-PE24-LR-LO10R.
[0382] Цитотоксическую активность GPC3-PE24-LR-LO10R сравнивали с таковой у GPC3-PE24-LR-LO10R-456A-длинный линкер на глипикан 3-положительной линии клеток рака печени HepG2. Вкратце, клетки HepG2 высевали по 6000 клеток/лунка в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP, и клетки инкубировали в течение 72 часов. В конце периода инкубации жизнеспособность клеток определяли с помощью анализа CELLTITERGLOW. Результаты приведены в таблице 26.
[0383] Как показано в таблице 26, для обеих молекул на клетках HepG2 наблюдались сопоставимые кривые "доза - ответ" для ингибирования жизнеспособности клеток. Значение IC50 для более полно деиммунизированного варианта РЕ с мутацией 456А и с более длинным линкером было даже немного ниже, чем для варианта LR-LO10R с коротким линкером. Нецелевой ("свободный РЕ24") или неправильно нацеленный РЕ24 ("CD33-Fab-PE"; HepG2-клетки не экспрессируют CD33) не показал какого-либо значительного снижения жизнеспособности клеток при концентрациях менее 30 мкМ. Таким образом, более полно деиммунизированный GPC3-нацеленный вариант LR-LO10R-456A-длинный линкер имел такую же или даже чуть более высокую цитотоксическую активность по сравнению с GPC3-нацеленным LR-LO10R-вариантом с коротким линкером. Из-за дополнительной 456А мутации в РЕ все В-клеточные эпитопы были удалены.
Пример 17
[0384] Этот пример показывает цитотоксичность деиммунизированных РЕ-гибридных белков с мутацией A458R.
[0385] Цитотоксичность SS1P, SS1-LR-GGS, SS1-LR-GGS-LO10, SS1-LR-GGS-LO10-A458R и SS1-LR-GGS-LO10-A458-456A измеряли способом WST. Результаты показаны в таблице 27.
[0386] Как показано в таблице 27, мутация A458R повышает активность SS1-LR-GGS-L010 на нескольких клеточных линиях. Добавление мутации 456А также повышает активность на нескольких клеточных линиях. А431/Н9 представляет собой плоскоклеточный рак, экспрессирующий мезотелин, а Hay представляет собой линию мезотелиомы. М30 также представляет собой клеточную линию мезотелиомы, a AGS представляет собой клеточную линию рака желудка. Hu-Meso представляет собой клетки от пациента с мезотелиомой, которые находились в культуре в течение нескольких месяцев.
Пример 18
[0387] Этот пример демонстрирует лечение опухолей НСС70 с помощью RG7787.
[0388] Самкам голых мышей инокулировали в интрамаммарный жир прокладку с клетками НСС70 в момент времени 0. НСС70 является клеточной линией рака молочной железы. Внутривенное введение RG7787 (2,5 мг/кг внутривенно) или носителя начинали на 6-й день и продолжали через день в течение всего 5 доз (стрелки). Оценивали размер опухоли. Результаты показаны на фиг. 24.
[0389] Как показано на фиг. 24, размер опухоли у мышей, получавших RG7787, был снижен по сравнению с контрольными мышами (получавшими носитель). Начиная с 10-го дня, между двумя группами наблюдается статистически значимая разница, на 14-й день р составляет менее0,00001.
Пример 19
[0390] Этот пример демонстрирует лечение опухолей KLM1 у мышей с помощью комбинации паклитаксела и RG7787.
[0391] Мышам в возрасте четырех недель и четырех дней вводили 4×106 клеток KLM1. KLM1 представляет собой клеточную линию рака поджелудочной железы, которая экспрессирует мезотелин. Через тринадцать дней мышам либо не вводили никакой агент, либо вводили паклитаксел (50 мг/кг), RG7787 (2,5 мг/кг) или комбинацию RG7787 (2,5 мг/кг) и паклитаксела (50 мг/кг). Размер опухоли оценивали в течение периода до 89 дней после введения. Результаты показаны на фиг. 23.
[0392] Как показано на фиг. 23, размер опухоли у мышей, которых лечили комбинацией паклитаксела и RG7787, уменьшался по сравнению с таковым у контрольных (нелеченных) мышей или у мышей, которым вводили только паклитаксел или только RG7787.
Пример 20
[0393] В данном примере показано лечение опухолей НСС70 у мышей с помощью комбинации паклитаксела и RG7787.
[0394] Самкам бестимусных голых мышей инокулировали клетки НСС70 в момент времени 0. Животным вводили носитель, RG7787 с внутрибрюшинным введением носителя, паклитаксел с внутривенным введением носителя или комбинацию паклитаксела и RG7787. Паклитаксел (50 мг/кг) вводили путем внутрибрюшинной инъекции в дни, отмеченные длинными стрелками. RG7787 (2,5 мг/кг) вводили внутривенно в дни, указанные короткими стрелками. Средние объемы опухолей с n равно 5 для мышей, получавших носитель, и n равно 6 для мышей, получавших RG7787, паклитаксел или комбинацию, отмечены. Результаты показаны на фиг. 25.
[0395] Как показано на фиг.25, размер опухоли у мышей, получавших комбинацию паклитаксела и RG7787, уменьшался по сравнению с контрольными мышами (носитель) или с мышами, которым вводили только паклитаксел или только RG7787.
Пример 21
[0396] Этот пример демонстрирует лечение опухолей MKN-28 у мышей с помощью комбинации паклитаксела и R205.
[0397] Бестимусным голым мышам инокулировали клетки MKN-28 в момент времени 0. MKN-28 представляет собой клеточную линию рака желудка, экспрессирующую мезотелин. Животным либо не вводили никакой агент, либо вводили только Roche 205 (R205 или 205), только паклитаксел (таксол) или комбинацию R205 и паклитаксела. Оценивали размер опухоли. Результаты показаны на фиг. 26.
Как показано на фиг.26, размер опухоли у мышей, которых лечили комбинацией паклитаксела и R205, уменьшался по сравнению с таковым у контрольных (нелеченных) мышей или у мышей, которым вводили только паклитаксел или только R205.
Пример 22
[0398] В этом примере показана противоопухолевая активность LMB-T18 in vivo.
Мышам с тяжелым комбинированным иммунодефицитом (severe combined immunodeficient, SCID) имплантировали клетки СА46. Через семь дней, когда объем опухоли превышал 100 мм3, мышам вводили PBS (контроль) или LMB-T18 (5 мг/кг × 4 или 7,5 мг/кг × 3) внутривенно. Мышам, получавшим 5,0 мг/кг, дозу вводили четыре раза, в дни 7, 9, 11 и 16, а группа с более высокой дозой получала 7,5 мг/кг три раза в дни 7, 9 и 11. Заметная регрессия опухолей наблюдалась у всех мышей (фиг.27Е) лишь с небольшой потерей веса (в среднем 6%). 5 из 7 мышей, получавших 5,0 мг/кг, сохранили полную регрессию опухоли на день 33, и 3 из 7 мышей сохранили полную регрессию опухоли в группе 7,5 мг/кг. Для оценки неспецифической токсичности LMB-T18 шести мышам с опухолями внутривенно вводили две дозы по 10 мг/кг QOD. Одна мышь продемонстрировала серьезную потерю веса и была подвергнута эвтаназии.
Пример 23
[0399] Этот пример демонстрирует, что LMB-T18 значительно уменьшил активацию Т-клеток.
[0400] Для того чтобы определить, уменьшает ли LMB-T18 стимуляцию Т-клеток или создает новые Т-клеточные эпитопы за счет мутаций, стимулировали РВМС от доноров с самым высоким ответом (n равно 13) и от пациентов с HCL и мезотелиомой (n равно 7) с помощью MP или LMB-T18. Клетки повторно стимулировали 39 новыми пептидами, представляющими различия между MP и LMB-T18. Наблюдалось снижение на 90% активации донорских Т-клеток (рменее0,0001 в t-тесте Стьюдента). Даже у пациентов с активированными Т-клетками наблюдалось снижение на 83% (рменее0,0001 в t-тесте Стьюдента). Кроме того, никакие новые эпитопы не были созданы за счет мутаций.
Пример 24
[0401] Этот пример демонстрирует, что LMB-T18 уменьшил связывание с антисывороткой от пациентов.
[0402] Антигенность LMB-T18 оценивали путем сравнения реактивности MP, HA22-LR и LMB-T18 в отношении сыворотки от пациентов с нейтрализующими антителами к MP. Связывание измеряли с помощью ICC-ELISA с сывороткой от 13 пациентов, леченных MP, оно показано на фиг. 27F. Было установлено, что как и HA22-LR, LMB-T18 значительно уменьшал связывание с сывороткой по сравнению с MP (рменее0,001 в одностороннем анализе ANOVA). Также было установлено, что LMB-T18 имел значительно более низкое связывание, чем HA22-LR (рменее0,001 в одностороннем анализе ANOVA), что указывает на то, что мутации в LMB-T18 снижают связывание с антисывороткой.
Пример 25
[0403] В этом примере показано получение анти-FAP-PE-вариантных химерных молекул.
[0404] Три анти-FAP-РЕ-вариантных химерных молекулы, содержащие:
(a) линкер, содержащий аминокислотную последовательность SEQ ID NO 36, РЕ, содержащий SEQ ID NO 37 (L010R-456A)), вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 94 (iFAP-PE24-LR-LO10R-456A-длинный линкер)
(b) линкер, содержащий аминокислотную последовательность SEQ ID NO 36, РЕ, содержащий SEQ ID NO 37 ((L010R-456A)), вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 294 (LCL4-PE24-LR-LO10R-456A-длинный-линкер) (в том числе VL-вариант SEQ ID NO 290), и
(c) линкер, содержащий аминокислотную последовательность SEQ ID NO 36, РЕ, содержащий SEQ ID NO 37 (Т-20), вариабельный домен тяжелой цепи VH SEQ ID NO 93 и вариабельный домен легкой цепи SEQ ID NO 290 (LCL4-T20);
были получены способом, аналогичным способу получения РЕ-вариантной химерной молекулы против мезотелина cFP-077, описанному в примере 12 (от клонирования до очистки), за исключением того, что описано ниже.
[0405] Анти-FAP-РЕ-вариантные химерные молекулы (b) и (с) включали модифицированный вариабельный домен легкой цепи (VL), в котором метионин в позиции 4 исходной VL-последовательности SEQ ID NO 94 заменяли лейцином, чтобы получить модифицированную VL-последовательность SEQ ID NO 290 ("LCL4"). Было обнаружено, что модифицированный вариабельный домен легкой цепи SEQ ID NO 290 уменьшает образование примесей, связанных с N-концевыми модификациями. Эти N-концевые модификации дают смесь вариантов с легкими цепями различной длины вследствие инициации экспрессии немодифицированной последовательности либо с N-концевого метионина, либо с метионина в позиции 4 в SEQ ID NO 94.
Предварительное культивирование:
[0406] Для предварительной ферментации использовали ту же среду с химически определенным составом (CD-PCMv2.20), которая описана в примере 12.
[0407] Культивирование проводили на ротационном шейкере в течение 8 часов при температуре 37°C и скорости 170 оборотов в минуту до получения оптической плотности (578 нм) 13,3 или 14,4. 150 мл культуры из предварительного культивирования использовали для инокуляции в партию среды для биореактора объемом 10 л.
Ферментация:
[0408] Для ферментации в ферментере BioStat С, DCU3, объемом 10 л (Sartorius, Мельзунген, Германия) использовали такую же парию среды с определенным химическим составом, которая описана в примере 12.
[0409] Один питательный раствор содержал 700 г/л глюкозы *H2O, 7,4 г/л MgSO4 *7H2O и 0,1 г/л FeSO4 *7H2O. Все компоненты растворяли в деионизированной воде. Щелочной раствор для регулирования pH представлял собой водный 12,5% (вес/объем) раствор NH3, дополненный 11,25 г/л L-метионина, 10 г/л лейцина и 10 г/л треонина.
[0410] Начиная с 6,24 л стерильной парии среды плюс 150 мл инокулята из предварительного культивирования, периодическую ферментацию проводили при 32°C, pH 6,9±0,2, противодавлении 800 мбар и начальной скорости аэрации 10 л/мин. Относительное значение растворенного кислорода (рО2) в ходе ферментации поддерживали на уровне 50% за счет увеличения скорости мешалки до 1500 оборотов в минуту. После того, как первоначально введенная глюкоза истощалась, что обозначалось резким повышением значений растворенного кислорода, температуру сдвигали на 32°C или 37°C, и через 15 минут ферментацию вводили в режим подпитки с началом введения обоих питательных растворов (60 и 14 г/ч, соответственно). Скорость подачи раствора увеличивали ступенчато с заранее определенным профилем подачи от 90 до 210 или 240 г/ч в течение 5,5 или 6,5 часов. Когда концентрация выделяемого газообразного диоксида углерода устанавливалась выше 2%, скорость аэрации постоянно увеличили с 10 до 20 л/мин в течение 5 часов. Экспрессию рекомбинантного белка индуцировали добавлением 3,6 г IPTG при оптической плотности примерно 40 или 120. Целевой белок экспрессировался в виде телец включения в цитоплазме.
[0411] После 24 часов культивирования была достигнута оптическая плотность 179 или 171, и цельный бульон охлаждали до температуры от 4 до 8°C. Бактерии собирали центрифугированием с помощью проточной центрифуги (4500 оборотов в минуту, 4°C, в течение 1 ч), и полученную биомассу хранили при -20°C до дальнейшей обработки (разрушения клеток).
Анализ образования продукта:
[0412] Специфические различия в сравнении со способом примера 12 описаны ниже:
[0413] Из каждого образца одинаковое количество клеток (ODцелевое равно 10) суспендировали в 5 мл PBS-буфера и разрушали путем обработки ультразвуком на льду. Затем 100 мкл каждой суспензии центрифугировали (8000 оборотов в минуту, 5 минут), и каждый супернатант отбирали и переносили в отдельную пробирку.
[0414] После добавления буфера Laemmli образцы нагревали в течение 45 мин при температуре 40°C в условиях интенсивного смешивания для солюбилизации и восстановления всех белков в образцах.
Подготовка препаратов телец включения:
[0415] Препараты телец включения (IBP) из ферментеров объемом 10 л обрабатывали способом, аналогичным способу, описанному в примере 12, за исключением того, что после разрушения бактериальных клеток добавляли дополнительную бензоазу (30 Ед/г сухой вес) и инкубировали в течение 60 минут при 25°C.
[0416] Солюбилизацию, ренатурацию и очистку проводили способом, аналогичным способу, описанному в примере 12. Были использованы следующие последовательности:
- Последовательность химерной полноразмерной тяжелой цепи iFAP-РЕ24-LR-LO10R-456А-длинный линкер и LCL4-PE24-LR-LO10R-456A-длинный линкер, содержащая вариабельный домен VH SEQ ID NO 93, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, and а РЕ comprising SEQ ID NO 37 (SEQ ID NO 291);
- Последовательность химерной конструкции тяжелой цепи LCL4-T20, содержащая полноразмерную тяжелую цепь, содержащую вариабельный домен VH SEQ ID NO 93, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и PE, содержащий SEQ ID NO 289 (T18/T20) (SEQ ID NO 292);
- Последовательность полноразмерной легкой цепи iFAP (SEQ ID NO 293), содержащая вариабельный домен легкой цепи SEQ ID NO 94 и константную область;
- Последовательность полноразмерной легкой цепи LCL4 (SEQ ID NO 294), содержащая вариабельный домен легкой цепи SEQ ID NO 290 и константную область; и
- Последовательность вариабельного домена легкой цепи SEQ ID NO 290 (с мутацией M4L в позиции 4 (в сравнении с SEQ ID NO 94).
Пример 26
[0417] Этот пример демонстрирует цитотоксичность анти-FAP-PE-вариантных химерных молекул iFAP-PE24-LR-LO10R-456A-длинный линкер, LCL4-PE24-LR-LO10R-456A-длинный линкер и LCL4-T20.
[0418] Цитотоксичность iFAP-PE24-LR-LO10R-456A-длинный линкер сравнивали с таковой у LCL4-PE24-LR-LO10R-456A-длинный линкер и LCL4-T20 ("cFP") в отношении FAP-положительной клеточной линии фибробластов MRC-5, FAP-положительной клеточной линии десмопластической меланомы LOX-IMVI и FAP-положительной клеточной линии саркомы OsA-CL. Вкратце, клетки высевали с плотностью 10000 клеток/лунка в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP и клетки инкубировали в течение 72 часов. В конце периода инкубации определяли жизнеспособность клеток с помощью анализа CELLTITER GLO. Результаты представлены в таблице 28 и таблице 29.
[0419] Как показано в таблице 28, наблюдались сравнимые величины IC50 для ингибирования жизнеспособности клеток на всех трех тестируемых клеточных линиях для iFAP-PE24-LR-LO10R-456A-длинный линкер (3 разных партии) и для LCL4-PE24-LR-LO10R-456A-длинный линкер. Как показано в таблице 29, LCL4-T20 также показала сильное ингибирование жизнеспособности клеток. Таким образом, iFAP-PE24-LR-L010 R-456А-длинный линкер, LCL4-PE24-LR-L010R-456A-длинный линкер и LCL4-T20 показали сильное цитотоксическое воздействие на FAP-положительные опухолевые клеточные линии и фибробласты.
Пример 27
[0420] В этом примере показано получение анти-CAIX-РЕ-вариантных химерных молекул.
[0421] Две анти-CAIX-РЕ-вариантные химерные молекулы, включающие:
(а) линкер, содержащий аминокислотную последовательность SEQ ID NO 36, РЕ, содержащий SEQ ID NO 37 (L010R-456A), вариабельный домен тяжелой цепи VH SEQ ID NO 125 и вариабельный домен легкой цепи SEQ ID NO 126; или
(b) линкер, содержащий аминокислотную последовательность SEQ ID NO 36, РЕ, содержащий SEQ ID NO 289 (Т-20), вариабельный домен тяжелой цепи VH SEQ ID NO 125 и вариабельный домен легкой цепи SEQ ID NO 126;
были получены способом, аналогичным способу, описанному для анти-мезотелин-РЕ-вариантной химерной молекулы cFP-077 из примера 12 (от клонирования до очистки), за исключением того, что описано ниже.
[0422] Образцы анализировали по OD 280 нм с помощью УФ-спектрофотометра для определения концентрации белка в растворе. Материалы для SDS-PAGE и устройство для окрашивания Кумасси приведены в таблице 30 ниже.
[0423] После добавления буфера Laemmli образцы нагревали в течение 45 мин при температуре 40°C в условиях интенсивного смешивания для солюбилизации и восстановления всех белков в образцах.
[0424] Образец доводили буфером до концентрации белка 1 мг/мл. Образец восстанавливали с помощью буфера для восстановления, содержащего 4 мл буфера для образцов (2×) и 1 мл восстанавливающего буфера (10×). Образцы восстанавливали путем разведения пробы 1:1 буфером для восстановления и инкубации образца в течение 10 минут при 70°C.
[0425] Гель-электрофорез проводили при 200 В в течение 40 минут. Гели окрашивали SIMPLY BLUE Safe Stain (Invitrogen, кат. NO LC6065).
Подготовка препаратов телец включения:
[0426] Препараты телец включения (IBP) из ферментеров объемом 10 л обрабатывали способом, аналогичным способу, описанному в примере 12, за исключением того, что после разрушения бактериальных клеток добавляли дополнительную бензоазу (30 Ед/г сухой вес) и инкубировали в течение 60 минут при 25°C.
[0427] Солюбилизацию, ренатурацию и очистку проводили способом, аналогичным способу, описанному в примере 12.
[0428] Были использованы следующие последовательности:
- Последовательность химерной конструкции тяжелой цепи CAIX-PE24-LR-LO10R-456A-длинный линкер (SEQ ID NO 295), содержащая вариабельный домен тяжелой цепи VH SEQ ID NO 125, линкер, содержащий аминокислотную последовательность SEQ ID NO 36, и РЕ, содержащий SEQ ID NO 37;
- Последовательность химерной конструкции тяжелой цепи CAIX-T20 (SEQ ID NO 296), содержащая вариабельный домен тяжелой цепи VH SEQ ID NO 125, линкер, содержащий аминокислотную последовательность SEQ ID NO 36 и РЕ, содержащий SEQ ID NO 289 (Т18/Т20); и
- Последовательность полноразмерной легкой цепи (SEQ ID NO 297), содержащая вариабельный домен легкой цепи SEQ ID NO 126) и константную область.
Пример 28
[0429] Этот пример демонстрирует цитотоксичность (уничтожение опухолевых клеток in vitro) анти-CAIX-РЕ-вариантных химерных молекул CAIX-PE24-LR-LO10R-456А-длинный линкер и CAIX-T20.
[0430] Цитотоксичность CAIX-PE24-LR-LO10R-456A-длинный линкер и CAIX-Т20 ("cFP") сравнивали в анализах клеточной жизнеспособности с помощью CAIX-экспрессирующих клеток RCC-MF. Вкратце, клетки высевали с плотностью 7500 клеток/лунка в 96-луночные планшеты. После культивирования в течение ночи в среду добавляли различные концентрации cFP и клетки инкубировали в течение 72 часов. В конце периода инкубации определяли жизнеспособность клеток с помощью анализа CELLTITER GLO. Результаты представлены в таблице 31.
[0431] Таким образом, CAIX-PE24-LR-LO10R-456A-длинный линкер и CAIX-Т20 показали мощное цитотоксическое воздействие на CAIX-положительные опухолевые клеточные линии.
[0432] Все ссылки, включая публикации, патентные заявки и патенты, процитированные в данном документе, включены в него посредством ссылки в той же степени, как если бы про каждую ссылку было отдельно и конкретно указано, что она включена в данный документ посредством ссылки и изложена в полном объеме.
[0433] Использование терминов в единственном числе и выражения "по меньшей мере один" и подобных ссылок в контексте описания изобретения (особенно в контексте следующей ниже формулы изобретения) должно толковаться как охватывающее как единственное, так и множественное число, если иное не указано в данном документе, или если это явно не противоречит контексту. Использование термина "по меньшей мере один" с последующим списком из одного или более чем одного элемента (например, "по меньшей мере один из А и В") должно быть истолковано как один элемент, выбранный из перечисленных элементов (А или В) или любая комбинация двух или более из перечисленных элементов (А или В), если иное не указано в данном документе, или если это явно не противоречит контексту. Термины "содержащий", "имеющий" и "включающий" должны быть истолкованы как открытые термины (т.е. означающие "включающий, но не ограничиваясь этим"), если не указано иное. Указание диапазонов значений в данном документе предназначено только для использования в качестве быстрого способа указать индивидуально на каждое отдельное значение, попадающее в диапазон, если в данном документе не указано иное, и каждое отдельное значение включено в описание, как если бы оно было индивидуально указано в данном документе. Все описанные в данном документе способы могут быть выполнены в любом подходящем порядке, если в данном документе не указано иное, или если это явно не противоречит контексту. Использование любого и всех примеров или выражений (например, "такой как") в данном документе предназначено только для лучшего освещения изобретения и не накладывает ограничений на объем изобретения, если не заявлено иное. Ни одно из выражений в описании не должно быть истолковано как указание на какой-либо не заявленный элемент как существенный для осуществления данного изобретения.
[0434] В данном документе описаны предпочтительные воплощения согласно данному изобретению, в том числе лучший способ осуществления изобретения, известный авторам данного изобретения. Вариации этих предпочтительных воплощений могут стать очевидны специалистам в данной области после прочтения приведенного выше описания. Авторы данного изобретения ожидают, что квалифицированные специалисты будут использовать такие вариации в зависимости от обстоятельств, и авторы данного изобретения подразумевают, что данное изобретение может быть осуществлено на практике другим путем, отличающимся от конкретно описанного в данном документе. Соответственно, данное изобретение включает все модификации и эквиваленты объекта изобретения, изложенного в формуле изобретения, прилагаемой к данному документу, в соответствии с действующим законодательством. Кроме того, любая комбинация описанных выше элементов во всех возможных вариантах охватывается изобретением, если иное не указано в данном документе, или если это явно не противоречит контексту.
Claims (129)
1. Экзотоксин А псевдомонад (РЕ, от англ. Pseudomonas exotoxin), характеризующийся цитотоксической активностью и сниженной иммуногенностью по сравнению с РЕ дикого типа, имеющий аминокислотную последовательность SEQ ID NO 1, где аминокислотный остаток R456 замещен на аланин, один или в сочетании одним или более чем одним из аминокислотных остатков F443, замещенным на аланин, L477, замещенным на гистидин, R494, замещенным на аланин, и L552, замещенным на глутаминовую кислоту или аспарагин, определенных относительно SEQ ID NO 1,
и, необязательно, может быть:
(i) дополнительная замена одного или более чем одного аминокислотного остатка в одном или более чем одном B-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, К590, Q592 и L597, определенного относительно SEQ ID NO 1, на остаток природной аминокислоты,
(ii) дополнительная замена одного или более чем одного аминокислотного остатка в одном или более чем одном T-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенного относительно SEQ ID NO 1,
(iii) делеция одного или более чем одного из смежных аминокислотных остатков среди остатков с 1 по 273 и с 285 по 394, определенных согласно SEQ ID NO 1, или
(iv) сочетание любого из (i)-(iii).
2. РЕ по п. 1, где РЕ имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном B-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, K590, Q592 и L597, определенного относительно SEQ ID NO 1, на остаток природной аминокислоты,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном T-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенного относительно SEQ ID NO 1,
(iii) делецию одного или более чем одного из смежных аминокислотных остатков среди остатков с 1 по 273 и с 285 по 394, определенных согласно SEQ ID NO 1, или
(iv) сочетание любого из (i)-(iii).
3. Выделенный мутантный экзотоксин А псевдомонад (РЕ), характеризующийся цитотоксической активностью и сниженной иммуногенностью по сравнению с РЕ дикого типа, имеющий последовательность следующей формулы:
R1 n-FCS-R2 n- R3 n-фyнкциoнaльный домен РЕ III
где n равно 1 для каждого из R1 и R2 и равно 0 или 1 для R3,
R1 представляет собой от 1 до 10 аминокислотных остатков FCS (от англ. furin cleavage sequence) представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет аминоконец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более чем один из смежных остатков среди остатков с 365 по 394 последовательности SEQ ID 1; и
функциональный домен РЕ III представляет собой остатки с 395 по 613 последовательности SEQ ID NO 1, где аминокислотный остаток R456 замещен на аланин один или в сочетании с одним или более чем одним из аминокислотных остатков: F443, замещенным на аланин; L477, замещенным на гистидин; R494, замещенным на аланин, и L552, замещенным на глутаминовую кислоту или аспарагин, определенных относительно SEQ ID NO 1,
и, необязательно, может быть:
(i) дополнительная замена одного или более чем одного аминокислотного остатка в одном или более чем одном B-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, K590, Q592 и L597, определенного относительно SEQ ID NO 1, на остаток природной аминокислоты,
(ii) дополнительная замена одного или более чем одного аминокислотного остатка в одном или более чем одном T-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенного относительно SEQ ID NO 1, или
(iii) вместе (i)-(ii).
4. Мутантный РЕ по п. 3, где РЕ имеет:
(i) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном B-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, K590, Q592 и L597, определенного относительно SEQ ID NO 1, на остаток природной аминокислоты,
(ii) дополнительную замену одного или более чем одного аминокислотного остатка в одном или более чем одном T-клеточном эпитопе, которая представляет собой замену одного или более чем одного аминокислотного остатка R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенного относительно SEQ ID NO 1, или
(iii) вместе (i) и (ii).
5. Мутантный РЕ по п. 3 или 4, характеризующийся тем, что FCS представлена формулой Р4-Р3-Р2-Р1, где Р4 представляет собой аминокислотный остаток на аминоконце, Р1 представляет собой аминокислотный остаток на карбоксильном конце, Р1 представляет собой остаток аргинина или лизина, и последовательность может расщепляться фурином на карбоксильном конце Р1.
6. Мутантный РЕ по п. 5, характеризующийся тем, что FCS: (i) дополнительно содержит аминокислотные остатки на аминоконце, представленные Р6-Р5, (ii) дополнительно содержит аминокислотные остатки на карбоксильном конце, представленные Р1'-Р2', (iii) если Р1 представляет собой остаток аргинина или лизина, то Р2' представляет собой триптофан, а Р4 представляет собой аргинин, валин или лизин, при условии, что если Р4 не является аргинином, то Р6 и Р2 являются основными остатками, и (iv) последовательность может расщепляться фурином на карбоксильном конце Р1.
7. Мутантный РЕ по п. 3 или 4, характеризующийся тем, что функциональный домен III РЕ состоит из последовательности остатков с 395 по 613 последовательности SEQ ID NO 1.
8. Мутантный РЕ по п. 3 или 4, где мутантный РЕ содержит между FCS и доменом III РЕ один или более чем один из смежных остатков с 365 по 394 последовательности SEQ ID NO 1.
9. Мутантный РЕ по п. 3 или 4, где FCS представляет собой SEQ ID NO 8.
10. Мутантный РЕ по п. 3 или 4, где R1 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 282, R2 представляет собой линкер с аминокислотной последовательностью SEQ ID NO 284 и FCS представляет собой SEQ ID NO 8.
11. Мутантный РЕ по п. 3 или 4, где n равен 0 для R3.
12. Мутантный РЕ по п. 3 или 4, где функциональный домен III РЕ содержит аминокислотную последовательность SEQ ID NO 37.
13. Мутантный РЕ по п. 3 или 4, где R1 n-FCS-R2 n представляет собой SEQ ID NO 36.
14. РЕ по любому из пп. 1-4, где дополнительная замена аминокислоты в одном или более чем одном B-клеточном эпитопе представляет собой замену аланином, глицином, серином или глутамином одного или более чем одного из аминокислотных остатков Е282, Е285, Р290, R313, N314, Р319, D324, Е327, Е331, Q332, D403, D406, R412, R427, Е431, R432, D461, R463, R467, R490, R505, R513, Е522, R538, Е548, R551, R576, K590, Q592 и L597, определенных относительно SEQ ID NO 1.
15. РЕ по любому из пп. 1-4, где РЕ имеет дополнительную замену аминокислоты в одном или более чем одном T-клеточном эпитопе и дополнительная замена аминокислоты в одном или более чем одном T-клеточном эпитопе представляет собой замену аланином, глицином, серином или глутамином одного или более чем одного из аминокислотных остатков R421, L422, L423, А425, R427, L429, Y439, Н440, F443, L444, А446, А447, I450, 463-519, R551, L552, Т554, I555, L556 и W558, определенных относительно SEQ ID NO 1.
16. РЕ по любому из пп. 1-4, где замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену аланином аминокислотного остатка R456; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену глутаминовой кислотой аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а дополнительная замена аминокислоты в одном или более чем одном B-клеточном эпитопе представляет собой:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538;
определенных относительно SEQ ID NO 1.
17. РЕ по любому из пп. 1-4, где замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка R456, РЕ имеет остаток аргинина в позиции 458, а дополнительная замена аминокислоты в одном или более чем одном B-клеточном эпитопе представляет собой:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538;
определенных относительно SEQ ID NO 1.
18. РЕ по любому из пп. 1-4, где замена одного или более чем одного из аминокислотных остатков F443, R456, L477, R494 и L552 представляет собой замену аланином аминокислотного остатка F443; замену аланином аминокислотного остатка R456; замену гистидином аминокислотного остатка L477; замену аланином аминокислотного остатка R494; и замену аспарагином аминокислотного остатка L552, РЕ имеет остаток аргинина в позиции 458, а дополнительная замена аминокислоты в одном или более чем одном В-клеточном эпитопе представляет собой:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538;
определенных относительно SEQ ID NO 1.
19. Мутантный РЕ по п. 3 или 4, где один или более чем один из аминокислотных остатков F443, L477, R494 и L552, определенных относительно SEQ ID NO 1, является замещенным.
20. Выделенный мутантный экзотоксин А псевдомонад (РЕ), характеризующийся цитотоксической активностью и сниженной иммуногенностью по сравнению с РЕ дикого типа, имеющий последовательность следующей формулы:
R1 n-FCS-R2 n- R3 n-фyнкциoнaльный домен III РЕ
где n равно 1 для каждого из R1 и R2 и равно 0 или 1 для R3,
R1 представляет собой от 1 до 10 аминокислотных остатков,
FCS представляет собой фурин-расщепляемую последовательность аминокислотных остатков, которая расщепляется фурином и имеет аминоконец и карбоксильный конец,
R2 представляет собой от 1 до 10 аминокислотных остатков;
R3 представляет собой 1 или более чем один из смежных остатков среди остатков с 365 по 394 SEQ ID 1; и
функциональный домен РЕ III представляет собой остатки с 395 по 613 SEQ ID NO 1, где РЕ включает аргинин в позиции 458 и замену на аланин в позиции R456 и где РЕ имеет:
(a) замену аланином аминокислотного остатка R427;
(b) замену аланином аминокислотного остатка R463;
(c) замену аланином аминокислотного остатка R467;
(d) замену аланином аминокислотного остатка R490;
(e) замену аланином аминокислотного остатка R505; и
(f) замену аланином аминокислотного остатка R538,
где позиции определены относительно SEQ ID NO 1.
21. Химерная молекула для ингибирования роста раковой клетки-мишени, содержащая (а) нацеливающий на указанную раковую клетку-мишень агент, конъюгированный непосредственно или опосредованно через линкер с (b) РЕ по любому из пп. 1-20.
22. Химерная молекула для ингибирования роста раковой клетки-мишени, содержащая (а) нацеливающий на указанную раковую клетку-мишень агент, слитый непосредственно или опосредованно через линкер с (b) РЕ по любому из пп. 1-20.
23. Химерная молекула по п. 21 или 22, где нацеливающий агент представляет собой моноклональное антитело или антигенсвязывающую часть моноклонального антитела.
24. Химерная молекула по п. 23, где моноклональное антитело или антигенсвязывающая часть моноклонального антитела специфически связывается с маркером клеточной поверхности, выбранным из группы, состоящей из: CD19, CD21, CD22, CD25, CD30, CD33, CD79b, рецептора трансферрина, рецептора эпидермального фактора роста (EGF, от англ. epidermal growth factor), мезотелина, кадгерина, антигена Льюиса Y, глипикана-3, белка активации фибробластов альфа (FAP, от англ. fibroblast activation protein alpha), простатического специфического мембранного антигена (PSMA, от англ. prostate specific membrane antigen), карбоангидразы IX (CA9 или CAIX, от англ. carbonic anhydrase), молекулы адгезии нервных клеток L1 (L1CAM, от англ. cell adhesion molecule), эндосиалина, HER3 (активированная конформация члена 3 семейства рецепторов эпидермального фактора роста), комплекса Alk1/BMP9 (киназа 1 анапластической лимфомы/костный морфогенетический белок 9), TPBG или 5Т4 гликопротеин трофобласта (TPBG или 5Т4, от англ. trophoblast glycoprotein), CD33 (связывающий сиаловые кислоты lg-подобный лектин 3, миелоидный антиген клеточной поверхности), CD123 (рецептор альфа интерлейкина 3), MUC1 (опухоль-ассоциированный эпителиальный муцин), ROR1 (рецепторный тирозинкиназоподобный поверхностный антиген), HER1 (активированная конформация рецептора эпидермального фактора роста) и CLL1 (семейство лектиновых доменов С-типа 12, член А).
25. Химерная молекула по п. 21 или 22, где нацеливающий агент выбран из группы, состоящей из: В3, RFB4, SS, SS1, MN, MB, HN1, HN2, MORAb-009, их антигенсвязывающих частей и антигенсвязывающей части НА22.
26. Химерная молекула по п. 21 или 22, где нацеливающий агент представляет собой гуманизированное SS1 или антигенсвязывающую часть гуманизированного SS1.
27. Химерная молекула по п. 21 или 22, где нацеливающий агент содержит:
(a) SEQ ID NO 31 и 34;
(b) SEQ ID NO 45 и 46;
(c) SEQ ID NO 61 и 62;
(d) SEQ ID NO 77 и 78;
(e) SEQ ID NO 93 и 94;
(f) SEQ ID NO 109 и 110;
(g) SEQ ID NO 125 и 126;
(h) SEQ ID NO 141 и 142;
(i) SEQ ID NO 157 и 158;
(j) SEQ ID NO 173 и 174;
(k) SEQ ID NO 49, 50, 53, 54, 57, и 58;
(l) SEQ ID NO 65, 66, 69, 70, 73, и 74;
(m) SEQ ID NO 81, 82, 85, 86, 89, и 90;
(n) SEQ ID NO 97, 98, 101, 102, 105, и 106;
(о) SEQ ID NO 113, 114, 117, 118, 121, и 122;
(p) SEQ ID NO 129, 130, 133, 134, 137, и 138;
(q) SEQ ID NO 145, 146, 149, 150, 153, и 154;
(r) SEQ ID NO 161, 162, 165, 166, 169, и 170;
(s) SEQ ID NO 177, 178, 181, 182, 185, и 186;
(t) SEQ ID NO 31-32 и 34-36;
(u) SEQ ID NO 33 и 38; или
(v) SEQ ID NO 93 и 290.
28. Химерная молекула по п. 21 или 22, где химерная молекула содержит линкер, содержащий SEQ ID NO 36.
29. Химерная молекула по п. 21 или 22, содержащая:
(a) SEQ ID NO 39 и 40;
(b) SEQ ID NO 41 и 42;
(c) SEQ ID NO 43 и 44;
(d) SEQ ID NO 291 и 293;
(e) SEQ ID NO 291 и 294;
(f) SEQ ID NO 292 и 294;
(g) SEQ ID NO 295 и 297; или
(h) SEQ ID NO 296 и 297.
30. Нуклеиновая кислота, кодирующая РЕ по любому из пп. 1-20.
31. Нуклеиновая кислота, кодирующая химерную молекулу по п. 22.
32. Рекомбинантный экспрессионный вектор, содержащий нуклеиновую кислоту по п. 30.
33. Рекомбинантный экспрессионный вектор, содержащий нуклеиновую кислоту по п. 31.
34. Клетка-хозяин для получения РЕ по любому из пп. 1-20, содержащая рекомбинантный экспрессионный вектор по п. 32, где указанная клетка-хозяин подходит для получения указанного РЕ и не является эмбриональной клеткой человека.
35. Клетка-хозяин для получения химерной молекулы по п. 22, содержащая рекомбинантный экспрессионный вектор по п. 33, где указанная клетка-хозяин подходит для получения указанной химерной молекулы и не является эмбриональной клеткой человека.
36. Фармацевтическая композиция для ингибирования роста раковых клеток, содержащая: эффективное количество (а) РЕ по любому из пп. 1-20, химерной молекулы по любому из пп. 21-29, нуклеиновой кислоты по п. 30 или 31, рекомбинантного экспрессионного вектора по п. 32 или 33, клетки-хозяина по п. 34 или 35 и (b) фармацевтически приемлемый носитель.
37. Применение РЕ по любому из пп. 1-20, химерной молекулы по любому из пп. 21-29, нуклеиновой кислоты по п. 30 или 31, рекомбинантного экспрессионного вектора по п. 32 или 33, клетки-хозяина по п. 34 или 35 или фармацевтической композиции по п. 36 для получения лекарственного средства для лечения или профилактики рака у млекопитающего.
38. Применение РЕ по любому из пп. 1-20, химерной молекулы по любому из пп. 21-29, нуклеиновой кислоты по п. 30 или 31, рекомбинантного экспрессионного вектора по п. 32 или 33, клетки-хозяина по п. 34 или 35 или фармацевтической композиции по п. 36 для получения лекарственного средства для ингибирования роста раковой клетки-мишени.
39. Применение по п. 38, где клетка-мишень экспрессирует маркер клеточной поверхности, выбранный из группы, состоящей из: CD19, CD21, CD22, CD25, CD30, CD33, CD79b, рецептора трансферрина, рецептора EGF, мезотелина, кадгерина, антигена Льюиса Y, глипикана-3, FAP (белка активации фибробластов альфа), PSMA (простатический специфический мембранный антиген), СА9 или CAIX (карбоангидраза IX), L1CAM (молекула адгезии нервных клеток L1), эндосиалина, HER3 (активированная конформация члена 3 семейства рецепторов эпидермального фактора роста), комплекса Alk1/BMP9 (киназа 1 анапластической лимфомы/костный морфогенетический белок 9), TPBG или 5Т4 (гликопротеин трофобласта), CD33 (связывающий сиаловые кислоты Ig-подобный лектин 3, миелоидный антиген клеточной поверхности), CD123 (рецептор альфа интерлейкина 3), MUC1 (опухоль-ассоциированный эпителиальный муцин), ROR1 (рецепторный тирозинкиназоподобный поверхностный антиген), HER1 (активированная конформация рецептора эпидермального фактора роста) и CLL1 (семейство лектиновых доменов С-типа 12, член А).
40. Способ получения РЕ по любому из пп. 1-20, включающий: (а) рекомбинантную экспрессию в подходящей клетке-хозяине РЕ по любому из пп. 1-20 и (b) очистку указанного РЕ, где указанная клетка-хозяин не является эмбриональной клеткой человека.
41. Способ получения химерной молекулы по п. 22, включающий: (а) рекомбинантную экспрессию в подходящей клетке-хозяине химерной молекулы по п. 22 и (b) очистку указанной химерной молекулы, где указанная клетка-хозяин не является эмбриональной клеткой человека.
42. Способ получения химерной молекулы по п. 21, включающий: (а) рекомбинантную экспрессию в подходящей клетке-хозяине РЕ по любому из пп. 1-20, (b) очистку указанного РЕ и (с) ковалентное связывание нацеливающего агента непосредственно или опосредованно через линкер с очищенным РЕ, где указанная клетка-хозяин не является эмбриональной клеткой человека.
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361887418P | 2013-10-06 | 2013-10-06 | |
| US61/887,418 | 2013-10-06 | ||
| US201361908464P | 2013-11-25 | 2013-11-25 | |
| US61/908,464 | 2013-11-25 | ||
| US201461982051P | 2014-04-21 | 2014-04-21 | |
| US61/982,051 | 2014-04-21 | ||
| US201462052665P | 2014-09-19 | 2014-09-19 | |
| US62/052,665 | 2014-09-19 | ||
| PCT/US2014/058941 WO2015051199A2 (en) | 2013-10-06 | 2014-10-03 | Modified pseudomonas exotoxin a |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2016114406A RU2016114406A (ru) | 2017-11-09 |
| RU2016114406A3 RU2016114406A3 (ru) | 2018-06-01 |
| RU2687143C2 true RU2687143C2 (ru) | 2019-05-07 |
Family
ID=51794961
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016114406A RU2687143C2 (ru) | 2013-10-06 | 2014-10-03 | Модифицированный экзотоксин а псевдомонад |
Country Status (8)
| Country | Link |
|---|---|
| US (4) | US9388222B2 (ru) |
| EP (1) | EP3038641B1 (ru) |
| JP (1) | JP6584012B2 (ru) |
| CN (1) | CN105849120A (ru) |
| AU (1) | AU2014329437B2 (ru) |
| CA (1) | CA2926215A1 (ru) |
| RU (1) | RU2687143C2 (ru) |
| WO (1) | WO2015051199A2 (ru) |
Families Citing this family (72)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MX2013012596A (es) | 2011-04-29 | 2014-08-21 | Selecta Biosciences Inc | Nanoportadores sintéticos tolerogénicos para generar linfocitos t reguladores cd8+. |
| BR112015027279A8 (pt) | 2013-05-03 | 2018-01-30 | Selecta Biosciences Inc | métodos e composições para acentuar células t reguladoras cd4+ |
| US20160074532A1 (en) | 2014-09-07 | 2016-03-17 | Selecta Biosciences, Inc. | Methods and compositions for attenuating gene editing anti-viral transfer vector immune responses |
| US9616114B1 (en) | 2014-09-18 | 2017-04-11 | David Gordon Bermudes | Modified bacteria having improved pharmacokinetics and tumor colonization enhancing antitumor activity |
| WO2016146833A1 (en) | 2015-03-19 | 2016-09-22 | F. Hoffmann-La Roche Ag | Biomarkers for nad(+)-diphthamide adp ribosyltransferase resistance |
| US10676723B2 (en) | 2015-05-11 | 2020-06-09 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| WO2016207324A1 (en) * | 2015-06-24 | 2016-12-29 | F. Hoffmann-La Roche Ag | Biomarkers for nad(+)−diphthamide adp ribosyltransferase sensitivity and resistance |
| BR112018002342A2 (pt) | 2015-08-04 | 2018-12-11 | Univ Duke | polímeros furtivos intrinsecamente desordenados e geneticamente modificados para entrega e métodos para uso dos mesmos |
| EP3340999A4 (en) | 2015-08-28 | 2019-06-12 | The General Hospital Corporation | AGONISTIC ANTI-TUMOR NECROSIS RECEPTOR 2 ANTIBODIES |
| WO2017055391A1 (en) | 2015-10-02 | 2017-04-06 | F. Hoffmann-La Roche Ag | Bispecific t cell activating antigen binding molecules binding mesothelin and cd3 |
| EP3184547A1 (en) | 2015-10-29 | 2017-06-28 | F. Hoffmann-La Roche AG | Anti-tpbg antibodies and methods of use |
| AU2016353067B2 (en) * | 2015-11-13 | 2023-10-05 | Sanford Research | Anti-BCMA polypeptides and proteins |
| US11752213B2 (en) | 2015-12-21 | 2023-09-12 | Duke University | Surfaces having reduced non-specific binding and antigenicity |
| WO2017159699A1 (en) * | 2016-03-15 | 2017-09-21 | Chugai Seiyaku Kabushiki Kaisha | Methods of treating cancers using pd-1 axis binding antagonists and anti-gpc3 antibodies |
| WO2017196847A1 (en) | 2016-05-10 | 2017-11-16 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Variable new antigen receptor (vnar) antibodies and antibody conjugates targeting tumor and viral antigens |
| US11467156B2 (en) | 2016-06-01 | 2022-10-11 | Duke University | Nonfouling biosensors |
| WO2017214182A1 (en) | 2016-06-07 | 2017-12-14 | The United States Of America. As Represented By The Secretary, Department Of Health & Human Services | Fully human antibody targeting pdi for cancer immunotherapy |
| BR112018077375A2 (pt) * | 2016-06-30 | 2019-10-01 | F. Hoffmann-La Roche Ag | kits, moléculas de anticorpo biespecífico trivalente, composição farmacêutica, vetor de expressão, célula hospedeira e método para a produção de uma molécula de anticorpo biespecífico trivalente |
| EP3494135A1 (en) | 2016-08-02 | 2019-06-12 | The United States of America, as represented by The Secretary, Department of Health and Human Services | Monoclonal antibodies targeting glypican-2 (gpc2) and use thereof |
| RU2019110848A (ru) | 2016-09-14 | 2020-10-15 | Дьюк Юниверсити | Наночастицы на основе триблочных полипептидов для доставки гидрофильных лекарственных средств |
| CN107841506B (zh) * | 2016-09-20 | 2021-03-16 | 上海恒润达生生物科技有限公司 | 靶向间皮素的嵌合抗原受体及其用途 |
| CN110023326A (zh) | 2016-09-23 | 2019-07-16 | 杜克大学 | 具有lcst行为的非结构化无重复多肽 |
| US11180535B1 (en) | 2016-12-07 | 2021-11-23 | David Gordon Bermudes | Saccharide binding, tumor penetration, and cytotoxic antitumor chimeric peptides from therapeutic bacteria |
| US11129906B1 (en) | 2016-12-07 | 2021-09-28 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| AU2017382883B2 (en) | 2016-12-21 | 2024-07-04 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Human monoclonal antibodies specific for FLT3 and uses thereof |
| US11648200B2 (en) | 2017-01-12 | 2023-05-16 | Duke University | Genetically encoded lipid-polypeptide hybrid biomaterials that exhibit temperature triggered hierarchical self-assembly |
| EP3592389B1 (en) | 2017-03-11 | 2025-05-07 | Cartesian Therapeutics, Inc. | Methods and compositions related to combined treatment with anti-inflammatories and synthetic nanocarriers comprising an immunosuppressant |
| CN108624607B (zh) * | 2017-03-16 | 2021-11-16 | 上海恒润达生生物科技股份有限公司 | 靶向mesothelin的嵌合抗原受体并对其双重修饰的方法和用途 |
| CN108624608B (zh) * | 2017-03-17 | 2021-11-16 | 上海恒润达生生物科技股份有限公司 | 靶向mesothelin的第四代嵌合抗原受体的制备方法和用途 |
| CN108728458B (zh) * | 2017-04-21 | 2021-11-16 | 上海恒润达生生物科技股份有限公司 | 靶向mesothelin的嵌合抗原受体并联合表达IL-15的方法和用途 |
| WO2018213320A1 (en) | 2017-05-15 | 2018-11-22 | Duke University | Recombinant production of hybrid lipid-biopolymer materials that self-assemble and encapsulate agents |
| CN108864287B (zh) * | 2017-05-16 | 2022-08-30 | 上海恒润达生生物科技股份有限公司 | 一种靶向Mesothelin的嵌合抗原受体并对其两种修饰的方法及其用途 |
| US11390683B2 (en) | 2017-05-18 | 2022-07-19 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Anti-mesothelin polypeptides and proteins |
| EP3625256A1 (en) | 2017-05-19 | 2020-03-25 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Human monoclonal antibody targeting tnfr2 for cancer immunotherapy |
| CN106990188B (zh) * | 2017-06-09 | 2019-11-15 | 齐齐哈尔医学院 | 一种绿脓杆菌外毒素a的高效液相色谱检测方法 |
| CA3067351A1 (en) * | 2017-06-15 | 2018-12-20 | Nai-Kong Cheung | Anti-l1-cam antibodies and uses thereof |
| US11680083B2 (en) | 2017-06-30 | 2023-06-20 | Duke University | Order and disorder as a design principle for stimuli-responsive biopolymer networks |
| WO2019005208A1 (en) | 2017-06-30 | 2019-01-03 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | ANTIBODIES TO HUMAN MESOTHELIN AND USES IN ANTICANCER THERAPY |
| CA3066953A1 (en) | 2017-06-30 | 2019-01-03 | Lentigen Technology, Inc. | Human monoclonal antibodies specific for cd33 and methods of their use |
| WO2019055955A1 (en) | 2017-09-18 | 2019-03-21 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | IMMUNOTOXINS WITH ALBUMIN BINDING DOMAIN |
| WO2019107962A2 (ko) | 2017-11-29 | 2019-06-06 | 아주대학교 산학협력단 | 항체와 생리활성물질의 접합방법 |
| KR102037336B1 (ko) | 2017-11-29 | 2019-10-29 | 아주대학교산학협력단 | 항체와 생리활성물질의 접합방법 |
| WO2019147954A1 (en) | 2018-01-26 | 2019-08-01 | Duke University | Albumin binding peptide-drug (aibiped) conjugates and methods of making and using same |
| WO2019183476A1 (en) * | 2018-03-23 | 2019-09-26 | Duke University | Sustained-release biopolymer-immunotoxin conjugates and methods of using same |
| IL320375A (en) * | 2018-03-29 | 2025-06-01 | Ambrx Inc | Drug conjugates - anti-PSMA antibody - of human origin and their uses for reducing or inhibiting the growth or progression of tumors in a cancer or cancerous tissue expressing PSMA |
| WO2019213150A1 (en) | 2018-04-30 | 2019-11-07 | Duke University | Stimuli-responsive peg-like polymer-based drug delivery platform |
| WO2020014482A1 (en) | 2018-07-12 | 2020-01-16 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Affinity matured cd22-specific monoclonal antibody and uses thereof |
| WO2020028806A1 (en) | 2018-08-02 | 2020-02-06 | Duke University | Dual agonist fusion proteins |
| CA3106544A1 (en) | 2018-08-08 | 2020-02-13 | Mitchell Ho | High affinity monoclonal antibodies targeting glypican-2 and uses thereof |
| CN113302205B (zh) * | 2018-11-15 | 2024-12-06 | 综合医院公司 | 激动性肿瘤坏死因子受体超家族多肽 |
| CA3125484A1 (en) | 2019-01-08 | 2020-07-16 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Cross-species single domain antibodies targeting mesothelin for treating solid tumors |
| EP3883971A1 (en) | 2019-01-22 | 2021-09-29 | The United States of America, as represented by the Secretary, Department of Health and Human Services | High affinity monoclonal antibodies targeting glypican-1 and methods of use |
| MA56467A (fr) * | 2019-07-02 | 2022-05-11 | Telix Int Pty Ltd | Anticorps dirigés contre caix avec une affinité réduite pour le récepteur fc néonatal |
| US11512314B2 (en) | 2019-07-12 | 2022-11-29 | Duke University | Amphiphilic polynucleotides |
| CN119899265A (zh) | 2019-10-22 | 2025-04-29 | 美国政府(由卫生和人类服务部的部长所代表) | 用于治疗多种实体瘤的靶向b7h3(cd276)的高亲和力纳米抗体 |
| IL301285A (en) | 2020-09-10 | 2023-05-01 | Precirix N V | A portion of an antibody against FAP |
| WO2022093745A1 (en) | 2020-10-26 | 2022-05-05 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Single domain antibodies targeting sars coronavirus spike protein and uses thereof |
| CA3202875A1 (en) | 2020-12-22 | 2022-06-30 | Huan Wang | Complex of anti-il-4r antibody or antigen-binding fragment thereof and medical use thereof |
| CN113201473B (zh) * | 2021-04-22 | 2022-06-07 | 广东省科学院微生物研究所(广东省微生物分析检测中心) | 香茅醇在制备促进铜绿假单胞菌毒力基因toxA表达的制剂中的应用 |
| WO2022232612A1 (en) | 2021-04-29 | 2022-11-03 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Lassa virus-specific nanobodies and methods of their use |
| US20240270851A1 (en) | 2021-06-09 | 2024-08-15 | The U.S.A., As Represented By The Secretary, Department Of Health And Human Services | Cross species single domain antibodies targeting pd-l1 for treating solid tumors |
| US20240417446A1 (en) | 2021-10-26 | 2024-12-19 | The U.S.A., As Represented By The Secretary, Department Of Health And Human Services | Single domain antibodies targeting the s2 subunit of sars-cov-2 spike protein |
| US20250018040A1 (en) | 2021-12-17 | 2025-01-16 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Servic | Anti-mesothelin polypeptides, proteins, and chimeric antigen receptors |
| KR102572039B1 (ko) * | 2022-04-18 | 2023-08-30 | 주식회사 노벨티노빌리티 | 슈도모나스 외독소 A를 포함하는 c-Kit 표적 면역접합체 |
| WO2023203135A1 (en) | 2022-04-22 | 2023-10-26 | Precirix N.V. | Improved radiolabelled antibody |
| WO2023213801A1 (en) | 2022-05-02 | 2023-11-09 | Precirix N.V. | Pre-targeting |
| WO2024020703A1 (en) | 2022-07-29 | 2024-02-01 | Zymeworks Bc Inc. | Multivalent and bispecific antibody constructs and methods of use thereof |
| WO2024050399A1 (en) | 2022-09-01 | 2024-03-07 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Single domain antibodies targeting hpv e6/e7 oncogenic peptide/mhc complexes |
| WO2024238346A1 (en) | 2023-05-12 | 2024-11-21 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Single domain antibodies that specifically bind the s2 subunit of sars-cov-2 spike protein and compositions and uses thereof |
| WO2025019228A1 (en) | 2023-07-20 | 2025-01-23 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Fully human monoclonal antibodies and chimeric antigen receptors against cd276 for the treatment of solid tumors |
| WO2025072772A2 (en) * | 2023-09-28 | 2025-04-03 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Recombinant fusion protein for treating cancer |
| WO2025171238A1 (en) | 2024-02-07 | 2025-08-14 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Monoclonal antibodies that bind the juxta-membrane region of mesothelin and uses thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007031741A1 (en) * | 2005-09-14 | 2007-03-22 | Cambridge Antibody Technology Limited | Pseudomonas exotoxin a cd4+ t-cell epitopes |
| WO2011032022A1 (en) * | 2009-09-11 | 2011-03-17 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Improved pseudomonas exotoxin a with reduced immunogenicity |
| WO2012170614A2 (en) * | 2011-06-07 | 2012-12-13 | Board Of Regents, The University Of Texas System | Dna methylation markers in non-small cell lung cancer and methods of using the same |
| WO2013040141A1 (en) * | 2011-09-16 | 2013-03-21 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Pseudomonas exotoxin a with less immunogenic b cell epitopes |
Family Cites Families (51)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4450150A (en) | 1973-05-17 | 1984-05-22 | Arthur D. Little, Inc. | Biodegradable, implantable drug delivery depots, and method for preparing and using the same |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| EP0173494A3 (en) | 1984-08-27 | 1987-11-25 | The Board Of Trustees Of The Leland Stanford Junior University | Chimeric receptors by dna splicing and expression |
| WO1987002671A1 (en) | 1985-11-01 | 1987-05-07 | International Genetic Engineering, Inc. | Modular assembly of antibody genes, antibodies prepared thereby and use |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| IN165717B (ru) | 1986-08-07 | 1989-12-23 | Battelle Memorial Institute | |
| US4892827A (en) | 1986-09-24 | 1990-01-09 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant pseudomonas exotoxins: construction of an active immunotoxin with low side effects |
| US5242824A (en) | 1988-12-22 | 1993-09-07 | Oncogen | Monoclonal antibody to human carcinomas |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| DE3920358A1 (de) | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| US5859205A (en) | 1989-12-21 | 1999-01-12 | Celltech Limited | Humanised antibodies |
| US5545806A (en) | 1990-08-29 | 1996-08-13 | Genpharm International, Inc. | Ransgenic non-human animals for producing heterologous antibodies |
| JP2938569B2 (ja) | 1990-08-29 | 1999-08-23 | ジェンファーム インターナショナル,インコーポレイティド | 異種免疫グロブリンを作る方法及びトランスジェニックマウス |
| US5608039A (en) | 1990-10-12 | 1997-03-04 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Single chain B3 antibody fusion proteins and their uses |
| US5846535A (en) | 1990-10-12 | 1998-12-08 | The United States Of America As Represented By The Department Of Health And Human Services | Methods for reducing tumor cell growth by using antibodies with broad tumor reactivity and limited normal tissue reactivity |
| US5889157A (en) | 1990-10-12 | 1999-03-30 | The United States Of America As Represented By The Department Of Health And Human Services | Humanized B3 antibody fragments, fusion proteins, and uses thereof |
| US5981726A (en) | 1990-10-12 | 1999-11-09 | The United States Of America As Represented By The Department Of Health And Human Services | Chimeric and mutationally stabilized tumor-specific B1, B3 and B5 antibody fragments; immunotoxic fusion proteins; and uses thereof |
| JP3266311B2 (ja) | 1991-05-02 | 2002-03-18 | 生化学工業株式会社 | 新規ポリペプチドおよびこれを用いる抗hiv剤 |
| WO1993011161A1 (en) | 1991-11-25 | 1993-06-10 | Enzon, Inc. | Multivalent antigen-binding proteins |
| CA2136724A1 (en) | 1992-06-18 | 1993-12-23 | Ira H. Pastan | Recombinant pseudomonas exotoxin with increased activity |
| US5639641A (en) | 1992-09-09 | 1997-06-17 | Immunogen Inc. | Resurfacing of rodent antibodies |
| US5747654A (en) | 1993-06-14 | 1998-05-05 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant disulfide-stabilized polypeptide fragments having binding specificity |
| US5888773A (en) | 1994-08-17 | 1999-03-30 | The United States Of America As Represented By The Department Of Health And Human Services | Method of producing single-chain Fv molecules |
| US6265150B1 (en) | 1995-06-07 | 2001-07-24 | Becton Dickinson & Company | Phage antibodies |
| US5714352A (en) | 1996-03-20 | 1998-02-03 | Xenotech Incorporated | Directed switch-mediated DNA recombination |
| ES2300122T3 (es) | 1997-03-20 | 2008-06-01 | The Government Of The Usa As Represented By The Secretary Of Department Of Health And Human Services | Anticuerpos recombinantes e inmunoconjugados dirigidos contra celulas y tumores portadores de cd-22. |
| CA2287084A1 (en) | 1997-04-10 | 1998-10-15 | Royal Netherlands Academy Of Arts And Sciences | Diagnosis method and reagents |
| DE19742706B4 (de) | 1997-09-26 | 2013-07-25 | Pieris Proteolab Ag | Lipocalinmuteine |
| US6809184B1 (en) | 1997-12-01 | 2004-10-26 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Antibodies, including FV molecules, and immunoconjugates having high binding affinity for mesothelin and methods for their use |
| US6296843B1 (en) | 1998-04-03 | 2001-10-02 | The Penn State Research Foundation | Mutagenized IL 13-based chimeric molecules |
| EP0972838B1 (en) | 1998-07-15 | 2004-09-15 | Roche Diagnostics GmbH | Escherichia coli host/vector system based on antibiotic-free selection by complementation of an auxotrophy |
| US6291245B1 (en) | 1998-07-15 | 2001-09-18 | Roche Diagnostics Gmbh | Host-vector system |
| US6818418B1 (en) | 1998-12-10 | 2004-11-16 | Compound Therapeutics, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| US7115396B2 (en) | 1998-12-10 | 2006-10-03 | Compound Therapeutics, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| DE60039510D1 (de) | 1999-05-27 | 2008-08-28 | Us Gov Health & Human Serv | Immunokonjugate mit hoher bindungsaffinität |
| JP2004511425A (ja) | 2000-02-08 | 2004-04-15 | ザ ペン ステート リサーチ ファウンデーション | 免疫療法に使用されるインターロイキン13受容体サブユニットアルファー2 |
| CA2421447C (en) | 2000-09-08 | 2012-05-08 | Universitat Zurich | Collections of repeat proteins comprising repeat modules |
| US7521054B2 (en) | 2000-11-17 | 2009-04-21 | The United States Of America As Represented By The Department Of Health And Human Services | Reduction of the nonspecific animal toxicity of immunotoxins by mutating the framework regions of the Fv to lower the isoelectric point |
| US7355012B2 (en) | 2001-09-26 | 2008-04-08 | United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Mutated anti-CD22 antibodies with increased affinity to CD22-expressing leukemia cells |
| AU2003239248A1 (en) | 2002-06-07 | 2003-12-22 | The Government Of The United States, As Represented By The Secretary Of The Department Of Health And | Anti-cd30 stalk and anti-cd30 antibodies suitable for use in immunotoxins |
| ATE416190T1 (de) | 2003-07-04 | 2008-12-15 | Affibody Ab | Polypeptide mit bindungsaffinität für her2 |
| WO2005019255A1 (en) | 2003-08-25 | 2005-03-03 | Pieris Proteolab Ag | Muteins of tear lipocalin |
| AU2004293471C1 (en) | 2003-11-25 | 2011-02-24 | The Government Of The United States, As Represented By The Secretary Of Health And Human Services | Mutated anti-CD22 antibodies and immunoconjugates |
| JP5006651B2 (ja) | 2003-12-05 | 2012-08-22 | ブリストル−マイヤーズ スクウィブ カンパニー | 2型血管内皮増殖因子受容体の阻害剤 |
| PL3006457T3 (pl) * | 2005-07-29 | 2018-05-30 | The Government Of The United States Of America, As Represented By The Secretary Of Health And Human Services | Zmutowane egzotoksyny Pseudomonas o zmniejszonej antygenowości |
| TW200726776A (en) | 2005-07-29 | 2007-07-16 | Friedrich Alexander University Of Erlangen Nuremberg | CD33-specific single-chain immunotoxin and methods of use |
| EP1958957A1 (en) | 2007-02-16 | 2008-08-20 | NascaCell Technologies AG | Polypeptide comprising a knottin protein moiety |
| PL2197903T3 (pl) * | 2007-09-04 | 2015-03-31 | Us Gov Health & Human Services | Delecje w domenie ii egzotoksyny a psuedomonas zmniejszające toksyczność niespecyficzną |
| CN103648525B (zh) * | 2011-05-06 | 2016-08-24 | 由卫生与公共服务部部长代表的美国政府 | 靶向间皮素的重组免疫毒素 |
| CA2838013C (en) * | 2011-06-09 | 2023-03-07 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Pseudomonas exotoxin a with less immunogenic t cell and/or b cell epitopes |
-
2014
- 2014-10-03 RU RU2016114406A patent/RU2687143C2/ru active
- 2014-10-03 WO PCT/US2014/058941 patent/WO2015051199A2/en not_active Ceased
- 2014-10-03 EP EP14789449.7A patent/EP3038641B1/en active Active
- 2014-10-03 JP JP2016520651A patent/JP6584012B2/ja not_active Expired - Fee Related
- 2014-10-03 AU AU2014329437A patent/AU2014329437B2/en active Active
- 2014-10-03 CA CA2926215A patent/CA2926215A1/en not_active Abandoned
- 2014-10-03 US US14/505,590 patent/US9388222B2/en active Active
- 2014-10-03 CN CN201480062185.7A patent/CN105849120A/zh active Pending
-
2016
- 2016-06-23 US US15/191,392 patent/US20170051072A1/en not_active Abandoned
-
2019
- 2019-06-03 US US16/429,829 patent/US20200181280A1/en not_active Abandoned
-
2020
- 2020-02-10 US US16/785,911 patent/US20210024648A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007031741A1 (en) * | 2005-09-14 | 2007-03-22 | Cambridge Antibody Technology Limited | Pseudomonas exotoxin a cd4+ t-cell epitopes |
| WO2011032022A1 (en) * | 2009-09-11 | 2011-03-17 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Improved pseudomonas exotoxin a with reduced immunogenicity |
| WO2012170614A2 (en) * | 2011-06-07 | 2012-12-13 | Board Of Regents, The University Of Texas System | Dna methylation markers in non-small cell lung cancer and methods of using the same |
| WO2013040141A1 (en) * | 2011-09-16 | 2013-03-21 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Pseudomonas exotoxin a with less immunogenic b cell epitopes |
Non-Patent Citations (3)
| Title |
|---|
| ONDA M. et al., An immunotoxin with greatly reduced immunogenicity by identification and removal of B-cell epitopes, PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, 2008, v.105, n.32, p. 11311-11316. * |
| ONDA M. et al., An immunotoxin with greatly reduced immunogenicity by identification and removal of B-cell epitopes, PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, 2008, v.105, n.32, p. 11311-11316. ЛЯМИН А.В. "Особенности биологических свойств и факторов патогенности штаммов Pseudomonas aeruginosa, выделенных из разных источников." Аспирант. вестн. Поволжья, 2010, 3-4: 220-223. * |
| ЛЯМИН А.В. "Особенности биологических свойств и факторов патогенности штаммов Pseudomonas aeruginosa, выделенных из разных источников." Аспирант. вестн. Поволжья, 2010, 3-4: 220-223. * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3038641A2 (en) | 2016-07-06 |
| US9388222B2 (en) | 2016-07-12 |
| RU2016114406A3 (ru) | 2018-06-01 |
| JP2016534985A (ja) | 2016-11-10 |
| AU2014329437B2 (en) | 2018-10-18 |
| CN105849120A (zh) | 2016-08-10 |
| US20150099707A1 (en) | 2015-04-09 |
| EP3038641B1 (en) | 2019-04-17 |
| JP6584012B2 (ja) | 2019-10-02 |
| US20210024648A1 (en) | 2021-01-28 |
| CA2926215A1 (en) | 2015-04-09 |
| US20170051072A1 (en) | 2017-02-23 |
| WO2015051199A2 (en) | 2015-04-09 |
| WO2015051199A3 (en) | 2015-08-27 |
| RU2016114406A (ru) | 2017-11-09 |
| US20200181280A1 (en) | 2020-06-11 |
| AU2014329437A1 (en) | 2016-04-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2687143C2 (ru) | Модифицированный экзотоксин а псевдомонад | |
| US20240101641A1 (en) | Tgf-b-receptor ectodomain fusion molecules and uses thereof | |
| JP6449359B2 (ja) | 免疫原性の低いt細胞及び/又はb細胞エピトープを有するシュードモナス外毒素a | |
| TWI772586B (zh) | 三鏈抗體、其製備方法及其用途 | |
| EP2755993B1 (en) | Pseudomonas exotoxin a with less immunogenic b cell epitopes | |
| JP7557377B2 (ja) | 三量体ポリペプチド複合体およびその使用 | |
| US12215164B2 (en) | Immunotoxins with albumin binding domain | |
| WO2019176866A1 (ja) | ウテログロビンを構造基盤とする二重特異性ポリペプチド |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| HC9A | Changing information about inventors |