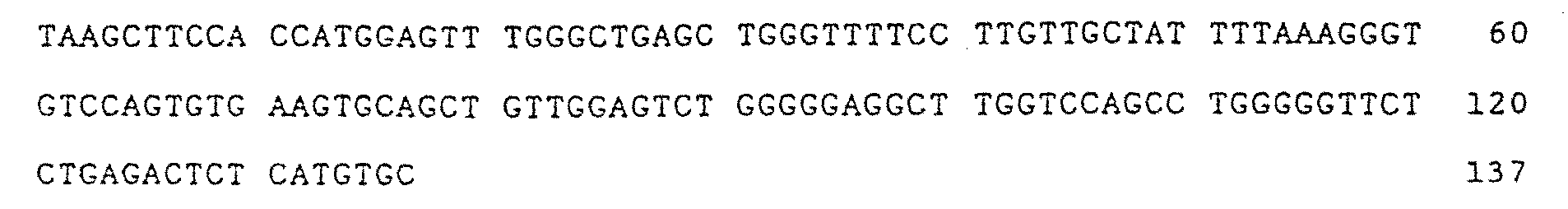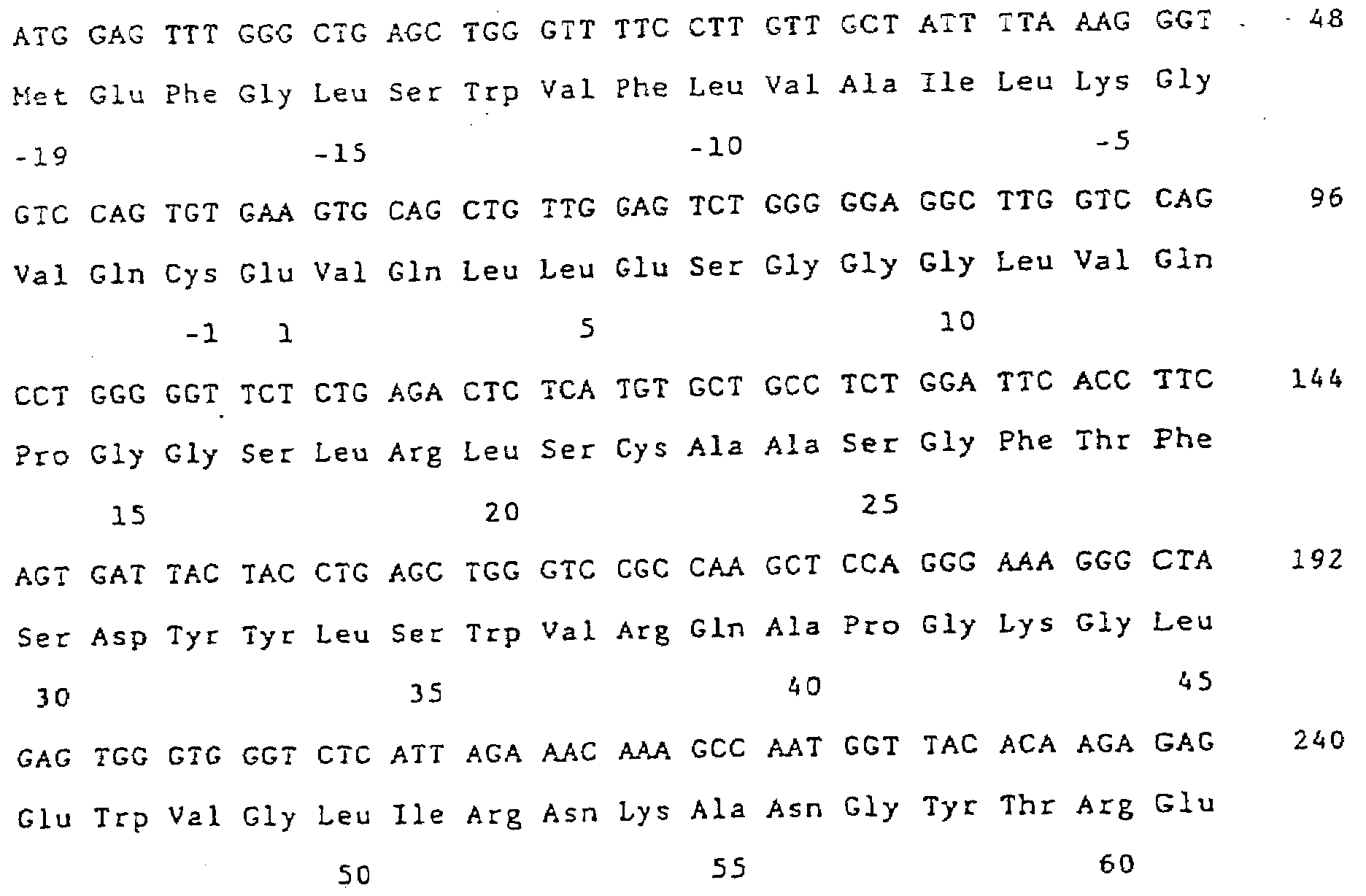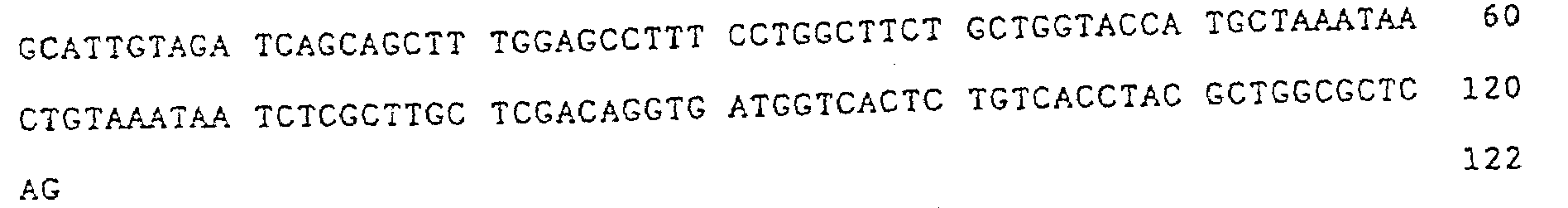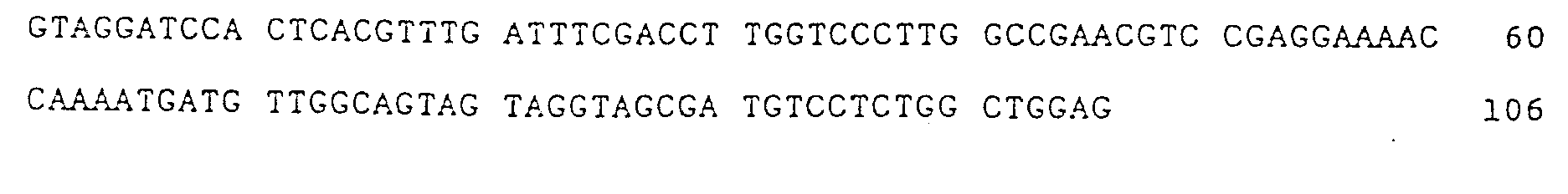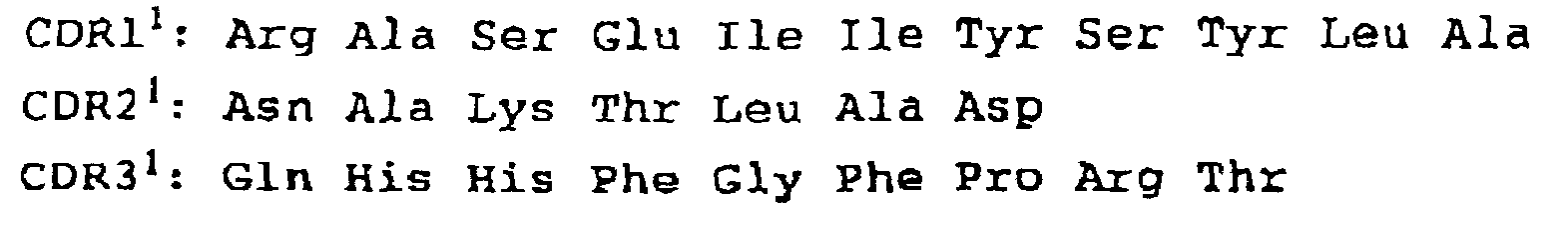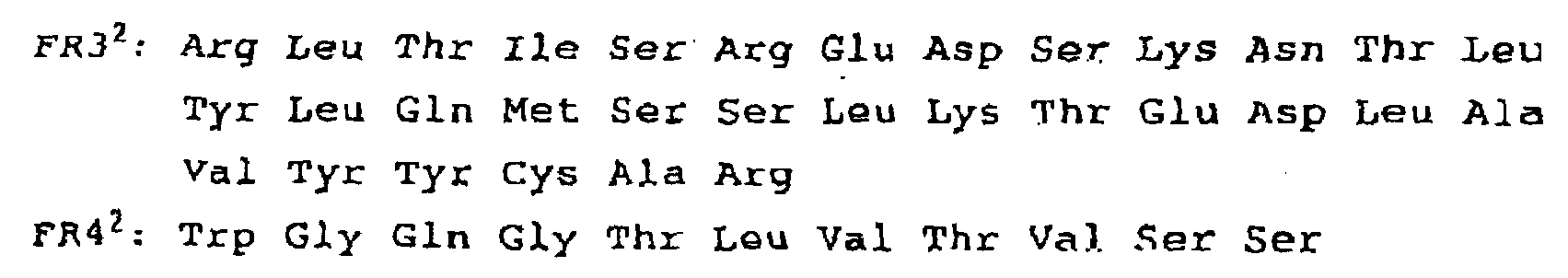KR100261941B1 - 사람의 인터루킨-8에 대한 재구성 사람항체 - Google Patents
사람의 인터루킨-8에 대한 재구성 사람항체 Download PDFInfo
- Publication number
- KR100261941B1 KR100261941B1 KR1019970700191A KR19970700191A KR100261941B1 KR 100261941 B1 KR100261941 B1 KR 100261941B1 KR 1019970700191 A KR1019970700191 A KR 1019970700191A KR 19970700191 A KR19970700191 A KR 19970700191A KR 100261941 B1 KR100261941 B1 KR 100261941B1
- Authority
- KR
- South Korea
- Prior art keywords
- chain
- region
- human
- sequence
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Description
Claims (24)
- 제1항에 있어서, 상기 HSGI가 REI 항체인 것인 L사슬 V영역.
- 제1항에 있어서, 서열번호 62 또는 65로 나타낸 아미노산 서열을 갖는 L사슬 V영역.
- 제1항 내지 제4항 중 어느 하나에 따른 V영역 및 불변(C) 영역으로 이루어진 사람의 IL-8에 대한 항체의 L사슬.
- 제5항에 있어서, C 영역은 Cκ인 것인 L사슬.
- 제7항에 있어서, HSGⅢ는 VDH26 항체 및/또는 4B4 항체인 것인 H사슬 V영역.
- 제7항에 있어서, 서열번호 38, 41, 44, 45, 48, 51, 54 또는 55로 나타낸 아미노산 서열을 갖는 H사슬 V영역.
- 제7항 내지 10항 중 어느 하나의 항에 따른 V영역 및 사람 항체로 부터 유도된 불변(C) 영역으로 이루어진 사람의 IL-8에 대한 항체의 H사슬.
- 제11항에 있어서, C영역은 Cκ인 것인 H사슬.
- 제5항 또는 제6항에 따른 두 개의 L 사슬 및 제11항 또는 제12항에 따른 두 개의 H사슬로 이루어진 사람의 IL-8에 대한 항체.
- F(ab')2, Fab, Fv 또는 단일 사슬 Fv 또는 제13항에 따른 항체의 단편.
- 제1항 내지 제4항 중 어느 하나의 항에 따른 L사슬 V영역을 코드하는 DNA.
- 제5항 또는 제6항에 따른 L사슬을 코드하는 DNA.
- 제7항 내지 제10항 중 어느 하나의 항에 따른 H사슬 V영역을 코드하는 DNA.
- 제11항 또는 제12항에 따른 H사슬을 코드하는 DNA.
- 제15항 또는 제16항에 따른 DNA로 이루어진 벡터.
- 제17항 또는 제18항에 따른 DNA로 이루어진 벡터.
- 제15항 또는 제16항에 따른 DNA 및 제94항 또는 제95항에 따른 DNA로 이루어진 벡터.
- 제19 및/또는 제20항에 따른 벡터로 트랜스펙션된 숙주 세포.
- 제19항에 따른 발현 벡터와 제20항에 따른 발현 벡터로 트랜스펙션된 숙주 세포를 배양하는 단계 및 목적하는 항체를 회수하는 단계로 이루어진 사람 IL-8에 대한 항체의 제조방법.
- 제21항에 따른 발현 벡터로 트랜스펙션된 숙주 세포를 배양하는 단계 및 목적하는 항체를 회수하는 단계로 이루어진 사람 IL-8에 대한 항체의 제조방법.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP16148194 | 1994-07-13 | ||
| JP1994/161481 | 1994-07-13 | ||
| JP28995194 | 1994-11-24 | ||
| JP1994/289951 | 1994-11-24 | ||
| JP1994/310785 | 1994-12-14 | ||
| JP31078594 | 1994-12-14 | ||
| PCT/JP1995/001396 WO1996002576A1 (en) | 1994-07-13 | 1995-07-12 | Reconstituted human antibody against human interleukin-8 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR100261941B1 true KR100261941B1 (ko) | 2000-07-15 |
Family
ID=27321865
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019970700191A Expired - Fee Related KR100261941B1 (ko) | 1994-07-13 | 1995-07-12 | 사람의 인터루킨-8에 대한 재구성 사람항체 |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US5994524A (ko) |
| EP (1) | EP0770628B9 (ko) |
| KR (1) | KR100261941B1 (ko) |
| AT (1) | ATE340590T1 (ko) |
| AU (1) | AU701342B2 (ko) |
| CA (1) | CA2194907A1 (ko) |
| DE (1) | DE69535243T2 (ko) |
| HU (1) | HU221385B1 (ko) |
| WO (1) | WO1996002576A1 (ko) |
| ZA (1) | ZA955832B (ko) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11454633B2 (en) | 2014-12-19 | 2022-09-27 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant Fc regions, and methods of use |
| US11780912B2 (en) | 2016-08-05 | 2023-10-10 | Chugai Seiyaku Kabushiki Kaisha | Composition for prophylaxis or treatment of IL-8 related diseases |
| US12116414B2 (en) | 2007-09-26 | 2024-10-15 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US12252532B2 (en) | 2015-12-25 | 2025-03-18 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies and methods of use |
| US12473375B2 (en) | 2006-03-31 | 2025-11-18 | Chugai Seiyaku Kabushiki Kaisha | Methods for controlling blood pharmacokinetics of antibodies |
Families Citing this family (385)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7041871B1 (en) | 1995-10-10 | 2006-05-09 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| US6300129B1 (en) * | 1990-08-29 | 2001-10-09 | Genpharm International | Transgenic non-human animals for producing heterologous antibodies |
| CA2181787A1 (en) * | 1994-03-03 | 1995-09-08 | Claire M. Doerschuk | Anti-il-8 monoclonal antibodies for treatment of inflammatory disorders |
| US20010006637A1 (en) * | 1996-04-19 | 2001-07-05 | Tohru Akahoshi | Rheumatoid arthritis remedy containing anti-il-8 antibody as active ingredient |
| US6497878B1 (en) | 1996-04-23 | 2002-12-24 | Chugai Seiyaku Kabushiki Kaisha | Treatment of cerebral disorders by inhibition of IL-8 binding to receptor |
| AU2405197A (en) * | 1996-04-23 | 1997-11-12 | Chugai Seiyaku Kabushiki Kaisha | Myocardial infarction remedy containing anti-il-8 antibody as active ingredient |
| AU709108B2 (en) * | 1996-06-26 | 1999-08-19 | Chugai Seiyaku Kabushiki Kaisha | Therapeutic agent for acute lung injury resulting from indirect causes comprising anti-IL-8 antibody as active ingredient |
| US20020006405A1 (en) * | 1996-10-22 | 2002-01-17 | Masaki Kitajima | Sepsis remedy comprising anti-il-8 antibody as active ingredient |
| US6025158A (en) * | 1997-02-21 | 2000-02-15 | Genentech, Inc. | Nucleic acids encoding humanized anti-IL-8 monoclonal antibodies |
| US6133426A (en) * | 1997-02-21 | 2000-10-17 | Genentech, Inc. | Humanized anti-IL-8 monoclonal antibodies |
| US7122636B1 (en) | 1997-02-21 | 2006-10-17 | Genentech, Inc. | Antibody fragment-polymer conjugates and uses of same |
| JP4108760B2 (ja) | 1997-02-21 | 2008-06-25 | ジェネンテック,インコーポレーテッド | 抗体フラグメント−ポリマー複合体およびヒト化抗il−8モノクローナル抗体 |
| WO1998042377A1 (fr) | 1997-03-21 | 1998-10-01 | Chugai Seiyaku Kabushiki Kaisha | Substances servant a la prevention ou au traitement de maladies liees a la cellule-t sensibilisee contenant comme principe actif des antagonistes de l'il-6 |
| CA2308007C (en) | 1997-10-14 | 2011-05-17 | Chugai Seiyaku Kabushiki Kaisha | Enhancer for antibody to lymphocytic tumors |
| US6468532B1 (en) | 1998-01-22 | 2002-10-22 | Genentech, Inc. | Methods of treating inflammatory diseases with anti-IL-8 antibody fragment-polymer conjugates |
| US6458355B1 (en) | 1998-01-22 | 2002-10-01 | Genentech, Inc. | Methods of treating inflammatory disease with anti-IL-8 antibody fragment-polymer conjugates |
| AU2559799A (en) * | 1998-01-22 | 1999-08-09 | Genentech Inc. | Antibody fragment-polymer conjugates and humanized anti-il-8 monoclonal antibodies and uses of same |
| US7005504B2 (en) | 1998-01-22 | 2006-02-28 | Genentech, Inc. | Antibody fragment-peg conjugates |
| AU770555B2 (en) * | 1998-08-17 | 2004-02-26 | Abgenix, Inc. | Generation of modified molecules with increased serum half-lives |
| JP4228111B2 (ja) * | 1998-08-24 | 2009-02-25 | メディカル セラピーズ リミテッド | 動脈硬化およびptca術後の血管再狭窄に対する予防・治療剤 |
| AU784460B2 (en) | 1999-08-23 | 2006-04-06 | Chugai Seiyaku Kabushiki Kaisha | HM1.24 antigen expression potentiators |
| JP3859512B2 (ja) | 1999-10-01 | 2006-12-20 | 中外製薬株式会社 | 血液凝固関連疾患の予防及び治療 |
| ATE420661T1 (de) | 2000-04-28 | 2009-01-15 | Chugai Pharmaceutical Co Ltd | Zellproliferation-inhibitoren |
| WO2002013865A1 (en) | 2000-08-16 | 2002-02-21 | Chugai Seiyaku Kabushiki Kaisha | Agents for ameliorating symptoms caused by joint diseases |
| EP1916303B1 (en) | 2000-11-30 | 2013-02-27 | Medarex, Inc. | Nucleic acids encoding rearranged human immunoglobulin sequences from transgenic transchromosomal mice |
| WO2002052005A1 (fr) | 2000-12-22 | 2002-07-04 | Kazusa Dna Research Institute Foundation | Genes et proteines codees par ceux-ci |
| JP3986439B2 (ja) | 2001-02-07 | 2007-10-03 | 中外製薬株式会社 | 造血器腫瘍の治療剤 |
| EP1970448A1 (en) | 2001-05-11 | 2008-09-17 | Kirin Pharma Kabushiki Kaisha | Human artificial chromosome containting human antibody lambda light chain and non-human animal containting the human artificial chromosome capable of genetic transmission |
| KR100453877B1 (ko) | 2001-07-26 | 2004-10-20 | 메덱스젠 주식회사 | 연쇄체화에 의한 면역 글로블린 융합 단백질의 제조 방법 및 이 방법에 의해 제조된 TNFR/Fc 융합 단백질, 상기 단백질을 코딩하는 DNA, 상기 DNA를 포함하는벡터, 및 상기 벡터에 의한 형질전환체 |
| PL213311B1 (pl) | 2002-02-14 | 2013-02-28 | Chugai Pharmaceutical Co Ltd | Preparat roztworu zawierajacego przeciwcialo |
| EP1485403A4 (en) * | 2002-03-15 | 2007-08-08 | Multicell Immunotherapeutics I | COMPOSITIONS AND METHOD FOR INTRODUCTION OR REINFORCEMENT OF ANTIBODY AND MAIN THISTOCOMPATIBILITY CLASS I OR CLASS II RESTRICTED T-CELL REACTIONS USING IMMUNOMODULATING, NON-CODING RNA MOTIVES |
| EP2258712A3 (en) | 2002-03-15 | 2011-05-04 | Multicell Immunotherapeutics, Inc. | Compositions and Methods to Initiate or Enhance Antibody and Major-histocompatibility Class I or Class II-restricted T Cell Responses by Using Immunomodulatory, Non-coding RNA Motifs |
| US20070037769A1 (en) * | 2003-03-14 | 2007-02-15 | Multicell Immunotherapeutics, Inc. | Compositions and methods to treat and control tumors by loading antigen presenting cells |
| CA2488441C (en) * | 2002-06-03 | 2015-01-27 | Genentech, Inc. | Synthetic antibody phage libraries |
| WO2004019966A1 (ja) | 2002-08-27 | 2004-03-11 | Chugai Seiyaku Kabushiki Kaisha | タンパク質溶液製剤の安定化方法 |
| WO2004022595A1 (ja) | 2002-09-04 | 2004-03-18 | Chugai Seiyaku Kabushiki Kaisha | MRL/lprマウスを用いた抗体の作製 |
| EP2261230B1 (en) | 2002-09-11 | 2017-05-10 | Chugai Seiyaku Kabushiki Kaisha | Protein purification method |
| JP4739763B2 (ja) | 2002-12-16 | 2011-08-03 | ゲンマブ エー/エス | インターロイキン8(il−8)に対するヒトモノクローナル抗体 |
| EP1613775B1 (en) * | 2003-03-26 | 2012-08-29 | Multicell Immunotherapeutics, Inc. | Selected rna motifs in anti-leukemia therapy |
| EP2228445A1 (en) | 2003-06-18 | 2010-09-15 | Chugai Seiyaku Kabushiki Kaisha | Fucose Transporter |
| KR20060069825A (ko) * | 2003-08-01 | 2006-06-22 | 제넨테크, 인크. | 제한된 다양성을 갖는 항체 cdr 폴리펩티드 서열 |
| US20080153104A1 (en) | 2003-08-08 | 2008-06-26 | Hiroyuki Aburantai | Gene Overexpressed in Cancer |
| US20050095627A1 (en) * | 2003-09-03 | 2005-05-05 | The Salk Institute For Biological Studies | Multiple antigen detection assays and reagents |
| WO2005035753A1 (ja) | 2003-10-10 | 2005-04-21 | Chugai Seiyaku Kabushiki Kaisha | 機能蛋白質を代替する二重特異性抗体 |
| US20080075712A1 (en) | 2003-10-14 | 2008-03-27 | Kunihiro Hattori | Double Specific Antibodies Substituting For Functional Proteins |
| FI122368B (fi) * | 2003-11-06 | 2011-12-30 | Valtion Teknillinen | Menetelmä huokoisen muovikalvon valmistamiseksi ja muovikalvo |
| US8101719B2 (en) | 2003-11-11 | 2012-01-24 | Chugai Seiyaku Kabushiki Kaisha | Humanized anti-CD47 antibody |
| CN102702353A (zh) | 2004-07-09 | 2012-10-03 | 中外制药株式会社 | 抗-磷脂酰肌醇蛋白聚糖3抗体 |
| JPWO2006067847A1 (ja) | 2004-12-22 | 2008-06-12 | 中外製薬株式会社 | フコーストランスポーターの機能が阻害された細胞を用いた抗体の作製方法 |
| DK1831258T4 (en) * | 2004-12-28 | 2023-08-28 | Innate Pharma Sa | Monoklonale antistoffer mod NKG2A |
| WO2006106905A1 (ja) | 2005-03-31 | 2006-10-12 | Chugai Seiyaku Kabushiki Kaisha | 会合制御によるポリペプチド製造方法 |
| CA2957144C (en) | 2005-04-08 | 2020-06-02 | Chugai Seiyaku Kabushiki Kaisha | Antibody substituting for function of blood coagulation factor viii |
| EP1900814A4 (en) | 2005-06-10 | 2010-07-21 | Chugai Pharmaceutical Co Ltd | SCREED SC (FV) 2-MUTANTE |
| US8945543B2 (en) | 2005-06-10 | 2015-02-03 | Chugai Seiyaku Kabushiki Kaisha | Stabilizer for protein preparation comprising meglumine and use thereof |
| JPWO2007046439A1 (ja) | 2005-10-18 | 2009-04-23 | 独立行政法人農業生物資源研究所 | 抗体を産生するトランスジェニックカイコとその製造方法 |
| US20090291437A1 (en) * | 2005-11-02 | 2009-11-26 | O'brien Sean | Methods for targeting quadruplex sequences |
| EP1957531B1 (en) | 2005-11-07 | 2016-04-13 | Genentech, Inc. | Binding polypeptides with diversified and consensus vh/vl hypervariable sequences |
| US20070237764A1 (en) * | 2005-12-02 | 2007-10-11 | Genentech, Inc. | Binding polypeptides with restricted diversity sequences |
| JP5231810B2 (ja) | 2005-12-28 | 2013-07-10 | 中外製薬株式会社 | 抗体含有安定化製剤 |
| JP5144499B2 (ja) | 2006-03-31 | 2013-02-13 | 中外製薬株式会社 | 二重特異性抗体を精製するための抗体改変方法 |
| AU2007235496B2 (en) | 2006-03-31 | 2013-11-21 | E. R. Squibb & Sons, L.L.C. | Transgenic animals expressing chimeric antibodies for use in preparing human antibodies |
| JP5311303B2 (ja) | 2006-04-25 | 2013-10-09 | 国立大学法人 東京大学 | アルツハイマー病および癌の治療薬 |
| US20100196336A1 (en) | 2006-05-23 | 2010-08-05 | Dongsu Park | Modified dendritic cells having enhanced survival and immunogenicity and related compositions and methods |
| WO2007142325A1 (ja) | 2006-06-08 | 2007-12-13 | Chugai Seiyaku Kabushiki Kaisha | 炎症性疾患の予防または治療剤 |
| WO2007145227A1 (ja) | 2006-06-14 | 2007-12-21 | Chugai Seiyaku Kabushiki Kaisha | 造血幹細胞増加促進剤 |
| US8221751B2 (en) | 2006-06-21 | 2012-07-17 | Oncotherapy Science, Inc. | Tumor-targeting monoclonal antibodies to FZD10 and uses thereof |
| BRPI0712953B8 (pt) | 2006-06-30 | 2021-05-25 | Novo Nordisk As | anticorpos anti-nkg2a, seu uso, e composição farmacêutica |
| BRPI0714209A2 (pt) | 2006-07-13 | 2014-06-24 | Chugai Pharmaceutical Co Ltd | Induzidor de morte celular |
| JP5175729B2 (ja) | 2006-07-21 | 2013-04-03 | 中外製薬株式会社 | 腎疾患治療剤 |
| ATE465179T1 (de) | 2006-07-24 | 2010-05-15 | Pasteur Institut | Antikörper, antikörperfragmente und scfv die an posttranslational modifizierte neurotrophine binden |
| US20100092457A1 (en) | 2006-08-14 | 2010-04-15 | Forerunner Pharma Research Co., Ltd. | Diagnosis and Treatment of Cancer Using Anti-Desmoglein-3 Antibodies |
| AU2007312367B2 (en) | 2006-10-12 | 2012-09-06 | Chugai Seiyaku Kabushiki Kaisha | Diagnosis and treatment of cancer using anti-EREG antibody |
| CA2666559A1 (en) | 2006-10-20 | 2008-04-24 | Forerunner Pharma Research Co., Ltd. | Pharmaceutical composition comprising anti-hb-egf antibody as active ingredient |
| CA2666809A1 (en) | 2006-10-20 | 2008-04-24 | Forerunner Pharma Research Co., Ltd. | Anti-cancer agent comprising anti-hb-egf antibody as active ingredient |
| CA2672581A1 (en) | 2006-12-14 | 2008-06-19 | Forerunner Pharma Research Co., Ltd. | Anti-claudin 3 monoclonal antibody and treatment and diagnosis of cancer using the same |
| US20100111851A1 (en) | 2007-01-05 | 2010-05-06 | The University Of Tokyo | Diagnosis and treatment of cancer by using anti-prg-3 antibody |
| DE602008006041D1 (de) | 2007-01-30 | 2011-05-19 | Forerunner Pharma Res Co Ltd | CHIMÄRER Fc GAMMA REZEPTOR UND VERFAHREN ZUR BESTIMMUNG VON ADCC-AKTIVITÄT UNTER VERWENDUNG DES REZEPTORS |
| CA2679266A1 (en) | 2007-02-27 | 2008-09-04 | Forerunner Pharma Research Co., Ltd. | Pharmaceutical composition comprising anti-grp78 antibody as active ingredient |
| CL2008000719A1 (es) | 2007-03-12 | 2008-09-05 | Univ Tokushima Chugai Seiyaku | Agente terapeutico para cancer resistente a agentes quimioterapeuticos que comprende un anticuerpo que reconoce hla de clase i como ingrediente activo; composicion farmaceutica que comprende dicho anticuerpo; y metodo para tratar cancer resistente a |
| JP5117765B2 (ja) | 2007-05-28 | 2013-01-16 | 国立大学法人 東京大学 | 抗robo1抗体を含むpet用腫瘍診断剤 |
| US8097422B2 (en) | 2007-06-20 | 2012-01-17 | Salk Institute For Biological Studies | Kir channel modulators |
| EP2175016A4 (en) | 2007-06-25 | 2012-03-28 | Forerunner Pharma Res Co Ltd | ANTI-PROMININ-1 ANTIBODY WITH ADCC ACTIVITY OR CDC ACTIVITY |
| US8536313B2 (en) | 2007-07-10 | 2013-09-17 | Shionogi & Co., Ltd. | Monoclonal antibody having neutralizing activity against MMP13 |
| CN101809162B (zh) | 2007-09-28 | 2013-06-05 | 中外制药株式会社 | 血浆中动力学被改善的磷脂酰肌醇蛋白聚糖3抗体 |
| SI2202307T2 (sl) | 2007-10-15 | 2021-11-30 | Chugai Seiyaku Kabushiki Kaisha | Postopek za proizvodnjo protitelesa |
| US8680243B2 (en) | 2007-11-14 | 2014-03-25 | Chugai Seiyaku Kabushiki Kaisha | Diagnosis and treatment of cancer using anti-GPR49 antibody |
| KR101568051B1 (ko) | 2007-11-15 | 2015-11-10 | 추가이 세이야쿠 가부시키가이샤 | Anexelekto에 결합하는 단일클론항체, 및 그의 이용 |
| KR20160074019A (ko) | 2007-12-05 | 2016-06-27 | 추가이 세이야쿠 가부시키가이샤 | 항nr10 항체 및 그의 이용 |
| MX2010006097A (es) | 2007-12-05 | 2010-08-04 | Chugai Pharmaceutical Co Ltd | Agentes terapeuticos para tratar el prurito. |
| PE20091174A1 (es) | 2007-12-27 | 2009-08-03 | Chugai Pharmaceutical Co Ltd | Formulacion liquida con contenido de alta concentracion de anticuerpo |
| RU2010133547A (ru) | 2008-01-11 | 2012-02-20 | Дзе Юниверсити Оф Токио (Jp) | Анти-cldn антитела |
| JP5774312B2 (ja) | 2008-01-24 | 2015-09-09 | ノボ・ノルデイスク・エー/エス | ヒト化抗ヒトnkg2aモノクローナル抗体 |
| JP6018361B2 (ja) | 2008-01-31 | 2016-11-02 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 制御性t細胞活性を抑制するための、ヒトcd39に対する抗体およびその使用 |
| CL2009000647A1 (es) | 2008-04-04 | 2010-06-04 | Chugai Pharmaceutical Co Ltd | Composicion farmaceutica para tratar o prevenir cancer hepatico que comprende una combinacion de un agente quimioterapeutico y un anticuerpo anti-glipicano 3; agente para atenuar un efecto secundario que comprende dicho anticuerpo; metodo para tratar o prevenir un cancer hepatico de un sujeto. |
| UA121453C2 (uk) | 2008-04-11 | 2020-06-10 | Чугей Сейяку Кабусікі Кайся | Спосіб одержання фармацевтичної композиції, яка містить антитіло |
| EP2116261A1 (en) | 2008-05-07 | 2009-11-11 | Institut Pasteur | Sub-region of a plasmodium protein with improved vaccine potential and medical uses thereof |
| EP2283862B1 (en) | 2008-06-02 | 2018-08-08 | The University of Tokyo | Combination treatment of cancer comprising anti-mfg-e8 antibody |
| US10611835B2 (en) | 2008-07-10 | 2020-04-07 | Toray Industries, Inc. | Pharmaceutical composition for treatment and prevention of cancer |
| BRPI0911926A2 (pt) | 2008-08-05 | 2020-08-18 | Toray Industries, Inc | composições farmacêuticas, anticorpos e usos de um anticorpo ou um fragmento do mesmo. |
| EP2343087B1 (en) | 2008-09-30 | 2018-07-18 | Oriental Yeast Co., Ltd. | Novel inducer of chondrocyte proliferation and differentiation |
| JP2012504946A (ja) | 2008-10-07 | 2012-03-01 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 血小板第4因子変異体1(pf4v1)に対する中和抗体およびそのフラグメント |
| JP5593488B2 (ja) | 2008-11-17 | 2014-09-24 | 独立行政法人国立がん研究センター | 癌間質の構成因子に対して特異的結合能を有する物質と抗腫瘍性化合物との複合体による新規の癌ターゲティング治療 |
| JP5756292B2 (ja) | 2008-12-22 | 2015-07-29 | 中外製薬株式会社 | 抗hs6st2抗体及びその用途 |
| EP2385114A4 (en) | 2008-12-25 | 2012-08-08 | Univ Tokyo | CANCER TREATMENT DIAGNOSIS WITH ANTI-TM4SF20 ANTIBODY |
| MX2011006908A (es) | 2008-12-26 | 2011-10-06 | Univ Tokio | Diagnosis y tratamiento del cancer utilizando el anticuerpo anti-lgr7. |
| WO2010087994A2 (en) | 2009-01-30 | 2010-08-05 | Whitehead Institute For Biomedical Research | Methods for ligation and uses thereof |
| JP2010210772A (ja) | 2009-03-13 | 2010-09-24 | Dainippon Screen Mfg Co Ltd | 液晶表示装置の製造方法 |
| EP2408818A1 (en) | 2009-03-17 | 2012-01-25 | Université de la Méditerranée | Btla antibodies and uses thereof |
| WO2010113117A2 (en) | 2009-03-30 | 2010-10-07 | Edimer Biotech S.A. | Preparation of isolated agonist anti-edar monoclonal antibodies |
| EP2420515A4 (en) | 2009-04-16 | 2013-08-28 | Univ Tokyo | DIAGNOSIS AND TREATMENT OF CANCER WITH ANTI-TMPRSS11E ANTIBODY |
| EP2426149A4 (en) | 2009-05-01 | 2013-01-23 | Univ Tokyo | ANTI-CADHERIN ANTIBODY |
| WO2010131733A1 (ja) | 2009-05-15 | 2010-11-18 | 中外製薬株式会社 | 抗axl抗体 |
| WO2010137654A1 (ja) | 2009-05-29 | 2010-12-02 | 株式会社未来創薬研究所 | Egfファミリーリガンドのアンタゴニストを成分とする医薬組成物 |
| EP2468771A4 (en) | 2009-08-17 | 2013-06-05 | Forerunner Pharma Res Co Ltd | PHARMACEUTICAL COMPOSITION WITH AN ANTIBODY TO HB-EGF AS AN ACTIVE SUBSTANCE |
| TW201118166A (en) | 2009-09-24 | 2011-06-01 | Chugai Pharmaceutical Co Ltd | HLA class I-recognizing antibodies |
| WO2011057188A1 (en) | 2009-11-06 | 2011-05-12 | Idexx Laboratories, Inc. | Canine anti-cd20 antibodies |
| JP5728718B2 (ja) | 2009-12-28 | 2015-06-03 | オンコセラピー・サイエンス株式会社 | 抗cdh3抗体およびその使用 |
| TWI505838B (zh) | 2010-01-20 | 2015-11-01 | Chugai Pharmaceutical Co Ltd | Stabilized antibody solution containing |
| CN102712769B (zh) | 2010-01-29 | 2014-12-03 | 东丽株式会社 | 聚乳酸系树脂片 |
| HRP20180952T1 (hr) | 2010-01-29 | 2018-07-27 | Chugai Seiyaku Kabushiki Kaisha | Anti-dll3 antitijelo |
| PT2532364T (pt) | 2010-02-04 | 2016-07-28 | Toray Industries | Composição farmacêutica que compreende anticorpos anti caprin-1 para o tratamento e/ou a prevenção de cancro |
| RU2567657C2 (ru) | 2010-02-04 | 2015-11-10 | Торэй Индастриз, Инк. | Фармацевтическая композиция для лечения и/или профилактики рака |
| CN102821789B (zh) | 2010-02-04 | 2016-03-02 | 东丽株式会社 | 癌的治疗和/或预防用药物组合物 |
| ES2583627T3 (es) | 2010-02-04 | 2016-09-21 | Toray Industries, Inc. | Composición farmacéutica para el tratamiento y/o la prevención del cáncer |
| US8828398B2 (en) | 2010-02-04 | 2014-09-09 | Toray Industries, Inc. | Pharmaceutical composition for treating and/or preventing cancer |
| US8815211B2 (en) | 2010-02-10 | 2014-08-26 | Fujifilm Ri Pharma Co., Ltd. | Radioactive metal-labeled anti-cadherin antibody |
| US20120321557A1 (en) | 2010-02-26 | 2012-12-20 | Forerunner Pharma Research Co., Ltd. | Anti-icam3 antibody and use thereof |
| WO2011108714A1 (ja) | 2010-03-04 | 2011-09-09 | 中外製薬株式会社 | 抗体定常領域改変体 |
| TWI667257B (zh) | 2010-03-30 | 2019-08-01 | 中外製藥股份有限公司 | 促進抗原消失之具有經修飾的FcRn親和力之抗體 |
| WO2011140182A2 (en) | 2010-05-04 | 2011-11-10 | Medimmune, Llc | Optimized degenerative muscle disease diagnostics and treatments |
| WO2011145085A2 (en) | 2010-05-21 | 2011-11-24 | Procognia (Israel) Ltd | Novel antibodies and methods of use for the treatment and diagnosis of cancer |
| WO2012005076A1 (ja) | 2010-07-08 | 2012-01-12 | 本田技研工業株式会社 | 高周波加熱用コイル |
| WO2012010696A1 (en) | 2010-07-23 | 2012-01-26 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for cancer management targeting co-029 |
| WO2012043747A1 (ja) | 2010-09-30 | 2012-04-05 | 独立行政法人理化学研究所 | グリオーマの治療方法、グリオーマの検査方法、所望の物質をグリオーマに送達させる方法、及びそれらの方法に用いられる薬剤 |
| CN103491978A (zh) | 2010-10-25 | 2014-01-01 | 明尼苏达大学评议会 | 用于治疗成胶质细胞瘤的治疗组合物 |
| HUE039375T2 (hu) | 2010-10-29 | 2018-12-28 | Perseus Proteomics Inc | Magas internalizálási kapacitású anti-CDH3 antitest |
| PH12013500974A1 (en) | 2010-11-17 | 2013-07-08 | Chugai Pharmaceutical Co Ltd | Multi-specific antigen-binding molecule having alternative function to function of blood coagulation factor viii |
| KR102385507B1 (ko) | 2010-11-30 | 2022-04-12 | 추가이 세이야쿠 가부시키가이샤 | 복수 분자의 항원에 반복해서 결합하는 항원 결합 분자 |
| MX349057B (es) | 2010-11-30 | 2017-07-07 | Chugai Pharmaceutical Co Ltd | Agente terapeutico que induce citotoxicidad. |
| WO2012080769A1 (en) | 2010-12-15 | 2012-06-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Anti-cd277 antibodies and uses thereof |
| EP2654789B1 (en) | 2010-12-22 | 2018-05-30 | Orega Biotech | Antibodies against human cd39 and use thereof |
| EP2659910B1 (en) | 2010-12-27 | 2016-11-09 | National University Corporation Nagoya University | Screening method for a compound capable of suppressing receptor tyrosine kinase-mediated pro-survival signaling in a cancer cell |
| EP2662385A4 (en) | 2011-01-07 | 2015-11-11 | Chugai Pharmaceutical Co Ltd | METHOD FOR IMPROVING THE PHYSICAL PROPERTIES OF ANTIBODIES |
| WO2012101125A1 (en) | 2011-01-24 | 2012-08-02 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Specific antibodies against human cxcl4 and uses thereof |
| EP2487242A1 (en) | 2011-02-09 | 2012-08-15 | Ruprecht-Karls-Universität Heidelberg | B-type plexin antagonists and uses thereof |
| CA2827923C (en) | 2011-02-25 | 2021-11-23 | Chugai Seiyaku Kabushiki Kaisha | Fc.gamma.riib-specific fc antibody |
| WO2012133782A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| WO2012133914A1 (ja) | 2011-03-31 | 2012-10-04 | オリエンタル酵母工業株式会社 | Ranklアンタゴニストを含む癌免疫増強剤 |
| ES2612914T3 (es) | 2011-03-31 | 2017-05-19 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos dirigidos contra Icos y usos de los mismos |
| CN103826657A (zh) | 2011-04-04 | 2014-05-28 | 衣阿华大学研究基金会 | 改进疫苗免疫原性的方法 |
| US10006879B2 (en) | 2011-04-12 | 2018-06-26 | Electronic Biosciences, Inc. | Site specific chemically modified nanopore devices |
| EP2700652B1 (en) | 2011-04-18 | 2018-12-19 | The University of Tokyo | Diagnosis and treatment of cancer using anti-itm2a antibody |
| KR102101806B1 (ko) | 2011-05-19 | 2020-04-20 | 인쎄름 (엥스띠뛰 나씨오날 드 라 쌍떼 에 드 라 흐쉐르슈 메디깔) | 항-인간-her3 항체 및 이의 용도 |
| CN103635487B (zh) | 2011-06-17 | 2016-10-12 | 诺沃—诺迪斯克有限公司 | 选择性消除侵蚀性细胞 |
| AU2012273954A1 (en) | 2011-06-22 | 2014-01-09 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Anti-Axl antibodies and uses thereof |
| US9409988B2 (en) | 2011-06-22 | 2016-08-09 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Anti-Axl antibodies and uses thereof |
| RU2641256C2 (ru) | 2011-06-30 | 2018-01-16 | Чугаи Сейяку Кабусики Кайся | Гетеродимеризованный полипептид |
| EP2543677A1 (en) | 2011-07-08 | 2013-01-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies for the treatment and prevention of thrombosis |
| EP2543678A1 (en) | 2011-07-08 | 2013-01-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies for the treatment and prevention of thrombosis |
| EP2543679A1 (en) | 2011-07-08 | 2013-01-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies for the treatment and prevention of thrombosis |
| JP6176849B2 (ja) | 2011-07-19 | 2017-08-09 | 中外製薬株式会社 | アルギニンアミドまたはその類似化合物を含む安定なタンパク質含有製剤 |
| WO2013017656A1 (en) | 2011-08-02 | 2013-02-07 | Medizinische Universität Wien | Antagonists of ribonucleases for treating obesity |
| JP6065592B2 (ja) | 2011-08-04 | 2017-01-25 | 東レ株式会社 | 癌の治療及び/又は予防用医薬組成物 |
| JP6065591B2 (ja) | 2011-08-04 | 2017-01-25 | 東レ株式会社 | 癌の治療及び/又は予防用医薬組成物 |
| CA2844040C (en) | 2011-08-04 | 2019-05-07 | Toray Industries, Inc. | Pharmaceutical composition for treatment and/or prophylaxis of cancer |
| WO2013017691A1 (en) | 2011-08-04 | 2013-02-07 | Medizinische Universität Innsbruck | Cahgt1p inhibitors for use in the treatment of candidiasis |
| JP5925783B2 (ja) | 2011-08-12 | 2016-05-25 | 国立感染症研究所長 | アスペルギルスフミガーツス感染症の検査、予防及び治療のための方法並びに組成物 |
| JP6101205B2 (ja) | 2011-08-23 | 2017-03-22 | 中外製薬株式会社 | 抗腫瘍活性を有する新規な抗ddr1抗体 |
| EP2749641B1 (en) | 2011-09-07 | 2021-06-02 | Chugai Seiyaku Kabushiki Kaisha | Cancer stem cell isolation |
| TWI681970B (zh) | 2011-09-30 | 2020-01-11 | 日商中外製藥股份有限公司 | 包含依離子濃度之條件對抗原之結合活性會改變之抗原結合分域、及於pH中性之條件下對FcRn有結合活性之FcRn結合分域、且誘導對標的抗原的免疫反應之抗原結合分子 |
| CN107287660A (zh) | 2011-09-30 | 2017-10-24 | 中外制药株式会社 | 离子浓度依赖性结合分子文库 |
| EP2762166B1 (en) | 2011-09-30 | 2019-09-18 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecules for promoting elimination of antigens |
| JP6322411B2 (ja) | 2011-09-30 | 2018-05-09 | 中外製薬株式会社 | 複数の生理活性を有する抗原の消失を促進する抗原結合分子 |
| TW201817745A (zh) | 2011-09-30 | 2018-05-16 | 日商中外製藥股份有限公司 | 具有促進抗原清除之FcRn結合域的治療性抗原結合分子 |
| WO2013051294A1 (ja) | 2011-10-05 | 2013-04-11 | 中外製薬株式会社 | 糖鎖受容体結合ドメインを含む抗原の血漿中からの消失を促進する抗原結合分子 |
| US20140302511A1 (en) | 2011-10-28 | 2014-10-09 | Pharmalogicals Research Pte. Ltd. | Cancer stem cell-specific molecule |
| ES2732712T3 (es) | 2011-10-31 | 2019-11-25 | Chugai Pharmaceutical Co Ltd | Molécula de unión a antígeno que tiene una conjugación regulada entre la cadena pesada y la cadena ligera |
| SG10201609301QA (en) | 2011-11-30 | 2016-12-29 | Chugai Pharmaceutical Co Ltd | Drug containing carrier into cell for forming immune complex |
| TWI593705B (zh) | 2011-12-28 | 2017-08-01 | Chugai Pharmaceutical Co Ltd | Humanized anti-epiregulin antibody and cancer therapeutic agent containing the antibody as an active ingredient |
| CA2862999A1 (en) | 2012-01-11 | 2013-07-18 | Arizona Board Of Regents, A Body Corporate Of The State Of Arizona Acting For And On Behalf Of Arizona State University | Bispecific antibody fragments for neurological disease proteins and methods of use |
| SG10201704849PA (en) | 2012-02-09 | 2017-07-28 | Chugai Pharmaceutical Co Ltd | Modified fc region of antibody |
| PT2824114T (pt) | 2012-02-21 | 2019-08-05 | Toray Industries | Composição farmacêutica para o tratamento do cancro |
| PL2818481T3 (pl) | 2012-02-21 | 2020-02-28 | Toray Industries, Inc. | Kompozycja farmaceutyczna do leczenia i/lub zapobiegania nowotworowi złośliwemu |
| JP6187255B2 (ja) | 2012-02-21 | 2017-08-30 | 東レ株式会社 | 癌の治療及び/又は予防用医薬組成物 |
| JP6187256B2 (ja) | 2012-02-21 | 2017-08-30 | 東レ株式会社 | 癌の治療及び/又は予防用医薬組成物 |
| CA2865158C (en) | 2012-02-24 | 2022-11-01 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting disappearance of antigen via fc.gamma.riib |
| WO2013147153A1 (ja) | 2012-03-29 | 2013-10-03 | 株式会社未来創薬研究所 | 抗lamp5抗体およびその利用 |
| PL2832366T3 (pl) | 2012-03-30 | 2018-04-30 | Toray Industries, Inc. | Kompozycja farmaceutyczna do leczenia i/lub zapobiegania rakowi pęcherzyka żółciowego |
| WO2013147169A1 (ja) | 2012-03-30 | 2013-10-03 | 東レ株式会社 | 肝臓癌の治療及び/又は予防用医薬組成物 |
| AU2012376421A1 (en) | 2012-04-04 | 2014-11-13 | Perseus Proteomics Inc. | Drug conjugate comprising anti-cdh3 (p-cadherin) antibody |
| JP6286757B2 (ja) | 2012-04-23 | 2018-03-07 | ジーンフロンティア株式会社 | 抗ヒトcd69抗体、及びその医薬用途 |
| EP2848633B1 (en) | 2012-05-11 | 2019-02-06 | Microbial Chemistry Research Foundation | Anti-cxadr antibody |
| DK2857419T3 (da) | 2012-05-30 | 2021-03-29 | Chugai Pharmaceutical Co Ltd | Antigen-bindende molekyle til eliminering af aggregerede antigener |
| CN107964042B (zh) | 2012-05-30 | 2022-04-19 | 中外制药株式会社 | 靶组织特异性抗原结合分子 |
| US11142563B2 (en) | 2012-06-14 | 2021-10-12 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule containing modified Fc region |
| EP2861998B1 (en) | 2012-06-18 | 2020-07-22 | Electronic Biosciences Inc. | Cell-free assay device and methods of use |
| EP2864355B1 (en) | 2012-06-25 | 2016-10-12 | Orega Biotech | Il-17 antagonist antibodies |
| EP2881467B1 (en) | 2012-07-30 | 2018-10-31 | National University Corporation Nagoya University | Monoclonal antibody against human midkine |
| JP6774164B2 (ja) | 2012-08-24 | 2020-10-21 | 中外製薬株式会社 | マウスFcγRII特異的Fc抗体 |
| AU2013306700B2 (en) | 2012-08-24 | 2019-05-02 | Chugai Seiyaku Kabushiki Kaisha | FcgammaRIIb-specific Fc region variant |
| ES2684552T3 (es) | 2012-09-03 | 2018-10-03 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos dirigidos contra ICOS para tratar la enfermedad de injerto contra hospedador |
| WO2014042251A1 (ja) | 2012-09-13 | 2014-03-20 | 中外製薬株式会社 | 遺伝子ノックイン非ヒト動物 |
| CN107501413A (zh) | 2012-09-27 | 2017-12-22 | 中外制药株式会社 | Fgfr3融合基因和以其作为标靶的药物 |
| WO2014050926A1 (ja) | 2012-09-28 | 2014-04-03 | 中外製薬株式会社 | 血液凝固反応の評価方法 |
| JP6361003B2 (ja) | 2012-11-09 | 2018-07-25 | ジーンフロンティア株式会社 | 癌治療のための抗adam28抗体 |
| EP2733153A1 (en) | 2012-11-15 | 2014-05-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for the preparation of immunoconjugates and uses thereof |
| TWI664192B (zh) | 2012-11-20 | 2019-07-01 | 法商賽諾菲公司 | 抗ceacam5抗體及其用途 |
| JP6441232B2 (ja) | 2012-12-27 | 2018-12-19 | サノフイSanofi | 抗lamp1抗体および抗体薬物コンジュゲート、ならびにその使用 |
| KR102249779B1 (ko) | 2012-12-27 | 2021-05-07 | 추가이 세이야쿠 가부시키가이샤 | 헤테로이량화 폴리펩티드 |
| EP2955226B1 (en) | 2013-02-08 | 2019-06-26 | Medical & Biological Laboratories Co., Ltd. | Antibodies to human nrg1 protein |
| CN105073988A (zh) | 2013-02-15 | 2015-11-18 | 株式会社英仙蛋白质科学 | 抗cdh3人源化抗体、其药剂偶联物以及它们的用途 |
| WO2014133093A1 (ja) | 2013-02-28 | 2014-09-04 | 独立行政法人国立がん研究センター | 不溶性フィブリンに対する抗体 |
| WO2014163101A1 (ja) | 2013-04-02 | 2014-10-09 | 中外製薬株式会社 | Fc領域改変体 |
| WO2014174596A1 (ja) | 2013-04-23 | 2014-10-30 | 株式会社医学生物学研究所 | ヘパリン結合上皮増殖因子様増殖因子に対する機能性モノクローナル抗体 |
| US9863953B2 (en) | 2013-05-16 | 2018-01-09 | Kyoto University | Method for determining prognosis of cancer |
| WO2014183885A1 (en) | 2013-05-17 | 2014-11-20 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antagonist of the btla/hvem interaction for use in therapy |
| WO2014208482A1 (ja) | 2013-06-24 | 2014-12-31 | 中外製薬株式会社 | ヒト化抗Epiregulin抗体を有効成分として含む腺癌以外の非小細胞肺癌の治療剤 |
| DK3031826T3 (en) | 2013-08-09 | 2018-12-17 | Toray Industries | Pharmaceutical composition for the treatment and / or prevention of cancer |
| JP6445440B2 (ja) | 2013-09-20 | 2018-12-26 | 中外製薬株式会社 | 抗プロテインc抗体による出血性疾患の治療 |
| SG10201803449VA (en) | 2013-09-27 | 2018-05-30 | Chugai Pharmaceutical Co Ltd | Method for producing polypeptide heteromultimer |
| JP6454893B2 (ja) | 2013-10-15 | 2019-01-23 | ジーンフロンティア株式会社 | アグリカナーゼ関連疾患の治療のためのアグリカナーゼ型adamts種に対するヒト抗体 |
| WO2015068781A1 (ja) | 2013-11-06 | 2015-05-14 | 国立大学法人大阪大学 | インフルエンザウイルスa型のグループ1に対して広域な中和活性を有する抗体 |
| ES2865196T3 (es) | 2013-11-07 | 2021-10-15 | Inst Nat Sante Rech Med | Anticuerpos anti-HER3 humana alostéricos de neuregulina |
| KR102551410B1 (ko) | 2013-11-11 | 2023-07-04 | 추가이 세이야쿠 가부시키가이샤 | 개변된 항체 가변영역을 포함하는 항원 결합 분자 |
| TWI664331B (zh) | 2013-12-04 | 2019-07-01 | 日商中外製藥股份有限公司 | 因應化合物濃度使抗原結合能力變化的抗原結合分子及其資料庫 |
| CN105849562B (zh) | 2013-12-24 | 2019-08-16 | 中外制药株式会社 | 可溶性gpc3蛋白质的测定方法 |
| JP6514645B2 (ja) | 2013-12-27 | 2019-05-15 | 中外製薬株式会社 | Fgfrゲートキーパー変異遺伝子およびそれを標的とする医薬 |
| KR102344170B1 (ko) | 2013-12-27 | 2021-12-27 | 추가이 세이야쿠 가부시키가이샤 | 등전점이 낮은 항체의 정제방법 |
| KR20160138494A (ko) | 2014-03-31 | 2016-12-05 | 데비오팜 인터네셔날 에스 에이 | Fgfr 융합물 |
| EP3131929B1 (en) | 2014-04-16 | 2022-06-01 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies for the prevention or the treatment of bleeding episodes |
| TW201625299A (zh) | 2014-06-20 | 2016-07-16 | Chugai Pharmaceutical Co Ltd | 用於因第viii凝血因子及/或活化的第viii凝血因子的活性降低或欠缺而發病及/或進展的疾病之預防及/或治療之醫藥組成物 |
| US10166304B2 (en) | 2014-07-11 | 2019-01-01 | Regents Of The University Of Minnesota | Antibody fragments for detecting cancer and methods of use |
| EP3185004A4 (en) | 2014-08-20 | 2018-05-30 | Chugai Seiyaku Kabushiki Kaisha | Method for measuring viscosity of protein solution |
| MA40764A (fr) | 2014-09-26 | 2017-08-01 | Chugai Pharmaceutical Co Ltd | Agent thérapeutique induisant une cytotoxicité |
| TWI880146B (zh) | 2014-11-11 | 2025-04-11 | 日商中外製藥股份有限公司 | 包含經改變之抗體可變區之抗原結合分子的資料庫 |
| CN114230667A (zh) | 2015-01-23 | 2022-03-25 | 赛诺菲 | 抗cd3抗体、抗cd123抗体和与cd3和/或cd123特异性结合的双特异性抗体 |
| CN114773470A (zh) | 2015-02-05 | 2022-07-22 | 中外制药株式会社 | 包含离子浓度依赖性的抗原结合结构域的抗体,fc区变体,il-8-结合抗体及其应用 |
| US10266584B2 (en) | 2015-02-09 | 2019-04-23 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Antibodies specific to glycoprotein (GP) of Ebolavirus and uses for the treatment and diagnosis of ebola virus infection |
| EP3280455A1 (en) | 2015-04-07 | 2018-02-14 | INSERM - Institut National de la Santé et de la Recherche Médicale | Non-invasive imaging of tumor pd-l1 expression |
| CA2978038A1 (en) | 2015-04-17 | 2016-10-20 | F. Hoffmann-La Roche Ag | Combination therapy with coagulation factors and multispecific antibodies |
| WO2017005847A1 (en) | 2015-07-07 | 2017-01-12 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies having specificity to myosin 18a and uses thereof |
| US10509035B2 (en) | 2015-08-07 | 2019-12-17 | Gamamabs Pharma Sa | Antibodies, antibody drug conjugates and methods of use |
| CN108271372B (zh) * | 2015-09-18 | 2021-07-09 | 中外制药株式会社 | Il-8-结合抗体及其应用 |
| EP3359573B1 (en) | 2015-10-01 | 2023-01-04 | The Whitehead Institute for Biomedical Research | Labeling of antibodies |
| EP4524161A3 (en) | 2015-10-08 | 2025-06-04 | Zymeworks BC Inc. | Antigen-binding polypeptide constructs comprising kappa and lambda light chains and uses thereof |
| WO2017060397A1 (en) | 2015-10-09 | 2017-04-13 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for predicting the survival time of subjects suffering from melanoma metastases |
| EP3370763B1 (en) | 2015-11-03 | 2024-04-10 | Regents of the University of Minnesota | Cd200 inhibitors and methods of use thereof |
| US11649293B2 (en) | 2015-11-18 | 2023-05-16 | Chugai Seiyaku Kabushiki Kaisha | Method for enhancing humoral immune response |
| WO2017086367A1 (ja) | 2015-11-18 | 2017-05-26 | 中外製薬株式会社 | 免疫抑制機能を有する細胞に対するt細胞リダイレクト抗原結合分子を用いた併用療法 |
| US20200270363A1 (en) | 2015-12-25 | 2020-08-27 | Chugai Seiyaku Kabushiki Kaisha | Antibody having enhanced activity, and method for modifying same |
| CA3013333A1 (en) | 2016-02-26 | 2017-08-31 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Antibodies having specificity for btla and uses thereof |
| RU2746754C2 (ru) | 2016-03-14 | 2021-04-20 | Чугаи Сейяку Кабусики Кайся | Индуцирующее повреждение клеток терапевтическое лекарственное средство, предназначенное для противораковой терапии |
| KR20180127971A (ko) | 2016-03-23 | 2018-11-30 | 맵스페이스 바이오사이언시즈 (쑤저우) 컴퍼니 리미티드 | 신규 항-pd-l1 항체 |
| RU2746123C2 (ru) | 2016-03-28 | 2021-04-07 | Торэй Индастриз, Инк. | Фармацевтическая композиция для лечения и/или предотвращения злокачественных опухолей |
| CN109661406A (zh) | 2016-07-29 | 2019-04-19 | 国家医疗保健研究所 | 靶向肿瘤相关巨噬细胞的抗体及其用途 |
| AU2017325240B9 (en) | 2016-09-06 | 2025-02-13 | Chugai Seiyaku Kabushiki Kaisha | Methods of using a bispecific antibody that recognizes coagulation factor IX and/or activated coagulation factor IX and coagulation factor X and/or activated coagulation factor X |
| SG10201607778XA (en) | 2016-09-16 | 2018-04-27 | Chugai Pharmaceutical Co Ltd | Anti-Dengue Virus Antibodies, Polypeptides Containing Variant Fc Regions, And Methods Of Use |
| WO2018079740A1 (ja) | 2016-10-28 | 2018-05-03 | 東レ株式会社 | 癌の治療及び/又は予防用医薬組成物 |
| US11773163B2 (en) | 2016-11-21 | 2023-10-03 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the prophylactic treatment of metastases |
| CA3039316A1 (en) | 2016-11-28 | 2018-05-31 | Chugai Seiyaku Kabushiki Kaisha | Ligand-binding molecule having adjustable ligand binding activity |
| EP4252629A3 (en) | 2016-12-07 | 2023-12-27 | Biora Therapeutics, Inc. | Gastrointestinal tract detection methods, devices and systems |
| EP3554541B1 (en) | 2016-12-14 | 2023-06-07 | Biora Therapeutics, Inc. | Treatment of a disease of the gastrointestinal tract with a chemokine/chemokine receptor inhibitor |
| EP3589654A1 (en) | 2017-03-02 | 2020-01-08 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies having specificity to nectin-4 and uses thereof |
| US10941203B2 (en) | 2017-03-15 | 2021-03-09 | Tsinghua University | Anti-TrkB agonist antibodies binding to D5 domain of TrkB and methods of promoting neuronal survival in motor neuron injury, stroke or glaucoma |
| BR112019018685A8 (pt) | 2017-03-16 | 2023-03-21 | Innate Pharma | Anticorpos, composição farmacêutica, kit, usos de um anticorpo e método in vitro de identificação ou seleção de um anticorpo |
| KR20190133005A (ko) | 2017-03-24 | 2019-11-29 | 젠야쿠코교가부시키가이샤 | 항 IgM/B 세포 표면 항원 이중 특이성 항체 |
| US20210107994A1 (en) | 2017-03-31 | 2021-04-15 | Public University Corporation Nara Medical University | Medicinal composition usable for preventing and/or treating blood coagulation factor ix abnormality, comprising multispecific antigen binding molecule replacing function of blood coagulation factor viii |
| CA3058541A1 (en) | 2017-04-14 | 2018-10-18 | Gamamabs Pharma | Amhrii-binding compounds for preventing or treating lung cancers |
| CN110891970B (zh) | 2017-04-14 | 2024-05-10 | 埃克塞里艾克西斯公司 | 用于预防或治疗癌症的amhrii结合化合物 |
| WO2018199214A1 (ja) | 2017-04-27 | 2018-11-01 | 中外製薬株式会社 | 薬物動態が改善された血液凝固第ix因子 |
| WO2019020480A1 (en) | 2017-07-24 | 2019-01-31 | INSERM (Institut National de la Santé et de la Recherche Médicale) | ANTIBODIES AND PEPTIDES FOR TREATING HCMV RELATED DISEASES |
| US11085929B2 (en) | 2017-08-31 | 2021-08-10 | Arizona Board Of Regents On Behalf Of Arizona State University | Nanoshell-structured material as co-matrix for peptide characterization in mass spectrometry |
| AU2018335955B2 (en) | 2017-09-21 | 2024-12-12 | Centre National De La Recherche Scientifique - Cnrs - | Antibodies having specificity for BTN2 and uses thereof |
| CA3080429A1 (en) * | 2017-11-01 | 2019-05-09 | Nantbio, Inc. | Il8 blocking emt pathway and overcoming cancer stem cells |
| TWI818934B (zh) | 2017-11-28 | 2023-10-21 | 日商中外製藥股份有限公司 | 可調整配體結合活性的配體結合分子 |
| TWI817974B (zh) | 2017-12-28 | 2023-10-11 | 日商中外製藥股份有限公司 | 細胞毒性誘導治療劑 |
| JP2021510697A (ja) | 2018-01-12 | 2021-04-30 | ブリストル−マイヤーズ スクイブ カンパニーBristol−Myers Squibb Company | がん処置のための坑il−8抗体及び坑pd−1抗体を用いる組合せ治療 |
| CN112119090B (zh) | 2018-03-15 | 2023-01-13 | 中外制药株式会社 | 对寨卡病毒具有交叉反应性的抗登革热病毒抗体及使用方法 |
| US12060427B2 (en) | 2018-03-28 | 2024-08-13 | Mitsubishi Tanabe Pharma Corporat | Drug conjugates of cMET monoclonal binding agents, and uses thereof |
| CN111936164B (zh) | 2018-03-30 | 2024-09-17 | 东丽株式会社 | 癌的治疗和/或预防用药物组合物 |
| RU2020136055A (ru) | 2018-04-06 | 2022-05-06 | Дана-Фарбер Кэнсер Инститьют, Инк. | Kir3dl3 в качестве рецептора hhla2, анти-hhla2-антител и его использование |
| ES2986389T3 (es) | 2018-05-21 | 2024-11-11 | Chugai Pharmaceutical Co Ltd | Formulación liofilizada sellada en un vial de vidrio |
| US11643458B2 (en) | 2018-05-31 | 2023-05-09 | Shionogi & Co., Ltd. | Monoclonal antibody against Nav1.7 |
| EA202092518A1 (ru) | 2018-06-18 | 2021-08-23 | Иннейт Фарма | Композиции и способы лечения рака |
| JP7182308B2 (ja) | 2018-07-27 | 2022-12-02 | 国立大学法人大阪大学 | 老化の抑制、加齢性の疾患もしくは症状の予防、改善、もしくは治療、または寿命の延長のための組成物 |
| US12319731B2 (en) | 2018-09-21 | 2025-06-03 | Institute Of Science Tokyo | Human monoclonal antibody binding specifically to human HMGB1, and pharmaceutical composition for treating or preventing Alzheimer's disease containing said human monoclonal antibody |
| WO2020094609A1 (en) | 2018-11-06 | 2020-05-14 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of acute myeloid leukemia by eradicating leukemic stem cells |
| US20220249814A1 (en) | 2018-11-19 | 2022-08-11 | Progenity, Inc. | Methods and devices for treating a disease with biotherapeutics |
| US20220064260A1 (en) | 2018-12-14 | 2022-03-03 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Isolated mhc-derived human peptides and uses thereof for stimulating and activating the suppressive function of cd8+cd45rclow tregs |
| JP6894086B2 (ja) | 2018-12-27 | 2021-06-23 | 塩野義製薬株式会社 | 新規抗ccr8抗体 |
| US11680105B2 (en) | 2019-01-17 | 2023-06-20 | Regents Of The University Of Minnesota | Antibody fragments for detecting cancer and methods of use |
| US20220089770A1 (en) | 2019-01-24 | 2022-03-24 | Chugai Seiyaku Kabushiki Kaisha | Novel cancer antigens and antibodies of said antigens |
| WO2020169472A2 (en) | 2019-02-18 | 2020-08-27 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods of inducing phenotypic changes in macrophages |
| KR20210134705A (ko) | 2019-02-28 | 2021-11-10 | 각코우호우진 쥰텐도 | 절단형의 변이형 Calreticulin에 결합하는 항체, 및 골수 증식성 종양의 진단, 예방 또는 치료약 |
| WO2020189748A1 (ja) | 2019-03-19 | 2020-09-24 | 中外製薬株式会社 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
| BR112021018611A2 (pt) | 2019-03-20 | 2021-11-23 | Imcheck Therapeutics Sas | Anticorpos tendo especificidade para btn2 e usos dos mesmos |
| JP2022526334A (ja) | 2019-03-25 | 2022-05-24 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 新たなタウ種を標的化することによるタウオパチー障害の処置の方法 |
| CA3136398A1 (en) | 2019-04-10 | 2020-10-15 | Chugai Seiyaku Kabushiki Kaisha | Method for purifying fc region-modified antibody |
| CN114206444B (zh) | 2019-04-18 | 2026-01-06 | Ac免疫有限公司 | 用于治疗和诊断的新分子 |
| AU2020288499A1 (en) | 2019-06-05 | 2022-01-27 | Chugai Seiyaku Kabushiki Kaisha | Antibody cleavage site-binding molecule |
| EP4007775A1 (en) | 2019-08-02 | 2022-06-08 | Orega Biotech | Novel il-17b antibodies |
| US12441788B2 (en) | 2019-09-27 | 2025-10-14 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Anti-müllerian inhibiting substance antibodies and uses thereof |
| WO2021058729A1 (en) | 2019-09-27 | 2021-04-01 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Anti-müllerian inhibiting substance type i receptor antibodies and uses thereof |
| EP3812008A1 (en) | 2019-10-23 | 2021-04-28 | Gamamabs Pharma | Amh-competitive antagonist antibody |
| JP2023503429A (ja) | 2019-11-22 | 2023-01-30 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 白血病幹細胞を根絶することによる、急性骨髄性白血病の処置のための、アドレノメデュリン阻害剤 |
| US20250340623A1 (en) | 2019-12-04 | 2025-11-06 | Ac Immune Sa | Novel Molecules for Therapy and Diagnosis |
| EP4072682A1 (en) | 2019-12-09 | 2022-10-19 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Antibodies having specificity to her4 and uses thereof |
| EP4309722A3 (en) | 2019-12-13 | 2024-08-07 | Biora Therapeutics, Inc. | Ingestible device for delivery of therapeutic agent to the gastrointestinal tract |
| MX2022010538A (es) | 2020-02-28 | 2022-09-21 | Genzyme Corp | Polipeptidos de union modificados para conjugacion optimizada con farmacos. |
| WO2021175954A1 (en) | 2020-03-04 | 2021-09-10 | Imcheck Therapeutics Sas | Antibodies having specificity for btnl8 and uses thereof |
| CA3175127A1 (en) | 2020-03-12 | 2021-09-16 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| EP4119156A4 (en) | 2020-03-12 | 2024-05-08 | Toray Industries, Inc. | MEDICINE FOR THE TREATMENT AND/OR PREVENTION OF CANCER |
| KR20220153615A (ko) | 2020-03-12 | 2022-11-18 | 도레이 카부시키가이샤 | 암의 치료 및/또는 예방을 위한 의약품 |
| US20230139178A1 (en) | 2020-03-12 | 2023-05-04 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| KR20220151684A (ko) | 2020-03-12 | 2022-11-15 | 도레이 카부시키가이샤 | 암의 치료 및/또는 예방을 위한 의약품 |
| CN115335082A (zh) | 2020-03-27 | 2022-11-11 | 光爱科技公司 | 用于杀死肿瘤细胞的医药品 |
| CA3173263A1 (en) | 2020-03-30 | 2021-10-07 | Yasuhiro Matsumura | Antibody drug conjugate |
| WO2021206078A1 (ja) | 2020-04-06 | 2021-10-14 | 株式会社PhotoQ3 | 腫瘍細胞を死滅させるための医薬 |
| JP2023106635A (ja) | 2020-04-17 | 2023-08-02 | 中外製薬株式会社 | 二重特異性抗原結合分子ならびに、それに関連する組成物、組成物の製造のための使用、キット、および方法 |
| MX2022013404A (es) | 2020-04-24 | 2022-11-14 | Sanofi Sa | Combinaciones antitumorales que contienen productos conjugados de anticuerpos anti-ceacam5, trifluridina y tipirazilo. |
| JP2023522392A (ja) | 2020-04-24 | 2023-05-30 | サノフイ | 抗ceacam5抗体コンジュゲートおよびフォルフィリを含有する抗腫瘍組み合わせ |
| IL297311A (en) | 2020-04-24 | 2022-12-01 | Sanofi Sa | Antitumor combinations containing conjugates of antibodies to ceacam5 and folfox |
| CA3180872A1 (en) | 2020-04-24 | 2021-10-28 | Sanofi | Antitumor combinations containing anti-ceacam5 antibody conjugates and cetuximab |
| CN115551553A (zh) | 2020-05-12 | 2022-12-30 | Inserm(法国国家健康医学研究院) | 治疗皮肤t细胞淋巴瘤和tfh起源淋巴瘤的新方法 |
| JP7752613B2 (ja) | 2020-05-22 | 2025-10-10 | 中外製薬株式会社 | 凝固第viii因子(f.viii)機能代替活性を有する物質を中和する抗体 |
| JP7690172B2 (ja) | 2020-06-24 | 2025-06-10 | 国立大学法人 東京大学 | 光増感色素 |
| JPWO2022004760A1 (ko) | 2020-06-30 | 2022-01-06 | ||
| WO2022025030A1 (ja) | 2020-07-28 | 2022-02-03 | 中外製薬株式会社 | 新規改変型抗体を含む、針シールドを備えた針付プレフィルドシリンジ製剤 |
| KR20230048059A (ko) | 2020-07-31 | 2023-04-10 | 추가이 세이야쿠 가부시키가이샤 | 키메라 수용체를 발현하는 세포를 포함하는 의약 조성물 |
| JP2023540732A (ja) | 2020-09-04 | 2023-09-26 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗ceacam5抗体及びコンジュゲート並びにそれらの使用 |
| EP3981789A1 (en) | 2020-10-12 | 2022-04-13 | Commissariat À L'Énergie Atomique Et Aux Énergies Alternatives | Anti-lilrb antibodies and uses thereof |
| EP4229082A1 (en) | 2020-10-16 | 2023-08-23 | AC Immune SA | Antibodies binding to alpha-synuclein for therapy and diagnosis |
| JPWO2022124247A1 (ko) | 2020-12-09 | 2022-06-16 | ||
| IL303758A (en) | 2020-12-18 | 2023-08-01 | Ac Immune Sa | Antibody delivery |
| WO2022159575A1 (en) | 2021-01-20 | 2022-07-28 | Bioentre Llc | Ctla4-binding proteins and methods of treating cancer |
| EP4360649A4 (en) | 2021-06-23 | 2025-06-25 | Toray Industries, Inc. | MEDICINE FOR THE TREATMENT AND/OR PREVENTION OF CANCER |
| JPWO2022270523A1 (ko) | 2021-06-23 | 2022-12-29 | ||
| AU2022320304A1 (en) | 2021-07-27 | 2024-02-29 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| US20250325663A1 (en) | 2021-07-27 | 2025-10-23 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| AU2022319362A1 (en) | 2021-07-27 | 2024-02-29 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| KR20240095160A (ko) | 2021-07-29 | 2024-06-25 | 인스티튜트 내셔널 드 라 싼테 에 드 라 리셰르셰 메디칼르 (인 썸) | 인간화된 항-인간 βig-h3 단백질 및 이의 용도 |
| EP4380691A1 (en) | 2021-08-06 | 2024-06-12 | Institut Régional du Cancer de Montpellier (ICM) | Methods for the treatment of cancer |
| US20250281630A1 (en) | 2021-09-03 | 2025-09-11 | Toray Industries, Inc. | Pharmaceutical composition for cancer treatment and/or prevention |
| JPWO2023048231A1 (ko) | 2021-09-24 | 2023-03-30 | ||
| CN118043031A (zh) | 2021-10-04 | 2024-05-14 | 诺华股份有限公司 | 表面活性剂稳定剂 |
| JPWO2023058723A1 (ko) | 2021-10-08 | 2023-04-13 | ||
| IL311683B1 (en) | 2021-11-01 | 2025-12-01 | Shionogi & Co | Novel nav1.7 monoclonal antibody |
| WO2023079057A1 (en) | 2021-11-05 | 2023-05-11 | Sanofi | Antitumor combinations containing anti-ceacam5 antibody-drug conjugates and anti-vegfr-2 antibodies |
| CN115466331B (zh) | 2021-11-18 | 2023-05-30 | 合源生物科技(天津)有限公司 | 靶向bcma的嵌合抗原受体及其应用 |
| EP4442274A4 (en) | 2021-12-01 | 2025-12-24 | Chugai Pharmaceutical Co Ltd | METHOD FOR PREPARING A FORMULATION CONTAINING AN ANTIBODY |
| WO2023171009A1 (ja) | 2022-03-09 | 2023-09-14 | 株式会社Cured | Eva1タンパク質に結合する、ヒト化抗体又はその機能的断片、抗体薬物複合体及びキメラ抗原受容体 |
| WO2023170239A1 (en) | 2022-03-09 | 2023-09-14 | Merck Patent Gmbh | Methods and tools for conjugation to antibodies |
| WO2023172968A1 (en) | 2022-03-09 | 2023-09-14 | Merck Patent Gmbh | Anti-gd2 antibodies, immunoconjugates and therapeutic uses thereof |
| WO2023192478A1 (en) | 2022-04-01 | 2023-10-05 | Bristol-Myers Squibb Company | Combination therapy with anti-il-8 antibodies and anti-pd-1 antibodies for treating cancer |
| JP7544986B2 (ja) | 2022-04-26 | 2024-09-03 | 中外製薬株式会社 | 医薬製剤含有フィルター内蔵シリンジ |
| JPWO2023234406A1 (ko) | 2022-06-03 | 2023-12-07 | ||
| JPWO2023238869A1 (ko) | 2022-06-07 | 2023-12-14 | ||
| WO2023240287A1 (en) | 2022-06-10 | 2023-12-14 | Bioentre Llc | Combinations of ctla4 binding proteins and methods of treating cancer |
| US20250367307A1 (en) | 2022-06-30 | 2025-12-04 | Toray Industries, Inc. | Pharmaceutical composition for cancer treatment and/or prevention |
| CN119768181A (zh) | 2022-08-24 | 2025-04-04 | 东丽株式会社 | 用于癌的治疗和/或预防的药品 |
| CN119744176A (zh) | 2022-08-24 | 2025-04-01 | 东丽株式会社 | 用于癌的治疗和/或预防的药品 |
| AU2023329558A1 (en) | 2022-08-24 | 2025-02-27 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| EP4582101A1 (en) | 2022-08-30 | 2025-07-09 | Toray Industries, Inc. | Medicament for treatment and/or prevention of cancer |
| KR20250053841A (ko) | 2022-08-30 | 2025-04-22 | 도레이 카부시키가이샤 | 암의 치료 및/또는 예방을 위한 의약품 |
| CA3267132A1 (en) | 2022-09-09 | 2024-03-14 | Regents Of The University Of Minnesota | ANTIBODIES DIRECTED AGAINST FENTANYL AND ITS ANALOGUES AND THEIR METHODS OF USE |
| CN120225559A (zh) | 2022-09-12 | 2025-06-27 | 国家健康与医学研究院 | 新型抗itgb8抗体及其用途 |
| KR20250116683A (ko) | 2022-11-25 | 2025-08-01 | 고꾸리쯔 다이가꾸 호우징 오사까 다이가꾸 | 혈액암에 대한 항체 |
| CN120302998A (zh) | 2022-12-23 | 2025-07-11 | 东丽株式会社 | 用于癌的治疗和/或预防的药品 |
| AU2024224961A1 (en) | 2023-02-21 | 2025-09-11 | Joint-Stock Company "Generium" | Pharmaceutical composition and method for the prophylaxis and treatment of a lysosomal enzyme deficiency in a subject with mucopolysaccharidosis type ii |
| KR20250154496A (ko) | 2023-03-01 | 2025-10-28 | 사노피 | Ceacam5를 발현하는 신경내분비암을 치료하기 위한 항-ceacam5 면역접합체의 용도 |
| EP4427763A1 (en) | 2023-03-06 | 2024-09-11 | Sanofi | Antitumor combinations containing anti-ceacam5 antibody-drug conjugates, anti-vegfr-2 antibodies and anti-pd1/pd-l1 antibodies |
| KR20250169564A (ko) | 2023-03-23 | 2025-12-03 | 사노피 | 암 치료법에서 환자 선택을 위한 CEACAM5 mRNA 검정 |
| JPWO2024214811A1 (ko) | 2023-04-14 | 2024-10-17 | ||
| WO2024251733A1 (en) | 2023-06-05 | 2024-12-12 | Sanofi | Antitumor combinations containing anti-ceacam5 antibody-drug conjugates, anti-pd1/pd-l1 antibodies and anti-ctla4 antibodies |
| WO2024261239A1 (en) | 2023-06-23 | 2024-12-26 | Imcheck Therapeutics | Bispecific antibodies targeting btn3a and the pd-1/pd-l1 inhibitory axis |
| WO2025012417A1 (en) | 2023-07-13 | 2025-01-16 | Institut National de la Santé et de la Recherche Médicale | Anti-neurotensin long fragment and anti-neuromedin n long fragment antibodies and uses thereof |
| WO2025032158A1 (en) | 2023-08-08 | 2025-02-13 | Institut National de la Santé et de la Recherche Médicale | Method to treat tauopathies |
| WO2025073890A1 (en) | 2023-10-06 | 2025-04-10 | Institut National de la Santé et de la Recherche Médicale | Method to capture circulating tumor extracellular vesicles |
| WO2025093720A1 (en) | 2023-11-02 | 2025-05-08 | Betasense Gmbh | Methods for determining misfolded alpha-synuclein in a sample |
| WO2025172525A1 (en) | 2024-02-15 | 2025-08-21 | Merck Patent Gmbh | Anti-gd2 antibodies and immunoconjugates for the treatment of gd2 positive cancer |
| WO2025210264A1 (en) | 2024-04-04 | 2025-10-09 | Merck Patent Gmbh | Antibody-drug-conjugates binding napi2b |
| WO2025242732A1 (en) | 2024-05-21 | 2025-11-27 | Institut National de la Santé et de la Recherche Médicale | Pan antibodies against sars-cov-2 spike protein and uses thereof for therapeutical purposes |
| WO2025242845A1 (en) | 2024-05-22 | 2025-11-27 | Merck Patent Gmbh | Colorectal cancer treatment |
| WO2025248097A2 (en) | 2024-05-31 | 2025-12-04 | Gamamabs Pharma | Humanized anti-human her3 antibodies and uses thereof |
| WO2025257181A1 (en) | 2024-06-11 | 2025-12-18 | Institut National de la Santé et de la Recherche Médicale | Antibodies targeting trans-active response dna-binding protein-43 (tdp-43) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62201598A (ja) * | 1986-02-28 | 1987-09-05 | Teijin Ltd | マウス−ヒトキメラ抗体h鎖、それをコ−ドするキメラdna配列、プラスミドおよび細胞 |
| JPH04141095A (ja) * | 1990-10-02 | 1992-05-14 | Chemo Sero Therapeut Res Inst | 組換え抗hiv改変抗体および改変抗体の調製方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| GB9014932D0 (en) * | 1990-07-05 | 1990-08-22 | Celltech Ltd | Recombinant dna product and method |
| IE913192A1 (en) * | 1990-09-12 | 1992-02-25 | Scripps Research Inst | Active site of interleukin-8: polypeptide analogs and¹antibodies |
| WO1995001997A1 (en) * | 1993-07-09 | 1995-01-19 | Smithkline Beecham Corporation | RECOMBINANT AND HUMANIZED IL-1β ANTIBODIES FOR TREATMENT OF IL-1 MEDIATED INFLAMMATORY DISORDERS IN MAN |
| CA2181787A1 (en) * | 1994-03-03 | 1995-09-08 | Claire M. Doerschuk | Anti-il-8 monoclonal antibodies for treatment of inflammatory disorders |
| US5874080A (en) * | 1994-03-03 | 1999-02-23 | Genentech, Inc. | Anti-IL-8 monoclonal antibodies for treatment of asthma |
-
1995
- 1995-07-12 KR KR1019970700191A patent/KR100261941B1/ko not_active Expired - Fee Related
- 1995-07-12 AU AU29363/95A patent/AU701342B2/en not_active Ceased
- 1995-07-12 US US08/765,783 patent/US5994524A/en not_active Expired - Lifetime
- 1995-07-12 AT AT95925116T patent/ATE340590T1/de not_active IP Right Cessation
- 1995-07-12 DE DE69535243T patent/DE69535243T2/de not_active Expired - Lifetime
- 1995-07-12 CA CA002194907A patent/CA2194907A1/en not_active Abandoned
- 1995-07-12 EP EP95925116A patent/EP0770628B9/en not_active Expired - Lifetime
- 1995-07-12 WO PCT/JP1995/001396 patent/WO1996002576A1/ja not_active Ceased
- 1995-07-12 HU HU9700093A patent/HU221385B1/hu not_active IP Right Cessation
- 1995-10-11 ZA ZA955832A patent/ZA955832B/xx unknown
-
1999
- 1999-10-12 US US09/416,557 patent/US6245894B1/en not_active Expired - Lifetime
-
2000
- 2000-12-07 US US09/730,857 patent/US20020082396A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62201598A (ja) * | 1986-02-28 | 1987-09-05 | Teijin Ltd | マウス−ヒトキメラ抗体h鎖、それをコ−ドするキメラdna配列、プラスミドおよび細胞 |
| JPH04141095A (ja) * | 1990-10-02 | 1992-05-14 | Chemo Sero Therapeut Res Inst | 組換え抗hiv改変抗体および改変抗体の調製方法 |
Non-Patent Citations (2)
| Title |
|---|
| J. Immunol Methods, vol.149, pp227-235 (1992. 5. 18) * |
| Nature, vol.332, pp323-327 (1988. 3. 24) * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12473375B2 (en) | 2006-03-31 | 2025-11-18 | Chugai Seiyaku Kabushiki Kaisha | Methods for controlling blood pharmacokinetics of antibodies |
| US12116414B2 (en) | 2007-09-26 | 2024-10-15 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US12122840B2 (en) | 2007-09-26 | 2024-10-22 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US11454633B2 (en) | 2014-12-19 | 2022-09-27 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant Fc regions, and methods of use |
| US12169205B2 (en) | 2014-12-19 | 2024-12-17 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant fc regions, and methods of use |
| US12252532B2 (en) | 2015-12-25 | 2025-03-18 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies and methods of use |
| US11780912B2 (en) | 2016-08-05 | 2023-10-10 | Chugai Seiyaku Kabushiki Kaisha | Composition for prophylaxis or treatment of IL-8 related diseases |
| US12516115B2 (en) | 2016-08-05 | 2026-01-06 | Chugai Seiyaku Kabushiki Kaisha | Composition for prophylaxis or treatment of IL-8 related diseases |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE340590T1 (de) | 2006-10-15 |
| CA2194907A1 (en) | 1996-02-01 |
| AU701342B2 (en) | 1999-01-28 |
| US6245894B1 (en) | 2001-06-12 |
| US20020082396A1 (en) | 2002-06-27 |
| EP0770628A1 (en) | 1997-05-02 |
| HU221385B1 (en) | 2002-09-28 |
| WO1996002576A1 (en) | 1996-02-01 |
| US5994524A (en) | 1999-11-30 |
| EP0770628B9 (en) | 2007-02-28 |
| ZA955832B (en) | 1996-04-10 |
| EP0770628B1 (en) | 2006-09-27 |
| HUT77420A (hu) | 1998-04-28 |
| DE69535243D1 (de) | 2006-11-09 |
| DE69535243T2 (de) | 2007-05-10 |
| EP0770628A4 (en) | 2004-10-27 |
| AU2936395A (en) | 1996-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100261941B1 (ko) | 사람의 인터루킨-8에 대한 재구성 사람항체 | |
| JP3176598B2 (ja) | ヒトインターロイキン−6受容体に対するキメラ抗体 | |
| US6316227B1 (en) | Nucleic acids encoding interleukin-5 specific recombinant antibodies | |
| US6024956A (en) | Method to treat inflammation with humanized anti-IL-8-antibodies | |
| US7183390B2 (en) | Humanized antibodies to gamma-interferon | |
| EP0627002B1 (en) | Cloning and expression of humanized monoclonal antibodies against human interleukin-4 | |
| JP3865418B2 (ja) | ヒトインターロイキン−8に対する再構成ヒト抗体 | |
| EP2567982A1 (en) | Antibody against carcinoembryonic antigen and uses thereof | |
| US6214973B1 (en) | Reshaped human antibody to human medulloblastoma cells | |
| RU2159776C2 (ru) | Реконструированные человеческие антитела к человеческому интерлейкину-8 | |
| KR100277769B1 (ko) | 항-파스 재조합 항체 및 이에 대한 디엔에이 | |
| JP3614183B2 (ja) | ヒトインターロイキン−6に対する再構成ヒト抗体 | |
| CN1817906B (zh) | 抗人副甲状腺激素相关蛋白的抗体 | |
| HK1008831B (en) | Cloning and expression of humanized monoclonal antibodies against human interleukin-4 | |
| MXPA98002536A (en) | Antibodies anti- |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| FPAY | Annual fee payment |
Payment date: 20030324 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee |
St.27 status event code: A-4-4-U10-U13-oth-PC1903 Not in force date: 20040426 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE |
|
| PC1903 | Unpaid annual fee |
St.27 status event code: N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 20040426 |