JP2022525149A - ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 - Google Patents
ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 Download PDFInfo
- Publication number
- JP2022525149A JP2022525149A JP2021555227A JP2021555227A JP2022525149A JP 2022525149 A JP2022525149 A JP 2022525149A JP 2021555227 A JP2021555227 A JP 2021555227A JP 2021555227 A JP2021555227 A JP 2021555227A JP 2022525149 A JP2022525149 A JP 2022525149A
- Authority
- JP
- Japan
- Prior art keywords
- subject
- treatment
- alvocidib
- aml
- days
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/453—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/661—Phosphorus acids or esters thereof not having P—C bonds, e.g. fosfosal, dichlorvos, malathion or mevinphos
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Dermatology (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
本出願は、2019年3月20日に出願された米国仮特許出願第62/821,342号、および2019年7月9日に出願された米国仮特許出願第62/871,934号の利益を主張する。これらの出願の教示全体は、参照により本明細書に組み込まれる。
したがって、以前のベネトクラクス処置に失敗したAML患者を処置するための治療法を開発することは非常に興味深く重要である。
(i)被験体(例えば、血液がんを有する患者)の腫瘍崩壊症候群(TLS)の発症を阻害する方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、アルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(ii)被験体(例えば、アルボシジブで処置される血液がん被験体)のTLSの重症度を低減する方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(iii)被験体(例えば、アルボシジブで処置される血液がん被験体)のTLSを処置する方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(iv)被験体(例えば、アルボシジブで処置される血液がん被験体)のTLSによる死亡率を低下させる方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(v)被験体(例えば、アルボシジブで処置される血液がん被験体)のTLSの発生率を低下させる方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(vi)被験体(例えば、アルボシジブで処置される血液がん被験体)のTLSを予防する方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
(vii)TLSを発症するリスクが高くない、被験体の血液がんを処置する方法であって、本明細書に開示される処置レジメンのいずれかに従って、ベネトクラクスの非存在下で、有効量のアルボシジブ(例えば、約50mg/m2に等しいかもしくはそれ未満、約15mg/m2~約40mg/m2または約25mg/m2の第1の用量で)および、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
原薬および原薬を含む医薬組成物
(i)治療薬
(ii)医薬組成物
AML被験体
ベネトクラクスが失敗したAMLを処置する方法
(i)アルボシジブ単剤療法を含む処置レジメン
(ii)低用量のシタラビンと組み合わせてアルボシジブを含む処置レジメン
-20mg/m2のシタラビンを、10連続日間、1日1回または2回(医師の選択による)、SC注射する。この投与量は、70歳を超えるAML患者に与えられ得る。
-20mg/m2のシタラビンを、4週間にわたって1週間に4日間、12時間離して2回に分けてSC注射する(CRまたは部分寛解(PR)患者の場合、シタラビンが維持処置として2日/週与えられ得る)。この投与量は、60歳を超えるAML患者に与えられ得る。
-修飾LDAC(mLDAC)シタラビン(20mg/m2 SC BID)および経口エトポシド(50mg PO BID)を14日間の第1のサイクル。この投与条件は、60歳を超える不適格AML患者(例えば、ECOG 2またはそれを超える)に適用され得る。
-シタラビン、20mg/m2、1日2回(BID)、SC、1日目から10日目、1日目+15日目のみ1時間IV。この投与条件は、ECOG≦2を有するAML患者に適用され得る。
-シタラビン、1日目~10日目、40mg/m2、1日1回、または20mg/m2、1日2回、SC、サイクル頻度28~42日毎。この投与条件は、不適格AML患者に適用され得る。
-シタラビン、20mg/m2 SC、1日2回、1~10日目(必要に応じて、1日1回経口のグラスデギブ100mgと組み合わせて)。この投与条件は、75歳を超えるAML患者に適用され得る。
(iii)低メチル化剤と組み合わせてアルボシジブを含む処置レジメン
(iv)アルボシジブを含む他の処置レジメン
腫瘍崩壊症候群(TLS)を軽減する方法
[0001]
本明細書で使用される場合、「TLS治療」という用語は、高カリウム血症、高尿酸血症、高リン血症、凝固障害、血清クレアチニンの増加、サイトカイン放出症候群、乏尿性腎不全(例えば、尿量が800mL/日未満)、心不整脈、テタニーおよび/または発作の処置を指す。このような処置は、予防的に、あるいは前記状態または障害のうちの1またはそれを超えるものの発症に応じて患者に投与され、このような処置は、1回または複数回、被験体に投与され得る。TLS治療には、それだけに限らないが、処置前IV水分供給、経口アロプリノール、経口リン酸塩吸着剤の予防的投与、および尿量が流入水分量と等しくなることを確実にするように注意深く監視することが含まれる。流入量が流出量より10%多い場合は、利尿剤の投与が推奨される。下痢に起因するものを含む過度の水分喪失の補充も、臨床的に特に指示がない限り、実験室異常に関連する以下の処置とともに推奨される:
・ カリウムレベルが4.0mEq/L超に上昇している場合、TLS以外の高カリウム血症の他に考えられる原因も、その使用の禁忌もない限り、患者は30gm用量のポリスチレンスルホン酸ナトリウムを受けるべきである。
・ カリウムレベルが5.0mEq/L超に上昇した場合、TLS以外の高カリウム血症の他に考えられる原因も、その使用の禁忌もない限り、患者は、30gm用量のポリスチレンスルホン酸ナトリウムに加えて、10単位のIV速効型インスリンおよび25gm(1アンプル)のIVデキストロース50%も受けるべきである。
・ カリウムレベルが5.5mEq/L超に上昇した場合、患者は緊急の断続的または連続的な透析を検討されるべきである。
・ リン酸カルシウム結晶の腎沈殿を回避するために、この設定ではカルシウム補給が症候性低カルシウム血症に対してのみ行われるべきである。
・ サイトカイン放出症候群の臨床的証拠を示す患者、または透析を必要とする高カリウム血症の患者は、少なくとも20mgのIVデキサメタゾンに相当する即時ステロイド療法を受ける。
ベネトクラクスが失敗したAMLの処置に使用するためのキット
一般的な技術
例示的実施形態
A1.急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で、有効量のアルボシジブを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
A2.1またはそれを超える以前の治療が、AMLを処置するための1またはそれを超える他の治療薬をさらに含む、請求項A1に記載の方法。
A3.AMLを処置するための1またはそれを超える他の治療薬が、アザシチジン、デシタビン、またはこれらの組み合わせである、請求項A2に記載の方法。
A4.上記方法が、AMLのための単独の処置剤としてアルボシジブを含む、請求項A1からA3のいずれか一項に記載の方法。
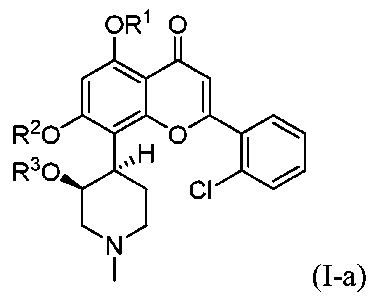
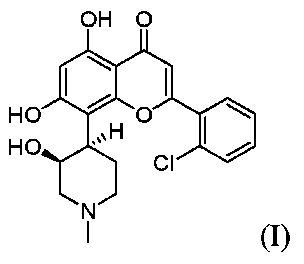
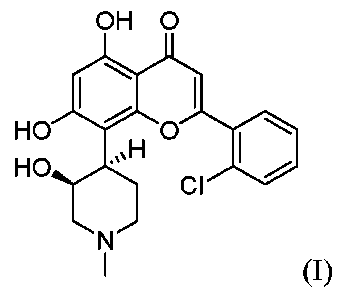
A5.アルボシジブが式(I)の構造を有する化合物:
A6.アルボシジブが式(I-b)の構造を有する化合物:
A7.被験体が、難治性AMLを有し、1またはそれを超える以前の治療が最大2サイクルのベネトクラクス処置を含む、請求項A1からA6のいずれか一項に記載の方法。
A8.被験体が、1またはそれを超える以前の治療後に再発AMLを有する、請求項A1からA6のいずれか一項に記載の方法。
A9.被験体が、約90日間~約18か月間の第1の完全寛解(CR1)期間後に再発AMLを有する、請求項A8に記載の方法。
A10.アルボシジブの有効量が、1週間に1回、約20mg/m2~約100mg/m2である、請求項A1からA9のいずれか一項に記載の方法。
A11.アルボシジブの有効量が、1週間に1回、約25mg/m2または約50mg/m2である、請求項A1からA10のいずれか一項に記載の方法。
A12.アルボシジブが、1週間に1回、約15分間~約1時間の静脈内ボーラスとして、約20mg/m2~約100mg/m2の用量で被験体に投与される、請求項A1からA11のいずれか一項に記載の方法。
A13.アルボシジブが、約30分間の静脈内ボーラスとして、約25mg/m2~約50mg/m2の用量で被験体に投与される、請求項A1からA10のいずれか一項に記載の方法。
A14.アルボシジブが、約25mg/m2または約50mg/m2の用量で被験体に投与される、請求項A13に記載の方法。
A15.アルボシジブが、処置サイクルとして、1週間に1回、約1~約4週間連続して被験体に投与され、これに約1~約3週間の休薬期間が続く、請求項A1からA14のいずれか一項に記載の方法。
A16.アルボシジブが、処置サイクルとして、1週間に1回、3週間連続して被験体に投与され、これに1週間の休薬期間が続く、請求項A15に記載の方法。
A17.上記方法が、1~8回の処置サイクルを含む、請求項A1からA16のいずれか一項に記載の方法。
A18.処置が被験体に実質的に利益を示さなくなるまで、複数の処置サイクルを含む、請求項A1からA16のいずれか一項に記載の方法。
A19.各処置サイクルが、(i)アルボシジブを約15分間~約1時間の静脈内ボーラスとして、約15mg/m2~約40mg/m2の用量で被験体に投与すること、および(ii)ステップ(i)の約1週間後、アルボシジブを、1週間に1回、2~4週間、約15分間~約1時間の静脈内ボーラスとして、約40mg/m2~約80mg/m2の用量で被験体に投与し、これに約2~約4週間の休薬期間が続くことを含む、請求項A15からA18のいずれか一項に記載の方法。
A20.各処置サイクルが4週間からなり、(i)アルボシジブを、第1週の初日に約30分間の静脈内ボーラスとして、約25mg/m2の用量で被験体に投与すること、および(ii)アルボシジブを、第2週の初日および第3週の初日に約30分間の静脈内ボーラスとして、約50mg/m2の用量で被験体に投与し、これに約1週間の休薬期間が続くことを含む、請求項A15からA19のいずれか一項に記載の方法。
A21.上記方法が、2~6回の処置サイクルを含む、請求項A15からA20のいずれか一項に記載の方法。
A22.上記方法が、3~5回の処置サイクルを含む、請求項A21に記載の方法。
A23.白血病芽球数の少なくとも約20%の減少を達成できない被験体でアルボシジブの投与を終了するステップをさらに含む、請求項A1からA22のいずれか一項に記載の方法。
A24.有効量のアシクロビル、トリメトプリム、スルファメトキサゾール、またはこれらの組み合わせを被験体に投与するステップをさらに含む、請求項A1からA23のいずれか一項に記載の方法。
A25.有効量のシプロフロキサシンを、好中球減少症を有する被験体に投与するステップをさらに含む、請求項A1からA24のいずれか一項に記載の方法。
A26.被験体が、顆粒球コロニー刺激因子を含む処置を受けていない、請求項A1からA25のいずれか一項に記載の方法。
A27.被験体がMCL-1依存性である、請求項A1からA26のいずれか一項に記載の方法。
A28.被験体がMCL-1依存性として特定されている、請求項A1からA27のいずれか一項に記載の方法。
A29.被験体が、被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項A28に記載の方法。
A30.式(I-b)の化合物またはその薬学的に許容され得る塩が、被験体に経口投与される、請求項A6に記載の方法。
A31.被験体が、アルボシジブを投与される前に測定可能残存病変(MRD)陽性である、請求項A1からA30のいずれか一項に記載の方法。
A32.被験体が、アルボシジブを投与された後に測定可能残存病変(MRD)陰性である、請求項A1からA31のいずれか一項に記載の方法。
A33.被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項A1からA32のいずれか一項に記載の方法。
A34.アルボシジブを被験体に投与する前に、被験体のMRD状態が検出される、請求項A33に記載の方法。
A35.アルボシジブを被験体に投与した後に、被験体のMRD状態が検出される、請求項A33に記載の方法。
A36.アルボシジブを被験体に投与する前後に、被験体のMRD状態が検出される、請求項A33からA35のいずれか一項に記載の方法。
A37.被験体が測定可能残存病変(MRD)陰性であると決定された場合、被験体へのアルボシジブの投与を終了するステップをさらに含む、請求項A1からA36のいずれか一項に記載の方法。
B1.急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で、
(i)第1の処置過程で有効量のアルボシジブを被験体に投与するステップと;
(ii)第2の処置過程で有効量のシタラビンを被験体に投与するステップと;
(iii)第3の処置過程で有効量のアルボシジブを被験体に投与するステップと
を含み;
被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
B2.1またはそれを超える以前の治療が、AMLを処置するための1またはそれを超える他の治療薬をさらに含む、請求項B1に記載の方法。
B3.1またはそれを超える他の治療薬が、アザシチジン、デシタビン、またはこれらの組み合わせを含む、請求項B2に記載の方法。
B4.アルボシジブが式(I)の構造を有する化合物:
B5.アルボシジブが式(I-b)の構造を有する化合物:
B6.ステップ(ii)がステップ(i)の後に実施され、ステップ(iii)がステップ(ii)の後に実施される、請求項B1からB5のいずれか一項に記載の方法。
B7.第1の処置過程におけるアルボシジブの有効量が、第3の処置過程におけるアルボシジブの有効量とは異なる、請求項B1からB6のいずれか一項に記載の方法。
B8.第1の処置過程におけるアルボシジブの有効量が、1日当たり約10mg/m2~約50mg/m2である、請求項B1からB7のいずれか一項に記載の方法。
B9.第1の処置過程におけるアルボシジブの有効量が、1日当たり約25mg/m2である、請求項B8に記載の方法。
B10.第1の処置過程が約1~約4日間からなる、請求項B1からB9のいずれか一項に記載の方法。
B11.第1の処置過程が1日間または2日間からなる、請求項B10に記載の方法。
B12.第2の処置過程におけるシタラビンの有効量が、1日当たり約10mg/m2~約100mg/m2である、請求項B1からB11のいずれか一項に記載の方法。
B13.第2の処置過程におけるシタラビンの有効量が、1日当たり約20mg/m2である、請求項B12に記載の方法。
B14.第2の処置過程が8~12日間からなる、請求項B1からB13のいずれか一項に記載の方法。
B15.第2の処置過程が10日間からなる、請求項B14に記載の方法。
B16.第3の処置過程におけるアルボシジブの有効量が、1日当たり約25mg/m2~約100mg/m2である、請求項B1からB15のいずれか一項に記載の方法。
B17.第3の処置過程におけるアルボシジブの有効量が、1日当たり約50mg/m2である、請求項B16に記載の方法。
B18.第3の処置過程が1~3日間からなる、請求項B1からB17のいずれか一項に記載の方法。
B19.第3の処置過程が1日間または2日間からなる、請求項B18に記載の方法。
B20.第1の処置過程が1日間からなり、これに、第2の処置過程の開始前の1日間の第1の休薬期間が続く、請求項B1からB19のいずれか一項に記載の方法。
B21.第2の処置過程が10日間からなり、これに、第3の処置過程の開始前の2日間の第2の休薬期間が続く、請求項B1からB20のいずれか一項に記載の方法。
B22.第3の処置過程が1日間からなり、これに、約13日間の第3の休薬期間が続く、請求項B1からB21のいずれか一項に記載の方法。
B23.複数の処置サイクルを含み、各処置サイクルが第1の処置過程、第2の処置過程、および第3の処置過程を含み、28日毎に繰り返される、請求項B1からB22のいずれか一項に記載の方法。
B24.各処置サイクルが以下を含む、請求項B23に記載の方法:
(i)アルボシジブを、約1~約3日間、約15分間~約1時間の静脈内ボーラスとして、約10mg/m2~約50mg/m2の1日量で被験体に投与し、これに約1~約3日間の第1の休薬期間が続くこと;
(ii)シタラビンを、8~12日間、約15mg/m2~約40mg/m2の1日量で皮下注射によって被験体に投与し、これに1~3日間の第2の休薬期間が続くこと;
(iii)アルボシジブを、約1~約3日間、約15分間~約1時間の静脈内ボーラスとして、約25mg/m2~約100mg/m2の1日量で被験体に投与し、これに約12~約14日間の第3の休薬期間が続くこと。
B25.各処置サイクルが以下を含む、請求項B24に記載の方法:
(i)アルボシジブを、第1の処置過程で、1日間、約30分間の静脈内ボーラスとして、約25mg/m2の1日量で被験体に投与し、これに1日間の第1の休薬期間が続くこと;
(ii)シタラビンを、第2の処置過程で、10日間、約20mg/m2の1日量で皮下注射によって被験体に投与し、これに2日間の第2の休薬期間が続くこと;
(iii)アルボシジブを、第3の処置過程で、1日間、約30分間の静脈内ボーラスとして、約50mg/m2の1日量で被験体に投与し、これに約13日間の第3の休薬期間が続くこと。
B26.各処置サイクルが28日間からなり、以下を含む、請求項B24またはB25に記載の方法:
(i)アルボシジブを、1日目に約30分間の静脈内ボーラスとして、約25mg/m2の1日量で被験体に投与し、これに2日目の第1の休薬期間が続くこと;
(ii)シタラビンを、3~12日目に約20mg/m2の1日量で皮下注射によって被験体に投与し、これに13~14日目の第2の休薬期間が続くこと;および
(iii)アルボシジブを、15日目に約30分間の静脈内ボーラスとして、約50mg/m2の1日量で被験体に投与し、これに16~28日目の第3の休薬期間が続くこと。
B27.ステップ(iii)がステップ(i)の後に実施され、ステップ(ii)がステップ(iii)の後に実施される、請求項B1からB5のいずれか一項に記載の方法。
B28.ステップ(i)、(ii)および(iii)が、1またはそれを超える休薬期間によって分離される、請求項B27に記載の方法。
B29.第1の処置過程におけるアルボシジブの有効量が、1日当たり約10mg/m2~約50mg/m2である、請求項B27または請求項B28に記載の方法。
B30.第1の処置過程におけるアルボシジブの有効量が約25mg/m2である、請求項B29に記載の方法。
B31.第1の処置過程が約1~4日間からなる、請求項B27からB29のいずれか一項に記載の方法。
B32.第1の処置過程が1日間または2日間からなる、請求項B31に記載の方法。
B33.第3の処置過程におけるアルボシジブの有効量が、1日当たり約25mg/m2~約100mg/m2である、請求項B27からB32のいずれか一項に記載の方法。
B34.第3の処置過程におけるアルボシジブの有効量が、1日当たり約50mg/m2である、請求項B33に記載の方法。
B35.第3の処置過程が1~3日間からなる、請求項B27からB34のいずれか一項に記載の方法。
B36.第3の処置過程が1日間または2日間からなる、請求項B35に記載の方法。
B37.第1の処置過程が1日間からなり、第3の処置過程が2日間からなる、または第1の処置過程が2日間からなり、第3の処置過程が1日間からなる、請求項B27からB36のいずれか一項に記載の方法。
B38.第2の処置過程におけるシタラビンの有効量が、1日当たり約10mg/m2~約100mg/m2である、請求項B27からB37のいずれか一項に記載の方法。
B39.第2の処置過程におけるシタラビンの有効量が、1日当たり約20mg/m2である、請求項B38に記載の方法。
B40.第2の処置過程が8~12日間からなる、請求項B38またはB39に記載の方法。
B41.第2の処置過程が10日間からなる、請求項B40に記載の方法。
B42.第2の処置過程におけるシタラビンの有効量が、10日間、1日1回または2回、20mg/m2である、請求項B1からB41のいずれか一項に記載の方法。
B43.第2の処置過程におけるシタラビンの有効量が、4日間、2つの用量に分けられる1日20mg/m2であり、上記2つの用量が12時間離して被験体に投与される、請求項B1からB42のいずれか一項に記載の方法。
B44.シタラビンが1週間に2日間被験体に投与される、請求項B43に記載の方法。
B45.第2の処置過程におけるシタラビンの有効量が、10日間、1日2回、20mg/m2である、請求項B1からB42のいずれか一項に記載の方法。
B46.第2の処置過程におけるシタラビンの有効量が、10日間、1日1回40mg/m2、または1日2回20mg/m2である、請求項B1からB41のいずれか一項に記載の方法。
B47.第1の処置過程、第3の処置過程、またはその両方におけるアルボシジブが、静脈内注入によって投与される、請求項B1からB46のいずれか一項に記載の方法。
B48.第1の処置過程、第3の処置過程、またはその両方におけるアルボシジブが、15分間~1時間の静脈内ボーラスとして投与される、請求項B47に記載の方法。
B49.第1の処置過程、第3の処置過程、またはその両方におけるアルボシジブが、30分間の静脈内ボーラスとして投与される、請求項B48に記載の方法。
B50.第2の処置過程におけるシタラビンが注射によって投与される、請求項B1からB49のいずれか一項に記載の方法。
B51.第2の処置過程におけるシタラビンが皮下注射によって投与される、請求項B50に記載の方法。
B52.少なくともアルボシジブの第1の投与前に、有効量の静脈内水分供給液、アロプリノール、リン酸塩吸着剤またはこれらの組み合わせを被験体に投与するステップをさらに含む、請求項B1からB51のいずれか一項に記載の方法。
B53.有効量の抗生物質、抗ウイルス剤、抗真菌剤またはこれらの組み合わせを被験体に投与するステップをさらに含む、請求項B1からB52のいずれか一項に記載の方法。
B54.被験体がMCL-1依存性である、請求項B1からB53のいずれか一項に記載の方法。
B55.被験体がMCL-1依存性として特定されている、請求項B1からB54のいずれか一項に記載の方法。
B56.被験体が、被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項B55に記載の方法。
B57.式(I-b)の化合物またはその薬学的に許容され得る塩が、被験体に経口投与される、請求項B5に記載の方法。
B58.被験体が、第1、第2および第3の処置過程を投与される前に測定可能残存病変(MRD)陽性である、請求項B1からB57のいずれか一項に記載の方法。
B59.被験体が、第1、第2および第3の処置過程を投与された後に測定可能残存病変(MRD)陰性である、請求項B1からB58のいずれか一項に記載の方法。
B60.被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項B1からB59のいずれか一項に記載の方法。
B61.第1、第2および第3の処置過程を被験体に投与する前に、被験体のMRD状態が検出される、請求項B60に記載の方法。
B62.第1、第2および第3の処置過程を被験体に投与した後に、被験体のMRD状態が検出される、請求項B60に記載の方法。
B63.第1、第2および第3の処置過程を被験体に投与する前後に、被験体のMRD状態が検出される、請求項B60からB62のいずれか一項に記載の方法。
B64.被験体が測定可能残存病変(MRD)陰性であると決定された場合、被験体への少なくとも第1および第3の処置過程の投与を終了するステップをさらに含む、請求項B1からB63のいずれか一項に記載の方法。
C1.急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で、
(i)第1の処置過程で有効量のデシタビンまたはアザシチジンを被験体に投与するステップと;
(ii)第2の処置過程で有効量のアルボシジブを被験体に投与するステップと
を含み;
被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
C2.1またはそれを超える以前の治療が、AMLを処置するための1またはそれを超える他の治療薬をさらに含む、請求項C1に記載の方法。
C3.1またはそれを超える他の治療薬が、アザシチジン(azacitibine)、デシタビン、またはこれらの組み合わせを含む、請求項C2に記載の方法。
C4.アルボシジブが式(I)の構造を有する化合物:
C5.アルボシジブが式(I-b)の構造を有する化合物:
C6.アルボシジブの有効量が、1日1回、約20mg/m2~約150mg/m2である、請求項C1からC5のいずれか一項に記載の方法。
C7.アルボシジブが、15分間~1時間の静脈内ボーラスとして被験体に投与される、請求項C6に記載の方法。
C8.アルボシジブの一部が、15分間~1時間の静脈内ボーラスとして被験体に投与され、残りのアルボシジブが、約3~約6時間の静脈内注入によって被験体に投与される、請求項C6に記載の方法。
C9.デシタビンの有効量が、1日1回、約15mg/m2~約40mg/m2である、請求項C1からC8のいずれか一項に記載の方法。
C10.デシタビンが静脈内注入によって被験体に投与される、請求項C1からC9のいずれか一項に記載の方法。
C11.アザシチジンの有効量が、1日1回、約50mg/m2~約100mg/m2である、請求項C1からC10のいずれか一項に記載の方法。
C12.アザシチジンが静脈内注射または皮下注射によって被験体に投与される、請求項C1からC11のいずれか一項に記載の方法。
C13.上記方法が、1またはそれを超える処置サイクルを含み、各治療サイクルが以下を含む、請求項C1からC12のいずれか一項に記載の方法:
(i)(a)デシタビンを、3~10日間、1日1回、約15mg/m2~約40mg/m2で、または(b)アザシチジンを、3~10日間、1日1回、約50mg/m2~約100mg/m2で、被験体に投与し;これに約1~約4日間の休薬期間が続くこと;および
(ii)アルボシジブを、1~3日間、1日1回、約20mg/m2~約100mg/m2の用量で、被験体に投与すること。
C14.各処置サイクルが28日間からなり、以下を含む、請求項C13に記載の方法:
(i)デシタビンを、1~5日目に、1日1回、約20mg/m2で被験体に投与し;これに6日目および7日目の第1の休薬期間が続くこと;および
(ii)アルボシジブを、8日目に約20mg/m2~約100mg/m2の用量で被験体に投与し;これに9~28日目の第2の休薬期間が続くこと。
C15.各処置サイクルが28日間からなり、以下を含む、請求項C13に記載の方法:
(i)アザシチジンを、1~5日目に、1日1回、約75mg/m2で被験体に投与し;これに6日目および7日目の第1の休薬期間が続くこと;および
(ii)アルボシジブを、8日目に約20mg/m2~約100mg/m2の用量で被験体に投与し;これに9~28日目の第2の休薬期間が続くこと。
C16.被験体がMCL-1依存性である、請求項C1からC15のいずれか一項に記載の方法。
C17.被験体がMCL-1依存性として特定されている、請求項C1からC16のいずれか一項に記載の方法。
C18.被験体が、被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項C17に記載の方法。
C19.式(I-b)の化合物またはその薬学的に許容され得る塩が、被験体に経口投与される、請求項C5に記載の方法。
C20.被験体が、第2の処置過程を投与される前に測定可能残存病変(MRD)陽性である、請求項C1からC19のいずれか一項に記載の方法。
C21.被験体が、第2の処置過程を投与された後に測定可能残存病変(MRD)陰性である、請求項C1からC20のいずれか一項に記載の方法。
C22.被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項C1からC21のいずれか一項に記載の方法。
C23.第2の処置過程を被験体に投与する前に、被験体のMRD状態が検出される、請求項C22に記載の方法。
C24.第2の処置過程を被験体に投与した後に、被験体のMRD状態が検出される、請求項C22に記載の方法。
C25.第2の処置過程を被験体に投与する前後に、被験体のMRD状態が検出される、請求項C22からC24のいずれか一項に記載の方法。
C26.被験体が測定可能残存病変(MRD)陰性であると決定された場合、被験体への少なくとも第2の処置過程の投与を終了するステップをさらに含む、請求項C1からC25のいずれか一項に記載の方法。
D1.血液がんを有する被験体の腫瘍崩壊症候群(TLS)の発症を阻害する方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、アルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D2.血液がんを有し、アルボシジブで処置されている被験体の腫瘍崩壊症候群(TLS)の重症度を低減する方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D3.血液がんを有し、アルボシジブで処置されている被験体の腫瘍崩壊症候群(TLS)を処置する方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D4.血液がんを有し、アルボシジブで処置されている被験体の腫瘍崩壊症候群(TLS)による死亡率を低下させる方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D5.血液がんを有し、アルボシジブで処置されている被験体の腫瘍崩壊症候群(TLS)の発生率を低下させる方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D6.血液がんを有し、アルボシジブで処置されている被験体の腫瘍崩壊症候群(TLS)を予防する方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D7.腫瘍崩壊症候群(TLS)を発症するリスクが高くない、被験体の血液がんを処置する方法であって、前記請求項のいずれか一項に示される条件に従って、ベネトクラクスの非存在下で、有効量のアルボシジブおよび、必要に応じて、シタラビンを被験体に投与するステップを含み、被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発血液がんを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
D8.血液がんが急性骨髄性白血病(AML)である、請求項D1からD7のいずれか一項に記載の方法。
D9.被験体が、TLSを発症するリスクがあると特定されている、請求項D1からD8のいずれか一項に記載の方法。
D10.1またはそれを超える以前の治療が、AMLを処置するための1またはそれを超える他の治療薬をさらに含む、請求項D1からD9のいずれか一項に記載の方法。
D11.1またはそれを超える他の治療薬が、アザシチジン、デシタビン、またはこれらの組み合わせを含む、請求項D10に記載の方法。
E1.急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で、
(i)第1の処置過程で有効量のアルボシジブを被験体に投与するステップと;
(ii)第2の処置過程でシタラビンを約500mg/m2~約3g/m2の1日量で被験体に投与するステップと;
(iii)第3の処置過程で有効量のアルボシジブを被験体に投与するステップと
を含み;
被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
E2.1またはそれを超える以前の治療が、1またはそれを超える他の治療薬をさらに含む、請求項E1に記載の方法。
E3.1またはそれを超える他の治療薬が、デシタビン、アザシチジン、またはこれらの組み合わせを含む、請求項E2に記載の方法。
E4.第2の処置過程におけるシタラビンの有効量が、1日当たり約1g/m2である、請求項E1からE3のいずれか一項に記載の方法。
E5.第2の処置過程が3~8日間からなる、請求項E1からE4のいずれか一項に記載の方法。
E6.第2の処置過程が5日間からなる、請求項E5に記載の方法。
E7.ステップ(i)およびステップ(iii)が、請求項B7からB11、B17からB22、B29からB36、およびB46からB48のいずれか一項に示されるように実施される、請求項E1からE6のいずれか一項に記載の方法。
E8.被験体がMCL-1依存性である、請求項E1からE7のいずれか一項に記載の方法。
E9.被験体がMCL-1依存性として特定されている、請求項E1からE8のいずれか一項に記載の方法。
E10.被験体が、被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項E9に記載の方法。
E11.被験体が、第1、第2および第3の処置過程を投与される前に測定可能残存病変(MRD)陽性である、請求項E1からE10のいずれか一項に記載の方法。
E12.被験体が、第1、第2および第3の処置過程を投与された後に測定可能残存病変(MRD)陰性である、請求項E1から11のいずれか一項に記載の方法。
E13.被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項E1からE12のいずれか一項に記載の方法。
E14.第1、第2および第3の処置過程を被験体に投与する前に、被験体のMRD状態が検出される、請求項E13に記載の方法。
E15.第1、第2および第3の処置過程を被験体に投与した後に、被験体のMRD状態が検出される、請求項E13に記載の方法。
E16.第1、第2および第3の処置過程を被験体に投与する前後に、被験体のMRD状態が検出される、請求項E13からE15のいずれか一項に記載の方法。
E17.被験体が測定可能残存病変(MRD)陰性であると決定された場合、被験体への少なくとも第1および第3の処置過程の投与を終了するステップをさらに含む、請求項E1からE16のいずれか一項に記載の方法。
F1.急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスおよびミトキサントロンの非存在下で、
(i)第1の処置過程で有効量のアルボシジブを被験体に投与するステップと;
(ii)第2の処置過程で有効量のシタラビンを被験体に投与するステップと
を含み
被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、この以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
F2.1またはそれを超える以前の治療が、AMLを処置するための1またはそれを超える他の治療薬をさらに含む、請求項F1に記載の方法。
F3.1またはそれを超える他の治療薬が、アザシチジン、デシタビン、またはこれらの組み合わせを含む、請求項F2に記載の方法。
F4.ステップ(i)がステップ(ii)の後に実施される、請求項F1からF3のいずれか一項に記載の方法。
F5.第2の処置過程におけるシタラビンの有効量が、1日当たり約10mg/m2~約100mg/m2である、請求項F1からF4のいずれか一項に記載の方法。
F6.第2の処置過程におけるシタラビンの有効量が、1日当たり約20mg/m2である、請求項F5に記載の方法。
F7.第2の処置過程が8~12日間からなる、請求項F1からF6のいずれか一項に記載の方法。
F8.ステップ(i)が、アルボシジブを、約1~4日間、1日当たり約25mg/m2~約100mg/m2の用量で被験体に投与することを含む、請求項F1からF7のいずれか一項に記載の方法。
F9.アルボシジブが、3日間、1日1回、約30分間の静脈内ボーラスとして1日当たり50mg/m2の用量で被験体に投与される、請求項F8に記載の方法。
F10.ステップ(i)がステップ(ii)の前に実施される、請求項F1からF3のいずれか一項に記載の方法。
F11.ステップ(i)が、アルボシジブを、約80mg/m2~約120mg/m2の1日量で被験体に投与することを含む、請求項F10に記載の方法。
F12.ステップ(i)で、アルボシジブが、1日1回、3連続日間被験体に投与され、これに2日間の休薬期間が続く、請求項F11に記載の方法。
F13.ステップ(ii)が、シタラビンを、約72時間の静脈内注射によって、約1g/m2~約3g/m2の用量で被験体に投与することを含む、請求項F10からF12のいずれか一項に記載の方法。
F14.被験体がMCL-1依存性である、請求項F1からF13のいずれか一項に記載の方法。
F15.被験体がMCL-1依存性として特定されている、請求項F1からF14のいずれか一項に記載の方法。
F16.被験体が、被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項F15に記載の方法。
F17.被験体が、第1および第2の処置過程を投与される前に測定可能残存病変(MRD)陽性である、請求項F1からF16のいずれか一項に記載の方法。
F18.被験体が、第1および第2の処置過程を投与された後に測定可能残存病変(MRD)陰性である、請求項F1からF17のいずれか一項に記載の方法。
F19.被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項F1からF18のいずれか一項に記載の方法。
F20.第1および第2の処置過程を被験体に投与する前に、被験体のMRD状態が検出される、請求項F19に記載の方法。
F21.第1および第2の処置過程を被験体に投与した後に、被験体のMRD状態が検出される、請求項F19に記載の方法。
F22.第1および第2の処置過程を被験体に投与する前後に、被験体のMRD状態が検出される、請求項F18からF20のいずれか一項に記載の方法。
F23.被験体が測定可能残存病変(MRD)陰性であると決定された場合、被験体への少なくとも第1の処置過程の投与を終了するステップをさらに含む、請求項F1からF22のいずれか一項に記載の方法。
実施例1.アルボシジブ単剤療法
実施例2.低用量シタラビンと組み合わせたアルボシジブ
a.75歳以上
b.集中導入化学療法の使用を妨げる以下の併存症のうちの少なくとも1つを有する18歳以上~65歳:
i.2または3の米国東海岸がん臨床試験グループ(ECOG)のパフォーマンスステータス;
ii.処置を必要とするうっ血性心不全(CHF)または駆出率50%以下または慢性安定狭心症の心臓病歴;
iii.65%以下の一酸化炭素肺拡散能(DLCO)または65%以下の1秒間での努力呼気量(FEV1);
iv.30mL/分以上~45ml/分未満のクレアチニンクリアランス;
v.1.5超~3.0以下×基準値上限(ULN)の総ビリルビンを伴う中等度の肝障害;
vi.医師が集中化学療法に適合しないと判断するその他のあらゆる併存症は、スクリーニング中および試験登録前に、治療医長によって審査および承認されなければならない。
1.18歳以上である
2.組織学またはフローサイトメトリーに基づいて、骨髄が5%を超える芽球を伴う急性前骨髄球性白血病(APL-M3)を除く、世界保健機関(WHO)の基準によって確立された病理学的に確認されたAMLの診断がある
3.アザシチジンまたはデシタビンと組み合わせた以前のベネトクラクスで進行を示した
4.2以下の米国東海岸がん臨床試験グループ(ECOG)のパフォーマンスステータス(PS)を有する
5.1.8mg/dL以下の血清クレアチニンレベルを有する
6.基準値上限(ULN)の5倍以下のアラニンアミノトランスフェラーゼ(ALT)/アスパラギン酸アミノトランスフェラーゼ(AST)レベルを有する
7.2.0mg/dL以下の総ビリルビンレベルを有する(ジルベール症候群、溶血、または白血病に続発する場合を除く)
8.心エコー検査(ECHO)またはマルチゲート収集法(MUGA)スキャンで45%を超える左心室駆出率(LVEF)を有する
9.不妊であるか、適切な避妊方法を使用することに同意する。性的に活発な患者とそのパートナーは、試験治療中およびその終了後6か月間、失敗率が低い有効な避妊方法を使用しなければならない
1.アルボシジブまたはいずれかの他のCDK阻害剤による以前の何らかの処置を受けた
2.化学療法、放射線療法、または免疫療法の併用が必要である
ヒドロキシウレアは、いずれかのアームの開始処置の開始前の夕方まで(ただし12時間以内ではない)許可される。
3.30,000/mm3を超える末梢芽球数を有する(上記の5番のようにヒドロキシウレアを使用する場合がある)
4.過去3週間以内に抗白血病治療を受けた(ヒドロキシウレアを除く、または患者が明確な難治性疾患を患っている場合を除く)。過去3週間以内に治療を受けた難治性患者は、メディカルモニターの事前承認が望ましい場合がある
5.急性前骨髄球性白血病(APL、M3)と診断された
6.活動性の中枢神経系(CNS)白血病を患っている
7.制御されていない播種性血管内凝固の証拠がある
8.活動的で制御されていない感染症を有する
9.他の生命を脅かす病気を有する
10.非黒色腫皮膚がんまたは子宮頸部上皮内新生物を除いて、過去6か月以内に、他の活動性悪性腫瘍を有しているか、または他の悪性腫瘍と診断されている
11.書面によるインフォームドコンセントを与える能力または試験プロトコルを遵守する能力を損なう可能性のある精神障害および/または精神病歴がある
12.妊娠中および/または授乳中である
13.最初の試験薬物投与前14日以内に何らかの生ワクチンを接種した
実施例3.低メチル化剤(HMA)と組み合わせたアルボシジブ
実施例4.ベネトクラクス併用療法による処置後の再発/難治性急性骨髄性白血病患者におけるアルボシジブの第2相試験
1.18歳以上である。
2.組織学またはフローサイトメトリーに基づいて、骨髄が5%を超える芽球を伴う急性前骨髄球性白血病(APL-M3)を除く、世界保健機関(WHO)の基準によって確立された病理学的に確認されたAMLの診断がある。
3.アザシチジンまたはデシタビンと組み合わせたベネトクラクスによる初期導入療法を受けており、難治性であった(CR/CRiを達成できなかった、もしくは90日未満の持続期間のCR/CRiを達成した)または再発した(90日以上の持続時間のCR/CRi後の疾患の再発)。
4.2以下の米国東海岸がん臨床試験グループ(ECOG)のパフォーマンスステータス(PS)を有する。
5.コッククロフト・ゴールトの式を使用して、30mL/分以上の糸球体濾過量(GFR)を有する。
6.基準値上限(ULN)の5倍以下のアラニンアミノトランスフェラーゼ(ALT)/アスパラギン酸アミノトランスフェラーゼ(AST)レベルを有する。
7.2.0mg/dL以下の総ビリルビンレベルを有する(ジルベール症候群、溶血、または白血病に続発する場合を除く)。
8.不妊であるか、適切な避妊方法を使用することに同意する:性的に活発な患者とそのパートナーは、試験登録前、試験参加期間中ならびに試験薬物の最後の投与後少なくとも3か月間(男性)および6か月間(女性)、失敗率が低い有効な避妊方法を使用しなければならない。
9.試験全体の要件を遵守することができる。
10.試験に関連する任意の手順の前に書面によるインフォームドコンセントを提出する:患者が試験参加のために再スクリーニングされた場合、またはプロトコルの修正により進行中の患者のケアが変更された場合、新たなインフォームドコンセントフォームに署名しなければならない。
1.アルボシジブもしくは別のCDK阻害剤による以前の処置を受けた、またはアザシチジンもしくはデシタビンと組み合わせた第一選択ベネトクラクス(venteoclax)以外の以前の抗白血病治療を受けた。
2.化学療法、放射線療法、または免疫療法の併用が必要である。ヒドロキシウレアは、いずれかのアームの開始処置の開始前の夕方まで(ただし12時間以内ではない)許可される。
3.試験処置開始の60日以内に同種幹細胞移植を受けた。同種幹細胞移植を受けた患者は、試験処置の時点で全ての免疫抑制剤をやめていなければならない。
4.移植片対宿主病の全身治療を受けている、または受けていた。
5.30,000/mm3を超える末梢芽球数を有する(上記の2番のようにヒドロキシウレアを使用する場合がある)
6.過去3週間以内に抗白血病治療を受けた(ヒドロキシウレアを除く、また患者が明確な難治性疾患を患っている場合を除く)。過去3週間以内に治療を受けた難治性患者は、メディカルモニターの事前承認が望ましい場合がある。
7.急性前骨髄球性白血病(APL-M3)と診断された。
8.活動性の中枢神経系(CNS)白血病を患っている。
9.制御されていない播種性血管内凝固の証拠がある。
10.活動的で制御されていない感染症を有する。
11.他の生命を脅かす病気を有する。
12.非黒色腫皮膚がんまたは子宮頸部上皮内新生物を除いて、過去6か月以内に、処置を要する他の活動性悪性腫瘍を有しているか、または他の悪性腫瘍と診断されている。
13.書面によるインフォームドコンセントを与える能力または試験プロトコルを遵守する能力を損なう可能性のある精神障害および/または精神病歴がある。
14.妊娠中および/または授乳中である。
15.最初の試験薬物投与前14日以内に生ワクチンを接種した。
b 30~60分間にわたってIVボーラスとして投与されるべきアルボシジブ
他の実施形態
Claims (96)
- 急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で有効量のアルボシジブを前記被験体に投与するステップを含み、前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスおよび低メチル化剤を含む、方法。
- 前記低メチル化剤が、アザシチジン、デシタビン、またはアザシチジンおよびデシタビンである、請求項1に記載の方法。
- ベネトクラクスおよび低メチル化剤を含む、前記1またはそれを超える以前の治療が、導入療法である、請求項1または2に記載の方法。
- 前記被験体が難治性AMLを有する、請求項1から5のいずれか一項に記載の方法。
- 前記被験体が耐性AMLを有する、請求項1から6のいずれか一項に記載の方法。
- 前記被験体が再発AMLを有する、請求項1から7のいずれか一項に記載の方法。
- 前記被験体が、約90日間~約18か月間の第1の完全寛解(CR1)期間後に再発AMLを有する、請求項8に記載の方法。
- AMLのための追加の化学療法剤の非存在下で、有効量のアルボシジブを前記被験体に投与するステップを含む、請求項1から9のいずれか一項に記載の方法。
- 有効量のシタラビンを前記被験体に投与するステップをさらに含む、請求項1から9のいずれか一項に記載の方法。
- AMLのための追加の化学療法剤の非存在下で、有効量のアルボシジブおよび有効量のシタラビンを前記被験体に投与するステップを含む、請求項11に記載の方法。
- 前記有効量が、1週間に1回、約20mg/m2~約100mg/m2のアルボシジブである、請求項1から12のいずれか一項に記載の方法。
- 前記有効量が、1週間に1回、約25mg/m2または約50mg/m2のアルボシジブである、請求項1から13のいずれか一項に記載の方法。
- 前記アルボシジブが、1週間に1回、約15分間~約1時間の静脈内ボーラスとして、約20mg/m2~約100mg/m2の用量で前記被験体に投与される、請求項1から13のいずれか一項に記載の方法。
- 前記アルボシジブが、1週間に1回、約30分間~約1時間の静脈内ボーラスとして、約25mg/m2~約50mg/m2の用量で前記被験体に投与される、請求項1から13および15のいずれか一項に記載の方法。
- 前記アルボシジブが、1週間に1回、約25mg/m2または約50mg/m2の用量で前記被験体に投与される、請求項1から13、15および16のいずれか一項に記載の方法。
- 前記アルボシジブが、処置サイクルとして、1週間に1回、3週間連続して前記被験体に投与され、これに1週間の休薬期間が続く、請求項1から10および13から17のいずれか一項に記載の方法。
- 前記方法が、1~8回の前記アルボシジブ処置サイクルを含む、請求項1から18のいずれか一項に記載の方法。
- 前記方法が、前記処置が前記被験体に実質的に利益を示さなくなるまで、複数の前記アルボシジブ処置サイクルを含む、請求項1から19のいずれか一項に記載の方法。
- 各処置サイクルが4週間からなり、(i)前記アルボシジブを、前記処置サイクルの第1週の初日に約30分間~約1時間の静脈内ボーラスとして、約25mg/m2の用量で前記被験体に投与すること、(ii)前記アルボシジブを、前記処置サイクルの第2週の初日および第3週の初日に約30分間~約1時間の静脈内ボーラスとして、約50mg/m2の用量で前記被験体に投与すること、ならびに(iii)前記処置サイクルの第4週の間の約1週間の休薬期間を含む、請求項18から20のいずれか一項に記載の方法。
- 前記有効量が、1週間に1回、約20mg/m2~約100mg/m2のアルボシジブ、および1日当たり約10mg/m2~約100mg/m2のシタラビンである、請求項11から17、19および20のいずれか一項に記載の方法。
- 前記有効量が、1週間に1回、約25mg/m2または約50mg/m2のアルボシジブ、および1日当たり約20mg/m2のシタラビンである、請求項22に記載の方法。
- 前記シタラビンが、1日当たり約10mg/m2~約100mg/m2の用量で前記被験体に投与される、請求項11から17、19、20、22および23のいずれか一項に記載の方法。
- 前記シタラビンが、1日当たり約20mg/m2の用量で前記被験体に投与される、請求項24に記載の方法。
- 前記シタラビンが注射によって投与される、請求項11から17、19、20および22から25のいずれか一項に記載の方法。
- 前記シタラビンが皮下注射によって投与される、請求項26に記載の方法。
- 各処置サイクルが4週間からなり、(i)前記アルボシジブを、前記処置サイクルの第1週の初日に約30分間~約1時間の静脈内ボーラスとして、約25mg/m2の用量で前記被験体に投与すること、(ii)前記シタラビンを、前記処置サイクルの第1週の3日目に始まる10日間、約20mg/m2の1日量で、皮下注射によって前記被験体に投与すること、(iii)前記アルボシジブを、第3週の初日に約30分間~約1時間の静脈内ボーラスとして、約50mg/m2の用量で前記被験体に投与すること、および(iv)前記処置サイクルの第4週の間の約1週間の休薬期間を含む、請求項11から17、19、20および22から27のいずれか一項に記載の方法。
- 急性骨髄性白血病(AML)の処置を必要とする被験体の急性骨髄性白血病(AML)を処置する方法であって、ベネトクラクスの非存在下で、
(i)第1の処置過程で有効量のアルボシジブを前記被験体に投与するステップと;
(ii)第2の処置過程で有効量のシタラビンを前記被験体に投与するステップと;
(iii)第3の処置過程で有効量のアルボシジブを前記被験体に投与するステップと
を含み;
前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスおよび低メチル化剤を含む、方法。 - ベネトクラクスおよび低メチル化剤を含む、前記1またはそれを超える以前の治療が、導入療法である、請求項29に記載の方法。
- 前記低メチル化剤が、アザシチジン、デシタビン、またはアザシチジンおよびデシタビンである、請求項30に記載の方法。
- ステップ(ii)がステップ(i)の後に実施され、ステップ(iii)がステップ(ii)の後に実施される、請求項29から33のいずれか一項に記載の方法。
- 前記第1の処置過程におけるアルボシジブの前記有効量が、前記第3の処置過程におけるアルボシジブの前記有効量とは異なる、請求項29から34のいずれか一項に記載の方法。
- 前記第1の処置過程におけるアルボシジブの前記有効量が、1日当たり約10mg/m2~約50mg/m2である、請求項29から35のいずれか一項に記載の方法。
- 前記第1の処置過程におけるアルボシジブの前記有効量が1日当たり約25mg/m2である、請求項36に記載の方法。
- 前記第1の処置過程が約1~約4日間からなる、請求項29から37のいずれか一項に記載の方法。
- 前記第1の処置過程が1日間または2日間からなる、請求項38に記載の方法。
- 前記第2の処置過程におけるシタラビンの前記有効量が、1日当たり約10mg/m2~約100mg/m2である、請求項29から39のいずれか一項に記載の方法。
- 前記第2の処置過程におけるシタラビンの前記有効量が、1日当たり約20mg/m2である、請求項40に記載の方法。
- 前記第2の処置過程が8~12日間からなる、請求項29から41のいずれか一項に記載の方法。
- 前記第2の処置過程が10日間からなる、請求項42に記載の方法。
- 前記第3の処置過程におけるアルボシジブの前記有効量が、1日当たり約25mg/m2~約100mg/m2である、請求項29から43のいずれか一項に記載の方法。
- 前記第3の処置過程におけるアルボシジブの前記有効量が1日当たり約50mg/m2である、請求項44に記載の方法。
- 前記第3の処置過程が1~3日間からなる、請求項29から45のいずれか一項に記載の方法。
- 前記第3の処置過程が1日間または2日間からなる、請求項46に記載の方法。
- 前記第1の処置過程が1日間からなり、これに、前記第2の処置過程の開始前の1日間の第1の休薬期間が続く、請求項29から47のいずれか一項に記載の方法。
- 前記第2の処置過程が10日間からなり、これに、前記第3の処置過程の開始前の2日間の第2の休薬期間が続く、請求項29から48のいずれか一項に記載の方法。
- 前記第3の処置過程が1日間からなり、これに、約13日間の第3の休薬期間が続く、請求項29から49のいずれか一項に記載の方法。
- 前記方法が、複数の処置サイクルを含み;各処置サイクルが前記第1の処置過程、前記第2の処置過程、および前記第3の処置過程を含み、各処置サイクルが28日毎に繰り返される、請求項29から50のいずれか一項に記載の方法。
- 各処置サイクルが、
(i)前記アルボシジブを、約1~約3日間、約15分間~約1時間の静脈内ボーラスとして、約10mg/m2~約50mg/m2の1日量で前記被験体に投与し、これに約1~約3日間の第1の休薬期間が続くこと;
(ii)前記シタラビンを、8~12日間、約15mg/m2~約40mg/m2の1日量で皮下注射によって前記被験体に投与し、これに1~3日間の第2の休薬期間が続くこと、および
(iii)前記アルボシジブを、約1~約3日間、約15分間~約1時間の静脈内ボーラスとして、約25mg/m2~約100mg/m2の1日量で前記被験体に投与し、これに約12~約14日間の第3の休薬期間が続くこと
を含む、請求項51に記載の方法。 - 各処置サイクルが、
(i)前記アルボシジブを、1日間、約30分間~約1時間の静脈内ボーラスとして、約25mg/m2の1日量で前記被験体に投与し、これに1日間の第1の休薬期間が続くこと;
(ii)前記シタラビンを、10日間、約20mg/m2の1日量で皮下注射によって前記被験体に投与し、これに2日間の第2の休薬期間が続くこと;および
(iii)前記アルボシジブを、1日間、約30分間~約1時間の静脈内ボーラスとして、約50mg/m2の1日量で前記被験体に投与し、これに約13日間の第3の休薬期間が続くこと
を含む、請求項51または52に記載の方法。 - 各処置サイクルが、
(i)前記アルボシジブを、前記処置サイクルの1日目に、約30分間~約1時間の静脈内ボーラスとして、約25mg/m2の1日量で前記被験体に投与し、これに前記処置サイクルの2日目の第1の休薬期間が続くこと;
(ii)前記シタラビンを、前記処置サイクルの3~12日目に、約20mg/m2の1日量で皮下注射によって前記被験体に投与し、これに前記処置サイクルの13~14日目の第2の休薬期間が続くこと;および
(iii)前記アルボシジブを、前記処置サイクルの15日目に、約30分間~約1時間の静脈内ボーラスとして、約50mg/m2の1日量で前記被験体に投与し、これに前記処置サイクルの16~28日目の第3の休薬期間が続くこと
を含む、請求項51から53のいずれか一項に記載の方法。 - 前記第1の処置過程、前記第3の処置過程、またはその両方における前記アルボシジブが、15分間~1時間の静脈内ボーラスとして投与される、請求項29から52のいずれか一項に記載の方法。
- 前記第1の処置過程、前記第3の処置過程、またはその両方における前記アルボシジブが、30分間~1時間の静脈内ボーラスとして投与される、請求項29から55のいずれか一項に記載の方法。
- 前記第2の処置過程における前記シタラビンが注射によって投与される、請求項29から51のいずれか一項に記載の方法。
- 前記第2の処置過程における前記シタラビンが皮下注射によって投与される、請求項57に記載の方法。
- 前記被験体がMCL-1依存性である、請求項1から58のいずれか一項に記載の方法。
- 前記被験体がMCL-1依存性として特定されている、請求項1から59のいずれか一項に記載の方法。
- 前記被験体が、前記被験体の骨髄試料を検査することによって、MCL-1依存性として特定されている、請求項60に記載の方法。
- 前記被験体が、前記アルボシジブを投与される前に測定可能残存病変(MRD)陽性である、請求項1から61のいずれか一項に記載の方法。
- 前記被験体が、前記アルボシジブを投与された後に測定可能残存病変(MRD)陰性である、請求項1から62のいずれか一項に記載の方法。
- 前記被験体の測定可能残存病変(MRD)状態を検出するステップをさらに含む、請求項1から63のいずれか一項に記載の方法。
- 前記アルボシジブを前記被験体に投与する前に、前記被験体のMRD状態が検出される、請求項64に記載の方法。
- 前記アルボシジブを前記被験体に投与した後に、前記被験体のMRD状態が検出される、請求項64に記載の方法。
- 前記アルボシジブを前記被験体に投与する前後に、前記被験体のMRD状態が検出される、請求項64から66のいずれか一項に記載の方法。
- 前記被験体が測定可能残存病変(MRD)陰性であると決定された場合、前記被験体への前記アルボシジブの投与を終了するステップをさらに含む、請求項1から67のいずれか一項に記載の方法。
- 難治性、耐性または再発急性骨髄性白血病(AML)の処置を必要とする被験体の難治性、耐性または再発急性骨髄性白血病(AML)を処置する方法であって、AMLのための追加の化学療法剤の非存在下で、有効量のアルボシジブを前記被験体に投与するステップを含み、前記被験体が、ベネトクラクスおよび低メチル化剤を含む導入療法後に、難治性、耐性または再発AMLを有する、方法。
- 約15mg/m2~約40mg/m2の前記アルボシジブが、28日の処置サイクルの1日目に、静脈内ボーラスによって投与され;
約40mg/m2~約80mg/m2の前記アルボシジブが、前記28日の処置サイクルの8日目および15日目に、静脈内ボーラスによって投与される、
請求項69または70に記載の方法。 - 難治性、耐性または再発急性骨髄性白血病(AML)の処置を必要とする被験体の難治性、耐性または再発急性骨髄性白血病(AML)を処置する方法であって、AMLのための追加の化学療法剤の非存在下で、
約15mg/m2~約40mg/m2の式(I)の構造を有する化合物:
約40mg/m2~約80mg/m2の式(I)の構造を有する前記化合物、またはその薬学的に許容され得る塩を、前記28日の処置サイクルの8日目および15日目に静脈内ボーラスによって
前記被験体に投与するステップを含み、
前記被験体が、ベネトクラクスおよびアザシチジン、またはベネトクラクスおよびデシタビンを含む導入療法後に、難治性、耐性または再発AMLを有する、方法。 - 約25mg/m2の前記アルボシジブが、28日の処置サイクルの1日目に、静脈内ボーラスによって投与され;
約50mg/m2の前記アルボシジブが、前記28日の処置サイクルの8日目および15日目に、静脈内ボーラスによって投与される、
請求項71または72に記載の方法。 - 前記静脈内ボーラスが約30分間~約60分間にわたって投与される、請求項69から72のいずれか一項に記載の方法。
- 難治性、耐性または再発急性骨髄性白血病(AML)の処置を必要とする被験体の難治性、耐性または再発急性骨髄性白血病(AML)を処置する方法であって、AMLのための追加の化学療法剤の非存在下で、有効量のアルボシジブおよび低用量シタラビンを前記被験体に投与するステップを含み、前記被験体が、ベネトクラクスおよび低メチル化剤を含む導入療法後に、難治性、耐性または再発AMLを有する、方法。
- 約15mg/m2~約40mg/m2の前記アルボシジブが、28日の処置サイクルの1日目に、静脈内ボーラスによって投与され;
約40mg/m2~約80mg/m2の前記アルボシジブが、前記28日の処置サイクルの15日目に、静脈内ボーラスによって投与される、
請求項75または76に記載の方法。 - 1日当たり約10mg/m2~約100mg/m2のシタラビンが、前記28日の処置サイクルの3、4、5、6、7、8、9、10、11および12日目に注射によって投与される、
請求項77に記載の方法。 - 難治性、耐性または再発急性骨髄性白血病(AML)の処置を必要とする被験体の難治性、耐性または再発急性骨髄性白血病(AML)を処置する方法であって、AMLのための追加の化学療法剤の非存在下で、
約15mg/m2~約40mg/m2の式(I)の構造を有する化合物:
1日当たり約10mg/m2~約100mg/m2のシタラビンを、前記28日の処置サイクルの3、4、5、6、7、8、9、10、11および12日目に注射によって;および
約40mg/m2~約80mg/m2の式(I)の構造を有する前記化合物、またはその薬学的に許容され得る塩を、前記28日の処置サイクルの8日目および15日目に静脈内ボーラスによって
前記被験体に投与するステップを含み、
前記被験体が、ベネトクラクスおよびアザシチジン、またはベネトクラクスおよびデシタビンを含む導入療法後に、難治性、耐性または再発AMLを有する、方法。 - 約25mg/m2の前記アルボシジブが、28日の処置サイクルの1日目に、静脈内ボーラスによって投与され;
約50mg/m2の前記アルボシジブが、前記28日の処置サイクルの15日目に、静脈内ボーラスによって投与される、
請求項77から79のいずれか一項に記載の方法。 - 前記静脈内ボーラスが約30分間~約60分間にわたって投与される、請求項77から80のいずれか一項に記載の方法。
- 1日当たり約20mg/m2のシタラビンが、前記28日の処置サイクルの3、4、5、6、7、8、9、10、11および12日目に注射によって投与される、
請求項78から81のいずれか一項に記載の方法。 - 前記シタラビンが皮下注射によって投与される、請求項75から82のいずれか一項に記載の方法。
- 前記被験体がヒトである、請求項1から83のいずれか一項に記載の方法。
- 前記低メチル化剤がアザシチジンまたはデシタビンである、請求項69から71、73から78および80から84のいずれか一項に記載の方法。
- 被験体の腫瘍崩壊症候群(TLS)の発症を阻害する方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 被験体の腫瘍崩壊症候群(TLS)の重症度を低減する方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 被験体の腫瘍崩壊症候群(TLS)による死亡率を低下させる方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、各被験体が独立に、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 被験体の腫瘍崩壊症候群(TLS)の発生率を低下させる方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、各被験体が独立に、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 被験体の腫瘍崩壊症候群(TLS)を予防する方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 腫瘍崩壊症候群(TLS)を発症するリスクが高くない、被験体のAMLを処置する方法であって、ベネトクラクスの非存在下で、アルボシジブを、約15mg/m2~約40mg/m2の第1の用量で前記被験体に投与するステップを含み、前記被験体が、1またはそれを超える以前の治療後に難治性、耐性または再発AMLを有し、前記以前の治療のうちの少なくとも1つがベネトクラクスを含む、方法。
- 前記1またはそれを超える以前の治療のうちの少なくとも1つがベネトクラクスおよび低メチル化剤を含む、請求項86から91のいずれか一項に記載の方法。
- 前記低メチル化剤が、アザシチジン、デシタビン、またはアザシチジンおよびデシタビンである、請求項92に記載の方法。
- アルボシジブの前記第1の用量が約25mg/m2である、請求項86から93のいずれか一項に記載の方法。
- ベネトクラクスの非存在下で、アルボシジブを、約40mg/m2~約100mg/m2の第2の用量で前記被験体に投与するステップをさらに含む、請求項86から94のいずれか一項に記載の方法。
- アルボシジブの前記第2の用量が約50mg/m2である、請求項95に記載の方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962821342P | 2019-03-20 | 2019-03-20 | |
| US62/821,342 | 2019-03-20 | ||
| US201962871934P | 2019-07-09 | 2019-07-09 | |
| US62/871,934 | 2019-07-09 | ||
| PCT/US2020/023939 WO2020191326A1 (en) | 2019-03-20 | 2020-03-20 | Treatment of acute myeloid leukemia (aml) with venetoclax failure |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022525149A true JP2022525149A (ja) | 2022-05-11 |
| JPWO2020191326A5 JPWO2020191326A5 (ja) | 2023-03-23 |
Family
ID=72519370
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021555227A Pending JP2022525149A (ja) | 2019-03-20 | 2020-03-20 | ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US11793802B2 (ja) |
| JP (1) | JP2022525149A (ja) |
| WO (1) | WO2020191326A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4086264B1 (en) | 2015-05-18 | 2023-10-25 | Sumitomo Pharma Oncology, Inc. | Alvocidib prodrugs having increased bioavailability |
| WO2017087885A1 (en) | 2015-11-19 | 2017-05-26 | Dana-Farber Cancer Institute, Inc. | Methods of identifying compounds that interfere with erg-driven misguidance of baf complexes in tmprss2-erg driven prostate cancers |
| US11279694B2 (en) | 2016-11-18 | 2022-03-22 | Sumitomo Dainippon Pharma Oncology, Inc. | Alvocidib prodrugs and their use as protein kinase inhibitors |
| JP7196160B2 (ja) | 2017-09-12 | 2022-12-26 | スミトモ ファーマ オンコロジー, インコーポレイテッド | Mcl-1阻害剤アルボシジブを用いた、bcl-2阻害剤に対して非感受性である癌の治療レジメン |
| CN112153984A (zh) | 2018-01-30 | 2020-12-29 | 福宏治疗公司 | 化合物及其用途 |
| AU2019391097B2 (en) | 2018-12-04 | 2025-07-03 | Sumitomo Pharma America, Inc. | CDK9 inhibitors and polymorphs thereof for use as agents for treatment of cancer |
| US12509453B2 (en) | 2019-01-29 | 2025-12-30 | Foghorn Therapeutics Inc. | BRM/BRG1 inhibitors and uses thereof |
| JP2022525149A (ja) | 2019-03-20 | 2022-05-11 | スミトモ ダイニッポン ファーマ オンコロジー, インコーポレイテッド | ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 |
| WO2021007316A1 (en) * | 2019-07-08 | 2021-01-14 | Sumitomo Dainippon Pharma Oncology, Inc. | Treatment of cancer |
| JP7561195B2 (ja) | 2020-01-29 | 2024-10-03 | フォグホーン セラピューティクス インコーポレイテッド | 化合物及びその使用 |
| US12383555B2 (en) | 2020-05-20 | 2025-08-12 | Foghorn Therapeutics Inc. | Methods of treating cancers |
| WO2024216151A1 (en) * | 2023-04-13 | 2024-10-17 | Foghorn Therapeutics Inc. | Combination therapy for treating hematological cancers |
| WO2024216136A1 (en) * | 2023-04-13 | 2024-10-17 | Foghorn Therapeutics Inc. | Combination therapy for the treatment of hematological cancers |
| WO2025014784A1 (en) * | 2023-07-07 | 2025-01-16 | Rigel Pharmaceuticals, Inc. | Treatment of acute myeloid leukemia with olutasidenib, venetoclax and a hypomethylating agent |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018516245A (ja) * | 2015-04-20 | 2018-06-21 | トレロ ファーマシューティカルズ, インコーポレイテッド | ミトコンドリアプロファイリングによるアルボシジブ応答の予測 |
Family Cites Families (271)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4048314A (en) | 1974-12-17 | 1977-09-13 | Delmar Chemicals Limited | Morpholino containing 4-arylpiperidine derivatives |
| FR2338043A1 (fr) | 1976-01-13 | 1977-08-12 | Delmar Chem | Derives de 4-arylpiperidine et procedes de production |
| US4132710A (en) | 1976-12-20 | 1979-01-02 | Ayerst, Mckenna And Harrison, Ltd. | [2]Benzopyrano[3,4-c]pyridines and process therefor |
| US4522811A (en) | 1982-07-08 | 1985-06-11 | Syntex (U.S.A.) Inc. | Serial injection of muramyldipeptides and liposomes enhances the anti-infective activity of muramyldipeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| DE3329186A1 (de) | 1983-08-12 | 1985-02-21 | Hoechst Ag, 6230 Frankfurt | Chromonalkaloid, verfahren zu seiner isolierung aus dysoxylum binectariferum, und seine verwendung als arzneimittel |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| IN164232B (ja) | 1986-04-11 | 1989-02-04 | Hoechst India | |
| FR2601675B1 (fr) | 1986-07-17 | 1988-09-23 | Rhone Poulenc Sante | Derives du taxol, leur preparation et les compositions pharmaceutiques qui les contiennent |
| FR2601676B1 (fr) | 1986-07-17 | 1988-09-23 | Rhone Poulenc Sante | Procede de preparation du taxol et du desacetyl-10 taxol |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| JP2691986B2 (ja) | 1987-08-28 | 1997-12-17 | チッソ株式会社 | ピリジン骨格を有する光学活性化合物の製造法 |
| DE3743824C2 (de) | 1987-12-23 | 1997-03-06 | Hoechst Ag | Verfahren zur enzymatischen Racematspaltung von racemischen Alkoholen mit/in Vinylestern durch Umesterung |
| GB8823869D0 (en) | 1988-10-12 | 1988-11-16 | Medical Res Council | Production of antibodies |
| US5284856A (en) | 1988-10-28 | 1994-02-08 | Hoechst Aktiengesellschaft | Oncogene-encoded kinases inhibition using 4-H-1-benzopyran-4-one derivatives |
| DE3836676A1 (de) | 1988-10-28 | 1990-05-03 | Hoechst Ag | Die verwendung von 4h-1-benzopyran-4-on-derivaten, neue 4h-1-benzopyran-4-on-derivate und diese enthaltende arzneimittel |
| GB8827305D0 (en) | 1988-11-23 | 1988-12-29 | British Bio Technology | Compounds |
| ES2096590T3 (es) | 1989-06-29 | 1997-03-16 | Medarex Inc | Reactivos biespecificos para la terapia del sida. |
| US5747641A (en) | 1989-12-21 | 1998-05-05 | Biogen Inc | Tat-derived transport polypeptide conjugates |
| US5804604A (en) | 1989-12-21 | 1998-09-08 | Biogen, Inc. | Tat-derived transport polypeptides and fusion proteins |
| DK0463151T3 (da) | 1990-01-12 | 1996-07-01 | Cell Genesys Inc | Frembringelse af xenogene antistoffer |
| JP2938569B2 (ja) | 1990-08-29 | 1999-08-23 | ジェンファーム インターナショナル,インコーポレイティド | 異種免疫グロブリンを作る方法及びトランスジェニックマウス |
| US5661016A (en) | 1990-08-29 | 1997-08-26 | Genpharm International Inc. | Transgenic non-human animals capable of producing heterologous antibodies of various isotypes |
| US5625126A (en) | 1990-08-29 | 1997-04-29 | Genpharm International, Inc. | Transgenic non-human animals for producing heterologous antibodies |
| US5545806A (en) | 1990-08-29 | 1996-08-13 | Genpharm International, Inc. | Ransgenic non-human animals for producing heterologous antibodies |
| JPH0641075A (ja) | 1990-09-01 | 1994-02-15 | Kazuo Achinami | 新規な1,4−ジヒドロピリジン化合物及びその製造方法 |
| MX9102128A (es) | 1990-11-23 | 1992-07-08 | Rhone Poulenc Rorer Sa | Derivados de taxano,procedimiento para su preparacion y composicion farmaceutica que los contiene |
| JPH05192145A (ja) | 1991-04-02 | 1993-08-03 | Hoechst Ag | 固定化生体触媒、その製造およびカラムリアクター中でのエステル合成におけるその使用 |
| CA2102511A1 (en) | 1991-05-14 | 1992-11-15 | Paul J. Higgins | Heteroconjugate antibodies for treatment of hiv infection |
| FI941572L (fi) | 1991-10-07 | 1994-05-27 | Oncologix Inc | Anti-erbB-2-monoklonaalisten vasta-aineiden yhdistelmä ja käyttömenetelmä |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| ATE503496T1 (de) | 1992-02-06 | 2011-04-15 | Novartis Vaccines & Diagnostic | Biosynthetisches bindeprotein für tumormarker |
| EP0652950B1 (en) | 1992-07-24 | 2007-12-19 | Amgen Fremont Inc. | Generation of xenogeneic antibodies |
| ATE139900T1 (de) | 1992-11-13 | 1996-07-15 | Idec Pharma Corp | Therapeutische verwendung von chimerischen und markierten antikörper gegen menschlichen b lymphozyt beschränkter differenzierung antigen für die behandlung von b-zell-lymphoma |
| US6177401B1 (en) | 1992-11-13 | 2001-01-23 | Max-Planck-Gesellschaft Zur Forderung Der Wissenschaften | Use of organic compounds for the inhibition of Flk-1 mediated vasculogenesis and angiogenesis |
| US5455258A (en) | 1993-01-06 | 1995-10-03 | Ciba-Geigy Corporation | Arylsulfonamido-substituted hydroxamic acids |
| IL112248A0 (en) | 1994-01-25 | 1995-03-30 | Warner Lambert Co | Tricyclic heteroaromatic compounds and pharmaceutical compositions containing them |
| GB9422836D0 (en) | 1994-11-11 | 1995-01-04 | Wainscoat James | Monitoring malignant disease |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US5863949A (en) | 1995-03-08 | 1999-01-26 | Pfizer Inc | Arylsulfonylamino hydroxamic acid derivatives |
| US5861510A (en) | 1995-04-20 | 1999-01-19 | Pfizer Inc | Arylsulfonyl hydroxamic acid derivatives as MMP and TNF inhibitors |
| DE69637481T2 (de) | 1995-04-27 | 2009-04-09 | Amgen Fremont Inc. | Aus immunisierten Xenomäusen stammende menschliche Antikörper gegen IL-8 |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US5747498A (en) | 1996-05-28 | 1998-05-05 | Pfizer Inc. | Alkynyl and azido-substituted 4-anilinoquinazolines |
| US5880141A (en) | 1995-06-07 | 1999-03-09 | Sugen, Inc. | Benzylidene-Z-indoline compounds for the treatment of disease |
| JPH11510386A (ja) | 1995-07-28 | 1999-09-14 | マリー キュリー キャンサー ケア | 輸送蛋白質およびそれらの使用 |
| GB9520822D0 (en) | 1995-10-11 | 1995-12-13 | Wellcome Found | Therapeutically active compounds |
| US5733920A (en) | 1995-10-31 | 1998-03-31 | Mitotix, Inc. | Inhibitors of cyclin dependent kinases |
| GB9624482D0 (en) | 1995-12-18 | 1997-01-15 | Zeneca Phaema S A | Chemical compounds |
| DE69624081T2 (de) | 1995-12-20 | 2003-06-12 | Agouron Pharmaceuticals, Inc. | Matrix-metalloprotease Inhibitoren |
| US5663425A (en) | 1996-01-26 | 1997-09-02 | Lignotech Usa, Inc. | Production of acid soluble humates |
| AU2195297A (en) | 1996-02-20 | 1997-09-02 | Sloan-Kettering Institute For Cancer Research | Combinations of pkc inhibitors and therapeutic agents for treating cancers |
| ES2169355T3 (es) | 1996-03-05 | 2002-07-01 | Astrazeneca Ab | Derivados de 4-anilinoquinazolina. |
| US6087366A (en) | 1996-03-07 | 2000-07-11 | The Trustees Of Columbia University In The City Of New York | Use of flavopiridol or a pharmaceutically acceptable salt thereof for inhibiting cell damage or cell death |
| US5849733A (en) | 1996-05-10 | 1998-12-15 | Bristol-Myers Squibb Co. | 2-thio or 2-oxo flavopiridol analogs |
| EP0818442A3 (en) | 1996-07-12 | 1998-12-30 | Pfizer Inc. | Cyclic sulphone derivatives as inhibitors of metalloproteinases and of the production of tumour necrosis factor |
| ES2191187T3 (es) | 1996-07-13 | 2003-09-01 | Glaxo Group Ltd | Compuestos heteroaromaticos biciclicos como inhibidores de la proteina tirosin-quinasa. |
| EP0912559B1 (en) | 1996-07-13 | 2002-11-06 | Glaxo Group Limited | Fused heterocyclic compounds as protein tyrosine kinase inhibitors |
| HRP970371A2 (en) | 1996-07-13 | 1998-08-31 | Kathryn Jane Smith | Heterocyclic compounds |
| EA199900036A1 (ru) | 1996-07-18 | 1999-06-24 | Пфайзер Инк | Ингибиторы металлопротеаз матрикса на основе фосфинатов, фармацевтическая композиция, способ лечения |
| PL331895A1 (en) | 1996-08-23 | 1999-08-16 | Pfizer | Arylosulphonylamino derivatives of hydroxamic acid |
| US5965703A (en) | 1996-09-20 | 1999-10-12 | Idun Pharmaceuticals | Human bad polypeptides, encoding nucleic acids and methods of use |
| US5908934A (en) | 1996-09-26 | 1999-06-01 | Bristol-Myers Squibb Company | Process for the preparation of chiral ketone intermediates useful for the preparation of flavopiridol and analogs |
| ID18494A (id) | 1996-10-02 | 1998-04-16 | Novartis Ag | Turunan pirazola leburan dan proses pembuatannya |
| US5916771A (en) | 1996-10-11 | 1999-06-29 | Abgenix, Inc. | Production of a multimeric protein by cell fusion method |
| DK0950059T3 (da) | 1997-01-06 | 2004-11-01 | Pfizer | Cycliske sulfonderivater |
| ATE248812T1 (de) | 1997-02-03 | 2003-09-15 | Pfizer Prod Inc | Arylsulfonylhydroxamsäurederivate |
| KR20000070751A (ko) | 1997-02-05 | 2000-11-25 | 로즈 암스트롱, 크리스틴 에이. 트러트웨인 | 세포 증식 억제제로서의 피리도[2,3-d]피리미딘 및 4-아미노피리미딘 |
| JP2000507975A (ja) | 1997-02-07 | 2000-06-27 | ファイザー・インク | N−ヒドロキシ−β−スルホニルプロピオンアミド誘導体類及びそれらのマトリックスメタロプロテイナーゼ阻害薬としての使用 |
| PL334997A1 (en) | 1997-02-11 | 2000-03-27 | Pfizer | Derivatives or arylosulphonyl-hydroxamic acid |
| GB9704444D0 (en) | 1997-03-04 | 1997-04-23 | Isis Innovation | Non-invasive prenatal diagnosis |
| EP0984930B1 (en) | 1997-05-07 | 2005-04-06 | Sugen, Inc. | 2-indolinone derivatives as modulators of protein kinase activity |
| WO1998054093A1 (en) | 1997-05-30 | 1998-12-03 | Merck & Co., Inc. | Novel angiogenesis inhibitors |
| BR9811868A (pt) | 1997-08-08 | 2000-08-15 | Pfizer Prod Inc | Derivados de ácido ariloxiarilsulfonilamino hidroxâmico |
| US6294532B1 (en) | 1997-08-22 | 2001-09-25 | Zeneca Limited | Oxindolylquinazoline derivatives as angiogenesis inhibitors |
| US7064193B1 (en) | 1997-09-17 | 2006-06-20 | The Walter And Eliza Hall Institute Of Medical Research | Therapeutic molecules |
| EP1017682A4 (en) | 1997-09-26 | 2000-11-08 | Merck & Co Inc | NEW ANGIOGENESIS INHIBITORS |
| WO1999016787A1 (en) | 1997-09-26 | 1999-04-08 | Washington University | Cell death agonists |
| CN1280580A (zh) | 1997-11-11 | 2001-01-17 | 辉瑞产品公司 | 用作抗癌药的噻吩并嘧啶和噻吩并吡啶衍生物 |
| GB9725782D0 (en) | 1997-12-05 | 1998-02-04 | Pfizer Ltd | Therapeutic agents |
| GB9800575D0 (en) | 1998-01-12 | 1998-03-11 | Glaxo Group Ltd | Heterocyclic compounds |
| RS49779B (sr) | 1998-01-12 | 2008-06-05 | Glaxo Group Limited, | Biciklična heteroaromatična jedinjenja kao inhibitori protein tirozin kinaze |
| DE19802449A1 (de) | 1998-01-23 | 1999-07-29 | Hoechst Marion Roussel De Gmbh | Verfahren zur Herstellung von (-)cis-3-Hydroxy-1-methyl-4-(2,4,6-trimethoxypyhenyl)-piperidin |
| US6437136B2 (en) | 1998-01-23 | 2002-08-20 | Aventis Pharma Deutschland Gmbh | Process for the preparation of (−)cis-3-hydroxy-1-methyl-4-(2,4,6-trimethoxyphenyl)piperidine |
| GB9801690D0 (en) | 1998-01-27 | 1998-03-25 | Pfizer Ltd | Therapeutic agents |
| DE19809649A1 (de) | 1998-03-06 | 1999-09-09 | Hoechst Marion Roussel De Gmbh | Verfahren zur enzymatischen Enantiomeren-Trennung von 3(R)- und 3(S)-Hydroxy-1-methyl-4-(2,4,6-trimethoxyphenyl)-1,2,3,6-tetrahydro-pyridin bzw. der Carbonsäureester |
| PA8469401A1 (es) | 1998-04-10 | 2000-05-24 | Pfizer Prod Inc | Derivados biciclicos del acido hidroxamico |
| PA8469501A1 (es) | 1998-04-10 | 2000-09-29 | Pfizer Prod Inc | Hidroxamidas del acido (4-arilsulfonilamino)-tetrahidropiran-4-carboxilico |
| US20020029391A1 (en) | 1998-04-15 | 2002-03-07 | Claude Geoffrey Davis | Epitope-driven human antibody production and gene expression profiling |
| HUP0103617A2 (hu) | 1998-05-29 | 2002-02-28 | Sugen, Inc. | Protein kinázt gátló, pirrolilcsoporttal helyettesített 2-indolszármazékok, e vegyületeket tartalmazó gyógyászati készítmények, valamint e vegyületek alkalmazása |
| UA60365C2 (uk) | 1998-06-04 | 2003-10-15 | Пфайзер Продактс Інк. | Похідні ізотіазолу, спосіб їх одержання, фармацевтична композиція та спосіб лікування гіперпроліферативного захворювання у ссавця |
| FR2780056B1 (fr) | 1998-06-18 | 2000-08-04 | Hoechst Marion Roussel Inc | Nouveau procede de preparation de derives de la 4-phenyl-1-2 3,6-tetrahydropyridine et les produits imtermediaires mis en oeuvre |
| PT1100589E (pt) | 1998-07-30 | 2005-05-31 | Sigma Tau Ind Farmaceuti | Utilizacao de propionil-l-carnitina e acetil-l-carnitina na preparacao de medicamentos com actividade anticancerigena |
| US6268499B1 (en) | 1998-08-10 | 2001-07-31 | Hoffman-La Roche Inc. | Process and intermediates for preparation of substituted piperidine-epoxides |
| AU1029500A (en) | 1998-08-29 | 2000-03-21 | Miklos Ghyczy | Pharmaceutical and/or diet product |
| ES2213985T3 (es) | 1998-11-05 | 2004-09-01 | Pfizer Products Inc. | Derivados de hidroxiamida de acido 5-oxo-pirrolidin-2-carboxilico. |
| UA71945C2 (en) | 1999-01-27 | 2005-01-17 | Pfizer Prod Inc | Substituted bicyclic derivatives being used as anticancer agents |
| US6399633B1 (en) | 1999-02-01 | 2002-06-04 | Aventis Pharmaceuticals Inc. | Use of 4-H-1-benzopryan-4-one derivatives as inhibitors of smooth muscle cell proliferation |
| IL129299A0 (en) | 1999-03-31 | 2000-02-17 | Mor Research Applic Ltd | Monoclonal antibodies antigens and diagnosis of malignant diseases |
| WO2000059526A1 (en) | 1999-04-07 | 2000-10-12 | Thomas Jefferson University | Enhancement of peptide cellular uptake |
| US6511993B1 (en) | 1999-06-03 | 2003-01-28 | Kevin Neil Dack | Metalloprotease inhibitors |
| WO2001012661A2 (en) | 1999-08-16 | 2001-02-22 | The Government Of The United States Of America, Asrepresented By The Secretary, Department Of Healthand Human Services, The National Institutes Of Health | RECEPTOR-MEDIATED UPTAKE OF AN EXTRACELLULAR BCL-xL FUSION PROTEIN INHIBITS APOPTOSIS |
| CA3016482A1 (en) | 1999-11-30 | 2001-06-07 | Mayo Foundation For Medical Education And Research | B7-h1, a novel immunoregulatory molecule |
| DE19959546A1 (de) | 1999-12-09 | 2001-06-21 | Rhone Poulenc Rorer Gmbh | Pharmazeutische Zubereitung zur Behandlung von Tumorerkrankungen |
| US6576647B2 (en) | 2000-01-18 | 2003-06-10 | Aventis Pharmaceuticals Inc. | Pseudopolymorph of (—)-cis-2-(2-chlorophenyl)-5,7-dihydroxy-8[4R-(3S-hydroxy -1-methyl)piperidinyl]-4H-1-benzopyran-4-one |
| US6821990B2 (en) | 2000-01-18 | 2004-11-23 | Aventis Pharma Deutschland Gmbh | Ethanol solvate of (-)-cis-2-(2-chlorophenyl)-5, 7-dihydroxy-8 [4R-(3S-hydroxy-1-M ethyl) piperidinyl]-4H-1-benzopyran-4-one |
| PT1255752E (pt) | 2000-02-15 | 2007-10-17 | Pharmacia & Upjohn Co Llc | Inibidores de proteína quinases: 2-indolinonas substituídas com pirrolo |
| FR2805538B1 (fr) | 2000-02-29 | 2006-08-04 | Hoechst Marion Roussel Inc | Nouveaux derives de flavones, leur procede de preparation, leur application a titre de medicaments, compositions pharmaceutiques et nouvelle utilisation |
| WO2001080896A2 (en) | 2000-04-21 | 2001-11-01 | Arch Development Corporation | Flavopiridol drug combinations and methods with reduced side effects |
| WO2002020568A2 (en) | 2000-09-06 | 2002-03-14 | Abbott Laboratories | Mutant peptides derived from bad and their use to identify substances which bind to a member of the bcl-2 family of proteins |
| CA2430376A1 (en) | 2000-12-08 | 2002-06-13 | David J. Carini | Semicarbazides and their uses as cyclin dependent kinase inhibitors |
| WO2002069995A2 (en) | 2001-02-16 | 2002-09-12 | Medical College Of Georgia Research Institute, Inc. | Use of trail and antiprogestins for treating cancer |
| AU2002303164A1 (en) | 2001-03-23 | 2002-10-08 | Protarga, Inc. | Fatty amine drug conjugates |
| WO2002076404A2 (en) | 2001-03-23 | 2002-10-03 | Protarga, Inc. | Fatty alcohol drug conjugates |
| US20030073661A1 (en) | 2001-09-24 | 2003-04-17 | Shigemi Matsuyama | Method of modulating or examining Ku70 levels in cells |
| KR20030026069A (ko) | 2001-09-24 | 2003-03-31 | 주식회사 엘지생명과학 | 티엔에프계 단백질과 플라보피리돌의 조합에 의한 암세포특이적인 세포사멸 유도용 조성물 |
| AU2002361589A1 (en) | 2001-11-06 | 2003-05-19 | Enanta Pharmaceuticals, Inc. | Methods and compositions for identifying peptide aptamers capable of altering a cell phenotype |
| EP1469871A4 (en) | 2001-12-31 | 2006-08-23 | Dana Farber Cancer Inst Inc | METHOD OF TREATING APOPTOSIS AND COMPOSITIONS THEREOF |
| WO2003074566A2 (en) | 2002-03-01 | 2003-09-12 | Immunomedics, Inc. | Rs7 antibodies |
| IL149820A0 (en) | 2002-05-23 | 2002-11-10 | Curetech Ltd | Humanized immunomodulatory monoclonal antibodies for the treatment of neoplastic disease or immunodeficiency |
| US20040106647A1 (en) | 2002-06-28 | 2004-06-03 | Schneider Michael D. | Modulators of Cdk9 as a therapeutic target in cardiac hypertrophy |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| US7884127B2 (en) | 2002-07-08 | 2011-02-08 | Pirimal Life Sciences Ltd. | Inhibitors of cyclin dependent kinases and their use |
| US7915301B2 (en) | 2002-07-08 | 2011-03-29 | Piramal Life Science Limited | Inhibitors of cyclin dependent kinases and their use |
| EP1590363A4 (en) | 2002-09-09 | 2006-11-02 | Dana Farber Cancer Inst Inc | BH3-PEPTIDES AND METHOD FOR THEIR USE |
| JP4511943B2 (ja) | 2002-12-23 | 2010-07-28 | ワイス エルエルシー | Pd−1に対する抗体およびその使用 |
| US20070032417A1 (en) | 2002-12-24 | 2007-02-08 | Walter And Eliza Hall Institute Of Medical Research | Peptides and therapeutic uses thereof |
| EP1620109A2 (en) | 2003-04-25 | 2006-02-01 | Gilead Sciences, Inc. | Kinase inhibitor phosphonate conjugates |
| US7452901B2 (en) | 2003-04-25 | 2008-11-18 | Gilead Sciences, Inc. | Anti-cancer phosphonate analogs |
| GB0315259D0 (en) | 2003-06-30 | 2003-08-06 | Cyclacel Ltd | Use |
| DK1648998T3 (en) | 2003-07-18 | 2015-01-05 | Amgen Inc | Specific binding agents for hepatocyte growth factor |
| CN1302004C (zh) | 2003-08-22 | 2007-02-28 | 浙江海正药业股份有限公司 | 一种阿糖胞苷的制备方法 |
| CN107090025A (zh) | 2003-11-05 | 2017-08-25 | 达纳-法伯癌症研究所股份有限公司 | 稳定的α螺旋肽及其用途 |
| EP1793823B1 (en) | 2004-09-21 | 2012-08-08 | Vion Pharmaceuticals, Inc. | Phosphate containing prodrugs of sulfonyl hydrazines as hypoxia-selective antineoplastic agents |
| WO2006069186A2 (en) | 2004-12-22 | 2006-06-29 | The Ohio State Research Foundation | Small molecule bcl-xl/bcl-2 binding inhibitors |
| WO2006101846A1 (en) | 2005-03-16 | 2006-09-28 | Aventis Pharmaceuticals Inc. | Dosing regimen of flavopiridol for treating cancer in particular cll |
| WO2006099667A1 (en) | 2005-03-21 | 2006-09-28 | The Walter And Eliza Hall Institute Of Medical Research | Prophylactic and therapeutic agents and uses therefor |
| PL2161336T5 (pl) | 2005-05-09 | 2017-10-31 | Ono Pharmaceutical Co | Ludzkie przeciwciała monoklonalne przeciwko białku Programmed Death 1 (PD-1) oraz sposoby leczenia raka z zastosowaniem samych przeciwciał anty-PD-1 lub w połączeniu z innymi środkami immunoterapeutycznymi |
| CN104356236B (zh) | 2005-07-01 | 2020-07-03 | E.R.施贵宝&圣斯有限责任公司 | 抗程序性死亡配体1(pd-l1)的人单克隆抗体 |
| US7750000B2 (en) | 2005-09-02 | 2010-07-06 | Bayer Schering Pharma Ag | Substituted imidazo[1,2b]pyridazines as kinase inhibitors, their preparation and use as medicaments |
| EP2008106A2 (en) | 2006-03-31 | 2008-12-31 | Dana-Farber Cancer Institute | Methods of determining cellular chemosensitivity |
| EP2026805A1 (en) | 2006-05-08 | 2009-02-25 | Astex Therapeutics Limited | Pharmaceutical combinations of diazole derivatives for cancer treatment |
| WO2008021484A2 (en) | 2006-08-16 | 2008-02-21 | Eutropics Pharmaceuticals | Assay system to identify therapeutic agents |
| KR101451290B1 (ko) | 2006-10-19 | 2014-10-15 | 시그날 파마소티칼 엘엘씨 | 헤테로아릴 화합물, 이들의 조성물 그리고 단백질 키나아제 억제제로서의 이들의 용도 |
| US20080214558A1 (en) | 2007-03-01 | 2008-09-04 | Supergen, Inc. | Pyrimidine-2,4-diamine derivatives and their use as jak2 kinase inhibitors |
| GB0706633D0 (en) | 2007-04-04 | 2007-05-16 | Cyclacel Ltd | Combination |
| US9244059B2 (en) | 2007-04-30 | 2016-01-26 | Immutep Parc Club Orsay | Cytotoxic anti-LAG-3 monoclonal antibody and its use in the treatment or prevention of organ transplant rejection and autoimmune disease |
| EP1987839A1 (en) | 2007-04-30 | 2008-11-05 | I.N.S.E.R.M. Institut National de la Sante et de la Recherche Medicale | Cytotoxic anti-LAG-3 monoclonal antibody and its use in the treatment or prevention of organ transplant rejection and autoimmune disease |
| DK2154971T3 (da) | 2007-05-15 | 2012-04-02 | Piramal Life Sciences Ltd | Synergistisk farmaceutisk kombination til behandling af cancer |
| RU2438664C2 (ru) | 2007-05-15 | 2012-01-10 | Пирамал Лайф Сайнсиз Лимитед | Синергическая фармацевтическая комбинация для лечения рака |
| CA2691357C (en) | 2007-06-18 | 2014-09-23 | N.V. Organon | Antibodies to human programmed death receptor pd-1 |
| WO2009014642A1 (en) | 2007-07-19 | 2009-01-29 | Amgen Inc. | Combination of a de novo purine biosynthesis inhibitor and a cyclin dependent kinase inhibitor for the treatment of cancer |
| US8921323B2 (en) | 2007-09-26 | 2014-12-30 | Dana Farber Cancer Institute, Inc. | Methods and compositions for modulating BCL-2 family polypeptides |
| EP2044949A1 (en) | 2007-10-05 | 2009-04-08 | Immutep | Use of recombinant lag-3 or the derivatives thereof for eliciting monocyte immune response |
| AU2008335772B2 (en) | 2007-12-10 | 2014-11-27 | Sunesis Pharmaceuticals, Inc. | Methods of using (+)-1,4-dihydro-7-[(3S,4S)-3- methoxy-4-(methylamino)-1-pyrrolidinyl]-4-oxo-1- (2-thiazolyl)-1,8-naphthyridine-3-carboxylic acid for treatment of antecedent hematologic disorders |
| EP2250180A1 (en) | 2008-02-08 | 2010-11-17 | Wyeth LLC | Phosphate derivatives of substituted benzoxazoles |
| EP3284828A1 (en) | 2008-05-07 | 2018-02-21 | Eutropics Pharmaceuticals, Inc. | Antibodies specific to heterodimers of bcl-2 family and uses thereof |
| PL2307002T3 (pl) | 2008-06-09 | 2013-05-31 | Cyclacel Ltd | Kombinacje sapacytabiny lub cndac z inhibitorami metylotransferazy dna, takimi jak decytabina i prokaina |
| AR072999A1 (es) | 2008-08-11 | 2010-10-06 | Medarex Inc | Anticuerpos humanos que se unen al gen 3 de activacion linfocitaria (lag-3) y los usos de estos |
| EP2328919A2 (en) | 2008-08-25 | 2011-06-08 | Amplimmune, Inc. | Pd-i antagonists and methods for treating infectious disease |
| TWI453207B (zh) | 2008-09-08 | 2014-09-21 | Signal Pharm Llc | 胺基三唑并吡啶,其組合物及使用其之治療方法 |
| US20100061982A1 (en) | 2008-09-10 | 2010-03-11 | Wyeth | 3-substituted-1h-indole, 3-substituted-1h-pyrrolo[2,3-b]pyridine and 3-substituted-1h-pyrrolo[3,2-b]pyridine compounds, their use as mtor kinase and pi3 kinase inhibitors, and their syntheses |
| CA2736829C (en) | 2008-09-12 | 2018-02-27 | Isis Innovation Limited | Pd-1 specific antibodies and uses thereof |
| CA2998281C (en) | 2008-09-26 | 2022-08-16 | Dana-Farber Cancer Institute, Inc. | Human anti-pd-1 antobodies and uses therefor |
| EP4331604B9 (en) | 2008-12-09 | 2025-07-23 | F. Hoffmann-La Roche AG | Anti-pd-l1 antibodies and their use to enhance t-cell function |
| JP2012517241A (ja) | 2009-02-11 | 2012-08-02 | アボット・ラボラトリーズ | Bcl−2ファミリー阻害剤耐性腫瘍及び癌を有する被験者を同定、分類及びモニターするための方法及び組成物 |
| LT3903829T (lt) | 2009-02-13 | 2023-06-12 | Immunomedics, Inc. | Imunokonjugatai su viduląsteliniu būdu skaldoma jungtimi |
| WO2010147961A1 (en) | 2009-06-15 | 2010-12-23 | Precision Therapeutics, Inc. | Methods and markers for predicting responses to chemotherapy |
| KR101424989B1 (ko) | 2009-11-05 | 2014-07-31 | 글락소스미스클라인 엘엘씨 | 벤조디아제핀 브로모도메인 억제제 |
| US20130017199A1 (en) | 2009-11-24 | 2013-01-17 | AMPLIMMUNE ,Inc. a corporation | Simultaneous inhibition of pd-l1/pd-l2 |
| CA2778714C (en) | 2009-11-24 | 2018-02-27 | Medimmune Limited | Targeted binding agents against b7-h1 |
| US20130011393A1 (en) | 2010-01-12 | 2013-01-10 | Johnathan Mark Lancaster | Bad pathway gene signature |
| US8993731B2 (en) | 2010-03-11 | 2015-03-31 | Ucb Biopharma Sprl | PD-1 antibody |
| US8372819B2 (en) | 2010-04-11 | 2013-02-12 | Salk Institute For Biological Studies | Methods and compositions for targeting skip |
| CA2799403C (en) | 2010-05-14 | 2020-01-21 | Dana-Farber Cancer Institute, Inc. | Compositions and methods for treating leukemia |
| WO2011153374A1 (en) | 2010-06-04 | 2011-12-08 | Syndax Pharmaceuticals Inc. | Prodrugs of azacitidine 5'-phosphate |
| JP6158511B2 (ja) | 2010-06-11 | 2017-07-05 | 協和発酵キリン株式会社 | 抗tim−3抗体 |
| CA2802344C (en) | 2010-06-18 | 2023-06-13 | The Brigham And Women's Hospital, Inc. | Bi-specific antibodies against tim-3 and pd-1 for immunotherapy in chronic immune conditions |
| US8907053B2 (en) | 2010-06-25 | 2014-12-09 | Aurigene Discovery Technologies Limited | Immunosuppression modulating compounds |
| SG180031A1 (en) | 2010-10-15 | 2012-05-30 | Agency Science Tech & Res | Combination treatment of cancer |
| AR084070A1 (es) | 2010-12-02 | 2013-04-17 | Constellation Pharmaceuticals Inc | Inhibidores del bromodominio y usos de los mismos |
| US8987271B2 (en) | 2010-12-22 | 2015-03-24 | Eutropics Pharmaceuticals, Inc. | 2,2′-biphenazine compounds and methods useful for treating disease |
| WO2012122370A2 (en) | 2011-03-08 | 2012-09-13 | Eutropics Pharmaceuticals, Inc. | Compositions and methods useful for treating diseases |
| PT2699264T (pt) | 2011-04-20 | 2018-05-23 | Medimmune Llc | Anticorpos e outras moléculas que ligam b7-h1 e pd-1 |
| WO2013006490A2 (en) | 2011-07-01 | 2013-01-10 | Cellerant Therapeutics, Inc. | Antibodies that specifically bind to tim3 |
| RU2604814C2 (ru) | 2011-07-24 | 2016-12-10 | Кьюртек Лтд. | Варианты гуманизированных иммуномодулирующих моноклональных антител |
| EP2561867A1 (en) | 2011-08-22 | 2013-02-27 | Lead Discovery Center GmbH | CDK9 inhibitors in the treatment of midline carcinoma |
| US9012215B2 (en) | 2011-09-22 | 2015-04-21 | The Johns Hopkins University | Methods for identifying leukemia stem cells and distinguishing them from normal hematopietic stem cells in patients with acute myeloid leukemia: uses in diagnosis, treatment, and research |
| US20130122492A1 (en) | 2011-11-14 | 2013-05-16 | Kellbenx Inc. | Detection, isolation and analysis of rare cells in biological fluids |
| ES2808152T3 (es) | 2011-11-28 | 2021-02-25 | Merck Patent Gmbh | Anticuerpos anti-PD-L1 y usos de los mismos |
| WO2013082660A1 (en) | 2011-12-09 | 2013-06-13 | Alfred Health | Prediction method |
| US20150110779A1 (en) | 2012-03-15 | 2015-04-23 | Bristol-Myers Squibb Company | Methods for predicting gastrointestinal immune-related adverse events (gi-irae) in patients treated with modulation of the co-stimulatory pathway |
| WO2013142281A1 (en) | 2012-03-20 | 2013-09-26 | Dana Farber Cancer Institute, Inc. | Inhibition of mcl-1 and/or bfl-1/a1 |
| EP2847592A4 (en) | 2012-05-10 | 2016-05-04 | Eutropics Pharmaceuticals Inc | SURROGATE FUNCTIONAL DIAGNOSTIC TEST FOR CANCER |
| JP2015519375A (ja) | 2012-05-31 | 2015-07-09 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Pd−l1に結合する抗原結合蛋白質 |
| WO2013182519A1 (en) | 2012-06-04 | 2013-12-12 | Universitaet Basel | Combination of lysosomotropic or autophagy modulating agents and a gsk-3 inhibitor for treatment of cancer |
| WO2013188355A1 (en) | 2012-06-12 | 2013-12-19 | Merck Sharp & Dohme Corp. | Cdk inhibitor for treating refractory chronic lymphocytic leukemia |
| US20150133450A1 (en) | 2012-06-20 | 2015-05-14 | Eutropics Pharmaceuticals, Inc. | Methods and compositions useful for treating diseases involving bcl-2 family proteins with quinoline derivatives |
| CA2875620A1 (en) | 2012-06-20 | 2013-12-27 | Cytospan Technologies Corporation | Apparatus and method for quantification of replicative lifespan and observation of senescence |
| UY34887A (es) | 2012-07-02 | 2013-12-31 | Bristol Myers Squibb Company Una Corporacion Del Estado De Delaware | Optimización de anticuerpos que se fijan al gen de activación de linfocitos 3 (lag-3) y sus usos |
| WO2014022758A1 (en) | 2012-08-03 | 2014-02-06 | Dana-Farber Cancer Institute, Inc. | Single agent anti-pd-l1 and pd-l2 dual binding antibodies and methods of use |
| US10393733B2 (en) | 2012-09-19 | 2019-08-27 | Dana-Farber Cancer Institute, Inc. | Dynamic BH3 profiling |
| US9241941B2 (en) | 2012-09-20 | 2016-01-26 | Memorial Sloan-Kettering Cancer Center | Methods for treatment of lymphomas with mutations in cell cycle genes |
| US9493454B2 (en) | 2012-09-26 | 2016-11-15 | Tolero Pharmaceuticals, Inc. | Multiple kinase pathway inhibitors |
| CN114507282B (zh) | 2012-10-04 | 2025-05-16 | 达纳-法伯癌症研究所公司 | 人单克隆抗-pd-l1抗体和使用方法 |
| WO2014059028A1 (en) | 2012-10-09 | 2014-04-17 | Igenica, Inc. | Anti-c16orf54 antibodies and methods of use thereof |
| WO2014065275A1 (ja) | 2012-10-23 | 2014-05-01 | 国立大学法人福井大学 | 腫瘍融解症候群の治療薬及び予防薬 |
| US20140287932A1 (en) | 2012-10-25 | 2014-09-25 | Whitehead Institute For Biomedical Research | Super-enhancers and methods of use thereof |
| US9765039B2 (en) | 2012-11-21 | 2017-09-19 | Zenith Epigenetics Ltd. | Biaryl derivatives as bromodomain inhibitors |
| AR093984A1 (es) | 2012-12-21 | 2015-07-01 | Merck Sharp & Dohme | Anticuerpos que se unen a ligando 1 de muerte programada (pd-l1) humano |
| JOP20200097A1 (ar) | 2013-01-15 | 2017-06-16 | Aragon Pharmaceuticals Inc | معدل مستقبل أندروجين واستخداماته |
| ES2808654T3 (es) | 2013-03-15 | 2021-03-01 | Glaxosmithkline Ip Dev Ltd | Proteínas de unión anti-LAG-3 |
| HUE053069T2 (hu) | 2013-05-02 | 2021-06-28 | Anaptysbio Inc | Programozott halál-1 (PD-1) ellen irányuló ellenanyagok |
| CA2913977C (en) | 2013-05-31 | 2022-11-29 | Sorrento Therapeutics, Inc. | Antigen binding proteins that bind pd-1 |
| WO2014209804A1 (en) | 2013-06-24 | 2014-12-31 | Biomed Valley Discoveries, Inc. | Bispecific antibodies |
| US20160178612A1 (en) | 2013-07-18 | 2016-06-23 | Eutropics Pharmaceuticals, Inc. | Differential bh3 mitochondrial profiling |
| US10732182B2 (en) | 2013-08-01 | 2020-08-04 | Eutropics Pharmaceuticals, Inc. | Method for predicting cancer sensitivity |
| PT3702373T (pt) | 2013-09-13 | 2022-09-27 | Beigene Switzerland Gmbh | Anticorpos anti-pd1 e a sua utilização como agentes terapêuticos e de diagnóstico |
| WO2015042249A1 (en) | 2013-09-19 | 2015-03-26 | Dana-Farber Cancer Institute, Inc. | Methods of bh3 profiling |
| WO2015047510A1 (en) | 2013-09-27 | 2015-04-02 | Immunomedics, Inc. | Anti-trop-2 antibody-drug conjugates and uses thereof |
| US10202454B2 (en) | 2013-10-25 | 2019-02-12 | Dana-Farber Cancer Institute, Inc. | Anti-PD-L1 monoclonal antibodies and fragments thereof |
| WO2015066305A1 (en) | 2013-10-30 | 2015-05-07 | Eutropics Pharmaceuticals, Inc. | Methods for determining chemosensitivity and chemotoxicity |
| MX379463B (es) | 2013-11-08 | 2025-03-10 | Dana Farber Cancer Inst Inc | Terapia de combinación para el cáncer usando inhibidores de la proteína bromodominio y extra-terminal. |
| WO2015081158A1 (en) | 2013-11-26 | 2015-06-04 | Bristol-Myers Squibb Company | Method of treating hiv by disrupting pd-1/pd-l1 signaling |
| SG10201804945WA (en) | 2013-12-12 | 2018-07-30 | Shanghai hengrui pharmaceutical co ltd | Pd-1 antibody, antigen-binding fragment thereof, and medical application thereof |
| US10407502B2 (en) | 2014-01-15 | 2019-09-10 | Kadmon Corporation, Llc | Immunomodulatory agents |
| TWI681969B (zh) | 2014-01-23 | 2020-01-11 | 美商再生元醫藥公司 | 針對pd-1的人類抗體 |
| TWI680138B (zh) | 2014-01-23 | 2019-12-21 | 美商再生元醫藥公司 | 抗pd-l1之人類抗體 |
| JOP20200094A1 (ar) | 2014-01-24 | 2017-06-16 | Dana Farber Cancer Inst Inc | جزيئات جسم مضاد لـ pd-1 واستخداماتها |
| KR20160106762A (ko) | 2014-01-28 | 2016-09-12 | 브리스톨-마이어스 스큅 컴퍼니 | 혈액 악성종양을 치료하기 위한 항-lag-3 항체 |
| JOP20200096A1 (ar) | 2014-01-31 | 2017-06-16 | Children’S Medical Center Corp | جزيئات جسم مضاد لـ tim-3 واستخداماتها |
| EP3110509B1 (en) | 2014-02-28 | 2020-08-19 | Merck Sharp & Dohme Corp. | Treating cancer with a combination comprising dinaciclib |
| LT3116909T (lt) | 2014-03-14 | 2020-02-10 | Novartis Ag | Antikūno molekulės prieš lag-3 ir jų panaudojimas |
| WO2015161247A1 (en) | 2014-04-17 | 2015-10-22 | Igenica Biotherapeutics, Inc. | Humanized anti-c16orf54 antibodies and methods of use thereof |
| EP3149042B1 (en) | 2014-05-29 | 2019-08-28 | Spring Bioscience Corporation | Pd-l1 antibodies and uses thereof |
| WO2015195163A1 (en) | 2014-06-20 | 2015-12-23 | R-Pharm Overseas, Inc. | Pd-l1 antagonist fully human antibody |
| TWI693232B (zh) | 2014-06-26 | 2020-05-11 | 美商宏觀基因股份有限公司 | 與pd-1和lag-3具有免疫反應性的共價結合的雙抗體和其使用方法 |
| CN110156892B (zh) | 2014-07-03 | 2023-05-16 | 百济神州有限公司 | 抗pd-l1抗体及其作为治疗剂及诊断剂的用途 |
| JO3663B1 (ar) | 2014-08-19 | 2020-08-27 | Merck Sharp & Dohme | الأجسام المضادة لمضاد lag3 وأجزاء ربط الأنتيجين |
| MX2017003645A (es) | 2014-09-17 | 2017-05-30 | Novartis Ag | Direccion de celulas citotoxicas con receptores quimericos para inmunoterapia adoptiva. |
| JP6877339B2 (ja) | 2014-10-14 | 2021-05-26 | ノバルティス アーゲー | Pd−l1に対する抗体分子およびその使用 |
| JP6930913B2 (ja) | 2014-10-14 | 2021-09-01 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニアThe Regents Of The University Of California | 炎症を阻害するためのcdk9及びbrd4阻害剤の使用法 |
| CA2964830C (en) | 2014-11-06 | 2024-01-02 | F. Hoffmann-La Roche Ag | Anti-tim3 antibodies and methods of use |
| WO2016073913A1 (en) | 2014-11-07 | 2016-05-12 | Tolero Pharmaceuticals, Inc. | Methods to target transcriptional control at super-enhancer regions |
| TWI595006B (zh) | 2014-12-09 | 2017-08-11 | 禮納特神經系統科學公司 | 抗pd-1抗體類和使用彼等之方法 |
| WO2016111947A2 (en) | 2015-01-05 | 2016-07-14 | Jounce Therapeutics, Inc. | Antibodies that inhibit tim-3:lilrb2 interactions and uses thereof |
| AU2016206882B2 (en) | 2015-01-12 | 2022-03-10 | Eutropics Pharmaceuticals, Inc. | Context dependent diagnostics test for guiding cancer treatment |
| EP3258941A4 (en) | 2015-02-17 | 2018-09-26 | Cantex Pharmaceuticals, Inc. | Treatment of cancers and hematopoietic stem cell disorders privileged by cxcl12-cxcr4 interaction |
| TW201639888A (zh) | 2015-03-06 | 2016-11-16 | 索倫多醫療公司 | 結合tim3之抗體治療劑 |
| AU2016232833A1 (en) | 2015-03-18 | 2017-10-12 | Dana-Farber Cancer Institute, Inc. | Selective Mcl-1 binding peptides |
| WO2016154380A1 (en) | 2015-03-24 | 2016-09-29 | Eutropics Pharmaceuticals, Inc. | Surrogate functional biomarker for solid tumor cancer |
| SMT202400420T1 (it) | 2015-04-01 | 2024-11-15 | Anaptysbio Inc | Anticorpi diretti contro la proteina dell’immunoglobulina delle cellule t e della mucina 3 (tim-3) |
| CA2983022C (en) | 2015-04-27 | 2023-03-07 | Dana-Farber Cancer Institute, Inc. | High throughput bh3 profiling: a rapid and scalable technology to bh3 profile on low numbers of cells |
| EP4086264B1 (en) | 2015-05-18 | 2023-10-25 | Sumitomo Pharma Oncology, Inc. | Alvocidib prodrugs having increased bioavailability |
| US10568887B2 (en) | 2015-08-03 | 2020-02-25 | Tolero Pharmaceuticals, Inc. | Combination therapies for treatment of cancer |
| WO2017075349A2 (en) | 2015-10-30 | 2017-05-04 | Massachusetts Institute Of Technology | Selective mcl-1 binding peptides |
| CN110461315B (zh) | 2016-07-15 | 2025-05-02 | 诺华股份有限公司 | 使用与激酶抑制剂组合的嵌合抗原受体治疗和预防细胞因子释放综合征 |
| US11279694B2 (en) | 2016-11-18 | 2022-03-22 | Sumitomo Dainippon Pharma Oncology, Inc. | Alvocidib prodrugs and their use as protein kinase inhibitors |
| MX2019007332A (es) | 2016-12-19 | 2019-11-18 | Tolero Pharmaceuticals Inc | Péptidos indicadores y métodos para caracterizar sensibilidad. |
| JP7196160B2 (ja) | 2017-09-12 | 2022-12-26 | スミトモ ファーマ オンコロジー, インコーポレイテッド | Mcl-1阻害剤アルボシジブを用いた、bcl-2阻害剤に対して非感受性である癌の治療レジメン |
| US20190314357A1 (en) | 2018-04-13 | 2019-10-17 | Tolero Pharmaceuticals, Inc. | Cyclin-dependent kinase inhibitors in combination with anthracyclines for treatment of cancer |
| US20210277037A1 (en) | 2018-06-21 | 2021-09-09 | Sumitomo Dainippon Pharma Oncology, Inc. | Deuterated alvocidib and alvocidib prodrugs |
| US20210379042A1 (en) | 2018-10-12 | 2021-12-09 | Sumitomo Dainippon Pharma Oncology, Inc. | Methods for monitoring tumor lysis syndrome |
| US20210353619A1 (en) | 2018-11-01 | 2021-11-18 | Oregon Health & Science University | Treatment for venetoclax-resistant and venetoclax-sensitive acute myeloid leukemia |
| JP7222673B2 (ja) | 2018-11-20 | 2023-02-15 | 株式会社日立製作所 | 粒子線治療装置およびその制御方法 |
| AU2019391097B2 (en) | 2018-12-04 | 2025-07-03 | Sumitomo Pharma America, Inc. | CDK9 inhibitors and polymorphs thereof for use as agents for treatment of cancer |
| US20200281949A1 (en) | 2018-12-07 | 2020-09-10 | Tolero Pharmaceuticals, Inc. | Methods for treating castration-resistant and castration-sensitive prostate cancer |
| JP2022525149A (ja) | 2019-03-20 | 2022-05-11 | スミトモ ダイニッポン ファーマ オンコロジー, インコーポレイテッド | ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 |
| WO2021007316A1 (en) | 2019-07-08 | 2021-01-14 | Sumitomo Dainippon Pharma Oncology, Inc. | Treatment of cancer |
| US20220257581A1 (en) | 2019-07-08 | 2022-08-18 | Sumitomo Dainippon Pharma Oncology, Inc. | Treatment of Cancer |
-
2020
- 2020-03-20 JP JP2021555227A patent/JP2022525149A/ja active Pending
- 2020-03-20 WO PCT/US2020/023939 patent/WO2020191326A1/en not_active Ceased
- 2020-03-20 US US17/435,264 patent/US11793802B2/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018516245A (ja) * | 2015-04-20 | 2018-06-21 | トレロ ファーマシューティカルズ, インコーポレイテッド | ミトコンドリアプロファイリングによるアルボシジブ応答の予測 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2020191326A8 (en) | 2020-10-29 |
| WO2020191326A1 (en) | 2020-09-24 |
| US11793802B2 (en) | 2023-10-24 |
| US20220125776A1 (en) | 2022-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2022525149A (ja) | ベネトクラクスが失敗した急性骨髄性白血病(aml)の処置 | |
| JP2025123379A (ja) | 異型braf変異を有するがんを処置するための組成物および方法 | |
| TWI620565B (zh) | 治療及預防移植物抗宿主病之方法 | |
| CA3109090A1 (en) | Diagnostic and therapeutic methods for the treatment of breast cancer | |
| CN110325191A (zh) | 以较少的副作用治疗egfr-驱动的癌症 | |
| JP2017502013A (ja) | Cdk阻害剤およびerk阻害剤の組み合わせを使用するがん処置 | |
| UA125216C2 (uk) | Комбінована терапія | |
| JP2024023480A (ja) | 癌治療のためのバイオマーカー | |
| KR20180124055A (ko) | 급성 골수성 백혈병의 치료를 위한 병용 요법 | |
| US20230000835A1 (en) | Lysine-specific histone demethylase inhibitors for the treatment of myeloproliferative neoplasms | |
| JP2017502016A (ja) | 1型mek阻害剤およびerk阻害剤の組み合わせを使用するがんの処置 | |
| TW202216156A (zh) | 全身紅斑性狼瘡之治療 | |
| KR20250145001A (ko) | 혈액암 환자를 치료하기 위한 방법 | |
| CN115737821B (zh) | 用于治疗aml和mds的rara激动剂 | |
| JP2025098099A (ja) | ブルトン型チロシンキナーゼ阻害剤の投薬 | |
| TW200808313A (en) | Compositions and methods for treating rheumatoid arthritis | |
| CN117838695A (zh) | 用于治疗骨髓增殖性肿瘤和与癌症相关的纤维化的pim激酶抑制剂 | |
| WO2023183822A1 (en) | Hematopoietic loss of y chromosome leads to cardiac fibrosis and dysfunction and is associated with death due to heart failure | |
| JP2024519342A (ja) | 自己免疫性、同種免疫性、炎症性、及びミトコンドリア性の状態を治療するための組成物、ならびにその使用 | |
| JP2020114857A (ja) | Raf阻害剤及びタキサンの組み合わせ | |
| WO2022036111A1 (en) | Methods and compositions for treating sickle cell disease | |
| WO2021092030A1 (en) | Dosing regimens for use in treating myelofibrosis and mpn-related disorders with navitoclax | |
| Tsunogai et al. | A novel NR3C2 mutation in a Japanese patient with the renal form of pseudohypoaldosteronism type 1 | |
| WO2025242178A1 (zh) | 度洛西汀及化疗药物用于制备用于治疗或预防癌症的医药组成物的用途 | |
| HK40105549A (zh) | 用地西他滨和西达尿苷治疗骨髓增生异常综合症的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230314 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230314 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20230627 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240304 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20241002 |