RU2242474C2 - Соединения, пригодные в качестве противовоспалительных агентов - Google Patents
Соединения, пригодные в качестве противовоспалительных агентов Download PDFInfo
- Publication number
- RU2242474C2 RU2242474C2 RU2001126337/04A RU2001126337A RU2242474C2 RU 2242474 C2 RU2242474 C2 RU 2242474C2 RU 2001126337/04 A RU2001126337/04 A RU 2001126337/04A RU 2001126337 A RU2001126337 A RU 2001126337A RU 2242474 C2 RU2242474 C2 RU 2242474C2
- Authority
- RU
- Russia
- Prior art keywords
- urea
- tert
- butyl
- naphthalen
- morpholin
- Prior art date
Links
- 0 **(C(NN)=*)N Chemical compound **(C(NN)=*)N 0.000 description 1
- WQZJJDJFWQEFOB-UHFFFAOYSA-N C=[Br]c(c1ccccc11)ccc1N Chemical compound C=[Br]c(c1ccccc11)ccc1N WQZJJDJFWQEFOB-UHFFFAOYSA-N 0.000 description 1
- UCPVBLRLRLJZRP-UHFFFAOYSA-N Nc1ccc(-c2ccc(CN3CCOCC3)nc2)c2ccccc12 Chemical compound Nc1ccc(-c2ccc(CN3CCOCC3)nc2)c2ccccc12 UCPVBLRLRLJZRP-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/16—Central respiratory analeptics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/08—Plasma substitutes; Perfusion solutions; Dialytics or haemodialytics; Drugs for electrolytic or acid-base disorders, e.g. hypovolemic shock
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/36—Radicals substituted by singly-bound nitrogen atoms
- C07D213/38—Radicals substituted by singly-bound nitrogen atoms having only hydrogen or hydrocarbon radicals attached to the substituent nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/76—Nitrogen atoms to which a second hetero atom is attached
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/04—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D307/10—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/12—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/34—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D307/38—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D307/52—Radicals substituted by nitrogen atoms not forming part of a nitro radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/08—Bridged systems
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Diabetes (AREA)
- Neurosurgery (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Hematology (AREA)
- Dermatology (AREA)
- Urology & Nephrology (AREA)
- Pain & Pain Management (AREA)
- Toxicology (AREA)
- Endocrinology (AREA)
- Oncology (AREA)
- Transplantation (AREA)
- Psychiatry (AREA)
- Pulmonology (AREA)
- Hospice & Palliative Care (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Emergency Medicine (AREA)
- Communicable Diseases (AREA)
- Obesity (AREA)
Abstract
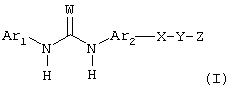
Изобретение относится к новым соединениям формулы (I)
в которой Ar1 означает пиразол, который может быть замещен одной или несколькими группами R1, R2 или R3; Ar2 означает нафтил, тетрагидронафтил, каждый из которых необязательно замещен 0-1 группами R2; Х означает С5-С8циклоалкенил, фенил, необязательно замещенный гидроксигруппой или С1-С4алкоксигруппой, фуран, пиридинонил, пиразолил, пиридинил, необязательно замещенный гидроксигруппой или С1-С4алкоксигруппой, пиперидинил; Y означает связь или насыщенную разветвленную или неразветвленную С1-С4углеродную цепь, при этом одна метиленовая группа необязательно заменена на NH, или а Y необязательно независимо замещен оксогруппой; Z означает морфолин, о-группу, пиридинил, фуранил, тетрагидрофуранил, тиоморфолинил, пентаметиленсульфид, пентаметиленсульфон, вторичный или третичный амин, причем атом азота аминогруппы ковалентно связан со следующими группами, выбранными из ряда, включающего C1-С3алкил и С1-С5алкоксиалкил; R1 означает С3-С10алкил, который необязательно частично или полностью галогенирован; R2 означает разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, галоген; R3 означает фенил, пиримидинил, пиразолил, которые замещены одним разветвленным или неразветвленным С1-С6алкилом, и пиридинил, необязательно замещенный С1-С3алкоксигруппой или аминогруппой, W означает O и его фармацевтически приемлемые соли. Соединения 1 ингибируют продуцирование цитокинов, что позволяет использовать их в фармацевтической композиции и для лечения заболевания опосредуемого цитокинами. 4 н. и 6 з.п. ф-лы, 1 табл.
Description
Сведения о дате заявки
По настоящей заявке испрашивается приоритет предварительных заявок на патент США 60/124148 от 12 марта 1999 г. и 60/165867 от 16 ноября 1999 г.
Область техники изобретения
Настоящее изобретение относится к новым соединениям, которые ингибируют продуцирование цитокинов, участвующих в воспалительных процессах, и поэтому могут применяться для лечения болезней и патологических состояний, сопровождающихся воспалением, таких как хронические воспалительные заболевания. Настоящее изобретение относится также к способам получения таких соединений и к фармацевтическим композициям, содержащим эти соединения.
Предпосылки создания изобретения
Фактор некроза опухоли (TNF) и интерлейкин-1 (IL-1) представляют собой важные биологические факторы, в целом называемые провоспалительными цитокинами. Наряду с некоторыми другими родственными молекулами они опосредуют воспалительную реакцию, связанную с иммунологическим распознаванием инфекционных агентов. Воспалительная реакция играет важную роль в ограничении развития патогенных инфекций и борьбе с ними.
Повышенные уровни провоспалительных цитокинов также связаны с многочисленными аутоиммунными болезнями, такими как синдром токсического шока, ревматоидный артрит, остеоартрит, диабет и воспалительное заболевание кишечника (С.A. Dinarello и др., Rev. Infect. Disease 6: 51, 1984). При таких болезнях хроническое усиление воспалительной реакции обостряет или вызывает многие наблюдаемые патологические проявления. Так, например, при ревматизме в синовиальную ткань проникают воспалительные клетки, что приводит к разрушению хряща и кости (А.Е. Koch и др., J. Invest. Med. 43: 28-38, 1995). При таких болезнях важным и признанным терапевтическим подходом, основанным на возможном использовании лекарственных средств, является уменьшение уровней провоспалительных цитокинов, таких как TNF (в виде выделенной из клеток формы также называемый TNFα) и IL-1β. В настоящее время проходят клинические испытания большое количество терапевтических средств, предназначенных для лечения опосредуемых цитокинами болезней. Для многочисленных аутоиммунных болезней была подтверждена эффективность применения моноклонального антитела к TNFα (Р. Heath, "CDP571: An Engineered Human IgG4 Anti-TNFα Antibody", материалы конференции IBC Meeting on Cytokine Antagonists, Филадельфия, шт. Пенсильвания, 24-25 апреля 1997 г.). Такие области применения включают лечение ревматоидного артрита, болезни Крона и язвенного колита (E.C.C. Rankin и др., British J. Rheum. 35: 334-342, 1997; W.A. Stack и др., Lancet 349: 521-524, 1997). Предполагается, что моноклональное антитело осуществляет свою функцию путем связывания как растворимого TNFα, так и связанного с мембраной TNF.
Был сконструирован рецептор растворимого TNFα, который взаимодействует с TNFα. Такой подход аналогичен подходу, описанному выше для моноклональных антител к TNFα; оба агента связываются с растворимым TNFα, снижая тем самым его концентрацию. Для одного из вариантов этой конструкции, названного Enbrel (фирма Immunex, Сиэтл, шт. Вашингтон), недавно в ходе фазы III клинических испытаний была продемонстрирована эффективность в отношении лечения ревматоидного артрита (Brower и др., Nature Biotechnology 15: 1240, 1997). Для другого варианта рецептора TNFα, Ro 45-2081 (фирма Hoffman-LaRoche Inc., Натли, шт. Нью-Джерси), была продемонстрирована эффективность его применения на различных моделях с использованием животных аллергического воспаления легкого и острого повреждения легкого. Ro 45-2081 представляет собой рекомбинантную химерную молекулу, сконструированную путем слияния растворимого человеческого рецептора TNF, имеющего молекулярную массу 55 кДа, с геном шарнирной области тяжелой цепи IgG1, который экспрессируется в эукариотических клетках (Renzetti и др., Inflamm. Res. 46: стр.143, 1997).
IL-1 в качестве иммунологической эффекторной молекулы участвует в развитии многочисленных болезней. Антагонист рецептора IL-1 (IL-1ra) изучали в клинических испытаниях на людях. Была продемонстрирована его эффективность в отношении лечения ревматоидного артрита (антрил, амген). На фазе III клинического испытания на людях IL-1ra приводил к уменьшению смертности пациентов, страдающих синдромом септического шока (Dinarello, Nutrution 11, 492, 1995). Остеоартрит представляет собой слабо прогрессирующую болезнь, характеризующуюся разрушением хряща сустава. IL-1 обнаружен в синовиальной жидкости и в хрящевом матриксе суставов, пораженных остеоартритом. На различных экспериментальных моделях артрита было установлено, что антагонисты IL-1 позволяют уменьшить разложение компонентов хрящевого матрикса (Chevalier, Biomed Pharmacother., 51, 58, 1997). В последнее время было установлено, что оксид азота, являющийся медиатором сердечно-сосудистого гомеостаза, передачи нервного импульса и иммунной функции, играет важную роль в модуляции восстановления кости. Сильными стимуляторами продуцирования NO являются цитокины, такие как IL-1 и TNF. NO представляет собой молекулу, обладающую важной регуляторной функцией в кости, которая оказывает влияние на клетки выстилки остеобласта и остеокласта (Evans и др., J. Bone Miner Res. 11, 300, 1996). Усиление разрушения бета-клеток, приводящее к развитию инсулинзависимого сахарного диабета, зависит от IL-1. Некоторые из таких повреждений могут быть опосредованы другими эффекторами, такими как простагландины и тромбоксаны. IL-1 может оказывать влияние на этот процесс путем контроля уровня экспрессии как циклооксигеназы II, так и индуцибельной синтетазы оксида азота (McDaniel и др., Proc. Soc. Exp. Biol. Med., 211, 24, 1996). Предполагается, что ингибиторы продуцирования цитокинов блокируют экспрессию индуцибельной циклооксигеназы (СОХ-2). Установлено, что экспрессия СОХ-2 увеличивается под действием цитокинов и предполагается, что она представляет собой изоформу циклооксигеназы, которая обусловливает воспаление (М.К. O'Banion и др., Proc. Natl. Acad. Sci. U.S.A., 89, 4888, 1992). Поэтому следует ожидать, что ингибиторы цитокинов, таких как IL-1, должны обладать эффективностью в отношении нарушений, которые в настоящее время лечат с использованием ингибиторов СОХ, таких как обычные нестероидные противовоспалительные лекарственные средства (НСПВЛС). Такие нарушения включают острую и хроническую боль, а также воспалительные симптомы и сердечно-сосудистые заболевания.
Было установлено, что уровень определенных цитокинов повышается при воспалительном заболевании кишечника (ВЗК). У пациентов, страдающих ВЗК, имеется дисбаланс IL-1 и IL-1ra в слизистой оболочке кишечника. Недостаточное продуцирование эндогенного IL-1ra может влиять на патогенез ВЗК (Cominelli и др., Aliment. Pharmacol. Ther. 10, 49, 1996). Болезнь Альцгеймера отличается присутствием отложений бета-амилоидного протеина, наличием нейрофибриллярных сплетений и холинергической дисфункции в области гиппокампа. Структурное и метаболическое нарушение, обнаруживаемое при болезни Альцгеймера вероятно обусловлено постоянным повышенным уровнем IL-1 (Holden и др., Med. Hypotheses, 45, 559, 1995). Установлено, что IL-1 играет определенную роль в патогенезе, обусловленном вирусом иммунодефицита человека (ВИЧ). Установлена четкая связь IL-1ra с острыми воспалениями, а также с различными стадиями болезни при патофизиологии ВИЧ-инфекций (Kreuzer и др., Clin. Exp. Immunol., 109, 54, 1997). IL-1 и TNF принимают участие в болезни периодонта. Процесс разрушения, связанный с болезнью периодонта, может быть обусловлен нарушением регуляции как IL-1, так и TNF (Howells, Oral Dis. 1, 266, 1995).
Провоспалительные цитокины, такие как TNFα and IL-1β, являются также важными медиаторами септического шока и связанной с ним сердечно-легочной дисфункции, острого респираторного дистресс-синдрома взрослых (РДСВ) и множественной недостаточности органов. TNFα также участвует в кахексии и деградации мышечной ткани, связанной с ВИЧ-инфекцией (Lahdiverta и др., Amer. J. Med., 85, 289, 1988). Ожирение сопровождается повышенной вероятностью возникновения инфекции, диабета и сердечно-сосудистых заболеваний. Установлено, что для каждого из указанных выше состояний имеются аномалии в уровне экспрессии TNFα (Loffreda и др., FASEB J. 12, 57, 1998). Предполагается, что повышенные уровни TNFα присутствуют и при других нарушениях, связанных с питанием, таких как нервная анорексия и булимия. Обнаружены патофизиологические параллели между нервной анорексией и раковой кахексией (Holden и др., Med. Hypotheses 47, 423, 1996). С использованием экспериментальной модели было установлено, что ингибитор продуцирования TNFα HU-211 улучшает реабилитацию после закрытой травмы головного мозга (Shohami и др., J. Neuroimmunol. 72, 169, 1997). Известно, что в развитии атеросклероза присутствует воспалительный компонент и предполагается, что такие цитокины, как IL-1 и TNF, стимулируют развитие болезни. На модели с использованием животных было установлено, что антагонист рецептора IL-1 ингибирует образование жировой прослойки (Elhage и др., Circulation, 97, 242, 1998).
Аномальная экспрессия индуцибельной синтетазы оксида азота (iNOS) сопровождалась развитием гипертензии у крыс со спонтанной гипертензией (Chou и др., Hypertension, 31, 643, 1998). IL-1 оказывает влияние на экспрессию iNOS и поэтому также может участвовать в патогенезе гипертензии (Singh и др., Amer. J. Hypertension, 9, 867, 1996).
Установлено, что IL-1 индуцирует развитие увеита у крыс, которое поддается ингибированию с помощью блокаторов IL-1 (Xuan и др., J. Ocular Pharmacol. and Ther., 14, 31, 1998). Продемонстрировано, что цитокины, включая IL-1, TNF и GM-CSF, стимулируют пролиферацию бластов острой миелогенной лейкемии (Bruserud, Leukemia Res. 20, 65, 1996). Установлено, что IL-1 имеет важное значение для развития как воспалительного, так и аллергического контактного дерматита. Сенсибилизация поверхности кожи может быть предотвращена путем введения моноклонального антитела к IL-1 перед нанесением аллергена на кожу (Muller и др., Am. J. Contact. Dermal. 7, 177, 1996). Результаты, полученные в опытах на мышах, у которых отсутствовал IL-1, свидетельствуют о том, что этот цитокин имеет решающее значение в развитии лихорадки (Kluger и др., Clin. Exp. Pharmacol. Physiol., 25, 141, 1998). Различные цитокины, включая TNF, IL-1, IL-6 и IL-8, инициируют острую фазу реакции, которая обычно характерна для лихорадки, при недомогании, миалгии, головных болях, клеточном гиперметаболизме и многочисленных эндокринных и ферментативных ответах (Beisel, Am. J. Clin. Nutr. 62, 813, 1995). После травмы или заражения патогенными организмами быстро начинается продуцирование этих воспалительных цитокинов.
Другие провоспалительные цитокины связаны с различными болезненными состояниями. Уровень IL-8 коррелирует с притоком нейтрофилов в места воспаления или повреждения. С использованием блокирующих антител к IL-8 было установлено, что IL-8 играет определенную роль в опосредуемом нейтрофилами повреждении ткани при остром воспалении (Harada и др., Molecular Medicine Today 2, 482, 1996). Таким образом, ингибитор продуцирования IL-8 может применяться для лечения болезней, которые в основном опосредуются нейтрофилами, таких как удар и инфаркт миокарда, возникшими в результате тромболитической терапии или независимо от нее, тепловое повреждение, респираторный дистресс-синдром взрослых (РДСВ), множественное повреждение органов в результате травмы, острый гломерулонефрит, дерматозы, включающие компоненты острого воспаления, острый гнойный менингит или другие нарушения центральной нервной системы, гемодиализ, лейкофериз, синдромы, связанные с трансфузией гранулоцитов, и некротический энтероколит.
Риновирус инициирует продуцирование различных провоспалительных цитокинов, преимущественно IL-8, что приводит к симптоматическим болезням, таким как острый ринит (Winther и др., Am. J. Rhinol. 12, 17, 1998).
Другие болезни, в развитии которых принимает участие IL-8, включают ишемию сердечной мышцы и реперфузию, воспалительные заболевания кишечника и многие другие болезни.
Провоспалительный цитокин IL-6 участвует в острой фазе реакции. IL-6 представляет собой фактор роста при многих онкологических болезнях, включая множественную миелому и родственные дискразии клеток плазмы (Treon и др., Current Opinion in Hematology 5: 42, 1998). Установлено, что он является важным медиатором воспаления в центральной нервной системе. Повышенные уровни IL-6 выявлены при некоторых неврологических нарушениях, включая комплекс деменций, связанных со СПИДом, болезнь Альцгеймера, рассеянный склероз, системную красную волчанку, травму ЦНС и вирусный и бактериальный менингит (Gruol и др., Molecular Neurobiology 15: 307, 1997). IL-6 также играет важную роль при остеопорозе. При моделировании на мышах было установлено, что он опосредует резорбцию кости и индуцирует активность остеокластов (Ershler и др., Development and Comparative Immunol. 21: 487, 1997). Выраженные различия уровней цитокинов, например уровней IL-6, обнаружены in vivo между остеокластами здоровой кости и кости пациентов, страдающих болезнью Пэджета (Mills и др., Calcif Tissue Int. 61, 16, 1997). Установлено, что многие цитокины участвуют в развитии раковой кахексии. Серьезность основных симптомов кахексии может быть снижена путем лечения с использованием антител к IL-6 или антагонистов рецептора IL-6 (Strassmann и др., Cytokins Mol. Ther. 1, 107, 1995). При некоторых инфекционных болезнях, таких как грипп, IL-6 и IFNα являются основными факторами как для формирования симптомов, так и для защиты хозяина (Hayden и др., J. Clin. Invest. 101, 643, 1998). Сверхэкспрессия IL-6 опосредует патологию многих болезней, включая множественную миелому, ревматоидный артрит, болезнь Кастлемана, псориаз и постменопаузальный остеопороз (Simpson и др., Protein Sci. 6, 929, 1997).
Соединения, которые оказывают влияние на продуцирование цитокинов, включая IL-6 и TNF, оказались эффективными в отношении блокирования пассивной кожной анафилаксии у мышей (Scholz и др., J. Med. Chem., 41, 1050, 1998).
GM-CSF представляет собой другой провоспалительный цитокин, связанный с многочисленными терапевтическими болезнями. Он влияет не только на пролиферацию и дифференциацию стволовых клеток, но и регулирует также некоторые другие клетки, участвующие в остром и хроническом воспалении. Предпринимались попытки лечения с использованием GM-CSF многих болезненных состояний, включая заживление ран, вызванных ожогом, рассасывание трансплантата кожи, а также мукозит, индуцированный цитостатическими агентами и радиотерапией (Masucci, Medical Oncology 13: 149, 1996). GM-CSF, вероятно, также играет определенную роль в репликации вируса иммунодефицита человека (ВИЧ) в клетках выстилки макрофагов при терапии СПИДа (Crowe и др., Journal of Leukocyte Biology 62, 41, 1997). Бронхиальная астма характеризуется наличием воспалительного процесса в легких. Участвующие при этом цитокины включают среди прочего GM-CSF (Lee, J. R. Coll. Physicians Lond., 32, 56, 1998).
Установлено, что интерферон γ (IFN-γ) участвует в развитии многих болезней. Он связан с повышенным отложением коллагена, которое представляет собой основной гистопатологический признак болезни "трансплантат против хозяина" (Parkman, Curr. Opin. Hematol., 5, 22, 1998). У одного из пациентов после трансплантации почки была диагностирована острая миелогенная лейкемия. Ретроспективный анализ цитокинов периферической крови выявил повышенные уровни GM-CSF и IFN-γ. Эти повышенные уровни коррелируют с увеличением количества лейкоцитов в периферической крови (Burke и др., Leuk. Lymphoma. 19, 173, 1995). Развитие инсулинзависимого диабета (типа 1) может коррелировать с накоплением в клетках панекреатического островка Т-клеток, которые продуцируют IFN-γ (Ablumunits и др., J. Autoimmun., 11, 73, 1998). IFN-γ наряду с TNF, IL-2 и IL-6 приводит к активации большинства периферических Т-клеток перед развитием повреждений в центральной нервной системе при таких болезнях, как рассеянный склероз (PC) и комплекс деменций, связанных со СПИДом (Martino et al., 1998, Ann Neurol. 43, 340). Атеросклеротические повреждения вызывают артериальную болезнь, которая может привести к инфаркту сердца и головного мозга. В областях таких повреждений присутствуют многие активированные иммунные клетки, в основном Т-клетки и макрофаги. Указанные клетки продуцируют большие количества провоспалительных цитокинов, таких как TNF, IL-1 и IFNγ. Предполагается, что эти цитокины участвуют в стимулировании апоптоза (т.е. запрограммированной гибели клеток) окружающих клеток гладкой мускулатуры сосудов, что приводит к атеросклеротическим повреждениям (Geng, Heart Vessels Suppl., 12, 76, 1997). В организме людей, страдающих аллергией, после заражения ядом осы (р. Vespula) продуцируется мРНК, специфичная для IFN-γ (Bonay и др., Clin. Exp. Immunol., 109, 342, 1997). Установлено, что после гиперчувствительной реакции замедленного типа увеличивается экспрессия многих цитокинов, включая IFN-γ, что свидетельствует о роли IFN-γ в развитии атопического дерматита (Szepietowski и др., Br. J. Dermatol. 137, 195, 1997). Для случаев заболевания фатальной церебральной малярией были проведены гистопатологические и иммуногистопатологические исследования. Был выявлен повышенный уровень IFN-γ по сравнению с другими цитокинами, что свидетельствует о его роли в развитии этой болезни (Udomsangpetch и др., Am. J. Trop. Med. Hyg. 57, 501, 1997). Установлено, что различные свободные радикалы участвуют в патогенезе различных инфекционных болезней. В качестве ответа на заражение определенными вирусами происходит активация пути синтеза оксида азота в результате индукции провоспалительных цитокинов, таких как IFN-γ (Akaike и др, Proc. Soc. Exp. Biol. Med. 217, 64, 1998). У пациентов, являющихся хроническими носителями вируса гепатита В (ВГВ), может развиться цирроз и карцинома клеток печени. Экспрессия вируса гена и его репликация в трансгенных мышах, зараженных ВГВ, может быть подавлена с помощью посттранскрибционного механизма, опосредуемого IFN-γ, TNF и IL-2 (Chisari и др., Springer Semin. Immunopathol. 17, 261, 1995). IFN-γ может избирательно ингибировать индуцированную цитокином резорбцию кости. Этот процесс происходит, вероятно, при участии оксида азота (NO), который представляет собой важный регуляторный агент, оказывающий влияние на восстановление кости. NO может участвовать в качестве медиатора болезни кости для таких болезней, как ревматоидный артрит, связанная с остеолизом опухоль и постменопаузальный остеопороз (Evans и др., J. Bone Miner Res. 11, 300, 1996). Исследования, проведенные на мышах с дефицитом гена, продемонстрировали, что зависящее от IL-12 продуцирование IFN играет решающую роль в борьбе с ростом паразитов на начальной стадии. Хотя этот процесс не зависит от оксида азота, эффективность борьбы с хронической инфекцией зависит, по-видимому, от NO (Alexander и др., Philos. Trans. R. Soc. Lond. В. Biol. Sci. 352, 1355, 1997). NO является важным сосудорасширяющим средством, при этом имеются подтверждения того, что он играет определенную роль в развитии сердечно-сосудистого шока (Kilbourn и др., Dis. Mon. 43, 277, 1997). IFN-γ участвует в развитии хронического воспаления кишечника при таких болезнях, как болезнь Крона и воспалительное заболевание кишечника (ВЗК), преимущественно вследствие присутствия CD4+-лимфоцитов, относящихся, как полагают, к ТН1-фенотипу (Sartor, Aliment Pharmacol. Ther. 10, приложение 2, 43, 1996). Повышенные уровни сыворотки IgE связаны с различными атопическими болезнями, такими как бронхиальная астма и атопический дерматит. Уровень IFN-γ отрицательно коррелирует с уровнем IgE в сыворотке, что свидетельствует о роли IFN-γ в развитии атопических болезней у пациентов (Teramoto и др., Clin. Exp. Allergy 28, 74, 1998).
Соединения, которые обладают способностью модулировать один или несколько из указанных выше воспалительных цитокинов, могут применяться для лечения болезней, опосредуемых высвобождением этих цитокинов. Так, например, в WO 98/52558 описаны производные гетероарилмочевины, которые могут применяться для лечения опосредуемых цитокинами болезней. В WO 99/23091 описан другой класс производных мочевины, которые могут применяться в качестве противовоспалительных агентов.
В патенте US 5162360 описаны (N-замещенный арил)-N'-гетероциклилзамещенные производные мочевины, которые могут применяться для лечения гиперхолестеромии и атеросклероза.
Процитированные выше публикации свидетельствуют о том, что ингибирование продуцирования цитокинов может иметь важное значение при различных болезненных состояниях. Некоторые терапевтические средства на основе протеина находятся в стадии разработки или разрешены к применению в определенных случаях. Терапевтические средства на основе протеина являются дорогостоящими, и для них характерны определенные проблемы, связанные с биологической доступностью и стабильностью. Поэтому существует необходимость в разработке новых ингибиторах цитокинов с малой молекулярной массой, обладающих оптимальной эффективностью, фармакокинетическими характеристиками и профилями безопасности.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
С учетом указанных выше публикаций в данной области техники существует необходимость в соединениях, которые ингибировали бы продуцирование цитокинов с целью лечения различных болезненных состояний.
Таким образом, в основу настоящего изобретения была положена задача получить новые соединения, которые ингибируют высвобождение воспалительных цитокинов, таких как интерлейкин 1 и фактор некроза опухоли.
Еще одной задачей изобретения является разработка способа лечения воспалительных заболеваний и патологических состояний, таких как хронические воспалительные заболевания, с использованием новых соединений по изобретению.
Задачей изобретения является далее разработка способа получения вышеуказанных новых соединений.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В соответствии с первым объектом в изобретении предлагаются соединения формулы (I)
в которой Ar1 выбран из группы, включающей пиррол, пирролидин, пиразол, имидазол, оксазол, тиазол, фуран и тиофен, при этом Ar1 может быть замещен одной или несколькими группами R1, R2 или R3,
Ar2 означает фенил, нафтил, хинолин, изохинолин, тетрагидронафтил, тетрагидрохинолин, тетрагидроизохинолин, бензимидазол, бензофуран, инданил, инденил или индол, каждый из которых необязательно замещен 0-3 группами R2,
Х означает
а) С5-С8циклоалкил или циклоалкенил, необязательно замещенный 0-2 оксогруппами или 0-3 разветвленными либо неразветвленными С1-С4алкильными, C1-С4алкокси- или C1-С4алкиламиноцепями или
б) фенил, фуран, тиофен, пиррол, имидазолил, пиридин, пиримидин, пиридинон, дигидропиридинон, малеимид, дигидромалеимид, пиперидин, пиперазин или пиразин, каждый из которых независимо друг от друга необязательно замещен 0-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный С1-С4алкил, C1-С4алкоксигруппу, гидроксигруппу, нитрил, моно- либо ди(С1-С3алкил)аминогруппу, группу С1-С6алкил-S(О)m или галоген,
Y означает связь или насыщенную или ненасыщенную разветвленную или неразветвленную С1-С4углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH, S(O), S(O)2 или S, а Y необязательно независимо замещен 0-2 оксогруппами и одной или несколькими разветвленными или неразветвленными С1-С4алкильными группами, которые могут быть замещены одним или несколькими атомами галогена,
Z означает
а) фенил, пиридин, пиримидин, пиридазин, имидазол, фуран, тиофен, пиран, которые необязательно замещены 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, гидроксигруппу, моно- либо ди(C1-С3алкил) аминогруппу, группу С1-С6алкил-S(O)m, группу СООН и фениламиногруппу, при этом фенильное кольцо необязательно замещено 1-2 заместителями, выбранными из галогена, С1-С6алкила и С1-С6алкоксигруппы,
б) тетрагидропиран, тетрагидрофуран, 1,3-диоксоланон, 1,3-диоксанон, 1,4-диоксан, морфолин, тиоморфолин, тиоморфолинсульфоксид, пиперидин, пиперидинон, пиперазин, тетрагидропиримидон, циклогексанон, циклогексанол, пентаметиленсульфид, пентаметиленсульфоксид, пентаметиленсульфон, тетраметиленсульфид, тетраметиленсульфоксид или тетраметиленсульфон, которые необязательно замещены 1-3 заместителями, выбранными из нитрила, C1-C6алкила, С1-С6алкоксигруппы, гидроксигруппы, моно- либо ди(С1-С3алкил)амино-С1-С3алкила, фениламино-С1-С3алкила и С1-С3алкокси-С1-С3алкила, или
в) С1-С6алкоксигруппу, вторичный или третичный амин, где аминный азот ковалентно связан с группами, выбранными из ряда, включающего C1-С3алкил, С1-С5алкоксиалкил, пиридинил-С1-С3алкил, имидазолил-C1-С3алкил, тетрагидрофуранил-С1-С3алкил, фениламиногруппу, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу С1-С6алкил-S(O)m и группу фенил-S(O)m, в которой фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
R1 означает
а) разветвленный или неразветвленный С3-С10алкил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 фенильными, нафтильными или гетероциклическими группами, выбранными из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, при этом каждый такой фенил, нафтил или гетероцикл, выбранный из описанного выше в этом абзаце ряда, замещен 0-5 заместителями, выбранными из группы, включающей галоген, разветвленный или неразветвленный C1-C6алкил, который необязательно частично или полностью галогенирован, С3-С8циклоалкил, С5-С8циклоалкенил, гидроксигруппу, нитрил, С1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, группу NH4C(O) и ди(С1-С3)алкиламинокарбонил,
б) С3-С7циклоалкил, выбранный из группы, включающей циклопропил, циклобутил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил и бициклогептанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 C1-С3алкильными группами, или аналог подобной циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы заменены на группы, независимо друг от друга выбранные из ряда, включающего О, S, CHOH, >C=O, >C=S и NH,
в) разветвленный С3-С10алкенил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из разветвленного или неразветвленного С1-С5алкила, фенила, нафтила или гетероциклических групп, при этом каждая такая гетероциклическая группа независимо выбрана из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, а каждая из указанных фенильных, нафтильных или гетероциклических групп замещена 0-5 заместителями, выбранными из группы, включающей галоген, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропил, циклобутил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, гидроксигруппу, нитрил, C1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, группу NH2C(O) и моно- либо ди(С1-С3)алкиламинокарбонил,
г) С5-С7циклоалкенил, выбранный из группы, включающей циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил и бициклогептенил, при этом каждая такая циклоалкенильная группа необязательно замещена 1-3 C1-С3алкильными группами,
д) нитрил или
е) разветвленный или неразветвленный C1-С6алкоксикарбонил, разветвленный или неразветвленный С1-С6алкиламинокарбонил, разветвленный или неразветвленный С1-С6алкилкарбониламино-С1-С3алкил,
R2 означает разветвленный или неразветвленный C1-С6алкил, который необязательно частично или полностью галогенирован, ацетил, ароил, разветвленную или неразветвленную С1-С4алкоксигруппу, которая необязательно частично или полностью галогенирована, галоген, метоксикарбонил или фенилсульфонил,
R3 означает
а) фенильную, нафтильную или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, тетрагидрофурил, изоксазолил, изотиазолил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, бензоксазолил, бензизоксазолил, бензпиразолил, бензотиофуранил, циннолинил, птериндинил, фталазинил, нафтилпиридинил, хиноксалинил, хинозолинил, пуринил и индазолил, при этом такая фенильная, нафтильная или гетероциклическая группа необязательно замещена 1-5 заместителями, выбранными из группы, включающей фенил, нафтил, гетероцикл, выбранный из описанного выше в этом абзаце ряда, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бициклопентил, бициклогексил, бициклогептил, фенил-C1-С5алкил, нафтил-C1-С5алкил, галоген, гидроксигруппу, нитрил, С1-С3алкилоксигруппу, которая необязательно может быть частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу, где гетероциклический фрагмент выбран из описанного выше в этом абзаце ряда, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, где гетероциклильный фрагмент выбран из описанного выше в этом абзаце ряда, группу NH2C(O), моно- либо ди(С1-С3)алкиламинокарбонил, С1-С5алкил-С(O)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, группу амино-S(O)2, группу ди(С1-С3алкиламино-S(O)2, R4-С1-С5алкил, R5-С1-С5алкоксигруппу, R6-C(O)-C1-С5алкил, группу R7-С1-С5алкил(R8)N, карбокси-моно- либо ди-С1-С5алкиламиногруппу,
б) конденсированный арил, выбранный из группы, включающей бензоциклобутанил, инданил, инденил, дигидронафтил, тетрагидронафтил, бензоциклогептанил и бензоциклогептенил, или конденсированный гетероциклил, выбранный из группы, включающей циклопентенопиридин, циклогексанопиридин, циклопентанопиримидин, циклогексанопиримидин, циклопентанопиразин, циклогексанопиразин, циклопентанопиридазин, циклогексанопиридазин, циклопентанохинолин, циклогексанохинолин, циклопентаноизохинолин, циклогексаноизохинолин, циклопентаноиндол, циклогексаноиндол, циклопентанобензимидазол, циклогексанобензимидазол, циклопентанобензоксазол, циклогексанобензоксазол, циклопентаноимидазол, циклогексаноимидазол, циклопентанотиофен и циклогексанотиофен, при этом указанные конденсированное арильное или конденсированное гетероциклильное кольца замещены 0-3 заместителями, выбранными из группы, включающей фенил, нафтил и гетероциклил, выбранный из группы, включающей пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, разветвленный или неразветвленный C1-С6алкил, который необязательно частично или полностью галогенирован, галоген, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероциклилоксигруппу, в которой гетероциклильный фрагмент выбран из описанной выше в этом абзаце группы, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, в которой гетероциклильный фрагмент выбран из описанной выше в этом абзаце группы, группу NH2C(O), моно- либо ди(С1-С3)алкиламинокарбонил, группу С1-С4алкил-ОС(O), разветвленный или неразветвленный С1-С5алкил-С(О)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, R9-С1-С5алкил, R10-С1-С5алкоксигруппу, R11-С(O)-С1-С5алкил и группу R12-C1-C5алкил(R13)N,
в) циклоалкил, выбранный из группы, включающей циклопентил, циклогексил, циклогептил, бициклопентил, бициклогексил и бициклогептил, при этом такой циклоалкил необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами,
г) С5-С7 циклоалкенил, выбранный из группы, включающей циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил и бициклогептенил, при этом такая циклоалкенильная группа необязательно замещена 1-3 C1-С3алкильными группами,
д) ацетил, ароил, алкоксикарбонилалкил или фенилсульфонил или
е) разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, или
R1 и R2 вместе могут необязательно образовывать конденсированное фенильное или пиридинильное кольцо,
R8 и R13 каждый независимо друг от друга выбран из группы, включающей водород и разветвленный или неразветвленный C1-С4алкил, который необязательно частично или полностью галогенирован,
R4, R5, R6, R7, R9, R10, R11 и R12 каждый независимо друг от друга выбран из группы, включающей морфолин, пиперидин, пиперазин, имидазол и тетразол,
m означает 0, 1 или 2,
W означает О или S,
и их фармацевтически приемлемые производные.
Согласно одному из вариантов осуществления изобретения предпочтительны соединения формулы (I), в которых Ar2 означает нафтил, тетрагидронафтил, инданил или инденил, а W означает О.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых Ar1 выбран из тиофена и пиразола,
Х означает С5-С7циклоалкил или С5-С7циклоалкенил, необязательно замещенный 0-2 оксогруппами или 0-3 разветвленными или неразветвленными C1-С4алкильными группами, С1-С4алкоксигруппами или С1-С4алкиламиногруппами, или Х означает фенил, пиридин, тетрагидропиридин, пиримидин, фуран или тиофен, каждый из которых независимо друг от друга необязательно замещен 0-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный С1-С4алкил, С1-С4алкоксигруппу, гидроксигруппу, нитрил, моно- либо ди(C1-С3алкил)аминогруппу, группу С1-С6алкил-S(O)m и галоген,
R1 означает разветвленный или неразветвленный С1-С4алкил, циклопропил или циклогексил, которые необязательно частично или полностью галогенированы и необязательно замещены 1-3 С1-С3алкильными группами,
R3 означает разветвленный или неразветвленный С1-С4алкил, фенил, пиримидинил, пиразолил или пиридинил, каждый из которых необязательно замещен, как это указано при описании первого объекта изобретения, алкоксикарбонилалкил или циклопропил либо циклопентил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен, как это указано при описании первого объекта изобретения.
Согласно еще одному варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых
Ar1 означает пиразол и
Х означает циклопентенил, циклогексенил или циклогептенил, необязательно замещенные оксогруппой или 0-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный С1-С4алкил, С1-С4алкоксигруппу и С1-С4алкиламиногруппу, или Х означает фенил, пиридин, фуран или тиофен, каждый из которых независимо друг от друга необязательно замещен 0-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный C1-С4алкил, C1-С4алкоксигруппу, гидроксигруппу, нитрил, моно- либо ди(С1-С3алкил) аминогруппу, группу С1-С6алкил-S(O)m и галоген.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых
Y означает -СН2-, -СН2СН2-, -CH2NH-, -CH2CH2NH- или связь и
Z означает фенил, имидазол, фуран, пиперазин, тетрагидропиран, морфолин, тиоморфолин, тиоморфолинсульфоксид, пиперидин, пиридин, вторичный или третичный амин, где аминный азот ковалентно связан с группами, выбранными из ряда, включающего C1-С3алкил и С1-С5алкоксиалкил, или означает далее фениламиногруппу, в которой фенильное кольцо необязательно замещено 1-2 заместителями, выбранными из галогена, C1-С6алкоксигруппы, гидроксигруппы и моно- либо ди(C1-С3алкил)аминогруппы, группу С1-С6алкил-S(O)m и группу фенил-S(О)m, в которой фенильное кольцо необязательно замещено 1-2 заместителями, выбранными из галогена, С1-С6алкоксигруппы, гидроксигруппы и моно- либо ди(С1-С3алкил)аминогруппы.
В соответствии еще с одним вариантом осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых
Ar1 означает 5-трет-бутилпиразол-3-ил, где пиразольное кольцо может быть замещено группой R3, при этом
R3 означает разветвленный или неразветвленный С1-С4алкил, фенил, пиримидинил, пиразолил или пиридинил, каждый из которых необязательно замещен, как это указано при описании первого объекта изобретения, алкоксикарбонил-алкил или циклопропил либо циклопентил, каждый из которых необязательно замещен, как это указано при описании первого объекта изобретения.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых Х означает пиридинил.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (I), в которых пиридинил присоединен к Ar1 в 3-м положении пиридинила.
В качестве примеров соединений формулы (I) по изобретению можно назвать следующие:
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-ил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(2-(морфолин-4-ил)этил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-диметиламинофенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-ил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилфур-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-метил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-фенил-2Н-пиразол-3-ил]-3-[4-(4-пиперидин-1-илметилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-фенил-2Н-пиразол-3-ил]-3-[4-(4-(4-метилпиперазин-1-ил)метилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3,4-ди(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-пиридин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-тетрагидропиран-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотетрагидротиофен-3-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(имидазол-1-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[2-(3-диметиламинометилфенил)-5-(1-метилциклогексил)-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[2-(5-(1-метилциклогексил)-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-метокси-5-(2-морфолин-4-илэтокси)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-морфолин-4-илэтокси)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-3-(диметиламино)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-3-(метилсульфонил)фенил)нафталин-1-ил]мочевину,
метиловый эфир 5-трет-бутил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}тиофен-2-карбоновой кислоты,
метиламид 5-трет-бутил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}тиофен-2-карбоновой кислоты,
метиловый эфир 5-трет-бутил-1-метил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}-1Н-пиррол-2-карбоновой кислоты,
метиламид 5-трет-бутил-1-метил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}-1Н-пиррол-2-карбоновой кислоты,
2-ацетиламино-N-(5-трет-бутил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}тиофен-2-илметил)ацетамид,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-морфолин-4-илциклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-морфолин-4-илциклогепт-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(2-морфолин-4-илэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-морфолин-4-илциклогепт-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(пиридин-4-илметиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(диметиламиноэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(пиридин-3-илметиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(фенилметиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-фенилэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-ниразол-3-ил]-3-[4-(3-(фуран-2-илметиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-пиридин-2-илэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-пиперидин-1-илэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-имидазол-4-илэтиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(пиридин-2-илметиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-(4-метоксифенил)этиламино)циклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-морфолин-4-илметил-3-оксоциклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(1-оксотетрагидротиофен-3-илметил)-3-оксоциклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(1-оксотиоморфолин-4-илметил)-3-оксоциклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-метилпиперазин-1-илметил)-3-оксоциклогекс-1-енил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-[6-оксо-1-(тетрагидропиран-4-илметил)-1,2,3,6-тетрагидропиридин-4-ил]нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(2-оксо-1-пиридин-4-илметилпиперидин-4-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-оксо-1-пиридин-4-ил-1,2,3,6-тетрагидропиридин-4-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-оксо-1-пиридин-4-ил-1,2,3,6-тетрагидропиридин-4-ил)нафталин-1-ил]мочевину,
метиловый эфир 5-трет-бутил-3-{3-[4-(6-оксо-1-пиридин-4-ил-1,2,3,6-тетрагидропиридин-4-ил)нафталин-1-ил]уреидо}тиофен-2-карбоновой кислоты,
метиловый эфир 5-трет-бутил-1-метил-3-{3-[4-(6-оксо-1-пиридин-4-ил-1,2,3,6-тетрагидропиридин-4-ил)нафталин-1-ил]уреидо]пиррол-2-карбоновой кислоты,
метиламид 5-трет-бутил-1-метил-3-{3-[4-(6-оксо-1-пиридин-4-ил-1,2,3,6-тетрагидропиридин-4-ил)нафталин-1-ил]уреидо]пиррол-2-карбоновой кислоты,
метиловый эфир 5-трет-бутил-3-{3-[4-(3-морфолин-4-илциклогекс-1-енил)нафталин-1-ил]уреидо}тиофен-2-карбоновой кислоты,
метиловый эфир 5-трет-бутил-1-метил-3-{3-[4-(3-морфолин-4-илциклогекс-1-енил)нафталин-1-ил]уреидо]пиррол-2-карбоновой кислоты и
метиламид 5-трет-бутил-1-метил-3-{3-[4-(3-морфолин-4-илциклогекс-1-енил)нафталин-1-ил]уреидо}пиррол-2-карбоновой кислоты, а также их фармацевтически приемлемые производные.
Согласно еще одному варианту осуществления изобретения в нем предлагаются также следующие соединения формулы (I):
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(2-(морфолин-4-ил)этил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилфур-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-метил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
а также их фармацевтически приемлемые производные.
Вторым объектом изобретения являются соединения формулы (Iа):
в которой Ar1 означает пиррол, пирролидин, пиразол, имидазол, оксазол, тиазол, фуран и тиофен, при этом Ar1 необязательно замещен одной или несколькими группами R1, R2 или R3,
Ar2 означает фенил, нафтил, хинолин, изохинолин, тетрагидронафтил, тетрагидрохинолин, тетрагидроизохинолин, бензимидазол, бензофуран, инданил, инденил и индол, каждый из которых необязательно замещен 0-3 группами R2,
Х означает
- С5-С8циклоалкил или циклоалкенил, необязательно замещенные 1-2 оксогруппами или 1-3 С1-С4алкильными, С1-С4алкокси- или С1-С4алкиламиноцепями, каждая из которых является разветвленной или неразветвленной,
- фенил, фуранил, тиенил, пирролил, пиразолил, имидазолил, пиридинил, тетрагидропиридинил, пиримидинил, пиридинонил, дигидропиридинонил, малеимидил, дигидромалеимидил, пиперидинил, бензимидазол, 3Н-имидазо[4,5-b]пиридин, пиперазинил, пиридазинил или пиразинил, каждый из которых независимо необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, С1-С4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу С1-С6алкил-S(O) и галоген,
Y означает связь или насыщенную либо ненасыщенную разветвленную или неразветвленную С1-С4-углеродную цепь, которая необязательно частично или полностью галогенирована, при этом один или более С-атомов необязательно заменены на О, N или S(O)m, а Y в каждом случае независимо необязательно замещен 1-2 оксогруппами, нитрилом, фенилом, гидроксигрупой или одной или несколькими С1-С4алкильными группами, необязательно замещенными одним или более атомами галогена,
Z означает
арил, инданил, гетероарил, выбранный из бензимидазолила, пиридинила, пиримидинила, пиридазинила, пиразинила, имидазолила, пиразолила, триазолила, тетразолила, фуранила, тиенила и пиранила, гетероцикл, выбранный из пиперазинила, тетрагидропиримидонила, циклогексанонила, циклогексанолила, 2-окса- либо 2-тиа-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетраметиленсульфидила, тетраметиленсульфоксидила либо тетраметиленсульфонила, тетрагидропиранила, тетрагидрофуранила, 1,3-диоксоланонила, 1,3-диоксанонила, 1,4-диоксанила, морфолиногруппы, тиоморфолиногруппы, тиоморфолиносульфоксидил, тиоморфолиносульфонила, пиперидинила, пиперидинонила, пирролидинила и диоксоланила,
при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, C1-С6алкоксигруппу, C1-С3алкокси-С1-С3алкил, C1-C6алкоксикарбонил, ароил, гетероароил, гетероциклС1-С3ацил, где гетероарил и гетероцикл имеют указанные выше в этом абзаце значения, C1-С3ацил, оксогруппу, гидроксигруппу, пиридинил-С1-С3алкил, имидазолил-C1-С3алкил, тетрагидрофуранил-C1-С3алкил, нитрил-C1-С3алкил, нитрил, карбоксигруппу, фенил, причем фенильное кольцо необязательно замещено 1-2 заместителями, выбранными из группы, включающей галоген, С1-С6алкоксигруппу, гидроксигруппу и моно- либо ди(С1-С3алкил)аминогруппу, группу амино-S(O)m, группу С1-С6алкил-S(O)m и группу фенил-S(О)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, или Z необязательно замещен 1-3 заместителями, выбранными из группы, включающей аминогруппу, аминокарбонил и амино-С1-С3алкил, где N-атом независимо необязательно моно- либо дизамещен аминоС1-С6алкилом, С1-С3алкилом, арилС0-С3алкилом, С1-С5алкоксиС1-С3алкилом, С1-С5алкоксигруппой, ароилом, C1-С3ацилом, группой С1-С3алкил-S(O)m- или группой арилС0-С3алкил-S(O)m-, при этом каждый из вышеуказанных алкилов и арилов, присоединенных к аминогруппе, необязательно замещен 1-2 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, гидроксигруппу и моно- либо ди(С1-С3алкил) аминогруппу,
или Z необязательно замещен 1-3 заместителями, выбранными из группы, включающей арил, гетероцикл или гетероарил, как они определены выше в этом абзаце, при этой каждый из укзанных заместителей в свою очередь необязательно замещен галогеном, C1-С6алкилом или С1-С6алкоксигруппой,
или Z означает гидроксигруппу, гидроксиС1-С3алкил, галоген, нитрил, аминогруппу, где N-атом независимо необязательно моно- либо дизамещен С1-С6алкилом, аминоС1-С6алкилом, арилС0-С3алкилом, С1-С5алкоксиС1-С3алкилом, C1-С5алкоксигруппой, ароилом, C1-С3ацилом, группой С1-С3алкил-S(O)m-, группой арилС0-С3алкил-S(О)m-, нитрилС1-С4алкилом или С1-С3алкоксиС1-С3алкилом, при этом каждый из вышеуказанных алкилов и арилов, присоединенных к аминогруппе, необязательно замещен 1-2 заместителями, выбранными из группы, включающей галоген, C1-С6алкил, C1-С6алкоксигруппу, гидроксигруппу и моно- либо ди(С1-С3алкил)аминогруппу, С1-С6алкоксигетероарилС0-С3алкилом, гетероарилС0-С3алкилом или гетероциклС0-С3алкилом, где гетероарил и гетероцикл имеют вышеуказанные в этом абзаце значения, или Z означает разветвленный или неразветвленный С1-С6алкил, С1-С6алкоксигруппу, С1-С3ациламиногруппу, нитрилС1-С4алкил, С1-С6алкил-S(O)m и фенил-S(O)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
R1 означает
а) разветвленный или неразветвленный С1-С10алкил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей фенил, нафтил и гетероциклические группы, выбранные из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, при этом каждая из указанных фенильных, нафтильных или гетероциклических групп, которые выбраны из вышеуказанного ряда, замещена 0-5 заместителями, выбранными из группы, включающей галоген, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, С3-С8циклоалкил, С5-С8циклоалкенил, гидроксигруппу, нитрил, С1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, группу NH2C(O) и ди(С1-3)алкиламинокарбонил,
б) С3-С7циклоалкил, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бициклопентил, бициклогексил и бициклогептил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 C1-С3алкильными группами, или аналог подобной циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы заменены на группы, независимо друг от друга выбранные из ряда, включающего О, S, СНОН, >С=O, >C=S и NH,
в) разветвленный С3-С10алкенил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный C1-С5алкил, фенил, нафтил и гетероциклические группы, где каждая такая гетероцикличесая группа независимо выбрана из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, а каждая из таких фенильных, нафтильных или гетероциклических групп замещена 0-5 заместителями, выбранными из группы, включающей галоген, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропил, циклобутил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, гидроксигруппу, нитрил, C1-C3алкоксигруппу, которая необязательно частично или полностью галогенирована, группу NH2C(O) и моно- либо ди(С1-С3)алкиламинокарбонил,
г) C5-С7циклоалкенил, выбранный из группы, включающей циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил и бициклогептенил, при этом каждая такая циклоалкенильная группа необязательно замещена 1-3 C1-С3алкильными группами,
д) нитрил или
е) разветвленный или неразветвленный С1-С6алкоксикарбонил, разветвленный или неразветвленный С1-С6алкиламинокарбонил, разветвленный или неразветвленный С1-С6алкилкарбониламино-С1-С3алкил,
R2 означает разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован и необязательно замещен нитрилом,
или R2 означает ацетил, ароил, разветвленную или неразветвленную С1-С4алкоксигруппу, которая необязательно частично или полностью галогенирована, галоген, метоксикарбонил или фенилсульфонил,
R3 означает
а) фенил, нафтил или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фуррит, тетрагидрофурил, изоксазолил, изотиазолил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, бензоксазолил, бензизоксазолил, бензпиразолил, бензотиофуранил, циннолинил, птериндинил, фталазинил, нафтилпиридинил, хиноксалинил, хиназолинил, пуринил и индазолил, при этом такая фенильная, нафтильная или гетероциклическая группа необязательно замещена 1-5 заместителями, выбранными из группы, включающей фенил, нафтил, гетероцикл, выбранный из описанного выше в этом абзаце ряда, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропил, циклобутил, циклопептил, циклогексил, циклогептил, бициклопентил, бициклогексил, бициклогептил, фенил-С1-С5алкил, нафтил-С1-С5алкил, галоген, гидроксигругтпу, оксогруппу, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, С1-С3алкоксиС1-С5алкил, C1-С3тиоалкил, С1-С3тиоалкилС1-С5алкил, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу, в которой гетероциклический фрагмент выбран из описанного выше в этом абзаце ряда, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, в которой гетероциклильный фрагмент выбран из описанного выше в этом абзаце ряда, группу NH2C(O), моно- либо ди(С1-С3)алкиламинокарбонил, С1-С5алкил-С(О)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, группу амино-S(O)2, группу ди(С1-С3)алкиламино-S(O)2, R4-С1-С5алкил, R5-C1-С5алкоксигруппу, R6-С(O)-С1-С5алкил, группу R7-С1-С5алкил(R8)N и карбокси-моно- либо ди(С1-С5)алкиламиногруппу,
б) конденсированный арил, выбранный из группы, включающей бензоциклобутанил, инданил, инденил, дигидронафтил, тетрагидронафтил, бензоциклогептанил и бензоциклогептенил, или конденсированный гетероциклил, выбранный из группы, включающей циклопентенопиридин, циклогексанопиридин, циклопентанопиримидин, циклогексанопиримидин, циклопентанопиразин, циклогексанопиразин, циклопентанопиридазин, циклогексанопиридазин, циклопентанохинолин, циклогексанохинолин, циклопентаноизохинолин, циклогексаноизохинолин, циклопентаноиндол, циклогексаноиндол, циклопентанобензимидазол, циклогексанобензимидазол, циклопентанобензоксазол, циклогексанобензоксазол, циклопентаноимидазол, циклогексаноимидазол, циклопентанотиофен и циклогексанотиофен, при этом указанные конденсированное арильное или конденсированное гетероциклильное кольца замещены 0-3 заместителями, независимо друг от друга выбранными из группы, включающей фенил, нафтил и гетероциклил, выбранный из группы, включающей пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, галоген, нитрил, C1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероциклилоксигруппу, в которой гетероциклильный фрагмент выбран из описанного выше ряда, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, в которой гетероциклильный фрагмент выбран из описанного выше ряда, группу NH2C(O), моно- либо ди(С1-С3)алкиламинокарбонил, группу С1-С4алкил-ОС(О), разветвленный или неразветвленный С1-С5алкил-С(O)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, R9-С1-С5алкил, R10-С1-С5алкоксигруппу, R11-C(O)-C1-С5алкил и группу R12-С1-С5алкил(R13)N,
в) циклоалкил, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бициклопентил, бициклогексил и бициклогептил, при этом такой циклоалкил необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами,
г) С5-С7циклоалкенил, выбранный из группы, включающей циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил и бициклогептенил, при этом такая циклоалкенильная группа необязательно замещена 1-3 C1-C3алкильными группами,
д) ацетил, ароил, С1-С6алкоксикарбонилС1-С6алкил или фенилсульфонил или
e) разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, или
R1 и R2 вместе необязательно образуют конденсированное фенильное или пиридинильное кольцо,
R8 и R13 каждый независимо друг от друга выбран из группы, включающей водород и разветвленный или неразветвленный C1-С4алкил, который необязательно частично или полностью галогенирован,
R4, R5, R6, R7, R9, R10, R11 и R12 каждый независимо друг от друга выбран из группы, включающей морфолин, пиперидин, пиперазин, имидазол и тетразол,
m означает 0, 1 или 2,
W означает О или S,
при этом Х непосредственно присоединен к одной или двум группам -Y-Z, и их фармацевтически приемлемые производные.
Согласно одному из вариантов осуществления изобретения предпочтительны соединения формулы (Iа), в которых Ar2 означает нафтил, тетрагидронафтил, инданил или инденил, а W означает О.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых
Ar1 означает тиофен или пиразол, каждый из которых независимо друг от друга замещен 1-3 группами R1, R2 или R3,
X означает
- С5-С7циклоалкил или циклоалкенил, необязательно замещенный 1-2 оксогруппами или 1-3 С1-С4алкильными, С1-С4алкокси- или С1-С4алкиламиноцепями, каждая из которых является разветвленной или неразветвленной,
- фенил, инданил, фуранил, тиенил, имидазолил, пиридинил, пиразинил, тетрагидрапиридинил, пиримидинил, пиридинонил, пиперидинил, бензимидазол или пиперазинил, каждый из которых независимо друг от друга необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, С1-С4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппуу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу C1-С6алкил-S(O)m и галоген,
Y означает связь или насыщенную либо ненасыщенную разветвленную или неразветвленную С1-С4-углеродную цепь, которая необязательно частично или полностью галогенирована, при этом один или более С-атомов необязательно заменены на О или N, а Y в каждом случае независимо необязательно замещен 1-2 оксогруппами, нитрилом, фенилом, гидроксигруппой или одной или более С1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена,
Z означает
- фенил, гетероарил, выбранный из пиридинила, имидазолила, фуранила и тиенила, гетероцикл, выбранный из пиперазинила, 2-окса-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетрагидрофуранила, морфолиногруппы, тиоморфолиногруппы и пиперидинила,
при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, C1-С3алкокси-С1-С3алкил, C1-С6алкоксикарбонил, ароил, морфолинокарбонил, С1-С3ацил, оксогруппу, гидроксигруппу, пиридинил-С1-С3алкил, имидазолил-С1-С3алкил, тетрагидрофуранил-С1-С3алкил, нитрил-C1-С3алкил, нитрил, карбоксигруппу, фенил, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу амино-S(O)m, группу С1-С6алкил-S(O)m и группу фенил-S(O)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
или Z необязательно замещен 1-3 заместителями, выбранными из группы, включающей аминогруппу, аминокарбонил и амино-С1-С3алкил, где N-атом в каждом случае независимо необязательно моно- либо дизамещен аминоС1-С6алкилом, С1-С3алкилом, арилС0-С3алкилом, C1-С5алкоксиС1-С3алкилом, С1-С5алкоксигруппой, ароилом, С1-С3ацилом, группой С1-С3алкил-S(O)m- или группой арилС0-С3алкил-S(О)m-, при этом каждый из указанных алкилов и арилов, присоединенных к аминогруппе, необязательно замещен 1-2 заместителями, выбранными из группы, включающей галоген, С1-С6алкил и C1-С6алкоксигруппу,
или Z необязательно замещен 1-3 арильными, гетероциклическими или гетероарильными группами, как это указано выше в этом абзаце, каждая из которых в свою очередь необязательно замещена галогеном, C1-С6алкилом или С1-С6алкоксигруппой,
или Z означает гидроксигруппу, гидроксиС1-С3алкил, галоген, нитрил, аминогруппу, где N-атом в каждом случае независимо необязательно моно- либо дизамещен ароилом, С1-С3ацилом, C1-С6алкилом, С1-С5алкоксиС1-С3алкилом, ниридинилС1-С3алкилом, тетрагидрафуранилС1-С3алкилом, нитрилС1-С4алкилом или фенилом, при этом фенильное кольцо необязательно замещено 1-2 заместителями, выбранными из группы, включающей галоген, С1-С6алкоксигруппу, гидроксигруппу и моно- либо ди(С1-С3алкил)аминогруппу,
или Z означает разветвленный или неразветвленный C1-С6алкил, С1-С6алкоксигруппу или нитрилС1-С4алкил,
R1 означает
- разветвленный либо неразветвленный необязательно частично или полностью галогенированный С1-С4алкил,
- циклопропил, циклобутил, циклопентил, циклогексил и циклогептил, которые необязательно частично или полностью галогенированы и необязательно замещены 1-3 C1-С3алкилъными группами, или аналог такой циклоалкильной группы, в которой 1-3 кольцевые метиленовые группы заменены на группы, независимо друг от друга выбранные из О, S и NH,
- разветвленный С3-С10алкенил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 разветвленными или неразветвленными C1-С5алкильными группами,
- циклопентенил и циклогексенил, необязательно замещенный 1-3 C1-С3алкильными группами,
R2 означает разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован и необязательно замещен нитрилом,
R3 означает
- фенилльную или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил, пиразинил, пиридазинил и пиразолил, при этом такая фенильная или гетероциклическая группа необязательно замещена 1-5 заместителями, выбранными из группы, включающей фенил, гетероцикл, выбранный из описанного выше в этом абзаце ряда, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бициклопентил, бициклогексил, бициклогептил, фенил-С1-С5алкил, нафтил-С1-С5алкил, галоген, гидроксигруппу, оксогруппу, нитрил, C1-C3алкоксигруппу, которая необязательно частично или полностью галогенирована, С1-С3алкоксиС1-С5алкил, С1-С3тиоалкил, С1-С3тиоалкилС1-С5алкил, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу, в которой гетероциклический фрагмент выбран из описанного выше в этом абзаце ряда, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, в которой гетероциклильный фрагмент выбран из описанного выше в этом абзаце ряда, группу NH2C(O), моно- либо ди(С1-С3)алкиламинокарбонил, С1-С5алкил-С(О)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, группу aмино-S(O)2, группу ди(С1-С3)алкиламино-S(О)2, R4-С1-С5алкил, R5-С1-С5алкоксигруппу, R6-C(O)-C1-С5алкил, группу R7-C1-C5алкил(R8)N и карбокси- моно- либо ди(С1-С5)-алкиламиногруппу,
- конденсированный арил, выбранный из группы, включающей бензоциклобутанил, инданил, инденил, при этом такой конденсированный арил замещен 0-3 заместителями, независимо друг от друга выбранными из группы, включающей фенил, нафтил и гетероциклил, выбранный из пиридинила, пиримидинила, пиразинила, пиридазииила, пирролила, имидазолила, пиразолила, тиенила, фурила, изоксазолила и изотиазолила, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, галоген, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероциклилоксигруппу, в которой гетероциклильный фрагмент выбран из описанной выше в этом абзаце группы, нитрогруппу, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, фениламиногруппу, нафтиламиногруппу, гетероциклиламиногруппу, в которой гетероциклильный фрагмент выбран из описанной выше в этом абзаце группы, группу NH2C(O), а моно- либо ди(С1-С3)алкиламинокарбонил, группу С1-С4алкил-ОС(O), разветвленный или неразветвленный С1-С5алкил-С(O)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, R9-C1-С5алкил, R10-C1-C5алкоксигруппу, R11-С(O0)-С1-С5алкил и группу R12-С1-С5алкил(R13)N,
- циклоалкил, выбранный из группы, включающей циклопропил, циклобутил, циклопентил, циклогексил и циклогептил, при этом такой циклоалкил необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами,
- С1-С6алкоксикарбонилС1-С6алкил, или
R1 и R2 вместе необязательно образуют конденсированное фенильное или пиридинильное кольцо,
R8 и R13 каждый независимо друг от друга выбран из группы, включающей водород и разветвленный или неразветвленный С1-С4алкил, который необязательно частично или полностью галогенирован,
R4, R5, R6, R7, R9, R10, R11 и R12 каждый независимо друг от друга выбран из группы, включающей морфолин, пиперидин, пиперазин, имидазол и тетразол,
при этом Х непосредственно присоединен к одной группе -Y-Z.
В следующем варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых Ar1 означает пиразол,
Х означает
- циклопентенил, циклогексенил, циклогептенил, необязательно замещенные оксогруппой или 1-3 С1-С4алкильными, С1-С4алкокси- или С1-С4алкиламиноцепями, каждая из которых является разветвленной или неразветвленной,
- фенил, фуранил, тиенил, пиридинил, пиразинил, пиперидинил или пиримидинил, каждый из которых независимо необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С2алкил, С1-С2алкоксигруппу, гидроксигруппу и галоген,
Z означает
фенил, гетероарил, выбранный из пиридинила, имидазолила и фуранила, гетероцикл, выбранный из 2-окса-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетрагидрофуранила, тетрагидропиранила, пиперазинила, морфолиногруппы, тиоморфолиногруппы, тиоморфолиносульфоксида и пиперидинила,
при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, C1-С3алкокси-С1-С3алкил, С1-С6алкоксикарбонил, ароил, морфолинокарбонил, С1-С3ацил, оксогруппу, гидроксигруппу, пиридинил-С1-С3алкил, имидазолил-С1-С3алкил, тетрагидрофуранил-С1-С3алкил, нитрил-С1-С3алкил, нитрил, карбоксигруппу, фенил, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу амино-S(O)m, группу С1-С6алкил-S(O)m, и группу фенил-S(О)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, или Z необязательно замещен 1-3 аминогруппами, аминокарбонильными группами или амино-С1-С3алкильными группами, где N-атом необязательно в каждом случае независимо моно- либо дизамещен аминоС1-С6алкилом, С1-С3алкилом, арилС0-С3алкилом, C1-С5алкоксиС1-С3алкилом, С1-С5алкоксигруппой, ароилом, C1-С3ацилом, группой С1-С3алкил-S(O)m-, пиридинилС0-С3алкилом, тетрагидрафуранилС0-С3алкилом или группой арилС0-С3алкил-S(O)m-, при этом каждый из вышеуказанных алкилов и арилов, присодиненных к аминогруппе,
необязательно замещен 1-2 атомами галогена, С1-С6алкильными группами или С1-С6алкоксигруппами,
или Z означает гидроксигруппу, гидроксиС1-С3алкил, галоген, нитрил, аминогруппу, где N-атом необязательно в каждом случае независимо моно- либо дизамещен С1-С6алкилом, пиридинилС0-С3алкилом, тетрагидрафуранилС0-С3алкилом, С1-С5алкоксиС1-С3алкилом, C1-C3ацилом, нитрилС1-С4алкилом или фенилом, при этом фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил) аминогруппами,
или Z означает разветвленный или неразветвленный С1-С6алкил, C1-C6алкоксигруппу или нитрилС1-С4алкил,
R1 означает
- разветвленный или неразветвленный С1-С4алкил, который необязательно частично или полностью галогенирован,
- циклопропил, циклобутил, циклопентанил, циклогексанил и циклогептанил, которые необязательно частично или полностью галогенированы и необязательно замещены 1-3 С1-С3алкильными группами, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы заменены на группы, независимо выбранные из О, S и NH,
- разветвленный С3-С10алкенил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 разветвленными или неразветвленными С1-С3алкильными группами,
- циклопентенил и циклогексенил, необязательно замещенные 1-3 С1-С3алкильными группами,
R2 означает разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован и необязательно замещен нитрилом,
R3 означает
- фенильную или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил, пиридазинил и пиразолил, при этом такая фенильная или гетероциклическая группа необязательно замещена 1-5 заместителями, выбранными из ряда, включающего фенил, гетероцикл, выбранный из описанной выше в этом абзаце группы, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, фенил-С1-С5алкил, галоген, гидроксигруппу, оксогруппу, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, С1-С3тиоалкил, С1-С3тиоалкилС1-С5алкил, аминогруппу, моно- либо ди(С1-С3)алкиламиногруппу, группу NH2C(O) или моно- либо ди(С1-С3)алкиламинокарбонил,
- С1-С6алкоксикарбонилС1-С6алкил,
или R3 означает циклопропил или циклопентил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами, или
R1 и R2 вместе необязательно образуют конденсированное фенильное или пиридинильное кольцо.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых
Y означает -CH2-, -О-(СН2)0-3-, -CH2CH2-, -CH2NH-, -CH2CH2-NH-, NH-CH2CH2-, -CH2-NH-CH2-, -NH-, -NH-C(O)-, -C(O)-, -CH(OH)-, -CH2(CH2CH3)- или связь,
X означает
- циклогексенил, необязательно замещенный оксогруппой или 1-3 С1-С4алкильными, С1-С4алкокси- или C1-С4алкиламиноцепями, каждая из которых является разветвленной или неразветвленной,
- фенил, пиридинил, пиразинил, пиперидинил или пиримидинил, каждый из которых необязательно независимо замещен 1-3 заместителями, выбранными из группы, включающей С1-С2алкил, С1-С2алкоксигруппу, гидроксигруппу и галоген,
Z означает
- фенил, гетероарил, выбранный из пиридинила, имидазолила и фуранила, гетероцикл, выбранный из 2-окса-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетрагидрофуранила, тетрагидроттиранила, пиперазинила, морфолиногруппы, тиоморфолиногруппы, тиоморфолиносульфоксида и ниперидинила, при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, C1-С3алкокси-С1-С3алкил, С1-С6алкоксикарбонил, ароил, морфолинокарбонил, C1-С3ацил, оксогруппу, гидроксигруппу, пиридинил-С1-С3алкил, имидазолил-С1-С3алкил, тетрагидрофуранил-С1-С3алкил, нитрил-С1-С3алкил, нитрил, карбоксигруппу, фенил, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу амино-S(O)m, группу С1-С6алкил-S(O)m и группу фенил-S(O)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил) аминогруппами, или Z необязательно замещен 1-3 аминогруппами или аминокарбонильными группами, где N-атом необязательно в каждом случае независимо моно- либо дизамещен аминоС1-С6алкилом, C1-С3алкилом, арилС0-С3алкилом, C1-С5алкоксиС1-С3алкилом, C1-C5алкоксигруппой, ароилом, С1-С3ацилом, группой С1-С3алкил-S(O)m- или группой арилС1-С3алкил-S(O)m-, при этом каждый из вышеуказанных алкилов и арилов, присоединенных к аминогруппе, необязательно замещен 1-2 атомами галогена, С1-С6алкильными группами или С1-С6алкоксигруппами, или Z означает гидроксигруппу, гидроксиС1-С3алкил, галоген, нитрил, аминогруппу, где N-атом необязательно в каждом случае независимо моно- либо дизамещен С1-С3алкилом, пиридинилС1-С2алкилом, тетрагидрафуранилС1-С2алкилом, С1-С3алкоксиС1-С3алкилом, С1-С3ацилом, нитрилС1-С4алкилом, фенилом, при этом фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил) аминогруппами, или Z означает разветвленный или неразветвленный C1-C6алкил, C1-С6алкоксигруппу или нитрилС1-С4алкил,
R1 означает разветвленный или неразветвленный С1-С4алкил, который необязательно частично или полностью галогенирован,
R2 означает разветвленный или неразветвленный С1-С3алкил, который необязательно частично или полностью галогенирован и необязательно замещен нитрилом,
R3 означает
- фенильную или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил и пиразолил, при этом такая фенильная или гетероциклическая группа необязательно замещена 1-5 заместителями, выбранными из ряда, включающего разветвленный или неразветвленный С1-С3алкил, который необязательно частично или полностью галогенирован, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, С1-С3тиоалкил, С1-С3тиоалкилС1-С5алкил, аминогруппу или группу NH2C(O),
- С1-С3алкоксикарбонил, или R3 означает циклопропил или циклопентил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами.
В соответствии еще с одним вариантом осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых
Ar1 означает 5-трет-бутилпиразол-3-ил, где пиразольное кольцо в каждом случае независимо замещено 1-2 группами R2 или R3,
Х означает
- циклогексенил,
- фенил, пиридинил, пиразинил, пиперидинил или пиримидинил, каждый из которых необязательно независимо замещен C1-С2алкоксигруппой или гидроксигруппой,
Z означает
фенил, гетероарил, выбранный из пиридинила и фуранила, гетероцикл, выбранный из 2-окса-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, тетрагидрофуранила, пиперазинила, морфолиногруппы, тиоморфолиногруппы и пиперидинила, при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, С1-С3алкоксигруппу, оксогруппу, гидроксигруппу и группу NH2C(O)-,
или Z означает гидрокси-С1-С3алкил, аминогруппу, где N-атом необязательно в каждом случае независимо моно- либо дизамещен пиридинилметилом, тетрагидрафуранилметилом, С1-С3алкокси-С1-С3алкилом, С1-С3ацилом или нитрил-С1-С4алкилом,
или Z означает нитрилС1-С4алкил,
R3 означает
- фенил или гетероциклическую группу, выбранную из ряда, включающего пиридинил, пиримидинил и пиразолил, при этом такая фенильная или гетероциклическая группа необязательно замещена 1-2 заместителями, выбранными из группы, включающей C1-С2алкил, который необязательно частично или полностью галогенирован, С1-С2алкоксигруппу, которая необязательно частично или полностью галогенирована, С1-С2тиоалкил, C1-С2тиоалкил-С1-С3алкил, аминогруппу и группу NH2C(O),
- С1-С3алкоксикарбонил,
или R3 означает циклопропил или циклопентил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых Х означает пиридинил.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (Ia), в которых пиридинил присоединен к Ar1 в 3-м положении пиридипила.
В качестве примеров соединений формулы (Ia) по изобретению можно назвать следующие:
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-ниразол-3-ил]-3-[3-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилфуран-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(4-морфолин-4-ил)этилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-диметиламинометилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-илметил)пиридин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-метил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)ниридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-(морфолин-4-ил)этиламино)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3,4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-метилпиперазин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(пиперидин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-(пиридин-2-ил)этиламино)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(2-(пиридин-4-ил)этиламинометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(пиридин-3-илметиламинометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3,4-диметоксифенилметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-оксо-1,6-дигидропиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)имидазол-1-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)имидазол-1-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(фуран-3-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутиламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(пиридин-3-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(4-метил-3-карбамилфенил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(имидазол-2-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-ниразол-3-ил]-3-[4-(4-(3-гидроксиморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-2-метоксиэтил-N-метиламинометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(4-гидроксиморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тетрагидрофуран-3-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-di-(2-метоксиэтил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(3-цианопропокси)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилниридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-морфолин-4-илметилпиперидин-1)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-ди(2-циaнoэтил)aминoмeтил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(1-морфолин-4-илиндан-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(фуран-2-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тиоморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3-карбоксамидоморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(2-метил-3-оксопиперазин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутилокси)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(фуран-2-илметил)-3-метоксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-карбонил)пиразин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-цианоэтил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метоксипиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-аминопиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-оксо-1,6-дигидропиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-ил-4-карбонил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(3-карбамилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(пиридин-3-илметил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(пиридин-2-илметил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(тетрагидрофуран-2-илметил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)-4-метоксипиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-морфолин-4-илпропил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(N-(3-метоксипропил)амино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метипиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(N-(3-метоксипропил)-N-метиламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1'-метил-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-бензил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-N-ди(2-цианоэтил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(4-карбамилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксо-тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1'-(3-цианопропил)-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-метансульфинилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-метансульфонилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-сульфонамидофенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-ил)карбонилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(5-(тетрагидротиопиран-4-иламино)пиразин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(метилкарбониламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-ил-4-карбонил)фенил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1'-(3-метилсульфанилпропил)-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-ил-карбонил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-илметил)пиразин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-аминопиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-метилпиперидин-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-ил-карбонил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-N,N-ди(2-метоксиэтил)аминометил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-илметил)пиразин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилтиопиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(пиридин-3-илокси)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(пиридин-3-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метоксипиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-карбамилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-аминониримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1'-метил-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-циклопропилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(пиридин-3-иламино)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(тиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-бензил-3Н-имидазо[4,5-b]пиридин-6-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(пиридин-3-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илкарбонил)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-н-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-амино-4-карбамилфенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(пиридин-3-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(гидроксипиридин-3-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевину, а также их фармацевтически приемлемые производные.
Согласно еще одному варианту осуществления изобретения в нем предлагаются также следующие соединения формулы (Iа):
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-илметил)пиридин-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-(пиридин-2-ил)этиламино)циклогексенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(пиридин-3-илметиламинометил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутиламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(4-метил-3-карбамилфенил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3-гидроксипиперидин-1-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(4-гидроксиморфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)циклогексенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тетрагидрофуран-3-илметил)-3-гидроксифенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-ди(2-метоксиэтил)аминометил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(3-цианопропокси)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-морфолин-4-илметилпиперидину1)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-ди(2-цианоэтил)аминометил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(фуран-2-илметил)-3-гидроксифенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тиоморфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3-карбоксамидопиперидин-1-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(2-метил-3-оксопиперазин-1-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутилокси)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-цианоэтил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метоксипиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-аминопиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-ил-4-карбонил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(пиридин-3-илметил)аминометил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(тетрагидрофуран-2-илметил)аминометил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)-4-метоксипиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-морфолин-4-илпропил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-1'-метил-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксо-тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(5-(тетрагидротиопиран-4-иламино)пиразин-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(метилкарбониламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-1'-(3-метилсульфанилпропил)-1'Н-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2H-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилтиопиримидин-5-ил)-2H-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-аминопиримидин-5-ил)-2H-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-1'-метил-1'H-[1,4']бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксо-тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(тиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-ил-карбонил)пиримидин-5-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевина
и их фармацевтически приемлемые производные.
В соответствии с третьим объектом изобретения в нем предлагаются далее соединения формулы (II):
в которой G означает
- ароматический С6-С10карбоцикл или насыщенный либо ненасыщенный неароматический С3-С10карбоцикл,
- 6-10-членный гетероарил, содержащий один или более гетероатомов, выбранных из О, N и S,
- 5-8-членный моноциклический гетероцикл, содержащий один или несколько гетероатомов, выбранных из О, N и S, или
- 8-11-членный бициклический гетероцикл, содержащий один или несколько гетероатомов, выбранных из О, N и S,
при этом G замещен одной или несколькими группами R1, R2 или R3,
Ar означает фенил, нафтил, хинолинил, изохинолинил, тетрагидронафтил, тетрагидрохинолинил, тетрагидроизохинолинил, бензимидазолил, бензофуранил, дигидробензофуранил, индолинил, бензотиенил, дигидробензотиенил, инданил, инденил или индолил, каждый из которых необязательно замещен одной или несколькими группами R4 или R5,
Х означает
- С5-С8 циклоалкил или циклоалкенил, необязательно замещенные 1-2 оксогруппами или 1-3 С1-C4алкильными, С1-С4алкокси- или С1-С4алкиламиноцепями,
- фенил, фуранил, тиенил, пирролил, пиразолил, имидазолил, пиридинил, пиримидинил, пиридинонил, дигидропиридинонил, малеимидил, дигидромалеимидил, пиперидинил, бензимидазол, 3Н-имидазо[4,5-b]пиридин, пиперазинил, пиридазинил или пиразинил,
Y означает связь или насыщенную либо ненасыщенную разветвленную или неразветвленную С1-C4-углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, N или S(O)m, a Y необязательно независимо замещен 1-2 оксогруппами, фенилом или одной или несколькими С1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена,
Z означает
- фенил, пиридинил, пиримидинил, пиридазинил, пиразинил, имидазолил, пиразолил, триазолил, тетразолил, фуранил, тиенил, пиранил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, гидроксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, группу С1-С6алкил-S(O)m, группу CN, группу CONH2, группу COOH и фениламиногруппу, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С4алкильными группами или С1-С6алкоксигруппами,
- тетрагидропиранил, тетрагидрофуранил, 1,3-диоксоланонил, 1,3-диоксанонил, 1,4-диоксанил, морфолинил, тиоморфолинил, тиоморфолиносульфоксидил, тиоморфолиносульфонил, пиперидинил, пиперидинонил, пиперазинил, тетрагидропиримидонил, циклогексанонил, циклогексанолил, пентаметиленсульфидил, пентаметиленсульфоксидил, пентаметиленсульфонил, тетраметиленсульфид, тетраметиленсульфоксидил или тетраметиленсульфонил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей нитрил, C1-С6алкил, С1-С6алкоксигруппу, гидроксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)амино-С1-С3алкил, группу CONH2, фениламино-С1-С3алкил и С1-С3алкокси-С1-С3алкил,
- галоген, С1-С4алкил, нитрил, аминогруппу, гидроксигруппу, С1-С6алкоксигруппу, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, моно- либо ди(С1-С3алкил)аминогруппу, вторичный или третичный амин, при этом аминный азот ковалентно связан с С1-С3алкилом или С1-С5алкоксиалкилом, пиридинил-C1-С3алкил, имидазолил-С1-С3алкил, тетрагидрофуранил-С1-С3алкил, нитрил-С1-С3алкил, карбоксамид-С1-С3алкил, фенил, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу С1-С6алкил-S(O)m или группу фенил-S(О)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
- С1-С6алкил-S(О)m и фенил-S(O)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
R1 в каждом случае независимо означает
- С1-С10алкил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей С3-С10циклоалканил, гидроксигруппу, фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиснил, фурил, изоксазолил и изотиазолил, при этом каждый из вышеуказанных заместителей необязательно замещен 1-5 заместителями, выбранными из галогена, С1-С6алкила, который необязательно частично или полностью галогенирован, С3-С8циклоалканила, С5-С8циклоалкенила, гидроксигруппы, нитрила, С1-С3алкоксигруппы, которая необязательно частично или полностью галогенирована, группы NH2C(O), моно- либо ди(С1-С3алкил)аминогруппы и моно- либо ди(С1-С3алкил)аминокарбонила,
- циклопропилоксигруппу, циклобутилоксигруппу, циклопентилоксигруппу, циклогексилоксигруппу или циклогептилоксигруппу, каждая из которых необязательно частично или полностью галогенирована и необязательно замещена 1-3 заместителями, выбранными из группы, включающей C1-С3алкил, который необязательно частично или полностью галогенирован, группу CN, гидроксиС1-С3алкил и арил или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S(O)m, CHOH, >C=O, >C=S или NH,
- фенилоксигруппу или бензилоксигруппу, каждая из которых необязательно частично или полностью галогенирована и необязательно замещена 1-3 заместителями, выбранными из группы, включающей С1-C3алкил, который необязательно частично или полностью галогенирован, группу CN, гидроксиС1-С3алкил и арил, или аналог такой циклоарильной группы, в котором 1-2 кольцевые метиленовые группы независимо заменены на N,
- циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил или бициклогептанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, группу CN, гидроксиС1-C3алкил и арил, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S(O)m, СHОН, >С=O, >C=S или NH,
- разветвленный или неразветвленный С3-С10алкенил, который в каждом случае необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный С1-С5алкил, фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, при этом каждый из указанных заместителей замещен 1-5 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил и бициклогептанил, гидроксигруппу, нитрил, C1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, группу NH2C(O) и моно- либо ди(С1-алкилС3аминокарбонил, при этом такой разветвленный или неразветвленный С3-С10алкенил необязательно прерван одним или несколькими гетероатомами, выбранными из О, N и S(O)m,
- циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил или бициклогептенил, при этом такая циклоалкенильная группа необязательно замещена 1-3 C1-С3алкильными группами,
- нитрил, галоген,
- метоксикарбонил, этоксикарбонил и пропоксикарбонил,
- силил, содержащий три С1-С4алкильные группы, которые необязательно частично или полностью галогенированы,
- С3-С6алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH или S(O)m, а указанная алкинильная группа необязательно независимо замещена 1-2 оксогруппами, пирролидинилом, пирролилом, одной или несколькими С1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена, нитрилом, морфолиногруппой, пинеридинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или моно- либо ди(С1-С3алкил)аминогруппой, необязательно замещенной одним или несколькими атомами галогена,
R2, R4 и R5 каждый означает
- разветвленный или неразветвленный C1-C6алкил, который необязательно частично или полностью галогенирован, ацетил, ароил, разветвленную или неразветвленную С1-С4алкоксигруппу, которая в каждом случае необязательно частично или полностью галогенирована, галоген, метоксикарбонил, группу C1-C3алкил-S(O)m, которая необязательно частично или полностью галогенирована, или фенилсульфонил,
- С1-С6алкоксигруппу, гидроксигруппу, аминогруппу, моно- либо ди(С1-С4алкил)аминогруппу, нитрил или галоген,
- группу OR6,
- нитрогруппу или
- группу моно- либо ди(С1-С4алкил)амино-S(O)2, которая необязательно частично или полностью галогенирована, или группу H2NSO2,
R3 в каждом случае независимо означает
- фенил, нафтил, морфолинил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, пирролидинил, имидазолил, пиразолил, тиазолил, оксазолил, триазолил, тетразолил, тиенил, фурил, тетрагидрофурил, изоксазолил, изотиазолил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, бензоксазолил, бензизоксазолил, бензпиразолил, бензотиофуранил, циннолинил, птериндинил, фталазинил, нафтилпиридинил, хиноксалинил, хиназолинил, пуринил или индазолил, при этом каждый из вышеуказанных радикалов необязательно замещен 1-3 заместителями, выбранными из группы, включающей фенил, нафтил, гетероцикл либо гетероарил, которые описаны выше в этом абзаце, разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, фенил-С1-С5алкил, нафтил-C1-С5алкил, галоген, гидроксигруппу, оксогруппу, нитрил, С1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу и гетероциклоксигруппу, где гетероциклический либо гетероарильный фрагмент описан выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу либо гетероцикламиногруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, C1-С5алкил-С(O)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3алкил)амино-С1-С5алкил, группу амино-S(O)2, группу ди(С1-С3алкил)амино-S(O)2, R7-С1-С5алкил, R8-С1-С5алкоксигруппу, R9-С(О)-С1-С5алкил, группу R10-C1-C5алкил(R11)N и карбокси-моно- либо ди(С1-С5алкил) аминогруппу,
- конденсированный арил, выбранный из бензоциклобутанила, инданила, инденила, дигидронафтила, тетрагидронафтила, бензоциклогептанила и бензоциклогептенила, или конденсированный гетероарил, выбранный из циклопентенопиридинила, циклогексанопиридинила, циклопентанопиримидинила, циклогексанопиримидинила, циклопентанопиразинила, циклогексанопиразинила, циклопентанопиридазинила, циклогексанопиридазинила, циклопентанохинолинила, циклогексанохинолинила, циклопентаноизохинолинила, циклогексаноизохинолинила, циклопентаноиндолила, циклогексаноиндолила, циклопентанобензимидазолила, циклогексанобензимидазолила, циклопентанобензоксазолила, циклогексанобензоксазолила, циклопентаноимидазолила, циклогексаноимидазолила, циклопентанотиенила и циклогексанотиенила, при этом конденсированное арильное или конденсированное гетероарильное кольцо независимо замещено 0-3 заместителями, выбранными из группы, включающей фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил, изотиазолил, С1-С6алкил, который необязательно частично или полностью галогенирован, галоген, нитрил, C1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу либо гетероциклоксигруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу либо гетероцикламиногруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, группу С1-С4алкил-ОС(O), С1-С5алкил-С(O)-С1-С4алкил, амино-C1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, R12-C1-С5алкил, R13-С1-С5алкоксигруппу, R14C(O)-C1-C-С5алкил и группу R15-С1-алкилС5(R16)N,
- циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил или бициклогептанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 С1-С3алкильными группами, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S, CHOH, >C=O, >C=S или NH,
- циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил или бициклогептенил, каждый из которых необязательно замещен 1-3 C1-С3алкильными группами,
- С1-С4алкилфенил-С(O)-С1-С4алкил-, С1-С4алкил-С(O)-С1-С4алкил- или С1-С4алкилфенил-S(O)m-С1-С4алкил-,
- С1-С6алкильную группу или разветвленную или неразветвленную С1-С6алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или С1-С6алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С5алкил)аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21)-, R22O-, R23R24NC(O)-, R26(CH2)mC(O)N(R21)- или R26C(O)(CH2)mN(R21)-,
- С2-С6алкенил, замещенный группой R23R24NС(O)-,
- С2-С6алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH, S(O)m, а указанная алкинильная группа необязательно независимо замещена 1-2 оксогруппами, пирролидинилом, пирролилом, морфолинилом, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом, одной или более C1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена, нитрилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолил, фенилом, пиридинилом, тетразолилом или моно- либо ди(С1-С4алкил)аминогруппой, которая может быть замещена одним или несколькими атомами галогена, или
- ароил,
R6 означает С1-С4алкил, который необязательно частично или полностью галогенирован и необязательно замещен группой R26,
R7, R8, R9, R10, R12, R13, R14, R15, R17, R19, R25, и R26 каждый независимо друг от друга означает нитрил, фенил, морфолиногруппу, пиперидинил, пиперазинил, имидазолил, пиридинил, тетразолил, аминогруппу или моно- либо ди(С1-С4алкил)аминогруппу, которая необязательно частично или полностью галогенирована,
R11 и R16 каждый независимо друг от друга означает водород или С1-С4алкил, который необязательно частично или полностью галогенирован,
R18 в каждом случае независимо означает водород или С1-С4алкил, который необязательно независимо замещен оксогруппой или группой R25,
R20 в каждом случае независимо означает C1-С10алкил, который необязательно частично или полностью галогенирован, фенил или пиридинил,
R21 в каждом случае независимо означает водород или С1-С3алкил, который необязательно частично или полностью галогенирован,
R22, R23 и R24 каждый независимо друг от друга означает водород, С1-С6алкил, который необязательно частично или полностью галогенирован, причем указанный С1-С6алкил необязательно прерван одним или несколькими атомами О, N или S, а также независимо необязательно замещен моно- либо ди(С1-С3алкил)аминокарбонилом, фенилом, пиридинилом, аминогруппой или моно- либо ди (С1-С4алкил) аминогруппой, при этом каждый из указанных заместителей необязательно частично или полностью галогенирован и необязательно замещен моно- либо ди(С1-С3алкил) аминогруппой, или
R23 и R24 вместе необязательно образуют гетероциклическое или гетероарильное кольцо,
m означает 0, 1 или 2 и
W означает О или S,
и их фармацевтически приемлемые производные.
Согласно одному из вариантов осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых
G означает
- фенил, нафтил, бензоциклобутанил, дигидронафтил, тетрагидронафтил, бензоциклогептанил, бензоциклогептенил, инданил, инденил,
- пиридинил, пиридонил, хинолинил, дигидрохинолинил, тетрагидрохиноил, изохинолинил, тетрагидроизохиноил, пиридазинил, пиримидинил, пиразинил, бензимидазолил, бензтиазолил, бензоксазолил, бензофуранил, бензотиофенил, бензпиразолил, дигидробензофуранил,
дигидробензотиофенил, бензооксазолонил, бензо[1,4]оксазин-3-онил, бензодиоксолил, бензо[1,3]диоксол-2-онил, бензофуран-3-онил, тетрагидробензопиранил, индолил, индолинил, индолонил, индолинонил, фталимидил, хромоил,
- оксетанил, пирролидинил, тетрагидрофуранил, тетрагидротиофенил, пиперидинил, пиперазинил, морфолинил, тетрагидропиранил, диоксанид, тетраметиленсульфонил, тетраметиленсульфоксидил, оксазолинил, тиазолинил, имидазолинил, тетрагидропиридинил, гомопиперидинил, пирролинил, тетрагидропиримидинил, декагидрохинолинил, декагидроизохинолинил, тиоморфолинил, тиазолидинил, дигидрооксазинил, дигидропиранил, оксоканил, гептаканил, тиоксанил либо дитианил,
при этом G замещен одной или несколькими группами R1, R2 или R3.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых
G означает фенил, пиридинил, пиридонил, нафтил, хинолинил, изохинолинил, пиразинил, бензимидазолил, бензоксазолил, бензофуранил, бензотиофенил, бензпиразолил, дигидробензофуранил, дигидробензотиофенил, инданил, инденил, индолил, индолинил, индолонил или индолинонил, при этом G замещен одной или несколькими группами R1, R2 или R3,
Ar означает нафтил, хинолинил, изохинолинил, тетрагидронафтил, тетрагидрохинолинил, тетрагидроизохинолинил, инданил, инденил или индолил, каждый из которых необязательно замещен одной или несколькими группами R4 или R5,
Х означает фенил, фуранил, тиенил, пирролил, пиразолил, имидазолил, пиридинил, пиримидинил, пиридинонил, дигидропиридинонил, малеимидил, дигидромалеимидил, пиперидинил, пиперазинил, пиридазинил или пиразинил,
Y означает связь или насыщенную или ненасыщенную С1-С4-углеродную цепь, при этом один из атомов углерода необязательно заменен на О, N или S(O)m, a Y необязательно независимо замещен 1-2 оксогруппами, фенилом или одной либо несколькими С1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена,
Z означает
- фенил, пиридинил, пиримидинил, пиридазинил, пиразинил, имидазолил, фуранил, тиенил, дигидротиазолил, дигидротиазолилсульфоксидил, пиранил, пирролидинил, которые необязательно замещены 1-3 заместителями, выбранными из группы, включающей нитрил, С1-С3алкил, C1-С3алкоксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, группу CONH2 и группу ОН,
- тетрагидропиранил, тетрагидрофуранил, 1,3-диоксоланонил, 1,3-диоксанонил, 1,4-диоксанил, морфолинил, тиоморфолинил, тиоморфолиносульфоксидил, пиперидинил, пиперидинонил, пиперазинил, тетрагидропиримидонил, пентаметиленсульфидил, пентаметиленсульфоксидил, пентаметиленсульфонил, тетраметиленсульфидил, тетраметиленсульфоксидил или тетраметиленсульфонил, которые необязательно замещены 1-3 заместителями, выбранными из группы, включающей нитрил, С1-С3алкил, C1-С3алкоксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, группу CONH2 и группу ОН,
- нитрил, С1-С6алкил-S(O)m, галоген, гидроксигруппу, С1-С4алкоксигруппу, аминогруппу, моно- либо ди(С1-С6алкил) аминогруппу, моно- либо ди(С1-С3алкил)аминокарбонил или группу NH2C(O),
R1 в каждом случае независимо означает
- C3-C6алкил, который необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей С3-С6циклоалкил, фенил, тиенил, фурил, изоксазолил и изотиазолил, где каждый из указанных заместителей необязательно замещен 1-3 заместителями, выбранными из галогена, С1-С3алкила, который необязательно частично или полностью галогенирован, гидроксигруппы, нитрила и С1-С3алкоксигруппы, которая необязательно частично или полностью галогенирована,
- циклопропил, циклобутил, циклопентанил, циклогексанил, бициклопентанил или бициклогексанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей C1-С3алкил, который необязательно частично или полностью галогенирован, группу CN, гидроксиС1-С3алкил и фенил, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S, СНОН, >С=O, >C=S или NH, или
- силил, содержащий три С1-С4алкильные группы, которые необязательно частично или полностью галогенированы,
R2 в каждом случае независимо означает галоген, C1-С3алкоксигруппу, группу С1-С3алкил-S(O)m, которая необязательно частично или полностью галогенирована, фенилсульфонил или нитрил,
R3 в каждом случае независимо означает
- фенил, морфолиногруппу, пиридинил, пиримидинил, пиразинил, пирролил, пирролидинил, имидазолил, пиразолил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы,
включающей фенил, нафтил, гетероцикл либо гетероарил, которые описаны выше в этом абзаце, С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, фенил-С1-С5алкиль, нафтил-С1-С5алкил, галоген, оксогруппуу, гидроксигруппу, нитрил, С1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу либо гетероциклоксигруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу либо гетероцикламиногруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, С1-С5алкил-С(O)-С1-С4алкил, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, группу моно- либо ди(С1-С3алкил)амино-S(O)2, R7-С1-С5алкил, R8-С1-С5алкоксигруппу, R9-С(O)-С1-С5алкил, группу R10-С1-С5алкил(R11)N и карбокси-моно- либо ди(С1-С5)-алкил-аминогруппу,
- C1-С3алкильную группу или С1-С4алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или C1-С6алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С5алкил) аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21))-, R22O-, R23R24NC(O)-, R26CH2C(O)N(R21)- или R26C(O)CH2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NC(O)-, или
- С2-С4алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована и необязательно независимо замещена 1-2 оксогруппами, пирролидинилом, пирролилом, морфолинилом, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или одной или несколькими С1-С4алкильными группами, которые необязательно замещены одним или несколькими атомами галогена, и
R23 и R24 вместе необязательно образуют имидазолильное, пиперидинильное, морфолинильное, пиперазинильное или пиридинильное кольцо.
Согласно еще одному варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых
G означает фенил, пиридинил, пиридонил, нафтил, хинолинил, изохинолинил, пиразинил, бензотиофенил, дигидробензофуранил, дигидробензотиофенил, инданил, индолил, индолинил, индолонил или индолинонил, при этом G замещен одной или несколькими группами R1, R2 или R3,
Ar означает нафтил,
Х означает фенил, имидазолил, пиридинил, пиримидинил, пиперидинил, пиперазинил, пиридазинил или пиразинил, каждый из которых необязательно независимо замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, С1-C4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу С1-С6алкил-S(O)m и галоген,
Y означает связь или насыщенную С1-С4-углеродную цепь, при этом один из атомов углерода необязательно заменен на О, N или S, а Y необязательно независимо замещен оксогруппой,
Z означает
- фенил, пиридинил, пиримидинил, пиридазинил, пиразинил, имидазолил, дигидротиазолил, дигидротиазолилсульфоксид, пиранил или пирролидинил, которые необязательно замещены 1-2 С1-С2алкильными группами или С1-С2алкоксигруппами,
- тетрагидропиранил, морфолинил, тиоморфолинил, тиоморфолиносульфоксидил, пиперидинил, пиперидипонил, пиперазинил или тетрагидропиримидонил, которые необязательно замещены 1-2 С1-С2алкильными группами или С1-С2алкоксигруппами, или
- C1-С3алкоксигруппу,
R1 в каждом случае независимо означает
- С3-С5алкил, который необязательно частично или полностью галогенирован и необязательно замещен фенилом, замещенным 0-3 заместителями, выбранными из группы, включающей галоген, C1-С3алкил, который необязательно частично или полностью галогенирован, гидроксигруппу, нитрил и C1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована,
- циклопропил, циклобутил, циклопентанил, циклогексанил, бициклопентанил или бициклогексанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей C1-C3алкил, который необязательно частично или полностью галогенирован, группу CN, гидроксиС1-С3алкил и фенил, или аналог циклопропила, циклобутила, циклопентанила, циклогексанила, бициклопентанила или бициклогексанила, где одна кольцевая метиленовая группа заменена на О, или
- силил, содержащий независимо три С1-С2алкильные группы, которые необязательно частично или полностью галогенированы,
R2 в каждом случае независимо означает бром, хлор, фтор, метоксигруппу, метилсульфонил или нитрил,
R3 в каждом случае независимо означает
- фенил, морфолиногруппу, пиридинил, пиримидинил, пирролидинил, 2,5-пирролидиндионил, имидазолил, пиразолил, при этом каждый из указанных радикалов необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, галоген, оксогруппу, гидроксигруппу, нитрил и С1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована,
- С1-С3алкильную группу или C1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или C1-С3алкильную группу, необязательно замещенную группой OR18,
- аминогруппу или моно- либо ди(С1-С3алкил)аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21)-, R22O-, R23R24NC(O)-, R26CH2C(O)N(R21)-, R26C(O)CH2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NC(O)-, или
- С2-С4алкинил, замещенный пирролидинилом или пирролилом, и R23 и R24 вместе необязательно образуют морфолиногруппу.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых
G означает фенил, пиридинил, пиридонил, нафтил, хинолинил, изохинолинил, дигидробензофуранил, инданил, индолинил, индолонил или индолинонил, при этом G замещен одной или несколькими группами R1, R2 или R3,
Ar означает 1-нафтил,
Х означает фенил, имидазолил, пиридинил, пиримидинил, пиперидинил, пиперазинил, пиридазинил или пиразинил,
Y означает связь или -СН2-, -СН2СН2-, -С(O)-, -О-, -S-, -NH-CH2CH2CH2-, -N(СН3)- либо -NH-,
R1 в каждом случае независимо означает
- С3-С5алкил, который необязательно частично или полностью галогенирован и необязательно замещен фенилом,
- циклопропил, циклопентанил, циклогексанил или бициклопентанил, необязательно замещенный 1-3 заместителями, выбранными из группы, включающей метил, который необязательно частично или полностью галогенирован, группу CN, гидроксиметил и фенил, либо 2-тетрагидрофуранил, замещенный метилом, или
- триметилсилил,
R3 в каждом случае независимо означает
- фенил, морфолинил, пиридинил, пиримидинил, пирролидинил, 2,5-пирролидиндионил, имидазолил или пиразолил, при этом каждый из указанных радикалов необязательно замещен С1-С2алкилом, который необязательно частично или полностью галогенирован,
- C1-С3алкильную группу или С1-С3алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена диэтиламиногруппой,
- OR18 или C1-С3алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С3алкил) аминогруппу, необязательно замещенную группой R19,
- СН3С(O)NН-, R22O-, R23R24NC(O)-, R26CH2C(O)N(R21)- или R26C(O)CH2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NС(O)-, или
- С2-С4алкинил, замещенный пирролидинилом или пирролилом,
R23 и R24 означают Н или R23 и R24 вместе необязательно образуют морфолиногруппу и
R26 означает морфолиногруппу.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых
G означает фенил, пиридинил или нафтил, при этом G замещен одной или несколькими группами R1, R2 или R3,
Х означает имидазолил или пиридинил,
Y означает -CH2-, -NH-CH2CH2CH2- или -NH-,
Z означает морфолиногруппу,
R1 в каждом случае независимо означает трет-бутил, втор-бутил, трет-амил или фенил,
R2 означает хлор и
R3 в каждом случае независимо означает метил, метоксигруппу, метоксиметил, гидроксипропил, ацетамид, морфолиногруппу или морфолинокарбонил.
В следующем варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых Х означает пиридинил.
В соответствии еще с одним вариантом осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (II), в которых пиридинил присоединен к Ar в 3-м положении пиридинила.
В качестве примеров соединений формулы (II) по изобретению можно назвать следующие:
1-(3-цианофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-фторфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-хлор-2-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-хлор-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3,4-диметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-иодфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил) нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-м-толил-мочевину,
1-(4-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-хлор-4-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-хлор-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,5-дихлорфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-нафталин-2-илмочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-фенилмочевину,
1-(3-хлорфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-хлор-3-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(2,4,6-трихлорфенил)мочевину,
1-(2-метил-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метил-2-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,3-дихлорфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метокси-5-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-хлор-6-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,4-дихлорфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метил-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,4-диметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,3-диметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-цианофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3,4,5-триметоксифенил)мочевину,
1-бифенил-4-ил-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,5-дифторфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-хлор-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-фтор-3-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-бензилоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-фтор-6-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-фтор-3-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(2,4,5-триметилфенил)мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-трифторметилфенил)мочевину,
1-(3-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-фтор-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метокси-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-фтор-5-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-этоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,5-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4,5-диметил-2-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-хлор-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-изопропил-6-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-дифторметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-изопропилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-этилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-этоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-бутоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
этиловый эфир 4-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-уреидо}бензойной кислоты,
1-(4-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,6-дибром-4-изопропилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-трифторметилсульфанилфенил)мочевину,
диметиловый эфир 5-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}изофталевой кислоты,
1-(3-циклопентилокси-4-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
этиловый эфир 3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензойной кислоты,
1-(5-трет-бутил-2-гидроксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-гидроксиметил-4-фенилциклогексил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метилсульфанил-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-пентилоксибифенил-3-ил)мочевину,
метиловый эфир 4-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензойной кислоты,
1-(2,5-диэтоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-бензотиазол-6-ил-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(2,5-диэтокси-4-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо]фенил)бензамид,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-феноксифенил)мочевину,
1-(5-этансульфонил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
4-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}-N-фенилбензамид,
1-(2-метил-1,3-диоксо-2,3-дигидро-1Н-изоиндол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,3-диметил-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-бутил-4-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо]бензолсульфонамид,
1-[3-(2-метил-[1,3]диоксолан-2-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-метокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,4-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метил-4-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метокси-4-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-хлор-2-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-хлор-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3,5-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-трифторметоксифенил)мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметилсульфанилфенил)мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(2-фенокси-фенил)мочевину,
1-(2-метокси-5-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-хлор-2,4-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3,5-бистрифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-трет-бутил-5-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-метилнафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метилбифенил-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-хлор-2,4-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-изопропил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-втор-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метокси-3-пропилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксиметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил)-3-(4-[6-[(3-метоксипропил)метиламино]пиридин-3-ил]нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метилфенил)-3-[4-(4-морфолин-4-илметилимидазол-1-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил)-3-{4-[6-(3-метоксипропиламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-морфолин-4-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-2-хлор-3-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметилфенил)мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-трифторметоксифенил)мочевину,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-гидроксипропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-морфолин-4-ил-3-оксопропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(морфолин-4-карбонил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид
и их фармацевтически приемлемые производные.
Помимо представленных выше в качестве примера соединений по описанным ниже общим методам синтеза могут быть получены также следующие возможные соединения формулы (II):
1-[4-(6-{[бис(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[4-(2-метил-3-оксопиперазин-1-илметил)фенил]нафталин-1-ил}мочевина,
1-[4-(6-{[бис-(2-метоксиэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксо-114-тиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-{4-[6-(1-оксо-114-тиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-[6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[4-(1-оксо-11-тиоморфолин-4-илметил)фенил]нафталин-1-ил}мочевина,
1-[4-(4-{[бис(2-цианоэтил)амино]метил}фенил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевина,
1-(2-метокси-5-пентафторэтилфенил)-3-[4-(4-морфолин-4-илметилпиперидин-1-ил)нафталин-1-ил]мочевина,
1-(2-метокси-5-трифторметилпиридин-3-ил)-3-{4-[2-(4-оксопиперидин-1-илметил)пиримидин-5-ил]нафталин-1-ил}мочевина,
1-(2-метокси-5-триметилсиланилфенил)-3-{4-[4-(тетрагидропиран-4-иламино)фенил]нафталин-1-ил}мочевина,
1-(3-метоксинафталин-2-ил)-3-[4-(4-морфолин-4-илметилпиперидин-1-ил)нафталин-1-ил]мочевина,
1-(3-метилнафталин-2-ил)-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(3-трет-бутил-5-метансульфинилфенил)-3-{4-[6-(1-метилпиперидин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(3-трет-бутилфенил)-3-[4-(3-пиридин-3-илпропокси)нафталин-1-ил]мочевина,
1-(3-трет-бутилфенил)-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(4-метоксибифенил-3-ил)-3-{4-[4-(тетрагидропиран-4-илметил)имидазол-1-ил]нафталин-1-ил}мочевина,
1-(4-метилбифенил-3-ил)-3-{4-[4-(2-пиридин-4-илэтил)пиперазин-1-ил]нафталин-1-ил}мочевина,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(пиридин-4-илметокси)нафталин-1-ил]мочевина,
1-(4-трет-бутилбифенил-2-ил)-3-{4-[2-(1-оксо-114-тиоморфолин-4-илметил)-3H-имидазол-4-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-гидроксифенил)-3-[4-(5-морфолин-4-илметилпиразин-2-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метокси-3-пропилфенил)-3-{4-[4-(пирролидин-1-карбонил)фенил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(4-тиоморфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[4-(тетрагидропиран-4-иламино)фенил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксипиридин-3-ил)-3-{4-[6-(4-оксопиперидин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метилбензоксазол-7-ил)-3-[4-(6-пиридин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-феноксифенил)-3-{4-[6-(тетрагидропиран-4-илокси)-пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-пирролидин-1-илфенил)-3-[4-(4-метокси-6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-пирролидин-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-3-циано-2-метоксифенил)-3-[4-[2-(2,6-диметилморфолин-4-илметил)пиримидин-5-ил]нафталин-1-ил]мочевина,
1-(5-трет-бутил-4'-диметиламинобифенил-3-ил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-(6-метокси-3,3-диметилиндан-5-ил)-3-{4-[4-(морфолин-4-карбонил)фенил]нафталин-1-ил}мочевина,
1-(6-трет-бутил-2-хлор-3-метилпиридин-4-ил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(6-трет-бутилбензо[1,3]диоксо1-4-ил)-3-{4-[6-(морфолин-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(7-метокси-1,4,4-триметил-1,2,3,4-тетрагидрохинолин-6-ил)-3-{4-[6-(тетрагидропиран-4-илокси)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(7-трет-бутил-2,4-диметил-бензоксазол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[2-метокси-5-(1-метил-1-фенилэтил)фенил]-3-{4-[6-(2-пиридин-4-илэтил)пиридазин-3-ил]нафталин-1-ил}мочевина,
1-[2-метокси-5-(1-метилциклогексил)фенил]-3-{4-[4-(1-метилпиперидин-4-илсульфанил)фенил]нафталин-1-ил}мочевина,
1-[2-метокси-5-(1-метилциклопропил)фенил]-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-[2-метокси-5-(2-метил-тетрагидрофуран-2-ил)фенил]-3-[4-(5-морфолин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевина,
1-[2-метокси-5-(3-трифторметилбицикло[1.1.1]пент-1-ил)фенил]-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-5-(1-метил-1Н-имидазол-4-ил)фенил]-3-[4-(5-морфолин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевина,
1-[3-трет-бутил-5-(2-пирролидин-1-илэтил)фенил]-3-{4-[6-(1-метилпиперидин-4-илокси)пиридин-3-ил]нафталин-1-ил}мочевина,
1-[3-трет-бутил-5-(3-пирролидин-1-илпроп-1-инил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[4-(6-имидазол-1-илметилпиридин-3-ил)нафталин-1-ил]-3-[2-метокси-5-(1-фенилциклопропил)фенил]мочевина,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(4-тиоморфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-[5-(1-цианоциклопропил)-2-метоксифенил]-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-[5-(1-гидроксиметилциклопропил)-2-метоксифенил]-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-1-(2-диэтиламиноэтил)-2-оксо-1,2-дигидропиридин-3-ил]-3-{4-[6-(1-метилпиперидин-4-илокси)пиридин-3-ил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(2-морфолин-4-илэтокси)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-{4-[4-(4-метилпиперазин-1-карбонил)фенил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-2-(2,5-диоксопирролидин-1-ил)фенил]-3-{4-[6-(1Н-имидазол-2-илметил)пиридин-3-ил]нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(5-пиридин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-морфолин-4-ил-2-оксоэтокси)фенил]-3-{4-[6-(2-пиридин-4-илэтил)пиридазин-3-ил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-2-(2-морфолин-4-ил-2-оксоэтиламино)фенил]-3-{4-[4-(1-метилпиперидин-4-иламино)пиперидин-1-ил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)фенил]-3-{4-[5-(2-пирролидин-1-илэтил)пиридин-2-ил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-2-метокси-3-(3-морфолин-4-ил-3-оксопропенил)фенил]-3-[4-(6-пирролидин-1-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-3-(2-диэтиламиноэтокси)-2-метоксифенил]-3-{4-[4-(тетрагидропиран-4-илокси)фенил]нафталин-1-ил}мочевина,
1-[5-трет-бутил-3-(2-пирролидин-1-илэтил)бензофуран-7-ил]-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-[6-трет-бутил-4-(2-диметиламиноэтил)-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил]-3-{4-[6-(тиоморфолин-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевина,
1-{5-трет-бутил-2-метокси-3-[2-(1-метилпиперидин-4-илокси)этил]фенил}-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
2-(4-трет-бутил-2-{3-[4-(5-пирролидин-1-илметилпиридин-2-ил)нафталин-1-ил]уреидо}фенокси)-N-метилацетамид,
2-[4-трет-бутил-2-(3-{4-[6-(2,6-диметилморфолин-4-илметил)-пиридин-3-ил]нафталин-1-ил}уреидо)фенокси]ацетамид,
3-(5-трет-бутил-2-метокси-3-{3-[4-(6-пирролидин-1-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)акриламид,
3-{3-трет-бутил-5-[3-(4-{4-[2-(1-оксо-114-тиазолидин-3-ил)этил]фенил}нафталин-1-ил)уреидо]фенил}-N,N-диметилпропионамид,
3-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}бензамид,
4-трет-бутил-2-{3-[4-(2-хлор-4-морфолин-4-илметилфенил)нафталин-1-ил]уреидо}бензамид,
N-(4-трет-бутил-2-{3-[4-(6-оксо-1,6-дигидропиридин-3-ил)нафталин-1-ил]уреидо}фенил)-2-морфолин-4-илацетамид,
N-[3-трет-бутил-5-(3-{4-[5-(тетрагидропиран-4-иламино)пиридин-2-ил]нафталин-1-ил}уреидо)фенил]-2-морфолин-4-илацетамид,
N-[4-трет-бутил-2-(3-{4-[4-(1-метилпиперидин-4-илокси)фенил]нафталин-1-ил}уреидо)фенил]ацетамид
и их фармацевтически приемлемые производные.
Согласно еще одному варианту осуществления изобретения в нем предлагаются также следующие соединения формулы (II):
1-(2-трет-бутил-5-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(3-метилнафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(3-трет-бутилфенил)-3-[4-(4-морфолин-4-илметилфенил) нафталин-1-ил]мочевина,
1-(3-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(4-метилбифенил-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-хлор-2,4-диметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-изопропил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-втор-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метокси-3-пропилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксиметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(4-тиоморфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[4-(тетрагидропиран-4-иламино)фенил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метилфенил)-3-(4-{6-[(3-метоксипропил)метиламино]пиридин-3-ил}-нафталин-1-ил)мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-(4-морфолин-4-илметилимидазол-1-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-(4-морфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-{4-[6-(3-метоксипропиламино)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-морфолин-4-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(6-трет-бутил-2-хлор-3-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(6-трет-бутил-2-хлор-3-метилпиридин-4-ил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[2-метокси-5-(1-метилциклопропил)фенил]-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметилфенил)мочевина,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(4-трифторметоксифенил)мочевина,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(4-тиоморфолин-4-илметилфенил)нафталин-1-ил]мочевина,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-(1-цианоциклопропил)-2-метоксифенил]-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(5-пиридин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(3-гидроксипропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(3-морфолин-4-ил-3-оксопропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(морфолин-4-карбонил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
2-[4-трет-бутил-2-(3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}уреидо)фенокси]ацетамид,
3-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}бензамид,
4-трет-бутил-2-{3-[4-(2-хлор-4-морфолин-4-илметилфенил)нафталин-1-ил]уреидо}бензамид
и их фармацевтически приемлемые производные.
В другом варианте осуществления изобретения в нем предлагаются далее следующие соединения формулы (II):
1-(2-трет-бутил-5-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(3-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(4-метилбифенил-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-изопропил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-втор-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксиметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилфенил)-3-(4-{6-[(3-метоксипропил)метиламино]пиридин-3-ил}нафталин-1-ил)мочевина,
1-(5-трет-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(3-гидроксипропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(морфолин-4-карбонил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид
и их фармацевтически приемлемые производные.
Четвертым объектом изобретения являются соединения формулы (III)
в которой Е означает углерод или содержащую гетероатом группу, выбранную из -О-,
-NH- и -S-,
G означает
- ароматический С6-С10карбоцикл или насыщенный или ненасыщенный неароматический C3-С10карбоцикл,
- 6-14-членный моноциклический, бициклический или трициклический гетероарил, содержащий один или несколько гетероатомов, выбранных из О, N и S,
- 6-8-членный моноциклический гетероцикл, содержащий один или несколько гетероатомов, выбранных из О, N и S, или
- 8-11-членный бициклический гетероцикл, содержащий один или несколько гетероатомов, выбранных из О, N и S,
при этом G необязательно замещен одной или несколькими группами R1, R2 или R3,
Ar означает фенил, нафтил, хинолинил, изохинолинил, тетрагидронафтил, тетрагидрохинолинил, тетрагидроизохинолинил, бензимидазолил, бензофуранил, дигидробензофуранил, индолинил, бензотиенил, дигидробензотиенил, инданил, инденил или индолил, каждый из которых необязательно замещен одной или несколькими группами R4 или R5,
Х означает
- С5-С8циклоалкил или циклоалкенил, необязательно замещенный 1-2 оксогруппами или 1-3 С1-С4алкильными, C1-С4алкокси- или C1-С4алкиламиноцепями, каждая из которых является разветвленной или неразветвленной,
- арил, фуранил, тиенил, пирролил, пиразолил, имидазолил, пиридинил, пиримидинил, пиридинонил, дигидропиридинонил, малеимидил, дигидромалеимидил, пиперидинил, бензимидазол, 3Н-имидазо[4,5-b]пиридин, пиперазинил, пиридазинил или пиразинил, каждый из которых необязательно независимо замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, С1-С4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу С1-С6алкил-S(O)m и галоген,
Y означает связь или насыщенную либо ненасыщенную разветвленную или неразветвленную C1-С4-углеродную цепь, которая необязательно частично или полностью галогенирована, при этом один или несколько С-атомов необязательно заменены на О, N или S(O)m, a Y необязательно независимо замещен 1-2 оксогруппами, нитрилом, фенилом или одной или несколькими C1-С4алкильными группами, которые необязательно замещены одним или несколькими атомами галогена,
Z означает
арил, гетероарил, выбранный из пиридинила, пиперазинила, пиримидинила, пиридазинила, пиразинила, имидазолила, пиразолила, триазолила, тетразолила, фуранила, тиенила и пиранила, гетероцикл, выбранный из тетрагидропиримидонила, циклогексанонила, циклогексанолила, 2-окса- или 2-тиа-5-азабицикло[2.2.1]гептанила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетраметиленсульфидила, тетраметиленсульфоксидила либо тетраметиленсульфонила, тетрагидропиранила, тетрагидрофуранила, 1,3-диоксоланонила, 1,3-диоксанонила, 1,4-диоксанила, морфолиногруппы, тиоморфолиногруппы, тиоморфолиносульфоксидила, тиоморфолиносульфонила, пиперидинила, пиперидинонила, пирролидинила и диоксоланила,
при этом каждая из вышеуказанных в качестве значений Z групп необязательно замещена 1-3 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, С1-С6алкоксигруппу, C1-С3алкокси-C1-С3алкил, C1-С6алкоксикарбонил, ароил, С1-С3ацил, оксогруппу, гидроксигруппу, пиридинил-С1-С3алкил, имидазолил-С1-С3алкил, тетрагидрофуранил-С1-С3алкил, нитрил -С1-С3алкил, нитрил, карбоксигруппу, фенил, где фенильное кольцо необязательно замещено 1-2 атомами галогена, С1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами, группу С1-С6алкил-S(O)m и группу фенил-S(О)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил) аминогруппами,
или Z необязательно замещен 1-3 аминогруппами или амино-С1-С3алкильными группами, при этом N-атом необязательно независимо моно- либо дизамещен аминоС1-С6алкилом, C1-С3алкилом, арилС0-С3алкилом, C1-С5алкоксиС1-С3алкилом, C1-С5алкоксигруппой, ароилом, C1-С3ацилом, группой С1-алкил-С3(О)m- или группой арилС0-С3алкил-S(О)m-, при этом каждый из указанных алкилов и арилов, присоединенных к аминогруппе, необязательно замещен 1-2 атомами галогена, С1-С6алкильными группами или C1-С6алкоксигруппами, или Z необязательно замещен 1-3 арильными группами, гетероциклическими или гетероарильными группами, которые описаны выше в этом абзаце, при этом каждая из указанных групп в свою очередь необязательно замещена галогеном, С1-С6алкилом или C1-С6алкоксигруппой,
или Z означает гидроксигруппу, галоген, нитрил, аминогруппу, где N-атом необязательно независимо моно- либо дизамещен С1-С3ацилом, C1-С6алкилом или С1-С3алкоксиС1-С3алкилом, разветвленный или неразветвленный С1-С3алкил, С1-С6алкоксигруппу, С1-С3ациламиногруппу, нитрилС1-С4алкил, группу С1-С6алкил-S(O)m или группу фенил-S(О)m, где фенильное кольцо необязательно замещено 1-2 атомами галогена, C1-С6алкоксигруппами, гидроксигруппами или моно- либо ди(С1-С3алкил)аминогруппами,
R1 в каждом случае независимо означает
разветвленный или неразветвленный C1-С10алкил, который необязательно частично или полностью галогенирован, при этом один или несколько С-атомов необязательно независимо заменены на О, N или S(O)m, a указанный С1-С10алкил необязательно замещен 1-3 заместителями, выбранными из группы, включающей С3-С10циклоалкил, гидроксигруппу, оксогруппу, фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, пирролидинил, имидазолил, пиразолил, тиенил, фурил, диоксоланил, изоксазолил и изотиазолил, причем каждый из указанных заместителей необязательно замещен 1-5 заместителями, выбранными из галогена, C1-С6алкила, который необязательно частично или полностью галогенирован, C3-С8циклоалканила, С5-С8циклоалкенила, гидроксигруппы, нитрила, С1-С3алкоксигруппы, которая необязательно частично или полностью галогенирована, группы NH2C(O), моно- либо ди(С1-С3алкил)аминогруппы и моно- либо ди(С1-С3алкил)аминокарбонила,
или R1 означает
- циклопропилоксигруппу, циклобутилоксигруппу, циклопентилоксигруппу, циклогексилоксигруппу или циклогептилоксигруппу, каждая из которых необязательно частично или полностью галогенирована и необязательно замещена 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, нитрил, гидроксиС1-С3алкил и арил, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S(O)m, CHOH, >C=O, >C=S или NH,
- фенилоксигруппу или бензилоксигруппу, каждая из которых необязательно частично или полностью галогенирована и необязательно замещена 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, нитрил, гидроксиС1-С3алкил и арил, или аналог такой циклоарильной группы, в котором 1-2 кольцевые метиленовые группы независимо заменены на N,
- циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, бициклопентанил, бициклогексанил или бициклогептанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, нитрил, гидроксиС1-С3алкил и арил, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S(O)m, CHOH, >C=O, >C=S или NH,
- разветвленный или неразветвленный С3-С10алкенил, который в каждом случае необязательно частично или полностью галогенирован и необязательно замещен 1-3 заместителями, выбранными из группы, включающей разветвленный или неразветвленный С1-С5алкил, фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил и изотиазолил, при этом каждый из указанных заместителей замещен 1-5 заместителями, выбранными из группы, включающей галоген, С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил либо бициклогептанил, гидроксигруппу, нитрил, C1-С3алкилоксигруппу, который необязательно частично или полностью галогенирован, группу NH2C(O) и моно- либо ди(С1-С3алкил)аминокарбонил, при этом указанный разветвленный или неразветвленный С3-С10алкенил необязательно прерван одним или несколькими гетероатомами, выбранными из О, N и S(O)m,
- циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил или бициклогептенил, при этом такая циклоалкепильная группа необязательно замещена 1-3 C1-С3алкильными группами,
- оксогруппу, нитрил, галоген,
- силил, содержащий три С1-С4алкильные группы, которые необязательно частично или полностью галогенированы, или
- С3-С6алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH или S(O)m, а указанная алкинильная группа необязательно независимо замещена 1-2 оксогруппами, гидроксигруппой, пирролидинилом, пирролилом, тетрагидропиранилом, одной или несколькими C1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена, нитрилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или моно- либо ди(С1-С3алкил)аминогруппой, необязательно замещенной одним или несколькими атомами галогена,
R2, R4 и R5 каждый означает
- разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, C1-С6ацил, ароил, разветвленную или неразветвленную С1-С4алкоксигруппу, которая в каждом случае необязательно частично или полностью галогенирована, галоген, метоксикарбонил, группу С1-С3алкил-S(O)m, которая необязательно частично или полностью галогенирована, или группу фенил-S(О)m,
- OR6, C1-C6алкоксигруппу, гидроксигруппу, нитрил, нитрогруппу, галоген или
- группу амино-S(O)m, где N-атом необязательно независимо моно- либо дизамещен C1-C6алкилом или арилС0-С3алкилом, или аминогруппу, где N-атом необязательно независимо моно- либо дизамещен С1-С3алкилом, арилС0-С3алкилом, С1-С6ацилом, группой С1-С6алкил-S(О)m- или группой арилС0-С3алкил-S(O)m-, при этом каждый из указанных в этом абзаце алкилов и арилов необязательно частично или полностью галогенирован и необязательно замещен 1-2 С1-С6алкильными группами или C1-С6алкоксигруппами,
R3 в каждом случае независимо означает
- фенил, нафтил, морфолиногруппу, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, пирролидинил, имидазолил, пиразолил, тиазолил, оксазолил, [1,3,4]оксадиазол, триазолил, тетразолил, тиенил, фурил, тетрагидрофурил, изоксазолил, изотиазолил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, бензоксазолил, бензизоксазолил, бензпиразолил, бензотиофуранил, циннолинил, птериндинил, фталазинил, нафтилпиридинил, хиноксалинил, хиназолинил, пуринил или индазолил, при этом каждый из вышеуказанных радикалов необязательно замещен 1-3 заместителями, выбранными из группы, включающей фенил, нафтил, гетероцикл либо гетероарил, которые описаны в этом абзаце, разветвленный или неразветвленный C1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, фенил-C1-С5алкил, нафтил-С1-С5алкил, галоген, гидроксигруппу, оксогруппу, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу либо гетероциклоксигруппу, где гетероциклический или гетероарильный фрагмент описан выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу либо гетероцикламиногруппу, где гетероциклический или гетероарильный фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, С1-С5алкил-С(О)-C1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1 -С5алкил)аминогруппу, моно- либо ди(С1-С3алкил)амино-С1-С5алкил, группу амино-S(О)2, группу ди(С1-С3алкил)амино-S(O)2, R7-С1-С5алкил, R8-С1-С5алкоксигруппу, R9-С(O)-С1-С5алкил, группу R10-C1-C5алкил(R11)N и карбокси-моно- либо ди(С1-С5алкил)аминогруппу,
- конденсированный арил, выбранный из бензоциклобутанила, инданила, инденила, дигидронафтила, тетрагидронафтила, бензоциклогептанила и бензоциклогептенила, или конденсированный гетероарил, выбранный из циклопентенопиридинила, циклогексанопиридинила, циклопентанопиримидинила, циклогексанопиримидинила, циклопентанопиразинила, циклогексанопиразинила, циклопентанопиридазинила, циклогексанопиридазинила, циклопентанохинолинила, циклогексанохинолинила, циклопентаноизохинолинила, циклогексаноизохинолинила, циклопентаноиндолила, циклогексаноиндолила, циклопентанобензимидазолила, циклогексанобензимидазолила, циклопентанобензоксазолила, циклогексанобензоксазолила, циклопентаноимидазолила, циклогексаноимидазолила, циклопентанотиенила и циклогексанотиенила, при этом указанное конденсированное арильное или конденсированное гетероарильное кольцо независимо замещено 0-3 заместителями, выбранными из группы, включающей фенил, нафтил, пиридинил, пиримидинил, пиразинил, пиридазинил, пирролил, имидазолил, пиразолил, тиенил, фурил, изоксазолил, изотиазолил, С1-С6алкил, который необязательно частично или полностью галогенирован, галоген, нитрил, C1-С3алкилоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу либо гетероциклоксигруппу, где гетероарильный или гетероциклический фрагмент описаны выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу либо гетероцикламиногруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, группу С1-С4алкил-ОС(O), С1-С5алкил-С(O)-С1-С4алкил, амино-С1-С5алкил, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, R12-C1-C5алкил, R13-С1-С5алкоксигруппу, R14-C(O)-C1-С5алкил и группу R15-С1-алкилС5R16)N,
- циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил или бициклогептанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 C1-С3алкильными группами, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S, CHOH, >C=O, >C=S или NH,
- циклопентенил, циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, бициклогексенил или бициклогептенил, каждый из которых необязательно замещен 1-3 C1-C3алкил группами,
- С1-С4алкилфенил-С(O)-С1-С4алкил-, С1-С4алкил-С(O)-С1-С4алкил- или С1-С4алкилфенил-S(O)m-С1-С4алкил-,
- С1-С6алкильную группу или разветвленную или неразветвленную C1-С6алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или С1-С6алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С5алкил)аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21)-, R22O-, R23R24NC(O)-, R26(CH2)mC(O)N(R21)-, R23R24NC(O)-C1-C3aлкoкcигруппу или R26С(O)(CH2)mN(R21)-,
- С2-С6алкенил, замещенный группой R23R24NС(O)-,
- С2-С6алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH, S(O)m, а указанная алкинильная группа необязательно независимо замещена 1-2 оксогруппами, пирролидинилом, пирролилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом, одной или несколькими С1-С4алкильными группами, которые необязательно замещены одним или несколькими атомами галогена, нитрилом, морфолиногрупой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или моно- либо ди(С1-С4алкил)аминогруппой, необязательно замещенной одним или несколькими атомами галогена,
- С1-С6ацил или ароил,
R6 означает С1-С4алкил, который необязательно частично или полностью галогенирован и необязательно замещен группой R26,
R7, R8, R9, R10, R12, R13, R14, R15, R17, R19, R25 и R26 кaждый независимо друг от друга означает нитрил, фенил, морфолиногруппу, пиперидинил, пиперазинил, имидазолил, пиридинил, тетразолил, аминогруппу или моно- либо ди(С1-С4алкил)аминогруппу, которая необязательно частично или полностью галогенирована,
R11 и R16 каждый независимо друг от друга означает водород или С1-С4алкил, который необязательно частично или полностью галогенирован,
R18 в каждом случае независимо означает водород или С1-С4алкил, который необязательно независимо замещен оксогруппой или группой R25,
R20 в каждом случае независимо означает С1-С10алкил, который необязательно частично или полностью галогенирован, фенил или пиридинил,
R21 в каждом случае независимо означает водород или C1-С3алкил, который необязательно частично или полностью галогенирован,
R22, R23 и R24 каждый независимо друг от друга означает водород, С1-С6алкил, который необязательно частично или полностью галогенирован, при этом указанный С1-С6алкил необязательно прерван одни или несколькими атомами О, N или S, а также независимо необязательно замещен моно- либо ди(С1-С3алкил)аминокарбонилом, фенилом, пиридинилом, аминогруппой или моно- либо ди(С1-С4алкил) аминогруппой, причем каждый из указанных радикалов необязательно частично или полностью галогенирован и необязательно замещен моно- либо ди(С1-С3алкил) аминогруппой, или
R23, и R24 вместе необязательно образуют гетероциклическое или гетероарильное кольцо,
m означает 0, 1 или 2 и
W означает О или S,
и их фармацевтически приемлемые производные.
В другом варианте осуществления изобретения среди указанных выше предпочтительны те соединения формулы (III), в которых
Е означает -СН2-, -NH- или -О-,
W означает О и
G означает
- фенил, нафтил, бензоциклобутанил, дигидронафтил, тетрагидронафтил, бензоциклогептанил, бензоциклогептенил, инданил, инденил,
- пиридинил, пиридонил, хинолинил, дигидрохинолинил, тетрагидрохиноил, изохинолинил, тетрагидроизохиноил, пиридазинил, пиримидинил, пиразинил, бензимидазолил, бензтиазолил, бензооксазолил, бензофуранил, бензотиофенил, бензпиразолил, дигидробензофуранил, дибензофуранил, дигидробензотиофенил, бензооксазолонил, бензо [1,4] оксазин-3-онил, бензодиоксолил, бензо[1,3]диоксол-2-онил, бензофуран-3-онил, тетрагидробензопиранил, индолил, 2,3-дигидро-1Н-индолил, индолинил, индолонил, индолинонил, фталимидил,
- оксетанил, пирролидинил, тетрагидрофуранил, тетрагидротиофенил, пиперидинил, пиперазинил, морфолино, тетрагидропиранил, диоксанил, тетраметиленсульфонил, тетраметиленсульфоксидил, оксазолинил, 3,4-дигидро-2Н-бензо[1,4]оксазинил, тиазолинил, имидазолинил, тетрагидропиридинил, гомопиперидинил, пирролинил, тетрагидропиримидинил, декагидрохинолинил, декагидроизохинолинил, тиоморфолиногруппу, тиазолидинил, дигидрооксазинил, дигидропиранил, оксоканил, гептаканил, тиоксанил или дитианил, при этом G необязательно замещен одной или несколькими группами R1, R2 или R3.
Согласно еще одному варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых
Е означает -NH-,
G означает фенил, пиридинил, пиридонил, нафтил, хинолинил, изохинолинил, пиразинил, бензимидазолил, бензооксазолил, бензооксазолонил, бензофуранил, бензотиофенил, бензопиразолил, дигидробензофуранил, дигидробензотиофенил, 3,4-дигидро-2Н-бензо[1,4]оксазинил, инданил, инденил, индолил, индолинил, индолонил, 2,3-дигидро-1Н-индолил или индолинонил, при этом G необязательно замещен одной или несколькими группами R1, R2 или R3,
Ar означает нафтил, хинолинил, изохинолинил, тетрагидронафтил, тетрагидрохинолинил, тетрагидроизохинолинил, инданил, инденил или индолил, каждый из которых необязательно замещен одной или несколькими группами R4 или R5,
Х означает фенил, фуранил, тиенил, пирролил, пиразолил, имидазолил, пиридинил, пиримидинил, пиридинонил, дигидропиридинонил, малеимидил, дигидромалеимидил, пиперидинил, пиперазинил, пиридазинил или пиразинил, каждый из которых необязательно независимо замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, C1-С4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу С1-С6алкил-S(O)m и галоген,
Y означает связь или насыщенную либо ненасыщенную С1-С4-углеродную цепь, где один или несколько С-атомов необязательно заменены на О, N или S(O)m, а Y необязательно независимо замещен 1-2 оксогруппами, нитрилом, фенилом или одной или несколькими С1-C4алкильными группами, необязательно замещенными одним или несколькими атомами галогена,
Z означает
фенил, гетероарил, выбранный из пиридинила, пиперазинила, пиримидинила, пиридазинила, пиразинила, имидазолила, фуранила, тиенила и пиранила, гетероцикл, выбранный из 2-окса-5-азабицикло[2.2.1]гептанила, тетрагидропиримидонила, пентаметиленсульфидила, пентаметиленсульфоксидила, пентаметиленсульфонила, тетраметиленсульфидила, тетраметиленсульфоксидила, тетраметиленсульфонила, тетрагидропиранила, тетрагидрофуранила, 1,3-диоксоланонила, 1,3-диоксанонила, 1,4-диоксанила, морфолиногруппы, тиоморфолиногруппы, тиоморфолиносульфоксидила, пиперидинила, пиперидинонила, дигидротиазолила, дигидротиазолилсульфоксидила, пирролидинила и диоксоланила, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей нитрил, С1-С3алкил, С1-С3алкоксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, группу CONH2 и группу ОН,
или Z необязательно замещен фенилом, гетероциклом или гетероарилом, как они определены выше в этом абзаце, каждый из которых в свою очередь необязательно замещен галогеном, C1-С3алкилом или С1-С3алкоксигруппой,
или Z означает нитрил, нитрилС1-С3алкил, группу С1-С6алкил-S(O)m, галоген, гидроксигруппу, C1-С3алкил, С1-С3ациламиногруппу, С1-С4алкоксигруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминокарбонил или аминогруппу, моно либо дизамещенную аминоС1-С6алкилом или С1-С3алкоксиС1-С3алкилом,
R1 в каждом случае независимо означает
- разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, при этом один или несколько С-атомов необязательно независимо заменены на О, N или S(O)m, a указанный С1-С6алкил необязательно замещен 1-3 заместителями, выбранными из группы, включающей С3-С6циклоалкил, оксогруппу, фенил, диоксоланил, пирролидинил, фурил, изоксазолил или изотиазолил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей галоген, С1-С3алкил, который необязательно частично или полностью галогенирован, гидроксигруппу, нитрил и С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована,
- циклопропил, циклобутил, циклопентанил, циклогексанил, бициклопентанил или бициклогексанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 C1-С3алкильными группами, которые необязательно частично или полностью галогенированы, нитрилом, гидроксиС1-С3алкилом или фенилом, или аналог такой циклоалкильной группы, в котором 1-3 кольцевые метиленовые группы независимо заменены на О, S, CHOH, >C=O, >C=S или NH,
- оксогруппу,
- С3-С6алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна или несколько метиленовых групп необязательно заменены на О, NH или S(O)m, а указанная алкинильная группа необязательно независимо замещена 1-2 оксогруппами, гидроксигруппой, пирролидинилом, пирролилом, тетрагидропиранилом, С1-С4алкилом, который необязательно замещен одним или несколькими атомами галогена, нитрилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или моно- или ди(С1-С3алкил)аминогруппой, которая необязательно замещена одним или несколькими атомами галогена, или
- силил, содержащий три С1-С4алкильные группы, которые необязательно частично или полностью галогенированы,
R2 в каждом случае независимо означает
- разветвленный или неразветвленный C1-С5алкил, который необязательно частично или полностью галогенирован, ацетил, ароил, разветвленную или неразветвленную С1-С4алкоксигруппу, которая в каждом случае необязательно частично или полностью галогенирована, галоген, метоксикарбонил, группу С1-С2алкил-S(O)m, которая необязательно частично или полностью галогенирована, или группу фенил-S(O)m,
- С1-С3алкоксигруппу, гидроксигруппу, нитрил, нитрогруппу, галоген или
- группу амино-S(О)m-, где N-атом необязательно независимо моно- или дизамещен С1-С3алкилом или арилС0-С3алкилом, или аминогруппу, где N-атом необязательно независимо моно- или дизамещен C1-С3алкилом, арилС0-С3алкилом, С1-С3ацилом, группой С1-С4алкил-S(O)m- или группой арилС0-С3алкил-S(О)m-, при этом каждый из указанных в этом абзаце алкилов и арилов необязательно частично или полностью галогенирован и необязательно замещен 1-2 C1-С3алкильными группами или С1-С3алкоксигруппами,
R3 в каждом случае независимо означает
- фенил, морфолиногруппу, пиридинил, пиримидинил, пиразинил, пирролил, пирролидинил, имидазолил, [1,3,4]оксадиазол, пиразолил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей фенил, нафтил, гетероцикл либо гетероарил, как они описаны выше в этом абзаце, С1-С6алкил, который необязательно частично или полностью галогенирован, циклопропанил, циклобутанил, циклопентанил, циклогексанил, циклогептанил, бициклопентанил, бициклогексанил, бициклогептанил, фенил-С1-С5алкил, нафтилC1-С5алкил, галоген, оксогруппу, гидроксигруппу, нитрил, С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована, фенилоксигруппу, нафтилоксигруппу, гетероарилоксигруппу либо гетероциклоксигруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, нитрогруппу, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, фениламиногруппу, нафтиламиногруппу, гетероариламиногруппу или гетероцикламиногруппу, где гетероарильный или гетероциклический фрагмент описан выше в этом абзаце, группу NH2C(O), моно- либо ди(С1-С3алкил)аминокарбонил, С1-С5алкил-С(O)-С1-С4алкил, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3)алкиламино-С1-С5алкил, группу моно- либо ди(С1-С3алкил)амино-S(O)2, R7-С1-С5алкил, R8-С1-С5алкоксигруппу, R9-С(O)-С1-С5алкил, группу R10-C1-C5алкил(R11)N и карбокси-моно- либо ди(С1-С5)-алкиламиногруппу,
- C1-С3алкильную группу или С1-С4алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или C1-C6алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-C5алкил)аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21)-, R22O-, R23R24NC(O)-, R26CH2(O)N(R21)-, R23R24NC(O)-C1-C2aлкoкcигруппу или R26C(O)CH2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NС(O)-,
- С2-С4алкинильную разветвленную или неразветвленную углеродную цепь, которая необязательно частично или полностью галогенирована, при этом одна из метиленовых групп необязательно заменена на О, и необязательно независимо замещена 1-2 оксогруппами, пирролидинилом, пирролилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или одной или несколькими С1-С4алкильными группами, необязательно замещенными одним или несколькими атомами галогена, или
- C1-С3ацил и
R23 и R24 вместе необязательно образуют имидазолильное, пиперидинильное, морфолиновое, пиперазинильное или пиридинильное кольцо.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых
G означает фенил, пиридинил, пиридонил, нафтил, хинолинил, изохинолинил, пиразинил, 3,4-дигидро-2Н-бензо[1,4]оксазинил, бензотиофенил, дигидробензофуранил, дигидробензотиофенил, бензоксазолил, инданил, индолил, индолинил, индолонил или индолинонил, при этом G необязательно замещен одной или несколькими группами R1, R2 или R3,
Ar означает нафтил,
Х означает фенил, имидазолил, пиридинил, пиримидинил, пиперидинил, пиперазинил, пиридазинил или пиразинил, каждый из которых необязательно независимо замещен 1-3 заместителями, выбранными из группы, включающей С1-С4алкил, С1-С4алкоксигруппу, гидроксигруппу, нитрил, аминогруппу, моно- либо ди(С1-С3алкил)аминогруппу, моно- либо ди(С1-С3алкиламино)карбонил, группу NH2C(O), группу С1-С6алкил-S(О)m и галоген,
Y означает связь или насыщенную С1-С4-углеродную цепь, где один или несколько С-атомов необязательно заменены на О, N или S, а Y необязательно независимо замещен нитрилом или оксогруппой,
Z означает фенил, пиридинил, пиримидинил, пиридазинил, пиразинил, имидазолил, дигидротиазолил, дигидротиазолилсульфоксид, пиранил, пирролидинил, фенилпиперазинил, тетрагидропиранил, тетрагидрофуранил, диоксоланил, 2-окса-5-азабицикло[2.2.1]гептанил, морфолиногруппу, тиоморфолиногруппу, тиоморфолиносульфоксидил, пиперидинил, пиперидинонил, пиперазинил или тетрагидропиримидонил, каждый из которых необязательно замещен 1-2С1-С2алкильными группами или C1-С2алкоксигруппами, или
Z означает гидроксигруппу, C1-С3алкил, C1-С3алкоксигруппу, С1-С3ациламиногруппу, С1-С3алкилсульфонил, нитрил-C1-С3алкил или аминогруппу, моно- или дизамещенную С1-С3алкоксиС1-С3алкилом,
R1 в каждом случае независимо означает
- разветвленный или неразветвленный C1-С5алкил, который необязательно частично или полностью галогенирован, при этом один или несколько С-атомов необязательно независимо заменены на О, N или S(O)m, a указанный С1-С5алкил необязательно замещен оксогруппой, диоксоланилом, пирролидинилом, фурилом или фенилом, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей галоген, С1-С3алкил, который необязательно частично или полностью галогенирован, гидроксигруппу, нитрил и С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована,
- циклопропил, циклобутил, циклопентанил, циклогексанил, бициклопентанил или бициклогексанил, каждый из которых необязательно частично или полностью галогенирован и необязательно замещен 1-3 C1-С3алкильными группами, которые необязательно частично или полностью галогенированы, нитрилом, гидроксиС1-С3алкилом или фенилом, или аналог циклопропила, циклобутила, циклопентанила, циклогексанила, бициклопентанила или бициклогексанила, в котором одна кольцевая метиленовая группа заменена на О,
- оксогруппу,
- С2-С4алкинил, который необязательно частично или полностью галогенирован, при этом одна или несколько метиленовых групп необязательно заменены на О, и необязательно независимо замещен 1-2 оксогруппами, гидроксигруппой, пирролидинилом, пирролилом, тетрагидропиранилом, С1-С4алкилом, который необязательно замещен одним или несколькими атомами галогена, нитрилом, морфолиногруппой, пиперидинилом, пиперазинилом, имидазолилом, фенилом, пиридинилом, тетразолилом или моно- либо ди(С1-С3алкил)аминогруппой, которая необязательно замещена одним или несколькими атомами галогена, или
- силил, содержащий три C1-С2алкильные группы, которые необязательно частично или полностью галогенированы,
R2 в каждом случае независимо означает С1-С4алкил, который необязательно частично или полностью галогенирован, С1-С4алкоксигруппу, которая необязательно частично или полностью галогенирована, бром, хлор, фтор, метоксикарбонил, группу метил-S(О)m либо этил-S(O)m, каждая из которых необязательно частично или полностью галогенирована, или группу фенил-S(О)m,
или R2 означает моно- или диС1-С3ациламиногруппу, группу амино-S(O)m или S(О)m-аминогруппу, где N-атом моно- или дизамещен C1-С3алкилом или фенилом, нитрил, нитрогруппу или аминогруппу,
R3 в каждом случае независимо означает
- фенил, морфолиногруппу, пиридинил, пиримидинил, пирролидинил, 2,5-пирролидиндионил, имидазолил, [1,3,4]оксадиазол, пиразолил, каждый из которых необязательно замещен 1-3 заместителями, выбранными из группы, включающей С1-С3алкил, который необязательно частично или полностью галогенирован, галоген, оксогруппу, гидроксигруппу, нитрил и С1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована,
- С1-С3алкильную группу или C1-С3алкоксигруппу, которая необязательно частично или полностью галогенирована или необязательно замещена группой R17,
- OR18 или C1-С3алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С3алкил)аминогруппу, необязательно замещенную группой R19,
- R20C(O)N(R21)-, R22O-, R23R24NC(O)-, R26CH2C(O)N(R21)-, NH2С(O)метоксигруппу или R25C(O)CH2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NС(O)-,
- С2-С1алкинил, замещенный пирролидинилом или пирролилом, или
- C1-C3ацил и
R23 и R24 вместе необязательно образуют морфолиногруппу.
В соответствии еще с одним вариантом осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых
G означает фенил, пиридинил, пиридонил, 2-нафтил, хинолинил, изохинолинил, дигидробензофуранил, инданил, 5-индолил, 3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил, бензооксалолил, 2,3-дигидробензооксазол-7-ил, 2-оксо-2,3-дигидро-1Н-индол-5-ил, индолинил, индолонил или индолинонил, при этом G необязательно замещен одной или несколькими группами R1, R2 или R3,
Ar означает 1-нафтил,
Х означает фенил, имидазолил, пиридинил, пиримидинил, пиперидинил, пиперазинил, пиридазинил или пиразинил,
Y означает связь или -СН2-, -СН2CH2-, -С(O)-, -О-, -S-, -NH-CH2CH2CH2-, -N(СН3)-, CH2(CN)CH2-NH-CH2 или -NH-,
Z означает морфолиногруппу, диоксоланил, тетрагидрофуранил, пиридинил, 2-окса-5-азабицикло[2.2.1]гептанил, C1-C3алкоксифенилпиперазинил, гидроксигруппу, С1-С3алкил, N,N-диС1-С3алкокси-С1-С3алкиламиногруппу, C1-С3ациламиногруппу, С1-С3алкилсульфонил или нитрилС1-С3алкил,
R1 в каждом случае независимо означает
- С1-С5алкил, который необязательно частично или полностью галогенирован, при этом один или несколько С-атомов необязательно независимо заменены на О или N, а указанный C1-С5алкил необязательно замещен оксогруппой, диоксоланилом, пирролидинилом, фурилом или фенилом, необязательно замещенным С1-С3алкоксигруппой,
- циклопропил, циклопентанил, циклогексанил и бициклопентанил, необязательно замещенный 1-3 метильными группами, которые необязательно частично или полностью галогенированы, нитрилом, гидроксиметилом или фенилом, или 2-тетрагидрофуранил, замещенный метилом,
- триметилсилил или
- пропинил, замещенный гидроксигруппой или тетрагидропиран-2-илоксигруппой,
R2 означает моно- либо диС1-С3ациламиногруппу, группу амино-S(O)m или S(O)m-аминогруппу, где N-атом моно- либо дизамещен C1-С3алкилом или фенилом, бром, хлор, фтор, нитрил, нитрогруппу, аминогруппу, метилсульфонил, который необязательно частично или полностью галогенирован, или фенилсульфонил,
R3 в каждом случае независимо означает
- фенил, морфолиногруппу, пиридинил, пиримидинил, пирролидинил, 2,5-пирролидинилдионил, имидазолил, [1,3,4]оксадиазол или пиразолил, каждый из которых необязательно замещен С1-С2алкилом, который необязательно частично или полностью галогенирован,
- С1-С3алкильную группу или С1-С3алкоксигруппу, каждая из которых необязательно частично или полностью галогенирована или необязательно замещена диэтиламиногруппой,
- OR18 или С1-С3алкил, необязательно замещенный группой OR18,
- аминогруппу или моно- либо ди(С1-С3алкил) аминогруппу, необязательно замещенную группой R19,
- СН3С(O)NH-, R22O-, R23R24NC(O)-, R26CH2C(O)N(R21)-, NH2С(O)метоксигруппу или R26С(O)СН2N(R21)-,
- С2-С4алкенил, замещенный группой R23R24NC(O)-,
- С2-С4алкинил, замещенный пирролидинилом или пирролилом, или
- С1-С2ацил и
R23 и R24 означают Н или R23 и R24 вместе необязательно образуют морфолиногруппу и
R26 означает морфолиногруппу.
В соответствии еще с одним вариантом осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых
G означает фенил, пиридинил, 5-индолил, 3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил, бензооксалолил, 2,3-дигидробензооксазол-7-ил, 2-оксо-2,3-дигидро-1Н-индол-5-ил или 2-нафтил, при этом G необязательно замещен одной или несколькими группами R1, R2 или R3,
Х означает имидазолил, пиридинил, пиримидинил или пиразинил,
Y означает связь, CH2(CN)CH2-NH-CH2, -CH2-, -NH-CH2CH2CH2- или -NH-,
Z означает морфолин-4-ил, диоксолан-2-ил, тетрагидрофуранил, пиридинил, 2-окса-5-азабицикло [2.2.1]гепт-5-ил, метоксифенилпиперазинил, гидроксигруппу, метил, N,N-диметоксиэтиламиногруппу, ацетиламиногруппу, метилсульфонил или цианоэтил,
R1 в каждом случае независимо означает трет-бутил, втор-бутил, трет-амил, фенил, тетрагидропиран-2-илоксипропинил, гидроксипропинил, тригалометил, 2,2-диэтилпропионил или циклогексанил,
R2 означает хлор, нитрогруппу, аминогруппу, нитрил, метилсульфониламиногруппу, диацетиламиногруппу, фенилсульфониламиногруппу, N,N-ди(метилсульфонил)аминогруппу, метилсульфонил или тригалометилсульфонил,
R3 в каждом случае независимо означает метил, C1-С3алкоксигруппу, метоксиметил, гидроксипропил, диметиламиногруппу, С1-C4алкиламиногруппу, NН2С(O)метоксигруппу, ацетил, пирролидинил, имидазолил, пиразолил, морфолиногруппу или морфолинокарбонил.
В другом варианте осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых Х означает пиридинил.
Согласно следующему варианту осуществления изобретения среди непосредственно указанных выше предпочтительны те соединения формулы (III), в которых пиридинил присоединен к Ar в 3-м положении пиридинила.
В качестве примеров соединений формулы(III) по изобретению можно назвать следующие:
1-(4-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил)-3-[4-(4-морфолин-4-илметилпиперидин-1-ил)нафталин-1-ил]мочевину,
1-(6-хлор-4-трифторметилпиридин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-дифторметоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-метилнафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[2-метокси-5-(1-метил-1-фенилэтил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
3-(5-{4-[3-(5-трет-бутил-2-метилфенил)уреидо]нафталин-1-ил}пиридин-2-иламино)пропиловый эфир (5-трет-бутил-2-метилфенил)карбаминовой кислоты,
1-(6-трет-бутилбензо[1,3]диоксол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1,3-бис[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,2-диметил-[1,3]диоксолан-4-илметил)-2-гидроксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-пирролидин-1-илэтокси)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-гидроксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,3-диметил-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(2-п-толилокси-5-трифторметилфенил)мочевину,
1-[2-(2-метоксифенокси)-5-трифторметилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-нафталин-1-илмочевину,
1-{5-трет-бутил-2-метил-3-[3-(тетрагидропиран-2-илокси)проп-1-инил]фенил}-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-{5-трет-бутил-2-[3-(тетрагидропиран-2-илокси)проп-1-инил]фенил}-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-гидроксиметил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метоксидибензофуран-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,5-ди-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-(4-бром-1-метил-1H-пиразол-3-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-гидрокси-5,6,7,8-тетрагидронафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(1-ацетил-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-оксазол-5-илфенил)мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-[1,3,4]оксадиазол-2-илфенил)мочевину,
1-(2-метокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
(4-трет-бутил-2-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид фуран-2-карбоновой кислоты,
1-(2-метокси-4-фениламинофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-метокси-2-метилфенил)-3-[4-(6-морфолин-4-илметилниридин-3-ил)нафталин-1-ил]мочевину,
1-(3-гидроксинафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N,N-диэтил-4-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензолсульфонамид,
1-(2,2-дифторбензо[1,3]диоксо1-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(1,1-диметилпропил)-2-феноксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(2,2-диметилпропионил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
изопропиловый эфир 2-хлор-5-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензойной кислоты,
1-(4-амино-3,5-дибромфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(3-гидроксипроп-1-инил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-гидроксипроп-1-инил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,2-диметил-[1,3]диоксолан-4-илметил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутокси-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(1-цианоциклопропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2-диэтиламино-этил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-[1,3]диоксолан-2-илпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-пирролидин-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-диметиламинофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-пропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-гидроксиметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
2-(5-трет-бутил-2-метоксифенил)-N-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]ацетамид,
1-(2-метокси-5-феноксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-циклопентилоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-пиридин-3-илпирролидин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-циклогексил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,4-диметокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метокси-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-метилпиридин-3-ил)нафталин-1-ил]мочевину,
N-ацетил-N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-(6-трет-бутил-4-метил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[6-трет-бутил-4-(2-морфолин-4-илэтил)-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-этоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-изопропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-имидазол-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-4-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)метансульфонамид,
1-(5-трет-бутил-3-этиламино-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)бис(метансульфон)амид,
1-[5-трет-бутил-2-(1-метил-1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метансульфинил-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-этансульфонил-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-{[бис(2-метоксиэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-диметиламинопирролидин-1-илметил)пиридин-3-ил}нафталин-1-ил}мочевину,
N-[1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)-пирролидин-3-ил]ацетамид,
1-(1-ацетил-3,3-диметил-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпирипин-3-ил)нафталин-1-ил]уреидо}фенил)пропионамид,
1-(5-трет-бутил-2-метилбензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметансульфонилфенил)мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)изобутирамид,
2-(4-трет-бутил-2-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенокси)ацетамид,
1-(5-трет-бутил-2-оксо-2,3-дигидробензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-пиано-2-метоксиметоксипиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-циано-2-гидроксипиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-3-циано-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(1,3,3-триметил-2,3-дигидро-1Н-индол-5-ил)мочевину,
1-(5-трет-бутилбензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)бензолсульфонамид,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид этансульфоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(4-морфолин-4-илметилпиперидин-1-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(1-метил-1Н-пиразол-4-ил)фенил]-3-[4-(4-морфолин-4-илметилпиперидин-1-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксипиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид 2,2,2-трифторэтансульфоновой кислоты,
N-(5-{4-[3-(5-трет-бутил-2-метилфенил)уреидо]нафталин-1-ил}пиразин-2-ил)метансульфонамид,
1-[4-(6-{[бис(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилпиперидин-1-илметил)-пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(тетрагидропиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)-(тетрагидрофуран-2-илметил)амино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метоксиметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(2-морфолин-4-илэтиламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
амид 1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперидин-3-карбоновой кислоты,
амид 1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперидин-4-карбоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксо-114-тиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-{4-[6-(4-ацетилпиперазин-1-илметил)-пиридин-3-ил]нафталин-1-ил}-3-(5-трет-бутил-2-метоксифенил)мочевину,
этиловый эфир 4-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперазин-1-карбоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(2-пиридин-3-илэтиламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(тетрагидрофуран-3-иламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)пиридин-3-илметиламино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(2-метилсульфанилэтиламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(2-пиперазин-1-илэтиламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-пиримидин-2-илпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-пиридин-2-илпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[4-(3-метоксифенил)-пиперазин-1-илметил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(морфолин-4-карбонил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-тиа-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(5-морфолин-4-илметилпиразин-2-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-ил)ацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-N-метилацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-2,2,2-трифторацетамид,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(пиридин-3-илокси)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(пиридин-3-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
3-трет-бутилфениловый эфир[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]карбаминовой кислоты,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)метансульфонамид
и их фармацевтически приемлемые производные.
Согласно еще одному варианту осуществления изобретения в нем предлагаются также следующие соединения формулы (III):
1-(3-метилнафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-гидроксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(2,3-диметил-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-{5-трет-бутил-2-метил-3-[3-(тетрагидропиран-2-илокси)проп-1-инил]фенил}-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(2-метокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-(2,2-диметилпропионил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-3-(3-гидроксипроп-1-инил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-2-(3-гидроксипроп-1-инил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-3-(2,2-диметил-[1,3]диоксолан-4-илметил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутокси-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-(1-цианоциклопропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[5-трет-бутил-3-(2-диэтиламиноэтил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-[1,3]диоксолан-2-илпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-пирролидин-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-диметиламинофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-пропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-гидроксиметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-циклогексил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(2,4-диметокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метокси-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-метилпиридин-3-ил)нафталин-1-ил]мочевина,
N-ацетил-N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-(6-трет-бутил-4-метил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-этоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-изопропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-имидазол-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-3-этиламино-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил}уреидо}фенил)бис(метансульфон)амид,
1-[5-трет-бутил-2-(1-метил-1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(2-метансульфинил-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[4-(6-{[бис-(2-метоксиэтил)амино]метил]пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевина,
N-[1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пирролидин-3-ил]ацетамид,
1-(1-ацетил-3,3-диметил-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)пропионамид,
1-(5-трет-бутил-2-метилбензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметансульфонилфенил)мочевина,
N-(5-трет-бутил-2-метокси-3-[3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)изобутирамид,
2-(4-трет-бутил-2-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенокси)ацетамид,
1-(5-трет-бутил-2-оксо-2,3-дигидробензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-3-циано-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутилбензоксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)бензолсульфонамид,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид этансульфоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксипиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид2,2,2-трифторэтансульфоновой кислоты,
N-(5-{4-[3-(5-трет-бутил-2-метилфенил)уреидо]нафталин-1-ил]пиразин-2-ил)метансульфонамид,
1-[4-(6-{[бис(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилпиперидин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(тетрагидропиран-4-иламино)пиридин-3-ил]нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)-(тетрагидрофуран-2-илметил)амино]метил}пиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метоксиметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
амид 1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперидин-3-карбоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксо-114-тиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилниридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(тетрагидрофуран-3-иламино)метил]пиридин-3-ил}нафталин-1-ил)мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)-пиридин-3-илметиламино]метил}пиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[4-(3-метоксифенил)пиперазин-1-илметил]пиридин-3-ил}-нафталин-1-ил)мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(морфолин-4-карбонил)пиридин-3-ил]нафталин-1-ил}мочевина,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(5-морфолин-4-илметилпиразин-2-ил)нафталин-1-ил]мочевина,
1-(6-трет-бутил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-ил)ацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-N-метилацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-2,2,2-трифторацетамид,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(пиридин-3-илокси)пиридин-3-ил]нафталин-1-ил}мочевина,
3-трет-бутилфениловый эфир[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]карбаминовой кислоты,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)метансульфонамид
и их фармацевтически приемлемые производные.
Помимо представленных выше в качестве примера соединений по описанным ниже общим методам синтеза могут быть получены также следующие возможные соединения формулы (III):
1-(5-трет-бутил-2-метилсульфанилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-хлорпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
1-(5-трет-бутил-2-метиламинопиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина,
N-(5-трет-бутил-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}-2-оксо-2Н-пиридин-1-ил)метансульфонамид,
амид 5-трет-бутил-7-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензоксазол-2-карбоновой кислоты,
2-(5-трет-бутил-7-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензоксазол-2-ил)ацетамид,
5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}бензамид
и их фармацевтически приемлемые производные.
Любые соединения по изобретению, содержащие один или более асимметричных атомов углерода, могут существовать в виде рацематов и рацемических смесей, отдельных энантиомеров, диастереомерных смесей и индивидуальных диастереомеров. Все подобные изомерные формы этих соединений включены в объем настоящего изобретения. Каждый стереогенный атом углерода может находиться в R- или S-конфигурации либо в сочетании таких конфигураций.
Некоторые из соединений формул (I), (Iа), (II) и (III) могут существовать более чем в одной таутомерной форме. Все подобные таутомеры включены в объем настоящего изобретения.
Все термины, используемые в настоящем описании, имеют, если не указано иное, общепринятые в данной области значения. Так, например, "С1-С4алкоксигруппа" представляет собой С1-С4алкил с концевым атомом кислорода, в частности метокси-, этокси-, пропокси-, пентокси- и гексоксигруппу. Все алкильные, алкенильные и алкинильные группы могут иметь разветвленную или неразветвленную цепь, если это возможно с точки зрения их структуры и если не указано иное. Ниже приведены определения других конкретных терминов, используемых в настоящем описании.
Термин "ароил" в контексте настоящего описания означает "бензоил" или "нафтоил".
Термин "карбоцикл" означает алифатический углеводородный радикал, содержащий от трех до двенадцати атомов углерода. Карбоциклы включают углеводородные кольца, содержащие от трех до десяти атомов углерода. Подобные карбоциклы могут представлять собой либо ароматические, либо неароматические кольцевые системы. Неароматические кольцевые системы могут быть моно- или полиненасыщенными. В качестве примеров предпочтительных карбоциклов можно назвать (но не ограничиваясь только ими) циклопропил, циклобутил, циклопентил, циклопентенил, циклогексил, циклогексенил, циклогептанил, циклогептенил, фенил, инданил, инденил, бензоциклобутанил, дигидронафтил, тетрагидронафтил, нафтил, декагидронафтил, бензоциклогептанил и бензоциклогептенил. Некоторые термины, которые относятся к циклоалкилу, такие как циклобутанил и циклобутил, могут использоваться как взаимозаменяющие понятия.
Термин "гетероцикл" относится к стабильному неароматическому 4-8-членному (однако более предпочтительно 5- или 6-членному) моноциклическому или неароматическому 8-11-членному бициклическому гетероциклическому радикалу, который может быть насыщенным либо ненасыщенным. Каждый гетероцикл состоит из атомов углерода и одного или более, предпочтительно 1-4, гетероатомов, выбранных из азота, кислорода и серы. Гетероцикл может быть присоединен через любой атом кольца, что приводит к образованию стабильной структуры. Если не указано иное, в качестве примеров гетероциклов можно назвать (но не ограничиваясь только ими) оксетанил, пирролидинил, тетрагидрофуранил, тетрагидротиофенил, пиперидинил, пиперазинил, морфолинил, тетрагидропиранил, диоксанил, тетраметиленсульфонил, тетраметиленсульфоксидил, оксазолинил, тиазолинил, имидазолинил, тетрагидропиридинил, гомопиперидинил, пирролинил, тетрагидропиримидинил, декагидрохинолинил, декагидроизохинолинил, тиазолидинил, дигидрооксазинил, дигидропиранил, оксоканил, гептаканил, тиоксанил, дитианил или 2-окса- или 2-тиа-5-азабицикло[2.2.1]гептанил.
Термин "гетероарил" означает ароматическое 5-8-членное моноциклическое или 8-11-членное бициклическое кольцо, содержащее 1-4 гетероатома, таких как N, О и S. Если не указано иное, к подобным гетероарилам относятся пиридинил, пиридонил, хинолинил, дигидрохинолинил, тетрагидрохиноил, изохинолинил, тетрагидроизохиноил, пиридазинил, пиримидинил, пиразинил, бензимидазолил, бензтиазолил, бензоксазолил, бензофуранил, бензотиофенил, бензпиразолил, дигидробензофуранил, дигидробензотиофенил, бензооксазолонил, бензо[1,4]оксазин-3-онил, бензодиоксолил, бензо[1,3]диоксол-2-онил, тетрагидробензопиранил, индолил, индолинил, индолонил, индолинонил, фталимидил.
Термин "гетероатом" в контексте настоящего описания относится к атомам, отличным от атома углерода, таким как О, N, S и Р.
Термин "арил" в контексте настоящего описания означает ароматический карбоцикл или гетероарил, которые определены выше.
Термины, которые являются аналогами вышеуказанных циклических остатков, такие как арилокси или гетероариламин, означают арил, гетероарил, гетероцикл, как они определены выше, присоединенные к их соответствующей группе.
В контексте настоящего описания понятия "азот" и "сера" включают любую окисленную форму азота и серы и кватернизованную форму любого азотистого основания.
Термин "галоген" в контексте настоящего описания означает бром, хлор, фтор или иод.
К соединениям по изобретению относятся только те соединения, которые рассматриваются как "химически стабильные" в том отношении, как это принято в данной области техники. Так, например, соединение, обладающее "плавающей валентностью" ("dangling valency"), или "карбанион" не подпадают под соединения по изобретению.
В объем изобретения включены также фармацевтически приемлемые производные соединений формул (I), (Iа), (II) и (III). Понятие "фармацевтически приемлемое производное" относится к любой фармацевтически приемлемой соли или фармацевтически приемлемому эфиру соединения по изобретению или к любому иному соединению, которое при введении пациенту способно превращаться (непосредственно или опосредованно) в соединение по изобретению, в его фармаколокически активный метаболит или фармаколокически активный остаток. Под "фармаколокически активным метаболитом" в этом отношении понимается любое соединение по изобретению, способное к метаболизму ферментативным или химическим путем. Примером таких соединений являются гидроксилированные или окисленные производные соединений формул (I), (Ia), (II) или (III).
Фармацевтически приемлемые соли соединений по изобретению включают соли, полученные из фармацевтически приемлемых неорганических и органических кислот и оснований. В качестве примера соответствующих кислот можно назвать соляную, бромистоводородную, серную, азотную, перхлорную, фумаровую, малеиновую, фосфорную, гликолевую, молочную, салициловую, янтарную, толуол-п-серную, винную, уксусную, лимонную, метансульфоновую, муравьиную, бензойную, малоновую, нафталин-2-серную и бензолсульфоновую кислоты. Помимо этого, могут использоваться и иные кислоты, например щавелевая кислота, которые хотя и не являются сами по себе фармацевтически приемлемыми, но тем не менее могут применяться для получения солей, пригодных для использования в качестве промежуточных продуктов в процессе получения соединений по изобретению и их фармацевтически приемлемых кислотно-аддитивных солей. К солям, полученным из соответствующих оснований, относятся соли щелочных металлов (например натрия), соли щелочноземельных металлов (например магния), соли аммония и N-(C1-C4aлкилъныe) соли.
Кроме того, к соединениям по изобретению относятся пролекарства соединений формул (I), (Ia), (II) и (III). Пролекарства представляют собой такие соединения, которые в результате простого химического превращения преобразуются в соединения по изобретению. Подобными простыми химическими превращениями являются гидролиз, окисление и восстановление. Так, в частности, при введении пролекарства по изобретению пациенту такое пролекарство может превращаться в соединение по изобретению, проявляя тем самым целевое фармакологическое действие.
Методы применения
В изобретении предлагаются методы применения соединений формул (I), (Iа), (II) и (III). Соединения по изобретению эффективно блокируют продуцирование клетками воспалительных цитокинов. Ингибирование продуцирования цитокинов представляет собой перспективный метод предупреждения и лечения различных болезней, связанных с избыточным продуцированием цитокинов, например болезней и патологических состояний, связанных с воспалением. Таким образом, соединения по изобретению могут применяться для лечения таких состояний. Эти состояния включают хронические воспалительные болезни, в том числе (но не ограничиваясь только ими) остеоартрит, рассеянный склероз, синдром Гийена-Барре, болезнь Крона, язвенный колит, псориаз, болезнь "трансплантат против хозяина", системную красную волчанку и инсулинзависимый сахарный диабет. Соединения по изобретению могут также применяться для лечения других нарушений, которые связаны с активностью провоспалительных цитокинов, присутствующих в повышенных концентрациях, таких как реакции на различные инфекционные агенты и многочисленные аутоиммунные заболевания, такие как ревматоидный артрит, синдром токсического шока, диабет и воспалительное заболевание кишечника, не относящиеся к перечисленным выше болезням, и которые описаны в разделе "Предпосылки создания изобретения".
Кроме того, поскольку соединения по изобретению являются ингибиторами продуцирования цитокинов, следует ожидать, что они должны блокировать экспрессию индуцибельной циклооксигеназы (СОХ-2). Установлено, что экспрессия СОХ-2 усиливается под действием цитокинов и предполагается, что эта циклооксигеназа представляет собой изоформу циклооксигеназы, которая ответственна за воспаление (М.К. O'Banion и др., Ргос. Natl. Acad. Sci. U.S.A., 89, 4888, 1992). Поэтому следует ожидать, что новые соединения по изобретению должны обладать эффективностью в отношении тех болезней, которые в настоящее время поддаются лечению ингибиторами СОХ, такими как обычные нестероидные противовоспалительные лекарственные средства (НСПВЛС). Такие нарушения включают острую и хроническую боль, а также воспалительные симптомы и сердечно-сосудистые заболевания.
Как указывалось в разделе "Предпосылки создания изобретения", IL-8 влияет на приток нейтрофилов в места воспаления или повреждения. Таким образом, в соответствии с еще одним объектом изобретения соединения по изобретению могут применяться для лечения болезней, которые в основном опосредуются нейтрофилами, таких как удар и инфаркт миокарда, возникшие в результате тромболитической терапии или независимо от нее, тепловое повреждение, респираторный дистресс-синдром взрослых (РДСВ), множественное повреждение органов в результате травмы, острый гломерулонефрит, дерматозы, включающие компоненты острого воспаления, острый гнойный менингит или другие нарушения центральной нервной системы, гемодиализ, лейкофериз, синдромы, связанные с трансфузией гранулоцитов, и некротический энтероколит.
Для терапевтических целей соединения по изобретению можно вводить в любой пригодной дозируемой форме любым обычным путем. К таким методам введения относятся (но не ограничиваясь только ими) внутривенный, внутримышечный, подкожный, интрасиновиальный, инфузия, подъязычный, чрезкожный, пероральный или введение путем ингаляции. Предпочтительными являются пероральный и внутривенный методы введения.
Соединения по изобретению можно вводить индивидуально или в сочетании с адъювантами, которые повышают стабильность ингибиторов, облегчают введение содержащих их фармацевтических композиций определенных типов, обеспечивают более высокую растворимость или диспергируемость, повышают ингибирующую активность, обеспечивают возможность вспомогательной терапии и т.п., а также с другими действующими веществами. При таких комбинированных терапиях предпочтительно используют меньшие дозы обычных терапевтических средств, что позволяет избежать возможных токсичных и вредных побочных действий, возникающих в том случае, когда такие агенты применяются для монотерапии. Соединения по изобретению могут быть объединены физическим путем с обычными терапевтическими средствами или другими адъювантами в одной фармацевтической композиции. Предпочтительно соединения следует вводить совместно в виде одной стандартной дозируемой формы. В конкретных вариантах осуществления фармацевтические композиции, включающие такие сочетания соединений, содержат по крайней мере приблизительно 5%, более предпочтительно по крайней мере приблизительно 20% (мас.%), соединения формулы (I), (Iа), (II) или (III) или комбинации этих соединений. Оптимальное процентное содержание (в мас.%) соединения по изобретению может варьироваться и должно определяться специалистами в данной области. В другом варианте соединения можно вводить по отдельности (либо последовательно, либо параллельно). Раздельное введение позволяет использовать более гибкий режим дозировки.
Как указывалось выше, дозируемые формы соединений по настоящему изобретению включают фармацевтически приемлемые носители и адъюванты, известные специалистам в данной области. Такие носители и адъюванты включают, например, ионообменные смолы, оксид алюминия, стеарат алюминия, лецитин, протеины из сыворотки, забуферивающие вещества, воду, соли или электролиты и соединения на основе целлюлозы. К предпочтительным дозируемым формам относятся таблетки, капсулы, каплетки, жидкости, растворы, суспензии, эмульсии, пастилки, сиропы, восстанавливаемые порошки, гранулы, суппозитории и трансдермальные бляшки. Методы приготовления таких дозируемых форм известны (см., например, Н.С. Ansel и N.G. Popovish, Pharmaceutical Dosage Forms and Drug Delivery Systems, 5-е изд., изд-во Lea and Febiger (1990)). Уровни доз и требования к ним являются хорошо известными в данной области, и их можно подбирать для конкретного пациента на основе доступных методов и средств. В определенных вариантах уровни доз составляют приблизительно 1-1000 мг/дозу для пациента весом 70 кг. Хотя может оказаться достаточным использовать одну дозу в день, тем не менее допустимо введение до 5 доз в день. При введении пероральным путем может потребоваться доза до 2000 мг/день. Специалист в данной области может самостоятельно определить, какие более низкие или более высокие дозы могут потребоваться в зависимости от конкретных факторов. Так, например, конкретные дозы и режимы введения могут зависеть от таких факторов, как общее состояние здоровья пациента, серьезность и протекание болезни у пациента или предрасположенность к ней, и они должны назначаться по решению лечащего врача.
Ниже изобретение проиллюстрировано на примерах. Эти примеры иллюстрируют предпочтительные варианты осуществления настоящего изобретения и не должны рассматриваться как ограничивающие каким-либо образом его объем.
Поскольку, как указано выше, приведенные ниже примеры носят иллюстративный характер, для специалистов в данной области очевидно, что при необходимости конкретные реагенты или условия проведения реакций для отдельных соединений можно соответствующим образом изменять. Исходные продукты, применяемые в описанных ниже реакциях, либо имеются в продаже, либо легко могут быть получены специалистами в данной области из имеющихся в продаже продуктов.
ОБЩИЕ МЕТОДЫ СИНТЕЗА
Соединения по изобретению можно получать по методу А, Б или В, как это проиллюстрировано на схеме I, предпочтительно по методу В. Дополнительно подобные методы описаны, например, в заявке PCT/US99/29165 и заявках на патент США 60/124148 и 60/165867. Каждая из указанных заявок в полном объеме включена в настоящее описание в качестве ссылки.
На приведенной выше схеме D соответствует радикалу Ar1 (для соединений формул I и Iа) или G (для соединения формулы II или III), D' представляет собой группу Ar2-X-Y-Z (или ее предшественник) для соединений формул I и Iа или группу Ar-X-Y-Z (или ее предшественник) для соединения формулы II или III.
Согласно методу А смесь амина формулы IV и изоцианата формулы V растворяют в непротонном безводном растворителе, таком как ТГФ, простой эфир, толуол, диоксан или этилацетат. Предпочтительным растворителем является ТГФ. Смесь перемешивают при температуре от 0 до 45°С, предпочтительно при 25°С, в течение 2-24 ч и удаляют летучие компоненты. В результате очистки остатка перекристаллизацией из пригодного для этой цели растворителя, такого как этилацетат/гексаны, этилацетат/метанол, ТГФ/петролейный эфир, этанол/вода, или хроматографией на силикагеле с использованием, например, гексанов и этилацетата в качестве элюентов, получают продукт формулы I, Iа, II или III (E означает NH).
Согласно методу Б амин формулы IV растворяют в галогенированном растворителе, таком как метиленхлорид, хлороформ или дихлорэтан. Предпочтительным растворителем является метиленхлорид. Смесь разбавляют водной щелочью, такой как бикарбонат натрия или карбонат калия, охлаждают на ледяной бане и добавляют фосген. Смесь интенсивно перемешивают в течение 5-30 мин, предпочтительно в течение 10 мин. Органический слой сушат с помощью такого агента, как MgSO4 или Na2SO4, и удаляют летучие компоненты с получением соответствующего изоцианата D-N=C=O. Затем этот изоцианат и амин формулы VI смешивают в непротонном безводном растворителе, таком как ТГФ, простой эфир, толуол, диоксан, метиленхлорид или этилацетат. Предпочтительным растворителем является ТГФ. Смесь перемешивают при температуре от 0 до 45°С, предпочтительно при 25°С, в течение 2-24 ч и удаляют летучие компоненты. В результате очистки остатка перекристаллизацией или хроматографией на силикагеле, как это указано выше, получают продукт формулы I, Ia, II или III (E означает NH).
Необходимый изоцианат можно получить также из карбоновой кислоты D-СО2Н взаимодействием с хлорформиатом, таким как этилхлорформиат, в присутствии приемлемого основания, такого как триэтиламин, в пригодном для этой цели растворителе, таком как ТГФ, при температуре примерно 0°С. Полученный смешанный ангидрид обрабатывают водным раствором азида натрия. При нагревании раствора полученного ацилазида в пригодном для этой цели растворителе, таком как толуол, примерно при температуре перегонки, происходит перегруппировка по реакции Курциуса, приводящая к получению in situ изоцианата D-N=C=O.
Согласно методу В амин формулы IV растворяют в приемлемом растворителе, таком как галогенированный растворитель, например метиленхлорид, хлороформ или дихлорэтан. Предпочтительным растворителем является метиленхлорид. При этом можно добавлять приемлемое основание, такое как триэтиламин, а затем фенилхлорформиат. Смесь перемешивают при температуре от 0 до 85°С, предпочтительно при температуре перегонки, в течение 2-24 ч и удаляют летучие компоненты с получением карбамата формулы VII. Этот карбамат и амин формулы VI смешивают в непротонном безводном растворителе, таком как ТГФ, простой эфир, толуол, диоксан, метиленхлорид или этилацетат. Предпочтительным растворителем является ТГФ. Смесь перемешивают при температуре от 0 до 110°С, предпочтительно при температуре перегонки, в течение 2-24 ч и удаляют летучие компоненты. После очистки остатка, как это описано выше, получают продукт формулы I, Ia, II или III (E означает NH). Этот метод можно осуществлять и в обратной последовательности, т.е. сначала можно получать карбамат из D'NH2 и подвергать этот карбамат взаимодействию с амином D-NH2. В примере 37 описан процесс синтеза соединения формулы III, в котором Е означает -О-, а в примере 38 рассмотрен синтез соединения формулы III, в котором Е означает -CH2-.
Способ, используемый для получения аминов формулы IV, зависит от природы целевой группы D. В целом промежуточные продукты формулы IV можно получать по методам, известным в данной области. Некоторые из подобных общих методов проиллюстрированы на приведенных ниже схемах. Соединения D'-NCO или D'-NH2 на схеме I являются коммерчески доступными соединениями или могут быть получены по методам, известным в данной области. Если D' является предшественником группы Ar2-X-Y-Z или Ar-X-Y-Z, то целевой конечный продукт формулы I, Ia, II или III можно получать по методам, известным в данной области. Иллюстративные примеры таких методов представлены в приведенном ниже разделе "Примеры синтеза".
Аминопиразолы формулы XV, необходимые для получения соединений формулы I или Iа, можно получать в соответствии со схемой II. Гидразин формулы X, несущий заместитель R3, можно получать по методу Г или Д. Согласно методу Г арилбромид формулы VIII растворяют в непротонном инертном растворителе, таком как ТГФ, 1,4-диоксан или диэтиловый эфир, и охлаждают до низкой температуры в инертной атмосфере. При этом предпочтительной для раствора является температура -77°С. После этого по каплям добавляют сильное основание, растворенное в непротонном инертном растворителе, таком как гексаны, ТГФ или простой эфир, поддерживая реакционную температуру ниже 0°С, предпочтительно ниже -60°С. Предпочтительными основаниями являются алкиллитиевые реагенты, наиболее предпочтительно втор-бутиллитий. После добавления основания реакционную смесь перемешивают в течение 30-90 мин до тех пор, пока не израсходуется исходный арилбромид. Далее добавляют избыток диалкилазодикарбоксилата, поддерживая реакционную температуру ниже 0°С, предпочтительно ниже -60°С. В качестве диалкилазодикарбоксилата предпочтительно использовать ди-трет-бутилазодикарбоксилат. Реакционную смесь перемешивают при пониженной температуре и по истечении 0,5-2 ч нагревают до комнатной температуры. Реакцию прекращают добавлением воды и продукт экстрагируют непротонным растворителем, таким как этилацетат, диэтиловый эфир или хлороформ. Органические слои сушат с помощью таких агентов, как MgSO4 или Na2SO4, и удаляют летучие компоненты. Остаток растворяют в протонном растворителе, таком как метанол или изопропанол, охлаждают, предпочтительно до 0-5°С, и обрабатывают кислотой. При этом предпочтительно использовать соляную, бромистоводородную, серную и трифторуксусную кислоту. Наиболее предпочтительна соляная кислота в газообразной форме. После добавления избытка кислоты смесь выдерживают при температуре перегонки растворителя до тех пор, пока не израсходуется весь исходный материал. После охлаждения полученную арилгидразинную соль формулы Х фильтруют и сушат.
Согласно методу Д ариламин, несущий заместитель R3 (формула IX), растворяют в концентрированной водной кислоте, такой как соляная, бромистоводородная или серная кислота, и охлаждают до температуры ледяной бани. При этом наиболее предпочтительна соляная кислота с коцентрацией от 3 н. до 8 н., более предпочтительно 6 н. Затем по каплям добавляют агент нитрозирования в воде, поддерживая пониженную температуру. Предпочтительной при этом является температура 0-5°С. Предпочтительным реагентом является нитрит натрия. Реакционную смесь перемешивают в течение 10-90 мин и затем добавляют восстановитель, поддерживая пониженную температуру. Предпочтительна при этом температура 0-5°С. В качестве восстановителя можно использовать цинк, железо, иодид самария и хлорид олова(II). Наиболее предпочтительным восстановителем является хлорид олова (II), растворенный в водной соляной кислоте с концентрацией от 3 н. до 8 н., более предпочтительно 6 н. Реакционную смесь перемешивают в течение 0,5-3 ч и затем реакцию прекращают добавлением щелочи с доведением значения рН до 12-14. При этом можно использовать такие щелочные реагенты, как гидроксид натрия, гидроксид калия, гидроксид лития и гидроксид кальция. Наиболее предпочтительным щелочным реагентом является гидроксид калия. Водный раствор экстрагируют непротонным органическим растворителем, таким как диэтиловый эфир, хлороформ, этилацетат и метиленхлорид. Органические слои сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты с получением арилгидразина (формула X), который можно использовать в последующей реакции без дополнительной очистки.
β-Кетонитрил, несущий заместитель R1 (формула XIV), можно получать в соответствии с методом Е или Ж. Согласно методу Е гидрид металла, такой как гидрид натрия, гидрид калия или гидрид лития, суспендируют в безводном инертном непротонном растворителе, таком как диэтиловый эфир, ТГФ и диоксан, при температуре в пределах от 35 до 85°С. Наиболее предпочтительным гидридом металла является гидрид натрия, а наиболее предпочтительным растворителем является ТГФ при температуре 75°С. Затем в безводном инетрном непротонном растворителе, таком как диэтиловый эфир, ТГФ или диоксан, растворяют алкиловый эфир, предпочтительно метиловый эфир (формула XI), и ацетонитрил и полученный раствор по каплям добавляют к вышеуказанной суспензии гидрида металла. Предпочтительным растворителем является ТГФ. Смесь выдерживают при повышенной температуре в течение 3-24 ч, охлаждают до комнатной температуры и разбавляют непротонным растворителем и водной кислотой. Затем органический слой промывают водой и рассолом, сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты с получением β-кетонитрила (формула XIV), который можно использовать далее без дополнительной очистки.
В другом варианте согласно методу Ж раствор сильного основания, такого как алкиллитий и амид металла, например н-бутиллитий, втор-бутиллитий, метиллитий и диизопропиламид лития, в безводном инертном непротонном растворителе, таком как диэтиловый эфир, ТГФ и диоксан, охлаждают до температуры ниже 0°С. Предпочтительным основанием является н-бутиллитий, предпочтительным растворителем является ТГФ, а предпочтительной температурой является температура в -77°С. Далее по каплям добавляют раствор цианоуксусной кислоты (формула XII) в безводном инертном непротонном растворителе, таком как диэтиловый эфир, ТГФ и диоксан, более предпочтительно ТГФ, поддерживая температуру реакции ниже 0°С, предпочтительно на уровне -77°С. Реакционную смесь перемешивают в течение 10-45 мин, нагревая ее до 0°С. Раствор дианиона цианоуксусной кислоты охлаждают до температуры ниже -25°С, предпочтительно до -77°C. Далее добавляют хлорангидрид алкиловой кислоты (формула XIII), растворенный в безводном инертном непротонном растворителе, таком как диэтиловый эфир, ТГФ и диоксан, более предпочтительно ТГФ. Реакционную смесь нагревают в течение 10-30 мин до 0°С и реакцию прекращают добавлением водной кислоты. Продукт экстрагируют органическим растворителем, таким как хлороформ, этилацетат, простой эфир и метиленхлорид. Объединенные органические экстракты сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты с получением β-кетонитрила (формула XIV), который можно использовать далее без дополнительной очистки.
Целевой аминопиразол (формула XV) можно получать затем в соответствии с методом З или И. Согласно методу З арилгидразин формулы Х и β-кетонитрил формулы XIV смешивают в органическом растворителе, таком как толуол, этанол, изопропанол или трет-бутанол. Предпочтительным растворителем является этанол. Далее добавляют кислоту, такую как соляная кислота, п-толуолсульфоновая кислота или серная кислота. Предпочтительной кислотой является коцентрированная соляная кислота. Далее смесь в течение 10-24 ч выдерживают с нагреванием при температуре 50-100°С, предпочтительно при 80°С, и затем охлаждают до комнатной температуры.
Смесь разбавляют непротонным органическим растворителем, таким как этилацетат, простой эфир, хлороформ или метиленхлорид, и промывают водной щелочью, такой как бикарбонат натрия и карбонат калия. Органический слой сушат с помощью таких агентов, как MgSO4 и Na4SО4, и удаляют летучие компоненты с получением остатка, который очищают перекристаллизацией или хроматографией на силикагеле с использованием гексанов и этилацетата в качестве элюентов. Далее фракции с высоким содержанием продукта собирают и удаляют летучие компоненты с получением целевого аминопиразола (формула XV).
В другом варианте согласно методу И арилгидразин формулы Х и β-кетонитрил формулы XIV смешивают в органическом растворителе, таком как толуол, этанол, изопропанол или трет-бутанол. Предпочтительным растворителем является толуол. Смесь выдерживают при температуре перегонки в течение 3-24 ч с азеотропным удалением воды и после переработки, описанной выше, получают аминопиразол формулы XV.
Другие необходимые аминогетероциклы, которые могут использоваться в синтезе соединений формулы I или Iа, можно получать по методам, известным в данной области и описанным в литературе. Приведенные на последующих схемах III-XV примеры носят иллюстративный характер, и поэтому, что очевидно для специалистов в данной области, конкретные реагенты и условия проведения реакций могут изменяться в зависимости от индивидуальных соединений. Промежуточные продукты, используемые в реакциях на приведенных ниже схемах, либо являются коммерчески доступными, либо могут быть простым путем получены специалистами в данной области из коммерчески доступных материалов.
На схеме III, метод К, проиллюстрирован общий процесс синтеза целевых аминотиофенов.
Смесь 1-арил-5-алкилбутан-1,4-диона (XVI) и сульфатирующего агента, такого как реагент Лавессона (Lawesson) или сульфид фосфора (V), предпочтительно реагент Лавессона, растворяют в непротонном безводном растворителе, таком как толуол, ТГФ или диоксан. Предпочтительным растворителем является толуол. Смесь выдерживают с нагреванием при повышенной температуре, предпочтительно при температуре перегонки растворителя, в течение 1-10 ч. После удаления летучих компонентов остаток очищают хроматографией на силикагеле с использованием гексанов и этилацетата в качестве элюента. Фракции с высоким содержанием продукта собирают и удаляют летучие компоненты с получением замещенного тиофена формулы XVII.
Этот замещенный тиофен формулы XVII растворяют в таком растворителе, как уксусный ангидрид или уксусная кислота. Предпочтительным растворителем является уксусный ангидрид. Смесь охлаждают до 0-30°С, предпочтительно до -10°С. Далее добавляют раствор концентрированной азотной кислоты в таком растворителе, как уксусный ангидрид или уксусная кислота, предпочтительно уксусный ангидрид, охлаждая смесь до 0-30°С, предпочтительно до -10°С. Далее смесь перемешивают в течение 10-120 мин, сливают на лед и экстрагируют непротонным растворителем, таким как диэтиловый эфир, хлороформ, этилацетат или метиленхлорид. Органические экстракты промывают водной щелочью, сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты. Остаток очищают хроматографией на силикагеле с использованием гексанов и этилацетата в качестве элюентов. Фракции с высоким содержанием продукта собирают и удаляют летучие компоненты с получением 2-арил-5-алкил-3-нитротиофена. Этот 2-арил-5-алкил-3-нитротиофен восстанавливают с помощью металла, такого как железо, олово или цинк, или каталитическим гидрированием. Предпочтительно для восстановления использовать железо в уксусной кислоте и проводить такое восстановление при температуре в интервале от 50 до 110°С, более предпочтительно при 100°С, в течение 5-30 мин. После охлаждения до комнатной температуры реакционную смесь разбавляют водой, нейтрализуют щелочью, такой как гидроксид натрия, гидроксид калия, карбонат калия или бикарбонат натрия, и экстрагируют непротонным растворителем, таким как диэтиловый эфир, этилацетат или метиленхлорид. Органические экстракты сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты с получением целевого аминотиофена формулы XVIII.
На схеме IV проиллюстрирован общий метод получения требуемых аминофуранов, как это описано у Stevenson и др. (J. Am. Chem. Soc., 1937, 59, 2525). При этом этилароилацетат (формула XIX) растворяют в непротонном растворителе, таком как простой эфир или ТГФ, и обрабатывают сильным основанием, таким как натрий, этоксид натрия или гидрид натрия, и полученный анион подвергают взаимодействию с бромметилалкилкетоном (формула XX) при пониженной температуре, например при 0°С. После перемешивания реакционной смеси до тех пор, пока не израсходуется весь исходный материал, ее сливают в холодную воду и экстрагируют непротонным растворителем. Затем объединенные экстракты сушат с помощью таких агентов, как MgSО4 или Na2SO4. Полученный дикетоэфир (формула XXI) можно использовать в последующем без дополнительной очистки или очищать перегонкой либо хроматографией на силикагеле. Далее дикетоэфир в протонном растворителе, таком как этанол, нагревают в присутствии минеральной кислоты, такой как серная или соляная кислота, в течение 5-10 ч и экстрагируют непротонным растворителем. Затем объединенные экстракты сушат с помощью таких агентов, как MgSO4 или Na2SO4. Полученный фурановый эфир (формула XXII) можно использовать в последующем без дополнительной очистки или очищать перегонкой либо хроматографией на силикагеле. Далее этот фурановый эфир в протонном растворителе, таком как этанол, обрабатывают гидразингидратом и смесь выдерживают с нагреванием в течение 2-5 дней. После этого гидразин выделяют по описанной выше методике и обрабатывают горячей муравьиной кислотой, после чего полученный фуранамин (формула XXIII) очищают перегонкой или хроматографией на силикагеле.
Замещенные 4-аминооксазолы можно синтезировать аналогично методу, описанному у Lakhan и др. (J. Het. Chem., 1988, 25, 1413) и проиллюстрированному на схеме V. При этом смесь ароилцианида (формула XXIV), альдегида, (формула XXV) и безводного ацетата аммония в уксусной кислоте выдерживают с нагреванием при 100-110°С в течение 3-6 ч, охлаждают до комнатной температуры и затем реакцию прекращают добавлением воды. После экстракции непротонным растворителем получают продукт формулы XXVI, который можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
Замещенные 3-аминопирролы (формула XXX) можно синтезировать аналогично методу, описанному у Aiello и др., J. Chem. Soc. Perkins Trans. I, 1981, 1. Этот метод проиллюстрирован на схеме VI. При этом смесь арилдиоксоалкана (формула XXVII) и амина (формула XXVIII) в уксусной кислоте выдерживают с нагреванием при 100-110°С в течение 3-6 ч и затем перерабатывают обычным образом. После этого полученный продукт (формула XXIX) в уксусной кислоте обрабатывают агентом нитрования, таким как азотная кислота или нитрат калия в концентрированной серной кислоте. Смесь сливают далее в холодную воду и экстрагируют непротонным растворителем. Затем объединенные экстракты сушат с помощью таких агентов, как MgSO4 и Na2SO4. Полученный после удаления летучих компонентов нитропиррол можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле. Этот нитропиррол восстанавливают до амина с помощью железа в уксусной кислоте или путем каталитического гидрирования с использованием палладия на активированном угле. Полученный аминопиррол (формула XXX) можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
Аналогичным образом смесь амина формулы XXXI и 3-арил-2,5-диоксоалкана (формула XXXII) в уксусной кислоте выдерживают с нагреванием при 80-110°С в течение 2-24 ч. Затем реакционную смесь разбавляют водой и экстрагируют органическим растворителем. После этого объединенные экстракты сушат с помощью таких агентов, как MgSO4 или Na2SO4, и затем удаляют летучие компоненты. Полученный пиррол обрабатывают агентом нитрования и затем по описанной выше методике восстанавливают до соединения формулы XXXIII. Полученный продукт можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле. Этот процесс проиллюстрирован на схеме VII.
Замещенные 5-аминотиазолы (формула XXXVII) можно получать аналогично методу, описанному у Gerwald и др., J. Prakl. Chem. 1973, 315, 539.
Как показано на схеме VIII, к смеси аминоцианида формулы XXXIV, альдегида формулы XXXV и серы в безводном растворителе, таком как этанол или метанол, но каплям добавляют основание, такое как триэтиламин. Смесь выдерживают с нагреванием при 50°С в течение 1-3 ч. После этого смесь охлаждают и удаляют избыток серы. Далее к смеси для ее нейтрализации добавляют уксусную кислоту и собирают твердое вещество. Полученный имин формулы XXXVI обрабатывают кислотой, такой как соляная или толуолсульфоновая кислота, в воде и органическом растворителе. После израсходования исходного материала реакционную смесь подвергают переработке, получая продукт формулы XXXVII, который можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
Замещенные 2-аминотиофены (формула XXXIX) можно синтезировать аналогично методу, описанному у Gewald и др. (J. Prakt. Chem., 1973, 315, 539) и проиллюстрированному на схеме IX. При этом смесь дизамещенной тиофен-3-карбоновой кислоты (формула XXXVIII) в протонном растворителе, таком как уксусная кислота, обрабатывают при температуре 0-50°С агентом нитрования, таким как азотная кислота или нитрат калия в концентрированной серной кислоте. После израсходования исходного материала реакционную смесь сливают на лед и продукт экстрагируют непротонным растворителем. Объединенные экстракты сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты. Полученный нитротиофен восстанавливают до амина с помощью железа в уксусной кислоте или каталитическим гидрированием с использованием палладия на активированном угле. Полученный аминотиофен можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
1,5-дизамещенные 3-аминопиразолы (формула XLII) можно получать в соответствии со схемой Х аналогично методу, описанному у Ege и др. (J. Het. Chem., 1982, 19, 1267). При этом к безводному трет-бутанолу добавляют калий и смесь охлаждают до 5°С. После этого добавляют гидразин формулы XL, a затем цианодибромалкан формулы XLI. Далее смесь в течение 3-10 ч нагревают с обратным холодильником при температуре перегонки. После этого смесь охлаждают до комнатной температуры и сливают на смесь воды со льдом. Полученный продукт экстрагируют органическим растворителем. Объединенные экстракты сушат с помощью таких агентов, как MgSO4 или Na2SO4, и удаляют летучие компоненты. Полученный продукт формулы XLII можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
2-амино-3,5-дизамещенные тиофены можно синтезировать в соответствии со схемой XI аналогично методу, описанному у Knoll и др., J. Prakt. Chem., 1985, 327, 463. При этом смесь замещенного N-(3-аминотиоакрилоил)формамидина (формула XLIII) и замещенного бромида (формула XLIV) в протонном растворителе, таком как метанол или этанол, нагревают, предпочтительно выдерживают при температуре перегонки, в течение 5-30 мин и затем охлаждают до температуры ниже комнатной. Полученный тиофенимин фильтруют и сушат. Далее тиофенимин формулы XLV обработкой водной кислотой превращают в тиофенамин (формула XLVI).
1,4-дизамещенные 2-аминопирролы (формула L) можно синтезировать аналогично методу, описанному у Brodrick и др. (J. Chem. Soc. Perkin Trans. I, 1975, 1910) и проиллюстрированному на схеме XII. При этом калиевую соль формилнитрила формулы XLVII в воде обрабатывают амином формулы XLVIII и уксусной кислотой и смесь выдерживают с нагреванием при 50-90°С в течение 5-30 мин. После охлаждения полученный аминонитрил формулы XLIX собирают фильтрацией и затем перемешивают при комнатной температуре в присутствии основания, такого как этанольный этоксид калия, в течение 2-5 ч и удаляют летучие компоненты. Остаток разбавляют водой и экстрагируют органическим растворителем. Объединенные экстракты сушат с помощью таких агентов, как MgSO4 и Na2SO4, и удаляют летучие компоненты. Полученный продукт (формула L) можно использовать в последующем без дополнительной очистки или очищать перекристаллизацией либо хроматографией на силикагеле.
1,2-дизамещенные 4-аминоимидазолы (формула LII) можно получать восстановлением соответствующего нитросоединения (формула LI), например с помощью железа в уксусной кислоте или каталитическим гидрированием, по методу, описанному у Al-Shaar и др. (J. Chem. Soc. Perkin Trans. I, 1992, 2779) и проиллюстрированному на схеме XIII.
2,4-дизамещенные 5-аминооксазолы (формула LVII) можно получать аналогично методу, описанному у Poupaert и др. (Synthesis, 1972, 622) и проиллюстрированному на схеме XIV. При этом хлорангидрид кислоты формулы LIII добавляют к охлажденной смеси 2-аминонитрила формулы LIV и основания, такого как триэтиламин, в непротонном растворителе, таком как ТГФ, бензол, толуол или простой эфир. Предпочтительна при этом температура 0°С. Смесь перемешивают в течение 12-24 ч и промывают водой. После удаления летучих компонентов полученный продукт формулы LV обрабатывают этилмеркаптаном и сухим хлористым водородом в сухом метиленхлориде в течение 5-30 мин. Твердый гидрохлорид 5-имино-1,3-оксазола (формула LVI) собирают фильтрацией, растворяют в сухом пиридине и раствор насыщают гидросульфидом в течение 4 ч при 0°С. Смесь разбавляют органическим растворителем, промывают водой и сушат. После удаления летучих компонентов получают 5-амино-1,3-оксазол (формула LVII), который можно использовать в последующем без дополнительной очистки или очищать хроматографией на силикагеле.
1,4-дизамещенные 2-аминопиразолы можно синтезировать в соответствии со схемой XV по методу, описанному у Lancini и др., J. Het. Chem., 1966, 3, 152. При этом к смеси замещенного аминокетона (формула LVIII) и цианамида в воде и уксусной кислоте добавляют водный гидроксид натрия до тех пор, пока значение рН не достигнет 4,5. После этого смесь выдерживают с нагреванием при 50-90°С в течение 1-5 ч, охлаждают и подщелачивают гидроксидом аммония. Полученный продукт формулы LIX собирают фильтрацией и сушат.
Ариламинное и гетероариламинное промежуточные продукты формулы IV (G-NH2) для синтеза соединений формул II и III являются либо коммерчески доступными продуктами, либо могут быть легко получены по методам, известным в данной области. Так, например, необходимые ариламины и гетероариламины можно получить нитрованием и восстановлением замещенного арильного или гетероарильного кольца, как это проиллюстрировано для синтеза некоторых 5-членных гетероциклических аминов (Ar1-NH2) на приведенных выше схемах. В другом варианте замещенный ариловый эфир можно превращать в ариламин, как это проиллюстрировано для замещенного фурана на приведенной выше схеме IV и описано ниже в примере 17. В разделе "Примеры синтеза" описаны процессы получения и других соединений G-NH2 и Ar1-NH2.
Методы, позволяющие получать промежуточные продукты формул V и VI (схема I, D' означает группу Ar-X-Y-Z или Ar2-X-Y-Z), описаны ниже.
Согласно методу Л (схема XVI) бромариламин формулы LX, который либо может быть коммерчески доступным продуктом, либо может быть легко получен специалистом в данной области, подвергают взаимодействию с циклоалкеноном формулы LXI в присутствии катализатора на основе переходного металла, например катализатора на основе палладия(II), такого как хлорид бис (трифенилфосфин) палладия (II), и в присутствии бис(трифенилфосфинового) хелатирующего агента, такого как 1,2-бис (дифенилфосфино) этан (ДФФЭ), 1,1'-бис(дифенилфосфино)ферроцен (ДФФФ) или 1,3-бис(дифенилфосфино)пропан (ДФФП), предпочтительно ДФФФ, и основания, предпочтительно бикарбоната натрия, в приемлемом растворителе, предпочтительно в ДМФ, при температуре примерно 150°С с получением соединения формулы LXII. Это соединение формулы LXII можно затем использовать (в виде соединения формулы VI) в методе Б (схема I) или превращать в изоцианат формулы LXIII взаимодействием с фосгеном или эквивалентом фосгена в присутствии основания, такого как бикарбонат натрия, в приемлемом растворителе, таком как дихлорметан, при температуре примерно 0°С и использовать (в виде соединения формулы V) в методе А. Полученный продукт формулы LXIV можно далее модифицировать методами, известными специалистам в данной области, с получением целевых соединений формулы I, как это описано в приведенных ниже примерах синтеза.
Согласно методу М бромид формулы LXV подвергают взаимодействию в присутствии сильного основания, такого как трет-бутиллитий, в приемлемом растворителе, таком как ТГФ, с хлоридом трибутилолова при температуре в интервале от примерно -50 до -100°С, предпочтительно примерно при -78°С, с получением соединения формулы LXVI. Это соединение формулы LXVI подвергают далее взаимодействию с соединением формулы LX в приемлемом растворителе, таком как ТГФ или 1,4-диоксан, в присутствии катализатора на основе переходного металла, предпочтительно тетракис (трифенилфосфин) палладия (0), при температуре от примерно 50 до 150°С, предпочтительно примерно при 100°С, в герметично укупоренной трубке с получением соединения формулы LXVII. Затем это соединение формулы LXVII можно использовать (в виде соединения формулы VI) в методе Б или В (схема I) или превращать в соответствующий изоцианат, как это описано для метода Л, и использовать (в виде соединения формулы V) в методе А.
На схеме XVII проиллюстрированы методы, позволяющие присоединять Y и Z к X. Согласно методу методу Н при необходимости получить продукт, в котором Y включает аминный азот, присоединенный к X, группу X, содержащую кетон, можно подвергать взаимодействию с группой Y-Z, содержащий концевой первичный или вторичный амин, в условиях гидроаминирования. Так, например, кетон формулы LXIV объединяют с первичным или вторичным амином в приемлемом растворителе, таком как ТГФ. Далее добавляют кислоту, такую как уксусная кислота, а затем приемлемый восстановитель, предпочтительно цианоборогидрид натрия или (триацетокси)борогидрид натрия, с получением целевого продукта формулы LXVIII.
На примере метода О проиллюстрирован процесс получения метиленовой группы для Y и первичного или вторичного амина для Z. При этом группу X, несущую альдегид и галоген, предпочтительно бром (формула LXIX), можно подвергать взаимодействию с первичным или вторичным амином в условиях гидроаминирования, как это описано для метода Н, с получением соединения формулы LXX. Этот промежуточный продукт можно затем использовать аналогично методу М.
Как и в рассмотренных выше случаях, дополнительные промежуточные продукты, соответствующие формулам V, VI и VII, можно синтезировать по методам, аналогичным описанным в литературе или известным специалистам в данной области. Несколько примеров подобного синтеза приведены ниже в разделе "Примеры синтеза".
ПРИМЕРЫ СИНТЕЗА
Пример 1
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-циклогексенон-3-ил)нафталин-1-ил]мочевина
Согласно описанному выше методу Л в герметично укупориваемую трубку объемом 350 мл в инертной атмосфере помещают 4-бром-1-нафтиламин (LXXI) (1,97 г, 8,9 ммоля, 1 экв.), 2-циклогексенон (1,65 г, 17,2 ммоля, 1,9 экв.), порошковый бикарбонат натрия (2,17 г, 25,8 ммоля, 2,9 экв.), 1,3-бис(дифенилфосфино)пропан (177 мг, 0,43 ммоля, 0,05 экв.), хлорид бис (трифенилфосфин) палладия (II) (302 мг, 0,43 ммоля, 0,05 экв.) и ДМФ (дегазированный, 100 мл). Смесь выдерживают с нагреванием при 150°С в течение 8 ч. После охлаждения вновь до окружающей температуры смесь разбавляют 100 мл EtOAc и фильтруют через диатомовую землю. После этого раствор переносят в делительную воронку и промывают водой (100 мл) и насыщенным рассолом (100 мл). После сушки над MgSO4 летучие компоненты удаляют в вакууме. Затем продукт очищают колоночной хроматографией с использованием EtOAc (от 10 до 50%) в гексанах в качестве элюента с получением 1,3 г материала, который перекристаллизовывают из горячей смеси EtOAc/гексаны с получением 800 мг соединения формулы LXXII (3,4 ммоля, выход 38%) в виде темно-коричневого твердого вещества.
Соединение формулы LXXII (100 мг, 0,42 ммоля, 1 экв.) растворяют в метиленхлориде (20 мл) и добавляют насыщенный водный раствор бикарбоната натрия (20 мл). Смесь интенсивно перемешивают при 0°С в течение 15 мин. Далее перемешивание прерывают и к органическому слою одной порцией с помощью шприца добавляют фосген (примерно 2,0-молярный раствор в толуоле, 0,63 мл, 1,26 ммоля, 3,0 экв.). Непосредственно после этого перемешивание возобновляют и продолжают при 0°С в течение 20 мин. Затем слои разделяют, после чего водную фазу экстрагируют метиленхлоридом (1×25 мл). Объединенные органические фазы сушат (Na2SO4), фильтруют и 3/4 растворителя удаляют в вакууме. Непосредственно после этого этот раствор изоцианата формулы LXXIII разбавляют безводным ТГФ (8 мл) и обрабатывают соединением формулы LXXIV при комнатной температуре (метод А). Далее смесь оставляют перемешиваться в течение ночи в атмосфере азота, после чего добавляют МеОН (2 мл) и летучие компоненты удаляют в вакууме. Таким путем получают указанное в заголовке соединение 1 в виде оранжевого/красного пенистого вещества (200 мг, 0,41 ммоля, 74%). Этот продукт дважды нерекристаллизовывают в течение ночи из EtOAc с получением 49 мг желтых кристаллов (tпл 168-170°С).
Пример 2
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-{4-[3-(морфолин-4-ил)циклогексен-1-ил]нафталин-1-ил}мочевина
Согласно описанному выше методу Н продукт из примера (1) (93 мг, 0,19 ммоля, 1 экв.) и морфолин (30 мкл, 0,34 ммоля, 1,8 экв.) растворяют в 1,0 мл безводного ТГФ и обрабатывают уксусной кислотой (16 мкл, 0,28 ммоля, 1,5 экв.) и (триацетокси)борогидридом натрия (80 мг, 0,39 ммоля, 2 экв.). Реакционную смесь перемешивают при комнатной температуре в течение 2 дней, а затем добавляют 5%-ный водный раствор NaOH (3 мл) и после этого реакционную смесь экстрагируют EtOAc (3×3 мл). Объединенные органические фазы промывают однократно водой, а затем рассолом, сушат (Na2SO4), фильтруют и растворители удаляют в вакууме. После колоночной хроматографии с использованием ЕtOAc/гексанов в качестве элюента получают 64 мг пенистого вещества желтовато-коричневого цвета (0,11 ммоля, 60%). Этот продукт повторно хроматографируют с использованием 5%-ного МеОН в метиленхлориде с получением указанного в заголовке соединения 2 в виде пенистого вещества светло-фиолетового цвета (50 мг).
Пример 3
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-{4-[5-(морфолин-4-илметил)фур-2-ил]нафталин-1-ил}мочевина
Согласно описанному выше методу О к смеси 5-бром-2-фуральдегида (LXXV) (1,76 г) и морфолина (1,00 мл) в 40 мл безводного ТГФ при комнатной температуре добавляют уксусную кислоту (0,60 мл), а затем триацетоксиборогидрид натрия (3,28 г). Смесь перемешивают при комнатной температуре в течение 3 ч и затем сливают в насыщенный раствор бикарбоната натрия (100 мл). После интенсивного перемешивания в течение 5 мин слои разделяют и водный слой экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 2,09 г (8,49 ммоля, выход 84%) соединения LXXVI.
Согласно описанному выше методу М соединение LXXVI (0,678 г, 2,76 ммоля) растворяют в 10 мл безводного ТГФ в атмосфере инертного газа и раствор охлаждают до -78°С. Далее по каплям добавляют трет-бутиллитий (4,0 мл 1,7-молярного раствора в пентане) и раствор перемешивают при -78°С в течение 30 мин. После этого добавляют хлорид трибутилолова (0,60 мл, 0,72 г, 2,2 ммоля) и раствор перемешивают еще в течение 30 мин при -78°С. Затем добавляют буфер с рН 7 (насыщ. NaH2PO4/Na2HPO4) (10 мл) и смесь нагревают до комнатной температуры. Слои разделяют и водный слой экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 0,526 г (1,15 ммоля, выход 42%) соединения LXXVII.
Это соединение LXXVII (0,399 г, 0,874 ммоля) и соединение LXXI (0,200 г, 0,901 ммоля) согласно описанному выше методу М растворяют в 10 мл безводного 1,4-диоксана в герметично укупориваемой трубке в атмосфере инертного газа. Раствор дегазируют и продувают азотом (дважды). Далее добавляют тетракис(трифенилфосфин)палладий (0) (0,057 г, 0,049 ммоля), после чего раствор дегазируют и вновь продувают азотом (дважды). Трубку герметично укупоривают и нагревают до 100°С в течение 24 ч. После охлаждения до комнатной температуры смесь разбавляют EtOAc, добавляют насыщенный водный раствор карбоната калия (10 мл) и смесь перемешивают в течение 1 ч при комнатной температуре. Далее смесь фильтруют через диатомовую землю и слои разделяют. Водный слой экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 0,314 г желтого масла, которое содержит соединение LXXVIII наряду с бромидом трибутилолова. Эту смесь используют на следующей стадии без дополнительной очистки.
Соединение LXXVIII (0,283 г, 0,917 ммоля) подвергают взаимодействию с фенилкарбаматом LXXIV (0,395 г, 1,13 ммоля) в соответствии с методом В. Полученный продукт очищают экспресс-хроматографией с получением указанного в заголовке соединения 3 в виде желтого твердого вещества (0,338 г, 0,600 ммоля, выход 65%), который дополнительно очищают перекристаллизацией с получением 0,131 г указанного в заголовке соединения 3 (tпл 144-146°С).
Пример 4
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-{4-[6-(морфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина
Аналогично методу, описанному у R.J. Chambers и A. Marfat (Synthetic Communications, 1997, 27, 515), смесь 2,5-дибромпиридина (LXXIX) (9,90 г, 41,78 ммоля), Рd(ДФФФ)Cl2 (1,51 г, 1,85 ммоля), безводного МеОН (40 мл), безводного ДМФ (40 мл) и безводного триэтиламина (12 мл) в течение 10 мин продувают в аппарате Парра потоком моноксида углерода и затем перемешивают при давлении моноксида углерода 80 фунтов/кв.дюйм при 50°С в течение 4 ч. Смесь разбавляют EtOAc (600 мл), промывают водой (2×100 мл) и рассолом (1×100 мл), сушат (сульфат натрия), фильтруют и упаривают досуха. Остаток очищают экспресс-хроматографией на силикагеле (40%-ный EtOAc в гексанах) с получением соединения LXXX в виде светло-оранжевого твердого вещества (3,733 г, 17,28 ммоля, 41%).
К раствору соединения LXXX (165,9 мг, 0,7679 ммоля) в безводном ТГФ (10 мл) при -78°С по каплям добавляют диизобутилалюминийгидрид (1,0-молярный раствор в ТГФ) (2,0 мл, 2,0 ммоля). Смесь перемешивают при -78°С в течение 2 ч, после чего добавляют насыщенный раствор карбоната калия (0,6 мл), смесь нагревают до комнатной температуры и перемешивают еще в течение 30 мин. Далее добавляют сульфат натрия и смесь перемешивают в течение 10 мин. Твердое вещество удаляют фильтрацией и фильтрат упаривают досуха. Остаток очищают экспресс-хроматографией на силикагеле (20%-ный EtOAc в гексанах) с получением альдегида LXXXI в виде белого твердого вещества (80 мг, 0,43 ммоля, 56%).
К раствору соединения LXXXI (367,7 мг, 2,0 ммоля) в безводном 1,2-дихлороэтане (10 мл) добавляют морфолин (0,20 мл, 0,20 г, 2,3 ммоля), а затем ледяную уксусную кислоту (0,12 мл, 0,13 г, 2,1 ммоля) и триацетоксиборогидрид натрия (625 мг, 2,95 ммоля). Смесь перемешивают при комнатной температуре в течение 30 мин. Далее добавляют насыщенный раствор бикарбоната натрия (10 мл) и смесь интенсивно перемешивают еще в течение 30 мин. Слои разделяют и водный слой экстрагируют EtOAc (3×20 мл). Объединенные органические слои промывают рассолом, сушат (сульфат натрия), фильтруют и упаривают досуха. После экспресс-хроматографии (1%-ный триэтиламин в EtOAc) остатка получают соединение LXXXII в виде светло-желтого масла (460,8 мг, 1,79 ммоля, 91%).
К раствору трет-бутиллития (1,42-молярный раствор в пентане) (2,80 мл, 3,98 ммоля) в безводном ТГФ (20 мл) при -78°С по каплям добавляют раствор соединения LXXXII (460,8 мг, 1,792 ммоля) в безводном ТГФ (10 мл) и смесь перемешивают при -78°С в течение 10 мин. Далее добавляют хлорид трибутилолова (0,49 мл, 0,59 г, 1,8 ммоля) и смесь перемешивают при -78°С еще в течение 15 мин. После этого добавляют буфер с рН 7 (насыщ. Na2HPO4/NaH2PO4) (10 мл) и смесь нагревают до комнатной температуры. Слои разделяют и водный слой экстрагируют EtOAc (3×20 мл). Объединенные органические слои промывают рассолом, сушат (сульфат натрия), фильтруют и упаривают досуха. После экспресс-хроматографии (EtOAc) остатка получают соединение LXXXIII в виде бесцветного масла (548,8 мг, 1,17 ммоля, 65%).
Дегазированный раствор соединения LXXXITI (302 мг, 0,646 ммоля), соединения LXXI (177 мг, 0,797 ммоля) и Pd(PPh3)4 (55 мг, 0,48 ммоля) в безводном 1,4-диоксане (10 мл) нагревают до 100°С в герметично укупоренной трубке в течение 16 ч. Черный осадок удаляют фильтрацией и трубку промывают EtOAc. Объединенные фильтраты перемешивают с раствором фторида калия (40%-ным) (10 мл) в течение 30 мин. Далее добавляют воду и рассол, слои разделяют и водный слой экстрагируют EtOAc (4×50 мл). Объединенные органические слои промывают рассолом, сушат (сульфат натрия), фильтруют и упаривают досуха. После экспресс-хроматографии (5%-ный МеОН и 1%-ный триэтиламин в EtOAc) остатка получают соединение LXXXIV в виде светло-коричневого твердого вещества (157,6 мг, 0,49 ммоля, 76%).
Соединение LXXXIV и фенилкарбамат LXIV подвергают взаимодействию в соответствии с методом В. После очистки экспресс-хроматографией с использованием 5%-ного МеОН и 1%-ного триэтиламина в EtOAc в качестве элюента с последующей перекристаллизацией из ЕtOAc/гексанов получают указанное в заголовке соединение 4 в виде белого твердого вещества (tпл 169-170°С).
Пример 5
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-{4-[3-(морфолин-4-ил)фенил]нафталин-1-ил}мочевина
3-броманилин (3,0 мл, 4,7 г, 28 ммолей), 2-бромэтиловый эфир (4,2 мл, 7,7 г, 33 ммоля) и диизопропилэтиламин (15 мл, 11 г, 86 ммолей) растворяют в безводном ДМФ (20 мл) в атмосфере инертного газа и нагревают до 100°С в течение 6 ч. После охлаждения до комнатной температуры смесь сливают в воду (300 мл) и экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 2,9 г (12 ммолей, выход 43%) соединения LXXXVI.
Соединение LXXXVI (1,73 г, 7,13 ммоля) растворяют в безводном ТГФ (30 мл) и охлаждают до -78°С. Далее по каплям добавляют трет-бутиллитий (10,0 мл 1,7-молярного раствора в пентане) и раствор перемешивают при -78°С в течение 30 мин. После этого добавляют хлорид трибутилолова (1,90 мл, 2,28 г, 7,00 ммолей) и раствор перемешивают еще в течение 45 мин при -78°С. Затем добавляют буфер с рН 7 (насыщ. NaH2PO4/Na2HPO4) (10 мл) и смесь нагревают до комнатной температуры. Слои разделяют и водный слой экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 2,28 г (5,36 ммоля, выход 77%) соединения LXXXVII.
Соединение LXXXVII (1,49 г, 3,51 ммоля) и соединение LXXI (0,69 г, 3,11 ммоля) растворяют в 20 мл безводного 1,4-диоксана в герметично укупориваемой трубке в атмосфере инертного газа. Далее раствор дегазируют и продувают азотом (дважды). После этого добавляют тетракис(трифенилфосфин)палладий (0) (0,21 г, 0,18 ммоля) и раствор вновь дегазируют и продувают азотом (дважды). Трубку герметично укупоривают и выдерживают с нагреванием при 100°С в течение 17 ч. После охлаждения до комнатной температуры смесь разбавляют ЕtОАс, добавляют насыщенный водный раствор карбоната калия (10 мл) и смесь перемешивают в течение 1 ч при комнатной температуре. После этого смесь фильтруют через диатомовую землю и слои разделяют. Водный слой экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат (Na2SO4), фильтруют и упаривают досуха. После очистки остатка экспресс-хроматографией получают 0,363 г (1,19 ммоля, 38%) соединения LXXXVIII.
Соединение LXXXVIII (0,360 г, 1,18 ммоля) в соответствии с методом В подвергают взаимодействию с фенилкарбаматом LXIV (0,69 г, 1,97 ммоля). Полученный продукт очищают экспресс-хроматографией с получением бесцветного твердого вещества (0,433 г, 0,77 ммоля, выход 66%), которое далее очищают перекристаллизацией из ЕtOAc/гексанов, получая 0,344 г указанного в заголовке соединения 5 (tпл 188-190°C).
В таблице представлены другие соединения по изобретению, которые получают по методам, аналогичным описанным выше.
Пример 16
1-[4-(6-{[бис-(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метилфенил)мочевина
К раствору 4-трет-бутилтолуола (33,7 ммоля) в ацетонитриле (150 мл) при 0°С добавляют тетрафторборат нитрил-иона (40,5 ммоля). После выдержки в течение 30 мин при комнатной температуре реакционную смесь разбавляют водой (50 мл) и экстрагируют EtOAc (3×30 мл). Объединенные органические экстракты промывают рассолом и сушат (MgSO4). Полученный после удаления летучих компонентов в вакууме остаток очищают экспресс-хроматографией с использованием 10%-ного метиленхлорида/петролейного эфира в качестве элюента с получением 4 -трет-бутил- 2-нитротолуола.
4-трет-бутил-2-нитротолуол (1,1 ммоля) растворяют в ДМФ (10 мл). Далее добавляют катализатор (10%-ный Pd/C, 5 мг), а затем добавляют ди-трет-бутилдикарбонат (1,4 ммоля). Эту смесь продувают аргоном, а затем выдерживают в атмосфере Н2 (1 атм) в течение 12 ч. Смесь фильтруют через подушку из диатомовой земли, фильтрат разбавляют водой и экстрагируют EtOAc (3×10мл). Объединенные органические экстракты промывают рассолом и сушат (MgSO4). После выпаривания летучих компонентов получают 265 мг N-Вос-5-трет-бутил-2-метиланилина в виде кристаллического твердого вещества.
К смеси N-Вос-5-трет-бутил-2-метиланилина (0,8 ммоля) и триэтиламина (0,22 моля) в бензоле (10 мл) при комнатной температуре с помощью шприца добавляют трихлорид бора (0,4 ммоля). Полученную неоднородную смесь перемешивают при 80°С в течение 30 мин. После этого удаляют источник тепла и добавляют аминонафталин LXXXIX (0,7 ммоля). Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. Затем реакционную смесь разбавляют водой (10 мл) и экстрагируют EtOAc (3×10 мл). Объединенные органические экстракты промывают рассолом и сушат (MgSO4). Полученный после удаления летучих компонентов в вакууме остаток очищают экспресс-хроматографией с использованием 10%-ного МеОН/ЕtOАс в качестве элюента с получением 300 мг целевой мочевины ХС.
Эту мочевину помещают в кислые условия для удаления ацеталя, который проявляет наличие альдегидной функции. К этому альдегиду в 1,2-дихлорэтане добавляют 1,25 эквивалента бис(2-цианоэтил)амина, а затем добавляют триацетоксиборогидрид натрия (1,5 эквивалента). После колоночной хроматографии (5%-ный MeOH/EtOAc) получают указанное в заголовке соединение 16.
Пример 17
1-(6-трет-бутил-2-хлор-3-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевина
К перемешиваемому раствору N-Вос-1-амино-4-бромнафталина (15,5 ммоля) в безводном ТГФ (40 мл) при -78°С добавляют н-BuLi (47 ммолей). Полученный желто-зеленый раствор перемешивают при -78°С в течение 2 ч, а затем переносят в раствор триметилбората (5,64 г, 54,2 ммоля) в безводном ТГФ (25 мл) при -42°С. Реакционной смеси дают нагреться до комнатной температуры в течение ночи по мере нагревания бани. После перемешивания в течение 16 ч добавляют 5%-ную водную НСl (25 мл) и смесь перемешивают в течение 15 мин. Водный слой насыщают NaCl и слои разделяют. Водную фазу экстрагируют диэтиловым эфиром (3×60 мл) и затем объединенные органические фазы экстрагируют 0,5-молярным раствором NaOH (6×30 мл).
Объединенные щелочные экстракты подкисляют с помощью 3М НСl (около 30 мл) примерно до рН 2 и суспензию экстрагируют диэтиловым эфиром (3×100 мл). Объединенные эфирные экстракты сушат (MgSO4), фильтруют и удаляют растворитель с получением бороновой кислоты XCI в виде бежевого твердого вещества (2,3 г), которую используют в дальнейшем без дополнительной очистки.
5-бром-2-(морфолин-4-илметил)пиридин (0,70 ммоля) и соединение XCI (0,70 ммоля) растворяют в двухфазной смеси диметоксиэтана (2 мл) и 2-молярного водного Na2CO3 (1 мл). Реакционную смесь продувают потоком N2 в течение 15 мин, добавляют Pd-катализатор и смесь выдерживают с нагреванием при 85°С в течение 16 ч. После этого реакционную смесь охлаждают до комнатной температуры и распределяют между водой (10 мл) и ЕtOАс (75 мл). Слои разделяют и органическую фазу промывают рассолом (20 мл), сушат (MgSO4), фильтруют и удаляют растворитель с получением коричневого твердого вещества. После колоночной хроматографии получают продукт XCII в виде бежевого твердого вещества.
Соединение XCII (0,50 ммоля) растворяют в 2 мл безводного диоксана и добавляют НСl (2,5 ммоля). Раствор перемешивают при комнатной температуре в течение 16 ч. Далее к полученной суспензии добавляют диэтиловый эфир (5 мл) и смесь охлаждают до 0°С. После нейтрализации водным NaOH и фильтрации получают 4-[6-(морфолин-4-илметил)пиридин-3-ил]-1-аминонафталин (XCIII) в виде светло-коричневого твердого вещества (100 мг).
Смесь метилового эфира 2-трет-бутил-6-хлор-5-метилпиридин-4-карбоновой кислоты (2,27 г, 9,39 ммоля) и моногидрата LiOH (2,36 г, 56,3 ммоля) в МеОН (30 мл) и воде (10 мл) перемешивают при комнатной температуре в течение 24 ч. Затем реакционную смесь концентрируют и очищают хроматографией на силикагеле (элюент: 5%-ная ТФУК в дихлорметане) с получением соответствующей карбоновой кислоты (1,41 г, 66,3%).
К перемешиваемому раствору полученной на предыдущей стадии карбоновой кислоты (0,54 г, 2,36 ммоля) и триэтиламина (0,66 мл, 4,75 ммоля) в ТГФ (6 мл) при -10°С по каплям добавляют этилхлорформиат (0,34 мл, 3,51 ммоля). Полученную смесь перемешивают при 0°С в течение 1 ч. После этого добавляют раствор азида натрия (0,40 г, 6,0 ммолей) в воде (2 мл) и перемешивание продолжают еще в течение 1 ч. Смесь экстрагируют толуолом. Органические фазы разделяют, сушат с помощью сульфата натрия и концентрируют до объема 15 мл. Концентрат нагревают с обратным холодильником в течение 2 ч, что сопровождается образованием in situ изоцианата, а затем добавляют раствор соединения XCIII (0,39 г, 1,23 ммоля) в дихлорметане (5 мл). Реакционную смесь перемешивают при комнатной температуре в течение ночи. После концентрирования и хроматографии на силикагеле (элюент: EtOAc) получают указанное в заголовке соединение 17 (0,60 г, 89,9%).
Пример 18
1-(5-трет-бутил-2-метилфенил)-3-(4-{6-[(3-метоксипропил)метиламино] пиридин-3-ил}нафталин-1-ил)мочевина
2,5-дибромпиридин (100 мг) нагревают в герметично укупоренной трубке до 115°С в присутствии 3-метоксипропил-1-метиламина (2 мл) в течение 48 ч с получением соединения XCIV. После реакции сочетания Судзуки (Suzuki) соединения XCIV с соединением XCI и удаления трет-бутилкарбамата (аналогично описанному в примере 17 процессу) получают целевой нафтиламин XCV.
5-трет-бутил-2-метиланилин (0,56 ммоля) растворяют в дихлорометане (20 мл). После этого добавляют равный объем насыщенного водного бикарбоната натрия и двухфазный раствор охлаждают до 0°С. На время добавления фосгена (1,93М в толуоле, 0,80 мл) перемешивание приостанавливают. Непосредственно после этого перемешивание возобновляют и продолжают в течение 15 мин с реакционной смесью при 0°С. Слои разделяют, органические фазы сушат над твердым сульфатом магния и раствор концентрируют примерно до объема 5 мл. Далее добавляют необходимый нафтиламин (XCVI, 0,47 ммоля) в 5 мл дихлорометана. Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. После экспресс-хроматографии с использованием 7%-ного МеОН/ЕtOАс в качестве элюента и последующего растирания с простым эфиром получают указанное в заголовке соединение 18.
Пример 19
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметилфенил)мочевина
Перемешиваемый раствор 3-трифторметиланилина (4,7 ммоля) в сухом ТГФ (30 мл) обрабатывают при 0°С фенилхлорформиатом (4,8 ммоля). Через 2 ч реакцию прекращают добавлением водного насыщенного раствора бикарбоната натрия и экстрагируют EtOAc. Объединенные органические слои промывают водным насыщенным раствором бикарбоната натрия и рассолом и сушат над твердым MgSO4. После концентрирования получают карбамат XCVI (97%). После этого смесь соединения XCIII (пример 17) (0,06 ммоля) и указанного карбамата (0,05 ммоля) нагревают в течение 2 дней в герметично укупоренной трубке. Затем реакционную смесь охлаждают до комнатной температуры. Далее добавляют PS-трисаминный (100 мг, фирма Argonaut) и PS-изоцианатный полимеры (150 мг, фирма Argonaut) и реакционную смесь взбалтывают в течение 3 дней. После этого реакционную смесь фильтруют и концентрируют с получением указанного в заголовке соединения 19.
В примерах 20-25 проиллюстрирован синтез арил- и гетероариламинов, которые могут использоваться в качестве промежуточного продукта IV в методах А-В (раздел "Общие методы синтеза") для получения соединений формулы II или III.
Пример 20
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]амин
Метил-4-трет-бутилфенилацетат (20 ммолей) растворяют в МеОН (160 мл) и обрабатывают водой (40 мл) и моногидратом LiOH (30 ммолей). После этого реакционную смесь оставляют перемешиваться при комнатной температуре в течение ночи. Затем под пониженным давлением удаляют летучие компоненты, образовавшийся остаток разбавляют водой и нейтрализуют до рН 4 с помощью 1 н. серной кислоты. Полученное твердое вещество отфильтровывают, промывают водой и сушат с получением 4-трет-бутилфенилуксусной кислоты в виде не совсем белого твердого вещества (3,8 г, 99%).
Безводный ДМФ (139 ммолей) охлаждают до 0°С и обрабатывают РОСl3 (79,6 ммоля). Через 5 мин добавляют 4-трет-бутилфенилуксусную кислоту (19,9 ммоля) и реакционный сосуд помещают в масляную баню с температурой 110°С. Реакционную смесь перемешивают в течение 2 ч, при этом все твердые вещества растворяются. После охлаждения до комнатной температуры реакционную смесь сливают в перемешиваемый раствор NaPF6 (19,8 ммоля) в воде (200 мл). По завершении выпадения осадка его отфильтровывают, промывают водой и сушат с получением соединения XCVII (7,8 г, 97%).
Соединение XCVII (5 ммолей) растворяют в EtOH (50 мл) и полученную суспензию обрабатывают гидразингидратом (5 ммолей). После этого реакционный сосуд помещают в масляную баню с температурой 90°С и реакционную смесь перемешивают при нагревании с обратным холодильником в течение 2 ч. После охлаждения реакционной смеси до комнатной температуры летучие компоненты удаляют под пониженным давлением. Остаток растворяют в ледяной воде, твердое вещество отфильтровывают, промывают водой и сушат, получая 4-(4-трет-бутилфенил)пиразол (973 мг, 97%).
Этот 4-(4-трет-бутилфенил)пиразол (0,5 ммоля) суспендируют в MeCN (2 мл), охлаждают до 0°С и обрабатывают NO2BF4 (0,6 ммоля). Реакционной смеси дают медленно нагреться до комнатной температуры и перемешивают при комнатной температуре (КТ) в течение 2 ч. После прекращения реакции добавлением водного NaHCO3 летучие компоненты удаляют под пониженным давлением. Остаток растворяют в воде и экстрагируют СН2Сl2. Органические фазы объединяют, сушат над MgSO4 и концентрируют с получением желтого масла, которое хроматографируют на силикагеле (элюент: CH2Cl2/EtOAc в соотношении 6:4), получая в результате 4-(4-трет-бутил-2-нитрофенил)пиразол в виде желтого кристаллического твердого вещества (71 мг, 58%).
4-(4-трет-бутил-2-нитрофенил)пиразол (0,27 ммоля) растворяют в ЕtОН (3 мл) и обрабатывают 10%-ным Pd/C (0,2 экв. в пересчете на массу нитросоединения), а затем NH4CO2H (2,7 ммоля). Через 30 мин катализатор отфильтровывают через слой диатомовой земли и фильтрат концентрируют под пониженным давлением. Остаток растворяют в воде, образовавшееся твердое вещество отфильтровывают, промывают водой и сушат (54 мг, 93%), получая указанное в заголовке соединение 20.
Пример 21
3-амино-2-метокси-5-трет-бутилпиридин
К гидроксиду аммония (25 мл, 11%) добавляют этилнитроацетат (3,3 мл, 4,0 г, 29,7 ммоля) и перемешивают в течение ночи, как это описано у A.V. Amet и др., Russian Chemical Bulletin, 1996, 45(2), 393-398. Далее реакционную смесь подщелачивают 4 н. соляной кислотой, экстрагируют простым эфиром (3×25 мл), а затем EtOAc (3×100 мл). Объединенные ЕtOАс-экстракты сушат (сульфат магния), фильтруют и упаривают досуха с получением нитроацетамида в виде бледно-желтого твердого вещества (1,7 г, 16,3 ммоля, 55%).
К 100 мл охлаждаемого льдом нитрометана в атмосфере азота медленно добавляют трихлоралюминий (45,5 г, 341 ммоль). После этого в течение часа по каплям добавляют раствор малононитрила (21,5 мл, 22,6 г, 341 ммоль) в 50 мл нитрометана, поддерживая температуру ниже 10°С. Затем медленно в течение 2,5 ч добавляют раствор трет-бутилхлорида (88 мл, 74,9 г, 809 ммолей) в 25 мл нитрометана, поддерживая температуру ниже 10°С. Реакционную смесь закрывают и помещают в морозильную камеру на 60 ч. После этого к реакционной смеси для подавления интенсивного протекания реакции по каплям в течение 4 ч добавляют насыщенный водный бикарбонат натрия (500 мл), поддерживая температуру ниже 10°С. Затем гетерогенную смесь нейтрализуют твердым бикарбонатом натрия (50 г). Слои разделяют и водный слой экстрагируют метиленхлоридом (3×250 мл). Объединенные органические экстракты сушат (сульфат магния) и концентрируют в вакууме с получением 42 г частично кристаллического коричневого масла. Остаток перегоняют в вакууме при 100°С. Первую фракцию собирают, после чего в конденсаторе начинается образование твердого вещества. Затем отключают подачу охлаждающей воды и конденсатор нагревают с помощью нагревательного пистолета для расплавления твердого вещества. Эту фракцию собирают до тех пор, пока в конденсаторе при пропускании через него охлаждающей воды не прекратится образование твердого вещества, с получением в результате целевого динитрила в виде плавящегося при малой температуре твердого вещества кремового цвета (19 г, 155 ммолей, 46%).
Раствор этого динитрила (961 мг, 7,9 ммоля) в безводных гексанах (50 мл) охлаждают в атмосфере азота до -70°С в бане из сухого льда/ацетона. После этого по каплям в течение 20 мин добавляют диизобутилалюминийгидрид (ДИБАГ) (17,5 мл, 1,0 М в циклогексане). Смесь перемешивают при -70°С в течение 45 мин, а затем при комнатной температуре в течение 5 ч. Реакционную смесь охлаждают до 0°С, после чего медленно добавляют 2-молярный водный раствор соляной кислоты (45 мл), поддерживая температуру ниже 10°С. Смесь перемешивают при комнатной температуре в течение 15 ч. Слои разделяют, и водный слой экстрагируют простым эфиром (3×25 мл). Объединенные органические экстракты сушат (сульфат магния), фильтруют и упаривают досуха с получением целевого диальдегида в виде вязкого желтого масла (600 мг, 4,68 ммоля, 60%).
Раствор этого альдегида (271 мг, 2,11 ммоля), нитроацетамида (223 мг, 2,14 ммоля) и пиперидина (20%-ного в EtOH) (250 мкл, 0,51 ммоля) в абсолютном EtOH (3 мл) выдерживают с нагреванием при 65°С в течение 3 ч. После охлаждения до комнатной температуры реакционную смесь концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (EtOAc) с получением целевого нитропиридона в виде желтого твердого вещества (280 мг, 1,43 ммоля, 67%).
Смесь этого нитропиридона (150 мг, 0,76 ммоля), пентахлорида фосфора (199 мг, 0,96 ммоля) и оксихлорида фосфора (1 капля) нагревают до температуры перегонки в герметично укупоренной трубке. Через 2 ч оксихлорид фосфора удаляют в вакууме и остаток перемешивают в ледяной воде (10 мл) в течение 18ч. После этого собирают целевой продукт в виде коричневого твердого вещества (95 мг, 0,44 ммоля, 58%).
К раствору 2-хлор-3-нитро-5-трет-бутилпиридина (30 мг, 0,14 ммоля) в безводном МеОН (1,5 мл) в атмосфере азота добавляют раствор метоксида натрия (1,57 г натрия в 40 мл безводного МеОН) (85 мкл, 0,14 ммоля). Реакционную смесь в течение ночи нагревают в герметично укупоренной трубке в масляной бане с температурой 80-90°С. После этого летучие компоненты удаляют в вакууме, остаток растворяют в EtOAc (15 мл), промывают водой (10 мл) и рассолом (10 мл), сушат (сульфат магния), фильтруют и упаривают досуха. После экспресс-хроматографии остатка на силикагеле (10%-ный EtOAc в гексанах) получают целевой 2-метокси-3-нитро-5-трет-бутилпиридин в виде стекловидного желтого твердого вещества (12 мг, 0,057 ммоля, 41%).
К суспензии полученного на предыдущей стадии промежуточного продукта (12 мг, 0,057 ммоля) и Pd/C (10%-ного, 14 мг) в абсолютном EtOH (1 мл) добавляют формиат аммония (22 мг, 0,35 ммоля) и смесь нагревают до 50°С в течение 1 ч. После охлаждения реакционную смесь фильтруют через диатомовую землю и промывают МеОН. Фильтрат упаривают досуха, получая указанное в заголовке соединение 21 в виде коричневого твердого вещества (10 мг, 0,055 ммоля, 100%).
Пример 22
N-ацетил-5-амино-3,3-диметилиндолин
Раствор оксиндола (5,0 г, 37,5 ммоля) в уксусном ангидриде (7,1 мл, 75,1 ммоля) и уксусной кислоте (25 мл) нагревают с обратным холодильником в течение 20 ч. После охлаждения до комнатной температуры реакционную смесь разбавляют водой (200 мл). Полученное твердое вещество отфильтровывают, промывают водой и сушат с получением N-ацетилоксиндола в виде белого твердого вещества (5,2 г, 79%).
Смесь этого N-ацетилоксиндола (2,0 г, 11,4 ммоля), иодметана (1,56 мл, 25,1 ммоля) и карбоната калия (3,1 г, 22,8 ммоля) в ДМСО (20 мл) перемешивают при комнатной температуре в течение 20 ч. После этого реакционную смесь разбавляют водой. Полученное твердое вещество отфильтровывают, промывают водой и сушат с получением N-ацетилдиметилоксиндола в виде оранжевого твердого вещества (1,9 г, 84%).
Раствор этого N-ацетилдиметилоксиндола (500 мг, 2,5 ммоля) в 3 н. растворе серной кислоты (7 мл) и ТГФ (7 мл) нагревают с обратным холодильником в течение 4 ч. После охлаждения до комнатной температуры реакционную смесь разбавляют простым эфиром. Эфирный слой промывают водой и рассолом, сушат (сульфат магния), фильтруют и концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (элюент: 30%-ный EtOAc в гексанах) с получением диметилоксиндола в виде красного твердого вещества (228 мг, 57%).
Раствор этого диметилоксиндола (220 мг, 1,4 ммоля) в толуоле (5 мл) обрабатывают 65%-ным раствором Red-Al в толуоле (0,64 мл, 2,05 ммоля) при 80°С. После перемешивания при 100°С в течение 4 ч реакцию прекращают добавлением 1 н. раствора гидроксида натрия. Органический слой отделяют, промывают водой и рассолом, сушат (сульфат натрия), фильтруют и концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (элюент: 25%-ный EtOAc в гексанах) с получением диметилиндолина в виде светло-голубого масла (121 мг, 60%).
Раствор этого диметилиндолина (65 мг, 0,44 ммоля) и триэтиламина (0,12 мл, 0,88 ммоля) в сухом дихлорометане (3 мл) обрабатывают ацетилхлоридом (0,05 мл, 0,66 ммоля) при 0°С. Смеси дают нагреться до комнатной температуры и перемешивают в течение 16 ч. Затем реакцию прекращают добавлением воды и продукт экстрагируют простым эфиром. Органический слой промывают водой и рассолом, сушат (сульфат натрия), фильтруют и концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (элюент: 30%-ный EtOAc в гексанах) с получением N-ацетилдиметилиндолина в виде светло-желтого масла (68 мг, 82%).
Раствор этого N-ацетилдиметилиндолина (65 мг, 0,34 ммоля) в уксусной кислоте (2 мл) обрабатывают дымящей азотной кислотой (24 мкл, 0,57 ммоля) при комнатной температуре и полученную смесь перемешивают в течение 1 ч. После этого реакцию прекращают добавлением насыщенного раствора бикарбоната натрия и продукт экстрагируют EtOAc. Органический слой промывают водой и рассолом, сушат (сульфат натрия), фильтруют и концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (элюент: 50%-ный EtOAc в гексанах) с получением целевого нитрованного индолина в виде светло-оранжевого твердого вещества (66 мг, 67%).
Смесь N-ацетил-3,3-диметил-5-нитроиндолина (64 мг, 0,27 ммоля), формиата аммония (86 мг, 1,36 ммоля) и 10%-ного палладия на угле (5 мг) в МеОН (5 мл) перемешивают при комнатной температуре в течение 2 ч. Реакционную смесь фильтруют через короткую пробку из диатомовой земли. После этого фильтрат концентрируют в вакууме. Остаток очищают экспресс-хроматографией на силикагеле (элюент: 50%-ный EtOAc в гексанах) с получением указанного в заголовке соединения 22 в виде белого твердого вещества (48 мг, 87%).
Пример 23
8-амино-6-трет-бутил-3-оксо-4-N-метилбензоксазин
К раствору 4-трет-бутил-2,6-динитрофенола (3,15 г, 13,13 ммоля) в 100 мл ацетонитрила добавляют формиат аммония (5,0 г, 78,8 ммоля) и 10%-ный палладий на угле (1,0 г). Смесь нагревают с обратным холодильником в течение 20 мин, после чего дают охладиться и фильтруют через диатомовую землю. Остаток промывают EtOAc и объединенные органические фазы упаривают в вакууме. Остаток растворяют в дихлорометане и фильтруют через короткую пробку из силикагеля. После удаления растворителя в вакууме получают 2-амино-4-трет-бутил-6-нитрофенол в виде рыжего твердого вещества (4,86 ммоля, выход 37%).
К раствору этого 2-амино-4-трет-бутил-6-нитрофенола (258 мг, 1,23 ммоля) и хлорида бензилтриэтиламмония (БТЭА) (280 мг, 1,23 ммоля) в 5 мл хлороформа добавляют тонкоизмельченный NaHCO3 (413 мг, 4,92 ммоля). Смесь охлаждают до 0°С и по каплям с помощью шприца в течение 15 мин добавляют α-хлорацетилхлорид (0,12 мл, 1,47 ммоля) в 1,5 мл хлороформа. По завершении добавления смесь оставляют перемешиваться при 0°С в течение 1 ч. Затем смеси дают нагреться до окружающей температуры и в завершение осторожно нагревают с обратным холодильником в течение 6 ч. Полученной сырой оранжевой смеси дают охладиться, после чего фильтруют через диатомовую землю для отделения белого осадка, который тщательно промывают большим количеством хлороформа. После удаления растворителя в вакууме маслянистый остаток обрабатывают водой (40 мл) и перемешивают шпателем, в результате чего образуется желтый осадок. Этот чистый 6-трет-бутил-8-нитро-3-оксобензоксазин фильтруют и сушат сначала в токе воздуха, а затем в вакууме (1,05 ммоля, 85%).
К раствору этого 6-трет-бутил-8-нитро-3-оксобензоксазина (51 мг, 0,20 ммоля) в 3,5 мл ДМФ при 0°С одной порцией добавляют гидрид натрия (10 мг, 60%-ная дисперсия в минеральном масле, 0,24 ммоля). Через 20 мин с помощью шприца добавляют метилиодид (20 мкл, 0,24 ммоля). Смеси дают медленно нагреться до окружающей температуры в течение ночи. К сырой смеси для прекращения реакции добавляют насыщенный водный раствор хлорида аммония и экстрагируют EtOAc (3×10 мл). Объединенные органические фазы промывают водой, а затем рассолом, после чего сушат над сульфатом натрия. После фильтрации и удаления растворителей в вакууме получают 6-трет-бутил-8-нитро-3-оксо-4-N-метилбензоксазин (100%).
Этот 6-трет-бутил-8-нитро-3-оксо-4-N-метилбензоксазин (53 мг, 0,2 ммоля) растворяют в 12,5 мл ацетонитрила. После этого добавляют циклогексен (0,20 мл, 2,0 ммоля) и 10%-ный палладий на угле (75 мг). Смесь нагревают с обратным холодильником в течение 1 ч, после чего охлаждают до окружающей температуры и фильтруют через диатомовую землю. Остаток промывают EtOAc и объединенные органические фазы упаривают в вакууме, получая указанное в заголовке соединение 23 (100%).
Пример 24
7-амино-5-трет-бутил-3Н-бензоксазол-2-он
К раствору 2-амино-4-трет-бутил-6-нитрофенола (300 мг, 1,43 ммоля) и пиридина (0,30 мл) в метиленхлориде (30 мл) добавляют 4-нитрофенилхлорформиат (280 мг, 1,39 ммоля). Смесь перемешивают в течение 24 ч. Полученный раствор промывают водным бикарбонатом натрия (2×20 мл), сушат над твердым сульфатом магния и концентрируют до получения оранжевого твердого вещества. После колоночной хроматографии (силикагель, элюент: 40%-ный ЕtOАс/петролейный эфир) получают 5-трет-бутил-7-нитро-3Н-бензоксазол-2-он (70%).
Этот 5-трет-бутил-7-нитро-3Н-бензоксазол-2-он (200 мг, 0,9 ммоля) растворяют в EtOH (10 мл). После этого добавляют циклогексен (4 мл) и 10%-ный палладий на угле (50 мг). Смесь нагревают с обратным холодильником в течение 3 ч, а затем охлаждают до окружающей температуры и фильтруют через диатомовую землю. После колоночной хроматографии (силикагель, элюент: 25%-ный ЕtOАс/петролейный эфир) получают указанное в заголовке соединение 24 (70%).
Пример 25
7-амино-5-трет-бутил-2-метилбензоксазол
2-амино-4-трет-бутил-6-нитрофенол растворяют в триэтилортоацетате (10 мл). Реакционную смесь перемешивают в течение ночи при 100°С. После выпаривания летучих компонентов в вакууме получают 5-трет-бутил-2-метил-7-нитробензоксазол (110 мг).
Этот 5-трет-бутил-2-метил-7-нитробензоксазол (100 мг, 0,4 ммоля) растворяют в EtOH (20 мл). После этого добавляют катализатор (10%-ный Pd/C, 100 мг), а затем формиат аммония (160 мг, 0,3 ммоля). Полученную гетерогенную смесь перемешивают при 100°С в течение 1 ч. После фильтрации и последующего упаривания получают указанное в заголовке соединение 25 (85 мг).
В примерах 26-29 рассмотрен синтез четырех гетероариламинов, которые могут использоваться в качестве промежуточного продукта IV в методах А-В (раздел "Общие методы синтеза") для получения соединений формулы I или Iа.
Пример 26
5-(5-амино-3-трет-бутилпиразол-1-ил)-2-метилбензамид
3-иод-4-метилфениламин (10 г, 43 ммоля) растворяют в 6 н. НСl (40 мл) и охлаждают до 0°С, интенсивно перемешивая в течение всего этого процесса. Нитрит натрия (2,9 г, 1,03 экв.) растворяют в воде (5 мл) и этот раствор добавляют по каплям к реакционной смеси. Через 30 мин с помощью капельной воронки добавляют дигидрат хлорида олова (II) (22,8 г, 1 моль) в 6 н. НСl (100 мл) и реакционную суспензию перемешивают при 0°С в течение 3 ч. После этого значение рН с помощью 40%-ного водного раствора гидроксида натрия устанавливают на 14 и водную смесь экстрагируют EtOAc (6×50 мл), сушат (MgSO4) и концентрируют с получением 3-иод-4-метилфенилгидразина (7 г, 57%). Этот материал используют непосредственно в последующей реакции без дополнительной очистки.
Раствор указанного выше фенилгидразина (5,08 г, 22 ммоля) и 4,4-диметил-3-оксопентаннитрила (3,06 г, 1,1 экв.) в EtOH (100 мл), содержащем конц. НСl (3 мл), нагревают с обратным холодильником в течение 17 ч, после чего охлаждают до комнатной температуры. Значение рН с помощью 40%-ного водного раствора гидроксида натрия устанавливают на 14. Водную смесь экстрагируют EtOAc (3×50 мл), сушат (MgSO4) и концентрируют с получением 5-трет-бутил-2-(3-иод-4-метилфенил)-2Н-пиразол-3-иламина (6,3 г, 86%). Этот материал используют непосредственно в последующей реакции без дополнительной очистки.
5-трет-бутил-2-(3-иод-4-метилфенил)-2Н-пиразол-3-иламин (2 г, 5,6 ммоля) объединяют с цианидом цинка (397 мг, 0,6 экв.) и тетракис(трифенилфосфин)палладием(0) (325 мг, 5 мол.%) в дезоксигенированном диметилформамиде (10 мл). Полученную желтую суспензию выдерживают с нагреванием при 100°С в течение 4 ч, охлаждают до комнатной температуры, а затем разбавляют рассолом и 2 н. НСl. Водную смесь экстрагируют EtOAc (6×10 мл), сушат (MgSO4) и концентрируют. Остаток очищают экспресс-хроматографией, элюируя смесью 20%-ный ЕtOАс/петролейный эфир, с получением 1,3 г (91%) целевого нитрила.
Этот нитрил (150 мг, 0,6 ммоля) в EtOH (5 мл) в течение 2 ч нагревают до 100°С в присутствии 10 н. NaOH. После этого реакционную смесь охлаждают до комнатной температуры, нейтрализуют 50%-ной НСl, экстрагируют EtOAc (6×10 мл), сушат (MgSO4) и концентрируют с получением указанного в заголовке соединения 26 (130 мг, 80%).
Пример 27
5-амино-2-метоксипиридин (5,0 г, 40 ммолей) растворяют в 6 н. НСl (10 мл) и охлаждают до 0°С, интенсивно перемешивая в течение всего этого процесса. Нитрит натрия (2,8 г, 41 ммоль) растворяют в воде (10 мл) и этот раствор добавляют к реакционному раствору. Через 30 мин добавляют дигидрат хлорида олова (II) (52 г, 230 ммолей) в 6 н. НСl (20 мл) и реакционную суспензию перемешивают при 0°С в течение 2,5 ч. Значение рН с помощью 40%-ного водного раствора гидроксида натрия устанавливают на 13. После этого добавляют этиловый эфир и смесь экстрагируют EtOAc (4×70 мл), сушат (MgSO4) и концентрируют с получением 5-гидразино-2-метоксипиридина в виде оранжевого твердого вещества (5,1 г).
Раствор 5-гидразино-2-метоксипиридина (2,5 г, 18 ммолей) и 4,4-диметил-3-оксопентаннитрила (2,3 г, 18 ммолей) в толуоле (50 мл) нагревают с обратным холодильником в течение 17 ч в колбе, оборудованной ловушкой Дина-Старка, а затем охлаждают до комнатной температуры. После этого реакционную смесь концентрируют и остаток очищают колоночной хроматографией на силикагеле, элюируя смесью 30%-ный EtOAc/петролейный эфир, с получением указанного в заголовке соединения 27 в виде желтовато-коричневого твердого вещества (3,5 г, 80%).
Пример 28
5-амино-3-трет-бутил-1-(2-пиридон-5-ил) пиразол
К раствору полученного в примере 27 продукта (0,6 г, 2,4 ммоля) в уксусной кислоте (3 мл) добавляют 48%-ный НВr в уксусной кислоте (3 мл). Реакционную смесь нагревают до 120°С в течение 15 мин, охлаждают до комнатной температуры и затем значение рН с помощью 10%-ного водного раствора гидроксида натрия устанавливают на 7,5. Водную смесь экстрагируют EtOAc (4×15 мл), сушат (MgSO4) и концентрируют с получением желтовато-коричневого твердого вещества. Указанное в заголовке соединение 28 (0,46 г, 82%) получают после перекристаллизации из простого эфира.
Пример 29
5-амино-3-трет-бутил-1-(2-цианоэтил)пиразол
Раствор 2-цианоэтилгидразина (3,0 г, 35 ммолей) и 4,4-диметил-3-оксопентаннитрила (4,2 г, 34 ммоля) в толуоле (50 мл) нагревают с обратным холодильником в течение 17 ч в колбе, оборудованной ловушкой Дина-Старка, а затем охлаждают до комнатной температуры. Суспензию фильтруют и фильтрат концентрируют. Колоночной хроматографией остатка на силикагеле с элюированием смесью 50%-ный EtOAc/петролейный эфир получают указанное в заголовке соединение 29 в виде бесцветного твердого вещества (2,6 г, 40%).
Пример 30
1-[5-трет-бутил-2-(2-метилтиопиримидин-5-ил)-2Н-пиразол-3-ил]-3-{4-[6-(морфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевина
Пинаколин (100 ммолей) и диэтилоксалат (120 ммолей) растворяют в ТГФ (200 мл), охлаждают до -78°С и обрабатывают гексаметилдисилазидом лития (Li-ГМДС, 120 ммолей, 1-молярный раствор в ТГФ). После этого ледяную баню удаляют и реакционной смеси дают нагреться до комнатной температуры. Через 2 ч удаляют летучие компоненты и сырой остаток растворяют в ледяном НОАс (200 мл). Затем добавляют гидразинмоногидрат (110 ммолей), реакционную смесь помещают в масляную баню с температурой 90°С и перемешивают в течение ночи. После этого НОАс удаляют под пониженным давлением и сырой остаток растворяют в водном NаНСО3, получая раствор с рН 6. Далее твердое вещество отфильтровывают, промывают водой и сушат с получением целевого пиразолового эфира (12,9 г, 66%).
КО-трет-Bu (67 ммолей) растворяют в ДМСО (120 мл). Далее одной порцией добавляют полученный на предыдущей стадии пиразоловый эфир (12 г, 61 ммоль) и реакционную смесь перемешивают в течение 15 мин. После этого добавляют трет-бутилбромацетат (92 ммоля) и реакционную смесь перемешивают при комнатной температуре в течение 45 мин. Затем ДМСО удаляют под пониженным давлением и сырой остаток разбавляют ледяной водой и экстрагируют CH2Cl2. Органические фазы объединяют, сушат над MgSO4 и концентрируют с получением изомерной смеси пиразолов в виде оранжевого масла (21 г). Целевой изомер выделяют в виде масла хроматографией на силикагеле, элюируя СН2Cl2 (13,3 г, 70%).
Пиразоловый диэфир (13,3 г, 43 ммоля) растворяют в чистой ТФУК (150 мл) и перемешивают при комнатной температуре в течение 3 ч. После этого удаляют летучие компоненты и сырой остаток разбавляют ледяной водой и экстрагируют СН2Сl2. Органические фазы объединяют, промывают водой, сушат над MgSO4 и концентрируют с получением целевой карбоновой кислоты в виде густого масла, которое частично кристаллизуется (10,2 г, 94%).
Безводный ДМФ (282 ммоля) охлаждают до 0°С и обрабатывают POCl3 (161 ммоль). Через 5 мин добавляют полученное на предыдущей стадии пиразольное производное уксусной кислоты (10,2 г, 40 ммолей) и суспензию помещают в масляную баню с температурой 110°С. После этого реакционную смесь перемешивают в течение 2 ч, при этом растворяется все твердое вещество. После охлаждения до комнатной температуры реакционную смесь сливают в перемешиваемый раствор NaPF6 (80 ммолей) в воде (400 мл). По завершении выпадения осадка его отфильтровывают, промывают водой и сушат, получая целевую винамидиниевую соль XCVIII (14,6 г, 78%).
Эту соль XCVIII (233 мг, 0,5 ммоля) растворяют в ДМСО (10 мл) и обрабатывают сульфатом S-метилизотиомочевины (0,25 ммоля) и К2СО3 (0,25 ммоля). После этого реакционную смесь помещают в масляную баню с температурой 90°С и перемешивают в течение 2 ч. После охлаждения реакционной смеси до комнатной температуры удаляют летучие компоненты под пониженным давлением. Остаток растворяют в ледяной воде и экстрагируют диэтиловым эфиром. Органические фазы объединяют, сушат над MgSO4 и концентрируют с получением коричневой смолы. Целевой этиловый эфир очищают хроматографией на силикагелевой колонке, элюируя смесью CH2Cl2/EtOAc в соотношении 1:1, с получением желтого масла, которое кристаллизуется при стоянии (157 мг, 98%).
Полученный на предыдущей стадии эфир (150 мг, 0,47 ммоля) растворяют в МеОН (4 мл) и воде (1 мл), обрабатывают моногидратом LiOH (0,7 ммоля) и перемешивают при комнатной температуре в течение ночи. После этого удаляют летучие компоненты и остаток разбавляют водой и нейтрализуют до рН 4 с помощью 1 н. серной кислоты. Твердое вещество отфильтровывают, промывают водой и сушат (113 мг, 82%).
Полученную карбоновую кислоту (105 мг, 0,36 ммоля) суспендируют в бензоле (4 мл) и обрабатывают триэтиламином (0,61 ммоля). Полученный раствор обрабатывают дифенилфосфорилазидом (ДФФА) (0,54 ммоля) и оставляют перемешиваться при комнатной температуре в течение 6 ч. Органические фазы промывают водным NaHCO3 и водой, сушат над MgSO4 и фильтруют. Полученный раствор обрабатывают соединением LXXXIV (пример 4) (115 мг, 0,36 ммоля) и реакционную смесь помещают на 1 ч в масляную баню с температурой 90°С. После этого удаляют летучие компоненты и сырой остаток очищают препаративной тонкослойной хроматографией на двух пластинах, элюируя смесью CH2Cl2/MeOH в соотношении 9:1, с получением указанного в заголовке соединения 30 в виде не совсем белого твердого вещества (61 мг, 28%).
Заменяя сульфат S-метилизотиомочевины, используемый в реакции с соединением XCVIII, можно получить другие замещенные пиримидины, соответствующие формуле XCVIV. Так, например, используя гидрохлорид ацетамида, можно получить 2-метилпиримидиновый аналог соединения XCVIV. Использование сульфата O-метилизотиомочевины и карбоната гуанидина позволяет получить соответственно 2-метоксипиримидиновый и 2-аминопиримидиновый аналоги. При замене сульфата S-метилизотиомочевины моногидратом гидразина или N-метилгидразином можно получить соответственно пиразол-4-ильное или 1-метилпиразол-4-ильное кольцо вместо замещенного пиримидина в соединении XCVIV. Каждый из подобных аналогов соединения XCVIV может использоваться в описанных выше методах для получения соответствующих аналогов соединения 30.
В примерах 31-36 описан синтез замещенных нафтиламинов, которые могут использоваться в качестве промежуточного продукта VI (D'-NH2), как это описано для методов Б и В в разделе "Общие методы синтеза", для получения различных соединений по изобретению.
Пример 31
5-(4-аминонафталин-1-ил)-2-пиридин-3-илметилфенол
В трубку с раствором 2,0 г 1-амино-4-бромнафталина (9,0 ммолей, 1 экв.) в 70 мл ДМФ добавляют 1,75 мл 2-циклогексен-1-она (18,0 ммолей, 2,0 экв.), 2,3 г бикарбоната натрия (27,0 ммолей, 3,0 экв.) и 186 мг 1,3-бис(дифенилфосфино)пропана (ДФФП, 0,45 ммоля, 0,05 экв.). Смесь в течение 15 мин барботируют сухим газообразным азотом, после чего добавляют 316 мг хлорида бис (трифенилфосфино) палладия (II) (0,45 ммоля, 0,05 экв.) и трубку герметично укупоривают. Смесь выдерживают с нагреванием при 150°С в течение 8 ч, а затем охлаждают до окружающей температуры, разбавляют EtOAc (150 мл) и фильтруют через диатомовую землю. Смесь промывают водой, а затем рассолом. Органический слой сушат (MgSO4), фильтруют и концентрируют. Сырое масло очищают колоночной хроматографией на SiO2, используя от 10 до 50% EtOAc в смесях гексанов в качестве элюентов, с получением 2,0 г густой жидкости, содержащей 3-(4-аминонафталин-1-ил)циклогекс-2-енон и ДМФ (соответственно в молярном отношении 1:2, 5,22 ммоля нафтиламина, выход 58% от теоретического).
К раствору 4,0 г 3-(4-аминонафталин-1-ил)циклогекс-2-енона в смеси с ДМФ (1:2, 10,4 ммоля, 1 экв.) в 50 мл толуола добавляют 2,72 г ди-трет-бутил-дикарбоната (12,5 ммоля, 1,2 экв.) и 1,5 мл триэтиламина (10,4 ммоля, 1 экв.). Смесь выдерживают с нагреванием при 100°С в течение ночи, после чего охлаждают до окружающей температуры. Далее реакционную смесь промывают 0,1%-ной водной НСl (2×50 мл), водой и рассолом, сушат (MgSO4), фильтруют и концентрируют. Сырой продукт осаждают и промывают 10%-ным EtOAc в гексане с получением после фильтрации 2,5 г целевого трет-бутилкарбамата (7,4 ммоля, выход 71% от теоретического).
К раствору 186 мг полученного на предыдущей стадии трет-бутилнафтилкарбамата (0,55 ммоля, 1 экв.) в 1,6 мл безводного трет-бутанола добавляют 52 мкл пиридин-3-карбоксальдегида (0,55 ммоля, 1 экв.) и 1,65 мл раствора трет-бутоксида калия (1,0М, 1,32 ммоля, 3 экв.). Эту смесь нагревают с обратным холодильником в течение ночи, а затем охлаждают. Далее добавляют МеОН (5 мл) и раствор НСl в диоксане (4,0 М) до тех пора, пока значение рН не установится примерно на 1, после чего реакционную смесь перемешивают в течение 1,5 ч при окружающей температуре. Затем в смесь для прекращения реакции добавляют насыщенный водный раствор NaHCO3 и экстрагируют EtOAc (2×50 мл). Водный слой обрабатывают 4 н. водным раствором NaOH до тех пора, пока значение рН не установится примерно на 12, и затем экстрагируют еще дважды. Объединенные органические экстракты промывают рассолом, сушат (MgSO4), фильтруют и концентрируют с получением смеси сырых продуктов, содержащей нафтиламин в виде все еще защищенного карбамата. После этого остаток растворяют в дихлорометане (3 мл), обрабатывают 2 мл ТФУК и оставляют перемешиваться на выходные дни при окружающей температуре. Затем реакцию в смеси прекращают и смесь нейтрализуют насыщенным водным NaHCO3, экстрагируют дихлорометаном (3×50 мл), сушат (MgSO4) и фильтруют. Далее летучие компоненты удаляют в вакууме и сырой продукт очищают колоночной хроматографией на SiO2, используя от 50 до 100% EtOAc в смесях гексанов в качестве элюента, с получением 35 мг указанного в заголовке соединения 31 (0,11 ммоля, выход 20% от теоретического).
Пример 32
5-(4-аминонафталин-1-ил)-2-(тетрагидрофуран-3-илметил)фенол
К раствору 3,16 г тетрагидро-3-фуроевой кислоты (27 ммолей, 1 экв.) в 25 мл безводного дихлорометана добавляют 7,85 г дициклогексилкарбодиимида (ДЦК, 38 ммолей, 1,4 экв.) и 4,54 мл триэтиламина (32,6 ммоля, 1,2 экв.). После этого добавляют гидрохлорид N-метилметаноламина, а затем 60 мг ДМАП ((4-диметиламино)пиридин). При этом происходит экзотермическая реакция и поэтому добавляют еще 25 мл дихлорометана. Смесь перемешивают при окружающей температуре в течение ночи, после чего фильтруют через диатомовую землю и концентрируют. Остаток обрабатывают простым эфиром, белое твердое вещество отфильтровывают и отбрасывают. Из маточного раствора удаляют растворитель, и остаток очищают колоночной хроматографией на SiO2, используя 15-25%-ный EtOAc в гексанах в качестве смесей элгоентов, с получением целевого амида в виде бесцветного масла (выход 55% от теоретического), который все еще содержит 10% дициклогексилмочевины. Этот продукт используют в последующей реакции без дополнительной очистки.
К раствору 1,0 г вышеуказанного амида (6,28 ммоля, 1 экв.) в 60 мл безводного ТГФ при -78°С по каплям с помощью шприца добавляют 12,6 мл 1,0-молярного раствора ДИБАГ в толуоле (12,6 ммоля, 2,0 экв.). После 30-минутного перемешивания при -78°С к реакционной смеси для прекращения реакции добавляют 50 мл МеОН и 50 мл воды. Реакционную смесь переносят в делительную воронку и добавляют 250 мл простого эфира. После этого добавляют 1 н. водный раствор НСl до тех пор, пока не растворится все твердое вещество. Слои разделяют и водную фазу дополнительно дважды экстрагируют простым эфиром порциями по 100 мл. Объединенные органические фазы промывают насыщенным водным раствором NaHCO3, а затем рассолом, сушат над Na2SO4, фильтруют и концентрируют. Сырой продукт очищают хроматографией на силикагеле с использованием 0-5%-ного МеОН в дихлорометане в качестве смесей элюентов. Таким путем получают целевой 3-тетрагидрофуроевый альдегид в виде легко улетучивающегося содержащего примеси бесцветного масла (200 мг).
К раствору 200 мг трет-бутилнафтилкарбамата (0,59 ммоля, 1 экв.) в 1,6 мл безводного трет-бутанола добавляют 200 мг полученного на предыдущей стадии 3-тетрагидрофуроеого альдегида (в избытке) и 1,78 мл раствора трет-бутоксида калия в трет-бутаноле (1,0 М, 1,78 ммоля, 3 экв.). Смесь выдерживают с нагреванием при 40°С в течение ночи, после чего охлаждают и прекращают реакцию добавлением насыщенного водного раствора NH4Cl. Полученный продукт экстрагируют смесью дихлорометана с метанолом (3×100 мл).
Объединенные экстракты промывают рассолом, сушат над MgSO4 и концентрируют. При этом согласно данным 1H-ЯМР-анализа расходуется только 10% енона. Остаток (300 мг) растворяют в 4,0 мл дихлорометана и обрабатывают 4 мл смеси дихлорометана с ТФУК в соотношении 1:1. Реакционную смесь перемешивают в течение 1,5 ч, после чего нейтрализуют насыщенным водным раствором NaHCO3, подщелачивают 4 н. раствором NaOH и экстрагируют дихлорметаном/метанолом (3×100 мл). Объединенные органические экстракты промывают рассолом, сушат (MgSO4), фильтруют и концентрируют. Сырой продукт очищают колоночной хроматографией на силикагеле, используя от 10 до 50% EtOAc в гексанах в качестве смесей элюентов, с получением указанного в заголовке соединения 32 (35 мг, 0,11 ммоля, выход 19% от теоретического).
Пример 33
4-[5-(4-аминонафталин-1-ил)пиридин-2-илокси]бутиронитрил
К раствору 2,5-дибромпиридина (500 мг, 2,1 ммоля) и 3-циано-1-пропанола (270 мг, 3,1 ммоля) в ДМСО (2 мл) добавляют 1М гексаметилдисилазид натрия (Na-ГМДС, 2,1 мл, 2,1 ммоля). После этого реакционную смесь перемешивают при комнатной температуре в течение ночи. Далее к реакционной смеси добавляют EtOAc и смесь промывают водой (2х10 мл). ЕtOАс-фракцию сушат над безводным сульфатом натрия и упаривают на роторном испарителе. Сырой продукт очищают колоночной экспресс-хроматографией на силикагеле, используя смесь 40%-ный EtOAc/гексаны, с получением 200 мг 5-бром-2-цианопропилоксипиридина в виде бледно-желтого твердого вещества (39,3%).
К полученному на предыдущей стадии промежуточному продукту (100 мг, 0,4 ммоля) и CBZ-защищенной нафтилбороновой кислоте XCVIX (полученной согласно методу получения Вос-аналога XCI в примере 17) (200 мг, 0,62 ммоля) в ДМЭ (4 мл) добавляют 2-молярный раствор карбоната натрия (2 мл). Раствор продувают азотом в течение 10 мин и затем добавляют тетракистрифенилфосфин палладия (20 мг). Реакционную смесь выдерживают с нагреванием при 90°С в течение 48ч, после чего охлаждают до комнатной температуры. Далее к реакционной смеси добавляют EtOAc и смесь промывают водой (2×10 мл). ЕtOАс-фракцию сушат над безводным сульфатом натрия, фильтруют и концентрируют. Сырой продукт очищают колоночной экспресс-хроматографией на силикагеле, элюируя смесью 40%-ный ЕtOАс/гексаны, с получением 70 мг продукта (39%).
К полученному на предыдущей стадии продукту реакции сочетания (70 мг, 0,16 ммоля) в EtOH (5 мл) добавляют циклогексен (263 мг, 3,2 ммоля) и 10%-ный Pd/C (20 мг). Реакционную смесь выдерживают с нагреванием в атмосфере азота в течение ночи и охлаждают до комнатной температуры. После этого реакционную смесь фильтруют через диатомовую землю, промывают МеОН и концентрируют. Сырой продукт очищают колоночной экспресс-хроматографией на силикагеле, элюируя смесью 50%-ный ЕtOАс/гексаны, с получением 15 мг указанного в заголовке соединения 33 (31%).
Пример 34
Дигидрохлорид [5-(4-аминонафталин-1-ил)пиридин-2-ил]-(тетрагидротиопиран-4-ил)амина
К тетрагидро-1,4-тиопирону (2,0 г, 17,2 ммоля) и гидрохлориду гидроксиламина (2,0 г, 28,7 ммоля) в EtOH (10 мл) добавляют тригидрат ацетата натрия (4,0 г, 29,4 ммоля) в 20 мл воды. Реакционную смесь нагревают с обратным холодильником в течение 3 ч, охлаждают до комнатной температуры и концентрируют на роторном испарителе до объема 15 мл. Остаток охлаждают в ледяной бане и фильтруют с получением 2,0 г оксимового продукта в виде белого твердого вещества с tпл 80-83°C (88,7%).
В сухую колбу, содержащую ТГФ (20 мл) и 1 М алюмогидрид лития (АГЛ) в диэтиловом эфире (19 мл) при комнатной температуре, добавляют полученный на предыдущей стадии оксим (500 мг, 3,82 ммоля). Реакционную смесь нагревают с обратным холодильником в течение 3 ч, охлаждают до комнатной температуры и реакцию избыточного АГЛ прекращают добавлением смеси льда с водой. После экстракции EtOAc и концентрирования получают 340 мг (76%) целевого 4-аминотетрагидротиопирана.
К полученному на предыдущей стадии амину (170 мг, 1,4 ммоля) в сухом пиридине (1 мл) добавляют 2,5-дибромпиридин (250 мг, 1,1 ммоля), после чего реакционную смесь выдерживают с нагреванием при 110-120°С в течение 5 дней. Затем реакционную смесь экстрагируют EtOAc, промывают водой, сушат над безводным сульфатом натрия и концентрируют с получением сырого продукта. Этот сырой продукт очищают колоночной экспресс-хроматографией на силикагеле, используя смесь 30%-ный EtOAc/гексаны в качестве элюента, с получением 100 мг чистого продукта (33,3%).
К полученному на предыдущей стадии промежуточному продукту (80 мг, 0,293 ммоля) и ВОС-защищенной нафтилбороновой кислоте XCI (пример 17) (140 мг, 0,488 ммоля) в ДМЭ (4 мл) добавляют 2М карбонат натрия (2 мл) и хлорид бис (трифенилфосфин) палладия (15 мг). Реакционную смесь выдерживают с нагреванием при 90°С в атмосфере азота в течение 18 ч и охлаждают до комнатной температуры. После этого реакционную смесь экстрагируют EtOAc, промывают водой, сушат над безводным сульфатом натрия и концентрируют с получением сырого продукта. Этот сырой продукт очищают колоночной экспресс-хроматографией на силикагеле, используя смесь 30%-ный EtOAc/гексаны в качестве элюента, с получением 110 мг чистого продукта ХСХ (86,0%)
К соединению ХСХ (35 мг, 0,08 ммоля) в диоксане (1 мл) добавляют смесь 4М HCl/диоксан (0,6 мл). Затем реакционную смесь перемешивают при комнатной температуре в течение 48 ч. После добавления диэтилового эфира получают продукт в виде гидрохлорида, который фильтруют с получением 18 мг (55%) указанного в заголовке соединения 34.
Пример 35
Дигидрохлорид [5-(4-аминонафталин-1-ил)пиридин-2-ил]-(тетрагидропиран-4-ил)амина
К 2-амино-5-бромпиридину (250 мг, 1,44 ммоля) и ВОС-защищенной нафтилбороновой кислоте XCI (пример 17) (688 мг, 2,4 ммоля) в 5 мл ДМЭ добавляют 2 М карбонат натрия (2,5 мл) и хлорид бис(трифенилфосфин)палладия (30 мг). Реакционную смесь выдерживают с нагреванием при 90°С в атмосфере азота в течение 18 ч и охлаждают до комнатной температуры. Затем реакционную смесь экстрагируют EtOAc, промывают водой, сушат над безводным сульфатом натрия и концентрируют. Остаток очищают колоночной экспресс-хроматографией на силикагеле, элюируя смесью 40%-ный EtOAc/гексаны, с получением 370 мг продукта реакции сочетания ХСХ (76,4%).
К этому промежуточному продукту (200 мг, 0,597 ммоля) и тетрагидропиранону (120 мг, 1,19 ммоля) в дихлорэтане (5 мл) добавляют ледяную уксусную кислоту (0,2 мл, 3,58 ммоля) и триацетоксиборогидрид натрия (380 мг, 1,79 ммоля). Реакционную смесь перемешивают при комнатной температуре в течение 48 ч, а затем экстрагируют EtOAc, промывают водой, сушат над безводным сульфатом натрия и концентрируют. Остаток очищают колоночной экспресс-хроматографией на силикагеле, элюируя смесью 50%-ный ЕtOАс/гексаны в качестве элюента, с получением 120 мг соединения XCXI (48,0%).
Полученное на предыдущей стадии соединение XCXI растворяют в дихлорметане (3 мл) и обрабатывают трифторуксусной кислотой (1 мл).
Реакционную смесь перемешивают в течение 3 ч и концентрируют. Остаток растворяют в EtOAc (20 мл), промывают раствором бикарбоната натрия, сушат над безводным сульфатом натрия и концентрируют с получением 90 мг указанного в заголовке соединения 35 (98,5%).
Пример 36
[5-(4-аминонафталин-1-ил)пиридин-2-ил]-(1-метилпиперидин-4-ил)амин
К смеси соединения ХСХ (пример 35) (110 мг, 0,33 ммоля) и 1-метил-4-пиперидона (80 мг, 0,7 ммоля) в дихлорэтане (6 мл) добавляют ледяную уксусную кислоту (120 мг, 2,0 ммоля) и триацетоксиборогидрид натрия (220 мг, 1,03 ммоля). Реакционную смесь перемешивают при комнатной температуре в течение 96 ч, а затем экстрагируют EtOAc, промывают водой, сушат над безводным сульфатом натрия и концентрируют. Остаток очищают колоночной экспресс-хроматографией на силикагеле, используя смесь 10% МеОН/СН2Сl2/0,1% ТЭА (триэтаноламин) в качестве элюента, с получением 60 мг чистого продукта (42,0%).
Полученный на предыдущей стадии продукт растворяют в дихлорметане (3 мл) и обрабатывают трифторуксусной кислотой (1 мл). Реакционную смесь перемешивают в течение 2,5 ч и концентрируют с получением 94 мг указанного в заголовке соединения 36 (100%).
Пример 37
В примере 37 проиллюстрирован синтез соединения формулы III, в которой Е означает О.
3-трет-бутилфениловый эфир [4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]карбаминовой кислоты
Соединение LXXXIV (пример 4) (100 мг, 0,31 ммоля) растворяют в дихлорметане (20 мл). После этого добавляют равный объем насыщенного водного бикарбоната натрия и двухфазный раствор охлаждают до 0°С. Далее на время добавления фосгена (1,93 М в толуоле, 0,40 мл) перемешивание останавливают. Сразу же после этого перемешивание реакционной смеси возобновляют и продолжают в течение 15 мин при 0°С. После этого слои разделяют, органические фазы сушат над твердым сульфатом магния и раствор концентрируют до объема примерно 5 мл. Затем добавляют 3-трет-бутилфенол (100 мг, 0,67 ммоля) в дихлорметане (5 мл). Реакционную смесь перемешивают при комнатной температуре в течение 19 ч. После экспресс-хроматографии с использованием EtOAc в качестве элюента получают 71 мг указанного в заголовке соединения 37.
Пример 38
В примере 38 проиллюстрирован синтез соединения формулы III, в которой Е означает CH2.
2-(5-трет-бутил-2-метоксифенил)-N-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]ацетамид
Соединение LXXXIV (пример 4) (100 мг, 0,4 ммоля) и натриевую соль 5-трет-бутил-2-метоксифенилуксусной кислоты (154 мг, 0,4 ммоля) растворяют в дихлорметане (15 мл). Далее добавляют гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (172 мг, 0,9 ммоля) и реакционную смесь перемешивают при окружающей температуре в течение 16 ч. После очистки жидкостной хроматографией высокого разрешения (ЖХВР) получают 30 мг указанного в заголовке соединения 38.
Аналогично описанным выше методам получают также следующие соединения:
1-(2-трет-бутил-5-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил]-3-{4-[6-(морфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метилбифенил-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
амид 1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперидин-3-карбоновой кислоты,
1-(5-изопропил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-втор-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксиметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(тетрагидрофуран-3-иламино)-метил]пиридин-3-ил]}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[4-(3-метоксифенил)пиперазин-1-илметил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(5-морфолин-4-илметилпиразин-2-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)-(тетрагидрофуран-2-илметил)амино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)пиридин-3-илметиламино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксо-1λ4-тиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)-пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилпиперидин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метоксиметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метил-3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-тиа-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-пиридин-2-илпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(морфолин-4-карбонил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(пиридин-3-илокси)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(тетрагидропиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метилфенил)-3-(4-{6-[(3-метоксипропил)метиламино]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-{[бис(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевину,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-гидроксипропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(морфолин-4-карбонил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-ил)ацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-N-метилацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-2,2,2-трифторацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)метансульфонамид.
Оценка биологических свойств
Ингибирование продуцирования TNF в ТНР-клетках
Ингибирование продуцирования цитокинов можно можно оценить путем измерения ингибирования TNFα в стимулированных с помощью липополисахаридов ТНР-клетках (см., например, W. Prichett и др., J. Inflammation, 45, 97, 1995). Все клетки и реагенты разбавляли средой RPMT 1640, содержащей феноловый красный и L-глутамин с добавлением еще одной порции L-глутамина (всего: 4 мМ), пенициллини и стрептомицина (по 50 ед./мл каждого) и фетальную бычью сыворотку (ФБС, 3%) (фирма GIBCO, все концентрации представляют собой конечные концентрации). Анализ проводили в стерильных условиях; только получение тестируемого соединения проводили в нестерильных условиях. Исходные маточные растворы готовили в ДМСО, а затем разбавляли средой RPMI 1640 до достижения концентрации, превышающей в 2 раза конечную требующуюся для анализа концентрацию.
Конфлуентные ТНР.1-клетки (конечная концентрация 2×106 клеток/мл, American Type Culture Company, Роквилл, шт. Мэриленд) вносили в 96-луночные полипропиленовые круглодонные планшеты для культивирования (типа Costar 3790; стерильные), содержащие 125 мкл тестируемого соединения (2-кратной концентрации) или носитель, представляющий собой ДМСО (контроли, чистые). Конечная концентрация ДМСО не превышала 0,2%. Смесь, содержащую клетки, подвергали предварительной инкубации в течение 30 мин при 37°С, 5% СО2, перед стимуляцией с помощью липополисахарида (ЛПС; конечная концентрация 1 мкг/мл; Siga L-2630, из серотипа 0111.В4 Е.соli; хранившийся при -80°С в виде маточного раствора с концентрацией 1 мг/мл в дистиллированной Н2О с постоянным наблюдением за присутствием эндотоксина). В контрольные образцы (нестимулированные) добавляли носитель, представляющий собой Н2О; конечный объем для инкубации составлял 250 мкл. Инкубацию в течение ночи (18-24 ч) проводили по описанной выше методике. Процесс прекращали путем центрифугирования планшетов при 1600 об/мин (400xg) в течение 5 мин при комнатной температуре; супернатанты переносили в чистые 96-луночные планшеты и хранили при -80°С до проведения анализа в отношении человеческого TNFα с помощью имеющегося в продаже набора для ELISA (типа Biosource #KHC3015, Камарильо, шт. Калифорния). Данные анализировали методом нелинейной регрессии (с использованием уравнения Хилла), получая зависимость реакции от дозы с помощью математического обеспечения SAS Software System (институт SAS, Inc., Кари, шт. Северная Каролина). Рассчитанное значение IC50 представляет собой концентрацию тестируемого соединения, которая приводит к 50%-ному уменьшению продуцирования TNFα по сравнению с максимальным значением.
С помощью этого метода анализа проводили оценку предпочтительных соединений, включая соединения, приведенные в примерах синтеза, и было установлено, что для них IC50 составляет менее 10 мкМ.
Ингибирование других цитокинов
Аналогичными методами с использованием клеток моноцитов периферической крови, соответствующих стимулов и имеющихся в продаже наборов для ELISA (или с помощью другого метода обнаружения, такого как радиоиммунный анализ), пригодных для конкретного цитокина, может быть продемонстрировано ингибирование IL-1β, GM-CSF, IL-6 и IL-8 (см., например, J.C. Lee и др., Int. J. Immunopharmacol., 10, 835, 1988).
Claims (12)
1. Соединение формулы (I)
в которой Ar1 означает пиразол, который может быть замещен одной или несколькими группами R1, R2 или R3;
Аr2 означает нафтил, тетрагидронафтил, каждый из которых необязательно замещен 0-1 группами R2;
Х означает С5-С8циклоалкенил, фенил, необязательно замещенный гидроксигруппой или С1-С4алкоксигруппой, фуранил, пиридинонил, пиразолил, пиридинил, необязательно замещенный гидроксигруппой или С1-С4алкоксигруппой, пиперидинил;
Y означает связь или насыщенную разветвленную или неразветвленную С1-С4углеродную цепь, при этом одна метиленовая группа необязательно заменена на NH или Y необязательно независимо замещен оксогруппой;
Z означает морфолино-группу, пиридинил, фуранил, тетрагидрофуранил, тиоморфолинил, пентаметиленсульфид, пентаметиленсульфон, вторичный или третичный амин, причем атом азота аминогруппы ковалентно связан со следующими группами, выбранными из ряда, включающего С1-С3алкил и С1-С5алкоксиалкил;
R1 означает С3-С10алкил, который необязательно частично или полностью галогенирован;
R2 означает разветвленный или неразветвленный С1-С6алкил, который необязательно частично или полностью галогенирован, галоген;
R3 означает фенил, пиримидинил, пиразолил, которые замещены одним разветвленным или неразветвленным С1-С6алкилом, и пиридинил, необязательно замещенный С1-С3алкоксигруппой или аминогруппой;
W означает О,
и его фармацевтически приемлемые соли.
2. Соединение по п.1, в котором Y означает -СН2-, -СН2СН2-, -CH2NH-, -CH2CH2NH- или связь и Z означает морфолин, пиридинил, фуранил, тетрагидрофуранил, тиоморфолинил, пентаметиленсульфид, пентаметиленсульфон, вторичный или третичный амин, причем атом азота аминогруппы ковалентно связан со следующими группами, выбранными из ряда, включающего С1-С3алкил и С1-С5алкоксиалкил.
3. Соединение по п.2, в котором Ar1 означает 5-трет-бутилпиразол-3-ил, где пиразольное кольцо может быть замещено группой R3, при этом R3 означает фенил, пиримидинил, пиразолил, которые замещены одним разветвленным или неразветвленным С1-С6алкилом, и пиридинил, необязательно замещенный C1-С3алкоксигруппой или аминогруппой.
4. Соединение по п.3, в котором Х означает пиридинил.
5. Соединение по п.4, в котором пиридинил присоединен к Аr1 в 3-м положении пиридинила.
6. Соединение формулы (I) по п.1, выбранное из группы, включающей
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-ил-метил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(2-(морфолин-4-ил)этил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-ил-метил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилпиридин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-морфолин-4-илметилфур-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-метил-2Н-пиразол-3-ил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(5-(морфолин-4-илметил)пиридин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(2-(пиридин-2-ил)этиламино)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(4-(пиридин-3-илметиламинометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(морфолин-4-ил-метил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутиламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(4-метил-3-карбамилфенил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3-гидроксипиперидин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(4-гидроксиморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(3-(морфолин-4-илметил)циклогексенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тетрагидрофуран-3-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-ди(2-метоксиэтил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(3-цианопропокси)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-морфолин-4-илметилпиперидинил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N,N-ди(2-цианоэтил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(фуран-2-илметил)-3-гидроксифенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(тиоморфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(3-карбоксамидопиперидин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(2-метил-3-оксопиперазин-1-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(4-гидроксибутилокси)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1’Н-[1,4’]бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-цианоэтил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метоксипиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-аминоупиридин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-ил-4-карбонил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(пиридин-3-илметил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(4-(N-(2-цианоэтил)-N-(тетрагидрофуран-2-илметил)аминометил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)-4-метоксипиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-морфолин-4-илпропил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1’-метил-1’Н-[1,4’]бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксо-тетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(5-(тетрагидротиопиран-4-иламино)пиразин-2-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(6-метилпиридин-3-ил)-2Н-пиразол-3-ил]-3-[4-(6-(метилкарбониламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1’-(3-метилсульфанилпропил)-1’Н-[1,4’]бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(тетрагидропиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилтиопиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-аминопиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(6-(морфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[3-трет-бутил-1’-метил-1’Н-[1,4’]бипиразол-5-ил]-3-[4-(6-(морфолин-4-илметил)фенил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(тиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илкарбонил)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-п-толил-2Н-пиразол-3-ил]-3-[4-(6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)-2Н-пиразол-3-ил]-3-[4-(2-(морфолин-4-илметил)пиримидин-5-ил)нафталин-1-ил]мочевину,
1-(2-трет-бутил-5-метилпиридин-4-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-трет-бутилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-метилбифенил-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(4-трет-бутилбифенил-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-изопропил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-втор-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксиметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилфенил)-3-(4-{6-[(3-метоксипропил)метиламино]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилпиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(1,1-диметилпропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(2-метилпиримидин-5-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-гидроксипропил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(морфолин-4-карбонил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-(3-метилнафталин-2-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-гидроксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,3-диметил-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-{5-трет-бутил-2-метил-3-[3-(тетрагидропиран-2-илокси)проп-1-инил]фенил}-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(2,2-диметилпропионил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(3-гидроксипроп-1-инил)-2-метилфенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-2-(3-гидроксипроп-1-инил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,2-диметил-[1,3]диоксолан-4-илметил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2,3-дигидроксипропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутокси-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-(1-цианоциклопропил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[5-трет-бутил-3-(2-диэтиламиноэтил)-2-метоксифенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-[1,3]диоксолан-2-илпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-пирролидин-1-ил-фенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-диметиламинофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-пропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-гидроксиметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-циклогексил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2,4-диметокси-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метокси-3-нитрофенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-метилпиридин-3-ил)нафталин-1-ил]мочевину,
N-ацетил-N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)ацетамид,
1-(6-трет-бутил-4-метил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-этокси-фенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-изопропоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-имидазол-1-илфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-3-этиламино-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)бис(метансульфон)амид,
1-[5-трет-бутил-2-(1-метил-1Н-пиразол-4-ил)фенил]-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(2-метансульфинил-5-трифторметилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-{[бис(2-метоксиэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевину,
N-[1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пирролидин-3-ил]ацетамид,
1-(1-ацетил-3,3-диметил-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)пропионамид,
1-(5-трет-бутил-2-метил-бензооксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]-3-(3-трифторметансульфонилфенил)мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)изобутирамид,
2-(4-трет-бутил-2-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенокси)ацетамид,
1-(5-трет-бутил-2-оксо-2,3-дигидробензооксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-3-циано-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутилбензооксазол-7-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)бензолсульфонамид,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид этансульфоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(2-морфолин-4-илметилпиримидин-5-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метилсульфанилфенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксипиридин-3-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)амид 2,2,2-трифторэтансульфоновой кислоты,
N-(5-{4-[3-(5-трет-бутил-2-метилфенил)уреидо]нафталин-1-ил}пиразин-2-ил)метансульфонамид,
1-[4-(6-{[бис(2-цианоэтил)амино]метил}пиридин-3-ил)нафталин-1-ил]-3-(5-трет-бутил-2-метоксифенил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-тиоморфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилпиперидин-1-илметил)-пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксотетрагидротиопиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(тетрагидропиран-4-иламино)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)-(тетрагидрофуран-2-илметил)амино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метоксиметилморфолин-4-илметил)-пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-метил-3-оксопиперазин-1-илметил)-пиридин-3-ил]нафталин-1-ил}мочевину,
амид 1-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-илметил)пиперидин-3-карбоновой кислоты,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(1-оксотиоморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(3,3-диметил-2-оксо-2,3-дигидро-1Н-индол-5-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(3-оксопиперазин-1-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[(тетрагидрофуран-3-иламино)метил]пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(6-{[(2-цианоэтил)пиридин-3-илметиламино]метил}пиридин-3-ил)нафталин-1-ил]мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2-окса-5-азабицикло[2.2.1]гепт-5-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(2,6-диметилморфолин-4-илметил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-(4-{6-[4-(3-метоксифенил)пиперазин-1-илметил]-пиридин-3-ил}нафталин-1-ил)мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(морфолин-4-карбонил)пиридин-3-ил]нафталин-1-ил}мочевину,
1-(5-трет-бутил-2-метоксифенил)-3-[4-(5-морфолин-4-илметилпиразин-2-ил)нафталин-1-ил]мочевину,
1-(6-трет-бутил-3-оксо-3,4-дигидро-2Н-бензо[1,4]оксазин-8-ил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
1-(3-амино-5-трет-бутил-2-метоксифенил)-3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]мочевину,
N-(5-{4-[3-(5-трет-бутил-2-метоксифенил)уреидо]нафталин-1-ил}пиридин-2-ил)ацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-N-метилацетамид,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)-2,2,2-трифторацетамид,
1-(5-трет-бутил-2-метоксифенил)-3-{4-[6-(пиридин-3-илокси)пиридин-3-ил]нафталин-1-ил}мочевину,
3-трет-бутилфениловый эфир [4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]карбаминовой кислоты,
N-(5-трет-бутил-2-метокси-3-{3-[4-(6-морфолин-4-илметилпиридин-3-ил)нафталин-1-ил]уреидо}фенил)метансульфонамид,
и их фармацевтически приемлемые соли.
7. Фармацевтическая композиция для лечения заболевания, опосредованного цитокинами и нейтрофилами, содержащая фармацевтически эффективное количество соединения по п.1.
8. Способ лечения заболевания, опосредуемого цитокинами, заключающийся во введении пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по п.1.
9. Способ по п.8, где указанное опосредуемое цитокинами заболевание представляет собой заболевание из группы, включающей ревматоидный артрит, остеоартрит, болезнь Крона, неспецифический язвенный колит, множественный склероз, синдром Гийена-Барре, псориаз, реакцию "трансплантат против хозяина", системную красную волчанку, диабет, токсический шок, остеопороз, болезнь Альцгеймера, острую и хроническую боль, контактный дерматит и атеросклероз.
10. Способ лечения опосредуемого нейтрофилами заболевания, выбранного из группы, включающей удар, инфаркт миокарда, термический ожог, респираторный дистресс-синдром взрослых (РДСВ), множественное повреждение в результате травмы, острый гломерулонефрит, дерматоз, сопровождающийся острыми воспалительными процессами, острый гнойный менингит, гемодиализ, лейкофериз (leukopheresis), связанные с трансфузией гранулоцитов синдромы и некротический энтероколит, заключающийся во введении пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по п.1.
Приоритет по пунктам:
12.03.1999 по пп.1-13;
16.11.1999 по пп.1-13.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12414899P | 1999-03-12 | 1999-03-12 | |
| US60/124,148 | 1999-03-12 | ||
| US16586799P | 1999-11-16 | 1999-11-16 | |
| US60/165,867 | 1999-11-16 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2004121842/04A Division RU2298008C2 (ru) | 1999-11-16 | 2000-02-16 | Соединения, содержащие их фармацевтические композиции, и способ лечения заболевания, опосредуемого цитокинами |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2001126337A RU2001126337A (ru) | 2003-07-10 |
| RU2242474C2 true RU2242474C2 (ru) | 2004-12-20 |
Family
ID=26822256
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2001126337/04A RU2242474C2 (ru) | 1999-03-12 | 2000-02-16 | Соединения, пригодные в качестве противовоспалительных агентов |
Country Status (35)
| Country | Link |
|---|---|
| US (5) | US6358945B1 (ru) |
| EP (1) | EP1165516B1 (ru) |
| JP (1) | JP4820488B2 (ru) |
| KR (1) | KR100709497B1 (ru) |
| CN (2) | CN1156452C (ru) |
| AR (1) | AR028473A1 (ru) |
| AT (1) | ATE278674T1 (ru) |
| AU (1) | AU771273B2 (ru) |
| BG (1) | BG65159B1 (ru) |
| BR (1) | BR0008922A (ru) |
| CA (1) | CA2362003C (ru) |
| CO (1) | CO5251387A1 (ru) |
| CZ (1) | CZ20013289A3 (ru) |
| DE (1) | DE60014603T2 (ru) |
| DK (1) | DK1165516T3 (ru) |
| EE (1) | EE04799B1 (ru) |
| ES (1) | ES2225095T3 (ru) |
| HK (1) | HK1043127B (ru) |
| HR (1) | HRP20010665A2 (ru) |
| HU (1) | HUP0202248A3 (ru) |
| ID (1) | ID30176A (ru) |
| IL (3) | IL144897A0 (ru) |
| NO (1) | NO321120B1 (ru) |
| NZ (2) | NZ514711A (ru) |
| PE (1) | PE20001484A1 (ru) |
| PL (1) | PL350357A1 (ru) |
| PT (1) | PT1165516E (ru) |
| RU (1) | RU2242474C2 (ru) |
| SG (1) | SG142120A1 (ru) |
| SI (1) | SI1165516T1 (ru) |
| SK (1) | SK12832001A3 (ru) |
| TR (1) | TR200102817T2 (ru) |
| UY (1) | UY26058A1 (ru) |
| WO (1) | WO2000055139A2 (ru) |
| YU (1) | YU64701A (ru) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2442777C2 (ru) * | 2006-01-31 | 2012-02-20 | Эррэй Биофарма Инк. | Ингибиторы киназ и способы их применения |
| RU2478639C2 (ru) * | 2005-05-24 | 2013-04-10 | Лаборатуар Сероно С.А. | Трициклические спиро-производные в качестве модуляторов crth2 |
| RU2489426C2 (ru) * | 2007-12-14 | 2013-08-10 | Актелион Фармасьютиклз Лтд | Производные аминопиразола |
| RU2496778C2 (ru) * | 2009-03-09 | 2013-10-27 | Тайхо Фармасьютикал Ко., Лтд. | Пиперазиновое соединение, ингибирующее простагландин-d-синтазу |
| RU2505538C2 (ru) * | 2008-02-05 | 2014-01-27 | Ф.Хоффманн-Ля Рош Аг | Новые пиридиноны и пиридазиноны |
Families Citing this family (145)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HU228769B1 (en) * | 1996-07-24 | 2013-05-28 | Celgene Corp | Substituted 2(2,6-dioxopiperidin-3-yl)phthalimides and -1-oxoisoindolines and their use for production of pharmaceutical compositions for mammals to reduce the level of tnf-alpha |
| US7517880B2 (en) | 1997-12-22 | 2009-04-14 | Bayer Pharmaceuticals Corporation | Inhibition of p38 kinase using symmetrical and unsymmetrical diphenyl ureas |
| US7329670B1 (en) | 1997-12-22 | 2008-02-12 | Bayer Pharmaceuticals Corporation | Inhibition of RAF kinase using aryl and heteroaryl substituted heterocyclic ureas |
| US8124630B2 (en) | 1999-01-13 | 2012-02-28 | Bayer Healthcare Llc | ω-carboxyaryl substituted diphenyl ureas as raf kinase inhibitors |
| JP2002534468A (ja) | 1999-01-13 | 2002-10-15 | バイエル コーポレイション | p38キナーゼ阻害剤としてのω−カルボキシアリール置換ジフェニル尿素 |
| ME00275B (me) * | 1999-01-13 | 2011-02-10 | Bayer Corp | ω-KARBOKSIARIL SUPSTITUISANI DIFENIL KARBAMIDI KAO INHIBITORI RAF KINAZE |
| EP1140840B1 (en) | 1999-01-13 | 2006-03-22 | Bayer Pharmaceuticals Corp. | -g(v)-carboxyaryl substituted diphenyl ureas as raf kinase inhibitors |
| CN1156452C (zh) * | 1999-03-12 | 2004-07-07 | 贝林格尔·英格海姆药物公司 | 作为消炎剂的化合物 |
| EP1466906A1 (en) * | 1999-03-12 | 2004-10-13 | Boehringer Ingelheim Pharmaceuticals Inc. | Heterocyclic urea and related compounds useful as anti-inflammatory agents |
| US7629360B2 (en) | 1999-05-07 | 2009-12-08 | Celgene Corporation | Methods for the treatment of cachexia and graft v. host disease |
| WO2001004115A2 (en) * | 1999-07-09 | 2001-01-18 | Boehringer Ingelheim Pharmaceuticals, Inc. | Novel process for synthesis of heteroaryl-substituted urea compounds |
| ATE375334T1 (de) * | 1999-11-16 | 2007-10-15 | Boehringer Ingelheim Pharma | Harnstoff derivate als entzündungshemmende mittel |
| US6635767B2 (en) | 2000-05-23 | 2003-10-21 | Boehringer Ingelheim Pharmaceuticals, Inc. | Synthesis of heteroarylamine intermediate compounds |
| US6822093B2 (en) | 2000-05-23 | 2004-11-23 | Boehringer Ingelheim Pharmaceuticals, Inc. | Synthesis of heteroarylamine intermediate compounds |
| US7235576B1 (en) | 2001-01-12 | 2007-06-26 | Bayer Pharmaceuticals Corporation | Omega-carboxyaryl substituted diphenyl ureas as raf kinase inhibitors |
| EP1362037A1 (en) | 2001-02-15 | 2003-11-19 | Boehringer Ingelheim Pharmaceuticals Inc. | Process for synthesis of heteroaryl-substituted urea compounds useful as antiinflammatory agents |
| US6949585B2 (en) | 2001-04-03 | 2005-09-27 | Eisai Co., Ltd. | Cyclooctanone derivatives and cyclodecanone derivative, and use thereof |
| EP1381594A1 (en) * | 2001-04-13 | 2004-01-21 | Boehringer Ingelheim Pharmaceuticals Inc. | Urea compounds useful as anti-inflammatory agents |
| US7371763B2 (en) * | 2001-04-20 | 2008-05-13 | Bayer Pharmaceuticals Corporation | Inhibition of raf kinase using quinolyl, isoquinolyl or pyridyl ureas |
| JP2004530690A (ja) | 2001-05-16 | 2004-10-07 | ベーリンガー インゲルハイム ファーマシューティカルズ インコーポレイテッド | 抗炎症性薬剤として有用なジアリールウレア誘導体 |
| US6953801B2 (en) | 2001-05-22 | 2005-10-11 | Neurogen Corporation | Melanin concentrating hormone receptor ligands: substituted 1-benzyl-4-aryl piperazine analogues |
| EP1935885A3 (en) * | 2001-05-22 | 2008-10-15 | Neurogen Corporation | Melanin concentrating hormone receptor ligands : substituted 1-benzyl-4-aryl piperazine analogues. |
| JP2004531571A (ja) * | 2001-05-25 | 2004-10-14 | ベーリンガー インゲルハイム ファーマシューティカルズ インコーポレイテッド | サイトカイン生産のインヒビターとしてのカルバメート及びオキサミド化合物 |
| AU2002310156A1 (en) | 2001-06-05 | 2002-12-16 | Boehringer Ingelheim Pharmaceuticals, Inc. | 1,4-disubstituted benzo-fused cycloalkyl urea compounds |
| US8329924B2 (en) * | 2001-06-11 | 2012-12-11 | Vertex Pharmaceuticals (Canada) Incorporated | Compounds and methods for the treatment or prevention of Flavivirus infections |
| AP1753A (en) * | 2001-06-11 | 2007-07-18 | Shire Biochem Inc | Thiophene derivatives as antiviral agents for flavvivirus infection |
| ATE343415T1 (de) | 2001-06-29 | 2006-11-15 | Ab Science | Die verwendung von c-kit hemmer zur behandlung von entzündlichen darmerkrankungen |
| JP2004537536A (ja) | 2001-06-29 | 2004-12-16 | アブ サイエンス | アレルギー疾患を治療するためのチロシンキナーゼ阻害剤の使用方法 |
| DK1401415T3 (da) | 2001-06-29 | 2006-10-16 | Ab Science | Anvendelse af N-phenyl-2-pyrimidinamin-derivater til behandling af inflammatoriske sygdomme |
| US7727731B2 (en) | 2001-06-29 | 2010-06-01 | Ab Science | Potent, selective and non toxic c-kit inhibitors |
| CA2452390A1 (en) * | 2001-06-29 | 2003-01-09 | Ab Science | Use of tyrosine kinase inhibitors for treating bone loss |
| WO2003006431A1 (en) * | 2001-07-11 | 2003-01-23 | Boehringer Ingelheim Pharmaceuticals, Inc. | A novel synthesis for heteroarylamine compounds |
| US6603000B2 (en) | 2001-07-11 | 2003-08-05 | Boehringer Ingelheim Pharmaceuticals, Inc. | Synthesis for heteroarylamine compounds |
| DE60219793T2 (de) * | 2001-07-11 | 2008-01-24 | Boehringer Ingelheim Pharmaceuticals, Inc., Ridgefield | Verfahren zur Behandlung von Cytokin-Vermittelten Erkrankungen |
| EP1709965A3 (en) | 2001-07-11 | 2006-12-27 | Boehringer Ingelheim Pharmaceuticals, Inc. | Methods of treating cytokine mediate diseases |
| TWI283665B (en) | 2001-09-13 | 2007-07-11 | Smithkline Beecham Plc | Novel urea compound, pharmaceutical composition containing the same and its use |
| US7211575B2 (en) | 2001-09-13 | 2007-05-01 | Boehringer Ingelheim Pharmaceuticals, Inc. | Methods of treating cytokine mediated diseases |
| US6825184B2 (en) * | 2001-10-18 | 2004-11-30 | Boehringer Ingelheim Pharmaceuticals, Inc. | 1,4-Disubstituted benzo-fused urea compounds |
| US20080108672A1 (en) * | 2002-01-11 | 2008-05-08 | Bernd Riedl | Omega-Carboxyaryl Substituted Diphenyl Ureas As Raf Kinase Inhibitors |
| PT1478358E (pt) | 2002-02-11 | 2013-09-11 | Bayer Healthcare Llc | Tosilato de sorafenib para o tratamento de doenças caracterizadas por angiogénese anormal |
| US20030216396A1 (en) | 2002-02-11 | 2003-11-20 | Bayer Corporation | Pyridine, quinoline, and isoquinoline N-oxides as kinase inhibitors |
| PT1580188E (pt) | 2002-02-11 | 2012-01-25 | Bayer Healthcare Llc | Aril-ureias como inibidores de cinases |
| DE60319066T2 (de) * | 2002-02-25 | 2009-02-26 | Boehringer Ingelheim Pharmaceuticals, Inc., Ridgefield | 1,4-disubstituierte benzokondensierte cycloalkyl-harnstoffverbindungen zur behandlung von zytokinvermittelten erkrankungen |
| JP2005528374A (ja) * | 2002-04-05 | 2005-09-22 | ベーリンガー インゲルハイム ファルマ ゲゼルシャフト ミット ベシュレンクテル ハフツング ウント コンパニー コマンディトゲゼルシャフト | 粘液分泌過多の治療方法 |
| US20030225089A1 (en) * | 2002-04-10 | 2003-12-04 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Pharmaceutical compositions based on anticholinergics and p38 kinase inhibitors |
| EP1497278B1 (en) * | 2002-04-11 | 2010-05-26 | Boehringer Ingelheim Pharmaceuticals Inc. | Heterocyclic amide derivatives as cytokine inhibitors |
| US20030236287A1 (en) * | 2002-05-03 | 2003-12-25 | Piotrowski David W. | Positive allosteric modulators of the nicotinic acetylcholine receptor |
| CA2490120C (en) * | 2002-06-19 | 2010-06-01 | Neurotech Co., Ltd. | Tetrafluorobenzyl derivatives and pharmaceutical composition for preventing and treating acute and chronic neurodegenerative diseases in central nervous system containing the same |
| US20040044020A1 (en) * | 2002-07-09 | 2004-03-04 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Pharmaceutical compositions based on novel anticholinergics and p38 kinase inhibitors |
| ES2278170T3 (es) * | 2002-07-09 | 2007-08-01 | BOEHRINGER INGELHEIM PHARMA GMBH & CO.KG | Composiciones farmaceuticas de anticolinergicos e inhibidores de la quinasa p38 en el tratamiento de enfermedades respiratorias. |
| EP1549621A1 (en) * | 2002-08-08 | 2005-07-06 | Boehringer Ingelheim Pharmaceuticals Inc. | Fluorinated phenyl-naphthalenyl-urea compounds as inhibitors of cytokines involved in inflammatory processes |
| US7232828B2 (en) * | 2002-08-10 | 2007-06-19 | Bethesda Pharmaceuticals, Inc. | PPAR Ligands that do not cause fluid retention, edema or congestive heart failure |
| US20040110755A1 (en) * | 2002-08-13 | 2004-06-10 | Boehringer Ingelheim Pharmaceuticals, Inc. | Combination therapy with p38 MAP kinase inhibitors and their pharmaceutical compositions |
| EP1545514A1 (en) * | 2002-08-14 | 2005-06-29 | Boehringer Ingelheim Pharmaceuticals Inc. | Anticoagulant and fibrinolytic therapy using p38 map kinase inhibitors |
| US7179836B2 (en) * | 2002-09-20 | 2007-02-20 | Smithkline Beecham Corporation | Chemical compounds |
| US7202259B2 (en) * | 2002-11-18 | 2007-04-10 | Euro-Celtique S.A. | Therapeutic agents useful for treating pain |
| US7022883B2 (en) * | 2002-11-22 | 2006-04-04 | Boehringer Ingelheim Pharmaceuticals, Inc. | Preparation of aryl intermediates |
| CN100413861C (zh) | 2002-12-10 | 2008-08-27 | 维勒凯姆制药股份有限公司 | 用于治疗或预防黄病毒感染的化合物 |
| US7144911B2 (en) | 2002-12-31 | 2006-12-05 | Deciphera Pharmaceuticals Llc | Anti-inflammatory medicaments |
| US7202257B2 (en) | 2003-12-24 | 2007-04-10 | Deciphera Pharmaceuticals, Llc | Anti-inflammatory medicaments |
| UY28213A1 (es) | 2003-02-28 | 2004-09-30 | Bayer Pharmaceuticals Corp | Nuevos derivados de cianopiridina útiles en el tratamiento de cáncer y otros trastornos. |
| US7135575B2 (en) * | 2003-03-03 | 2006-11-14 | Array Biopharma, Inc. | P38 inhibitors and methods of use thereof |
| RU2357957C2 (ru) * | 2003-03-03 | 2009-06-10 | Эррэй Биофарма, Инк. | Ингибиторы р38 и способы их применения |
| EP1608648B1 (en) | 2003-03-12 | 2012-07-18 | Pfizer Products Inc. | Pyridyloxymethyl and benzisoxazole azabicyclic derivatives |
| GB2400101A (en) * | 2003-03-28 | 2004-10-06 | Biofocus Discovery Ltd | Compounds capable of binding to the active site of protein kinases |
| JPWO2004101529A1 (ja) * | 2003-05-19 | 2006-07-13 | 小野薬品工業株式会社 | 含窒素複素環化合物およびその医薬用途 |
| DK1636585T3 (da) * | 2003-05-20 | 2008-05-26 | Bayer Pharmaceuticals Corp | Diarylurinstoffer med kinasehæmmende aktivitet |
| PT1663978E (pt) * | 2003-07-23 | 2008-02-15 | Bayer Pharmaceuticals Corp | Omega-carboxiaril difenil ureia substituída por flúor para o tratamento e a prevenção de doenças e estados patológicos |
| RU2006108864A (ru) * | 2003-08-22 | 2007-09-27 | Берингер Ингельхайм Фармасьютиклз, Инк. (Us) | Способы лечения хронического обструктивного заболевания легких (хозл) и легочной гипертензии |
| KR100886002B1 (ko) * | 2004-01-30 | 2009-03-03 | 유로-셀띠끄 소시에떼 아노님 | 4-테트라졸릴-4-페닐피페리딘 화합물의 제조방법 |
| MXPA06012394A (es) * | 2004-04-30 | 2007-01-31 | Bayer Pharmaceuticals Corp | Derivados de pirazolilurea sustituidos utiles en el tratamiento de cancer. |
| US7550499B2 (en) * | 2004-05-12 | 2009-06-23 | Bristol-Myers Squibb Company | Urea antagonists of P2Y1 receptor useful in the treatment of thrombotic conditions |
| PT1761520E (pt) * | 2004-06-23 | 2008-09-15 | Lilly Co Eli | Inibidores de quinase |
| US20060035893A1 (en) | 2004-08-07 | 2006-02-16 | Boehringer Ingelheim International Gmbh | Pharmaceutical compositions for treatment of respiratory and gastrointestinal disorders |
| CA2580844A1 (en) | 2004-09-20 | 2006-03-30 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives and their use as mediators of stearoyl-coa desaturase |
| JP4958785B2 (ja) | 2004-09-20 | 2012-06-20 | ゼノン・ファーマシューティカルズ・インコーポレイテッド | 複素環誘導体およびステアロイル−CoAデサチュラーゼインヒビターとしてのそれらの使用 |
| US7767677B2 (en) | 2004-09-20 | 2010-08-03 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives and their use as stearoyl-CoA desaturase inhibitors |
| CN101084211A (zh) | 2004-09-20 | 2007-12-05 | 泽农医药公司 | 杂环衍生物及其作为治疗剂的用途 |
| US7919496B2 (en) | 2004-09-20 | 2011-04-05 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives for the treatment of diseases mediated by stearoyl-CoA desaturase enzymes |
| WO2006034441A1 (en) | 2004-09-20 | 2006-03-30 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives and their use as stearoyl-coa desaturase inhibitors |
| AR051094A1 (es) | 2004-09-20 | 2006-12-20 | Xenon Pharmaceuticals Inc | Derivados heterociclicos y su uso como inhibidores de la estearoil-coa desaturasa |
| US7612200B2 (en) * | 2004-12-07 | 2009-11-03 | Locus Pharmaceuticals, Inc. | Inhibitors of protein kinases |
| CA2589271A1 (en) * | 2004-12-07 | 2006-06-15 | Locus Pharmaceuticals, Inc. | Urea inhibitors of map kinases |
| PE20060777A1 (es) | 2004-12-24 | 2006-10-06 | Boehringer Ingelheim Int | Derivados de indolinona para el tratamiento o la prevencion de enfermedades fibroticas |
| WO2006078621A2 (en) * | 2005-01-19 | 2006-07-27 | Bristol-Myers Squibb Company | 2-phenoxy-n- (1, 3 , 4-thiadizol-2-yl) pyridin-3-amine derivatives and related compounds as p2y1 receptor inhibitors for the treatment of thromboembolic disorders |
| ES2415742T3 (es) * | 2005-05-13 | 2013-07-26 | Vertex Pharmaceuticals (Canada) Incorporated | Compuestos y procedimientos para el tratamiento o prevención de infecciones por flavivirus |
| EP2540296A1 (en) | 2005-06-03 | 2013-01-02 | Xenon Pharmaceuticals Inc. | Arminothiazole derivatives as human stearoyl-coa desaturase inhibitors |
| ES2360818T3 (es) | 2005-06-27 | 2011-06-09 | Bristol-Myers Squibb Company | Miméticos de urea lineal antagonistas del receptor p2y, útiles en el tratamiento de afecciones trombóticas. |
| US7728008B2 (en) * | 2005-06-27 | 2010-06-01 | Bristol-Myers Squibb Company | N-linked heterocyclic antagonists of P2Y1 receptor useful in the treatment of thrombotic conditions |
| US7700620B2 (en) * | 2005-06-27 | 2010-04-20 | Bristol-Myers Squibb Company | C-linked cyclic antagonists of P2Y1 receptor useful in the treatment of thrombotic conditions |
| WO2007002634A1 (en) * | 2005-06-27 | 2007-01-04 | Bristol-Myers Squibb Company | Carbocycle and heterocycle antagonists of p2y1 receptor useful in the treatment of thrombotic conditions |
| DE102005037499A1 (de) * | 2005-08-09 | 2007-02-15 | Merck Patent Gmbh | Pyrazolderivate |
| US20070298129A1 (en) * | 2005-08-24 | 2007-12-27 | Neurotech Pharmaceuticals Co., Ltd. | Compounds and compositions for treating neuronal death or neurological dysfunction |
| US20070049565A1 (en) * | 2005-08-24 | 2007-03-01 | Neurotech Pharmaceuticals Co., Ltd. | Combination of cell necrosis inhibitor and lithium for treating neuronal death or neurological dysfunction |
| WO2007044490A2 (en) * | 2005-10-06 | 2007-04-19 | Boehringer Ingelheim International Gmbh | Process for making heteroaryl amine intermediate compounds |
| EP1973408A2 (en) * | 2006-01-04 | 2008-10-01 | Locus Pharmaceuticals, Inc. | Inhibitors of protein kinases |
| WO2007109434A1 (en) * | 2006-03-17 | 2007-09-27 | Boehringer Ingelheim International Gmbh | Besylate salt form of 1- (5-tert-butyl-2-p-t0lyl-2h-pyraz0l-3-yl) -3- (4- (6- (morpholin-4-yl-methyl) -pyrid in- 3 -yl) -naphthalen- 1-yl) -urea and polymorphs thereof |
| US7960569B2 (en) * | 2006-10-17 | 2011-06-14 | Bristol-Myers Squibb Company | Indole antagonists of P2Y1 receptor useful in the treatment of thrombotic conditions |
| AP2579A (en) | 2006-11-15 | 2013-01-29 | Virochem Pharma Inc | Thiophene analogues for the treatment or prevention of flavivirus infections |
| EP1992344A1 (en) | 2007-05-18 | 2008-11-19 | Institut Curie | P38 alpha as a therapeutic target in pathologies linked to FGFR3 mutation |
| KR100852962B1 (ko) * | 2007-11-12 | 2008-08-20 | 주식회사 뉴로테크 | 2-하이드록시-5-페닐알킬아미노벤조산 유도체 및 이의 염의제조방법 |
| EP2240451B1 (en) | 2008-01-04 | 2017-08-09 | Intellikine, LLC | Isoquinolinone derivatives substituted with a purine useful as PI3K inhibitors |
| US8193182B2 (en) | 2008-01-04 | 2012-06-05 | Intellikine, Inc. | Substituted isoquinolin-1(2H)-ones, and methods of use thereof |
| GB0905955D0 (en) | 2009-04-06 | 2009-05-20 | Respivert Ltd | Novel compounds |
| BR112012022910B1 (pt) | 2010-03-12 | 2021-08-10 | Omeros Corporation | Compostos inibidores de pde10, composição farmacêutica compreendendo os referidos compostos e uso dos mesmos para tratar distúrbios neurológicos em um animal de sangue quente |
| US9024041B2 (en) | 2010-04-08 | 2015-05-05 | Respivert Ltd. | P38 MAP kinase inhibitors |
| JP5973426B2 (ja) | 2010-06-17 | 2016-08-23 | レスピバート・リミテツド | P38mapk阻害剤を含む呼吸器用製剤 |
| AR084824A1 (es) | 2011-01-10 | 2013-06-26 | Intellikine Inc | Procesos para preparar isoquinolinonas y formas solidas de isoquinolinonas |
| ES2659763T3 (es) * | 2011-02-14 | 2018-03-19 | The Regents Of The University Of Michigan | Composiciones y procedimientos para el tratamiento de obesidad y trastornos relacionados |
| US9199975B2 (en) | 2011-09-30 | 2015-12-01 | Asana Biosciences, Llc | Biaryl imidazole derivatives for regulating CYP17 |
| US8809372B2 (en) | 2011-09-30 | 2014-08-19 | Asana Biosciences, Llc | Pyridine derivatives |
| US8476303B2 (en) * | 2011-10-31 | 2013-07-02 | Florida A&M University Board of Trustees | N-aminopyrrolylmethyltetrahydropyridines as anti-cancer agents |
| US8461179B1 (en) | 2012-06-07 | 2013-06-11 | Deciphera Pharmaceuticals, Llc | Dihydronaphthyridines and related compounds useful as kinase inhibitors for the treatment of proliferative diseases |
| US8828998B2 (en) * | 2012-06-25 | 2014-09-09 | Infinity Pharmaceuticals, Inc. | Treatment of lupus, fibrotic conditions, and inflammatory myopathies and other disorders using PI3 kinase inhibitors |
| WO2014033446A1 (en) | 2012-08-29 | 2014-03-06 | Respivert Limited | Kinase inhibitors |
| WO2014033447A2 (en) | 2012-08-29 | 2014-03-06 | Respivert Limited | Kinase inhibitors |
| EP2890701B1 (en) | 2012-08-29 | 2017-03-29 | Respivert Limited | Kinase inhibitors |
| RU2702908C2 (ru) | 2012-11-01 | 2019-10-14 | Инфинити Фармасьютикалз, Инк. | Лечение злокачественных опухолей с использованием модуляторов изоформ pi3-киназы |
| AU2014246866B2 (en) | 2013-04-02 | 2018-05-10 | Oxular Acquisitions Limited | Kinase inhibitor |
| EP2981534B1 (en) | 2013-04-02 | 2017-07-19 | Topivert Pharma Limited | Kinase inhibitors based upon n-alkyl pyrazoles |
| US9365581B2 (en) | 2013-05-02 | 2016-06-14 | The Regents Of The University Of Michigan | Deuterated amlexanox |
| WO2015092423A1 (en) | 2013-12-20 | 2015-06-25 | Respivert Limited | Urea derivatives useful as kinase inhibitors |
| US20150320755A1 (en) | 2014-04-16 | 2015-11-12 | Infinity Pharmaceuticals, Inc. | Combination therapies |
| NZ716494A (en) | 2014-04-28 | 2017-07-28 | Omeros Corp | Processes and intermediates for the preparation of a pde10 inhibitor |
| NZ716462A (en) | 2014-04-28 | 2017-11-24 | Omeros Corp | Optically active pde10 inhibitor |
| MA40775A (fr) | 2014-10-01 | 2017-08-08 | Respivert Ltd | Dérivé d'acide 4-(4-(4-phényluréido-naphtalén -1-yl) oxy-pyridin-2-yl) amino-benzoïque utilisé en tant qu'inhibiteur de la kinase p38 |
| AU2016250843A1 (en) | 2015-04-24 | 2017-10-12 | Omeros Corporation | PDE10 inhibitors and related compositions and methods |
| JP2018535969A (ja) | 2015-11-04 | 2018-12-06 | オメロス コーポレーション | Pde10阻害剤の固体状態形態 |
| WO2017132538A1 (en) | 2016-01-29 | 2017-08-03 | The Regents Of The University Of Michigan | Amlexanox analogs |
| WO2017174995A1 (en) | 2016-04-06 | 2017-10-12 | Respivert Limited | Kinase inhibitors |
| CN109640999A (zh) | 2016-06-24 | 2019-04-16 | 无限药品股份有限公司 | 组合疗法 |
| CN106632403B (zh) * | 2017-01-23 | 2018-09-11 | 牡丹江医学院 | 一种手术用止痛消炎药及其制备方法 |
| US10364245B2 (en) | 2017-06-07 | 2019-07-30 | Chiesi Farmaceutici S.P.A. | Kinase inhibitors |
| JP7569688B2 (ja) | 2017-12-22 | 2024-10-18 | ハイバーセル,インコーポレイテッド | ホスファチジルイノシトールリン酸キナーゼ阻害剤としてのアミノピリジン誘導体 |
| SG11202007198WA (en) | 2018-01-31 | 2020-08-28 | Deciphera Pharmaceuticals Llc | Combination therapy for the treatment of gastrointestinal stromal tumors |
| CA3089630A1 (en) | 2018-01-31 | 2019-08-08 | Deciphera Pharmaceuticals, Llc | Combination therapy for the treatment of mastocytosis |
| WO2020185812A1 (en) | 2019-03-11 | 2020-09-17 | Teva Pharmaceuticals International Gmbh | Solid state forms of ripretinib |
| TW202112767A (zh) | 2019-06-17 | 2021-04-01 | 美商佩特拉製藥公司 | 作為磷脂酸肌醇磷酸激酶抑制劑之胺基吡啶衍生物 |
| KR20220045189A (ko) | 2019-08-12 | 2022-04-12 | 데시페라 파마슈티칼스, 엘엘씨. | 위장관 기질 종양을 치료하는 방법 |
| TWI878335B (zh) | 2019-08-12 | 2025-04-01 | 美商迪賽孚爾製藥有限公司 | 治療胃腸道基質瘤方法 |
| SMT202400484T1 (it) | 2019-12-30 | 2025-01-14 | Deciphera Pharmaceuticals Llc | Composizioni di 1-(4-bromo-5-(1-etil-7-(metilammino)-2-osso-1,2-diidro-1,6-naftiridin-3-il)-2-fluorofenil)-3-fenilurea |
| SMT202300467T1 (it) | 2019-12-30 | 2024-01-10 | Deciphera Pharmaceuticals Llc | Formulazioni di inibitori di chinasi amorfi e loro procedimenti d’uso |
| WO2021178907A1 (en) * | 2020-03-05 | 2021-09-10 | Janpix, Ltd. | Stat inhibitory compounds and compositions |
| US11779572B1 (en) | 2022-09-02 | 2023-10-10 | Deciphera Pharmaceuticals, Llc | Methods of treating gastrointestinal stromal tumors |
| CN116987041A (zh) * | 2023-08-02 | 2023-11-03 | 河北科技大学 | 一种转移氢化法制备5-(2-氨基-4-氯苯基)四氮唑的方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5162360A (en) * | 1991-06-24 | 1992-11-10 | Warner-Lambert Company | 2-heteroatom containing urea and thiourea ACAT inhibitors |
| RU2114633C1 (ru) * | 1990-10-01 | 1998-07-10 | Рисерч Дивелопмент Фаундейшн | Композиция для воздействия на опухолевые клетки |
| WO1998052558A1 (en) * | 1997-05-23 | 1998-11-26 | Bayer Corporation | INHIBITION OF p38 KINASE ACTIVITY BY ARYL UREAS |
| WO1999023091A1 (en) * | 1997-11-03 | 1999-05-14 | Boehringer Ingelheim Pharmaceuticals, Inc. | Aromatic heterocyclic compounds as anti-inflammatory agents |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE293352C (ru) | ||||
| US4105766A (en) | 1977-08-19 | 1978-08-08 | Sterling Drug Inc. | 4,5-Dihydro-5-oxopyrazolo[1,5-a]quinazoline-3-carboxylic acid derivatives |
| HU185294B (en) | 1980-12-29 | 1984-12-28 | Chinoin Gyogyszer Es Vegyeszet | Process for producing substituted urea derivatives |
| JPS61228444A (ja) | 1985-04-02 | 1986-10-11 | Fuji Photo Film Co Ltd | ハロゲン化銀カラ−写真感光材料 |
| EP0272866A1 (en) | 1986-12-23 | 1988-06-29 | Merck & Co. Inc. | 1,4-Benzodiazepines with 5-membered heterocyclic rings |
| GB8908869D0 (en) | 1989-04-19 | 1989-06-07 | Shell Int Research | A process for the preparation of aromatic ureas |
| WO1991004027A1 (en) | 1989-09-15 | 1991-04-04 | Pfizer Inc. | New n-aryl and n-heteroarylamide and urea derivatives as inhibitors of acyl coenzyme a: cholesterol acyl transferase (acat) |
| DD293352A5 (de) | 1990-04-06 | 1991-08-29 | Adw,Zi Fuer Organische Chemie,De | Verfahren zur herstellung von 2,2-disubstituierten 1-acyl- und/oder 9-acyl-2,3-dihydro-imidazo/1,2-a/benzimidazol-3-onen |
| MX9300141A (es) | 1992-01-13 | 1994-07-29 | Smithkline Beecham Corp | Compuestos de imidazol novedosos, procedimiento para su preparacion y composiciones farmaceuticas que lo contienen. |
| BR9306421A (pt) | 1992-05-28 | 1998-09-15 | Pfizer | Novos derivados n-aril e n-heteroariluréia como inbidores da acilcoenzima a:colesterol aciltransferase (acat) |
| US5342942A (en) | 1992-06-09 | 1994-08-30 | Warner-Lambert Company | Pyrazoloquinazolone derivatives as neurotrophic agents |
| GB9302275D0 (en) | 1993-02-05 | 1993-03-24 | Smithkline Beecham Plc | Novel compounds |
| WO1994022872A1 (fr) | 1993-03-30 | 1994-10-13 | Yoshitomi Pharmaceutical Industries, Ltd. | Inhibiteur d'adhesion cellulaire et compose a base de thienotriazolodiazepine |
| PT724588E (pt) | 1993-09-17 | 2000-05-31 | Smithkline Beecham Corp | Proteina de ligacao a farmacos |
| US5869043A (en) | 1993-09-17 | 1999-02-09 | Smithkline Beecham Corporation | Drug binding protein |
| US5783664A (en) | 1993-09-17 | 1998-07-21 | Smithkline Beecham Corporation | Cytokine suppressive anit-inflammatory drug binding proteins |
| JPH11503110A (ja) * | 1995-02-17 | 1999-03-23 | スミスクライン・ビーチャム・コーポレイション | Il−8受容体拮抗剤 |
| US5739143A (en) | 1995-06-07 | 1998-04-14 | Smithkline Beecham Corporation | Imidazole compounds and compositions |
| IL118544A (en) | 1995-06-07 | 2001-08-08 | Smithkline Beecham Corp | History of imidazole, the process for their preparation and the pharmaceutical preparations containing them |
| CZ183198A3 (cs) * | 1995-12-14 | 1998-10-14 | Merck And Co., Inc. | Nepeptidové deriváty, antagonizující hormon, uvolňující gonadotropin a farmaceutický prostředek |
| US6074862A (en) | 1995-12-20 | 2000-06-13 | Signal Pharmaceuticals Inc. | Mitogen-activated protein kinase kinase MEK6 and variants thereof |
| EP0888335A4 (en) | 1996-03-13 | 2002-01-02 | Smithkline Beecham Corp | NEW PYRIMIDINE COMPOUNDS AND THEIR USE IN THE TREATMENT OF CYTOKININ MEDIATOR DISEASES |
| JP2000507545A (ja) | 1996-03-25 | 2000-06-20 | スミスクライン・ビーチャム・コーポレイション | Cns損傷についての新規な治療 |
| EP0889888A4 (en) | 1996-03-25 | 2003-01-08 | Smithkline Beecham Corp | NEW TREATMENT OF LESIONS IN THE CENTRAL NERVOUS SYSTEM |
| PL192628B1 (pl) * | 1996-04-23 | 2006-11-30 | Vertex Pharma | Pochodne mocznika, kompozycje farmaceutyczne i zastosowanie związku i kompozycji |
| WO1997044467A1 (en) | 1996-05-20 | 1997-11-27 | Signal Pharmaceuticals, Inc. | MITOGEN-ACTIVATED PROTEIN KINASE p38-2 AND METHODS OF USE THEREFOR |
| US5948885A (en) | 1996-05-20 | 1999-09-07 | Signal Pharmaceuticals, Inc. | Mitogen-activated protein kinase p38-2 and methods of use therefor |
| EP0906307B1 (en) | 1996-06-10 | 2005-04-27 | Merck & Co., Inc. | Substituted imidazoles having cytokine inhibitory activity |
| CA2258728C (en) | 1996-06-19 | 2011-09-27 | Rhone Poulenc Rorer Limited | Substituted azabicylic compounds and their use as inhibitors of the production of tnf and cyclic amp phosphodiesterase |
| ATE230403T1 (de) * | 1996-07-23 | 2003-01-15 | Neurogen Corp | Einige amido- und ammo- substituierte benzylaminderivate: eine neue klasse von neuropeptid y1 spezifische ligande |
| WO1998007425A1 (en) | 1996-08-21 | 1998-02-26 | Smithkline Beecham Corporation | Imidazole compounds, compositions and use |
| DE69731964T2 (de) | 1996-10-09 | 2005-12-08 | Medical Research Council | Map-kinase: polypeptide, polynukleotide und ihre verwendung |
| WO1998024768A1 (en) | 1996-12-03 | 1998-06-11 | Banyu Pharmaceutical Co., Ltd. | Novel urea derivatives |
| US6147080A (en) | 1996-12-18 | 2000-11-14 | Vertex Pharmaceuticals Incorporated | Inhibitors of p38 |
| US6376214B1 (en) | 1997-02-18 | 2002-04-23 | Smithkline Beecham Corporation | DNA encoding a novel homolog of CSBP/p38 MAP kinase |
| WO1998050346A2 (en) * | 1997-04-18 | 1998-11-12 | Smithkline Beecham Plc | Acetamide and urea derivatives, process for their preparation and their use in the treatment of cns disorders |
| WO1998047868A1 (en) * | 1997-04-18 | 1998-10-29 | Smithkline Beecham Plc | Heterocycle-containing urea derivatives as 5ht1a, 5ht1b and 5ht1d receptor antagonists |
| JP2001526643A (ja) * | 1997-04-18 | 2001-12-18 | スミスクライン・ビーチャム・パブリック・リミテッド・カンパニー | 5ht1a、5ht1bおよび5ht1d受容体アンタゴニスト活性を合わせ持つ化合物を含む二環式アリールまたは二環式複素環 |
| ATE399007T1 (de) | 1997-05-23 | 2008-07-15 | Bayer Pharmaceuticals Corp | Raf kinase hemmer |
| US6093742A (en) | 1997-06-27 | 2000-07-25 | Vertex Pharmaceuticals, Inc. | Inhibitors of p38 |
| US5851812A (en) | 1997-07-01 | 1998-12-22 | Tularik Inc. | IKK-β proteins, nucleic acids and methods |
| DE69819903T2 (de) * | 1997-08-09 | 2004-11-11 | Smithkline Beecham P.L.C., Brentford | Bicyclische verbindungen als liganden der 5-ht1 rezeptoren |
| CA2223075A1 (en) | 1997-12-02 | 1999-06-02 | Smithkline Beecham Corporation | Drug binding protein |
| SK285371B6 (sk) | 1997-12-22 | 2006-12-07 | Bayer Corporation | Aryl- a heteroaryl-substituované heterocyklické močoviny, ich použitie a farmaceutické kompozície sich obsahom |
| WO1999032110A1 (en) | 1997-12-22 | 1999-07-01 | Bayer Corporation | INHIBITION OF p38 KINASE ACTIVITY USING ARYL AND HETEROARYL SUBSTITUTED HETEROCYCLIC UREAS |
| DE1041982T1 (de) | 1997-12-22 | 2001-06-07 | Bayer Corp., Pittsburgh | HEMMUNG DER p38 KINASE AKTIVITÄT DURCH SUBSTITUIERTEN HETEROCYCLISCHEN HARNSTOFFEN |
| NZ505844A (en) | 1997-12-22 | 2003-10-31 | Bayer Ag | Inhibition of raf kinase using substituted heterocyclic ureas |
| PT1042305E (pt) | 1997-12-22 | 2005-10-31 | Bayer Pharmaceuticals Corp | Inibicao de quinase p38 utilizando difenilureias simetricas e assimetricas |
| WO1999046244A1 (en) | 1998-03-12 | 1999-09-16 | Novo Nordisk A/S | Modulators of protein tyrosine phosphatases (ptpases) |
| US6506747B1 (en) * | 1998-06-05 | 2003-01-14 | Boehringer Ingelheim Pharmaceuticals, Inc. | Substituted 1-(4-aminophenyl)pyrazoles and their use as anti-inflammatory agents |
| AU3126700A (en) * | 1998-12-18 | 2000-07-03 | Du Pont Pharmaceuticals Company | N-ureidoalkyl-piperidines as modulators of chemokine receptor activity |
| UA73492C2 (en) | 1999-01-19 | 2005-08-15 | Aromatic heterocyclic compounds as antiinflammatory agents | |
| CN1156452C (zh) * | 1999-03-12 | 2004-07-07 | 贝林格尔·英格海姆药物公司 | 作为消炎剂的化合物 |
-
2000
- 2000-02-16 CN CNB008048134A patent/CN1156452C/zh not_active Expired - Fee Related
- 2000-02-16 TR TR2001/02817T patent/TR200102817T2/xx unknown
- 2000-02-16 DE DE60014603T patent/DE60014603T2/de not_active Expired - Lifetime
- 2000-02-16 SG SG200304005-2A patent/SG142120A1/en unknown
- 2000-02-16 DK DK00907295T patent/DK1165516T3/da active
- 2000-02-16 HK HK02104955.3A patent/HK1043127B/zh not_active IP Right Cessation
- 2000-02-16 EP EP00907295A patent/EP1165516B1/en not_active Expired - Lifetime
- 2000-02-16 HU HU0202248A patent/HUP0202248A3/hu not_active Application Discontinuation
- 2000-02-16 RU RU2001126337/04A patent/RU2242474C2/ru not_active IP Right Cessation
- 2000-02-16 ID IDW00200101981A patent/ID30176A/id unknown
- 2000-02-16 PL PL00350357A patent/PL350357A1/xx not_active Application Discontinuation
- 2000-02-16 AU AU28817/00A patent/AU771273B2/en not_active Ceased
- 2000-02-16 CN CNA031278329A patent/CN1511830A/zh active Pending
- 2000-02-16 AT AT00907295T patent/ATE278674T1/de active
- 2000-02-16 ES ES00907295T patent/ES2225095T3/es not_active Expired - Lifetime
- 2000-02-16 YU YU64701A patent/YU64701A/sh unknown
- 2000-02-16 EE EEP200100483A patent/EE04799B1/xx not_active IP Right Cessation
- 2000-02-16 NZ NZ514711A patent/NZ514711A/xx unknown
- 2000-02-16 JP JP2000605569A patent/JP4820488B2/ja not_active Expired - Lifetime
- 2000-02-16 BR BR0008922-2A patent/BR0008922A/pt not_active IP Right Cessation
- 2000-02-16 SI SI200030564T patent/SI1165516T1/xx unknown
- 2000-02-16 WO PCT/US2000/003865 patent/WO2000055139A2/en not_active Ceased
- 2000-02-16 HR HR20010665A patent/HRP20010665A2/hr not_active Application Discontinuation
- 2000-02-16 CZ CZ20013289A patent/CZ20013289A3/cs unknown
- 2000-02-16 NZ NZ528846A patent/NZ528846A/en unknown
- 2000-02-16 PT PT00907295T patent/PT1165516E/pt unknown
- 2000-02-16 US US09/505,582 patent/US6358945B1/en not_active Expired - Lifetime
- 2000-02-16 IL IL14489700A patent/IL144897A0/xx active IP Right Grant
- 2000-02-16 SK SK1283-2001A patent/SK12832001A3/sk unknown
- 2000-02-16 KR KR1020017011599A patent/KR100709497B1/ko not_active Expired - Fee Related
- 2000-02-16 CA CA002362003A patent/CA2362003C/en not_active Expired - Lifetime
- 2000-03-08 CO CO00016936A patent/CO5251387A1/es not_active Application Discontinuation
- 2000-03-10 UY UY26058A patent/UY26058A1/es not_active Application Discontinuation
- 2000-03-10 PE PE2000000212A patent/PE20001484A1/es not_active Application Discontinuation
- 2000-03-10 AR ARP000101080A patent/AR028473A1/es not_active Application Discontinuation
-
2001
- 2001-08-14 IL IL144897A patent/IL144897A/en not_active IP Right Cessation
- 2001-09-05 BG BG105880A patent/BG65159B1/bg unknown
- 2001-09-11 NO NO20014412A patent/NO321120B1/no unknown
- 2001-09-25 US US09/962,057 patent/US6656933B2/en not_active Expired - Lifetime
- 2001-09-25 US US09/962,709 patent/US6660732B2/en not_active Expired - Lifetime
-
2003
- 2003-04-28 US US10/424,613 patent/US7026476B2/en not_active Expired - Lifetime
- 2003-07-21 US US10/624,289 patent/US7019006B2/en not_active Expired - Lifetime
-
2006
- 2006-04-10 IL IL174917A patent/IL174917A0/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2114633C1 (ru) * | 1990-10-01 | 1998-07-10 | Рисерч Дивелопмент Фаундейшн | Композиция для воздействия на опухолевые клетки |
| US5162360A (en) * | 1991-06-24 | 1992-11-10 | Warner-Lambert Company | 2-heteroatom containing urea and thiourea ACAT inhibitors |
| WO1998052558A1 (en) * | 1997-05-23 | 1998-11-26 | Bayer Corporation | INHIBITION OF p38 KINASE ACTIVITY BY ARYL UREAS |
| WO1999023091A1 (en) * | 1997-11-03 | 1999-05-14 | Boehringer Ingelheim Pharmaceuticals, Inc. | Aromatic heterocyclic compounds as anti-inflammatory agents |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2478639C2 (ru) * | 2005-05-24 | 2013-04-10 | Лаборатуар Сероно С.А. | Трициклические спиро-производные в качестве модуляторов crth2 |
| RU2442777C2 (ru) * | 2006-01-31 | 2012-02-20 | Эррэй Биофарма Инк. | Ингибиторы киназ и способы их применения |
| RU2489426C2 (ru) * | 2007-12-14 | 2013-08-10 | Актелион Фармасьютиклз Лтд | Производные аминопиразола |
| RU2505538C2 (ru) * | 2008-02-05 | 2014-01-27 | Ф.Хоффманн-Ля Рош Аг | Новые пиридиноны и пиридазиноны |
| RU2496778C2 (ru) * | 2009-03-09 | 2013-10-27 | Тайхо Фармасьютикал Ко., Лтд. | Пиперазиновое соединение, ингибирующее простагландин-d-синтазу |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2242474C2 (ru) | Соединения, пригодные в качестве противовоспалительных агентов | |
| CA2352524C (en) | Aromatic heterocyclic compounds as antiinflammatory agents | |
| US7211575B2 (en) | Methods of treating cytokine mediated diseases | |
| RU2298008C2 (ru) | Соединения, содержащие их фармацевтические композиции, и способ лечения заболевания, опосредуемого цитокинами | |
| EP1466906A1 (en) | Heterocyclic urea and related compounds useful as anti-inflammatory agents | |
| EP1690854A1 (en) | Heterocyclic urea and related compounds useful as anti-inflammatory agents | |
| AU2004200240B2 (en) | Compounds useful as anti-inflammatory agents | |
| MXPA01009163A (es) | Compuestos utiles como antiinflamatorios |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20080217 |