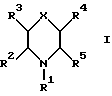
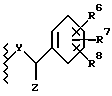
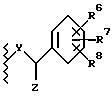
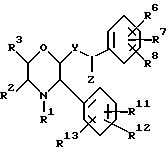
RU2140914C1 - Замещенные гетероциклы или их фармацевтически приемлемая соль, фармацевтическая композиция для блокады рецепторов нейрокинина-1 у млекопитающих, способ для блокады рецепторов нейрокинина-1 у млекопитающих - Google Patents
Замещенные гетероциклы или их фармацевтически приемлемая соль, фармацевтическая композиция для блокады рецепторов нейрокинина-1 у млекопитающих, способ для блокады рецепторов нейрокинина-1 у млекопитающих Download PDFInfo
- Publication number
- RU2140914C1 RU2140914C1 RU94046364A RU94046364A RU2140914C1 RU 2140914 C1 RU2140914 C1 RU 2140914C1 RU 94046364 A RU94046364 A RU 94046364A RU 94046364 A RU94046364 A RU 94046364A RU 2140914 C1 RU2140914 C1 RU 2140914C1
- Authority
- RU
- Russia
- Prior art keywords
- trifluoromethyl
- benzyloxy
- bis
- phenylmorpholine
- phenyl
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 46
- 125000000623 heterocyclic group Chemical group 0.000 title claims abstract description 23
- 241000124008 Mammalia Species 0.000 title claims abstract description 9
- 108010040718 Neurokinin-1 Receptors Proteins 0.000 title claims abstract description 7
- 102000002002 Neurokinin-1 Receptors Human genes 0.000 title claims abstract description 7
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 7
- 150000003839 salts Chemical class 0.000 title claims description 32
- 150000001875 compounds Chemical class 0.000 claims abstract description 64
- 230000000903 blocking effect Effects 0.000 claims abstract description 5
- -1 3,5-bis (trifluoromethyl) benzyloxy Chemical group 0.000 claims description 100
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 91
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 43
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 37
- 125000005843 halogen group Chemical group 0.000 claims description 32
- 125000001424 substituent group Chemical group 0.000 claims description 27
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 23
- 125000004043 oxo group Chemical group O=* 0.000 claims description 17
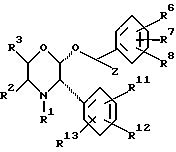
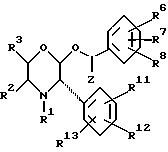
- FUQXMZQIUQTJPV-UHFFFAOYSA-N 2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(COC2C(NCCO2)C=2C=CC=CC=2)=C1 FUQXMZQIUQTJPV-UHFFFAOYSA-N 0.000 claims description 15
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 claims description 15
- FUQXMZQIUQTJPV-DLBZAZTESA-N (2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@@H](NCCO2)C=2C=CC=CC=2)=C1 FUQXMZQIUQTJPV-DLBZAZTESA-N 0.000 claims description 9
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 claims description 7
- FUQXMZQIUQTJPV-IAGOWNOFSA-N (2s,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@H](NCCO2)C=2C=CC=CC=2)=C1 FUQXMZQIUQTJPV-IAGOWNOFSA-N 0.000 claims description 6
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 6
- 125000002883 imidazolyl group Chemical group 0.000 claims description 6
- 125000003386 piperidinyl group Chemical group 0.000 claims description 6
- 125000004076 pyridyl group Chemical group 0.000 claims description 6
- AOWGLTSPUDFTLW-NXOUGTEYSA-N (2r,3r,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@H]1[C@H](NC[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-NXOUGTEYSA-N 0.000 claims description 5
- PUZOQLKLCNWXCR-UUWFMWQGSA-N (2r,3s,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@@H]1OC[C@H](N[C@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-UUWFMWQGSA-N 0.000 claims description 5
- AOWGLTSPUDFTLW-OCBCSQNSSA-N (2r,3s,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@H]1[C@@H](NC[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-OCBCSQNSSA-N 0.000 claims description 5
- AOWGLTSPUDFTLW-PJSAGSTRSA-N (2s,3r,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@@H]1[C@H](NC[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-PJSAGSTRSA-N 0.000 claims description 5
- PUZOQLKLCNWXCR-OCBCSQNSSA-N (2s,3s,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@H]1OC[C@H](N[C@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-OCBCSQNSSA-N 0.000 claims description 5
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 5
- 239000001257 hydrogen Substances 0.000 claims description 5
- 229910052739 hydrogen Inorganic materials 0.000 claims description 5
- HKQKWZAMVUVBGL-VQTJNVASSA-N methyl 2-[(2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetate Chemical compound O([C@H]1OCCN([C@H]1C=1C=CC=CC=1)CC(=O)OC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 HKQKWZAMVUVBGL-VQTJNVASSA-N 0.000 claims description 5
- AOWGLTSPUDFTLW-RZAIGCCYSA-N (2s,3r,6s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@@H]1[C@H](NC[C@@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-RZAIGCCYSA-N 0.000 claims description 4
- AOWGLTSPUDFTLW-UUWFMWQGSA-N (2s,3s,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@@H]1[C@@H](NC[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-UUWFMWQGSA-N 0.000 claims description 4
- BJGPOQZAOCLNIE-DHIUTWEWSA-N 6-[(2s,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]hexanoic acid Chemical compound O([C@H]1OCCN([C@@H]1C=1C=CC=CC=1)CCCCCC(=O)O)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 BJGPOQZAOCLNIE-DHIUTWEWSA-N 0.000 claims description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 4
- 125000001425 triazolyl group Chemical group 0.000 claims description 4
- PUZOQLKLCNWXCR-RZAIGCCYSA-N (2r,3r,5s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@@H]1OC[C@@H](N[C@@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-RZAIGCCYSA-N 0.000 claims description 3
- PUZOQLKLCNWXCR-IGNZVWTISA-N (2r,3s,5s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@@H]1OC[C@@H](N[C@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-IGNZVWTISA-N 0.000 claims description 3
- AOWGLTSPUDFTLW-UYHISHBKSA-N (2r,3s,6s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@H]1[C@@H](NC[C@@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-UYHISHBKSA-N 0.000 claims description 3
- ICJXTVCDDLEZHJ-DLBZAZTESA-N (2s,3s)-2-[(3,5-dichlorophenyl)methoxy]-3-phenylmorpholine Chemical compound ClC1=CC(Cl)=CC(CO[C@@H]2[C@@H](NCCO2)C=2C=CC=CC=2)=C1 ICJXTVCDDLEZHJ-DLBZAZTESA-N 0.000 claims description 3
- AOWGLTSPUDFTLW-IGNZVWTISA-N (2s,3s,6s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@@H]1[C@@H](NC[C@@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-IGNZVWTISA-N 0.000 claims description 3
- SRIOHIXTSHGWLJ-UHFFFAOYSA-N 2-[2-[3,5-bis(trifluoromethyl)phenyl]ethyl]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CCC2C(NCCO2)C=2C=CC=CC=2)=C1 SRIOHIXTSHGWLJ-UHFFFAOYSA-N 0.000 claims description 3
- 150000002367 halogens Chemical class 0.000 claims description 3
- RSRSCNFYBRQXAD-DNQXCXABSA-N methyl 6-[(2s,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]hexanoate Chemical compound O([C@H]1OCCN([C@@H]1C=1C=CC=CC=1)CCCCCC(=O)OC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 RSRSCNFYBRQXAD-DNQXCXABSA-N 0.000 claims description 3
- PUZOQLKLCNWXCR-PJSAGSTRSA-N (2r,3r,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@@H]1OC[C@H](N[C@@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-PJSAGSTRSA-N 0.000 claims description 2
- AOWGLTSPUDFTLW-JBBXEZCESA-N (2r,3r,6s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenylmorpholine Chemical compound O([C@H]1[C@H](NC[C@@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 AOWGLTSPUDFTLW-JBBXEZCESA-N 0.000 claims description 2
- PUZOQLKLCNWXCR-NXOUGTEYSA-N (2s,3r,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@H]1OC[C@H](N[C@@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-NXOUGTEYSA-N 0.000 claims description 2
- MQHWDFVGDXXXRC-BJKOFHAPSA-N (2s,3s)-4-benzyl-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-(4-fluorophenyl)morpholine Chemical compound C1=CC(F)=CC=C1[C@@H]1N(CC=2C=CC=CC=2)CCO[C@@H]1OCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 MQHWDFVGDXXXRC-BJKOFHAPSA-N 0.000 claims description 2
- PUZOQLKLCNWXCR-UYHISHBKSA-N (2s,3s,5s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-5-methyl-3-phenylmorpholine Chemical compound O([C@H]1OC[C@@H](N[C@H]1C=1C=CC=CC=1)C)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PUZOQLKLCNWXCR-UYHISHBKSA-N 0.000 claims description 2
- GFOCXNQTHDSCRO-RTBURBONSA-N 2-[(2s,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetamide Chemical compound O([C@H]1OCCN([C@@H]1C=1C=CC=CC=1)CC(=O)N)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 GFOCXNQTHDSCRO-RTBURBONSA-N 0.000 claims description 2
- JHHZUJYNSIUXII-FZKQIMNGSA-N (2R,5S)-4-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-2-methyl-5-phenylmorpholine Chemical compound FC(C=1C=C(CON2[C@H](CO[C@@H](C2)C)C2=CC=CC=C2)C=C(C1)C(F)(F)F)(F)F JHHZUJYNSIUXII-FZKQIMNGSA-N 0.000 claims 1
- FGNKYBCTXIEACK-DLBZAZTESA-N (2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-(4-fluorophenyl)morpholine Chemical compound C1=CC(F)=CC=C1[C@H]1[C@@H](OCC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)OCCN1 FGNKYBCTXIEACK-DLBZAZTESA-N 0.000 claims 1
- LEMUQYVGNWVOOC-RBUKOAKNSA-N 2-[(2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetic acid Chemical compound O([C@H]1OCCN([C@H]1C=1C=CC=CC=1)CC(=O)O)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 LEMUQYVGNWVOOC-RBUKOAKNSA-N 0.000 claims 1
- UDECBHOWPWFZBK-UHFFFAOYSA-N 4-[[3-tert-butyl-5-(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound C(C)(C)(C)C=1C=C(CON2C(COCC2)C2=CC=CC=C2)C=C(C=1)C(F)(F)F UDECBHOWPWFZBK-UHFFFAOYSA-N 0.000 claims 1
- 239000004098 Tetracycline Substances 0.000 claims 1
- 125000004430 oxygen atom Chemical group O* 0.000 claims 1
- 229960002180 tetracycline Drugs 0.000 claims 1
- 229930101283 tetracycline Natural products 0.000 claims 1
- 235000019364 tetracycline Nutrition 0.000 claims 1
- 150000003522 tetracyclines Chemical class 0.000 claims 1
- 239000000126 substance Substances 0.000 abstract description 52
- 239000005557 antagonist Substances 0.000 abstract description 19
- 230000036407 pain Effects 0.000 abstract description 14
- 208000002193 Pain Diseases 0.000 abstract description 11
- 102000005962 receptors Human genes 0.000 abstract description 11
- 108020003175 receptors Proteins 0.000 abstract description 11
- 208000019695 Migraine disease Diseases 0.000 abstract description 10
- 208000006673 asthma Diseases 0.000 abstract description 9
- 230000000694 effects Effects 0.000 abstract description 6
- 108010072901 Tachykinin Receptors Proteins 0.000 abstract description 5
- 102000007124 Tachykinin Receptors Human genes 0.000 abstract description 5
- 206010027599 migraine Diseases 0.000 abstract description 5
- 239000003795 chemical substances by application Substances 0.000 abstract description 4
- 230000008901 benefit Effects 0.000 abstract description 3
- 206010002383 Angina Pectoris Diseases 0.000 abstract description 2
- 108090000312 Calcium Channels Proteins 0.000 abstract description 2
- 102000003922 Calcium Channels Human genes 0.000 abstract description 2
- 208000024172 Cardiovascular disease Diseases 0.000 abstract description 2
- 208000028867 ischemia Diseases 0.000 abstract description 2
- 230000002757 inflammatory effect Effects 0.000 abstract 1
- 206010025482 malaise Diseases 0.000 abstract 1
- 239000000203 mixture Substances 0.000 description 173
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 165
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 144
- 239000000243 solution Substances 0.000 description 132
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 126
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 116
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 113
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 68
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 52
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 50
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 48
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 48
- 238000003818 flash chromatography Methods 0.000 description 46
- 239000012044 organic layer Substances 0.000 description 46
- 238000001228 spectrum Methods 0.000 description 46
- 239000010410 layer Substances 0.000 description 45
- 239000000741 silica gel Substances 0.000 description 45
- 229910002027 silica gel Inorganic materials 0.000 description 45
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 42
- 239000000463 material Substances 0.000 description 39
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 36
- 239000000047 product Substances 0.000 description 36
- 102100024304 Protachykinin-1 Human genes 0.000 description 35
- 239000007864 aqueous solution Substances 0.000 description 35
- 239000003921 oil Substances 0.000 description 34
- 235000019198 oils Nutrition 0.000 description 34
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 32
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 31
- 239000003480 eluent Substances 0.000 description 31
- 239000011541 reaction mixture Substances 0.000 description 31
- QDZOEBFLNHCSSF-PFFBOGFISA-N (2S)-2-[[(2R)-2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-1-[(2R)-2-amino-5-carbamimidamidopentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-N-[(2R)-1-[[(2S)-1-[[(2R)-1-[[(2S)-1-[[(2S)-1-amino-4-methyl-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]pentanediamide Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](N)CCCNC(N)=N)C1=CC=CC=C1 QDZOEBFLNHCSSF-PFFBOGFISA-N 0.000 description 30
- QTBSBXVTEAMEQO-UHFFFAOYSA-N acetic acid Substances CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 29
- 101800003906 Substance P Proteins 0.000 description 28
- 229920006395 saturated elastomer Polymers 0.000 description 28
- 239000007787 solid Substances 0.000 description 28
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 25
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 25
- 235000019341 magnesium sulphate Nutrition 0.000 description 25
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 22
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 22
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 22
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 21
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 21
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 21
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 21
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 21
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 20
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 19
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 18
- 125000004093 cyano group Chemical group *C#N 0.000 description 18
- 238000004458 analytical method Methods 0.000 description 17
- 238000006243 chemical reaction Methods 0.000 description 17
- 208000035475 disorder Diseases 0.000 description 16
- 239000000706 filtrate Substances 0.000 description 16
- 239000000725 suspension Substances 0.000 description 15
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 14
- 210000004027 cell Anatomy 0.000 description 14
- 229910052757 nitrogen Inorganic materials 0.000 description 14
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 13
- 239000012267 brine Substances 0.000 description 13
- 201000010099 disease Diseases 0.000 description 13
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 13
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 12
- 230000029936 alkylation Effects 0.000 description 12
- 238000005804 alkylation reaction Methods 0.000 description 12
- 238000004587 chromatography analysis Methods 0.000 description 12
- 229910052938 sodium sulfate Inorganic materials 0.000 description 12
- 235000011152 sodium sulphate Nutrition 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- 102000003141 Tachykinin Human genes 0.000 description 11
- 229910000027 potassium carbonate Inorganic materials 0.000 description 11
- 239000011780 sodium chloride Substances 0.000 description 11
- 108060008037 tachykinin Proteins 0.000 description 11
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 10
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 10
- 229960000583 acetic acid Drugs 0.000 description 10
- 150000001414 amino alcohols Chemical class 0.000 description 10
- 238000003756 stirring Methods 0.000 description 10
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- 239000004480 active ingredient Substances 0.000 description 9
- 239000000843 powder Substances 0.000 description 9
- 125000006239 protecting group Chemical group 0.000 description 9
- UWCWUCKPEYNDNV-LBPRGKRZSA-N 2,6-dimethyl-n-[[(2s)-pyrrolidin-2-yl]methyl]aniline Chemical compound CC1=CC=CC(C)=C1NC[C@H]1NCCC1 UWCWUCKPEYNDNV-LBPRGKRZSA-N 0.000 description 8
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 8
- 208000018522 Gastrointestinal disease Diseases 0.000 description 8
- 101000600903 Homo sapiens Substance-P receptor Proteins 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 8
- 238000009835 boiling Methods 0.000 description 8
- 238000002329 infrared spectrum Methods 0.000 description 8
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 8
- 239000002609 medium Substances 0.000 description 8
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 8
- 239000012299 nitrogen atmosphere Substances 0.000 description 8
- 239000007858 starting material Substances 0.000 description 8
- DYLIWHYUXAJDOJ-OWOJBTEDSA-N (e)-4-(6-aminopurin-9-yl)but-2-en-1-ol Chemical compound NC1=NC=NC2=C1N=CN2C\C=C\CO DYLIWHYUXAJDOJ-OWOJBTEDSA-N 0.000 description 7
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 7
- 101000831616 Homo sapiens Protachykinin-1 Proteins 0.000 description 7
- 102400000097 Neurokinin A Human genes 0.000 description 7
- HEAUFJZALFKPBA-YRVBCFNBSA-N Neurokinin A Chemical compound C([C@@H](C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)C(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CC=1NC=NC=1)C(C)O)C1=CC=CC=C1 HEAUFJZALFKPBA-YRVBCFNBSA-N 0.000 description 7
- 101800000399 Neurokinin A Proteins 0.000 description 7
- 102100037346 Substance-P receptor Human genes 0.000 description 7
- 230000010933 acylation Effects 0.000 description 7
- 238000005917 acylation reaction Methods 0.000 description 7
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 7
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzenecarboxaldehyde Natural products O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 7
- 239000002775 capsule Substances 0.000 description 7
- 238000009472 formulation Methods 0.000 description 7
- 235000017557 sodium bicarbonate Nutrition 0.000 description 7
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 7
- 239000003826 tablet Substances 0.000 description 7
- HXKKHQJGJAFBHI-GSVOUGTGSA-N (2R)-1-aminopropan-2-ol Chemical compound C[C@@H](O)CN HXKKHQJGJAFBHI-GSVOUGTGSA-N 0.000 description 6
- DLXNVSRGOHFBDV-UHFFFAOYSA-N (3Z)-3-amino-2-chloro-3-(methylhydrazinylidene)propanoic acid Chemical compound CNNC(C(Cl)C(=O)O)=N DLXNVSRGOHFBDV-UHFFFAOYSA-N 0.000 description 6
- 208000024827 Alzheimer disease Diseases 0.000 description 6
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 6
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 6
- 125000000217 alkyl group Chemical group 0.000 description 6
- 235000019270 ammonium chloride Nutrition 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 210000003169 central nervous system Anatomy 0.000 description 6
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 6
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 150000002780 morpholines Chemical class 0.000 description 6
- 150000007524 organic acids Chemical class 0.000 description 6
- KJIFKLIQANRMOU-UHFFFAOYSA-N oxidanium;4-methylbenzenesulfonate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1 KJIFKLIQANRMOU-UHFFFAOYSA-N 0.000 description 6
- 208000033808 peripheral neuropathy Diseases 0.000 description 6
- 108090000765 processed proteins & peptides Proteins 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 238000001953 recrystallisation Methods 0.000 description 6
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 6
- ADNPLDHMAVUMIW-CUZNLEPHSA-N substance P Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 ADNPLDHMAVUMIW-CUZNLEPHSA-N 0.000 description 6
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 6
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 5
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 5
- 239000003377 acid catalyst Substances 0.000 description 5
- 238000007792 addition Methods 0.000 description 5
- 150000001413 amino acids Chemical group 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 238000001816 cooling Methods 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 238000001640 fractional crystallisation Methods 0.000 description 5
- 208000027866 inflammatory disease Diseases 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 229910052744 lithium Inorganic materials 0.000 description 5
- VSEAAEQOQBMPQF-UHFFFAOYSA-N morpholin-3-one Chemical compound O=C1COCCN1 VSEAAEQOQBMPQF-UHFFFAOYSA-N 0.000 description 5
- 210000003097 mucus Anatomy 0.000 description 5
- 230000001272 neurogenic effect Effects 0.000 description 5
- 201000008482 osteoarthritis Diseases 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 206010039073 rheumatoid arthritis Diseases 0.000 description 5
- QBERHIJABFXGRZ-UHFFFAOYSA-M rhodium;triphenylphosphane;chloride Chemical compound [Cl-].[Rh].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 QBERHIJABFXGRZ-UHFFFAOYSA-M 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 5
- CYBHDFOHUGLNEW-RJGXRXQPSA-N (2r,3s,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3,5-diphenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@H]2[C@@H](N[C@@H](CO2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 CYBHDFOHUGLNEW-RJGXRXQPSA-N 0.000 description 4
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 4
- 125000006729 (C2-C5) alkenyl group Chemical group 0.000 description 4
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N 1,1-dimethoxyethane Chemical class COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- 201000003883 Cystic fibrosis Diseases 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 4
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 4
- NHXYSAFTNPANFK-HDMCBQFHSA-N Neurokinin B Chemical compound C([C@@H](C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCSC)NC(=O)[C@@H](N)CC(O)=O)C1=CC=CC=C1 NHXYSAFTNPANFK-HDMCBQFHSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 206010003246 arthritis Diseases 0.000 description 4
- 235000019445 benzyl alcohol Nutrition 0.000 description 4
- 229960004217 benzyl alcohol Drugs 0.000 description 4
- 230000027455 binding Effects 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 125000001309 chloro group Chemical group Cl* 0.000 description 4
- 238000011097 chromatography purification Methods 0.000 description 4
- GKIRPKYJQBWNGO-OCEACIFDSA-N clomifene Chemical compound C1=CC(OCCN(CC)CC)=CC=C1C(\C=1C=CC=CC=1)=C(\Cl)C1=CC=CC=C1 GKIRPKYJQBWNGO-OCEACIFDSA-N 0.000 description 4
- 238000002425 crystallisation Methods 0.000 description 4
- 230000008025 crystallization Effects 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 239000000284 extract Substances 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 4
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 4
- 239000008101 lactose Substances 0.000 description 4
- 235000019359 magnesium stearate Nutrition 0.000 description 4
- WNPORCRRSCZMSO-UHFFFAOYSA-N n-[(z)-(1-amino-2-chloroethylidene)amino]formamide Chemical compound ClCC(/N)=N\NC=O WNPORCRRSCZMSO-UHFFFAOYSA-N 0.000 description 4
- 201000001119 neuropathy Diseases 0.000 description 4
- 230000007823 neuropathy Effects 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 4
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 4
- 239000006187 pill Substances 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 125000000168 pyrrolyl group Chemical group 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 238000007363 ring formation reaction Methods 0.000 description 4
- 230000028327 secretion Effects 0.000 description 4
- 230000020341 sensory perception of pain Effects 0.000 description 4
- 239000012279 sodium borohydride Substances 0.000 description 4
- 229910000033 sodium borohydride Inorganic materials 0.000 description 4
- 238000001890 transfection Methods 0.000 description 4
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 4
- 230000024883 vasodilation Effects 0.000 description 4
- CYBHDFOHUGLNEW-DNVJHFABSA-N (2r,3r,5s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3,5-diphenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@H]2[C@H](N[C@H](CO2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 CYBHDFOHUGLNEW-DNVJHFABSA-N 0.000 description 3
- LTOTYONEVCMJJL-TZMCWYRMSA-N (2s)-2-[[(2r)-2-hydroxypropyl]-prop-2-enylamino]-2-phenylacetaldehyde Chemical compound C[C@@H](O)CN(CC=C)[C@H](C=O)C1=CC=CC=C1 LTOTYONEVCMJJL-TZMCWYRMSA-N 0.000 description 3
- AAZRMYIAKWXBIF-DNQXCXABSA-N (2s,3r)-4-benzyl-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@H](N(CC=3C=CC=CC=3)CCO2)C=2C=CC=CC=2)=C1 AAZRMYIAKWXBIF-DNQXCXABSA-N 0.000 description 3
- LMEFHDJFPPYPBL-SJORKVTESA-N (2s,3r)-4-benzyl-3-phenylmorpholin-2-ol Chemical compound O([C@@H]([C@H]1C=2C=CC=CC=2)O)CCN1CC1=CC=CC=C1 LMEFHDJFPPYPBL-SJORKVTESA-N 0.000 description 3
- CYBHDFOHUGLNEW-ZLNRFVROSA-N (2s,3r,5s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3,5-diphenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@H](N[C@H](CO2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 CYBHDFOHUGLNEW-ZLNRFVROSA-N 0.000 description 3
- CYBHDFOHUGLNEW-VABKMULXSA-N (2s,3s,5r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3,5-diphenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@@H](N[C@@H](CO2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 CYBHDFOHUGLNEW-VABKMULXSA-N 0.000 description 3
- OIYANYVIFQBNMS-LLVKDONJSA-N (3S)-4-methyl-3-phenylmorpholine Chemical compound C1(=CC=CC=C1)[C@@H]1N(CCOC1)C OIYANYVIFQBNMS-LLVKDONJSA-N 0.000 description 3
- GSZAAEJBPFTBKG-INIZCTEOSA-N (3s)-4-benzyl-3-(4-fluorophenyl)morpholin-2-one Chemical compound C1=CC(F)=CC=C1[C@H]1C(=O)OCCN1CC1=CC=CC=C1 GSZAAEJBPFTBKG-INIZCTEOSA-N 0.000 description 3
- JMVUVZICZVJGJY-INIZCTEOSA-N (3s)-4-benzyl-3-phenylmorpholin-2-one Chemical compound O=C([C@@H]1C=2C=CC=CC=2)OCCN1CC1=CC=CC=C1 JMVUVZICZVJGJY-INIZCTEOSA-N 0.000 description 3
- HVHZEKKZMFRULH-UHFFFAOYSA-N 2,6-ditert-butyl-4-methylpyridine Chemical compound CC1=CC(C(C)(C)C)=NC(C(C)(C)C)=C1 HVHZEKKZMFRULH-UHFFFAOYSA-N 0.000 description 3
- LOUZEJGRHQDABV-UHFFFAOYSA-N 2-bromo-2-phenylacetaldehyde Chemical class O=CC(Br)C1=CC=CC=C1 LOUZEJGRHQDABV-UHFFFAOYSA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- OZPICOPIYPCOIS-UHFFFAOYSA-N 6-[2-[3,5-bis(trifluoromethyl)phenyl]ethenyl]-5-phenylmorpholin-3-one Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(C=CC2C(NC(=O)CO2)C=2C=CC=CC=2)=C1 OZPICOPIYPCOIS-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 208000009079 Bronchial Spasm Diseases 0.000 description 3
- 208000014181 Bronchial disease Diseases 0.000 description 3
- 206010006482 Bronchospasm Diseases 0.000 description 3
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 3
- RENMDAKOXSCIGH-UHFFFAOYSA-N Chloroacetonitrile Chemical compound ClCC#N RENMDAKOXSCIGH-UHFFFAOYSA-N 0.000 description 3
- 206010009900 Colitis ulcerative Diseases 0.000 description 3
- 208000011231 Crohn disease Diseases 0.000 description 3
- 201000004624 Dermatitis Diseases 0.000 description 3
- 201000010374 Down Syndrome Diseases 0.000 description 3
- 101000990055 Homo sapiens CMRF35-like molecule 1 Proteins 0.000 description 3
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 3
- 206010065390 Inflammatory pain Diseases 0.000 description 3
- 102000046798 Neurokinin B Human genes 0.000 description 3
- 101800002813 Neurokinin-B Proteins 0.000 description 3
- QHUBYMGFBNYCJF-BFHBGLAWSA-N O[C@@H](CNC(C1=CC=CC=C1)C=O)C Chemical compound O[C@@H](CNC(C1=CC=CC=C1)C=O)C QHUBYMGFBNYCJF-BFHBGLAWSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 206010039966 Senile dementia Diseases 0.000 description 3
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- BJTWPJOGDWRYDD-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenyl]methanol Chemical compound OCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 BJTWPJOGDWRYDD-UHFFFAOYSA-N 0.000 description 3
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 3
- 239000000908 ammonium hydroxide Substances 0.000 description 3
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 3
- 229940035676 analgesics Drugs 0.000 description 3
- 150000008064 anhydrides Chemical class 0.000 description 3
- 239000000730 antalgic agent Substances 0.000 description 3
- 239000008346 aqueous phase Substances 0.000 description 3
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 3
- 230000005540 biological transmission Effects 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 235000011089 carbon dioxide Nutrition 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 238000002512 chemotherapy Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- SIPUZPBQZHNSDW-UHFFFAOYSA-N diisobutylaluminium hydride Substances CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 125000001207 fluorophenyl group Chemical group 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 239000012458 free base Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- CWWARWOPSKGELM-SARDKLJWSA-N methyl (2s)-2-[[(2s)-2-[[2-[[(2s)-2-[[(2s)-2-[[(2s)-5-amino-2-[[(2s)-5-amino-2-[[(2s)-1-[(2s)-6-amino-2-[[(2s)-1-[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-5 Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)OC)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 CWWARWOPSKGELM-SARDKLJWSA-N 0.000 description 3
- 230000001537 neural effect Effects 0.000 description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 description 3
- 125000002971 oxazolyl group Chemical group 0.000 description 3
- 229910000343 potassium bisulfate Inorganic materials 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- 208000023504 respiratory system disease Diseases 0.000 description 3
- 239000012312 sodium hydride Substances 0.000 description 3
- 229910000104 sodium hydride Inorganic materials 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000000829 suppository Substances 0.000 description 3
- 230000005062 synaptic transmission Effects 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- 210000001835 viscera Anatomy 0.000 description 3
- LTOTYONEVCMJJL-OCCSQVGLSA-N (2r)-2-[[(2r)-2-hydroxypropyl]-prop-2-enylamino]-2-phenylacetaldehyde Chemical compound C[C@@H](O)CN(CC=C)[C@@H](C=O)C1=CC=CC=C1 LTOTYONEVCMJJL-OCCSQVGLSA-N 0.000 description 2
- XDXNSQTXGXCNRF-IPHXSNPTSA-N (2r,3r,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenyl-4-prop-2-enylmorpholine Chemical compound O([C@H]1[C@H](N(CC=C)C[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XDXNSQTXGXCNRF-IPHXSNPTSA-N 0.000 description 2
- XDXNSQTXGXCNRF-GQWLDOHISA-N (2r,3s,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenyl-4-prop-2-enylmorpholine Chemical compound O([C@H]1[C@@H](N(CC=C)C[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XDXNSQTXGXCNRF-GQWLDOHISA-N 0.000 description 2
- LCRCODPYSHSWAR-AWEZNQCLSA-N (2s)-2-(benzylazaniumyl)-2-phenylacetate Chemical compound [NH2+]([C@H](C(=O)[O-])C=1C=CC=CC=1)CC1=CC=CC=C1 LCRCODPYSHSWAR-AWEZNQCLSA-N 0.000 description 2
- NVBABMBPLPCEBT-ZETCQYMHSA-N (2s)-2-azido-2-(4-fluorophenyl)acetic acid Chemical compound [N-]=[N+]=N[C@H](C(=O)O)C1=CC=C(F)C=C1 NVBABMBPLPCEBT-ZETCQYMHSA-N 0.000 description 2
- XDXNSQTXGXCNRF-LPTQZCDUSA-N (2s,3r,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenyl-4-prop-2-enylmorpholine Chemical compound O([C@@H]1[C@H](N(CC=C)C[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XDXNSQTXGXCNRF-LPTQZCDUSA-N 0.000 description 2
- FCODJGJNKUESIL-BJKOFHAPSA-N (2s,3s)-4-benzyl-2-[(3,5-dichlorophenyl)methoxy]-3-phenylmorpholine Chemical compound ClC1=CC(Cl)=CC(CO[C@@H]2[C@@H](N(CC=3C=CC=CC=3)CCO2)C=2C=CC=CC=2)=C1 FCODJGJNKUESIL-BJKOFHAPSA-N 0.000 description 2
- XDXNSQTXGXCNRF-NQERJWCQSA-N (2s,3s,6r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-6-methyl-3-phenyl-4-prop-2-enylmorpholine Chemical compound O([C@@H]1[C@@H](N(CC=C)C[C@H](O1)C)C=1C=CC=CC=1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XDXNSQTXGXCNRF-NQERJWCQSA-N 0.000 description 2
- VSNNLLQKDRCKCB-UHFFFAOYSA-N (3,5-dichlorophenyl)methanol Chemical compound OCC1=CC(Cl)=CC(Cl)=C1 VSNNLLQKDRCKCB-UHFFFAOYSA-N 0.000 description 2
- OJOFMLDBXPDXLQ-VIFPVBQESA-N (4s)-4-benzyl-1,3-oxazolidin-2-one Chemical compound C1OC(=O)N[C@H]1CC1=CC=CC=C1 OJOFMLDBXPDXLQ-VIFPVBQESA-N 0.000 description 2
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 2
- PAAZPARNPHGIKF-UHFFFAOYSA-N 1,2-dibromoethane Chemical class BrCCBr PAAZPARNPHGIKF-UHFFFAOYSA-N 0.000 description 2
- RYHRCYSIWGQBNC-DNQXCXABSA-N 1-[(2s,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]-2-pyridin-3-ylethanone Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@H](N(CCO2)C(=O)CC=2C=NC=CC=2)C=2C=CC=CC=2)=C1 RYHRCYSIWGQBNC-DNQXCXABSA-N 0.000 description 2
- GDUHZPGTYUAZSE-UHFFFAOYSA-N 1-amino-4-[3,5-bis(trifluoromethyl)phenyl]-1-phenylbut-3-en-2-ol Chemical compound C=1C=CC=CC=1C(N)C(O)C=CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 GDUHZPGTYUAZSE-UHFFFAOYSA-N 0.000 description 2
- PJUPKRYGDFTMTM-UHFFFAOYSA-N 1-hydroxybenzotriazole;hydrate Chemical compound O.C1=CC=C2N(O)N=NC2=C1 PJUPKRYGDFTMTM-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- JTNCEQNHURODLX-UHFFFAOYSA-N 2-phenylethanimidamide Chemical compound NC(=N)CC1=CC=CC=C1 JTNCEQNHURODLX-UHFFFAOYSA-N 0.000 description 2
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- 108060003345 Adrenergic Receptor Proteins 0.000 description 2
- 102000017910 Adrenergic receptor Human genes 0.000 description 2
- 206010002091 Anaesthesia Diseases 0.000 description 2
- 208000019901 Anxiety disease Diseases 0.000 description 2
- KPYSYYIEGFHWSV-UHFFFAOYSA-N Baclofen Chemical compound OC(=O)CC(CN)C1=CC=C(Cl)C=C1 KPYSYYIEGFHWSV-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 201000004813 Bronchopneumonia Diseases 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- 206010010741 Conjunctivitis Diseases 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 208000032131 Diabetic Neuropathies Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 206010020772 Hypertension Diseases 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 206010021639 Incontinence Diseases 0.000 description 2
- ZGUNAGUHMKGQNY-ZETCQYMHSA-N L-alpha-phenylglycine zwitterion Chemical compound OC(=O)[C@@H](N)C1=CC=CC=C1 ZGUNAGUHMKGQNY-ZETCQYMHSA-N 0.000 description 2
- 239000012448 Lithium borohydride Substances 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 229910021380 Manganese Chloride Inorganic materials 0.000 description 2
- GLFNIEUTAYBVOC-UHFFFAOYSA-L Manganese chloride Chemical compound Cl[Mn]Cl GLFNIEUTAYBVOC-UHFFFAOYSA-L 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- 206010028813 Nausea Diseases 0.000 description 2
- 108010040722 Neurokinin-2 Receptors Proteins 0.000 description 2
- 108090000189 Neuropeptides Proteins 0.000 description 2
- QHUBYMGFBNYCJF-FTNKSUMCSA-N O[C@H](CNC(C1=CC=CC=C1)C=O)C Chemical compound O[C@H](CNC(C1=CC=CC=C1)C=O)C QHUBYMGFBNYCJF-FTNKSUMCSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- 208000028017 Psychotic disease Diseases 0.000 description 2
- 206010039424 Salivary hypersecretion Diseases 0.000 description 2
- HEMHJVSKTPXQMS-DYCDLGHISA-M Sodium hydroxide-d Chemical compound [Na+].[2H][O-] HEMHJVSKTPXQMS-DYCDLGHISA-M 0.000 description 2
- 102100037342 Substance-K receptor Human genes 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 201000006704 Ulcerative Colitis Diseases 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- INAPMGSXUVUWAF-GCVPSNMTSA-N [(2r,3s,5r,6r)-2,3,4,5,6-pentahydroxycyclohexyl] dihydrogen phosphate Chemical compound OC1[C@H](O)[C@@H](O)C(OP(O)(O)=O)[C@H](O)[C@@H]1O INAPMGSXUVUWAF-GCVPSNMTSA-N 0.000 description 2
- RXDLGFMMQFNVLI-UHFFFAOYSA-N [Na].[Na].[Ca] Chemical compound [Na].[Na].[Ca] RXDLGFMMQFNVLI-UHFFFAOYSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- BHELZAPQIKSEDF-UHFFFAOYSA-N allyl bromide Chemical compound BrCC=C BHELZAPQIKSEDF-UHFFFAOYSA-N 0.000 description 2
- VZTDIZULWFCMLS-UHFFFAOYSA-N ammonium formate Chemical compound [NH4+].[O-]C=O VZTDIZULWFCMLS-UHFFFAOYSA-N 0.000 description 2
- 239000003708 ampul Substances 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 229960000794 baclofen Drugs 0.000 description 2
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 2
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 2
- 230000002051 biphasic effect Effects 0.000 description 2
- XGIUDIMNNMKGDE-UHFFFAOYSA-N bis(trimethylsilyl)azanide Chemical compound C[Si](C)(C)[N-][Si](C)(C)C XGIUDIMNNMKGDE-UHFFFAOYSA-N 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- UORVGPXVDQYIDP-UHFFFAOYSA-N borane Chemical compound B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 150000001649 bromium compounds Chemical class 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000000480 calcium channel blocker Substances 0.000 description 2
- 125000002837 carbocyclic group Chemical group 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- QOPVNWQGBQYBBP-UHFFFAOYSA-N chloroethyl chloroformate Chemical compound CC(Cl)OC(Cl)=O QOPVNWQGBQYBBP-UHFFFAOYSA-N 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 238000012258 culturing Methods 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 2
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 2
- 235000019797 dipotassium phosphate Nutrition 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 210000001198 duodenum Anatomy 0.000 description 2
- 229940009662 edetate Drugs 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000012259 ether extract Substances 0.000 description 2
- 230000002964 excitative effect Effects 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 239000012065 filter cake Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- 230000002496 gastric effect Effects 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 239000012362 glacial acetic acid Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 150000004678 hydrides Chemical class 0.000 description 2
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 2
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 2
- 230000008105 immune reaction Effects 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 150000004694 iodide salts Chemical class 0.000 description 2
- PGLTVOMIXTUURA-UHFFFAOYSA-N iodoacetamide Chemical compound NC(=O)CI PGLTVOMIXTUURA-UHFFFAOYSA-N 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000001786 isothiazolyl group Chemical group 0.000 description 2
- 125000000842 isoxazolyl group Chemical group 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 150000002596 lactones Chemical class 0.000 description 2
- 239000012280 lithium aluminium hydride Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 230000033001 locomotion Effects 0.000 description 2
- 239000011565 manganese chloride Substances 0.000 description 2
- 235000002867 manganese chloride Nutrition 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- UKVIEHSSVKSQBA-UHFFFAOYSA-N methane;palladium Chemical compound C.[Pd] UKVIEHSSVKSQBA-UHFFFAOYSA-N 0.000 description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 2
- YDCHPLOFQATIDS-UHFFFAOYSA-N methyl 2-bromoacetate Chemical compound COC(=O)CBr YDCHPLOFQATIDS-UHFFFAOYSA-N 0.000 description 2
- WFJRIDQGVSJLLH-UHFFFAOYSA-N methyl n-aminocarbamate Chemical compound COC(=O)NN WFJRIDQGVSJLLH-UHFFFAOYSA-N 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- KRKPYFLIYNGWTE-UHFFFAOYSA-N n,o-dimethylhydroxylamine Chemical compound CNOC KRKPYFLIYNGWTE-UHFFFAOYSA-N 0.000 description 2
- WPBBCIADLPYGDP-FCHUYYIVSA-N n-(3-aminopropyl)-2-[(2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetamide Chemical compound O([C@H]1OCCN([C@H]1C=1C=CC=CC=1)CC(=O)NCCCN)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 WPBBCIADLPYGDP-FCHUYYIVSA-N 0.000 description 2
- 230000008693 nausea Effects 0.000 description 2
- 210000000653 nervous system Anatomy 0.000 description 2
- 208000015122 neurodegenerative disease Diseases 0.000 description 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 125000001715 oxadiazolyl group Chemical group 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 150000004885 piperazines Chemical class 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- LJCNRYVRMXRIQR-OLXYHTOASA-L potassium sodium L-tartrate Chemical compound [Na+].[K+].[O-]C(=O)[C@H](O)[C@@H](O)C([O-])=O LJCNRYVRMXRIQR-OLXYHTOASA-L 0.000 description 2
- 229940074439 potassium sodium tartrate Drugs 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- NSETWVJZUWGCKE-UHFFFAOYSA-N propylphosphonic acid Chemical compound CCCP(O)(O)=O NSETWVJZUWGCKE-UHFFFAOYSA-N 0.000 description 2
- 125000003373 pyrazinyl group Chemical group 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- 230000000241 respiratory effect Effects 0.000 description 2
- 208000026451 salivation Diseases 0.000 description 2
- 201000000980 schizophrenia Diseases 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- VATDYQWILMGLEW-UHFFFAOYSA-N sec-butyllithium Chemical compound [Li]C(C)CC VATDYQWILMGLEW-UHFFFAOYSA-N 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 235000009518 sodium iodide Nutrition 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 235000011006 sodium potassium tartrate Nutrition 0.000 description 2
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 2
- 235000019345 sodium thiosulphate Nutrition 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 239000013076 target substance Substances 0.000 description 2
- 229940095064 tartrate Drugs 0.000 description 2
- JDJUXEBWGNEEDT-UHFFFAOYSA-N tert-butyl n-[4-[3,5-bis(trifluoromethyl)phenyl]-2-oxo-1-phenylbut-3-enyl]carbamate Chemical compound C=1C=CC=CC=1C(NC(=O)OC(C)(C)C)C(=O)C=CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 JDJUXEBWGNEEDT-UHFFFAOYSA-N 0.000 description 2
- DPKBAXPHAYBPRL-UHFFFAOYSA-M tetrabutylazanium;iodide Chemical compound [I-].CCCC[N+](CCCC)(CCCC)CCCC DPKBAXPHAYBPRL-UHFFFAOYSA-M 0.000 description 2
- RWRDLPDLKQPQOW-UHFFFAOYSA-N tetrahydropyrrole Natural products C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 2
- 125000003831 tetrazolyl group Chemical group 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 125000000464 thioxo group Chemical group S=* 0.000 description 2
- 206010044008 tonsillitis Diseases 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- XFNJVJPLKCPIBV-UHFFFAOYSA-N trimethylenediamine Chemical compound NCCCN XFNJVJPLKCPIBV-UHFFFAOYSA-N 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 239000011995 wilkinson's catalyst Substances 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical compound CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- RCIVUMDLBQZEHP-UHFFFAOYSA-N (2-methylpropan-2-yl)oxycarbamic acid Chemical compound CC(C)(C)ONC(O)=O RCIVUMDLBQZEHP-UHFFFAOYSA-N 0.000 description 1
- XHNJTWCNBDADLM-OCCSQVGLSA-N (2R)-2-[[(2R)-2-hydroxypropyl]-propan-2-ylamino]-2-phenylacetaldehyde Chemical compound O[C@@H](CN([C@H](C1=CC=CC=C1)C=O)C(C)C)C XHNJTWCNBDADLM-OCCSQVGLSA-N 0.000 description 1
- LTOTYONEVCMJJL-JSGCOSHPSA-N (2r)-2-[[(2s)-2-hydroxypropyl]-prop-2-enylamino]-2-phenylacetaldehyde Chemical compound C[C@H](O)CN(CC=C)[C@@H](C=O)C1=CC=CC=C1 LTOTYONEVCMJJL-JSGCOSHPSA-N 0.000 description 1
- BKMMTJMQCTUHRP-GSVOUGTGSA-N (2r)-2-aminopropan-1-ol Chemical compound C[C@@H](N)CO BKMMTJMQCTUHRP-GSVOUGTGSA-N 0.000 description 1
- FUQXMZQIUQTJPV-SJORKVTESA-N (2r,3r)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@H]2[C@H](NCCO2)C=2C=CC=CC=2)=C1 FUQXMZQIUQTJPV-SJORKVTESA-N 0.000 description 1
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- HXKKHQJGJAFBHI-VKHMYHEASA-N (2s)-1-aminopropan-2-ol Chemical compound C[C@H](O)CN HXKKHQJGJAFBHI-VKHMYHEASA-N 0.000 description 1
- LTOTYONEVCMJJL-GXTWGEPZSA-N (2s)-2-[[(2s)-2-hydroxypropyl]-prop-2-enylamino]-2-phenylacetaldehyde Chemical compound C[C@H](O)CN(CC=C)[C@H](C=O)C1=CC=CC=C1 LTOTYONEVCMJJL-GXTWGEPZSA-N 0.000 description 1
- IJXJGQCXFSSHNL-MRVPVSSYSA-N (2s)-2-amino-2-phenylethanol Chemical compound OC[C@@H](N)C1=CC=CC=C1 IJXJGQCXFSSHNL-MRVPVSSYSA-N 0.000 description 1
- AAZRMYIAKWXBIF-BJKOFHAPSA-N (2s,3s)-4-benzyl-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CO[C@@H]2[C@@H](N(CC=3C=CC=CC=3)CCO2)C=2C=CC=CC=2)=C1 AAZRMYIAKWXBIF-BJKOFHAPSA-N 0.000 description 1
- JMVUVZICZVJGJY-MRXNPFEDSA-N (3r)-4-benzyl-3-phenylmorpholin-2-one Chemical compound O=C([C@H]1C=2C=CC=CC=2)OCCN1CC1=CC=CC=C1 JMVUVZICZVJGJY-MRXNPFEDSA-N 0.000 description 1
- HEAUFJZALFKPBA-JPQUDPSNSA-N (3s)-3-[[(2s,3r)-2-[[(2s)-6-amino-2-[[(2s)-2-amino-3-(1h-imidazol-5-yl)propanoyl]amino]hexanoyl]amino]-3-hydroxybutanoyl]amino]-4-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[2-[[(2s)-1-[[(2s)-1-amino-4-methylsulfanyl-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amin Chemical compound C([C@@H](C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)C(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)C1=CC=CC=C1 HEAUFJZALFKPBA-JPQUDPSNSA-N 0.000 description 1
- RFSVEDOANSSCGG-SFHVURJKSA-N (4s)-4-acetyl-4-benzyl-3-(4-fluorophenyl)-1,3-oxazolidin-2-one Chemical compound C([C@]1(C(=O)C)N(C(=O)OC1)C=1C=CC(F)=CC=1)C1=CC=CC=C1 RFSVEDOANSSCGG-SFHVURJKSA-N 0.000 description 1
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 1
- BKMMTJMQCTUHRP-VKHMYHEASA-N (S)-2-aminopropan-1-ol Chemical compound C[C@H](N)CO BKMMTJMQCTUHRP-VKHMYHEASA-N 0.000 description 1
- ODIGIKRIUKFKHP-UHFFFAOYSA-N (n-propan-2-yloxycarbonylanilino) acetate Chemical compound CC(C)OC(=O)N(OC(C)=O)C1=CC=CC=C1 ODIGIKRIUKFKHP-UHFFFAOYSA-N 0.000 description 1
- AEMWUHCKKDPRSK-UHFFFAOYSA-N (ne)-n-diazo-2,4,6-tri(propan-2-yl)benzenesulfonamide Chemical compound CC(C)C1=CC(C(C)C)=C(S(=O)(=O)N=[N+]=[N-])C(C(C)C)=C1 AEMWUHCKKDPRSK-UHFFFAOYSA-N 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- APQIUTYORBAGEZ-UHFFFAOYSA-N 1,1-dibromoethane Chemical compound CC(Br)Br APQIUTYORBAGEZ-UHFFFAOYSA-N 0.000 description 1
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- 125000005940 1,4-dioxanyl group Chemical group 0.000 description 1
- ATLQGZVLWOURFU-UHFFFAOYSA-N 1-(bromomethyl)-3,5-bis(trifluoromethyl)benzene Chemical compound FC(F)(F)C1=CC(CBr)=CC(C(F)(F)F)=C1 ATLQGZVLWOURFU-UHFFFAOYSA-N 0.000 description 1
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 1
- NYYLZXREFNYPKB-UHFFFAOYSA-N 1-[ethoxy(methyl)phosphoryl]oxyethane Chemical compound CCOP(C)(=O)OCC NYYLZXREFNYPKB-UHFFFAOYSA-N 0.000 description 1
- IGNPOXGBNFMJHE-UHFFFAOYSA-N 1-azabicyclo[2.2.2]octan-2-amine Chemical compound C1CN2C(N)CC1CC2 IGNPOXGBNFMJHE-UHFFFAOYSA-N 0.000 description 1
- UALFYMMGEYDHHJ-UHFFFAOYSA-N 1-azabicyclo[3.2.2]nonan-3-amine Chemical class C1C(N)CC2CCN1CC2 UALFYMMGEYDHHJ-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical compound CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- VUQPJRPDRDVQMN-UHFFFAOYSA-N 1-chlorooctadecane Chemical class CCCCCCCCCCCCCCCCCCCl VUQPJRPDRDVQMN-UHFFFAOYSA-N 0.000 description 1
- XYHKNCXZYYTLRG-UHFFFAOYSA-N 1h-imidazole-2-carbaldehyde Chemical compound O=CC1=NC=CN1 XYHKNCXZYYTLRG-UHFFFAOYSA-N 0.000 description 1
- JVSFQJZRHXAUGT-UHFFFAOYSA-N 2,2-dimethylpropanoyl chloride Chemical compound CC(C)(C)C(Cl)=O JVSFQJZRHXAUGT-UHFFFAOYSA-N 0.000 description 1
- ZIIUUSVHCHPIQD-UHFFFAOYSA-N 2,4,6-trimethyl-N-[3-(trifluoromethyl)phenyl]benzenesulfonamide Chemical compound CC1=CC(C)=CC(C)=C1S(=O)(=O)NC1=CC=CC(C(F)(F)F)=C1 ZIIUUSVHCHPIQD-UHFFFAOYSA-N 0.000 description 1
- UWKQJZCTQGMHKD-UHFFFAOYSA-N 2,6-di-tert-butylpyridine Chemical compound CC(C)(C)C1=CC=CC(C(C)(C)C)=N1 UWKQJZCTQGMHKD-UHFFFAOYSA-N 0.000 description 1
- MGKPFALCNDRSQD-UHFFFAOYSA-N 2-(4-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=C(F)C=C1 MGKPFALCNDRSQD-UHFFFAOYSA-N 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical compound O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- HOBFSNNENNQQIU-UHFFFAOYSA-N 2-[(2-methylpropan-2-yl)oxycarbonylamino]-2-phenylacetic acid Chemical compound CC(C)(C)OC(=O)NC(C(O)=O)C1=CC=CC=C1 HOBFSNNENNQQIU-UHFFFAOYSA-N 0.000 description 1
- FJUPKIPPLZPSDY-UHFFFAOYSA-N 2-[(3-tert-butyl-5-methylphenyl)methoxy]-4-methyl-3-phenylmorpholine Chemical compound CN1C(C(OCC1)OCC1=CC(=CC(=C1)C)C(C)(C)C)C1=CC=CC=C1 FJUPKIPPLZPSDY-UHFFFAOYSA-N 0.000 description 1
- TUHKIFKLUZKZDP-LJQANCHMSA-N 2-[(3S)-3-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetic acid Chemical compound FC(C=1C=C(CO[C@@]2(N(CCOC2)CC(=O)O)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F TUHKIFKLUZKZDP-LJQANCHMSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- IJXJGQCXFSSHNL-UHFFFAOYSA-N 2-amino-2-phenylethanol Chemical compound OCC(N)C1=CC=CC=C1 IJXJGQCXFSSHNL-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- FUSFWUFSEJXMRQ-UHFFFAOYSA-N 2-bromo-1,1-dimethoxyethane Chemical class COC(CBr)OC FUSFWUFSEJXMRQ-UHFFFAOYSA-N 0.000 description 1
- YOETUEMZNOLGDB-UHFFFAOYSA-N 2-methylpropyl carbonochloridate Chemical compound CC(C)COC(Cl)=O YOETUEMZNOLGDB-UHFFFAOYSA-N 0.000 description 1
- PAEXAIBDCHBNDC-UHFFFAOYSA-N 2-pyridin-4-ylacetic acid Chemical compound OC(=O)CC1=CC=NC=C1 PAEXAIBDCHBNDC-UHFFFAOYSA-N 0.000 description 1
- LDWLIXZSDPXYDR-UHFFFAOYSA-N 3,5-bis(trifluoromethyl)benzaldehyde Chemical compound FC(F)(F)C1=CC(C=O)=CC(C(F)(F)F)=C1 LDWLIXZSDPXYDR-UHFFFAOYSA-N 0.000 description 1
- HYCKBFLTZGORKA-HNPMAXIBSA-N 3,7-dihydropurin-6-one;1-[(2r,4s,5r)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound O=C1NC=NC2=C1NC=N2.O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 HYCKBFLTZGORKA-HNPMAXIBSA-N 0.000 description 1
- LULAYUGMBFYYEX-UHFFFAOYSA-N 3-chlorobenzoic acid Chemical compound OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 1
- IVLICPVPXWEGCA-UHFFFAOYSA-N 3-quinuclidinol Chemical class C1C[C@@H]2C(O)C[N@]1CC2 IVLICPVPXWEGCA-UHFFFAOYSA-N 0.000 description 1
- BBDCCXMBOJDLMO-UHFFFAOYSA-N 4-benzyl-1-(2-chloroethyl)piperidine Chemical compound C1CN(CCCl)CCC1CC1=CC=CC=C1 BBDCCXMBOJDLMO-UHFFFAOYSA-N 0.000 description 1
- UZOVYGYOLBIAJR-UHFFFAOYSA-N 4-isocyanato-4'-methyldiphenylmethane Chemical compound C1=CC(C)=CC=C1CC1=CC=C(N=C=O)C=C1 UZOVYGYOLBIAJR-UHFFFAOYSA-N 0.000 description 1
- FHQRDEDZJIFJAL-UHFFFAOYSA-N 4-phenylmorpholine Chemical compound C1COCCN1C1=CC=CC=C1 FHQRDEDZJIFJAL-UHFFFAOYSA-N 0.000 description 1
- SUSANAYXICMXBL-UHFFFAOYSA-N 4-prop-2-enylmorpholine Chemical compound C=CCN1CCOCC1 SUSANAYXICMXBL-UHFFFAOYSA-N 0.000 description 1
- 102000040125 5-hydroxytryptamine receptor family Human genes 0.000 description 1
- 108091032151 5-hydroxytryptamine receptor family Proteins 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 206010065040 AIDS dementia complex Diseases 0.000 description 1
- 208000007848 Alcoholism Diseases 0.000 description 1
- 206010027654 Allergic conditions Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 102000013455 Amyloid beta-Peptides Human genes 0.000 description 1
- 108010090849 Amyloid beta-Peptides Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 108010001478 Bacitracin Proteins 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 208000014644 Brain disease Diseases 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 206010006458 Bronchitis chronic Diseases 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- RWZMGMWTRFGIIA-JTQLQIEISA-N C1(=CC=CC=C1)N1CCOC[C@@H]1C Chemical compound C1(=CC=CC=C1)N1CCOC[C@@H]1C RWZMGMWTRFGIIA-JTQLQIEISA-N 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- 206010007572 Cardiac hypertrophy Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 206010059109 Cerebral vasoconstriction Diseases 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 208000006561 Cluster Headache Diseases 0.000 description 1
- 208000027932 Collagen disease Diseases 0.000 description 1
- 208000013586 Complex regional pain syndrome type 1 Diseases 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZGUNAGUHMKGQNY-SSDOTTSWSA-N D-alpha-phenylglycine Chemical compound OC(=O)[C@H](N)C1=CC=CC=C1 ZGUNAGUHMKGQNY-SSDOTTSWSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 208000016192 Demyelinating disease Diseases 0.000 description 1
- 206010012305 Demyelination Diseases 0.000 description 1
- 206010012442 Dermatitis contact Diseases 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 102000015554 Dopamine receptor Human genes 0.000 description 1
- 108050004812 Dopamine receptor Proteins 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- GEXNFXWEJMCWRV-SCLBCKFNSA-N FC(C=1C=C(CON2[C@H](COC[C@@H]2C)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F Chemical compound FC(C=1C=C(CON2[C@H](COC[C@@H]2C)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F GEXNFXWEJMCWRV-SCLBCKFNSA-N 0.000 description 1
- PVTOOIOSQVTXIE-DHIUTWEWSA-N FC(C=1C=C(CON2[C@H](COC[C@@H]2C2=CC=CC=C2)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F Chemical compound FC(C=1C=C(CON2[C@H](COC[C@@H]2C2=CC=CC=C2)C2=CC=CC=C2)C=C(C=1)C(F)(F)F)(F)F PVTOOIOSQVTXIE-DHIUTWEWSA-N 0.000 description 1
- 208000001640 Fibromyalgia Diseases 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- WZELXJBMMZFDDU-UHFFFAOYSA-N Imidazol-2-one Chemical compound O=C1N=CC=N1 WZELXJBMMZFDDU-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 208000027601 Inner ear disease Diseases 0.000 description 1
- 108010076876 Keratins Proteins 0.000 description 1
- 102000011782 Keratins Human genes 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- 102000014415 Muscarinic acetylcholine receptor Human genes 0.000 description 1
- 108050003473 Muscarinic acetylcholine receptor Proteins 0.000 description 1
- RIXRAKOSCNUQBZ-WMZOPIPTSA-N N(=[N+]=[N-])[C@@H]1[C@](N(C(O1)=O)C(C)=O)(CC1=CC=CC=C1)C1=CC=C(C=C1)F Chemical compound N(=[N+]=[N-])[C@@H]1[C@](N(C(O1)=O)C(C)=O)(CC1=CC=CC=C1)C1=CC=C(C=C1)F RIXRAKOSCNUQBZ-WMZOPIPTSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 208000007920 Neurogenic Inflammation Diseases 0.000 description 1
- 102000028517 Neuropeptide receptor Human genes 0.000 description 1
- 108070000018 Neuropeptide receptor Proteins 0.000 description 1
- 102000003797 Neuropeptides Human genes 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 102000010175 Opsin Human genes 0.000 description 1
- 108050001704 Opsin Proteins 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 102000015439 Phospholipases Human genes 0.000 description 1
- 108010064785 Phospholipases Proteins 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 206010036376 Postherpetic Neuralgia Diseases 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 208000003782 Raynaud disease Diseases 0.000 description 1
- 208000012322 Raynaud phenomenon Diseases 0.000 description 1
- 201000001947 Reflex Sympathetic Dystrophy Diseases 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 208000005392 Spasm Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 108090000253 Thyrotropin Receptors Proteins 0.000 description 1
- 102100029337 Thyrotropin receptor Human genes 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 208000024780 Urticaria Diseases 0.000 description 1
- RQBGLYREDLMZMC-UHFFFAOYSA-N [N].C1COCCN1 Chemical group [N].C1COCCN1 RQBGLYREDLMZMC-UHFFFAOYSA-N 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 150000001241 acetals Chemical class 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 229940081735 acetylcellulose Drugs 0.000 description 1
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 1
- 229960004373 acetylcholine Drugs 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 239000000674 adrenergic antagonist Substances 0.000 description 1
- 201000007930 alcohol dependence Diseases 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 1
- 229960000723 ampicillin Drugs 0.000 description 1
- 239000002269 analeptic agent Substances 0.000 description 1
- 230000036592 analgesia Effects 0.000 description 1
- 229940075564 anhydrous dibasic sodium phosphate Drugs 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- CELPHAGZKFMOMR-UHFFFAOYSA-N azanium;dichloromethane;methanol;hydroxide Chemical compound [NH4+].[OH-].OC.ClCCl CELPHAGZKFMOMR-UHFFFAOYSA-N 0.000 description 1
- 125000002393 azetidinyl group Chemical group 0.000 description 1
- 150000001540 azides Chemical class 0.000 description 1
- 229960003071 bacitracin Drugs 0.000 description 1
- 229930184125 bacitracin Natural products 0.000 description 1
- CLKOFPXJLQSYAH-ABRJDSQDSA-N bacitracin A Chemical compound C1SC([C@@H](N)[C@@H](C)CC)=N[C@@H]1C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]1C(=O)N[C@H](CCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2N=CNC=2)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)NCCCC1 CLKOFPXJLQSYAH-ABRJDSQDSA-N 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 150000003935 benzaldehydes Chemical class 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 125000005872 benzooxazolyl group Chemical group 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 150000003938 benzyl alcohols Chemical class 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000012148 binding buffer Substances 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- AZWXAPCAJCYGIA-UHFFFAOYSA-N bis(2-methylpropyl)alumane Chemical compound CC(C)C[AlH]CC(C)C AZWXAPCAJCYGIA-UHFFFAOYSA-N 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- 239000012888 bovine serum Substances 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 206010006451 bronchitis Diseases 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 230000004856 capillary permeability Effects 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 210000000748 cardiovascular system Anatomy 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- FOCAUTSVDIKZOP-UHFFFAOYSA-M chloroacetate Chemical class [O-]C(=O)CCl FOCAUTSVDIKZOP-UHFFFAOYSA-M 0.000 description 1
- 229940089960 chloroacetate Drugs 0.000 description 1
- 208000007451 chronic bronchitis Diseases 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 208000018912 cluster headache syndrome Diseases 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 208000010247 contact dermatitis Diseases 0.000 description 1
- 230000001595 contractor effect Effects 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000000994 depressogenic effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- OKKJLVBELUTLKV-MICDWDOJSA-N deuteriomethanol Chemical compound [2H]CO OKKJLVBELUTLKV-MICDWDOJSA-N 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- 125000002720 diazolyl group Chemical group 0.000 description 1
- LMEDOLJKVASKTP-UHFFFAOYSA-N dibutyl sulfate Chemical group CCCCOS(=O)(=O)OCCCC LMEDOLJKVASKTP-UHFFFAOYSA-N 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- GAFRWLVTHPVQGK-UHFFFAOYSA-N dipentyl sulfate Chemical compound CCCCCOS(=O)(=O)OCCCCC GAFRWLVTHPVQGK-UHFFFAOYSA-N 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- XPPKVPWEQAFLFU-UHFFFAOYSA-J diphosphate(4-) Chemical compound [O-]P([O-])(=O)OP([O-])([O-])=O XPPKVPWEQAFLFU-UHFFFAOYSA-J 0.000 description 1
- 235000011180 diphosphates Nutrition 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000003291 dopaminomimetic effect Effects 0.000 description 1
- 238000007877 drug screening Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 208000024732 dysthymic disease Diseases 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 230000002327 eosinophilic effect Effects 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 150000002148 esters Chemical group 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- VCAIPSUUTZJHRP-UHFFFAOYSA-N ethyl 2-oxoimidazole-4-carboxylate Chemical compound CCOC(=O)C1=NC(=O)N=C1 VCAIPSUUTZJHRP-UHFFFAOYSA-N 0.000 description 1
- VEUUMBGHMNQHGO-UHFFFAOYSA-N ethyl chloroacetate Chemical compound CCOC(=O)CCl VEUUMBGHMNQHGO-UHFFFAOYSA-N 0.000 description 1
- PQVSTLUFSYVLTO-UHFFFAOYSA-N ethyl n-ethoxycarbonylcarbamate Chemical compound CCOC(=O)NC(=O)OCC PQVSTLUFSYVLTO-UHFFFAOYSA-N 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 230000004438 eyesight Effects 0.000 description 1
- 208000006275 fascioliasis Diseases 0.000 description 1
- 230000003176 fibrotic effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- XZBIXDPGRMLSTC-UHFFFAOYSA-N formohydrazide Chemical compound NNC=O XZBIXDPGRMLSTC-UHFFFAOYSA-N 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 230000030135 gastric motility Effects 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 239000010460 hemp oil Substances 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229940094991 herring sperm dna Drugs 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 125000004634 hexahydroazepinyl group Chemical group N1(CCCCCC1)* 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 108091008039 hormone receptors Proteins 0.000 description 1
- 102000056136 human TACR1 Human genes 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 239000008172 hydrogenated vegetable oil Substances 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 230000007365 immunoregulation Effects 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 229960000367 inositol Drugs 0.000 description 1
- 239000002917 insecticide Substances 0.000 description 1
- 239000002198 insoluble material Substances 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 208000001286 intracranial vasospasm Diseases 0.000 description 1
- 230000004410 intraocular pressure Effects 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 208000023589 ischemic disease Diseases 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 210000001630 jejunum Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229940040692 lithium hydroxide monohydrate Drugs 0.000 description 1
- GLXDVVHUTZTUQK-UHFFFAOYSA-M lithium hydroxide monohydrate Substances [Li+].O.[OH-] GLXDVVHUTZTUQK-UHFFFAOYSA-M 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- DXGFMDOTPXBTFD-UHFFFAOYSA-N methanesulfonic acid;naphthalene-1-sulfonic acid Chemical compound CS(O)(=O)=O.C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 DXGFMDOTPXBTFD-UHFFFAOYSA-N 0.000 description 1
- AGJSNMGHAVDLRQ-HUUJSLGLSA-N methyl (2s)-2-[[(2r)-2-[[(2s)-2-[[(2r)-2-amino-3-sulfanylpropanoyl]amino]-3-methylbutanoyl]amino]-3-(4-hydroxy-2,3-dimethylphenyl)propanoyl]amino]-4-methylsulfanylbutanoate Chemical compound SC[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(=O)N[C@@H](CCSC)C(=O)OC)CC1=CC=C(O)C(C)=C1C AGJSNMGHAVDLRQ-HUUJSLGLSA-N 0.000 description 1
- AGJSNMGHAVDLRQ-IWFBPKFRSA-N methyl (2s)-2-[[(2s)-2-[[(2s)-2-[[(2r)-2-amino-3-sulfanylpropanoyl]amino]-3-methylbutanoyl]amino]-3-(4-hydroxy-2,3-dimethylphenyl)propanoyl]amino]-4-methylsulfanylbutanoate Chemical compound SC[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(=O)N[C@@H](CCSC)C(=O)OC)CC1=CC=C(O)C(C)=C1C AGJSNMGHAVDLRQ-IWFBPKFRSA-N 0.000 description 1
- HKQKWZAMVUVBGL-UHFFFAOYSA-N methyl 2-[2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetate Chemical compound C=1C=CC=CC=1C1N(CC(=O)OC)CCOC1OCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 HKQKWZAMVUVBGL-UHFFFAOYSA-N 0.000 description 1
- KYLVAMSNNZMHSX-UHFFFAOYSA-N methyl 6-bromohexanoate Chemical compound COC(=O)CCCCCBr KYLVAMSNNZMHSX-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 230000027939 micturition Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000036457 multidrug resistance Effects 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- JMQYWICJKKYOSR-LEWJYISDSA-N n-(2-aminoethyl)-2-[(2s,3s)-2-[[3,5-bis(trifluoromethyl)phenyl]methoxy]-3-phenylmorpholin-4-yl]acetamide Chemical compound O([C@H]1OCCN([C@H]1C=1C=CC=CC=1)CC(=O)NCCN)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 JMQYWICJKKYOSR-LEWJYISDSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 230000003533 narcotic effect Effects 0.000 description 1
- 239000000025 natural resin Substances 0.000 description 1
- 208000004296 neuralgia Diseases 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 230000002981 neuropathic effect Effects 0.000 description 1
- 239000002858 neurotransmitter agent Substances 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229940127240 opiate Drugs 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- UUEVFMOUBSLVJW-UHFFFAOYSA-N oxo-[[1-[2-[2-[2-[4-(oxoazaniumylmethylidene)pyridin-1-yl]ethoxy]ethoxy]ethyl]pyridin-4-ylidene]methyl]azanium;dibromide Chemical compound [Br-].[Br-].C1=CC(=C[NH+]=O)C=CN1CCOCCOCCN1C=CC(=C[NH+]=O)C=C1 UUEVFMOUBSLVJW-UHFFFAOYSA-N 0.000 description 1
- 230000008058 pain sensation Effects 0.000 description 1
- 230000008533 pain sensitivity Effects 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- NXJCBFBQEVOTOW-UHFFFAOYSA-L palladium(2+);dihydroxide Chemical compound O[Pd]O NXJCBFBQEVOTOW-UHFFFAOYSA-L 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000004115 pentoxy group Chemical group [*]OC([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000008447 perception Effects 0.000 description 1
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 1
- 125000005460 perfluorocycloalkyl group Chemical group 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 210000001428 peripheral nervous system Anatomy 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L peroxydisulfate Chemical compound [O-]S(=O)(=O)OOS([O-])(=O)=O JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 150000005331 phenylglycines Chemical group 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- PEUGKEHLRUVPAN-UHFFFAOYSA-N piperidin-3-amine Chemical class NC1CCCNC1 PEUGKEHLRUVPAN-UHFFFAOYSA-N 0.000 description 1
- 229950010765 pivalate Drugs 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- CHKVPAROMQMJNQ-UHFFFAOYSA-M potassium bisulfate Chemical compound [K+].OS([O-])(=O)=O CHKVPAROMQMJNQ-UHFFFAOYSA-M 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000035935 pregnancy Effects 0.000 description 1
- 238000012746 preparative thin layer chromatography Methods 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 239000002599 prostaglandin synthase inhibitor Substances 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 150000003235 pyrrolidines Chemical class 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000029058 respiratory gaseous exchange Effects 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000001953 sensory effect Effects 0.000 description 1
- 230000013707 sensory perception of sound Effects 0.000 description 1
- 230000009209 sensory transmission Effects 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 230000035943 smell Effects 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 210000003594 spinal ganglia Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 230000010473 stable expression Effects 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000008174 sterile solution Substances 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000003890 substance P antagonist Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 150000003457 sulfones Chemical class 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 210000000331 sympathetic ganglia Anatomy 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 210000001258 synovial membrane Anatomy 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000002462 tachykinin receptor antagonist Substances 0.000 description 1
- LFKDJXLFVYVEFG-UHFFFAOYSA-N tert-butyl carbamate Chemical group CC(C)(C)OC(N)=O LFKDJXLFVYVEFG-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000005958 tetrahydrothienyl group Chemical group 0.000 description 1
- 125000004299 tetrazol-5-yl group Chemical group [H]N1N=NC(*)=N1 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- DUYAAUVXQSMXQP-UHFFFAOYSA-M thioacetate Chemical compound CC([S-])=O DUYAAUVXQSMXQP-UHFFFAOYSA-M 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-M toluene-4-sulfonate Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-M 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- JLTRXTDYQLMHGR-UHFFFAOYSA-N trimethylaluminium Chemical compound C[Al](C)C JLTRXTDYQLMHGR-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 125000000430 tryptophan group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C2=C([H])C([H])=C([H])C([H])=C12 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 230000002455 vasospastic effect Effects 0.000 description 1
- 208000027491 vestibular disease Diseases 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
- 150000003738 xylenes Chemical class 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/28—1,4-Oxazines; Hydrogenated 1,4-oxazines
- C07D265/30—1,4-Oxazines; Hydrogenated 1,4-oxazines not condensed with other rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/28—1,4-Oxazines; Hydrogenated 1,4-oxazines
- C07D265/30—1,4-Oxazines; Hydrogenated 1,4-oxazines not condensed with other rings
- C07D265/32—1,4-Oxazines; Hydrogenated 1,4-oxazines not condensed with other rings with oxygen atoms directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D279/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one sulfur atom as the only ring hetero atoms
- C07D279/10—1,4-Thiazines; Hydrogenated 1,4-thiazines
- C07D279/12—1,4-Thiazines; Hydrogenated 1,4-thiazines not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Pulmonology (AREA)
- Pain & Pain Management (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Vascular Medicine (AREA)
- Urology & Nephrology (AREA)
- Rheumatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Описываются новые замещенные гетероциклы общей формулы I, где значения R1-R5, Х указаны в п.1 формулы изобретения, которые являются антагонистами тахикининового рецептора и эффективны при лечении воспалительных заболеваний, болей или мигрени и астмы. Кроме того, некоторые из этих веществ являются агентами, блокирующими кальциевый канал, и являются полезными при лечении сердечно-сосудистых нарушений, таких, как ангина, гипертония и ишемия. Описывается также Фармацевтическая композиция на основе соединений формулы I и способ для блокады рецепторов нейрокинина-1 у млекопитающих. 3 с. и 6 з.п. ф-лы, 1 табл.
Description
Эта заявка является частичным продолжением совместно поданной заявки, порядковый N 07/971448, зарегистрированной 4 ноября 1992, которая является частичным продолжением совместно поданной заявки, порядковый N 07/905976, поданной 29 июня 1992.
Это изобретение относится к новым веществам, представленным структурной формулой I:
в которой R1, R2, R3, R4, R5 и X определены в последующем.
в которой R1, R2, R3, R4, R5 и X определены в последующем.
Это изобретение также связано с фармацевтическими рецептурами, которые включают эти новые вещества в качестве активных компонентов, и с применением новых веществ и их рецептур при лечении определенных нарушений.
Вещества этого изобретения являются антагонистами тахикининового рецептора и являются эффективными при лечении воспалительных заболеваний, болей или мигрени и астмы.
Кроме того, некоторые из этих веществ являются агентами, блокирующими кальциевый канал, и являются полезными при лечении сердечно-сосудистых нарушений, таких как ангина, гипертония и ишемия.
Фон изобретения
Исторически обезболивание в центральной нервной системе было достигнуто с помощью опиатов и их аналогов, которые являются наркотическими веществами, и периферически, с помощью ингибиторов циклооксигеназы, которые обладают побочным действием на желудок. Антагонисты вещества P могут вызвать обезболивание как центральной, так и периферической нервной системы. Кроме того, антагонисты вещества P являются ингибиторами нейрогенного воспаления.
Исторически обезболивание в центральной нервной системе было достигнуто с помощью опиатов и их аналогов, которые являются наркотическими веществами, и периферически, с помощью ингибиторов циклооксигеназы, которые обладают побочным действием на желудок. Антагонисты вещества P могут вызвать обезболивание как центральной, так и периферической нервной системы. Кроме того, антагонисты вещества P являются ингибиторами нейрогенного воспаления.
Нейропептидные рецепторы для вещества P (нейрокинин-1, NK-1) широко распределены по всей нервной системе млекопитающих (особенно, в мозговых и спинальных нервных узлах), в циркуляторной системе и периферических тканях (особенно в двенадцатиперстной кишке и тощей кишке) и вовлечены в регулирование ряда разнообразных биологических процессов. Последние включают восприятие обоняния, видения, слуха и боли, контроль движения, желудочную подвижность, расширение сосудов, слюновыделение и мочеиспускание (Б.Пернов, Pharmacol. Rev. 1983. т. 35, с.85 - 141). Подтипы рецепторов NK1 и NK2 вовлечены в синаптическую трансмиссию (Ланеувилль и др., Life Sci., т.42, с. 1295-1305, 1988).
Рецептор для вещества P является членом сверхсемейства G протеин-спаренных рецепторов. Это сверхсемейство является весьма разнообразной группой рецепторов в терминах активирующих лигандов и биологических функций. В дополнение к тахикининовым рецепторам, это рецепторное сверхсемейство включает опсины, адрэнергические рецепторы, мускариновые рецепторы, допаминовые рецепторы, серотониновые рецепторы, тироид-стимулирующий гормонный рецептор, лютеинизирующий гормон-хориогонадотропный гормонный рецептор, продукт онкогена ras, рецепторы дрожжевого фактора скрещивания, рецептор Dictyostellium cAMP и рецепторы для других гормонов и нейротрансмиттеров (смотри А.Д.Хершей и др., J.Biol.Chem., 1991, т.226, с.4366-4373).
Вещество P (также называемое здесь как "SP") представляет собой ундекапептид естественного происхождения, принадлежащий к тахикининовому семейству пептидов, причем последние называют таким образом из-за их быстрого сокращающего действия на гладкую мышечную ткань вне сосудов. Тахикинины отличаются сохраненной карбоксил- терминальной последовательностью Phe- X -Gly - Leu - Met - NH2.
В дополнение к SP, известные тахикинины млекопитающего включают нейрокинин A и нейрокинин B. В современной номенклатуре рецепторы для SP, нейрокинина A и нейрокинина B обозначаются как NK-1, NK-2 и NK-3, соответственно.
Более конкретно, вещество P представляет собой фармакологически активный нейропептид, который продуцируется у млекопитающих и обладает характерной аминокислотной последовательностью, которая показана ниже:
Arg - Pro - Lys - Pro - Gln - Gln - Phe - Phe - Gly - Leu - Met - NH2 (Чанг и др., Nature New Biol., т.232, с. 86, 1971; Д.Ф.Вебер и др., патент США N 4680 283).
Arg - Pro - Lys - Pro - Gln - Gln - Phe - Phe - Gly - Leu - Met - NH2 (Чанг и др., Nature New Biol., т.232, с. 86, 1971; Д.Ф.Вебер и др., патент США N 4680 283).
Нейрокинин A обладает следующей аминокислотной последовательностью:
His - Lys - Thr - Asp - Ser - Phe - Val - Gly - Leu - Met - NH2.
His - Lys - Thr - Asp - Ser - Phe - Val - Gly - Leu - Met - NH2.
Нейрокинин B обладает следующей аминокислотной последовательностью: Asp - Met - His - Asp - Phe - Phe - Val - Gly - Leu - Met - NH2.
Вещество P действует как сосудорасширяющий агент, депрессант, стимулирующий слюновыделение и продуцирующий повышенную капиллярную проницаемость. Оно также способно продуцировать как обезболивание, так и сверхальгезию у млекопитающих, в зависимости от дозы и болевой восприимчивости животного (смотри Р.С.А. Фредериксон и др., Science, т. 199, с. 1359, 1978, П. Оеме и др. , Science, т. 208, с.305, 1980) и играет роль в сенсорной трансмиссии и восприятии боли (Т.М. Джесселл, Advan, Biochem. Psychopharmacol., т. 28, с. 189, 1981). Например, полагают, что вещество P, наряду с другими веществами, вовлечено в нейротрансмиссию болевых ощущений [доклад Отсуки и др., "Роль вещества P в качестве сенсорного трансмиттера в спинном мозге и симпатетических ганглиях" в Симпозиуме Фонда Циба 91, 1982. Вещество P в Нервной Системе, с. 13-34 (опубликовано фирмой Питман) и статья Отсуки и Янагисавы, "Действительно ли вещество P действует как болевой трансмиттер?" TIPS (декабрь 1987) т. 8, с. 506-510]. В частности, было показано, что вещество P принимает участие в передаче боли при мигрени (смотри Б.Е.Б. Сандберг и др., J. of Medicinal Chemistry, 25, c. 1009, 1982) и при артрите (Левин и др. Science, 1984, т. 226, с.547-549). Эти пептиды также были вовлечены в желудочно-кишечные нарушения и заболевания желудочно-кишечного тракта, такие как воспалительное заболевание кишечника, язвенный колит и болезнь Крона и др. (смотри Мантых и др., Neuroscience, т.25, N 3, с. 817 - 37, 1988 и Д. Реголи в сборнике "Тенденции в кластерной головной боли", ред. Ф.Сикутери и др., издательство "Эльзевир Сайентифик Паблишерз, Амстердам, 1987, с. 85-95).
Кроме того, предполагалось, что существует нейрогенный механизм для артрита, в котором вещество P может играть роль (Кидд и др., "Нейрогенный механизм для симметричного артрита" в Lancet, 11 ноября 1989 и Гронблад и др., "Нейропептиды в синовиуме пациентов с ревматоидным артритом и остеоартритом" В J.Rheumatol., 1988, т. 15, N 12, с.1870-10). Поэтому полагают, что вещество P вовлечено в воспалительную реакцию при таких заболеваниях, как ревматоидный артрит и остеоартрит (О.Бирн и др., в Arthritis & Rheumatism, 1990, т. 33, с.1023-8). Другие болезненные области, при которых тахикининовые антагонисты считаются полезными, являются аллергические состояния (Хамелет и др. , Can.J.Pharmacol. Physiol., 1988, т. 66, с. 1361 - 7), иммунорегуляция (Лотц и др., Science, 1988, т.241, с. 1218 - 21, Кимбалл и др., J. Immunol., 1988, т.141, N 10, с.3564-9 и А.Перианин и др., Biochem. Biophys.Res.Commun. , т. 161, с. 520, 1989), расширение сосудов, спазм бронхов, рефлексный или нейрональный контроль внутренностей (Мантых и др., PNAS, 1988, т.85, с. 3235-9) и, возможно, прекращение или замедление нейродегенеративных изменений, передаваемых β--амилоидом (Янкнер и др., Science, 1990, т.250, с.279-82), при старческом слабоумии типа Альцхаймера, болезни Альцхаймера и синдроме Дауна. Вещество P также может играть роль в демиелинизационных заболеваниях, таких как множественный склероз [Дж.Лубер-Народ и др., стендовый доклад, представленный на 18-й Конгресс C.I.N.P, 28 июня - 2 июля 1992, в печати] . Антагонисты, селективные для рецептора нейрокинина - 1 (NK-1) или нейрокинина - 2 (NK-2), могут быть полезны при лечении астматического заболевания (Фроссард и др., Life Sci., т.49, с. 1941 - 1953, 1991; Адвениер и др. , Biochem. Biophys. Res.Commun., т.184, N 3, с. 1418-24, 1992).
Антагонисты вещества P могут быть полезными при перенесении нейрогенного выделения слизи в дыхательных путях млекопитающего и при симптоматическом облегчении при заболеваниях, характеризующихся выделением слизи, в частности, в циститном фиброзе [С.Рамнарин и др., абстракт, представленный на Международную конференцию 1993 ALA/ATS, 16-19 мая 1993, будет опубликован в журнале Am.Rev. of Respiratory Dis., май 1993, в печати].
В недавнем прошлом были предприняты некоторые попытки предоставления пептидно-подобных веществ, которые являются антагонистами для вещества P и других тахикининовых пептидов, для того, чтобы более эффективно излечивать различные нарушения и заболевания, перечисленные выше. Смотрите, например, заявки на Европейские патенты (публикации ЕРО NN 0347 802, 0401 177 и 0412 452), в которых раскрыты различные пептиды в качестве антагонистов нейрокинина А. Аналогично, в публикации Европатента N 0336230 описаны гептапептиды, которые являются антагонистами вещества P, полезными при лечении астмы. В патенте США N 4680 283 фирмы Мерк также раскрыты пептидные аналоги вещества P.
Определенные ингибиторы тахикинина были описаны в патенте США N 4501 733 посредством замещения остатков в последовательности вещества P на триптофановые остатки.
Дополнительный класс антагонистов тахикининового рецептора, включающий мономерное или димерное звено гекса- или гептапептида в линейной или циклической форме, описан в патенте Великобритании A - 2216 529.
Пептидноподобная природа таких веществ делает их слишком лабильными с точки зрения обмена веществ, чтобы они могли служить в качестве практических терапевтических агентов при лечении заболеваний.
Непептидные антагонисты настоящего изобретения, с другой стороны, не обладают этим недостатком, поскольку можно ожидать, что они будут более стабильными с точки зрения обмена веществ, чем рассмотренные ранее агенты.
В этой области техники известно, что баклофен [ (аминоэтил)-4-хлорбензолпропановая кислота] в центральной нервной системе эффективно блокирует возбуждающую активность вещества P, но, поскольку во многих областях возбуждающие отклики на другие вещества, такие как ацетилхлолин и глутамат, также ингибируются, баклофен не рассматривался как специфический антагонист вещества P. В патентных заявках фирмы Пфайзер WIPO (публикации Пи-Си-Ти WO 90/05525, WO 90/05729, WO 91/18899, WO 92/12151 и Wo 92/12152) и публикациях (Science, т. 251, с. 435-437, 1991; Science, т.251, с. 437-439, 1991; J. Med, Chem., т. 35, с. 2591-2600, 1992) раскрыты производные 2-арилметил-3-замещенного аминохинуклидина, которые описаны как эффективные антагонисты вещества P для лечения желудочно-кишечных нарушений, нарушений центральной нервной системы, воспалительных заболеваний и боли или мигрени. В заявке на Европатент фирмы Глаксо (публикация EPO N 0360390) раскрыты различные спиролактам-замещенные аминокислоты и пептиды, которые являются антагонистами или агонистами вещества P. В патентной заявке фирмы Пфайзер WIPO (публикация Пи-Си-Ти WO 92/06079) описаны конденсированно-циклические аналоги азотсодержащих неароматических гетероциклов, как полезные для лечения заболеваний, передаваемых посредством избытка вещества P. В патентной заявке фирмы Пфайзер WIPO (публикации Пи-Си-Ти WO 92/15585) раскрыты производные 1-азабицикло[3,2,2]нонан-3-амина как антагонисты вещества P. В публикации Санофи (Life Sci., т. 50, PL 101-6, 1992) описана производная 4-фенилиперидина как антагониста рецептора нейрокинина A (NK2).
Хаусон и др. (Biorg. & Med. Chem. Lett, т. 2, N 6, с. 559 - 64, 1992) описали определенные 3-амино-3-оксихинуклидиновые соединения и их связывание с рецепторами вещества P. В публикации EPO 0499313 раскрыты определенные 3-гидрокси- и 3-тио-азабициклические соединения в качестве антагонистов тахикинина. В патенте США N 3506673 описаны определенные 3-гидроксихинуклидиновые соединения в качестве стимуляторов центральной нервной системы. В патентной заявке фирмы Пфайзер (EPO публикация 0436334) раскрыты определенные 3-аминопиперидиновые соединения в качестве антагонистов вещества P. В патенте США N 5064838 раскрыты определенные 1,4-дизамещенные пиперидинильные соединения в качестве анальгетиков. В публикации Пи-Си-ТИ N WO 92/12128 раскрыты определенные пиперидиновые и пирролидиновые соединения в качестве анальгетиков. Пейронел и др. (Biorg & Med. Chem. Lett., т. 2, N 1, с. 37-40, 1992) описали пирролидиновое соединение с конденсированными кольцами в качестве антагониста вещества P. В публикации EPO N 0360390 раскрыты определенные спиролактамовые производные в качестве антагонистов вещества P. В патенте США N 4804661 раскрыты определенные пиперазиновые соединения в качестве анальгетиков. В патенте США N 4943578 раскрыты определенные пиперазиновые соединения, эффективные при лечении боли. В публикации Пи-Си-Ти N WO 92/01679 раскрыты определенные 1,4-дизамещенные пиперазины, полезные при лечении мозговых нарушений, в которые вовлечен допаминэргический дефицит.
Подробное описание изобретения
Новые вещества этого изобретения представлены структурной формулой I:
или их фармацевтически приемлемыми солями, в которой:
R1 выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 независимо выбирают из:
I) атома водорода
II) C1-C6-алкила,
III) гидрокси- C1-C6-алкила и
IV) фенила,
i) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
n) гетероцикла, в котором гетероцикл выбирают из группы, состоящей из:
A) бензимидазолила,
B) бензофуранила,
C) бензотиофенила,
D) бензооксазолила,
E) фуранила,
F) имидазолила,
G) индолила,
H) изоксазолила,
I) изотиазолила,
J) оксадиазолила,
K) оксазолила,
L) пиразинила,
M) пиразолила,
N) пиридила,
O) пиримидила,
P) пирролила,
Q) хинолила,
R) тетразолила,
S) тиадизолила,
T) тиазолила,
U) тиенила,
V) триазолила,
W) азетидинила,
X) 1,4-диоксанила,
Y) гексагидроазепинила,
Z) оксанила,
AA) пиперазинила,
AB) пиперидинила,
AC) пирролидинила,
AD) тетрагидрофуранила и
AE) тетрагидротиенила,
и в котором гетероцикл является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила, незамещенного или замещенного атомом галогена, трифторметилом, метокси-группой или фенилом,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) гидрокси-,
V) тиоксо-,
VI) группы - SR9, в которой R9 такой, как определено выше,
VII) атома галогена,
VIII) циано-,
IX) фенила,
X) трифторметила,
XI) группы - (CH2)m - NR9R10, в которой m представляет собой 0, 1 или 2 и R9 и R10 такие, как определено выше,
XII) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
XIII) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
XIV) группы - CO2R9, в которой R9 такой, как определено выше,
XV) группы - (CH2)m - OR9, в которой m и R9 такие, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
k) гетероцикла, в котором гетероцикл является таким, как определено выше,
4) C2-C6 - алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
R2 и R3 выбирают независимо из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6 - алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) C2-C6 - алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
и группы R1 и R2 могут быть объединены вместе, образуя гетероциклическое кольцо, выбранное из группы, состоящей из:
a) пирролидинила,
b) пиперидинила,
c) пирролила,
d) пиридинила,
e) имидазолила,
f) оксазолила и
g) диазолила,
и в котором гетероциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) группы -NR9R10, в которой R9 и R10 такие, как определено выше,
V) атома галогена и
VI) трифторметила,
и группы R2 и R3 могут быть объединены вместе, образуя карбоциклическое кольцо, выбранное из группы, состоящей из:
a) циклопентила,
b) циклогексила,
c) фенила,
и в котором карбоциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
IV) атома галогена и
V) трифторметила,
и группы R2 и R3 могут быть объединены вместе, образуя гетероциклическое кольцо, выбранное из группы, состоящей из:
a) пирролидинила,
b) пиперидинила,
c) пирролила,
d) пиридинила,
e) имидазолила,
f) фуранила,
g) оксазолила,
h) тиенила и
i) тиазолила,
и в котором гетероциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
V) атома галогена и
VI) трифторметила;
X выбирают из группы, состоящей из: -O-, -S-, -SO- и SO2;
R4 выбирают из группы, состоящей из:
1)
,
2) -Y- C1-C8-алкила, в котором алкил является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) -Y-C2-C6-алкенила, в котором алкенил является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) -O(CO) - фенила, где фенил является незамещенным или замещенным одним или несколькими радикалами R6, R7 и R8; R5 выбирают из группы, состоящей из:
1) фенила, незамещенного или замещенного одним или несколькими радикалами R11, R12 и R13,
2) C1-C8-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) C2-C6-алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
f) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) гетероцикл, в котором гетероцикл такой, как определено выше;
R6, R7, R8 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы -(CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
6) атома галогена,
7) циано-,
8) нитро-,
9) трифторметила,
10) -SR14, в которой R14 является атомом водорода или C1-C6-алкилом,
11) -SOR14, в которой R14 такой, как определено выше,
12) -SO2R14, в которой R14 такой, как определено выше,
13) -NR9COR10, в которой R9 и R10 такие, как определено выше,
14) группы -CONR9COR10, в которой R9 и R10 такие, как определено выше,
15) группы -NR9R10, в которой R9 и R10 такие, как определено выше,
16) группы -NR9CO2R10, в которой R9 и R10 такие, как определено выше,
17) гидрокси-,
18) C1-C6-алкокси-,
19) - COR9, в которой R9 такой, как определено выше,
20) - CO2R9, в которой R9 такой, как определено выше;
R11, R12 и R13 независимо выбирают из определений радикалов R6, R7 и R8;
Y выбирают из группы, состоящей из: простой связи, -O-, -S-, -CO-, -CH2-, -CHR15- и -CR15R16-, в которой R15 и R16 независимо выбирают из группы, состоящей из:
a) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
I) гидрокси-группы,
II) оксо-группы,
III) C1-C6-алкокси-,
IV) фенил-C1-C3-алкокси-,
V) фенила,
VI) циано-,
VII) атома галогена,
VIII) группы NR9R10, в которой R9 и R10 такие, как определено выше,
IX) группы NR9COR10, в которой R9 и R10 такие, как определено выше,
X) группы NR9CO2R10, в которой R9 и R10 такие, как определено выше,
XI) группы CONR9R10, в которой R9 и R10 такие, как определено выше,
XII) - COR9, в которой R9 такой, как определено выше,
XIII) - CO2R9, в которой R9 такой, как определено выше;
b) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
I) гидрокси-группы,
II) C1-C6-алкокси-,
III) C1-C6-алкила,
IV) C2-C5-алкенила,
V) атома галогена,
VI) циано-,
VII) нитро-,
VIII) трифторметила,
IX) - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
X) - NR9COR10, в которой R9 и R10 такие, как определено выше,
XI) - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
XII) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
XIII) - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
XIV) - COR9, в которой R9 такой, как определено выше,
XV) - CO2R9, в которой R9 такой, как определено выше,
Z выбирают из:
1) атома водорода,
2) C1-C4-алкила и
3) гидрокси-группы, при условии, что если Y представляет собой -O-, то Z отличается от гидрокси-группы, или если Y представляет собой -CHR15-, тогда Z и R15 могут быть объединены вместе, образуя двойную связь.
Новые вещества этого изобретения представлены структурной формулой I:
или их фармацевтически приемлемыми солями, в которой:
R1 выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 независимо выбирают из:
I) атома водорода
II) C1-C6-алкила,
III) гидрокси- C1-C6-алкила и
IV) фенила,
i) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
n) гетероцикла, в котором гетероцикл выбирают из группы, состоящей из:
A) бензимидазолила,
B) бензофуранила,
C) бензотиофенила,
D) бензооксазолила,
E) фуранила,
F) имидазолила,
G) индолила,
H) изоксазолила,
I) изотиазолила,
J) оксадиазолила,
K) оксазолила,
L) пиразинила,
M) пиразолила,
N) пиридила,
O) пиримидила,
P) пирролила,
Q) хинолила,
R) тетразолила,
S) тиадизолила,
T) тиазолила,
U) тиенила,
V) триазолила,
W) азетидинила,
X) 1,4-диоксанила,
Y) гексагидроазепинила,
Z) оксанила,
AA) пиперазинила,
AB) пиперидинила,
AC) пирролидинила,
AD) тетрагидрофуранила и
AE) тетрагидротиенила,
и в котором гетероцикл является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила, незамещенного или замещенного атомом галогена, трифторметилом, метокси-группой или фенилом,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) гидрокси-,
V) тиоксо-,
VI) группы - SR9, в которой R9 такой, как определено выше,
VII) атома галогена,
VIII) циано-,
IX) фенила,
X) трифторметила,
XI) группы - (CH2)m - NR9R10, в которой m представляет собой 0, 1 или 2 и R9 и R10 такие, как определено выше,
XII) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
XIII) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
XIV) группы - CO2R9, в которой R9 такой, как определено выше,
XV) группы - (CH2)m - OR9, в которой m и R9 такие, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
k) гетероцикла, в котором гетероцикл является таким, как определено выше,
4) C2-C6 - алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
R2 и R3 выбирают независимо из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6 - алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) C2-C6 - алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
и группы R1 и R2 могут быть объединены вместе, образуя гетероциклическое кольцо, выбранное из группы, состоящей из:
a) пирролидинила,
b) пиперидинила,
c) пирролила,
d) пиридинила,
e) имидазолила,
f) оксазолила и
g) диазолила,
и в котором гетероциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) группы -NR9R10, в которой R9 и R10 такие, как определено выше,
V) атома галогена и
VI) трифторметила,
и группы R2 и R3 могут быть объединены вместе, образуя карбоциклическое кольцо, выбранное из группы, состоящей из:
a) циклопентила,
b) циклогексила,
c) фенила,
и в котором карбоциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
IV) атома галогена и
V) трифторметила,
и группы R2 и R3 могут быть объединены вместе, образуя гетероциклическое кольцо, выбранное из группы, состоящей из:
a) пирролидинила,
b) пиперидинила,
c) пирролила,
d) пиридинила,
e) имидазолила,
f) фуранила,
g) оксазолила,
h) тиенила и
i) тиазолила,
и в котором гетероциклическое кольцо является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
V) атома галогена и
VI) трифторметила;
X выбирают из группы, состоящей из: -O-, -S-, -SO- и SO2;
R4 выбирают из группы, состоящей из:
1)
,
2) -Y- C1-C8-алкила, в котором алкил является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) -Y-C2-C6-алкенила, в котором алкенил является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) -O(CO) - фенила, где фенил является незамещенным или замещенным одним или несколькими радикалами R6, R7 и R8; R5 выбирают из группы, состоящей из:
1) фенила, незамещенного или замещенного одним или несколькими радикалами R11, R12 и R13,
2) C1-C8-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
k) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
l) группы - COR9, в которой R9 такой, как определено выше,
m) группы - CO2R9, в которой R9 такой, как определено выше,
3) C2-C6-алкенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) C2-C6-алкинила,
5) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) C1-C6-алкокси-,
c) C1-C6-алкила,
d) C2-C5-алкенила,
f) фенила,
f) циано-,
g) атома галогена,
h) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - COR9, в которой R9 такой, как определено выше,
j) группы - CO2R9, в которой R9 такой, как определено выше,
4) гетероцикл, в котором гетероцикл такой, как определено выше;
R6, R7, R8 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гидрокси-группы,
b) оксо-группы,
c) C1-C6-алкокси-,
d) фенил-C1-C3-алкокси-,
e) фенила,
f) циано-,
g) атома галогена,
h) группы - NR9R10, в которой R9 и R10 такие, как определено выше,
i) группы - NR9COR10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
e) атома галогена,
f) циано-,
g) нитро-,
h) трифторметила,
i) группы -(CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
j) группы - NR9COR10, в которой R9 и R10 такие, как определено выше,
k) группы - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
l) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
m) группы - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
n) группы - COR9, в которой R9 такой, как определено выше,
o) группы - CO2R9, в которой R9 такой, как определено выше,
6) атома галогена,
7) циано-,
8) нитро-,
9) трифторметила,
10) -SR14, в которой R14 является атомом водорода или C1-C6-алкилом,
11) -SOR14, в которой R14 такой, как определено выше,
12) -SO2R14, в которой R14 такой, как определено выше,
13) -NR9COR10, в которой R9 и R10 такие, как определено выше,
14) группы -CONR9COR10, в которой R9 и R10 такие, как определено выше,
15) группы -NR9R10, в которой R9 и R10 такие, как определено выше,
16) группы -NR9CO2R10, в которой R9 и R10 такие, как определено выше,
17) гидрокси-,
18) C1-C6-алкокси-,
19) - COR9, в которой R9 такой, как определено выше,
20) - CO2R9, в которой R9 такой, как определено выше;
R11, R12 и R13 независимо выбирают из определений радикалов R6, R7 и R8;
Y выбирают из группы, состоящей из: простой связи, -O-, -S-, -CO-, -CH2-, -CHR15- и -CR15R16-, в которой R15 и R16 независимо выбирают из группы, состоящей из:
a) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
I) гидрокси-группы,
II) оксо-группы,
III) C1-C6-алкокси-,
IV) фенил-C1-C3-алкокси-,
V) фенила,
VI) циано-,
VII) атома галогена,
VIII) группы NR9R10, в которой R9 и R10 такие, как определено выше,
IX) группы NR9COR10, в которой R9 и R10 такие, как определено выше,
X) группы NR9CO2R10, в которой R9 и R10 такие, как определено выше,
XI) группы CONR9R10, в которой R9 и R10 такие, как определено выше,
XII) - COR9, в которой R9 такой, как определено выше,
XIII) - CO2R9, в которой R9 такой, как определено выше;
b) фенила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
I) гидрокси-группы,
II) C1-C6-алкокси-,
III) C1-C6-алкила,
IV) C2-C5-алкенила,
V) атома галогена,
VI) циано-,
VII) нитро-,
VIII) трифторметила,
IX) - (CH2)m - NR9R10, в которой m, R9 и R10 такие, как определено выше,
X) - NR9COR10, в которой R9 и R10 такие, как определено выше,
XI) - NR9CO2R10, в которой R9 и R10 такие, как определено выше,
XII) группы - CONR9R10, в которой R9 и R10 такие, как определено выше,
XIII) - CO2NR9R10, в которой R9 и R10 такие, как определено выше,
XIV) - COR9, в которой R9 такой, как определено выше,
XV) - CO2R9, в которой R9 такой, как определено выше,
Z выбирают из:
1) атома водорода,
2) C1-C4-алкила и
3) гидрокси-группы, при условии, что если Y представляет собой -O-, то Z отличается от гидрокси-группы, или если Y представляет собой -CHR15-, тогда Z и R15 могут быть объединены вместе, образуя двойную связь.
Вещества настоящего изобретения имеют асимметрические центры, и это изобретение включает все оптические изомеры и их смеси.
В дополнение, вещества с углерод-углеродными двойными связями могут существовать в Z- и E-формах, причем все изомерные формы этих соединений включены в настоящее изобретение.
Когда любая переменная (например, алкил, арил, R6 и R7, R8, R11, R12, R13 и др.) встречается более одного раза в любой переменной или в формуле I, ее определение в каждом случае является независимым от ее определения в каждом другом случае.
Используемый здесь термин "алкил" включает те алкильные группы с указанным числом атомов углерода, имеющие либо линейную, разветвленную либо циклическую конфигурацию. Примеры "алкила" включают метил, этил, пропил, изопропил, бутил, изо-, втор- и трет-бутил, пентил, гексил, гептил, 3-этилбутил, циклопропил, циклобутил, циклопентил, циклогексил, цилкогептил, норборнил и т.п. Термин "алкокси" представляет алкильную группу с указанным числом атомов углерода, присоединенную через кислородный мостик, такую как метокси, этокси, пропокси, бутокси и пентокси. "Алкенил" подразумевает включение углеводородных цепочек с указанным числом атомов углерода, имеющих либо линейную, разветвленную либо циклическую конфигурацию и по меньшей мере одну ненасыщенность, которая может находиться в любом месте вдоль цепочки, такой как этенил, пропенил, бутенил, пентенил, диметилпентенил и т.п., и включает E- и Z-формы, где они применимы. Используемые здесь термины "атом галогена" или "галоидо" означают фторо-, хлоро-, бромо- и иодо.
Термин "арил" означает фенил или нафтил или незамещенный или замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из галоидо-, C1-C4-алкила, C1-C4-алкокси-, нитро-, трифторметила, C1-C4-алкилтио-, гидроксигруппы, -NR6R6-, -CO2R6, C1-C4-перфторалкила, C3-C6-перфторциклоалкила и тетразол-5-ила.
Термин "гетероарил" означает незамещенный, монозамещенный или дизамещенный пяти- или шестичленный ароматический гетероцикл, включающий от 1 до 3 гетероатомов, выбранных из группы кислорода, азота и серы, и в которых заместители являются членами, выбранными из группы, состоящей из -OH, -SH, C1-C4-алкила, C1-C4-алкокси, нитро-, галоидо-, трифторметила, -N(R9R10)-CO2R9 и конденсированной бензо-группы.
Как могут понять специалисты в этой области техники, фармацевтически приемлемые соли включают, но не ограничиваются солями с неорганическими кислотами, такими как гидрохлорид, сульфат, фосфат, дифосфат, гидробромид и нитрат, или солями с органическими кислотами, такими как малат, малеат, фумарат, тартрат, сукцинат, цитрат, ацетат, лактат, метансульфонат, пара-толуолсульфонат, 2-гидроэтилсульфонат, памоат, салицилат и стеарат. Аналогично фармацевтически приемлемые катионы включают, но не ограничиваются натрием, калием, кальцием, алюминием, литием и аммонием.
В соединениях формулы I является предпочтительным, чтобы: R1 был выбран из группы, состоящей из:
1) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гетероцикла, в котором гетероцикл выбирают из группы, состоящей из:
A) бензимидазолила,
B) имидазолила,
C) изоксазолила,
D) изотиазолила,
E) оксадиазолила,
F) пиразинила,
G) пиразолила,
H) пиридила,
I) пирролила,
J) тетразолила,
K) тиадизолила,
L) триазолила и
M) пиперидинила,
и в котором гетероцикл является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила, незамещенного или замещенного атомом галогена, трифторметилом, метокси-группой или фенилом,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) тиоксо-,
V) циано-,
VI группы -SCH3,
VII) фенила,
VIII) гидрокси-,
IX) трифторметила,
X) группы -(CH2)m-NR9R10, в которой m представляет собой 0, 1 или 2 и в которой R9 и R10 независимо выбирают из: атома водорода, C1-C6-алкила, гидро-C1-C6-алкила и фенила,
XI) группы -NR9COR10, в которой R9 и R10 такие, как определено выше,
XII) группы -CONR9R10, в которой R9 и R10 такие, как определено выше,
R2 и R3 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила,
3) C2-C6-алкенила и
4) фенила;
X представляет собой -O-;
R4 представляет собой:
,
R5 является фенилом, незамещенным или замещенным галогеном;
R6, R7 и R8 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила,
3) атома галогена и
4) трифторметила;
Y представляет собой -O-; и
Z представляет собой атом водорода или C1-C4-алкил.
1) C1-C6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из:
a) гетероцикла, в котором гетероцикл выбирают из группы, состоящей из:
A) бензимидазолила,
B) имидазолила,
C) изоксазолила,
D) изотиазолила,
E) оксадиазолила,
F) пиразинила,
G) пиразолила,
H) пиридила,
I) пирролила,
J) тетразолила,
K) тиадизолила,
L) триазолила и
M) пиперидинила,
и в котором гетероцикл является незамещенным или замещенным одним или несколькими заместителями, выбранными из:
I) C1-C6-алкила, незамещенного или замещенного атомом галогена, трифторметилом, метокси-группой или фенилом,
II) C1-C6-алкокси-,
III) оксо-группы,
IV) тиоксо-,
V) циано-,
VI группы -SCH3,
VII) фенила,
VIII) гидрокси-,
IX) трифторметила,
X) группы -(CH2)m-NR9R10, в которой m представляет собой 0, 1 или 2 и в которой R9 и R10 независимо выбирают из: атома водорода, C1-C6-алкила, гидро-C1-C6-алкила и фенила,
XI) группы -NR9COR10, в которой R9 и R10 такие, как определено выше,
XII) группы -CONR9R10, в которой R9 и R10 такие, как определено выше,
R2 и R3 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила,
3) C2-C6-алкенила и
4) фенила;
X представляет собой -O-;
R4 представляет собой:
,
R5 является фенилом, незамещенным или замещенным галогеном;
R6, R7 и R8 независимо выбирают из группы, состоящей из:
1) атома водорода,
2) C1-C6-алкила,
3) атома галогена и
4) трифторметила;
Y представляет собой -O-; и
Z представляет собой атом водорода или C1-C4-алкил.
Вариантом воплощения новых веществ этого изобретения
является то вещество, в котором X представляет собой -O-, R4 является группой -YCHZ-фенил и R5 является фенилом структурной формулы:
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
является то вещество, в котором X представляет собой -O-, R4 является группой -YCHZ-фенил и R5 является фенилом структурной формулы:
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
Другим вариантом воплощения новых веществ этого изобретения является то вещество, в котором X представляет собой -S-, R4 является группой -YCHZ-фенил и R5 является фенилом структурной формулы:
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
Другим вариантом воплощения новых веществ этого изобретения является то вещество, в котором X представляет собой -SO-, R4 является группой -YCHZ-фенил и R5 является фенилом структурной формулы:
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12, R13 и Z такие, как определено выше.
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12, R13 и Z такие, как определено выше.
Другим вариантом воплощения новых веществ этого изобретения является то вещество, в котором X представляет собой -SO2-, R4 является группой -YCHZ-фенил и R5 является фенилом структурной формулы:
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
или его фармацевтически приемлемая соль, в котором R1, R2, R3, R6, R7, R8, R11, R12 и R13 и Z такие, как определено выше.
В веществах настоящего изобретения предпочтительным вариантом воплощения является то вещество, в котором R1 выбирают из следующей группы заместителей:
β2-
Конкретные вещества в пределах объема настоящего изобретения включюат:
1) (+/-)2-(3,5-бис(трифторметил)бензилокси)-3-фенилморфолин;
2) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3R)-фенил-(6R)- метилморфолин;
3) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3S)-фенил-(6R)- метилморфолин;
4) (+/-)-2-(3,5-бис(трифторметил)бензилокси)-3-фенил-4- метилкарбоксамидоморфолин;
5) (+/-)-2-(3,5-бис(трифторметил)бензилокси)-3-фенил-4- метоксикарбонилметилморфолин;
6) 2-(2-(3,5-бис(трифторметил)фенил)этенил)-3-фенил-5- оксоморфолин;
7) 3-фенил-2-(2-(3,5-бис(трифторметил)фенил)этил)-морфолин;
8) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
9) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин;
10) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолин;
11) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин;
12) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин;
13) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин;
14) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин;
15) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин;
16) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- фенилморфолин;
17) 4-(3-(1,2,4-триазоло)метил)-2-(S)-(3,5-бис(трифторметил) бензилокси)-3-(S)-фенилморфолин;
18) 4-(3-(5-оксо-1H,4H,-1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
19) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
20) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
21) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин;
22) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин;
23) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)- метилморфолин;
24) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)- метилморфолин;
25) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(S)- метилморфолин;
26) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- фенилморфолин;
27) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-фенилморфолин;
28) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5- (S)-фенилморфолин;
29) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5- (S)-фенилморфолин;
30) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-3- (S)-фенил-4-(3-(1,2,4-триазоло)метил)-морфолин;
31) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-4- (3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-3-(S)-фенилморфолин;
32) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
33) 4-(3-(1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
34) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
35) 4-(2-(имидазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
36) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
37) 4-(аминокарбонил)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
38) 4-(2-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
39) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
40) 4-(2-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолин;
41) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолин;
42) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((6-гидрокси)гексил)-3-(R)-фенилметилморфолин;
43) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (5-метиламинокарбонил)пентил)-3-(R)-фенилметилморфолин;
44) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
45) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2- (3,5-диметил)бензилокси)-3-фенилморфолин;
46) 4-(3-(1,2,4-триазоло)метил)-2- (3,5-ди(третбутил)бензилокси)-3-фенилморфолин;
47) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2- (3,5-ди(третбутил)бензилокси)-3-фенилморфолин;
48) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
49) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолин;
50) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилморфолин;
51) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-(трифторметил)-5-метилбензилокси)-3-фенилморфолин;
52) 4-(3-(1,2,4-триазоло)метил)-2- (3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолин;
53) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолин;
54) 4-(2-(имидазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
55) 4-(4-(имидазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
56) 4-(2-(имидазоло)метил)-2-(3,5-ди-(трет-бутил)бензилокси)- 3-фенилморфолин;
57) 4-(4-(имидазоло)метил)-2-(S)-(3,5-дитрет- бутил)бензилокси)-3-фенилморфолин;
58) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
59) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
60) 4-(2-(имидазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилметилморфолин;
61) 4-(4-(имидазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилметилморфолин;
62) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5- (трифторметил)бензилокси)-3-фенилморфолин;
62а) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5- (трифторметил)-5-метилбензилокси)-3-фенилметилморфолин;
63) 2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолин;
64) 2-(S)-(3,5-дихлорбензилокси)-4-(3-(5-оксо-1,2,4- триазоло)-метил-3-(S)-фенилморфолин;
65) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метоксикарбонилметил)-3-(S)-фенилморфолин;
66) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (карбоксиметил)-3-(S)-фенилморфолин;
67) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((2-аминоэтил)-аминокарбонилметил)-3-(S)-фенилморфолин;
68) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((3-аминопропил)аминокарбонилметил)-3-(S)-фенилморфолин;
69) 4-бензил-5-(S),6-(R)-(диметил)-3-(S)-фенилморфолинон и 4-бензил-5-(R),6-(S)-(диметил)-3-(S)-фенилморфолинон;
70) 2-(R)-(3,5-бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
71) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
72) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4- (3-(1,2,4-триазоло)метил)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
73) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4- (3-(5-оксо-1,2,4-триазоло)метил)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
74) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (3-(1,2,4-триазоло)метил)-[5-(R),6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
75) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (3-(5-оксо-1,2,4-триазоло)метил)-[5-(R),6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
76) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (2-(1-(4-бензил)пиперидино)этил)-3-(S)-фенилморфолин;
77) 3-(S)-(4-фторфенил)-4-бензил-2-фенилморфолинон;
78) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-бензилморфолин;
79) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-морфолин;
80) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метилморфолин;
81) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((3-пиридил)-метилкарбонил)-3-(R)-фенилморфолин;
82) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метоксикарбонилпентил)-3-(R)-фенилморфолин;
83) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (карбоксипентил)-3-(R)-фенилморфолин;
84) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метиламинокарбоксипентил)-6-оксо-гексил)-3-(R)-фенилморфолин
и их фармацевтически приемлемые соли.
β2-
Конкретные вещества в пределах объема настоящего изобретения включюат:
1) (+/-)2-(3,5-бис(трифторметил)бензилокси)-3-фенилморфолин;
2) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3R)-фенил-(6R)- метилморфолин;
3) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3S)-фенил-(6R)- метилморфолин;
4) (+/-)-2-(3,5-бис(трифторметил)бензилокси)-3-фенил-4- метилкарбоксамидоморфолин;
5) (+/-)-2-(3,5-бис(трифторметил)бензилокси)-3-фенил-4- метоксикарбонилметилморфолин;
6) 2-(2-(3,5-бис(трифторметил)фенил)этенил)-3-фенил-5- оксоморфолин;
7) 3-фенил-2-(2-(3,5-бис(трифторметил)фенил)этил)-морфолин;
8) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
9) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин;
10) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолин;
11) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин;
12) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин;
13) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин;
14) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин;
15) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин;
16) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- фенилморфолин;
17) 4-(3-(1,2,4-триазоло)метил)-2-(S)-(3,5-бис(трифторметил) бензилокси)-3-(S)-фенилморфолин;
18) 4-(3-(5-оксо-1H,4H,-1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
19) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
20) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин;
21) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин;
22) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин;
23) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)- метилморфолин;
24) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)- метилморфолин;
25) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(S)- метилморфолин;
26) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- фенилморфолин;
27) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-фенилморфолин;
28) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5- (S)-фенилморфолин;
29) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5- (S)-фенилморфолин;
30) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-3- (S)-фенил-4-(3-(1,2,4-триазоло)метил)-морфолин;
31) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-4- (3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-3-(S)-фенилморфолин;
32) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
33) 4-(3-(1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
34) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
35) 4-(2-(имидазоло)метил)-2-(S)- (3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
36) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
37) 4-(аминокарбонил)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(R)-фенилморфолин;
38) 4-(2-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
39) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенилморфолин;
40) 4-(2-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолин;
41) 4-(4-(имидазоло)метил)-2-(S)-(3,5- бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолин;
42) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((6-гидрокси)гексил)-3-(R)-фенилметилморфолин;
43) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (5-метиламинокарбонил)пентил)-3-(R)-фенилметилморфолин;
44) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
45) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2- (3,5-диметил)бензилокси)-3-фенилморфолин;
46) 4-(3-(1,2,4-триазоло)метил)-2- (3,5-ди(третбутил)бензилокси)-3-фенилморфолин;
47) 4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метил)-2- (3,5-ди(третбутил)бензилокси)-3-фенилморфолин;
48) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
49) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолин;
50) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилморфолин;
51) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-(трифторметил)-5-метилбензилокси)-3-фенилморфолин;
52) 4-(3-(1,2,4-триазоло)метил)-2- (3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолин;
53) 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-2- (3-трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолин;
54) 4-(2-(имидазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
55) 4-(4-(имидазоло)метил)-2-(3,5-диметил)бензилокси)- 3-фенилморфолин;
56) 4-(2-(имидазоло)метил)-2-(3,5-ди-(трет-бутил)бензилокси)- 3-фенилморфолин;
57) 4-(4-(имидазоло)метил)-2-(S)-(3,5-дитрет- бутил)бензилокси)-3-фенилморфолин;
58) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
59) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин;
60) 4-(2-(имидазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилметилморфолин;
61) 4-(4-(имидазоло)метил)-2-(3-(трифторметил)-5- метилбензилокси)-3-фенилметилморфолин;
62) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5- (трифторметил)бензилокси)-3-фенилморфолин;
62а) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5- (трифторметил)-5-метилбензилокси)-3-фенилметилморфолин;
63) 2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолин;
64) 2-(S)-(3,5-дихлорбензилокси)-4-(3-(5-оксо-1,2,4- триазоло)-метил-3-(S)-фенилморфолин;
65) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метоксикарбонилметил)-3-(S)-фенилморфолин;
66) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (карбоксиметил)-3-(S)-фенилморфолин;
67) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((2-аминоэтил)-аминокарбонилметил)-3-(S)-фенилморфолин;
68) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((3-аминопропил)аминокарбонилметил)-3-(S)-фенилморфолин;
69) 4-бензил-5-(S),6-(R)-(диметил)-3-(S)-фенилморфолинон и 4-бензил-5-(R),6-(S)-(диметил)-3-(S)-фенилморфолинон;
70) 2-(R)-(3,5-бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
71) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
72) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4- (3-(1,2,4-триазоло)метил)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
73) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4- (3-(5-оксо-1,2,4-триазоло)метил)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолинон;
74) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (3-(1,2,4-триазоло)метил)-[5-(R),6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
75) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (3-(5-оксо-1,2,4-триазоло)метил)-[5-(R),6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолинон;
76) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (2-(1-(4-бензил)пиперидино)этил)-3-(S)-фенилморфолин;
77) 3-(S)-(4-фторфенил)-4-бензил-2-фенилморфолинон;
78) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-бензилморфолин;
79) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-морфолин;
80) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)- (4-фторфенил)-4-(3-(5-оксо-1H,4H-1,2,4-триазоло)метилморфолин;
81) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- ((3-пиридил)-метилкарбонил)-3-(R)-фенилморфолин;
82) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метоксикарбонилпентил)-3-(R)-фенилморфолин;
83) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (карбоксипентил)-3-(R)-фенилморфолин;
84) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4- (метиламинокарбоксипентил)-6-оксо-гексил)-3-(R)-фенилморфолин
и их фармацевтически приемлемые соли.
Испытания тахикининового антагонизма
Вещества этого изобретения являются полезными для антагонизации тахикининов, в частности, вещества P и нейрокинина A, при лечении желудочно-кишечных нарушений, нарушений центральной нервной системы, воспалительных заболеваний, боли или мигрени и астмы у млекопитающих, нуждающихся в таком лечении. Эта активность может быть продемонстрирована следующим испытанием.
Вещества этого изобретения являются полезными для антагонизации тахикининов, в частности, вещества P и нейрокинина A, при лечении желудочно-кишечных нарушений, нарушений центральной нервной системы, воспалительных заболеваний, боли или мигрени и астмы у млекопитающих, нуждающихся в таком лечении. Эта активность может быть продемонстрирована следующим испытанием.
А. Рецепторная экспрессия в клетках COS
Для того, чтобы временно выразить клонированный рецептор человеческого нейрокинина-1 (NK1R) в клетках COS, цДНК для человеческого NKIR был клонирован в вектор экспрессии pCDM9, который был произведен из вектора pCDM8 (Инвитроген) путем вставки гена, стойкого к ампициллину (нуклеотид от 1973 до 2964 от Блюскрипт sK+), в сайт Sac II. Трансфекция 20 мкг плазмида ДНК в 10 млн. клеток COS была осуществлена путем электропорации в 800 мкл трансфекционного буфера (135 ммоль/л хлорида натрия, 1,2 ммоль/л хлорида кальция, 1,2 ммоль/л хлорида магния, 2,4 ммоль/л моногидрофосфата калия, 0,6 ммоль/л гидрофосфата калия, 10 ммоль/л глюкозы, 10 ммоль/л буфера Хепес с pH 7,4) при 260 в и 950 мкФ, используя Генезаппер Ай-Би-Ай (фирма Ай-Би-Ай, Нью-Хэйвен, Коннектикут). Эти клетки культивировали в 10% сыворотки плода теленка, 2 ммоль/л глутамина, 100 ед/мл пенициллина - стрептомицина и 90% среды DMEM (фирма G IBCO, Гранд Айленд, Нью-Йорк) в 5% диоксида углерода при 37oC до связывающего анализа.
Для того, чтобы временно выразить клонированный рецептор человеческого нейрокинина-1 (NK1R) в клетках COS, цДНК для человеческого NKIR был клонирован в вектор экспрессии pCDM9, который был произведен из вектора pCDM8 (Инвитроген) путем вставки гена, стойкого к ампициллину (нуклеотид от 1973 до 2964 от Блюскрипт sK+), в сайт Sac II. Трансфекция 20 мкг плазмида ДНК в 10 млн. клеток COS была осуществлена путем электропорации в 800 мкл трансфекционного буфера (135 ммоль/л хлорида натрия, 1,2 ммоль/л хлорида кальция, 1,2 ммоль/л хлорида магния, 2,4 ммоль/л моногидрофосфата калия, 0,6 ммоль/л гидрофосфата калия, 10 ммоль/л глюкозы, 10 ммоль/л буфера Хепес с pH 7,4) при 260 в и 950 мкФ, используя Генезаппер Ай-Би-Ай (фирма Ай-Би-Ай, Нью-Хэйвен, Коннектикут). Эти клетки культивировали в 10% сыворотки плода теленка, 2 ммоль/л глутамина, 100 ед/мл пенициллина - стрептомицина и 90% среды DMEM (фирма G IBCO, Гранд Айленд, Нью-Йорк) в 5% диоксида углерода при 37oC до связывающего анализа.
Б. Стабильная экспрессия в клетках COS
Для того, чтобы основать стабильную клеточную линию, выражающую клонированный рецептор человеческого нейрокинина-1, цДНК была субклонирована в вектор pR с CMV (Инвитроген). Трансфекцию 20 мкг плазмида ДНК в клетки СНО была осуществлена путем электропорации в 800 мкл трансфекционного буфера, дополненного 0,625 мг/мл ДНК спермы сельди, при 260 в и 950 мкФ, используя Генезаппер Ай-Би-Ай (фирма Ай-Би-Ай). Трансфектированные клетки культивировали в среде CHO [10% сыворотки плода теленка, 2 ммоль/ л глутамина, 100 ед/мл пенициллина-стрептомицина, 1/500 гипоксантин-тимидина, (АТСС), 90% среды IMDM (фирма JRH Биосайенсиз, Ленекса, Канзас), 0,7 мг/мл G418 (фирма GIBCO)] в 5% диоксида углерода при 37oC до тех пор, пока колонии станут видимыми. Каждая колония была выделена и размножена. Клеточный клон с наибольшим количеством человеческого NK 1 R был выбран для последующих приложений, таких как скрининг медикаментов.
Для того, чтобы основать стабильную клеточную линию, выражающую клонированный рецептор человеческого нейрокинина-1, цДНК была субклонирована в вектор pR с CMV (Инвитроген). Трансфекцию 20 мкг плазмида ДНК в клетки СНО была осуществлена путем электропорации в 800 мкл трансфекционного буфера, дополненного 0,625 мг/мл ДНК спермы сельди, при 260 в и 950 мкФ, используя Генезаппер Ай-Би-Ай (фирма Ай-Би-Ай). Трансфектированные клетки культивировали в среде CHO [10% сыворотки плода теленка, 2 ммоль/ л глутамина, 100 ед/мл пенициллина-стрептомицина, 1/500 гипоксантин-тимидина, (АТСС), 90% среды IMDM (фирма JRH Биосайенсиз, Ленекса, Канзас), 0,7 мг/мл G418 (фирма GIBCO)] в 5% диоксида углерода при 37oC до тех пор, пока колонии станут видимыми. Каждая колония была выделена и размножена. Клеточный клон с наибольшим количеством человеческого NK 1 R был выбран для последующих приложений, таких как скрининг медикаментов.
B. Протокол испытания с использованием клеток COS или CHO
Связывающий анализ человеческого NKIR, выраженного либо в клетках COS, либо в клетках CHO, основан на использовании вещества P и изотопом 125 иода (125 I-SP, от фирмы Дюпон, Бостон, Массачузетс) в качестве радиоактивного меченого лиганда, который конкурирует с немеченым веществом P или любым другим лигандом для связывания с человеческим NKI R. Монослой клеточных культур COS или CHO был диссоциирован посредством неферментативного раствора (среда Спешиэлти, Лавалетт, Нью-Джерси) и повторно суспендирован в подходящем объеме связывающего буфера [50 ммоль/л буфера Трис с pH 7,5, 5 ммоль/л дихлорида марганца, 150 ммоль/л хлорида натрия, 0,04 мг/мл бацитрацина, 0,004 мг/мл лейпептина, 0,2 мг/мл белка бычьей сыворотки, 0,01 ммоль/л фосфорамидона], так чтобы 200 мкл суспензии клеток могли бы вызвать радиоактивность специфического связывания 125 I-Sp около 10000 импульсов/мин (приблизительно от 50000 до 200000 клеток). В связывающем анализе добавляли 200 мкл клеток в пробирку, содержащую 20 мкл раствора от 1,5 до 2,5 наномоль/л 125 I-Sp и 20 мкг немеченого вещества P или любого другого испытуемого вещества. Пробирки были культивированы при 4oC или при комнатной температуре в течение 1 ч при осторожном встряхивании. Связанную радиоактивность отделяли от несвязанной радиоактивности с помощью фильтра CF/C (фирма Брандел, Гэйтербсург, Мэриленд), который был предварительно увлажнен 0,1% полиэтиленимина. Фильтр промывали 3 раза 3 мл промывочного буфера (50 ммоль/л буфера Трис с pH 7,5, 5 ммоль/л дихлорида марганца, 150 ммоль/л хлорида натрия), и определяли его радиоактивность гамма-счетчиком.
Связывающий анализ человеческого NKIR, выраженного либо в клетках COS, либо в клетках CHO, основан на использовании вещества P и изотопом 125 иода (125 I-SP, от фирмы Дюпон, Бостон, Массачузетс) в качестве радиоактивного меченого лиганда, который конкурирует с немеченым веществом P или любым другим лигандом для связывания с человеческим NKI R. Монослой клеточных культур COS или CHO был диссоциирован посредством неферментативного раствора (среда Спешиэлти, Лавалетт, Нью-Джерси) и повторно суспендирован в подходящем объеме связывающего буфера [50 ммоль/л буфера Трис с pH 7,5, 5 ммоль/л дихлорида марганца, 150 ммоль/л хлорида натрия, 0,04 мг/мл бацитрацина, 0,004 мг/мл лейпептина, 0,2 мг/мл белка бычьей сыворотки, 0,01 ммоль/л фосфорамидона], так чтобы 200 мкл суспензии клеток могли бы вызвать радиоактивность специфического связывания 125 I-Sp около 10000 импульсов/мин (приблизительно от 50000 до 200000 клеток). В связывающем анализе добавляли 200 мкл клеток в пробирку, содержащую 20 мкл раствора от 1,5 до 2,5 наномоль/л 125 I-Sp и 20 мкг немеченого вещества P или любого другого испытуемого вещества. Пробирки были культивированы при 4oC или при комнатной температуре в течение 1 ч при осторожном встряхивании. Связанную радиоактивность отделяли от несвязанной радиоактивности с помощью фильтра CF/C (фирма Брандел, Гэйтербсург, Мэриленд), который был предварительно увлажнен 0,1% полиэтиленимина. Фильтр промывали 3 раза 3 мл промывочного буфера (50 ммоль/л буфера Трис с pH 7,5, 5 ммоль/л дихлорида марганца, 150 ммоль/л хлорида натрия), и определяли его радиоактивность гамма-счетчиком.
Активация фосфолипазы Си посредством NKIR также могла быть измерена в клетках CHO, выражающих человеческий NKI R, посредством определения накопления инозитол-монофосфата, который является продуктом распада IP3. Клетки CHO были посеяны в 12-луночной пластине в количестве 250000 клеток в лунке. После культивирования в среде CHO в течение 4 суток, клетки нагружали 0,025 мк Кюри/мл тритий - миоинозитола посредством культивирования в течение ночи. Внеклеточную радиоактивность удаляли путем промывки раствором соли, забуферированным фосфатом. В лунку добавляли хлористый литий в окончательной концентрации 0,1 ммоль/л с испытуемым веществом или без него, и культивирование продолжали при 37oC в течение 15 мин. В лунку добавляли вещество P в окончательной концентрации 0,3 нмоль/л, чтобы активировать человеческий NKI R. Спустя 30 мин культивирования при 37oC среду удаляли и добавляли 0,1 н. соляную кислоту. Каждую лунку озвучивали при 4oC и экстрагировали смесью хлорофором/метанол 1: 1. Водную фазу подавали на 1 мл ионообменной колонки Доуэкс Эй-Джи IX8. Колонку промывали 0,1 н. муравьиной кислотой и затем смесью растворов 0,025 моль/л формиата аммония и 0,1 н. муравьиной кислоты. Инозитолмонофосфат элюировали смесью растворов 0,2 мол/л формиата аммония и 0,1 н. муравьиной кислоты и количественно определяли счетчиком бета-частиц.
Вещества настоящего изобретения были полезны при предупреждении и лечении большого множества клинических состояний, которые характеризуются наличием избытка тахикининовой активности, в частности вещества P.
Эти состояния могут включать нарушения центральной нервной системы, такие как беспокойство, депрессия, психоз и шизофрения; нейродегенеративные нарушения, такие как связанное со СПИДом слабоумие, старческое слабоумие типа Альцхаймера и синдром Дауна; демиелизационные заболевания, такие как множественный склероз и амиотрофический латеральный склероз (АЛС; болезнь Лоу Герига) и другие нейропатологические нарушения, такие как периферическая нейропатия, например нейропатия, связанная со СПИДом, диабетическая нейропатия, хемотерапически индуцированная нейропатия и постгерпетическая и другие виды невралгии; респираторные заболевания, такие как хроническое обструктивное заболевание дыхательных путей, бронхопневмония, бронхоспазм и астма; заболевания, характеризующиеся нейрогенным выделением слизи, такое как циститный фиброз; воспалительные заболевания, такие как воспалительное заболевание кишечника, псориаз, фиброзитис, остеоартрит и ревматоидный артрит; аллергии, такие как экзема и ринит; нарушения сверхчувствительности, такие как сумах укореняющийся; офтальмические заболевания, такие как конъюнктивит, весенний конъюнктивит и т.п.; кожные заболевания, такие как контактный дерматит, атропический дерматит, уртикария и другие экзематоидные дерматиты; наркотические нарушения, такие как алкоголизм; соматические нарушения, связанные со стрессом; рефлексная симпатетическая дистрофия, такая как ручно/плечевой синдром; дистимовые нарушения, вредные иммунологические реакции, такие как отторжение трансплантированных тканей и нарушения, связанные с иммунным усилением или подавлением, такое как системный волчаночный эритематоз; желудочно-кишечные нарушения и заболевания желудочно-кишечного тракта, такие как нарушения, связанные с нейрональным контролем внутренностей, такие как язвенный колит, болезнь Крона и недержание, тошнота, включая острую, замедленную и предупреждающую тошноту, например, вызванную хемотерапией, радиацией, токсинами, беременностью, вестибулярными нарушениями, движением, хирургией, мигренью и изменениями внутричерепного давления, нарушения функции мочевого пузыря, такое как гиперрефлексия сбрасывающего клапана мочевого пузыря; фиброзные и коллагеновые заболевания, такие как склеродерма и эозинофиловый фасциолиаз; нарушения кровотока, вызванные расширением сосудов и сосудоспастическими заболеваниями, такими как ангина, мигрень и болезнь Рейно; и боль или ноцицепция, например, которые приписываются или связаны с любым из указанных выше состояний, особенно передача боли при мигрени. Поэтому эти вещества легко могут быть приспособлены для терапевтического использования при лечении физиологических нарушений, связанных с избыточным стимулированием тахикининовых рецепторов, особенно нейрокинина-1, и в качестве антагонистов нейрокинина-1, для контроля и/или лечения любого из указанных выше клинических состояний у млекопитающих, включая людей.
Например, вещества настоящего изобретения могут быть приемлемо использованы для лечения нарушений центральной нервной системы, таких как беспокойство, психоз и шизофрения; нейродегенеративных нарушений, таких как старческое слабоумие типа Альцхаймера, болезнь Альцхаймера и синдром Дауна; респираторные заболевания, в частности те, которые связаны с избыточным выделением слизи, такие как хроническое препятствующее заболевание дыхательных путей, бронхопневмония, хронический бронхит, циститный фиброз и астма, и бронхоспазм; воспалительные заболевания, такие как воспалительное заболевание кишечника, остеоартрит и ревматоидный артрит; вредные иммунологические реакции, такие как отторжение трансплантированной ткани; желудочно-кишечные нарушения и заболевания желудочно-кишечного тракта, такие как нарушения, связанные с нейрональным контролем внутренностей, такие как язвенный колит, болезнь Крона и недержание, нарушения кровотока, вызванные расширением сосудов, и боль или ноцицепция, например, та, которая приписывается или связана с любым из указанных выше состояний, или с передачей боли при мигрени.
В качестве агентов, блокирующих кальциевые каналы, некоторые из веществ настоящего изобретения являются полезными при предупреждении или лечении клинических состояний, которые извлекают пользу из ингибирования переноса ионов кальция через плазменную мембрану клеток. Эти состояния включают заболевания и нарушения сердечно-сосудистой системы, такие как грудная жаба, инфаркт миокарда, сердечная аритмия, гипертрофия сердца, сердечно-сосудистый спазм, гипертония, цереброваскулярный спазм и другие ишемические заболевания. Более того, эти вещества могут быть способны снижать повышенное внутриглазное давление при их местном назначении в гипертонический глаз в растворе с подходящим офтальмическим носителем. Кроме того, эти вещества могут быть полезными при возвращении полилекарственной стойкости в опухолевых клетках путем повышения эффективности хемотерапевтических агентов. В дополнение, эти вещества могут обладать активностью при блокировании кальциевых каналов в мозговых мембранах насекомых, и поэтому они могут быть полезными в качестве инсектицидов.
Вещества настоящего изобретения являются особенно эффективными при лечении боли или ноцицепции и/или воспаления и связанных с ним нарушений, таких как, например: нейропатия, такая как диабетическая или периферическая нейропатия и нейропатия, вызванная хемотерапией, постгерпетическая невралгия и другие; астма, остеоартрит, ревматоидный артрит, и особенно мигрень. Вещества настоящего изобретения, в частности, также полезны при лечении заболеваний, характеризующихся нейрогенным выделением слизи, особенно при циститном фиброзе.
При лечении указанных выше клинических состояний вещества этого изобретения могут быть использованы в композициях, таких как таблетки, капсулы или эликсиры для перорального назначения, свечи для ректального назначения, стерильные растворы или суспензии для парэнтерального или внутримышечного назначения и тому подобное.
Фармацевтические композиции этого изобретения могут применяться в форме фармацевтического препарата, например в твердой, полутвердой или жидкой форме, которая содержит одно или несколько веществ настоящего изобретения, в качестве активного компонента, в смеси с органическим или неорганическим носителем или средой для лекарства, пригодной для наружного энтерального или парэнтерального применения. Активный компонент может быть компаундирован, например, с обычными нетоксичными, фармацевтически приемлемыми носителями в таблетки, лепешки, капсулы, свечи, растворы, эмульсии, суспензии и любые другие формы, пригодные для использования. Возможные для использования носители представляют собой воду, глюкозу, лактозу, смолу акации, желатин, маннитол, крахмальную пасту, трисиликат магния, тальк, кукурузный крахмал, кератин, коллоидный диоксид кремния, картофельный крахмал, мочевину и другие носители, пригодные для применения в производимых препаратах, в твердой, полутвердой или жидкой форме и дополнительно могут быть использованы вспомогательные, стабилизирующие, загущающие и окрашивающие агенты и ароматизирующие вещества. Активное целевое вещество включается в фармацевтическую композицию в количестве, которое достаточно для получения желаемого эффекта на протекание или состояние заболевания.
Для приготовления твердых композиций, таких как таблетки, принципиальный активный компонент смешивается с фармацевтическим носителем, например, с традиционными таблетирующими ингредиентами, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальций-фосфат или смолы, и с другими фармацевтическими разбавителями, например, водой, чтобы сформовать предварительную рецептурную композицию, содержащую гомогенную смесь вещества настоящего изобретения, или его нетоксической фармацевтически приемлемой соли. Когда эти предварительные композиции называются гомогенными, это означает, что активный компонент равномерно диспергирован по всей композиции, так что эта композиция легко может быть подразделена на одинакового эффективные формы единичной дозировки, такие как таблетки, пилюли и капсулы. Затем эту твердую предварительно составленную композицию подразделяют на формы единичной дозировки описанного выше типа, которые содержат от 0,1 до примерно 500 мг активного компонента настоящего изобретения. Эти таблетки или пилюли новой композиции могут быть покрыты или иным образом компаундированы для того, чтобы предоставить форму дозировки, обеспечивающую преимущество продолжительного действия. Например, таблетка или пилюля может включать внутреннюю дозировку и внешний дозировочный компонент, причем последний имеет форму покрытия поверх внутренней дозы. Эти два компонента могут быть разделены желудочным слоем, который служит для ограничения распада в желудке и позволяет внутреннему компоненту пройти нетронутым в двенадцатиперстную кишку, или для замедления его выделения. Для таких желудочных слоев или покрытий может использоваться множество материалов, такие материалы включают ряд полимерных кислот и смесей полимерных кислот с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы.
Жидкие формы, в которые новые композиции настоящего изобретения могут быть введены для перорального или инъекционного назначения, включают водный раствор, соответственно отдушенные сиропы, водные или масляные суспензии и отдушенные эмульсии со съедобными маслами, такими как масло семян хлопка, конопляное масло, масло кокосового ореха или масло земляного ореха, а также эликсиры и аналогичные фармацевтические носители. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические или натуральные смолы, такие как смолы трагаканта и акации, альгинат, декстран, натрий карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин.
Композиции для ингаляции или вдувании включают растворы и суспензии в фармацевтически приемлемых водных или органических растворителях или их смесях, и порошки. Жидкие или твердые композиции могут содержать подходящие фармацевтически приемлемые среды для лекарства, которые изложены выше. Предпочтительно композиции назначаются перорально или носовым респираторным способом для локального или системного эффекта. Композиции в предпочтительно стерильных фармацевтически приемлемых растворителях могут быть распылены с помощью инертных газов. Распыленные растворы могут вдыхаться непосредственно из распыляющего устройства, или это распыляющее устройство может быть присоединено к лицевой маске, тенту или к дыхательной машине с пульсирующим положительным давлением. Растворные, суспензионные или порошковые композиции могут назначаться предпочтительно перорально или через нос из устройств, которые подают рецептуру соответствующим образом.
Для лечения клинических состояний и указанных выше заболеваний вещества этого изобретения могут назначаться перорально, местно, парэнтерально, путем ингаляционной струи или ректально в рецептурах дозировочной единицы, содержащей традиционные нетоксичные фармацевтически приемлемые носители, стимуляторы и носители. Используемый здесь термин парэнтерально означает подкожные инъекции, внутривенные, внутримышечные, внутригрудинные инъекционные или инфузионные методики.
Для лечения определенных состояний может быть желательным использование вещества настоящего изобретения и сочетании с другим фармакологически активным агентом. Например, для лечения распираторных заболеваний, таких как астма, вещество настоящего изобретения может использоваться в сочетании с расширителем бронхов, таким как агонист адрэнергического рецептора или тахикининовый антагонист, который действует как рецепторы NK-2. Вещество настоящего изобретения и расширитель бронхов могут назначаться пациенту одновременно, последовательно или в сочетании.
Вещества этого изобретения могут назначаться пациентам (животным и человеку), нуждающимся в таком лечении, в дозировках, которые будут обеспечивать оптимальную фармацевтическую эффективность. Эта дозировка может изменяться от пациента к пациенту, в зависимости от характера и серьезности заболевания, веса пациента, специальных диет, которым будет следовать пациент, конкурирующего лечения и других факторов, которые будут признаны специалистами в этой области медицины.
При лечении состояния, связанного с избытком тахикининов, подходящий уровень дозировки обычно будет составлять примерно от 0,001 до 50 мг/кг веса тела пациента в сутки, причем эта дозировка может назначаться в одной или нескольких дозах. Предпочтительно, уровень дозировки будет составлять примерно от 0,01 до 25 мг/кг в сутки; более предпочтительно примерно от 0,05 до 10 мг/кг в сутки. Например, при лечении состояний, включающих нейротрансмиссию ощущения боли, подходящий уровень дозировки составляет примерно от 0,001 до 25 мг/кг в сутки, предпочтительно примерно от 0,005 до 10 мг/кг в сутки, и особенно около 0,005 до 5 мг/кг в сутки. Эти вещества могут назначаться в режиме от 1 до 4 раз в сутки, предпочтительно, один или два раза в сутки.
Несколько способов получения веществ этого изобретения проиллюстрированы в следующих Схемах и Примерах, в которых радикалы R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12 и R13 имеют указанные выше значения.
В табл. 1 приведены сокращения, использованные в схемах и примерах.
α-
Вещества настоящего изобретения, в которых X = Y = 0, могут быть приготовлены по общему маршруту, изложенному в схеме 1. Таким образом, соответственно замещенный альфа-бромфенилацетальдегид, диметилацеталь 1 (приготовленный с использованием метода Джейкобса в журнале J. Amer. Chem. Soc., 1953, т. 75, с. 5500) может быть превращен в дибензилацеталь II посредством перемешивания I и небольшого избытка бензилового спирта в присутствии кислотного катализатора с сопутствующим удалением метанола. Алкилирование замещенного аминоспирта бромистым бензилом II может дать N-алкиламиноспирт III; использование хирального аминоспирта может привести к образованию диастереоизомеров, причем они могут быть разделены на этой стадии /или позднее/ с использованием стандартных хроматографических методов. Алкилирование или ацилирование вещества III по атому азота может дать диалкил- или ацил/алкил-аминоспирт IV, в которых группа R1 может служить защищающей группой или использоваться как, или вводиться в заместитель в окончательное целевое вещество. Циклизация с образованием замещенного морфолина V может быть реализована путем нагревания раствора IV и кислотного катализатора. Диастереомеры V, которые могут образоваться, могут быть выделены с использованием стандартных хроматографических методов. Если R1 является защищающей группой, она может быть удалена с использованием известных методик /Гриин Т. В. , Вутс П.Г.М. "Защитные группы в органическом синтезе", 2-е издание, изд. Джон Уилей энд Санз, Инк., Нью-Йорк, 1991/. Если приготовление соединений I-V приводит к образованию энантиомеров, они могут быть разделены посредством алкилирования или ацилирования V /R1=H/ со вспомогательным хиральным агентом, разделения полученных таким образом диастереоизомеров с использованием известных хроматографических методов, и удаления вспомогательного хирального агента с получением энантиомеров вещества V. Альтернативно, диастереоизомеры V могут быть разделены путем фракционной кристаллизации их подходящего растворителя диастереоизомерных солей, полученных из V и хиральной органической кислоты.
Вещества настоящего изобретения, в которых X=0 и Y = CH2, могут быть приготовлены по общему маршруту, изложенному в схеме 2. Таким образом, N-метокси-N-метиламид защищенного фенилглицина VI /приготовлен из карбоновой кислоты через смешанный ангидрид в соответствии с методикой Рапопорта в журнале J. Org Chem., 1985, т. 50, с. 3972/ может быть использован для ацилирования енолята лития метилдиэтилфосфоната, чтобы получить кетофосфонат VII. Натриевая соль VII может быть конденсирована с соответственно замещенным бензальдегидом, чтобы получить альфа, бетаненасыщенный кетон VIII. Восстановление этого кетона и удаление трет-бутилкарбаматной защищающей группы может дать аминоспирт IX. Диастереомеры, которые могут образоваться, могут быть разделены на этой стадии /или позднее/ с использованием стандартных хроматографических методик. Этерификация IX по Вильямсону с использованием замещенного хлорацетата и с последующим нагреванием может привести к образованию морфолинона X. Восстановление двойной связи и амидной карбонильной группы может быть осуществлено непосредственным образом с получением замещенного морфолина XI. Если приготовление соединений VI-XI приводит к образованию энантиомеров, то они могут быть разделены посредством алкилирования или ацилирования XI (R1=H) вспомогательным хиральным агентом, выделением полученных таким образом диастереомеров с использованием известных хроматографических методов и удаления вспомогательного хирального агента, чтобы получить энантиомеры XI. Альтернативно, диастереомеры XI могут быть разделены путем фракционной кристаллизации из подходящего растворителя диастереомерных солей, образованных веществом XI и хиральной органической кислотой. Если желательно, чтобы R1 отличался от атома водорода, морфолиновый атом азота в соединении XI может быть дополнительно функционализирован с использованием стандартных методов алкилирования или ацилирования вторичных аминов. Если желательно, чтобы R2 отличался от атома водорода, морфолинон X может быть переработан в карбинолкарбамат (R1=RO2C, R2=OH) - промежуточное вещество, которое может быть алкилировано и будет учтено для изменения в R2.
Вещества настоящего изобретения, в которых X=S-(O)n (n=0, 1, 2) и Y = 0, могут быть приготовлены по общему маршруту, изложенному в схеме 3. Таким образом спирт IV (приготовленный в схеме 1) может быть превращен в тиоацетат XII с использованием известных методик (Р.П. Воланте. Tetrahedron Zett, 1981, т. 22, с. 3119). Расщепление сложноэфирной функции, для предоставления тиола XIII, может быть осуществлено с водным основанием или восстановительно, в зависимости от ограничений, накладываемых другими присутствующими функциональными группами. Циклизация XIII в тиоморфолин XIV может быть выполнена путем нагревания раствора XIII и кислотного катализатора. Окисление XIV с использованием метапериодата натрия в уксусной кислоте может предоставить сульфоксид или сульфон XV. Диастереомеры XIV или XV, которые могут образоваться, могут быть разделены с использованием стандартных хроматографических методов. Если R1 является защищающей группой, она может быть удалена с использованием известных методик (Т.В. Гриин, Вутс П.Г. М. Защищающие группы в органическом синтезе, 2-е изд., Дж. Уилей энд Санз, Инк., Нью-Йорк, 1991). Если приготовление соединений XII-XI приводит к образованию энантиомеров, то они могут быть разделены путем алкилирования или ацилирования соединений XIV или XV (R1=H) вспомогательным хиральным агентом, выделения диастереомеров, полученных таким образом, с использованием известных хроматографических методов, и удаление вспомогательного хирального агента с получением энантиомеров XIV или XV. Альтернативно, диастереомеры XIV или XV могут быть разделены посредством фракционной кристаллизации из подходящего растворителя диастереомерных солей, образованных соединением XIV или XV и хиральной органической кислотой.
Вещества настоящего изобретения, в которых X=Y=0, также могут быть получены по общему маршруту, изложенному в схеме 4. Таким образом, соответственно замещенный диметилацеталь альфа-бромацетальдегида (приготовлен с использованием метода Джейкобса из журнала J.Am. Chem. Soc., 1953, т. 75, с. 5500) может быть превращен в ацеталь путем перемешивания с небольшим избытком подходящего спирта в присутствии кислотного катализатора с сопутствующим удалением метанола. Алкилирование замещенного аминоспирта бромидом может быть N-алкиламиноспирт. Использование хирального аминоспирта привело бы к образованию диастереомеров, которые могут быть разделены на этой стадии (или позднее), с использованием стандартных хроматографических методов. Алкилирование или ацилирование по атому азота может дать диалкил- или ацил/алкиламиноспирт, в котором группа R1 может служить в качестве защищающей группы или может использоваться или перерабатываться в заместитель в окончательном целевом соединении. Циклизация с получением замещенного морфолина может быть реализована путем нагревания раствора с кислотным катализатором. Диастереомеры, которые могут образоваться, могут быть разделены с использованием стандартных хроматографических методов. Если R1 является защищающей группой, она может быть удалена с использованием известных методик (Гриин Т. В. , П. Г. М. Вутс, Защищающие группы в органическом синтезе, 2-е изд. , Нью-Йорк, 1991). Если приготовление таких соединений приводит к образованию энантиомеров, они могут быть разделены путем алкилирования или ацилирования конечного продукта (R1=H) вспомогательным хиральным агентом, разделения диастереомеров, полученных таким образом, с использованием известных хроматографических методов, и удаления вспомогательного хирального агента, чтобы получить целевые энантиомеры. Альтернативно, эти диастереомеры могут быть разделены путем фракционной кристаллизации из подходящего растворителя диастереомерных солей, образованных соединением с хиральной органической кислотой.
Один метод синтеза энантиомерно чистых замещенных морфолинов иллюстрируется в схеме 5. Защита энантиомерно чистого фенилглицина, как //-бензил-производной с последующим двойным алкилированием 1,2-дибромэтановой производной, приводит к морфолинону. Восстановление активным гидридным реагентом, таким как диизобутилалюминийгидрид, литийалюминийгидрид, литий-(три-втор-бутил)боргидрид/L-Селектрид, торговой знак/ или другим восстанавливающим агентом приводит преимущественно к 2,3-транс-морфолиновым производным. Алкилирование спирта, удаление защищающей группы при атоме азота (например, гидрирующим палладиевым катализатором или 1-хлорэтилхлорформиатом (Олофсон в журнале J. Org Chem, 1984, с. 2081 и 2795)) и алкилирование по азоту производит 2,3-транс-соединениям.
Один способ получения энантиомерно чистых 2,3-цис-морфолинов проиллюстрирован в схеме 6. На первой стадии образование трифторметансульфонатного эфира подходящего бензилового спирта (особенно бензиловых спиртов, которые замещены электроно-акцепторными группами, такими как -нитро, фторо-, хлоро-, бромо-, -COR, трифторметил и др.) проводится в присутствии нереакционноспособного основания, в инертном растворителе. Кроме того, могут использоваться другие отщепляемые группы, такие как иодид, мезилат, тозилат, пара-нитрофенилсульфонат и т. п. Подходящие основания включают 2,6-ди-трет-бутилпиридин, 2,6-ди-трет-бутил-4-метилпиридин, диизопропилэтиламин, карбонат калия, карбонат натрия и т.п. Подходящие растворители включают толуол, гексаны, бензол, четыреххлористый углерод, дихлорметан, хлороформ, дихлорэтан и т. п. и их смеси. Затем отфильтрованный раствор трифлата добавляют к раствору промежуточного соединения, образовавшегося при контактировании морфолинона с активным гидридным реагентом, таким как диизобутилалюминийгидрид, литийалюминийгидрид или литий-три(вторбутил)боргидрид (L-Cелектрид) при низкой температуре, предпочтительно от -78oC до -20oC. Спустя несколько часов при низкой температуре, обработка и очистка обеспечивают преимущественно 2,3-цис-замещенные продукты, которые могут привести к конечным соединениям, как показано на схеме 6.
Энантиомерно чистые фенилглицины, замещенные при фенильном кольце, могут быть приготовлены по методике, показанной в схеме 7 (Д.А. Эванс и др., J. Am. Chem. Soc., 1990, т. 112, с. 4011).
Методы получения алкилирующих по атому азота агентов R1CH2X, применяемых в схеме 5 и схеме 6, базируются на известных литературных методах (для R1 = 3-/1,2,4-триазолил/ или 5-/1,2,4-триазолил-3-он/-ил и X = хлор, смотри Янагисава И.; И. Хирата. И. Ишин, J. Medicinal Chemistry, 1984, 27, с. 849; для R1 = 4((2H)-имидазол-2-он)-ил или 5-(4-этоксикарбонил-(2H)-имидазол-2-он)-ил и X = бромо-, см. Р.Душинский, Л.А. Долан, J. Am. Chem. Soc, 1948, т. 70, с. 657).
Целевые вещества формулы I, полученные в соответствии с реакциями, которые пояснены выше, могут быть выделены и очищены традиционным образом, например, экстракцией, осаждением, фракционной кристаллизацией, перекристаллизацией, хроматографией и т.п. Вещества настоящего изобретения способны образовывать соли с различными неорганическими и органическими кислотами и основаниями и такие соли также охватываются этим изобретением. Примеры таких кислотных аддитивных солей включают ацетат, адипинат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, этансульфонат, фумарат, полусульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, метансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, оксалат, памоат, персульфат, пикрат, пивалат, пропионат, сукцинат, тартрат, тозилат и ундеканоат. Основные соли включают соли аммония, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочноземельных металлов, таких как кальций и магний, соли с органическими основаниями, такими как дициклогексиламин, N-метил-D-глюкамин, и соли с аминокислотами, такими как аргинин, лизин и т.п. Кроме того, основные азотсодержащие группы могут быть кватернизованы с такими агентами, как галогениды низших алкилов, как например метил-, этил-, пропил- и бутилхлорид, бромиды и иодиды; диалкилсульфатами, подобными диметил-, диэтил, дибутил- и диамилсульфату; длинноцепочечными галогенидами, такими как децил-, лаурил-, миристил- и стеарилхлориды, бромиды и иодиды; аралкилгалогенидами, подобными бензилбромиду и другим. Нетоксичные физиологически приемлемые соли являются предпочтительными, хотя другие соли также являются полезными, как например при выделении или очистке продукта.
Эти соли могут быть образованы традиционным образом, как например путем взаимодействия свободно основной формы продукта с одним или несколькими эквивалентами подходящей кислоты в растворителе или среде, в которой соль является нерастворимой, или в таком растворителе, как вода, которая удаляется в вакууме, или путем сушки с вымораживанием или путем обмена анионов существующих солей на другой анион на подходящей ионо-обменной смоле.
Хотя описанные здесь реакционные схемы являются разумно обобщенными, специалист в этой области химии поймет, что одна или несколько функциональных групп, присутствующих в данном соединении формулы I, могут сделать эту молекулу несовместимой с конкретной синтетической последовательностью.
В таком случае могут использоваться альтернативные маршруты, измененный порядок стадий или стратегия защиты и снятия защиты. Во всех случаях конкретные условия реакции, включая реагенты, растворитель, температуру и время реакции, должны выбираться таким образом, чтобы они были согласованы с природой функциональной группы, присутствующей в молекуле.
Следующие примеры даны в целях иллюстрации настоящего изобретения, и они не должны рассматриваться как ограничивающие объем и замысел настоящего изобретения.
Пример 1.
(+/-)-альфа-Бромфенилацетальдегид, 3,5-бис(трифторметил)бензилацеталь
Раствор 2,50 г (10,2 ммоль) диметилацеталя альфа-бром-фенилацетальдегида, 8,00 г (32,8 ммоль) 3,5-бис(трифторметил)-бензилового спирта и 0,50 г (2,6 ммоль) моногидрата пара-толуолсульфокислоты в 10 мл толуола перемешивают в вакууме (35 мм рт.ст.) при комнатной температуре в течение 3 суток. Реакционную смесь распределяют между 100 мл эфира и 50 мл насыщенного водного раствора бикарбоната натрия, и слои разделяют. Органический слой промывают 25 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 200 г силикагеля с использованием в качестве элюента смеси 9:1 (по объему) гексана и хлористого метилена получают 5,41 г (81%) указанного в заголовке соединения в виде твердого вещества с температурой плавления (Т.пл.) 79-82oC.
Раствор 2,50 г (10,2 ммоль) диметилацеталя альфа-бром-фенилацетальдегида, 8,00 г (32,8 ммоль) 3,5-бис(трифторметил)-бензилового спирта и 0,50 г (2,6 ммоль) моногидрата пара-толуолсульфокислоты в 10 мл толуола перемешивают в вакууме (35 мм рт.ст.) при комнатной температуре в течение 3 суток. Реакционную смесь распределяют между 100 мл эфира и 50 мл насыщенного водного раствора бикарбоната натрия, и слои разделяют. Органический слой промывают 25 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 200 г силикагеля с использованием в качестве элюента смеси 9:1 (по объему) гексана и хлористого метилена получают 5,41 г (81%) указанного в заголовке соединения в виде твердого вещества с температурой плавления (Т.пл.) 79-82oC.
Спектр ПМР: 4,47 и 4,62 (AB кв., 2H, J = 12,5), 4,78-4,93 (2H), 5,09 и 5,21 (AB кв. , 2H, J = 7,7), 7,31 - 7,44 (м, 7H), 7,70 (≈c, 1H), 7,82 (≈с, 1H), 7,84 (≈c, 2H).
ИК-спектр (в тонкой пленке) 1363, 1278, 1174, 1130, 704, 682.
Анализ, вычислено для C26H17BrF12O2:
C - 46,76; H - 2,23; Br - 11,64; F - 33,70;
найдено: C - 46,65; H - 2,56; Br - 11,94; F - 34,06.
C - 46,76; H - 2,23; Br - 11,64; F - 33,70;
найдено: C - 46,65; H - 2,56; Br - 11,94; F - 34,06.
Список сокращений, используемых в ПМР-спектрах:
д - дублет,
кв. - квартет,
м - мультиплет,
с - синглет,
т - триплет,
шир. - широкий.
д - дублет,
кв. - квартет,
м - мультиплет,
с - синглет,
т - триплет,
шир. - широкий.
Пример 2.
(+/-)-N-(2-Гидроксиэтил)-фенилглициналь, 3,5-бис-(трифторметил) бензилацеталь
Раствор 1,50 г (2,2 ммоль) (+/-)-δбромфенилацетальдегида, 3,5-бис(трифторметил)бензилацеталя (пример 1), 100 мг (0,67 ммоль) иодида натрия и 3 мл этаноламина в 6 мл изопропанола нагревают до кипения с обратным холодильником в течение 20 ч. Раствор охлаждают и концентрируют до ≈25% от первоначального объема в вакууме. Концентрированный раствор растворяют в 1-молярном гидроксиде калия (120 мл), и раствор распределяют между 50 мл эфира и 20 мл двухнормального водного раствора гидроксида натрия, и слои разделяют. Органический слой промывают 20 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 65: 35 (по объему) эфира и гексана получают 1,18 г (83%) указанного в заголовке соединения в виде масла.
Раствор 1,50 г (2,2 ммоль) (+/-)-δбромфенилацетальдегида, 3,5-бис(трифторметил)бензилацеталя (пример 1), 100 мг (0,67 ммоль) иодида натрия и 3 мл этаноламина в 6 мл изопропанола нагревают до кипения с обратным холодильником в течение 20 ч. Раствор охлаждают и концентрируют до ≈25% от первоначального объема в вакууме. Концентрированный раствор растворяют в 1-молярном гидроксиде калия (120 мл), и раствор распределяют между 50 мл эфира и 20 мл двухнормального водного раствора гидроксида натрия, и слои разделяют. Органический слой промывают 20 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 65: 35 (по объему) эфира и гексана получают 1,18 г (83%) указанного в заголовке соединения в виде масла.
Спектр ПМР: 2,66 (шир. с., 2H), 2,61 и 2,68 (дд AB кв., 2H, J (AB)=12,4, J (2,61)=6,8, 6,2, J (2,68)=6,2, 6,2), 3,57 и 3,66 (дд AB кв., 2H, J (AB) = 10,8, J (3,57)=6,2, 6,2), J (3,66)=6,8, 6,2), 4,02 (д, 1H, J = 7,0), 4,37 и 4,64 (AB кв. , 2H, J = 12,5), 4,80 и 4,87 (AB кв., 2H, J = 12,8), 4,87 (д, 1H, J = 7,0), 7,31-7,40 (7H), 7,73 (≈ c, 1H), 7,81 (≈c, 3H).
ИК-спектр (в чистом виде) 3342, 1456, 1373, 1278, 1173, 1128, 704, 682.
МС-ББА-650 (M+I)+
Анализ, вычислено для C28H23F12NO3:
C - 51,78; H - 3,57; N - 2,16; F - 35,11;
найдено: C - 51,80; H - 3,67; N - 2,10, F - 35,41.
Анализ, вычислено для C28H23F12NO3:
C - 51,78; H - 3,57; N - 2,16; F - 35,11;
найдено: C - 51,80; H - 3,67; N - 2,10, F - 35,41.
Пример 3.
(+/-)-N-(2-Гидроксиэтил)-N-(проп-2-енил)фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь
Смесь 1,45 г (2,2 ммоль) (+/-)-N-(2-Гидроксиэтил)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталя (пример 2), 1,0 г (7,2 ммоль) карбоната калия, 3,0 мл (35,0 ммоль) аллилбромида и 15 мл этанола перемешивают при 60oC в течение 20 ч. Смесь охлаждают, распределяют между 100 мл эфира и 25 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния. Водный слой экстрагируют 100 мл эфира; эфирный экстракт сушат и объединяют с первоначальным органическим слоем. Объединенные органические слои концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 4:1 (по объему) гексана и эфира получают 1,36 г (88%) указанного в заголовке соединения в виде масла.
Смесь 1,45 г (2,2 ммоль) (+/-)-N-(2-Гидроксиэтил)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталя (пример 2), 1,0 г (7,2 ммоль) карбоната калия, 3,0 мл (35,0 ммоль) аллилбромида и 15 мл этанола перемешивают при 60oC в течение 20 ч. Смесь охлаждают, распределяют между 100 мл эфира и 25 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния. Водный слой экстрагируют 100 мл эфира; эфирный экстракт сушат и объединяют с первоначальным органическим слоем. Объединенные органические слои концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 4:1 (по объему) гексана и эфира получают 1,36 г (88%) указанного в заголовке соединения в виде масла.
Спектр ПМР: 2,40 (дт, 1H, J = 13,2 и 2,8), 2,93 - 3,08 (3H), 3,30 (ддт, 1H, J = 12,0, 2,8 и 1,6), 3,54 (шир. м, 2H), 3,65 (дт, 1H, J = 10,0, 2,8), 4,23 (д, 1H, J = 8,4), 4,52 и 4,58 (AB кв.:, 2H, J = 12,4), 4,85 и 4,95 (AB кв. , 2H, J = 12,4), 5,25 (д, 1H, J = 9,6), 5,28 (д, 1H, J = 16,4), 5,39 (д, 1H, J = 8,4), 5,81 (м, 1H), 7,24 - 7,40 (7H), 7,68 (с, 1H), 7,86 (с. 2H).
ИК-спектр (в чистом виде) 3457, 1362, 1278, 1132, 1056, 759, 705, 682.
МС-ББА-690 (M+I)+
Анализ, вычислено для C31H27F12NO3:
C - 53,99, H - 3,95, N - 2,03, F - 33,07;
найдено: C - 54,11, H - 4,08, N - 1,78, F - 32,75.
Анализ, вычислено для C31H27F12NO3:
C - 53,99, H - 3,95, N - 2,03, F - 33,07;
найдено: C - 54,11, H - 4,08, N - 1,78, F - 32,75.
Пример 4.
(+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенилморфолин
Стадия А.
Стадия А.
Раствор 850 мг (1,2 ммоль( (+/-)-N-(2-Гидроксиэтил)-N-(проп-2-енил) фенилглициналь, 3,5-бис-(трифторметил)бензилацеталя (пример 3) и 700 мг (3,7 ммоль) моногидрата пара-толуолсульфокислоты нагревают при кипении в течение 1,5 ч. Реакционную смесь охлаждают и распределяют между 100 мл эфира и 25 мл насыщенного водного раствора бикарбоната натрия. Слои разделяют, органический слой промывают 25 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 30 г силикагеля с использованием в качестве элюента смеси 50:1 (по объему) гексана и эфира получают 426 мг (78%) N-аллилморфолинов, которые были использованы на следующей стадии без дальнейшей очистки.
Стадия Б.
В двухгорлую колбу, снабженную пробкой и коротким устройством для перегонки, загружают раствор N-аллилморфолина со стадии А примера 4 (540 мг, 1,2 ммоль) и 80 мг (0,09 ммоль) хлористого трис(трифенилфосфин)родия (катализатор Уилкинсона) в 25 мл смеси 4:1 (по объему) ацетонитрила и воды. Эту реакционную смесь нагревают до кипения и позволяют растворителю отгоняться из реакционной смеси. Объем реакционной смеси поддерживают между 10-20 мл путем добавления растворителя через закрытый пробкой вход. Спустя 1 ч реакционную смесь обрабатывают дополнительной порцией 80 мг катализатора Уилкинсона. Спустя 6 ч реакционную смесь охлаждают и распределяют между 75 мл эфира и 50 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния. Водный слой экстрагируют 75 мл эфира; эфирный экстракт сушат и объединяют с первоначальным органическим слоем. Объединенные органические слои концентрируют в вакууме. В результате флэш-хроматографии на 35 г силикагеля с использованием в качестве элюента смеси 1:1 (по объему) эфира и гексана получают 200 мг трансизомера и 130 мг смеси цис- и транс-изомеров (в сумме 68%). Хроматографическая очистка смеси на 8 г силикагеля с использованием в качестве элюента смеси 4:1 (по объему) гексана и эфира дает 64 мг цис-V и 57 мг смеси цис- и транс-изомеров указанного в заголовке соединения.
Спектр ПМР для транс-V: 2,03 (шир. с, 1H), 2,94 (ддд, 1H, J = 11,0, 2,5 и 2,5), 3,08 (дт, 1H, J = 11,0, 3,2), 3,71 (д, 1H, J = 7,0), 3,83 (дт, 1H, J = 11,2, 2,8), 4,05 (ддд, 1H, J = 11,2, 3,2 и 3,2), 4,43 (д, 1H, J = 7,0), 4,53 и 4,88 (AB кв., 2H, J = 13,3), 7,26 - 7,45 (7H), 7,70 (с, 1H).
ИК-спектр (в чистом виде) 3333, 2859, 1456, 1374, 1278, 1131, 1082, 757, 702, 682.
МС-ББА-406 (M+I)+
Анализ, вычислено для C19H17F6NO4:
C - 56,30, H - 4,23; N - 3,46; F - 28,12;
найдено: C - 56,39; H - 4,28; N - 3,36; F - 28,32.
Анализ, вычислено для C19H17F6NO4:
C - 56,30, H - 4,23; N - 3,46; F - 28,12;
найдено: C - 56,39; H - 4,28; N - 3,36; F - 28,32.
Спектр ПМР для цис-V: 2,10 (шир. с, 1H), 3,13 (дд, 1H, J = 12,4, 3,0), 3,26 (дт, 1H, J = 12,4, 3,6), 3,65 (дд, 1H, J = 11,6 и 3,6), 4,07 (дт, 1H, J = 11,6, 3,0), 4,14 (д, 1H, J = 2,40, 4,52 и 4,82 (AB кв., 2H, J = 13,6), 4,76 (д, 1H, J = 2,4), 7,30-7,42 (6H), 7,70 (с , 1H).
МС-ББА-406 (M+1)+.
Пример 5.
(+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенил-4- метилкарбоксамидоморфолин
Раствор 105 мг (0,26 ммоль) транс-изомера (+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенилморфолина (пример 4) и 0,09 мл (0,50 ммоль) N, N-диизопропилэтиламина в 3 мл ацетонитрила обрабатывают 90 мг (0,5 ммоль) иодацетамида, и образовавшийся раствор перемешивают при комнатной температуре в течение 16 ч. Раствор концентрируют в вакууме и остаток распределяют между 20 мл этилацетата и 10 мл 0,5-нормального водного раствора гидросульфата калия. Слои разделяют, органический слой промывают 10 мл 5%-го водного раствора тиосульфата натрия, 10 мл насыщенного водного раствора бикарбоната натрия, 10 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии на 5 мг силикагеля с использованием в качестве элюента смеси 2:1 (по объему) этилацетата и гексана получают 99 мг (82%) транс-изомера указанного в заголовке соединения в виде масла.
Раствор 105 мг (0,26 ммоль) транс-изомера (+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенилморфолина (пример 4) и 0,09 мл (0,50 ммоль) N, N-диизопропилэтиламина в 3 мл ацетонитрила обрабатывают 90 мг (0,5 ммоль) иодацетамида, и образовавшийся раствор перемешивают при комнатной температуре в течение 16 ч. Раствор концентрируют в вакууме и остаток распределяют между 20 мл этилацетата и 10 мл 0,5-нормального водного раствора гидросульфата калия. Слои разделяют, органический слой промывают 10 мл 5%-го водного раствора тиосульфата натрия, 10 мл насыщенного водного раствора бикарбоната натрия, 10 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии на 5 мг силикагеля с использованием в качестве элюента смеси 2:1 (по объему) этилацетата и гексана получают 99 мг (82%) транс-изомера указанного в заголовке соединения в виде масла.
Спектр ПМР: 2,56 (дт, 1H, J=3,2 и 11,6), 2,67 и 3,16 (AB кв., 2H, J= 16,4), 2,96 (дт, 1H, J=12,0, 1,6), 3,30 (д, 1H, J=7,0), 3,86 (дт, 1H, J=3,2, 12,0), 4,08 (ддт, 1H, J=11,6, 3,2 и 1,6), 4,48 и 4,84 (AB кв., 2H, J=13,2), 4,49 (д, 1H, J= 7,0), 5,98 (шир.с, 1H), 6,83 (шир.с., 1H), 7,33 (≈с, 7H), 7,70 (с, 1H).
ИК-спектр (в чистом виде) 3445, 2838, 1682, 1278, 1132, 760, 704, 682.
МС-ББА - 463 (M+1)+.
Анализ, вычислено для C12H20F6NO3:
C - 54,54; H - 4,36; N - 6,06; F - 24,65;
найдено: C - 54,54; H - 4,52; N - 5,61; F - 24,45.
C - 54,54; H - 4,36; N - 6,06; F - 24,65;
найдено: C - 54,54; H - 4,52; N - 5,61; F - 24,45.
Аналогичный эксперимент был проведен с 40 мг (0,99 ммоль) цис-изомера (+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3- фенилморфолина (пример 4) с использованием 0,035 мл (0,2 ммоль) N,N-диизопропилэтиламина и 37 мг (0,2 ммоль) иодацетамида в этой реакции. Обработка и флеш-хроматография смеси дает 30 мг (65%) цис-изомера указанного в заголовке соединения в виде масла.
Спектр ПМР: 2,54 и 3,04 (АВ кв., 2H, J=16,8), 2,63 (дт, 1H, J=12,0, 3,6), 3,04 (д, 1H, J=11,6), 3,65 (д, 1H, J=2,8), 3,71 (ддт, 1H, J=11,6, 3,2, 1,2), 4,21 (дт, 1H, J=1,6, 2,4), 4,44 и 4,89 (АВ кв., 2H, J=13,6), 4,71 д, 1H, J= 2,8), 5,86 (шир.с., 1H), 7,15 (шир.с, 1H), 7,27-7,45 (7H), 7,73 (с, 1H).
МС-ББА- 463 (M+1)+.
Пример 6.
(+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенил-4- (метоксикарбонилметил)морфолин
Раствор 150 мг (0,37 ммоль) транс-изомера (+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенилморфолина (пример 4, R1=H) и 0,18 мл (1,0 ммоль) N, N-диизопропилэтиламина в 2 мл ацетонитрила обрабатывают 0,095 мл (1,0 ммоль) метилбромацетата, и образовавшийся раствор перемешивают при комнатной
температуре в течение 20 ч. Раствор концентрируют в вакууме, и остаток распределяют между 20 мл этилацетата и 5 мл 0,5-нормального водного раствора гидросульфата калия. Слои разделяют, органический слой промывают 10 мл 5%-го водного раствора тиосульфата натрия, 10 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии на 10 г силикагеля с использованием в качестве элюента смеси 4: 1 (по объему) гексанов и эфира получают 164 мг (93%) транс-изомера указанного в заголовке соединения в виде масла.
Раствор 150 мг (0,37 ммоль) транс-изомера (+/-)-2-(3,5-бис-(трифторметил)бензилокси)-3-фенилморфолина (пример 4, R1=H) и 0,18 мл (1,0 ммоль) N, N-диизопропилэтиламина в 2 мл ацетонитрила обрабатывают 0,095 мл (1,0 ммоль) метилбромацетата, и образовавшийся раствор перемешивают при комнатной
температуре в течение 20 ч. Раствор концентрируют в вакууме, и остаток распределяют между 20 мл этилацетата и 5 мл 0,5-нормального водного раствора гидросульфата калия. Слои разделяют, органический слой промывают 10 мл 5%-го водного раствора тиосульфата натрия, 10 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии на 10 г силикагеля с использованием в качестве элюента смеси 4: 1 (по объему) гексанов и эфира получают 164 мг (93%) транс-изомера указанного в заголовке соединения в виде масла.
Спектр ПМР: 2,79 (дт, 1H, J=3,2 и 11,2), 2,93 (дт, 1H, J=11,2, 1,6), 3,52 (д, 1H, J=7,2), 3,63 (с, 3H), 3,92 (дт, 1H, J=2,8, 11,6), 4,04 (ддд, 1H, J= 11,6, 3,2 и 1,6), 4,45 и 4,84 (АВ кв., 2H, J=13,2), 4,46 (д, 1H, J= 7,2), 7,31-7,38 (м, 6H), 7,68 (с, 1H).
ИК-спектр (в чистом виде) 2861, 1744, 1455, 1375, 1346, 1278, 1170, 887, 759, 704, 682.
МС-ББА- 478 (M+1)+.
Анализ, вычислено для C221H21F6NO4:
C - 55,35, H - 4,43, N - 2,93, F - 23,88;
найдено: C - 55,74, H - 4,50, N - 2,79, F - 24,01.
C - 55,35, H - 4,43, N - 2,93, F - 23,88;
найдено: C - 55,74, H - 4,50, N - 2,79, F - 24,01.
Пример 7.
N-Метокси-N-метил-(N-трет-бутоксикарбонил)-фенилглицинамид
Раствор 20,0 г (79,7 ммоль) (N-трет-бутоксикарбонил)-фенилглицина в 150 мл этилацетата при -10oC обрабатывают 8,8 мл (79,7 ммоль) 4-метилморфолина. По каплям добавляют за 10 мин 10,3 мл изобутилхлорформиата (79,7 ммоль), поддерживая температуру при -10oC. Образовавшуюся суспензию перемешивают на холоду 15 минут. Реакционную смесь обрабатывают 11,6 г (119,0 ммоль) хлористоводородного N, O-диметилгидроксиламина. Добавляют вторую порцию 4-метилморфолина (13 мл, 119 ммоль), и смесь перемешивают при -10oC 15 минут и при 25oC в течение 2 ч. Реакционную смесь распределяют между 100 мл этилацетата и 100 мл 10%-го водного раствора лимонной кислоты и слои разделяют. Органический слой промывают 100 мл насыщенного водного раствора бикарбоната натрия, 100 мл насыщенного водного раствора хлорида аммония, сушат над сульфатом магния и концентрируют в вакууме. Кристаллизация из гексанов при -20oC в течение 72 ч дает 8,0 г (34%) указанного в заголовке соединения в виде твердого вещества.
Раствор 20,0 г (79,7 ммоль) (N-трет-бутоксикарбонил)-фенилглицина в 150 мл этилацетата при -10oC обрабатывают 8,8 мл (79,7 ммоль) 4-метилморфолина. По каплям добавляют за 10 мин 10,3 мл изобутилхлорформиата (79,7 ммоль), поддерживая температуру при -10oC. Образовавшуюся суспензию перемешивают на холоду 15 минут. Реакционную смесь обрабатывают 11,6 г (119,0 ммоль) хлористоводородного N, O-диметилгидроксиламина. Добавляют вторую порцию 4-метилморфолина (13 мл, 119 ммоль), и смесь перемешивают при -10oC 15 минут и при 25oC в течение 2 ч. Реакционную смесь распределяют между 100 мл этилацетата и 100 мл 10%-го водного раствора лимонной кислоты и слои разделяют. Органический слой промывают 100 мл насыщенного водного раствора бикарбоната натрия, 100 мл насыщенного водного раствора хлорида аммония, сушат над сульфатом магния и концентрируют в вакууме. Кристаллизация из гексанов при -20oC в течение 72 ч дает 8,0 г (34%) указанного в заголовке соединения в виде твердого вещества.
Спектр ПМР: 1,40 (с, 9H), 3,2 (с, 3H), 3,40 (с, 3H), 5,8 (м, 2H), 7,40 (м, 5H).
Пример 8.
Диэтил (2-оксо-3-трет-бутоксикарбамидо-3-фенил)-пропилфосфонат
Раствор 7,45 мл (51,0 ммоль) диэтилметилфосфоната в тетрагидрофуране при -78oC обрабатывают 31,8 мл (51,0 ммоль) 1,6-молярного раствора н-бутиллития в гексане, и образовавшуюся смесь перемешивают на холоду 30 минут. Добавляют раствор N-метокси-N-метил-(N-трет-бутоксикарбонил)-фенилглицинамида (4,0 г, 14,0 ммоль) из примера 7 в 20 мл тетрагидрофурана, и реакционную смесь перемешивают при -78oC 15 мин и при 25oC 15 мин. Реакцию прерывают, добавляя 150 мл насыщенного водного раствора хлорида аммония, разбавляют 300 мл этилацетата и слоя разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на силикагеле с использованием в качестве элюента смеси 7:3 и затем 4:1 (по объему) этилацетата и гексана получают 4,8 г (92%) транс-изомера указанного в заголовке соединения в виде масла.
Раствор 7,45 мл (51,0 ммоль) диэтилметилфосфоната в тетрагидрофуране при -78oC обрабатывают 31,8 мл (51,0 ммоль) 1,6-молярного раствора н-бутиллития в гексане, и образовавшуюся смесь перемешивают на холоду 30 минут. Добавляют раствор N-метокси-N-метил-(N-трет-бутоксикарбонил)-фенилглицинамида (4,0 г, 14,0 ммоль) из примера 7 в 20 мл тетрагидрофурана, и реакционную смесь перемешивают при -78oC 15 мин и при 25oC 15 мин. Реакцию прерывают, добавляя 150 мл насыщенного водного раствора хлорида аммония, разбавляют 300 мл этилацетата и слоя разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на силикагеле с использованием в качестве элюента смеси 7:3 и затем 4:1 (по объему) этилацетата и гексана получают 4,8 г (92%) транс-изомера указанного в заголовке соединения в виде масла.
Спектр ПМР: 1,2-1,42 (15H), 2,84 (дд, 1H), 3,20 (дд, 1H), 4,0-4,20 (м, 4H), 5,50 (д, 1H), 5,94 (шир.с., 1H), 7,32 (м, 5H).
Пример 9.
N-трет-Бутоксикарбонил-1-фенил-2-оксо-4-(3,5-бис-(трифторметил) фенил)бут-3-енамин
Раствор 4,80 г (12,5 ммоль) диэтил (2-оксо-3-трет-бутоксикарбамидо-3-фенил)-пропилфосфоната (пример 8) в 20 мл тетрагидрофурана по каплям добавляют к суспензии 1,05 г (26,3 ммоль, 60%-ная дисперсия в минеральном масле) гидрида натрия в 30 мл тетрагидрофурана при 0oC. Спустя 30 минут медленно добавляют 2,06 мл (12,5 ммоль) 3,5-бис-(трифторметил)бензальдегида, и образовавшуюся смесь перемешивают на холоду 15 мин. Реакцию прерывают, добавляя 50 мл насыщенного водного раствора хлорида аммония, разбавляют 50 мл этилацетата, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на силикагеле с использованием в качестве элюента смеси 19:1 и затем 9:1 (по объему) этилацетата и петролейного эфира получают 3,3 г (56%) указанного в заголовке соединения в виде твердого вещества.
Раствор 4,80 г (12,5 ммоль) диэтил (2-оксо-3-трет-бутоксикарбамидо-3-фенил)-пропилфосфоната (пример 8) в 20 мл тетрагидрофурана по каплям добавляют к суспензии 1,05 г (26,3 ммоль, 60%-ная дисперсия в минеральном масле) гидрида натрия в 30 мл тетрагидрофурана при 0oC. Спустя 30 минут медленно добавляют 2,06 мл (12,5 ммоль) 3,5-бис-(трифторметил)бензальдегида, и образовавшуюся смесь перемешивают на холоду 15 мин. Реакцию прерывают, добавляя 50 мл насыщенного водного раствора хлорида аммония, разбавляют 50 мл этилацетата, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на силикагеле с использованием в качестве элюента смеси 19:1 и затем 9:1 (по объему) этилацетата и петролейного эфира получают 3,3 г (56%) указанного в заголовке соединения в виде твердого вещества.
Спектр ПМР: 1,40 (с, 9H), 5,38 (д, 1H), 5,90 (д, 1H), 6,80 (д, 1H), 7,39 (м, 5H), 7,70 (с, 1H), 7,84 (с, 3H).
Пример 10.
Хлористоводородный 1-фенил-2-гидрокси-4-(3,5-бис-(трифторметил) фенил)бут-3-енамин
Раствор 1,0 г (2,1 ммоль) N-трет-бутоксикарбонил-1-фенил- 2-оксо-4-(3,5-бис-(трифторметил)фенил)бут-3-енамина (пример 9) в 30 мл метанола при 0oC обрабатывают 241 мг (6,3 ммоль) боргидрида натрия. Спустя 30 минут реакцию прерывают, добавляя 50 мл воды, и концентрируют в вакууме, удаляя метанол. Смесь распределяют между 100 мл этилацетата и 50 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате кристаллизации из смеси эфира и гексанов получают 680 мг (68%) указанного в заголовке соединения в виде смеси 5:1 диастереомеров (каждый защищен трет-бутоксикарбаматом).
Раствор 1,0 г (2,1 ммоль) N-трет-бутоксикарбонил-1-фенил- 2-оксо-4-(3,5-бис-(трифторметил)фенил)бут-3-енамина (пример 9) в 30 мл метанола при 0oC обрабатывают 241 мг (6,3 ммоль) боргидрида натрия. Спустя 30 минут реакцию прерывают, добавляя 50 мл воды, и концентрируют в вакууме, удаляя метанол. Смесь распределяют между 100 мл этилацетата и 50 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате кристаллизации из смеси эфира и гексанов получают 680 мг (68%) указанного в заголовке соединения в виде смеси 5:1 диастереомеров (каждый защищен трет-бутоксикарбаматом).
Спектр ПМР (* указывает резонансы меньшего диастереомера):
1,40 (с, 9H), 4,60 (дд, 1H), 4,90 (шир.с., 1H), 5,20 (шир.д., 1H), 6,30 (дд, 1H), 6,40 (дд, 1H*), 6,70 (дд, 1H), 6,80 (дд, 1H*), 7,40 (м, 5H), 7,80 (м, 3H).
1,40 (с, 9H), 4,60 (дд, 1H), 4,90 (шир.с., 1H), 5,20 (шир.д., 1H), 6,30 (дд, 1H), 6,40 (дд, 1H*), 6,70 (дд, 1H), 6,80 (дд, 1H*), 7,40 (м, 5H), 7,80 (м, 3H).
Раствор указанного в заголовке соединения, защищенного трет-бутоксикарбонилом в метаноле (насыщенном хлористым водородом), выдерживают в течение 72 ч. Раствор концентрируют в вакууме. В результате перекристаллизации образовавшегося твердого вещества из смеси эфира и гексанов получают 500 мг (80%) гидрохлорида указанного в заголовке соединения в виде твердого вещества.
Спектр ПМР: 4,20 (шир. с, 1H), 4,40 (д, 1H), 6,20 (дд, 1H), 6,60 (дд, 1H), 7,30 (м, 5H), 7,80 (м, 3H).
Гидрохлорид указанного соединения растворяют в этилацетате и 1 н. водном растворе гидроксида натрия. Слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме, получая указанное в заголовке соединение в виде свободного основания.
Пример 11.
2-(2-(3,5-бис-(трифторметил)фенил)этенил)-3-фенил-5-оксоморфолин
Раствор 1,95 г (5,2 ммоль) 1-фенил-2-гидрокси-4-(3,5-бис-(трифторметил)фенил)бут-3-енамина (пример 10) в 20 мл толуола добавляют к суспензии 250 мг (6,2 ммоль, 60%-ная дисперсия в минеральном масле) гидрида натрия в 30 мл толуола, и образовавшуюся смесь перемешивают при комнатной температуре 15 мин. Медленно добавляют раствор 0,6 мл (1,15 миллимоль) этилхлорацетата в 5 мл толуола и образовавшуюся смесь нагревают при температуре кипения в течение 3 ч. Реакционную смесь охлаждают, прерывают реакцию, добавляя 50 мл насыщенного водного раствора хлорида аммония, разбавляют 50 мл этилацетата, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии с использованием в качестве элюента смеси 4: 1, затем 3:1 и 1:1 (по объему) этилацетата и гексана, и затем элюируя чистым этилацетатом, получают 300 мг транс-изомера и 800 мг цис-изомера соединения, указанного в заголовке и (суммарно 55%), оба изомера в твердом виде.
Раствор 1,95 г (5,2 ммоль) 1-фенил-2-гидрокси-4-(3,5-бис-(трифторметил)фенил)бут-3-енамина (пример 10) в 20 мл толуола добавляют к суспензии 250 мг (6,2 ммоль, 60%-ная дисперсия в минеральном масле) гидрида натрия в 30 мл толуола, и образовавшуюся смесь перемешивают при комнатной температуре 15 мин. Медленно добавляют раствор 0,6 мл (1,15 миллимоль) этилхлорацетата в 5 мл толуола и образовавшуюся смесь нагревают при температуре кипения в течение 3 ч. Реакционную смесь охлаждают, прерывают реакцию, добавляя 50 мл насыщенного водного раствора хлорида аммония, разбавляют 50 мл этилацетата, и слои разделяют. Органический слой сушат над сульфатом магния и концентрируют в вакууме. В результате флеш-хроматографии с использованием в качестве элюента смеси 4: 1, затем 3:1 и 1:1 (по объему) этилацетата и гексана, и затем элюируя чистым этилацетатом, получают 300 мг транс-изомера и 800 мг цис-изомера соединения, указанного в заголовке и (суммарно 55%), оба изомера в твердом виде.
Спектр ПМР для цис-изомера: 1,20-1,40 (м, 1H), 1,5-1,62 (м, 1H), 2,6 - 2,98 (м, 2H), 3,86 (дт, 1H), 4,24 (д, 1H), 4,34 (дд, 1H), 4,45 (д, 1H), 6,40 (шир. с, 1H), 7,24 (м, 2H), 7,40 (м, 3H), 7,50 (с, 2H), 7,70 (с, 1H).
Пример 12.
3-фенил-2-(2-(3,5-бис-(трифторметил)фенил)этил)-морфолин
Раствор 0,095 г (0,23 ммоль) 2-(2-(3,5-бис-(трифторметил)- фенил)этенил)-3-фенил-5-оксоморфолина (пример 11) в 10 мл смеси 1 : 1 (по объему) этанола и этилацетата обрабатывают с 10 мг гидроксида палладия, и образовавшуюся смесь перемешивают в атмосфере водорода в течение 2 ч. Катализатор отфильтровывают, и фильтрат концентрируют в вакууме. Сырой продукт используют непосредственно без дополнительной очистки.
Раствор 0,095 г (0,23 ммоль) 2-(2-(3,5-бис-(трифторметил)- фенил)этенил)-3-фенил-5-оксоморфолина (пример 11) в 10 мл смеси 1 : 1 (по объему) этанола и этилацетата обрабатывают с 10 мг гидроксида палладия, и образовавшуюся смесь перемешивают в атмосфере водорода в течение 2 ч. Катализатор отфильтровывают, и фильтрат концентрируют в вакууме. Сырой продукт используют непосредственно без дополнительной очистки.
Раствор 65 мг этого сырого морфолинона в 10 мл тетрагидрофурана обрабатывают 0,84 мл 1-молярного раствора комплекса боран*тетрагидрофуран в тетрагидрофуране, и образовавшийся раствор кипятят в течение 16 ч. Реакцию прерывают добавлением 10 мл метанола и 70 мг карбоната калия, и полученную смесь нагревают при кипении в течение 3 ч. Все летуче вещества удаляют в вакууме, и остаток распределяют между 20 мл этилацетата и 10 мл насыщенного водного раствора хлорида аммония. Органический слой отделяют, сушат над карбонатом натрия и концентрируют в вакууме. Остаток растворяют в метаноле, насыщенном хлористым водородом, и концентрируют в вакууме. Остаток растворяют с эфиром; полученное твердое вещество отфильтровывают и сушат, получая 32 мг (46%) гидрохлорида указанного в заголовке соединения с т.пл. 114 - 116oC.
Спектр ПМР: 1,42 (м, 1H), 1,66 - 1,84 (м, 1H), 2,7 - 2,94 (м, 2H), 3,00 (м, 1H), 3,3 - 3,46 (м, 1H), 3,8 - 3,94 (м, 2H), 4,10 (м, 1H), 4,20 (д, 1H), 7,40 (м, 3H), 7,64 (м, 3H), 7,64 (м, 5H).
MC-Cl 402 (M + 1)+
Пример 13.
Пример 13.
N-бензил-(S)-фенилглицин
Раствор 1,51 г (10 ммоль) S-фенилглицина в 5 мл 2-нормального водного раствора гидроксида натрия обрабатывают 1,0 мл (10 ммоль) бензальдегида и перемешивают при комнатной температуре 20 минут. Раствор разбавляют 5 мл метанола, охлаждают до 0oC и осторожно обрабатывают 200 мг (5,3 ммоль) боргидрида натрия. Удаляют охлаждающую баню, и реакционную смесь перемешивают при комнатной температуре 1,5 ч. Реакционную смесь разбавляют 20 мл воды и экстрагируют 2 раза по 25 мл хлористого метилена. Водный слой подкисляют концентрированной соляной кислотой до pH 6, и выпавший твердый осадок отфильтровывают, промывают 50 мл воды 50 мл смеси 1 : 1 (по объему) метанола и этилового эфира и 50 мл эфира и сушат, получая 1,83 г (76%) продукта с т. плавления 230 - 232oC.
Раствор 1,51 г (10 ммоль) S-фенилглицина в 5 мл 2-нормального водного раствора гидроксида натрия обрабатывают 1,0 мл (10 ммоль) бензальдегида и перемешивают при комнатной температуре 20 минут. Раствор разбавляют 5 мл метанола, охлаждают до 0oC и осторожно обрабатывают 200 мг (5,3 ммоль) боргидрида натрия. Удаляют охлаждающую баню, и реакционную смесь перемешивают при комнатной температуре 1,5 ч. Реакционную смесь разбавляют 20 мл воды и экстрагируют 2 раза по 25 мл хлористого метилена. Водный слой подкисляют концентрированной соляной кислотой до pH 6, и выпавший твердый осадок отфильтровывают, промывают 50 мл воды 50 мл смеси 1 : 1 (по объему) метанола и этилового эфира и 50 мл эфира и сушат, получая 1,83 г (76%) продукта с т. плавления 230 - 232oC.
Анализ, вычислено для C15H15NO2:
C - 74,66, H - 6,27, N - 5,81;
найдено C - 74,17, H - 6,19, N - 5,86.
C - 74,66, H - 6,27, N - 5,81;
найдено C - 74,17, H - 6,19, N - 5,86.
Пример 14.
3-(S)-фенил-4-бензил-2-морфолинон
Смесь 4,0 г (16,6 ммоль) N-бензил-S-фенилглицина (из примера 13), 5,00 г (36 ммоль) карбоната калия, 10 мл дибромэтана и 25 мл диметилформамида перемешивают при 100oC в течение 20 ч. Смесь охлаждают и распределяют между 200 мл этилового эфира и 100 мл воды. Слои разделяют, и органический слой промывают 3 раза по 50 мл воды, сушат над сульфатом магния и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 125 г силикагеля, который элюируют смесью 9 : 1, затем 4 : 1 (по объему) гексана и эфира, и получают 2,41 г (54%) продукта в твердом виде с т.пл. 98 - 100oC.
Смесь 4,0 г (16,6 ммоль) N-бензил-S-фенилглицина (из примера 13), 5,00 г (36 ммоль) карбоната калия, 10 мл дибромэтана и 25 мл диметилформамида перемешивают при 100oC в течение 20 ч. Смесь охлаждают и распределяют между 200 мл этилового эфира и 100 мл воды. Слои разделяют, и органический слой промывают 3 раза по 50 мл воды, сушат над сульфатом магния и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 125 г силикагеля, который элюируют смесью 9 : 1, затем 4 : 1 (по объему) гексана и эфира, и получают 2,41 г (54%) продукта в твердом виде с т.пл. 98 - 100oC.
MC-ББА: m/z 268 (M + H, 100%).
Спектр ПМР (в дейтерохлороформе), 200 МГц, м.д.): 2,54 - 2,68 (м, 1H), 2,96 (дт, J = 12,8 и 2,8, 1H), 3,14 (дт, J = 13,3, 1H), 3,75 (д, J = 13,3, 1H), 4,23 (с, 1H), 4,29 - 4,38 (м, 1H), 4,53 (дт, J = 3,2 и 11,0), 7,2 - 7,56 (м, 10H).
Анализ, вычислено для C17H17NO2:
C - 78,38; H - 6,41; N - 5,24,
найдено: C - 76,06; H - 6,40; N - 5,78.
C - 78,38; H - 6,41; N - 5,24,
найдено: C - 76,06; H - 6,40; N - 5,78.
Пример 15.
2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолин
Стадия А.
Стадия А.
3,5-бис-(трифторметил)бензиловый спирт, трифторметансульфонатный эфир
Раствор 1,0 г (4,1 ммоль) 3,5-бис-(трифторметил)бензилового спирта и 1,05 г (5,12 ммоль) 2,6-ди-трет-бутил-4-метилпиридина в 45 мл осушенного четыреххлористого углерода в атмосфере азота обрабатывают 0,74 мл (4,38 ммоль) ангидрида трифторметансульфокислоты при комнатной температуре. Вскоре после добавления ангидрида образуется белый осадок. Спустя 90 мин суспензию отфильтровывают в атмосфере азота на фильтре Шленка, и фильтрат концентрируют в вакууме. Остаток, который представляет собой двухфазное масло, растворяют в 10 мл сухого толуола в атмосфере азота. Полученный прозрачный раствор был использован немедленно на стадии Б ниже.
Раствор 1,0 г (4,1 ммоль) 3,5-бис-(трифторметил)бензилового спирта и 1,05 г (5,12 ммоль) 2,6-ди-трет-бутил-4-метилпиридина в 45 мл осушенного четыреххлористого углерода в атмосфере азота обрабатывают 0,74 мл (4,38 ммоль) ангидрида трифторметансульфокислоты при комнатной температуре. Вскоре после добавления ангидрида образуется белый осадок. Спустя 90 мин суспензию отфильтровывают в атмосфере азота на фильтре Шленка, и фильтрат концентрируют в вакууме. Остаток, который представляет собой двухфазное масло, растворяют в 10 мл сухого толуола в атмосфере азота. Полученный прозрачный раствор был использован немедленно на стадии Б ниже.
Стадия Б.
4-Бензил-2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)- фенилморфолин
Раствор 0,50 г (1,87 ммоль) N-бензил-3-(S)-фенилморфолин-2- она (из примера 14) в 10 мл сухого ТГФ охлаждают до -75oC в атмосфере азота и обрабатывают по каплям 2,06 мл (2,06 ммоль) 1-молярным раствором три(втор-бутил)боргидрида лития (L-Селектрид) в тетрагидрофуране. После перемешивания раствора при -75oC в течение 30 мин через полую трубочку добавляют раствор 3,5-бис-(трифторметил)бензиловый спирт - трифторметансульфонатного эфира в толуоле, так чтобы внутренняя температура поддерживалась ниже -60oC. Образовавшийся раствор перемешивают при -75oC 1 ч и затем при температуре между -38oC и -50oC в течение 2 ч. Затем раствор выливают в смесь 25 мл этилацетата и 20 мл насыщенного водного раствора бикарбоната натрия, и слои разделяют. Водную фазу экстрагируют 2 раза по 30 мл этилацетата, объединенные органические слои сушат над сульфатом натрия, смесь фильтруют, и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 130 г силикагеля, который элюируют 2 литрами смеси 100 : 5 гексана и этилацетата, получая 0,68 г (73%) масла, которое по данным ПМР-спектра является смесью 20 : 1 цис-: транс-морфолинов.
Раствор 0,50 г (1,87 ммоль) N-бензил-3-(S)-фенилморфолин-2- она (из примера 14) в 10 мл сухого ТГФ охлаждают до -75oC в атмосфере азота и обрабатывают по каплям 2,06 мл (2,06 ммоль) 1-молярным раствором три(втор-бутил)боргидрида лития (L-Селектрид) в тетрагидрофуране. После перемешивания раствора при -75oC в течение 30 мин через полую трубочку добавляют раствор 3,5-бис-(трифторметил)бензиловый спирт - трифторметансульфонатного эфира в толуоле, так чтобы внутренняя температура поддерживалась ниже -60oC. Образовавшийся раствор перемешивают при -75oC 1 ч и затем при температуре между -38oC и -50oC в течение 2 ч. Затем раствор выливают в смесь 25 мл этилацетата и 20 мл насыщенного водного раствора бикарбоната натрия, и слои разделяют. Водную фазу экстрагируют 2 раза по 30 мл этилацетата, объединенные органические слои сушат над сульфатом натрия, смесь фильтруют, и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 130 г силикагеля, который элюируют 2 литрами смеси 100 : 5 гексана и этилацетата, получая 0,68 г (73%) масла, которое по данным ПМР-спектра является смесью 20 : 1 цис-: транс-морфолинов.
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ основной (цис-изомер): 2,37 (т. д. , J = 12, 3,6, 1H), 2,86 (≈ т, J = 13, 2H), 3,57 (д, J = 2,6, 1H), 3,63 (д. кв, J = 11,3, 1,6, 1H), 3,89 (д, J = 13,3, 1H), 4,12 (тд, J = 11,6, 2,4, 1H), 4,40 (д, J = 13,6, 1H), 4,69 (д, J = 2,9, 1H), 4,77 (д, J = 13,6, 1H), 7,2 - 7,4 (м, 8H), 7,43 (с, 2H), 7,55 (шир. д., 2H), 7,69 (с, 1H).
Стадия В.
2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолин
Смесь 0,68 г (1,37 ммоль) 4-бензил-2-(S)-3,5-бис- (трифторметил)бензилокси)-3-(S)-фенилморфолина и 280 мг катализатора 10% палладия на угле в 36 мл смеси 97 : 3 этанола и воды перемешивают при давлении водорода 1 атмосфера в течение 15 ч. Смесь фильтруют через Целит, лепешку на фильтре тщательно промывают этанолом, и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 68 г силикагеля, который элюируют 1 литром смеси 25 : 75 гексана и диэтилового эфира, получая 0,443 г (30%) масла, которое по данным ПМР-спектра является чистым цис-морфолином.
Смесь 0,68 г (1,37 ммоль) 4-бензил-2-(S)-3,5-бис- (трифторметил)бензилокси)-3-(S)-фенилморфолина и 280 мг катализатора 10% палладия на угле в 36 мл смеси 97 : 3 этанола и воды перемешивают при давлении водорода 1 атмосфера в течение 15 ч. Смесь фильтруют через Целит, лепешку на фильтре тщательно промывают этанолом, и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 68 г силикагеля, который элюируют 1 литром смеси 25 : 75 гексана и диэтилового эфира, получая 0,443 г (30%) масла, которое по данным ПМР-спектра является чистым цис-морфолином.
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,8 (шир. с, 1H), 3,10 (дд, J = 12,5, 2,9, 1H), 3,24 (тд, J = 12,2, 3,6, 1H), 3,62 (дд, J = 11,3, 2,5, 1H), 4,04 (тд, J = 11,7, 7,3, 1H), 4,11 (д, J = 2,4, 1H), 4,49 (д, J = 13,5, 1H), 4,74 (д, J = 2,5, 1H), 4,80 (д, J = 13,3, 1H), 7,25 - 7,40 (м, 5H), 7,40 (с, 2H), 7,68 (с, 1H).
Анализ, вычислено для C19H17F6NO2:
C - 56,30; H - 4,23; N - 3,46; F - 28,12;
найдено: C - 56,20; H - 4,29; N - 3,34; F - 27,94.
C - 56,30; H - 4,23; N - 3,46; F - 28,12;
найдено: C - 56,20; H - 4,29; N - 3,34; F - 27,94.
Пример 16.
2-(R)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенилморфолин
Указанное в заголовке вещество было приготовлено из (R)-фенилглицина, используя методики примеров 13, 14 и 15.
Указанное в заголовке вещество было приготовлено из (R)-фенилглицина, используя методики примеров 13, 14 и 15.
Пример 17.
4-(3-(1,2,4-Триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)- бензилокси)-3-(S)-фенилморфолин
Стадия A.
Стадия A.
N-формил-2-хлорацетамидразон
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 30 мл сухого метанола охлаждают до 0oC в атмосфере азота и обрабатывают 0,1 г (1,8 ммоль) метоксида натрия. Смеси дают нагреться до комнатной температуры, и ее перемешивают 30 мин и добавляют 0,106 мл (1,8 ммоль) уксусной кислоты. Затем в образовавшийся раствор добавляют 3,9 г (64,9 моль) гидразида муравьиной кислоты, и этот материал перемешивают 30 мин. Реакционную смесь концентрируют в вакууме до твердого вещества, которое используют как таковое на стадии Б ниже.
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 30 мл сухого метанола охлаждают до 0oC в атмосфере азота и обрабатывают 0,1 г (1,8 ммоль) метоксида натрия. Смеси дают нагреться до комнатной температуры, и ее перемешивают 30 мин и добавляют 0,106 мл (1,8 ммоль) уксусной кислоты. Затем в образовавшийся раствор добавляют 3,9 г (64,9 моль) гидразида муравьиной кислоты, и этот материал перемешивают 30 мин. Реакционную смесь концентрируют в вакууме до твердого вещества, которое используют как таковое на стадии Б ниже.
Стадия Б.
4-(3-(1,2,4-Триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)- бензилокси)-3-(S)-фенилморфолин
Раствор 0,295 г (0,73 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина (из примера 15) в 10 мл сухого диметилформамида обрабатывают, 0,302 г (2,18 ммоль) безводного карбоната калия и затем добавляют 0,168 г (1,24 ммоль) N-формил-2-хлорацетамидразона (из примера 17, стадия А), и суспензию перемешивают при 60oC в течение 4 ч. Затем смесь нагревают до 120oC в течение 4,5 ч. После охлаждения реакционную смесь разбавляют 80 мл этилацетата, и органический слой промывают 3 раза по 20 мл воды. Органический слой сушат под сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 67 г силикагеля, который элюируют 1,5 литрами смеси 100 : 2 хлористого метилена и метанола, получая 0,22 г желтого вещества, которое было перекристаллизовано из смеси гексан/хлористый метилен, получая 0,213 г (60%) белого кристаллического вещества с т. пл. 134 - 135oC.
Раствор 0,295 г (0,73 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина (из примера 15) в 10 мл сухого диметилформамида обрабатывают, 0,302 г (2,18 ммоль) безводного карбоната калия и затем добавляют 0,168 г (1,24 ммоль) N-формил-2-хлорацетамидразона (из примера 17, стадия А), и суспензию перемешивают при 60oC в течение 4 ч. Затем смесь нагревают до 120oC в течение 4,5 ч. После охлаждения реакционную смесь разбавляют 80 мл этилацетата, и органический слой промывают 3 раза по 20 мл воды. Органический слой сушат под сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 67 г силикагеля, который элюируют 1,5 литрами смеси 100 : 2 хлористого метилена и метанола, получая 0,22 г желтого вещества, которое было перекристаллизовано из смеси гексан/хлористый метилен, получая 0,213 г (60%) белого кристаллического вещества с т. пл. 134 - 135oC.
Спектр МС-ББА: m/z 487 (M + H, 100%), 259 (35%), 243 (65%), 227 (50%), 174 (25%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 2,67 (т.д., J = 11,9, 3,4, 1H), 2,90 (шир. д., J = 11,7, 1H), 3,43 (д, J = 15,2, 1H), 3,66 (≈ дд, J = 13, 1,9, 2H), 3,88 (д, J = 15,1, 1H), 4,17 (тд, J = 11,7, 2,3, 1H), 4,42 (д, J = 13,5, 1H), 4,69 (д, J = 2,6, 1H), 4,77 (д, J = 13,5, 1H), 7,30 - 7,50 (м, 7H), 7,70 (с, 1H), 7,94 (с, 1H).
Пример 18.
4-(3-(5-Оксо-1H,4H-1,2,4-триазоло)метил)-2-(S)- (3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолин
Стадия А.
Стадия А.
N-Метилкарбокси-2-хлорацетамидразон
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 35 мл сухого метанола охлаждают до 0oC и обрабатывают 0,105 г (1,9 ммоль) метоксида натрия. Удаляют баню со льдом, и смеси дают перемешаться при комнатной температуре в течение 30 мин. Затем к реакционной смеси добавляют 0,110 мл (1,9 ммоль) уксусной кислоты и после этого добавляют 5,8 г (64,9 ммоль) метилгидразинкарбоксилата. После перемешивания 30 мин, при комнатной температуре суспензию концентрируют в вакууме и помещают на ночь в линию высокого вакуума, получая 10,5 г (98%) желтого порошка, который используется на стадии B ниже.
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 35 мл сухого метанола охлаждают до 0oC и обрабатывают 0,105 г (1,9 ммоль) метоксида натрия. Удаляют баню со льдом, и смеси дают перемешаться при комнатной температуре в течение 30 мин. Затем к реакционной смеси добавляют 0,110 мл (1,9 ммоль) уксусной кислоты и после этого добавляют 5,8 г (64,9 ммоль) метилгидразинкарбоксилата. После перемешивания 30 мин, при комнатной температуре суспензию концентрируют в вакууме и помещают на ночь в линию высокого вакуума, получая 10,5 г (98%) желтого порошка, который используется на стадии B ниже.
Спектр ПМР (в дейтерометаноле, 400 МГц, м.д.): δ 3,71 (с, 3H), 4,06 (с, 2H).
Стадия Б.
4-(2-(N-Метилкарбокси-ацетамидразоно-2-(S)-(3,5-бис-(трифторметил) бензилокси)-3-(S)-фенилморфолин
Раствор 2,30 г (5,7 ммоль) (2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина (из примера 15), 1,13 г (6,8 ммоль) N-метилкарбокси-2-хлорацетамидразона (со стадии А) и 1,5 мл (8,6 ммоль) N,N-диизопропилэтиламина в 25 мл сухого ацетонитрила перемешивают при комнатной температуре в течение 20 ч. Выпавший в осадок продукт отфильтровывают, промывают 5 мл охлажденного льдом ацетонитрила и сушат, получая 1,83 г белого твердого вещества. Фильтрат концентрируют в вакууме, и остаток распределяют между 50 мл хлористого метилена и 20 мл воды. Слои разделяют, и органический слой экстрагируют 50 мл хлористого метилена. Экстракт сушат, объединяют с первоначальным органическим слоем, и объединенные органические слои концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 30 г силикагеля, который элюируют смесью 50:1:0,1 (по объему) хлористого метилена/метанола/гидроксида аммония, получая дополнительно 1,09 г продукта (суммарно 96%).
Раствор 2,30 г (5,7 ммоль) (2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина (из примера 15), 1,13 г (6,8 ммоль) N-метилкарбокси-2-хлорацетамидразона (со стадии А) и 1,5 мл (8,6 ммоль) N,N-диизопропилэтиламина в 25 мл сухого ацетонитрила перемешивают при комнатной температуре в течение 20 ч. Выпавший в осадок продукт отфильтровывают, промывают 5 мл охлажденного льдом ацетонитрила и сушат, получая 1,83 г белого твердого вещества. Фильтрат концентрируют в вакууме, и остаток распределяют между 50 мл хлористого метилена и 20 мл воды. Слои разделяют, и органический слой экстрагируют 50 мл хлористого метилена. Экстракт сушат, объединяют с первоначальным органическим слоем, и объединенные органические слои концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 30 г силикагеля, который элюируют смесью 50:1:0,1 (по объему) хлористого метилена/метанола/гидроксида аммония, получая дополнительно 1,09 г продукта (суммарно 96%).
Спектр МС-ББА: m/z 535 (M+H, 100%), 462 (16%), 291 (30%), 226 (35%), 173 (25%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 2,53 (дт. J = 3,5, 12,2, 1H), 2,59 (д, J = 14,6, 1H), 2,94 (д, J = 11,8, 1H), 3,37 (д, J = 14,6, 1H), 3,58 (д, J = 2,8, 1H), 3,62 - 3,72 (м, 1H), 3,75 (с, 3H), 4,16 (дт, J = 2,2, 11,8, 1H), 4,44 (д, J = 13,2, 1H), 4,70 (д, J = 2,8, 1H), 4,79 (д, J = 13,2), 5,55 (шир, с, 2H), 7,30 - 7,46 (м, 7H), 7,72 (с, 1H).
Стадия B.
2-(S)-(3,5-бис-(трифторметил)бензилокси)-4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метил)-3-(S)-фенилморфолин
Раствор 2,89 г (5,4 ммоль)-4-(2-(N-Метилкарбокси-ацетамидразоно-2-(S)-(3,5-бис-(трифторметил) бензилокси)-3-(S)-фенилморфолина (стадия Б) в 36 мл ксилолов нагревают при кипячении в течение 1,5 ч. Раствор охлаждают и концентрируют в вакууме. Остаток растворяют в 50 мл смеси 3:1 (по объему) гексанов и этилацетата, что вызывает кристаллизацию продукта. Продукт фильтруют и сушат, получая 1,85 г твердого вещества. Перекристаллизация этого твердого вещества из 30 мл смеси 4:1 (по объему) гексана/этилацетата дает 1,19 г чистого продукта в виде белого кристаллического вещества с т.пл. 156-157oC. Все маточные растворы стадии кристаллизации были объединены и сконцентрированы в вакууме. Остаток очищают методом флэш-хроматографии на 30 г силикагеля, который элюируют смесью 50:1:0,1 (по объему) хлористого метилена/метанола/гидроксида аммония, получая дополнительно 0,69 г твердого вещества. Три перекристаллизации из 20 мл смеси 4:1 гексана и этилацетата дают дополнительно 0,39 г чистого продукта в виде белого твердого вещества (суммарно 58%).
Раствор 2,89 г (5,4 ммоль)-4-(2-(N-Метилкарбокси-ацетамидразоно-2-(S)-(3,5-бис-(трифторметил) бензилокси)-3-(S)-фенилморфолина (стадия Б) в 36 мл ксилолов нагревают при кипячении в течение 1,5 ч. Раствор охлаждают и концентрируют в вакууме. Остаток растворяют в 50 мл смеси 3:1 (по объему) гексанов и этилацетата, что вызывает кристаллизацию продукта. Продукт фильтруют и сушат, получая 1,85 г твердого вещества. Перекристаллизация этого твердого вещества из 30 мл смеси 4:1 (по объему) гексана/этилацетата дает 1,19 г чистого продукта в виде белого кристаллического вещества с т.пл. 156-157oC. Все маточные растворы стадии кристаллизации были объединены и сконцентрированы в вакууме. Остаток очищают методом флэш-хроматографии на 30 г силикагеля, который элюируют смесью 50:1:0,1 (по объему) хлористого метилена/метанола/гидроксида аммония, получая дополнительно 0,69 г твердого вещества. Три перекристаллизации из 20 мл смеси 4:1 гексана и этилацетата дают дополнительно 0,39 г чистого продукта в виде белого твердого вещества (суммарно 58%).
Спектр МС-ББА: m/z 503 (M+H), 259 (55%), 226 (40%), 160 (30%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): -α- 2,57 (≈ т, J = 9,6, 1H), 2,87 - 2,97 (м, 2H), 3,58 - 3,71 (м, 3H), 4,18 (≈ т, J = 10,4, 1H), 4,46 (д, J = 13,6), 4,68 (д, J = 2,8, 1H), 4,85 (д, J = 13,6, 1H), 7,30 - 7,45 (м, 7H), 7,65 (с, 1H), 10,40 (шир, с., 1H), 10,73 (шир, с., 1H).
Пример 19.
N-(2-(R)-Гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил) бензилацеталь
Раствор 1,0 г (1,5 ммоль) (+/-)γбромфенилацетальдегида, 3,5-бис(трифторметил)бензилацеталя (пример 1), 1,25 мл (R)-1-амино-2-пропанола, 225 мг (1,5 ммоль) иодида натрия и 3,75 мл изопропанола нагревают до кипения с обратным холодильником в течение 20 ч. Раствор охлаждают и концентрируют до ≈ 25% от первоначального объема в вакууме. Концентрированный раствор распределяют между 50 мл эфира и 20 мл двухнормального водного раствора гидроксида натрия, и слои разделяют. Органический слой промывают 20 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 65:35 (по объему) эфира и гексана получают 948 мг (95%) продукта в виде смеси 1:1 неразделимых диастереомеров.
Раствор 1,0 г (1,5 ммоль) (+/-)γбромфенилацетальдегида, 3,5-бис(трифторметил)бензилацеталя (пример 1), 1,25 мл (R)-1-амино-2-пропанола, 225 мг (1,5 ммоль) иодида натрия и 3,75 мл изопропанола нагревают до кипения с обратным холодильником в течение 20 ч. Раствор охлаждают и концентрируют до ≈ 25% от первоначального объема в вакууме. Концентрированный раствор распределяют между 50 мл эфира и 20 мл двухнормального водного раствора гидроксида натрия, и слои разделяют. Органический слой промывают 20 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 65:35 (по объему) эфира и гексана получают 948 мг (95%) продукта в виде смеси 1:1 неразделимых диастереомеров.
Спектр МС-ББА: m/z 664 (M+H, 25%), 420 (20%), 226 (100%).
Пример 20.
N-(2-(S)-Гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил) бензилацеталь
Заменяя (R)-1-амино-2-пропанол на (S)-1-амино-2-пропанол в опыте, аналогичном предшествующему примеру, получают 940 мг продукта в виде смеси 1:1 диастереомеров.
Заменяя (R)-1-амино-2-пропанол на (S)-1-амино-2-пропанол в опыте, аналогичном предшествующему примеру, получают 940 мг продукта в виде смеси 1:1 диастереомеров.
Пример 21.
N-(2-(R)-Гидроксипропил)-N-(проп-2-енил)-(R)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь и N-(2-(R)-Гидроксипропил)-N-(проп-2-енил)-(S)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь
Смесь 933 г (1,40 ммоль) N-(2-(R)-Гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил) бензилацеталя (из примера 19), 1 мл бромистого аллила, 600 мг (4,3 ммоль) карбоната калия и 5 мл этанола перемешивают при 60oC в течение 20 ч. Смесь охлаждают, распределяют между 100 мл этилового эфира и 25 мл воды, и слои разделяют. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 20:1 (по объему) эфира и гексанов получают 380 мг (R,R)-аминоспирта (Rf = 0,72 с элюентом - смесью 3: 2 (по объему) эфира и гексанов), 220 мг (R,S)-аминоспирта (Rf = 0,62 с элюентом - смесью 3:2 (по объему) эфира и гексанов) и 285 мг смеси диастереомерных аминоспиртов.
Смесь 933 г (1,40 ммоль) N-(2-(R)-Гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил) бензилацеталя (из примера 19), 1 мл бромистого аллила, 600 мг (4,3 ммоль) карбоната калия и 5 мл этанола перемешивают при 60oC в течение 20 ч. Смесь охлаждают, распределяют между 100 мл этилового эфира и 25 мл воды, и слои разделяют. В результате флэш-хроматографии на 50 г силикагеля с использованием в качестве элюента смеси 20:1 (по объему) эфира и гексанов получают 380 мг (R,R)-аминоспирта (Rf = 0,72 с элюентом - смесью 3: 2 (по объему) эфира и гексанов), 220 мг (R,S)-аминоспирта (Rf = 0,62 с элюентом - смесью 3:2 (по объему) эфира и гексанов) и 285 мг смеси диастереомерных аминоспиртов.
Для (R,R)-аминоспирта:
МС-ББА (FAB): m/z 704 (M+H)
ИК (чистый) 3476, 2932, 1624, 1454, 1361, 1278, 1175, 1132, 760, 704, 682
Спектр ПМР (CDCl3, 400 МГц, м.д.): 1,12 (д, 3H, J = 6,4), 2,19 и 2,62 (дАВ кв., 2H, JAB = 13,0, J2,19 = 2,3, J2,62 = 10,4), 2,97 (дд, 1H, J= 14,0, 8,8 δ), 3,25 - 3,30 (м, 1H), 3,76 (с, 1H), 3,77 - 3,85 (м, 1H), 4,21 (д, 1H, J = 8,8), 4,49 и 4,55 (АВ кв. 2H, J = 12,4), 4,86 и 4,92 (АВ кв, 2H, J = 12,4), 5,27 - 5,33 (м, 2H), 5,39 (д, 1H, J = 8,8), 5,79 - 5,89 (м, 1H), 7,21 - 7,26 (м, 4H), 7,35 - 7,40 (м, 3H), 7,67 (с, 1H), 7,81 (с, 1H), 7,85 (с, 2H).
МС-ББА (FAB): m/z 704 (M+H)
ИК (чистый) 3476, 2932, 1624, 1454, 1361, 1278, 1175, 1132, 760, 704, 682
Спектр ПМР (CDCl3, 400 МГц, м.д.): 1,12 (д, 3H, J = 6,4), 2,19 и 2,62 (дАВ кв., 2H, JAB = 13,0, J2,19 = 2,3, J2,62 = 10,4), 2,97 (дд, 1H, J= 14,0, 8,8 δ), 3,25 - 3,30 (м, 1H), 3,76 (с, 1H), 3,77 - 3,85 (м, 1H), 4,21 (д, 1H, J = 8,8), 4,49 и 4,55 (АВ кв. 2H, J = 12,4), 4,86 и 4,92 (АВ кв, 2H, J = 12,4), 5,27 - 5,33 (м, 2H), 5,39 (д, 1H, J = 8,8), 5,79 - 5,89 (м, 1H), 7,21 - 7,26 (м, 4H), 7,35 - 7,40 (м, 3H), 7,67 (с, 1H), 7,81 (с, 1H), 7,85 (с, 2H).
Анализ:
Вычислено для C32H29F12NO3:
C 54,63, H 4,15, N 1,99, F 32,41.
Вычислено для C32H29F12NO3:
C 54,63, H 4,15, N 1,99, F 32,41.
Найдено: C 54,72, H 3,94, N 1,95, F 32,17.
Для (R,S)-аминоспирта:
МС-ББА (FAB): m/z 704 (M+I)
ИК (чистый) 3451, 2931, 1624, 1454, 1362, 1277, 704, 683.
МС-ББА (FAB): m/z 704 (M+I)
ИК (чистый) 3451, 2931, 1624, 1454, 1362, 1277, 704, 683.
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,09 (д, 3H, J = 6,0), 2,48 и 2,71 (дАВ кв. 2H, JАВ = 13,2, J2,48 = 9,6, J2,62 = 3,6), 3,05 (дд, 1H, J = 14,4, 6,8), 3,34 - 3,39 (м, 1H), 3,35 (с, 1H), 3,76-3,81 (м, 1H), 4,21 (д, 1H, J = 8,4), 4,50 и 4,54 (АВ кв, 2H, J = 12,8), 4,86 и 4,96 (АВ кв, 2H, J = 12,4), 5,10 - 5,17 (м, 2H), 5,39 (д, 1H, J= 8,4), 5,68 - 5,78 (м, 1H), 7,23 - 7,32 (м, 4H), 7,34 - 7,39 (м, 3H), 7,69 (с, 1H), 7,83 (с, 1H), 7,86 (с, 2H).
Анализ:
Вычислено для C32H29F12NO3: C 54,63, H 4,15; N 1,99, F 32,41.
Вычислено для C32H29F12NO3: C 54,63, H 4,15; N 1,99, F 32,41.
Найдено: C 54,80, H 4,16, N 1,90, F 32,36.
Пример 22.
N-(2-(R)-Гидроксипропил)-N-(проп-2-енил)-(S)-фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталь и N-(2-(S)-Гидроксипропил)-N- (проп-2-енил)-(R)-фенилглициналь, 3,5-бис(трифторметил)бензилацеталь
Заменяя 880 мг (1,33 ммоль) N-(2-(S)-гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь (пример 20) на N-(2-(R)-гидроксипропил)фенилглициналь, 3,5-бис-(три-фторметил)бензилацеталь в методиках предыдущего примера, получают 281 мг (S,S)-аминоспирта (Rf = 0,72 с элюентом - смесью 3:2 (по объему) эфира и гексанов), 367 мг
(S,R)-аминоспирта (Rf = 0,62 с элюентом - смесью 3:2 (по объему) эфира и гексанов) и 197 мг смеси диастереомерных аминоспиртов.
Заменяя 880 мг (1,33 ммоль) N-(2-(S)-гидроксипропил)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь (пример 20) на N-(2-(R)-гидроксипропил)фенилглициналь, 3,5-бис-(три-фторметил)бензилацеталь в методиках предыдущего примера, получают 281 мг (S,S)-аминоспирта (Rf = 0,72 с элюентом - смесью 3:2 (по объему) эфира и гексанов), 367 мг
(S,R)-аминоспирта (Rf = 0,62 с элюентом - смесью 3:2 (по объему) эфира и гексанов) и 197 мг смеси диастереомерных аминоспиртов.
Пример 23.
2-(R)-3,5-Бис-(трифторметил)-бензилокси)-3-(R)-фенил-6-(R)- метилморфолин и (2-(S)-(3,5-Бис-(трифторметил)бензилокси)- 3-(R)-фенил-6-(R)-метилморфолин
Стадия А.
Стадия А.
2(R)-(3,5-Бис-(трифторметил)-бензилокси)-3-(R)-фенил-4- (2-пропенил)-6-(R)-метилморфолин и 2-(S)-(3,5-Бис-(трифторметил)бензилокси)- 3-(R)-фенил-4-(2-пропенил)-6- (R)-метилморфолин
Раствор 355 мг (0,50 ммоль) N-(2-(R)-гидроксипропил)- -N-(2-пропенил)-(R)-фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталя (из примера 21), и 285 мг (1,5 ммоль) моногидрата пара-толуолсульфокислоты в 5 мл толуола нагревают при кипении в течение 40 мин. Раствор охлаждают и распределяют между 40 мл этилового эфира и 15 мл насыщенного водного раствора бикарбоната натрия. Слои разделяют; органический слой промывают 10 мл насыщенного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 10 г силикагеля с использованием в качестве элюента смеси 19: 1 (по объему) гексанов и эфира получают 122 мг (2R, 3R, 6R)-продукта (Rf = 0,53 с элюентом - смесью 4:1 (по объему) гексанов и эфира) и 62 мг (2S, 3R, 6R)-продукта (Rf = 0,23 с элюентом - смесью 4:1 (по объему) гексанов и эфира).
Раствор 355 мг (0,50 ммоль) N-(2-(R)-гидроксипропил)- -N-(2-пропенил)-(R)-фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталя (из примера 21), и 285 мг (1,5 ммоль) моногидрата пара-толуолсульфокислоты в 5 мл толуола нагревают при кипении в течение 40 мин. Раствор охлаждают и распределяют между 40 мл этилового эфира и 15 мл насыщенного водного раствора бикарбоната натрия. Слои разделяют; органический слой промывают 10 мл насыщенного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 10 г силикагеля с использованием в качестве элюента смеси 19: 1 (по объему) гексанов и эфира получают 122 мг (2R, 3R, 6R)-продукта (Rf = 0,53 с элюентом - смесью 4:1 (по объему) гексанов и эфира) и 62 мг (2S, 3R, 6R)-продукта (Rf = 0,23 с элюентом - смесью 4:1 (по объему) гексанов и эфира).
Для (2R, 3R, 6R) продукта:
Спектр МС-ББА: m/z 460 (M+H, 65%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,35 (д, 3H, J = 6,4), 2,53 и 2,63 (дАВ кв. 2H, JАВ = 12,0, J2,53 = 3,2, J2,63 = 6,8), 2,83 - 2,96 (м, 2H), 3,60 (д, 1H, J = 4,0), 4,27 - 4,32 (м, 1H), 4,57 и 4,84 (АВ кв. 2H, J = 13,2), 4,87 (д, 1H, J = 4,0), 5,08 - 5,13 (м, 2H), 5,76 - 5,86 (м, 1H), 7,31 - 7,37 (м, 3H), 7,50 - 7,52 (м, 2H), 7,58 (с.2H), 7,71 (с, 1H).
Спектр МС-ББА: m/z 460 (M+H, 65%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,35 (д, 3H, J = 6,4), 2,53 и 2,63 (дАВ кв. 2H, JАВ = 12,0, J2,53 = 3,2, J2,63 = 6,8), 2,83 - 2,96 (м, 2H), 3,60 (д, 1H, J = 4,0), 4,27 - 4,32 (м, 1H), 4,57 и 4,84 (АВ кв. 2H, J = 13,2), 4,87 (д, 1H, J = 4,0), 5,08 - 5,13 (м, 2H), 5,76 - 5,86 (м, 1H), 7,31 - 7,37 (м, 3H), 7,50 - 7,52 (м, 2H), 7,58 (с.2H), 7,71 (с, 1H).
для (2S, 3R, 6R) продукта:
МС-ББА (FAB): m/z 460 (M + H, 65%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,37 (д, 3H, J = 6,8), 2,48 - 2,50 (м, 2H), 2,74 и 3,01 (дт, кв, 2H, J = 6,4, 1,2, 12,4), 3,84 (д, 1H, J = 3,6), 3,92 - 3,99 (м, 1H), 4,70 и 4,93 (АВ кв, 2H, J = 13,6), 4,97 (д, 1H, J = 3,6), 5,08 - 5,14 (м, 2H), 5,74 - 5,84 (м, 1H), 7,28 - 7,36 (м, 3H), 7,43 - 7,46 (м, 2H), 7,64 (с, 2H), 7,75 (с, 1H).
МС-ББА (FAB): m/z 460 (M + H, 65%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,37 (д, 3H, J = 6,8), 2,48 - 2,50 (м, 2H), 2,74 и 3,01 (дт, кв, 2H, J = 6,4, 1,2, 12,4), 3,84 (д, 1H, J = 3,6), 3,92 - 3,99 (м, 1H), 4,70 и 4,93 (АВ кв, 2H, J = 13,6), 4,97 (д, 1H, J = 3,6), 5,08 - 5,14 (м, 2H), 5,74 - 5,84 (м, 1H), 7,28 - 7,36 (м, 3H), 7,43 - 7,46 (м, 2H), 7,64 (с, 2H), 7,75 (с, 1H).
Стадия Б.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин
Раствор 115 мг (0,25 ммоль) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 23, стадия А) и 230 мг (0,25 ммоль) хлористого трис(трифенилфосфин)родия в 15 мл смеси 4:1 (по объему) ацетонитрила и воды нагревают до кипения в течение 30 мин. Реакционную смесь охлаждают и распределяют между 50 мл этилацетата и 15 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния. Водный слой экстрагируют 2 раза по 25 мл этилацетата; экстракты сушат и объединяют с первоначальным органическим слоем. Объединенные органические слои концентрируют в вакууме. Остаток фильтруют через слой силикагеля (≈ 20 г), используя в качестве растворителя смесь 2:1 эфира и гексанов. Фильтрат концентрируют. В результате флэш-хроматографии на 5 г силикагеля с использованием в качестве элюента смеси 17:3 (по объему) гексанов и эфира получают 676 мг (64%) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолина в виде масла.
Раствор 115 мг (0,25 ммоль) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 23, стадия А) и 230 мг (0,25 ммоль) хлористого трис(трифенилфосфин)родия в 15 мл смеси 4:1 (по объему) ацетонитрила и воды нагревают до кипения в течение 30 мин. Реакционную смесь охлаждают и распределяют между 50 мл этилацетата и 15 мл воды, и слои разделяют. Органический слой сушат над сульфатом магния. Водный слой экстрагируют 2 раза по 25 мл этилацетата; экстракты сушат и объединяют с первоначальным органическим слоем. Объединенные органические слои концентрируют в вакууме. Остаток фильтруют через слой силикагеля (≈ 20 г), используя в качестве растворителя смесь 2:1 эфира и гексанов. Фильтрат концентрируют. В результате флэш-хроматографии на 5 г силикагеля с использованием в качестве элюента смеси 17:3 (по объему) гексанов и эфира получают 676 мг (64%) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолина в виде масла.
MC-ББА: m/z 420 (M+H, 90%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,21 (д, 3H, J = 6,4), 2,02 (шир., с, 1H), 2,67 и 2,77 (дAB, кв, 2H, JAB = 13,2, J2,67 = 8,8, J2,77 = 3,2), 3,89 (д, 1H, J = 2,4,), 4,07-4,15 (м, 1H), 4,68 и 4,90 (AB кв., 2H, J = 12,8), 5,03 (д, 1H, J = 2,4), 7,28-7,38 (м, 3H), 7,51-7,53 (м, 2H), 7,77 (с, 2H), 7,79 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,21 (д, 3H, J = 6,4), 2,02 (шир., с, 1H), 2,67 и 2,77 (дAB, кв, 2H, JAB = 13,2, J2,67 = 8,8, J2,77 = 3,2), 3,89 (д, 1H, J = 2,4,), 4,07-4,15 (м, 1H), 4,68 и 4,90 (AB кв., 2H, J = 12,8), 5,03 (д, 1H, J = 2,4), 7,28-7,38 (м, 3H), 7,51-7,53 (м, 2H), 7,77 (с, 2H), 7,79 (с, 1H).
Стадия В.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолин
Аналогичная реакция была проведена с использованием 55 мг (0,12 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 23, стадия А) и 111 мг (0,12 ммоль) хлористого трис(трифенилфоcфин)родия в 12 мл смеси 4:1 (по объему) ацетонитрила и воды. В результате флэш-хроматографии на 4 г силикагеля с использованием в качестве элюента смеси 50:1 (по объему) хлористого метилена и ацетонитрила получают 14 мг (28%) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолина в виде масла.
Аналогичная реакция была проведена с использованием 55 мг (0,12 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 23, стадия А) и 111 мг (0,12 ммоль) хлористого трис(трифенилфоcфин)родия в 12 мл смеси 4:1 (по объему) ацетонитрила и воды. В результате флэш-хроматографии на 4 г силикагеля с использованием в качестве элюента смеси 50:1 (по объему) хлористого метилена и ацетонитрила получают 14 мг (28%) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(R)- метилморфолина в виде масла.
MC-ББА: m/z 420 (M+H, 90%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,39 (д, 3H, J = 6,8), 1,92 (шир.с, 1H), 2,84 и 2,95 (дAB, кв, 2H, JAB = 12,8, J2,84 = 6,4, J2,95 = 3,6), 3,93-4,00 (м, 1H), 4,07 (д, 1H, J = 2,8), 4,68 и 4,95 (AB кв., 2H, J = 13,2), 4,93 (д, 1H, J = 2,8), 7,28-7,37 (м, 3H), 7,48-7,52 (м, 2H), 7,55 (с, 2H), 7,72 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,39 (д, 3H, J = 6,8), 1,92 (шир.с, 1H), 2,84 и 2,95 (дAB, кв, 2H, JAB = 12,8, J2,84 = 6,4, J2,95 = 3,6), 3,93-4,00 (м, 1H), 4,07 (д, 1H, J = 2,8), 4,68 и 4,95 (AB кв., 2H, J = 13,2), 4,93 (д, 1H, J = 2,8), 7,28-7,37 (м, 3H), 7,48-7,52 (м, 2H), 7,55 (с, 2H), 7,72 (с, 1H).
Пример 24.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин и 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолин
Заменяя 350 мг N-(2-(S)гидроксипропил)-N-(2-пропенил)-(S)- фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь (из примера 22) на N-(2-(R)-гидроксипропил)-N-(2-пропенил)-(R)- фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь в эксперименте, аналогичном предыдущему примеру, получают 50 мг 2-(S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолина и 14 мг 2-(S)-3,5-Бис-(трифторметил/бензилокси)-3-(S)-фенил-6-(S)- метилморфолина.
Заменяя 350 мг N-(2-(S)гидроксипропил)-N-(2-пропенил)-(S)- фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь (из примера 22) на N-(2-(R)-гидроксипропил)-N-(2-пропенил)-(R)- фенилглициналь, 3,5-бис-(трифторметил)бензилацеталь в эксперименте, аналогичном предыдущему примеру, получают 50 мг 2-(S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(S)- метилморфолина и 14 мг 2-(S)-3,5-Бис-(трифторметил/бензилокси)-3-(S)-фенил-6-(S)- метилморфолина.
Пример 25.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин и 2-(S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин
Стадия А.
Стадия А.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2- пропенил)-6-(R)-метилморфолин и 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2- пропенил)-6-(R)-метилморфолин
Указанные в заголовке вещества были приготовлены по способу, аналогичному описанному в примере 23, стадия А. Циклизация 300 мг (0,43 ммоль) N-(2-(R)-гидроксипропил)-N-(2-пропенил)-(S)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталя (из примера 23) была осуществлена с использованием 246 мг (1,29 ммоль) моногидрата пара-толуолсульфокислоты в 5 мл толуола. В результате флэш-хроматографии на 8 г силикагеля с использованием в качестве элюента смеси 20: 1 (по объему) гексанов и эфира получают 149 мг продуктов в виде неразделимых диастереомеров.
Указанные в заголовке вещества были приготовлены по способу, аналогичному описанному в примере 23, стадия А. Циклизация 300 мг (0,43 ммоль) N-(2-(R)-гидроксипропил)-N-(2-пропенил)-(S)-фенилглициналь, 3,5-бис-(трифторметил)бензилацеталя (из примера 23) была осуществлена с использованием 246 мг (1,29 ммоль) моногидрата пара-толуолсульфокислоты в 5 мл толуола. В результате флэш-хроматографии на 8 г силикагеля с использованием в качестве элюента смеси 20: 1 (по объему) гексанов и эфира получают 149 мг продуктов в виде неразделимых диастереомеров.
Спектр MC-ББА: m/Z 460 (M+H, 65%).
Стадия Б.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин и 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолин
Раствор 150 мг (0,33 ммоль) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина и 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 25, стадия А) и 318 мг (0,32 ммоль) хлористого трис(трифенилфосфин)родия в 20 мл смеси 4:1 (по объему) ацетонитрила и воды нагревают до кипения в течение 1 час. В результате флэш-хроматографии на 5 г силикагеля с использованием в качестве элюента смеси 90:1 (по объему) гексанов и эфира получают 35 мг продуктов в виде смеси и 26 мг 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (Rf = 0,22 с элюентом - смесью 3: 2 (по объему) гексанов и эфира). Хроматографическая очистка смеси на 5 г силикагеля с использованием смеси 20:1 (по объему) дает 14 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина (Rf = 0,53 с элюентом - смесью 4 : 1 (по объему) гексанов и эфира) и 17 мг 2-(R)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (суммарный выход 41%).
Раствор 150 мг (0,33 ммоль) 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина и 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-4-(2-пропенил)- 6-(R)-метилморфолина (из примера 25, стадия А) и 318 мг (0,32 ммоль) хлористого трис(трифенилфосфин)родия в 20 мл смеси 4:1 (по объему) ацетонитрила и воды нагревают до кипения в течение 1 час. В результате флэш-хроматографии на 5 г силикагеля с использованием в качестве элюента смеси 90:1 (по объему) гексанов и эфира получают 35 мг продуктов в виде смеси и 26 мг 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (Rf = 0,22 с элюентом - смесью 3: 2 (по объему) гексанов и эфира). Хроматографическая очистка смеси на 5 г силикагеля с использованием смеси 20:1 (по объему) дает 14 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина (Rf = 0,53 с элюентом - смесью 4 : 1 (по объему) гексанов и эфира) и 17 мг 2-(R)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (суммарный выход 41%).
Для (2R, 3S, 6R) продукта:
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,30 (д, 3H, J = 6,4), 1,74 (шир.с, 1H), 2,73 и 2,98 (дAB, кв, 2H, JAB = 11,6, J2,73 = 10,0, J2,98 = 2,4), 3,65 (д, 1H, J = 7,2), 3,89-3,94 (м, 1H), 4,45 (д, 1H, J = 7,2), 4,53 и 4,90 (AB кв, 2H, J = 13,2), 7,28-7,38 (м, 3H), 7,41-7,43 (м, 2H), 7,45 (с, 2H), 7,70 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,30 (д, 3H, J = 6,4), 1,74 (шир.с, 1H), 2,73 и 2,98 (дAB, кв, 2H, JAB = 11,6, J2,73 = 10,0, J2,98 = 2,4), 3,65 (д, 1H, J = 7,2), 3,89-3,94 (м, 1H), 4,45 (д, 1H, J = 7,2), 4,53 и 4,90 (AB кв, 2H, J = 13,2), 7,28-7,38 (м, 3H), 7,41-7,43 (м, 2H), 7,45 (с, 2H), 7,70 (с, 1H).
Для (2S, 3S, 6R) продукта:
Спектр МС - ББА: m/Z 420 (M + H, 90%).
Спектр МС - ББА: m/Z 420 (M + H, 90%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) 1,20 (д, 3H, J = 6,4), 2,04 (шир.с, 1H), 2,84 и 3,15 (дAB, кв, 2H, JAB = 12,8, J2,84 = 10,8, J3,15 = 2,8), 4,08 (д, 1H, J = 2,8), 4,08-4,15 (м, 1H), 4,53 и 4,80 (AB кв, 2H, J = 13,2), 4,79 (д, 1H, J = 2,8), 7,28-7,38 (м, 5H), 7,43 (с, 2H), 7,70 (с, 1H)
(тд, J = 11 Гц и 3 Гц, 1H), 3,68 (д, J = 7 Гц, 1H), 3,81 (тд, J = 11 Гц и 3 Гц, 1H), 4,01 (м, 1H), 4,44 (д, J = 7 Гц), 4,5 (д, J = 13 Гц, 1H), 4,85 (д, J = 13 Гц, 1H), 7,28-7,42 (м, 7H), 7,67 (с, 1H).
(тд, J = 11 Гц и 3 Гц, 1H), 3,68 (д, J = 7 Гц, 1H), 3,81 (тд, J = 11 Гц и 3 Гц, 1H), 4,01 (м, 1H), 4,44 (д, J = 7 Гц), 4,5 (д, J = 13 Гц, 1H), 4,85 (д, J = 13 Гц, 1H), 7,28-7,42 (м, 7H), 7,67 (с, 1H).
Пример 26.
2-(S)-(3,5-Бис)-(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолин и 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)- фенил-6-(S)-метилморфолин
Заменяя 250 мг N-(2-(S)-гидроксипропил)-N-(2-пропил)-(S)- фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталь (из примера 22) на N-(2-(R)-гидроксипропил)-N-(2-пропил)-(R)-фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталь в эксперименте, аналогичном предыдущему примеру, получают 42 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолина и 17 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолина.
Заменяя 250 мг N-(2-(S)-гидроксипропил)-N-(2-пропил)-(S)- фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталь (из примера 22) на N-(2-(R)-гидроксипропил)-N-(2-пропил)-(R)-фенилглициналь, 3,5-бис-(трифторметил)-бензилацеталь в эксперименте, аналогичном предыдущему примеру, получают 42 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолина и 17 мг 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)-фенил-6-(S)- метилморфолина.
Пример 27.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин, 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)- фенил-5-(R)-метилморфолин, 2-(R или S)-3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин и 2-(S или R)-3,5-Бис-(трифторметил/бензилокси)-3-(R)-фенил-5-(R)- метилморфолин
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (R)-2-амино-1-пропанол предоставляет смесь 55 мг материала с высоким значением Rf и 56 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия А (выше), чтобы получить 10 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин) и 7 мг материала с низким значением Rf (2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин). Материал с низким значением Rf (после объединения с дополнительными 30 мг материала) обрабатывают в соответствии с методикой примера 23, стадия А (выше), чтобы получить 24 мг материала с высоким значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин) и 18 мг материала с низким значением Rf (2-(S или R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин).
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (R)-2-амино-1-пропанол предоставляет смесь 55 мг материала с высоким значением Rf и 56 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия А (выше), чтобы получить 10 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин) и 7 мг материала с низким значением Rf (2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин). Материал с низким значением Rf (после объединения с дополнительными 30 мг материала) обрабатывают в соответствии с методикой примера 23, стадия А (выше), чтобы получить 24 мг материала с высоким значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин) и 18 мг материала с низким значением Rf (2-(S или R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин).
2-(R)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенил-5- (R)-метилморфолин)
MC-ББА (FAB): m/z 420 (M+H, 100%), 227 (50%), 192 (75%), 176 (65%).
MC-ББА (FAB): m/z 420 (M+H, 100%), 227 (50%), 192 (75%), 176 (65%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 0,98 (д, 3H, J = 6,3), 3,16-3,20 (м, 1H), 3,43-3,47 (м, 1H), 3,79 (д, 1H, J = 7,5 Гц), 3,91 (дд, 1H, J = 3,2 и 11,5 Гц), 4,51 (д, 2H, J = 13,4 Гц), 4,85 (д, 1H, J = 13,2 Гц), 7,29-7,45 (м, 7H), 7,67 (с, 1H).
2-(S)-(3,5-Бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)- метилморфолин
MC-ББА (FAB): m/z 420 (M+H, 48%), 227 (35%), 192 (39%), 176 (100%).
MC-ББА (FAB): m/z 420 (M+H, 48%), 227 (35%), 192 (39%), 176 (100%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,10 (д, 3H, J = 6,4), 3,23-3,26 (м, 1H), 3,56-3,61 (м, 2H), 4,17 (д, 1H, J = 2,3 Гц), 4,51 (д, 1H, J = 13,7 Гц), 4,71 (д, 1H, J = 2,4 Гц), 4,78 (д, 1H, J = 13,5 Гц), 7,28-7,39 (м, 7H), 7,68 (с, 1H).
2-(R или S)-(3,5-Бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин
MC-ББА (FAB): m/z 281 (35%), 221 (55%), 207 (45%), 192 (40%), 147 (100%).
MC-ББА (FAB): m/z 281 (35%), 221 (55%), 207 (45%), 192 (40%), 147 (100%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,13 (д, 3H, J = 6,6 Гц), 3,10-3,14 (м, 1H), 3,66 (дд, 1H, J = 6,6 и 11,4 Гц), 3,76 (дд, 1H, J = 3,5 и 11,2 Гц), 4,04 (д, 1H, J = 4,0 Гц), 4,61 (д, 1H, J = 13,2 Гц), 4,74 (д, 1H, J = 3,9 Гц), 4,89 (з, 1H, 13,2 Гц), 7,26-7,35 (м, 3H), 7,47-7,49 (м, 2H), 7,64 (с, 1H), 7,74 (с, 1H).
2-(R или S)-(3,5-Бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)- метилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): 1,36 (д. 3H, J = 6,7 Гц), 3,27-3,31 (м, 1H), 3,39 (дд, 1H, J = 2,2 и 11,3 Гц), 4,16 (дд, 1H, J = 3,2 и 11,0 Гц), 4,37 (д, 1H, J = 2,3 Гц), 4,53 (д, 1H, J = 13,5 Гц), 4,75 (д, 1H, J = 2,5 Гц), 4,81 (д, 1H, 13,6 Гц), 7,26-7,35 (м, 3H), 7,26-7,43 (м, 7H), 7,68 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): 1,36 (д. 3H, J = 6,7 Гц), 3,27-3,31 (м, 1H), 3,39 (дд, 1H, J = 2,2 и 11,3 Гц), 4,16 (дд, 1H, J = 3,2 и 11,0 Гц), 4,37 (д, 1H, J = 2,3 Гц), 4,53 (д, 1H, J = 13,5 Гц), 4,75 (д, 1H, J = 2,5 Гц), 4,81 (д, 1H, 13,6 Гц), 7,26-7,35 (м, 3H), 7,26-7,43 (м, 7H), 7,68 (с, 1H).
Пример 28.
2-(R или S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин, 2-(S или R)-(3,5-Био-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин и 2-(R)-(3,5-Бис-(трифторметил)бензилокси-3-(R)-5-(S)-метилморфолин
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (S)-2-амино-1-пропанол представляет смесь 78 мг материала с высоким значением Rf и 70 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A (выше), чтобы получить менее чем 1 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин) и 9 мг материала с низким значением Rf (2-(S)-(3,5-Био-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 20 мг материала с высоким значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин) и 14 мг материала с низким значением Rf (2-(S или R)-(3,5-Бис-(трифторметил)бензилокси-3-(S)-фенил-5-(S)-метилморфолин).
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (S)-2-амино-1-пропанол представляет смесь 78 мг материала с высоким значением Rf и 70 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A (выше), чтобы получить менее чем 1 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин) и 9 мг материала с низким значением Rf (2-(S)-(3,5-Био-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 20 мг материала с высоким значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин) и 14 мг материала с низким значением Rf (2-(S или R)-(3,5-Бис-(трифторметил)бензилокси-3-(S)-фенил-5-(S)-метилморфолин).
2-(R или S)-(3,5-Бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин
МС-ББА (FAB): m/z 420 (M+H, 60%), 227 (68%), 192 (56%), 176 (100%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) δ 1,12 (д, 3H, J = 6,6 Гц), 3,09 - 3,14 (м, 1H), 3,65 (дд, 1H, J = 6,6 и 11,0 Гц), 3,75 (дд, 1H, J = 3,6 и 11,1 Гц), 4,04 (д, 1H, J = 3,9 Гц), 4,61 (д, 1H, J = 13,2 Гц), 4,73 (д, 1H, J = 3,9 Гц), 4,89 (д, 1H, 13,2 Гц), 7,28-7,35 (м, 3H), 7,47 (д, 2H, 7,0 Гц), 7,64 (с, 1H), 7,74 (с, 1H).
МС-ББА (FAB): m/z 420 (M+H, 60%), 227 (68%), 192 (56%), 176 (100%)
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) δ 1,12 (д, 3H, J = 6,6 Гц), 3,09 - 3,14 (м, 1H), 3,65 (дд, 1H, J = 6,6 и 11,0 Гц), 3,75 (дд, 1H, J = 3,6 и 11,1 Гц), 4,04 (д, 1H, J = 3,9 Гц), 4,61 (д, 1H, J = 13,2 Гц), 4,73 (д, 1H, J = 3,9 Гц), 4,89 (д, 1H, 13,2 Гц), 7,28-7,35 (м, 3H), 7,47 (д, 2H, 7,0 Гц), 7,64 (с, 1H), 7,74 (с, 1H).
2-(S или R)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолин
МС-ББА (FAB): m/z 420 (M+H, 50%), 227 (45%), 192 (40%), 176 (100%).
МС-ББА (FAB): m/z 420 (M+H, 50%), 227 (45%), 192 (40%), 176 (100%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,36 (д, 3H, J = 6,9 Гц), 3,27-3,29 (м, 1H), 3,39 (д, 1H, J = 2,2 и 11,1 Гц), 4,15 (дд, 1H, J = 3,3 и 11,1 Гц), 4,37 (д, 1H, J = 2,5 Гц), 4,52 (д, 1H, J = 13,3 Гц), 4,75 (д, 1H, J = 2,4 Гц), 4,81 (д, 1H, 13,5 Гц), 7,28-7,43 (м, 7H), 7,68 (с, 1H).
2-(R)-(3,5-Бис(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-метилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,10 (д, 3H, J = 6,4 Гц), 3,22-3,25 (м, 1H), 3,55-3,60 (м, 2H), 4,17 (д, 1H, J = 2,3 Гц), 4,51 (д, 1H, J = 13,5 Гц), 4,71 (д, 1H, J = 2,4 Гц), 4,77 (д, 1H, J = 13,6 Гц), 7,28-7,38 (м, 7H), 7,67 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,10 (д, 3H, J = 6,4 Гц), 3,22-3,25 (м, 1H), 3,55-3,60 (м, 2H), 4,17 (д, 1H, J = 2,3 Гц), 4,51 (д, 1H, J = 13,5 Гц), 4,71 (д, 1H, J = 2,4 Гц), 4,77 (д, 1H, J = 13,6 Гц), 7,28-7,38 (м, 7H), 7,67 (с, 1H).
Пример 29.
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин, 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин и 2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(R)-фенилморфолин
Проведение последовательности, описанной в примере 149, с заменой (R)-1-амино-2-пропанола на (R)-2-амино-2-фенилэтанол представляет смесь 62 мг материала с высоким значением Rf и 52 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой применения 23, стадия A (выше), чтобы получить 16 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин) и 4 мг материала с низким значением Rf (2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 4 мг продукта (2-(R или S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(R)-фенил-5-(R)-фенилморфолин).
Проведение последовательности, описанной в примере 149, с заменой (R)-1-амино-2-пропанола на (R)-2-амино-2-фенилэтанол представляет смесь 62 мг материала с высоким значением Rf и 52 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой применения 23, стадия A (выше), чтобы получить 16 мг материала с высоким значением Rf (2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин) и 4 мг материала с низким значением Rf (2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 4 мг продукта (2-(R или S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(R)-фенил-5-(R)-фенилморфолин).
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) δ 3,62 (т, 1H, J = 10,7 и 21,5 Гц), 3,93 (д, 1H, J = 7,4 Гц), 3,99 (дд, 1H, J = 3,1 и 11,2 Гц), 4,18 (дд, 1H, J = 3,0 и 10,2 Гц), 4,46 (д, 1H, J = 7,4 Гц), 4,53 (д, 1H, J = 13,5 Гц), 4,89 (д, 1H, J = 13,3 Гц), 7,28-7,55 (м, 12H), 7,69 (с, 1H). 2-(S)-(3,5)-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,67 (дд, 1H, J = 3,5 и 11,0 Гц), 3,89 (д, 1H, J = 10,8 и 21,6 Гц), 4,25 (дд, 1H, J = 3,3 и 11,0 Гц), 4,34 (д, 1H, J = 2,2 Гц), 4,52 (д, 1H, J = 13,8 Гц), 4,78-4,87 (м, 2H), 7,28-7,51 (м, 12H), 7,69 (с, 1H)
2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(R)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 4,10-4,25 (м, 2H), 4,30-4,38 (м, 1H), 4,48-4,54 (м, 1H), 4,59-4,66 (м, 1H), 4,86-5,00 (м, 2H), 7,25-7,74 (м, 13H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.) δ 3,62 (т, 1H, J = 10,7 и 21,5 Гц), 3,93 (д, 1H, J = 7,4 Гц), 3,99 (дд, 1H, J = 3,1 и 11,2 Гц), 4,18 (дд, 1H, J = 3,0 и 10,2 Гц), 4,46 (д, 1H, J = 7,4 Гц), 4,53 (д, 1H, J = 13,5 Гц), 4,89 (д, 1H, J = 13,3 Гц), 7,28-7,55 (м, 12H), 7,69 (с, 1H). 2-(S)-(3,5)-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,67 (дд, 1H, J = 3,5 и 11,0 Гц), 3,89 (д, 1H, J = 10,8 и 21,6 Гц), 4,25 (дд, 1H, J = 3,3 и 11,0 Гц), 4,34 (д, 1H, J = 2,2 Гц), 4,52 (д, 1H, J = 13,8 Гц), 4,78-4,87 (м, 2H), 7,28-7,51 (м, 12H), 7,69 (с, 1H)
2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(R)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 4,10-4,25 (м, 2H), 4,30-4,38 (м, 1H), 4,48-4,54 (м, 1H), 4,59-4,66 (м, 1H), 4,86-5,00 (м, 2H), 7,25-7,74 (м, 13H).
Пример 30
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин, 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин, 2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин и 2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (S)-2-амино-2-фенилэтанол представляет смесь 75 мг материала с высоким значением Rf и 64 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A (выше), чтобы получить 23 мг материала с высоким значением Rf (2-(S)-(3,5-(Бис-(трифторметил)-
бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин [L-740, 390]) и 7 мг материала с низким значением Rf 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)- фенилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 26 мг продукта с более высоким Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси-3-(S)фенил-5-(S)-фенилморфолин) и 6 мг продукта с пониженным значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин).
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин, 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин, 2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин и 2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин
Проведение последовательности, описанной в примере 19, с заменой (R)-1-амино-2-пропанола на (S)-2-амино-2-фенилэтанол представляет смесь 75 мг материала с высоким значением Rf и 64 мг материала с низким значением Rf. Материал с высоким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A (выше), чтобы получить 23 мг материала с высоким значением Rf (2-(S)-(3,5-(Бис-(трифторметил)-
бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин [L-740, 390]) и 7 мг материала с низким значением Rf 2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)- фенилморфолин). Материал с низким значением Rf обрабатывают в соответствии с методикой примера 23, стадия A, чтобы получить 26 мг продукта с более высоким Rf (2-(R или S)-(3,5-Бис-(трифторметил)бензилокси-3-(S)фенил-5-(S)-фенилморфолин) и 6 мг продукта с пониженным значением Rf (2-(R или S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин).
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин
Спектр ПМР (дейтерохлороформе, 400 МГц, м.д.): δ 3,60-3,74 (м, 1H), 3,94 (д, 1H, J = 7,6 Гц), 4,00 (дд, 1H, J = 3,2 и 11,3 Гц), 4,18-4,21 (м, 1H), 4,50-4,55 (м, 2H), 4,89 (м, 1H), 7,26-7,55 (м, 12H), 7,69 (с, 1H).
Спектр ПМР (дейтерохлороформе, 400 МГц, м.д.): δ 3,60-3,74 (м, 1H), 3,94 (д, 1H, J = 7,6 Гц), 4,00 (дд, 1H, J = 3,2 и 11,3 Гц), 4,18-4,21 (м, 1H), 4,50-4,55 (м, 2H), 4,89 (м, 1H), 7,26-7,55 (м, 12H), 7,69 (с, 1H).
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц м.д.): δ 3,68 (дд, 1H, J = 3,0 и 11,0 Гц), 3,88-3,94 (м, 1H), 4,26-4,30 (м, 1H), 4,36 (с, 1H), 4,52 (д, 1H, J = 13,5 Гц), 4,77-4,86 (м, 2H), 7,27-7,51 (м, 12H), 7,69 (с, 1H).
Спектр ПМР (в дейтерохлороформе, 400 МГц м.д.): δ 3,68 (дд, 1H, J = 3,0 и 11,0 Гц), 3,88-3,94 (м, 1H), 4,26-4,30 (м, 1H), 4,36 (с, 1H), 4,52 (д, 1H, J = 13,5 Гц), 4,77-4,86 (м, 2H), 7,27-7,51 (м, 12H), 7,69 (с, 1H).
2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)фенил-5-(S)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,93-3,95 (м, 1H), 4,06-4,21 (м, 2H), 4,38-4,42 (м, 1H), 4,59-4,68 (м, 2H), 4,83-4,94 (м, 2H), 7,25-7,81 (м, 13H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,93-3,95 (м, 1H), 4,06-4,21 (м, 2H), 4,38-4,42 (м, 1H), 4,59-4,68 (м, 2H), 4,83-4,94 (м, 2H), 7,25-7,81 (м, 13H).
2-(R или S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-фенилморфолин
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,43-3,59 (м, 2H), 3,82 (д, 1H, J = 7,2 Гц), 4,25 (д, 1H, J = 12,5 Гц), 4,52-4,63 (м, 3H), 4,80-4,90 (шир. с, 1H), 7,11-7,81 (м, 13H).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 3,43-3,59 (м, 2H), 3,82 (д, 1H, J = 7,2 Гц), 4,25 (д, 1H, J = 12,5 Гц), 4,52-4,63 (м, 3H), 4,80-4,90 (шир. с, 1H), 7,11-7,81 (м, 13H).
Пример 31.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-3-(S)-фенил- 4-(3-(1,2,4-триазоло)метилформолин
В соответствии с методикой, приведенной в примере 17, стадия Б, 98 мг (0,24 ммоль) 2-(S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(S)-фенил-6-(R)-метилморфолина (из примера 25 выше), 38 мг (0,28 ммоль) N-формил-2-хлорацетамидразона (из примера 17, стадия А) и 97 мг (0,7 ммоль) безводного карбоната калия дают после флэш-хроматографии на 28 мг силикагеля, элюируемого 1 л смеси 100:4:0,5 хлористый метилен/метанол/водный аммиак, светло-желтое твердое вещество, которое после перекриcталлизации из смеси гексаны/хлористый метилен, обеспечивает 77 мг (66%) 2-(S)-3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-3-(S)-фенил-4-(3- (1,2,4-триазоло)-метилморфолина в виде белого кристаллического порошка.
В соответствии с методикой, приведенной в примере 17, стадия Б, 98 мг (0,24 ммоль) 2-(S)-(3,5-Бис-(трифторметил)-бензилокси)-3-(S)-фенил-6-(R)-метилморфолина (из примера 25 выше), 38 мг (0,28 ммоль) N-формил-2-хлорацетамидразона (из примера 17, стадия А) и 97 мг (0,7 ммоль) безводного карбоната калия дают после флэш-хроматографии на 28 мг силикагеля, элюируемого 1 л смеси 100:4:0,5 хлористый метилен/метанол/водный аммиак, светло-желтое твердое вещество, которое после перекриcталлизации из смеси гексаны/хлористый метилен, обеспечивает 77 мг (66%) 2-(S)-3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-3-(S)-фенил-4-(3- (1,2,4-триазоло)-метилморфолина в виде белого кристаллического порошка.
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,17 (д, 3H, J = 6,3), 2,29 (т, J = 11,1, 1H), 2,92 (д, J = 11,1, 1H), 3,42 (д, J = 15,3, 1H), 3,58 (с, 1H), 3,88 (д, J = 15,4, 1H), 4,20-4,33 (м, 1H), 4,43 (д, 13,5, 1H), 4,71 (д, J = 2,4, 1H), 4,74 (д, J = 13,3, 1H), 7,30-7,55 (м, 7H), 7,69 (с, 1H), 7,95 (с, 1H).
Пример 32.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-4-(3-(5-оксо- 1H, 4H-(1,2,4-триазоло)метил-3-(S)-фенилморфолин
Смесь 96 мг (0,23 ммоль) 2-(S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (из примера 25 выше), 46 мг (0,28 ммоль) N-метилкарбокси-2-хлорацетамидразона и 95 мг (0,69 ммоль) безводного карбоната калия в 3 мл сухого диметилформамида перемешивают при 60oC в течение 90 мин и затем при 120oC в течение 2 ч. Смесь охлаждают до комнатной температуры, растворяют в 15 мл этилацетата и промывают 3 раза по 10 мл воды. Объединенные водные слои повторно экстрагируют 10 мл этилацетата. Объединенные органические слои промывают 10 мл рассола, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 28 мг силикагеля, который элюируют 1 литром смеси 100:4 хлористого метилена и метанола, получая 65 мг (55%) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-4-(3-(5-оксо- 1H, 4H-(1,2,4-триазоло)метил-3-(S)-фенилморфолин в виде светло-желтого твердого порошка.
Смесь 96 мг (0,23 ммоль) 2-(S)-3,5-Бис-(трифторметил)бензилокси)-3-(S)-фенил-6-(R)- метилморфолина (из примера 25 выше), 46 мг (0,28 ммоль) N-метилкарбокси-2-хлорацетамидразона и 95 мг (0,69 ммоль) безводного карбоната калия в 3 мл сухого диметилформамида перемешивают при 60oC в течение 90 мин и затем при 120oC в течение 2 ч. Смесь охлаждают до комнатной температуры, растворяют в 15 мл этилацетата и промывают 3 раза по 10 мл воды. Объединенные водные слои повторно экстрагируют 10 мл этилацетата. Объединенные органические слои промывают 10 мл рассола, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 28 мг силикагеля, который элюируют 1 литром смеси 100:4 хлористого метилена и метанола, получая 65 мг (55%) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-6-(R)-метил-4-(3-(5-оксо- 1H, 4H-(1,2,4-триазоло)метил-3-(S)-фенилморфолин в виде светло-желтого твердого порошка.
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ 1,18 (д, 3H, J = 6,2), 2,15 (т, J = 11,1, 1H), 2,89 (д, J = 14, 2H), 3,49 (д, J = 2,2, 1H), 3,61 (д, J = 14,4, 1H), 4,20-4,30 (м, 1H), 4,45 (д, J = 13,6, 1H), 4,67 (д, J = 2,5, 1H), 4,79 (д, J = 13,5, 1H), 7,25-7,50 (м, 7H), 7,62 (с, 1H), 10,07 (с, 1H), 10,35 (с, 1H).
Пример 33.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)- фенилморфолин.
Стадия А.
4-Бензил-2-(S)-гидрокси-3-(R)-фенилморфолин
Раствор 3,72 г (13,9 ммоль) 4-бензил-3-(R)-фенил-2-морфолинона, приготовленного из 3-(R)-фенилглицина, как описано в примере 14, в 28 мл хлористого метилена охлаждают в бане при -78oC в атмосфере азота и добавляют 14 мл 1,5-молярного раствора диизобутилалюминийгидрида (21 ммоль) в толуоле. После перемешивания образовавшегося раствора в течение 0,5 ч, ему дают нагреться до -50oC и выдерживают при этой температуре 0,5 ч. Реакцию прерывают путем добавления 10 мл водного раствора калий-натрий тартрата. Смесь разбавляют хлористым метиленом, и разделяют слои. Водный слой экстрагируют 3 раза хлористым метиленом. Органические слои промывают рассолом, сушат над сульфатом натрия и фильтруют. Концентрирование фильтрата дает 3,32 г (88%) 4-бензил-2-(S)-гидрокси-3-(R)-фенилморфолина, пригодного для использования на следующей стадии.
Раствор 3,72 г (13,9 ммоль) 4-бензил-3-(R)-фенил-2-морфолинона, приготовленного из 3-(R)-фенилглицина, как описано в примере 14, в 28 мл хлористого метилена охлаждают в бане при -78oC в атмосфере азота и добавляют 14 мл 1,5-молярного раствора диизобутилалюминийгидрида (21 ммоль) в толуоле. После перемешивания образовавшегося раствора в течение 0,5 ч, ему дают нагреться до -50oC и выдерживают при этой температуре 0,5 ч. Реакцию прерывают путем добавления 10 мл водного раствора калий-натрий тартрата. Смесь разбавляют хлористым метиленом, и разделяют слои. Водный слой экстрагируют 3 раза хлористым метиленом. Органические слои промывают рассолом, сушат над сульфатом натрия и фильтруют. Концентрирование фильтрата дает 3,32 г (88%) 4-бензил-2-(S)-гидрокси-3-(R)-фенилморфолина, пригодного для использования на следующей стадии.
Спектр ПМР (CDCl3)
2,28 (м, 1H), 2,71 (м, 1H), 2,91 (д, J = 13 Гц, 1H), 3,09 (д, J = 6 Гц, 1H), 3,69 (д, J = 13 Гц, 1H), 3,82 (тд, J = 10 Гц и 2 Гц, 1H), 3,91 (д, J = 10 Гц, 1H), 4,73 (т, J = 6 Гц, 1H), 7,2-7,52 (м, 10H).
2,28 (м, 1H), 2,71 (м, 1H), 2,91 (д, J = 13 Гц, 1H), 3,09 (д, J = 6 Гц, 1H), 3,69 (д, J = 13 Гц, 1H), 3,82 (тд, J = 10 Гц и 2 Гц, 1H), 3,91 (д, J = 10 Гц, 1H), 4,73 (т, J = 6 Гц, 1H), 7,2-7,52 (м, 10H).
Стадия Б.
4-Бензил -2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(R)- фенилморфолин
К суспензии 0,592 г (14,8 ммоль) гидрида натрия в 30 мл сухого тетрагидрофурана при 0oC добавляют 3,32 г (12,3 ммоль) 4-бензил-2-(S)-гидрокси-3-(R)-фенилморфолина, приготовленного на стадии А. Спустя 15 мин добавляют 0,915 г тетрабутиламмонийиодида (2,47 ммоль) и 2,4 мл (13 ммоль) 3,5-бис-(трифторметил)бензилбромида. Образовавшуюся смесь перемешивают при температуре ледяной бани в течение 1 ч, затем выливают в насыщенный водный раствор бикарбоната натрия и экстрагируют этилацетатом. Органические соли объединяют, промывают рассолом, сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме. Остаток очищают хроматографически на ЖХВР системы "Ватерз Преп500", используя смесь 50% этилацетат/гексан, чтобы выделить 3,6 г (59%) 4-Бензил-2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина.
К суспензии 0,592 г (14,8 ммоль) гидрида натрия в 30 мл сухого тетрагидрофурана при 0oC добавляют 3,32 г (12,3 ммоль) 4-бензил-2-(S)-гидрокси-3-(R)-фенилморфолина, приготовленного на стадии А. Спустя 15 мин добавляют 0,915 г тетрабутиламмонийиодида (2,47 ммоль) и 2,4 мл (13 ммоль) 3,5-бис-(трифторметил)бензилбромида. Образовавшуюся смесь перемешивают при температуре ледяной бани в течение 1 ч, затем выливают в насыщенный водный раствор бикарбоната натрия и экстрагируют этилацетатом. Органические соли объединяют, промывают рассолом, сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме. Остаток очищают хроматографически на ЖХВР системы "Ватерз Преп500", используя смесь 50% этилацетат/гексан, чтобы выделить 3,6 г (59%) 4-Бензил-2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина.
Спектр ПМР (в дейтерохлороформе):
2,3 (тд, J = 11 Гц, 1H), 2,71 (д, J = 11 Гц, 1H), 2,90 (д, J = 13 Гц, 1H), 3,22 (д, J = 7,3 Гц, 1H), 3,75 (м, 2H), 3,93 (м, 1H), 4,43 (д, J = 13 Гц, 1H), 4,45 (д, J = 7,3, 1H), 4,82 (д, J = 13 Гц, 1H), 7,19-7,5 (м, 12H), 7,67 (с, 1H).
2,3 (тд, J = 11 Гц, 1H), 2,71 (д, J = 11 Гц, 1H), 2,90 (д, J = 13 Гц, 1H), 3,22 (д, J = 7,3 Гц, 1H), 3,75 (м, 2H), 3,93 (м, 1H), 4,43 (д, J = 13 Гц, 1H), 4,45 (д, J = 7,3, 1H), 4,82 (д, J = 13 Гц, 1H), 7,19-7,5 (м, 12H), 7,67 (с, 1H).
Стадия В.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(R)-фенилморфолин
Раствор 3,6 г (7,27 ммоль) 4-бензил-2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина в 100 мл этанола и 5 мл воды, содержащей 720 мг катализатора 10% палладия на угле, гидрируют в автоклаве Парра в течение 36 ч. Катализатор отфильтровывают и тщательно промывают этилацетатом. Фильтрат концентрируют, и остаток распределяют между водой и этилацетатом. Органический слой промывают рассолом, сушат над сульфатом натрия, фильтруют и концентрируют. Остаток очищают методом флэш-хроматографии, используя градиент 10-60% этилацетат/гексан, чтобы выделить 2,05 г (70%) 2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина.
Раствор 3,6 г (7,27 ммоль) 4-бензил-2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина в 100 мл этанола и 5 мл воды, содержащей 720 мг катализатора 10% палладия на угле, гидрируют в автоклаве Парра в течение 36 ч. Катализатор отфильтровывают и тщательно промывают этилацетатом. Фильтрат концентрируют, и остаток распределяют между водой и этилацетатом. Органический слой промывают рассолом, сушат над сульфатом натрия, фильтруют и концентрируют. Остаток очищают методом флэш-хроматографии, используя градиент 10-60% этилацетат/гексан, чтобы выделить 2,05 г (70%) 2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолина.
Спектр ПМР (CDCl3): 1,92 (шир. с, 1H), 2,91 (м, 1H), 3,05 (тд, J = 11 Гц и 3 Гц, 1H), 3,68 (д, J = 7 Гц, 1H), 3,81 (тд, J = 11 Гц и 3 Гц, 1H), 4,01 (м, 1H), 4,44 (д, J = 7 Гц), 4,5 (д, J = 13 Гц, 1H), 4,85 (д, J = 13 Гц, 1H), 7,28 - 7,42 (м, 7H), 7,67 (с, 1H).
Пример 34.
4-(3-(1,2,4-Триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)- бензилокси)-3-(R)-фенилморфолин
Указанное в заголовке вещество было получено по методике примера 17, стадия Б, используя продукт примера 33, стадия В, в качестве исходного материала.
Указанное в заголовке вещество было получено по методике примера 17, стадия Б, используя продукт примера 33, стадия В, в качестве исходного материала.
Спектр ПМР (дейтерохлороформ):
1,75 (шир. с, 1H), 2,61 (тд, J = 12 Гц и 2 Гц, 1H), 2,83 (д, J = 12 Гц, 1H), 3,33 (д, J = 7 Гц, 1H), 3,48 (д, J = 15 Гц, 1H), 3,78 (д, J = 15 Гц, 1H), 3,85 (м, 1H), 3,99 (м, 1H), 4,44 (д, J = 13 Гц, 1H), 4,49 (д, J = 7 Гц, 1H), 4,81 (д, J = 13 Гц, 1H), 7,23-7,45 (м, 7H), 7,67 с, 1H), 7,96 (с, 1H).
1,75 (шир. с, 1H), 2,61 (тд, J = 12 Гц и 2 Гц, 1H), 2,83 (д, J = 12 Гц, 1H), 3,33 (д, J = 7 Гц, 1H), 3,48 (д, J = 15 Гц, 1H), 3,78 (д, J = 15 Гц, 1H), 3,85 (м, 1H), 3,99 (м, 1H), 4,44 (д, J = 13 Гц, 1H), 4,49 (д, J = 7 Гц, 1H), 4,81 (д, J = 13 Гц, 1H), 7,23-7,45 (м, 7H), 7,67 с, 1H), 7,96 (с, 1H).
Пример 35.
4-(3-(5-Оксо-1H,4H-1,2,4-триазоло)метил)-2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(R)-фенилморфолин
Указанное в заголовке вещества было получено по методике примера 18, стадии Б и В, используя продукт примера 33, стадия В, в качестве исходного материала.
Указанное в заголовке вещества было получено по методике примера 18, стадии Б и В, используя продукт примера 33, стадия В, в качестве исходного материала.
Пример 36.
4-(2-(Имидазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)- 3-(S)-фенилморфолин
Раствор 101 мг (0,25 ммоль) 2-(S)-(3,5-бис-(трифторметил)- бензилокси)-3-(S)-фенилморфолина (пример 15), 98 мг (1,0 ммоль) имидазол-2-карбоксальдегида и 5 капель ледяной уксусной кислоты в 3 мл метанола обрабатывают 1,5 мл одномолярного раствора цианоборгидрида натрия в тетрагидрофуране. Спустя 16 ч реакцию прерывают, добавляя 5 мл насыщенного водного раствора бикарбоната натрия, и смесь распределяют между 40 мл этилацетата и 20 мл воды. Отделяют органический слой, сушат его над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 8 г силикагеля, элюируемого смесью 50: 1: 0,1 хлористый метилен/метанол/гидроксид аммония, получают 54 мг (выход 44%) указанного в заголовке соединения в виде белого кристаллического вещества.
Раствор 101 мг (0,25 ммоль) 2-(S)-(3,5-бис-(трифторметил)- бензилокси)-3-(S)-фенилморфолина (пример 15), 98 мг (1,0 ммоль) имидазол-2-карбоксальдегида и 5 капель ледяной уксусной кислоты в 3 мл метанола обрабатывают 1,5 мл одномолярного раствора цианоборгидрида натрия в тетрагидрофуране. Спустя 16 ч реакцию прерывают, добавляя 5 мл насыщенного водного раствора бикарбоната натрия, и смесь распределяют между 40 мл этилацетата и 20 мл воды. Отделяют органический слой, сушат его над сульфатом магния и концентрируют в вакууме. В результате флэш-хроматографии на 8 г силикагеля, элюируемого смесью 50: 1: 0,1 хлористый метилен/метанол/гидроксид аммония, получают 54 мг (выход 44%) указанного в заголовке соединения в виде белого кристаллического вещества.
Спектр ПМР (CDCl3)
2,60 (дт, J = 3,2 Гц и 12,4 Гц, 1H), 2,85 (д, J = 12,4 Гц, 1H), 3,28 (д, J = 14,4 Гц, 1H), 3,59 (д, J = 2,8 Гц, 1H), 3,66 (дд, J = 2,0, 11,6 Гц, 1H), 3,84 (д, J = 14,4 Гц, 1H), 3,94 ( ≈ с, 2H), 4,14 (дт, J = 2,0, 12,0 Гц, 1H), 4,43 (д, J = 13,6 Гц, 1H), 4,71 (д, J = 2,8 Гц, 1H), 4,78 (д, J = 13,6 Гц, 1H), 6,99 (≈ с, 2H), 7,25-7,48 (м, 6H), 7,72 (с, 1H),
Спектр МС-ББА (FAB): m/z 486 (100%, M+H)
Пример 37.
2,60 (дт, J = 3,2 Гц и 12,4 Гц, 1H), 2,85 (д, J = 12,4 Гц, 1H), 3,28 (д, J = 14,4 Гц, 1H), 3,59 (д, J = 2,8 Гц, 1H), 3,66 (дд, J = 2,0, 11,6 Гц, 1H), 3,84 (д, J = 14,4 Гц, 1H), 3,94 ( ≈ с, 2H), 4,14 (дт, J = 2,0, 12,0 Гц, 1H), 4,43 (д, J = 13,6 Гц, 1H), 4,71 (д, J = 2,8 Гц, 1H), 4,78 (д, J = 13,6 Гц, 1H), 6,99 (≈ с, 2H), 7,25-7,48 (м, 6H), 7,72 (с, 1H),
Спектр МС-ББА (FAB): m/z 486 (100%, M+H)
Пример 37.
4-(2-(Имидазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)- 3-(R)-фенилморфолин
Указанное в заголовке вещество было получено по методике примера 36, используя подходящие исходные материалы.
Указанное в заголовке вещество было получено по методике примера 36, используя подходящие исходные материалы.
Спектр ПМР (CDCl3)
2,53 (тд, J = 11 Гц и 3 Гц, 1H), 2,74 (д, J = 12 Гц, 1H), 3,23 (д, J = 7 Гц, 1H), 3,32 (д, J = 15 Гц, 1H), 3,66 (д, J = 15 Гц, 1H), 3,77 (тд, J = 11 Гц и 2 Гц, 1H), 3,99 (м, 1H), 4,44 (м, 2H), 4,8 (д, J = 13,0 Гц, 1H), 6,94 (с, 2H), 7,2 - 7,45 (м, 7H ), 7,67 (с, 1H).
2,53 (тд, J = 11 Гц и 3 Гц, 1H), 2,74 (д, J = 12 Гц, 1H), 3,23 (д, J = 7 Гц, 1H), 3,32 (д, J = 15 Гц, 1H), 3,66 (д, J = 15 Гц, 1H), 3,77 (тд, J = 11 Гц и 2 Гц, 1H), 3,99 (м, 1H), 4,44 (м, 2H), 4,8 (д, J = 13,0 Гц, 1H), 6,94 (с, 2H), 7,2 - 7,45 (м, 7H ), 7,67 (с, 1H).
Пример 38
4-(5-(Имидазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)- 3-(R)-фенилморфолин
Указанное в заголовке вещество было получено по методике примера 36, используя подходящие исходные материалы.
4-(5-(Имидазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)- 3-(R)-фенилморфолин
Указанное в заголовке вещество было получено по методике примера 36, используя подходящие исходные материалы.
Спектр ПМР (CDCl3)
2,47 (тд, J = 12 Гц и 3 Гц, 1H), 2,83 (д, J = 12 Гц, 1H), 3,2 (м, 2H), 3,61 (д, J = 14 Гц, 1H), 3,79 (тд, J = 12 Гц и 2 Гц, 1H), 3,96 (м, 1H), 4,44 (м, 2H), 4,80 (д, J = 13 Гц, 1H), 6,81 (с, 1H), 7,28-7,45 (м, 7H), 7,60 (с, 1H), 7,66 (с, 1H).
2,47 (тд, J = 12 Гц и 3 Гц, 1H), 2,83 (д, J = 12 Гц, 1H), 3,2 (м, 2H), 3,61 (д, J = 14 Гц, 1H), 3,79 (тд, J = 12 Гц и 2 Гц, 1H), 3,96 (м, 1H), 4,44 (м, 2H), 4,80 (д, J = 13 Гц, 1H), 6,81 (с, 1H), 7,28-7,45 (м, 7H), 7,60 (с, 1H), 7,66 (с, 1H).
Пример 39.
4-(Аминокарбонилметил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)- 3-(R)-фенилморфолин
Указанное в заголовке вещество было получено по методике примера 15, используя подходящие исходные материалы.
Указанное в заголовке вещество было получено по методике примера 15, используя подходящие исходные материалы.
Спектр ПМР (CDCl3)
2,54 (тд, J = 11 Гц и 2 Гц, 1H), 2,64 (д, J = 17 Гц, 1H), 2,93 (д, J = 12 Гц, 1H), 3,14 (д, J = 17 Гц, 1H), 3,27 (д, J = 7 Гц, 1H), 3,83 (тд, J = 11 Гц и 2 Гц, 1H), 4,05 (м, 1H), 4,46 (м, 2H), 4,81 (д, J = 13 Гц, 1H), 5,62 (шир. с, 1H), 6,80 (шир. с, 1H), 7,28-7,32 (м, 7H), 7,67 (с, 1H).
2,54 (тд, J = 11 Гц и 2 Гц, 1H), 2,64 (д, J = 17 Гц, 1H), 2,93 (д, J = 12 Гц, 1H), 3,14 (д, J = 17 Гц, 1H), 3,27 (д, J = 7 Гц, 1H), 3,83 (тд, J = 11 Гц и 2 Гц, 1H), 4,05 (м, 1H), 4,46 (м, 2H), 4,81 (д, J = 13 Гц, 1H), 5,62 (шир. с, 1H), 6,80 (шир. с, 1H), 7,28-7,32 (м, 7H), 7,67 (с, 1H).
Примеры 40-43.
4-(3-(1,2,4-Триазоло)метил-2-(3-(трет-бутил)-5- метилбензилокси)-3-фенилморфолин, 4-(3-(5-Оксо-1H,4H-1,2,4-триазоло)- метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолин, 4-(2-(Имидазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)- 3-фенилморфолин, 4-(4-(Имидазоло)метил)-2-(3-трет-бутил)-5-метилбензилокси)-3-фенилморфолин
Указанные в заголовке вещества были получены (каждое) по методикам примеров 15, 17 и 18, используя соответственно замещенные исходные материалы и реагенты.
Указанные в заголовке вещества были получены (каждое) по методикам примеров 15, 17 и 18, используя соответственно замещенные исходные материалы и реагенты.
Пример 44.
2-(S)-(3,5-Дихлорбензилокси)-3-(S)-фенилморфолин
Стадия А.
Стадия А.
3,5-Дихлорбензиловый спирт, трифторметансульфонатный эфир
Раствор 6,09 г (34,4 ммоль) 3,5-дихлорбензилового спирта и 8,48 г (41,3 ммоль) 2,6-ди-трет-бутил-4-метилпиридина в 280 мл осушенного четыреххлористого углерода в атмосфере азота обрабатывают 5,95 мл (35,4 ммоль) ангидрида трифторметансульфокислоты, при комнатной температуре. Вскоре после добавления ангидрида образуется белый осадок. Спустя 90 мин суспензию отфильтровывают в атмосфере азота на фильтре Шленка, и фильтрат концентрируют в вакууме. Остаток, который представляет собой двухфазное масло, растворяют в 60 мл сухого толуола в атмосфере азота. Полученный прозрачный раствор был использован немедленно на стадии Б ниже.
Раствор 6,09 г (34,4 ммоль) 3,5-дихлорбензилового спирта и 8,48 г (41,3 ммоль) 2,6-ди-трет-бутил-4-метилпиридина в 280 мл осушенного четыреххлористого углерода в атмосфере азота обрабатывают 5,95 мл (35,4 ммоль) ангидрида трифторметансульфокислоты, при комнатной температуре. Вскоре после добавления ангидрида образуется белый осадок. Спустя 90 мин суспензию отфильтровывают в атмосфере азота на фильтре Шленка, и фильтрат концентрируют в вакууме. Остаток, который представляет собой двухфазное масло, растворяют в 60 мл сухого толуола в атмосфере азота. Полученный прозрачный раствор был использован немедленно на стадии Б ниже.
Стадия Б.
4-Бензил-2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолин
Раствор 5,11 г (19,1 ммоль) N-бензил-3-(S)-фенилморфолин-2-она (из примера 14) в 100 мл сухого ТГФ охлаждают до -75oC в атмосфере азота и обрабатывают по каплям 20,5 мл (20,5 ммоль) 1-молярного раствора три (втор-бутил)боргидрида лития (L-Селектрид) в тетрагидрофуране. После перемешивания раствора при -75oC в течение 30 мин, через полую трубочку добавляют раствор 3,5-дихлорбензиловый спирт-трифторметансульфонатного эфира в толуоле (из примера 44, стадия А), так чтобы внутренняя температура поддерживалась ниже -60oC. Образовавшийся раствор перемешивают при -75oC 1 ч и затем при температуре между -38oC и -50oC в течение 9 ч. Затем раствор обрабатывают 14 мл водного аммиака и хранят при -20oC 12 ч. Затем раствор выливают в смесь 50 мл этилацетата и 100 мл воды, и слои разделяют. Водную фазу экстрагируют 2 раза по 100 мл этилацетата, каждый экстракт промывают рассолом, объединенные органические слои сушат над сульфатом натрия, смесь фильтруют и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 235 г силикагеля, который элюируют 1,5 литрами смеси 100:2 гексана и этилацетата, затем 1,5 литрами смеси 100:3 гексана и этилацетата, затем 1,9 литрами смеси 100: 5 гексана и этилацетата, чтобы получить 4,4 г (54%) масла, которое по данным ПМР-спектра является смесью 8:1 цис-: транс-морфолинов.
Раствор 5,11 г (19,1 ммоль) N-бензил-3-(S)-фенилморфолин-2-она (из примера 14) в 100 мл сухого ТГФ охлаждают до -75oC в атмосфере азота и обрабатывают по каплям 20,5 мл (20,5 ммоль) 1-молярного раствора три (втор-бутил)боргидрида лития (L-Селектрид) в тетрагидрофуране. После перемешивания раствора при -75oC в течение 30 мин, через полую трубочку добавляют раствор 3,5-дихлорбензиловый спирт-трифторметансульфонатного эфира в толуоле (из примера 44, стадия А), так чтобы внутренняя температура поддерживалась ниже -60oC. Образовавшийся раствор перемешивают при -75oC 1 ч и затем при температуре между -38oC и -50oC в течение 9 ч. Затем раствор обрабатывают 14 мл водного аммиака и хранят при -20oC 12 ч. Затем раствор выливают в смесь 50 мл этилацетата и 100 мл воды, и слои разделяют. Водную фазу экстрагируют 2 раза по 100 мл этилацетата, каждый экстракт промывают рассолом, объединенные органические слои сушат над сульфатом натрия, смесь фильтруют и фильтрат концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 235 г силикагеля, который элюируют 1,5 литрами смеси 100:2 гексана и этилацетата, затем 1,5 литрами смеси 100:3 гексана и этилацетата, затем 1,9 литрами смеси 100: 5 гексана и этилацетата, чтобы получить 4,4 г (54%) масла, которое по данным ПМР-спектра является смесью 8:1 цис-: транс-морфолинов.
Спектр MC ББА: m/z 430, 428, 426 (M+H, ≈ 60%), 268 (M-ArCH2, 100%), 252 (M-ArCH2O, 75%), 222 (20%), 159 (45%).
Спектр ПМР (в дейтерохлороформе, 400 МГц, м.д.): δ основной (цис-изомер):
2,32 (т. д., J = 12, 3,6 1H), 2,84 (≈ т, J = 13, 2H), 3,52 (д, J = 2,6, 1H), 3,55 (д.кв, J = 11,3, 1,6, 1H), 3,91 (д, J = 13,3, 1H), 4,12 (тд, J = 11,6, 2,4, 1H), 4,29 (д, J = 13,6, 1H), 4,59 (д, J = 2,9, 1H), 4,60 (д, J = 13,6), 6,70 (с, 2H), 7,13 (т, J = 1,9, 1H), 7,2-7,6 (м, 8H), 7,53 (шир.д., 2H).
2,32 (т. д., J = 12, 3,6 1H), 2,84 (≈ т, J = 13, 2H), 3,52 (д, J = 2,6, 1H), 3,55 (д.кв, J = 11,3, 1,6, 1H), 3,91 (д, J = 13,3, 1H), 4,12 (тд, J = 11,6, 2,4, 1H), 4,29 (д, J = 13,6, 1H), 4,59 (д, J = 2,9, 1H), 4,60 (д, J = 13,6), 6,70 (с, 2H), 7,13 (т, J = 1,9, 1H), 7,2-7,6 (м, 8H), 7,53 (шир.д., 2H).
Стадия В.
2=(S)-(3,5-Дихлорбензилокси)-3-(S)-фенилморфолин
Раствор 0,33 г (0,77 ммоль) 4-бензил-2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолина (из примера 44, стадия В) и 0,22 г (1,54 ммоль) 1-хлорэтилхлорформиата в 4,5 мл 1,2-дихлорэтана помещают в ампулу, выдерживающую давление. Ампулу опускают в масляную баню, которая нагрета до 110oC. После перемешивания в течение 60 ч раствор охлаждают и концентрируют в вакууме. Остаток растворяют в 7 мл метанола и образовавшийся раствор нагревают при кипячении 30 мин. Смесь охлаждают и обрабатывают несколькими каплями концентрированного водного аммиака, и раствор концентрируют. Остаток частично очищают методом флэш-хроматографии на 67 г силикагеля, который элюируют 1,5 литрами смеси 100:1 хлористого метилена и метанола, причем богатые фракции очищают методом флэш-хроматографии на 32 г силикагеля, элюируемого смесью 50: 50 гексана и этилацетата и затем смесью 50:50:5 гексана:этилацетата и метанола, чтобы получить 0,051 г (20%) масла, которое по данным ПМР-спектра является чистым цис-морфолином.
Раствор 0,33 г (0,77 ммоль) 4-бензил-2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолина (из примера 44, стадия В) и 0,22 г (1,54 ммоль) 1-хлорэтилхлорформиата в 4,5 мл 1,2-дихлорэтана помещают в ампулу, выдерживающую давление. Ампулу опускают в масляную баню, которая нагрета до 110oC. После перемешивания в течение 60 ч раствор охлаждают и концентрируют в вакууме. Остаток растворяют в 7 мл метанола и образовавшийся раствор нагревают при кипячении 30 мин. Смесь охлаждают и обрабатывают несколькими каплями концентрированного водного аммиака, и раствор концентрируют. Остаток частично очищают методом флэш-хроматографии на 67 г силикагеля, который элюируют 1,5 литрами смеси 100:1 хлористого метилена и метанола, причем богатые фракции очищают методом флэш-хроматографии на 32 г силикагеля, элюируемого смесью 50: 50 гексана и этилацетата и затем смесью 50:50:5 гексана:этилацетата и метанола, чтобы получить 0,051 г (20%) масла, которое по данным ПМР-спектра является чистым цис-морфолином.
Спектр MC-ББА: m/z 468, 466, 464 (макс. 8%), 338, 340 (M+H, 25%), 178 (20%), 162 (100%), 132 (20%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 1,89 (шир.с, 1H), 3,08 (дд, J = 12,5, 2,9, 1H), 3,23 (тд, J = 12,2, 3,6, 1H), 3,59 (дд, J = 11,3, 2,5, 1H), 4,03 (тд, J = 11,7, 3, 1H), 4,09 (д, J = 2,4, 1H), 4,37 (д, J = 13,5, 1H), 4,62 (д, J = 13,3, 1H), 4,67 (д, J = 2,5, 1H), 6,72 (д, J = 1,8, 2H), 7,14 (д, J = 1,8, 1H), 7,25-7,40 (м, 5H).
Пример 45.
2-(S)-(3,5-Дихлорбензилокси)-4-(3-(5-Оксо-1H, 4H-1,2,4-триазоло) метил)-3-(S)-фенилморфолин
Стадия А.
Стадия А.
N-Метилкарбокси-2-хлорацетамидразон
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 35 мл сухого метанола охлаждают до 0oC и обрабатывают 0,105 г (1,9 ммоль) метоксида натрия. Удаляют баню со льдом, и смеси дают перемешаться при комнатной температуре в течение 30 мин. Затем к реакционной смеси добавляют 0,110 мл (1,9 ммоль) уксусной кислоты и после этого добавляют 5,8 г (64,9 ммоль) метилгидразинкарбоксилата. После перемешивания 30 мин при комнатной температуре суспензию концентрируют в вакууме и помещают на ночь в линию высокого вакуума, получая 10,5 г (98%) желтого порошка, который используется как на стадии В ниже.
Раствор 5 г (66,2 ммоль) хлорацетонитрила в 35 мл сухого метанола охлаждают до 0oC и обрабатывают 0,105 г (1,9 ммоль) метоксида натрия. Удаляют баню со льдом, и смеси дают перемешаться при комнатной температуре в течение 30 мин. Затем к реакционной смеси добавляют 0,110 мл (1,9 ммоль) уксусной кислоты и после этого добавляют 5,8 г (64,9 ммоль) метилгидразинкарбоксилата. После перемешивания 30 мин при комнатной температуре суспензию концентрируют в вакууме и помещают на ночь в линию высокого вакуума, получая 10,5 г (98%) желтого порошка, который используется как на стадии В ниже.
Стадия Б.
4-(2-(N-Метилкарбокси-ацетамидразоно-2-(S)-(3,5- ихлорбензилокси)-3-(S)-фенилморфолин
Раствор 0,05 г (0,15 ммоль) 2-(S)-3,5-дихлорбензилокси)- -3-(S)-фенилморфолина (из примера 44, стадия С), 0,034 г (0,21 моль) N-метилкарбокси-2-хлорацетамидразона (со стадии А) и 0,044 мл (0,25 ммоль) N,N-диизопропилэтиламина в 1 мл ацетонитрила перемешивают при комнатной температуре в течение 3 ч. Смесь распределяют между 20 мл хлористого метилена и 10 мл воды. Слои разделяют, органический слой сушат над сульфатом натрия и затем концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 35 г силикагеля, который элюируют 1 л смеси 50:1 хлористого метилена и метанола, затем 500 мл смеси 25:1:0,05 хлористый метилен/метанол/гидроксид аммония, получая 70 мг продукта (≈ 100%) в виде белого твердого вещества.
Раствор 0,05 г (0,15 ммоль) 2-(S)-3,5-дихлорбензилокси)- -3-(S)-фенилморфолина (из примера 44, стадия С), 0,034 г (0,21 моль) N-метилкарбокси-2-хлорацетамидразона (со стадии А) и 0,044 мл (0,25 ммоль) N,N-диизопропилэтиламина в 1 мл ацетонитрила перемешивают при комнатной температуре в течение 3 ч. Смесь распределяют между 20 мл хлористого метилена и 10 мл воды. Слои разделяют, органический слой сушат над сульфатом натрия и затем концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 35 г силикагеля, который элюируют 1 л смеси 50:1 хлористого метилена и метанола, затем 500 мл смеси 25:1:0,05 хлористый метилен/метанол/гидроксид аммония, получая 70 мг продукта (≈ 100%) в виде белого твердого вещества.
Спектр MC-ББА: m/z 469 (M+H, 60%), 467 (M+H, 100%), 291 (40%), 160 (20%), 1558 (25%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 2,48 (тд, J = 3,5, 12,2, 1H), 2,53 (д, J = 14,6, 1H), 2,90 (д, J = 11,8, 1H), 3,37 (д, J = 14,6, 1H), 3,52 (д, J = 2,8, 1H), 3,62 (дм, J = 11,4, 1H), 3,75 (с, 1H), 4,14 (тд, J = 2,2, 11,8, 1H), 4,28 (д, J = 13,5, 1H), 4,58 (д, J = 13,6), 4,60 (д, J = 2,8, 1H), 5,45 (шир.с, 2H), 6,74 (д, J = 1,9, 2H), 7,15 (т, J = 1,9, 1H), 7,30-7,46 (м, 6H).
Стадия В.
2-(S)-(3,5-Дихлорбензилокси)-4-(3-(5-оксо-1H, 4H-1,2,4-триазоло) метил)-3-(S)-фенилморфолин
Раствор 0,069 г (0,15 ммоль) 4-(2-(N-метилкарбоксиацетамидразоно)-2-(S)-(3,5-дихлорбензилокси)-3- (S)-фенилморфолина (со стадии Б) в 6 мл ксилолов нагревают при кипячении в течение 2 ч. Раствор охлаждают и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 35 г силикагеля, который элюируют 500 мл смеси 50:1:0,1 хлористого метилена/метанола/водного аммиака, затем 500 мл смеси 20:1:0,1 хлористого метилена/метанола/водного аммиака, получая 56 мг (88%) продукта в виде белого порошка.
Раствор 0,069 г (0,15 ммоль) 4-(2-(N-метилкарбоксиацетамидразоно)-2-(S)-(3,5-дихлорбензилокси)-3- (S)-фенилморфолина (со стадии Б) в 6 мл ксилолов нагревают при кипячении в течение 2 ч. Раствор охлаждают и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 35 г силикагеля, который элюируют 500 мл смеси 50:1:0,1 хлористого метилена/метанола/водного аммиака, затем 500 мл смеси 20:1:0,1 хлористого метилена/метанола/водного аммиака, получая 56 мг (88%) продукта в виде белого порошка.
Спектр MC-ББА: m/z 437 (M+H, 65%), 435 (M+H, 100%), 259 (85%), 161 (55%)
Спектр ПМР (CDCl3, 400 МГц, м.д.): α 2,53 (т, J = 11,7, 3,6, 1H), 2,88 (д, J = 11,6, 1H), 2,96 (д, J = 14,3, 1H), 3,54 (д, J = 2,6, 1H), 3,63 (дд, J = 11,6, 1,9, 1H), 3,68 (д, J = 14,6, 1H), 4,16 (т, J = 11,7, 2,2, 1H), 4,30 (д, J = 13,6), 4,58 (д, J = 2,7, 1H), 4,67 (д, J = 13,6, 1H), 6,65 (д, J = 1,8, 2H), 7,07 (т, J = 1,9, 1H), 7,29-7,44 (м, 5H), 10,25 (шир.с, 1H), 10,75 (шир.с, 1H).
Спектр ПМР (CDCl3, 400 МГц, м.д.): α 2,53 (т, J = 11,7, 3,6, 1H), 2,88 (д, J = 11,6, 1H), 2,96 (д, J = 14,3, 1H), 3,54 (д, J = 2,6, 1H), 3,63 (дд, J = 11,6, 1,9, 1H), 3,68 (д, J = 14,6, 1H), 4,16 (т, J = 11,7, 2,2, 1H), 4,30 (д, J = 13,6), 4,58 (д, J = 2,7, 1H), 4,67 (д, J = 13,6, 1H), 6,65 (д, J = 1,8, 2H), 7,07 (т, J = 1,9, 1H), 7,29-7,44 (м, 5H), 10,25 (шир.с, 1H), 10,75 (шир.с, 1H).
Пример 46.
2-(S)-(3,5-Бис-трифторметил)бензилокси)-4-метоксикарбонилметил)- 3-(S)-фенилморфолин
Раствор 300 мг (0,74 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина из примера 15, стадия В) и 0,35 мл (2,0 ммоль) N,N-диизопропилэтиламина в 5 мл сухого ацетонитрила обрабатывают 0,19 мл (2,0 ммоль) метилбромацетата, и смесь перемешивают при комнатной температуре в течение 16 ч. Затем раствор концентрируют в вакууме, и остаток распределяют между 30 мл эфира и 15 мл 0,5 н. водного раствора бисульфата калия. Слои разделяют, и органический слой промывают 10 мл рассола и сушат над сульфатом магния. После фильтрации органическую фазу концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 20 г силикагеля, который элюируют смесью 80:20 гексанов и эфира, получая 351 мг продукта (99%).
Раствор 300 мг (0,74 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина из примера 15, стадия В) и 0,35 мл (2,0 ммоль) N,N-диизопропилэтиламина в 5 мл сухого ацетонитрила обрабатывают 0,19 мл (2,0 ммоль) метилбромацетата, и смесь перемешивают при комнатной температуре в течение 16 ч. Затем раствор концентрируют в вакууме, и остаток распределяют между 30 мл эфира и 15 мл 0,5 н. водного раствора бисульфата калия. Слои разделяют, и органический слой промывают 10 мл рассола и сушат над сульфатом магния. После фильтрации органическую фазу концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 20 г силикагеля, который элюируют смесью 80:20 гексанов и эфира, получая 351 мг продукта (99%).
[δ]D = +147,3o (C = 1,6, в хлороформе).
Спектр MC-ББА: m/z 478 (M+H, 40%), 477 (65%), 418 (50%), 250 (95%), 234 (90%), 227 (100%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 3,02 (шир.д., 2H), 3,13 (д, J = 16,9, 1H), 3,36 (д, J = 16,8), 3,62 (с, 3H), 3,69 (дт, J = 11,7, 2,2, 1H), 4,03 (шир. с, 1H), 4,23-4,32 (м, 1H), 4,44 (д, J = 13,3, 1H), 4,68 (д, J = 2,6, 1H), 4,81 (д, J = 13,5, 1H), 7,30-7,38 (м, 3H), 7,4-7,5 (м, 3H), 7,70 (с, 1H).
Анализ,
вычислено для C22H21F6NO4: C 55,35, H 4,43, N 2,93, F 23,88;
найдено: C 55,09, H 4,43, N 2,83, F 24,05.
вычислено для C22H21F6NO4: C 55,35, H 4,43, N 2,93, F 23,88;
найдено: C 55,09, H 4,43, N 2,83, F 24,05.
Пример 47.
2-(S)-(3,5-Бис-трифторметил)бензилокси)-4-(карбоксилметил)- 3-(S)-фенилморфолин
Раствор 16 мг (0,034 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) в 2 мл тетрагидрофурана и 0,5 мл воды обрабатывают 0,027 мл (0,067 ммоль) 2,5 н. водного раствора гидроксида натрия, и смесь перемешивают при комнатной температуре в течение 5 ч. Смесь обрабатывают 2 каплями 2 н. соляной кислоты и 3 мл воды, и раствор экстрагируют 15 мл смеси 1:1 гексанов и этилацетата. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 13 г силикагеля, который элюируют 250 мл смеси 100:3:0,1 хлористый метилен-метанол:уксусная кислота, затем 100 мл смеси 50:2:0,1 хлористый метилен:метанол:уксусная кислота, получая 14 мг масла (90%).
Раствор 16 мг (0,034 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) в 2 мл тетрагидрофурана и 0,5 мл воды обрабатывают 0,027 мл (0,067 ммоль) 2,5 н. водного раствора гидроксида натрия, и смесь перемешивают при комнатной температуре в течение 5 ч. Смесь обрабатывают 2 каплями 2 н. соляной кислоты и 3 мл воды, и раствор экстрагируют 15 мл смеси 1:1 гексанов и этилацетата. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают методом флэш-хроматографии на 13 г силикагеля, который элюируют 250 мл смеси 100:3:0,1 хлористый метилен-метанол:уксусная кислота, затем 100 мл смеси 50:2:0,1 хлористый метилен:метанол:уксусная кислота, получая 14 мг масла (90%).
Спектр MC-ББА: m/z 464 (M+H, 90%), 420 (M-CO2, 10%), 227 (ArCH2, 35%), 220 (M-OCH2Ar, 100%), 161 20%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 2,9 (≈ д, 2H), 3,03 (д, 1H), 3,33 (д, 1H), 3,72 (д, 1H), 3,90 (д, 1H), 4,25 (т, 1H), 4,44 (д, 1H), 4,71 (д, 1H), 4,79 (д, 1H), 7,3-7,4 (м, 5H), 7,44 (с, 2H), 7,71 (с, 1H).
Пример 48.
2-(S)-(3,5-Бис-трифторметил)бензилокси)-4-((2-аминоэтил) аминокарбонилметил)-3-(S)-фенилморфолин
Раствор 54 мг (0,11 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) и 0,15 мл этилендиамина (2,3 ммоль) в 1 мл метанола перемешивают при 55oC в течение 48 ч. Смесь концентрируют, и остаток очищают методом флэш-хроматографии на 16 г силикагеля, который элюируют 500 мл смеси 50:40:0,1 хлористый метилен:метанол:водный аммиак, получая 57 мг масла (100%). Это масло растворяют в эфире и обрабатывают эфиром, насыщенным газообразным хлористым водородом. После концентрирования в вакууме получают 58 мг (95%) устойчивого масла.
Раствор 54 мг (0,11 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) и 0,15 мл этилендиамина (2,3 ммоль) в 1 мл метанола перемешивают при 55oC в течение 48 ч. Смесь концентрируют, и остаток очищают методом флэш-хроматографии на 16 г силикагеля, который элюируют 500 мл смеси 50:40:0,1 хлористый метилен:метанол:водный аммиак, получая 57 мг масла (100%). Это масло растворяют в эфире и обрабатывают эфиром, насыщенным газообразным хлористым водородом. После концентрирования в вакууме получают 58 мг (95%) устойчивого масла.
Спектр MC-ББА (свободное основание): m/z 506 (M+H, 100%), 418 (15%), 262 (35%), 227 (30%), 173 (40%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 2,56 (д, J = 15,5, 1H), 2,59 (т.д., J = 12,0, 3,6, 1H), 2,82 (т, J = 6,5, 2H), 2,96 (д, J = 11,8, 1H), 3,21 (д, J = 15,8, 1H), 3,25-3,40 (м, 2H), 3,65 (д, J = 2,6, 1H), 3,67 (≈ дг, J = 11,4, ≈ 2, 1H), 4,18 (т.д., J = 11,8, 2,6, 1H), 4,33 (д, J = 13,5, 1H), 4,69 (д, J = 2,7, 1H), 4,79 (д, J = 13,5, 1H), 7,25-7,40 (м, 5H), 7,46 (с, 2H), 7,59 (ш.т., 1H), 7,71 (с, 1H).
Пример 49.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-((3-аминопропил) аминокарбонилметил)-3-(S)-фенилморфолин
Раствор 59 мг (0,12 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) и 0,21 мл 1,3-пропилендиамина (2,5 ммоль) в 1 мл метанола перемешивают при 55oC в течение 72 ч. Смесь концентрируют, и остаток очищают методом флэш-хроматографии на 16 г силикагеля, который элюируют 500 мл смеси 10:1:0,05 хлористый метилен:метанол:водный аммиак, получая 56 мг масла (88%). Это масло растворяют в хлористом метилене и обрабатывают хлористым метиленом, насыщенным газообразным хлористым водородом. После концентрирования в вакууме получают белую пасту.
Раствор 59 мг (0,12 ммоль) 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(метоксикарбонилметил)- 3-(S)-фенилморфолина (из примера 46) и 0,21 мл 1,3-пропилендиамина (2,5 ммоль) в 1 мл метанола перемешивают при 55oC в течение 72 ч. Смесь концентрируют, и остаток очищают методом флэш-хроматографии на 16 г силикагеля, который элюируют 500 мл смеси 10:1:0,05 хлористый метилен:метанол:водный аммиак, получая 56 мг масла (88%). Это масло растворяют в хлористом метилене и обрабатывают хлористым метиленом, насыщенным газообразным хлористым водородом. После концентрирования в вакууме получают белую пасту.
Спектр MC-ББА (свободное основание): m/z 520 (M+H, 100%), 418 (10%), 276 (30%), 227 (20%), 174 (30%).
Спектр ПМР (CDCl3, 400 МГц, м.д.): δ 1,64 (пентет, J = 6,6, 2H), 2,53 (т, J = 15,5, 1H), 2,58 (тд, J = 12,0, 3,6, 1H), 2,73 (т, J = 6,5, 2H), 2,92 (д, J = 11,8, 1H), 3,19 (д, J = 15,8, 1H), 3,25-3,40 (м, 2H), 3,62 (д, J = 2,6, 1H), 3,65 (≈ дт, J = 11,4, ≈ 2, 1H), 4,16 (тд, J = 11,8, 2,6, 1H), 4.41(д, J = 13,5, 1H), 4,68 (д, J= 2,7, 1H), 4,79 (д, J= 13,5 1H), 7,25-7,40 (м, 5H), 7,45 (с, 2H), 7,57 (шир. т., 1H), 7,70 (с. 1H).
Пример 50.
4-бензил-5-(S), 6-(R)-(диметил)-3-(S)-фенилморфолинон-2
4-бензил-5-(R), 6-(S)-(диметил)-3-(S)-фенилморфолинон-2
К суспензии 1,7 г (7,0 ммоль) N -бензил-(S)- фенилглицина (пример 13) в 15 мл хлористого метилена при 0oC добавляют 6,9 мл (13,9 ммоль) 2-млоярного раствора триметилалюминия в толуоле. Спустя 1 ч при 0oC по каплям добавляют 0,625 мл (7,0 ммоль) (+/-)-транс-2,3-эпоккибутана (растворен в 2 мл хлористого метилена), и затем оставляют перемешиваться при 22oC, 16 ч. Затем реакционную смесь переносят в другую колбу, содержащую 30 мл смеси 1:1 гексана и хлористого метилена и 30 мл 1-молярного раствора калий-натрий тартрата, и перемешивают при 22oC 2 ч. Слои разделяют, и водный слой экстрагируют хлористым метиленом 3 раза по 100 мл. Объединенные органические слои промывают 25 мл насыщенного раствора хлорида натрия, сушат над безводным сульфатом натрия, фильтруют концентрируют в вакууме.
4-бензил-5-(R), 6-(S)-(диметил)-3-(S)-фенилморфолинон-2
К суспензии 1,7 г (7,0 ммоль) N -бензил-(S)- фенилглицина (пример 13) в 15 мл хлористого метилена при 0oC добавляют 6,9 мл (13,9 ммоль) 2-млоярного раствора триметилалюминия в толуоле. Спустя 1 ч при 0oC по каплям добавляют 0,625 мл (7,0 ммоль) (+/-)-транс-2,3-эпоккибутана (растворен в 2 мл хлористого метилена), и затем оставляют перемешиваться при 22oC, 16 ч. Затем реакционную смесь переносят в другую колбу, содержащую 30 мл смеси 1:1 гексана и хлористого метилена и 30 мл 1-молярного раствора калий-натрий тартрата, и перемешивают при 22oC 2 ч. Слои разделяют, и водный слой экстрагируют хлористым метиленом 3 раза по 100 мл. Объединенные органические слои промывают 25 мл насыщенного раствора хлорида натрия, сушат над безводным сульфатом натрия, фильтруют концентрируют в вакууме.
Неочищенный спирт растворяют в 25 мл толуола, обрабатывают 93 мг (0,49 ммоль) п-толуолсульфокислоты и нагревают при 50oC 20 ч. Затем реакционную смесь охлаждают и концентрируют в вакууме. Остаток распределяют между 15 мл диэтилового эфира и 10 мл насыщенного водного раствора бикарбоната натрия. Слои разделяют, и органический слой промывают 3 раза по 10 мл воды. Объединенные органические слои промывают 25 мл насыщенного раствора хлорида натрия, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Очистка методом флэш-хроматографии на 145 г силикагеля с использованием смеси 1:4 (по объему) этилацетата и гексана в качестве элюента дает 567 мг лактона с высоким значением Rf (изомер А) и 388 мг лактона с низким значением Rf (изомер Б).
Спектр ПМР (CDCl3, 400 МГц) δ изомер А: 1,04 (д, 3H, J= 8,0 Гц), 1,24 (д, 3H, J= 8,0 Гц), 2,92 (шир, кв. д), 1H) 3,41 (д, 1H, J = 16,0 Гц), 3,62 (д, 1H, J= 16,0 Гц), 4,38 (с, 1H), 4,96 (шир, кв. д. 1H), 7,20 - 7,42 (м, 8H), 7,58-7,64 (м, 2H), изомер В: 1,04 (д, 3H, J = 10,0 Гц), 1,39 (д, 3H, J= 10,0 Гц), 3,06 (шир. кв. д, 1H), 3,53 (д, 1H, J = 16,0 Гц), 3,81 (д, 1H, J = 16,0 Гц), 4,33 (с. 1H), 4,67 (шир, кв. д. 1H), 7,18 -7,50 (м, 10H).
Спектр МС-ББА: m/z 478 (M+H, 40%), 477 (65%), 418 (50%), 250 (95%), 234 (90%), 227 (100%).
Пример 51.
2(R)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин
Стадия А.
Стадия А.
4-бензил-2-(R)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин.
В соответствии с методикой примера 15, стадия Б 251 мг (0,85 ммоль) изомера А из примера 50 (4-бензил-[5-(S), 6(R) или 5-(R), 6(S)-диметил)-3-(S)-фенилморфолинон) получают 238 мг (53%) продукта в виде масла.
Спектр ПМР (400 МГц, CDCl3) δ 1,03 (д, 3H, J = 6,7 Гц), 1,13 (д, 3H, J= 6,6 Гц), 2,61 (кв, д, 1H, J = 2,2 и 6,6 Гц), 3,26 (д, 1H, J= 13,9 Гц), 3,55 (д, 1H, J = 13,9 Гц), 3,63 (д, 1H, J= 7,6 Гц), 4,01 (кв. д. 1H, J = 2,3 и 6,6 Гц), 4,44 (д. 1H, J = 13,1 Гц), 4,53 (д, 1H, J = 7,7 Гц), 4,71 (с, 1H), 4,85 (д, 1H, J= 13,2 Гц), 7,20-7,35 (м, 9H), 7,46-7,48 (м, 2H), 7,67 (с, 1H), 7,81 (с, 1H).
Спектр МС-ББА: m/z 523 (M+H, 100%), 296 (95%), 280 (40%), 227 (50%)
Стадия Б
2-(R)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин.
Стадия Б
2-(R)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин.
В соответствии с методикой примера 15, стадия В 260 мг исходного материала из стадии А [произведен из изомера А в примере 50 (4-бензил-2-(R)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6-(R) или 5(R),6(S)-диметил]-8-(S)-фенилморфолино)] получают 122 мг (57%) продукта в виде масла.
Спектр ПМР (400 МГц, CDCl3) δ 1,19 (д, 3H, J = 6,5 Гц), 1,27 (д, 3H, J = 6,7 Гц), 2,97 (кв. д. 1H, J = 2,9 и 6,9 Гц), 3,96 (д, 1H, J= 7,7 Гц), 4,08 - 4,11 (м, 2H), 4,39 (д, 1H, J = 7,7 Гц), 4,50 (д, 1H, J= 13,3 Гц), 4,88 (д, 1H, J = 13,2 Гц), 7,27-7,33 (м, 3H), 7,40-7,42 (м, 4H), 7,67 (с, 1H).
МС-ББА: m/z 433 (M+H, 45%), 227 (35%), 206 (40%), 190 (100%).
Пример 52.
2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S), 6(R)-диметил]-3-(S)-фенилморфолин
Стадия А
4-бензил-2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6(R)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 15, стадия Б 449 мг (1,52 ммоль) изомера Б из примера 50 (4-бензил-[5-(R), 6-(S) или 5-(S), 6(R)-(диметил)] -3-(S)-фенилморфолинон) получают 400 мг (31%) продукта в виде масла.
Стадия А
4-бензил-2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6(R)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 15, стадия Б 449 мг (1,52 ммоль) изомера Б из примера 50 (4-бензил-[5-(R), 6-(S) или 5-(S), 6(R)-(диметил)] -3-(S)-фенилморфолинон) получают 400 мг (31%) продукта в виде масла.
Спектр ПМР (CDCl3, 400 МГц) δ: 0,90 (д, 3H, J= 6,8 Гц), 1,37 (д, 3H, J = 6,6 Гц), 2,86-2,89 (шир. кв. д, 1H), 3,47 (д, 1H, J = 15,0 Гц), 3,82-3,85 (м, 2H), 3,99-4,02 (шир. кв. д, 1H), 4,45 (д, 1H, J= 13,6 Гц), 4,81 (д, 1H, J= 2,0 Гц), 4,87 (д, 1H, J= 13,5 Гц), 7,17-7,83 (м, 13H)
Стадия Б
2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 15, стадия В 400 мг исходного материала из стадии А [произведен из изомера Б в примере 50 (4-бензил-2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S), 6(R) -диметил]-3-(S)-фенилморфолино)] получают 230 мг (69%) продукта в виде масла.
Стадия Б
2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(S), 6(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 15, стадия В 400 мг исходного материала из стадии А [произведен из изомера Б в примере 50 (4-бензил-2-(S)-(3,5-Бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S), 6(R) -диметил]-3-(S)-фенилморфолино)] получают 230 мг (69%) продукта в виде масла.
Спектр ПМР (CDCl3, 400 МГц) δ: 1,08 (д, 3H, J = 6,7 Гц), 1,38 (д, 3H, J = 7,0 Гц), 3,41 - 3,45 (шир. кв. д, 1H), 3,85-3,89 (шир. кв. д., 1H), 4,16 (д, 1H, J = 2,9 Гц), 4,49 (д, 1H, J= 13,6 Гц), 4,71 (д, 1H, J = 2,9 Гц), 4,82 (д, 1H, J = 13,6 Гц), 7,25-7,36 (м, 7H), 7,66 (с. 1H)
Спектр МС-ББА: m/z 434 (M+H, 35%), 227 (40%), 206 (40%), 190 (100%)
Пример 53.
Спектр МС-ББА: m/z 434 (M+H, 35%), 227 (40%), 206 (40%), 190 (100%)
Пример 53.
2-(R)-(3,5-Бис(трифторметил)бензилокси)-4-(3-(1,2,4-триазоло) -метил)-[5-(S), 6(R) или 5-(R),6(S)-диметил]-3-(S)-фенилморфолин
Смесь 62 мг (0,14 ммоль) 2-(R)-(3,5-бис)трифторметил)-бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолина (из примера 51, стадия Б), 62 мг (0,45 ммоль) безводного карбоната калия и 26 мг (0,19 ммоль)
N-формил-2-хлорацетамидразона (из примера 17, стадия А) в 2 мл диметилформамида нагревают при 60oC в течение 2 ч и затем при 118oC в течение 4,5 ч. Затем смеси дают охладиться до комнатной температуры и реакцию прерывают, добавляя 5 мл воды и разбавляют 15 мл этилацетата. Слои разделяют, и органический промывают 2 раза по 10 мл этилацетатом. Объединенные органические слои промывают 10 мл рассола, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Очистка методом флэш-хроматографии на 42 г силикагеля, с использованием в качестве элюента смеси 95:5 хлористого метилена и метанола, дает 42 мг прозрачного масла.
Смесь 62 мг (0,14 ммоль) 2-(R)-(3,5-бис)трифторметил)-бензилокси)-[5-(S), 6-(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолина (из примера 51, стадия Б), 62 мг (0,45 ммоль) безводного карбоната калия и 26 мг (0,19 ммоль)
N-формил-2-хлорацетамидразона (из примера 17, стадия А) в 2 мл диметилформамида нагревают при 60oC в течение 2 ч и затем при 118oC в течение 4,5 ч. Затем смеси дают охладиться до комнатной температуры и реакцию прерывают, добавляя 5 мл воды и разбавляют 15 мл этилацетата. Слои разделяют, и органический промывают 2 раза по 10 мл этилацетатом. Объединенные органические слои промывают 10 мл рассола, сушат над безводным сульфатом магния, фильтруют и концентрируют в вакууме. Очистка методом флэш-хроматографии на 42 г силикагеля, с использованием в качестве элюента смеси 95:5 хлористого метилена и метанола, дает 42 мг прозрачного масла.
Спектр ПМР (CDCl3, 400 Гц, м.д.) δ 1,13 (д, 3H, J = 6,5 Гц), 1,19 (д, 3H, J= 6,5 Гц), 2,65 (кв, д, 1H, J = 1,9 и 6,5 Гц), 3,58 (д, 1H, J = 15,5 Гц), 3,65 (д, 1H, J = 7,7 Гц), 3,75 (д, 1H, J= 15,4 Гц), 4,06 (кв, д, 1H, J = 2,2 и 6,6 Гц), 4,45 (д, 1H, J = 13,2 Гц), 4,54 (д, 1H, J = 7,7 Гц), 4,84 (д, 1H, J = 13,2 Гц), 7,28 - 7,37 (м, 7H), 7,67 (с, 1H), 7,89 (с, 1H).
Спектр МС-ББА: m/Z 516 (M+H, 52%), 287 (28%), 271 (100%), 227 (40%), 202 (38%).
Пример 54
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4- триазоло)метил)-[5-(S), 6-(R) или 5-(R), 6-(S)-диметил]-3-(S)-фенилморфолин
Раствор 96 мг (0,22 ммоль) 2-(R)-(3,5-бис(трифторметил)-бензилокси)-[5-(S), 6(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолина (из примера 51, стадия Б), 92 мг (0,66 ммоль) карбоната калия и 48 мг (0,28 ммоль) N-метил-карбокси-2-хлорацетамидразона (со стадии А примера 18) в 4 мл диметилформамида нагревают при 60oC 1,5 ч и при 120oC в течение 3,5 ч. Смесь охлаждают до комнатной температуры и распределяют между 15 мл воды и 25 мл этилацетата. Водный слой экстрагируют 3 раза по 10 мл этилацетата, объединенные органические слои промывают 10 мл рассола, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток частично очищают методом флэш-хроматографии на 42 г силикагеля, который элюируют 2 л смеси 98:2 (по объему) хлористого метилена и метанола; богатые фракции очищают в тех же условиях, получая 38 мг прозрачного масла (33%).
2-(R)-(3,5-Бис-(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4- триазоло)метил)-[5-(S), 6-(R) или 5-(R), 6-(S)-диметил]-3-(S)-фенилморфолин
Раствор 96 мг (0,22 ммоль) 2-(R)-(3,5-бис(трифторметил)-бензилокси)-[5-(S), 6(R) или 5-(R), 6(S)-диметил]-3-(S)-фенилморфолина (из примера 51, стадия Б), 92 мг (0,66 ммоль) карбоната калия и 48 мг (0,28 ммоль) N-метил-карбокси-2-хлорацетамидразона (со стадии А примера 18) в 4 мл диметилформамида нагревают при 60oC 1,5 ч и при 120oC в течение 3,5 ч. Смесь охлаждают до комнатной температуры и распределяют между 15 мл воды и 25 мл этилацетата. Водный слой экстрагируют 3 раза по 10 мл этилацетата, объединенные органические слои промывают 10 мл рассола, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток частично очищают методом флэш-хроматографии на 42 г силикагеля, который элюируют 2 л смеси 98:2 (по объему) хлористого метилена и метанола; богатые фракции очищают в тех же условиях, получая 38 мг прозрачного масла (33%).
Спектр ПМР (CDCl3, 400 МГц) δ: 1,09 (д, 3H, J = 6,5 Гц), 1,20 (д, 3H, J = 6,6 Гц), 2,64 (кв, д, 1H, J= 2,4 и 6,6 Гц), 3,33 (с, 1H), 3,56 (д, 1H, J = 7,6 Гц), 4,11 (кв, д, 1H, J = 2,4 и 6,6 Гц), 4,41 (д, 1H, J = 13,2 Гц), 4,57 (д, 1H, J = 7,7 Гц), 4,82 (д, 1H, J = 13,2 Гц), 7,25-7,30 (м, 5H), 7,40 (д, 2H, J= 5,7 Гц), 7,65 (с, 1H), 9,46 (с, 1H), 10,51 (с, 1H).
Спектр МС-ББА: M/Z 531 (M+H, 98%), 287 (100%), 227 (80%), 189 (65%)
Пример 55.
Пример 55.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(3''-(1,2,4- триазоло)метил)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 53, 75 мг (0,17 ммоль) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина (из примера 52, стадия Б) обеспечивают, после флэш-хроматографической очистки на 73 г силикагеля с использованием в качестве элюента смеси 38 : 2 (по объему) хлористого метилена и метанола, 46 мг желтого масла (52%).
В соответствии с методикой примера 53, 75 мг (0,17 ммоль) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина (из примера 52, стадия Б) обеспечивают, после флэш-хроматографической очистки на 73 г силикагеля с использованием в качестве элюента смеси 38 : 2 (по объему) хлористого метилена и метанола, 46 мг желтого масла (52%).
Спектр ПМР (CDCl3, 400 МГц) δ: 1,04 (д, 3H, J = 6,6 Гц), 1,46 (д, 3H, J = 6,7 Гц), 3,05 - 3,08 (м, 1H), 3,74 - 3,81 (м, 2H), 3,91 - 3,95 (м, 2H), 4,41 (д, 1H, J = 13,2 Гц), 4,69 (д, 1H, J = 3,2 Гц), 4,82 (д, 1H, J = 13,5 Гц), 7,31 - 7,35 (м, 5H), 7,43 - 7,45 (м, 2H), 7,68 (с, 1H), 7,91 (с, 1H).
Масс-спектр (EI): m/z 432 (36%), 287 (60%), 270 (65%), 227 (30%), 187 (48%), 83 (100%).
Пример 56.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(3-(5-оксо- 1,2,4-триазоло)метил)-[5-(R),6-(S) или 5-(S), 6-(R)-диметил]-3-(S)-фенилморфолин
В соответствии с методикой примера 54, 86 мг (0,2 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S), 6-(R)-диметил]-3-(S)-фенилморфолина (из примера 47, стадия Б) обеспечивают, после флэш-хроматографической очистки на 73 г силикагеля с использованием в качестве элюента смеси 95:5 (по объему) хлористого метилена и метанола, 32 мг желтого масла (30%).
В соответствии с методикой примера 54, 86 мг (0,2 ммоль) 2-(S)-(3,5-бис-(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S), 6-(R)-диметил]-3-(S)-фенилморфолина (из примера 47, стадия Б) обеспечивают, после флэш-хроматографической очистки на 73 г силикагеля с использованием в качестве элюента смеси 95:5 (по объему) хлористого метилена и метанола, 32 мг желтого масла (30%).
Спектр ПМР (CDCl3, 400 МГц) δ: 1,03 (д, 3H, J = 6,7 Гц), 1,40 (д, 3H, J = 6,8 Гц), 3,00 (кв. д, 3H, J = 3,8 и 6,8 Гц), 3,44 (д, 1H, J = 16,1 Гц), 3,63 (д, 1H, J = 16,0 Гц), 3,82 (д, 1H, J = 3,3 Гц), 3,95 (кв. д, 1H, J = 3,7 и 6,7 Гц), 4,43 (д, 1H, J = 13,5 Гц), 4,73 (д, 1H, J = 3,3 Гц), 4,84 (д, 1H, J = 13,6 Гц), 7,28 - 7,47 (м, 7H), 7,68 (с, 1H), 9,52 (д, 2H).
Масс МС-ББА: m/z 531 (M + H, 100%), 287 (55%), 227 (25%), 147 (50%).
Пример 57.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(2-(1-4- бензил)пиперидино)этил)-3-(S)-фенилморфолин
К раствору 50 мг (0,12 ммоль) 2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(S)-фенилморфолина и 50 мг (0,18 ммоль) 4-бензил-1-(2-хлорэтил)пиперидина в 0,5 мл ацетонитрила при комнатной температуре добавляют 65 мкл (0,36 ммоль) диизопропилэтиламина. Спустя 60 ч по данным тонкослойной хроматографии (ТСХ) реакция завершилась неполностью. Реакционную смесь разбавляют хлористым метиленом, промывают водой, затем рассолом, сушат над сульфатом натрия и выпаривают. Методом препаративной ТСХ получают 36 мг (50%) указанного в заголовке вещества в виде масла.
К раствору 50 мг (0,12 ммоль) 2-(S)-(3,5-бис- (трифторметил)бензилокси)-3-(S)-фенилморфолина и 50 мг (0,18 ммоль) 4-бензил-1-(2-хлорэтил)пиперидина в 0,5 мл ацетонитрила при комнатной температуре добавляют 65 мкл (0,36 ммоль) диизопропилэтиламина. Спустя 60 ч по данным тонкослойной хроматографии (ТСХ) реакция завершилась неполностью. Реакционную смесь разбавляют хлористым метиленом, промывают водой, затем рассолом, сушат над сульфатом натрия и выпаривают. Методом препаративной ТСХ получают 36 мг (50%) указанного в заголовке вещества в виде масла.
Спектр ПМР (CDCl3, 400 МГц) δ: 1,1 - 1,4 (м, 2H), 1,4 - 1,65 (2м, 4H), 1,65 - 2,05 (м, 3H), 2,05 - 2,3 (м, 1H), 2,35 - 2,5 (м, и д., J = 7 Гц, 3H), 2,55 (шир. т, J = 11 Гц, 1H), 2,65 - 2,8 (м, 2H), 3,09 (д, J = 11 Гц, 1H), 3,50 (д, J = 2,5 Гц, 1H), 3,66 (дд, J = 2 или 11 Гц, 1H), 4,15 (дт, J = 2 и 12 Гц, 1H), 4,38 и 4,75 (AB кв, J = 13 Гц, 2H), 4,61 (д, J = 2,5 Гц, 1H), 7,06 (д, J = 7 Гц, 2H), 7,15 (т, J = 7 Гц, 1H), 7,2 - 7,35 (м, 5H), 7,36 (м, 4H), 7,75 (с, 1H).
Пример 58.
(S)-(4-Фторфенил)глицин
Стадия А.
Стадия А.
3-(4-Фторфенил)ацетил-4-(S)-бензил-2-оксазолидинон
Высушенную в печи трехгорлую колбу емкостью 1 л, снабженную перегородкой, вводом азота, термометром и магнитной мешалкой, продувают азотом и загружают в нее раствор 5,09 г (33 ммоль) 4-фторфенилуксусной кислоты в 100 мл безводного эфира. Раствор охлаждают до -10oC и обрабатывают 5,6 мл (40 ммоль) триэтиламина и затем 4,3 мл (35 ммоль) триметилацетилхлорида. Сразу же образуется белый осадок. Образовавшуюся смесь перемешивают при -10oC в течение 40 мин, затем охлаждают до -78oC.
Высушенную в печи трехгорлую колбу емкостью 1 л, снабженную перегородкой, вводом азота, термометром и магнитной мешалкой, продувают азотом и загружают в нее раствор 5,09 г (33 ммоль) 4-фторфенилуксусной кислоты в 100 мл безводного эфира. Раствор охлаждают до -10oC и обрабатывают 5,6 мл (40 ммоль) триэтиламина и затем 4,3 мл (35 ммоль) триметилацетилхлорида. Сразу же образуется белый осадок. Образовавшуюся смесь перемешивают при -10oC в течение 40 мин, затем охлаждают до -78oC.
Высушенную в печи круглодонную колбу емкостью 0,25 л, снабженную перегородкой и магнитной мешалкой, продувают азотом и загружают в нее раствор 5,31 г (30 ммоль) 4-(S)-бензил-2-оксазолидинона в 40 мл сухого тетрагидрофурана. Раствор перемешивают в бане с сухим льдом в ацетоне 10 минут, затем медленно добавляют 18,8 мл 1,6-молярного раствора н-бутиллития в гексане. Спустя 10 минут добавляют раствор литированного оксазолидинона через полую трубочку к смеси в трехгорлой колбе. Удаляют охлаждающую баню, и дают нагреться полученной смеси до 0oC. Реакцию прерывают добавлением 100 мл насыщенного водного раствора хлорида аммония, смесь переносят в колбу емкостью 1 л и эфир и тетрагидрофуран удаляют в вакууме. Концентрированную смесь распределяют между 300 мл хлористого метилена и 50 мл воды, и слои разделяют. Органический слой промывают 2-нормальным раствором соляной кислоты (200 мл), насыщенным водным раствором бикарбоната натрия (300 мл), сушат над сульфатом магния и концентрируют в вакууме. Флэш-хроматография на 400 г силикагеля с использованием в качестве элюента смеси 3 : 2 (по объему) гексанов и эфира дает 8,95 г масла, которое медленно отвердевает при стоянии. При перекристаллизации из смеси 10 : 1 гексанов и эфира получают 7,89 г (83%) указанного в заголовке соединения в виде белого твердого вещества с т. пл. 64 - 66oC.
Спектр МС-ББА: m/z 314 (M + H, 100%), 177 (M-ArCH2CO + H, 85%).
Спектр ПМР (400 МГц, CDCl3) δ: 2,76 (дд, 1H, J = 13,2, 9,2 Гц), 3,26 (дд, J = 13,2, 3,2), 4,16 - 4,34 (м, 4H), 4,65 - 4,70 (м, 1H), 7,02 - 7,33 (м, 9H).
Анализ:
Вычислено для C18H16FNO3: C 69,00, H 5,15, N 4,47, F 6,06.
Вычислено для C18H16FNO3: C 69,00, H 5,15, N 4,47, F 6,06.
Найдено: C 68,86, H 5,14, N 4,48, F 6,08.
Стадия Б.
3-((S)-Азидо-(4-фторфенил)ацетил-4-(S)-4-бензил-2-оксазолидинон
Высушенную в печи трехгорлую колбу емкостью 1 л, снабженную перегородкой, вводом азота, термометром и магнитной мешалкой, продувают азотом и загружают в нее 58 мл 1-молярного раствора бис(триметилсилил)амида в толуоле и 85 мл тетрагидрофурана. Этот раствор охлаждают до -78oC. Высушенную в печи круглодонную колбу емкостью 0,25 л, снабженную перегородкой и магнитной мешалкой, продувают азотом и загружают в нее раствор 7,20 г (23 ммоль) 3-(4-фторфенил)ацетил-4-(S)-бензил-2-оксазолидинона (из примера 58, стадии А) в 40 мл тетрагидрофурана. Ацилоксазолидиноновый раствор перемешивают в бане с сухим льдом в ацетоне 10 минут, затем переносят через трубочку в раствор с бис(триметилсилил)амидом с такой скоростью, чтобы температура внутри смеси поддерживалась ниже -70oC. Ацилоксазолидиноновую колбу промывают 15 мл тетрагидрофурана, и эту промывочную жидкость добавляют через трубочку в реакционную смесь, и образовавшуюся смесь перемешивают при -78oC в течение 30 мин.
Высушенную в печи трехгорлую колбу емкостью 1 л, снабженную перегородкой, вводом азота, термометром и магнитной мешалкой, продувают азотом и загружают в нее 58 мл 1-молярного раствора бис(триметилсилил)амида в толуоле и 85 мл тетрагидрофурана. Этот раствор охлаждают до -78oC. Высушенную в печи круглодонную колбу емкостью 0,25 л, снабженную перегородкой и магнитной мешалкой, продувают азотом и загружают в нее раствор 7,20 г (23 ммоль) 3-(4-фторфенил)ацетил-4-(S)-бензил-2-оксазолидинона (из примера 58, стадии А) в 40 мл тетрагидрофурана. Ацилоксазолидиноновый раствор перемешивают в бане с сухим льдом в ацетоне 10 минут, затем переносят через трубочку в раствор с бис(триметилсилил)амидом с такой скоростью, чтобы температура внутри смеси поддерживалась ниже -70oC. Ацилоксазолидиноновую колбу промывают 15 мл тетрагидрофурана, и эту промывочную жидкость добавляют через трубочку в реакционную смесь, и образовавшуюся смесь перемешивают при -78oC в течение 30 мин.
Высушенную в печи круглодонную колбу емкостью 0,25 л, снабженную перегородкой и магнитной мешалкой, продувают азотом и загружают в нее раствор 10,89 г (35,0 ммоль) 2,4,6-триизопропилфенилсульфонилазида в 40 мл тетрагидрофурана. Азидный раствор перемешивают в бане с сухим льдом в ацетоне 10 минут, затем переносят через трубочку в реакционную смесь с такой скоростью, чтобы температура внутри смеси поддерживалась ниже -70oC. Спустя 2 минуты реакцию прерывают добавлением 6,0 мл ледяной уксусной кислоты, удаляют охлаждающую баню, и смесь перемешивают при комнатной температуре 18 ч. Закаленную реакционную смесь распределяют между 300 мл этилацетата и 300 мл 50%-го водного раствора бикарбоната натрия. Отделяют органический слой, сушат его над сульфатом магния и концентрируют в вакууме. Флэш-хроматография на 500 г силикагеля с использованием в качестве элюента смеси 2 : 1 и затем 1 : 1 (по объему) гексанов и хлористого метилена дает 5,45 г (67%) указанного в заголовке соединения в виде масла.
ИК-спектр (в чистом виде), см-1: 2104, 1781, 1702.
Спектр ПМР (400 МГц, CDCl3): δ 2,86 (дд, 1H, J = 13,2, 9,6 Гц), 3,40 (дд, J = 13,2, 3,2), 4,09 - 4,19 (м, 2H), 4,62 - 4,68 (м, 1H), 6,14 (с, 1H), 7,07 - 7,47 (м, 9H).
Анализ:
Вычислено для C18H15FN4O3: C 61,01, H 4,27, N 15,81, F 4,36.
Вычислено для C18H15FN4O3: C 61,01, H 4,27, N 15,81, F 4,36.
Найдено: C 60,99, H 4,19, N 15,80, F 5,34.
Стадия В.
(S)-Азидо-(4-фторфенил)уксусная кислота
Раствор 5,4 г (15,2 ммоль) 3-((S)-Азидо-(4-фторфенил)ацетил- 4-(S)-бензил-2-оксазолидинона (из примера 58, стадия Б) в 200 мл смеси 3 : 1 (по объему) тетрагидрофурана и воды перемешивают в бане со льдом 10 минут. В один прием добавляют 1,28 г (30,4 ммоль) моногидрата гидроксида лития, и образовавшуюся смесь перемешивают на холоду 30 минут. Реакционную смесь распределяют между 100 мл хлористого метилена и 100 мл 25%-го водного бикарбоната натрия, и слои разделяют. Водный слой промывают 2 раза по 100 мл хлористым метиленом и подкисляют до pH 2 двухнормальным раствором соляной кислоты. Образовавшуюся смесь экстрагируют 2 раза по 100 мл этилацетата. Экстракты объединяют, промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме, получая 2,30 г масла (77%), которое используется на следующей стадии без дополнительной очистки.
Раствор 5,4 г (15,2 ммоль) 3-((S)-Азидо-(4-фторфенил)ацетил- 4-(S)-бензил-2-оксазолидинона (из примера 58, стадия Б) в 200 мл смеси 3 : 1 (по объему) тетрагидрофурана и воды перемешивают в бане со льдом 10 минут. В один прием добавляют 1,28 г (30,4 ммоль) моногидрата гидроксида лития, и образовавшуюся смесь перемешивают на холоду 30 минут. Реакционную смесь распределяют между 100 мл хлористого метилена и 100 мл 25%-го водного бикарбоната натрия, и слои разделяют. Водный слой промывают 2 раза по 100 мл хлористым метиленом и подкисляют до pH 2 двухнормальным раствором соляной кислоты. Образовавшуюся смесь экстрагируют 2 раза по 100 мл этилацетата. Экстракты объединяют, промывают 50 мл насыщенного водного раствора хлорида натрия, сушат над сульфатом магния и концентрируют в вакууме, получая 2,30 г масла (77%), которое используется на следующей стадии без дополнительной очистки.
ИК-спектр (в чистом виде), см-1: 2111, 1724.
Спектр ПМР (CDCl3, 400 МГц) δ: 5,06 (с, 1H), 7,08-7,45 (м, 4H), 8,75 (шир.с., 1H).
Стадия Г.
(S)-(4-Фторфенил)глицин
Смесь 2,30 г (11,8 ммоль) (S)-азидо-(4-фторфенил)уксусной кислоты (из примера 58, стадия B), 250 мг катализатора палладий-на-угле и 160 мг смеси 3:1 (по объему) воды и уксусной кислоты перемешивают при атмосферном давлении водорода 18 ч. Реакционную смесь фильтруют через Целит, причем колбу и лепешку на фильтре хорошо промывают 1 литром смеси 3:1 (по объему) воды и уксусной кислоты. Фильтрат концентрируют в вакууме примерно до объема 50 мл. Добавляют 300 мг толуола, и смесь концентрируют, получая твердое вещество. Это вещество суспендируют в смеси 1:1 (по объему) метанола и эфира, фильтруют и сушат, получая 1,99 г (100%) указанного в заголовке соединения.
Смесь 2,30 г (11,8 ммоль) (S)-азидо-(4-фторфенил)уксусной кислоты (из примера 58, стадия B), 250 мг катализатора палладий-на-угле и 160 мг смеси 3:1 (по объему) воды и уксусной кислоты перемешивают при атмосферном давлении водорода 18 ч. Реакционную смесь фильтруют через Целит, причем колбу и лепешку на фильтре хорошо промывают 1 литром смеси 3:1 (по объему) воды и уксусной кислоты. Фильтрат концентрируют в вакууме примерно до объема 50 мл. Добавляют 300 мг толуола, и смесь концентрируют, получая твердое вещество. Это вещество суспендируют в смеси 1:1 (по объему) метанола и эфира, фильтруют и сушат, получая 1,99 г (100%) указанного в заголовке соединения.
Спектр ПМР (400 МГц, D2O+NaOD): δ 3,97 (с, 1H), 6,77 (≈т, 2H, J=8,8), 7,01 (≈т, 2H, J=5,6).
Пример 59.
3-(S)-(4-Фторфенил)-4-бензил-2-морфолинон
Стадия А.
Стадия А.
N-Бензил (S)-(4-фторфенил)глицин
Раствор 1,87 г (11,05 ммоль) (S)-(4-фторфенил)глицина (из примера 58) и 1,12 мл (11,1 ммоль) бензальдегида в 11,1 мл 1 н. водного раствора гидроксида натрия и 11 мл метанола при 0oC обрабатывают 165 мг (4,4 ммоль) боргидрида натрия. Удаляют охлаждающую баню, и образовавшуюся смесь перемешивают 30 минут при комнатной температуре. В реакционную смесь добавляют
вторые порции (1,12 мл (11,1 ммоль)) бензальдегида и (165 мг (4,4 ммоль)) боргидрида натрия, и перемешивание продолжают 1,5 ч. Реакционную смесь распределяют между 100 мл эфира и 50 мл воды, и слои разделяют. Водный слой отделяют и фильтруют, чтобы удалить небольшие количества нерастворимого материала. Фильтрат подкисляют до pH 5 двухнормальным раствором соляной кислоты, и выпавшее в осадок твердое вещество фильтруют, хорошо промывают водой, затем эфиром и сушат, получая 1,95 г указанного в заголовке соединения.
Раствор 1,87 г (11,05 ммоль) (S)-(4-фторфенил)глицина (из примера 58) и 1,12 мл (11,1 ммоль) бензальдегида в 11,1 мл 1 н. водного раствора гидроксида натрия и 11 мл метанола при 0oC обрабатывают 165 мг (4,4 ммоль) боргидрида натрия. Удаляют охлаждающую баню, и образовавшуюся смесь перемешивают 30 минут при комнатной температуре. В реакционную смесь добавляют
вторые порции (1,12 мл (11,1 ммоль)) бензальдегида и (165 мг (4,4 ммоль)) боргидрида натрия, и перемешивание продолжают 1,5 ч. Реакционную смесь распределяют между 100 мл эфира и 50 мл воды, и слои разделяют. Водный слой отделяют и фильтруют, чтобы удалить небольшие количества нерастворимого материала. Фильтрат подкисляют до pH 5 двухнормальным раствором соляной кислоты, и выпавшее в осадок твердое вещество фильтруют, хорошо промывают водой, затем эфиром и сушат, получая 1,95 г указанного в заголовке соединения.
Спектр ПМР (400 МГц, D2O+NaOD): δ 3,33 (АВ кв., 2H, J=8,4), 3,85 (с, 1H), 6,79-7,16 (м, 4H).
Стадия Б.
3-(S)-(4-Фторфенил)-4-бензил-2-морфолинон
Смесь 1,95 г (7,5 ммоль) N-бензил (S)-(4-фторфенил)глицина, 3,9 мл (22,5 ммоль) N, N-диизопропилэтиламина, 6,5 мл (75 ммоль) 1,2-дибромэтана и 40 мл диметилформамида перемешивают при 100oC 20 часов (все твердые вещества растворяются при нагревании). Реакционную смесь охлаждают и концентрируют в вакууме. Остаток распределяют между 250 мл эфира и 100 мл 0,5 н. раствора бисульфата калия, и слои разделяют. Органический слой промывают 100 мл насыщенного водного раствора бикарбоната натрия, водой (3 раза по 150 мл), сушат над сульфатом магния и концентрируют в вакууме. Флеш-хроматография на 125 мг силикагеля с использованием в качестве элюента смеси 3:1 (по объему) гексанов и эфира дает 1,58 г (74%) указанного в заголовке соединения в виде масла.
Смесь 1,95 г (7,5 ммоль) N-бензил (S)-(4-фторфенил)глицина, 3,9 мл (22,5 ммоль) N, N-диизопропилэтиламина, 6,5 мл (75 ммоль) 1,2-дибромэтана и 40 мл диметилформамида перемешивают при 100oC 20 часов (все твердые вещества растворяются при нагревании). Реакционную смесь охлаждают и концентрируют в вакууме. Остаток распределяют между 250 мл эфира и 100 мл 0,5 н. раствора бисульфата калия, и слои разделяют. Органический слой промывают 100 мл насыщенного водного раствора бикарбоната натрия, водой (3 раза по 150 мл), сушат над сульфатом магния и концентрируют в вакууме. Флеш-хроматография на 125 мг силикагеля с использованием в качестве элюента смеси 3:1 (по объему) гексанов и эфира дает 1,58 г (74%) указанного в заголовке соединения в виде масла.
Спектр ПМР (400 МГц, CDCl3): δ 2,65 (дт, 1H, J=3,2, 12,8), 3,00 (дт, 1H, J=12,8, 2,8), 3,16 (д, 1H, J=13,6), 3,76 (д, 1H, J=13,6), 4,24 (с, 1H), 4,37 (дт, 1H, J=13,2, 3,2), 4,54 (дт, 1H, J=2,8, 13,2), 7,07-7,56 (м, 9H).
Пример 60.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-4-(фторфенил)- 4-бензилморфолин
Указанное в заголовке соединение было получено с выходом 72% из 3-(S)-(4-фторфенил)-4-бензил-2-морфолинона (из примера 59), используя методики, аналогичные методикам примера 15, стадии А и Б.
Указанное в заголовке соединение было получено с выходом 72% из 3-(S)-(4-фторфенил)-4-бензил-2-морфолинона (из примера 59), используя методики, аналогичные методикам примера 15, стадии А и Б.
Спектр ПМР (200 МГц, CDCl3): δ 2,37 (дт, 1H, J=3,6, 11,8), 2,83-2,90 (м, 2H), 3,55-3,63 (м, 2H), 3,85 (д, 1H, J=13,4), 4,14 (дт, 1H, J=2,0, 11,8), 4,44 (д, 1H, J=13,6), 4,66 (д, 1H, J=2,8), 4,79 (д, 1H, J=13,4), 7,00-7,70 (12H).
Пример 61.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-4-(фторфенил)- 4-морфолин
Указанное в заголовке соединение было получено с выходом 70% из 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-4-(фторфенил)-4-бензилморфолина (из примера 60), используя методику, аналогичную методике примера 15, стадия В.
Указанное в заголовке соединение было получено с выходом 70% из 2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-4-(фторфенил)-4-бензилморфолина (из примера 60), используя методику, аналогичную методике примера 15, стадия В.
Спектр МС-ББА: m/z 424 (M+H, 40%)
Спектр ПМР (400 МГц, CDCl3): δ 1,80 (шир.с., 1H), 3,11 (≈дд, 1H, J=2,2, 12,4), 3,25 (дт, 1H, J=3,6, 12,4), 3,65 (≈дд, 1H, J=3,6, 11,4), 4,05 (дт, 1H, J=2,2, 11,8), 4,11 (д, 1H, J=2,2), 4,53 (д, 1H, J=13,6), 4,71 (д, 1H, J= 2,2), 4,83 (д, 1H, J=13,6), 7,04 (т, 2H, J=7,2), 7,3-7,37 (м, 2H), 7,42 (с, 2H), 7,72 (с, 1H).
Спектр ПМР (400 МГц, CDCl3): δ 1,80 (шир.с., 1H), 3,11 (≈дд, 1H, J=2,2, 12,4), 3,25 (дт, 1H, J=3,6, 12,4), 3,65 (≈дд, 1H, J=3,6, 11,4), 4,05 (дт, 1H, J=2,2, 11,8), 4,11 (д, 1H, J=2,2), 4,53 (д, 1H, J=13,6), 4,71 (д, 1H, J= 2,2), 4,83 (д, 1H, J=13,6), 7,04 (т, 2H, J=7,2), 7,3-7,37 (м, 2H), 7,42 (с, 2H), 7,72 (с, 1H).
Пример 62.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-3-(S)-4-(фторфенил)- 4-(3-(5-оксо-1H, 4H-1,2,4-триазоло)метилморфолин
Указанное в заголовке соединение было получено с выходом 69% из 2-(S)-(3,5-бис-(трифторфенил)бензилокси)-3-(S)-4-(фторфенил)- 4-морфолина (из примера 61), используя методику, аналогичную методике примера 18.
Указанное в заголовке соединение было получено с выходом 69% из 2-(S)-(3,5-бис-(трифторфенил)бензилокси)-3-(S)-4-(фторфенил)- 4-морфолина (из примера 61), используя методику, аналогичную методике примера 18.
Спектр МС-ББА: m/z 521 (M+H, 100%)
Спектр ПМР (400 МГц, CDCl3): δ 2,55 (дт, 1H, J=3,6, 12,0), 2,91 (д, 1H, J= 11,6), 2,93 (д, 1H, J=14,4), 3,57 (д, 1H, J=2,8), 3,59 (д, 1H, J=14,4), 3,67-3,70 (м, 1H), 4,18 (дт, 1H, J=2,4, 11,6), 4,48 (д, 1H, J=13,6), 4,65 (д, 1H, J= 2,8), 4,84 (д, 1H, J=13,6), 7,07 (т, 2H, J=8,4), 7,40 (с, 2H), 7,45-7,48 (м, 2H), 7,68 (с, 1H), 10,04 (шир.с, 1H), 10,69 (шир.с., 1H).
Спектр ПМР (400 МГц, CDCl3): δ 2,55 (дт, 1H, J=3,6, 12,0), 2,91 (д, 1H, J= 11,6), 2,93 (д, 1H, J=14,4), 3,57 (д, 1H, J=2,8), 3,59 (д, 1H, J=14,4), 3,67-3,70 (м, 1H), 4,18 (дт, 1H, J=2,4, 11,6), 4,48 (д, 1H, J=13,6), 4,65 (д, 1H, J= 2,8), 4,84 (д, 1H, J=13,6), 7,07 (т, 2H, J=8,4), 7,40 (с, 2H), 7,45-7,48 (м, 2H), 7,68 (с, 1H), 10,04 (шир.с, 1H), 10,69 (шир.с., 1H).
Анализ:
Вычислено для C22H19F7N4O3: C 50,78, H 3,68, N 10,77, F 25,55.
Вычислено для C22H19F7N4O3: C 50,78, H 3,68, N 10,77, F 25,55.
Найдено: C 50,89, H 3,76, N 10,62, F 25,56.
Пример 63.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-((3-пиридил) метилкарбонил)-3-(R)-фенилморфолин
Раствор 55 мг (0,315 ммоль) 4-пиридилуксусной кислоты в 1 мл хлористого метилена, содержащего 79 мкл (0,175 ммоль) N-метилморфолина, 53 мг (0,37 ммоль) гидрата 1-гидроксибензотриазола и 73 мг (0,37 ммоль) гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида, перемешивают 10 минут. Добавляют раствор 2-(S)-(3,5-Бис-(трифторфенил)бензилокси)-3-(R)-фенилморфолина (из примера 33) в 1 мл хлористого метилена. После перемешивания смеси в течение 2 часов, ее распределяют между водой и хлористым метиленом. Органический слой промывают водой, рассолом и сушат посредством фильтрации через сульфат натрия. Фильтрат концентрируют, и остаток очищают путем флеш-хроматографии, используя смесь 70% этилацетат/гексан, чтобы получить 152 мг продукта (выход 100%).
Раствор 55 мг (0,315 ммоль) 4-пиридилуксусной кислоты в 1 мл хлористого метилена, содержащего 79 мкл (0,175 ммоль) N-метилморфолина, 53 мг (0,37 ммоль) гидрата 1-гидроксибензотриазола и 73 мг (0,37 ммоль) гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида, перемешивают 10 минут. Добавляют раствор 2-(S)-(3,5-Бис-(трифторфенил)бензилокси)-3-(R)-фенилморфолина (из примера 33) в 1 мл хлористого метилена. После перемешивания смеси в течение 2 часов, ее распределяют между водой и хлористым метиленом. Органический слой промывают водой, рассолом и сушат посредством фильтрации через сульфат натрия. Фильтрат концентрируют, и остаток очищают путем флеш-хроматографии, используя смесь 70% этилацетат/гексан, чтобы получить 152 мг продукта (выход 100%).
Спектр ПМР (400 МГц, CDCl3): δ 3,0-3,85 (м, 5H), 3,95 и 4,4 (шир.с, 1H), 4,66 (д, J=13 Гц, 1H), 4,82 (д, J=13 Гц, 1H), 5,0 и 5,9 (шир.с., 1H), 5,23 (с, 1H), 7,1-7,65 (м, 7H), 7,8 (м, 3H), 8,43 (шир.с., 2H).
Пример 64.
2-(S)-(3,5-Бис-(трифторметил)бензилокси)-4-(метокарбонилпентил)-3- (R)-фенилморфолин
К раствору 259 мг (0,64 ммоль) 2-(S)-3,5-бис-(трифторметил)бензилокси)-3-(R)-фенилморфолина (из примера 33) в 2 мл диметилформамида добавляют 160 мг (0,77 ммоль) метилового эфира 6-бромгексановой кислоты, 155 мг (1,12 ммоль) карбоната калия и 2 кристалла иодистого тетра-н-бутиламмония. Образовавшийся раствор нагревают 36 часов в бане при 60oC, в этот период по данным ТСХ реакция не завершилась. Температуру бани повышают до 100oC. Спустя 3 ч реакционную смесь охлаждают и разбавляют этилацетатом. Этилацетатный раствор 2 раза промывают водой, рассолом и сушат над сульфатом натрия. Фильтрат концентрируют, и остаток очищают путем флеш-хроматографии, используя смесь 30% этилацетат/гексан, чтобы выделить 220 мг продукта (выход 65%).
К раствору 259 мг (0,64 ммоль) 2-(S)-3,5-бис-(трифторметил)бензилокси)-3-(R)-фенилморфолина (из примера 33) в 2 мл диметилформамида добавляют 160 мг (0,77 ммоль) метилового эфира 6-бромгексановой кислоты, 155 мг (1,12 ммоль) карбоната калия и 2 кристалла иодистого тетра-н-бутиламмония. Образовавшийся раствор нагревают 36 часов в бане при 60oC, в этот период по данным ТСХ реакция не завершилась. Температуру бани повышают до 100oC. Спустя 3 ч реакционную смесь охлаждают и разбавляют этилацетатом. Этилацетатный раствор 2 раза промывают водой, рассолом и сушат над сульфатом натрия. Фильтрат концентрируют, и остаток очищают путем флеш-хроматографии, используя смесь 30% этилацетат/гексан, чтобы выделить 220 мг продукта (выход 65%).
Спектр ПМР (400 МГц, CDCl3): δ 1,0-1,4 (м, 4H), 1,47 (м, J=8 Гц, 2H), 1,95 (м, 1H), 2,2 (т, J=8 Гц, 2H), 2,35 (м, 2H), 2,9 (д, J=13 Гц, 1H), 3,07 (д, J=7 Гц, 1H), 3,62 (с, 3H), 3,81 (тд, J=8 Гц и 2 Гц, 1H), 4,04 (дд, J=10 Гц и 2 Гц, 1H), 4,36 (д, J=7 Гц, 1H), 4,4 (д, J= 13 Гц, 1H), 4,79 (д, J=13,0 Гц, 1H), 7,2-7,4 (м, 7H), 7,66 (с, 1H).
Пример 65.
2-(S)-(3,5-Бис(трифторметил)бензилокси)-4-(карбоксипентил)-3(R)- фенилморфолин
Раствор 0,15 г (0,28 ммоль) 2-(S)-(3,5-бис(трифторметил)-бензилокси)-4-(метоксикарбонилпентил)- 3-(R)-фенилморфолина (из примера 64) в 3 мл метанола омыляют путем обработки 0,5 мл 5-нормального раствора гидроксида натрия в течение 40 минут при 65oC. Раствор охлаждают, концентрируют и остаток разбавляют водой. Водный раствор доводят до значения pH 6 добавлением 2-нормальной соляной кислоты и экстрагируют этилацетатом. Органический слой промывают рассолом, сушат и концентрируют. Остаток флеш-хроматографии на колонке, элюируемой 50% смеси этилацетат/гексан, обеспечивает 0,13 г (89%) продукта.
Раствор 0,15 г (0,28 ммоль) 2-(S)-(3,5-бис(трифторметил)-бензилокси)-4-(метоксикарбонилпентил)- 3-(R)-фенилморфолина (из примера 64) в 3 мл метанола омыляют путем обработки 0,5 мл 5-нормального раствора гидроксида натрия в течение 40 минут при 65oC. Раствор охлаждают, концентрируют и остаток разбавляют водой. Водный раствор доводят до значения pH 6 добавлением 2-нормальной соляной кислоты и экстрагируют этилацетатом. Органический слой промывают рассолом, сушат и концентрируют. Остаток флеш-хроматографии на колонке, элюируемой 50% смеси этилацетат/гексан, обеспечивает 0,13 г (89%) продукта.
Спектр ПМР (400 МГц, CDCl3): δ 1,0-1,5 (м, 4H), 1,5 (м, 2H), 2,2 (м, 2H), 2,35 (м, 2H), 2,9 (д, J=13 Гц, 1H), 3,08 (д, J=7 Гц, 1H), 3,82 (т, J=8 Гц, 1H), 4,09 (д, J=7 Гц, 1H), 4,38 (с, 1H), 4,4 (д, J=13 Гц, 1H), 4,79 (д, J=13 Гц, 1H), 7,2-7,4 (м, 7H), 7,66 (с, 1H).
Пример 66.
2-(S)-(3,5-Бис(трифторметил)бензилокси)-4-(метиламино-карбонилпентил)- 6-оксо-гексил)-3-(R)-фенилморфолин
Раствор 116 мг (0,22 ммоль) 2-(S)-(3,5-бис(трифторметил)-бензилокси)-4-(карбоксипентил)-3-(R)- фенилморфолина (из примера 65) в 1 мл хлористого метилена обрабатывают 40 мг (0,29 ммоль) гидрата 1-гидроксибензотриазола, 57 мг (0,29 ммоль) гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида и 0,037 мл N-метилморфолина. Спустя 10 минут добавляют 0,027 мл (0,3 ммоль) водного 40% метиламина, и образовавшуюся смесь перемешивают 4 часа. Реакционную смесь разбавляют водой и экстрагируют хлористым метиленом. Объединенные хлористометиленовые слои промывают водой, рассолом и сушат над сульфатом натрия, и фильтрат концентрируют. Очистка остатка на флеш-хроматографической колонке с этилацетатом обеспечивает 0,10 г продукта.
Раствор 116 мг (0,22 ммоль) 2-(S)-(3,5-бис(трифторметил)-бензилокси)-4-(карбоксипентил)-3-(R)- фенилморфолина (из примера 65) в 1 мл хлористого метилена обрабатывают 40 мг (0,29 ммоль) гидрата 1-гидроксибензотриазола, 57 мг (0,29 ммоль) гидрохлорида 1-этил-3-(3-диметиламинопропил)карбодиимида и 0,037 мл N-метилморфолина. Спустя 10 минут добавляют 0,027 мл (0,3 ммоль) водного 40% метиламина, и образовавшуюся смесь перемешивают 4 часа. Реакционную смесь разбавляют водой и экстрагируют хлористым метиленом. Объединенные хлористометиленовые слои промывают водой, рассолом и сушат над сульфатом натрия, и фильтрат концентрируют. Очистка остатка на флеш-хроматографической колонке с этилацетатом обеспечивает 0,10 г продукта.
Спектр ПМР (400 МГц, CDCl3): δ 1,0-1,4 (м, 4H), 1,47 (м, 2H), 1,95 (м, 1H), 2,04 (т, J=8 Гц, 2H), 2,35 (м, 2H), 2,74 (д, J=5 Гц, 3H), 2,89 (д, J=12 Гц, 1H), 3,08 (д, J=7 Гц, 1H), 3,81 (т, J=7 Гц, 1H), 4,02 (д, J=11 Гц, 1H), 4,36 (д, J= 7 Гц, 1H), 4,39 (д, J=13 Гц, 1H), 4,79 (д, J=13 Гц, 1H), 5,03 (шир.с., 1H), 7,2-7,4 (м, 7H), 7,65 (с, 1H).
Пример 67.
Типичные фармацевтические композиции, содержащие вещество изобретения
А. Капсулы сухого наполнения, содержащего 50 мг активного компонента в капсуле
Компонент - Количество в капсуле, мг
Активный компонент - 50
Лактоза - 149
Стеарат магния - 1
Капсула (размер N 1) - 200
Активный компонент может быть измельчен до порошка N 60, при этом лактоза и стеарат магния могут быть пропущены через промокательную ткань N 60 на порошок. Затем объединенные компоненты могут быть перемешаны примерно в течение 10 минут и заполнены в сухую желатиновую капсулу N 1.
А. Капсулы сухого наполнения, содержащего 50 мг активного компонента в капсуле
Компонент - Количество в капсуле, мг
Активный компонент - 50
Лактоза - 149
Стеарат магния - 1
Капсула (размер N 1) - 200
Активный компонент может быть измельчен до порошка N 60, при этом лактоза и стеарат магния могут быть пропущены через промокательную ткань N 60 на порошок. Затем объединенные компоненты могут быть перемешаны примерно в течение 10 минут и заполнены в сухую желатиновую капсулу N 1.
Б. Таблетки
Типичная таблетка может содержать активный компонент (25 мг), предварительно желатинированный крахмал (82 мг, фармакопея США), микрокристаллическую целлюлозу (82 мг) и стеарат магния (1 мг).
Типичная таблетка может содержать активный компонент (25 мг), предварительно желатинированный крахмал (82 мг, фармакопея США), микрокристаллическую целлюлозу (82 мг) и стеарат магния (1 мг).
В. Свечи
Типичные свечные рецептуры для ректального назначения содержат активный компонент (0,08-1,0 мг), динатрий-кальций эдетат (0,25-0,5 мг) и полиэтиленгликоль (775-1600 мг). Другие свечные рецептуры могут быть произведены путем замены, например, динатрий-кальций эдетата на бутилированный гидрокситолуол (0,04-0,08 мг) и полиэтиленгликоля на гидрированное растительное масло (675-1400 мг), такое как Саппокайр Эл, Векобии Эф-Эс, Векобии Эм, Вайтпсолз и т.п.
Типичные свечные рецептуры для ректального назначения содержат активный компонент (0,08-1,0 мг), динатрий-кальций эдетат (0,25-0,5 мг) и полиэтиленгликоль (775-1600 мг). Другие свечные рецептуры могут быть произведены путем замены, например, динатрий-кальций эдетата на бутилированный гидрокситолуол (0,04-0,08 мг) и полиэтиленгликоля на гидрированное растительное масло (675-1400 мг), такое как Саппокайр Эл, Векобии Эф-Эс, Векобии Эм, Вайтпсолз и т.п.
Г. Инъекции
Типичная рецептура для инъекции содержит безводный двухосновной натрийфосфат активного компонента (11,4 мг), бензиловый спирт (0,01 мл) и воду для инъекции (1,0 мл).
Типичная рецептура для инъекции содержит безводный двухосновной натрийфосфат активного компонента (11,4 мг), бензиловый спирт (0,01 мл) и воду для инъекции (1,0 мл).
Хотя предшествующее описание раскрывает принципы настоящего изобретения с помощью примеров, предоставленных в целях иллюстрации, можно понять, что практика изобретения охватывает все случайные вариации, приспособления, модификации, исключения или добавления процедур и протоколов, описанных здесь, так как они входят в объем следующих притязаний и их эквивалентов.
Claims (8)
1. Замещенные гетероциклы общей структурной формулы
или их фармацевтически приемлемая соль, в которой R1 выбирают из группы, состоящей из: 1) атома водорода; 2) С1 - С6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из а) фенила, б) группы -NR9R10, в) группы -CO2R9, г) группы -CONR9R10, д) гетероцикла, который выбирают из группы, состоящей из: А) триазолила, В) имидазолила, С) пиперидинила, Д) пиридила, и в которой указанный гетероцикл является незамещенным или замещенным оксо-группой или С1 - С6-алкилом, замещенным фенилом; 3) С2 - С6-алкенила;
R2 и R3 выбирают независимо из атома водорода или С1 - С6-алкила;
Х представляет -0-;
R4 представляет группу
где Y выбирают из -O-, -CH2-, -CHR15, Z - атом водорода, или если Y представляет собой -CHR15, то Z и R15, объединенные вместе, образуют двойную связь;
R5 представляет собой фенил, возможно замещенный атомами галогена;
R6, R7 и R8 независимо выбирают из группы, состоящей из водорода, С1 - С6-алкила, атома галогена или трифторметила;
R9 и R10 независимо выбирают из атома водорода или С1 - С6-алкила.
или их фармацевтически приемлемая соль, в которой R1 выбирают из группы, состоящей из: 1) атома водорода; 2) С1 - С6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из а) фенила, б) группы -NR9R10, в) группы -CO2R9, г) группы -CONR9R10, д) гетероцикла, который выбирают из группы, состоящей из: А) триазолила, В) имидазолила, С) пиперидинила, Д) пиридила, и в которой указанный гетероцикл является незамещенным или замещенным оксо-группой или С1 - С6-алкилом, замещенным фенилом; 3) С2 - С6-алкенила;
R2 и R3 выбирают независимо из атома водорода или С1 - С6-алкила;
Х представляет -0-;
R4 представляет группу
где Y выбирают из -O-, -CH2-, -CHR15, Z - атом водорода, или если Y представляет собой -CHR15, то Z и R15, объединенные вместе, образуют двойную связь;
R5 представляет собой фенил, возможно замещенный атомами галогена;
R6, R7 и R8 независимо выбирают из группы, состоящей из водорода, С1 - С6-алкила, атома галогена или трифторметила;
R9 и R10 независимо выбирают из атома водорода или С1 - С6-алкила.
2. Соединение по п.1, в котором R1 выбирают из группы, состоящей из: 1) атома водорода, 2) С1 - С6-алкила, незамещенного или замещенного одним или несколькими заместителями, выбранными из: а) гетероцикла, в котором гетероцикл выбран из группы, состоящей из: имидазолила, пиридила, триазолила и пиперидинила, и в котором гетероцикл является незамещенным или замещенным оксо-группой или С1 - С6-алкилом, замещенным фенилом; R2 и R3 независимо выбирают из атома водорода или С1 - С6-алкила, Х представляет собой -О-, R4 представляет собой группу:
R5 является фенилом, незамещенным или замещенным галогеном; R6, R7 и R8 независимо выбирают из группы, состоящей из: атома водорода, С1 - С6-алкила, атома галогена и трифторметила; Y представляет собой -О-; и Z - атом водорода.
R5 является фенилом, незамещенным или замещенным галогеном; R6, R7 и R8 независимо выбирают из группы, состоящей из: атома водорода, С1 - С6-алкила, атома галогена и трифторметила; Y представляет собой -О-; и Z - атом водорода.
7. Соединение по п.1, которое выбирают из группы, состоящей из: 1) 2-(3,5-бис(трифторметил)бензилокси)-3-фенилморфолина; 2) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3R)-фенил-(6R)-метилморфолина; 3) (2R, S)-(3,5-бис(трифторметил)бензилокси)-(3S)-фенил-(6R)-метилморфолина; 5) (+/-)-2-(3,5-бис(трифторметил)бензилокси)-3-фенил-4-метоксикарбонилметилморфолина; 7) 3-фенил-2-(2-(3,5-бис(трифторметил)фенил)этил)-морфолина; 8) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(S)-метилморфолина; 9) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)-метилморфолина; 10) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(S)-метилморфолина; 11) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(S)-метилморфолина; 12) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)-метилморфолина; 13) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-метилморфолина; 14) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(R)-метилморфолина; 15) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(R)-метилморфолина; 16) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолина;
17) 4-(3-(1,2,4-триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина; 18) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина; 19) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)-метилморфолина; 20) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)-метилморфолина; 21) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 22) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 23) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолина; 24) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолина; 25) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-метилморфолина; 30) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-3-(S)-фенил-4-(3(1,2,4-триазоло)метил)-морфолина; 31) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-3-(S)-фенилморфолина; 32) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина;
33) 4-(3-(1,2,4-триазоло)метил)2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 34) 4(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 35) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 36) 4-(4-имидазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 37) 4-(аминокарбонилметил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 38) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолина; 39) 4-(4-имидазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолина; 40) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 41) 4-(4-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 44) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 45) 4(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)2-(3,5-диметил)бензилокси)-3-фенилморфолина; 46) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 47) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 48)
4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 49) 4-(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 50) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трифторметил)-5-метилбензилокси)-3-фенилморфолина; 51) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(3-(трифторметил)-5-метилбензилокси)-3-фенилморфолина; 52) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 53) 4-(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 54) 4-(2-(имидазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 55) 4-(4-(имидазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 56) 4-(2-(имидазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 57) 4-(4-(имидазоло)метил)-2-(S)-(3,5-ди(трет-бутил)-бензилокси)-3-фенилморфолина; 58) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 59) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 62)
4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси-3-фенилморфолина; 62а) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 63) 2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолина; 64) 2-(S)-(3,5-дихлорбензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-3-(S)-фенилморфолина; 65) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(метоксикарбонилметил)-3-(S)-фенилморфолина; 66) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(карбоксиметил)-3-(S)-фенилморфолина; 70) 2-(R)-(3,5-бис(трифторметил)бензилокси)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 71) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина; 72) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4-(3-(1,2,4-триазоло)метил)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 73) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 74) 2-(S)-(3.5-бис(трифторметил)бензилокси)-4-(3-(1,2,4-триазоло)метил)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина;
75) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина; 76) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(2-(1-(4-бензил)пиперидино)этил)-3-(S)-фенилморфолина; 78) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)-4-бензилморфолина; 79) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)морфолина; 80) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)-4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)морфолина; 82) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(метоксикарбонилпентил)-3-(R)-фенилморфолина; 83) 2-(S)-(3,5бис(трифторметил)бензилокси)-4-(карбоксипентил)-3-(R)-фенилморфолина; или его фармацевтически приемлемая соль.
17) 4-(3-(1,2,4-триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина; 18) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(S)-(3,5-бис-(трифторметил)бензилокси)-3-(S)-фенилморфолина; 19) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)-метилморфолина; 20) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-6-(R)-метилморфолина; 21) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 22) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 23) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолина; 24) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-5-(S)-метилморфолина; 25) 2-(R)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенил-5-(S)-метилморфолина; 30) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-3-(S)-фенил-4-(3(1,2,4-триазоло)метил)-морфолина; 31) 2-(S)-(3,5-бис(трифторметил)бензилокси)-6-(R)-метил-4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-3-(S)-фенилморфолина; 32) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина;
33) 4-(3-(1,2,4-триазоло)метил)2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 34) 4(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 35) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 36) 4-(4-имидазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 37) 4-(аминокарбонилметил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(R)-фенилморфолина; 38) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолина; 39) 4-(4-имидазоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенилморфолина; 40) 4-(2-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 41) 4-(4-(имидизоло)метил)-2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-фенил-6-(R)-метилморфолина; 44) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 45) 4(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)2-(3,5-диметил)бензилокси)-3-фенилморфолина; 46) 4-(3-(1,2,4-триазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 47) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 48)
4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 49) 4-(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 50) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трифторметил)-5-метилбензилокси)-3-фенилморфолина; 51) 4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)-2-(3-(трифторметил)-5-метилбензилокси)-3-фенилморфолина; 52) 4-(3-(1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 53) 4-(3-(5-оксо-1Н,4Н-1,2,4-триазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 54) 4-(2-(имидазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 55) 4-(4-(имидазоло)метил)-2-(3,5-диметил)бензилокси)-3-фенилморфолина; 56) 4-(2-(имидазоло)метил)-2-(3,5-ди(трет-бутил)бензилокси)-3-фенилморфолина; 57) 4-(4-(имидазоло)метил)-2-(S)-(3,5-ди(трет-бутил)-бензилокси)-3-фенилморфолина; 58) 4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 59) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5-метилбензилокси)-3-фенилморфолина; 62)
4-(2-(имидазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси-3-фенилморфолина; 62а) 4-(4-(имидазоло)метил)-2-(3-(трет-бутил)-5-(трифторметил)бензилокси)-3-фенилморфолина; 63) 2-(S)-(3,5-дихлорбензилокси)-3-(S)-фенилморфолина; 64) 2-(S)-(3,5-дихлорбензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-3-(S)-фенилморфолина; 65) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(метоксикарбонилметил)-3-(S)-фенилморфолина; 66) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(карбоксиметил)-3-(S)-фенилморфолина; 70) 2-(R)-(3,5-бис(трифторметил)бензилокси)-[5-(S),6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 71) 2-(S)-(3,5-бис(трифторметил)бензилокси)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина; 72) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4-(3-(1,2,4-триазоло)метил)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 73) 2-(R)-(3,5-бис(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-[5-(S), 6-(R) или 5-(R),6-(S)-диметил]-3-(S)-фенилморфолина; 74) 2-(S)-(3.5-бис(трифторметил)бензилокси)-4-(3-(1,2,4-триазоло)метил)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина;
75) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(3-(5-оксо-1,2,4-триазоло)метил)-[5-(R), 6-(S) или 5-(S),6-(R)-диметил]-3-(S)-фенилморфолина; 76) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(2-(1-(4-бензил)пиперидино)этил)-3-(S)-фенилморфолина; 78) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)-4-бензилморфолина; 79) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)морфолина; 80) 2-(S)-(3,5-бис(трифторметил)бензилокси)-3-(S)-(4-фторфенил)-4-(3-(5-оксо-1Н, 4Н-1,2,4-триазоло)метил)морфолина; 82) 2-(S)-(3,5-бис(трифторметил)бензилокси)-4-(метоксикарбонилпентил)-3-(R)-фенилморфолина; 83) 2-(S)-(3,5бис(трифторметил)бензилокси)-4-(карбоксипентил)-3-(R)-фенилморфолина; или его фармацевтически приемлемая соль.
8. Фармацевтическая композиция для блокады рецепторов нейрокинина-1 у млекопитающих, включающая фармацевтически приемлемый носитель и эффективное количество соединения по п.1.
9. Способ для блокады рецепторов нейрокинина-1 у млекопитающих, отличающийся тем, что назначают соединение по п.1 в эффективном количестве.
Приоритет по признакам:
29.06.92 по признакам п.1, кроме R1 - тетероцикл, по п.7 в отношении соединений 1 - 15 и по признакам пп.8 и 9;
04.11.92 по признакам п.1 касается каждого гетероцикла в R1, по признакам пп.2 - 6 и п.7 в отношении соединений 16 - 62;
19.05.93 по признаку п.7 в отношении соединений 63 - 84.
29.06.92 по признакам п.1, кроме R1 - тетероцикл, по п.7 в отношении соединений 1 - 15 и по признакам пп.8 и 9;
04.11.92 по признакам п.1 касается каждого гетероцикла в R1, по признакам пп.2 - 6 и п.7 в отношении соединений 16 - 62;
19.05.93 по признаку п.7 в отношении соединений 63 - 84.
Applications Claiming Priority (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US90597692A | 1992-06-29 | 1992-06-29 | |
| US905,976 | 1992-06-29 | ||
| US97144892A | 1992-11-04 | 1992-11-04 | |
| US971,448 | 1992-11-04 | ||
| US6191493A | 1993-05-19 | 1993-05-19 | |
| US905976 | 1993-05-19 | ||
| US971448 | 1993-05-19 | ||
| US061,914 | 1993-05-19 | ||
| US061914 | 1993-05-19 | ||
| PCT/US1993/006181 WO1994000440A1 (en) | 1992-06-29 | 1993-06-29 | Morpholine and thiomorpholine tachykinin receptor antagonists |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU94046364A RU94046364A (ru) | 1996-10-10 |
| RU2140914C1 true RU2140914C1 (ru) | 1999-11-10 |
Family
ID=27370159
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU94046364A RU2140914C1 (ru) | 1992-06-29 | 1993-06-29 | Замещенные гетероциклы или их фармацевтически приемлемая соль, фармацевтическая композиция для блокады рецепторов нейрокинина-1 у млекопитающих, способ для блокады рецепторов нейрокинина-1 у млекопитающих |
Country Status (33)
| Country | Link |
|---|---|
| EP (1) | EP0577394B1 (ru) |
| JP (1) | JP2634372B2 (ru) |
| KR (1) | KR100301212B1 (ru) |
| CN (1) | CN1049431C (ru) |
| AT (1) | ATE186532T1 (ru) |
| AU (1) | AU4656193A (ru) |
| BG (1) | BG62963B1 (ru) |
| BR (1) | BR1100375A (ru) |
| CA (1) | CA2099233A1 (ru) |
| CY (1) | CY2200B1 (ru) |
| CZ (1) | CZ288530B6 (ru) |
| DE (1) | DE69326977T2 (ru) |
| DK (1) | DK0577394T3 (ru) |
| DZ (1) | DZ1700A1 (ru) |
| ES (1) | ES2141133T3 (ru) |
| FI (1) | FI111363B (ru) |
| GR (1) | GR3031824T3 (ru) |
| HR (1) | HRP931003B1 (ru) |
| HU (1) | HU219713B (ru) |
| IL (1) | IL106142A (ru) |
| LV (1) | LV12568B (ru) |
| MX (1) | MX9303888A (ru) |
| MY (1) | MY108836A (ru) |
| NO (1) | NO305698B1 (ru) |
| NZ (1) | NZ254476A (ru) |
| RO (1) | RO114448B1 (ru) |
| RU (1) | RU2140914C1 (ru) |
| SI (1) | SI9300346B (ru) |
| SK (1) | SK281093B6 (ru) |
| TW (1) | TW358808B (ru) |
| WO (1) | WO1994000440A1 (ru) |
| YU (1) | YU49036B (ru) |
| ZA (1) | ZA934624B (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2304435C2 (ru) * | 2001-07-10 | 2007-08-20 | Ф.Хоффманн-Ля Рош Аг | Применение антагонистов рецептора nk-1 для лечения черепно-мозговой и спинномозговой травмы или повреждения нервной ткани |
| RU2307651C2 (ru) * | 2001-04-05 | 2007-10-10 | Тиога Фармасьютиклз, Инк. | Каппа-опиатные агонисты для лечения заболеваний мочевого пузыря |
Families Citing this family (116)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5719147A (en) * | 1992-06-29 | 1998-02-17 | Merck & Co., Inc. | Morpholine and thiomorpholine tachykinin receptor antagonists |
| US6048859A (en) | 1992-06-29 | 2000-04-11 | Merck & Co., Inc. | Morpholine and thiomorpholine tachykinin receptor antagonists |
| US5637699A (en) * | 1992-06-29 | 1997-06-10 | Merck & Co., Inc. | Process for preparing morpholine tachykinin receptor antagonists |
| IL111960A (en) * | 1993-12-17 | 1999-12-22 | Merck & Co Inc | Morpholines and thiomorpholines their preparation and pharmaceutical compositions containing them |
| ATE364606T1 (de) * | 1993-12-29 | 2007-07-15 | Merck Sharp & Dohme | Substituierte morpholinderivate und ihre verwendung als arzneimittel |
| US5610165A (en) * | 1994-02-17 | 1997-03-11 | Merck & Co., Inc. | N-acylpiperidine tachykinin antagonists |
| IL112778A0 (en) * | 1994-03-04 | 1995-05-26 | Merck & Co Inc | Substituted heterocycles, their preparation and pharmaceutical compositions containing them |
| JPH10500944A (ja) * | 1994-05-05 | 1998-01-27 | メルク シヤープ エンド ドーム リミテツド | モルホリン誘導体及びタキキニンのアンタゴニストとしてのそれらの使用 |
| PT777659E (pt) * | 1994-08-15 | 2001-09-28 | Merck Sharp & Dohme | Derivados de morfolina e sua utilizacao como agentes terapeuticos |
| GB9417956D0 (en) * | 1994-09-02 | 1994-10-26 | Merck Sharp & Dohme | Therapeutic agents |
| US5457107A (en) * | 1994-09-16 | 1995-10-10 | Merck & Co., Inc. | Polymorphic form of a tachykinin receptor antagonist |
| FR2728165A1 (fr) * | 1994-12-19 | 1996-06-21 | Oreal | Utilisation d'un antagoniste de substance p pour le traitement des rougeurs cutanees d'origine neurogene |
| GB9426103D0 (en) * | 1994-12-23 | 1995-02-22 | Merck Sharp & Dohme | Therapeutic agents |
| GB9426102D0 (en) * | 1994-12-23 | 1995-02-22 | Merck Sharp & Dohme | Pharmacuetical compositions |
| FR2729954B1 (fr) * | 1995-01-30 | 1997-08-01 | Sanofi Sa | Composes heterocycliques substitues, procede pour leur preparation et compositions pharmaceutiques les contenant |
| DE19504627A1 (de) * | 1995-02-13 | 1996-08-14 | Bayer Ag | Verfahren und neue Zwischenprodukte zur Herstellung von Triazolinonen |
| GB9505492D0 (en) * | 1995-03-18 | 1995-05-03 | Merck Sharp & Dohme | Therapeutic agents |
| GB9505491D0 (en) * | 1995-03-18 | 1995-05-03 | Merck Sharp & Dohme | Therapeutic agents |
| US5861510A (en) * | 1995-04-20 | 1999-01-19 | Pfizer Inc | Arylsulfonyl hydroxamic acid derivatives as MMP and TNF inhibitors |
| GB9511031D0 (en) * | 1995-06-01 | 1995-07-26 | Merck Sharp & Dohme | Chemical process |
| GB9513121D0 (en) * | 1995-06-28 | 1995-08-30 | Merck Sharp & Dohme | Therapeutic agents |
| GB9513117D0 (en) * | 1995-06-28 | 1995-08-30 | Merck Sharp & Dohme | Therapeutic agents |
| GB9513118D0 (en) * | 1995-06-28 | 1995-08-30 | Merck Sharp & Dohme | Therapeutic agents |
| GB9523244D0 (en) * | 1995-11-14 | 1996-01-17 | Merck Sharp & Dohme | Therapeutic agents |
| DE59605542D1 (de) * | 1996-01-19 | 2000-08-10 | Lonza Ag | Verfahren zur Herstellung von optisch aktivem 3-Chinuclidinol |
| GB9603137D0 (en) * | 1996-02-15 | 1996-04-17 | Merck Sharp & Dohme | Therapeutic agents |
| GB9603136D0 (en) * | 1996-02-15 | 1996-04-17 | Merck Sharp & Dohme | Therapeutic agents |
| US6423708B1 (en) | 1996-09-30 | 2002-07-23 | Pfizer Inc | Aralkyl and aralkylidene heterocyclic lactams and imides |
| UA56185C2 (ru) | 1996-09-30 | 2003-05-15 | Пфайзер Інк. | Аралкил- и аралкилиденгетероциклические лактамы и имиды, фармацевтическая композиция и способ лечения |
| US6117855A (en) | 1996-10-07 | 2000-09-12 | Merck Sharp & Dohme Ltd. | Use of a NK-1 receptor antagonist and an antidepressant and/or an anti-anxiety agent |
| ES2267153T3 (es) * | 1996-10-07 | 2007-03-01 | MERCK SHARP & DOHME LTD. | Antagonistas del receptor nk-1 penetrantes del snc como agentes antidepresivos y/o antiansiedad. |
| US5750549A (en) * | 1996-10-15 | 1998-05-12 | Merck & Co., Inc. | Cycloalkyl tachykinin receptor antagonists |
| EP0942735A1 (en) * | 1996-12-02 | 1999-09-22 | MERCK SHARP & DOHME LTD. | Use of nk-1 receptor antagonists for treating schizophrenic disorders |
| AU731672B2 (en) * | 1996-12-02 | 2001-04-05 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating bipolar disorders |
| PT942729E (pt) * | 1996-12-02 | 2004-12-31 | Merck Sharp & Dohme | Utilizacao de antagonistas de receptores nk-1 para tratamento de doencas do stresse |
| DE69733148T2 (de) * | 1996-12-02 | 2006-02-02 | Merck Sharp & Dohme Ltd., Hoddesdon | Die verwendung von nk-1 rezeptorantagonisten für die behandlung von kognitiven störungen |
| CA2273809A1 (en) * | 1996-12-02 | 1998-06-11 | Merck Sharp & Dohme Limited | Use of nk-1 receptor antagonists for treating movement disorders |
| WO1998024444A1 (en) * | 1996-12-02 | 1998-06-11 | Merck Sharp & Dohme Limited | Use of nk-1 receptor antagonists for treating substance use disorders |
| AU736042B2 (en) * | 1996-12-02 | 2001-07-26 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating major depressive disorders with anxiety |
| US6100256A (en) * | 1996-12-02 | 2000-08-08 | Merck Sharp & Dohme Ltd. | Use of NK-1 receptors antagonists for treating schizophrenic disorders |
| JP2001504851A (ja) * | 1996-12-02 | 2001-04-10 | メルク シヤープ エンド ドーム リミテツド | 性的機能不全の治療のためのnk−1受容体拮抗薬の使用 |
| JP2001504848A (ja) * | 1996-12-02 | 2001-04-10 | メルク シヤープ エンド ドーム リミテツド | 重症不安障害の治療のためのnk−1受容体拮抗薬の使用 |
| US6613765B1 (en) | 1996-12-02 | 2003-09-02 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating major depressive disorders |
| US5977104A (en) * | 1996-12-02 | 1999-11-02 | Merck Sharp & Dohme Ltd. | Use of NK-1 receptor antagonists for treating bipolar disorders |
| US6114315A (en) * | 1996-12-02 | 2000-09-05 | Merck Sharp & Dohme Ltd. | Use of NK-1 receptor antagonists for treating major depressive disorders with anxiety |
| WO1998024438A1 (en) * | 1996-12-02 | 1998-06-11 | Merck Sharp & Dohme Limited | Use of nk-1 receptor antagonists for treating major depressive disorders |
| RU2184538C2 (ru) * | 1997-01-09 | 2002-07-10 | Бифодан А/С | Применение дихлорбензилового спирта для получения лекарственного средства для местного лечения воспаления и лекарственное средство, содержащее дихлорбензиловый спирт |
| JP2001524960A (ja) * | 1997-04-24 | 2001-12-04 | メルク シヤープ エンド ドーム リミテツド | 摂食障害を治療するためのnk−1受容体拮抗薬の使用 |
| ZA985765B (en) | 1997-07-02 | 1999-08-04 | Merck & Co Inc | Polymorphic form of a tachykinin receptor antagonist. |
| GB9716463D0 (en) * | 1997-08-04 | 1997-10-08 | Merck Sharp & Dohme | Therapeutic agents |
| WO1999007376A1 (en) * | 1997-08-04 | 1999-02-18 | Merck Sharp & Dohme Limited | Use of nk-1 receptor antagonists for treating mania |
| AU737019B2 (en) * | 1997-08-04 | 2001-08-09 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating aggressive behaviour disorders |
| GB9716457D0 (en) * | 1997-08-04 | 1997-10-08 | Merck Sharp & Dohme | Therapeutic agents |
| US6156749A (en) * | 1997-12-01 | 2000-12-05 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating movement disorders |
| US6087348A (en) * | 1997-12-01 | 2000-07-11 | Merck Sharp & Dohme Ltd. | Use of NK-1 receptor antagonists for treating stress disorders |
| US6271230B1 (en) | 1997-12-01 | 2001-08-07 | Merck Sharp & Dohme Limited | Use of NK-1 receptor antagonists for treating cognitive disorders |
| GB9810920D0 (en) * | 1998-05-21 | 1998-07-22 | Merck Sharp & Dohme | Therapeutic use |
| GB9816897D0 (en) * | 1998-08-04 | 1998-09-30 | Merck Sharp & Dohme | Therapeutic use |
| GB9819888D0 (en) * | 1998-09-11 | 1998-11-04 | Merck Sharp & Dohme | Chemical synthesis |
| US6218390B1 (en) * | 1998-12-17 | 2001-04-17 | Synaptic Pharmaceutical Corporation | Morpholinone and morpholine derivatives and uses thereof |
| DE60013942T2 (de) * | 1999-03-30 | 2006-02-23 | Pfizer Products Inc., Groton | Verfahren zur Herstellung von cyclischen Thioamiden |
| RU2309953C2 (ru) | 1999-11-03 | 2007-11-10 | Эймр Текнолоджи, Инк. | Арил- и гетероарилзамещенные тетрагидроизохинолины, фармацевтическая композиция и способ лечения на их основе |
| US7163949B1 (en) | 1999-11-03 | 2007-01-16 | Amr Technology, Inc. | 4-phenyl substituted tetrahydroisoquinolines and use thereof |
| ATE253561T1 (de) * | 1999-11-29 | 2003-11-15 | Hoffmann La Roche | 2-(3,5-bis-trifluoromethyl-phenyl)-n-methyl-n-( - morpholin-4-yl-4-o-tolyl-pyridin-3-yl)- isobutyramid |
| WO2002004455A2 (en) | 2000-07-11 | 2002-01-17 | Albany Molecular Research, Inc | 4-phenyl substituted tetrahydroisoquinolines and therapeutic use thereof |
| GB0022988D0 (en) * | 2000-09-19 | 2000-11-01 | Merck Sharp & Dohme | Therapeutic agents |
| US6638981B2 (en) | 2001-08-17 | 2003-10-28 | Epicept Corporation | Topical compositions and methods for treating pain |
| MXPA05003830A (es) * | 2002-10-11 | 2005-06-23 | Cytokinetics Inc | Compuestos, composiciones y metodos. |
| KR20060124770A (ko) | 2004-03-17 | 2006-12-05 | 화이자 프로덕츠 인코포레이티드 | 벤질(이덴)-락탐 유도체 |
| US7541357B2 (en) | 2004-07-15 | 2009-06-02 | Amr Technology, Inc. | Aryl- and heteroaryl-substituted tetrahydroisoquinolines and use thereof to block reuptake of norepinephrine, dopamine, and serotonin |
| EP1888050B1 (en) | 2005-05-17 | 2012-03-21 | Merck Sharp & Dohme Ltd. | cis-4-[(4-chlorophenyl)sulfonyl]-4-(2,5-difluorophenyl)cyclohexanepropanoic acid for the treatment of cancer |
| JP5258561B2 (ja) | 2005-07-15 | 2013-08-07 | アルバニー モレキュラー リサーチ, インコーポレイテッド | アリール置換およびヘテロアリール置換テトラヒドロベンズアゼピンならびにノルエピネフリン、ドーパミンおよびセロトニンの再取り込みを遮断するためのその使用 |
| CN101277960A (zh) | 2005-09-29 | 2008-10-01 | 默克公司 | 作为黑皮质素-4受体调节剂的酰化螺哌啶衍生物 |
| GB0603041D0 (en) | 2006-02-15 | 2006-03-29 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| EP2698157B1 (en) | 2006-09-22 | 2015-05-20 | Merck Sharp & Dohme Corp. | Method of treatment using fatty acid synthesis inhibitors |
| US20110218176A1 (en) | 2006-11-01 | 2011-09-08 | Barbara Brooke Jennings-Spring | Compounds, methods, and treatments for abnormal signaling pathways for prenatal and postnatal development |
| EP2109608B1 (en) | 2007-01-10 | 2011-03-23 | Istituto di Richerche di Biologia Molecolare P. Angeletti S.p.A. | Amide substituted indazoles as poly(adp-ribose)polymerase (parp) inhibitors |
| JP2010516731A (ja) | 2007-01-24 | 2010-05-20 | グラクソ グループ リミテッド | 2−メトキシ−5−(5−トリフルオロメチル−テトラゾール−1−イル)−ベンジル]−(2s−フェニル−ピペリジン−3s−イル)−アミンを含む医薬組成物 |
| JP5319518B2 (ja) | 2007-04-02 | 2013-10-16 | Msd株式会社 | インドールジオン誘導体 |
| US20100197564A1 (en) * | 2007-04-19 | 2010-08-05 | Schering Corporation | Diaryl morpholines as cb1 modulators |
| US8389553B2 (en) | 2007-06-27 | 2013-03-05 | Merck Sharp & Dohme Corp. | 4-carboxybenzylamino derivatives as histone deacetylase inhibitors |
| WO2009104080A2 (en) | 2008-02-20 | 2009-08-27 | Targia Pharmaceuticals | Cns pharmaceutical compositions and methods of use |
| US8598184B2 (en) | 2008-03-03 | 2013-12-03 | Tiger Pharmatech | Protein kinase inhibitors |
| WO2009124756A1 (en) * | 2008-04-08 | 2009-10-15 | European Molecular Biology Laboratory (Embl) | Use of aprepitant and derivatives thereof for the treatment of cancer |
| AR071997A1 (es) | 2008-06-04 | 2010-07-28 | Bristol Myers Squibb Co | Forma cristalina de 6-((4s)-2-metil-4-(2-naftil)-1,2,3,4-tetrahidroisoquinolin-7-il)piridazin-3-amina |
| US9156812B2 (en) | 2008-06-04 | 2015-10-13 | Bristol-Myers Squibb Company | Crystalline form of 6-[(4S)-2-methyl-4-(2-naphthyl)-1,2,3,4-tetrahydroisoquinolin-7-yl]pyridazin-3-amine |
| WO2010114780A1 (en) | 2009-04-01 | 2010-10-07 | Merck Sharp & Dohme Corp. | Inhibitors of akt activity |
| EP2429293B1 (en) | 2009-05-12 | 2014-10-29 | Bristol-Myers Squibb Company | CRYSTALLINE FORMS OF (S)-7-([1,2,4]TRIAZOLO[1,5-a]PYRIDIN-6-YL)-4-(3,4-DICHLOROHPHENYL)-1,2,3,4-TETRAHYDROISOQUINOLINE AND USE THEREOF |
| DK2429296T3 (en) | 2009-05-12 | 2018-03-12 | Albany Molecular Res Inc | 7 - ([1,2,4,] TRIAZOLO [1,5, -A] PYRIDIN-6-YL) -4- (3,4-DICHLORPHENYL) -1,2,3,4- TETRAHYDROISOQUINOLINE AND USE thereof |
| KR20120034644A (ko) | 2009-05-12 | 2012-04-12 | 알바니 몰레큘라 리써치, 인크. | 아릴, 헤테로아릴, 및 헤테로사이클 치환된 테트라하이드로이소퀴놀린 및 이의 용도 |
| BR112012008849A2 (pt) | 2009-10-14 | 2015-09-22 | Schering Corp | composto, composição farmacêutica, e, uso de um composto |
| WO2011163330A1 (en) | 2010-06-24 | 2011-12-29 | Merck Sharp & Dohme Corp. | Novel heterocyclic compounds as erk inhibitors |
| EP2601293B1 (en) | 2010-08-02 | 2017-12-06 | Sirna Therapeutics, Inc. | RNA INTERFERENCE MEDIATED INHIBITION OF CATENIN (CADHERIN-ASSOCIATED PROTEIN), BETA 1 (CTNNB1) GENE EXPRESSION USING SHORT INTERFERING NUCLEIC ACID (siNA) |
| JP2013537423A (ja) | 2010-08-17 | 2013-10-03 | メルク・シャープ・エンド・ドーム・コーポレイション | 低分子干渉核酸(siNA)を用いたB型肝炎ウイルス(HBV)遺伝子発現のRNA干渉媒介性阻害 |
| EP2608669B1 (en) | 2010-08-23 | 2016-06-22 | Merck Sharp & Dohme Corp. | NOVEL PYRAZOLO[1,5-a]PYRIMIDINE DERIVATIVES AS mTOR INHIBITORS |
| WO2012030685A2 (en) | 2010-09-01 | 2012-03-08 | Schering Corporation | Indazole derivatives useful as erk inhibitors |
| US9242981B2 (en) | 2010-09-16 | 2016-01-26 | Merck Sharp & Dohme Corp. | Fused pyrazole derivatives as novel ERK inhibitors |
| WO2012058210A1 (en) | 2010-10-29 | 2012-05-03 | Merck Sharp & Dohme Corp. | RNA INTERFERENCE MEDIATED INHIBITION OF GENE EXPRESSION USING SHORT INTERFERING NUCLEIC ACIDS (siNA) |
| WO2012087772A1 (en) | 2010-12-21 | 2012-06-28 | Schering Corporation | Indazole derivatives useful as erk inhibitors |
| CN103732592A (zh) | 2011-04-21 | 2014-04-16 | 默沙东公司 | 胰岛素样生长因子-1受体抑制剂 |
| US9023865B2 (en) | 2011-10-27 | 2015-05-05 | Merck Sharp & Dohme Corp. | Compounds that are ERK inhibitors |
| US20150299696A1 (en) | 2012-05-02 | 2015-10-22 | Sirna Therapeutics, Inc. | SHORT INTERFERING NUCLEIC ACID (siNA) COMPOSITIONS |
| EP2900241B1 (en) | 2012-09-28 | 2018-08-08 | Merck Sharp & Dohme Corp. | Novel compounds that are erk inhibitors |
| AU2013352568B2 (en) | 2012-11-28 | 2019-09-19 | Merck Sharp & Dohme Llc | Compositions and methods for treating cancer |
| TW201429969A (zh) | 2012-12-20 | 2014-08-01 | Merck Sharp & Dohme | 作爲hdm2抑制劑之經取代咪唑吡啶 |
| EP2951180B1 (en) | 2013-01-30 | 2018-05-02 | Merck Sharp & Dohme Corp. | 2,6,7,8 substituted purines as hdm2 inhibitors |
| EP3041938A1 (en) | 2013-09-03 | 2016-07-13 | Moderna Therapeutics, Inc. | Circular polynucleotides |
| US10975084B2 (en) | 2016-10-12 | 2021-04-13 | Merck Sharp & Dohme Corp. | KDM5 inhibitors |
| EP3706742B1 (en) | 2017-11-08 | 2023-03-15 | Merck Sharp & Dohme LLC | Prmt5 inhibitors |
| WO2019094312A1 (en) | 2017-11-08 | 2019-05-16 | Merck Sharp & Dohme Corp. | Prmt5 inhibitors |
| BR112021002267A8 (pt) | 2018-08-07 | 2023-02-07 | Merck Sharp & Dohme | Inibidores de prmt5 |
| WO2020033282A1 (en) | 2018-08-07 | 2020-02-13 | Merck Sharp & Dohme Corp. | Prmt5 inhibitors |
| WO2020033284A1 (en) | 2018-08-07 | 2020-02-13 | Merck Sharp & Dohme Corp. | Prmt5 inhibitors |
| MX2022011545A (es) | 2020-04-03 | 2022-11-09 | Nerre Therapeutics Ltd | Un antagonista de receptor de nk-1 para tratar una enfermedad que se selecciona de sepsis, choque septico, síndrome de dificultad respiratoria aguda (ards) 0 síndrome de disfunción orgánica múltiple (mcds). |
| IL298589A (en) | 2020-06-02 | 2023-01-01 | Nerre Therapeutics Ltd | Neurokinin (nk)-1 receptor antagonists for use in the treatment of pulmonary fibrosis conditions promoted by mechanical injury to the lungs |
| CN115650969B (zh) * | 2022-10-29 | 2024-10-01 | 河南师范大学 | 一种α-取代-β-胺氧基取代吗啉类化合物的合成方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2534915A1 (fr) * | 1982-10-26 | 1984-04-27 | Lafon Labor | Nouveaux derives de 2-(phenoxymethyl)-morpholine, utilisation en therapeutique et procede de preparation |
| EP0436334A2 (en) * | 1990-01-04 | 1991-07-10 | Pfizer Inc. | 3-Aminopiperidine derivatives and related nitrogen containing heterocycles |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4476311A (en) * | 1980-03-12 | 1984-10-09 | The Purdue Frederick Company | Analgesic 4-carboxy-pyrrolidin-2-one compound |
| JPS5739599A (en) * | 1980-08-20 | 1982-03-04 | Fuji Machine Mfg | Method and device for automatically mounting leadless electronic part on printed board or like |
| EP0600952B1 (en) * | 1991-08-20 | 1996-04-17 | MERCK SHARP & DOHME LTD. | Azacyclic compounds, processes for their preparation and pharmaceutical compositions containing them |
-
1993
- 1993-06-25 CA CA002099233A patent/CA2099233A1/en not_active Abandoned
- 1993-06-25 IL IL106142A patent/IL106142A/xx not_active IP Right Cessation
- 1993-06-28 MY MYPI93001250A patent/MY108836A/en unknown
- 1993-06-28 HR HR931003 patent/HRP931003B1/xx not_active IP Right Cessation
- 1993-06-28 MX MX9303888A patent/MX9303888A/es unknown
- 1993-06-28 ZA ZA934624A patent/ZA934624B/xx unknown
- 1993-06-29 DE DE69326977T patent/DE69326977T2/de not_active Expired - Lifetime
- 1993-06-29 WO PCT/US1993/006181 patent/WO1994000440A1/en not_active Ceased
- 1993-06-29 YU YU45293A patent/YU49036B/sh unknown
- 1993-06-29 ES ES93305086T patent/ES2141133T3/es not_active Expired - Lifetime
- 1993-06-29 RO RO94-02095A patent/RO114448B1/ro unknown
- 1993-06-29 DZ DZ930080A patent/DZ1700A1/fr active
- 1993-06-29 JP JP5212045A patent/JP2634372B2/ja not_active Expired - Lifetime
- 1993-06-29 SI SI9300346A patent/SI9300346B/sl unknown
- 1993-06-29 SK SK1600-94A patent/SK281093B6/sk not_active IP Right Cessation
- 1993-06-29 CZ CZ19943330A patent/CZ288530B6/cs not_active IP Right Cessation
- 1993-06-29 EP EP93305086A patent/EP0577394B1/en not_active Expired - Lifetime
- 1993-06-29 AT AT93305086T patent/ATE186532T1/de active
- 1993-06-29 DK DK93305086T patent/DK0577394T3/da active
- 1993-06-29 HU HU9403804A patent/HU219713B/hu unknown
- 1993-06-29 NZ NZ254476A patent/NZ254476A/en not_active IP Right Cessation
- 1993-06-29 KR KR1019940704776A patent/KR100301212B1/ko not_active Expired - Lifetime
- 1993-06-29 RU RU94046364A patent/RU2140914C1/ru active
- 1993-06-29 AU AU46561/93A patent/AU4656193A/en not_active Abandoned
- 1993-06-29 CN CN93109517A patent/CN1049431C/zh not_active Expired - Lifetime
- 1993-08-17 TW TW082106583A patent/TW358808B/zh not_active IP Right Cessation
-
1994
- 1994-12-19 BG BG99274A patent/BG62963B1/bg unknown
- 1994-12-28 FI FI946133A patent/FI111363B/fi not_active IP Right Cessation
- 1994-12-28 NO NO945064A patent/NO305698B1/no not_active IP Right Cessation
-
1997
- 1997-04-30 BR BR1100375-8A patent/BR1100375A/pt active IP Right Grant
-
1999
- 1999-11-11 GR GR990402842T patent/GR3031824T3/el unknown
-
2000
- 2000-09-07 LV LVP-00-118A patent/LV12568B/lv unknown
- 2000-11-02 CY CY0000052A patent/CY2200B1/xx unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2534915A1 (fr) * | 1982-10-26 | 1984-04-27 | Lafon Labor | Nouveaux derives de 2-(phenoxymethyl)-morpholine, utilisation en therapeutique et procede de preparation |
| EP0436334A2 (en) * | 1990-01-04 | 1991-07-10 | Pfizer Inc. | 3-Aminopiperidine derivatives and related nitrogen containing heterocycles |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2307651C2 (ru) * | 2001-04-05 | 2007-10-10 | Тиога Фармасьютиклз, Инк. | Каппа-опиатные агонисты для лечения заболеваний мочевого пузыря |
| RU2304435C2 (ru) * | 2001-07-10 | 2007-08-20 | Ф.Хоффманн-Ля Рош Аг | Применение антагонистов рецептора nk-1 для лечения черепно-мозговой и спинномозговой травмы или повреждения нервной ткани |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2140914C1 (ru) | Замещенные гетероциклы или их фармацевтически приемлемая соль, фармацевтическая композиция для блокады рецепторов нейрокинина-1 у млекопитающих, способ для блокады рецепторов нейрокинина-1 у млекопитающих | |
| US5637699A (en) | Process for preparing morpholine tachykinin receptor antagonists | |
| KR100335704B1 (ko) | 모르폴린및티오모르폴린타키키닌수용체길항제 | |
| JP3073770B2 (ja) | モルホリンタキキニン受容体拮抗薬のプロドラッグ | |
| US5872116A (en) | Morpholine and thiomorpholine tachykinin receptor antagonists | |
| US6638930B2 (en) | Morpholine and thiomorpholine tachykinin receptor antagonists | |
| HK1009268B (en) | Morpholine and thiomorpholine tachykinin receptor antagonists | |
| HK1009046B (en) | Morpholine tachykinin receptor antagonists |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PD4A | Correction of name of patent owner | ||
| PC43 | Official registration of the transfer of the exclusive right without contract for inventions |
Effective date: 20130530 |
|
| PD4A | Correction of name of patent owner |