전술된 일반적인 설명 및 하기 상세한 설명 모두는 단지 예시적이고 설명적인 것이며, 청구될 때 본 발명을 제한하지 않음이 이해되어야 한다. 본원에서, 단수의 사용은 달리 구체적으로 언급되지 않으면 복수를 포함한다. 본원에서 사용된 바와 같이, "또는"의 사용은 달리 언급되지 않으면 "및/또는"를 의미한다. 더욱이, 용어 "포함하는" 뿐만 아니라 다른 형태, 예컨대 "포함한다" 및 "포함된"의 사용은 제한적인 것이 아니다. 또한, 용어들 예컨대 "요소" 또는 "성분"은, 달리 구체적으로 언급되지 않으면 하나의 단위를 포함하는 요소 및 성분 둘 모두 및 1 초과의 하부단위를 포함하는 요소 및 성분을 포함한다.
본원에서 사용된 섹션 제목은 단지 조직상의 목적을 위한 것이고, 기재된 요지를 제한하는 것으로 해석되서는 안 된다. 특허, 특허 출원, 기사, 서적 및 논문을 포함하지만 이들로 제한되는 것은 아닌, 본 출원에 인용된, 모든 문서 또는 문서들의 부분은, 임의의 목적을 위하여 이들의 전문이 참고로 명백하게 편입된다.
정의
구체적인 정의가 제공되지 않는 한, 본 명세서에 기술된 분석 화학, 합성 유기 화학, 및 의학 및 약제학적 화학과 관련하여 이용된 명명법, 및 그의 절차 및 기술은 본 기술분야에서 잘 알려지고 통상적으로 사용되는 것들이다. 화학적 합성 및 화학적 분석을 위해서는 표준 기술이 사용될 수 있다. 특정 그와 같은 기술 및 절차는 예를 들면 하기에서 발견될 수 있다: "Carbohydrate Modifications in Antisense Research" Edited by Sangvi and Cook, American Chemical Society , Washington D.C., 1994; "Remington's Pharmaceutical Sciences," Mack Publishing Co., Easton, Pa., 21st edition, 2005; 및 "Antisense Drug Technology, Principles, Strategies, and Applications" Edited by Stanley T. Crooke, CRC Press, Boca Raton, Florida; 및 Sambrook et al., "Molecular Cloning, A laboratory Manual," 2nd Edition, Cold Spring Harbor Laboratory Press, 1989 (이들은 임의의 목적을 위해 참고로 본원에 편입되어 있음). 허용되는 경우에, 모든 특허, 특허출원, 공개된 특허출원 및 다른 저널 출판물을 포함하여 (단, 이들로 제한되지는 않는다) 본 출원에서 인용된 모든 문서, 또는 문서의 일부분, 유전자은행 (GENBANK) 수탁 번호 및 국립 바이오테크놀로지 정보 센터(National Center for Biotechnology Information; NCBI) 및 본 명세서에서 전체적으로 언급된 다른 데이터와 같은 데이터베이스를 통해 수득될 수 있는 관련된 서열 정보는 온전하게 뿐만 아니라 여기에서 거론된 문서의 일부분에 대한 참고로 포함된다.
달리 지적되지 않으면, 하기 용어들은 하기 의미를 갖는다:
본원에서 사용된 바와 같이, "뉴클레오시드"는 핵염기 모이어티 및 당 모이어티를 포함하는 화합물을 의미한다. 뉴클레오시드는, 비제한적으로, 하기를 포함한다: 자연 발생 뉴클레오시드 (DNA 및 RNA에서 발견됨) 및 변형된 뉴클레오시드. 뉴클레오시드는 포스페이트 모이어티에 연결될 수 있다.
본원에서 사용된 바와 같이, "화학적 변형"은 자연 발생 대응물과 비교할 때 화합물에서 화학적 차이를 의미한다. 올리고뉴클레오티드의 화학적 변형은 뉴클레오시드 변형 (당 모이어티 변형 및 핵염기 변형 포함) 및 뉴클레오시드간 연결 변형을 포함한다. 올리고뉴클레오티드에 관하여, 화학적 변형은 핵염기 서열에서 단지 차이를 포함하지 않는다.
본원에서 사용된 바와 같이, "푸라노실"은 4개 탄소 원자 및 하나의 산소 원자를 포함하는 5-원 환을 포함하는 구조를 의미한다.
본원에서 사용된 바와 같이, "자연 발생 당 모이어티"는 자연 발생 RNA에서 발견된 리보푸라노실 또는 자연 발생 DNA로서 발견된 데옥시리보푸라노실을 의미한다.
본원에서 사용된 바와 같이, "당 모이어티"는 뉴클레오시드의 자연 발생 당 모이어티 또는 변형된 당 모이어티를 의미한다.
본원에서 사용된 바와 같이, "변형된 당 모이어티"는 치환된 당 모이어티 또는 당 대용물을 의미한다.
본원에서 사용된 바와 같이, "치환된 당 모이어티"는 자연 발생 당 모이어티가 아닌 푸라노실을 의미한다. 치환된 당 모이어티는 2'-위치, 3'-위치, 5'-위치 및/또는 4'-위치에서 치환체를 포함하는 푸라노실을 비제한적으로 포함한다. 특정 치환된 당 모이어티는 이환식 당 모이어티이다.
본원에서 사용된 바와 같이, "2'-치환된 당 모이어티"는 H 또는 OH 이외의 2'-위치에서 치환체를 포함하는 푸라노실을 의미한다. 달리 지적되지 않으면, 2'-치환된 당 모이어티는 이환식 당 모이어티가 아니다 (즉, 2'-치환된 당 모이어티의 2'-치환체는 푸라노실 환의 또 하나의 원자에 대해 가교를 형성하지 않는다.
본원에서 사용된 바와 같이, "MOE"는 -OCH2CH2OCH3를 의미한다.
본원에서 사용된 바와 같이, "2'-F 뉴클레오시드"는 2' 위치에서 불소를 포함하는 당을 포함하는 뉴클레오시드를 의미한다. 달리 지적되지 않으면, 2'-F 뉴클레오시드 중 불소는 (천연 리보오스의 OH를 대체하는) 리보 위치에 있다.
본원에서 사용된 바와 같이 용어 "당 대용물"은 푸라노실을 포함하지 않고 뉴클레오시드의 자연 발생 당 모이어티를 대체할 수 있는 구조를 의미하고, 이로써 수득한 뉴클레오시드 하부-단위는 함께 연결될 수 있고/거나 다른 뉴클레오시드에 연결되어 상보적 올리고머 화합물을 혼성화할 수 있는 올리고머 화합물을 형성할 수 있다. 그와 같은 구조는 푸라노실보다 상이한 원자를 포함하는 환 (예를 들면, 4, 6, 또는 7-원 환); 비-산소 원자 (예를 들면, 탄소, 황, 또는 질소)에 의한 푸라노실의 산소의 대체; 또는 원자의 수의 변화 및 산소의 대체 둘 모두를 포함한다. 그와 같은 구조는 치환된 당 모이어티를 대신하는 것 (예를 들면, 추가의 치환체를 임의로 포함하는 6-원 탄소환식 이환식 당 대용물)에 상응하는 치환을 또한 포함할 수 있다. 당 대용물은 또한 더 많은 복합 당 대체물질 (예를 들면, 펩티드 핵산의 비-환계)를 포함한다. 당 대용물은 비제한적으로 모폴리노, 사이클로헥세닐 및 사이클로헥시톨을 포함한다.
본원에서 사용된 바와 같이, "이환식 당 모이어티"는 이환식 구조가 되는, 제2 환을 형성하기 위해 4 내지 7 원 환의 2 개의 원자를 연결하는 가교를 포함하는 (비제한적으로 푸라노실을 포함하는) 4 내지 7 원 환을 포함하는 변형된 당 모이어티를 의미한다. 특정 구현예에서, 4 내지 7 원 환은 당 환이다. 특정 구현예에서 4 내지 7 원 환은 푸라노실이다. 특정 그와 같은 구현예에서, 가교는 푸라노실의 2'-탄소 및 4'-탄소를 연결한다.
본원에서 사용된 바와 같이, "뉴클레오티드"는 포스페이트 연결 그룹을 추가로 포함하는 뉴클레오시드를 의미한다. 본원에서 사용된 바와 같이, "연결된 뉴클레오시드"는 포스페이트 연결에 의해 연결되거나 그렇지 않을 수 있고 따라서, 비제한적으로 "연결된 뉴클레오티드"를 포함한다. 본원에서 사용된 바와 같이, "연결된 뉴클레오시드"는 연속적 서열로 연결된 뉴클레오시드이다 (즉 추가의 뉴클레오시드는 연결된 것들 사이에 존재하지 않는다).
본원에서 사용된 바와 같이, "핵염기"는 올리고뉴클레오티드에 편입될 수 있는 뉴클레오시드를 만들기 위해 당 모이어티에 연결될 수 있는 원자의 그룹을 의미하고, 상기 원자의 그룹은 또 하나의 올리고뉴클레오티드 또는 핵산의 상보적 자연 발생 핵염기와 결합할 수 있다. 핵염기는 자연 발생일 수 있거나 변형될 수 있다. "핵염기 서열"은 임의의 당, 연결 및/또는 핵염기 변형에 독립적인 인접 핵염기의 순서를 의미한다.
본원에서 사용된 바와 같이 용어들, "비변형된 핵염기" 또는 "자연 발생 핵염기"는 RNA 또는 DNA의 자연 발생 헤테로환식 핵염기: 퓨린계 아데닌 (A) 및 구아닌 (G), 및 피리미딘계 티민 (T), 시토신 (C) (5-메틸 C 포함), 및 우라실 (U)을 의미한다.
본원에서 사용된 바와 같이, "변형된 핵염기"는 자연 발생 핵염기가 아닌 임의의 핵염기를 의미한다.
본원에서 사용된 바와 같이, "변형된 뉴클레오시드"는 자연 발생 RNA 또는 DNA 뉴클레오시드와 비교하여 적어도 하나의 화학적 변형을 포함하는 뉴클레오시드를 의미한다. 변형된 뉴클레오시드는 변형된 당 모이어티 및/또는 변형된 핵염기를 포함한다.
본원에서 사용된 바와 같이, "이환식 뉴클레오시드" 또는 "BNA"는 이환식 당 모이어티를 포함하는 뉴클레오시드를 의미한다.
본원에서 사용된 바와 같이, "제한된 에틸 뉴클레오시드" 또는 "cEt"는 4'-CH(CH3)-O-2'가교를 포함하는 이환식 당 모이어티를 포함하는 뉴클레오시드를 의미한다.
본원에서 사용된 바와 같이, "잠겨진 핵산 뉴클레오시드" 또는 "LNA"는 4'-CH2-O-2'가교를 포함하는 이환식 당 모이어티를 포함하는 뉴클레오시드를 의미한다.
본원에서 사용된 바와 같이, "2'-치환된 뉴클레오시드"는 H 또는 OH 외에 2'-위치에서 치환체를 포함하는 뉴클레오시드 의미한다. 달리 지적되지 않으면, 2'-치환된 뉴클레오시드는 이환식 뉴클레오시드가 아니다.
본원에서 사용된 바와 같이, "데옥시뉴클레오시드"는 자연 발생 데옥시리보뉴클레오시드 (DNA)에서 발견되는 바와 같이, 2'-H 푸라노실 당 모이어티를 포함하는 뉴클레오시드를 의미한다. 특정 구현예에서, 2'-데옥시뉴클레오시드는 변형된 핵염기를 포함할 수 있거나 RNA 핵염기 (예를 들면, 우라실)를 포함할 수 있다.
본원에서 사용된 바와 같이, "올리고뉴클레오티드"는 복수의 연결된 뉴클레오시드를 포함하는 화합물을 의미한다. 특정 구현예에서, 올리고뉴클레오티드는 1 이상의 비변형된 리보뉴클레오시드 (RNA) 및/또는 비변형된 데옥시리보뉴클레오시드 (DNA) 및/또는 1 이상의 변형된 뉴클레오시드를 포함한다.
본원에서 사용된 바와 같이 "올리고뉴클레오시드"는, 뉴클레오시드간 연결의 특정 것도 인 원자를 함유하지 않는 올리고뉴클레오티드를 의미한다. 본원에서 사용된 바와 같이, 올리고뉴클레오티드는 올리고뉴클레오시드를 포함한다.
본원에서 사용된 바와 같이, "변형된 올리고뉴클레오티드"는 적어도 하나의 변형된 뉴클레오시드 및/또는 적어도 하나의 변형된 뉴클레오시드간 연결을 포함하는 올리고뉴클레오티드를 의미한다.
본원에서 사용된 바와 같이, "연결" 또는 "연결 그룹"은 원자의 2 이상의 다른 그룹과 함께 연결되는 원자의 그룹을 의미한다.
본원에서 사용된 바와 같이 "뉴클레오시드간 연결"은 올리고뉴클레오티드에서 인접한 뉴클레오시드 사이의 공유 결합을 의미한다.
본원에서 사용된 바와 같이 "자연 발생 뉴클레오시드간 연결"은 3' 내지 5' 포스포디에스테르 연결을 의미한다.
본원에서 사용된 바와 같이, "변형된 뉴클레오시드간 연결"은 자연 발생 뉴클레오시드간 연결 이외의 임의의 뉴클레오시드간 연결을 의미한다.
본원에서 사용된 바와 같이, "말단 뉴클레오시드간 연결"은 올리고뉴클레오티드 또는 그것의 규정된 영역의 마지막 2 개의 뉴클레오시드의 사이의 연결을 의미한다.
본원에서 사용된 바와 같이, "인 연결 그룹"은 인 원자를 포함하는 연결기를 의미한다. 인 연결 그룹는 하기 식을 갖는 그룹을 비제한적으로 포함한다:
상기 식 중에서,
Ra 및 Rd 각각은, 독립적으로, O, S, CH2, NH, 또는 NJ1이고 여기서 J1은 C1-C6 알킬 또는 치환된 C1-C6 알킬이고;
Rb 는 O 또는 S이고;
Rc은 OH, SH, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, 아미노 또는 치환된 아미노이고; 그리고
J1은 Rb는 O 또는 S이다.
인 연결 그룹는 비제한적으로, 하기를 포함한다: 포스포디에스테르, 포스포로티오에이트, 포스포로디티오에이트, 포스포네이트, 포스포르아미데이트, 포스포로티오아미데이트, 티오알킬포스포네이트, 포스포트리에스테르, 티오노알킬포스포트리에스테르 및 보라노포스페이트.
본원에서 사용된 바와 같이, "뉴클레오시드간 인 연결 그룹"은 2 개의 뉴클레오시드를 직접적으로 연결하는 인 연결 그룹를 의미한다.
본원에서 사용된 바와 같이, "비-뉴클레오시드간 인 연결 그룹"은 2 개의 뉴클레오시드를 직접적으로 연결하지 않는 인 연결 그룹를 의미한다. 특정 구현예에서, 비-뉴클레오시드간 인 연결 그룹는 뉴클레오시드를 뉴클레오시드 이외의 그룹에 연결한다. 특정 구현예에서, 비-뉴클레오시드간 인 연결 그룹는 2 개의 그룹을 연결하고, 이것 중 특정 것도 뉴클레오시드가 아니다.
본원에서 사용된 바와 같이, "중성 연결 그룹"은 충전되지 않은 연결기를 의미한다. 중성 연결 그룹는 비제한적으로 하기를 포함한다: 포스포트리에스테르, 메틸포스포네이트, MMI (-CH2-N(CH3)-O-), 아미드-3 (-CH2-C(=O)-N(H)-), 아미드-4 (-CH2-N(H)-C(=O)-), 포름아세탈 (-O-CH2-O-), 및 티오포름아세탈 (-S-CH2-O-). 추가의 중성 연결 그룹는 실록산 (디알킬실록산), 카복실레이트 에스테르, 카복사마이드, 설파이드, 설포네이트 에스테르 및 아미드를 포함하는 비이온성 연결을 포함한다 (참고 예를 들면: Carbohydrate Modifications in Antisense Research; Y.S. Sanghvi and P.D. Cook Eds. ACS Symposium Series 580; Chapters 3 and 4, (pp. 40-65)). 추가의 중성 연결 그룹는 혼합된 N, O, S 및 CH2 성분 부분을 포함하는 비이온성 연결을 포함한다.
본원에서 사용된 바와 같이, "뉴클레오시드간 중성 연결 그룹"는 2 개의 뉴클레오시드를 직접적으로 연결하는 중성 연결 그룹를 의미한다.
본원에서 사용된 바와 같이, "비-뉴클레오시드간 중성 연결 그룹"는 2 개의 뉴클레오시드를 직접적으로 연결하지 않는 중성 연결 그룹를 의미한다. 특정 구현예에서, 비-뉴클레오시드간 중성 연결 그룹는 뉴클레오시드를 뉴클레오시드 이외의 그룹에 연결한다. 특정 구현예에서, 비-뉴클레오시드간 중성 연결 그룹는 2 개의 그룹을 연결하고, 이것 중 특정 것도 뉴클레오시드가 아니다.
본원에서 사용된 바와 같이, "올리고머 화합물"은 2 이상의 하부구조를 포함하는 폴리머 구조를 의미한다. 특정 구현예에서, 올리고머 화합물은 올리고뉴클레오티드를 포함한다. 특정 구현예에서, 올리고머 화합물은 1 이상의 콘주게이트 그룹 및/또는 말단기를 포함한다. 특정 구현예에서, 올리고머 화합물은 올리고뉴클레오티드로 구성된다. 올리고머 화합물은 또한 자연 발생 핵산을 포함한다. 특정 구현예에서, 올리고머 화합물은 1 이상의 연결된 단량체 하부단위의 골격을 포함하고, 여기서 각각의 연결된 단량체 하부단위는 헤테로환 염기 모이어티에 직접적으로 또는 간접적으로 부착된다. 특정 구현예에서, 올리고머 화합물은 헤테로환 염기 모이어티에 연결되지 않는 단량체 하부단위를 또한 포함할 수 있고, 그렇게 함으로써 무염기성 부위를 제공한다. 특정 구현예에서, 단량체 하부단위, 당 모이어티 또는 대용물 및 헤테로환 염기 모이어티를 잇는 연결은 독립적으로 변형될 수 있다. 특정 구현예에서, 헤테로환 염기를 포함할 수 있거나 그렇지 않는 연결-당 단위는, 모방체 예컨대 펩티드 핵산 중 단량체로 치환될 수 있다.
본원에서 사용된 바와 같이, "말단기"는 올리고뉴클레오티드의 3' 말단 또는 5' 말단 중 하나 또는 둘 모두에 부착된 1 이상의 원자를 의미한다. 특정 구현예에서 말단기는 콘주게이트 그룹이다. 특정 구현예에서, 말단기는 1 이상의 말단기 뉴클레오시드를 포함한다.
본원에서 사용된 바와 같이, "콘주게이트" 또는 "콘주게이트 그룹"은 올리고뉴클레오티드 또는 올리고머 화합물에 결합된 원자 또는 원자의 그룹을 의미한다. 일반적으로, 콘주게이트 그룹은 약동학적, 약력학적, 결합, 흡수, 세포성 분포, 세포성 흡수, 전하 및/또는 청소능 특성을 비제한적으로 포함하는, 부착된 화합물의 1 이상의 특성을 변형시킨다.
본원에서 사용된 바와 같이, 콘주게이트 그룹의 문맥 중 "콘주게이트 링커" 또는 "링커"는 임의의 원자 또는 원자의 그룹을 포함하고 (1) 올리고뉴클레오티드를 콘주게이트 그룹의 또 하나의 부분 또는 (2) 콘주게이트 그룹의 2 이상의 부분에 공유 결합하는 콘주게이트 그룹의 구분을 의미한다.
콘주게이트 그룹은 올리고머 화합물 예컨대 안티센스 올리고뉴클레오티드에 대한 공유 결합을 형성하는 결합을 제공하는 라디칼로서 본원에서 보여진다. 특정 구현예에서, 올리고머 화합물 상의 부착점은 올리고머 화합물의 3' 말단 뉴클레오시드의 3'-하이드록실 그룹의 3'-산소 원자이다. 특정 구현예에서 올리고머 화합물 상의 부착점은 올리고머 화합물의 5' 말단 뉴클레오시드의 5'-하이드록실 그룹의 5'-산소 원자이다. 특정 구현예에서, 올리고머 화합물에 대한 부착을 형성하는 결합은 절단가능 결합이다. 특정 그와 같은 구현예에서, 그와 같은 절단가능 결합은 절단가능 모이어티의 모두 또는 일부를 구성한다.
특정 구현예에서, 콘주게이트 그룹은 절단가능 모이어티 (예를 들면, 절단가능 결합 또는 절단가능 뉴클레오시드) 및 탄수화물 클러스터 부분, 예컨대 GalNAc 클러스터 부분을 포함한다. 그와 같은 탄수화물 클러스터 부분은 하기를 포함한다: 표적 모이어티, 및 임의로, 콘주게이트 링커. 특정 구현예에서, 탄수화물 클러스터 부분은 리간드의 수 및 동일성에 의해 확인된다. 예를 들면, 특정 구현예에서, 탄수화물 클러스터 부분은 3 개의 GalNAc 그룹을 포함하고 "GalNAc3"로 칭한다. 특정 구현예에서, 탄수화물 클러스터 부분은 4 개의 GalNAc 그룹을 포함하고 "GalNAc4"로 칭한다. (특정 연결기, 분지화 및 콘주게이트 링커 그룹을 갖는) 구체적인 탄수화물 클러스터 부분은 본원에서 기재되어 있고, 로마 숫자 그 다음 하첨자 "a"로 지정된다. 따라서 "GalNac3-1a"는 3 개의 GalNAc 그룹을 갖는 콘주게이트 그룹 및 구체적으로 확인된 연결 그룹, 분지화 및 연결기의 구체적인 탄수화물 클러스터 부분을 의미한다. 그와 같은 탄수화물 클러스터 단편은 절단가능 모이어티, 예컨대 절단가능 결합 또는 절단가능 뉴클레오시드를 통해 올리고머 화합물에 부착된다.
본원에서 사용된 바와 같이, "절단가능 모이어티"는 생리적 조건 하에서 분열될 수 있는 결합 또는 그룹을 의미한다. 특정 구현예에서, 절단가능 모이어티는 세포 또는 아-세포성 구획, 예컨대 용해소체 내에서 절단된다. 특정 구현예에서, 절단가능 모이어티는 내인성 효소, 예컨대 뉴클레아제에 의해 절단된다. 특정 구현예에서, 절단가능 모이어티는 1, 2, 3, 4, 또는 그 초과의 4 개의 절단가능 결합을 갖는 원자의 그룹을 포함한다.
본원에서 사용된 바와 같이, "절단가능 결합"은 분열될 수 있는 임의의 화학 결합을 의미한다. 특정 구현예에서, 절단가능 결합은 하기 중으로부터 선택된다: 아미드, 폴리아미드, 에스테르, 에테르, 포스포디에스테르의 에스테르 하나 또는 둘 모두, 포스페이트 에스테르, 카바메이트, 디-설파이드, 또는 펩티드.
본원에서 사용된 바와 같이, "탄수화물 클러스터"는 스캐폴드 또는 링커 그룹에 부착된 1 이상의 탄수화물 잔기를 갖는 화합물을 의미한다. 예를 들면 하기 (참고: Maier et al., "Synthesis of Antisense Oligonucleotides Conjugated to a Multivalent Carbohydrate Cluster for Cellular Targeting," Bioconjugate Chemistry, 2003, (14): 18-29, 이것은 그 전체가 참고로 본원에 편입되어 있음, 또는 Rensen et al., "Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asiaglycoprotein Receptor," J. Med . Chem . 2004, (47): 5798-5808 (탄수화물 콘주게이트 클러스터의 예시로)).
본원에서 사용된 바와 같이, "변형된 탄수화물"은 자연 발생 탄수화물에 대해 1 이상의 화학적 변형을 갖는 임의의 탄수화합물을 의미한다.
본원에서 사용된 바와 같이, "탄수화물 유도체"는 탄수화물을 개시 물질 또는 중간체로서 사용하여 합성될 수 있는 임의의 화합물을 의미한다.
본원에서 사용된 바와 같이, "탄수화물"은 자연 발생 탄수화물, 변형된 탄수화물, 또는 탄수화물 유도체를 의미한다.
"보호기"는 본 분야의 숙련가에게 알려진 임의의 화합물 또는 보호기를 의미한다. 보호기의 비-제한적인 예는 하기에서 발견될 수 있다: "Protective Groups in Organic Chemistry", T. W. Greene, P. G. M. Wuts , ISBN 0-471-62301-6, John Wiley & Sons, Inc, New York (이의 전문이 본원에 참조로 인용됨).
본원에서 사용된 바와 같이, "단일가닥"은 그것의 보체에 대해 혼성화되지 않고 안정한 자가-이중나선를 형성하기 위한 충분한 자가-상보성이 없는 올리고머 화합물을 의미한다. 본원에서 사용된 바와 같이, "이중가닥"은 서로 혼성화된 한 쌍의 올리고머 화합물 또는 헤어핀 구조를 형성하는 단일 자가-상보적 올리고머 화합물을 의미한다.
특정 구현예에서, 이중-가닥 올리고머 화합물은 제 1 및 제 2 올리고머 화합물을 포함한다. 본원에서 사용된 바와 같이, "안티센스 화합물"은, 적어도 하나의 안티센스 활성이 생기는, 혼성화할 수 있는 표적 핵산에 대해 상보적인 올리고뉴클레오티드의 적어도 부분을 포함하거나 이로 이루어진 화합물을 의미한다.
본원에서 사용된 바와 같이, "안티센스 활성"은 그것의 표적 핵산에 대한 안티센스 화합물의 혼성화가 그 원인인 임의의 검출가능한 및/또는 측정가능한 변화를 의미한다. 특정 구현예에서, 안티센스 활성은 표적 핵산 전사체 (예를 들면 mRNA)의 양 또는 활성의 조절을 포함한다. 특정 구현예에서, 안티센스 활성은 전-mRNA의 스플라이싱의 조절을 포함한다.
본원에서 사용된 바와 같이, "RNase H 기반 안티센스 화합물"이란, 안티센스 화합물을 의미하고, 여기서 안티센스 화합물의 안티센스 활성의 적어도 일부는 표적 핵산에 대한 안티센스 화합물의 혼성화 및 RNase H에 의한 표적 핵산의 차후의 절단이 그 원인이다.
본원에서 사용된 바와 같이, "RISC 기반 안티센스 화합물"은 안티센스 화합물을 의미하고, 여기서 안티센스 화합물의 안티센스 활성의 적어도 일부는 RNA 유도된 사일런싱 복합체 (RISC)가 그 원인이다.
본원에서 사용된 바와 같이, "검출" 또는 "측정"이란, 검출 또는 측정을 위한 시험 또는 검정이 수행된다는 것을 의미한다. 그와 같은 검출 및/또는 측정으로 값이 제로일 수 있다. 따라서, 검출 또는 측정용 시험으로 활성 없음 (활성 제로)을 발현하면, 그럼에도 불구하고 상기 활성을 검출 또는 측정하는 단계가 수행되었다.
본원에서 사용된 바와 같이, "검출가능한 및/또는 측정가능한 활성"이란, 제로가 아닌 통계적으로 유의미한 활성을 의미한다.
본원에서 사용된 바와 같이, "본질적으로 변하지 않는다"란, 특히 훨씬 더 변하는 또 하나의 파라미터에 대해 특정한 파라미터의 변화가 거의 없거나 없다는 것을 의미한다. 특정 구현예에서, 파라미터는, 5% 미만 변할 때 본질적으로 변하지 않는다. 특정 구현예에서, 파라미터는, 2-배 미만 변하지만 또 하나의 파라미터가 적어도 10-배 변한다면 본질적으로 변하지 않는다. 예를 들면, 특정 구현예에서, 안티센스 활성은 표적 핵산의 양의 변화이다. 특정 그와 같은 구현예에서, 비-표적 핵산의 양은, 그것이 표적 핵산보다 훨씬 더 적게 변하지만 그 변화가 제로일 필요는 없다면, 본질적으로 변하지 않는다.
본원에서 사용된 바와 같이, "발현"은, 유전자가 결국 단백질로 되는 과정을 의미한다. 발현은, 비제한적으로, 전사, 후-전사 변형 (예를 들면, 5'-캡의 스플라이싱, 폴리아데닐화, 부가), 및 번역을 포함한다.
본원에서 사용된 바와 같이, "표적 핵산"은, 안티센스 화합물이 원하는 안티센스 활성이 생기도록 혼성화하는 것으로 의도된 핵산 분자를 의미한다. 안티센스 올리고뉴클레오티드는 생리적 조건 하에서 혼성화를 허용하기 위해 그것의 표적 핵산에 대해 충분한 상보성을 갖는다.
본원에서 사용된 바와 같이, "핵염기 상보성" 또는 "상보성"은, 핵염기를 참조할 때, 또 하나의 핵염기와 염기 짝짓기할 수 있는 핵염기를 의미한다. 예를 들면, DNA에서, 아데닌 (A)은 티민 (T)에 대해 상보적이다. 예를 들면, RNA에서, 아데닌 (A)은 우라실 (U)에 대해 상보적이다. 특정 구현예에서, 상보적 핵염기는 그것의 표적 핵산의 핵염기와 염기 짝짓기할 수 있는 안티센스 화합물의 핵염기를 의미한다. 예를 들면, 안티센스 화합물의 특정 위치에 있는 핵염기가 표적 핵산의 특정 위치에서 핵염기와 수소 결합할 수 있다면, 이때 올리고뉴클레오티드와 표적 핵산 사아의 수소 결합의 위치는 핵염기쌍에서 상보적인 것으로 간주된다. 특정 변형을 포함하는 핵염기는 대응물 핵염기와 쌍을 이루는 능력을 유지할 수 있고 따라서, 여전히 핵염기 상보성을 유지할 수 있다.
본원에서 사용된 바와 같이, 핵염기에 관한 "비-상보적"이란, 수소 결합을 서로 형성하지 않는 한 쌍의 핵염기를 의미한다.
본원에서 사용된 바와 같이, 올리고머 화합물 (예를 들면, 연결된 뉴클레오시드, 올리고뉴클레오티드, 또는 핵산)에 관한 "상보적"이란, 핵염기 상보성을 통해 또 하나의 올리고머 화합물 또는 그것의 영역과 혼성화하기 위한 그와 같은 올리고머 화합물 또는 그것의 영역의 투여량을 의미한다. 상보적 올리고머 화합물은 각각의 뉴클레오시드에서 핵염기 상보성을 가질 필요는 없다. 오히려, 일부 미스매치가 용인된다. 특정 구현예에서, 상보적 올리고머 화합물 또는 영역은 핵염기의 70%에서 상보적이다 (70% 상보적). 특정 구현예에서, 상보적 올리고머 화합물 또는 영역은 80% 상보적이다. 특정 구현예에서, 상보적 올리고머 화합물 또는 영역은 90% 상보적이다. 특정 구현예에서, 상보적 올리고머 화합물 또는 영역은 95% 상보적이다. 특정 구현예에서, 상보적 올리고머 화합물 또는 영역은 100% 상보적이다.
본원에서 사용된 바와 같이, "미스매치"는, 제 1 및 제 2 올리고머 화합물이 정렬될 때 제 2 올리고머 화합물의 상응하는 위치에서 핵염기와 짝짓기할 수 없는 제 1 올리고머 화합물의 핵염기를 의미한다. 제 1 및 제 2 올리고머 화합물 중 하나 또는 둘 모두는 올리고뉴클레오티드일 수 있다.
본원에서 사용된 바와 같이, "혼성화"는 상보적 올리고머 화합물 (예를 들면, 안티센스 화합물 및 그것의 표적 핵산)의 짝짓기를 의미한다. 특정한 기전에 제한되지 않으면서, 짝짓기의 가장 공통의 기전은 상보적 핵염기 사이의 왓슨-크릭, 휴그스틴 또는 역전된 휴그스틴 수소 결합일 수 있는 수소 결합을 수반한다.
본원에서 사용된 바와 같이, "특이적으로 혼성화하는"이란, 또 하나의 핵산 부위에 혼성화하는 것보다 더 큰 친화성으로 하나의 핵산 부위에 혼성화하기 위한 올리고머 화합물의 능력을 의미한다.
본원에서 사용된 바와 같이, 올리고뉴클레오티드 또는 그것의 부분에 대한"완전히 상보적"이란, 올리고뉴클레오티드 또는 그것의 부분의 각각의 핵염기가 상보적 핵산 또는 그것의 인접부의 핵염기와 짝짓기할 수 있다는 것을 의미한다. 따라서, 완전히 상보적 영역은 하나의 가닥에서 미스매치 또는 비혼성화된 핵염기를 포함하지 않는다.
본원에서 사용된 바와 같이, "퍼센트 상보성"은 표적 핵산의 동등-길이부에 대해 상보적인 올리고머 화합물의 핵염기의 백분율을 의미한다. 퍼센트 상보성은 올리고머 화합물의 총 길이로, 표적 핵산에서 상응하는 위치에서 핵염기에 대해 상보적인 올리고머 화합물의 핵염기의 수를 나누어서 계산된다.
본원에서 사용된 바와 같이, "퍼센트 동일성"은 제 1 핵산에서 핵염기의 총수에 의해 분할된, 제 2 핵산에서의 상응하는 위체에서 핵염기와 동일한 (화학적 변형에 독립적인) 유형인 제 1 핵산에서 핵염기의 수를 의미한다.
본원에서 사용된 바와 같이, "조절"은 조절 전의 분자, 기능, 또는 활성의 양 또는 품질과 비교할 때, 분자, 기능, 또는 활성의 양 또는 품질의 변화를 의미한다. 예를 들면, 조절은 유전자 발현에서 변화, 증가 (자극 또는 유도) 또는 축소감소 (억제 또는 축소)를 포함한다. 추가 예로서, 발현의 조절은 전-mRNA 처리의 스플라이스 부위 선택의 변화를 포함할 수 있고, 조절의 부재에서의 양과 비교하여 특정한 스플라이스 -변이체의 절대적인 또는 상대적인 양이 변한다.
본원에서 사용된 바와 같이, "화학적 모티프"는 올리고뉴클레오티드 또는 그것의 영역에서 화학적 변형의 패턴을 의미한다. 모티프는 특정 뉴클레오시드 및/또는 올리고뉴클레오티드의 특정 연결 그룹에서의 변형에 의해 규정될 수 있다.
본원에서 사용된 바와 같이, "뉴클레오시드 모티프"는 올리고뉴클레오티드 또는 그것의 영역에서 뉴클레오시드 변형의 패턴을 의미한다. 그와 같은 올리고뉴클레오티드의 연결은 변형 또는 비변형될 수 있다. 달리 지적되지 않으면, 뉴클레오시드를 단지 기재하는 본원의 모티프는 뉴클레오시드 모티프인 것으로 의도된다. 따라서, 그와 같은 경우에, 연결은 제한되지 않는다.
본원에서 사용된 바와 같이, "당 모티프"는 올리고뉴클레오티드 또는 그것의 영역에서 당 변형의 패턴을 의미한다.
본원에서 사용된 바와 같이, "연결 모티프"는 올리고뉴클레오티드 또는 그것의 영역에서 연결 변형의 패턴을 의미한다. 그와 같은 올리고뉴클레오티드의 뉴클레오시드는 변형 또는 비변형될 수 있다. 달리 지적되지 않으면, 연결을 단지 기재하는 본원의 모티프는 연결 모티프인 것으로 의도된다. 따라서, 그와 같은 경우에, 뉴클레오시드는 제한되지 않는다.
본원에서 사용된 바와 같이, "핵염기 변형 모티프"는 올리고뉴클레오티드에 따른 핵염기에 대한 변형의 패턴을 의미한다. 달리 지적되지 않으면, 핵염기 변형 모티프는 핵염기 서열에 독립적이다.
본원에서 사용된 바와 같이, "서열 모티프"는 올리고뉴클레오티드 또는 그것의 부분을 따라 배열된 핵염기의 패턴을 의미한다. 달리 지적되지 않으면, 서열 모티프는 화학적 변형에 독립적이고 따라서 화학적 변형을 포함하지 않으면서 화학적 변형의 임의의 조합을 가질 수 있다.
본원에서 사용된 바와 같이, "유형"의 뉴클레오시드 또는 뉴클레오시드에 관한 "변형의 유형"은 뉴클레오시드의 화학적 변형을 의미하고 변형된 및 비변형된 뉴클레오시드를 포함한다. 따라서, 달리 지적되지 않으면, "제 1 형의 변형을 갖는 뉴클레오시드"는 비변형된 뉴클레오시드일 수 있다.
본원에서 사용된 바와 같이, "상이하게 변형된"은 변형의 부재를 포함하여, 서로 상이한 화학적 변형 또는 화학적 치환체를 의미한다. 따라서, 예를 들면, MOE 뉴클레오시드 및 비변형된 DNA 뉴클레오시드는, DNA 뉴클레오시드는 비변형될지라도 "상이하게 변형"된다. 마찬가지로, DNA 및 RNA는, 둘 모두가 자연 발생 비변형된 뉴클레오시드일지라도, "상이하게 변형"된다. 동일한, 그러나 상이한 핵염기를 포함하는 뉴클레오시드는 상이하게 변형되지 않는다. 예를 들면, 2'-OMe 변형된 당 및 비변형된 아데닌 핵염기를 포함하는 뉴클레오시드 및 2'-OMe 변형된 당 및 비변형된 티민 핵염기를 포함하는 뉴클레오시드는 상이하게 변형되지 않는다.
본원에서 사용된 바와 같이, "동일한 유형의 변형"은 변형의 부재를 포함하여 서로 동일한 변형을 의미한다. 따라서, 예를 들면, 2 개의 비변형된 DNA 뉴클레오시드는, DNA 뉴클레오시드가 비변형될지라도 "동일한 유형의 변형"를 갖는다. 동일한 유형 변형을 갖는 그와 같은 뉴클레오시드는 상이한 핵염기를 포함할 수 있다.
본원에서 사용된 바와 같이, "별개의 영역"는 올리고뉴클레오티드의 부분을 의미하고, 상기 화학적 변형 또는 임의의 인접하는 구분의 화학적 변형의 모티프는 별개의 영역이 서로 구별되도록 하는 적어도 하나의 차이를 포함한다.
본원에서 사용된 바와 같이, "약제학적으로 허용가능한 담체 또는 희석제"는 동물에게 투여하는데 사용하기에 적당한 임의의 물질을 의미한다. 특정 구현예에서, 약제학적으로 허용가능한 담체 또는 희석제는 멸균한 염수이다. 특정 구현예에서, 그와 같은 멸균한 염수는 약품 등급 염수이다.
본원에서 사용된 바와 같이 용어 "대사성 장애"는 대사의 조절 장애 - 에너지를 생산하기 위해 음식의 분해와 연관된 화학 반응의 복합 세트를 주로 특징으로 하는 질환 또는 병태를 의미한다.
본원에서 사용된 바와 같이, 용어 "심혈관 질환” 또는 "심혈관 장애”는 심장 또는 혈관의 손상된 기능을 주요하게 특징으로 하는 질환 또는 병태를 의미한다. 심혈관 질환 또는 장애의 예시는, 비제한적으로, 동맥류, 협심증, 부정맥, 죽상경화증, 뇌혈관 질환 (뇌졸중), 관상동맥 심장병, 고혈압, 이상지질혈증, 고지혈증, 및 고콜레스테롤혈증을 포함한다.
본원에서 사용된 바와 같이 용어 "단환식 또는 다환식 환계"는 단일 또는 다환식 라디칼 환계로부터 선택된 모든 환계를 포함하는 것을 의미하고, 상기 환은 융합 또는 연결되고, 지방족, 지환족, 아릴, 헤테로아릴, 아랄킬, 아릴알킬, 헤테로환식, 헤테로아릴, 헤테로방향족 및 헤테로아릴알킬로부터 개별적으로 선택된 단일 및 혼합된 환계를 포함하는 것을 의미한다. 그와 같은 단환식 또는 다환식 환형 구조는, 각각이 동일한 수준의 포화를 갖거나, 각각이, 독립적으로, 완전 포화된, 부분적으로 포화된 또는 완전 불포화된을 포함하는 가변 포화도를 갖는 환을 함유할 수 있다. 각각의 환은 C, N, O 및 S로부터 선택된 환 원자를 포함하여 헤테로환식 환 뿐만 아니라 혼합된 모티프 예컨대 벤즈이미다졸에서 존재할 수 있는 C 환 원자만을 포함하는 환을 얻을 수 있고, 여기서 하나의 환은 유일한 탄소 환 원자를 가지며 융합 환은 2 개의 질소 원자를 갖는다. 단환 또는 다환식 환계는 치환체 그룹 예컨대 환 중의 하나에 부착된 2 =O 그룹을 갖는 프탈이미드로 추가로 치환될 수 있다. 단환 또는 다환식 환계는 다양한 전략을 사용하여 예컨대 직접적으로 환 원자를 통해 모 분자에 부착될 수 있고, 다중 환 원자를 통해, 치환체 그룹을 통해 또는 이작용성 연결 모이어티를 통해 융합될 수 있다.
본원에서 사용된 바와 같이, "프로드럭"은 불활성 이하 활성 형태의 화합물을 의미하고, 이 화합물은, 대상체에 투여될 때, 대사작용되어 활성, 또는 더 많은 활성, 화합물 (예를 들면, 약물)을 형성한다.
본원에서 사용된 바와 같이, "치환체" 및 "치환체 그룹"은, 명명된 모 화합물의 원자 또는 그룹을 대체하는 원자 또는 그룹을 의미한다. 예를 들면 변형된 뉴클레오시드의 치환체는 자연 발생 뉴클레오시드에서 발견된 원자 또는 그룹과 상이한 임의의 원자 또는 그룹이다 (예를 들면, 변형된 2'-치환체는 H 또는 OH 이외의 뉴클레오시드의 2'-위치에 있는 임의의 원자 또는 그룹이다). 치환체 그룹은 보호 또는 비보호될 수 있다. 특정 구현예에서, 본 개시내용의 화합물은 모 화합물의 하나 또는 하나 초과의 위치에서 치환체를 갖는다. 치환체는 또한, 다른 치환체 그룹으로 추가로 치환될 수 있고 직접적으로 또는 연결 그룹 예컨대 알킬 또는 하이드로카르빌 그룹을 통해 모 화합물에 부착될 수 있다.
마찬가지로, 본원에서 사용된 바와 같이, 화학적 작용기에 관한 "치환체"는 명명된 작용기에 통상적으로 존재하는 원자 또는 원자의 그룹과 상이한 원자 또는 원자의 그룹을 의미한다. 특정 구현예에서, 치환체는 작용기의 수소 원자를 대체한다 (예를 들면, 특정 구현예에서, 치환된 메틸 그룹의 치환체는 비치환된 메틸 그룹의 수소 원자 중의 하나는 대체하는 수소 이외의 원자 또는 그룹이다). 달리 지적되지 않으면, 치환체로서 잘 받아들이는 그룹은 비제한적으로, 하기를 포함한다: 할로겐, 하이드록실, 알킬, 알케닐, 알키닐, 아실 (-C-(O)-Raa), 카복실 (-C(O)O-Raa), 지방족 그룹, 지환족 그룹, 알콕시, 치환된 옥시 (-O-Raa), 아릴, 아랄킬, 헤테로환식 라디칼, 헤테로아릴, 헤테로아릴알킬, 아미노 (-N(Rbb)-(Rcc)), 이미노(=NRbb), 아미도 (-C(O)N-(Rbb)(Rcc) 또는 -N(Rbb)C(O)Raa), 아지도 (-N3), 니트로 (-NO2), 시아노 (-CN), 카바미도 (-OC(O)N(Rbb)(Rcc) 또는 -N(Rbb)-C(O)-ORaa), 우레이도 (-N(Rbb)C(O)-N(Rbb)(Rcc)), 티오우레이도 (-N(Rbb)C-(S)N(Rbb)-(Rcc)), 구아니디닐 (-N(Rbb)-C(=NRbb)-N(Rbb)(Rcc)), 아미디닐 (-C(=NRbb)N(Rbb)(Rcc) 또는 -N(Rbb)C(=NRbb)(Raa)), 티올 (-SRbb), 설피닐 (-S(O)Rbb), 설포닐 (-S(O)2Rbb) 및 설폰아미딜 (-S(O)2N(Rbb)(Rcc) 또는 -N(Rbb)-S-(O)2Rbb. 여기서 각각의 Raa, Rbb 및 Rcc는, 독립적으로, H, 임의로 연결된 화학적 작용기 또는 추가 치환체 그룹이고, 바람직한 목록은 비제한적으로, 알킬, 알케닐, 알키닐, 지방족, 알콕시, 아실, 아릴, 아랄킬, 헤테로아릴, 지환족, 헤테로환식 및 헤테로아릴알킬을 포함한다. 본원에서 기재된 화합물 내의 선택된 치환체는 반복되는 정도로 존재한다.
본원에서 사용된 바와 같이, "알킬"은, 본원에서 사용된 바와 같이, 최대 24 개의 탄소 원자를 함유하는 포화된 직쇄형 또는 분지형 탄화수소 라디칼을 의미한다. 알킬 그룹의 예는 비제한적으로, 하기를 포함한다: 메틸, 에틸, 프로필, 부틸, 이소프로필, n-헥실, 옥틸, 데실, 도데실 등. 알킬기는 전형적으로 1 내지 약 24 개의 탄소 원자, 더욱 전형적으로 1 내지 약 12의 탄소 원자 (C1-C12 알킬)를 포함하고, 1 내지 약 6 개의 탄소 원자가 더 바람직하다.
본원에서 사용된 바와 같이, "알케닐"은, 최대 24 개의 탄소 원자를 함유하고 적어도 하나의 탄소-탄소 이중 결합을 갖는, 직쇄형 또는 분지형 탄화수소 사슬 라디칼을 의미한다. 알케닐 그룹의 예는 비제한적으로, 하기를 포함한다: 에테닐, 프로페닐, 부테닐, 1-메틸-2-부텐-1-일, 디엔 예컨대 1,3-부타디엔 등. 알케닐 그룹은 전형적으로 2 내지 약 24 개의 탄소 원자, 더욱 전형적으로 2 내지 약 12의 탄소 원자를 포함하고 2 내지 약 6 개의 탄소 원자가 더 바람직하다. 알케닐 그룹은, 본원에서 사용된 바와 같이, 1 이상의 추가 치환체 그룹을 임의로 포함할 수 있다.
본원에서 사용된 바와 같이, "알키닐"은, 최대 24 개의 탄소 원자를 함유하고 적어도 하나의 탄소-탄소 삼중결합을 갖는 직쇄형 또는 분지형 탄화수소 라디칼을 의미한다. 알키닐 그룹의 예는, 비제한적으로, 하기를 포함한다: 에티닐, 1-프로피닐, 1-부티닐, 등. 알키닐 그룹은 전형적으로 2 내지 약 24 개의 탄소 원자, 더욱 전형적으로 2 내지 약 12의 탄소 원자를 포함하고 2 내지 약 6 개의 탄소 원자가 더 바람직하다. 알키닐 그룹은, 본원에서 사용된 바와 같이, 1 이상의 추가 치환체 그룹을 임의로 포함할 수 있다.
본원에서 사용된 바와 같이, "아실"은, 유기산으로부터 하이드록실 그룹의 제거에 의해 형성될 라디칼을 의미하고 일반식 -C(O)-X (여기서 X은 전형적으로 지방족, 지환족 또는 방향족임)을 갖는다. 예들은 지방족 카보닐, 방향족 카보닐, 지방족 설포닐, 방향족 설피닐, 지방족 설피닐, 방향족 포스페이트, 지방족 포스페이트 등을 포함한다. 아실 그룹은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "지환족"은 환형 환계를 의미하고, 상기 환은 지방족이다. 환계는 1 이상의 환을 포함할 수 있고, 여기서 적어도 하나의 환은 지방족이다. 바람직한 지환족은 환 중 약 5 내지 약 9 개의 탄소 원자를 갖는 환을 포함한다. 지환족은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "지방족"은 최대 24 개의 탄소 원자를 함유하는 직쇄형 또는 분지형 탄화수소 라디칼을 의미하고, 상기 임의의 2 개의 탄소 원자 사이의 포화는 단일, 이중 또는 삼중결합이다. 지방족 그룹은 바람직하게는 1 내지 약 24 개의 탄소 원자, 더욱 전형적으로 1 내지 약 12의 탄소 원자를 함유하고, 1 내지 약 6 개의 탄소 원자가 더 바람직하다. 지방족 그룹의 직쇄형 또는 분지형 사슬은 질소, 산소, 황 및 인을 포함하는 1 이상의 헤테로원자로 방해될 수 있다. 헤테로원자에 의해 방해된 그와 같은 지방족 그룹은 비제한적으로, 폴리알콕시, 예컨대 폴리알킬렌 글리콜, 폴리아민, 및 폴리이민을 포함한다. 지방족 그룹은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "알콕시"는 알킬 그룹과 산소 원자 사이에 형셩된 라디칼을 의미하고, 상기 산소 원자는 알콕시 그룹을 모 분자에 부착하도록 사용된다. 알콕시 그룹의 예는 비제한적으로, 하기를 포함한다: 메톡시, 에톡시, 프로폭시, 이소프로폭시, n-부톡시, sec-부톡시, tert-부톡시, n-펜톡시, 네오펜톡시, n-헥소시 등. 알콕시 그룹은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "아미노알킬"은 아미노 치환된 C1-C12 알킬 라디칼을 의미한다. 라디칼의 알킬부는 모 분자와 공유 결합을 형성한다. 아미노 그룹은 임의의 위치에 있을 수 있고 아미노알킬 그룹은 알킬 및/또는 아미노 부분에서 추가 치환체 그룹으로 치환될 수 있다.
본원에서 사용된 바와 같이, "아랄킬" 및 "아릴알킬"은 C1-C12 알킬 라디칼에 공유 결합된 방향족 그룹을 의미한다. 수득한 아랄킬 (또는 아릴알킬) 그룹의 알킬 라디칼 부는 모 분자와 공유 결합을 형성한다. 예는 제한 없이, 벤질, 페네틸 등을 포함한다. 아랄킬 그룹은, 본원에서 사용된 바와 같이, 알킬, 아릴, 또는 라디칼 그룹을 형성하는 둘 모두 그룹에 부착된 추가 치환체 그룹을 임의로 포함한다.
본원에서 사용된 바와 같이, "아릴" 및 "방향족"은 1 이상의 방향족 환을 갖는, 단환 또는 다환식 탄소환식 환계 라디칼을 의미한다. 아릴 그룹의 예는 비제한적으로, 하기를 포함한다: 페닐, 나프틸, 테트라하이드로나프틸, 인다닐, 이데닐 등. 바람직한 아릴 환계는 1 이상의 환 중 약 5 내지 약 20 개의 탄소 원자를 갖는다. 아릴 그룹은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "할로" 및 "할로겐"은, 불소, 염소, 브롬 및 요오드로부터 선택된 원자를 의미한다.
본원에서 사용된 바와 같이, "헤테로아릴," 및 "헤테로방향족"은, 단일- 또는 다중-환형 방향족 환, 환계 또는 융합 환계를 포함하는 라디칼을 의미하고, 여기서 환 중 적어도 하나는 방향족이고 1 이상의 헤테로원자를 포함한다. 헤테로아릴은 또한, 융합 환 중 1 이상이 헤테로원자를 함유하지 않는 시스템을 포함하는 융합 환계를 포함하는 것을 의미한다. 헤테로아릴 그룹은 전형적으로, 황, 질소 또는 산소로부터 선택된 하나 이상의 환 원자를 포함한다. 헤테로아릴 그룹의 예는 비제한적으로, 하기를 포함한다: 피리디닐, 피라지닐, 피리미디닐, 피롤릴, 피라졸릴, 이미다졸릴, 티아졸릴, 옥사졸릴, 이속사졸릴, 티아디아졸릴, 옥사디아졸릴, 티오페닐, 푸라닐, 퀴놀리닐, 이소퀴놀리닐, 벤즈이미다졸릴, 벤조옥사졸릴, 퀴녹살리닐 등. 헤테로아릴 라디칼은 연결 모이어티 예컨대 지방족 그룹 또는 헤테로 원자를 통해 모 분자에 부착될 수 있다. 헤테로아릴 그룹은, 본원에서 사용된 바와 같이, 임의로 추가 치환체 그룹을 포함할 수 있다.
본원에서 사용된 바와 같이, "콘주게이트 화합물"은 임의의 원자, 원자의 그룹, 또는 콘주게이트 그룹으로서 사용하기에 적당한 연결된 원자의 그룹을 의미한다. 특정 구현예에서, 콘주게이트 화합물은 약동학적, 약력학적, 결합, 흡수, 세포성 분포, 세포성 흡수, 전하 및/또는 청소능 특성을 비제한적으로 포함하는 1 이상의 특성을 보유하거나 부여할 수 있다.
본원에서 사용된 바와 같이, 달리 지적되지 않으면 또는 변형된, 용어 "이중-가닥"은 서로 혼성화된 2 개의 별개의 올리고머 화합물을 의미한다. 그와 같은 이중가닥 화합물은 하나 또는 둘 모두 가닥 (오버행)의 하나 또는 둘 모두 말단에서 1 이상의 또는 비-혼성화 뉴클레오시드 및/또는 1 이상의 내부 비-혼성화 뉴클레오시드 (미스매치)를 가질 수 있고, 단, 생리적으로 관련된 조건 하에서 혼성화를 유지하기 위한 충분한 상보성이 있다.
본원에서 사용된 바와 같이, "2'-O-메톡시에틸" (또한 2'-MOE 및 2'-O(CH2)2-OCH3)은 푸로실 환의 2' 위치의 O-메톡시-에틸 변형을 나타낸다. 2'-O-메톡시에틸 변형된 당은 변형된 당이다.
본원에서 사용된 바와 같이, "2'-O-메톡시에틸 뉴클레오티드"는 2'-O-메톡시에틸 변형된 당 모이어티를 포함하는 뉴클레오티드를 의미한다.
"3' 표적 부위" 또는 "3' 정지 부위"는 특정한 안티센스 화합물의 3'-모스트 (most) 뉴클레오티드에 대해서 상보적인 표적 핵산의 뉴클레오티드를 나타낸다.
본원에서 사용된 바와 같이, "5' 표적 부위" 또는 "5 개시 부위"는 특정한 안티센스 화합물의 5'-모스트 (most) 뉴클레오티드에 대해서 상보적인 표적 핵산의 뉴클레오티드를 나타낸다.
본원에서 사용된 바와 같이, "5-메틸시토신"은 5' 위치에 부착된 메틸 기에 의해서 변형된 시토신을 의미한다. 5-메틸시토신은 변형된 핵염기이다.
본원에서 사용된 바와 같이, "약"은 값의 ±10% 내인 것을 의미한다. 예를 들어, "마커는 약 50% 만큼 증가될 수 있다"라고 언급된 경우에, 이것은 마커가 45%-55% 사이로 증가할 수 있음을 시사한다.
본원에서 사용된 바와 같이, "활성 약제학적 작용제"는 개체에게 투여하였을 때 치료학적 이점을 제공하는 약제학적 조성물의 물질 또는 물질들을 의미한다. 예를 들어, 특정 구현예에서는 ANGPTL3에 대해 표적화된 안티센스 올리고뉴클레오티드가 활성 약제학적 작용제이다.
본원에서 사용된 바와 같이, "활성 표적 영역" 또는 "표적 영역"은 하나 이상의 활성 안티센스 화합물이 표적화된 영역을 의미한다.
본원에서 사용된 바와 같이, "활성 안티센스 화합물"은 표적 핵산 수준 또는 단백질 수준을 감소시키는 안티센스 화합물을 의미한다.
본원에서 사용된 바와 같이, "지방생성(adipogenesis)"은 지방전구세포로부터 지방 세포의 발달을 의미한다. "지질생성"은 지방의 생산 또는 형성, 또는 지방 변성 또는 지방 침윤을 의미한다.
본원에서 사용된 바와 같이, "지방과다" 또는 "비만"은 비만인 상태, 또는 무지방 체질량 (lean body mass)과 관련하여 과도하게 많은 양의 체지방 또는 지방 조직을 나타낸다. 체지방의 양은 신체 전체에 걸친 지방의 분포 및 지방 조직 침착물의 크기 및 질량 둘 다에 대한 관심을 포함한다. 체지방 분포는 피부-접힘 (skin-fold) 척도, 허리 엉덩이 둘레율, 또는 초음파, 전산화 단층촬영법, 또는 자기 공명 영상과 같은 기술에 의해서 추정될 수 있다. 질환 제어 및 예방 센터(the Center for Disease Control and Prevention)에 따르면, 30 또는 그 이상의 체질량 지수 (BMI)를 갖는 개체는 비만인 것으로 간주된다. 본 명세서에서 사용된 것으로서 용어 "비만"은 신체 내에서 지방 조직의 과도한 축적의 결과로 물리적 필요성을 초과하는 체지방의 증가가 있는 상태를 포함한다. 용어 "비만"은 비제한적으로 하기 병태를 포함한다: 성인형 비만; 영양 비만; 내인성 또는 대사성 비만; 내분비 비만; 가족성 비만; 고인슐린 비만; 과형성-비대성 비만; 성기능저하 비만; 갑상선기능부전 비만; 평생 동안 비만; 병적 비만 및 외인성 비만.
본원에서 사용된 바와 같이, "동시에 투여된"은 둘 모두의 약리적 효과가 동시에 환자에서 나타나는 임의의 방식으로 2 종의 제제의 공-투여를 의미한다. 수반되는 투여는, 둘 제제가 단일 약제학적 조성물에서, 동일한 투여 형태로, 또는 동일한 투여 경로에 의해 투여되는 것을 요구하지는 않는다. 둘 제제 모두의 효과는 동시에 자체로 나타날 필요는 없다. 효과는 일정 기간 동안 단지 중첩될 필요는 있고 동일한 시(공)간에 걸칠 필요는 없다.
본원에서 사용된 바와 같이, "투여하는"은 제제를 동물에게 제공하는 것을 의미하며, 의료 전문가에 의한 투여 및 자가-투여를 포함하지만 이들로 제한되지는 않는다.
본원에서 사용된 바와 같이, "제제"는 포유동물에게 투여될 때 치료적 이점을 제공할 수 있는 활성 물질을 의미한다. "제1 제제"는 본 발명의 치료학적 화합물을 의미한다. 예를 들어, 제1 제제는 ANGPTL3를 표적으로 한 안티센스 올리고뉴클레오티드일 수 있다. "제2 제제"는 본 발명의 제2 치료학적 화합물 (예를 들어, ANGPTL3을 표적으로 하는 제2 안티센스 올리고뉴클레오티드) 및/또는 비-ANGPTL3 치료학적 화합물을 의미한다.
본원에서 사용된 바와 같이, "개선"은 연관된 질환, 장애 또는 병태의 적어도 하나의 지표, 징후 또는 증상을 약화시키는 것을 나타낸다. 표지자의 중증도는 당해분야의 숙련가에게 공지된 주관적 또는 객관적인 방안에 의해 결정될 수 있다.
"ANGPTL3"은 ANGPTL3의 임의의 핵산 또는 단백질을 의미한다.
"ANGPTL3 발현"은 ANGPTL3을 암호화한 유전자로부터 전사된 mRNA의 수준 또는 mRNA로부터 번역된 단백질의 수준을 의미한다. ANGPTL3 발현은 노던 또는 웨스턴 블럿과 같은 본 기술분야에서 공지된 방법에 의해서 측정될 수 있다.
본원에서 사용된 바와 같이, “ANGPTL3 핵산"은 ANGPTL3를 암호화하는 임의 핵산을 의미한다. 예를 들어, 특정 구현예에서, ANGPTL3 핵산은 ANGPTL3을 암호화한 DNA 서열, ANGPTL3을 암호화한 DNA (인트론 및 엑손을 포함하는 게놈 DNA를 포함)로부터 전사된 RNA 서열, 및 ANGPTL3을 암호화한 mRNA 서열을 포함한다. "ANGPTL3 mRNA"는 ANGPTL3 단백질을 암호화한 mRNA를 의미한다.
본원에서 사용된 바와 같이, "동물"은 인간 또는 비-인간 동물을 의미하고, 이 동물은, 비제한적으로, 마우스, 래트, 토끼, 개, 고양이, 돼지, 및 원숭이 및 침팬지를 비제한적으로 포함하는 비-인간 영장류를 포함한다.
본원에서 사용된 바와 같이, “apoB-함유 지질단백질"은, 이의 단백질 성분으로서의 아포지질단백질 B을 갖는 임의의 지질단백질을 의미하고, LDL, VLDL, IDL, 및 지질단백질(a)을 포함하는 것으로 이해되며, 지질 저하제 및 요법에 의하여 일반적으로 표적화될 수 있다. "ApoB-100-함유 LDL"은 LDL을 함유하는 ApoB-100 동형체를 의미한다.
본원에서 사용된 바와 같이, "죽상동맥경화증"은, 큰 및 중간-크기의 동맥에 영향을 미치는 동맥의 경화가 지방 축적의 존재를 특징으로 한다는 것을 의미한다. 지방 축적은 "죽종" 또는 "플라크"로 불리고, 이것은 콜레스테롤 및 다른 지방, 칼슘 및 반흔 조직으로 주로 구성되고, 동맥의 라이닝을 손상시킨다.
본원에서 사용된 바와 같이, "심대사성 질환" 또는 "심대사성 장애"은 심혈관계 및 대사계 둘 다에 관한 질환 또는 장애이다. 심대사성 질환 또는 장애는, 비제한적으로, 당뇨병 및 이상지질혈증을 포함한다.
본원에서 사용된 바와 같이, “공-투여"는 개체에게 두 개 이상의 제제를 투여하는 것을 의미한다. 두 개 이상의 제제는 단일 약제학적 조성물 내에 존재할 수 있거나, 별개의 약제학적 조성물 내에 존재할 수 있다. 두 개 이상의 제제 각각은 동일하거나 상이한 투여 경로를 통해서 투여될 수 있다. 공-투여는 병행 또는 순차적 투여를 포함한다.
본원에서 사용된 바와 같이, "콜레스테롤"은 모든 동물 조직의 세포막에서 발견되는 스테롤 분자이다. 콜레스테롤은 반드시 초저밀도 지방단백질 (VLDL), 중간 밀도 지방단백질 (IDL), 저밀도 지방단백질 (LDL), 및 고밀도 지방단백질 (HDL)을 포함한 지방단백질에 의해서 동물의 혈장 내로 수송되어야 한다. "혈장 콜레스테롤"은 혈장 또는 혈청 내에 존재하는 모든 지방단백질 (VDL, IDL, LDL, HDL) 에스테르화 및/또는 비-에스테르화된(non-estrified) 콜레스테롤의 합계를 나타낸다.
본원에서 사용된 바와 같이, "콜레스테롤 흡수 억제제" 식이로부터 수득된 외인성 콜레스테롤의 흡수를 억제하는 제제이다.
본원에서 사용된 바와 같이, "관상동맥 심장병 (CHD)"는, 종종 죽상동맥경화증의 결과인, 혈액 및 산소를 심장에 공급하는 작은 혈관의 협소화를 의미한다.
본원에서 사용된 바와 같이, "진성 당뇨병" 또는 "당뇨병"은 무질서한 대사 및 불충분한 수준의 인슐린 또는 감소된 인슐린 민감도로부터 야기된 비정상적인 고혈당 (고혈당증)을 특징으로 하는 증후군을 의미한다. 특징적인 증상은 고혈당 수준으로 인한 과도한 소변 생산 (다뇨증), 증가된 배뇨를 보충하려고 하는 과도한 갈증 및 증가된 유액 섭취 (조갈증), 눈의 광학에 대한 고혈당 영향으로 인한 흐릿한 시력, 원인불명 체중 감소, 및 무기력이다.
본원에서 사용된 바와 같이, "당뇨병성 이상지질혈증" 또는 "이상지질혈증을 갖는 2형 당뇨병"은 2형 당뇨병, 감소된 HDL-C, 상승된 트리글리세라이드, 및 상승된 작은, 조밀한 LDL 입자를 특징으로 하는 병태를 의미한다.
본원에서 사용된 바와 같이, "희석제"는 약리적 활성은 없지만 약제학적으로 필요한 또는 바람직한 조성물 중 성분을 의미한다. 예를 들면, 주입된 조성물 중 희석제는 액체, 예를 들면 염수 용액일 수 있다.
본원에서 사용된 바와 같이, "이상지질혈증"은 지질 및/또는 지질단백질 과잉생산 또는 결핍을 포함하는, 지질 및/또는 지질단백질 대사의 장애를 의미한다. 이상지질혈증은 콜레스테롤 및 트리글리세라이드 뿐만 아니라 저-밀도 지방단백질 (LDL) 콜레스테롤과 같은 지방단백질의 상승으로 나타날 수 있다.
본원에서 사용된 바와 같이, "투여량 단위"는 약제가 제공된 형태, 예를 들면 알약, 정제, 또는 당해기술에서 공지된 다른 투여량 단위를 의미한다. 특정 구현예에서, 투여량 단위는 동결건조된 안티센스 올리고뉴클레오티드를 함유하는 바이알이다. 특정 구현예에서, 투여량 단위는 재구성된 안티센스 올리고뉴클레오티드을 함유하는 바이알이다.
본원에서 사용된 바와 같이, "투여(dose)"는 단일 투여로, 또는 명시된 기간 내에 제공된 약제의 명시된 양을 의미한다. 특정 구현예에서, 투여량은 1, 2, 또는 초과의 볼러스, 정제, 또는 주사로 투여될 수 있다. 예를 들면, 특정 구현예에서 피하 투여를 원하면, 원하는 투여량은 단일 주사에 의해 쉽게 수용되지 않는 용적을 필요로 하고, 따라서, 2 이상의 주사가 사용되어 원하는 투여량을 달성할 수 있다. 특정 구현예에서, 약제는 장시간에 걸쳐 또는 연속적으로 주입에 의해 투여된다. 투여량은 시간, 일, 주, 또는 개월 당 약제의 양으로서 언급될 수 있다. 투여량은 mg/kg 또는 g/kg으로 표현될 수 있다.
본원에서 사용된 바와 같이, "효과적인 양" 또는 "치료적으로 효과적인 양"은 제제가 필요한 개체에서 원하는 생리적 결과를 유발하는데 충분한 활성 약제의 양을 의미한다. 유효량은 치료될 개체의 건강 및 신체 조건, 치료될 개체의 분류군, 조성물의 제형, 개체의 의학적 상태의 평가, 및 그 밖의 다른 관련된 인자에 따라 개체들 사이에서 달라질 수 있다.
본원에서 사용된 바와 같이, "글루코오스"는 에너지의 공급원 및 대사성 중간체로서 세포에 의해 사용된 단당류이다. "혈장 글루코스"는 혈장에 존재하는 글루코오스를 의미한다.
본원에서 사용된 바와 같이, "고밀도 지질단백질-C" 또는 "HDL-C"는 고밀도 지질단백질 입자와 연관된 콜레스테롤을 의미한다. 혈청 (또는 혈장) 중 HDL-C의 농도는 전형적으로 mg/dL 또는 nmol/L로 정량화된다. "혈청 HDL-C" 및 "혈장 HDL-C"는 혈청 및 혈장 각각에서 HDL-C를 의미한다.
본원에서 사용된 바와 같이, "HMG-CoA 환원효소 억제제"는 효소 HMG-CoA 환원효소의 억제를 통해 작용하는 제제, 예컨대 아토르바스타틴, 로수바스타틴, 플루바스타틴, 로바스타틴, 프라바스타틴, 및 심바스타틴을 의미한다.
본원에서 사용된 바와 같이, "고콜레스테롤혈증"은 하기의 지침에 따라, 상승된 콜레스테롤 또는 순환 (혈장) 콜레스테롤, LDL-콜레스테롤 및 VLDL-콜레스테롤을 특징으로 하는 병태를 의미한다: the Expert Panel Report of the National Cholesterol Educational Program (NCEP) of Detection, Evaluation of Treatment of high cholesterol in adults (참고: Arch. Int. Med. (1988) 148, 36-39).
본원에서 사용된 바와 같이, "고지혈증" 또는 "고지방혈증"은 상승된 혈청 지질 또는 순환 (혈장) 지질을 특징으로 하는 병태이다. 이러한 병태는 비정상적으로 고농도인 지방을 나타낸다. 순환 혈액 내의 지질 분획은 콜레스테롤, 저밀도 지방단백질, 초저밀도 지방단백질 및 트리글리세라이드이다.
본원에서 사용된 바와 같이, "초고트리글리세라이드혈증"은 상승된 트리글리세라이드 수준을 특징으로 하는 병태를 의미한다.
본원에서 사용된 바와 같이, "동정하는 것" 또는 "대사성 또는 심혈관 질환을 갖는 대상체를 선택하는 것"은 대사 질환, 심혈관 질환, 또는 대사성 질환으로 진단된 대상체를 동정 또는 선택하거나, 대사 질환, 심혈관 질환, 또는 대사 증후군, 예컨대 비제한적으로 고콜레스테롤혈증, 고혈당증, 고지혈증, 고트리글리세라이드혈증, 고혈압, 증가된 인슐린 내성, 감소된 인슐린 민감성, 정상 체중 초과, 및/또는 정상 체지방 함량 초과 또는 이들의 특정 조합의 임의의 증후군을 갖는 대상체를 동정 또는 선택하는 것을 의미한다. 이러한 동정은 혈청 또는 순환 (혈장) 혈액-글루코스의 측정, 혈청 또는 순환 (혈장) 트리글리세라이드의 측정, 혈압의 측정, 체지방 함량의 측정, 체중의 측정 등과 같은 표준 임상 시험 또는 평가를 포함하는 (단, 이들로 제한되지는 않는다) 특정 방법에 의해서라도 달성될 수 있다.
본원에서 사용된 바와 같이, "동정하는 것" 또는 "당뇨병성 대상체를 선택하는 것"은 당뇨병성으로 동정된 대상체를 동정 또는 선택하는 것, 또는 예컨대, 비제한적으로, 적어도 110 mg/dL의 공복 혈당, 당뇨, 다뇨증, 조갈증, 증가된 인슐린 내성, 및/또는 감소된 인슐린 민감성을 갖는 임의의 증상의 당뇨병 (1형 또는 2형)을 갖는 대상체를 동정 또는 선택하는 것을 의미한다.
본원에서 사용된 바와 같이, "동정하는 것" 또는 "비만 대상체를 선택하는 것"은, 비만으로 동정된 대상체를 동정 또는 선택하는 것, 또는 30 초과의 BMI, 및/또는 남성에서 102 cm 초과의 허리둘레, 또는 여성에서 88 cm 초과의 허리둘레를 갖는 대상체를 동정 또는 선택하는 것을 의미한다.
본원에서 사용된 바와 같이, "동정하는 것" 또는 "이상지질혈증 대상체를 선택하는 것"은, 지질 및/또는 지질단백질 대사 장애 (지질 및/또는 지질단백질 과잉생산 또는 결핍 포함)으로 동정된 대상체를 동정 또는 선택하는 것을 포함한다. 이상지질혈증은 콜레스테롤 및 트리글리세라이드 뿐만 아니라 저-밀도 지방단백질 (LDL) 콜레스테롤과 같은 지방단백질의 상승으로 나타날 수 있다.
본원에서 사용된 바와 같이, 증가된 지방과다를 갖는 대상체를 "동정하는 것" 또는 "선택하는 것"은, 신체 전체의 지방 분포 및 지방질 조직 침전물의 크기 및 질량에 대한 우려를 포함하는 체내 지방 (또는 지방과다)의 증가된 양을 갖는 대상체를 동정 또는 선택하는 것을 의미한다. 체지방 분포는 피부-접힘 (skin-fold) 척도, 허리 엉덩이 둘레율, 또는 초음파, 전산화 단층촬영법, 또는 자기 공명 영상과 같은 기술에 의해서 추정될 수 있다. 질환 제어 및 예방 센터(the Center for Disease Control and Prevention)에 따르면, 30 또는 그 이상의 체질량 지수 (BMI)를 갖는 개체는 비만인 것으로 간주된다.
본원에서 사용된 바와 같이, "개선된 심혈관 결과"는 부정적인 심혈관 사건의 발생, 또는 그것의 위험의 감소를 의미한다. 부정적인 심혈관 사건의 예는, 비제한적으로, 사망, 재경색, 뇌졸중, 심장성 충격, 폐 부종, 심장정지, 및 심방 율동부정을 포함한다.
본원에서 사용된 바와 같이, "바로 인접한"은 바로 인접한 요소들 사이에 개입성 요소가 없는 것을 의미한다.
본원에서 사용된 바와 같이, "개체" 또는 "대상체" 또는 "동물"은 치료 또는 요법에 대해 선택된 인간 또는 비-인간 동물을 의미한다.
본원에서 사용된 바와 같이, "인슐린 내성"은 정상적인 양의 인슐린이 세포, 예컨대 지방, 근육 및/또는 간 세포로부터 정상 인슐린 반응을 생산하는데 부적절한 상태로서 규정된다. 지장 세포에서의 인슐린 내성은 보관된 트리글리세라이드의 가수분해를 야기하고, 이것은 혈장에서 유리 지방산을 상승시킨다. 근육 중 인슐린 내성은 글루코오스 흡수를 감소시키고, 반면에 간에서의 인슐린 내성은 글루코오스 저장을 감소시키고, 이들 둘 모두의 효과는 혈당을 상승시키는데 기여한다. 인슐린 내성으로 인한 높은 혈장 수준의 인슐린 및 글루코오스는 종종 대사성 증후군 및 2형 당뇨병을 초래한다.
본원에서 사용된 바와 같이, "인슐린 민감도"는 개체가 어떻게 글루코오스를 효과적으로 처리하는 지에 대한 측정이다. 높은 인슐린 민감도를 갖는 개체는 효과적으로 글루코오스를 처리하고 반면에 낮은 인슐린 민감도를 갖는 개체는 효과적으로 글루코오스를 처리하지 못한다.
본원에서 사용된 바와 같이, "정맥내 투여"는 정맥 내로의 투여를 의미한다.
본원에서 사용된 바와 같이, "지질-저하"는 대상체에서 1 이상의 지질의 감소를 의미한다. 지질-저하는 경시적으로 하나 이상의 투여량과 함께 발생할 수 있다.
본원에서 사용된 바와 같이, "지질-저하제"는, 대상체 내의 지질 저하를 달성하기 위하여 대상체에 제공된 제제, 예를 들면, ANGPTL3-특이적 조절물질을 의미한다. 예를 들어, 특정 구현예에서, 지질-저하 제제는 대상체에서 apoB, apoC-Ⅲ, 총 콜레스테롤, LDL-C, VLDL-C, IDL-C, 비-HDL-C, 트리글리세라이드, 소형의 밀집된 LDL 입자, 및 Lp(a) 중의 하나 이상을 감소시키기 위해서 제공된다.
본원에서 사용된 바와 같이, "지질-저하 요법"은 대상체에서 하나 이상의 지질을 감소시키기 위해서 대상체에게 제공된 치료학적 레지멘을 의미한다. 특정 구현예에서, 지질-저하 요법은 대상체에서 apoB, apoC-Ⅲ, 총 콜레스테롤, LDL-C, VLDL-C, IDL-C, 비-HDL-C, 트리글리세라이드, 소형의 밀집된 LDL 입자, 및 Lp(a) 중의 하나 이상을 감소시키기 위해서 제공된다.
본원에서 사용된 바와 같이, "지질단백질", 예컨대 VLDL, LDL 및 HDL은, 혈청, 혈장 및 림프에서 발견되는 단백질의 그룹을 의미하고 지질 수송을 위해 중요하다. 각 지질단백질의 화학 조성은 HDL이 보다 높은 비율의 지질에 대한 단백질을 갖고, 반면 VLDL은 보다 낮은 비율의 지질에 대한 단백질을 갖는다는 점에서 상이하다.
본원에서 사용된 바와 같이, "저밀도 지질단백질-콜레스테롤 (LDL-C)"는 저밀도 지질단백질 입자에서 운반된 콜레스테롤을 의미한다. 혈청 (또는 혈장)에서의 LDL-C의 농도는 전형적으로 mg/dL 또는 nmol/L로 정량화된다. "혈청 LDL-C" 및 "혈장 LDL-C"는 혈청 및 혈장 각각에서 LDL-C를 의미한다.
본원에서 사용된 바와 같이, "주요 위험 인자"는 특정한 질환 또는 병태에 대한 고위험에 기여하는 인자를 의미한다. 특정 구현예에서, 관상동맥 심장 질환에 대한 주요 위험 인자에는 비제한적으로, 담배 흡연, 고혈압, 낮은 HDL-C, 관상동맥 심장 질환의 가족력, 연령, 및 본 명세서에 개시된 다른 인자가 포함된다.
본원에서 사용된 바와 같이, "대사성 장애" 또는 "대사성 질환"은 대사성 기능의 변경 또는 방해를 특징으로 하는 병태를 의미한다. "대사성" 및 "대사"는 당해기술에서 잘 알려진 용어들이고 일반적으로 살아있는 유기체 내에서 일어나는 생화학적 과정의 전체 범위를 포함한다. 대사성 장애는, 비제한적으로, 고혈당증, 전당뇨병, 당뇨병 (I형 및 2형), 비만, 인슐린 내성, 대사성 증후군 및 2형 당뇨병에 기인한 이상지질혈증을 포함한다.
본원에서 사용된 바와 같이, "대사성 증후군"은 대상 기원의 지질 및 비-지질 심혈관 위험 인자의 군집화를 특징으로 하는 병태를 의미한다. 특정 구현예에서, 대사성 증후군은 하기 인자 중 임의의 3 개에 의해 확인된다: 남성 102 cm 초과 또는 여성 88 cm 초과의 허리 둘레; 적어도 150 mg/dL의 혈청 트리글리세라이드; 남성에서는 40 mg/dL 또는 여성에서는 50 mg/dL 미만의 HDL-C; 적어도 130/85 mmHg의 혈압; 및 적어도 110 mg/dL의 공복 혈당. 이들 결정요인은 임상 실시예서 쉽게 측정될 수 있다 (JAMA, 2001, 285: 2486-2497).
본원에서 사용된 바와 같이, "혼합된 이상지질혈증"은 상승된 콜레스테롤 및 상승된 트리글리세라이드를 특징으로 하는 병태를 의미한다.
본원에서 사용된 바와 같이, "MTP 억제제" 효소 마이크로솜 트리글리세라이드 전이 단백질을 억제하는 제제를 의미한다.
본원에서 사용된 바와 같이, "비-알코올성 지방간 질환" 또는 "NAFLD"는 과도한 알코올 사용 (예를 들어, 20 g/일 이상의 알코올 소비)에 기인하지 않는 간의 지방성 염증을 특징으로 하는 병태를 의미한다. 특정 구현예에서, NAFLD는 인슐린 내성 및 대사 증후군과 관련된다. NAFLD는 간세포에서의 단순 트리글리세라이드 축적 (간 지방증)으로부터 염증 (지방간염), 섬유증, 및 경화증이 있는 간 지방증까지의 범위의 질환 스펙트럼을 포함한다.
본원에서 사용된 바와 같이, "비-알코올성 지방간염" (NASH)은 트리글리세라이드의 침착을 넘어서는 NAFLD의 진행으로부터 일어난다. 괴사, 염증 및 섬유증을 유도할 수 있는 "제2 히트 (second hit)"가 NASH의 진화에 필요하다. 제2-히트의 후보는 광범한 카테고리로 그룹화될 수 있다: 산화적 스트레스를 야기하는 인자 및 전염증성 사이토킨의 발현을 촉진시키는 인자. 증가된 간 트리글리세라이드은 동물 및 인간의 간세포 내 증가된 산화적 스트레스를 야기하고, 이는 간 트리글리세라이드 축적, 산화적 스트레스, 및 NASH에 대한 간 지방증의 진행 사이의 잠재적인 인과 및 효과 관계를 지시한다 (Browning and Horton, J Clin Invest, 2004, 114, 147-152). 초고트리글리세라이드혈증 및 과지방산혈증은 말초 조직 내 트리글리세라이드 축적을 야기할 수 있다 (Shimamura et al., Biochem Biophys Res Commun, 2004, 322, 1080-1085).
본원에서 사용된 바와 같이, "핵산"은 단량체 뉴클레오티드로 구성된 분자를 의미한다. 핵산에는 리보핵산 (RNA), 데옥시리보핵산 (DNA), 단일-가닥 핵산, 이중-가닥 핵산, 소형 개입성 리보핵산 (siRNA), 및 마이크로RNA (miRNA)가 포함된다. 핵산은 또한 단일 분자 내에 이들 요소의 조합을 포함할 수도 있다.
본원에서 사용된 바와 같이, “비경구 투여"는 소화관을 통한 것 이외의 방식에 의한 투여를 의미한다. 비경구 투여는 국소 투여, 피하 투여, 정맥내 투여, 근육내 투여, 동맥내 투여, 복강내 투여, 또는 두개내 투여, 예를 들면 척추강내 또는 뇌심실내 투여를 포함한다. 투여는 연속적이거나, 만성적이거나, 단기간이거나 간헐적일 수 있다.
본원에서 사용된 바와 같이, "약제"는 개체에게 투여될 때 치료적 이점을 제공하는 물질을 의미한다. 예를 들어, 특정 구현예에서, ANGPTL3에 대해서 표적화된 안티센스 올리고뉴클레오티드가 약제학적 작용제이다.
본원에서 사용된 바와 같이, "약제학적 조성물"은 개체에게 투여하기에 적합한 물질의 혼합물을 의미한다. 예를 들어, 약제학적 조성물은 하나 이상의 활성 작용제 및 멸균 수용액을 포함할 수 있다.
본원에서 사용된 바와 같이, "약제학적으로 허용가능한 담체"는 올리고뉴클레오티드의 구조 또는 기능을 저해하지 않는 매질 또는 희석제를 의미한다. 이러한 담체 중의 특정 것은 약제학적 조성물을 예를 들어, 대상체에 의한 경구 섭취를 위한 정제, 환제, 당의정, 캅셀제, 액체, 겔, 시럽, 슬러리, 현탁제 및 로젠지로 제형화되도록 할 수 있다. 그와 같은 특정 담체는 약제학적 조성물로 하여금 주사 또는 주입을 위하여 제형화되게 한다. 예를 들어, 약제학적으로 허용가능한 담체는 멸균 수용액일 수 있다.
본원에서 사용된 바와 같이, "약제학적으로 허용가능한 염"은 안티센스 올리고뉴클레오티드의 생리적으로 및 약제학적으로 허용가능한 염, 즉, 모 화합물의 원하는 생물학적 활성을 유지하고 원하지 않는 독물학적 효과를 그것에 부여하지 않는 염을 의미한다.
본원에서 사용된 바와 같이, "부분"은 핵산의 인접 (즉 연결된) 핵염기의 규정된 수를 의미한다. 특정 구현예에서, 구분은 표적 핵산의 인접 핵염기의 규정된 수이다. 특정 구현예에서, 부분은 안티센스 화합물의 인접 핵염기의 규정된 수를 의미한다.
본원에서 사용된 바와 같이, "예방한다"는 극히 작은 시간으로부터 규정되지 않은 시간 동안 질환, 장애, 또는 병태의 개시 또는 발달을 지연 또는 예방하는 것을 의미한다. 예방한다란 또한 질환, 장애, 또는 병태를 발달시킬 위험을 감소시킨다는 것을 의미한다.
본원에서 사용된 바와 같이, "부작용"은 원하는 효과 이외에 치료에 기인하는 생리적 반응을 의미한다. 특정 구현예에서, 부작용은 주사 부위 반응, 간 기능 시험 이상, 신장 기능 이상, 간독성, 신장 독성, 중추신경계 이상, 근병증, 및 권태감을 포함한다. 예를 들어, 혈청 내의 증가된 아미노트랜스페라제 수준은 간독성 또는 간 기능 이상을 나타낼 수 있다. 예를 들어, 증가된 빌리루빈은 간독성 또는 간 기능 이상을 나타낼 수 있다.
본원에서 사용된 바와 같이, "스타틴"은 HMG-CoA 환원효소의 활성을 억제하는 제제를 의미한다.
본원에서 사용된 바와 같이, "피하 투여"는 피부 바로 하기의 투여를 의미한다.
본원에서 사용된 바와 같이, "표적으로 하는" 또는 "표적화된"은 표적 핵산에 특이적으로 혼성화하고 원하는 효과를 유도하는 안티센스 화합물의 설계 및 선택의 과정을 의미한다.
본원에서 사용된 바와 같이, "표적 핵산", "표적 RNA", 및 "표적 RNA 전사체"는 모두 안티센스 화합물에 의해서 표적화될 수 있는 핵산을 나타낸다.
본원에서 사용된 바와 같이, "표적 영역"은 적어도 하나의 확인가능한 구조, 기능, 또는 특징을 갖는 표적 핵산의 부분으로서 규정된다.
본원에서 사용된 바와 같이, "표적 분절"은 하나 이상의 안티센스 화합물이 표적화된 표적 핵산의 뉴클레오티드의 서열을 의미한다. "5'표적 부위" 또는 "5'개시 부위"는 표적 분절의 5'-모스트 뉴클레오티드를 지칭한다. "3'표적 부위" 또는 "3'정지 부위"는 표적 분절의 3'-모스트 뉴클레오티드를 지칭한다.
본원에서 사용된 바와 같이, "치료적으로 효과적인 양"은 치료적 이점을 개체에게 제공하는 제제의 양을 의미한다.
본원에서 사용된 바와 같이, "치료적 생활방식 변화"는 낮은 지방/지방 조직 질량 및/또는 콜레스테롤에 대해 의도된 식이 및 생활방식 변화를 의미한다. 이러한 변화는 심장 질환이 발생할 위험을 감소시킬 수 있으며, 총 1일 칼로리, 총 지방, 포화 지방, 다중불포화 지방, 단일불포화 지방, 탄수화물, 단백질, 콜레스테롤, 불용성 섬유의 식이성 섭취에 대한 추천뿐만 아니라 신체 활동에 대한 추천을 포함한다.
본원에서 사용된 바와 같이, "트리글리세라이드"는 3 개의 지방산 분자와 조합된 글리세롤로 이루어진 지질 또는 중성 지방을 의미한다.
본원에서 사용된 바와 같이, "제2형 당뇨병" (또한, "제2형 진성 당뇨병" 또는 "진성 당뇨병, 제2형"으로 공지되며, 이전에는 "진성 당뇨병 제2형", "비-인슐린-의존성 당뇨병 (NIDDM)", "비만 관련된 당뇨병", 또는 "성년-발병 당뇨병"으로 불림)은 주로 인슐린 내성, 상대적 인슐린 결핍, 및 고혈당증을 특징으로 하는 대사 장애이다.
본원에서 사용된 바와 같이, "치료하다"는 질환, 장애 또는 병태의 변경 또는 개선을 달성하기 위해서 동물에게 약제학적 조성물을 투여하는 것을 나타낸다.
특정 구현예
특정 구현예에서, ANGPTL3는 유전자은행 수탁 번호 NM_014495.2 (서열번호: 1과 같이 본원에 포함)에 제시된 서열을 갖는다. 특정 구현예에서, ANGPTL3는 유전자은행 수탁 번호 NT_032977.9 뉴클레오티드 33032001 내지 33046000 (본원에서 서열번호: 2와 같이 포함)에 제시된 서열을 갖는다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고, 서열번호: 1-2의 동등 길이 부분에 상보적인 적어도 8개의 인접 핵염기를 포함한다.
특정 구현예에서, 본 화합물은 당해기술에서 공지된 ANGPTL3에 대해 표적화된 siRNA 또는 안티센스 올리고뉴클레오티드 및 본원에서 기재된 콘주게이트 그룹을 포함한다. 콘주게이션에 적당한 ANGPTL3에 대해 표적화된 안티센스 올리고뉴클레오티드의 예는 하기에서 개시된 것들을 비제한적으로 포함한다: US 8,653,047 (WO 2011/085271), 이것은 그 전체가 참고로 본원에 편입되어 있다. 특정 구현예에서, 본 화합물은 서열번호: 34-111 중 임의의 것의 핵염기 서열을 갖는 안티센스 올리고뉴클레오티드 (US 8,653,047 에 개시됨) 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 본 화합물은 서열번호: 34-111 중 임의의 것의 핵염기 서열을 갖는 siRNA 센스 또는 안티센스 가닥 (US 8,653,047 에 개시됨) 및 콘주게이트 그룹을 포함한다. 모든 상기 언급된 참조된 서열번호의 핵염기 서열은 본원에 참고로 편입되어 있다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 ANGPTL3에 대해 표적화된 길이로 12 내지 30 개의 연결된 뉴클레오시드로 이루어진다. ANGPTL3 표적은 서열번호: 1-2 중 임의의 하나로부터 선택된 서열을 가질 수 있다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 1140 내지 1159의 동등 길이 부분과 상보적인 적어도 8개의 인접 핵염기의 부분을 포함하는 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다. 특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 1의 핵염기 1140 내지 1159의 동등 길이 부분에 상보적인 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20개의 인접 핵염기이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 1140 내지 1159에 상보적인 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 1907 내지 1926의 동등 길이 부분과 상보적인 적어도 8개의 인접 핵염기의 부분을 포함하는 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다. 특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 1의 핵염기 1907 내지 1926의 동등 길이 부분에 상보적인 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20개의 인접 핵염기이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 1907 내지 1926에 상보적인 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 147 내지 162의 동등 길이 부분과 상보적인 적어도 8개의 인접 핵염기의 부분을 포함하는 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다. 특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 1의 핵염기 147 내지 162의 동등 길이 부분에 상보적인 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 또는 적어도 16개의 인접 핵염기이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 서열번호: 1의 핵염기 147 내지 162에 상보적인 핵염기 서열을 포함하며, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1과 적어도 80% 상보적이다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 12 내지 30, 15 내지 30, 18 내지 24, 19 내지 22, 13 내지 25, 14 내지 25, 15 내지 25 또는 16 내지 24개의 연결된 뉴클레오시드로 구성된다. 특정 구현예에서, 변형된 올리고뉴클레오티드는 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 또는 30개의 연결된 뉴클레오시드 또는 이들 값들 중 임의의 2개로 정의된 범위로 구성된다. 특정 구현예에서, 변형된 올리고뉴클레오티드의 길이는 16개의 연결된 뉴클레오시드이다. 특정 구현예에서, 변형된 올리고뉴클레오티드의 길이는 20개의 연결된 뉴클레오시드이다.
변형된 올리고뉴클레오티드가 서열번호: 1 또는 2의 동등 길이 부분에 대해 상보성인 적어도 8개, 적어도 9개, 적어도 10개, 적어도 11개, 적어도 12개, 적어도 13개, 적어도 14개, 적어도 15개, 적어도 16개, 적어도 17개, 적어도 18개, 적어도 19개, 또는 적어도 20개의 인접 핵염기의 일부를 포함하는 핵염기 서열을 포함한다.
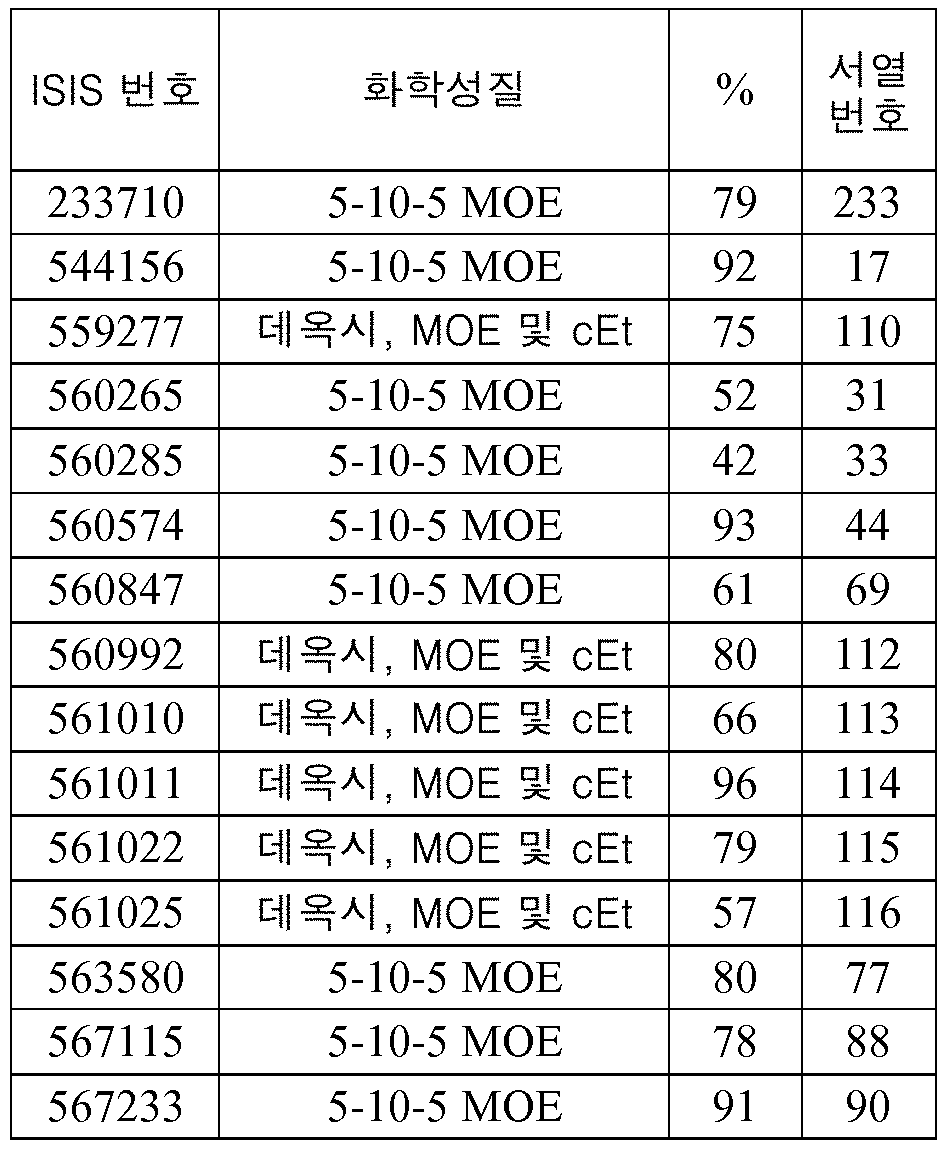
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지고 하기 서열번호 중 임의의 것으로부터 선택된 핵염기 서열의 적어도 8개, 적어도 9개, 적어도 10개, 적어도 11개, 적어도 12개, 적어도 13개, 적어도 14개, 적어도 15개, 적어도 16개, 적어도 17개, 적어도 18개, 적어도 19, 또는 20개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다: 15-27, 30-73, 75-85, 87-232, 238, 240-243, 245-247, 249-262, 264-397, 399-469, 471-541, 543-600, 604-760, 762-819, 821-966, 968-971, 973-975, 977-990, 992-1110, 1112-1186, 1188-1216, 1218-1226, 1228-1279, 1281-1293, 1295-1304, 1306-1943, 1945-1951, 1953-1977, 1979-1981, 1983-2044, 2046-2097, 2099-2181, 2183-2232, 2234-2238, 2240-2258, 2260-2265, 2267-2971, 2973-2976, 2978-4162, 4164-4329, 4331-4389, 4391-4394, 4396-4877.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 77의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 563580 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 563580 및 콘주게이트 그룹으로 이루어진다.
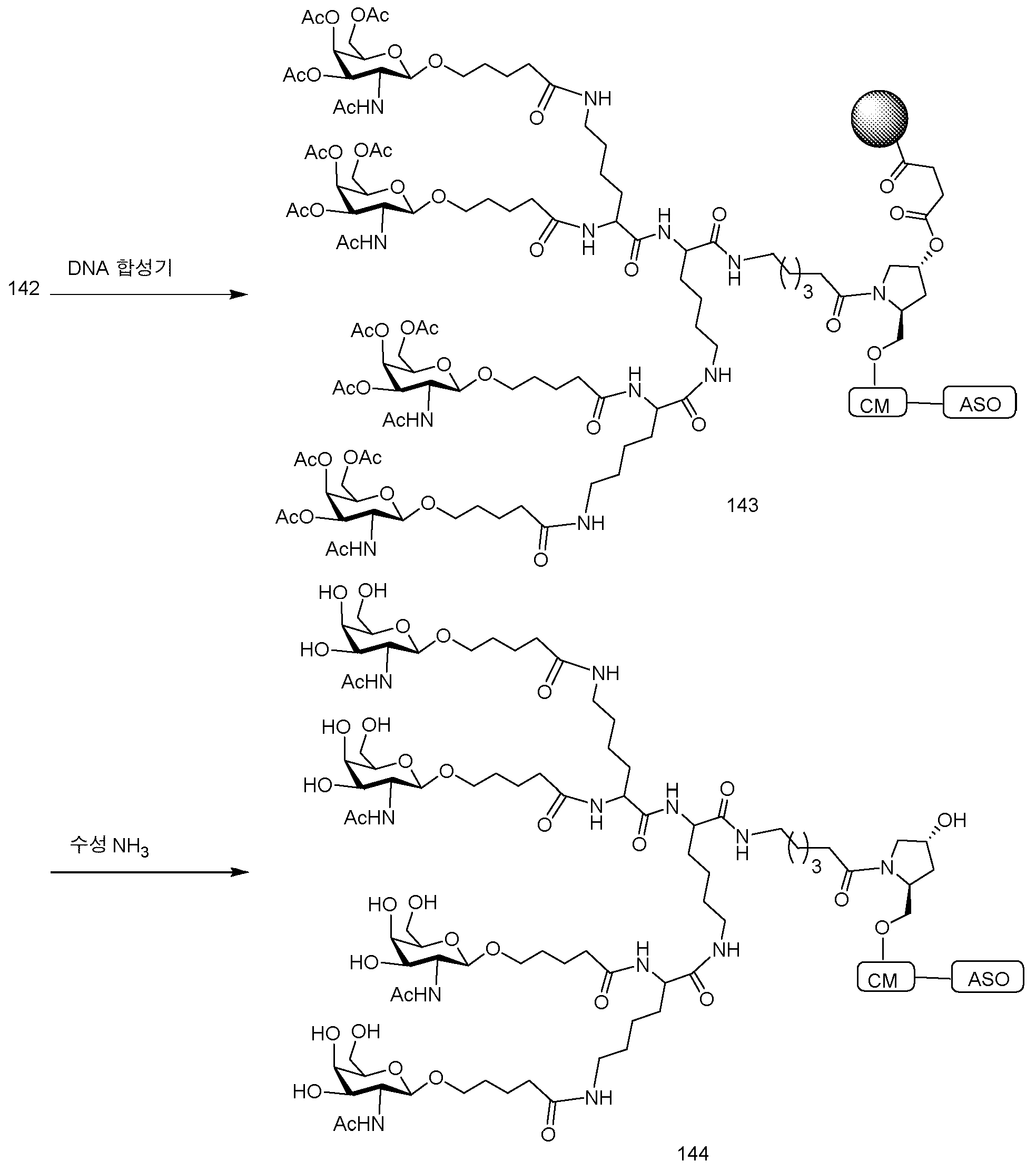
특정 구현예에서, 본 개시내용은 하기 구조로 나타낸 콘주게이트된 안티센스 화합물을 제공한다. 특정 구현예에서, 안티센스 화합물은 5'-X를 갖는 변형된 올리고뉴클레오티드 ISIS 563580를 포함하고, 여기서 X는 GalNAc를 포함하는 콘주게이트 그룹이다. 특정 구현예에서, 안티센스 화합물은 5'-X를 갖는 변형된 올리고뉴클레오티드 ISIS 563580로 구성되고, 여기서 X는 GalNAc를 포함하는 콘주게이트 그룹이다.
특정 구현예에서, 본 개시내용은 하기 구조로 나타낸 콘주게이트된 안티센스 화합물을 제공한다. 특정 구현예에서, 안티센스 화합물은 콘주게이트된 변형된 올리고뉴클레오티드 ISIS 703801을 포함한다. 특정 구현예에서, 안티센스 화합물은 콘주게이트된 변형된 올리고뉴클레오티드 ISIS 703801로 이루어진다.
특정 구현예에서, 본 개시내용은 하기 구조로 나타낸 콘주게이트된 안티센스 화합물을 제공한다. 특정 구현예에서, 안티센스 화합물은 콘주게이트된 변형된 올리고뉴클레오티드 ISIS 703802을 포함한다. 특정 구현예에서, 안티센스 화합물은 콘주게이트된 변형된 올리고뉴클레오티드 ISIS 703802로 이루어진다.
특정 구현예에서, 본 개시내용은 하기 구조로 나타낸 콘주게이트된 안티센스 화합물을 제공한다. 특정 구현예에서, 안티센스 화합물은 서열번호: 77의 핵염기 서열을 갖는 변형된 올리고뉴클레오티드를 포함하며, 이는 윙의 당 변형에서의 가변성을 갖는 5'-GalNAc를 갖는다. 특정 구현예에서, 안티센스 화합물은 서열번호: 77의 핵염기 서열을 갖는 변형된 올리고뉴클레오티드로 이루어지며, 이는 윙의 당 변형에서의 가변성을 갖는 5'-GalNAc를 갖는다.
여기서 R1은 -OCH2CH2OCH3 (MOE)이고 R2는 H이거나; 또는 R1 및 R2는 함께 가교를 형성하고, 여기서 R1은 -O-이고 R2는 -CH2-, -CH(CH3)-, 또는 -CH2CH2-이고, 그리고 R1 및 R2는 직접적으로 연결되고, 이로써 수득한 가교는 하기로부터 선택되고: -O-CH2-, -O-CH(CH3)-, 및 -O-CH2CH2-;
그리고 동일한 환 상의 R3 및 R4의 각각의 쌍에 대해, 독립적으로 각각의 환에 대해: 둘 중 하나의 R3은 H 및 -OCH2CH2OCH3로부터 선택되고 R4는 H이거나; 또는 R3 및 R4는 함께 가교를 형성하고, 여기서 R3은 -O-이고, 그리고 R4는 CH2-, -CH(CH3)-, 또는 -CH2CH2-이고 R3 및 R4는 직접적으로 연결되고, 이로써 수득한 가교는 하기로부터 선택되고: -O-CH2-, -O-CH(CH3)-, 및 -O-CH2CH2-;
그리고 R5는 H 및 -CH3로부터 선택되고;
그리고 Z는 S- 및 O-로부터 선택된다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 20의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 544199 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 544199 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 35의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 560400 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 560400 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 90의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 567233 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 567233 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 93의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 567320 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 567320 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 94의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 적어도 16, 적어도 17, 적어도 18, 적어도 19, 또는 20 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 567321 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 567321 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 110의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 또는 16 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 559277 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 559277 및 콘주게이트 그룹으로 이루어진다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하고, 상기 변형된 올리고뉴클레오티드는 12 내지 30 개의 연결된 뉴클레오시드로 이루어지고 서열번호: 114의 핵염기 서열의 적어도 8, 적어도 9, 적어도 10, 적어도 11, 적어도 12, 적어도 13, 적어도 14, 적어도 15, 또는 16 개의 인접 핵염기를 포함하는 핵염기 서열을 갖는다. 특정 구현예에서, 본 화합물은 ISIS 561011 및 콘주게이트 그룹을 포함한다. 특정 구현예에서, 상기 화합물은 ISIS 561011 및 콘주게이트 그룹으로 이루어진다.
특정 구현예에서, 상기 변형된 올리고뉴클레오티드의 핵염기 서열은 서열번호: 1-2에 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 100% 상보적이다 (변형된 올리고뉴클레오티드의 전체에 걸쳐 측정된 바와 같음).
특정 구현예에서, 본원에 개시된 화합물은 단일-가닥 올리고뉴클레오티드이다. 특정 구현예에서, 본원에 개시된 화합물은 단일-가닥 변형된 올리고뉴클레오티드이다.
특정 구현예에서, 변형된 올리고뉴클레오티드의 적어도 하나의 뉴클레오시드간 연결은 변형된 뉴클레오시드간 연결이다. 특정 구현예에서, 변형된 뉴클레오시드간 연결은 포스포로티오에이트 뉴클레오시드간 연결이다. 특정 구현예에서, 상기 변형된 올리고뉴클레오티드의 적어도 1, 적어도 2, 적어도 3, 적어도 4, 적어도 5, 적어도 6, 적어도 7, 적어도 8, 적어도 9 또는 적어도 10 개의 뉴클레오시드간 연결은 포스포로티오에이트 뉴클레오시드간 연결이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 뉴클레오시드간 연결이다. 특정 구현예에서, 변형된 올리고뉴클레오티드는 적어도 1, 적어도 2, 적어도 3, 적어도 4, 적어도 5, 적어도 6, 적어도 7, 적어도 8, 적어도 9 또는 적어도 10 개의 포스포디에스테르 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 상기 변형된 올리고뉴클레오티드의 각각의 뉴클레오시드간 연결은 포스포디에스테르 뉴클레오시드간 연결 및 포스포로티오에이트 뉴클레오시드간 연결로부터 선택된다.
특정 구현예에서, 상기 변형된 올리고뉴클레오티드의 적어도 하나의 뉴클레오시드는 변형된 당을 포함한다. 특정 구현예에서, 상기 적어도 하나의 변형된 당은 이환식 당이다. 적어도 하나의 변형된 당이 2'-O-메톡시에틸, 제한된 에틸, 3'-플루오로-HNA 또는 4'-(CH2)n-O-2' 가교(bridge)이고, 여기서 n이 1 또는 2인 화합물이다.
특정 구현예에서, 상기 변형된 올리고뉴클레오티드의 적어도 하나의 뉴클레오시드는 변형된 핵염기를 포함한다. 특정 구현예에서, 변형된 핵염기는 5-메틸시토신이다.
본원에 개시된 특정 구현예는 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 화합물 또는 조성물을 제공하며, 상기 변형된 올리고뉴클레오티드는 하기를 갖는다: a) 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; b) 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 및 c) 연결된 뉴클레오시드로 이루어진 3' 윙 분절. 상기 갭 분절은 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각 윙 분절의 각각의 뉴클레오시드는 변형된 당을 포함한다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 12 내지 30개의 연결된 뉴클레오시드로 이루어지며, 하기를 포함한다: 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절은 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각 윙 분절의 각 뉴클레오시드는 변형된 당을 포함한다.
특정 구현예에서, 본원에 개시된 화합물 또는 조성물은 서열번호: 1-2의 동등 길이 부분에 상보적인 적어도 8개의 인접 핵염기를 포함하는 핵염기 서열을 갖는 20개의 연결된 뉴클레오시드로 이루어진 변형된 올리고뉴클레오티드를 포함하고, 상기 변형된 올리고뉴클레오티드는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 20개의 연결된 뉴클레오시드로 이루어지며, 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 본원에 개시된 화합물 또는 조성물은 서열번호: 77의 선택된 핵염기 서열의 적어도 8개의 인접 핵염기를 포함하는 핵염기 서열을 갖는 20개의 연결된 뉴클레오시드로 이루어진 변형된 올리고뉴클레오티드를 포함하고, 상기 변형된 올리고뉴클레오티드는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 77의 핵염기 서열을 갖는 20개의 연결된 뉴클레오시드로 이루어지며, 이는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 본원에 개시된 화합물 또는 조성물은 서열번호: 20의 선택된 핵염기 서열의 적어도 8개의 인접 핵염기를 포함하는 핵염기 서열을 갖는 20개의 연결된 뉴클레오시드로 이루어진 변형된 올리고뉴클레오티드를 포함하고, 상기 변형된 올리고뉴클레오티드는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 20의 핵염기 서열을 갖는 20개의 연결된 뉴클레오시드로 이루어지며, 이는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 5개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 5개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절의 각각의 뉴클레오시드가 2'-O-메톡시에틸 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 본원에 개시된 화합물 또는 조성물은 서열번호: 110의 선택된 핵염기 서열의 적어도 8개의 인접 핵염기를 포함하는 핵염기 서열을 갖는 16개의 연결된 뉴클레오시드로 이루어진 변형된 올리고뉴클레오티드를 포함하고, 상기 변형된 올리고뉴클레오티드는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 3개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 3개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절은 2'-O-메톡시에틸 당 및 적어도 하나의 cEt 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 변형된 올리고뉴클레오티드는 서열번호: 110의 핵염기 서열을 갖는 16개의 연결된 뉴클레오시드로 이루어지며, 이는 하기를 포함한다: 10개의 연결된 데옥시뉴클레오시드로 이루어진 갭 분절; 3개의 연결된 뉴클레오시드로 이루어진 5' 윙 분절; 3개의 연결된 뉴클레오시드로 이루어진 3' 윙 분절; 여기서 상기 갭 분절이 5' 윙 분절과 3' 윙 분절 사이에 위치하고, 각각의 윙 분절은 2'-O-메톡시에틸 당 및 적어도 하나의 cEt 당을 포함하고, 여기서 적어도 하나의 뉴클레오시드간 연결이 포스포로티오에이트 연결이며, 여기서 각각의 시토신 잔기가 5-메틸시토신이다. 특정 구현예에서, 각각의 뉴클레오시드간 연결은 포스포로티오에이트 연결이다.
특정 구현예에서, 콘주게이트 그룹은 변형된 올리고뉴클레오티드의 5' 말단에서 변형된 올리고뉴클레오티드에 연결된다. 특정 구현예에서, 콘주게이트 그룹은 변형된 올리고뉴클레오티드의 3' 말단에서 변형된 올리고뉴클레오티드에 연결된다.
특정 구현예에서, 콘주게이트 그룹은 정확하게 하나의 리간드를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 1 이상의 리간드를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 정확하게 2 개의 리간드를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 2 이상의 리간드를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 3 개 이상의 리간드를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 정확하게 3 개의 리간드를 포함한다. 특정 구현예에서, 각각의 리간드는 하기 중으로부터 선택되는 화합물: 다당류, 변형된 다당류, 만노스, 갈락토오스, 만노스 유도체, 갈락토오스 유도체, D-만노파이라노스, L-만노파이라노스, D-아라비노오스, L-갈락토오스, D-자일로푸라노스, L-자일로푸라노스, D-글루코오스, L-글루코오스, D-갈락토오스, L-갈락토오스, α-D-만노푸라노스, β-D-만노푸라노스, α-D-만노파이라노스, β-D-만노파이라노스, α-D-글루코파이라노스, β-D-글루코파이라노스, α-D-글루코푸라노스, β-D-글루코푸라노스, α-D-프룩토푸라노스, α-D-프룩토파이라노스, α-D-갈락토파이라노스, β-D-갈락토파이라노스, α-D-갈락토푸라노스, β-D-갈락토푸라노스, 글루코사민, 시알산, α-D-갈락토사민, N-아세틸갈락토사민, 2-아미노-3-O-[(R)-1-카복시에틸]-2-데옥시-β-D-글루코파이라노스, 2-데옥시-2-메틸아미노-L-글루코파이라노스, 4,6-디데옥시-4-포름아미도-2,3-디-O-메틸-D-만노파이라노스, 2-데옥시-2-설포아미노-D-글루코파이라노스, N-글라이콜로일-α-뉴라민산, 5-티오-β-D-글루코파이라노스, 메틸 2,3,4-트리-O-아세틸-1-티오-6-O-트리틸-α-D-글루코피라노사이드, 4-티오-β-D-갈락토파이라노스, 에틸 3,4,6,7-테트라-O-아세틸-2-데옥시-1,5-디티오-α-D-글루코-헵토피라노사이드, 2,5-안하이드로-D-알로노니트릴, 리보오스, D-리보오스, D-4-티오리보오스, L-리보오스, L-4-티오리보오스. 특정 구현예에서, 각각의 리간드는 N-아세틸 갈락토사민이다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 인 연결 그룹 또는 중성 연결 그룹 중 적어도 하나를 포함한다.
특정 구현예에서, 콘주게이트 그룹은 하기 중으로부터 선택된 구조를 포함한다:
상기 식 중에서, n은 1 내지 12이고; 그리고
m은 1 내지 12이다.
특정 구현예에서, 콘주게이트 그룹은 하기 중으로부터 선택된 구조를 갖는 연결기를 갖는다:
여기서 L은 인 연결 그룹 또는 중성 연결 그룹이고;
Z1 는 C(=O)O-R2 이고;
Z2 는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고;
R2는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고; 그리고
각각의 m1은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m1은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 콘주게이트 그룹은 하기 중으로부터 선택된 구조를 갖는 연결기를 갖는다:
여기서 Z2는 H 또는 CH3이고; 그리고
각각의 m1은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m1은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 콘주게이트 그룹은 하기 중으로부터 선택된 구조를 갖는 연결기를 갖는다:
상기 식 중에서, n은 1 내지 12이고; 그리고
m은 1 내지 12이다.
특정 구현예에서, 콘주게이트 그룹은 변형된 올리고뉴클레오티드에 공유결합된다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고;
각각의 n은 독립적으로 0 또는 1이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고;
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
C는 콘주게이트 링커이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
D는 분지화 그룹이고;
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 본 화합물은 하기 식으로 나타낸 구조를 갖는다:
상기 식 중에서,
A는 변형된 올리고뉴클레오티드이고;
D는 분지화 그룹이고;
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 L은, 독립적으로, 인 연결 그룹 또는 중성 연결 그룹이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 피롤리딘을 포함한다. 특정 구현예에서, 콘주게이트 링커는 피롤리딘을 포함하지 않는다.
특정 구현예에서, 콘주게이트 링커는 PEG를 포함한다.
특정 구현예에서, 콘주게이트 링커는 아미드를 포함한다. 특정 구현예에서, 콘주게이트 링커는 적어도 2 개의 아미드를 포함한다. 특정 구현예에서, 콘주게이트 링커는 아미드를 포함하지 않는다. 특정 구현예에서, 콘주게이트 링커는 폴리아미드를 포함한다.
특정 구현예에서, 콘주게이트 링커는 아민을 포함한다.
특정 구현예에서, 콘주게이트 링커는 1 이상의 이황화 결합을 포함한다.
특정 구현예에서, 콘주게이트 링커는 단백질 결합 모이어티를 포함한다. 특정 구현예에서, 단백질 결합 모이어티는 지질을 포함한다. 특정 구현예에서, 단백질 결합 모이어티는 하기 중으로부터 선택된다: 콜레스테롤, 콜산, 아다만탄 아세트산, 1-피렌 부티르산, 디하이드로테스토스테론, 1,3-비스-O(헥사데실)글리세롤, 제라닐옥시헥실 그룹, 헥사데실글리세롤, 보르네올, 멘톨, 1,3-프로판디올, 헵타데실 그룹, 팔미트산, 미리스트산, O3-(올레오일)리토콜산, O3-(올레오일)콜렌산, 디메톡시트리틸, 또는 펜옥사진), 비타민 (예를 들면, 폴레이트, 비타민 A, 비타민 E, 바이오틴, 피리독살), 펩티드, 탄수화물 (예를 들면, 단당류, 디사카라이드, 트리사카라이드, 테트라사카라이드, 올리고당, 다당류), 엔도솜분해적 구성성분, 스테로이드 (예를 들면, 우바올, 헤시게닌, 디오스게닌), 테르펜 (예를 들면, 트리테르펜, 예를 들면, 사르사사포게닌, 프리델린, 에피프리에델라놀 유도된 리토콜산), 또는 양이온성 지질. 특정 구현예에서, 단백질 결합 모이어티는 하기 중으로부터 선택된다: C16 내지 C22 장쇄 포화된 또는 불포화된 지방산, 콜레스테롤, 콜산, 비타민 E, 아다만탄 또는 1-펜타플루오로프로필.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이고; 그리고 p는 1 내지 6이다.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, n은 1 내지 20이다.
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 n은 독립적으로, 0, 1, 2, 3, 4, 5, 6, 또는 7이다.
특정 구현예에서, 콘주게이트 링커는 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 구조 중 하나를 갖는다:
상기 식 중에서, 각각의 A1은 독립적으로, O, S, C=O 또는 NH이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기 구조 중 하나를 갖는다:
상기 식 중에서, 각각의 A1은 독립적으로, O, S, C=O 또는 NH이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 에테르를 포함한다.
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이고; 그리고
m은 2 내지 6이다.
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기를 포함한다:
상기 식 중에서, 각각의 j는 정수 1 내지 3이고; 그리고
각각의 n은 정수 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기를 포함한다:
특정 구현예에서, 각각의 연결기는 하기 중으로부터 선택된다:
상기 식 중에서, L은 인 연결 그룹 및 중성 연결 그룹으로부터 선택되고;
Z1 는 C(=O)O-R2 이고;
Z2는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고;
R2는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고; 그리고
각각의 m1은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m1은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 각각의 연결기는 하기 중으로부터 선택된다:
여기서 Z2는 H 또는 CH3이고; 그리고
각각의 m2은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m2은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 각각의 연결기는 하기 중으로부터 선택된다:
상기 식 중에서, n은 1 내지 12이고; 그리고
m은 1 내지 12이다.
특정 구현예에서, 적어도 하나의 연결기는 에틸렌 글리콜을 포함한다.
특정 구현예에서, 적어도 하나의 연결기는 아미드를 포함한다. 특정 구현예에서, 적어도 하나의 연결기는 폴리아미드를 포함한다.
특정 구현예에서, 적어도 하나의 연결기는 아민을 포함한다.
특정 구현예에서, 적어도 2 개의 연결기는 서로 상이하다. 특정 구현예에서, 모든 연결기는 서로 동일하다.
특정 구현예에서, 각각의 연결기는 하기 중으로부터 선택된다:
여기서 각각의 n은, 독립적으로, 1 내지 20이고; 그리고
각각의 p는 1 내지 약 6이다.
특정 구현예에서, 각각의 연결기는 하기 중으로부터 선택된다:
특정 구현예에서, 각각의 연결기는 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 각각의 연결기는 하기 구조를 갖는다:
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
; 여기서 각각의 n은 독립적으로, 0, 1, 2, 3, 4, 5, 6, 또는 7이다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 리간드는 갈락토오스이다.
특정 구현예에서, 리간드는 만노스-6-포스페이트이다.
특정 구현예에서, 각각의 리간드는 하기 중으로부터 선택된다:
상기 식 중에서, 각각의 R1은 OH 및 NHCOOH로부터 선택된다.
특정 구현예에서, 각각의 리간드는 하기 중으로부터 선택된다:
특정 구현예에서, 각각의 리간드는 하기 구조를 갖는다:
특정 구현예에서, 각각의 리간드는 하기 구조를 갖는다:
특정 구현예에서, 콘주게이트 그룹은 세포-표적화 모이어티를 포함한다.
특정 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는 세포-표적화 모이어티를 포함한다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
특정 구현예에서, 세포-표적화 모이어티는 하기를 포함한다:
상기 식 중에서, 각각의 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택된다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
상기 식 중에서, 각각의 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택된다.
특정 구현예에서, 세포-표적화 모이어티는 하기 구조를 갖는다:
상기 식 중에서, 각각의 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택된다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
특정 구현예에서, 콘주게이트 그룹은 하기 중으로부터 선택된 절단가능 모이어티를 포함한다: 포스포디에스테르, 아미드, 또는 에스테르.
특정 구현예에서, 콘주게이트 그룹은 포스포디에스테르 절단가능 모이어티를 포함한다.
특정 구현예에서, 콘주게이트 그룹은 절단가능 모이어티를 포함하지 않고, 상기 콘주게이트 그룹은 콘주게이트 그룹과 올리고뉴클레오티드 사이의 포스포로티오에이트 연결을 포함한다.
특정 구현예에서, 콘주게이트 그룹은 아미드 절단가능 모이어티를 포함한다.
특정 구현예에서, 콘주게이트 그룹은 에스테르 절단가능 모이어티를 포함한다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고;
Z는 H 또는 연결된 고형 지지체이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고;
Z는 H 또는 연결된 고형 지지체이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 본 화합물은 하기 구조를 갖는다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, 콘주게이트 그룹은 하기를 포함한다:
여기서 Q13 는 H 또는 O(CH2)2-OCH3 이고;
A는 변형된 올리고뉴클레오티드이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 구현예에서, Bx는 아데닌, 구아닌, 티민, 우라실, 또는 시토신, 또는 5-메틸 시토신 중으로부터 선택된다. 특정 구현예에서, Bx는 아데닌이다. 특정 구현예에서, Bx는 티민이다. Q13 는 H 또는 O(CH2)2-OCH3 이고; 특정 구현예에서, Q13은 H이다.
본 발명의 특정 구현예는 본원에서 개시된 조성물 또는 화합물을 포함하는 프로드럭을 제공한다. 특정 구현예는 ANGPTL3 발현을 억제하기 위하여 본원에 기재된 콘주게이트된 안티센스 화합물 및 조성물을 사용하는 방법을 제공한다. 특정 구현예에서, 콘주게이트된 안티센스 화합물 또는 조성물은 ANGPTL3을 적어도 5%, 적어도 10%, 적어도 20%, 적어도 30%, 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90% 또는 적어도 95% 만큼 억제한다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 50% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 55% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 60% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 65% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 70% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 75% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 80% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 85% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 90% 만큼 감소시킨다. 바람직한 구현예에서, 변형된 올리고뉴클레오티드 및 콘주게이트 그룹을 포함하는 안티센스 화합물은 ANGPTL3를 적어도 95% 만큼 감소시킨다.
특정 구현예에서, 본원에 기술된 콘주게이트된 안티센스 화합물 또는 조성물은 20μM 미만, 10μM 미만, 8μM 미만, 5μM 미만, 2μM 미만, 1μM 미만, 또는 0.8μM 미만의 시험관내 IC50을 갖는다 (실시예 2 내지 3 및 7 내지 10에 기술된 바와 같은 Hep3B 세포주 내에서).
특정 구현예에서, 본원에 기술된 콘주게이트된 안티센스 화합물 또는 조성물은 파라미터(실시예 13에 기술된 바와 같음)에 의해 측정하는 경우 점도가 40 cP 미만, 35 cP 미만, 30 cP 미만, 25 cP 미만, 20 cP 미만, 또는 15 cP 미만임으로 인해 효과적이다.
특정 구현예에서, 본원에 기술된 콘주게이트된 안티센스 화합물 또는 조성물은은 실시예에 기술된 생체내 내성 측정으로 입증된 바와 같이, 고도로 내성이다. 특정 구현예에서, 본원에 기술된 바와 같은 특정의 콘주게이트된 안티센스 화합물은 염수 치료된 동물보다 4배, 3배, 2배 또는 1.5배 이하의 ALT 및/또는 AST 값에 있어서의 증가를 가짐에 의해 입증되는 바와 같이, 고도로 내성이다.
본원에 기술된 특정 구현예는 본원에서 개시된 콘주게이트된 안티센스 화합물의 염을 제공한다. 특정 구현예에서, 본원에 개시된 화합물 또는 조성물은 콘주게이트 그룹 및 변형된 올리고뉴클레오티드의 염을 포함한다.
특정 구현예에서, 본원에 개시된 콘주게이트된 안티센스 화합물 또는 조성물은 추가로, 약제학적으로 허용가능한 담체 또는 희석제를 포함한다.
특정 구현예에서, 동물은 인간이다
본원에 개시된 특정 구현예는 본원에 개시된 콘주게이트된 안티센스 화합물 또는 조성물을 동물에게 투여하는 단계를 포함하는 방법을 제공한다. 특정 구현예에서, 콘주게이트된 안티센스 화합물 또는 조성물은 치료성이다. 특정 구현예에서, 콘주게이트된 안티센스 화합물 또는 조성물을 투여하는 것은 ANGPTL3과 관련된 질환을 치료하거나, 예방하거나, 또는 이의 진행을 지연시킨다. 특정 구현예에서, 상기 질환은 상승된 ANGPTL3에 관한 것이다. 특정 구현예에서, 콘주게이트된 안티센스 화합물 또는 조성물의 투여는 심혈관성 및/또는 대사성 질환을 치료하거나, 개선하거나, 또는 이의 진행을 지연시킨다.
본원에 개시된 특정 구현예는 심혈관성 및/또는 대사성 질환의 치료 방법을 제공하며, 이는 하기를 포함한다: 심혈관성 및/또는 대사성 질환을 갖는 인간을 동정하는 단계, 및 심혈관성 및/또는 대사성 질환에 대하여 상기 인간을 치료하기 위하여, 상기 인간에게 본원에 개시된 콘주게이트된 안티센스 화합물 또는 조성물 중 임의의 것의 치료적 유효량을 투여하는 단계.
특정 구현예는 요법에 사용하기 위한 본원에 기술된 콘주게이트된 안티센스 화합물 및 조성물을 제공한다. 특정 구현예에서, 요법은 ANGPTL3과 관련된 질환의 치료, 예방, 또는 이의 진행의 지연에 시용된다. 특정 구현예에서, 요법은 상승된 ANGPTL3과 관련된 질환의 치료, 예방, 또는 이의 진행의 지연에 시용된다.
특정 구현예에서, 질환은 심혈관 및/또는 대사성 질환, 장애 또는 병태이다. 특정 구현예에서, 대사성 및/또는 심혈관 질환은, 비제한적으로, 비만, 당뇨병, 인슐린 내성, 죽상경화증, 이상지질혈증, 지방이영양증, 관상동맥 심장병, 비-알코올성 지방간 질환 (NAFLD), 비알코올성 지방간염 (NASH) 과지방산혈증 또는 대사성 증후군, 또는 이들의 조합을 포함한다. 이상지질혈증은 고지혈증일 수 있다. 고지혈증은 조합된 고지혈증, 결합성 고지혈증 (CHL), 고콜레스테롤혈증, 초고트리글리세라이드혈증, 또는 둘 모두 고콜레스테롤혈증 및 초고트리글리세라이드혈증일 수 있다. 조합된 고지혈증은 가족성 또는 비-가족성일 수 있다. 고콜레스테롤혈증은 가족성 동종 고콜레스테롤혈증 (HoFH), 가족성 이형 고콜레스테롤혈증 (HeFH)일 수 있다. 초고트리글리세라이드혈증 가족성 카일로마이크론혈증 증후군 (FCS) 또는 고지질단백혈증 유형 IV일 수 있다. NAFLD는 간 지방증 또는 지방간염일 수 있다. 당뇨병은 이상지질혈증을 갖는 2형 당뇨병 또는 2형 당뇨병일 수 있다. 인슐린 내성은 이상지질혈증과 더불어 인슐린 내성일 수 있다.
특정 구현예에서, 본원에 개시된 콘주게이트된 안티센스 화합물 또는 조성물은 제1 제제로 지정되고, 본원에 개시된 방법 또는 용도는 제2 제제를 투여하는 단계를 추가로 포함한다. 특정 구현예에서, 제 1 제제 및 제2 제제는 공동 투여된다. 특정 구현예에서, 제 1 제제 및 제2 제제는 공동 투여되거나 수반하여 투여된다.
특정 구현예에서, 제2 제제는 글루코오스-저하제이다. 글루코오스 저하제는, 비제한적으로, 치료 생활방식 변화, PPAR 작용제, 디펩티딜 펩티다아제 (IV) 억제제, GLP-1 유사체, 인슐린 또는 인슐린 유사체, 인슐린 분비촉진제, SGLT2 억제제, 인간 아밀린 유사체, 바이구아나이드, 알파-글루코시다제 억제제, 또는 이들의 조합을 포함할 수 있다. 글루코오스-저하제는, 비제한적으로 메트포르민, 설포닐우레아, 로시글리타존, 메글리티나이드, 티아졸리딘디온, 알파-글루코시다제 억제제 또는 이들의 조합을 포함할 수 있다. 설포닐우레아는 아세토헥사마이드, 클로르프로파마이드, 톨부타마이드, 톨라자마이드, 글리메피라이드, 글리피자이드, 글리부라이드, 또는 글리클라자이드일 수 있다. 메글리티나이드는 나테글리나이드 또는 레파글리나이드일 수 있다. 티아졸리딘디온은 피오글리타존 또는 로시글리타존일 수 있다. 알파-글루코시다제는 아카르보스 또는 미글리톨일 수 있다.
특정 구현예에서, 제2 제제는 지질-저하 요법이다. 특정 구현예에서, 지질 저하 요법은 하기를 비제한적으로 포함할 수 있다: 치료적 생활방식 변화, HMG-CoA 환원효소 억제제, 콜레스테롤 흡수 억제제, MTP 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (MTP에 표적화됨)), ApoB 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (ApoB에 표적화됨)), ApoC3 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (ApoC3에 표적화됨)), PCSK9 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (PCSK9에 표적화됨)), CETP 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (CETP에 표적화됨)), 피브레이트, 유익한 오일 (예를 들면, 크릴(krill) 또는 물고기 오일 (예를 들면, VascepaR),아마씨 오일, 또는 기타 오메가-3 지방산 풍부 오일 예컨대 α-리놀렌산 (ALA), 도코사헥사에노산 (DHA) 또는 에이코사펜타에노산 (EPA)), 또는 이들의 임의의 조합. HMG-CoA 환원효소 억제제는 아토르바스타틴, 로수바스타틴, 플루바스타틴, 로바스타틴, 프라바스타틴, 또는 심바스타틴일 수 있다. 콜레스테롤 흡수 억제제는 에제티마이브일 수 있다. 피브레이트는 페노파이브레이트, 베자피브레이트, 시프로피브레이트, 클로파이브레이트, 젬피브로질 등일 수 있다.
특정 구현예에서, 투여는 비경구 투여를 포함한다. 특정 구현예에서, 투여는 피하 투여를 포함한다.
특정 구현예에서, 본원에 개시된 콘주게이트된 안티센스 화합물을 투여하는 것은 트리글리세라이드 수준, 콜레스테롤 수준, 인슐린 내성, 글루코오스 수준 또는 이들의 조합을 포함하는 지질 수준의 감소를 초래한다. 상기 수준 중 하나 이상은 독립적으로 적어도 5%, 적어도 10%, 적어도 20%, 적어도 30%, 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90% 또는 적어도 95% 만큼 감소할 수 있다. 콘주게이트된 안티센스 화합물을 투여하는 것은 향상된 인슐린 민감성 또는 간 인슐린 민감성을 초래할 수 있다. 본원에 개시된 콘주게이트된 안티센스 화합물을 투여하는 것은 죽상경화판, 비만, 글루코오스, 지질, 글루코오스 내성, 콜레스테롤의 감소, 또는 인슐린 민감성 또는 이들의 임의의 조합의 향상을 초래할 수 있다.
특정 구현예는 ANGPTL3와 관련된 질환 중 하나 이상을 치료, 개선, 지연 또는 예방하기 위한 약제의 제조에서의, 본원에서 기재된 콘주게이트된 안티센스 화합물의 용도를 제공한다. 특정 구현예는 대사성 질환 또는 심혈관 질환 중 하나 이상을 치료, 개선, 또는 예방을 위한 약제의 제조에서의 본원에 기재된 바와 같은 콘주게이트된 안티센스 화합물의 용도를 제공한다.
특정 구현예는 본원에 기재된 바와 같은 대사성 질환 또는 심혈관 질환 중 하나 이상을 치료, 예방, 또는 개선하기 위한 키트를 제공하고, 상기 키트는 하기를 포함한다: a) 본원에 기재된 바와 같은 콘주게이트된 안티센스 화합물; 및 임의로 b) 본원에 기재된 바와 같은 부가적 제제 또는 요법. 상기 키트는 대사성 질환 또는 심혈관 질환 중 하나 이상을 치료, 예방, 또는 개선하기 위하여 상기 키트를 사용하기 위한 설명서 또는 표지를 추가로 포함할 수 있다.
안티센스 화합물
올리고머 화합물은, 비제한적으로, 올리고뉴클레오티드, 올리고뉴클레오티드, 올리고뉴클레오티드 유사체, 올리고뉴클레오티드 모방체, 안티센스 화합물, 안티센스 올리고뉴클레오티드, 및 siRNA를 포함한다. 올리고머 화합물은 표적 핵산에 대한 "안티센스"일 수 있고, 이것은 수소 결합을 통해 표적 핵산에 대한 혼성화를 경험할 수 있다는 것을 의미한다.
특정 구현예에서, 안티센스 화합물은, 5'에서 3' 방향으로 쓰여질 때, 그것이 표적화된 표적 핵산의 표적 분절의 역보체를 포함하는 핵염기 서열을 갖는다. 그와 같은 특정 구현예에서, 안티센스 올리고뉴클레오티드는, 5'에서 3' 방향으로 쓰여질 때, 그것이 표적화된 표적 핵산의 표적 분절의 역보체를 포함하는 핵염기 서열을 갖는다.
특정 구현예에서, ANGPTL3 핵산에 표적화된 안티센스 화합물은 그 길이가 10 내지 30 개의 뉴클레오티드이다. 환언하면, 안티센스 화합물은 10 내지 30개의 연결된 핵염기이다. 다른 구현예에서, 안티센스 화합물은 하기로 이루어진 변형된 올리고뉴클레오티드를 포함한다: 8 내지 80, 10 내지 80, 12 내지 50, 12 내지 30, 15 내지 30, 18 내지 24, 19 내지 22, 또는 20개의 연결된 핵염기. 특정 구현예에서, 안티센스 화합물은 그 길이가 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 또는 80개 연결된 핵염기 또는 상기 값 중 임의의 2개에 의하여 정의된 범위로 이루어진 변형된 올리고뉴클레오티드를 포함한다.
특정 구현예에서, 안티센스 화합물은 단축된 또는 절단된 변형된 올리고뉴클레오티드를 포함한다. 단축된 또는 절단된 변형된 올리고뉴클레오티드는 5' 말단 (5' 절단), 또는 대안적으로 3' 말단 (3' 절단)로부터 결실된 단일 뉴클레오시드를 가질 수 있다. 단축된 또는 절단된 올리고뉴클레오티드는 5' 말단으로부터 결실된 2 개의 뉴클레오시드를 가질 수 있고, 또는 대안적으로 3' 말단으로부터 결실된 2개의 하부단위를 가질 수 있다. 대안적으로, 결실된 뉴클레오시드는, 예를 들면, 5' 말단으로부터 결실된 하나 이상의 뉴클레오시드 및 3' 말단로부터 결실된 하나 이상의 뉴클레오시드을 갖는 안티센스 화합물에서 변형된 올리고뉴클레오티드를 통해 분산될 수 있다.
단일 부가적 뉴클레오시드가 늘어난 올리고뉴클레오티드에서 존재할 때, 부가적 뉴클레오시드는 올리고뉴클레오티드의 5' 또는 3' 말단에서 위치할 수 있다. 2 개 이상의 부가적 뉴클레오시드가 존재할 때, 부가된 뉴클레오시드는, 예를 들면, 올리고뉴클레오티드의 5' 말단 (5' 부가), 또는 대안적으로 3' 말단 (3' 부가)에 부가된 2개의 뉴클레오시드를 갖는 올리고뉴클레오티드에서 서로 인접할 수 있다. 대안적으로, 부가된 뉴클레오시드는, 예를 들면, 5' 말단에 부가된 하나 이상의 뉴클레오시드 및 3' 말단에 부가된 하나 이상의 뉴클레오시드 및/또는 중앙 부분에 부가된 하나 이상에 뉴클레오시드를 갖는 올리고뉴클레오티드에서 안티센스 화합물을 통해 분산될 수 있다.
안티센스 화합물, 예컨대 안티센스 올리고뉴클레오티드의 길이를 증가 또는 감소시키고/시키거나 활성을 제거하지 않으면서 미스매치 염기를 도입할 수 있다. 예를 들어, 다음을 참고하며: Woolf et al. 예를 들면, Woolf et al. (Proc. Natl. Acad. Sci. USA 89:7305-7309, 1992)에서, 길이가 13-25 핵염기인 일련의 안티센스 올리고뉴클레오티드는 그것의 능력에 대해 시험되어 난모세포 주입 모델에서 표적 RNA의 절단을 유도했다. 안티센스 올리고뉴클레오티드의 말단 근처의 8 또는 11 미스매치 염기를 가지며 그 길이가 25개 핵염기인 안티센스 올리고뉴클레오티드는 미스매치를 함유하지 않는 안티센스 올리고뉴클레오티드보다 더 적을지라도 표적 mRNA의 직접적인 특이적 절단이 가능했다. 마찬가지로, 표적 특이적 절단은 1 또는 3 미스매치를 갖는 것을 포함하는 13개 핵염기 안티센스 올리고뉴클레오티드를 사용하여 달성되었다.
Gautschi 등 (J.Natl. Cancer Inst. 93:463-471, March 2001)는 bcl-2 및 bcl-xL 둘 다의 시험관내 및 생체내 발현을 감소시키기 위해 bcl-2 mRNA에 대해100% 상보성을 가지며 bcl-xL mRNA에 대한 3 개의 미스매치를 갖는 올리고뉴클레오티드의 능력을 실증했다. 더욱이, 이러한 올리고뉴클레오티드는 생체내 강력한 항-종양 활성을 실증했다.
Maher 및 Dolnick (Nuc. Acid. Res. 16:3341-3358, 1988) 는 토끼 망상적혈구 검정에서 인간 DHFR의 번역을 저지하는 그것의 능력에 대한, 각각의 탠덤 안티센스 올리고뉴클레오티드의 2개 또는 3개 서열로 구성된, 일련의 탠덤 14 핵염기 안티센스 올리고뉴클레오티드 및, 28 및 42 핵염기 안티센스 올리고뉴클레오티드를 시험했다. 각각의 3 개의 14 핵염기 안티센스 올리고뉴클레오티드 단독은 28 또는 42 핵염기 안티센스 올리고뉴클레오티드보다 더 보통의 수준일지라로 번역을 억제할 수 있었다.
특정 안티센스 화합물 모티프 및 기전
특정 구현예에서, 안티센스 화합물은, 안티센스 화합물 특성 예컨대 증대된 억제 활성, 표적 핵산에 대핸 증가된 결합 친화도, 또는 생체내 뉴클레아제에 의한 분해에 대한 내성을 부여하기 위해 패턴, 또는 모티프에서 마련된 화학적으로 변형된 하부단위를 갖는다.
키메라 안티센스 화합물은 전형적으로 뉴클레아제 분해에 대한 증가된 내성, 증가된 세포 흡수, 표적 핵산의 증가된 결합 친화도, 및/또는 증가된 억제 활성을 부여하기 위해 변형된 적어도 하나의 영역을 함유한다. 키메라성 안티센스 화합물의 제2 영역은 또 하나의 원하는 특성을 부여할 수 있고, 예를 들면, RNA:DNA 이중나선의 RNA 가닥을 절단하는 세포성 엔도뉴클레아제 RNase H에 대한 대체물로서 쓰인다.
안티센스 활성은 안티센스 화합물 (예를 들면, 올리고뉴클레오티드)과 표적 핵산과의 혼성화를 수반하는 임의의 기전으로부터 유래할 수 있고, 상기 혼성화는 궁극적으로 생물학적 효과를 야기한다. 특정 구현예에서, 표적 핵산의 양 및/또는 활성이 조절된다. 특정 구현예에서, 표적 핵산의 양 및/또는 활성이 감소된다. 특정 구현예에서, 안티센스 화합물의 표적 핵산에의 혼성화는 표적 핵산 분해를 야기하지 않는다. 특정 구현예에서, 안티센스 화합물의 표적 핵산에의 혼성화는 표적 핵산 분해를 야기하지 않는다. 특정 그와 같은 구현예에서, 표적 핵산 (점유)과 혼성화된 안티센스 화합물의 존재는 안티센스 활성의 조절을 야기한다. 특정 구현예에서, 특정한 화학적 모티프 또는 화학적 변형의 패턴을 갖는 안티센스 화합물은 하나 이상의 기전을 활용하는데 특히 적합하다. 특정 구현예에서, 안티센스 화합물은 1 초과의 기전을 통해 기능하고/거나 설명되지 않았던 기전을 통해 기능한다. 따라서, 본원에서 기재된 안티센스 화합물은 특정한 기전에 의해 제한되지 않는다.
안티센스 기전은, 비제한적으로 하기를 포함한다: RNase H 매개된 안티센스; RISC 경로를 이용하고 siRNA, ssRNA 및 microRNA 기전을 비제한적으로 포함하는 RNAi 기전; 및 점유 기반 기전. 특정 안티센스 화합물은 1 초과 그와 같은 기전을 통해 및/또는 추가의 기전을 통해 작용할 수 있다.
RNaseH
-
매개된
안티센스
특정 구현예에서, 안티센스 활성은 RNase H에 의한 표적 RNA의 분해로부터 적어도 부분적으로 유래한다. RNase H는 RNA:DNA 이중나선의 RNA 가닥을 절단하는 세포성 엔도뉴클레아제이다. "DNA-유사"한 단일가닥 안티센스 화합물이 포유동물 세포에서 RNase H 활성을 유도하는 것으로 당해기술에서 공지되어 있다. 따라서, 적어도 일부의 DNA 또는 DNA-유사 뉴클레오시드를 포함하는 안티센스 화합물은 RNase H를 활성화시킬 수 있고, 이것으로 표적 핵산이 절단된다. 특정 구현예에서, RNase H 를 이용하는 안티센스 화합물은 하나 이상의 변형된 뉴클레오시드를 포함한다. 특정 구현예에서, 그와 같은 안티센스 화합물은 1 내지 8개의 변형된 뉴클레오시드 중 적어도 하나의 블록을 포함한다. 특정 그와 같은 구현예에서, 변형된 뉴클레오시드는 RNase H 활성을 지지하지 않는다. 특정 구현예에서, 그와 같은 안티센스 화합물은 본원에 기재된 바와 같은 갭머이다. 특정 그와 같은 구현예에서, 상기 갭머의 갭은 DNA 뉴클레오시드를 포함한다. 특정 그와 같은 구현예에서, 상기 갭머의 갭은 DNA-유사 뉴클레오시드를 포함한다. 특정 그와 같은 구현예에서, 상기 갭머의 갭은 DNA 뉴클레오시드 및 DNA-유사 뉴클레오시드를 포함한다.
갭머 모티프를 갖는 특정 안티센스 화합물은 키메라성 안티센스 화합물인 것으로 간주된다. 갭머에서 RNaseH 절단을 지지하는 복수의 뉴클레오티드를 갖는 내부 영역은 내부 영역의 뉴클레오시드로부터 화학적으로 뚜렷한 복수의 뉴클레오티드를 갖는 외부 영역 사이에 배치된다. 갭머 모티프를 갖는 안티센스 올리고뉴클레오티드의 경우에, 갭 분절은 일반적으로 엔도뉴클레아제 절단의 기질로서 쓰이지만, 윙 분절은 변형된 뉴클레오시드를 포함한다. 특정 구현예에서, 갭머의 영역은 각각의 뚜렷한 영역을 포함하는 당 모이어티의 유형에 의해 분화된다. 갭머의 영역을 분화시키기 위해 사용된 당 모이어티의 유형은 일부 구현예에서 하기를 포함할 수 있다: β-D-리보뉴클레오시드, β-D-데옥시리보뉴클레오시드, 2'-변형된 뉴클레오시드 (그와 같은 2'-변형된 뉴클레오시드는 기타 중에서 2'-MOE 및 2'-O-CH3를 포함할 수 있다), 및 이환식 당 변형된 뉴클레오시드 (그와 같은 이환식 당 변형된 뉴클레오시드는 제한된 에틸을 갖는 것을 포함할 수 있다). 특정 구현예에서, 윙 중 뉴클레오시드는, 예를 들면 2'-MOE 및 이환식 당 모이어티 예컨대 제한된 에틸 또는 LNA을 포함하는, 몇 개의 변형된 당 모이어티를 포함할 수 있다. 특정 구현예에서, 윙은 몇 개의 변형된 및 비변형된 당 모이어티를 포함할 수 있다. 특정 구현예에서, 윙은 2'-MOE 뉴클레오시드, 이환식 당 모이어티 예컨대 제한된 에틸 뉴클레오시드 또는 LNA 뉴클레오시드, 및 2'-데옥시뉴클레오시드의 다양한 조성물을 포함할 수 있다.
각각의 뚜렷한 영역은 균일한 당 모이어티, 변이체, 또는 교대 당 모이어티를 포함할 수 있다. 윙-갭-윙 모티프는 "X-Y-Z"로서 빈번히 기재되고, 여기서 "X"는 5'-윙의 길이를 나타내고, "Y"는 갭의 길이를 나타내고, "Z"는 3'-윙의 길이를 나타낸다. "X" 및 "Z"는 균일한, 변이체, 또는 교대 당 모이어티를 포함할 수 있다. 특정 구현예에서, "X" 및 "Y"는 하나 이상의 2'-데옥시뉴클레오시드를 포함할 수 있다. "Y"는 2'-데옥시뉴클레오시드를 포함할 수 있다. 본원에서 사용된 바와 같이, "X-Y-Z"로서 기재된 갭머는, 캡이 각각의 5'-윙 및 3' 윙에 바로 인접하여 배치되는 정도의 배치를 갖는다. 따라서, 개재 뉴클레오티드는 5'-윙 및 갭, 또는 갭 및 3'-윙 사이에 존재하지 않는다. 본원에 기재된 안티센스 화합물의 임의의 것은 갭머 모티프를 가질 수 있다. 특정 구현예에서, "X" 및 "Z"는 동일하고, 다른 구현예에서 y는 상이하다. 특정 구현예에서, "Y"는 8 내지 15 뉴클레오시드이다. X, Y, 또는 Z는 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30 또는 그 초과의 뉴클레오시드 중 임의의 것일 수 있다.
특정 구현예에서, 안티센스 화합물은 ANGPTL3 핵산에 표적화되고, 갭이 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 또는 16개의 연결된 뉴클레오시드로 구성된 갭머 모티프를 갖는다.
특정 구현예에서, 안티센스 올리고뉴클레오티드는 하기와 같은 화학식 A에 기술된 당 모티프를 갖는다: (J)m-(B)n-(J)p-(B)r-(A)t-(D)g-(A)v-(B)w-(J)x-(B)y-(J)z
상기 식 중에서,
각각의 A는 독립적으로 2'-치환된 뉴클레오시드이고;
각각의 B는 독립적으로 이환식 뉴클레오시드이고;
각각의 J는 독립적으로 2'-치환된 뉴클레오시드 또는 2'-데옥시뉴클레오시드이고;
각각의 D는 2'-데옥시뉴클레오시드이고;
m는 0 내지 4이고; n는 0 내지 2이고; p는 0 내지 2이고; r는 0 내지 2이고; t는 0 내지 2이고; v는 0 내지 2이고; w는 0 내지 4이고; x는 0 내지 2이고; y는 0 내지 2이고; z는 0 내지 4이고; G는 6-14이고;
단,
m, n, 및 r 중 적어도 하나는 0 이외의 것이고;
w 및 y 중 적어도 하나는 0 이외의 것이고;
m, n, p, r, 및 t의 합은 2 내지 5이고; 그리고
v, w, x, y, 및 z의 합은 2 내지 5이다.
RNAi 화합물
특정 구현예에서, 안티센스 화합물은 이중-가닥 RNA 화합물 (또한 일명 단-간섭 RNA 또는 siRNA) 및 단일-가닥 RNAi 화합물 (또는 ssRNA)를 포함하는 간섭 RNA 화합물 (RNAi)이다. 그와 같은 화합물은 표적 핵산을 분해 및/또는 격리하기 위해 RISC 경로를 통해 적어도 부분적으로 작용한다 (따라서, 마이크로RNA/마이크로RNA-모방 화합물을 포함한다). 특정 구현예에서, 안티센스 화합물은 그와 같은 기전에 특히 적합하도록 하기 위한 변형을 포함한다.
1.
ssRNA
화합물
특정 구현예에서, 단일-가닥 RNAi 화합물 (ssRNA)로서 사용하는데 특히 적합한 것들을 포함하는 안티센스 화합물은 변형된 5'-말단을 포함한다. 특정 그와 같은 구현예에서, 5'-말단은 변형된 포스페이트 모이어티를 포함한다. 특정 구현예에서, 그와 같은 변형된 포스페이트는 안정화된다 (예를 들면, 비변형된 5'-포스페이트와 비교하여 분해/절단에 대해 내성이 있다). 특정 구현예에서, 그와 같은 5'-말단 뉴클레오시드는 5'-인 모이어티를 안정화시킨다. 특정 변형된 5'-말단 뉴클레오시드는 당해기술, 예를 들면 WO/2011/139702에서 발견될 수 있다.
특정 구현예에서, ssRNA 화합물의 5'-뉴클레오시드는 식 IIc를 갖는다:
상기 식 중에서,
T1 은 임의로 보호된 인 모이어티이고;
T2 는 IIc의 화합물을 올리고머 화합물에 연결시키는 뉴클레오시드간 연결 그룹이고;
A는 하기의 식 중 하나를 갖는다:
Q1 및 Q2 는 각각, 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐, 치환된 C2-C6 알키닐 또는 N(R3)(R4)이고;
Q3 는 O, S, N(R5) 또는 C(R6)(R7)이고;
각각의 R3, R4 R5, R6 및 R7은 독립적으로, H, C1-C6 알킬, 치환된 C1-C6 알킬 또는 C1-C6 알콕시이고;
M3 는 O, S, NR14, C(R15)(R16), C(R15)(R16)C(R17)(R18), C(R15)=C(R17), OC(R15)(R16) 또는 OC(R15)(Bx2)이고;
R14는 H, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
R15, R16, R17 및 R18은 각각, 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
Bx1는 헤테로환 염기 모이어티이다.
또는 만약 Bx2이 존재한다면, Bx2 는 헤테로환식 염기 모이어티이고, Bx1 은 H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
J4, J5, J6 및 J7 은 각각, 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
또는 J4 는 J5 또는 J7 중 하나와 가교를 형성하고 여기서 상기 가교는 하기로부터 선택된 1 내지 3개의 연결된 2가 라디칼 그룹을 포함하고: O, S, NR19, C(R20)(R21), C(R20)=C(R21), C[=C(R20)(R21)], 그리고 C(=O), J5, J6 및 J7 중 다른 두개는 각각, 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
각각의 R19, R20 및 R21은, 독립적으로, H, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고;
G는 H, OH, 할로겐, 또는 O-[C(R8)(R9)]n-[(C=O)m-X1]j-Z이고;
각각의 R8 및 R9은, 독립적으로, H, 할로겐, C1-C6 알킬 또는 치환된 C1-C6 알킬이고;
X1 는 O, S 또는 N(E1)이고;
Z는 H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐, 치환된 C2-C6 알키닐 또는 N(E2)(E3)이고;
E1, E2 및 E3 은 각각, 독립적으로, H, C1-C6 알킬 또는 치환된 C1-C6 알킬이고;
n은 1 내지 약 6이고;
m은 0 또는 1이고;
j는 0 또는 1이고;
각각의 치환된 그룹은, 하기로부터 독립적으로 선택된 하나 이상의 임의로 보호된 치환체 그룹을 포함한다: 할로겐, OJ1, N(J1)(J2), =NJ1, SJ1, N3, CN, OC(=X2)J1, OC(=X2)-N(J1)(J2) 및 C(=X2)N(J1)(J2);
X2는 O, S 또는 NJ3이고;
각각의 J1, J2 및 J3 은, 독립적으로, H 또는 C1-C6 알킬이고; 그리고
j가 1이면, Z는 할로겐 또는 N(E2)(E3) 이외의 것이고; 그리고
상기 올리고머 화합물은 8 내지 40개의 단량체 하부단위를 포함하고 적어도 일부의 표적 핵산과 혼성화가능하다.
특정 구현예에서, M3 는 O, CH=CH, OCH2 또는 OC(H)(Bx2) 이다. 특정 구현예에서, M3 은 O이다.
각각의 J4, J5, J6 및 J7은, 독립적으로, H이다. 특정 구현예에서, J4 는 J5 또는 J7 중 하나와의 가교를 형성한다.
특정 구현예에서, A는 하기의 식 중 하나를 갖는다:
상기 식 중에서,
Q1 및 Q2 은 각각, 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시 또는 치환된 C1-C6 알콕시이다. 특정 구현예에서, Q1 및 Q2 은 각각 H이다. 특정 구현예에서, Q1 및 Q2 은 각각, 독립적으로, H 또는 할로겐이다. 특정 구현예에서, Q1 및 Q2 은 H이고, Q1 및 Q2 중 다른 하나는, F, CH3 또는 OCH3 이다.
특정 구현예에서, T1 은 하기 식을 갖는다:
상기 식 중에서,
Ra 및 Rc 각각은, 독립적으로, 보호된 하이드록실, 보호된 티올, C1-C6 알킬, 치환된 C1-C6 알킬, C1-C6 알콕시, 치환된 C1-C6 알콕시, 보호된 아미노 또는 치환된 아미노이고; 그리고
Rb은 O 또는 S이다. 특정 구현예에서, Rb은 O이고, Ra 및 Rc 각각은, 독립적으로, OCH3, OCH2CH3 또는 CH(CH3)2이다.
특정 구현예에서, G 는 할로겐, OCH3, OCH2F, OCHF2, OCF3, OCH2CH3, O(CH2)2F, OCH2CHF2, OCH2CF3, OCH2-CH=CH2, O(CH2)2-OCH3, O(CH2)2-SCH3, O(CH2)2-OCF3, O(CH2)3-N(R10)(R11), O(CH2)2-ON(R10)(R11), O(CH2)2-O(CH2)2-N(R10)(R11), OCH2C(=O)-N(R10)(R11), OCH2C(=O)-N(R12)-(CH2)2-N(R10)(R11) 또는 O(CH2)2-N(R12)-C(=NR13)[N(R10)(R11)]이고, 여기서 R10, R11, R12 및 R13 은 각각, 독립적으로, H 또는 C1-C6 알킬이다. 특정 구현예에서, G 는 할로겐, OCH3, OCF3, OCH2CH3, OCH2CF3, OCH2-CH=CH2, O(CH2)2-OCH3, O(CH2)2-O(CH2)2-N(CH3)2, OCH2C(=O)-N(H)CH3, OCH2C(=O)-N(H)-(CH2)2-N(CH3)2 또는 OCH2-N(H)-C(=NH)NH2 이다. 특정 구현예에서, G 는 F, OCH3 또는 O(CH2)2-OCH3 이다. 특정 구현예에서, G 는 O(CH2)2-OCH3 이다.
특정 구현예에서, 5'-말단 뉴클레오시드는 식 IIe를 갖는다:
특정 구현예에서, ssRNA에 대해 특히 적합한 것을 포함하는 안티센스 화합물은 정의된 패턴 또는 당 변형 모티프에서 올리고뉴클레오티드와 함께 마련된 변형된 당 모이어티 및/또는 천연 발생 당 모이어티 또는 그것의 영역 중 하나 이상의 유형을 포함한다. 그와 같은 모티프는 본원에서 논의된 당 변형 및/또는 다른 공지된 당 변형 중 임의의 것을 포함할 수 있다.
특정 구현예에서, 그와 같은 모티프는 본원에서 논의된 당 변형 및/또는 다른 공지된 당 변형 중 임의의 것을 포함할 수 있다. 특정 그와 같은 구현예에서, 상기 영역의 각각의 뉴클레오시드는 동일한 RNA-유사 당 변형을 포함한다. 특정 구현예에서, 상기 영역의 각각의 뉴클레오시드는 2'-F 뉴클레오시드이다. 특정 구현예에서, 상기 영역의 각각의 뉴클레오시드는 2'-OMe 뉴클레오시드이다. 특정 구현예에서, 상기 영역의 각각의 뉴클레오시드는 2'-MOE 뉴클레오시드이다. 특정 구현예에서, 상기 영역의 각각의 뉴클레오시드는 cEt 뉴클레오시드이다. 특정 구현예에서, 상기 영역의 각각의 뉴클레오시드는 LNA 뉴클레오시드이다. 특정 구현예에서, 균일한 영역은 모든 또는 본질적으로 모든 올리고뉴클레오티드를 구성한다. 특정 구현예에서, 영역은 1 내지 4개의 말단 뉴클레오시드를 제외하고 전체 올리고뉴클레오티드를 구성한다.
특정 구현예에서, 올리고뉴클레오티드는 교대 당 변형의 하나 이상의 영역을 포함하고, 상기 뉴클레오시드는 제1 유형의 당 변형을 갖는 뉴클레오티드 및 제2 유형의 당 변형을 갖는 뉴클레오티드 둘 사이를 교대한다. 특정 구현예에서, 둘 유형 모두의 뉴클레오시드는 RNA-유사 뉴클레오시드이다. 특정 구현예에서, 교대 뉴클레오시드는 하기로부터 선택된다: 2'-OMe, 2'-F, 2'-MOE, LNA, 및 cEt. 특정 구현예에서, 교대 변형은 2'-F 및 2'-OMe이다. 그와 같은 영역은 인접될 수 있거나 상이하게 변형된 뉴클레오시드 또는 콘주게이트된 뉴클레오시드에 의해 방해될 수 있다.
특정 구현예에서, 교대 변형 각각의 교대 영역은 단일 뉴클레오시드로 구성된다 (즉, 패턴은 (AB)xAy이고, 여기서 A는 제1 유형의 당 변형을 갖는 뉴클레오시드이고 B는 제2 유형의 당 변형을 갖는 뉴클레오시드이고; X는 1 내지 20이고 y는 0 또는 1이다). 특정 구현예에서, 교대 모티프 중 하나 이상의 교대 영역은 단일 초과의 뉴클레오시드의 유형을 포함한다. 예를 들면, 올리고뉴클레오티드 하기 뉴클레오시드 모티프 중 임의의 하나 이상의 영역을 포함할 수 있다:
AABBAA;
ABBABB;
AABAAB;
ABBABAABB;
ABABAA;
AABABAB;
ABABAA;
ABBAABBABABAA;
BABBAABBABABAA; 또는
ABABBAABBABABAA;
여기서 A는 제1 유형의 뉴클레오시드이고 B은 제2 유형의 뉴클레오시드이다. 특정 구현예에서, A 및 B 각각은 2'-F, 2'-OMe, BNA, 및 MOE로부터 선택된다.
특정 구현예에서, 그와 같은 교대 모티프를 갖는 올리고뉴클레오티드는 변형된 5' 말단 뉴클레오시드, 예컨대 식 IIc 또는 IIe의 것들 것 또한 포함한다.
특정 구현예에서, 올리고뉴클레오티드는 2-2-3 모티프을 갖는 영역을 포함한다. 그와 같은 영역은 하기 모티프를 포함한다:
-(A)2-(B)x-(A)2-(C)y-(A)3-
상기 식 중에서, A는 제1 유형의 변형된 뉴클레오시드이고;
B 및 C는, A보다 상이하게 변형된 뉴클레오시드이고, 그러나, B 및 C는 서로 동일 또는 상이한 변형을 가질 수 있고;
X 및 y는 1 내지 15이다.
특정 구현예에서, A는 2'-OMe 변형된 뉴클레오시드이다. 특정 구현예에서, B 및 C 둘 모두는 2'-F 변형된 뉴클레오시드이다. 특정 구현예에서, A는 2'-OMe 변형된 뉴클레오시드이고 B 및 C 둘 모두는 2'-F 변형된 뉴클레오시드이다.
특정 구현예에서, 올리고뉴클레오티드는 하기 당 모티프를 갖는다:
5'-(Q)-(AB)xAy-(D)z
상기 식 중에서,
Q는 안정된 포스페이트 모이어티를 포함하는 뉴클레오시드이다. 특정 구현예에서, Q은 식 IIc 또는 IIe를 갖는 뉴클레오시드이고;
A는 제1 유형의 변형된 뉴클레오시드이고;
B는 제2 유형의 변형된 뉴클레오시드;
D은 그것에 인접한 뉴클레오시드로부터 상이한 변형을 포함하는 변형된 뉴클레오시드이다. 따라서, y가 0이면, 이때 D는 B보다 상이하게 변형되어야 하고, y가 1이면, 이때 D는 A보다 상이하게 변형되어야 한다. 특정 구현예에서, D는 A 및 B 둘 모두와 상이하다.
X는 5 내지 15이고;
Y는 0 또는 1이고;
Z는 0 내지 4이다.
특정 구현예에서, 올리고뉴클레오티드는 하기 당 모티프를 갖는다:
5'-(Q)-(A)x-(D)z
상기 식 중에서,
Q는 안정된 포스페이트 모이어티를 포함하는 뉴클레오시드이다. 특정 구현예에서, Q은 식 IIc 또는 IIe를 갖는 뉴클레오시드이고;
A는 제1 유형의 변형된 뉴클레오시드이고;
D은 A로부터 상이한 변형을 포함하는 변형된 뉴클레오시드이다.
X는 11 내지 30이고;
Z는 0 내지 4이다.
특정 구현예에서 상기 모티프 중 A, B, C, 및 D는 하기로부터 선택된다: 2'-OMe, 2'-F, 2'-MOE, LNA, 및 cEt. 특정 구현예에서, D는 말단 뉴클레오시드를 나타낸다. 특정 구현예에서, 그와 같은 말단 뉴클레오시드는 표적 핵산에 혼성화하도록 설계되지 않는다 (하지만 하나 이상은 우연히 혼성화한다). 특정 구현예에서, 각각의 D 뉴클레오시드의 핵염기는, 표적 핵산의 상응하는 위치에서 핵염기의 동일성과는 무관하게 아데닌이다. 특정 구현예에서 각각의 D 뉴클레오시드의 핵염기는 티민이다.
특정 구현예에서, ssRNA로서 사용하는데 특히 적합한 것을 포함하는 안티센스 화합물은 정의된 패턴 또는 변형된 뉴클레오시드간 연결 모티프에서 올리고뉴클레오티드 또는 그것의 영역을 따라 마련된 변형된 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 교대 뉴클레오시드간 연결 모티프를 갖는 영역을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 균일하게 변형된 뉴클레오시드간 연결의 영역을 포함한다. 특정 그와 같은 구현예에서, 올리고뉴클레오티드는 포스포로티오에이트 뉴클레오시드간 연결에 의해 균일하게 연결된 영역을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 포스포로티오에이트 뉴클레오시드간 연결에 의해 균일하게 연결된다. 특정 구현예에서, 올리고뉴클레오티드의 각각의 뉴클레오시드간 연결은 포스포디에스테르 및 포스포로티오에이트로부터 선택된다. 특정 구현예에서, 올리고뉴클레오티드의 각각의 뉴클레오시드간 연결은 포스포디에스테르 및 포스포로티오에이트로부터 선택되고 적어도 하나의 뉴클레오시드간 연결은 포스포로티오에이트이다.
특정 구현예에서, 올리고뉴클레오티드는 적어도 6 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 8 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 10 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 6개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 8개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 10개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 하나의 12개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 그와 같은 구현예에서, 적어도 하나의 그와 같은 블록은 올리고뉴클레오티드의 3' 말단에 위치한다. 특정 그와 같은 구현예에서, 적어도 하나의 그와 같은 블록은 올리고뉴클레오티드의 3' 말단의 3개의 뉴클레오시드 내에 위치한다.
본원에서 기재된 다양한 당 모티프 중 임의의 것을 갖는 올리고뉴클레오티드는 임의의 연결 모티프를 가질 수 있다. 상기에서 기재된 것들을 비제한적으로 포함하는, 예를 들면, 올리고뉴클레오티드는, 하기의 비제한적인 표로부터 선택된 연결 모티프를 가질 수 있다:
2.
siRNA
화합물
특정 구현예에서, 안티센스 화합물은 이중나선 RNAi 화합물 (siRNA)이다. 상기 구현예에서, 하나 또는 양 가닥은 ssRNA를 위해 상기된 임의의 변형 모티프를 포함할 수 있다. 특정 구현예에서, ssRNA 화합물은 비변형된 RNA일 수 있다. 특정 구현예에서, siRNA 화합물은 비변형된 RNA 뉴클레오시드 및 변형된 뉴클레오시드간 연결을 포함할 수 있다.
여러 구현예는 이중가닥 조성물에 관한 것이고, 여기서, 각각의 가닥은 하나 이상의 변형되거나 비변형된 뉴클레오시드의 위치에 의해 정의되는 모티프를 포함한다. 특정 구현예에서, 이중나선 영역을 형성하기 위해 완전히 또는 적어도 부분적으로 혼성화하는 제1 및 제2 올리고머 화합물을 포함하고 핵산 표적에 상보적이고 여기에 혼성화하는 영역을 추가로 포함하는 조성물이 제공된다. 상기 조성물은 핵산 표적에 완전하거나 부분적 상보성을 갖는 안티센스 가닥인 제1 올리고머 화합물 및 제1 올리고머 화합물에 대한 하나 이상의 상보성 영역을 가져 적어도 하나의 이중나선 영역을 형성하는 센스 가닥인 제2 올리고머 화합물을 포함하는 것이 적합하다.
여러 구현예의 조성물은 핵산 표적에 혼성화하여 이의 정상 기능을 상실시킴에 의해 유전자 발현을 조절한다. 특정 구현예에서, 표적 핵산은 ANGPTL3이다. 특정 구현예에서, 표적화된 ANGPTL3의 분해는 본 발명의 조성물과 함께 형성되는 활성화된 RISC 복합체에 의해 촉진된다.
여러 구현예는 이중가닥의 조성물에 관한 것이고, 여기서, 가닥 중 하나는 예를 들어, 반대 가닥의 RISC(또는 절단) 복합체로의 우선적 로딩에 영향을 주는데 유용하다. 상기 조성물은 선택된 핵산 분자를 표적화하고 하나 이상의 유전자의 발현을 조절하기 위해 유용하다. 일부 구현예에서, 본 발명의 조성물은 표적 RNA 부분에 혼성화하여 상기 표적 RNA의 정상 기능을 상실시킨다.
특정 구현예는 이중가닥의 조성물에 관한 것이고, 여기서, 양 가닥은 헤미머 모티프, 완전히 변형된 모티프, 위치적으로 변형된 모티프 또는 교대 모티프를 포함한다. 본 발명의 조성물의 각각의 가닥을 변형시켜 예를 들어, siRNA 경로에서 특정 역할을 완수할 수 있다. 각각 가닥에 상이한 모티프 또는 각각의 가닥에서 상이한 화학적 변형을 갖는 동일한 모티프의 사용은 센스 가닥의 혼입을 억제하면서 RISC 복합체에 대해 안티센스 가닥을 표적화할 수 있게 한다. 상기 모델내에서, 각각의 가닥은 독립적으로 변형시켜 이것이 이의 특정 역할을 위해 증진될 수 있도록 한다. 상기 안티센스 가닥은 5' 말단에서 변형시켜 RISC의 하나의 영역에서 이의 역할을 증진시킬 수 있고 3' 말단은 상이하게 변형시켜 RISC의 상이한 영역에서 이의 역할을 증진시킬 수 있다.
이중가닥 올리고뉴클레오티드 분자는 자가-상보성 센스 및 안티센스 영역을 포함하는 이중가닥 폴리뉴클레오티드 분자일 수 있고 여기서, 상기 안티센스 영역은 이의 표적 핵산 분자 또는 이의 부분에서 뉴클레오티드 서열에 상보적인 뉴클레오티드 서열을 포함하고 상기 센스 영역은 표적 핵산 서열 또는 이의 부분에 상응하는 뉴클레오티드 서열을 갖는다. 이중-가닥 올리고뉴클레오티드 분자 2개의 별개의 올리고뉴클레오티드로부터 어셈블리될 수 있고, 하나의 가닥은 센스 가닥이고 다른 하나는 안티센스 가닥이고, 여기서 상기 안티센스 및 센스 가닥은 자가-상보적이고 (즉 각각의 가닥은 다른 가닥 내의 뉴클레오티드 서열과 상보적인 뉴클레오티드 서열을 포함한다); 예컨대 안티센스 가닥 및 센스 가닥은 이중나선 또는 이중-가닥 구조, 예를 들면 상기 이중-가닥 영역은 약 15 내지 약 30개, 예를 들면, 약 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 또는 30개의 염기쌍을 형성하며; 안티센스 가닥은 표적 핵산 분자 내의 뉴클레오티드 서열 또는 이의 부분 내의 뉴클레오티드 서열에 상보적인 뉴클레오티드 서열을 포함하고, 센스 가닥은 표적 핵산 서열 또는 이의 부분 (예를 들면, 이중-가닥 올리고뉴클레오티드 분자의 약 15 내지 약 25개 이상의 뉴클레오티드는 표적 핵산 또는 이의 부분에 상보적이다)을 포함한다. 대안적으로, 이중가닥 올리고뉴클레오티드는 단일 올리고뉴클레오티드로부터 어셈블리되고, 여기서, siRNA의 자가-상보성 센스 및 안티센스 영역은 핵산 기반 또는 비-핵산 기반 링커(들)에 의해 연결된다.
이중가닥의 올리고뉴클레오티드는 자가-상보성 센스 및 안티센스 영역을 갖는, 이중나선, 비대칭 이중나선, 헤어핀 또는 비대칭 헤어핀 2차 구조를 갖는 폴리뉴클레오티드일 수 있고, 여기서, 상기 안티센스 영역은 별도의 표적 핵산 분자 또는 이의 부분에서 뉴클레오티드 서열에 상보적인 뉴클레오티드 서열을 포함하고, 상기 센스 영역은 표적 핵산 서열 또는 이의 부분에 상응하는 뉴클레오티드 서열을 갖는다. 이중가닥의 올리고뉴클레오티드는 2개 이상의 루프 구조 및 자가 상보성 센스 및 안티센스 영역을 포함하는 스템을 갖는 환형 단일-가닥 폴리뉴클레오티드일 수 있고, 여기서, 상기 안티센스 영역은 표적 핵산 분자 또는 이의 부분에서 뉴클레오티드 서열에 상보적인 뉴클레오티드 서열을 포함하고 상기 센스 영역은 표적 핵산 서열 또는 이의 부분에 상응하는 뉴클레오티드 서열을 갖고, 여기서, 환형 폴리뉴클레오티드는 RNAi를 매개할 수 있는 활성 siRNA 분자를 생성하기 위해 생체내 또는 시험관내 가공될 수 있다.
특정 구현예에서, 이중가닥 올리고뉴클레오티드는 별도의 센스 및 안티센스 서열 또는 영역을 포함하고, 상기 센스 및 안티센스 영역은 당업계에 공지된 바와 같이 뉴클레오티드 또는 비-뉴클레오티드 링커 분자에 의해 공유적으로 연결되거나 대안적으로 이온 상호작용, 수소 결합, 반데르 발스 상호작용, 소수성 상호작용 및/또는 스택킹 상호작용에 의해 비공유적으로 연결된다. 특정 구현예에서, 이중가닥 올리고뉴클레오티드는 표적 유전자의 뉴클레오티드 서열에 상보적인 뉴클레오티드 서열을 포함한다. 또 다른 구현예에서, 이중가닥 올리고뉴클레오티드는 표적 유전자의 발현을 억제시키는 방식으로 표적 유전자의 뉴클레오티드 서열과 상호작용한다.
본원에 사용된 바와 같은, 이중가닥 올리고뉴클레오티드는 RNA만을 함유하는 상기 분자에 제한될 필요는 없지만 화학적으로 변형된 뉴클레오티드 및 비-뉴클레오티드를 추가로 포함한다. 특정 구현예에서, 짧은 간섭 핵산 분자는 2'-하이드록시 (2'-OH) 함유 뉴클레오티드가 없다. 특정 구현예에서, 짧은 간섭 핵산은 임의로 임의의 리보뉴클레오티드(예를 들어, 2'-OH 그룹을 갖는 뉴클레오티드)를 포함하지 않는다. 그러나, RNAi를 지지하기 위한 분자내 리보뉴클레오티드의 존재를 요구하지 않는 상기 이중가닥 올리고뉴클레오티드는 부착된 링커 또는 링커들 또는 다른 부착되거나 연합된 그룹, 모이어티 또는 2'-OH 기를 갖는 하나 이상의 뉴클레오티드를 함유하는 쇄를 가질 수 있다. 임의로, 이중가닥 올리고뉴클레오티드는 뉴클레오티드 위치 중 약 5, 10, 20, 30, 40, 또는 50%에서 리보뉴클레오티드를 포함할 수 있다. 본원에 사용된 바와 같은 용어 siRNA는 서열 특이적 RNAi, 예를 들어, 짧은 간섭 RNA (siRNA), 이중가닥 RNA (dsRNA), 마이크로-RNA (miRNA), 짧은 헤어핀 RNA (shRNA), 짧은 간섭 올리고뉴클레오티드, 짧은 간섭 핵산, 짧은 간섭 변형된 올리고뉴클레오티드, 화학적으로 변형된 siRNA, 전사 후 유전자 사일런싱 RNA(ptgsRNA), 및 기타를 매개할 수 있는 핵산 분자를 기재하기 위해 사용되는 다른 용어와 동등한 것으로 의미된다. 추가로, 본원에 사용된 바와 같은 용어 RNAi는 전사후 유전자 사일런싱, 번역 억제 또는 후생유전학과 같은 서열 특이적 RNA 간섭을 기재하기 위해 사용되는 다른 용어와 동등한 것으로 의미된다. 예를 들어, 이중가닥 올리고뉴클레오티드는 전사후 수준 및 전사전 수준 둘다에서 유전자를 후생유전학적으로 사일런싱하기 위해 사용될 수 있다. 비제한적인 실시예에서, 본 발명의 siRNA 분자에 의한 유전자 발현의 후생유전학적 조절은 유전자 발현을 변화시키기 위해 염색질 구조 또는 메틸화 패턴의 siRNA 매개된 변형으로부터 비롯될 수 있다(문헌참조: 예를 들어, Verdel et al., (2004) Science 303:672-676; Pal-Bhadra et al. 2004, Science, 303, 669-672; Allshire, 2002, Science, 297, 1818-1819; Volpe et al., 2002, Science, 297, 1833-1837; Jenuwein, 2002, Science, 297, 2215-2218; 및 Hall et al., 2002, Science, 297, 2232-2237).
본원에 제공된 여러 구현예의 화합물 및 조성물은 예를 들어, "헤어핀" 또는 스템-루프 이중가닥 RNA 효과기 분자를 포함하는 dsRNA-매개된 유전자 사일런싱 또는 RNAi 기전, 예를 들어, "헤어핀" 또는 스템-루프(stem-loop) 이중-가닥 RNA 효과기 분자에 의해 ANGPTL3를 표적화할 수 있는 것으로 고려되고, 여기서, 자가-상보성 서열을 갖는 단일 RNA 가닥으로 이중가닥 배좌 또는 RNA의 2개의 별도 가닥을 포함하는 이중나선 dsRNA 효과기 분자를 추정할 수 있다. 다양한 구현예에서, 상기 dsRNA는 전체적으로 리보뉴클레오티드로 이루어지거나, 예를 들어, 2000년 4월 19일자로 출원된 WO 00/63364, 또는 1999년 4월 21일자로 출원된 미국 시리즈 번호 60/130,377에 의해 기재된 바와 같은, 리보뉴클레오티드 및 데옥시뉴클레오티드의 혼합물, 예컨대 RNA/DNA 혼성체로 이루어진다. 상기 dsRNA 또는 dsRNA 효과기 분자는 분자의 하나의 분절에서의 뉴클레오티드가 상기 분자의 또 다른 분절에서 뉴클레오티드와 염기 쌍을 형성하도록 자가-상보성 영역을 갖는 단일 분자일 수 있다. 다양한 구현예에서, 단일 분자로 이루어진 dsRNA는 전반적으로 리보뉴클레오티드로 이루어지거나 데옥시리보뉴클레오티드 영역에 상보적인 리보뉴클레오티드 영역을 포함한다. 대안적으로, 상기 dsRNA는 서로 상보성 영역을 갖는 2개의 상이한 가닥을 포함할 수 있다.
다양한 구현예에서, 양 가닥은 전반적으로 리보뉴클레오티드로 이루어지고, 하나의 가닥은 전반적으로 리보뉴클레오티드로 이루어지고 하나의 가닥은 전반적으로 데옥시리보뉴클레오티드로 이루어지거나, 하나 또는 양 가닥은 리보뉴클레오티드와 데옥시리보뉴클레오티드의 혼합물을 함유한다. 특정 구현예에서, 상보성 영역은 서로에 대해서 및 표적 핵산 서열에 대해서 적어도 70, 80, 90, 95, 98, 또는 100% 상보적이다. 특정 구현예에서, 이중가닥 배좌로 존재하는 dsRNA 영역은 적어도 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 50, 75,100, 200, 500, 1000, 2000 또는 5000개 뉴클레오티드를 포함하거나 모든 뉴클레오티드를 cDNA로 포함하거나 다른 표적 핵산 서열은 dsRNA로 제공된다. 일부 구현예에서, dsRNA는 단일 가닥 말단과 같은 임의의 단일 가닥 영역을 함유하지 않거나 dsRNA는 헤어핀이다. 다른 구현예에서, dsRNA는 하나 이상의 단일-가닥 영역 또는 오버행을 갖는다. 특정 구현예에서, RNA/DNA 혼성체는 안티센스 가닥 또는 영역인 DNA 가닥 또는 영역(예를 들어,표적 핵산과 적어도 70, 80, 90, 95, 98, 또는 100% 상보성을 갖는다) 및 센스 가닥 또는 영역인 RNA 가닥 또는 영역 (예를 들어, 표적 핵산과 적어도 70, 80, 90, 95, 98, 또는 100%의 동일성을 갖는다), 및 그 반대의 경우를 포함한다.
다양한 구현예에서, RNA/DNA 혼성체는 본원에 기재된 방법 또는 2000년 4월 19일자로 출원된 WO 00/63364 또는 1999년 4월 21일자로 출원된 미국 시리즈 번호 60/130,377에서 기술된 것들과 같은 효소적 또는 화학적 합성 방법을 사용하여 시험관내 제조된다. 다른 구현예에서, 시험관내 합성된 DNA 가닥은 DNA 가닥의 세포로의 형질전환 전, 형질전환 후 또는 형질전환과 동시에 생체내 또는 시험관내에서 제조된 RNA 가닥과 복합체화된다. 또 다른 구현예에서, dsRNA는 센스 및 안티센스 영역을 함유하는 단일 환형 핵산이거나, dsRNA는 환형 핵산 및 제2 환형 핵산 또는 선형 핵산을 포함한다 (문헌참조: 예를 들어, 2000년 4월 19일에 출원된 WO 00/63364 또는 1999년 4월 21일자로 출원된 미국 시리즈 번호 60/130,377). 예시적인 환형 핵산은 라리아트(lariat) 구조를 포함하고, 여기서, 뉴클레오티드의 유리된 5' 포스포릴 그룹은 루프 백 양상으로 또 다른 뉴클레오티드의 2' 하이드록실 그룹에 연결된다.
다른 구현예에서, dsRNA는 하나 이상의 변형된 뉴클레오티드를 포함하고, 여기서, 당에서 2' 위치는 할로겐(예를 들어, 불소 그룹)을 함유하거나, 상응하는 2' 위치가 수소 또는 하이드록실 그룹을 함유하는 상응하는 dsRNA와 비교하여 시험관내 또는 생체내 dsRNA의 반감기를 증가시키는 알콕시 그룹(예를 들어, 메톡시 그룹)을 함유한다. 또 다른 구현예에서, dsRNA는 천연적으로 존재하는 포스포디에스테르 연결체 이외의 인접한 뉴클레오티드 사이에 하나 이상의 연결체를 포함한다. 상기 연결체의 예는 포스포르아미드, 포스포로티오에이트 및 포스포로디티오에이트 연결체를 포함한다. dsRNA는 또한 미국 특허 번호 6,673,661에 교시된 화학적으로 변형된 핵산 분자일 수 있다. 다른 구현예에서, dsRNA는 예를 들어, 2000년 4월 19일자로 출원된 WO 00/63364 또는 19, 2000, 또는 미국 시리즈 번호 1999년 4월 21일자로 출원된 60/130,377에 의해 기재된 바와 같은 하나 또는 2개의 캡핑된 가닥을 함유한다.
다른 구현예에서, dsRNA는 WO 00/63364에 개시된 적어도 부분적인 dsRNA 분자 중 임의의 것일 수 있고, 뿐만 아니라 미국 임시 출원 60/399,998; 및 미국 임시 출원 60/419,532, 및 PCT/US2003/033466에 개시된 dsRNA 분자 중 임의의 것일 수 있고, 이의 교시는 본원에 참조로 편입된다. 임의의 dsRNA는 본원에 기재된 방법 또는 WO 00/63364에 기재된 것들과 같은 표준 방법을 사용하여 시험관내 또는 생체내에서 발현될 수 있다.
점유
특정 구현예에서, 안티센스 화합물은 RNase H를 통한 절단 또는 표적 핵산을 유도하거나 RISC 경로를 통해 절단 또는 격리를 유도할 것으로 예상되지 않는다. 특정 상기 구현예에서, 안티센스 활성은 점유로부터 비롯될 수 있고, 여기서, 혼성화된 안티센스 화합물의 존재는 표적 핵산의 활성을 붕괴시킨다. 특정 상기 구현예에서, 안티센스 화합물은 균일하게 변형되거나 혼합된 변형 및/또는 변형되고 비변형된 뉴클레오시드를 포함할 수 있다.
표적 핵산, 표적 영역 및 뉴클레오티드 서열
ANGPTL3를 암호화하는 뉴클레오티드 서열은 비제한적으로 하기를 포함한다: 유전자은행 수탁 번호 NM_014495.2에서 제시된 인간 서열 (서열번호: 1로 본원에 포함) 또는 유전자 은행 수탁 번호 NT_032977.9 뉴클레오티드 33032001 내지 33046000 (본원에서 서열번호: 2와 같이 포함). 본원에 함유된 실시예에서 각각의 서열번호로 제시된 서열은 당 모이어티, 뉴클레오시드간 연결, 또는 핵염기에 대한 임의의 변형에 독립적인 것으로 이해된다. 그것으로서, 서열번호에 의해 규정된 안티센스 화합물은 당 모이어티, 뉴클레오시드간 연결, 또는 핵염기에 대한 하나 이상의 변형을 독립적으로 포함할 수 있다. ISIS 번호 (Isis No)에 의해 기재된 안티센스 화합물은 핵염기 서열 및 모티프의 조합을 나타낸다.
특정 구현예에서, 표적 영역은 표적 핵산의 구조적으로 규정된 영역이다. 예를 들면, 표적 영역은 3' UTR, 5' UTR, 엑손, 인트론, 엑손/인트론 콘주게이트, 암호화 영역, 번역 개시 영역, 번역 종료 영역, 또는 다른 규정된 핵산 영역을 포함할 수 있다. ANGPTL3에 대한 구조적으로 규정된 영역은 서열 데이타베이스 예컨대 NCBI로부터의 승인 번호에 의해 수득될 수 있고 그와 같은 정보는 본원에 참고로 포함되어 있다. 특정 구현예에서, 표적 영역은 표적 영역내의 하나의 표적 분절의 5' 표적 부위로부터 표적 영역내의 또 다른 표적 분절의 3' 표적 부위로의 서열을 포괄할 수 있다.
특정 구현예에서, "표적 분절"는 핵산 내 더 작은, 하위-부분의 표적 영역이다. 예를 들면 "표적 분절"은 하나 이상의 안티센스 화합물이 표적화된 표적 핵산의 뉴클레오티드의 서열일 수 있다. "5' 표적 부위" 또는 "5' 정지 부위"은 표적 분절의 5'-모스트 뉴클레오티드를 지칭한다. "3' 표적 부위" 또는 "3' 정지 부위"은 표적 분절의 3'-모스트 뉴클레오티드를 지칭한다.
표적화는 안티센스 화합물이 혼성화하는 적어도 하나의 표적 분절의 결정을 포함하고, 이로써 원하는 효과가 발생한다. 특정 구현예에서, 원하는 효과는 mRNA 표적 핵산 수준의 감소이다. 특정 구현예에서, 원하는 효과는 표적 핵산 또는 표적 핵산과 연관된 표현형 변화에 의해 암호화된 단백질의 수준의 감소이다.
표적 영역은 하나 이상의 표적 분절을 함유할 수 있다. 표적 영역 내의 다중 표적 분절은 중첩성일 수 있다. 대안적으로, 이들은 비-중첩성일 수 있다. 특정 구현예에서, 표적 영역 내의 표적 분절은 약 300개 이하의 뉴클레오티드에 의해 분리된다. 특정 구현예에서, 표적 영역 내의 표적 분절은 표적 핵산 상의 약 250, 200, 150, 100, 90, 80, 70, 60, 50, 40, 30, 20, 또는 10 또는 그 이하의 뉴클레오티드이고, 이전의 값의 임의의 2개에 의해 규정된 범위인 수많은 뉴클레오티드에 의해 분리된다. 특정 구현예에서, 표적 영역 내의 표적 분절은 표적 핵산 상의 약 5개 이하의 뉴클레오티드에 의해 분리된다. 특정 구현예에서, 표적 분절은 인접한다. 본원에서 열거된 5' 표적 부위 또는 3' 표적 부위의 임의의 것인 개시 핵산을 갖는 범위에 의해 규정된 표적 영역이 고려된다.
적당한 표적 분절은 5' UTR, 암호화 영역, 3' UTR, 인트론, 엑손, 또는 엑손/인트론 콘주게이트 내에서 발견될 수 있다. 개시 코돈 또는 정지 코돈을 함유하는 표적 분절은 또한 적당한 표적 분절이다. 적당한 표적 분절은 특정의 구조적으로 규정된 영역 예컨대 개시 코돈 또는 정지 코돈을 명시적으로 제외할 수 있다.
적당한 표적 분절의 결정은 게놈 도처의 다른 서열에 대한 표적 핵산의 서열의 비교를 포함할 수 있다. 예를 들면, BLAST 알고리즘은 상이한 핵산 중에서 유사성의 영역을 동정하기 위해 사용될 수 있다. 이러한 비교는 선택된 표적 핵산 이외의 서열 (즉, 비-표적 또는 오프-타겟(off-target) 서열)과 비특이적 방식으로 혼성화할 수 있는 안티센스 화합물의 서열의 선택을 방지할 수 있다.
활성 표적 영역 내의 안티센스 화합물의 활성의 변화 (예를 들면, 표적 핵산 수준의 퍼센트 감소에 의해 규정된 바와 같이)가 있을 수 있다. 특정 구현예에서, ANGPTL3 mRNA 수준의 감소는 ANGPTL3 단백질 발현의 억제를 가리킨다. ANGPTL3 단백질의 수준 감소는 또한 표적 mRNA 발현의 억제를 가리킨다. 더욱이, 표현형 변화, 예컨대 콜레스테롤, LDL, 트리글리세라이드, 또는 글루코오스 수준 감소는 ANGPTL3 mRNA 및/또는 단백질 발현의 억제를 가리킬 수 있다.
혼성화
일부 구현예에서, 혼성화는 본원에 개시된 안티센스 화합물 및 ANGPTL3 핵산 사이에서 발생한다. 혼성화의 가장 일반적인 기전은 핵산 분자의 상보적 핵염기 사이의 수소 결합 (예를 들면, 왓슨-크릭(Watson-Crick), 후그스텐(Hoogsteen) 또는 역전된 후그스텐(Hoogsteen) 수소 결합)을 수반한다.
혼성화는 가변 조건 하에서 발생할 수 있다. 엄격한 조건은 서열-의존적이고 혼성화될 핵산 분자의 성질 및 조성에 의해 결정된다.
서열이 표적 핵산과 특이적으로 혼성화할 수 있는 지를 측정하는 방법은 당해기술에 공지되어 있다 (Sambrooke 및 Russell, Molecular Cloning: A Laboratory Manual, 3rd Ed., 2001). 특정 구현예에서, 본원에서 제공된 안티센스 화합물은 ANGPTL3 핵산과 특이적으로 혼성화할 수 있다.
상보성
안티센스 화합물 및 표적 핵산은, 충분한 수의 안티센스 화합물의 핵염기가 표적 핵산의 상응하는 핵염기와 수소결합하여 이로써 원하는 효과가 발생할 수 있을 때 (예를 들면, 표적 핵산, 예컨대 ANGPTL3 핵산의 안티센스 억제), 서로 상보적이다.
더욱이, 안티센스 화합물은 ANGPTL3 핵산의 하나 이상의 분절 상에서 혼성화될 수 있고 이로써 개재 또는 인접한 분절은 혼성화 사건 (예를 들면, 루프 구조, 미스매치 또는 헤어핀 구조)에 관여하지 않는다.
특정 구현예에서, 본원에 제공된 안티센스 화합물, 또는 이의 특정 부분은, ANGPTL3 핵산, 표적 영역, 표적 분절, 또는 이의 특정 부분에 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100%, 또는 적어도 상기와 같이 상보적이다. 특정 구현예에서, 본원에 제공된 안티센스 화합물, 또는 이의 특정 부분은, 서열번호: 1 내지 2의 하나 이상의 서열과 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100%, 또는 적어도 상기와 같이 상보적이다. 표적 핵산을 갖는 안티센스 화합물의 퍼센트 상보성은 일상적인 방법을 사용하여 결정될 수 있다.
예를 들면, 20개 안티센스 화합물의 핵염기 중 18개는 표적 영역에 대해 상보적이고 따라서 특이적으로 혼성화하는, 안티센스 화합물은 90 퍼센트 상보성을 나타낼 것이다. 이러한 예시에서, 잔류 비-상보적 핵염기는 무리를 이루거나 상보적 핵염기와 함께 사이에 배치될 수 있고, 서로 또는 상보적 핵염기에 인접할 필요가 없다. 그것으로서, 표적 핵산에 완전한 상보성을 갖는 2 개의 영역에 의해 플랭킹된 4 개의 비-상보적 핵염기를 갖는 길이가 18개의 핵염기인 안티센스 화합물은 표적 핵산에 77.8% 전체 상보성을 가질 것이며, 따라서 본 발명의 범위 내에 있을 것이다. 표적 핵산의 영역을 갖는 안티센스 화합물의 퍼센트 상보성은 당해기술에서 공지된 BLAST 프로그램 (기본적 국소 정렬 연구 도구) 및 PowerBLAST 프로그램을 사용하여 일상적으로 결정될 수 있다 (Altschul 등, J. Mol. Biol., 1990, 215, 403 410; Zhang and Madden, Genome Res., 1997, 7, 649 656). 퍼센트 상동성, 서열 동일성 또는 상보성은 Smith 및 Waterman (Adv. Appl. Math., 1981, 2, 482 489)의 알고리즘을 사용하는 디폴트 세팅을 사용하여, 예를 들면, 갭(Gap) 프로그램(Wisconsin Sequence Analysis Package, Version 8 for Unix, Genetics Computer Group, University Research Park, Madison Wis.)에 의해 측정될 수 있다.
특정 구현예에서, 본원에서 제공된 안티센스 화합물, 또는 이의 명시된 부분은 표적 핵산, 또는 명시된 이의 부분에 대해 완전 상보적 (즉, 100% 상보적)이다. 예를 들면, 안티센스 화합물은 ANGPTL3 핵산, 또는 이의 표적 영역, 또는 표적 분절 또는 표적 서열에 대해 완전히 상보적일 수 있다. 본원에서 사용된 바와 같이, "완전히 상보적"은, 안티센스 화합물의 각각의 핵염기가 표적 핵산의 상응하는 핵염기와 정확한 염기 짝짓기를 할수 있다는 것을 의미한다. 예를 들면, 20 핵염기 안티센스 화합물은, 안티센스 화합물에 대해 완전 상보적인 표적 핵산의 상응하는 20 핵염기 부분이 있는 한, 400 핵염기 길이인 표적 서열에 대해 완전 상보적이다. 완전 상보성은 제 1 및/또는 제 2 핵산의 명시된 부분을 참조하여 또한 사용될 수 있다. 예를 들면, 30 핵염기 안티센스 화합물의 20 핵염기 부분은 400개 핵염기 길이인 표적 서열에 대해 "완전히 상보적"일 수 있다. 30 핵염기 올리고뉴클레오티드의 20 핵염기 부분은, 표적 서열이 상응하는 20 핵염기 부분을 갖고, 이때 각각의 핵염기가 안티센스 화합물의 20 핵염기 부분에 대해 상보적이라면, 표적 서열에 대해 완전히 상보적이다. 동시에, 전체 30 핵염기 안티센스 화합물은, 안티센스 화합물의 잔류 10 핵염기가 표적 서열에 대해 또한 상보적인지에 따라 표적 서열에 대해 또한 완전히 상보적일 수 있다.
비-상보적 핵염기의 위치는 안티센스 화합물의 5' 말단 또는 3' 말단에 있을 수 있다. 대안적으로, 비-상보적 핵염기 또는 핵염기들은 안티센스 화합물의 내부 위치에 있을 수 있다. 두개 이상의 비-상보적 핵염기가 존재할 때, 이들은 인접하거나(즉, 연결되거나), 또는 비-인접할 수 있다. 일 구현예에서, 비-상보적 핵염기는 갭머 안티센스 올리고뉴클레오티드의 윙 분절에 위치한다.
특정 구현예에서, 길이가 10, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20개이거나, 또는 최대로 상기 길이인 안티센스 화합물은 표적 핵산, 예컨대 ANGPTL3 핵산, 또는 명시된 이의 부분에 대해 6 이하, 5 이하, 4 이하, 3 이하, 2 이하, 또는 1 이하의 비-상보적 핵염기(들)을 포함한다.
특정 구현예에서, 길이가 10, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 또는 30개이거나, 또는 최대로 상기 길이인 안티센스 화합물은 표적 핵산, 예컨대 ANGPTL3 핵산, 또는 명시된 이의 부분에 대해 6 이하, 5 이하, 4 이하, 3 이하, 2 이하, 또는 1 이하의 비-상보적 핵염기(들)을 포함한다.
본원에서 제공된 안티센스 화합물은 또한 표적 핵산의 부분에 대해 상보적인 것을 포함한다. 본원에서 사용된 바와 같이, "부분"은 표적 핵산의 영역 또는 분절 내의 규정된 수의 인접한 (즉, 연결된) 핵염기를 의미한다. "부분"은 또한 규정된 수의 안티센스 화합물의 인접한 핵염기를 의미할 수 있다. 특정 구현예에서, 안티센스 화합물은 표적 분절의 적어도 8 핵염기 부분에 대해 상보적이다. 특정 구현예에서, 안티센스 화합물은 표적 분절의 적어도 10 핵염기 부분에 대해 상보적이다. 특정 구현예에서, 안티센스 화합물은 표적 분절의 적어도 15 핵염기 부분에 대해 상보적이다. 표적 분절의 적어도 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 또는 그 초과, 또는 이들 값의 임의의 2 개에 의해 규정된 범위의 핵염기 부분에 대해 상보적인 안티센스 화합물이 또한 고려된다.
동일성
본원에서 제공된 안티센스 화합물은 특정한 뉴클레오티드 서열, 서열번호, 또는 특정 서열번호로 나타내는 화합물, 또는 이의 부분에 대한 규정된 퍼센트 동일성을 또한 가질 수 있다. 본원에서 사용된 바와 같이, 안티센스 화합물은, 동일한 핵염기 짝짓기 능력을 갖는다면, 본원에 개시된 서열과 동일하다. 예를 들면, 우라실 및 티미딘 둘 다 아데닌과 쌍을 이루므로, 개시된 DNA 서열에서 티미딘 대신에 우라실을 함유하는 RNA가 DNA 서열과 동일한 것으로 간주된다. 본원에 기재된 안티센스 화합물 뿐만 아니라 본원에서 제공된 안티센스 화합물에 대해 비-동일한 염기를 갖는 화합물의 단축된 및 늘어난 버전이 또한 고려된다. 비-동일한 염기는 안티센스 화합물에 도처에서 분산되거나 서로 인접할 수 있다. 안티센스 화합물의 퍼센트 동일성은 비교되는 서열에 대해 동일한 염기 짝짓기를 갖는 염기의 수에 따라 산출된다.
특정 구현예에서, 안티센스 화합물, 또는 이의 부분은, 본원에 개시된 안티센스 화합물 또는 서열번호, 또는 이의 부분의 하나 이상과 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98%, 적어도 99% 또는 100% 동일하다.
변형
뉴클레오시드는 염기-당 조합이다. 뉴클레오시드의 핵염기 (또한 염기로서 공지됨) 부분은 보통 헤테로환 염기 모이어티이다. 뉴클레오티드는 뉴클레오시드의 당 부분에 공유 연결된 인산기를 추가로 포함하는 뉴클레오시드이다. 펜토푸라노실 당을 포함하는 뉴클레오시드에 대해, 인산기는 당의 2', 3' 또는 5' 히드록실 모이어티에 연결될 수 있다. 올리고뉴클레오티드는 서로에 대한 인접한 뉴클레오시드의 공유연결을 통해 형성되어, 선형 폴리머 올리고뉴클레오티드를 형성한다. 올리고뉴클레오티드 구조 내에, 인산기는 통상적으로 올리고뉴클레오티드의 뉴클레오시드간 연결을 형성하는 것으로 간주된다.
안티센스 화합물에 대한 변형은 뉴클레오시드간 연결, 당 모이어티, 또는 핵염기에 대한 치환 또는 변화를 포괄한다. 변형된 안티센스 화합물은 바람직한 특성 예컨대, 예를 들면, 증대된 세포 흡수, 핵산 표적에 대한 증대된 친화도, 뉴클레아제의 존재에서의 증가된 안정성, 또는 증가된 억제 활성 때문에 천연 형태와 비교하여 종종 바람직하다.
화학적으로 변형된 뉴클레오시드는 그것의 표적 핵산에 대해, 단축된 또는 절단된 안티센스 올리고뉴클레오티드의 결합 친화도를 증가시키기 위해 또한 이용될 수 있다. 결과적으로, 비교할만한 결과는 그와 같은 화학적으로 변형된 뉴클레오시드를 갖는 더 짧은 안티센스 화합물로 종종 수득될 수 있다.
변형된 뉴클레오시드간 연결
RNA 및 DNA의 "천연적으로 발생하는 뉴클레오시드간 연결"은 3' 내지 5' 포스포디에스테르 연결을 의미한다. 하나 이상의 변형된, 즉 비-천연 발생, 뉴클레오시드간 연결을 갖는 안티센스 화합물은 바람직한 특성 예컨대, 예를 들면, 증대된 세포 흡수, 표적 핵산에 대한 증대된 친화도, 및 뉴클라아제의 존재에서 증가된 안정성 때문에 천연 발생 뉴클레오시드간 연결을 갖는 안티센스 화합물과 비교하여 종종 선택된다.
변형된 뉴클레오시드간 연결을 갖는 올리고뉴클레오티드는 인 원자를 보유하는 뉴클레오시드간 연결 뿐만 아니라 인 원자를 갖지 않는 뉴클레오시드간 연결을 포함한다. 대표적인 인을 함유하는 뉴클레오시드간 연결은, 비제한적으로, 포스포디에스테르, 포스포트리에스테르, 메틸포스포네이트, 포스포르아미데이트, 및 포스포로티오에이트를 포함한다. 인-함유 및 비-인-함유 연결의 제조 방법은 공지되어 있다.
특정 구현예에서, ANGPTL3 핵산에 표적화된 안티센스 화합물은 하나 이상의 변형된 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 변형된 뉴클레오시드간 연결은 포스포로티오에이트 연결이다. 특정 구현예에서, 안티센스 화합물의 각각의 뉴클레오시드간 연결은 포스포로티오에이트 뉴클레오시드간 연결이다.
특정 구현예에서, 올리고뉴클레오티드는 규정된 패턴 또는 변형된 뉴클레오시드간 연결 모티프에서 올리고뉴클레오티드 또는 그것의 영역을 따라 배열된 변형된 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 뉴클레오시드간 연결은 갭핑된 모티프에서 배열되어 있다. 그러한 구현예에서, 2개 윙 영역 중 각각에서 뉴클레오시드간 연결은 갭 영역에서의 뉴클레오시드간 연결과 상이하다. 그러한 구현예에서, 윙 영역 중에서 뉴클레오시드간 연결은 포스포디에스테르이고, 갭에서의 뉴클레오시드간 연결은 포스포로티오에이트이다. 뉴클레오시드 모티프는 독립적으로 선택되며, 따라서 갭핑된 뉴클레오시드간 연결을 갖는 그러한 올리고뉴클레오티드는 갭핑된 뉴클레오시드를 가지지 않을 수 있고, 만약 그것이 갭핑된 뉴클레오시드를 갖지 않는다면, 윙 및 갭 길이는 동일하거나 동일하지 않을 수 있다.
특정 구현예에서, 올리고뉴클레오티드는 교대 뉴클레오시드간 연결 모티프를 갖는 영역을 포함한다. 특정 구현예에서, 본 발명의 올리고뉴클레오티드는 균일하게 변형된 뉴클레오시드간 연결의 영역을 포함한다. 특정 그와 같은 구현예에서, 올리고뉴클레오티드는 포스포로티오에이트 뉴클레오시드간 연결에 의해 균일하게 연결된 영역을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 포스포로티오에이트에 의해 균일하게 연결된다. 특정 구현예에서, 올리고뉴클레오티드의 각각의 뉴클레오시드간 연결은 포스포디에스테르 및 포스포로티오에이트로부터 선택된다. 특정 구현예에서, 올리고뉴클레오티드의 각각의 뉴클레오시드간 연결은 포스포디에스테르 및 포스포로티오에이트로부터 선택되고 적어도 하나의 뉴클레오시드간 연결은 포스포로티오에이트이다.
특정 구현예에서, 올리고뉴클레오티드는 적어도 6 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 8 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 10 개의 포스포로티오에이트 뉴클레오시드간 연결을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 6개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 8개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 10개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 하나의 블록을 포함한다. 특정 구현예에서, 올리고뉴클레오티드는 적어도 하나의 12개의 연속적인 포스포로티오에이트 뉴클레오시드간 연결의 적어도 블록을 포함한다. 특정 그와 같은 구현예에서, 적어도 하나의 그와 같은 블록은 올리고뉴클레오티드의 3' 말단에 위치한다. 특정 그와 같은 구현예에서, 적어도 하나의 그와 같은 블록은 올리고뉴클레오티드의 3' 말단의 3개의 뉴클레오시드 내에 위치한다.
특정 구현예에서, 올리고뉴클레오티드는 1 이상의 메틸포스포네이트 연결을 포함한다. 특정 구현예에서, 갭머 뉴클레오시드 모티프를 갖는 올리고뉴클레오티드는 1 또는 2의 메틸포스포네이트 연결을 제외한 모든 포스포로티오에이트 연결을 포함하는 연결 모티프를 포함한다. 특정 구현예에서, 하나의 메틸포스포네이트 연결은 갭머 뉴클레오시드 모티프를 갖는 올리고뉴클레오티드의 중앙 갭 내에 있다.
특정 구현예에서, 뉴클레아제 내성을 유지하기 위하여 포스포로티오에이트 뉴클레오시드간 연결 및 포스포디에스테르 뉴클레오시드간 연결의 수를 배열하는 것이 바람직하다. 특정 구현예에서, 뉴클레아제 내성을 유지하기 위하여 포스포로티오에이트 뉴클레오시드간 연결의 수 및 위치와 포스포디에스테르 뉴클레오시드간 연결의 수 및 위치를 배열하는 것이 바람직하다. 특정 구현예에서, 포스포로티오에이트 뉴클레오시드간 연결의 수는 감소할 수 있고, 포스포디에스테르 뉴클레오시드간 연결의 수는 증가할 수 있다. 특정 구현예에서, 여전히 뉴클레아제 내성을 유지하는 동안, 포스포로티오에이트 뉴클레오시드간 연결의 수는 감소할 수 있고, 포스포디에스테르 뉴클레오시드간 연결의 수는 증가할 수 있다. 특정 구현예에서, 뉴클레아제 내성을 유지하는 동안 포스포로티오에이트 뉴클레오시드간 연결의 수를 감소시키는 것이 바람직하다. 특정 구현예에서, 뉴클레아제 내성을 유지하기 위하여 포스포디에스테르 뉴클레오시드간 연결의 수를 증가시키는 것이 바람직하다.
변형된 당 모이어티
안티센스 화합물은 임의로 하나 이상의 뉴클레오시드를 함유할 수 있으며, 여기서 당 그룹은 변형되었던 것이다. 그와 같은 당 변형된 뉴클레오시드는 안티센스 화합물에 대한 증대된 뉴클레아제 안정성, 증가된 결합 친화도, 또는 일부 다른 유익한 생물학적 특성을 부여할 수 있다. 특정 구현예에서, 뉴클레오시드는 화학적으로 변형된 리보푸라노스 환 모이어티를 포함한다. 화학적으로 변형된 리보푸라노스 환의 예는 비제한적으로 하기를 포함한다: 치환체 그룹의 부가 (5' 및 2' 치환체 그룹, 이환식 핵산 (BNA)를 형성하기 위한 비-제미널(geminal) 환 원자의 가교, 리보실 환 산소 원자의 S, N(R), 또는 C(R1)(R2)의 교체 포함) (R, R1 및 R2각각은 독립적으로 H, C1-C12 알킬 또는 보호기로부터 선택된다) 및 이들의 조합. 화학적으로 변형된 당의 예시는 하기를 포함한다: 2'-F-5'-메틸 치환된 뉴클레오시드 (참고, PCT 국제 출원 WO 2008/101157, 다른 개시된 5', 2'-비스 치환된 뉴클레오시드에 대해 8/21/08에 공개됨), 또는 2'-위치에서 추가 치환에 의해 S에 의한 리보실 환 산소 원자의 교체 (참고, 공개된 미국 특허 출원 US2005/0130923, 2005년 6월 16일에 공개됨), 또는 대안적으로, BNA의 5'-치환 (참고, PCT 국제 출원 WO 2007/134181, 11/22/07에 공개됨, LNA는, 예를 들면, 5'-메틸 또는 5'-비닐 그룹으로 치환됨).
변형된 당 모이어티를 갖는 뉴클레오시드의 예는 5'-비닐, 5'-메틸 (R 또는 S), 4'-S, 2'-F, 2'-OCH3, 2'-OCH2CH3, 2'-OCH2CH2F 및 2'-O(CH2)2OCH3 치환체 그룹을 포함하는 뉴클레오시드를 비제한적으로 포함한다. 2' 위치에서의 치환체는 알릴, 아미노, 아지도, 티오, O-알릴, O-C1-C10 알킬, OCF3, OCH2F, O(CH2)2SCH3, O(CH2)2-O-N(Rm)(Rn), O-CH2-C(=O)-N(Rm)(Rn), 및 O-CH2-C(=O)-N(Rl)-(CH2)2-N(Rm)(Rn)로부터 선택될 수 있고, 여기서 각각의 Rl, Rm 및 Rn은 독립적으로, H 또는 치환된 또는 비치환된 C1-C10 알킬이다.
본원에서 사용된 바와 같이, "이환식 뉴클레오시드"는 이환식 당 모이어티를 포함하는 변형된 뉴클레오시드를 의미한다. 이환식 핵산 (BNA)의 예는 4' 및 2' 리보실 환 원자 사이의 가교를 포함하는 뉴클레오시드를 비제한적으로 포함한다. 특정 구현예에서, 본원에서 제공된 안티센스 화합물은 하나 이상의 BNA 뉴클레오시드를 포함하고, 여기서 상기 가교는 하기 화학식 중 하나를 포함한다: 4'-(CH2)-O-2' (LNA); 4'-(CH2)-S-2'; 4'-(CH2)2-O-2' (ENA); 4'-CH(CH3)--O-2' 및 4'-C-H(CH2OCH3)--O-2' (및 이의 유사체, 참고: 미국 특허 7,399,845, 2008년 7월 15일 발행됨); 4'-C(CH3)(CH3)--O-2' (및 이의 유사체, 참고: PCT/US2008/068922, WO/2009/006478로서 2009년 1월 8일 공보됨); 4'-CH2-N(OCH3)-2' (및 이의 유사체, 참고: PCT/US2008/064591, WO/2008/150729로서 2008년 12월 11일 공보됨); 4'-CH2-O-N(CH3)-2' (참고: 국제 출원 공보 US2004-0171570, 2004년 9월 23일 공보됨); 4'-CH2-N(R)-O-2', 여기서 R은 H, C1-C12 알킬, 또는 보호기 (참고: 미국 특허 7,427,672, 2008년 9월 23일 발행됨); 4'-CH2-C-(H)(CH3)-2' (참고: Zhou et al., J. Org. Chem., 2009, 74, 118-134); 및 4'-CH2-C-(=CH2)-2' (및 이의 유사체, 참고: PCT/US2008/066154, WO 2008/154401로서 2008년 12월 8일 공보됨)이다.
이환식 뉴클레오티드와 관련된 추가적인 보고는 다음 출판 문헌에서 발견될 수 있다 (예를 들어, 참고: Srivastava et al., J. Am. Chem. Soc., 2007, 129(26) 8362-8379; Frieden et al., Nucleic Acids Research, 2003, 21, 6365-6372; Elayadi et al., Curr. Opinion Invens. Drugs, 2001, 2, 558-561; Braasch et al., Chem. Biol., 2001, 8, 1-7; Orum et al., Curr. Opinion Mol. Ther., 2001, 3, 239-243; Wahlestedt et al., Proc. Natl. Acad. Sci. U. S. A., 2000, 97, 5633-5638; Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; 미국 특허 번호: 7,741,457; 7,399,845; 7,053,207; 7,034,133; 6,794,499; 6,770,748; 6,670,461; 6,525,191; 6,268,490; 미국 특허 공보 번호: US2008-0039618; US2007-0287831; US2004-0171570; 미국 특허 출원 시리즈 번호: 61/097,787; 61/026,995; 및 국제 출원: WO 2009/006478; WO 2008/154401; WO 2008/150729; WO 2009/100320; WO 2011/017521; WO 2009/067647; WO 2010/036698; WO 2007/134181; WO 2005/021570; WO 2004/106356; WO 99/14226. 각각의 상기 이환식 뉴클레오시드는 예를 들면 α-L-리보푸라노스 및 β-D-리보푸라노스를 포함하는 하나 이상의 입체화학적 당 배치를 갖도록 제조될 수 있다 (참고 PCT 국제 출원 PCT/DK98/00393, WO 99/14226로서 1999년 3월 25일 공개).
본원에서 사용된 바와 같이, "단환식 뉴클레오시드"는 이환식 당 모이어티가 아닌 변형된 당 모이어티를 포함하는 뉴클레오시드를 의미한다. 특정 구현예에서, 뉴클레오시드의 당 모이어티, 또는 당 모이어티 유사체는 임의의 위치에서 변형 또는 치환될 수 있다.
본원에서 사용된 바와 같이, "4'-2' 이환식 뉴클레오시드" 또는 "4' 내지 2' 이환식 뉴클레오시드"는 당 환의 2' 탄소 원자 및 4' 탄소 원자를 연결하는 가교를 포함하는 푸라노스 환을 포함하는 이환식 뉴클레오시드를 의미한다.
특정 구현예에서, BNA 뉴클레오시드의 이환식 당 모이어티는, 비제한적으로, 펜토푸라노실 당 모이어티의 탄소 원자의 4' 및 2' 위치 사이의 적어도 하나의 가교를 갖는 화합물을 포함하고, 여기서 그와 같은 가교는 독립적으로, -[C(Ra)(Rb)]n-, -C(Ra)=C(Rb)-, -C(Ra)=N-, -C(=NRa)-, -C(=O)-, -C(=S)-, -O-, -Si(Ra)2-, -S(=O)x-, 및 -N(Ra)-로부터 독립적으로 선택된 1개 또는 2 내지 4개의 연결된 기를 포함하고; 여기서 x 는 0, 1, 또는 2이고; n 은 1, 2, 3, 또는 4이고; 각각의 Ra 및 Rb는, 독립적으로, H, 보호기, 하이드록실, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C5-C20 아릴, 치환된 C5-C20 아릴, 헤테로사이클 라디칼, 치환된 헤테로사이클 라디칼, 헤테로아릴, 치환된 헤테로아릴, C5-C7 지환족 라디칼, 치환된 C5-C7 지환족 라디칼, 할로겐, OJ1, NJ1J2, SJ1, N3, COOJ1, 아실 (C(=O)-H), 치환된 아실, CN, 설포닐 (S(=O)2-J1), 또는 설폭실 (S(=O)-J1)이고;
그리고 J1 및 J2 각각은 독립적으로, H, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C5-C20 아릴, 치환된 C5-C20 아릴, 아실 (C(=O)-H), 치환된 아실, 헤테로환 라디칼, 치환된 헤테로환 라디칼, C1-C12 아미노알킬, 치환된 C1-C12 아미노알킬 또는 보호기이다.
특정 구현예에서, 이환식 당 모이어티의 가교는, -[C(Ra)(Rb)]n-, -[C(Ra)(Rb)]n-O-, -C(RaRb)-N(R)-O- 또는 -C(RaRb)-O-N(R)-이다. 특정 구현예에서, 가교는 4'-CH2-2', 4'-(CH2)2-2', 4'-(CH2)3-2', 4'-CH2-O-2', 4'-(CH2)2-O-2', 4'-CH2-O-N(R)-2' 및 4'-CH2-N(R)-O-2'- 이고, 이때 각각의 R은 독립적으로, H, 보호기, 또는 C1-C12 알킬이다.
특정 구현예에서, 이환식 뉴클레오시드는 이성질체 배치에 의하여 추가로 정의된다. 예를 들어, 4'-(CH2)-O-2' 가교를 포함하는 뉴클레오시드는, α-L 배위 또는 β-D 배위일 수 있다. 이전에, α-L-메틸렌옥시 (4'-CH2-O-2') BNA'는 안티센스 활성을 보여준 안티센스 올리고뉴클레오티드에 통합되었다 (Frieden et al., Nucleic Acids Research, 2003, 21, 6365-6372).
특정 구현예에서, 이환식 뉴클레오시드는 4' 내지 2' 가교를 갖는 것들을 포함하고, 그러한 가교는 비제한적으로, α-L-4'-(CH2)-O-2', β-D-4'-CH2-O-2', 4'-(CH2)2-O-2', 4'-CH2-O-N(R)-2', 4'-CH2-N(R)-O-2', 4'-CH(CH3)-O-2', 4'-CH2-S-2', 4'-CH2-N(R)-2', 4'-CH2-CH(CH3)-2', 및 4'-(CH2)3-2'를 포함하고, 여기서 R은 H, 보호기 또는 C1-C12 알킬이다.
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
-Qa-Qb-Qc- 는 -CH2-N(Rc)-CH2-, -C(=O)-N(Rc)-CH2-, -CH2-O-N(Rc)-, -CH2-N(Rc)-O- 또는 -N(Rc)-O-CH2 이고;
Rc 는 C1-C12 알킬 또는 아미노 보호기이고; 그리고
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
Za는 C1-C6 알킬, C2-C6 알케닐, C2-C6 알키닐, 치환된 C1-C6 알킬, 치환된 C2-C6 알케닐, 치환된 C2-C6 알키닐, 아실, 치환된 아실, 치환된 아미드, 티올, 또는 치환된 티올이다.
일 구현예에서, 각각의 치환된 그룹은, 독립적으로, 할로겐, 옥소, 하이드록실, OJc, NJcJd, SJc, N3, OC(=X)Jc, 및 NJeC(=X)NJcJd로부터 독립적으로 선택된 치환체 그룹으로 단일 또는 다중 치환되고, 여기서 각각의 Jc, Jd 및 Je는, 독립적으로, H, C1-C6 알킬, 또는 치환된 C1-C6 알킬이고 X는 O 또는 NJc이다.
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
Zb는 C1-C6 알킬, C2-C6 알케닐, C2-C6 알키닐, 치환된 C1-C6 알킬, 치환된 C2-C6 알케닐, 치환된 C2-C6 알키닐, 또는 치환된 아실(C(=O)-)이다.
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
Rd는 C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐, 또는 치환된 C2-C6 알키닐이고;
각각의 qa, qb, qc 및 qd는 독립적으로, H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐, C1-C6 알콕실, 치환된 C1-C6 알콕실, 아실, 치환된 아실, C1-C6 아미노알킬 또는 치환된 C1-C6 아미노알킬이다;
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
qa, qb , qe 및 qf 각각은, 독립적으로, 수소, 할로겐, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C1-C12 알콕시, 치환된 C1-C12 알콕시, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)-NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)-NJjJk 또는 N(H)C(=S)NJjJk 이고;
또는 qe 및 qf는 함께 =C(qg)(qh)이고;
qg 및 qh 각각은, 독립적으로, H, 할로겐, C1-C12 알킬, 또는 치환된 C1-C12 알킬이다.
4'-CH2-O-2'가교를 가지는 아데닌, 시토신, 구아닌, 5-메틸-시토신, 티민 및 우라실 이환식 뉴클레오시드의 합성 및 제조와 함께, 이들의 올리고머화, 및 핵산 인식 특성이 설명되어 있다 (Koshkin et al., Tetrahedron, 1998, 54, 3607-3630). 이환식 뉴클레오시드의 합성이 WO 98/39352 및 WO 99/14226에 또한 설명되어 있다.
4'→ 2' 가교 기, 예컨대, 4'-CH2-O-2' 및 4'-CH2-S-2'를 갖는 다양한 이환식 뉴클레오시드의 유사체가 또한 제조되었다(Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222). 핵산 중합효소에 대한 기질로서 사용하기 위한 이환식 뉴클레오시드를 포함하는 올리고데옥시리보뉴클레오티드 이중구조의 제조가 또한 설명되어 있다 (Wengel et al., WO 99/14226). 더욱이, 2'-아미노-BNA, 신규 형태적으로 제한된 고-친화도 올리고뉴클레오티드 유사체의 합성은 당해기술에 기재되었다 (참고: Singh et al., J. Org. Chem., 1998, 63, 10035-10039). 또한, 2'-아미노- 및 2'-메틸아미노-BNA'가 제조되었고 상보적 RNA 및 DNA 가닥을 갖는 그것의 이중나선의 열 안정성은 이전에 보고되었다.
특정 구현예에서, 이환식 뉴클레오시드는 하기 화학식을 갖는다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
Ta 및 Tb 각각은, 독립적으로 H, 하이드록실 보호기, 콘주게이트 그룹, 반응성 인 그룹, 인 모이어티, 또는 지지 매질에 대한 공유 부착(covalent attachment)이고;
qi, qj, qk 및 ql 각각은, 독립적으로, 수소, 할로겐, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C1-C12 알콕실, 치환된 C1-C12 알콕실, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)-NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)-NJjJk 또는 N(H)C(=S)NJjJk 이고; 그리고
qi 및 qj 또는 ql 및 qk 는 함께 =C(qg)(qh)이고, 여기서 qg 및 qh은 각각 독립적으로 H, 할로겐, C1-C12 알킬 또는 치환된 C1-C12 알킬이다.
4'-(CH2)3-2'가교를 갖는 하나의 탄소환식 이환식 뉴클레오시드 및 알케닐 유사체, 가교 4'-CH=CH-CH2-2'가 기재되었다 (참고: Frier et al., Nucleic Acids Research, 1997, 25(22), 4429-4443 및 Albaek et al., J. Org . Chem ., 2006, 71, 7731-7740). 탄소환식 이환식 뉴클레오시드의 합성 및 제조는 그것의 올리고머화 및 생화학적 연구와 함께 또한 기재되었다 (참고: Srivastava et al., J. Am. Chem. Soc . 2007, 129(26), 8362-8379).
특정 구현예에서, 이환식 뉴클레오시드는, 비제한적으로, (A) α-L-메틸렌옥시 (4'-CH2-O-2') BNA, (B) β-D-메틸렌옥시 (4'-CH2-O-2') BNA, (C) 에틸렌옥시 (4'-(CH2)2-O-2') BNA, (D) 아미노옥시 (4'-CH2-O-N(R)-2') BNA, (E) 옥시아미노 (4'-CH2-N(R)-O-2') BNA, 및 (F) 메틸(메틸렌옥시) (4'-CH(CH3)-O-2') BNA (또한 제한된 에틸 또는 cEt로 지칭됨), (G) 메틸렌-티오 (4'-CH2-S-2') BNA, (H) 메틸렌-아미노 (4'-CH2-N(R)-2') BNA, (I) 메틸 탄소환식 (4'-CH2-CH(CH3)-2') BNA, (J) 프로필렌 탄소환식 (4'-(CH2)3-2') BNA 및 (K) 비닐 BNA를, 이하에서 묘사된 바와 같이 포함한다:
여기서 Bx는 염기 모이어티이고 R은, 독립적으로, H, 보호기 또는 C1-C6 알킬 또는 C1-C6 알콕시이다.
본원에서 사용된 바와 같이, "변형된 테트라하이드로피란 뉴클레오시드" 또는 "변형된 THP 뉴클레오시드"는 노말 뉴클레오시드에서 펜토푸라노실 잔기를 대체하기 위해 치환된 6-원 테트라하이드로피란 "당"을 갖는 뉴클레오시드를 의미하고, 당 대용물로 지칭될 수 있다. 변형된 THP 뉴클레오시드는, 비제한적으로, 헥시톨 핵산 (HNA), 아니톨 핵산 (ANA), 만니톨 핵산 (MNA)로서 당해 분야에서 불리는 것들 (참고 Leumann, Bioorg. Med . Chem ., 2002, 10, 841-854) 또는 플루오로 HNA (F-HNA) (하기 예시된 바와 같이 테트로하이드로피라닐 환계를 갖는다)을 포함한다.
특정 구현예에서, 당 대용물은 하기 화학식으로부터 선택된다:
상기 식 중에서,
Bx는 헤테로환 염기 모이어티이고;
T3 및 T4 각각은, 독립적으로, 테트라하이드로피란 뉴클레오시드 유사체를 올리고머 화합물에 연결시키는 뉴클레오시드간 연결 그룹이거나 T3 및 T4 중 하나는 테트라하이드로피란 뉴클레오시드 유사체를 올리고머 화합물 또는 올리고뉴클레오티드에 연결시키는 뉴클레오시드간 연결 그룹이고, 그리고 T3 및 T4 중 다른 것은 H, 히드록실 보호기, 연결된 콘주게이트 그룹, 또는 5' 또는 3'-말단기이고;
q1, q2, q3, q4, q5, q6 및 q7 각각은 독립적으로 H, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고; 그리고
R1 및 R2 중 한쪽은 수소이고 다른 쪽은 할로겐, 치환된 또는 비치환된 알콕시, NJ1J2, SJ1, N3, OC(=X)J1, OC(=X)NJ1J2, NJ3C(=X)NJ1J2 및 CN으로부터 선택되되, 여기서 X는 O, S 또는 NJ1이고 각각의 J1, J2 및 J3은, 독립적으로, H 또는 C1-C6 알킬이다.
특정 구현예에서, q1, q2, q3, q4, q5, q6 및 q7는 각각 H이다. 특정 구현예에서, q1, q2, q3, q4, q5, q6 및 q7 중 적어도 하나는 H 이외의 것이다. 특정 구현예에서, q1, q2, q3, q4, q5, q6 및 q7 중 적어도 하나는 메틸이다. 특정 구현예에서, R1 및 R2 중 하나가 F인 THP 뉴클레오시드가 제공된다. 특정 구현예에서, R1은 플루오로이고 R2는 H이며; R1은 메톡시이고 R2는 H이며, 그리고 R1은 메톡시에톡시이고 R2는 H이다.
특정 구현예에서, 당 대용물은 5개 초과의 원자를 갖고 1개 초과의 헤테로원자를 갖는 환을 포함한다. 예를 들어, 모폴리노 변형된 당 모이어티를 포함하는 뉴클레오시드 및 올리고머 화합물에서의 그들의 용도가 보고되었다 (예를 들어 참고: Braasch et al., Biochemistry, 2002, 41, 4503-4510; 및 미국 특허 5,698,685; 5,166,315; 5,185,444; 및 5,034,506). 본원에서 사용된 바와 같이, "모폴리노"는 하기 구조를 갖는 당 대용물을 의미한다:
특정 구현예에서, 모폴리노는, 상기 모폴리노 구조로부터의 다양한 치환체 그룹을 부가하거나 변경시킴으로써 변형될 수 있다. 그와 같은 당 대용물은 본원에서 "변형된 모폴리노"라 칭한다.
하기와 같은 변형의 조합이 또한 비제한적으로 제공된다: 2'-F-5'-메틸 치환된 뉴클레오시드 (참고 다른 개시된 5', 2'-비스 치환된 뉴클레오시드에 대해 8/21/08에 공개된 PCT 국제 출원 WO 2008/101157) 및 2'-위치에서의 리보실 환 산소 원자 대신에 S에 의한 대체 및 추가 치환 (참고 2005년 6월 16일에 공개된 미국 특허 출원 US2005-0130923) 또는 대안적으로 이환식 핵산의 5'-치환 (참고 11/22/07에 공개된 PCT 국제 출원 WO 2007/134181, 여기서 4'-CH2-O-2' 이환식 뉴클레오시드는 5' 위치에서 5'-메틸 또는 5'-비닐기로 추가로 치환된다). 탄소환식 이환식 뉴클레오시드의 합성 및 제조는 그것의 올리고머화 및 생화학적 연구와 함께 또한 기재되었다 (참고, 예를 들면, Srivastava et al., J. Am. Chem. Soc. 2007, 129(26), 8362-8379).
특정 구현예에서, 안티센스 화합물은 하나 이상의 변형된 사이클로헥세닐 뉴클레오시드를 포함하고, 이는 천연 발생 뉴클레오시드에 존재하는 펜토푸라노실 대신 6-원 사이클로헥세닐을 갖는 뉴클레오시드이다. 변형된 사이클로헥세닐 뉴클레오시드는 당업계에서 다음에 기술된 것들을 비제한적으로 포함한다(예를 들어 일반적으로 보유된, 다음 참고: 공개된 PCT 출원 WO 2010/036696 (2010년 4월 10일 발표), Robeyns et al., J. 변형된 사이클로헥시닐 뉴클레오시드는 당업계에서 다음에 기술된 것들을 비제한적으로 포함한다: (예를 들어 일반적으로 보유된, 다음 참고: 공개된 PCT 출원 WO 2010/036696 (2010년 4월 10일 발표), Robeyns
et al., J. Am. Chem . Soc ., 2008,
130(6), 1979-1984;
et al., Tetrahedron Letters, 2007,
48, 3621-3623; Nauwelaerts
et al., J. Am. Chem . Soc., 2007,
129(30), 9340-9348; Gu
et al.,,
Nucleosides , Nucleotides & Nucleic Acids, 2005,
24(5-7), 993-998; Nauwelaerts
et al., Nucleic Acids Research, 2005,
33(8), 2452-2463; Robeyns et al.,
Acta Crystallographica , Section F: Structural Biology and Crystallization Communications, 2005,
F61(6), 585-586; Gu
et al., Tetrahedron, 2004,
60(9), 2111-2123; Gu
et al., Oligonucleotides, 2003,
13(6), 479-489; Wang
et al., J. Org . Chem ., 2003,
68, 4499-4505; Verbeure
et al., Nucleic Acids Research, 2001,
29(24), 4941-4947; Wang
et al., J. Org . Chem., 2001,
66, 8478-82; Wang
et al.,
Nucleosides, Nucleotides & Nucleic Acids, 2001,
20(4-7), 785-788; Wang
et al., J. Am. Chem ., 2000,
122, 8595-8602; 공개 PCT 출원, WO 06/047842; 및 공개 PCT 출원 WO 01/049687; 각각의 내용은 본원에 그 전체가 참고로 편입되어 있다). 특정 변형된 사이클로헥세닐 뉴클레오시드는 하기 화학식 X를 가진다.
상기 식 중에서, 화학식 X의 적어도 하나의 사이클로헥세닐 뉴클레오시드 유사체 각각에 대해 독립적으로:
Bx는 헤테로환 염기 모이어티이다.
T3 및 T4 각각은, 독립적으로, 사이클로헥세닐 뉴클레오시드 유사체를 이의 안티센스 화합물에 연결시키는 뉴클레오시드간 연결 그룹이거나 T3 및 T4 중 하나는 테트라하이드로피란 뉴클레오시드 유사체를 안티센스 화합물에 연결시키는 뉴클레오시드간 연결 그룹이고, 그리고 T3 및 T4 중 다른 것은 H, 히드록실 보호기, 연결된 콘주게이트 그룹, 또는 5' 또는 3'-말단기이고;
q1, q2, q3, q4, q5, q6, q7, q8 및 q9 는 각각, 독립적으로, H, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐, 치환된 C2-C6 알키닐 또는 다른 당 치환체 그룹이다.
많은 다른 단환식, 이환식 및 삼환식 환계가 당업계에 공지되어 있고, 본 명세서에 제공된 바와 같은 올리고머 화합물로의 혼입을 위하여 뉴클레오시드를 변형시키도록 이용될 수 있는 당 대용물로서 적절하다(예를 들어, 하기 리뷰 논문 참고: Leumann, Christian J. Bioorg . & Med . Chem ., 2002, 10, 841-854). 그러한 환 시스템은 활성을 더욱 향상시키기 위하여 다양한 추가적인 치환을 거칠 수 있다.
본원에서 사용된 바와 같이, "2'-변형된 당"은 2' 위치에서 변형된 푸라노실 당을 의미한다. 특정 구현예에서, 그러한 변형은 하기를 비제한적으로 포함하는 치환체로부터 선택된다: 치환된 및 비치환된 알콕시, 치환된 및 비치환된 티오알킬, 치환된 및 비치환된 아미노 알킬, 치환된 및 비치환된 알킬, 치환된 및 비치환된 알릴, 및 치환된 및 비치환된 알키닐을 비제한적으로 포함하는 할라이드. 특정 구현예에서, 2' 변형은 하기를 비제한적으로 포함하는 치환체로부터 선택된다: O[(CH2)nO]mCH3, O(CH2)nNH2, O(CH2)nCH3, O(CH2)nF, O(CH2)nONH2, OCH2C(=O)N(H)CH3 , 및 O(CH2)nON[(CH2)nCH3]2, 여기서 n 및 m은 1 내지 약 10이다. 다른 2'-치환체 그룹은 또한 하기로부터 선택될 수 있다: C1-C12 알킬; 치환된 알킬; 알케닐; 알키닐; 알카릴; 아랄킬; O-알카릴 또는 O-아랄킬; SH, SCH3, OCN, Cl, Br, CN, F, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2; 헤테로사이클로알킬; 헤테로사이클로알카릴; 아미노알킬아미노; 폴리알킬아미노; 치환된 실릴; RNA 절단 그룹; 리포터 그룹; 삽입제; 약력학적 특성을 개선하는 그룹; 및 안티센스 화합물의 약동학적 특성을 개선하는 그룹, 및 유사한 특성을 갖는 다른 치환체. 특정 구현예에서, 변형된 뉴클레오시드는 2'-MOE 측쇄를 포함한다 (참고: Baker et al., J. Biol . Chem ., 1997, 272, 11944-12000). 그와 같은 2'-MOE 치환은 비변형된 뉴클레오시드 및 다른 변형된 뉴클레오시드, 예컨대 2'- O-메틸, O-프로필, 및 O-아미노프로필과 비교하여 개선된 결합 친화도를 갖는 것으로 기재되었다. 2'-MOE 치환체를 갖는 올리고뉴클레오티드는 또한 생체내 사용을 위해 유망한 특징을 갖는 유전자 발현의 안티센스 억제제인 것으로 나타나 있다 (참고, Martin, Helv. Chim . Acta, 1995, 78, 486-504; Altmann et al., Chimia, 1996, 50, 168-176; Altmann et al., Biochem . Soc . Trans., 1996, 24, 630-637; 및 Altmann et al., Nucleosides Nucleotides, 1997, 16, 917-926).
본원에서 사용된 바와 같이, "2'-변형된" 또는 "2'-치환된"은 H 또는 OH 이외의 2' 위치에서 치환체를 포함하는 당을 포함하는 뉴클레오시드를 의미한다. 2'-변형된 뉴클레오시드는, 비제한적으로, 이환식 뉴클레오시드를 포함하고, 여기서 당 환의 2 개의 탄소 원자를 연결하는 가교는 당 환의 2' 탄소 및 다른 탄소; 그리고 뉴클레오시드를 비-가교 2' 치환체, 예컨대 알릴, 아미노, 아지도, 티오, O-알릴, O-C1-C10 알킬, -OCF3, O-(CH2)2-O-CH3, 2'-O(CH2)2SCH3, O-(CH2)2-O-N(Rm)(Rn), 또는 O-CH2-C(=O)-N(Rm)(Rn)와 연결하고, 여기서 각각의 Rm 및 Rn는, 독립적으로, H 또는 치환된 또는 비치환된 C1-C10 알킬이다. 2'-변형된 뉴클레오시드는 예를 들면, 당의 다른 위치에서 및/또는 핵염기에서 다른 변형을 추가로 포함할 수 있다.
본원에서 사용된 바와 같이, "2'-F"는 당 환의 2' 위치에서 플루오로 기를 포함하는 당을 포함하는 뉴클레오시드를 의미한다.
본원에서 사용된 바와 같이, "2'-OMe" 또는 "2'-OCH3" 또는 "2'-O-메틸” 또는 “2'-메톡시” 각각은 당 환의 2' 위치에서 -OCH3 기를 포함하는 당을 포함하는 뉴클레오시드를 지칭한다.
본원에서 사용된 바와 같이, “MOE” 또는 “2'-MOE” 또는 “2'-OCH2CH2OCH3” 또는 “2'-O-메톡시에틸” 각각은 당 환의 2' 위치에서 -OCH2CH2OCH3 기를 포함하는 당을 포함하는 뉴클레오시드를 지칭한다.
변형된 당류의 제조 방법은 당해분야의 숙련가에게 잘 공지되어 있다. 이러한 변형 당의 제조를 교시하는 일부 대표적인 미국 특허는, 제한 없이, 미국 특허 제4,981,957호; 제5,118,800호; 제5,319,080호; 제5,359,044호; 제5,393,878호; 제5,446,137호; 제5,466,786호; 제5,514,785호; 제5,519,134호; 제5,567,811호; 제5,576,427호; 제5,591,722호; 제5,597,909호; 제5,610,300호; 제5,627,053호; 제5,639,873호; 제5,646,265호; 제5,670,633호; 제5,700,920호; 제5,792,847호 및 제6,600,032호 및 2005년 6월 2일에 출원되고 2005년 12월 22일에 WO 2005/121371로서 공개된 국제 출원 PCT/US 2005/019219를 포함하고, 이들 중 특정한 것은 본 출원과 공동으로 소유되며, 이들 각각은 그 전체가 본 명세서에 참고로 편입된다.
본 명세서에서 이용되는 바와 같이, "올리고뉴클레오티드"는 복수의 연결된 뉴클레오시드를 포함하는 화합물을 지칭한다. 소정의 실시형태에 있어서, 복수의 뉴클레오시드 중 하나 이상이 변형된다. 특정 구현예에서, 올리고뉴클레오티드는 하나 이상의 리보뉴클레오시드(RNA) 및/또는 데옥시리보뉴클레오시드(DNA)를 포함한다.
변형된 당 모이어티를 갖는 뉴클레오티드에서, 핵염기 모이어티 (천연, 변형된, 또는 이들의 조합)은 적절한 핵산 표적과의 혼성화를 위해 유지된다.
특정 구현예에서, 안티센스 화합물은 하나 이상의 변형된 당 모이어티를 갖는 뉴클레오시드를 포함한다. 특정 구현예에서, 변형된 당 모이어티는 2'-MOE이다. 특정 구현예에서, 2'-MOE 변형된 뉴클레오시드는 갭머 모티프에서 배열된다. 특정 구현예에서, 상기 변형된 당 모이어티는 (4'-CH(CH3)-O-2') 가교기를 갖는 이환식 뉴클레오시드이다. 특정 구현예에서, 상기 (4'-CH(CH3)-O-2') 변형된 뉴클레오시드는 갭머 모티프의 윙에 걸쳐 배열된다.
변형된
핵염기
핵염기 (또는 염기) 변형 또는 치환은, 자연 발생 또는 합성 비변형된 핵염기와 구조적으로 구별할 수 있고 기능적으로 교환가능하다. 천연 및 변형된 핵염기 모두는 수소 결합에 참여할 수 있다. 그와 같은 핵염기 변형은 뉴클레아제 안정성, 결합 친화도 또는 일부 다른 유익한 생물학적 특성을 안티센스 화합물에 부여할 수 있다. 변형된 핵염기는 합성 및 천연 핵염기 예컨대, 예를 들면, 5-메틸시토신 (5-me-C)를 포함한다. 5-메틸시토신 치환을 포함하는 임의의 핵염기 치환은, 표적 핵산에 대한 안티센스 화합물의 결합 친화도를 증가시키는데 특히 유용하다. 예를 들면, 5-메틸시토신 치환은 0.6-1.2℃ 까지 핵산 이중나선 안정성을 증가시키는 것으로 보였다 (Sanghvi, Y.S., Crooke, S.T. and Lebleu, B., eds., Antisense Research and Applications, CRC Press, Boca Raton, 1993, pp. 276-278).
추가의 변형된 핵염기는 하기를 포함한다: 5-하이드록시메틸 시토신, 잔틴, 하이포잔틴, 2-아미노아데닌, 6-메틸 및 아데닌 및 구아닌, 2-프로필의 다른 알킬 유도체 및 아데닌 및 구아닌, 2-티오우라실, 2-티오티민 및 2-티오시토신, 5-할로우라실 및 시토신, 5-프로피닐 (-C≡C-CH3) 우라실 및 시토신의 다른 알킬 유도체 및 피리미딘 염기, 6-아조 우라실, 시토신 및 티민, 5-우라실 (슈도우라실), 4-티오우라실, 8-할로, 8-아미노, 8-티올, 8-티오알킬, 8-하이드록실의 다른 알키닐 유도체 및 다른 8-치환된 아데닌 및 구아닌, 5-할로 특히 5-브로모, 5-트리플루오로메틸 및 다른 5-치환된 우라실 및 시토신, 7-메틸구아닌 및 7-메틸아데닌, 2-F-아데닌, 2-아미노-아데닌, 8-아자구아닌 및 8-아자아데닌, 7-데아자구아닌 및 7-데아자아데닌 및 3-데아자구아닌 및 3-데아자아데닌.
퓨린 또는 피리미딘 염기가 다른 헤테로환으로 대체된 헤테로환 염기 모이어티, 예를 들어 7-데아자-아데닌, 7-데아자구아노신, 2-아미노피리딘 및 2-피리돈이 또한 포함될 수 있다. 안티센스 화합물의 결합 친화도를 증가시키는데 특히 유용한 핵염기는 5-치환된 피리미딘, 6-아자피리미딘 및 N-2, N-6 및 O-6 치환된 퓨린을 포함하고, 이것은 2 아미노프로필아데닌, 5-프로피닐우라실 및 5-프로피닐시토신을 포함한다.
특정 구현예에서, ANGPTL3 핵산에 표적화된 안티센스 화합물은 하나 이상의 변형된 핵염기를 포함한다. 특정 구현예에서, ANGPTL3 핵산에 표적화된 단축되거나 갭-넓어진 안티센스 올리고뉴클레오티드는 하나 이상의 변형된 핵염기를 포함한다. 특정 구현예에서, 변형된 핵염기는 5-메틸시토신이다. 특정 구현예에서, 각각의 시토신은 5-메틸시토신이다.
약제학적 조성물을
제형화하기
위한 조성물 및 방법
안티센스 올리고뉴클레오티드는 약제학적 조성물 또는 제형의 제조를 위한 약제학적으로 허용가능한 활성 또는 불활성 물질과 혼합될 수 있다. 조성물 및 약제학적 조성물의 제형 방법은 수많은 기준에 의존하고, 이 기준은, 비제한적으로, 투여 경로, 질환 정도, 또는 투여될 투여량을 포함한다.
ANGPTL3 핵산에 표적화된 안티센스 화합물은 안티센스 화합물을 적당한 약제학적으로 허용가능한 희석제 또는 담체와 조합하여 약제학적 조성물에서 이용될 수 있다. 약제학적으로 허용가능한 희석제는 포스페이트-완충 식염수 (PBS)를 포함한다. PBS는 비경구로 전달될 조성물에서 사용하기에 적당한 희석제이다. 따라서, 일 구현예에서, ANGPTL3 핵산에 표적화된 안티센스 화합물 및 약제학적으로 허용가능한 희석제를 포함하는 약제학적 조성물이 본원에 기재된 방법에서 이용된다. 특정 구현예에서, 약제학적으로 허용가능한 희석제는 PBS이다. 특정 구현예에서, 안티센스 화합물은 안티센스 올리고뉴클레오티드이다.
안티센스 화합물을 포함하는 약제학적 조성물은 임의의 약제학적으로 허용가능한 염, 에스테르, 또는 그와 같은 에스테르의 염, 또는 인간을 포함하는 동물에게 투여시, (직접적으로 또는 간접적으로) 생물학적 활성 대사물 또는 그의 잔류물을 제공할 수 있는 임의의 다른 올리고뉴클레오티드을 포함한다. 따라서, 예를 들면, 본 개시내용은 또한 안티센스 화합물의 약제학적으로 허용가능한 염, 프로드럭, 그와 같은 프로드럭의 약제학적으로 허용가능한 염, 및 다른 생물동등체에 관한 것이다. 적당한 약제학적으로 허용가능한 염은, 비제한적으로, 하기를 포함한다: 나트륨 및 칼륨 염.
프로드럭은 활성 안티센스 화합물을 형성하도록 내인성 뉴클레아제에 의해 절단된 안티센스 화합물의 하나 또는 둘 모두의 말단에서 부가적 뉴클레오시드의 통합을 포함할 수 있다.
콘주게이트된
안티센스
화합물
안티센스 화합물은 수득한 안티센스 올리고뉴클레오티드의 활성, 세포 분포 또는 세포 흡수를 향상시키는 하나 이상의 모이어티 또는 콘주게이트에 공유연결될 수 있다. 전형적인 콘주게이트 그룹은 콜레스테롤 모이어티 및 지질 모이어티를 포함한다. 부가적 콘주게이트 그룹은 탄수화물, 인지질, 바이오틴, 펜아진, 폴레이트, 펜안트리딘, 안트라퀴논, 아크리딘, 플루오레신, 로다민, 쿠마린, 및 염료를 포함한다.
안티센스 화합물은 특성 예컨대, 예를 들면, 뉴클레아제 안정성을 향상시키기 위해 안티센스 화합물의 하나 또는 둘 모두 말단에 일반적으로 부착된 하나 이상의 안정화 그룹을 갖도록 또한 변형될 수 있다. 안정화 그룹에 캡 구조가 포함된다. 이들 말단 변형은 엑소뉴클레아제 분해로부터 말단 핵산을 갖는 안티센스 화합물을 보호하고, 세포 내에서 전달 및/또는 국재화를 도울 수 있다. 캡은 5'-말단 (5'-캡), 또는 3'-말단 (3'-캡)에서 존재할 수 있고, 또는 말단 둘에서 존재할 수 있다. 캡 구조는 당해기술에서 잘 공지되어 있고, 예를 들면, 반전된 데옥시 무염기성 캡을 포함한다. 뉴클레아제 안정성을 부여하기 위해 캡 안티센스 화합물의 하나 또는 둘 모두의 말단을 캡핑하기 위해 사용될 수 있는 추가의 3' 및 5'-안정화 그룹은 WO 03/004602 (2003년 1월 16일 공개)에서 개시된 것을 포함한다.
특정 구현예에서, 본 개시내용은 하기 식으로 나타낸 콘주게이트된 안티센스 화합물을 제공한다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는 것으로 제공된다:
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는 것으로 제공된다:
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는 것으로 제공된다:
본 개시내용은 하기의 비제한적인 넘버링된 구현예를 제공한다:
상기 식 중에서,
T2 는 뉴클레오시드, 뉴클레오티드, 단량체 하부단위, 또는 올리고머 화합물이다.
특정한 변수의 1 초과 (예를 들면, 1 초과 "m" 또는 "n")를 갖는 구현예에서, 달리 지적되지 않으면, 각각의 그와 같은 특정한 변수는 독립적으로 선택된다. 따라서, 1 초과 n을 갖는 구조에 대해, 각각의 n은 선택된 독립적으로 선택되고, 이로써, 서로 동일하거나 그렇지 않을 수 있다.
i.
특정 절단가능
모이어티
특정 구현예에서, 절단가능 모이어티는 절단가능 결합이다. 특정 구현예에서, 절단가능 모이어티는 절단가능 결합을 포함한다. 특정 구현예에서, 콘주게이트 그룹은 절단가능 모이어티를 포함한다. 특정 그와 같은 구현예에서, 절단가능 모이어티는 안티센스 올리고뉴클레오티드에 부착된다. 특정 그와 같은 구현예에서, 절단가능 모이어티는 세포-표적화 모이어티에 직접적으로 부착된다. 특정 그와 같은 구현예에서, 절단가능 모이어티는 콘주게이트 링커에 부착된다. 특정 구현예에서, 절단가능 모이어티는 포스페이트 또는 포스포디에스테르를 포함한다. 특정 구현예에서, 절단가능 모이어티는 절단가능 뉴클레오시드 또는 뉴클레오시드 유사체이다. 특정 구현예에서, 뉴클레오시드 또는 뉴클레오시드 유사체는 퓨린, 치환된 퓨린, 피리미딘 또는 치환된 피리미딘로부터 선택된 임의로 보호된 헤테로환 염기를 포함한다. 특정 구현예에서, 절단가능 모이어티는 우라실, 티민, 시토신, 4-N-벤조일시토신, 5-메틸시토신, 4-N-벤조일-5-메틸시토신, 아데닌, 6-N-벤조일아데닌, 구아닌 및 2-N-이소부티릴구아닌로부터 선택된 임의로 보호된 헤테로환 염기를 포함하는 뉴클레오시드이다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 연결에 의해 안티센스 올리고뉴클레오티드의 3' 위치에 부착되고 포스포디에스테르 또는 포스포로티오에이트 연결에 의해 링커에 부착된 2'-데옥시 뉴클레오시드이다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 연결에 의해 안티센스 올리고뉴클레오티드의 3' 위치에 부착되고 포스포디에스테르 또는 포스포로티오에이트 연결에 의해 링커에 부착된 2'-데옥시 아데노신이다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 연결에 의해 안티센스 올리고뉴클레오티드의 3' 위치에 부착되고 포스포디에스테르 또는 포스포로티오에이트 연결에 의해 링커에 부착된 2'-데옥시 아데노신이다.
특정 구현예에서, 절단가능 모이어티는 안티센스 올리고뉴클레오티드의 3' 위치에 부착된다. 특정 구현예에서, 절단가능 모이어티는 안티센스 올리고뉴클레오티드의 5' 위치에 부착된다. 특정 구현예에서, 절단가능 모이어티는 안티센스 올리고뉴클레오티드의 2' 위치에 부착된다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 연결에 의해 안티센스 올리고뉴클레오티드에 부착된다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 또는 포스포로티오에이트 연결에 의해 링커에 부착된다. 특정 구현예에서, 절단가능 모이어티는 포스포디에스테르 연결에 의해 링커에 부착된다. 특정 구현예에서, 콘주게이트 그룹은 절단가능 모이어티를 포함하지 않는다.
특정 구현예에서, 절단가능 모이어티는, 표적화된 세포에 의해 내면화된 직후에 복합물이 동물에게 투여된 후에 절단된다. 세포 내에서 절단가능 모이어티는 절단되고 그렇게 함으로써 활성 안티센스 올리고뉴클레오티드를 방출한다. 이론에 의해 제한되지를 바라지 않지만 절단가능 모이어티가 세포 내의 1 이상의 뉴클레아제에 의해 절단되는 것으로 믿는다. 특정 구현예에서, 1 이상의 뉴클레아제는 절단가능 모이어티와 링커 사이의 포스포디에스테르 연결을 절단한다. 특정 구현예에서, 절단가능 모이어티는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 Bx, Bx1, Bx2, 및 Bx3은 독립적으로 헤테로환 염기 모이어티이다. 특정 구현예에서, 절단가능 모이어티는 하기 중으로부터 선택된 구조를 갖는다:
i.
특정 링커
특정 구현예에서, 콘주게이트 그룹은 링커를 포함한다. 특정 그와 같은 구현예에서, 링커는 절단가능 모이어티에 공유결합된다. 특정 그와 같은 구현예에서, 링커는 안티센스 올리고뉴클레오티드에 공유결합된다. 특정 구현예에서, 링커는 세포-표적화 모이어티에 공유결합된다. 특정 구현예에서, 링커는 추가로, 고형 지지체에 대한 공유 결합을 포함한다. 특정 구현예에서, 링커는 추가로, 단백질 결합 모이어티에 대한 공유 결합을 포함한다. 특정 구현예에서, 링커는 추가로, 고형 지지체에 대한 공유결합을 포함하고, 추가로, 단백질 결합 모이어티에 대한 공유 결합을 포함한다. 특정 구현예에서, 링커는 연결된 리간드의 부착을 위한 다중 위치를 포함한다. 특정 구현예에서, 링커는 연결된 리간드의 부착을 위한 다중 위치를 포함하고 분지화 그룹에 부착되지 않는다. 특정 구현예에서, 링커는 추가로, 1 이상의 절단가능 결합을 포함한다. 특정 구현예에서, 콘주게이트 그룹은 링커를 포함하지 않는다.
특정 구현예에서, 링커는 알킬, 아미드, 이황화, 폴리에틸렌 글리콜, 에테르, 티오에테르 (-S-) 및 하이드록실아미노 (-O-N(H)-) 그룹으로부터 선택된 그룹을 포함하는 적어도 하나의 선형 그룹을 포함한다. 특정 구현예에서, 선형 그룹은 알킬, 아미드 및 에테르 그룹으로부터 선택된 그룹을 포함한다. 특정 구현예에서, 선형 그룹은 알킬 및 에테르 그룹으로부터 선택된 그룹을 포함한다. 특정 구현예에서, 선형 그룹은 적어도 하나의 인 연결 그룹를 포함한다. 특정 구현예에서, 선형 그룹은 적어도 하나의 포스포디에스테르 그룹을 포함한다. 특정 구현예에서, 선형 그룹은 적어도 하나의 중성 연결 그룹를 포함한다. 특정 구현예에서, 선형 그룹은 세포-표적화 모이어티 및 절단가능 모이어티에 공유결합된다. 특정 구현예에서, 선형 그룹은 세포-표적화 모이어티 및 안티센스 올리고뉴클레오티드에 공유결합된다. 특정 구현예에서, 선형 그룹은 세포-표적화 모이어티, 절단가능 모이어티 및 고형 지지체에 공유결합된다. 특정 구현예에서, 선형 그룹은 세포-표적화 모이어티, 절단가능 모이어티, 고형 지지체 및 단백질 결합 모이어티에 공유결합된다. 특정 구현예에서, 선형 그룹은 1 이상의 절단가능 결합을 포함한다.
특정 구현예에서, 링커는 스캐폴드 그룹에 공유결합된 선형 그룹을 포함한다. 특정 구현예에서, 스캐폴드는 알킬, 아미드, 디설파이드, 폴리에틸렌 글리콜, 에테르, 티오에테르 및 하이드록실아미노 그룹으로부터 선택된 그룹을 포함하는 분지된 지방족 그룹을 포함한다. 특정 구현예에서, 스캐폴드는 알킬, 아미드 및 에테르 그룹으로부터 선택된 그룹을 포함하는 분지된 지방족 그룹을 포함한다. 특정 구현예에서, 스캐폴드는 적어도 하나의 단환 또는 다환식 환계를 포함한다. 특정 구현예에서, 스캐폴드는 적어도 2 개의 단환 또는 다환식 환계를 포함한다. 특정 구현예에서, 선형 그룹은 스캐폴드 그룹에 공유결합되고 스캐폴드 그룹은 절단가능 모이어티 및 링커에 공유결합된다. 특정 구현예에서, 선형 그룹은 스캐폴드 그룹에 공유결합되고 스캐폴드 그룹은 절단가능 모이어티, 링커 및 고형 지지체에 공유결합된다. 특정 구현예에서, 선형 그룹은 스캐폴드 그룹에 공유결합되고 스캐폴드 그룹은 절단가능 모이어티, 링커 및 단백질 결합 모이어티에 공유결합된다. 특정 구현예에서, 선형 그룹은 스캐폴드 그룹에 공유결합되고, 스캐폴드 그룹은 절단가능 모이어티, 링커, 단백질 결합 모이어티 및 고형 지지체에 공유결합된다. 특정 구현예에서, 스캐폴드 그룹은 1 이상의 절단가능 결합을 포함한다.
특정 구현예에서, 링커는 단백질 결합 모이어티를 포함한다. 특정 구현예에서, 단백질 결합 모이어티는 하기를 비제한적으로 포함하는 지질이다: 콜레스테롤, 콜산, 아다만탄 아세트산, 1-피렌 부티르산, 디하이드로테스토스테론, 1,3-비스-O(헥사데실)글리세롤, 제라닐옥시헥실 그룹, 헥사데실글리세롤, 용뇌, 멘톨, 1,3-프로판디올, 헵타데실 그룹, 팔미트산, 미리스트산, O3-(올레오일)리토콜산, O3-(올레오일)콜렌산, 디메톡시트리틸, 또는 펜옥사진), 비타민 (예를 들면, 폴레이트, 비타민 A, 비타민 E, 바이오틴, 피리독살), 펩티드, 탄수화물 (예를 들면, 단당류, 디사카라이드, 트리사카라이드, 테트라사카라이드, 올리고당, 다당류), 엔도솜분해적 구성성분, 스테로이드 (예를 들면, 우바올, 헤시게닌, 디오스게닌), 테르펜 (예를 들면, 트리테르펜, 예를 들면, 사르사사포게닌, 프리델린, 에피프리에델라놀 유도된 리토콜산), 또는 양이온성 지질. 특정 구현예에서, 단백질 결합 모이어티는 C16 내지 C22 장쇄 포화된 또는 불포화된 지방산, 콜레스테롤, 콜산, 비타민 E, 아다만탄 또는 1-펜타플루오로프로필이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 n은, 독립적으로, 1 내지 20이고; 그리고 p는 1 내지 6이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, n은 1 내지 20이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 L은, 독립적으로, 인 연결 그룹 또는 중성 연결 그룹이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, n은 1 내지 20이다.
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 구조를 갖는다:
특정 구현예에서, 콘주게이트 링커는 하기 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 링커는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 n은 독립적으로, 0, 1, 2, 3, 4, 5, 6, 또는 7이다.
ii.
특정 세포-
표적화
모이어티
특정 구현예에서, 콘주게이트 그룹은 세포-표적화 모이어티를 포함한다. 특정 그와 같은 세포-표적화 모이어티는 안티센스 화합물의 세포성 흡수를 증가시킨다. 특정 구현예에서, 세포-표적화 모이어티는 분지화 그룹, 1 이상의 연결기, 및 1 이상의 리간드를 포함한다. 특정 구현예에서, 세포-표적화 모이어티는 분지화 그룹, 1 이상의 연결기, 1 이상의 리간드 및 1 이상의 절단가능 결합을 포함한다.
1.
특정
분지화
그룹
특정 구현예에서, 콘주게이트 그룹은 분지화 그룹 및 적어도 2 개의 연결된 리간드를 포함하는 표적 모이어티를 포함한다. 특정 구현예에서, 분지화 그룹은 콘주게이트 링커를 첨부한다. 특정 구현예에서, 분지화 그룹은 절단가능 모이어티를 첨부한다. 특정 구현예에서, 분지화 그룹은 안티센스 올리고뉴클레오티드를 첨부한다. 특정 구현예에서, 분지화 그룹은 링커 및 각각의 연결된 리간드에 공유결합된다. 특정 구현예에서, 분지화 그룹은 알킬, 아미드, 디설파이드, 폴리에틸렌 글리콜, 에테르, 티오에테르 및 하이드록실아미노 그룹으로부터 선택된 그룹을 포함하는 분지된 지방족 그룹을 포함한다. 특정 구현예에서, 분지화 그룹은 알킬, 아미드 및 에테르 그룹으로부터 선택된 그룹을 포함한다. 특정 구현예에서, 분지화 그룹은 알킬 및 에테르 그룹으로부터 선택된 그룹을 포함한다. 특정 구현예에서, 분지화 그룹은 단환 또는 다환식 환계를 포함한다. 특정 구현예에서, 분지화 그룹은 1 이상의 절단가능 결합을 포함한다. 특정 구현예에서, 콘주게이트 그룹은 분지화 그룹을 포함하지 않는다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
j는 1 내지 3이고; 그리고
m은 2 내지 6이다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이고; 그리고
m은 2 내지 6이다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 A1은 독립적으로, O, S, C=O 또는 NH이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 A1은 독립적으로, O, S, C=O 또는 NH이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, A1은 O, S, C=O 또는 NH이고; 그리고
각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 분지화 그룹은 하기 중으로부터 선택된 구조를 갖는다:
2.
특정
연결기
특정 구현예에서, 콘주게이트 그룹은 분지화 그룹에 공유결합된 1 이상의 연결기를 포함한다. 특정 구현예에서, 콘주게이트 그룹은 연결 그룹에 공유결합된 1 이상의 연결기를 포함한다. 특정 구현예에서, 각각의 연결기는 임의의 조합으로 알킬, 에테르, 티오에테르, 디설파이드, 아미드 및 폴리에틸렌 글리콜 그룹으로부터 선택된 1 이상의 그룹을 포함하는 선형 지방족 그룹이다. 특정 구현예에서, 각각의 연결기는 임의의 조합으로 알킬, 치환된 알킬, 에테르, 티오에테르, 디설파이드, 아미드, 포스포디에스테르 및 폴리에틸렌 글리콜 그룹으로부터 선택된 1 이상의 그룹을 포함하는 선형 지방족 그룹이다. 특정 구현예에서, 각각의 연결기는 임의의 조합으로 알킬, 에테르 및 아미드 그룹으로부터 선택된 1 이상의 그룹을 포함하는 선형 지방족 그룹이다. 특정 구현예에서, 각각의 연결기는 임의의 조합으로 알킬, 치환된 알킬, 포스포디에스테르, 에테르 및 아미드 그룹으로부터 선택된 1 이상의 그룹을 포함하는 선형 지방족 그룹이다. 특정 구현예에서, 각각의 연결기는 임의의 조합으로 알킬 및 포스포디에스테르로부터 선택된 1 이상의 그룹을 포함하는 선형 지방족 그룹이다. 특정 구현예에서, 각각의 연결기는 적어도 하나의 인 연결 그룹 또는 중성 연결 그룹를 포함한다.
특정 구현예에서, 연결기는 1 이상의 절단가능 결합을 포함한다. 특정 구현예에서, 연결기는 아미드 또는 에테르 그룹을 통해 분지화 그룹에 부착된다. 특정 구현예에서, 연결기는 포스포디에스테르 그룹을 통해 분지화 그룹에 부착된다. 특정 구현예에서, 연결기는 인 연결 그룹 또는 중성 연결 그룹를 통해 분지화 그룹에 부착된다. 특정 구현예에서, 연결기는 에테르 그룹을 통해 분지화 그룹에 부착된다. 특정 구현예에서, 연결기는 아미드 또는 에테르 그룹을 통해 리간드에 부착된다. 특정 구현예에서, 연결기는 에테르 그룹을 통해 리간드에 부착된다. 특정 구현예에서, 연결기는 아미드 또는 에테르 그룹을 통해 리간드에 부착된다. 특정 구현예에서, 연결기는 에테르 그룹을 통해 리간드에 부착된다.
특정 구현예에서, 각각의 연결기는 리간드와 분지화 그룹 사이에 약 8 내지 약 20 개의 원자의 사슬 길이를 포함한다. 특정 구현예에서, 각각의 연결기 그룹은 리간드와 분지화 그룹 사이에 약 10 내지 약 18 개의 원자의 사슬 길이를 포함한다. 특정 구현예에서, 각각의 연결기 그룹은 약 13 개의 원자의 사슬 길이를 포함한다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
여기서 각각의 n은, 독립적으로, 1 내지 20이고; 그리고
각각의 p는 1 내지 약 6이다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
여기서 L은 인 연결 그룹 또는 중성 연결 그룹이고;
Z1 는 C(=O)O-R2 이고;
Z2는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고;
R2는 H, C1-C6 알킬 또는 치환된 C1-C6 알키(alky)이고; 그리고
각각의 m1은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m1은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
여기서 Z2는 H 또는 CH3이고; 그리고
각각의 m1은, 독립적으로, 0 내지 20이고, 여기서 적어도 하나의 m1은 각각의 연결기에 대해 0 초과이다.
특정 구현예에서, 연결기는 하기 중으로부터 선택된 구조를 갖는다:
; 여기서 각각의 n은 독립적으로, 0, 1, 2, 3, 4, 5, 6, 또는 7이다.
특정 구현예에서, 연결기는 인 연결 그룹를 포함한다. 특정 구현예에서, 연결기는 임의의 아미드 결합을 포함하지 않는다. 특정 구현예에서, 연결기는 인 연결 그룹를 포함하고 임의의 아미드 결합을 포함하지 않는다.
3.
특정 리간드
특정 구현예에서, 본 개시내용은 리간드를 제공하고, 여기서 각각의 리간드는 연결기에 공유결합된다. 특정 구현예에서, 표적 세포 상의 적어도 하나의 유형의 수용체에 대한 친화성을 갖는 각각의 리간드가 선택된다. 특정 구현예에서, 포유동물 간 세포의 표면 상의 적어도 하나의 유형의 수용체에 대한 친화성을 갖는 리간드가 선택된다. 특정 구현예에서, 간 아시알로당단백질 수용체 (ASGP-R)에 대해 친화성을 갖는 리간드가 선택된다. 특정 구현예에서, 각각의 리간드는 탄수화물이다. 특정 구현예에서, 각각의 리간드는, 갈락토오스, N-아세틸 갈락토오스아민, 만노스, 글루코오스, 글루코사몬 및 푸코스로부터 독립적으로 선택된다. 특정 구현예에서, 각각의 리간드는 N-아세틸 갈락토오스아민 (GalNAc)이다. 특정 구현예에서, 표적 모이어티는 2 내지 6 개의 리간드를 포함한다. 특정 구현예에서, 표적 모이어티는 3 개의 리간드를 포함한다. 특정 구현예에서, 표적 모이어티는 3 N-아세틸 갈락토오스아민 리간드를 포함한다.
특정 구현예에서, 리간드는 탄수화물, 탄수화물 유도체, 변형된 탄수화물, 다가 탄수화물 클러스터, 다당류, 변형된 다당류, 또는 다당류 유도체이다. 특정 구현예에서, 리간드는 아미노 당 또는 티오 당이다. 예를 들면, 아미노 당은 당해기술에서 공지된 임의의 수의 화합물, 예를 들면 글루코사민, 시알산, α-D-갈락토사민, N-아세틸갈락토사민, 2-아세트아미도-2-데옥시-D-갈락토파이라노스 (GalNAc), 2-아미노-3-O-[(R)-1-카복시에틸]-2-데옥시-β-D-글루코파이라노스 (β-뮤람산), 2-데옥시-2-메틸아미노-L-글루코파이라노스, 4,6-디데옥시-4-포름아미도-2,3-디-O-메틸-D-만노파이라노스, 2-데옥시-2-설포아미노-D-글루코파이라노스 및 N-설포-D-글루코사민, 및 N-글리콜로일-α-뉴라민산으로부터 선택될 수 있다. 예를 들면, 티오 당류는 5-티오-β-D-글루코파이라노스, 메틸 2,3,4-트리-O-아세틸-1-티오-6-O-트리틸-α-D-글루코피라노사이드, 4-티오-β-D-갈락토파이라노스, 및 에틸 3,4,6,7-테트라-O-아세틸-2-데옥시-1,5-디티오-α-D-글루코-헵토피라노사이드로 이루어진 그룹으로부터 선택될 수 있다.
특정 구현예에서, "GalNac" 또는 "Gal-NAc"는 N-아세틸 갈락토사민으로서 문헌에서 통상적으로 칭해지는 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스를 의미한다. 특정 구현예에서, "N-아세틸 갈락토사민"는 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스를 의미한다. 특정 구현예에서, "GalNac" 또는 "Gal-NAc"는 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스를 의미한다. 특정 구현예에서, "GalNac" 또는 "Gal-NAc"는 β-유형: 2-(아세틸아미노)-2-데옥시-β-D-갈락토파이라노스 및 α-유형: 2-(아세틸아미노)-2-데옥시-β-D-갈락토파이라노스를 포함하는, 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스를 의미한다. 특정 구현예에서, β-유형: 2-(아세틸아미노)-2-데옥시-β-D-갈락토파이라노스 및 α-유형: 2-(아세틸아미노)-2-데옥시-β-D-갈락토파이라노스 둘 모두는 상호교환적으로 사용될 수 있다. 따라서, 하나의 형태가 묘사된 구조에서, 이들 구조는 다른 형태를 또한 포함하는 것으로 의도된다. 예를 들면, α-유형: 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스의 구조가 보여지는 경우, 이러한 구조는 다른 형태를 또한 포함하는 것으로 의도된다. 특정 구현예에서, 특정 바람직한 구현예에서, β-형 2-(아세틸아미노)-2-데옥시-D-갈락토파이라노스는 바람직한 구현예이다.
특정 구현예에서 1 이상의 리간드는 하기 중으로부터 선택된 구조를 갖는다:
상기 식 중에서, 각각의 R1은 OH 및 NHCOOH로부터 선택된다.
특정 구현예에서 1 이상의 리간드는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서 1 이상의 리간드는 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서 1 이상의 리간드는 하기 중으로부터 선택된 구조를 갖는다:
iii.
특정
콘주게이트
특정 구현예에서, 콘주게이트 그룹은 상기의 구조적 특징을 포함한다. 특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 포함한다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 포함한다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
상기 식 중에서, 각각의 n은, 독립적으로, 1 내지 20이다.
Z는 H 또는 연결된 고형 지지체이고;
Q는 안티센스 화합물이고;
X는 O 또는 S이고; 그리고
Bx는 헤테로환 염기 모이어티이다.
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 포함한다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 포함한다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 그와 같은 구현예에서, 콘주게이트 그룹은 하기 구조를 갖는다:
특정 구현예에서, 콘주게이트는 피롤리딘을 포함하지 않는다.
b.
특정
콘주게이트된
안티센스
화합물
특정 구현예에서, 콘주게이트는 뉴클레오시드의 2', 3', 또는 5' 위치에서 안티센스 올리고뉴클레오티드의 뉴클레오시드에 결합된다. 특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
C는 콘주게이트 링커이고
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 그와 같은 구현예에서, 콘주게이트 링커는 적어도 하나의 절단가능 결합을 포함한다.
특정 그와 같은 구현예에서, 분지화 그룹은 적어도 하나의 절단가능 결합을 포함한다.
특정 구현예에서 각각의 연결기는 적어도 하나의 절단가능 결합을 포함한다.
특정 구현예에서, 콘주게이트는 뉴클레오시드의 2', 3', 또는 5' 위치에서 안티센스 올리고뉴클레오티드의 뉴클레오시드에 결합된다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
C는 콘주게이트 링커이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트는 뉴클레오시드의 2', 3', 또는 5' 위치에서 안티센스 올리고뉴클레오티드의 뉴클레오시드에 결합된다. 특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
C는 콘주게이트 링커이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
B는 절단가능 모이어티이고;
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 식 중에서,
A는 안티센스 올리고뉴클레오티드이고;
D는 분지화 그룹이고
각각의 E는 연결기이고;
각각의 F는 리간드이고; 그리고
q는 정수 1 내지 5이다.
특정 그와 같은 구현예에서, 콘주게이트 링커는 적어도 하나의 절단가능 결합을 포함한다.
특정 구현예에서 각각의 연결기는 적어도 하나의 절단가능 결합을 포함한다.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 중으로부터 선택된 구조를 갖는다:
.
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 중으로부터 선택된 구조를 갖는다:
특정 구현예에서, 콘주게이트된 안티센스 화합물은 하기 구조를 갖는다:
상기 언급된 콘주게이트, 콘주게이트된 안티센스 화합물, 연결기, 링커, 분지화 그룹, 리간드, 절단가능 모이어티 뿐만 아니라 다른 변형 중 특정 것의 제조를 교시하는 대표적인 미국 특허들, 미국 특허 출원 공보, 및 국제 특허 출원 공보는 비제한적으로, 하기를 포함한다: US 5,994,517, US 6,300,319, US 6,660,720, US 6,906,182, US 7,262,177, US 7,491,805, US 8,106,022, US 7,723,509, US 2006/0148740, US 2011/0123520, WO 2013/033230 및 WO 2012/037254, 이들 각각은 그 전체가 참고로 본원에 편입되어 있다.
상기 언급된 콘주게이트, 콘주게이트된 안티센스 화합물, 연결기, 링커, 분지화 그룹, 리간드, 절단가능 모이어티 뿐만 아니라 다른 변형의 특정 것의 제조를 교시하는 대표적인 공보는 비제한적으로, 하기를 포함한다: BIESSEN et al., "The Cholesterol Derivative of a Triantennary Galactoside with High Affinity for the Hepatic Asialoglycoprotein Receptor: a Potent Cholesterol Lowering Agent" J. Med. Chem. (1995) 38:1846-1852, BIESSEN et al., "Synthesis of Cluster Galactosides with High Affinity for the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (1995) 38:1538-1546, LEE et al., "New and more efficient multivalent glyco-ligands for asialoglycoprotein receptor of mammalian hepatocytes" Bioorganic & Medicinal Chemistry (2011) 19:2494-2500, RENSEN et al., "Determination of the Upper Size Limit for Uptake and Processing of Ligands by the Asialoglycoprotein Receptor on Hepatocytes in Vitro and in Vivo" J. Biol. Chem. (2001) 276(40):37577-37584, RENSEN et al., "Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (2004) 47:5798-5808, SLIEDREGT et al., "Design and Synthesis of Novel Amphiphilic Dendritic Galactosides for Selective Targeting of Liposomes to the Hepatic Asialoglycoprotein Receptor" J. Med. Chem. (1999) 42:609-618, 및 Valentijn et al., “Solid-phase synthesis of lysine-based cluster galactosides with high affinity for the Asialoglycoprotein Receptor” Tetrahedron, 1997, 53(2), 759-770, (이들 각각은 본원에 그 전문이 참조로 편입됨).
특정 구현예에서, 콘주게이트된 안티센스 화합물은 RNase H 기반 올리고뉴클레오티드 (예컨대 갭머) 또는 스플라이스 조절 올리고뉴클레오티드 (예컨대 완전 변형된 올리고뉴클레오티드) 및 적어도 1, 2, 또는 3개의 GalNAc 그룹을 포함하는 임의의 콘주게이트 그룹을 포함한다. 특정 구현예에서 콘주게이트된 안티센스 화합물은 하기 참조 중 임의의 것에서 발견된 임의의 콘주게이트 그룹을 포함한다: Lee, Carbohydr Res, 1978, 67, 509-514; Connolly et al., J Biol Chem, 1982, 257, 939-945; Pavia et al., Int J Pep Protein Res, 1983, 22, 539-548; Lee et al., Biochem, 1984, 23, 4255-4261; Lee et al., Glycoconjugate J, 1987, 4, 317-328; Toyokuni et al., Tetrahedron Lett, 1990, 31, 2673-2676; Biessen et al., J Med Chem, 1995, 38, 1538-1546; Valentijn et al., Tetrahedron, 1997, 53, 759-770; Kim et al., Tetrahedron Lett, 1997, 38, 3487-3490; Lee et al., Bioconjug Chem, 1997, 8, 762-765; Kato et al., Glycobiol, 2001, 11, 821-829; Rensen et al., J Biol Chem, 2001, 276, 37577-37584; Lee et al., Methods Enzymol, 2003, 362, 38-43; Westerlind et al., Glycoconj J, 2004, 21, 227-241; Lee et al., Bioorg Med Chem Lett, 2006, 16(19), 5132-5135; Maierhofer et al., Bioorg Med Chem, 2007, 15, 7661-7676; Khorev et al., Bioorg Med Chem, 2008, 16, 5216-5231; Lee et al., Bioorg Med Chem, 2011, 19, 2494-2500; Kornilova et al., Analyt Biochem, 2012, 425, 43-46; Pujol et al., Angew Chemie Int Ed Engl, 2012, 51, 7445-7448; Biessen et al., J Med Chem, 1995, 38, 1846-1852; Sliedregt et al., J Med Chem, 1999, 42, 609-618; Rensen et al., J Med Chem, 2004, 47, 5798-5808; Rensen et al., Arterioscler Thromb Vasc Biol, 2006, 26, 169-175; van Rossenberg et al., Gene Ther, 2004, 11, 457-464; Sato et al., J Am Chem Soc, 2004, 126, 14013-14022; Lee et al., J Org Chem, 2012, 77, 7564-7571; Biessen et al., FASEB J, 2000, 14, 1784-1792; Rajur et al., Bioconjug Chem, 1997, 8, 935-940; Duff et al., Methods Enzymol, 2000, 313, 297-321; Maier et al., Bioconjug Chem, 2003, 14, 18-29; Jayaprakash et al., Org Lett, 2010, 12, 5410-5413; Manoharan, Antisense Nucleic Acid Drug Dev, 2002, 12, 103-128; Merwin et al., Bioconjug Chem, 1994, 5, 612-620; Tomiya et al., Bioorg Med Chem, 2013, 21, 5275-5281; 국제 출원 WO1998/013381; WO2011/038356; WO1997/046098; WO2008/098788; WO2004/101619; WO2012/037254; WO2011/120053; WO2011/100131; WO2011/163121; WO2012/177947; WO2013/033230; WO2013/075035; WO2012/083185; WO2012/083046; WO2009/082607; WO2009/134487; WO2010/144740; WO2010/148013; WO1997/020563; WO2010/088537; WO2002/043771; WO2010/129709; WO2012/068187; WO2009/126933; WO2004/024757; WO2010/054406; WO2012/089352; WO2012/089602; WO2013/166121; WO2013/165816; 미국 특허 4,751,219; 8,552,163; 6,908,903; 7,262,177; 5,994,517; 6,300,319; 8,106,022; 7,491,805; 7,491,805; 7,582,744; 8,137,695; 6,383,812; 6,525,031; 6,660,720; 7,723,509; 8,541,548; 8,344,125; 8,313,772; 8,349,308; 8,450,467; 8,501,930; 8,158,601; 7,262,177; 6,906,182; 6,620,916; 8,435,491; 8,404,862; 7,851,615; 공보된 미국 특허 출원 공보 US2011/0097264; US2011/0097265; US2013/0004427; US2005/0164235; US2006/0148740; US2008/0281044; US2010/0240730; US2003/0119724; US2006/0183886; US2008/0206869; US2011/0269814; US2009/0286973; US2011/0207799; US2012/0136042; US2012/0165393; US2008/0281041; US2009/0203135; US2012/0035115; US2012/0095075; US2012/0101148; US2012/0128760; US2012/0157509; US2012/0230938; US2013/0109817; US2013/0121954; US2013/0178512; US2013/0236968; US2011/0123520; US2003/0077829; US2008/0108801; 및 US2009/0203132; (이들 각각은 본원에 그 전문이 참조로 편입됨).
세포 배양물 및
안티센스
화합물 처리
ANGPTL3 핵산의 수준, 활성 또는 발현에 대한 안티센스 화합물의 효과는 다양한 세포 유형에서 시험관내에서 시험될 수 있다. 그와 같은 분석을 위해 사용된 세포 유형은 상업적 판매인 (예를 들면 American Type Culture Collection, Manassus, VA; Zen-Bio, Inc., Research Triangle Park, NC; Clonetics Corporation, Walkersville, MD)으로부터 이용가능하고 세포는 상업적으로 이용가능한 시약을 사용하여 판매인의 지침에 따라 배양된다 (예를 들면 Invitrogen Life Technologies, Carlsbad, CA). Invitrogen Life Technologies, Carlsbad, CA). 예시적인 세포 유형은, 비제한적으로, HepG2 세포 Hep3B 세포, Huh7 (간세포 암종) 세포, 일차 간세포, A549 세포, GM04281 섬유아세포 및 LLC-MK2 세포를 포함한다.
안티센스
올리고뉴클레오티드의
시험관내
시험
다른 안티센스 화합물에 의한 치료를 위해 적절하게 변형될 수 있는 안티센스 올리고뉴클레오티드에 의한 세포의 치료 방법이 본원에 기재되어 있다.
일반적으로, 세포는, 세포가 배양물에서 대략 60-80% 밀집도에 도달할 때 안티센스 올리고뉴클레오티드로 치료된다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위해 통상적으로 사용된 하나의 시약은 양이온성 지질 형질감염 시약 LIPOFECTIN® (Invitrogen, Carlsbad, CA)을 포함한다. 안티센스 올리고뉴클레오티드는 안티센스 올리고뉴클레오티드의 원하는 최종 농도 및 2 내지 12 ug/mL / 100 nM 안티센스 올리고뉴클레오티드 범위인 LIPOFECTIN® 농도를 달성하기 위해 OPTI-MEM® 1 (Invitrogen, Carlsbad, CA) 중에서 LIPOFECTIN®와 혼합된다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위해 사용된 또 하나의 시약은 LIPOFECTAMINE 2000® (Invitrogen, Carlsbad, CA)을 포함한다. 안티센스 올리고뉴클레오티드는 안티센스 올리고뉴클레오티드의 원하는 농도 및 2 내지 12 ug/mL / 100 nM 안티센스 올리고뉴클레오티드 범위인 LIPOFECTAMINE® 농도를 달성하기 위해 OPTI-MEM® 1 감소된 혈청 배지 (Invitrogen, Carlsbad, CA)에서 LIPOFECTAMINE 2000®와 혼합된다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위해 사용된 또 하나의 시약은 Cytofectin® (Invitrogen, Carlsbad, CA)를 포함한다. 안티센스 올리고뉴클레오티드는 안티센스 올리고뉴클레오티드의 원하는 농도 및 2 내지 12 ug/mL / 100 nM 안티센스 올리고뉴클레오티드 범위인 Cytofectin® 농도를 달성하기 위해 OPTI-MEM® 1 감소된 혈청 배치 (Invitrogen, Carlsbad, CA)에서 Cytofectin®와 혼합된다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위해 사용된 또 하나의 시약은 Oligofectamine™ (Life Technologies, Carlsbad, CA)을 포함한다. 안티센스 올리고뉴클레오티드는 안티센스 올리고뉴클레오티드의 원하는 농도 및 0.2 내지 0.8 μL / 100 nM 안티센스 올리고뉴클레오티드 범위인 Oligofectamine™ 농도를 달성하기 위해 Opti-MEM™-1 감소된 혈청 배지 (Life Technologies, Carlsbad, CA)에서 Oligofectamine™와 혼합된다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위한 기타 시약은 FuGENE 6 (Roche 진단 Corp., Indianapolis, IN)를 포함한다. 안티센스 올리고머 화합물을 FuGENE 6 대 올리고머 화합물 1 내지 4 μL의 FuGENE 6 (100 nM 당)로 원하는 농도의 올리고뉴클레오티드를 달성하기 위하여 1 mL 무혈청 RPMI 중 FuGENE 6을 혼합하였다.
안티센스 올리고뉴클레오티드를 배양 세포에 도입하기 위해 사용된 또 하나의 기술은 전기천공을 포함한다 (Sambrook 및 Russell, Molecular Cloning: A Laboratory Manual, 3rd Ed., 2001).
세포는 일상적인 방법에 의해 안티센스 올리고뉴클레오티드로 치료된다. 세포는 전형적으로 안티센스 올리고뉴클레오티드 치료 16-24 시간 후에 수확되고, 그 시간에 표적 핵산의 RNA 또는 단백질 수준은 당해분야에서 공지되고 본원에 기재된 방법으로 측정된다. 일반적으로, 치료가 다중 복제물에서 수행될 때, 데이터는 복제물 치료의 평균으로서 제공된다.
사용된 안티센스 올리고뉴클레오티드의 농도는 세포주에서 세포주로 변한다. 특정한 세포주에 대한 최적의 안티센스 올리고뉴클레오티드 농도를 측정하는 방법은 당해기술에 공지되어 있다. 안티센스 올리고뉴클레오티드는 LIPOFECTAMINE2000®, 리포펙틴 또는 사이토펙틴으로 형질감염될 때 1 nM 내지 300 nM 범위의 농도에서 전형적으로 사용된다. 안티센스 올리고뉴클레오티드는 전기천공을 사용하여 형질감염될 때 625 내지 20,000 nM 범위의 고농도에서 사용된다.
RNA 단리
RNA 분석은 총 세포 RNA 또는 폴리(A)+ mRNA에 대해 수행될 수 있다. RNA 단리 방법은 당해기술에서 잘 알려진 (Sambrook 및 Russell, Molecular Cloning: A Laboratory Manual, 3rd Ed., 2001). RNA는 제조자의 추천된 프로토콜에 따라 당해기술에서 공지된 방법, 예를 들면, TRIZOL® 시약 (Invitrogen, Carlsbad, CA)을 사용하여 제조된다.
표적 수준 또는 발현의 억제 분석
ANGPTL3 핵산의 수준 또는 발현 억제는 당해 기술에 공지된 다양한 방식으로 검정될 수 있다 (Sambrook 및 Russell, Molecular Cloning: A Laboratory Manual, 3rd Ed., 2001). 예를 들면, 표적 핵산 수준은, 예를 들면, 노던 블랏 분석, 경쟁적 폴리머라제 연쇄 반응 (PCR), 또는 정량적 실시간 PCR에 의해 정량화될 수 있다. RNA 분석은 총 세포 RNA 또는 폴리(A)+ mRNA에 대해 수행될 수 있다. RNA 단리의 방법은 당해기술에 공지되어 있다. 노던 블랏 분석은 당해기술에서 또한 일상적이다. 정량적 실시간 PCR은 상업적으로 이용가능한 ABI PRISM® 7600, 7700, 또는 7900 서열 검출 시스템 (PE-Applied Biosystems, Foster City, CA로부터 이용가능)을 사용하여 편리하게 달성될 수 있고 제조자의 지침에 따라 사용된다.
표적 RNA 수준의 정량적 실시간
PCR
분석
표적 RNA 수준의 정량화는 제조자의 지침에 따라 ABI PRISM® 7600, 7700, 또는 7900 서열 검출 시스템 (PE-Applied Biosystems, Foster City, CA)을 사용하여 정량적 실시간 PCR에 의해 달성될 수 있다. 정량적 실시간 PCR의 방법은 당해기술에 공지되어 있다.
실시간 PCR 전에, 단리된 RNA에 대해 역전사효소 (RT) 반응이 수행되고, 이 반응은 상보적 DNA (cDNA)을 생산하고 그 다음 실시간 PCR 증폭에 대한 기질로서 사용된다. RT 및 실시간 PCR 반응은 동일 샘플 웰에서 순차적으로 수행된다. RT 및 실시간 PCR 시약은 Invitrogen (Carlsbad, CA)로부터 수득된다. RT, 실시간-PCR 반응은 당해분야의 숙련가에게 공지된 방법에 의해 수행된다.
실시간 PCR에 의해 수득된 유전자 (또는 RNA) 표적 양은, 발현이 일정한 유전자, 예컨대 사이클로필린 A 또는 GADPH의 발현 수준을 사용하거나, 리보그린® (Life TechnologiesTM, Inc. Carlsbad, CA)을 사용하여 총 RNA를 정량화하여 정규화될 수 있다. 사이클로필린 A 또는 GADPH 발현은 실시간 PCR에 의해, 표적과 동시에, 다중화, 또는 별도로 시행하여 정량화될 수 있다. 총 RNA는 리보그린® RNA 정량화 시약을 사용하여 정량화될 수 있다. 리보그린®에 의한 RNA 정량화 방법은 하기에서 교시된다: Jones, L.J., et al, (Analytical Biochemistry, 1998, 265, 368-374). CYTOFLUOR® 4000 기기 (PE Applied Biosystems)는 리보그린® 형광을 측정하기 위해 사용된다.
실시간 PCR 프로브 및 프라이머를 설계하는 방법은 당해기술에 공지되어 있고 소프트웨어 예컨대 PRIMER EXPRESS® 소프트웨어 (Applied Biosystems, Foster City, CA)의 사용을 포함할 수 있다 실시간 PCR에 사용된 프로브 및 프라이머는 ANGPTL3 특이적 서열에 혼성화하기 위하여 설계되었고, 하기 실시예에서 개시된다. 표적 특이적 PCR 프로브는 5' 말단에 공유적으로 연결된 FAM 및 3' 말단에 공유적으로 연결된 TAMRA 또는 MGB를 가질 수 있고, 여기서 FAM은 형광 염료이고, TAMRA 또는 MGB는 켄쳐 염료(quencher dye)이다.
단백질 수준 분석
ANGPTL3 핵산의 안티센스 억제는 ANGPTL3 단백질 수준을 측정하여 평가될 수 있다. ANGPTL3의 단백질 수준은 당해기술에 공지된 다양한 방식, 예컨대 면역침전, 웨스턴 블랏 분석 (면역블로팅), 효소-결합 면역흡착 검정 (ELISA), 정량적 단백질 검정, 단백질 활성 검정 (예를 들면, 카스파제 활성 검정), 면역조직화학, 면역세포화학 또는 형광-활성화된 세포 분류 (FACS)으로 평가 또는 정량화될 수 있다 (Sambrook 및 Russell, Molecular Cloning: A Laboratory Manual, 3rd Ed., 2001). 표적에 대해 지향된 항체는 다양한 공급원, 예컨대 항체의 MSRS 카탈로그 (Aerie Corporation, Birmingham, MI)으로부터 동정 및 수득될 수 있고, 또는 당해기술에 잘 공지된 종래의 단클론성 또는 다클론성 항체 생성 방법을 통해 제조될 수 있다.
안티센스
화합물의
생체내
시험
안티센스 화합물, 예를 들면, 안티센스 올리고뉴클레오티드는, ANGPTL3의 발현을 억제하고 표현형 변화를 생성하기 위해 그것의 능력을 평가하기 위해 동물에서 시험된다. 시험은 정상동물, 또는 실험 질환 모델에서 수행될 수 있다. 동물에의 투여에 대해, 안티센스 올리고뉴클레오티드는 약제학적으로 허용가능한 희석제, 예컨대 포스페이트-완충 식염수에서 제형된다. 투여는 비경구 투여 경로를 포함한다. 안티센스 올리고뉴클레오티드에 의한 치료 기간 다음에, RNA는 조직으로부터 단리되고 ANGPTL3 핵산 발현의 변화가 측정된다. ANGPTL3 단백질 수준의 변화가 또한 측정된다.
특정 징후
특정 구현예에서, 개체를 치료하는 방법이 본원에서 제공되고, 이 방법은 본원에 기재된 바와 같은 하나 이상의 약제학적 조성물을 투여하는 것을 포함한다. 특정 구현예에서, 개체는 대사성 질환 및/또는 심혈관 질환을 갖는다. 특정 구현예에서, 개체는 다음을 갖는다: 고지혈증 (예를 들면, 가족성 또는 비-가족성), 고콜레스테롤혈증 (예를 들면, 가족성 동종 고콜레스테롤혈증 (HoFH), 가족성 이형 고콜레스테롤혈증 (HeFH)), 이상지질혈증, 지방이영양증, 초고트리글리세라이드혈증 (예를 들면, 이종 LPL 결핍, 동종 LPL 결핍), 관상동맥 질환 (CAD), 가족성 카일로마이크론혈증 증후군 (FCS), 고지질단백혈증 유형 IV), 대사성 증후군, 비-알콜성 지방간 질환 (NAFLD), 비-알콜성 지방간염 (NASH), 당뇨병 (예를 들면, 2형 당뇨병, 이상지질혈증을 갖는 2형 당뇨병), 인슐린 내성 (예를 들어, 이상지질혈증을 갖는 인슐린 내성), 혈관벽 증점제, 고혈압 (예를 들면, 폐 동맥 고혈압), 경화증 (예를 들면, 죽상경화증, 전신 경화증, 진행성 피부 경화증 및 증식성 폐쇄성 맥관병증 예컨대 디지털 궤양 및 폐 혈관 관여) 및 이의 조합.
특정 구현예에서, 본원에 기재된 ANGPTL3에 표적화된 화합물은 동물에서 지질 및/또는 에너지 대사를 조절한다. 특정 구현예에서, 본원에 기재된 ANGPTL3에 표적화된 화합물은 고콜레스테롤혈증, 이상지질혈증, 지방이영양증, 초고트리글리세라이드혈증, 대사성 증후군, NAFLD,NASH 및/또는 당뇨병의 생리적 마커 또는 표현형을 조절한다. 예를 들면, 동물에게 화합물을 투여하는 것은 VLDL, 비-에스테르화된 지방산 (NEFA), LDL, 콜레스테롤, 트리글리세라이드, 글루코오스, 인슐린 또는 ANGPTL3 수준 중 하나 이상을 조절할 수 있다. 특정 구현예에서, 생리적 마커 또는 표현형 조절은 상기 화합물에 의한 ANGPTL3의 억제와 연관될 수 있다.
특정 구현예에서, 본원에 기술된 ANGPTL3에 표적화된 화합물은 하기 중 하나 이상을 감소시키고/시키거나 예방한다: 간 TG 축적 (즉 간지방증), 죽상동맥 경화증, 혈관벽 비후화 (예를 들면, 동맥 내중막 비후화), 조합된 고지혈증 (예를 들면, 가족성 또는 비-가족성), 고콜레스테롤혈증 (예를 들면, 가족성 동종 고콜레스테롤혈증 (HoFH), 가족성 이형 고콜레스테롤혈증 (HeFH)), 이상지질혈증, 지방이영양증, 초고트리글리세라이드혈증 (예를 들면, 이종 LPL 결핍, 동종 LPL 결핍, 가족성 카일로마이크론혈증 증후군 (FCS), 고지질단백혈증 유형 IV), 대사성 증후군, 비-알콜성 지방간 질환 (NAFLD), 비-알콜성 지방간염 (NASH), 당뇨병 (예를 들면, 유형 2 당뇨병, 이상지질혈증을 갖는 유형 2 당뇨병), 인슐린 내성 (예를 들면, 이상지질혈증을 갖는 인슐린 내성), 고혈압 및 경화증, 또는 이의 임의의 조합. 특정 구현예에서, 본원에 기재된 ANGPTL3에 표적화된 화합물은 인슐린 민감성을 향상시킨다.
특정 구현예에서, ANGPTL3 핵산에 표적화된 안티센스 화합물의 투여로 적어도 약 15% 만큼, 적어도 약 20% 만큼, 적어도 약 25% 만큼, 적어도 약 30% 만큼, 적어도 약 35% 만큼, 적어도 약 40% 만큼, 적어도 약 45% 만큼, 적어도 약 50% 만큼, 적어도 약 55% 만큼, 적어도 약 60% 만큼, 적어도 약 65% 만큼, 적어도 약 70% 만큼, 적어도 약 75% 만큼, 적어도 약 80% 만큼, 적어도 약 85% 만큼, 적어도 약 90% 만큼, 적어도 약 95% 만큼 또는 적어도 약 99% 만큼 또는 이들 값의 임의의 2 개에 의해 규정된 범위 까지 ANGPTL3 발현의 감소를 초래한다.
특정 구현예에서, ANGPTL3에 대해 표적화된 안티센스 화합물을 포함하는 약제학적 조성물은 대사성 질환 또는 심혈관 질환을 앓고 있거나 그것에 민감한 환자를 치료하기 위한 약제의 제조를 위해 사용된다. 특정 구현예에서, ANGPTL3를 표적화하는 안티센스 화합물을 포함하는 약제학적 조성물은 하기를 앓고 있거나, 또는 이에 취약한 환자를 치료하기 위한 약제의 제조에 사용된다: 조합된 고지혈증 (예를 들면, 가족성 또는 비-가족성), 고콜레스테롤혈증 (예를 들면, 가족성 동종 고콜레스테롤혈증 (HoFH), 가족성 이형 고콜레스테롤혈증 (HeFH)), 이상지질혈증, 지방이영양증, 초고트리글리세라이드혈증 (예를 들면, 가족성 카일로마이크론혈증 증후군 (FCS), 고지질단백혈증 유형 IV), 대사성 증후군, 비-알콜성 지방간 질환 (NAFLD), 비-알콜성 지방간염 (NASH), 당뇨병 (예를 들면, 유형 2 당뇨병, 이상지질혈증을 갖는 유형 2 당뇨병), 인슐린 내성 (예를 들면, 이상지질혈증을 갖는 인슐린 내성), 혈관벽 증점제, 고혈압 및 경화증, 또는 이의 임의의 조합.
투여
특정 구현예에서, 본원에 기술된 화합물 및 조성물은 비경구로 투여된다.
특정 구현예에서, 비경구 투여는 주입에 의한 것이다. 주입은 만성적이거나, 연속적이거나, 단기간이거나 간헐적일 수 있다. 특정 구현예에서, 주입된 약제학적 제제는 펌프로 전달된다.
특정 구현예에서, 비경구 투여는 주사에 의한 것이다. 이러한 주사는 주사기로 투여될 수 있다. 특정 구현예에서, 비경구 투여는 주사에 의한 것이다. 특정 구현예에서, 주사는 조직 또는 장기로 직접 투여된다. 특정 구현예에서, 주사는 피하로 주사된다.
임의의 병용 요법
특정 구현예에서, 변형된 올리고뉴클레오티드를 포함하는 제1 제제는 하나 이상의 제2 제제와 함께 공-투여된다. 특정 구현예에서, 그와 같은 제2 제제는 본원에 기재된 제1 제제로서 동일한 질환, 장애, 또는 병태를 치료하기 위해 설계된다. 특정 구현예에서, 그와 같은 제2 제제는 본원에 기재된 제1 제제로서 상이한 질환, 장애, 또는 병태를 치료하기 위해 설계된다. 특정 구현예에서, 그와 같은 제2 제제는 본원에 기재된 바와 같은 하나 이상의 약제학적 조성물의 원하지 않는 부작용을 치료하기 위해 설계된다. 특정 구현예에서, 제2 제제는 제1 제제의 원하지 않는 효과를 치료하기 위해 제1 제제와 공-투여된다. 특정 구현예에서, 제2 제제는 조합 효과를 얻기 위해 제1 제제와 공-투여된다. 특정 구현예에서, 제2 제제는 상승작용 효과를 얻기 위해 제1 제제와 공-투여된다.
특정 구현예에서, 제 1 제제 및 하나 이상의 제2 제제는 동시에 투여된다. 특정 구현예에서, 제 1 제제 및 하나 이상의 제2 제제는 상이한 시간에 투여된다. 특정 구현예에서, 제 1 제제 및 하나 이상의 제2 제제는 단일 약제학적 제형으로 함께 제조된다. 특정 구현예에서, 제 1 제제 및 하나 이상의 제2 제제는 별도로 제조된다.
특정 구현예에서, 제2 제제는, 비제한적으로, 글루코오스-저하제를 포함한다. 글루코오스 저하제는, 비제한적으로, 치료 생활방식 변화, PPAR 작용제, 디펩티딜 펩티다아제 (IV) 억제제, GLP-1 유사체, 인슐린 또는 인슐린 유사체, 인슐린 분비촉진제, SGLT2 억제제, 인간 아밀린 유사체, 바이구아나이드, 알파-글루코시다제 억제제, 또는 이들의 조합을 포함할 수 있다. 글루코오스-저하제는, 비제한적으로 메트포르민, 설포닐우레아, 로시글리타존, 메글리티나이드, 티아졸리딘디온, 알파-글루코시다제 억제제 또는 이들의 조합을 포함할 수 있다. 설포닐우레아는 아세토헥사마이드, 클로르프로파마이드, 톨부타마이드, 톨라자마이드, 글리메피라이드, 글리피자이드, 글리부라이드, 또는 글리클라자이드일 수 있다. 메글리티나이드는 나테글리나이드 또는 레파글리나이드일 수 있다. 티아졸리딘디온은 피오글리타존 또는 로시글리타존일 수 있다. 알파-글루코시다제는 아카르보스 또는 미글리톨일 수 있다. 특정 구현예에서, 지질 저하 요법은 하기를 비제한적으로 포함할 수 있다: 치료적 생활방식 변화, 니아신, HMG-CoA 환원효소 억제제, 콜레스테롤 흡수 억제제, MTP 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 안티센스 화합물 (MTP에 표적화됨)), 피브레이트, PCSK9 억제제 (예를 들면, PCSK9 항체, 폴리펩티드, 소분자 핵산 화합물 (PCSK9에 표적화됨)), CETP 억제제 (예를 들면, 소분자 예컨대 토르세트라핍 및 아나세트라핍, 폴리펩티드, 항체 또는 핵산 화합물 (CETP에 표적화됨)), apoC-III 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 핵산 화합물 (apoC-III에 표적화됨)), apoB 억제제 (예를 들면, 소분자, 폴리펩티드, 항체 또는 핵산 화합물 (apoB에 표적화됨)), 오메가-3 지방산 내 풍부한 유익 지방, 오메가-3 지방산 또는 이들의 임의의 조합. HMG-CoA 환원효소 억제제는 아토르바스타틴, 로수바스타틴, 플루바스타틴, 로바스타틴, 프라바스타틴, 심바스타틴 등일 수 있다. 콜레스테롤 흡수 억제제는 에제티마이브일 수 있다. 피브레이트는 페노파이브레이트, 베자피브레이트, 시프로피브레이트, 클로파이브레이트, 젬피브로질 등일 수 있다. 오메가-3 지방산 내 풍부한 유익 오일은 크릴, 어류 (예를 들면, VascepaR), 아마씨유 등일 수 있다. 오메가-3 지방산은 ALA, DHA, EPA 등일 수 있다.
특정 화합물
인간 ANGPTL3를 표적화하는 안티센스 올리고뉴클레오티드는 이전의 공보(참조: 2011년 7월 14일자로 공개된 PCT 특허 공보 제WO 2011/085271호, 이의 전문은 본원에 참고로 포함되어 있다)에 기술되어 있다. 시험관내에서 최고로 가장 강력한 10개의 안티센스 화합물을 포함하는, 상기 문헌에 기술된 수개의 올리고뉴클레오티드(233676, 233690, 233710, 233717, 233721, 233722, 337459, 337460, 337474, 337477, 337478, 337479, 337481, 337484, 337487, 337488, 337490, 337491, 337492, 337497, 337498, 337503, 337505, 337506, 337508, 337513, 337514, 337516, 337520, 337521, 337525, 337526 및 337528)가 하기 및 미국 시리즈 번호 61/920,652에 기술된 안티센스 화합물에 대한 선택 시험관내 스크린 전체에서 벤취마크로서 사용되었다. 제WO 2011/085271호에 기술된 가장 강력한 화합물 중에서, ISIS 233722는 ANGPTL3을 억제하는 이의 능력에 있어서 매우 가변적임이 밝혀졌다. 따라서, 일부 시험관내 연구에서 초기 포함되어 있다고 해도, 233722는 추가의 연구용 벤취마크로서 선택되지 않았다. 이전에 동정된 강력한 시험관내 벤취마크 화합물 중에서, 5개(233710, 233717, 337477, 337478, 337479 및 337487)가 huANGPTL3 형질전환 마우스에서 이후 기술된 바와 같이, 생체내 시험을 위해 선택되어 인간 mRNA 전사체 및 단백질 발현을 감소시키는데 있어서 가장 강력한지를 평가하였다(실시예 126). ANGPTL3 수준 (233710)을 감소시키는데 있어서 최대 초기 생체내 효능을 지닌 안티센스 올리고뉴클레오티드를 이후 기술된 새로운 안티센스 화합물의 생체내 평가용 벤취마크로서 사용하였다.
특정 구현예에서, 본원에 기술된 안티센스 화합물은 제WO 2011/085271호 및 미국 시리즈 번호 61/920,652에 기술된 안티센스 화합물에 대한 하나 이상의 개선된 특성으로부터 유리하다. 이들 개선된 특성은 본원의 실시예에서 입증되어 있으며, 실시예의 비-전면적인 요약이 참고 용이성을 위해 하기에 제공된다.
본원에 기술된 제1의 스크린에서, 인간 ANGPTL3을 표적화하는 약 3000개의 새로이 설계된 5-10-5 MOE 갭머 안티센스 화합물을 시험관내에서 인간 ANGPTL3 mRNA에 있어서 이들의 효과에 대해 Hep3B 세포내에서 시험하였다(실시예 116). 새로운 안티센스 화합물의 mRNA 억제 수준은 선택 연구에서 벤취마크로서 사용된 미리 설계된 일부의 안티센스 화합물 (233717, 337484, 337487, 337492 및 337516)로 평가하였다. 이러한 제1의 스크리닝으로부터 약 3000개의 새로이 설계된 안티센스 화합물 중에서, 약 85개의 안티센스 화합물을 시험관내 투여량-의존성 억제 연구를 위해 선택하여 이들의 최대 억제 농도의 1/2(IC50)을 측정하였다(실시예 117-118). 이들의 최대 억제 농도의 1/2(IC50)에 대해 시험한 약 85개의 새로운 안티센스 화합물 중에서, ANGPTL3의 강력한 투여량-의존성 감소를 입증한 약 38개의 안티센스 화합물을 벤취마크로서 사용된 안티센스 화합물 233710을 사용하여 마우스(실시예 126-127)에서 생체내 효능 및 내성(ALT 및 AST) 시험을 위해 선택하였다.
본원에 기술된 제2의 스크린에서, MOE 갭머 모티프 또는 혼합 모티프(데옥시, 5-10-5 MOE 및 cET 갭머)를 지닌 인간 ANGPTL3을 표적화하는 약 2000개의 새로이 설계된 안티센스 화합물을 또한 시험관내에서 인간 ANGPTL3 mRNA에 대한 이들의 효과에 대해 Hep3B 세포 속에서 시험하였다(실시예 119-121). 새로운 안티센스 화합물의 억제 수준을 선택 연구에서 벤취마크로서 사용된 일부 이전에 설계된 안티센스 화합물(233717, 337487, 337513, 337514 및 337516)로 평가하였다. 이러한 제2의 스크리닝으로부터 약 2000개의 새로이 설계된 안티센스 화합물 중에서, 약 147개의 안티센스 화합물을 시험관내 투여량-의존성 억제 연구를 위해 선택하여 이들의 최대 억제 농도의 1/2(IC50)을 측정하였다(실시예 122-125). 이들의 최대 억제 농도의 1/2(IC50)에 대해 시험한 약 147개의 새로운 안티센스 화합물 중에서, ANGPTL3의 강력한 투여량-의존성 감소를 입증한 약 73개의 안티센스 화합물을 벤취마크로서 사용된 안티센스 화합물 233710을 사용하여 마우스(실시예 126-127)에서 생체내 효능 및 내성(예를 들어, ALT 및 AST) 시험을 위해 선택하였다.
마우스에서 효능 및 내성에 대해 시험한 스크린 1 및 2로부터의 약 111개의 안티센스 화합물 중 24개를 알라닌 트랜스아미나제(ALT), 아스파르테이트 트랜스아미나제(AST), 알부민 및 빌리루빈, 및 또한 신장 대사 마커 BUN 및 크레아티닌 및 기관 중량(실시예 127)와 같은 간 대사 마커를 평가함으로써 마우스내에서 보다 광범위한 내성 시험을 위해 선택하였다.
생체내 뮤린 연구와 병행하여, 17개의 안티센스 화합물을 점도 시험을 위해 선택하였다(실시예 128). 일반적으로, 점도에 최적이 아니었던 안티센스 화합물은 추가의 연구에서 상향으로 취해지지 않았다.
마우스 내성 연구의 결과를 기반으로 하여, 20개의 안티센스 화합물을 래트에서 생체내 내성 시험을 위해 선택하였다(실시예 129). 래트에서, ALT, AST, 알부민 및 빌리루빈과 같은 간 대사 마커, 체중 및 기관 중량, 및 또한 BUN, 크레아티닌 및 총 단백질/크레아티닌 비와 같은 신장 대사 마커를 측정하여 생체내에서 화합물의 내성을 측정하였다.
래트에서 시험한 20개의 안티센스 화합물을 또한 레서스 원숭이 ANGPTL3 유전자 서열에 대한 교차-반응성에 대해 평가하였다(실시예 130). 당해 연구에서 안티센스 화합물은 시노몰구스 원숭이에서 시험되었지만, 시노몰구스 원숭이 ANGPTL3 서열은 전장의 화합물의 서열과의 비교를 위하여 이용가능하지 않았으므로, 안티센스 화합물의 서열을 밀접하게 관련된 레서스 원숭이의 것과 비교하였다. 8개의 안티센스 화합물의 서열은 레서스 ANGPTL3 유전자 서열과 0 내지 2개의 미스매치를 가졌음이 밝혀졌으며 시노몰구스 원숭이에서 추가로 연구되었다(실시예 130). 8개의 안티센스 화합물(ISIS 563580, ISIS 560400, ISIS 567320, ISIS 567321, ISIS 544199, ISIS 567233, ISIS 561011 및 ISIS 559277)을 ANGPTL3 mRNA 및 단백질 발현의 억제 및 또한 원숭이에서 내성에 대해 시험하였다. 내성 연구에서, 체중, 간 대사 마커(ALT, AST 및 빌리루빈), 신장 대사 마커(BUN 및 크레아티닌), 혈액학 매개변수(혈액 세포 수, 헤모글로빈 및 헤마토크리트), 및 전-염증성 마커(CRP 및 C3)를 측정하였다. 또한, 간 및 신장 속에 존재하는 전장 올리고뉴클레오티드 농도를 측정하여 신장/간에서 전장 올리고뉴클레오티드의 비를 계산하였다.
시노몰구스 원숭이에서 측정된, 강력하고 내성있는 안티센스 화합물, ISIS 563580의 서열을, 실시예 113-115 및 131에서 나타난 바와 같이, GalNAc 콘주게이트 및/또는 골격 화학성질의 변화로 추가로 변형시키고, 증가된 효력에 대하여 평가하였다.
따라서, 하나 이상의 개선된 특징, 예를 들면, 제WO 2011/085271호 및 미국 시리즈 번호 61/920,652에 기술된 안티센스 화합물과 비교하여 개선된 특징을 지닌 안티센스 화합물이 본원에 제공된다. 특정 구현예에서, 서열번호: 1 및 2 중의 어느 하나의 뉴클레오티드의 영역에 표적화되거나, 이와 구체적으로 혼성화된, 본원에 기술된 바와 같은 변형된 올리고뉴클레오티드를 포함하는 안티센스 화합물이 본원에 제공된다.
특정 구현예에서, 본원에 기술된 바와 같은 특정의 안티센스 화합물은 ANGPTL3 발현을 억제하는데 있어서의 이의 효능으로 인해 효과적이다. 특정 구현예에서, 화합물 또는 조성물은 ANGPTL3를 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90% 또는 적어도 95%까지 억제한다.
특정 구현예에서, 본원에 기술된 특정의 안티센스 화합물은 인간 세포, 예를 들면, Hep3B 세포주에서 시험하는 경우(실시예 117-118 및 122-125에 기술된 바와 같이) 20μM 미만, 10μM 미만, 8μM 미만, 5μM 미만, 2μM 미만, 1μM 미만, 0.9μM 미만, 0.8μM 미만, 0.7μM 미만, 0.6μM, 또는 0.5μM 미만의 시험관내 IC50로 인해 효과적이다. 특정 구현예에서, 1.0 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 15, 20, 24, 34, 35, 36, 37, 42, 43, 44, 47, 50, 51, 57, 58, 60, 77, 79, 82, 87, 88, 90, 91, 93, 94, 100, 101, 104, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 169, 170, 177, 188, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 및 232. 특정 구현예에서, 0.9 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 15, 20, 35, 36, 42, 43, 44, 50, 57, 60, 77, 79, 87, 88, 90, 91, 93, 94, 101, 104, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 177, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 및 232. 특정 구현예에서, 0.8 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 15, 20, 35, 36, 42, 43, 44, 50, 57, 60, 77, 79, 87, 88, 90, 91, 93, 94, 101, 104, 110, 111, 112, 113, 114, 115, 116, 117, 118, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 177, 209, 210, 211, 212, 213, 214, 215, 217, 218, 219, 220, 221, 222, 223, 224, 225, 228, 229, 230, 231, 및 232. 특정 구현예에서, 0.7 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 15, 20, 36, 42, 43, 57, 60, 114, 117, 127, 131, 177, 209, 210, 211, 212, 213, 214, 215, 217, 218, 219, 220, 221, 222, 223, 224, 225, 228, 229, 230, 231, 및 232. 특정 구현예에서, 0.6 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 15, 20, 36, 42, 43, 57, 60, 114, 117, 127, 131, 177, 209, 210, 211, 212, 213, 215, 217, 218, 219, 220, 221, 222, 224, 225, 228, 229, 230, 231, 및 232. 특정 구현예에서, 0.5 μM 미만의 IC50를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 43, 114, 117, 127, 131, 177, 209, 210, 211, 212, 215, 217, 218, 219, 220, 221, 222, 229, 230, 및 232.
특정 구현예에서, 본원에 기술된 바와 같은 특정의 안티센스 화합물은 검정(실시예 128에 기술된 바와 같음)에 의해 측정하는 경우 점도가 40 cP 미만, 35 cP 미만, 30 cP 미만, 25 cP 미만, 20 cP 미만, 15 cP 미만, 또는 10 cP 미만임으로 인해 효과적이다. 40 cP보다 큰 점도를 갖는 올리고뉴클레오티드는 최적 미만의 점도를 가질 것이다. 특정 구현예에서, 20 cP 미만의 점도를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 16, 18, 20, 34, 35, 36, 38, 49, 77, 90, 93, 및 94. 특정 구현예에서, 15 cP 미만의 점도를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 16, 18, 20, 34, 35, 38, 49, 90, 93, 및 94. 특정 구현예에서, 10 cP 미만의 점도를 갖는 바람직한 안티센스 화합물은 하기 서열번호를 포함한다: 18, 34, 35, 49, 90, 93, 및 94.
특정 구현예에서, 본원에 기술된 바와 같은 특정의 안티센스 화합물은 실시예에 기술된 생체내 내성 측정으로 입증된 바와 같이, 고도로 내성이다. 특정 구현예에서, 본원에 기술된 바와 같은 특정의 안티센스 화합물은 염수 치료된 동물보다 3배, 2배 또는 1.5배 이하의 ALT 및/또는 AST 값에 있어서의 증가를 가짐에 의해 입증되는 바와 같이, 고도로 내성이다.
특정 구현예에서, 본원에 기술된 바와 같은 특정의 안티센스 화합물은 50% 이상의 억제 효능, 1μM 미만의 시험관내 IC50, 20 cP 미만의 점도, 및 ALT 및/또는 AST에 있어서 3배 이하의 증가 중 하나 이상를 가짐으로 인해 효과적이다.
특정 구현예에서, ISIS 563580(서열번호: 77)가 바람직하다. 당해 화합물은 ANGPTL3 형질전환 마우스에서 강력한 억제제이고 가장 내성인 안티센스 화합물임이 밝혀졌다. 이는 약 16.83cP의 허용되는 점도 및 시험관내에서 0.8μM 미만의 IC50 값을 가졌다. 마우스에서, 이는 염수 치료된 동물보다 ALT 및/또는 AST 수준에 있어서 3배 이하로 증가되었다. 또한, 원숭이에서, 이는 ANGPTL3을 억제하는데 있어서 가장 내성이고 강력한 화합물 중에 있었으며, 전장 올리고뉴클레오티드 농도의 가장 좋은 비를 가졌다.
특정 구현예에서, ISIS 544199(서열번호: 20)가 바람직하다. 당해 화합물은 강력하고 내성인 안티센스 화합물임이 밝혀졌다. 이는 약 1.7 cP의 허용되는 점도 및 시험관내에서 0.5 μM 미만의 IC50 값을 가졌다. 마우스에서, 이는 염수 치료된 동물보다 ALT 및/또는 AST 수준에 있어서 3배 이하로 증가되었다. 또한, 원숭이에서, 이는 ANGPTL3를 억제하는데 있어서 가장 강력한 화합물중에 있었으며 전장 올리고뉴클레오티드 농도의 우수한 비를 가졌다.
특정 구현예에서, ISIS 559277(서열번호: 110)가 바람직하다. 당해 화합물은 강력하고 내성인 안티센스 화합물임이 밝혀졌다. 이는, 시험관내에서 IC50 값이 0.8μM 미만이었다. 마우스에서, 이는 염수 치료된 동물보다 ALT 및/또는 AST 수준에 있어서 3배 이하로 증가되었다. 또한, 원숭이에서, 이는 ANGPTL3를 억제하는데 있어서 가장 강력한 화합물 중에 있었으며 전장 올리고뉴클레오티드 농도의 우수한 비를 가졌다.
특정 구현예에서, GalNAc 콘주게이트된 안티센스 화합물, ISIS 658501(서열번호: 4912)가 바람직하다. 이러한 안티센스 화합물은 이의 모체 화합물 ISIS 563580 (서열번호: 77)보다 더욱 강력한 것으로 나타났다 (억제 수준에 의하여 나타난 바와 같이).
특정 구현예에서, GalNAc 콘주게이트된 안티센스 화합물, ISIS 703801(서열번호: 77)가 바람직하다. 이러한 안티센스 화합물은 이의 모체 화합물 ISIS 563580 (서열번호: 77)보다 더욱 강력한 것으로 나타났다. ISIS 703801은 1의 ID50 값을 갖고, 한편 ISIS 563580은 6의 ID50 값을 갖는다.
특정 구현예에서, GalNAc 콘주게이트된 안티센스 화합물, ISIS 703802(서열번호: 77)가 바람직하다. 이러한 안티센스 화합물은 이의 모체 화합물 ISIS 563580 (서열번호: 77) 보다 더욱 강력한 것으로 나타났다. ISIS 703802은 0.3의 ID50 값을 갖고, 한편 ISIS 563580은 6의 ID50 값을 갖는다.
실시예
하기 실시예는 본 개시내용의 특정 구현예를 설명하고 제한하지는 않는다. 게다가, 특정 구현예가 제공되는 경우, 본 발명자들 특정 구현예의 포괄적인 적용을 고려했다. 예를 들면, 특정한 모티프를 갖는 올리고뉴클레오티드의 개시내용은 동일한 또는 유사한 모티프를 갖는 추가의 올리고뉴클레오티드에 대한 합리적인 지지를 제공한다. 그리고, 예를 들면, 특정한 고-친화성 변형이 특정한 위치에서 나타나는 경우, 동일한 위치에서의 다른 고-친화성 변형은, 달리 지적되지 않으면 적당한 것으로 고려된다.
실시예
1:
포스포아미다이트
, 화합물 1, 1a, 및 2의 제조를 위한 일반 방법
화합물 1, 1a 및 2를 본원 명세서에서 기술된 바와 같이, 본 분야에서 잘 알려진 절차에 따라 제조하였다 (참고: Seth et al., Bioorg. Med. Chem., 2011, 21(4), 1122-1125, J. Org. Chem., 2010, 75(5), 1569-1581, Nucleic Acids Symposium Series, 2008, 52(1), 553-554); 및 또한 참고: 공보된 PCT 국제 출원 (WO 2011/115818, WO 2010/077578, WO2010/036698, WO2009/143369, WO 2009/006478, 및 WO 2007/090071), 및 미국 특허 7,569,686).
실시예
2: 화합물 7의 제조
화합물 3 (2-아세트아미도-1,3,4,6-테트라-O-아세틸-2-데옥시-β-D갈락토파이라노스 또는 갈락토사민 펜타아세테이트)는 시판되고 있다. 화합물 5은 공개된 절차에 따라 제조되었다 (Weber et al., J. Med. Chem., 1991, 34, 2692).
실시예
3: 화합물 11의 제조
화합물 8 및 9는 시판되고 있다.
실시예
4: 화합물 18의 제조
화합물 11은 실시예 3에서 실증된 절차에 따라 제조되었다. 화합물 14는 시판되고 있다. 화합물 17은 하기에 의해 보고된 유사한 절차를 사용하여 제조되었다: Rensen et al., J. Med . Chem ., 2004, 47, 5798-5808.
실시예
5: 화합물 23의 제조
화합물 19 및 21는 시판되고 있다.
실시예
6: 화합물 24의 제조
화합물 18 및 23는 실시예 4 및 5에서 실증된 절차에 따라 제조되었다.
실시예
7: 화합물
25의 제조
화합물 24은 실시예 6에서 실증된 절차에 따라 제조되었다.
실시예
8: 화합물 26의 제조
화합물 24은 실시예 6에서 실증된 절차에 따라 제조된다.
실시예
9: GalNAc
3
-
1를
3' 말단에서 포함하는
콘주게이트된
ASO의
일반적인 제조, 화합물 29
상기 보호된 GalNAc 3 - 1는 하기 구조를 갖는다:
콘주게이트 그룹 GalNAc3-1의 GalNAc3 클러스터 부분 (GalNAc3-1a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 여기서 GalNAc3-1a은 하기 화학식을 갖는다:
고형 지지체 결합된 보호된 GalNAc 3 -1, 화합물 25는 실시예 7에서 실증된 절차에 따라 제조되었다. GalNAc 3 -1을 3' 말단에서 포함하는 올리고머 화합물 29는 자동화된 DNA/RNA 합성에서 표준 절차를 사용하여 제조되었다 (참고: Dupouy et al., Angew . Chem . Int . Ed., 2006, 45, 3623-3627). 포스포르아미다이트 빌딩 블록, 화합물 1 및 1a는 실시예 1에서 실증된 절차에 따라 제조되었다. 실증된 포스포르아미다이트는 대표적이고, 다른 포스포르아미다이트 빌딩 블록이 사용되어 소정의 순서 및 조성을 갖는 올리고머 화합물을 제조할 수 있는 것처럼 한정으로서 의도되지 않는다는 것을 의미한다. 고형 지지체에 부가된 포스포르아미다이트의 순서 및 양은 조정되어 본원에서 기재된 갭핑된 올리고머 화합물을 제조할 수 있다. 그와 같은 갭핑된 올리고머 화합물은 임의의 주어진 표적에 의해 지시되는 바와 같이 소정의 조성물 및 염기 서열을 가질 수 있다.
실시예
10: GalNAc
3
-
1를
5' 말단에서 포함하는
콘주게이트된
ASO의
일반적인 제조, 화합물 34
UnylinkerTM 30는 시판되고 있다. GalNAc 3 -1을 5' 말단에서 포함하는 올리고머 화합물 34는 자동화된 DNA/RNA 합성에서 표준 절차를 사용하여 제조되었다 (참고: Dupouy et al., Angew . Chem . Int . Ed., 2006, 45, 3623-3627). 포스포르아미다이트 빌딩 블록, 화합물 1 및 1a는 실시예 1에서 실증된 절차에 따라 제조되었다. 실증된 포스포르아미다이트는 대표적이고, 다른 포스포르아미다이트 빌딩 블록이 사용되어 소정의 순서 및 조성을 갖는 올리고머 화합물을 제조할 수 있는 것처럼 한정으로서 의도되지 않는다는 것을 의미한다. 고형 지지체에 부가된 포스포르아미다이트의 순서 및 양은 조정되어 본원에서 기재된 갭핑된 올리고머 화합물을 제조할 수 있다. 그와 같은 갭핑된 올리고머 화합물은 임의의 주어진 표적에 의해 지시되는 바와 같이 소정의 조성물 및 염기 서열을 가질 수 있다.
실시예
11: 화합물
39의 제조
화합물 4, 13 및 23는 실시예 2, 4, 및 5에서 실증된 절차에 따라 제조되었다. 화합물 35는 하기에서 공지된 유사한 절차를 사용하여 제조된다: Rouchaud et al., Eur. J. Org. Chem., 2011, 12, 2346-2353.
실시예
12: 화합물
40의 제조
화합물 38은 실시예 11에서 실증된 절차에 따라 제조된다.
실시예
13: 화합물
44의 제조
화합물 23 및 36은 실시예 5 및 11에서 실증된 절차에 따라 제조된다. 화합물 41는 하기에서 공지된 유사한 절차를 사용하여 제조된다: WO 2009082607.
실시예
14: 화합물
45의 제조
화합물 43은 실시예 13에서 실증된 절차에 따라 제조된다.
실시예
15: 화합물
47의 제조
화합물 46는 상업적으로 이용가능하다.
실시예
16: 화합물
53의 제조
화합물 48 및 49는 시판되고 있다. 화합물 17 및 47은 실시예 4 및 15에서 실증된 절차에 따라 제조된다.
실시예
17: 화합물
54의 제조
화합물 53은 실시예 16에서 실증된 절차에 따라 제조된다.
실시예
18: 화합물
55의 제조
화합물 53은 실시예 16에서 실증된 절차에 따라 제조된다.
실시예
19: 3
' 고체상 기술을 통해 위치에서
GalNAc
3
-1을 포함하는
콘주게이트된
ASO의 일반적인 제조 방법 (ISIS 647535, 647536 및 651900의 제조)
달리 언급되지 않으면, 올리고머 화합물의 합성을 위해 사용된 모든 시약 및 용액은 상업적 공급원으로부터 구매된다. 표준 포스포르아미다이트 빌딩 블록 및 고체 지지체는, 예를 들면 T, A, G, 및 mC 잔기를 포함하는 뉴클레오시드 잔기의 혼입을 위해 사용된다. 무수 아세토니트릴 중의 포스포르아미다이트의 0.1 M 용액을 β-D-2'-데옥시리보뉴클레오시드 및 2'-MOE에 사용하였다.
ASO 합성은 ABI 394 합성기 (1-2 μmol 규모) 상에서, 또는 칼럼에 충전된
GalNAc 3 -1 로딩된 VIMAD 고형 지지체 (110 μmol/g, Guzaev 등, 2003) 상에서 포스포르아미다이트 커플링 방법에 의해 GE Healthcare Bioscience
올리고파일럿 합성기 (40-200 μmol 규모) 상에서 수행되었다. 커플링 단계의 경우, 포스포르아미다이트를 고체 지지체의 로딩에 대해 4배 과량으로 전달하였고, 포스포르아미다이트 응축을 10분 동안 수행하였다. 모든 다른 단계는 제조자에 의해 공급된 표준 프로토콜을 따랐다. 톨루엔 중 6% 디클로로아세트산의 용액은 디메톡시트리틸 (DMT) 그룹을 뉴클레오티드의 5'-하이드록실 그룹로부터 제거하기 위해 사용되었다. 무수 CH
3CN 중 4,5-디시아노이미다졸 (0.7 M)은 커플링 단계 동안에 활성제로서 사용되었다. 포스포로티오에이트 연결을 3분의 접촉 시간 동안에 1:1 피리딘/CH3CN 중의 크산탄 하이드라이드의 0.1 M 용액을 이용한 황화에 의해 도입하였다. 6% 물을 함유하는 CH
3CN 중의 20%
tert-부틸하이드로퍼옥사이드의 용액을 산화제로서 사용하여 12분의 접촉 시간으로 포스포디에스테르 뉴클레오시드간 연결을 제공하였다.
원하는 서열이 조립된 후, 시아노에틸 포스페이트 보호 그룹은 45 분의 접촉 시간과 함께 트리에틸아민 및 아세토니트릴의 1:1 (v/v) 혼합물을 사용하여 탈보호되었다. 상기 고체-지지체 결합된 ASO를 암모니아수 (28-30 중량 %)에 현탁시키고 55℃ 에서 6시간 동안 가열하였다.
그리고 나서, 미결합된 ASO를 여과하고 암모니아를 가열로 제거하였다. 잔류물을 강한 음이온 교환 칼럼 상에서 고압 액체 크로마토그래피에 의해 정제하였다(GE Healthcare Bioscience, Source 30Q, 30 μm, 2.54 x 8 cm, A = 30% 수성 CH3CN 중의 100 mM 암모늄 아세테이트, B = A 중의 1.5 M NaBr, 60분에 0-40%의 B, 유량 14 mL min-1, λ = 260 nm). 잔류물을 역상 칼럼 상의 HPLC에 의해 탈염하여, 고체 지지체 상의 초기 로딩을 기준으로 15-30%의 단리된 수율로 원하는 ASO를 얻었다. ASO를 Agilent 1100 MSD 시스템을 갖는 이온-쌍-HPLC 커플링된 MS 분석에 의해 규명하였다.
콘주게이트를 포함하지 않는 안티센스 올리고뉴클레오티드는 당해기술에서 잘 알려진 표준 올리고뉴클레오티드 합성 절차를 사용하여 합성되었다.
이들 방법을 사용하여, ApoC III을 표적으로 하는 3 개의 별개의 안티센스 화합물이 제조되었다. 하기의 표 17에서 요약된 바와 같이, 각각의 ApoC III를 표적으로 하는 3 개의 안티센스 화합물은 동일한 핵염기 서열을 가졌고; ISIS 304801는 모든 포스포로티오에이트 연결을 갖는 5-10-5 MOE 갭머이고; ISIS 647535은 ISIS 304801와 동일하고, 단, 3' 말단에서 콘주게이트된 GalNAc 3 -1을 가졌고; 그리고 ISIS 647536은 ISIS 647535와 동일하고, 단, 상기 화합물의 특정 뉴클레오시드간 연결은 포스포디에스테르 연결이다. 표 17에서 추가로 요약된 바와 같이, SRB-1을 표적으로 하는 2 개의 별개의 안티센스 화합물이 합성되었다. ISIS 440762는 모든 포스포로티오에이트 뉴클레오시드간 연결을 갖는 2-10-2 cEt 갭머였고; ISIS 651900는 ISIS 440762와 동일하고, 단, 3'-말단에서 GalNAc 3 -1을 포함했다.
표 17
ApoC III 및 SRB-1을 표적으로 하는 변형된 ASO
하첨자: 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "k"는 6'-(S)-CH3 이환식 뉴클레오시드 (예를 들면 cEt)를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다. "GalNAc 3 -1"는 실시예 9에서 이전에 보여진 구조를 갖는 콘주게이트 그룹을 나타낸다. GalNAc 3 -1은 ASO를 “GalNAc 3 -1 a "인 것으로 지정된 콘주게이트의 나머지에 연결하는 절단가능 아데노신을 포함하는 것에 주목한다. 이러한 명명법은 콘주게이트의 일부인 아테노신을 포함하는 완전한 핵염기 서열을 보여주기 위해 상기 표에서 사용된다. 따라서, 상기 표에서, 서열은 "GalNAc 3 - 1"와 함께 생략된 "A do "로 종료되는 바와 같이 또한 열거될 수 있었다. 절단가능 뉴클레오시드 또는 절단가능 모이어티가 없는 콘주게이트 그룹의 부분을 나타내기 위해 하첨자 "a"를 사용하는 이러한 관례는 이들 실시예를 통해 사용된다. 절단가능 모이어티가 없는 콘주게이트 그룹의 이러한 부분은 "클러스터" 또는 "콘주게이트 클러스터" 또는 "GalNAc3 클러스터"로서 본원에서 칭해진다. 특정 예에서 그것의 클러스터 및 그것의 절단가능 모이어티를 별도로 제공하여 콘주게이트 그룹을 기재하는 것이 편리하다.
실시예
20:
huApoC
III 형질전환 마우스에서 인간
ApoC
III의 투여량-의존적 안티센스 억제
인간 ApoC III를 각각 표적으로 하고 상기에서 기재된 ISIS 304801 및 ISIS 647535는, 별도로 시험되었고 인간 ApoC III 형질전환 마우스에서 인간 ApoC III을 억제하기 위한 그것의 능력에 대한 투여량-의존적 연구에서 평가되었다.
치료
인간 ApoCIII 형질전환 마우스는 12-시간 명/암 사이클에서 유지되었고 임의로 Teklad 실험실 초우에 공급되었다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. ASO는 PBS에서 제조되었고 0.2 마이크론 필터을 통해 여과하여 멸균되었다. ASO는 주사를 위해 0.9% PBS에서 용해되었다.
인간 ApoC III 형질전환 마우스에게 복강내로 2 주 동안 1주 1회 ISIS 304801 또는 647535가 0.08, 0.25로 주입되었다. 0.75, 2.25 또는 6.75 μmol/kg 또는 PBS 대조군으로서. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마지막 투여량의 투여 48 시간 후, 혈액을 각 마우스로부터 뽑고 그리고 마우스는 희생되었고 조직은 수집되었다.
ApoC
III
mRNA
분석
마우스의 간 중 ApoC III mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린(RIBOGREEN)® RNA 정량화 시약을 사용하여 측정되었다 (Molecular Probes, Inc. Eugene, OR). ApoC III mRNA 수준은 PBS-처리된 대조군에 대한 정규화 전에 (리보그린을 사용하여) 총 RNA에 대해 결정되었다. 하기의 결과는 PBS-처리된 대조군에 대해 정규화된, 각 처리 그룹에 대한 ApoC III mRNA 수준의 평균 퍼센트로버 제공되고, "PBS %"로서 나타낸다. 각 ASO의 반 최대 효과적인 투여량 (ED50)은 하기의 표 18에서 또한 제공된다.
실증된 바와 같이, 안티센스 화합물 둘 모두는 PBS 대조군에 대한 ApoC III RNA를 감소시켰다. 게다가, GalNAc 3 -1 (ISIS 647535)에 콘주게이트된 안티센스 화합물은 GalNAc 3 -1 콘주게이트 (ISIS 304801)가 없는 안티센스 화합물보다 실질적으로 더 강했다.
표 18
인간 ApoC III 형질전환 마우스에서 ApoC III mRNA 수준에 대한 ASO 처리의 효과
ApoC
III 단백질 분석 (
비탁
(
Turbidometric
) 검정)
혈장 ApoC III 단백질 분석은 하기에 의해 보고된 절차를 사용하여 결정되었다: Graham 등, Circulation Research, 2013년 3월 29일 인쇄 전에 온라인에서 공개.
마우스로부터 단리된 대략 100 μl의 혈장은 Olympus 임상 분석기 및 시판되는 비탁 ApoC III 검정을 사용하여 희석없이 분석되었다 (Kamiya, Cat# KAI-006, Kamiya Biomedical, Seattle, WA). 검정 프로토콜은 판매인에 의해 기재된 바와 같이 수행되었다.
하기의 표 19에서 보여진 바와 같이, 안티센스 화합물 둘 모두는 PBS 대조군에 대한 ApoC III 단백질을 감소시켰다. 게다가, GalNAc 3 -1 (ISIS 647535)에 콘주게이트된 안티센스 화합물은 GalNAc 3 -1 콘주게이트 (ISIS 304801)가 없는 안티센스 화합물보다 실질적으로 더 강했다.
표 19
인간 ApoC III 형질전환 마우스에서 ApoC III 혈장 단백질 수준에 대한 ASO 처리의 효과
혈장 트리글리세라이드 및 콜레스테롤은 블라이 및 다이어 (Bligh, E.G. and Dyer, W.J. Can. J. Biochem. Physiol. 37: 911-917, 1959)(Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959)(Bligh, E and Dyer, W, Can J Biochem Physiol, 37, 911-917, 1959)의 방법에 의해 추출되었고, Beckmann Coulter 임상 분석기 및 시판되는 시약을 사용하여 측정되었다.
트리글리세라이드 수준은 PBS 주입된 마우스에 대해 측정되었고 "PBS %"로서 나타낸다. 결과는 표 20에서 제공된다. 실증된 바와 같이, 안티센스 화합물 둘 모두는 트리글리세라이드 수준을 감소시켰다. 게다가, GalNAc 3 -1 (ISIS 647535)에 콘주게이트된 안티센스 화합물은 GalNAc 3 -1 콘주게이트 (ISIS 304801)가 없는 안티센스 화합물보다 실질적으로 더 강했다.
표 20
형질전환 마우스에서 트리글리세라이드 수준에 대한 ASO 처리의 효과
혈장 샘플은 HPLC에 의해 분석되어 총 콜레스테롤 및 콜레스테롤 (HDL 및 LDL)의 상이한 분획의 양을 결정했다. 결과는 표 21 및 22에서 제공된다. 실증된 바와 같이, 안티센스 화합물 둘 모두는 총 콜레스테롤 수준을 감소시켰고; 둘 모두는 LDL을 감소시켰고; 그리고 둘 모두는 HDL을 상승시켰다. 게다가, GalNAc 3 -1 (ISIS 647535)에 콘주게이트된 안티센스 화합물은 GalNAc 3 -1 콘주게이트 (ISIS 304801)가 없는 안티센스 화합물보다 실질적으로 더 강했다. HDL의 증가 및 LDL 수준의 감소는 ApoC III의 안티센스 억제의 심혈관 유익한 효과이다.
표 21
형질전환 마우스에서 총 콜레스테롤 수준에 대한 ASO 처리의 효과
표 22
형질전환 마우스에서 HDL 및 LDL 콜레스테롤 수준에 대한 ASO 처리 효과
약동학 분석 (PK)
ASO의 PK가 또한 평가되었다. 간 및 신장 샘플은 다져졌고 표준 프로토콜을 사용하여 추출되었다. 샘플은 IP-HPLC-MS을 이용하여 MSD1 상에서 분석되었다. 전장 ISIS 304801 및 647535의 조직 수준 (μg/g)은 측정되었고 결과는 표 23에서 제공된다. 실증된 바와 같이, 총 전장 안티센스 화합물의 간 농도는 2 개의 안티센스 화합물에 대해 유사했다. 따라서, GalNAc 3 -1 콘주게이트된 안티센스 화합물기 (상기의 RNA 및 단백질 데이터에 의해 실질되는 바와 같이) 간에서 활성이 더 많을 지라도, 간에서 실질적으로 더 높은 농도로 존재하지 않는다. 사실상, 계산된 EC50 (표 23에서 제공)은, 콘주게이트된 화합물의 효능의 관찰된 증가가 증가된 축적에 전적으로 기인할 수 없다는 것을 확인해 준다. 이러한 결과는, 콘주게이트가 안티센스 화합물의 세포로의 생산적인 흡수를 가능하게 개선하여 간 축적 단독 이외의 기전에 의해 효능을 개선했다는 것을 암시한다.
상기 결과는 또한, 신장 중 GalNAc 3 -1 콘주게이트된 안티센스 화합물의 농도가 GalNAc 콘주게이트가 없는 안티센스 화합물의 농도보다 더 낮다는 것을 보여준다. 이것은 몇 개의 유익한 치료적 연루성을 갖는다. 신장에서의 활성이 추구되지 않는 치료적 징후에 대해, 신장에의 노출은 상응하는 이점 없이 신장 독성을 위태롭게 한다. 게다가, 신장의 고농도는 전형적으로 화합물의 소변으로 손실을 야기하고, 이로써 더 빠른 청소능을 얻는다. 따라서, 비-신장 표적에 대해, 신장 축적은 원치 않는다. 이들 데이터는, GalNAc 3 -1 콘주게이션이 신장 축적을 축소시킨다는 것을 암시한다.
표 23
형질전환 마우스에서 ASO 처리의 PK 분석
ISIS 647535의 대사물이 또한 확인되었고, 그것의 질량은 고분해능 질량 분광분석법 분석에 의해 확인되었다. 관찰된 대사물의 절단 부위 및 구조는 하기에서 보여진다. 전장 ASO의 상대 %는 표준 절차를 사용하여 계산되었고 결과는 표 23a에서 제공된다. ISIS 647535의 주요 대상물은 하기에서 보여진 절단 부위 A에서의 절단을 야기하는 전체 콘주게이트 (즉 ISIS 304801)가 없는 전장 ASO였다. 게다가, 다른 절단 부위로부터 수득된 추가 대상물이 또한 관찰되었다. 이들 결과는, 다른 절단가능 결합 예컨대 에스테르, 펩티드, 이황화, 포스포르아미데이트 또는 아실-하이드라존을 GalNAc 3 - 1 당과 ASO (이것은 세포 내의 효소에 의해 절단될 수 있거나, 사이토졸의 환원 환경에서 전달될 수 있거나 엔도솜 및 리소좀 내의 산성 pH에 대해 불안정함) 사이에 도입하는 것이 또한 유용할 수 있다는 것을 암시한다.
표 23a
ISIS 647535의 관찰된 전장 대사물
실시예
21: 단일 투여 연구에서 인간
ApoC
III 형질전환 마우스에서 인간
ApoC
III의
안티센스
억제
인간 ApoC III를 표적으로 하고 표 17에서 기재된 ISIS 304801, 647535 및 647536 각각은, 인간 ApoC III 형질전환 마우스 인간 ApoC III을 억제하기 위해 그것의 능력에 대한 단일 투여 연구에서 추가로 평가되었다.
치료
인간 ApoCIII 형질전환 마우스는 12-시간 명/암 사이클에서 유지되었고 임의로 Teklad 실험실 초우에 공급되었다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. ASO는 PBS에서 제조되었고 0.2 마이크론 필터을 통해 여과하여 멸균되었다. ASO는 주사를 위해 0.9% PBS에서 용해되었다.
인간 ApoC III 형질전환 마우스에게 복강내로 1 회 하기에서 보여진 투여량으로 ISIS 304801, 647535 또는 647536 (상기에서 기재됨) 또는 PBS 처리된 대조군이 주입되었다. 처리 그룹은 3마리의 동물로 구성되었고 대조군 그룹은 4 마리의 동물로 구성되었다. 처리 전에 뿐만 아니라 마지막 투여량 후에, 혈액을 각 마우스로부터 채혈하고 혈장 샘플을 분석하였다. 마우스는 마지막 투여 72 시간 후에 희생되었다.
샘플을 수집하고 분석하여 HDL 및 LDL 분획을 포함하는 간; 혈장 트리글리세라이드; 및 콜레스테롤에서 ApoC III mRNA 및 단백질 수준을 측정하고, 상기에서 기재된 바와 같이 평가하였다 (실시예 20). 이들 분석으로부터의 데이터는 하기의 표 24-28에서 제공된다. 혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. ALT 및 AST 수준은, 안티센스 화합물이 모든 투여된 투여량으로 용인되었다는 것을 보여주었다.
이들 결과는 GalNAc 3 -1 콘주게이트 (ISIS 304801)가 없는 안티센스 화합물과 비교하여 3' 말단 (ISIS 647535 및 647536)에서 GalNAc 3 -1 콘주게이트를 포함하는 안티센스 화합물에 대한 효능의 개선을 보여준다. 게다가, GalNAc 3 -1 콘주게이트 및 일부 포스포디에스테르 연결을 포함하는 ISIS 647536은 동일한 콘주게이트를 포함하는 ISIS 647535만큼 강력했고, ASO 내의 모든 뉴클레오시드간 연결은 포스포로티오에이트이다.
표 24
인간 ApoC III 형질전환 마우스에서 ApoC III mRNA 수준에 대한 ASO 처리의 효과
표 25
인간 ApoC III 형질전환 마우스에서 ApoC III 혈장 단백질 수준에 대한 ASO 처리의 효과
표 26
형질전환 마우스에서 트리글리세라이드 수준에 대한 ASO 처리의 효과
표 27
형질전환 마우스에서 총 콜레스테롤 수준에 대한 ASO 처리의 효과
표 28
형질전환 마우스에서 HDL 및 LDL 콜레스테롤 수준에 대한 ASO 처리 효과
이들 결과는, GalNAc 3 -1 콘주게이트가 안티센스 화합물의 효능을 개선한다는 것을 확인한다. 결과는 또한, GalNAc 3 -1 콘주게이트된 안티센스 화합물의 동등한 효능을 보여주고, 여기서 안티센스 올리고뉴클레오티드는 혼합된 연결 (6개의 포스포디에스테르 연결을 갖는 ISIS 647536) 및 동일한 안티센스 화합물의 완전한 포스포로티오에이트 버전 (ISIS 647535)을 갖는다.
포스포로티오에이트 연결은 안티센스 화합물에 대한 몇 개의 특성을 제공한다. 예를 들면, 뉴클레아제 소화에서 저장하고 단백질에 결합하고, 이것은 신장/소변에서보다 간에서 화합물의 축적을 야기한다. 이들은, 특히 간에서 조짐을 치료할 때 바람직한 특성이다. 그러나, 포스포로티오에이트 연결은 또한 염증성 반응과 연관되었다. 따라서, 화합물 중 포스포로티오에이트 연결의 수를 감소시키는 것은 염증의 위험, 뿐만 아니라 간에서 저농도의 화합물을 감소시키고, 신장 및 소변에서 농도를 증가시키고, 뉴클레아제의 존재에서의 안정성을 증가시키고, 더 낮은 전체 효능을 낮추는 것으로 기대된다. 본 결과는, 특정 포스포로티오에이트 연결이 포스포디에스테르 연결로 대체되었던 GalNAc 3 -1 콘주게이트된 안티센스 화합물이 완전한 포스포로티오에이트 연결을 갖는 대응물로서 간에서 표적에 대항하여 강력하다는 것을 보여준다. 그와 같은 화합물은 전염증이 덜한 것으로 기재된다 (PS의 축소를 보여주는 실험은 감소된 염증성 효과를 야기한다는 것을 기재하는 실시예 24 참고).
실시예
22:
생체내
에서
SRB
-1을 표적으로 하는
GalNAc
3
-1
콘주게이트된
변형된
ASO의
효과
SRB-1을 표적으로 하고 표 17에서 기재된 ISIS 440762 및 651900 각각을 대상으로 Balb/c 마우스에서 SRB-1을 억제하는 그 능력을 투여량-의존적 연구에서 평가하였다.
치료
6주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 440762, 651900 또는 PBS 처리된 대조군을 하기에 제시된 투여량으로 피하로 1회 주입하였다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 48 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 내에서의 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). SRB-1 mRNA 수준을 PBS-처리된 대조군에 대해 정규화하기 전에 총 RNA에 대해 결정하였다(리보그린을 이용하여). 하기의 결과는 PBS-처리된 대조군에 정규화된, 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 제시되어 있고, "PBS %"로서 표시되어 있다.
표 29에서 입증된 바와 같이, 두 안티센스 화합물들은 SRB-1 mRNA 수준을 낮추었다. 게다가, GalNAc 3 -1 (ISIS 651900) 콘주게이트를 포함하는 안티센스 화합물은 GalNAc 3 -1 콘주게이트 (ISIS 440762)가 없는 안티센스 화합물보다 실질적으로 더 강했다. 이들 결과는, GalNAc 3 -1 콘주게이트의 효능 이점이 상이한 표적에 대해 상보적이고 상이한 화학적으로 변형된 뉴클레오시드를 갖는 안티센스 올리고뉴클레오티드를 사용하여 관찰된다는 것을 입증하고, 이러한 예에서 변형된 뉴클레오시드는 제한된 에틸 당 모이어티 (이환식 당 모이어티)를 포함한다.
표 29
Balb/c 마우스에서 SRB-1 mRNA 수준에 대한 ASO 처리의 효과
실시예
23: 인간
말초 혈액
단핵
세포 (
hPBMC
) 검정 프로토콜
hPBMC 검정은 BD Vautainer CPT 튜브 방법을 사용하여 수행하였다. 미국 보건 클리닉(US HealthWorks clinic) (Faraday & El Camino Real, Carlsbad)에서 고지에 의한 동의로 자원된 공여체로부터 전혈 샘플을 얻어 4-15 BD 진공채혈기 CPT 8 ml 튜브 (VWR Cat.# BD362753)에 모았다. 각 공여체에 대한 CPT 튜브에서의 대략적인 개시되는 총 전혈액량을 PBMC 검정 데이터 시트를 사용하여 기록하였다.
튜브를 8-10회 뒤집어 원심분리 바로 전에 혈액 샘플을 재혼합하였다. CPT 튜브를브레이크 없이(2700 RPM Beckman Allegra 6R)1500-1800 RCF에서 30분간 수평 (swing-out) 로터에서 실온(18-25 oC)에서 원심분리하였다. 세포를 버피 코트 계면 (피콜 및 폴리머 겔 층 사이)로부터 회수하고; 멸균한 50 ml 원뿔형 튜브로 옮기고 5 CPT 튜브/50 ml 원뿔형 튜브/공여체까지 모았다. 그리고 나서, 세포를 PBS (Ca++, Mg++없음; GIBCO)로 2회 세정하였다. 튜브를 50 ml까지 가득 채우고몇 번 뒤집어 혼합하였다. 그리고 나서, 샘플을 330 x g에서 15분 동안 실온에서 원심분리하고(Beckman Allegra 6R에서 1215 RPM), 펠렛을 건드리지 않고 가능한 한 많은 상청액을 흡인하였다. 튜브를 와류시켜 세포 펠렛을 제거하고 RPMI+10% FBS+펜/스트렙 (~1 ml / 10 ml 시작하는 전혈량)에서 세포를 재현탁시켰다. 60 μl 샘플을 600 μl VersaLyse 시약 (Beckman Coulter Cat# A09777)을 갖는 샘플 바이알 (Beckman Coulter) 내로 피펫팅하고 10-15초 동안 부드럽게 볼텍싱하였다. 샘플을 10분 동안 실온에서 10분 동안 배양하고 다시 혼합한 후 계수하였다. 세포 현탁액을 PBMC 세포형 (1:11의 희석 인자가 다른 파라미터를 이용하여 보관되었음)을 이용하여 Vicell XR 세포 생존력 분석기 (Beckman Coulter) 상에서 계수하였다. 생존 세포/ml 및 생존력을 기록하였다. 세포 현탁액을 1 x 107 생존 PBMC/ RPMI+ 10% FBS+펜/스트렙 중에서의 ml로 희석하였다.
세포를 50 μl/웰의 96-웰 조직 배양판 (Falcon Microtest)에 5 x 105로 플레이팅하였다. RPMI+10% FBS+펜/스트렙에 희석된 50 μl/웰의 2x 농도 올리고/대조군을 실험 템플레이트 (100 μl/웰 총)에 따라 부가하였다. 플레이트를 진탕기에 놓고 대략 1분간 혼합하였다. 37 ℃에서 24시간 동안 배양한 후; 5% CO2, 플레이트를 400 x g에서 10분 동안 원심분리한 다음 MSD 사이토카인 검정 (즉 인간 IL-6, IL-10, IL-8 및 MCP-1)을 위해 상청액을 제거하였다.
실시예
24:
GalNAc
3
-1
콘주게이트된
ASO를
위한
hPBMC
검정에서의
전염증
효과의 평가
표 30에 열거된 안티센스 올리고뉴클레오티드 (ASO)에 대해 실시예 23에서 기재된 프로토콜을 사용하여 hPBMC 검정에서의 전염증 효과를 평가하였다. ISIS 353512는 검정에서의 IL-6 방출에 대한 고반응군인 것으로 알려진 내부 표준이다. hPBMC를 신선한, 지원된 공여체로부터 단리하고 0, 0.0128, 0.064, 0.32, 1.6, 8, 40 및 200 μM 농도의 ASO로 처리하였다. 24시간 처리 후, 사이토카인 수준을 측정하였다.
IL-6의 수준을 일차 판독으로서 사용하였다. EC50 및 Emax를 표준 절차를 이용하여 계산하였다. 결과는 두 공여체로부터 Emax/EC50의 평균 비로서 표현되고 "Emax/EC50"로 나타내어진다. 더 낮은 비율은 전염증 반응에서 상대적 감소를 가리키고 더 높은 비율은 전염증 반응에서 상대적 증가를 가리킨다.
시험 화합물과 관련하여, 가장 낮은 전염증 화합물은 PS/PO 연결된 ASO (ISIS 616468)였다. GalNAc 3 -1 콘주게이트된 ASO인 ISIS 647535는그의 비-콘주게이트된 대응물 ISIS 304801보다 약간 덜 전염증이었다. 이들 결과는, 일부 PO 연결의 혼입이 전염증 반응을 감소시키며 GalNAc 3 -1 콘주게이트의 부가가 화합물을 더 전염증성으로 만들며 전염증 반응을 감소시킬 수 있음을 가리킨다. 따라서, 당업자라면 혼합된 PS/PO 연결 및 GalNAc 3 -1 콘주게이트 모두를 포함하는 안티센스 화합물이 GalNAc 3 -1 콘주게이트를 갖거나 갖지 않는 완벽한 PS 연결된 안티센스 화합물과 비교하여 더 낮은 전염증 반응을 생성할 것임을 예상할 것이다. 이들 결과는, GalNAc 3- 1 콘주게이트된 안티센스 화합물, 특히 감소된 PS 함량을 갖는 화합물이 덜 전염증이라는 것을 보여준다.
함께, 이들 결과는, GalNAc 3 -1 콘주게이트된 화합물, 특히 감소된 PS 함량을 갖는 화합물이 GalNAc 3 -1 콘주게이트가 없는 대응되는 완전한 PS 안티센스 화합물보다 더 높은 투여량으로 투여될 수 있음을 제시한다. 이들 화합물의 경우 반감기가 실질적으로 상이할 것으로 예상되지 않으므로, 그러한 더 높은 투여는 덜 빈번한 투여를 야기할 것이다. 사실상 그러한 투여는 훨씬 덜 빈번할 수 있는데, GalNAc 3 -1 콘주게이트된 화합물이 더 강하고(실시예 20-22 참고), 화합물의 농도가 효능에 기초하여 원하는 수준 이하로 떨어지면 재-투여이 필요하기 때문이다.
표 30
변형된 ASO
하첨자: 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "k"는 6'-(S)-CH3 이환식 뉴클레오시드 (예를 들면 cEt)를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다. "A do '-GalNAc 3 -1 a "는, 명시된 바와 같이, 안티센스 올리고뉴클레오티드의 3'-말단에 부착된 실시예 9에 나타난 구조 GalNAc 3 -1를 갖는 콘주게이트를 가리킨다.
표 31
hPBMC 검정에서 ApoC III를 표적으로 하는 ASO의 전염증 효과
실시예
25:
시험관내
에서
인간
ApoC
III을 표적으로 하는
GalNAc
3
-1
콘주게
이트된 변형된 ASO의 효과
상기 기재된 ISIS 304801 및 647535를 시험관내에서 시험하였다. 웰당 25,000 세포의 밀도로 형질전환 마우스 유래의 일차 간세포 세포를 0.03,0.08, 0.24, 0.74, 2.22, 6.67 및 20 μM 농도의 변형된 올리고뉴클레오티드로 처리하였다. 대략 16시간의 처리 기간 후, RNA를 상기 세포로부터 단리하고 mRNA 수준을 정량적 실시간 PCR에 의해 측정하고 hApoC III mRNA 수준을, 리보그린에 의해 측정된 바와 같이, 총 RNA 함량에 따라 조정하였다.
IC50을 표준 방법을 사용하여 계산하였고 그 결과가 표 32에서 제시되어 있다. 예시된 바와 같이, 대조군 ISIS 304801과 비교하여 ISIS 647535로 처리된 세포에서 비교할만한 효능이 관찰되었다.
표 32
일차 간세포에서 인간 ApoC III를 표적으로 하는 변형된 ASO
이 실험에서, 생체내에서 관찰된 GalNAc 3 -1 콘주게이션의 큰 효능 이점은 시험관내에서 관찰되지 않았다. 시험관내에서 일차 간세포에서의 차후의 자유 흡수 실험은 GalNAc 콘주게이트가 없는 올리고뉴클레오티드(실시예 60, 82, 및 92 참고)와 비교하여 다양한 GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드의 증가된 효능을 나타내지 않았다.
실시예
26: ApoC
III
ASO
활성에 대한 PO/PS 연결의 효과
인간 ApoC III 형질전환 마우스에게 25 mg/kg의 ISIS 304801, 또는 ISIS 616468 (모두 상기에 기재됨)를 1회 복강내로 주입하거나 PBS 처리된 대조군은 2주간 주당 1회 주입하였다. 처리 그룹은 3마리의 동물로 구성되었고 대조군 그룹은 4 마리의 동물로 구성되었다. 처리 전에 뿐만 아니라 마지막 투여량 후에, 혈액을 각 마우스로부터 채혈하고 혈장 샘플을 분석하였다. 마우스를 마지막 투여 72시간 후에 희생시켰다.
샘플을 수집하고 상기에서 기재된 바와 같이(실시예 20) 간에서의 ApoC III 단백질 수준을 분석하였다. 이들 분석으로부터의 데이터가 하기 표 33에 나타나 있다.
이들 결과는 전체 PS (ISIS 304801) 대비 윙에서 PO/PS (ISIS 616468)를 갖는 안티센스 화합물의 효능 감소를 보여준다.
표 33
인간 ApoC III 형질전환 마우스에서 ApoC III 단백질 수준에 대한 ASO 처리의 효과
실시예
27: 화합물
56
화합물 56은 Glen Research사부터 상업적으로 이용가능하거나 문헌[Shchepinov 등, Nucleic Acids Research, 1997, 25(22), 4447-4454]에 의해 보고된 공개된 과정에 따라 제조할 수 있다.
실시예
28: 화합물
60의 제조
화합물 4를 실시예 2에서 예시된 과정에 따라 제조하였다. 화합물 57는 상업적으로 이용가능하다. 화합물 60을 구조적 분석에 의해 확인하였다.
화합물 57은 대표적인 것으로 여겨지며, 소정의 조성물을 갖는 포스포르아미다이트를 제조하는데 사용될 수 있는 본 명세서에서 제공된 것들을 포함하나 이제 제한되지 않는 다른 단일보호된 치환된 또는 비치환된 알킬 디올로서 제한되는 것으로 의도되지 않는다.
실시예
29: 화합물
63의 제조
화합물 61 및 62를 하기에 의해 보고된 것과 유사한 과정을 이용하여 제조한다: Tober et al., Eur . J. Org . Chem ., 2013, 3, 566-577; 및 Jiang et al., Tetrahedron, 2007, 63(19), 3982-3988.
대안적으로, 화합물 63을 Kim et al., Synlett , 2003, 12, 1838-1840; 및 Kim et al., 공개된 PCT 국제 출원, WO 2004063208에 의해 과학 및 특허 문헌에 보고된 것과 유사한 과정을 이용하여 제조한다. 실시예 30: 화합물 63b의 제조
화합물 63a를 하기에 의해 보고된 것들과 유사한 과정을 이용하여 제조한다: Hanessian et al., Canadian Journal of Chemistry, 1996, 74(9), 1731-1737.
실시예
31: 화합물
63d의 제조
화합물 63c를 Chen et al., Chinese Chemical Letters, 1998, 9(5), 451-453에 의해 보고된 것들과 유사한 과정을 이용하여 제조한다.
실시예
32: 화합물
67의 제조
화합물 64는 실시예 2에 예시된 과정에 따라 제조하였다. 화합물 65는 Or et al., 공개된 PCT 국제 출원, WO 2009/003009에 의해 보고된 것들과 유사한 과정을 이용하여 제조된다. 화합물 65에 대해 사용된 보호 그룹은 대표적인 것을 의미하며, 사용될 수 있는 본원 명세서에 제시된 것을 포함하나 이에 제한되지 않는 다른 보호 그룹으로서 제한되지 않는 것으로 의도된다.
실시예
33: 화합물
70의 제조
화합물 64는 실시예 2에 예시된 과정에 따라 제조하였다. 화합물 68는 상업적으로 이용가능하다. 화합물 68에 대해 사용된 보호 그룹은 대표적인 것을 의미하며, 사용될 수 있는 본원 명세서에서 제공된 것들 것 포함하나 이에 제한되지 않는 다른 보호 그룹으로서 제한되는 것으로 의도되지 않는다.
실시예
34: 화합물
75a의 제조
화합물 75를 Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454에 의해 공개된 과정을 이용하여 제조한다.
실시예
35: 화합물
79의 제조
화합물 76을 Shchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454에 의해 공개된 과정을 이용하여 제조하였다.
실시예
36: 화합물
79a의 제조
화합물 77은 실시예 35에서 실증된 절차에 따라 제조된다.
실시예
37: 고체
지지체를 통해 5' 말단에
포스포디에스테르
연결된
GalNAc
3
-2
콘주게이트를
포함하는
콘주게이트된
올리고머 화합물 82의 일반적인 제조 방법 (방법 I)
여기서 GalNAc3-2은 하기 구조의 화학식을 갖는다:
콘주게이트 그룹 GalNAc3-2의 GalNAc3 클러스터 부분 (GalNAc3-2a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 여기서 GalNAc3-2a은 하기 화학식을 갖는다:
VIMAD-결합된 올리고머 화합물 79b를 하기에 대한 표준 과정을 이용하여 제조하였다: 자동화된 DNA/RNA 합성 (참고: Dupouy et al., Angew . Chem . Int . Ed., 2006, 45, 3623-3627). 포스포르아미다이트 화합물 56 및 60을 각각 실시예 27 및 28에 예시된 과정에 따라 제조하였다. 실증된 포스포르아미다이트는 대표적인 것으로 여겨지며, 5' 말단에 포스포디에스테르 연결된 콘주게이트 그룹을 갖는 올리고머 화합물을 제조하는데 사용될 수 있는 본 명세서에서 제공된 것들을 포함하나 이에 제한되지 않는 다른 포스포르아미다이트 빌딩 블록으로 한정되는 것으로 의도되지 않는다. 고체 지지체에 부가된 포스포르아미다이트의 순서 및 양은 임의의 소정의 순서 및 조성을 갖는 본원에서 기재된 올리고머 화합물을 제조하기 위해 조정될 수 있다.
실시예
38: 5
' 말단에
포스포디에스테르
연결된
GalNAc
3
-2
콘주게이트를
포함하는 올리고머 화합물 82의 대안적인 제조 방법 (방법 II)
VIMAD-결합된 올리고머 화합물 79b를 하기에 대한 표준 과정을 이용하여 제조하였다: 자동화된 DNA/RNA 합성 (참고: Dupouy et al., Angew . Chem . Int . Ed., 2006, 45, 3623-3627). GalNAc3-2 클러스터 포스포르아미다이트인 화합물 79를 실시예 35에 예시된 과정에 따라 제조하였다. 이 대안적인 방법은 합성의 최종 단계에서 포스포디에스테르 연결된 GalNAc3-2 콘주게이트의 올리고머 화합물에의 1-단계 설치를 허용한다. 예시된 포스포르아미다이트는 대표적인 것으로 여겨지며, 5' 말단에 포스포디에스테르 콘주게이트를 갖는 올리고머 화합물을 제조하는데 사용될 수 있는 본 명세서에서 제공된 것들을 포함하나 이에 제한되지 않는 다른 포스포르아미다이트 빌딩 블록으로서 한정되는 것으로 의도되지 않는다. 고체 지지체에 부가된 포스포르아미다이트의 순서 및 양은 임의의 소정의 순서 및 조성을 갖는 본원에서 기재된 올리고머 화합물을 제조하기 위해 조정될 수 있다.
실시예
39: 고체
지지체를
통한
5' 말단에 (5' 말단 부착을 위해 변형된
GalNAc
3
-1)
GalNAc
3
-3
콘주게이트를
포함하는 올리고머 화합물 83h의 일반적인 제조 방법
화합물 18을 실시예 4에 예시된 과정에 따라 제조하였다. 화합물 83a 및 83b는 상업적으로 이용가능하다. 포스포디에스테르 연결된 헥실아민을 포함하는 올리고머 화합물 83e를 표준 올리고뉴클레오티드 합성 과정을 이용하여 제조하였다. 암모니아수를 이용한 상기 보호된 올리고머 화합물의 처리는 5'-GalNAc3-3 콘주게이트된 올리고머 화합물 (83h)을 제공하였다.
여기서 GalNAc3-3은 하기 구조의 화학식을 갖는다:
콘주게이트 그룹 GalNAc3-3의 GalNAc3 클러스터 부분 (GalNAc3-3a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 여기서 GalNAc3-3a은 하기 화학식을 갖는다:
실시예
40: 고체
지지체를
통해
3' 말단에
포스포디에스테르
연결된
GalNAc
3
-4
콘주게이트를
포함하는 올리고머 화합물 89의 일반적인 제조 방법
여기서 GalNAc3-4은 하기 구조의 화학식을 갖는다:
여기서 CM은 절단가능 모이어티이다. 특정 구현예에서, 절단가능 모이어티는 하기와 같다:
콘주게이트 그룹 GalNAc3-4의 GalNAc3 클러스터 부분 (GalNAc3-4a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 여기서 GalNAc3-4a은 하기 화학식을 갖는다:
보호된 Unylinker 관능화된 고체 지지체 화합물 30은 상업적으로 이용가능하다. 화합물 84는 문헌에 의해 보고된 것과 유사한 과정을 이용하여 제조된다: (hchepinov et al., Nucleic Acids Research, 1997, 25(22), 4447-4454; Shchepinov et al., Nucleic Acids Research, 1999, 27, 3035-3041; 및 Hornet et al., Nucleic Acids Research, 1997, 25, 4842-4849 참고).
포스포르아미다이트 빌딩 블록, 화합물 60 및 79a를 실시예 28 및 36에 예시된 과정에 따라 제조한다. 예시된 포스포르아미다이트는 대표적인 것으로 여겨지며, 소정의 순서 및 조성으로 3' 말단에 포스포디에스테르 연결된 콘주게이트를 갖는 올리고머 화합물을 제조하는데 사용될 수 있는 다른 포스포르아미다이트 빌딩 블록로서 제한되는 것으로 의도되지 않는다. 고체 지지체에 부가된 포스포르아미다이트의 순서 및 양은 임의의 소정의 순서 및 조성을 갖는 본원에서 기재된 올리고머 화합물을 제조하기 위해 조정될 수 있다.
실시예
41: 고체상
기술을
통해
5' 위치에
포스포디에스테르
연결된
GalNAc
3
-2 (
실시예
37 참고,
Bx는
아데닌임)
콘주게이트를
포함하는
ASO의
일반적인 제조 방법(ISIS 661134의 제조)
달리 언급되지 않으면, 올리고머 화합물의 합성을 위해 사용된 모든 시약 및 용액은 상업적 공급원으로부터 구매된다. 표준 포스포르아미다이트 빌딩 블록 및 고체 지지체는, 예를 들면 T, A, G, 및 mC 잔기를 포함하는 뉴클레오시드 잔기의 혼입을 위해 사용된다. 사용된 포스포르아미다이트 화합물 56 및 60을 5' 말단에 포스포디에스테르 연결된 GalNAc3-2 콘주게이트를 합성하기 위해 사용하였다. 무수 아세토니트릴 중의 포스포르아미다이트의 0.1 M 용액을 β-D-2'-데옥시리보뉴클레오시드 및 2'-MOE에 사용하였다.
ASO 합성을 칼럼 내에 패킹된 VIMAD 고체 지지체 (110 μmol/g, Guzaev et al., 2003) 상의 포스포르아미다이트 커플링 방법에 의해 ABI 394 합성기 (1-2 μmol 크기) 또는 GE Healthcare Bioscience
올리고파일럿 합성기 (40-200 μmol 크기) 상에서 수행하였다. 커플링 단계의 경우, 포스포르아미다이트를 고체 지지체의 초기 로딩에 대해 4배 과량으로 전달하였고, 포스포르아미다이트 커플링을 10분 동안 수행하였다. 모든 다른 단계는 제조자에 의해 공급된 표준 프로토콜을 따랐다. 톨루엔 중의 6% 디클로로아세트산 용액을 뉴클레오티드의 5'-하이드록실 그룹으로부터 디메톡시트리틸 (DMT) 그룹을 제거하는데 사용하였다. 무수 CH
3CN 중 4,5-디시아노이미다졸 (0.7 M)은 커플링 단계 동안에 활성제로서 사용되었다. 포스포로티오에이트 연결을 3분의 접촉 시간 동안에 1:1 피리딘/CH3CN 중의 크산탄 하이드라이드의 0.1 M 용액을 이용한 황화에 의해 도입하였다. 6% 물을 함유하는 CH3CN 중의 20% tert-부틸하이드로퍼옥사이드의 용액을 산화제로서 사용하여 12분의 접촉 시간으로 포스포디에스테르 뉴클레오시드간 연결을 제공하였다.
원하는 서열이 조립된 후, 시아노에틸 포스페이트 보호 그룹을 45분의 접촉 시간으로 톨루엔 (v/v) 중의 20% 디에틸아민을 이용하여 탈보호화시켰다. 상기 고체-지지체 결합된 ASO를 암모니아수 (28-30 중량 %)에 현탁시키고 55℃ 에서 6시간 동안 가열하였다.
그리고 나서, 미결합된 ASO를 여과하고 암모니아를 가열로 제거하였다. 잔류물을 강한 음이온 교환 칼럼 상에서 고압 액체 크로마토그래피에 의해 정제하였다(GE Healthcare Bioscience, Source 30Q, 30 μm, 2.54 x 8 cm, A = 30% 수성 CH3CN 중의 100 mM 암모늄 아세테이트, B = A 중의 1.5 M NaBr, 60분에 0-40%의 B, 유량 14 mL min-1, λ = 260 nm). 잔류물을 역상 칼럼 상의 HPLC에 의해 탈염하여, 고체 지지체 상의 초기 로딩을 기준으로 15-30%의 단리된 수율로 원하는 ASO를 얻었다. ASO를 Agilent 1100 MSD 시스템을 갖는 이온-쌍-HPLC 커플링된 MS 분석에 의해 규명하였다.
표 34
SRB
-
1를
표적화하는
5' 위치에
포스포디에스테르
연결된
GalNAc
3
-2
콘주게이트를
포함하는
ASO
하첨자: 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "k"는 6'-(S)-CH3 이환식 뉴클레오시드 (예를 들면 cEt)를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다. "GalNAc3-2a"의 구조가 실시예 37에 나타나 있다.
실시예
42: 고체상
기술을 통해 5' 위치에
GalNAc
3
-3
콘주게이트를
포함하는
ASO의
일반적인 제조 방법(ISIS 661166의 제조)
ISIS 661166을 위한 합성을 실시예 39 및 41에 예시된 것과 유사한 과정을 이용하여 수행하였다.
ISIS 661166은 5-10-5 MOE 갭머이며, 상기 5' 위치는 GalNAc3-3 콘주게이트를 포함한다. ASO를 Agilent 1100 MSD 시스템을 갖는 이온-쌍-HPLC 커플링된 MS 분석에 의해 규명하였다.
표 34a
Malat
-1을
표적화하는
헥실아미노
포스포디에스테르
연결을 통한 5' 위치에서의
GalNAc
3
-3
콘주게이트를
포함하는
ASO
하첨자:“e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다. "5'-GalNAc3-3a"의 구조가 실시예 39에 나타나 있다.
실시예
43:
생체내
에서
SRB
-1을
표적화하는
5' 말단에서의
포스포디에스테르
연결된
GalNAc
3
-2 (
실시예
37 및 41 참고,
Bx는
아데닌임)의 투여량-의존적 연구
5' 말단에 포스포디에스테르 연결된 GalNAc3-2 콘주게이트를 포함하는 ISIS 661134 (실시예 41 참고)를 마우스에서 SRB-1의 안티센스 억제를 위해 투여량-의존적 연구에서 시험하였다. 비콘주게이트된 ISIS 440762 및 651900 (3' 말단에 GalNAc3-1 콘주게이트, 실시예 9 참고)을 비교를 위해 연구에 포함시켰고, 이들은 앞서 표 17에 기재되어 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 440762, 651900, 661134 또는 PBS 처리된 대조군으로 하기 제시된 투여량으로 피하로 1회 주입하였다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). SRB-1 mRNA 수준을 PBS-처리된 대조군에 대해 정규화하기 전에 총 RNA에 대해 결정하였다(리보그린을 이용하여). 하기의 결과는 PBS-처리된 대조군에 정규화된, 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 제시되어 있고, "PBS %"로서 표시되어 있다. ED50은 전에 기재된 것과 유사한 방법을 사용하여 측정되었고 하기에서 제공된다.
표 35에 예시된 바와 같이, 안티센스 올리고뉴클레오티드 처리는 SRB-1 mRNA 수준을 투여량-의존적 방식으로 낮추었다. 사실상, 5' 말단에 포스포디에스테르 연결된 GalNAc3-2 콘주게이트를 포함하는 안티센스 올리고뉴클레오티드 (ISIS 661134) 또는 3' 말단에 연결된 GalNAc3-1 콘주게이트를 포함하는 안티센스 올리고뉴클레오티드(ISIS 651900)는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 440762)와 비교하여 실질적인 효능 개선을 나타내었다. 게다가, 5' 말단에 포스포디에스테르 연결된 GalNAc3-2 콘주게이트를 포함하는 ISIS 661134는 3' 말단에 GalNAc3-1 콘주게이트를 포함하는 ISIS 651900과 비교하여 효능이 동등하였다.
표 35
SRB
-1을 표적으로 하는
GalNAc
3
-1 또는
GalNAc
3
-2를 함유하는
ASO
3'GalNAc3-1 및 5'GalNAc3-2에 대한 구조는 실시예 9 및 37에 앞서 기술되었다.
약동학 분석 (PK)
고투여량 그룹 (7 mg/kg)으로부터의 ASO의 PK를 조사하고 실시예 20에 예시된 것과 동일한 방식으로 평가하였다. 간 샘플을 민싱(minced)하고 표준 프로토콜을 사용하여 추출하였다. 661134 (5' GalNAc3-2) 및 ISIS 651900 (3' GalNAc3-1)의 전장 대사물을 확인하고 이들의 질량을 고분해능 질량 분광분석법 분석에 의해 확인하였다. 상기 결과는 5' 말단에 포스포디에스테르 연결된 GalNAc3-2 콘주게이트를 포함하는 ASO (ISIS 661134)에 대해 검출된 주요 대사물이 ISIS 440762였음을 보여주었다 (데이터 도시되지 않음). 검출가능한 수준에서 추가의 대사물이 관찰되지 않았다. 그의 대응물과 달리, 표 23a에서 이전에 보고된 것과 유사한 추가의 대사물이 3' 말단에 GalNAc3-1 콘주게이트를 갖는 ASO에 대해 관찰되었다(ISIS 651900). 이들 결과는, 포스포디에스테르 연결된 GalNAc3-1 또는 GalNAc3-2 콘주게이트를 갖는 것이 그것의 효능을없애지 않고 ASO의 PK 프로파일을 개선할 수 있음을 제시한다.
실시예
44: SRB
-1을
표적화하는
3' 말단에
GalNAc
3
-1
콘주게이트를
포함하는
ASO
(실시예 9 참고)의
안티센스
억제에 대한 PO/PS 연결의 효과
각각 SRB-1을 표적화하는 3' 말단에 GalNAc3-1 콘주게이트를 포함하는 ISIS 655861 및 655862를 대상으로 단일 투여 연구에서 마우스에서 SRB-1을 억제하는 이들의 능력을 시험하였다. 모 비콘주게이트된 화합물인 ISIS 353382를 비교를 위해 연구에 포함시켰다.
ASO는 5-10-5 MOE 갭머이며, 상기 갭 영역은 10개의 2'-데옥시리보뉴클레오시드를 포함하고 각 윙 영역은 5개의 2'-MOE 변형된 뉴클레오시드를 포함한다. ASO를 실시예 19에서 앞서 예시된 것과 유사한 방법을 이용하여 제조하였고 이는 하기 표 36에 기술되어 있다.
표 36
SRB
-
1를
표적화하는
3' 말단에
GalNAc
3
-1
콘주게이트를
포함하는 변형된
ASO
하첨자: “e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다. "GalNAc3-1"의 구조가 실시예 9에 나타나 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 353382, 655861, 655862 또는 PBS 처리된 대조군으로 하기에 제시된 투여량으로 피하로 1회 주입하였다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 처리 전에 뿐만 아니라 마지막 투여량 후에, 혈액을 각 마우스로부터 채혈하고 혈장 샘플을 분석하였다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). SRB-1 mRNA 수준을 PBS-처리된 대조군에 대해 정규화하기 전에 총 RNA에 대해 결정하였다(리보그린을 이용하여). 하기의 결과는 PBS-처리된 대조군에 정규화된, 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 제시되어 있고, "PBS %"로서 표시되어 있다. ED50은 전에 기재된 것과 유사한 방법을 사용하여 측정되었고 하기에서 보고된다.
표 37에서 예시된 바와 같이, 안티센스 올리고뉴클레오티드 처리는 PBS 처리된 대조군과 비교하여 투여량-의존 방식으로 SRB-1 mRNA 수준을 낮추었다. 사실상, 3' 말단에 GalNAc3-1 콘주게이트를 포함하는 안티센스 올리고뉴클레오티드 (ISIS 655861 및 655862)는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 353382)와 비교하여 실질적인 효능 개선을 나타내었다. 게다가, 혼합된 PS/PO 연결을 갖는 ISIS 655862는전체 PS (ISIS 655861)와 비교하여 효능 개선을 나타내었다.
표 37
SRB
-
1를
표적화하는
3' 말단에
GalNAc
3
-1
콘주게이트를
포함하는
ASO의
안티센스
억제에 대한 PO/PS 연결의 효과
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 장기 중량을 또한 평가하였다. 상기 결과는 PBS 대조군과 비교하여 ASO 처리된 마우스에서 트랜스아미나제 수준 (표 38) 또는 장기 중량 (데이터 도시되지 않음)의 상승이 관찰되지 않았음을 입증하였다 (데이터 도시되지 않음). 게다가, 혼합된 PS/PO 연결을 갖는 ASO (ISIS 655862)는 전체 PS (ISIS 655861)와 비교하여 유사한 트랜스아미나제 수준을 나타내었다.
표 38
SRB
-
1를
표적화하는
3' 말단에
GalNAc
3
-1
콘주게이트를
포함하는
ASO의
트랜
스아미나제 수준에 대한 PO/PS 연결의 효과
실시예
45:
PFP
에스테르, 화합물 110a의 제조
화합물 4 (9.5g, 28.8 mmol)를 개별적으로 화합물 103a 또는 103b (38 mmol), 및 디클로로메탄 (200 mL) 중 TMSOTf (0.5 eq.) 및 분자체로 처리하고, 16시간 동안 실온에서 교반하였다. 이 때, 유기 층을 셀라이트를 통해 여과한 다음 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (2%-->10% 메탄올/디클로로메탄)로 정제하여 >80% 수율로 화합물 104a 및 104b를 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 104a 및 104b를 화합물 100a-d (실시예 47)와 동일한 조건으로 처리하여>90% 수율로 화합물 105a 및 105b를 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 105a 및 105b를 화합물 901a-d와 동일한 조건 하에서 화합물 90으로 개별적으로 처리하여, 화합물 106a (80%) 및 106b (20%)를 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 106a 및 106b를 화합물 96a-d (실시예 47)와 동일한 조건 하에서 처리하여 107a (60%) 및 107b (20%)를 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 107a 및 107b를 화합물 97a-d (실시예 47)와 동일한 조건 하에서 처리하여, 화합물 108a 및 108b를 40-60% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 108a (60%) 및 108b (40%)을 화합물 100a-d (실시예 47)와 동일한 조건으로처리하여, 화합물 109a 및 109b를 >80% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 109a를 화합물 101a-d (실시예 47)와 동일한 조건 하에서 처리하여, 화합물 110a를 30-60% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다. 대안적으로, 화합물 110b는 화합물 109b로 시작하는 개시되는 유사한 방식으로 제조될 수 있다.
실시예
46:
PFP
에스테르 (올리고뉴클레오티드
111)과의
콘주게이션을
위한 일반적인 절차; ISIS 666881 (
GalNAc
3
-
10)의
제조
5'-헥실아미노 변형된 올리고뉴클레오티드를 합성하고 표준 고체상 올리고뉴클레오티드 과정을 이용하여 정제하였다. 5'-헥실아미노 변형된 올리고뉴클레오티드를 0.1 M 나트륨 테트라보레이트, pH 8.5 (200 μL)에 용해시키고 DMSO (50 μL)에 용해된 3 당량의 선택된 PFP 에스테르화된 GalNAc3 클러스터를 부가하였다. 만약 PFP 에스테르가 ASO 용액 부가시 침전되면, 모든 PFP 에스테르가 용액 내에 있을 때까지 DMSO를 부가하였다. 반응은 실온에서 약 16시간 혼합 후 완료하였다. 수득한 용액을 12 mL의 물로 희석한 다음 스핀 필터에서 3000 Da의 질량 컷오프로 3000 rpm으로 스핀다운하였다. 이 과정을 2회 반복하여 소분자 불순물을 제거하였다. 그 다음 용액을 동결건조하고 농축된 암모니아수에서 재용해하고 실온에서 2.5시간 동안 혼합한 다음 진공에서 농축하여 대부분의 암모니아를 제거하였다. 콘주게이트된 올리고뉴클레오티드를 정제하고 RP-HPLC로 탈염하고 동결건조하여 GalNAc3 콘주게이트된 올리고뉴클레오티드를 제공하였다.
올리고뉴클레오티드 111은 GalNAc3-10과 콘주게이트된다. 콘주게이트 그룹 GalNAc3-10의 GalNAc3 클러스터 부분 (GalNAc3-10a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 하기 GalNAc3-10을 이용하여 합성된 올리고뉴클레오티드 (ISIS 666881)에서 나타난 바와 같은 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-10 (GalNAc3-10a-CM-) 의 구조는 하기와 같다:
일반적인 절차에 따라 ISIS 666881을 제조하였다. 5'-헥실아미노 변형된 올리고뉴클레오티드 ISIS 660254을 합성하고 표준 고체상 올리고뉴클레오티드 과정을 이용하여 정제하였다. ISIS 660254 (40 mg, 5.2 μmol)을 0.1 M 나트륨 테트라보레이트, pH 8.5 (200 μL)에 용해시키고 DMSO (50 μL)에 용해된 3 당량의 PFP 에스테르 (화합물 110a)를 부가하였다. PFP 에스테르는 PFP 에스테르를 완전히 용해시키기 위해 추가의 DMSO (600 μL)를 필요로 하는 ASO 용액에 부가시 침전되었다. 상기 반응을 실온에서 16시간 혼합한 후 완료하였다. 상기 용액을 물로 12 mL 총 용적으로 희석하고 스핀 필터에서 3000 Da의 질량 컷오프로 3000 rpm으로 스핀다운하였다. 이 과정을 2회 반복하여 소분자 불순물을 제거하였다. 용액을 동결건조하고 실온에서 2.5시간 동안 혼합하면서 농축된 암모니아수에 재용해한 다음 진공에서 농축하여 대부분의 암모니아를 제거하였다. 콘주게이트된 올리고뉴클레오티드를 정제하고 RP-HPLC로 탈염하고 동결건조하여 중량으로 90% 수율로 ISIS 666881를 얻었다 (42 mg, 4.7 μmol).
GalNAc
3
-10
콘주게이트된
올리고뉴클레오티드
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
실시예
47:
GalNAc
3
-
8를
포함하는 올리고뉴클레오티드 102의 제조
3가산 90 (4 g, 14.43 mmol)을 DMF (120 mL) 및 N,N-디이소프로필에틸아민 (12.35 mL, 72 mmol)에 용해시켰다. 펜타플루오로페닐 트리플루오로아세테이트 (8.9 mL, 52 mmol)를 아르곤 하에 적가하고, 반응을 실온에서 30분 동안 교반하였다. Boc-디아민 91a 또는 91b (68.87 mmol)를 N,N-디이소프로필에틸아민 (12.35 mL, 72 mmol)과 함께 부가하고, 반응을 실온에서 16시간 동안 교반하였다. 이때, DMF를 >75% 감압 하에서 환원시킨 다음 상기 혼합물을 디클로로메탄에 용해시켰다. 유기층을 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 오일 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (2%-->10% 메탄올/디클로로메탄)로 정제하여 화합물 92a 및 92b를 대략적인 80% 수율로 생성하였다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 92a 또는 92b (6.7 mmol)를 20 mL의 디클로로메탄 및 20 mL의 트리플루오로아세트산으로 실온에서 16시간 동안 처리하였다. 얻어진 용액을 증발시킨 다음 메탄올에 용해시키고 DOWEX-OH 수지로 30분 동안 처리하였다. 얻어진 용액을 여과하고 오일 감압 하에서 환원하여 화합물 93a 및 93b를 85-90% 수율로 얻었다.
화합물 7 또는 64 (9.6 mmol)를 DMF (20 mL) 중의 HBTU (3.7g, 9.6 mmol) 및 N,N-디이소프로필에틸아민 (5 mL)로 15분 동안 처리하였다. 여기에 화합물 93a 또는 93b (3 mmol) 중 하나를 첨가하고, 실온에서 16시간 동안 교반하였다. 이때, DMF를 >75% 감압 하에서 환원시킨 다음 상기 혼합물을 디클로로메탄에 용해시켰다. 유기층을 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 오일 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (5%-->20% 메탄올/디클로로메탄)에 의해 정제하여 화합물 96a-d를 20-40% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 96a-d (0.75 mmol)를 개별적으로, 에탄올 (75 mL)에서 3시간 동안 라니 니켈에 대해 수소첨가하였다. 이때, 촉매를 셀라이트를 통해 여과에 의해 제거하고, 에탄올을 감압 하에서 제거하여 화합물 97a-d를 80-90% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 23 (0.32g, 0.53 mmol)을 DMF (30mL) 중에서 HBTU (0.2g, 0.53 mmol) 및 N,N-디이소프로필에틸아민 (0.19 mL, 1.14 mmol)으로 15분 동안 처리하였다. 여기에 화합물 97a-d (0.38 mmol)를 개별적으로 첨가하고, 실온에서 16시간 동안 교반하였다. 이때, DMF를 >75% 감압 하에서 환원시킨 다음 상기 혼합물을 디클로로메탄에 용해시켰다. 유기층을 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 오일 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (2%-->20% 메탄올/디클로로메탄)에 의해 정제하여 화합물 98a-d를 30-40% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 99 (0.17g, 0.76 mmol)을 DMF (50mL) 중에서 HBTU (0.29 g, 0.76 mmol) 및 N,N-디이소프로필에틸아민 (0.35 mL, 2.0 mmol)으로 15분 동안 처리하였다. 여기에 화합물 97a-d (0.51 mmol)를 개별적으로 첨가하고, 실온에서 16시간 동안 교반하였다. 이때, DMF를 >75% 감압 하에서 환원시킨 다음 상기 혼합물을 디클로로메탄에 용해시켰다. 유기층을 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 오일 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (5%-->20% 메탄올/디클로로메탄)에 의해 정제하여 화합물 100a-d를 40-60% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 100a-d (0.16 mmol)를 개별적으로, 메탄올/에틸 아세테이트 (1:1, 50 mL) 중에서 3시간 동안 10% Pd(OH)2/C에 대해 수소첨가하였다. 이때, 촉매를 셀라이트를 통한 여과에 의해 제거하고, 유기물을 감압 하에서 제거하여 화합물 101a-d를 80-90% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
화합물 101a-d (0.15 mmol)를 개별적으로DMF (15 mL) 및 피리딘 (0.016 mL, 0.2 mmol)에 용해시켰다. 펜타플루오로페닐 트리플루오로아세테이트 (0.034 mL, 0.2 mmol)를 아르곤 하에서 적가하고, 반응을 실온에서 30분 동안 교반하였다. 이때, DMF를 >75% 감압 하에서 환원시킨 다음 상기 혼합물을 디클로로메탄에 용해시켰다. 유기층을 중탄산나트륨, 물 및 염수로 세정하였다. 그 다음 유기층을 분리하고 황산나트륨 상에서 건조하고, 여과하고 오일 감압 하에서 환원시켰다. 얻어진 오일을 실리카겔 크로마토그래피 (2%-->5% 메탄올/디클로로메탄)에 의해 정제하여 화합물 102a-d를약 80% 수율로 얻었다. LCMS 및 양성자 NMR은 상기 구조와 일치하였다.
GalNAc3-8 콘주게이트 그룹을 포함하는 올리고머 화합물 102를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-8의 GalNAc3 클러스터 부분 (GalNAc3-8a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 바람직한 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다.
GalNAc3-8 (GalNAc3-8a-CM-) 의 구조는 하기와 같다:
실시예
48:
GalNAc
3
-
7를
포함하는 올리고뉴클레오티드 119의 제조
화합물 112를 하기 문헌에 기재된 과정에 따라 합성하였다: (J. Med . Chem . 2004, 47, 5798-5808).
화합물 112 (5 g, 8.6 mmol)를 1:1 메탄올/에틸 아세테이트 (22 mL/22 mL)에 용해시켰다. 탄소상 수산화팔라듐 (0.5 g)을 부가하였다. 반응 혼합물을 실온에서 수소 하에서 12시간 동안 교반하였다. 반응 혼합물을 셀라이트의 패드를 통해 여과하고 1:1 메탄올/에틸 아세테이트로 패드로 세정하였다. 여과물과 세정물을 조합하고 농축 건조하여 화합물 105a (정량적)를 얻었다. 상기 구조를 LCMS에 의해 확인하였다.
화합물 113 (1.25 g, 2.7 mmol), HBTU (3.2 g, 8.4 mmol) 및 DIEA (2.8 mL, 16.2 mmol)를 무수 DMF (17 mL)에 용해시키고상기 반응 혼합물을 실온에서 5분 동안 교반하였다. 여기에 무수 DMF (20 mL) 중의 화합물 105a (3.77 g, 8.4 mmol)의 용액을 부가하였다. 상기 반응을 실온에서 6시간 동안 교반하였다. 용매를 감압 하에서 제거하여 오일을 얻었다. 잔류물을 CH2Cl2 (100 mL)에 용해시키고 수성 포화된 NaHCO3 용액 (100 mL) 및 염수 (100 mL)로 세정하였다. 유기상을 분리하고, 건조시키고 (Na2SO4), 여과하고 증발시켰다. 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하고 디클로로메탄 중의 10 내지 20 % MeOH로 용출시켜 화합물 114 (1.45 g, 30%)를 얻었다. 구조를 LCMS 및 1H NMR 분석에 의해 확인하였다.
화합물 114 (1.43 g, 0.8 mmol)를 1:1 메탄올/에틸 아세테이트 (4 mL/4 mL)에 용해시켰다. 탄소상 팔라듐 (습식 0.14 g)을 부가하였다. 반응 혼합물을 수소로 씻어내고 실온에서 수소 하에서 12시간 동안 교반하였다. 반응 혼합물을 셀라이트의 패드를 통해 여과하였다. 셀라이트 패드를 메탄올/에틸 아세테이트 (1:1)로 세정하였다. 여과물과 세정물을 함께 조합하고 감압 하에서 증발시켜 화합물 115 (정량적)를 얻었다. 구조를 LCMS 및 1H NMR 분석에 의해 확인하였다.
화합물 83a (0.17 g, 0.75 mmol), HBTU (0.31 g, 0.83 mmol) 및 DIEA (0.26 mL, 1.5 mmol)를 무수 DMF (5 mL)에 용해시키고 상기 반응 혼합물을 실온에서 5분 동안 교반하였다. 여기에 무수 DMF 중의 화합물 115 (1.22 g, 0.75 mmol)의 용액을 부가하고 반응을 실온에서 6시간 동안 교반하였다. 용매를 감압 하에서 제거하고 잔류물을 CH2Cl2에 용해시켰다. 유기층을 수성 포화된 NaHCO3 용액 및 염수로 세정하고 무수 Na2SO4 상에서 건조시키고 여과하였다. 유기층을 농축 건조하고 수득된 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하고 디클로로메탄 중의 3 내지 15 % MeOH로 용출시켜 화합물 116 (0.84 g, 61%)을 얻었다. 구조를 LC MS 및 1H NMR 분석에 의해 확인하였다.
화합물 116 (0.74 g, 0.4 mmol)를 1:1 메탄올/에틸 아세테이트 (5 mL/5 mL)에 용해시켰다. 탄소상 팔라듐 (습성, 0.074 g)을 부가하였다. 반응 혼합물을 수소로 씻어내고 실온에서 수소 하에서 12시간 동안 교반하였다. 반응 혼합물을 셀라이트의 패드를 통해 여과하였다. 셀라이트 패드를 메탄올/에틸 아세테이트 (1:1)로 세정하였다. 여과물과 세정물을 함께 조합하고 감압 하에서 증발시켜 화합물 117 (0.73 g, 98%)을 얻었다. 구조를 LCMS 및 1H NMR 분석에 의해 확인하였다.
화합물 117 (0.63 g, 0.36 mmol)을 무수 DMF (3 mL)에 용해시켰다. 이용액에 N,N-디이소프로필에틸아민 (70 μL, 0.4 mmol) 및 펜타플루오로페닐 트리플루오로아세테이트 (72 μL, 0.42 mmol)를 부가하였다. 상기 반응 혼합물을 실온에서 12시간 동안 교반하고 수성 포화된 NaHCO3 용액에 부었다. 상기 혼합물을 디클로로메탄으로 추출하고, 염수로 세정하고 무수 Na2SO4 상에서 건조시켰다. 상기 디클로로메탄 용액을 농축 건조하고 실리카겔 칼럼 크로마토그래피로 정제하고 디클로로메탄 중 5 내지 10 % MeOH로 용출하여 화합물 118 (0.51 g, 79%)을 얻었다. 구조를 LCMS 및 1H 및 1H 및 19F NMR에 의해 확인하였다.
GalNAc3-7 콘주게이트 그룹을 포함하는 올리고머 화합물 119를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-7의 GalNAc3 클러스터 부분 (GalNAc3-7a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다.
GalNAc3-7 (GalNAc3-7a-CM-) 의 구조는 하기와 같다:
실시예
49:
GalNAc
3
-5를 포함하는 올리고뉴클레오티드 132의 제조
화합물 120 (14.01 g, 40 mmol) 및 HBTU (14.06 g, 37 mmol)를 무수 DMF (80 mL)에 용해시켰다. 트리에틸아민 (11.2 mL, 80.35 mmol)을 부가하고 5분 동안 교반하였다. 상기 반응 혼합물을 빙욕에서 냉각하고 무수 DMF (20 mL) 중의 화합물 121 (10 g, mmol)의 용액을 부가하였다. 추가의 트리에틸아민 (4.5 mL, 32.28 mmol)을 부가하고 반응 혼합물을 18시간 동안 아르곤 대기 하에서 교반하였다. 반응을 TLC (에틸 아세테이트:헥산; 1:1; Rf = 0.47)에 의해 관찰하였다. 용매를 감압 하에서 제거하였다. 잔류물을 EtOAc (300 mL)에서 취하고 1M NaHSO4 (3 x 150 mL), 수성 포화된 NaHCO3 용액 (3 x 150 mL) 및 염수 (2 x 100 mL)로 세정하였다. 유기층을 Na2SO4로 건조시켰다. 건조제를 여과로 제거하고 유기층을 회전식 증발로 농축하였다. 조 혼합물을 실리카겔 칼럼 크로마토그래피로 정제하고 헥산 중 35 50% EtOAc를 사용하여 용출하여 화합물 122 (15.50 g, 78.13%)를 얻었다. 구조를 LCMS 및 1H NMR 분석에 의해 확인하였다. 질량 m/z 589.3 [M + H]+.
물 (20 mL) 및 THF (10 mL) 중의 LiOH (92.15 mmol)의 용액을 메탄올 (15 mL)에 용해된 화합물 122 (7.75 g,13.16 mmol)의 냉각된 용액에 첨가하였다. 상기 반응 혼합물을 실온에서 45분 동안 교반하고 TLC (EtOAc:헥산; 1:1)로 관찰하였다. 상기 반응 혼합물을 감압 하에서 절반 용적으로 농축하였다. 남아있는 용액을 빙욕에서 냉각하고 농축된 HCl를 부가하여 중화하였다. 상기 반응 혼합물을 희석하고, EtOAc (120 mL)로 추출하고 염수 (100 mL)로 세정하였다. 에멀젼 형성하고 밤새 정치하여 제거하였다. 유기층을 분리하고, (Na2SO4)로 건조시키고, 여과하고 증발시켜 화합물 123 (8.42 g)을 얻었다. 잔류 염은 과다 질량의 원인인 것 같다. LCMS는 구조와 일치한다. 생성물을 임의의 추가 정제없이 사용하였다. M.W.cal:574.36; M.W.fd:575.3 [M + H]+.
화합물 126를 하기 문헌에 기재된 과정에 따라 합성하였다: (J. Am. Chem . Soc. 2011, 133, 958-963).
화합물 123(7.419 g, 12.91 mmol), HOBt (3.49 g, 25.82 mmol) 및 화합물 126 (6.33 g, 16.14 mmol)을 DMF (40 mL)에 용해시키고 수득한 반응 혼합물을 빙욕에서 냉각하였다. 여기에 N,N-디이소프로필에틸아민 (4.42 mL, 25.82 mmol), PyBop (8.7 g, 16.7 mmol) 그 다음 Bop 커플링 시약 (1.17 g, 2.66 mmol)을 아르곤 대기 하에서부가하였다. 얼음 수조를 제거하고 용액을 실온으로 가온하였다. 반응을 TLC (DCM:MeOH:AA; 89:10:1)에 의해 결정된 바와 같이 1시간 후에 완료시켰다. 상기 반응 혼합물을 감압 하에서 농축하였다. 잔류물을 EtOAc (200 mL)에 용해시키고 1 M NaHSO4 (3x100 mL), 수성 포화된 NaHCO3 (3x100 mL) 및 염수 (2x100 mL)로 세정하였다. 유기상을 분리하고, 건조시키고 (Na2SO4), 여과하고 농축시켰다. 잔류물을 50% 헥산/EtOAC 내지 100% EtOAc의 구배로 실리카겔 칼럼 크로마토그래피에 의해 정제하여 백색 포말로서 화합물 127 (9.4 g)을 얻었다. LCMS 및 1H NMR은 구조와 일치하였다. 질량 m/z 778.4 [M + H]+.
트리플루오로아세트산 (12 mL)을 디클로로메탄 (12 mL) 중의 화합물 127 (1.57 g, 2.02 mmol)의 용액에 첨가하고 실온에서 1시간 동안 교반하였다. 상기 반응 혼합물을 감압 하에서 톨루엔 (30 mL)으로 공-증발시켜 건조하였다. 수득된 잔류물을 아세토니트릴 (30 mL) 및 톨루엔 (40 mL)으로 2회 공-증발시켜 화합물 128 (1.67 g)을 트리플루오로 아세테이트 염으로서 얻었고 다음 단계 동안에 추가 정제없이 사용하였다. LCMS 및 1H NMR은 구조와 일치하였다. 질량 m/z 478.2 [M + H]+.
화합물 7 (0.43 g, 0.963 mmol), HATU (0.35 g, 0.91 mmol), 및 HOAt (0.035 g, 0.26 mmol)을 함께 조합하고 둥근바닥 플라스크에서 감압 하에서 P2O5로 4시간 동안 건조시킨 다음 무수 DMF (1 mL)에 용해시키고 5분 동안 교반하였다. 여기에 무수 DMF (0.2 mL) 및 N,N-디이소프로필에틸아민 (0.2 mL) 중의 화합물 128 (0.20 g, 0.26 mmol)의 용액을 부가하였다. 상기 반응 혼합물을 실온에서 아르곤 대기 하에서 교반하였다. 반응을 LCMS 및 TLC (7% MeOH/DCM)에 의해 결정된 바와 같이 30분 후에 완료시켰다. 상기 반응 혼합물을 감압 하에서 농축하였다. 잔류물을 DCM (30 mL)에 용해시키고 1 M NaHSO4 (3x20 mL), 수성 포화된 NaHCO3 (3 x 20 mL) 및 염수 (3x20 mL)로 세정하였다. 유기상을 분리하고, 건조시키고 (Na2SO4), 여과하고 농축시켰다. 잔류물을 디클로로메탄 중의 5-15% MeOH를 이용한 실리카겔 칼럼 크로마토그래피에 의해 정제하여 화합물 129 (96.6 mg)를 얻었다. LC MS 및 1H NMR은 구조와 일치한다. 질량 m/z 883.4 [M + 2H]+.
화합물 129 (0.09 g, 0.051 mmol)를 20 mL 섬광 바이알 내에서 메탄올 (5 mL)에 용해시켰다. 여기에 소량의 10% Pd/C (0.015 mg)를 부가하고 반응 용기를 H2 가스로 씻어 내었다. 상기 반응 혼합물을 실온에서 H2 대기 하에서 18시간 동안 교반하였다. 상기 반응 혼합물을 셀라이트의 패드를 통해 여과하고 셀라이트 패드를 메탄올로 세정하였다. 여과물 및 세정물을 모으고 감압 하에서 농축하여 화합물 130 (0.08 g)을 얻었다. LCMS 및 1H NMR은 구조와 일치하였다. 생성물을 추가 정제없이 사용하였다. 질량 m/z 838.3 [M + 2H]+.
10 mL 표시된 둥근바닥 플라스크에 화합물 130 (75.8 mg, 0.046 mmol), 0.37 M 피리딘/DMF (200 μL) 및 교반 바를 부가하였다. 이 용액에 0.7 M 펜타플루오로페닐 트리플루오로아세테이트/DMF (100 μL)를 교반하면서 적가하였다. 반응을 LC MS에 의해 결정된 바와 같이 1시간 후에 완료하였다. 용매를 감압 하에서 제거하고 잔류물을 CHCl3 (~ 10 mL)에 용해시켰다. 유기층을 NaHSO4 (1 M, 10 mL), 수성 포화된 NaHCO3 (10 mL) 및 염수 (10 mL)에 대해 각각 3회 분할하였다. 유기상을 분리하고 Na2SO4 상에서 건조시키고, 여과하고 농축하여 화합물 131 (77.7 mg)을 얻었다. LCMS는 구조와 일치한다. 추가 정제없이 사용하였다. 질량 m/z 921.3 [M + 2H]+.
GalNAc3-5 콘주게이트 그룹을 포함하는 올리고머 화합물 132를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-5의 GalNAc3 클러스터 부분 (GalNAc3-5a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다.
GalNAc3-5 (GalNAc3-5a-CM-) 의 구조는 하기와 같다:
실시예
50:
GalNAc
4
-
11를
포함하는 올리고뉴클레오티드 144의 제조
화합물 134의 합성. 메리필드 플라스크에 아세토니트릴, 디메틸포름아미드, 디클로로메탄 및 아세토니트릴로 세정된 아미노메틸 VIMAD 수지 (2.5 g, 450 μmol/g)를 부가하였다. 상기 수지를 아세토니트릴 (4 mL)에서 팽창시켰다. 화합물 133을 20 (1.0 mmol, 0.747 g), TBTU (1.0 mmol, 0.321 g), 아세토니트릴 (5 mL) 및 DIEA (3.0 mmol, 0.5 mL)를 첨가하여 100 mL 둥근바닥 플라스크에서 전-활성화시켰다. 이 용액을 5분 동안 교반한 다음, 흔들면서 메리필드 플라스크에 첨가하였다. 상기 현탁액을 3시간 동안 교반하였다. 상기 반응 혼합물을 빼내고 수지를 아세토니트릴, DMF 및 DCM으로 세정하였다. 새로운 수지 로딩을 DCM 중에서 500 nm (소멸 계수 = 76000)에서 DMT 양이온의 흡광도를 측정하여 정량화하였고 238 μmol/g인 것으로 결정되었다. 상기 수지를 아세트산 무수물 용액에서 10분간 3회 현탁시켜 캠핑하였다.
고체 지지체 결합된 화합물 141을 반복적인 Fmoc-기반 고체상 펩티드 합성 방법을 사용하여 합성하였다. 소량의 고체 지지체를 빼내고, 암모니아수 (28-30 wt%)에서 6시간 동안 현탁시켰다. 절단된 화합물을 LC-MS에 의해 분석하였고 상기 관찰된 질량은 구조와 일치하였다. 질량 m/z 1063.8 [M + 2H]+.
고체 지지체 결합된 화합물 142를 고체상 펩티드 합성 방법을 사용하여 합성하였다.
고체 지지체 결합된 화합물 143을 DNA 합성기 상에서 표준 고체상 합성을 사용하여 합성하였다.
고체 지지체 결합된 화합물 143을 암모니아수 (28-30 wt%)에 현탁시키고 55 oC 에서 16시간 동안 가열하였다. 상기 용액을 냉각하고 고체 지지체를 여과하였다. 상기 여과물을 농축하고 잔류물을 물에서 용해시키고 강한 음이온 교환 칼럼 상에서 HPLC로 정제하였다. 전장 화합물 144을 함유하는 분획들을 모으고 탈염하였다. 수득한 GalNAc4-11 콘주게이트된 올리고머 화합물을 LC-MS로 분석하였고, 상기 관찰된 질량은 구조와 일치하였다.
콘주게이트 그룹 GalNAc4-11의 GalNAc4 클러스터 부분 (GalNAc4-11a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다.
GalNAc4-11 (GalNAc4-11a-CM) 의 구조는 하기와 같다:
실시예
51:
GalNAc
3
-
6를
포함하는 올리고뉴클레오티드 155의 제조
화합물 146을 문헌에 기재된 바와 같이 합성하였다: (Analytical Biochemistry 1995, 229, 54-60).
화합물 4 (15 g, 45.55 mmol) 및 화합물 35b (14.3 그램, 57 mmol)를 CH2Cl2 (200 ml)에 용해시켰다. 활성화된 분자체 (4 Å. 2 g, 분말화됨)를 첨가하고, 반응을 30분 동안 질소 대기 하에서 교반하였다. TMS-OTf를 첨가하고(4.1 ml, 22.77 mmol), 반응을 밤새 실온에서 교반하였다. 완료되자마자, 상기 반응을 포화된 수성 NaHCO3의 용액 (500 ml) 및 부서진 얼음 (~ 150 g) 내로 부어 켄칭하였다. 유기층을 단리하고, 염수로 세정하고, MgSO4로 건조하고, 여과하고, 감압 하에서 농축하여 오렌지색 오일을 얻었다. 조 물질을 실리카겔 칼럼 크로마토그래피로 정제하고 CH2Cl2 중의 2-10% MeOH로 용출시켜 화합물 112 (16.53 g, 63%)를 얻었다. LCMS 및 1HNMR은 예상된 화합물과 일치하였다.
화합물 112 (4.27 g, 7.35 mmol)를 1:1 MeOH/EtOAc (40 ml)에 용해시켰다. 상기 용액에 아르곤 스트림을 15분간 기포발생시켜 상기 반응 혼합물을 퍼징하였다. 펄만 촉매 (탄소상 수산화팔라듐, 400 mg)를 부가하고, 수소 가스로 30분 동안 용액에 거품을 일으켰다. 완료시 (CH2Cl2 중의 TLC 10% MeOH, 및 LCMS), 촉매를 셀라이트의 패드를 통해 여과로 제거하였다. 상기 여과물을 회전식 증발로 농축하고, 진공 하에서 잠시 건조하여 화합물 105a (3.28 g)를 얻었다. LCMS 및 1H NMR은 원하는 생성물과 일치하였다.
화합물 147 (2.31 g, 11 mmol)을 무수 DMF (100 mL)에 용해시켰다. N,N-디이소프로필에틸아민 (DIEA, 3.9 mL, 22 mmol)을 부가한 다음 HBTU (4 g, 10.5 mmol)를 부가하였다. 반응 혼합물을 ~ 15 분 동안 질소 하에서 교반하였다. 여기에, 건조 DMF 중의 화합물 105a (3.3 g, 7.4 mmol)의 용액을 부가하고 질소 대기 하에서 2시간 동안 교반하였다. 반응을 EtOAc로 희석하고 포화된 수성 NaHCO3 및 염수로 세정하였다. 유기상을 분리하고, 건조시키고 (MgSO4), 여과하고, 농축하여 오렌지색 시럽을 얻었다. 조 물질을 CH2Cl2 중의 칼럼 크로마토그래피 2-5 % MeOH에 의해 정제하여 화합물 148(3.44 g, 73 %)을 얻었다. LCMS 및 1H NMR은 예상된 화합물과 일치하였다.
화합물 148 (3.3 g, 5.2 mmol)을 1:1 MeOH/EtOAc (75 ml) 중에 용해시켰다. 상기 용액에 아르곤 스트림을 15분간 기포발생시켜 상기 반응 혼합물을 퍼징하였다. 펄만 촉매 (탄소상 수산화팔라듐)을 부가하였다 (350 mg). 수소 가스로 30분 동안 용액에 거품을 일으켰다. 완료시 (DCM 중의 TLC 10% MeOH, 및 LCMS), 촉매를 셀라이트의 패드를 통해 여과로 제거하였다. 상기 여과물을 회전식 증발로 농축하고, 고진공 하에서 간단히 건조하여 화합물 149 (2.6 g)를 얻었다. LCMS는 원하는 생성물과 일치하였다. 잔류물을 건조 DMF (10 ml)에 용해시키고 이것을 다음 단계에서 즉시 사용하였다.
화합물 146 (0.68 g, 1.73 mmol)을 건조 DMF (20 ml)에 용해시켰다. 여기에, DIEA (450 μL, 2.6 mmol, 1.5 eq.) 및 HBTU (1.96 g, 0.5.2 mmol)를 부가하였다. 상기 반응 혼합물을 15분 동안 실온에서 질소 하에서 교반하였다. 무수 DMF (10 mL) 중의 화합물 149 (2.6 g)의 용액을 부가하였다. 반응의 pH을 DIEA (필요한 경우)를 첨가하여 pH = 9-10으로 조정하였다. 반응을 실온에서 질소 하에서 2시간 동안 교반하였다. 완료시, 반응을 EtOAc (100 mL)로 희석하고, 수성 포화된 수성 NaHCO3 및 염수로 세정하였다. 유기상을 분리하고, 건조시키고 (MgSO4), 여과하고 농축시켰다. 조 물질을 실리카겔 칼럼 크로마토그래피로 정제하고 CH2Cl2 중의 2-10% MeOH로 용출시켜 화합물 150 (0.62 g, 20 %)를 얻었다. LCMS 및 1H NMR은 예상된 화합물과 일치하였다.
화합물 150 (0.62 g)을 1:1 MeOH/ EtOAc (5 L)에 용해시켰다. 상기 용액에 아르곤 스트림을 15분간 기포발생시켜 상기 반응 혼합물을 퍼징하였다. 펄만 촉매 (탄소상 수산화팔라듐)을 부가하였다 (60 mg). 수소 가스로 30분 동안 용액에 거품을 일으켰다. 완료시 (DCM 중 TLC 10% MeOH, 및 LCMS), 촉매를 여과 (주사기-팁 테플론 필터, 0.45 μm)에 의해 제거하였다. 여과물을 회전식 증발로 농축하고, 고진공 하에서 간단히 건조하여 화합물 151 (0.57 g)을 얻었다. LCMS는 원하는 생성물과 일치하였다. 생성물을 4 mL 건조 DMF에서 용해시키고 다음 단계에서 즉시 사용하였다.
화합물 83a (0.11 g, 0.33 mmol)을 무수 DMF (5 mL)에서 용해시키고 N,N-디이소프로필에틸아민 (75 μL, 1 mmol) 및 PFP-TFA (90 μL, 0.76 mmol)를 부가하였다. 상기 반응 혼합물은 접촉시 자홍색으로 변하였고, 그 다음 30분 동안 점차 오렌지색으로 변하였다. 반응의 진행을 TLC 및 LCMS로 관찰하였다. 완료시 (PFP 에스테르의 형성), DMF 중의 화합물 151(0.57 g, 0.33 mmol)의 용액을 부가하였다. 반응의 pH를 N,N-디이소프로필에틸아민 (필요한 경우)을 첨가하여 pH = 9-10으로 조정하였다. 반응 혼합물을 질소 하에서 ~ 30분 동안 교반하였다. 완료시, 대다수의 용매를 감압 하에서 제거하였다. 잔류물을 CH2Cl2로 희석하고 수성 포화된 NaHCO3 및 염수로 세정하였다. 유기상을 분리하고, MgSO4 상에서 건조시키고, 여과하고, 농축하여 오렌지색 시럽을 얻었다. 잔류물을 실리카겔 칼럼 크로마토그래피 (CH2Cl2 중 2-10 % MeOH)에 의해 정제하여 화합물 152(0.35 g, 55 %)를 얻었다. LCMS 및 1H NMR은 예상된 화합물과 일치하였다.
화합물 152 (0.35 g, 0.182 mmol)를 1:1 MeOH/EtOAc (10 mL)에 용해시켰다. 상기 용액에 아르곤 스트림을 15분간 기포발생시켜 상기 반응 혼합물을 퍼징하였다. 펄만 촉매 (탄소상 수산화팔라듐)을 부가하였다 (35 mg). 용액에 수소 가스를 30분간 기포발생시켰다. 완료시 (DCM 중 TLC 10% MeOH, 및 LCMS), 촉매를 여과 (주사기-팁 테플론 필터, 0.45 μm)에 의해 제거하였다. 상기 여과물을 회전식 증발로 농축하고, 고진공 하에서 잠시 건조하여 화합물 153 (0.33 g, 정량적)을 얻었다. LCMS는 원하는 생성물과 일치하였다.
화합물 153 (0.33 g, 0.18 mmol)을 교반하면서 질소 하에서 무수 DMF (5 mL)에 용해시켰다. 여기에 N,N-디이소프로필에틸아민 (65 μL, 0.37 mmol) 및 PFP-TFA (35 μL, 0.28 mmol)를 부가하였다. 반응 혼합물을 질소 하에서 ~ 30분 동안 교반하였다. 반응 혼합물은 접촉시 자홍색으로 변하였고, 점차 오렌지색으로 변하였다. 더 많은 N,-디이소프로필에틸아민을 첨가하여 상기 반응 혼합물의 pH를 pH = 9-10으로 유지시켰다. 반응의 진행을 TLC 및 LCMS로 관찰하였다. 완료시, 대다수의 용매를 감압 하에서 제거하였다. 잔류물을 CH2Cl2 (50 mL)로 희석하고 수성 포화된 NaHCO3 및 염수로 세정하였다. 유기층을 MgSO4 상에서 건조시키고, 여과하고, 농축하여 오렌지색 시럽을 얻었다. 조 물질을 칼럼 크로마토그래피로 정제하고 CH2Cl2 중의 2-10% MeOH로 용출시켜 화합물 154 (0.29 g, 79 %)를 얻었다. LCMS 및 1H NMR은 예상된 화합물과 일치하였다.
GalNAc3-6 콘주게이트 그룹을 포함하는 올리고머 화합물 155를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-6의 GalNAc3 클러스터 부분 (GalNAc3-6a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다.
GalNAc3-6 (GalNAc3-6a-CM-) 의 구조는 하기와 같다:
실시예
52:
GalNAc
3
-9를 포함하는 올리고뉴클레오티드 160의 제조
화합물 156를 하기 문헌에 기재된 과정에 따라 합성하였다: (J. Med . Chem . 2004, 47, 5798-5808).
화합물 156(18.60 g, 29.28 mmol)을 메탄올 (200 mL)에 용해시켰다. 탄소상 팔라듐 (6.15 g, 10 wt%, 로딩 (건조 기준), 매트릭스 탄소 분말, 습성)을 부가하였다. 상기 반응 혼합물을 실온에서 수소 하에서 18시간 동안 교반하였다. 상기 반응 혼합물을 셀라이트의 패드를 통해 여과하고 셀라이트 패드를 메탄올로 철저히 세정하였다. 조합된 여과물을 세정하고 농축 건조하였다. 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하고 디클로로메탄 중의 5-10 % 메탄올로 용출시켜 화합물 157 (14.26 g, 89%)을 얻었다. 질량 m/z 544.1 [M-H]-.
화합물 157 (5 g, 9.17 mmol)을 무수 DMF (30 mL)에 용해시켰다. HBTU (3.65 g, 9.61 mmol) 및 N,N-디이소프로필에틸아민 (13.73 mL, 78.81 mmol)을 부가하고 상기 반응 혼합물을 실온에서 5분 동안 교반하였다. 여기에, 화합물 47 (2.96 g, 7.04 mmol)의 용액을 부가하였다. 반응을 실온에서 8시간 동안 교반하였다. 상기 반응 혼합물을 포화된 NaHCO3 수용액에 부었다. 상기 혼합물을 에틸 아세테이트로 추출하고 유기층을 염수로 세정하고 건조시키고 (Na2SO4 상에서), 여과하고 증발시켰다. 수득된 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하고 헥산 중의 50% 에틸 아세테이트로 용출시켜 화합물 158 (8.25g, 73.3%)을 얻었다. 구조를 MS 및 1H NMR 분석에 의해 확인하였다.
화합물 158 (7.2 g, 7.61 mmol)을 감압 하에서 P2O5로 건조시켰다. 상기 건조된 화합물을 무수 DMF (50 mL)에 용해시켰다. 여기에, 1H-테트라졸 (0.43 g, 6.09 mmol) 및 N-메틸이미다졸 (0.3 mL, 3.81 mmol) 및 2-시아노에틸-N,N,N',N'-테트라이소프로필 포스포로디아미다이트 (3.65 mL, 11.50 mmol)를 부가하였다. 상기 반응 혼합물을 아르곤 대기 하에서 4시간 동안 교반하였다. 상기 반응 혼합물을 에틸 아세테이트 (200 mL)로 희석하였다. 상기 반응 혼합물을 포화된 NaHCO3 및 염수로 세정하였다. 유기상을 분리하고, 건조시키고 (Na2SO4), 여과하고 증발시켰다. 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하고 헥산 중의 50-90 % 에틸 아세테이트로 용출시켜 화합물 159 (7.82 g, 80.5%)를 얻었다. 구조를 LCMS 및 31P NMR 분석에 의해 확인하였다.
GalNAc3-9 콘주게이트 그룹을 포함하는 올리고머 화합물 160을 표준 올리고뉴클레오티드 합성 과정을 이용하여 제조하였다. 화합물 159의 3 단위를 고체 지지체에 커플링시킨 다음 뉴클레오티드 포스포르아미다이트에 커플링시켰다. 암모니아수를 이용한 상기 보호된 올리고머 화합물의처리는 화합물 160을 생성하였다. 콘주게이트 그룹 GalNAc3-9의 GalNAc3 클러스터 부분 (GalNAc3-9a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-9 (GalNAc3-9a-CM) 의 구조는 하기와 같다:
실시예
53: 화합물 18 (
GalNAc
3
-1a 및
GalNAc
3
-3a)의 제조를 위한 대안적인 절차
락톤 161을 디아미노 프로판 (3-5 eq) 또는 단일-Boc 보호된 디아미노 프로판 (1 eq)과 반응시켜 알코올 162a 또는 162b를 제공하였다. 비보호된 프로판디아민이 상기 반응에 사용되는 경우, 과잉 디아민을 고진공 하에서 증발에 의해 제거하였고, 162a 내의 유리 아미노 그룹을 CbzCl을 이용하여 보호하여 칼럼 크로마토그래피에 의해 정제 후백색 고체물로서 162b를 제공하였다. 알코올 162b를 TMSOTf의 존재하에 화합물 4와 추가 반응시켜 163a를 제공하였고, 이는 촉매적 수소첨가를 이용한 Cbz 그룹의 제거에 의해 163b로 전환되었다. 펜타플루오로페닐 (PFP) 에스테르 164를 3가산 113 (참고 실시예 48)을 DMF (0.1 내지 0.5 M) 중의 PFPTFA (3.5 eq) 및 피리딘 (3.5 eq)과 반응시켜 제조하였다. 상기 트리에스테르 164를 아민 163b (3-4 eq) 및 DIPEA (3-4 eq)와 직접 반응시켜 화합물 18을 제공하였다. 상기 방법은 중간체의 정제를 상당히 용이하게 하며 실시예 4에 기재된 과정을 이용하여 형성된 부산물의 형성을 최소화한다.
실시예
54: 화합물 18 (
GalNAc
3
-1a 및
GalNAc
3
-3a)의 제조를 위한 대안적인 절차
triPFP 에스테르 164를 상기 실시예 53에 개괄된 절차를 이용하여 산 113으로부터 제조하였고 모노-Boc 보호된 디아민과 반응시켜 165를 본질적으로 정량적 수율로 제공하였다. 상기 Boc 그룹을 염산 또는 트리플루오로아세트산으로 제거하여 트리아민을 제공하였고, 이를 적당한 염기, 예컨대 DIPEA의 존재하에 PFP 활성화된 산 166과 반응시켜 화합물 18을 제공하였다.
PFP 보호된 Gal-NAc 산 166을 DMF 중 PFPTFA (1-1.2 eq) 및 피리딘 (1-1.2 eq)으로 처리하여 상응하는 산으로부터 제조하였다. 전구체 산을 결국, 아세토니트릴 및 물 중의 TEMPO (0.2 eq) 및 BAIB를 아용한 산화에 의해 상응하는 알코올로부터 제조하였다. 전구체 알코올을 실시예 47에 앞서 기재된 조건을 이용하여 1,6-헥산디올 (또는 1,5-펜탄디올 또는 다른 n 값에 대한 다른 디올) (2-4 eq) 및 TMSOTf와의 반응에 의해 당 중간체 4로부터 제조하였다.
실시예
55:
생체내
에서
SRB
-1을 표적으로 하는 3' 또는 5'-
콘주게이트
그룹 (GalNAc
3
-1, 3, 8 및 9의 비교)을 포함하는 올리고뉴클레오티드의 투여량-의존적 연구
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 비콘주게이트된 ISIS 353382는 표준으로서 포함된다. 각각의 다양한 GalNAc3 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 (절단가능 모이어티)에 의해 각 올리고뉴클레오티드의 3' 또는 5' 말단에서 부착되었다.
표 39
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다. "GalNAc3-9"의 구조가 실시예 52에 나타나 있다. "GalNAc3-3"의 구조가 실시예 39에 나타나 있다. "GalNAc3-8"의 구조가 실시예 47에 나타나 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 353382, 655861, 664078, 661161, 665001 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 40에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. 사실상, 3' 말단에서 포스포디에스테르 연결된 GalNAc3-1 및 GalNAc3-9 콘주게이트 (ISIS 655861 및 ISIS 664078) 및 5' 말단에서 연결된 GalNAc3-3 및 GalNAc3-8 콘주게이트 (ISIS 661161 및 ISIS 665001)을 포함하는 안티센스 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 353382)와 비교하여 효능의 실질적인 개선을 보여주었다. 더욱이, 3' 말단에서 GalNAc3-9 콘주게이트를 포함하는 ISIS 664078은 3' 말단에서 GalNAc3-1 콘주게이트를 포함하는 ISIS 655861와 비교하여 본질적으로 동등하게 강력했다. GalNAc3-3 또는 GalNAc3-9, 각각을 포함하는 5' 콘주게이트된 안티센스 올리고뉴클레오티드, ISIS 661161 및 ISIS 665001은, 3' 콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 655861 및 ISIS 664078)와 비교하여 증가된 효능을 가졌다.
표 40
SRB
-1을 표적으로 하는
GalNAc
3
-1, 3, 8 또는 9를 함유하는
ASO
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화를 염수 그룹으로부터 유의미한 변화 없이 평가했다. ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표에서 보여진다.
표 41
실시예
56:
생체내
에서
SRB
-1을 표적으로 하는 3' 또는 5'-
콘주게이트
그룹 (GalNAc
3
-1, 2, 3, 5, 6, 7 및 10의 비교)을 포함하는 올리고뉴클레오티드의 투여량-의존적 연구
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 비콘주게이트된 ISIS 353382는 표준으로서 포함된다. 각각의 다양한 GalNAc3 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 (절단가능 모이어티)에 의해 각 올리고뉴클레오티드의 5' 말단에서 부착되었고, 단 3' 말단에서 부착된 GalNAc3 콘주게이트 그룹을 갖는 ISIS 655861는 제외된다.
표 42
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다. "GalNAc3-2a"의 구조가 이미 실시예 37에 나타나 있다. "GalNAc3-3a"의 구조가 이미 실시예 39에 나타나 있다. "GalNAc3-5a"의 구조가 이미 실시예 49에 나타나 있다. "GalNAc3-6a"의 구조가 이미 실시예 51에 나타나 있다. "GalNAc3-7a"의 구조가 이미 실시예 48에 나타나 있다. "GalNAc3-10a"의 구조가 이미 실시예 46에 나타나 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 353382, 655861, 664507, 661161, 666224, 666961, 666981, 666881 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 43에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. 사실상, 콘주게이트된 안티센스 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 353382) 와 비교하여 효능의 실질적인 개선을 보여주었다. 5' 콘주게이트된 안티센스 올리고뉴클레오티드는 3' 콘주게이트된 안티센스 올리고뉴클레오티드와 비교하여 효능의 약간의 증가를 보여주었다.
표 43
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화를 염수 그룹으로부터 유의미한 변화 없이 평가했다. ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 44에서 보여진다.
표 44
실시예
57:
생체내
에서
ApoC
III을 표적으로 하는 3'-
콘주게이트
그룹을 포함하는 올리고뉴클레오티드의 작용 연구의 지속 시간
마우스에게 하기에서 명시된 투여량이 1 회 주입되었고 42 일의 과정 동안 ApoC-III 및 혈장 트리글리세라이드 (혈장 TG) 수준에 대해 모니터링되었다. 연구는 각 그룹에서 인간 APOC-III을 발현시키는 3 개의 형질전환 마우스을 사용하여 수행되었다.
표 45
ApoC
III를 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다.
표 46
ApoC
III
mRNA
(
1 일째
염수
%
) 및 혈장 TG 수준 (
1 일째
염수
%
)
상기 표에서 보여질 수 있는 바와 같이, 작용의 지속시간은 비콘주게이트된 올리고뉴클레오티드와 비교하여 3'-콘주게이트 그룹의 부가와 함께 증가되었다. 콘주게이트된 완벽한 PS 올리고뉴클레오티드 647535와 비교하여 콘주게이트된 혼합된 PO/PS 올리고뉴클레오티드 647536에 대한 작용의 지속시간이 추가로 증가되었다.
실시예
58:
생체내
에서
SRB
-1을 표적으로 하는 3'-
콘주게이트
그룹 (
GalNAc
3
-1 및 GalNAc
4
-11의 비교)을 포함하는 올리고뉴클레오티드의 투여량-의존적 연구
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 비콘주게이트된 ISIS 440762은 비콘주게이트된 표준으로서 포함되었다. 각각의 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 절단가능 모이어티에 의해 각 올리고뉴클레오티드의 3' 말단에서 부착되었다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다. "GalNAc3-11a"의 구조가 이미 실시예 50에 나타나 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 440762, 651900, 663748 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 47에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. 3' 말단(ISIS 651900 및 ISIS 663748)에서 포스포디에스테르 연결된 GalNAc3-1 및 GalNAc4-11 콘주게이트를 포함하는 안티센스 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 440762) 와 비교하여 효능의 실질적인 개선을 보여주었다. 2 개의 콘주게이트된 올리고뉴클레오티드, GalNAc3-1 및 GalNAc4-11는, 동등하게 강력했다.
표 47
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "k"는 6'-(S)-CH3 이환식 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화를 염수 그룹으로부터 유의미한 변화 없이 평가했다. ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 48에서 보여진다.
표 48
실시예
59:
생체내
FXI을
표적으로 하는
GalNAc
3
-1
콘주게이트된
ASO의
효과
하기에서 열거된 올리고뉴클레오티드는 마우스에서 FXI의 안티센스 억제에 대한 다중 투여량 연구에서 시험되었다. ISIS 404071은 비콘주게이트된 표준으로서 포함되었다. 각각의 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 절단가능 모이어티에 의해 각 올리고뉴클레오티드의 3' 말단에서 부착되었다.
표 49
FXI를
표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다.
치료
6 주령 수컷 Balb/c 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 피하로 매주 2회 3 주 동안 하기에서 보여진 투여량으로 ISIS 404071, 656172, 656173 또는 PBS 처리된 대조군이 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 FXI mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 혈장 FXI 단백질 수준은 ELISA을 사용하여 또한 측정되었다. FXI mRNA 수준은 PBS-처리된 대조군에 대한 정규화 전에 (리보그린®를 사용하여) 총 RNA에 대해 결정되었다. 하기의 결과는 각 처리 그룹에 대한 FXI mRNA 수준의 평균 퍼센트로저 제공된다. 데이터는 PBS-처리된 대조군에 대해 정규화되었고 "% PBS"로 나타낸다. ED50은 전에 기재된 것과 유사한 방법을 사용하여 측정되었고 하기에서 제공된다.
표 50
인자 XI
mRNA
(염수
%
)
표 50에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 FXI mRNA 수준을 감소시켰다. 3'-GalNAc3-1 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 404071) 와 비교하여 효능의 실질적인 개선을 보여주었다. 2 개의 콘주게이트된 올리고뉴클레오티드 사이에 효능의 개선이 추가로, PS 연결의 일부를 PO (ISIS 656173)로 치환하여 제공되었다.
표 50a에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 FXI 단백질 수준을 감소시켰다. 3'-GalNAc3-1 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 404071) 와 비교하여 효능의 실질적인 개선을 보여주었다. 2 개의 콘주게이트된 올리고뉴클레오티드 사이에 효능의 개선이 추가로, PS 연결의 일부를 PO (ISIS 656173)로 치환하여 제공되었다.
표 50a
인자 XI 단백질 (염수
%
)
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈, 총 알부민, CRE 및 BUN가 또한 평가되었다. 체중의 변화를 염수 그룹으로부터 유의미한 변화 없이 평가했다. ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표에서 보여진다.
표 51
실시예
60:
시험관내
SRB
-1을 표적으로 하는
콘주게이트된
ASO의
효과
하기에서 열거된 올리고뉴클레오티드는 일차 마우스 간세포에서 SRB-1의 안티센스 억제에 대한 다중 투여량 연구에서 시험되었다. ISIS 353382은 비콘주게이트된 표준으로서 포함되었다. 각각의 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 절단가능 모이어티에 의해 각 올리고뉴클레오티드의 3' 또는 5' 말단에서 부착되었다.
표 52
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다. "GalNAc3-3a"의 구조가 이미 실시예 39에 나타나 있다. "GalNAc3-8a"의 구조가 이미 실시예 47에 나타나 있다. "GalNAc3-9a"의 구조가 이미 실시예 52에 나타나 있다. "GalNAc3-6a"의 구조가 이미 실시예 51에 나타나 있다. "GalNAc3-2a"의 구조가 이미 실시예 37에 나타나 있다. "GalNAc3-10a"의 구조가 이미 실시예 46에 나타나 있다. "GalNAc3-5a"의 구조가 이미 실시예 49에 나타나 있다. "GalNAc3-7a"의 구조가 이미 실시예 48에 나타나 있다.
치료
상기 열거된 올리고뉴클레오티드는 25,000 세포/웰의 밀도에서 플레이팅된 일차 마우스 간세포 세포에서 시험관내에서 시험되었고, 0.03, 0.08, 0.24, 0.74, 2.22, 6.67 또는 20 nM 변형된 올리고뉴클레오티드로 처리되었다. 대략 16 시간의 처리 기간 후, RNA는 세포로부터 단리되었고 mRNA 수준은 정량적 실시간 PCR에 의해 측정되었고 SRB-1 mRNA 수준은 리보그린®에 의해 측정된 바와 같이 총 RNA 함량에 따라 조정되었다.
IC50을 표준 방법을 사용하여 계산하였고 그 결과가 표 53에서 제시되어 있다. 이 결과는, 시약 또는 전기천공 기술이 올리고뉴클레오티드의 세포로의 유입을 인공적으로 촉진하기 위해 사용되지 않은 유리 흡수 조건 하에서, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트를 포함하지 않는 모 올리고뉴클레오티드 (ISIS 353382)보다 간세포에서 유의미하게 더 강했다는 것을 보여준다.
표 53
실시예
61: GalNAc
3
-12를 포함하는 올리고머 화합물 175의 제조
화합물 169는 상업적으로 이용가능하다. 화합물 172를, 벤질 (퍼플루오로페닐) 글루타레이트를 화합물 171에 부가하여 제조했다. 벤질 (퍼플루오로페닐) 글루타레이트를, DMF 중 PFP-TFA 및 DIEA을 5-(벤질옥시)-5-옥소펜탄산에 부가하여 제조했다. GalNAc3-12 콘주게이트 그룹을 포함하는 올리고머 화합물 175를 실시예 46에 예시된 일반적인 과정을 이용하여 화합물 174로부터 제조하였다. 콘주게이트 그룹 GalNAc3-12의 GalNAc3 클러스터 부분 (GalNAc3-12a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-.다. GalNAc3-12 (GalNAc3-12a-CM-) 의 구조는 하기와 같다:
실시예
62:
GalNAc
3
-
13를
포함하는 올리고머 화합물 180의 제조
화합물 176은 실시예 2에서 보여진 일반적인 절차를 사용하여 제조되었다. GalNAc3-13 콘주게이트 그룹을 포함하는 올리고머 화합물 180를 실시예 49에 예시된 일반적인 과정을 이용하여 화합물 177로부터 제조하였다. 콘주게이트 그룹 GalNAc3-13의 GalNAc3 클러스터 부분 (GalNAc3-13a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-.이다. GalNAc3-13 (GalNAc3-13a-CM-) 의 구조는 하기와 같다:
실시예
63:
GalNAc
3
-14를 포함하는 올리고머 화합물 188의 제조
화합물 181 및 185는 시판되고 있다. GalNAc3-14 콘주게이트 그룹을 포함하는 올리고머 화합물 188를 실시예 46에 예시된 일반적인 과정을 이용하여 화합물 187로부터 제조하였다. 콘주게이트 그룹 GalNAc3-14의 GalNAc3 클러스터 부분 (GalNAc3-14a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-14 (GalNAc3-14a-CM-) 의 구조는 하기와 같다:
실시예
64:
GalNAc
3
-15를 포함하는 올리고머 화합물 197의 제조
화합물 189는 상업적으로 이용가능하다. 화합물 195은 실시예 31에서 보여진 일반적인 절차를 사용하여 제조되었다. GalNAc3-15 콘주게이트 그룹을 포함하는 올리고머 화합물 197은, 표준 올리고뉴클레오티드 합성 절차를 사용하여 화합물 194 및 195로부터 제조되었다. 콘주게이트 그룹 GalNAc3-15의 GalNAc3 클러스터 부분 (GalNAc3-15a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-15 (GalNAc3-15a-CM-) 의 구조는 하기와 같다:
실시예
65:
생체내
에서
SRB
-1을 표적으로 하는 5'-
콘주게이트
그룹 (GalNAc
3
-3, 12, 13, 14, 및 15의 비교)을 포함하는 올리고뉴클레오티드의 투여량-의존적 연구
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 비콘주게이트된 ISIS 353382는 표준으로서 포함된다. 각각의 GalNAc3 콘주게이트 그룹은 포스포디에스테르 연결된 2'-데옥시아데노신 뉴클레오시드 절단가능 모이어티에 의해 각 올리고뉴클레오티드의 5' 말단에서 부착되었다.
표 54
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-3a"의 구조가 이미 실시예 39에 나타나 있다. "GalNAc3-12a"의 구조가 실시예 61에 나타나 있다. "GalNAc3-13a"의 구조가 실시예 62에 나타나 있다. "GalNAc3-14a"의 구조가 실시예 63에 나타나 있다. "GalNAc3-15a"의 구조가 실시예 64에 나타나 있다.
치료
6 내지 8 주령 C57bl6 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 하기에서 보여진 투여량으로 ISIS 353382, 661161, 671144, 670061, 671261, 671262, 또는 염수가 1 회 또는 2 회 피하로 주입되었다. 2 회 투여된 마우스는 제 1 투여량 3일 후에 제 2 투여량을 수용했다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 55에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. 표적 녹다운의 유의미한 차이는 단회 투여량을 수용한 동물과 2 회 투여량을 수용한 동물 사이에 관찰되지 않았다 (참고 ISIS 353382 투여량 30 및 2 x 15 mg/kg; 및 ISIS 661161 투여량 5 및 2 x 2.5 mg/kg). 포스포디에스테르 연결된 GalNAc3-3, 12, 13, 14, 및 15 콘주게이트을 포함하는 안티센스 올리고뉴클레오티드는 비콘주게이트된 안티센스 올리고뉴클레오티드 (ISIS 335382) 와 비교하여 효능의 실질적인 개선을 보여주었다.
표 55
SRB
-1
mRNA
(
%
염수)
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화는 염수 그룹으로부터 유의미한 차이 없이 평가되었다 (데이터 도시되지 않음). ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 56에서 보여진다.
표 56
실시예
66: 5'
-
GalNAc
3
클러스터를 포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제에 대한 다양한 절단가능
모이어티의
효과
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 각각의 GalNAc3 콘주게이트 그룹은 포스포디에스테르 연결된 뉴클레오시드 절단가능 모이어티(CM)에 의해 각 올리고뉴클레오티드의 5' 말단에서 부착되었다.
표 57
SRB
-1을 표적으로 하는 변형된
ASO
대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-3a"의 구조가 이미 실시예 39에 나타나 있다. "GalNAc3-13a"의 구조가 실시예 62에 나타나 있다.
치료
6 내지 8 주령 C57bl6 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 ISIS 661161, 670699, 670700, 670701, 671165, 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 간 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 58에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. 다양한 절단가능 모이어티 모두을 포함하는 안티센스 올리고뉴클레오티드는 유사한 효능을 보여주었다.
표 58
SRB
-1
mRNA
(
%
염수)
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화는 염수 그룹으로부터 유의미한 차이 없이 평가되었다 (데이터 도시되지 않음). ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 56에서 보여진다.
표 59
실시예
67:
GalNAc
3
-
16를
포함하는 올리고머 화합물 199의 제조
GalNAc3-16 콘주게이트 그룹을 포함하는 올리고머 화합물 199를 실시예 7 및 9에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-16의 GalNAc3 클러스터 부분 (GalNAc3-16a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-16 (GalNAc3-16a-CM-)의 구조는 이하에서 보여진다:
실시예
68:
GalNAc
3
-
17를
포함하는 올리고머 화합물 200의 제조
GalNAc3-17 콘주게이트 그룹을 포함하는 올리고머 화합물 200를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-17의 GalNAc3 클러스터 부분 (GalNAc3-17a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-17 (GalNAc3-17a-CM-) 의 구조는 하기와 같다:
실시예
69:
GalNAc
3
-
18를
포함하는 올리고머 화합물 201의 제조
GalNAc3-18 콘주게이트 그룹을 포함하는 올리고머 화합물 201를 실시예 46에 예시된 일반적인 과정을 이용하여 제조하였다. 콘주게이트 그룹 GalNAc3-18의 GalNAc3 클러스터 부분 (GalNAc3-18a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-18 (GalNAc3-18a-CM-) 의 구조는 하기와 같다:
실시예
70:
GalNAc
3
-19를 포함하는 올리고머 화합물 204의 제조
GalNAc3-19 콘주게이트 그룹을 포함하는 올리고머 화합물 204를 실시예 52에 예시된 일반적인 과정을 이용하여 화합물 64로부터 제조하였다. 콘주게이트 그룹 GalNAc3-19의 GalNAc3 클러스터 부분 (GalNAc3-19a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-19 (GalNAc3-19a-CM-) 의 구조는 하기와 같다:
실시예
71:
GalNAc
3
-
20를
포함하는 올리고머 화합물 210의 제조
화합물 205을, 트리플릭산 무수물을 6-아미노헥산산에 부가하여 제조된 아세토니트릴에서 PFP-TFA 및 DIEA을 6-(2,2,2-트리플루오로아세트아미도)헥산산에 부가하여 제조했다. 반응 혼합물을 80 oC로 가열하고, 그 다음 실온으로 온도를 낮추었다. GalNAc3-20 콘주게이트 그룹을 포함하는 올리고머 화합물 210를 실시예 52에 예시된 일반적인 과정을 이용하여 화합물 208로부터 제조하였다. 콘주게이트 그룹 GalNAc3-20의 GalNAc3 클러스터 부분 (GalNAc3-20a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-20 (GalNAc3-20a-CM-) 의 구조는 하기와 같다:
실시예
72:
GalNAc
3
-
21를
포함하는 올리고머 화합물 215의 제조
화합물 211는 상업적으로 이용가능하다. GalNAc3-21 콘주게이트 그룹을 포함하는 올리고머 화합물 215를 실시예 52에 예시된 일반적인 과정을 이용하여 화합물 213로부터 제조하였다. 콘주게이트 그룹 GalNAc3-21의 GalNAc3 클러스터 부분 (GalNAc3-21a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-21 (GalNAc3-21a-CM-) 의 구조는 하기와 같다:
실시예
73:
GalNAc
3
-22를 포함하는 올리고머 화합물 221의 제조
화합물 220은 디이소프로필암모늄 테트라졸라이드를 사용하여 화합물 219로부터 제조되었다. GalNAc3-21 콘주게이트 그룹을 포함하는 올리고머 화합물 221를 실시예 52에 예시된 일반적인 과정을 이용하여 화합물 220로부터 제조하였다. 콘주게이트 그룹 GalNAc3-22의 GalNAc3 클러스터 부분 (GalNAc3-22a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 절단가능 모이어티는 -P(=O)(OH)-Ad-P(=O)(OH)-이다. GalNAc3-22 (GalNAc3-22a-CM-) 의 구조는 하기와 같다:
실시예
74: 5'
-
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제에 대한 다양한 절단가능
모이어티의
효과
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다. 각각의 GalNAc3 콘주게이트 그룹은 각 올리고뉴클레오티드의 5' 말단에서 부착되었다.
표 60
SRB
-1을 표적으로 하는 변형된
ASO
모든 표에서, 대문자는 각 뉴클레오시드에 대한 핵염기를 나타내고 mC는 5-메틸 시토신을 나타낸다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)을 나타내고; 그리고 "o'"는 -O-P(=O)(OH)-를 나타낸다. 콘주게이트 그룹은 굵은 글자체이다.
"GalNAc3-3a"의 구조가 이미 실시예 39에 나타나 있다. GalNAc3-17a의 구조는 실시예 68에서 이미 나타나 있고, GalNAc3-18a의 구조는 실시예 69에서 나타나 있다.
치료
6 내지 8 주령 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 표 60에서 열거된 올리고뉴클레오티드 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 61에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다. GalNAc 콘주게이트를 포함하는 안티센스 올리고뉴클레오티드 유사한 효능을 보여주었고 GalNAc 콘주게이트가 없는 모 올리고뉴클레오티드보다 유의미하게 더 강했다.
표 61
SRB
-1
mRNA
(
%
염수)
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 염수 주입된 마우스에 대해 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화를 염수 그룹으로부터 유의미한 변화 없이 평가했다 (데이터 도시되지 않음). ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 62에서 보여진다.
표 62
실시예
75: 5
'-
콘주게이트
그룹을 포함하는 올리고뉴클레오티드의
약력학적
분석
상기 표 54, 57 및 60 중 ASO의 PK를, 실시예 65, 66, 및 74에서 기재된 처리 절차에 따라 수득된 간 샘플을 사용하여 평가했다. 간 샘플을 다지고 표준 프로토콜을 사용하여 추출하고 내부 표준과 함께 IP-HPLC-MS로 분석했다. 모든 대사물의 조합된 조직 수준 (㎍/g)은 적절한 UV 피크를 통합하여 측정되었고, (이 경우에 Isis 번호 353382인 "모") 콘주게이트를 누락한 전장 ASO의 조직 수준을 적절한 추출된 이온 크로마토그램 (EIC)를 사용하여 측정했다.
표 63
간 중 PK 분석
상기 표 63의 결과는, 특히 GalNAc3 콘주게이트 그룹의 유무에 따라 올리고뉴클레오티드 사이의 투여의 차이를 고려할 때, 올리고뉴클레오티드 투여로부터 72 시간 후에 GalNAc3 콘주게이트 그룹 (ISIS 353382)를 포함하지 않는 모 올리고뉴클레오티드보다 GalNAc3 콘주게이트 그룹을 포함하는 올리고뉴클레오티드의 간 조직 수준이 더 크다는 것을 보여준다. 더욱이, 72 시간까지, GalNAc3 콘주게이트 그룹을 포함하는 각 올리고뉴클레오티드의 40-98%는 대사작용되어 모 화합물을 얻었고, 이것은, GalNAc3 콘주게이트 그룹이 올리고뉴클레오티드로부터 절단되었다는 것을 나타낸다.
실시예
76:
GalNAc
3
-
23를
포함하는 올리고머 화합물 230의 제조
화합물 222는 상업적으로 이용가능하다. 44.48 ml (0.33 mol)의 화합물 222를 피리딘 (500mL) 중 토실 클로라이드 (25.39 g, 0.13 mol)로 16 시간 동안 처리했다. 그 다음 반응을 증발시켜 오일을 얻고, EtOAc에서 용해시키고 물, 포화 NaHCO3, 염수로 세정하고, Na2SO4 상에서 건조시켰다. 에틸 아세테이트를 농축 건조하고 칼럼 크로마토그래피로 정제하고, EtOAc/헥산 (1:1) 그 다음 CH2Cl2 중 10% 메탄올로 용출하여 화합물 223을 무색 오일로서 얻었다. LCMS 및 NMR은 구조와 일치했다. 10 g (32.86 mmol)의 1-토실트리에틸렌 글리콜 (화합물 223)을 DMSO (100mL) 중 아지드화나트륨 (10.68 g, 164.28 mmol)로 실온에서 17 시간 동안 처리했다. 그 다음 반응 혼합물을 물에 붓고, EtOAc로 추출했다. 유기 층을 물로 3 회 세정하고 Na2SO4 상에서 건조시켰다. 유기 층을 농축 건조하여 5.3g의 화합물 224 (92%)을 얻었다. LCMS 및 NMR은 구조와 일치했다. 1-아지도트리에틸렌 글리콜 (화합물 224, 5.53 g, 23.69 mmol) 및 화합물 4 (6 g, 18.22 mmol)을 4A 분자체 (5g), 및 디클로로메탄 (100mL) 중 TMSOTf (1.65 ml, 9.11 mmol)로 불활성 대기 하에서 처리했다. 14 시간 후, 반응을 여과하여 체를 제거하고, 유기 층을 포화 NaHCO3, 염수로 세정하고, Na2SO4 상에서 건조시켰다. 유기 층을 농축 건조하고 칼럼 크로마토그래피로 정제하고, 디클로로메탄 중 2 내지 4% 메탄올의 구배로 용출하여 화합물 225를 얻었다. LCMS 및 NMR은 구조와 일치했다. 화합물 225 (11.9 g, 23.59 mmol)을 펄만 촉매 상에서 EtOAc/메탄올 (4:1, 250mL)에서 수소첨가했다. 8 시간 후, 촉매를 여과로 제거하고 용매를 제거하고 건조시켜 화합물 226을 얻었다. LCMS 및 NMR은 구조와 일치했다.
화합물 227를 산출하기 위해, DMF (100mL) 중 니트로메탄트리스프로피온산 (4.17 g, 15.04 mmol) 및 휘니그 염기 (10.3 ml, 60.17 mmol)의 용액을 펜타플루오로트리플루오로 아세테이트 (9.05 ml, 52.65 mmol)로 적가 처리했다. 30 분 후, 반응을 빙수에 붓고 EtOAc로 추출했다. 유기 층을 물, 염수로 세정하고 Na2SO4 상에서 건조시켰다. 유기 층을 농축 건조하고 그 다음 헵탄으로부터 재결정화하여 화합물 227을 백색 고형물로서 얻었다. LCMS 및 NMR은 구조와 일치했다. 화합물 227(1.5 g, 1.93 mmol) 및 화합물 226 (3.7 g, 7.74 mmol)을 실온에서 아세토니트릴 (15 mL)에서 2 시간 동안 교반했다. 그 다음 반응을 증발 건조하고 디클로로메탄 중 2 내지 10% 메탄올의 구배로 용출하는 칼럼 크로마토그래피로 정제하여 화합물 228을 얻었다. LCMS 및 NMR은 구조와 일치했다. 화합물 228 (1.7 g, 1.02 mmol)을 에탄올 (100mL) 중 라니 니켈 (약 2g 습성)로 수소의 대기에서 처리했다. 12 시간 후, 촉매를 여과로 제거하고 유기 층을 증발시켜 고형물을 얻었고, 이것을 직접적으로 다음 단계에서 사용했다. LCMS 및 NMR은 구조와 일치했다. 이러한 고형물 (0.87 g, 0.53 mmol)을 DMF (5mL) 중 벤질글루타르산 (0.18 g, 0.8 mmol), HBTU (0.3 g, 0.8 mmol) 및 DIEA (273.7 μl, 1.6 mmol)로 처리했다. 16 시간 후, DMF를 감압 하에서 65에서 제거하여 오일을 얻었고, 오일을 디클로로메탄에서 용해시켰다. 유기 층을 포화 NaHCO3, 염수로 세정하고, Na2SO4 상에서 건조시켰다. 유기 층의 증발 후, 화합물을 칼럼 크로마토그래피로 정제하고 디클로로메탄 중 2 내지 20% 메탄올의 구배로 용출하여 커플링된 생성물을 얻었다. LCMS 및 NMR은 구조와 일치했다. 벤질 에스테르를 수소 대기 하에서 1 시간 동안 펄만 촉매로 탈보호했다. 그 다음 촉매를 여과로 제거하고 용매를 제거하고 건조시켜 산을 얻었다. LCMS 및 NMR은 구조와 일치했다. 산 (486 mg, 0.27 mmol)을 건조 DMF (3 mL)에서 용해시켰다. 피리딘(53.61 μl, 0.66 mmol)을 부가하고 반응을 아르곤으로 퍼지했다. 펜타플루오로트리플루오로 아세테이트 (46.39 μl, 0.4 mmol)을 반응 혼합물에 서서히 부가했다. 반응의 색상은 담황색에서 암적색으로 변했고, 옅은 연기가 생겼고, 이것을 아르곤의 스트림으로 없앴다. 반응을 실온에서 1 시간 동안 교반되도록 했다 (반응의 완료는 LCMS으로 확인되었다). 용매를 감압 (회전증발기) 하에서 70 ℃에서 제거했다. 잔류물을 DCM으로 희석하고 1N NaHSO4, 염수로 세정하고, 포화된 중탄산나트륨 및 염수로 다시 세정했다. 유기물을 Na2SO4 상에서 건조하고, 여과하고, 농축 건조하여 225 mg의 화합물 229를 잘 부서지는 황색 포말로서 얻었다. LCMS 및 NMR은 구조와 일치했다.
GalNAc3-23 콘주게이트 그룹을 포함하는 올리고머 화합물 230은, 실시예 46에서 실증된 일반적인 절차를 사용하여 화합물 229로부터 제조되었다. GalNAc3-23 콘주게이트 그룹의 GalNAc3 클러스터 부분 (GalNAc3-23a)은 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc3-23 (GalNAc3-23a-CM) 의 구조는 하기와 같다:
실시예
77:
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
표 64
SRB
-1을 표적으로 하는 변형된
ASO
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-9a의 구조는 실시예 52에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, GalNAc3-19a의 구조는 실시예 70에서 나타나 있고, GalNAc3-20a의 구조는 실시예 71에서 나타나 있고, GalNAc3-23a의 구조는 실시예 76에서 나타나 있다.
치료
6 내지 8 주령 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME) 각각에게 하기에서 보여진 투여량으로 표 64에서 열거된 올리고뉴클레오티드 또는 염수가 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 72 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군에 대해 정규화된 각 처리 그룹에 대한 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 65에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다.
표 65
SRB
-1
mRNA
(
%
염수)
혈청 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 표준 프로토콜을 사용하여 또한 측정되었다. 총 빌리루빈 및 BUN가 또한 평가되었다. 체중의 변화가 평가되었고, 염수 그룹으로부터 유의미한 변화는 없었다 (데이터 도시되지 않음). ALT, AST, 총 빌리루빈 및 BUN 값은 하기의 표 66에서 보여진다.
표 66
실시예
78:
GalNAc
3
콘주게이트를
포함하는
안지오텐시노겐을
표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기에서 열거된 올리고뉴클레오티드는 정상혈압 스프래그 다우리 래트에서 안지오텐시노겐 (AGT)의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
표 67
AGT을
표적으로 하는 변형된
ASO
"GalNAc3-1a"의 구조가 이미 실시예 9에 나타나 있다.
치료
6 주령, 수컷 스프래그 다우리 래트 각각에게 피하로 주당 1회 하기에서 보여진 투여량으로, 총 3 회 투여량 동안, 표 67에서 열거된 올리고뉴클레오티드 또는 PBS가 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 래트는 최종 투여량 후 72 시간에 희생되었다. AGT 간 mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc. Eugene, OR)을 사용하여 측정되었다. AGT 혈장 단백질 수준은 총 안지오텐시노겐 ELISA (카탈로그 # JP27412, IBL International, Toronto, ON)을 1:20,000 희석된 혈장과 함께 사용하여 측정되었다. 하기의 결과는 간에서 AGT mRNA 수준 또는 PBS 대조군에 대해 정규화된 각 처리 그룹의 혈장에서 AGT 단백질 수준의 평균 퍼센트로서 나타낸다.
표 68에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 AGT 간 mRNA 및 혈장 단백질 수준을 감소시켰고, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트가 없는 모 올리고뉴클레오티드 보다 유의미하게 더 강했다.
표 68
AGT
간
mRNA
및 혈장 단백질 수준
혈장 및 체중 중 간 트랜스아미나제 수준, 알라닌 트랜스아미나제 (ALT) 및 아스파르테이트 트랜스아미나제 (AST)는, 또한 표준 프로토콜을 사용하여 희생 시에 측정되었다. 결과는 하기의 표 69에서 보여준다.
표 69
간 트랜스아미나제 수준 및
래트
체중
실시예
79:
GalNAc
3
콘주게이트를
포함하는
APOC
-III을 표적으로 하는 올리고뉴클레오티드의
생체내
작용의 지속시간
하기의 표 70에서 열거된 올리고뉴클레오티드는 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
표 70
APOC
-III을 표적으로 하는 변형된
ASO
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, GalNAc3-13a의 구조는 실시예 62에서 나타나 있다.
치료
인간 APOC-III을 발현시키는 6 내지 8 주령 형질전환 마우스 각각에게 표 70에서 열거된 올리고뉴클레오티드 또는 PBS가 피하로 1 회 주입되었다. 각 처리 그룹은 3 마리의 동물로 구성되었다. 투여 전에 채혈하여 기준선을 결정하고 투여 후 72 시간, 1 주, 2 주, 3 주, 4 주, 5 주, 및 6 주에서 결정했다. 혈장 트리글리세라이드 및 APOC-III 단백질 수준은 실시예 20에서 기재된 바와 같이 측정되었다. 하기의 결과는 기준선 수준에 대해 정규화된 각 처리 그룹의 혈장 트리글리세라이드 및 APOC-III 수준의 평균 퍼센트로서 나타내고, 이것은, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드가, 모의 투여량이 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드의 투여량의 3 배일지라도, 콘주게이트 그룹 (ISIS 304801)없는 모 올리고뉴클레오티드보다 더 긴 작용의 지속시간을 나타낸다는 것을 보여준다.
표 71
형질전환 마우스 중 혈장
트리글리세라이드
및
APOC
-III 단백질 수준
실시예
80:
GalNAc
3
콘주게이트를
포함하는 알파-1
항트립신(A1AT)을
표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기의 표 72에서 열거된 올리고뉴클레오티드는 마우스에서 A1AT 의투여량-의존적 억제에 대한 연구에서 시험되었다.
표 72
A1AT을
표적으로 하는 변형된
ASO
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, 그리고 GalNAc3-13a의 구조는 실시예 62에서 나타나 있다.
치료
6 주령, 수컷 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME) 각각에게 피하로 주당 1회 하기에서 보여진 투여량으로, 총 3 회 투여량 동안, 표 72에서 열거된 올리고뉴클레오티드 또는 PBS가 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 72 시간 후에 희생되었다. A1AT 간 mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc. Eugene, OR)을 사용하여 측정되었다. A1AT 혈장 단백질 수준은 마우스 알파 1-항트립신 ELISA을 사용하여 결정되었다 (카탈로그 # 41-A1AMS-E01, Alpco, Salem, NH). 하기의 결과는 PBS 대조군에 대해 정규화된 각 처리 그룹에 대한 A1AT 간 mRNA 및 혈장 단백질 수준의 평균 퍼센트로부터 나타낸다.
표 73에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 A1AT 간 mRNA 및 A1AT 혈장 단백질 수준을 감소시켰다. GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 모 (ISIS 476366)보다 유의미하게 더 강했다.
표 73
A1AT
간
mRNA
및 혈장 단백질 수준
혈장 중 간 트랜스아미나제 및 BUN 수준은 표준 프로토콜을 사용하여 희생 시에 측정되었다. 체중 및 장기 중량이 또한 측정되었다. 결과는 하기의 표 74에서 보여진다. 체중은 기준선에 대한 %로서 보여진다. 장기 중량은 PBS 대조군 그룹에 대한 체중의 %로서 보여진다.
표 74
실시예
81:
GalNAc
3
클러스터를 포함하는
A1AT을
표적으로 하는 올리고뉴클레오티드의
생체내
작용의 지속시간
표 72에서 열거된 올리고뉴클레오티드는 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
치료
6 주령, 수컷 C57BL/6 마우스 각각에게 표 72에서 열거된 올리고뉴클레오티드 또는 PBS를 피하로 1 회 주입했다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 혈액을 투여 전날에 취하여 기준선을 결정했고 투여 후 5, 12, 19, 및 25 일에서 결정했다. 혈장 A1AT 단백질 수준은 ELISA을 통해 측정되었다 (참고 실시예 80). 하기의 결과는 기준선 수준에 대해 정규화된 각 처리 그룹에 대한 혈장 A1AT 단백질 수준의 평균 퍼센트로서 나타낸다. 이 결과는, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드가 더 강했고 GalNAc 콘주게이트 (ISIS 476366) 없는 모보다 더 긴 작용의 지속시간을 가졌다는 것을 보여준다. 더욱이, 5'-GalNAc 콘주게이트 (ISIS 678381, 678382, 678383, 및 678384)을 포함하는 올리고뉴클레오티드는 3'-GalNAc 콘주게이트 (ISIS 656326)을 포함하는 올리고뉴클레오티드보다 더욱 더 긴 작용의 지속시간과 함께 일반적으로 더욱 더 강했다.
표 75
마우스 중 혈장
A1AT
단백질 수준
실시예
82:
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는
올리고뉴
클레오티드에 의한
시험관내
안티센스
억제
일차 마우스 간 간세포는 96 웰 플레이트에서 15,000 세포/웰에서 처리 2시간 전에 씨딩되었다. 표 76에서 열거된 올리고뉴클레오티드는 2, 10, 50, 또는 250 nM에서 Williams E 배지에서 부가되었고 세포는 밤새 37 oC에서 5% CO2에서 인큐베이션되었다. 세포는 올리고뉴클레오티드 부가 다음 16 시간 동안 용해되었고, 총 RNA는 RNease 3000 BioRobot (Qiagen)를 사용하여 정제되었다. SRB-1 mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc. Eugene, OR)을 사용하여 측정되었다. IC50 값은 Prism 4 소프트웨어 (GraphPad)를 사용하여 측정되었다. 이 결과는, 다양한 상이한 GalNAc 콘주게이트 그룹 및 다양한 상이한 절단가능 모이어티를 포함하는 올리고뉴클레오티드가 GalNAc 콘주게이트 그룹 (ISIS 353382 및 666841)이 없는 모 올리고뉴클레오티드보다 시험관내 유리 흡수 실험에서 유의미하게 더 강하다는 것을 보여준다.
표 76
시험관내
SRB
-1 발현의 억제
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-5a의 구조는 실시예 49에서 나타나 있고, GalNAc3-6a의 구조는 실시예 51에서 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 나타나 있고, GalNAc3-8a의 구조는 실시예 47에서 나타나 있고, GalNAc3-9a의 구조는 실시예 52에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, GalNAc3-12a의 구조는 실시예 61에서 나타나 있고, GalNAc3-13a의 구조는 실시예 62에서 나타나 있고, GalNAc3-14a의 구조는 실시예 63에서 나타나 있고, GalNAc3-15a의 구조는 실시예 64에서 나타나 있고, GalNAc3-17a의 구조는 실시예 68에서 나타나 있고, GalNAc3-18a의 구조는 실시예 69에서 나타나 있고, GalNAc3-19a의 구조는 실시예 70에서 나타나 있고, GalNAc3-20a의 구조는 실시예 71에서 나타나 있고, GalNAc3-23a의 구조는 실시예 76에서 나타나 있다.
실시예
83:
GalNAc
3
클러스터를 포함하는 인자 XI를 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기의 표 77에서 열거된 올리고뉴클레오티드는 마우스에서 인자 XI의 투여량-의존적 억제에 대한 연구에서 시험되었다.
표 77
인자 XI를 표적으로 하는 변형된 올리고뉴클레오티드
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, 그리고 GalNAc3-13a의 구조는 실시예 62에서 나타나 있다.
치료
6 내지 8 주령 마우스 각각에게 피하로 주당 1회 하기에서 보여진 투여량으로, 총 3 회 투여량 동안, 하기에서 열거된 올리고뉴클레오티드는 또는 PBS가 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스를 최종 투여로부터 72시간 후 희생시켰다. 인자 XI 간 mRNA 수준은 실시간 PCR을 사용하여 측정되었고 표준 프로토콜에 따라 사이클로필린에 대해 정규화되었다. 간 트랜스아미나제, BUN, 및 빌리루빈이 또한 측정되었다. 하기의 결과는 PBS 대조군에 대해 정규화된 각 처리 그룹에 대한 평균 퍼센트로서 나타낸다.
표 78에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 인자 XI 간 mRNA를 감소시켰다. 이 결과는, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트 (ISIS 404071)가 없는 모보다 더 강했다는 것을 보여준다. 더욱이, 5'-GalNAc 콘주게이트 (ISIS 663086, 678347, 678348, 및 678349)을 포함하는 올리고뉴클레오티드는 3'-GalNAc 콘주게이트 (ISIS 656173)을 포함하는 올리고뉴클레오티드보다 더욱 더 강했다.
표 78
인자 XI 간
mRNA
, 간 트랜스아미나제, BUN, 및 빌리루빈 수준
실시예
84:
GalNAc
3
콘주게이트를
포함하는 인자 XI를 표적으로 하는 올리고뉴클레오티드의
생체내
작용의 지속시간
표 77에서 열거된 올리고뉴클레오티드는 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
치료
6 내지 8 주령 마우스 각각에게 표 77에서 열거된 올리고뉴클레오티드 또는 PBS를 피하로 1 회 주입했다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 혈액을 투여 전날에 꼬리 채혈에 의해 취해서 기준선을 결정하고 투여 후 3, 10, 및 17 일에서 측정했다. 혈장 인자 XI 단백질 수준은 인자 XI 포획 및 바이오티닐화된 검출 항체 (R & D SYSTEMS, Minneapolis, MN (카탈로그 # AF2460 및 # BAF2460, 각각)) 및 OptEIA 시약 세트 B (카탈로그 # 550534, BD Biosciences, San Jose, CA)를 사용하여 ELISA에 의해 측정되었다. 하기의 결과는 기준선 수준에 대해 정규화된 각 처리 그룹에 대한 혈장 인자 XI 단백질 수준의 평균 퍼센트로서 나타낸다. 이 결과는, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드가 GalNAc 콘주게이트 (ISIS 404071) 없는 모보다 더 긴 작용의 지속시간과 함께 더 강했다는 것을 보여준다. 더욱이, 5'-GalNAc 콘주게이트 (ISIS 663086, 678347, 678348, 및 678349)을 포함하는 올리고뉴클레오티드는 3'-GalNAc 콘주게이트 (ISIS 656173)을 포함하는 올리고뉴클레오티드보다 더욱 더 긴 작용의 지속시간과 함께 더 더욱 더 강했다.
표 79
마우스 중 혈장 인자 XI 단백질 수준
실시예
85:
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
표 76에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
치료
6 내지 8 주령 C57BL/6 마우스 각각에게 피하로 주당 1회 하기에서 보여진 투여량으로, 총 3 회 투여량 동안, 표 76에서 열거된 올리고뉴클레오티드 또는 염수가 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 후 48 시간에 희생되었고 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하여 SRB-1 mRNA 수준을 측정했다 (Molecular Probes, Inc. Eugene, OR). 하기의 결과는 염수 대조군으로 정규화된 각 처리 그룹에 대한 간 SRB-1 mRNA 수준의 평균 퍼센트로서 나타낸다.
표 80 ?? 81에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 SRB-1 mRNA 수준을 감소시켰다.
표 80
간 중
SRB
-1
mRNA
표 81
간 중
SRB
-1
mRNA
간 트랜스아미나제 수준, 총 빌리루빈, BUN, 및 체중은 표준 프로토콜을 사용하여 또한 측정되었다. 각 처리 그룹의 평균 값은 하기의 표 82에서 보여진다.
표 82
실시예
86:
GalNAc
3
클러스터를 포함하는
TTR를
표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기의 표 83에서 열거된 올리고뉴클레오티드는 인간 TTR 유전자를 발현시키는 형질전환 마우스에서 인간 트랜스티레틴 (TTR)의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
치료
8 주령 TTR 형질전환 마우스 각각에게 피하로 주당 1회 3 주 동안, 총 3 회 투여량 동안, 하기의 표에서 열거된 올리고뉴클레오티드 및 투여량 또는 PBS가 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 72 시간 후에 희생되었다. 꼬리 채혈은 실험을 통해 다양한 시점에서 수행되었고, 혈장 TTR 단백질, ALT, 및 AST 수준은 측정되고 표 85-87에서 보고되었다. 상기 동물이 희생된 후, 혈장 ALT, AST, 및 인간 TTR 수준은 체중, 장기 중량, 및 간 인간 TTR mRNA 수준에서와 같이 측정되었다. TTR 단백질 수준은 임상 분석기 (AU480, Beckman Coulter, CA)를 사용하여 측정되었다. 간 인간 TTR mRNA 수준을 측정하기 위하여 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하였다 (Molecular Probes, Inc. Eugene, OR). 표 84-87에서 제공된 결과는 각 처리 그룹의 평균 값이다. mRNA 수준은 PBS 그룹의 평균에 대한 평균 값이다. 혈장 단백질 수준은 기준선에서 PBS 그룹의 평균 값에 대한 평균 값이다. 체중은 각 개별적인 처리 그룹에 대한 희생까지 기준선으로부터의 평균 퍼센트 체중 변화이다. 보여진 장기 중량은 동물의 체중으로 정규화되고, 그 다음 각 처리 그룹의 평균 정규화된 장기 중량은 PBS 그룹의 평균 정규화된 장기 중량에 대해 나타낸다.
표 84 내지 87에서, "BL"는 제 1 투여량 직전에 취한 기준선, 측정을 나타낸다. 표 84 ?? 85에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 TTR 발현 수준을 감소시켰다. GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트 (ISIS 420915)가 없는 모보다 더 강했다. 더욱이, GalNAc 콘주게이트 및 혼합된 PS/PO 뉴클레오시드간 연결를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트 및 완벽한 PS 연결을 포함하는 올리고뉴클레오티드.
표 83
인간
TTR을
표적으로 하는 올리고뉴클레오티드
표 85에 대한 범례는 실시예 74에서 발견될 수 있다. "GalNAc3-1"의 구조가 실시예 9에 나타나 있다. “GalNAc3-3a"의 구조가 실시예 39에 나타나 있다. “GalNAc3-7a"의 구조가 실시예 48에 나타나 있다. “GalNAc3-10a"의 구조가 실시예 46에 나타나 있다. “GalNAc3-13a"의 구조가 실시예 62에 나타나 있다. “GalNAc3-19a"의 구조가 실시예 70에 나타나 있다.
표 84
생체내
인간
TTR의
안티센스
억제
표 85
생체내
인간
TTR의
안티센스
억제
표 86
트랜스아미나제
수준, 체중 변화, 및 장기 중량
표 87
트랜스아미나제
수준, 체중 변화, 및 장기 중량
실시예
87:
GalNAc
3
클러스터를 포함하는
TTR을
표적으로 하는 올리고뉴클레오티드의 단회 투여량에 의한
생체내
작용의 지속시간
ISIS 번호 420915 및 660261 (참고 표 83)은 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다. ISIS 번호 420915, 682883, 및 682885 (참고 표 83)은 또한 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
치료
인간 TTR을 발현시키는 8 주령, 수컷 형질전환 마우스 각각에게 100 mg/kg ISIS 번호 420915 또는 13.5 mg/kg ISIS 번호 660261가 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 꼬리 채혈은 투여 전에 수행되어 기준선을 결정했고 투여 3, 7, 10, 17, 24, 및 39 일 후에 측정했다. 혈장 TTR 단백질 수준은 실시예 86에서 기재된 바와 같이 측정되었다. 하기의 결과는 기준선 수준에 대해 정규화된 각 처리 그룹에 대한 혈장 TTR 수준의 평균 퍼센트로서 나타낸다.
표 88
혈장
TTR
단백질 수준
치료
인간 TTR을 발현시키는 암컷 형질전환 마우스 각각에게 100 mg/kg ISIS 번호 420915, 10.0 mg/kg ISIS 번호 682883, 또는 10.0 mg/kg 682885가 피하로 한번 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 꼬리 채혈은 투여 전에 수행되어 기준선을 결정했고 투여 3, 7, 10, 17, 24, 및 39 일 후에 측정했다. 혈장 TTR 단백질 수준은 실시예 86에서 기재된 바와 같이 측정되었다. 하기의 결과는 기준선 수준에 대해 정규화된 각 처리 그룹에 대한 혈장 TTR 수준의 평균 퍼센트로서 나타낸다.
표 89
혈장
TTR
단백질 수준
표 88 및 89의 결과는, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드가 콘주게이트가 없는 모 올리고뉴클레오티드 (ISIS 420915)보다 더 긴 지속시간과 함께 더 강하다는 것을 보여준다.
실시예
88:
GalNAc
3
콘주게이트를
포함하는
SMN을
표적으로 하는 올리고뉴클레오티드에 의한
생체내
스플라이싱
조절
표 90에서 열거된 올리고뉴클레오티드는 마우스에서 운동 뉴런 (SMN)의 인간 생존의 스플라이싱 조절에 대해 시험되었다.
표 90
SMN를
표적으로 하는 변형된
ASO
"GalNAc3-7a"의 구조가 이미 실시예 48에 나타나 있다. "X"는 Gene Tools (Philomath, OR)에 의해 산출된 5' 일차 아민을 나타내고, GalNAc3-7b는 이하에서 보여진 바와 같은 링커의 -NH-C6-O 부분이 없는 GalNAc3-7a의 구조를 나타낸다:
ISIS 번호 703421 및 703422는 모플리노 올리고뉴클레오티드이고, 여기서 2 개의 올리고뉴클레오티드의 각 뉴클레오티드는 모폴리노 뉴클레오티드이다.
치료
인간 SMN를 발현시키는 6 주령 형질전환 마우스는 표 91에서 열거된 올리고뉴클레오티드 또는 염수가 피하로 한번 주입되었다. 각 처리 그룹은 2 마리 수컷 및 2 마리 암컷으로 구성되었다. 마우스는 투여 3 일 후에 희생되어 표준 프로토콜에 따라 실시간 PCR을 사용하여 엑손 7 유무에 따른 간 인간 SMN mRNA 수준을 측정했다. 총 RNA는 리보그린 시약을 사용하여 측정되었다. SMN mRNA 수준은 총 mRNA로 정규화되었고, 염수 처리 그룹의 평균으로 추가로 정규화되었다. 엑손 7 포함 SMN mRNA 대 엑손 7 누락 SMN mRNA의 수득한 평균 비는 표 91에서 보여진다. 이 결과는, 스플라이싱을 조절하고 GalNAc 콘주게이트를 포함하는 완전히 변형된 올리고뉴클레오티드가 GlaNAc 콘주게이트가 없는 모 올리고뉴클레오티드보다 간에서 스플라이싱을 변경할 때 유의미하게 더 강하다는 것을 보여준다. 더욱이, 이러한 추세는 2'-MOE 및 모폴리노 변형된 올리고뉴클레오티드를 포함하는 다중 변형 화학을 위해 유지된다.
표 91
생체내
에서
인간
SMN을
표적으로 하는 올리고뉴클레오티드의 효과
실시예
89:
GalNAc
3
콘주게이트를
포함하는
아포지질단백질
A (
아포
(a))을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기의 표 92에서 열거된 올리고뉴클레오티드는 형질전환 마우스에서 아포(a)의 투여량-의존적 억제에 대한 연구에서 시험되었다.
표 92
아포(a)를
표적으로 하는 변형된
ASO
“GalNAc3-7a"의 구조가 실시예 48에 나타나 있다.
치료
8 주령, 암컷 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME) 각각에게 피하로 주당 1회 하기에서 보여진 투여량으로, 총 6 번 투여량 동안에, 표 92에서 열거된 올리고뉴클레오티드 또는 PBS가 주입되었다. 각 처리 그룹은 3 내지 4 마리의 동물로 구성되었다. 꼬리 채혈은 제 1 투여량 전날에 및 각 투여량 다음 매주 수행되어 혈장 아포(a) 단백질 수준을 측정했다. 마우스는 최종 투여 2 일 후에 희생되었다. 아포(a) 간 mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc. Eugene, OR)을 사용하여 측정되었다. 아포(a) 혈장 단백질 수준은 ELISA를 사용하여 측정되었고, 간 트랜스아미나제 수준이 측정되었다. 표 93의 mRNA 및 혈장 단백질 결과는 PBS 처리된 그룹에 대한 처리 그룹 평균 퍼센트로서 나타낸다. 혈장 단백질 수준은 PBS 그룹의 기준선 (BL) 값으로 추가로 정규화되었다. 평균 절대적인 트랜스아미나제 수준 및 체중 (기준선 평균에 대한 %)은 표 94에서 보고된다.
표 93에서 실증된 바와 같이, 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 아포(a) 간 mRNA 및 혈장 단백질 수준을 감소시켰다. 더욱이, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트가 없는 모 올리고뉴클레오티드보다 더 긴 작용의 지속시간과 함께 유의미하게 더 강했다. 표 94에서 실증된 바와 같이, 트랜스아미나제 수준 및 체중은 올리고뉴클레오티드에 의해 영향을 받지 않았고, 이것은, 올리고뉴클레오티드가 잘 용인되었다는 것을 나타낸다.
표 93
아포
(a) 간
mRNA
및 혈장 단백질 수준
표 94
실시예
90:
GalNAc
3
클러스터를 포함하는
TTR를
표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
하기의 표 95에서 열거된 올리고뉴클레오티드는 인간 TTR 유전자를 발현시키는 형질전환 마우스에서 인간 트랜스티레틴 (TTR)의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
치료
TTR 형질전환 마우스 각각에게 피하로 주당 1회 3 주 동안, 총 3 회 투여량 동안, 표 96에서 열거된 올리고뉴클레오티드 및 투여량 또는 PBS이 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 제 1 투여량 전에, 꼬리 채혈이 수행되어 기준선 (BL)에서 혈장 TTR 단백질 수준을 측정했다. 마우스는 최종 투여 72 시간 후에 희생되었다. TTR 단백질 수준은 임상 분석기 (AU480, Beckman Coulter, CA)를 사용하여 측정되었다. 간 인간 TTR mRNA 수준을 측정하기 위하여 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약을 사용하였다 (Molecular Probes, Inc. Eugene, OR) . 표 96에서 제공된 결과는 각 처리 그룹의 평균 값이다. mRNA 수준은 PBS 그룹의 평균에 대한 평균 값이다. 혈장 단백질 수준은 기준선에서 PBS 그룹의 평균 값에 대한 평균 값이다. "BL"는 제 1 투여량 직전에 취한 기준선, 측정을 나타낸다. 표 96에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 TTR 발현 수준을 감소시켰다. GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트 (ISIS 420915)가 없는 모보다 더 강했고, 포스포디에스테르 또는 데옥시아데노신 절단가능 모이어티를 포함하는 올리고뉴클레오티드는 콘주게이트가 없는 모체와 비교하여 효능의 유의미한 개선을 보여주었다 (참고 ISIS 번호 682883 및 666943 vs 420915 및 실시예 86 및 87 참고).
표 95
인간
TTR을
표적으로 하는 올리고뉴클레오티드
표 95에 대한 범례는 실시예 74에서 발견될 수 있다. “GalNAc3-3a"의 구조가 실시예 39에 나타나 있다. “GalNAc3-7a"의 구조가 실시예 48에 나타나 있다. “GalNAc3-10a"의 구조가 실시예 46에 나타나 있다. “GalNAc3-13a"의 구조가 실시예 62에 나타나 있다.
표 96
생체내
인간
TTR의
안티센스
억제
실시예
91: 비-인간 영장류에서
GalNAc3
콘주게이트를
포함하는 인자 VII를 표적으로 하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
하기의 표 97에서 열거된 올리고뉴클레오티드는 원숭이에서 인자 VII의 안티센스 억제에 대해 비-말단, 투여량 단계적 확대 연구에서 시험되었다.
치료
비-나이브 원숭이 각각에게 0, 15, 및 29일에 상승하는 투여량의 표 97에서 열거된 올리고뉴클레오티드 또는 PBS가 피하로 주입되었다. 각 처리 그룹은 4 마리의 수컷 및 1 마리의 암컷으로 구성되었다. 제 1 투여량 전에 및 그 후 다양한 시점에서, 채혈이 수행되어 혈장 인자 VII 단백질 수준을 측정했다. 인자 VII 단백질 수준은 ELISA에 의해 측정되었다. 표 98에서 제공된 결과는 기준선 (BL)에서 PBS 그룹의 평균 값에 대한 각 처리 그룹의 평균 값이고, 상기 측정은 제 1 투여량 직전에 취해졌다. 표 98에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식으로 인자 VII 발현 수준을 감소시켰고, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트가 없는 올리고뉴클레오티드와 비교하여 원숭이에서 유의미하게 더 강했다.
표 97
인자 VII을 표적으로 하는 올리고뉴클레오티드
표 97에 대한 범례는 실시예 74에서 발견될 수 있다. “GalNAc3-10a"의 구조가 실시예 46에 나타나 있다.
표 98
인자 VII 혈장 단백질 수준
실시예
92:
GalNAc
3
콘주게이트를
포함하는
Apo
-
CIII을
표적으로 하는
안티센스
올리고뉴클레오티드에 의한 일차 간세포에서의
안티센스
억제
일차 마우스 간세포는 15,000 세포/웰에서 96-웰 플레이트에서 씨딩되었고, 마우스 ApoC-III을 표적으로 하는, 표 99에서 열거된 올리고뉴클레오티드는, 0.46, 1.37, 4.12, 또는 12.35, 37.04, 111.11, 또는 333.33 nM 또는 1.00 μm에서 부가되었다. 24 시간 동안 올리고뉴클레오티드와 함께 인큐베이션한 후, 세포는 용해되었고 총 RNA는 RNeasy (Qiagen)를 사용하여 정제되었다. ApoC-III mRNA 수준은 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc.)을 사용하여 측정되었다. IC50 값은 Prism 4 소프트웨어 (GraphPad)를 사용하여 측정되었다. 이 결과는, 절단가능 모이어티가 포스포디에스테르 또는 포스포디에스테르-연결된 데옥시아데노신인 지와는 무관하게, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 콘주게이트가 없는 모 올리고뉴클레오티드보다 유의미하게 더 강했다는 것을 보여준다.
표 99
마우스 일차 간세포 중 마우스
APOC
-III 발현의 억제
GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 나타나 있고, GalNAc3-10a의 구조는 실시예 46에서 나타나 있고, GalNAc3-13a의 구조는 실시예 62에서 나타나 있고, 그리고 GalNAc3-19a의 구조는 실시예 70에서 나타나 있다.
실시예
93: 혼합된 윙 및 5'-
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
표 100에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
표 100
SRB
-1을 표적으로 하는 변형된
ASO
GalNAc3-3a의 구조는 이미 실시예 39에서 나타나 있고, GalNAc3-7a의 구조는 이미 실시예 48에서 나타나 있다. 하첨자: "e"는 2'-MOE 변형된 뉴클레오시드를 나타내고; "d"는 β-D-2'-데옥시리보뉴클레오시드를 나타내고; "k"는 6'-(S)-CH3 이환식 뉴클레오시드 (cEt)를 나타내고; "s"는 포스포로티오에이트 뉴클레오시드간 연결 (PS)을 나타내고; "o"는 포스포디에스테르 뉴클레오시드간 연결 (PO)를 나타낸다. 상첨자 "m"은 5-메틸시토신을 나타낸다.
치료
6 내지 8 주령 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 표 100에서 열거된 올리고뉴클레오티드 또는 염수가 하기에서 보여진 투여량으로 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 72 시간 후에 희생되었다. 간 SRB-1 mRNA 수준은 실시간 PCR를 사용하여 측정되었다. SRB-1 mRNA 수준은 표준 프로토콜에 따라 사이클로필린 mRNA 수준에 대해 정규화되었다. 결과는 염수 대조군 그룹에 대한 각 처리 그룹을 위해 SRB-1 mRNA 수준의 평균 퍼센트로서 제공된다. 표 101에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식으로 SRB-1 mRNA 수준을 감소시켰고, GalNAc 콘주게이트를 포함하고 완전한 cEt 또는 혼합된 당 변형이었던 윙을 갖는 갭머 올리고뉴클레오티드는 콘주게이트가 없고 완전한 cEt 변형된 윙을 포함하는 모 올리고뉴클레오티드보다 유의미하게 더 강했다.
체중, 간 트랜스아미나제, 총 빌리루빈, 및 BUN가 또한 측정되었고, 각 처리 그룹에 대한 평균 값은 표 101에서 보여진다. 체중은 올리고뉴클레오티드 투여량 직전에 측정된 기준선 체중 (% BL)에 대한 평균 퍼센트 체중로서 보여진다.
표 101
SRB
-1
mRNA
, ALT,
AST
, BUN, 및 총 빌리루빈 수준 및 체중
실시예
94: 2'
-당 변형 및 5'-
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
표 102에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
표 102
SRB
-1을 표적으로 하는 변형된
ASO
하첨자 "m"은 2'-O-메틸 변형된 뉴클레오시드를 나타낸다. 완전한 표 범례에 대한 실시예 74 참고. GalNAc3-3a의 구조는 실시예 39에서 이미 나타나 있고, GalNAc3-7a의 구조는 이미 실시예 48에서 나타나 있다.
치료
이러한 연구는 실시예 93에서 기재된 프로토콜을 사용하여 완료되었다. 결과는 하기의 표 103에서 보여지고 GalNAc 콘주게이트를 포함하는 2'-MOE 및 2'-OMe 변형된 올리고뉴클레오티드 둘 모두가 콘주게이트가 없는 각 모 올리고뉴클레오티드보다 유의미하게 더 강했다는 것을 보여준다. 체중, 간 트랜스아미나제, 총 빌리루빈, 및 BUN 측정의 결과는, 모든 화합물이 용인되었다는 것을 명시했다.
표 103
SRB
-1
mRNA
실시예
95: 이환식 뉴클레오시드 및 5'-
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
표 104에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
표 104
SRB
-1을 표적으로 하는 변형된
ASO
하첨자 "g"는 플루오로-HNA 뉴클레오시드를 나타내고, 하첨자 "l"는 2'-O-CH2-4'가교를 포함하는 잠겨진 뉴클레오시드를 나타낸다. 다른 약어에 대한 실시예 74 표 범례 참고. GalNAc3-1a의 구조는 실시예 9에서 이미 나타나 있고, GalNAc3-3a의 구조는 실시예 39에서 이미 나타나 있고, GalNAc3-7a의 구조는 실시예 48에서 이미 나타나 있다.
치료
이러한 연구는 실시예 93에서 기재된 프로토콜을 사용하여 완료되었다. 결과는 하기의 표 105에서 보여지고 GalNAc 콘주게이트 및 다양한 이환식 뉴클레오시드 변형을 포함하는 올리고뉴클레오티드가 콘주게이트가 없고 이환식 뉴클레오시드 변형을 포함하는 모 올리고뉴클레오티드보다 유의미하게 더 강했다는 것을 보여준다. 더욱이, GalNAc 콘주게이트 및 플루오로-HNA 변형을 포함하는 올리고뉴클레오티드는 콘주게이트가 없고 플루오로-HNA 변형을 포함하는 모 올리고뉴클레오티드보다 유의미하게 더 강했다. 체중, 간 트랜스아미나제, 총 빌리루빈, 및 BUN 측정의 결과는, 모든 화합물이 용인되었다는 것을 명시했다.
표 105
SRB
-1
mRNA
, ALT,
AST
, BUN, 및 총 빌리루빈 수준 및 체중
실시예
96:
GalNAc
3
콘주게이트
그룹을 포함하는
안티센스
올리고뉴클레오티드의 혈장 단백질 결합
ApoC-III을 표적으로 하는 표 70에서 열거된 올리고뉴클레오티드 및 아포(a)을 표적으로 하는 표 106에서의 올리고뉴클레오티드는 한외여과 검정에서 시험되어 혈장 단백질 결합을 평가했다.
표 106
아포(a)을
표적으로 하는 변형된 올리고뉴클레오티드
표 범례에 대한 실시예 74 참조. "GalNAc3-7a"의 구조가 이미 실시예 48에 나타나 있다.
Ultrafree-MC 한외여과 장치 (30,000 NMWL, 저-결합 재생된 셀룰로오스 막, 밀리포어, Bedford, MA)을 300 μL의 0.5% Tween 80으로 전-컨디셔닝하고 10 분 동안 2000 g에서 원심분리하고, 그 다음 H2O 중 대조 올리고뉴클레오티드의 300μL의 300 μg/mL 용액으로 전-컨디셔닝하고 16 분 동안 2000 g에서 원심분리했다. 본 연구에서 사용될 표 70 및 106으로부터의 각 시험 올리고뉴클레오티드의 필터에 대한 비-특이적 결합을 평가하기 위해, H2O 중 올리고뉴클레오티드의 300 μL의 250 ng/mL 용액을 pH 7.4에서 전-컨디셔닝된 필터 내에 두었고 16 분 동안 2000 g에서 원심분리했다. 비여과된 및 여과된 샘플을 ELISA 검정로 분석하여 올리고뉴클레오티드 농도를 측정했다. 3개의 복제물을 사용하여 각 샘플에 대한 평균 농도를 얻었다. 미여과된 샘플에 대한 여과된 샘플의 평균 농도를 사용하여 혈장의 부재에서 필터를 통해 회수된 올리고뉴클레오티드의 퍼센트를 결정한다 (% 회수율).
정상, 무약물 인간 지원자, 시노몰구스 원숭이, 및 CD-1 마우스로부터의 K3-EDTA에서 수집된 냉동된 전체의 혈장 샘플을, Bioreclamation LLC (Westbury, NY)로부터 구매했다. 시험 올리고뉴클레오티드를 1.2 mL 분취량의 혈장에 2 개의 농도 (5 및 150 μg/mL)에서 부가했다. 분취량 (300 μL)의 각 스파이킹된 혈장 샘플을 전-컨디셔닝된 필터 장치에 내에 두고 37°에서 30 분 동안 인큐베이션하고, 즉시 그 다음 2000 g에서 16 분 동안 원심분리했다. 분취량의 여과된 및 미여과된 스파이킹된 혈장 샘플을 ELISA로 분석하여 각 샘플 중 올리고뉴클레오티드 농도를 측정했다. 농도 당 3 개의 복제물을 사용된 각 샘플 중 결합된 및 미결합된 올리고뉴클레오티드의 평균 백분율을 측정했다. 미여과된 샘플의 농도에 대한 여과된 샘플의 평균 농도는 사용되어 혈장 단백질에 결합되지 않는 혈장(미결합된 %) 중 올리고뉴클레오티드의 퍼센트를 측정한다. 최종 미결합된 올리고뉴클레오티드 값은 각 올리고뉴클레오티드에 대해 % 미결합된 %를 % 회수율로 나누어서 비-특이적 결합을 위해 수정된다. 최종 % 결합된 올리고뉴클레오티드 값은 100에서 최종 % 미결합된 값을 빼서 결정된다. 결과는 각 종의 혈장에서 시험된2 개의 올리고뉴클레오티드의 농도 시험 (5 및 150 μg/mL)에 대해 표 107에서 보여진다. 이 결과는, GalNAc 콘주게이트 그룹이 혈장 단백질 결합에 대한 유의미한 영향을 갖지 않는다는 것을 보여준다. 더욱이, 완벽한 PS 뉴클레오시드간 연결 및 혼합된 PO/PS 연결 둘 모두를 갖는 올리고뉴클레오티드는 혈장 단백질에 결합하고, 완벽한 PS 연결을 갖는 것은 혼합된 PO/PS 연결을 갖는 것보다 어느 정도 더 큰 정도로 혈장 단백질에 결합한다.
표 107
혈장 단백질에
결합된
변형된 올리고뉴클레오티드의 퍼센트
실시예
97:
GalNAc
3
콘주게이트
그룹을 포함하는
TTR을
표적으로 하는 변형된 올리고뉴클레오티드
GalNAc 콘주게이트를 포함하는 표 108에서 보여진 올리고뉴클레오티드는 설계되어 TTR을 표적으로 했다.
표 108
TTR을
표적으로 하는 변형된 올리고뉴클레오티드
표 108에 대한 범례는 실시예 74에서 발견될 수 있다. "GalNAc3-1"의 구조가 실시예 9에 나타나 있다. “GalNAc3-3a"의 구조가 실시예 39에 나타나 있다. “GalNAc3-7a"의 구조가 실시예 48에 나타나 있다. “GalNAc3-10a"의 구조가 실시예 46에 나타나 있다. “GalNAc3-13a"의 구조가 실시예 62에 나타나 있다. “GalNAc3-19a"의 구조가 실시예 70에 나타나 있다.
실시예
98:
hPMBC
검정에서
GalNAc
콘주게이트를
포함하는 올리고뉴클레오티드의 전-염증 효과의 평가
표 109에서 열거된 올리고뉴클레오티드는 실시예 23 및 24에서 기재된 바와 같이 hPMBC 검정에서 전-염증 효과에 대해 시험되었다. (올리고뉴클레오티드의 기술에 대하여, 표 30, 83, 95, 및 108 참고). ISIS 353512는 양성 대조군으로서 사용된 고반응군이고, 다른 올리고뉴클레오티드는 표 83, 95, 및 108에서 기재되어 있다. 표 109에서 보여진 이러한 결과는 하나의 지원자 공여체로부터의 혈액을 사용하여 수득되었다. 이 결과는, 혼합된 PO/PS 뉴클레오시드간 연결을 갖는 올리고뉴클레오티드가 완벽한 PS 연결을 갖는 동일한 올리고뉴클레오티드와 비교하여 유의미하게 더 낮은 전-염증 반응을 생산했다는 것을 보여준다. 더욱이, GalNAc 콘주게이트 그룹은 이러한 검정에서 유의미한 효과를 가지지 않았다.
표 109
실시예
99:
아시알로당단백질
수용체에 대한
GalNAc
콘주게이트를
포함하는 올리고뉴클레오티드의 결합 친화성
아시알로당단백질 수용체에 대한 표 110에서 열거된 올리고뉴클레오티드의 결합 친화성 (올리고뉴클레오티드의 설명에 대한 표 76 참고)은 경쟁적 수용체 결합 검정에서 시험되었다. 경쟁자 리간드, α1-산 당단백질 (AGP)는, 50 mM 나트륨 아세테이트 버퍼 (pH 5)에서 1 U 뉴라미니다제-아가로스와 함께 16 시간 동안 37℃에서 인큐베이션되었고, > 90% 탈시알릴화는 시알산 검정 또는 크기 배제 크로마토그래피 (SEC)에 의해 확인되었다. 요오드 모노클로라이드는 사용되어 Atsma 등에 의한 절차에 따라 AGP를 요오드화했다 (참고: J Lipid Res. 1991 Jan; 32(1):173-81). 이러한 방법에서, 탈시알릴화된 α1-산 당단백질 (de-AGP)을 0.25 M NaOH 중 10 mM 염화요오드, Na125I, 및 1 M 글리신에 부가했다. 10 분 동안 실온에서 인큐베이션한 후, 125I -표지된 de-AGP를, 3 KDMWCO 스핀 칼럼을 시용하여 혼합물을 2회 농축하여 유리 125I로부터 분리했다. 단백질을, Agilent SEC-3 칼럼 (7.8x300mm) 및 β-RAM 계수기가 구비된 HPLC 시스템 상에서 표지 효율 및 순도에 대해 시험했다. 125I-표지된 de-AGP 및 ASO를 함유하는 다양한 GalNAc-클러스터를 이용하는 경쟁 실험을 하기와 같이 수행했다. 인간 HepG2 세포 (106 세포/ml)을 2 mL의 적절한 성장 배지에서 6-웰 플레이트 상에서 플레이팅했다. 10% 우태 혈청 (FBS), 2 mM L-글루타민 및 10mM HEPES로 보강된 MEM 배지를 사용했다. 세포를 16-20 시간 동안 37℃에서 5% 및 10% CO2 각각과 함께 인큐베이션했다. 세포를 실험 전에 FBS가 없는 배지로 세정했다. 세포를, 적절한 성장 배지를 2% FBS, 10-8 M 125I-표지된 de-AGP와 함게 함유하는 1ml 경쟁 혼합물 및 10-11 내지 10-5 범위의 농도에서 ASO를 함유하는 GalNAc-클러스터로 30 분 동안 37˚C에서 인큐베이션했다. 비-특이적 결합을 10-2 M GalNAc 당의 존재에서 결정했다. 세포를 FBS가 없는 배지로 2회 세정하여 미결합된 125I-표지된 de-AGP 및 경쟁자 GalNAc ASO를 제거했다. 세포를, 1% β-머캅토에탄올을 함유하는 Qiagen's RLT 버퍼를 사용하여 용해시켰다. 용해물을 짧은 10 분 동결/융해 사이클 후 둥근바닥 검정 튜브로 이동시키고 γ-계수기 상에서 검정했다. 비-특이적 결합을 공제한 후 125I 단백질 카운트를 최저 GalNAc-ASO 농도 카운트의 값으로 나누었다. 억제 곡선 비선형회귀 알고리즘을 사용하는 단일 부위 경쟁적 결합 방정식에 따라 적합화되어 결합 친화성 (KD's)을 계산했다.
표 110의 결과는 5 개의 상이한 날에 수행된 실험으로부터 수득되었다. 상첨자 "a"로 나타낸 올리고뉴클레오티드에 대한 결과는 2 개의 상이한 날에 실험 시행의 평균이다. 이 결과는, 5'-말단 상에 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 3'-말단 상에 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드보다 1.5 내지 16-배 더 큰 친화성을 갖는 인간 HepG2 세포 상에서 아시알로당단백질 수용체를 결합햇다는 것을 보여준다.
표 110
아시알로당단백질
수용체 결합 검정 결과
실시예
100:
생체내
에서
아포(a)
를
표적으로 하는
GalNAc
콘주게이트
그룹을 포함하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
하기의 표 111a에서 열거된 올리고뉴클레오티드는 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
표 111a
아포(a)를
표적으로 하는 변형된
ASO
“GalNAc3-7a"의 구조가 실시예 48에 나타나 있다.
치료
인간 아포(a)을 발현시키는 암컷 형질전환 마우스 각각에게, 피하로 주당 1회, 총 6 번 투여량 동안에, 표 111b에서 열거된 올리고뉴클레오티드 및 투여량 또는 PBS이 주입되었다. 각 처리 그룹은 3 마리의 동물로 구성되었다. 혈액을, 투여 전날에 뽑아서 아포(a) 단백질의 기준선 수준을 혈장에서 그리고 제 1 투여량 다음72 시간, 1 주, 및 2 주에서 측정했다. 추가의 채혈은 제 1 투여량 다음 3 주, 4 주, 5 주, 및 6 주에서 일어날 것이다. 혈장 아포(a) 단백질 수준은 ELISA를 사용하여 측정되었다. 표 111b의 결과는 기준선 수준 (% BL)에 대해 정규화된, 각 처리 그룹에 대한 혈장 아포(a) 단백질 수준의 평균 퍼센트로서 제공되고, 이 결과는, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드가 아포(a) 발현에서 강력한 축소를 나타내었다는 것을 보여준다. 이러한 강력한 효과는 완벽한 PS 뉴클레오시드간 연결을 포함하는 올리고뉴클레오티드 및 혼합된 PO 및 PS 연결을 포함하는 올리고뉴클레오티드에 대해 관찰되었다.
표 111b
아포
(a) 혈장 단백질 수준
실시예
101: 안정한
모이어티를
통해 연결된
GalNAc
클러스터를 포함하는 올리고뉴클레오티드에 의한
안티센스
억제
표 112에서 열거된 올리고뉴클레오티드는 마우스 APOC-III 발현의 억제에 대해 생체내에서 시험되었다. C57Bl/6 마우스 각각에게 표 112에서 열거된 올리고뉴클레오티드 또는 PBS를 피하로 1 회 주입했다. 각 처리 그룹은 4 마리의 동물로 구성되었다. ISIS 440670로 처리된 각각의 마우스는 2, 6, 20, 또는 60 mg/kg의 투여량을 수용했다. ISIS 680772 또는 696847로 처리된 각각의 마우스는 0.6, 2, 6, 또는 20 mg/kg을 수용했다. ISIS 696847의 GalNAc 콘주게이트 그룹은 쉽게 절단가능 포스포디에스테르 함유 연결 대신에 안정한 모이어티, 포스포로티오에이트 연결을 통해 연결된다. 동물은 투여량 후 72 시간에 희생되었다. 간 APOC-III mRNA 수준은 실시간 PCR를 사용하여 측정되었다. APOC-III mRNA 수준은 표준 프로토콜에 따라 사이클로필린 mRNA 수준에 대해 정규화되었다. 결과는 염수 대조군 그룹에 대한 각 처리 그룹을 위해 APOC-III mRNA 수준의 평균 퍼센트로서 표 112에서 제공된다. 이 결과는, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드가 콘주게이트 그룹이 없는 올리고뉴클레오티드보다 유의미하게 더 강했다는 것을 보여준다. 더욱이, 절단가능 모이어티 (ISIS 680772)를 통해 올리고뉴클레오티드에 연결된 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 안정한 모이어티 (ISIS 696847)를 통해 올리고뉴클레오티드에 연결된 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드보다 더욱 더 강했다.
표 112
마우스
APOC
-III를 표적으로 하는 변형된 올리고뉴클레오티드
“GalNAc3-7a"의 구조가 실시예 48에 나타나 있다.
실시예
102:
GalNAc
콘주게이트를
포함하는
안티센스
올리고뉴클레오티드의 간에서의 분포
GalNAc 콘주게이트를 포함하지 않는 ISIS 353382 (참고 표 36) 및 GalNAc 콘주게이트를 포함하는 ISIS 655861 (참고 표 36)의 간 분포는 평가되었다. 수컷 Balb/c 마우스에게 표 113에서 열거된 투여량으로 ISIS 353382 또는 655861을 피하로 1회 주입했다. 각각의 처리 그룹은 2 마리의 동물로 구성된 ISIS 655861에 대한 18 mg/kg 그룹을 제외하고 3 마리의 동물로 구성되었다. 동물을 투여 48 시간 후에 희생시켜 올리고뉴클레오티드의 간 분포를 측정했다. 세포 당 안티센스 올리고뉴클레오티드 분자의 수를 측정하기 위해, 루테늄 (II) 트리스-바이피리딘 태그 (MSD TAG, 중간 규모발견)을 안티센스 올리고뉴클레오티드를 검출하기 위해 사용된 올리고뉴클레오티드 프로브에 콘주게이트된다. 표 113에 존재하는 결과는 세포 당 올리고뉴클레오티드 분자의 수백만 단위로 각 처리 그룹에 대한 올리고뉴클레오티드의 평균 농도이다. 이 결과는, 동등 투여량에서, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드가 GalNAc 콘주게이트를 포함하지 않는 올리고뉴클레오티드보다 전체 간 및 간세포에서 더 높은 농도로 존재한다는 것을 보여준다. 더욱이, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트를 포함하지 않는 올리고뉴클레오티드 보다 더 낮은 비-실질 간 세포 중 농도로 존재했다. 그리고 간세포 및 비-실질 간 세포 중 ISIS 655861의 농도는 세포에 대해 유사했지만, 간은 용적으로 대략 80% 간세포이다. 따라서, 간에 존재했던 대다수의 ISIS 655861 올리고뉴클레오티드는 간세포에서 발견되었고, 반면에 간에 존재했던 대다수의 ISIS 353382 올리고뉴클레오티드는 비-실질 간 세포에서 발견되었다.
표 113
실시예
103:
GalNAc
3
콘주게이트를
포함하는
APOC
-III을 표적으로 하는 올리고뉴클레오티드의
생체내
작용의 지속시간
하기의 표 114에서 열거된 올리고뉴클레오티드는 마우스에서 작용의 지속시간에 대한 단회 투여량 연구에서 시험되었다.
표 114
APOC
-III을 표적으로 하는 변형된
ASO
GalNAc3-3a의 구조는 실시예 39에서 이미 나타나 있고, GalNAc3-19a는 실시예 70에서 나타나 있다.
치료
인간 APOC-III을 발현시키는 암컷 형질전환 마우스 각각에게 표 114에서 열거된 올리고뉴클레오티드 또는 PBS를 피하로 1 회 주입했다. 각 처리 그룹은 3 마리의 동물로 구성되었다. 투여 전에 채혈하여 투여 다음에 기준선 및 3, 7, 14, 21, 28, 35, 및 42 일에서 측정했다. 혈장 트리글리세라이드 및 APOC-III 단백질 수준은 실시예 20에서 기재된 바와 같이 측정되었다. 표 115에서의 결과는 기준선 수준에 대해 정규화된, 각 처리 그룹에 대한 혈장 트리글리세라이드 및 APOC-III 수준의 평균 퍼센트로서 제공된다. 실시예 79의 표 71의 결과와 하기의 표 115의 결과와의 비교는, 포스포디에스테르와 포스포로티오에이트 뉴클레오시드간 연결의 혼합물을 포함하는 올리고뉴클레오티드가 포스포로티오에이트 뉴클레오시드간 연결만을 포함하는 동등한 올리고뉴클레오티드보다 작용의 증가된 지속시간을 나타냈다는 것을 보여준다.
표 115
형질전환 마우스 중 혈장
트리글리세라이드
및
APOC
-III 단백질 수준
실시예
104: 5'
-
GalNAc
2
콘주게이트를
포함하는 올리고뉴클레오티드의 합성
화합물 120은 시판되고 있고, 화합물 126의 합성은 실시예 49에서 기재되어 있다. 화합물 120 (1 g, 2.89 mmol) 및 HBTU (0.39 g, 2.89 mmol) 및 HOBt (1.64 g, 4.33 mmol)를 DMF (10 mL에 용해시키고. N,N-N,N-디이소프로필에틸아민 1.75 mL, 10.1 mmo)을 부가하였다. 약 5 분 후, 아미노헥산산 벤질 에스테르 (1.36 g, 3.46 mmol)을 반응에 부가했다. 3 시간 후, 반응 혼합물을 100 mL의 1 M NaHSO4에 붓고 2 x 50 mL 에틸 아세테이트로 추출했다. 유기 층들을 조합하고 3 x 40 mL 포화 NaHCO3 및 2 x 염수로 세정하고, Na2SO4로 건조시키고, 여과하고 농축했다. 생성물을 실리카겔 칼럼 크로마토그래피 (DCM:EA:Hex, 1:1:1)로 정제하여 화합물 231을 얻었다. LCMS 및 NMR은 구조와 일치했다. 화합물 231 (1.34 g, 2.438 mmol)을 디클로로메탄 (10 mL)에서 용해시키고 트리플루오르아세트산 (10 mL)을 부가했다. 실온에서 2 시간 동안 교반한 후, 반응 혼합물을 감압 하에서 농축하고 톨루엔 (3 x 10 mL)로 공-증발시켰다. 잔류물을 감압 하에서 건조하여 화합물 232을 트리플루오르아세테이트 염으로서 얻었다. 화합물 166의 합성은 실시예 54에서 기재되어 있다. 화합물 166 (3.39 g, 5.40 mmol)을 DMF (3 mL)에서 용해시켰다. 화합물 232 (1.3 g, 2.25 mmol)의 용액을 DMF (3 mL)에서 용해시키고 N,N-디이소프로필에틸아민 (1.55 mL)을 부가했다. 반응을 실온에서 30 분 동안 교반하고, 그 다음 물 (80 mL)에 붓고 수성 층을 EtOAc (2x100 mL)로 추출했다. 유기 상을 분리하고 포화 수성 NaHCO3 (3 x 80 mL), 1 M NaHSO4 (3 x 80 mL) 및 염수 (2 x 80 mL)로 세정하고, 그 다음 건조시키고 (Na2SO4), 여과하고, 농축했다. 잔류물을 실리카겔 칼럼 크로마토그래피로 정제하여 화합물 233을 얻었다. LCMS 및 NMR은 구조와 일치했다. 화합물 233 (0.59 g, 0.48 mmol)을 메탄올 (2.2 mL) 및 에틸 아세테이트 (2.2 mL)에서 용해시켰다. 탄소상 팔라듐 (10 wt% Pd/C, 습성, 0.07 g)을 부가하고, 반응 혼합물을 수소 대기 하에서 3 시간 동안 교반했다. 반응 혼합물을 셀라이트의 패드를 통해 여과하고 농축하여 카복실산을 얻었다. 카복실산 (1.32 g, 1.15 mmol, 클러스터 유리 산)을 DMF (3.2 mL)에서 용해시켰다. 이것에 N,N-디이소프로필에틸아민 (0.3 mL, 1.73 mmol) 및 PFPTFA (0.30 mL, 1.73 mmol)을 부가했다. 실온에서 30 분 교반 후 반응 혼합물을 물 (40 mL)에 붓고 EtOAc (2 x 50 mL)로 추출했다. 표준 워크업은 상기에서 기재된 바와 같이 완료되어 화합물 234를 산출했다. LCMS 및 NMR은 구조와 일치했다. 올리고뉴클레오티드 235는 실시예 46에서 기재된 일반적인 절차를 사용하여 제조되었다. 콘주게이트 그룹 GalNAc2-24의 GalNAc2 클러스터 부분 (GalNAc2-24a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc2-24 (GalNAc2-24a-CM) 의 구조는 하기와 같다:
실시예
105:
GalNAc
1
-25
콘주게이트를
포함하는 올리고뉴클레오티드의 합성
화합물 166의 합성은 실시예 54에서 기재되어 있다. 올리고뉴클레오티드 236는 실시예 46에서 기재된 일반적인 절차를 사용하여 제조되었다.
대안적으로, 올리고뉴클레오티드 236은 하기에서 보여진 도식을 사용하여 합성되었고, 및 화합물 238은 사용되어 실시예 10에서 기재된 절차를 사용하여 올리고뉴클레오티드 236을 형성했다.
콘주게이트 그룹 GalNAc1-25의 GalNAc1 클러스터 부분 (GalNAc1-25a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc1-25 (GalNAc1-25a-CM) 의 구조는 하기와 같다:
실시예
106: 5'
-
GalNAc
2
또는 5'-
GalNAc
3
콘주게이트를
포함하는
SRB
-1을 표적으로 하는 올리고뉴클레오티드에 의한
생체내
안티센스
억제
표 116 및 117에서 열거된 올리고뉴클레오티드는 마우스에서 SRB-1의 안티센스 억제에 대한 투여량-의존적 연구에서 시험되었다.
치료
6 주령, 수컷 C57BL/6 마우스 (Jackson Laboratory, Bar Harbor, ME)에게 2, 7, 또는 20 mg/kg의 ISIS 번호 440762; 또는 0.2, 0.6, 2, 6, 또는 20 mg/kg의 ISIS 번호 686221, 686222, 또는 708561; 또는 염수가 피하로 1회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스는 최종 투여 72 시간 후에 희생되었다. 간 SRB-1 mRNA 수준은 실시간 PCR를 사용하여 측정되었다. SRB-1 mRNA 수준은 표준 프로토콜에 따라 사이클로필린 mRNA 수준에 대해 정규화되었다. 안티센스 올리고뉴클레오티드는 투여량-의존 방식으로 SRB-1 mRNA 수준을 감소시켰고, ED50 결과는 표 116 및 117에서 제공된다. 이전의 연구는, 3가 GalNAc-콘주게이트된 올리고뉴클레오티드가 결국 1가 GalNAc 콘주게이트된 올리고뉴클레오티드로부터 유의미하게 더 강했던 2가 GalNAc-콘주게이트된 올리고뉴클레오티드보다 유의미하게 더 강했다는 것을 보여주었지만, (참고, 예를 들면, Khorev et al., Bioorg . & Med . Chem., Vol. 16, 5216-5231 (2008)), 1가, 2가, 및 3가 GalNAc 클러스터를 포함하는 안티센스 올리고뉴클레오티드에 의한처리는 표 116 및 117에서 보여진 바와 같은 유사한 효능으로 SRB-1 mRNA 수준을 감소시켰다.
표 116
SRB
-1을 표적으로 하는 변형된 올리고뉴클레오티드
표 범례에 대한 실시예 93 참조. GalNAc3-13a의 구조는 실시예 62에서 이미 나타나 있고, GalNAc2-24a의 구조는 실시예 104에서 나타나 있다.
표 117
SRB
-1을 표적으로 하는 변형된 올리고뉴클레오티드
표 범례에 대한 실시예 93 참조. GalNAc1-25a의 구조가 실시예 105에 나타나 있다.
간 중 표 116 및 117에서의 올리고뉴클레오티드의 농도는 실시예 75에서 기재된 절차를 사용하여 또한 평가되었다. 하기의 표 117a 및 117b에서 보여진 결과는 μg 올리고뉴클레오티드 / 간 조직의 그램의 단위로 UV에 의해 측정된 바와 같이, 각 처리 그룹에 대한 평균 총 안티센스 올리고뉴클레오티드 조직 수준이다. 이 결과는, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드가 GalNAc 콘주게이트 그룹이 없는 올리고뉴클레오티드의 동일한 투여량보다 유의미하게 더 높은 수준에서 간에서 축적된다는 것을 보여준다. 더욱이, 그의 각 콘주게이트 그룹 모두 중 1, 2 또는 3 개의 GalNAc 리간드를 포함하는 안티센스 올리고뉴클레오티드는 유사한 수준으로 간에서 축적된다. 이러한 결과는 상기에서 인용된 Khorev 등 문헌 참조의 관점에서 놀랍고 상기 표 116 및 117에서 보여진 활성 데이터와 일치한다.
표 117a
GalNAc
2
또는
GalNAc
3
콘주게이트
그룹을 포함하는 올리고뉴클레오티드의 간 농도
표 117b
GalNAc
1
콘주게이트
그룹을 포함하는 올리고뉴클레오티드의 간 농도
실시예
107:
GalNAc
1
-26 또는
GalNAc
1
-27
콘주게이트를
포함하는 올리고뉴클레오티드의 합성
올리고뉴클레오티드 239는 DMF 중 HBTU 및 DIEA를 사용하여 화합물 47 (참고 실시예 15)의 산 64 (참고 실시예 32)에의 커플링을 통해 합성된다. 수득한 아미드 함유 화합물은 포스피틸화되고, 그 다음 실시예 10에서 기재된 절차를 사용하여 올리고뉴클레오티드의 5'-말단에 부가된다. 콘주게이트 그룹 GalNAc1-26의 GalNAc1 클러스터 부분 (GalNAc1-26a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc1-26 (GalNAc1-26a-CM) 의 구조는 하기와 같다:
GalNAc1 콘주게이트 그룹을 올리고뉴클레오티드의 3'-말단에 부가하기 위해, 화합물 47 및 64의 반응으로부터 형성된 아미드는 실시예 7에서 기재된 절차를 사용하여 고형 지지체에 부가된다. 그 다음 올리고뉴클레오티드 합성은 실시예 9에서 기재된 절차를 사용하여 완료되어 올리고뉴클레오티드 240을 형성한다.
콘주게이트 그룹 GalNAc1-27의 GalNAc1 클러스터 부분 (GalNAc1-27a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc1-27 (GalNAc1-27a-CM) 의 구조는 하기와 같다:
실시예
108:
생체내
에서
아포(a)
를
표적으로 하는
GalNAc
콘주게이트
그룹을 포함하는 올리고뉴클레오티드에 의한
생체내
의
안티센스
억제
하기의 표 118에서 열거된 올리고뉴클레오티드는 마우스에서 단회 투여량 연구에서 시험되었다.
표 118
아포(a)를
표적으로 하는 변형된
ASO
“GalNAc3-7a"의 구조가 실시예 48에 나타나 있다.
치료
인간 아포(a)를 발현시키는 수컷 형질전환 마우스 각각에게, 올리고뉴클레오티드가 그리고 표 119에서 열거된 투여량으로 또는 PBS가 피하로 1 회 주입되었다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 혈액은 혈장 중 아포(a) 단백질의 기준선 수준을 측정하기 위해 투여 전 날 및 제 1 투여량 다음 1 주에 뽑았다. 추가의 채혈은 대략 8 주 동안 매주 일어날 것이다. 혈장 아포(a) 단백질 수준은 ELISA를 사용하여 측정되었다. 표 119의 결과는 기준선 수준 (% BL)으로 정규화된, 각 처리 그룹에 대한 혈장 아포(a) 단백질 수준의 평균 퍼센트로서 제공된다. 이 결과는, 안티센스 올리고뉴클레오티드가 아포(a) 단백질 발현을 축소시킨다는 것을 보여준다. 더욱이, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 콘주게이트 그룹을 포함하지 않는 올리고뉴클레오티드보다 아포(a) 발현에서 더욱 더 강한 축소를 나타내었다.
표 119
아포(a) 혈장 단백질 수준
실시예 109: GalNAc
1
-28 또는 GalNAc
1
-29 콘주게이트를 포함하는 올리고뉴클레오티드의 합성
올리고뉴클레오티드 241은 실시예 71에서 기재된 것과 유사한 절차를 사용하여 합성되어 포스포르아미다이트 중간체를 형성하고, 그 다음 실시예 10에서 기재된 절차를 사용하여 올리고뉴클레오티드를 합성한다. 콘주게이트 그룹 GalNAc1-28의 GalNAc1 클러스터 부분 (GalNAc1-28a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc1-28 (GalNAc1-28a-CM) 의 구조는 하기와 같다:
GalNAc1 콘주게이트 그룹을 올리고뉴클레오티드의 3'-말단에 부가하기 위해, 실시예 71에서 기재된 것과 유사한 절차가 사용되어 하이드록실 중간체를 형성하고, 그 다음 이것은 실시예 7에서 기재된 절차를 사용하여 고형 지지체에 부가된다. 그 다음 올리고뉴클레오티드 합성은 실시예 9에서 기재된 절차를 사용하여 완료되어 올리고뉴클레오티드 242를 형성한다.
콘주게이트 그룹 GalNAc1-29의 GalNAc1 클러스터 부분 (GalNAc1-29a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. GalNAc1-29 (GalNAc1-29a-CM) 의 구조는 하기와 같다:
실시예 110: GalNAc
1
-30 콘주게이트를 포함하는 올리고뉴클레오티드의 합성
GalNAc1-30 콘주게이트 그룹을 포함하는 올리고뉴클레오티드 246(여기서 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택됨)는, 상기에 보여진 바와 같이 합성된다. 콘주게이트 그룹 GalNAc1-30의 GalNAc1 클러스터 부분 (GalNAc1-30a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, Y는 절단가능 모이어티의 일부이다. 특정 구현예에서, Y는 안정한 모이어티의 일부이고 절단가능 모이어티는 올리고뉴클레오티드 상에 존재한다. "GalNAc1-30a"의 구조가 하기에 나타나 있다.
실시예 111: GalNAc
2
-31 또는 GalNAc
2
-32 콘주게이트를 포함하는 올리고뉴클레오티드의 합성
GalNAc2-31 콘주게이트 그룹을 포함하는 올리고뉴클레오티드 250(여기서 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택됨)는, 상기에 보여진 바와 같이 합성된다. 콘주게이트 그룹 GalNAc2-31의 GalNAc2 클러스터 부분 (GalNAc2-31a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 올리고뉴클레오티드의 5'-말단에 직접적으로 인접한 Y-함유 그룹은 절단가능 모이어티의 일부이다. 특정 구현예에서, 올리고뉴클레오티드의 5'-말단에 직접적으로 인접한 Y-함유 그룹은 안정한 모이어티의 일부이고 절단가능 모이어티는 올리고뉴클레오티드 상에 존재한다. "GalNAc2-31a"의 구조가 하기에 나타나 있다.
GalNAc2-32 콘주게이트를 포함하는 올리고뉴클레오티드의 합성은 하기에서 보여진다.
GalNAc2-32 콘주게이트 그룹을 포함하는 올리고뉴클레오티드 252(여기서 Y는 O, S, 치환된 또는 비치환된 C1-C10 알킬, 아미노, 치환된 아미노, 아지도, 알케닐 또는 알키닐로부터 선택됨)는, 상기에 보여진 바와 같이 합성된다. 콘주게이트 그룹 GalNAc2-32의 GalNAc2 클러스터 부분 (GalNAc2-32a)은 올리고뉴클레오티드 상에 존재하는 임의의 절단가능 모이어티와 조합되어 다양한 콘주게이트 그룹을 제공할 수 있다. 특정 구현예에서, 올리고뉴클레오티드의 5'-말단에 직접적으로 인접한 Y-함유 그룹은 절단가능 모이어티의 일부이다. 특정 구현예에서, 올리고뉴클레오티드의 5'-말단에 직접적으로 인접한 Y-함유 그룹은 안정한 모이어티의 일부이고 절단가능 모이어티는 올리고뉴클레오티드 상에 존재한다. "GalNAc2-32a"의 구조가 하기에 나타나 있다.
실시예 112: GalNAc
1
콘주게이트를 포함하는 올리고뉴클레오티드의 합성
SRB-1를 표적으로 하는 표 120 중 올리고뉴클레오티드는 1 개의 GalNAc 리간드를 함유하는 콘주게이트 그룹을 포함하는 올리고뉴클레오티드의 효능을 추가 시험하기 위해 GalNAc1 콘주게이트 그룹으로 합성되었다.
표 120
실시예 113: 안지오포이에틴-유사 3을 표적화하고 GalNAc 콘주게이트 그룹을 포함하는 안티센스 올리고뉴클레오티드
표 121에서의 올리고뉴클레오티드를 안지오포이에틴-유사 3 (ANGPTL3)에 표적화되도록 설계하였다.
표 121
실시예 114: 인간 ANGPTL3을 표적으로 하는 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드에 의한
생체내
의 안티센스 억제
인간 ANGPTL3을 발현하는, 6 주령, 수컷 형질전환 C57Bl/6 마우스에게 복강내로 주당 1회 하기에서 보여진 투여량으로, 총 2 회 투여량 동안, 표 122에서 열거된 (그리고 표 121에서 열거된) 올리고뉴클레오티드 또는 PBS를 주사하였다. 각 처리 그룹은 4 마리의 동물로 구성되었다. 마우스를 최종 투여로부터 2 일 후 희생시켰다. ANGPTL3 간 mRNA 수준을 표준 프로토콜에 따라 실시간 PCR 및 리보그린® RNA 정량화 시약 (Molecular Probes, Inc. Eugene, OR)을 사용하여 측정하였다. 하기의 결과를 PBS 대조군에 대해 정규화된 각 처리 그룹에 대한 간 중의 ANGPTL3 mRNA 수준의 평균 퍼센트로서 나타내었다.
표 122에서 실증된 바와 같이, 안티센스 올리고뉴클레오티드에 의한 처리는 투여량-의존 방식에서 ANGPTL3 간 mRNA 수준을 감소시켰고, GalNAc 콘주게이트를 포함하는 올리고뉴클레오티드는 GalNAc 콘주게이트가 없는 모 올리고뉴클레오티드 보다 유의미하게 더 강했다.
표 122
ANGPTL3 간 mRNA 수준
간 알라닌 트랜스아미나제 (ALT) 수준을 표준 프로토콜을 사용하여 희생 시에 또한 측정하였다. 결과는, 처리 그룹 중 어느 그륩도 상승된 ALT 수준을 갖지 않았으며, 이는 상기 올리고뉴클레오티드가 양호한 내성을 갖는다는 것을 나타낸다.
실시예 115: 마우스 ANGPTL3을 표적으로 하는 GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드에 의한
생체내
의 안티센스 억제
하기의 표 123에서 열거된 올리고뉴클레오티드는 마우스에서 투여량 의존적 연구에서 시험되었다.
표 123
마우스
ANGPTL3을
표적으로 하는 변형된
ASO
“GalNAc3-7a"의 구조가 실시예 48에 나타나 있다.
저밀도 지단백질 수용체 녹아웃 (LDLR-/-) 마우스에, 표 123에 열거된 올리고뉴클레오티드 또는 PBS로 하기에 나타낸 투여량으로 1주일에 1회 복강내 주사하기 전에, 1주간 서양식 식이로 먹이공급하였다. 각 처리 그룹은 5 마리의 동물로 구성되었다. 혈액을 혈장 중 트리글리세라이드의 기준선 수준을 측정하기 위해 제1 투여가 투여된 후, 그리고 제1 투여로부터 2주 후에 채취하였다. 표 124의 결과는 기준선 수준 (% BL)으로 정규화된, 각 처리 그룹에 대한 혈장 트리글리세라이드 수준의 평균 퍼센트로서 제공되며, 이 결과는, 안티센스 올리고뉴클레오티드가 트리글리세라이드 발현을 투여량 의존적 방식으로 감소시킨다는 것을 보여준다. 더욱이, GalNAc 콘주게이트 그룹을 포함하는 올리고뉴클레오티드는 콘주게이트 그룹을 포함하지 않는 올리고뉴클레오티드보다 트리글리세라이드에서 더욱 더 강한 축소를 나타내었다.
표 124
혈장 트리글리세라이드 (TG) 수준
실시예 116: Hep3B 세포내에서 MOE 갭머(gapmer)에 의한 인간 안지오포이에틴-유사 3의 안티센스 억제
안티센스 올리고뉴클레오티드를 안지오포이에틴-유사 3(ANGPTL3) 핵산을 표적화하도록 설계하여 시험관내 ANGPTL3 mRNA에 대한 이의 효과에 대해 시험하였다. 상기 안티센스 올리고뉴클레오티드를 유사한 배양 조건을 갖는 일련의 평행 실험에서 효력을 시험하였다. 각 실험에 대한 결과는 하기 나타난 별개의 표에서 제시된다. 웰당 20,000 세포의 밀도로 배양된 Hep3B 세포를 전기천공을 사용하여 4,500 nM 안티센스 올리고뉴클레오티드로 형질감염시켰다. 대략 24시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB (정방향 서열 CCGTGGAAGACCAATATAAACAATT, 서열번호: 4로 본원에 지정됨; AGTCCTTCTGAGCTGATTTTCTATTTCT; 역방향 서열, 본원에서 서열번호: 5로 같이 지정됨; 프로브 서열 AACCAACAGCATAGTCAAATA, 본원에서 서열번호: 6으로 지정됨) 을 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준을 리보그린®에 의해 측정한 것으로서 총 RNA 함량에 따라 조절하였다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
하기 표에서 새로이 설계된 키메라 안티센스 올리고뉴클레오티드를 5-10-5 MOE 갭머로 설계하였다. 5-10-5 MOE 갭머는, 길이가 20개 뉴클레오티드이고, 여기서 중심 갭 분절은 10개의 2' 데옥시뉴클레오시드를 포함하며 각각 5개의 뉴클레오티드를 포함하는 5' 방향 및 3' 방향에서 윙 분절에 의해 플랭킹되어 있다. 5' 윙 분절 내의 각 뉴클레오시드 및 3' 윙 분절 내의 각각의 뉴클레오시드는 2'-MOE 변형을 갖는다. 각각의 갭머 전체에 걸쳐 뉴클레오시드간 연결은 포스포로티오에이트(P=S) 연결이다. 각각의 갭머 전체에 걸쳐 모든 시토신 잔기는 5-메틸시토신이다. "개시 부위"는, 갭머가 인간 유전자 서열내에서 표적화된 5'-대부분의 뉴클레오시드를 나타낸다. "정지 부위"는, 갭머가 인간 유전자 서열내에서 표적화된 3'-대부분의 뉴클레오시드를 나타낸다. 하기 표에 열거된 각각의 갭머는 본원에 개시된 서열번호: 1과 같이 지정된 인간 ANGPTL3 mRNA (유전자은행 수탁 번호 NM_014495.2) 또는 인간 ANGPTL3 게놈 서열 (서열번호: 2와 같이 본원에 지정됨; 33032001 내지 33046000로부터 절단된 유전자 은행 수탁 번호 NT_032977.9)에 표적화된다. 'n/a'는 안티센스 올리고뉴클레오티드가 100% 상보성을 갖는 특정 유전자 서열을 표적화하지 않는다는 것이다.
표 125
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 126
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 127
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 128
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 129
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 130
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 131
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 132
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 133
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 134
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 135
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 136
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 137
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
표 138
서열번호: 1 및 2를 표적화하는 5-10-5 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
실시예
117:
MOE
갭머에
의한
Hep3B
세포내에서
인간
ANGPTL3의
투여량-의존성
안티센스
억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 위에서 기술된 연구로부터의 5-10-5 MOE 갭머를 선택하고 Hep3B 세포내에서 다양한 투여량으로 시험하였다. 세포를 웰당 20,000개의 세포의 밀도에서 플레이팅하고 하기 표에 명시된 바와 같이, 0.75μM, 1.50μM, 3.00μM, 6.00μM 및 12.00μM 농도의 안티센스 올리고뉴클레오티드를 사용한 전기천공을 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 139
실시예 118: MOE 갭머에 의한 Hep3B 세포내에서 인간 ANGPTL3의 투여량-의존성 안티센스 억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 위에서 기술된 연구로부터의 5-10-5 MOE 갭머를 선택하고 Hep3B 세포내에서 다양한 투여량으로 시험하였다. 세포를 웰당 20,000개 세포의 밀도에서 플레이팅하고 하기 표에 명시된 바와 같이, 0.813μM, 1.625μM, 3.25μM, 6.50μM 및 13.00μM 농도의 안티센스 올리고뉴클레오티드를 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 140
표 141
표 142
표 143
표 144
표 145
표 146
표 147
실시예 119: 데옥시, MOE 및 (S)-cEt 갭머에 의한 Hep3B 세포내에서 인간 ANGPTL3의 안티센스 억제
추가의 안티센스 올리고뉴클레오티드를 ANGPTL3 핵산을 표적화하도록 설계하여 시험관내 ANGPTL3 mRNA에 대한 이의 효과에 대해 시험하였다. 웰당 20,000개의 세포의 밀도에서 배양된 Hep3B 세포를 4,500nM의 안티센스 올리고뉴클레오티드를 사용한 전기천공을 사용하여 형질감염시켰다. 대략 24시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준을 리보그린®에 의해 측정한 것으로서 총 RNA 함량에 따라 조절하였다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
하기 표에서 새로이 설계된 키메라 안티센스 올리고뉴클레오티드를 데옥시, MOE, 및 (S)-cEt 올리고뉴클레오티드로서 설계하였다. 데옥시, MOE 및 (S)-cEt 올리고뉴클레오티드는, 길이가 16개 뉴클레오티드이며, 여기서 당해 뉴클레오시드는 MOE 당 변형, (S)-cEt 당 변형, 또는 데옥시 당 잔기를 갖는다. 각각의 안티센스 올리고뉴클레오티드의 당 변형은 'eek-d10-kke'로서 기술되며, 여기서, 'k'는 (S)-cEt 당 변형을 나타내고; 'd'는 데옥시리보스를 나타내고; 수는 데옥시리보스 당 잔기의 수를 나타내며; 'e'는 MOE 당 변형을 나타낸다. 각각의 올리고뉴클레오티드 전체에서 뉴클레오시드간 연결은 포스포로티오에이트(P=S) 연결이다. 각각의 올리고뉴클레오티드 전체에서 모든 시토신 잔기는 5-메틸시토신이다. "개시 부위"는, 올리고뉴클레오티드가 인간 유전자 서열내에서 표적화된 5'-대부분의 뉴클레오시드를 나타낸다. "정지 부위"는, 올리고뉴클레오티드가 인간 유전자 서열내에서 표적화된 3'-대부분의 뉴클레오시드를 나타낸다. 하기 표에 열거된 각각의 올리고뉴클레오티드는 본원에 개시된 서열번호: 1과 같이 지정된 인간 ANGPTL3 mRNA (유전자은행 수탁 번호 NM_014495.2) 또는 인간 ANGPTL3 게놈 서열 (서열번호: 2와 같이 본원에 지정됨; 33032001 내지 33046000로부터 절단된 유전자 은행 수탁 번호 NT_032977.9)에 표적화된다. 'n/a'는 안티센스 올리고뉴클레오티드가 100% 상보성을 갖는 특정 유전자 서열을 표적화하지 않는다는 것이다.
표 148
서열번호: 1 및 2를 표적화하는 데옥시, MOE 및 cEt 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
표 149
서열번호: 1 및 2를 표적화하는 데옥시, MOE 및 (S)-cEt 갭머에 의한 ANGPTL3 mRNA의 억제
실시예 120: 데옥시, MOE 및 (S)-cEt 갭머에 의한 Hep3B 세포내에서 인간 ANGPTL3의 안티센스 억제
추가의 안티센스 올리고뉴클레오티드를 ANGPTL3 핵산을 표적화하도록 설계하여 시험관내 ANGPTL3 mRNA에 대한 이의 효과에 대해 시험하였다. 5-10-5 MOE 갭머인 ISIS 337487 및 ISIS 233717을 또한 벤치마크 올리고뉴클레오티드로서 검정에 포함시켰다. 웰당 20,000 세포의 밀도로 배양된 Hep3B 세포를 전기천공을 사용하여 4,500 nM 안티센스 올리고뉴클레오티드로 형질감염시켰다. 대략 24시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준을 리보그린®에 의해 측정한 것으로서 총 RNA 함량에 따라 조절하였다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
하기 표에서 새로이 설계된 키메라 안티센스 올리고뉴클레오티드를 데옥시, MOE, 및 (S)-cEt 올리고뉴클레오티드 또는 5-10-5 MOE 갭머로 설계하였다. 데옥시, MOE 및 (S)-cEt 올리고뉴클레오티드는, 길이가 16개 뉴클레오티드이며, 여기서 뉴클레오시드는 MOE 당 변형, (S)-cEt 당 변형, 또는 데옥시 당 잔기를 갖는다. 각각의 안티센스 올리고뉴클레오티드의 당 변형은 'eek-d10-kke'로 기술되어 있으며, 여기서 'k'는 (S)-cEt 당 변형이고; 'd'는 데옥시리보스를 나타내며; 수는 데옥시리보스 당 잔기의 수를 나타내고; 'e'는 MOE 변형을 나타낸다. 5-10-5 MOE 갭머는, 길이가 20개 뉴클레오티드이고, 여기서 중심 갭 분절은 10개의 2' 데옥시뉴클레오시드를 포함하며 각각 5개의 뉴클레오티드를 포함하는 5' 방향 및 3' 방향에서 윙 분절에 의해 플랭킹되어 있다. 각각의 올리고뉴클레오티드 전체에서 뉴클레오시드간 연결은 포스포로티오에이트(P=S) 연결이다. 각각의 올리고뉴클레오티드 전체에서 모든 시토신 잔기는 5-메틸시토신이다. "개시 부위"는, 올리고뉴클레오티드가 인간 유전자 서열내에서 표적화된 5'-대부분의 뉴클레오시드를 나타낸다. "정지 부위"는, 올리고뉴클레오티드가 인간 유전자 서열내에서 표적화된 3'-대부분의 뉴클레오시드를 나타낸다. 하기 표에 열거된 각각의 올리고뉴클레오티드는 본원에 개시된 서열번호: 1과 같이 지정된 인간 ANGPTL3 mRNA (유전자은행 수탁 번호 NM_014495.2) 또는 인간 ANGPTL3 게놈 서열 (서열번호: 2와 같이 본원에 지정됨; 33032001 내지 33046000로부터 절단된 유전자 은행 수탁 번호 NT_032977.9)에 표적화된다. 'n/a'는 안티센스 올리고뉴클레오티드가 100% 상보성을 갖는 특정 유전자 서열을 표적화하지 않는다는 것이다.
표 150
서열번호: 1 및 2를 표적화하는 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
표 151
서열번호: 1 및 2를 표적화하는 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
표 152
서열번호: 1 및 2를 표적화하는 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
표 153
서열번호: 1 및 2를 표적화하는 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
표 154
서열번호: 1 및 2를 표적화하는 올리고뉴클레오티드에 의한 ANGPTL3 mRNA의 억제
실시예 121: MOE 갭머에 의한 Hep3B 세포내에서 인간 ANGPTL3의 안티센스 억제
추가의 안티센스 올리고뉴클레오티드를 ANGPTL3 핵산을 표적화하도록 설계하여 시험관내 ANGPTL3 mRNA에 대한 이의 효과에 대해 시험하였다. 웰당 20,000 세포의 밀도로 배양된 Hep3B 세포를 전기천공을 사용하여 4,500 nM 안티센스 올리고뉴클레오티드로 형질감염시켰다. 대략 24시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준을 리보그린®에 의해 측정한 것으로서 총 RNA 함량에 따라 조절하였다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
하기 표에서 새로이 설계된 키메라 안티센스 올리고뉴클레오티드를 5-10-5 MOE 또는 3-10-4 MOE 갭머로 지정하였다. 5-10-5 MOE 갭머는, 길이가 20개 뉴클레오티드이고, 여기서 중심 갭 분절은 10개의 2' 데옥시뉴클레오시드를 포함하며 각각 5개의 뉴클레오티드를 포함하는 5' 방향 및 3' 방향에서 윙 분절에 의해 플랭킹되어 있다. 3-10-4 MOE 갭머는, 길이가 17개 뉴클레오티드이고, 여기서 중심 갭 분절은 10개의 2' 데옥시뉴클레오시드를 포함하고 각각 3개 및 4개의 뉴클레오티드를 포함하는 5' 방향 및 3' 방향에서 윙 분절에 의해 플랭킹되어 있다. 5' 윙 분절 내의 각 뉴클레오시드 및 3' 윙 분절 내의 각각의 뉴클레오시드는 2'-MOE 변형을 갖는다. 5' 윙 분절 내의 각 뉴클레오시드 및 3' 윙 분절 내의 각각의 뉴클레오시드는 2'-MOE 변형을 갖는다. 각각의 갭머 전체에 걸쳐 뉴클레오시드간 연결은 포스포로티오에이트(P=S) 연결이다. 각각의 갭머 전체에 걸쳐 모든 시토신 잔기는 5-메틸시토신이다. "개시 부위"는, 갭머가 인간 유전자 서열내에서 표적화된 5'-대부분의 뉴클레오시드를 나타낸다. "정지 부위"는, 갭머가 인간 유전자 서열내에서 표적화된 3'-대부분의 뉴클레오시드를 나타낸다. 하기 표에 열거된 각각의 갭머는 본원에 개시된 서열번호: 1과 같이 지정된 인간 ANGPTL3 mRNA (유전자은행 수탁 번호 NM_014495.2) 또는 인간 ANGPTL3 게놈 서열 (서열번호: 2와 같이 본원에 지정됨; 33032001 내지 33046000로부터 절단된 유전자 은행 수탁 번호 NT_032977.9)에 표적화된다. 'n/a'는 안티센스 올리고뉴클레오티드가 100% 상보성을 갖는 특정 유전자 서열을 표적화하지 않는다는 것이다.
표 155
서열번호: 1 및 2를 표적화하는 MOE 갭머에 의한 ANGPTL3 mRNA의 억제
실시예 122: Hep3B 세포내에서 인간 ANGPTL3의 투여량-의존적인 안티센스 억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 상기 기술된 연구로부터 데옥시, MOE, 및 cEt 올리고뉴클레오티드를 선택하여 Hep3B 세포내에서 다양한 투여량으로 시험하였다. ISIS 233717 및 ISIS 337847, 5-10-5 MOE 갭머 둘 다를 또한 본 연구에 포함시켰다. 상기 안티센스 올리고뉴클레오티드를 유사한 배양 조건을 갖는 일련의 평행 실험에서 효력을 시험하였다. 각각의 실험의 결과를 하기 별도의 표에 나타낸다.
세포를 웰당 20,000개 세포의 밀도로 플레이팅하고 하기 표에 명시한 바와 같이, 0.813μM, 1.625μM, 3.25μM, 6.500μM 및 13.00μM 농도의 안티센스 올리고뉴클레오티드를 사용하는 전기천공을 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 156
표 157
표 158
표 159
실시예 123: Hep3B 세포내에서 인간 ANGPTL3의 투여량-의존적인 안티센스 억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 상기 기술된 연구로부터 데옥시, MOE, 및 cEt 올리고뉴클레오티드를 선택하여 Hep3B 세포내에서 다양한 투여량으로 시험하였다. ISIS 337847, 5-10-5 MOE 갭머를 또한 당해 연구에 포함시켰다. 상기 안티센스 올리고뉴클레오티드를 유사한 배양 조건을 갖는 일련의 평행 실험에서 효력을 시험하였다. 각각의 실험의 결과를 하기 별도의 표에 나타낸다.
세포를 웰당 20,000개 세포의 밀도에서 플레이팅하고 하기 표에 명시된 바와 같이, 0.160μM, 0.481μM, 1.444μM, 4.333μM 및 13.00μM 농도의 안티센스 올리고뉴클레오티드를 사용한 전기천공을 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 160
표 161
표 162
실시예 124: MOE 갭머에 의한 Hep3B 세포내에서 인간 ANGPTL3의 투여량-의존성 안티센스 억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 상기 기술된 연구로부터의 MOE 갭머를 선택하여 Hep3B 세포내에서 다양한 투여량으로 시험하였다. 세포를 웰당 20,000개 세포의 밀도에서 플레이팅하고 하기 표에 명시된 바와 같이, 0.160μM, 0.481μM, 1.444μM, 4.333μM 및 13.00μM 농도의 안티센스 올리고뉴클레오티드를 사용한 전기천공을 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 163
실시예 125: 데옥시, MOE 및 cEt 올리고뉴클레오티드에 의한 Hep3B 세포내에서 인간 ANGPTL3의 투여량-의존적인 안티센스 억제
ANGPTL3 mRNA의 유의미한 시험관내 억제를 나타내는 상기 기술된 연구로부터 데옥시, MOE, 및 cEt 올리고뉴클레오티드를 선택하여 Hep3B 세포내에서 다양한 투여량으로 시험하였다. 세포를 웰당 20,000개 세포의 밀도에서 플레이팅하고 하기 표에 명시된 바와 같이, 0.111μM, 0.333μM, 1.00μM, 3.00μM 및 9.00μM 농도의 안티센스 올리고뉴클레오티드를 사용한 전기천공을 사용하여 형질감염시켰다. 대략 16시간의 처리 기간 후, RNA를 세포로부터 단리하고 ANGPTL3 mRNA 수준을 정량적인 실시간 PCR로 측정하였다. 인간 프라이머 프로브 세트 RTS3492_MGB를 사용하여 mRNA 수준을 측정하였다. ANGPTL3 mRNA 수준은 리보그린®에 의해서 측정되는 바와 같은 총 RNA 함량에 따라 조정되었다. 결과는 치료되지 않은 대조군 세포에 대해, ANGPTL3의 억제 퍼센트로 나타낸다.
각각의 올리고뉴클레오티드의 절반 최대 억제 농도 (IC50)를 하기 표에 또한 제시하였다. ANGPTL3 mRNA 수준은 안티센스 올리고뉴클레오티드 치료된 세포내에서 투여량-의존적 방식으로 유의미하게 감소하였다.
표 164
표 165
표 166
표 167
실시예 126: huANGPTL3 형질전환 마우스내에서 인간 ANGPTL3의 안티센스 억제
상기 연구에 기술된 안티센스 올리고뉴클레오티드를 인간 ANGPTL3 삽입유전자를 지닌 C57Bl/6 마우스(Tg 마우스)내에서 인간 ANGPTL3 mRNA 전사체를 감소시키는 이들의 능력에 대해 추가로 평가하였다.
연구 1
암컷 Tg 마우스를 12-시간의 명/암 주기에서 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머의 복강내 주사를 50mg/kg의 투여량에서 주당 1회로 2주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를, RTS3492_MGB를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. mRNA 수준을 또한 인간 프라이머 프로브 세트 RTS1984 (정방향 서열 CTTCAATGAAACGTGGGAGAACT, 본원에 서열번호: 7로 본원에서 지정됨; 역방향 서열 TCTCTAGGCCCAACCAAAATTC, 서열번호: 8로 본원에서 지정됨; 프로브 서열 AAATATGGTTTTGGGAGGCTTGAT, 서열번호: 9로 본원에서 지정됨)로 측정하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 168
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다.
표 169
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
10일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 170
제10일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 2
수컷 Tg 마우스를 12-시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머의 복강내 주사를 50mg/kg의 투여량에서 주당 1회로 2주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 RTS1984를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 171
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다.
표 172
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
8일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 173
제8일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구3
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머의 복강내 주사를 2.5mg/kg, 12.5 mg/kg, 또는 25 mg/kg의 투여량으로 주당 1회 3주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다 (정방향 서열 AAATTTTAGCCAATGGCCTCC, 서열번호: 10으로 본원에서 지정됨; TGTCATTAATTTGGCCCTTCG, 역방향 서열, 서열번호: 11로 본원에서 지정됨; 프로브 서열 TCAGTTGGGACATGGTCTTAAAGACTTTGTCC, 서열번호: 12로 지정됨). 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다. 각 갭머의 ED50은 또한 하기 표에 나타난다.‘n.d.'는, ED50이 측정되지 않았다는 것을 나타낸다.
표 174
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다. ‘n.d.'는, ED50이 측정되지 않았다는 것을 나타낸다.
표 175
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
17일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 176
제17일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 4
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 177
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
혈장 화학성질 마커
10일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 178
제10일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 5
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머 또는 데옥시, MOE, 및 cEt 갭머의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 RTS1984를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 179
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
혈장 화학성질 마커
9일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 180
제9일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 6
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 데옥시, MOE, 및 cEt 올리고뉴클레오티드의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. ISIS 233710, 5-10-5 MOE 갭머를 또한 벤치마크로서 포함시켰다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, 수개의 ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의적인 감소를 생성하였다.
표 181
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, 수개의 ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다.
표 182
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
10일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 183
제10일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 7
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 데옥시, MOE, 및 cEt 올리고뉴클레오티드의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. ISIS 233710, 5-10-5 MOE 갭머를 또한 벤치마크로서 포함시켰다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 184
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다. 이 경우, '0' 값은, ISIS 올리고뉴클레오티드 중의 일부를 사용한 처리가 발현을 억제하지 않았으며; 일부 예에서, 발현의 증가된 수준이 기록될 수 있음을 내포한다.
표 185
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
9일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 186
제9일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 8
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 데옥시, MOE, 및 cEt 올리고뉴클레오티드의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. ISIS 233710, 5-10-5 MOE 갭머를 또한 벤치마크로서 포함시켰다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다.
표 187
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 수준을 생성하였음을 나타낸다.
표 188
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
8일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 189
제8일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 9
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 데옥시, MOE, 및 cEt 올리고뉴클레오티드의 복강내 주사를 25mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. ISIS 233710, 5-10-5 MOE 갭머를 또한 벤치마크로서 포함시켰다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의적인 감소를 생성하였다. 이 경우, '0' 값은, ISIS 올리고뉴클레오티드 중의 일부를 사용한 처리가 발현을 억제하지 않았으며; 일부 예에서, 발현의 증가된 수준이 기록될 수 있음을 내포한다.
표 190
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 당해 결과는, ISIS 올리고뉴클레오티드를 사용한 처리가 감소된 ANGPTL3 단백질 수준을 생성하였음을 나타낸다. 이 경우, '0' 값은, ISIS 올리고뉴클레오티드 중의 일부를 사용한 처리가 발현을 억제하지 않았으며; 일부 예에서, 발현의 증가된 수준이 기록될 수 있음을 내포한다.
표 191
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
혈장 화학성질 마커
9일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 192
제9일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
연구 10
수컷 및 암컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
마우스의 그룹에게 5-10-5 MOE 갭머 또는 데옥시, MOE, 및 cEt 올리고뉴클레오티드의 복강내 주사를 5mg/kg, 12.5 mg/kg, 또는 25 mg/kg의 투여량으로 주당 1회로 2주 동안 제공하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 hANGPTL3_LTS01022과 RTS3492_MGB도 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드 중의 일부를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의적인 감소를 생성하였다.
표 193
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
혈장 화학성질 마커
8일째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 194
제8일에서의 형질전환 마우스 내에서의 혈장 트랜스아미나제 수준(IU/L)
실시예 127: CD1 마우스내에서 인간 ANGPTL3을 표적화하는 안티센스 올리고뉴클레오티드의 내성
CD1® 마우스(Charles River, MA)는 다중목적 마우스 모델이고, 흔히 안전성 및 효능 시험에 이용된다. 상기 마우스를 상기 기재된 연구로부터 선택된 ISIS 안티센스 올리고뉴클레오티드로 처리하고 다양한 혈장 화학 마커의 수준 변화를 평가하였다.
연구 1
수컷 CD1 마우스(처리 그룹 당 1마리의 동물)에게 200mg/kg의 단일 투여량의 데옥시, MOE, 및 cEt 올리고뉴클레오티드를 복강내 주사하였다. 1마리의 수컷 CD1 마우스에게 단일 투여량의 PBS를 피하 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
4일 째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 195
제4일에서의 CD1 마우스 내에서의 혈장 트랜스아미나제 수준
체중
체중을 ISIS 올리고뉴클레오티드의 1일 투여량 후 1일째에 측정하고 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 196
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 체중 (g)
연구 2
수컷 CD1 마우스(처리 그룹 당 1마리의 동물)에게 200mg/kg의 단일 투여량의 데옥시, MOE 및 cEt 올리고뉴클레오티드를 복강내 주사하였다. 1마리의 수컷 CD1 마우스에게 단일 투여량의 PBS를 피하 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
5일 째에 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여 트랜스아미나제(ALT 및 AST)의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 197
제5일에서의 CD1 마우스 내에서의 혈장 트랜스아미나제 수준
체중
체중을 ISIS 올리고뉴클레오티드의 1일 투여량 후 5일째에 측정하고 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 198
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 체중 (g)
연구 3
수컷 CD1 마우스(처리 그룹 당 4마리의 동물)에게 주당 1회로 6주 동안 100mg/kg의 5-10-5 MOE 갭머를 복강내 주사하였다. 4마리의 수컷 CD1 마우스의 1개 그룹에게 PBS를 주당 1회로 6주 동안 복강내 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 다양한 간 및 신장 기능 마커의 혈장 수준을 45일째에 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 199
제45일에서의 CD1 마우스 내에서의 혈장 화학성질 마커 수준
체중
체중을 43일째에 측정하여 하기 표에 나타내었다. 신장, 간 및 비장 중량을 45일째에 연구 말기에 측정하였다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 200
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 중량 (g)
연구 4
수컷 CD1 마우스(처리 그룹 당 4마리의 동물)에게 주당 1회로 6주 동안 제공된 50mg/kg 또는 100mg/kg의 5-10-5 MOE 갭머 또는 데옥시, MOE 및 cEt 올리고뉴클레오티드를 복강내 주사하였다. 4마리의 수컷 CD1 마우스의 1개 그룹에게 PBS를 주당 1회로 6주 동안 복강내 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 다양한 간 및 신장 기능 마커의 혈장 수준을 46일째에 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 201
제45일에서의 CD1 마우스 내에서의 혈장 화학성질 마커 수준
체중
체중을 44일째에 측정하여 하기 표에 나타내었다. 신장, 간 및 비장 중량을 46일째에 연구 말기에 측정하였다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 202
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 중량 (g)
연구 5
수컷 CD1 마우스(처리 그룹 당 4마리의 동물)에게 주당 1회로 6주 동안 제공된 50mg/kg의 데옥시, MOE 및 cEt 올리고뉴클레오티드를 복강내 주사하였다. 4마리의 수컷 CD1 마우스의 1개 그룹에게 PBS를 주당 1회로 6주 동안 복강내 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 다양한 간 및 신장 기능 마커의 혈장 수준을 43일째에 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 이들 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 203
제43일에서의 CD1 마우스 내에서의 혈장 화학성질 마커 수준
체중
체중을 41일째에 측정하여 하기 표에 나타내었다. 신장, 간 및 비장 중량을 43일째에 연구 말기에 측정하였다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 204
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 중량 (g)
실시예 128: 인간 ANGPTL3을 표적화하는 ISIS 안티센스 올리고뉴클레오티드의 점도의 측정
상기 기술된 연구로부터 선택된 안티센스 올리고뉴클레오티드의 점도를 40 이상의 센티포이즈(cP)를 갖는 안티센스 올리고뉴클레오티드를 스크리닝할 목적으로 측정하였다. 40 cP보다 큰 점도를 갖는 올리고뉴클레오티드는 최적 미만의 점도를 가질 것이다.
ISIS 올리고뉴클레오티드(32-35 mg)를 개량하여 유리 바이알에 넣고, 120 μL 물을 첨가하고 상기 바이알을 500C에서 가열함으로써 안티센스 올리고뉴클레오티드를 용액으로 용해시켰다. 미리 가열된 샘플의 일부(75 μL)를 마이크로-점도계(Cambridge)로 피펫팅하였다. 마이크로-점도계의 온도를 250C로 설정하고 샘플의 점도를 측정하였다. 또 다른 부분의 (20 μL)의 전-가열된 샘플을, 850C에서 260 nM에서 UV 판독을 위해 10 mL의 물에 피펫팅했다 (Cary UV 장치). 결과는 하기 표에 나타내었으며, 여기서 각각의 안티센스 올리고뉴클레오티드의 농도는 350mg/ml이었으며, 안티센스 올리고뉴클레오티드 용액의 대부분이 상기 기술된 기준 내에서 이들의 점도에 있어서 최적임을 나타낸다.
표 205
인간 ANGPTL3을 표적화하는 ISIS 안티센스 올리고뉴클레오티드의 점도
실시예 129: 스프라그-도울리 래트에서 인간 ANGPTL3을 표적화하는 안티센스 올리고뉴클레오티드의 내성
스프라그-도울리 래트는 안전성 및 효능 평가에 사용되는 다목적 모델이다. 래트를 상기 실시예에 기술된 연구로부터의 ISIS 안티센스 올리고뉴클레오티드로 치료하고 다양한 혈장 화학 마커의 수준에 있어서의 변화를 평가하였다.
연구 1
수컷 스프라그-도울리 래트를 12-시간의 명/암 주기에 유지시키고 퓨리나 정상 래트 사료, 식이 5001을 자유로이 공급하였다. 각각 4마리의 스프라그-도울리 래트의 그룹에게 PBS 또는 100mg/kg의 5-10-5 MOE 갭머를 주당 1회로 6주 동안 피하 주사하였다. 마지막 투여량 후 48시간 째에, 래트를 안락사시키고 혈장을 추가의 분석을 위해 수거하였다.
간 기능
간 기능에 있어서 ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 트랜스아미나제의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 혈장 수준의 ALT(알라닌 트랜스아미나제) 및 AST(아스파타제 트랜스아미나제)를 45일째에 측정하여 결과를 하기 표에 IU/L로 표시하여 나타낸다. 빌리루빈의 혈장 수준을 또한 동일한 임상 화학 분석기를 사용하여 측정하고 결과를 또한 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 206
스프라그-도울리 래트의 간 기능 마커
신장 기능
신장 기능에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위해, 혈액 우레아 질소(BUN) 및 크레아티닌의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과를 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 신장 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다. 총 뇨 단백질 및 뇨 크레아티닌 수준을 측정하고, 크레아티닌에 대한 총 뇨 단백질의 비를 평가하였다. 결과는 하기 표에 나타내었다.
표 207
스프라그-도울리 래트의 신장 기능 혈장 마커 (mg/dL)
표 208
스프라그-도울리 래트의 신장 기능 소변 마커
장기 중량
체중을 42일째에 측정하여 하기 표에 나타내었다. 간, 비장 및 신장 중량을 45일째에 연구 말기에 측정하고, 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 209
스프라그-도울리 래트의 몸체 및 장기 중량 (g)
연구 2
수컷 스프라그-도울리 래트를 12-시간의 명/암 주기에 유지시키고 퓨리나 정상 래트 사료, 식이 5001을 자유로이 공급하였다. 각각 4마리의 스프라그-도울리 래트의 그룹에게 PBS 또는 50mg/kg 또는 100mg/kg의 5-10-5 MOE 갭머 또는 데옥시, MOE 및 cEt 올리고뉴클레오티드를 주당 1회로 6주 동안 피하 주사하였다. 마지막 투여량 후 48시간 째에, 래트를 안락사시키고 혈장을 추가의 분석을 위해 수거하였다.
간 기능
간 기능에 있어서 ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 트랜스아미나제의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 혈장 수준의 ALT(알라닌 트랜스아미나제) 및 AST(아스파타제 트랜스아미나제)를 44일째에 측정하여 결과를 하기 표에 IU/L로 표시하여 나타낸다. 빌리루빈의 혈장 수준을 또한 동일한 임상 화학 분석기를 사용하여 측정하고 결과를 또한 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 210
스프라그-도울리 래트의 간 기능 마커
신장 기능
신장 기능에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위해, 제44일에 혈액 우레아 질소(BUN) 및 크레아티닌의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과를 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 신장 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다. 총 뇨 단백질 및 뇨 크레아티닌 수준을 측정하고, 크레아티닌에 대한 총 뇨 단백질의 비를 평가하였다. 결과는 하기 표에 나타내었다.
표 211
스프라그-도울리 래트의 신장 기능 혈장 마커 (mg/dL)
표 212
스프라그-도울리 래트의 신장 기능 소변 마커
장기 중량
체중을 42일째에 측정하여 하기 표에 나타내었다. 간, 비장 및 신장 중량을 44일째에 연구 말기에 측정하고, 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 213
스프라그-도울리 래트의 몸체 및 장기 중량 (g)
연구3
수컷 스프라그-도울리 래트를 12-시간의 명/암 주기에 유지시키고 퓨리나 정상 래트 사료, 식이 5001을 자유로이 공급하였다. 각각 4마리의 스프라그-도울리 래트의 그룹에게 PBS 또는 50mg/kg의 데옥시, MOE 및 cEt 올리고뉴클레오티드를 주당 1회로 6주 동안 피하 주사하였다. 마지막 투여량 후 48시간 째에, 래트를 안락사시키고 혈장을 추가의 분석을 위해 수거하였다.
간 기능
간 기능에 있어서 ISIS 올리고뉴클레오티드의 효능을 평가하기 위해, 트랜스아미나제의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 혈장 수준의 ALT(알라닌 트랜스아미나제) 및 AST(아스파타제 트랜스아미나제)를 44일째에 측정하여 결과를 하기 표에 IU/L로 표시하여 나타낸다. 빌리루빈의 혈장 수준을 또한 동일한 임상 화학 분석기를 사용하여 측정하고 결과를 또한 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 간 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다.
표 214
스프라그-도울리 래트의 간 기능 마커
신장 기능
신장 기능에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위해, 제44일에 혈액 우레아 질소(BUN) 및 크레아티닌의 혈장 수준을 자동화된 임상 화학 분석기(뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과를 하기 표에 mg/dL로 표시하여 나타낸다. 안티센스 올리고뉴클레오티드에 대한 예상 범위를 벗어나는 신장 기능 마커 중 임의의 수준에 있어서의 임의의 변화를 유발하는 ISIS 올리고뉴클레오티드는 추가의 연구에서 배제시켰다. 총 뇨 단백질 및 뇨 크레아티닌 수준을 측정하고, 크레아티닌에 대한 총 뇨 단백질의 비를 평가하였다. 결과는 하기 표에 나타내었다.
표 215
스프라그-도울리 래트의 신장 기능 혈장 마커 (mg/dL)
표 216
스프라그-도울리 래트의 신장 기능 소변 마커
장기 중량
체중을 42일째에 측정하여 하기 표에 나타내었다. 간, 비장 및 신장 중량을 44일째에 연구 말기에 측정하고, 하기 표에 나타내었다. 안티센스 올리고뉴클레오티드에 대해 예상되는 범위를 벗어나 특정 장기 중량 변화를 야기한 ISIS 올리고뉴클레오티드를 추가 연구에서 제외시켰다.
표 217
스프라그-도울리 래트의 몸체 및 장기 중량 (g)
실시예 130: 시노몰구스 원숭이에서 인간 ANGPTL3를 표적으로 하는 ISIS 안티센스 올리고뉴클레오티드의 효과
시노몰구스 원숭이를 상기 실시예에 기술된 연구로부터 선택된 ISIS 안티센스 올리고뉴클레오티드로 치료하였다. 안티센스 올리고뉴클레오티드 효능 및 내성, 및 또한 간 및 신장에서 이들의 약력학적 프로파일을 평가하였다.
이 연구가 착수될 시점에, 시노몰구스 원숭이 게놈 서열은 미국 국립생물공학정보센터(NCBI) 데이터베이스에서 이용할 수 없었으므로, 시노몰구스 원숭이 유전자 서열과의 교차-반응성은 확인할 수 없었다. 대신에, 시노몰구스 원숭이에서 사용된 ISIS 안티센스 올리고뉴클레오티드의 서열을 상동성을 위해 레서스 서열과 비교하였다. 레서스 서열과 상동인 ISIS 올리고뉴클레오티드는 또한 시노몰구스 원숭이 서열과 완전히 교차-반응하는 것으로 예상된다. 시험한 인간 안티센스 올리고뉴클레오티드는 레서스 게놈 서열(본원에서 서열번호: 3으로 지정된, 뉴클레오티드 3049001 내지 3062000로부터 절단된(truncated) 유전자은행 수탁 번호 제NW_001108682.1호)과 교차 반응성이다. 인간 올리고뉴클레오티드와 레서스 서열 사이의 상보성이 크면 클수록, 아마도 인간 올리고뉴클레오티드가 레서스 서열과 더 교차-반응할 수 있다. 서열번호: 3에 대한 각 올리고뉴클레오티드의 개시 및 정지 부위는 하기 표에 제시되어 있다. "개시 부위"는, 갭머가 레서스 원숭이 유전자 서열내에서 표적화된 5'-최대 뉴클레오티드를 나타낸다. '미스매치(mismatch)'는 레서스 게놈 서열과 미스매치된 인간 올리고뉴클레오티드내 핵염기의 수를 나타낸다.
표 218
레서스 ANGPTL3 유전자 서열 (서열번호: 3)에 상보적인 안티센스 올리고뉴클레오티드
치료
연구 전에, 원숭이를 적어도 30일의 기간 동안 격리실에 유지시키고, 이 동안에 동물을 일반적인 건강에 대해 매일 관찰하였다. 원숭이들은 2-4세였고 체중은 2 내지 4 kg 사이였다. 5마리의 무작위로 지정된 수컷 시노몰구스 원숭이 각각의 9개 그룹에게 ISIS 올리고뉴클레오티드 또는 PBS를 시계 방향으로 등위의 4개 부위(즉, 좌측, 상부, 우측, 및 하부)에, 투여량당 1개 부위씩 피하 주사하였다. 원숭이에게 부하 투여량의 PBS 또는 40mg/kg의 ISIS 올리고뉴클레오티드를 첫번째 주 동안 매 2일마다(1, 3, 5, 및 7일) 제공하고 주당 1회로 12주 동안(14, 21, 28, 35, 42, 49, 56, 63, 70, 77, 및 84일) PBS 또는 40mg/kg의 ISIS 올리고뉴클레오티드를 연속 투여하였다.
연구 기간 동안, 원숭이를 매일 2회 질환 또는 고통에 대해 관찰하였다. 치료, 손상 또는 병으로 인해 순간적이거나 가벼운 통증 또는 고통 이상을 경험하는 특정 동물은 연구 지도자와 협의한 후 통증을 완화시키기 위해 수의과 직원에 의해 승인받은 진통제 또는 제제로 처리하였다. 건강하지 못하거나 가능한 빈사 상태에 있는 특정 동물은 추가 관찰 및 가능한 안락사를 확인하였다. 예를 들면, ISIS 567321 치료 그룹에서 1마리의 동물이 45일째에 빈사상태인 것으로 밝혀져서 종결하였다. 동물의 계획된 안락사를 86일(마지막 투여량 후 대략 48 시간째)째에 케타민/크실라진-유도된 마취 및 나트륨 펜토바르비탈의 투여 후 방혈에 의해 수행하였다. 본 실시예에 기재된 프로토콜은 동물실험윤리위원회(IACUC)에 의해 승인되었다.
간 표적 감소
RNA 분석
86일째에, RNA을 간으로부터 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 하기 표에 나타낸 바와 같이, ISIS 안티센스 올리고뉴클레오티드를 사용한 처리는 PBS 대조군과 비교시 ANGPTL3 mRNA의 유의미한 감소를 생성하였다. ANGPTL3 mRNA 수준의 분석은, 레서스 서열과 둘 다 완전히 교차-반응성인, ISIS 544199 및 ISIS 559277이 발현 수준을 유의미하게 감소시킴을 나타낸다. 미스매치된 원숭이 서열을 표적화하는, 다른 ISIS 올리고뉴클레오티드는 또한 ANGPTL3 mRNA 수준을 감소시킬 수 있다.
표 219
PBS 대조군과 비교시 시노몰구스 원숭이 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
대략 1mL의 혈액을 85일째에 모든 이용가능한 동물로부터 수집하여 EDTA의 칼륨 염을 함유하는 튜브 속에 두었다. 혈액 샘플을 빙상 속에 두고 원심분리(4℃에서 10분 동안 3000 rpm)하여 혈장을 수집하였다.
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 혈장 ANGPTL3의 분석은, ISIS 563580, 544199 및 ISIS 559277이 지연된 방식으로 단백질 수준을 감소시킴을 나타내었다. 다른 ISIS 올리고뉴클레오티드 또한 ANGPTL3 수준을 감소시킬 수 있었다.
표 220
시노몰구스 원숭이 내 혈장 단백질 수준 (ng/mL)
내성 연구
체중 측정
동물의 전체적인 건강에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 체격 및 체중을 측정하고 하기 표에 나타내었다. 당해 결과는, 체중에 있어서 안티센스 올리고뉴클레오티드를 사용한 처리의 효과가 안티센스 올리고뉴클레오티드에 대해 예측된 범위 내에 있었음을 나타낸다. 구체적으로, ISIS 563580을 사용한 처리는 또한 원숭이의 체중의 측면에서 매우 내성이었다.
표 221
시노몰구스 원숭이 내 최종 체중 (g)
간 기능
간 기능에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 혈액 샘플을 모든 연구 그룹으로부터 수집하였다. 혈액 샘플을 요측피정맥, 복재정맥, 또는 대퇴 정맥으로부터 투여 후 48시간째에 수집하였다. 상기 원숭이들은 채혈에 앞서 밤새 단식시켰다. 혈액을 혈청 분리를 위해 항응고제없이 튜브 속에 수집하였다. 튜브를 실온에서 최소 90분 동안 유지시킨 후 원심분리(10분 동안 대략 3,000 rpm에서)하여 혈청을 수집하였다. 다양한 간 기능 마커의 수준을 Toshiba 200FR NEO Chemistry 분석기(Toshiba Co., Japan)를 사용하여 측정하였다. ALT 및 AST의 혈장 수준을 측정하고 결과는 하기 표에 IU/L로 표시하여 나타낸다. 간 기능 마커인, 빌리루빈을 유사하게 측정하여 하기 표에 mg/dL로 표시하여 나타낸다. 당해 결과는, 대부분의 안티센스 올리고뉴클레오티드가 안티센스 올리고뉴클레오티드에 대해 예측된 범위를 벗어나는 이외의 간 기능에 효과가 없었음을 나타낸다. 구체적으로, ISIS 563580을 사용한 처리는 원숭이에서 간 기능의 측면에서 매우 내성이었다.
표 222
시노몰구스 원숭이 혈장 내 ALT 수준 (IU/L)
표 223
시노몰구스 원숭이 혈장 내 AST 수준 (IU/L)
표 224
시노몰구스 원숭이 혈장 내 빌리루빈 수준 (mg/dL)
신장 기능
신장 기능에 있어서 ISIS 올리고뉴클레오티드의 효과를 평가하기 위하여, 혈액 샘플을 모든 연구 그룹으로부터 수집하였다. 혈액 샘플을 요측피정맥, 복재정맥, 또는 대퇴 정맥으로부터 투여 후 48시간째에 수집하였다. 상기 원숭이들은 채혈에 앞서 밤새 단식시켰다. 혈액을 혈청 분리를 위해 항응고제없이 튜브 속에 수집하였다. 튜브를 실온에서 최소 90분 동안 유지시킨 후 원심분리(10분 동안 대략 3,000 rpm에서)하여 혈청을 수집하였다. BUN 및 크레아티닌의 수준을 도시바 200FR NEO 화학 분석기(제조원: 일본 소재의 Toshiba Co.)를 사용하여 측정하였다. 결과를 하기 표에 mg/dL로 표시하여 나타낸다.
혈장 화학은, 대부분의 ISIS 올리고뉴클레오티드가 안티센스 올리고뉴클레오티드에 대한 예측된 범위를 벗어나는 신장 기능에 임의의 영향도 미치지 않았음을 나타낸다. 구체적으로, ISIS 563580을 사용한 처리는 원숭이에서 신장 기능의 측면에서 매우 내성이었다.
표 225
시노몰구스 원숭이 내 혈장 BUN 수준 (mg/dL)
표 226
시노몰구스 원숭이 내 혈장 크레아티닌 수준 (mg/dL)
혈액학
혈액학적 매개변수에 있어서 시노몰구스 원숭이에서 ISIS 올리고뉴클레오티드의 임의의 효과도 평가하기 위해, 대략 0.5mL의 혈액의 혈액 샘플을 K2-EDTA를 함유하는 튜브 속에 이용가능한 연구 동물 각각으로부터 수집하였다. 샘플을 적혈구(RBC) 수, 백혈구(WBC) 수, 단핵구, 호중구, 림프구의 것과 같은 개개의 백혈구 수, 및 혈소판 수, 헤모글로빈 함량 및 헤마토크리트를 ADVIA120 혈액학 분석기(제조원: 미국 소재의Bayer)를 사용하여 분석하였다. 데이타는 하기 표에 나타낸다.
상기 데이터는, 올리고뉴클레오티드가 당해 투여량에서 안티센스 올리고뉴클레오티드에 대해 예측된 범위를 벗어나는 혈액학적 매개변수내에서 임의의 변화도 유발하지 않았음을 나타낸다. 구체적으로, ISIS 563580을 사용한 처리는 원숭이의 혈액학적 매개변수의 측면에서 매우 내성이었다.
표 227
시노몰구스 원숭이에서 혈구 수
표 228
시노몰구스 원숭이 혈액학적 파라미터
전-염증성 분자에 있어서의 효과
시노몰구스 원숭이에서 ISIS 올리고뉴클레오티드의 염증 효과를 평가하기 위하여, 혈액 샘플을 투여 전 84일째에 C-반응성 단백질 및 C3 수준의 분석을 위해 취하였다. 각 동물로부터 약 1.5 mL의 혈액을 수집하였고, 혈청 분리를 위해 이를 혈액 응고 방지제가 없는 튜브에 넣었다. 상기 튜브를 최소 90분 동안 실온에서 유지시킨 다음, 10분 동안 실온에서 3,000 rpm에서 원심분리하여 혈청을 얻었다. 염증의 마커로서 제공되는, C-반응성 단백질(CRP) 및 상보체 C3를 도시바 200FR NEO 화학 분석기(제조원: 일본 소재의 Toshiba Co.)를 사용하여 측정하였다. 당해 결과는, ISIS 563580을 사용한 처리가 원숭이에서 매우 내성이었음을 나타낸다.
표 229
시노몰구스 원숭이 혈장에서의 C-반응성 단백질 수준 (mg/L)
표 230
시노몰구스 원숭이 혈장 내 C3 수준 (mg/dL)
올리고뉴클레오티드 농도의 측정
전장 올리고뉴클레오티드의 농도를 측정하였다. 사용된 방법은 종래 공개된 방법(Leeds 등, 1996; Geary 등, 1999)의 변형이며, 이는 페놀-클로로포름 추출 후 고체상 추출로 구성되어 있다. 내부 표준물(ISIS 355868, 27-머 2'-O-메톡시에틸 변형된 포스포로티오에이트 올리고뉴클레오티드, GCGTTTGCTCTTCTTCTTGCGTTTTTT, 본원에서 서열번호: 13으로 지정됨) 을 추출 전에 가하였다. 조직 샘플 농도를 대략 1.14 μg/g의 정량화의 하한(LLOQ)으로 보정 곡선을 사용하여 계산하였다. 결과는 하기 표에 ㎍/g 간 또는 신장으로 표시하여 나타내었다. 신장 대 간내의 전장 올리고뉴클레오티드의 농도 비를 계산하였다. ISIS 563580의 치료 후 신장 대 간 내의 전장 올리고뉴클레오티드의 농도 비는 평가된 다른 화합물과 비교하여 가장 최적임이 밝혀졌다.
표 231
올리고뉴클레오티드 전장 농도
실시예 131: GalNAc 콘주게이트 그룹을 포함하는 ISIS 올리고뉴클레오티드 및 GalNAc 콘주게이트 그룹을 포함하지 않는 ISIS 올리고뉴클레오티드에 의한, huANGPTL3 형질전환 마우스에서의 인간 ANGPTL3의 안티센스 억제 비교
GalNAc3-7a를 포함하는 안티센스 올리고뉴클레오티드를, Tg 마우스에서의 인간 ANGPTL3 mRNA 전사체를 감소시키는 이들의 능력에 대하여 이들의 비-콘주게이트된 대상체와 비교하여 평가하였다. 서열번호: 1을 표적화하는 갭머는 하기 표 및 표 121에 기술되어 있다. 골격 화학성질 칼럼의 부호는 하기와 같다: ‘s'는 티오에이트 에스테르이고,‘o'는 포스페이트 에스테르이다.
표 232
ISIS 올리고뉴클레오티드
암컷 및 수컷 Tg 마우스를 12 시간의 명/암 주기에 유지시켰다. 동물은 실험의 개시 전 연구 시설에서 적어도 7일 동안 순응되었다. 안티센스 올리고뉴클레오티드(ASO)를 완충된 염수(PBS) 속에서 제조하고 0.2 마이크론 여과기를 통해 여과하여 멸균시켰다. 올리고뉴클레오티드를 주사용 0.9% PBS 속에 용해시켰다.
4마리 마우스의 그룹에게 ISIS 563580를 5 mg/kg, 10 mg/kg, 15 mg/kg, 또는 30 mg/kg의 투여량으로 주당 1회 2주 동안 피하로 주사하였다. 4마리 마우스의 그룹에게 ISIS 703801 또는 ISIS 703802를 0.3 mg/kg, 1 mg/kg, 3 mg/kg, 또는 10 mg/kg의 투여량으로 주당 1회 2주 동안 복강내 주사하였다. 마우스의 한 그룹에게는 PBS의 피하 주사를 주당 1회로 2주 동안 제공하였다. PBS-주사된 그룹은, 상응하는 올리고뉴클레오티드-치료된 그룹을 비교하는 대조군 그룹으로 제공하였다.
RNA 분석
처리 기간 말기에, RNA를 인간 프라이머 프로브 세트 hANGPTL3_LTS01022를 지닌 ANGPTL3의 mRNA 발현의 측정의 실시간 PCR 분석을 위해 간 조직으로부터 추출하였다. 결과는 PBS 대조군과 비교시 mRNA의 변화 퍼센트로서 나타내고, 리보그린®로 정규화하였다. 0의 값은, 단순하게, 안티센스 올리고뉴클레오티드가 측정가능한 수준에서 발현을 억제하지 않았다는 것을 나타내었다.
결과는, 상기 콘주게이트된 화합물이, 이들의 비-콘주게이트된 화합물 보다, 억제 퍼센트 및 ID50 값으로부터 명백하게 ANGPTL3 발현을 감소시키는데 훨씬 더 강력하다는 것을 예증한다. 혼합 골격 화학성질 (703802)를 갖는 콘주게이트된 올리고뉴클레오티드는 전장 포스포로티오에이트 골격 화학성질 (703801)을 갖는 콘주게이트된 올리고뉴클레오티드보다 발현을 억제함에 있어 더욱 강력하였다.
표 233
PBS 대조군과 비교시 형질전환 마우스 간 내에서의 ANGPTL3 mRNA의 억제율%
단백질 분석
인간 ANGPTL3 단백질 수준을 시판되는 ELISA 키트(미네소타주 미네아폴리스 소재의 R&D Systems에 의한 제품 번호 #DANL30)를 사용하여 1:20,000로 희석된 형질전환된 혈장 샘플로 제조업자가 기술한 프로토콜을 사용하여 정량화하였다. 결과는 하기 표에 나타내었다. 0의 값은, 단순하게, 안티센스 올리고뉴클레오티드가 측정가능한 수준에서 발현을 억제하지 않았다는 것을 나타내었다.
결과는, 상기 콘주게이트된 화합물이, 이들의 비-콘주게이트된 화합물 보다, 억제 퍼센트로부터 명백하게 ANGPTL3 발현을 감소시키는데 더 강력하다는 것을 예증한다. 혼합 골격 화학성질 (703802)를 갖는 콘주게이트된 올리고뉴클레오티드는 전장 포스포로티오에이트 골격 화학성질 (703801)을 갖는 콘주게이트된 올리고뉴클레오티드보다 발현을 억제함에 있어 더욱 강력하였다.
표 234
형질전환 마우스 내에서의 혈장 단백질 수준 억제율%
실시예 132: CD1 마우스내에서 인간 ANGPTL3을 표적화하는 GalNAc 콘주게이트된 안티센스 올리고뉴클레오티드의 내성
수컷 CD1 마우스 (처리 그룹 당 4개 동물)에 ISIS 703802를 하기 표와 같이 6주간 다양한 투여량으로 피하 주사하였다 (제 1, 제 3, 제 5, 제 8, 제 14, 제 21, 제 28, 제 35 및 제 42일) 4마리의 수컷 CD1 마우스의 1개 그룹에게 PBS를 6주 동안 피하 주사하였다. 마우스를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
혈장 화학성질 마커
ISIS 703802의 효능을 평가하기 위해, 다양한 간 및 신장 기능 마커의 혈장 수준을 44일째에 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 결과는 하기 표에 나타내었다. ISIS 703802는 높은 투여량에서 조차 내성있는 화합물인 것으로 나타났다.
표 235
제44일에서의 CD1 마우스 내에서의 혈장 화학성질 마커 수준
체중
몸체, 신장, 간 및 비장 중량을 44일째에 연구 말기에 측정하였다. ISIS 703802는, 높은 투여량으로 투여되었을 때 조차, 몸체 및 장기 중량을 유의미하게 변화시키지 않았다.
표 236
안티센스 올리고뉴클레오티드 처리 후 CD1 마우스의 중량 (g)
실시예 133: 스프라그-도울리 래트 내에서 인간 ANGPTL3을 표적화하는 GalNAc 콘주게이트된 안티센스 올리고뉴클레오티드의 내성
스프라그-도울리 래트는 안전성 및 효능 평가에 사용되는 다목적 모델이다. 수컷 스프라그-도울리 래트를 12-시간의 명/암 주기에 유지시키고 퓨리나 정상 래트 사료, 식이 5001을 자유로이 공급하였다. 4마리의 스프라그-도울리 래트 그룹에 ISIS 703802를 하기 표와 같이 6주간 다양한 투여량으로 피하 주사하였다 (제 1, 제 3, 제 5, 제 8, 제 14, 제 21, 제 28, 제 35 및 제 42일) 4마리의 래트의 1개 그룹에게 PBS를 6주 동안 피하 주사하였다. 래트를 마지막 투여량 후 48시간에 안락사시키고, 추가 분석을 위해 장기 및 혈장을 수확하였다.
간 및 신장 기능
간 기능에 있어서 ISIS 703802의 효능을 평가하기 위해, 트랜스아미나제의 혈장 수준을 자동화된 임상 화학 분석기(제조원: 뉴욕주 멜빌 소재의 Hitachi Olympus AU400e)를 사용하여 측정하였다. 혈장 수준의 ALT(알라닌 트랜스아미나제) 및 AST(아스파타제 트랜스아미나제)를 44일째에 측정하여 결과를 하기 표에 IU/L로 표시하여 나타낸다.
ISIS 703802의 신장 기능 상에서의 효과를 평가하기 위하여, 알부민, 혈액 우레아 질소 (BUN), 크레아티닌 및 빌리루빈의 혈장 수준을, 상동한 임상 화학성질 분석기를 사용하여 측정하였고, 결과를 g/dL 또는 mg/dL로 표시된 하기 표에 제시하였다.
ISIS 703802의 신장 기능 상에서의 효능을 추가로 평가하기 위하여, 뇨 단백질 및 뇨 크레아티닌 수준을 측정하고, 크레아티닌에 대한 총 뇨 단백질의 비를 평가하였다. 결과는 하기 표에 나타내었다.
ISIS 703802는 높은 투여량에서 조차 내성있는 화합물인 것으로 나타났다.
표 237
제44일에서의 스프라그-도울리 래트 혈장에서의 간 및 신장 기능 마커
표 238
제44일에서의 스프라그-도울리 래트의 신장 기능 뇨 마커 (mg/dL)
장기 중량
몸체, 간, 비장 및 신장 중량을 44일째에 연구 말기에 측정하고, 하기 표에 나타내었다. ISIS 703802는, 높은 투여량으로 투여되었을 때 조차 몸체, 신장, 및 간 중량을 유의미하게 변화시키지 않았다.
표 239
스프라그-도울리 래트의 몸체 및 장기 중량 (g)