JP7525558B2 - 二重特異性t細胞アクチベーターで武装したアデノウイルス - Google Patents
二重特異性t細胞アクチベーターで武装したアデノウイルス Download PDFInfo
- Publication number
- JP7525558B2 JP7525558B2 JP2022130173A JP2022130173A JP7525558B2 JP 7525558 B2 JP7525558 B2 JP 7525558B2 JP 2022130173 A JP2022130173 A JP 2022130173A JP 2022130173 A JP2022130173 A JP 2022130173A JP 7525558 B2 JP7525558 B2 JP 7525558B2
- Authority
- JP
- Japan
- Prior art keywords
- bispecific
- cells
- cell
- seq
- adenovirus
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/76—Viruses; Subviral particles; Bacteriophages
- A61K35/761—Adenovirus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/521—Chemokines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/521—Chemokines
- C07K14/522—Alpha-chemokines, e.g. NAP-2, ENA-78, GRO-alpha/MGSA/NAP-3, GRO-beta/MIP-2alpha, GRO-gamma/MIP-2beta, IP-10, GCP-2, MIG, PBSF, PF-4, KC
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7156—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for interferons [IFN]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
- C12N15/861—Adenoviral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5256—Virus expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55522—Cytokines; Lymphokines; Interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/58—Medicinal preparations containing antigens or antibodies raising an immune response against a target which is not the antigen used for immunisation
- A61K2039/585—Medicinal preparations containing antigens or antibodies raising an immune response against a target which is not the antigen used for immunisation wherein the target is cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/76—Viruses; Subviral particles; Bacteriophages
- A61K35/768—Oncolytic viruses not provided for in groups A61K35/761 - A61K35/766
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/90—Fusion polypeptide containing a motif for post-translational modification
- C07K2319/92—Fusion polypeptide containing a motif for post-translational modification containing an intein ("protein splicing")domain
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10311—Mastadenovirus, e.g. human or simian adenoviruses
- C12N2710/10321—Viruses as such, e.g. new isolates, mutants or their genomic sequences
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10311—Mastadenovirus, e.g. human or simian adenoviruses
- C12N2710/10332—Use of virus as therapeutic agent, other than vaccine, e.g. as cytolytic agent
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/10011—Adenoviridae
- C12N2710/10311—Mastadenovirus, e.g. human or simian adenoviruses
- C12N2710/10341—Use of virus, viral particle or viral elements as a vector
- C12N2710/10343—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/60—Vector systems having a special element relevant for transcription from viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2840/00—Vectors comprising a special translation-regulating system
- C12N2840/44—Vectors comprising a special translation-regulating system being a specific part of the splice mechanism, e.g. donor, acceptor
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Virology (AREA)
- Microbiology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Description
5’ITR-B1-BA-B2-BX-BB-BY-B3-3’ITR(I)
式中、
B1は結合であるか、又はE1A、E1B又はE1A-E1Bを含み、
BAは、-E2B-L1-L2-L3-E2A-L4を含み、
B2は結合であるか、又はE3を含み、
BXは結合であるか、又は制限部位、1つ又は複数の導入遺伝子、又はその両方を含むDNA配列であり、
BBはL5を含み、
BYは結合であるか、又は制限部位、1つ又は複数の導入遺伝子、又はその両方を含むDNA配列であり、
B3は結合であるか、又はE4を含み、
アデノウイルスは、少なくとも2つの結合ドメインを含む二重特異性T細胞アクチベーターをコードし、前記ドメインのうちの少なくとも1つは、対象のT細胞などの対象の免疫細胞上の表面抗原に特異的であり、
アデノウイルスはEnAd又はAd11である、式(I)の配列を含むアデノウイルスを提供する。
1.式(I):
5’ITR-B1-BA-B2-BX-BB-BY-B3-3’ITR(I)
式中、
B1は結合であるか、又はE1A、E1B又はE1A-E1Bを含み、
BAは、-E2B-L1-L2-L3-E2A-L4を含み、
B2は結合であるか、又はE3を含み、
BXは結合であるか、又は制限部位、1つ又は複数の導入遺伝子、又はその両方を含むDNA配列であり、
BBはL5を含み、
BYは結合であるか、又は制限部位、1つ又は複数の導入遺伝子、又はその両方を含むDNA配列であり、
B3は結合であるか、又はE4を含み、
アデノウイルスは、少なくとも2つの結合ドメインを含む二重特異性T細胞アクチベーターをコードし、前記ドメインの少なくとも1つは、対象のT細胞などの対象の免疫細胞上の表面抗原に特異的であり、
アデノウイルスはEnAd又はAd11である、式(I)の配列を含むアデノウイルスを提供する。
2.アデノウイルスはEnAdである、段落1に記載のアデノウイルス。
3.表面抗原がCD3、TCR-α及びTCR-βなどのT細胞受容体複合体(TCR)の成分である、段落1又は2に記載のアデノウイルス。
4.表面抗原がCD3-ε、CD3-γ、及びCD3-δ、特にCD3-εのようなCD3である、段落3に記載のアデノウイルス。
5.結合ドメインの1つが、CEA、MUC-1、EpCAM、HER受容体HER1、HER2、HER3、HER4、PEM、A33、G250、炭水化物抗原Ley、LeX、Leb、PSMA、TAG-72、STEAP1、CD166、CD24、CD44、E-カドヘリン、SPARC、ErbB2及びErbB3などの腫瘍抗原に特異的である、段落1~4のいずれか一段落に記載のアデノウイルス。
6.結合ドメインの1つがEpCAM、例えば配列番号28に記載のアミノ酸配列を含むEpCAMに特異的である、段落5に記載のアデノウイルス。
7.結合ドメインのうちの1つが腫瘍間質抗原、例えば線維芽細胞活性化タンパク質(FAP)、TREM1、IGFBP7、FSP-1、血小板由来成長因子-α受容体(PDGFR-α)、血小板由来成長因子-β受容体(PDGFR-β)及びビメンチンに特異的である、段落1~4のいずれか一項に記載のアデノウイルス。
8.結合ドメインのうちの1つがFAP、例えば配列番号30に記載のアミノ酸配列を含むFAPに特異的である、段落7に記載のアデノウイルス。
9.間質抗原が抗原であり、骨髄由来サプレッサー細胞抗原、腫瘍関連マクロファージ、及びそれらの組み合わせから選択される、段落7又は8に記載のアデノウイルス。
10.抗原がCD163、CD206、CD68、CD11c、CD11b、CD14、CSF1受容体、CD15、CD33、CD66b及びそれらの2つ以上の組み合わせから選択される、段落9に記載のアデノウイルス。
11.二重特異性T細胞アクチベーター中の結合ドメインの1つが、CD31、CD2及びCD277などの非TCR活性化タンパク質に特異的である、段落1~3及び5~10のいずれか一段落に記載のアデノウイルス。
12.BX又はBYの少なくとも一方が結合ではない、段落1~11のいずれか一段落に記載のアデノウイルス。
13.アデノウイルスがキメラである、段落1~12のいずれか一段落に記載のアデノウイルス。
14.アデノウイルスが腫瘍溶解性である、段落1~13のいずれか一段落に記載のアデノウイルス。
15.アデノウイルスの複製が可能である、段落1~14のいずれか一段落に記載のアデノウイルス。
16.アデノウイルスに複製能力がある、段落13に記載のアデノウイルス。
17.アデノウイルスが複製能欠損型である、段落1~14のいずれか一段落に記載のアデノウイルス。
18.BXが、1つ又は複数の導入遺伝子又は導入遺伝子カセットを含む、段落1~17のいずれか一段落に記載のアデノウイルス。
19.BYが1つ又は複数の導入遺伝子又は導入遺伝子カセットを含む、段落1~16のいずれか一段落に記載のアデノウイルス。
20.1つ又は複数の導入遺伝子又は導入遺伝子カセットが、内因性プロモーターなどの内因性又は外因性プロモーターの制御下にある、段落1~19のいずれか一段落に記載のアデノウイルス。
21.導入遺伝子又は導入遺伝子カセットがE4プロモーター及び主要後期プロモーター、特に主要後期プロモーターからなる群から選択される内因性プロモーターの制御下にある、段落20に記載のアデノウイルス。
22.導入遺伝子又は導入遺伝子カセットが、CMVなどの外因性プロモーターの制御下にある、段落19に記載のアデノウイルス。
23.導入遺伝子カセットが、
a.スプライスアクセプター配列、
b.内部リボソーム進入配列又は高い自己切断効率のAペプチド、
c.Kozak配列、及び
d.それらの組み合わせから独立して選択される調節エレメントをさらに含む、段落1~22のいずれか一段落に記載のアデノウイルス。
24.導入遺伝子カセットがタンパク質コード配列の開始点にあるコザック配列を含む、段落23に記載のアデノウイルス。
25.導入遺伝子カセットが高い自己切断効率のAペプチドをコードする、請求項1~24のいずれか一項に記載のアデノウイルス。
26.導入遺伝子カセットがポリアデニル化配列をさらに含む、段落1~25のいずれか一段落に記載のアデノウイルス。
27.導入遺伝子カセットが、DNA配列の「末端」及び/又はDNA配列の「末端」に制限部位をさらに含む、段落1~26のいずれか一段落に記載のアデノウイルス。
28.少なくとも1つの導入遺伝子カセットがモノシストロニックmRNAをコードする、段落1~27のいずれかに記載のアデノウイルス。
29.二重特異性T細胞アクチベーターが短い半減期、例えば48時間以下を有する、段落1~28のいずれか一段落に記載のアデノウイルス。
30.二重特異性T細胞アクチベーターが、E1、E3、BX、BY及びそれらの組み合わせから選択される領域にコードされている、段落1~29のいずれか一段落に記載のアデノウイルス。
31.二重特異性T細胞アクチベーターが、例えば主要後期プロモーターの制御下で、少なくともBX位にコードされている、段落30に記載のアデノウイルス。
32.アデノウイルスが、第2の二重特異性T細胞アクチベーターをさらにコードする、段落1~29のいずれか一段落に記載のアデノウイルス。
33.第1の二重特異性T細胞アクチベーター分子が腫瘍抗原、例えば腫瘍抗原(例えば本明細書に記載のもの)に特異的であり、第2の二重特異性T細胞アクチベーター分子が腫瘍間質抗原、例えば間質抗原(例えば本明細書に記載のもの)に特異的である、段落32に記載のアデノウイルス。
34.アデノウイルスがサイトカイン又はケモカイン又は免疫調節剤(サイトカイン又はケモカインなど)をさらに含む、段落1~33のいずれか一段落に記載のアデノウイルス。
35.サイトカイン又はケモカインは、MIP1α、IL-1α、IL-1β、IL-6、IL-9、IL-12、IL-13、IL-17、IL-18、IL-22、IL-23、IL-24、IL-25、IL-26、IL-27、IL-33、IL-35、IL-2、IL-4、IL-5、IL-7、IL-10、IL-15、IL-21、IL-25、IL-1RA、IFNα、IFNβ、IFNγ、TNFα、リンホトキシンα(LTA)、Flt3L、GM-CSF、IL-8、CCL2、CCL3、CCL5、CCL17、CCL20、CCL22、CXCL9、CXCL10、CXCL11、CXCL13、CXCL12、CCL2、CCL19、CCL21、(例えば、IL-1α、IL-1β、IL-6、IL-9、IL-12、IL-13、IL)-17、IL-18、IL-22、IL-23、IL-24、IL-25、IL-26、IL-27、IL-33、IL-35、IL-2、IL-4、IL-5、IL-7、IL-10、IL-15、IL-21、IL-25、IL-1RA、IFNα、IFNβ、IFNγ、TNFα、リンホトキシンα(LTA)、GM-CSF、IL-8、CCL2、CCL3、CCL5、CCL17、CCL20、CCL22、CXCL9、CXCL10、CXCL11、CXCL13、CXCL12、CCL2、CCL19、CCL21)、例えばIL-12、IL-18、IL-22、IL-7、IL-15など、IL-21、IFNγ、TNFα、リンホトキシンα(LTA)、CCL3、CCL5、CXCL9、CXCL10、CXCL12、CCL2、CCL19及びCCL21から選択される、段落34に記載のアデノウイルス。
36.アデノウイルスが、抗体もしくは抗体フラグメントなどの免疫調節剤、又はCTLA-4、PD-1、PD-L1、PD-L2、VISTA、B7-H3、B7-H4、HVEM、ILT-2、ILT-3、ILT-4、TIM-3、LAG-3、BTLA、LIGHT又はCD160、例えばCTLA-4、PD-1、PD-L1及びPD-L2に対する、又はCD28、CD80、CD86、CD83、ICOS、B7H2、TL1A及び4-1BBなどの共刺激分子に対する、チェックポイントタンパク質に特異的な、タンパク質もしくはペプチドリガンドをさらに含む、段落1~35のいずれか一段落に記載のアデノウイルス。
37.二重特異性T細胞アクチベーターが、配列番号8、13もしくは18のいずれか1つに記載のアミノ酸配列を含むVHドメイン、又はこれと少なくとも95%同一のアミノ酸配列を含む、段落1~36のいずれか一段落に記載のアデノウイルス。
38.二重特異性T細胞アクチベーターが、配列番号9、12、もしくは17のいずれか1つに記載のアミノ酸配列を含むVLドメイン、又はこれと少なくとも95%同一のアミノ酸配列を含む、段落1~37のいずれか一段落に記載のアデノウイルス。
39.二重特異性T細胞アクチベーターが、配列番号7、11もしくは16のいずれか1つに記載のアミノ酸配列を含むscFv、又はこれと少なくとも95%同一のアミノ酸配列を含む、段落1~36のいずれか一段落に記載のアデノウイルス。
40.二重特異性T細胞アクチベーターが、配列番号2もしくは4に記載のアミノ酸配列、又はこれと少なくとも95%同一であるアミノ酸配列、例えば配列番号73もしくは75に記載のアミノ酸配列を含む、段落1~39のいずれか一段落に記載のアデノウイルス。
41.アデノウイルスが、配列番号34~37のいずれか1つに記載のDNA配列、又はこれと少なくとも95%同一のDNA酸配列、例えば配列番号79~82のいずれか1つに記載のDNA配列を含む、段落1~40のいずれか一段落に記載のアデノウイルス。
42.段落1~41のいずれか一段落に記載のアデノウイルス及び希釈剤又は担体を含む組成物。
43.患者を治療する方法であって、段落1~41のいずれか一段落に記載のアデノウイルス又は段落42の組成物の治療有効量を投与することを含む方法。
44.癌、特に固形腫瘍の治療のための、段落43に記載の方法。
一実施形態では、本開示によるアデノウイルスは、少なくとも1つのさらなる導入遺伝子、例えば1、2、3又は4つのさらなる導入遺伝子をコードする。
一実施形態では、異なる切断ペプチドが各遺伝子間でコードされている。
一実施形態では、すべての導入遺伝子がウイルス内の1箇所にあり、例えばBYに位置している。
i)スプライスアクセプター配列、
ii)内部リボソーム進入配列又は高い自己切断効率の2Aペプチド、
iii)Kozak配列、及び
iv)それらの組み合わせから独立して選択される調節エレメントをさらに含む。
従って、一実施形態では、導入遺伝子カセットは、i)又はii)又はiii)又はiv)を含む。
表1
本開示はまた、本明細書に開示されているプラスミドなどのウイルス又はウイルス成分/構築物の新規配列に関する。
5’ITR-B1-BA-B2-BX-BB-BY-B3-3’ITR(I)
式中、B1はE1A、E1B又はE1A-E1Bを含み、BAはE2B-L1-L2-L3-E2A-L4を含み、B2は結合であるか又はE3を含み、BXは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えば外因性プロモーターの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、BBはL5を含み、BYは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、B3は結合であるか又はE4を含み、ここで、BX及びBYの少なくとも一方は結合ではなく、導入遺伝子又は制限部位又はその両方を含み、少なくとも2つの結合ドメインを含む多重特異性抗原分子をコードし、前記ドメインの少なくとも1つは対象のT細胞上の表面抗原に対して特異的である、式(I)の配列を含むゲノムを含む。一実施形態では、アデノウイルスは、B1 BXが結合である式(I)の配列を含むゲノムを含む。
5’ITR-BA-B2-BX-BB-BY-B3-3’ITR(Ia)
式中、BAはE2B-L1-L2-L3-E2A-L4を含み、B2は結合であるか又はE3を含み、BXは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えば外因性プロモーターの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、BBはL5を含み、BYは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子、)又はその両方を含むDNA配列であり、B3は結合であるか又はE4を含み、ここで、BX及びBYの少なくとも一方は結合ではなく、少なくとも1つは導入遺伝子などの導入遺伝子又は制限部位を含む、式(Ia)の配列を含むゲノムを含む。
5’ITR-BA-BX-BB-BY-B3-3’ITR Ib(Ib)
式中、BAはE2B-L1-L2-L3-E2A-L4を含み、BXは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えば外因性プロモーターの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、BBはL5を含み、BYは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、B3は結合であるか又はE4を含み、ここで、BX及びBYの少なくとも一方は結合ではなく、導入遺伝子などの導入遺伝子又は制限部位又はその両方を含む、式(Ib)の配列を含むゲノムを含む。
5’ITR-BA-B2-BX-BB-BY-3’ITR(Ic)
式中、BAはE2B-L1-L2-L3-E2A-L4を含み、B2はE3であり、BXは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えば外因性プロモーターの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、BBはL5を含み、BYは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、ここで、BX及びBYの少なくとも一方は結合ではなく、導入遺伝子などの導入遺伝子又は制限部位又はその両方を含む、式(Ic)の配列を含むゲノムを含む。
5’ITR-B1-BA-BX-BB-BY-B3-3’ITR(Id)
式中、B1はE1A、E1B、又はE1A-E1Bを含み、BAはE2B-L1-L2-L3-E2A-L4を含み、BXは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えば外因性プロモーターの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、BBはL5を含み、BYは結合であるか又は制限部位、1つ又は複数の導入遺伝子(特に、例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする導入遺伝子)又はその両方を含むDNA配列であり、B3は結合であるか又はE4を含み、ここで、BX及びBYの少なくとも一方は結合ではなく、導入遺伝子、制限部位、又はその両方を含む、式(Id)の配列を含むゲノムを含む。
5’ITR-B1-BA-B2-BB-BY-3’ITR(Ie)
式中、B1はE1A、E1B、又はE1A-E1Bを含み、BAはE2B-L1-L2-L3-E2A-L4を含み、B2はE3を含み、BBはL5を含み、BYは結合であるか又は(例えばMPLのような内因性プロモーターの制御下又はCMVプロモーターなどの外因性プロモータの制御下にある)本開示による少なくとも1つの二重特異性T細胞アクチベーターをコードする1つ又は複数の導入遺伝子を含むDNA配列であり、ここで、BX及びBYの少なくとも一方は結合ではなく、導入遺伝子、制限部位、又はその両方を含む、式(Ie)の配列を含むゲノムを含む。
本明細書で使用されるプロモーターは、特定の1つ又は複数の遺伝子の転写を開始するDNAの領域を意味する。プロモーターは一般に、それらが転写する遺伝子に近接して、DNA上の同じ鎖上及び上流(すなわち5’)に位置する。これに関連して用いられる近位とは、プロモーターとして機能するのに十分近いことを意味する。一実施形態では、プロモーターは転写開始部位の100bp以内にある。従って、本明細書中で使用される内因性プロモーターは、導入遺伝子が挿入されているアデノウイルス(又は構築物)中に天然に存在する(すなわち原産の)プロモーターを指す。1つ又は複数の実施形態において、使用される内因性プロモーターは、ウイルスゲノム中のその元の位置にあるウイルス中の天然に存在するプロモーターであり、特にこれは、導入遺伝子又は導入遺伝子の発現に使用される一次又は唯一のプロモーターである。一実施形態では、導入遺伝子の翻訳及び任意選択で転写を促進するために使用される内因性プロモーターは、1つの常在するものであり、すなわちアデノウイルスのゲノムに組み込まれたものであって、組換え技術によって以前に導入されたものではない。
本明細書で使用される「遺伝子発現の調節因子」(又は調節因子/調節エレメント)は、典型的には転写又は翻訳を開始又は増強することによって遺伝子発現において役割を果たすプロモーター、エンハンサー又はスプライスアクセプター配列などの遺伝的特徴を指す。
本明細書中に記載されるように、ウイルス中の少なくとも1つの導入遺伝子は二重特異性T細胞アクチベーターをコードし、ここで1つの結合ドメインはT細胞表面抗原に特異的である。第2の結合ドメインは、適切な抗原、例えば病原体抗原、癌抗原、間質抗原を標的とし得る。
本開示はまた、本明細書中に記載されるようなウイルスの医薬製剤にも関する。
さらなる態様において、本開示は、治療、特に癌の治療に使用するための本明細書に記載のウイルス又はその製剤に及ぶ。
配列番号1 N末端シグナル配列及びC末端デカHis親和性タグを有する、抗EpCAM 二重特異性T細胞アクチベーター DNAコード配列
配列番号2 N末端シグナル配列及びC末端デカHis親和性タグを有する、抗EpCAM 二重特異性T細胞アクチベーター タンパク質配列
配列番号3 N末端シグナル配列及びC末端デカHis親和性タグを有する、抗FAP 二重特異性T細胞アクチベーター DNAコード配列
配列番号4 N末端シグナル配列及びC末端デカHis親和性タグを有する、抗FAP 二重特異性T細胞アクチベーター アミノ酸配列
配列番号5 N末端シグナル配列及びC末端デカHis親和性タグを有する、コントロール(抗FHA)二重特異性T細胞アクチベーター DNAコード配列
配列番号6 N末端シグナル配列及びC末端デカHis親和性タグを有する、コントロール(抗FHA)二重特異性T細胞アクチベーター アミノ酸配列
配列番号7 抗CD3 ScFv のアミノ酸配列
配列番号8 抗CD3 VH
配列番号9 抗CD3 VL
配列番号10 抗CD3 ScFvリンカー配列
配列番号11 抗FAP ScFv
配列番号12 抗FAP VLドメイン
配列番号13 抗FAP VHドメイン
配列番号14 抗FAP及び抗EpCAMリンカー配列
配列番号15 二重特異性T細胞アクチベーターリーダー配列
配列番号16 抗EpCAM ScFv
配列番号17 抗EpCAM VL
配列番号18 抗EpCAM VH
配列番号19 コントロール二重特異性T細胞アクチベーター(抗FHA)
配列番号20 コントロール(抗FHA)のScFv
配列番号21 コントロール(抗FHA)VL
配列番号22 コントロール(抗FHA)VH
配列番号23 コントロール(抗FHA)ScFvリンカー配列
配列番号24 デカ-Hisタグ配列
配列番号25 FAP 二重特異性T細胞アクチベーター-P2A-RFP(斜字体=リーダー、太字=フリン切断部位、下線=P2A配列、小文字=RFP)
配列番号26 コントロール(抗FHA)二重特異性T細胞アクチベーター-P2A-RFP(斜字体=リーダー、太字=フリン切断部位、下線=P2A配列、小文字=RFP)
配列番号27 ヒトEpCAMのDNAコード配列
配列番号28 ヒトEpCAMのアミノ酸配列
配列番号29 ヒトFAPのDNAコード配列
配列番号30 ヒトFAPのアミノ酸配列
配列番号31 CMVプロモーター配列
配列番号32 SV40後期ポリアデニル化配列
配列番号33 Null配列
配列番号34 NG-601(EnAd-CMV-EpCAM二重特異性T細胞アクチベーター)
配列番号35 NG-602(EnAd-SA-EpCAM二重特異性T細胞アクチベーター)
配列番号36 NG-605(EnAd-CMV-FAP二重特異性T細胞アクチベーター)
配列番号37 NG-606(EnAd-SA-FAP二重特異性T細胞アクチベーター)
配列番号38 EnAdゲノム
配列番号39 EnAdゲノムの塩基対28166~28366に対応しかつこれを含むBX DNA配列
配列番号40 EnAdゲノムの塩基対29345~29379に対応し、かつこれを含むBY DNA配列
配列番号41 HISタグ
配列番号42 スプライスアクセプター配列
配列番号43 SV40ポリアデニル化配列
配列番号44 EpCam 二重特異性T細胞アクチベーター核酸配列(OKT3)
配列番号45 FAP 二重特異性T細胞アクチベーター核酸配列(OKT3)
配列番号46 FAP 二重特異性T細胞アクチベーター核酸配列(aCD3)
配列番号47 NG-611導入遺伝子カセット
配列番号48 NG-612導入遺伝子カセット
配列番号49 NG-613 導入遺伝子カセット
配列番号50 制限部位挿入物(BX)
配列番号51 制限部位挿入物(BY)
配列番号52 CMVプロモーター配列
配列番号53 PGKプロモーター配列
配列番号54 CBAプロモーター配列
配列番号55 短いスプライスアクセプター(SSA)DNA配列
配列番号56 スプライスアクセプター(SA)DNA配列
配列番号57 分岐スプライスアクセプター(bSA)DNA配列
配列番号58 コザック配列(null配列)
配列番号59 開始コドンの例
配列番号60 内部リボソーム進入配列(IRES)
配列番号61 P2Aペプチド
配列番号62 F2Aペプチド
配列番号63 E2Aペプチド
配列番号64 T2Aペプチド
配列番号65 ポリアデニル化(ポリA)配列
配列番号66 リーダー配列
配列番号67 リーダー配列
配列番号68 IFNΓアミノ酸配列
配列番号69 IFNαアミノ酸配列
配列番号70 TNFαアミノ酸配列
配列番号71 EnAdゲノム(塩基対10355~5068)のE2B領域に対応するDNA配列
配列番号72 N末端シグナル配列及びC末端デカHis親和性タグを有する、抗EpCAM 二重特異性T細胞アクチベーター DNAコード配列
配列番号73 N末端シグナル配列を有するが、C末端デカHis親和性タグを有さない、抗EpCAM 二重特異性T細胞アクチベータータンパク質配列
配列番号74 N末端シグナル配列を有するが、C末端デカHis親和性タグを有さない、抗FAP 二重特異性T細胞アクチベーター DNAコード配列
配列番号75 N末端シグナル配列を有するが、C末端デカHis親和性タグを有さない、抗FAP 二重特異性T細胞アクチベーターアミノ酸配列
配列番号76 N末端シグナル配列を有するが、C末端デカHisの親和性タグを有さない、コントロール(抗FHA)の二重特異性T細胞アクチベーター DNAコード配列
配列番号77 N末端シグナル配列を有するが、C末端デカHis親和性タグを有さないコントロール(抗FHA)二重特異性T細胞アクチベーターアミノ酸配列
配列番号78 C末端デカHis親和性タグを有さない、コントロール二重特異性T細胞アクチベーター(抗FHA)
配列番号79 デカHis親和性タグを有さない、NG-601(EnAd-CMV-EpCAM二重特異性T細胞アクチベーター)
配列番号80 デカHis親和性タグを有さない、NG-602(EnAd-SA-EpCAM二重特異性T細胞アクチベーター)
配列番号81 デカHis親和性タグを有さない、NG-605(EnAd-CMV-FAP二重特異性T細胞アクチベーター)
配列番号82 デカHis親和性タグを有さない、NG-606(EnAd-SA-FAP二重特異性T細胞アクチベーター)
配列番号83 EpCam 二重特異性T細胞アクチベーター核酸配列(OKT3)
配列番号84 Null配列
配列番号85 FAP 二重特異性T細胞アクチベーター核酸配列(OKT3)
配列番号86 Null配列
配列番号87 FAP 二重特異性T細胞アクチベーター核酸配列(aCD3)
配列番号88 NG-611導入遺伝子カセット
配列番号89 NG-612導入遺伝子カセット
配列番号90 NG-613導入遺伝子カセット
配列番号91 NG-614導入遺伝子カセット
配列番号92 NG-617導入遺伝子カセット
配列番号93 EpCam 二重特異性T細胞アクチベーターアミノ酸配列(OKT3)
配列番号94 FAP 二重特異性T細胞アクチベーターアミノ酸配列(OKT3)
配列番号95 FAP 二重特異性T細胞アクチベーターアミノ酸配列(aCD3)
配列番号96 NG-611ゲノム
配列番号97 NG-612ゲノム
配列番号98 NG-613ゲノム
配列番号99 NG-614ゲノム
配列番号100 NG-617ゲノム
配列番号101 NG-615ゲノム
配列番号102 NG-640ゲノム
配列番号103 NG-641ゲノム
配列番号104 Null配列
配列番号105 Flt3L核酸配列
配列番号106 Null配列
配列番号107 MIP1α核酸配列
配列番号108 フレキシブルリンカー配列
配列番号109 IFNα核酸配列
配列番号110 CXCL10核酸配列
配列番号111 CXCL9核酸配列
配列番号112 NG-615導入遺伝子カセット
配列番号113 NG-640導入遺伝子カセット
配列番号114 NG-641導入遺伝子カセット
配列番号115 FLT3Lアミノ酸配列
配列番号116 MIP1αアミノ酸配列
配列番号117 IFNαアミノ酸配列
配列番号118 CXCL9アミノ酸配列
配列番号119 CXCL10アミノ酸配列
配列番号120 NG-618ゲノム
配列番号121 NG-618 EpCam 二重特異性T細胞アクチベーター核酸配列
配列番号122 NG-618 FAP 二重特異性T細胞アクチベーター核酸配列
配列番号123 NG-618導入遺伝子カセット
配列番号124~297 リンカー配列
配列番号298 NG-616ゲノム
この実施例に記載したように、組換え二重特異性T細胞アクチベーターを設計し、タンパク質を産生した。
二重特異性T細胞アクチベーターは、特異性の異なる2本の一本鎖抗体フラグメント(ScFv)を、柔軟なGly4Serリンカーと連結することによって生成される。ScFvは、親モノクローナル抗体からのVH及びVLドメインをリンカーによって連結することによって生成される。各二重特異性T細胞アクチベーターは、哺乳動物分泌のためのN末端シグナル配列及び検出及び精製のためのC末端デカヒスチジン親和性タグを用いて設計された。二重特異性T細胞アクチベーターは標準的なDNAクローニング技術によって操作され、タンパク質発現ベクターに挿入された(図1)。抗EpCAM 二重特異性T細胞アクチベーターは、特許WO2005040220(その中の配列番号63)からのものであり、シグナル配列及び親和性タグが付加されている。抗FAP 二重特異性T細胞アクチベーターは、シグナル配列及び親和性タグを付加して、特許WO2010037835A2からの抗FAP ScFv及び特許WO2005040220(その中の配列番号63)からの抗CD3 ScFvを用いて新たに作成された。コントロール二重特異性T細胞アクチベーターは、Husseinら、2007年からの抗FHA(Bordetella pertussis由来の糸状赤血球凝集素)ScFv(Hussein AHら、(2007)“Construction and characterization of single-chain variable fragment antibodies directed against the Bordetella pertussis surface adhesins filamentous hemagglutinin and pertactin”.Infect Immunity 75、5476~5482)及び特許WO2005040220(その中の配列番号63)からの抗CD3 ScFvを、シグナル配列及び親和性タグを加えて使用した。これらの二重特異性T細胞アクチベーターのDNAコード配列及びアミノ酸配列は、配列番号1~6である。
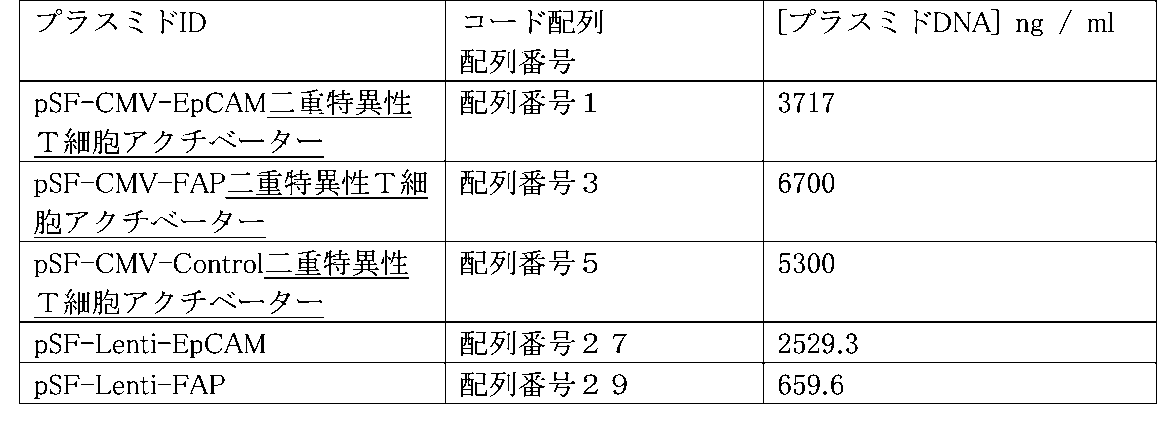
タンパク質発現を駆動するためにCMVプロモーター(配列番号31)を使用して、それぞれの配列をpSF-CMVベクターにクローニングすることによって、組換え二重特異性T細胞アクチベータータンパク質を産生した(図1)。プラスミド、pSF-CMV-EpCAM二重特異性T細胞アクチベーター、pSF-CMV-FAP二重特異性T細胞アクチベーター及びpSF-CMV-Control二重特異性T細胞アクチベーター(表2)のプラスミドDNAの濃度をNanoDropにより測定した。空のpSF-CMVベクターはネガティブコントロールとして含む。それぞれ54.7μgを4mLのOptiMEMで希釈した。109.2μgのPEI(線状、MW25000、Polysciences、米国)を4mLのOptiMEM培地で希釈し、4mlの希釈DNAと混合してDNA-PEI複合体を生成した(DNA:PEI比1:2(w/w))。室温で20分間インキュベートした後、混合物をOptiMEMで18mLまで補充し、このトランスフェクション混合物を90%の集密度でAd293細胞を含むT175フラスコに加えた。細胞をトランスフェクション混合物と共に37℃、5%CO2で4時間インキュベートした後、30mLの細胞培地(グルタミン補充DMEM高グルコース、フェノールレッド不含)を細胞に加え、フラスコを37℃、5%CO2で48時間インキュベートした。効率的なトランスフェクション効率を確保するために、別の細胞のフラスコにpSF-CMV-GFPを並行してトランスフェクトした。分泌タンパク質を回収するために、トランスフェクトした細胞の上清を回収し、細胞成分を除去するために4℃で5分間350gで遠心分離した(Allegra X-15R、Beckman Coulter)。上清を10k MWCO Amicon Ultra-15遠心フィルターユニット(Millipore)に移した。4750rpm及び4℃で回転させた後、50倍高い濃度を得るためにフロースルーを用いて保持液の体積を調整した。濃縮タンパク質のアリコートを-80℃で保存した。
表2
命名構築物において接頭辞として使用される「p」は、構築物がプラスミドであることを示す。
二重特異性T細胞アクチベーターを検出するために、C末端デカヒスチジン親和性タグを、ウエスタンブロッティングの技術を用いて抗His抗体でプローブすることができる。タンパク質サンプルを溶解緩衝液で、β-メルカプトエタノール及びSDSを含む2.5μLの6×Laemmli SDSサンプル緩衝液を含む15μLの最終容量に調整した。サンプルを95℃で5分間インキュベートしてタンパク質を変性させ、15ウェルの10%プレキャストポリアクリルアミドゲル(Mini-PROTEAN TGX Precast Gels、BioRad、英国)にロードした。Mini-PROTEAN Tetra System(BioRad、UK)内の1×ランニングバッファー中でゲルを180 Vで45分間泳動した。SDSゲルからのタンパク質を、Mini Trans-Blot Cell(BioRad、英国)内の1×転写緩衝液中、300mA及び4℃で90分間の湿式エレクトロブロッティングによってニトロセルロース膜上に転写した。熱を制限するためにアイスパックの存在下で移動を行った。次いでニトロセルロース膜を室温で1時間シェーカー上でPBS-T中の5%ミルクでブロッキングし、抗His(C末端)抗体(マウスα- 6xHis、クローン3D5、Invitrogen、UK、#46~0693))でプローブし、PBS/5%ミルクで1:5000に希釈した。振盪機上で一晩4℃でインキュベートした後、膜を洗浄し、HRP標識ポリクローナル二次α-マウス-免疫グロブリン-抗体(PBS/5%ミルク中1:10.000、Dako、#P0161)で1時間室温でプローブした。視覚化のために、SuperSignal West Dura Extended Duration Substrate(Thermo Fisher Scientific、英国)を製造元の指示に従って適用し、X線フィルムに露光し、自動フィルムプロセッサーで現像した。結果は、二重特異性T細胞アクチベーター発現プラスミドをトランスフェクトしたが、親ベクターはトランスフェクトしていないAd293細胞からの二重特異性T細胞アクチベータータンパク質の発現及び分泌を示した。
組換え二重特異性T細胞アクチベータータンパク質の量を測定するために、ドットブロットの技術を用いて二重特異性T細胞アクチベーターシグナルをHisタグ付き(C末端10His)タンパク質標準物質(10×Hisタグ付きヒトカテプシンD、Biolegend、#556704)と比較した。二重特異性T細胞アクチベーターサンプル及びタンパク質標準物質の2倍段階希釈物を調製し、それぞれ1.5μLをニトロセルロース膜に直接塗布し、20分間風乾した。次いで、ウエスタンブロッティングについて上述したブロッキング及び染色プロトコルを実施した。タンパク質標準物質のモル濃度は、250μg/ mLの二重特異性T細胞アクチベーター濃度を表すように調整した。結果(図2A)は、二重特異性T細胞アクチベーター発現プラスミドをトランスフェクトしたAd293細胞からの二重特異性T細胞アクチベータータンパク質の発現及び分泌を実証した。
FAP 二重特異性T細胞アクチベーターのFAP結合活性及びpSF-CMV-FAP二重特異性T細胞アクチベーター又はpSF-CMV-Control二重特異性T細胞アクチベーターでトランスフェクトした細胞から分泌されたコントロール(抗FHA)二重特異性T細胞アクチベーター(配列番号4及び6)は、酵素結合免疫吸着検定法(ELISA)によって評価した。空のpSF-CMVベクター上清をネガティブコントロールとして含めた。PBS緩衝液中のヒトFAP/セプラーゼタンパク質(100ng/ウェル、Sino Biological Inc、10464-H07H-10)で4℃で一晩コーティングすることによって、ELISAプレート(Nunc Immuno MaxiSorp 96ウェルマイクロプレート)を調製した。その後の全ての結合工程の間に、プレートをPBS 0.05%Tween 20で洗浄した。プレートを、PBS 0.05%Tween 20中5%BSAで、室温で1時間ブロッキングした。一定量の二重特異性T細胞アクチベータータンパク質、又は空のpSF-CMVベクターをトランスフェクトしたウェルから採取したタンパク質を、PBS/5% BSA/0.05% Tween 20で10倍希釈した。全てのサンプルをFAPコートプレートに添加し、室温で2時間インキュベートした。検出抗体である抗His(C末端)抗体(マウス抗6xHis、クローン3D5、Invitrogen、英国、#46~0693)を1:1000に希釈し、室温で1時間適用した。次いで、HRP結合抗マウスFc(PBS/5%ミルク中1:1000、Dako)を室温で1時間適用した後、HRP基質溶液3.3.5.5’-テトラメチルエチレンジアミン(TMB、Thermo-Fisher)を用いてHRP検出を実施した。停止溶液を使用して反応を停止させ、発色をプレートリーダーで450nmで測定した。450nmでの吸光度をFAP 二重特異性T細胞アクチベーター、コントロール二重特異性T細胞アクチベーター及び空のベクター上清についてプロットしたところ、FAP 二重特異性T細胞アクチベーターのFAPタンパク質への特異的結合が示された。結果(図2B)は、組換えFAPタンパク質へのコントロール二重特異性T細胞アクチベーターではなく、FAP 二重特異性T細胞アクチベーターの特異的結合を示す。
EpCAM 二重特異性T細胞アクチベーターのEpCAM結合活性及びpSF-CMV-EpCAM二重特異性T細胞アクチベーター又はpSF-CMV-Control二重特異性T細胞アクチベーターでトランスフェクトした細胞から分泌されたコントロール二重特異性T細胞アクチベーター(配列番号2及び6)は、酵素結合免疫吸着検定法(ELISA)によって評価した。空のpSF-CMVベクター上清をネガティブコントロールとして含める。PBS緩衝液中のヒトEpCAM/TROP-1タンパク質(50ng/ウェル、Sino Biological Inc、#10694-H02H-50)で4℃で一晩コーティングすることによって、ELISAプレート(A Nunc Immuno MaxiSorp 96ウェルマイクロプレート)を調製した。その後の全ての結合工程の間に、プレートをPBS 0.05%Tween 20で洗浄した。プレートを、PBS 0.05%Tween 20中5%BSAで、室温で1時間ブロッキングした。一定量の二重特異性T細胞アクチベータータンパク質、又は空のpSF-CMVベクターをトランスフェクトしたウェルから採取したタンパク質を、PBS/5% BSA/0.05% Tween 20で10倍希釈した。全てのサンプルをEpCAM被覆プレートに添加し、室温で2時間インキュベートした。検出抗体である抗His(C末端)抗体(マウス抗6xHis、クローン3D5、Invitrogen、英国、#46~0693)を1:5000に希釈し、室温で1時間適用した。次いで、HRP結合抗マウスFc(PBS/5%ミルク中1:1000、Dako)を室温で1時間適用した後、HRP基質溶液3.3.5.5’-テトラメチルエチレンジアミン(TMB、Thermo-Fisher)を用いてHRP検出を実施した。停止溶液を使用して反応を停止させ、発色をプレートリーダーで450nmで測定した。450nmでの吸光度をEpCAM 二重特異性T細胞アクチベーター、コントロール二重特異性T細胞アクチベーター及び空のベクター上清についてプロットしたところ、EpCAM 二重特異性T細胞アクチベーターの組換えEpCAMへの特異的結合が実証された。結果(図2C)は、EpCAM 二重特異性T細胞アクチベーターの特異的結合を示し、コントロール二重特異性T細胞アクチベーターの組換えEpCAMタンパク質への特異的結合は示さない。
二重特異性T細胞アクチベーター導入遺伝子保有EnAdウイルスを構築する前に、組換え二重特異性T細胞アクチベータータンパク質の機能活性をいくつかの異なるアッセイで評価した。
健康なドナーの新鮮なヒト血液サンプルから、又はオックスフォードのNHS Blood and Transplant UKから入手した全血白血球コーンからのいずれかからの、ヒトPBMCを密度勾配遠心分離によって単離した。いずれの場合も、サンプルをPBSで1:2に希釈し、この混合物25mLを50mLのFalconチューブ中の13mLのFicoll(1.079g/mL、Ficoll-Paque Plus、GE Healthcare)上に重層した。相分離を維持するために最低の減速設定でサンプルを22℃で30分間1600rpmで遠心分離した(Allegra X-15R、Beckman Coulter)。遠心分離後、4層は、上部に血漿層を、続いてPBMC含有界面、フィコール層、及び底部に赤血球及び顆粒球の層を含むことが観察できた。パスツールピペットを用いてPBMCを回収し、PBS(室温で10分間1200rpm)で2回洗浄し、10%FBSを補充したRPMI培地に再懸濁した。
製造元のプロトコルに従って、Pan T細胞単離キット(Miltenyi Biotec、#130-096-535)を使用して、非CD3細胞を枯渇させることにより、PBMCからCD3陽性(CD3+)T細胞を抽出した。
チャーチル病院(オックスフォード大学病院)腫瘍病棟の卵巣癌、膵臓癌、乳癌及び胃癌を含むがこれらに限定されない複数の適応症を有する患者から、一次ヒト腹水サンプルを受け取った。受け取ると、保存と将来の分析のために、細胞及び液体画分を、-20℃で凍結した流体のアリコートで、分離した。製造元の指示に従って、細胞画分を赤血球溶解緩衝液(Roche、#11814389001)で処理して赤血球を除去した。各サンプル中に存在する細胞型を、EpCAM、EGFR、FAP、CD45、CD11b、CD56、CD3、CD4、CD8、PD1及びCTLA4について染色することによって決定し、フローサイトメトリーによって分析した。次いで細胞をエクスビボ T細胞活性化及び標的細胞溶解実験のために新鮮に使用した。場合によっては、後の実験で使用するために、細胞を10% FBSを補ったDMEM中で継代した。
表3で特定されるように、別段の記載がない限り、すべての細胞株は、10%(v/v)のウシ胎児血清(FBS、ギブコ(商標))及び1%、(v/v)のペニシリン/ストレプトマイシン(10mg/mL、Sigma-Aldrich社、英国)で補充し、DMEM(Sigma-Aldrich社、英国)又はRPMI培地(Sigma-Aldrich社、英国)で、加湿インキュベーター(MCO-17AIC、三洋)内で、37℃で及び5% CO2で維持した。トリプシン/EDTA(0.05%トリプシン、0.02% EDTA、Sigma-Aldrich、英国)による酵素的解離によって密集度に達する前に、細胞を2~3日毎に分割した。このプロセスでは、培地を吸引し、細胞を15mlのPBSで洗浄し、続いて細胞を2mLのトリプシン/EDTAで2~10分間37℃で処理した。トリプシンを10% FBSを含む10mLのDMEMで中和し、細胞の一部を新しい培地を含む新しいフラスコに移した。日常的な細胞培養のために、2% FBSを含む感染及びウイルスプラスミドトランスフェクションのため、ならびにFBSを含まない組換え二重特異性T細胞アクチベータープラスミドトランスフェクションのために、培地に10% FBSを補った。
表3
2つの条件が比較されている場合は、t検定を使用して統計分析が行われた。他の全ての場合において、統計分析は一元配置分散分析を用いて行った。
正常ヒト皮膚線維芽細胞(NHDF)の存在下又は非存在下でFAP 二重特異性T細胞アクチベーターがT細胞活性化を誘導する能力を比較した。ヒトCD3+T細胞(96ウェルU底プレート中、1ウェルあたり70,000細胞)を培地単独又は300ng/mLのFAP又はコントロール二重特異性T細胞アクチベーターの存在下で、単独で又はNHDF細胞(10:1 T:NHDF)と共培養した。細胞を37℃で24時間共培養し、続いて無酵素細胞解離緩衝液(Thermo、#13151014)で採取した。次いで、CD45+T細胞上のCD69(図3A)及びCD25(図3B)の発現レベルを、抗体染色及びフローサイトメトリーによって分析し、幾何平均蛍光(gMFI)値として表した。プレート固定化抗CD3抗体(7.5μg/mL)をT細胞活性化のためのポジティブコントロールとして使用した。FAP 二重特異性T細胞アクチベーターは、T細胞上の活性化マーカーCD69及びCD25の発現を選択的に誘導し、それがT細胞を活性化することができたことを示している。
実施例2の実験と同様の一連の実験を行って、組換えEpCAM 二重特異性T細胞アクチベータータンパク質を特徴付けた。
EpCAM陽性DLD細胞株の存在下又は非存在下でEpCAM 二重特異性T細胞アクチベーターがT細胞活性化を誘導する能力を比較した。ヒトCD3+T細胞(96ウェルU底プレート中、1ウェルあたり70,000細胞)を培地単独又は600ng/mLのEpCAM又はコントロール二重特異性T細胞アクチベーターの存在下で、単独又はDLD細胞(10:1 T:DLD)と共培養した。細胞を37℃で24時間共培養し、続いて無酵素細胞解離緩衝液を用いて採取した。次いで、CD45+T細胞上のCD69及びCD25の発現レベルを、抗体染色及びフローサイトメトリーによって分析し、データを幾何平均蛍光(gMFI)値として表した。プレート固定化抗CD3抗体(7.5μg/mL)をT細胞活性化のポジティブコントロールとして使用した。EpCAM 二重特異性T細胞アクチベーターはT細胞上の活性化マーカーCD69及びCD25の発現を選択的に誘導し、それがT細胞を活性化することができたことを示している(図4B及びC)。
この実施例では、組換えFAP 二重特異性T細胞アクチベーター活性化T細胞が、線維芽細胞標的細胞の死滅を誘導する能力を評価した。
実施例4と同様の研究を用いて、標的腫瘍細胞の死滅を誘導する組換えEpCAM 二重特異性T細胞アクチベーター活性化T細胞の能力を評価した。
DLD腫瘍細胞(7,000細胞)を、培地単独又は300ng/mLのコントロールもしくはEpCAM 二重特異性T細胞アクチベーターの存在下で、U底96ウェルプレートのウェル中で70,000個のT細胞と共培養した。24時間の共培養の後、上清を回収し、細胞傷害性をLDHアッセイにより測定した。図8Bの結果は、EpCAM 二重特異性T細胞アクチベーターがDLD細胞の溶解を有意に増加させたことを示す(DLD細胞上のEpCAM発現を図8Cに示す)。
FAPを発現する安定なCHO及びAd293細胞株を、親非トランスフェクト細胞と比較することによってFAP 二重特異性T細胞アクチベーターのFAP抗原特異性を実証するための手段として生成した。
FAP遺伝子のタンパク質配列は、NCBIデータベース(配列番号30)から得られ、Oxford Genetics Ltd(オックスフォード、英国)によって合成されたDNAコード配列を生成するために逆転写された。FAP遺伝子を、pSF-Lenti-FAPベクターを産生する標準的なクローニング技術によってpSF-Lentiベクターにクローニングした。HEK293T細胞を、pSF-CMV-HIV-Gag-Pol、pSF-CMV-VSV-G、pSF-CMV-HIV-Revと共にレンチウイルスFAP発現ベクターでトランスフェクトした。リポフェクタミン2000を、トランスフェクション試薬として使用し、1:2のDNA:リポフェクタミン比でベクターDNAに添加し、37℃で細胞と共にインキュベートした。レンチウイルスを含む上清を48時間後に回収し、ポリブレンと混合した(最終濃度、8μg/mL)。レンチウイルス/ポリブレン混合物を、播種したAd293又はCHO細胞に添加し、37℃でインキュベートした。4日目に、上清をピューロマイシン(Ad293について2μg/mL及びCHOについて7.5μg/mL)を含有する培地と交換した。次に安定な変異体をクローン選択し、親細胞株又は安定にトランスフェクトした変異体のFAP発現を、FAP又は同位体対照抗体で染色することによって決定し、フローサイトメトリーによって分析した(図11A)。
CHO又はCHO-FAP細胞(7,000細胞)を、培地単独又は2μg/mLコントロールもしくはFAP 二重特異性T細胞アクチベーターの存在下で、U底96ウェルプレートのウェル中で、単独で又はヒトT細胞(70,000個)と共培養した。24時間のインキュベーション後、上清を回収し、標的細胞の細胞傷害性を、実施例4に記載のようにLDH細胞傷害性アッセイによって測定した(図11B)。T細胞活性化はまた、フローサイトメトリーによってCD69及びCD25の発現レベルを分析することによっても決定された(図12)。細胞傷害性は、CHO-FAP細胞をT細胞及びFAP 二重特異性T細胞アクチベーターと共に培養した場合にのみ観察された。これは、FAP 二重特異性T細胞アクチベーターが媒介するT細胞活性化及び標的細胞溶解が非常に特異的であり、FAP発現細胞に限定され、FAP陰性親細胞株ではないことを示している。
EpCAMを発現する安定なCHO及びAd293細胞株は、親非トランスフェクト細胞と比較することによって、EpCAM 二重特異性T細胞アクチベーターのEpCAM抗原特異性を実証するための手段として生成した。
EpCAM遺伝子のタンパク質配列は、NCBIデータベース(配列番号28)から得られ、Oxford Genetics Ltd(オックスフォード、英国)によって合成されたDNAコード配列を生成するために逆転写された。EpCAM遺伝子を、pSF-Lenti-EpCAMベクターを産生する標準的なクローニング技術によってpSF-Lentiベクターにクローニングした。HEK293T細胞を、pSF-CMV-HIV-Gag-Pol、pSF-CMV-VSV-G、pSF-CMV-HIV-Revと共にレンチウイルスEpCAM発現ベクターでトランスフェクトした。リポフェクタミン2000をトランスフェクション試薬として使用し、1:2のDNA:リポフェクタミン比でベクターDNAに添加し、37℃で細胞と共にインキュベートした。レンチウイルスを含む上清を48時間後に回収し、ポリブレンと混合した(最終濃度、8μg/mL)。レンチウイルス/ポリブレン混合物を、播種したAd293又はCHO細胞に添加し、37℃でインキュベートした。4日目に、上清をピューロマイシン(Ad293について2μg/mL及びCHOについて7.5μg/mL)を含有する培地と交換した。次に安定な変異体をクローン選択し、親細胞株又は安定にトランスフェクトした変異体のEpCAM発現を、EpCAM又は同位体対照抗体で染色することによって決定し、フローサイトメトリーによって分析した(図13A)。
CHO又はCHO-EpCAM細胞(7,000細胞)を、培地単独又は2μg/mLコントロールもしくはEpCAM 二重特異性T細胞アクチベーターの存在下で、U底96ウェルプレートのウェル中で、単独で又はヒトT細胞(70,000個)と共培養した。24時間のインキュベーション後、上清を回収し、標的細胞の細胞傷害性をLDH細胞傷害性アッセイによって測定した(図13B)。T細胞活性化はまた、フローサイトメトリーによってCD69及びCD25の発現レベルを分析することによっても決定された(図14)。細胞傷害性は、CHO-EpCAM細胞をT細胞及びEpCAM 二重特異性T細胞アクチベーターと共に培養した場合にのみ観察された。これは、EpCAM 二重特異性T細胞アクチベーター媒介T細胞活性化及び標的細胞溶解が非常に特異的であり、EpCAM発現細胞に限定され、EpCAM陰性の親細胞株ではないことを示している。
さらなる実験において、組換えFAP 二重特異性T細胞アクチベータータンパク質がCD4又はCD8 T細胞を活性化する能力及びこれらのT細胞サブセットのそれぞれがNHDF細胞を溶解する能力を評価した。CD3+T細胞(35,000個)を、U底96ウェルプレートのウェル中で300ng/mLのコントロール又はFAP 二重特異性T細胞アクチベーターの存在下で、7,000個のNHDF細胞と共培養し、37℃で24時間インキュベートした。細胞を採取し、CD4又はCD8ならびにCD69及びCD25について抗体で染色し、フローサイトメトリーにより分析した。結果(図15A)は、FAP 二重特異性T細胞アクチベーターがCD4+及びCD8+T細胞の両方において活性化マーカーCD69及びCD25の増加を誘導することを実証した。
EpCAM 二重特異性T細胞アクチベーターがCD4+又はCD8+T細胞を活性化する能力及び各サブセットのDLD腫瘍細胞を溶解する能力を評価した。CD3+T細胞(35,000個)を、U底96ウェルプレートのウェル中で300ng/mLのコントロール又はEpCAM 二重特異性T細胞アクチベーターの存在下で、7,000個のDLD細胞と共培養し、37℃で24時間インキュベートした。細胞を採取し、CD4又はCD8ならびにCD69及びCD25について抗体で染色し、フローサイトメトリーにより分析した。結果(図16A)は、EpCAM 二重特異性T細胞アクチベーターがCD4+及びCD8+T細胞の両方において活性化マーカーCD69及びCD25の増加を誘導したことを実証した。
原発性悪性腹水からの自己腫瘍関連リンパ球のFAP 二重特異性T細胞アクチベーター媒介活性化の特徴付け
癌患者由来の細胞を用いて二重特異性T細胞アクチベータータンパク質の活性を評価するために、CD3+T細胞とFAP+細胞の両方を含む一次悪性腹水のサンプルを試験のために得た。未精製腹水細胞(従って、受け取ったときから変わらない)を、100%腹水又は500ng/mLコントロール又はFAP 二重特異性T細胞アクチベーターの存在下で、1%ヒト血清を補充した培地のいずれかに、U底96ウェルプレートのウェル当たり250,000細胞で播種した。未処置ウェルをネガティブコントロールとして用いた。37℃で5日間インキュベートした後、総細胞集団を採取し、CD3+T細胞の数(図17A)及びCD3+T細胞上のCD25の発現レベルを決定した(図17B)。1ウェルあたりの総細胞数は精密計数ビーズを用いて決定した。結果は、FAP 二重特異性T細胞アクチベーターが癌患者由来の腫瘍関連T細胞のT細胞活性化の有意な増加をもたらしたことを実証している。
以下に記載する方法を用いて、組換え二重特異性T細胞アクチベーター発現EnAdウイルスを操作し、産生し、そして精製した。
EnAdは、E2B領域におけるAd11pに対するAd3の頻繁な非相同的ヌクレオチド置換、ほぼ完全なE3欠失、及びE4orf4にマッピングされたより小さなE4欠失を含む、複製能力のあるキメラグループBアデノウイルスである(Kuhnら、Directed evolution generates a novel oncolytic virus for the treatment of colon cancer、PLoS One、2008年6月18日; 3(6):e2409)。この研究で使用したアデノウイルスのゲノムの略図を図18Aに示す。
表4
プラスミドEnAd2.4-CMV-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-SA-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-CMV-FAP二重特異性T細胞アクチベーター、pEnAd2.4-SA-FAP二重特異性T細胞アクチベーター、pEnAd2.4-CMV-コントロール二重特異性T細胞アクチベーター、pEnAd2.4-SA-コントロール二重特異性T細胞アクチベーターは、ライナーウイルスゲノムを生成するために、酵素AscIでの制限消化によって線状化された。消化したDNAをイソプロパノール抽出により精製し、300μl>95%分子生物学グレードのエタノール及び10μlの3M酢酸ナトリウム中で、-20℃で16時間沈殿させた。沈殿したDNAを14000rpmで5分間遠心分離することによってペレット化し、500μlの70%エタノールで洗浄した後、再び14000rpmで5分間遠心分離した。きれいなDNAペレットを風乾し、100μLの水に再懸濁した。6.25μgのDNAを、OptiMEM中でリポフェクタミントランスフェクション試薬15.6μLと混合し、20分間室温でインキュベートした。次いで、トランスフェクション混合物を、80%の密集度まで増殖させたAd293細胞を含むT-25フラスコに加えた。細胞をトランスフェクション混合物と共に37℃で4時間インキュベートした後、5%CO2 4mlの細胞培地(10% FBSを補充したグルタミンを含むDMEM高グルコース)を細胞に加え、フラスコを37℃、5%CO2でインキュベートした。トランスフェクトしたAd293細胞を24時間ごとにモニターし、48~72時間ごとに追加の培地を補充した。細胞単層における有意な細胞変性効果(CPE)の観察によってウイルスの産生をモニターした。広範囲のCPEが観察されたら、3回の凍結融解サイクルによってAd293細胞からウイルスを採取した。収集した溶解物を段階希釈し、Ad293細胞を再感染させ、単一のプラークを含むウェルを収集することによって、単一のウイルスクローンを選択した。ウイルスストックを増幅するために、感染が完全CPEに達したら、Ad293細胞の連続感染を行った。増幅中の生存ウイルス産生は、細胞単層中の有意なCPEの観察によって確認された。
強力なウイルスストックを増幅したら、二重塩化セシウム密度勾配遠心分離(バンディング)によってウイルスを精製して、NG-601、NG-602、NG-603、NG-604、NG-605及びNG-606ウイルスストックを生成した。製造元の指示に従って、これらのストックをmicoBCAアッセイ(Life Technologies)によって力価測定した(表5)。
表5
NG-601、NG-602、NG-603、NG-604、NG-605及びNG-606ウイルスの活性は、下記の方法を用いて特徴付けられた。
NG-601、NG-602、NG-603、NG-604、NG-605、NG-606又はEnAdが複製する能力を、A549肺癌細胞の感染によって分析し、qPCRによって評価した。A549細胞を24ウェルプレートのウェルに、2×105細胞/ウェルの細胞密度で播種した。細胞を細胞当たり100ウイルス粒子(ppc)で感染させるか又は未感染のままにする前に、プレートを37℃、5%CO2で18時間インキュベートした。感染の24、48又は72時間後にウェルを採取し、製造元のプロトコルに従ってPureLinkゲノムDNAミニキット(Invitrogen)を用いてDNAを精製した。全ウイルスゲノムを、表6に詳述した反応混合物中のEnAdヘキソン遺伝子特異的プライマー-プローブセットを用いて、各抽出サンプル又は標準物質を用いてqPCRにより定量化した。qPCRは表7のプログラムに従って実施した。
表6
細胞当たりの検出されたウイルスゲノムの数の定量化は、NG-601、NG-602、NG-603、NG-604、NG-605、NG-606及びEnAdウイルス複製がA549細胞株において同程度であることを実証した(図19A)。
ウイルスNG-601、NG-602、NG-605、NG-606が機能的二重特異性T細胞アクチベーターを産生するかどうかを決定するために、標的細胞としてCHO、CHO-EpCAM及びCHO-FAP細胞株を使用する、T細胞活性化アッセイを実施した。培養液中で100倍希釈したAd293ウイルス上清を含むU底96ウェルプレートのウェル中で、10,000個の標的細胞を50,000個のCD3+T細胞と共培養し、37℃、5%CO2で24時間インキュベートした。T細胞を採取し、CD25及びCD69に特異的な抗体で染色し、フローサイトメトリーにより分析した。結果(図20A及び20B)は、ウイルスNG-601及びNG-602が、CHO-EpCAM細胞と共培養するとT細胞を活性化する機能的二重特異性T細胞アクチベーター導入遺伝子を発現し、NG-605及びNG-606が、CHO-FAP細胞と共培養するとT細胞を活性化したが、CHO細胞と共培養すると活性化しなかった機能的二重特異性T細胞アクチベーター導入遺伝子を発現することを示した。
ヒト結腸癌細胞株DLDのNG-601、NG-602、NG-605、NG-606感染による二重特異性T細胞アクチベーター発現量を評価した。DLD細胞を、1ウェルあたり1.2×106細胞の密度で6ウェル培養プレートに播種した。播種18時間後、DLD細胞を100ppcでEnAd、NG-601、NG-602、NG-603、NG-604、NG-605、NG-606に感染させた。上清をウェルから回収する前に細胞を72時間培養し、細胞破片を除去するために1200rpmで5分間遠心分離した。次いで、清澄化した上清を、公知濃度の組み換え二重特異性T細胞アクチベーターを用いて作成した標準曲線と比較して細胞傷害性を用いて殺傷アッセイに使用し、ウイルス上清中の二重特異性T細胞アクチベーターの量を決定した。
FAP又はコントロール二重特異性T細胞アクチベーターをコードすることに加えて、NG-607、NG-608、NG-609、NG-610ウイルスはまた、蛍光顕微鏡法(配列番号25及び26、表4)を用いた感染細胞の視覚化のために、赤色蛍光タンパク質(RFP)導入遺伝子を担持する。これらのウイルスの機能活性は、下記の方法を用いて特徴付けられた。
ウイルスNG-607、NG-608、NG-609及びNG-610がそれらの二重特異性T細胞アクチベーター導入遺伝子を産生する能力をAd293細胞の感染によって評価した。Ad293細胞を1×106細胞/ウェルで6ウェルプレートにプレーティングした。細胞を100ppcでウイルスに感染させる前、又は未感染のままにする前に、プレートを37℃、5%CO2で24時間インキュベートした。感染後48時間で、プラークを蛍光水銀灯で照射し、写真撮影した(図23)。結果は、ウイルスNG-607、NG-608、NG-609及びNG-610がRFP導入遺伝子を発現することを示唆した。
次の一連の実験では、EnAd及びFAP、又はコントロール二重特異性T細胞アクチベーターウイルスNG-603、NG-604、NG-605、NG-606、NG-607、NG-608、NG-609、NG-610が、腫瘍細胞及び線維芽細胞を含む標的細胞を死滅させる能力評価した。
この一連の実験では、EnAd及びEpCAM又はコントロール二重特異性T細胞アクチベーターウイルスNG-601、NG-602、NG-603及びNG-604が腫瘍細胞及び線維芽細胞を含む標的細胞を死滅させる能力を評価した。
CD3+T細胞の存在下又は非存在下で、EnAd及びNG-601、NG-602、NG-603及びNG-604が、DLD腫瘍細胞を死滅させる能力をxCELLigence技術を用いて評価した。DLD細胞を1.2×104細胞/ウェルで48ウェルEプレートにプレーティングした。細胞を100ppcでEnAdに感染させるか、又は未感染のままにする前に、プレートを37℃、5%CO2で18時間インキュベートした。感染の2時間後、75,000個のCD3+T細胞を必要なウェルに加えた。XCELLigenceを用いて、15分ごとに標的細胞の細胞傷害性を測定した。結果(図30)は、NG-601及びNG-602が、T細胞依存的に、有意により迅速なDLD細胞傷害性をもたらすことを示す。
この実施例では、EnAd、NG-603、NG-604、NG-605及びNG-606による癌患者からのFAP+原発性悪性腹水由来の自己由来腫瘍関連リンパ球の活性化を評価した。さらなる分析に適していると考えられる患者サンプルは、CD3+T細胞及びFAP+細胞を含むものであった。
細胞株
HEK293A、DLD、SKOV3、MCF7、A431、A549、及びPC3細胞(ATCC)は、Roswell Park Memorial Institute(RPMI-1640、Sigma-Aldrich、英国)のDulbecco’s Modified Eagle’s Medium(DMEM、Sigma-Aldrich、英国)及びCHO細胞(ATCC)で培養した。増殖培地には、10%(v/v)ウシ胎児血清(FBS、Gibco、英国)及び1%(v/v)ペニシリン/ストレプトマイシン(10 mg/mL、Sigma-Aldrich)を補充し、細胞を加湿雰囲気中で37℃、5% CO2で維持した。ウイルス感染及びウイルスプラスミドトランスフェクションのために、細胞を2% FBSを補充したDMEM中で維持した。組換え二重特異性T細胞アクチベータープラスミドトランスフェクションのために、細胞をFBSなしでDMEM中に維持した。標的細胞株のEpCAM発現をフローサイトメトリーによって決定した。
EpCAM遺伝子のタンパク質配列(配列番号4072)は、NCBIデータベース及びOxford Genetics Ltd(Oxford、英国)によって合成されたDNAから得た。EpCAM遺伝子は、pSF-Lenti-EpCAMベクターを生成する標準的なクローニング技術によって、pSF-Lentiベクターにクローニングされた。HEK293T細胞を、pSF-CMVHIV-Gag-Pol、pSF-CMV-VSV-G、pSF-CMV-HIV-Rev(Oxford Genetics Ltd)と共に、レンチウイルスEpCAM発現ベクターを伴うLipofectamine 2000を用いてトランスフェクトした。レンチウイルスを含む上清を、48時間後に回収し、ポリブレン(8μg/mL)と混合した。レンチウイルス/ポリブレン混合物を、CHO細胞に添加し、37℃でインキュベートした。4日目に、上清を7.5μg/mLピューロマイシンを含有する培地と交換した。次に安定な変異体をクローン選択し、親細胞株又は安定にトランスフェクトした変異体のEpCAM発現を、EpCAM又は同位体対照抗体での抗体染色によって決定し、フローサイトメトリーによって分析した。陽性クローンを拡大し、さらなる実験に使用した。
PBMCを、NHS Blood and Transplant UK(Oxford、英国)から入手した全血白血球円錐体から密度勾配遠心分離(Boyum、1968)によって単離した。血液をPBSで1:2に希釈し、Ficoll(1,079 g/mL、Ficoll-Paque Plus、GE Healthcare)上に重層した後、400 gで30分間、22℃で低減速で遠心分離した。遠心分離後、PBMCを回収し、PBSで2回洗浄し(300 g、室温で10分間)、10% FBSで補充したRPMI-1640培地に再懸濁した。PBMCからCD3陽性T細胞を抽出するために、非CD3細胞を、Pan T Cell Isolation Kit(Miltenyi Biotec、#130-096-535)を、製造元のプロトコルに従って使用し、除去した。CD4及びCD8陽性T細胞をさらに単離するために、CD3 T細胞をCD4+Microbeads(Miltenyi Biotec、#130-045-101)を使用して、さらにもう1回精製した。
卵巣癌、膵臓癌、乳癌及び肺癌を含むがこれらに限定されない進行癌の複数の適応症を有する患者からのインフォームド・コンセントの後、原発性ヒト悪性腹水及び胸水サンプルを、オックスフォード大学病院のチャーチル病院(Oxford、英国)から受け取った。この研究は、オックスフォード病理組織学研究センターの研究倫理委員会によって承認された。受け取り次第、細胞画分と液体画分を分離し、液体を直ちに使用するか、又はアリコートを将来の分析のために-20℃で保存した。細胞画分を、製造元の指示に従って、赤血球溶解緩衝液(Roche、英国)で処理した。細胞数及び生存率は、トリパンブルー染色によって決定した。各サンプル中に存在する細胞型を、EpCAM、EGFR、FAP、CD45、CD11b、CD56、CD3、CD4、CD8、PD1及びCTLA4に対する抗体染色によって決定し、フローサイトメトリーによって分析した。エクスビボでのT細胞活性化及び標的細胞溶解実験には、新鮮な細胞と液体を使用した。場合によっては、接着細胞を10% FBSを補充したDMEM中で継代し、後で使用するために増殖させた。
二重特異性T細胞アクチベーターは、異なる特異性の2つのscFvを柔軟なGSリンカーで連結することによって生成された。各scFvは、親モノクローナル抗体由来のVHドメイン及びVLドメインをリンカーによって連結することによって生成される。各二重特異性T細胞アクチベーターは、哺乳動物の分泌のための免疫グロブリン軽鎖(Ig)N末端シグナル配列と、検出と精製のためのC末端デカヒスチジン親和性タグを保有した。二重特異性T細胞アクチベーターは、標準的なDNAクローニング技術によって操作され、サイトメガロウイルス(CMV)プロモーター駆動の構成的タンパク質発現及び分泌のためのタンパク質発現ベクター(pSFCMV-Amp)に挿入された。pSF-CMV-EpCAM二重特異性T細胞アクチベーター又はpSF-CMV-コントロール二重特異性T細胞アクチベータープラスミドDNAを、ポリエチレンイミン(PEI、リニア、MW 25000、Polysciences、米国)を用いて以下の条件下でHEK293A細胞にトランスフェクトした:55μgのプラスミドDNA:110μg PEI(DNA:PEI比は1:2(w/w))を細胞に加え、37℃で4時間インキュベートした後、新鮮な無血清DMEMと交換し、さらに37℃、5% CO2で48時間インキュベートした。トランスフェクション効率を確実にするために、細胞をpSF-CMV-GFPと並行してトランスフェクトした。分泌タンパク質を回収するために、トランスフェクトされた細胞の上清を集め、細胞成分を除去するために、350g、4℃で5分間遠心分離した。上清を10,000 MWCO Amicon Ultra-15遠心フィルターユニット(Millipore)に移した。4750 g、4℃で遠心した後、50倍高い濃度を得るためにフロースルーを用いて保持液の体積を調整した。濃縮タンパク質のアリコートを-80℃で保存した。
プラスミドpEnAd2.4-CMV-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-SA-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-CMV-コントロール二重特異性T細胞アクチベーター、pEnAd2.4-SA-コントロール二重特異性T細胞アクチベーターは、EpCAM 二重特異性T細胞アクチベーター又はコントロール二重特異性T細胞アクチベーターをコードする導入遺伝子カセットを、ギブソンアセンブリ技術を用いた基本的なEnAdプラスミドpEnAd2.4に直接挿入することによって生成した。導入遺伝子カセットは、5 ’短いスプライスアクセプター配列又は外因性CMVプロモーターを含み、その後下流にEpCAM又はコントロール二重特異性T細胞アクチベーター cDNA配列及び3’ポリアデニル化配列が続く。挿入された導入遺伝子カセットの概略図を図18に示す。プラスミドの正しい構築はDNA配列決定により確認された。プラスミドEnAd2.4-CMV-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-SA-EpCAM二重特異性T細胞アクチベーター、pEnAd2.4-CMV-コントロール二重特異性T細胞アクチベーター及びpEnAd2.4-SA-コントロール二重特異性T細胞アクチベーターは、HEK293A細胞へのトランスフェクションの前に、酵素AscIによる制限消化によって線状化された。細胞単層における細胞変性効果(CPE)の観察によってウイルスの産生をモニターした。広範囲のCPEが観察されたら、3回の凍結融解サイクルでHEK293A細胞からウイルスを回収した。収集した溶解物を段階希釈し、HEK293A細胞を再感染させ、単一のプラークを含むウェルを収集することによって、単一のウイルスクローンを選択した。ウイルスストックを増幅するために、感染が完全CPEに達したら、HEK293A細胞の連続感染を行った。強力なウイルスストックが増幅されたら、二重塩化セシウムバンディングによってウイルスを精製し、EnAd-CMVEpCAM二重特異性T細胞アクチベーター、EnAd-SA-EpCAM二重特異性T細胞アクチベーター、EnAd-CMV-コントロール二重特異性T細胞アクチベーター、EnAd-SA-コントロール二重特異性T細胞アクチベーターウイルスストックを生成した。製造元の指示に従って、これらのストックをTCID 50及びピコグリーンアッセイ(Life Technologies)によって力価測定した。
二重特異性T細胞アクチベーターを介したサイトカインの放出を評価するために、DLD細胞(20,000個)を、96ウェル平底プレート中で単独で、又は2ng/μLのEpCAM又はコントロール二重特異性T細胞アクチベーターと共に、100,000個のCD3+T細胞とプレーティングした。37℃、5% CO2で48時間インキュベートした後、上清を回収し、細胞成分を遠心分離で除去し、アリコートを-20℃で保存した。組換えウイルスからの二重特異性T細胞アクチベーター導入遺伝子発現を評価するために、HEK293A(1e6)又はDLD細胞(1.2e6)を、EnAd-CMV-EpCAM二重特異性T細胞アクチベーター、EnAd-SA-EpCAM二重特異性T細胞アクチベーター、EnAd-CMVコントロール二重特異性T細胞アクチベーター、EnAd-SA-コントロール二重特異性T細胞アクチベーター又は100vp/細胞のEnAdで感染させた。細胞を72時間培養し、その時点で細胞変性効果(CPE)が進行した。上清を回収し、300 gで5分間遠心して細胞片を除去し、将来の分析のために-20℃で保存した。
イムノブロッティング
ドットブロットを用いて、プラスミドトランスフェクションから産生された組換え二重特異性T細胞アクチベーターの濃度を測定した。各二重特異性T細胞アクチベーター及びタンパク質標準(10×Hisタグ付き(C末端)ヒトカテプシンD、Biolegend、#556704)の2倍段階希釈物を調製した。タンパク質標準のモル濃度は、100μg/ mLの二重特異性T細胞アクチベーター濃度を表すように調整した。各サンプル及びタンパク質標準物質2μLを、ニトロセルロース膜に直接塗布した。膜を風乾し、C末端Hisタグタンパク質を検出するために、α-6xHis(C末端)抗体(1:5000、クローン3D5、Invitrogen、英国、#46-0693)でブロッキング及びプローブし、続いて洗浄して抗マウス二次抗体(1:10000、Dako、#P0161)とインキュベートし、SuperSignal West Dura Extended Duration Substrate(Thermo Fisher、#34075)を製造元の指示に従って、適用することによって検出した。ウイルス感染HEK293A細胞の上清を、二重特異性T細胞アクチベーター発現についてウエスタンブロッティングによって分析した。上清をSDS-PAGEによって分画し、製造元のプロトコル(Bio-Rad)に従って、ニトロセルロース膜に転写した。膜をさらに上記のドットブロットプロトコルと同様に処理した。
EpCAM結合を評価するために、ヒトEpCAM/TROP-1タンパク質(50 ng/ウェル、Sino Biological Inc、#10694-H02H-50)で、4℃で一晩コーティングすることによって、ELISAプレートを調製した。プレートを5% BSAで周囲温度で1時間ブロッキングした後、希釈したEpCAM 二重特異性T細胞アクチベーター-、コントロール二重特異性T細胞アクチベーター-及び空のpSF-CMVベクタートランスフェクトHEK293A上清とインキュベートした(2時間、室温)。プレートをPBS-Tで3回洗浄し、その後に起こる結合ステップの後毎に洗浄した。プレートを抗His(C末端)抗体(1:5000、クローン3D5、#46-0693、Invitrogen、英国)と共に室温で1時間、続いてHRP結合抗マウスFc(1:1000、PBS/5%ミルク、Dako)と共に室温で1時間インキュベートした。HRP検出は3.3.5.5’-テトラメチルエチレンジアミン(TMB、Thermo-Fisher)を使用して行い、反応を停止させるために停止溶液を使用した。450nmでの吸光度をWallac 1420プレートリーダー(Perkin Elmer)で測定した。
フローサイトメトリー分析をFACSCaliburフローサイトメーター(BD Biosciences)で行い、データをFlowJo v10.0.7r2ソフトウェア(TreeStar Inc.、米国)で処理した。異なる細胞集団の分類のために、CD45(HI30、Biolegend)、CD11b(ICRF44、Biolegend)、EpCAM(9C4、Biolegend)及びFAP(427819、R&D Systems)に特異的な抗体を用いた。T細胞集団の分析には、異なる蛍光色素分子に結合した以下の抗体クローンを使用した:CD69(FN50、Biolegend)、CD25(BC96、Biolegend)、IFNγ(4S.B3、Biolegend)、αCD107a抗体(H4A3、Biolegend)、CD3(HIT3a、Biolegend)、CD4(OKT4、Biolegend)、CD8a(HIT8a、Biolegend)、PD1(H4A3、Biolegend)。各場合において、適切なアイソタイプ対照抗体を使用した。
CD69及びCD25発現レベル
組み換えEpCAM 二重特異性T細胞アクチベーター又はEpCAM 二重特異性T細胞アクチベーターウイルスがT細胞活性化を誘導する能力は、CD69及びCD25の表面発現によって評価された。PBMC又は腹水サンプル由来のヒトCD3細胞(96ウェル平底プレートで75,000細胞/ウェル)を、培地のみ、EpCAMもしくはコントロール二重特異性T細胞アクチベータータンパク質(2ng/μL)又は組換えウイルス(100vp/細胞)の存在下で、単独で又はDLD、SKOV、CHO、CHOEpCAMもしくは腹水標的細胞(15,000個)と共に培養した。場合によっては、抗PD1(Invivogen、#hpd1ni-mab7)抗体を終濃度2.5μg/ mLで添加した。T細胞活性化のポジティブコントロールとして、CD3細胞をCD3/CD28ダイナビーズ(Thermo Fisher、#11131D)と共にインキュベートした。特に明記しない限り、細胞を37℃で24時間培地で培養し、続いて無酵素細胞解離緩衝液(Gibco、#13151014)を用いて回収した。全細胞をCD69、CD25、CD3、CD4又はCD8の表面発現について抗体で染色し、フローサイトメトリーによって分析した。T細胞活性化(CD69、CD25)に対する腹水の影響を、RPMI-1640又は悪性腹水サンプルから分離された液体中で、プレート固定化CD3抗体(7.5μg/ mL、HIT3a、Biolegend、#300313)とインキュベートすることによって、CD3精製PBMC(100,000個)をポリクローナル活性化することによって調査した。
EpCAM 二重特異性T細胞アクチベーターがT細胞活性を誘導する能力は、T細胞をDLD細胞(平底96ウェルプレートで、200,000個のCD3細胞/ウェル、40,000個のDLD細胞/ウェル)及び2ng/μLの組換えEpCAM又はコントロール二重特異性T細胞アクチベーターと、6時間共培養することによる、IFNγ発現によって評価された。ポジティブコントロールとして、T細胞を可溶性PMA/イオノマイシン細胞活性化カクテル(Biolegend、#423301)で刺激した。Brefeldin A(GolgiPlug、BD Biosciences)を回収の5時間前に培地に添加し、その時点でCD3+T細胞を回収し、細胞内でIFNγ発現について染色し、フローサイトメトリーによって分析した。
T細胞増殖を研究するために、100,000個のCFSE標識(CellTrace CFSEキット、Invitrogen、#C34554)CD3+T細胞を、2ng/μLのEpCAM又はコントロール二重特異性T細胞アクチベーターと共に、96ウェルプレートフォーマットで、20,000個のDLD細胞とインキュベートした。
培地単独又は2 ng/μLのコントロールもしくはEpCAM 二重特異性T細胞アクチベーターの存在下、平底96ウェルプレートでDLD細胞(15,000細胞/ウェル)を75,000個のCD3+T細胞と共培養した。αCD107a又はアイソタイプ対照抗体を、培地に直接添加した。モネンシン(GolgiStop、BD Biosciences)を、37℃及び5% CO2で1時間インキュベートした後、その後さらに5時間インキュベートした後に添加した。続いて細胞を採取し、CD3、CD4又はCD8について染色し、フローサイトメトリーによって分析した。
DLD/PBMC又は胸水細胞の培養物から採取した上清中のサイトカインを、LEGENDplexヒトTヘルパーサイトカインパネル(Biolegend、#740001)及び製造元の指示に従ってフローサイトメトリーを用いて定量化した。解析に含まれるサイトカインには、IL-2、IL-4、IL-5、IL-6、IL-9、IL-10、IL-13、IL-17A、IL-17F、IL-21、IL-22、IFNγ及びTNFαがある。
組換え二重特異性T細胞アクチベーター又はウイルスによって媒介される標的細胞の細胞傷害性は、LDH放出又はMTSアッセイによって評価された。標的細胞(DLD、SKOV、HT-29、A431、A549、PC3、CHO、CHO-EpCAM)を、培地単独、希釈上清又はウイルス(100vp/細胞)の存在下で、平底96ウェルプレートでCD3、CD4又はCD8 T細胞(E:T 5:1)と共培養した。24時間共培養した後(特に明記しない限り)、上清と細胞を回収し、細胞傷害性を、LDHアッセイ(CytoTox 96非放射性細胞傷害性アッセイ、Promega、#G1780)又はMTS生存アッセイ(CellTiter 96 Cell Proliferation Assay、Promega、#G3580)により、製造元の指示に従って決定した。ウイルス感染DLD細胞から産生された二重特異性T細胞アクチベーターの量は、希釈されたウイルス上清によって誘導された細胞傷害性を、組換え二重特異性T細胞アクチベーターを用いて生成された標準曲線のそれと比較することによって決定された。
EnAd-CMV-EpCAM二重特異性T細胞アクチベーター、EnAd-SA-EpCAM二重特異性T細胞アクチベーター、EnAd-CMV-コントロール二重特異性T細胞アクチベーター、EnAd-SAコントロール二重特異性T細胞アクチベーター又はEnAdがそれぞれのゲノムを複製する能力を、100vp/細胞で感染する前に、DLD細胞を24ウェルプレート(150,000細胞/ウェル)に18時間、37℃、5% CO2で播種することによって分析した。感染の24及び72時間後にウェルを採取し、PureLinkゲノムDNAミニキット(Invitrogen、#K182001)を製造元のプロトコルに従って使用し、DNAを精製した。全ウイルスゲノムを、特異的プライマー-プローブセット(プライマー:TACATGCACATCGCCGGA/CGGGCGAACTGCACCA、プローブ:CCGGACTCAGGTACTCCGAAGCATCCT)を用いてEnAdヘキソンに対するqPCRにより定量化した。
明視野及び蛍光画像をZeiss Axiovert 25顕微鏡で捕捉した。タイムラプスビデオを得て、EnAd又はEnAd-CMVEpCAM二重特異性T細胞アクチベーターによる標的細胞のウイルス性又はT細胞媒介溶解性を観察した。感染していない細胞をネガティブコントロールとして使用した。NHDF細胞を、CellTracker Orange CMTMR色素(Life Technologies、#C2927)で染色し、CD3+細胞をCellTrace Violet Cell Proliferation Kit(Life Technologies、#C34557)で製造元のプロトコルに従って染色した。染色したNHDFを24ウェルプレートに7,500細胞/ウェルで、SKOV3と共培養して13,500細胞/ウェルで、プレーティングした。プレートを37℃、5% CO2で18時間インキュベートした。次に、細胞を300ng/mLのEpCAM 二重特異性T細胞アクチベーターで処理するか、100 vp/細胞のEnAd又はEnAd2.4-CMV-EpCAM二重特異性T細胞アクチベーターで感染させるか、未処置のままにした。2時間のインキュベーション後、1.5μMのCellEvent Caspase 3-7試薬(Life Technologies、#C10423)に加えて、100,000個の染色CD3+を必要なウェルに加えた。画像をNikon TE 2000-E Eclipse倒立顕微鏡(10倍光学対物レンズ)で、15分間隔で96時間撮影した。ImageJソフトウェアを使用して、タイムラプスビデオ(12フレーム/秒)を生成した。
比較されている2つ以上の実験条件のすべての場合において、統計分析はTukey’s Post Hoc分析を用いた一元配置分散分析検定を用いて行われた。全てのデータは平均±SDとして提示されている。使用した有意水準はP=0.01~0.05(*)、0.001~0.01(**)、0.0001~0.001(***)であった。明記しない限り、全てのインビトロ実験は3回行った。
EpCAMを標的とする二重特異性T細胞アクチベーターは、CD3ε及びEpCAMに特異的な2つのscFvを柔軟なグリシン-セリン(GS)リンカーと連結することによって操作された。CD3ε及び無関係の抗原(百日咳菌の線維状赤血球凝集素アドヘシン(FHA))を認識するコントロール二重特異性T細胞アクチベーターもまた産生した。両方の二重特異性T細胞アクチベーターは、哺乳動物分泌のためのN末端シグナル配列及び検出及び精製のためのC末端デカヒスチジン親和性タグを含むように操作された(図45A)。組み換え二重特異性T細胞アクチベーターの機能を特徴付けるために、それらをCMV最初期プロモーター(それぞれpSF-CMV-EpCAM二重特異性T細胞アクチベーター及びpSF-CMV-コントロール二重特異性T細胞アクチベーター)の転写制御下で、発現ベクターにクローニングした。
PBMC由来T細胞を活性化するための組換えEpCAM 二重特異性T細胞アクチベータータンパク質の能力は、表面にEpCAMを発現することが知られているヒトDLD結腸直腸癌細胞の培養物に未刺激ヒト初代CD3+細胞を添加することによって評価した(Karlssonら、2008)。2.5ng/mlのEpCAM 二重特異性T細胞アクチベーター(形質導入HEK293A細胞からの上清として)の添加は、T細胞活性化マーカーCD69及びCD25の有意な増加をもたらした(図45B及びC)が、コントロール二重特異性T細胞アクチベーターは効果がなかった。
ほとんどのヒト上皮細胞はEpCAMを発現するため、EpCAM 二重特異性T細胞アクチベーターの効果が
どのT細胞型がEpCAM 二重特異性T細胞アクチベーターによって活性化されるかを決定するために、PBMC由来T細胞をDLD細胞とインキュベートし、フロー解析の前に二重特異性T細胞アクチベーターを用いて活性化した。活性化CD4細胞の割合は一般的にわずかに高かったが、CD4+及びCD8+細胞の両方がCD69及びCD25の高レベルの発現を示した(図49A)。EpCAM 二重特異性T細胞アクチベーター媒介T細胞増殖をCFSE染色を用いて評価し(図49B)、CD197a/LAMP1の発現による脱顆粒(図49C)、そして再び同様のレベルの活性化がCD4+及びCD8+細胞の両方で見られた。最後に、達成された腫瘍細胞の細胞傷害性のレベルを、精製CD4+及びCD8+サブセットを活性化するためにEpCAM 二重特異性T細胞アクチベーターを用いて比較した。すべてのT細胞調製物は同様の細胞傷害性を示し(図49D)、これはCD4+及びCD8+細胞の両方が観察された二重特異性T細胞アクチベーター媒介細胞傷害性に寄与し得ることを示した。
エナデノチュシレブ(EnAdenotucirev)(EnAd)は、腫瘍溶解性アデノウイルスであり、モザイクE2B領域、ほぼ完全なE3欠失及びE4orf4にマッピングされたより小さなE4欠失を有するグループBタイプ11及びタイプ3アデノウイルスのキメラである(Kuhn 2008)。現在癌治療のためにいくつかの初期段階臨床試験を受けているこのウイルスは、優れた全身薬物動態及び有望な臨床活性を、導入遺伝子のコード化及び発現の可能性と組み合わせている(Calvo 2014、Boni 2014)。EpCAM 二重特異性T細胞アクチベーターは、Gibsonアセンブリによってウイルス骨格に挿入されたシャトルベクターを使用して、ファイバー遺伝子のすぐ下流のEnAd内にコードされた(図18)。二重特異性T細胞アクチベーターは、CMV最初期プロモーター(EnAd-CMV-EpCAM 二重特異性T細胞アクチベーター)の転写制御下に置くか、アデノウイルス主要後期プロモーターのスプライスアクセプター部位(MLP;EnAd-SA-EpCAM 二重特異性T細胞アクチベーター)の下流に置いた。前者の構成では、ウイルスが首尾よく細胞に感染するときはいつでも二重特異性T細胞アクチベーターが発現されるべきであるのに対して、MLPスプライスアクセプター部位からの発現は、ウイルス複製を許容する細胞においてMLPが活性化されるときにのみ起こる。2つの対応する対照ウイルスを生成するために(CD3及びFHAを認識する)コントロール二重特異性T細胞アクチベーターも導入した。
EnAd-EpCAM 二重特異性T細胞アクチベーター感染HEK293A細胞の上清を、PBMC由来T細胞の有無にかかわらず、CHO及びCHO-EpCAM細胞の培養液に加え、T細胞活性化及びCHO/CHO-EpCAM細胞に対する細胞傷害性を24時間後に測定した。CHO細胞の場合、CD25のT細胞発現の増加は見られず(図51D)、いかなる処理でも細胞傷害性は観察されなかった(図51E)。しかしながら、CHO-EpCAM細胞と共にインキュベートしたT細胞は、EnAd-CMV-EpCAM 二重特異性T細胞アクチベーター又はEnAd-SA-EpCAM 二重特異性T細胞アクチベーターウイルスのいずれかに感染したHEK293A細胞からの上清を用いてCD25発現の実質的な増加を示した(図51D)。予想通り、これは、EnAd-CMV-EpCAM 二重特異性T細胞アクチベーター又はEnAd-SA-EpCAM 二重特異性T細胞アクチベーターウイルスのいずれかに感染した293A細胞からの上清の存在下で、T細胞を添加した場合にのみ、CHO-EpCAM細胞に対する選択的細胞傷害性に変換された(図51E)。決定的には、T細胞の非存在下で、又はその細胞がコントロール二重特異性T細胞アクチベーターを発現するEnAdに感染していたHEK293Aからの上清を使用する場合、細胞傷害性はなかった。
一部の細胞、特にSKOV3卵巣癌細胞は部分的に耐性があり、よりゆっくりと死滅するが、EnAdはほとんどの癌細胞を直接腫瘍溶解によって迅速に死滅させる(Kuhn 2008)。従って、T細胞の細胞傷害性活性化をもたらすEpCAM 二重特異性T細胞アクチベーターを分泌するためにEndを武装させることの結果は、SKOV3細胞において特に明白であり得ると推論した。それゆえ、細胞は播種の24時間後にウイルス(100 vp/細胞)にさらされ、細胞死はxCELLigenceシステムによってモニターされた。PBMC由来T細胞を2時間後にSKOV3細胞培養液に添加した(又は添加しない)。T細胞の非存在下では、腫瘍細胞は約72時間増殖したが(図53Aの増加するCell Indexシグナルにより明白)、その後細胞増殖はプラトーに達し、ウイルス感染とは無関係に、少なくとも160時間まで安定していた。親EnAdを含む試験したウイルスはすべて、測定した時間中に観察可能な標的細胞の細胞傷害性を誘導しなかった。しかし、PBMC由来のT細胞と共培養すると、CMVとSAの両方のEpCAM 二重特異性T細胞アクチベーター武装ウイルスは、T細胞の添加後CMV駆動の誘導溶解は16時間以内、SAは44時間以内など、迅速なSKOV3溶解を誘導する(図53B)。重要なことに、親EnAd又は非特異的二重特異性T細胞アクチベーター対照ウイルスは、T細胞を添加したとしても、この期間内に標的細胞溶解を示さなかった。この結果は、感染後24、48及び96時間に細胞傷害性を測定し、上記と同一の共培養を設定したLDHアッセイによって確認された(図48)。これらの結果は、ウイルスを発現するEpCAM 二重特異性T細胞アクチベーターが、コントロール二重特異性T細胞アクチベーターウイルスよりも有意に速い速度で細胞傷害性を誘導した、DLD細胞における同様の知見によってさらに支持される(図50A+B)。
EpCAM陽性腫瘍細胞と原発性線維芽細胞(コントロールとして、非EpCAM発現細胞)を含む3つの悪性腹膜腹水サンプルの臨床サンプルをエクスビボで増殖させ、混合した初代細胞集団をPBMC由来T細胞とインキュベートし、培養液中の遊離二重特異性T細胞アクチベーター又は100 vp/細胞のEnAd-EpCAM二重特異性T細胞アクチベーターで処理した。72時間後、EpCAM陽性標的細胞(図55A)又は非標的線維芽細胞活性化タンパク質(FAP)陽性線維芽細胞(図55B)のレベルをフローサイトメトリーで測定した。T細胞の活性化は、CD25発現を測定することによって分析した(図55C)。遊離EpCAM 二重特異性T細胞アクチベーター及びEpCAM 二重特異性T細胞アクチベーター発現ウイルスは、T細胞活性化を誘導し、EpCAM陽性腫瘍細胞の枯渇を引き起こし、初代FAP陽性(EpCAM陰性)線維芽細胞は数に変化を示さなかった。これはすべての患者のサンプルで観察され、他の治療法はいずれも有意な効果を示さなかった。これは、EpCAM 二重特異性T細胞アクチベーター(又はそれをコードする腫瘍溶解性ウイルス)が、PBMC由来T細胞によるヒト卵巣腹水腫瘍細胞に対する活性化及び選択的細胞傷害性を媒介することができることを示す。
臨床的に関連性のある別の状況で、EpCAM 二重特異性T細胞アクチベーター発現ウイルスの影響を調べるために、様々な悪性腫瘍患者から胸水のサンプルをいくつか入手した。初回スクリーニング時(例を図52に示す)には、さらなる分析に適していると考えられるサンプルは、CD3及びEpCAM陽性細胞を含むものであった。最初の単離後に内因性T細胞によるPD1の発現も評価したところ、PBMC由来T細胞の10%のみがPD1を発現するのに対して、悪性滲出液サンプルT細胞はすべてPD1に対して少なくとも40%陽性であり、時に100%にまで高く達することもあった(図54)。未精製の全細胞(遠心分離によって単離し、再懸濁した)を、500ng/mLの遊離EpCAM 二重特異性T細胞アクチベーター又は100vp/細胞ウイルスをコードする二重特異性T細胞アクチベーターの存在下で、100%胸水中で一定濃度でインキュベートした。5日後、総細胞集団を採取し、CD3+細胞の総数(図57A)を測定した。
腫瘍溶解性ウイルスは、単一の標的化自己増幅剤内にいくつかの治療法を組み合わせるための興味深い新しい戦略を提供する(Keller&Bell、2016; Seymour&Fisher、2016)。それらは癌細胞内で選択的に増殖し、細胞から細胞へと広がるため、一部の腫瘍溶解性ウイルスは、ウイルス粒子が死にかけている細胞から逃げるのを許容するプロセスの一部として、非アポトーシス死経路(Ingemarsdotterら、2010; Li ら、2013)による細胞死を媒介すると考えられている。特にEnAdは、壊死症又は虚血性細胞死として知られる炎症誘発プロセスによって細胞を死滅させる(Dyer、2017)。この非アポトーシス死のメカニズムは、ATP、HMGB1、カルレティキュリン(損傷関連分子パターンとして知られる、
患者の悪性滲出液によるヒトT細胞活性化及び標的細胞の細胞傷害性の免疫抑制
悪性滲出液は、後期転移性癌患者で一般的に観察される免疫応答が抑制された潜在的免疫寛容の環境を表す。抗炎症性サイトカインと考えられるIL-10の量を、ヒトIL-10 ELISA MAXキット(Biolegend、430604)を用いて、正常血清又は患者の悪性滲出液(A、腹膜腹水、P、胸水)中で測定した。滲出液中のIL-10レベル(88.1~633.4pg/mL)は、正常血清(7.2~10pg/mL)で測定された値をはるかに超えていた。図58を参照のこと。
FAP 二重特異性T細胞アクチベーターは異なるドナーT細胞によるT細胞の活性化とFAP+細胞の死滅を媒介する
他の実験では、実施例2に記載の方法を用いて、NHDF及びT細胞の共培養物中で試験した組換えFAP 二重特異性T細胞アクチベータータンパク質のT細胞活性化特性を、CD3/CD28ダイナビーズを用いたコントロール二重特異性T細胞アクチベーター及びポリクローナルT細胞活性化と比較して、さらに評価した。
異なる潰瘍患者由来の原発性悪性腹水サンプル中の細胞に対するFAP 二重特異性T細胞アクチベーター及びEnAd-FAP 二重特異性T細胞アクチベーターウイルスの影響
実施例16に記載した研究の後継として、さらなる癌患者からの新鮮な原発性悪性腹膜腹水をEnAd FAP 二重特異性T細胞アクチベーターウイルス活性の研究のために得た。EpCAM+腫瘍細胞とFAP+線維芽細胞の両方を含む3人の患者サンプルを、エクスビボで増殖させ、混合(付着)細胞集団をPBMC由来T細胞及び未修飾又はEnAdウイルスを発現する二重特異性T細胞アクチベーターと共に培養した。72時間後、全細胞を採取し、フローサイトメトリーによってFAP+(図70A)及びEpCAM+細胞(図70B)の数を決定した。さらに、T細胞の活性化状態(CD25発現による)を測定した(図70C)。EnAd-CMV-FAP二重特異性T細胞アクチベーター及びEnAd-SA-FAP二重特異性T細胞アクチベーターの両方による感染は、すべての患者サンプルにおいてT細胞活性化及びFAP+細胞枯渇を誘導し、EpCAM+腫瘍細胞のレベルに有意な変化はなかった。親EnAd又は対照ウイルスは、観察可能なT細胞活性化を誘導せず、FAP+細胞数は未感染対照と同じままであった。
EnAd‐FAP二重特異性T細胞アクチベーター媒介腫瘍溶解及びT細胞刺激は、患者の腹水症におけるCD11b+TAMをより活性化した表現型に偏らせる
T細胞のFAP 二重特異性T細胞アクチベーター媒介活性化によるIFNγ、TNFα及びIL-2を含むTh1サイトカインの産生、及びその後のFAP+線維芽細胞の除去(及びそれに伴うTGFβ1の減少)が、免疫抑制及び発がん性から抗腫瘍活性に向けての腫瘍微小環境における他のシフトと関連しているかどうかを調べるために、分離されていない腹水細胞サンプルにおける腫瘍関連マクロファージ(TAM)に対する効果を評価した。未精製の患者の腹水細胞全体を50%腹水にプレーティングし、遊離コントロール又はFAP 二重特異性T細胞アクチベーターで処理するか、又はEnAd-SAコントロール二重特異性T細胞アクチベーター又はEnAd-SA-FAP二重特異性T細胞アクチベーターウイルスに感染させた(100 vp/細胞)。並行して、いくつかの細胞をIFNγで処理して活性化CD11b骨髄性細胞表現型を誘導した。3日間インキュベートした後、T細胞の活性化状態を最初に測定した。CD25+細胞をフローサイトメトリーにより測定し、IFNγ分泌をELISAにより測定した。
EnAd ‐ FAP二重特異性T細胞アクチベーターは、腫瘍浸潤リンパ球を活性化し、固形前立腺腫瘍生検においてエクスビボで細胞傷害性を誘導する
組織切片培養は、多様な組織、器官及び腫瘍の最も現実的な前臨床モデルの1つを提供する。この臨床的に極めて関連性の高い状況におけるウイルスを発現するFAP 二重特異性T細胞アクチベーターの活性を評価するために、切除されたヒト前立腺由来の悪性及び良性前立腺組織が、いくつかの対でパンチ生検によって研究された。最初のスクリーニングで、前立腺組織は、散在したCD8 T細胞を含む間質の広い領域の間に散在したEpCAM+腫瘍細胞の円環(図76A)を有することが再現可能に示された(図76B)。FAP染色は、腫瘍領域に隣接する線維芽細胞で見られた(図76C)。
単一の二重特異性T細胞アクチベーターをコードする5つのウイルス(NG-611、NG-612、NG-613、NG-614、NG-617)が生成された(表8)。
表8
プラスミドpEnAd2.4を、合成導入遺伝子カセット(それぞれ配列番号88~92)の直接挿入によりプラスミドpNG-611、pNG-612、pNG-613、pNG-614及びpNG-617を生成するために使用した。pNG-611導入遺伝子カセットは、二重特異性T細胞アクチベーター(配列番号93)を標的とするEpCamをコードし、pNG-612、pNG-613及びpNG-617導入遺伝子カセットは、配列番号94の二重特異性T細胞アクチベーターを標的とするFAPをコードし、pNG-614導入遺伝子カセットは、配列番号95の二重特異性T細胞アクチベーターを標的とするFAPをコードする。導入遺伝子カセットの概略図を図77A~Cに示す。プラスミドDNAの構築は制限分析及びDNA配列決定により確認した。
1ppcのNG-611、NG-612、NG-617、エナデノチュシレブ(enadenotucirev)で72時間感染させた、又は未感染のままにしたA549細胞を、qPCRによるウイルスDNAの定量化に使用した。細胞上清を回収し、1200rpmで5分間遠心分離することによって清澄化した。製造元のプロトコルに従って、Qiagen DNeasyキットを用いて45μLの上清からDNAを抽出した。エナデノチュシレブ(Enadenotucirev)ウイルス粒子(2.5e10-2.5e5vp)を用いた標準曲線もまた作成し、DNeasyキットを用いて抽出した。抽出された各サンプル又は標準物質は、初期遺伝子E3に設定されたウイルス遺伝子特異的プライマー-プローブを用いてqPCRにより分析された。
癌細胞感染
A549細胞を24ウェルプレートに2.5e5細胞/ウェルの密度で播種した。細胞を1ppcのNG-611、NG-612、エナデノチュシレブ(enadenotucirev)に感染させるか、又は未感染のままにする前に、プレートを37℃、5% CO2で4時間インキュベートした。感染後24、48又は72時間に細胞から上清を回収し、1200rpmで5分間遠心分離することにより清澄化し、瞬間凍結した。
FAPを発現する肺線維芽細胞株MRC-5、又はEpCamを発現する卵巣癌細胞、SKOV3を、それぞれ48ウェルプレートに5.7e4細胞/ウェル及び1.2e5細胞/ウェルの密度で播種した。プレートを、37℃、5% CO2で4時間インキュベートした後、培地をA549プレートから回収した150μL/ウェルの解凍上清と交換した。次いで、ヒトPBMCドナーから単離した精製CD3 T細胞もプレートに添加して、2:1のT細胞対MRC-5又はSKOV3の比を得た。共培養物を37℃、5% CO2で16時間インキュベートした後、細胞上清をELISA分析のために収集し、T細胞をフローサイトメトリー分析のために収集した。非接着細胞を含む培地を共培養ウェルから取り出し、遠心分離した(300×g)。上清を注意深く除去し、PBS 5% BSAで1/2に希釈し、ELISA分析のために保存した。接着細胞単層をPBSで1回洗浄した後、トリプシンを用いて剥離した。トリプシンを10% FBS RPMI培地を用いて不活性化し、細胞を培養上清から集めた細胞ペレットに添加した。細胞を遠心分離し(300×g)、上清を捨て、細胞ペレットを200μLのPBS中で洗浄した。細胞を再度遠心分離し、次いでLive/Dead Aqua(Life tech)を含む50μLのPBSに室温で15分間再懸濁した。直接結合抗体のパネルで染色する前に、細胞をFAC緩衝液中で1回洗浄した:AF700にコンジュゲートした抗CD3;BV421にコンジュゲートした抗CD25;PE/CY5にコンジュゲートした抗HLA-DR;BV605にコンジュゲートした抗CD40L;PEにコンジュゲートした抗CD69及びFITCにコンジュゲートした抗CD107a。各共培養条件からの細胞のサンプルもまた、関連するアイソタイプ対照抗体で染色された。全ての染色は、FAC緩衝液中、全容量50μL/ウェルで15分間、4℃で行った。次に、細胞をFAC緩衝液(200μL)で2回洗浄した後、200μLのFAC緩衝液に再懸濁し、フローサイトメトリー(Attune)で分析した。
T細胞活性化のフローサイトメトリー分析は、生きた単一細胞上のT細胞活性化マーカーCD25、CD69、HLA-DR及びCD40L又はT細胞脱顆粒マーカーCD107aの発現によって評価した。これらのデータは、EpCam+SKOV3細胞と共培養したとき、NG-611上清を細胞に添加すると、NG-612、エナデノチュシレブ(enadenotucirev)又は未処置対照上清と比較して、CD25、CD69、HLA-DR、CD40L又は細胞表面CD107aを発現するT細胞の数が有意に増加することを示した(図78)。これらすべてのマーカーについて、24時間感染させたA549細胞からの上清によってはほとんどT細胞活性化が刺激されなかったが、感染後48時間までに、上清はすべてのマーカーにわたって有意なT細胞活性化を刺激した。これは感染後72時間の時点でも同様であった。
NSGマウスヒト化CD34+造血幹細胞(Jackson Labsから)を、HCT116腫瘍細胞と共に、生着後18週目に、両脇腹の皮下に移植した。腫瘍が80~400mm3に達したら、各処置群が同等の腫瘍体積分布を有するようにマウスをグループ分けし、1グループ当たり7匹のマウスにした。マウスに生理食塩水、エナデノチュシレブ(enadenotucirev)又はNG-611のいずれかを、注射当たり5×109粒子、腫瘍当たり2回注射で腫瘍内注射した。両脇腹の腫瘍を治療した。腫瘍体積を週に3~4回測定し、NG-611処置が投与後20日までの間、エナデノチュシレブ(enadenotucirev)又は未処置の対照と比較して、有意な抗腫瘍応答をもたらすことを実証した(図82a)。投与20日後、各群の4匹のマウスからの1つの腫瘍をフローサイトメトリーのために処理し、一方残りの腫瘍はドライアイス上で凍結した。
腫瘍サンプルは切除直後に少量のRPMI培地中で機械的に分離した。次いで、分離した腫瘍を70μmセルストレーナーに通し、300gで10分間遠心した。細胞ペレットをLive/Dead Aqua(Life tech)を含む100μLのPBSに氷上で15分間再懸濁した。直接結合抗体のパネルで染色する前に、細胞をFACs緩衝液(5% BSA PBS)で1回洗浄した:抗CD8(RPA-T8、AF700);抗CD4(RPA-T4、PE);抗CD45(2D1、APC-Fire 750);抗CD3(OKT3、PerCP-Cy5.5);抗CD25(M-A251、PE-Dazzle 594);抗CD69(FN50、APC);抗HLA-DR(L243、BV605);抗CD107a(H4A3、FITC)。腫瘍細胞懸濁液のプールも、関連アイソタイプ対照抗体で染色した。全ての染色は、4℃で20分間、50μL/ウェルの総容量でFAC緩衝液中で実施した。細胞をFAC緩衝液(200μL)で3回洗浄した後、200μLのFAC緩衝液に再懸濁し、フローサイトメトリー(Attune)で分析した。FAC分析は、腫瘍中のCD4 T細胞に対するCD8 T細胞の比が、エナデノチュシレブ(enadenotucirev)処置又は未処置対照と比較して、NG-611処置腫瘍において有意に増加したことを示した(図82b)。
FAP 二重特異性T細胞アクチベーター及び免疫調節タンパク質をコードする3つのウイルス(NG-615、NG-640及びNG-641)が生成された(表9)。
表9
プラスミドpEnAd2.4を使用して、合成導入遺伝子カセット(それぞれ配列番号112~114)の直接挿入により、プラスミドpNG-615、pNG-616、pNG-640及びpNG-641を生成した。NG-615及びNG-616は、FAP標的二重特異性T細胞アクチベーター(配列番号94)、Flt3L(配列番号115)、MIP1α(配列番号116)及びIFNα(配列番号117)をコードする4つの導入遺伝子を含む。NG-640及びNG-641は、FAP標的二重特異性T細胞アクチベーター(配列番号94)、CXCL9(配列番号118)及びCXCL10(配列番号119)をコードし、NG-641はまた、IFNα(配列番号117)をコードする第4の導入遺伝子を含む。導入遺伝子カセットの概略図を図83A~Cに示す。プラスミドDNAの構築は制限分析及びDNA配列決定により確認した。
癌細胞感染
1ppcのNG-615、エナデノチュシレブ(enadenotucirev)で72時間感染させた、又は未感染のままにしたA549細胞を、qPCRによるウイルスDNAの定量化及びELISAによる導入遺伝子発現の分析に使用した。細胞上清を回収し、1200rpmで5分間遠心分離することによって清澄化した。45μLの上清をDNA分析に使用し、残りの上清をELISAに使用した。
製造元のプロトコルに従って、Qiagen DNeasyキットを使用して上清サンプルからDNAを抽出した。エナデノチュシレブ(Enadenotucirev)ウイルス粒子(2.5e10-2.5e5vp)を用いた標準曲線もまた作成し、DNeasyキットを用いて抽出した。抽出された各サンプル又は標準物質は、初期遺伝子E3に設定されたウイルス遺伝子特異的プライマー-プローブを用いてqPCRにより分析された。細胞あたりの検出されたウイルスゲノムの数の定量化は、NG-615がA549細胞株において親ウイルスのエナデノチュシレブ(enadenotucirev)と同等のレベルで有意なゲノム複製を示したことを実証した(図84)。これらのデータは、二重特異性T細胞アクチベーター及び3つの免疫調節導入遺伝子の包含がウイルス複製活性に有意な影響を及ぼさないことを示した。未感染細胞ではウイルスゲノムは検出されなかった。
IFNα ELISAは、Verikine Human IFN alpha キット(Pbl assay science)を使用して実施し、MIP1α ELISAは、ヒトCCL3 Quantikine ELISAキット(R&D systems)を使用して実施し、Flt3L ELISAは、Flt3LヒトELISAキット(Abcam)を使用して実施した。全てのアッセイは製造元のプロトコルに従って実施した。
癌細胞感染
A549細胞を24ウェルプレートに2.5e5細胞/ウェルの密度で播種した。細胞を1ppcのNG-612、NG-615、エナデノチュシレブ(enadenotucirev)に感染させるか、又は未感染のままにする前に、プレートを37℃、5% CO2で4時間インキュベートした。感染後24、48又は72時間に細胞から上清を回収し、1200rpmで5分間遠心分離することにより清澄化し、瞬間凍結した。
FAPを発現する肺線維芽細胞株MRC-5を、48ウェルプレートに5.7e4細胞/ウェルの密度で播種した。プレートを、37℃、5% CO2で4時間インキュベートした後、培地をA549プレートから回収した150μL/ウェルの解凍上清と交換した。次いで、ヒトPBMCドナーから単離された精製CD3 T細胞もプレートに添加して、2:1のT細胞対MRC-5の比を得た。細胞上清をELISA分析のために収集し、T細胞を実施例29に詳述した方法に従ってフローサイトメトリー分析のために回収する前に、共培養物を37℃、5% CO2で16時間インキュベートした。
T細胞活性化のフローサイトメトリー分析は、生きたCD3+単一細胞上のT細胞活性化マーカーCD25、CD69、HLA-DR及びCD40L、又はT細胞脱顆粒マーカーCD107aの発現によって評価した。これらのデータは、FAP+MRC-5細胞と共培養したとき、NG-615又は612上清を添加すると、エナデノチュシレブ(enadenotucirev)又は未処置対照上清と比較して、CD25、CD69、HLA-DR、CD40L又はCD107aを発現するT細胞の数が、有意に増加したことを示した(図86)。
IFNγ発現の検出のために、共培養上清を5% BSA/PBSアッセイ緩衝液(1:10~1:1000の範囲内)に希釈し、ELISAをヒトIFNガンマQuantikine キット(RandD Systems)を用いて、製造元のプロトコルに従って行った。標準曲線から内挿することによって、分泌されたIFNγの濃度を決定した。IFNγの発現は、NG-612又はNG-615に感染したA549上清を用いた共培養の上清中でのみ検出することができた(図87)。
一方がEpCamを標的とし(EpCam 二重特異性T細胞アクチベーター)、他方がFAPを標的とする(FAP 二重特異性T細胞アクチベーター)2つの二重特異性T細胞アクチベーター分子をコードするウイルスNG-618が生成された(表10)。
表10
プラスミドpEnAd2.4を使用して、合成導入遺伝子カセット(配列番号123)の直接挿入により、プラスミドpNG-618を生成した。NG-618ウイルスは、EpCam標的二重特異性T細胞アクチベーター(配列番号93)及びFAP標的二重特異性T細胞アクチベーター(配列番号95)をコードする2つの導入遺伝子を含む。導入遺伝子カセットの概略図を図88に示す。プラスミドDNAの構築は制限分析及びDNA配列決定により確認した。
癌細胞感染
A549細胞を1.2e6細胞/ウェルの密度で6ウェルプレートに播種した。細胞をNG-611、NG-612、NG-618、エナデノチュシレブ(enadenotucirev)に感染させるか、又は未感染のままにする前に、プレートを37℃、5% CO2で4時間インキュベートした。感染後72時間で、細胞から上清を回収し、1200rpmで5分間遠心分離することによって清澄化した。
FAPを発現する肺線維芽細胞系MRC-5及びEpCamを発現するA549細胞を、24ウェルプレートに1.5e5細胞/ウェルの密度で播種した。MRC-5及びA549細胞もまた1:1の比率で混合し、1.5e5細胞/ウェルの総細胞密度で24プレートに播種した。培地をA549プレートから回収した300μL/ウェルの解凍上清と交換する前に、プレートを37℃、5% CO2で4時間インキュベートした。次いで、ヒトPBMCドナーから単離された精製CD3 T細胞もプレートに添加して、2:1のT細胞対MRC-5又はSKOV3細胞の比を得た。細胞上清をELISA分析用に収集し、T細胞、MRC-5細胞及びA549細胞をフローサイトメトリー分析用に収集する前に、共培養物を37℃、5% CO2で16時間インキュベートした。
MRC-5又はSKOV細胞の表面上のそれぞれ検出可能なFAP又はEpCamのフローサイトメトリー分析は、直接結合抗体のパネルで染色する前に、細胞をFAC緩衝液中で1回洗浄することによって評価した:AF647とコンジュゲートした抗FAP; PEとコンジュゲートした抗EpCam。分析は、ウイルスを発現するFAP-二重特異性T細胞アクチベーター、NG-618に感染した細胞からの上清とインキュベートしたMRC-5細胞ではFAP発現がもはや検出できないが、EnAdで処置した細胞又は未処置細胞からの上清でインキュベートした>80%の細胞上では検出されたことを示した。(図89A)。これらのデータは、NG-618ウイルスによって産生されたFAP-二重特異性T細胞アクチベーターが、抗FAP抗体の結合を妨げるMRC-5細胞上のそのFAP標的に結合することを示す。生きた大きな単一細胞のSKOV細胞を、検出可能なEpCamの発現について評価した。ウイルスを発現するEpCam-二重特異性T細胞アクチベーター、NG-618に感染した細胞からの上清(17%の細胞)とインキュベートしたSKOV細胞では、EpCam発現は低レベルでしか検出できなかったが、EnAdで処置した細胞又は未処置細胞からの上清でインキュベートした>40%の細胞上では検出された(図89B)。まとめると、これらのデータは、NG-618がEpCam及びFAP標的タンパク質に結合する二重特異性T細胞アクチベーター分子を産生することを示す。
T細胞活性化のフローサイトメトリー分析は、生きたCD3+単一細胞上のT細胞活性化マーカーCD25、CD69、HLA-DR及びCD40L、又はT細胞脱顆粒マーカーCD107aの発現によって評価した。これらのデータは、FAP+MRC-5細胞と共培養したとき、NG-618上清を細胞に添加しすると、エナデノチュシレブ(enadenotucirev)又は未処置対応上清と比較して、CD25、CD40L又はCD107aを発現するT細胞数が有意に増加したことを示した(図90)。NG-618上清をEpCam+SKOV3細胞に添加した場合、エナデノチュシレブ(enadenotucirev)又は未処置の対照上清と比較して、CD25、CD40L又はCD107aを発現するT細胞の数もまた有意に増加した(図91)。これらのデータは、NG-618ウイルスによって発現された両方の二重特異性T細胞アクチベーター分子が、T細胞活性化の誘導に関して機能的であることを実証している。
MRC-5及びSKOV細胞生存率のフローサイトメトリー分析は、Live/Dead Aqua(Life tech)を含む50μLのPBS中で、室温で15分間細胞を染色することによって評価した。直接結合抗体のパネルで染色する前に、細胞をFAC緩衝液中で1回洗浄した:AF647にコンジュゲートした抗FAP;PEとコンジュゲートした抗EpCam。MRC-5及びSKOV細胞生存率は、NG-618上清サンプルとのインキュベーション後に有意に減少したが、有意な細胞死は、エナデノチュシレブ(enadenotucirev)又は未処置の対照上清において検出されなかった(図92)。これらのデータは、標的細胞のT細胞媒介細胞死滅を誘導するための、FAP及びEpCam標的二重特異性T細胞アクチベーターを同時発現したNG-618の機能的能力を実証する。
配列番号25:FAP 二重特異性T細胞アクチベーター-P2A-RFP(斜字体=リーダー、太字=フリン切断部位、下線=P2A配列、小文字=RFP)
MGWSCIILFLVATATGVHSDIVMTQSPDSLAVSLGERATINCKSSQSLLYSRNQKNYLAWYQQKPGQPPKLLIFWASTRESGVPDRFSGSGFGTDFTLTISSLQAEDVAVYYCQQYFSYPLTFGQGTKVEIKGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCKTSRYTFTEYTIHWVRQAPGQRLEWIGGINPNNGIPNYNQKFKGRVTITVDTSASTAYMELSSLRSEDTAVYYCARRRIAYGYDEGHAMDYWGQGTLVTVSSGGGGSDVQLVQSGAEVKKPGASVKVSCKASGYTFTRYTMHWVRQAPGQGLEWIGYINPSRGYTNYADSVKGRFTITTDKSTSTAYMELSSLRSEDTATYYCARYYDDHYCLDYWGQGTTVTVSSGEGTSTGSGGSGGSGGADDIVLTQSPATLSLSPGERATLSCRASQSVSYMNWYQQKPGKAPKRWIYDTSKVASGVPARFSGSGSGTDYSLTINSLEAEDAATYYCQQWSSNPLTFGGGTKVEIKHHHHHHHHHHRRKRGSGATNFSLLKQAGDVEENPGPmselikenmhmklymegtvnnhhfkctsegegkpyegtqtmkikvveggplpfafdilatsfmygskafinhtqgipdffkqsfpegftwerittyedggvltatqdtsfqngciiynvkingvnfpsngpvmqkktrgweantemlypadgglrghsqmalklvgggylhcsfkttyrskkpaknlkmpgfhfvdhrlerikeadketyveqhemavakycdlpsklghr
配列番号26:コントロール(抗FHA)二重特異性T細胞アクチベーター-P2A-RFP (斜字体 =リーダー、太字 =フリン切断部位、下線=P2A配列、小文字=RFP)
MGWSCIILFLVATATGVHSELDIVMTQAPASLAVSLGQRATISCRASKSVSSSGYNYLHWYQQKPGQPPKLLIYLASNLESGVPARFSGSGSGTDFTLNIHPVEEEDAATYYCQHSREFPLTFGAGTKLEIKSSGGGGSGGGGGGSSRSSLEVQLQQSGPELVKPGASVKISCKTSGYTFTGYTMHWVRQSHGKSLEWIGGINPKNGGIIYNQKFQGKATLTVDKSSSTASMELRSLTSDDSAVYYCARRVYDDYPYYYAMDYWGQGTSVTVSSAKTTPPSVTSGGGGSDVQLVQSGAEVKKPGASVKVSCKASGYTFTRYTMHWVRQAPGQGLEWIGYINPSRGYTNYADSVKGRFTITTDKSTSTAYMELSSLRSEDTATYYCARYYDDHYCLDYWGQGTTVTVSSGEGTSTGSGGSGGSGGADDIVLTQSPATLSLSPGERATLSCRASQSVSYMNWYQQKPGKAPKRWIYDTSKVASGVPARFSGSGSGTDYSLTINSLEAEDAATYYCQQWSSNPLTFGGGTKVEIKHHHHHHHHHHRRKRGSGATNFSLLKQAGDVEENPGPmselikenmhmklymegtvnnhhfkctsegegkpyegtqtmkikvveggplpfafdilatsfmygskafinhtqgipdffkqsfpegftwerittyedggvltatqdtsfqngciiynvkingvnfpsngpvmqkktrgweantemlypadgglrghsqmalklvgggylhcsfkttyrskkpaknlkmpgfhfvdhrlerikeadketyveqhemavakycdlpsklghr
配列番号33:スプライスアクセプター配列
CAGG
配列番号55:短いスプライスアクセプター(SSA)DNA配列(null配列)
CAGG
配列番号58:コザック配列(null配列)
CCACC
Claims (22)
- 腫瘍溶解性アデノウイルスであって、
式(I):
5’ITR-B1-BA-B2-BX-BB-BY-B3-3’ITR(I)
式中、
B1は結合であるか、又はE1A、E1B若しくはE1A-E1Bを含み、
BAは、-E2B-L1-L2-L3-E2A-L4を含み、
B2は結合であるか、又はE3を含み、
BXは結合であるか、又は制限部位、1つ又は複数の導入遺伝子、若しくはその両方を含むDNA配列であり、
BBはL5を含み、
BY は、1つ若しくは複数の導入遺伝子を含むDNA配列であり、
B3 は、E4を含み、
ここで、腫瘍溶解性アデノウイルスは、BY位に、主要後期プロモーターの制御下において、少なくとも2つの結合ドメインを含む二重特異性T細胞アクチベーターをコードし、
ここで前記結合ドメインの1つは、T細胞受容体複合体(TCR)の成分に特異的であり、
前記結合ドメインの1つは、CEA、MUC-1、EpCAM、HER 受容体HER1、HER2、HER3及びHER4、PEM、A33、G250、炭水化物抗原Ley、Lex及びLeb、PSMA、TAG-72、STEAP1、CD166、CD24、CD44、E-カドヘリン並びにSPARCから成る群より選ばれる腫瘍抗原に特異的であり、
前記アデノウイルスはエナデノチュシレブ(enadenotucirev)(EnAd)又は血清型11のアデノウイルス(Ad11)である、式(I)の配列を含む腫瘍溶解性アデノウイルス。 - 前記アデノウイルスがEnAdである、請求項1に記載の腫瘍溶解性アデノウイルス。
- 前記T細胞受容体複合体(TCR)の成分がCD3である、請求項1又は2に記載の腫瘍溶解性アデノウイルス。
- 前記TCRの成分が、CD3ε、CD3γ又はCD3δである、請求項3に記載の腫瘍溶解性アデノウイルス。
- 前記腫瘍抗原が、CEA、MUC-1、EpCAM、HER 受容体HER2、HER3及びHER4、PEM、A33、G250、炭水化物抗原Ley、Lex及びLeb、PSMA、TAG-72、STEAP1、CD166、CD24、CD44、E-カドヘリン、SPARC、ErbB2並びにErbB3から成る群より選ばれる、請求項1~4のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- 前記腫瘍抗原が、EpCAMである、請求項1~5のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- 前記アデノウイルスに複製能力がある、請求項1~6のいずれかに記載の腫瘍溶解性アデノウイルス。
- 前記アデノウイルスが第2の二重特異性T細胞アクチベーターをさらにコードする、請求項1~7のいずれかに記載の腫瘍溶解性アデノウイルス。
- 前記第2の二重特異性T細胞アクチベーターがBY位にコードされている、請求項8に記載の腫瘍溶解性アデノウイルス。
- 前記コードされた二重特異性T細胞アクチベーターが、配列番号8に記載の可変重鎖のアミノ酸配列の3つの相補性決定領域(CDR)を含むVHドメイン、及び配列番号9に記載の可変軽鎖のアミノ酸配列の3つのCDR配列を含むVLドメインを含む、請求項1~9のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- 前記コードされた二重特異性T細胞アクチベーターが、配列番号8に記載のアミノ酸配列又はそれと少なくとも95%同一であるアミノ酸配列を含むVHドメイン、及び配列番号9に記載のアミノ酸配列又はそれと少なくとも95%同一である配列を含むVLドメインを含む、請求項10記載の腫瘍溶解性アデノウイルス。
- 前記コードされた二重特異性T細胞アクチベーターが、配列番号18に記載の可変重鎖のアミノ酸配列の3つの相補性決定領域(CDR)を含むVHドメイン、及び配列番号17に記載の可変軽鎖のアミノ酸配列の3つのCDR配列を含むVLドメインを含む、請求項1~11のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- 前記コードされた二重特異性T細胞アクチベーターが、配列番号18に記載のアミノ酸配列、又はそれと少なくとも95%同一であるアミノ酸配列を含むVHドメイン、及び配列番号17に記載のアミノ酸配列又はそれと少なくとも95%同一である配列を含むVLドメインを含む、請求項12に記載の腫瘍溶解性アデノウイルス。
- 前記腫瘍溶解性アデノウイルスが、配列番号34、35、79、80又は96に示される配列を含む、請求項1に記載の腫瘍溶解性アデノウイルス。
- 前記腫瘍溶解性アデノウイルスが2、3又は4のさらなる導入遺伝子をコードする、請求項1~14のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- 前記さらなる導入遺伝子が、サイトカイン、ケモカイン及び免疫調節剤の1つ又は複数をコードする、請求項15に記載の腫瘍溶解性アデノウイルス。
- 前記さらなる導入遺伝子の全てがBY位にコードされている、請求項15又は16に記載の腫瘍溶解性アデノウイルス。
- 前記サイトカイン又は前記ケモカインが、MIP1α、IL-1α、IL-1β、IL-6、IL-9、IL-12、IL-13、IL-17、IL-18、IL-22、IL-23、IL-24、IL-25、IL-26、IL-27、IL-33、IL-35、IL-2、IL-4、IL-5、IL-7、IL-10、IL-15、IL-21、IL-25、IL-1RA、IFNα、IFNβ、IFNγ、TNFα、リンホトキシンα(LTA)、Flt3L、GM-CSF、IL-8、CCL2、CCL3、CCL5、CCL17、CCL20、CCL22、CXCL9、CXCL10、CXCL11、CXCL13、CXCL12、CCL2、CCL19及びCCL21から選択される、請求項16又は17に記載の腫瘍溶解性アデノウイルス。
- 請求項1~18のいずれか1項に記載の腫瘍溶解性アデノウイルス、及び希釈剤又は担体を含む、組成物。
- がん治療用である請求項19に記載の組成物。
- 治療用である、請求項1~18のいずれか1項に記載の腫瘍溶解性アデノウイルス。
- がん治療用である、請求項21に記載の腫瘍溶解性アデノウイルス。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024114614A JP2024147722A (ja) | 2016-08-29 | 2024-07-18 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
Applications Claiming Priority (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1614607.8A GB201614607D0 (en) | 2016-08-29 | 2016-08-29 | Modified adenovirus |
| GB1614607.8 | 2016-08-29 | ||
| GBGB1700663.6A GB201700663D0 (en) | 2017-01-13 | 2017-01-13 | Modified adenovirus |
| GB1700663.6 | 2017-01-13 | ||
| GBGB1706219.1A GB201706219D0 (en) | 2017-04-19 | 2017-04-19 | Modified adenovirus |
| GB1706219.1 | 2017-04-19 | ||
| GBGB1713765.4A GB201713765D0 (en) | 2017-08-28 | 2017-08-28 | Modified adenovirus |
| GB1713765.4 | 2017-08-28 | ||
| PCT/EP2017/071674 WO2018041838A1 (en) | 2016-08-29 | 2017-08-29 | Adenovirus armed with bispecific t cell engager (bite) |
| JP2019532192A JP7212620B2 (ja) | 2016-08-29 | 2017-08-29 | 二重特異性t細胞アクチベーターで武装したアデノウイルス |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019532192A Division JP7212620B2 (ja) | 2016-08-29 | 2017-08-29 | 二重特異性t細胞アクチベーターで武装したアデノウイルス |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024114614A Division JP2024147722A (ja) | 2016-08-29 | 2024-07-18 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022166209A JP2022166209A (ja) | 2022-11-01 |
| JP7525558B2 true JP7525558B2 (ja) | 2024-07-30 |
Family
ID=59923381
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019532192A Active JP7212620B2 (ja) | 2016-08-29 | 2017-08-29 | 二重特異性t細胞アクチベーターで武装したアデノウイルス |
| JP2019507924A Pending JP2019532621A (ja) | 2016-08-29 | 2017-08-29 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
| JP2022130173A Active JP7525558B2 (ja) | 2016-08-29 | 2022-08-17 | 二重特異性t細胞アクチベーターで武装したアデノウイルス |
| JP2024114614A Pending JP2024147722A (ja) | 2016-08-29 | 2024-07-18 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019532192A Active JP7212620B2 (ja) | 2016-08-29 | 2017-08-29 | 二重特異性t細胞アクチベーターで武装したアデノウイルス |
| JP2019507924A Pending JP2019532621A (ja) | 2016-08-29 | 2017-08-29 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024114614A Pending JP2024147722A (ja) | 2016-08-29 | 2024-07-18 | 二重特異性T細胞エンゲージャー(BiTE)で武装したアデノウイルス |
Country Status (18)
| Country | Link |
|---|---|
| US (3) | US12258417B2 (ja) |
| EP (3) | EP4273252A3 (ja) |
| JP (4) | JP7212620B2 (ja) |
| KR (2) | KR102427563B1 (ja) |
| CN (4) | CN110214025B (ja) |
| AU (2) | AU2017320776B2 (ja) |
| BR (1) | BR112019003866A2 (ja) |
| CA (2) | CA3033267A1 (ja) |
| CL (1) | CL2019000510A1 (ja) |
| CO (1) | CO2019002371A2 (ja) |
| ES (1) | ES2983916T3 (ja) |
| IL (2) | IL264902B2 (ja) |
| MX (2) | MX2019002328A (ja) |
| MY (1) | MY197324A (ja) |
| PH (1) | PH12019500436A1 (ja) |
| SG (2) | SG11201901715UA (ja) |
| WO (2) | WO2018041838A1 (ja) |
| ZA (1) | ZA201900644B (ja) |
Families Citing this family (49)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12466897B2 (en) | 2011-10-10 | 2025-11-11 | Xencor, Inc. | Heterodimeric human IgG1 polypeptides with isoelectric point modifications |
| US10968276B2 (en) | 2013-03-12 | 2021-04-06 | Xencor, Inc. | Optimized anti-CD3 variable regions |
| US9605084B2 (en) | 2013-03-15 | 2017-03-28 | Xencor, Inc. | Heterodimeric proteins |
| US11053316B2 (en) | 2013-01-14 | 2021-07-06 | Xencor, Inc. | Optimized antibody variable regions |
| US10738132B2 (en) | 2013-01-14 | 2020-08-11 | Xencor, Inc. | Heterodimeric proteins |
| US10858417B2 (en) | 2013-03-15 | 2020-12-08 | Xencor, Inc. | Heterodimeric proteins |
| PL3021859T3 (pl) | 2013-10-25 | 2018-06-29 | Psioxus Therapeutics Limited | Adenowirusy onkolityczne wyposażone w geny heterolityczne |
| LT3122781T (lt) | 2014-03-28 | 2020-03-25 | Xencor, Inc. | Bispecifiniai antikūnai, kurie jungiasi prie cd38 ir cd3 |
| US10259887B2 (en) | 2014-11-26 | 2019-04-16 | Xencor, Inc. | Heterodimeric antibodies that bind CD3 and tumor antigens |
| IL252467B (en) | 2014-11-26 | 2022-06-01 | Xencor Inc | Heterodimeric antibodies that bind cd3 and cd38 |
| TN2017000223A1 (en) | 2014-11-26 | 2018-10-19 | Xencor Inc | Heterodimeric antibodies that bind cd3 and tumor antigens |
| PT3288573T (pt) | 2015-04-30 | 2020-03-25 | Psioxus Therapeutics Ltd | Adenovírus oncolítico que codifica uma proteína b7 |
| KR20180085800A (ko) | 2015-12-07 | 2018-07-27 | 젠코어 인코포레이티드 | Cd3 및 psma에 결합하는 이종이합체성 항체 |
| WO2017103291A1 (en) | 2015-12-17 | 2017-06-22 | Psioxus Therapeutics Limited | Virus encoding an anti-tcr-complex antibody or fragment |
| MA45255A (fr) | 2016-06-14 | 2019-04-17 | Xencor Inc | Anticorps inhibiteurs de points de contrôle bispécifiques |
| CA3029328A1 (en) | 2016-06-28 | 2018-01-04 | Xencor, Inc. | Heterodimeric antibodies that bind somatostatin receptor 2 |
| IL264902B2 (en) | 2016-08-29 | 2023-11-01 | Akamis Bio Ltd | Adenovirus with bispecific T cell activator |
| GB201713765D0 (en) | 2017-08-28 | 2017-10-11 | Psioxus Therapeutics Ltd | Modified adenovirus |
| WO2019023483A1 (en) * | 2017-07-26 | 2019-01-31 | Oncorus, Inc. | ONCOLYTIC VIRAL VECTORS AND USES THEREOF |
| US11312770B2 (en) | 2017-11-08 | 2022-04-26 | Xencor, Inc. | Bispecific and monospecific antibodies using novel anti-PD-1 sequences |
| JP7765181B2 (ja) | 2017-12-19 | 2025-11-06 | ゼンコア インコーポレイテッド | 改変されたil-2 fc融合タンパク質 |
| JP2021508477A (ja) * | 2017-12-29 | 2021-03-11 | オンコラス, インコーポレイテッド | 治療用ポリペプチドの腫瘍溶解性ウイルス送達 |
| US10982006B2 (en) | 2018-04-04 | 2021-04-20 | Xencor, Inc. | Heterodimeric antibodies that bind fibroblast activation protein |
| EP3781130A4 (en) * | 2018-04-11 | 2022-01-26 | Precision Molecular Inc. | THERAPEUTIC CONSTRUCTS FOR TREATMENT OF CANCER |
| CA3097741A1 (en) | 2018-04-18 | 2019-10-24 | Xencor, Inc. | Tim-3 targeted heterodimeric fusion proteins containing il-15/il-15ra fc-fusion proteins and tim-3 antigen binding domains |
| CN112867734A (zh) | 2018-04-18 | 2021-05-28 | Xencor股份有限公司 | 包含IL-15/IL-15Ra Fc融合蛋白和PD-1抗原结合结构域的靶向PD-1的异源二聚体融合蛋白及其用途 |
| EP3847186A4 (en) * | 2018-09-05 | 2022-05-18 | Memorial Sloan Kettering Cancer Center | Pleural effusion-based methods for assessing immunoresponsive cell activity |
| AU2019355971B2 (en) | 2018-10-03 | 2025-05-08 | Xencor, Inc. | IL-12 heterodimeric Fc-fusion proteins |
| CN109709341B (zh) * | 2019-01-17 | 2020-12-15 | 浙江大学 | 骨关节炎第二亚型的生物标记物以及用途 |
| KR20210128399A (ko) * | 2019-02-20 | 2021-10-26 | 더 리서치 인스티튜트 앳 네이션와이드 칠드런스 하스피탈 | 암-표적화되고, 바이러스-암호화된, 조절 가능한 t 세포 (catvert) 또는 nk 세포 (catvern) 링커 |
| BR112021016955A2 (pt) | 2019-03-01 | 2021-11-23 | Xencor Inc | Composição, composição de ácido nucleico, composição de vetor de expressão, vetor de expressão, célula hospedeira, métodos de produção de um domínio de ligação de membro de família 3 de pirofosfatase/fosfodiesterase de ectonucleotídeo e de tratamento de um câncer, anticorpo anti-enpp3, e, anticorpo heterodimérico |
| BR112021022682A2 (pt) | 2019-05-14 | 2022-02-22 | Provention Bio Inc | Métodos e composições para prevenir diabetes do tipo 1 |
| US11919956B2 (en) | 2020-05-14 | 2024-03-05 | Xencor, Inc. | Heterodimeric antibodies that bind prostate specific membrane antigen (PSMA) and CD3 |
| CA3182445A1 (en) | 2020-06-11 | 2021-12-16 | Francisco Leon | Methods and compositions for preventing type 1 diabetes |
| WO2022033468A1 (zh) * | 2020-08-14 | 2022-02-17 | 上海行深生物科技有限公司 | 水疱性口炎病毒及其治疗用途 |
| KR20230166150A (ko) | 2020-08-19 | 2023-12-06 | 젠코어 인코포레이티드 | 항-cd28 조성물 |
| WO2022067005A1 (en) * | 2020-09-27 | 2022-03-31 | Genentech, Inc. | High throughput multiparametric immune cell engager screening assay |
| EP4247850A1 (en) | 2020-11-20 | 2023-09-27 | Simcere Innovation, Inc. | Armed dual car-t compositions and methods for cancer immunotherapy |
| WO2022148736A1 (en) * | 2021-01-05 | 2022-07-14 | Transgene | Vectorization of muc1 t cell engager |
| GB202102049D0 (en) | 2021-02-13 | 2021-03-31 | Psioxus Therapeutics Ltd | Viruses |
| US11739144B2 (en) | 2021-03-09 | 2023-08-29 | Xencor, Inc. | Heterodimeric antibodies that bind CD3 and CLDN6 |
| KR20230154311A (ko) | 2021-03-10 | 2023-11-07 | 젠코어 인코포레이티드 | Cd3 및 gpc3에 결합하는 이종이량체 항체 |
| CN115161293B (zh) * | 2021-04-01 | 2024-11-15 | 南京惟亚德生物医药有限公司 | 一种编码双特异性t细胞衔接子的溶瘤痘苗病毒及其制备方法和应用 |
| EP4482859A1 (en) | 2022-02-27 | 2025-01-01 | Boehringer Ingelheim International GmbH | Bispecific antibodies against cd277 and a tumor-antigen |
| WO2024022602A1 (en) | 2022-07-28 | 2024-02-01 | Akamis Bio Ltd | Virus encoding transgenes to complement cellular therapy |
| WO2024047114A1 (en) * | 2022-08-31 | 2024-03-07 | Universität Zürich | Adenoviral-based in situ delivery of bispecific t cell engagers |
| AU2024277678A1 (en) | 2023-05-25 | 2025-11-27 | Dispatch Biotherapeutics, Inc. | Synthetic cancer antigens as targets for treating cancers |
| WO2025171383A2 (en) | 2024-02-09 | 2025-08-14 | Dispatch Biotherapeutics, Inc. | Engineered cancer antigens and related methods and uses |
| WO2025171388A1 (en) | 2024-02-09 | 2025-08-14 | Dispatch Biotherapeutics, Inc. | Engineered cancer antigens with modified domains and related methods and uses |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007537714A (ja) | 2003-10-16 | 2007-12-27 | マイクロメット アクツィエン ゲゼルシャフト | 多重特異的脱免疫cd3−結合物質 |
| WO2015059303A1 (en) | 2013-10-25 | 2015-04-30 | Psioxus Therapeutics Limited | Oncolytic adenoviruses armed with heterologous genes |
| JP2016007217A (ja) | 2008-10-01 | 2016-01-18 | アムゲン リサーチ (ミュンヘン) ゲーエムベーハー | PSCA×CD3、CD19×CD3、C−MET×CD3、エンドシアリン×CD3、EpCAM×CD3、IGF−1R×CD3、またはFAPアルファ×CD3の異種間特異的二重特異性単鎖抗体 |
| WO2016030489A2 (en) | 2014-08-27 | 2016-03-03 | Psioxus Therapeutics Limited | A process for the production of adenovirus |
Family Cites Families (98)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0170269A3 (en) | 1984-08-02 | 1987-09-23 | Kao Corporation | Medicated cosmetic compositions |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| GB8928874D0 (en) | 1989-12-21 | 1990-02-28 | Celltech Ltd | Humanised antibodies |
| GB9113120D0 (en) | 1991-06-18 | 1991-08-07 | Kodak Ltd | Photographic processing apparatus |
| US5358866A (en) | 1991-07-03 | 1994-10-25 | The United States Of America As Represented By The Department Of Health And Human Services | Cytosine deaminase negative selection system for gene transfer techniques and therapies |
| US5846945A (en) | 1993-02-16 | 1998-12-08 | Onyx Pharmaceuticals, Inc. | Cytopathic viruses for therapy and prophylaxis of neoplasia |
| FR2705361B1 (fr) | 1993-05-18 | 1995-08-04 | Centre Nat Rech Scient | Vecteurs viraux et utilisation en thérapie génique. |
| KR100356615B1 (ko) | 1993-07-13 | 2003-04-03 | 아방티 파르마 소시에테 아노님 | 결함아데노바이러스벡터및유전자치료에서그의사용 |
| US5631236A (en) | 1993-08-26 | 1997-05-20 | Baylor College Of Medicine | Gene therapy for solid tumors, using a DNA sequence encoding HSV-Tk or VZV-Tk |
| US5595756A (en) | 1993-12-22 | 1997-01-21 | Inex Pharmaceuticals Corporation | Liposomal compositions for enhanced retention of bioactive agents |
| US5830686A (en) | 1994-01-13 | 1998-11-03 | Calydon | Tissue-specific enhancer active in prostate |
| US5677170A (en) | 1994-03-02 | 1997-10-14 | The Johns Hopkins University | In vitro transposition of artificial transposons |
| US5587299A (en) | 1994-04-20 | 1996-12-24 | Memorial Sloan-Kettering Cancer Center | Isolated nucleic acid molecule coding for fibroblast activation protein alpha and uses thereof |
| DE19648650C2 (de) | 1996-01-29 | 1998-07-02 | Schering Ag | Puffersysteme und deren Verwendung zur Stabilisierung pharmazeutischer Zubereitung |
| US7732129B1 (en) | 1998-12-01 | 2010-06-08 | Crucell Holland B.V. | Method for the production and purification of adenoviral vectors |
| US5877011A (en) | 1996-11-20 | 1999-03-02 | Genzyme Corporation | Chimeric adenoviral vectors |
| CN1242051A (zh) | 1996-12-31 | 2000-01-19 | 昂尼克斯药物公司 | 用于肿瘤治疗和预防的致细胞病变病毒 |
| ATE374821T1 (de) | 1997-02-20 | 2007-10-15 | Univ Johns Hopkins Med | Mutationen in atp-abhängigen transpositionsproteinen die die zielortspezifität reduzieren |
| US20030044384A1 (en) | 1997-10-09 | 2003-03-06 | Pro-Virus, Inc. | Treatment of neoplasms with viruses |
| HUP0003911A3 (en) | 1997-10-09 | 2007-11-28 | Pro Virus | Treatment of neoplasms with viruses |
| US6291214B1 (en) | 1998-05-11 | 2001-09-18 | Glaxo Wellcome Inc. | System for generating recombinant viruses |
| US20020019051A1 (en) | 1998-05-27 | 2002-02-14 | Monika Lusky | Chimeric adenoviral vectors |
| US20030017138A1 (en) | 1998-07-08 | 2003-01-23 | Menzo Havenga | Chimeric adenoviruses |
| CN1110553C (zh) | 1998-07-15 | 2003-06-04 | 杭州赛狮生物技术开发有限公司 | 基因工程腺病毒及其用途 |
| US6455314B1 (en) | 1998-09-11 | 2002-09-24 | Genvec, Inc. | Alternatively targeted adenovirus |
| CA2354024C (en) | 1998-12-09 | 2009-12-22 | Jeffrey Schlom | A recombinant vector expressing multiple costimulatory molecules and uses thereof |
| ATE332364T1 (de) | 1999-02-22 | 2006-07-15 | Transgene Sa | Verfahren zur gewinnung von purifizierter virenzuammensetzung |
| CN1347450A (zh) | 1999-04-09 | 2002-05-01 | 阿文蒂斯药物股份有限公司 | 用于保存感染性重组腺病毒的组合物 |
| PT1818408E (pt) | 1999-05-17 | 2011-11-15 | Crucell Holland Bv | Adenovírus recombinante do serótipo ad11 |
| JP2003501041A (ja) | 1999-06-01 | 2003-01-14 | ユニバーシティ オブ ワシントン | 細胞特異的な感染およびゲノム組み込みのためのキメラファイバータンパク質を発現する組換えアデノウイルスベクター |
| ES2308989T3 (es) | 1999-08-09 | 2008-12-16 | Targeted Genetics Corporation | Aumento de la expresion de una secuencia nucleotidica heterologa a partir de vectores viricos recombinantes que contienen una secuencia que forman pares de bases intracatenarios. |
| US7396679B2 (en) | 1999-11-15 | 2008-07-08 | Onyx Pharmaceuticals, Inc. | Oncolytic adenovirus |
| US7063835B2 (en) | 2000-01-21 | 2006-06-20 | Biovex Limited | Virus strains |
| US7456009B2 (en) | 2000-03-07 | 2008-11-25 | Merck & Co., Inc. | Adenovirus formulations |
| AU2001265154A1 (en) | 2000-05-31 | 2001-12-11 | Genvec, Inc. | Method and composition for targeting an adenoviral vector |
| CA2412377A1 (en) | 2000-06-06 | 2001-12-13 | Bristol-Myers Squibb Company | B7-related nucleic acids and polypeptides and their uses for immunomodulation |
| US20030031675A1 (en) | 2000-06-06 | 2003-02-13 | Mikesell Glen E. | B7-related nucleic acids and polypeptides useful for immunomodulation |
| ATE449859T1 (de) | 2001-01-04 | 2009-12-15 | Goeran Wadell | Virusvektor zur gentherapie |
| US20050175589A1 (en) | 2001-07-13 | 2005-08-11 | Btg International Limited | Anti-neoplastic viral agents |
| AR039067A1 (es) | 2001-11-09 | 2005-02-09 | Pfizer Prod Inc | Anticuerpos para cd40 |
| EP1327688A1 (en) | 2002-01-14 | 2003-07-16 | Vereniging Voor Christelijk Wetenschappelijk Onderwijs | Adenoviruses with enhanced lytic potency |
| CA2474777A1 (en) | 2002-02-01 | 2003-08-07 | Transgene S.A. | Adenoviral vectors for modulating the cellular activities associated with pods |
| AU2003223775A1 (en) | 2002-04-30 | 2003-11-17 | Duke University | Adeno-associated viral vectors and methods for their production from hybrid adenovirus and for their use |
| US20040167088A1 (en) | 2003-02-25 | 2004-08-26 | Genvec, Inc. | Method of using adenoviral vectors with increased persistence in vivo |
| WO2004087930A1 (en) | 2003-03-28 | 2004-10-14 | Saint Louis University | Adenovirus replication-competent vectors expressing trail |
| US20050136035A1 (en) | 2003-06-03 | 2005-06-23 | Derek Ko | Cell specific replication-competent viral vectors comprising a self processing peptide cleavage site |
| JP2007536898A (ja) | 2003-07-01 | 2007-12-20 | セルテック アール アンド ディ リミテッド | 修飾抗体Fabフラグメント |
| GB0315457D0 (en) | 2003-07-01 | 2003-08-06 | Celltech R&D Ltd | Biological products |
| GB0315450D0 (en) | 2003-07-01 | 2003-08-06 | Celltech R&D Ltd | Biological products |
| JP2007530004A (ja) | 2003-07-18 | 2007-11-01 | オニックス ファーマシューティカルズ,インコーポレイティド | 疾患を処置するためのサブグループbアデノウイルスベクター |
| WO2005086922A2 (en) | 2004-03-10 | 2005-09-22 | Board Of Regents, University Of Texas System | Oncolytic adenovirus armed with therapeutic genes |
| WO2005107474A2 (en) | 2004-04-30 | 2005-11-17 | Introgen Therapeutics, Inc. | Oncolytic adenovirus armed with therapeutic genes |
| GB0411186D0 (en) | 2004-05-19 | 2004-06-23 | Celltech R&D Ltd | Biological products |
| KR101169109B1 (ko) | 2004-05-26 | 2012-07-26 | 싸이오서스 테라퓨틱스 엘티디. | 암 치료에 사용하기 위한 키메릭 아데노바이러스 |
| CN100361710C (zh) | 2004-06-07 | 2008-01-16 | 成都康弘生物科技有限公司 | 肿瘤细胞专一表达免疫调节因子gm-csf的溶瘤性腺病毒重组体的构建及其应用 |
| US20060292682A1 (en) | 2004-07-22 | 2006-12-28 | Hawkins Lynda K | Addition of transgenes into adenoviral vectors |
| CA2589602A1 (en) | 2004-09-01 | 2006-04-13 | Genvec, Inc. | Adenoviral vectors able to transduce apcs, potential use in immune response generation |
| EP1819823A2 (en) | 2004-12-01 | 2007-08-22 | Bayer Schering Pharma Aktiengesellschaft | Generation of replication competent viruses for therapeutic use |
| US20060205080A1 (en) | 2005-03-01 | 2006-09-14 | David Frey | Formulations for therapeutic viruses having enhanced storage stability |
| BRPI0615400A2 (pt) | 2005-08-31 | 2011-05-17 | Genvec Inc | vacinas para malária baseadas em vetor adenoviral |
| CN1961961B (zh) | 2005-11-11 | 2010-05-26 | 深圳市源兴生物医药科技有限公司 | 一种药物制剂及其制备方法 |
| DE102005055128B4 (de) | 2005-11-15 | 2015-04-02 | Universität Rostock | Viraler Vektor, dessen Verwendung zur Therapie von Leberzellkarzinomen und pharmazeutische Mittel umfassend den Vektor |
| ES2304281B1 (es) | 2006-02-01 | 2009-08-12 | Dnatrix Inc. | Adenovirus oncoliticos para el tratamiento del cancer. |
| WO2008080003A2 (en) | 2006-12-22 | 2008-07-03 | Bayer Schering Pharma Aktiengesellschaft | Generation of oncolytic adenoviruses and uses thereof |
| ES2667729T3 (es) | 2007-09-26 | 2018-05-14 | Ucb Biopharma Sprl | Fusiones de anticuerpos con doble especificidad |
| US20110034560A1 (en) | 2008-01-29 | 2011-02-10 | Sven Jacobson | Liquid formulations of compounds active at sulfonylurea receptors |
| WO2009143610A1 (en) | 2008-05-27 | 2009-12-03 | Oncolytics Biotech Inc. | Modulating interstitial pressure and oncolytic viral delivery and distribution |
| HUE033438T2 (en) | 2008-09-26 | 2017-11-28 | Ucb Biopharma Sprl | Biological products |
| CN101381742A (zh) | 2008-10-23 | 2009-03-11 | 浙江理工大学 | 晚期启动子靶向性调控溶瘤腺病毒pCN305载体及其构建方法与应用 |
| ES2385251B1 (es) | 2009-05-06 | 2013-05-06 | Fundació Privada Institut D'investigació Biomèdica De Bellvitge | Adenovirus oncolíticos para el tratamiento del cáncer. |
| US20100297072A1 (en) | 2009-05-19 | 2010-11-25 | Depinho Ronald A | Combinations of Immunostimulatory Agents, Oncolytic Virus, and Additional Anticancer Therapy |
| AU2010301105A1 (en) | 2009-10-02 | 2012-04-19 | Ludwig Institute For Cancer Research Ltd. | Anti-fibroblast activation protein antibodies and methods and uses thereof |
| UY33492A (es) * | 2010-07-09 | 2012-01-31 | Abbott Lab | Inmunoglobulinas con dominio variable dual y usos de las mismas |
| CN103237889B (zh) | 2010-08-16 | 2017-04-05 | 萨克生物研究学院 | 腺病毒组装方法 |
| RS56879B1 (sr) | 2011-08-23 | 2018-04-30 | Roche Glycart Ag | Bispecifične molekule koje vezuju antigen za aktiviranje t ćelija |
| EP2780020A4 (en) | 2011-11-14 | 2016-03-02 | Regenerative Sciences Llc | SUSPENDED PARTICLE DISTRIBUTION SYSTEMS AND METHODS |
| CN102586327B (zh) | 2012-01-18 | 2013-09-11 | 陕西师范大学 | 一步法构建携带外源基因的d24纤维蛋白修饰的条件复制型腺病毒载体及其应用 |
| EP2809682B1 (en) * | 2012-02-03 | 2020-04-08 | F.Hoffmann-La Roche Ag | Bispecific antibody molecules with antigen-transfected t-cells and their use in medicine |
| KR102125658B1 (ko) | 2012-05-04 | 2020-06-22 | 화이자 인코포레이티드 | 전립선 관련된 항원 및 백신 기재 면역치료 요법 |
| US9314519B2 (en) | 2012-08-21 | 2016-04-19 | Intervet Inc. | Liquid stable virus vaccines |
| JP2016512199A (ja) * | 2013-03-05 | 2016-04-25 | ベイラー カレッジ オブ メディスンBaylor College Of Medicine | 腫瘍溶解性ウイルス |
| KR20180058870A (ko) | 2013-03-06 | 2018-06-04 | 아담 제이 사이먼 | 뇌 건강의 다중 모드 생리학적 평가를 위한 폼 팩터 |
| GB201322851D0 (en) | 2013-12-23 | 2014-02-12 | Psioxus Therapeutics Ltd | Method |
| GB201318793D0 (en) | 2013-10-24 | 2013-12-11 | Plaquetec Ltd | Vascular Biomarkers |
| KR20160137946A (ko) | 2013-11-22 | 2016-12-02 | 디엔에이트릭스, 인코포레이티드 | 면역 세포 자극성 수용체 작용제(들)를 발현하는 아데노바이러스 |
| SI3560954T1 (sl) | 2014-04-03 | 2021-11-30 | Igm Biosciences, Inc. | Spremenjena J-veriga |
| GB201406608D0 (en) | 2014-04-12 | 2014-05-28 | Psioxus Therapeutics Ltd | Virus |
| GB201503500D0 (en) | 2015-03-02 | 2015-04-15 | Ucl Business Plc | Cell |
| JP6754532B2 (ja) | 2015-03-17 | 2020-09-16 | ティーアイエルティー・バイオセラピューティクス・オーワイTILT Biotherapeutics Oy | 二重特異性抗体をコードする腫瘍溶解性アデノウイルスおよびそれに関連する方法と使用 |
| PT3288573T (pt) | 2015-04-30 | 2020-03-25 | Psioxus Therapeutics Ltd | Adenovírus oncolítico que codifica uma proteína b7 |
| WO2017103291A1 (en) | 2015-12-17 | 2017-06-22 | Psioxus Therapeutics Limited | Virus encoding an anti-tcr-complex antibody or fragment |
| WO2017161360A2 (en) | 2016-03-18 | 2017-09-21 | Nant Holdings Ip, Llc | Multimodal vector for dendritic cell infection |
| IL264902B2 (en) | 2016-08-29 | 2023-11-01 | Akamis Bio Ltd | Adenovirus with bispecific T cell activator |
| GB201713765D0 (en) | 2017-08-28 | 2017-10-11 | Psioxus Therapeutics Ltd | Modified adenovirus |
| EP3529361B1 (en) | 2016-10-20 | 2021-03-24 | Alpine Immune Sciences, Inc. | Secretable variant immunomodulatory proteins and engineered cell therapy |
| WO2018083258A1 (en) | 2016-11-03 | 2018-05-11 | Psioxus Therapeutics Limited | Oncolytic adenovirus encoding at least three transgenes |
| WO2018083259A1 (en) | 2016-11-03 | 2018-05-11 | Psioxus Therapeutics Limited | Oncolytic adenovirus encoding transgenes |
| WO2018083257A1 (en) | 2016-11-03 | 2018-05-11 | Psioxus Therapeutics Limited | Oncolytic adenovirus encoding transgenes |
-
2017
- 2017-08-29 IL IL264902A patent/IL264902B2/en unknown
- 2017-08-29 EP EP23170482.6A patent/EP4273252A3/en active Pending
- 2017-08-29 IL IL303187A patent/IL303187A/en unknown
- 2017-08-29 ES ES17771344T patent/ES2983916T3/es active Active
- 2017-08-29 JP JP2019532192A patent/JP7212620B2/ja active Active
- 2017-08-29 CN CN201780057768.4A patent/CN110214025B/zh active Active
- 2017-08-29 SG SG11201901715UA patent/SG11201901715UA/en unknown
- 2017-08-29 MX MX2019002328A patent/MX2019002328A/es unknown
- 2017-08-29 EP EP17771343.5A patent/EP3503918B1/en active Active
- 2017-08-29 SG SG11201901716TA patent/SG11201901716TA/en unknown
- 2017-08-29 BR BR112019003866-3A patent/BR112019003866A2/pt unknown
- 2017-08-29 JP JP2019507924A patent/JP2019532621A/ja active Pending
- 2017-08-29 EP EP17771344.3A patent/EP3503919B1/en active Active
- 2017-08-29 MY MYPI2019000750A patent/MY197324A/en unknown
- 2017-08-29 CA CA3033267A patent/CA3033267A1/en not_active Abandoned
- 2017-08-29 KR KR1020197008941A patent/KR102427563B1/ko active Active
- 2017-08-29 US US16/329,125 patent/US12258417B2/en active Active
- 2017-08-29 WO PCT/EP2017/071674 patent/WO2018041838A1/en not_active Ceased
- 2017-08-29 AU AU2017320776A patent/AU2017320776B2/en active Active
- 2017-08-29 CN CN202410962886.1A patent/CN119592523A/zh active Pending
- 2017-08-29 CA CA3034517A patent/CA3034517A1/en active Pending
- 2017-08-29 US US16/329,098 patent/US12049513B2/en active Active
- 2017-08-29 WO PCT/EP2017/071655 patent/WO2018041827A1/en not_active Ceased
- 2017-08-29 CN CN202410956740.6A patent/CN119614520A/zh active Pending
- 2017-08-29 CN CN201780056486.2A patent/CN109862912B/zh active Active
- 2017-08-29 KR KR1020227026101A patent/KR102491752B1/ko active Active
-
2019
- 2019-01-30 ZA ZA2019/00644A patent/ZA201900644B/en unknown
- 2019-02-26 CL CL2019000510A patent/CL2019000510A1/es unknown
- 2019-02-26 MX MX2023008779A patent/MX2023008779A/es unknown
- 2019-02-28 PH PH12019500436A patent/PH12019500436A1/en unknown
- 2019-03-14 CO CONC2019/0002371A patent/CO2019002371A2/es unknown
-
2022
- 2022-08-17 JP JP2022130173A patent/JP7525558B2/ja active Active
-
2024
- 2024-06-14 US US18/744,059 patent/US20250026851A1/en active Pending
- 2024-07-18 JP JP2024114614A patent/JP2024147722A/ja active Pending
-
2025
- 2025-01-09 AU AU2025200140A patent/AU2025200140A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007537714A (ja) | 2003-10-16 | 2007-12-27 | マイクロメット アクツィエン ゲゼルシャフト | 多重特異的脱免疫cd3−結合物質 |
| JP2016007217A (ja) | 2008-10-01 | 2016-01-18 | アムゲン リサーチ (ミュンヘン) ゲーエムベーハー | PSCA×CD3、CD19×CD3、C−MET×CD3、エンドシアリン×CD3、EpCAM×CD3、IGF−1R×CD3、またはFAPアルファ×CD3の異種間特異的二重特異性単鎖抗体 |
| WO2015059303A1 (en) | 2013-10-25 | 2015-04-30 | Psioxus Therapeutics Limited | Oncolytic adenoviruses armed with heterologous genes |
| WO2016030489A2 (en) | 2014-08-27 | 2016-03-03 | Psioxus Therapeutics Limited | A process for the production of adenovirus |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7525558B2 (ja) | 二重特異性t細胞アクチベーターで武装したアデノウイルス | |
| CA2927968C (en) | Oncolytic adenoviruses armed with heterologous genes | |
| AU2016372576A1 (en) | Virus encoding an anti-TCR-complex antibody or fragment | |
| WO2018083257A1 (en) | Oncolytic adenovirus encoding transgenes | |
| WO2018083258A1 (en) | Oncolytic adenovirus encoding at least three transgenes | |
| HK40104373A (en) | Adenovirus armed with bispecific t cell engager (bite) | |
| EA043895B1 (ru) | Аденовирус, вооруженный биспецифичным активатором т-клеток | |
| HK40011114A (en) | Adenovirus armed with bispecific t cell engager | |
| NZ791667A (en) | Adenovirus armed with bispecific T-cell activator | |
| HK1224946A1 (en) | Oncolytic adenoviruses armed with heterologous genes | |
| HK1224946B (en) | Oncolytic adenoviruses armed with heterologous genes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220819 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220819 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230928 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231221 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240328 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240524 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240621 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240718 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7525558 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |