JP2025516649A - Shp2阻害剤およびpd-l1結合アンタゴニストを含む方法および組成物 - Google Patents
Shp2阻害剤およびpd-l1結合アンタゴニストを含む方法および組成物 Download PDFInfo
- Publication number
- JP2025516649A JP2025516649A JP2024566593A JP2024566593A JP2025516649A JP 2025516649 A JP2025516649 A JP 2025516649A JP 2024566593 A JP2024566593 A JP 2024566593A JP 2024566593 A JP2024566593 A JP 2024566593A JP 2025516649 A JP2025516649 A JP 2025516649A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- atezolizumab
- administered
- pharma
- acceptable salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Mycology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Endocrinology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
Abstract
Description
SHP2阻害剤(例えば、化合物1)およびPD-L1結合アンタゴニスト(例えば、アテゾリズマブ)を含む併用療法、ならびにそのような併用療法を使用する方法が本明細書に提供される。
配列表
本出願は、EFS-Webを介して提出されたASCIIテキスト形式の配列表のコンピュータ可読形式(CRF)を参照により組み込む。EFS-Webを介して提出された配列表テキストファイル、表題P37266_SEQ_LISTING_ST26.txt、ファイルサイズ18キロバイト、2023年4月25日作成。
本出願は、EFS-Webを介して提出されたASCIIテキスト形式の配列表のコンピュータ可読形式(CRF)を参照により組み込む。EFS-Webを介して提出された配列表テキストファイル、表題P37266_SEQ_LISTING_ST26.txt、ファイルサイズ18キロバイト、2023年4月25日作成。
タンパク質チロシンリン酸化は、がんの病因において中心的な役割を果たす。SSHP2(Src相同性-2ドメイン含有タンパク質チロシンホスファターゼ-2)は、PTPN11遺伝子によってコードされるタンパク質チロシンホスファターゼであり、RAS/Raf/MAPK、PI3K/AKT、Jak/STATおよびPD-1/PDL-1経路(J Med Chem.2020;63:11368-11396)等のいくつかの細胞内発癌性シグナル伝達経路の中心ノードとして機能する。SHP2の機能変異の獲得および/または過剰発現、遺伝子発達疾患(例えば、ヌーナン症候群)および様々なタイプのがん(例えば、乳がん、黒色腫、非小細胞肺腺癌(NSCL)およびその他)に関連している(Eur J Med Genet.2015;58(10):509-25;Pharmacol Res.2020;152:104595-104605)。基礎条件下では、SHP2は、SHP2の触媒活性が抑制された自己阻害型配座で存在する。白血病において、よりまれには固形腫瘍において検出されているSHP2における体細胞のミスセンス変異は、SHP2の自己阻害型立体配座を不安定化し、それにより、異常な過剰活性化をもたらす。
したがって、肺がん、頭頸部がん、および他の固形腫瘍等のがんを処置するための効果的な治療法および併用療法が必要とされている。
したがって、肺がん、頭頸部がん、および他の固形腫瘍等のがんを処置するための効果的な治療法および併用療法が必要とされている。
J Med Chem.2020;63:11368-11396
Eur J Med Genet.2015;58(10):509-25
Pharmacol Res.2020;152:104595-104605
本明細書では、当技術分野におけるこれらおよび他の課題に対する解決策が提供される。
一態様では、(a)本明細書に記載の化合物1またはその薬学的に許容され得る塩と、(b)本明細書に記載のPD-L1結合アンタゴニストとを含む併用療法が本明細書に提供される。
別の態様では、肺がん、頭頸部がんまたは黒色腫の処置を必要とする患者における肺がん、頭頸部がんまたは黒色腫を処置する方法であって、処置期間中に、本明細書に記載の(a)化合物1またはその薬学的に許容され得る塩と、(b)PD-L1結合アンタゴニストとを含む有効量の併用療法を投与することを含む方法が本明細書に提供される。いくつかの実施形態では、肺がんは、非小細胞肺がん(NSCLC)である。いくつかの実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC:head and neck squamous cell carcinoma)である。いくつかの実施形態では、黒色腫は、BRAF野生型(WT)黒色腫である。
別の態様では、肺がん、頭頸部がん、または黒色腫の処置を必要とする患者における肺がん、頭頸部がん、または黒色腫を処置する方法であって、有効量の本明細書に記載の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニストとを含む処置レジメンを患者に投与することを含む、方法が本明細書に提供される。いくつかの実施形態では、肺がんは、非小細胞肺がん(NSCLC)である。いくつかの実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC)である。いくつかの実施形態では、黒色腫は、BRAF野生型(WT)黒色腫である。
更に別の態様では、本明細書に記載の肺がん、頭頸部がんまたは黒色腫を処置するための、本明細書に記載の化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法の使用(U1)が本明細書に提供される。いくつかの実施形態では、肺がんは、非小細胞肺がん(NSCLC)である。いくつかの実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC)である。いくつかの実施形態では、黒色腫は、BRAF野生型(WT)黒色腫である。
更に別の態様では、肺がん、頭頸部がんまたは黒色腫を処置するための医薬品を製造するための、本明細書に記載の化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法の使用(U5)が本明細書に提供される。いくつかの実施形態では、肺がんは、非小細胞肺がん(NSCLC)である。いくつかの実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC)である。いくつかの実施形態では、黒色腫は、BRAF野生型(WT)黒色腫である。
更に別の態様では、肺がん、頭頸部がんまたは黒色腫の処置における使用のための、本明細書に記載の化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法が本明細書に提供される。いくつかの実施形態では、肺がんは、非小細胞肺がん(NSCLC)である。いくつかの実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC)である。いくつかの実施形態では、黒色腫は、BRAF野生型(WT)黒色腫である。
任意の特定の要素または行為の説明を容易に識別するために、参照番号の最上位桁は、その要素が最初に導入される図番号を指す。
別段の定義がない限り、本明細書で使用される全ての技術用語および科学用語は、当業者によって一般的に理解されている意味と同じ意味を有する。例えば、Singleton et al.,DICTIONARY OF MICROBIOLOGY AND MOLECULAR BIOLOGY 2nd ed.,J.Wiley&Sons(New York,NY 1994);Sambrook et al.,MOLECULAR CLONING,A LABORATORY MANUAL,Cold Springs Harbor Press(Cold Springs Harbor,NY 1989)を参照されたい。本発明の実施においては、本明細書に記載されるものと類似したまたは同等の任意の方法、装置、および材料を使用することができる。
以下の定義は、本明細書で頻繁に用いられる特定の用語の理解を容易にするために提供されており、本開示の範囲を限定することを意味するものではない。本明細書で言及されている全ての参照文献は、その全体が参照により組み込まれる。
本明細書で使用される場合、特に明記されていない限り、「約」および「およそ」という用語は、組成物または剤形の成分の用量、量、または重量パーセントを指すときには、指定された用量、量、または重量パーセントから得られるものと同等の薬理的効果を提供するために、当業者によって認識される用量、量、または重量パーセントを意味する。同等の用量、量、または重量パーセントは、指定された用量、量、または重量パーセントの30%、20%、15%、10%、5%、1%、またはそれ未満以内であり得る。
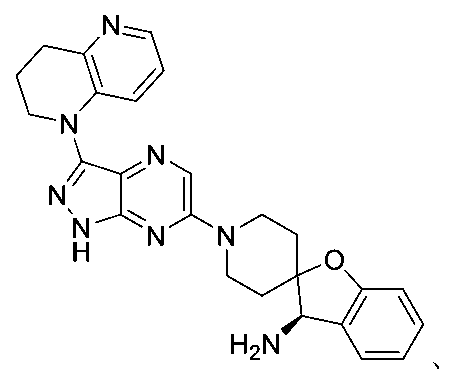
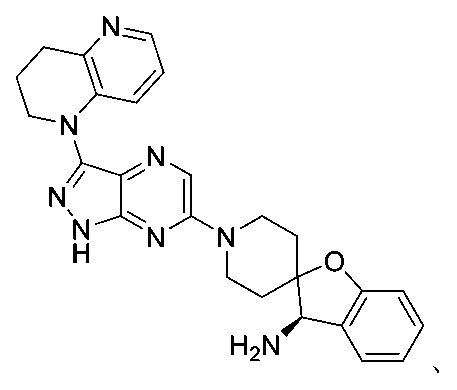
「化合物1」は、構造:
、
を有し、化学名(R)-1’-(3-(3,4-ジヒドロ-1,5-ナフチリジン-1(2H)-イル)-1H-ピラゾロ[3,4-b]ピラジン-6-イル)-3H-スピロ[ベンゾフラン-2,4’-ピペリジン]-3-アミンを有する化合物を指す。
を有し、化学名(R)-1’-(3-(3,4-ジヒドロ-1,5-ナフチリジン-1(2H)-イル)-1H-ピラゾロ[3,4-b]ピラジン-6-イル)-3H-スピロ[ベンゾフラン-2,4’-ピペリジン]-3-アミンを有する化合物を指す。
「薬学的に許容され得る」という用語は、動物、例えばヒトに適切に投与された場合に、副作用、アレルギー反応、または他の副反応を生み出さない、分子実体および組成を指す。
本発明の化合物は、薬学的に許容され得る塩等の塩の形態であってもよい。「薬学的に許容され得る塩」は、酸付加塩と塩基付加塩の両方を含む。「薬学的に許容され得る酸付加塩」とは、塩酸、臭化水素酸、硫酸、硝酸、炭酸、リン酸等の無機酸と共に形成される、遊離塩基の生物学的有効性および性質を保持し、かつ生物学的または別様において望ましい塩を意味し、有機酸は、ギ酸、酢酸、プロピオン酸、グリコール酸、グルコン酸、乳酸、ピルビン酸、シュウ酸、リンゴ酸、マレイン酸、マロン酸、コハク酸、フマル酸、酒石酸、クエン酸、アスパラギン酸、アスコルビン酸、グルタミン酸、アントラニル酸、安息香酸、ケイ皮酸、マンデル酸、エンボニン酸、フェニル酢酸、メタンスルホン酸、エタンスルホン酸、ベンゼンスルホン酸、p-トルエンスルホン酸、サリチル酸等の有機酸の脂肪族、脂環式、芳香族、芳香脂肪族、複素環式、カルボン酸、およびスルホン酸の部類から選択され得る。
「薬学的に許容され得る塩基付加塩」という用語は、ナトリウム、カリウム、リチウム、アンモニウム、カルシウム、マグネシウム、鉄、亜鉛、銅、マンガン、アルミニウムの塩等の無機塩基から誘導されるものを含む。具体的な塩基付加塩は、アンモニウム塩、カリウム塩、ナトリウム塩、カルシウム塩、およびマグネシウム塩である。薬学的に許容され得る有機無毒性塩基に由来する塩としては、一級、二級、および三級アミン、天然に存在する置換アミン、環式アミン、および塩基性イオン交換樹脂を含む置換アミン、例えばイソプロピルアミン、トリメチルアミン、ジエチルアミン、トリエチルアミン、トリプロピルアミン、エタノールアミン、2-ジエチルアミノエタノール、トロメタミン、ジシクロヘキシルアミン、リジン、アルギニン、ヒスチジン、カフェイン、プロカイン、ヒドラバミン、コリン、ベタイン、エチレンジアミン、グルコサミン、メチルグルカミン、テオブロミン、プリン、ピペラジン、ピペリジン、N-エチルピペリジン、ポリアミン樹脂等の塩が挙げられる。具体的な有機無毒性塩基としては、イソプロピルアミン、ジエチルアミン、エタノールアミン、トロメタミン、ジシクロヘキシルアミン、コリン、およびカフェインが挙げられる。
いくつかの実施形態では、塩は、塩酸塩、臭化水素酸塩、トリフルオロ酢酸塩、硫酸塩、リン酸塩、酢酸塩、フマル酸塩、マレイン酸塩、酒石酸塩、乳酸塩、クエン酸塩、ピルビン酸塩、コハク酸塩、シュウ酸塩、メタンスルホン酸塩、p-トルエンスルホン酸塩、重硫酸塩、ベンゼンスルホン酸塩、エタンスルホン酸塩、マロン酸塩、キシナホ酸塩、アスコルビン酸塩、オレイン酸塩、ニコチン酸塩、サッカリン酸塩、アジピン酸塩、ギ酸塩、グリコール酸塩、パルミチン酸塩、L-乳酸塩、D-乳酸塩、アスパラギン酸塩、リンゴ酸塩、L-酒石酸塩、D-酒石酸塩、ステアリン酸塩、フロ酸塩(例えば、2-フロ酸塩または3-フロ酸塩)、ナパジシル酸塩(ナフタレン-1,5-ジスルホン酸塩、またはナフタレン-1(スルホン酸)-5-スルホン酸塩)、エジシル酸塩(エタン-1,2-ジスルホン酸塩、またはエタン-1-(スルホン酸)-2-スルホン酸塩)、イソチオン酸塩(2-ヒドロキシエチルスルホン酸塩)、2-メシチレンスルホン酸塩、2-ナフタレンスルホン酸塩、2,5-ジクロロベンゼンスルホン酸塩、D-マンデル酸塩、L-マンデル酸塩、ケイ皮酸塩、安息香酸塩、アジピン酸塩、エシル酸塩、マロン酸塩、メシチル酸塩(2-メシチレンスルホン酸塩)、ナプシル酸塩(2-ナフタレンスルホン酸塩)、カンシル酸塩(カンファー10-スルホン酸塩、例えば(1S)-(+)-10-カンファー-スルホン酸塩)、グルタミン酸塩、グルタル酸塩、馬尿酸(2-(ベンゾイルアミノ)酢酸塩)、オロチン酸塩、キシル酸塩(p-キシレン-2-スルホン酸塩)、およびパモ酸塩(2,2’-ジヒドロキシ-1,1’-ジナフチルメタン-3,3’-ジカルボン酸塩)から選択される。
「阻害する」および「低減/減少させる」という用語、またはこれらの用語のあらゆる変形は、所望の結果を達成するための、測定可能なあらゆる低減/減少または完全な阻害を含む。例えば、約、最大で約、または少なくとも約5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%、またはそれ以上、またはこれらの任意の範囲変数の減少、通常と比較しての活性の低下が存在し得る。
「PD-L1結合アンタゴニスト」、「PD-L1阻害剤」、および「PD-L1遮断抗体」という用語は、本明細書では互換的に使用され、PD-L1とその結合パートナーのうちのいずれか1つ以上、例えば、PD-1および/またはB7-1との相互作用に起因するシグナル伝達を低減する、遮断する、阻害する、消失させる、または妨害する分子を指す。いくつかの例では、PD-L1結合アンタゴニストは、PD-L1のその結合パートナーへの結合を阻害する分子である。具体的な態様では、PD-L1結合アンタゴニストは、PD-L1のPD-1および/またはB7-1への結合を阻害する。いくつかの例では、PD-L1結合アンタゴニストは、抗PD-L1抗体、その抗原結合断片、イムノアドヘシン、融合タンパク質、オリゴペプチド、ならびにPD-L1とその結合パートナーのうちの1つ以上、例えば、PD-1および/またはB7-1との相互作用に起因するシグナル伝達を減少させる、遮断する、阻害する、抑止する、または干渉する他の分子を含む。一例では、PD-L1結合アンタゴニストは、機能不全のT細胞を機能不全にしないようにする(例えば、抗原認識に対するエフェクター応答を増強する)ように、PD-L1を介するシグナル伝達を介してTリンパ球上で発現される細胞表面タンパク質によってまたはそれを介して媒介される負の共刺激性シグナルを低減する。いくつかの例では、PD-L1結合アンタゴニストはPD-L1に結合する。いくつかの例では、PD-L1結合アンタゴニストは、抗PD-L1抗体(例えば、抗PD-L1アンタゴニスト抗体)である。例示的な抗PD-L1アンタゴニスト抗体としては、アテゾリズマブ、MDX-1105、MEDI4736(デュルバルマブ)、MSB0010718C(アベルマブ)、SHR-1316、CS1001、エンバホリマブ、TQB2450、ZKAB001、LP-002、CX-072、IMC-001、KL-A167、APL-502、コシベリマブ、ロダポリマブ、FAZ053、TG-1501、BGB-A333、BCD-135、AK-106、LDP、GR1405、HLX20、MSB2311、RC98、PDL-GEX、KD036、KY1003、YBL-007およびHS-636が挙げられる。好ましい態様では、PD-L1結合アンタゴニストは、アテゾリズマブである。
「プログラム死リガンド1」および「PD-L1」という用語は、本明細書では、天然配列のヒトPD-L1ポリペプチドを指す。天然配列PD-L1ポリペプチドは、Uniprot受託番号Q9NZQ7で提供される。例えば、天然配列PD-L1は、Uniprot受託番号Q9NZQ7-1(アイソフォーム1)に記載のアミノ酸配列を有し得る。別の例において、天然配列PD-L1は、Uniprot受託番号Q9NZQ7-2(アイソフォーム2)に記載のアミノ酸配列を有し得る。更に別の例において、天然配列PD-L1は、Uniprot受託番号Q9NZQ7-3(アイソフォーム3)に記載のアミノ酸配列を有し得る。PD-L1はまた、当技術分野において「プログラム細胞死1リガンド1」、「PDCD1LG1」、「CD274」、「B7-H」、および「PDL1」とも称される。
Kabatナンバリングシステムは、一般に、可変ドメイン中の残基(およそ軽鎖の残基1~107および重鎖の残基1~113)を指す場合に使用される(例えば、Kabat et al.,Sequences of Immunological Interest.5th Ed.Public Health Service,National Institutes of Health,Bethesda,Md.(1991))。「EUナンバリングシステム」または「EU指標」は、一般に、免疫グロブリン重鎖定常領域における残基について言及する際に使用される(例えば、上記のKabat et al.で報告されるEU指標)。「KabatにおけるようなEUインデックス」は、ヒトIgG1 EU抗体の残基ナンバリングを指す。
本明細書の目的では、「アテゾリズマブ」は、PD-L1に結合し、配列番号1の重鎖配列および配列番号2の軽鎖配列を含むFc操作ヒト化非グリコシル化IgG1カッパ免疫グロブリンである。アテゾリズマブは、Fc領域アミノ酸残基のEUナンバリングを使用して重鎖上の297位に単一のアミノ酸置換(アスパラギンをアラニンへ)(N297A)を含み、Fc受容体への最小限の結合を有する非グリコシル化抗体をもたらす。アテゾリズマブは、2015年1月16日に発行されたWHO Drug Information(International Nonproprietary Names for Pharmaceutical Substances),Proposed INN:List 112,Vol.28,No.4にも記載されている(485頁を参照)。
いくつかの例では、抗PD-L1抗体は、(a)配列番号1または配列番号1の配列と少なくとも95%の配列同一性(例えば、少なくとも95%、96%、97%、98%、または99%の配列同一性)を有するアミノ酸配列を含むVH、(b)配列番号2の配列に対して少なくとも95%の配列同一性(例えば、少なくとも95%、96%、97%、98%、または99%の配列同一性)を有するアミノ酸配列もしくは配列番号2を含むVL、または(c)(a)に記載のVHおよび(b)に記載のVLを含む。
一実施形態では、抗PD-L1抗体は、以下を含むアテゾリズマブを含む:
(a)重鎖(VH)アミノ酸配列:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG(配列番号1)、および
(b)軽鎖(VL)アミノ酸配列:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号2)。
(a)重鎖(VH)アミノ酸配列:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG(配列番号1)、および
(b)軽鎖(VL)アミノ酸配列:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号2)。
「がん」という用語は、身体の一部における異常細胞の制御されていない分裂によって引き起こされる疾患を指す。一例では、がんは、肺がんである。別の例では、がんは、非小細胞肺がん(NSCLC:non-small cell lung cancer)である。一例では、がんは、頭頸部がんである。別の例では、がんは、頭頸部扁平上皮癌(HNSCC)である。一例では、がんは、黒色腫である。別の例では、がんは、BRAF野生型(WT)黒色腫である。
本明細書で使用される場合、「処置すること」は、有効量の治療剤(例えば、アテゾリズマブまたは化合物1)または治療剤の組み合わせ(例えば、アテゾリズマブおよび化合物1)による有効ながん処置を含む。処置は、第一選択処置(例えば、患者は以前に処置されていない可能性がある、または事前の全身療法を受けたことがない)または第二選択処置もしくはそれ以降の治療であり得る。例えば、患者は、がん性細胞の増殖の低減(または破壊)、疾患に起因する症候の軽減、疾患に罹患している者の生活の質の向上、疾患の処置に必要な他の薬物治療の用量の低減、および/または患者の生存期間の延長を含むが、これらに限定されない、本明細書に記載のがんに関連する1つ以上の症候が軽減または排除された場合、「処置」に成功する。
疾患の「進行の遅延」という用語は、本明細書に記載のがんの発症を先延ばしにする、妨げる、遅延させる、遅らせる、安定化する、および/または延期することを指す。この遅延は、処置されている本明細書に記載のがんおよび/または患者の病歴に応じて、様々な時間長であり得る。当業者には明らかであるように、十分または有意な遅延は、患者ががんを発症しないという点で予防を事実上包含し得る。
本明細書において、「有効量」は、治療結果を達成する本明細書に記載の治療剤(例えば、アテゾリズマブおよび/または化合物1)の量を指す。いくつかの例では、治療剤または治療剤の組み合わせの有効量は、本明細書に提供される臨床エンドポイントを達成する薬剤または薬剤の組み合わせの量である。本明細書における有効量は、患者の疾患状態、年齢、性別、および体重、ならびに患者における所望の応答を誘発する薬剤の能力等の要因に応じて異なり得る。有効量は、治療上有益な作用が処置の何らかの毒性作用または有害作用を上回るものでもある。いくつかの実施形態では、有効量の薬物は、がん細胞の数を減少させ、腫瘍サイズを低減させ、がん細胞の末梢器官への浸潤を阻害し(すなわち、遅らせるか、または停止し)、腫瘍転移を阻害し(すなわち、遅らせるか、または停止し)、腫瘍成長を阻害し(すなわち、遅らせるか、または停止し)、および/または疾患に関連する症候のうちの1つ以上を軽減する効果を有し得る。有効量を1回以上の投与で投与することができる。本明細書に記載の薬物、化合物、医薬組成物または併用療法の有効量は、直接的または間接的に治療的処置を達成するのに十分な量であり得る。
「客観的奏効率」または「ORR」は、RECIST v1.1に従って治験責任医師によって決定される、34週間離れた2回の連続した機会における確定された完全奏効または部分奏効を有する患者の割合を指す。
「奏効期間」または「DOR」とは、記録された客観的奏効の最初の発生から、RECIST v1.1に従って治験責任医師によって決定された疾患の進行、または何らかの原因による死亡のうち、いずれか早い方までの時間を指す。
「無増悪生存」または「PFS」とは、登録から、RECIST v1.1を使用して治験責任医師が決定した、最初の記録された疾患の進行の発生または何らかの原因による死亡のうち、いずれか早い方の日付までの時間を指す。
本明細書で使用される場合、「完全奏効」および「CR」は、全ての標的病変の消失および(該当する場合)腫瘍マーカーレベルの正常化を指す。
本明細書で使用される場合、「部分奏効」および「PR」は、1つ以上の非標的病変の持続および/または(適用可能な場合)腫瘍マーカーレベルの正常限界を超える維持を指す。PRは、CRの不存在下での標的病変の直径の合計の330%の低減、新たな病変、および非標的病変における明確な進行も指し得る。
「投与期間」または「サイクル」とは、本明細書に記載の1つ以上の薬剤(例えば、化合物1およびアテゾリズマブ)の投与を含む期間、および本明細書に記載の1つ以上の薬剤の投与を含まない任意の期間を指す。例えば、サイクルは合計21日間とすることができ、サイクルの各日に本明細書に記載の1つ以上の薬剤(例えば、化合物1およびアテゾリズマブ)の投与を含む。別の例では、サイクルは合計28日間とすることができ、21日間および7日間の休薬期間にわたる本明細書に記載の1つ以上の薬剤(例えば、化合物1およびアテゾリズマブ)の投与を含む。「休薬期間」は、本明細書に記載の薬剤の少なくとも1つ(すなわち、化合物1およびアテゾリズマブ)が投与されない期間を指す。一実施形態では、休薬期間は、本明細書に記載の薬剤(すなわち、化合物1およびアテゾリズマブ)のいずれも投与されない期間を指す。本明細書で提供される休薬期間は、いくつかの例では、化合物1またはアテゾリズマブではない別の薬剤の投与を含むことができる。このような場合には、休薬期間中の別の薬剤の投与は、本明細書に記載の薬剤の投与の妨害になったり、不利益を与えたりすべきではない。一例では、本明細書で使用されるサイクルは、休薬期間のない21日間のサイクルを指す。
「投薬レジメン」とは、1つまたは複数のサイクルを含む、本明細書に記載の薬剤の投与期間を指し、各サイクルは、本明細書に記載の薬剤の投与を異なる回数または異なる量で含むことができる。
「QD」は、本明細書に記載の薬剤を1日1回投与することを指す。
「BID」は、本明細書に記載の薬剤を1日2回投与することを指す。
「Q3W」は、本明細書に記載の薬剤を3週間に1回投与することを指す。
「PO」は、本明細書に記載の薬剤の経口投与を指す。
「IV」は、本明細書に記載の任意の薬剤の静脈内投与を指す。
「患者」という用語は、ヒト患者を指す。患者は成人であってもよい。
「抗体」という用語は、具体的には、それらが所望の生物学的活性を示す限り、モノクローナル抗体(全長モノクローナル抗体等)、ポリクローナル抗体、多重特異性抗体(例えば、二重特異性抗体)、および抗体断片を包含する。一例では、抗体は完全長モノクローナル抗体である。
本明細書で使用される場合、IgG「アイソタイプ」または「サブクラス」という用語は、それらの定常領域の化学的および抗原的特性によって定義される免疫グロブリンのサブクラスのうちのいずれかを意味する。
それらの重鎖の定常ドメインのアミノ酸配列に応じて、抗体(免疫グロブリン)は、異なるクラスに割り当てられ得る。免疫グロブリンには5つの主なクラス:IgA、IgD、IgE、IgG、およびIgMがあり、これらのいくつかは、サブクラス(アイソタイプ)、例えば、IgG1、IgG2、IgG3、IgG4、IgA1、およびIgA2に更に分けられる場合がある。免疫グロブリンの異なるクラスに対応する重鎖定常ドメインは、それぞれ、α、γ、ε、γ、およびμと呼ばれる。免疫グロブリンの異なるクラスのサブユニット構造および三次元立体配置は周知であり、一般的に、例えば、Cellular and Mol.Immunology,4th ed.(W.B.Saunders,Co.,2000)に記載されている。抗体は、抗体と1以上の他のタンパク質もしくはペプチドとの共有的または非共有的結合により形成される、より大きな融合分子の一部であってもよい。
「全長抗体」、「インタクトな抗体」、および「全抗体」という用語は、以下に記載の抗体断片ではない、その実質的にインタクトな形態の抗体を指すために本明細書で同義に使用される。この用語は、Fc領域を含む抗体を指す。
「Fc領域」という用語は、本明細書では定常領域の少なくとも一部分を含有する免疫グロブリン重鎖のC末端領域を定義するために使用される。この用語は、ネイティブ配列Fc領域と変異体Fc領域を含む。一態様では、ヒトIgG重鎖Fc領域は、Cys226から、またはPro230から、重鎖のカルボキシル末端までに及ぶ。しかしながら、宿主細胞によって産生される抗体は、重鎖のC末端から1つ以上の、特に1つまたは2つのアミノ酸の翻訳後開裂を受けてもよい。したがって、完全長重鎖をコードする特定の核酸分子の発現によって宿主細胞によって産生される抗体は、完全長重鎖を含み得るか、または完全長重鎖の切断されたバリアントを含み得る。これは、重鎖の最後の2つのC末端アミノ酸がグリシン(G446)とリジン(K447)である場合にも当てはまる。したがって、Fc領域のC末端リジン(K447)、またはC末端グリシン(G446)およびリジン(K447)が存在してもよく、または存在していなくてもよい。Fc領域を含む重鎖のアミノ酸配列は、別途示されない限り、本明細書ではC末端リジン(K447)なしで示される。一態様では、本明細書に開示される抗体に含まれる、本明細書で明記したFc領域を含む重鎖は、更なるC末端グリシン-リジンジペプチド(G446およびK447)を含む。一態様では、本明細書に開示される抗体に含まれる、本明細書で明記したFc領域を含む重鎖は、更なるC末端グリシン残基(G446)を含む。一態様では、本明細書に開示される抗体に含まれる、本明細書で明記したFc領域を含む重鎖は、更なるC末端リジン残基(K447)を含む。一実施形態では、Fc領域は、重鎖の単一アミノ酸置換N297Aを含む。本明細書で特に明記されない限り、Fc領域または定常領域におけるアミノ酸残基のナンバリングは、Kabat et al.,Sequences of Proteins of Immunological Interest,5th Ed.Public Health Service,National Institutes of Health,Bethesda,MD,1991に記載されるような、EUナンバリング方式(EUインデックスとも呼ばれる)に従う。
「ネイキッド抗体」は、異種部分(例えば、細胞傷害性部分)または放射性標識にコンジュゲートしていない抗体を指す。ネイキッド抗体は、薬学的組成物で存在してもよい。
「抗体断片」は、好ましくはその抗原結合領域を含む、インタクトな抗体の一部を含む。いくつかの例では、本明細書に記載の抗体断片は、抗原結合断片である。抗体断片の例としては、Fab、F(ab’)2、およびFv断片、ダイアボディ、直鎖状抗体、一本鎖抗体分子(例えば、scFv)、ならびに抗体断片から形成される多重特異性抗体が挙げられる。
「モノクローナル抗体」という用語は、本明細書で使用される場合、実質的に均一な抗体の集合から得られる抗体を指し、すなわち、例えば、天然に存在する変異またはモノクローナル抗体調製物の製造中に生じる変異を含む、可能性のあるバリアント抗体(そのようなバリアントは一般的に少量存在する)を除いて、集合を構成する個々の抗体は同一であるおよび/または同じエピトープを結合する。様々な決定基(エピトープ)に対する様々な抗体を通常含むポリクローナル抗体調製物とは対照的に、モノクローナル抗体調製物の各モノクローナル抗体は、抗原上の単一の決定基に対するものである。したがって、修飾語「モノクローナル」は、抗体の実質的に均一な集合から得られる抗体の特徴を示し、任意の特定の方法による抗体の産生を必要とするように解釈すべきではない。例えば、本発明に従って使用されるモノクローナル抗体は、ハイブリドーマ法、組換えDNA法、ファージディスプレイ法、およびヒト免疫グロブリン遺伝子座の全部または一部を含むトランスジェニック動物を利用する方法を含むがこれらに限定されない種々の技術によって作製されてもよい。
本明細書で使用される場合、「超可変領域」または「HVR」という用語は、配列において超可変性であり、抗原結合特異性を決定する、抗体可変ドメインの領域、例えば「相補性決定領域」(CDR)のそれぞれを指す。
一般に、抗体は6つのCDRを含み、3つがVHにあり(CDR-H1、CDR-H2、CDR-H3)、3つがVLにある(CDR-L1、CDR-L2、CDR-L3)。本明細書における例示的なCDRとしては、
(a)アミノ酸残基26-32(L1)、50-52(L2)、91-96(L3)、26-32(H1)、53-55(H2)および96-101(H3)で生じる超可変ループ(Chothia and Lesk,J.Mol.Biol.196:901-917(1987));
(b)アミノ酸残基24-34(L1)、50-56(L2)、89-97(L3)、31-35b(H1)、50-65(H2)および95-102(H3)に生じるCDR(Kabat et al.,Sequences of Proteins of Immunological Interest,5th Ed.Public Health Service,National Institutes of Health,Bethesda,MD(1991));ならびに
(c)アミノ酸残基27c-36(L1)、46-55(L2)、89-96(L3)、30-35b(H1)、47-58(H2)および93-101(H3)で生じる抗原接触(MacCallum et al.J.Mol.Biol.262:732-745(1996))が挙げられる。
(a)アミノ酸残基26-32(L1)、50-52(L2)、91-96(L3)、26-32(H1)、53-55(H2)および96-101(H3)で生じる超可変ループ(Chothia and Lesk,J.Mol.Biol.196:901-917(1987));
(b)アミノ酸残基24-34(L1)、50-56(L2)、89-97(L3)、31-35b(H1)、50-65(H2)および95-102(H3)に生じるCDR(Kabat et al.,Sequences of Proteins of Immunological Interest,5th Ed.Public Health Service,National Institutes of Health,Bethesda,MD(1991));ならびに
(c)アミノ酸残基27c-36(L1)、46-55(L2)、89-96(L3)、30-35b(H1)、47-58(H2)および93-101(H3)で生じる抗原接触(MacCallum et al.J.Mol.Biol.262:732-745(1996))が挙げられる。
特に指示がない限り、CDRは、上記Kabat et al.に従い決定される。当業者は、CDRの表記は、上記Chothia、上記McCallum、または、任意の他の、科学的に認可された命名システムに従い決定することができることを理解するであろう。
「フレームワーク」または「FR」は、相補性決定領域(CDR)以外の可変ドメイン残基を指す。可変ドメインのFRは、一般的に4つのFRドメイン:FR1、FR2、FR3およびFR4からなる。したがって、CDRおよびFR配列は、一般的に、VH(またはVL)において次の配列で出現する:FR1-CDR-H1(CDR-L1)-FR2-CDR-H2(CDR-L2)-FR3-CDR-H3(CDR-L3)-FR4。
「Kabatにおけるような可変ドメイン残基ナンバリング」または「Kabatにおけるようなアミノ酸位置ナンバリング」という用語、およびそれらの変形は、Kabat et al.,(上記参照)における抗体の編集物の重鎖可変ドメインまたは軽鎖可変ドメインに使用されるナンバリングシステムを指す。このナンバリング方式を使用して、実際の直鎖状アミノ酸配列は、可変ドメインのFRもしくはHVRの短縮、またはそれへの挿入に対応する、より少ないアミノ酸または追加のアミノ酸を含み得る。例えば、重鎖可変ドメインは、H2の残基52の後に単一のアミノ酸挿入(Kabatに従う残基52a)を含み、重鎖FR残基82の後に挿入された残基(例えば、Kabatに従う残基82a、82b、および82c等)を含み得る。残基のKabatナンバリングは、所与の抗体に対して、抗体の配列と「標準の」Kabatによってナンバリングされた配列との相同領域での整列によって決定され得る。
「パッケージ添付文書」との用語は、治療製品の市販パッケージに通常含まれる指示を指すために用いられ、このような治療製品に関する適応症、使用、投薬量、投与、併用療法、禁忌および/または警告に関する情報を含有する。
本明細書で使用される場合、「と組み合わせて」とは、別の処置様式に加えて1つの処置様式、例えば、PD-1軸結合アンタゴニスト(例えば、アテゾリズマブ)および化合物1またはその薬学的に許容され得る塩の投与を含む処置レジメンの投与を指す。したがって、「と組み合わせて」とは、患者への他の処置様式の投与前、投与中、または投与後の1つの処置様式の投与を指す。
1つ以上の他の薬物と「同時に」投与される薬物は、同一処置サイクル中、1つ以上の他の薬物と同じ処置日に、また必要に応じて1つ以上の他の薬物と同じ時間に投与される。例えば、3週間ごとに付与されるがん療法の場合、同時に投与される薬物はそれぞれ、3週間のサイクルの1日目に投与される。
併用療法
化合物1またはその薬学的に許容され得る塩およびPD-L1結合アンタゴニストを含む併用療法(組成物)が本明細書に提供される。
化合物1またはその薬学的に許容され得る塩およびPD-L1結合アンタゴニストを含む併用療法(組成物)が本明細書に提供される。
いくつかの例では、PD-L1結合アンタゴニストは抗PD-L1抗体である。様々な抗PD-L1抗体が本明細書において企図され、記載される。本明細書の例のいずれにおいても、単離された抗PD-L1抗体は、ヒトPD-L1、例えば、UniProtKB/Swiss-Prot受託番号Q9NZQ7-1に示されるようなヒトPD-L1、またはそのバリアントに結合することができる。いくつかの例では、抗PD-L1抗体は、PD-L1とPD-1との間および/またはPD-L1とB7-1との間の結合を阻害することができる。いくつかの例では、抗PD-L1抗体はモノクローナル抗体である。いくつかの例では、抗PD-L1抗体は、Fab断片、Fab’-SH断片、Fv断片、scFv断片、および(Fab’)2断片片からなる群から選択される抗体断片である。いくつかの例では、抗PD-L1抗体はヒト化抗体である。いくつかの例では、抗PD-L1抗体は、ヒト抗体である。例示的な抗PD-L1抗体としては、アテゾリズマブ、MDX-1105、MEDI4736(デュルバルマブ)、MSB0010718C(アベルマブ)、SHR-1316、CS1001、エンバホリマブ、TQB2450、ZKAB001、LP-002、CX-072、IMC-001、KL-A167、APL-502、コシベリマブ、ロダポリマブ、FAZ053、TG-1501、BGB-A333、BCD-135、AK-106、LDP、GR1405、HLX20、MSB2311、RC98、PDL-GEX、KD036、KY1003、YBL-007およびHS-636が挙げられる。本発明の方法において有用な抗PD-L1抗体およびそれらを作製する方法の例は、国際公開第2010/077634号および米国特許第8217149号に記載されており、これらの各々は、参照によりその全体が本明細書に援用される。好ましい一実施形態では、PD-L1結合アンタゴニストは、抗PD-L1抗体を含む。より好ましい実施形態では、抗PD-L1抗体は、アテゾリズマブである。
いくつかの例では、抗PD-L1抗体は、
(a)それぞれ、GFTFSDSWIH(配列番号3)、AWISPYGGSTYYADSVKG(配列番号4)およびRHWPGGFDY(配列番号5)のHVR-H1、HVR-H2およびHVR-H3配列、ならびに
(b)それぞれ、RASQDVSTAVA(配列番号6)、SASFLYS(配列番号7)およびQQYLYHPAT(配列番号8)のHVR-L1、HVR-L2およびHVR-L3配列を含む。
(a)それぞれ、GFTFSDSWIH(配列番号3)、AWISPYGGSTYYADSVKG(配列番号4)およびRHWPGGFDY(配列番号5)のHVR-H1、HVR-H2およびHVR-H3配列、ならびに
(b)それぞれ、RASQDVSTAVA(配列番号6)、SASFLYS(配列番号7)およびQQYLYHPAT(配列番号8)のHVR-L1、HVR-L2およびHVR-L3配列を含む。
一実施形態では、抗PD-L1抗体は、
(a)以下のアミノ酸配列を含む、重鎖可変領域(VH):
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSS(配列番号9)、および
(b)以下のアミノ酸配列を含む、軽鎖可変領域(VL):
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKR(配列番号10)を含む。
(a)以下のアミノ酸配列を含む、重鎖可変領域(VH):
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSS(配列番号9)、および
(b)以下のアミノ酸配列を含む、軽鎖可変領域(VL):
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKR(配列番号10)を含む。
いくつかの例では、抗PD-L1抗体は、(a)配列番号9の配列に対して少なくとも95%の配列同一性(例えば、少なくとも95%、96%、97%、98%、もしくは99%の配列同一性)を有するアミノ酸配列、もしくは配列番号9の配列を含むVHドメイン;(b)配列番号10の配列に対して少なくとも95%の配列同一性(例えば、少なくとも95%、96%、97%、98%、もしくは99%の配列同一性)を有するアミノ酸配列、もしくは配列番号10の配列を含むVLドメイン;または(a)のVHおよび(b)のVLを含む。
一実施形態では、抗PD-L1抗体は、以下を含むアテゾリズマブを含む:
(a)重鎖アミノ酸配列:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG(配列番号1)、および
(b)軽鎖アミノ酸配列:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号2)。
(a)重鎖アミノ酸配列:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSDSWIHWVRQAPGKGLEWVAWISPYGGSTYYADSVKGRFTISADTSKNTAYLQMNSLRAEDTAVYYCARRHWPGGFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG(配列番号1)、および
(b)軽鎖アミノ酸配列:
DIQMTQSPSSLSASVGDRVTITCRASQDVSTAVAWYQQKPGKAPKLLIYSASFLYSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYLYHPATFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号2)。
いくつかの例では、抗PD-L1抗体はアベルマブ(CAS登録番号:1537032-82-8)である。MSB0010718Cとしても知られるアベルマブは、ヒトモノクローナルIgG1抗PD-L1抗体(Merck KGaA、Pfizer)である。
いくつかの例では、抗PD-L1抗体は、デュルバルマブ(CAS登録番号:1428935-60-7)である。MEDI4736としても知られるデュルバルマブは、国際公開第2011/066389号および米国特許出願公開第2013/034559号に記載されている、Fc最適化ヒトモノクローナルIgG1カッパ抗PD-L1抗体(MedImmune、AstraZeneca)である。
いくつかの例では、抗PD-L1抗体はMDX-1105(Bristol Myers Squibb)である。BMS-936559としても知られているMDX-1105は、国際公開第2007/005874号に記載されている抗PD-L1抗体である。
いくつかの例では、抗PD-L1抗体はLY3300054(Eli Lilly)である。いくつかの例では、抗PD-L1抗体はSTI-A1014(Sorrento)である。STI-A1014はヒト抗PD-L1抗体である。いくつかの例では、抗PD-L1抗体はKN035(Suzhou Alphamab)である。KN035は、ラクダファージディスプレイライブラリーから生成されたシングルドメイン抗体(dAB)である。
いくつかの例では、抗PD-L1抗体は、(例えば、腫瘍微小環境中のプロテアーゼによって)切断されると、抗体抗原結合ドメインを活性化して、例えば、非結合性立体部位を除去することによって、その抗原を結合させることができるようにする、切断可能な部位またはリンカーから構成される。いくつかの例では、抗PD-L1抗体はCX-072(CytomX Therapeutics)である。
いくつかの例では、抗PD-L1抗体は、6つのHVR配列(例えば、3つの重鎖HVRおよび3つの軽鎖HVR)、および/または米国特許出願公開第20160108123号、国際公開第2016/000619号、国際公開第2012/145493号、米国特許第9,205,148号、国際公開第2013/181634号、または国際公開第2016/061142号に記載される抗PD-L1抗体からの重鎖可変ドメインおよび軽鎖可変ドメインを含む。
なお更なる特定の態様では、抗PD-L1抗体は、低下したまたは最小のエフェクター機能を有する。なお更に具体的な一態様では、最小のエフェクター機能は、「エフェクターなしのFc突然変異」またはグリコシル化突然変異から生じる。なお更なる事例では、エフェクターなしのFc突然変異は、定常領域内のN297AまたはD265A/N297A置換である。なお更なる例では、エフェクターレスFc変異は、定常領域内のN297A置換である。いくつかの例では、単離された抗PD-L1抗体は、非グリコシル化されている。抗体のグリコシル化は、典型的には、N結合型またはO結合型のいずれかである。N結合型とは、炭水化物部分のアスパラギン残基の側鎖への結合を指す。トリペプチド配列であるアスパラギン-X-セリンおよびアスパラギン-X-スレオニン(ここで、Xは、プロリン以外の任意のアミノ酸である)は、アスパラギン側鎖への炭水化物部分の酵素的結合のための認識配列である。よって、ポリペプチドにおけるこれらトリペプチド配列のいずれかの存在が、潜在的なグリコシル化部位を作る。O結合型グリコシル化とは、糖類、N-アセチルガラクトサミン、ガラクトース、またはキシロースのうちの1つのヒドロキシアミノ酸、最も一般的にはセリンまたはトレオニンへの結合を指すが、5-ヒドロキシプロリンまたは5-ヒドロキシリジンも使用され得る。抗体からのグリコシル化部位の除去は、(N結合型グリコシル化部位について)上述のトリペプチド配列のうちの1種が除去されるようにアミノ酸配列を改変することによって好都合に達成される。この改変は、グリコシル化部位内のアスパラギン、セリンまたはトレオニン残基の別のアミノ酸残基(例えば、グリシン、アラニンまたは保存的置換)との置換によって行われ得る。
一態様では、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法が本明細書に提供される。一実施形態では、本明細書に記載の併用療法は、本明細書に記載の特定の種類の肺がん、頭頸部がん、および/または黒色腫の処置に有用である。一実施形態では、肺がんはNSCLCである。一実施形態では、頭頸部がんは、HNSCCである。一実施形態では、黒色腫は、BRAFT WT黒色腫である。一実施形態では、化合物1は、遊離塩基である。別の実施形態では、化合物1は、化合物1の薬学的に許容され得る塩である。
一態様では、最初の21日サイクルの1~21日目にQD投与される化合物1またはその薬学的に許容され得る塩と、抗PD-L1抗体とを含む併用療法(例えば、組成物)が本明細書に提供される。
一態様では、最初の21日サイクルの1~21日目にQD投与される化合物1またはその薬学的に許容され得る塩と、第1の21日サイクルの1日目にQ3W投与されるアテゾリズマブとを含む併用療法が本明細書に提供される。
一態様では、最初の21日サイクルの1~21日目にQD投与される化合物1またはその薬学的に許容され得る塩と、第1の21日サイクルの1日目にQ2W投与されるアテゾリズマブとを含む併用療法が本明細書に提供される。そのような一実施形態では、アテゾリズマブは、840mgの量でQ2W投与される。そのような一実施形態では、アテゾリズマブは添付文書に従ってQ2W投与される。
本明細書に記載の併用療法の一実施形態では、化合物1またはその薬学的に許容され得る塩は、固定用量のQD投与として投与される。一実施形態では、投与は経口(PO)であり、化合物1またはその薬学的に許容され得る塩は、錠剤またはカプセル剤として製剤化される。そのような一実施形態では、化合物1またはその薬学的に許容され得る塩は、フィルムコーティング錠として製剤化(および投与)される。別のそのような実施形態では、化合物1は、カプセル剤として投与される。
本明細書に記載の併用療法の一実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg~250mg、5mg~200mg、5mg~150mg、5mg~125mg、5mg~120mg、5mg~110mg、5mg~100mg、5mg~80mg、5mg~75mg、5mg~60mg、5mg~50mg、5mg~40mg、5mg~20mg、5mg~10mg、20mg~250mg、20mg~200mg、20mg~150mg、20mg~100mg、20mg~80mg、20mg~75mg、20mg~60mg、20mg~40mg、40mg~250mg、40mg~200mg、40mg~150mg、40mg~100mg、40mg~80mg、40mg~60mg、60mg~250mg、60mg~200mg、60mg~150mg、60mg~100mg、または60mg~80mg QDの量で投与される。
本明細書に記載の併用療法の一実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg~250mg、5mg~200mg、5mg~150mg、5mg~125mg、5mg~120mg、5mg~110mg、5mg~100mg、5mg~80mg、5mg~75mg、5mg~60mg、5mg~50mg、5mg~40mg、5mg~20mg、5mg~10mg、20mg~250mg、20mg~200mg、20mg~150mg、20mg~100mg、20mg~80mg、20mg~75mg、20mg~60mg、20mg~40mg、40mg~250mg、40mg~200mg、40mg~150mg、40mg~100mg、40mg~80mg、40mg~60mg、60mg~250mg、60mg~200mg、60mg~150mg、60mg~100mg、または60mg~80mg BIDの量で投与される。
別の実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg、10mg、20mg、40mg、50mg、60mg、80mg、100mg、120mgまたは150mg QDの量で投与される。別の実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg、10mg、20mg、40mg、50mg、60mg、80mg、100mg、120mgまたは150mg BIDの量で投与される。別の実施形態では、化合物1またはその薬学的に許容され得る塩は、約20mg、40mg、50mg、60mgまたは80mg QDの量で投与される。別の実施形態では、化合物1またはその薬学的に許容され得る塩は、約20mg、40mg、50mg、60mgまたは80mg BIDの量で投与される。
本明細書に記載の併用療法の一実施形態では、PD-L1結合アンタゴニストは添付文書に従って投与される。好ましい実施形態では、PD-L1結合アンタゴニストはアテゾリズマブである。
一般的な提案として、ヒトに投与されるPD-L1結合アンタゴニスト(例えば、アテゾリズマブ)の治療有効量は、1回以上の投与によるかどうかにかかわらず、患者の体重の約0.01mg/kg~約50mg/kgの範囲となる。
いくつかの例示的実施形態では、PD-L1結合アンタゴニストは、約0.01mg/kg~約45mg/kg、約0.01mg/kg~約40mg/kg、約0.01mg/kg~約35mg/kg、約0.01mg/kg~約30mg/kg、約0.01mg/kg~約25mg/kg、約0.01mg/kg~約20mg/kg、約0.01mg/kg~約15mg/kg、約0.01mg/kg~約10mg/kg、約0.01mg/kg~約5mg/kg、または約0.01mg/kg~約1mg/kgの用量で投与され、例えば、毎日、毎週、2週間ごと、3週間ごと、または4週間ごとに投与される。
一例では、PD-L1結合アンタゴニストは、約100mg、約200mg、約300mg、約400mg、約500mg、約600mg、約700mg、約800mg、約900mg、約1000mg、約1100mg、約1200mg、約1300mg、約1400mg、または約1500mgの用量でヒトに投与される。いくつかの例では、PD-L1結合アンタゴニストは、3週間ごとに約1000mg~約1400mg(例えば、3週間ごとに約1100mg~約1300mg、例えば、3週間ごとに約1150mg~約1250mg)の用量で投与され得る。
好ましい一実施形態では、本明細書に記載の併用療法は、本明細書に記載の化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、アテゾリズマブは、2週間ごとに約840mg、3週間ごとに約1200mg、または4週間ごとに約1680mgの用量で患者に静脈内投与される。好ましい一実施形態では、本明細書に記載の併用療法は、本明細書に記載の化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、アテゾリズマブは患者に静脈内で約1200mgの用量でQ3W投与される。
一実施形態では、本明細書に記載の併用療法は、肺がんを処置するために使用される。特定の一実施形態では、併用療法は、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブを含み、併用療法は、肺がんを処置するためのものである。そのような一実施形態では、肺がんは非小細胞肺癌腫(NSCLC)である。そのような一実施形態では、NSCLCは局所進行性または転移性NSCLCである。別のそのような実施形態では、NSCLCは、EGFRまたはALKの変化を有さない。
一実施形態では、本明細書に記載される併用療法は、頭頸部がんを処置するために使用される。そのような一実施形態では、頭頸部がんは、頭頸部扁平上皮癌(HNSCC)である。特定の一実施形態では、併用療法は、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブを含み、併用療法は、HNSCCを処置するためのものである。そのような一実施形態では、HNSCCは、中咽頭、口腔、喉頭、または下咽頭を含む再発性または転移性のHNSCCである。
一実施形態では、本明細書に記載の併用療法は、黒色腫を処置するために使用される。特定の一実施形態では、併用療法は、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブを含み、併用療法は、黒色腫を処置するためのものである。そのような一実施形態では、黒色腫は、局所的に進行した黒色腫または転移性(例えば、再発性またはデノボ(de novo)ステージIV)黒色腫である。別のそのような実施形態では、黒色腫は、切除不能な局所進行型(例えば、ステージIII)皮膚黒色腫である。そのような実施形態では、黒色腫は、BRAF WT黒色腫である。
更に別の態様では、本明細書に記載の肺がんの処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが、第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細書に提供される。一実施形態では、肺がんはNSCLCである。
更に別の態様では、本明細書に記載の頭頸部がんの処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが、第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細書に提供される。一実施形態では、頭頸部がんは、HNSCCである。
更に別の態様では、本明細書に記載の黒色腫の処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが、第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細書に提供される。一実施形態では、黒色腫は、BRAFT WT黒色腫である。
更に別の態様では、本明細書に記載の肺がんの処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが、第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細書に提供される。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。
更に別の態様では、本明細書に記載の頭頸部がんの処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが、第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細書に提供される。一実施形態では、頭頸部がんは、HNSCCである。
更に別の態様では、本明細書に記載の黒色腫の処置に有用な併用療法であって、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含み、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが、第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細書に提供される。一実施形態では、黒色腫は、BRAFT WT黒色腫である。
更に別の態様では、肺がんの処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細に提供される。一実施形態では、肺がんはNSCLCである。
更に別の態様では、頭頸部がんの処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細に提供される。一実施形態では、頭頸部がんは、HNSCCである。
更に別の態様では、黒色腫の処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが第1の21日サイクルの1日目にQ3W投与される、併用療法が本明細に提供される。一実施形態では、黒色腫は、BRAFT WT黒色腫である。
更に別の態様では、肺がんの処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細に提供される。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。
更に別の態様では、頭頸部がんの処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細に提供される。一実施形態では、頭頸部がんは、HNSCCである。
更に別の態様では、黒色腫の処置における使用のための化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法であって、化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、アテゾリズマブが第1の21日サイクルの1日目に約1200mgの量でQ3W投与される、併用療法が本明細に提供される。一実施形態では、黒色腫は、BRAFT WT黒色腫である。
処置方法
肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)または黒色腫(例えば、BRAFT WT黒色腫)の処置を必要とする患者においてそれらを処置する方法も本明細書に提供される。一実施形態では、本方法は、化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニストとを含む、有効量の併用療法を投与することを含む。別の実施形態では、本方法は、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む、有効量の併用療法を投与することを含む。
肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)または黒色腫(例えば、BRAFT WT黒色腫)の処置を必要とする患者においてそれらを処置する方法も本明細書に提供される。一実施形態では、本方法は、化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニストとを含む、有効量の併用療法を投与することを含む。別の実施形態では、本方法は、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む、有効量の併用療法を投与することを含む。
一態様では、肺がんの処置を必要とする患者における肺がんを処置する方法であって、化合物1またはその薬学的に許容され得る塩とPD-L1結合アンタゴニストとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。別の態様では、肺がんの処置を必要とする患者における肺がんを処置する方法であって、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。一実施形態では、肺がんはNSCLCである。
一態様では、頭頸部がんの処置を必要とする患者における頭頸部がんを処置する方法であって、化合物1またはその薬学的に許容され得る塩とPD-L1結合アンタゴニストとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。別の態様では、頭頸部がんの処置を必要とする患者における頭頸部がんを処置する方法であって、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。一実施形態では、頭頸部がんは、HNSCCである。
一態様では、黒色腫の処置を必要とする患者における黒色腫を処置する方法であって、化合物1またはその薬学的に許容され得る塩とPD-L1結合アンタゴニストとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。別の態様では、黒色腫の処置を必要とする患者における黒色腫を処置する方法であって、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む、有効量の併用療法を投与することを含む方法が本明細書に提供される。一実施形態では、黒色腫は、BRAFT WT黒色腫である。
本明細書に記載の方法の一実施形態では、化合物1またはその薬学的に許容され得る塩は、固定用量のQD投与として投与される。本明細書に記載の方法の別の実施形態では、化合物1またはその薬学的に許容され得る塩は、固定用量のBID投与として投与される。一実施形態では、投与は経口(PO)であり、化合物1またはその薬学的に許容され得る塩は、錠剤またはカプセル剤として製剤化される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg~250mg、5mg~200mg、5mg~150mg、5mg~125mg、5mg~120mg、5mg~110mg、5mg~100mg、5mg~80mg、5mg~75mg、5mg~60mg、5mg~50mg、5mg~40mg、5mg~20mg、5mg~10mg、20mg~250mg、20mg~200mg、20mg~150mg、20mg~100mg、20mg~80mg、20mg~75mg、20mg~60mg、20mg~40mg、40mg~250mg、40mg~200mg、40mg~150mg、40mg~100mg、40mg~80mg、40mg~60mg、60mg~250mg、60mg~200mg、60mg~150mg、60mg~100mg、または60mg~80mg QDの量で投与される。
別の実施形態では、化合物1またはその薬学的に許容され得る塩は、錠剤として製剤化され、約5mg~100mg QDの量で投与される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約10mgの量でQD投与される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約20mgの量でQD投与される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約40mgの量でQD投与される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約60mgの量でQD投与される。一実施形態では、化合物1またはその薬学的に許容され得る塩は、約80mgの量でQD投与される。
本明細書に記載の方法の一実施形態では、化合物1またはその薬学的に許容され得る塩は、約5mg~250mg、5mg~200mg、5mg~150mg、5mg~125mg、5mg~120mg、5mg~110mg、5mg~100mg、5mg~80mg、5mg~75mg、5mg~60mg、5mg~50mg、5mg~40mg、5mg~20mg、5mg~10mg、20mg~250mg、20mg~200mg、20mg~150mg、20mg~100mg、20mg~80mg、20mg~75mg、20mg~60mg、20mg~40mg、40mg~250mg、40mg~200mg、40mg~150mg、40mg~100mg、40mg~80mg、40mg~60mg、60mg~250mg、60mg~200mg、60mg~150mg、60mg~100mg、または60mg~80mg BIDの量で投与される。
本明細書に記載の方法の一実施形態では、アテゾリズマブは、約0.01mg/kg~約45mg/kg、約0.01mg/kg~約40mg/kg、約0.01mg/kg~約35mg/kg、約0.01mg/kg~約30mg/kg、約0.01mg/kg~約25mg/kg、約0.01mg/kg~約20mg/kg、約0.01mg/kg~約15mg/kg、約0.01mg/kg~約10mg/kg、約0.01mg/kg~約5mg/kg、または約0.01mg/kg~約1mg/kgの用量で投与され、例えば、毎日、毎週、2週間ごと、3週間ごと、または4週間ごとに投与される。
一例では、アテゾリズマブは、約100mg、約200mg、約300mg、約400mg、約500mg、約600mg、約700mg、約800mg、約900mg、約1000mg、約1100mg、約1200mg、約1300mg、約1400mg、または約1500mgの用量でヒトに投与される。いくつかの例では、アテゾリズマブは、3週間ごとに約1000mg~約1400mg(例えば、3週間ごとに約1100mg~約1300mg、例えば、3週間ごとに約1150mg~約1250mg)の用量で投与され得る。
本明細書に記載の方法の好ましい一実施形態では、化合物1またはその薬学的に許容され得る塩は本明細書に記載されるように投与され、アテゾリズマブは患者に静脈内に約1200mgの用量でQ3W投与される。
一実施形態では、本明細書に記載の方法は、慣らし期間を更に含む。慣らし期間は、約1~14日の長さであり得る。そのような一実施形態では、慣らし期間は14日間を含む。別のそのような実施形態では、慣らし期間は14日間であり、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブが慣らし期間の1日目に投与される。そのような一実施形態では、化合物1またはその薬学的に許容され得る塩は、慣らし期間の8日目に単独で投与され、その後QD投与される。
本明細書で提供される方法は、投薬レジメンの一部として、本明細書に記載の併用療法の投与を含み得る。そのような一実施形態では、投薬レジメンは、1回以上のサイクルを含む。別の実施形態では、投薬レジメンは、少なくとも2サイクルを含む。別の態様では、本明細書で提供される投薬レジメンは、2、3、4、5、6、8、10、12、16、18、20、24、30、36、42、48、54、60、66または72回のサイクルを含む。更に別の実施形態では、投薬レジメンは、約2~72、2~66、2~60、2~54、2~48、2~42、2~36、2~30、2~24、2~18、2~12または2~6回のサイクルを含む。一実施形態では、投薬レジメンは、所望の応答(例えば、PFS、OS、ORR、および/またはDOR)が所望の転帰に達するまでの(例えば、本明細書に記載の対照と比較して、PFS、OS、ORR、および/またはDORが増加)、本明細書に記載の併用療法の任意の回数のサイクルでの投与を含む。別の実施形態では、投薬レジメンは、毒性が発現するか、またはその他患者が更なる投与を妨げる1つまたは複数の有害事象(AE)を経験するまで、任意の回数のサイクルでの本明細書に記載の併用療法の投与を含む。更に別の実施形態では、投薬レジメンは、疾患進行までの任意のサイクル数での本明細書に記載の併用療法の投与を含む。
本明細書に記載の方法の一実施形態では、患者には、合計で1~50用量、例えば、1~50用量、1~45用量、1~40用量、1~35用量、1~30用量、1~25用量、1~20用量、1~15用量、1~10用量、1~5用量、2~50用量、2~45用量、2~40用量、2~35用量、2~30用量、2~25用量、2~20用量、2~15用量、2~10用量、2~5用量、3~50用量、3~45用量、3~40用量、3~35用量、3~30用量、3~25用量、3~20用量、3~15用量、3~10用量、3~5用量、4~50用量、4~45用量、4~40用量、4~35用量、4~30用量、4~25用量、4~20用量、4~15用量、4~10用量、4~5用量、5~50用量、5~45用量、5~40用量、5~35用量、5~30用量、5~25用量、5~20用量、5~15用量、5~10用量、10~50用量、10~45用量、10~40用量、10~35用量、10~30用量、10~25用量、10~20用量、10~15用量、15~50用量、15~45用量、15~40用量、15~35用量、15~30用量、15~25用量、15~20用量、20~50用量、20~45用量、20~40用量、20~35用量、20~30用量、20~25用量、25~50用量、25~45用量、25~40用量、25~35用量、25~30用量、30~50用量、30~45用量、30~40用量、30~35用量、35~50用量、35~45用量、35~40用量、40~50用量、40~45用量、または45~50用量のアテゾリズマブが投与される。好ましい一実施形態では、用量は静脈内投与される。
特定の実施形態では、本明細書に記載の併用療法の治療剤(例えば、化合物1またはその薬学的に許容され得る塩、およびアテゾリズマブ)は、当技術分野で公知の任意の適切な方法で投与され得る。例えば、アテゾリズマブは、化合物1またはその薬学的に許容され得る塩として連続的に(異なる日に)、または同時に(同日または同じ処置サイクル中に)投与され得る。一実施形態では、アテゾリズマブは、化合物1またはその薬学的に許容され得る塩の投与後に投与される。いくつかの例では、アテゾリズマブは、化合物1の投与後に投与され、またはその薬学的に許容され得る塩は同日に投与され得る。一実施形態では、アテゾリズマブは、化合物1またはその薬学的に許容され得る塩を投与した後、同日に投与され得る。例えば、化合物1またはその薬学的に許容され得る塩は、各サイクルの1日目にアテゾリズマブを投与する前に各サイクルの1日目に投与することができ、次いで、化合物1またはその薬学的に許容され得る塩は、21日サイクルの次の20日間QD投与される。
好ましい実施形態では、アテゾリズマブは静脈内投与される。一例では、アテゾリズマブは60分かけて静脈内投与され得、初回注入が許容され得る場合、その後の注入は全て30分かけて送達され得る。いくつかの例では、PD-1軸結合アンタゴニストは、静脈内プッシュまたはボーラスとして投与されない。
また、肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)または黒色腫(例えば、BRAFT WT黒色腫)の処置を必要とする患者において肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)または黒色腫(例えば、BRAFT WT黒色腫)を処置するための方法であって、有効量の化合物1またはその薬学的に許容され得る塩およびPD-L1結合アンタゴニスト(例えば、アテゾリズマブ)を含む処置レジメンを患者に投与することを含む方法が本明細書に提供される。そのような方法の別の実施形態では、化合物1またはその薬学的に許容され得る塩は、本明細書に記載のQDで、および本明細書に記載の量(例えば、5mg~100mg)で投与される。そのような方法の別の実施形態では、アテゾリズマブは、本明細書に記載のQ3Wで、および本明細書に記載の量(例えば1200mg)で投与される。別のそのような実施形態では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、処置レジメンの開始前に、本明細書に記載の慣らし期間の構成要素として投与される。そのような方法では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、本明細書に記載されるように投与され得る。
さらに、肺がんの処置を必要とする患者において肺がんを処置するための方法であって、有効量の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニスト(例えば、アテゾリズマブ)とを含む処置レジメンを患者に投与することを含む方法が、本明細書に提供される。そのような方法の別の実施形態では、化合物1またはその薬学的に許容され得る塩は、本明細書に記載のQDで、および本明細書に記載の量(例えば、5mg~100mg)で投与される。そのような方法の別の実施形態では、アテゾリズマブは、本明細書に記載のQ3Wで、および本明細書に記載の量(例えば1200mg)で投与される。別のそのような実施形態では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、処置レジメンの開始前に、本明細書に記載の慣らし期間の構成要素として投与される。そのような方法では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、本明細書に記載されるように投与され得る。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。
なお更に、本明細書に記載の頭頸部がんの処置を必要とする患者において頭頸部がんを処置する方法であって、有効量の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニスト(例えば、アテゾリズマブ)とを含む処置レジメンを患者に投与することを含む方法が、本明細書において提供される。そのような方法の別の実施形態では、化合物1またはその薬学的に許容され得る塩は、本明細書に記載のQDで、および本明細書に記載の量(例えば、5mg~100mg)で投与される。そのような方法の別の実施形態では、アテゾリズマブは、本明細書に記載のQ3Wで、および本明細書に記載の量(例えば1200mg)で投与される。別のそのような実施形態では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、処置レジメンの開始前に、本明細書に記載の慣らし期間の構成要素として投与される。そのような方法では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、本明細書に記載されるように投与され得る。一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。
また、本明細書に記載の黒色腫の処置を必要とする患者において黒色腫を処置するための方法であって、有効量の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニスト(例えば、アテゾリズマブ)とを含む処置レジメンを患者に投与することを含む方法が、本明細書に提供される。そのような方法の別の実施形態では、化合物1またはその薬学的に許容され得る塩は、本明細書に記載のQDで、および本明細書に記載の量(例えば、5mg~100mg)で投与される。そのような方法の別の実施形態では、アテゾリズマブは、本明細書に記載のQ3Wで、および本明細書に記載の量(例えば1200mg)で投与される。別のそのような実施形態では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、処置レジメンの開始前に、本明細書に記載の慣らし期間の構成要素として投与される。そのような方法では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブは、本明細書に記載されるように投与され得る。一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
いくつかの例では、本明細書に記載の処置レジメンは、1つ以上の追加の療法の投与を含み、追加の療法は、1つ以上の副作用制限剤(例えば、処置の副作用の発生および/または重症度を軽減することを意図した薬剤、例えば、抗悪心剤、胃酸抑制剤、コルチコステロイド(例えば、プレドニゾンまたは同等物、例えば1~2mg/kg/日の用量)、ホルモン補充薬(複数可)等)である。
本明細書に記載の方法のいくつかの実施形態では、患者は、PD-L1陽性またはPD-L1状態について評価される。一実施形態では、PD-L1陽性またはPD-L1状態は、IHCに基づく試験によって評価される。一実施形態では、患者は、PD-L1陽性である。一実施形態では、患者は、PD-L1 high状態で評価されたNSCLCを有する。別の実施形態では、患者は、PD-L1 low状態で評価されたNSCLCを有する。そのような一実施形態では、患者は、EGFRおよびALK野生型状態のNSCLCを有する。
PD-L1の発現は、本明細書に記載されている使用のための方法および組成物のいずれかに従って処置された患者において評価され得る。使用のための方法および組成物は、患者から得られた生物学的試料(例えば、腫瘍試料)中のPD-L1の発現レベルを決定することを含み得る。他の例では、患者から得られた生物学的試料(例えば、腫瘍試料)中のPD-L1の発現レベルは、処置開始前または処置開始後に決定されている。PD-L1発現は、任意の適切なアプローチを使用して決定され得る。例えば、PD-L1発現は、米国特許出願公開第2018/0030138号および第2018/0037655号に記載されているように決定され得る。任意の適切な腫瘍試料、例えばホルマリン固定パラフィン包埋(FFPE)腫瘍試料、保管腫瘍試料、新鮮腫瘍試料または凍結腫瘍試料が使用され得る。
例えば、PD-L1の発現は、検出可能なPD-L1発現レベルを発現する腫瘍浸潤免疫細胞に含まれる腫瘍試料の割合に関して、検出可能なPD-L1発現レベルを発現する腫瘍試料中の腫瘍浸潤免疫細胞の割合として、および/または検出可能なPD-L1発現レベルを発現する腫瘍試料中の腫瘍細胞の割合として決定され得る。前述の例のいずれにおいても、腫瘍浸潤免疫細胞によって構成される腫瘍試料のパーセンテージは、患者から得られた腫瘍試料の切片において、腫瘍浸潤免疫細胞によって覆われる腫瘍領域のパーセンテージ(例えば、抗PD-L1抗体(例えば、SP142抗体)を使用してIHCによって評定されるように)に関してであり得ることが理解されるべきである。例えば、SP142(Ventana)、SP263(Ventana)、22C3(Dako)、28-8(Dako)、E1L3N(Cell Signaling Technology)、4059(ProSci,Inc.)、h5H1(Advanced Cell Diagnostics)および9A11を含む任意の適切な抗PD-L1抗体を使用してもよい。いくつかの例では、抗PD-L1抗体はSP142である。他の例では、抗PD-L1抗体はSP263である。
いくつかの例では、患者から得られる腫瘍試料は、腫瘍試料中の1%未満の腫瘍細胞、腫瘍試料中の1%以上の腫瘍細胞、腫瘍試料中の1%~5%未満の腫瘍細胞、腫瘍試料中の5%以上の腫瘍細胞、腫瘍試料中の5%~50%未満の腫瘍細胞または腫瘍試料中の50%以上の腫瘍細胞において、検出可能なPD-L1発現レベルを有する。
いくつかの例では、患者から得られた腫瘍試料は、腫瘍試料の1%未満、腫瘍試料の1%超、腫瘍試料の1%~5%未満、腫瘍試料の5%超、腫瘍試料の5%~10%未満、または腫瘍試料の10%超を構成する腫瘍浸潤免疫細胞中の検出可能なPD-L1発現レベルを有する。
いくつかの例では、腫瘍試料は、表Aおよび/または表Bにそれぞれ示される診断評定のための基準に従って、腫瘍浸潤免疫細胞および/または腫瘍細胞におけるPD-L1陽性についてスコア化され得る。
本明細書に記載の併用療法を投与することによって、本明細書に記載の患者において腫瘍増殖を阻害する方法または腫瘍退縮を生じる方法もまた、本明細書に提供される。一実施形態では、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブを、本明細書に記載される1回以上の21日サイクルで投与することを含む併用療法を投与することによって、腫瘍成長の阻害を必要とする患者において腫瘍成長を阻害する方法が本明細書に提供される。
一実施形態では、本明細書に記載の1回以上の21日サイクルで、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを投与することを含む併用療法を投与することによって、本明細書に記載の肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)、または黒色腫(例えば、BRAFT WT黒色腫)を有する患者における腫瘍退縮を生じさせるかまたは改善する方法が本明細書に提供される。
さらに、本明細書に記載の肺がん(例えば、NSCLC)、頭頸部がん(例えば、HNSCC)または黒色腫(例えば、BRAFT WT黒色腫)の処置のための、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブを含む本明細書に記載の併用療法(組成物)の使用が本明細書に提供される。
一実施形態では、本明細書に記載の肺がんの処置のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)の使用(U1)が本明細書に提供される。そのような一実施形態では、肺がんはNSCLCである。いくつかの実施形態では、NSCLCは、本明細書に記載の局所進行性NSCLCまたは転移性NSCLCである。
一実施形態では、本明細書に記載の頭頸部がんの処置のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)の使用(U2)が本明細書に提供される。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。
一実施形態では、本明細書に記載の黒色腫の処置のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)の使用(U3)が本明細書に提供される。一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法の使用(U4)であって、(i)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、使用が本明細書に提供される。そのような一実施形態では、使用は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、使用は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、使用は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法の使用(U5)であって、(i)第1の21日サイクルの1~21日目に約5~100mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目に約1200mgのアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、使用が本明細書に提供される。そのような一実施形態では、投薬レジメンは、本明細書に記載のサイクルを2回以上含む。そのような一実施形態では、使用は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、使用は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、使用は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法の使用(U6)が本明細書に提供される。そのような一実施形態では、使用は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、使用は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、使用は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法の使用(U7)であって、(i)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、を含む投薬レジメンを更に含む、使用が本明細書に提供される。そのような一実施形態では、使用は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、使用は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、使用は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法の使用(U7)であって、(i)第1の21日サイクルの1~21日目に約5~100mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目に約1200mgのアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、使用が本明細書に提供される。そのような一実施形態では、投薬レジメンは、本明細書に記載のサイクルを2回以上含む。そのような一実施形態では、使用は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、使用は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、使用は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
一実施形態では、本明細書に記載の肺がんの処置における使用(U1)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)が本明細書に提供される。そのような一実施形態では、肺がんはNSCLCである。いくつかの実施形態では、NSCLCは、本明細書に記載の局所進行性NSCLCまたは転移性NSCLCである。
一実施形態では、本明細書に記載の頭頸部がんの処置における使用(U2)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)が本明細書に提供される。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。
一実施形態では、本明細書に記載の黒色腫の処置における使用(U3)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法(組成物)が本明細書に提供される。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置における使用(U4)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法であって、(i)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、併用療法が本明細書に提供される。そのような一実施形態では、処置は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、処置は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、処置は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置における使用(U5)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法であって、(i)第1の21日サイクルの1~21日目に約5~100mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目に約1200mgのアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、併用療法が本明細書に提供される。そのような一実施形態では、投薬レジメンは、本明細書に記載のサイクルを2回以上含む。そのような一実施形態では、処置は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、処置は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、処置は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造における使用(U6)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法が本明細書に提供される。そのような一実施形態では、処置は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、処置は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、処置は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造における使用(U7)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法であって、(i)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、を含む投薬レジメンを含む、併用療法が本明細書に提供される。そのような一実施形態では、処置は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、処置は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、処置は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
さらに、本明細書に記載の肺がん、頭頸部がん、または黒色腫の処置のための医薬品の製造における使用(U7)のための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む本明細書に記載の併用療法であって、(i)第1の21日サイクルの1~21日目に約5~100mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(ii)第1の21日サイクルの1日目に約1200mgのアテゾリズマブをQ3W投与することと、を更に含む、投薬レジメンを含む、併用療法が本明細書に提供される。そのような一実施形態では、投薬レジメンは、本明細書に記載のサイクルを2回以上含む。そのような一実施形態では、処置は、肺がんの処置を含む。そのような一実施形態では、肺がんは、本明細書に記載のNSCLCである。別のそのような実施形態では、処置は、頭頸部がんの処置を含む。そのような一実施形態では、頭頸部がんは、本明細書に記載のHNSCCである。別のそのような実施形態では、処置は、本明細書に記載の黒色腫の処置を含む。そのような一実施形態では、黒色腫は、本明細書に記載されるBRAFT WT黒色腫である。
併用処置の開発は、例えば、許容され得る毒性を維持しつつ有効性の改善につながり得る併用療法のための作用物質の選択を含めて、課題を有している。1つの特定の課題は、併用の漸増的な毒性を識別する必要性である。本明細書に記載の方法の一実施形態では、本明細書に記載の併用療法(例えば、化合物1またはその薬学的に許容され得る塩、およびアテゾリズマブ)は、時差投薬スケジュールを含む投薬レジメンで投与される。そのような一実施形態では、患者は、対照(例えば、SOC療法、本明細書に記載の1つの薬剤(例えば、化合物1もしくはその薬学的に許容され得る塩、またはアテゾリズマブ)単独による処置)に匹敵する有害事象(AE:adverse event)の数またはグレードの低下を有する。
有害事象が発生した場合、次の4つの選択肢が存在すると一般的に理解されている:(1)任意の付随療法を用いてそのまま処置を継続;(2)投薬レジメンにおける1つ以上の薬剤の用量を調整;(3)投薬レジメンにおける1つ以上の薬剤の投与を一時中断;または、(4)投薬レジメンにおける1つ以上の薬剤の投与を中止。一実施形態では、化合物1またはその薬学的に許容され得る塩の量は変更されない。別の実施形態では、投与されるアテゾリズマブの量は変更されない。一実施形態では、アテゾリズマブの投与が中断される場合、化合物1またはその薬学的に許容され得る塩の次の投与は、アテゾリズマブの投与が再開されるのと同じ日に行われる。
本明細書に記載の患者は、本明細書に記載のもの等の1つ以上の有害事象(AE)を経験する可能性がある。一実施形態では、本明細書に記載の患者は、末梢浮腫、骨髄抑制(例えば、血小板減少症および/または貧血)、胃腸毒性(例えば、下痢、悪心および/または嘔吐)、発疹、肝臓トランスアミナーゼの上昇、心筋症、眼毒性または光毒性を経験する。別の実施形態では、本明細書に記載の患者は、注入関連反応(IRR)および免疫介在性肝炎、間質性肺炎、大腸炎、膵炎、真性糖尿病、甲状腺機能低下症、甲状腺機能亢進症、副腎機能不全、下垂体炎、ギラン・バレー症候群、筋無力症症候群または重症筋無力症、髄膜脳炎、心筋炎、腎炎および筋炎のうちの1つ以上を経験する。免疫介在性反応は、任意の器官系を伴い得、血球貪食性リンパ組織球症(HLH)およびマクロファージ活性化症候群(MAS)をもたらし得る。そのような一実施形態では、患者は、心臓毒性、肺毒性、腎毒性、血栓塞栓性毒性、または眼毒性のうちの1つ以上を経験しない。
いくつかの実施形態では、本明細書に記載の患者に、以下を含む1つ以上の併用療法を投与することもできる:(a)経口避妊薬;(b)ホルモン補充療法;(c)予防的または治療的な抗凝固療法(例えば、安定な用量のワーファリンまたは低分子量ヘパリン);ワクチン接種(インフルエンザ、COVID-19等)、ただし、生弱毒化ワクチンは許可されていない;(d)食欲刺激剤として投与される酢酸メゲストロール;(e)ミネラルコルチコイド(例えば、フルドロコルチゾン);(f)慢性閉塞性肺疾患または喘息のために投与される吸入または低用量コルチコステロイド;(g)起立性低血圧または副腎皮質機能不全のために投与される低用量コルチコステロイド;(h)緩和的放射線療法(例えば、既知の骨転移の処置または疼痛の症候性軽減);(i)局所療法(例えば、外科手術、定位的放射線手術、放射線療法、高周波アブレーション);(j)抗ヒスタミン薬、解熱薬および/または鎮痛薬による前投薬(例えば、アセトアミノフェン、イブプロフェン、ジフェンヒドラミン)、および/またはH2受容体アンタゴニスト(例えば、ファモチジン、シメチジン)。
本明細書に記載の患者は、特定の実施形態では、(a)強力/中程度のCYP3A4阻害剤(例えば、アタザナビル、リトナビル、インジナビル、ネルフィナビル、サキナビル、クラリスロマイシン、テリスロマイシン、エリスロマイシン、トロレアンドマイシン、フルコナゾール、イトラコナゾール、ケトコナゾール、ボリコナゾール、ポサコナゾール、アプレピタント、コニバプタン、フルボキサミン、ジルチアゼム、ネファゾドン、ミベフラジル、ベラパミル、およびグレープフルーツジュースまたはグレープフルーツサプリメント);(b)強力/中程度のCYP3A4誘導剤(例えば、リファンピン、カルバマゼピン、フェニトイン、オクスカルバゼピン、フェノバルビタール、エファビレンツ、ネビラピン、エトラビリン、モダフィニル、ハイパーフォリン(セントジョーンズワート)およびシプロテロン);(c)化学療法;(d)ホルモン療法;(e)免疫療法;(f)放射線療法;(g)薬草療法);(h)生弱毒化ワクチン;全身免疫賦活剤(例えば、インターフェロンおよびIL-2);(i)プロトンポンプ阻害剤;(j)カンナビジオール生成物;または(k)H2遮断薬および制酸薬を含む併用治療を受けなくてもよい。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、以下のいずれかを有する局所進行性または転移性固形腫瘍(例えば、本明細書に記載のNSCLC、HNSCC、黒色腫)を有する:(a)少なくとも1つの利用可能な標準療法後に進行するか、または(b)承認された標準療法が無効もしくは容認できないことが証明されているか、または不適切であると考えられる。
本明細書に記載の方法の一実施形態では、患者は肺がんを有し、事前の全身療法を受けていない。そのような一実施形態では、肺がんは、本明細書に記載の局所進行性または転移性肺がんである。
本明細書に記載の方法の一実施形態では、患者はNSCLCを有し、事前の全身療法を受けていない。そのような一実施形態では、NSCLCは、本明細書に記載の局所進行性または転移性NSCLCである。
本明細書に記載の方法の別の実施形態では、患者は、本明細書に記載のNSCLCを有し、EGFRおよび/またはALKの変化がない。そのような一実施形態では、患者試料(例えば、腫瘍組織の生検)を、EGFRおよび/またはALKの変化の有無について試験する。別のそのような実施形態では、患者は、PD-L1陽性である。そのような実施形態では、患者は、本明細書に記載されるようIHC分析を行うことによってPD-L1陽性であると判定される。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、組織学的に確認された再発性または転移性頭頸部がんを有する。そのような一実施形態では、頭頸部がんは、中咽頭、口腔、喉頭、または下咽頭を含む。そのような一実施形態では、頭頸部がんは、治癒的療法に適していないと考えられる中咽頭、口腔、喉頭、または下咽頭を含む。本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、本明細書に記載の頭頸部がんを有し、頭頸部がんを処置するための事前の全身療法を受けていない。本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、頭頸部がんを有し、中咽頭癌について局所ヒトパピローマウイルス(HPV)の存在/非存在についての試験を受けたことがある。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、組織学的に確認された再発性または転移性のHNSCCを有する。そのような一実施形態では、HNSCCは、中咽頭、口腔、喉頭、または下咽頭を含む。そのような一実施形態では、HNSCCは、治癒的療法に適していないと考えられる中咽頭、口腔、喉頭、または下咽頭を含む。本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、本明細書に記載されるHNSCCを有し、かつ、HNSCCを処置するための事前の全身療法を受けていない。本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、HNSCCを有し、中咽頭癌について局所ヒトパピローマウイルス(HPV)の存在/非存在についての試験を受けたことがある。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、本明細書に記載の黒色腫を有し、抗PD-1または抗PD-L1療法を含む事前処置に対してまたはその後に疾患が進行している。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、本明細書に記載のBRAFT WT黒色腫を有し、抗PD-1または抗PD-L1療法を含む事前処置に対してまたはその後に疾患が進行している。
一実施形態では、本明細書に記載の患者は、既知で未処置のまたは活動性の中枢神経系(CNS)転移(進行しているか、または対症療法のために抗痙攣薬もしくはコルチコステロイドを必要とする)を有していない。患者は、そのような患者が処置されたCNS転移の病歴を有する場合、本明細書に記載の方法を使用して処置してもよく、そのような患者は以下を有する:(1)CNS外の測定可能または評価可能な疾患;(2)頭蓋内出血または脊髄出血の既往なし;(3)CNS転移の治療としてのコルチコステロイドに対する継続的な必要性がなく、コルチコステロイドは、本明細書に記載の併用療法の投与の2週間前に中止され、CNS転移に起因する進行中の症候はない;(4)本明細書に記載のサイクル1の1日目の前の7日間以内の定位放射線照射または14日間以内の全脳放射線照射なし;および(5)CNS向け治療の完了とスクリーニング放射線学的研究との間の暫定的な進行の証拠はない。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、軟髄膜疾患または癌性髄膜炎を有さない。別の実施形態では、本明細書に記載の患者は、制御されていない高血圧を有していない。別の実施形態では、本明細書に記載の患者は活動性結核感染症を有さない。別の実施形態では、本明細書に記載の患者は、HBVについて積極的に処置されていない。
本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、スクリーニング眼科検査時に、網膜静脈閉塞症(RVO)、中心性漿液性網膜症(CSR)、RVOもしくはCSRの素因、または網膜症を含む眼科疾患を有していない。
本明細書に記載の方法の一実施形態では、本明細書に記載の患者は、本明細書に記載の処置開始前4週間以内に、診断以外の主要な外科的処置を受けていない。
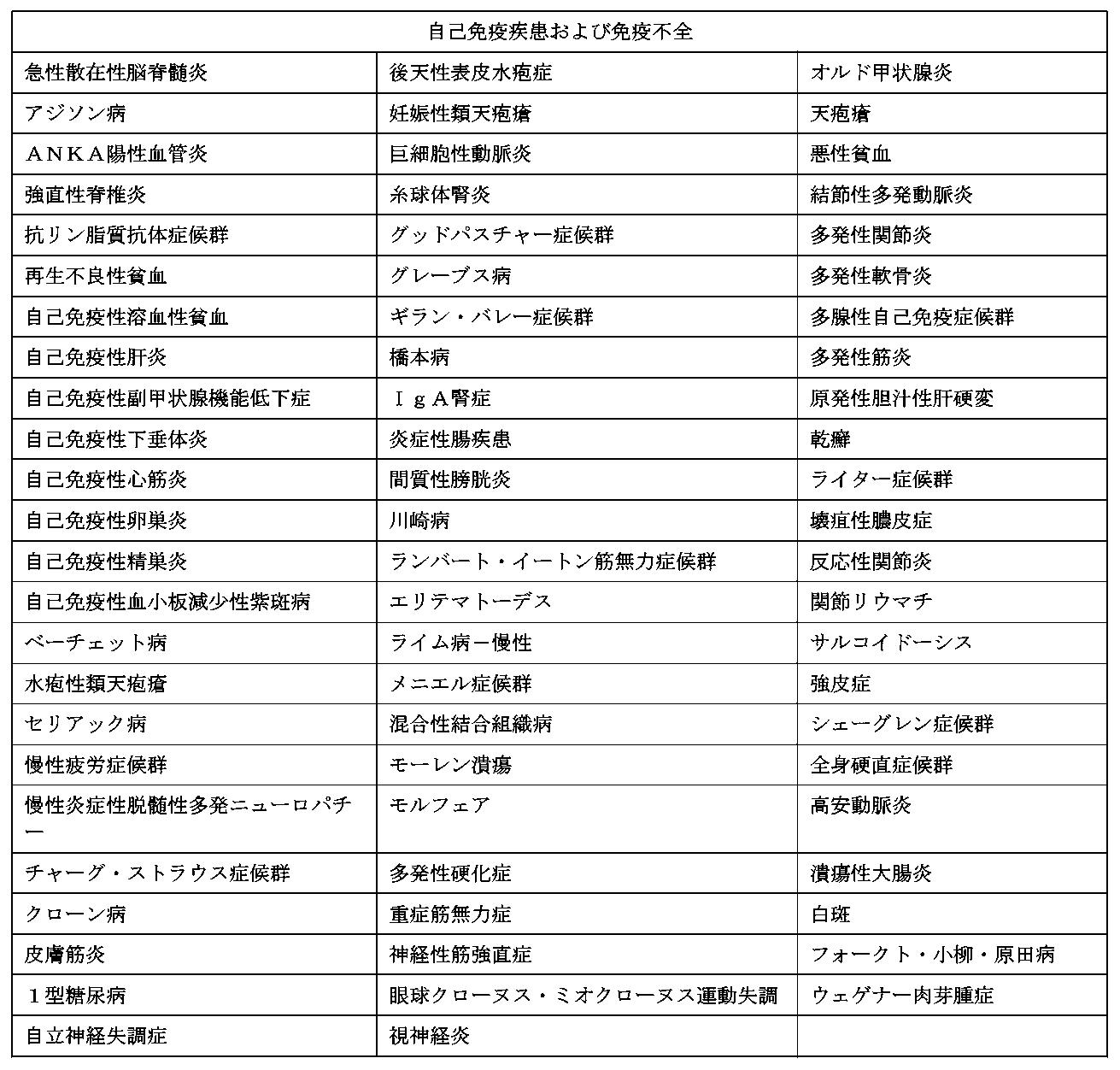
本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、重症筋無力症、筋炎、自己免疫性肝炎、全身性エリテマトーデス、関節リウマチ、炎症性腸疾患、抗リン脂質抗体症候群、ウェゲナー肉芽腫症、シェーグレン症候群、ギラン・バレー症候群、または多発性硬化症を含むがこれらに限定されない、活動性自己免疫疾患もしくは免疫不全、またはそれらの病歴を有していない。いくつかの実施形態では、そのような自己免疫疾患を有する患者は、以下の場合、本明細書に記載される方法に従って処置することができる:
・そのような患者が、自己免疫関連甲状腺機能低下症の病歴を有し、甲状腺補充ホルモンで処置されている;
・そのような患者が、制御された1型糖尿病を有し、インスリンレジメンで処置されている;
・そのような患者は、皮膚症状のみ(例えば、乾癬性関節炎を有する患者は除外される)を伴う湿疹、乾癬、慢性単純性苔癬または白斑を有し、(i)発疹は患者の体表面積の10%未満を覆い、(ii)処置は低効力の局所コルチコステロイドのみを使用し、(iii)過去12ヶ月以内にソラレン+紫外線A照射、メトトレキサート、レチノイド、生物学的薬剤、経口カルシニューリン阻害剤、または高効力もしくは経口のコルチコステロイドを必要とする基礎疾患の急性増悪の発生はなかった。
・そのような患者が、自己免疫関連甲状腺機能低下症の病歴を有し、甲状腺補充ホルモンで処置されている;
・そのような患者が、制御された1型糖尿病を有し、インスリンレジメンで処置されている;
・そのような患者は、皮膚症状のみ(例えば、乾癬性関節炎を有する患者は除外される)を伴う湿疹、乾癬、慢性単純性苔癬または白斑を有し、(i)発疹は患者の体表面積の10%未満を覆い、(ii)処置は低効力の局所コルチコステロイドのみを使用し、(iii)過去12ヶ月以内にソラレン+紫外線A照射、メトトレキサート、レチノイド、生物学的薬剤、経口カルシニューリン阻害剤、または高効力もしくは経口のコルチコステロイドを必要とする基礎疾患の急性増悪の発生はなかった。
本明細書に記載の方法の別の実施形態では、患者は、特発性肺線維症、器質化肺炎(例えば、閉塞性細気管支炎)、薬物誘発性間質性肺炎もしくは特発性間質性肺炎の病歴、または胸部コンピュータ断層撮影スキャンのスクリーニングでの活動性間質性肺炎の証拠を有していない。
別の実施形態では、本明細書に記載の患者は、内分泌感受性がん(例えば、前立腺がん、子宮内膜がん、ホルモン受容体陽性乳がん)に対するゴナドトロピン放出ホルモン(GnRH)アゴニストまたはアンタゴニストを用いたホルモン療法を除いて、本明細書に記載の併用療法の投与前3週間以内に抗がん療法としての化学療法、免疫療法、または生物学的療法による処置を受けておらず、または本明細書に記載の併用療法の投与前2週間以内に内分泌療法を受けていない。
本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、本明細書に記載の処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内にH2遮断薬または制酸薬による事前処置を受けていない。本明細書に記載の方法の別の実施形態では、本明細書に記載の患者は、本明細書に記載の処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内に、軽度または中程度のCYP3A4阻害剤または軽度または中程度のCYP3A4誘導剤による事前処置を受けていない。
キット
本明細書に記載の併用療法は、投与のための本明細書に記載の1つ以上の薬剤を含むキットとして提供され得る。一実施形態では、キットは、本明細書に記載のアテゾリズマブと組み合わせて投与するための化合物1またはその薬学的に許容され得る塩を含む。別の実施形態では、キットは、アテゾリズマブと共に包装された化合物1またはその薬学的に許容され得る塩を含み、該キットは、各薬剤の別々の処方された投与量を含む。
本明細書に記載の併用療法は、投与のための本明細書に記載の1つ以上の薬剤を含むキットとして提供され得る。一実施形態では、キットは、本明細書に記載のアテゾリズマブと組み合わせて投与するための化合物1またはその薬学的に許容され得る塩を含む。別の実施形態では、キットは、アテゾリズマブと共に包装された化合物1またはその薬学的に許容され得る塩を含み、該キットは、各薬剤の別々の処方された投与量を含む。
化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニスト(例えば、アテゾリズマブ)とを含む製造品またはキットも本明細書に提供される。いくつかの例では、製造品は、本明細書に記載されるような肺がん、頭頸部がんまたは黒色腫を処置するためにPD-L1結合アンタゴニストを使用するための説明書を含む添付文書を更に含む。そのような一実施形態では、肺がんはNSCLCである。そのような一実施形態では、頭頸部がんはHNSCCである。そのような一実施形態では、黒色腫は、BRAFT WT黒色腫である。一実施形態では、製造品は、本明細書に記載のNSCLC、HNSCCまたはBRAFT WT黒色腫を本明細書に記載の患者において処置するために、アテゾリズマブを化合物1またはその薬学的に許容され得る塩と組み合わせて使用するための説明書を含む添付文書を更に含む。
いくつかの例では、PD-L1結合アンタゴニスト(例えば、アテゾリズマブ)および化合物1またはその薬学的に許容され得る塩は、同じ容器または別々の容器に入っている。好適な容器としては、例えば、ボトル、バイアル、袋、およびシリンジが挙げられる。容器は、ガラス、プラスチック(ポリ塩化ビニルもしくはポリオレフィン等)、または金属合金(ステンレス鋼もしくはハステロイ等)等の様々な材料から形成され得る。いくつかの例では、容器は、製剤を保持し、容器上のラベルまたは容器に関連するラベルは、使用上の指示を示し得る。製造品またはキットは、他の緩衝液、希釈剤、フィルタ、針、シリンジ、および使用説明書付きの添付文書を含む、商業的観点および使用者の観点から望ましい他の材料を更に含み得る。いくつかの例では、製造品は、1つ以上の別の薬剤(例えば、更なる化学療法剤または抗新生物剤)を更に含む。1つ以上の薬剤に好適な容器としては、例えば、ボトル、バイアル、袋、およびシリンジが挙げられる。
本明細書に記載の製造品またはキットのいずれかは、本明細書に記載の化合物1またはその薬学的に許容され得る塩、および/またはPD-L1結合アンタゴニスト(例えば、アテゾリズマブ)を、本明細書に記載の方法のいずれかに従って患者に投与するための説明書を含む場合がある。
実施形態
以下に、本発明の例示的な実施形態を提供する。
以下に、本発明の例示的な実施形態を提供する。
実施形態2.前記PD-L1結合アンタゴニストが、抗PD-L1抗体である、実施形態1に記載の併用療法。
実施形態3.前記抗PD-L1抗体がアテゾリズマブである、実施形態1または2に記載の併用療法。
実施形態4.化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが前記第1の21日サイクルの1日目に投与される、実施形態3に記載の併用療法。
実施形態5.化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にBID投与され、アテゾリズマブが前記第1の21日サイクルの1日目に投与される、実施形態3に記載の併用療法。
実施形態6.化合物1またはその薬学的に許容され得る塩が、錠剤またはカプセル剤として経口投与される、実施形態1~5のいずれか1つに記載の併用療法。
実施形態7.化合物1またはその薬学的に許容され得る塩が約5mg~100mgの量で投与される、実施形態1~6のいずれか1つに記載の併用療法。
実施形態8.化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、実施形態1~7のいずれか1つに記載の併用療法。
実施形態9.アテゾリズマブが約800mg~約1400mgの量でQ3W投与される、実施形態3~8のいずれか1つに記載の併用療法。
実施形態10.アテゾリズマブが、各サイクルの1日目に約1200mgの量で投与される、実施形態3~9のいずれか1つに記載の併用療法。
実施形態11.前記第1の21日サイクルの開始前に、化合物1またはその薬学的に許容され得る塩が投与され、続いてアテゾリズマブが840mgの量で投与される、実施形態5~10のいずれか1つに記載の併用療法。
実施形態12.前記併用療法が、それを必要とする患者に投与され、前記患者が肺がん、頭頸部がん、または黒色腫を有する、実施形態1~11のいずれか1つに記載の併用療法。
実施形態13.前記患者が、PD-L1陽性である、実施形態12に記載の併用療法。
実施形態14.前記患者が、PD-L1-highである、実施形態12または13に記載の併用療法。
実施形態15.前記患者が、PD-L1-lowである、実施形態12~14のいずれか1つに記載の併用療法。
実施形態16.前記PD-L1陽性が、PD-L1免疫組織化学(IHC)アッセイによって判定される、実施形態13~15のいずれか1つに記載の併用療法。
実施形態17.前記患者が、非小細胞肺がん(NSCLC)、頭頸部扁平上皮癌(HNSCC)、またはBRAF WT黒色腫を有する、実施形態12~15のいずれか1つに記載の併用療法。
実施形態18.肺がん、頭頸部がん、または黒色腫の処置を必要とする患者における肺がん、頭頸部がん、または黒色腫を処置する方法であって、処置期間中に、
(a)化合物1
またはその薬学的に許容され得る塩と、
(b)PD-L1結合アンタゴニストと、
を含む、有効量の併用療法を投与することを含む、方法。
(a)化合物1
(b)PD-L1結合アンタゴニストと、
を含む、有効量の併用療法を投与することを含む、方法。
実施形態19.PD-L1結合アンタゴニストが、抗PD-L1抗体である、実施形態18に記載の方法。
実施形態20.前記抗PD-L1抗体がアテゾリズマブである、実施形態18に記載の方法。
実施形態21.前記処置期間が、
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、実施形態20に記載の方法。
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、実施形態20に記載の方法。
実施形態22.前記処置期間が、
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をBID投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、実施形態20に記載の方法。
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をBID投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、実施形態20に記載の方法。
実施形態23.化合物1またはその薬学的に許容され得る塩が、錠剤またはカプセル剤として経口投与される、実施形態18~22のいずれか1つに記載の方法。
実施形態24.化合物1またはその薬学的に許容され得る塩が、約5mg~100mgの量で投与される、実施形態18~23のいずれか1つに記載の方法。
実施形態25.化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、実施形態18~24のいずれか1つに記載の方法。
実施形態26.アテゾリズマブが、約800mg~約1400mgの量でQ3W投与される、実施形態20~25のいずれか1つに記載の方法。
実施形態27.アテゾリズマブが、各サイクルの1日目に約1200mgの量で投与される、実施形態20~26のいずれか1つに記載の方法。
実施形態28.前記方法が、化合物1またはその薬学的に許容され得る塩を第1のサイクルの開始前に投与し、続いてアテゾリズマブを840mgの量で投与することを含む慣らし期間を更に含む、実施形態20~27のいずれか1つに記載の方法。
実施形態29.前記慣らし期間が、1~14日間を含む、実施形態28に記載の方法。
実施形態30.前記慣らし期間が14日間であり、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブが前記慣らし期間の1日目に投与される、実施形態28または29に記載の方法。
実施形態31.化合物1またはその薬学的に許容され得る塩が、前記慣らし期間の8日目から開始してQD投与される、実施形態29または30に記載の方法。
実施形態32.前記患者がPD-L1陽性である、実施形態18~28のいずれか1つに記載の方法。
実施形態33.前記患者がPD-L1-highである、実施形態18~28または32のいずれか1つに記載の方法。
実施形態34.前記患者がPD-L1-lowである、実施形態18~28または32~33のいずれか1つに記載の方法。
実施形態35.前記PD-L1陽性が、PD-L1免疫組織化学(IHC)アッセイによって判定される、実施形態18~28または32~34のいずれか1つに記載の方法。
実施形態36.前記肺がんが、非小細胞肺がん(NSCLC)である、実施形態18~35のいずれか1つに記載の方法。
実施形態37.前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、実施形態18~35のいずれか1つに記載の方法。
実施形態38.前記黒色腫が、BRAF WT黒色腫である、実施形態18~35のいずれか1つに記載の方法。
実施形態39.肺がん、頭頸部がん、または黒色腫の処置を必要とする患者における肺がん、頭頸部がん、または黒色腫を処置する方法であって、有効量の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニストとを含む処置レジメンを前記患者に投与することを含む、方法。
実施形態40.PD-L1結合アンタゴニストが、抗PD-L1抗体である、実施形態39に記載の方法。
実施形態41.抗PD-L1抗体がアテゾリズマブである、実施形態39または40に記載の方法。
実施形態42.(a)化合物1またはその薬学的に許容され得る塩が、前記第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、
(b)アテゾリズマブが、前記第1の21日サイクルの1日目に1200mgの量で投与される、
実施形態41に記載の方法。
(b)アテゾリズマブが、前記第1の21日サイクルの1日目に1200mgの量で投与される、
実施形態41に記載の方法。
実施形態43.化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、実施形態39~42のいずれか1つに記載の方法。
実施形態44.前記肺がんが、非小細胞肺がん(NSCLC)である、実施形態39~43のいずれか1つに記載の方法。
実施形態45.前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、実施形態39~43のいずれか1つに記載の方法。
実施形態46.前記黒色腫が、BRAFT WT黒色腫である、実施形態39~43のいずれか1つに記載の方法。
実施形態47.本明細書に記載の肺がん、頭頸部がん、または黒色腫を処置するための、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む併用療法の使用(U1)。
実施形態48.投薬レジメンであって、(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、を含む投薬レジメンを更に含む、実施形態47に記載の使用。
実施形態49.(a)前記第1の21日サイクルの1~21日目に約50mg~500mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(b)前記第1の21日サイクルの1日目に約1200mgのアテゾリズマブを投与することと、を更に含む、実施形態47または48に記載の使用。
実施形態50.肺がん、頭頸部がん、または黒色腫を処置するための医薬品を製造するための、化合物1またはその薬学的に許容され得る塩と、アテゾリズマブとを含む併用療法の使用(U5)。
実施形態51.(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(b)前記第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、を含む投薬レジメンを更に含む、実施形態50に記載の使用。
実施形態52.(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、を含む投薬レジメンを更に含む、実施形態50または51に記載の使用。
実施形態53.(a)第1の21日サイクルの1~21日目に約50mg~500mgの化合物1またはその薬学的に許容され得る塩をQD投与することと、(b)前記第1の21日サイクルの1日目に約1200mgのアテゾリズマブを投与することと、を更に含む、実施形態50~52のいずれか1つに記載の使用。
実施形態54.投薬レジメンが、2サイクル以上を含む、実施形態50~53のいずれか1つに記載の使用。
実施形態55.化合物1が、約5mg~100mgの量で投与される、実施形態47~54のいずれか1つに記載の使用。
実施形態56.化合物1が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、実施形態47~55のいずれか1つに記載の使用。
実施形態57.前記肺がんが、非小細胞肺がん(NSCLC)である、実施形態47~56のいずれか1つに記載の使用。
実施形態58.前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、実施形態47~56のいずれか1つに記載の使用。
実施形態59.前記黒色腫が、BRAFT WT黒色腫である、実施形態47~56のいずれか1つに記載の使用。
実施形態60.肺がん、頭頸部がん、または黒色腫の処置における使用のための、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む、併用療法。
実施形態61.(a)化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、(b)アテゾリズマブが、前記第1の21日サイクルの1日目にQ3W投与される、実施形態60に記載の併用療法。
実施形態62.(a)化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、(b)アテゾリズマブが、前記第1の21日サイクルの1日目に投与される、実施形態60または61に記載の併用療法。
実施形態63.(a)第1の21日サイクルの1~21日目に約50mg~500mgの化合物1またはその薬学的に許容され得る塩がQD投与され、(b)前記第1の21日サイクルの1日目に約1200mgのアテゾリズマブが当紆余される、実施形態60~62のいずれか1つに記載の併用療法。
実施形態64.投薬レジメンが、2サイクル以上を含む、実施形態60~63のいずれか1つに記載の併用療法。
実施形態65.化合物1が、約5mg~100mgの量で投与される、実施形態60~64のいずれか1つに記載の併用療法。
実施形態66.化合物1が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、実施形態60~65のいずれか1つに記載の併用療法。
実施形態67.前記肺がんが、非小細胞肺がん(NSCLC)である、実施形態60~66のいずれか1つに記載の併用療法。
実施形態68.前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、実施形態60~66のいずれか1つに記載の併用療法。
実施形態69.前記黒色腫が、BRAFT WT黒色腫である、実施形態60~66のいずれか1つに記載の併用療法。
以下の実施例は、限定ではなく、例示として提示されている。
実施例1:インビトロおよびインビボでの特性評価
薬剤。化合物1を、60mg/kgの濃度で50mMクエン酸ナトリウム緩衝液(pH3.0)に製剤化した。抗PD-L1 mAb(Mu IgG2a抗PD-L1、以下、抗PD-L1と称する)および抗gp120アイソタイプ対照(Mu IgG1抗gp120;以下、アイソタイプ対照と称する)を、20mM酢酸ヒスチジン、240mMスクロース、0.02% Tween 20(商標)、pH5.5の緩衝液中の溶液として製剤化した。経口投与ビヒクル対照は、50mMクエン酸ナトリウム緩衝液、pH3.0であった。
細胞株。EMT6乳癌細胞株をインビトロで培養し、対数増殖期に採取し、インビボ接種のために、Matrigel(商標)(BD Biosciences;カリフォルニア州サンノゼ)を体積比1:1で含有するハンクス平衡塩類溶液(HBSS)に再懸濁した。動物にそれぞれ、乳腺(5個、左)中に100mLの体積で0.1×106個の細胞を接種した。
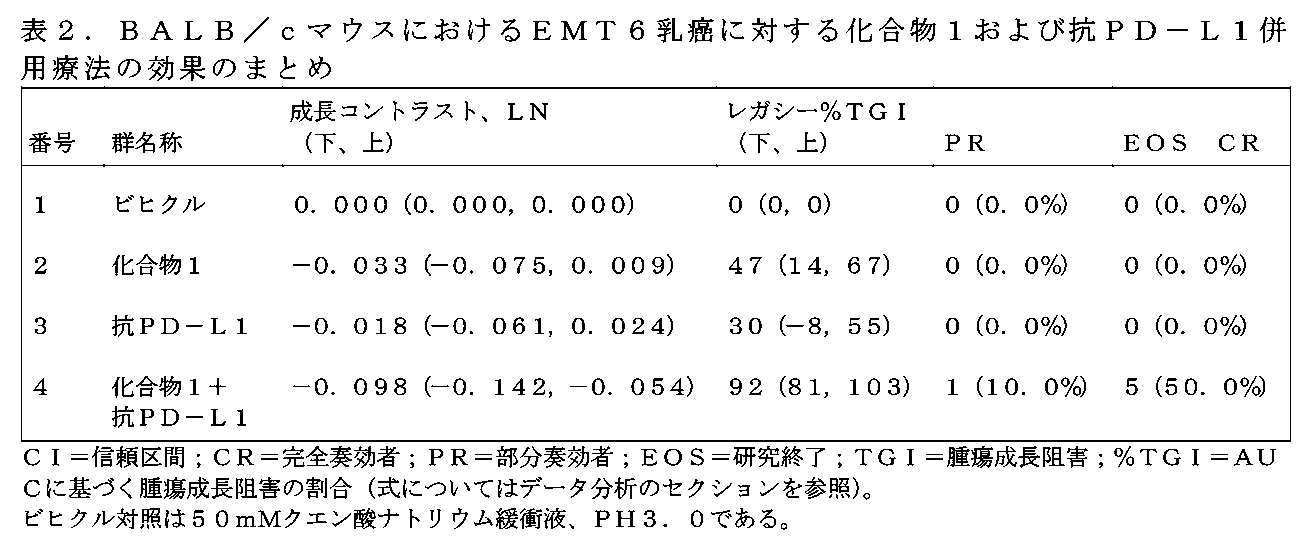
マウス腫瘍モデル。141~196mm3の範囲の腫瘍を有する10.6週齢のBalb/cマウスを、それぞれ10匹のマウスからなる4つの研究群に均等に分配した。全ての群にわたる平均腫瘍体積は、投薬開始時に165mm3であった。平均開始重量は、19.94gであった。全ての濃度を20gの平均体重に基づいて計算し、10%の体重減少または体重増加について調整した。様々な群のマウスは、表1に記載の処置レジメンを受けた。マウスに、合計28日間、または罹患の最初の徴候時に、または体重減少が投与開始時の体重の20%以上であった場合に安楽死させるまで投薬した。この研究は、28日間を超えて、処置の中止後、応答の持続性をチェックするために延長され、102日目に終了し、残りのマウスは全て安楽死させた。
腫瘍および体重の測定。腫瘍体積を、Ultra Cal-IVノギス(モデル54-10-111;Fred V.Fowler Co.;マサチューセッツ州ニュートン)を使用して2つの垂直寸法(長さおよび幅)で測定し、腫瘍体積を以下の式に従って計算した:
腫瘍サイズ(mm3)=(より長い測定値×より短い測定値2)×0.5
腫瘍サイズ(mm3)=(より長い測定値×より短い測定値2)×0.5
研究中にそれらの開始体積に対して50%超退縮した腫瘍を部分奏効者(PR)として分類し、完全退縮に対応する最終腫瘍体積を有する腫瘍を完全奏効者(CR)として分類した。動物の体重を、Adventura Pro AV812スケール(Ohaus Corporation;ニュージャージー州パインブルック)を使用して測定し、各群の体重の変化率を計算し、プロットした(図4を参照)。パーセント重量変化を、以下の式を使用して計算した。
体重変化(%)=[(現在の体重/初回体重)-1)×100]
体重変化(%)=[(現在の体重/初回体重)-1)×100]
成長分析および群比較。腫瘍は一般に指数関数的成長を示すため、分析前に腫瘍体積を自然対数変換に供した。R(バージョン3.6.2)(R統計コンピューティング財団;オーストリア国ウィーン)のカスタマイズされた関数のパッケージを使用して、腫瘍増殖の分析および比較を行い、これは、オープンソースパッケージ(例えば、lme4、mgcv、gamm4、multcomp、setting、およびplyr)からのソフトウェアと、tidyverse(例えば、magrittr、dplyr、tidyr、およびggplot2)からのいくつかのパッケージとが統合されている(Forrest et al.;Cancer Res 2020;80(22):5089-97)。0(最小)から8mm3(最大値)までの全ての生腫瘍体積測定値を、完全な腫瘍非存在を反映すると判断して、自然対数変換の前に8mm3に変換した。次いで、一般化された加法混合モデル(GAMM)を適用して、自動的に生成されたスプライン基底を有する回帰スプラインを使用して、経時的な変換された腫瘍体積の変化を記述した。このアプローチは、同じ研究対象からの反復測定および研究終了前の中程度の脱落の両方に対処する。
腫瘍成長阻害率(TGI:tumor growth inhibition)は、処置群の曲線下面積(AUC)と、腫瘍体積を元の尺度に逆変換して、開始腫瘍負荷量を補正し、共通の期間にわたって平均化した後の参照群との間の百分率差を表す。陽性値は抗腫瘍効果を示し、100%は静止を示し、100%超の値は退縮を示す(陰性値は腫瘍促進効果を示す)。95%信頼区間は、パラメトリックブートストラッピングを使用して、データのフィッティングされたモデルおよび変動性測定値に基づく。成長コントラストは、処置群と参照群の適合間の曲線下面積(AUC)に基づく成長速度(時間積分されたエンドポイントゲイン(eGalT:endpoint Gain Integrated in Time))の差を表す。AUCベースの成長速度を計算するために、群AUC値を開始時腫瘍負荷量に対して補正し、勾配等価正規化に供した。腫瘍が対数線形増殖(すなわち、フィッティングは自然対数スケール上の線である)を示す場合、AUCの勾配当量正規化は、適合の勾配の計算をもたらす。腫瘍が非対数線形成長(すなわち、適合は自然対数スケールで湾曲している)を示す場合、勾配当量正規化は、当てはめのために観察されたベースライン補正AUCを得るために必要な一定の対数線形成長速度の計算をもたらす。数学的には、この正規化は、各推定ベースライン補正AUC値を共通の研究期間の二乗の半分で割ることによって達成され、1日当たりの自然対数単位の単位をもたらす。ビヒクル対照は、0の成長コントラスト(GR)値に対応する。GR値が負であるほど、抗腫瘍効果は大きくなる。95%信頼区間は、データの適合モデルおよび変動性測定値に基づく。
選択された1日目AUCからその最終測定時点までの各個々の腫瘍の増殖速度は、最初に腫瘍体積を自然対数変換に供した後のこの時間範囲における腫瘍体積プロファイルのAUCから計算される。AUCから成長速度を得るために、この期間に関連する腫瘍負荷量を開始するためにAUCを補正し、次いで、勾配等価正規化に供する。ベースライン補正されたAUC値は、この正規化工程において指定された期間の二乗の半分で除算される。このメトリックのデフォルト単位は、元のスケールでの指数関数的増加が自然対数スケールで線形であるので、1日当たりの自然対数単位である。正の値は増殖を示し、負の値は退縮を示し、0は静止を示す。値がより正の値であるほど、腫瘍がより速く成長している。値が負の値であるほど、腫瘍の退縮が速くなる。個々のAUCに基づく成長速度は、群比較の目的のために計算されない。
抗腫瘍効果を、化合物1の単剤(60mg/kg、PO、QD)、抗PD-L1(10mg/kg、IV、最初の用量、次いで5mg/kg、IP、週2回、または化合物1と抗PD-L1との組み合わせによる処置後のEMT6乳癌を有するBalb/cマウスにおいて評価した。単剤処置は有効性をもたらさず、化合物1はビヒクル対照に対して47%のTGIおよび-0.033GRをもたらし、抗PD-L1は30%のTGIおよび-0.022GRをもたらした。対照的に、化合物1と抗PD-L1との組み合わせは、ビヒクル対照に対して、20日間の投薬後に腫瘍静止に近い抗腫瘍応答の増強を示し、92%のTGIおよび-0.098GRをもたらした。さらに、1/10 PRおよび5/10 CRを用いた28日間の投薬処置の中止後、持続的な抗腫瘍効果が観察された(図1、図2、図3を参照)。体重の変化率によって判定したところ、全ての処置は忍容性が良好であった。
腫瘍免疫プロファイリング。抗腫瘍免疫を、ビヒクルおよびアイソタイプ対照抗体、単一薬剤化合物1(60mg/kg、PO、QD)、抗PD-L1抗体(10mg/kg、IV、最初の用量、次いで5mg/kg、IP、週に2回)、または化合物1と抗PD-L1との組み合わせのいずれかによる7日間の処置後の腫瘍細胞および腫瘍浸潤免疫細胞のフローサイトメトリー免疫プロファイリングによってEMT6乳房腫瘍において評価した。
MHC-IおよびPD-L1の発現について評価した腫瘍細胞(CD45陰性細胞)は、化合物1単独および抗PD-L1と組み合わせた処置群において、ビヒクル群のものに対して、MHC-I(それぞれp=0.0354およびp=0.0044)およびPD-L1(それぞれp=0.0127およびp=0.0018)の両方の発現の平均蛍光強度(MFI)の有意な増加があったことを明らかにした(図4を参照)。
化合物1単独または抗PD-L1抗体と組み合わせて処置したマウス由来の腫瘍では、ビヒクル群に対して、MDSC(それぞれp=0.0058およびp=0.0083)およびTAM(それぞれp=0.0072およびp=0.0098)の頻度が低下した(図5A)。さらに、ビヒクル群に対して、化合物1単独または抗PD-L1と組み合わせて処置したマウスの腫瘍微小環境におけるマクロファージのM1集団(それぞれp=0.0033およびp=0.0162)の頻度の増加およびマクロファージのM2集団(それぞれp=0.0036およびp=0.0007)の代償的減少、ならびに組み合わせ(p=0.0033)におけるM1/M2比の増加があった。骨髄由来樹状細胞(DC)は、いずれの処置群においても変化を示さなかった。これらのデータは、化合物1によるSHP2阻害が腫瘍MDSCを減少させ、TAMの表現型を歪めてより炎症誘発性になることを実証している。
TおよびNK細胞活性に対するSHP2阻害の効果を決定するために、CD4+およびCD8+T細胞ならびにNK細胞集団を含む腫瘍浸潤リンパ球(TIL)を評価した。化合物1と抗PD-L1の組み合わせ群では、化合物1単独または抗PDL1抗体と組み合わせて処置したマウスでは、ビヒクル群(CD8、p=0.0058およびp=0.008;CD4、p=0.0067およびp=0.002;NK、それぞれp=0.013およびp=0.024)と比較して増加した(図5B)。
腫瘍由来T細胞からのインターフェロンガンマ(IFNg)、腫瘍壊死因子アルファ(TNFa)およびグランザイムB(GZMB)を含むサイトカインおよびエフェクター分子の発現を、PMA/イオノマイシン(図6A)を使用する再刺激条件下で評価することによって、TILの活性化状態を評価した。化合物1単独または抗PD-L1抗体と組み合わせて処置したマウス由来の腫瘍由来CD8+T細胞上のIFNgおよびTNFaの両方の発現は、ビヒクル群(IFNg、p=0.0002およびp=0.0001;TNFa、それぞれp=0.0016およびp=0.0035)に対して増加し(図6A)、これらのT細胞がより活性であることと一致した。化合物1および抗PD-L1で処置したマウス由来の腫瘍におけるGZMBを発現するCD8+T細胞の頻度も、ビヒクル群に対して増加した(p=0.0137)。(図6A)。腫瘍浸潤CD8+T細胞(IFNgおよびTNFaを発現する)の多機能性は、ビヒクル群に対して、マウスを化合物1単独または抗PD-L1抗体と組み合わせて処置した場合に増加した(それぞれp=0.0008およびp=0.0011)。
T細胞活性化および疲弊のマーカーも評価して、化合物1単独または抗PD-L1抗体と組み合わせた化合物1によるSHP2阻害が腫瘍内のCD8+T細胞の表現型を変化させたかどうかを決定した。化合物1および抗PDL1抗体で処置したマウス由来の腫瘍は、活性化マーカーKi-67(p=0.0127)、CD69(p=0.0009)およびICOS(p=0.001)を発現するCD8+T細胞の総数の増加を示した(図6B)。これらのデータは、化合物1単独または抗PD-L1と組み合わせた化合物1によるSHP2阻害が、EMT6腫瘍においてNK細胞ならびにCD4+およびCD8+T細胞活性化の有意な増加をもたらすことを実証している。
これらの研究は、抗PD-L1抗体と組み合わせた60mg/kg、QDでの化合物1によるSHP2阻害が、EMT6同系腫瘍モデルにおいて有意な抗腫瘍活性を実証することを集合的に実証する。28日間の投薬間隔中に観察された抗腫瘍活性の増加に加えて、研究終了時(102日目)に6/10(60%)のORRおよび5/10(50%)のCRを有する永続的奏効者の数の増加もあった。これらのデータは、SHP2阻害剤化合物1を抗PD-L1抗体と組み合わせることが、EMT6同系腫瘍モデルにおいて忍容性が高く、有効な併用レジメンであることを実証した。
これらのデータは、SHP2阻害剤化合物1を抗PD-L1抗体と組み合わせることが、腫瘍細胞において観察される薬力学的変化、ならびに単剤単独に対してかなりの数の動物において集合的に深く持続的な腫瘍阻害を促進する腫瘍微小環境を通じて抗腫瘍免疫応答を促進することを実証している。
実施例2:
化合物1は、0.7nMの50%(IC50)の阻害濃度を有する組換えヒトSHP2の強力なアロステリック阻害剤である。これは、多数の非臨床がんモデルにおいて特徴付けられている。化合物1はまた、細胞ベースのアッセイにおいてSHP2の強力な阻害剤であることが実証されている。細胞におけるSHP2阻害を、EGFR増幅KYSE-520細胞において1.3nMのIC50値でThr202/Tyr204におけるERK1/2リン酸化のレベルを測定することによって決定した。一連のキナーゼ、受容体、イオンチャネルおよび輸送体に対する選択性の包括的な評価は、化合物1がSHP2を選択的に阻害することを実証した。
化合物1の抗増殖効果は、2Dおよび足場非依存性3Dフォーマットを使用して複数のがん細胞株において評価されている。NSCLC、食道扁平上皮癌、結腸直腸癌、膵管腺癌、胆管癌、および2Dまたは3Dアッセイで試験した他の腫瘍細胞株のパネルの中で、化合物1は、1nM未満のIC50値で多数の細胞株の増殖を阻害した。抗増殖効果は、RAS/MAPKシグナル伝達経路に様々な異常を有する細胞株で見られた。これらのインビトロ結果は、化合物1が様々な腫瘍タイプにわたって広範な抗腫瘍効果の可能性を有することを示唆している。
化合物1はまた、複数の異種移植モデルにおいてインビボ抗腫瘍活性について試験されている。単一薬剤化合物1の経口投与は、例えばKRAS変異NSCLC(NCI-H358)およびEGFR増幅食道扁平上皮癌(KYSE-520)のヒト腫瘍異種移植モデルにおいて有意な抗腫瘍効果を示した。用量依存的な抗腫瘍活性が、十分に忍容された用量レベルで認められた。薬物動態、薬力学および効力の比較は、SHP2阻害の程度および持続時間が抗腫瘍活性のレベルと直接相関することを示した。まとめると、これらのインビトロおよびインビボ研究は、抗腫瘍剤としての化合物1の臨床評価を裏付けている。
アテゾリズマブは、PD-L1を標的とし、PD-L1と、その受容体であるPD-1およびB7-1(CD80としても知られる。両方ともT細胞上に発現される阻害性受容体として機能する)との間の相互作用を阻害するヒト化IgG1モノクローナル抗体である。アテゾリズマブによるPD-L1結合の治療的遮断は、腫瘍特異的T-細胞応答の大きさおよび質を増強し、抗腫瘍活性の改善をもたらすことが示されている。アテゾリズマブは、Fc受容体への結合が最小限であり、したがって、検出可能なFcエフェクター機能および活性化エフェクターT細胞の関連する抗体-媒介性クリアランスを排除する。
アテゾリズマブは、非臨床モデルおよびがん患者の両方において抗腫瘍活性を示し、多種多様な悪性腫瘍における潜在的な治療法として研究されている。アテゾリズマブは、単剤として進行がんにおいて、またアジュバント療法の状況において、ならびに化学療法、標的療法およびがん免疫療法と組み合わせて研究されている。アテゾリズマブは、局所進行性または転移性尿路上皮癌腫、NSCLC、小細胞肺がん腫、トリプルネガティブ乳がん、黒色腫および肝細胞癌腫の処置のために(単剤としておよび/または他の抗がん療法と組み合わせて)承認されている。
アテゾリズマブとの併用療法の理論的根拠。腫瘍免疫療法の分野で出現している有望な臨床データは、がんに対するT細胞応答の増強に焦点を当てた療法が、進行性悪性腫瘍を有する患者において有意な生存利益をもたらし得ることを実証している。PD-L1経路は、慢性感染症やがん等の慢性抗原刺激状態において免疫応答を一時的に弱める免疫チェックポイントとして機能する。PD-L1経路の中断は、腫瘍特異的T細胞免疫を回復させるための1つの経路を表す。
非臨床薬力学(PD)および有効性研究において、チェックポイント阻害(抗PD-L1)と組み合わせたSHP2阻害剤化合物1(60mg QDで)は、EMT6乳がん同系モデルにおける腫瘍微小環境の炎症状態の増加をもたらし、より強い抗腫瘍応答をもたらす免疫系による腫瘍の効果的な関与を可能にした。(実施例1を参照)。腫瘍細胞では、化合物1+抗PD-L1は腫瘍MHC IおよびPD-L1発現を増加させた。化合物1は単独で、または抗PD-L1と組み合わせて、MDSCおよびTAMの減少をもたらした。さらに、残りのTAMは炎症促進性M1表現型に向かって歪んでいた。化合物1単独および抗PD-L1と組み合わせて、CD4+およびCD8+T細胞ならびに腫瘍に存在するNK細胞の増加も促進した。化合物1と抗PD-L1との組み合わせは、増殖性マーカーKi-67およびCD69ならびにT細胞成熟マーカーICOS1の増加を含む、腫瘍におけるCD8+T細胞の活性化状態の増加を促進した。化合物1および抗PD-L1は、EMT6腫瘍モデルにおいて強力な併用有効性を示し、いずれかの単剤に対してより深くより持続的な応答をもたらす。
高いPD-L1発現は、免疫チェックポイント阻害剤(CPI)療法に対する応答を予測することができる。PD-L1発現の増加、腫瘍細胞への抗原提示、およびCD8+T細胞の浸潤および活性化の増強を促進するその能力により、SHP2阻害は腫瘍におけるPD-L1遮断と相乗作用し得る。アテゾリズマブは、進行した悪性腫瘍を有する患者において活性を実証した。客観的応答は、例えば、肺がん(例えば、NSCLC)、尿路上皮癌、RCC、黒色腫(例えば、BRAFT WT黒色腫)、結腸直腸がん、頭頸部がん(例えば、HNSCC)、胃がん、乳がんおよび肉腫を含む広範囲の悪性腫瘍にわたって観察されている。
抗PD-1/PD-L1活性に応答する疾患特異的悪性腫瘍を有する患者は、本明細書に記載の併用療法から利益を得る可能性が高い。一次処置設定におけるPD-L1陽性NSCLCおよびPD-L1陽性転移性頭頸部扁平上皮癌(HNSCC)は抗PD-1/PD-L1剤に反応性であり、単剤抗PD-1/PD-L1療法は、利益を提供することが示されている認識されている標準治療レジメンである。これらの疾患には複数の処置タイプが利用可能であるが(化学療法、免疫療法)、これらの患者は、満たされていないニーズが高い不治の疾患を有する。
第二選択またはそれ以降の転移性処置の状況におけるBRAFV600野生型(BRAF WT)黒色腫の患者も処置される。これらの患者は不治の疾患を有し、抗CTLA4処置の有無にかかわらず、抗PD-L1療法の使用後に承認された治療法はない。典型的には、これらの患者は追加のCPI処置で処置され得る。研究により、奏効率の範囲(4%~36%)が示されており、これは、再処置がいくらかの限定された利益をもたらし得ることを示している。アテゾリズマブへの化合物1の添加は、更なる抗腫瘍活性を提供し得る。
アテゾリズマブは、一般に忍容性が良好であった。免疫介在性の可能性がある原因が免疫療法剤と一致する有害事象(発疹、インフルエンザ様疾患の内分泌不全症、肝炎または高トランスアミナーゼ血症、間質性肺炎、大腸炎、および重症筋無力症を含む)が観察されている。
化合物1およびアテゾリズマブは、放射線写真データおよび臨床状態の統合評価後に治験責任医師によって決定される許容できない毒性または臨床的利益の喪失まで投与される(例えば、疾患に続発する疼痛等の症候性の悪化)。化合物1およびアテゾリズマブによる処置は、明らかな放射線撮影による疾患進行を超えて継続し得る。
一例では、本明細書に記載の化合物1とアテゾリズマブの組み合わせによる処置は、14日間の慣らし期間とそれに続く本明細書に記載の処置期間とからなる。慣らし期間中、患者は、以下に概説するように、1日目および8日目に処置を受ける。
・1日目:化合物1錠剤60mg PO QD、続いてアテゾリズマブ840mg IV
・8日目:化合物1カプセル剤60mg PO QD
・1日目:化合物1錠剤60mg PO QD、続いてアテゾリズマブ840mg IV
・8日目:化合物1カプセル剤60mg PO QD
14日間の慣らし期間が完了すると、患者は処置期間に入る。サイクル1の1日目から開始して、以下に概説するように、患者は21日サイクルで処置を受ける。
・化合物1カプセル剤(割り当てられた用量、例えば、20mg、40mg、60mg)、各サイクルの1~21日目にPO QD投与
・各サイクルの1日目にアテゾリズマブ1200mg IV
・化合物1カプセル剤(割り当てられた用量、例えば、20mg、40mg、60mg)、各サイクルの1~21日目にPO QD投与
・各サイクルの1日目にアテゾリズマブ1200mg IV
アテゾリズマブと組み合わせた化合物1の活性は、ORR、DOR、PFS、PFSレート、およびOSレートについて、RECIST v1.1に従って評価される。
選択基準:患者は、本明細書に記載の処置のための以下の基準を満たさなければならない:
・インフォームドコンセント書類の署名時の年齢が18歳以上
・RECIST v1.1による測定疾患
・ECOGパフォーマンスステータス0または1
・平均余命12週間以上
・処置開始前14日以内に得られた十分な血液学的機能および終末器官機能:
oANC≧1.5×109/L(1500/mL)
oWBC≧2,500/mL
oリンパ球数≧0.5×109/L(500/mL)
o血小板数≧100×109/L(100,000/mL)
oヘモグロビン≧90g/L(9g/dL)
o血清アルブミン≧25g/L(2.5g/dL)
oAST、ALT、およびALP≦2.5×ULN、ただし、以下の例外がある。
・記録された肝臓転移を有する患者:ASTおよびALT≦5×ULN
・記録された肝臓転移または骨転移を有する患者:ALP≦5×ULN
o総ビリルビン≦1.5×ULN、ただし、以下の例外がある。
・既知のギルバート病患者:総ビリルビン≦3×ULN
o測定または計算されたクレアチニンクリアランス≧50mL/分(Cockcroft-Gault式を使用して計算):
・スクリーニング時の陰性HIV検査
・スクリーニング時のB型肝炎表面抗原(HBsAg)陰性
・スクリーニング時のB型肝炎表面抗体(HBsAb)陽性検査、または以下のいずれかを伴うスクリーニング時のHBsAb陰性:
o総B型肝炎コア抗体(HBcAb)陰性
o陽性の全HBcAb検査とそれに続く定量的B型肝炎ウイルス(HBV)DNA<500IU/mL
oHBV DNA検査を、HBsAg検査陰性、HBsAb検査陰性、および総HBcAb検査陽性の患者に対して実施しなければならない。
・スクリーニング時にC型肝炎ウイルス(HCV)抗体検査陰性、またはスクリーニング時にHCV抗体検査陽性後、HCV RNA検査陰性
oHCV RNA検査を、HCV抗体検査が陽性の患者に対して行われなければならない。
・組織学的に確認された局所進行性または転移性の固形腫瘍であって、少なくとも1つの利用可能な標準治療後に進行しているか、または承認された標準療法が無効もしくは容認できないことが証明されているもの、標準療法が不適切であると考えられているもの、または治験薬が認識されている標準治療であるもの
・インフォームドコンセント書類の署名時の年齢が18歳以上
・RECIST v1.1による測定疾患
・ECOGパフォーマンスステータス0または1
・平均余命12週間以上
・処置開始前14日以内に得られた十分な血液学的機能および終末器官機能:
oANC≧1.5×109/L(1500/mL)
oWBC≧2,500/mL
oリンパ球数≧0.5×109/L(500/mL)
o血小板数≧100×109/L(100,000/mL)
oヘモグロビン≧90g/L(9g/dL)
o血清アルブミン≧25g/L(2.5g/dL)
oAST、ALT、およびALP≦2.5×ULN、ただし、以下の例外がある。
・記録された肝臓転移を有する患者:ASTおよびALT≦5×ULN
・記録された肝臓転移または骨転移を有する患者:ALP≦5×ULN
o総ビリルビン≦1.5×ULN、ただし、以下の例外がある。
・既知のギルバート病患者:総ビリルビン≦3×ULN
o測定または計算されたクレアチニンクリアランス≧50mL/分(Cockcroft-Gault式を使用して計算):
・スクリーニング時のB型肝炎表面抗原(HBsAg)陰性
・スクリーニング時のB型肝炎表面抗体(HBsAb)陽性検査、または以下のいずれかを伴うスクリーニング時のHBsAb陰性:
o総B型肝炎コア抗体(HBcAb)陰性
o陽性の全HBcAb検査とそれに続く定量的B型肝炎ウイルス(HBV)DNA<500IU/mL
oHBV DNA検査を、HBsAg検査陰性、HBsAb検査陰性、および総HBcAb検査陽性の患者に対して実施しなければならない。
・スクリーニング時にC型肝炎ウイルス(HCV)抗体検査陰性、またはスクリーニング時にHCV抗体検査陽性後、HCV RNA検査陰性
oHCV RNA検査を、HCV抗体検査が陽性の患者に対して行われなければならない。
・組織学的に確認された局所進行性または転移性の固形腫瘍であって、少なくとも1つの利用可能な標準治療後に進行しているか、または承認された標準療法が無効もしくは容認できないことが証明されているもの、標準療法が不適切であると考えられているもの、または治験薬が認識されている標準治療であるもの
NSCLCのための追加の選択基準
・組織学的に確認された局所進行性または転移性NSCLC
・局所進行性または転移性NSCLCに対する事前の全身療法なし(補助療法は許容される)
・中央検査室または現場検査室の試験によって評価されるEGFRおよびALKの変化ならびにPD-L1状態の決定に適した代表的な腫瘍検体の利用可能性
・EGFRおよびALKの変化または患者が標的治療剤にアクセスすることができる他の既知の発癌性ドライバー変異の非存在
・PD-L1陽性
・組織学的に確認された局所進行性または転移性NSCLC
・局所進行性または転移性NSCLCに対する事前の全身療法なし(補助療法は許容される)
・中央検査室または現場検査室の試験によって評価されるEGFRおよびALKの変化ならびにPD-L1状態の決定に適した代表的な腫瘍検体の利用可能性
・EGFRおよびALKの変化または患者が標的治療剤にアクセスすることができる他の既知の発癌性ドライバー変異の非存在
・PD-L1陽性
HNSCCの追加の選択基準
・治癒的療法に適していないと考えられる中咽頭、口腔、喉頭、または下咽頭を含む組織学的に確認された再発性または転移性のHNSCC
・中咽頭癌に対する局所ヒトパピローマウイルス(HPV)状態試験の既知の結果
・再発性または転移性のHNSCCに対する事前の全身療法なし
・中央検査室または現場の実験室のIHCに基づく試験によって評価されるPD-L1状態の決定に適した代表的な腫瘍検体の利用可能性
・PD-L1陽性
・治癒的療法に適していないと考えられる中咽頭、口腔、喉頭、または下咽頭を含む組織学的に確認された再発性または転移性のHNSCC
・中咽頭癌に対する局所ヒトパピローマウイルス(HPV)状態試験の既知の結果
・再発性または転移性のHNSCCに対する事前の全身療法なし
・中央検査室または現場の実験室のIHCに基づく試験によって評価されるPD-L1状態の決定に適した代表的な腫瘍検体の利用可能性
・PD-L1陽性
黒色腫の追加の選択基準
・米国がん合同委員会(American Joint Committee on Cancer)第8版によって定義された、抗PD-1療法または抗PD-L1療法を含む処置中またはその後に進行した、組織学的に確認された局所進行性または転移性(再発性またはデノボス(de novo)ステージIV)または切除不能な局所進行性(ステージIII)皮膚BRAF WT黒色腫(臨床検査改善法(CLIA:Clinical Laboratory Improvement Amendments)または同等に認定された研究室での局所有効性試験によって実証されたもの)
・患者は研究登録時に進行性疾患を有していなければならない。
・米国がん合同委員会(American Joint Committee on Cancer)第8版によって定義された、抗PD-1療法または抗PD-L1療法を含む処置中またはその後に進行した、組織学的に確認された局所進行性または転移性(再発性またはデノボス(de novo)ステージIV)または切除不能な局所進行性(ステージIII)皮膚BRAF WT黒色腫(臨床検査改善法(CLIA:Clinical Laboratory Improvement Amendments)または同等に認定された研究室での局所有効性試験によって実証されたもの)
・患者は研究登録時に進行性疾患を有していなければならない。
除外基準:以下の基準のいずれかを満たす患者は除外される:
・症候性、未処置、または活発に進行する中枢神経系(CNS)転移。
・処置されたCNS病変を有する無症候性患者は、以下の基準の全てが満たされるならば適格である:
oRECIST v1.1による測定可能な疾患はCNS外に存在しなければならない。
o患者は頭蓋内出血または脊髄出血の病歴がない。
o患者は、処置前7日以内に定位放射線療法、処置前14日以内に全脳放射線療法、または処置前28日以内に神経外科的切除を受けていない
oCNS疾患の治療としてのコルチコステロイドの継続的な必要性はない。
o患者が抗痙攣療法を受けている場合、用量は安定であると見なされる。
o転移は小脳またはテント上領域に限定される(すなわち、中脳、橋、延髄、または脊髄への転移がない)。
oCNS向け処置の完了と研究処置の開始との間の中間進行の証拠はない。
・軟膜疾患または癌性髄膜炎
・スクリーニング眼科検査における、網膜静脈閉塞症(RVO)、中心性漿液性網膜症(CSR)、RVOもしくはCSRの素因、または網膜症を含む眼科疾患の病歴または所見
・制御されていない高血圧
・正常な施設内下限未満または50%未満の左室駆出率
・キメラもしくはヒト化抗体または融合タンパク質に対する重症アレルギーアナフィラキシー反応の病歴
・チャイニーズハムスター卵巣細胞生成物またはアテゾリズマブ製剤の任意の成分に対する既知の過敏症
・化合物1製剤の任意の成分に対する既知のアレルギーまたは過敏症
・制御されていない胸水、心膜滲出液、または反復性の排液治療を必要とする腹水(毎月1回またはより頻繁に)
・ウイルス性もしくはその他の肝炎、現在のアルコール乱用、または硬変を含む、臨床的に顕著な肝疾患の病歴
・制御されていないまたは症候性の高カルシウム血症(イオン化カルシウム>1.5mmol/L、カルシウム>12mg/dL、または補正カルシウム>ULN)
・重症筋無力症、筋炎、自己免疫性肝炎、全身性エリテマトーデス、関節リウマチ、炎症性腸疾患、抗リン脂質抗体症候群、ウェゲナー肉芽腫症、シェーグレン症候群、ギラン・バレー症候群、または多発性硬化症を含むがこれらに限定されない自己免疫疾患または免疫不全が活動が活動性であるもの、またはその病歴、ただし、以下を除く:
o甲状腺補充ホルモンを服用している自己免疫関連甲状腺機能低下症の既往歴を有する患者は、研究に適格である。
oインスリンレジメンを受けている、制御された1型糖尿病患者は研究に適格である。
o湿疹、乾癬、慢性単純性苔癬、または皮膚症状のみを伴う白斑(例えば、乾癬性関節炎を有する患者は除外される)を有する患者は、以下の条件の全てが満たされるならば、研究に適格である:
・発疹が覆っている体表面積は10%未満でなければならない
・疾患はベースラインで十分に制御されており、低効力の局所コルチコステロイドのみを必要とする
・過去12ヶ月以内にソラレン+紫外線A照射、メトトレキサート、レチノイド、生物学的薬剤、経口カルシニューリン阻害剤、または高効力もしくは経口コルチコステロイドを必要とする基礎症状の急性増悪の発生がない。
・特発性肺線維症、器質化肺炎(例えば、閉塞性細気管支炎)、薬物誘発性間質性肺炎、もしくは特発性間質性肺炎の病歴、またはスクリーニング胸部コンピュータ断層撮影(CT)スキャンでの活動性間質性肺炎の証拠
・放射線領域における放射線間質性肺炎(線維症)の既往歴は許容される
・活動性結核
・診断以外の処置前4週間以内の主要な外科的処置
・事前の同種異系幹細胞または固形臓器移植
・HBVのための抗ウイルス療法による現在の処置
・化学療法、免疫療法、生物学的療法、または3週間以内もしくは処置前の5回の薬物消失半減期のいずれか短い方の抗がん療法としての治験薬による処置;または内分泌感受性がん(例えば、前立腺がん、子宮内膜がん、ホルモン受容体陽性乳がん)に対するゴナドトロピン放出ホルモンアゴニストもしくはアンタゴニストを用いたホルモン療法を除く、処置前2週間以内の内分泌療法
・処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内の強力なCYP3A4阻害剤または強力なCYP3A4誘導剤による処置
・研究薬の開始に先立つ2週以内の治療用経口またはIV抗生物質による処置
・本研究で調査中のがんおよび転移または死亡のリスクが無視できる(例えば、5年OS率>90%)悪性腫瘍、例えば適切に処置された子宮頸部上皮内癌腫、非黒色腫皮膚癌腫、限局性前立腺がん、上皮内乳管癌腫、またはステージI子宮がんを除いて、スクリーニング前5年以内の悪性腫瘍の病歴
・異常なECGの病歴または存在
・処置前の4週間以内の弱毒化生ワクチンによる処置
・フリデリシアの式を使用することによって補正されたQT間隔(QTcF)>440msであり、少なくとも2つのECGが30分超離れていることによって実証される
・心室性不整脈の病歴または構造的心疾患(例えば、重症左室収縮機能不全、左室肥大)、冠動脈心疾患(症候性または診断試験によって実証された虚血を伴う)、臨床的に有意な電解質異常(例えば、低カリウム血症、低マグネシウム血症、低カルシウム血症)、または原因不明の突然死もしくはQT延長症候群の家族歴等の心室性不整脈の危険因子
・QT間隔を延ばすことが十分に知られた投薬による現在の処置
・研究薬の開始前の14日以内のH2遮断薬または制酸薬による処置または5回の薬物消失半減期のいずれか長い方
・処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内の軽度もしくは中程度のCYP3A4阻害剤または軽度もしくは中程度のCYP3A4誘導剤(詳細はセクション4.4.2.4を参照)による処置
・処置前の14日以内の任意の薬草療法による処置または5つの薬物消失半減期のうちのいずれか長い方
・症候性、未処置、または活発に進行する中枢神経系(CNS)転移。
・処置されたCNS病変を有する無症候性患者は、以下の基準の全てが満たされるならば適格である:
oRECIST v1.1による測定可能な疾患はCNS外に存在しなければならない。
o患者は頭蓋内出血または脊髄出血の病歴がない。
o患者は、処置前7日以内に定位放射線療法、処置前14日以内に全脳放射線療法、または処置前28日以内に神経外科的切除を受けていない
oCNS疾患の治療としてのコルチコステロイドの継続的な必要性はない。
o患者が抗痙攣療法を受けている場合、用量は安定であると見なされる。
o転移は小脳またはテント上領域に限定される(すなわち、中脳、橋、延髄、または脊髄への転移がない)。
oCNS向け処置の完了と研究処置の開始との間の中間進行の証拠はない。
・軟膜疾患または癌性髄膜炎
・スクリーニング眼科検査における、網膜静脈閉塞症(RVO)、中心性漿液性網膜症(CSR)、RVOもしくはCSRの素因、または網膜症を含む眼科疾患の病歴または所見
・制御されていない高血圧
・正常な施設内下限未満または50%未満の左室駆出率
・キメラもしくはヒト化抗体または融合タンパク質に対する重症アレルギーアナフィラキシー反応の病歴
・チャイニーズハムスター卵巣細胞生成物またはアテゾリズマブ製剤の任意の成分に対する既知の過敏症
・化合物1製剤の任意の成分に対する既知のアレルギーまたは過敏症
・制御されていない胸水、心膜滲出液、または反復性の排液治療を必要とする腹水(毎月1回またはより頻繁に)
・ウイルス性もしくはその他の肝炎、現在のアルコール乱用、または硬変を含む、臨床的に顕著な肝疾患の病歴
・制御されていないまたは症候性の高カルシウム血症(イオン化カルシウム>1.5mmol/L、カルシウム>12mg/dL、または補正カルシウム>ULN)
・重症筋無力症、筋炎、自己免疫性肝炎、全身性エリテマトーデス、関節リウマチ、炎症性腸疾患、抗リン脂質抗体症候群、ウェゲナー肉芽腫症、シェーグレン症候群、ギラン・バレー症候群、または多発性硬化症を含むがこれらに限定されない自己免疫疾患または免疫不全が活動が活動性であるもの、またはその病歴、ただし、以下を除く:
o甲状腺補充ホルモンを服用している自己免疫関連甲状腺機能低下症の既往歴を有する患者は、研究に適格である。
oインスリンレジメンを受けている、制御された1型糖尿病患者は研究に適格である。
o湿疹、乾癬、慢性単純性苔癬、または皮膚症状のみを伴う白斑(例えば、乾癬性関節炎を有する患者は除外される)を有する患者は、以下の条件の全てが満たされるならば、研究に適格である:
・発疹が覆っている体表面積は10%未満でなければならない
・疾患はベースラインで十分に制御されており、低効力の局所コルチコステロイドのみを必要とする
・過去12ヶ月以内にソラレン+紫外線A照射、メトトレキサート、レチノイド、生物学的薬剤、経口カルシニューリン阻害剤、または高効力もしくは経口コルチコステロイドを必要とする基礎症状の急性増悪の発生がない。
・特発性肺線維症、器質化肺炎(例えば、閉塞性細気管支炎)、薬物誘発性間質性肺炎、もしくは特発性間質性肺炎の病歴、またはスクリーニング胸部コンピュータ断層撮影(CT)スキャンでの活動性間質性肺炎の証拠
・放射線領域における放射線間質性肺炎(線維症)の既往歴は許容される
・活動性結核
・診断以外の処置前4週間以内の主要な外科的処置
・事前の同種異系幹細胞または固形臓器移植
・HBVのための抗ウイルス療法による現在の処置
・化学療法、免疫療法、生物学的療法、または3週間以内もしくは処置前の5回の薬物消失半減期のいずれか短い方の抗がん療法としての治験薬による処置;または内分泌感受性がん(例えば、前立腺がん、子宮内膜がん、ホルモン受容体陽性乳がん)に対するゴナドトロピン放出ホルモンアゴニストもしくはアンタゴニストを用いたホルモン療法を除く、処置前2週間以内の内分泌療法
・処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内の強力なCYP3A4阻害剤または強力なCYP3A4誘導剤による処置
・研究薬の開始に先立つ2週以内の治療用経口またはIV抗生物質による処置
・本研究で調査中のがんおよび転移または死亡のリスクが無視できる(例えば、5年OS率>90%)悪性腫瘍、例えば適切に処置された子宮頸部上皮内癌腫、非黒色腫皮膚癌腫、限局性前立腺がん、上皮内乳管癌腫、またはステージI子宮がんを除いて、スクリーニング前5年以内の悪性腫瘍の病歴
・異常なECGの病歴または存在
・処置前の4週間以内の弱毒化生ワクチンによる処置
・フリデリシアの式を使用することによって補正されたQT間隔(QTcF)>440msであり、少なくとも2つのECGが30分超離れていることによって実証される
・心室性不整脈の病歴または構造的心疾患(例えば、重症左室収縮機能不全、左室肥大)、冠動脈心疾患(症候性または診断試験によって実証された虚血を伴う)、臨床的に有意な電解質異常(例えば、低カリウム血症、低マグネシウム血症、低カルシウム血症)、または原因不明の突然死もしくはQT延長症候群の家族歴等の心室性不整脈の危険因子
・QT間隔を延ばすことが十分に知られた投薬による現在の処置
・研究薬の開始前の14日以内のH2遮断薬または制酸薬による処置または5回の薬物消失半減期のいずれか長い方
・処置前の14日以内または5回の薬物消失半減期のいずれか長い方の期間内の軽度もしくは中程度のCYP3A4阻害剤または軽度もしくは中程度のCYP3A4誘導剤(詳細はセクション4.4.2.4を参照)による処置
・処置前の14日以内の任意の薬草療法による処置または5つの薬物消失半減期のうちのいずれか長い方
以下の表に列挙される免疫不全または自己免疫疾患の病歴を有する患者は、研究への参加から除外される。この除外に対する可能な例外は、自己免疫疾患の臨床的疑いが低い、アトピー性疾患または小児関節痛等の実体の病歴を有する患者であり得る。安定した用量の甲状腺補充ホルモンを受ける自己免関連甲状腺機能低下症の病歴を有する患者は、この研究に適格であり得る。さらに、感染因子の処置時に消散した急性感染性疾患の一過性の自己免疫症状は排除されない(例えば、急性ライム関節炎)。
研究処置製剤、包装および取扱い。化合物1は、カプセル剤(10mgおよび25mg)および錠剤(20mg)として供給される。化合物1は、カプセル剤または錠剤の形態で経口投与される。処置期間中、化合物1は、各21日サイクルの1~21日目に毎日ほぼ同じ時間に服用しなければならない。カプセル剤または錠剤を、完全に嚥下しなければならず、噛んだり、砕いたり、開封したりしてはならない。服用し忘れた用量は、計画された投薬時間の4時間後まで投与され得る。化合物1の用量を服用し忘れた場合(すなわち、予定投薬時間後4時間以内に服用されなかった)、またはその用量を服用したときに嘔吐が起こった場合、次の予定された用量で投与を再開しなければならない。
別段の指示がない限り、化合物1を、約240mLの水と共に絶食状態(食事または軽食の1時間前または2時間後)に摂取しなければならない。患者は外来ベースで自己投与する。患者は、放射線写真データおよび臨床状態の統合評価後に治験責任医師によって決定される許容できない毒性または臨床的利益の喪失まで化合物1を受ける(詳細についてはセクション3.1.3を参照)。
アテゾリズマブは、1200mg/20mLバイアル内のIV製剤として供給される。アテゾリズマブは、化合物1の投与後、各21日サイクルの1日目に1200mgの固定用量でIV注入によって投与される。アテゾリズマブ投与の開始は、化合物1の経口投与後約30分でなければならない。アテゾリズマブの投与は、訓練された人員ならびに潜在的に重篤な反応を管理するための適切な機器および薬剤に直ちにアクセスできる監視された設定で行われる。アテゾリズマブ注入は、本明細書に概説される説明書に従って投与される。アテゾリズマブの用量変更は許可されない。
本明細書に記載の患者は、本明細書に記載の14日間の慣らし期間に参加し、そのような患者は、慣らし期間の1日目に840mgの固定用量でIV注入によって投与されるアテゾリズマブを受ける。用量設定段階および用量拡大段階の処置期間中、全ての患者は、許容できない毒性または臨床的利益の喪失まで、各21日サイクルの1日目に1200mgの固定用量でIV注入によって投与されるアテゾリズマブを受ける。
アテゾリズマブは、化合物1の投与後に投与される。アテゾリズマブ注入は、化合物1の投与の30分後に開始しなければならない。
アテゾリズマブの投与は、訓練された人員ならびに潜在的に重篤な反応を管理するための適切な機器および薬剤に直ちにアクセスできる監視された設定で行われる。アテゾリズマブ注入は、表3に概説される説明書に従って投与される。
許可された治療。患者は、研究中に以下の治療法を使用することが許される。
・経口避妊薬
・ホルモン補充療法
・予防的または治療的抗凝固療法(安定用量のワーファリンまたは低分子量ヘパリン等)
・しかしながら、生弱毒化ワクチンのワクチン接種は許可されていない
・酢酸メゲストロール
・ミネラルコルチコイド(例えば、フルドロコルチゾン)
・吸入または低用量コルチコステロイド
・低用量コルチコステロイド
・以下に概説する緩和的放射線療法(例えば、既知の骨転移の処置または疼痛の症候性軽減):
・抗ヒスタミン剤、解熱剤、および/または鎮痛剤による前投薬は、治験責任医師の裁量で、2回目以降のアテゾリズマブ注入のためにのみ投与され得る。
・経口避妊薬
・ホルモン補充療法
・予防的または治療的抗凝固療法(安定用量のワーファリンまたは低分子量ヘパリン等)
・しかしながら、生弱毒化ワクチンのワクチン接種は許可されていない
・酢酸メゲストロール
・ミネラルコルチコイド(例えば、フルドロコルチゾン)
・吸入または低用量コルチコステロイド
・低用量コルチコステロイド
・以下に概説する緩和的放射線療法(例えば、既知の骨転移の処置または疼痛の症候性軽減):
・抗ヒスタミン剤、解熱剤、および/または鎮痛剤による前投薬は、治験責任医師の裁量で、2回目以降のアテゾリズマブ注入のためにのみ投与され得る。
注入に関連する症状を経験する患者は、アセトアミノフェン、イブプロフェン、ジフェンヒドラミン、および/またはH2受容体アンタゴニスト(例えば、ファモチジン、シメチジン)、または現場の標準慣行による同等の薬物を用いた対症療法処置され得る。呼吸困難、低血圧症、喘鳴、気管支痙攣、頻脈、酸素飽和度低下、または呼吸促拍によって現れる重篤な点滴関連事象は、臨床的に適応がある支持療法(例えば、酸素補充およびb2アドレナリン作用性アゴニスト)によって管理されなければならない。
注意を要する治療。全身性コルチコステロイド、免疫抑制薬、およびTNF-a阻害剤は、アテゾリズマブによる処置の潜在的に有益な免疫学的効果を減弱させ得る。したがって、全身性コルチコステロイド、免疫抑制薬、またはTNF-a阻害剤が日常的に投与される状況では、抗ヒスタミン剤を含む代替物を検討しなければならない。
禁止される治療。以下の併用療法の使用は、以下に記載されるように禁止される:
・治験治療(治験実施計画書で定められた研究処置以外)は、処置前の3週間以内または5回の薬物消失半減期以内に禁止される。
・がんの処置を目的とした併用療法(限定されないが、化学療法、ホルモン療法、免疫療法、放射線療法、および薬草療法を含む)は、保健当局が承認しているか実験的であるかにかかわらず、処置前および処置中に禁止される。
・生ワクチン、弱毒化ワクチン
・全身免疫賦活剤(インターフェロンおよびIL-2を含むがこれらに限定されない)
・プロトンポンプ阻害剤
・カンナビジオール生成物
・強力なCYP3A4阻害剤または強力なCYP3A4誘導剤
・治験治療(治験実施計画書で定められた研究処置以外)は、処置前の3週間以内または5回の薬物消失半減期以内に禁止される。
・がんの処置を目的とした併用療法(限定されないが、化学療法、ホルモン療法、免疫療法、放射線療法、および薬草療法を含む)は、保健当局が承認しているか実験的であるかにかかわらず、処置前および処置中に禁止される。
・生ワクチン、弱毒化ワクチン
・全身免疫賦活剤(インターフェロンおよびIL-2を含むがこれらに限定されない)
・プロトンポンプ阻害剤
・カンナビジオール生成物
・強力なCYP3A4阻害剤または強力なCYP3A4誘導剤
慣らし期間中の全ての患者について、慣らし期間前の14日間または5回の薬物消失半減期のいずれか長い方の期間内に以下の併用療法の使用を禁止する。
・H2遮断薬および制酸薬
・軽度または中程度のCYP3A4阻害剤または軽度または中程度のCYP3A4誘導剤
・全ての薬草療法
・H2遮断薬および制酸薬
・軽度または中程度のCYP3A4阻害剤または軽度または中程度のCYP3A4誘導剤
・全ての薬草療法
化合物1に関連するリスク。化合物1の投与は、以下を含む可逆的かつ監視可能な事象に関連している:末梢浮腫、骨髄抑制(例えば、血小板減少症、貧血)、胃腸毒性(例えば、下痢、悪心および嘔吐)、肝トランスアミナーゼの上昇および発疹。
MAPK経路クラス阻害剤に関連するリスク。MAPK経路阻害剤の投与は、心筋症、網膜症、心筋症、CPK増加、血栓塞栓事象、光毒性、および生殖毒性に関連している。化合物1を用いた非臨床安全性試験は、心臓、肺、腎臓、血栓塞栓性または眼毒性の証拠を示さなかった。
アテゾリズマブに関連するリスク。アテゾリズマブは、以下のようなリスクと関連している:注入関連反応(IRR)および免疫介在性肝炎、間質性肺炎、大腸炎、膵炎、真性糖尿病、甲状腺機能低下症、甲状腺機能亢進症、副腎機能不全、下垂体炎、ギラン・バレー症候群、筋無力症症候群または重症筋無力症、髄膜脳炎、心筋炎、腎炎および筋炎。免疫介在性反応は、任意の器官系を伴い得、血球貪食性リンパ組織球症(HLH)およびマクロファージ活性化症候群(MAS)をもたらし得る。
有害事象。有害事象は、原因の属性にかかわらず、併用療法dhで本明細書に記載の薬剤を投与された臨床試験対象における任意の不都合な医学的事象を指すと本明細書で定義される。「重症」および「重篤」という用語は、同義語ではない。重症度とは、有害事象の強度(例えば、軽症、中等度、もしくは重症と評価されるかまたはNCI CTCAEによる;セクション5.3.3を参照)を指し、その事象自体は比較的軽微な医学的意義(例えば、それ以上の所見のない重症の頭痛)のものであってもよい。
監視すべき有害事象としては、末梢浮腫、下痢、呼吸困難、肝炎またはALTもしくはASTの上昇、間質性肺炎、何らかの血栓塞栓性事象、全身性エリテマトーデス、過敏症を示唆する事象(例えば、IRR、CRS、HLH、およびMAS)、腎炎、眼毒性(例えば、ブドウ膜炎、網膜炎、視神経炎)、心臓障害(例えば、心房細動、心筋炎、心膜炎)、血管炎、自己免疫性溶血性貧血および重症皮膚反応(例えば、スティーブンス・ジョンソン症候群、水疱性皮膚炎、中毒性表皮壊死症)が挙げられる。
本明細書および特許請求の範囲を通して、「含む(comprise/comprises、およびcomprising)という語は、文脈上矛盾する場合を除き、非限定的な意味で使用される。本明細書に記載の実施形態は、「からなる」および/または「から本質的になる」実施形態を含むものと理解される。
値の範囲が提供される場合、文脈が明確な別段の指示がない限り、範囲の上限および下限と、その記載された範囲内の任意の他の記載された値または介在する値との間の、下限の単位の10分の1までの各介在値が、本明細書に包含されるものと理解されたい。より小さい範囲に独立して含めることができるこれらの小さい範囲の上限および下限もまた、記載された範囲における具体的に除かれる限界値を条件として、本明細書に包含される。記載された範囲に限界値の一方または両方が含まれる場合、それらの含まれる限界値のいずれかまたは両方を除く範囲もまた、本明細書に含まれる。
本明細書に記載された発明の多くの修正および他の実施形態は、これらの発明が、前述の説明および関連する図面に提示された教示の恩恵を受けて関連する当業者には思い浮かぶであろう。したがって、本発明は、開示された具体的な実施形態に限定されるべきではなく、変更および他の実施形態は、添付の特許請求の範囲内に含まれることが意図されていることを理解されたい。本明細書には特定の用語が用いられているが、それらは包括的および説明的意味でのみ使用されているのであって、限定を目的としない。
Claims (69)
- 前記PD-L1結合アンタゴニストが、抗PD-L1抗体である、請求項1に記載の併用療法。
- 前記抗PD-L1抗体が、アテゾリズマブである、請求項1または2に記載の併用療法。
- 化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にQD投与され、アテゾリズマブが前記第1の21日サイクルの1日目に投与される、請求項3に記載の併用療法。
- 化合物1またはその薬学的に許容され得る塩が、第1の21日サイクルの1~21日目にBID投与され、アテゾリズマブが前記第1の21日サイクルの1日目に投与される、請求項3に記載の併用療法。
- 化合物1またはその薬学的に許容され得る塩が、錠剤またはカプセル剤として経口投与される、請求項1~5のいずれか一項に記載の併用療法。
- 化合物1またはその薬学的に許容され得る塩が約5mg~100mgの量で投与される、請求項1~6のいずれか一項に記載の併用療法。
- 化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、請求項1~7のいずれか一項に記載の併用療法。
- アテゾリズマブが、約800mg~約1400mgの量でQ3W投与される、請求項3~8のいずれか一項に記載の併用療法。
- アテゾリズマブが、各サイクルの1日目に約1200mgの量で投与される、請求項3~9のいずれか一項に記載の併用療法。
- 前記第1の21日サイクルの開始前に、化合物1またはその薬学的に許容され得る塩が投与され、続いてアテゾリズマブが840mgの量で投与される、請求項5~10のいずれか一項に記載の併用療法。
- 前記併用療法が、それを必要とする患者に投与され、前記患者が肺がん、頭頸部がん、または黒色腫を有する、請求項1~11のいずれか一項に記載の併用療法。
- 前記患者が、PD-L1陽性である、請求項12に記載の併用療法。
- 前記患者が、PD-L1-highである、請求項12または13に記載の併用療法。
- 前記患者が、PD-L1-lowである、請求項12~14のいずれか一項に記載の併用療法。
- 前記PD-L1陽性が、PD-L1免疫組織化学(IHC)アッセイによって判定される、請求項13~15のいずれか一項に記載の併用療法。
- 前記患者が、非小細胞肺がん(NSCLC)、頭頸部扁平上皮癌(HNSCC)、またはBRAF WT黒色腫を有する、請求項12~15のいずれか一項に記載の併用療法。
- 前記PD-L1結合アンタゴニストが、抗PD-L1抗体である、請求項18に記載の方法。
- 前記抗PD-L1抗体が、アテゾリズマブである、請求項18に記載の方法。
- 前記処置期間が、
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、請求項20に記載の方法。 - 前記処置期間が、
(a)第1の21日サイクルの1~21日目に化合物1またはその薬学的に許容され得る塩をBID投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む、請求項20に記載の方法。 - 化合物1またはその薬学的に許容され得る塩が、錠剤またはカプセル剤として経口投与される、請求項18~22のいずれか一項に記載の方法。
- 化合物1またはその薬学的に許容され得る塩が、約5mg~100mgの量で投与される、請求項18~23のいずれか一項に記載の方法。
- 化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、請求項18~24のいずれか一項に記載の方法。
- アテゾリズマブが、約800mg~約1400mgの量でQ3W投与される、請求項20~25のいずれか一項に記載の方法。
- アテゾリズマブが、各サイクルの1日目に約1200mgの量で投与される、請求項20~26のいずれか一項に記載の方法。
- 前記方法が、化合物1またはその薬学的に許容され得る塩を第1のサイクルの開始前に投与し、続いてアテゾリズマブを840mgの量で投与することを含む慣らし期間を更に含む、請求項20~27のいずれか一項に記載の方法。
- 前記慣らし期間が、1~14日間を含む、請求項28に記載の方法。
- 前記慣らし期間が14日間であり、化合物1またはその薬学的に許容され得る塩およびアテゾリズマブが前記慣らし期間の1日目に投与される、請求項28または29に記載の方法。
- 化合物1またはその薬学的に許容され得る塩が、前記慣らし期間の8日目から開始してQD投与される、請求項28または29に記載の方法。
- 前記患者がPD-L1陽性である、請求項18~28のいずれか一項に記載の方法。
- 前記患者がPD-L1-highである、請求項18~28または32のいずれか一項に記載の方法。
- 前記患者がPD-L1-lowである、請求項18~28または32~33のいずれか一項に記載の方法。
- 前記PD-L1陽性が、PD-L1免疫組織化学(IHC)アッセイによって判定される、請求項18~28または32~34のいずれか一項に記載の方法。
- 前記肺がんが、非小細胞肺がん(NSCLC)である、請求項18~35のいずれか一項に記載の方法。
- 前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、請求項18~35のいずれか一項に記載の方法。
- 前記黒色腫が、BRAF WT黒色腫である、請求項18~35のいずれか一項に記載の方法。
- 肺がん、頭頸部がん、または黒色腫の処置を必要とする患者における肺がん、頭頸部がん、または黒色腫を処置する方法であって、有効量の化合物1またはその薬学的に許容され得る塩と、PD-L1結合アンタゴニストとを含む処置レジメンを前記患者に投与することを含む、方法。
- 前記PD-L1結合アンタゴニストが、抗PD-L1抗体である、請求項39に記載の方法。
- 前記抗PD-L1抗体が、アテゾリズマブである、請求項39または40に記載の方法。
- (a)化合物1またはその薬学的に許容され得る塩が、前記第1の21日サイクルの1~21日目に約5mg~100mgの量でQD投与され、
(b)アテゾリズマブが、前記第1の21日サイクルの1日目に1200mgの量で投与される、
請求項41に記載の方法。 - 化合物1またはその薬学的に許容され得る塩が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、請求項39~42のいずれか一項に記載の方法。
- 前記肺がんが、非小細胞肺がん(NSCLC)である、請求項39~43のいずれか一項に記載の方法。
- 前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、請求項39~43のいずれか一項に記載の方法。
- 前記黒色腫が、BRAFT WT黒色腫である、請求項39~43のいずれか一項に記載の方法。
- 本明細書に記載の肺がん、頭頸部がん、または黒色腫を処置するための、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む併用療法の使用。
- (a)化合物1またはその薬学的に許容され得る塩を第1の21日サイクルの1~21日目にQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を含む投薬レジメンを更に含む、請求項47に記載の使用。 - (a)約50mg~500mgの化合物1またはその薬学的に許容され得る塩を第1の21日サイクルの1~21日目にQD投与することと、
(b)約1200mgのアテゾリズマブを前記第1の21日サイクルの1日目に投与することと、
を更に含む、請求項47または48に記載の使用。 - 肺がん、頭頸部がん、または黒色腫を処置するための医薬品を製造するための、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む併用療法の使用。
- (a)化合物1またはその薬学的に許容され得る塩を第1の21日サイクルの1~21日目にQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブをQ3W投与することと、
を更に含む、請求項50に記載の使用。 - (a)化合物1またはその薬学的に許容され得る塩を第1の21日サイクルの1~21日目にQD投与することと、
(b)前記第1の21日サイクルの1日目にアテゾリズマブを投与することと、
を更に含む、請求項50または51に記載の使用。 - (a)約50mg~500mgの化合物1またはその薬学的に許容され得る塩を第1の21日サイクルの1~21日目にQD投与することと、
(b)約1200mgのアテゾリズマブを前記第1の21日サイクルの1日目に投与することと、
を更に含む、請求項50~52のいずれか一項に記載の使用。 - 投薬レジメンが、2サイクル以上を含む、請求項50~53のいずれか一項に記載の使用。
- 化合物1が、約5mg~100mgの量で投与される、請求項47~54のいずれか一項に記載の使用。
- 化合物1が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、請求項47~55のいずれか一項に記載の使用。
- 前記肺がんが、非小細胞肺がん(NSCLC)である、請求項47~56のいずれか一項に記載の使用。
- 前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、請求項47~56のいずれか一項に記載の使用。
- 前記黒色腫が、BRAFT WT黒色腫である、請求項47~56のいずれか一項に記載の使用。
- 肺がん、頭頸部がん、または黒色腫の処置における使用のための、化合物1またはその薬学的に許容され得る塩とアテゾリズマブとを含む、併用療法。
- (a)化合物1またはその薬学的に許容され得る塩が第1の21日サイクルの1~21日目にQD投与され、
(b)アテゾリズマブが前記第1の21日サイクルの1日目にQ3W投与される、
請求項60に記載の併用療法。 - (a)化合物1またはその薬学的に許容され得る塩が第1の21日サイクルの1~21日目にQD投与され、
(b)アテゾリズマブが前記第1の21日サイクルの1日目に投与される、
請求項60または61に記載の併用療法。 - (a)約50mg~500mgの化合物1またはその薬学的に許容され得る塩が第1の21日サイクルの1~21日目にQD投与され、
(b)約1200mgのアテゾリズマブが前記第1の21日サイクルの1日目に投与される、
請求項60~62のいずれか一項に記載の方法。 - 投薬レジメンが、2サイクル以上を含む、請求項60~63のいずれか一項に記載の併用療法。
- 化合物1が、約5mg~100mgの量で投与される、請求項60~64のいずれか一項に記載の併用療法。
- 化合物1が、約5mg、10mg、20mg、40mg、60mg、80mgまたは100mgの量で投与される、請求項60~65のいずれか一項に記載の併用療法。
- 前記肺がんが、非小細胞肺がん(NSCLC)である、請求項60~66のいずれか一項に記載の併用療法。
- 前記頭頸部がんが、頭頸部扁平上皮癌(HNSCC)である、請求項60~66のいずれか一項に記載の併用療法。
- 前記黒色腫が、BRAFT WT黒色腫である、請求項60~66のいずれか一項に記載の併用療法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202263341361P | 2022-05-12 | 2022-05-12 | |
| US63/341,361 | 2022-05-12 | ||
| PCT/US2023/066920 WO2023220703A1 (en) | 2022-05-12 | 2023-05-12 | Methods and compositions comprising a shp2 inhibitor and a pd-l1 binding antagonist |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2025516649A true JP2025516649A (ja) | 2025-05-30 |
Family
ID=86710772
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024566593A Pending JP2025516649A (ja) | 2022-05-12 | 2023-05-12 | Shp2阻害剤およびpd-l1結合アンタゴニストを含む方法および組成物 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20250312339A1 (ja) |
| EP (1) | EP4522173A1 (ja) |
| JP (1) | JP2025516649A (ja) |
| KR (1) | KR20250012585A (ja) |
| CN (1) | CN119183377A (ja) |
| AR (1) | AR129314A1 (ja) |
| AU (1) | AU2023269154A1 (ja) |
| CA (1) | CA3248752A1 (ja) |
| TW (1) | TW202408523A (ja) |
| WO (1) | WO2023220703A1 (ja) |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104356236B (zh) | 2005-07-01 | 2020-07-03 | E.R.施贵宝&圣斯有限责任公司 | 抗程序性死亡配体1(pd-l1)的人单克隆抗体 |
| EP4331604B9 (en) | 2008-12-09 | 2025-07-23 | F. Hoffmann-La Roche AG | Anti-pd-l1 antibodies and their use to enhance t-cell function |
| CA2778714C (en) | 2009-11-24 | 2018-02-27 | Medimmune Limited | Targeted binding agents against b7-h1 |
| PT2699264T (pt) | 2011-04-20 | 2018-05-23 | Medimmune Llc | Anticorpos e outras moléculas que ligam b7-h1 e pd-1 |
| JP2015519375A (ja) | 2012-05-31 | 2015-07-09 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Pd−l1に結合する抗原結合蛋白質 |
| CN110156892B (zh) | 2014-07-03 | 2023-05-16 | 百济神州有限公司 | 抗pd-l1抗体及其作为治疗剂及诊断剂的用途 |
| JP6877339B2 (ja) | 2014-10-14 | 2021-05-26 | ノバルティス アーゲー | Pd−l1に対する抗体分子およびその使用 |
| HRP20201900T4 (hr) | 2015-05-12 | 2024-06-07 | F. Hoffmann - La Roche Ag | Terapeutski i dijagnostički postupci kod raka |
| IL294138A (en) | 2015-05-29 | 2022-08-01 | Genentech Inc | Therapeutic and diagnostic methods for cancer |
| KR20210089716A (ko) * | 2018-11-07 | 2021-07-16 | 상하이 린진 바이오파마 씨오., 엘티디. | 질소 함유 축합 헤테로고리 shp2억제제 화합물, 제조방법 및 용도 |
| KR20220066923A (ko) * | 2019-09-24 | 2022-05-24 | 릴레이 테라퓨틱스, 인크. | Shp2 포스파테이스 억제제 및 이의 제조 및 사용 방법 |
-
2023
- 2023-05-12 CN CN202380040108.0A patent/CN119183377A/zh active Pending
- 2023-05-12 KR KR1020247040965A patent/KR20250012585A/ko active Pending
- 2023-05-12 EP EP23729279.2A patent/EP4522173A1/en active Pending
- 2023-05-12 CA CA3248752A patent/CA3248752A1/en active Pending
- 2023-05-12 JP JP2024566593A patent/JP2025516649A/ja active Pending
- 2023-05-12 TW TW112117719A patent/TW202408523A/zh unknown
- 2023-05-12 US US18/864,984 patent/US20250312339A1/en active Pending
- 2023-05-12 AR ARP230101183A patent/AR129314A1/es unknown
- 2023-05-12 AU AU2023269154A patent/AU2023269154A1/en active Pending
- 2023-05-12 WO PCT/US2023/066920 patent/WO2023220703A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2023220703A1 (en) | 2023-11-16 |
| TW202408523A (zh) | 2024-03-01 |
| US20250312339A1 (en) | 2025-10-09 |
| EP4522173A1 (en) | 2025-03-19 |
| AU2023269154A1 (en) | 2024-10-10 |
| KR20250012585A (ko) | 2025-01-24 |
| AR129314A1 (es) | 2024-08-14 |
| CN119183377A (zh) | 2024-12-24 |
| CA3248752A1 (en) | 2023-11-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7749667B2 (ja) | 肺がんを治療するためのkrasg12c阻害剤及びpd-l1結合アンタゴニストを含む方法及び組成物 | |
| US12409178B2 (en) | Methods and compositions comprising a KRasG12C inhibitor and a VEGF inhibitor for treating solid tumors | |
| AU2021397214B2 (en) | Methods and compositions comprising a krasg12c inhibitor and a egfr-inhibitor for treating solid tumors | |
| JP2024529451A (ja) | がんを治療するための方法及び組成物 | |
| JP2025516649A (ja) | Shp2阻害剤およびpd-l1結合アンタゴニストを含む方法および組成物 | |
| KR20240028452A (ko) | 암을 치료하기 위한 방법 및 조성물 | |
| US20230090868A1 (en) | Anti-cd30 antibody-drug conjugates and their use for the treatment of non-hodgkin lymphoma | |
| HK40113732A (zh) | 包含shp2抑制剂和pd-l1结合拮抗剂的方法和组合物 | |
| HK40093627A (zh) | 用於治疗肺癌的方法以及包含krasg12c抑制剂和pd-l1结合拮抗剂的组合物 | |
| WO2023144973A1 (ja) | 抗vegf抗体及びパクリタキセルと組み合わせて使用する抗pd-l1抗体を含む医薬組成物 | |
| HK40109234A (zh) | 用於治疗癌症的方法和组合物 | |
| EA048671B1 (ru) | Конъюгаты антител к тканевому фактору с лекарственными средствами и их применение при лечении рака |