JP2007500686A - 新規の6−フェニルフェナントリジン - Google Patents
新規の6−フェニルフェナントリジン Download PDFInfo
- Publication number
- JP2007500686A JP2007500686A JP2006521590A JP2006521590A JP2007500686A JP 2007500686 A JP2007500686 A JP 2007500686A JP 2006521590 A JP2006521590 A JP 2006521590A JP 2006521590 A JP2006521590 A JP 2006521590A JP 2007500686 A JP2007500686 A JP 2007500686A
- Authority
- JP
- Japan
- Prior art keywords
- phenyl
- hydrogen
- substituted
- alkoxy
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- XXWONCALJGBUFK-UHFFFAOYSA-N 6-phenylphenanthridine Chemical compound C1=CC=CC=C1C1=NC2=CC=CC=C2C2=CC=CC=C12 XXWONCALJGBUFK-UHFFFAOYSA-N 0.000 title description 5
- 150000001875 compounds Chemical class 0.000 claims abstract description 144
- 229910052739 hydrogen Inorganic materials 0.000 claims description 60
- 239000001257 hydrogen Substances 0.000 claims description 60
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 53
- -1 C 1 -C 4 - alkyl Chemical group 0.000 claims description 46
- 150000003839 salts Chemical class 0.000 claims description 39
- 150000002431 hydrogen Chemical group 0.000 claims description 25
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 25
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 17
- 238000011282 treatment Methods 0.000 claims description 17
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 16
- 238000000034 method Methods 0.000 claims description 16
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 16
- 229910052736 halogen Inorganic materials 0.000 claims description 15
- 150000002367 halogens Chemical group 0.000 claims description 15
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 14
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 14
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 13
- 239000008194 pharmaceutical composition Substances 0.000 claims description 13
- 125000004104 aryloxy group Chemical group 0.000 claims description 12
- 201000010099 disease Diseases 0.000 claims description 12
- 125000003118 aryl group Chemical group 0.000 claims description 8
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 8
- 229910052757 nitrogen Inorganic materials 0.000 claims description 8
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 7
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 7
- 230000002265 prevention Effects 0.000 claims description 7
- 125000000217 alkyl group Chemical group 0.000 claims description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 6
- 238000004519 manufacturing process Methods 0.000 claims description 6
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 claims description 6
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 5
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 5
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 claims description 4
- 229910052801 chlorine Inorganic materials 0.000 claims description 4
- 125000005002 aryl methyl group Chemical group 0.000 claims description 3
- 239000000460 chlorine Substances 0.000 claims description 3
- 125000001153 fluoro group Chemical group F* 0.000 claims description 3
- 125000004076 pyridyl group Chemical group 0.000 claims description 3
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 claims description 2
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 claims description 2
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 claims description 2
- 125000006283 4-chlorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1Cl)C([H])([H])* 0.000 claims description 2
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims description 2
- 125000004195 4-methylpiperazin-1-yl group Chemical group [H]C([H])([H])N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000004199 4-trifluoromethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C(F)(F)F 0.000 claims description 2
- YSNIPFQCRHRGSO-UHFFFAOYSA-N 5-[[6-chloro-5-[4-(2-hydroxyphenyl)phenyl]-1H-benzimidazol-2-yl]oxy]-N-hydroxy-2-methylbenzamide Chemical compound ClC=1C(=CC2=C(NC(=N2)OC=2C=CC(=C(C(=O)NO)C=2)C)C=1)C1=CC=C(C=C1)C1=C(C=CC=C1)O YSNIPFQCRHRGSO-UHFFFAOYSA-N 0.000 claims description 2
- 125000005083 alkoxyalkoxy group Chemical group 0.000 claims description 2
- 125000005530 alkylenedioxy group Chemical group 0.000 claims description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 2
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 2
- 125000002757 morpholinyl group Chemical group 0.000 claims description 2
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 claims description 2
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 claims description 2
- 229940124531 pharmaceutical excipient Drugs 0.000 claims description 2
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 230000000241 respiratory effect Effects 0.000 claims description 2
- 208000018569 Respiratory Tract disease Diseases 0.000 claims 1
- 239000003937 drug carrier Substances 0.000 claims 1
- 239000003112 inhibitor Substances 0.000 abstract description 8
- 101100296719 Caenorhabditis elegans pde-4 gene Proteins 0.000 abstract 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 48
- 102000004861 Phosphoric Diester Hydrolases Human genes 0.000 description 20
- 108090001050 Phosphoric Diester Hydrolases Proteins 0.000 description 20
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 18
- 239000000203 mixture Substances 0.000 description 17
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 239000002904 solvent Substances 0.000 description 13
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 12
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 10
- 230000005764 inhibitory process Effects 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 238000002844 melting Methods 0.000 description 9
- 230000008018 melting Effects 0.000 description 9
- 239000002253 acid Substances 0.000 description 8
- 230000003287 optical effect Effects 0.000 description 8
- BIVMWDQSMDXTCT-VXGBXAGGSA-N (1r,2r)-2-(3,4-dimethoxyphenyl)cyclohexan-1-amine Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H]1[C@H](N)CCCC1 BIVMWDQSMDXTCT-VXGBXAGGSA-N 0.000 description 7
- 239000000443 aerosol Substances 0.000 description 7
- 238000003556 assay Methods 0.000 description 7
- 239000002585 base Substances 0.000 description 7
- 239000007858 starting material Substances 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- IVOMOUWHDPKRLL-KQYNXXCUSA-N Cyclic adenosine monophosphate Chemical compound C([C@H]1O2)OP(O)(=O)O[C@H]1[C@@H](O)[C@@H]2N1C(N=CN=C2N)=C2N=C1 IVOMOUWHDPKRLL-KQYNXXCUSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- IVOMOUWHDPKRLL-UHFFFAOYSA-N UNPD107823 Natural products O1C2COP(O)(=O)OC2C(O)C1N1C(N=CN=C2N)=C2N=C1 IVOMOUWHDPKRLL-UHFFFAOYSA-N 0.000 description 6
- 208000010668 atopic eczema Diseases 0.000 description 6
- 229940095074 cyclic amp Drugs 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- CKUUWZSXSMTFIO-RYUDHWBXSA-N 1,2-dimethoxy-4-[(1s,2s)-2-nitrocyclohexyl]benzene Chemical compound C1=C(OC)C(OC)=CC=C1[C@H]1[C@@H]([N+]([O-])=O)CCCC1 CKUUWZSXSMTFIO-RYUDHWBXSA-N 0.000 description 5
- 239000000706 filtrate Substances 0.000 description 5
- 239000005022 packaging material Substances 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- 125000003762 3,4-dimethoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 229960000583 acetic acid Drugs 0.000 description 4
- 230000000172 allergic effect Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 238000000921 elemental analysis Methods 0.000 description 4
- 230000002401 inhibitory effect Effects 0.000 description 4
- 239000000825 pharmaceutical preparation Substances 0.000 description 4
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 125000006239 protecting group Chemical group 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 208000017520 skin disease Diseases 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- SYJMYDMKPSZMSB-AATRIKPKSA-N 1,2-dimethoxy-4-[(e)-2-nitroethenyl]benzene Chemical compound COC1=CC=C(\C=C\[N+]([O-])=O)C=C1OC SYJMYDMKPSZMSB-AATRIKPKSA-N 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- FVZFPSTZUVPBRE-DNQXCXABSA-N 4-benzoyl-n-[(1r,2r)-2-(3,4-dimethoxyphenyl)cyclohexyl]benzamide Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H]1[C@H](NC(=O)C=2C=CC(=CC=2)C(=O)C=2C=CC=CC=2)CCCC1 FVZFPSTZUVPBRE-DNQXCXABSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 229940123932 Phosphodiesterase 4 inhibitor Drugs 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000003431 cross linking reagent Substances 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 230000004054 inflammatory process Effects 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000003208 petroleum Substances 0.000 description 3
- 229940127557 pharmaceutical product Drugs 0.000 description 3
- 239000002587 phosphodiesterase IV inhibitor Substances 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 210000002345 respiratory system Anatomy 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 102000003390 tumor necrosis factor Human genes 0.000 description 3
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 2
- CKUUWZSXSMTFIO-VXGBXAGGSA-N 1,2-dimethoxy-4-[(1r,2r)-2-nitrocyclohexyl]benzene Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H]1[C@H]([N+]([O-])=O)CCCC1 CKUUWZSXSMTFIO-VXGBXAGGSA-N 0.000 description 2
- HFGWXWJFQQCBEY-VXGBXAGGSA-N 1,2-dimethoxy-4-[(1r,6r)-6-nitrocyclohex-3-en-1-yl]benzene Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H]1[C@H]([N+]([O-])=O)CC=CC1 HFGWXWJFQQCBEY-VXGBXAGGSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 2
- 208000002874 Acne Vulgaris Diseases 0.000 description 2
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 2
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- 0 CC(C1c2c3cc(*)c(*)c2)C(*)(*)C(*)(*)C(*)C1N=C3/C(/C=C1)=C/*(*)/C=C/[C@]1(C)C(*)=NO* Chemical compound CC(C1c2c3cc(*)c(*)c2)C(*)(*)C(*)(*)C(*)C1N=C3/C(/C=C1)=C/*(*)/C=C/[C@]1(C)C(*)=NO* 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 101100135868 Dictyostelium discoideum pde3 gene Proteins 0.000 description 2
- 208000010228 Erectile Dysfunction Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 2
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 2
- 206010040070 Septic Shock Diseases 0.000 description 2
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 2
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 2
- 235000011054 acetic acid Nutrition 0.000 description 2
- 206010000496 acne Diseases 0.000 description 2
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 2
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 150000001718 carbodiimides Chemical class 0.000 description 2
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 150000008280 chlorinated hydrocarbons Chemical class 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 210000001508 eye Anatomy 0.000 description 2
- 238000005755 formation reaction Methods 0.000 description 2
- 239000012362 glacial acetic acid Substances 0.000 description 2
- 208000019622 heart disease Diseases 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 208000026278 immune system disease Diseases 0.000 description 2
- 201000001881 impotence Diseases 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 239000012442 inert solvent Substances 0.000 description 2
- 229940047124 interferons Drugs 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 238000011835 investigation Methods 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000001630 malic acid Substances 0.000 description 2
- 235000011090 malic acid Nutrition 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000006199 nebulizer Substances 0.000 description 2
- 210000000440 neutrophil Anatomy 0.000 description 2
- 150000002923 oximes Chemical class 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- 239000003380 propellant Substances 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 238000000967 suction filtration Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 235000002906 tartaric acid Nutrition 0.000 description 2
- 239000011975 tartaric acid Substances 0.000 description 2
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 125000005500 uronium group Chemical group 0.000 description 2
- WJUFSDZVCOTFON-UHFFFAOYSA-N veratraldehyde Chemical compound COC1=CC=C(C=O)C=C1OC WJUFSDZVCOTFON-UHFFFAOYSA-N 0.000 description 2
- BIVMWDQSMDXTCT-RYUDHWBXSA-N (1s,2s)-2-(3,4-dimethoxyphenyl)cyclohexan-1-amine Chemical compound C1=C(OC)C(OC)=CC=C1[C@H]1[C@@H](N)CCCC1 BIVMWDQSMDXTCT-RYUDHWBXSA-N 0.000 description 1
- XUJHKPSBHDQIOD-UHFFFAOYSA-N (2-bromo-7,7-dimethyl-3-oxo-4-bicyclo[2.2.1]heptanyl)methanesulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)C(Br)C1C2(C)C XUJHKPSBHDQIOD-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- NWZSZGALRFJKBT-KNIFDHDWSA-N (2s)-2,6-diaminohexanoic acid;(2s)-2-hydroxybutanedioic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O.NCCCC[C@H](N)C(O)=O NWZSZGALRFJKBT-KNIFDHDWSA-N 0.000 description 1
- AAWZDTNXLSGCEK-LNVDRNJUSA-N (3r,5r)-1,3,4,5-tetrahydroxycyclohexane-1-carboxylic acid Chemical compound O[C@@H]1CC(O)(C(O)=O)C[C@@H](O)C1O AAWZDTNXLSGCEK-LNVDRNJUSA-N 0.000 description 1
- IWYDHOAUDWTVEP-SSDOTTSWSA-N (R)-mandelic acid Chemical compound OC(=O)[C@H](O)C1=CC=CC=C1 IWYDHOAUDWTVEP-SSDOTTSWSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- USVVENVKYJZFMW-ONEGZZNKSA-N (e)-carboxyiminocarbamic acid Chemical class OC(=O)\N=N\C(O)=O USVVENVKYJZFMW-ONEGZZNKSA-N 0.000 description 1
- 125000004815 1,2-dimethylethylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([*:2])C([H])([H])[H] 0.000 description 1
- QTCAZWCRONJAQN-ZJSXRUAMSA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-(2-methylpropoxy)ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C1=CC=CC(C(C)=NOCC(C)C)=C1 QTCAZWCRONJAQN-ZJSXRUAMSA-N 0.000 description 1
- IAABRTXCOVUUMR-SHQCIBLASA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(3-chlorophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC1=CC=CC(Cl)=C1 IAABRTXCOVUUMR-SHQCIBLASA-N 0.000 description 1
- HDHWZPFGVGMLIQ-SHQCIBLASA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(3-fluorophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC1=CC=CC(F)=C1 HDHWZPFGVGMLIQ-SHQCIBLASA-N 0.000 description 1
- OYOWPARFPFXBIA-SHQCIBLASA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(4-chlorophenyl)methoxy]ethanimine Chemical compound ClC1=CC=C(CON=C(C)C2=CC(=CC=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=C1 OYOWPARFPFXBIA-SHQCIBLASA-N 0.000 description 1
- OXVQDFCAPSGXOZ-LEAFIULHSA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(4-methoxyphenyl)methoxy]ethanimine Chemical compound C1=CC(OC)=CC=C1CON=C(C)C1=CC=CC(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)=C1 OXVQDFCAPSGXOZ-LEAFIULHSA-N 0.000 description 1
- RELCRCRJGCNAFU-SHQCIBLASA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(4-nitrophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC1=CC=C([N+]([O-])=O)C=C1 RELCRCRJGCNAFU-SHQCIBLASA-N 0.000 description 1
- FTNOYSVAWGDPCG-LEAFIULHSA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[2-[3-(trifluoromethyl)phenoxy]ethoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCCOC1=CC=CC(C(F)(F)F)=C1 FTNOYSVAWGDPCG-LEAFIULHSA-N 0.000 description 1
- KJWIQARDXHFSLY-WIYYLYMNSA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-methoxyethanimine Chemical compound CON=C(C)C1=CC=CC(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)=C1 KJWIQARDXHFSLY-WIYYLYMNSA-N 0.000 description 1
- WCVINGMEQIELNQ-SHQCIBLASA-N 1-[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-phenylmethoxyethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC1=CC=CC=C1 WCVINGMEQIELNQ-SHQCIBLASA-N 0.000 description 1
- UGXLKVSPFXZPLM-LEAFIULHSA-N 1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-n-[(3-methoxyphenyl)methoxy]ethanimine Chemical compound COC1=CC=CC(CON=C(C)C=2C=C(C=CC=2)C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)=C1 UGXLKVSPFXZPLM-LEAFIULHSA-N 0.000 description 1
- CDXVFZNKWYKDGZ-SHQCIBLASA-N 1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-n-[[4-(trifluoromethyl)phenyl]methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC1=CC=C(C(F)(F)F)C=C1 CDXVFZNKWYKDGZ-SHQCIBLASA-N 0.000 description 1
- FICVABVZKOEDLK-YIXXDRMTSA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(2-chlorophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=CC=C1Cl FICVABVZKOEDLK-YIXXDRMTSA-N 0.000 description 1
- SHVREFRBJPEMHJ-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(2-methoxyphenyl)methoxy]ethanimine Chemical compound COC1=CC=CC=C1CON=C(C)C1=CC=C(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)C=C1 SHVREFRBJPEMHJ-SHQCIBLASA-N 0.000 description 1
- LHJFGOQHBVSMMJ-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(3-fluorophenyl)methoxy]ethanimine Chemical compound FC=1C=C(CON=C(C)C2=CC=C(C=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=CC1 LHJFGOQHBVSMMJ-SHQCIBLASA-N 0.000 description 1
- DNZUWSYNFJLURA-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[(4-nitrophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=C([N+]([O-])=O)C=C1 DNZUWSYNFJLURA-SHQCIBLASA-N 0.000 description 1
- LPVJGWHRNGRILF-LEAFIULHSA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[2-[3-(trifluoromethyl)phenoxy]ethoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCCOC1=CC=CC(C(F)(F)F)=C1 LPVJGWHRNGRILF-LEAFIULHSA-N 0.000 description 1
- JFWPSCITBRDORA-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[[3-(trifluoromethyl)phenyl]methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=CC(C(F)(F)F)=C1 JFWPSCITBRDORA-SHQCIBLASA-N 0.000 description 1
- XAZIGVPDNLRKFS-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-[[4-(trifluoromethyl)phenyl]methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=C(C(F)(F)F)C=C1 XAZIGVPDNLRKFS-SHQCIBLASA-N 0.000 description 1
- LPCZTURZPMZHSN-DENIHFKCSA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-ethoxyethanimine Chemical compound C1=CC(C(C)=NOCC)=CC=C1C(C1=CC(OC)=C(OC)C=C11)=N[C@H]2[C@@H]1CCCC2 LPCZTURZPMZHSN-DENIHFKCSA-N 0.000 description 1
- COXPHOSUGJYSMR-WIYYLYMNSA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-methoxyethanimine Chemical compound C1=CC(C(C)=NOC)=CC=C1C(C1=CC(OC)=C(OC)C=C11)=N[C@H]2[C@@H]1CCCC2 COXPHOSUGJYSMR-WIYYLYMNSA-N 0.000 description 1
- VTGZCMVKPJNHLJ-ZEQKJWHPSA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-phenoxyethanimine Chemical compound C1(=CC=CC=C1)ON=C(C)C1=CC=C(C=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC VTGZCMVKPJNHLJ-ZEQKJWHPSA-N 0.000 description 1
- UHUYCQAVDIHCHQ-SHQCIBLASA-N 1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-N-phenylmethoxyethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=CC=C1 UHUYCQAVDIHCHQ-SHQCIBLASA-N 0.000 description 1
- MJOWZIUMLHAMBR-ZJSXRUAMSA-N 1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-n-(2-methylpropoxy)ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C1=CC=C(C(C)=NOCC(C)C)C=C1 MJOWZIUMLHAMBR-ZJSXRUAMSA-N 0.000 description 1
- XUQJUCBQRWUIDT-LEAFIULHSA-N 1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-n-(2-phenoxyethoxy)ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCCOC1=CC=CC=C1 XUQJUCBQRWUIDT-LEAFIULHSA-N 0.000 description 1
- UCWLRLJRKQYKQC-SHQCIBLASA-N 1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-n-[(4-chlorophenyl)methoxy]ethanimine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=C(Cl)C=C1 UCWLRLJRKQYKQC-SHQCIBLASA-N 0.000 description 1
- YGTUPRIZNBMOFV-UHFFFAOYSA-N 2-(4-hydroxybenzoyl)benzoic acid Chemical compound OC(=O)C1=CC=CC=C1C(=O)C1=CC=C(O)C=C1 YGTUPRIZNBMOFV-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- HVAUUPRFYPCOCA-AREMUKBSSA-N 2-O-acetyl-1-O-hexadecyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCOC[C@@H](OC(C)=O)COP([O-])(=O)OCC[N+](C)(C)C HVAUUPRFYPCOCA-AREMUKBSSA-N 0.000 description 1
- UVDWQLRXDVCEJQ-GRKNLSHJSA-N 2-[1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-1-(4-phenylpiperazin-1-yl)ethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC(=O)N(CC1)CCN1C1=CC=CC=C1 UVDWQLRXDVCEJQ-GRKNLSHJSA-N 0.000 description 1
- KOJQZFUMEHKRDM-RCZVLFRGSA-N 2-[1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-1-morpholin-4-ylethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC(=O)N1CCOCC1 KOJQZFUMEHKRDM-RCZVLFRGSA-N 0.000 description 1
- USNWPYXVAUAMLH-ZEQKJWHPSA-N 2-[1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-n-(2-methoxyphenyl)acetamide Chemical compound COC1=CC=CC=C1NC(=O)CON=C(C)C1=CC=CC(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)=C1 USNWPYXVAUAMLH-ZEQKJWHPSA-N 0.000 description 1
- HDUVLUDNIFXJBY-LEAFIULHSA-N 2-[1-[3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-n-[(4-chlorophenyl)methyl]acetamide Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(C)=NOCC(=O)NCC1=CC=C(Cl)C=C1 HDUVLUDNIFXJBY-LEAFIULHSA-N 0.000 description 1
- PENUOFMFIFNBKK-GRKNLSHJSA-N 2-[1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-1-(4-phenylpiperazin-1-yl)ethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC(=O)N(CC1)CCN1C1=CC=CC=C1 PENUOFMFIFNBKK-GRKNLSHJSA-N 0.000 description 1
- NRXVHBSKCVOVEG-RCZVLFRGSA-N 2-[1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-1-morpholin-4-ylethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC(=O)N1CCOCC1 NRXVHBSKCVOVEG-RCZVLFRGSA-N 0.000 description 1
- DYTVVSNRZLMFBZ-ZEQKJWHPSA-N 2-[1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxy-n-(2-methoxyphenyl)acetamide Chemical compound COC1=CC=CC=C1NC(=O)CON=C(C)C1=CC=C(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)C=C1 DYTVVSNRZLMFBZ-ZEQKJWHPSA-N 0.000 description 1
- WXHLLJAMBQLULT-UHFFFAOYSA-N 2-[[6-[4-(2-hydroxyethyl)piperazin-1-yl]-2-methylpyrimidin-4-yl]amino]-n-(2-methyl-6-sulfanylphenyl)-1,3-thiazole-5-carboxamide;hydrate Chemical compound O.C=1C(N2CCN(CCO)CC2)=NC(C)=NC=1NC(S1)=NC=C1C(=O)NC1=C(C)C=CC=C1S WXHLLJAMBQLULT-UHFFFAOYSA-N 0.000 description 1
- UOXJNGFFPMOZDM-UHFFFAOYSA-N 2-[di(propan-2-yl)amino]ethylsulfanyl-methylphosphinic acid Chemical compound CC(C)N(C(C)C)CCSP(C)(O)=O UOXJNGFFPMOZDM-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- NPFVRBCDMFKOPY-UHFFFAOYSA-N 3-(4-imidazol-1-ylthiophen-2-yl)-4-methyl-4,5-dihydro-1h-pyridazin-6-one Chemical compound CC1CC(=O)NN=C1C1=CC(N2C=NC=C2)=CS1 NPFVRBCDMFKOPY-UHFFFAOYSA-N 0.000 description 1
- ALKYHXVLJMQRLQ-UHFFFAOYSA-N 3-Hydroxy-2-naphthoate Chemical compound C1=CC=C2C=C(O)C(C(=O)O)=CC2=C1 ALKYHXVLJMQRLQ-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- SQDOBUNREMZFPN-DNQXCXABSA-N 3-benzoyl-n-[(1r,2r)-2-(3,4-dimethoxyphenyl)cyclohexyl]benzamide Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H]1[C@H](NC(=O)C=2C=C(C=CC=2)C(=O)C=2C=CC=CC=2)CCCC1 SQDOBUNREMZFPN-DNQXCXABSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 102000004008 5'-Nucleotidase Human genes 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 208000004998 Abdominal Pain Diseases 0.000 description 1
- 206010052613 Allergic bronchitis Diseases 0.000 description 1
- 206010049153 Allergic sinusitis Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 1
- 208000032492 Bacterial toxic-shock syndrome Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- 238000006407 Bischler-Napieralski reaction Methods 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- VGUMJNBFEROQFM-DENIHFKCSA-N C(C)ON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC Chemical compound C(C)ON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC VGUMJNBFEROQFM-DENIHFKCSA-N 0.000 description 1
- JHJDLRDSSGDAFW-ZEQKJWHPSA-N C1(=CC=CC=C1)ON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC Chemical compound C1(=CC=CC=C1)ON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC JHJDLRDSSGDAFW-ZEQKJWHPSA-N 0.000 description 1
- XCVYOAJWDNTBGG-LEAFIULHSA-N COC1=CC=C(CON=C(C)C2=CC=C(C=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=C1 Chemical compound COC1=CC=C(CON=C(C)C2=CC=C(C=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=C1 XCVYOAJWDNTBGG-LEAFIULHSA-N 0.000 description 1
- AECMOXXPFHCAEH-GLOUMADESA-N COC=1C=C(C=CC1OC)[C@@H]1[C@@H](CCCC1)N.COC=1C=C(C=CC1OC)[C@@H]1[C@@H](CCCC1)N Chemical compound COC=1C=C(C=CC1OC)[C@@H]1[C@@H](CCCC1)N.COC=1C=C(C=CC1OC)[C@@H]1[C@@H](CCCC1)N AECMOXXPFHCAEH-GLOUMADESA-N 0.000 description 1
- YZWDRENVCKOTTP-YLJYHZDGSA-N COC=1C=C2C(=N[C@@H]3CCCC[C@@H]3C2=CC1OC)C=1C=C(C=CC1)C(C)=NO Chemical compound COC=1C=C2C(=N[C@@H]3CCCC[C@@H]3C2=CC1OC)C=1C=C(C=CC1)C(C)=NO YZWDRENVCKOTTP-YLJYHZDGSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- LSPHULWDVZXLIL-UHFFFAOYSA-N Camphoric acid Natural products CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- VOPWNXZWBYDODV-UHFFFAOYSA-N Chlorodifluoromethane Chemical compound FC(F)Cl VOPWNXZWBYDODV-UHFFFAOYSA-N 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 206010009137 Chronic sinusitis Diseases 0.000 description 1
- AFNMQDGKOANXDU-SHQCIBLASA-N ClC=1C=C(CON=C(C)C2=CC=C(C=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=CC1 Chemical compound ClC=1C=C(CON=C(C)C2=CC=C(C=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=CC1 AFNMQDGKOANXDU-SHQCIBLASA-N 0.000 description 1
- 208000002881 Colic Diseases 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- AAWZDTNXLSGCEK-UHFFFAOYSA-N Cordycepinsaeure Natural products OC1CC(O)(C(O)=O)CC(O)C1O AAWZDTNXLSGCEK-UHFFFAOYSA-N 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 241000271532 Crotalus Species 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- DIWVBIXQCNRCFE-UHFFFAOYSA-N DL-alpha-Methoxyphenylacetic acid Chemical compound COC(C(O)=O)C1=CC=CC=C1 DIWVBIXQCNRCFE-UHFFFAOYSA-N 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 206010012442 Dermatitis contact Diseases 0.000 description 1
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 1
- 208000006926 Discoid Lupus Erythematosus Diseases 0.000 description 1
- 206010014561 Emphysema Diseases 0.000 description 1
- FRTXWMGXOGCFSG-SHQCIBLASA-N FC(C=1C=C(CON=C(C)C2=CC(=CC=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=CC1)(F)F Chemical compound FC(C=1C=C(CON=C(C)C2=CC(=CC=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=CC1)(F)F FRTXWMGXOGCFSG-SHQCIBLASA-N 0.000 description 1
- QCKYCOUFYKJJBH-SHQCIBLASA-N FC1=CC=C(CON=C(C)C2=CC(=CC=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=C1 Chemical compound FC1=CC=C(CON=C(C)C2=CC(=CC=C2)C2=N[C@@H]3CCCC[C@@H]3C3=CC(=C(C=C23)OC)OC)C=C1 QCKYCOUFYKJJBH-SHQCIBLASA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical class NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 208000000913 Kidney Calculi Diseases 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 208000026139 Memory disease Diseases 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- 101000909851 Mycobacterium tuberculosis (strain ATCC 25618 / H37Rv) cAMP/cGMP dual specificity phosphodiesterase Rv0805 Proteins 0.000 description 1
- IFHNNJMSCHMBKF-SHQCIBLASA-N N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=C(F)C=C1 Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(C)=NOCC1=CC=C(F)C=C1 IFHNNJMSCHMBKF-SHQCIBLASA-N 0.000 description 1
- YIQQKHURCQRCLD-YLJYHZDGSA-N N-[1-[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylidene]hydroxylamine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C1=CC=C(C(C)=NO)C=C1 YIQQKHURCQRCLD-YLJYHZDGSA-N 0.000 description 1
- CBAKUQYQYIQGKX-ZJSXRUAMSA-N N-[[3-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-phenylmethylidene]hydroxylamine Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(=NO)C1=CC=CC=C1 CBAKUQYQYIQGKX-ZJSXRUAMSA-N 0.000 description 1
- MSSDWAHXSSFFDE-ZJSXRUAMSA-N N-[[4-[(4aR,10bR)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-phenylmethylidene]hydroxylamine Chemical compound COC=1C=C2C(=N[C@@H]3CCCC[C@@H]3C2=CC1OC)C1=CC=C(C=C1)C(=NO)C1=CC=CC=C1 MSSDWAHXSSFFDE-ZJSXRUAMSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 208000000592 Nasal Polyps Diseases 0.000 description 1
- 206010029148 Nephrolithiasis Diseases 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- OGQGGBSVFAOAFF-LEAFIULHSA-N O(C1=CC=CC=C1)CCON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC Chemical compound O(C1=CC=CC=C1)CCON=C(C)C1=CC(=CC=C1)C1=N[C@@H]2CCCC[C@@H]2C2=CC(=C(C=C12)OC)OC OGQGGBSVFAOAFF-LEAFIULHSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 206010037093 Pruritus genital Diseases 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 208000006311 Pyoderma Diseases 0.000 description 1
- AAWZDTNXLSGCEK-ZHQZDSKASA-N Quinic acid Natural products O[C@H]1CC(O)(C(O)=O)C[C@H](O)C1O AAWZDTNXLSGCEK-ZHQZDSKASA-N 0.000 description 1
- 239000007868 Raney catalyst Substances 0.000 description 1
- NPXOKRUENSOPAO-UHFFFAOYSA-N Raney nickel Chemical compound [Al].[Ni] NPXOKRUENSOPAO-UHFFFAOYSA-N 0.000 description 1
- 229910000564 Raney nickel Inorganic materials 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- 206010039793 Seborrhoeic dermatitis Diseases 0.000 description 1
- 206010039966 Senile dementia Diseases 0.000 description 1
- 229920005654 Sephadex Polymers 0.000 description 1
- 239000012507 Sephadex™ Substances 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 206010042496 Sunburn Diseases 0.000 description 1
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- 241000906446 Theraps Species 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 206010044248 Toxic shock syndrome Diseases 0.000 description 1
- 231100000650 Toxic shock syndrome Toxicity 0.000 description 1
- 206010052779 Transplant rejections Diseases 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 102000011017 Type 4 Cyclic Nucleotide Phosphodiesterases Human genes 0.000 description 1
- 108010037584 Type 4 Cyclic Nucleotide Phosphodiesterases Proteins 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 201000004810 Vascular dementia Diseases 0.000 description 1
- 102100026383 Vasopressin-neurophysin 2-copeptin Human genes 0.000 description 1
- JPUJWHOKGSAARG-VXGBXAGGSA-N [(1r,2r)-2-nitrocyclohexyl]benzene Chemical compound [O-][N+](=O)[C@@H]1CCCC[C@@H]1C1=CC=CC=C1 JPUJWHOKGSAARG-VXGBXAGGSA-N 0.000 description 1
- IQMPXCWPLKIDFM-ZJSXRUAMSA-N [3-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-phenylmethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=1)=CC=CC=1C(=O)C1=CC=CC=C1 IQMPXCWPLKIDFM-ZJSXRUAMSA-N 0.000 description 1
- FFDSXMWUQGJKFO-ZJSXRUAMSA-N [4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]-phenylmethanone Chemical compound N([C@@H]1CCCC[C@@H]1C=1C=C(C(=CC=11)OC)OC)=C1C(C=C1)=CC=C1C(=O)C1=CC=CC=C1 FFDSXMWUQGJKFO-ZJSXRUAMSA-N 0.000 description 1
- CLZISMQKJZCZDN-UHFFFAOYSA-N [benzotriazol-1-yloxy(dimethylamino)methylidene]-dimethylazanium Chemical compound C1=CC=C2N(OC(N(C)C)=[N+](C)C)N=NC2=C1 CLZISMQKJZCZDN-UHFFFAOYSA-N 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 230000002009 allergenic effect Effects 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 208000004631 alopecia areata Diseases 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- VZTDIZULWFCMLS-UHFFFAOYSA-N ammonium formate Chemical compound [NH4+].[O-]C=O VZTDIZULWFCMLS-UHFFFAOYSA-N 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical class CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 1
- 230000002917 arthritic effect Effects 0.000 description 1
- 238000011914 asymmetric synthesis Methods 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 201000005008 bacterial sepsis Diseases 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000004067 bulking agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- LSPHULWDVZXLIL-QUBYGPBYSA-N camphoric acid Chemical compound CC1(C)[C@H](C(O)=O)CC[C@]1(C)C(O)=O LSPHULWDVZXLIL-QUBYGPBYSA-N 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 230000002490 cerebral effect Effects 0.000 description 1
- 150000001793 charged compounds Chemical group 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 208000027157 chronic rhinosinusitis Diseases 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 239000005515 coenzyme Substances 0.000 description 1
- 230000037410 cognitive enhancement Effects 0.000 description 1
- 206010009887 colitis Diseases 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 208000010247 contact dermatitis Diseases 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 208000004921 cutaneous lupus erythematosus Diseases 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000004850 cyclobutylmethyl group Chemical group C1(CCC1)C* 0.000 description 1
- 125000001352 cyclobutyloxy group Chemical group C1(CCC1)O* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000003113 cycloheptyloxy group Chemical group C1(CCCCCC1)O* 0.000 description 1
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 1
- 125000001887 cyclopentyloxy group Chemical group C1(CCCC1)O* 0.000 description 1
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000131 cyclopropyloxy group Chemical group C1(CC1)O* 0.000 description 1
- 210000000172 cytosol Anatomy 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 201000010064 diabetes insipidus Diseases 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- FAMRKDQNMBBFBR-BQYQJAHWSA-N diethyl azodicarboxylate Substances CCOC(=O)\N=N\C(=O)OCC FAMRKDQNMBBFBR-BQYQJAHWSA-N 0.000 description 1
- 125000004786 difluoromethoxy group Chemical group [H]C(F)(F)O* 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- YWEUIGNSBFLMFL-UHFFFAOYSA-N diphosphonate Chemical compound O=P(=O)OP(=O)=O YWEUIGNSBFLMFL-UHFFFAOYSA-N 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- FAMRKDQNMBBFBR-UHFFFAOYSA-N ethyl n-ethoxycarbonyliminocarbamate Chemical compound CCOC(=O)N=NC(=O)OCC FAMRKDQNMBBFBR-UHFFFAOYSA-N 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 229940044627 gamma-interferon Drugs 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 229950006191 gluconic acid Drugs 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- YPGCWEMNNLXISK-UHFFFAOYSA-N hydratropic acid Chemical compound OC(=O)C(C)C1=CC=CC=C1 YPGCWEMNNLXISK-UHFFFAOYSA-N 0.000 description 1
- IKDUDTNKRLTJSI-UHFFFAOYSA-N hydrazine monohydrate Substances O.NN IKDUDTNKRLTJSI-UHFFFAOYSA-N 0.000 description 1
- 230000001969 hypertrophic effect Effects 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 230000031891 intestinal absorption Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000000654 isopropylidene group Chemical group C(C)(C)=* 0.000 description 1
- 208000018934 joint symptom Diseases 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 150000002617 leukotrienes Chemical class 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229960003194 meglumine Drugs 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- ZGQXYNYDTKDVPB-LEAFIULHSA-N methyl 4-[[1-[4-[(4ar,10br)-8,9-dimethoxy-1,2,3,4,4a,10b-hexahydrophenanthridin-6-yl]phenyl]ethylideneamino]oxymethyl]benzoate Chemical compound C1=CC(C(=O)OC)=CC=C1CON=C(C)C1=CC=C(C=2C3=CC(OC)=C(OC)C=C3[C@H]3CCCC[C@H]3N=2)C=C1 ZGQXYNYDTKDVPB-LEAFIULHSA-N 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 229950002910 motapizone Drugs 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 230000021962 pH elevation Effects 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 210000003800 pharynx Anatomy 0.000 description 1
- RDOWQLZANAYVLL-UHFFFAOYSA-N phenanthridine Chemical group C1=CC=C2C3=CC=CC=C3C=NC2=C1 RDOWQLZANAYVLL-UHFFFAOYSA-N 0.000 description 1
- UHZYTMXLRWXGPK-UHFFFAOYSA-N phosphorus pentachloride Chemical compound ClP(Cl)(Cl)(Cl)Cl UHZYTMXLRWXGPK-UHFFFAOYSA-N 0.000 description 1
- DLYUQMMRRRQYAE-UHFFFAOYSA-N phosphorus pentoxide Inorganic materials O1P(O2)(=O)OP3(=O)OP1(=O)OP2(=O)O3 DLYUQMMRRRQYAE-UHFFFAOYSA-N 0.000 description 1
- 229920000137 polyphosphoric acid Polymers 0.000 description 1
- 150000007519 polyprotic acids Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000007112 pro inflammatory response Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 108010043671 prostatic acid phosphatase Proteins 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 230000036387 respiratory rate Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 201000003068 rheumatic fever Diseases 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 208000008742 seborrheic dermatitis Diseases 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000036303 septic shock Effects 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 206010040560 shock Diseases 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000003998 snake venom Substances 0.000 description 1
- 150000003385 sodium Chemical class 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 210000001635 urinary tract Anatomy 0.000 description 1
- 230000000304 vasodilatating effect Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
- C07D221/06—Ring systems of three rings
- C07D221/10—Aza-phenanthrenes
- C07D221/12—Phenanthridines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Pulmonology (AREA)
- Dermatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Other In-Based Heterocyclic Compounds (AREA)
Abstract
一定の式(I)で示され、式中のR1、R2、R3、R31、R4、R5、R51、R6、R7及びR8は明細書中に記載の意味を有する化合物は新規の効果的なPDE4阻害剤である。
Description
発明の適用分野
本発明は、医薬品組成物の製造のための医薬品工業で使用される新規の6−フェニルフェナントリジンに関する。
本発明は、医薬品組成物の製造のための医薬品工業で使用される新規の6−フェニルフェナントリジンに関する。
公知の背景技術
国際出願WO97/28131号(=USP6,191,138号)、WO97/35854号(=USP6,127,378号)、WO99/05113号(=USP6,121,279号)、WO99/05111号(=USP6,410,551号)、WO00/42018号、WO00/42020号、WO02/05616号及びWO02/06238号はPDE4インヒビターとしての6−フェニルフェナントリジンを記載している。
国際出願WO97/28131号(=USP6,191,138号)、WO97/35854号(=USP6,127,378号)、WO99/05113号(=USP6,121,279号)、WO99/05111号(=USP6,410,551号)、WO00/42018号、WO00/42020号、WO02/05616号及びWO02/06238号はPDE4インヒビターとしての6−フェニルフェナントリジンを記載している。
発明の開示
ここで、今までに知られた6−フェニルフェナントリジンとは6−フェニル環で予想されない緻密な置換型の点で異なる、以下に詳細に説明する新規の6−フェニルフェナントリジンが驚くべき特に有利な特性を有することが判明した。
ここで、今までに知られた6−フェニルフェナントリジンとは6−フェニル環で予想されない緻密な置換型の点で異なる、以下に詳細に説明する新規の6−フェニルフェナントリジンが驚くべき特に有利な特性を有することが判明した。
このように、本発明は、式I
R1はヒドロキシル、C1〜C4−アルコキシ、C3〜C7−シクロアルコキシ、C3〜C7−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであり、
R2はヒドロキシル、C1〜C4−アルコキシ、C3〜C7−シクロアルコキシ、C3〜C7−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであるか、又は
R1及びR2は一緒になってC1〜C2−アルキレンジオキシ基であり、
R3は水素又はC1〜C4−アルキルであり、
R31は水素又はC1〜C4−アルキルであるか、又は
R3及びR31は一緒になってC1〜C4−アルキレン基であり、
R4は水素又はC1〜C4−アルキルであり、
R5は水素であり、
R51は水素であるか、又は
R5及びR51は一緒になって付加的な結合を表し、
R6は水素、ハロゲン、ニトロ、C1〜C4−アルキル、トリフルオロメチル又はC1〜C4−アルコキシであり、
R7はC1〜C4−アルキル、C3〜C7−シクロアルキル、C3〜C7−シクロアルキルメチル、ピリジニル、フェニル又はR71及び/又はR72で置換されたフェニルであり、その際、
R71はハロゲン、ヒドロキシル、シアノ、トリフルオロメチル、カルボキシル、ニトロ、C1〜C4−アルキル又はC1〜C4−アルコキシであり、
R72はC1〜C4−アルコキシ、C1〜C4−アルキル又はハロゲンであり、
R8は水素、フェニル、C1〜C4−アルキル、アリールオキシ−C2〜C4−アルキル又はR9で置換されたC1〜C4−アルキルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はハロゲン又はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はフェニル、アリール−C1〜C4−アルキル又はR911で置換されたフェニルであり、その際、
アリールはフェニル又はR81で置換されたフェニルであり、
R911はC1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、その両者が結合される窒素原子を含んで、1−ピロリジニル基、1−ピペリジニル基、1−ピペラジニル基、4−メチルピペラジン−1−イル基、4−フェニルピペラジン−1−イル基、1−ヘキサヒドロアゼピニル基又は4−モルホリニル基を表し、
R93はニトロ、C1〜C4−アルキル、C1〜C4−アルコキシカルボニル、ハロゲン、トリフルオロメチル、C1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシである]の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体に関する。
C1〜C4−アルキルは、直鎖状又は分枝鎖状の1〜4個の炭素原子を有するアルキル基を表す。挙げられる例は、ブチル、イソブチル、s−ブチル、t−ブチル、プロピル、イソプロピル及び、有利にはエチル基及びメチル基である。
C1〜C4−アルコキシは、酸素原子の他に直鎖状又は分枝鎖状の1〜4個の炭素原子を有するアルキル基を有する基を表す。挙げられる例は、ブトキシ、イソブトキシ、s−ブトキシ、t−ブトキシ、プロポキシ、イソプロポキシ及び、有利にはエトキシ基及びメトキシ基である。
C3〜C7−シクロアルコキシは、シクロプロピルオキシ、シクロブチルオキシ、シクロペンチルオキシ、シクロヘキシルオキシ及びシクロヘプチルオキシを表し、そのうちシクロプロピルオキシ、シクロブチルオキシ及びシクロペンチルオキシが有利である。
C3〜C7−シクロアルキルメトキシは、シクロプロピルメトキシ、シクロブチルメトキシ、シクロペンチルメトキシ、シクロヘキシルメトキシ及びシクロヘプチルメトキシを表し、そのうちシクロプロピルメトキシ、シクロブチルメトキシ及びシクロペンチルメトキシが有利である。
完全に又は大部分がフッ素置換されたC1〜C4−アルコキシとしては、例えば2,2,3,3,3−ペンタフルオロプロポキシ、ペルフルオロエトキシ、1,2,2−トリフルオロエトキシ、特に1,1,2,2−テトラフルオロエトキシ、2,2,2−トリフルオロエトキシ、トリフルオロメトキシ及び、有利にはジフルオロメトキシ基が挙げられる。この関連で、“大部分が”とは、C1〜C4−アルコキシ基の水素原子の半分より多くがフッ素原子により置換されていることを意味する。
C1〜C2−アルキレンジオキシは、例えばメチレンジオキシ[−O−CH2−O−]基及びエチレンジオキシ[−O−CH2−CH2−O−]基を表す。
R3及びR31が一緒になってC1〜C4−アルキレンを意味する場合に、式Iの化合物中の1位及び4位はC1〜C4−アルキレン架橋によって互いに結合されており、その際、C1〜C4−アルキレンは直鎖状又は分枝鎖状の1〜4個の炭素原子を有するアルキレン基を表す。挙げられる例は、メチレン基[−CH2−]、エチレン基[−CH2−CH2−]、トリメチレン基[−CH2−CH2−CH2−]、1,2−ジメチル−エチレン基[−CH(CH3)−CH(CH3)−]及びイソプロピリデン基[−C(CH3)2−]である。
C3〜C7−シクロアルキルは、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル及びシクロヘプチルを表し、そのうちシクロプロピル、シクロブチル及びシクロペンチルが有利である。
C3〜C7−シクロアルキルメチルは、前記のC3〜C7−シクロアルキル基の1つにより置換されているメチル基を表す。有利にはC3〜C5−シクロアルキルメチル基、シクロプロピルメチル、シクロブチルメチル及びシクロペンチルメチルが挙げられる。
C1〜C4−アルコキシカルボニルは、前記C1〜C4−アルコキシ基の1つが結合されているカルボニル基を表す。挙げられる例は、メトキシカルボニル[CH3O−C(O)−]及びエトキシカルボニル[CH3CH2O−C(O)−]基である。
R9で置換されたC1〜C4−アルキルは、R9によって表される基の1つによって置換された前記のC1〜C4−アルキル基の1つを表す。挙げられる例は、R9で置換されたエチル基、有利にはR9で置換されたメチル基である。
アリールは、フェニル又はR81で置換されたフェニル基を表す。
アリール−C1〜C4−アルキルは、前記のアリール基の1つにより置換されている前記のC1〜C4−アルキル基の1つを表す。挙げられる例は、アリールエチル基及びアリールメチル基である。
アリールオキシは、フェノキシ又は又はR81で置換されたフェノキシ基を表す。
アリールオキシ−C2〜C4−アルキルは、前記のアリールオキシ基の1つによって置換されたC2〜C4−アルキル基を表す。有利には、2−アリールオキシエチル基が挙げられるべきである。
本発明の意味上の範囲内ではハロゲンは、臭素、塩素又はフッ素である。
本発明の範囲内でのピリジニルは、ピリジン−2−イル、ピリジン−3−イル又はピリジン−4−イルである。
式Iの化合物の置換基R6及び−C(R7)=N−O−R8は、6−フェニル環がフェナントリジン環系に結合されている結合位置に対してオルト位、メタ位又はパラ位で結合されていてよい。式Iで示され、式中、R6が水素であり、かつ−C(R7)=N−O−R8がメタ位又はパラ位で結合されている化合物が有利である。
当業者は、非環C=N二重結合を有する化合物は、立体化学において通常の慣習に従ってZ/E異性体と示される2つの立体異性体形で存在しうることを認識している。オキシムC=N二重結合に関して、このように本発明は、任意の可能なZ/E異性体及びそれらの混合物に関する。
式Iの化合物の可能な塩(置換基に依存して)は全ての酸付加塩又は塩基との全ての塩である。薬学で慣用に使用される無機酸及び有機酸との塩基の薬理学的に認容性の塩を特に挙げることができる。これらの好適なものは、塩酸、臭化水素酸、リン酸、硝酸、硫酸、酢酸、クエン酸、D−グルコン酸、安息香酸、2−(4−ヒドロキシベンゾイル)安息香酸、酪酸、スルホサリチル酸、マレイン酸、ラウリン酸、リンゴ酸、フマル酸、コハク酸、シュウ酸、酒石酸、エンボン酸、ステアリン酸、トルエンスルホン酸、メタンスルホン酸又は3−ヒドロキシ−2−ナフトエ酸のような酸との、一方では、水不溶性の酸付加塩、特に水溶性の酸付加塩であり、その際、前記の酸は塩調製において(一塩基酸又は多塩基酸のどちらが考慮されるかに依存して、そしてどの塩が望ましいかに依存して)等モル量比又はそれとは異なる比で使用できる。
他方で塩基との塩も適当である。挙げられる塩基との塩の例は、アルカリ金属(リチウム、ナトリウム、カリウム)又はカルシウム、アルミニウム、マグネシウム、チタン、アンモニウム、メグルミン又はグアニジニウムの塩であり、その際、ここでもまた塩基は塩調製において等モル量比又はそれとは異なる比で使用される。
本発明による化合物の工業的規模での製造においてプロセス生成物として、例えば最初に得ることができる薬理学的に非認容性の塩は当業者に公知の方法によって薬理学的に認容性の塩に変換される。
本発明による化合物及びその塩は、例えばこれらが結晶形で単離される場合に種々の溶剤量を有してよいことは当業者には知られている。従ってまた本発明は、式Iの化合物の全ての溶媒和物及び、特に全ての水和物、及びまた式Iの化合物の塩の全ての溶媒和物及び、特に全ての水和物を包含する。
強調されるべき式Iの化合物は、式中、
R1はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R2はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R3は水素であり、
R31は水素であり、
R4は水素又はC1〜C2−アルキルであり、
R5は水素であり、
R51は水素であるか、又は
R5及びR51は一緒になって付加的な結合を表し、
R6は水素であり、
R7はC1〜C4−アルキル又はフェニルであり、
R8は水素、フェニル、C1〜C4−アルキル、アリールオキシ−C2〜C4−アルキル又はR9で置換されたC1〜C2−アルキルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はハロゲン又はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリール−C1〜C2−アルキル又はR911で置換されたフェニルであり、その際、
アリールはフェニル又はR81で置換されたフェニルであり、
R911はC1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−メチルピペラジン−1−イル基、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、C1〜C4−アルコキシカルボニル、ハロゲン、トリフルオロメチル、C1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシである化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
R1はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R2はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R3は水素であり、
R31は水素であり、
R4は水素又はC1〜C2−アルキルであり、
R5は水素であり、
R51は水素であるか、又は
R5及びR51は一緒になって付加的な結合を表し、
R6は水素であり、
R7はC1〜C4−アルキル又はフェニルであり、
R8は水素、フェニル、C1〜C4−アルキル、アリールオキシ−C2〜C4−アルキル又はR9で置換されたC1〜C2−アルキルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はハロゲン又はトリフルオロメチルであり、
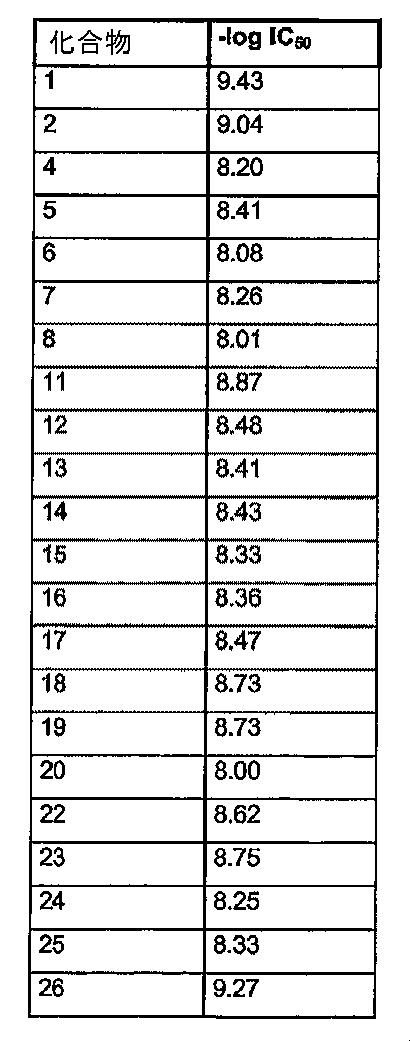
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリール−C1〜C2−アルキル又はR911で置換されたフェニルであり、その際、
アリールはフェニル又はR81で置換されたフェニルであり、
R911はC1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−メチルピペラジン−1−イル基、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、C1〜C4−アルコキシカルボニル、ハロゲン、トリフルオロメチル、C1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシである化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
より強調されるべき式Iの化合物は、式中、
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はC1〜C2−アルキル又はフェニルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、アリールオキシエチル又はR9で置換されたメチルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリールメチル又はR911で置換されたフェニルであり、その際、
アリールは塩素置換されたフェニルであり、
R911はメトキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、メトキシカルボニル、クロロ、フルオロ、トリフルオロメチル又はメトキシである化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はC1〜C2−アルキル又はフェニルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、アリールオキシエチル又はR9で置換されたメチルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリールメチル又はR911で置換されたフェニルであり、その際、
アリールは塩素置換されたフェニルであり、
R911はメトキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、メトキシカルボニル、クロロ、フルオロ、トリフルオロメチル又はメトキシである化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
特に強調されるべき式Iの化合物は、式中、
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はメチルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、フェノキシエチル、3−トリフルオロメチルフェノキシエチル又はR9で置換されたメチルであり、その際、
R9はフェニル、4−ニトロフェニル、4−メトキシカルボニルフェニル、4−クロロフェニル、3−クロロフェニル、2−クロロフェニル、4−フルオロフェニル、3−フルオロフェニル、4−トリフルオロメチルフェニル、3−トリフルオロメチルフェニル、4−メトキシフェニル、2−メトキシフェニル又はC(O)N(R91)R92であり、その際、
R91は2−メトキシフェニル又は4−クロロベンジルであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表すか、又は
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はフェニルであり、
R8は水素である化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はメチルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、フェノキシエチル、3−トリフルオロメチルフェノキシエチル又はR9で置換されたメチルであり、その際、
R9はフェニル、4−ニトロフェニル、4−メトキシカルボニルフェニル、4−クロロフェニル、3−クロロフェニル、2−クロロフェニル、4−フルオロフェニル、3−フルオロフェニル、4−トリフルオロメチルフェニル、3−トリフルオロメチルフェニル、4−メトキシフェニル、2−メトキシフェニル又はC(O)N(R91)R92であり、その際、
R91は2−メトキシフェニル又は4−クロロベンジルであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表すか、又は
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はフェニルであり、
R8は水素である化合物並びにそれらの塩及びこれらの化合物のE/Z異性体である。
本発明の化合物の特定の一実施態様には、式Iで示され、式中、R1及びR2がC1〜C2−アルコキシである化合物が含まれる。
本発明の化合物の別の特定の一実施態様には、式Iで示され、式中、R1及びR2がC1〜C2−アルコキシであり、かつR3、R31、R4、R5及びR51が水素である化合物が含まれる。
本発明の化合物の特定の一実施態様には、式Iで示され、式中、R1及びR2がC1〜C2−アルコキシであり、かつR3、R31、R4、R5、R51及びR6が水素である化合物が含まれる。
なおも本発明の化合物の特定の一実施態様には、式Iで示され、式中、R1及びR2がC1〜C2−アルコキシであり、かつR3、R31、R4、R5、R51及びR6が水素であり、かつR7がメチルである化合物が含まれる。
なおも更に本発明の化合物の特定の一実施態様には、式Iで示され、式中、R1及びR2がC1〜C2−アルコキシであり、かつR3、R31、R4、R5、R51及びR6が水素であり、かつR7がフェニルである化合物が含まれる。
式Iの化合物は、少なくとも4a位及び10b位にキラル中心を有し、かつ置換基R3、R31、R4、R5及びR51の意味によっては更なるキラル中心を1位、2位、3位及び4位に有するキラル化合物である。
従って本発明は純粋形並びに任意の混合比での全ての考えられる立体異性体を含む。
式Iの有利な化合物は、4a位及び10b位の水素原子が互いにシス位にある化合物である。純粋なシス−ジアステレオマー、純粋なシス−エナンチオマー及びその任意の混合比での混合物及び、例えばラセミ体が本願では特に有利である。本文中で特に有利な化合物は、式Iで示され、4a位及び10b位に関して、式I*:
例えば式I*の化合物において、R3、R31、R4、R5及びR51が水素の意味を有する場合には、カーン−インゴールド及びプレローグの規則に従う立体配置は4a位においてRであり、かつ10b位においてRである。
エナンチオマーは自体公知のように分割できる(例えば適当なジアステレオマー化合物の調製及び分割によって)。例えば、エナンチオマー分割は、式Vで示され、R1、R2、R3、R31、R4及びR5が前記の意味を有する出発化合物の段階で実施してよい。
エナンチオマーの分割は、例えば式Vで示されるラセミ化合物と光学活性酸、有利にはカルボン酸との塩形成を実施し、引き続き塩の分割及び該塩からの所望の化合物の遊離を行うことによって実施してよい。この文脈で述べられた光学活性カルボン酸の例は、マンデル酸、酒石酸、O,O′−ジベンゾイル酒石酸、ショウノウ酸、キニン酸、グルタミン酸、リンゴ酸、ショウノウスルホン酸、3−ブロモショウノウスルホン酸、α−メトキシフェニル酢酸、α−メトキシ−α−トリフルオロメチルフェニル酢酸及び2−フェニルプロピオン酸のエナンチオマー形である。選択的に、式Vのエナンチオマー純粋な出発化合物は、不斉合成によって製造できる。エナンチオマー純粋な出発化合物並びに式Iのエナンチオマー純粋な化合物は、キラル分割カラム上でのクロマトグラフィー分割によって、キラル補助試薬による誘導体化、引き続きのジアステレオマー分割及びキラル補助基の除去によって、又は適当な溶剤からの(分別)結晶化によって得ることもできる。
本発明による化合物は、例えば以下の実施例に記載されるように、引き続き明記される反応式1と2に示される反応段階に従って製造できる。
反応式1は、例として、式Iで示され、その式中のR1、R2、R3、R31、R4、R5、R51、R6、R7及びR8が前記の意味を有する化合物についての、式IIで示され、その式中のR1、R2、R3、R31、R4、R5、R51、R6及びR7が前記の意味を有するケト化合物から出発する2つの選択的な合成経路を示している。
一方で、前記の式Iの化合物は、前記の式IIの化合物と式IIIで示され、その式中のR8が前記の意味を有する化合物とのオキシム形成反応によって得られる。前記反応は、例えば以下の実施例に記載されるように又は当業者に公知のように実施できる。
他方で、前記の式Iの化合物は、前記の式IIの化合物から出発する2段階法で得ることもできる:まず、式IIの化合物をヒドロキシルアミンでで相応の式IIaの化合物に変換し、次いで得られた式IIaの化合物を式IIIaで示され、その式中のR8が前記の意味を有し、かつXが適当な離脱基を表す化合物と反応させて、所望の式Iの化合物を得られる。この両方の反応は、当業者に公知のように実施できる。
式IIIの化合物は市販されているか、又は当業者に公知のように製造することができる。
式IIIaの化合物は公知であるか、又は公知の方法に従って製造することができる。
式IIで示され、その式中のR1、R2、R3、R3、R31、R4、R5、R51、R6及びR7が前記の意味を有する化合物は、国際出願WO00/42042号から公知であるか、又はそこに記載されるのと同様の又は類似のように製造することができる。しかしながら有利には、式IIの化合物は、以下の実施例に例として示される方法に従って得られる。更なる詳細について、式IIの化合物に好適な合成経路は以下の反応式2に概略する。前記の反応式2の第一段階では、式Vで示され、その式中のR1、R2、R3、R31、R4、R5及びR51が前記の意味を有する化合物を、式VIで示され、その式中のR6及びR7が前記の意味を有し、かつXが好適な離脱基、有利には塩素原子を表す化合物と反応させて、式IVで示され、その式中のR1、R2、R3、R31、R4、R5、R51、R6及びR7が前記の意味を有する化合物が得られる。
選択的に、式IVで示され、式中、R1、R2、R3、R31、R4、R51、R6及びR7は前記の意味を有する化合物は、例えば式Vで示され、式中、R1、R2、R3、R31、R4、R5及びR51は前記の意味を有する化合物と式VIで示され、R6及びR7は前記の意味を有し、かつXはヒドロキシルである化合物から、当業者に公知のアミド結合架橋試薬と反応させることによって製造することもできる。当業者に公知のアミド結合架橋試薬の挙げられる例は、カルボジイミド(例えばジシクロヘキシルカルボジイミド又は、有利には1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩)、アゾジカルボン酸誘導体(例えばジエチルアゾジカルボキシレート)、ウロニウム塩[例えばO−(ベンゾトリアゾール−1−イル)−N,N,N′,N′−テトラメチルウロニウムテトラフルオロボレート又はO−(ベンゾトリアゾール−1−イル)−N,N,N′,N′−テトラメチルウロニウムヘキサフルオロホスフェート]及びN,N’−カルボニルジイミダゾールである。本発明の範囲において、有利なアミド結合架橋試薬はウロニウム塩及び、有利にはカルボジイミド、有利には1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩である。
式VIで示され、式中、R6及びR7が前記の意味を有する化合物は公知であるか、又は公知のように製造できる。
反応式2において後続の工程に示されるように、式IIで示され、その式中のR1、R2、R3、R31、R4、R5、R51、R6及びR7は前記の意味を有する化合物は、式VIの相応の化合物の縮合環化によって得ることができる。前記の環状縮合は、当業者に自体公知のように又は以下の実施例に例として記載されるように、Bischler-Napieralski(例えばJ.Chem.Soc., 1956, 4280-4282に記載されるように)に従って適当な縮合剤、例えばポリリン酸、五塩化リン、五酸化リン又はオキシ塩化リンの存在下に、適当な不活性溶剤、例えば塩素化炭化水素、例えばクロロホルム中で又は環状炭化水素、例えばトルエン又はキシレン中で、又は別の不活性溶剤、例えばアセトニトリル中で、又は更なる溶剤を使用せず、過剰の縮合剤を使用して、低減された温度で、又は室温で、又は高められた温度で、又は使用される溶剤又は縮合剤の沸点で実施される。
式Vの出発化合物の純粋なエナンチオマーの製造は、例えば国際出願WO00/42020号に既に記載されているか、又はその製造は以下の実施例に従って実施することができる。
更に当業者には、多数の反応中心が出発化合物又は中間体化合物に存在する場合には、1つ以上の反応中心を反応が所望の反応中心だけで行われるように保護基で封鎖する必要があることもあることは知られている。多数の証明された保護基の使用のための詳細な記載は、例えば“Protective Groups in Organic Synthesis”、T.Greene and P.Wuts著(John Wiley & Sons, Inc. 1999, 3rd Ed)又は“Protecting Groups(Thieme Foundations Organic Chemistry Series N Group)”、P.Kocienski著(Thieme Medical Publishers, 2000)で述べられている。
本発明による物質の単離及び精製は、自体公知の方法で、例えば真空中で溶剤を留去し、そして得られた残留物を適当な溶剤から再結晶させるか、又は慣用の精製法の1つ、例えば適当な担体材料上でのカラムクロマトグラフィーを実施することによって行われる。
塩は、遊離の化合物を所望の酸又は塩基を含有する適当な溶剤(例えばケトン、例えばアセトン、メチルエチルケトン又はメチルイソブチルケトン、エーテル、例えばジエチルエーテル、テトラヒドロフラン又はジオキサン、塩素化炭化水素、塩化メチレン又はクロロホルム又は低分子量の脂肪族アルコール、例えばエタノール又はイソプロパノール)中に、又は所望の酸又は塩基がその後に添加される溶剤中に溶解させることによって得られる。塩は、付加塩のための非溶剤を用いる濾過、再沈殿、沈殿又は溶剤の蒸発によって得られる。得られた塩を、アルカリ性化又は酸性化によって遊離の化合物に変換してよく、該化合物はまた塩に変換してもよい。前記のように、薬理学的に認容性でない塩を薬理学的に認容性の塩に変換することができる。
場合により式Iの化合物をその塩に変換できるか、又は場合により式Iの化合物の塩を遊離の化合物に変換することができる。
当業者はその知識に基づいて、本発明の明細書中に示され記載されたこれらの合成経路に基づいて、式Iの化合物に関して他の可能な合成経路をどのように見いだすかを知っている。全てのこれらの他の可能な合成経路もまた本発明を構成する部分である。
以下の実施例は本発明をより詳細に説明するものであり、それを制限するものではない。同様に製造方法が明記されていない式Iの他の化合物は、同様に又は当業者に公知の方法で慣用の処理技術を用いて製造できる。
この実施例において、m.p.は融点を表し、hは時間を表し、minは分を表し、EFは実験式を表し、MWは分子量を表し、MSは質量スペクトルを表し、Mは分子イオンを表し、calc.は計算値を表し、fnd.は実測値を表す。
この実施例に挙げられる化合物及びそれらの塩及びE/Z異性体は本発明の有利な対象である。
実施例
最終生成物:
1. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノンオキシム
200mgの(4aR,10bR)−8,9−ジメトキシ−6−(4−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン(化合物A1)及び300mgの炭酸水素ナトリウムを5mlのエタノール中に懸濁させ、230mgのヒドロキシルアミン塩酸塩で処理し、そして室温で1.5時間撹拌する。反応混合物を濾過し、濾液を濃縮させ、そして残留物をシリカゲル(石油エーテル/酢酸エチル/トリエチルアミン 6:3:1)上でクロマトグラフィーする。640mgの表題化合物が得られる。融点189〜192℃。
最終生成物:
1. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノンオキシム
200mgの(4aR,10bR)−8,9−ジメトキシ−6−(4−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン(化合物A1)及び300mgの炭酸水素ナトリウムを5mlのエタノール中に懸濁させ、230mgのヒドロキシルアミン塩酸塩で処理し、そして室温で1.5時間撹拌する。反応混合物を濾過し、濾液を濃縮させ、そして残留物をシリカゲル(石油エーテル/酢酸エチル/トリエチルアミン 6:3:1)上でクロマトグラフィーする。640mgの表題化合物が得られる。融点189〜192℃。
MS:計算値:C23H26N2O3(378.48) 実測値:[M+1]379.2
以下に記載される適切な出発化合物A1又はA2又はA3又はA4から出発して、以下の化合物は、実施例1の手順と同様にして、好適なO−置換されたヒドロキシルアミンを反応相手として使用して得られる。
以下に記載される適切な出発化合物A1又はA2又はA3又はA4から出発して、以下の化合物は、実施例1の手順と同様にして、好適なO−置換されたヒドロキシルアミンを反応相手として使用して得られる。
2. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−1−フェニル−メタノンオキシム
MS:計算値:C28H28N2O3(440.55) 実測値:[M+1]441.3
3. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−メチルオキシム
MS:計算値:C24H28N2O3(392.5) 実測値:[M+1]393.2
4. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−ベンジルオキシム
MS:計算値:C30H32N2O3(468.6) 実測値:[M+1]469.2
5. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−ニトロベンジル)−オキシム
MS:計算値:C30H31N3O5(513.6) 実測値:[M+1]514.2
6. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−エチルオキシム
MS:計算値:C25H30N2O3(406.53) 実測値:[M+1]407.2
7. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−フェニルオキシム
MS:計算値:C29H30N2O3(454.57) 実測値:[M+1]455.0
8. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−イソブチルオキシム
MS:計算値:C27H34N2O3(434.58) 実測値:[M+1]435.2
9. 4−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシメチル}−安息香酸メチルエステル
MS:計算値:C32H34N2O5(526.64) 実測値:[M+1]527.3
10. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−(4−フェニルピペラジン−1−イル)−エタノン
MS:計算値:C35H40N4O4(580.73) 実測値:[M+1]581.3
11. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−N−(2−メトキシフェニル)−アセトアミド
MS:計算値:C32H35N3O5(541.65) 実測値:[M+1]542.3
12. N−(4−クロロベンジル)−2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシ}−アセトアミド
MS:計算値:C32H34ClN3O4(560.1) 実測値:[M+1]560.3
13. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−クロロ−ベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
14. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
15. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−メトキシ−ベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
16. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−(4−フルオロベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
17. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−フルオロベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
18. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
19. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−フェノキシエチル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
20. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−[2−(3−トリフルオロメチルフェノキシ)−エチル]−オキシム
MS:計算値:C32H33F3N2O4(566.63) 実測値:[M+1]567.2
21. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
22. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
23. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−メトキシベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.3
24. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−モルホリン−4−イル−エタノン
MS:計算値:C29H35N3O5(505.62) 実測値:[M+1]506.3
25. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノンオキシム
MS:計算値:C23H26N2O3(378.48) 実測値:[M+1]379.4
26. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−1−フェニル−メタノンオキシム
MS:計算値:C28H28N2O3(440.55) 実測値:[M+1]441.3
27. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−ベンジルオキシム
MS:計算値:C30H32N2O3(468.6) 実測値:[M+1]469.2
28. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−メチルオキシム
MS:計算値:C24H28N2O3(392.5) 実測値:[M+1]393.2
29. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−クロロ−ベンジル)オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
30. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−メトキシ−ベンジル)オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
31. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−モルホリン−4−イル−エタノン
MS:計算値:C29H35N3O5(505.62) 実測値:[M+1]506.2
32. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−ニトロ−ベンジル)−オキシム
MS:計算値:C30H31N3O5(513.6) 実測値:[M+1]514.2
33. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−エチルオキシム
MS:計算値:C25H30N2O3(406.53) 実測値:[M+1]407.2
34. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−フェニルオキシム
MS:計算値:C29H30N2O3(454.57) 実測値:[M+1]455.0
35. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−イソブチルオキシム
MS:計算値:C27H34N2O3(434.58) 実測値:[M+1]435.2
36. 4−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシメチル}−安息香酸メチルエステル
MS:計算値:C32H34N2O5(526.64) 実測値:[M+1]527.2
37. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−(4−フェニルピペラジン−1−イル)−エタノン
MS:計算値:C35H40N4O4(580.73) 実測値:[M+1]581.3
38. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−N−(2−メトキシフェニル)−アセトアミド
MS:計算値:C32H35N3O5(541.65) 実測値:[M+1]542.3
39. N−(4−クロロベンジル)−2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシ}−アセトアミド
MS:計算値:C32H34ClN3O4(560.1) 実測値:[M+1]560.3
40. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−クロロ−ベンジル)オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
41. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−トリフルオロメチル−ベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
42. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−メトキシ−ベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
43. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−フルオロ−ベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
44. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−フルオロ−ベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
45. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
46. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−フェノキシエチル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.7
47. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−[2−(3−トリフルオロメチル−フェノキシ)−エチル]−オキシム
MS:計算値:C32H33F3N2O4(566.63) 実測値:[M+1]567.2
48. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
出発化合物:
A1. (4aR,10bR)−8,9−ジメトキシ−6−(4−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A1はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−アセトベンザミド(化合物B1)から実施例A2に記載されるのと同様にして製造される。
MS:計算値:C28H28N2O3(440.55) 実測値:[M+1]441.3
3. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−メチルオキシム
MS:計算値:C24H28N2O3(392.5) 実測値:[M+1]393.2
4. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−ベンジルオキシム
MS:計算値:C30H32N2O3(468.6) 実測値:[M+1]469.2
5. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−ニトロベンジル)−オキシム
MS:計算値:C30H31N3O5(513.6) 実測値:[M+1]514.2
6. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−エチルオキシム
MS:計算値:C25H30N2O3(406.53) 実測値:[M+1]407.2
7. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−フェニルオキシム
MS:計算値:C29H30N2O3(454.57) 実測値:[M+1]455.0
8. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−イソブチルオキシム
MS:計算値:C27H34N2O3(434.58) 実測値:[M+1]435.2
9. 4−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシメチル}−安息香酸メチルエステル
MS:計算値:C32H34N2O5(526.64) 実測値:[M+1]527.3
10. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−(4−フェニルピペラジン−1−イル)−エタノン
MS:計算値:C35H40N4O4(580.73) 実測値:[M+1]581.3
11. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−N−(2−メトキシフェニル)−アセトアミド
MS:計算値:C32H35N3O5(541.65) 実測値:[M+1]542.3
12. N−(4−クロロベンジル)−2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシ}−アセトアミド
MS:計算値:C32H34ClN3O4(560.1) 実測値:[M+1]560.3
13. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−クロロ−ベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
14. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
15. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−メトキシ−ベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
16. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−(4−フルオロベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
17. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−フルオロベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
18. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
19. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−フェノキシエチル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
20. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−[2−(3−トリフルオロメチルフェノキシ)−エチル]−オキシム
MS:計算値:C32H33F3N2O4(566.63) 実測値:[M+1]567.2
21. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
22. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
23. 1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−メトキシベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.3
24. 2−{1−[4−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−モルホリン−4−イル−エタノン
MS:計算値:C29H35N3O5(505.62) 実測値:[M+1]506.3
25. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノンオキシム
MS:計算値:C23H26N2O3(378.48) 実測値:[M+1]379.4
26. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−1−フェニル−メタノンオキシム
MS:計算値:C28H28N2O3(440.55) 実測値:[M+1]441.3
27. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−ベンジルオキシム
MS:計算値:C30H32N2O3(468.6) 実測値:[M+1]469.2
28. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−メチルオキシム
MS:計算値:C24H28N2O3(392.5) 実測値:[M+1]393.2
29. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−クロロ−ベンジル)オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
30. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−メトキシ−ベンジル)オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
31. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−モルホリン−4−イル−エタノン
MS:計算値:C29H35N3O5(505.62) 実測値:[M+1]506.2
32. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−ニトロ−ベンジル)−オキシム
MS:計算値:C30H31N3O5(513.6) 実測値:[M+1]514.2
33. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−エチルオキシム
MS:計算値:C25H30N2O3(406.53) 実測値:[M+1]407.2
34. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−フェニルオキシム
MS:計算値:C29H30N2O3(454.57) 実測値:[M+1]455.0
35. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エタノン O−イソブチルオキシム
MS:計算値:C27H34N2O3(434.58) 実測値:[M+1]435.2
36. 4−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシメチル}−安息香酸メチルエステル
MS:計算値:C32H34N2O5(526.64) 実測値:[M+1]527.2
37. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−1−(4−フェニルピペラジン−1−イル)−エタノン
MS:計算値:C35H40N4O4(580.73) 実測値:[M+1]581.3
38. 2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]エチリデンアミノオキシ}−N−(2−メトキシフェニル)−アセトアミド
MS:計算値:C32H35N3O5(541.65) 実測値:[M+1]542.3
39. N−(4−クロロベンジル)−2−{1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エチリデンアミノオキシ}−アセトアミド
MS:計算値:C32H34ClN3O4(560.1) 実測値:[M+1]560.3
40. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−クロロ−ベンジル)オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
41. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−トリフルオロメチル−ベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
42. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−メトキシ−ベンジル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.2
43. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−フルオロ−ベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
44. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(3−フルオロ−ベンジル)−オキシム
MS:計算値:C30H31FN2O3(486.59) 実測値:[M+1]487.2
45. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−クロロベンジル)−オキシム
MS:計算値:C30H31ClN2O3(503.05) 実測値:[M+1]503.2
46. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(2−フェノキシエチル)−オキシム
MS:計算値:C31H34N2O4(498.63) 実測値:[M+1]499.7
47. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−[2−(3−トリフルオロメチル−フェノキシ)−エチル]−オキシム
MS:計算値:C32H33F3N2O4(566.63) 実測値:[M+1]567.2
48. 1−[3−((4aR,10bR)−8,9−ジメトキシ−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン−6−イル)−フェニル]−エタノン O−(4−トリフルオロメチルベンジル)−オキシム
MS:計算値:C31H31F3N2O3(536.6) 実測値:[M+1]537.2
出発化合物:
A1. (4aR,10bR)−8,9−ジメトキシ−6−(4−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A1はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−アセトベンザミド(化合物B1)から実施例A2に記載されるのと同様にして製造される。
実験式:C23H25NO3;分子量:363.46
元素分析:計算値:C76.01H6.93N3.85
実測値:C75.77H6.98N3.82
旋光度:[α]20 D=−97.4゜(c=0.2、エタノール)
A2. (4aR,10bR)−8,9−ジメトキシ−6−(4−ベンゾイルフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
7.1gのN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−ベンゾイルベンザミド(化合物B2)を100mlのアセトニトリル及び5.0mlの塩化ホスホリル中に溶解させ、そして80℃で一晩撹拌する。該反応混合物を減圧下に濃縮させ、そして残留物を炭酸水素ナトリウム飽和溶液と酢酸エチルで抽出する。石油エーテル(低級)/酢酸エチル/トリエチルアミンを6/3/1の比率で用いるシリカゲル上でのクロマトグラフィーと生成物分画の濃縮の後に、5.3gの表題化合物が得られる。
元素分析:計算値:C76.01H6.93N3.85
実測値:C75.77H6.98N3.82
旋光度:[α]20 D=−97.4゜(c=0.2、エタノール)
A2. (4aR,10bR)−8,9−ジメトキシ−6−(4−ベンゾイルフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
7.1gのN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−ベンゾイルベンザミド(化合物B2)を100mlのアセトニトリル及び5.0mlの塩化ホスホリル中に溶解させ、そして80℃で一晩撹拌する。該反応混合物を減圧下に濃縮させ、そして残留物を炭酸水素ナトリウム飽和溶液と酢酸エチルで抽出する。石油エーテル(低級)/酢酸エチル/トリエチルアミンを6/3/1の比率で用いるシリカゲル上でのクロマトグラフィーと生成物分画の濃縮の後に、5.3gの表題化合物が得られる。
実験式:C28H27NO3;分子量:425.53
元素分析×0.08H2O:計算値:C78.77H6.41N3.28
実測値:C78.55H6.64N3.50
旋光度:[α]20 D=−70.6゜(c=0.2、エタノール)
A3. (4aR,10bR)−8,9−ジメトキシ−6−(3−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A3はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル−3−アセトベンザミド(化合物B3)から実施例A2に記載されるのと同様に製造される。
元素分析×0.08H2O:計算値:C78.77H6.41N3.28
実測値:C78.55H6.64N3.50
旋光度:[α]20 D=−70.6゜(c=0.2、エタノール)
A3. (4aR,10bR)−8,9−ジメトキシ−6−(3−アセトフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A3はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル−3−アセトベンザミド(化合物B3)から実施例A2に記載されるのと同様に製造される。
融点:112.5〜114℃
実験式:C23H25NO3;分子量:363.46
元素分析:計算値:C76.01H6.93N3.85
実測値:C75.62H6.90N3.83
旋光度:[α]20 D=−168.7゜(c=0.2、エタノール)
A4. (4aR,10bR)−8,9−ジメトキシ−6−(3−ベンゾイルフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A4はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル−3−ベンゾイルベンザミド(化合物B4)から実施例A2に記載されるのと同様に製造される。
実験式:C23H25NO3;分子量:363.46
元素分析:計算値:C76.01H6.93N3.85
実測値:C75.62H6.90N3.83
旋光度:[α]20 D=−168.7゜(c=0.2、エタノール)
A4. (4aR,10bR)−8,9−ジメトキシ−6−(3−ベンゾイルフェニル)−1,2,3,4,4a,10b−ヘキサヒドロフェナントリジン
化合物A4はN−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル−3−ベンゾイルベンザミド(化合物B4)から実施例A2に記載されるのと同様に製造される。
実験式:C28H27NO3;分子量:425.53
元素分析×0.15H2O:計算値:C78.54H6.43N3.27
実測値:C78.39H6.58N3.40
旋光度:[α]20 D=−96.8゜(c=0.2、エタノール)
B1. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−アセトベンザミド
化合物B1は(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシルアミン(化合物C1)から実施例B2に記載されるのと同様に製造される。
元素分析×0.15H2O:計算値:C78.54H6.43N3.27
実測値:C78.39H6.58N3.40
旋光度:[α]20 D=−96.8゜(c=0.2、エタノール)
B1. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−アセトベンザミド
化合物B1は(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシルアミン(化合物C1)から実施例B2に記載されるのと同様に製造される。
融点:129〜137℃
旋光度:[α]20 D=−180.4゜(c=0.2、エタノール)
B2. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−ベンゾイルベンザミド
4.0gの(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシルアミン(化合物C1)を40mlの塩化メチレンと10.0mlのトリエチルアミン中に溶解させる。4.9gのベンゾフェノン−4−カルボニル塩化物を100mlの塩化メチレン中に溶かした溶液を室温で滴加し、そして該混合物を、一晩撹拌した後に、それぞれ50mlの水、2Nの塩酸、炭酸水素ナトリウム飽和溶液、そして再び水で抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして濃縮させる。7.78gの表題化合物が結晶化油として得られる。
旋光度:[α]20 D=−180.4゜(c=0.2、エタノール)
B2. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−4−ベンゾイルベンザミド
4.0gの(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシルアミン(化合物C1)を40mlの塩化メチレンと10.0mlのトリエチルアミン中に溶解させる。4.9gのベンゾフェノン−4−カルボニル塩化物を100mlの塩化メチレン中に溶かした溶液を室温で滴加し、そして該混合物を、一晩撹拌した後に、それぞれ50mlの水、2Nの塩酸、炭酸水素ナトリウム飽和溶液、そして再び水で抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして濃縮させる。7.78gの表題化合物が結晶化油として得られる。
融点:119〜122.5℃
旋光度:[α]20 D=−151.7゜(c=0.2、エタノール)
B3. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−3−アセトベンザミド、つまり化合物B3は化合物C1から実施例B2に記載されるのと同様に製造される。
旋光度:[α]20 D=−151.7゜(c=0.2、エタノール)
B3. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−3−アセトベンザミド、つまり化合物B3は化合物C1から実施例B2に記載されるのと同様に製造される。
固化油
旋光度:[α]20 D=−127.1゜(c=0.2、エタノール)
B4. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−3−ベンゾイルベンザミド、つまり化合物B4は化合物C1から実施例B2に記載されるのと同様に製造される。
旋光度:[α]20 D=−127.1゜(c=0.2、エタノール)
B4. N−[(1R,2R)−2−(3,4−ジメトキシフェニル)シクロヘキシル]−3−ベンゾイルベンザミド、つまり化合物B4は化合物C1から実施例B2に記載されるのと同様に製造される。
油
旋光度:[α]20 D=−162.9゜(c=0.2、エタノール)
C1. (1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミン
(1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンと(1S,2S)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミン(化合物D1)との12.0gのラセミ体混合物及び6.2gの(−)−マンデル酸を420mlのジオキサン及び60mlのテトラヒドロフラン中に溶解させ、そして該溶液を室温で一晩撹拌する。固体を吸引濾過し、乾燥させ、100mlの炭酸水素ナトリウム飽和溶液で処理し、そして酢酸エチルで抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして減圧下に濃縮させる。4.8gの表題化合物(融点80〜81.5℃)が得られる。
旋光度:[α]20 D=−162.9゜(c=0.2、エタノール)
C1. (1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミン
(1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンと(1S,2S)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミン(化合物D1)との12.0gのラセミ体混合物及び6.2gの(−)−マンデル酸を420mlのジオキサン及び60mlのテトラヒドロフラン中に溶解させ、そして該溶液を室温で一晩撹拌する。固体を吸引濾過し、乾燥させ、100mlの炭酸水素ナトリウム飽和溶液で処理し、そして酢酸エチルで抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして減圧下に濃縮させる。4.8gの表題化合物(融点80〜81.5℃)が得られる。
比旋光度:[α]20 D=−58.5℃(c=1、エタノール)
D1. (1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンと(1S,2S)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンとのラセミ体混合物
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキシル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキシル)ベンゼンとのラセミ体混合物(化合物E1)125g及び120gの亜鉛粉末又は顆粒を1300mlのエタノール中に懸濁する。220mlの酢酸を沸点加熱して滴加する。沈殿物を吸引濾過により分離し、そしてエタノールで洗浄し、かつ濾液を減圧下に濃縮する。残留物を塩酸中に取り、そしてトルエンで抽出する。水相を50%濃度の水酸化ナトリウム溶液を用いてアルカリ性にし、沈殿物を吸引濾過により分離し、そして濾液をトルエンで抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして濃縮させる。98gの表題化合物が結晶油として得られる。
D1. (1R,2R)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンと(1S,2S)−2−(3,4−ジメトキシフェニル)−シクロヘキシルアミンとのラセミ体混合物
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキシル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキシル)ベンゼンとのラセミ体混合物(化合物E1)125g及び120gの亜鉛粉末又は顆粒を1300mlのエタノール中に懸濁する。220mlの酢酸を沸点加熱して滴加する。沈殿物を吸引濾過により分離し、そしてエタノールで洗浄し、かつ濾液を減圧下に濃縮する。残留物を塩酸中に取り、そしてトルエンで抽出する。水相を50%濃度の水酸化ナトリウム溶液を用いてアルカリ性にし、沈殿物を吸引濾過により分離し、そして濾液をトルエンで抽出する。有機相を水で硫酸ナトリウムを使用して乾燥させ、そして濃縮させる。98gの表題化合物が結晶油として得られる。
選択的に:
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキシル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキシル)ベンゼンとのラセミ体混合物(化合物E1)8.5gを400mlのメタノール中に溶解させ、そして室温で7mlのヒドラジン水和物及び2.5gのラネーニッケルにより少しずつ8時間にわたり処理する。室温で一晩撹拌した後に、反応混合物を濾過し、濾液を濃縮させ、そして残留物をシリカゲル上でトルエン/酢酸エチル/トリエチルアミンの混合物(4/2/0.5)を用いてクロマトグラフィーを行う。表題化合物が油状物として得られる。
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキシル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキシル)ベンゼンとのラセミ体混合物(化合物E1)8.5gを400mlのメタノール中に溶解させ、そして室温で7mlのヒドラジン水和物及び2.5gのラネーニッケルにより少しずつ8時間にわたり処理する。室温で一晩撹拌した後に、反応混合物を濾過し、濾液を濃縮させ、そして残留物をシリカゲル上でトルエン/酢酸エチル/トリエチルアミンの混合物(4/2/0.5)を用いてクロマトグラフィーを行う。表題化合物が油状物として得られる。
E1. 1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキシル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキシル)ベンゼンとのラセミ体混合物
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンとのラセミ体混合物(化合物F1)8.4gを450mlのメタノール中に溶解させ、そして2mlの濃塩酸で処理し、かつ10%濃度のPd/C500mgを添加して水素化させる。該反応混合物を濾過し、そして濾液を濃縮させる。融点:84〜86.5℃
F1. 1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)ベンゼンとのラセミ体混合物
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンとのラセミ体混合物(化合物G1)10.0g及び20.0gの水酸化カリウムを150mlのメタノール及び35mlのジメチルホルムアミド中に溶解させる。60mlのエタノール中の17.5mlの濃硫酸の溶液を次いで、初期温度が4℃を超過しないように滴加する。1時間撹拌した後に、該混合物を1lの氷水に添加し、沈殿物を吸引濾過し、水で洗浄し、そして乾燥させ、粗生成物をエタノール中で再結晶させる。8.6gの表題化合物(融点82.5〜84℃)が得られる。
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンとのラセミ体混合物(化合物F1)8.4gを450mlのメタノール中に溶解させ、そして2mlの濃塩酸で処理し、かつ10%濃度のPd/C500mgを添加して水素化させる。該反応混合物を濾過し、そして濾液を濃縮させる。融点:84〜86.5℃
F1. 1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)ベンゼンとのラセミ体混合物
1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)]ベンゼンとのラセミ体混合物(化合物G1)10.0g及び20.0gの水酸化カリウムを150mlのメタノール及び35mlのジメチルホルムアミド中に溶解させる。60mlのエタノール中の17.5mlの濃硫酸の溶液を次いで、初期温度が4℃を超過しないように滴加する。1時間撹拌した後に、該混合物を1lの氷水に添加し、沈殿物を吸引濾過し、水で洗浄し、そして乾燥させ、粗生成物をエタノール中で再結晶させる。8.6gの表題化合物(融点82.5〜84℃)が得られる。
G1. 1,2−ジメトキシ−4−((1R,2R)−2−ニトロシクロヘキセ−4−エニル)ベンゼンと1,2−ジメトキシ−4−((1S,2S)−2−ニトロシクロヘキセ−4−エニル)ベンゼンとのラセミ体混合物
50.0gの3,4−ジメトキシ−ω−ニトロスチレン(化合物H1)及び1.0g(9.1ミリモル)のヒドロキノンを200mlの無水トルエン中に懸濁させ、そして−70℃で55.0g(1.02モル)の液状1,3−ブタジエンで処理する。該混合物を160℃で6日間オートクレーブ中で撹拌し、次いで冷却する。幾らかの溶剤を回転蒸発器上で除去し、そして得られた沈殿物を吸引濾過し、そしてエタノール中で再結晶させる。融点:113.5〜115.5℃
H1. 3,4−ジメトキシ−ω−ニトロスチレン
207.0gの3,4−ジメトキシベンズアルデヒド、100.0gの酢酸アンモニウム及び125mlのニトロメタンを1.0lの氷酢酸中で3〜4時間にわたり沸騰するまで加熱する。氷浴中で冷却した後に、沈殿物を吸引濾過し、氷酢酸及び石油エーテルですすぎ、そして乾燥させる。融点:140〜141℃
収量:179.0g
産業上利用性
本発明による化合物は、工業的利用を可能にする有用な薬理学的特性を有する。選択的環状ヌクレオチドホスホジエステラーゼ(PDE)インヒビター(特にタイプ4)として、これらは一方で気管支治療薬(拡張拡張を原因とするが、その呼吸数又は呼吸力の増大作用をも原因とする気道障害の治療のため)として、そしてその血管拡張作用のため勃起不全の解除のために適しているが、他方では、特に疾患、特に例えば気道(喘息予防)、皮膚、腸管、眼、CNS及び関節の炎症状態の治療のために適当であり、これらはメディエーター、例えばヒスタミン、PAF(血小板活性因子)、アラキドン酸代謝物、例えばロイコトリエン及びプロスタグランジン、サイトカイン、インターロイキン、ケモカイン、α−インターフェロン、β−インターフェロン及びγ−インターフェロン、腫瘍壊死因子(TNF)又は酸素フリーラジカル及びプロテアーゼによって媒介される。本願明細書では、本発明による化合物は低い毒性、良好な腸内吸収(高い生物学的利用能)、広い治療範囲及び重篤な副作用の不在によって特徴付けられる。
50.0gの3,4−ジメトキシ−ω−ニトロスチレン(化合物H1)及び1.0g(9.1ミリモル)のヒドロキノンを200mlの無水トルエン中に懸濁させ、そして−70℃で55.0g(1.02モル)の液状1,3−ブタジエンで処理する。該混合物を160℃で6日間オートクレーブ中で撹拌し、次いで冷却する。幾らかの溶剤を回転蒸発器上で除去し、そして得られた沈殿物を吸引濾過し、そしてエタノール中で再結晶させる。融点:113.5〜115.5℃
H1. 3,4−ジメトキシ−ω−ニトロスチレン
207.0gの3,4−ジメトキシベンズアルデヒド、100.0gの酢酸アンモニウム及び125mlのニトロメタンを1.0lの氷酢酸中で3〜4時間にわたり沸騰するまで加熱する。氷浴中で冷却した後に、沈殿物を吸引濾過し、氷酢酸及び石油エーテルですすぎ、そして乾燥させる。融点:140〜141℃
収量:179.0g
産業上利用性
本発明による化合物は、工業的利用を可能にする有用な薬理学的特性を有する。選択的環状ヌクレオチドホスホジエステラーゼ(PDE)インヒビター(特にタイプ4)として、これらは一方で気管支治療薬(拡張拡張を原因とするが、その呼吸数又は呼吸力の増大作用をも原因とする気道障害の治療のため)として、そしてその血管拡張作用のため勃起不全の解除のために適しているが、他方では、特に疾患、特に例えば気道(喘息予防)、皮膚、腸管、眼、CNS及び関節の炎症状態の治療のために適当であり、これらはメディエーター、例えばヒスタミン、PAF(血小板活性因子)、アラキドン酸代謝物、例えばロイコトリエン及びプロスタグランジン、サイトカイン、インターロイキン、ケモカイン、α−インターフェロン、β−インターフェロン及びγ−インターフェロン、腫瘍壊死因子(TNF)又は酸素フリーラジカル及びプロテアーゼによって媒介される。本願明細書では、本発明による化合物は低い毒性、良好な腸内吸収(高い生物学的利用能)、広い治療範囲及び重篤な副作用の不在によって特徴付けられる。
それらのPDE阻害特性のため、本発明による化合物はヒト医学及び獣医学において療法剤として使用でき、その際、これらは、例えば以下の疾患の治療及び予防のために使用できる:種々の原因(気管支炎、アレルギー性気管支炎、気管支喘息、肺気腫、COPD)による急性および慢性の(特に炎症性およびアレルギー誘発性)気道障害、皮膚病(特に増殖性、炎症性およびアレルギー性)、例えば乾癬(尋常性)、中毒性湿疹およびアレルギー接触性湿疹、アトピー性湿疹、脂漏性湿疹、単純苔癬、日焼け、肛門性器領域の痒み症、円形脱毛症、肥厚性瘢痕、円板状エリテマトーデス、ろ胞性および広範囲の膿皮症、内因性および外因性座瘡、酒土性座瘡および他の増殖性、炎症性およびアレルギー性の皮膚疾患、TNFおよびロイコトリエンの過剰放出に基づく障害、例えば関節性の障害(リウマチ様関節炎、リウマチ様脊椎炎、変形性関節症および他の関節の症状)、免疫系の障害(AIDS、多発性硬化症)、移植片対宿主反応、移植拒否反応、ショック症状(敗血症性ショック、エンドトキシンショック、グラム陰性菌性敗血症、トキシックショック症候群およびARDS(成人呼吸窮迫症候群))、ならびに胃腸領域における全身性炎症(クローン病および潰瘍性大腸炎)、上部気道(咽頭、鼻)領域および隣接領域(副鼻腔、目)でのアレルギー性および/または慢性の免疫不全性反応に基づく疾患、例えばアレルギー性鼻炎/アレルギー性副鼻腔炎、慢性鼻炎/慢性副鼻腔炎、アレルギー性結膜炎および鼻ポリープ、さらにはPDEインヒビターによって治療することができる心臓疾患、例えば心不全、またはPDEインヒビターの組織弛緩作用から治療することができる疾患、例えば、勃起機能不全または腎臓結石に関連する腎臓および尿管の疝痛。更に、本発明の化合物は、尿崩症、真性糖尿病、白血病、骨粗鬆症及び大脳の代謝抑制に関連する症状、例えば大脳老化、老年性痴呆(アルツハイマー氏病)、パーキンソン氏病又は多発拘束性痴呆に関連する記憶障害の治療に有用であり、また中枢神経系の障害、例えば、鬱病又は動脈硬化性痴呆の治療並びに認知強化のために有用である。
更に本発明は前記の疾患の1つ以上に罹患するヒトを含む哺乳動物の治療のための方法に関する。本方法は、治療学的に有効な、かつ薬理学的に有効かつ認容性の量の本発明による1種以上の化合物を病気の哺乳動物に投与することを特徴とする。
更に本発明は病気、特に前記の病気の治療及び/又は予防における使用のための本発明による化合物に関する。
更に本発明は、PDE阻害特性、PDE4阻害特性を有する本発明による化合物に関する。
また本発明は、前記の病気の治療及び/又は予防のために使用される医薬品組成物の製造のための、本発明による化合物の使用に関する。
更に本発明は、前記の病気の治療及び/又は予防のための、1種以上の本発明による化合物を含有する医薬品組成物に関する。
更に、本発明は、包装材料及びその包装材料中に包含される医薬品からなる製品であって、該医薬品はタイプ4の環状ヌクレオチドホスホジエステラーゼ(PDE4)の作用に拮抗するため、PDE4に媒介される疾患の症状の改善のために治療学的に有効であり、かつ該包装材料は、該医薬品がPDE4に媒介される疾患の予防又は治療のために有用である旨を示すラベル又は添付文書を含み、かつ前記の医薬品が本発明による式Iの少なくとも1種の化合物を含有する製品に関する。包装材料、ラベル及び添付文書は、その他の点で、関連の利用性を有する医薬品のための標準的な包装材料、ラベル及び添付文書として一般に考慮されるものに対応又は類似するものである
該医薬品組成物は、自体公知かつ当業者によく知られた方法によって製造される。医薬品組成物としては、本発明による化合物(=有効化合物)はそれ自体で、又は有利には適当な医薬品助剤及び/又は賦形剤と組み合わせて、例えば錠剤、被覆錠剤、カプセル剤、カプレット剤、坐剤、パッチ剤(例えばTTS)、乳剤、懸濁剤、ゲル剤又は液剤の形で使用され、その際、有効化合物の含有率は有利には0.1〜95%であり、かつ助剤及び/又は賦形剤の適当な選択によって、有効化合物に厳密に適合された、及び/又は作用の所望の開始に厳密に適合された医薬品投与形(例えば遅延放出形又は腸溶形)を達成できる。
該医薬品組成物は、自体公知かつ当業者によく知られた方法によって製造される。医薬品組成物としては、本発明による化合物(=有効化合物)はそれ自体で、又は有利には適当な医薬品助剤及び/又は賦形剤と組み合わせて、例えば錠剤、被覆錠剤、カプセル剤、カプレット剤、坐剤、パッチ剤(例えばTTS)、乳剤、懸濁剤、ゲル剤又は液剤の形で使用され、その際、有効化合物の含有率は有利には0.1〜95%であり、かつ助剤及び/又は賦形剤の適当な選択によって、有効化合物に厳密に適合された、及び/又は作用の所望の開始に厳密に適合された医薬品投与形(例えば遅延放出形又は腸溶形)を達成できる。
当業者はその専門知識により所望の医薬品製剤に適した助剤又は賦形剤に精通している。溶剤、ゲル形成剤、軟膏基材及び他の有効化合物の他に、賦形剤、例えば酸化防止剤、分散剤、乳化剤、保存剤、溶解剤、着色剤、錯化剤又は侵透促進剤を使用してよい。
本発明による医薬品組成物の投与は、この分野で利用できる一般的に許容される任意の様式で実施できる。好適な投与様式の実例は、例えば静脈内、経口、経鼻、非経口、局所、経皮及び直腸内の送達である。経口送達が有利である。
呼吸管の疾患の治療のために、本発明による化合物を、有利には吸入によってエーロゾルの形で投与する;固体、液体又は混合組成のエーロゾル粒子は有利には0.5〜10μm、有利には2〜6μmの直径を有する。
エーロゾルの発生は、例えば圧力駆動のジェット噴霧器又は超音波噴霧器、有利には噴射剤駆動の計量供給エーロゾルによるか、又は吸入カプセルからの微粉化有効化合物の噴射剤不使用の投与によって実施できる。
使用される吸入系に依存して、有効化合物の他に該投与形は付加的に所望の賦形剤、例えば噴射剤(例えば計量供給エーロゾルの場合にFrigen)、界面活性剤、乳化剤、安定化剤、保存剤、フレーバー又は増量剤(例えば粉末吸入器の場合にラクトース)又は、適宜更なる有効化合物を含有する。
吸入の目的のために、多くの装置を利用でき、それを用いて最適な粒度を有するエーロゾルを発生させ、かつ患者にできる限り正しい吸入技術を使用して投与できる。アダプタ(スペーサ、エキスパンダ)及び洋ナシ型容器(例えばNebulator(R)、Volumatic(R))並びに計量供給エーロゾルのための、特に粉末吸入器の場合に吹き付け噴霧(puffer spray)を放出する自動装置(Autohaler(R))を使用する他に、種々の技術的解決策(例えばDiskhaler(R)、Rotadisk(R)、Turbohaler(R)又はEP0505321号に記載される吸入器)が利用でき、それを用いて有効化合物の最適な投与を達成できる。
皮膚病の治療のためには、本発明による化合物を、特に局所適用のために適当な医薬品組成物の形で適用する。該医薬品組成物の製造のために、本発明による化合物(=有効化合物)を有利には適当な製薬学的賦形剤と混合し、更に加工して適当な医薬品製剤を得る。適当な医薬品製剤は、例えば粉剤、乳剤、懸濁剤、スプレー剤、オイル剤、軟膏剤、脂肪軟膏剤、クリーム剤、ペースト剤、ゲル剤又は液剤である。
本発明による医薬品組成物は自体公知の方法によって製造される。有効化合物の投与は、PDEインヒビターについて慣用のオーダーで行われる。従って皮膚病の治療のための局所適用形(例えば軟膏)は有効化合物を、例えば0.1〜99%の濃度で含有する。吸入による投与のための用量は慣用に1日あたり0.1〜3mgである。全身治療(経口又は静脈内)の場合の慣用の用量は1日あたり0.03〜3mg/kgである。
生物学的調査
セカンドメッセンジャーのサイクリックAMP(cAMP)は炎症細胞及び免疫応答を担う細胞の阻害に関してよく知られている。PDE4補酵素は免疫疾患の開始及び伝播に関連する細胞において広範に発現され(H Tenor and C Schudt, in "Phosphodiestarase Inhibitors", 21-40, "The Handbook of Immunopharmacology", Academic Press, 1996)、かつその阻害は細胞内cAMP濃度の増大をもたらし、従って細胞活性の阻害をもたらす(JE Souness et al., Immunopharmacology 47: 127-162, 2000)。
セカンドメッセンジャーのサイクリックAMP(cAMP)は炎症細胞及び免疫応答を担う細胞の阻害に関してよく知られている。PDE4補酵素は免疫疾患の開始及び伝播に関連する細胞において広範に発現され(H Tenor and C Schudt, in "Phosphodiestarase Inhibitors", 21-40, "The Handbook of Immunopharmacology", Academic Press, 1996)、かつその阻害は細胞内cAMP濃度の増大をもたらし、従って細胞活性の阻害をもたらす(JE Souness et al., Immunopharmacology 47: 127-162, 2000)。
種々の動物モデルにおけるインビボでのPDE4インヒビターの抗炎症能力が記載されている(MM Teixeira, TiPS 18: 164-170, 1997)。細胞レベルでの(インビボ)PDE4阻害の調査のために、多くの種々の前炎症反応を測定できる。例は好中性(C Schudt et al., Arch Pharmacol 344: 682-690, 1991)又は好酸性(A Hatzelmann et al., Brit J Pharmacol 114: 821-831, 1995)の顆粒球のスーパーオキシド産生であり、これはルミノールで増強される化学発光として、又は単球、マクロファージ又は樹状細胞における腫瘍壊死因子αの合成として測定できる(Gantner et al., Brit J Pharmacol 121: 221-231, 1997, and Pulmonary Pharmacol Therap 12: 377-386, 1999)。更にPDE4インヒビターの免疫調節能力はサイトカイン合成又は増殖のようなT細胞応答の阻害から明らかである(DM Essayan, Biochem Pharmacol 57: 965-973, 1999)。前記の前炎症メディエーターの分泌を阻害する物質はPDE4を阻害する物質である。従って本発明による化合物によるPDE4阻害は炎症プロセス抑制の主要な指標である。
PDE4活性の阻害の測定方法
PDE4活性をThompson他(Adv Cycl Nucl Res 10: 69-92, 1979)に記載のようにして幾つかの変更を加えて(Bauer and Schwabe, Naunyn-Schmiedeberg's Arch Pharmacol 311: 193-198, 1980)測定した。200μlの最終アッセイ容量(96ウェルのマイクロタイタープレート)で、アッセイ混合物は20mMのTris(pH7.4)、5mMのMgCl2、0.5μMのcAMP、[3H]cAMP(約30000cpm/アッセイ)、試験化合物及びSchudt他(Naunyn-Schmiedeberg's Arch Pharmacol 344: 682-690, 1991)によって記載されるように主にPDE4活性を有するヒト好中球由来のサイトゾルのアリコートを含有し、汚染された血小板に由来するPDE3活性を抑制するためにPDE3特異的インヒビターのモタピゾン(1μM)を含んでいた。化合物の連続希釈をDMSO中に作成し、そして更にアッセイ物において1:100(v/v)の希釈を行って、それ自体によりPDE4活性に僅かにのみ影響するDMSO濃度1%(v/v)で所望の最終濃度のインヒビターを得た。
PDE4活性をThompson他(Adv Cycl Nucl Res 10: 69-92, 1979)に記載のようにして幾つかの変更を加えて(Bauer and Schwabe, Naunyn-Schmiedeberg's Arch Pharmacol 311: 193-198, 1980)測定した。200μlの最終アッセイ容量(96ウェルのマイクロタイタープレート)で、アッセイ混合物は20mMのTris(pH7.4)、5mMのMgCl2、0.5μMのcAMP、[3H]cAMP(約30000cpm/アッセイ)、試験化合物及びSchudt他(Naunyn-Schmiedeberg's Arch Pharmacol 344: 682-690, 1991)によって記載されるように主にPDE4活性を有するヒト好中球由来のサイトゾルのアリコートを含有し、汚染された血小板に由来するPDE3活性を抑制するためにPDE3特異的インヒビターのモタピゾン(1μM)を含んでいた。化合物の連続希釈をDMSO中に作成し、そして更にアッセイ物において1:100(v/v)の希釈を行って、それ自体によりPDE4活性に僅かにのみ影響するDMSO濃度1%(v/v)で所望の最終濃度のインヒビターを得た。
37℃で5分間プレインキュベートした後に、基質(cAMP)を添加することで反応を開始させ、そしてアッセイ物を37℃で更に15分間インキュベートする。50μlの0.2NのHClを添加して反応を停止させ、そしてアッセイ物を氷上に約10分間放置する。25μgの5′−ヌクレオチダーゼ(ガラガラヘビのヘビ毒)と一緒に37℃で10分間インキュベートした後に、アッセイ物をQAEセファデックスA−25(1mlの床容量)上にロードした。カラムを2mlの30mMのギ酸アンモニウム(pH6.0)で溶出させ、そして溶出物の放射活性を計数した。結果を全放射活性の5%未満であるブランク値(変性タンパク質の存在下に測定した)について補正した。加水分解された環状ヌクレオチドの量は元の基質濃度の30%を超過しなかった。本発明による化合物のPDE4活性の阻害についてのIC50値を濃度−阻害曲線から非線形回帰によって測定した。
本発明による化合物について測定された代表的な阻害値は以下の表Aからわかり、そこでは化合物の番号は実施例の番号に相当する。
表A
PDE4活性の阻害
PDE4活性の阻害
Claims (11)
- 式I
R1はヒドロキシル、C1〜C4−アルコキシ、C3〜C7−シクロアルコキシ、C3〜C7−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであり、
R2はヒドロキシル、C1〜C4−アルコキシ、C3〜C7−シクロアルコキシ、C3〜C7−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであるか、又は
R1及びR2は一緒になってC1〜C2−アルキレンジオキシ基であり、
R3は水素又はC1〜C4−アルキルであり、
R31は水素又はC1〜C4−アルキルであるか、又は
R3及びR31は一緒になってC1〜C4−アルキレン基であり、
R4は水素又はC1〜C4−アルキルであり、
R5は水素であり、
R51は水素であるか、又は
R5及びR51は一緒になって付加的な結合を表し、
R6は水素、ハロゲン、ニトロ、C1〜C4−アルキル、トリフルオロメチル又はC1〜C4−アルコキシであり、
R7はC1〜C4−アルキル、C3〜C7−シクロアルキル、C3〜C7−シクロアルキルメチル、ピリジニル、フェニル又はR71及び/又はR72で置換されたフェニルであり、その際、
R71はハロゲン、ヒドロキシル、シアノ、トリフルオロメチル、カルボキシル、ニトロ、C1〜C4−アルキル又はC1〜C4−アルコキシであり、
R72はC1〜C4−アルコキシ、C1〜C4−アルキル又はハロゲンであり、
R8は水素、フェニル、C1〜C4−アルキル、アリールオキシ−C2〜C4−アルキル又はR9で置換されたC1〜C4−アルキルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はハロゲン又はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はフェニル、アリール−C1〜C4−アルキル又はR911で置換されたフェニルであり、その際、
アリールはフェニル又はR81で置換されたフェニルであり、
R911はC1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、その両者が結合される窒素原子を含んで、1−ピロリジニル基、1−ピペリジニル基、1−ピペラジニル基、4−メチルピペラジン−1−イル基、4−フェニルピペラジン−1−イル基、1−ヘキサヒドロアゼピニル基又は4−モルホリニル基を表し、
R93はニトロ、C1〜C4−アルキル、C1〜C4−アルコキシカルボニル、ハロゲン、トリフルオロメチル、C1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C4−アルコキシである]の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体。 - 式Iで示され、式中、
R1はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R2はC1〜C2−アルコキシ、C3〜C5−シクロアルコキシ、C3〜C5−シクロアルキルメトキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R3は水素であり、
R31は水素であり、
R4は水素又はC1〜C2−アルキルであり、
R5は水素であり、
R51は水素であるか、又は
R5及びR51は一緒になって付加的な結合を表し、
R6は水素であり、
R7はC1〜C4−アルキル又はフェニルであり、
R8は水素、フェニル、C1〜C4−アルキル、アリールオキシ−C2〜C4−アルキル又はR9で置換されたC1〜C2−アルキルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はハロゲン又はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリール−C1〜C2−アルキル又はR911で置換されたフェニルであり、その際、
アリールはフェニル又はR81で置換されたフェニルであり、
R911はC1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−メチルピペラジン−1−イル基、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、C1〜C4−アルコキシカルボニル、ハロゲン、トリフルオロメチル、C1〜C4−アルコキシ又は完全にもしくは大部分がフッ素置換されたC1〜C2−アルコキシである、請求項1記載の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体。 - 式Iで示され、式中、
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はC1〜C2−アルキル又はフェニルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、アリールオキシエチル又はR9で置換されたメチルであり、その際、
アリールオキシはフェノキシ又はR81で置換されたフェノキシであり、その際、
R81はトリフルオロメチルであり、
R9はフェニル、C(O)N(R91)R92又はR93で置換されたフェニルであり、その際、
R91はアリールメチル又はR911で置換されたフェニルであり、その際、
アリールは塩素置換されたフェニルであり、
R911はメトキシであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表し、
R93はニトロ、メトキシカルボニル、クロロ、フルオロ、トリフルオロメチル又はメトキシである、請求項1記載の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体。 - 式Iで示され、式中、
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はメチルであり、
R8は水素、フェニル、メチル、エチル、イソブチル、フェノキシエチル、3−トリフルオロメチルフェノキシエチル又はR9で置換されたメチルであり、その際、
R9はフェニル、4−ニトロフェニル、4−メトキシカルボニルフェニル、4−クロロフェニル、3−クロロフェニル、2−クロロフェニル、4−フルオロフェニル、3−フルオロフェニル、4−トリフルオロメチルフェニル、3−トリフルオロメチルフェニル、4−メトキシフェニル、2−メトキシフェニル又はC(O)N(R91)R92であり、その際、
R91は2−メトキシフェニル又は4−クロロベンジルであり、
R92は水素であるか、又は
R91及びR92は一緒になって、両者が結合される窒素原子を含んで、4−フェニルピペラジン−1−イル基又は4−モルホリニル基を表すか、又は
R1はメトキシであり、
R2はメトキシであり、
R3、R31、R4、R5及びR51は水素であり、
R6は水素であり、
R7はフェニルであり、
R8は水素である、請求項1記載の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体。 - 式Iで示され、式中、4a位及び10b位の水素原子が互いにシス位にある、請求項1から4までのいずれか1項記載の化合物並びにそれらの塩及びこれらの化合物のE/Z異性体。
- 疾病の治療又は予防において使用するための、請求項1記載の式Iの化合物。
- 請求項1記載の式Iの化合物1種以上と一緒に慣用の医薬品賦形剤及び/又はビヒクルを含有する医薬品組成物。
- 呼吸器疾患及び/又は皮膚病の治療又は予防のための医薬品組成物の製造のための、請求項1記載の式Iの化合物及び/又はそれらの薬理学的に認容性の塩の使用。
- 患者の病気を治療するための方法において、前記患者に請求項1記載の式Iの化合物の治療学的有効量を投与することを含む方法。
- 患者の気道疾患を治療するための方法において、前記患者に請求項1記載の式Iの化合物の治療学的有効量を投与することを含む方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP03017338 | 2003-07-31 | ||
| PCT/EP2004/051680 WO2005012253A1 (en) | 2003-07-31 | 2004-07-30 | Novel 6-phenylphenanthridines |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007500686A true JP2007500686A (ja) | 2007-01-18 |
Family
ID=34112458
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006521590A Withdrawn JP2007500686A (ja) | 2003-07-31 | 2004-07-30 | 新規の6−フェニルフェナントリジン |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20060189641A1 (ja) |
| EP (1) | EP1658271A1 (ja) |
| JP (1) | JP2007500686A (ja) |
| CA (1) | CA2533636A1 (ja) |
| WO (1) | WO2005012253A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007500685A (ja) * | 2003-07-31 | 2007-01-18 | アルタナ ファルマ アクチエンゲゼルシャフト | 新規の6−フェニルフェナントリジン |
| GB0601951D0 (en) | 2006-01-31 | 2006-03-15 | Novartis Ag | Organic compounds |
| AU2007315234A1 (en) | 2006-10-30 | 2008-05-08 | Novartis Ag | Heterocyclic compounds as antiinflammatory agents |
| AU2008307195B2 (en) | 2007-10-04 | 2012-11-22 | F. Hoffmann-La Roche Ag | Cyclopropyl aryl amide derivatives and uses thereof |
| CN101910153B (zh) | 2008-01-11 | 2014-01-22 | 诺华股份有限公司 | 作为激酶抑制剂的嘧啶类 |
| UY33597A (es) | 2010-09-09 | 2012-04-30 | Irm Llc | Compuestos y composiciones como inhibidores de la trk |
| WO2012034095A1 (en) | 2010-09-09 | 2012-03-15 | Irm Llc | Compounds and compositions as trk inhibitors |
| BR112013021638A2 (pt) | 2011-02-25 | 2016-08-02 | Irm Llc | "compostos inibidores de trk, seu uso e composições que os compreendem" |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9412672D0 (en) * | 1994-06-23 | 1994-08-10 | Celltech Ltd | Chemical compounds |
| BR9707233A (pt) * | 1996-01-31 | 1999-07-20 | Byk Gulden Lomberg Chem Fab | Fenantridinas |
| US6127378A (en) * | 1996-03-26 | 2000-10-03 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Phenanthridines substituted in the 6 position |
| EP0889886B1 (de) * | 1996-03-26 | 2002-09-18 | ALTANA Pharma AG | Neue in 6-position substituierte phenanthridine |
| FR2754260B1 (fr) * | 1996-10-04 | 1998-10-30 | Adir | Nouveaux derives substitues de biphenyle ou de phenylpyridine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| AU756349B2 (en) * | 1997-07-25 | 2003-01-09 | Altana Pharma Ag | Substituted 6-phenylphenanthridines |
| ATE260899T1 (de) * | 1997-07-25 | 2004-03-15 | Altana Pharma Ag | Neue tetrazolderivate |
| AU2904300A (en) * | 1999-01-15 | 2000-08-01 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Polysubstituted 6-phenylphenanthridines with pde-iv inhibiting activity |
| CA2359449A1 (en) * | 1999-01-15 | 2000-07-20 | Beate Gutterer | Phenanthridine-n-oxides with pde-iv inhibiting activity |
| DK1147089T3 (da) * | 1999-01-15 | 2006-04-10 | Altana Pharma Ag | Phenylphenanthridiner med PDE-IV-inhiberende virkning |
| WO2002005616A1 (en) * | 2000-07-14 | 2002-01-24 | Altana Pharma Ag | Novel 6-phenylphenanthridines |
-
2004
- 2004-07-30 US US10/565,526 patent/US20060189641A1/en not_active Abandoned
- 2004-07-30 WO PCT/EP2004/051680 patent/WO2005012253A1/en not_active Ceased
- 2004-07-30 CA CA002533636A patent/CA2533636A1/en not_active Abandoned
- 2004-07-30 EP EP04766388A patent/EP1658271A1/en not_active Withdrawn
- 2004-07-30 JP JP2006521590A patent/JP2007500686A/ja not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| EP1658271A1 (en) | 2006-05-24 |
| WO2005012253A1 (en) | 2005-02-10 |
| CA2533636A1 (en) | 2005-02-10 |
| US20060189641A1 (en) | 2006-08-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4653314B2 (ja) | Pde−iv阻害作用を有するフェニルフェナントリジン | |
| JP4555684B2 (ja) | Pde4阻害剤としての、ピロリジンジオンにより置換されたピペリジン−フタラゾン | |
| JP4587295B2 (ja) | Pde4インヒビターとしての3−ヒドロキシ−6−フェニルフェナントリジン | |
| JP2005537312A (ja) | 新規のフェナントリジン | |
| JP4587294B2 (ja) | Pde4インヒビターとしての2−ヒドロキシ−6−フェニルフェナントリジン | |
| JP4223075B2 (ja) | 気管支治療薬としてのベンゾナフチリジン | |
| JP4141501B2 (ja) | 新規の6位置換フェナントリジン | |
| JP2005538137A (ja) | ピペリジン−n−オキシド誘導体 | |
| JP2002513793A (ja) | 新規n−オキシド | |
| JP2001510827A (ja) | 置換6−フェニルフェナントリジン | |
| JPH11505236A (ja) | フェニルジヒドロベンゾフラン | |
| JP2001510825A (ja) | 新規テトラゾール誘導体 | |
| AU757198B2 (en) | Benzamides with tetrahydrofuranyloxy substitutents as phosphodiesterase 4 inhibitors | |
| JP2002534506A (ja) | Pde−iv抑制作用を有する多重に置換された6−フェニルフェナントリジン | |
| US6214839B1 (en) | Substituted 6-alkylphenanthridines | |
| JP2003502278A (ja) | 新規のn−オキシド | |
| JP2002534507A (ja) | 新規6−アリールフェナントリジン | |
| JP4248245B2 (ja) | 6−フェニルベンゾナフチリジン | |
| JP2002534505A (ja) | 新規フェナントリジン−n−オキシド | |
| JP2007500685A (ja) | 新規の6−フェニルフェナントリジン | |
| EP1303506B1 (en) | 6-heteroarylphenanthridines | |
| JP2007500686A (ja) | 新規の6−フェニルフェナントリジン | |
| JP2002519423A (ja) | Ped阻害作用を有する新規ベンゾオキサゾール | |
| JP2003519686A (ja) | フェナントリジン−n−オキシド | |
| JP2008532980A (ja) | アミド置換された6−フェニルフェナントリジン |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070727 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20091127 |