KR20180038834A - 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 - Google Patents
유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 Download PDFInfo
- Publication number
- KR20180038834A KR20180038834A KR1020160129959A KR20160129959A KR20180038834A KR 20180038834 A KR20180038834 A KR 20180038834A KR 1020160129959 A KR1020160129959 A KR 1020160129959A KR 20160129959 A KR20160129959 A KR 20160129959A KR 20180038834 A KR20180038834 A KR 20180038834A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- unsubstituted
- independently
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 C*(*)c1cccc2c1c(cccc1)c1[s]2 Chemical compound C*(*)c1cccc2c1c(cccc1)c1[s]2 0.000 description 3
- QIGMSDDNSGIBTA-UHFFFAOYSA-N Brc1cc(-c2cccc3c2c(cccc2)c2[s]3)ccc1 Chemical compound Brc1cc(-c2cccc3c2c(cccc2)c2[s]3)ccc1 QIGMSDDNSGIBTA-UHFFFAOYSA-N 0.000 description 1
- WEBZPWOIHJAAEC-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2c(c(cccc3)c3[s]3)c3ccc2)nc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2c(c(cccc3)c3[s]3)c3ccc2)nc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)n1 WEBZPWOIHJAAEC-UHFFFAOYSA-N 0.000 description 1
- PZPGMNWRISZFOW-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2c(c3ccccc3[s]3)c3ccc2)nc(-c2cc(-c3cccc(-c4ccccc4)c3)ccc2)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2c(c3ccccc3[s]3)c3ccc2)nc(-c2cc(-c3cccc(-c4ccccc4)c3)ccc2)n1 PZPGMNWRISZFOW-UHFFFAOYSA-N 0.000 description 1
- VEMDAMFBPQKZLL-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cc(cccc3)c3cc2)nc(-c2c(c3ccccc3[s]3)c3ccc2)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cc(cccc3)c3cc2)nc(-c2c(c3ccccc3[s]3)c3ccc2)n1 VEMDAMFBPQKZLL-UHFFFAOYSA-N 0.000 description 1
- NLVFMJANPXBHOQ-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cccc3ccccc23)nc(-c2c(c3ccccc3[s]3)c3ccc2)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cccc3ccccc23)nc(-c2c(c3ccccc3[s]3)c3ccc2)n1 NLVFMJANPXBHOQ-UHFFFAOYSA-N 0.000 description 1
- CWEICZPGILOQEQ-UHFFFAOYSA-N c(cc1)ccc1-c1cccc(-c2nc(-c3c(c4ccccc4[s]4)c4ccc3)nc(-c3cccc(-c4ccccc4)c3)n2)c1 Chemical compound c(cc1)ccc1-c1cccc(-c2nc(-c3c(c4ccccc4[s]4)c4ccc3)nc(-c3cccc(-c4ccccc4)c3)n2)c1 CWEICZPGILOQEQ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- H01L51/0074—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- H01L51/0067—
-
- H01L51/0073—
-
- H01L51/5024—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/653—Aromatic compounds comprising a hetero atom comprising only oxygen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K99/00—Subject matter not provided for in other groups of this subclass
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/90—Multiple hosts in the emissive layer
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
상기 화학식 1 및 2에 대한 상세 내용은 명세서에서 정의한 바와 같다.
Description
| 합성실시예 | 사용 중간체 (사용량) | 생성물 구조 |
수득량 (수율) |
LC/MS M+1=g/mol |
|
| 보론 중간체 | 할로겐 중간체 | ||||
| 합성실시예 1 | M-8 (6.8g) |
M-18 (12.6g) |
A-2 | 15.5g (91%) |
568.32 |
| 합성실시예 2 | M-13 (11.6g) |
M-21 (10.3g) |
A-21 | 15.2g (89%) |
568.25 |
| 합성실시예 3 | M-14 (11.6g) |
M-18 (12.6g) |
A-43 | 17.8g (92%) |
644.28 |
| 합성실시예 4 | M-4 (6.4g) |
M-20 (12.6g) |
A-63 | 14.6g (88%) |
552.19 |
| 합성실시예 5 | M-12 (11.1g) |
M-15 (14.8g) |
A-98 | 18.3g (87%) |
702.29 |
| 합성실시예 6 | M-4 (6.4g) |
M-19 (12.6g) |
D-14 | 14.0g (85%) |
551.31 |
| 합성실시예 7 | M-14 (11.6g) |
2,4-디클로로-6-페닐-1,3,5-트리아진 (3.4g) |
B-9 | 8.9g (87%) |
685.21 |
| 합성실시예 8 | M-4 (6.4g) |
M-22 (5.7g) |
B-107 | 8.7g (90%) |
642.22 |
| 합성실시예 9 | M-4 (6.4g) |
M-17 (5.9g) |
C-27 | 8.1g (82%) |
656.30 |
| 합성실시예 10 | M-12 (11.1g) |
4,6-디클로로-2-페닐피리미딘 (3.4g) |
E-21 | 8.0g (83%) |
641.20 |
| 실시예 | 제1호스트 | 제2 호스트 | 제1호스트: 제2호스트 (wt/wt) |
구동 전압 (V) |
발광 효율 (cd/A) |
색 | 수명T95 (h) |
| 실시예 1 | A-43 | HT-130 | 3:7 | 4.85 | 41.5 | 녹색 | 395 |
| 실시예 2 | A-63 | HT-130 | 3:7 | 4.94 | 45.6 | 녹색 | 424 |
| 실시예 3 | A-98 | HT-130 | 3:7 | 4.68 | 47.8 | 녹색 | 585 |
| 실시예 5 | B-9 | HT-130 | 3:7 | 4.98 | 49.0 | 녹색 | 405 |
| 실시예 6 | C-27 | HT-31 | 3:7 | 4.70 | 48.7 | 녹색 | 480 |
| 실시예 7 | A-98 | HT-31 | 1:1 | 4.45 | 46.2 | 녹색 | 505 |
| 실시예 8 | A-43 | HT-138 | 3:7 | 4.88 | 42.5 | 녹색 | 400 |
| 실시예 9 | A-63 | HT-138 | 3:7 | 4.90 | 46.9 | 녹색 | 420 |
| 실시예 10 | A-98 | HT-138 | 3:7 | 4.70 | 49.8 | 녹색 | 580 |
| 실시예 12 | B-9 | HT-138 | 3:7 | 5.00 | 50.0 | 녹색 | 415 |
| 실시예 13 | C-27 | HT-138 | 3:7 | 4.69 | 49.9 | 녹색 | 470 |
| 실시예 14 | A-98 | HT-138 | 1:1 | 4.50 | 46.7 | 녹색 | 510 |
| 비교예 5 | ET-2 | HT-130 | 3:7 | 5.45 | 45.0 | 녹색 | 360 |
| 비교예 6 | ET-3 | HT-130 | 3:7 | 5.37 | 44.2 | 녹색 | 290 |
| 비교예 7 | ET-2 | HT-130 | 1:1 | 5.25 | 44.0 | 녹색 | 330 |
| 실시예 | 제1호스트 | 제2 호스트 | 제1호스트: 제2호스트 (wt/wt) |
구동 전압 (V) |
발광 효율 (cd/A) |
색 | 수명T95 (h) |
| 실시예 4 | D-14 | HT-130 | 3:7 | 5.10 | 46.9 | 녹색 | 365 |
| 실시예 11 | D-14 | HT-138 | 3:7 | 5.15 | 47.5 | 녹색 | 370 |
| 비교예 1 | ET-1 | - | - | 5.85 | 24.8 | 녹색 | 55 |
| 비교예 4 | ET-1 | HT-130 | 3:7 | 5.95 | 39.5 | 녹색 | 125 |
| 실시예 | 제1호스트 | 제2 호스트 | 제1호스트: 제2호스트 (wt/wt) |
구동 전압 (V) |
발광 효율 (cd/A) |
색 | 수명T95 (h) |
| 실시예 15 | B-9 | - | - | 4.25 | 26.9 | 녹색 | 180 |
| 실시예 16 | A-98 | - | - | 4.15 | 29.1 | 녹색 | 210 |
| 비교예 1 | ET-1 | - | - | 5.85 | 24.8 | 녹색 | 55 |
| 비교예 2 | ET-2 | - | - | 5.25 | 25.5 | 녹색 | 160 |
| 비교예 3 | ET-3 | - | - | 5.15 | 24.0 | 녹색 | 115 |
105: 유기층
110: 음극
120: 양극
130: 발광층
140: 정공 보조층
Claims (12)
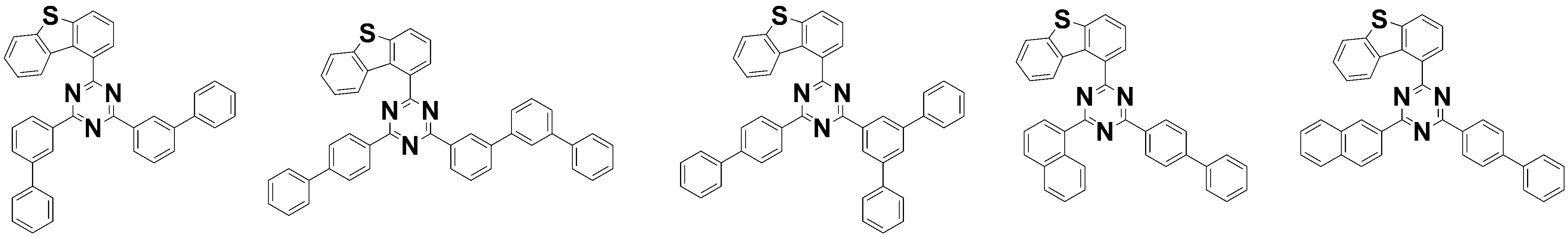
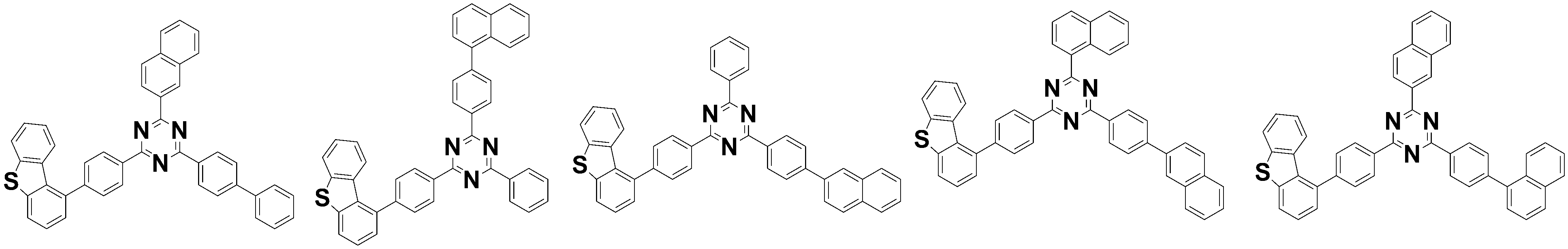
- 하기 화학식 1로 표현되는 제1 호스트 화합물; 및 하기 화학식 2로 표현되는 제2 호스트 화합물
을 포함하는 유기 광전자 소자용 조성물:
[화학식 1]
상기 화학식 1에서,
X는 O 또는 S이고,
L1 내지 L3은 각각 독립적으로 단일결합, 또는 치환 또는 비치환된 C6 내지 C20 아릴렌기이고,
X1 내지 X3은 각각 독립적으로 N 또는 CRa이고,
X1 내지 X3 중 적어도 둘은 N이고,
R1 내지 R3은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 치환 또는 비치환된 C6 내지 C12 아릴기, 또는 이들의 조합이고,
Ra는 수소, 중수소, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기, 또는 이들의 조합이고,
Rb, 및 Rc은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기, 또는 이들의 조합이고,
상기 화학식 1의 "치환"이란, 적어도 하나의 수소가 중수소, C6 내지 C30 아릴기, 디벤조퓨란일기, 또는 디벤조티오펜일기로 치환된 것을 의미하고;
[화학식 2]
상기 화학식 2에서,
Y1 및 Y2는 각각 독립적으로 단일 결합, 치환 또는 비치환된 C6 내지 C30 아릴렌기, 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기, 또는 이들의 조합이고,
Z1 및 Z2은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 또는 이들의 조합이고,
R4 내지 R9은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 C2 내지 C30 헤테로고리기, 또는 이들의 조합이고,
m은 0 내지 2의 정수 중 하나이고;
상기 화학식 2의 "치환"이란, 적어도 하나의 수소가 중수소, C1 내지 C4 알킬기, C6 내지 C18 아릴기, 또는 C2 내지 C30 헤테로아릴기로 치환된 것을 의미한다. - 제1항에 있어서,
상기 화학식 1은 하기 화학식 1-A, 화학식 1-B, 및 화학식 1-C 중 어느 하나로 표현되는 유기 광전자 소자용 조성물:
[화학식 1-A] [화학식 1-B] [화학식 1-C]
상기 화학식 1-A, 화학식 1-B, 및 화학식 1-C에서,
X는 O 또는 S이고,
L1 내지 L3은 각각 독립적으로 단일결합, 또는 치환 또는 비치환된 C6 내지 C20 아릴렌기이고,
R1 내지 R3은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C10 알킬기, 치환 또는 비치환된 C6 내지 C12 아릴기, 또는 이들의 조합이고,
Ra는 수소, 중수소, 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기, 또는 이들의 조합이고,
Rb, 및 Rc은 각각 독립적으로 치환 또는 비치환된 C6 내지 C30 아릴기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 디벤조티오펜일기, 또는 이들의 조합이다. - 제1항에 있어서,
상기 Ra는 수소, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트레닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기, 또는 치환 또는 비치환된 디벤조티오펜일기이고,
상기 Rb 및 Rc는 각각 독립적으로, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 페난트레닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기, 또는 치환 또는 비치환된 디벤조티오펜일기인 유기 광전자 소자용 조성물. - 제1항에 있어서,
L1 내지 L3은 각각 독립적으로 단일결합, para-페닐렌기, meta-페닐렌기, 또는 바이페닐렌기이고,
R1 내지 R3은 각각 독립적으로 수소이고,
상기 Ra는 수소, 또는 페닐기이고,
상기 Rb 및 Rc는 각각 독립적으로, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기, 또는 치환 또는 비치환된 디벤조티오펜일기이며,
상기 "치환"이란, 적어도 하나의 수소가 페닐기, 바이페닐기, 터페닐기, 나프틸기, 트리페닐렌기, 디벤조퓨란일기, 또는 디벤조티오펜일기로 치환된 것을 의미하는 것인 유기 광전자 소자용 조성물. - 제1항에 있어서,
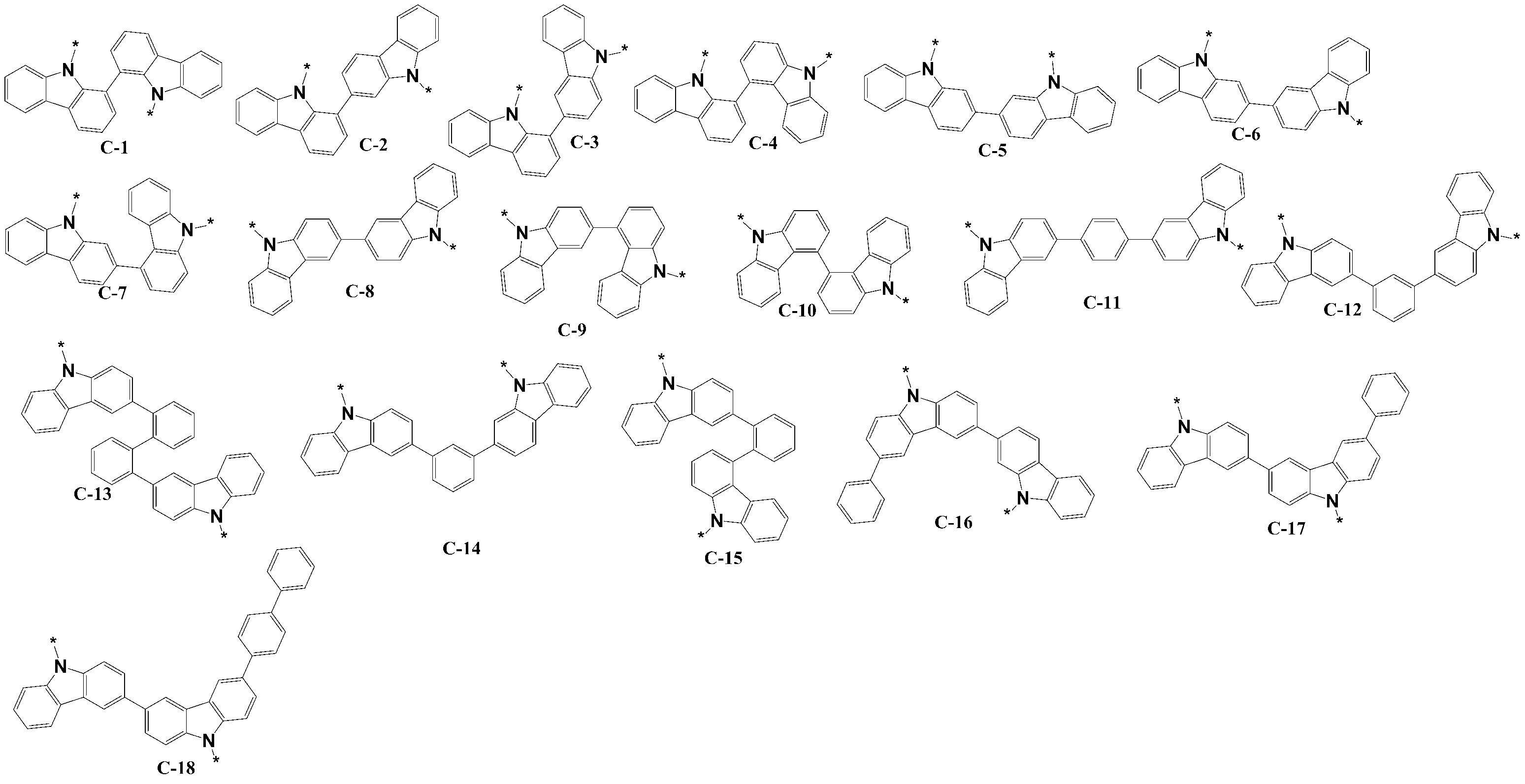
상기 화학식 2의 Z1 및 Z2은 각각 독립적으로, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 나프틸기, 치환 또는 비치환된 안트라세닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 퀴나졸일기, 치환 또는 비치환된 디벤조티오펜일기, 치환 또는 비치환된 디벤조퓨란일기, 치환 또는 비치환된 카바졸일기, 치환 또는 비치환된 플루오레닐기, 또는 이들의 조합인 유기 광전자 소자용 조성물. - 제7항에 있어서,
상기 화학식 2는 상기 그룹 Ⅲ의 화학식 C-8 또는 화학식 C-17로 표현되고,
상기 *-Y1-Z1 및 *-Y2-Z2은 상기 그룹 Ⅳ의 B-1 내지 B-6에서 선택되는 유기 광전자 소자용 조성물. - 제1항에 있어서,
상기 화학식 1은 하기 화학식 1-A 또는 화학식 1-B로 표현되고,
상기 화학식 2는 하기 화학식 C-8 또는 화학식 C-17로 표현되며,
상기 화학식 2의 *-Y1-Z1 및 *-Y2-Z2은 B-1, B-2, B-3, B-5 및 B-6에서 선택되는 유기 광전자 소자용 조성물:
[화학식 1-A] [화학식 1-B]
상기 화학식 1-A, 및 화학식 1-B에서,
X는 O 또는 S이고,
L1 내지 L3은 각각 독립적으로 단일결합, para-페닐렌기, meta-페닐렌기, 또는 바이페닐렌기이고,
R1 내지 R3은 각각 독립적으로 수소이고,
상기 Ra는 수소, 또는 페닐기이고,
상기 Rb 및 Rc는 각각 독립적으로, 치환 또는 비치환된 페닐기, 치환 또는 비치환된 바이페닐기, 치환 또는 비치환된 터페닐기, 치환 또는 비치환된 트리페닐렌기, 치환 또는 비치환된 디벤조퓨란일기, 또는 치환 또는 비치환된 디벤조티오펜일기이며,
상기 "치환"이란, 적어도 하나의 수소가 페닐기, 바이페닐기, 터페닐기, 나프틸기, 트리페닐렌기, 디벤조퓨란일기, 또는 디벤조티오펜일기로 치환된 것을 의미한다. - 서로 마주하는 양극과 음극, 그리고
상기 양극과 상기 음극 사이에 위치하는 적어도 한 층의 유기층을 포함하고,
상기 유기층은 제1항 내지 제9항 중 어느 한 항에 따른 유기 광전자 소자용 조성물을 포함하는 유기 광전자 소자. - 제10항에 있어서,
상기 유기층은 발광층을 포함하고,
상기 유기 광전자 소자용 조성물은 상기 발광층의 호스트로서 포함되는 유기 광전자 소자. - 제10항에 따른 유기 광전자 소자를 포함하는 표시장치.
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160129959A KR20180038834A (ko) | 2016-10-07 | 2016-10-07 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| CN201780059494.2A CN109791981A (zh) | 2016-10-07 | 2017-05-24 | 用于有机光电子元件的组合物、有机光电子元件及显示器件 |
| PCT/KR2017/005409 WO2018066783A1 (ko) | 2016-10-07 | 2017-05-24 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| US16/332,843 US20190214573A1 (en) | 2016-10-07 | 2017-05-24 | Composition for organic optoelectronic device, organic optoelectronic device, and display device |
| US18/210,280 US12289993B2 (en) | 2016-10-07 | 2023-06-15 | Composition for organic optoelectronic device, organic optoelectronic device, and display device |
| US18/387,540 US12225815B2 (en) | 2016-10-07 | 2023-11-07 | Composition for organic optoelectronic device, organic optoelectronic device, and display device |
| US18/387,545 US12310232B2 (en) | 2016-10-07 | 2023-11-07 | Composition for organic optoelectronic device, organic optoelectronic device, and display device |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160129959A KR20180038834A (ko) | 2016-10-07 | 2016-10-07 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180038834A true KR20180038834A (ko) | 2018-04-17 |
Family
ID=61831364
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160129959A Ceased KR20180038834A (ko) | 2016-10-07 | 2016-10-07 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
Country Status (4)
| Country | Link |
|---|---|
| US (4) | US20190214573A1 (ko) |
| KR (1) | KR20180038834A (ko) |
| CN (1) | CN109791981A (ko) |
| WO (1) | WO2018066783A1 (ko) |
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019209037A1 (ko) * | 2018-04-25 | 2019-10-31 | 주식회사 엘지화학 | 화합물 및 이를 포함한 유기 발광 소자 |
| WO2019212289A1 (ko) * | 2018-05-04 | 2019-11-07 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2020032428A1 (ko) * | 2018-08-09 | 2020-02-13 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물을 포함하는 유기전기소자 및 그 전자 장치 |
| WO2020032424A1 (ko) * | 2018-08-09 | 2020-02-13 | 덕산네오룩스 주식회사 | 이종 화합물의 혼합물을 호스트로 포함하는 유기전기소자 및 그 전자 장치 |
| KR20200029784A (ko) * | 2018-09-11 | 2020-03-19 | 두산솔루스 주식회사 | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 |
| DE102021108423A1 (de) | 2020-04-06 | 2021-10-07 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20210124018A (ko) | 2020-04-06 | 2021-10-14 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료, 및 이를 포함하는 유기 전계 발광 소자 |
| KR20210133891A (ko) * | 2020-04-29 | 2021-11-08 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2022055155A1 (ko) * | 2020-09-11 | 2022-03-17 | 엘티소재주식회사 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| DE102021126733A1 (de) | 2020-10-19 | 2022-04-21 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20220051794A (ko) | 2020-10-19 | 2022-04-26 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| DE102022113160A1 (de) | 2021-05-26 | 2022-12-01 | Rohm And Haas Electronic Materials Korea Ltd. | Mehrere wirtsmaterialien, organische elektrolumineszierende verbindung und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20220159884A (ko) | 2021-05-26 | 2022-12-05 | 롬엔드하스전자재료코리아유한회사 | 복수 종의 호스트 재료, 유기 전계 발광 화합물, 및 이를 포함하는 유기 전계 발광 소자 |
| US12096688B2 (en) | 2020-07-03 | 2024-09-17 | Samsung Sdi Co., Ltd. | Composition for organic optoelectronic device, organic optoelectronic device and display device |
| US12120900B2 (en) | 2018-09-14 | 2024-10-15 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting device, light-emitting apparatus, electronic device, and lighting device |
| US12507589B2 (en) | 2018-09-04 | 2025-12-23 | Lg Chem, Ltd. | Organic light emitting device |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101849747B1 (ko) | 2016-07-20 | 2018-05-31 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| US11807632B2 (en) * | 2018-10-22 | 2023-11-07 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting device comprising the same |
| CN111808082B (zh) * | 2019-04-11 | 2023-10-17 | 北京鼎材科技有限公司 | 一种发光材料及其应用 |
| CN112851645B (zh) * | 2019-11-28 | 2023-06-23 | 南京高光半导体材料有限公司 | 一种基于三嗪环结构的有机电致发光材料及有机电致发光器件 |
| KR102495278B1 (ko) * | 2020-03-23 | 2023-02-01 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102645135B1 (ko) | 2020-06-02 | 2024-03-06 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102689562B1 (ko) | 2020-06-09 | 2024-07-26 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102689558B1 (ko) | 2020-06-30 | 2024-07-26 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102689561B1 (ko) * | 2020-07-29 | 2024-07-26 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102761653B1 (ko) * | 2020-09-04 | 2025-01-31 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| US20240107884A1 (en) * | 2021-02-19 | 2024-03-28 | Lg Chem, Ltd. | Organic light emitting device |
| KR102807138B1 (ko) * | 2021-02-25 | 2025-05-12 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102787040B1 (ko) * | 2021-02-26 | 2025-03-25 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102756338B1 (ko) * | 2021-12-10 | 2025-01-21 | 엘티소재주식회사 | 헤테로고리 화합물, 이를 포함하는 유기 발광 소자 및 유기 발광 소자의 유기물층용 조성물 |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004346082A (ja) * | 2003-09-16 | 2004-12-09 | Tetsuya Nishio | 第3級アミン化合物およびそれを使用した有機半導体装置 |
| US7651791B2 (en) | 2005-12-15 | 2010-01-26 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and electroluminescence device employing the same |
| KR101288304B1 (ko) * | 2006-01-27 | 2013-07-18 | 삼성디스플레이 주식회사 | 유기 발광 화합물 및 이를 구비한 유기 발광 소자 |
| KR100910150B1 (ko) | 2008-04-02 | 2009-08-03 | (주)그라쎌 | 신규한 유기 발광 화합물 및 이를 발광재료로서 채용하고있는 유기 발광 소자 |
| US8759818B2 (en) | 2009-02-27 | 2014-06-24 | E I Du Pont De Nemours And Company | Deuterated compounds for electronic applications |
| TWI492944B (zh) | 2010-05-21 | 2015-07-21 | Semiconductor Energy Lab | 三唑衍生物,以及使用此三唑衍生物之發光元件、發光裝置、電子裝置與照明裝置 |
| EP2590967B1 (en) | 2010-07-08 | 2019-05-15 | UDC Ireland Limited | Use of dibenzofurans and dibenzothiophenes substituted by nitrogen-bonded five-membered heterocyclic rings in organic electronics |
| JP6007467B2 (ja) | 2010-07-27 | 2016-10-12 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、 |
| US20120085992A1 (en) * | 2010-09-30 | 2012-04-12 | The Regents Of The University Of California | Furan Conjugated Polymers Useful for Photovoltaic Applications |
| TWI520952B (zh) | 2010-11-18 | 2016-02-11 | 半導體能源研究所股份有限公司 | 二唑衍生物,及使用該二唑衍生物之發光元件,發光裝置,電子裝置,和照明裝置 |
| KR101910030B1 (ko) | 2010-11-30 | 2018-10-19 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 벤조옥사졸 유도체, 발광 소자, 발광 장치, 전자기기 및 조명 장치 |
| WO2012087960A1 (en) | 2010-12-20 | 2012-06-28 | E. I. Du Pont De Nemours And Company | Triazine derivatives for electronic applications |
| JP2012197496A (ja) | 2011-03-22 | 2012-10-18 | Sumitomo Electric Ind Ltd | 複合部材 |
| US9466802B2 (en) * | 2011-09-12 | 2016-10-11 | Nippon Steel & Sumikin Chemical Co., Ltd. | Organic electroluminescent element |
| KR102191022B1 (ko) | 2012-04-18 | 2020-12-14 | 에스에프씨 주식회사 | 이형고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR101423067B1 (ko) | 2012-10-04 | 2014-07-29 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP6357422B2 (ja) | 2012-12-17 | 2018-07-11 | 新日鉄住金化学株式会社 | 有機電界発光素子 |
| WO2014123369A1 (ko) | 2013-02-06 | 2014-08-14 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 전자 소자 |
| JP6317544B2 (ja) * | 2013-02-15 | 2018-04-25 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および電子機器 |
| CN103232843B (zh) | 2013-04-18 | 2015-02-25 | 烟台万润精细化工股份有限公司 | 一种电致发光材料及其应用 |
| KR101672074B1 (ko) | 2013-05-07 | 2016-11-02 | 주식회사 엘지화학 | 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 |
| KR101649683B1 (ko) * | 2013-09-06 | 2016-08-19 | 제일모직 주식회사 | 유기광전자소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR101618409B1 (ko) | 2013-10-10 | 2016-05-04 | 주식회사 두산 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20150074603A (ko) * | 2013-12-24 | 2015-07-02 | 희성소재 (주) | 플루오렌계 화합물 및 이를 이용한 유기발광소자 |
| KR101788094B1 (ko) | 2014-01-09 | 2017-10-19 | 제일모직 주식회사 | 유기 화합물, 유기 광전자 소자 및 표시 장치 |
| EP2907815B1 (en) * | 2014-02-12 | 2023-12-06 | Samsung Electronics Co., Ltd. | Condensed cyclic compound and organic light-emitting device including the same |
| KR20150110101A (ko) * | 2014-03-24 | 2015-10-02 | (주)피엔에이치테크 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| KR101537500B1 (ko) | 2014-04-04 | 2015-07-20 | 주식회사 엘지화학 | 유기 발광 소자 |
| EP3140302B1 (de) * | 2014-05-05 | 2019-08-21 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| EP3180411B1 (de) | 2014-08-13 | 2018-08-29 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| US10749113B2 (en) * | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP6575921B2 (ja) | 2015-09-15 | 2019-09-18 | エルジー・ケム・リミテッド | ヘテロ環化合物およびこれを含む有機発光素子 |
| TWI789025B (zh) * | 2016-08-19 | 2023-01-01 | 日商九州有機光材股份有限公司 | 電荷輸送材料、化合物、延遲螢光材料及有機發光元件 |
-
2016
- 2016-10-07 KR KR1020160129959A patent/KR20180038834A/ko not_active Ceased
-
2017
- 2017-05-24 US US16/332,843 patent/US20190214573A1/en not_active Abandoned
- 2017-05-24 WO PCT/KR2017/005409 patent/WO2018066783A1/ko not_active Ceased
- 2017-05-24 CN CN201780059494.2A patent/CN109791981A/zh active Pending
-
2023
- 2023-06-15 US US18/210,280 patent/US12289993B2/en active Active
- 2023-11-07 US US18/387,545 patent/US12310232B2/en active Active
- 2023-11-07 US US18/387,540 patent/US12225815B2/en active Active
Cited By (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111971289A (zh) * | 2018-04-25 | 2020-11-20 | 株式会社Lg化学 | 化合物和包含其的有机发光器件 |
| KR20190124162A (ko) * | 2018-04-25 | 2019-11-04 | 주식회사 엘지화학 | 화합물 및 이를 포함한 유기 발광 소자 |
| CN111971289B (zh) * | 2018-04-25 | 2023-12-08 | 株式会社Lg化学 | 化合物和包含其的有机发光器件 |
| US11980089B2 (en) | 2018-04-25 | 2024-05-07 | Lg Chem, Ltd. | Compound and organic light emitting device comprising same |
| WO2019209037A1 (ko) * | 2018-04-25 | 2019-10-31 | 주식회사 엘지화학 | 화합물 및 이를 포함한 유기 발광 소자 |
| WO2019212289A1 (ko) * | 2018-05-04 | 2019-11-07 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US12268087B2 (en) | 2018-05-04 | 2025-04-01 | Duk San Neolux Co., Ltd. | Compound for organic electronic element, organic electronic element using same and electronic device thereof |
| WO2020032428A1 (ko) * | 2018-08-09 | 2020-02-13 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물을 포함하는 유기전기소자 및 그 전자 장치 |
| KR20200017727A (ko) * | 2018-08-09 | 2020-02-19 | 덕산네오룩스 주식회사 | 이종 화합물의 혼합물을 호스트로 포함하는 유기전기소자 및 그 전자 장치 |
| WO2020032424A1 (ko) * | 2018-08-09 | 2020-02-13 | 덕산네오룩스 주식회사 | 이종 화합물의 혼합물을 호스트로 포함하는 유기전기소자 및 그 전자 장치 |
| US12507589B2 (en) | 2018-09-04 | 2025-12-23 | Lg Chem, Ltd. | Organic light emitting device |
| KR20200029784A (ko) * | 2018-09-11 | 2020-03-19 | 두산솔루스 주식회사 | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 |
| US12120900B2 (en) | 2018-09-14 | 2024-10-15 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting device, light-emitting apparatus, electronic device, and lighting device |
| KR20240068613A (ko) | 2020-04-06 | 2024-05-17 | 듀폰스페셜티머터리얼스코리아 유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료, 및 이를 포함하는 유기 전계 발광 소자 |
| KR20240069703A (ko) | 2020-04-06 | 2024-05-20 | 듀폰스페셜티머터리얼스코리아 유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료, 및 이를 포함하는 유기 전계 발광 소자 |
| KR20250179699A (ko) | 2020-04-06 | 2025-12-30 | 듀폰스페셜티머터리얼스코리아 유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료, 및 이를 포함하는 유기 전계 발광 소자 |
| DE102021108423A1 (de) | 2020-04-06 | 2021-10-07 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20210124018A (ko) | 2020-04-06 | 2021-10-14 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료, 및 이를 포함하는 유기 전계 발광 소자 |
| KR20210133891A (ko) * | 2020-04-29 | 2021-11-08 | 주식회사 엘지화학 | 유기 발광 소자 |
| US12096688B2 (en) | 2020-07-03 | 2024-09-17 | Samsung Sdi Co., Ltd. | Composition for organic optoelectronic device, organic optoelectronic device and display device |
| CN116075508A (zh) * | 2020-09-11 | 2023-05-05 | Lt素材株式会社 | 杂环化合物及包括其的有机发光元件 |
| WO2022055155A1 (ko) * | 2020-09-11 | 2022-03-17 | 엘티소재주식회사 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20220034663A (ko) * | 2020-09-11 | 2022-03-18 | 엘티소재주식회사 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| JP2023542097A (ja) * | 2020-09-11 | 2023-10-05 | エルティー・マテリアルズ・カンパニー・リミテッド | ヘテロ環化合物およびそれを含む有機発光素子 |
| DE102021126733A1 (de) | 2020-10-19 | 2022-04-21 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20220051794A (ko) | 2020-10-19 | 2022-04-26 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| KR20220159884A (ko) | 2021-05-26 | 2022-12-05 | 롬엔드하스전자재료코리아유한회사 | 복수 종의 호스트 재료, 유기 전계 발광 화합물, 및 이를 포함하는 유기 전계 발광 소자 |
| DE102022113160A1 (de) | 2021-05-26 | 2022-12-01 | Rohm And Haas Electronic Materials Korea Ltd. | Mehrere wirtsmaterialien, organische elektrolumineszierende verbindung und diese umfassende organische elektrolumineszierende vorrichtung |
Also Published As
| Publication number | Publication date |
|---|---|
| US20240090325A1 (en) | 2024-03-14 |
| US20240099129A1 (en) | 2024-03-21 |
| US12289993B2 (en) | 2025-04-29 |
| US20230329097A1 (en) | 2023-10-12 |
| US12310232B2 (en) | 2025-05-20 |
| WO2018066783A1 (ko) | 2018-04-12 |
| US20190214573A1 (en) | 2019-07-11 |
| US12225815B2 (en) | 2025-02-11 |
| CN109791981A (zh) | 2019-05-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20180038834A (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR101947747B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102146792B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시 장치 | |
| KR101888934B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시장치 | |
| KR102368409B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR101958833B1 (ko) | 유기 광전자 소자 및 표시 장치 | |
| TW202026290A (zh) | 用於有機光電裝置的化合物和組成物及有機光電裝置和顯示裝置 | |
| KR102232510B1 (ko) | 인광 호스트용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102063663B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR20130077473A (ko) | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 | |
| KR101986261B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 및 이를 포함하는 유기 광전자 소자 및 표시장치 | |
| KR20240010328A (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102118142B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시 장치 | |
| KR101627754B1 (ko) | 화합물, 이를 포함하는 유기 광전자 소자 및 표시장치 | |
| KR102160270B1 (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102094942B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102018238B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR101962756B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102129508B1 (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102146790B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102011907B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102005867B1 (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102787040B1 (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102922958B1 (ko) | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 | |
| KR102430047B1 (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20161007 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20171130 Comment text: Request for Examination of Application Patent event code: PA02011R01I Patent event date: 20161007 Comment text: Patent Application |
|
| PG1501 | Laying open of application | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20190122 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20190611 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20190122 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |