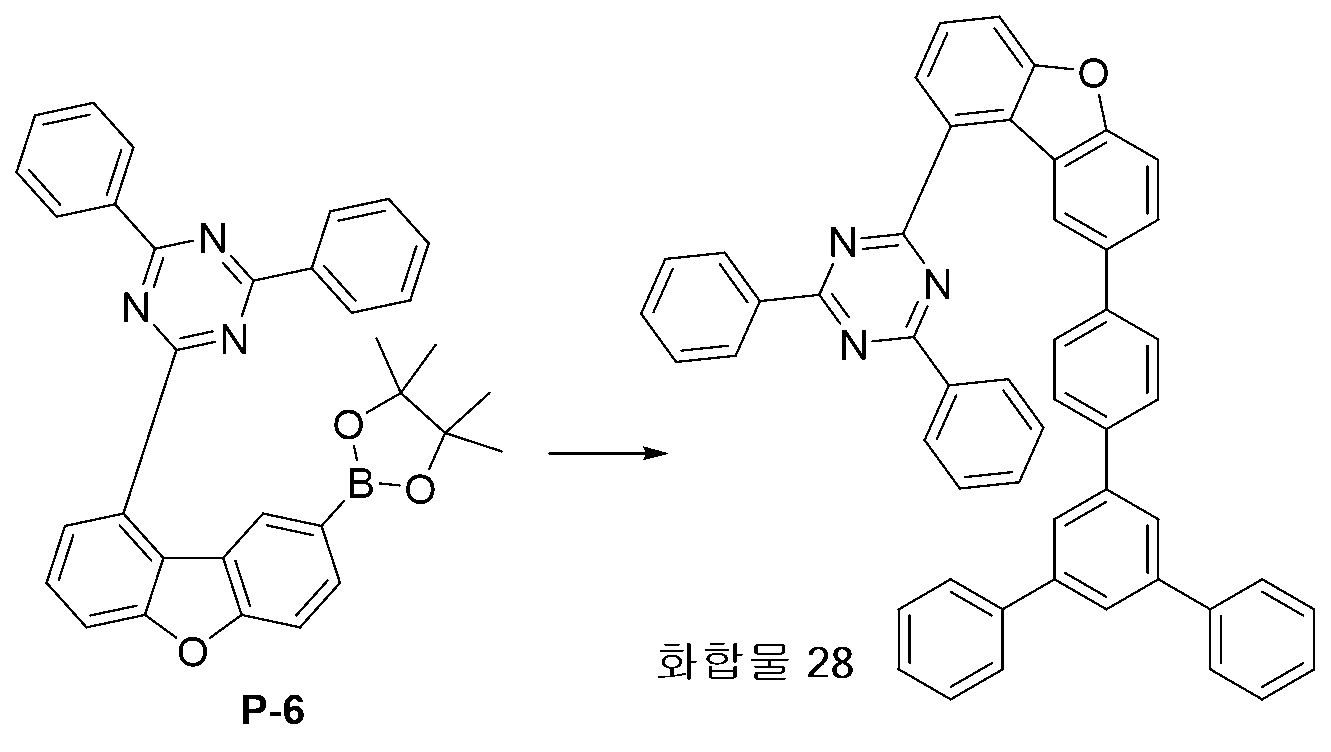
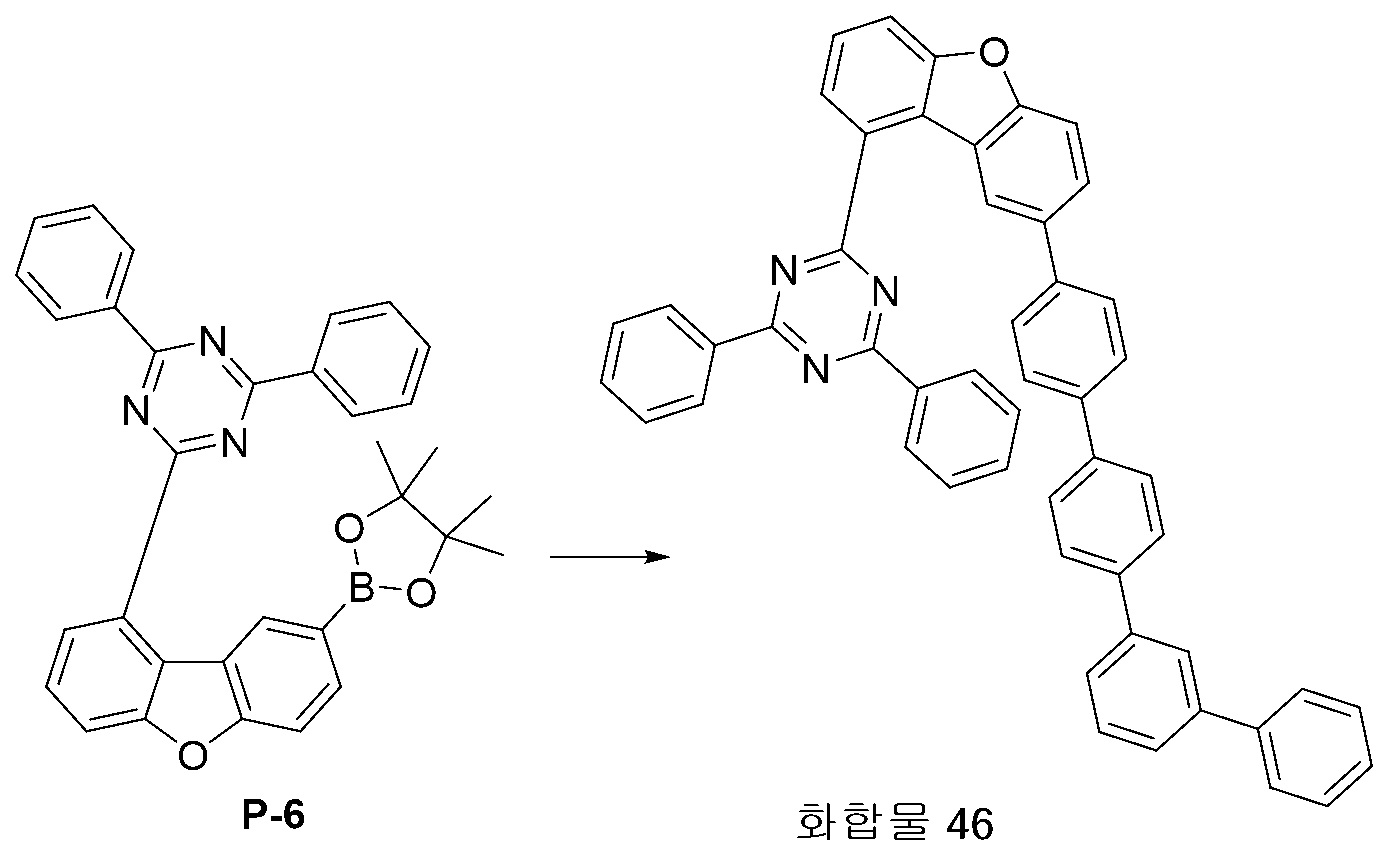
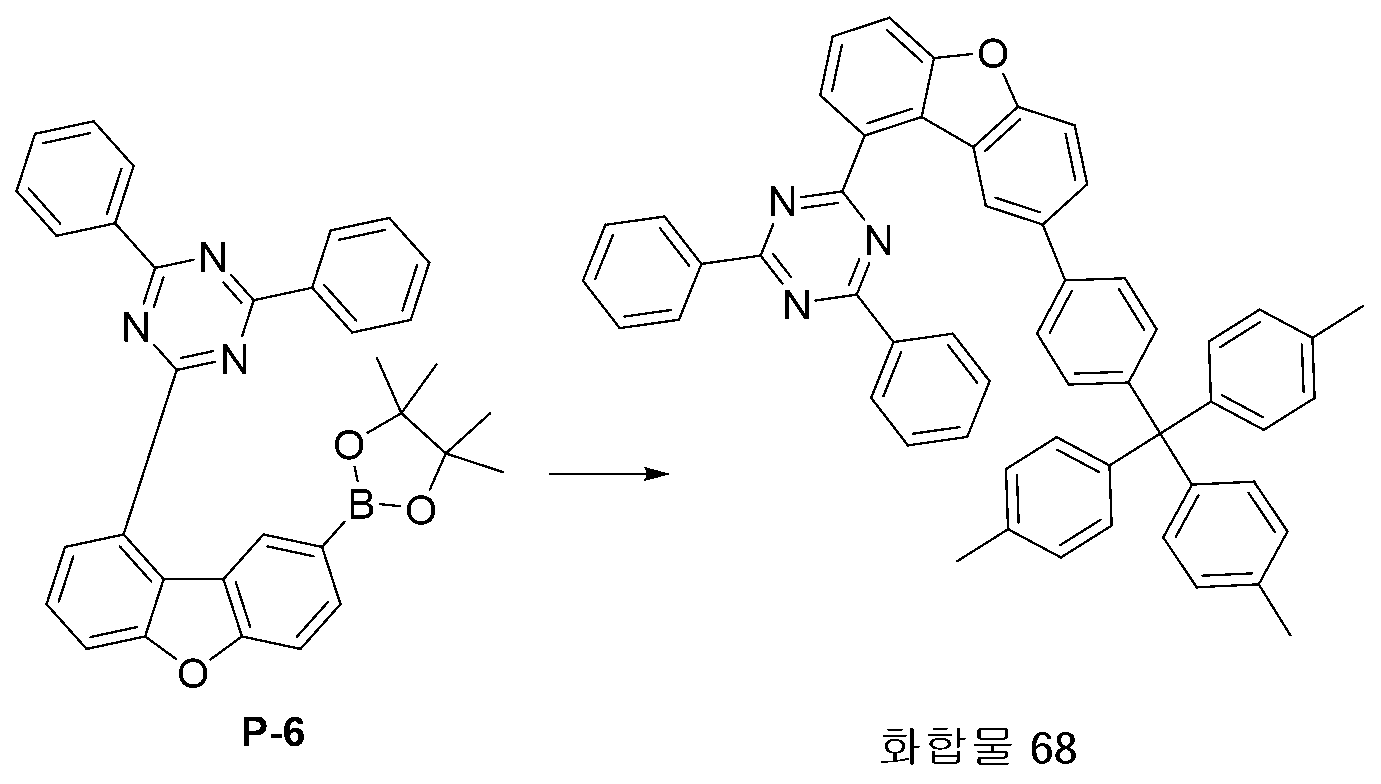
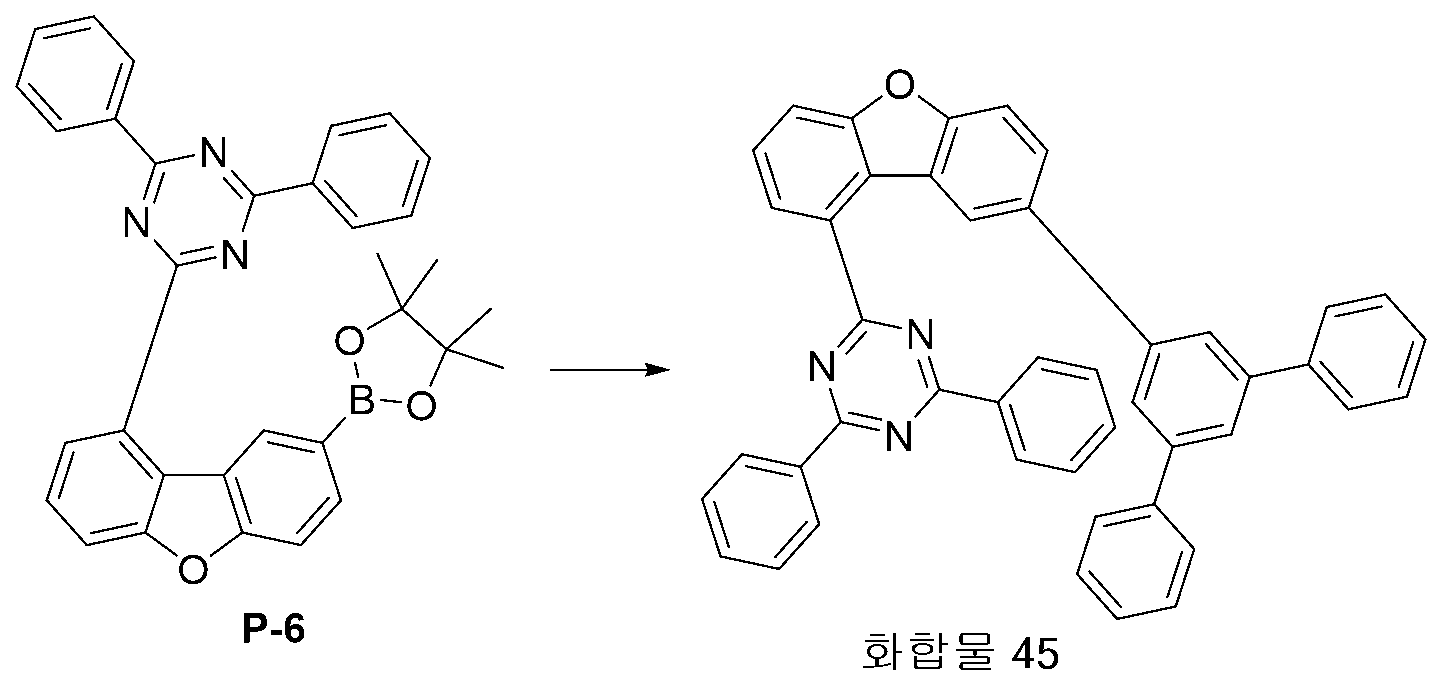
KR101849747B1 - 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 - Google Patents
신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 Download PDFInfo
- Publication number
- KR101849747B1 KR101849747B1 KR1020170075029A KR20170075029A KR101849747B1 KR 101849747 B1 KR101849747 B1 KR 101849747B1 KR 1020170075029 A KR1020170075029 A KR 1020170075029A KR 20170075029 A KR20170075029 A KR 20170075029A KR 101849747 B1 KR101849747 B1 KR 101849747B1
- Authority
- KR
- South Korea
- Prior art keywords
- compound
- mmol
- group
- substituted
- unsubstituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000002391 heterocyclic compounds Chemical class 0.000 title abstract description 4
- 150000001875 compounds Chemical class 0.000 claims description 411
- 125000003118 aryl group Chemical group 0.000 claims description 44
- 239000000463 material Substances 0.000 claims description 43
- 229910052757 nitrogen Inorganic materials 0.000 claims description 27
- 239000011368 organic material Substances 0.000 claims description 25
- 125000000217 alkyl group Chemical group 0.000 claims description 21
- 238000000034 method Methods 0.000 claims description 16
- 229910052760 oxygen Inorganic materials 0.000 claims description 16
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 14
- 229910052739 hydrogen Inorganic materials 0.000 claims description 14
- 239000001257 hydrogen Substances 0.000 claims description 14
- 229910052717 sulfur Inorganic materials 0.000 claims description 14
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 13
- 125000000449 nitro group Chemical class [O-][N+](*)=O 0.000 claims description 12
- 229910052736 halogen Inorganic materials 0.000 claims description 11
- 150000002367 halogens Chemical class 0.000 claims description 11
- 125000005842 heteroatom Chemical group 0.000 claims description 11
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 11
- 125000003342 alkenyl group Chemical group 0.000 claims description 9
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 9
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical class C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 claims description 9
- 125000001072 heteroaryl group Chemical group 0.000 claims description 6
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 5
- 229910052799 carbon Inorganic materials 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 4
- 125000000732 arylene group Chemical group 0.000 claims description 4
- 235000010290 biphenyl Nutrition 0.000 claims description 4
- 125000006653 (C1-C20) heteroaryl group Chemical group 0.000 claims description 3
- 125000004104 aryloxy group Chemical group 0.000 claims description 3
- 125000005549 heteroarylene group Chemical group 0.000 claims description 3
- 229910052710 silicon Inorganic materials 0.000 claims description 3
- 125000004438 haloalkoxy group Chemical group 0.000 claims description 2
- 125000001188 haloalkyl group Chemical group 0.000 claims description 2
- 125000004957 naphthylene group Chemical group 0.000 claims description 2
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 2
- 239000000126 substance Substances 0.000 claims description 2
- UFHFLCQGNIYNRP-VVKOMZTBSA-N Dideuterium Chemical compound [2H][2H] UFHFLCQGNIYNRP-VVKOMZTBSA-N 0.000 claims 5
- 239000004305 biphenyl Substances 0.000 claims 1
- 150000002894 organic compounds Chemical class 0.000 claims 1
- 230000015572 biosynthetic process Effects 0.000 description 194
- 238000003786 synthesis reaction Methods 0.000 description 193
- 238000002360 preparation method Methods 0.000 description 179
- 239000010410 layer Substances 0.000 description 108
- -1 heterocyclic compound compound Chemical class 0.000 description 74
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 73
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 54
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 48
- SQTPFYJEKHTINP-UHFFFAOYSA-N 2-bromophenanthrene Chemical compound C1=CC=C2C3=CC=C(Br)C=C3C=CC2=C1 SQTPFYJEKHTINP-UHFFFAOYSA-N 0.000 description 45
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 38
- 239000000203 mixture Substances 0.000 description 34
- 230000000052 comparative effect Effects 0.000 description 33
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 28
- 239000012044 organic layer Substances 0.000 description 27
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 26
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 24
- OHVLMTFVQDZYHP-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CN1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O OHVLMTFVQDZYHP-UHFFFAOYSA-N 0.000 description 23
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 23
- 238000006243 chemical reaction Methods 0.000 description 23
- 125000004432 carbon atom Chemical group C* 0.000 description 22
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 22
- 239000002019 doping agent Substances 0.000 description 20
- UZVGSSNIUNSOFA-UHFFFAOYSA-N dibenzofuran-1-carboxylic acid Chemical compound O1C2=CC=CC=C2C2=C1C=CC=C2C(=O)O UZVGSSNIUNSOFA-UHFFFAOYSA-N 0.000 description 18
- 238000002347 injection Methods 0.000 description 18
- 239000007924 injection Substances 0.000 description 18
- 239000011541 reaction mixture Substances 0.000 description 18
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 16
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 15
- 239000007787 solid Substances 0.000 description 15
- 238000003756 stirring Methods 0.000 description 14
- 239000000758 substrate Substances 0.000 description 14
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 12
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 12
- UBJFKNSINUCEAL-UHFFFAOYSA-N lithium;2-methylpropane Chemical compound [Li+].C[C-](C)C UBJFKNSINUCEAL-UHFFFAOYSA-N 0.000 description 11
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 11
- 235000019341 magnesium sulphate Nutrition 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- DDGPPAMADXTGTN-UHFFFAOYSA-N 2-chloro-4,6-diphenyl-1,3,5-triazine Chemical compound N=1C(Cl)=NC(C=2C=CC=CC=2)=NC=1C1=CC=CC=C1 DDGPPAMADXTGTN-UHFFFAOYSA-N 0.000 description 10
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 10
- 238000000151 deposition Methods 0.000 description 10
- 125000001424 substituent group Chemical group 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- 229910052782 aluminium Inorganic materials 0.000 description 9
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 9
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 9
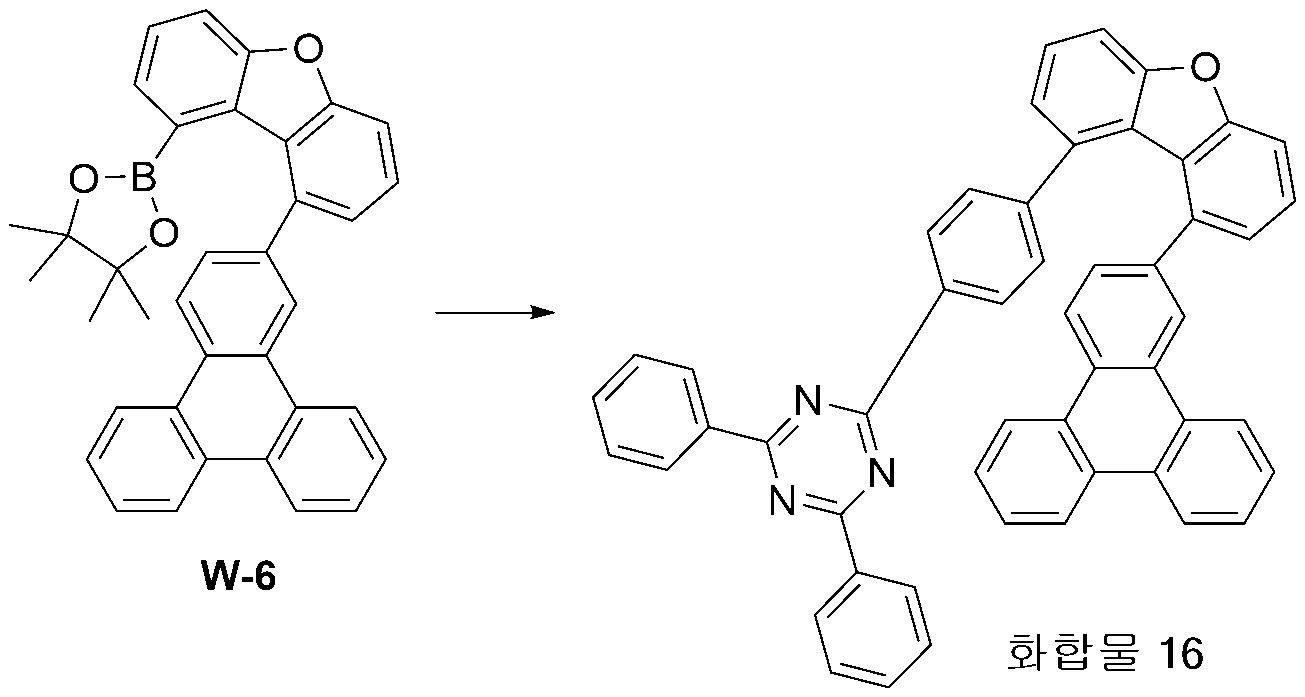
- VXLBBSLCTFTKOE-UHFFFAOYSA-N 4,4,5,5-tetramethyl-2-triphenylen-2-yl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(C=2C(=CC=CC=2)C=2C3=CC=CC=2)C3=C1 VXLBBSLCTFTKOE-UHFFFAOYSA-N 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- 239000002253 acid Substances 0.000 description 8
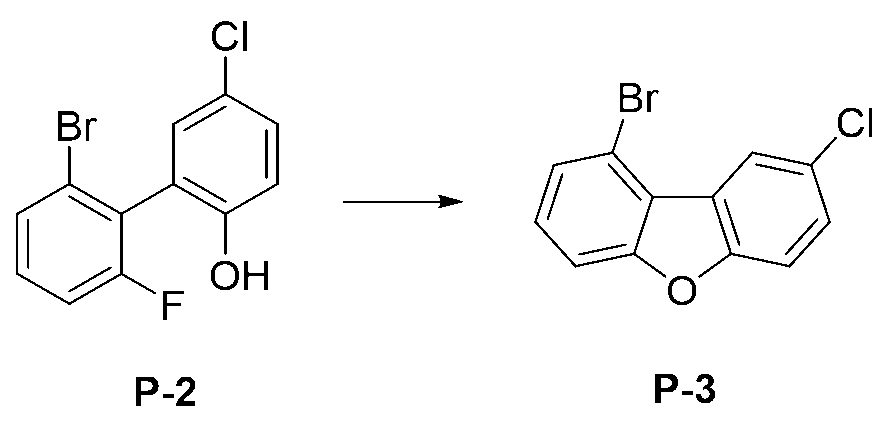
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 7
- 230000008021 deposition Effects 0.000 description 7
- 125000000623 heterocyclic group Chemical group 0.000 description 7
- 230000005525 hole transport Effects 0.000 description 7
- 229910052751 metal Inorganic materials 0.000 description 7
- 239000002184 metal Substances 0.000 description 7
- FIDRAVVQGKNYQK-UHFFFAOYSA-N 1,2,3,4-tetrahydrotriazine Chemical compound C1NNNC=C1 FIDRAVVQGKNYQK-UHFFFAOYSA-N 0.000 description 6
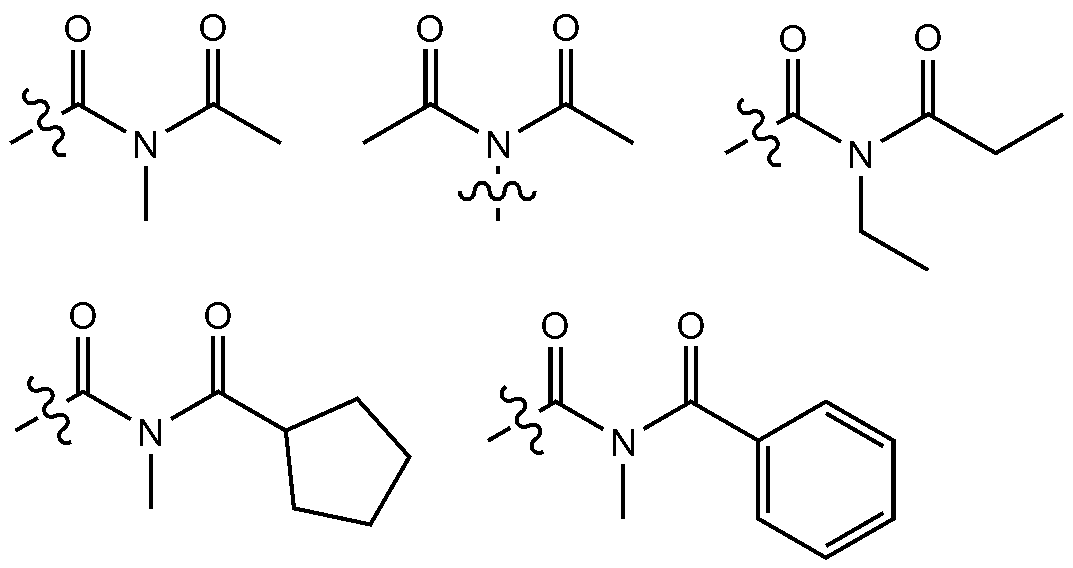
- 0 CC(N(C)*=O)=O Chemical compound CC(N(C)*=O)=O 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 239000010406 cathode material Substances 0.000 description 6
- 235000011056 potassium acetate Nutrition 0.000 description 6
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 230000032258 transport Effects 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 5
- 239000007864 aqueous solution Substances 0.000 description 5
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 5
- 239000012153 distilled water Substances 0.000 description 5
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 5
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 4
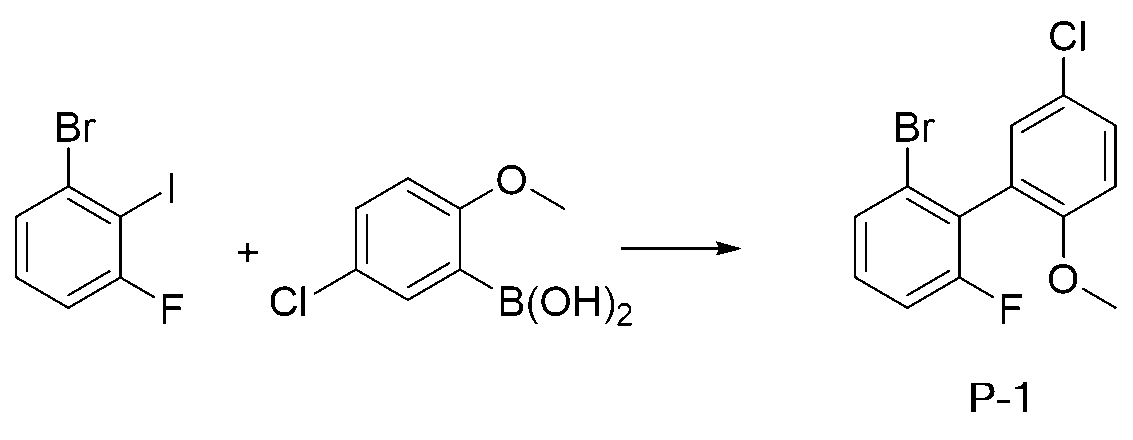
- FXEGEEUPPGLIIC-UHFFFAOYSA-N 1-bromo-3-fluoro-2-iodobenzene Chemical compound FC1=CC=CC(Br)=C1I FXEGEEUPPGLIIC-UHFFFAOYSA-N 0.000 description 4
- NTEIZPBYXABJKN-UHFFFAOYSA-N 2-(4-chlorophenyl)-4,6-diphenyl-1,3,5-triazine Chemical compound C1=CC(Cl)=CC=C1C1=NC(C=2C=CC=CC=2)=NC(C=2C=CC=CC=2)=N1 NTEIZPBYXABJKN-UHFFFAOYSA-N 0.000 description 4
- 229940126062 Compound A Drugs 0.000 description 4
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 4
- 150000004982 aromatic amines Chemical class 0.000 description 4
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 229940125904 compound 1 Drugs 0.000 description 4
- 229940125782 compound 2 Drugs 0.000 description 4
- 229940125844 compound 46 Drugs 0.000 description 4
- JNGZXGGOCLZBFB-IVCQMTBJSA-N compound E Chemical compound N([C@@H](C)C(=O)N[C@@H]1C(N(C)C2=CC=CC=C2C(C=2C=CC=CC=2)=N1)=O)C(=O)CC1=CC(F)=CC(F)=C1 JNGZXGGOCLZBFB-IVCQMTBJSA-N 0.000 description 4
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical group C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 4
- 238000004821 distillation Methods 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- DQYBDCGIPTYXML-UHFFFAOYSA-N ethoxyethane;hydrate Chemical compound O.CCOCC DQYBDCGIPTYXML-UHFFFAOYSA-N 0.000 description 4
- 229910052763 palladium Inorganic materials 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 4
- 125000003373 pyrazinyl group Chemical group 0.000 description 4
- NHDIQVFFNDKAQU-UHFFFAOYSA-N tripropan-2-yl borate Chemical compound CC(C)OB(OC(C)C)OC(C)C NHDIQVFFNDKAQU-UHFFFAOYSA-N 0.000 description 4
- 238000010792 warming Methods 0.000 description 4
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 3
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 3
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 3
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 3
- FMBVAOHFMSQDGT-UHFFFAOYSA-N (5-chloro-2-methoxyphenyl)boronic acid Chemical compound COC1=CC=C(Cl)C=C1B(O)O FMBVAOHFMSQDGT-UHFFFAOYSA-N 0.000 description 3
- DEVSOMFAQLZNKR-RJRFIUFISA-N (z)-3-[3-[3,5-bis(trifluoromethyl)phenyl]-1,2,4-triazol-1-yl]-n'-pyrazin-2-ylprop-2-enehydrazide Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(C2=NN(\C=C/C(=O)NNC=3N=CC=NC=3)C=N2)=C1 DEVSOMFAQLZNKR-RJRFIUFISA-N 0.000 description 3
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 3
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 3
- FMKGJQHNYMWDFJ-CVEARBPZSA-N 2-[[4-(2,2-difluoropropoxy)pyrimidin-5-yl]methylamino]-4-[[(1R,4S)-4-hydroxy-3,3-dimethylcyclohexyl]amino]pyrimidine-5-carbonitrile Chemical compound FC(COC1=NC=NC=C1CNC1=NC=C(C(=N1)N[C@H]1CC([C@H](CC1)O)(C)C)C#N)(C)F FMKGJQHNYMWDFJ-CVEARBPZSA-N 0.000 description 3
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 3
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 3
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
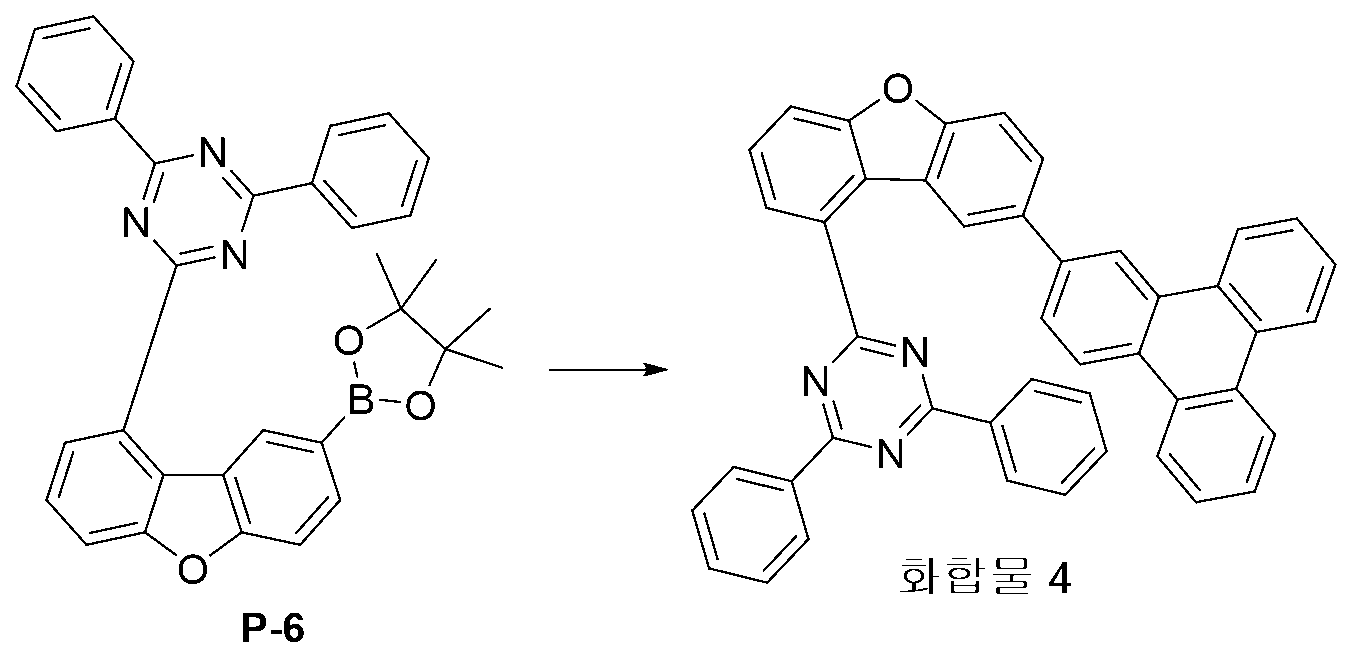
- LLKCLITYYLAQEO-UHFFFAOYSA-N CC1(C)OB(c2ccc3[o]c4cccc(-c5nc(-c6ccccc6)nc(-c6ccccc6)n5)c4c3c2)OC1(C)C Chemical compound CC1(C)OB(c2ccc3[o]c4cccc(-c5nc(-c6ccccc6)nc(-c6ccccc6)n5)c4c3c2)OC1(C)C LLKCLITYYLAQEO-UHFFFAOYSA-N 0.000 description 3
- KCBAMQOKOLXLOX-BSZYMOERSA-N CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O Chemical compound CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O KCBAMQOKOLXLOX-BSZYMOERSA-N 0.000 description 3
- PKMUHQIDVVOXHQ-HXUWFJFHSA-N C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O Chemical compound C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O PKMUHQIDVVOXHQ-HXUWFJFHSA-N 0.000 description 3
- 229940127007 Compound 39 Drugs 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- LVDRREOUMKACNJ-BKMJKUGQSA-N N-[(2R,3S)-2-(4-chlorophenyl)-1-(1,4-dimethyl-2-oxoquinolin-7-yl)-6-oxopiperidin-3-yl]-2-methylpropane-1-sulfonamide Chemical compound CC(C)CS(=O)(=O)N[C@H]1CCC(=O)N([C@@H]1c1ccc(Cl)cc1)c1ccc2c(C)cc(=O)n(C)c2c1 LVDRREOUMKACNJ-BKMJKUGQSA-N 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- PSLUFJFHTBIXMW-WYEYVKMPSA-N [(3r,4ar,5s,6s,6as,10s,10ar,10bs)-3-ethenyl-10,10b-dihydroxy-3,4a,7,7,10a-pentamethyl-1-oxo-6-(2-pyridin-2-ylethylcarbamoyloxy)-5,6,6a,8,9,10-hexahydro-2h-benzo[f]chromen-5-yl] acetate Chemical compound O([C@@H]1[C@@H]([C@]2(O[C@](C)(CC(=O)[C@]2(O)[C@@]2(C)[C@@H](O)CCC(C)(C)[C@@H]21)C=C)C)OC(=O)C)C(=O)NCCC1=CC=CC=N1 PSLUFJFHTBIXMW-WYEYVKMPSA-N 0.000 description 3
- 125000002877 alkyl aryl group Chemical group 0.000 description 3
- 229910045601 alloy Inorganic materials 0.000 description 3
- 239000000956 alloy Substances 0.000 description 3
- 125000003710 aryl alkyl group Chemical group 0.000 description 3
- 125000001769 aryl amino group Chemical group 0.000 description 3
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 3
- 125000006267 biphenyl group Chemical group 0.000 description 3
- 125000000319 biphenyl-4-yl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 229940126543 compound 14 Drugs 0.000 description 3
- 229940126142 compound 16 Drugs 0.000 description 3
- 229940125810 compound 20 Drugs 0.000 description 3
- 229940125833 compound 23 Drugs 0.000 description 3
- 229940125961 compound 24 Drugs 0.000 description 3
- 229940125846 compound 25 Drugs 0.000 description 3
- 229940126214 compound 3 Drugs 0.000 description 3
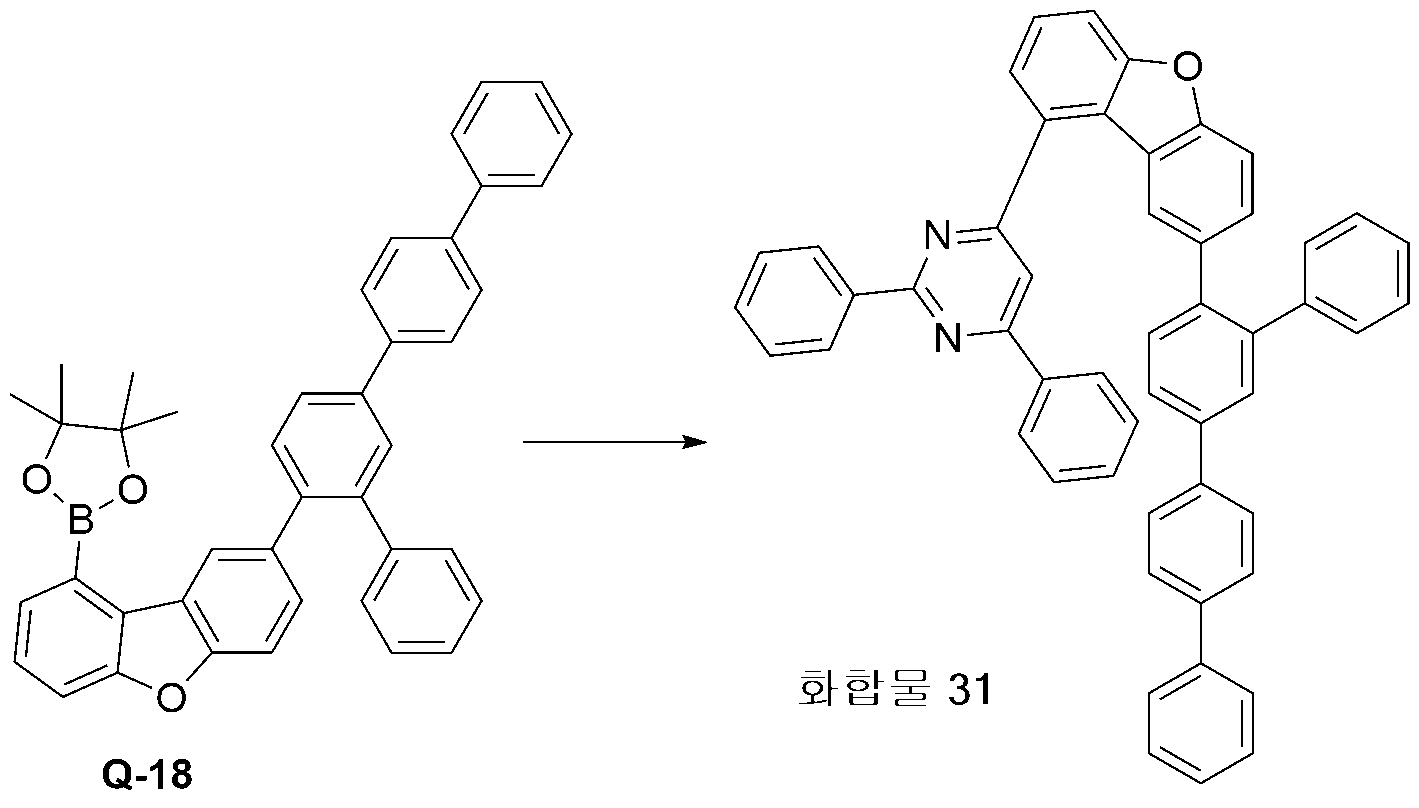
- 229940125877 compound 31 Drugs 0.000 description 3
- 229940125807 compound 37 Drugs 0.000 description 3
- 229940127113 compound 57 Drugs 0.000 description 3
- 229940126179 compound 72 Drugs 0.000 description 3
- 229920001940 conductive polymer Polymers 0.000 description 3
- 229910052805 deuterium Inorganic materials 0.000 description 3
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 3
- BJXYHBKEQFQVES-NWDGAFQWSA-N enpatoran Chemical compound N[C@H]1CN(C[C@H](C1)C(F)(F)F)C1=C2C=CC=NC2=C(C=C1)C#N BJXYHBKEQFQVES-NWDGAFQWSA-N 0.000 description 3
- 125000004185 ester group Chemical group 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 3
- 238000004770 highest occupied molecular orbital Methods 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 3
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 3
- 229910000027 potassium carbonate Inorganic materials 0.000 description 3
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 3
- 229910052709 silver Inorganic materials 0.000 description 3
- 239000004332 silver Substances 0.000 description 3
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- RMVRSNDYEFQCLF-UHFFFAOYSA-N thiophenol Chemical compound SC1=CC=CC=C1 RMVRSNDYEFQCLF-UHFFFAOYSA-N 0.000 description 3
- WLPUWLXVBWGYMZ-UHFFFAOYSA-N tricyclohexylphosphine Chemical compound C1CCCCC1P(C1CCCCC1)C1CCCCC1 WLPUWLXVBWGYMZ-UHFFFAOYSA-N 0.000 description 3
- PXFBSZZEOWJJNL-UHFFFAOYSA-N triphenylen-2-ylboronic acid Chemical compound C1=CC=C2C3=CC(B(O)O)=CC=C3C3=CC=CC=C3C2=C1 PXFBSZZEOWJJNL-UHFFFAOYSA-N 0.000 description 3
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 2
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 2
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 2
- BKWVXPCYDRURMK-UHFFFAOYSA-N (2,6-dimethoxyphenyl)boronic acid Chemical compound COC1=CC=CC(OC)=C1B(O)O BKWVXPCYDRURMK-UHFFFAOYSA-N 0.000 description 2
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- GCTFTMWXZFLTRR-GFCCVEGCSA-N (2r)-2-amino-n-[3-(difluoromethoxy)-4-(1,3-oxazol-5-yl)phenyl]-4-methylpentanamide Chemical compound FC(F)OC1=CC(NC(=O)[C@H](N)CC(C)C)=CC=C1C1=CN=CO1 GCTFTMWXZFLTRR-GFCCVEGCSA-N 0.000 description 2
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 2
- YJLIKUSWRSEPSM-WGQQHEPDSA-N (2r,3r,4s,5r)-2-[6-amino-8-[(4-phenylphenyl)methylamino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CNC1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O YJLIKUSWRSEPSM-WGQQHEPDSA-N 0.000 description 2
- VIJSPAIQWVPKQZ-BLECARSGSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-4-methylpentanoyl]amino]-4,4-dimethylpentanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(C)=O VIJSPAIQWVPKQZ-BLECARSGSA-N 0.000 description 2
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 2
- KSYYRNDZOSXTFU-UHFFFAOYSA-N (3-bromo-2-methoxyphenyl)boronic acid Chemical compound COC1=C(Br)C=CC=C1B(O)O KSYYRNDZOSXTFU-UHFFFAOYSA-N 0.000 description 2
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 2
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 2
- OOKAZRDERJMRCJ-KOUAFAAESA-N (3r)-7-[(1s,2s,4ar,6s,8s)-2,6-dimethyl-8-[(2s)-2-methylbutanoyl]oxy-1,2,4a,5,6,7,8,8a-octahydronaphthalen-1-yl]-3-hydroxy-5-oxoheptanoic acid Chemical compound C1=C[C@H](C)[C@H](CCC(=O)C[C@@H](O)CC(O)=O)C2[C@@H](OC(=O)[C@@H](C)CC)C[C@@H](C)C[C@@H]21 OOKAZRDERJMRCJ-KOUAFAAESA-N 0.000 description 2
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 2
- OMBVEVHRIQULKW-DNQXCXABSA-M (3r,5r)-7-[3-(4-fluorophenyl)-8-oxo-7-phenyl-1-propan-2-yl-5,6-dihydro-4h-pyrrolo[2,3-c]azepin-2-yl]-3,5-dihydroxyheptanoate Chemical compound O=C1C=2N(C(C)C)C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C(C=3C=CC(F)=CC=3)C=2CCCN1C1=CC=CC=C1 OMBVEVHRIQULKW-DNQXCXABSA-M 0.000 description 2
- STPKWKPURVSAJF-LJEWAXOPSA-N (4r,5r)-5-[4-[[4-(1-aza-4-azoniabicyclo[2.2.2]octan-4-ylmethyl)phenyl]methoxy]phenyl]-3,3-dibutyl-7-(dimethylamino)-1,1-dioxo-4,5-dihydro-2h-1$l^{6}-benzothiepin-4-ol Chemical compound O[C@H]1C(CCCC)(CCCC)CS(=O)(=O)C2=CC=C(N(C)C)C=C2[C@H]1C(C=C1)=CC=C1OCC(C=C1)=CC=C1C[N+]1(CC2)CCN2CC1 STPKWKPURVSAJF-LJEWAXOPSA-N 0.000 description 2
- VUEGYUOUAAVYAS-JGGQBBKZSA-N (6ar,9s,10ar)-9-(dimethylsulfamoylamino)-7-methyl-6,6a,8,9,10,10a-hexahydro-4h-indolo[4,3-fg]quinoline Chemical compound C1=CC([C@H]2C[C@@H](CN(C)[C@@H]2C2)NS(=O)(=O)N(C)C)=C3C2=CNC3=C1 VUEGYUOUAAVYAS-JGGQBBKZSA-N 0.000 description 2
- UWRZIZXBOLBCON-VOTSOKGWSA-N (e)-2-phenylethenamine Chemical class N\C=C\C1=CC=CC=C1 UWRZIZXBOLBCON-VOTSOKGWSA-N 0.000 description 2
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical compound C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 2
- KKHFRAFPESRGGD-UHFFFAOYSA-N 1,3-dimethyl-7-[3-(n-methylanilino)propyl]purine-2,6-dione Chemical compound C1=NC=2N(C)C(=O)N(C)C(=O)C=2N1CCCN(C)C1=CC=CC=C1 KKHFRAFPESRGGD-UHFFFAOYSA-N 0.000 description 2
- XJKSTNDFUHDPQJ-UHFFFAOYSA-N 1,4-diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=C(C=2C=CC=CC=2)C=C1 XJKSTNDFUHDPQJ-UHFFFAOYSA-N 0.000 description 2
- WTAPZWXVSZMMDG-UHFFFAOYSA-N 1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].C=1C=CC=CC=1C=CC(=O)C=CC1=CC=CC=C1 WTAPZWXVSZMMDG-UHFFFAOYSA-N 0.000 description 2
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- QXOGPTXQGKQSJT-UHFFFAOYSA-N 1-amino-4-[4-(3,4-dimethylphenyl)sulfanylanilino]-9,10-dioxoanthracene-2-sulfonic acid Chemical compound Cc1ccc(Sc2ccc(Nc3cc(c(N)c4C(=O)c5ccccc5C(=O)c34)S(O)(=O)=O)cc2)cc1C QXOGPTXQGKQSJT-UHFFFAOYSA-N 0.000 description 2
- CTPUUDQIXKUAMO-UHFFFAOYSA-N 1-bromo-3-iodobenzene Chemical compound BrC1=CC=CC(I)=C1 CTPUUDQIXKUAMO-UHFFFAOYSA-N 0.000 description 2
- AZUUTAFMFQSXMA-UHFFFAOYSA-N 1-chloro-3-fluoro-2-iodobenzene Chemical compound FC1=CC=CC(Cl)=C1I AZUUTAFMFQSXMA-UHFFFAOYSA-N 0.000 description 2
- HZNVUJQVZSTENZ-UHFFFAOYSA-N 2,3-dichloro-5,6-dicyano-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(C#N)=C(C#N)C1=O HZNVUJQVZSTENZ-UHFFFAOYSA-N 0.000 description 2
- WGFNXGPBPIJYLI-UHFFFAOYSA-N 2,6-difluoro-3-[(3-fluorophenyl)sulfonylamino]-n-(3-methoxy-1h-pyrazolo[3,4-b]pyridin-5-yl)benzamide Chemical compound C1=C2C(OC)=NNC2=NC=C1NC(=O)C(C=1F)=C(F)C=CC=1NS(=O)(=O)C1=CC=CC(F)=C1 WGFNXGPBPIJYLI-UHFFFAOYSA-N 0.000 description 2
- VCUXVXLUOHDHKK-UHFFFAOYSA-N 2-(2-aminopyrimidin-4-yl)-4-(2-chloro-4-methoxyphenyl)-1,3-thiazole-5-carboxamide Chemical compound ClC1=CC(OC)=CC=C1C1=C(C(N)=O)SC(C=2N=C(N)N=CC=2)=N1 VCUXVXLUOHDHKK-UHFFFAOYSA-N 0.000 description 2
- KWXFBIBEVROWEF-UHFFFAOYSA-N 2-(3-bromophenyl)triphenylene Chemical group BrC1=CC=CC(C=2C=C3C4=CC=CC=C4C4=CC=CC=C4C3=CC=2)=C1 KWXFBIBEVROWEF-UHFFFAOYSA-N 0.000 description 2
- PYRKKGOKRMZEIT-UHFFFAOYSA-N 2-[6-(2-cyclopropylethoxy)-9-(2-hydroxy-2-methylpropyl)-1h-phenanthro[9,10-d]imidazol-2-yl]-5-fluorobenzene-1,3-dicarbonitrile Chemical compound C1=C2C3=CC(CC(C)(O)C)=CC=C3C=3NC(C=4C(=CC(F)=CC=4C#N)C#N)=NC=3C2=CC=C1OCCC1CC1 PYRKKGOKRMZEIT-UHFFFAOYSA-N 0.000 description 2
- VVCMGAUPZIKYTH-VGHSCWAPSA-N 2-acetyloxybenzoic acid;[(2s,3r)-4-(dimethylamino)-3-methyl-1,2-diphenylbutan-2-yl] propanoate;1,3,7-trimethylpurine-2,6-dione Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O.CN1C(=O)N(C)C(=O)C2=C1N=CN2C.C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 VVCMGAUPZIKYTH-VGHSCWAPSA-N 0.000 description 2
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 2
- NPRYCHLHHVWLQZ-TURQNECASA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynylpurin-8-one Chemical compound NC1=NC=C2N(C(N(C2=N1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C NPRYCHLHHVWLQZ-TURQNECASA-N 0.000 description 2
- YUQUNWNSQDULTI-UHFFFAOYSA-N 2-bromobenzenethiol Chemical compound SC1=CC=CC=C1Br YUQUNWNSQDULTI-UHFFFAOYSA-N 0.000 description 2
- GEDOYYDMCZUHNW-UHFFFAOYSA-N 2-bromotriphenylene Chemical group C1=CC=C2C3=CC(Br)=CC=C3C3=CC=CC=C3C2=C1 GEDOYYDMCZUHNW-UHFFFAOYSA-N 0.000 description 2
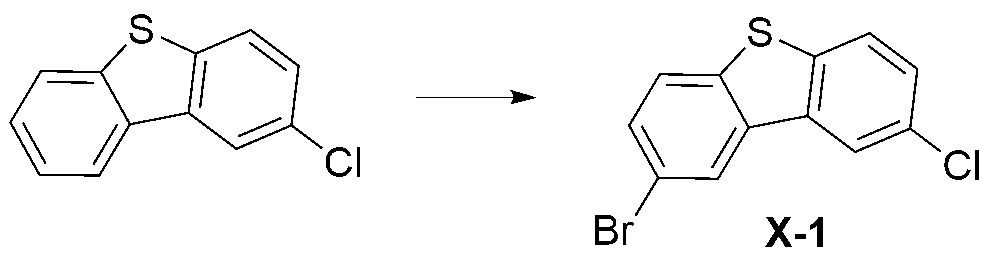
- ZNJQWPJMTIZOHA-UHFFFAOYSA-N 2-chlorodibenzothiophene Chemical compound C1=CC=C2C3=CC(Cl)=CC=C3SC2=C1 ZNJQWPJMTIZOHA-UHFFFAOYSA-N 0.000 description 2
- LFOIDLOIBZFWDO-UHFFFAOYSA-N 2-methoxy-6-[6-methoxy-4-[(3-phenylmethoxyphenyl)methoxy]-1-benzofuran-2-yl]imidazo[2,1-b][1,3,4]thiadiazole Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(C=1)=CC=CC=1OCC1=CC=CC=C1 LFOIDLOIBZFWDO-UHFFFAOYSA-N 0.000 description 2
- QENGPZGAWFQWCZ-UHFFFAOYSA-N 3-Methylthiophene Chemical compound CC=1C=CSC=1 QENGPZGAWFQWCZ-UHFFFAOYSA-N 0.000 description 2
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 description 2
- ICESCNGNKLTYAZ-UHFFFAOYSA-N 4,4,5,5-tetramethyl-2-phenanthren-2-yl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C2C3=CC=CC=C3C=CC2=C1 ICESCNGNKLTYAZ-UHFFFAOYSA-N 0.000 description 2
- MINMDCMSHDBHKG-UHFFFAOYSA-N 4-[4-[[6-methoxy-2-(2-methoxyimidazo[2,1-b][1,3,4]thiadiazol-6-yl)-1-benzofuran-4-yl]oxymethyl]-5-methyl-1,3-thiazol-2-yl]morpholine Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(=C(S1)C)N=C1N1CCOCC1 MINMDCMSHDBHKG-UHFFFAOYSA-N 0.000 description 2
- WYFCZWSWFGJODV-MIANJLSGSA-N 4-[[(1s)-2-[(e)-3-[3-chloro-2-fluoro-6-(tetrazol-1-yl)phenyl]prop-2-enoyl]-5-(4-methyl-2-oxopiperazin-1-yl)-3,4-dihydro-1h-isoquinoline-1-carbonyl]amino]benzoic acid Chemical compound O=C1CN(C)CCN1C1=CC=CC2=C1CCN(C(=O)\C=C\C=1C(=CC=C(Cl)C=1F)N1N=NN=C1)[C@@H]2C(=O)NC1=CC=C(C(O)=O)C=C1 WYFCZWSWFGJODV-MIANJLSGSA-N 0.000 description 2
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 2
- MJDDVTZXYXHTRY-UHFFFAOYSA-N 4-chloro-2,6-diphenylpyrimidine Chemical compound N=1C(Cl)=CC(C=2C=CC=CC=2)=NC=1C1=CC=CC=C1 MJDDVTZXYXHTRY-UHFFFAOYSA-N 0.000 description 2
- XFJBGINZIMNZBW-CRAIPNDOSA-N 5-chloro-2-[4-[(1r,2s)-2-[2-(5-methylsulfonylpyridin-2-yl)oxyethyl]cyclopropyl]piperidin-1-yl]pyrimidine Chemical compound N1=CC(S(=O)(=O)C)=CC=C1OCC[C@H]1[C@@H](C2CCN(CC2)C=2N=CC(Cl)=CN=2)C1 XFJBGINZIMNZBW-CRAIPNDOSA-N 0.000 description 2
- RSIWALKZYXPAGW-NSHDSACASA-N 6-(3-fluorophenyl)-3-methyl-7-[(1s)-1-(7h-purin-6-ylamino)ethyl]-[1,3]thiazolo[3,2-a]pyrimidin-5-one Chemical compound C=1([C@@H](NC=2C=3N=CNC=3N=CN=2)C)N=C2SC=C(C)N2C(=O)C=1C1=CC=CC(F)=C1 RSIWALKZYXPAGW-NSHDSACASA-N 0.000 description 2
- HCCNBKFJYUWLEX-UHFFFAOYSA-N 7-(6-methoxypyridin-3-yl)-1-(2-propoxyethyl)-3-(pyrazin-2-ylmethylamino)pyrido[3,4-b]pyrazin-2-one Chemical compound O=C1N(CCOCCC)C2=CC(C=3C=NC(OC)=CC=3)=NC=C2N=C1NCC1=CN=CC=N1 HCCNBKFJYUWLEX-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- AVYARGMBGHVCMO-UHFFFAOYSA-N Brc1cccc2c1c(cc(cc1)-c3cc4ccccc4c4c3cccc4)c1[o]2 Chemical compound Brc1cccc2c1c(cc(cc1)-c3cc4ccccc4c4c3cccc4)c1[o]2 AVYARGMBGHVCMO-UHFFFAOYSA-N 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- JQUCWIWWWKZNCS-LESHARBVSA-N C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F Chemical compound C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F JQUCWIWWWKZNCS-LESHARBVSA-N 0.000 description 2
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 2
- XIZWXBVOGDHRRN-UHFFFAOYSA-N CC1(C)OB(c2c(c(cc(cc3)-c(cc4)cc5c4c4ccccc4c4ccccc54)c3[o]3)c3ccc2)OC1(C)C Chemical compound CC1(C)OB(c2c(c(cc(cc3)-c(cc4)cc5c4c4ccccc4c4ccccc54)c3[o]3)c3ccc2)OC1(C)C XIZWXBVOGDHRRN-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 229940126657 Compound 17 Drugs 0.000 description 2
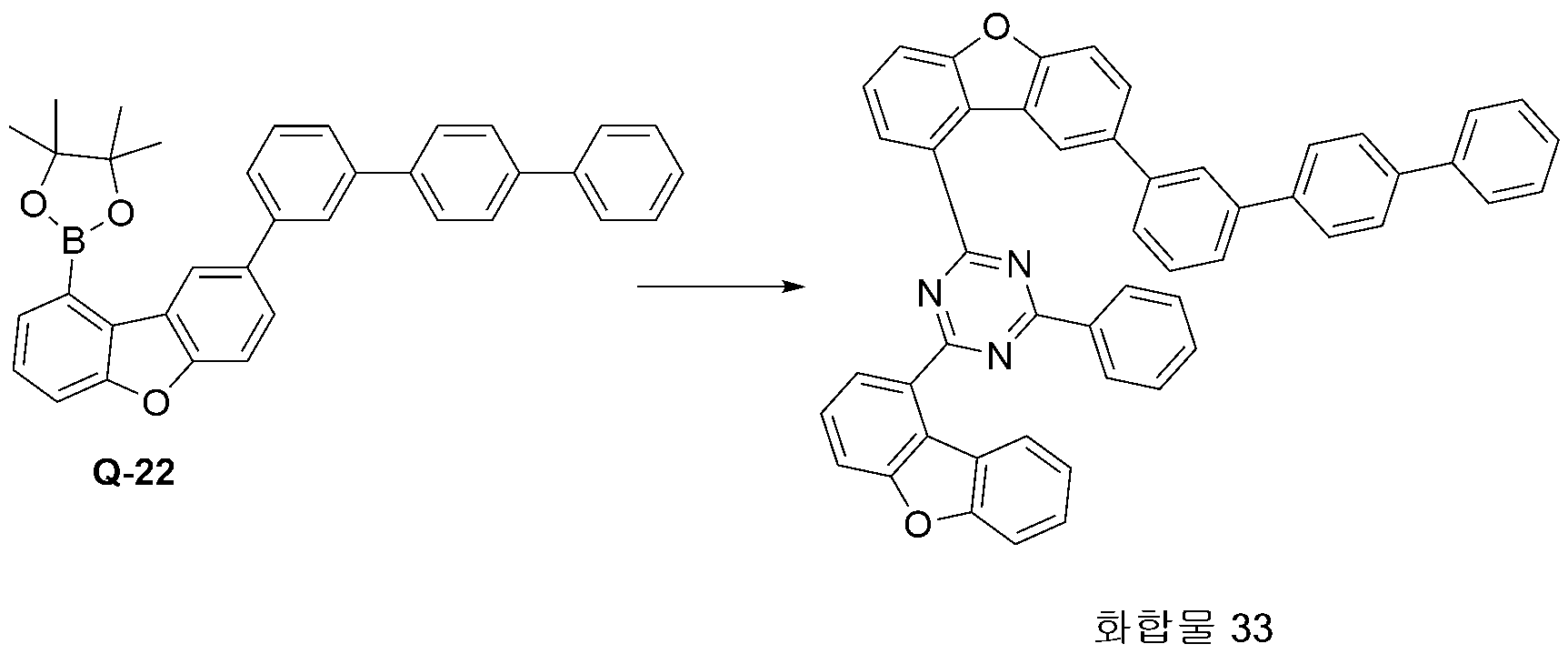
- 229940126639 Compound 33 Drugs 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 2
- QOVYHDHLFPKQQG-NDEPHWFRSA-N N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O Chemical compound N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O QOVYHDHLFPKQQG-NDEPHWFRSA-N 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 2
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 2
- SPXSEZMVRJLHQG-XMMPIXPASA-N [(2R)-1-[[4-[(3-phenylmethoxyphenoxy)methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound C(C1=CC=CC=C1)OC=1C=C(OCC2=CC=C(CN3[C@H](CCC3)CO)C=C2)C=CC=1 SPXSEZMVRJLHQG-XMMPIXPASA-N 0.000 description 2
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 2
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 239000010405 anode material Substances 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 125000005264 aryl amine group Chemical group 0.000 description 2
- 125000003609 aryl vinyl group Chemical group 0.000 description 2
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- 229940125773 compound 10 Drugs 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 229940125758 compound 15 Drugs 0.000 description 2
- 229940126086 compound 21 Drugs 0.000 description 2
- 229940126208 compound 22 Drugs 0.000 description 2
- 229940125851 compound 27 Drugs 0.000 description 2
- 229940127204 compound 29 Drugs 0.000 description 2
- 229940125878 compound 36 Drugs 0.000 description 2
- 229940127573 compound 38 Drugs 0.000 description 2
- 229940126540 compound 41 Drugs 0.000 description 2
- 229940125936 compound 42 Drugs 0.000 description 2
- 229940127271 compound 49 Drugs 0.000 description 2
- 229940125898 compound 5 Drugs 0.000 description 2
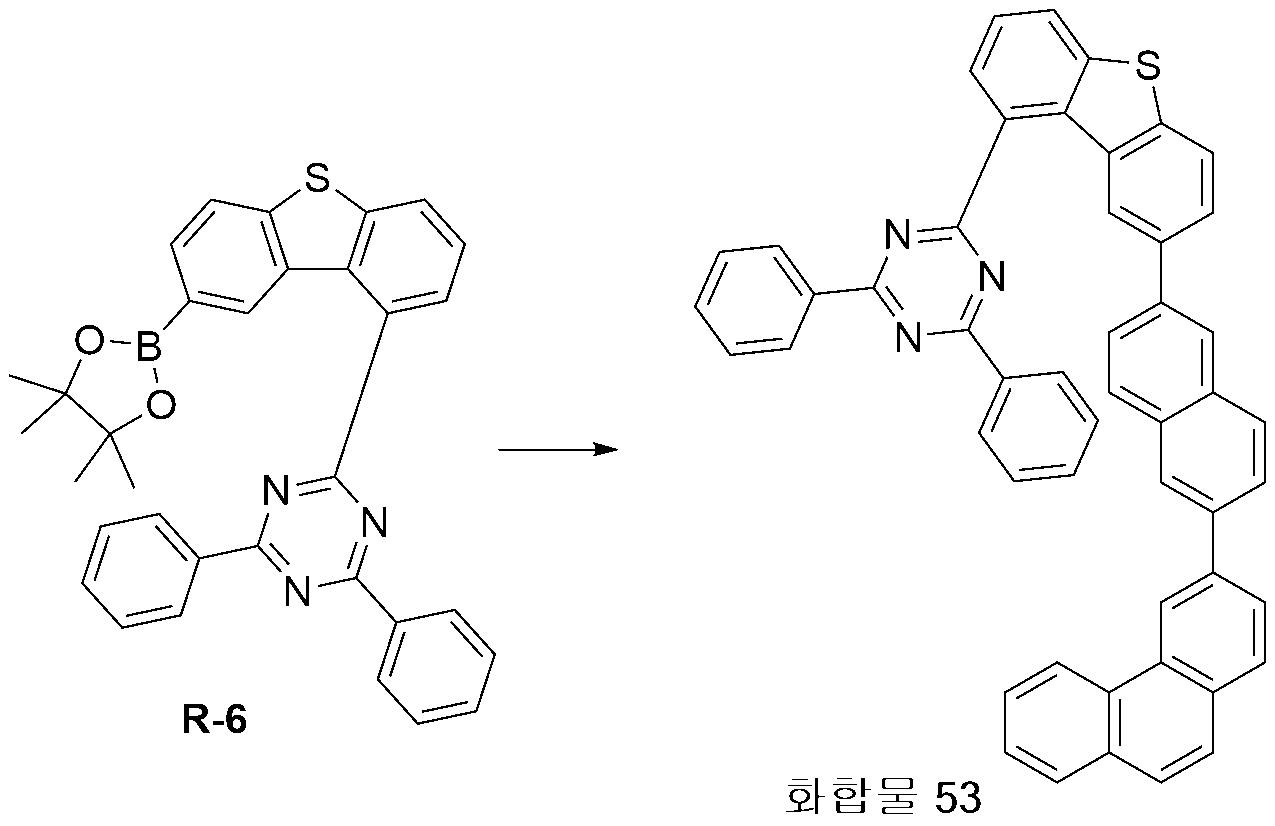
- 229940126545 compound 53 Drugs 0.000 description 2
- 229940125900 compound 59 Drugs 0.000 description 2
- 239000003599 detergent Substances 0.000 description 2
- ZXHUJRZYLRVVNP-UHFFFAOYSA-N dibenzofuran-4-ylboronic acid Chemical compound C12=CC=CC=C2OC2=C1C=CC=C2B(O)O ZXHUJRZYLRVVNP-UHFFFAOYSA-N 0.000 description 2
- GWNFQAKCJYEJEW-UHFFFAOYSA-N ethyl 3-[8-[[4-methyl-5-[(3-methyl-4-oxophthalazin-1-yl)methyl]-1,2,4-triazol-3-yl]sulfanyl]octanoylamino]benzoate Chemical compound CCOC(=O)C1=CC(NC(=O)CCCCCCCSC2=NN=C(CC3=NN(C)C(=O)C4=CC=CC=C34)N2C)=CC=C1 GWNFQAKCJYEJEW-UHFFFAOYSA-N 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 150000002219 fluoranthenes Chemical class 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- 125000005241 heteroarylamino group Chemical group 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 2
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- ZBELDPMWYXDLNY-UHFFFAOYSA-N methyl 9-(4-bromo-2-fluoroanilino)-[1,3]thiazolo[5,4-f]quinazoline-2-carboximidate Chemical compound C12=C3SC(C(=N)OC)=NC3=CC=C2N=CN=C1NC1=CC=C(Br)C=C1F ZBELDPMWYXDLNY-UHFFFAOYSA-N 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 239000011259 mixed solution Substances 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- VQSRKMNBWMHJKY-YTEVENLXSA-N n-[3-[(4ar,7as)-2-amino-6-(5-fluoropyrimidin-2-yl)-4,4a,5,7-tetrahydropyrrolo[3,4-d][1,3]thiazin-7a-yl]-4-fluorophenyl]-5-methoxypyrazine-2-carboxamide Chemical compound C1=NC(OC)=CN=C1C(=O)NC1=CC=C(F)C([C@@]23[C@@H](CN(C2)C=2N=CC(F)=CN=2)CSC(N)=N3)=C1 VQSRKMNBWMHJKY-YTEVENLXSA-N 0.000 description 2
- 239000007773 negative electrode material Substances 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- PIDFDZJZLOTZTM-KHVQSSSXSA-N ombitasvir Chemical compound COC(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@H]1C(=O)NC1=CC=C([C@H]2N([C@@H](CC2)C=2C=CC(NC(=O)[C@H]3N(CCC3)C(=O)[C@@H](NC(=O)OC)C(C)C)=CC=2)C=2C=CC(=CC=2)C(C)(C)C)C=C1 PIDFDZJZLOTZTM-KHVQSSSXSA-N 0.000 description 2
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 2
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 2
- 238000005240 physical vapour deposition Methods 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920000553 poly(phenylenevinylene) Polymers 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 239000002002 slurry Substances 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- 125000004306 triazinyl group Chemical group 0.000 description 2
- 150000003852 triazoles Chemical group 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 229910000404 tripotassium phosphate Inorganic materials 0.000 description 2
- 235000019798 tripotassium phosphate Nutrition 0.000 description 2
- 229910052725 zinc Inorganic materials 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- 239000011787 zinc oxide Substances 0.000 description 2
- ROEQGIFOWRQYHD-UHFFFAOYSA-N (2-methoxyphenyl)boronic acid Chemical compound COC1=CC=CC=C1B(O)O ROEQGIFOWRQYHD-UHFFFAOYSA-N 0.000 description 1
- NZRRMTBNTSBIFH-UHFFFAOYSA-N (4-chloro-2-methoxyphenyl)boronic acid Chemical compound COC1=CC(Cl)=CC=C1B(O)O NZRRMTBNTSBIFH-UHFFFAOYSA-N 0.000 description 1
- XPEIJWZLPWNNOK-UHFFFAOYSA-N (4-phenylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=CC=C1 XPEIJWZLPWNNOK-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- 125000000355 1,3-benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- BMZVDHQOAJUZJL-UHFFFAOYSA-N 1,3-dibromo-2-methoxybenzene Chemical compound COC1=C(Br)C=CC=C1Br BMZVDHQOAJUZJL-UHFFFAOYSA-N 0.000 description 1
- KZEVSDGEBAJOTK-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[5-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CC=1OC(=NN=1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O KZEVSDGEBAJOTK-UHFFFAOYSA-N 0.000 description 1
- YIWGJFPJRAEKMK-UHFFFAOYSA-N 1-(2H-benzotriazol-5-yl)-3-methyl-8-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carbonyl]-1,3,8-triazaspiro[4.5]decane-2,4-dione Chemical compound CN1C(=O)N(c2ccc3n[nH]nc3c2)C2(CCN(CC2)C(=O)c2cnc(NCc3cccc(OC(F)(F)F)c3)nc2)C1=O YIWGJFPJRAEKMK-UHFFFAOYSA-N 0.000 description 1
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 1
- NKPFKBYFBCNTPS-UHFFFAOYSA-N 1-[[4-(2-chlorophenyl)-1,2,3,4-tetrahydronaphthalen-1-yl]methyl]dibenzofuran Chemical compound ClC1=C(C=CC=C1)C1CCC(C2=CC=CC=C12)CC1=CC=CC=2OC3=C(C=21)C=CC=C3 NKPFKBYFBCNTPS-UHFFFAOYSA-N 0.000 description 1
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 1
- KTADSLDAUJLZGL-UHFFFAOYSA-N 1-bromo-2-phenylbenzene Chemical group BrC1=CC=CC=C1C1=CC=CC=C1 KTADSLDAUJLZGL-UHFFFAOYSA-N 0.000 description 1
- ZARGVWJSXZDKRE-UHFFFAOYSA-N 1-bromo-4-phenylnaphthalene Chemical compound C12=CC=CC=C2C(Br)=CC=C1C1=CC=CC=C1 ZARGVWJSXZDKRE-UHFFFAOYSA-N 0.000 description 1
- FIJIRZKOKTVVOZ-UHFFFAOYSA-N 1-bromo-4-tritylbenzene Chemical compound C1=CC(Br)=CC=C1C(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 FIJIRZKOKTVVOZ-UHFFFAOYSA-N 0.000 description 1
- RGJXEFKYMBTAOM-UHFFFAOYSA-N 1-bromophenanthrene Chemical compound C1=CC2=CC=CC=C2C2=C1C(Br)=CC=C2 RGJXEFKYMBTAOM-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical compound C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000006023 1-pentenyl group Chemical group 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- MYKQKWIPLZEVOW-UHFFFAOYSA-N 11h-benzo[a]carbazole Chemical group C1=CC2=CC=CC=C2C2=C1C1=CC=CC=C1N2 MYKQKWIPLZEVOW-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical group C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- LDXJRKWFNNFDSA-UHFFFAOYSA-N 2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound C1CN(CC2=NNN=C21)CC(=O)N3CCN(CC3)C4=CN=C(N=C4)NCC5=CC(=CC=C5)OC(F)(F)F LDXJRKWFNNFDSA-UHFFFAOYSA-N 0.000 description 1
- OVNPUJOZNPAVJQ-UHFFFAOYSA-N 2-(3-chlorophenyl)-4,6-diphenyl-1,3,5-triazine Chemical compound ClC1=CC=CC(C=2N=C(N=C(N=2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 OVNPUJOZNPAVJQ-UHFFFAOYSA-N 0.000 description 1
- VWVRASTUFJRTHW-UHFFFAOYSA-N 2-[3-(azetidin-3-yloxy)-4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound O=C(CN1C=C(C(OC2CNC2)=N1)C1=CN=C(NC2CC3=C(C2)C=CC=C3)N=C1)N1CCC2=C(C1)N=NN2 VWVRASTUFJRTHW-UHFFFAOYSA-N 0.000 description 1
- SXAMGRAIZSSWIH-UHFFFAOYSA-N 2-[3-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,2,4-oxadiazol-5-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NOC(=N1)CC(=O)N1CC2=C(CC1)NN=N2 SXAMGRAIZSSWIH-UHFFFAOYSA-N 0.000 description 1
- NPHULPIAPWNOOH-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-(2,3-dihydroindol-1-ylmethyl)pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)CN1CCC2=CC=CC=C12 NPHULPIAPWNOOH-UHFFFAOYSA-N 0.000 description 1
- XXZCIYUJYUESMD-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-(morpholin-4-ylmethyl)pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)CN1CCOCC1 XXZCIYUJYUESMD-UHFFFAOYSA-N 0.000 description 1
- WWSJZGAPAVMETJ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-ethoxypyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)OCC WWSJZGAPAVMETJ-UHFFFAOYSA-N 0.000 description 1
- LPZOCVVDSHQFST-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-ethylpyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)CC LPZOCVVDSHQFST-UHFFFAOYSA-N 0.000 description 1
- FYELSNVLZVIGTI-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-5-ethylpyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1CC)CC(=O)N1CC2=C(CC1)NN=N2 FYELSNVLZVIGTI-UHFFFAOYSA-N 0.000 description 1
- JQMFQLVAJGZSQS-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JQMFQLVAJGZSQS-UHFFFAOYSA-N 0.000 description 1
- IHCCLXNEEPMSIO-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperidin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 IHCCLXNEEPMSIO-UHFFFAOYSA-N 0.000 description 1
- ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2 ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 0.000 description 1
- JVKRKMWZYMKVTQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JVKRKMWZYMKVTQ-UHFFFAOYSA-N 0.000 description 1
- YJLUBHOZZTYQIP-UHFFFAOYSA-N 2-[5-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NN=C(O1)CC(=O)N1CC2=C(CC1)NN=N2 YJLUBHOZZTYQIP-UHFFFAOYSA-N 0.000 description 1
- VHVYSMMZHORFKU-UHFFFAOYSA-N 2-bromo-1,3-dimethoxybenzene Chemical compound COC1=CC=CC(OC)=C1Br VHVYSMMZHORFKU-UHFFFAOYSA-N 0.000 description 1
- MBHPOBSZPYEADG-UHFFFAOYSA-N 2-bromo-9,9-dimethylfluorene Chemical compound C1=C(Br)C=C2C(C)(C)C3=CC=CC=C3C2=C1 MBHPOBSZPYEADG-UHFFFAOYSA-N 0.000 description 1
- 125000006276 2-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C(*)C([H])=C1[H] 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- PRKTYWJFCODJOA-UHFFFAOYSA-N 2-chlorodibenzofuran Chemical compound C1=CC=C2C3=CC(Cl)=CC=C3OC2=C1 PRKTYWJFCODJOA-UHFFFAOYSA-N 0.000 description 1
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000005916 2-methylpentyl group Chemical group 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- DXIJHCSGLOHNES-UHFFFAOYSA-N 3,3-dimethylbut-1-enylbenzene Chemical compound CC(C)(C)C=CC1=CC=CC=C1 DXIJHCSGLOHNES-UHFFFAOYSA-N 0.000 description 1
- DMEVMYSQZPJFOK-UHFFFAOYSA-N 3,4,5,6,9,10-hexazatetracyclo[12.4.0.02,7.08,13]octadeca-1(18),2(7),3,5,8(13),9,11,14,16-nonaene Chemical group N1=NN=C2C3=CC=CC=C3C3=CC=NN=C3C2=N1 DMEVMYSQZPJFOK-UHFFFAOYSA-N 0.000 description 1
- YLZOPXRUQYQQID-UHFFFAOYSA-N 3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]propan-1-one Chemical compound N1N=NC=2CN(CCC=21)CCC(=O)N1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F YLZOPXRUQYQQID-UHFFFAOYSA-N 0.000 description 1
- KYSRSEHFLTYWQI-UHFFFAOYSA-N 3-(3-bromophenyl)phenanthrene Chemical compound BrC1=CC=CC(C=2C=C3C4=CC=CC=C4C=CC3=CC=2)=C1 KYSRSEHFLTYWQI-UHFFFAOYSA-N 0.000 description 1
- PJTJCHPUFYMUNO-UHFFFAOYSA-N 3-(6-bromonaphthalen-2-yl)phenanthrene Chemical compound C1=CC=C2C3=CC(C4=CC5=CC=C(C=C5C=C4)Br)=CC=C3C=CC2=C1 PJTJCHPUFYMUNO-UHFFFAOYSA-N 0.000 description 1
- WCXFCLXZMIFHBU-UHFFFAOYSA-N 3-bromofluoranthene Chemical compound C12=CC=CC=C2C2=CC=CC3=C2C1=CC=C3Br WCXFCLXZMIFHBU-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- UCFSYHMCKWNKAH-UHFFFAOYSA-N 4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound CC1(C)OBOC1(C)C UCFSYHMCKWNKAH-UHFFFAOYSA-N 0.000 description 1
- JOQIJIMZTPMLCY-UHFFFAOYSA-N 4,5-dihydro-1-benzothiophene Chemical compound C1=CCCC2=C1SC=C2 JOQIJIMZTPMLCY-UHFFFAOYSA-N 0.000 description 1
- XSJLDNSNUICSQC-UHFFFAOYSA-N 4,6-dibromodibenzofuran Chemical compound O1C2=C(Br)C=CC=C2C2=C1C(Br)=CC=C2 XSJLDNSNUICSQC-UHFFFAOYSA-N 0.000 description 1
- BWRMZQGIDWILAU-UHFFFAOYSA-N 4,6-diphenylpyrimidine Chemical compound C1=CC=CC=C1C1=CC(C=2C=CC=CC=2)=NC=N1 BWRMZQGIDWILAU-UHFFFAOYSA-N 0.000 description 1
- DDTHMESPCBONDT-UHFFFAOYSA-N 4-(4-oxocyclohexa-2,5-dien-1-ylidene)cyclohexa-2,5-dien-1-one Chemical compound C1=CC(=O)C=CC1=C1C=CC(=O)C=C1 DDTHMESPCBONDT-UHFFFAOYSA-N 0.000 description 1
- GJXAVNQWIVUQOD-UHFFFAOYSA-N 4-bromodibenzothiophene Chemical compound S1C2=CC=CC=C2C2=C1C(Br)=CC=C2 GJXAVNQWIVUQOD-UHFFFAOYSA-N 0.000 description 1
- NJESAUCSIMQRGL-UHFFFAOYSA-N 4-bromophenanthrene Chemical compound C1=CC=CC2=C3C(Br)=CC=CC3=CC=C21 NJESAUCSIMQRGL-UHFFFAOYSA-N 0.000 description 1
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 1
- WTFUTSCZYYCBAY-SXBRIOAWSA-N 6-[(E)-C-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-N-hydroxycarbonimidoyl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C/C(=N/O)/C1=CC2=C(NC(O2)=O)C=C1 WTFUTSCZYYCBAY-SXBRIOAWSA-N 0.000 description 1
- DFGKGUXTPFWHIX-UHFFFAOYSA-N 6-[2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]acetyl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)C1=CC2=C(NC(O2)=O)C=C1 DFGKGUXTPFWHIX-UHFFFAOYSA-N 0.000 description 1
- SYPFPEMDKAKIFM-UHFFFAOYSA-N 7-(4-bromophenyl)-10-phenylfluoranthene Chemical compound BrC1=CC=C(C=C1)C1=C2C3=CC=CC4=CC=CC(C2=C(C=C1)C1=CC=CC=C1)=C43 SYPFPEMDKAKIFM-UHFFFAOYSA-N 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- GXVYYKSNVXVMNS-UHFFFAOYSA-N 9-(3-bromophenyl)phenanthrene Chemical compound BrC1=CC=CC(C=2C3=CC=CC=C3C3=CC=CC=C3C=2)=C1 GXVYYKSNVXVMNS-UHFFFAOYSA-N 0.000 description 1
- JZAFCDUOMYNXTO-UHFFFAOYSA-N 9-(4-bromophenyl)phenanthrene Chemical compound C1=CC(Br)=CC=C1C1=CC2=CC=CC=C2C2=CC=CC=C12 JZAFCDUOMYNXTO-UHFFFAOYSA-N 0.000 description 1
- RSQXKVWKJVUZDG-UHFFFAOYSA-N 9-bromophenanthrene Chemical compound C1=CC=C2C(Br)=CC3=CC=CC=C3C2=C1 RSQXKVWKJVUZDG-UHFFFAOYSA-N 0.000 description 1
- PWJXTSSQVFCSQT-UHFFFAOYSA-N B1CCOC1 Chemical compound B1CCOC1 PWJXTSSQVFCSQT-UHFFFAOYSA-N 0.000 description 1
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical group N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 1
- JFDOROOGDGZSCH-UHFFFAOYSA-N BrC1=C(C=CC=C1)C1=C(C=CC=C1)C1=CC=CC=2C3=CC=CC=C3C=CC1=2 Chemical compound BrC1=C(C=CC=C1)C1=C(C=CC=C1)C1=CC=CC=2C3=CC=CC=C3C=CC1=2 JFDOROOGDGZSCH-UHFFFAOYSA-N 0.000 description 1
- VEKSNOZYUGKSOF-UHFFFAOYSA-N Brc(cc1)cc2c1[s]c1c2c(-c2nc(-c(cccc3)c3-c3ccccc3)nc(-c3ccccc3)n2)ccc1 Chemical compound Brc(cc1)cc2c1[s]c1c2c(-c2nc(-c(cccc3)c3-c3ccccc3)nc(-c3ccccc3)n2)ccc1 VEKSNOZYUGKSOF-UHFFFAOYSA-N 0.000 description 1
- XGMDXENWGFMDDW-UHFFFAOYSA-N Brc1cccc(Sc(cccc2)c2Br)c1 Chemical compound Brc1cccc(Sc(cccc2)c2Br)c1 XGMDXENWGFMDDW-UHFFFAOYSA-N 0.000 description 1
- CJJVNVKOQMJMBT-UHFFFAOYSA-N Brc1cccc2c1c(cc(cc1)-c(cc3)cc4c3c3ccccc3c3ccccc43)c1[o]2 Chemical compound Brc1cccc2c1c(cc(cc1)-c(cc3)cc4c3c3ccccc3c3ccccc43)c1[o]2 CJJVNVKOQMJMBT-UHFFFAOYSA-N 0.000 description 1
- ZQIJGJTWYKZOSG-UHFFFAOYSA-N Brc1cccc2c1c1cc(-c(cccc3)c3-c(cccc3)c3-c3ccccc3)ccc1[o]2 Chemical compound Brc1cccc2c1c1cc(-c(cccc3)c3-c(cccc3)c3-c3ccccc3)ccc1[o]2 ZQIJGJTWYKZOSG-UHFFFAOYSA-N 0.000 description 1
- KYPNFEBMMQFIDM-UHFFFAOYSA-N Brc1cccc2c1c1cc(I)ccc1[o]2 Chemical compound Brc1cccc2c1c1cc(I)ccc1[o]2 KYPNFEBMMQFIDM-UHFFFAOYSA-N 0.000 description 1
- IXDHQBLCJJNKCW-UHFFFAOYSA-N C(C1=CC=CC=C1)(C1=CC=CC=C1)(C1=CC=CC=C1)C=1C=C(C=CC1)B(O)O Chemical compound C(C1=CC=CC=C1)(C1=CC=CC=C1)(C1=CC=CC=C1)C=1C=C(C=CC1)B(O)O IXDHQBLCJJNKCW-UHFFFAOYSA-N 0.000 description 1
- QEEIPLARTAMSRN-UHFFFAOYSA-N C(CC(c1nc(-c2c(c(cc(cc3)-c4cc5ccc(c6ccccc6cc6)c6c5cc4)c3[o]3)c3ccc2)nc(-c2ccccc2)n1)=C1)c2c1c(cccc1)c1[s]2 Chemical compound C(CC(c1nc(-c2c(c(cc(cc3)-c4cc5ccc(c6ccccc6cc6)c6c5cc4)c3[o]3)c3ccc2)nc(-c2ccccc2)n1)=C1)c2c1c(cccc1)c1[s]2 QEEIPLARTAMSRN-UHFFFAOYSA-N 0.000 description 1
- YPQXILCAWCYGHJ-UHFFFAOYSA-N C1=C(C=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)C1=CC=C(C=C1)B(O)O Chemical compound C1=C(C=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)C1=CC=C(C=C1)B(O)O YPQXILCAWCYGHJ-UHFFFAOYSA-N 0.000 description 1
- ODPJQTGHDFWLPR-UHFFFAOYSA-N CC(N(C)C(C1CCCC1)=O)=O Chemical compound CC(N(C)C(C1CCCC1)=O)=O ODPJQTGHDFWLPR-UHFFFAOYSA-N 0.000 description 1
- ZSBDPRIWBYHIAF-UHFFFAOYSA-N CC(NC(C)=O)=O Chemical compound CC(NC(C)=O)=O ZSBDPRIWBYHIAF-UHFFFAOYSA-N 0.000 description 1
- ZLANEMJAZDBYFH-UHFFFAOYSA-N CC1(C)OB(c2c(c3cc(-c(cc4)ccc4-c4ccccc4)ccc3[o]3)c3ccc2)OC1(C)C Chemical compound CC1(C)OB(c2c(c3cc(-c(cc4)ccc4-c4ccccc4)ccc3[o]3)c3ccc2)OC1(C)C ZLANEMJAZDBYFH-UHFFFAOYSA-N 0.000 description 1
- BKHRYWPRYDRELJ-UHFFFAOYSA-N CC1(C)OB(c2c(c3cc(-c4cc(cccc5)c5c5c4cccc5)ccc3[o]3)c3ccc2)OC1(C)C Chemical compound CC1(C)OB(c2c(c3cc(-c4cc(cccc5)c5c5c4cccc5)ccc3[o]3)c3ccc2)OC1(C)C BKHRYWPRYDRELJ-UHFFFAOYSA-N 0.000 description 1
- GPGBYRJEYUTDLX-UHFFFAOYSA-N CC1(C)OB(c2c(c3cc(-c4cc5ccc(c6ccccc6cc6)c6c5cc4)ccc3[o]3)c3ccc2)OC1(C)C Chemical compound CC1(C)OB(c2c(c3cc(-c4cc5ccc(c6ccccc6cc6)c6c5cc4)ccc3[o]3)c3ccc2)OC1(C)C GPGBYRJEYUTDLX-UHFFFAOYSA-N 0.000 description 1
- XEWGNBHQEUQVAS-UHFFFAOYSA-N CC1(C)OB(c2c(c3cc(-c4ccccc4-c(cccc4)c4-c4ccccc4)ccc3[o]3)c3ccc2)OC1(C)C Chemical compound CC1(C)OB(c2c(c3cc(-c4ccccc4-c(cccc4)c4-c4ccccc4)ccc3[o]3)c3ccc2)OC1(C)C XEWGNBHQEUQVAS-UHFFFAOYSA-N 0.000 description 1
- ZDNKFEKWLKIJPV-UHFFFAOYSA-N CC1(C)OB(c2cccc3c2c(cccc2-c(cc4)ccc4-c(cc4)ccc4-c4ccccc4)c2[o]3)OC1(C)C Chemical compound CC1(C)OB(c2cccc3c2c(cccc2-c(cc4)ccc4-c(cc4)ccc4-c4ccccc4)c2[o]3)OC1(C)C ZDNKFEKWLKIJPV-UHFFFAOYSA-N 0.000 description 1
- GCCHEFAXUVFOKS-UHFFFAOYSA-N CCC(N(CC)C(C)=O)=O Chemical compound CCC(N(CC)C(C)=O)=O GCCHEFAXUVFOKS-UHFFFAOYSA-N 0.000 description 1
- RIDYSAUBERCXSL-UHFFFAOYSA-N CN(C=O)C(c1ccccc1)=O Chemical compound CN(C=O)C(c1ccccc1)=O RIDYSAUBERCXSL-UHFFFAOYSA-N 0.000 description 1
- CNTHVKVOYCUDQU-UHFFFAOYSA-N COc1cccc(OC)c1-c(c(F)ccc1)c1Cl Chemical compound COc1cccc(OC)c1-c(c(F)ccc1)c1Cl CNTHVKVOYCUDQU-UHFFFAOYSA-N 0.000 description 1
- LKUZYIOHNJDVHO-UHFFFAOYSA-N COc1ccccc1-c(c(F)ccc1)c1Br Chemical compound COc1ccccc1-c(c(F)ccc1)c1Br LKUZYIOHNJDVHO-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- KBYZBOKBZLTSPI-UHFFFAOYSA-N Clc(cc1)cc2c1[o]c1c2c(-c2nc(-c3ccccc3)nc(-c3ccccc3)n2)ccc1 Chemical compound Clc(cc1)cc2c1[o]c1c2c(-c2nc(-c3ccccc3)nc(-c3ccccc3)n2)ccc1 KBYZBOKBZLTSPI-UHFFFAOYSA-N 0.000 description 1
- WXKGFVXGRJHAML-UHFFFAOYSA-N Clc(cc1[o]c2ccc3)ccc1c2c3Br Chemical compound Clc(cc1[o]c2ccc3)ccc1c2c3Br WXKGFVXGRJHAML-UHFFFAOYSA-N 0.000 description 1
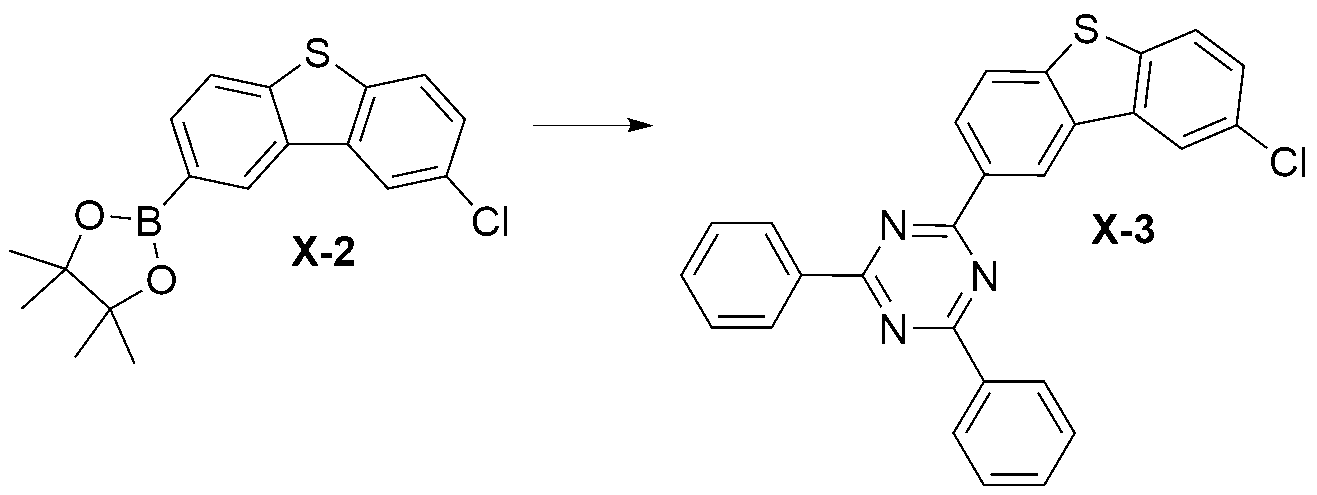
- XTPCMQVNRYXXIT-UHFFFAOYSA-N Clc(cc1c2c3)ccc1[s]c2ccc3-c1nc(-c2ccccc2)nc(-c2ccccc2)n1 Chemical compound Clc(cc1c2c3)ccc1[s]c2ccc3-c1nc(-c2ccccc2)nc(-c2ccccc2)n1 XTPCMQVNRYXXIT-UHFFFAOYSA-N 0.000 description 1
- JYMUQMRITLCSFT-UHFFFAOYSA-N Clc1cccc2c1c1cccc(-c(cc3)ccc3-c(cc3)ccc3-c3ccccc3)c1[o]2 Chemical compound Clc1cccc2c1c1cccc(-c(cc3)ccc3-c(cc3)ccc3-c3ccccc3)c1[o]2 JYMUQMRITLCSFT-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 229910052688 Gadolinium Inorganic materials 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 1
- NIPNSKYNPDTRPC-UHFFFAOYSA-N N-[2-oxo-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 NIPNSKYNPDTRPC-UHFFFAOYSA-N 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- VCUFZILGIRCDQQ-KRWDZBQOSA-N N-[[(5S)-2-oxo-3-(2-oxo-3H-1,3-benzoxazol-6-yl)-1,3-oxazolidin-5-yl]methyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C1O[C@H](CN1C1=CC2=C(NC(O2)=O)C=C1)CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F VCUFZILGIRCDQQ-KRWDZBQOSA-N 0.000 description 1
- CNJMGYWSOGWUFO-UHFFFAOYSA-N OB(c1cccc([o]c2c3)c1c2ccc3Cl)O Chemical compound OB(c1cccc([o]c2c3)c1c2ccc3Cl)O CNJMGYWSOGWUFO-UHFFFAOYSA-N 0.000 description 1
- GVKDYOVTRHDDPI-UHFFFAOYSA-N Oc(cccc1O)c1-c(c(F)ccc1)c1Cl Chemical compound Oc(cccc1O)c1-c(c(F)ccc1)c1Cl GVKDYOVTRHDDPI-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- YXLXNENXOJSQEI-UHFFFAOYSA-L Oxine-copper Chemical compound [Cu+2].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 YXLXNENXOJSQEI-UHFFFAOYSA-L 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- NRCMAYZCPIVABH-UHFFFAOYSA-N Quinacridone Chemical compound N1C2=CC=CC=C2C(=O)C2=C1C=C1C(=O)C3=CC=CC=C3NC1=C2 NRCMAYZCPIVABH-UHFFFAOYSA-N 0.000 description 1
- 229910052772 Samarium Inorganic materials 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 229910052769 Ytterbium Inorganic materials 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- JAWMENYCRQKKJY-UHFFFAOYSA-N [3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-ylmethyl)-1-oxa-2,8-diazaspiro[4.5]dec-2-en-8-yl]-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]methanone Chemical compound N1N=NC=2CN(CCC=21)CC1=NOC2(C1)CCN(CC2)C(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F JAWMENYCRQKKJY-UHFFFAOYSA-N 0.000 description 1
- MKYMRPWGXSEFKE-UHFFFAOYSA-N [3-(4-phenylphenyl)phenyl]boronic acid Chemical compound OB(O)C1=CC=CC(C=2C=CC(=CC=2)C=2C=CC=CC=2)=C1 MKYMRPWGXSEFKE-UHFFFAOYSA-N 0.000 description 1
- 125000005332 alkyl sulfoxy group Chemical group 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 150000001454 anthracenes Chemical class 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 150000003974 aralkylamines Chemical group 0.000 description 1
- 125000005165 aryl thioxy group Chemical group 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 150000001556 benzimidazoles Chemical class 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 229910052790 beryllium Inorganic materials 0.000 description 1
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 1
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 1
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 150000001638 boron Chemical class 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- LUUVFHQMDMVIKH-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)c(cccc2)c2c1-c(cc1)cc2c1[o]c1cccc(-c3nc(-c4ccccc4)nc(-c4ccccc4)n3)c21 Chemical compound c(cc1)ccc1-c(cc1)c(cccc2)c2c1-c(cc1)cc2c1[o]c1cccc(-c3nc(-c4ccccc4)nc(-c4ccccc4)n3)c21 LUUVFHQMDMVIKH-UHFFFAOYSA-N 0.000 description 1
- COWGRJFVTTZJDP-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)cc(-c(cc2)cc3c2[s]c2cccc(-c4nc(-c5ccccc5)nc(-c(cccc5)c5-c5ccccc5)n4)c32)c1-c1ccccc1 Chemical compound c(cc1)ccc1-c(cc1)cc(-c(cc2)cc3c2[s]c2cccc(-c4nc(-c5ccccc5)nc(-c(cccc5)c5-c5ccccc5)n4)c32)c1-c1ccccc1 COWGRJFVTTZJDP-UHFFFAOYSA-N 0.000 description 1
- QCRYBZZSTGYUNF-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1ccc2[o]c3cccc(-c4nc(-c5ccccc5)nc(-c(cc5)ccc5-c5cccc(-c6ccccc6)c5)n4)c3c2c1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1ccc2[o]c3cccc(-c4nc(-c5ccccc5)nc(-c(cc5)ccc5-c5cccc(-c6ccccc6)c5)n4)c3c2c1 QCRYBZZSTGYUNF-UHFFFAOYSA-N 0.000 description 1
- BPWIIYGDWYVBHM-UHFFFAOYSA-N c(cc1)ccc1-c1c(-c(cc2)cc3c2[s]c2cccc(-c(cc4)ccc4-c4nc(-c5ccc6[s]c7ccccc7c6c5)nc(-c5ccccc5)n4)c32)c(cccc2)c2c2c1cccc2 Chemical compound c(cc1)ccc1-c1c(-c(cc2)cc3c2[s]c2cccc(-c(cc4)ccc4-c4nc(-c5ccc6[s]c7ccccc7c6c5)nc(-c5ccccc5)n4)c32)c(cccc2)c2c2c1cccc2 BPWIIYGDWYVBHM-UHFFFAOYSA-N 0.000 description 1
- RTXYJPZSOJEMRE-UHFFFAOYSA-N c(cc1)ccc1-c1cc(c2cc(-c(cc3)cc4c3[s]c3c4c(-c(cc4)ccc4-c4nc(-c5ccccc5)nc(-c(cc5)cc6c5[s]c5ccccc65)n4)ccc3)ccc2cc2)c2cc1 Chemical compound c(cc1)ccc1-c1cc(c2cc(-c(cc3)cc4c3[s]c3c4c(-c(cc4)ccc4-c4nc(-c5ccccc5)nc(-c(cc5)cc6c5[s]c5ccccc65)n4)ccc3)ccc2cc2)c2cc1 RTXYJPZSOJEMRE-UHFFFAOYSA-N 0.000 description 1
- QKMIYNCHEGCTOI-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c(cc2)cc3c2[s]c2c3cccc2)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4cc(cccc5)c5c5c4cccc5)c2[s]3)n1 Chemical compound c(cc1)ccc1-c1nc(-c(cc2)cc3c2[s]c2c3cccc2)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4cc(cccc5)c5c5c4cccc5)c2[s]3)n1 QKMIYNCHEGCTOI-UHFFFAOYSA-N 0.000 description 1
- VBKPQTODWWZBTC-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c(cc2)cc3c2[s]c2c3cccc2)nc(-c2cc(-c3cccc4c3c3cc(-c5cc(cccc6)c6c6c5cccc6)ccc3[s]4)ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c(cc2)cc3c2[s]c2c3cccc2)nc(-c2cc(-c3cccc4c3c3cc(-c5cc(cccc6)c6c6c5cccc6)ccc3[s]4)ccc2)n1 VBKPQTODWWZBTC-UHFFFAOYSA-N 0.000 description 1
- CEAFABTZRJWKSW-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c(cc2)cc3c2c(cccc2)c2[s]3)nc(-c(cccc2)c2-c2c(c3cc(-c4cc(cccc5)c5c5c4cccc5)ccc3[s]3)c3ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c(cc2)cc3c2c(cccc2)c2[s]3)nc(-c(cccc2)c2-c2c(c3cc(-c4cc(cccc5)c5c5c4cccc5)ccc3[s]3)c3ccc2)n1 CEAFABTZRJWKSW-UHFFFAOYSA-N 0.000 description 1
- JENUNGBPBSHZRA-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c(cc2)cc3c2c2ccccc2[s]3)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4cc5ccccc5c5c4cccc5)c2[s]3)n1 Chemical compound c(cc1)ccc1-c1nc(-c(cc2)cc3c2c2ccccc2[s]3)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4cc5ccccc5c5c4cccc5)c2[s]3)n1 JENUNGBPBSHZRA-UHFFFAOYSA-N 0.000 description 1
- LCDDLSVRARTBFH-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2c(c(cc(cc3)-c4cc(cccc5)c5c5c4cccc5)c3[s]3)c3ccc2)nc(-c2cccc3c2c2ccccc2[s]3)n1 Chemical compound c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2c(c(cc(cc3)-c4cc(cccc5)c5c5c4cccc5)c3[s]3)c3ccc2)nc(-c2cccc3c2c2ccccc2[s]3)n1 LCDDLSVRARTBFH-UHFFFAOYSA-N 0.000 description 1
- ZADQQQXGUYRAKT-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2c(c(cccc3)c3[s]3)c3ccc2)nc(-c2cccc(-c3c(c4cc(-c5cccc6c5ccc5c(cccc7)c7ccc65)ccc4[s]4)c4ccc3)c2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2c(c(cccc3)c3[s]3)c3ccc2)nc(-c2cccc(-c3c(c4cc(-c5cccc6c5ccc5c(cccc7)c7ccc65)ccc4[s]4)c4ccc3)c2)n1 ZADQQQXGUYRAKT-UHFFFAOYSA-N 0.000 description 1
- FKTZOLHOHHGUFD-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2c(c3cc(-c(cccc4-5)c4-c4cccc6cccc-5c46)ccc3[s]3)c3ccc2)nc(-c(cc2)cc3c2[s]c2ccccc32)n1 Chemical compound c(cc1)ccc1-c1nc(-c2c(c3cc(-c(cccc4-5)c4-c4cccc6cccc-5c46)ccc3[s]3)c3ccc2)nc(-c(cc2)cc3c2[s]c2ccccc32)n1 FKTZOLHOHHGUFD-UHFFFAOYSA-N 0.000 description 1
- WDJMFPNGUVTJTI-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2c(c3ccccc3[s]3)c3ccc2)nc(-c2cc(-c3cccc4c3c3cc(-c5cc6ccccc6c6ccccc56)ccc3[s]4)ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2c(c3ccccc3[s]3)c3ccc2)nc(-c2cc(-c3cccc4c3c3cc(-c5cc6ccccc6c6ccccc56)ccc3[s]4)ccc2)n1 WDJMFPNGUVTJTI-UHFFFAOYSA-N 0.000 description 1
- MXQWGHIVGHGHHJ-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2c3[s]c(cccc4)c4c3ccc2)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4c(cccc5)c5c(cccc5)c5c4)c2[s]3)n1 Chemical compound c(cc1)ccc1-c1nc(-c2c3[s]c(cccc4)c4c3ccc2)nc(-c(cc2)ccc2-c2cccc3c2c(cc(cc2)-c4c(cccc5)c5c(cccc5)c5c4)c2[s]3)n1 MXQWGHIVGHGHHJ-UHFFFAOYSA-N 0.000 description 1
- GPWDUFWRJFHLHL-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2c3[s]c4ccccc4c3ccc2)nc(-c2ccccc2-c2c(c3cc(-c4c(cccc5)c5c(cccc5)c5c4)ccc3[s]3)c3ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2c3[s]c4ccccc4c3ccc2)nc(-c2ccccc2-c2c(c3cc(-c4c(cccc5)c5c(cccc5)c5c4)ccc3[s]3)c3ccc2)n1 GPWDUFWRJFHLHL-UHFFFAOYSA-N 0.000 description 1
- RUKQMTLMYLKWCQ-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2ccc(c3ccccc3[s]3)c3c2)nc(-c2c(c3cc(-c4cc5c(cccc6)c6c(cccc6)c6c5cc4)ccc3[o]3)c3ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2ccc(c3ccccc3[s]3)c3c2)nc(-c2c(c3cc(-c4cc5c(cccc6)c6c(cccc6)c6c5cc4)ccc3[o]3)c3ccc2)n1 RUKQMTLMYLKWCQ-UHFFFAOYSA-N 0.000 description 1
- HLAXGONHWMXGRR-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2ccc3[s]c(cccc4)c4c3c2)nc(-c2cc(-c3cccc4c3c(cc(cc3)-c5ccc(ccc6c(cccc7)c7ccc66)c6c5)c3[s]4)ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2ccc3[s]c(cccc4)c4c3c2)nc(-c2cc(-c3cccc4c3c(cc(cc3)-c5ccc(ccc6c(cccc7)c7ccc66)c6c5)c3[s]4)ccc2)n1 HLAXGONHWMXGRR-UHFFFAOYSA-N 0.000 description 1
- ZQVNJTUWMFGXLZ-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2cccc(-c3c(c4cc(-c5ccc-6c7c5cccc7-c5c-6cccc5)ccc4[s]4)c4ccc3)c2)nc(-c2ccc(c3ccccc3[s]3)c3c2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2cccc(-c3c(c4cc(-c5ccc-6c7c5cccc7-c5c-6cccc5)ccc4[s]4)c4ccc3)c2)nc(-c2ccc(c3ccccc3[s]3)c3c2)n1 ZQVNJTUWMFGXLZ-UHFFFAOYSA-N 0.000 description 1
- NKPQSAPNFFXEIW-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2cccc3c2[s]c2c3cccc2)nc(-c2cc(-c3c(c(cc(cc4)-c(cccc5-6)c5-c5cccc7cccc-6c57)c4[s]4)c4ccc3)ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2cccc3c2[s]c2c3cccc2)nc(-c2cc(-c3c(c(cc(cc4)-c(cccc5-6)c5-c5cccc7cccc-6c57)c4[s]4)c4ccc3)ccc2)n1 NKPQSAPNFFXEIW-UHFFFAOYSA-N 0.000 description 1
- YBYDWYYNZRAHFO-UHFFFAOYSA-N c(cc1)ccc1-c1nc(-c2cccc3c2[s]c2ccccc32)nc(-c2cc(-c3c(c4cc(-c5cc(cccc6)c6c6c5cccc6)ccc4[s]4)c4ccc3)ccc2)n1 Chemical compound c(cc1)ccc1-c1nc(-c2cccc3c2[s]c2ccccc32)nc(-c2cc(-c3c(c4cc(-c5cc(cccc6)c6c6c5cccc6)ccc4[s]4)c4ccc3)ccc2)n1 YBYDWYYNZRAHFO-UHFFFAOYSA-N 0.000 description 1
- CEIGRHPZXHKWBK-UHFFFAOYSA-N c1ccc(C(c2ccccc2)(c2ccccc2)c(cc2)ccc2-c(cc2)cc3c2[o]c2cccc(-c4nc(-c5ccccc5)nc(-c5ccccc5)n4)c32)cc1 Chemical compound c1ccc(C(c2ccccc2)(c2ccccc2)c(cc2)ccc2-c(cc2)cc3c2[o]c2cccc(-c4nc(-c5ccccc5)nc(-c5ccccc5)n4)c32)cc1 CEIGRHPZXHKWBK-UHFFFAOYSA-N 0.000 description 1
- UHOVQNZJYSORNB-UHFFFAOYSA-N c1ccccc1 Chemical compound c1ccccc1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 150000001716 carbazoles Chemical class 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- XOYLJNJLGBYDTH-UHFFFAOYSA-M chlorogallium Chemical compound [Ga]Cl XOYLJNJLGBYDTH-UHFFFAOYSA-M 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 150000004826 dibenzofurans Chemical class 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- LYINKTVZUSKQEQ-UHFFFAOYSA-N furan-3-one Chemical compound O=C1COC=C1 LYINKTVZUSKQEQ-UHFFFAOYSA-N 0.000 description 1
- 150000002240 furans Chemical class 0.000 description 1
- UIWYJDYFSGRHKR-UHFFFAOYSA-N gadolinium atom Chemical compound [Gd] UIWYJDYFSGRHKR-UHFFFAOYSA-N 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- QFWPJPIVLCBXFJ-UHFFFAOYSA-N glymidine Chemical compound N1=CC(OCCOC)=CN=C1NS(=O)(=O)C1=CC=CC=C1 QFWPJPIVLCBXFJ-UHFFFAOYSA-N 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 150000002431 hydrogen Chemical group 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000005462 imide group Chemical group 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910003437 indium oxide Inorganic materials 0.000 description 1
- PJXISJQVUVHSOJ-UHFFFAOYSA-N indium(iii) oxide Chemical compound [O-2].[O-2].[O-2].[In+3].[In+3] PJXISJQVUVHSOJ-UHFFFAOYSA-N 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000011133 lead Substances 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- SFMJNHNUOVADRW-UHFFFAOYSA-N n-[5-[9-[4-(methanesulfonamido)phenyl]-2-oxobenzo[h][1,6]naphthyridin-1-yl]-2-methylphenyl]prop-2-enamide Chemical compound C1=C(NC(=O)C=C)C(C)=CC=C1N1C(=O)C=CC2=C1C1=CC(C=3C=CC(NS(C)(=O)=O)=CC=3)=CC=C1N=C2 SFMJNHNUOVADRW-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 150000002790 naphthalenes Chemical class 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000002560 nitrile group Chemical group 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical group [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- 150000002964 pentacenes Chemical class 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- LUYQYZLEHLTPBH-UHFFFAOYSA-N perfluorobutanesulfonyl fluoride Chemical compound FC(F)(F)C(F)(F)C(F)(F)C(F)(F)S(F)(=O)=O LUYQYZLEHLTPBH-UHFFFAOYSA-N 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N perylene Chemical compound C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- FVDOBFPYBSDRKH-UHFFFAOYSA-N perylene-3,4,9,10-tetracarboxylic acid Chemical compound C=12C3=CC=C(C(O)=O)C2=C(C(O)=O)C=CC=1C1=CC=C(C(O)=O)C2=C1C3=CC=C2C(=O)O FVDOBFPYBSDRKH-UHFFFAOYSA-N 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- 150000002987 phenanthrenes Chemical class 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- XPPWLXNXHSNMKC-UHFFFAOYSA-N phenylboron Chemical group [B]C1=CC=CC=C1 XPPWLXNXHSNMKC-UHFFFAOYSA-N 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920002098 polyfluorene Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920000123 polythiophene Polymers 0.000 description 1
- 150000004032 porphyrins Chemical class 0.000 description 1
- 239000007774 positive electrode material Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000003220 pyrenes Chemical class 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- YYMBJDOZVAITBP-UHFFFAOYSA-N rubrene Chemical compound C1=CC=CC=C1C(C1=C(C=2C=CC=CC=2)C2=CC=CC=C2C(C=2C=CC=CC=2)=C11)=C(C=CC=C2)C2=C1C1=CC=CC=C1 YYMBJDOZVAITBP-UHFFFAOYSA-N 0.000 description 1
- KZUNJOHGWZRPMI-UHFFFAOYSA-N samarium atom Chemical compound [Sm] KZUNJOHGWZRPMI-UHFFFAOYSA-N 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 150000003413 spiro compounds Chemical class 0.000 description 1
- 125000003003 spiro group Chemical group 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 238000010345 tape casting Methods 0.000 description 1
- JLBRGNFGBDNNSF-UHFFFAOYSA-N tert-butyl(dimethyl)borane Chemical group CB(C)C(C)(C)C JLBRGNFGBDNNSF-UHFFFAOYSA-N 0.000 description 1
- UOHMMEJUHBCKEE-UHFFFAOYSA-N tetramethylbenzene Natural products CC1=CC=C(C)C(C)=C1C UOHMMEJUHBCKEE-UHFFFAOYSA-N 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- IBBLKSWSCDAPIF-UHFFFAOYSA-N thiopyran Chemical compound S1C=CC=C=C1 IBBLKSWSCDAPIF-UHFFFAOYSA-N 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 1
- KWQNQSDKCINQQP-UHFFFAOYSA-K tri(quinolin-8-yloxy)gallane Chemical compound C1=CN=C2C(O[Ga](OC=3C4=NC=CC=C4C=CC=3)OC=3C4=NC=CC=C4C=CC=3)=CC=CC2=C1 KWQNQSDKCINQQP-UHFFFAOYSA-K 0.000 description 1
- LALRXNPLTWZJIJ-UHFFFAOYSA-N triethylborane Chemical group CCB(CC)CC LALRXNPLTWZJIJ-UHFFFAOYSA-N 0.000 description 1
- WXRGABKACDFXMG-UHFFFAOYSA-N trimethylborane Chemical group CB(C)C WXRGABKACDFXMG-UHFFFAOYSA-N 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- MXSVLWZRHLXFKH-UHFFFAOYSA-N triphenylborane Chemical group C1=CC=CC=C1B(C=1C=CC=CC=1)C1=CC=CC=C1 MXSVLWZRHLXFKH-UHFFFAOYSA-N 0.000 description 1
- 238000001771 vacuum deposition Methods 0.000 description 1
- 238000005292 vacuum distillation Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- NAWDYIZEMPQZHO-UHFFFAOYSA-N ytterbium Chemical compound [Yb] NAWDYIZEMPQZHO-UHFFFAOYSA-N 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- VWQVUPCCIRVNHF-UHFFFAOYSA-N yttrium atom Chemical compound [Y] VWQVUPCCIRVNHF-UHFFFAOYSA-N 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
- HTPBWAPZAJWXKY-UHFFFAOYSA-L zinc;quinolin-8-olate Chemical compound [Zn+2].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 HTPBWAPZAJWXKY-UHFFFAOYSA-L 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H01L51/0073—
-
- H01L51/0074—
-
- H01L51/5012—
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/90—Multiple hosts in the emissive layer
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/81—Anodes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/80—Constructional details
- H10K50/805—Electrodes
- H10K50/82—Cathodes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
도 2는 기판(1), 양극(2), 정공 주입층(5), 정공 수송층(6), 발광층(7), 전자수송층(8) 및 음극(4)로 이루어진 유기 발광 소자의 예를 도시한 것이다.
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@50mA/cm2) |
| 실시예 1 | 화합물1:YGD-1 (400)12% |
2.99 | 62.8 | (0.46,0.54) | 47.5 |
| 실시예 2 | 화합물2:YGD-1 (400)12% |
2.99 | 64.1 | (0.46,0.53) | 50.5 |
| 실시예 3 | 화합물3:YGD-1 (400)16% |
2.97 | 65.0 | (0.46,0.52) | 47.0 |
| 실시예 4 | 화합물4:YGD-1 (400)12% |
3.15 | 62.8 | (0.46,0.53) | 78.6 |
| 실시예 5 | 화합물5:YGD-1 (400)14% |
3.11 | 53.8 | (0.47,0.52) | 46.4 |
| 실시예 6 | 화합물6:YGD-1 (400)12% |
3.23 | 62.7 | (0.47,0.53) | 49.9 |
| 실시예 7 | 화합물7:YGD-1 (400)12% |
3.20 | 63.1 | (0.46,0.53) | 50.3 |
| 실시예 8 | 화합물8:YGD-1 (400)16% |
3.30 | 55.7 | (0.47,0.52) | 87.9 |
| 실시예 9 | 화합물9:YGD-1 (400)16% |
2.97 | 64.2 | (0.46,0.54) | 70.5 |
| 실시예 10 | 화합물10:YGD-1 (400)16% |
3.12 | 60.3 | (0.47,0.53) | 47.7 |
| 실시예 11 | 화합물11:YGD-1 (400)16% |
2.89 | 63.0 | (0.46,0.53) | 69.8 |
| 실시예 12 | 화합물14:YGD-1 (400)16% |
3.08 | 56.1 | (0.45,0.54) | 47.6 |
| 실시예 13 | 화합물15:YGD-1 (400)12% |
3.00 | 63.0 | (0.46,0.53) | 47.1 |
| 실시예 14 | 화합물16:YGD-1 (400)12% |
3.28 | 63.2 | (0.46,0.53) | 41.8 |
| 실시예 15 | 화합물12:YGD-1 (200:200)16% |
3.55 | 65.9 | (0.46,0.52) | 126.2 |
| 실시예 16 | 화합물13:PH-1:YGD-1 (160:240)16% |
3.51 | 67.2 | (0.46,0.53) | 116.0 |
| 실시예 17 | 화합물4:PH-2:YGD-1 (160:240)12% |
3.57 | 67.7 | (0.46,0.53) | 191.9 |
| 실시예 18 | 화합물17:PH-2:YGD-1 (200:200)16% |
3.53 | 67.8 | (0.47,0.53) | 125.1 |
| 실시예 19 | 화합물18:PH-2:YGD-1 (160:240)12% |
3.56 | 70.2 | (0.45,0.53) | 132.8 |
| 실시예 20 | 화합물19:PH-2:YGD-1 (200:200)15% |
3.50 | 68.9 | (0.46,0.53) | 352.0 |
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@50mA/cm2) |
| 실시예 21 | 화합물20:PH-3:YGD-1 (160:240)12% |
3.64 | 65.4 | (0.45,0.54) | 155.7 |
| 실시예 22 | 화합물21:PH-2:YGD-1 (200:200)14% |
3.58 | 64.1 | (0.46,0.54) | 100.3 |
| 실시예 23 | 화합물22:PH-3:YGD-1 (200:200)16% |
3.60 | 66.5 | (0.46,0.54) | 115.6 |
| 실시예 24 | 화합물23:PH-2:YGD-1 (160:240)12% |
3.71 | 66.8 | (0.46,0.53) | 180.3 |
| 실시예 25 | 화합물24:PH-2:YGD-1 (160:240)12% |
3.48 | 67.1 | (0.46,0.53) | 230.7 |
| 실시예 26 | 화합물25:YGD-1 (400)16% |
3.12 | 60.3 | (0.46,0.52) | 48.3 |
| 실시예 27 | 화합물26:YGD-1 (400)12% |
3.01 | 61.7 | (0.48,0.51) | 84.9 |
| 실시예 28 | 화합물27:YGD-1 (400)16% |
2.98 | 58.5 | (0.48,0.51) | 76.1 |
| 실시예 29 | 화합물28:YGD-1 (400)16% |
3.00 | 67.1 | (0.47,0.52) | 87.2 |
| 실시예 30 | 화합물29:YGD-1 (400)16% |
3.04 | 65.4 | (0.46,0.53) | 68.1 |
| 실시예 31 | 화합물30:YGD-1 (400)16% |
3.01 | 66.1 | (0.46,0.52) | 73.6 |
| 실시예 32 | 화합물31:YGD-1 (400)12% |
3.12 | 60.2 | (0.46,0.53) | 77.2 |
| 실시예 33 | 화합물32:YGD-1 (400)12% |
3.08 | 64.2 | (0.45,0.53) | 76.8 |
| 실시예 34 | 화합물33:YGD-1 (400)16% |
3.11 | 52.6 | (0.45,0.53) | 46.2 |
| 실시예 35 | 화합물34:YGD-1 (400)16% |
2.97 | 59.9 | (0.46,0.54) | 74.3 |
| 실시예 36 | 화합물35:YGD-1 (400)12% |
3.04 | 62.4 | (0.45,0.53) | 79.8 |
| 실시예 37 | 화합물36:YGD-1 (400)16% |
3.10 | 59.15 | (0.45,0.55) | 48.4 |
| 실시예 38 | 화합물37:YGD-1 (400)14% |
3.01 | 59.2 | (0.45,0.53) | 44.1 |
| 실시예 39 | 화합물38:PH-1:YGD-1 (200:200)12% |
3.52 | 67.2 | (0.46,0.53) | 160.3 |
| 실시예 40 | 화합물39:PH-2:YGD-1 (160:240)16% |
3.49 | 72.4 | (0.45,0.54) | 265.8 |
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@50mA/cm2) |
| 실시예 41 | 화합물40:PH-3:YGD-1 (200:200)16% |
3.61 | 62.6 | (0.44,0.54) | 102.8 |
| 실시예 42 | 화합물41:PH-2:YGD-1 (160:240)16% |
3.48 | 65.1 | (0.47,0.53) | 272.1 |
| 실시예 43 | 화합물42:PH-2:YGD-1 (160:240)12% |
3.52 | 67.7 | (0.45,0.54) | 326.1 |
| 실시예 44 | 화합물43:PH-3:YGD-1 (160:240)12% |
3.55 | 62.4 | (0.45,0.53) | 239.8 |
| 실시예 45 | 화합물44:PH-3:YGD-1 (200:200)16% |
3.60 | 60.0 | (0.46,0.52) | 154.2 |
| 실시예 46 | 화합물46:PH-1:YGD-1 (160:240)16% |
3.62 | 64.68 | (0.45,0.53) | 175.3 |
| 실시예 47 | 화합물28:PH-2:YGD-1 (160:240)16% |
3.51 | 67.9 | (0.45,0.54) | 330.2 |
| 실시예 48 | 화합물81:PH-2:YGD-1 (160:240)12% |
3.53 | 65.3 | (0.47,0.54) | 289.6 |
| 실시예 49 | 화합물45:PH-2:YGD-1 (160:240)12% |
3.50 | 68.1 | (0.45,0.52) | 349.8 |
| 비교예 1 | 화합물A:YGD-1 (400)12% |
3.21 | 61.9 | (0.46,0.53) | 25.9 |
| 비교예 2 | 화합물B:YGD-1 (400)12% |
3.17 | 56.2 | (0.47,0.52) | 27.3 |
| 비교예 3 | 화합물C:YGD-1 (400)12% |
2.92 | 62.2 | (0.48,0.50) | 20.3 |
| 비교예 4 | 화합물D:YGD-1 (400)12% |
3.11 | 67.3 | (0.48,0.53) | 26.2 |
| 비교예 5 | 화합물E:YGD-1 (400)12% |
4.73 | 28.11 | (0.47,0.51) | 22.2 |
| 비교예 6 | 화합물F:YGD-1 (400)12% |
3.15 | 53.2 | (0.48,0.50) | 27.5 |
| 비교예 7 | 화합물G:YGD-1 (400)12% |
3.14 | 52.7 | (0.49,0.50) | 26.9 |
| 비교예 8 | 화합물H:YGD-1 (400)12% |
3.14 | 56.8 | (0.49,0.50) | 28.9 |
| 비교예 9 | 화합물I:YGD-1 (400)12% |
3.0 | 60 | (0.46,0.53) | 31.5 |
| 비교예 10 | 화합물A:PH-1:YGD-1 (160:240)16% |
3.63 | 64.3 | (0.47,0.53) | 63.2 |
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@20mA/cm2) |
| 실시예 50 | 화합물47:GD-1 (400)5% |
4 | 50.8 | (0.349,0.612) | 52.9 |
| 실시예 51 | 화합물48:GD-1 (400)5% |
4.01 | 51.1 | (0.350,0.610) | 66.4 |
| 실시예 52 | 화합물49:GD-1 (400)7% |
3.98 | 51.2 | (0.350,0.611) | 59.65 |
| 실시예 53 | 화합물50:GD-1 (400)5% |
4.11 | 51.8 | (0.348,0.612) | 51.8 |
| 실시예 54 | 화합물51:GD-1 (400)5% |
4.09 | 50.2 | (0.345,0.612) | 51.4 |
| 실시예 55 | 화합물52:GD-1 (400)7% |
4.1 | 50.8 | (0.348.0.610) | 51.5 |
| 실시예 56 | 화합물16:GD-1 (400)5% |
4.08 | 49.1 | (0.349,0.610) | 46.7 |
| 실시예 57 | 화합물53:GD-1 (400)7% |
4.02 | 51.8 | (0.348,0.612) | 55.5 |
| 실시예 58 | 화합물20:GD-1 (400)5% |
3.97 | 52.8 | (0.349,0.611) | 67.7 |
| 실시예 59 | 화합물54:GD-1 (400)5% |
4.01 | 52.4 | (0.350,0.613) | 66.2 |
| 실시예 60 | 화합물46:GD-1 (400)5% |
4.0 | 52.9 | (0.349,0.612) | 65.6 |
| 실시예 61 | 화합물55:GD-1 (400)5% |
3.99 | 52.7 | (0.350,0.611) | 65.8 |
| 실시예 62 | 화합물56:GD-1 (400)10% |
3.99 | 52.4 | (0.347,0.612) | 51.3 |
| 실시예 63 | 화합물4:PH-2:GD-1 (200:200)5% |
3.71 | 55.1 | (0.351,0.609) | 110.2 |
| 실시예 64 | 화합물57:PH-3:GD-1 (200:200)5% |
4.07 | 52.9 | (0.348,0.612) | 79.9 |
| 실시예 65 | 화합물58:PH-1:GD-1 (200:200)5% |
4.2 | 51.7 | (0.347,0.610) | 88.7 |
| 실시예 66 | 화합물6:PH-2:GD-1 (200:200)5% |
4.21 | 53.4 | (0.347,0.613) | 100.1 |
| 실시예 67 | 화합물50:PH-2:GD-1 (160:240)7% |
4.17 | 58.1 | (0.348,0.612) | 78.9 |
| 실시예 68 | 화합물60:PH-2:GD-1 (160:240)5% |
4.23 | 51.7 | (0.347,0.611) | 89.2 |
| 실시예 69 | 화합물61:PH-3:GD-1 (200:200)5% |
4.11 | 54.2 | (0.351,0.613) | 106.2 |
| 실시예 70 | 화합물62:PH-2:GD-1 (160:240)5% |
4.22 | 51.9 | (0.351,0.613) | 170.7 |
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@20mA/cm2) |
| 실시예 71 | 화합물63:PH-3:GD-1 (200:200)5% |
4.31 | 54.2 | (0.349,0.613) | 134.9 |
| 실시예 72 | 화합물64:PH-1:GD-1 (160:240)7% |
4.30 | 54.3 | (0.347,0.612) | 135.4 |
| 실시예 73 | 화합물65:PH-2:GD-1 (200:200)5% |
4.19 | 52.9 | (0.351,0.613) | 170.9 |
| 실시예 74 | 화합물66:PH-1:GD-1 (160:240)10% |
3.92 | 52.3 | (0.351,0.613) | 171.4 |
| 실시예 75 | 화합물67:PH-2:GD-1 (200:200)5% |
4.12 | 54.9 | (0.350,0.611) | 128.2 |
| 실시예 76 | 화합물68:PH-1:GD-1 (160:240)5% |
3.76 | 56.8 | (0.352,0.609) | 104 |
| 실시예 77 | 화합물69:PH-2:GD-1 (160:240)7% |
4.10 | 55.1 | (0.351,0.613) | 103.2 |
| 실시예 78 | 화합물70:PH-1:GD-1 (160:240)5% |
4.17 | 56.53 | (0.351,0.613) | 104.5 |
| 실시예 79 | 화합물71:PH-3:GD-1 (200:200)7% |
4.24 | 54.6 | (0.346,0.612) | 137.9 |
| 실시예 80 | 화합물72:PH-2:GD-1 (200:200)5% |
4.32 | 56.1 | (0.350,0.612) | 158.8 |
| 실시예 81 | 화합물73:PH-2:GD-1 (160:240)5% |
4.42 | 51.24 | (0.346,0.611) | 102.5 |
| 실시예 82 | 화합물74:PH-2:GD-1 (160:240)10% |
4.13 | 54.7 | (0.350,0.611) | 119.9 |
| 실시예 83 | 화합물75:PH-3:GD-1 (200:200)7% |
4.43 | 50.35 | (0.346,0.613) | 95.2 |
| 실시예 84 | 화합물76:PH-3:GD-1 (160:240)10% |
4.14 | 52.8 | (0.346,0.612) | 105.7 |
| 실시예 85 | 화합물77:PH-1:GD-1 (200:200)5% |
4.35 | 56.4 | (0.347,0.611) | 62.9 |
| 실시예 86 | 화합물78:PH-1:GD-1 (200:200)5% |
3.92 | 54 | (0.352,0.609) | 81.2 |
| 실시예 87 | 화합물79:PH-3:GD-1 (160:240)5% |
4.16 | 56.13 | (0.351,0.613) | 104.3 |
| 실시예 88 | 화합물80:PH-1:GD-1 (160:240)5% |
4.32 | 50.89 | (0.346,0.611) | 100.4 |
| 실시예 89 | 화합물59:PH-1:GD-1 (160:240)6% |
4.29 | 53.7 | (0.347,0.614) | 92.6 |
| 실시예 90 | 화합물45:PH-1:GD-1 (160:240)7% |
4.31 | 57.3 | (0.350,0.611) | 168.1 |
| No. | 호스트: 도펀트 (두께, Å)도펀트함량 |
전압(V) (@10mA/cm2) |
효율(Cd/A) (@10mA/cm2) |
색좌표 (x,y) |
수명(T95, h) (@20mA/cm2) |
| 비교예 11 | 화합물A:GD-1 (400)5% |
4.18 | 51.2 | (0.351,0.609) | 18.3 |
| 비교예 12 | 화합물B:GD-1 (400)5% |
4.16 | 46.1 | (0.352,0.611) | 23.1 |
| 비교예 13 | 화합물C:GD-1 (400)5% |
4.10 | 61.8 | (0.351,0.610) | 16.3 |
| 비교예 14 | 화합물D:GD-1 (400)5% |
4.21 | 62.4 | (0.351,0.609) | 19.8 |
| 비교예 15 | 화합물E:GD-1 (400)5% |
5.80 | 37.1 | (0.350,0.611) | 14.7 |
| 비교예 16 | 화합물F:GD-1 (400)5% |
4.08 | 44.0 | (0.352,0.609) | 22.8 |
| 비교예 17 | 화합물G:GD-1 (400)5% |
4.09 | 43.2 | (0.352,0.609) | 22.0 |
| 비교예 18 | 화합물H:GD-1 (400)5% |
4.19 | 51.0 | (0.352,0.610) | 27.1 |
| 비교예 19 | 화합물I:GD-1 (400)5% |
4.1 | 47 | (0.349,0.611) | 32.2 |
3: 발광층 4: 음극
5: 정공 주입층 6: 정공 수송층
7: 발광층 8: 전자 수송층
Claims (13)
- 하기 화학식 1로 표시되는 화합물:
[화학식 1]
상기 화학식 1에서,
X1은 O 또는 S이고,
L1 및 L2는 각각 독립적으로, 단일 결합; 치환 또는 비치환된 C6-60 아릴렌; 또는 치환 또는 비치환된 O, N, Si 및 S로 구성되는 군으로부터 선택되는 헤테로원자를 1개 이상 포함하는 C1-60 헤테로아릴렌이고,
Y1 내지 Y3는 각각 독립적으로, N 또는 CR3이되, Y1 내지 Y3 중 적어도 하나는 N이고,
Ar1a 및 Ar1b는 각각 독립적으로, 치환 또는 비치환된 C6-60 아릴; 또는 치환 또는 비치환된 N, O 및 S로 구성되는 군으로부터 선택되는 헤테로원자를 1개 내지 3개 포함하는 C1-60 헤테로아릴이고,
R1 내지 R3는 각각 독립적으로, 수소; 중수소; 할로겐; 시아노; 니트로; 아미노; 치환 또는 비치환된 C1-60 알킬; 치환 또는 비치환된 C1-60 할로알킬; 치환 또는 비치환된 C1-60 알콕시; 치환 또는 비치환된 C1-60 할로알콕시; 치환 또는 비치환된 C3-60 사이클로알킬; 치환 또는 비치환된 C2-60 알케닐; 치환 또는 비치환된 C6-60 아릴; 치환 또는 비치환된 C6-60 아릴옥시; 또는 치환 또는 비치환된 N, O 및 S로 구성되는 군으로부터 선택되는 헤테로원자를 1개 이상 포함하는 C1-60 헤테로아릴이고,
n1 및 n2는 각각 독립적으로, 0 내지 3의 정수이고,
Ar2는 하기로 구성되는 군으로부터 선택되는 어느 하나이다:
상기에서,
Z11 내지 Z14는 각각 독립적으로, 수소; 중수소; 할로겐; 시아노; 니트로; 아미노; 치환 또는 비치환된 C1-60 알킬; 치환 또는 비치환된 C1-60 할로알킬; Si(Q1)(Q2)(Q3); C(Q4)(Q5)(Q6) 및 C6-60 아릴이고,
여기서, Q1 내지 Q6은 각각 독립적으로, 수소; 중수소; 할로겐; 시아노; 니트로; 아미노; 치환 또는 비치환된 C1-20 알킬; 또는 치환 또는 비치환된 C6-20 아릴이고,
c11은 0 내지 5의 정수이고,
c12는 0 내지 7의 정수이고,
c13는 0 내지 9의 정수이고,
c14는 0 내지 4의 정수이고,
c15는 0 내지 3의 정수이고,
c16은 0 내지 11의 정수이고,
c17은 0 내지 9의 정수이고,
c18은 0 내지 6의 정수이고,
c19는 0 내지 13의 정수이다.
- 제1항에 있어서,
L1 및 L2는 각각 독립적으로, 단일 결합; 치환 또는 비치환된 페닐렌; 치환 또는 비치환된 나프틸렌; 또는 치환 또는 비치환된 바이페닐릴렌인, 화합물.
- 제1항에 있어서,
Y1은 N이고, Y2는 N이고, Y3는 N이거나;
Y1은 N이고, Y2는 N이고, Y3는 CH이거나;
Y1은 N이고, Y2는 CH이고, Y3는 N이거나;
Y1은 N이고, Y2는 CH이고, Y3는 CH이거나; 또는
Y1은 CH이고, Y2는 CH이고, Y3는 N인, 화합물.
- 제1항에 있어서,
Ar1a 및 Ar1b는 각각 독립적으로, 하기로 구성되는 군으로부터 선택되는 어느 하나인, 화합물:
상기에서,
X2는 O, S, NZ4, 또는 CZ5Z6이고,
Z1 내지 Z6은 각각 독립적으로, 수소; 중수소; 할로겐; 시아노; 니트로; 아미노; 치환 또는 비치환된 C1-20 알킬; 치환 또는 비치환된 C1-20 할로알킬; 치환 또는 비치환된 C6-20 아릴; 또는 치환 또는 비치환된 N, O 및 S로 구성되는 군으로부터 선택되는 헤테로원자를 1개 이상 포함하는 C1-20 헤테로아릴이고,
c1은 0 내지 5의 정수이고,
c2는 0 내지 4의 정수이고,
c3는 0 내지 3의 정수이다.
- 삭제
- 제1항에 있어서,
R1 및 R2는 각각 독립적으로, 수소; 중수소; 시아노; 또는 치환 또는 비치환된 C1-10 알킬인, 화합물.
- 제1 전극; 상기 제1 전극과 대향하여 구비된 제2 전극; 및 상기 제1 전극과 상기 제2 전극 사이에 구비된 1층 이상의 유기물 층을 포함하는 유기 발광 소자로서, 상기 유기물 층 중 1층 이상은 제1항 내지 제6항 및 제8항 내지 제10항 중 어느 하나의 항에 따른 화합물을 포함하는 것인, 유기 발광 소자.
- 제11항에 있어서,
상기 화합물을 포함하는 유기물층은 발광층인, 유기 발광 소자.
- 제12항에 있어서,
상기 화합물은 호스트 물질로 사용되는, 유기 발광 소자.
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201780004123.4A CN108368078B (zh) | 2016-07-20 | 2017-06-15 | 杂环化合物和包含其的有机发光器件 |
| EP17831215.3A EP3480194B1 (en) | 2016-07-20 | 2017-06-15 | Heterocyclic compounds and organic light-emitting devices using same |
| US15/771,066 US11903311B2 (en) | 2016-07-20 | 2017-06-15 | Heterocyclic compound and organic light emitting device comprising the same |
| PCT/KR2017/006274 WO2018016742A1 (ko) | 2016-07-20 | 2017-06-15 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| JP2019502221A JP7210856B2 (ja) | 2016-07-20 | 2017-06-15 | 新規なヘテロ環式化合物およびこれを利用した有機発光素子 |
| TW106121583A TWI653233B (zh) | 2016-07-20 | 2017-06-28 | 新式雜環化合物以及包含此化合物的有機發光裝置 |
| JP2020210801A JP7205037B2 (ja) | 2016-07-20 | 2020-12-18 | 新規なヘテロ環式化合物およびこれを利用した有機発光素子 |
| US17/842,520 US12167689B2 (en) | 2016-07-20 | 2022-06-16 | Heterocyclic compound and organic light emitting device comprising the same |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20160092202 | 2016-07-20 | ||
| KR1020160092202 | 2016-07-20 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180010130A KR20180010130A (ko) | 2018-01-30 |
| KR101849747B1 true KR101849747B1 (ko) | 2018-05-31 |
Family
ID=61070679
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020170075029A Active KR101849747B1 (ko) | 2016-07-20 | 2017-06-14 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US11903311B2 (ko) |
| EP (1) | EP3480194B1 (ko) |
| JP (2) | JP7210856B2 (ko) |
| KR (1) | KR101849747B1 (ko) |
| CN (1) | CN108368078B (ko) |
| TW (1) | TWI653233B (ko) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11453659B2 (en) | 2019-06-28 | 2022-09-27 | Samsung Sdi Co., Ltd. | Compound for organic optoelectronic device, composition for organic optoelectronic device, organic optoelectronic device and display device |
| US12522591B2 (en) | 2019-08-26 | 2026-01-13 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
Families Citing this family (60)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101849747B1 (ko) * | 2016-07-20 | 2018-05-31 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| TWI789025B (zh) * | 2016-08-19 | 2023-01-01 | 日商九州有機光材股份有限公司 | 電荷輸送材料、化合物、延遲螢光材料及有機發光元件 |
| KR102003351B1 (ko) * | 2017-01-20 | 2019-07-23 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR102232510B1 (ko) * | 2017-05-26 | 2021-03-26 | 삼성에스디아이 주식회사 | 인광 호스트용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102107085B1 (ko) * | 2017-07-14 | 2020-05-06 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102418440B1 (ko) | 2017-09-29 | 2022-07-07 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2019066242A1 (ko) * | 2017-09-29 | 2019-04-04 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN108424420B (zh) * | 2017-09-30 | 2021-01-12 | 北京绿人科技有限责任公司 | 含有硅原子的三嗪化合物及其应用和一种有机电致发光器件 |
| KR102134383B1 (ko) * | 2017-12-12 | 2020-07-15 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102154083B1 (ko) * | 2017-12-29 | 2020-09-09 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| JP7551273B2 (ja) * | 2018-01-11 | 2024-09-17 | 三星電子株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子用組成物、及び有機エレクトロルミネッセンス素子 |
| US11706977B2 (en) * | 2018-01-11 | 2023-07-18 | Samsung Electronics Co., Ltd. | Heterocyclic compound, composition including the same, and organic light-emitting device including the heterocyclic compound |
| KR102125962B1 (ko) * | 2018-01-17 | 2020-06-23 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| KR101857632B1 (ko) * | 2018-02-02 | 2018-05-14 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN111712938B (zh) | 2018-02-20 | 2025-01-14 | 出光兴产株式会社 | 有机电致发光元件和电子设备 |
| WO2019163826A1 (ja) * | 2018-02-20 | 2019-08-29 | 出光興産株式会社 | 新規化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR102123015B1 (ko) * | 2018-03-06 | 2020-06-15 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| US12063855B2 (en) | 2018-03-29 | 2024-08-13 | Duk San Neolux Co., Ltd. | Compound for organic electric element, organic electric element using the same, and electronic device therefor |
| KR102720177B1 (ko) * | 2018-03-29 | 2024-10-21 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2019190101A1 (ko) * | 2018-03-29 | 2019-10-03 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102206482B1 (ko) * | 2018-04-24 | 2021-01-22 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| WO2019209031A1 (ko) * | 2018-04-24 | 2019-10-31 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR102202771B1 (ko) | 2018-04-25 | 2021-01-14 | 주식회사 엘지화학 | 화합물 및 이를 포함한 유기 발광 소자 |
| KR20190127272A (ko) * | 2018-05-04 | 2019-11-13 | 덕산네오룩스 주식회사 | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2019231210A1 (ko) * | 2018-05-29 | 2019-12-05 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019235845A1 (ko) * | 2018-06-05 | 2019-12-12 | 주식회사 엘지화학 | 화합물 및 이를 포함한 유기 발광 소자 |
| KR102217250B1 (ko) * | 2018-06-12 | 2021-02-18 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102288989B1 (ko) | 2018-08-22 | 2021-08-11 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| KR102701149B1 (ko) | 2018-09-07 | 2024-09-03 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 축합 다환 화합물 |
| KR102611314B1 (ko) * | 2018-09-11 | 2023-12-07 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR102495276B1 (ko) * | 2018-11-07 | 2023-02-01 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR102638577B1 (ko) | 2018-11-15 | 2024-02-20 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN111909213B (zh) * | 2019-05-09 | 2024-02-27 | 北京夏禾科技有限公司 | 一种含有三个不同配体的金属配合物 |
| CN110156777A (zh) * | 2019-05-21 | 2019-08-23 | 吉林工程技术师范学院 | 一种三嗪衍生物及其有机电致发光器件 |
| CN110256412B (zh) * | 2019-06-27 | 2022-04-05 | 武汉天马微电子有限公司 | 一种化合物、有机电致发光器件及显示装置 |
| US12435073B2 (en) | 2019-08-19 | 2025-10-07 | Idemitsu Kosan Co., Ltd. | Compound, material for organic electroluminescent element, organic electroluminescent element, and electronic device |
| CN112679548B (zh) | 2019-10-18 | 2023-07-28 | 北京夏禾科技有限公司 | 具有部分氟取代的取代基的辅助配体的有机发光材料 |
| TW202130783A (zh) | 2019-11-04 | 2021-08-16 | 德商麥克專利有限公司 | 有機電致發光裝置 |
| TW202136471A (zh) * | 2019-12-17 | 2021-10-01 | 德商麥克專利有限公司 | 有機電致發光裝置用的材料 |
| CN118084980A (zh) | 2020-01-10 | 2024-05-28 | 北京夏禾科技有限公司 | 有机发光材料 |
| CN113121609B (zh) | 2020-01-16 | 2024-03-29 | 北京夏禾科技有限公司 | 一种金属配合物、包含其的电致发光器件及其用途 |
| CN113939508B (zh) * | 2020-03-09 | 2024-10-29 | 株式会社Lg化学 | 新型化合物及包含其的有机发光器件 |
| KR20220151192A (ko) | 2020-03-11 | 2022-11-14 | 메르크 파텐트 게엠베하 | 유기 전계 발광 장치 |
| JP7293565B2 (ja) * | 2020-03-11 | 2023-06-20 | エルジー・ケム・リミテッド | 有機発光素子 |
| KR102787035B1 (ko) * | 2020-09-09 | 2025-03-25 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| US20230232717A1 (en) * | 2020-09-28 | 2023-07-20 | Lt Materials Co., Ltd. | Organic light-emitting device, composition for organic layer of organic lightemitting device, and method for manufacturing organic light-emitting device |
| CN114621198B (zh) * | 2020-12-11 | 2025-01-21 | 北京夏禾科技有限公司 | 有机电致发光材料及其器件 |
| CN114835686B (zh) * | 2021-02-02 | 2024-10-11 | 江苏三月科技股份有限公司 | 一种含有菲与三嗪结构的化合物及其应用 |
| US20240107884A1 (en) * | 2021-02-19 | 2024-03-28 | Lg Chem, Ltd. | Organic light emitting device |
| CN115148914B (zh) * | 2021-03-30 | 2025-02-25 | 北京夏禾科技有限公司 | 一种电致发光器件 |
| WO2022216019A1 (ko) * | 2021-04-05 | 2022-10-13 | 주식회사 엘지화학 | 유기 발광 소자 |
| US20240138256A1 (en) * | 2021-04-05 | 2024-04-25 | Lg Chem, Ltd. | Organic light emitting device |
| CN116491244A (zh) * | 2021-04-27 | 2023-07-25 | 株式会社Lg化学 | 有机发光器件 |
| CN113549059B (zh) * | 2021-06-18 | 2023-04-28 | 陕西莱特光电材料股份有限公司 | 有机化合物及包含其的电子器件和电子装置 |
| KR20230013465A (ko) * | 2021-07-19 | 2023-01-26 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| KR102746268B1 (ko) * | 2021-12-03 | 2024-12-26 | 엘티소재주식회사 | 헤테로고리 화합물, 이를 포함하는 유기 발광 소자, 및 유기물층용 조성물 |
| CN114213373B (zh) * | 2021-12-17 | 2023-06-16 | 江苏广域化学有限公司 | 二苯并呋喃类衍生物的合成方法 |
| US20240365660A1 (en) * | 2021-12-22 | 2024-10-31 | Lg Chem, Ltd. | Novel compound and organic light emitting device comprising the same |
| CN116751177B (zh) * | 2022-03-03 | 2025-12-16 | 阜阳欣奕华新材料科技股份有限公司 | 一种蒽类化合物、中间体、蒽类混合物、有机电致发光器件和显示装置 |
| WO2025143781A1 (ko) * | 2023-12-27 | 2025-07-03 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Family Cites Families (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5831654B2 (ja) * | 1977-11-26 | 1983-07-07 | 富士通株式会社 | 磁気デイスク塗膜組成物 |
| JPS5831654U (ja) | 1981-08-26 | 1983-03-01 | 三菱電機株式会社 | 操作コイルリ−ド |
| JPS607467U (ja) | 1983-06-27 | 1985-01-19 | 松下電工株式会社 | 水栓の弁構造 |
| KR100430549B1 (ko) | 1999-01-27 | 2004-05-10 | 주식회사 엘지화학 | 신규한 착물 및 그의 제조 방법과 이를 이용한 유기 발광 소자 및 그의 제조 방법 |
| DE10135513B4 (de) | 2001-07-20 | 2005-02-24 | Novaled Gmbh | Lichtemittierendes Bauelement mit organischen Schichten |
| US20060088728A1 (en) * | 2004-10-22 | 2006-04-27 | Raymond Kwong | Arylcarbazoles as hosts in PHOLEDs |
| EP2185532B1 (en) | 2007-08-08 | 2016-11-09 | Universal Display Corporation | Benzo-fused thiophene compounds comprising a triphenylene group |
| KR101431644B1 (ko) | 2009-08-10 | 2014-08-21 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| JP6007467B2 (ja) | 2010-07-27 | 2016-10-12 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、 |
| KR101600453B1 (ko) | 2013-09-13 | 2016-03-08 | 주식회사 엠비케이 | 신규한 유기발광화합물 및 이를 포함하는 유기전기발광소자 |
| KR102140018B1 (ko) * | 2013-12-17 | 2020-07-31 | 삼성전자주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| KR20150074603A (ko) * | 2013-12-24 | 2015-07-02 | 희성소재 (주) | 플루오렌계 화합물 및 이를 이용한 유기발광소자 |
| KR101788094B1 (ko) | 2014-01-09 | 2017-10-19 | 제일모직 주식회사 | 유기 화합물, 유기 광전자 소자 및 표시 장치 |
| KR102280686B1 (ko) | 2014-02-11 | 2021-07-22 | 삼성전자주식회사 | 카바졸계 화합물 및 이를 포함한 유기 발광 소자 |
| US9190620B2 (en) | 2014-03-01 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3140302B1 (de) | 2014-05-05 | 2019-08-21 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| KR101764969B1 (ko) | 2014-05-26 | 2017-08-04 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US9997716B2 (en) | 2014-05-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR101579289B1 (ko) | 2014-06-30 | 2015-12-22 | 희성소재 (주) | 헤테로고리 화합물 및 이를 이용한 유기발광소자 |
| US10297762B2 (en) | 2014-07-09 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN106661006B (zh) | 2014-07-29 | 2019-11-08 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| EP3180411B1 (de) | 2014-08-13 | 2018-08-29 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| EP2991128B1 (en) | 2014-08-29 | 2017-04-12 | Samsung Electronics Co., Ltd. | Organic light-emitting device |
| US10749113B2 (en) * | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN112480089A (zh) | 2014-12-29 | 2021-03-12 | 东进世美肯株式会社 | 新颖化合物及包含其的有机发光器件 |
| WO2016108596A2 (ko) | 2014-12-29 | 2016-07-07 | 주식회사 동진쎄미켐 | 신규한 화합물 및 이를 포함하는 유기발광소자 |
| US9406892B2 (en) | 2015-01-07 | 2016-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP5831654B1 (ja) * | 2015-02-13 | 2015-12-09 | コニカミノルタ株式会社 | 芳香族複素環誘導体、それを用いた有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| US11522140B2 (en) | 2015-08-17 | 2022-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN108350352B (zh) | 2015-11-02 | 2021-03-30 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| JP6754185B2 (ja) | 2015-12-10 | 2020-09-09 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、表示装置、照明装置及び電子デバイス用有機機能性材料 |
| CN108884087A (zh) | 2016-04-11 | 2018-11-23 | 默克专利有限公司 | 包含二苯并呋喃和/或二苯并噻吩结构的杂环化合物 |
| KR101849747B1 (ko) | 2016-07-20 | 2018-05-31 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR20180038834A (ko) * | 2016-10-07 | 2018-04-17 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| KR101885898B1 (ko) * | 2016-11-16 | 2018-08-06 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102022689B1 (ko) * | 2017-03-30 | 2019-09-18 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102107085B1 (ko) * | 2017-07-14 | 2020-05-06 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102134383B1 (ko) * | 2017-12-12 | 2020-07-15 | 주식회사 엘지화학 | 유기 발광 소자 |
-
2017
- 2017-06-14 KR KR1020170075029A patent/KR101849747B1/ko active Active
- 2017-06-15 CN CN201780004123.4A patent/CN108368078B/zh active Active
- 2017-06-15 JP JP2019502221A patent/JP7210856B2/ja active Active
- 2017-06-15 US US15/771,066 patent/US11903311B2/en active Active
- 2017-06-15 EP EP17831215.3A patent/EP3480194B1/en active Active
- 2017-06-28 TW TW106121583A patent/TWI653233B/zh active
-
2020
- 2020-12-18 JP JP2020210801A patent/JP7205037B2/ja active Active
-
2022
- 2022-06-16 US US17/842,520 patent/US12167689B2/en active Active
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11453659B2 (en) | 2019-06-28 | 2022-09-27 | Samsung Sdi Co., Ltd. | Compound for organic optoelectronic device, composition for organic optoelectronic device, organic optoelectronic device and display device |
| US12522591B2 (en) | 2019-08-26 | 2026-01-13 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
Also Published As
| Publication number | Publication date |
|---|---|
| CN108368078A (zh) | 2018-08-03 |
| EP3480194A1 (en) | 2019-05-08 |
| JP7210856B2 (ja) | 2023-01-24 |
| CN108368078B (zh) | 2019-05-21 |
| TWI653233B (zh) | 2019-03-11 |
| US12167689B2 (en) | 2024-12-10 |
| US20220336757A1 (en) | 2022-10-20 |
| EP3480194B1 (en) | 2021-09-08 |
| TW201811773A (zh) | 2018-04-01 |
| JP7205037B2 (ja) | 2023-01-17 |
| KR20180010130A (ko) | 2018-01-30 |
| US20180337348A1 (en) | 2018-11-22 |
| JP2019524741A (ja) | 2019-09-05 |
| JP2021073177A (ja) | 2021-05-13 |
| US11903311B2 (en) | 2024-02-13 |
| EP3480194A4 (en) | 2019-05-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101849747B1 (ko) | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 | |
| KR102447008B1 (ko) | 유기 발광 소자 | |
| KR102446400B1 (ko) | 유기 발광 소자 | |
| JP7187752B2 (ja) | 新規な化合物およびこれを利用した有機発光素子 | |
| KR20200085232A (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| WO2018016742A1 (ko) | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 | |
| KR101929448B1 (ko) | 신규한 화합물 및 이를 포함하는 유기발광 소자 | |
| KR102123015B1 (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| KR20190079571A (ko) | 유기 발광 소자 | |
| KR102235480B1 (ko) | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 | |
| KR102278532B1 (ko) | 신규한 화합물 및 이를 이용한 유기발광 소자 | |
| JP7680140B2 (ja) | 新規な化合物およびこれを利用した有機発光素子 | |
| KR102278531B1 (ko) | 신규한 화합물 및 이를 이용한 유기발광 소자 | |
| KR101983340B1 (ko) | 헤테로고리 화합물 및 이를 이용하는 유기발광소자 | |
| KR102521059B1 (ko) | 신규한 화합물 및 이를 이용한 유기발광 소자 | |
| KR101964437B1 (ko) | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 | |
| KR20180131412A (ko) | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20170614 |
|
| PA0201 | Request for examination | ||
| A302 | Request for accelerated examination | ||
| PA0302 | Request for accelerated examination |
Patent event date: 20171026 Patent event code: PA03022R01D Comment text: Request for Accelerated Examination Patent event date: 20170614 Patent event code: PA03021R01I Comment text: Patent Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20171116 Patent event code: PE09021S01D |
|
| PG1501 | Laying open of application | ||
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20180330 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20180411 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20180411 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| PR1001 | Payment of annual fee |
Payment date: 20210322 Start annual number: 4 End annual number: 4 |
|
| PR1001 | Payment of annual fee |
Payment date: 20240320 Start annual number: 7 End annual number: 7 |