본 개시내용은 고도의 미소위성체 불안정성 (MSI-H)을 나타내는 결장직장암으로부터 유래된 종양을 앓는 대상체에게 프로그램화된 사멸-1 수용체 (PD-1)에 특이적으로 결합하고 PD-1 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-PD-1 항체")의 치료 유효량을 투여하는 것 포함하는, 상기 대상체를 치료하는 방법에 관한 것이다. 일부 실시양태에서, 방법은 세포독성 T-림프구 항원-4 (CTLA-4)에 특이적으로 결합하고 CTLA-4 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-CTLA-4 항체")의 치료 유효량을 투여하는 것을 추가로 포함한다.
일부 실시양태에서, 결장직장암은 직장암, 결장암 또는 그의 임의의 조합이다. 한 실시양태에서, 투여는 결장직장암을 치료한다.
일부 실시양태에서, 항-PD-1 항체는 인간 PD-1에의 결합에 대해 니볼루맙과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 니볼루맙과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분이다. 일부 실시양태에서, 항-PD-1 항체는 인간 IgG1 또는 IgG4 이소형의 중쇄 불변 영역을 포함한다. 한 실시양태에서, 항-PD-1 항체는 니볼루맙이다. 또 다른 실시양태에서, 항-PD-1 항체는 펨브롤리주맙이다.
특정 실시양태에서, 항-PD-1 항체는 약 1, 2 또는 3주마다 1회 적어도 약 0.1 mg/kg 내지 적어도 약 10.0 mg/kg 체중 범위의 용량으로 투여된다. 한 실시양태에서, 항-PD-1 항체 (예를 들어, 니볼루맙)는 약 3주마다 1회 적어도 약 1 mg/kg 체중의 용량으로 투여된다. 또 다른 실시양태에서, 항-PD-1 항체 (예를 들어, 니볼루맙)는 약 3주마다 1회 적어도 약 3 mg/kg 체중의 용량으로 투여된다. 또 다른 실시양태에서, 항-PD-1 항체 (예를 들어, 니볼루맙)는 약 2주마다 1회 적어도 약 3 mg/kg 체중의 용량으로 투여된다. 다른 실시양태에서, 항-PD-1 항체 (예를 들어, 펨브롤리주맙)는 3주마다 적어도 약 200 mg 또는 3주마다 2 mg/kg (최대 200 mg)의 용량으로 투여된다. 일부 실시양태에서, 항-PD-1 항체 (예를 들어, 아벨루맙)는 2주마다 10 mg/kg의 용량으로 투여된다. 특정 실시양태에서, 항-PD-1 항체는 균일 용량으로 투여된다. 실시양태에서, 항-PD-1 항체는 적어도 약 200 mg, 적어도 약 220 mg, 적어도 약 240 mg, 적어도 약 260 mg, 적어도 약 280 mg, 적어도 약 300 mg, 적어도 약 320 mg, 적어도 약 340 mg, 적어도 약 360 mg, 적어도 약 380 mg, 적어도 약 400 mg, 적어도 약 420 mg, 적어도 약 440 mg, 적어도 약 460 mg, 적어도 약 480 mg, 적어도 약 500 mg, 적어도 약 550 mg, 적어도 약 600 mg, 적어도 약 650 mg, 적어도 700 mg, 적어도 750 mg, 또는 적어도 800 mg의 균일 용량으로 투여된다. 일부 실시양태에서, 항-PD-1 항체는 임상 이익이 관찰되는 한 또는 다루기 힘든 독성 또는 질환 진행이 발생할 때까지 투여된다.
일부 실시양태에서, 항-CTLA-4 항체는 인간 CTLA-4에의 결합에 대해 이필리무맙과 교차-경쟁한다. 한 실시양태에서, 항-CTLA-4 항체는 이필리무맙과 동일한 에피토프에 결합한다. 일부 실시양태에서, 항-CTLA-4 항체는 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분이다. 특정 실시양태에서, 항-CTLA-4 항체는 인간 IgG1 또는 IgG2 이소형의 중쇄 불변 영역을 포함한다. 한 실시양태에서, 항-CTLA-4 항체는 이필리무맙이다. 또 다른 실시양태에서, 항-CTLA-4 항체는 트레멜리무맙이다.
일부 실시양태에서, 항-CTLA-4 항체는 약 1, 2 또는 3주마다 1회 적어도 약 0.01 mg/kg 내지 적어도 약 10 mg/kg 체중 범위의 용량으로 투여된다. 한 실시양태에서, 항-CTLA-4 항체는 약 3주마다 1회 적어도 약 1 mg/kg 체중의 용량으로 투여된다. 또 다른 실시양태에서, 항-CTLA-4 항체는 약 3주마다 1회 적어도 약 3 mg/kg 체중의 용량으로 투여된다. 일부 실시양태에서, 항-CTLA-4 항체는 임상 이익이 관찰되는 한 또는 다루기 힘든 독성 또는 질환 진행이 발생할 때까지 투여된다.
일부 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 정맥내 투여를 위해 제제화된다. 특정 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 순차적으로 투여된다. 한 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 서로 30분 이내에 투여된다. 한 실시양태에서, 항-PD-1 항체는 항-CTLA-4 항체 전에 투여된다. 또 다른 실시양태에서, 항-CTLA-4 항체는 항-PD-1 항체 전에 투여된다. 특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 개별 조성물로 공동으로 투여된다. 다른 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 공동 투여를 위해 단일 조성물로서 혼합된다.
한 실시양태에서, 항-PD-1 항체는 치료량 미만의 용량으로 투여된다. 또 다른 실시양태에서, 항-CTLA-4 항체는 치료량 미만의 용량으로 투여된다. 추가 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 각각 치료량 미만의 용량으로 투여된다.
특정 실시양태에서, 대상체는 PD-L1, PD-L2 또는 둘 다를 발현하는 종양을 갖는다. 실시양태에서, 대상체는 초기 투여 후 적어도 약 1개월, 적어도 약 2개월, 적어도 약 3개월, 적어도 약 4개월, 적어도 약 5개월, 적어도 약 6개월, 적어도 약 7개월, 적어도 약 8개월, 적어도 약 9개월, 적어도 약 10개월, 적어도 약 11개월, 적어도 약 1년, 적어도 약 18개월, 적어도 약 2년, 적어도 약 3년, 적어도 약 4년, 또는 적어도 약 5년의 무진행 생존을 나타낸다.
본 개시내용은 (a) 약 0.1 mg/kg 내지 약 10 mg/kg 범위의 투여량의 항-PD-1 항체; (b) 약 0.1 mg/kg 내지 약 10 mg/kg 범위의 투여량의 항-CTLA-4 항체; 및 (c) 본원에 개시된 임의의 방법에서 항-PD-1 항체 및 항-CTLA-4 항체를 사용하는 것에 대한 지침서를 포함하는, 암을 앓는 대상체를 치료하기 위한 키트에 관한 것이다.
일부 실시양태에서, 대상체는 미소위성체 안정한 (MSS) 종양 또는 미소위성체 불안정성-높은 (MSI-H) 종양을 갖는다. 특정 실시양태는 항-PD-1 항체 및/또는 항-CTLA-4 항체의 투여 전에 종양의 미소위성체 상태를 측정하는 것을 추가로 포함한다. 실시양태에서, 종양은 MSS 종양 또는 MSI-H 종양이다. 한 실시양태에서, 대상체는 결장직장암을 앓는다. 또 다른 실시양태에서, 대상체는 결장암을 앓는다. 또 다른 실시양태에서, 대상체는 직장암을 앓는다.
실시양태
E1. 결장직장암으로부터 유래된 종양을 앓는 대상체에게 프로그램화된 사멸-1 수용체 (PD-1)에 특이적으로 결합하고 PD-1 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-PD-1 항체")의 치료 유효량을 투여하는 것 포함하며, 여기서 종양은 고도의 미소위성체 불안정성 ("MSI-H")을 나타내는 것인, 상기 대상체를 치료하는 방법.
E2. 실시양태 E1에 있어서, 종양이 결장암인 방법.
E3. 실시양태 E1에 있어서, 종양이 직장암인 방법.
E4. 실시양태 E1 내지 E3 중 어느 하나에 있어서, 종양이 (a) 종양은 적어도 2종, 적어도 3종, 적어도 4종 또는 적어도 5종의 DNA 미스매치 복구 유전자 ("MMR 유전자")에서 배선 변경을 포함함; (b) 종양은 5종 이상의 MMR 유전자의 적어도 30%에서 배선 변경을 포함함; (c) DNA MMR 유전자에 의해 코딩되는 적어도 1종의 단백질이 종양에서 검출되지 않음; 및 (d) 그의 임의의 조합으로 이루어진 군으로부터 선택된 1개 이상의 특징을 나타내는 것인 방법.
E5. 실시양태 E4에 있어서, DNA MMR 유전자가 MSH2, MLH1, MSH6, PMS2, PMS1 또는 그의 임의의 조합을 포함하는 것인 방법.
E6. 실시양태 E4에 있어서, (a) 또는 (b)에서의 배선 변경이 폴리머라제 연쇄 반응에 의해 측정되는 것인 방법.
E7. 실시양태 E4에 있어서, DNA MMR 유전자에 의해 코딩되는 적어도 1종의 단백질이 면역조직화학에 의해 검출되는 것인 방법.
E8. 실시양태 E1 내지 E7 중 어느 하나에 있어서, 대상체가 치료의 투여 후 적어도 약 1개월, 적어도 약 2개월, 적어도 약 3개월, 적어도 약 4개월, 적어도 약 5개월, 적어도 약 6개월, 적어도 약 7개월, 적어도 약 8개월, 적어도 약 9개월, 적어도 약 10개월, 적어도 약 11개월, 또는 적어도 약 12개월의 무진행 생존을 나타내는 것인 방법.
E9. 실시양태 E1 내지 E8 중 어느 하나에 있어서, 대상체가 치료의 투여 후 적어도 약 1개월, 적어도 약 2개월, 적어도 약 3개월, 적어도 약 4개월, 적어도 약 5개월, 적어도 약 6개월, 적어도 약 7개월, 적어도 약 8개월, 적어도 약 9개월, 적어도 약 10개월, 적어도 약 11개월, 또는 적어도 약 12개월의 전체 생존을 나타내는 것인 방법.
E10. 실시양태 E1 내지 E9 중 어느 하나에 있어서, 투여가 암을 치료하는 것인 방법.
E11. 실시양태 E1 내지 E10 중 어느 하나에 있어서, 항-PD-1 항체가 인간 PD-1에의 결합에 대해 니볼루맙과 교차-경쟁하는 것인 방법.
E12. 실시양태 E1 내지 E11 중 어느 하나에 있어서, 항-PD-1 항체가 니볼루맙과 동일한 에피토프에 결합하는 것인 방법.
E13. 실시양태 E1 내지 E12 중 어느 하나에 있어서, 항-PD-1 항체가 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분인 방법.
E14. 실시양태 E1 내지 E13 중 어느 하나에 있어서, 항-PD-1 항체가 인간 IgG1 또는 IgG4 이소형의 중쇄 불변 영역을 포함하는 것인 방법.
E15. 실시양태 E1 내지 E14 중 어느 하나에 있어서, 항-PD-1 항체가 니볼루맙인 방법.
E16. 실시양태 E1 내지 E14 중 어느 하나에 있어서, 항-PD-1 항체가 펨브롤리주맙인 방법.
E17. 실시양태 E1 내지 E16 중 어느 하나에 있어서, 항-PD-1 항체가 약 1, 2 또는 3주마다 1회 적어도 약 0.1 mg/kg 내지 적어도 약 10.0 mg/kg 체중 범위의 용량으로 투여되는 것인 방법.
E18. 실시양태 E17에 있어서, 항-PD-1 항체가 약 3주마다 1회 약 3 mg/kg 체중의 용량으로 투여되는 것인 방법.
E19. 실시양태 E1 내지 E18 중 어느 하나에 있어서, CTLA-4에 특이적으로 결합하고 CTLA-4 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-CTLA-4 항체")의 치료 유효량을 투여하는 것을 추가로 포함하는 방법.
E20. 실시양태 E19에 있어서, 항-CTLA-4 항체가 인간 CTLA-4에의 결합에 대해 이필리무맙과 교차-경쟁하는 것인 방법.
E21. 실시양태 E19 또는 E20에 있어서, 항-CTLA-4 항체가 이필리무맙과 동일한 에피토프에 결합하는 것인 방법.
E22. 실시양태 E19 내지 E21 중 어느 하나에 있어서, 항-CTLA-4 항체가 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분인 방법.
E23. 실시양태 E19 내지 E22 중 어느 하나에 있어서, 항-CTLA-4 항체가 인간 IgG1 또는 IgG2 이소형의 중쇄 불변 영역을 포함하는 것인 방법.
E24. 실시양태 E19 내지 E23 중 어느 하나에 있어서, 항-CTLA-4 항체가 이필리무맙인 방법.
E25. 실시양태 E19 내지 E23 중 어느 하나에 있어서, 항-CTLA-4 항체가 트레멜리무맙인 방법.
E26. 실시양태 E19 내지 E25 중 어느 하나에 있어서, 항-CTLA-4 항체가 약 1, 2 또는 3주마다 1회 적어도 약 0.1 mg/kg 내지 적어도 약 10.0 mg/kg 체중 범위의 용량으로 투여되는 것인 방법.
E27. 실시양태 E26에 있어서, 항-CTLA-4 항체가 약 3주마다 1회 약 1 mg/kg 체중의 용량으로 투여되는 것인 방법.
E28. 실시양태 E19 내지 E25 중 어느 하나에 있어서, 항-PD-1 항체가 약 1 mg/kg 체중의 용량으로 투여되고, 항-CTLA-4 항체가 약 1 mg/kg 체중의 용량으로 투여되는 것인 방법.
E29. 실시양태 E19 내지 E25 중 어느 하나에 있어서, 항-PD-1 항체가 약 1 mg/kg 체중의 용량으로 투여되고, 항-CTLA-4 항체가 약 3 mg/kg 체중의 용량으로 투여되는 것인 방법.
E30. 실시양태 E19 내지 E25 중 어느 하나에 있어서, 항-PD-1 항체가 약 3 mg/kg 체중의 용량으로 투여되고, 항-CTLA-4 항체가 약 1 mg/kg 체중의 용량으로 투여되는 것인 방법.
E31. 실시양태 E19 내지 E25 중 어느 하나에 있어서, 항-PD-1 항체가 약 3 mg/kg 체중의 용량으로 투여되고, 항-CTLA-4 항체가 약 3 mg/kg 체중의 용량으로 투여되는 것인 방법.
E32. 실시양태 E19 내지 E31 중 어느 하나에 있어서, 항-PD-1 항체 및 항-CTLA-4 항체의 투여 후 항-PD-1 항체 단독요법이 이어지는 것인 방법.
E33. 실시양태 E32에 있어서, 항-PD-1 항체 단독요법이 약 1 mg/kg 체중의 용량으로 항-PD-1 항체를 투여하는 것을 포함하는 것인 방법.
E34. 실시양태 E32에 있어서, 항-PD-1 항체 단독요법이 약 3 mg/kg 체중의 용량으로 항-PD-1 항체를 투여하는 것을 포함하는 것인 방법.
E35. 실시양태 E32에 있어서, 항-PD-1 항체 단독요법이 약 4 mg/kg 체중의 용량으로 항-PD-1 항체를 투여하는 것을 포함하는 것인 방법.
E36. 실시양태 E19 내지 E35 중 어느 하나에 있어서, 항-PD-1 항체 및 항-CTLA-4 항체가 약 1, 2, 3 또는 4주마다 1회 투여되는 것인 방법.
E37. 실시양태 E32 내지 E35 중 어느 하나에 있어서, 항-PD-1 항체 단독요법이 약 1, 2, 3 또는 4주마다 1회 투여되는 것인 방법.
E38. 실시양태 E1 내지 E37 중 어느 하나에 있어서, 대상체가 치료의 초기 투여 후 약 4주, 약 5주, 약 6주, 약 7주, 약 8주, 약 9주, 약 10주, 약 11주, 약 12주, 약 18주, 약 24주, 약 30주, 또는 약 36주에 치료에 대한 완전 반응 또는 부분 반응을 나타내는 것인 방법.
E39. 실시양태 E19 내지 E38 중 어느 하나에 있어서, 항-PD-1 및 항-CTLA-4 항체가 정맥내 투여를 위해 제제화되는 것인 방법.
E40. 실시양태 E19 내지 E39 중 어느 하나에 있어서, 항-PD-1 및 항-CTLA-4 항체가 순차적으로 투여되는 것인 방법.
E41. 실시양태 E19 내지 E40 중 어느 하나에 있어서, 항-PD-1 및 항-CTLA-4 항체가 서로 30분 이내에 투여되는 것인 방법.
E42. 실시양태 E19 내지 E41 중 어느 하나에 있어서, 항-PD-1 항체가 항-CTLA-4 항체 전에 투여되는 것인 방법.
E43. 실시양태 E19 내지 E41 중 어느 하나에 있어서, 항-CTLA-4 항체가 항-PD-1 항체 전에 투여되는 것인 방법.
E44. 실시양태 E1 내지 E39 중 어느 하나에 있어서, 항-PD-1 항체 및 항-CTLA-4 항체가 개별 조성물로 공동으로 투여되는 것인 방법.
E45. 실시양태 E1 내지 E39 중 어느 하나에 있어서, 항-PD-1 항체 및 항-CTLA-4 항체가 공동 투여를 위해 단일 조성물로서 혼합되는 것인 방법.
E46. (a) 0.1 mg/kg 내지 10 mg/kg 체중 범위의 투여량의 항-PD-1 항체; (b) 0.1 mg/kg 내지 10 mg/kg 체중 범위의 투여량의 항-CTLA-4 항체; 및 (c) 실시양태 E1 내지 E45 중 어느 하나의 방법에서 항-PD-1 항체 및 항-CTLA-4 항체를 사용하는 것에 대한 지침서를 포함하는, 고도의 미소위성체 불안정성 ("MSI-H")을 나타내는, 결장직장암으로부터 유래된 종양을 앓는 환자를 치료하기 위한 키트.
본 개시내용은 대상체에게 항-프래그램화된 사멸-1 (PD-1) 항체를 투여하는 것을 포함하는, 대상체에서 결장직장암을 치료하는 방법에 관한 것이다. 일부 실시양태에서, 결장직장암은 고도의 미소위성체 불안정성 (MSI-H)을 나타낸다. 일부 실시양태에서, 방법은 항-세포독성 T-림프구 항원-4 (CTLA-4) 항체를 투여하는 것을 추가로 포함한다. 일부 실시양태에서, 결장직장암은 직장암, 결장암 또는 그의 임의의 조합이다.
용어
본 개시내용이 보다 용이하게 이해될 수 있도록, 특정 용어가 먼저 정의된다. 본 출원에 사용된 바와 같이, 본원에 달리 명백하게 제공된 경우를 제외하고는, 각각의 하기 용어는 하기 제시된 의미를 가질 것이다. 추가의 정의가 본 출원 전반에 걸쳐 제시된다.
본원에서 사용된 경우의 용어 "및/또는"은 2개의 명시된 특색 또는 성분 각각을 함께 또는 따로따로 구체적으로 개시하는 것으로서 여겨져야 한다. 따라서, 본원에서 "A 및/또는 B"와 같은 어구에서 사용된 용어 "및/또는"은 "A 및 B", "A 또는 B", "A" (단독), 및 "B" (단독)를 포함하는 것으로 의도된다. 마찬가지로, "A, B, 및/또는 C"와 같은 어구에서 사용된 용어 "및/또는"은 하기 측면 각각을 포괄하는 것으로 의도된다: A, B, 및 C; A, B, 또는 C; A 또는 C; A 또는 B; B 또는 C; A 및 C; A 및 B; B 및 C; A (단독); B (단독); 및 C (단독).
측면이 언어 "포함하는"을 사용하여 본원에 기재된 경우에, "로 이루어진" 및/또는 "로 본질적으로 이루어진"과 관련하여 기재된 다른 유사한 측면이 또한 제공되는 것으로 이해된다.
달리 정의되지 않는 한, 본원에 사용된 모든 기술 과학 용어는 본 개시내용이 관련된 관련 기술분야의 통상의 기술자에 의해 통상적으로 이해되는 것과 동일한 의미를 갖는다. 예를 들어, 문헌 [the Concise Dictionary of Biomedicine and Molecular Biology, Juo, Pei-Show, 2nd ed., 2002, CRC Press; The Dictionary of Cell and Molecular Biology, 3rd ed., 1999, Academic Press; 및 the Oxford Dictionary Of Biochemistry And Molecular Biology, Revised, 2000, Oxford University Press]은 통상의 기술자에게 본 개시내용에 사용된 많은 용어에 대한 일반 사전을 제공한다.
단위, 접두어, 및 기호는 시스템 인터내셔날 드 유니테스 (SI) 허용 형태로 나타내어진다. 수치 범위는 범위를 정의하는 수를 포함한다. 본원에 제공된 표제는 본 개시내용의 다양한 측면을 제한하는 것이 아니며, 이는 본 명세서를 전체로서 참조할 수 있다. 따라서, 바로 하기에 정의되는 용어는 본 명세서를 그 전체로 참조하여 보다 충분히 정의된다.
"투여하는"은 관련 기술분야의 통상의 기술자에게 공지된 다양한 방법 및 전달 시스템 중 어느 것을 사용하여 치료제를 대상체에게 물리적으로 도입하는 것을 지칭한다. 항-PD-1 항체에 대한 예시적인 투여 경로는 정맥내, 근육내, 피하, 복강내, 척수 또는 다른 비경구 투여 경로, 예를 들어 주사 또는 주입에 의한 투여를 포함한다. 본원에 사용된 어구 "비경구 투여"는 통상적으로 주사에 의한, 경장 및 국소 투여 이외의 다른 투여 방식을 의미하고, 비제한적으로, 정맥내, 근육내, 동맥내, 척수강내, 림프내, 병변내, 피막내, 안와내, 심장내, 피내, 복강내, 경기관, 피하, 각피하, 관절내, 피막하, 지주막하, 척수내, 경막외 및 흉골내 주사 및 주입, 뿐만 아니라 생체내 전기천공을 포함한다. 치료제는 비-비경구 경로를 통해 또는 경구로 투여될 수 있다. 다른 비-비경구 경로는 국소, 표피 또는 점막 투여 경로, 예를 들어 비강내, 질, 직장, 설하 또는 국소 투여 경로를 포함한다. 투여는 또한, 예를 들어 1회, 복수회, 및/또는 1회 이상의 연장된 기간에 걸쳐 수행될 수 있다.
본원에 사용된 "유해 사건" (AE)은 의학적 치료의 사용과 연관된, 임의의 바람직하지 않고 일반적으로 의도되지 않거나 원하지 않는 징후 (비정상적 실험실 발견 포함), 증상, 또는 질환이다. 의학적 치료는 1건 이상의 연관된 AE를 가질 수 있고 각각의 AE는 동일하거나 상이한 수준의 중증도를 가질 수 있다. "유해 사건을 변경할" 수 있는 방법에 대한 언급은 상이한 치료 요법의 사용과 연관된 1건 이상의 AE의 발생률 및/또는 중증도를 감소시키는 치료 요법을 의미한다.
"항체" (Ab)는 비제한적으로, 항원에 특이적으로 결합하고 디술피드 결합에 의해 상호연결된 적어도 2개의 중쇄 (H) 및 2개의 경쇄 (L)를 포함하는 당단백질 이뮤노글로불린, 또는 그의 항원-결합 부분을 포함할 것이다. 각각의 H 쇄는 중쇄 가변 영역 (본원에서 VH로 약칭됨) 및 중쇄 불변 영역을 포함한다. 중쇄 불변 영역은 적어도 3개의 불변 도메인, CH1, CH2 및 CH3을 포함한다. 각각의 경쇄는 경쇄 가변 영역 (본원에서 VL로 약칭됨) 및 경쇄 불변 영역을 포함한다. 경쇄 불변 영역은 1개의 불변 도메인, CL을 포함한다. VH 및 VL 영역은 프레임워크 영역 (FR)으로 명명되는 보다 보존된 영역이 산재되어 있는, 상보성 결정 영역 (CDR)으로 명명되는 초가변성 영역으로 추가로 세분될 수 있다. 각각의 VH 및 VL은 아미노-말단에서 카르복시-말단으로 하기 순서로 배열된 3개의 CDR 및 4개의 FR을 포함한다: FR1, CDR1, FR2, CDR2, FR3, CDR3, 및 FR4. 중쇄 및 경쇄의 가변 영역은 항원과 상호작용하는 결합 도메인을 함유한다. 항체의 불변 영역은 면역계의 다양한 세포 (예를 들어, 이펙터 세포) 및 전형적 보체계의 제1 성분 (C1q)을 포함한 숙주 조직 또는 인자에 대한 이뮤노글로불린의 결합을 매개할 수 있다.
이뮤노글로불린은 IgA, 분비형 IgA, IgG 및 IgM을 포함하나 이에 제한되지는 않는, 임의의 통상적으로 공지된 이소형으로부터 유래될 수 있다. IgG 하위부류는 또한 관련 기술분야의 통상의 기술자에게 널리 공지되어 있고, 인간 IgG1, IgG2, IgG3 및 IgG4를 포함하나 이에 제한되지는 않는다. "이소형"은 중쇄 불변 영역 유전자에 의해 코딩되는 항체 부류 또는 하위부류 (예를 들어, IgM 또는 IgG1)를 지칭한다. 용어 "항체"는, 예로서, 자연 발생 및 비-자연 발생 항체 둘 다; 모노클로날 및 폴리클로날 항체; 키메라 및 인간화 항체; 인간 또는 비-인간 항체; 완전 합성 항체; 및 단일 쇄 항체를 포함한다. 비-인간 항체는 인간에서 그의 면역원성이 감소하도록 재조합 방법에 의해 인간화될 수 있다. 명백하게 언급되지 않는 경우, 및 문맥상 달리 나타내지 않는 한, 용어 "항체"는 또한 상기 언급된 이뮤노글로불린 중 어느 것의 항원-결합 단편 또는 항원-결합 부분을 포함하고, 1가 및 2가 단편 또는 부분, 및 단일 쇄 항체를 포함한다.
"단리된 항체"는 상이한 항원 특이성을 갖는 다른 항체가 실질적으로 없는 항체를 지칭한다 (예를 들어, PD-1에 특이적으로 결합하는 단리된 항체는 PD-1 이외의 다른 항원에 특이적으로 결합하는 항체가 실질적으로 없음). 그러나, PD-1에 특이적으로 결합하는 단리된 항체는 다른 항원, 예컨대 상이한 종으로부터의 PD-1 분자와 교차-반응성을 가질 수 있다. 더욱이, 단리된 항체는 다른 세포 물질 및/또는 화학물질이 실질적으로 없을 수 있다.
용어 "모노클로날 항체" ("mAb")는 단일 분자 조성의 항체 분자, 즉, 1차 서열이 본질적으로 동일하고 특정한 에피토프에 대해 단일 결합 특이성 및 친화도를 나타내는 항체 분자의 비-자연 발생 제제를 지칭한다. 모노클로날 항체는 단리된 항체의 예이다. 모노클로날 항체는 하이브리도마, 재조합, 트랜스제닉, 또는 관련 기술분야의 통상의 기술자에게 공지된 다른 기술에 의해 생산될 수 있다.
"인간" 항체 (HuMAb)는 프레임워크 및 CDR 둘 다가 인간 배선 이뮤노글로불린 서열로부터 유래된 것인 가변 영역을 갖는 항체를 지칭한다. 추가로, 항체가 불변 영역을 함유하는 경우에, 불변 영역도 또한 인간 배선 이뮤노글로불린 서열로부터 유래된다. 본 개시내용의 인간 항체는 인간 배선 이뮤노글로불린 서열에 의해 코딩되지 않는 아미노산 잔기 (예를 들어, 시험관내 무작위 또는 부위-특이적 돌연변이유발에 의해 또는 생체내 체세포 돌연변이에 의해 도입된 돌연변이)를 포함할 수 있다. 그러나, 본원에 사용된 용어 "인간 항체"는 또 다른 포유동물 종, 예컨대 마우스의 배선으로부터 유래된 CDR 서열이 인간 프레임워크 서열 상에 그라프팅된 것인 항체를 포함하는 것으로 의도되지는 않는다. 용어 "인간" 항체 및 "완전 인간" 항체는 동의어로 사용된다.
"인간화 항체"는 비-인간 항체의 CDR 밖의 아미노산 중 일부, 대부분 또는 모두가 인간 이뮤노글로불린으로부터 유래된 상응하는 아미노산으로 대체된 것인 항체를 지칭한다. 인간화 형태의 항체의 한 실시양태에서, CDR 밖의 아미노산 중 일부, 대부분 또는 모두는 인간 이뮤노글로불린으로부터의 아미노산으로 대체된 반면에 1개 이상의 CDR 내의 일부, 대부분 또는 모든 아미노산은 변화되지 않는다. 특정한 항원에 결합하는 항체의 능력을 제거하지 않는 한, 아미노산의 적은 부가, 결실, 삽입, 치환 또는 변형은 허용가능하다. "인간화" 항체는 원래 항체의 경우와 유사한 항원 특이성을 유지한다. 일부 실시양태에서, 인간화 항체의 CDR은 비-인간, 포유동물 항체로부터의 CDR을 함유한다. 다른 실시양태에서, 인간화 항체의 CDR은 조작된, 합성 항체로부터의 CDR을 함유한다.
"키메라 항체"는 가변 영역은 한 종으로부터 유래되고 불변 영역은 또 다른 종으로부터 유래된 것인 항체, 예컨대 가변 영역은 마우스 항체로부터 유래되고 불변 영역은 인간 항체로부터 유래된 것인 항체를 지칭한다.
"항-항원" 항체는 항원에 특이적으로 결합하는 항체를 지칭한다. 예를 들어, 항-PD-1 항체는 PD-1에 특이적으로 결합하고 항-CTLA-4 항체는 CTLA-4에 특이적으로 결합한다.
항체의 "항원-결합 부분" (또한 "항원-결합 단편"으로 불림)은 전체 항체에 의해 결합되는 항원에 특이적으로 결합하는 능력을 유지하는 항체의 1개 이상의 단편을 지칭한다.
"암"은 신체 내 비정상 세포의 비제어된 성장을 특징으로 하는 다양한 질환의 광범위한 군을 지칭한다. "암" 또는 "암 조직"은 종양을 포함할 수 있다. 비조절된 세포 분열 및 성장은 이웃 조직을 침습하는 악성 종양의 형성을 일으키고 또한 림프계 또는 혈류를 통해 신체의 원위 부분으로 전이할 수 있다. 전이 후, 원위 종양은 원래, 전이전 종양"으로부터 유래된" 것으로 언급될 수 있다. 예를 들어, 결장직장암"으로부터 유래된 종양"은 전이된 결장직장암의 결과인 종양을 지칭한다. 원위 종양이 전이전 종양으로부터 유래되기 때문에, 종양"으로부터 유래된" 것은 또한 전이전 종양을 포함할 수 있으며, 예를 들어 결장직장암으로부터 유래된 종양은 결장직장암을 포함할 수 있다.
"세포독성 T-림프구 항원-4" (CTLA-4)는 CD28 패밀리에 속하는 면역억제 수용체를 지칭한다. CTLA-4는 생체내 T 세포 상에서 독점적으로 발현되고, 2종의 리간드인 CD80 및 CD86 (또한 각각 B7-1 및 B7-2로 불림)에 결합한다. 본원에 사용된 용어 "CTLA-4"는 인간 CTLA-4 (hCTLA-4), hCTLA-4의 변이체, 이소형 및 종 상동체, 및 hCTLA-4와 적어도 1개의 공통 에피토프를 갖는 유사체를 포함한다. 완전한 hCTLA-4 서열은 진뱅크 수탁 번호 AAB59385 하에 찾아볼 수 있다.
용어 "면역요법"은 면역 반응을 유도하거나, 증진시키거나, 억제하거나 또는 달리 변형시키는 것을 포함하는 방법에 의해, 질환을 앓거나, 질환에 걸릴 위험이 있거나 또는 질환의 재발을 앓고 있는 대상체를 치료하는 것을 지칭한다.
대상체의 "치료" 또는 "요법"은 질환과 연관된 증상, 합병증, 상태 또는 생화학적 징후의 발병, 진행, 발달, 중증도 또는 재발을 역전시키거나, 완화시키거나, 호전시키거나, 억제하거나, 저속화하거나 또는 방지하는 것을 목적으로 대상체에 대해 수행되는 임의의 유형의 시술 또는 과정, 또는 그에 대한 활성제의 투여를 지칭한다.
본원에 사용된 "PD-L1 양성" 또는 "PD-L2 양성"은 "적어도 약 1%의 PD-L1 및/또는 PD-L2 발현"과 상호교환가능하게 사용될 수 있다. 한 실시양태에서, PD-L1 및/또는 PD-L2 발현은 관련 기술분야에 공지된 임의의 방법에 의해 사용될 수 있다. 또 다른 실시양태에서, PD-L1 및/또는 PD-L2 발현은 자동화 계내 혼성화 (IHC)에 의해 측정된다. PD-L1 및/또는 PD-L2 양성 종양은 따라서 자동화 IHC에 의해 측정된 바와 같이 적어도 약 1%, 적어도 약 2%, 적어도 약 5%, 적어도 약 10%, 또는 적어도 약 20%, 적어도 약 25%, 적어도 약 30%, 적어도 약 40%, 적어도 약 50%, 적어도 약 60%, 적어도 약 70%, 적어도 약 75%, 적어도 약 80%, 적어도 약 85%, 적어도 약 90%, 적어도 약 95%, 또는 약 100%의 PD-L1 및/또는 PD-L2 발현 종양 세포를 가질 수 있다. 특정 실시양태에서, "PD-L1 양성"은 세포의 표면 상에 PD-L1을 발현하는 적어도 100개의 세포가 존재한다는 것을 의미한다. 다른 실시양태에서, "PD-L2 양성"은 세포의 표면 상에 PD-L2를 발현하는 적어도 100개의 세포가 존재한다는 것을 의미한다.
"프로그램화된 사멸-1" (PD-1)은 CD28 패밀리에 속하는 면역억제 수용체를 지칭한다. PD-1은 생체내 이전에 활성화된 T 세포 상에서 우세하게 발현되고, 2종의 리간드, PD-L1 및 PD-L2에 결합한다. 본원에 사용된 용어 "PD-1"은 인간 PD-1 (hPD-1), hPD-1의 변이체, 이소형 및 종 상동체, 및 hPD-1과 적어도 1개의 공통 에피토프를 갖는 유사체를 포함한다. 완전한 hPD-1 서열은 진뱅크 수탁 번호 U64863 하에 찾아볼 수 있다.
"프로그램화된 사멸 리간드-1" (PD-L1)은 PD-1에 대한 결합 시 T 세포 활성화 및 시토카인 분비를 하향 조절하는, PD-1에 대한 2종의 세포 표면 당단백질 리간드 중 하나이다 (다른 것은 PD-L2임). 본원에 사용된 용어 "PD-L1"은 인간 PD-L1 (hPD-L1), hPD-L1의 변이체, 이소형 및 종 상동체, 및 hPD-L1과 적어도 1개의 공통 에피토프를 갖는 유사체를 포함한다. 완전한 hPD-L1 서열은 진뱅크 수탁번호 Q9NZQ7 하에 찾아볼 수 있다.
"대상체"는 임의의 인간 또는 비-인간 동물을 포함한다. 용어 "비-인간 동물"은 척추동물, 예컨대 비-인간 영장류, 양, 개, 및 설치류, 예컨대 마우스, 래트, 및 기니 피그를 포함하나 이에 제한되지는 않는다. 일부 실시양태에서, 대상체는 인간이다. 용어 "대상체" 및 "환자"는 본원에서 상호교환가능하게 사용된다.
약물 또는 치료제의 "치료 유효량" 또는 "치료 유효 투여량"은, 단독으로 사용되거나 또는 또 다른 치료제와 조합되어 사용되는 경우에, 질환의 발병에 대해 대상체를 보호하거나, 또는 질환 증상의 중증도의 감소, 질환 무증상 기간의 빈도 및 지속기간의 증가, 또는 앓고 있는 질환으로 인한 손상 또는 장애의 방지에 의해 입증되는 질환 퇴행을 촉진하는 약물의 임의의 양이다. 질환 퇴행을 촉진하는 치료제의 능력은 숙련된 진료의에게 공지된 다양한 방법을 사용하여, 예컨대 임상 시험 동안 인간 대상체에서, 인간에서의 효능을 예측하는 동물 모델 시스템에서, 또는 시험관내 검정에서 작용제의 활성을 검정함으로써 평가될 수 있다.
본원에 사용된 "치료량 미만의 용량"은 과다증식성 질환 (예를 들어, 암)의 치료를 위해 단독으로 투여되는 경우 치료 화합물 (예를 들어, 항체)의 통상적 또는 전형적 용량보다 더 낮은 치료 화합물의 용량을 의미한다.
예로서, "항암제"는 대상체에서 암 퇴행을 촉진한다. 일부 실시양태에서, 치료 유효량의 약물은 암을 제거하는 지점까지 암 퇴행을 촉진한다. "암 퇴행을 촉진하는"은 치료 유효량의 약물을 단독으로 또는 항암제와 조합하여 투여하여 종양 성장 또는 크기의 감소, 종양의 괴사, 적어도 1종의 질환 증상의 중증도의 감소, 질환 무증상 기간의 빈도 및 지속기간의 증가, 또는 앓고 있는 질환으로 인한 손상 또는 장애의 방지를 유발하는 것을 의미한다. 추가로, 치료와 관련한 용어 "유효한" 및 "유효성"은 약리학적 유효성 및 생리학적 안전성 둘 다를 포함한다. 약리학적 유효성은 환자에서 암 퇴행을 촉진하는 약물의 능력을 지칭한다. 생리학적 안전성은 약물의 투여로부터 유발되는 세포, 기관 및/또는 유기체 수준에서의 독성의 수준 또는 다른 유해 생리학적 효과 (유해 효과)를 지칭한다.
종양의 치료에 대한 예로서, 치료 유효량의 항암제는 비치료 대상체에 비해 적어도 약 10%, 적어도 약 20%, 적어도 약 30%, 적어도 약 40%, 적어도 약 50%, 적어도 약 60%, 적어도 약 70%, 적어도 약 80%, 적어도 약 90%, 또는 약 100%만큼 세포 성장 또는 종양 성장을 억제한다.
본 개시내용의 다른 실시양태에서, 종양 퇴행은 적어도 약 20일, 적어도 약 30일, 적어도 약 40일, 적어도 약 50일, 또는 적어도 약 60일의 기간 동안 관찰되고 계속될 수 있다. 이들 치료 유효성의 최고의 측정에도 불구하고, 면역요법 약물의 평가는 또한 "면역-관련" 반응 패턴을 감안해야 한다.
"면역-관련" 반응 패턴은 암-특이적 면역 반응을 유도함으로써 또는 천연 면역 과정을 변형시킴으로써 항종양 효과를 생성하는 면역요법제로 치료된 암 환자에서 종종 관찰되는 임상 반응 패턴을 지칭한다. 이 반응 패턴은, 전통적인 화학요법제의 평가에서는 질환 진행으로 분류되고 약물 실패와 동의어인 종양 부담의 초기 증가 또는 새로운 병변의 출현에 이어지는 유익한 치료 효과를 특징으로 한다. 따라서, 면역요법제의 적절한 평가는 표적 질환에 대한 이들 작용제의 효과의 장기간 모니터링을 요구할 수 있다.
약물의 치료 유효량은 "예방 유효량"을 포함하며, 이는 암이 발생할 위험이 있는 대상체 (예를 들어, 전-악성 상태를 갖는 대상체) 또는 암의 재발을 앓을 위험이 있는 대상체에게 단독으로 또는 항암제와 조합되어 투여되는 경우에, 암의 발생 또는 재발을 억제하는 약물의 임의의 양이다. 일부 실시양태에서, 예방 유효량은 암의 발생 또는 재발을 전적으로 방지한다. 암의 발생 또는 재발을 "억제하는"은 암의 발생 또는 재발 가능성을 경감시키거나, 또는 암의 발생 또는 재발을 전적으로 방지하는 것을 의미한다.
본원에 지칭된 용어 "중량-기준 용량"은 환자에게 투여되는 용량이 환자의 중량을 기준으로 하여 계산된다는 것을 의미한다. 예를 들어, 60 kg 체중을 갖는 환자가 3 mg/kg의 항-PD-1 항체를 요구하는 경우에, 투여를 위해 항-PD-1 항체의 적절한 양 (즉, 180 mg)을 계산하고 사용할 수 있다.
본 개시내용의 방법과 관련하여 용어 "고정 용량"의 사용은 단일 조성물 중에 2종 이상의 상이한 항체 (예를 들어, 항-PD-1 항체 및 항-CTLA-4 항체)가 서로 특정한 (고정) 비로 조성물 중에 존재한다는 것을 의미한다. 일부 실시양태에서, 고정 용량은 항체의 중량 (예를 들어, mg)을 기준으로 한다. 특정 실시양태에서, 고정 용량은 항체의 농도 (예를 들어, mg/ml)를 기준으로 한다. 일부 실시양태에서, 제1 항체 (예를 들어, 항-PD-1 항체) (mg) 대 제2 항체 (예를 들어, 항-CTLA-4 항체) (mg)의 비는 적어도 약 1:1, 약 1:2, 약 1:3, 약 1:4, 약 1:5, 약 1:6, 약 1:7, 약 1:8, 약 1:9, 약 1:10, 약 1:15, 약 1:20, 약 1:30, 약 1:40, 약 1:50, 약 1:60, 약 1:70, 약 1:80, 약 1:90, 약 1:100, 약 1:120, 약 1:140, 약 1:160, 약 1:180, 약 1:200, 약 200:1, 약 180:1, 약 160:1, 약 140:1, 약 120:1, 약 100:1, 약 90:1, 약 80:1, 약 70:1, 약 60:1, 약 50:1, 약 40:1, 약 30:1, 약 20:1, 약 15:1, 약 10:1, 약 9:1, 약 8:1, 약 7:1, 약 6:1, 약 5:1, 약 4:1, 약 3:1, 또는 약 2:1이다. 예를 들어, 항-PD-1 항체 및 항-CTLA-4 항체의 3:1 비는 바이알이 약 240 mg의 항-PD-1 항체 및 80 mg의 항-CTLA-4 항체 또는 약 3 mg/ml의 항-PD-1 항체 및 1 mg/ml의 항-CTLA-4 항체를 함유할 수 있다는 것을 의미할 수 있다.
본 개시내용의 방법 및 투여량과 관련하여 용어 "균일 용량"의 사용은 환자의 중량 또는 체표면적 (BSA)과 무관하게 환자에게 투여되는 용량을 의미한다. 따라서 균일 용량은 mg/kg 용량으로 제공되는 것이 아니라, 오히려 작용제 (예를 들어, 항-CTLA-4 항체 및/또는 항-PD-1 항체)의 절대량으로서 제공된다. 예를 들어, 60 kg 사람 및 100 kg 사람은 동일한 용량의 항체 (예를 들어, 240 mg의 항-PD1 항체)를 받을 것이다.
대안적 사용 (예를 들어, "또는")은 대안 중 하나, 둘 다, 또는 그의 임의의 조합을 의미하는 것으로 이해되어야 한다. 본원에 사용된 단수 형태는 임의의 언급되거나 열거된 성분 중 "하나 이상"을 지칭하는 것으로 이해되어야 한다.
용어 "약" 또는 "본질적으로 포함하는"은 관련 기술분야의 통상의 기술자에 의해 결정된 바와 같은 특정한 값 또는 조성에 대한 허용 오차 범위 내의 값 또는 조성을 지칭하며, 이는 부분적으로 값 또는 조성이 측정 또는 결정되는 방법, 즉 측정 시스템의 한계에 좌우될 것이다. 예를 들어, "약" 또는 "본질적으로 포함하는"은 관련 기술분야에서의 실시에 따라 1 또는 1 초과의 표준 편차 내에 있음을 의미할 수 있다. 대안적으로, "약" 또는 "본질적으로 포함하는"은 최대 20%의 범위를 의미할 수 있다. 추가로, 특히 생물학적 시스템 또는 과정과 관련하여, 그 용어는 값의 최대 한 자릿수 배수 또는 최대 5-배를 의미할 수 있다. 특정한 값 또는 조성이 본 출원 및 청구범위에서 제공되는 경우에, 달리 언급되지 않는 한, "약" 또는 "본질적으로 포함하는"의 의미는 그러한 특정한 값 또는 조성에 대한 허용 오차 범위 내에 있는 것으로 가정되어야 한다.
본원에 사용된 용어 "약 매주 1회", "약 2주마다 1회", 또는 임의의 다른 유사한 투여 간격 용어는 대략적인 횟수를 의미한다. "약 매주 1회"는 7일 ± 1일마다, 즉, 6일마다 내지 8일마다를 포함할 수 있다. "약 2주마다 1회"는 14일 ± 3일마다, 즉, 11일마다 내지 17일마다를 포함할 수 있다. 유사한 근사법이, 예를 들어 약 3주마다 1회, 약 4주마다 1회, 약 5주마다 1회, 약 6주마다 1회, 및 약 12주마다 1회에 대해 적용된다. 일부 실시양태에서, 약 6주마다 1회 또는 약 12주마다 1회의 투여 간격은, 제1 용량이 제1주 중 임의의 날에 투여될 수 있고, 이어서 다음 용량이 각각 제6주 또는 제12주 중 임의의 날에 투여될 수 있다는 것을 의미한다. 다른 실시양태에서, 약 6주마다 1회 또는 약 12주마다 1회의 투여 간격은, 제1 용량이 제1주의 특정한 날 (예를 들어, 월요일)에 투여되고, 이어서 다음 용량이 각각 제6주 또는 제12주의 동일한 날 (즉, 월요일)에 투여된다는 것을 의미한다.
본원에 기재된 임의의 농도 범위, 백분율 범위, 비 범위 또는 정수 범위는 달리 나타내지 않는 한, 언급된 범위 내의 임의의 정수 값, 및 적절한 경우에, 그의 분율 (예컨대 정수의 1/10 및 1/100)을 포함하는 것으로 이해되어야 한다.
본 개시내용의 다양한 측면이 하기 서브섹션에 추가로 상세하게 기재되어 있다.
표 1. 약어의 목록
본 개시내용의 방법
본 개시내용은 결장직장암으로부터 유래된 종양을 앓는 대상체에게 프로그램화된 사멸-1 수용체 (PD-1)에 특이적으로 결합하고 PD-1 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-PD-1 항체") 또는 프로그램화된 사멸 리간드 1 (PD-L1)에 특이적으로 결합하고 PD-L1 활성을 억제하는 항체 또는 그의 항원-결합 부분 ("항-PD-L1 항체")의 치료 유효량을 투여하는 것을 포함하는, 상기 대상체를 치료하는 방법에 관한 것이다.
일부 실시양태에서, 요법은 결장직장암인 암으로부터 유래된 종양을 치료한다. 일부 실시양태에서, 결장직장암은 결장암이다. 다른 실시양태에서, 결장직장암은 직장암이다. 특정 실시양태에서, 결장직장암은 미소위성체 불안정성 (MSI)을 갖는다 (문헌 [Pawlik et al., Dis. Markers 20(4-5): 199-206 (2004)] 참조). 다른 실시양태에서, 결장직장암은 높은 미소위성체 불안정성 (MSI-H)을 갖는다.
결장암은 다음 5개의 병기로 존재한다: 0기 (상피내 암종), I기, II기, III기 및 IV기. 다음 6가지 유형의 표준 치료가 결장암에 사용된다: 1) 국부 절제, 문합술을 사용한 결장의 절제, 또는 결장조루술을 사용한 결장의 절제를 포함한 수술; 2) 고주파 절제; 3) 동결수술; 4) 화학요법; 5) 방사선 요법; 및 6) 모노클로날 항체 및 혈관신생 억제제를 포함한 표적화 요법. 일부 실시양태에서, 본 개시내용의 조합 요법은 표준 관리 요법과 함께 결장암을 치료한다.
직장암은 다음 5개의 병기로 존재한다: 0기 (상피내 암종), I기, II기, III기 및 IV기. 다음 6가지 유형의 표준 치료가 직장암에 사용된다: 1) 폴립절제술, 국부 절제, 절제, 고주파 절제, 동결수술 및 골반 내용제거술을 포함한 수술; 2) 방사선 요법; 3) 화학요법; 및 4) 모노클로날 항체 요법을 포함한 표적화 요법. 일부 실시양태에서, 본 개시내용의 방법은 표준 관리 요법과 함께 직장암을 치료한다.
결장직장암에서, MSI-H는 면역 침윤 및 면역 체크포인트 조절제의 발현의 증가와 연관된다. 따라서, 본 개시내용의 방법은 고도의 미소위성체 불안정성 (MSI-H)을 나타내는 결장직장암의 치료를 포함한다. 일부 실시양태에서, 항-PD-1 항체는 CTLA-4에 특이적으로 결합하는 항체 또는 그의 항원-결합 부분 ("항-CTLA-4 항체")의 치료 유효량과 조합되어 투여된다.
미소위성체 불안정성은 손상된 DNA 미스매치 복구 (MMR)로부터 유발되는 유전적 과다돌연변이성의 상태이다. MSI의 존재는 MMR이 정상적으로 기능하지 않는 표현형 증거를 나타낸다. 대부분의 경우에, MSI 종양에서의 불안정성에 대한 유전적 기초는 다음 5종의 인간 MMR 유전자 중 어느 하나에서의 유전성 배선 변경이다: MSH2, MLH1, MSH6, PMS2 및 PMS1. 특정 실시양태에서, 종양 치료를 받는 대상체는 고도의 미소위성체 불안정성 (MSI-H)을 갖고, 유전자 MSH2, MLH1, MSH6, PMS2 또는 PMS1에서 적어도 1종의 돌연변이를 갖는다. 다른 실시양태에서, 대조군 내 종양 치료를 받는 대상체는 미소위성체 불안정성을 갖지 않고 (MSS 또는 MSI 안정한), 유전자 MSH2, MLH1, MSH6, PMS2 및 PMS1에서 돌연변이를 갖지 않는다.
본 개시내용은 또한 단독으로 또는 항-CTLA-4 항체와 조합되어 투여된 항-PD-1 항체에 반응하는 대상체를 확인하는 것을 포함하며, 여기서 대상체는 MSI-H 종양을 갖는 것인, 종양, 예를 들어 결장에서의 종양을 치료하는 방법에 관한 것이다. 일부 실시양태에서, 본 개시내용은 (i) MSI-H 종양인 종양을 갖는 대상체를 확인하고, (ii) 대상체에게 유효량의 항-PD-1 항체를 단독으로 또는 유효량의 항-CTLA-4 항체와 조합하여 투여하는 것을 포함하는, 종양, 예를 들어 결장에서의 종양을 치료하는 방법을 제공한다. 본원에 사용된, MSI-H 종양은 적어도 약 30% 초과의 불안정한 MSI 바이오마커를 갖는 종양을 의미한다. 일부 실시양태에서, 결장직장암은 적어도 2종, 적어도 3종, 적어도 4종 또는 적어도 5종의 MMR 유전자에서 배선 변경이 검출되는 경우에 MSI-H이다. 다른 실시양태에서, 결장직장암은 5종 이상의 MMR 유전자의 적어도 30%에서 배선 변경이 검출되는 경우에 MSI-H이다. 일부 실시양태에서, MMR 유전자에서의 배선 변경은 폴리머라제 연쇄 반응에 의해 측정된다. 다른 실시양태에서, 결장직장암은 DNA MMR 유전자에 의해 코딩되는 적어도 1종의 단백질이 종양에서 검출되지 않는 경우에 MSI-H이다. 일부 실시양태에서, DNA MMR 유전자에 의해 코딩되는 적어도 1종의 단백질은 면역조직화학에 의해 검출된다. 특정 실시양태에서, 본 개시내용은 1) 종양의 미소위성체 상태를 확인 하고, 2) 대상체에게 미소위성체 상태에 기초하여 요법을 투여하는 것을 포함하는, 암을 치료하는 방법에 관한 것이다. 일부 실시양태에서, 대상체는 MSI-H를 갖는다.
일부 실시양태에서, 결장직장암은 직장암, 결장암 또는 그의 임의의 조합이다. 특정 실시양태에서, 대상체는 1, 2, 3, 4, 5종 또는 그 초과의 선행 암 치료를 받았다. 다른 실시양태에서, 대상체는 치료-나이브이다. 일부 실시양태에서, 대상체는 다른 암 치료를 진행하였다. 실시양태에서, 암은 재발하였다. 일부 실시양태에서, 암은 전이성이다. 다른 실시양태에서, 암은 전이성이 아니다.
일부 실시양태에서, 결장직장암은 조직학적으로 확인된다. 특정 실시양태에서, 결장직장암은 전이성 또는 재발성이다. 실시양태에서, 대상체는 표준 요법의 마지막 투여 동안, 그 후에 진행하였거나, 또는 그에 불내성이었다. 특정 실시양태에서, 대상체는 미소위성체 불안정성을 갖는다. 다른 실시양태에서, 결장직장암은 고도의 미소위성체 불안정성 (MSI-H)을 갖는다.
다른 실시양태에서, MSI-H를 갖는 결장직장암은 PD-L1을 발현한다. 또 다른 실시양태에서, MSI-H를 갖는 결장직장암은 적어도 1%, 적어도 2%, 적어도 3%, 적어도 4%, 적어도 5%, 적어도 10%, 적어도 20%, 적어도 30%, 적어도 40%, 또는 적어도 50% 막 PD-L1을 발현한다.
일부 실시양태에서, 본 방법은 유효량의 항-PD-1 항체를 투여하는 것을 포함한다. 다른 실시양태에서, 본 방법은 유효량의 항-PD-1 항체 및 유효량의 항-CTLA-4 항체를 투여하는 것을 포함한다. 항-PD-1 항체 및/또는 항-CTLA-4 항체의 유효량은 균일 용량 또는 중량 기준 용량일 수 있다.
실시양태에서, 본 개시내용은 항-PD-1 길항제를 항-CTLA-4 항체와 조합하여 투여하여 암을 치료하는 것을 포함하는, 결장직장암으로부터 유래된 종양을 앓는 대상체를 치료하는 방법을 포함한다. 본원에 지칭된 "항-PD-1 길항제"는 PD-1/PD-L1의 신호 경로가 차단되도록 PD-1 (수용체)과 PD-L1 (리간드) 사이의 상호작용을 억제하는 임의의 분자를 포함한다. 다른 실시양태에서, 항-PD-1 길항제는 PD-1-Fc 융합 단백질이다. 특정 실시양태에서, 항-PD-1 길항제는 PD-1과 PD-L1 사이의 상호작용을 억제 또는 방지하는 항-PD-1 융합 단백질, 안티센스 분자, 소분자, 리보자임 또는 나노바디를 포함한다.
특정 실시양태에서, 본 개시내용의 요법 (예를 들어, 단독 또는 항-CTLA-4 항체와 조합된 항-PD-1 항체의 투여)은 대상체의 생존 기간을 효과적으로 증가시킨다. 예를 들어, 대상체의 생존 기간은 적어도 약 1개월, 적어도 약 2개월, 적어도 약 3개월, 적어도 약 4개월, 적어도 약 5개월, 적어도 약 6개월, 적어도 약 7개월, 적어도 약 8개월, 적어도 약 9개월, 적어도 약 10개월, 적어도 약 11개월 또는 적어도 약 1년 또는 그 초과만큼 증가된다.
특정 실시양태에서, 본 개시내용의 요법은 대상체의 무진행 생존 기간을 효과적으로 증가시킨다. 예를 들어, 대상체의 무진행 생존은 적어도 약 1개월, 적어도 약 2개월, 적어도 약 3개월, 적어도 약 4개월, 적어도 약 5개월, 적어도 약 6개월, 적어도 약 7개월, 적어도 약 8개월, 적어도 약 9개월, 적어도 약 10개월, 적어도 약 11개월 또는 적어도 약 1년만큼 증가된다. 특정 실시양태에서, 본 개시내용의 요법은 대상체 군에서 반응률을 효과적으로 증가시킨다. 예를 들어, 대상체 군에서의 반응률은 적어도 약 2%, 적어도 약 3%, 적어도 약 4%, 적어도 약 5%, 적어도 약 10%, 적어도 약 15%, 적어도 약 20%, 적어도 약 25%, 적어도 약 30%, 적어도 약 35%, 적어도 약 40%, 적어도 약 45%, 적어도 약 50%, 적어도 약 55%, 적어도 약 60%, 적어도 약 70%, 적어도 약 75%, 적어도 약 80%, 적어도 약 85%, 적어도 약 90%, 적어도 약 95%, 적어도 약 99% 또는 약 100%만큼 증가된다.
일부 실시양태에서, 항-PD-1 항체는 정맥내 투여를 위해 제제화된다. 일부 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 정맥내 투여를 위해 제제화된다. 특정 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 순차적으로 투여된다. 실시양태에서, 항-PD-1 및 항-CTLA-4 항체는 서로 30분 이내에 투여된다. 한 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분은 항-CTLA-4 항체 또는 그의 항원-결합 부분 전에 투여된다. 또 다른 실시양태에서, 항-CTLA-4 항체 또는 그의 항원-결합 부분은 항-PD-1 항체 또는 그의 항원-결합 부분 전에 투여된다. 또 다른 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분 및 항-CTLA-4 항체 또는 그의 항원-결합 부분은 개별 조성물로 공동으로 투여된다. 추가 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분 및 항-CTLA-4 항체 또는 그의 항원-결합 부분은 공동 투여를 위해 단일 조성물로서 혼합된다.
일부 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 고정 용량으로 투여된다.
일부 실시양태에서, 암은 미소위성체 안정한 (MSS) (또는 "MSI 안정한") 암이고, 따라서 미소위성체 불안정성을 갖지 않는다. 다른 실시양태에서, 암은 고도의 미소위성체 불안정성 (MSI-H)을 갖는다.
항-PD-1 항체 및 항-PD-L1 항체
본 개시내용의 요법은 항-PD-1 항체 또는 그의 항원-결합 부분을 이용할 수 있다. PD-1은 활성화된 T 및 B 세포에 의해 발현되는 주요 면역 체크포인트 수용체이고 면역억제를 매개한다. PD-1은 CD28, CTLA-4, ICOS, PD-1 및 BTLA를 포함하는 CD28 패밀리의 수용체의 구성원이다. 항원-제시 세포 뿐만 아니라 많은 인간 암에서 발현되는 PD-1에 대한 2종의 세포 표면 당단백질 리간드인 프로그램화된 사멸 리간드-1 (PD-L1) 및 프로그램화된 사멸 리간드-2 (PD-L2)가 확인되었으며, 이는 PD-1에 결합 시 T 세포 활성화 및 시토카인 분비를 하향-조절하는 것으로 밝혀졌다. PD-1/PD-L1 상호작용의 억제는 전임상 모델에서 강력한 항종양 활성을 매개한다.
개시된 방법에서 사용하기에 적합한 항-PD-1 항체는, PD-1에 높은 특이성 및 친화도로 결합하고, PD-L1의 결합을 차단하고, PD-1 신호전달 경로의 면역억제 효과를 억제하는 항체이다. 본원에 개시된 임의의 치료 방법에서, 항-PD-1 또는 항-PD-L1 "항체"는 각각 PD-1 또는 PD-L1 수용체에 결합하며, 리간드 결합을 억제하고 면역계를 상향조절하는데 있어서 전체 항체의 경우와 유사한 기능적 특성을 나타내는 항원-결합 부분을 포함한다. 특정 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분은 인간 PD-1에의 결합에 대해 니볼루맙과 교차-경쟁한다. 다른 실시양태에서, 항-PD-L1 항체 또는 그의 항원-결합 단편은 인간 PD-L1에의 결합에 대해 BMS-936559, MPDL3280A, MEDI4736, 또는 MSB0010718C와 경쟁한다.
다른 실시양태에서, 항-PD-1 항체 또는 항-PD-L1 항체 또는 그의 항원-결합 부분은 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분이다. 인간 대상체를 치료하기 위한 특정 실시양태에서, 항체는 인간화 항체이다. 인간 대상체를 치료하기 위한 다른 실시양태에서, 항체는 IgG1, IgG2, IgG3 또는 IgG4 이소형의 인간 항체가 사용될 수 있다.
특정 실시양태에서, 항-PD-1 항체 또는 항-PD-L1 항체 또는 그의 항원-결합 부분은 인간 IgG1 또는 IgG4 이소형의 중쇄 불변 영역을 포함한다. 특정의 다른 실시양태에서, 항-PD-1 항체 또는 항-PD-L1 항체 또는 그의 항원-결합 부분의 IgG4 중쇄 불변 영역의 서열은 힌지 영역 내의 세린 잔기를, IgG1 이소형 항체 내의 상응하는 위치에서 통상적으로 발견되는 프롤린 잔기로 대체한 S228P 돌연변이를 함유한다. 니볼루맙에 존재하는 이 돌연변이는 내인성 IgG4 항체와의 Fab 아암 교환을 방지하는 반면에, 야생형 IgG4 항체와 연관된 Fc 수용체를 활성화시키는데 있어서 낮은 친화도를 유지한다 (Wang et al., In vitro characterization of the anti-PD-1 antibody nivolumab, BMS-936558, and in vivo toxicology in non-human primates, Cancer Imm Res, 2(9):846-56 (2014)). 또 다른 실시양태에서, 항체는 인간 카파 또는 람다 불변 영역인 경쇄 불변 영역을 포함한다. 다른 실시양태에서, 항-PD-1 항체 또는 항-PD-L1 항체 또는 그의 항원-결합 부분은 모노클로날 항체 또는 그의 항원-결합 부분이다.
고친화도로 PD-1에 특이적으로 결합하는 인간 모노클로날 항체는 미국 특허 번호 8,008,449에 개시되었다. 다른 항-PD-1 모노클로날 항체는, 예를 들어 미국 특허 번호 6,808,710, 7,488,802, 8,168,757 및 8,354,509 및 PCT 공개 번호 WO 2012/145493에 기재되었다. 미국 특허 번호 8,008,449에 개시된 각각의 항-PD-1 인간 모노클로날 항체는 하기 특징 중 1개 이상을 나타내는 것으로 입증되었다: (a) 비아코어 바이오센서 시스템을 사용하여 표면 플라즈몬 공명에 의해 결정된 바와 같이, 1 x 10-7 M 이하의 KD로 인간 PD-1에 결합함; (b) 인간 CD28, CTLA-4 또는 ICOS에 실질적으로 결합하지 않음; (c) 혼합 림프구 반응 (MLR) 검정에서 T-세포 증식을 증가시킴; (d) MLR 검정에서 인터페론-γ 생산을 증가시킴; (e) MLR 검정에서 IL-2 분비를 증가시킴; (f) 인간 PD-1 및 시노몰구스 원숭이 PD-1에 결합함; (g) PD-L1 및/또는 PD-L2의 PD-1에의 결합을 억제함; (h) 항원-특이적 기억 반응을 자극함; (i) 항체 반응을 자극함; 및/또는 (j) 생체내 종양 세포 성장을 억제함. 본 개시내용에서 사용가능한 항-PD-1 항체는 인간 PD-1에 특이적으로 결합하고 상기 특징 중 적어도 1개, 적어도 2개, 적어도 3개, 적어도 4개 또는 적어도 5개를 나타내는 모노클로날 항체를 포함한다. 일부 실시양태에서, 항-PD-1 항체는 니볼루맙을 포함한다. 한 실시양태에서, 항-PD-1 항체는 펨브롤리주맙을 포함한다.
한 실시양태에서, 항-PD-1 항체는 니볼루맙이다. 니볼루맙 (또한 "옵디보(OPDIVO)®"로 공지됨; 이전에 5C4, BMS-936558, MDX-1106, 또는 ONO-4538로 명명됨)은 PD-1 리간드 (PD-L1 및 PD-L2)와의 상호작용을 선택적으로 방지함으로써 항종양 T-세포 기능의 하향-조절을 차단하는 완전 인간 IgG4 (S228P) PD-1 면역 체크포인트 억제제 항체이다 (미국 특허 번호 8,008,449; 문헌 [Wang et al., 2014 Cancer Immunol Res. 2(9):846-56]). 니볼루맙은 신세포 암종 (신장 선암종 또는 부신종), 흑색종 및 비소세포 폐암 (NSCLC)을 포함한 다양한 진행성 고형 종양에서 활성을 나타냈다 (Topalian et al., 2012a; Topalian et al., 2014; Drake et al., 2013; WO 2013/173223). 또 다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 니볼루맙과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 니볼루맙과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 니볼루맙과 동일한 CDR을 갖는다.
또 다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 펨브롤리주맙과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 펨브롤리주맙과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 펨브롤리주맙과 동일한 CDR을 갖는다. 또 다른 실시양태에서, 항-PD-1 항체는 펨브롤리주맙이다. 펨브롤리주맙 (또한 "키트루다(KEYTRUDA)®", 람브롤리주맙, 및 MK-3475로 공지됨)은 인간 세포 표면 수용체 PD-1 (프로그램화된 사멸-1 또는 프로그램화된 세포 사멸-1)에 대해 지시된 인간화 모노클로날 IgG4 항체이다. 펨브롤리주맙은, 예를 들어 미국 특허 번호 8,900,587에 기재되어 있으며; 또한 www.cancer.gov/drugdictionary?cdrid=695789 (마지막 접근: 2014년 12월 14일)를 참조한다. 펨브롤리주맙은 재발성 또는 불응성 흑색종 및 진행성 NSCLC의 치료를 위한 것으로 FDA에 의해 승인되었다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 MEDI0680과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 MEDI0680과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 MEDI0680과 동일한 CDR을 갖는다. 다른 실시양태에서, 항-PD-1 항체는 PD-1 수용체에 대한 모노클로날 항체인 MEDI0680 (이전에 AMP-514)이다. MEDI0680은, 예를 들어 미국 특허 번호 8,609,089 B2 또는 www.cancer.gov/drugdictionary?cdrid=756047 (마지막 접근 2014년 12월 14일)에 기재되어 있다.
특정 실시양태에서, 면역 체크포인트 억제제는 B7-DC Fc 융합 단백질인 AMP-224이다. AMP-224는 미국 공개 번호 2013/0017199 또는 http://www.cancer.gov/publications/dictionaries/cancer-drug?cdrid=700595 (마지막 접근 2015년 7월 8일)에 논의되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 BGB-A317과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 BGB-A317과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 BGB-A317과 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간화 모노클로날 항체인 BGB-A317이다. BGB-A317은 미국 공개 번호 2015/0079109에 기재되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 INCSHR1210 (SHR-1210)과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 INCSHR1210 (SHR-1210)과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 INCSHR1210 (SHR-1210)과 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간 모노클로날 항체인 INCSHR1210 (SHR-1210)이다. INCSHR1210 (SHR-1210)은 WO2015/085847에 기재되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 REGN-2810과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 REGN-2810과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 REGN-2810과 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간 모노클로날 항체인 REGN-2810이다. REGN-2810은 WO2015/112800에 기재되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 PDR001과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 PDR001과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 PDR001과 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간화 모노클로날 항체인 PDR001이다. PDR001은 WO2015/112900에 기재되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 TSR-042 (ANB011)와 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 TSR-042 (ANB011)와 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 TSR-042 (ANB011)와 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간화 모노클로날 항체인 TSR-042 (ANB011)이다. TSR-042 (ANB011)는 WO2014/179664에 기재되어 있다.
다른 실시양태에서, 항-PD-1 항체 (또는 그의 항원-결합 부분)는 STI-1110과 교차-경쟁한다. 일부 실시양태에서, 항-PD-1 항체는 STI-1110과 동일한 에피토프에 결합한다. 특정 실시양태에서, 항-PD-1 항체는 STI-1110과 동일한 CDR을 갖는다. 특정 실시양태에서, 항-PD-1 항체는 인간 모노클로날 항체인 STI-1110이다. STI-1110은 WO2014/194302에 기재되어 있다.
개시된 방법에서 사용가능한 항-PD-1 항체는 또한, 인간 PD-1에 특이적으로 결합하고, 인간 PD-1에의 결합에 대해 니볼루맙과 교차-경쟁하는 단리된 항체를 포함한다 (예를 들어, 미국 특허 번호 8,008,449; WO 2013/173223 참조). 항체가 항원에의 결합에 대해 교차-경쟁하는 능력은 이들 항체가 항원의 동일한 에피토프 영역에 결합하고 그러한 특정한 에피토프 영역에 대한 다른 교차-경쟁 항체의 결합을 입체적으로 방해한다는 것을 나타낸다. 이들 교차-경쟁 항체는 그가 PD-1의 동일한 에피토프 영역에 결합하는데 있어서 니볼루맙의 경우와 매우 유사한 기능적 특성을 갖는 것으로 예상된다. 교차-경쟁 항체는 표준 PD-1 결합 검정, 예컨대 비아코어 분석, ELISA 검정 또는 유동 세포측정법에서 니볼루맙과 교차-경쟁하는 그의 능력에 기초하여 용이하게 확인될 수 있다 (예를 들어, WO 2013/173223 참조).
특정 실시양태에서, 인간 PD-1에의 결합에 대해 니볼루맙과 교차-경쟁하거나, 또는 그와 동일한 인간 PD-1의 에피토프 영역에 결합하는 항체는 모노클로날 항체이다. 인간 대상체에 대한 투여의 경우, 이들 교차-경쟁 항체는 키메라 항체일 수 있거나, 또는 인간화 또는 인간 항체일 수 있다. 이러한 키메라, 인간화 또는 인간 모노클로날 항체는 관련 기술분야에 널리 공지된 방법에 의해 제조 및 단리될 수 있다.
본 개시내용의 방법에서 사용가능한 항-PD-1 항체는 또한 상기 항체의 항원-결합 부분을 포함한다. 항체의 항원-결합 기능이 전장 항체의 단편에 의해 수행될 수 있다는 것은 충분히 입증되었다. 용어 항체의 "항원-결합 부분" 내에 포괄된 결합 단편의 예는 (i) VL, VH, CL 및 CH1 도메인으로 이루어진 1가 단편인 Fab 단편; (ii) 힌지 영역에서 디술피드 가교에 의해 연결된 2개의 Fab 단편을 포함하는 2가 단편인 F(ab')2 단편; (iii) VH 및 CH1 도메인으로 이루어진 Fd 단편; 및 (iv) 항체의 단일 아암의 VL 및 VH 도메인으로 이루어진 Fv 단편, 또는 그의 임의의 조합을 포함한다.
특정 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분은 인간 IgG1 또는 IgG4 이소형의 중쇄 불변 영역을 포함한다. 특정의 다른 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분의 IgG4 중쇄 불변 영역의 서열은 힌지 영역 내의 세린 잔기를, IgG1 이소형 항체 내의 상응하는 위치에서 통상적으로 발견되는 프롤린 잔기로 대체한 S228P 돌연변이를 함유한다. 니볼루맙에 존재하는 이 돌연변이는 내인성 IgG4 항체와의 Fab 아암 교환을 방지하는 반면에, 야생형 IgG4 항체와 연관된 Fc 수용체를 활성화시키는데 있어서 낮은 친화도를 유지한다 (Wang et al., 2014). 또 다른 실시양태에서, 항체는 인간 카파 또는 람다 불변 영역인 경쇄 불변 영역을 포함한다. 다른 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분은 모노클로날 항체 또는 그의 항원-결합 부분이다. 항-PD-1 항체의 투여를 포함하는 본원에 기재된 임의의 치료 방법의 특정 실시양태에서, 항-PD-1 항체는 니볼루맙이다. 다른 실시양태에서, 항-PD-1 항체는 펨브롤리주맙이다. 다른 실시양태에서, 항-PD-1 항체는 미국 특허 번호 8,008,449에 기재된 인간 항체 17D8, 2D3, 4H1, 4A11, 7D3 및 5F4로부터 선택된다. 또 다른 실시양태에서, 항-PD-1 항체는 MEDI0680 (이전에 AMP-514), AMP-224, 또는 BGB-A317이다.
다른 실시양태에서, 항-PD-1 항체 또는 그의 항원-결합 부분은 키메라, 인간화 또는 인간 모노클로날 항체 또는 그의 부분이다. 인간 대상체를 치료하기 위한 특정 실시양태에서, 항체는 인간화 항체이다. 인간 대상체를 치료하기 위한 다른 실시양태에서, 항체는 인간 항체이다. IgG1, IgG2, IgG3 또는 IgG4 이소형의 항체가 사용될 수 있다.
특정 실시양태에서, 방법에 사용된 항-PD-1 항체는 또 다른 PD-1 또는 항-PD-L1 길항제로 대체될 수 있다. 예를 들어, 항-PD-L1 항체가 PD-1과 PD-L1 사이의 상호작용을 방지함으로써, PD-1의 신호전달 경로에 유사한 효과를 발휘하기 때문에, 항-PD-L1 항체는 본원에 개시된 방법에서 항-PD-1 항체의 사용을 대체할 수 있다. 따라서, 한 실시양태에서, 본 개시내용은 결장직장암으로부터 유래된 종양을 앓는 대상체에게 프로그램화된 사멸-리간드 1 (PD-L1) 수용체에 특이적으로 결합하고 PD-L1 활성을 억제하는 항체 또는 그의 항원-결합 부분 (항-PD-L1 항체)인 항암제의 치료 유효량을 투여하는 것을 포함하는, 상기 대상체를 치료하는 방법에 관한 것이다. 다른 실시양태에서, 본 개시내용은 결장직장암으로부터 유래된 종양을 앓는 대상체에게 치료 유효량의 항-PD-L1 항체를 항-CTLA-4 항체와 조합하여 투여하는 것을 포함하는, 상기 대상체를 치료하는 방법에 관한 것이다. 특정 실시양태에서, 항-PD-L1 Ab는 BMS-936559 (이전에 12A4 또는 MDX-1105) (예를 들어 미국 특허 번호 7,943,743; WO 2013/173223 참조)이다. 다른 실시양태에서, 항-PD-L1 Ab는 MPDL3280A (또한 RG7446 또는 아테졸리주맙으로 공지됨) (예를 들어 [Herbst]; 미국 특허 번호 8,217,149 참조), MEDI4736 (또한 두르발루맙으로 불림; [Khleif, 2013], 미국 특허 번호 8,779,108 또는 US 2014/0356353 (2014년 5월 6일 출원) 참조), 또는 MSB0010718C (또한 아벨루맙으로 불림; US 2014/0341917 참조)이다. 다른 실시양태에서, 항-PD-L1 항체는 CX-072 (또한 시톰엑스로 불림; WO2016/149201 참조)이다.
항-CTLA-4 항체
일부 실시양태에서, 본 개시내용의 방법은 항-PD-1 항체 또는 항-PD-L1 항체 및 항-CTLA-4 항체의 조합 요법일 수 있다. 본 개시내용의 항-CTLA-4 항체는 인간 CTLA-4에 결합하여 CTLA-4와 인간 B7 수용체와의 상호작용을 파괴할 수 있다. CTLA-4와 B7과의 상호작용은 CTLA-4 수용체를 보유하는 T-세포의 불활성화를 일으키는 신호를 전달하기 때문에, 상호작용의 파괴는 이러한 T 세포의 활성화를 효과적으로 유도, 증진 또는 연장시킴으로써, 면역 반응을 유도, 증진 또는 연장시킨다.
고친화도로 CTLA-4에 특이적으로 결합하는 인간 모노클로날 항체는 미국 특허 번호 6,984,720 및 7,605,238에 개시되었다. 다른 항-PD-1 모노클로날 항체는, 예를 들어 미국 특허 번호 5,977,318, 6,051,227, 6,682,736, 및 7,034,121에 기재되었다. 미국 특허 번호 6,984,720 및 7,605,238에 개시된 항-PD-1 인간 모노클로날 항체는 하기 특징 중 1개 이상을 나타내는 것으로 입증되었다: (a) 비아코어 분석에 의해 결정된 바와 같이 적어도 약 107 M-1, 또는 약 109 M-1, 또는 약 1010 M-1 to 1011 M-1 또는 그 초과의 평형 회합 상수 (Ka)에 의해 반영되는 결합 친화도로 인간 CTLA-4에 특이적으로 결합함; (b) 적어도 약 103, 약 104, 또는 약 105 m-1 s-1의 동역학적 회합 상수 (ka); (c) 적어도 약 103, 약 104, 또는 약 105 m-1 s-1의 동역학적 해리 상수 (k d ); 및 (d) CTLA-4의 B7-1 (CD80) 및 B7-2 (CD86)에 대한 결합을 억제함. 본 개시내용에 유용한 항-CTLA-4 항체는 인간 CTLA-4에 특이적으로 결합하고 상기 특징 중 적어도 1개, 적어도 2개, 또는 적어도 3개를 나타내는 모노클로날 항체를 포함한다.
예시적인 임상 항-CTLA-4 항체는 미국 특허 번호 6,984,720에 개시된 바와 같은 인간 모노클로날 항체 10D1 (현재 이필리무맙으로 공지되고 예르보이®로서 시판됨)이다. 이필리무맙은 본원에 개시된 방법에 사용하기 위한 항-CTLA-4 항체이다. 이필리무맙은 CTLA-4의 그의 B7 리간드에의 결합을 차단함으로써 T 세포 활성화를 자극하고 진행성 흑색종을 갖는 환자의 전체 생존 (OS)을 개선시키는 완전 인간 IgG1 모노클로날 항체이다.
본 방법에 유용한 또 다른 항-CTLA-4 항체는 트레멜리무맙 (또한 CP-675,206으로 공지됨)이다. 트레멜리무맙은 인간 IgG2 모노클로날 항-CTLA-4 항체이다. 트레멜리무맙은 WO/2012/122444, 미국 공개 번호 2012/263677, 또는 WO 공개 번호 2007/113648 A2에 기재되어 있다.
개시된 조성물에 유용한 항-CTLA-4 항체는 또한, 인간 CTLA-4에 특이적으로 결합하고 인간 CTLA-4에의 결합에 대해 이필리무맙 또는 트레멜리무맙과 교차-경쟁하거나 또는 이필리무맙 또는 트레멜리무맙과 동일한 인간 CTLA-4의 에피토프 영역에 결합하는 단리된 항체를 포함한다. 특정 실시양태에서, 인간 CTLA-4에의 결합에 대해 이필리무맙 또는 트레멜리무맙과 교차-경쟁하거나, 또는 그와 동일한 인간 CTLA-4의 에피토프 영역에 결합하는 항체는 인간 IgG1 이소형의 중쇄를 포함하는 항체이다. 인간 대상체에 대한 투여의 경우, 이들 교차-경쟁 항체는 키메라 항체, 또는 인간화 또는 인간 항체이다. 유용한 항-CTLA-4 항체는 또한, 상기 항체의 항원-결합 부분, 예컨대 Fab, F(ab')2, Fd, 또는 Fv 단편을 포함한다.
암 및 표준 관리 요법
일부 실시양태에서, 본원에 개시된 방법은 표준 관리 요법 대신에 사용된다. 특정 실시양태에서, 표준 관리 요법은 본원에 개시된 임의의 방법과 조합되어 사용된다. 상이한 유형의 암에 대한 표준 관리 요법은 관련 기술분야의 통상의 기술자에게 널리 공지되어 있다. 예를 들어, 미국 내 21개 주요 암 센터의 연합인 국립 종합 암 네트워크 (NCCN)는 광범위한 암에 대한 표준 관리 치료에 관한 상세한 최신 정보를 제공하는 NCCN 종양학 임상 관리기준 가이드라인 (NCCN 가이드라인즈(NCCN GUIDELINES)®)을 공개한다 (NCCN 가이드라인즈® (2014) 참조).
제약 조성물 및 투여량
본 개시내용의 치료제는 조성물, 예를 들어 항체 및 제약상 허용되는 담체를 포함하는 제약 조성물 중에 구성될 수 있다. 본원에 사용된 "제약상 허용되는 담체"는 생리학상 상용성인 임의의 및 모든 용매, 분산 매질, 코팅, 항박테리아제 및 항진균제, 등장화제 및 흡수 지연제 등을 포함한다. 일부 실시양태에서, 항체를 함유하는 조성물에 대한 담체는 정맥내, 근육내, 피하, 비경구, 척수 또는 표피 투여 (예를 들어, 주사 또는 주입에 의함)에 적합하다. 본 개시내용의 제약 조성물은 1종 이상의 제약상 허용되는 염, 항산화제, 수성 및 비수성 담체, 및/또는 아주반트, 예컨대 보존제, 습윤제, 유화제 및 분산제를 포함할 수 있다.
투여 요법은 최적의 목적하는 반응, 예를 들어 최대의 치료 반응 및/또는 최소의 유해 효과를 제공하도록 조정된다. 일부 실시양태에서, 항-PD-1 항체는 중량-기준 용량으로 투여된다. 항-PD-1 항체의 투여의 경우, 투여량은 적어도 약 0.01 내지 적어도 약 20 mg/kg, 적어도 약 0.1 내지 적어도 약 10 mg/kg 대상체 체중의 범위일 수 있다. 예를 들어, 투여량은 적어도 약 0.1 mg/kg, 적어도 약 0.3 mg/kg, 적어도 약 1 mg/kg, 적어도 약 2 mg/kg, 적어도 약 3 mg/kg, 적어도 약 5 mg/kg, 또는 적어도 약 10 mg/kg 체중일 수 있다. 특정 실시양태에서, 항-PD-1 항체의 투여량은 3 mg/kg 체중이다. 특정 실시양태에서, 항-PD-1 항체는 균일 용량으로 투여된다. 특정 실시양태에서, 항-PD-1 항체의 균일 용량은 적어도 약 100-300 mg, 예컨대 적어도 약 200-300 mg, 적어도 약 220-260 mg, 적어도 약 230-250 mg 또는 적어도 약 240 mg, 예컨대 적어도 약 60 mg, 적어도 약 80 mg, 적어도 약 100 mg, 적어도 약 120 mg, 적어도 약 140 mg, 적어도 약 160 mg, 적어도 약 180 mg, 적어도 약 200 mg, 적어도 약 220 mg, 적어도 약 240 mg, 적어도 약 260 mg, 적어도 약 280 mg 또는 적어도 약 300 mg의 용량 (예를 들어, 균일 용량)이다. 일부 실시양태에서, 항-PD-1 항체는 항-CTLA-4 항체와 함께 고정 용량으로 투여된다. 일부 실시양태에서, 항-PD-1 항체 (mg) 대 항-CTLA-4 항체 (mg)의 비는 적어도 약 1:1, 약 1:2, 약 1:3, 약 1:4, 약 1:5, 약 1:6, 약 1:7, 약 1:8, 약 1:9, 약 1:10, 약 1:15, 약 1:20, 약 1:30, 약 1:40, 약 1:50, 약 1:60, 약 1:70, 약 1:80, 약 1:90, 약 1:100, 약 1:120, 약 1:140, 약 1:160, 약 1:180, 약 1:200, 약 200:1, 약 180:1, 약 160:1, 약 140:1, 약 120:1, 약 100:1, 약 90:1, 약 80:1, 약 70:1, 약 60:1, 약 50:1, 약 40:1, 약 30:1, 약 20:1, 약 15:1, 약 10:1, 약 9:1, 약 8:1, 약 7:1, 약 6:1, 약 5:1, 약 4:1, 약 3:1, 또는 약 2:1이다.
투여 스케줄은 전형적으로 항체의 전형적인 약동학적 특성에 기초하여 지속적인 수용체 점유율 (RO)을 유발하는 노출을 달성하도록 설계된다. 예시적인 치료 요법은 1주 1회, 약 2주마다 1회, 약 3주마다 1회, 약 4주마다 1회, 약 1개월에 1회, 약 3-6개월 또는 더 긴 기간마다 1회 투여하는 것을 수반한다. 특정 실시양태에서, 항-PD-1 항체, 예컨대 니볼루맙은 대상체에게 약 2주마다 1회 투여된다. 다른 실시양태에서, 항체는 약 3주마다 1회 투여된다. 투여량 및 스케줄링은 치료 과정 동안 변경될 수 있다.
다른 항암제와 조합되어 사용되는 경우, 항-PD-1 항체의 투여량은 단독요법 용량과 비교하여 더 낮아질 수 있다. 전형적인 3 mg/kg 미만, 그러나 0.001 mg/kg 이상인 니볼루맙의 투여량이 치료량 미만의 투여량이다. 본원의 방법에서 사용되는 항-PD-1 항체의 치료량 미만의 용량은 0.001 mg/kg 초과 및 3mg/kg 미만이다. 일부 실시양태에서, 치료량 미만의 용량은 약 0.001 mg/kg 내지 약 1 mg/kg, 약 0.01 mg/kg 내지 약 1 mg/kg, 약 0.1 mg/kg 내지 약 1 mg/kg, 또는 약 0.001 mg/kg 내지 약 0.1 mg/kg 체중이다. 일부 실시양태에서, 치료량 미만의 용량은 적어도 약 0.001 mg/kg, 적어도 약 0.005 mg/kg, 적어도 약 0.01 mg/kg, 적어도 약 0.05 mg/kg, 적어도 약 0.1 mg/kg, 적어도 약 0.5 mg/kg, 또는 적어도 약 1.0 mg/kg 체중이다. 0.3 mg/kg 내지 10 mg/kg의 니볼루맙 투여를 받은 15명의 대상체로부터의 수용체-점유율 데이터는, 이 용량 범위에서 PD-1 점유율이 용량-비의존성인 것으로 보인다는 것을 나타낸다. 모든 용량에 걸쳐, 평균 점유율은 85% (범위, 70% 내지 97%)이고, 이때 평균 플래토 점유율은 72% (범위, 59% 내지 81%)였다. 일부 실시양태에서, 0.3 mg/kg 투여는 최대 생물학적 활성에 이르기에 충분한 노출을 가능하게 할 수 있다.
일부 실시양태에서, 항-CTLA-4 항체는 중량-기준 용량으로 투여된다. 항-CTLA-4 항체의 투여의 경우 투여량은 약 0.01 내지 약 20 mg/kg, 약 0.05 내지 약 20 mg/kg, 약 0.1 내지 약 20 mg/kg, 약 0.1 내지 약 15 mg/kg, 약 0.1 내지 약 10 mg/kg, 약 0.1 내지 약 5 mg/kg, 및 약 1 내지 약 10 mg/kg 대상체 체중 범위일 수 있다. 예를 들어, 투여량은 약 0.05 mg/kg, 약 0.1 mg/kg, 약 0.5 mg/kg, 약 1 mg/kg, 약 2 mg/kg, 약 3 mg/kg, 약 4 mg/kg, 약 5 mg/kg, 약 6 mg/kg, 약 7 mg/kg, 약 8 mg/kg, 약 9 mg/kg, 약 10 mg/kg, 약 11 mg/kg, 약 12 mg/kg, 약 13 mg/kg, 약 14 mg/kg, 약 15 mg/kg 또는 약 20 mg/kg 대상체 체중일 수 있다. 일부 실시양태에서, 항-CTLA-4 항체의 투여량은 0.1 mg/kg 체중이다. 다른 실시양태에서, 항-CTLA-4 항체의 투여량은 1 mg/kg 체중이다. 추가 실시양태에서, 항-CTLA-4 항체의 투여량은 10 mg/kg 체중이다. 특정 실시양태에서, 항-CTLA-4 항체는 균일 용량으로 투여된다. 실시양태에서, 항-CTLA-4의 균일 용량은 적어도 약 60-1500 mg, 예컨대 적어도 약 100-1400 mg, 적어도 약 100-1000 mg, 적어도 약 200-1000 mg 또는 적어도 약 200-500 mg, 예컨대 적어도 약 60 mg, 적어도 약 80 mg, 적어도 약 100 mg, 적어도 약 120 mg, 적어도 약 140 mg, 적어도 약 160 mg, 적어도 약 180 mg, 적어도 약 200 mg, 적어도 약 220 mg, 적어도 약 240 mg, 적어도 약 260 mg, 적어도 약 280 mg, 적어도 약 300 mg, 적어도 약 320 mg, 적어도 약 340 mg, 적어도 약 360 mg, 적어도 약 380 mg, 적어도 약 400 mg, 적어도 약 420 mg, 적어도 약 440 mg, 적어도 약 460 mg, 적어도 약 480 mg, 적어도 약 500 mg, 적어도 약 600 mg, 적어도 약 700 mg, 적어도 약 800 mg, 적어도 약 900 mg, 적어도 약 1000 mg, 적어도 약 1100 mg, 적어도 약 1200 mg, 적어도 약 1300 mg, 적어도 약 1400 mg, 또는 적어도 약 1500 mg의 용량 (예를 들어, 균일 용량)이다.
예시적인 치료 요법은 1주 1회, 약 2주마다 1회, 약 3주마다 1회, 약 4주마다 1회, 약 1개월에 1회, 약 3-6개월 또는 더 긴 기간마다 1회 투여하는 것을 수반한다. 특정 실시양태에서, 항-CTLA-4 항체는 약 3주마다 1회 투여된다.
일부 실시양태에서, 항-CTLA-4 항체의 치료량 미만의 용량이 본원의 방법에 사용된다. 본원의 방법에 사용된 항-CTLA-4 항체의 치료량 미만의 투여량은 0.001 mg/kg 초과 및 10 mg/kg 미만이다. 일부 실시양태에서, 치료량 미만의 용량은 약 0.001 mg/kg 내지 약 10 mg/kg, 약 0.01 mg/kg 내지 약 10 mg/kg, 약 0.01 mg/kg 내지 약 1 mg/kg, 약 0.1 mg/kg 내지 약 1 mg/kg, 또는 약 0.001 mg/kg 내지 약 0.1 mg/kg 체중이다. 일부 실시양태에서, 치료량 미만의 용량은 적어도 약 0.001 mg/kg, 적어도 약 0.005 mg/kg, 적어도 약 0.01 mg/kg, 적어도 약 0.05 mg/kg, 적어도 약 0.1 mg/kg, 적어도 약 0.5 mg/kg, 적어도 약 1.0 mg/kg, 적어도 약 2 mg/kg, 적어도 약 3 mg/kg, 적어도 약 4 mg/kg, 적어도 약 5 mg/kg, 적어도 약 6 mg/kg, 적어도 약 7 mg/kg, 적어도 약 8 mg/kg, 적어도 약 9 mg/kg, 또는 적어도 약 10 mg/kg 체중이다. 일부 실시양태에서, 치료량 미만의 용량은 약 10 mg/kg, 약 5 mg/kg, 약 2 mg/kg, 약 1 mg/kg, 약 0.1 mg/kg, 또는 약 0.01 mg/kg 체중이다.
특정 실시양태에서, 적어도 약 0.1 내지 약 10 mg/kg의 적어도 항-CTLA-4 항체 및 적어도 약 0.1 내지 약 10 mg/kg의 항-PD1 항체는 약 3주마다 1회 대상체에게 투여된다. 특정 실시양태에서, 적어도 약 1 mg/kg의 항-CTLA-4 항체 및 적어도 약 1 mg/kg의 항-PD1 항체는 약 3주마다 1회 대상체에게 투여된다. 특정 실시양태에서, 적어도 약 1 mg/kg의 항-CTLA-4 항체 및 적어도 약 3 mg/kg의 항-PD1 항체는 약 3주마다 1회 대상체에게 투여된다. 특정 실시양태에서, 적어도 약 3 mg/kg의 항-CTLA-4 항체 및 적어도 약 1 mg/kg의 항-PD-1 항체는 약 3주마다 1회 대상체게 투여된다. 특정 실시양태에서, 적어도 약 3 mg/kg의 항-CTLA-4 항체 및 적어도 약 3 mg/kg의 항-PD1 항체는 약 3주마다 1회 대상체에게 투여된다. 실시양태에서, 항-CTLA-4 항체는 이필리무맙이다. 일부 실시양태에서, 항-PD-1 항체는 니볼루맙이다.
특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체의 조합은 총 12주 동안 약 3주마다 1회 대상체에게 정맥내로 투여된다. 일부 실시양태에서, 12주 주기는 3 또는 4회 반복된다. 일부 실시양태에서, 대상체는 총 12주 동안 3주마다 항-PD-1 항체 및 항-CTLA-4 항체의 조합으로 치료되고, 3회의 12-주 주기가 수행된다. 실시양태에서, 대상체는 총 12주 동안 3주마다 항-PD-1 항체 및 항-CTLA-4 항체의 조합으로 치료되고, 4회의 12-주 주기가 수행된다. 실시양태에서, 대상체는 12회의 12-주 주기 동안 항-PD1 항체로 치료된다.
특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체의 투여 후 항-PD-1 항체 단독요법이 이어진다. 일부 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체의 조합 요법 후 항체 단독요법은 항-PD-1 항체를 약 1 mg/kg 체중, 약 2 mg/kg 체중, 약 3 mg/kg 체중, 약 4 mg/kg 체중, 약 5 mg/kg 체중, 약 6 mg/kg 체중, 약 7 mg/kg 체중, 약 8 mg/kg 체중, 약 9 mg/kg 체중, 또는 약 10 mg/kg 체중의 용량으로 투여하는 것을 포함한다. 일부 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체의 조합 요법 후에 제공되는 항-PD-1 단독요법은 약 1, 2, 3 또는 4주마다 1회 투여된다. 특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체의 조합 요법 후에 제공되는 항-PD-1 항체 단독요법은 2주마다 1회 약 3 mg/kg 체중의 용량으로 투여된다.
다른 실시양태에서, 항-PD-1 항체는 3주마다 1회 3 mg/kg으로 투여되고, 항-CTLA-4 항체는 3주마다 1회 1 mg/kg으로 투여된다. 특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 각각 1회 용량, 각각에 대해 2회 용량, 각각에 대해 3회 용량, 각각에 대해 4회 용량, 각각에 대해 5회 용량, 각각에 대해 6회 용량, 각각에 대해 7회 용량, 각각에 대해 8회 용량, 각각에 대해 9회 용량, 또는 각각에 대해 10회 용량에 대해 조합되어 투여된다. 특정한 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 각각에 대해 4회 용량에 대해 조합되어 투여된다. 특정 실시양태에서, 대상체는 항-PD-1 항체 및 항-CTLA-4 항체의 조합 요법 전 및/또는 후에, 2주마다 1회 3 mg/kg의 용량의 항-PD-1 항체가 투여된다. 특정한 실시양태에서, MSI-H를 갖는 결장직장암을 앓는 대상체는 초기 단계 (예를 들어, 항-PD-1 항체 단독요법, 예를 들어 2주마다 1회 3 mg/kg의 용량의 니볼루맙), 조합 단계 (예를 들어, 항-PD-1 항체 및 항-CTLA-4 항체 조합, 예를 들어 3주마다 1회 3 mg/kg의 용량의 니볼루맙 및 매주 1회 1 mg/kg의 용량의 이필리무맙), 및 최종 단계 (예를 들어, 항-PD-1 항체 단독요법, 예를 들어 2주마다 1회 3 mg/kg의 용량의 니볼루맙)로 치료된다.
치료는 임상 이익이 관찰되는 한 또는 허용되지 않는 독성 또는 질환 진행이 발생할 때까지 계속될 수 있다. 특정 실시양태에서, 항-PD-1 항체는 임상 시험에서 단독요법으로서 가장 높은 효능을 생성하는 것으로 밝혀진 투여량, 예를 들어 약 3주마다 1회 투여되는 약 3 mg/kg의 니볼루맙 (Topalian et al., 2012 N Engl J Med 366:2443-54; Topalian et al., 2012 Curr Opin Immunol 24:207-12), 또는 유의하게 더 낮은 용량으로, 즉 치료량 미만의 용량으로 투여될 수 있다.
본 개시내용의 제약 조성물 중 활성 성분의 실제 투여량 수준은 환자에게 과도하게 독성이지 않으면서, 특정한 환자, 조성물 및 투여 방식에 대해 목적하는 치료 반응을 달성하는데 효과적인 활성 성분의 양을 수득하도록 달라질 수 있다. 선택된 투여량 수준은 사용되는 본 개시내용의 특정한 조성물의 활성, 투여 경로, 투여 시간, 사용되는 특정한 화합물의 배출 속도, 치료 지속기간, 사용되는 특정한 조성물과 조합되어 사용되는 다른 약물, 화합물 및/또는 물질, 치료되는 환자의 연령, 성별, 체중, 상태, 전반적 건강 및 과거 병력, 및 의학 기술분야에 널리 공지되어 있는 기타 인자를 포함한 다양한 약동학적 인자에 좌우될 것이다. 본 개시내용의 조성물은 관련 기술분야에 널리 공지된 다양한 방법 중 1종 이상을 사용하여 1종 이상의 투여 경로를 통해 투여될 수 있다. 통상의 기술자에 의해 인지될 바와 같이, 투여 경로 및/또는 방식은 목적하는 결과에 따라 달라질 것이다.
키트
또한 치료 용도를 위한 항-PD-1 항체 및 또 다른 항암제를 포함하는 키트가 본 개시내용의 범주 내에 있다. 키트는 전형적으로, 키트의 내용물의 의도된 사용을 나타내는 라벨 및 사용에 대한 지침서를 포함한다. 용어 라벨은 키트 상에 또는 키트와 함께 공급되거나, 또는 달리 키트에 동반되는 임의의 문서 또는 기록물을 포함한다. 따라서, 본 개시내용은 (a) 약 0.1 mg/kg 내지 약 10 mg/kg 범위의 투여량의 항-PD-1 항체 또는 그의 항원-결합 부분; 및 (b) 본원에 개시된 임의의 단독요법 방법에서 항-PD-1 항체를 사용하는 것에 대한 지침서를 포함하는, 결장직장암으로부터 유래된 종양을 앓는 대상체를 치료하기 위한 키트를 제공한다. 다른 실시양태에서, 결장직장암으로부터 유래된 종양을 앓는 대상체를 치료하기 위한 키트는 (a) 약 0.1 mg/kg 내지 약 10 mg/kg 범위의 투여량의 항-PD-1 항체 또는 그의 항원-결합 부분; 및 (b) 약 0.1 mg/kg 내지 약 10 mg/kg 범위의 투여량의 항-CTLA-4 항체 또는 그의 항원-결합 부분; 및 (c) 본원에 개시된 임의의 조합 요법 방법에서 항-PD-1 항체 및 항-CTLA-4 항체를 사용하는 것에 대한 지침서를 포함한다. 특정 실시양태에서, 항-PD-1 항체 및 항-CTLA-4 항체는 단위 투여 형태로 공동-패키징될 수 있다. 인간 환자를 치료하기 위한 특정 실시양태에서, 키트는 본원에 개시된 항-인간 PD-1 항체, 예를 들어 니볼루맙, 펨브롤리주맙, MEDI0608 (이전에 AMP-514), AMP-224 또는 BGB-A317을 포함한다. 다른 실시양태에서, 키트는 본원에 개시된 항-인간 CTLA-4 항체, 예를 들어 이필리무맙 또는 트레멜리무맙을 포함한다.
본 개시내용은 추가의 제한으로 해석되어서는 안되는 하기 실시예에 의해 추가로 예시된다. 본 출원 전반에 걸쳐 인용된 모든 참고문헌의 내용은 명백히 본원에 참조로 포함된다.
보다 먼저 제출된 출원에 대한 상호-참조: 본 출원은 2016년 6월 3일 출원된 미국 가출원 번호 62/345,662에 대한 우선권을 주장하며, 상기 가출원은 그 전문이 본원에 참조로 포함된다.
실시예
실시예 1
높은 미소위성체 불안정성을 갖는 및 갖지 않는 전이성 결장직장암을 갖는 환자의 치료에서의 니볼루맙 ± 이필리무맙의 임상 사례 연구
환자는 하기 기준에 기초하여 본 연구에 포함시키기에 적격이었다: 1) 조직학적으로 확인된 결장직장암; 2) 고형 종양의 반응 평가 기준 (RECIST) 1.1에 의해 측정가능한 재발성 또는 전이성 질환; 3) 환자는 동부 협동 종양학 그룹 (ECOG) 점수 0-1을 갖는 적어도 18세의 성인임; 및 4) ≥ 1종의 선행 치료 요법 후 (미소위성체 불안정성-높은 환자의 경우) 또는 최근의 치료 후 (모든 환자의 경우) 질환 진행 또는 화학요법을 받는데 불내성 또는 거부. 환자는 하기 기준에 기초하여 연구로부터 배제되었다: 1) 중추 신경계 침범; 2) 3년 이내 악성종양의 병력; 3) 자가면역 질환의 활성 또는 병력; 4) 코르티코스테로이드를 포함한 면역억제 의약을 사용한 치료에 대한 필요; 또는 5) T-세포 공동자극 또는 면역 체크포인트 경로를 표적화하는 선행 치료.
환자의 결장직장암은 폴리머라제 연쇄 반응 (PCR)에 의해 시험된 5종의 유전자좌 중에서 2종 이상의 마커가 불안정성을 나타낸 경우 또는 5종 이상의 유전자좌가 시험되었을 때 마커의 적어도 30%가 불안정성을 나타낸 경우 미소위성체 불안정성-높은 (MSI-H) 것으로 결정되었다. 환자의 결장직장암은 또한 면역조직화학 (IHC)에 의해 1종 이상의 마커의 상실이 존재한 경우 MSI-H인 것으로 결정되었다.
비-MSI-H이고 0-1의 ECOG 수행 상태를 갖는 3L 이후의 결장암을 갖는 환자를 환자의 미소위성체 안정한 (MSS) 코호트에 포함시키기 위해 선택하였다. 선택된 MSS 환자에게 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 1 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 이러한 치료의 초기 단계로부터 6주 이상 후에, 초기 치료 요법을 허용한 MSS 환자를 2개의 치료군으로 분할하였다. 하나의 치료군에서, 10명의 MSS 환자에게 총 4회 용량에 대해 3주마다 1회 3 mg/kg 이필리무맙과 조합된 1 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 제2 치료군에서, 10명의 MSS 환자에게 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 3 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg을 투여하였다. 종합적으로, 이들 치료군은 MSS 환자에서 독립적 안전성 부문으로서의 역할을 하였고, MSI-H 환자에서 사용하기 위한 이필리무맙과 조합된 니볼루맙의 용량에 관한 정보를 제공하였다. 도 1은 MSS 코호트에서의 환자에 대한 전체 연구 설계를 보여준다.
적어도 1개의 표적 병변을 갖고 0-1의 ECOG 수행 상태를 갖는, 전이성 질환에 대한 적어도 1종의 선행 치료를 받은 제2 MSI-H 결장암을 갖는 환자를 환자의 MSI-H 코호트에 포함시키기 위해 선택하였다. 19명의 MSI-H 환자에게 치료의 초기 단독요법 단계 (m단계 1)에서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 이어서, 양성 반응을 나타내는 특정 MSI-H 환자를 치료의 조합 요법 단계 (c단계 1)에 포함시키기 위해 선택하였다. 이어서, 19명의 이들 MSI-H 환자에게 c단계 1에서 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 3 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. c단계 1로부터의 양성 반응을 갖는 다수의 환자가 현재 조합 요법의 제2 단계 (c단계 2)에 등록되고 있다. c단계 2에서, 48명의 환자 (c단계 1로부터의 19명의 환자 플러스 29명의 추가의 환자)는 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 3 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 받을 것이다. m단계 1에서 양성 반응을 나타내는 환자의 별개의 군을 단독요법의 제2 단계 (m단계 2)에 포함시키기 위해 선택하였다. m단계 2에서, 48명의 환자 (m단계 1로부터의 19명의 환자 플러스 29명의 새로운 환자)에게 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 도 2는 MSI-H 코호트에서의 환자에 대한 전체 연구 설계를 보여준다.
이 연구의 1차 종점은 MSI-H 환자에서 RECIST 1.1을 사용하여 연구자-평가된 객관적 반응률 (ORR)을 결정하는 것이었다. 이 연구의 2차 종점은 환자에서 독립적 방사선학 검토 위원회-평가된 ORR을 결정하는 것이었다. 이 연구의 탐색적 종점은 안전성 및 내약성, MSS 환자에서의 무진행 생존 (PFS), 전체 생존 (OS), 연구자-평가된 ORR, 및 바이오마커의 평가를 포함하였다.
이 연구 동안 수집된 환자 인구통계는 중앙 연령, 65세 이하의 환자의 수, 남성 환자의 수, 특정한 인종의 환자의 수, 및 0 또는 1의 ECOG 점수를 갖는 환자의 수를 포함하였다. 표 1은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자와 비교하여 3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대한 인구통계를 제시한다. 표 2는 또한 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSS 환자와 비교하여 1 mg/kg 니볼루맙을 3 mg/kg 이필리무맙과 조합하여 받는 MSS 환자에 대한 인구통계를 제시한다.
표 2. MSI-H 또는 MSS 결장직장암을 갖는 환자에 대한 인구통계.
질환 특징 및 선행 요법에 대해 수집된 데이터는 진단시 특정한 질환 병기를 갖는 환자의 수, 특정한 돌연변이 상태를 갖는 환자의 수, 선행 치료를 받는 환자의 수, 선행 수술을 받는 환자의 수, 및 선행 방사선요법을 받는 환자의 수를 포함하였다. 표 3은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자와 비교하여 3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대한 질환 특징 및 선행 요법을 제시한다. 표 3은 또한 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSS 환자와 비교하여 1 mg/kg 니볼루맙을 3 mg/kg 이필리무맙과 조합하여 받는 MSS 환자에 대한 질환 특징 및 선행 요법을 제시한다.
표 3. MSI-H 또는 MSS 결장직장암을 갖는 환자에 대한 질환 특징 및 선행 요법.
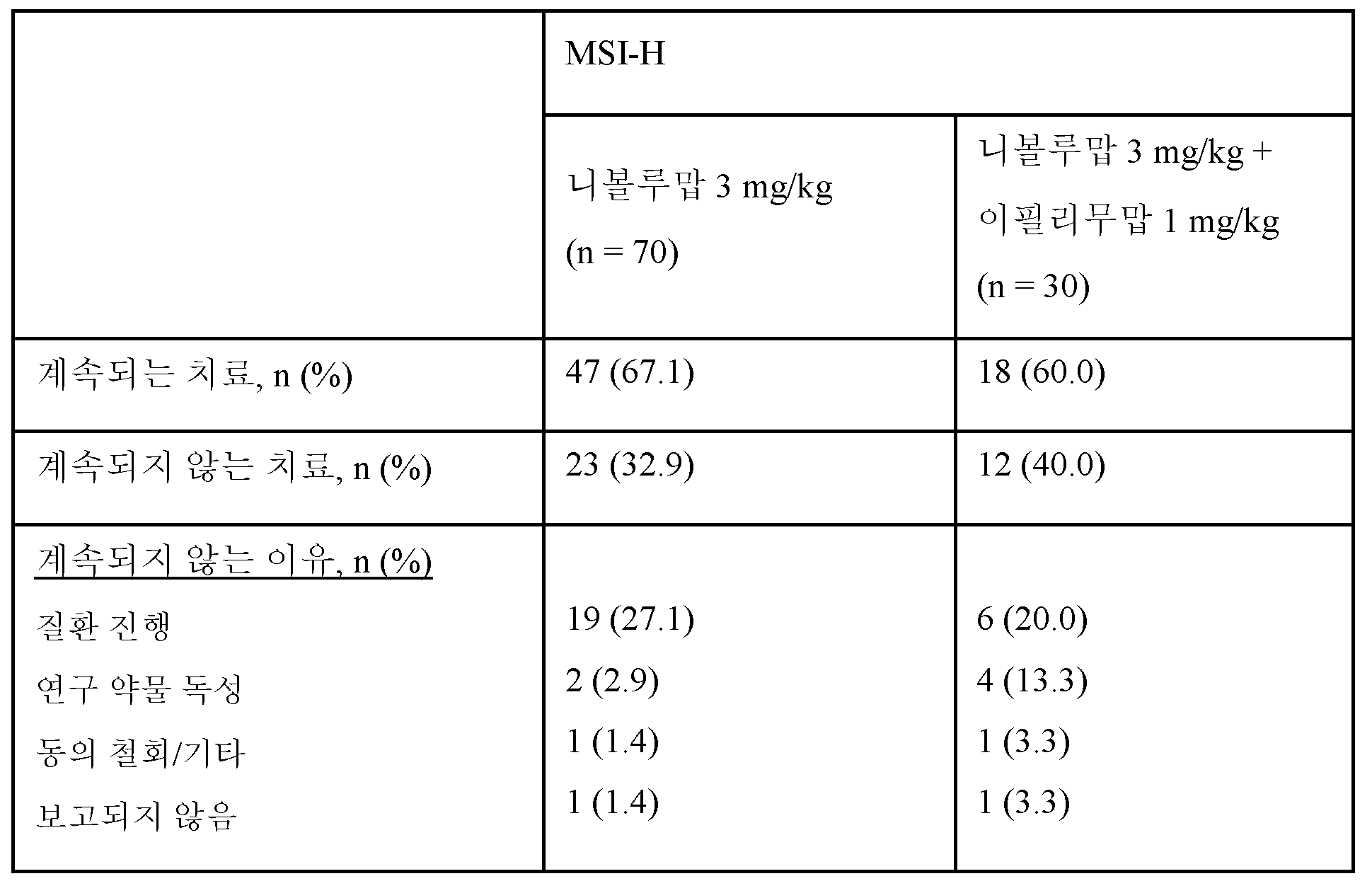
이 연구에서 수집된 MSI-H 환자의 배치에 관한 데이터는 치료가 계속되는 환자의 수, 치료가 계속되지 않는 환자의 수, 및 질환 진행, 연구 약물 독성, 동의 철회 또는 다른 이유로 인해, 또는 보고되지 않은 이유로 치료가 계속되지 않는 환자의 수를 포함하였다. 표 4는 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자와 비교하여 3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대한 환자 배치를 제시한다.
표 4. MSI-H 환자 배치.
3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에서의 연구자-평가된 최상의 전체 반응을 객관적 반응률, 중앙 반응까지의 시간 및 중앙 반응 지속기간에 의해 결정하였다. 표 5에 제시된 바와 같이, 47명의 환자 중 12명 (25.5%)은 3 mg/kg 니볼루맙 단독요법에 대해 객관적 반응을 나타냈으며, 이때 중앙 반응까지의 시간은 치료 후 2.12개월에 발생하였다. 도 3은 3 mg/kg 니볼루맙 단독요법을 받는 개별 환자에 대한 기준선으로부터의 퍼센트 변화를 보여준다.
표 5. 니볼루맙 단독요법을 받는 MSI-H 환자에서의 연구자-평가된 최상의 전체 반응.
3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자에서의 연구자-평가된 최상의 전체 반응을 객관적 반응률, 중앙 반응까지의 시간 및 중앙 반응 지속기간에 의해 결정하였다. 표 6에 제시된 바와 같이, 27명의 환자 중 9명 (33.3%)은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 사용한 치료에 대해 객관적 반응을 나타냈으며, 이때 중앙 반응까지의 시간은 치료 후 2.73개월에 발생하였다. 도 4는 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 개별 환자에 대한 기준선으로부터의 퍼센트 변화를 보여준다.
표 6. 니볼루맙을 이필리무맙과 조합하여 받는 MSI-H 환자에서의 연구자-평가된 최상의 전체 반응.
3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대한 표적 병변 크기의 최상의 감소를, 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자에 대한 표적 병변 크기의 최상의 감소와 비교하였다. 도 5에 제시된 바와 같이, 3 mg/kg 니볼루맙 단독요법을 받는 환자의 56%가 기준선으로부터 표적 병변 크기의 감소를 나타냈고, 반면에 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 환자의 81%가 기준선으로부터 표적 병변 크기의 감소를 나타냈다.
연구자-평가된 PFS를, 3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대해서는 6개월, 9개월 및 12개월에 측정하고, 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자에 대해서는 6개월에 측정하였다. 표 7에 제시된 바와 같이, 3 mg/kg 니볼루맙 단독요법을 받는 환자의 45.9%가 6개월에 무진행 생존을 나타냈고, 반면에 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 환자의 66.6%가 6개월에 무진행 생존을 나타냈다. 도 6은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 경우와 비교하여 3 mg/kg 니볼루맙 단독요법을 받는 경우에 무진행 생존을 나타내는 환자의 백분율을 보여준다.
표 7. MSI-H 환자에서의 연구자-평가된 무진행 생존.
OS를, 3 mg/kg 니볼루맙 단독요법을 받는 MSI-H 환자에 대해서는 6개월, 9개월 및 12개월에 측정하고, 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자에 대해서는 6개월 및 9개월에 측정하였다. 표 8에 제시된 바와 같이, 3 mg/kg 니볼루맙 단독요법을 받는 환자의 75.0%가 6개월에 무진행 생존을 나타냈고, 반면에 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 환자의 85.1%가 6개월에 무진행 생존을 나타냈다. 9개월에, 3 mg/kg 니볼루맙 단독요법을 받는 환자의 65.6%가 무진행 생존을 나타냈고, 반면에 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 환자의 85.1%가 무진행 생존을 나타냈다. 도 7은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 경우와 비교하여 3 mg/kg 니볼루맙 단독요법을 받는 경우에 전체 생존을 나타내는 환자의 백분율을 보여준다.
표 8. MSI-H 환자에서의 전체 생존.
MSS 결장직장암 환자에서의 치료 효능을 ORR, PFS 및 OS에 의해 측정하였다. 표 9는 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSS 환자와 비교하여 1 mg/kg 니볼루맙을 3 mg/kg 이필리무맙과 조합하여 받는 MSS 환자에서의 효능 데이터의 요약을 제시한다.
표 9. MSS 결장직장암 환자에서의 효능의 요약.
MSI-H 결장직장암 환자의 ≥ 15%에서 관찰된 치료-관련 유해 사건은 피로, 설사, 소양증, 오심, 발열 및 구토를 포함하였다. 표 10은 3 mg/kg 니볼루맙을 1 mg/kg 이필리무맙과 조합하여 받는 MSI-H 환자와 비교하여 3 mg/kg 니볼루맙을 받는 MSI-H 환자의 ≥ 15%에서의 치료-관련 유해 사건을 제시한다.
표 10. MSI-H 환자의 ≥ 15%에서의 치료-관련 유해 사건.
MSS 결장직장암 환자의 ≥ 15%에서 관찰된 치료-관련 유해 사건은 설사, 무력증, 오심, 발열, 구토, 피로, 피부 건조 및 기침을 포함하였다.
이 연구의 결과는 MSI-H 상태를 갖는 환자에서 니볼루맙 단독요법의 고무적인 활성을 입증하였다. 니볼루맙 및 이필리무맙의 조합은 또한 유망한 예비 활성을 입증하였다. 이 연구의 결과는 니볼루맙 단독요법 및 니볼루맙 + 이필리무맙 조합 요법에 대한 반응이 지속적이었다는 것을 나타냈다. 니볼루맙 및 니볼루맙과 이필리무맙의 조합은 임상 이익과 관련하여 허용되는 안전성 프로파일을 입증하였고, 다른 고형 종양에서의 관찰과 일치하였다. 이러한 결과는 고무적이고, MSI-H 전이성 결장직장암 및 잠재적으로 미스매치 복구 결함을 갖는 다른 종양을 갖는 환자에서 니볼루맙 단독요법 및 니볼루맙 + 이필리무맙 조합 요법의 계속된 평가를 지지한다.
실시예 2
결함성 DNA 미스매치 복구/높은 미소위성체 불안정성 전이성 결장직장암을 갖는 환자의 치료에서의 니볼루맙 + 이필리무맙의 확장된 임상 사례 연구
실시예 1에 기재된 임상 사례 연구에 추가로, 이필리무맙과 조합된 니볼루맙의 효능 및 안전성을, 데이터 컷-오프 적어도 6개월 전에 제1 치료 용량을 받은 DNA 미스매치 복구-결함성/미소위성체 불안정성-높은 (dMMR/MSI-H) 전이성 결장직장암 (mCRC)을 갖는 환자의 확장된 집단에서 연구하였다. 환자는 하기 기준에 기초하여 이 연구에 포함시키기에 적격이었다: 1) 조직학적으로 확인된 전이성/재발성 결장직장암; 2) 지역 실험실에 의해 나타내어진 dMMR/MSI-H; 및 3) 적어도 1차의 선행 요법.
도 8은 치료의 단독요법 부문 또는 조합 요법 부문에 포함된 환자에 대한 전체 연구 설계를 보여준다. 간략하게, 단독요법 부문에 포함된 환자에게 치료의 단계 1에서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 19명의 확인된 반응자 중 적어도 7명이 존재한 경우에, 치료의 제2 단계 동안 등록을 계속하였다. 치료의 단계 2에서, 환자에게 2주마다 1회 3 mg/kg 니볼루맙 투여하였다. 환자는 치료의 단계 1에서 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 3 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 투여하는 별개의 조합 부문을 포함하였다. 19명의 확인된 반응자 중 적어도 7명이 존재한 경우, 치료의 제2 단계 동안 등록을 계속하였다. 치료의 단계 2에서, 환자에게 총 4회 용량에 대해 3주마다 1회 1 mg/kg 이필리무맙과 조합된 3 mg/kg 니볼루맙, 이어서 2주마다 1회 3 mg/kg 니볼루맙을 투여하였다. 연구 설계에 관한 추가의 세부사항은 문헌 [Overman M et al., J Clin Oncol. 2017; 35: (suppl 4S; abstract 519) 및 Overman M et al., Ann Oncol. 2016; 27 (6): 149-206 (abstract 479P)]에 기재되어 있다.
이 연구의 1차 종점은 RECIST 1.1을 사용하여 연구자-평가된 객관적 반응률 (ORR)을 결정하는 것이었다. 다른 주요 종점은 맹검 독립적 중앙기관 검토 (BICR)에 의한 ORR의 결정 및 무진행 생존 (PFS), 전체 생존 (OS) 및 안전성의 평가를 포함하였다. 종양 영상화 평가를 24주 동안 6주마다 수행하고, 이후 질환 진행 또는 중단까지 12주마다 수행하였다. 진행 이후의 치료는 환자가 연구 요법으로부터 이익을 얻고 있는 것으로 연구자에 의해 결정되었고 환자가 동의를 제공한 경우에 허용되었다.
니볼루맙 단독요법을 사용한 연구자-평가된 반응을 74명의 환자에 대해 결정하였다. 니볼루맙 단독요법은 지속적인 반응, 지속적 질환 제어 및 74%의 12-개월 전체 생존 (OS)율을 입증하였다. 니볼루맙 단독요법을 받는 환자에서의 객관적 반응률 (ORR)은 31%였으며, 이때 중앙 반응까지의 시간 (TTR)은 2.8개월이었다. 중앙 반응 지속기간 (DOR)은 니볼루맙 단독요법을 받는 환자에서는 도달되지 않았으며, 이때 83% (19/23명)가 반응 진행중이었다. 도 9에 제시된 바와 같이, 니볼루맙 단독요법을 받는 환자의 62%는 기준선으로부터의 종양 부담의 감소를 나타냈다. 니볼루맙 단독요법에 관한 추가의 세부사항은 문헌 [Overman M et al., J Clin Oncol. 2017; 35: (suppl 4S; abstract 519)]에 제공된다.
이 연구 동안 수집된 환자 인구통계는 중앙 연령, 65세 이하의 환자의 수, 남성 환자의 수, 특정한 인종의 환자의 수, 0 또는 1의 ECOG 점수를 갖는 환자의 수, 초기 진단에서의 특정한 질환 병기에 있는 환자의 수, 린치 증후군의 특정한 임상 병력을 갖는 환자의 수, 특정한 BRAF 또는 KRAS 돌연변이 상태를 갖는 환자의 수, 기준선에서 ≥ 1% 또는 < 1 %의 종양 PD-L1 발현을 갖는 환자의 수, 특정 선행 차수의 요법을 갖는 환자의 수, 및 선행 방사선요법을 갖는 환자의 수를 포함하였다. 표 11은 3 mg/kg 니볼루맙 + 1 mg/kg 이필리무맙을 사용한 조합 요법을 받는 84명의 dMMR/MSI-H 전이성 결장직장암 환자에 대한 기준선 환자 인구통계 및 질환 특징을 제시한다.
표 11. 니볼루맙 + 이필리무맙 조합 요법을 받는 환자에 대한 기준선 환자 인구통계 및 질환 특징.
이 연구에서 수집된 dMMR/MSI-H 전이성 결장직장암 환자의 배치에 관한 데이터는 받은 용량의 수, 치료가 계속되는 환자의 수, 치료가 중단된 환자의 수, 및 특정한 이유로 치료를 중단하는 환자의 수를 포함하였다. 제1 용량에서 데이터 컷-오프까지의 중앙 시간은 6.3-19.4개월의 범위로 8.6개월이었다. 표 12는 3 mg/kg 니볼루맙 + 1 mg/kg 이필리무맙을 사용한 조합 요법을 받는 84명의 dMMR/MSI-H 전이성 결장직장암 환자에 대한 환자 배치를 제시한다.
표 12. 니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에 대한 환자 배치.
연구자-평가된 객관적 반응률 (ORR), 최상의 전체 반응, ≥ 12주 동안 질환 제어를 갖는 환자의 수, 중앙 반응까지의 시간 (TTR), 및 중앙 반응 지속기간 (DOR)을 니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에 대해 결정하였다. 최상의 전체 반응을 완전 완화, 부분 완화, 안정 질환 또는 진행성 질환을 갖는 환자의 수를 측정함으로써 결정하였다. 표 13에 제시된 바와 같이, 연구자-평가된 ORR은 환자의 55%에서 달성되었고, 질환 제어율 (DCR)은 79%였다.
표 13. 니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에 대한 반응 및 질환 제어의 요약.
표적 병변 크기의 최상의 감소 및 시간 경과에 따른 종양 부담의 변화를 니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에 대해 결정하였다. 도 10에 제시된 바와 같이, 환자의 80%가 기준선으로부터의 종양 부담의 감소를 나타냈다. 시간 경과에 따른 종양 부담의 변화의 환자-특이적 특징이 도 11에 제시된다. 데이터 베이스 컷-오프 시에, 85% (39/46명) 반응이 진행중이었다.
무진행 생존 (PFS) 및 전체 생존 (OS)을 니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에 대해 평가하였다. 제1 용량에서 사망 또는 마지막으로 알려진 살아있는 날까지의 중앙 시간은 이들 환자에 대해 0.1개월 내지 20.1개월의 범위로 8.7개월이었다. 도 12A에 제시된 바와 같이, 9-개월 PFS율은 77%였고, 반면에 6-개월 및 12-개월 PFS율은 또한 각각 77% (95% CI에서 66.5%, 85.1%)였다. 개월 단위의 중앙 PFS는 데이터 컷-오프 시에 도달되지 않았다 (11.47, 95% CI에서 평가가능하지 않음). 도 12B에 제시된 바와 같이, 9-개월 OS율은 88%였고, 반면에 6-개월 OS율은 89% (95% CI에서 80.2%, 94.2%)이고 12-개월 OS율은 88% (95% CI에서 78.1%, 93.1%)였다. 개월 단위의 중앙 OS는 데이터 컷-오프 시에 도달되지 않았다 (평가가능하지 않음, 95% CI에서 평가가능하지 않음).
니볼루맙 + 이필리무맙 조합 요법을 받는 dMMR/MSI-H 전이성 결장직장암 환자에서 관찰된 치료-관련 유해 사건 (TRAE)은 설사, 피로, 아스파르테이트 아미노트랜스퍼라제 증가, 발열, 소양증, 알라닌 아미노트랜스퍼라제 증가, 오심, 갑상선기능항진증 및 갑상선기능저하증을 포함하였다. 모든 유해 사건은 다루기 쉬웠으며, 이때 등급 3/4 TRAE가 환자의 29%에서 보고되었다. 어떤 치료-관련 사망도 보고되지 않았다.
이 연구의 결과는 니볼루맙 + 이필리무맙을 사용한 조합 요법이 dMMR/MSI-H 전이성 결장직장암을 갖는 사전치료된 환자에서 지속적인 반응, 지속적 질환 제어 및 고무적인 생존 데이터를 제공하였다는 것을 입증하였다. 니볼루맙 + 이필리무맙을 사용한 조합 요법은 또한 다루기 쉬운 안전성 프로파일을 입증하였다. 이러한 결과는 고무적이고, dMMR/MSI-H 전이성 결장직장암 및 잠재적으로 다른 종양을 갖는 환자에서 니볼루맙 + 이필리무맙을 사용한 조합 요법의 계속된 평가를 지지한다.