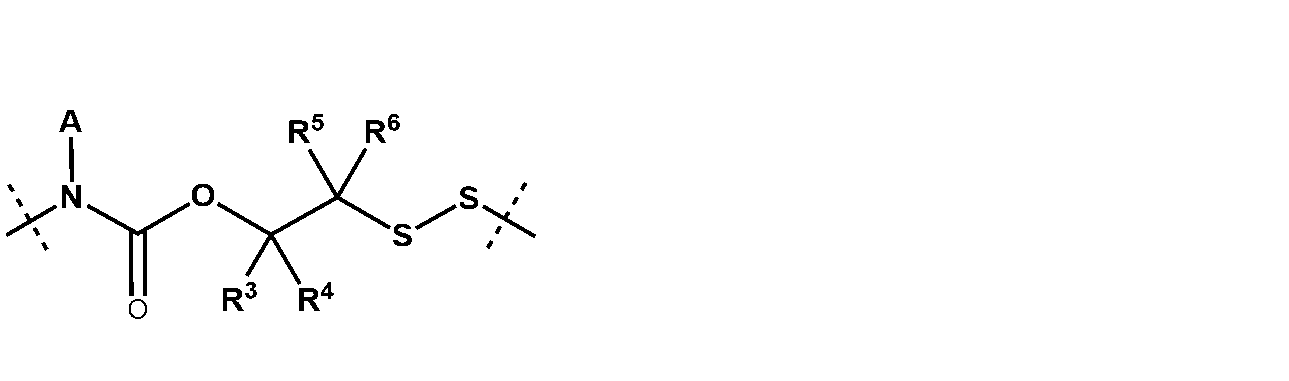JP7675060B2 - 治療薬としての微小管標的化剤のペプチドコンジュゲート - Google Patents
治療薬としての微小管標的化剤のペプチドコンジュゲート Download PDFInfo
- Publication number
- JP7675060B2 JP7675060B2 JP2022501186A JP2022501186A JP7675060B2 JP 7675060 B2 JP7675060 B2 JP 7675060B2 JP 2022501186 A JP2022501186 A JP 2022501186A JP 2022501186 A JP2022501186 A JP 2022501186A JP 7675060 B2 JP7675060 B2 JP 7675060B2
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- compound
- independently selected
- alkyl
- halo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/04—1,3-Oxazines; Hydrogenated 1,3-oxazines
- C07D265/12—1,3-Oxazines; Hydrogenated 1,3-oxazines condensed with carbocyclic rings or ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/537—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines spiro-condensed or forming part of bridged ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D498/18—Bridged systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Description
R1は、5~50アミノ酸を有するペプチドであり、
R2は、小分子微小管標的化部分であり、及び
Lは、部分R1及びR2に共有結合されるリンカーである。
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、小分子微小管標的化部分であり、及び
Lは、部分R1及びR2に共有結合されるリンカーである。
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、部分R1及びR2に共有結合されるリンカーである。
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、部分R1及びR2に共有結合されるリンカーである。
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、
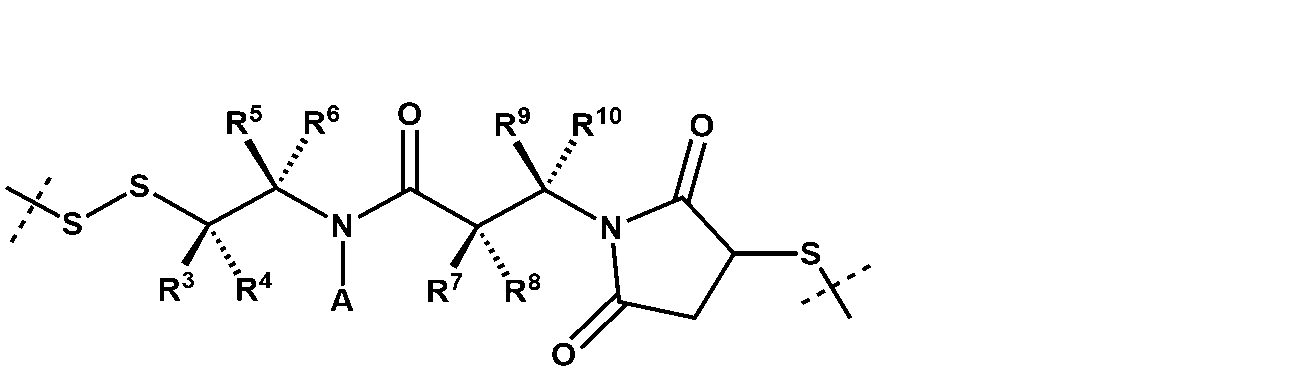
式中、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRC1C(O)NRc1Rd1から選択され、ここで、前記C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR5は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R4及びR6は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R5及びR6は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR8は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR9は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R8及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R9及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Zは、C6-10アリールまたは5~10員ヘテロアリールであり、ここで、5~10員ヘテロアリールは、少なくとも1つの環形成炭素原子と、N、O、及びSから独立して選択された1、2、3、または4の環形成ヘテロ原子とを有し、ここで、C6-10アリールまたは5~10員ヘテロアリールはそれぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Aは、HまたはC1-4アルキルであり、
Ra1、Rb1、Rc1、及びRd1はそれぞれ、独立して、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から選択され、ここで、前記C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよく、及び
nは、0、1、または2である。
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、5~10員ヘテロアリール、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、ここで、前記C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R3及びR5は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R4及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R5及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR8は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR9は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R8及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R9及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
Aは、HまたはC1-4アルキルであり、及び
Ra1、Rb1、Rc1、及びRd1はそれぞれ、独立して、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から選択され、ここで、前記C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよい。
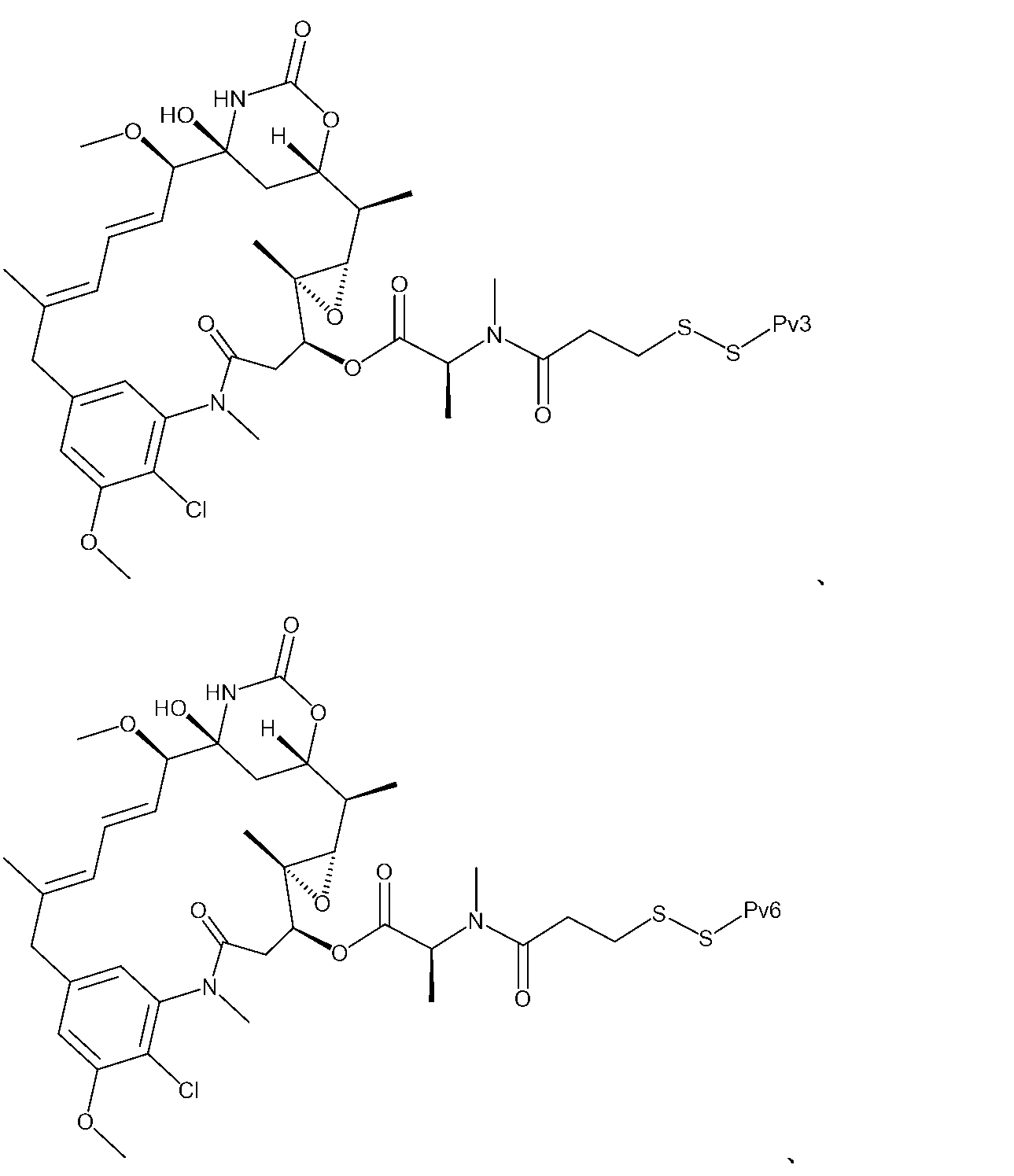
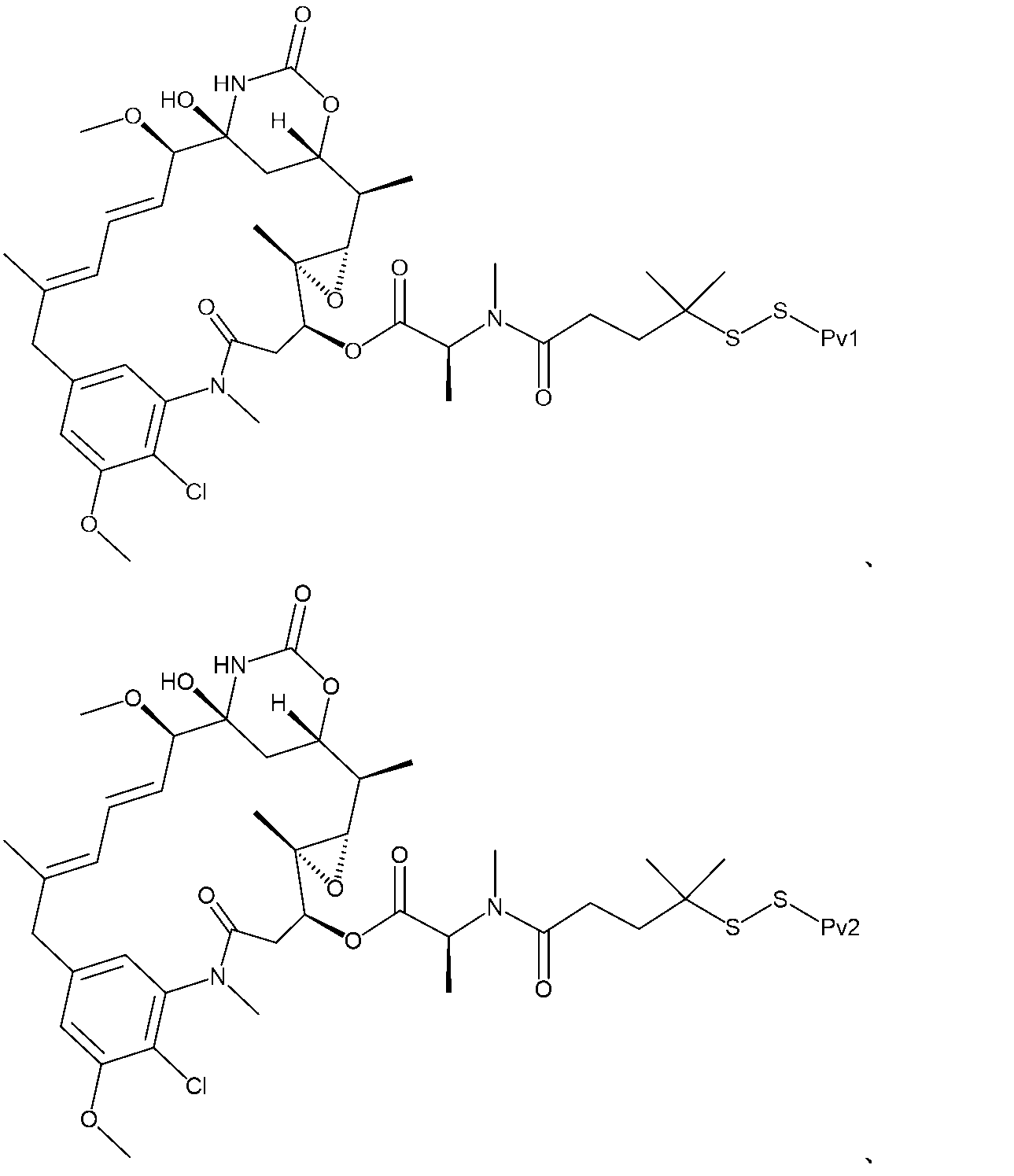
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)、及び
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3);
Ac-AAEQNPIYWARYADWLFTTPLLLLDLALLVDADEGTKCG(配列番号4;Pv4);
AAEQNPIYWARYADWLFTTPLLLLDLALLVDADEGTC(配列番号5;Pv5);ならびに
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)のうちの少なくとも1つを含むペプチドであり、
ここで、R1は、R1のシステイン残基を介してLに結合している。
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)、
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)、及び
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)のうちの少なくとも1つを含むペプチドであり、
ここで、R1は、R1のシステイン残基を介してLに結合している。
各Rqは、独立して、OH、CN、-COOH、NH2、ハロ、C1-6ハロアルキル、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルコキシ、C1-6アルキルチオ、フェニル、5~6員のヘテロアリール、4~6員のヘテロシクロアルキル、C3~6シクロアルキル、NH(C1-6アルキル)、及びN(C1-6アルキル)2から選択され、ここで、RqのC1-6アルキル、フェニル、C3-6シクロアルキル、4~6員ヘテロシクロアルキル、及び5~6員のヘテロアリールは、それぞれハロ、OH、CN、-COOH、NH2、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C1-4ハロアルコキシ、フェニル、C3-10シクロアルキル、5もしくは6員ヘテロアリールまたは4~6員ヘテロシクロアルキルで置換され、及び
2つのRq基は、それらが結合している鎖原子とともに、フェニル、5~6員のヘテロアリール、4~6員のヘテロシクロアルキル、またはC3-6シクロアルキル環を形成できる。
R1はペプチドであり、
R2は、小分子微小管標的化部分であり、
Aは、HまたはC1-4アルキルであり、
環Yは、単環式C5-7シクロアルキル環または単環式5~7員ヘテロシクロアルキル環であり、
各RYは独立して、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、
または2つの隣接するRYは、それらが結合している原子と共に、縮合単環式C5-7シクロアルキル環、縮合単環式5~7員ヘテロシクロアルキル環、縮合C6-10アリール環、または縮合した6~10員のヘテロアリール環を形成し、それぞれが、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択された1、2、または3の置換基で置換されていてもよく、
Ra1、Rb1、Rc1、及びRd1は、それぞれ独立して、H、C1-4アルキル、C2-4アルケニル、C2-4アルキニルから選択され、それぞれ、ハロ、OH、CN、及びNO2から独立して選択された1、2、または3の置換基で置換されていてもよく、及び
mは、0、1、2、または3である。
その塩を含む本発明の化合物は、既知の有機合成技術を使用して調製することができ、以下のスキームのような多くの可能な合成経路のいずれかに従って合成することができる。
本明細書で提供されるのは、がんまたは神経変性疾患などの疾患の治療における式(I)の化合物の使用である。本発明の別の態様は、がんなどの酸性または低酸素性の病組織が関与する疾患の治療における式(I)の化合物の使用である。低酸素症とアシドーシスは、がんを含む多くの疾患のプロセスの生理学的マーカーである。がんでは、低酸素症は固形腫瘍内の酸性環境の発達に関与する1つのメカニズムである。その結果、セル内の通常のpHを維持するために、水素イオンをセルから(例えば、プロトンポンプによって)除去しなければならない。この水素イオンの輸出の結果として、がん細胞は、正常細胞と比較した場合、細胞膜脂質二重層全体のpH勾配が増加し、細胞外環境のpHが低くなる。細胞毒性剤の有効性と治療指数を改善するための1つのアプローチは、この生理学的特性を活用して、健康な組織上の低酸素細胞に化合物を選択的に送達することである。
本発明の医薬組成物を調製するために、式(I)の化合物またはその薬学的に許容される塩を、従来の医薬配合技術に従って、医薬担体と密接に混合する有効成分として組み合わせる。この担体は、投与に望まれる調製物の形態に応じて、例えば、経口または非経口など、様々な形態をとることができる。経口剤形で組成物を調製する際に、例えば、懸濁液、秘薬、及び溶液などの経口液体調製物の場合、水、グリコール、油、アルコール、香味剤、防腐剤、着色剤などの通常の医薬媒体のいずれかを使用することができ、または、例えば、粉末、カプセル、及び錠剤などの経口固形製剤の場合、デンプン、糖、希釈剤、造粒剤、潤滑剤、結合剤、崩壊剤などの担体を使用することができる。投与が容易であるため、錠剤及びカプセルは最も有利な経口投与単位形態であり、その場合、固形医薬担体が明らかに使用される。所望される場合、錠剤は、標準技術によって糖コーティングまたは腸溶コーティングされ得る。非経口剤の場合、担体は、通常、滅菌水を含むが、他の成分、例えば、溶解性を助けるか、または保存のための成分が含まれ得る。注射可能な懸濁液も調製することができ、その場合、適切な液体担体、懸濁剤などを使用することができる。製薬及び医療分野の当業者は、治療される特定の疾患または状態に適した本発明の医薬組成物の投与量を容易に決定することができるであろう。
DCM:ジクロロメタン
TFA:トリフルオロ酢酸
DIPEA:ジイソプロピルエチルアミン
DMA:ジメチルアセトアミド
DME:ジメトキシエタン
DMF:ジメチルホルムアミド
DMSO:メチルスルホキシド
DTT:ジチオスレイトール
MSD:質量分析検出器
Et2O:エチルエーテル
EtOAc:酢酸エチル
EtOH:エチルアルコール
HATU:O-(7-アザ-ベンゾトリアゾール-1-イル)-N,N,N’,N’-テトラメチルウロニウムヘキサフルオロホスフェート
HOBt:1-ヒドロキシベンゾトリアゾール
RP:逆相
HPLC:高速液体クロマトグラフィー
IPA:イソプロパノール
LAH:水素化アルミニウムリチウム
N-BuLi:n-ブチルリチウム
LC-MS:液体クロマトグラフィー質量分析
LDA:リチウムジイソプロイルエチルアミド
Me:メチル
MeOH:メタノール
MTBE:メチルt-ブチルエーテル
NMP:N-メチルピロリジン
Ph:フェニル
PNPC:パラ-ニトロフェニルクロロホルメート
RTまたはrt:室温
SFC:超臨界流体クロマトグラフィー
TBAI:ヨウ化テトラブチルアンモニウム
TBME:tert-ブチルメチルエーテル
tBu:ターシャリーブチル
THF:テトラヒドロフラン
TEA:トリエチルアミン
TMEDA:テトラメチルエチレンジアミン
GSH:グルタチオン
GS:硫黄で結合したグルタチオン
LiOH:水酸化リチウム
DPPA:ジフェニルホスホリルアジド
Sn(Bu)2(ラウリン酸)2:ジブチルスズジラウレート
PBS:リン酸緩衝生理食塩水
ACN:アセトニトリル
AcOH:酢酸
EEDQ:N-エトキシカルボニル-2-エトキシ-1,2-ジヒドロキノリン
DMAP:4-ジメチルアミノピリジン
EDC:1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド
A:SunfireC18 150×4.6mm;H2O/アセトニトリルw/TFA修飾子(0.05%);流量:1ml/分;波長=217nM。
Maldi-TOF(マトリックス支援レーザー 脱離/イオン化-飛行時間;Matrix-assisted laser desorption/ionization-Time of Flight)質量分析は、Applied Biosystems Voyager System6268で測定した。サンプルは、ABサイエンスプレート(部品番号V700666)上でα-シアノヒドロキシ桂皮酸のマトリックスとして調製した。
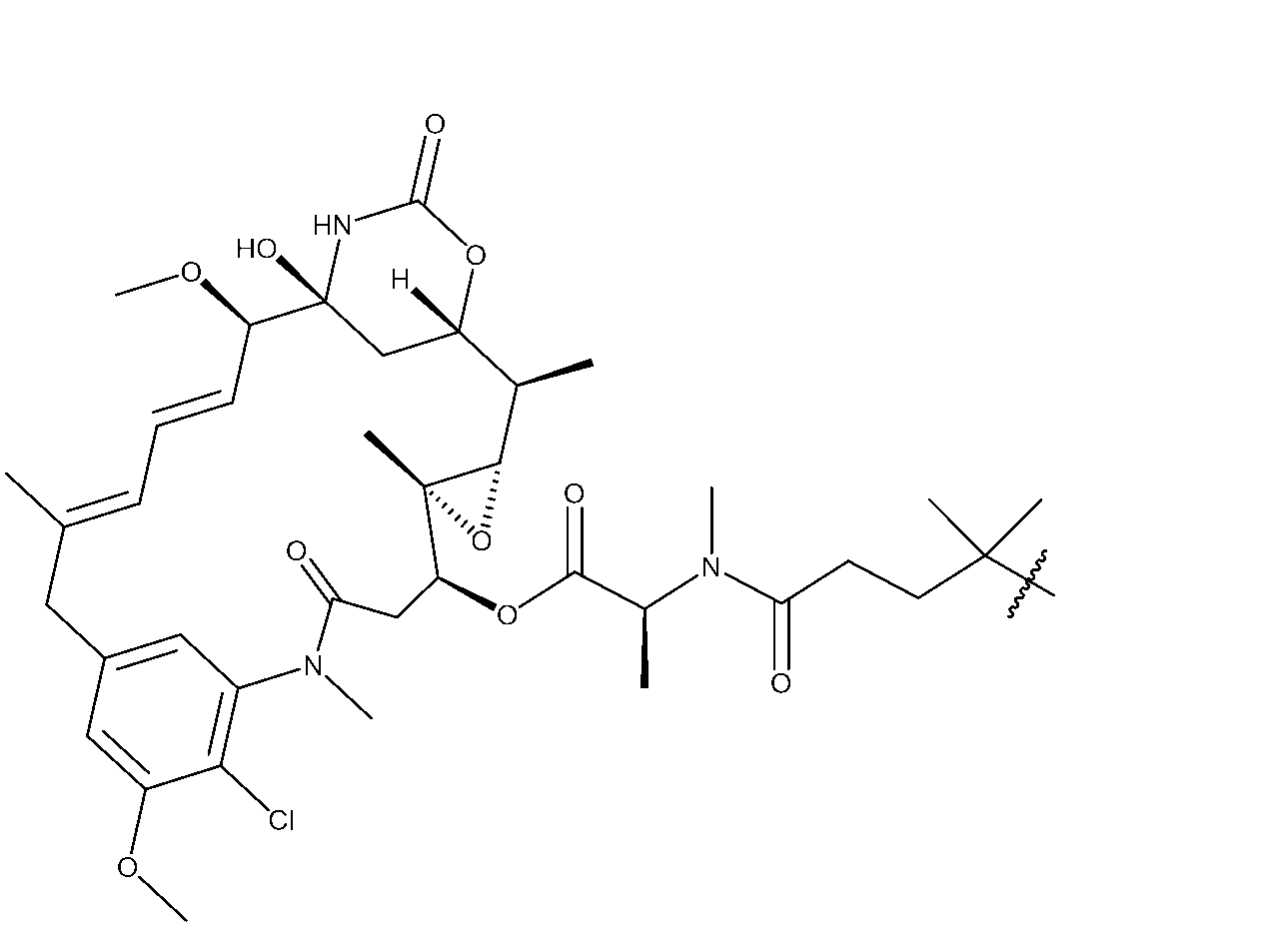
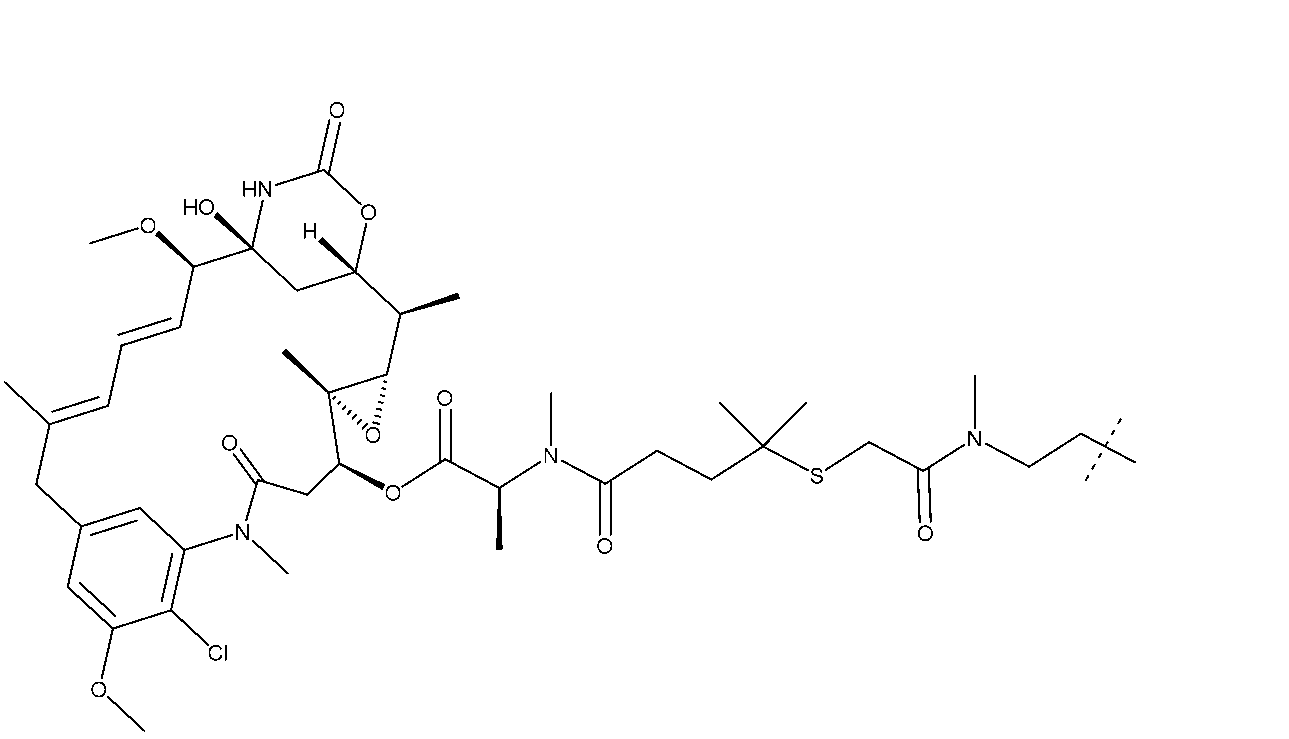
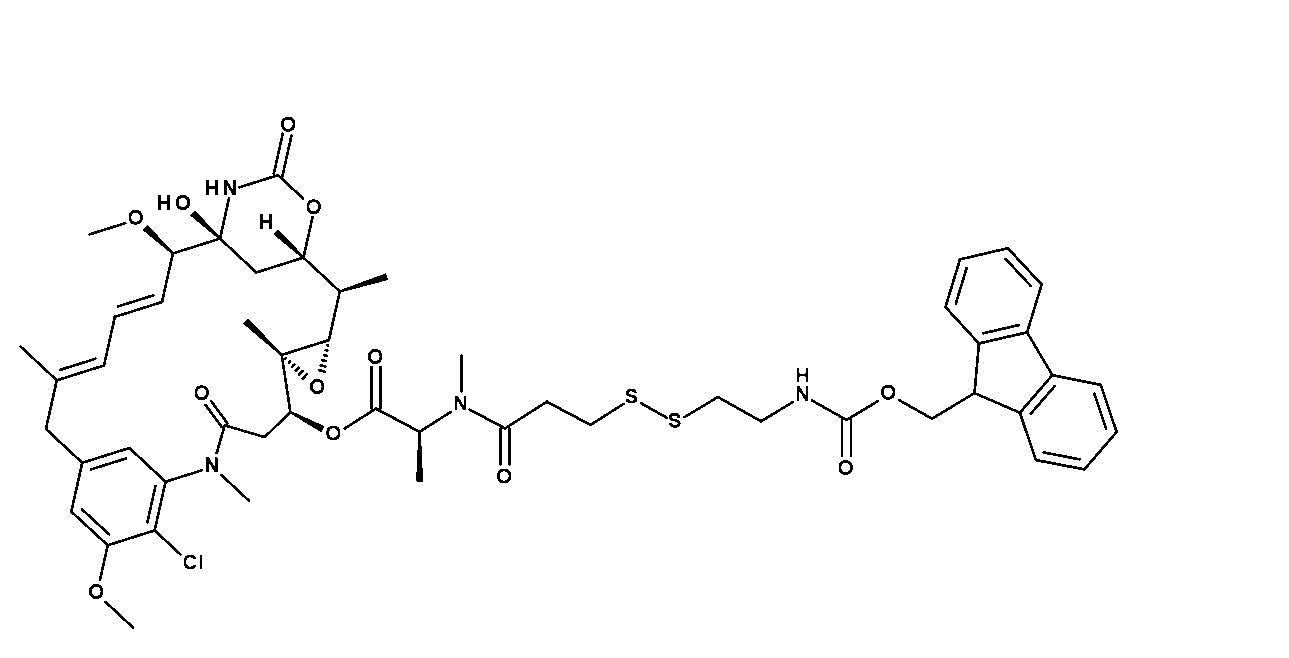
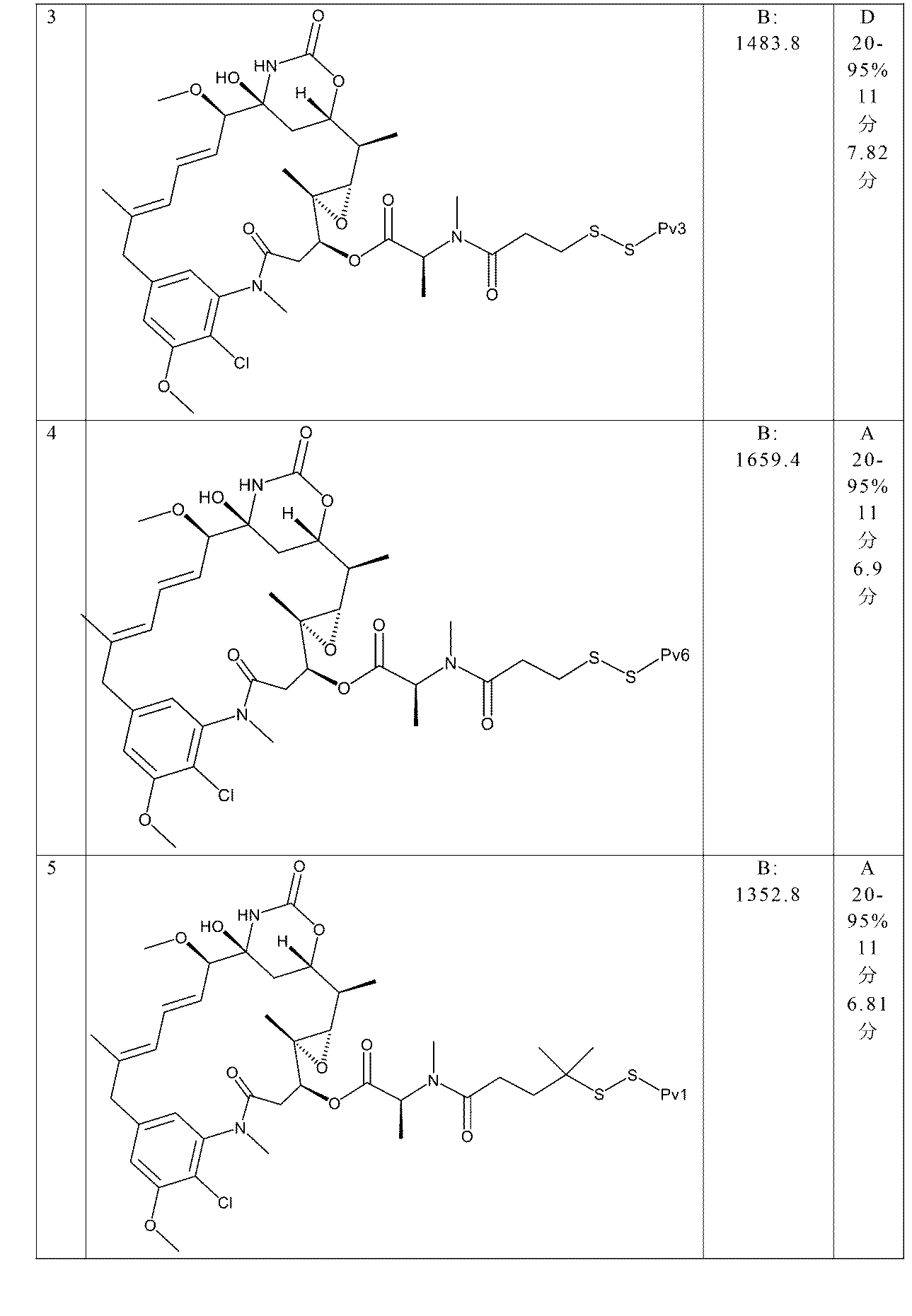
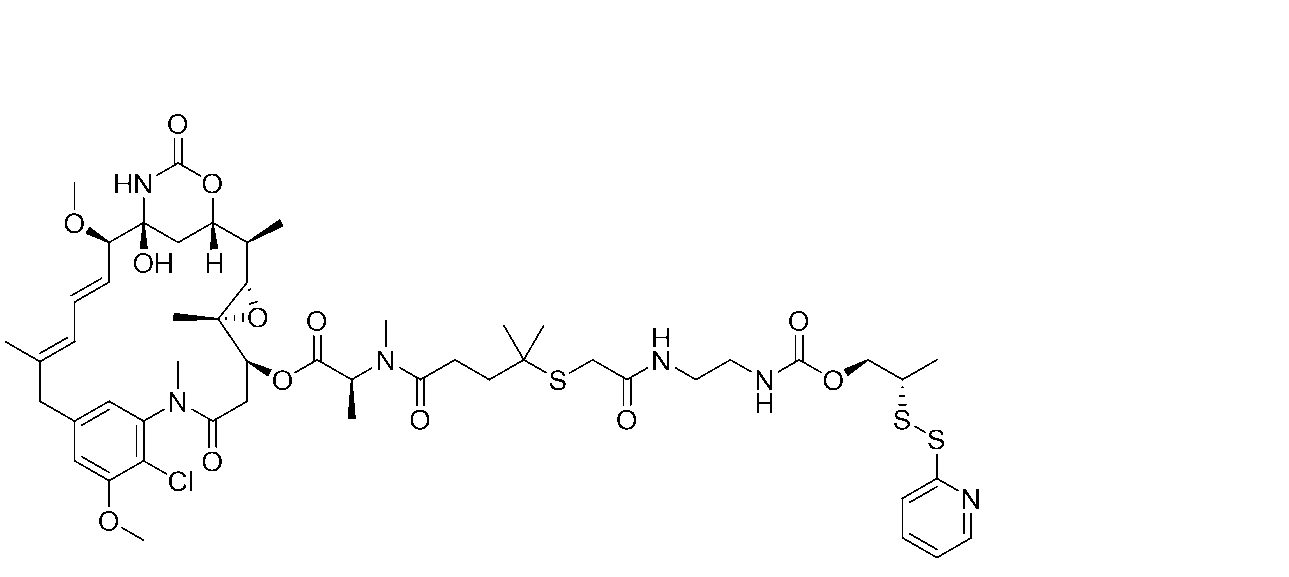
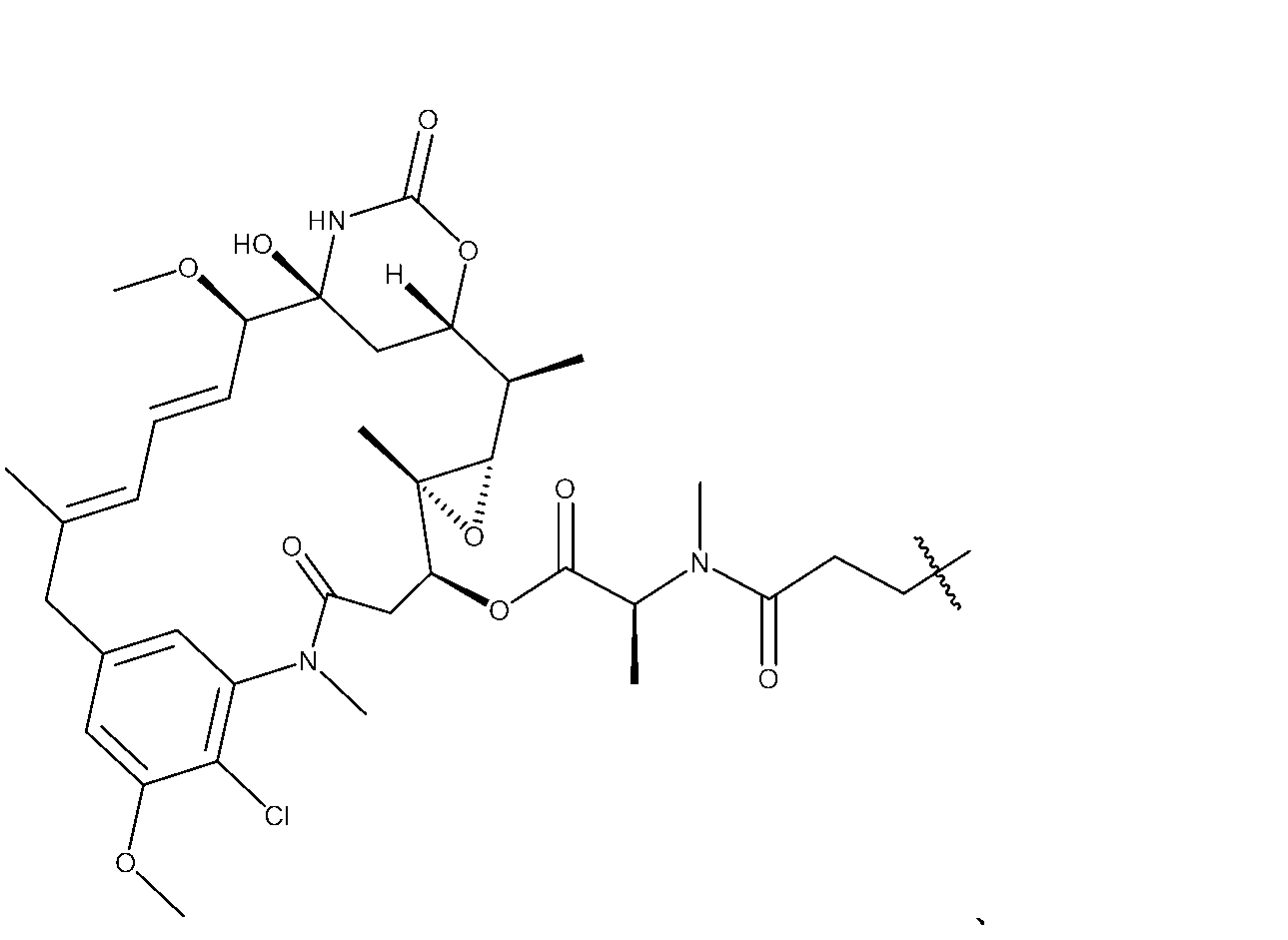
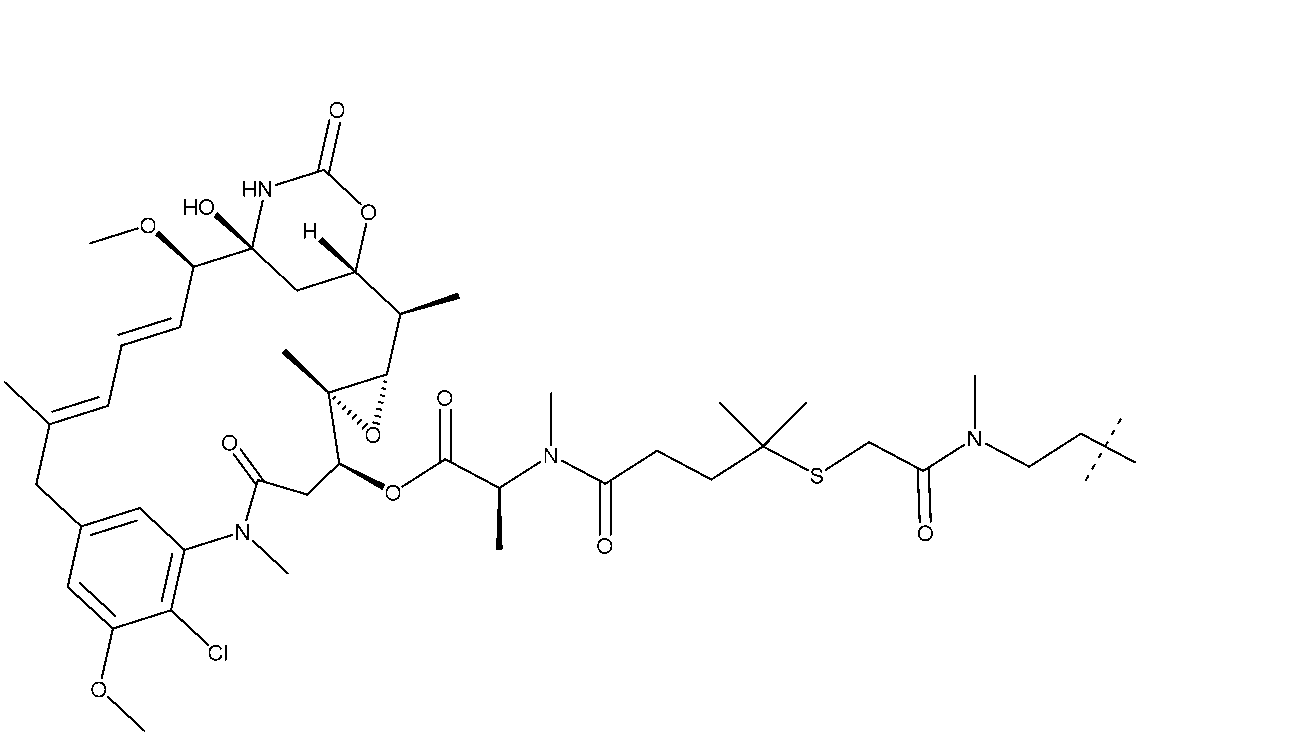
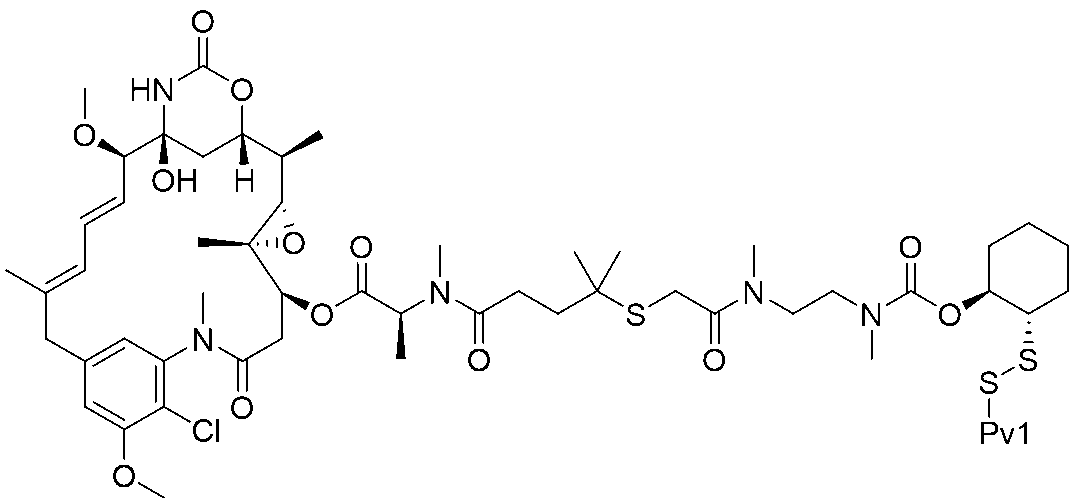
3mLの2:1CH3CN/H2O中のPv1(50.0mg、1.48e-5mоl)及び[(1S,2R,3S,6S,16E,18E,20R,21S)-11-クロロ-21-ヒドロキシ-12,20-ジメトキシ-2,5,9,16-テトラメチル-8,23-ジオキソ-4,24-ジオキサ-9,22-ジアザテトラシクロ[19.3.1.110,14.03,5]ヘキサコサ-10,12,14(26),16,18-ペンタエン-6-イル](2S)-2-[メチル-(4-メチル-4-スルファニル-ペンタノイル)アミノ]プロパノエート(0.0150g、1.92e-5mоl)に、N-メチルモルホリン(0.0600mL、0.000546mоl)を加えた。混合物を36時間撹拌した。LC-MS分析は、所望の物質の形成を示した。混合物をGilson分取HPLC(Sunfire C18 30×150mm;20~80%CH3CN/H2O w/0.05%TFA、16分間実行、13.5分)で精製して、目的のコンジュゲートを得た。混合物をGilson分取HPLC(Sunfire C18 30×150mm;20~72%CH3CN/H2O w/0.05%TFA、15分間実行、12.5分;保持時間:6.847分)で精製して、化合物5(0.0322g、7.94e-6mоl、収率:53.8%)を得た。ESI(m/z=3)1352.8。
ステップ1:Pv1-S-ピリジルの調製
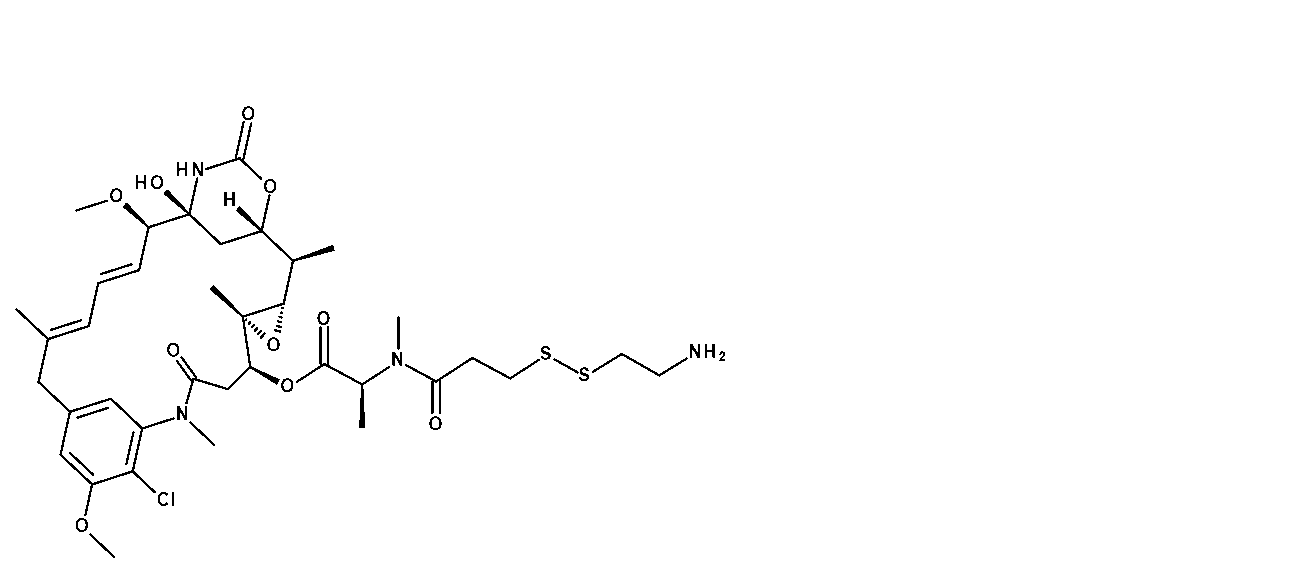
ペプチドPv1及び2,2’-ジピリジルジスルフィドをMeOHに溶解し、反応物を一晩撹拌した。LC-MSは、所望の生成物が形成されたことを示した。反応混合物を濃縮し、残留物をDMSOに取り、逆相カラムクロマトグラフィー(40~75%ACN/H2O(0.5%AcOH)、15分)によって精製して、212mgの所望の生成物を得た。
Pv1-SPyr(25.0mg、736e-6mоl)及び[(1S,2R,3S,6S,16E,18E,20R,21S)-11-クロロ-21-ヒドロキシ-12,20-ジメトキシ-2,5,9,16-テトラメチル-8,23-ジオキソ-4,24-ジオキサ-9,22-ジアザテトラシクロ[19.3.1.110,14.03,5]ヘキサコサ-10,12,14(26),16,18-ペンタエン-6-イル](2S)-2-[メチル-(4-メチル-4-スルファニル-ペンタノイル)アミノ]プロパノエート(0.00864g、1.11e-5mоl)を含むバイアルに、1mLの脱気したDMF及び0.5mLの脱気したH2Oを加えた。これにCH3CO2H(0.017mL、0.000295mol)を加えた。混合物を72時間撹拌した。LC-MSは、所望の生成物の形成を示した。混合物をGilson分取HPLC(Sunfire C18 30×150mm;20~80CH3CN/H2Ow/0.5%AcOH、16分間実行、12.9分)で精製し、化合物5(0.00750g、1.85e-6mоl、収率:25.1%)を得た。
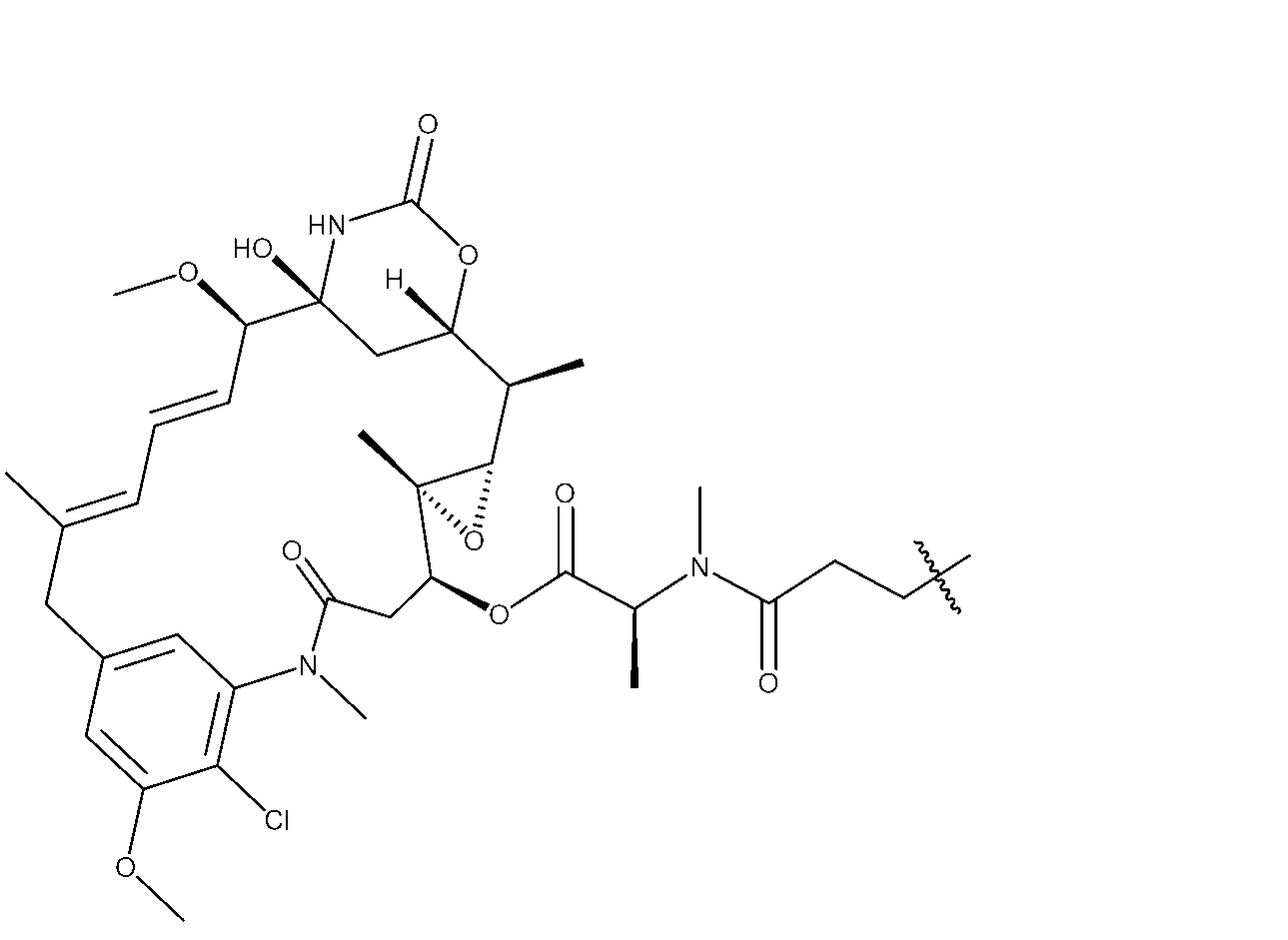
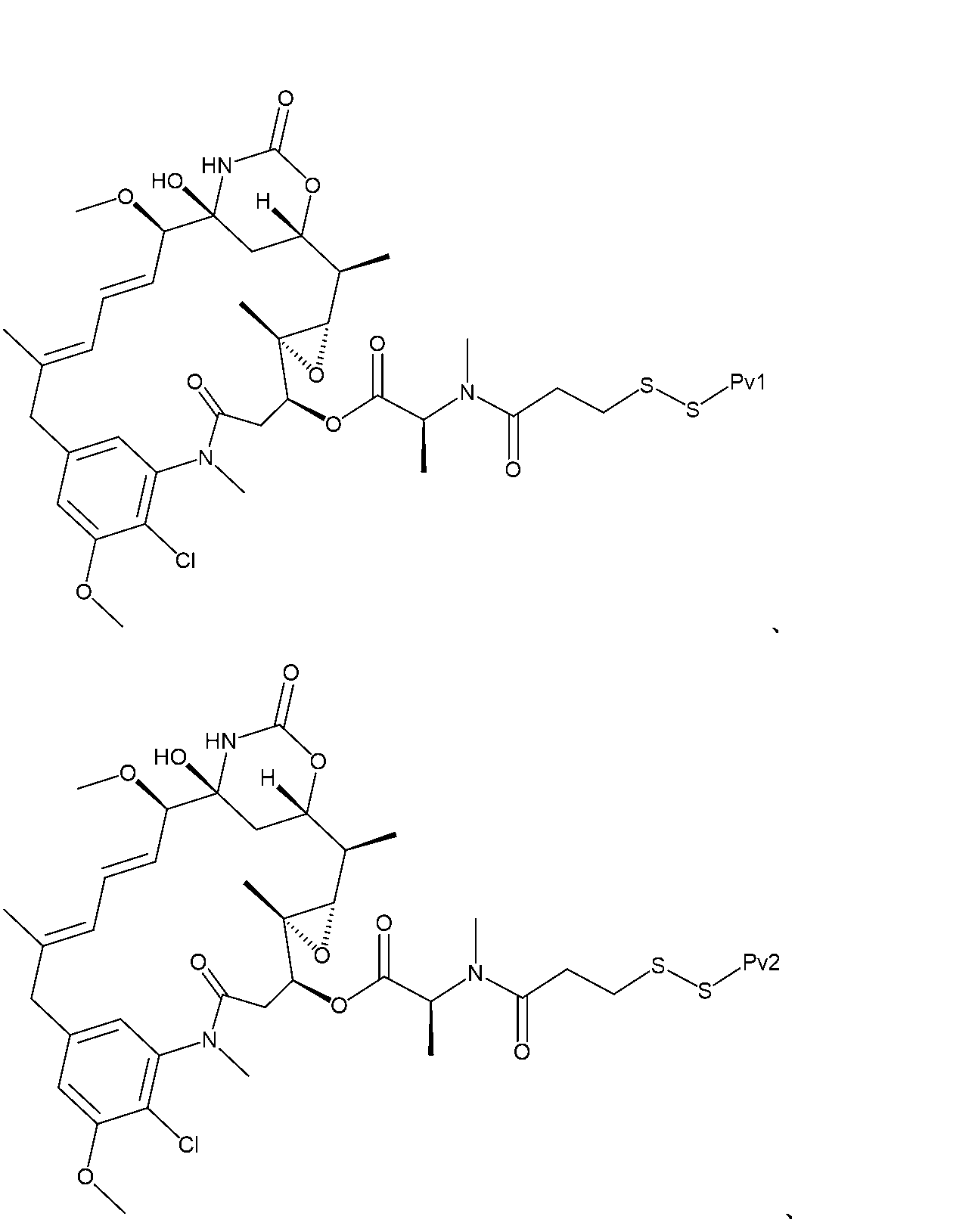
DMF(1mL)中の(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(2S,18S)-2,3,7,7-テトラメチル-4,10,15-トリオキソ-18-(ピリジン-2-イルジスルファネイル)-16-オキサ-8-チア-3,11,14-トリアザノナデカノエート(17.7mg、0.0857mmоl)の溶液を重炭酸ナトリウム(1.8mg、0.0214mmоl)及び水(50mL)で処理した。得られた溶液をペプチドPv1(31.5mg、0.0899mmol)で処理し、室温で3時間撹拌した後、逆相カラムRediSep C18(15.5g)に適用し、酢酸アンモニウム(10mM)を含む水中のアセトニトリル(30%~70%)の勾配で溶出した。画分を組み合わせて凍結し、凍結乾燥して白色の固体として18.7mg(収率50%)の生成物を得た。254nmでのHPLC純度:99%。保持時間:6.49分(方法G)。LCMS:2138.0(M+2H)/2+,1425.3(M+3H)/3+。
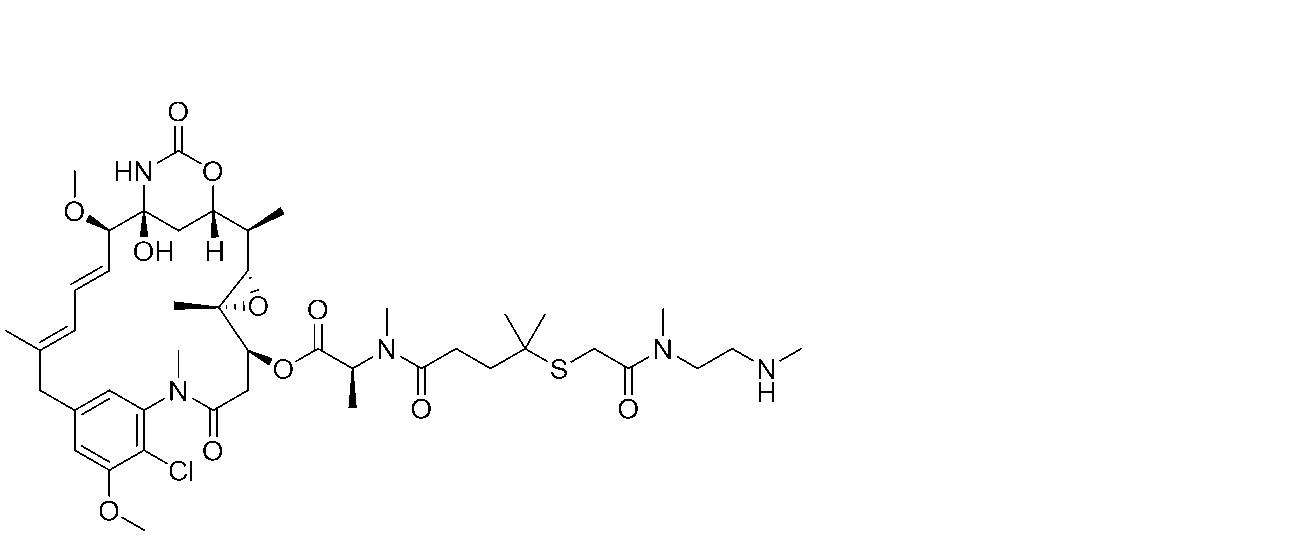
(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イルN-(4-((4-((2-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)エチル)アミノ)-4-オキソブチル)ジスルファネイル)-4-メチルペンタノイル)-N-メチル-L-アラニネート(6mg、0.006mmоl)及びPv1ペプチド(22.3mg、0.006mmоl)の溶液をDMF(0.12mL)に溶解し、トリエチルアミン(0.001mL)で処理した。30分後、反応混合物をRediSEP C8(15.5g)カラムに直接ロードし、TFA(0.05%)を含む水中のアセトニトリル(35%~75%)の勾配で溶出して、16mg(収率64%)の表題化合物を得た。254nmでのHPLC純度:98%。保持時間:6.19分(方法G)。LCMS:2150.2(M+2H)/2+,1433.3(M+3H)/3+。
(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(S)-1-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)-16,16,20,21-テトラメチル-10,19-ジオキソ-3,6-ジオキサ-14,15-ジチア-9,20-ジアザドコサン-22-オエート(15mg、0.014mmоl)及びPv1ペプチド(52mg、0.015mmоl)の溶液をDMF(0.28mL)に溶解し、トリエチルアミン(0.006mL)で処理した。30分後、反応混合物をRediSEP C8(15.5g)カラムに直接ロードし、TFA(0.05%)を含む水中のアセトニトリル(35%~60%)の勾配で溶出して、25mg(収率34%)を得た。254nmでのHPLC純度:98%。保持時間:6.26分(方法G)。LCMS:2194.0(M+2H)/2+,1463.0(M+3H)/3+。
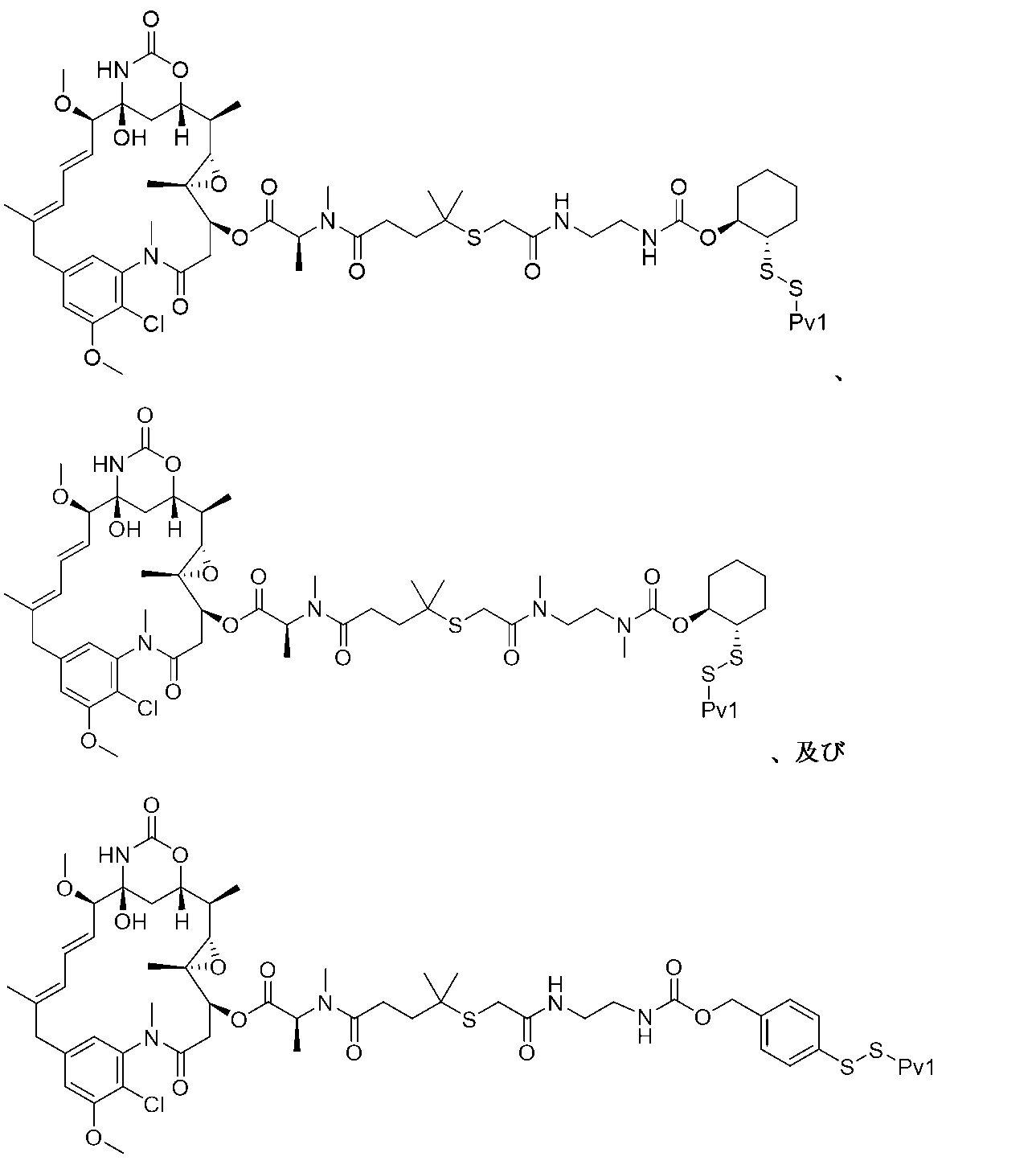
14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(S)-1-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)-16,16,20,21-テトラメチル-10,19-ジオキソ-3,6-ジオキサ-14,15-ジチア-9,20-ジアザドコサン-22-オエート(18mg、0.017mmоl)及びPv1ペプチド(63mg、0.019mmоl)の溶液をDMF(0.34mL)に溶解し、トリエチルアミン(0.007mL)で処理した。30分後、反応混合物をRediSEP C8(15.5g)カラムに直接ロードし、TFA(0.05%)を含む水中のアセトニトリル(35%~60%)の勾配で溶出して、25mg(収率34%)の表題生成物を得た。254nmでのHPLC純度:99%。保持時間:6.24分(方法G)。LCMS:2172.0(M+2H)/2+,1448.7(M+3H)/3+。
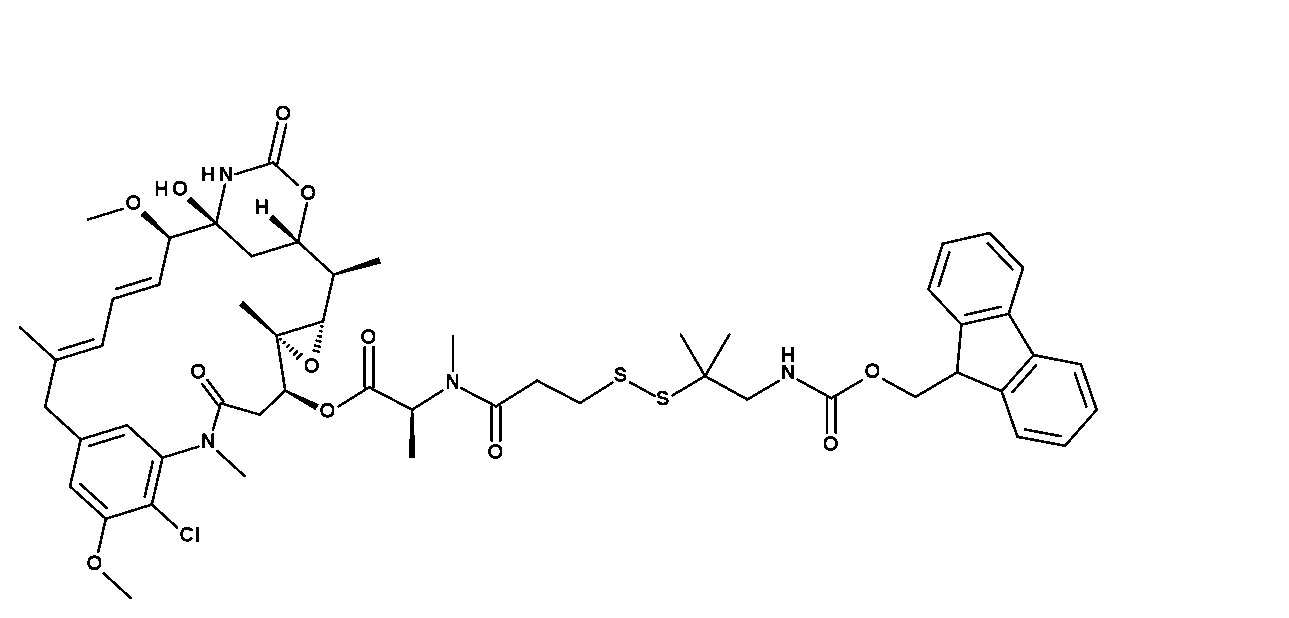
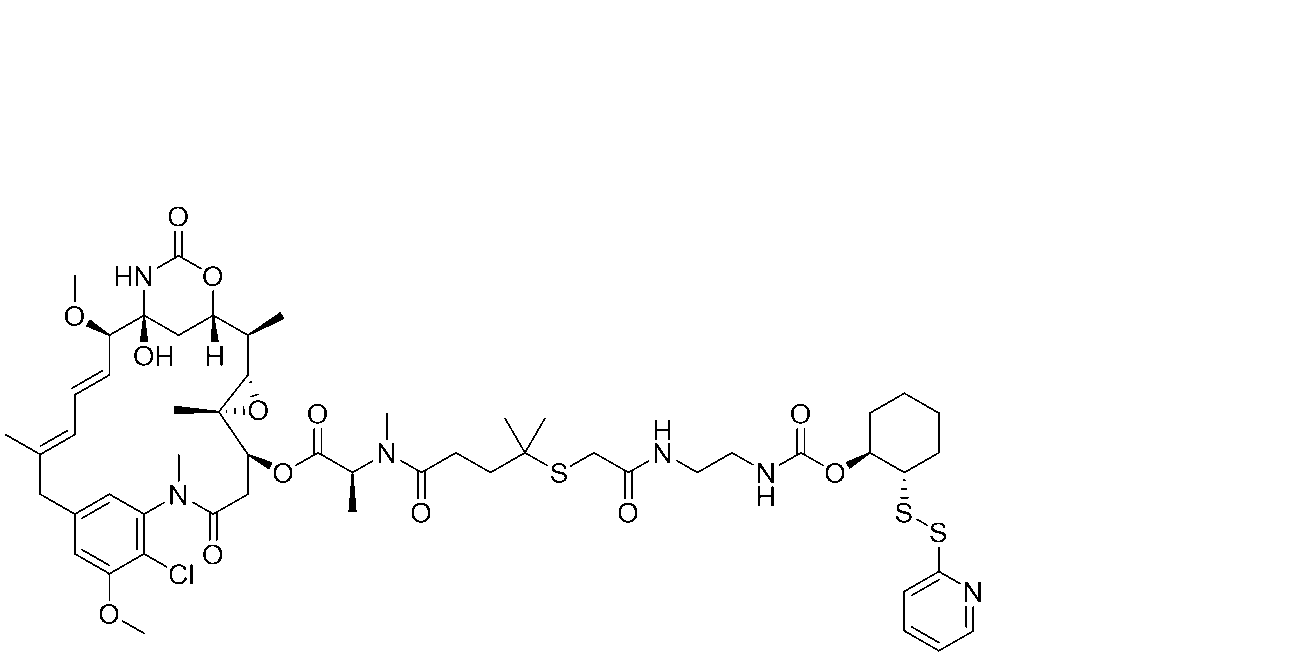
(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(S)-9,9,13,14-テトラメチル-1,6,12-トリオキソ-1-(((1S,2S)-2-(ピリジン-2-イルジスルファネイル)シクロヘキシル)オキシ)-8-チア-2,5,13-トリアザペンタデカン-15-オエート(17mg、0.015mmоl)及びPv1ペプチド(47mg、0.013mmоl)の溶液をDMF(0.34mL)に溶解し、トリエチルアミン(0.007mL)で処理した。30分後、反応混合物をRediSEP C8(15.5g)カラムに直接ロードし、TFA(0.05%)を含む水中のアセトニトリル(35%~60%)の勾配で溶出して、28mg(収率37%)を得た。254nmでのHPLC純度:99%。保持時間:7.36分(方法G)。LCMS:2158.0(M+2H)/2+,1439.0(M+3H)/3+。
(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(S)-2,5,9,9,13,14-ヘキサメチル-1,6,12-トリオキソ-1-(((1S,2S)-2-(ピリジン-2-イルジスルファネイル)シクロヘキシル)オキシ)-8-チア-2,5,13-トリアザペンタデカン-15-オエート(16mg、0.014mmоl)及びPv1ペプチド(52mg、0.015mmоl)の溶液をDMF(0.28mL)に溶解し、トリエチルアミン(0.008mL)で処理した。30分後、反応混合物をRediSEP C8(15.5g)カラムに直接ロードし、TFA(0.05%)を含む水中のアセトニトリル(35%~60%)の勾配で溶出して、32mg(収率44%)の表題生成物を得た。254nmでのHPLC純度:99%。保持時間:6.86分(方法G)。LCMS:2172.0(M+2H)/2+,1448.4(M+3H)/3+。
DMF(1mL)中の(14S,16S,32S,33S,2R,4S,10E,12E,14R)-86-クロロ-14-ヒドロキシ-85,14-ジメトキシ-33,2,7,10-テトラメチル-12,6-ジオキソ-7-アザ-1(6,4)-オキサジナナ-3(2,3)-オキシラナ-8(1,3)-ベンゼナシクロテトラデカファン-10,12-ジエン-4-イル(S)-11,11,15,16-テトラメチル-1-(4-((5-ニトロピリジン-2-イル)ジスルファネイル)フェニル)-3,8,14-トリオキソ-2-オキサ-10-チア-4,7,15-トリアザヘプタデカン-17-オエート(10.3mg、0.00857mmоl)の溶液を重炭酸ナトリウム(1.8mg、0.0214mmоl)及び水(50mL)で処理した。得られた溶液をペプチドPv1(31.5mg、0.0899mmol)で処理し、室温で3時間撹拌した後、逆相カラムRediSep C18(15.5g)に適用し、酢酸アンモニウム(10mM)を含む水中のアセトニトリル(30%~70%)の勾配で溶出した。画分を組み合わせて凍結し、凍結乾燥して白色の固体として18.7mg(収率50%)の生成物を得た。254nmでのHPLC純度:99%。保持時間:6.63分(方法G)。MSデータ,2162.4(M+2H)/2+,1441.8(M+3H)/3+,1082.6(M+4H)/4+,1435.7(M+3H-H2O)/3+。
細胞を96ウェルの黒い壁の透明な底板(Griener)に、ウェルあたり2500個のDLD-1 WT細胞、ウェルあたり5000個のFaDu及びHeLa細胞、ウェルあたり3000個のHCT116で、10%FBS含有増殖培地にプレーティングした。細胞を室温で60分間接着させた後、37℃の5%CO2インキュベーターに戻した。24時間後、培地を除去し、様々な薬物濃度を含む新鮮な増殖培地で置き換えた。各薬物濃度を3回加えた。薬物で処理されていない対照には、増殖培地のみが含まれていた。細胞をインキュベーターに戻した。薬物添加の96時間後、細胞を4%パラホルムアルデヒドで20分間固定し、1μg/mLのヘキストで染色した。プレートをCytation5オートイメージャー(BioTek)で画像化し、CellProfiler(http://cellprofiler.org)を使用して細胞をカウントした。細胞増殖遅延パーセントが計算され、GraphPadPrismを使用してデータがプロットされた。
蛍光ベースのチューブリン重合アッセイ(細胞骨格カタログ番号BK011P)を実行して、インビトロチューブリン重合に対する非結合DM4及び化合物5の影響を定量化した。DM4及び化合物5は、DMSOで10mMのストックとして調製し、DMSOの最終濃度が0.2%になるように、超純水で10Xから200、50、及び5μMに希釈した。キット試薬を急速に解凍し、早期重合を防ぐために氷上で冷たく保った。チューブリン反応混合物は、精製ブタ脳チューブリン、GTP、及びグリセロール緩衝液をすべて1Xキット緩衝液で混合し、最終濃度が2mg/mLチューブリン、1mM GTP、及び15%グリセロールになるように氷上で調製した。5μLのDM4、化合物5、またはDMSO対照を、事前に温めた黒色のハーフウェル反応プレートに37℃で1分以内で加え、蒸発させないように温めた。50μLのチューブリン反応混合物を各ウェルに迅速に添加し、すぐに事前に温めたCytation 5イメージングリーダー(BioTek)に入れた。動的読み取りは、360励起/450発光で37℃で2時間実行され、重合が発生するときに蛍光レポーターが微小管に組み込まれることによる蛍光の増強を追跡するために、2.5分ごとに読み取りが行われた。
結合実験は、BiacoreS200機器を使用して実行された。ストレプトアビジンが予め固定化されたシリーズSセンサーチップは、50mM NaOH中の1M NaClでコンディショニングされた。HeLa細胞に由来するビオチン標識ヒトチューブリンを、HBS-P+緩衝液中125μg/mLの濃度で10μl/分の流量でセンサーチップに固定化した。タンパク質の最後の3000RU(応答ユニット)をチップに直接固定した。チューブリンを固定化した後、センサーチップを50%イソプロパノール、50mM NaOH、及び1M NaClで洗浄し、続いてアッセイ緩衝液で4時間平衡化した。ストレプトアビジン-ビオチンキャプチャーブランク(リファレンスFC)を使用して、非特異的結合をモニターした。
6週齢のメスの無胸腺ヌードFoxnnuマウスは、Taconic Labs(カタログ番号NCRNU-F)から入手し、使い捨てケージシステムのAlphaDri寝具にケージごとに5匹収容した。結腸直腸癌に由来するヒトHCT116細胞を、フェノールレッドを含まないマトリゲルで1:1に希釈し、100μLで2.5x106細胞の密度で各マウスの左脇腹に皮下移植した。異種移植片が100~200mm3の平均体積に達したとき、マウスをランダムに群分けをし、以下の表に詳述されているように処理した。マウスに、腹腔内(IP)投与量のビヒクル、または0.21、0.29、0.35、0.42μmоl/kgの化合物5(1.1、1.4、1、7、または2mg/kg化合物5に相当)もしくは0.42μmоl/kgの非抱合体型DM4(0.33mg/kgの非結合DM4に相当)を投与した。用量は、クエン酸緩衝液中の5%マンニトールで0.1mg/μLのDMSOストックを希釈することによって調製し、2回目と3回目の投与の間に2日間隔で12mL/kg(25gマウスあたり300μL)の量でQDX4を投与した。異種移植腫瘍はノギスで測定し、体積は楕円体体積の式:体積=π/6x(長さ)x(幅)2を使用して計算した。動物の体重は、腫瘍体積の評価と同時に測定した。動物は、死亡、腫瘍サイズが2000mm3を超える、または体重減少が20%を超える場合に研究から除外した。カプランマイヤー分析を使用して、死亡または研究からの除外に基づいて生存率を評価した。
マウス乳癌に由来し、近赤外蛍光タンパク質(iRFP)をトランスフェクトしたマウス4T1-iRFPがん細胞を、5%CO2の加湿雰囲気下で37℃で単層として培養した。移植の1及び3日前に細胞を継代し、細胞の生存率を維持するために必要に応じて培地を2~3日ごとに交換した。細胞が80%のコンフルエンシーを超えないようにした。移植の日に、細胞をトリプシン処理し、完全培地で洗浄し、1200rpmで5分間の遠心分離によってペレット化した。上澄みをデカントし、細胞を滅菌PBSで3回洗浄し、遠心分離によりペレット化した。最後の遠心分離中に、トリパンブルー排除を使用して生存率を決定した。細胞を滅菌PBSに再懸濁し、最終濃度を5x105細胞/100μLにした。細胞は27ゲージの針で滅菌1ccツベルクリン注射器に引き込まれた。気泡を取り除き、余分な細胞混合物をコニカルチューブに戻し、各シリンジに100μLの注入量を残した。100μLの細胞を、6週齢のメスの無胸腺ヌードFoxnnuマウス(Taconic Labsカタログ番号NCRNU-F)の内側尾静脈に直接注入した。
本発明は、以下の態様および実施態様を含む。
[項1]
式(I)
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、
式中、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、ここで、前記C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR5は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R4及びR6が、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R5及びR6は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR8は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR9が、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R8及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R9及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Zは、C6-10アリールまたは5~10員ヘテロアリールであり、前記5~10員ヘテロアリールは、少なくとも1つの環形成炭素原子と、N、O、及びSから独立して選択された1、2、3、または4の環形成ヘテロ原子とを有し、前記C6-10アリールまたは5~10員ヘテロアリールはそれぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Aは、HまたはC1-4アルキルであり、
Ra1、Rb1、Rc1、及びRd1はそれぞれ、独立して、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から選択され、ここで、前記C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよく、及び
nは、0、1、または2である、前記化合物またはその薬学的に許容される塩。
[項2]
R1は、酸性または低酸素性マントルを有する細胞膜をわたってR2L-を選択的に送達することができるペプチドであり、
R2は、
Lは、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、5~10員ヘテロアリール、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、ここで、前記C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R3及びR5は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R4及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R5及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR8は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR9は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R8及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R9及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
Aは、HまたはC1-4アルキルであり、及び
Ra1、Rb1、Rc1、及びRd1はそれぞれ、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から独立して選択され、ここで、前記C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよい、項1に記載の化合物、またはその薬学的に許容される塩。
[項3]
前記R7が、約6.0未満のpHを有する酸性または低酸素性マントルを有する細胞膜を横切ってR2L-を選択的に送達することができるペプチドである、項1または2に記載の化合物、またはその薬学的に許容される塩。
[項4]
前記R7が、以下の配列
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)、及び
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)、及び
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)のうちの少なくとも1つを含むペプチドであり、
ここで、前記R1が、R1のシステイン残基を介してLに結合している、項1または2に記載の化合物またはその薬学的に許容される塩。
[項5]
前記R1が、少なくとも以下の配列
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)
を含むペプチドである、項1または2に記載の化合物またはその薬学的に許容される塩。
[項6]
前記R1が、少なくとも以下の配列
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2、Pv2)
を含むペプチドである、項1または2に記載の化合物またはその薬学的に許容される塩。
[項7]
前記R1が、少なくとも以下の配列
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)
を含むペプチドである、項1または2に記載の化合物またはその薬学的に許容される塩。
[項8]
前記R1が、少なくとも以下の配列
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)
を含むペプチドである、項1または2に記載の化合物またはその薬学的に許容される塩。
[項9]
前記R2が、
[項10]
前記R2が、
[項11]
前記R2が、
[項12]
前記R2が、
[項13]
前記Lが、
[項14]
前記Lが、
[項15]
前記Lが、
[項16]
前記Lが、
[項17]
前記Lが、
[項18]
前記Lが、
[項19]
前記R3、R4、R5、R6、R7、R8、R9、及びR10がそれぞれ独立して、H及びC1-4アルキルから選択される、項1~18のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項20]
前記R3、R4、R5、R6、R7、R8、R9、及びR10がそれぞれHである、項1~18のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項21]
前記AがHである、項1~20のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項22]
前記AがCH3である、項1~20のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項23]
前記Zがフェニルである、項1~22のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項24]
前記nが0である、項1~23のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項25]
前記nが1である、項1~23のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項26]
前記nが2である、項1~23のいずれか一項に記載の化合物またはその薬学的に許容される塩。
[項27]
[項28]
[項29]
項1~28のいずれか一項に記載の化合物またはその薬学的に許容される塩を含む医薬組成物。
[項30]
治療有効量の項1~28のいずれか一項に記載の化合物またはその医薬的に許容される塩を患者に投与することを含む、がんの治療を必要とする前記患者のがんを治療する方法。
[項31]
前記がんは、膀胱癌、骨癌、神経膠腫、乳癌、子宮頸癌、結腸癌、結腸直腸癌、子宮内膜癌、上皮癌、食道癌、ユーイング肉腫、膵臓癌、胆嚢癌、胃癌、胃腸腫瘍、頭頸部癌、腸癌、カポジ肉腫、腎臓癌、喉頭癌、肝臓癌、肺癌、メラノーマ、前立腺癌、直腸癌、腎明細胞癌、皮膚癌、胃癌、精巣癌、甲状腺癌、及び子宮癌から選択される、項30に記載の方法。
[項32]
前記がんが、肺癌、結腸直腸癌、及び胃癌から選択される、項30に記載の方法。
Claims (32)
- 式(I)
R1は、以下の配列:
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)、
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)、及び
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)のうちの少なくとも1つを含むペプチドであり、
ここで、R 1 が、R 1 のシステイン残基を介してLに結合しており、
R2は、
Lは、
式中、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、ここで、C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR5は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R4及びR6が、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R5及びR6は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR8は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R7及びR9が、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R8及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R9及びR10は、それらが結合している炭素原子と共に、C3-14シクロアルキル基または4~14員ヘテロシクロアルキル基を形成し、それぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Zは、C6-10アリールまたは5~10員ヘテロアリールであり、5~10員ヘテロアリールは、少なくとも1つの環形成炭素原子と、N、O、及びSから独立して選択された1、2、3、または4の環形成ヘテロ原子とを有し、C6-10アリールまたは5~10員ヘテロアリールはそれぞれ、C1-4アルキル、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
Aは、HまたはC1-4アルキルであり、
Ra1、Rb1、Rc1、及びRd1はそれぞれ、独立して、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から選択され、ここで、C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよく、及び
nは、0、1、または2である、化合物またはその薬学的に許容される塩。 - R1は、以下の配列:
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)、
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2;Pv2)、
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)、及び
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)のうちの少なくとも1つを含むペプチドであり、
ここで、R 1 が、R 1 のシステイン残基を介してLに結合しており、
R2は、
Lは、
R3、R4、R5、R6、R7、R8、R9、及びR10はそれぞれ、独立して、H、C1-4アルキル、C1-4アルケニル、C6-10アリール、5~10員ヘテロアリール、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から選択され、ここで、C1-4アルキル、C1-4アルケニル、C6-10アリール、及び5~10員ヘテロアリールはそれぞれ、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよく、
または、R3及びR4は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R3及びR5は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R4及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R5及びR6は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR8は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R7及びR9は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R8及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
または、R9及びR10は、それらが結合している炭素原子と共に、ハロ、CN、NO2、ORa1、SRa1、C(O)Rb1、C(O)NRc1Rd1、C(O)ORa1、OC(O)Rb1、OC(O)NRc1Rd1、NRc1Rd1、NRc1C(O)Rb1、NRc1C(O)ORa1、及びNRc1C(O)NRc1Rd1から独立して選択される1、2、または3置換基で置換されていてもよいC3-7シクロアルキル基を形成し、
Aは、HまたはC1-4アルキルであり、及び
Ra1、Rb1、Rc1、及びRd1はそれぞれ、H、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、OH、CN、NO2、及びCO2CH3から独立して選択され、ここで、C1-6アルキル及びC2-6アルケニルは、それぞれ、OH、CN、NO2、またはCO2CHで置換されていてもよい、請求項1に記載の化合物、またはその薬学的に許容される塩。 - R1が、少なくとも以下の配列:
ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1;Pv1)
を含むペプチドである、請求項1または2に記載の化合物またはその薬学的に許容される塩。 - R1が、少なくとも以下の配列:
AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2、Pv2)
を含むペプチドである、請求項1または2に記載の化合物またはその薬学的に許容される塩。 - R1が、少なくとも以下の配列:
ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3;Pv3)
を含むペプチドである、請求項1または2に記載の化合物またはその薬学的に許容される塩。 - R1が、少なくとも以下の配列:
AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6;Pv6)
を含むペプチドである、請求項1または2に記載の化合物またはその薬学的に許容される塩。 - R3、R4、R5、R6、R7、R8、R9、及びR10がそれぞれ独立して、H及びC1-4アルキルから選択される、請求項1~16のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- R3、R4、R5、R6、R7、R8、R9、及びR10がそれぞれHである、請求項1~16のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- AがHである、請求項1~18のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- AがCH3である、請求項1~18のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- Zがフェニルである、請求項1~20のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- nが0である、請求項1~21のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- nが1である、請求項1~21のいずれか一項に記載の化合物またはその薬学的に許容される塩。
- nが2である、請求項1~21のいずれか一項に記載の化合物またはその薬学的に許容される塩。
-
式中、
Pv1が、少なくとも配列:ADDQNPWRAYLDLLFPTDTLLLDLLWCG(配列番号1)を含むペプチドであり、
Pv2が、少なくとも配列:AEQNPIYWARYADWLFTTPLLLLDLALLVDADECG(配列番号2)を含むペプチドであり、
Pv3が、少なくとも配列:ADDQNPWRAYLDLLFPTDTLLLDLLWDADECG(配列番号3)を含むペプチドであり、そして
Pv6が、少なくとも配列:AAEQNPIYWWARYADWLFTTPLLLLDLALLVDADEGTCG(配列番号6)を含むペプチドである、請求項1に記載の化合物、またはそのいずれかの薬学的に許容される塩。 - 請求項1~28のいずれか一項に記載の化合物またはその薬学的に許容される塩を含む医薬組成物。
- 請求項1~28のいずれか一項に記載の化合物またはその医薬的に許容される塩を含む、がんを治療するための医薬。
- がんが、膀胱癌、骨癌、神経膠腫、乳癌、子宮頸癌、結腸癌、結腸直腸癌、子宮内膜癌、上皮癌、食道癌、ユーイング肉腫、膵臓癌、胆嚢癌、胃癌、胃腸腫瘍、頭頸部癌、腸癌、カポジ肉腫、腎臓癌、喉頭癌、肝臓癌、肺癌、メラノーマ、前立腺癌、直腸癌、腎明細胞癌、皮膚癌、胃癌、精巣癌、甲状腺癌、及び子宮癌から選択される、請求項30に記載の医薬。
- がんが、肺癌、結腸直腸癌、及び胃癌から選択される、請求項30に記載の医薬。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962872638P | 2019-07-10 | 2019-07-10 | |
| US62/872,638 | 2019-07-10 | ||
| US202063041324P | 2020-06-19 | 2020-06-19 | |
| US63/041,324 | 2020-06-19 | ||
| PCT/US2020/041348 WO2021007402A1 (en) | 2019-07-10 | 2020-07-09 | Peptide conjugates of microtubule-targeting agents as therapeutics |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022541747A JP2022541747A (ja) | 2022-09-27 |
| JPWO2021007402A5 JPWO2021007402A5 (ja) | 2023-07-18 |
| JP7675060B2 true JP7675060B2 (ja) | 2025-05-12 |
Family
ID=71944331
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022501186A Active JP7675060B2 (ja) | 2019-07-10 | 2020-07-09 | 治療薬としての微小管標的化剤のペプチドコンジュゲート |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US11555019B2 (ja) |
| EP (1) | EP3996749A1 (ja) |
| JP (1) | JP7675060B2 (ja) |
| KR (1) | KR20220051332A (ja) |
| CN (1) | CN114302744B (ja) |
| AU (1) | AU2020311925A1 (ja) |
| BR (1) | BR112022000297A2 (ja) |
| CA (1) | CA3146385A1 (ja) |
| CL (1) | CL2022000043A1 (ja) |
| CO (1) | CO2022001315A2 (ja) |
| CR (1) | CR20220057A (ja) |
| EC (1) | ECSP22010121A (ja) |
| IL (1) | IL289659B1 (ja) |
| MX (1) | MX2022000450A (ja) |
| MY (1) | MY209459A (ja) |
| PE (1) | PE20220485A1 (ja) |
| PH (1) | PH12022550037A1 (ja) |
| TW (1) | TW202116356A (ja) |
| WO (1) | WO2021007402A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112020013672A2 (pt) | 2018-01-05 | 2020-12-01 | Cybrexa 1, Inc. | compostos, composições, e métodos para tratamento de doenças que envolvem tecidos afetados por ácidos ou hipoxia |
| CA3146560A1 (en) | 2019-07-10 | 2021-01-14 | Cybrexa 2, Inc. | Peptide conjugates of cytotoxins as therapeutics |
| JP7675060B2 (ja) | 2019-07-10 | 2025-05-12 | サイブレクサ 3,インコーポレイテッド | 治療薬としての微小管標的化剤のペプチドコンジュゲート |
| PE20240119A1 (es) | 2021-01-08 | 2024-01-22 | Cybrexa 2 Inc | Proceso para preparar un resto enlazador de conjugados |
| CN118574642A (zh) * | 2021-11-17 | 2024-08-30 | 赛博克萨4公司 | 作为治疗剂的肽微管蛋白抑制剂的肽缀合物 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004520450A (ja) | 2001-05-31 | 2004-07-08 | イムノージェン インコーポレーテッド | メイタンシノイドと細胞結合剤との細胞傷害性コンジュゲートを製造する方法 |
| US20170267727A1 (en) | 2016-03-04 | 2017-09-21 | Lehigh University | Conjugates of pH Low Insertion Peptide and Monomethyl Auristatins in the Treatment of Solid Tumors |
| WO2018023098A1 (en) | 2016-07-29 | 2018-02-01 | Memorial Sloan Kettering Cancer Center | Radiolabeled ligands for targeted pet/spect imaging and methods of their use |
| JP2018535212A (ja) | 2015-10-28 | 2018-11-29 | ターベダ セラピューティクス インコーポレイテッドTarveda Therapeutics,Inc. | Sstr標的化コンジュゲート及び粒子並びにその製剤 |
Family Cites Families (111)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5637770A (en) | 1991-01-16 | 1997-06-10 | Daiichi Pharmaceutical Co., Ltd. | Hexa-cyclic compound |
| US6504029B1 (en) | 1995-04-10 | 2003-01-07 | Daiichi Pharmaceutical Co., Ltd. | Condensed-hexacyclic compounds and a process therefor |
| CA2225465A1 (en) | 1995-08-02 | 1997-02-13 | Newcastle University Ventures Limited | Benzimidazole compounds |
| DK0897924T3 (da) | 1996-04-26 | 2001-11-19 | Daiichi Seiyaku Co | Fremgangsmåde til fremstilling af tetrahydroindoliziner |
| TW409058B (en) | 1996-06-06 | 2000-10-21 | Daiichi Seiyaku Co | Method for preparation of a drug complex |
| TW527183B (en) | 1996-06-06 | 2003-04-11 | Daiichi Seiyaku Co | Drug complex |
| IN189180B (ja) | 1997-07-09 | 2003-01-04 | Chong Kun Dang Corp | |
| MY132496A (en) | 1998-05-11 | 2007-10-31 | Vertex Pharma | Inhibitors of p38 |
| KR100581443B1 (ko) | 1998-05-22 | 2006-05-23 | 다이이찌 세이야꾸 가부시기가이샤 | 약물복합체 |
| CA2348931A1 (en) | 1998-10-30 | 2000-05-11 | Daiichi Pharmaceutical Co., Ltd. | Dds compound and method for measurement thereof |
| JP2002528531A (ja) | 1998-11-03 | 2002-09-03 | ビーエーエスエフ アクチェンゲゼルシャフト | 置換2−フェニルベンズイミダゾール、その製造法および使用 |
| WO2000042040A1 (en) | 1999-01-11 | 2000-07-20 | Agouron Pharmaceuticals, Inc. | Tricyclic inhibitors of poly(adp-ribose) polymerases |
| DE19920936A1 (de) | 1999-05-07 | 2000-11-09 | Basf Ag | Heterozyklisch substituierte Benzimidazole, deren Herstellung und Anwendung |
| ECSP003637A (es) | 1999-08-31 | 2002-03-25 | Agouron Pharma | Inhibidores triciclicos de poli (adp-ribosa) polimerasas |
| US6699876B2 (en) | 1999-11-18 | 2004-03-02 | Les Laboratoires Servier | Camptothecin analogue compounds |
| BR0016328A (pt) | 1999-12-13 | 2002-08-27 | Lilly Co Eli | Pró-drogas de fosfato de pseudomicina |
| WO2001068145A2 (en) * | 2000-03-15 | 2001-09-20 | Bristol-Myers Squibb Pharma Company | Peptidase-cleavable, targeted antineoplastic drugs and their therapeutic use |
| KR20030023697A (ko) | 2000-07-13 | 2003-03-19 | 다이이찌 세이야꾸 가부시기가이샤 | Dds 화합물을 함유하는 의약 조성물 |
| US7151102B2 (en) | 2000-10-30 | 2006-12-19 | Kudos Pharmaceuticals Limited | Phthalazinone derivatives |
| CA2476182A1 (en) | 2002-03-01 | 2003-09-12 | The Administrators Of The Tulane Educational Fund | Conjugates of therapeutic or cytotoxic agents and biologically active peptides |
| MXPA04008999A (es) | 2002-03-20 | 2004-12-07 | Squibb Bristol Myers Co | Profarmacos de fosfato de fluorooxindoles. |
| ES2357057T3 (es) | 2002-04-30 | 2011-04-15 | Kudos Pharmaceuticals Limited | Derivados de ftalazinona. |
| US7449464B2 (en) | 2003-03-12 | 2008-11-11 | Kudos Pharmaceuticals Limited | Phthalazinone derivatives |
| EP1611137A1 (en) | 2003-03-31 | 2006-01-04 | Pfizer Inc. | Salts of tricyclic inhibitors of poly(adp-ribose) polymerases |
| EP2281577B1 (en) | 2003-05-14 | 2016-11-16 | ImmunoGen, Inc. | Drug conjugate composition |
| US8088387B2 (en) | 2003-10-10 | 2012-01-03 | Immunogen Inc. | Method of targeting specific cell populations using cell-binding agent maytansinoid conjugates linked via a non-cleavable linker, said conjugates, and methods of making said conjugates |
| US7276497B2 (en) | 2003-05-20 | 2007-10-02 | Immunogen Inc. | Cytotoxic agents comprising new maytansinoids |
| CA2525130C (en) | 2003-05-20 | 2014-04-15 | Immunogen, Inc. | Improved cytotoxic agents comprising new maytansinoids |
| PT1660095E (pt) | 2003-07-25 | 2010-04-19 | Pfizer | Inibidores tricíclicos de parp |
| GB0317466D0 (en) | 2003-07-25 | 2003-08-27 | Univ Sheffield | Use |
| NZ547984A (en) | 2003-12-01 | 2009-03-31 | Kudos Pharm Ltd | DNA damage repair inhibitors for treatment of cancer |
| CA2556752C (en) | 2004-02-23 | 2016-02-02 | Genentech, Inc. | Heterocyclic self-immolative linkers and conjugates |
| US8288557B2 (en) | 2004-07-23 | 2012-10-16 | Endocyte, Inc. | Bivalent linkers and conjugates thereof |
| WO2006033007A2 (en) | 2004-09-22 | 2006-03-30 | Pfizer Inc. | Polymorphic and amorphous forms of the phosphate salt of 8-fluoro-2-{4-[(methylamino)methyl]phenyl}-1,3,4,5-tetrahydro-6h-azepino[5,4,3-cd]indol-6-one |
| WO2006033003A1 (en) | 2004-09-22 | 2006-03-30 | Pfizer, Inc. | Method of preparing poly(adp-ribose) polymerases inhibitors |
| EP1793830A2 (en) | 2004-09-22 | 2007-06-13 | Pfizer, Inc. | Therapeutic combinations comprising poly(adp-ribose) polymerases inhibitor |
| EA013323B1 (ru) | 2004-12-09 | 2010-04-30 | Сентокор, Инк. | Иммуноконъюгаты против интегрина, способы и варианты применения |
| AU2006206428B2 (en) | 2005-01-18 | 2009-07-16 | The Board Of Governors For Higher Education | Selective delivery of molecules into cells or marking of cells in diseased tissue regions using environmentally senstive transmembrane peptide |
| US7301019B2 (en) | 2005-01-21 | 2007-11-27 | Immunogen, Inc. | Method for the preparation of maytansinoid esters |
| EP2468304A3 (en) | 2005-02-11 | 2012-09-26 | ImmunoGen, Inc. | Process for preparing stable drug conjugates |
| US9707302B2 (en) | 2013-07-23 | 2017-07-18 | Immunomedics, Inc. | Combining anti-HLA-DR or anti-Trop-2 antibodies with microtubule inhibitors, PARP inhibitors, bruton kinase inhibitors or phosphoinositide 3-kinase inhibitors significantly improves therapeutic outcome in cancer |
| BRPI0608175A2 (pt) | 2005-04-15 | 2009-11-10 | Immunogen Inc | método de eliminação de população de células heterogêneas ou mistas em tumores, assim como compostos maitansinóides |
| CA2893252C (en) | 2005-08-24 | 2018-05-29 | Immunogen, Inc. | Process for preparing antibody maytansinoid conjugates |
| CN101316834A (zh) | 2005-09-29 | 2008-12-03 | 艾博特公司 | 在2位取代有苯基的1h-苯并咪唑-4-甲酰胺是强效parp抑制剂 |
| PL1945647T3 (pl) | 2005-11-08 | 2012-04-30 | Immunogen Inc | Procesy wytwarzania maytansinolu |
| RS53082B (sr) | 2006-01-17 | 2014-06-30 | Abbvie Bahamas Ltd. | Kombinovana terapija sa parp inhibitorima |
| WO2007131133A2 (en) | 2006-05-04 | 2007-11-15 | Genentech, Inc. | Methods and compositions relating to zpa polypeptides |
| TWI404716B (zh) | 2006-10-17 | 2013-08-11 | Kudos Pharm Ltd | 酞嗪酮(phthalazinone)衍生物 |
| EP2109608B1 (en) | 2007-01-10 | 2011-03-23 | Istituto di Richerche di Biologia Molecolare P. Angeletti S.p.A. | Amide substituted indazoles as poly(adp-ribose)polymerase (parp) inhibitors |
| WO2008114114A2 (en) | 2007-03-16 | 2008-09-25 | Pfizer Products Inc. | Poly(adp-ribose) polymerases inhibitor for treating ophthalmic condition |
| CA2690943A1 (en) | 2007-06-25 | 2008-12-31 | Endocyte, Inc. | Conjugates containing hydrophilic spacer linkers |
| US8067613B2 (en) | 2007-07-16 | 2011-11-29 | Abbott Laboratories | Benzimidazole poly(ADP ribose)polymerase inhibitors |
| EP3838298B1 (en) | 2007-08-17 | 2025-02-26 | Purdue Research Foundation | Psma binding ligand-linker conjugates and methods for using |
| EP2276506A4 (en) | 2008-04-30 | 2014-05-07 | Immunogen Inc | EFFICIENT CONJUGATES AND HYDROPHILIC BINDER |
| ES2617619T3 (es) | 2008-06-05 | 2017-06-19 | Janssen Pharmaceutica, N.V. | Combinaciones de fármacos que comprenden un inhibidor de DGAT y un agonista de PPAR |
| KR102444399B1 (ko) | 2009-06-03 | 2022-09-16 | 이뮤노젠 아이엔씨 | 메이탄시노이드의 제조방법 |
| US9353140B2 (en) | 2009-11-25 | 2016-05-31 | Academia Sinica | BQC-G, a tumor-selective anti-cancer prodrug |
| JP5745283B2 (ja) | 2010-02-12 | 2015-07-08 | ファイザー・インク | 8−フルオロ−2−{4−[(メチルアミノ)メチル]フェニル}−1,3,4,5−テトラヒドロ−6H−アゼピノ[5,4,3−cd]インドール−6−オンの塩および多形体 |
| US20120322741A1 (en) | 2010-02-25 | 2012-12-20 | Purdue Research Foundation | Psma binding ligand-linker conjugates and methods for using |
| MX2012011171A (es) | 2010-03-31 | 2013-02-01 | Gilead Pharmasset Llc | Fosforamidatos de nucleosido. |
| EP2566335B1 (en) | 2010-05-05 | 2016-06-29 | Prolynx Llc | Controlled release of active compounds from macromolecular conjugates |
| WO2012047354A2 (en) | 2010-07-13 | 2012-04-12 | Rhode Island Board Of Governors For Higher Education | Environmentally sensitive compositions |
| EP2603201B1 (en) | 2010-08-13 | 2020-03-11 | Rhode Island Board of Governors for Higher Education | Liposome compositions and methods of use thereof |
| MX2013005046A (es) | 2010-11-03 | 2013-12-12 | Immunogen Inc | Agentes citotoxicos que comprenden nuevos derivados de ansamitocina. |
| CN107537040A (zh) | 2011-03-29 | 2018-01-05 | 伊缪诺金公司 | 通过一步法制备类美登素抗体缀合物 |
| SG193996A1 (en) | 2011-03-29 | 2013-11-29 | Immunogen Inc | Preparation of maytansinoid antibody conjugates by a one-step process |
| DK2750713T3 (en) | 2011-10-14 | 2015-12-21 | Medimmune Ltd | PYRROLOBENZODIAZEPINS AND CONJUGATES THEREOF |
| KR102853456B1 (ko) | 2012-10-11 | 2025-09-01 | 다이이찌 산쿄 가부시키가이샤 | 글리신아미드 화합물의 제조 방법 |
| WO2014061277A1 (ja) | 2012-10-19 | 2014-04-24 | 第一三共株式会社 | 親水性構造を含むリンカーで結合させた抗体-薬物コンジュゲート |
| US9180203B2 (en) | 2012-10-23 | 2015-11-10 | The Johns Hopkins University | Self-assembling drug amphiphiles and methods for synthesis and use |
| WO2014093343A2 (en) | 2012-12-10 | 2014-06-19 | Massachusetts Institute Of Technology | Multistage nanoparticle drug delivery system for the treatment of solid tumors |
| US9814784B2 (en) | 2013-01-03 | 2017-11-14 | Celltrion, Inc. | Antibody-linker-drug conjugate, preparation method therefor, and anticancer drug composition containing same |
| WO2014134483A2 (en) | 2013-02-28 | 2014-09-04 | Immunogen, Inc. | Conjugates comprising cell-binding agents and cytotoxic agents |
| CN111569086B (zh) | 2013-12-19 | 2024-06-21 | 西雅图基因公司 | 与目标-药物偶联物并用的亚甲基氨基甲酸酯连接物 |
| US20180163271A1 (en) | 2014-01-16 | 2018-06-14 | Clovis Oncology, Inc. | Use of PARP Inhibitors to Treat Breast or Ovarian Cancer Patients Showing a Loss of Heterozygosity |
| JOP20200096A1 (ar) | 2014-01-31 | 2017-06-16 | Children’S Medical Center Corp | جزيئات جسم مضاد لـ tim-3 واستخداماتها |
| JP2017114763A (ja) | 2014-03-26 | 2017-06-29 | 第一三共株式会社 | 抗cd98抗体−薬物コンジュゲート |
| AU2015245122B2 (en) | 2014-04-10 | 2019-10-24 | Daiichi Sankyo Company, Limited | Anti-HER3 antibody-drug conjugate |
| US11185594B2 (en) | 2014-04-10 | 2021-11-30 | Daiichi Sankyo Company, Limited | (Anti-HER2 antibody)-drug conjugate |
| US20170151339A1 (en) | 2014-06-30 | 2017-06-01 | Tarveda Therapeutics, Inc. | Targeted conjugates and particles and formulations thereof |
| CN113209033A (zh) | 2014-08-22 | 2021-08-06 | 克洛维斯肿瘤有限公司 | Rucaparib的高剂量强度片剂 |
| AU2015318018B2 (en) | 2014-09-16 | 2017-05-11 | Synermore Biologics (Suzhou) Co. Ltd. | Anti-EGFR antibody and uses of same |
| PT3204018T (pt) | 2014-10-07 | 2021-11-12 | Immunomedics Inc | Uso neoadjuvante de conjugados anticorpo-fármaco |
| AU2015349985A1 (en) | 2014-11-19 | 2017-05-25 | Immunogen, Inc. | Process for preparing cell-binding agent-cytotoxic agent conjugates |
| JO3705B1 (ar) | 2014-11-26 | 2021-01-31 | Bayer Pharma AG | إندازولات مستبدلة جديدة، عمليات لتحضيرها، مستحضرات دوائية تحتوي عليها واستخدامها في إنتاج أدوية |
| KR102407261B1 (ko) | 2015-02-27 | 2022-07-06 | 서울대학교산학협력단 | 나노 항암제형 및 그 제조 방법 |
| MA43354A (fr) | 2015-10-16 | 2018-08-22 | Genentech Inc | Conjugués médicamenteux à pont disulfure encombré |
| US10435428B2 (en) | 2015-11-24 | 2019-10-08 | Theravance Biopharma R&D Ip, Llc | Prodrugs of a JAK inhibitor compound for treatment of gastrointestinal inflammatory disease |
| KR102498258B1 (ko) | 2016-01-20 | 2023-02-10 | 삼성디스플레이 주식회사 | 표시 장치 |
| JP2019510085A (ja) | 2016-03-08 | 2019-04-11 | ロス ガトス ファーマスーティカルズ, インク.Los Gatos Pharmaceuticals, Inc. | 癌治療のためのナノ粒子ならびに方法および化合物 |
| EP3442592A4 (en) | 2016-04-13 | 2019-11-27 | Tarveda Therapeutics, Inc. | NEUROTENSIN RECEPTOR BINDING CONJUGATES AND FORMULATIONS THEREOF |
| GB201608885D0 (en) | 2016-05-20 | 2016-07-06 | Univ Birmingham | Treatment |
| US20190133980A1 (en) | 2016-06-02 | 2019-05-09 | Yale University | Compositions and methods for targeting and treating homologous recombination-deficient tumors |
| PT3502122T (pt) | 2016-08-16 | 2021-11-25 | Aist | Péptido que visa tumor maligno |
| US11779662B2 (en) * | 2016-09-22 | 2023-10-10 | University Of Rhode Island Board Of Trustees | Fluorescent compound comprising a fluorophore conjugated to a pH-triggered polypeptide |
| JP7058666B2 (ja) | 2016-11-25 | 2022-04-22 | マブウェル (シャンハイ) バイオサイエンス カンパニー リミテッド | 抗体-薬物複合体化のための二置換マレインアミドリンカーならびにその調製方法および使用 |
| EP3554638B1 (en) | 2016-12-19 | 2022-02-02 | Morehouse School of Medicine | Compositions and methods for treating diseases by inhibiting exosome release |
| EP3634498A4 (en) | 2017-06-09 | 2021-08-25 | Rhode Island Council on Postsecondary Education | BOUND COMPOUNDS AND OTHER PH ACTIVATED COMPOUNDS |
| KR102422860B1 (ko) | 2017-08-31 | 2022-07-19 | 다이이찌 산쿄 가부시키가이샤 | 항체-약물 콘주게이트의 신규 제조 방법 |
| BR112020013672A2 (pt) | 2018-01-05 | 2020-12-01 | Cybrexa 1, Inc. | compostos, composições, e métodos para tratamento de doenças que envolvem tecidos afetados por ácidos ou hipoxia |
| KR20200109345A (ko) | 2018-01-12 | 2020-09-22 | 프로린크스 엘엘시 | 상승적 암 치료 |
| HRP20230787T1 (hr) | 2018-05-18 | 2023-10-27 | Glycotope Gmbh | Anti-muc1 antitijelo |
| TWI851577B (zh) | 2018-06-07 | 2024-08-11 | 美商思進公司 | 喜樹鹼結合物 |
| CN109232719B (zh) | 2018-09-21 | 2021-06-29 | 中国科学院理化技术研究所 | 一种pH响应的抗菌肽及其制备方法和应用 |
| WO2020160009A1 (en) * | 2019-01-28 | 2020-08-06 | Rhode Island Council On Postsecondary Education | Phlip® targeted delivery of potent cytotoxic compounds |
| KR102679892B1 (ko) | 2019-03-29 | 2024-07-02 | 메디뮨 리미티드 | 화합물 및 이의 접합체 |
| CA3146560A1 (en) | 2019-07-10 | 2021-01-14 | Cybrexa 2, Inc. | Peptide conjugates of cytotoxins as therapeutics |
| JP7675060B2 (ja) | 2019-07-10 | 2025-05-12 | サイブレクサ 3,インコーポレイテッド | 治療薬としての微小管標的化剤のペプチドコンジュゲート |
| PE20240119A1 (es) | 2021-01-08 | 2024-01-22 | Cybrexa 2 Inc | Proceso para preparar un resto enlazador de conjugados |
| CN117897175A (zh) | 2021-04-29 | 2024-04-16 | 美商斯布雷克萨二号公司 | 拓扑异构酶i抑制剂的肽缀合物的给药方案 |
| CN118574642A (zh) | 2021-11-17 | 2024-08-30 | 赛博克萨4公司 | 作为治疗剂的肽微管蛋白抑制剂的肽缀合物 |
-
2020
- 2020-07-09 JP JP2022501186A patent/JP7675060B2/ja active Active
- 2020-07-09 CA CA3146385A patent/CA3146385A1/en active Pending
- 2020-07-09 CN CN202080057629.3A patent/CN114302744B/zh active Active
- 2020-07-09 CR CR20220057A patent/CR20220057A/es unknown
- 2020-07-09 KR KR1020227004520A patent/KR20220051332A/ko active Pending
- 2020-07-09 PE PE2022000038A patent/PE20220485A1/es unknown
- 2020-07-09 US US16/924,445 patent/US11555019B2/en active Active
- 2020-07-09 EP EP20750936.5A patent/EP3996749A1/en active Pending
- 2020-07-09 BR BR112022000297A patent/BR112022000297A2/pt unknown
- 2020-07-09 WO PCT/US2020/041348 patent/WO2021007402A1/en not_active Ceased
- 2020-07-09 MY MYPI2022000121A patent/MY209459A/en unknown
- 2020-07-09 MX MX2022000450A patent/MX2022000450A/es unknown
- 2020-07-09 PH PH1/2022/550037A patent/PH12022550037A1/en unknown
- 2020-07-09 AU AU2020311925A patent/AU2020311925A1/en active Pending
- 2020-07-09 TW TW109123266A patent/TW202116356A/zh unknown
-
2022
- 2022-01-06 IL IL289659A patent/IL289659B1/en unknown
- 2022-01-07 CL CL2022000043A patent/CL2022000043A1/es unknown
- 2022-02-09 CO CONC2022/0001315A patent/CO2022001315A2/es unknown
- 2022-02-09 EC ECSENADI202210121A patent/ECSP22010121A/es unknown
-
2023
- 2023-01-11 US US18/152,987 patent/US12234212B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004520450A (ja) | 2001-05-31 | 2004-07-08 | イムノージェン インコーポレーテッド | メイタンシノイドと細胞結合剤との細胞傷害性コンジュゲートを製造する方法 |
| JP2018535212A (ja) | 2015-10-28 | 2018-11-29 | ターベダ セラピューティクス インコーポレイテッドTarveda Therapeutics,Inc. | Sstr標的化コンジュゲート及び粒子並びにその製剤 |
| US20170267727A1 (en) | 2016-03-04 | 2017-09-21 | Lehigh University | Conjugates of pH Low Insertion Peptide and Monomethyl Auristatins in the Treatment of Solid Tumors |
| WO2018023098A1 (en) | 2016-07-29 | 2018-02-01 | Memorial Sloan Kettering Cancer Center | Radiolabeled ligands for targeted pet/spect imaging and methods of their use |
Non-Patent Citations (4)
| Title |
|---|
| Cancer Letters,2011年,307,pp.113-118 |
| J. Med. Chem.,2019年,62,pp.2708-2719 |
| J.Med. Chem.,2006年,49,pp.4392-4408 |
| PNAS,2018年,115(12),E2811-E2818 |
Also Published As
| Publication number | Publication date |
|---|---|
| PE20220485A1 (es) | 2022-04-04 |
| CA3146385A1 (en) | 2021-01-14 |
| TW202116356A (zh) | 2021-05-01 |
| WO2021007402A1 (en) | 2021-01-14 |
| EP3996749A1 (en) | 2022-05-18 |
| ECSP22010121A (es) | 2022-05-31 |
| US12234212B2 (en) | 2025-02-25 |
| MX2022000450A (es) | 2022-04-25 |
| US11555019B2 (en) | 2023-01-17 |
| CN114302744B (zh) | 2025-08-26 |
| PH12022550037A1 (en) | 2023-04-12 |
| KR20220051332A (ko) | 2022-04-26 |
| US20210009536A1 (en) | 2021-01-14 |
| CR20220057A (es) | 2022-07-19 |
| CL2022000043A1 (es) | 2022-08-19 |
| IL289659B1 (en) | 2026-01-01 |
| BR112022000297A2 (pt) | 2022-03-15 |
| JP2022541747A (ja) | 2022-09-27 |
| CN114302744A (zh) | 2022-04-08 |
| CO2022001315A2 (es) | 2022-05-10 |
| AU2020311925A1 (en) | 2022-02-03 |
| US20240067616A1 (en) | 2024-02-29 |
| MY209459A (en) | 2025-07-09 |
| IL289659A (en) | 2022-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7673041B2 (ja) | 治療薬としての細胞毒素のペプチドコンジュゲート | |
| TWI820077B (zh) | 治療涉及酸性或缺氧性患病組織之疾病之化合物、組合物及方法 | |
| JP7675060B2 (ja) | 治療薬としての微小管標的化剤のペプチドコンジュゲート | |
| JPWO2021007435A5 (ja) | ||
| US20230416331A1 (en) | Peptide conjugates of peptidic tubulin inhibitors as therapeutics | |
| WO2022155172A1 (en) | Peptide conjugates of therapeutics |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230707 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230707 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240610 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240618 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240917 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241114 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241217 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250305 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20250403 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250425 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7675060 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |