JP2010233575A - 新規抗igf−ir抗体およびその使用 - Google Patents
新規抗igf−ir抗体およびその使用 Download PDFInfo
- Publication number
- JP2010233575A JP2010233575A JP2010124341A JP2010124341A JP2010233575A JP 2010233575 A JP2010233575 A JP 2010233575A JP 2010124341 A JP2010124341 A JP 2010124341A JP 2010124341 A JP2010124341 A JP 2010124341A JP 2010233575 A JP2010233575 A JP 2010233575A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- sequence
- igf
- seq
- receptor
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Dermatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Mycology (AREA)
- Molecular Biology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
【解決手段】ヒトインスリン様増殖因子I受容体(IGF−IR)と特異的に結合することができる新規な抗体、特にマウス起源のモノクローナル抗体、キメラモノクローナル抗体およびヒト化モノクローナル抗体。
【効果】IGF−IRの過剰発現および/もしくは異常な活性化に関連した病気、ならびに/またはIGF1もしくはIGF2のIGF−IRとの相互作用が介在するシグナル変換経路の過反応に関連した病気の予防または治療が可能となる。
【選択図】なし
【効果】IGF−IRの過剰発現および/もしくは異常な活性化に関連した病気、ならびに/またはIGF1もしくはIGF2のIGF−IRとの相互作用が介在するシグナル変換経路の過反応に関連した病気の予防または治療が可能となる。
【選択図】なし
Description
本発明は、ヒトインスリン様増殖因子I受容体IGF−IRと特異的に結合することができ、および/またはそのIGF−IR受容体のチロシンキナーゼ活性を特異的に阻害することができる新規な抗体、特にマウス起源のモノクローナル抗体、キメラモノクローナル抗体およびヒト化モノクローナル抗体、ならびにこれらの抗体をコードするアミノ酸および核酸配列に関する。本発明はまた、IGF−IRを過剰発現する癌またはその受容体の過剰発現に関連した病状の予防的および/または治療的処置に向けた薬剤としてのこれら抗体の使用、ならびにIGF−IR受容体の過剰発現に関連した疾患の診断のための方法またはキットに関する。本発明は、このような抗体を抗EGFR抗体および/または化合物および/または抗癌剤または毒素と結合した薬剤と組み合わせて含む製品および/または組成物、ならびに特定の癌の予防および/または治療のためのその使用に関する。
IGF−IRと呼ばれるインスリン様増殖因子I受容体はインスリン受容体IRと70%の相同性を有するチロシンキナーゼ活性をもった受容体である。IGF−IRは分子量約350,000の糖タンパク質である。これはヘテロ四量体の受容体であり、ジスルフィド架橋によってハーフリンクしたその各々は細胞外α−サブユニットおよび膜貫通型β−サブユニットからなっている(図1を参照)。IGF−IRは極めて高いアフィニティー(Kd #1 nM)によってIGF IおよびIGF IIと結合するが、インスリンとも同様に100〜1000分の1より小さいアフィニティーによって結合することができる 。逆に、IGFは100倍低いアフィニティーによってしかインスリン受容体と結合しないが、IRは極めて高いアフィニティーによってインスリンと結合する。相同性の低いゾーンがα−サブユニットおよびβ−サブユニットのC末端部分に位置するシステインに富む領域に関係しているが、IGF−IRのチロシンキナーゼドメインとIRのチロシンキナーゼドメインとは極めて高い配列相同性を有している。α−サブユニットに見られる配列の違いはリガンドの結合ゾーンに存在するため、それがIGFおよびインスリン各々に対するIGF−IRおよびIRの相対アフィニティーの原点にある。β−サブユニットのC末端部分における違いは2つの受容体のシグナル伝達経路の相違をもたらす;IGF−IRは有糸分裂誘発作用、分化作用および抗アポトーシス作用を媒介するが、一方、IRの活性化は主として代謝経路のレベルでの作用と関係している(Baserga et al., Biochim. Biophys. Acta, 1332: F105-126頁, 1997; Baserga R., Exp. Cell. Res., 253: 1-6頁, 1999)。
細胞質チロシンキナーゼタンパク質はリガンドの受容体の細胞外ドメインとの結合によって活性化される。キナーゼの活性化に伴ってIRS−1、IRS−2、ShcおよびGrb10をはじめとする異なる細胞内基質の刺激が生じる(Peruzzi F. et al., J. Cancer Res. Clin. Oncol., l25: 166-173頁, 1999)。IGF−IRの2つの主要な基質がIRSおよびShcであり、これらは数多くの下流のエフェクターの活性化によってIGFのこの受容体との結合に関連した大多数の増殖および分化作用を媒介する(図2)。従って、基質のアベイラビリティーがIGF−IRの活性化に関連した最終的な生物学的作用を決定することがある。IRS−1が優位を占める場合には、細胞は増殖し、変化する傾向がある。Shcが優位を占める場合には、細胞は分化する傾向がある(Valentinis B. et al., J. Biol. Chem. 274: 12423-12430頁, 1999)。アポトーシスに対する防御作用に主として関わる経路はホスファチジルイノシトール 3−キナーゼ(PT 3−キナーゼ)経路であると思われる(Prisco M. et al., Horm. Metab. Res., 31: 80-89頁, 1999; Peruzzi F. et al., J. Cancer Res. Clin. Oncol., 125: 166-173頁, 1999)。
発癌におけるIGF系の役割はここ10年で集中的な調査の対象となってきている。この関心によって、その有糸分裂誘発性および抗アポトーシス性に加えて、IGF−IRが形質転換された表現型の確立および維持に必要であると思われるという事実の発見につながった。実際には、幅広い種類の細胞において、IGF−IRの過剰発現または構成的活性化がウシ胎児血清不含培地での維持とは関係のなく、細胞の増殖を誘導し、ヌードマウスにおいて腫瘍の形成を誘導することが十分に確立された。過剰発現された遺伝子の幅広い種類の産物がかなり多くの増殖因子の受容体をはじめとする細胞を形質転換し得るため、このこと自体に独自性はない。しかしながら、IGF−IRが形質転換において果たす主要な役割をはっきりと示した非常に重要な発見が、IGF−IRをコードする遺伝子が不活性化されたR細胞がウシパピローマウイルスのE5タンパク質などの、一般に細胞を形質転換することができる異なる薬剤、EGFRまたはPDGFRの過剰発現、SV40のT抗原、活性化したrasまたはこれらの2つの因子の組合せによる形質転換に全く不応であることの立証となった(Sell C. et al., Proc. Natl. Acad. Sci., USA, 90: 11217-11221頁, 1993; Sell C. et al., Mol. Cell. Biol., 14: 3604-3612頁, 1994; Morrione A. J., Virol., 69: 5300-5303頁, 1955; Coppola D. et al., Mol. Cell. Biol., 14: 4588-4595頁, 1994; DeAngelis T et al., J. Cell. Physiol., 164: 214-221頁, 1995)。
IGF−IRは幅広い種類の腫瘍および腫瘍系において発現され、IGFはIGF−IRとの結合を介して腫瘍増殖を増幅する。IGF−IRの発癌における役割に有利なその他の議論は受容体に対して向けられたマウスモノクローナル抗体を使用またはIGF−IRのネガティブドミナントを使用した研究から生まれる。実際には、IGF−IRに対して向けられたマウスモノクローナル抗体が数多くの細胞系の培養増殖および腫瘍細胞のin vivo増殖を阻害する(Arteaga C. et al., Cancer Res., 49: 6237-6241頁, 1989; Li et al., Biochem. Biophys. Res. Com., 196: 92-98頁, 1993; Zia F et al., J. Cell. Biol., 24: 269-275頁, 1996; Scotlandi K et al., Cancer Res., 58: 4127-4131頁, 1998)。また、Jiang et al.の研究(Oncogene, 18: 6071-6077頁, 1999)においてもIGF−IRのネガティブドミナントが腫瘍増殖を阻害することができるということが示された。
本発明の目的は、IGF−IRを特異的かつ高いアフィニティーによって認識するマウスモノクローナル抗体、好ましくは、キメラ化抗体またはヒト化抗体を利用可能とすることである。この抗体はインスリンのIR受容体とはほとんどまたは全く相互に作用しない。その結合によって、主としてIGFI/IGF−IRおよびIGF2/IGF−IR相互作用によって活性化されたシグナル変換経路との相互作用によってIGF−IRを発現する腫瘍の増殖をin vitroで阻害することができる。この抗体は、in vivoにおいて、エストロゲン依存性乳房腫瘍および前立腺腫瘍をはじめとする、IGF−IRを発現するあらゆるタイプの腫瘍において活性であり得る。現在利用可能な抗IGF−IRモノクローナル抗体(MAbまたはMABと記載)の場合はそうではない。実際には、IGF−IRのドメインを指すαIR3は、エストロゲン依存性乳房腫瘍(MCF−7)の増殖を完全にin vitro阻害するが、in vivoの対応するモデルに対する効果はない(Arteaga C. et al., J. Clin. Invest. 84: 1418-1423頁, 1989)。同様に、マウスモノクローナル1H7由来のscFv−Fc断片は乳房腫瘍MCF−7に対して弱い活性しかないが、アンドロゲン非依存性前立腺腫瘍に対しては完全に不活性である(Li S. L. et al., Cancer Immunol. Immunother., 49: 243-252頁, 2000)。
発明者らは、驚くべきことに、キメラ抗体(C7C10と呼ばれる)および各々、h7C10ヒト化型1およびh7C10ヒト化型2と呼ばれる2種類のヒト化抗体、マウスモノクローナル抗体の誘導体7C10が、IGF−IRを認識し、上記のあらゆる基準、すなわち、インスリンでの受容体の非認識、誘導されるIGF1および/またはIGF2増殖のin vitro遮断、ならびに、骨肉腫および非小細胞肺腫瘍など、さらに、より詳しくはエストロゲン依存性乳房腫瘍MCF−7およびアンドロゲン非依存性前立腺腫瘍DU−145であるIGF−IRを発現する異なる腫瘍の増殖のin vivo阻害に対応することを立証した。また、驚くべきことに、抗体7C10によるMCF−7細胞の腫瘍増殖のin vivo阻害の強度は、エストロゲン依存性乳房腫瘍の処置においての参照化合物の1つであるタモキシフェンで認められるものと同程度であるか、またはかなり上回るものでさえある。さらに、これらの抗体がIGF−IRおよび受容体の第一の基質IRS−1のβ鎖のチロシンのリン酸化を阻害することがわかった。さらに、これらの抗体が、一般的に、細胞の表面での受容体の迅速な再生を可能にする天然リガンドで認められることとは相違して、受容体の内在化およびその分解を引き起こすことも確立された。これらの抗体はそれらのペプチド性配列および核の配列、特に、IGF−IRに対するそれらの相補性(CDR)を決定するそれらの領域の配列によって特徴づけることができた。
よって、第一の態様によれば、本発明は、ヒトインスリン様増殖因子I受容体と特異的に結合することができ、必要に応じて、好ましくはさらにIGF−IRのリガンドIGF1および/またはIGF2の自然結合を阻害することができ、および/または前記IGF−IR受容体のチロシンキナーゼ活性を特異的に阻害することができる、単離された抗体またはその機能的断片であって、配列番号2、4もしくは6のアミノ酸配列の相補性決定領域(CDR)、または配列番号2、4もしくは6の配列との最適なアライメントにおいて少なくとも80%、好ましくは85%、90%、95%および98%の同一性を有する配列の少なくとも1つのCDRから選択される少なくとも1つのCDRを含んでなる軽鎖を含んでなるか、あるいは、配列番号8、10および12のアミノ酸配列のCDR、または配列番号8、10および12の配列との最適なアライメントにおいて少なくとも80%、好ましくは85%、90%、95%および98%の同一性を有する配列の少なくとも1つのCDRから選択される少なくとも1つのCDRを含んでなる重鎖を含んでなる、単離された抗体またはその機能的断片に関する。
本明細書において、「結合すること(to bind)」と「結合すること(to attach)」とは同じ意味を有し、互換的に用いられる。
本明細書において、抗体化合物またはそれらの配列と結合するポリペプチド、ポリペプチド配列、ペプチドおよびタンパク質という用語は互換的に用いられる。
本発明が天然抗体に関するものではないこと、すなわち、それらはそれらの天然環境には存在しないが、それらは天然源からの精製によって単離し、または準備することができ、あるいは遺伝子組換えによって、または化学合成によって準備することができ、その結果、それらがさらに記載する非天然アミノ酸を含み得ることをここで理解しなければならない。
CDR領域またはCDRとは、Kabatらによって定義された免疫グロブリンの重鎖および軽鎖の超可変領域(Kabat et al., Sequences of proteins of immunological interest, 第5版, U.S. Department of Health and Human Services, NIH, 1991、および以降の版)を示すものである。3つの重鎖CDRおよび3つの軽鎖CDRが存在する。CDRという用語は、本明細書において、場合によっては、それが認識する抗原またはエピトープに対する抗体のアフィニティーによる結合を担う大多数のアミノ酸残基を含むこれらの領域の1つまたはいくつか、あるいはこれらの領域の全てを示すために用いられる。
本発明において、2つの核酸配列またはアミノ酸配列間の「同一性の割合(パーセント)」とは、比較される2つの配列間の、最良アライメント(最適アライメント)において得られた同一ヌクレオチドの割合(パーセント)または同一アミノ酸残基の割合(パーセント)を示すものであり、この割合(パーセント)は純粋に統計的であり、2つの配列間の相違はランダムに、かつ、それらの全長にわたって分布している。2つの核酸配列またはアミノ酸配列間の配列比較は、従来どおりに、それらを最善の方法でアラインした後にこれらの配列を比較することによって実施され、その比較はセグメントによってまたは「比較ウィンドウ」によって実施することができる。比較のための配列の最適アライメントは、手動に加え、Smith and Waterman (1981)の局所的相同性アルゴリズム[Ad. App. Math. 2: 482頁]によって、Neddleman and Wunsch (1970)の局所的相同性アルゴリズム[J. Mol. Biol. 48: 443頁]によって、Pearson and Lipman (1988)の類似検索方法[Proc. Natl. Acad. Sci. USA 85: 2444頁]によって、これらのアルゴリズム(Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Madison, WIのGAP、BESTFIT、FASTAおよびTFASTA、あるいはBLAST NまたはBLAST P比較ソフトウェアにより)を用いるコンピュータソフトウェアを用いて実施することができる。
2つの核酸配列またはアミノ酸配列間の同一性の割合(パーセント)は最善の方法でアラインしたこれらの2つの配列を比較することにより決定されるが、その際、これらの2つの配列間の最適アライメントでは、比較する核酸配列またはアミノ酸配列が参照配列に対して付加または欠失を含んでなる場合がある。同一性の割合(パーセント)は、2つの配列間でヌクレオチドまたはアミノ酸残基が同一である同一位置の数を求め、この同一位置数を比較ウィンドウの全位置数で除し、これらの2つの配列間の同一性の割合(パーセント)を得るために得られた結果に100を乗じて計算される。
例えば、サイト http://www.ncbi.nlm.nih.gov/gorf/b12.htmlで入手可能なBLASTプログラム、「BLAST 2 sequences」(Tatusova et al., "Blast 2 sequences - a new tool for comparing protein and nucleotide sequences", FEMS Microbiol Lett. 174: 247-250頁)を使用することが可能であり、このプログラムで使用するパラメーターはデフォルト(特に、パラメーターに関しては「オープンギャップペナルティ」:5、および「エクステンションギャップペナルティ」:2;選択されるマトリックスは、例えば、プログラムによって提示されるマトリックス「BLOSUM 62」である)で与えられるものであり、比較する2つの配列間の同一性の割合(パーセント)はプログラムによって直接算出される。
参照アミノ酸配列と少なくとも80%、好ましくは85%、90%、95%および98%の同一性を有するアミノ酸配列には、参照配列に対して特定の改変、特に、少なくとも1つのアミノ酸の欠失、付加、または置換、末端切断もしくは延長を有するものが好ましい。1以上の連続したまたは不連続なアミノ酸の置換の場合、置換されるアミノ酸が「等価な」アミノ酸に置き換えられる置換が好ましい。「等価なアミノ酸」とは、本明細書において、対応する抗体の生物活性を本質的に改変することなく、基本構造のアミノ酸の1つと置き換えることができる、後に、特に、実施例にて記載するようなアミノ酸を示すものである。
これらの等価なアミノ酸は、それらが置き換わるアミノ酸とのそれらの構造類似性、または実施が可能な異なる抗体間の生物活性の比較試験の結果のいずれかに応じて決めることができる。
一例として、対応する改変された抗体の生物活性に著しい変化をもたらすことなく、実施することができる置換の可能性を挙げる。例えば、ロイシンはバリンまたはイソロイシンに、アスパラギン酸はグルタミン酸に、グルタミンはアスパラギンに、アルギニンはリジンに、などと置き換えることができ、当然ながら、逆の置換も同じ条件下で考えられる。
本発明による抗体は、好ましくは、当業者には周知の標準的方法によって得ることができる特定のモノクローナル抗体、特に、マウス起源のモノクローナル抗体、キメラモノクローナル抗体またはヒト化モノクローナル抗体である。
一般に、モノクローナル抗体またはその機能的断片、特に、マウス起源のものの製造については、特に、マニュアル"Antibodies"(Harlow and Lane, Antibodies: A Laboratory Manual, Cold Spring Harbor laboratory, Cold Spring Harbor NY, 726頁, 1988)に記載の技術またはKohler and Milstein(Nature, 256: 495-497頁, 1975)によって記載されたハイブリドーマからの製造技術を参照することができる。
本発明によるモノクローナル抗体は、例えば、その本発明によるモノクローナル抗体が特異的に認識するエピトープを含むIGF−IR受容体またはその断片の1つに対する免疫がある動物細胞から得ることができる。そのIGF−IR受容体またはその断片の1つは、特に、IGF−IR受容体をコードするcDNA配列に含まれる核酸配列からの遺伝子組換えによる、またはIGF−IR受容体のペプチド配列に含まれるアミノ酸配列からのペプチド合成による一般的な方法によって作製することができる。
本発明によるモノクローナル抗体は、例えば、その本発明によるモノクローナル抗体が特異的に認識するエピトープを含むIGF−IR受容体またはその断片の1つがその上に予め固定化されているアフィニティーカラムで精製することができる。より詳しくは、そのモノクローナル抗体を、Aタンパク質および/またはGタンパク質でのクロマトグラフィー、その後の、残留タンパク質混入物質、ならびにDNAおよびLPSを排除することを目的としたイオン交換クロマトグラフィーの実施または非実施、本質的にその後の、ダイマーまたはその他のマルチマーの存在に起因して起こり得る会合体を排除するためのセファロースゲルでの排除クロマトグラフィーの実施または非実施によって精製することができる。さらに好ましい方法では、これらの技術全てを同時にまたは連続的に用いることができる。
キメラ抗体またはヒト化抗体もまた、本発明の抗体に含まれる。
キメラ抗体とは、特定種の抗体由来の天然の可変(軽鎖および重鎖)領域をその特定種とは異種の種の抗体の軽鎖および重鎖定常領域と組み合わせて含む抗体を示すものである。
本発明によるキメラタイプの抗体またはその断片は、遺伝子組換え技術を用いて作製することができる。例えば、キメラ抗体は、プロモーター、ならびに本発明による非ヒト、特に、マウスモノクローナル抗体の可変領域をコードする配列、およびヒト抗体の定常領域をコードする配列を含む組換えDNAをクローニングすることによって作製することができる。このような組換え遺伝子によってコードされる本発明によるキメラ抗体は、例えば、マウス−ヒトキメラであり、この抗体の特異性はマウスDNA由来の可変領域によって決定され、そのイソタイプはヒトDNA由来の定常領域によって決定される。キメラ抗体の製造方法については、例えば、文献、verhoeyn et al.(BicEssays, 8: 74頁, 1988)を参照することができる。
ヒト化抗体とは、非ヒト起源の抗体由来のCDR領域を含み、抗体分子の他の部分が1つの(またはいくつかの)ヒト抗体に由来する抗体を示すものである。さらに、骨格のセグメントの残基のいくつか(FRと呼ばれる)が結合アフィニティーを維持するよう改変されていてもよい(Jones et al., Nature, 321: 522-525頁, 1986; verhoeyen et al., Science, 239: 1534-1536頁, 1988; Riechmann et al., Nature, 332: 323-327, 1988)。
本発明によるヒト化抗体またはその断片は、当業者に公知の技術によって作製することができる(例えば、文献、Singer et al., J. Inmun. 150: 2844-2857頁, 1992; Mountain et al., Biotechnol. Genet. Eng. Rev., 10: 1-142頁, 1992; またはBebbington et al., Bio/Technology, 10: 169-175頁, 1992に記載のものなど)。このような本発明によるヒト化抗体は、in vitroでの診断法、またはin vivoでの予防的および/または治療的処置での使用に好適である。
本発明による抗体の機能的断片とは、特に、Fv、scFv(scは単鎖)、Fab、F(ab’)2、Fab’、scFv−Fc断片またはダイアボディ、またはポリ(エチレン)グリコール(「ペグ化」)のようなポリ(アルキレン)グリコールの付加などの化学修飾によって、またはリポソームへの組込みによって半減期を延長した断片(Fv−PEG、scFv−PEG、Fab−PEG、F(ab’)2−PEGまたはFab’−PEGと呼ばれるペグ化断片)(「PEG」はポリ(エチレン)グリコール)といった抗体断片を示すものであり、その断片は配列番号2、4、6、8、10または12の配列の特徴的なCDRの少なくとも1つを有し、特に、一般に、その由来となる抗体の部分活性、例えば、特に、IGF−IR受容体を認識し、それと結合し、必要に応じて、IGF−IR受容体の活性を阻害する能力さえ発揮し得る。
好ましくは、その機能的断片がそれらの由来となる抗体の重または軽可変鎖の部分配列から構成されるか、またはそれを含んでなり、その部分配列がその由来となる抗体と同じ結合特異性と十分なアフィニティー、好ましくは、IGF−IR受容体に対して、その由来となる抗体のアフィニティーと少なくとも同等〜1/100、より好ましくは、少なくとも1/10のアフィニティーを保持するのに十分なものである。
このような機能的断片は、その由来となる抗体の配列の最低5個のアミノ酸、好ましくは、10、15、25、50および100個の連続したアミノ酸を含む。
好ましくは、これらの機能的断片は、一般に、それらの由来となる抗体と同じ結合特異性を有するFv、scFv、Fab、F(ab’)2、F(ab')、scFv−Fcタイプまたはダイアボディの断片である。本発明によれば、本発明による抗体断片は、上記のような抗体から、ペプシンまたはパパインのような酵素による消化などの方法によって、および/または化学的還元によるジスルフィド架橋の切断によって得ることができる。別法では、本発明に含まれる抗体断片を当業者にはまた周知の遺伝子組換え技術によって、あるいは、例えば、Applied Biosystemsなどの会社から提供されるものなどの自動ペプチド合成装置を用いたペプチド合成によって得ることができる。
より好ましくは、本発明は、遺伝子組換えによって、または化学合成によって得られた本発明による抗体またはその機能的断片、特に、キメラ抗体またはヒト化抗体を包含する。
好ましい実施態様によれば、本発明は、配列番号12の配列、または配列番号12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の少なくとも1つのCDRを含んでなる重鎖を含んでなる、本発明による抗体またはその機能的断片に関する。
6つの短いCDR配列のうち、重鎖の3番目のCDR(CDRH3)は多様なサイズを有する(本質的にはそれをもたらす遺伝子の配列機構によって多様化)。知られている最長サイズは26であるが、2アミノ酸ほど短いこともある。機能上、CDRH3は抗体の特異性決定において部分的に役割を果たす(Segal et al., PNAS, 71: 4298-4302,頁 1974; Amit et al., Science, 233: 747-753頁, 1986; Chothia et al., J. Mol. Biol., 196: 901-917頁, 1987; Chothia et al., Nature, 342: 877-883頁, 1989; Caton et al., J. Immunol., 144: 1965-1968頁, 1990; Sharon et al., PNAS, 87: 4814-4817頁, 1990; Sharon et al., J. Immunol., 144: 4863-4869頁, 1990; Kabat et al., J. Immunol., 147: 1709-1719頁, 1991)。
抗体結合部位の構築にはCDRの低い割合のアミノ酸しか貢献しないが、これらの残基が極めて特異的な立体配座に維持されなければならないことは知られている。
より好ましくは、本発明は、配列番号8、10および12の配列の3つのCDRのうち少なくとも2つもしくは3つのCDR、または各々が配列番号8、10および12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRのうち少なくとも2つもしくは3つのCDRを含んでなる重鎖を含んでなる、本発明による抗体またはその機能的断片に関する。
同様に好ましい実施態様によれば、本発明は、配列番号2、4もしくは6の配列のCDR、または配列番号2、4もしくは6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列のCDRから選択される少なくとも1つのCDRを含んでなる軽鎖を含んでなる、本発明による抗体またはその機能的断片に関する。
より好ましい実施態様によれば、本発明は、配列番号2、4および6の配列の3つのCDRのうち少なくとも2つもしくは3つのCDR、または各々が配列番号2、4および6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRのうち少なくとも2つもしくは3つのCDRを含んでなる軽鎖を含んでなる、本発明による抗体またはその機能的断片に関する。
より好ましくは、本発明による抗体またはその機能的断片は、配列番号8、10および12の配列の3つのCDR、または各々が配列番号8、10および12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRを含んでなる重鎖を含んでなり、かつ、さらに、配列番号2、4および6の配列の3つのCDR、または各々が配列番号2、4および6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRを含んでなる軽鎖を含んでなる。
他の態様によれば、本発明は、ヒトインスリン受容体IRと結合しないか、または有意に結合しないことを特徴とする、本発明の抗体またはその機能的断片に関する。
好ましくは、本発明による機能的断片は、Fv断片、Fab断片、F(ab’)2断片、Fab'断片、scFv断片、scFv−Fc断片およびダイアボディから選択されるもの、またはペグ化断片などの化学修飾、特に、ペグ化によって、またはリポソームへの組込みによって半減期を延長させた機能的断片とされる。
他の態様によれば、本発明は、本発明によるモノクローナル抗体を分泌することができるマウスハイブリドーマ、特に、2001年9月19日にCentre National de Culture De Microorganisme(CNCM, National Center of Microorganism Culture)(Institut Pasteur, Paris, France)に番号I−2717として寄託されているようなマウス起源のハイブリドーマに関する。
2001年9月19日にCNCMに番号I−2717として寄託されたハイブリドーマによって分泌される、本明細書において7C10と呼ばれるモノクローナル抗体またはその機能的断片は、当然ながら本発明に包含される。
特定の実施態様によれば、本発明は、前記抗体が、配列番号54のアミノ酸配列、もしくは配列番号54の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる配列の軽鎖、または/および、配列番号69のアミノ酸配列、もしくは配列番号69の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる配列の重鎖を含んでなるものである、本発明によるマウス抗体またはその機能的断片に関する。
同様の特定の態様によれば、本発明は、前記抗体が、さらにマウスとは異種の種、特にヒトの抗体に由来する軽鎖および重鎖定常領域を含んでなるものであり、好ましくは、ヒト抗体由来の軽鎖および重鎖定常領域が、それぞれκ領域およびγ−1、γ−2またはγ-4領域である、本発明によるキメラ抗体またはその機能的断片に関する。
同様の特定の態様によれば、本発明は、前記抗体が、軽鎖および/または重鎖の骨格セグメントFR1〜FR4(実施例12および13、表5および6にて以下で記載するようなもの)がそれぞれヒト抗体軽鎖および/または重鎖の骨格セグメントFR1〜FR4に由来するものである軽鎖および/または重鎖を含んでなるものである、本発明によるヒト化抗体またはその機能的断片に関する。
好ましい実施態様によれば、本発明によるヒト化抗体またはその機能的断片において、前記ヒト化抗体は、配列番号61もしくは65のアミノ酸配列、または配列番号61もしくは65の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる軽鎖、または/および、配列番号75、79もしくは83のアミノ酸配列、または配列番号75、79もしくは83の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる重鎖を含んでなるものとされる。
好ましくは、本発明によるヒト化抗体またはその機能的断片において、前記ヒト化抗体は、配列番号65のアミノ酸配列を含んでなる軽鎖、および配列番号79または83、好ましくは配列番号83のアミノ酸配列を含んでなる配列の重鎖を含んでなるものとされる。
新規の態様によれば、本発明は、以下の核酸:
(a)本発明による抗体またはその機能的断片をコードする核酸、DNAまたはRNA、
(b)前記(a)に記載の核酸に相補的な核酸、および
(c)配列番号1、3、5、7、9、もしくは11の核酸配列、または配列番号1、3、5、7、9、もしくは11の配列との最適なアライメントにおいて少なくとも80%、好ましくは、85%、90%、95%および98%の同一性を有する配列の少なくとも1つのCDRと、高度ストリンジェンシー条件下でハイブリダイズすることができる少なくとも18個のヌクレオチドからなる核酸
から選択される、単離された核酸に関する。
(a)本発明による抗体またはその機能的断片をコードする核酸、DNAまたはRNA、
(b)前記(a)に記載の核酸に相補的な核酸、および
(c)配列番号1、3、5、7、9、もしくは11の核酸配列、または配列番号1、3、5、7、9、もしくは11の配列との最適なアライメントにおいて少なくとも80%、好ましくは、85%、90%、95%および98%の同一性を有する配列の少なくとも1つのCDRと、高度ストリンジェンシー条件下でハイブリダイズすることができる少なくとも18個のヌクレオチドからなる核酸
から選択される、単離された核酸に関する。
核酸、核配列または核酸配列、ポリヌクレオチド、オリゴヌクレオチド、ポリヌクレオチド配列、ヌクレオチド配列とは、本発明においては区別せずに使用され、改変または非改変ヌクレオチドの正確な連鎖を示すものであり、核酸の断片または領域を定義することを可能にし、非天然ヌクレオチドを含むかまたは含まず、二本鎖DNA、一本鎖DNAはもちろんのこと、そのDNAの転写産物に相当することもある。
本発明が、それらの天然の染色体環境における、すなわち、自然な状態でのヌクレオチド配列に関するものではないこともここで理解しなければならない。本発明は、単離され、および/または精製された配列に関するものであり、すなわち、それらは直接的または間接的に、例えばコピーによって、選択されたものであり、それらの環境は少なくとも部分的に改変されている。よって、本明細書において、それは、例えば、宿主細胞を用いた遺伝子組換えによって得られる、または化学合成によって得られる単離核酸もまた示すものである。
好適な配列との最適なアライメントにおいて少なくとも80%、好ましくは、85%、90%、95%および98%の同一性の割合(パーセント)を有する核配列とは、参照核配列に対して特定の改変、例えば、特に、欠失、末端切断、延長、キメラ融合および/または置換、特に、点置換を有する核配列を示すものである。好ましくは、それは、それに含まれる配列が、遺伝子コードの縮重に関連する参照配列と同じアミノ酸配列をコードする配列、または参照配列と、好ましくは、高ストリンジェンシー条件下、特に、以下に記載するような条件下で特異的にハイブリダイズすることができる相補配列に関する。
高ストリンジェンシー条件下でのハイブリダイゼーションは、温度条件およびイオン強度条件によって相補的DNAの2断片間でのハイブリダイゼーションの維持を可能にするようにそれらを選択することを示す。例として、上記のポリヌクレオチド断片を定義することを目的としたハイブリダイゼーション工程の高ストリンジェンシー条件は、以下のものが有利である。
DNA−DNAまたはDNA−RNAハイブリダイゼーションは2工程で実施される:(1)5×SSC(1×SSCは0.15M NaCl+0.015Mクエン酸ナトリウム溶液に相当する)、50%のホルムアミド、7%のドデシル硫酸ナトリウム(SDS)、10×Denhardt’s、5%の硫酸デキストランおよび1%のサケ精子DNAを含有するリン酸バッファー(20mM,pH7.5)中、42℃にて3時間のプレハイブリダイゼーション;(2)プローブのサイズに応じた温度(すなわち、プローブサイズ>100ヌクレオチドの場合には42℃)にて20時間の実際のハイブリダイゼーション、その後の2×SSC+2%SDSで20℃にて20分の2回洗浄、0.1×SSC+0.1%SDSで20℃にて20分の1回洗浄。最終洗浄は、プローブサイズ>100ヌクレオチドの場合、0.1×SSC+0.1%SDSで60℃にて30分間実施する。より大きなサイズまたはより小さなサイズのオリゴヌクレオチドの場合には、当業者ならば、規定サイズのポリヌクレオチドの上記高ストリンジェンシーハイブリダイゼーション条件を、Sambrookらの教示(1989, Molecular cloning: a laboratory manual. 第2版 Cold Spring Harbor)に従って適合させることができる。
本発明はまた、本発明による核酸を含んでなるベクターに関する。
本発明は、特に、本発明によるヌクレオチド配列を含むクローニングベクターおよび/または発現ベクターに関する。
本発明によるベクターは、好ましくは、所定の宿主細胞におけるヌクレオチド配列の発現および/または分泌を可能にするエレメントを含む。そのため、ベクターは、プロモーター、翻訳開始および終結シグナル、ならびに転写調節の好適な領域を含む必要がある。それは安定した形で宿主細胞中に維持されなければならず、所望により、翻訳されたタンパク質の分泌を指示する特定のシグナルを有していてもよい。これらの様々なエレメントは、用いる宿主細胞に応じて当業者により選択され、最適化される。この目的のために、本発明によるヌクレオチド配列は、選択された宿主の自己複製ベクターに挿入してもよいし、または選択された宿主の組換え型ベクターとしてもよい。
このようなベクターは、当業者によって現在使用される方法によって作製され、得られたクローンはリポフェクチン、エレクトロポレーション、熱衝撃、または化学的手法などの標準的方法によって好適な宿主に導入することができる。
本発明によるベクターは、例えば、プラスミドまたはウイルス起源のベクターである。それらは宿主細胞を形質転換して本発明によるヌクレオチド配列をクローニングする、または発現させるのに有用である。
本発明はまた、本発明によるベクターによって形質転換された、またはこれを含んでなる宿主細胞を包含する。
宿主細胞は、原核生物または真核生物系、例えば、細菌細胞から選択することができるが、同様に酵母細胞または動物細胞、特に、哺乳類細胞から選択することもできる。また、昆虫細胞または植物細胞を使用することもできる。
本発明はまた、本発明に従って形質転換された少なくとも1つの細胞を含んでなる、ヒトを除く動物に関する。
他の態様によれば、本発明は、以下の工程:
(a)本発明による宿主細胞を、培地および好適な培養条件において培養する工程、および
(b)このようにして産生した抗体またはその機能的断片を、培養培地または培養した前記細胞から回収する工程
を含んでなる、本発明による抗体またはその機能的断片の製造方法に関する。
(a)本発明による宿主細胞を、培地および好適な培養条件において培養する工程、および
(b)このようにして産生した抗体またはその機能的断片を、培養培地または培養した前記細胞から回収する工程
を含んでなる、本発明による抗体またはその機能的断片の製造方法に関する。
本発明による形質転換細胞は、本発明による組換えポリペプチドの製造方法に使用することができる。本発明によるベクターおよび/または本発明によるベクターによって形質転換された細胞を使用する、組換え型の本発明によるポリペプチドの製造方法は、それ自体が本発明に包含される。好ましくは、本発明によるベクターによって形質転換された細胞を、ポリペプチドの発現を可能にする条件下で培養し、組換えペプチドを回収する。
上述のように、宿主細胞は原核生物または真核生物系から選択することができる。特に、このような原核生物または真核生物系での分泌を促進する本発明によるヌクレオチド配列を同定することができるため、このような配列を有する本発明によるベクターは、分泌されるよう意図された組換えタンパク質の作製に有利に用いることができる。実際には、目的のこれらの組換えタンパク質の精製は、それらが宿主細胞内部よりもむしろ細胞培養物の上清に存在することによって容易になる。
また、化学合成によっても本発明によるポリペプチドを作製することができる。このような製造方法もまた、本発明の1つの態様である。当業者ならば、化学合成の方法、例えば、固相を使用する技術(特に、Steward et al., 1984, Solid phase peptide synthesis, Pierce Chem. Company, Rockford, 111, 第2版, (1984)を参照)または部分固相を用いる、断片の縮合による、または溶液中での古典的な合成による技術は理解している。化学合成によって得られた、対応する非天然アミノ酸を含み得るポリペプチドもまた、本発明に包含される。
本発明による方法によって得ることができる抗体またはその機能的断片もまた、本発明に包含される。
第二の実施態様によれば、本発明はさらに、ヒト上皮細胞増殖因子受容体(EGFR)と特異的に結合することができ、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害することができるものである、上述の本発明による抗体またはその機能的断片に関する。
一般に、増殖因子は正常細胞の増殖および分化の調節に関与する小タンパク質である。また、これらの増殖因子のいくつかは、細胞形質転換の開始および維持において重要な役割を果たし、オートクライン因子またはパラクライン因子として機能することができる。これは、特に、上述のIGF1に加えて、特に、腫瘍表現型の発現、腫瘍の進行および転移の発生に関与すると思われる上皮細胞増殖因子(EGF)にもあてはまる。
EGFおよびIGF1は、本明細書においてEGFRおよびIGF−IRと呼ばれるそれぞれの受容体を介してその作用を発揮する。2つの事例において、このことは数多くの癌でその過剰発現が報告されているチロシンキナーゼ活性を有する膜受容体に関係している。しかしながら、これら2つの受容体の相互作用が解明されておらず、これに関して種々のチームによって実施された研究において、これら2つの受容体の連携に関して矛盾する結果が得られていることに留意する必要がある。
前立腺腫瘍細胞で実施された研究では、抗EGFRモノクローナル抗体(本明細書において「MAB」または「MAb」と呼ばれる)によるオートクリンループEGF/EGFRの中断が、DU145細胞のIGF1に対する応答の完全喪失によって明示されることを示している(Connolly J. M. and Rose D, P., Prostate, Apr. 24 (4): 167-75頁, 1994; Putz T. et al., Cancer Res., Jan. 1, 59 (1): 227-33頁, 1999)。これらの結果からは、EGFに対する受容体の遮断が2つの受容体(EGFRおよびIGF−IR)の活性化によって生じる形質転換シグナルの完全阻害を得るのに十分なものであることが示唆される。一方、他の研究(Pietrzkowski et al., Cell Growth Differ, Apr., 3 (4):199-205頁, 1992; Coppola et al., Mol Cell Biol., Jul., 14 (7): 4588-95頁, 1994)では、IGF−IRは、その作用を媒介する役割としては、機能的EGFRの存在を必要としないが、EGFRの過剰発現はその有糸分裂誘発性および形質転換能を発揮するのに機能的IGF−IRの存在を必要とすることが示された。この2つ目の一連の研究は、2つの受容体に同時に作用することを目的として選択的にIGF−IRを遮断する傾向がある方法とより同調している。
驚くべきことに、発明者らは初めて、IGF1および/またはIGF2のIGF−IR受容体との結合およびEGFのEGFR受容体との結合の同時阻害によって、これら2つの受容体を発現する腫瘍を有するヌードマウスにおけるin vivo腫瘍増殖に対して得られるこれら2つの作用の有意な相乗効果が可能となることを立証した。この作用の相乗効果を説明することができるより有望な仮説の1つは、2つの増殖因子EGFおよびIGF1(および/またはIGF2)自身が、正常細胞の腫瘍特性を有する細胞への形質転換において、および/または特定の腫瘍、特に、2つの受容体EGFRおよびIGF−IRを過剰発現し、および/またはこれら2つの受容体、特に、これらの受容体のチロシンキナーゼ活性のレベルにて介在する変換シグナルの過剰活性化を有する腫瘍に関する腫瘍細胞の成長および/または増殖において相乗効果を発揮するというものである。
この実施態様の好ましい態様によれば、本発明は、EGFのEGFRとの結合を特異的に阻害し、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害する第二のモチーフを含んでなる二重特異性抗体からなるものである、上述のような抗体に関する。
「第二のモチーフ」という用語は、上記の、特に、EGFRと特異的に結合することができる断片、特に、抗EGFR抗体の可変鎖のCDR領域、またはこの特異的な結合を行うのに十分な長さのこのCDR領域の断片の1つ、あるいは抗EGFR抗体のいくつかのCDR領域を含んでなるアミノ酸の配列を示すものである。
二重特異性または二価性抗体は、同じ分子内に2つの異なる可変領域を併せ持つ第二世代のモノクローナル抗体である(Hollinger and Bohlen 1999 Cancer and metastasis rev. 18: 411-419頁)。それらの用途は、新しいエフェクター機能を補充し、または腫瘍細胞表面のいくつかの分子をターゲッティングするそれらの能力から、診断分野および治療分野の両方において実証されている。これらの抗体は、化学的手法(Glennie MJ et al. 1987 J. Immunol. 139, 2367-2375頁; Repp R. et al. 1995 J. Hemat. 377-382頁)または体細胞法(Staerz U. D. and Bevan M. J. 1986 PNAS 83, 1453-1457頁; Suresh M. R. et al. 1986 Method Enzymol. 121: 210-228頁)によるだけでなく、選択的に、ヘテロ二量化の強化を可能にし、それによって求められている抗体の精製方法を容易にする遺伝子工学技術(Merchand et al. 1998 Nature Biotech. 16: 677-681頁)によっても得ることができる。
これらの二重特異性抗体は、完全IgGとして、二重特異性Fab’2として、Fab'PEGとして、またはダイアボディとして、あるいは二重特異性scFvとしてだけでなく、ターゲッティングされた各抗原に対する2つの結合部位が存在する四価二重特異性抗体(Park et al. 2000 Mol. Immunol. 37 (18): 1123-30頁)または上述のようなその断片としても構築することができる。
二重特異性抗体の製造および投与は、2種類の特異的な抗体の製造よりも負担が少ないという事実からの経済上の利点に加え、このような二重特異性抗体の使用は処置の毒性を軽減するという利点も有している。これは、二重特異性抗体の使用が循環抗体総量の低減を可能にし、結果として、起こり得る毒性を軽減させていることによるものである。
本発明の好ましい実施態様によれば、二重特異性抗体は、二価または四価抗体である。
実際問題として、四価二重特異性抗体の使用への関心は、それが二価抗体と比較して、各標的、本発明においてはIGF−IRおよびEGFRのそれぞれに対する2つの結合部位が存在することから、より大きなアビディティを有することである。
上記の抗IGF−IR抗体の機能的断片の選択と同様に、第二のモチーフは、Fv断片、Fab断片、F(ab’)2断片、Fab’断片、scFv断片、scFv−Fc断片およびダイアボディから選択され、またはペグ化断片、例えば、Fv−PEG、scFv−PEG、Fab−PEG、F(ab’)2−PEGまたはFab’−PEGなどの、半減期を延長した形態とされる。本発明のさらに好ましい態様によれば、第二の抗EGFRモチーフは、マウスモノクローナル抗体225、そのマウス−ヒトキメラ誘導体C225、またはこの抗体225由来のヒト化抗体に由来するものである。
さらに他の態様によれば、本発明は、薬剤としての、本発明による抗体またはその機能的断片、好ましくは、上記のようなヒト化抗体に関する。以下の説明における抗体は、抗IGF−IR抗体、ならびに二重特異性抗IGF−IR/EGFR抗体として理解しなければならない。
本発明はまた、有効成分として、好ましくは賦形剤および/または医薬上許容されるビヒクルと混合した、本発明による抗体またはその機能的断片からなる化合物を含んでなる医薬組成物に関する。
さらに他の実施態様によれば、本発明はまた、EGFのヒト上皮細胞増殖因子受容体(EGFR)との結合を特異的に阻害することができ、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害することができる化合物から選択される第二の化合物を含んでなる、上述の医薬組成物に関する。
本発明の好ましい態様では、第二の化合物は、EGFのEGFRとの結合を競合によって阻害することができる単離された抗EGFR抗体またはその機能的断片から選択される。より詳しくは、抗EGFR抗体は、モノクローナル抗EGFR抗体、キメラ抗EGFR抗体もしくはヒト化抗EGFR抗体、またはその機能的断片から選択される。さらに詳しくは、抗EGFR抗体の機能的断片は、Fv断片、Fab断片、F(ab’)2断片、Fab'断片、scFv−Fc断片もしくはダイアボディから選択され、またはペグ化断片などの半減期を延長した断片とされる。前記抗体は、さらに好ましくは、マウスモノクローナル抗体225、そのマウス−ヒトキメラ誘導体C225(IMC−C225とも呼ばれる)、またはこの抗体225由来のヒト化抗体からなる。
本発明の他の実施態様によれば、同時使用、個別使用または逐次使用を目的とした組合せ製品として、細胞傷害性薬剤/細胞増殖抑制剤、ならびに/またはIGF−Iに対する受容体および/もしくはEGFに対する受容体のそれぞれのチロシンキナーゼ活性の阻害剤をさらに含んでなる、上記のような組成物が提供される。
「同時使用」とは、本発明による組成物の2種類の化合物の単一および同一医薬形態での投与と解釈される。
「個別使用」とは、本発明による組成物の2種類の化合物の異なる医薬形態での同時投与と解釈される。
「逐次使用」とは、本発明による組成物の2種類の化合物の各々が異なる医薬形態での連続的な投与と解釈される。
「逐次使用」とは、本発明による組成物の2種類の化合物の各々が異なる医薬形態での連続的な投与と解釈される。
一般に、本発明による組成物は癌の治療効果をかなり高める。言い換えれば、本発明による抗IGF−IR抗体の治療効果は、意外にも、細胞傷害性薬剤の投与によって増強される。本発明による組成物によって生まれるもう1つの重要なそれに続く利点は、副次的効果、特に、細胞傷害性薬剤の効果が現れる危険性、を回避する、または減少させることを可能にするより低い有効用量の有効成分の使用の可能性に関係する。
さらに、本発明によるこの組成物は、期待される治療効果がより迅速に達成されることを可能にする。
特に好ましい実施態様では、本発明による組合せ製品としての組成物において、細胞傷害性薬剤/細胞増殖抑制剤は、DNAと相互作用する薬剤、代謝拮抗物質、トポイソメラーゼIもしくはII阻害剤、または紡錘体形成阻害剤もしくは安定化剤、あるいは化学療法に用いることができる薬剤から選択されるものとされる。このような細胞傷害性薬剤/細胞増殖抑制剤は、上記種類の細胞傷害性薬剤のそれぞれに関しては、例えば、VIDALの2001年版、癌腫学および血液学コラム「細胞傷害性物質」の一部としてある化合物をテーマにした頁に挙げられており、本書に関して引用したこれらの細胞傷害性化合物は好ましい細胞傷害性薬剤として本明細書にて挙げている。
特に好ましい実施態様では、本発明による組合せ製品としての組成物において、細胞傷害性薬剤は、同時使用を目的とした抗体と化学的に結合しているものとされる。
特に好ましい実施態様では、本発明による組成物において、細胞傷害性薬剤/細胞増殖抑制剤は、紡錘体形成阻害剤または安定化剤、好ましくはビノレルビンおよび/またはビンフルニンおよび/またはビンクリスチンから選択されるものとされる。
細胞傷害性薬剤と本発明による抗体との結合を容易にするためには、特に、結合する2種類の化合物間にポリ(エチレン)グリコールのようなポリ(アルキレン)グリコールあるいはアミノ酸などのスペーサー分子を導入することができるし、または、もう1つの実施態様では、本発明による抗体と反応することができる官能基を導入した細胞傷害性薬剤の有効な誘導体を用いることができる。これらの結合技術は当業者には周知であり、本明細書では取り上げていない。
もう1つの好ましい実施態様では、IGF−Iに対する受容体および/またはEGFに対する受容体のチロシンキナーゼ活性の阻害剤は、誘導天然薬剤、ジアニリノフタルイミド、ピラゾロ−またはピロロピリドピリミジンあるいはキナジリンからなる群から選択される。このような阻害剤は当業者には周知であり、文献(Ciardiello F., Drugs 2000, Suppl. 1, 25-32頁)にて記載されている。
EGFRのその他の阻害剤としては、限定されるものではないが、抗EGFRモノクローナル抗体C225および22Mab(ImClone Systems Incorporated)、ABX−EGF(Abgenix/Cell Genesys)、EMD−7200(Merck KgaA)または化合物ZD−1834、ZD−1838およびZD−1839(AstraZeneca)、PKI−166(Novartis)、PKI−166/CGP−75166(Novartis)、PTK 787(Novartis)、CP 701(Cephalon)、レフルノマイド(Pharmacia/Sugen)、CI−1033(Warner-Lambert Parke-Davis)、CI−1033/PD 183、805(Warner-Lambert Parke-Davis)、CL−387、785(Wyeth-Ayerst)、BBR−1611(Boehringer Mannheim GmbH/Roche)、ナアミジナA(Bristol-Myers Squibb)、RC−3940−II(Pharmacia)、BIBX−1382(Boehringer Ingelheim)、OLX−103(Merck & Co)、VRCTC−310(Ventech Research)、EGF融合毒素(Seragen Inc.)、DAB−389(Seragen/Lilgand)、ZM−252808(Imperial Cancer Research Fund)、RG−50864(INSERM)、LFM−A12(Parker Hughes Cancer Center)、WHI−P97(Parker Hughes Cancer Center)、GW−282974(Glaxo)、KT−8391(Kyowa Hakko)または「EGFRワクチン」(York Medical/Centro de Immunologia Molecular)が挙げられる。
本発明のさらにもう1つの実施態様によれば、上記のような組成物はまた、さらに、癌、特に、HER2/neu受容体および受容体IGF−IRおよび/またはEGFRを過剰発現する癌、例えば、特に、乳癌、の予防および治療に向けた同時使用、個別使用または逐次使用を目的とした組合せ製品として、HER2/neu受容体の細胞外ドメインに対する他の抗体化合物を含んでなっていてもよい。
抗HER2/neu抗体を本発明による抗IGF−IR抗体と組み合わせることでの予想外の利益の妥当性を示す、特に、Albanell et at.(J. of the National Cancer Institute, 93 (24): 1830-1831頁, 2001)およびLu et al.(J. of the National Cancer Institute, 93 (24): 1852-1857頁, 2001)の出版物を参照のこと。
特に、本発明による組成物の抗HER2/neu抗体は、トラスツズマブ(Trastuzumab)と呼ばれる(ヘルセプチンとも呼ばれる)抗体である。
本発明は、もう1つの態様において、抗体またはその機能的断片の少なくとも1つが細胞毒素および/または放射性元素と結合していることを特徴とする組成物に関する。
好ましくは、毒素または放射性元素は、IGF−IR受容体および/またはEGFR受容体を発現する細胞の少なくとも1つの細胞活性を阻害することができるものとされ、より好ましくは、その細胞の成長または増殖を抑制し、特に、その細胞を完全に不活性化することができるものとされる。
また、好ましくは、毒素は、腸内細菌毒素、特に、シュードモナス(Pseudomonas)外毒素Aとされる。
好ましくは、治療に使用する抗体と結合する放射性元素(または放射性同位元素)は、γ線を放つ放射性同位元素とされ、好ましくは、ヨウ素131、イットリウム90、金199、パラジウム100、銅67、ビスマス217およびアンチモン211とされる。βおよびα線を放つ放射性同位元素もまた治療に用いることができる。
本発明による少なくとも1つの抗体またはその機能的断片と結合した毒素または放射性元素とは、毒素または放射性元素が少なくとも1つの抗体と、特に、結合分子を導入してまたはしない2つの化合物の共有結合によって結合可能であることを示すものである。
化学的(共有的)、静電的または非共有的に複合体の成分の全てまたは一部の結合を可能にする薬剤のうち、特に、ベンゾキノン、カルボジイミド、より詳しくは、EDC(塩酸1−エチル−3−[3−ジメチル−アミノプロピル]−カルボジイミド)、ジマレイミド、ジチオビス−ニトロ安息香酸(DTNB)、N−スクシンイミジル S−アセチル チオ−アセテート(SATA)、紫外線(U.V.)と反応する1以上のフェニルアジド基を有する架橋剤、好ましくは、N−[−4−(アジドサリチルアミノ)ブチル]−3’−(2’−ピリジルジチオ)−ピロピオンアミド(APDP)、N−スクシンイミド−イル3−(2−ピリジルジチオ)プロピオネート(SPDP)、6−ヒドラジノ−ニコチンアミド(HYNIC)が挙げられる。
特に、放射性元素の結合のもう1つの形式が二価イオンキレート化剤の使用にある。
これらのキレート化合物のうち、金属、特に、放射性金属の結合用に開発されたEDTA(エチレンジアミン四酢酸)から生じるキレート化合物またはDTPA(ジエチレントリアミン五酢酸)から生じるキレート化合物、および免疫グロブリンを挙げることができる。例えば、DTPAおよびその誘導体が炭素鎖にある異なる基と置き換わり、リガンド金属複合体の安定性および剛性を高めることができる(Krejcarek et al. (1977); Brechbiel et al. (1991); Gansow (1991); 米国特許第4 831 175号)。
例えば、長い間、医薬品において、生物学においては遊離形としてまたは金属イオンとの複合体のいずれかとして広く用いられてきたジエチレントリアミン五酢酸(DTPA)およびその誘導体は、金属イオンと安定したキレート化合物を形成し、治療目的または診断目的のタンパク質、例えば、癌治療における放射免疫複合体の開発用の抗体と結合する(Meases et al. (1984); Gansow et al. (1990)という注目すべき特徴を備えている。
また、好ましくは、本発明の複合体を形成する少なくとも1つの抗体がその機能的断片、特に、そのFc部分の切断された断片、例えば、scFv断片から選択される。
本発明はさらに、薬剤の製造のための、本発明による組成物の使用を包含する。
より詳しくは、もう1つの実施態様によれば、本発明は、IGF−IR受容体および/もしくはEGFR受容体の過剰発現および/もしくは異常な活性化によって引き起こされる病気、ならびに/または1−IGF1もしくはIGF2のIGF−IRとの相互作用および/もしくはEGFのEGFRおよび/もしくはHER2/neuとの相互作用が介在するシグナル変換経路の過反応に関連した病気の予防または治療に向けた薬剤の製造のための、抗体またはその機能的断片および/または組成物の使用に関する。
好ましくは、本発明による使用において、薬剤の投与は、インスリン受容体(IR)の阻害、すなわち、薬剤が存在することによる、特に、薬剤のIRとの結合に関連した競合的阻害によるIR受容体のその天然リガンドとの相互作用の阻害に関連した副次的効果を引き起こさない、またはわずかしか引き起こさない。
本発明はさらに、正常細胞の、腫瘍特性を有する細胞、好ましくは、IGF依存性細胞、特に、IGF1および/またはIGF2依存性細胞、および/またはEGF依存性細胞、および/またはHER2/neu依存性細胞への形質転換を阻害することを目的とした薬剤の製造のための、本発明による抗体またはその機能的断片、好ましくは、ヒト化されたもの、および/または組成物の使用を包含する。
本発明はまた、腫瘍細胞、好ましくは、IGF依存性細胞、特に、IGF1および/またはIGF2依存性細胞、および/またはEGF依存性細胞、および/またはエストロゲン依存性細胞、および/またはHER2/neu依存性細胞の成長および/または増殖を阻害することを目的とした薬剤の製造のための、本発明による抗体またはその機能的断片、好ましくは、ヒト化されたもの、および/または組成物の使用に関する。
一般に、本発明は、癌、好ましくは、IGF−IRおよび/またはEGFRを発現する癌および/または、好ましくは、IGF1またはIGF2のIGF−IRとの相互作用、例えば、IRS1の過剰発現など、および/またはEGFのEGFRとの相互作用が介在するシグナル変換経路の過反応を示す癌、の予防または治療に向けた薬剤の製造のための、本発明による抗体またはその機能的断片、好ましくは、ヒト化されたもの、および/または組成物の使用に関する。
本発明はまた、乾癬、その上皮細胞の過剰増殖がIGF−IRおよび/またはEGFRの発現または過剰発現および/またはIGF−IRのその天然リガンドとの相互作用および/またはEFGRのその天然リガンドとの相互作用が介在するシグナル変換経路の過反応と関連している可能性がある乾癬(Wraight C. J. et al. Nat. Biotechnol., 2000, 18 (5): 521-526頁. 乾癬における上皮細胞の過剰増殖のインスリン様増殖因子I受容体アンチセンスオリゴヌクレオチドによる逆転)の予防または治療に向けた薬剤の製造のための、本発明による抗体またはその機能的断片、好ましくは、ヒト化されたもの、および/または組成物の使用に関する。
予防および/または治療することができる癌としては、前立腺癌、骨肉腫、肺癌、乳癌、子宮内膜癌または結腸癌、あるいはIGF−IRを過剰発現するその他の癌が好ましい。
さらにもう1つの態様によれば、本発明は、IGF−IR受容体および/またはEGFR受容体の異常な存在が疑われる生物学的サンプルから、IGF−IR受容体および/またはEGFR受容体の過剰発現または過少発現、好ましくは過剰発現に関連した病気を、好ましくはin vitroにて診断する方法であって、生物学的サンプルを、必要に応じて標識することが可能である本発明による抗体またはその機能的断片と接触させることを特徴とする方法に関する。
好ましくは、その診断方法において、IGF−IR受容体および/またはEGFR受容体の過剰発現に関連した病気は、癌である。
抗体またはその機能的断片が検出可能なおよび/または定量可能なシグナルを得るためには、免疫複合体または標識抗体として存在してもよい。
本発明の標識された抗体またはその機能的断片としては、例えば、ペルオキシダーゼ、アルカリ性ホスファターゼ、α−D−ガラクトシダーゼ、グルコースオキシダーゼ、グルコースアミラーゼ、炭酸脱水酵素、アセチルコリンエステラーゼ、リゾチーム、リンゴ酸デヒドロゲナーゼまたはグルコース6−リン酸デヒドロゲナーゼなどの酵素と結合するか、またはビオチン、ジゴキシゲニンまたは5−ブロモデオキシウリジンなどの分子が結合する免疫複合体と呼ばれる抗体などが挙げられる。また、蛍光標識を本発明の抗体またはその機能的断片と結合してもよく、それらとしては、特に、フルオレセインおよびその誘導体、蛍光色素、ローダミンおよびその誘導体、GFP(GFPは「緑色蛍光タンパク質」)、ダンシル、ウンベリフェロンなどが挙げられる。このような複合体では、本発明の抗体またはその機能的断片を当業者には公知の方法によって作製することができる。それらは直接、またはスペーサー基またはグルタルアルデヒドのようなポリアルデヒド、エチレンジアミン四酢酸(EDTA)、ジエチレントリアミン五酢酸(DPTA)などの結合基を介して、または治療用複合体についての上記のものなどのカップリング剤の存在下にて、酵素または蛍光標識と結合させることができる。フルオレセインタイプの標識を有する複合体はイソチオシアネートとの反応によって作製することができる。
また、その他の複合体としては、ルミノールおよびジオキセタン類などの化学発光標識、ルシフェラーゼおよびルシフェリンなどの生物発光標識、あるいはヨウ素123、ヨウ素125、ヨウ素126、ヨウ素133、臭素77、テクネチウム99m、インジウム111、インジウム113m、ガリウム67、ガリウム68、ルテニウム95、ルテニウム97、ルテニウム103、ルテニウム105、水銀107、水銀203、レニウム99m、レニウム101、レニウム105、スカンジウム47、テルル121m、テルル122m、テルル125m、ツリウム165、ツリウム167、ツリウム168、フッ素18、イットリウム199、ヨウ素131などの放射性標識が挙げられる。治療用放射性同位元素の、直接または上記のEDTA、DTPAなどのキレート剤による抗体との結合についての、存在する当業者に公知の方法を、診断に用いることができる放射性元素に用いてよい。また、クロラミンT法[Hunter W. M. and Greenwood F. C. (1962) Nature 194: 495頁]によるNa[I125]での標識あるいはCrockford et al.(米国特許第4 424 200号)の技術によってまたはHnatowich(米国特許第4 479 930号)によって記載されるようなDTPAにより結合されるテクネチウム99mでの標識もまた挙げることができる。
例えば、本発明による抗体またはその機能的断片は、生物学的サンプルのIGF−IR受容体および/またはEGFR受容体の過剰発現または過少発現、好ましくは、過剰発現の検出方法および/もしくは定量方法に使用することができ、その方法は以下の工程:
(a)生物学的サンプルを、本発明による抗体またはその機能的断片と接触させる工程、および
(b)形成される可能性のあるIGF−IRおよび/またはEGFR/抗体複合体を実証する工程
を含んでなる。
(a)生物学的サンプルを、本発明による抗体またはその機能的断片と接触させる工程、および
(b)形成される可能性のあるIGF−IRおよび/またはEGFR/抗体複合体を実証する工程
を含んでなる。
特定の実施態様では、本発明による抗体またはその機能的断片を、IGFおよび/またはEGF依存性癌の予防的および/または治療的処置あるいは乾癬の予防的および/または治療的処置の効果をモニタリングするための、生物学的サンプルからのIGF−IR受容体および/またはEGFR受容体の検出方法および/もしくは定量方法に使用することができる。
より一般的には、本発明による抗体またはその機能的断片は、IGF−IR受容体および/またはEGFR受容体の発現を定性的および/または定量的に観察する必要のある状況で有利に使用することができる。
好ましくは、生物学的サンプルは、血清などの体液、全血、細胞、組織サンプルまたはヒト起源の生検からなる。
このような検出および/または投与を実施するためには任意の手順または従来の試験を用いてもよい。上記の試験は競合試験またはサンドウィッチ試験、あるいは抗体−抗原タイプの免疫複合体の形成に依存した当業者に公知の試験であってよい。本発明の適用後に、抗体またはその機能的断片を固定化してもよいし、または標識してもよい。この固定は当業者に公知の数多くの支持体上で行うことができる。これらの支持体はとしては、特に、ガラス、ポリスチレン、ポリプロピレン、ポリエチレン、デキストラン、ナイロン、または自然のままの細胞または改変細胞が挙げられる。これらの支持体は可溶性でも不溶性でもよい。
一例として、好ましい方法は免疫蛍光検査、またはラジオイムノアッセイ(RIA)技術または等価物によるELISA技術での酵素抗体法である。
よって、本発明はまた、IGF−IR受容体および/もしくはEGFR受容体の過剰発現もしくは過少発現によって引き起こされる病気の診断方法、または生物学的サンプルのIGF−IR受容体および/もしくはEGFR受容体の過剰発現もしくは過少発現、好ましくは、その受容体の過剰発現の検出方法および/もしくは定量方法を実施するのに必要なキットまたはセットであって、以下の要素:
(a)本発明による抗体またはその機能的断片、
(b)所望により、 免疫学的反応に適した培地を形成するための試薬、
(c)所望により、免疫学的反応によって生じるIGF−IR/抗体および/またはEGFR/抗体複合体の実証を可能にする試薬
を含んでなる、キットまたはセットを包含する。
(a)本発明による抗体またはその機能的断片、
(b)所望により、 免疫学的反応に適した培地を形成するための試薬、
(c)所望により、免疫学的反応によって生じるIGF−IR/抗体および/またはEGFR/抗体複合体の実証を可能にする試薬
を含んでなる、キットまたはセットを包含する。
本発明はさらに、癌、特に、細胞傷害性薬剤または抗HER2/neu抗体が一般に処方される癌、特に、その癌の腫瘍細胞がIGF−IR受容体および/またはEGFR受容体を発現または過剰発現する癌の予防または治療に向けた薬剤の製造のための、本発明による組合せ製品としての組成物の使用に関する。
本発明はまた、生物活性のある化合物の、IGF−IR受容体および/またはEGFR受容体を発現または過剰発現する細胞への特異的ターゲッティングを目的とする薬剤の製造のための、本発明による抗体の使用に関する。
本明細書において、生物活性のある化合物とは、細胞活性、特に、その成長、その増殖、転写または遺伝子翻訳を調節する、特に、阻害することができる化合物を示すものである。
本発明はまた、本発明による抗体またはその機能的断片、好ましくは、標識したもの、特に、放射性標識したものを含んでなるin vivo診断試薬、および、特に、IGF−IR受容体および/またはEGER受容体の細胞による発現または過剰発現に関連した癌の検出を目的とした医学的画像化におけるその使用に関する。
本発明はまた、本発明による組合せ製品としての組成物または薬剤としての、抗IGF−IRおよび/またはEGFR/毒素複合体または放射性元素に関する。
好ましくは、本発明による組合せ製品としての組成物または複合体は、賦形剤および/または医薬上許容されるビヒクルと混合される。
本明細書において、医薬上許容されるビヒクルとは、二次反応を誘発しない、例えば、活性化合物の投与を容易にし、そのライフスパンおよび/または体内でのその効果を長期化し、溶液中のその溶解度を高め、あるいはその保持を改善することを可能にする、医薬組成物の一部になる化合物または化合物の組合せを示すものである。これらの医薬上許容されるビヒクルは周知であり、選択された活性化合物の性質および投与の様式に応じて当業者が適合させる。
好ましくは、これらの化合物は全身経路によって、特に、静脈内経路によって、筋肉内、皮内、腹腔内または皮下経路によって、または経口経路によって投与される。より好ましくは、本発明の抗体を含んでなる組成物を逐次的に数回投与する。
その投与の様式、用量および最適な医薬形態は患者に適合させる、治療の確立において一般に考慮する基準、例えば、患者の年齢または体重、患者の一般的な状態の重篤度、治療に対する耐性および言及した副次的効果など、に従って決定することができる。
本発明のその他の特徴および利点は、下記実施例および以下にその説明を示す図面の説明にて示している。
実施例1:マウスモノクローナル抗体(MAb)の作製および選抜
IGF−IRに対して特異的に向けられ、IRを認識しないMAbの作製を目的として、6スクリーニング工程を含んでなるプロトコールを構想した。
IGF−IRに対して特異的に向けられ、IRを認識しないMAbの作製を目的として、6スクリーニング工程を含んでなるプロトコールを構想した。
このプロトコールは:
マウスに組換えIGF−IRで免疫性を与えて、ハイブリドーマを作製し、
培養物上清を免疫付与に役立つ組換えタンパク質についてELISAによりスクリーニングし、
ハイブリドーマ陽性の全ての上清をMCF−7腫瘍細胞表面で過剰発現される天然受容体についてELISAにより試験し、
IGF−IRまたはIR各々を発現するバキュロウイルスに感染した昆虫細胞でのIGF−IRおよびIRの認識差に関する2種類の最初のスクリーニングにてハイブリドーマ陽性の上清を評価し、
この工程で選抜された抗体がMCF−7細胞の誘導されたIGF1増殖をin vitroにて阻害できることを実証し、
腫瘍MCF−7の増殖に対する影響という点から保持された候補のヌードマウスにおけるin vivo活性を保証する
ことにある。
マウスに組換えIGF−IRで免疫性を与えて、ハイブリドーマを作製し、
培養物上清を免疫付与に役立つ組換えタンパク質についてELISAによりスクリーニングし、
ハイブリドーマ陽性の全ての上清をMCF−7腫瘍細胞表面で過剰発現される天然受容体についてELISAにより試験し、
IGF−IRまたはIR各々を発現するバキュロウイルスに感染した昆虫細胞でのIGF−IRおよびIRの認識差に関する2種類の最初のスクリーニングにてハイブリドーマ陽性の上清を評価し、
この工程で選抜された抗体がMCF−7細胞の誘導されたIGF1増殖をin vitroにて阻害できることを実証し、
腫瘍MCF−7の増殖に対する影響という点から保持された候補のヌードマウスにおけるin vivo活性を保証する
ことにある。
これらの異なる工程および得られた結果の全てを以下の実施例1にて簡単に説明する。
免疫付与工程では、マウスに皮下経路により8μgの組換えIGF−IRを2回注射した。雌ラットの細胞のマウス骨髄腫Sp20Ag14の細胞との融合3日前に、3μgの組換え受容体の静脈注射によりマウスを刺激した。 融合14日後、上清のハイブリドーマを組換えIGF−IRにより感作されたプレートにおいてELISAによりスクリーニングした。陽性であることが分かった上清のハイブリドーマを保持し、増幅した後に、産生した抗体もまた、天然IGF−IRを認識することができることを実証するためにFACScanで試験した。これをを行うために、ELISAにて選抜したハイブリドーマによって産生された培養上清各々とともにIGF−IRを過剰発現するエストロゲン依存性乳房腫瘍由来のMCF−7細胞をインキュベートした。細胞表面の天然/MAb受容体複合体は蛍光色素と結合した二次抗種(anti-species)抗体によって顕示された。図3A〜3Cはハイブリドーマ7C10の上清(図3C)で得られたヒストグラムタイプと細胞標識単独+二次抗体の場合(図3A)または対照のイソタイプを用いた標識の場合(図3B)との比較を示す。
選抜のこの工程にて、MAbを分泌し、同時に、組換え受容体および天然受容体を認識するハイブリドーマだけを選抜し、クローニングした。これらのハイブリドーマによって分泌されるMAbを産生させ、次いで、精製した後に、同時に2種類の受容体を認識するハイブリドーマを排除するために、上記の方法に従って、IGF−IRまたはIRを発現するSf9昆虫細胞にてFACScanで試験した。図4Aは非感染細胞+二次抗体(1)、αIR3で標識した非感染細胞+二次抗体(2)および抗IR抗体で標識した非感染細胞+二次抗体(3)各々に対応するヒストグラム1、2、3を完全再編したものを示す。この最初の結果はこれらの非感染昆虫細胞の表面において検出可能なIGF−IRおよびIRが存在しないことを十分に示している。図4BはIGF−IRを発現するバキュロウイルスに感染した細胞の標識を示す。この2番目の図では、正の対照として用いたαIR3が、予想どおりに細胞を十分に標識付けしている(ピーク2)が、一方、抗IRは細胞単独のピークに重なっている(ピーク3)。最後に、図4Cでは、抗IRは予想どおりにIRを発現するSf9細胞を十分に標識付けしている(ピーク3)が、意外なことに、文献にて、IGF−IRに対して特異的であると記載されるαIR3もまたIRを認識すると考えられる(ピーク2)ことが示される。
この3番目のスクリーニング系で得られた結果を表1にまとめ、IGF−IRの認識およびIRの非認識の基準を満たすMAb:7C10の製造を示す。MAb 7C10のイソタイプ割り出しからそれがIgG1を含むことが分かった。
MAbの選抜に提供された最後の2つのスクリーニングは、後者のものが細胞系MCF−7においてIGF−1によって誘導されるin vitroおよびin vivo細胞増殖をかなり阻害することができることを実証することにあった。
in vitro選抜では、MCF−7細胞を接種し、ウシ胎児血清を除いた後、漸増濃度のIGF−1(1〜50ng/ml)の存在下、最終濃度10μg/mlまで添加する調べる7C10抗体の存在または不在下でインキュベートした。この試験では、αIR3 MAb市販品を正の対照として用い、7G3 MAb(7C10と同時に単離され、天然受容体を弱く認識する(FACSでのMFIはMAb 7C10の200に対して50))を対照のイソタイプとして用いる。細胞増殖をβカウンターにて、細胞によるトリチウム化したチミジンの取り込みにより推定する。結果を増殖指数として表す。図5にて示されたデータからは、IGF1は用量依存的にMCF−7細胞の増殖を刺激することができることが分かる。正の対照として用いたMAb αIR3はIGF−1によって誘導されるMCF−7細胞の増殖を完全に阻害する。同様に、MAb 7C10はIGF−1によって誘導されるMCF−7細胞の増殖を有意に阻害する。最後に、イソタイプ対照として用いるMAb 7G3は、予想どおりにMCF−7細胞のin vitro腫瘍細胞増殖に対する影響なくうまくいく。
確立された腫瘍モデルにてin vivo選抜を実施した。これを行うために、ヌードマウスはマウスモデルにおける腫瘍の調査に不可欠な徐放性エストロゲン皮下埋め込みを受けた。エストロゲンの埋め込み24時間後、5.106MCF−7細胞をマウスの右側皮下に移植する。この細胞移植5日後、腫瘍は測定可能であり、6マウス群をランダムに形成する。週2回、5〜6週間、250μg/1回用量/マウスの用量にてマウスの処置を行った。対照群では、マウス対照イソタイプと同様にマウスを処置する。図6Aにて示された結果からは、抗体7C10によって誘導される腫瘍増殖の極めて有意な阻害が示される。通常IGF1に対する受容体のドメインの参照としても用いられ、エストロゲン依存性腫瘍の増殖に対してin vivoでの活性を有さないことで知られているαIR3に関して入手可能なデータを参照する場合、この活性はとりわけ予想外のことである(図6Bを参照)。同様に、マウスMAb 1H7由来の組換え抗体scFv−Fcで得られた結果(図6Cを参照)と比較すると、MAb 7C10はMCF−7細胞の増殖のin vivo阻害においてはるかに有効である。
実施例2:腫瘍MCF−7のin vivo増殖に対する7C10およびタモキシフェンの効果の比較
エストロゲン依存性乳癌に関する抗体7C10による処置の有効性を決定する目的として、7C10を乳癌の治療に現在用いられているタモキシフェン化合物と局部進行および/または転移性進行の発展および再発の予防に関して比較した(VIDAL 2000, 1975-1976頁参照)。
エストロゲン依存性乳癌に関する抗体7C10による処置の有効性を決定する目的として、7C10を乳癌の治療に現在用いられているタモキシフェン化合物と局部進行および/または転移性進行の発展および再発の予防に関して比較した(VIDAL 2000, 1975-1976頁参照)。
ホルモン依存性乳癌では、エストロゲンに対する受容体(ER)の発現およびIGF−IRの発現間に重大な関連が存在する(Surmacz E. et al., Breast Cancer Res. Treat., Feb., 47 (3): 255-267頁, 1998)。さらに、エストロゲン(E2)はIGF1(IGF−IまたはIGFIと記載している場合もある)と相乗作用して細胞増殖を刺激すると思われる。E2による処置によってIGF−IRのmRNAレベル、ならびにタンパク質の発現レベルが約10倍高まることが実際に示されている(Lee A. V. et al., Mol. Endocrinol., May, 13 (5): 787-796頁, 1999)。この高まりではIGF−IRのリン酸化の有意な増加が認められる。さらに、E2はリン酸化されるIGF−IRの基質の1つであるIRS−1(「IRS−1」は「インスリン受容体基質−1」)の発現を有意に刺激する。
タモキシフェンはE2依存性乳癌を患う患者に向けたホルモン療法に長年の間広く用いられてきた(Forbes J. F., Semin. Oncol., Feb., 24 (1st Suppl. 1): S1-5-S1-19, 1997)。この分子はエストラジオールと競合して、これのその受容体との結合を阻害する(Jordan V. C., Breast Cancer Res. Treat., 31 (1): 41-52頁, 1994)。タモキシフェンが受容体の発現およびそのリン酸化を阻害することによりIGF−IR依存性増殖を阻害することができることがさらに実証された(Guvakova M. A. et al., Cancer Res., July 1, 57 (13): 2606-2610頁, 1997)。これらのデータは総じて、IGF−IRがE2/ER相互作用によって誘導される増殖の重要なメディエーターであることを示しているように思われる。
タモキシフェンの長期使用は子宮内膜癌(Fisher et al., J. of National Cancer Institute, 86, 7: 527-537頁, 1994; VIDAL 2000, 1975-1976)およびE2非依存性乳癌の付帯再発(Li C. I. et al., J. Natl. Cancer Inst., July 4, 93 (13): 1008-1013頁, 2001)の危険性の著しい増加と関連している。これに関連して、MCF−7モデルで抗体7C10およびタモキシフェンのin vivo抗腫瘍効果の比較を実施し、媒介するER増殖におけるIGF−IRと関連した活性の一部を決定した。これを行うために、ヌードマウスでの、この動物種におけるE2依存性ヒト腫瘍の確立に不可欠な持続性放出型エストラジオール粒子(0.72mg/錠剤、60日間作用)の埋め込み24時間後、7.106MCF−7細胞をこれらの同じマウスのsc(皮下に)移植した。この移植の5日後、腫瘍は測定可能であり、6マウス群を形成する。これらの群を各々、1)250μg/マウスの用量にて、週2回、ip(腹腔内)注射される7C10抗体により、2)3%のヒドロキシプロピルセルロース(HPC)を含有するPBSに含まれた10μgのタモキシフェンによりipにて、または3)タモキシフェンが溶けた溶媒(ヒドロキシプロピルセルロース)により処置する。タモキシフェンを週末を除いて毎日、4週間投与する。MAb 7C10により処置したマウスはまた、毎日、3%HPCを含有するPBSの注射も受ける。溶媒単独では腫瘍増殖に対する影響がないことを実証するために、予め試験を行った。
図7にて示された結果からは、MAb 7C10が腫瘍MCF−7の増殖を有意にin vivo阻害することができることが分かる(アスタリスク(*)はt検定における比較対照群/7C10群に相当する)。驚くべきことに、抗体7C10は腫瘍増殖の阻害に関してタモキシフェンよりも有意に効果があると思われ(サークル(°)はt検定における比較タモキシフェン群/7C10群に相当する)、タモキシフェンでの処置の代わりにMAbによるこの種の処置を用いてもよいことが示唆される。
実施例3:異なる起源のヒト腫瘍に対するMAb 7C10のin vivoにおける抗腫瘍活性の実証
a)3種類の腫瘍モデルにおける抗体7C10のin vivo活性
IGF1に対する受容体を発現するその他の腫瘍に対する7C10抗体の活性を一般化するために、アンドロゲン非依存性前立腺腫瘍モデルDU145(DU−145とも記載)、SKES−1骨肉腫モデルおよび非小細胞肺腫瘍モデルA549において7C10をin vivoで試験した。プロトコールはMCF−7に関し以上で記載したものと同様であり、図8A〜8Cにて示された結果からは、3種類の腫瘍モデルにおいてのこのMABの有意な活性が示される。MAB 1H7の単鎖scFvはアンドロゲン非依存性前立腺腫瘍モデルにおいて活性がないため、前立腺腫瘍モデルにて観察された活性は極めて特に注目すべきである(Li et al., 2000)
a)3種類の腫瘍モデルにおける抗体7C10のin vivo活性
IGF1に対する受容体を発現するその他の腫瘍に対する7C10抗体の活性を一般化するために、アンドロゲン非依存性前立腺腫瘍モデルDU145(DU−145とも記載)、SKES−1骨肉腫モデルおよび非小細胞肺腫瘍モデルA549において7C10をin vivoで試験した。プロトコールはMCF−7に関し以上で記載したものと同様であり、図8A〜8Cにて示された結果からは、3種類の腫瘍モデルにおいてのこのMABの有意な活性が示される。MAB 1H7の単鎖scFvはアンドロゲン非依存性前立腺腫瘍モデルにおいて活性がないため、前立腺腫瘍モデルにて観察された活性は極めて特に注目すべきである(Li et al., 2000)
b)同所移植モデルA549における抗体7C10のin vivo活性
上記の従来の異種移植片モデルでは転移性播種についての薬剤の試験ができない。実際に、s.c.(皮下に)移植した腫瘍は注入した位置に限局された状態のままであるため、実際にはヒトの場合の状況を反映していない。我々の抗体を現実に近いモデルにて評価するために、A549細胞を胸腔内位置に移植した。このモデルは十分に記載されており(Clin. Cancer Res. 2000 Jan; 6 (1): 297-304頁)、縦隔、肺、心臓および脊椎転移について、ヒトで観察されるものに近い転移性播種の観察がなされる。実施した試験では、106 A549細胞を雌ヌードマウスに胸腔内注射した。移植7日後、マウスを22匹からなる2群に分けた。これらの群の一方は500μg/マウスの抗原投与を受けた後、週2回、250μgの7C10/1回用量の割合で処置した。もう1つの群は対照イソタイプ9G4と同じスキームによって処置した。図31はMAB 7C10により処置したマウスにおいて生存の有意な延長を示し、このことからこの抗体が転移性播種においてある作用を有し得ることが分かる。
上記の従来の異種移植片モデルでは転移性播種についての薬剤の試験ができない。実際に、s.c.(皮下に)移植した腫瘍は注入した位置に限局された状態のままであるため、実際にはヒトの場合の状況を反映していない。我々の抗体を現実に近いモデルにて評価するために、A549細胞を胸腔内位置に移植した。このモデルは十分に記載されており(Clin. Cancer Res. 2000 Jan; 6 (1): 297-304頁)、縦隔、肺、心臓および脊椎転移について、ヒトで観察されるものに近い転移性播種の観察がなされる。実施した試験では、106 A549細胞を雌ヌードマウスに胸腔内注射した。移植7日後、マウスを22匹からなる2群に分けた。これらの群の一方は500μg/マウスの抗原投与を受けた後、週2回、250μgの7C10/1回用量の割合で処置した。もう1つの群は対照イソタイプ9G4と同じスキームによって処置した。図31はMAB 7C10により処置したマウスにおいて生存の有意な延長を示し、このことからこの抗体が転移性播種においてある作用を有し得ることが分かる。
実施例4:in vivoにおけるMAb 7C10のナベルビンとの比較;2種類の処置の併用効果
ナベルビンは非小細胞肺癌および転移性乳癌に適応とされる化学療法用化合物である。7C10およびナベルビンの比較試験、ならびに2種類の製品間で起こり得る相乗効果を腫瘍モデルA549にて試験した。この試験では、5.106A549細胞ををマウスの右側皮下に移植する。細胞移植5日後、腫瘍は測定可能であり、MAbおよび/またはナベルビンによる処置を開始する。抗体は常に250μg/1回用量/マウス、週2回、腹腔内にて投与する。ナベルビンに関しては、マウスの最大許容量または10mg/kg、腹腔内にて投与する。この処置では、7日おきに3回の注入を行う。同時投与では、注入前に2種類の製品を混合する。
ナベルビンは非小細胞肺癌および転移性乳癌に適応とされる化学療法用化合物である。7C10およびナベルビンの比較試験、ならびに2種類の製品間で起こり得る相乗効果を腫瘍モデルA549にて試験した。この試験では、5.106A549細胞ををマウスの右側皮下に移植する。細胞移植5日後、腫瘍は測定可能であり、MAbおよび/またはナベルビンによる処置を開始する。抗体は常に250μg/1回用量/マウス、週2回、腹腔内にて投与する。ナベルビンに関しては、マウスの最大許容量または10mg/kg、腹腔内にて投与する。この処置では、7日おきに3回の注入を行う。同時投与では、注入前に2種類の製品を混合する。
図9にて示された結果からは、驚くべきことに、このモデルにおいて、抗体7C10がナベルビンでの従来の処置と同じくらい有効であることが分かる。2種類の製品の極めて有意な相乗効果もまた、72日で測定可能な腫瘍を有する7マウスのうちの5マウスにて観察される。
実施例5:MCF−7腫瘍のIGF2誘導性増殖のin vitro阻害の試験
上記のように、IGF−IRは数多くの腫瘍によって過剰発現されるが、さらに乳癌および結腸癌の大部分において、特に、増殖シグナルがIGF−II(IGF−IIまたはIGFIIと記載している場合もある)を介してこの受容体に送られることも記載されてきた。そのため、MAb 7C10がまた確実にin vitroにてMCF−7腫瘍で誘導されるIGF2増殖を阻害し得ることも必要である。これを行うために、細胞を96−ウェルプレートに接種し、ウシ胎児血清を除き、10μg/mlの濃度にて添加する調べるMAbの存在および不在下で最終濃度の培地ml当たり200ngのIGF2を添加して刺激した。図10にて示された結果からは、IGF2がIGF1と同様に、MCF−7細胞の増殖を有意に刺激することが分かる。対照のイソタイプ、9G4を添加した場合は依然この刺激への影響はない。De Leon et al.(Growth Factors, 6: 327-334頁, 1992)によってすでに記載されているように、MAb αIR3の添加によって認められた影響はない。一方、7C10はIGF2によって誘導される増殖を完全に阻害する。その活性は1H7のものよりも有意に優れている。
上記のように、IGF−IRは数多くの腫瘍によって過剰発現されるが、さらに乳癌および結腸癌の大部分において、特に、増殖シグナルがIGF−II(IGF−IIまたはIGFIIと記載している場合もある)を介してこの受容体に送られることも記載されてきた。そのため、MAb 7C10がまた確実にin vitroにてMCF−7腫瘍で誘導されるIGF2増殖を阻害し得ることも必要である。これを行うために、細胞を96−ウェルプレートに接種し、ウシ胎児血清を除き、10μg/mlの濃度にて添加する調べるMAbの存在および不在下で最終濃度の培地ml当たり200ngのIGF2を添加して刺激した。図10にて示された結果からは、IGF2がIGF1と同様に、MCF−7細胞の増殖を有意に刺激することが分かる。対照のイソタイプ、9G4を添加した場合は依然この刺激への影響はない。De Leon et al.(Growth Factors, 6: 327-334頁, 1992)によってすでに記載されているように、MAb αIR3の添加によって認められた影響はない。一方、7C10はIGF2によって誘導される増殖を完全に阻害する。その活性は1H7のものよりも有意に優れている。
実施例6:キメラ7C10(C7C10)抗体およびヒト化(h7C10)抗体の生物活性
a)in vitroにおけるMCF−7モデルでの7C10/C7C10および7C10/h7C10の比較
上記のように、MCF−7モデルにおいてキメラ型のMAb 7C10および精製ヒト化型1(本明細書においては7H2HMと記載)をin vitroにて試験した。図11および12各々にて示された結果からは、これら2種類のものがMCF−7腫瘍のIGF1誘導性増殖を阻害するというそれらの特性を完全に保持していることが分かる。
a)in vitroにおけるMCF−7モデルでの7C10/C7C10および7C10/h7C10の比較
上記のように、MCF−7モデルにおいてキメラ型のMAb 7C10および精製ヒト化型1(本明細書においては7H2HMと記載)をin vitroにて試験した。図11および12各々にて示された結果からは、これら2種類のものがMCF−7腫瘍のIGF1誘導性増殖を阻害するというそれらの特性を完全に保持していることが分かる。
b)IGF1のその受容体との結合によって誘導されるシグナルの変換に対するMAb 7C10および7C10の比較効果
系統MCF−7においてin vitroにて誘導されたIGF1増殖の阻害活性はMAb7C10のその受容体との結合時にIGF1が介在するシグナルの変換の阻害の翻訳のはずである。この仮説を実証するために、MCF−7細胞を調べる抗体の存在またはの不在下、IGF1を加えてまたは加えずにインキュベートした。短時間のインキュベーションの後、細胞を溶解し、β鎖を免疫沈降させ、このサブユニットのリン酸化を抗ホスホチロシンキナーゼ抗体を用いて推定した。図13にて示された結果からは、無関係のマウス抗体(9G4)またはヒト抗体(スキームではIgG1と記載)とは異なり、7C10またはh7C10の結合によってIGF−IRのβサブユニットのリン酸化を有意に阻害することが分かる。
系統MCF−7においてin vitroにて誘導されたIGF1増殖の阻害活性はMAb7C10のその受容体との結合時にIGF1が介在するシグナルの変換の阻害の翻訳のはずである。この仮説を実証するために、MCF−7細胞を調べる抗体の存在またはの不在下、IGF1を加えてまたは加えずにインキュベートした。短時間のインキュベーションの後、細胞を溶解し、β鎖を免疫沈降させ、このサブユニットのリン酸化を抗ホスホチロシンキナーゼ抗体を用いて推定した。図13にて示された結果からは、無関係のマウス抗体(9G4)またはヒト抗体(スキームではIgG1と記載)とは異なり、7C10またはh7C10の結合によってIGF−IRのβサブユニットのリン酸化を有意に阻害することが分かる。
c)7H2HM抗体のADCC機構への関与
パラグラフb)での上記のシグナル変換の阻害は抗体7C10および7H2HMの生物活性に関与する作用の重要な機構である。しかしながら、ヒトへの投与ではイソタイプIgG1の抗体7H2HMがADCC(抗体依存性細胞傷害作用)タイプの機構によって細胞溶解を誘導し得るであろうと考えられる。この点を実証するために、ヒトドナーの末梢血由来のNK(ナチュラルキラー)細胞を5.105細胞当たり10μgの7H2HM抗体とともに4時間、予めインキュベートしたA549細胞またはMCF−7細胞の存在下に置き、51Cr(50μg)で標識する。この試験では、ヘルセプチン(図32Aおよび32Bではh4D5と記載)を試験の正の対照として用いる。図32A〜32Dからは、予想どおりにヘルセプチンが2種類の細胞A549およびMCF−7において有意なADCCを誘導すること(各々図32Aおよび32Bを参照)が分かる。7H2HMもまた、A549細胞においてADCCを誘導することができる(図32Cを参照)が、MCF7細胞におけるこの現象の大きさは小さいものである(図32Dを参照)。
パラグラフb)での上記のシグナル変換の阻害は抗体7C10および7H2HMの生物活性に関与する作用の重要な機構である。しかしながら、ヒトへの投与ではイソタイプIgG1の抗体7H2HMがADCC(抗体依存性細胞傷害作用)タイプの機構によって細胞溶解を誘導し得るであろうと考えられる。この点を実証するために、ヒトドナーの末梢血由来のNK(ナチュラルキラー)細胞を5.105細胞当たり10μgの7H2HM抗体とともに4時間、予めインキュベートしたA549細胞またはMCF−7細胞の存在下に置き、51Cr(50μg)で標識する。この試験では、ヘルセプチン(図32Aおよび32Bではh4D5と記載)を試験の正の対照として用いる。図32A〜32Dからは、予想どおりにヘルセプチンが2種類の細胞A549およびMCF−7において有意なADCCを誘導すること(各々図32Aおよび32Bを参照)が分かる。7H2HMもまた、A549細胞においてADCCを誘導することができる(図32Cを参照)が、MCF7細胞におけるこの現象の大きさは小さいものである(図32Dを参照)。
d)抗体7C10および7H2HMの細胞周期に対する効果
系統MCF−7においてin vitroにて観察される細胞増殖の阻害は細胞周期に対する効果により明らかになるはずである。この事柄に答えるために、4.105細胞を6−ウェルプレートに接種する。接種24時間後、ウシ血清を除き、調べる抗体の存在または不在下でIGF1を添加する。24時間のインキュベーション後、細胞周期の試験用に細胞を回収する。図33BはIGF1の不在下でのMCF−7細胞の周期および増殖の開始(図33Aを参照)と比較した、IGF1のMCF−7細胞の周期および増殖の開始に対する効果を示している。増殖因子の添加後、G0/G1期(88.2%〜56.3%)の有意な減少〜 S期(7.8%〜31%)およびG2/M期(4%〜12.7%)のその恩恵が観察される。抗体7C10および7H2HMの添加により(図33Cを参照)、周期開始の有意な阻害が認められる。マウス抗体およびそのヒト化相同体が細胞周期に対して同程度の活性を有するということも注意すべきである。正の対照として取り入れたαIR3は、この試験において7C10および7H2HMよりも少し活性が低いと思われる。対照のイソタイプとして用いた抗体9G4には細胞周期に及ぼす効果はない。
系統MCF−7においてin vitroにて観察される細胞増殖の阻害は細胞周期に対する効果により明らかになるはずである。この事柄に答えるために、4.105細胞を6−ウェルプレートに接種する。接種24時間後、ウシ血清を除き、調べる抗体の存在または不在下でIGF1を添加する。24時間のインキュベーション後、細胞周期の試験用に細胞を回収する。図33BはIGF1の不在下でのMCF−7細胞の周期および増殖の開始(図33Aを参照)と比較した、IGF1のMCF−7細胞の周期および増殖の開始に対する効果を示している。増殖因子の添加後、G0/G1期(88.2%〜56.3%)の有意な減少〜 S期(7.8%〜31%)およびG2/M期(4%〜12.7%)のその恩恵が観察される。抗体7C10および7H2HMの添加により(図33Cを参照)、周期開始の有意な阻害が認められる。マウス抗体およびそのヒト化相同体が細胞周期に対して同程度の活性を有するということも注意すべきである。正の対照として取り入れたαIR3は、この試験において7C10および7H2HMよりも少し活性が低いと思われる。対照のイソタイプとして用いた抗体9G4には細胞周期に及ぼす効果はない。
e)iモデルA549における抗体7C10および7H2HMのn vivo比較活性
ヒト化抗体7H2HMのin vivo活性を確認するため、後者を非小細胞肺腫瘍モデルA549において7C10と比較した。この試験は、抗体量が250μg/1回用量、週2回の代わりに125μg/1回用量、週2回であること、および大量の7H2HMが入手不可能であるという事実を除いて、上記のとおり正確に実施した。抗体9G4を7C10に対するイソタイプの対照として用い、イソタイプの無関係のヒト免疫グロブリンIgG1(以下ではHIgG1と呼ばれる)をヒト化抗体7H2HMに対する対照として用いた。
ヒト化抗体7H2HMのin vivo活性を確認するため、後者を非小細胞肺腫瘍モデルA549において7C10と比較した。この試験は、抗体量が250μg/1回用量、週2回の代わりに125μg/1回用量、週2回であること、および大量の7H2HMが入手不可能であるという事実を除いて、上記のとおり正確に実施した。抗体9G4を7C10に対するイソタイプの対照として用い、イソタイプの無関係のヒト免疫グロブリンIgG1(以下ではHIgG1と呼ばれる)をヒト化抗体7H2HMに対する対照として用いた。
図34Aからは、9G4およびHIgG1対照曲線間に有意差がないことが分かる。予想どおりに、マウス抗体7C10において腫瘍増殖の有意な阻害が認められる。ヒト化抗体7H2HMに関しては、認められた活性がそのマウス対照物において認められるものと厳密に同じ強さのものである。このデータはin vitroでの上記の観察結果に加えて、ヒト化によって作製された抗体の特性が改変されないことを示している。また、マウスの異種移植片モデルでは、ヒト化抗体の活性がシグナルの変換の阻害機構に完全に関連していると思われる。実際には、ADCCがヌードマウスにおける腫瘍増殖の阻害に影響を及ぼしている場合には、マウス抗体およびヒト化抗体の活性間に差が認められるであろう。
また、in vivo試験をMCF−7乳房腫瘍モデルにおいて実施し、この試験により、予想どおりに、抗体7H2HMがこの腫瘍の増殖のin vivo阻害に関し、マウス抗体7C10と完全に同程度であることが示される(図34B)。
f)7H2HMおよびナベルビン間の相乗効果の実証
7C10で得られた結果の再現を目的として、そのヒト化相同体:抗体7H2HMについて実施例4に記載のプロトコールを繰り返した。
図35Aおよび35Bにて示された結果からは、7C10の場合と同様に、ヒト化抗体7H2HMおよびナベルビン間の有意な相乗効果が示されることが分かる。
7C10で得られた結果の再現を目的として、そのヒト化相同体:抗体7H2HMについて実施例4に記載のプロトコールを繰り返した。
図35Aおよび35Bにて示された結果からは、7C10の場合と同様に、ヒト化抗体7H2HMおよびナベルビン間の有意な相乗効果が示されることが分かる。
g)in vitroにおけるMCF−7細胞のアポトーシスに対する抗体7C10および7H2HMの効果
上記のように、IGF−IRが細胞表面で過剰発現される場合にはこれによってアポトーシスからの保護を与えることができる。さらに、これらの実施例において、抗体7C10および7H2HMが化学療法の活性化合物を増強することができることも示された。抗体7C10および7H2HMのアポトーシス誘導能を調べ、化学療法に関するそれらの相乗効果の可能性を一部説明するために、MCF−7細胞においてドキソルビシン、この細胞系のアポトーシスをin vitroにて誘導することが知られている薬剤の存在または不在下で試験を行った。これらの試験では、MCF−7細胞を2.104/cm2にてペトリ皿に接種し、フェノールレッド不含の10%のウシ胎児血清(FCS)を補給したRPMIで24時間培養する。その後、細胞をPBSで2回洗浄し、FCSを含まない培地での培養を再開する。それらには抗体を10μg/mlにて添加する前に37℃にて10分の適応時間が考慮される。さらに37℃にて10分後、組換えIGF−I(Sigma)を培養培地に最終濃度50ng/mlまで添加する。細胞を再び37℃にて1時間放置して、抗体およびIGF−Iの結合を可能にする。最後に、ドキソルビシン(Sigma)を培養培地に2μg/mlにて添加し、細胞を37℃にて24時間インキュベートする。
上記のように、IGF−IRが細胞表面で過剰発現される場合にはこれによってアポトーシスからの保護を与えることができる。さらに、これらの実施例において、抗体7C10および7H2HMが化学療法の活性化合物を増強することができることも示された。抗体7C10および7H2HMのアポトーシス誘導能を調べ、化学療法に関するそれらの相乗効果の可能性を一部説明するために、MCF−7細胞においてドキソルビシン、この細胞系のアポトーシスをin vitroにて誘導することが知られている薬剤の存在または不在下で試験を行った。これらの試験では、MCF−7細胞を2.104/cm2にてペトリ皿に接種し、フェノールレッド不含の10%のウシ胎児血清(FCS)を補給したRPMIで24時間培養する。その後、細胞をPBSで2回洗浄し、FCSを含まない培地での培養を再開する。それらには抗体を10μg/mlにて添加する前に37℃にて10分の適応時間が考慮される。さらに37℃にて10分後、組換えIGF−I(Sigma)を培養培地に最終濃度50ng/mlまで添加する。細胞を再び37℃にて1時間放置して、抗体およびIGF−Iの結合を可能にする。最後に、ドキソルビシン(Sigma)を培養培地に2μg/mlにて添加し、細胞を37℃にて24時間インキュベートする。
同様に、ナベルビンを10μg/mlの濃度にて用いて試験を実施した。
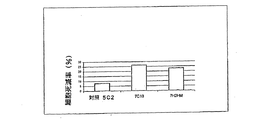
アネキシンV−FITC(20分間、4℃)およびDAPI(2μg/ml)で標識した後、フローサイトメトリー解析により細胞の生存の解析を行う。検討する死細胞の割合(パーセント)は標識された集団アネキシン+I/DAPI+である。抗体5C2を対照のイソタイプとして用いる。
アネキシンV−FITC(20分間、4℃)およびDAPI(2μg/ml)で標識した後、フローサイトメトリー解析により細胞の生存の解析を行う。検討する死細胞の割合(パーセント)は標識された集団アネキシン+I/DAPI+である。抗体5C2を対照のイソタイプとして用いる。
図36にて示された結果からは、ドキソルビシンがMCF−7細胞の8%でアポトーシスを誘導することが分かる。抗体7C10およびドキソルビシンを併用して細胞を処置すると、細胞死の有意な増加が認められる。同じ効果が抗体7H2HMでも示される。抗体をナベルビンと組み合わせた場合も同様の結果が認められた。
実施例7:モノクローナル抗体(MAb)7C10重鎖および軽鎖の可変領域をコードする遺伝子のクローニング戦略
TRI REAGENT(商標)(供給業者によって与えられた使用説明書に従う、SIGMA,. T9424)を用いて107細胞の抗体7C10を分泌するハイブリドーマからトータルRNAを抽出した。Amersham-Pharmaciaの「第1鎖cDNA合成」キット(#27-9621-01、供給業者によって与えられた使用説明書に従う)を用いて第1cDNA鎖を合成した。2鎖の反応にはキットに含まれるオリゴヌクレオチドNot I−d(T)18を準備した。
TRI REAGENT(商標)(供給業者によって与えられた使用説明書に従う、SIGMA,. T9424)を用いて107細胞の抗体7C10を分泌するハイブリドーマからトータルRNAを抽出した。Amersham-Pharmaciaの「第1鎖cDNA合成」キット(#27-9621-01、供給業者によって与えられた使用説明書に従う)を用いて第1cDNA鎖を合成した。2鎖の反応にはキットに含まれるオリゴヌクレオチドNot I−d(T)18を準備した。
このようにして得られたcDNA:mRNAハイブッドをMAb 7C10の重鎖および軽鎖をコードする遺伝子のPCRによる増幅に用いた。PCRはマウス免疫グロブリンの重鎖および軽(κ)鎖に特異的なオリゴヌクレオチドの組合せを用いて実施した。5’末端に相当するプライマーはシグナルペプチドに相当する領域でハイブリダイズする(重鎖に関しては表2、軽鎖に関しては表3)。データバンクで見つけられる多数のマウス抗体配列からこれらのプライマーをまとめた(Jones S. T. et al., Bio/Technology 9: 88-89頁, 1991)。3’末端に相当するプライマーは重鎖(V−Cジャンクションからさほど離れていないサブクラスIgG1のCH1ドメイン、MHC−1プライマー 表4)および軽鎖(V−Cジャンクションからさほど離れていないκドメイン、MKCプライマー 表4)の定常領域でハイブリダイズする。
実施例8:マウスハイブリドーマ7C10からクローニングした免疫グロブリンの配列
上記の増幅戦略に従って、「pGEM(登録商標)−T Easyベクター系」(Promega)を用いて重鎖(VH)および軽鎖(VL)の可変領域に相当するPCR産物をクローニングした。7C10 VLの場合、MKCプライマーをMKV1およびMKV2プライマーと組み合わせてPCR産物を得た。7C10 VHの場合、MHC−1プライマーをMHV8およびMHV12プライマーと組み合わせてPCR産物を得た。pGem−T easyベクターでクローニングしたPCR産物の詳細な配列決定では、軽鎖の場合、2つの異なる配列が示され、重鎖の場合、1つの独自の配列が示された。
上記の増幅戦略に従って、「pGEM(登録商標)−T Easyベクター系」(Promega)を用いて重鎖(VH)および軽鎖(VL)の可変領域に相当するPCR産物をクローニングした。7C10 VLの場合、MKCプライマーをMKV1およびMKV2プライマーと組み合わせてPCR産物を得た。7C10 VHの場合、MHC−1プライマーをMHV8およびMHV12プライマーと組み合わせてPCR産物を得た。pGem−T easyベクターでクローニングしたPCR産物の詳細な配列決定では、軽鎖の場合、2つの異なる配列が示され、重鎖の場合、1つの独自の配列が示された。
a)オリゴMKV1から単離された可変領域
得られたDNA配列は機能的Igの可変領域の特徴を示している。そのため、この新規な配列が7C10 VLをコードするものであると考えられる。7C10 VLをコードするcDNAのDNA(配列番号48および50)およびアミノ酸(配列番号49)配列を図14に示す。
得られたDNA配列は機能的Igの可変領域の特徴を示している。そのため、この新規な配列が7C10 VLをコードするものであると考えられる。7C10 VLをコードするcDNAのDNA(配列番号48および50)およびアミノ酸(配列番号49)配列を図14に示す。
b)オリゴMKV2から単離された可変領域
この軽鎖をコードする遺伝子は、7C10 ハイブリドーマの作製に用いたマウス骨髄腫Sp2/Oag14がその一部である最初のMOPC−21腫瘍由来の標準的な融合相手の全てに存在する異常なmRNA転写物由来のものである。この配列はVおよびJ遺伝子間の異常な組換え(リーディングフレームの変化に関連する4ヌクレオチド塩基の欠失)および23位にある一定のシステインのチロシンへの変化を含んでいる。これらの変化は、この軽鎖がメッセンジャーRNAに転写されるにもかかわらず機能しないことを示唆する。この擬似軽鎖のDNA配列は示していない。
この軽鎖をコードする遺伝子は、7C10 ハイブリドーマの作製に用いたマウス骨髄腫Sp2/Oag14がその一部である最初のMOPC−21腫瘍由来の標準的な融合相手の全てに存在する異常なmRNA転写物由来のものである。この配列はVおよびJ遺伝子間の異常な組換え(リーディングフレームの変化に関連する4ヌクレオチド塩基の欠失)および23位にある一定のシステインのチロシンへの変化を含んでいる。これらの変化は、この軽鎖がメッセンジャーRNAに転写されるにもかかわらず機能しないことを示唆する。この擬似軽鎖のDNA配列は示していない。
c)オリゴMHV8およびMHV12から単離された可変領域
これら2つのオリゴで得られたDNA配列は同一であり、オリゴ自身によってコードされる配列とは区別される。この配列はモノクローナル抗体7C10のものであると考えられる機能的重鎖をコードする新規の配列である。7C10 VHをコードするcDNAのDNA(配列番号51および53)およびアミノ酸(配列番号52)配列を図15に示す。
これら2つのオリゴで得られたDNA配列は同一であり、オリゴ自身によってコードされる配列とは区別される。この配列はモノクローナル抗体7C10のものであると考えられる機能的重鎖をコードする新規の配列である。7C10 VHをコードするcDNAのDNA(配列番号51および53)およびアミノ酸(配列番号52)配列を図15に示す。
実施例9:キメラマウス−ヒト遺伝子の構築
ヒト定常領域κおよびγ−1各々と連結されるマウス7C10領域VLおよびVHを有するようにキメラ抗体7C10を構築した。哺乳類細胞における発現用ベクターへのそれらのクローニングが可能となるよう7C10 VLおよびVHをコードするDNAにフランキングする配列の5’および3’末端を改変するためにオリゴを用いた。これらのベクターは強力なプロモーターHCMVを用いてキメラ抗体7C10の重鎖および軽鎖を効率的に転写する。また、これらのベクターは、DNAの効率的な複製を、結果として、cos細胞におけるタンパク質の一時的発現として可能にするSV40の複製起点も含んでいる。
ヒト定常領域κおよびγ−1各々と連結されるマウス7C10領域VLおよびVHを有するようにキメラ抗体7C10を構築した。哺乳類細胞における発現用ベクターへのそれらのクローニングが可能となるよう7C10 VLおよびVHをコードするDNAにフランキングする配列の5’および3’末端を改変するためにオリゴを用いた。これらのベクターは強力なプロモーターHCMVを用いてキメラ抗体7C10の重鎖および軽鎖を効率的に転写する。また、これらのベクターは、DNAの効率的な複製を、結果として、cos細胞におけるタンパク質の一時的発現として可能にするSV40の複製起点も含んでいる。
実施例10:キメラ抗体7C10のIGF−1受容体の発現および認識活性の評価
キメラ7C10抗体をコードするDNAを含む2種類のプラスミドをcos−7細胞(ATCC番号CRL−1651)にトランスフェクトし、組換え抗体の一時的発現を調べた。72時間のインキュベーション後、培養培地を取り出し、細胞残屑を除去するために遠心分離し、ヒトIgG1の産生(実施例16を参照)およびIGF−1に対する受容体の認識(実施例17を参照)についてELISA技術により解析した。
キメラ7C10抗体をコードするDNAを含む2種類のプラスミドをcos−7細胞(ATCC番号CRL−1651)にトランスフェクトし、組換え抗体の一時的発現を調べた。72時間のインキュベーション後、培養培地を取り出し、細胞残屑を除去するために遠心分離し、ヒトIgG1の産生(実施例16を参照)およびIGF−1に対する受容体の認識(実施例17を参照)についてELISA技術により解析した。
ヒトIgG1/κ濃度の測定に関するELISA試験からは、cos−7細胞におけるキメラ抗体7C10の発現が多数の抗体で認められる値と同程度である300〜500ng/mm間であることが分かった。
IGF−1に対する受容体の認識に関するELISA試験からは、キメラ抗体がそれを特異的かつ優れた相対アビディティにて認識することが分かった(図3A、3Bおよび3Cを参照)。このことによって7C10抗体の適したVHおよびVLが確認されたという有効な証拠が提供される。さらに、このキメラ型の7C10はヒト化型のアフィニティーの評価において必須のツールであると思われる。
実施例11:マウス抗体7C10の可変領域の分子モデリング
「CDR移植」によるヒト化方法を手助けし、改良するために、マウス抗体7C10のVLおよびVH領域の分子モデルを構築した。モデルは重鎖1AY1および軽鎖2PCPの結晶構造に基づく。
「CDR移植」によるヒト化方法を手助けし、改良するために、マウス抗体7C10のVLおよびVH領域の分子モデルを構築した。モデルは重鎖1AY1および軽鎖2PCPの結晶構造に基づく。
実施例12:抗体7C10の軽鎖可変領域(7C10 VL)のCDR移植によるヒト化方法
a)7C10 VLのアミノ酸配列の全ての既知マウスVL配列との比較
CDR移植によるヒト化の予備工程として、7C10 VLのアミノ酸配列をまず、Kabatのデータバンク(インターネットアドレス:ftp://ftp.ebi.ac,uk/pub/database/kabat/fasta_format/, データの最終更新日 1999年)に存在する全てのマウスVL配列と比較した。このことによって、7C10 VLがKabat et al.(In Sequences of proteins of immunological interest(第5版), NIH publication No.91-3242,, US Department of Health and Human Services, Public Health Service, National Institutes of Health, Bethesda, 1991)によって定義されたκ軽鎖のサブグループIIに属することが確認された。最大95%に及ぶ配列同一性を有するマウスのモノクローナル抗体VL領域が確認された(DRB1−4.3(配列番号55):95%およびC94−5B11'CL(配列番号56):95%、図17を参照)。7C10 VL配列の通常の残基から同定を試みるために、7C10 VLのアミノ酸配列(配列番号54)をKabatによって定義されたマウスκ鎖のサブグループIIのコンセンサス配列(配列番号57)とアラインした(図17を参照)。
a)7C10 VLのアミノ酸配列の全ての既知マウスVL配列との比較
CDR移植によるヒト化の予備工程として、7C10 VLのアミノ酸配列をまず、Kabatのデータバンク(インターネットアドレス:ftp://ftp.ebi.ac,uk/pub/database/kabat/fasta_format/, データの最終更新日 1999年)に存在する全てのマウスVL配列と比較した。このことによって、7C10 VLがKabat et al.(In Sequences of proteins of immunological interest(第5版), NIH publication No.91-3242,, US Department of Health and Human Services, Public Health Service, National Institutes of Health, Bethesda, 1991)によって定義されたκ軽鎖のサブグループIIに属することが確認された。最大95%に及ぶ配列同一性を有するマウスのモノクローナル抗体VL領域が確認された(DRB1−4.3(配列番号55):95%およびC94−5B11'CL(配列番号56):95%、図17を参照)。7C10 VL配列の通常の残基から同定を試みるために、7C10 VLのアミノ酸配列(配列番号54)をKabatによって定義されたマウスκ鎖のサブグループIIのコンセンサス配列(配列番号57)とアラインした(図17を参照)。
Kabatの位置番号3では、Kabatに従ってκ軽鎖のサブグループIIに通常存在するバリン(V)(71%)がロイシン(L)に置き換えられている。この位置のロイシンは、例えば、DRB1−4.3およびC94−5B11'CLにおいて認められ、珍しくはない。分子モデルによれば、この残基が特定の役割を果たすとは考えられない。そのため、ヒト化型におけるこの残基の保存は考えない。
Kabatの位置番号7では、Kabatに従ってκ軽鎖のサブグループIIに通常存在するトレオニン(T)(66%)がイソロイシン(I)に置き換えられている。この位置のイソロイシンは、全ての既知マウスVL配列では15倍認められ、ヒトVL配列では全く認められないため、比較的珍しい。分子モデルによれば、この残基(17)は分子の表面の方に向いているが、CDRとは接触しない(最も近いCDRの残基がKabatの位置番号42のアルギニンである)ことが分かる。さらに、この残基17が直接抗原と接触するとはほとんど考えられない。そのため、いずれにしても最初はヒト化型におけるこの残基の保存は考えない。
Kabatの位置番号77では、Kabatに従ってκ軽鎖のサブグループIIに通常存在するアルギニン(R)(95.5%)がセリン(S)に置き換えられている。この位置のセリンは、珍しくはない。
b)7C10 VLのアミノ酸配列の全ての既知ヒトVL配列との比較
「CDR移植」の最良のヒト候補を同定するために、7C10 VLと可能な限り最高の相同性を有するヒト起源のκ VL領域を求めた。この目的を達するために、マウスκ 7C10 VLのアミノ酸配列をKabatのデータバンクに存在する全てのヒトκ VL配列と比較した。マウス7C10 VLはKabat et al.(1991)によって定義されたサブグループIIのヒトκ VL領域と最高の配列相同性を有した。ヒト起源のモノクローナル抗体のVH領域は可変領域を構成する112個のアミノ酸全てに対して最大75.9%に及ぶ配列同一性を有する(GM607(配列番号58)、図18を参照)ことが確認された。76%の配列同一性を有するヒト起源の生殖細胞系統、DPK15/A19(配列番号59)(図18を参照)もまた同定された、GM607(Klobeck et al., 1984)。それゆえ、GM607をマウス7C10 VLのCDRを受け入れることができるヒト配列(Kabatの定義に従う)として選択した。GM607配列のヒトサブグループIIのコンセンサス配列のもの(配列番号60)との比較(図18)によっては、フレームワーク領域(Rch)内の特定の残基は同定できず、その事実によってGM607がCDR移植の優れた候補であることが示される。
「CDR移植」の最良のヒト候補を同定するために、7C10 VLと可能な限り最高の相同性を有するヒト起源のκ VL領域を求めた。この目的を達するために、マウスκ 7C10 VLのアミノ酸配列をKabatのデータバンクに存在する全てのヒトκ VL配列と比較した。マウス7C10 VLはKabat et al.(1991)によって定義されたサブグループIIのヒトκ VL領域と最高の配列相同性を有した。ヒト起源のモノクローナル抗体のVH領域は可変領域を構成する112個のアミノ酸全てに対して最大75.9%に及ぶ配列同一性を有する(GM607(配列番号58)、図18を参照)ことが確認された。76%の配列同一性を有するヒト起源の生殖細胞系統、DPK15/A19(配列番号59)(図18を参照)もまた同定された、GM607(Klobeck et al., 1984)。それゆえ、GM607をマウス7C10 VLのCDRを受け入れることができるヒト配列(Kabatの定義に従う)として選択した。GM607配列のヒトサブグループIIのコンセンサス配列のもの(配列番号60)との比較(図18)によっては、フレームワーク領域(Rch)内の特定の残基は同定できず、その事実によってGM607がCDR移植の優れた候補であることが示される。
c)ヒト化型の7C10 VL
ヒト化方法の次の工程は、マウス7C10 VLのCDRの選択したヒト軽鎖、GM607(Klobeck et al., 1964)のフレームワーク領域(Rch)との結合にあった。方法のこの工程において、分子の3次元構造の維持(CDRの正規構造(canonical structure)、VH/VLインターフェイス、など)または抗原との結合においてある役割を果たし得るように保持されるマウス残基の選択には7C10のマウスFv領域の分子モデルが特に有用である。Rchにおいて、マウス(7C10 VL)およびヒト(GM607)アミノ酸間の違いを綿密に調べた(表5を参照)。さらに、必要に応じて、同定されたマウス配列7C10 VLの特定の残基(実施例12.aを参照)を検討した。
ヒト化方法の次の工程は、マウス7C10 VLのCDRの選択したヒト軽鎖、GM607(Klobeck et al., 1964)のフレームワーク領域(Rch)との結合にあった。方法のこの工程において、分子の3次元構造の維持(CDRの正規構造(canonical structure)、VH/VLインターフェイス、など)または抗原との結合においてある役割を果たし得るように保持されるマウス残基の選択には7C10のマウスFv領域の分子モデルが特に有用である。Rchにおいて、マウス(7C10 VL)およびヒト(GM607)アミノ酸間の違いを綿密に調べた(表5を参照)。さらに、必要に応じて、同定されたマウス配列7C10 VLの特定の残基(実施例12.aを参照)を検討した。
7C10 VLの「CDR移植」によってヒト化した最初の型、ヒト1では、GM607のフレームワーク領域(Rch)内に1つの変化がなし遂げられている。この変化はRch1に位置する残基2(Kabatの命名)に関係する。この残基は、実際には、7C10 VLのCDR1の正規構造構成の一部になるため、その適したコンホメーションにおいてこのループを維持するのに重要である。そのため、マウス7C10 VL配列のこの位置に存在するバリンはヒト化型のこの同じ位置に維持されている(アミノ酸配列(配列番号61)に関しては表5および図19を、DNA配列(配列番号62および64)およびペプチドシグナルを含んでなるアミノ酸配列(配列番号63)に関しては図20を参照)。
7C10 VLの「CDR移植」によってヒト化した2番目の型、ヒト2では、ヒト軽鎖GM607のRch内に受けた変化はない。そのため、Rchの全ての残基が、マウス7C10 VLに存在するバリンをヒト軽鎖GM607のこの同じ位置に見られるイソロイシンに置き換えるために変異させた残基2をはじめとするヒト起源のものである(アミノ酸配列(配列番号65)に関しては表5および図19を、DNA配列(配列番号66および68)およびペプチドシグナルを含んでなるアミノ酸配列(配列番号67)に関しては図21を参照)。そのため、このヒト型2はRchの全ての残基がヒト起源の軽鎖、GM607のものであることから、完全にヒト化されている(当然ながら、CDR自体とは区別される)。
説明:1列目(Kabat)はKabat et al. (1991)によるアミノ酸残基の位置を示し;2列目(#)は通常の配列でのアミノ酸残基の位置を示し;3列目(FRまたはCDR)は骨格のセグメント(FR1、FR2、FR3およびFR4)およびCDRセグメント(CDR1、CDR2およびCDR3)(「CDR」は「相補性決定領域」)を容易に確認するために作成し、3つのCDRが4つのFRを隔てている;4列目(マウス軽鎖 7C10)はマウス抗体7C10のVL領域のアミノ酸配列(配列番号54)を示し;5列目(ヒト生殖細胞系統DPK15/A19)は生殖細胞系統のκ II ヒトV軽鎖のアミノ酸配列(配列番号59)を示し;6列目(GM607)はヒト抗体GM607のVL領域のアミノ酸配列(配列番号58)を示し;7および8列目(再構築したヒト7C10 1および2)はヒト化1および2抗体7C10 VLのアミノ酸配列(各々、配列番号61および65)を示す。「*」はChothia et al. (Nature, 342, 877-883頁, 1989)によって定義されるようなCDRループの正規構造の一部を示す。
実施例13:抗体7C10の重鎖可変領域(7C10 VH)のCDR移植によるヒト化方法
a)7C10 VHのアミノ酸配列の全ての既知マウスVH配列との比較
CDR移植によるヒト化の予備工程として、7C10 VHのアミノ酸配列をまず、Kabatデータバンク(インターネットアドレス:ftp://ftp.ebi.ac,uk/pub/database/kabat/fasta_format/, データの最終更新日 1999年)に存在する全てのマウスVH配列と比較した。このことによって、7C10 VHがKabat et al.(1991)によって定義された重鎖のサブグループI(A)に属することが確認された。最大90.5%に及ぶ配列同一性を有するマウスのモノクローナル抗体VH領域が確認された(AN03’CL(配列番号70)、図22を参照)。7C10 VH配列の通常の残基から同定を試みるために、我々は7C10 VHのアミノ酸配列(配列番号69)をKabatによって定義されたマウス重鎖のサブグループI(A)のコンセンサス配列(配列番号71)とアラインした(図22を参照)。
a)7C10 VHのアミノ酸配列の全ての既知マウスVH配列との比較
CDR移植によるヒト化の予備工程として、7C10 VHのアミノ酸配列をまず、Kabatデータバンク(インターネットアドレス:ftp://ftp.ebi.ac,uk/pub/database/kabat/fasta_format/, データの最終更新日 1999年)に存在する全てのマウスVH配列と比較した。このことによって、7C10 VHがKabat et al.(1991)によって定義された重鎖のサブグループI(A)に属することが確認された。最大90.5%に及ぶ配列同一性を有するマウスのモノクローナル抗体VH領域が確認された(AN03’CL(配列番号70)、図22を参照)。7C10 VH配列の通常の残基から同定を試みるために、我々は7C10 VHのアミノ酸配列(配列番号69)をKabatによって定義されたマウス重鎖のサブグループI(A)のコンセンサス配列(配列番号71)とアラインした(図22を参照)。
残基17(Kabatの番号付け)、サブグループI(A)のコンセンサス配列ではThr、7C10 VHではSer、は定常領域との結合では分子の表面に位置する。この残基は重要であるとは考えられない。
残基27(Kabatの番号付け)、サブグループI(A)のコンセンサス配列ではAsp、7C10 VHではTyr、はCDR1の標準残基である。この位置のTyrは珍しくなく、その適したコンホメーションにおいてCDR1を維持するのに重要であるといえる。
残基84(Kabatの番号付け)、サブグループI(A)のコンセンサス配列ではThr、7C10 VHではAsn。AsnはマウスVHでは93倍、ヒトVHでは3倍認められた。分子モデルによれば、これはパラトープから遠く離れた表面残基である。
アミノ酸の番号付けはKabat et al. (1991)のものである。7C10 VHおよびKabat マウスサブグループI(A)(配列番号57)間で異なるフレームワーク領域(CDRとは区別される)内の残基に下線を付けている。AN03’CLは represents マウス抗体重鎖の配列(Kabatデータバンクでのアクセス番号はP001289である)を表す。
b)7C10 VHのアミノ酸配列の全ての既知ヒトVH配列との比較
「CDR移植」の最良のヒト候補を同定するために、7C10 VHと可能な限り最高の相同性を有するヒト起源のVH領域を求めた。この目的を達するために、マウス7C10 VHのアミノ酸配列をKabatのデータバンクに存在する全てのヒトVH配列と比較した。マウス7C10 VHはKabat et al.(1991)によって定義されたサブグループIIのヒトVH領域と最高の配列相同性を有した。ヒト起源のモノクローナル抗体のVH領域は可変遺伝子によってコードされた(すなわち、CDR3および領域Jとは区別される)98個のアミノ酸全てに対して最大67.3%に及ぶ配列同一性を有する(ヒトVH FUR1’CL(配列番号73)、図23を参照)ことが確認された。68.4%の配列同一性を有するヒト起源の生殖細胞系統、4.22 VH IV(Sanz et al., 1989)もまたVH
「CDR移植」の最良のヒト候補を同定するために、7C10 VHと可能な限り最高の相同性を有するヒト起源のVH領域を求めた。この目的を達するために、マウス7C10 VHのアミノ酸配列をKabatのデータバンクに存在する全てのヒトVH配列と比較した。マウス7C10 VHはKabat et al.(1991)によって定義されたサブグループIIのヒトVH領域と最高の配列相同性を有した。ヒト起源のモノクローナル抗体のVH領域は可変遺伝子によってコードされた(すなわち、CDR3および領域Jとは区別される)98個のアミノ酸全てに対して最大67.3%に及ぶ配列同一性を有する(ヒトVH FUR1’CL(配列番号73)、図23を参照)ことが確認された。68.4%の配列同一性を有するヒト起源の生殖細胞系統、4.22 VH IV(Sanz et al., 1989)もまたVH
FUR1’CLに対するものと同じ基準に従って同定された(ヒト生殖細胞(配列番号74)、図23を参照)。4.22 VH IVおよびVH FUR1’CLの配列のヒトサブグループIIのコンセンサス配列のもの(ヒト Kabat sg II(配列番号72)、図23および表6を参照)との比較によって、4.22 VH IVではフレームワーク領域(Rch)内の非定型残基は同定できなかったが、VH FUR1’CLによってコードされた配列では2つの非定型残基(Kabatの命名によれば、各々、81および82A位のGlnおよびArg)の存在が同定されたことから、VH FUR1’CLよりもむしろ、生殖細胞系統4.22 VH IVによってコードされた配列をマウス7C10 VHのCDRを受け入れることができるヒト配列(Kabatの定義に従う)として選択した。
c)ヒト化型の7C10 VH
ヒト化方法の次の工程は、マウス7C10 VHのCDRのヒト生殖細胞系統4.22 VH IV(Sanz et al., 1989)のフレームワーク領域(Rch)との結合にあった。方法のこの工程において、分子の3次元構造の維持(CDRの正規構造、VH/VLインターフェイス、など)または抗原(パラトープに属する)との結合においてある役割を果たし得るように保持されるマウス残基の選択には7C10のマウスFv領域の分子モデルが特に有用である。Rchにおいて、マウス(7C10 VH)およびヒト(4.22 VH IV)アミノ酸間の違いを綿密に調べた(表6を参照)。さらに、必要に応じて、同定されたマウス7C10 VH配列の特定の残基(実施例8.aを参照)を検討した。
ヒト化方法の次の工程は、マウス7C10 VHのCDRのヒト生殖細胞系統4.22 VH IV(Sanz et al., 1989)のフレームワーク領域(Rch)との結合にあった。方法のこの工程において、分子の3次元構造の維持(CDRの正規構造、VH/VLインターフェイス、など)または抗原(パラトープに属する)との結合においてある役割を果たし得るように保持されるマウス残基の選択には7C10のマウスFv領域の分子モデルが特に有用である。Rchにおいて、マウス(7C10 VH)およびヒト(4.22 VH IV)アミノ酸間の違いを綿密に調べた(表6を参照)。さらに、必要に応じて、同定されたマウス7C10 VH配列の特定の残基(実施例8.aを参照)を検討した。
7C10 VHの「CDR移植」によってヒト化した最初の型、ヒト1では、4.22 VH IVのフレームワーク領域(Rch)内に4つの変化がなし遂げられている(アミノ酸配列(配列番号75)に関しては表6、図24を、DNA配列(配列番号76および78)およびペプチドシグナルを含んでなるアミノ酸配列(配列番号77)に関しては図25を参照)。これら4つの変化は以下の残基に関係する:
・Rch1に位置する残基30(Kabatの命名)。この残基は、実際には、(Chothia et al., 1989によって定義されるように)7C10 VHのCDR1の構造構成の一部になるため、その正確なコンホメーションにおいてこのループを維持するのに重要である。そのため、マウス配列7C10 VHのこの位置に存在するThrはヒト化型のこの同じ位置に維持されている。
・Rch1に位置する残基30(Kabatの命名)。この残基は、実際には、(Chothia et al., 1989によって定義されるように)7C10 VHのCDR1の構造構成の一部になるため、その正確なコンホメーションにおいてこのループを維持するのに重要である。そのため、マウス配列7C10 VHのこの位置に存在するThrはヒト化型のこの同じ位置に維持されている。
・Rch2に位置する残基48(Kabatの命名)。この残基は、分子モデルによれば、後者に直接接触しないが、CDRに近く、それらの最終的なコンホメーションに影響を及ぼすこともある。そのため、マウス配列7C10 VHのこの位置に存在するメチオニンはヒト化型1のこの同じ位置に維持されている。
・Rch3に位置する残基67(Kabatの命名)。この残基はCDRに近く、分子モデルによれば、CDR2のリジン60(Kabatの命名)と接触することもある。そのため、マウス配列7C10 VHのこの位置に存在するイソロイシンはヒト化型1のこの同じ位置に維持されている。
・Rch3に位置する残基71(Kabatの命名)。この残基はCDR2の正規構造構成の一部になるため、その正確なコンホメーションにおいてこのループを維持するのに重要である。そのため、マウス配列7C10 VHのこの位置に存在するアルギニンはヒト化型1のこの同じ位置に維持されている。
7C10 VHの「CDR移植」によってヒト化した2番目の型、ヒト2では、4.22 VH IVのフレームワーク領域(Rch)内に2つの変化がなし遂げられている。これら2つの変化はヒト化型1ですでに説明した残基30および71(Kabatの命名)に関係する(アミノ酸配列(配列番号79)に関しては表6および図24を、DNA配列(配列番号80および82)およびペプチドシグナルを含んでなるアミノ酸配列(配列番号81)に関しては図26を参照)。
7C10 VHの「CDR移植」によってヒト化した3番目の型、ヒト3では、4.22 VH IVのRch内に受けた変化はない。そのため、Rchの全ての残基が、残基30、48、67および71(Kabatの命名)をはじめとする維持されたヒト起源のものである(アミノ酸配列(配列番号83)に関しては表6および図24を、DNA配列(配列番号84および86)およびペプチドシグナルを含んでなるアミノ酸配列(配列番号85)に関しては図27を参照)。そのため、このヒト型3はRchの全ての残基が生殖細胞系統、4.22 VH IVのVH遺伝子によってコードされたものであることから、完全にヒト化されている(当然ながら、Kabatによって定義されたCDR自体とは区別される)。
説明:1列目(Kabat)はKabat et al. (1991)によるアミノ酸残基の位置を示し;2列目(FRまたはCDR)は骨格のセグメント(FR1、FR2、FR3およびFR4)およびCDRセグメント(CDR1、CDR2およびCDR3)を容易に確認するために作成し、3つのCDRが4つのFRを隔てている;3列目(マウス重鎖 7C10)はマウス抗体7C10のVH領域のアミノ酸配列(配列番号69)を示し;4列目(生殖細胞系統4.22 VH IV)は遺伝子4.22 VH IV(Sanz et al., 1989)のアミノ酸配列(配列番号74)を示し;5列目(ヒトFUR1’CL VH、kabatのアクセス番号N020619)はアミノ酸配列(配列番号73)を示し[欠文]IgMK ヒト起源の抗ラミンB(Mariette et al., 1993);6、7および8列目(再構築したヒト7C10 1、2および3)は型1(配列番号75)、2(配列番号79)および3(配列番号83)各々の再構築ヒト7C10のVH領域のアミノ酸配列を示す。「*」はChothia et al. (1989)によって定義されるようなCDRループの正規構造の一部を示す。
実施例14:オリゴヌクレオチドのアセンブリによるヒト化型1の7C10 VLおよびVHをコードする遺伝子の構築
a)原理
ヒト化可変領域をコードする遺伝子(リーダーペプチド+可変領域 VHの場合はVDJまたはVKの場合はVJ)をストレプトアビジンでコーティングした磁気ビーズ上での固相アセンブリによって合成した。ヒト化7C10 VH(445塩基対)およびヒト化7C10 VL(433塩基対)をコードする遺伝子を、2配列に存在し、遺伝子のほぼ中間に(VLおよびVH各々に対する遺伝子の5’末端に対して200および245ヌクレオチドに)位置するKpnI制限部位の存在によって2つのDNA断片を融合することによって構築した。一緒に融合される2断片自身が、それらが延長中にオーバーラップするように2つずつ(一方のオリゴが50%の相同性を有するセンス、もう一方がアンチセンス)ハイブリダイズされたリン酸化オリゴヌクレオチド(約30〜35量体)を用いることにあるアセンブリ技術により構成される。5’位置でビオチン化した最初のオリゴヌクレオチドを磁気ビーズと結合した後、リン酸化オリゴヌクレオチド対を1つずつ添加する。酵素T4 DNAリガーゼによって隣り合って並んだリン酸化オリゴヌクレオチド間のホスホジエステル結合が形成される。
a)原理
ヒト化可変領域をコードする遺伝子(リーダーペプチド+可変領域 VHの場合はVDJまたはVKの場合はVJ)をストレプトアビジンでコーティングした磁気ビーズ上での固相アセンブリによって合成した。ヒト化7C10 VH(445塩基対)およびヒト化7C10 VL(433塩基対)をコードする遺伝子を、2配列に存在し、遺伝子のほぼ中間に(VLおよびVH各々に対する遺伝子の5’末端に対して200および245ヌクレオチドに)位置するKpnI制限部位の存在によって2つのDNA断片を融合することによって構築した。一緒に融合される2断片自身が、それらが延長中にオーバーラップするように2つずつ(一方のオリゴが50%の相同性を有するセンス、もう一方がアンチセンス)ハイブリダイズされたリン酸化オリゴヌクレオチド(約30〜35量体)を用いることにあるアセンブリ技術により構成される。5’位置でビオチン化した最初のオリゴヌクレオチドを磁気ビーズと結合した後、リン酸化オリゴヌクレオチド対を1つずつ添加する。酵素T4 DNAリガーゼによって隣り合って並んだリン酸化オリゴヌクレオチド間のホスホジエステル結合が形成される。
このようにde novo合成した遺伝子は(選択した発現ベクターと適合する制限酵素での消化により)直接クローニングすることができるし、またはPCRにより増幅して酵素消化による指向性クローニングへの準備としてより多くの材料を得ることができる。このようにde novoアセンブリによって構築された遺伝子の配列はDNAの自動配列決定により確認する。
b)de novoアセンブリ技術の試験プロトコール
5’位置でリン酸化されるか、または5’位置でビオチン化された、100μM濃度に調整済みのオリゴヌクレオチドをMWG Biotechに注文した(ヒト化7C10 VLの構築の場合には表7の使用オリゴヌクレオチドの配列を、ヒト化 7C10 VHの構築の場合には表8のものを参照)。表9に記載のスキームに従って、オリゴヌクレオチドを対にハイブリダイズした(等モル混合物、T4 DNAリガーゼバッファー中センスオリゴおよアンチセンスオリゴ各々500pmolを95℃に5分間加熱した後、ベンチで周囲温度まで冷却する)。
5’位置でリン酸化されるか、または5’位置でビオチン化された、100μM濃度に調整済みのオリゴヌクレオチドをMWG Biotechに注文した(ヒト化7C10 VLの構築の場合には表7の使用オリゴヌクレオチドの配列を、ヒト化 7C10 VHの構築の場合には表8のものを参照)。表9に記載のスキームに従って、オリゴヌクレオチドを対にハイブリダイズした(等モル混合物、T4 DNAリガーゼバッファー中センスオリゴおよアンチセンスオリゴ各々500pmolを95℃に5分間加熱した後、ベンチで周囲温度まで冷却する)。
第一のビオチン化オリゴヌクレオチドをストレプトアビジンでコーティングした磁気ビーズ(Dynabeads M-280 ストレプトアビジン, Dynal product No.112-05)と結合させる。このために、15mM NaCl溶液中500pmoLのビオチン化オリゴヌクレオチドを、予め100μlのTE 1Xバッファー(Tris−EDTA 100Xバッファー:1M Tris-HCl、pH 8、0.1M EDTA, Sigma T-9285)で2回洗浄した、50μlのデカントしたビーズ(マグネットホルダーを使用)に添加する。37℃で15分間のインキュベーションの後、ビーズを洗浄バッファー(10mM Tris-HCl pH 7.6、10mM EDTAおよび50mM NaCl)で2回洗浄し、次いで、ハイブリダイズしたオリゴ−ヌクレオチド対を1つずつ添加する。オリゴヌクレオチド対を再添加するたびに、混合物を95℃に5分間加熱した後、ベンチで周囲温度まで冷却する。一度、周囲温度に到達したら、2μlの10U/μl T4 DNAリガーゼ(Biolabs)を添加し、混合物を37℃で20分間インキュベートする。次いで、ビーズを洗浄し(洗浄バッファー)た後、以下のオリゴヌクレオチド対を連続して添加する。
最後の非対合オリゴ(アンチセンス)を以下の様式でアセンブリする。5μlのオリゴ(500pmol)および43μlのT4 DNAリガーゼバッファーをデカントしたビーズに添加した後、混合物を95℃に5分間加熱し、ベンチで周囲温度まで冷却する。一度、周囲温度に到達したら、2μlのT4 DNAリガーゼを添加し、混合物を37℃で20分間インキュベートする。次いで、ビーズを洗浄バッファーで2回、次ぎに、TE 1Xバッファーで2回洗浄する。
その後、ビーズはde novoアセンブリした遺伝子のクローニングおよび配列決定を行うまで4℃にて保存してもよい。
実施例15:特異的突然変異誘発によるヒト化型2の7C10 VLおよび7C10 VHならびにヒト化型3の7C10 VHをコードする遺伝子の構築
ヒト化型1の残基48および67(Kabatの命名に従う)の特異的突然変異誘発によって、ヒト化型2の7C10 VHを得た。この特異的突然変異誘発はStratageneの系QuikChange(商標)部位特異的突然変異誘発(キット #200518)を製造業者が記載するプロトコールに従って用いて実施した。構築は2工程で実施し、まず、型1の残基48をプライマー対、7C10Hヒト化1QCM48センスおよびアンチセンス(表10を参照)を用いて変異させ、続いて、残基48で変異させたこの型自身をプライマー対、7C10Hヒト化1QCI67センスおよびアンチセンス(表10を参照)を用いて残基67で変異させた。
ヒト化型1の残基48および67(Kabatの命名に従う)の特異的突然変異誘発によって、ヒト化型2の7C10 VHを得た。この特異的突然変異誘発はStratageneの系QuikChange(商標)部位特異的突然変異誘発(キット #200518)を製造業者が記載するプロトコールに従って用いて実施した。構築は2工程で実施し、まず、型1の残基48をプライマー対、7C10Hヒト化1QCM48センスおよびアンチセンス(表10を参照)を用いて変異させ、続いて、残基48で変異させたこの型自身をプライマー対、7C10Hヒト化1QCI67センスおよびアンチセンス(表10を参照)を用いて残基67で変異させた。
同様に、系QuikChange(商標)を用いたヒト化型2の残基30および71(Kabatの命名に従う)の部位特異的変異によって、ヒト化型3の7C10 VHを得た。この構築は2工程で実施する。まず、型2の残基30をプライマー対、7C10Hヒト化QCT30センスおよびアンチセンス(表10を参照)を用いて変異させた。続いて、残基30で変異させたこの型自身をプライマー対、7C10Hヒト化1V67QCR71センスおよびアンチセンス(表10を参照)を用いて残基71で変異させた。
系QuikChange(商標)を用いたヒト化型1の残基2(Kabatの命名に従う)の部位特異的変異によって、ヒト化型2の7C10 VLを得た。型1の残基2をプライマー対、7C10Lヒト化1QCV2センスおよびアンチセンス(表10を参照)を用いて変異させた。
実施例16:エレクトロポレーションによるcos7細胞のトランスフェクション
キメラまたはヒト化型抗体7C10の重鎖および軽鎖を有する哺乳類発現ベクターを、cos7細胞において、組換え抗体7C10の一時的発現について試験した。BioRad instrument(Gene Pulsar)を用いたエレクトロポレーションによってDNAをcos細胞に導入した。DNA(各ベクター10μg)は0.8mlアリコートのcos細胞にPBSバッファー1ml当たり1×107細胞の濃度にて添加する(Ca++およびMg++なし)。パルス 1900ボルトおよび電気容量 25μFを供給した。次いで、トランスフェクトしたcos細胞を8mlの5%ウシ血清含有DMEM培地に添加し、37℃で72時間インキュベートする。次いで、上清を回収し、細胞残屑を除去するために遠心分離し、ELISAによりIgG1/ヒトκタイプの組換え抗体7C10のその濃度の大きさについて試験する。
キメラまたはヒト化型抗体7C10の重鎖および軽鎖を有する哺乳類発現ベクターを、cos7細胞において、組換え抗体7C10の一時的発現について試験した。BioRad instrument(Gene Pulsar)を用いたエレクトロポレーションによってDNAをcos細胞に導入した。DNA(各ベクター10μg)は0.8mlアリコートのcos細胞にPBSバッファー1ml当たり1×107細胞の濃度にて添加する(Ca++およびMg++なし)。パルス 1900ボルトおよび電気容量 25μFを供給した。次いで、トランスフェクトしたcos細胞を8mlの5%ウシ血清含有DMEM培地に添加し、37℃で72時間インキュベートする。次いで、上清を回収し、細胞残屑を除去するために遠心分離し、ELISAによりIgG1/ヒトκタイプの組換え抗体7C10のその濃度の大きさについて試験する。
実施例17:cos形質転換体の上清に存在する組換え抗体IgG1/ヒトκの濃度を測定するためのELISA法
cos7細胞における一時的発現によって生じた上清をIgG1/ヒトκタイプの7C10抗体の存在について試験した。IgG1/ヒトκ免疫グロブリンの検出を目的として、96−ウェルELISAプレート(Maxisorb, Nunc)をヤギ抗ヒトIgGポリクローナル抗体(γ Fc断片に対して特異的, Jackson Immuno-Research Laboratories Inc., #109-005-098)でコーティングした。cos細胞の上清を連続希釈し、コーティングしたウェルに添加した。37℃で1時間インキュベートし、洗浄した後に、ペルオキシダーゼと結合したヤギ抗ヒト軽κ鎖ポリクローナル抗体(HRP, Sigma, A-7164)を添加した。37℃で45分間インキュベートし、洗浄した後に、TMB基質(KPL #50-76-04)を添加した。10分間のインキュベーションの後に、1M硫酸の添加により反応を停止させ、450nmにて光学密度を読み取った。既知濃度の精製ヒトIgG1/ヒトκ免疫グロブリン(Sigma, 1-3889)を標準参照抗体として用いた。
cos7細胞における一時的発現によって生じた上清をIgG1/ヒトκタイプの7C10抗体の存在について試験した。IgG1/ヒトκ免疫グロブリンの検出を目的として、96−ウェルELISAプレート(Maxisorb, Nunc)をヤギ抗ヒトIgGポリクローナル抗体(γ Fc断片に対して特異的, Jackson Immuno-Research Laboratories Inc., #109-005-098)でコーティングした。cos細胞の上清を連続希釈し、コーティングしたウェルに添加した。37℃で1時間インキュベートし、洗浄した後に、ペルオキシダーゼと結合したヤギ抗ヒト軽κ鎖ポリクローナル抗体(HRP, Sigma, A-7164)を添加した。37℃で45分間インキュベートし、洗浄した後に、TMB基質(KPL #50-76-04)を添加した。10分間のインキュベーションの後に、1M硫酸の添加により反応を停止させ、450nmにて光学密度を読み取った。既知濃度の精製ヒトIgG1/ヒトκ免疫グロブリン(Sigma, 1-3889)を標準参照抗体として用いた。
実施例18:ヒトIgG1/κタイプの7C10組換え抗体のIGF−1に対する受容体(IGF−IR)に関する認識活性を測定するためのELISA法
cos7培養物上清をELISA法によりIGF−1 Rを認識するそれらの能力について試験した。96−ウェルELISAプレート(Dynex Immulon 2HB)を4℃にて一晩のインキュベーションにより、0.31ng/μlのIGF−1 R(ヒトインスリン様増殖因子I可溶性受容体, R & D Systems, #391-GR)を含有するPBS溶液、各ウェル当たり100μlでコーティングした。0.05%Tween20を含有するPBSでの洗浄後、プレートを0.5%ゼラチン溶液を含有するPBS溶液を添加し、37℃で1時間インキュベートして飽和させた。PBSで3回洗浄した後、調べるcos上清のサンプルを予め0.1%ゼラチンおよび0.05%Tween20を含有するPBSで連続希釈し、それをプレートに添加した。37℃で1時間インキュベートし、続いて、3回洗浄した(0.05%Tween20を含有するPBS)後、ペルオキシダーゼと結合した抗ヒトIgG抗体(Fc断片に対して特異的)(HRP, Jackson Immuno-Research Laboratories Inc., #109-035-098)を添加した(0.1%ゼラチンおよび0.05%Tween20を含有するPBSにて1/5000に希釈)。37℃で45分間インキュベートし、3回洗浄した(0.05%Tween20を含有するPBS)後に、TMB基質(KPL #50-76-04)を添加した。10分間のインキュベーションの後に、1M硫酸の添加により反応を停止させ、450nmにて光学密度を読み取った。
cos7培養物上清をELISA法によりIGF−1 Rを認識するそれらの能力について試験した。96−ウェルELISAプレート(Dynex Immulon 2HB)を4℃にて一晩のインキュベーションにより、0.31ng/μlのIGF−1 R(ヒトインスリン様増殖因子I可溶性受容体, R & D Systems, #391-GR)を含有するPBS溶液、各ウェル当たり100μlでコーティングした。0.05%Tween20を含有するPBSでの洗浄後、プレートを0.5%ゼラチン溶液を含有するPBS溶液を添加し、37℃で1時間インキュベートして飽和させた。PBSで3回洗浄した後、調べるcos上清のサンプルを予め0.1%ゼラチンおよび0.05%Tween20を含有するPBSで連続希釈し、それをプレートに添加した。37℃で1時間インキュベートし、続いて、3回洗浄した(0.05%Tween20を含有するPBS)後、ペルオキシダーゼと結合した抗ヒトIgG抗体(Fc断片に対して特異的)(HRP, Jackson Immuno-Research Laboratories Inc., #109-035-098)を添加した(0.1%ゼラチンおよび0.05%Tween20を含有するPBSにて1/5000に希釈)。37℃で45分間インキュベートし、3回洗浄した(0.05%Tween20を含有するPBS)後に、TMB基質(KPL #50-76-04)を添加した。10分間のインキュベーションの後に、1M硫酸の添加により反応を停止させ、450nmにて光学密度を読み取った。
実施例19:「CDR移植」による異なる型のヒト化7C10抗体によるIGF1−Rの認識活性の測定
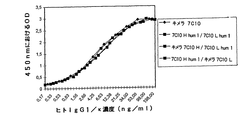
まず、我々はIGF−1受容体に対するヒト化型1の7C10の重鎖および軽鎖の認識活性をキメラ型と比較した。図28は、前もって、ELISAによりそのIgG1/ヒトκ濃度を測定した(実施例17を参照)cos7細胞の上清のIGF−1Rの認識に関するELISA試験の結果を示す(実施例18を参照)。調べた4種類の組換え抗体の滴定曲線は完全に重なり、このことから、IGF−IRに対するそれらの相対アフィニティーが極めて類似していることが分かる。それゆえ、このことから、ヒト化軽鎖1(フレームワーク領域内に存在する1マウス残基)とヒト化重鎖1(フレームワーク領域内に存在する4マウス残基)を組み合わせて構成されたヒト化型1の7C1が、IGF−1受容体を特異的に認識し、キメラ抗体(マウス可変領域)のものと極めて類似したアフィニティーを有するという結論に達する。
まず、我々はIGF−1受容体に対するヒト化型1の7C10の重鎖および軽鎖の認識活性をキメラ型と比較した。図28は、前もって、ELISAによりそのIgG1/ヒトκ濃度を測定した(実施例17を参照)cos7細胞の上清のIGF−1Rの認識に関するELISA試験の結果を示す(実施例18を参照)。調べた4種類の組換え抗体の滴定曲線は完全に重なり、このことから、IGF−IRに対するそれらの相対アフィニティーが極めて類似していることが分かる。それゆえ、このことから、ヒト化軽鎖1(フレームワーク領域内に存在する1マウス残基)とヒト化重鎖1(フレームワーク領域内に存在する4マウス残基)を組み合わせて構成されたヒト化型1の7C1が、IGF−1受容体を特異的に認識し、キメラ抗体(マウス可変領域)のものと極めて類似したアフィニティーを有するという結論に達する。
続いて、我々はIGF−IRの認識に及ぼす7C10のヒト化軽鎖の残基2(Kabatの命名に従う)の影響(ヒト化型1対ヒト化型2、図19を参照)を調べた。図29は、前もって、ELISAによりそのIgG1/ヒトκ濃度を測定した(実施例17を参照)cos7細胞の上清のIGF−IRの認識に関するELISA試験の結果を示す(実施例18を参照)。2種類のヒト化型1および2の軽鎖を連続的にヒト化7C10 VH 1と組み合わせた。2種類の組合せの滴定曲線を重ね合わることによって、ヒト化型1の1つのバリンからヒト化型2のイソロイシンへと変化した軽鎖残基2の変異により、IGF1受容体の認識の相対アフィニティーに及ぼす影響が明らかにないことが分かる。よって、ヒト化型2の7C10軽鎖はマウス残基(CDRとは区別される)が全く保存されない1つの型を形成する。完全にヒト化されたこの型は、7C10 VLの好ましい型の典型である。
完全ヒト化型の7C10軽鎖(ヒト化型2、上記参照)を3種類のヒト化型の7C10重鎖と組み合わせて試験した。図30は、前もって、ELISAによりそのIgG1/ヒトκ濃度を測定した(実施例17を参照)cos7細胞の上清のIGF−1Rの認識に関するELISA試験の結果を示す(実施例18を参照)。滴定曲線は極めて類似しており、キメラ抗体の参照曲線と実質的に重なり、このことから、3種類のヒト化型1、2および3の7C10 VHがヒト化7C10 VL 2と組み合わせた場合にはIGF−IRに対して同一の相対アフィニティーを与えることが分かる。しかしながら、同時に行ったその他のELISA試験(結果は示さない)では、残基71(Kabatの命名)のアルギニン(マウス)からバリン(ヒト)への点変異には対応する抗体のIGF−1Rに対するアフィニティーの少しの低下を伴うことを明らかにしているが、ヒト化7C10 VH 2がIGF−1Rに対してヒト化7C10 VH 1と同じ相対アフィニティーを有すると考えるに値する。よって、このヒト化型2はそれだけが2つのマウスアミノ酸(残基30および71、図24を参照)を有することから型1に対して好ましい。マウス残基(CDRとは区別される)を全く含まないヒト化型3もまたそれだけがアフィニティーの最小限の低下しか生じないと思われることから好ましい。
要するに、本発明の抗体7C10の2種類のヒト化型が特に好ましいと思われる。 ヒト化7C10 VH 2(2つの保存されたマウス残基)とヒト化7C10 VL 2(マウス残基が全く保存されない)との組合せによって構成された型およびヒト化7C10 VH 3(マウス残基が全く保存されない)とヒト化7C10 VL 2(マウス残基が全く保存されない)との組合せによって構成されたもう1つの型。この最後の型は、重鎖および軽鎖に同時に存在するマウス残基がないことから、最終的なヒト化型を構成している。
実施例20:A549細胞の表面におけるEGFRおよびIGF−IRの発現
IGF−IRおよびEGFR各々に対して向けられた2種類のMABの同時投与によって得られた作用の相乗効果を、A549細胞(肺癌細胞系)の皮下注射(s.c.)によって確立された非小細胞肺腫瘍を有するヌードマウスにて調べた。
IGF−IRおよびEGFR各々に対して向けられた2種類のMABの同時投与によって得られた作用の相乗効果を、A549細胞(肺癌細胞系)の皮下注射(s.c.)によって確立された非小細胞肺腫瘍を有するヌードマウスにて調べた。
まず、これをマウスに注入する前のA549細胞の表面における2つの受容体 IGF−IRおよびEGFRを確認するために、これらの細胞のFACSでの読み取りのために標識化をマウス7C10抗IGF−IR MAB(図37B)およびマウス225抗EGFR MAB(図37D)各々で行った。これを行うために、細胞を4℃で30分間、10%FCS(ウシ胎児血清)PBS溶液で飽和させ、洗浄した後、目的のMABとともに4℃で30分間インキュベートした。新たに3回洗浄した後、FITC(フルオレセインイソチオシアネート)と結合した二次抗種抗体を添加する。30分間のインキュベーションの後、FACS(蛍光活性化細胞選別装置)での読み取りを520nmにて(励起 488nm)行う。
図37A〜37Dにて示された結果からは、A549細胞がそれらの表面にEGFおよびIGF1に対する受容体を同程度の数有していることが分かる。その2つについての各受容体の分布に関しては集団は均一である。イソタイプの対照(図37C)を使用することによって標識の特異性を確認する。これらの結果は2種類のIGF−IR受容体およびEGFR受容体に対する作用の相乗効果の試験用およびこれら2つの受容体の連携の試験用モデルとしてのA549細胞の使用の正当性を実証するものである。
実施例21:抗腫瘍処置におけるin vivoにてヌードマウスに同時投与した抗IGF−IR MABおよび抗EGFR MABの作用の相乗効果
この試験のため、ヌードマウスに5.106 A549細胞をs.c.移植する。細胞移植5日後、腫瘍を測定し、腫瘍体積に関しての均質なマウス群を形成する。この群から、6マウス群をランダムに形成する。これらのマウスを、腹腔内にて(i.p.)、週2回、MAB 7C10および225各々により個別に250μg/マウスの用量にて、または2種類のMABの同時投与により処置する。MAB 9G4を試験のイソタイプ対照として投与する。
この試験のため、ヌードマウスに5.106 A549細胞をs.c.移植する。細胞移植5日後、腫瘍を測定し、腫瘍体積に関しての均質なマウス群を形成する。この群から、6マウス群をランダムに形成する。これらのマウスを、腹腔内にて(i.p.)、週2回、MAB 7C10および225各々により個別に250μg/マウスの用量にて、または2種類のMABの同時投与により処置する。MAB 9G4を試験のイソタイプ対照として投与する。
図38にて示された結果からは、単独投与した抗体7C10および225各々によってin vivo腫瘍増殖の有意な減少を誘導することができることが分かる。調べた2種類のMABが腫瘍A549の増殖に対して同等の活性を有することにも注目すべきである。文献に対して驚くべきことに、2種類のMABの同時投与において観察される有意な相乗効果(t検定での各動態倍率においてp≦0.01 )によって、in vivoにおける腫瘍の最適増殖に2種類の受容体の連携があること、および、文献でのデータに反して、2つの軸のうちの一方の遮断ではもう1つのものが媒介する増殖を完全に阻害するには不十分であることが示唆される。
実施例22:A549細胞を同所移植したマウスに同時投与されたマウス抗体7C10および225の抗腫瘍活性の試験
抗腫瘍活性の評価での同所移植モデルの使用は、腫瘍の転移性播種のプロセスに関して特定の利益を提供する。IGF−IRおよびEGFR各々に対して向けられた抗体混合物の抗腫瘍活性を評価するために、106 A549細胞(非小細胞肺癌)をヌードマウスの胸腔内に移植した。この種の腫瘍移植がもたらす影響はヒトで観察されるものと同様の転移性播種であり、動物の死を誘導するということも注意すべきである。図39からは、抗体225および7C10単独での投与によって観察する生存において同程度の有意な増加がなされることが分かる。驚くべきことに、これら2種類の抗体の同時投与によって動物の生存がかなり増加し、このことにより、この処置が腫瘍細胞の転移性播種に影響を及ぼし得ることが示唆される。
抗腫瘍活性の評価での同所移植モデルの使用は、腫瘍の転移性播種のプロセスに関して特定の利益を提供する。IGF−IRおよびEGFR各々に対して向けられた抗体混合物の抗腫瘍活性を評価するために、106 A549細胞(非小細胞肺癌)をヌードマウスの胸腔内に移植した。この種の腫瘍移植がもたらす影響はヒトで観察されるものと同様の転移性播種であり、動物の死を誘導するということも注意すべきである。図39からは、抗体225および7C10単独での投与によって観察する生存において同程度の有意な増加がなされることが分かる。驚くべきことに、これら2種類の抗体の同時投与によって動物の生存がかなり増加し、このことにより、この処置が腫瘍細胞の転移性播種に影響を及ぼし得ることが示唆される。
実施例23:7C10および7H2HMがIGF−IRおよびIRS−Iのβ鎖のチロシンのリン酸化を阻害する
MCF7細胞を5.104細胞/cm2(75cm2プレート, COSTAR)にてフェノールレッド不含の、5mMのグルタミン、ペニシリン/ストレプトマイシン(各々、100U/100μg/ml)および10%のウシ胎児血清と合せた20mlのRPMIで24時間培養する。PBSで3回洗浄した後、細胞をフェノールレッド不含の、ウシ胎児血清を除き、5mMのグルタミン、ペニシリン/ストレプトマイシン、0.5μg/mlのウシ血清アルブミン(Sigma A-8022)および5μg/mlのトランスフェリン(Sigma T8158)と合せた培地(RPMI)で12時間インキュベートした。
MCF7細胞を5.104細胞/cm2(75cm2プレート, COSTAR)にてフェノールレッド不含の、5mMのグルタミン、ペニシリン/ストレプトマイシン(各々、100U/100μg/ml)および10%のウシ胎児血清と合せた20mlのRPMIで24時間培養する。PBSで3回洗浄した後、細胞をフェノールレッド不含の、ウシ胎児血清を除き、5mMのグルタミン、ペニシリン/ストレプトマイシン、0.5μg/mlのウシ血清アルブミン(Sigma A-8022)および5μg/mlのトランスフェリン(Sigma T8158)と合せた培地(RPMI)で12時間インキュベートした。
活性化では、細胞をまず、遮断抗体(10μg/ml)とともに37℃で2分間インキュベートした後、IGF−I(Sigma 13769、50ng/ml)をさらに2分間添加した。インキュベーション培地を吸引して反応を停止させ、プレートを氷上に置いた。プロテアーゼ阻害剤(50ml当たり1錠剤, Boehringer Ref.: 1697 498)、およびホスファターゼ阻害剤(Calbiochem Ref.: 524625 (1/100))と合せた0.5mlの溶解バッファー(50mM tris−HCl pH 7.5、150mM NaCl、1%Nonidet P40、0.5%デオキシコール酸ナトリウム)の添加により細胞を可溶化した。細胞をこすり落とし、懸濁物を回収し、攪拌装置に4℃で1.5時間置いた。この溶液を12,000rpmにて10分間(4℃)遠心分離し、BCAによって上清のタンパク質濃度を定量した。
免疫沈降では、細胞溶解物のタンパク質の500μgを抗IGF−IR(Santa cruz Ref.: sc-713)と混合し、攪拌装置にて4℃で1.5時間インキュベートした。プロテインA−アガロース(Boehringer Ref.: 1 134 515)を添加して免疫沈降物を回収し、攪拌装置にて4℃で一晩中インキュベートした。IRS−1の免疫沈降では、アガロースビーズ(Santa cruz Ref.: 559Ac)と結合した抗IRS−1抗体を用いた。アガロースビーズを1mlの溶解バッファーで2回、洗浄バッファー1(プロテアーゼ阻害剤およびホスファターゼ阻害剤と合せた50mM tris−HCl pH 7.5;500mM NaCl;0.1%Nonidet P40;0.05%デオキシコール酸ナトリウム(Boehringer 1 332 597))で2回、洗浄バッファー2(プロテアーゼ阻害剤およびホスファターゼ阻害剤1/100と合せた50mM tris−HCl;0.1%Nonidet P40;0.05%デオキシコール酸ナトリウム(Boehringer 1 332 597))で1回洗浄した。免疫沈降物をLaemmliバッファーに再懸濁し、100℃に5分間加熱した。ポリアクリルアミドSDSゲル(8%Novex EC6015)での電気泳動により上清を解析した。タンパク質をニトロセルロース膜に移し、その後にHRPと結合した抗ホスホチロシン抗体(upstate Biotechnology 4G10)またはIGF−IRまたは抗IRS−1(Santa Cruz Ref.: sc 8038) のβ抗鎖のいずれか、続いてHRPと結合した抗ウサギ抗体での免疫ブロットを続けた。この影響は化学発光(Amersham RPN 2209)、その後のKodak X-マットARフィルムでのオートラジオグラフィーによって明らかになった。
図40Aは、刺激していないMCF7細胞(0)またはIGF−1(50ng/ml)単独(0+IGF−I)で刺激したか、またはモノクローナルまたはヒト化抗IGF−IR抗体(10μg/ml)7C10、1H7、7H2HMと組み合わせて刺激したMCF7細胞を示す。抗体9G4またはhIgG1は試験の負の対照として用いたイソタイプIgG1のマウスまたはヒト免疫グロブリンである。IGF−IRのβ鎖を免疫沈降し、リン酸化抗チロシン抗体を用いてブロットした。得られた結果からは、モノクローナルまたはヒト化抗IG−IR 7C10、1H7および7H2HM抗体がIGF−IRのβ鎖のチロシンのリン酸化を阻害することが分かる。
図40Bは、刺激していないMCF7細胞(0)またはIGF−1(50ng/ml)単独(0+IGF−I)で刺激したか、またはモノクローナルまたはヒト化抗IGF−IR抗体(10μg/ml)7C10、1H7、7H2HMと組み合わせて刺激したMCF7細胞を示す。上記のように、抗体9G4またはhIgG1は試験の負の対照として用いたイソタイプIgG1のマウスまたはヒト免疫グロブリンである。IRS−1を免疫沈降し、リン酸化抗チロシン抗体を用いてブロットした。得られた結果からは、モノクローナル抗体7C10、7H2HMおよび1H7がIRS−1のチロシンのリン酸化を阻害することが分かる。
実施例24:7C10および7H2HMがIGF−IRの内在化を誘導する
MCF7細胞およびA549細胞を10%のウシ胎児血清を含有するPBS(FACSバッファー)中1.107細胞/mlに懸濁した。1.106細胞を10μg/mlのモノクローナル抗体(7C10、7G3、9G4)または20μg/mlの7H2HMとともに37℃で30分間インキュベートした。洗浄後、細胞をビオチン化抗IGF−IR(モノクローナル抗体12B1)で4℃で30分間標識し、最後にストレプトアビジン−488 alexa Fluor(登録商標)の複合体とともに4℃で30分間インキュベートした。細胞を残屑の除去後、CellquestソフトウェアによるFACScan(Becton-Dickinson,. Enembogegem, Belgium)により解析した。
MCF7細胞およびA549細胞を10%のウシ胎児血清を含有するPBS(FACSバッファー)中1.107細胞/mlに懸濁した。1.106細胞を10μg/mlのモノクローナル抗体(7C10、7G3、9G4)または20μg/mlの7H2HMとともに37℃で30分間インキュベートした。洗浄後、細胞をビオチン化抗IGF−IR(モノクローナル抗体12B1)で4℃で30分間標識し、最後にストレプトアビジン−488 alexa Fluor(登録商標)の複合体とともに4℃で30分間インキュベートした。細胞を残屑の除去後、CellquestソフトウェアによるFACScan(Becton-Dickinson,. Enembogegem, Belgium)により解析した。
図41は、着色のないA549細胞(第一のピーク)、7C10または7H2HMとともにインキュベートしたA549細胞(第二のピーク)および無関係のマウスまたはラットのIgG1とともにインキュベートしたA549細胞(第3のピーク)を示している。細胞を予め7C10または7H2HMとともにインキュベートした場合に細胞によるIGF−IRの表面発現の2単位の低下が見られる。
実施例25:7C10および7H2HMがIGF−IRの分解を誘導する
MCF−7細胞を10.104細胞/cm2にて(75cm2, Costar)15mlの完全培地で24時間培養した。次ぎに、この培養物をPBSで3回洗浄し、血清を除いた培地で12時間インキュベートした。次ぎに、細胞を25μg/mlのシクロヘキシミド単独とともに、または10μg/mlのモノクローナル抗体7C10、9G4、7G3もしくはIGF-I(50ng/ml)とともにインキュベートした。特定の試験では、モノクローナル抗体とのインキュベーションの前に、細胞をMG−132(10μM, Calbiochem 474791)により37℃で1時間処置し、プロテアソーム活性を阻害した。インキュベーション後、細胞を洗浄し、溶解バッファーの添加により可溶化した。20μgのタンパク質を8%SDSのポリアクリルアミドゲルでの電気泳動により解析し、ニトロセルロース膜に移し、その後、さらに以上に記載のようなIGF−IRのβ抗鎖免疫ブロットを続けた。
MCF−7細胞を10.104細胞/cm2にて(75cm2, Costar)15mlの完全培地で24時間培養した。次ぎに、この培養物をPBSで3回洗浄し、血清を除いた培地で12時間インキュベートした。次ぎに、細胞を25μg/mlのシクロヘキシミド単独とともに、または10μg/mlのモノクローナル抗体7C10、9G4、7G3もしくはIGF-I(50ng/ml)とともにインキュベートした。特定の試験では、モノクローナル抗体とのインキュベーションの前に、細胞をMG−132(10μM, Calbiochem 474791)により37℃で1時間処置し、プロテアソーム活性を阻害した。インキュベーション後、細胞を洗浄し、溶解バッファーの添加により可溶化した。20μgのタンパク質を8%SDSのポリアクリルアミドゲルでの電気泳動により解析し、ニトロセルロース膜に移し、その後、さらに以上に記載のようなIGF−IRのβ抗鎖免疫ブロットを続けた。
IGF−IRの完全性のウエスタンブロットによる解析(図42A)から、7C10および7H2HMは受容体の分解を誘導するが、天然リガンドは後者の分解を全くもたらさないことが分かる。イソタイプ対照として用いた無関係の抗体9G4では受容体の分解は認められない。図42Bは、それに関連して、分解がプロテアソーム阻害剤MG132によって(インキュベーション時間 2時間)阻害されることを実証している。
同様の結果がヒト化抗体7H2HMでも認められた(図42C)。
Claims (54)
- ヒトインスリン様増殖因子I受容体(IGF−IR)と結合し、必要に応じて、そのリガンドIGF1および/またはIGF2の自然結合を阻害することができ、および/または前記IGF−IR受容体のチロシンキナーゼ活性を特異的に阻害することができる、単離された抗体またはその機能的断片であって、
配列番号2、4もしくは6の配列の相補性決定領域(CDR)、または配列番号2、4もしくは6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の少なくとも1つのCDRから選択される少なくとも1つのCDRを含んでなる軽鎖を含んでなるか、あるいは、配列番号8、10および12の配列のCDR、または配列番号8、10および12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の少なくとも1つのCDRから選択される少なくとも1つのCDRを含んでなる重鎖を含んでなる、単離された抗体またはその機能的断片。 - 配列番号12の配列、または配列番号12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の少なくとも1つのCDRを含んでなる重鎖を含んでなる、請求項1に記載の抗体またはその機能的断片。
- 配列番号8、10および12の配列の3つのCDRのうち少なくとも2つもしくは3つのCDR、または各々が配列番号8、10および12の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRのうち少なくとも2つもしくは3つのCDRを含んでなる重鎖を含んでなる、請求項1または2に記載の抗体またはその機能的断片。
- 配列番号2、4もしくは6の配列のCDR、または配列番号2、4もしくは6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列のCDRから選択される少なくとも1つのCDRを含んでなる軽鎖を含んでなる、請求項1〜3のいずれか一項に記載の抗体またはその機能的断片。
- 配列番号2、4および6の配列の3つのCDRのうち少なくとも2つもしくは3つのCDR、または各々が配列番号2、4および6の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の3つのCDRのうち少なくとも2つもしくは3つのCDRを含んでなる軽鎖を含んでなる、請求項1〜4のいずれか一項に記載の抗体またはその機能的断片。
- ヒトインスリン受容体(IR)と有意に結合しないことを特徴とする、請求項1〜5のいずれか一項に記載の抗体またはその機能的断片。
- 機能的断片が、Fv断片、Fab断片、F(ab’)2断片、Fab'断片、scFv断片、scFv−Fc断片およびダイアボディから選択されるもの、またはペグ化断片などの半減期を延長させた断片である、請求項1〜6のいずれか一項に記載の抗体。
- 請求項1〜6のいずれか一項に記載の抗体を分泌することができる、マウスハイブリドーマ。
- 2001年9月19日にCNCM(Institut Pasteur, Paris)に番号I−2717として寄託された、請求項8に記載のマウスハイブリドーマ。
- 請求項9に記載のハイブリドーマによって分泌される抗体またはその機能的断片。
- 前記抗体が、配列番号54のアミノ酸配列、もしくは配列番号54の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる配列の軽鎖、または/および、配列番号69のアミノ酸配列、もしくは配列番号69の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる配列の重鎖を含んでなるものである、請求項1〜7のいずれか一項に記載の抗体またはその機能的断片。
- 前記抗体がキメラ抗体であり、マウスとは異種の種の抗体に由来する軽鎖および重鎖定常領域をさらに含んでなるものである、請求項11に記載の抗体またはその機能的断片。
- 異種の種がヒトである、請求項12に記載のキメラ抗体またはその機能的断片。
- ヒト抗体由来の軽鎖および重鎖定常領域が、それぞれκ領域およびγ−1、γ−2またはγ-4領域である、請求項13に記載のキメラ抗体またはその機能的断片。
- 前記抗体がヒト化抗体であり、軽鎖および/または重鎖の骨格セグメントFR1〜FR4が、それぞれヒト抗体軽鎖および/または重鎖の骨格セグメントFR1〜FR4に由来するものである軽鎖および/または重鎖を含んでなるものである、請求項1〜7のいずれか一項に記載の抗体またはその機能的断片。
- 前記抗体が、配列番号61もしくは65のアミノ酸配列、または配列番号61もしくは65の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる軽鎖、または/および、配列番号75、79もしくは83のアミノ酸配列、または配列番号75、79もしくは83の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列を含んでなる重鎖を含んでなるものである、請求項15に記載のヒト化抗体またはその機能的断片。
- 前記抗体が、配列番号65のアミノ酸配列を含んでなる軽鎖、および配列番号79または83、好ましくは配列番号83のアミノ酸配列を含んでなる配列の重鎖を含んでなるものである、請求項15または16に記載のヒト化抗体またはその機能的断片。
- 以下の核酸:
(a)請求項1〜7および請求項10〜17のいずれか一項に記載の抗体またはその機能的断片をコードする核酸、DNAまたはRNA、
(b)前記(a)に記載の核酸に相補的な核酸、および
(c)配列番号1、3、5、7、9、もしくは11の核酸配列、または配列番号1、3、5、7、9、もしくは11の配列との最適なアライメントにおいて少なくとも80%の同一性を有する配列の少なくとも1つのCDRと、高度ストリンジェンシー条件下でハイブリダイズすることができる少なくとも18個のヌクレオチドからなる核酸
から選択される、単離された核酸。 - 請求項18に記載の核酸を含んでなる、ベクター。
- 請求項19に記載のベクターを含んでなる、宿主細胞。
- 請求項19に記載のベクターによって形質転換された少なくとも1つの細胞を含んでなる、ヒトを除くトランスジェニック動物。
- 以下の工程:
(a)請求項20に記載の細胞を、培地および好適な培養条件において培養する工程、および
(b)このようにして産生した抗体またはその機能的断片を、培養培地または培養した前記細胞から回収する工程
を含んでなる、請求項1〜7および請求項10〜17のいずれか一項に記載の抗体またはその機能的断片の製造方法。 - 請求項22に記載の方法によって得ることができる、抗体またはその機能的断片。
- さらに、ヒト上皮細胞増殖因子受容体と特異的に結合することができ、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害することができるものである、請求項1〜7、請求項10〜17および請求項23のいずれか一項に記載の抗体またはその機能的断片。
- 二重特異性抗体からなるものであり、かつ、EGFのヒト上皮細胞増殖因子受容体(EGFR)との結合を特異的に阻害し、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害する第二のモチーフを含んでなるものである、請求項24に記載の抗体。
- 二価または四価である、請求項25に記載の抗体。
- 第二のモチーフが、Fv断片、Fab断片、F(ab’)2断片、Fab’断片、Fab’PEG断片、scFv断片、scFv−Fc断片およびダイアボディから選択されるもの、または半減期を延長した形態である、請求項25または26に記載の抗体。
- 第二の抗EGFRモチーフが、マウスモノクローナル抗体225、そのマウス−ヒトキメラ誘導体C225、またはこの抗体225由来のヒト化抗体に由来するものである、請求項25〜27のいずれか一項に記載の抗体。
- 薬剤としての、請求項1〜7、請求項10〜17および請求項23〜27のいずれか一項に記載の抗体またはその機能的断片。
- 有効成分として、請求項1〜7、請求項10〜17および請求項23〜29のいずれか一項に記載の抗体またはその機能的断片からなる化合物を含んでなる、組成物。
- EGFのヒト上皮細胞増殖因子受容体(EGFR)との結合を特異的に阻害することができ、および/またはそのEGFR受容体のチロシンキナーゼ活性を特異的に阻害することができる化合物から選択される第二の化合物を含んでなる、請求項30に記載の組成物。
- 第二の化合物が、EGFのEGFRとの結合を競合によって阻害することができる単離された抗EGFR抗体またはその機能的断片から選択されるものである、請求項31に記載の組成物。
- 抗EGFR抗体が、モノクローナル抗EGFR抗体、キメラ抗EGFR抗体もしくはヒト化抗EGFR抗体、またはその機能的断片から選択されるものである、請求項32に記載の組成物。
- 抗EGFR抗体の機能的断片が、Fv断片、Fab断片、F(ab’)2断片、Fab'断片、scFv−Fc断片およびダイアボディから選択されるもの、またはペグ化断片などの半減期を延長した断片である、請求項32または33に記載の組成物。
- 抗EGFR抗体が、マウスモノクローナル抗体225、そのマウス−ヒトキメラ誘導体C225、または前記抗体225由来のヒト化抗体である、請求項32〜34のいずれか一項に記載の組成物。
- 同時使用、個別使用または逐次使用を目的とした組合せ製品として、細胞傷害性薬剤/細胞増殖抑制剤、ならびに/またはIGF−Iに対する受容体および/もしくはEGFに対する受容体のそれぞれのチロシンキナーゼ活性の阻害剤をさらに含んでなる、請求項30〜35のいずれか一項に記載の組成物。
- 細胞傷害性薬剤/細胞増殖抑制剤が、DNAと相互作用する薬剤、代謝拮抗物質、トポイソメラーゼIもしくはII阻害剤、または紡錘体形成阻害剤もしくは安定化剤、あるいは化学療法に用いることができる薬剤から選択されるものである、請求項36に記載の組成物。
- 細胞傷害性薬剤/細胞増殖抑制剤が、同時使用を目的とした組成物の少なくとも1つのエレメントと化学的に結合しているものである、請求項36または37に記載の組成物。
- 細胞傷害性薬剤/細胞増殖抑制剤が、紡錘体形成阻害剤または安定化剤、好ましくはビノレルビン、ビンフルニンまたはビンクリスチンから選択されるものである、請求項37または38に記載の組成物。
- IGF−Iに対する受容体および/またはEGFに対する受容体のそれぞれのチロシンキナーゼ活性の阻害剤が、誘導天然薬剤、ジアニリノフタルイミド、ピラゾロ−もしくはピロロピリドピリミジンまたはキナジリンからなる群から選択されるものである、請求項36〜39のいずれか一項に記載の組成物。
- 癌の予防および治療に向けた同時使用、個別使用または逐次使用を目的とした組合せ製品として、HER2/neu受容体の細胞外ドメインに対する他の抗体化合物をさらに含んでなる、請求項30〜40のいずれか一項に記載の組成物。
- HER2/neu受容体の細胞膜外ドメインに対する抗体が、トラスツズマブ、またはその機能的断片である、請求項41に記載の組成物。
- 抗体またはその機能的断片の少なくとも1つが、細胞毒素および/または放射性元素と結合しているものである、請求項30〜42のいずれか一項に記載の組成物。
- 薬剤としての、請求項30〜43のいずれか一項に記載の組成物。
- IGF−IR受容体および/もしくはEGFR受容体の過剰発現および/もしくは異常な活性化に関連した病気、ならびに/またはIGF1もしくはIGF2のIGF−IRとの相互作用および/もしくはEGFのEGFRとの相互作用が介在するシグナル変換経路の過反応に関連した病気の予防または治療に向けた薬剤の製造のための、請求項1〜7、請求項10〜17および請求項23〜29のいずれか一項に記載の抗体もしくはその機能的断片、および/または請求項30〜44のいずれか一項に記載の組成物の使用。
- 薬剤の投与が、インスリン受容体(IR)の阻害に関連した副次的効果を引き起こさない、またはわずかしか引き起こさない、請求項45に記載の使用。
- 正常細胞の、腫瘍特性を有する細胞、好ましくは、IGF依存性細胞、特に、IGF1および/またはIGF2依存性細胞、および/またはEGF依存性細胞、および/またはHER2/neu依存性細胞への形質転換を阻害することを目的とした薬剤の製造のための、請求項45または46に記載の使用。
- 腫瘍細胞、好ましくは、IGF依存性細胞、特に、IGF1および/またはIGF2依存性細胞、および/またはEGF依存性細胞、および/またはHER2/neu依存性細胞の成長および/または増殖を阻害することを目的とした薬剤の製造のための、請求項45〜47のいずれか一項に記載の使用。
- 癌の予防および治療を目的とする薬剤の製造のための、請求項45〜48のいずれか一項に記載の使用。
- 癌が、前立腺癌、骨肉腫、肺癌、乳癌、子宮内膜癌または結腸癌から選択される癌である、請求項49に記載の使用。
- 乾癬の予防および治療を目的とする薬剤の製造のための、請求項45〜48のいずれか一項に記載の使用。
- IGF−IR受容体および/またはEGFR受容体の異常な存在が疑われる生物学的サンプルから、IGF−IR受容体および/またはEGFR受容体の過剰発現または過少発現によって引き起こされる病気をin vitroで診断する方法であって、
前記生物学的サンプルを、必要に応じて標識することが可能である請求項1〜7、請求項10〜17および請求項23〜29のいずれか一項に記載の抗体と接触させることを特徴とする、方法。 - IGF−IR受容体および/もしくはEGFR受容体の過剰発現もしくは過少発現によって引き起こされる病気の診断方法、または生物学的サンプルのIGF−IR受容体および/もしくはEGFR受容体の過剰発現もしくは過少発現、好ましくはその受容体の過剰発現の検出方法および/もしくは定量方法を実施するためのキットまたはセットであって、以下の要素:
(a)請求項1〜7、請求項10〜17および請求項23〜29のいずれか一項に記載の抗体またはその機能的断片、
(b)所望により、 免疫学的反応に適した培地を形成するための試薬、
(c)所望により、免疫学的反応によって生じるIGF−IR/抗体および/またはEGFR/抗体複合体の実証を可能にする試薬
を含んでなる、キットまたはセット。 - 生物活性のある化合物の、IGF−IR受容体および/またはEGFR受容体を発現または過剰発現する細胞への特異的ターゲッティングを目的とする薬剤の製造のための、請求項1〜7、請求項10〜17および請求項23〜29のいずれか一項に記載の抗体またはその機能的断片の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0200654A FR2834900B1 (fr) | 2002-01-18 | 2002-01-18 | Nouvelles compositions a activite anti-igf-ir et anti-egfr et leurs applications |
| FR0200653A FR2834990A1 (fr) | 2002-01-18 | 2002-01-18 | Nouveaux anticorps anti-igf-ir et leurs applications |
| FR0205753A FR2834991B1 (fr) | 2002-01-18 | 2002-05-07 | Nouveaux anticorps anti-igf-ir et leurs applications |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003560053A Division JP4606739B2 (ja) | 2002-01-18 | 2003-01-20 | 新規抗igf−ir抗体およびその使用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010233575A true JP2010233575A (ja) | 2010-10-21 |
Family
ID=27248849
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003560053A Expired - Lifetime JP4606739B2 (ja) | 2002-01-18 | 2003-01-20 | 新規抗igf−ir抗体およびその使用 |
| JP2010124341A Pending JP2010233575A (ja) | 2002-01-18 | 2010-05-31 | 新規抗igf−ir抗体およびその使用 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003560053A Expired - Lifetime JP4606739B2 (ja) | 2002-01-18 | 2003-01-20 | 新規抗igf−ir抗体およびその使用 |
Country Status (16)
| Country | Link |
|---|---|
| EP (3) | EP1461359B1 (ja) |
| JP (2) | JP4606739B2 (ja) |
| CN (1) | CN100410275C (ja) |
| AT (1) | ATE357460T1 (ja) |
| AU (2) | AU2003216748B2 (ja) |
| BR (1) | BRPI0306973B8 (ja) |
| CA (1) | CA2473039C (ja) |
| CY (1) | CY1106662T1 (ja) |
| DE (1) | DE60312639T2 (ja) |
| DK (1) | DK1461359T3 (ja) |
| ES (2) | ES2427964T3 (ja) |
| MX (1) | MXPA04006980A (ja) |
| PT (1) | PT1461359E (ja) |
| SI (1) | SI1461359T1 (ja) |
| WO (1) | WO2003059951A2 (ja) |
| ZA (1) | ZA200405402B (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023027085A (ja) * | 2017-04-21 | 2023-03-01 | ジェネンテック, インコーポレイテッド | 疾患の治療のためのklk5アンタゴニストの使用 |
Families Citing this family (150)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10201182A1 (de) | 2002-01-14 | 2003-07-24 | Cfs Gmbh Kempten | Positioniersystem |
| US7553485B2 (en) | 2002-01-18 | 2009-06-30 | Pierre Fabre Medicament | Anti-IGF-IR and/or anti-insulin/IGF-I hybrid receptors antibodies and uses thereof |
| NZ554740A (en) | 2002-05-24 | 2009-01-31 | Schering Corp | Neutralizing human anti-IGFR antibody |
| US7538195B2 (en) | 2002-06-14 | 2009-05-26 | Immunogen Inc. | Anti-IGF-I receptor antibody |
| US8034904B2 (en) | 2002-06-14 | 2011-10-11 | Immunogen Inc. | Anti-IGF-I receptor antibody |
| US8663650B2 (en) | 2003-02-21 | 2014-03-04 | Ac Immune Sa | Methods and compositions comprising supramolecular constructs |
| ATE549359T1 (de) | 2003-04-02 | 2012-03-15 | Hoffmann La Roche | Antikörper gegen den insulinähnlichen wachstumsfaktor i-rezeptor und deren verwendungen |
| WO2005016970A2 (en) | 2003-05-01 | 2005-02-24 | Imclone Systems Incorporated | Fully human antibodies directed against the human insulin-like growth factor-1 receptor |
| US7579157B2 (en) * | 2003-07-10 | 2009-08-25 | Hoffmann-La Roche Inc. | Antibody selection method against IGF-IR |
| CN1835975B (zh) | 2003-08-13 | 2012-11-21 | 辉瑞产品公司 | 经修饰的人类igf-1r抗体 |
| WO2005047512A2 (en) | 2003-11-12 | 2005-05-26 | Shering Corporation | Plasmid system for multigene expression |
| AR046639A1 (es) | 2003-11-21 | 2005-12-14 | Schering Corp | Combinaciones terapeuticas de anticuerpo anti- igfr1 |
| WO2005058967A2 (en) * | 2003-12-16 | 2005-06-30 | Pierre Fabre Medicament | Novel anti-insulin/igf-i hybrid receptor or anti-insulin/igf-i hybrid receptor and igf-ir antibodies and uses thereof |
| MXPA06011199A (es) * | 2004-03-31 | 2007-04-16 | Genentech Inc | Anticuerpos anti-tgf-beta humanizados. |
| CN101014365B (zh) | 2004-07-16 | 2011-04-13 | 辉瑞产品公司 | 使用抗-igf-1r抗体联合治疗非血液的恶性肿瘤 |
| AU2011236042B2 (en) * | 2004-07-29 | 2013-09-05 | Pierre Fabre Medicament | Novel anti-IGF-IR antibodies and uses thereof |
| FR2873699B1 (fr) * | 2004-07-29 | 2009-08-21 | Pierre Fabre Medicament Sa | Nouveaux anticorps anti igf ir rt leurs utilisations |
| WO2006060419A2 (en) * | 2004-12-03 | 2006-06-08 | Schering Corporation | Biomarkers for pre-selection of patients for anti-igf1r therapy |
| MY146381A (en) | 2004-12-22 | 2012-08-15 | Amgen Inc | Compositions and methods relating relating to anti-igf-1 receptor antibodies |
| US20060233810A1 (en) * | 2005-04-15 | 2006-10-19 | Yaolin Wang | Methods and compositions for treating or preventing cancer |
| CA2612449A1 (en) | 2005-06-17 | 2006-12-28 | Imclone Systems Incorporated | Receptor antagonists for treatment of metastatic bone cancer |
| WO2007000328A1 (en) * | 2005-06-27 | 2007-01-04 | Istituto Di Ricerche Di Biologia Molecolare P Angeletti Spa | Antibodies that bind to an epitope on insulin-like growth factor 1 receptor and uses thereof |
| FR2888850B1 (fr) | 2005-07-22 | 2013-01-11 | Pf Medicament | Nouveaux anticorps anti-igf-ir et leurs applications |
| EA017812B1 (ru) * | 2005-12-08 | 2013-03-29 | Медарекс, Инк. | Выделенное моноклональное антитело или его антигенсвязывающий участок, которые связываются с протеинтирозинкиназой 7 ( ptk7) человека, и их применение |
| EP1984011A4 (en) | 2006-02-03 | 2010-08-18 | Imclone Llc | IGF-IR ANTAGONISTS AS AUXILIARIES FOR THE TREATMENT OF PROSTATE CANCER |
| GB0603041D0 (en) | 2006-02-15 | 2006-03-29 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| WO2007093008A1 (en) * | 2006-02-17 | 2007-08-23 | Adelaide Research & Innovation Pty Ltd | Antibodies to insulin-like growth factor i receptor |
| US7846724B2 (en) | 2006-04-11 | 2010-12-07 | Hoffmann-La Roche Inc. | Method for selecting CHO cell for production of glycosylated antibodies |
| CA2653745C (en) * | 2006-06-02 | 2013-11-19 | Pfizer Products Inc. | Circulating tumor cell assay |
| EP2032989B2 (en) | 2006-06-30 | 2015-10-28 | Merck Sharp & Dohme Corp. | Igfbp2 biomarker |
| FR2906533B1 (fr) | 2006-09-28 | 2013-02-22 | Pf Medicament | Procede de generation d'anticorps actifs contre un antigene de resistance,anticorps obtenus par ledit procede et leurs utilisations |
| JP2010511060A (ja) * | 2006-11-29 | 2010-04-08 | ジェネンテック インコーポレイテッド | 神経膠腫の診断及び治療方法 |
| WO2008076278A2 (en) * | 2006-12-13 | 2008-06-26 | Schering Corporation | Methods of cancer treatment with igf1r inhibitors |
| EP2109608B1 (en) | 2007-01-10 | 2011-03-23 | Istituto di Richerche di Biologia Molecolare P. Angeletti S.p.A. | Amide substituted indazoles as poly(adp-ribose)polymerase (parp) inhibitors |
| EP2559771A3 (en) | 2007-05-17 | 2013-06-12 | Bristol-Myers Squibb Company | Biomarkers and methods for determining sensitivity to insulin growth factor-1 receptor modulators |
| JP2010528583A (ja) * | 2007-06-11 | 2010-08-26 | エーシー イミューン ソシエテ アノニム | アミロイドβに対するヒト化抗体 |
| SG182192A1 (en) * | 2007-06-12 | 2012-07-30 | Ac Immune Sa | Humanized antibodies to amyloid beta |
| PE20090368A1 (es) | 2007-06-19 | 2009-04-28 | Boehringer Ingelheim Int | Anticuerpos anti-igf |
| CA2694990A1 (en) * | 2007-07-31 | 2009-02-05 | Merck Sharp & Dohme Corp. | Igf-1r specific antibodies useful in the detection and diagnosis of cellular proliferative disorders |
| CA2701032C (en) | 2007-09-27 | 2021-01-26 | Amgen Inc. | Pharmaceutical formulations |
| ES2962777T3 (es) | 2007-11-15 | 2024-03-21 | Amgen Inc | Formulación acuosa de anticuerpos estabilizada por antioxidantes para la administración parenteral |
| RU2011116112A (ru) * | 2008-09-26 | 2012-11-10 | Роше Гликарт Аг (Ch) | Биспецифические анти-egfr/анти-igf-1r антитела |
| CN103396488A (zh) | 2008-12-12 | 2013-11-20 | 贝林格尔.英格海姆国际有限公司 | 抗igf抗体 |
| AR075982A1 (es) | 2009-03-31 | 2011-05-11 | Roche Glycart Ag | Terapia de combinacion de un anticuerpo afucosilado y una o mas de las citoquinas seleccionadas de gm- csf humano, m -csf humano y/o il-3 humano y composicion |
| WO2010146059A2 (en) | 2009-06-16 | 2010-12-23 | F. Hoffmann-La Roche Ag | Biomarkers for igf-1r inhibitor therapy |
| US8470297B1 (en) | 2009-09-10 | 2013-06-25 | Merck Sharp & Dohme Corp. | FDG-pet evaluation of Ewing's sarcoma sensitivity |
| AU2010310457B2 (en) | 2009-10-23 | 2015-07-02 | Amgen Inc. | Vial adapter and system |
| MX2012004682A (es) | 2009-10-26 | 2012-09-07 | Hoffmann La Roche | Metodo para la produccion de una inmunoglobulina glicosilada. |
| WO2011053779A2 (en) | 2009-10-30 | 2011-05-05 | Bristol-Myers Squibb Company | Methods for treating cancer in patients having igf-1r inhibitor resistance |
| EP2507392A4 (en) | 2009-11-30 | 2013-06-05 | Merck Sharp & Dohme | METHOD OF IDENTIFYING AND TREATING PATIENTS SENSITIVE TO ANTI-IGF-1R INHIBITION THERAPY |
| WO2011083391A2 (en) | 2010-01-05 | 2011-07-14 | Pfizer Inc. | Biomarkers for anti-igf-ir cancer therapy |
| PT2575935E (pt) | 2010-06-07 | 2015-10-20 | Amgen Inc | Dispositivo de administração de medicamento |
| EP3441085A1 (en) | 2010-06-25 | 2019-02-13 | Vaccibody AS | Homodimeric protein constructs |
| JP2014510265A (ja) | 2011-02-02 | 2014-04-24 | アムジェン インコーポレイテッド | Igf−1rの阻害に関する方法および組成物 |
| MX341790B (es) | 2011-03-31 | 2016-09-02 | Amgen Inc | Adaptador de viales y sistema. |
| CA3021845C (en) | 2011-04-20 | 2022-03-29 | Amgen Inc. | Autoinjector apparatus |
| WO2013056069A1 (en) | 2011-10-13 | 2013-04-18 | Bristol-Myers Squibb Company | Methods for selecting and treating cancer in patients with igf-1r/ir inhibitors |
| SMT201800287T1 (it) | 2011-10-14 | 2018-07-17 | Amgen Inc | Iniettore e metodo di assiemaggio |
| US9700619B2 (en) | 2011-11-11 | 2017-07-11 | Duke University | Combination drug therapy for the treatment of solid tumors |
| US8980259B2 (en) | 2012-07-20 | 2015-03-17 | Novartis Ag | Combination therapy |
| CN102793922A (zh) * | 2012-08-14 | 2012-11-28 | 四川汇宇制药有限公司 | 一种治疗哺乳动物体内肿瘤疾病的方法 |
| AU2013348071B2 (en) | 2012-11-21 | 2018-05-24 | Amgen Inc. | Drug delivery device |
| US20140255413A1 (en) | 2013-03-07 | 2014-09-11 | Boehringer Ingelheim International Gmbh | Combination therapy for neoplasia treatment |
| JP6336564B2 (ja) | 2013-03-15 | 2018-06-06 | アムゲン・インコーポレーテッド | 薬物カセット、自動注入器、および自動注入器システム |
| TWI639453B (zh) | 2013-03-15 | 2018-11-01 | 美商安美基公司 | 用於注射器之匣盒 |
| JP6643977B2 (ja) | 2013-03-15 | 2020-02-12 | アムゲン・インコーポレーテッド | 体輪郭に適応可能な自動注入機デバイス |
| CN113559363B (zh) | 2013-03-22 | 2023-10-31 | 美国安进公司 | 注射器及装配方法 |
| CN103319597B (zh) * | 2013-05-13 | 2014-10-22 | 杭州德同生物技术有限公司 | 一种抗胰岛素样生长因子-1受体抗体及其编码基因和应用 |
| CN103319598B (zh) * | 2013-05-13 | 2014-10-22 | 杭州德同生物技术有限公司 | 抗胰岛素样生长因子-1受体抗体及其编码基因和应用 |
| WO2015035332A1 (en) * | 2013-09-09 | 2015-03-12 | Canimguide Therapeutics Ab | Immune system modulators |
| EP3789064B1 (en) | 2013-10-24 | 2024-11-27 | Amgen Inc. | Injector and method of assembly |
| WO2015061389A1 (en) | 2013-10-24 | 2015-04-30 | Amgen Inc. | Drug delivery system with temperature-sensitive control |
| WO2015119906A1 (en) | 2014-02-05 | 2015-08-13 | Amgen Inc. | Drug delivery system with electromagnetic field generator |
| SG11201609219QA (en) | 2014-05-07 | 2016-12-29 | Amgen Inc | Autoinjector with shock reducing elements |
| US20170124285A1 (en) | 2014-06-03 | 2017-05-04 | Amgen Inc. | Devices and methods for assisting a user of a drug delivery device |
| MX392725B (es) | 2014-10-14 | 2025-03-24 | Amgen Inc | Dispositivo de inyeccion de farmaco con indicadores visuales y audibles. |
| JP6716566B2 (ja) | 2014-12-19 | 2020-07-01 | アムジエン・インコーポレーテツド | 近接センサ付き薬物送達装置 |
| WO2016100055A1 (en) | 2014-12-19 | 2016-06-23 | Amgen Inc. | Drug delivery device with live button or user interface field |
| US10583245B2 (en) | 2015-02-17 | 2020-03-10 | Amgen Inc. | Drug delivery device with vacuum assisted securement and/or feedback |
| ES2905870T3 (es) | 2015-02-27 | 2022-04-12 | Amgen Inc | Dispositivo de suministro de fármacos que tiene un mecanismo de protección de aguja con un umbral de resistencia ajustable al movimiento de la protección de aguja |
| AU2016229309B2 (en) | 2015-03-06 | 2021-12-02 | Canimguide Therapeutics Ab | Immune system modulators and compositions |
| WO2017039786A1 (en) | 2015-09-02 | 2017-03-09 | Amgen Inc. | Syringe assembly adapter for a syringe |
| WO2017100501A1 (en) | 2015-12-09 | 2017-06-15 | Amgen Inc. | Auto-injector with signaling cap |
| WO2017120178A1 (en) | 2016-01-06 | 2017-07-13 | Amgen Inc. | Auto-injector with signaling electronics |
| JP2019505512A (ja) | 2016-01-08 | 2019-02-28 | バッシボディ アクスイェ セルスカプ | 治療用抗癌ネオエピトープワクチン |
| ES2814287T3 (es) | 2016-03-15 | 2021-03-26 | Amgen Inc | Reducir la probabilidad de rotura de cristal en dispositivos de administración de fármaco |
| WO2017189089A1 (en) | 2016-04-29 | 2017-11-02 | Amgen Inc. | Drug delivery device with messaging label |
| US11389588B2 (en) | 2016-05-02 | 2022-07-19 | Amgen Inc. | Syringe adapter and guide for filling an on-body injector |
| AU2017263558B2 (en) | 2016-05-13 | 2022-12-22 | Amgen Inc. | Vial sleeve assembly |
| US11238150B2 (en) | 2016-05-16 | 2022-02-01 | Amgen Inc. | Data encryption in medical devices with limited computational capability |
| EP3465124B1 (en) | 2016-06-03 | 2026-02-11 | Amgen Inc. | Impact testing apparatuses and methods for drug delivery devices |
| WO2017222951A1 (en) | 2016-06-23 | 2017-12-28 | Merck Sharp & Dohme Corp. | 3-aryl and heteroaryl substituted 5-trifluoromethyl oxadiazoles as histone deacetylase 6 (hdac6) inhibitors |
| WO2018004842A1 (en) | 2016-07-01 | 2018-01-04 | Amgen Inc. | Drug delivery device having minimized risk of component fracture upon impact events |
| US20190328965A1 (en) | 2016-08-17 | 2019-10-31 | Amgen Inc. | Drug delivery device with placement detection |
| EP3532127A1 (en) | 2016-10-25 | 2019-09-04 | Amgen Inc. | On-body injector |
| EP3570917A1 (en) | 2017-01-17 | 2019-11-27 | Amgen Inc. | Injection devices and related methods of use and assembly |
| WO2018152073A1 (en) | 2017-02-17 | 2018-08-23 | Amgen Inc. | Insertion mechanism for drug delivery device |
| AU2018220538B2 (en) | 2017-02-17 | 2023-12-14 | Amgen Inc. | Drug delivery device with sterile fluid flowpath and related method of assembly |
| WO2018165143A1 (en) | 2017-03-06 | 2018-09-13 | Amgen Inc. | Drug delivery device with activation prevention feature |
| IL268478B2 (en) | 2017-03-07 | 2023-10-01 | Amgen Inc | Inserting a needle using super pressure |
| MX2019010671A (es) | 2017-03-09 | 2019-10-21 | Amgen Inc | Mecanismo de insercion para dispositivo de administracion de farmacos. |
| KR102651078B1 (ko) | 2017-03-28 | 2024-03-22 | 암겐 인코포레이티드 | 플런저 로드 및 주사기 조립 시스템 및 방법 |
| CA3061982A1 (en) | 2017-06-08 | 2018-12-13 | Amgen Inc. | Syringe assembly for a drug delivery device and method of assembly |
| EP3634546A1 (en) | 2017-06-08 | 2020-04-15 | Amgen Inc. | Torque driven drug delivery device |
| AU2018288604B2 (en) | 2017-06-22 | 2023-12-21 | Amgen Inc. | Device activation impact/shock reduction |
| MA49461A (fr) | 2017-06-23 | 2020-04-29 | Amgen Inc | Dispositif électronique d'administration de médicament comprenant un bouchon activé par un ensemble commutateur |
| JP7408398B2 (ja) | 2017-07-14 | 2024-01-05 | アムジエン・インコーポレーテツド | 二重ねじりばねシステムを有する針挿入後退システム |
| WO2019018169A1 (en) | 2017-07-21 | 2019-01-24 | Amgen Inc. | PERMEABLE GAS SEALING ELEMENT FOR MEDICINE CONTAINER AND METHODS OF ASSEMBLY |
| MA49677A (fr) | 2017-07-25 | 2021-04-21 | Amgen Inc | Dispositif d'administration de médicament avec module d'engrenage et procédé d'assemblage associé |
| JP7242562B2 (ja) | 2017-07-25 | 2023-03-20 | アムジエン・インコーポレーテツド | 容器アクセスシステムを有する薬物送達デバイス及び関連する組立方法 |
| US12318593B2 (en) | 2017-08-09 | 2025-06-03 | Amgen Inc. | Hydraulic-pneumatic pressurized chamber drug delivery system |
| WO2019036181A1 (en) | 2017-08-18 | 2019-02-21 | Amgen Inc. | BODY INJECTOR WITH STERILE ADHESIVE PATCH |
| US11103636B2 (en) | 2017-08-22 | 2021-08-31 | Amgen Inc. | Needle insertion mechanism for drug delivery device |
| MA50611A (fr) | 2017-10-04 | 2020-08-12 | Amgen Inc | Adaptateur d'écoulement destiné à un dispositif d'administration de médicament |
| CN111132711B (zh) | 2017-10-06 | 2022-07-01 | 安进公司 | 带有联锁组件的药物递送装置及相关组装方法 |
| EP3694578B1 (en) | 2017-10-09 | 2025-09-24 | Amgen Inc. | Drug delivery device with drive assembly and related method of assembly |
| IL273663B2 (en) | 2017-11-03 | 2025-05-01 | Amgen Inc | System and methods for disinfecting a drug delivery device |
| ES2994389T3 (en) | 2017-11-06 | 2025-01-23 | Amgen Inc | Drug delivery device with placement and flow sensing |
| WO2019090303A1 (en) | 2017-11-06 | 2019-05-09 | Amgen Inc. | Fill-finish assemblies and related methods |
| MA50557A (fr) | 2017-11-10 | 2020-09-16 | Amgen Inc | Pistons pour dispositifs d'administration de médicament |
| JP7370969B2 (ja) | 2017-11-16 | 2023-10-30 | アムジエン・インコーポレーテツド | 薬物送達デバイスの扉ラッチ機構 |
| JP7747438B2 (ja) | 2017-11-16 | 2025-10-01 | アムジエン・インコーポレーテツド | 失速及び終点検出を有するオートインジェクタ |
| US10835685B2 (en) | 2018-05-30 | 2020-11-17 | Amgen Inc. | Thermal spring release mechanism for a drug delivery device |
| US11083840B2 (en) | 2018-06-01 | 2021-08-10 | Amgen Inc. | Modular fluid path assemblies for drug delivery devices |
| US12303677B2 (en) | 2018-07-24 | 2025-05-20 | Amgen Inc. | Hybrid drug delivery devices with optional grip portion and related method of preparation |
| WO2020023451A1 (en) | 2018-07-24 | 2020-01-30 | Amgen Inc. | Delivery devices for administering drugs |
| MA53379A (fr) | 2018-07-24 | 2021-06-02 | Amgen Inc | Dispositifs d'administration pour l'administration de médicaments |
| WO2020023336A1 (en) | 2018-07-24 | 2020-01-30 | Amgen Inc. | Hybrid drug delivery devices with grip portion |
| MA53320A (fr) | 2018-07-31 | 2021-11-03 | Amgen Inc | Ensemble de trajet de fluide pour dispositif d'administration de médicament |
| US12097263B2 (en) | 2018-08-02 | 2024-09-24 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating myotonic dystrophy |
| US12018087B2 (en) | 2018-08-02 | 2024-06-25 | Dyne Therapeutics, Inc. | Muscle-targeting complexes comprising an anti-transferrin receptor antibody linked to an oligonucleotide and methods of delivering oligonucleotide to a subject |
| US12370264B1 (en) | 2018-08-02 | 2025-07-29 | Dyne Therapeutics, Inc. | Complexes comprising an anti-transferrin receptor antibody linked to an oligonucleotide and method of delivering oligonucleotide to a subject |
| US11911484B2 (en) | 2018-08-02 | 2024-02-27 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating myotonic dystrophy |
| MA53724A (fr) | 2018-09-24 | 2021-12-29 | Amgen Inc | Systèmes et procédés de dosage interventionnel |
| CA3110371A1 (en) | 2018-09-28 | 2020-04-02 | Amgen Inc. | Muscle wire escapement activation assembly for a drug delivery device |
| CN117159846A (zh) | 2018-10-02 | 2023-12-05 | 安进公司 | 具有内部力传递的用于药物递送的注射系统 |
| WO2020072846A1 (en) | 2018-10-05 | 2020-04-09 | Amgen Inc. | Drug delivery device having dose indicator |
| AR116704A1 (es) | 2018-10-15 | 2021-06-02 | Amgen Inc | Dispositivo de administración de fármacos con mecanismo de amortiguación |
| SG11202101824VA (en) | 2018-10-15 | 2021-03-30 | Amgen Inc | Platform assembly process for drug delivery device |
| IL281908B2 (en) | 2018-11-01 | 2025-06-01 | Amgen Inc | Drug delivery devices with partial drug delivery member retraction |
| ES3010833T3 (en) | 2018-11-01 | 2025-04-04 | Amgen Inc | Drug delivery devices with partial drug delivery member retraction |
| TWI831847B (zh) | 2018-11-01 | 2024-02-11 | 美商安進公司 | 部分針頭縮回之藥物遞送裝置及其操作方法 |
| US20220160972A1 (en) | 2019-04-24 | 2022-05-26 | Amgen Inc. | Syringe sterilization verification assemblies and methods |
| EP4017560A2 (en) | 2019-08-23 | 2022-06-29 | Amgen, Inc | Drug delivery device with configurable needle shield engagement components and related methods |
| IL294479A (en) * | 2020-01-10 | 2022-09-01 | Dyne Therapeutics Inc | Muscle targeting complexes and uses thereof for treating myotonic dystrophy |
| AU2021205346A1 (en) * | 2020-01-10 | 2022-09-01 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating dystrophinopathies |
| MX2023013640A (es) | 2021-05-21 | 2023-11-30 | Amgen Inc | Metodo de optimizacion de una receta de llenado para un contenedor de medicamento. |
| US11633498B2 (en) | 2021-07-09 | 2023-04-25 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating myotonic dystrophy |
| US11969475B2 (en) | 2021-07-09 | 2024-04-30 | Dyne Therapeutics, Inc. | Muscle targeting complexes and uses thereof for treating facioscapulohumeral muscular dystrophy |
| CA3255934A1 (en) | 2022-04-15 | 2023-10-19 | Dyne Therapeutics, Inc. | MUSCLE TARGETTING COMPLEXES AND FORMULATIONS FOR THE TREATMENT OF MYOTONIC DYSTROPHY |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11507535A (ja) * | 1995-06-07 | 1999-07-06 | イムクローン システムズ インコーポレイテッド | 腫瘍の成長を抑制する抗体および抗体フラグメント類 |
| JP2003533987A (ja) * | 2000-05-19 | 2003-11-18 | イス ケミカル カンパニー リミテッド | 表皮成長因子収容体に対するヒト化抗体 |
| SV2007000775A (es) * | 2001-01-05 | 2007-03-15 | Pfizer | Anticuerpos contra el receptor del factor de crecimiento similar a insulina |
-
2003
- 2003-01-20 CA CA2473039A patent/CA2473039C/fr not_active Expired - Lifetime
- 2003-01-20 BR BRPI0306973A patent/BRPI0306973B8/pt not_active IP Right Cessation
- 2003-01-20 ES ES06126430T patent/ES2427964T3/es not_active Expired - Lifetime
- 2003-01-20 EP EP03712270A patent/EP1461359B1/fr not_active Expired - Lifetime
- 2003-01-20 ES ES03712270T patent/ES2283759T3/es not_active Expired - Lifetime
- 2003-01-20 DK DK03712270T patent/DK1461359T3/da active
- 2003-01-20 DE DE60312639T patent/DE60312639T2/de not_active Expired - Lifetime
- 2003-01-20 EP EP06126430.5A patent/EP1806364B1/fr not_active Expired - Lifetime
- 2003-01-20 WO PCT/FR2003/000178 patent/WO2003059951A2/fr not_active Ceased
- 2003-01-20 CN CNB038024489A patent/CN100410275C/zh not_active Expired - Lifetime
- 2003-01-20 AU AU2003216748A patent/AU2003216748B2/en not_active Expired
- 2003-01-20 AT AT03712270T patent/ATE357460T1/de active
- 2003-01-20 EP EP06126429A patent/EP1798242B1/fr not_active Expired - Lifetime
- 2003-01-20 PT PT03712270T patent/PT1461359E/pt unknown
- 2003-01-20 JP JP2003560053A patent/JP4606739B2/ja not_active Expired - Lifetime
- 2003-01-20 MX MXPA04006980A patent/MXPA04006980A/es active IP Right Grant
- 2003-01-20 SI SI200330732T patent/SI1461359T1/sl unknown
-
2004
- 2004-07-07 ZA ZA2004/05402A patent/ZA200405402B/en unknown
-
2007
- 2007-06-15 CY CY20071100801T patent/CY1106662T1/el unknown
-
2009
- 2009-04-24 AU AU2009201674A patent/AU2009201674B2/en not_active Expired
-
2010
- 2010-05-31 JP JP2010124341A patent/JP2010233575A/ja active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023027085A (ja) * | 2017-04-21 | 2023-03-01 | ジェネンテック, インコーポレイテッド | 疾患の治療のためのklk5アンタゴニストの使用 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4606739B2 (ja) | 新規抗igf−ir抗体およびその使用 | |
| US7241444B2 (en) | Anti-IGF-IR antibodies and uses thereof | |
| TWI414532B (zh) | 抗第1型類胰島素生長因子接受器之抗體及其之使用 | |
| CN101939336B (zh) | Axl抗体 | |
| KR101671039B1 (ko) | 항 cxcr4 항체 및 그들의 암의 치료를 위한 용도 | |
| KR101838310B1 (ko) | 암의 치료를 위한 인간화 항-cxcr4 항체들 | |
| EP3741777A1 (en) | Pd-l1 antibody, antigen-binding fragment thereof, and pharmaceutical use thereof | |
| JP2022514786A (ja) | Muc18に特異的な抗体 | |
| US20080063639A1 (en) | Method for the treatment of psoriasis comprising novel anti-IGF-IR antibodies | |
| WO2020063660A1 (zh) | 抗ox40抗体、其抗原结合片段及其医药用途 | |
| FR2834990A1 (fr) | Nouveaux anticorps anti-igf-ir et leurs applications | |
| KR102728505B1 (ko) | 향상된 암세포 사멸효능을 갖는 비대칭 항체 | |
| US20240383998A1 (en) | Asymmetric antibody with improved cytotoxicity against cancer cells | |
| US20240141061A1 (en) | Novel antibody against cd55 and use thereof | |
| HK1078590B (en) | Novel anti-igf-ir antibodies and uses thereof | |
| HK1147275B (en) | Axl antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A132 Effective date: 20120706 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20121005 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20121011 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130319 |