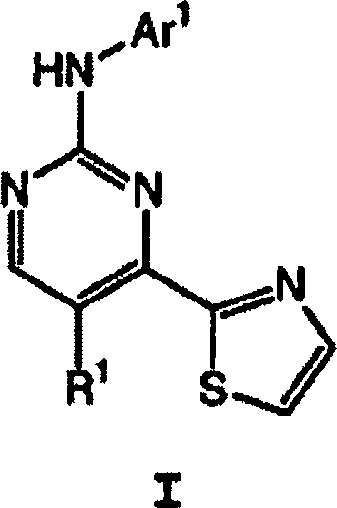
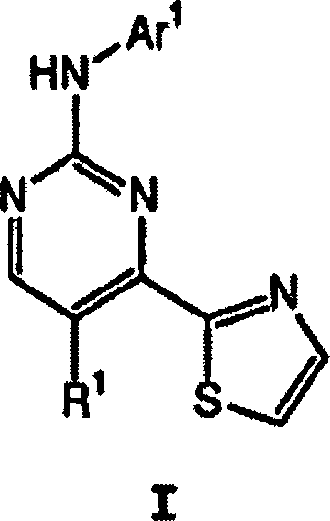
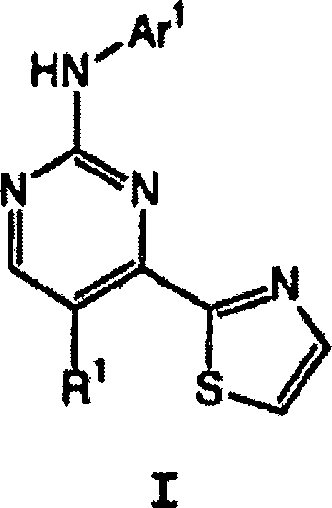
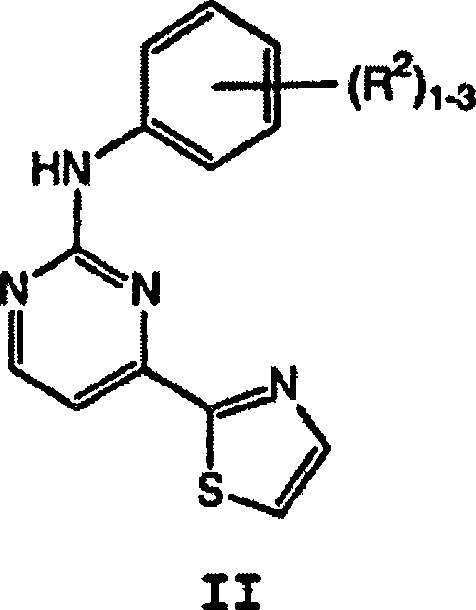
DE60214703T2 - Thiazolverbindungen, die sich als inhibitoren von proteinkinasen eignen - Google Patents
Thiazolverbindungen, die sich als inhibitoren von proteinkinasen eignen Download PDFInfo
- Publication number
- DE60214703T2 DE60214703T2 DE60214703T DE60214703T DE60214703T2 DE 60214703 T2 DE60214703 T2 DE 60214703T2 DE 60214703 T DE60214703 T DE 60214703T DE 60214703 T DE60214703 T DE 60214703T DE 60214703 T2 DE60214703 T2 DE 60214703T2
- Authority
- DE
- Germany
- Prior art keywords
- disease
- treating
- compound
- optionally substituted
- agent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 102000001253 Protein Kinase Human genes 0.000 title claims abstract description 24
- 108060006633 protein kinase Proteins 0.000 title claims abstract description 24
- 239000003112 inhibitor Substances 0.000 title abstract description 19
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical class C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 108
- 239000000203 mixture Substances 0.000 claims abstract description 62
- 101150110875 Syk gene Proteins 0.000 claims abstract description 36
- 108090000461 Aurora Kinase A Proteins 0.000 claims abstract description 34
- 102100032311 Aurora kinase A Human genes 0.000 claims abstract description 31
- 238000011282 treatment Methods 0.000 claims abstract description 29
- 102000001267 GSK3 Human genes 0.000 claims abstract description 23
- 108060006662 GSK3 Proteins 0.000 claims abstract description 23
- 230000001404 mediated effect Effects 0.000 claims abstract description 21
- 238000000034 method Methods 0.000 claims abstract description 21
- NFVJNJQRWPQVOA-UHFFFAOYSA-N n-[2-chloro-5-(trifluoromethyl)phenyl]-2-[3-(4-ethyl-5-ethylsulfanyl-1,2,4-triazol-3-yl)piperidin-1-yl]acetamide Chemical compound CCN1C(SCC)=NN=C1C1CN(CC(=O)NC=2C(=CC=C(C=2)C(F)(F)F)Cl)CCC1 NFVJNJQRWPQVOA-UHFFFAOYSA-N 0.000 claims abstract description 21
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 66
- 229910052757 nitrogen Inorganic materials 0.000 claims description 46
- -1 CO 2 CH 3 Chemical group 0.000 claims description 44
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 37
- 125000001931 aliphatic group Chemical group 0.000 claims description 36
- 229910052760 oxygen Inorganic materials 0.000 claims description 30
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 29
- 201000010099 disease Diseases 0.000 claims description 29
- 239000001301 oxygen Substances 0.000 claims description 28
- 230000000694 effects Effects 0.000 claims description 23
- 125000005842 heteroatom Chemical group 0.000 claims description 20
- 229910052717 sulfur Inorganic materials 0.000 claims description 19
- 239000011593 sulfur Substances 0.000 claims description 19
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 18
- 125000003118 aryl group Chemical group 0.000 claims description 16
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 16
- 239000003795 chemical substances by application Substances 0.000 claims description 15
- 239000004480 active ingredient Substances 0.000 claims description 14
- 239000003814 drug Substances 0.000 claims description 14
- 229910052736 halogen Inorganic materials 0.000 claims description 13
- 150000002367 halogens Chemical class 0.000 claims description 13
- 229910052739 hydrogen Inorganic materials 0.000 claims description 12
- 125000002950 monocyclic group Chemical group 0.000 claims description 12
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims description 12
- 229940124597 therapeutic agent Drugs 0.000 claims description 12
- 239000012472 biological sample Substances 0.000 claims description 11
- 229920006395 saturated elastomer Polymers 0.000 claims description 11
- 208000024827 Alzheimer disease Diseases 0.000 claims description 10
- 208000006673 asthma Diseases 0.000 claims description 10
- 201000006417 multiple sclerosis Diseases 0.000 claims description 10
- 150000003839 salts Chemical class 0.000 claims description 10
- 125000001072 heteroaryl group Chemical group 0.000 claims description 9
- 239000001257 hydrogen Substances 0.000 claims description 9
- 229910002091 carbon monoxide Inorganic materials 0.000 claims description 8
- 206010012601 diabetes mellitus Diseases 0.000 claims description 8
- 125000002619 bicyclic group Chemical group 0.000 claims description 7
- 208000035475 disorder Diseases 0.000 claims description 7
- 230000002401 inhibitory effect Effects 0.000 claims description 7
- 239000003981 vehicle Substances 0.000 claims description 7
- 206010028980 Neoplasm Diseases 0.000 claims description 6
- 208000024172 Cardiovascular disease Diseases 0.000 claims description 5
- 125000001118 alkylidene group Chemical group 0.000 claims description 5
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 claims description 5
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 5
- 201000000980 schizophrenia Diseases 0.000 claims description 5
- 208000018737 Parkinson disease Diseases 0.000 claims description 4
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 4
- 201000011510 cancer Diseases 0.000 claims description 4
- 125000006569 (C5-C6) heterocyclic group Chemical group 0.000 claims description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 3
- 206010020880 Hypertrophy Diseases 0.000 claims description 3
- 208000029462 Immunodeficiency disease Diseases 0.000 claims description 3
- 108010025020 Nerve Growth Factor Proteins 0.000 claims description 3
- 102000007072 Nerve Growth Factors Human genes 0.000 claims description 3
- 102000000551 Syk Kinase Human genes 0.000 claims description 3
- 108010016672 Syk Kinase Proteins 0.000 claims description 3
- 230000000172 allergic effect Effects 0.000 claims description 3
- 239000002260 anti-inflammatory agent Substances 0.000 claims description 3
- 229940125708 antidiabetic agent Drugs 0.000 claims description 3
- 239000003472 antidiabetic agent Substances 0.000 claims description 3
- 208000010668 atopic eczema Diseases 0.000 claims description 3
- 125000001246 bromo group Chemical group Br* 0.000 claims description 3
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 3
- 125000001153 fluoro group Chemical group F* 0.000 claims description 3
- 208000014951 hematologic disease Diseases 0.000 claims description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 3
- 230000002519 immonomodulatory effect Effects 0.000 claims description 3
- 229940125721 immunosuppressive agent Drugs 0.000 claims description 3
- 239000003018 immunosuppressive agent Substances 0.000 claims description 3
- 208000019423 liver disease Diseases 0.000 claims description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 3
- 239000003900 neurotrophic factor Substances 0.000 claims description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 3
- 206010065040 AIDS dementia complex Diseases 0.000 claims description 2
- 208000006011 Stroke Diseases 0.000 claims description 2
- 239000002246 antineoplastic agent Substances 0.000 claims description 2
- 208000015114 central nervous system disease Diseases 0.000 claims description 2
- 229940127089 cytotoxic agent Drugs 0.000 claims description 2
- 229940079593 drug Drugs 0.000 claims description 2
- 239000003937 drug carrier Substances 0.000 claims description 2
- 125000001188 haloalkyl group Chemical group 0.000 claims description 2
- 125000002346 iodo group Chemical group I* 0.000 claims description 2
- 229940124599 anti-inflammatory drug Drugs 0.000 claims 2
- 230000001028 anti-proliverative effect Effects 0.000 claims 2
- 239000013543 active substance Substances 0.000 claims 1
- 239000002671 adjuvant Substances 0.000 claims 1
- 208000028683 bipolar I disease Diseases 0.000 claims 1
- 230000000973 chemotherapeutic effect Effects 0.000 claims 1
- 239000004744 fabric Substances 0.000 claims 1
- 230000001225 therapeutic effect Effects 0.000 claims 1
- 102000002254 Glycogen Synthase Kinase 3 Human genes 0.000 description 22
- 108010014905 Glycogen Synthase Kinase 3 Proteins 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 125000001424 substituent group Chemical group 0.000 description 20
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 17
- 235000002639 sodium chloride Nutrition 0.000 description 15
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 13
- 230000005764 inhibitory process Effects 0.000 description 13
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 12
- 239000000243 solution Substances 0.000 description 11
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- 238000003556 assay Methods 0.000 description 9
- 102000004877 Insulin Human genes 0.000 description 8
- 108090001061 Insulin Proteins 0.000 description 8
- 210000004027 cell Anatomy 0.000 description 8
- 125000000623 heterocyclic group Chemical group 0.000 description 8
- 229940125396 insulin Drugs 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 7
- 125000000217 alkyl group Chemical group 0.000 description 7
- 210000004369 blood Anatomy 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 229940088598 enzyme Drugs 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 125000005843 halogen group Chemical group 0.000 description 6
- 239000011541 reaction mixture Substances 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
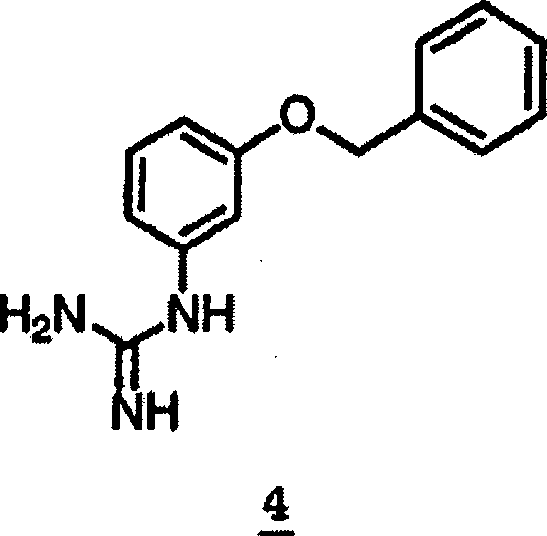
- FDLXZFWWHUOYOB-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)guanidine Chemical compound NC(N)=NC1=CC=CC(OCC=2C=CC=CC=2)=C1 FDLXZFWWHUOYOB-UHFFFAOYSA-N 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 125000006367 bivalent amino carbonyl group Chemical group [H]N([*:1])C([*:2])=O 0.000 description 5
- 210000003979 eosinophil Anatomy 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 125000001624 naphthyl group Chemical group 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 235000019198 oils Nutrition 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 108090000765 processed proteins & peptides Proteins 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 0 *CCN1CN(CCCOC2C=C(C(*)C3=NC=CC(c4ncc[s]4)N3)C=CC2)CC1 Chemical compound *CCN1CN(CCCOC2C=C(C(*)C3=NC=CC(c4ncc[s]4)N3)C=CC2)CC1 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- MOMFXATYAINJML-UHFFFAOYSA-N 2-Acetylthiazole Chemical compound CC(=O)C1=NC=CS1 MOMFXATYAINJML-UHFFFAOYSA-N 0.000 description 4
- 229920002527 Glycogen Polymers 0.000 description 4
- 108010050904 Interferons Proteins 0.000 description 4
- 102000014150 Interferons Human genes 0.000 description 4
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 description 4
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 4
- 108091000080 Phosphotransferase Proteins 0.000 description 4
- 230000006907 apoptotic process Effects 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 239000003246 corticosteroid Substances 0.000 description 4
- 229960001334 corticosteroids Drugs 0.000 description 4
- 239000002270 dispersing agent Substances 0.000 description 4
- 239000002552 dosage form Substances 0.000 description 4
- 239000000284 extract Substances 0.000 description 4
- 229940096919 glycogen Drugs 0.000 description 4
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 4
- 229940047124 interferons Drugs 0.000 description 4
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 4
- BOPGDPNILDQYTO-NNYOXOHSSA-N nicotinamide-adenine dinucleotide Chemical compound C1=CCC(C(=O)N)=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=NC=NC(N)=C3N=C2)O)O1 BOPGDPNILDQYTO-NNYOXOHSSA-N 0.000 description 4
- 102000020233 phosphotransferase Human genes 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 3
- 102000004000 Aurora Kinase A Human genes 0.000 description 3
- 102000015735 Beta-catenin Human genes 0.000 description 3
- 108060000903 Beta-catenin Proteins 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- XZMCDFZZKTWFGF-UHFFFAOYSA-N Cyanamide Chemical compound NC#N XZMCDFZZKTWFGF-UHFFFAOYSA-N 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- 206010014950 Eosinophilia Diseases 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 3
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 3
- 239000007995 HEPES buffer Substances 0.000 description 3
- 102000000589 Interleukin-1 Human genes 0.000 description 3
- 108010002352 Interleukin-1 Proteins 0.000 description 3
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 3
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 102000013009 Pyruvate Kinase Human genes 0.000 description 3
- 108020005115 Pyruvate Kinase Proteins 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 230000002159 abnormal effect Effects 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- ZRALSGWEFCBTJO-UHFFFAOYSA-N anhydrous guanidine Natural products NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 3
- 229940045988 antineoplastic drug protein kinase inhibitors Drugs 0.000 description 3
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 3
- 125000003710 aryl alkyl group Chemical group 0.000 description 3
- 239000007853 buffer solution Substances 0.000 description 3
- 150000001721 carbon Chemical group 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000000753 cycloalkyl group Chemical group 0.000 description 3
- 229960004397 cyclophosphamide Drugs 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 125000004475 heteroaralkyl group Chemical group 0.000 description 3
- 150000002431 hydrogen Chemical class 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000002207 metabolite Substances 0.000 description 3
- SMHUCMRAVFJCSW-UHFFFAOYSA-N n-(3-phenylmethoxyphenyl)-4-(1,3-thiazol-2-yl)pyrimidin-2-amine Chemical compound C=1C=CC=CC=1COC(C=1)=CC=CC=1NC(N=1)=NC=CC=1C1=NC=CS1 SMHUCMRAVFJCSW-UHFFFAOYSA-N 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 229930029653 phosphoenolpyruvate Natural products 0.000 description 3
- DTBNBXWJWCWCIK-UHFFFAOYSA-N phosphoenolpyruvic acid Chemical compound OC(=O)C(=C)OP(O)(O)=O DTBNBXWJWCWCIK-UHFFFAOYSA-N 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000003909 protein kinase inhibitor Substances 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 230000035939 shock Effects 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000011550 stock solution Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 102000013498 tau Proteins Human genes 0.000 description 3
- 108010026424 tau Proteins Proteins 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 description 2
- 125000000389 2-pyrrolyl group Chemical group [H]N1C([*])=C([H])C([H])=C1[H] 0.000 description 2
- FHCSBLWRGCOVPT-UHFFFAOYSA-N AZD2858 Chemical compound C1CN(C)CCN1S(=O)(=O)C1=CC=C(C=2N=C(C(N)=NC=2)C(=O)NC=2C=NC=CC=2)C=C1 FHCSBLWRGCOVPT-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 102100030013 Endoribonuclease Human genes 0.000 description 2
- 101710199605 Endoribonuclease Proteins 0.000 description 2
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 2
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 108010001483 Glycogen Synthase Proteins 0.000 description 2
- 102000009438 IgE Receptors Human genes 0.000 description 2
- 108010073816 IgE Receptors Proteins 0.000 description 2
- 108010005716 Interferon beta-1a Proteins 0.000 description 2
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 101710113029 Serine/threonine-protein kinase Proteins 0.000 description 2
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 2
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 2
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 2
- 229960002170 azathioprine Drugs 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 235000019445 benzyl alcohol Nutrition 0.000 description 2
- 238000004166 bioassay Methods 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 230000022131 cell cycle Effects 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 230000036755 cellular response Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 208000029742 colonic neoplasm Diseases 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 229940099112 cornstarch Drugs 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 2
- ADEBPBSSDYVVLD-UHFFFAOYSA-N donepezil Chemical compound O=C1C=2C=C(OC)C(OC)=CC=2CC1CC(CC1)CCN1CC1=CC=CC=C1 ADEBPBSSDYVVLD-UHFFFAOYSA-N 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 238000001952 enzyme assay Methods 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 229940126864 fibroblast growth factor Drugs 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 230000004190 glucose uptake Effects 0.000 description 2
- 125000005456 glyceride group Chemical group 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- 125000005114 heteroarylalkoxy group Chemical group 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 230000004770 neurodegeneration Effects 0.000 description 2
- 210000002682 neurofibrillary tangle Anatomy 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 235000021317 phosphate Nutrition 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- 238000011321 prophylaxis Methods 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 238000005956 quaternization reaction Methods 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 229960001940 sulfasalazine Drugs 0.000 description 2
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 2
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 125000004192 tetrahydrofuran-2-yl group Chemical group [H]C1([H])OC([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 2
- 229940099259 vaseline Drugs 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical compound CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- SEUSFEKWVIFWTN-UHFFFAOYSA-N 2-aminopyrimidine-5-carbonitrile Chemical class NC1=NC=C(C#N)C=N1 SEUSFEKWVIFWTN-UHFFFAOYSA-N 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- WWHZKHHZRIJLEM-UHFFFAOYSA-N 2-phenylmethoxyguanidine Chemical compound NC(N)=NOCC1=CC=CC=C1 WWHZKHHZRIJLEM-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- IGPFOKFDBICQMC-UHFFFAOYSA-N 3-phenylmethoxyaniline Chemical compound NC1=CC=CC(OCC=2C=CC=CC=2)=C1 IGPFOKFDBICQMC-UHFFFAOYSA-N 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-M 3-phenylpropionate Chemical compound [O-]C(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-M 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 239000005541 ACE inhibitor Substances 0.000 description 1
- 102000004146 ATP citrate synthases Human genes 0.000 description 1
- 108090000662 ATP citrate synthases Proteins 0.000 description 1
- 108091006112 ATPases Proteins 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102000057290 Adenosine Triphosphatases Human genes 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 229940077274 Alpha glucosidase inhibitor Drugs 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 229940123208 Biguanide Drugs 0.000 description 1
- 208000020925 Bipolar disease Diseases 0.000 description 1
- 201000004569 Blindness Diseases 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 208000019838 Blood disease Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- 229940127291 Calcium channel antagonist Drugs 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 229920001268 Cholestyramine Polymers 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 102000005636 Cyclic AMP Response Element-Binding Protein Human genes 0.000 description 1
- 108010045171 Cyclic AMP Response Element-Binding Protein Proteins 0.000 description 1
- 102000008130 Cyclic AMP-Dependent Protein Kinases Human genes 0.000 description 1
- 108010049894 Cyclic AMP-Dependent Protein Kinases Proteins 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 229930105110 Cyclosporin A Natural products 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 241000792859 Enema Species 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- XBGGUPMXALFZOT-VIFPVBQESA-N Gly-Tyr Chemical compound NCC(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 XBGGUPMXALFZOT-VIFPVBQESA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102000019058 Glycogen Synthase Kinase 3 beta Human genes 0.000 description 1
- 108010051975 Glycogen Synthase Kinase 3 beta Proteins 0.000 description 1
- AEMRFAOFKBGASW-UHFFFAOYSA-M Glycolate Chemical compound OCC([O-])=O AEMRFAOFKBGASW-UHFFFAOYSA-M 0.000 description 1
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 1
- 101001050288 Homo sapiens Transcription factor Jun Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229940122355 Insulin sensitizer Drugs 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 102000003996 Interferon-beta Human genes 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 108090000862 Ion Channels Proteins 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 102100040243 Microtubule-associated protein tau Human genes 0.000 description 1
- 101710115937 Microtubule-associated protein tau Proteins 0.000 description 1
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical compound CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 1
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 1
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 102000005877 Peptide Initiation Factors Human genes 0.000 description 1
- 108010044843 Peptide Initiation Factors Proteins 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 102000007327 Protamines Human genes 0.000 description 1
- 108010007568 Protamines Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 102000009096 Proto-Oncogene Proteins c-myb Human genes 0.000 description 1
- 108010087776 Proto-Oncogene Proteins c-myb Proteins 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- FTALBRSUTCGOEG-UHFFFAOYSA-N Riluzole Chemical compound C1=C(OC(F)(F)F)C=C2SC(N)=NC2=C1 FTALBRSUTCGOEG-UHFFFAOYSA-N 0.000 description 1
- 102000014400 SH2 domains Human genes 0.000 description 1
- 108050003452 SH2 domains Proteins 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 229940100389 Sulfonylurea Drugs 0.000 description 1
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 102100023132 Transcription factor Jun Human genes 0.000 description 1
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 1
- 230000007488 abnormal function Effects 0.000 description 1
- 229940124532 absorption promoter Drugs 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 229940009456 adriamycin Drugs 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 239000003888 alpha glucosidase inhibitor Substances 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- DKNWSYNQZKUICI-UHFFFAOYSA-N amantadine Chemical compound C1C(C2)CC3CC2CC1(N)C3 DKNWSYNQZKUICI-UHFFFAOYSA-N 0.000 description 1
- 229960003805 amantadine Drugs 0.000 description 1
- DZHSAHHDTRWUTF-SIQRNXPUSA-N amyloid-beta polypeptide 42 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 DZHSAHHDTRWUTF-SIQRNXPUSA-N 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 230000000719 anti-leukaemic effect Effects 0.000 description 1
- 229940125681 anticonvulsant agent Drugs 0.000 description 1
- 239000001961 anticonvulsive agent Substances 0.000 description 1
- 229940082992 antihypertensives mao inhibitors Drugs 0.000 description 1
- 229940125688 antiparkinson agent Drugs 0.000 description 1
- 239000000939 antiparkinson agent Substances 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 229940039856 aricept Drugs 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229940003504 avonex Drugs 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- 229940097320 beta blocking agent Drugs 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-N beta-phenylpropanoic acid Natural products OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 1
- 150000004283 biguanides Chemical class 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000004979 bone marrow derived macrophage Anatomy 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 229960002802 bromocriptine Drugs 0.000 description 1
- OZVBMTJYIDMWIL-AYFBDAFISA-N bromocriptine Chemical compound C1=CC(C=2[C@H](N(C)C[C@@H](C=2)C(=O)N[C@]2(C(=O)N3[C@H](C(N4CCC[C@H]4[C@]3(O)O2)=O)CC(C)C)C(C)C)C2)=C3C2=C(Br)NC3=C1 OZVBMTJYIDMWIL-AYFBDAFISA-N 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000000480 calcium channel blocker Substances 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 229960004205 carbidopa Drugs 0.000 description 1
- TZFNLOMSOLWIDK-JTQLQIEISA-N carbidopa (anhydrous) Chemical compound NN[C@@](C(O)=O)(C)CC1=CC=C(O)C(O)=C1 TZFNLOMSOLWIDK-JTQLQIEISA-N 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000011712 cell development Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000008727 cellular glucose uptake Effects 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 239000000544 cholinesterase inhibitor Substances 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 230000015271 coagulation Effects 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 125000000392 cycloalkenyl group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 230000009849 deactivation Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 1
- 235000019797 dipotassium phosphate Nutrition 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 229940043264 dodecyl sulfate Drugs 0.000 description 1
- 230000007783 downstream signaling Effects 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 239000013583 drug formulation Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 239000007920 enema Substances 0.000 description 1
- 229940095399 enema Drugs 0.000 description 1
- JRURYQJSLYLRLN-BJMVGYQFSA-N entacapone Chemical compound CCN(CC)C(=O)C(\C#N)=C\C1=CC(O)=C(O)C([N+]([O-])=O)=C1 JRURYQJSLYLRLN-BJMVGYQFSA-N 0.000 description 1
- 229960003337 entacapone Drugs 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 108010074605 gamma-Globulins Proteins 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 229940080856 gleevec Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 230000004153 glucose metabolism Effects 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 229960003878 haloperidol Drugs 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000018706 hematopoietic system disease Diseases 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 125000001183 hydrocarbyl group Chemical group 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 1
- 230000006951 hyperphosphorylation Effects 0.000 description 1
- 230000003463 hyperproliferative effect Effects 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007919 intrasynovial administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 229940042472 mineral oil Drugs 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000002899 monoamine oxidase inhibitor Substances 0.000 description 1
- 229960005127 montelukast Drugs 0.000 description 1
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 1
- 230000004118 muscle contraction Effects 0.000 description 1
- 229960004866 mycophenolate mofetil Drugs 0.000 description 1
- RTGDFNSFWBGLEC-SYZQJQIISA-N mycophenolate mofetil Chemical compound COC1=C(C)C=2COC(=O)C=2C(O)=C1C\C=C(/C)CCC(=O)OCCN1CCOCC1 RTGDFNSFWBGLEC-SYZQJQIISA-N 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 230000016273 neuron death Effects 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 231100000344 non-irritating Toxicity 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 1
- KVWDHTXUZHCGIO-UHFFFAOYSA-N olanzapine Chemical compound C1CN(C)CCN1C1=NC2=CC=CC=C2NC2=C1C=C(C)S2 KVWDHTXUZHCGIO-UHFFFAOYSA-N 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 229960004851 pergolide Drugs 0.000 description 1
- YYPWGCZOLGTTER-MZMPZRCHSA-N pergolide Chemical compound C1=CC=C2[C@H]3C[C@@H](CSC)CN(CCC)[C@@H]3CC3=CN=C1[C]32 YYPWGCZOLGTTER-MZMPZRCHSA-N 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L peroxydisulfate Chemical compound [O-]S(=O)(=O)OOS([O-])(=O)=O JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 208000025712 phagocytic cell dysfunction Diseases 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- LFGREXWGYUGZLY-UHFFFAOYSA-N phosphoryl Chemical group [P]=O LFGREXWGYUGZLY-UHFFFAOYSA-N 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 229950010765 pivalate Drugs 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 1
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940113124 polysorbate 60 Drugs 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 229960003089 pramipexole Drugs 0.000 description 1
- FASDKYOPVNHBLU-ZETCQYMHSA-N pramipexole Chemical compound C1[C@@H](NCCC)CCC2=C1SC(N)=N2 FASDKYOPVNHBLU-ZETCQYMHSA-N 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 229950008679 protamine sulfate Drugs 0.000 description 1
- 230000009822 protein phosphorylation Effects 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- ZTHJULTYCAQOIJ-WXXKFALUSA-N quetiapine fumarate Chemical compound [H+].[H+].[O-]C(=O)\C=C\C([O-])=O.C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12.C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12 ZTHJULTYCAQOIJ-WXXKFALUSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 239000002287 radioligand Substances 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 229940038850 rebif Drugs 0.000 description 1
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 1
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 1
- 229940100618 rectal suppository Drugs 0.000 description 1
- 239000006215 rectal suppository Substances 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000022983 regulation of cell cycle Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 229960004181 riluzole Drugs 0.000 description 1
- 229940106887 risperdal Drugs 0.000 description 1
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 description 1
- 229960002052 salbutamol Drugs 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 230000000698 schizophrenic effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000005204 segregation Methods 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 229940035004 seroquel Drugs 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 229910021653 sulphate ion Inorganic materials 0.000 description 1
- 230000003319 supportive effect Effects 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 229960001967 tacrolimus Drugs 0.000 description 1
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 210000001138 tear Anatomy 0.000 description 1
- 125000004187 tetrahydropyran-2-yl group Chemical group [H]C1([H])OC([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 229940124788 therapeutic inhibitor Drugs 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 230000014621 translational initiation Effects 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 229940039925 zyprexa Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/26—Psychostimulants, e.g. nicotine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/12—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/56—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6561—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Cardiology (AREA)
- Physical Education & Sports Medicine (AREA)
- Pulmonology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Psychology (AREA)
- Biochemistry (AREA)
- Hospice & Palliative Care (AREA)
- Heart & Thoracic Surgery (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Gastroenterology & Hepatology (AREA)
- Transplantation (AREA)
- Dermatology (AREA)
- Rheumatology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
- QUERVERWEIS ZU VERWANDTER ANMELDUNG
- Die vorliegende Anmeldung beansprucht die Priorität der am 1. Juni 2001 eingereichten provisorischen US-Patentanmeldung 60/295,158, deren Inhalt hiermit durch Bezugnahme aufgenommen ist.
- BEREICH DER ERFINDUNG
- Die vorliegende Erfindung betrifft Verbindungen, die Proteinkinaseinhibitoren sind, pharmazeutisch annehmbare Zusammensetzungen, die die Verbindungen beinhalten, sowie Verfahren für deren Verwendung. Insbesondere sind die Verbindungen Inhibitoren von GSK-3, Aurora2 und Syk Proteinkinasen und sind zur Behandlung oder Minderung der Schwere einer Reihe verschiedener Krankheiten und Zuständen von Nutzen, wie Diabetes, die Alzheimer-Krankheit, Schlaganfall, proliferative Störungen und Asthma.
- HINTERGRUND DER ERFINDUNG
- Die Suche nach neuen therapeutischen Wirkstoffen wurde in den vergangenen Jahren durch ein besseres Verständnis der Struktur von Enzymen und anderen Biomolekülen, die mit Zielkrankheiten assoziiert sind, sehr unterstützt. Eine bedeutende Klasse von Enzymen, die Gegenstand umfangreicher Studien ist, sind die Proteinkinasen.
- Proteinkinasen vermitteln die intrazelluläre Signaltransduktion. Sie tun dies, indem sie einen Phosphoryltransfer von einem Nucleosidtriphosphat zu einem Proteinakzeptor bewirken, der in einem Signalweg involviert ist. Es gibt eine Reihe von Kinasen und Wegen, über die extrazelluläre und andere Stimuli eine Vielfalt von zellulären Reaktionen innerhalb der Zelle auslösen. Zu Beispielen für solche Stimuli gehören Umwelt- und chemische Stresssignale (z.B. osmotischer Schock, Hitzeschock, UV-Strahlung, bakterielles Endotoxin, H2O2), Cytokine (z.B. Interleukin-1 (IL-1) und Tumornekrosefaktor α (TNF-α)) und Wachstumsfaktoren (z.B. Granulozytenmakrophagenkolonie-stimulierender Faktor (GM-CSF) und Fibroblastenwachstumsfaktor (FGF). Ein extrazellulärer Stimulus kann eine oder mehrere zelluläre Reaktionen in Bezug auf Zellwachstum, Migration, Differenzierung, Sekretion von Hormonen, Aktivierung von Transkriptionsfaktoren, Muskelkontraktion, Glukosestoffwechsel, Proteinsynthesekontrolle und Zellzyklusregulation bewirken.
- Viele Krankheiten und Zustände sind mit anormalen zellulären Reaktionen assoziiert, die durch Proteinkinase-vermittelte Ereignisse ausgelöst werden. Zu diesen Krankheiten gehören Autoimmunkrankheiten, Entzündungskrankheiten, neurologische und neurodegenerative Krankheiten, Krebs, Herz-Kreislauf-Erkrankungen, Allergien und Asthma, die Alzheimer-Krankheit oder hormonell bedingte Krankheiten. Demzufolge wird in der Arzneimittelchemie ein erheblicher Aufwand betrieben, um Proteinkinaseinhibitoren zu finden, die als therapeutische Wirkstoffe wirksam sind.
- Die
US 5958935 betrifft die Verwendung und Herstellung von substituierten 2-Anilinopyrimidenen als selektive Proteinkinaseinhibitoren. Die pharmazeutischen Zusammensetzungen dieser Verbindungen werden in der Prophylaxe und Behandlung von Immunkrankheiten, Hyperproliferationsstörungen und anderen Krankheiten eingesetzt, bei denen vermutlich eine unangemessene Kinasewirkung involviert ist. - Die WO 00/78731 betrifft die Herstellung und medizinische Verwendung von 5-Cyano-2-aminopyrimidinderivaten. Diese Verbindungen sind potente und selektive Inhibitoren von Rezeptortyrosin-Kinasen, insbesondere KDR-Kinase und/oder FGFr-Kinase, die in der Angiogenese involviert und zur Prophylaxe und Behandlung assoziierter Erkrankungszustände von Nutzen sind.
- Glycogensynthasekinase-3 (GSK-3) ist eine Serin/Threoninproteinkinase, die aus α und β Isoformen besteht, die jeweils durch verschiedene Gene kodiert sind [Coghlan et al., Chemistry & Biology, 7, 793–803 (2000); Kim und Kimmel, Curr. Opinion Genetics Dev., 10, 508–514 (2000)]. GSK-3 wird mit verschiedenen Krankheiten in Verbindung gebracht, wie Diabetes, die Alzheimer-Krankheit, Störungen des Zentralnervensystems, wie manischdepressive Störungen und neurodegenerative Krankheiten, und Kardiomycete-Hypertrophie [WO 99/65897; WO 00/38675; und Haq et al., J. Cell. Biol. (2000) 151, 117]. Diese Krankheiten können durch die anormale Funktion bestimmter Zellsignalwege, in denen GSK-3 eine Rolle spielt, verursacht werden oder in dieser resultieren. Es wurde gefunden, dass GSK-3 die Aktivität einer) Reihe von Regulatorproteinen phosporyliert und moduliert. Hierzu gehören Glycogensynthase, die das geschwindigkeitsbegrenzende Enzym ist, das zur Glycogensynthese notwendig ist, das Mikrotubuli-assoziierte Protein Tau, der Gentranskriptionsfaktor β-Catenin, der Translationsinitiationsfaktor e1F2B, sowie ATP-Citratlyase, Axin, Hitzeschockfaktor-1, c-Jun, c-Myc, c-Myb, CREB und CEPBα. Diese verschiedenen Targets implizieren GSK-3 in vielen Aspekten des Zellstoffwechsels, der Proliferation, Differenzierung und Entwicklung.
- In einem GSK-3-vermittelten Weg, der für die Behandlung von Typ II Diabetes relevant ist, führt eine Insulin-induzierte Signalisierung zur zellulären Glucoseaufnahme und Glycogensynthese. Entlang dieses Wegs ist GSK-3 ein negativer Regulator des Insulin induzierten Signals. Normalerweise verursacht die Anwesenheit von Insulin die Inhibition einer GSK-3-vermittelten Phosphorylierung und Deaktivierung der Glycogensynthase. Die Inhibition von GSK-3 fuhrt zu einer verstärkten Glycogensynthese und Glucoseaufnahme [Klein et al., PNAS, 93, 8455–9 (1996); Cross et al., Biochem. J., 303, 21–26 (1994); Cohen, Biochem. Soc. Trans., 21, 555–567 (1993); Massillon et al., Biochem J. 299, 123–128 (1994)]. Bei einem Diabetiker mit beeinträchtigter Insulinreaktion kommt es jedoch trotz des Vorhandenseins relativ hoher Insulinwerte im Blut zu keiner verstärkten Glycogensynthese und Glucoseaufnahme. Dies fuhrt zu anormal hohen Glucosewerten im Blut, deren akute und langfristige Auswirkungen schließlich zu einer Herz-Kreislauf-Erkrankung, einem Nierenversagen und Erblindung führen können. Bei solchen Patienten kommt es nicht zur normalen Insulin-induzierten Inhibition von GSK-3. Es wurde außerdem berichtet, dass bei Patienten mit Typ II Diabetes, GSK-3 überexprimiert ist [WO 00/38675]. Therapeutische Inhibitoren von GSK-3 sind daher zur Behandlung von Diabetikern, die an einer beeinträchtigten Reaktion auf Insulin leiden, möglicherweise nützlich.
- GSK-3 Aktivität wird auch mit der Alzheimer-Krankheit in Verbindung gebracht. Diese Krankheit ist durch das allgemein bekannte β-Amyloidpeptid und die Bildung von intrazellulären Alzheimer-Fibrillen (neurofibrillary tangle) gekennzeichnet. Die Alzheimer-Fibrillen enthalten hyperphosphoryliertes Tau-Protein, wobei Tau an anormalen Stellen phosphoryliert ist. Es wurde gezeigt, dass GSK-3 diese anormalen Stellen in Zell- und Tiermodellen phosphoryliert. Ferner wurde gezeigt, dass durch die Inhibition von GSK-3 die Hyperphosphorylierung von Tau in Zellen verhindert wird [Lovestone et al., Current Biology 4, 1077–86 (1994); Brownlees et al., Neuroreport 8, 3251–55 (1997)]. Man geht daher davon aus, dass GSK-3 Aktivität die Erzeugung der Alzheimer-Fibrillen und das Voranschreiten der Alzheimer-Krankheit unterstützen kann.
- Ein weiteres Substrat von GSK-3 ist β-Catenin, das nach der Phosphorylierung durch GSK-3 abgebaut wird. In Verbindung mit schizophrenen Patienten wurde über reduzierte (β-Catenin-Werte berichtet, die auch mit anderen Krankheiten assoziiert werden, die mit einer Zunahme des Neuronentods zusammenhängen [Zhong et al., Nature, 395, 698–702 (1998); Takashima et al., PNAS, 90, 7789–93 (1993); Pei et al., J. Neuropathol. Exp, 56, 70–78 (1997)].
- Aurora-2 ist eine Serin/Threoninproteinkinase, die mit humanem Krebs in Verbindung gebracht wird, wie Kolon-, Brust- und anderen festen Tumoren. Diese Kinase ist in Proteinphosphorylierungsereignissen involviert, die den Zellzyklus regulieren. Im Speziellen spielt Aurora-2 eine Rolle bei der Steuerung der akkuraten Segregation von Chromosomen im Laufe der Mitose. Eine Fehlregulation des Zellzyklus kann zu Zellproliferation und anderen Anomalien führen. Es wurde gefunden, dass das Aurora-2 Protein in humanem Kolonkrebsgewebe überexprimiert ist [Bischoff et al., EMBO J., 17, 3052–3065 (1998); Schumacher et al., J. Cell Biol., 143, 1635–1646 (1998); Kimura et al., J. Biol. Chem., 272, 13766–13771 (1997)].
- Syk ist eine Tyrosinkinase, die eine entscheidende Rolle bei der FcεRI-vermittelten Mastzellen-Degranulation und der Eosinophilen-Aktivierung spielt. Demzufolge wird Syk Kinase mit verschiedenen allergischen Störungen in Verbindung gebracht, insbesondere mit Asthma.
- Es hat sich gezeigt, dass Syk an die phosphorylierte Gammakette des FcεRI-Rezeptors über N-terminale SH2-Domänen bindet und für die stromabwärtige Signalisierung wesentlich ist [Taylor et al, Mol Cell Biol 1995; 15:4149].
- Es wird angenommen, dass die Inhibierung der Eosinophilen-Apoptose der Hauptmechanismus für die Entwicklung von Blut- und Gewebe-Eosinophilie bei Asthma ist. IL-5 und GM-CSF werden bei Asthma hinaufreguliert und verursachen wohl Blut- und Gewebe-Eosinophilie durch die Inhibierung von Eosinophilen-Apoptose. Es wird angenommen, dass die Inhibierung der Eosinophilen-Apoptose der Hauptmechanismus für die Entwicklung von Blut- und Gewebe-Eosinophilie bei Asthma ist. Es wurde berichtet, dass Syk Kinase zur Verhinderung von Eosinophilen-Apoptose durch Cytokine (unter Verwendung von Antisense) erforderlich ist [Yousefi et al, J Exp Med 1996; 183:1407].
- Die Rolle von Syk bei der FcγR-abhängigen und unabhängigen Reaktion in von Knochenmark stammenden Makrophagen wurde unter Verwendung bestrahlter Mauschimären bestimmt, die mit fötalen Leberzellen von Syk -/- Embryos rekonstituiert wurden. Syk-defiziente Makrophagen wiesen eine durch FcγR induzierte fehlerhafte Phagozytose, aber eine normale Phagozytose als Reaktion auf das Komplement auf [Kiefer et al, Mol Cell Biol 1998; 18:4209]. Es wurde außerdem berichtet, dass aerosoliertes Syk-Antisense Syk-Expression und Mediatorfreisetzung von Makrophagen unterdrückt [Stenton et al, J Immunology 2000; 164: 3790].
- In Anbetracht des Mangels an derzeit verfügbaren Behandlungsmöglichkeiten für die Mehrzahl der mit Proteinkinasen, insbesondere GSK-3, Aurora-2 und Syk, verbundenen Krankheiten gibt es noch immer einen großen Bedarf an neuen therapeutischen Wirkstoffen, die diese Proteintargets inhibieren.
- ZUSAMMENFASSUNG DER ERFINDUNG
-
- Die vorliegende Erfindung stellt außerdem eine pharmazeutisch annehmbare Zusammensetzung bereit, die eine Verbindung der Formel I beinhaltet.
- Die Verbindungen und pharmazeutisch annehmbaren Zusammensetzungen der vorliegenden Erfindung sind als Inhibitoren von GSK-3, Aurora-2 und Syk Proteinkinasen von Nutzen. Folglich sind sie auch in Verfahren zur Behandlung oder Minderung der Schwere einer Auswahl von Störungen, wie allergische Krankheiten, proliferativen Störungen, Krebs, neurodegenerative Störungen und Diabetes, von Nutzen.
- BESCHREIBUNG DER ERFINDUNG
- Die vorliegende Erfindung betrifft eine Verbindung der Formel I: oder ein pharmazeutisch annehmbares Derivat davon, wobei:
R1 aus R, Halogen, CN, NO2 oder TR ausgewählt ist;
T eine gegebenenfalls substituierte C1-C4 Alkylidenkette ist, wobei bis zu zwei Methyleneinheiten von T gegebenenfalls und unabhängig durch O, N(R), C(O), S, SO oder SO2 ersetzt sind;
jedes R unabhängig aus Wasserstoff oder einer gegebenenfalls substituierten C1-6 aliphatischen Gruppe ausgewählt ist, wobei:
zwei an dasselbe Stickstoffatom gebundene R gegebenenfalls mit dem Stickstoff zusammengefasst werden, um einen 3–7 gliedrigen, gesättigten, teilweise ungesättigten oder völlig ungesättigten Ring mit 0–2 Heteroatomen zusätzlich zum darin gebundenen Stickstoff zu bilden, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind;
Ar1 ein gegebenenfalls substituierter Ring ist, der ausgewählt ist aus: - (a) einem 3–8 gliedrigen, monozyklischen oder 8–10 gliedrigen, bizyklischen, gesättigten, teilweise ungesättigten oder Aryl-Ring;
- (b) einem 3–7 gliedrigen, heterozyklischen Ring mit 1–3 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; oder
- (c) einem 5–6 gliedrigen, monozyklischen oder 8–10 gliedrigen, bizyklischen Heteroaryl-Ring mit 1–4 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind, wobei:
- (a) einer Gruppe, die aus QR, Ar2 oder QAr2 ausgewählt ist; und
- (b) bis zu vier R2 Gruppen;
- (a) einem 3–8 gliedrigen, monozyklischen oder 8–10 gliedrigen, bizyklischen, gesättigten, teilweise ungesättigten oder Aryl-Ring;
- (b) einem 3–7 gliedrigen, heterozyklischen Ring mit 1–3 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; oder
- (c) einem 5–6 gliedrigen, monozyklischen oder 8–10 gliedrigen, bizyklischen Heteroaryl-Ring mit 1–4 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind, wobei:
- Es treffen die hierin benutzten folgenden Definitionen zu, sofern nicht anders angegeben.
- Der Ausdruck „gegebenenfalls substituiert" und der Ausdruck „substituiert oder nicht substituiert" sind untereinander austauschbar. Sofern nicht anders angegeben, kann eine gegebenenfalls substituierte Gruppe einen Substituenten an jeder substituierbaren Position der Gruppe haben und jede Substitution ist von der anderen unabhängig.
- Der hierin benutzte Begriff „aliphatisch" oder „aliphatische Gruppe" bedeutet eine geradkettige oder verzweigte C1-C8 Kohlenwasserstoffkette, die völlig gesättigt ist oder die eine oder mehrere Ungesättigtheitseinheiten enthält, oder einen monozyklischen C3-C8 Kohlenwasserstoff oder bizyklischen C8-C12 Kohlenwasserstoff, der völlig gesättigt ist oder der eine oder mehrere Ungesättigtheitseinheiten enthält, der jedoch nicht aromatisch ist (hierin auch als „Carbozyklus" oder „Cycloalkyl" bezeichnet), der eine einzelne Verknüpfungsstelle zum Rest des Moleküls hat, wobei jeder individuelle Ring in dem bizyklischen Ringsystem 3–7 Glieder hat. Zu geeigneten aliphatischen Gruppen gehören zum Beispiel unter anderem lineare oder verzweigte oder Alkyl-, Alkenyl-, Alkynylgruppen und Hybride davon wie (Cycloalkyl)alkyl, (Cycloalkenyl)alkyl oder (Cycloalkyl)alkenyl.
- Die Begriffe „Alkyl", „Alkoxy", „Hydroxyalkyl", „Alkoxyalkyl" und „Alkoxycarbonyl", die alleine oder als Teil eines größeren Anteils benutzt werden, schließen sowohl gerade als auch verzweigte Ketten ein, die ein bis zwölf Kohlenstoffatome enthalten. Die Begriffe „Alkenyl" und „Alkynyl", die alleine oder als ein Teil eines größeren Anteils benutzt werden, schließen sowohl gerade als auch verzweigte Ketten ein, die zwei bis zwölf Kohlenstoffatome enthalten.
- Der Begriff „Heteroatom" bedeutet Stickstoff, Sauerstoff oder Schwefel und beinhaltet jede beliebige oxydierte Form von Stickstoff und Schwefel und die quaternisierte Form jedes beliebigen basischen Stickstoffs. Außerdem schließt der Begriff „Stickstoff" einen substituierbaren Stickstoff eines heterozyklischen Rings ein. In einem gesättigten oder teilweise ungesättigten Ring mit 0–3 Heteroatomen, die aus Sauerstoff, Schwefel oder Stickstoff ausgewählt sind, kann der Stickstoff zum Beispiel N (wie in 3,4-Dihydro-2H-pyrrolyl), NH (wie in Pyrrolidinyl) oder NR+ (wie in N-substituiertem Pyrrolidinyl) sein.
- Der Begriff „Aryl", der alleine oder als Teil eines größeren Anteils benutzt wird, wie in „Aralkyl", Aralkoxy" oder „Aryloxyalkyl", betrifft monozyklische, bizyklische und trizyklische Ringsysteme mit insgesamt fünf bis vierzehn Ringgliedern, wobei wenigstens ein Ring in dem System aromatisch ist und wobei jeder Ring in dem System 3 bis 7 Ringglieder enthält. Der Begriff „Aryl" und der Begriff „Arylring" sind untereinander austauschbar. Der Begriff „Aryl" bezieht sich außerdem auf die im Folgenden definierten Heteroarylringsysteme.
- Der hierin verwendete Begriff „Heterozyklus", „Heterocyclyl" oder „heterozyklisch" steht für nicht aromatische, monozyklische, bizyklische oder trizyklische Ringsysteme mit fünf bis vierzehn Ringgliedern, bei denen ein oder mehrere Ringglieder ein Heteroatom ist/sind, wobei jeder Ring in dem System 3 bis 7 Ringglieder enthält.
- Der Begriff „Heteroaryl", der alleine oder als ein Teil eines größeren Anteils benutzt wird, wie in „Heteroaralkyl" oder „Heteroarylalkoxy", bezieht sich auf monozyklische, bizyklische und trizyklische Ringsysteme mit insgesamt fünf bis vierzehn Ringgliedern, wobei wenigstens ein Ring in dem System aromatisch ist, wenigstens ein Ring in dem System ein oder mehrere Heteroatome enthält, und wobei jeder Ring in dem System 3 bis 7 Ringglieder enthält. Der Begriff „Heteroaryl" und der Begriff „Heteroarylring" oder der Begriff „heteroaromatisch" sind untereinander austauschbar.
- Eine Aryl-(einschließlich Aralkyl, Aralkoxy, Aryloxyalkyl und dergleichen) oder Heteroaryl-(einschließlich Heteroaralkyl und Heteroarylalkoxy und dergleichen)-Gruppe kann einen oder mehrere Substituenten enthalten. Geeignete Substituenten auf dem ungesättigten Kohlenstoffatom einer Aryl-, Heteroaryl-, Aralkyl- oder Heteroaralkylgruppe sind ausgewählt aus Halogen, -Ro, -ORo, -SRo, 1,2-Methylendioxy, 1,2-Ethylendioxy, Phenyl (Ph), gegebenenfalls substituiert durch Ro, -O(Ph), gegebenenfalls substituiert durch Ro, -CH2(Ph), gegebenenfalls substituiert durch Ro, -CH2CH2(Ph), gegebenenfalls substituiert durch Ro, -NO2, -CN, -N(Ro)2, -NRoC(O)Ro, -NRoC(O)N(Ro)2, -NRoCO2Ro, -NRoNRoC(O)Ro, -NRoNRoC(O)N(Ro)2, -NRoNRoCO2Ro, -C(O)C(O)Ro, -C(O)CH2C(O)Ro, -CO2Ro, -C(O)Ro, -C(O)N(Ro)2, -OC(O)N(Ro)2, -S(O)2Ro, -SO2N(Ro)2, -S(O)Ro, -NRoSO2N(Ro)2, -NRoSO2Ro, -C(=S)N(Ro)2, -C(=NH)-N(Ro)2 oder -(CH2)yNHC(O)Ro, wobei jedes Ro unabhängig aus Wasserstoff, gegebenenfalls substituiertem C1-6 Aliphat, einem nicht substituierten 5–6 gliedrigen Heteroaryl- oder heterozyklischen Ring, Phenyl, -O(Ph) oder -CH2(Ph) ausgewählt ist. Fakultative Substituenten auf der aliphatischen Gruppe von Ro sind aus NH2, NH(C1-4 Aliphat), N(C1-4 Aliphat)2, Halogen, C1-4 Aliphat, OH, O(C1-4 Aliphat), NO2, CN, CO2H, CO2(C1-4 Aliphat), O(Halo C1-4 Aliphat) oder Halo-C1-4-Aliphat ausgewählt.
- Eine aliphatische Gruppe oder ein nicht aromatischer heterozyklischer Ring kann einen oder mehrere Substituenten enthalten. Geeignete Substituenten auf dem gesättigten Kohlenstoff einer aliphatischen Gruppe oder eines nicht aromatischen heterozyklischen Rings sind aus den oben für den ungesättigten Kohlenstoff einer Aryl- oder Heteroarylgruppe aufgeführten und den Folgenden ausgewählt: =O, =S, =NNHR*, =NN(R*)2, =NNHC(O)R*, =NNHCO2(Alkyl), =NNHSO2(Alkyl) oder =NR*, wobei jedes R* unabhängig aus Wasserstoff oder einer gegebenenfalls substituierten C1-6 aliphatischen Gruppe ausgewählt ist. Fakultative Substituenten auf der aliphatischen Gruppe von R* sind aus NH2, NH(C1-4 Aliphat), N(C1-4 Aliphat)2, Halogen, C1-4 Aliphat, OH, O(C1-4 Aliphat), NO2, CN, CO2H, CO2(C1-4 Aliphat), O(Halo C1-4 Aliphat) oder Halo(C1-4 Aliphat) ausgewählt.
- Fakultative Substituenten auf dem Stickstoff eines nicht aromatischen heterozyklischen Rings sind ausgewählt aus
-R+, -N(R+)2, -C(O)R+, -CO2R+, -C(O)C(O)R+, -C(O)CH2C(O)R+, -SO2R+, -SO2N(R+)2, -C(=S)N(R+)2, -C(=NH)-N(R+)2 oder NR+SO2R+;
wobei R+ Wasserstoff, eine gegebenenfalls substituierte C1-6 aliphatische Gruppe, gegebenenfalls substituiertes Phenyl, gegebenenfalls substituiertes -O(Ph), gegebenenfalls substituiertes -CH2(Ph), gegebenenfalls substituiertes -CH2CH2(Ph) oder ein nicht substituierter 5–6 gliedriger Heteroaryl- oder heterozyklischer Ring ist. Fakultative Substituenten auf der aliphatischen Gruppe oder dem Phenylring von R+ sind ausgewählt aus NH2, NH(C1-4 Aliphat), N(C1-4 Aliphat)2, Halogen, C1-4 Aliphat, OH, O(C1-4 Aliphat), NO2, CN, CO2H, CO2(C1-4 Aliphat), O(Halo C1-4 Aliphat) oder Halo(C1-4 alphatisch). - Der Begriff „Alkylidenkette" betrifft eine gerade oder verzweigte Kohlenstoffkette, die völlig gesättigt sein kann oder eine oder mehrere Ungesättigtheitseinheiten haben kann und die zwei Verknüpfungsstellen zum Rest des Moleküls hat.
- Eine Kombination von Substituenten oder Variablen ist nur dann zulässig, wenn eine solche Kombination in einer stabilen oder chemisch realisierbaren Verbindung resultiert. Eine stabile oder chemisch realisierbare Verbindung ist eine Verbindung, die nicht wesentlich verändert wird, wenn sie mindestens eine Woche lang bei einer Temperatur von 4O°C oder weniger ohne Feuchtigkeit oder andere chemisch reaktive Bedingungen gehalten wird.
- Dem Fachmann wird es verständlich sein, dass bestimmte Verbindungen der vorliegenden Erfindung in tautomeren Formen vorliegen können, wobei alle diese tautomeren Formen der Verbindungen innerhalb des Umfangs der Erfindung liegen.
- Sofern nicht anders angegeben, sind die hierin dargestellten Strukturen auch so zu verstehen, dass sie alle stereochemischen Formen der Struktur beinhalten; d.h. die R- und S-Konfigurationen für jedes Asymmetriezentrum. Folglich liegen einzelne stereochemische Isomere sowie enantiomere und diastereomere Gemische der vorliegenden Verbindungen innerhalb des Umfangs der Erfindung. Sofern nicht anders angegeben, sind die hierin dargestellten Strukturen auch so zu verstehen, dass sie Verbindungen beinhalten, die sich nur in der Anwesenheit von einem oder mehreren isotopisch angereicherten Atom(en) unterscheiden. Zum Beispiel liegen Verbindungen, die die vorliegenden Strukturen, mit Ausnahme des Ersatzes eines Wasserstoffs durch ein Deuterium oder Tritium oder des Ersatzes eines Kohlenstoffs durch einen 13C- oder 14C-angereicherten Kohlenstoff, aufweisen, innerhalb des Umfangs der Erfindung. Solche Verbindungen sind zum Beispiel als analytische Werkzeuge oder Sonden in biologischen Assays von Nutzen.
- Gemäß einer Ausgestaltung betrifft die vorliegende Erfindung eine Verbindung der Formel I: oder ein pharmazeutisch annehmbares Derivat davon, wobei R1 und Ar1 der obigen Definition entsprechen, unter der Bedingung, dass, wenn Ar1 Phenyl mit zwei R2 Substituenten ist, die beiden R2 nicht gleichzeitig OR in der meta- und para-Stellung von Ar1 sind.
-
- Bevorzugte Ar1 Gruppen der Formel I sind gegebenenfalls substituierte Ringe, die ausgewählt sind aus:
- (a) einem Phenyl-, Indanyl- oder Naphthylring;
- (b) einem 5–6 gliedrigen, heterozyklischen Ring mit 1–3 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; oder
- (c) einem 5–6 gliedrigen, monozyklischen oder 9–10 gliedrigen, bizyklischen Heteroarylring mit 1–2 Heteroatomen, die unabhängig aus Sauerstoff, Stickstoff oder Schwefel ausgewählt sind.
- Mehr bevorzugte Ar1 Gruppen der Formel I sind Ringe, die ausgewählt sind aus:
- (a) einem Phenyl-, Indanyl- oder Naphthylring;
- (b) einem 5–6 gliedrigen, heterozyklischen Ring mit 1–3 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; oder
- (c) einem 5–6 gliedrigen, monozyklischen Heteroarylring mit 1–2 Stickstoffatomen, wobei:
- (a) einer Gruppe, die aus QR, Ar2 oder QAr2 ausgewählt ist; und
- (b) bis zur vier R2 Gruppen.
- Die am meisten bevorzugten Ar1 Ringe sind aus substituiertem Phenyl, Indanyl, Naphthyl, Pyrimidinyl oder Pyridyl ausgewählt. Bevorzugte R2 Substituenten auf Ar1 sind Halogen, CN, CO2R, R, NO2, OR, Haloalkyl, SO2N(R)2 oder N(R)2. Mehr bevorzugte R2 Substituenten auf Ar1 sind Fluor, Iod, Chlor, Brom, CO2CH3, Methyl, Ethyl, t-Butyl, NH2, NHMe, N(Me)2, OH, OCH3, OCH2CH3, CF3, SO2NH2 oder SO2NHMe. Andere bevorzugte Verbindungen schließen solche ein, bei denen zwei R2 zusammengefasst werden, um einen Methylendioxy- oder einen Ethylendioxysubstituenten zu bilden.
- Bevorzugte QR oder QAr2 Substituenten auf Ar1 der Formel I sind solche, bei denen Q eine C1- 4 Alkylidenkette ist, wobei eine oder zwei Methyleneinheiten von Q gegebenenfalls durch O, NR, NRCO, NRCO2, NRSO2 oder CONR ersetzt sind, wobei jedes R Wasserstoff oder eine gegebenenfalls substituierte C1-4 aliphatische Gruppe ist und wobei Ar2 ein 3–6 gliedriger, carbozyklischer Ring oder ein gegebenenfalls substituierter Phenyl-, 5–6 gliedriger, heterozyklischer oder Heteroarylring mit einem bis zwei Heteroatomen ist, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind.
- Die Ar2 Gruppe des QAr2-Restes der Formel I ist gegebenenfalls durch R, OR, N(R)2, SO2R, Halogen, NO2, CN, SR, SO2N(R)2, CO2R, C(O)R oder Oxo substituiert. Mehr bevorzugte QAr2-Gruppen der Formel I sind ausgewählt aus O(CH2)3pyrrolidin-1-yl, O(CH2)2morpholin-4-yl, O(CH2)3(4-hydroxyethylpiperazin-1-yl), O(CH2)3piperazin-1-yl, O(CH2)3(4-hydroxymethylpiperidin-1-yl), O(CH2)3(4-hydroxypiperidin-1-yl), NHCOCH2pyridin-2-yl, NHCOCH2(2-aminothiazol-4-yl), NHCOCH2cyclopropyl, NHCO(CH2)2(piperazin-2,5-dion-3-yl), NHCOpyrrolidin-1-yl, NHCOmorpholin-4-yl, NHCO2CH2tetrahydrofuran-2-yl, NHCO2tetrahydrofuran-2-yl, NHCO2tetrahydropyran-4-yl, NHCO2CH2tetrahydropyran-2-yl, Ophenyl, OCH2(cyclohexyl), OCH2phenyl, OCH2(3-CN-phenyl), OCH2(2-NO2-phenyl), OCH2(3-NH2-phenyl), OCH2(4-CO2R-phenyl), OCH2-pyridyl, OCH2(mono-, di- oder tri-halogeniertes Phenyl), OCH2(C1-C6 aliphatisches, substituiertes Phenyl), OCH2CH2-Pyrrolyl, OCH2-Pyrrolyl und OCH2(Phenyl, substituiert durch ein oder zwei R2).
- Bevorzugte Ar2-Substituenten auf Ar1 der Formel I sind gegebenenfalls substituierte Ringe, die ausgewählt sind aus:
- (a) einem Phenyl-, Indanyl- oder Naphthylring;
- (b) einem 5–6 gliedrigen, heterozyklischen Ring mit 1–3 Heteroatomen, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; oder
- (c) einem 5–6 gliedrigen, monozyklischen oder 9–10 gliedrigen, bizyklischen Heteroarylring mit 1–2 Heteroatomen, die unabhängig aus Sauerstoff, Stickstoff oder Schwefel ausgewählt sind, wobei:
- Mehr bevorzugte Ar2-Substituenten auf Ar1 der Formel I sind gegebenenfalls substituierte Ringe, die aus Phenyl, Pyridyl, Indolyl, Naphthyl oder Benzo[1,3]dioxolyl ausgewählt sind.
- Bevorzugte R2 Gruppen, sofern vorhanden, auf dem Ar2-Substituenten auf Ar1 der Formel I sind aus R, Halogen, NO2, CN, OR, SR, N(R)2, C(O)R, SO2N(R)2 oder SO2R ausgewählt. Mehr bevorzugte R2-Gruppen, sofern vorhanden, auf dem Ar2 Substituenten auf Ar1 der Formel I sind aus Methyl, Ethyl, t-Butyl, Fluor, Chlor, Brom, CF3, OMe, OEt, CN, SO2Me, SO2NH2, NH2, NHMe, N(Me)2, SMe, SEt, OH, C(O)Me, NO2 oder CH2OH ausgewählt.
-
- Bevorzugte Ar1-Gruppen der Formel Ia sind die oben für die Formel I beschriebenen.
-
- Bevorzugte R2-Gruppen der Formel II sind die oben für die Formel I beschriebenen und beinhalten solche, bei denen zwei R2 zusammengefasst werden, um einen Methylendioxy- oder Ethylendioxy-Substituenten zu bilden.
-
- Bevorzugte R2-Gruppen der Formel IIa oder IIA' sind die oben für die Verbindungen der Formel I beschriebenen.
- Bevorzugte QR- und QAr2-Gruppen der Formel IIa oder IIa' sind die oben für die Verbindungen der Formel I beschriebenen.
-
- Bevorzugte R2 und QAr2 Gruppen der Formel III sind die oben für die Formel I beschriebenen.
- Bevorzugte R1-Gruppen der Formel III sind aus Wasserstoff, N(R)2, SR, OR oder TR ausgewählt. Mehr bevorzugte R1-Gruppen sind aus OH, OCH3, CH2OH, CH2OCH3, CH2NH2 oder CH2NHCH3 ausgewählt.
-
- Bevorzugte R2 und Ar2 Gruppen der Formel IV sind die oben für die Verbindungen der Formel I beschriebenen.
- Beispielhafte Strukturen der Formel I sind in der folgenden Tabelle 1 enthalten.
- Beispielhafte Strukturen der Formeln IIa und IIa' sind in der folgenden Tabelle 2 enthalten.
-
- Reagenzien und Bedingungen: (a) DMF-DMA, THF, 12–18 Stunden, Raumtemperatur; (b) H2NCN, 4N HCl in Dioxan, 12–18 Stunden, 120°C; (c) Ethanol, Rückfluss, 12–18 Stunden.
- Das obige Schema I stellt einen allgemeinen Syntheseweg dar, der zur Herstellung von Verbindungen der Formel I verwendet werden kann.
- Im Schritt (a) wird eine Lösung aus 2-Acetylthiazol (1) in THF mit Dimethylformamid-Dimethylacetal behandelt und das resultierende Gemisch wird über Nacht bei Raumtemperatur gerührt. Das Reaktionsgemisch wird in vacuo konzentriert und das Konzentrat mit Diethylether verrieben, um 2 zu erhalten.
- Zur Herstellung des Intermediats 4 von Anilin 3 in Schritt (b) wird ein Gemisch aus 3 und Cyanamid in HCl (4N in Dioxan) über Nacht auf 120°C erhitzt. Nach dem Abkühlen auf Raumtemperatur wird durch eine wässrige Aufarbeitung die gewünschte Guanidinverbindung 4 erhalten. Der Fachmann wird erkennen, dass eine große Auswahl von Arylguanidinen im Schritt (b) hergestellt und somit zur Herstellung von Verbindungen der Formel I mit einer großen Vielfalt von Ar1 Ringen verwendet werden kann.
- In Schritt (c) wird Guanidin 4 mit Enaminon 2 in Ethanol in einem versiegelten Röhrchen kombiniert. Das resultierende Gemisch wird über Nacht auf Rückfluss erhitzt, anschließend konzentriert, und das Rohprodukt wird durch Säulenchromatographie gereinigt, um die gewünschte Pyrimidinverbindung 5 zu erhalten. Die Details der zur Herstellung dieser Verbindungen verwendeten Bedingungen sind in den Beispielen dargelegt.
- Die Aktivität einer Verbindung, die in der vorliegenden Erfindung als Inhibitor von GSK3, Aurora2 oder Syk Proteinkinase verwendet wird, kann in vitro, in vivo oder in einer Zelllinie gemäß Verfahren, die in der Technik bekannt sind, und den in den folgenden Beispielen beschriebenen Verfahren untersucht werden. In-vitro-Untersuchungen schließen Untersuchungen ein, die die Inhibition der Phosphorylierungsaktivität oder ATPase-Aktivität von aktivierter GSK3, Aurora2 oder Syk Proteinkinase bestimmen. Alternative In-vitro-Untersuchungen bestimmen quantitativ die Fähigkeit des Inhibitors, sich an GSK3, Aurora2 oder Syk Proteinkinase zu binden. Die Inhibitorbindung kann durch radioaktive Markierung des Inhibitors vor der Bindung, Isolierung des Inhibitor/GSK3-, Inhibitor/Aurora2- oder Inhibitor/Syk-Komplexes und Bestimmen der Menge der gebundenen radioaktiven Markierung gemessen werden. Alternativ kann die Inhibitorbindung mit einem Kompetitionsexperiment bestimmt werden, bei dem neue Inhibitoren mit GSK3, Aurora2 oder Syk Proteinkinase, gebunden an bekannte Radioliganden, inkubiert werden. Detaillierte Bedingungen für die Untersuchung einer Verbindung, die in der vorliegenden Erfindung als Inhibitor von GSK3, Aurora2 oder Syk Proteinkinase verwendet wird, sind in den folgenden Beispielen dargelegt.
- Gemäß einer weiteren Ausgestaltung stellt die vorliegende Erfindung eine Zusammensetzung oder eine pharmazeutisch annehmbare Zusammensetzung bereit, die eine erfindungsgemäße Verbindung oder ein pharmazeutisch annehmbares Derivat davon und einen pharmazeutisch annehmbaren Träger, Hilfsstoff oder ein solches Vehikel beinhaltet. Die Menge der Verbindung in den erfindungsgemäßen Zusammensetzungen ist derart, dass sie nachweislich eine Proteinkinase, insbesondere GSK3, Aurora2 oder Syk Proteinkinase, in einer biologischen Probe oder in einem Patienten inhibiert. Vorzugsweise wird die erfindungsgemäße Zusammensetzung zur Verabreichung an einen Patienten formuliert, der eine solche Zusammensetzung benötigt. Am meisten bevorzugt wird die erfindungsgemäße Zusammensetzung zur oralen Verabreichung an einen Patienten formuliert.
- Der hierin verwendete Begriff „Patient" bedeutet ein Tier, vorzugsweise ein Säugetier, und am meisten bevorzugt einen Menschen.
- Der Ausdruck „pharmazeutisch annehmbarer Träger, Hilfsstoff oder ein solches Vehikel" bezieht sich auf einen nicht toxischen Träger, Hilfsstoff oder ein solches Vehikel, der/das die pharmakologische Aktivität der Verbindung, mit der er/sie formuliert wird, nicht zerstört. Zu pharmazeutisch annehmbaren Trägern, Hilfsstoffen oder Vehikeln, die in den erfindungsgemäßen Zusammensetzungen verwendet werden können, gehören unter anderem Ionenaustauscher, Aluminiumoxid, Aluminiumstearat, Lecithin, Serumproteine wie Humanserumalbumin, Puffersubstanzen wie Phosphate, Glycin, Sorbinsäure, Kaliumsorbat, partielle Glyceridgemische von gesättigten pflanzlichen Fettsäuren, Wasser, Salze oder Elektrolyte, wie Protaminsulfat, Dinatriumhydrogenphosphat, Kaliumhydrogenphosphat, Natriumchlorid, Zinksalze, Kolloidsilika, Magnesiumtrisilikat, Polyvinylpyrrolidon, Substanzen auf Cellulosebasis, Polyethylenglykol, Natriumcarboxymethylcellulose, Polyacrylate, Wachse, Polyethylen-Polyoxypropylen-Blockpolymere, Polyethylenglykol und Wollfett.
- Der hierin verwendete Ausdruck „nachweislich inhibieren" bedeutet eine messbare Veränderung der GSK3, Aurora2 oder Syk Proteinkinaseaktivität zwischen einer Probe, die die Zusammensetzung und eine GSK3, Aurora2 oder Syk Proteinkinase beinhaltet, und einer äquivalenten Probe, die GSK3, Aurora2 oder Syk Proteinkinase ohne die Zusammensetzung aufweist.
- Ein „pharmazeutisch annehmbares Derivat" bedeutet ein beliebiges nicht toxisches Salz, einen Ester, ein Salz eines Esters oder ein anderes Derivat einer Verbindung der vorliegenden Erfindung, das nach der Verabreichung an einen Empfänger entweder direkt oder indirekt eine erfindungsgemäße Verbindung oder einen inhibitorisch aktiven Metabolit oder Rest davon bereitstellen kann. Der hierin verwendete Ausdruck „inhibitorisch aktiver Metabolit oder Rest davon" bedeutet, dass ein Metabolit oder Rest davon ebenfalls ein Inhibitor einer GSK3, Aurora2 oder Syk Proteinkinase ist.
- Pharmazeutisch annehmbare Salze der erfindungsgemäßen Verbindungen schließen die von pharmazeutisch annehmbaren anorganischen und organischen Säuren und Basen gewonnenen ein. Beispiele für geeignete saure Salze sind Acetat, Adipat, Alginat, Aspartat, Benzoat, Benzolsulfonat, Bisulfat, Butyrat, Citrat, Camphorat, Camphorsulfonat, Cyclopentanpropionat, Digluconat, Dodecylsulfat, Ethansulfonat, Format, Fumarat, Glucoheptanoat, Glycerophosphat, Glycolat, Hemisulfat, Heptanoat, Hexanoat, Hydrochlorid, Hydrobromid, Hydroiodid, 2-Hydroxyethansulfonat, Lactat, Maleat, Malonat, Methansulfonat, 2-Naphthalensulfonat, Nicotinat, Nitrat, Oxalat, Palmoat, Pectinat, Persulfat, 3-Phenylpropionat, Phosphat, Picrat, Pivalat, Propionat, Salicylat, Succinat, Sulfat, Tartrat, Thiocyanat, Tosylat und Undecanoat. Andere Säuren wie Oxalsäure, die zwar selbst nicht pharmazeutisch akzeptabel sind, können jedoch zur Herstellung von Salzen verwendet werden, die als Intermediate zur Gewinnung der erfindungsgemäßen Verbindungen und ihrer pharmazeutisch annehmbaren Säureadditionsalze von Nutzen sind.
- Zu Salzen, die von geeigneten Basen gewonnen werden, gehören Alkalimetall (z.B. Natrium und Kalium), Erdalkalimetall (z.B. Magnesium), Ammonium und N+(C1-4 alkyl)4 Salze. Die vorliegende Erfindung sieht außerdem die Quaternisierung beliebiger Gruppen, die basischen Stickstoff enthalten, der hierin offenbarten Verbindungen vor. Wasser- oder öllösliche oder -dispergierbare Produkte können durch eine solche Quaternisierung erhalten werden.
- Die erfindungsgemäßen Zusammensetzungen können oral, parenteral, per Inhalationsspray, topisch, rektal, nasal, bukkal, vaginal oder über ein implantiertes Reservoir verabreicht werden. Der hierin verwendete Begriff „parenteral" schließt subkutane, intravenöse, intramuskuläre, intraartikuläre, intrasynoviale, intrasternale, intrathekale, intrahepatische, intraläsionale und intrakraniale Injektions- oder Infusionstechniken ein. Vorzugsweise werden die Zusammensetzungen oral, intraperitoneal oder intravenös verabreicht. Sterile injizierbare Formen der erfindungsgemäßen Zusammensetzungen können wässrige oder ölige Suspensionen sein. Diese Suspensionen können gemäß in der Technik bekannten Methoden unter Verwendung geeigneter Dispergier- oder Benetzungsmittel und Suspendiermittel formuliert werden. Das sterile, injizierbare Präparat kann auch eine sterile, injizierbare Lösung oder Suspension in einem nicht toxischen, parenteral akzeptablen Verdünnungsmittel oder Lösungsmittel sein, zum Beispiel eine Lösung in 1,3-Butandiol. Zu den akzeptablen Vehikeln und Lösungsmitteln, die verwendet werden können, gehören Wasser, Ringer-Lösung und isotonische Natriumchloridlösung. Außerdem werden sterile, feste Öle konventionell als Lösungsmittel oder Suspendiermedium verwendet.
- Zu diesem Zweck kann jedes milde, feste Öl verwendet werden, einschließlich synthetischer Mono- oder Diglyceride. Fettsäuren wie Ölsäure und ihre Glyceridderivate sind zur Herstellung von injizierbaren Materialien nützlich, wie auch natürliche pharmazeutisch annehmbare Öle wie Olivenöl oder Rizinusöl, vor allem in ihren polyoxyethylierten Versionen. Diese Öllösungen oder -suspensionen können auch ein langkettiges Alkoholverdünnungsmittel oder -dispergiermittel enthalten, wie Carboxymethylcellulose oder ähnliche Dispergiermittel, die gewöhnlich zur Formulierung pharmazeutisch annehmbarer Dosierungsformen verwendet werden, einschließlich Emulsionen und Suspensionen. Andere üblicherweise verwendete Tenside wie Tweens, Spans und andere Emulgatoren oder Bioverfügbarkeitsförderer, die gewöhnlich zur Herstellung pharmazeutisch annehmbarer Feststoffe, Flüssigkeiten oder anderer Dosierungsformen verwendet werden, können auch zur Formulierung verwendet werden.
- Die pharmazeutisch annehmbaren Zusammensetzungen der vorliegenden Erfindung können oral in jeder beliebigen oral akzeptablen Dosierungsform verabreicht werden, einschließlich unter anderem Kapseln, Tabletten, wässriger Suspensionen oder Lösungen. Im Falle von Tabletten für die orale Einnahme werden gewöhnlich Träger wie Lactose und Maisstärke verwendet. Gewöhnlich werden auch Gleitmittel wie Magnesiumstearat zugegeben. Zur oralen Verabreichung in Kapselform sind Lactose und getrocknete Maisstärke nützliche Streckmittel. Sind wässrige Suspensionen für den oralen Gebrauch erforderlich, dann wird der aktive Bestandteil mit Emulgatoren und Suspendiermitteln kombiniert. Bei Bedarf können auch bestimmte Süßungsmittel, Aromastoffe oder Farbstoffe zugegeben werden.
- Alternativ können die pharmazeutisch akzeptablen Zusammensetzungen der vorliegenden Erfindung in Form von Suppositorien rektal verabreicht werden. Diese können durch Vermischen des Mittels mit einem geeigneten nicht reizenden Exzipienten hergestellt werden, der bei Raumtemperatur fest und bei Rektaltemperatur flüssig ist und folglich im Rektum schmilzt, um den Wirkstoff freizusetzen. Zu solchen Materialien gehören Kakaobutter, Bienenwachs und Polyethylenglykole.
- Die pharmazeutisch annehmbaren Zusammensetzungen der vorliegenden Erfindung können auch topisch verabreicht werden, vor allem dann, wenn das Behandlungsziel Bereiche oder Organe einschließt, die durch eine topische Anwendung ohne weiteres erreichbar sind, einschließlich Erkrankungen am Auge, der Haut oder des unteren Darmtraktes. Geeignete topische Formulierungen können für jeden/jedes dieser Bereiche oder Organe ohne weiteres hergestellt werden.
- Die topische Anwendung im unteren Darmtrakt kann anhand einer rektalen Suppositorienformulierung (siehe oben) oder einer geeigneten Einlaufformulierung erfolgen. Topisch können auch transdermale Pflaster verwendet werden.
- Für topische Anwendungen können die pharmazeutisch annehmbaren Zusammensetzungen in einer geeigneten Salbe formuliert werden, die die aktive Komponente suspendiert oder gelöst in einem oder mehreren Trägern enthält. Träger für die topische Verabreichung der erfindungsgemäßen Verbindungen sind unter anderem Mineralöl, flüssiges Vaselin, weißes Vaselin, Propylenglykol, Polyoxyethylen, Polyoxypropylenverbindung, Emulgierwachs und Wasser. Alternativ können die pharmazeutisch annehmbaren Zusammensetzungen in einer geeigneten Lotion oder Creme formuliert werden, in der die aktiven Komponenten in einem oder mehreren pharmazeutisch annehmbaren Trägern suspendiert oder gelöst enthalten sind. Zu geeigneten Trägern gehören, ohne darauf beschränkt zu sein, Mineralöl, Sorbitanmonostearat, Polysorbat 60, Cetylesterwachs, Cetearylalkohol, 2-Octyldodecanol, Benzylalkohol und Wasser.
- Für den Gebrauch am Auge können die pharmazeutisch annehmbaren Zusammensetzungen als mikronisierte Suspensionen in isotonischer, pH-eingestellter, steriler Salzlösung oder vorzugsweise als Lösungen in isotonischer, pH-eingestellter, steriler Salzlösung mit oder ohne Konservierungsmittel wie Benzylalkoniumchlorid formuliert werden. Alternativ können die pharmazeutisch annehmbaren Zusammensetzungen für die Benutzung am Auge in einer Salbe wie Vaselin formuliert werden.
- Die pharmazeutisch annehmbaren Zusammensetzungen der vorliegenden Erfindung können auch nasal durch Aerosol oder Inhalation verabreicht werden. Solche Zusammensetzungen werden gemäß den auf dem Gebiet der Arzneimittelformulierung allgemein bekannten Methoden hergestellt und können als Lösungen in Salzlösung unter Verwendung von Benzylalkohol oder anderen geeigneten Konservierungsmitteln, Absorptionsförderern zur Verbesserung der Bioverfügbarkeit, Fluorkohlenwasserstoffen und/oder anderen konventionellen Solubilisierungs- oder Dispergiermitteln hergestellt werden.
- Am meisten bevorzugt werden die pharmazeutisch annehmbaren Zusammensetzungen der vorliegenden Erfindung für die orale Verabreichung formuliert.
- Die Menge der erfindungsgemäßen Verbindungen, die mit den Trägermaterialien kombiniert werden kann, um eine Zusammensetzung in einer einzelnen Dosierungsform zu produzieren, variiert je nach dem behandelten Wirt und der jeweiligen Verabreichungsmethode. Vorzugsweise sollten die Zusammensetzungen so formuliert werden, dass einem Patienten, der diese Zusammensetzungen erhält, eine Inhibitordosis zwischen 0,01 und 100 mg/kg Körpergewicht/Tag verabreicht werden kann.
- Es ist auch zu verstehen, dass ein bestimmter Dosierungs- und Behandlungsplan für jeden speziellen Patienten von einer Vielzahl von Faktoren abhängig ist, einschließlich Aktivität der spezifischen verwendeten Verbindung, das Alter, das Körpergewicht, der allgemeine Gesundheitszustand, das Geschlecht, die Ernährung, der Verabreichungszeitpunkt, die Ausscheidungsrate, die Wirkstoffkombination und die Beurteilung des behandelnden Arztes und die Schwere der jeweiligen behandelten Krankheit. Die Menge einer erfindungsgemäßen Verbindung in der Zusammensetzung ist außerdem von der jeweiligen Verbindung in der Zusammensetzung abhängig.
- Je nach dem/der jeweiligen zu behandelnden oder vermeidenden Zustand oder Krankheit, können auch zusätzliche therapeutische Wirkstoffe, die normalerweise zur Behandlung oder Vermeidung dieses Zustands verabreicht werden, in den erfindungsgemäßen Zusammensetzungen vorhanden sein. Wie hierin verwendet, sind zusätzliche therapeutische Wirkstoffe, die normalerweise zur Behandlung oder Vermeidung einer speziellen Krankheit oder eines Zustands verabreicht werden, als „für die/den behandelte(n) Krankheit oder Zustand geeignet" bekannt.
- Bei der Behandlung von Diabetes können zum Beispiel andere antidiabetische Mittel mit den erfindungsgemäßen Verbindungen zur Behandlung von Diabetes kombiniert werden. Zu diesen Mitteln gehören unter anderem Insulin in injizierbarer oder inhalierbarer Form, Insulinanaloga, Glitazone, Sulfonylharnstoffe, Alphaglucosidase-Inhibitoren, Biguanide und Insulinsensibilisatoren.
- Weitere Beispiele für Mittel, mit denen die erfindungsgemäßen Inhibitoren ebenfalls kombiniert werden können, sind unter anderem: Chemotherapeutika wie GleevecTM, Adriamycin, Dexamethason, Vincristin, Cyclophosphamid, Fluoruracil, Topotecan, Taxol, Interferone und Platinderivate; Behandlungsmittel für die Alzheimer-Krankheit wie Aricept• und Excelon•; Behandlungsmittel für die Parkinsonsche Krankheit wie L-DOPA/Carbidopa, Entacapon, Ropinrol, Pramipexol, Bromocriptin, Pergolid, Trihexephendyl und Amantadin; Mittel zur Behandlung multipler Sklerose (MS) wie Beta-Interferon (z.B. Avonex• und Rebif•), Copaxon• und Mitoxantron; Behandlungsmittel für Asthma wie Albuterol und Singulair•; Mittel zur Behandlung von Schizophrenie wie Zyprexa, Risperdal, Seroquel und Haloperidol; entzündungshemmende Mittel wie Corticosteroide, TNF-Blocker, IL-1 RA, Azathioprin, Cyclophosphamid und Sulfasalazin; immunomodulatorische und immunosuppressive Mittel wie Cyclosporin, Tacrolimus, Rapamycin, Mycophenolat Mofetil, Interferone, Corticosteroide, Cyclophophamid, Azathioprin und Sulfasalazin; neurotrophische Faktoren wie Acetylcholinesteraseinhibitoren, MAO-Inhibitoren, Interferone, Antikrampfmittel, Ionenkanalblocker, Riluzol und Anti-Parkinsonmittel; Mittel zur Behandlung von Herz-Kreislauf-Erkrankungen wie Beta-Blocker, ACE-Inhibitoren, Diuretika, Nitrate, Calciumkanalblocker und Statine; Mittel zur Behandlung von Lebererkrankungen wie Corticosteroide, Cholestyramin, Interferone und antivirale Mittel; Mittel zur Behandlung von Blutkrankheiten wie Corticosteroide, Antileukämika und Wachstumsfaktoren; und Mittel zur Behandlung von Immundefizienzkrankheiten wie Gammaglobulin.
- Die Menge des zusätzlichen therapeutischen Wirkstoffs in den erfindungsgemäßen Zusammensetzungen ist nicht höher als die Menge, die normalerweise in einer Zusammensetzung verabreicht würde, die diesen therapeutischen Wirkstoff als einzigen aktiven Wirkstoff enthält. Vorzugsweise liegt die Menge des zusätzlichen therapeutischen Wirkstoffs in den gegenwärtig offenbarten Zusammensetzungen zwischen etwa 50 % und 100 % der Menge, die normalerweise in einer Zusammensetzung vorliegt, die diesen Wirkstoff als einzigen therapeutisch aktiven Wirkstoff enthält.
- Gemäß einer weiteren Ausgestaltung betrifft die Erfindung ein Verfahren zum Inhibieren von GSK3 Proteinkinaseaktivität in einer biologischen Probe, das den Schritt des Inkontaktbringens der biologischen Probe mit einer erfindungsgemäßen Verbindung oder einer Zusammensetzung aufweist, die die Verbindung enthält.
- Gemäß einer weiteren Ausgestaltung betrifft die Erfindung ein Verfahren zum Inhibieren von Aurora2 Proteinkinaseaktivität in einer biologischen Probe, das den Schritt des Inkontaktbringens der biologischen Probe mit einer erfindungsgemäßen Verbindung oder einer Zusammensetzung aufweist, die die Verbindung enthält.
- Gemäß einer weiteren Ausgestaltung betrifft die Erfindung ein Verfahren zum Inhibieren von Syk Proteinkinaseaktivität in einer biologischen Probe, das den Schritt des Inkontaktbringens der biologischen Probe mit einer erfindungsgemäßen Verbindung oder einer Zusammensetzung aufweist, die die Verbindung enthält.
- Der hierin benutzte Begriff „biologische Probe" schließt unter anderem Zellkulturen oder Extrakte davon, Biopsiematerial von einem Säugetier oder Extrakte davon, sowie Blut, Speichel, Urin, Fäzes, Sperma, Tränenflüssigkeit oder andere Körperflüssigkeiten oder Extrakte davon ein.
- Die Inhibition von GSK3, Aurora2 oder Syk Proteinkinaseaktivität in einer biologischen Probe ist für viele Zwecke nützlich, die der fachkundigen Person bekannt sind. Beispiele für solche Zwecke sind unter anderem Bluttransfusionen, Organtransplantationen, biologische Testmaterialaufbewahrung und biologische Assays.
- Gemäß einer weiteren Ausgestaltung stellt die Erfindung ein Verfahren zur Behandlung oder Minderung der Schwere einer/eines GSK3-vermittelten Krankheit oder Zustands bei einem Patienten bereit, das den Schritt des Verabreichens einer erfindungsgemäßen Zusammensetzung an den Patienten aufweist.
- Der hierin benutzte Ausdruck „GSK3-vermittelte Krankheit" oder „GSK3-vermittelter Zustand" bezieht sich auf jede beliebige Krankheit oder jeden beliebigen anderen schädigenden Zustand, bei der/dem GSK3 Proteinkinase bekanntlich eine Rolle spielt. Zu solchen Zuständen gehören unter anderem Diabetes, neurodegenerative Störungen, die Alzheimer-Krankheit, die Huntington-Krankheit, die Parkinsonsche Krankheit, AIDS-assozüerte Dementia, amyotrophe Lateralsklerose (AML), multiple Sklerose (MS), Schizophrenie, Schlaganfall, Kardiomycete-Hypertrophie und Alopecia.
- Gemäß einer weiteren Ausgestaltung stellt die Erfindung ein Verfahren zur Behandlung oder Minderung der Schwere einer/eines Aurora2-vermittelten Krankheit oder Zustands bei einem Patienten bereit, das den Schritt des Verabreichens einer erfindungsgemäßen Zusammensetzung an den Patienten aufweist.
- Der hierin benutzte Ausdruck „Aurora2-vermittelte Krankheit" oder „Aurora2-vermittelter Zustand" bezieht sich auf jede beliebige Krankheit oder jeden beliebigen anderen schädigenden Zustand, bei der/dem Aurora2 Proteinkinase bekanntermaßen eine Rolle spielt. Zu solchen Zuständen gehören unter anderem Krebserkrankungen wie Kolon- und Brustkrebs. Gemäß einer weiteren Ausgestaltung stellt die Erfindung ein Verfahren zur Behandlung oder Minderung der Schwere einer/eines Syk-vermittelten Krankheit oder Zustands bei einem Patienten bereit, das den Schritt des Verabreichens einer erfindungsgemäßen Zusammensetzung an den Patienten aufweist.
- Der hierin benutzte Ausdruck „Syk-vermittelte Krankheit" oder „Syk-vermittelter Zustand" bezieht sich auf jede beliebige Krankheit oder jeden beliebigen anderen schädigenden Zustand, bei der/dem Syk Proteinkinase bekanntermaßen eine Rolle spielt. Zu solchen Zuständen gehören unter anderem allergische Störungen, insbesondere Asthma.
- In einer alternativen Ausgestaltung schließen die erfindungsgemäßen Verfahren, die Zusammensetzungen verwenden, die keinen zusätzlichen therapeutischen Wirkstoff enthalten, den zusätzlichen Schritt des getrennten Verabreichens eines zusätzlichen therapeutischen Wirkstoffs an den Patienten ein. Werden diese zusätzlichen therapeutischen Wirkstoffe getrennt verabreicht, dann können sie dem Patienten vor, sequentiell mit oder nach der Verabreichung der erfindungsgemäßen Zusammensetzungen verabreicht werden.
- Damit die hierin beschriebene Erfindung besser nachvollziehbar ist, werden die folgenden Beispiele gegeben. Es ist zu verstehen, dass diese Beispiele lediglich illustrativ sind und nicht als die vorliegende Erfindung in irgendeiner Weise beschränkend auszulegen sind.
- 3-Dimethylamino-1-thiazol-2-yl-propanon (2): Zu einer Lösung aus 2-Acetylthiazol (500 mg, 3,93 mmol) in 2 ml THF wurde Dimethylformamid-Dimethylacetal (1,6 ml, 7,86 mmol) gegeben, und die resultierende Lösung wurde über Nacht bei Raumtemperatur gerührt. Das Reaktionsgemisch wurde verdampft und der Rest mit Ethylacetat verrieben, und das Produkt wurde durch Filtration isoliert. Der filtrierte Feststoff wurde mit Diethylether gewaschen und getrocknet, um 2 (400 mg) als gelben Feststoff zu erhalten.
- N-(3-Benzyloxy-phenyl)-guanidin (4): 3-Benzyloxyanilin (1 g, 5 mmol) und Cyanamid (420 mg, 10 mmol) wurden in 4 ml 4N HCl in Dioxan gelöst und über Nacht auf 120°C erhitzt. Das Reaktionsgemisch wurde auf Raumtemperatur gekühlt, mit Wasser abgeschreckt und mit Diethylether extrahiert. Die wässrige Lage wurde mit 2N NaOH basisch gemacht und dreimal mit Dichlormethan extrahiert. Die organischen Extrakte wurden kombiniert und mit Lake gewaschen, über MgSO4 getrocknet und konzentriert, um 4 (450 mg) als hellbraunen Feststoff zu erhalten.
- (3-Benzyloxy-phenyl)-(4-thiazol-2-yl-pyrimidin-2-yl)-amin (I-7): Eine Lösung aus 3-Benzyloxyguanidin 4 (50 mg, 0,20 mmol) und Enaminon 2 (50 mg, 0,27 mmol) in Ethanol (3 ml) wurde unter Rückfluss in einem versiegelten Röhrchen über Nacht erhitzt. Das Reaktionsgemisch wurde konzentriert und der Rest wurde durch Säulenchromatographie gereinigt, um die Verbindung I-7 (20 mg) zu erhalten. M + 1 (beobachtet) 347,1. Rt = 4,28 Minuten.
- Beispiel 4
- Wir haben weitere Verbindungen der Formel I mit Verfahren hergestellt, die im Wesentlichen den in den obigen Beispielen 1–3 und den im Schema I illustrierten ähnlich sind. Die Charakterisierungsdaten für diese Verbindungen sind in der folgenden Tabelle 3 aufgeführt und beinhalten LC/MS (M + 1 beobachtet), HPLC und 1HNMR Daten.
- Der Begriff „Rt (min)" bezieht sich auf die mit der Verbindung assoziierte Retentionszeit in Minuten unter Anwendung des folgenden HPLC-Verfahrens. Die Rt wurde mit einer Waters ODS-AQ (2 × 50 mm) Säule bei Umgebungstemperatur mit einem Gradient von 10→90 % CH3CN in Wasser über einen Zeitraum von 5 Minuten bestimmt, wobei die Absorbanz als Durchschnitt von 190–380 nM in 4 nM Schritten nachgewiesen wurde.
- Der Buchstabe „Y" bedeutet, dass 1HNMR-Daten erhalten wurden und mit der zugeordneten Struktur übereinstimmten. Die Verbindungsnummern entsprechen den in Tabelle 1 aufgeführten Verbindungsnummern.
- Beispiel 5
- GSK-3 Inhibierungsuntersuchung
- Verbindungen wurden im Hinblick auf ihre Fähigkeit zur Inhibierung von GSK3-β-(AA 1-420)-Aktivität mit einem standardmäßigen gekoppelten Enzymsystem gescreent (Fox et al. (1998) Protein Sci. 7, 2249). Die Reaktionen fanden in einer Lösung statt, die 100 mM HEPES (pH 7,5), 10 mM MgCl2, 25 mM NaCl, 300 μM NADH, 1 mM DTT und 1,5 % DMSO enthielt. Endgültige Substratkonzentrationen im Assay waren 10 μM ATP (Sigma Chemicals, St Louis, MO) und 300 μM Peptid (HSSPHQS(PO3H3)EDEEE, American Peptide, Sunnyvale, CA). Die Reaktionen fanden bei 30°C und 60 nM GSK-3β statt. Die Endkonzentrationen der Komponenten des gekoppelten Enzymsystems lagen bei 2,5 mM Phosphoenolpyruvat, 300 μM NADH, 30 μg/ml Pyruvatkinase und 10 μg/ml Lactatdehydrogenase.
- Es wurde eine Untersuchungs-Vorratspufferlösung hergestellt, die alle oben aufgeführten Reagenzien enthielt, mit Ausnahme von ATP und der Testverbindung von Interesse. 59 μl des Testreaktionsgemischs wurden in eine 96-Kammern-1/2-Durchmesser-Platte (Corning, Corning, NY) gegeben und anschließend mit 1 μl einer 2 mM DMSO-Vorratslösung behandelt, die die Testverbindung enthielt (endgültige Konzentration der Verbindung 30 μM). Die Platte wurde ~10 Minuten lang bei 30°C inkubiert, anschließend wurde die Reaktion durch die Zugabe von 7 μl ATP initiiert (Endkonzentration 10 μM). Die Reaktionsgeschwindigkeiten wurden mit einem Molecular Devices Spectramax Plattenleser (Sunnyvale, CA) über einen Lesezeitraum von 5 Minuten bei 30°C erhalten. Verbindungen, die eine Inhibierung von mehr als 50 % gegenüber Standardkammern aufwiesen, die DMSO, aber keine Verbindung enthielten, wurden titriert und es wurden die Ki-Werte ermittelt.
- Tabelle 4 zeigt die Ergebnisse der Aktivität ausgewählter Verbindungen der vorliegenden Erfindung in GSK3-Inhibierungsuntersuchung. Die Verbindungsnummern entsprechen den Verbindungsnummern in Tabelle 1. Verbindungen mit einem Ki-Wert von weniger als 0,1 Mikromol (μM) sind mit „A" bewertet, Verbindungen mit einem Ki zwischen 0,1 und 1 μM sind mit „B" bewertet und Verbindungen mit einem Ki von mehr als 1 μM sind mit „C" bewertet.
- Beispiel 6
- Aurora2-Inhibitionsassay
- Verbindungen wurden in der folgenden Weise im Hinblick auf ihre Fähigkeit zur Inhibition von Aurora2 mit einer standardmäßigen gekoppelten Enzymuntersuchung gescreent (Fox et al (1998) Protein Sci 7, 2249). Zu einer Untersuchungs-Vorratspufferlösung mit 0,1 M HEPES 7,5, 10 mM MgCl2, 1 mM DTT, 25 mM NaCl, 2,5 mM Phosphoenolpyruvat, 300 mM NADH, 30 mg/ml Pyruvatkinase, 10 mg/ml Lactatdehydrogenase, 40 mM ATP und 800 μM Peptid (LRRASLG, American Peptide, Sunnyvale, CA) wurde eine DMSO-Lösung einer erfindungsgemäßen Verbindung bis auf eine Endkonzentration von 30 μM gegeben. Das resultierende Gemisch wurde 10 Minuten lang bei 30°C inkubiert. Die Reaktion wurde durch die Zugabe von 10 μl Aurora2-Vorratslösung initiiert, um eine Endkonzentration von 70 nM in der Untersuchung zu erhalten. Die Reaktionsgeschwindigkeiten wurden durch Beobachten der Absorbanz bei 340 nm über einen Lesezeitraum von 5 Minuten bei 30°C mit einem BioRad Ultramark Plattenleser (Hercules, CA) erhalten. Die IC50-Werte wurden anhand der Geschwindigkeitsdaten in Abhängigkeit der Inhibitorkonzentration ermittelt.
- In Tabelle 5 sind die Ergebnisse der Aktivität ausgewählter Verbindungen der vorliegenden Erfindung im Aurora2-Inhibitionsassay enthalten. Die Verbindungsnummern entsprechen den Verbindungsnummern in Tabelle 1. Verbindungen mit einem IC50-Wert von weniger als 0,5 Mikromol (μM) sind mit „A" bewertet, Verbindungen mit einem IC50 zwischen 0,5 und 2 μM sind mit „B" bewertet und Verbindungen mit einem IC50 von mehr als 2 μM sind mit „C" bewertet.
- Beispiel 7
- Syk-Inhibierungsuntersuchung
- Verbindungen wurden im Hinblick auf ihre Fähigkeit zur Inhibierung von Syk mit einem standardmäßigen gekoppelten Enzymassay gescreent (Fox et al. (1998) Protein Sci. 7, 2249). Reaktionen wurden in 100 mM HEPES, pH 7,5, 10 mM MgCl2, 25 mM NaCl, 1 mM DTT und 1,5 % DMSO ausgeführt. Die endgültigen Substratkonzentrationen in der Untersuchung lagen bei 200 μM ATP (Sigma Chemical Co.) und 4 μM Poly-Gly-Tyr-Peptid (Sigma Chemical Co.). Untersuchungen wurden bei 30°C und 200 nM Syk durchgeführt. Die Endkonzentrationen der Komponenten des gekoppelten Enzymsystems lagen bei 2,5 mM Phosphoenolpyruvat, 300 μM NADH, 30 μg/ml Pyruvatkinase und 10 μg/ml Lactatdehydrogenase.
- Es wurde eine Assay-Vorratspufferlösung hergestellt, die alle oben aufgeführten Reagenzien enthielt, mit Ausnahme von Syk, DTT und der Testverbindung von Interesse. 56 μl des Testreaktionsgemischs wurden in eine 96-Kammern-Platte gegeben, anschließend wurde 1 μl einer 2 mM DMSO Vorratslösung dazugegeben, die die Testverbindung enthielt (Endkonzentration der Verbindung 30 μM). Die Platte wurde ~10 Minuten lang bei 30°C vorinkubiert und die Reaktion wurde durch Zugeben von 10 μl des Enzyms initiiert (Endkonzentration 25 nM). Die Reaktionsgeschwindigkeiten wurden mit einem BioRad Ultramark Plattenleser (Hercules, CA) über einen Lesezeitraum von 5 Minuten bei 30°C erhalten. Verbindungen, die eine Inhibierung von >50 % gegenüber Standardkammern aufwiesen, die DMSO, aber keine Verbindung enthielten, wurden titriert und die IC50-Werte wurden mit einem ähnlichen Protokoll ermittelt.
- In Tabelle 6 sind die Ergebnisse der Aktivität ausgewählter Verbindungen der vorliegenden Erfindung im Syk-Inhibitionsassay enthalten. Die Verbindungsnummern entsprechen den Verbindungsnummern in Tabelle 1. Verbindungen mit einem IC50-Wert von weniger als 0,5 Mikromol (μM) sind mit „A" bewertet, Verbindungen mit einem IC50 zwischen 0,5 und 2 μM sind mit „B" bewertet und Verbindungen mit einem IC50 von mehr als 2 μM sind mit „C" bewertet.
- Während wir eine Reihe von Ausgestaltungen der vorliegenden Erfindung beschrieben haben, es ist aber offensichtlich, dass unsere grundlegenden Beispiele verändert werden können, um andere Ausgestaltungen unter Verwendung der erfindungsgemäßen Verbindungen und Verfahren bereitzustellen. Es ist daher verständlich, dass der Umfang der vorliegenden Erfindung anhand der beiliegenden Ansprüche und nicht durch die beispielhaft wiedergegebenen spezifischen Ausgestaltungen zu definieren.
Ar1 gegebenenfalls durch einen bis vier Substituenten substituiert ist, die aus der Gruppe bestehend aus Folgendem ausgewählt sind:
jedes Q unabhängig aus einer Valenzbindung oder einer gegebenenfalls substituierten C1-6 Alkylidenkette ausgewählt ist, wobei:
eine oder zwei nicht benachbarte Methyleneinheiten von Q gegebenenfalls und unabhängig durch -O-, -S-, -NR-, -C(O)-, -CO2-, -C(O)NR-, -OC(O)NR-, -C(O)C(O)-, -C(O)C(O)-, -NRC(O)-, NRCO2-, -NRC(O)NR-, -S(O)-, -SO2-, NRSO2-, -SO2NR- oder -NRSO2NR- ersetzt sind;
jedes Ar2 ein gegebenenfalls substituierter Ring ist, welcher unabhängig ausgewählt ist aus:
Ar2 gegebenenfalls durch eine bis vier R2 Gruppen substituiert ist; und
jedes R2 unabhängig aus R, Halogen, NO2, CN, OR, SR, N(R)2, NRCOR, NRCON(R)2, NRCO2R, C(O)R, CO2R, CON(R)2, OC(O)N(R)2, SOR, SO2R, SO2N(R)2, NRSO2R, NRSO2N(R)2, C(O)C(O)R oder C(O)CH2C(O)R ausgewählt ist, wobei:
zwei R2 an benachbarten Positionen auf Ar1 oder Ar2 gegebenenfalls zusammengefasst werden, um einen gesättigten, teilweise ungesättigten oder völlig ungesättigten 4–6 gliedrigen Ring mit 0–3 Heteroatomen zu bilden, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind.
Ar1 durch einen bis vier Substituenten substituiert ist, die ausgewählt sind aus der Gruppe bestehend aus:
Ar2 gegebenenfalls durch 1–2 R2 Gruppen substituiert ist.
Claims (15)
- Eine Verbindung der Formel IIa oder IIa' oder ein pharmazeutisch annehmbares Salz davon, wobei: jedes R unabhängig aus Wasserstoff oder einer gegebenenfalls substituierten C1-6 aliphatischen Gruppe ausgewählt ist, wobei: zwei an das selbe Stickstoffatom gebundene R sind, die gegebenenfalls mit dem Stickstoff zusammengefasst werden können, um einen 3–7 gliedrigen gesättigten, teilweise ungesättigten oder völlig ungesättigten Ring mit 0–2 Heteroatomen zusätzlich zum darin gebundenen Stickstoff zu bilden, die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind; jedes Q unabhängig aus einer Valenzbindung oder einer gegebenenfalls substituierten C1-6Alkylidenkette ausgewählt ist, wobei: eine oder zwei nicht-benachbarte Methyleneinheiten von Q gegebenenfalls und unabhängig durch -O-, -S-, -NR-, -C(O)-, -CO2-, -C(O)NR-, -OC(O)NR-, -C(O)C(O)- -NRC(O)-, NRCO2-, -NRC(O)NR-, S(O)-, -SO2-, -NRSO2-, -SO2NR-, oder NRSO2NR- ersetzt sind; jedes Ar2 ein gegebenenfalls substituierter Ring ist, welcher unabhängig ausgewählt ist aus: (a) einem 3–8 gliedrigen monozyklischen oder 8–10 gliedrigen bizyklischen gesättigten, teilweise ungesättigten oder Aryl-Ring (b) einem 3–7 gliedrigen heterozyklischen Ring mit 1–3 Heteroatomen die unabhängig aus Stickstoff, Sauerstoff, oder Schwefel ausgewählt sind, oder (c) einem 5–6 gliedrigen monozyklischen oder 8–10 gliedrigen bizyklischen Heteroaryl-Ring mit 1–4 Heteroatomen die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind, wobei: Ar2 gegebenenfalls durch eine bis vier R2 Gruppen substituiert ist, wobei jedes R2 unabhängig aus R, Halogen, NO2, CN, OR, SR, N(R)2, NRCOR, NRCON(R)2, NRCO2R, C(O)R, CO2R, CON(R)2, OC(O)N(R)2, SOR, SO2R, SO2N(R)2, NRSO2R, NRSO2N(R)2, C(O)C(O)R, oder C(O)CH2C(O)R ausgewählt ist; unter der Bedingung, dass wenn Ar1 ein Phenyl ist, zwei R2 nicht gleichzeitig OR in der meta und para Position von Ar1 sind.
- Verbindung nach Anspruch 1, wobei R2 aus Halogen, CN, CO2R, R, NO2, OR, Haloalkyl, SO2N(R)2 oder N(R)2 ausgewählt ist.
- Verbindung nach Anspruch 2, wobei R2 aus Fluor, Iod, Chlor, Brom, CO2CH3, Methyl, Ethyl, t-Butyl, NH2, NHMe, N(Me)2, OH, OCH3, OCH2CH3, CF3, SO2NH2, oder SO2NHMe ausgewählt ist.
- Verbindung nach Anspruch 1, wobei Q eine C1-4 Alkylidenkette ist, wobei eine oder zwei Methyleneinheiten von Q gegebenenfalls durch O, NR, NRCO, NRCO2, NRSO2, oder CONR ersetzt sind, wobei jedes R Wasserstoff oder eine gegebenenfalls substituierte C1-4 aliphatische Gruppe ist, und wobei Ar2 ein 3–6 gliedriger carbozyklischer Ring oder ein gegebenenfalls substituiertes Phenyl, 5–6 gliedriger heterozyklischer oder Heteroaryl Ring mit einem oder zwei Heteroatomen die unabhängig aus Stickstoff, Sauerstoff oder Schwefel ausgewählt sind, ist
- Verbindung nach Anspruch 1, wobei die Ar2 Gruppe des QAr2 Restes gegebenenfalls mit R, OR, N(R)2, SO2R, Halogen, NO2, CN, SR, SO2N(R)2, CO2R, C(O)R, oder Oxo substituiert ist.
- Zusammensetzung die eine Verbindung nach Anspruch 1, in einer Menge um nachweislich GSK3, Aurora2 oder Syk Proteinkinase Aktivität zu inhibieren, und einen pharmazeutisch annehmbaren Träger, Hilfsstoff oder Vehikel aufweist.
- Zusammensetzung nach Anspruch 8, die weiters einen zusätzlichen therapeutischen Wirkstoff der aus einem antidiabetischen Wirkstoff, einem chemotherapeutischen oder antiproliferativen Wirkstoff, einem Wirkstoff zum Behandeln der Alzheimer Krankheit, einem Wirkstoff zum Behandeln der Parkinson Krankheit, einem Wirkstoff zum Behandeln von Multiple Sklerose (MS), zur Behandlung von Asthma, einem Wirkstoff zum Behandeln von Schizophrenie, einem antiinflammatorischen Wirkstoff, einem immunomodulatorischen oder immununosuppresiven Wirkstoff, einem neurotrophischen Faktor, einem Wirkstoff zum Behandeln kardiovaskulärer Krankheiten, einem Wirkstoff zum Behandeln von Leberkrankheiten, einem Wirkstoff zum Behandeln von Blutkrankheiten, oder einem Wirkstoff zum Behandeln von Immundefizienz-Krankheiten ausgewählt ist, aufweist.
- Verfahren zum Inhibieren von GSK3, Aurora2 oder Syk Kinase Aktivität in einer biologischen Probe, welche den Schritt des Kontaktierens der biologischen Probe mit a) einer Zusammensetzung nach Anspruch 8, oder b) einer Verbindung nach Anspruch 1 aufweist.
- Zusammensetzung nach Anspruch 8, oder einer Verbindung nach Anspruch 1 zur Verwendung in der Behandlung oder Verminderung der Schwere einer(s) durch GSK3-, Aurora2-, oder Syk-vermittelten Krankheit oder Zustandes bei einem Patienten.
- Zusammensetzung oder Verbindung nach Anspruch 11, für die Verwendung in der Behandlung oder Verminderung der Schwere einer durch GSK3-vermittelten Krankheit, wobei die GSK3-vermittelte Krankheit aus Diabetes, einer neurodegenerativen Störung, einer Krankheit des Zentralnervensystems, Alzheimer Krankheit, Huntington, Parkinson, AIDS assoziierte Dementia, amyotrophe Lateralsklerose (AML), multiple Sklerose, Schlaganfall, Schizophrenie, Kardiomycete-Hypertrophie, manisch-depressive Krankheit oder Calvities ausgewählt ist.
- Zusammensetzung oder eine Verbindung nach Anspruch 11, für die Verwendung in der Behandlung oder Verminderung der Schwere einer Aurora2-vermittelten Krankheit, wobei die Aurora2-vermittelte Krankeit Krebs ist.
- Zusammensetzung oder eine Verbindung nach Anspruch 11, für die Verwendung in der Behandlung oder Verminderung der Schwere einer Syk-vermittelten Krankheit, wobei die Syk-vermittelte Krankeit eine allergische Störung ist.
- Zusammensetzung oder Verbindung nach Anspruch 11, für die Verwendung mit einem zusätzlichen therapeutischen Wirkstoff der aus einem antidiabetischen Wirkstoff, einem chemotherapeutischen oder antiproliferativen Wirkstoff, für die Behandlung der Alzheimer Krankheit, für die Behandlung der Parkinson Krankheit, einem Wirkstoff zum Behandeln von Multiple Sklerose (MS), zur Behandlung von Asthma, einem Wirkstoff zum Behandeln von Schizophrenie, einem antiinflammatorischen Wirkstoff, einem immunomodulatorischen oder immununosuppresiven Wirkstoff, einem neurotrophischen Faktor, einem Wirkstoff zum Behandeln kardiovaskulärer Krankheiten, einem Wirkstoff zum Behandeln von Leberkrankheiten, einem Wirkstoff zum Behandeln von Blutkrankheiten, oder einem Wirkstoff zum Behandeln von Immundefizienz-Krankheiten ausgewählt ist.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US29515801P | 2001-06-01 | 2001-06-01 | |
| US295158P | 2001-06-01 | ||
| PCT/US2002/016352 WO2002096905A1 (en) | 2001-06-01 | 2002-05-23 | Thiazole compounds useful as inhibitors of protein kinases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60214703D1 DE60214703D1 (de) | 2006-10-26 |
| DE60214703T2 true DE60214703T2 (de) | 2007-09-13 |
Family
ID=35781455
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60214703T Expired - Lifetime DE60214703T2 (de) | 2001-06-01 | 2002-05-23 | Thiazolverbindungen, die sich als inhibitoren von proteinkinasen eignen |
Country Status (8)
| Country | Link |
|---|---|
| US (2) | US7256190B2 (de) |
| EP (1) | EP1392684B1 (de) |
| JP (2) | JP4523271B2 (de) |
| AT (1) | ATE339418T1 (de) |
| CA (1) | CA2446756C (de) |
| DE (1) | DE60214703T2 (de) |
| ES (1) | ES2274035T3 (de) |
| WO (1) | WO2002096905A1 (de) |
Families Citing this family (100)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2242771T5 (es) * | 2000-09-15 | 2011-10-14 | Vertex Pharmaceuticals Incorporated | Compuestos de pirazol útiles como inhibidores de proteína quinasas. |
| TWI329105B (en) * | 2002-02-01 | 2010-08-21 | Rigel Pharmaceuticals Inc | 2,4-pyrimidinediamine compounds and their uses |
| NZ537752A (en) | 2002-07-29 | 2006-12-22 | Rigel Pharmaceuticals Inc | Use of 2,4-pyrimidinediamine compounds in the preparation of medicaments for treating autoimmune diseases |
| AU2003288956A1 (en) * | 2002-10-30 | 2004-06-07 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of rock and other protein kinases |
| GB0229581D0 (en) * | 2002-12-19 | 2003-01-22 | Cyclacel Ltd | Use |
| WO2004071440A2 (en) | 2003-02-06 | 2004-08-26 | Bristol-Myers Squibb Company | Thiazolyl-based compounds useful as kinase inhibitors |
| WO2004080977A1 (en) * | 2003-03-12 | 2004-09-23 | Vertex Pharmaceuticals Incorporated | 4-substituted-5-cyano-1h-pyrimidin-6-(thi)ones as gsk-3 inhibitors |
| ATE396731T1 (de) * | 2003-03-25 | 2008-06-15 | Vertex Pharma | Thiazole zur verwendung als inhibitoren von protein-kinasen |
| ATE482200T1 (de) | 2003-05-01 | 2010-10-15 | Bristol Myers Squibb Co | Als kinaseinhibitoren geeignete arylsubstituierte pyrazolamidverbindungen |
| JP4886511B2 (ja) | 2003-07-30 | 2012-02-29 | ライジェル ファーマシューティカルズ, インコーポレイテッド | 2,4−ピリミジンジアミン化合物による自己免疫疾患の治療または予防方法 |
| EP1694686A1 (de) | 2003-12-19 | 2006-08-30 | Takeda San Diego, Inc. | Kinaseinhibitoren |
| GB0402653D0 (en) * | 2004-02-06 | 2004-03-10 | Cyclacel Ltd | Compounds |
| US20050250829A1 (en) * | 2004-04-23 | 2005-11-10 | Takeda San Diego, Inc. | Kinase inhibitors |
| JPWO2005113550A1 (ja) * | 2004-05-20 | 2008-03-27 | 三菱ウェルファーマ株式会社 | アミノピリミジン誘導体及びその医薬としての用途 |
| GB0411791D0 (en) * | 2004-05-26 | 2004-06-30 | Cyclacel Ltd | Compounds |
| EP1778669A2 (de) | 2004-08-18 | 2007-05-02 | Takeda San Diego, Inc. | Kinase-inhibitoren |
| EP1799656A4 (de) * | 2004-08-25 | 2009-09-02 | Targegen Inc | Heterocyclische verbindungen und anwendungsverfahren |
| US7285569B2 (en) | 2004-09-24 | 2007-10-23 | Hoff Hoffmann-La Roche Inc. | Tricycles, their manufacture and use as pharmaceutical agents |
| AR050948A1 (es) | 2004-09-24 | 2006-12-06 | Hoffmann La Roche | Derivados de ftalazinona; su obtencion y su utilizacion en la fabricacion de medicamentos para el tratamiento del cancer. |
| RU2007114080A (ru) | 2004-10-13 | 2008-11-27 | Вайет (Us) | N-бензилсульфонил-замещенные аналоги анилинопиримидина |
| DE602005023333D1 (de) | 2004-10-15 | 2010-10-14 | Takeda Pharmaceutical | Kinaseinhibitoren |
| WO2006093247A1 (ja) * | 2005-02-28 | 2006-09-08 | Japan Tobacco Inc. | Syk阻害活性を有する新規なアミノピリジン化合物 |
| RU2363699C2 (ru) * | 2005-02-28 | 2009-08-10 | Джапан Тобакко Инк. | Новое производное аминопиридина с ингибиторной активностью в отношении syk. |
| KR20070113286A (ko) | 2005-04-14 | 2007-11-28 | 에프. 호프만-라 로슈 아게 | 아미노피라졸 유도체, 이의 제조 및 약학 제제로서의 용도 |
| CA2607901C (en) | 2005-06-13 | 2016-08-16 | Rigel Pharmaceuticals, Inc. | Methods and compositions for treating degenerative bone disorders using a syk inhibitory 2,4-pyrimidinediamine |
| EP1734251B1 (de) * | 2005-06-17 | 2007-01-24 | MAGNETI MARELLI POWERTRAIN S.p.A. | Brennstoffeinspritzventil |
| KR100674813B1 (ko) * | 2005-08-05 | 2007-01-29 | 일양약품주식회사 | N-페닐-2-피리미딘-아민 유도체 및 그의 제조방법 |
| US8119655B2 (en) | 2005-10-07 | 2012-02-21 | Takeda Pharmaceutical Company Limited | Kinase inhibitors |
| GB0520958D0 (en) | 2005-10-14 | 2005-11-23 | Cyclacel Ltd | Compound |
| US7572809B2 (en) | 2005-12-19 | 2009-08-11 | Hoffmann-La Roche Inc. | Isoquinoline aminopyrazole derivatives |
| WO2007132221A1 (en) * | 2006-05-12 | 2007-11-22 | Cyclacel Limited | Combined anticancer pyrimidine-thiazole aurora kinase inhibitors |
| MX2009003673A (es) * | 2006-10-04 | 2009-04-22 | Pfizer Prod Inc | Derivados de piridido[4,3-d]pirimidin-4(3h)-ona como antagonistas de los receptores de calcio. |
| EA200970361A1 (ru) | 2006-10-09 | 2010-02-26 | Такеда Фармасьютикал Компани Лимитед | Ингибиторы киназы |
| EP2223925A1 (de) * | 2006-10-09 | 2010-09-01 | Takeda Pharmaceutical Company Limited | Kinase-Inhibitoren |
| JP5160637B2 (ja) * | 2007-05-04 | 2013-03-13 | アイアールエム・リミテッド・ライアビリティ・カンパニー | c−kitおよびPDGFRキナーゼインヒビターとしての化合物および組成物 |
| WO2009046416A1 (en) * | 2007-10-05 | 2009-04-09 | Targegen Inc. | Anilinopyrimidines as jak kinase inhibitors |
| ES2617622T3 (es) | 2008-02-15 | 2017-06-19 | Rigel Pharmaceuticals, Inc. | Compuestos de pirimidin-2-amina y su uso como inhibidores de JAK cinasas |
| EP2177510A1 (de) | 2008-10-17 | 2010-04-21 | Universität des Saarlandes | Allosterische Proteinkinasemodulatoren |
| US8765747B2 (en) | 2009-06-12 | 2014-07-01 | Dana-Farber Cancer Institute, Inc. | Fused 2-aminothiazole compounds |
| EP2512246B1 (de) | 2009-12-17 | 2015-09-30 | Merck Sharp & Dohme Corp. | Aminopyrimidine als syk-hemmer |
| US8759366B2 (en) | 2009-12-17 | 2014-06-24 | Merck Sharp & Dohme Corp. | Aminopyrimidines as SYK inhibitors |
| EP2519517B1 (de) | 2009-12-29 | 2015-03-25 | Dana-Farber Cancer Institute, Inc. | Typ-ii-raf-kinase-hemmer |
| WO2012060847A1 (en) | 2010-11-07 | 2012-05-10 | Targegen, Inc. | Compositions and methods for treating myelofibrosis |
| CA2826286C (en) | 2011-01-31 | 2021-09-21 | Intellect Neurosciences Inc. | Treatment of tauopathies |
| EP2489663A1 (de) | 2011-02-16 | 2012-08-22 | Almirall, S.A. | Verbindungen als Syk-Kinasehemmer |
| US9120785B2 (en) | 2011-05-10 | 2015-09-01 | Merck Sharp & Dohme Corp. | Pyridyl aminopyridines as Syk inhibitors |
| KR20140028062A (ko) | 2011-05-10 | 2014-03-07 | 머크 샤프 앤드 돔 코포레이션 | Syk 억제제로서의 아미노피리미딘 |
| WO2012154518A1 (en) | 2011-05-10 | 2012-11-15 | Merck Sharp & Dohme Corp. | Bipyridylaminopyridines as syk inhibitors |
| EP2554662A1 (de) | 2011-08-05 | 2013-02-06 | M Maria Pia Cosma | Verfahren zur Behandlung von Netzhautdegenerationserkrankungen |
| WO2013052393A1 (en) | 2011-10-05 | 2013-04-11 | Merck Sharp & Dohme Corp. | 3-PYRIDYL CARBOXAMIDE-CONTAINING SPLEEN TYROSINE KINASE (Syk) INHIBITORS |
| WO2013052391A1 (en) | 2011-10-05 | 2013-04-11 | Merck Sharp & Dohme Corp. | PHENYL CARBOXAMIDE-CONTAINING SPLEEN TYROSINE KINASE (Syk) INHIBITORS |
| WO2013052394A1 (en) | 2011-10-05 | 2013-04-11 | Merck Sharp & Dohme Corp. | 2-pyridyl carboxamide-containing spleen tyrosine kinase (syk) inhibitors |
| US9382239B2 (en) | 2011-11-17 | 2016-07-05 | Dana-Farber Cancer Institute, Inc. | Inhibitors of c-Jun-N-terminal kinase (JNK) |
| CN104302640A (zh) | 2012-03-16 | 2015-01-21 | 埃克希金医药品有限公司 | 3,5-二氨基吡唑激酶抑制剂 |
| US9096579B2 (en) | 2012-04-20 | 2015-08-04 | Boehringer Ingelheim International Gmbh | Amino-indolyl-substituted imidazolyl-pyrimidines and their use as medicaments |
| MX371331B (es) | 2012-04-24 | 2020-01-27 | Vertex Pharma | Inhibidores de la proteina cinasa dependiente de acido desoxirribonucleico(adn-pk). |
| WO2014031438A2 (en) * | 2012-08-20 | 2014-02-27 | Merck Sharp & Dohme Corp. | SUBSTITUTED PHENYL SPLEEN TYROSINE KINASE (Syk) INHIBITORS |
| EP2909194A1 (de) | 2012-10-18 | 2015-08-26 | Dana-Farber Cancer Institute, Inc. | Hemmer der cyclinabhängigen kinase 7 (cdk7) |
| WO2014063061A1 (en) | 2012-10-19 | 2014-04-24 | Dana-Farber Cancer Institute, Inc. | Hydrophobically tagged small molecules as inducers of protein degradation |
| US10000483B2 (en) | 2012-10-19 | 2018-06-19 | Dana-Farber Cancer Institute, Inc. | Bone marrow on X chromosome kinase (BMX) inhibitors and uses thereof |
| US9624210B2 (en) | 2012-12-12 | 2017-04-18 | Merck Sharp & Dohme Corp. | Amino-pyrimidine-containing spleen tyrosine kinase (Syk) inhibitors |
| EP2934525B1 (de) | 2012-12-21 | 2019-05-08 | Merck Sharp & Dohme Corp. | Thiazolsubstituierte aminopyridine als milztyrosinkinasehemmer |
| SI3527563T1 (sl) | 2013-03-12 | 2022-01-31 | Vertex Pharmaceuticals Incorporated | Inhibitorji DNA-PK |
| EP2988744A4 (de) | 2013-04-26 | 2016-11-02 | Merck Sharp & Dohme | Thiazolsubstituierte aminoheteroaryle als milztyrosinkinasehemmer |
| US9499534B2 (en) | 2013-04-26 | 2016-11-22 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminopyrimidines as spleen tyrosine kinase inhibitors |
| NZ631142A (en) | 2013-09-18 | 2016-03-31 | Axikin Pharmaceuticals Inc | Pharmaceutically acceptable salts of 3,5-diaminopyrazole kinase inhibitors |
| DK3424920T3 (da) | 2013-10-17 | 2020-06-08 | Vertex Pharma | Co-krystaller af (s)-n-methyl-8-(1-((2'-methyl-[4,5'-bipyrimidin]-6-yl)amino)propan-2-yl)quinolin-4-carboxamid og deuterede derivater deraf som dna-pk-inhibitorer |
| WO2015058126A1 (en) | 2013-10-18 | 2015-04-23 | Syros Pharmaceuticals, Inc. | Heteroaromatic compounds useful for the treatment of prolferative diseases |
| AU2014337044A1 (en) | 2013-10-18 | 2016-05-05 | Dana-Farber Cancer Institute, Inc. | Polycyclic inhibitors of cyclin-dependent kinase 7 (CDK7) |
| US9670196B2 (en) | 2013-12-20 | 2017-06-06 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminoheteroaryls as Spleen Tyrosine Kinase inhibitors |
| WO2015095445A1 (en) | 2013-12-20 | 2015-06-25 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors |
| EP3082807B1 (de) | 2013-12-20 | 2018-07-04 | Merck Sharp & Dohme Corp. | Thiazolsubstituierte aminoheteroaryle als milztyrosinkinasehemmer |
| US9775839B2 (en) | 2014-03-13 | 2017-10-03 | Merck Sharp & Dohme Corp. | 2-pyrazine carboxamides as spleen tyrosine kinase inhibitors |
| HRP20190039T1 (hr) | 2014-04-04 | 2019-03-08 | Syros Pharmaceuticals, Inc. | Inhibitori ciklin-ovisne kinaze 7 (cdk7) |
| WO2015155738A2 (en) | 2014-04-09 | 2015-10-15 | Christopher Rudd | Use of gsk-3 inhibitors or activators which modulate pd-1 or t-bet expression to modulate t cell immunity |
| WO2015164604A1 (en) | 2014-04-23 | 2015-10-29 | Dana-Farber Cancer Institute, Inc. | Hydrophobically tagged janus kinase inhibitors and uses thereof |
| US10017477B2 (en) | 2014-04-23 | 2018-07-10 | Dana-Farber Cancer Institute, Inc. | Janus kinase inhibitors and uses thereof |
| WO2015191630A1 (en) | 2014-06-10 | 2015-12-17 | Sanford-Burnham Medical Research Institute | Metabotropic glutamate receptor negative allosteric modulators (nams) and uses thereof |
| WO2016105528A2 (en) | 2014-12-23 | 2016-06-30 | Dana-Farber Cancer Institute, Inc. | Inhibitors of cyclin-dependent kinase 7 (cdk7) |
| HUE049801T2 (hu) | 2014-12-23 | 2020-10-28 | Sma Therapeutics Inc | 3,5-diaminopirazol kináz inhibitorok |
| HK1246645A1 (zh) | 2015-03-27 | 2018-09-14 | 达纳-法伯癌症研究所股份有限公司 | 细胞周期蛋白依赖性激酶的抑制剂 |
| US10702527B2 (en) | 2015-06-12 | 2020-07-07 | Dana-Farber Cancer Institute, Inc. | Combination therapy of transcription inhibitors and kinase inhibitors |
| JP7028766B2 (ja) | 2015-09-09 | 2022-03-02 | ダナ-ファーバー キャンサー インスティテュート, インコーポレイテッド | サイクリン依存性キナーゼの阻害剤 |
| EP3231434A1 (de) | 2016-04-14 | 2017-10-18 | Fundacio Centre de Regulacio Genomica | Verfahren zur behandlung von parkinsonismus |
| JP2019529475A (ja) | 2016-09-27 | 2019-10-17 | バーテックス ファーマシューティカルズ インコーポレイテッドVertex Pharmaceuticals Incorporated | Dna損傷剤とdna−pk阻害剤との組合せ物を使用する、がんを処置するための方法 |
| WO2018217766A1 (en) | 2017-05-22 | 2018-11-29 | Whitehead Institute For Biomedical Research | Kcc2 expression enhancing compounds and uses thereof |
| US12187701B2 (en) | 2018-06-25 | 2025-01-07 | Dana-Farber Cancer Institute, Inc. | Taire family kinase inhibitors and uses thereof |
| US11066404B2 (en) | 2018-10-11 | 2021-07-20 | Incyte Corporation | Dihydropyrido[2,3-d]pyrimidinone compounds as CDK2 inhibitors |
| CA3124422A1 (en) | 2018-12-28 | 2020-07-02 | Dana-Farber Cancer Institute, Inc. | Inhibitors of cyclin-dependent kinase 7 and uses thereof |
| WO2020168197A1 (en) | 2019-02-15 | 2020-08-20 | Incyte Corporation | Pyrrolo[2,3-d]pyrimidinone compounds as cdk2 inhibitors |
| US11472791B2 (en) | 2019-03-05 | 2022-10-18 | Incyte Corporation | Pyrazolyl pyrimidinylamine compounds as CDK2 inhibitors |
| US11919904B2 (en) | 2019-03-29 | 2024-03-05 | Incyte Corporation | Sulfonylamide compounds as CDK2 inhibitors |
| CA3135170A1 (en) | 2019-04-05 | 2020-10-08 | Tauc3 Biologics Limited | Anti-tauc3 antibodies and uses thereof |
| US11440914B2 (en) | 2019-05-01 | 2022-09-13 | Incyte Corporation | Tricyclic amine compounds as CDK2 inhibitors |
| WO2020223558A1 (en) | 2019-05-01 | 2020-11-05 | Incyte Corporation | Tricyclic amine compounds as cdk2 inhibitors |
| CA3150681A1 (en) | 2019-08-14 | 2021-02-18 | Incyte Corporation | Imidazolyl pyrimidinylamine compounds as cdk2 inhibitors |
| WO2021072232A1 (en) | 2019-10-11 | 2021-04-15 | Incyte Corporation | Bicyclic amines as cdk2 inhibitors |
| US11981671B2 (en) | 2021-06-21 | 2024-05-14 | Incyte Corporation | Bicyclic pyrazolyl amines as CDK2 inhibitors |
| US12084453B2 (en) | 2021-12-10 | 2024-09-10 | Incyte Corporation | Bicyclic amines as CDK12 inhibitors |
| US11976073B2 (en) | 2021-12-10 | 2024-05-07 | Incyte Corporation | Bicyclic amines as CDK2 inhibitors |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9523675D0 (en) * | 1995-11-20 | 1996-01-24 | Celltech Therapeutics Ltd | Chemical compounds |
| GB9914258D0 (en) * | 1999-06-18 | 1999-08-18 | Celltech Therapeutics Ltd | Chemical compounds |
| GB9924862D0 (en) * | 1999-10-20 | 1999-12-22 | Celltech Therapeutics Ltd | Chemical compounds |
| MY130778A (en) * | 2001-02-09 | 2007-07-31 | Vertex Pharma | Heterocyclic inhibitiors of erk2 and uses thereof |
| WO2002079197A1 (en) * | 2001-03-29 | 2002-10-10 | Vertex Pharmaceuticals Incorporated | Inhibitors of c-jun n-terminal kinases (jnk) and other protein kinases |
| MXPA03009378A (es) * | 2001-04-13 | 2004-01-29 | Vertex Pharma | Inhibidores de cinasas c-jun n-terminales (jnk) y otras proteinas cinasas. |
| JP4316893B2 (ja) * | 2001-05-16 | 2009-08-19 | バーテックス ファーマシューティカルズ インコーポレイテッド | Srcおよび他のプロテインキナーゼのインヒビター |
| US6762179B2 (en) * | 2001-05-31 | 2004-07-13 | Vertex Pharmaceuticals Incorporated | Thiazole compounds useful as inhibitors of protein kinase |
| US20030207873A1 (en) * | 2002-04-10 | 2003-11-06 | Edmund Harrington | Inhibitors of Src and other protein kinases |
-
2002
- 2002-05-23 WO PCT/US2002/016352 patent/WO2002096905A1/en not_active Ceased
- 2002-05-23 AT AT02737123T patent/ATE339418T1/de not_active IP Right Cessation
- 2002-05-23 DE DE60214703T patent/DE60214703T2/de not_active Expired - Lifetime
- 2002-05-23 EP EP02737123A patent/EP1392684B1/de not_active Expired - Lifetime
- 2002-05-23 ES ES02737123T patent/ES2274035T3/es not_active Expired - Lifetime
- 2002-05-23 JP JP2003500084A patent/JP4523271B2/ja not_active Expired - Fee Related
- 2002-05-23 CA CA2446756A patent/CA2446756C/en not_active Expired - Fee Related
-
2004
- 2004-07-13 US US10/891,912 patent/US7256190B2/en not_active Expired - Fee Related
-
2007
- 2007-06-15 US US11/763,693 patent/US7488727B2/en not_active Expired - Fee Related
-
2009
- 2009-08-21 JP JP2009192633A patent/JP2009269932A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP1392684A1 (de) | 2004-03-03 |
| CA2446756A1 (en) | 2002-12-05 |
| WO2002096905A1 (en) | 2002-12-05 |
| JP4523271B2 (ja) | 2010-08-11 |
| US20050004152A1 (en) | 2005-01-06 |
| DE60214703D1 (de) | 2006-10-26 |
| WO2002096905A8 (en) | 2005-07-28 |
| CA2446756C (en) | 2011-03-08 |
| JP2006516110A (ja) | 2006-06-22 |
| ATE339418T1 (de) | 2006-10-15 |
| US20070249645A1 (en) | 2007-10-25 |
| JP2009269932A (ja) | 2009-11-19 |
| HK1065033A1 (en) | 2005-02-08 |
| US7488727B2 (en) | 2009-02-10 |
| US7256190B2 (en) | 2007-08-14 |
| EP1392684B1 (de) | 2006-09-13 |
| ES2274035T3 (es) | 2007-05-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60214703T2 (de) | Thiazolverbindungen, die sich als inhibitoren von proteinkinasen eignen | |
| DE60126658T2 (de) | Pyrazolverbindungen als proteinkinasehemmer | |
| DE60214198T2 (de) | Isoxazolyl-pyrimidines als inhibitoren von src- und lck-protein-kinasen | |
| DE60122176T2 (de) | Isoxazole und ihre verwendung als erk-inhibitoren | |
| DE60314603T2 (de) | Zusammensetzungen brauchbar als protein-kinase-inhibitoren | |
| EP1265889B1 (de) | Arzneimittel gegen virale erkrankungen | |
| DE60319430T2 (de) | Pyridino2,3-d pyrimidin-derivate als selektive kdr- und fgfr-inhibitoren | |
| DE60316013T2 (de) | Heteroaryl-pyrimidinderivate als jak-inhibitoren | |
| US6762179B2 (en) | Thiazole compounds useful as inhibitors of protein kinase | |
| DE60214701T2 (de) | Inhibitoren von c-jun-n-terminalen-kinasen (jnk) und anderen proteinkinasen | |
| DE60226154T2 (de) | Von pyrazol abgeleitete kinaseinhibitoren und deren verwendung | |
| DE60120193T2 (de) | Pyrazolverbindungen als protein-kinasehemmer | |
| DE60309701T2 (de) | 2-ureido-6-heteroaryl-3h-benzoimidazol-4-carbonsäurederivate und verwandte verbindungen als gyrase und/oder topoisomerase iv inhibitoren zur behandlung von bakteriellen infektionen | |
| DE60319255T2 (de) | Pyrimidoverbindungen mit antiproliferativer wirkung | |
| DE10013126A1 (de) | Arzneimittel gegen virale Erkrankungen | |
| DE60129154T2 (de) | Neuartige verbindungen | |
| JP2007513172A (ja) | 複素環式プロテインキナーゼインヒビターおよびその使用 | |
| DE102010034699A1 (de) | Pyrimidinderivate | |
| WO2001045712A1 (de) | Arzneimittelkombinationen gegen virale erkrankungen | |
| DE10012824A1 (de) | Arzneimittel gegen virale Erkrankungen | |
| DE10013125A1 (de) | Arzneimittel gegen virale Erkrankungen | |
| DE60226225T2 (de) | Phtalazine derivate mit angiogenesis inhibierender wirkung | |
| DE60110592T2 (de) | Pharmazeutische zusammensetzung enthaltend ein farnesyl-transferase hemmenden 1,2-annellierten chinolin enantiomer | |
| WO1998032755A1 (de) | Purindione als phosphodiesterasehemmer | |
| HK1065033B (en) | Thiazole compounds useful as inhibitors of protein kinases |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition |