KR20140028062A - Syk 억제제로서의 아미노피리미딘 - Google Patents
Syk 억제제로서의 아미노피리미딘 Download PDFInfo
- Publication number
- KR20140028062A KR20140028062A KR1020137032289A KR20137032289A KR20140028062A KR 20140028062 A KR20140028062 A KR 20140028062A KR 1020137032289 A KR1020137032289 A KR 1020137032289A KR 20137032289 A KR20137032289 A KR 20137032289A KR 20140028062 A KR20140028062 A KR 20140028062A
- Authority
- KR
- South Korea
- Prior art keywords
- mmol
- methyl
- thiazol
- ethyl
- amino
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000003112 inhibitor Substances 0.000 title abstract description 52
- 150000005005 aminopyrimidines Chemical class 0.000 title 1
- -1 pyrimidine amines Chemical class 0.000 claims abstract description 170
- 238000011282 treatment Methods 0.000 claims abstract description 25
- 208000006673 asthma Diseases 0.000 claims abstract description 19
- 206010039073 rheumatoid arthritis Diseases 0.000 claims abstract description 18
- 230000001404 mediated effect Effects 0.000 claims abstract description 17
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 14
- 201000011510 cancer Diseases 0.000 claims abstract description 10
- 150000001875 compounds Chemical class 0.000 claims description 138
- 150000003839 salts Chemical class 0.000 claims description 63
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 48
- 125000000217 alkyl group Chemical group 0.000 claims description 42
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 36
- 229910052799 carbon Inorganic materials 0.000 claims description 29
- 239000008194 pharmaceutical composition Substances 0.000 claims description 28
- 229910052739 hydrogen Inorganic materials 0.000 claims description 24
- 201000010099 disease Diseases 0.000 claims description 23
- 238000000034 method Methods 0.000 claims description 22
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 13
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 12
- 229910052736 halogen Inorganic materials 0.000 claims description 11
- 150000002367 halogens Chemical class 0.000 claims description 11
- 239000003937 drug carrier Substances 0.000 claims description 5
- 125000002853 C1-C4 hydroxyalkyl group Chemical group 0.000 claims description 4
- 125000003545 alkoxy group Chemical group 0.000 claims description 4
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 4
- 150000001721 carbon Chemical group 0.000 claims description 3
- 125000006367 bivalent amino carbonyl group Chemical group [H]N([*:1])C([*:2])=O 0.000 claims description 2
- 230000002265 prevention Effects 0.000 claims description 2
- 125000003831 tetrazolyl group Chemical group 0.000 claims description 2
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 abstract description 9
- 102000000551 Syk Kinase Human genes 0.000 abstract description 9
- 108010016672 Syk Kinase Proteins 0.000 abstract description 9
- 230000006806 disease prevention Effects 0.000 abstract description 4
- 102000004190 Enzymes Human genes 0.000 abstract description 3
- 108090000790 Enzymes Proteins 0.000 abstract description 3
- 230000003389 potentiating effect Effects 0.000 abstract description 2
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 276
- 239000000203 mixture Substances 0.000 description 166
- 239000000243 solution Substances 0.000 description 143
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 133
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 118
- 235000019439 ethyl acetate Nutrition 0.000 description 112
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 108
- 238000006243 chemical reaction Methods 0.000 description 108
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical group ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 101
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 96
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 92
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 84
- 239000000741 silica gel Substances 0.000 description 61
- 229910002027 silica gel Inorganic materials 0.000 description 61
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 56
- 239000011541 reaction mixture Substances 0.000 description 51
- 239000012044 organic layer Substances 0.000 description 50
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 49
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 49
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 48
- NZNMSOFKMUBTKW-UHFFFAOYSA-N Cyclohexanecarboxylic acid Natural products OC(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-N 0.000 description 44
- 239000000543 intermediate Substances 0.000 description 44
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 43
- 239000012267 brine Substances 0.000 description 43
- 239000010410 layer Substances 0.000 description 43
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 43
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 42
- 235000019341 magnesium sulphate Nutrition 0.000 description 42
- NZNMSOFKMUBTKW-UHFFFAOYSA-M cyclohexanecarboxylate Chemical compound [O-]C(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-M 0.000 description 37
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 36
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 34
- 238000004587 chromatography analysis Methods 0.000 description 32
- 230000002829 reductive effect Effects 0.000 description 32
- 239000007787 solid Substances 0.000 description 32
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 30
- VZFUCHSFHOYXIS-UHFFFAOYSA-N cycloheptane carboxylic acid Natural products OC(=O)C1CCCCCC1 VZFUCHSFHOYXIS-UHFFFAOYSA-N 0.000 description 29
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 28
- 230000000694 effects Effects 0.000 description 25
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 25
- 229910052938 sodium sulfate Inorganic materials 0.000 description 25
- 235000011152 sodium sulphate Nutrition 0.000 description 25
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 24
- 238000007792 addition Methods 0.000 description 22
- 239000000460 chlorine Substances 0.000 description 22
- 239000003921 oil Substances 0.000 description 22
- 239000000047 product Substances 0.000 description 22
- 238000003756 stirring Methods 0.000 description 22
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 22
- 235000019198 oils Nutrition 0.000 description 21
- 238000000746 purification Methods 0.000 description 21
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 20
- 238000003818 flash chromatography Methods 0.000 description 20
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 20
- 239000012453 solvate Substances 0.000 description 20
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 19
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 19
- 239000000843 powder Substances 0.000 description 19
- 229910052757 nitrogen Inorganic materials 0.000 description 18
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 17
- 235000011121 sodium hydroxide Nutrition 0.000 description 17
- 239000000725 suspension Substances 0.000 description 17
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 16
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 16
- 239000012074 organic phase Substances 0.000 description 16
- 229920006395 saturated elastomer Polymers 0.000 description 16
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 15
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 15
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Natural products CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 14
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 14
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 14
- 206010039085 Rhinitis allergic Diseases 0.000 description 14
- 201000010105 allergic rhinitis Diseases 0.000 description 14
- 239000012530 fluid Substances 0.000 description 14
- 238000009472 formulation Methods 0.000 description 14
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 14
- 239000008101 lactose Substances 0.000 description 14
- 229960001375 lactose Drugs 0.000 description 14
- 239000011734 sodium Substances 0.000 description 14
- 239000002904 solvent Substances 0.000 description 14
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 13
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 13
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 13
- 208000035475 disorder Diseases 0.000 description 13
- 239000003814 drug Substances 0.000 description 13
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 13
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 12
- 229910052786 argon Inorganic materials 0.000 description 12
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 12
- 239000012071 phase Substances 0.000 description 12
- 238000004808 supercritical fluid chromatography Methods 0.000 description 12
- UNCQVRBWJWWJBF-UHFFFAOYSA-N 2-chloropyrimidine Chemical compound ClC1=NC=CC=N1 UNCQVRBWJWWJBF-UHFFFAOYSA-N 0.000 description 11
- 239000002253 acid Substances 0.000 description 11
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 11
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 11
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 10
- 210000003719 b-lymphocyte Anatomy 0.000 description 10
- 238000012512 characterization method Methods 0.000 description 10
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 10
- 239000003607 modifier Substances 0.000 description 10
- 239000002245 particle Substances 0.000 description 10
- 239000000377 silicon dioxide Substances 0.000 description 10
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 10
- 208000023275 Autoimmune disease Diseases 0.000 description 9
- 101150003085 Pdcl gene Proteins 0.000 description 9
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 9
- 239000012230 colorless oil Substances 0.000 description 9
- 238000004440 column chromatography Methods 0.000 description 9
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 9
- 239000002552 dosage form Substances 0.000 description 9
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 9
- 239000000546 pharmaceutical excipient Substances 0.000 description 9
- 230000002441 reversible effect Effects 0.000 description 9
- 125000001424 substituent group Chemical group 0.000 description 9
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 9
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 8
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 8
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 8
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 8
- 239000000443 aerosol Substances 0.000 description 8
- 150000001336 alkenes Chemical class 0.000 description 8
- 238000001816 cooling Methods 0.000 description 8
- 238000002425 crystallisation Methods 0.000 description 8
- 230000008025 crystallization Effects 0.000 description 8
- 125000000753 cycloalkyl group Chemical group 0.000 description 8
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 8
- 239000000706 filtrate Substances 0.000 description 8
- 239000008241 heterogeneous mixture Substances 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- 238000010992 reflux Methods 0.000 description 8
- 229910000029 sodium carbonate Inorganic materials 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- XMYKNCNAZKMVQN-UHFFFAOYSA-N 3-aminopyridine-2-carboxaldehyde thiosemicarbazone Chemical compound NC(=S)NN=CC1=NC=CC=C1N XMYKNCNAZKMVQN-UHFFFAOYSA-N 0.000 description 7
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 7
- 108010087819 Fc receptors Proteins 0.000 description 7
- 102000009109 Fc receptors Human genes 0.000 description 7
- 206010020751 Hypersensitivity Diseases 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 7
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 7
- 230000011664 signaling Effects 0.000 description 7
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 7
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 6
- 208000031981 Thrombocytopenic Idiopathic Purpura Diseases 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 6
- 150000001412 amines Chemical class 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 238000004128 high performance liquid chromatography Methods 0.000 description 6
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 6
- 230000007062 hydrolysis Effects 0.000 description 6
- 238000006460 hydrolysis reaction Methods 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 229940098779 methanesulfonic acid Drugs 0.000 description 6
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 6
- 230000001225 therapeutic effect Effects 0.000 description 6
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 6
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 6
- FZRBTBCCMVNZBD-UHFFFAOYSA-N 2-chloro-4-(trifluoromethyl)pyrimidine Chemical compound FC(F)(F)C1=CC=NC(Cl)=N1 FZRBTBCCMVNZBD-UHFFFAOYSA-N 0.000 description 5
- VMMAHBOAJLYGKQ-HAQNSBGRSA-N CCCCOC(=O)[C@H]1CC[C@H](C(C)=O)CC1 Chemical compound CCCCOC(=O)[C@H]1CC[C@H](C(C)=O)CC1 VMMAHBOAJLYGKQ-HAQNSBGRSA-N 0.000 description 5
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 5
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical class [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 5
- 229920002472 Starch Polymers 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 208000026935 allergic disease Diseases 0.000 description 5
- 201000003710 autoimmune thrombocytopenic purpura Diseases 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 230000003915 cell function Effects 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 239000003085 diluting agent Substances 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 210000003630 histaminocyte Anatomy 0.000 description 5
- 239000004615 ingredient Substances 0.000 description 5
- 150000002576 ketones Chemical class 0.000 description 5
- DBTNVRCCIDISMV-UHFFFAOYSA-L lithium;magnesium;propane;dichloride Chemical compound [Li+].[Mg+2].[Cl-].[Cl-].C[CH-]C DBTNVRCCIDISMV-UHFFFAOYSA-L 0.000 description 5
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 5
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 5
- 231100000252 nontoxic Toxicity 0.000 description 5
- 230000003000 nontoxic effect Effects 0.000 description 5
- 235000011056 potassium acetate Nutrition 0.000 description 5
- 125000006239 protecting group Chemical group 0.000 description 5
- 230000019491 signal transduction Effects 0.000 description 5
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 5
- 235000017557 sodium bicarbonate Nutrition 0.000 description 5
- 235000010265 sodium sulphite Nutrition 0.000 description 5
- 239000008107 starch Substances 0.000 description 5
- 235000019698 starch Nutrition 0.000 description 5
- 229940124597 therapeutic agent Drugs 0.000 description 5
- FPVKHBSQESCIEP-UHFFFAOYSA-N (8S)-3-(2-deoxy-beta-D-erythro-pentofuranosyl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol Natural products C1C(O)C(CO)OC1N1C(NC=NCC2O)=C2N=C1 FPVKHBSQESCIEP-UHFFFAOYSA-N 0.000 description 4
- BTTNYQZNBZNDOR-UHFFFAOYSA-N 2,4-dichloropyrimidine Chemical compound ClC1=CC=NC(Cl)=N1 BTTNYQZNBZNDOR-UHFFFAOYSA-N 0.000 description 4
- BZHGSZDEICTDRN-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-1-methylcyclohexan-1-ol Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(C)(O)CC2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 BZHGSZDEICTDRN-UHFFFAOYSA-N 0.000 description 4
- OZBUFFXESDBEHG-FXILSDISSA-N 4-[[(2e,4e,6e,8e)-3,7-dimethyl-9-(2,6,6-trimethylcyclohexen-1-yl)nona-2,4,6,8-tetraenoyl]amino]benzoic acid Chemical compound C=1C=C(C(O)=O)C=CC=1NC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OZBUFFXESDBEHG-FXILSDISSA-N 0.000 description 4
- DWUPYMSVAPQXMS-UHFFFAOYSA-N 5-bromo-1,3-thiazole Chemical compound BrC1=CN=CS1 DWUPYMSVAPQXMS-UHFFFAOYSA-N 0.000 description 4
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Natural products N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 4
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 4
- 206010009900 Colitis ulcerative Diseases 0.000 description 4
- 206010010741 Conjunctivitis Diseases 0.000 description 4
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 4
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 4
- HKVAMNSJSFKALM-GKUWKFKPSA-N Everolimus Chemical compound C1C[C@@H](OCCO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 HKVAMNSJSFKALM-GKUWKFKPSA-N 0.000 description 4
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 4
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 4
- 206010021143 Hypoxia Diseases 0.000 description 4
- 206010021245 Idiopathic thrombocytopenic purpura Diseases 0.000 description 4
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical group COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 4
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- LFTLOKWAGJYHHR-UHFFFAOYSA-N N-methylmorpholine N-oxide Chemical compound CN1(=O)CCOCC1 LFTLOKWAGJYHHR-UHFFFAOYSA-N 0.000 description 4
- 201000004681 Psoriasis Diseases 0.000 description 4
- 206010039710 Scleroderma Diseases 0.000 description 4
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 4
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 4
- 201000006704 Ulcerative Colitis Diseases 0.000 description 4
- 239000013543 active substance Substances 0.000 description 4
- 235000019270 ammonium chloride Nutrition 0.000 description 4
- 230000001363 autoimmune Effects 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 239000012455 biphasic mixture Substances 0.000 description 4
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 4
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 238000004132 cross linking Methods 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 4
- JBDSSBMEKXHSJF-UHFFFAOYSA-M cyclopentanecarboxylate Chemical compound [O-]C(=O)C1CCCC1 JBDSSBMEKXHSJF-UHFFFAOYSA-M 0.000 description 4
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 229960000684 cytarabine Drugs 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- AXAZMDOAUQTMOW-UHFFFAOYSA-N dimethylzinc Chemical compound C[Zn]C AXAZMDOAUQTMOW-UHFFFAOYSA-N 0.000 description 4
- 239000007884 disintegrant Substances 0.000 description 4
- 238000010828 elution Methods 0.000 description 4
- FJKIXWOMBXYWOQ-UHFFFAOYSA-N ethenoxyethane Chemical compound CCOC=C FJKIXWOMBXYWOQ-UHFFFAOYSA-N 0.000 description 4
- MNJVRJDLRVPLFE-UHFFFAOYSA-N etoricoxib Chemical compound C1=NC(C)=CC=C1C1=NC=C(Cl)C=C1C1=CC=C(S(C)(=O)=O)C=C1 MNJVRJDLRVPLFE-UHFFFAOYSA-N 0.000 description 4
- 239000012065 filter cake Substances 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 125000001188 haloalkyl group Chemical group 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 239000001257 hydrogen Substances 0.000 description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 229940043355 kinase inhibitor Drugs 0.000 description 4
- 239000000314 lubricant Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000002480 mineral oil Substances 0.000 description 4
- 235000010446 mineral oil Nutrition 0.000 description 4
- WOFMFGQZHJDGCX-ZULDAHANSA-N mometasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(Cl)[C@@]4(C)C=CC(=O)C=C4CC[C@H]3[C@@H]2C[C@H]1C)C(=O)CCl)C(=O)C1=CC=CO1 WOFMFGQZHJDGCX-ZULDAHANSA-N 0.000 description 4
- NAOFLFFIGTWCPY-UHFFFAOYSA-N n-[3-methyl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound C=1C(B2OC(C)(C)C(C)(C)O2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 NAOFLFFIGTWCPY-UHFFFAOYSA-N 0.000 description 4
- 229910000489 osmium tetroxide Inorganic materials 0.000 description 4
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 4
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 4
- FPVKHBSQESCIEP-JQCXWYLXSA-N pentostatin Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC[C@H]2O)=C2N=C1 FPVKHBSQESCIEP-JQCXWYLXSA-N 0.000 description 4
- 229960002340 pentostatin Drugs 0.000 description 4
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 4
- UAJUXJSXCLUTNU-UHFFFAOYSA-N pranlukast Chemical compound C=1C=C(OCCCCC=2C=CC=CC=2)C=CC=1C(=O)NC(C=1)=CC=C(C(C=2)=O)C=1OC=2C=1N=NNN=1 UAJUXJSXCLUTNU-UHFFFAOYSA-N 0.000 description 4
- 229940002612 prodrug Drugs 0.000 description 4
- 239000000651 prodrug Substances 0.000 description 4
- 229960004641 rituximab Drugs 0.000 description 4
- BPRHUIZQVSMCRT-VEUZHWNKSA-N rosuvastatin Chemical compound CC(C)C1=NC(N(C)S(C)(=O)=O)=NC(C=2C=CC(F)=CC=2)=C1\C=C\[C@@H](O)C[C@@H](O)CC(O)=O BPRHUIZQVSMCRT-VEUZHWNKSA-N 0.000 description 4
- 229960004017 salmeterol Drugs 0.000 description 4
- 238000010898 silica gel chromatography Methods 0.000 description 4
- 239000002002 slurry Substances 0.000 description 4
- 229910000104 sodium hydride Inorganic materials 0.000 description 4
- 208000011580 syndromic disease Diseases 0.000 description 4
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 4
- 229960003087 tioguanine Drugs 0.000 description 4
- MNRILEROXIRVNJ-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=NC=N[C]21 MNRILEROXIRVNJ-UHFFFAOYSA-N 0.000 description 4
- 230000009466 transformation Effects 0.000 description 4
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 4
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 4
- 239000003039 volatile agent Substances 0.000 description 4
- YIZRPAWCIFTHNA-UHFFFAOYSA-N 3-bromo-5-methylaniline Chemical compound CC1=CC(N)=CC(Br)=C1 YIZRPAWCIFTHNA-UHFFFAOYSA-N 0.000 description 3
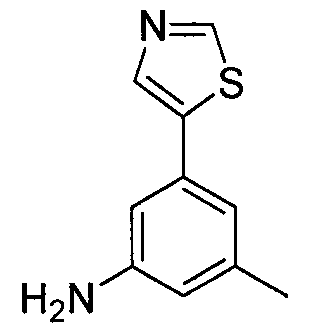
- VLUHONKZQKGGOJ-UHFFFAOYSA-N 3-methyl-5-(1,3-thiazol-5-yl)aniline Chemical compound CC1=CC(N)=CC(C=2SC=NC=2)=C1 VLUHONKZQKGGOJ-UHFFFAOYSA-N 0.000 description 3
- VGEGVYAUXCVIKQ-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-1-methylcyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(C)(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 VGEGVYAUXCVIKQ-UHFFFAOYSA-N 0.000 description 3
- XPGYMSWIVDGLSA-UHFFFAOYSA-N 4-[hydroxy-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]-3,3-dimethylcyclohexan-1-ol Chemical compound C=1C(C=2SC(=NC=2)C(O)C2C(CC(O)CC2)(C)C)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 XPGYMSWIVDGLSA-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 3
- 102000015790 Asparaginase Human genes 0.000 description 3
- 108010024976 Asparaginase Proteins 0.000 description 3
- 108091008875 B cell receptors Proteins 0.000 description 3
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 3
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 3
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 208000011231 Crohn disease Diseases 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 3
- 108010092160 Dactinomycin Proteins 0.000 description 3
- 201000004624 Dermatitis Diseases 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 108091000080 Phosphotransferase Proteins 0.000 description 3
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 3
- 206010057190 Respiratory tract infections Diseases 0.000 description 3
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 3
- 238000006069 Suzuki reaction reaction Methods 0.000 description 3
- CBPNZQVSJQDFBE-FUXHJELOSA-N Temsirolimus Chemical compound C1C[C@@H](OC(=O)C(C)(CO)CO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 CBPNZQVSJQDFBE-FUXHJELOSA-N 0.000 description 3
- 229940123464 Thiazolidinedione Drugs 0.000 description 3
- 208000007536 Thrombosis Diseases 0.000 description 3
- 102000004357 Transferases Human genes 0.000 description 3
- 108090000992 Transferases Proteins 0.000 description 3
- 206010052779 Transplant rejections Diseases 0.000 description 3
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 3
- OKJPEAGHQZHRQV-UHFFFAOYSA-N Triiodomethane Natural products IC(I)I OKJPEAGHQZHRQV-UHFFFAOYSA-N 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 208000024780 Urticaria Diseases 0.000 description 3
- 229940022663 acetate Drugs 0.000 description 3
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 3
- 239000000048 adrenergic agonist Substances 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 201000009961 allergic asthma Diseases 0.000 description 3
- 230000000172 allergic effect Effects 0.000 description 3
- 229960003272 asparaginase Drugs 0.000 description 3
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 208000010668 atopic eczema Diseases 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 3
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 3
- 206010006451 bronchitis Diseases 0.000 description 3
- 229960004117 capecitabine Drugs 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 230000004663 cell proliferation Effects 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- IMZMKUWMOSJXDT-UHFFFAOYSA-N cromoglycic acid Chemical compound O1C(C(O)=O)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=CC=CC2=C1C(=O)C=C(C(O)=O)O2 IMZMKUWMOSJXDT-UHFFFAOYSA-N 0.000 description 3
- XUUBDTZZIFDAPD-KXNXZCPBSA-N cyclohexanecarboxylic acid;(1s,2s)-2-(methylamino)-1-phenylpropan-1-ol Chemical compound OC(=O)C1CCCCC1.CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 XUUBDTZZIFDAPD-KXNXZCPBSA-N 0.000 description 3
- 229960004397 cyclophosphamide Drugs 0.000 description 3
- 229960000640 dactinomycin Drugs 0.000 description 3
- 229960000975 daunorubicin Drugs 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- ZOCHARZZJNPSEU-UHFFFAOYSA-N diboron Chemical compound B#B ZOCHARZZJNPSEU-UHFFFAOYSA-N 0.000 description 3
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Chemical group CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 3
- 238000005906 dihydroxylation reaction Methods 0.000 description 3
- 150000002009 diols Chemical class 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 229960000390 fludarabine Drugs 0.000 description 3
- 229960000289 fluticasone propionate Drugs 0.000 description 3
- WMWTYOKRWGGJOA-CENSZEJFSA-N fluticasone propionate Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O WMWTYOKRWGGJOA-CENSZEJFSA-N 0.000 description 3
- 235000013355 food flavoring agent Nutrition 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 3
- 229960005277 gemcitabine Drugs 0.000 description 3
- 238000005469 granulation Methods 0.000 description 3
- 230000003179 granulation Effects 0.000 description 3
- 238000002868 homogeneous time resolved fluorescence Methods 0.000 description 3
- 230000007954 hypoxia Effects 0.000 description 3
- 239000005457 ice water Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 208000027866 inflammatory disease Diseases 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 3
- 206010023332 keratitis Diseases 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229910052749 magnesium Inorganic materials 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 229960004961 mechlorethamine Drugs 0.000 description 3
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical compound ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 description 3
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 3
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 3
- 229960000485 methotrexate Drugs 0.000 description 3
- LSEFCHWGJNHZNT-UHFFFAOYSA-M methyl(triphenyl)phosphanium;bromide Chemical compound [Br-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(C)C1=CC=CC=C1 LSEFCHWGJNHZNT-UHFFFAOYSA-M 0.000 description 3
- 201000006417 multiple sclerosis Diseases 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- LLCYYUOGLULSRC-UHFFFAOYSA-N n-(3-bromo-5-methylphenyl)-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound CC1=CC(Br)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 LLCYYUOGLULSRC-UHFFFAOYSA-N 0.000 description 3
- HUASEJWIDXNZRZ-UHFFFAOYSA-N n-[3-methyl-5-(1,3-thiazol-5-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound C=1C(C=2SC=NC=2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 HUASEJWIDXNZRZ-UHFFFAOYSA-N 0.000 description 3
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 210000000440 neutrophil Anatomy 0.000 description 3
- 239000012299 nitrogen atmosphere Substances 0.000 description 3
- 230000000414 obstructive effect Effects 0.000 description 3
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 3
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 3
- 239000010452 phosphate Substances 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 102000020233 phosphotransferase Human genes 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 239000011591 potassium Substances 0.000 description 3
- 229910052700 potassium Inorganic materials 0.000 description 3
- 229910000027 potassium carbonate Inorganic materials 0.000 description 3
- 230000000770 proinflammatory effect Effects 0.000 description 3
- 239000003380 propellant Substances 0.000 description 3
- LJXQPZWIHJMPQQ-UHFFFAOYSA-N pyrimidin-2-amine Chemical compound NC1=NC=CC=N1 LJXQPZWIHJMPQQ-UHFFFAOYSA-N 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 239000012312 sodium hydride Substances 0.000 description 3
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical class [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000002889 sympathetic effect Effects 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- 229960000235 temsirolimus Drugs 0.000 description 3
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 230000001732 thrombotic effect Effects 0.000 description 3
- 238000000844 transformation Methods 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 3
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 2
- VZUKBNZKASVATD-RQJHMYQMSA-N (1r,3s)-3-acetyl-2,2-dimethylcyclobutane-1-carboxylic acid Chemical compound CC(=O)[C@H]1C[C@@H](C(O)=O)C1(C)C VZUKBNZKASVATD-RQJHMYQMSA-N 0.000 description 2
- IYXUFOCLMOXQSL-UHFFFAOYSA-N (2,2-difluoroacetyl) 2,2-difluoroacetate Chemical compound FC(F)C(=O)OC(=O)C(F)F IYXUFOCLMOXQSL-UHFFFAOYSA-N 0.000 description 2
- XXYGHWQHTRONLX-UHFFFAOYSA-N 1,4-dioxaspiro[4.5]decan-8-yl-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methanol Chemical compound C=1C(C=2SC(=NC=2)C(O)C2CCC3(CC2)OCCO3)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 XXYGHWQHTRONLX-UHFFFAOYSA-N 0.000 description 2
- HJTAZXHBEBIQQX-UHFFFAOYSA-N 1,5-bis(chloromethyl)naphthalene Chemical compound C1=CC=C2C(CCl)=CC=CC2=C1CCl HJTAZXHBEBIQQX-UHFFFAOYSA-N 0.000 description 2
- WQZYJXYZSGVBNX-UHFFFAOYSA-N 1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]-1-[4-(2h-tetrazol-5-yl)cyclohexyl]ethanol Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 WQZYJXYZSGVBNX-UHFFFAOYSA-N 0.000 description 2
- DMXVRUGSSAPNCE-UHFFFAOYSA-N 1-bromo-3-(difluoromethyl)-5-nitrobenzene Chemical compound [O-][N+](=O)C1=CC(Br)=CC(C(F)F)=C1 DMXVRUGSSAPNCE-UHFFFAOYSA-N 0.000 description 2
- 125000004776 1-fluoroethyl group Chemical group [H]C([H])([H])C([H])(F)* 0.000 description 2
- DGHHQBMTXTWTJV-BQAIUKQQSA-N 119413-54-6 Chemical compound Cl.C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 DGHHQBMTXTWTJV-BQAIUKQQSA-N 0.000 description 2
- 125000004778 2,2-difluoroethyl group Chemical group [H]C([H])(*)C([H])(F)F 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- YYTUPWKEZBXDOA-UHFFFAOYSA-N 2-chloro-4-(difluoromethyl)pyrimidine Chemical compound FC(F)C1=CC=NC(Cl)=N1 YYTUPWKEZBXDOA-UHFFFAOYSA-N 0.000 description 2
- NWKPCTJWFJSBAY-UHFFFAOYSA-N 2-chloro-4-propan-2-yloxypyrimidine Chemical compound CC(C)OC1=CC=NC(Cl)=N1 NWKPCTJWFJSBAY-UHFFFAOYSA-N 0.000 description 2
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 2
- APOYTRAZFJURPB-UHFFFAOYSA-N 2-methoxy-n-(2-methoxyethyl)-n-(trifluoro-$l^{4}-sulfanyl)ethanamine Chemical compound COCCN(S(F)(F)F)CCOC APOYTRAZFJURPB-UHFFFAOYSA-N 0.000 description 2
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 2
- OMHYJQZNAXHGQH-UHFFFAOYSA-N 3-bromo-5-(difluoromethyl)aniline Chemical compound NC1=CC(Br)=CC(C(F)F)=C1 OMHYJQZNAXHGQH-UHFFFAOYSA-N 0.000 description 2
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 2
- CHEAWEQNYGMNIW-UHFFFAOYSA-N 4-[1-[5-[3-(difluoromethyl)-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=2)C(F)F)SC=1C(O)(C)C1CCC(C(O)=O)CC1 CHEAWEQNYGMNIW-UHFFFAOYSA-N 0.000 description 2
- SLIJRVWIGDCBNY-UHFFFAOYSA-N 4-[2-fluoro-1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(CF)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 SLIJRVWIGDCBNY-UHFFFAOYSA-N 0.000 description 2
- KYYIFVGLZAJMDL-UHFFFAOYSA-N 4-[[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(CC3CCC(CC3)C(O)=O)=NC=2)=CC(C)=CC=1NC1=NC=CC(C)=N1 KYYIFVGLZAJMDL-UHFFFAOYSA-N 0.000 description 2
- QLAPEAYGMXJPRF-UHFFFAOYSA-N 4-[hydroxy-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxamide Chemical compound C=1C(C=2SC(=NC=2)C(O)C2CCC(CC2)C(N)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 QLAPEAYGMXJPRF-UHFFFAOYSA-N 0.000 description 2
- JMIDSPIKSGTNFP-UHFFFAOYSA-N 4-[hydroxy-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 JMIDSPIKSGTNFP-UHFFFAOYSA-N 0.000 description 2
- AQUYZYWOJKHFFX-UHFFFAOYSA-N 4-acetylcyclohexane-1-carbonitrile Chemical compound CC(=O)C1CCC(C#N)CC1 AQUYZYWOJKHFFX-UHFFFAOYSA-N 0.000 description 2
- TVZGACDUOSZQKY-LBPRGKRZSA-N 4-aminofolic acid Chemical compound C1=NC2=NC(N)=NC(N)=C2N=C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 TVZGACDUOSZQKY-LBPRGKRZSA-N 0.000 description 2
- RNYOUYQUNNCUQB-UHFFFAOYSA-N 4-cyclopropyl-5-fluoro-n-[3-methyl-5-(1,3-thiazol-5-yl)phenyl]pyrimidin-2-amine Chemical compound C=1C(C=2SC=NC=2)=CC(C)=CC=1NC(N=1)=NC=C(F)C=1C1CC1 RNYOUYQUNNCUQB-UHFFFAOYSA-N 0.000 description 2
- CMSGDCCPUJIGNT-UHFFFAOYSA-N 4-methoxycarbonyl-4-methylcyclohexane-1-carboxylic acid Chemical compound COC(=O)C1(C)CCC(C(O)=O)CC1 CMSGDCCPUJIGNT-UHFFFAOYSA-N 0.000 description 2
- PNGFYXGXKPJJJS-UHFFFAOYSA-N 4-methyl-n-[3-methyl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]pyrimidin-2-amine Chemical compound C=1C(B2OC(C)(C)C(C)(C)O2)=CC(C)=CC=1NC1=NC=CC(C)=N1 PNGFYXGXKPJJJS-UHFFFAOYSA-N 0.000 description 2
- IDPUKCWIGUEADI-UHFFFAOYSA-N 5-[bis(2-chloroethyl)amino]uracil Chemical compound ClCCN(CCCl)C1=CNC(=O)NC1=O IDPUKCWIGUEADI-UHFFFAOYSA-N 0.000 description 2
- XAUDJQYHKZQPEU-KVQBGUIXSA-N 5-aza-2'-deoxycytidine Chemical compound O=C1N=C(N)N=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 XAUDJQYHKZQPEU-KVQBGUIXSA-N 0.000 description 2
- ICSLJIQRUZFXPE-UHFFFAOYSA-N 5-bromo-2-(bromomethyl)-1,3-thiazole Chemical compound BrCC1=NC=C(Br)S1 ICSLJIQRUZFXPE-UHFFFAOYSA-N 0.000 description 2
- AAGYYOJOECDYOQ-UHFFFAOYSA-N 5-bromo-2-(diethoxyphosphorylmethyl)-1,3-thiazole Chemical compound CCOP(=O)(OCC)CC1=NC=C(Br)S1 AAGYYOJOECDYOQ-UHFFFAOYSA-N 0.000 description 2
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- SHGAZHPCJJPHSC-ZVCIMWCZSA-N 9-cis-retinoic acid Chemical compound OC(=O)/C=C(\C)/C=C/C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-ZVCIMWCZSA-N 0.000 description 2
- BUROJSBIWGDYCN-GAUTUEMISA-N AP 23573 Chemical compound C1C[C@@H](OP(C)(C)=O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 BUROJSBIWGDYCN-GAUTUEMISA-N 0.000 description 2
- 102100033350 ATP-dependent translocase ABCB1 Human genes 0.000 description 2
- 229930024421 Adenine Natural products 0.000 description 2
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- WSVLPVUVIUVCRA-KPKNDVKVSA-N Alpha-lactose monohydrate Chemical compound O.O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O WSVLPVUVIUVCRA-KPKNDVKVSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 108020004491 Antisense DNA Proteins 0.000 description 2
- 108020005544 Antisense RNA Proteins 0.000 description 2
- 102000001381 Arachidonate 5-Lipoxygenase Human genes 0.000 description 2
- 108010093579 Arachidonate 5-lipoxygenase Proteins 0.000 description 2
- BFYIZQONLCFLEV-DAELLWKTSA-N Aromasine Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC(=C)C2=C1 BFYIZQONLCFLEV-DAELLWKTSA-N 0.000 description 2
- 201000001320 Atherosclerosis Diseases 0.000 description 2
- 208000003950 B-cell lymphoma Diseases 0.000 description 2
- 108010006654 Bleomycin Proteins 0.000 description 2
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 2
- SLIJRVWIGDCBNY-ZBVLSHQLSA-N C=1C(C=2SC(=NC=2)C(O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)C(O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 SLIJRVWIGDCBNY-ZBVLSHQLSA-N 0.000 description 2
- BHERIRZHLGQHFV-RTNKVPBISA-N C=1C(C=2SC(=NC=2)[C@@](O)(C2CC2)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)[C@@](O)(C2CC2)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 BHERIRZHLGQHFV-RTNKVPBISA-N 0.000 description 2
- SLIJRVWIGDCBNY-GTAYFMOCSA-N C=1C(C=2SC(=NC=2)[C@@](O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)[C@@](O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 SLIJRVWIGDCBNY-GTAYFMOCSA-N 0.000 description 2
- BHERIRZHLGQHFV-XVNUGVHUSA-N C=1C(C=2SC(=NC=2)[C@](O)(C2CC2)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)[C@](O)(C2CC2)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 BHERIRZHLGQHFV-XVNUGVHUSA-N 0.000 description 2
- SLIJRVWIGDCBNY-UBMNLSNXSA-N C=1C(C=2SC(=NC=2)[C@](O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)[C@](O)(CF)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 SLIJRVWIGDCBNY-UBMNLSNXSA-N 0.000 description 2
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- LUKZNWIVRBCLON-GXOBDPJESA-N Ciclesonide Chemical compound C1([C@H]2O[C@@]3([C@H](O2)C[C@@H]2[C@@]3(C[C@H](O)[C@@H]3[C@@]4(C)C=CC(=O)C=C4CC[C@H]32)C)C(=O)COC(=O)C(C)C)CCCCC1 LUKZNWIVRBCLON-GXOBDPJESA-N 0.000 description 2
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 2
- 101000582926 Dictyostelium discoideum Probable serine/threonine-protein kinase PLK Proteins 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical group COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- 108010008165 Etanercept Proteins 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- 108700012941 GNRH1 Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 description 2
- 108010069236 Goserelin Proteins 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 2
- 108010047761 Interferon-alpha Proteins 0.000 description 2
- 102000006992 Interferon-alpha Human genes 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 102000042838 JAK family Human genes 0.000 description 2
- 108091082332 JAK family Proteins 0.000 description 2
- 102000010638 Kinesin Human genes 0.000 description 2
- 108010063296 Kinesin Proteins 0.000 description 2
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 2
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 2
- 108010043135 L-methionine gamma-lyase Proteins 0.000 description 2
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 2
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 2
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 2
- 240000007472 Leucaena leucocephala Species 0.000 description 2
- 108010000817 Leuprolide Proteins 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- OUSFTKFNBAZUKL-UHFFFAOYSA-N N-(5-{[(5-tert-butyl-1,3-oxazol-2-yl)methyl]sulfanyl}-1,3-thiazol-2-yl)piperidine-4-carboxamide Chemical compound O1C(C(C)(C)C)=CN=C1CSC(S1)=CN=C1NC(=O)C1CCNCC1 OUSFTKFNBAZUKL-UHFFFAOYSA-N 0.000 description 2
- VJBOUZNIABXECL-UFXILDGNSA-N N=1C=C(Br)SC=1C(O)(C)[C@H]1CC[C@H](NS(C)(=O)=O)CC1 Chemical compound N=1C=C(Br)SC=1C(O)(C)[C@H]1CC[C@H](NS(C)(=O)=O)CC1 VJBOUZNIABXECL-UFXILDGNSA-N 0.000 description 2
- FRDNSUXMEZUIJU-WYTSPMRSSA-N N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](CO)CC1 Chemical compound N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](CO)CC1 FRDNSUXMEZUIJU-WYTSPMRSSA-N 0.000 description 2
- VFMFRAOIYNWZGI-WYTSPMRSSA-N N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](NS(C)(=O)=O)CC1 Chemical compound N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](NS(C)(=O)=O)CC1 VFMFRAOIYNWZGI-WYTSPMRSSA-N 0.000 description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 2
- 108091034117 Oligonucleotide Proteins 0.000 description 2
- 235000019502 Orange oil Nutrition 0.000 description 2
- 229930012538 Paclitaxel Natural products 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 229940079156 Proteasome inhibitor Drugs 0.000 description 2
- 102000001253 Protein Kinase Human genes 0.000 description 2
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 2
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 206010063837 Reperfusion injury Diseases 0.000 description 2
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 208000005392 Spasm Diseases 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 208000006011 Stroke Diseases 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 2
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 206010046851 Uveitis Diseases 0.000 description 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 2
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 2
- 206010047249 Venous thrombosis Diseases 0.000 description 2
- NZDMRJGAFPUTMZ-UHFFFAOYSA-N [1-(3,4-dihydroxyphenyl)-1-hydroxybutan-2-yl]azanium;chloride Chemical compound [Cl-].CCC([NH3+])C(O)C1=CC=C(O)C(O)=C1 NZDMRJGAFPUTMZ-UHFFFAOYSA-N 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- MXRQMVJXZTTXCN-WJXBOPMLSA-N [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)[C@@](C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 Chemical compound [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)[C@@](C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 MXRQMVJXZTTXCN-WJXBOPMLSA-N 0.000 description 2
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 2
- 229960000643 adenine Drugs 0.000 description 2
- 229940126157 adrenergic receptor agonist Drugs 0.000 description 2
- 239000004479 aerosol dispenser Substances 0.000 description 2
- 235000010419 agar Nutrition 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 229960001445 alitretinoin Drugs 0.000 description 2
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 2
- 239000013566 allergen Substances 0.000 description 2
- 208000002205 allergic conjunctivitis Diseases 0.000 description 2
- 230000007815 allergy Effects 0.000 description 2
- 229960000473 altretamine Drugs 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 229960003896 aminopterin Drugs 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 230000001399 anti-metabolic effect Effects 0.000 description 2
- 230000001028 anti-proliverative effect Effects 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 239000003816 antisense DNA Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- GOLCXWYRSKYTSP-UHFFFAOYSA-N arsenic trioxide Inorganic materials O1[As]2O[As]1O2 GOLCXWYRSKYTSP-UHFFFAOYSA-N 0.000 description 2
- 206010003246 arthritis Diseases 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 238000000668 atmospheric pressure chemical ionisation mass spectrometry Methods 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- 208000024998 atopic conjunctivitis Diseases 0.000 description 2
- 201000008937 atopic dermatitis Diseases 0.000 description 2
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 2
- 235000012216 bentonite Nutrition 0.000 description 2
- 239000000440 bentonite Substances 0.000 description 2
- 229910000278 bentonite Inorganic materials 0.000 description 2
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 229960001561 bleomycin Drugs 0.000 description 2
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 2
- 229960001467 bortezomib Drugs 0.000 description 2
- 230000031709 bromination Effects 0.000 description 2
- 238000005893 bromination reaction Methods 0.000 description 2
- 229960004436 budesonide Drugs 0.000 description 2
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 2
- 229910000024 caesium carbonate Inorganic materials 0.000 description 2
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 2
- 235000013539 calcium stearate Nutrition 0.000 description 2
- 239000008116 calcium stearate Substances 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 229960004562 carboplatin Drugs 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 210000000845 cartilage Anatomy 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 230000036755 cellular response Effects 0.000 description 2
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 2
- 229960004630 chlorambucil Drugs 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 229960003728 ciclesonide Drugs 0.000 description 2
- VZUKBNZKASVATD-UHFFFAOYSA-N cis-nor-pinonic acid Natural products CC(=O)C1CC(C(O)=O)C1(C)C VZUKBNZKASVATD-UHFFFAOYSA-N 0.000 description 2
- 229960002436 cladribine Drugs 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 239000003184 complementary RNA Substances 0.000 description 2
- 238000007906 compression Methods 0.000 description 2
- 230000006835 compression Effects 0.000 description 2
- 230000000875 corresponding effect Effects 0.000 description 2
- 239000003246 corticosteroid Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 229940111134 coxibs Drugs 0.000 description 2
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- VUSWCWPCANWBFG-UHFFFAOYSA-M cyclohex-3-ene-1-carboxylate Chemical compound [O-]C(=O)C1CCC=CC1 VUSWCWPCANWBFG-UHFFFAOYSA-M 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexyloxide Natural products O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 description 2
- WLVKDFJTYKELLQ-UHFFFAOYSA-N cyclopropylboronic acid Chemical compound OB(O)C1CC1 WLVKDFJTYKELLQ-UHFFFAOYSA-N 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 239000002254 cytotoxic agent Substances 0.000 description 2
- 231100000599 cytotoxic agent Toxicity 0.000 description 2
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 229960003603 decitabine Drugs 0.000 description 2
- 230000005595 deprotonation Effects 0.000 description 2
- 238000010537 deprotonation reaction Methods 0.000 description 2
- 230000002074 deregulated effect Effects 0.000 description 2
- 229910052805 deuterium Inorganic materials 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 208000037765 diseases and disorders Diseases 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 239000003534 dna topoisomerase inhibitor Substances 0.000 description 2
- 229960004679 doxorubicin Drugs 0.000 description 2
- 239000000428 dust Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 150000002118 epoxides Chemical class 0.000 description 2
- 229960001433 erlotinib Drugs 0.000 description 2
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 2
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 2
- DGKKLYPEMLTKGS-MYQWFSQQSA-N ethyl (1r,2s,4r)-4-[(1r)-1-(5-bromo-1,3-thiazol-2-yl)-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1[C@H](C)[C@H](C(=O)OCC)CC[C@H]1[C@@](C)(O)C1=NC=C(Br)S1 DGKKLYPEMLTKGS-MYQWFSQQSA-N 0.000 description 2
- DGKKLYPEMLTKGS-DZHLUBAWSA-N ethyl (1s,2r,4s)-4-[(1r)-1-(5-bromo-1,3-thiazol-2-yl)-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical class C1[C@@H](C)[C@@H](C(=O)OCC)CC[C@@H]1[C@@](C)(O)C1=NC=C(Br)S1 DGKKLYPEMLTKGS-DZHLUBAWSA-N 0.000 description 2
- JOKGYRVJJHYJRY-UHFFFAOYSA-N ethyl 3-acetylbicyclo[3.1.0]hexane-6-carboxylate Chemical compound C1C(C(C)=O)CC2C(C(=O)OCC)C21 JOKGYRVJJHYJRY-UHFFFAOYSA-N 0.000 description 2
- JDOMFPBSHJBRJR-UHFFFAOYSA-N ethyl 4-[(5-bromo-1,3-thiazol-2-yl)methylidene]cyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OCC)CCC1=CC1=NC=C(Br)S1 JDOMFPBSHJBRJR-UHFFFAOYSA-N 0.000 description 2
- UFBBTXVCZARYFX-UHFFFAOYSA-N ethyl 4-[[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]methylidene]cyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OCC)CCC1=CC1=NC=C(C=2C=C(NC=3N=C(C)C=CN=3)C=C(C)C=2)S1 UFBBTXVCZARYFX-UHFFFAOYSA-N 0.000 description 2
- ZNEPDYMOZIYBHP-UHFFFAOYSA-N ethyl 4-[hydroxy(1,3-thiazol-2-yl)methyl]cyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OCC)CCC1C(O)C1=NC=CS1 ZNEPDYMOZIYBHP-UHFFFAOYSA-N 0.000 description 2
- PRZDWMBBAYQZOR-UHFFFAOYSA-N ethyl 4-formylcyclohexane-1-carboxylate Chemical compound CCOC(=O)C1CCC(C=O)CC1 PRZDWMBBAYQZOR-UHFFFAOYSA-N 0.000 description 2
- ZXYAWONOWHSQRU-UHFFFAOYSA-N ethyl 4-oxocyclohexanecarboxylate Chemical compound CCOC(=O)C1CCC(=O)CC1 ZXYAWONOWHSQRU-UHFFFAOYSA-N 0.000 description 2
- LIQODXNTTZAGID-OCBXBXKTSA-N etoposide phosphate Chemical compound COC1=C(OP(O)(O)=O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 LIQODXNTTZAGID-OCBXBXKTSA-N 0.000 description 2
- 229960000752 etoposide phosphate Drugs 0.000 description 2
- 229960005167 everolimus Drugs 0.000 description 2
- 229960000255 exemestane Drugs 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000011049 filling Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 125000003709 fluoroalkyl group Chemical group 0.000 description 2
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 2
- 229960002848 formoterol Drugs 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 229960002584 gefitinib Drugs 0.000 description 2
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 239000003862 glucocorticoid Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 229930195712 glutamate Natural products 0.000 description 2
- 229940049906 glutamate Drugs 0.000 description 2
- KWIUHFFTVRNATP-UHFFFAOYSA-N glycine betaine Chemical compound C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 2
- 229960003690 goserelin acetate Drugs 0.000 description 2
- FFUAGWLWBBFQJT-UHFFFAOYSA-N hexamethyldisilazane Chemical compound C[Si](C)(C)N[Si](C)(C)C FFUAGWLWBBFQJT-UHFFFAOYSA-N 0.000 description 2
- UUVWYPNAQBNQJQ-UHFFFAOYSA-N hexamethylmelamine Chemical compound CN(C)C1=NC(N(C)C)=NC(N(C)C)=N1 UUVWYPNAQBNQJQ-UHFFFAOYSA-N 0.000 description 2
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- LWRDQHOZTAOILO-UHFFFAOYSA-N incadronic acid Chemical compound OP(O)(=O)C(P(O)(O)=O)NC1CCCCCC1 LWRDQHOZTAOILO-UHFFFAOYSA-N 0.000 description 2
- 229950006971 incadronic acid Drugs 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 102000006495 integrins Human genes 0.000 description 2
- 108010044426 integrins Proteins 0.000 description 2
- 229960004768 irinotecan Drugs 0.000 description 2
- GURKHSYORGJETM-WAQYZQTGSA-N irinotecan hydrochloride (anhydrous) Chemical compound Cl.C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 GURKHSYORGJETM-WAQYZQTGSA-N 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 230000000155 isotopic effect Effects 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 229960003881 letrozole Drugs 0.000 description 2
- HPJKCIUCZWXJDR-UHFFFAOYSA-N letrozole Chemical compound C1=CC(C#N)=CC=C1C(N1N=CN=C1)C1=CC=C(C#N)C=C1 HPJKCIUCZWXJDR-UHFFFAOYSA-N 0.000 description 2
- 150000002617 leukotrienes Chemical class 0.000 description 2
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 2
- 229960004338 leuprorelin Drugs 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 239000012280 lithium aluminium hydride Substances 0.000 description 2
- 206010025135 lupus erythematosus Diseases 0.000 description 2
- VFZXMEQGIIWBFJ-UHFFFAOYSA-M magnesium;cyclopropane;bromide Chemical compound [Mg+2].[Br-].C1C[CH-]1 VFZXMEQGIIWBFJ-UHFFFAOYSA-M 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 238000001819 mass spectrum Methods 0.000 description 2
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 description 2
- 229960004296 megestrol acetate Drugs 0.000 description 2
- 229960001924 melphalan Drugs 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- WSFSSNUMVMOOMR-BJUDXGSMSA-N methanone Chemical compound O=[11CH2] WSFSSNUMVMOOMR-BJUDXGSMSA-N 0.000 description 2
- SJFNDMHZXCUXSA-UHFFFAOYSA-M methoxymethyl(triphenyl)phosphanium;chloride Chemical compound [Cl-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(COC)C1=CC=CC=C1 SJFNDMHZXCUXSA-UHFFFAOYSA-M 0.000 description 2
- ZXHKOSDXLQCBGD-AATRIKPKSA-N methyl (e)-2,2-dimethyl-5-oxohex-3-enoate Chemical compound COC(=O)C(C)(C)\C=C\C(C)=O ZXHKOSDXLQCBGD-AATRIKPKSA-N 0.000 description 2
- JTNLHWBSJAHYHF-UHFFFAOYSA-N methyl 2-(2-acetylcyclopropyl)-2-methylpropanoate Chemical compound COC(=O)C(C)(C)C1CC1C(C)=O JTNLHWBSJAHYHF-UHFFFAOYSA-N 0.000 description 2
- IKBVIZKEHQOMEQ-UHFFFAOYSA-N methyl 4-acetyl-1-methylcyclohexane-1-carboxylate Chemical compound COC(=O)C1(C)CCC(C(C)=O)CC1 IKBVIZKEHQOMEQ-UHFFFAOYSA-N 0.000 description 2
- CGDYCFGASIFAAA-UHFFFAOYSA-N methyl 4-carbonochloridoyl-1-methylcyclohexane-1-carboxylate Chemical compound COC(=O)C1(C)CCC(C(Cl)=O)CC1 CGDYCFGASIFAAA-UHFFFAOYSA-N 0.000 description 2
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 2
- 231100000782 microtubule inhibitor Toxicity 0.000 description 2
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 description 2
- 229960004857 mitomycin Drugs 0.000 description 2
- 230000000394 mitotic effect Effects 0.000 description 2
- 230000008600 mitotic progression Effects 0.000 description 2
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 2
- 229960001156 mitoxantrone Drugs 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 229960002744 mometasone furoate Drugs 0.000 description 2
- 239000012452 mother liquor Substances 0.000 description 2
- UBVHBYRYYQOCPQ-UHFFFAOYSA-N n-(3-bromo-5-methylphenyl)-4-(difluoromethyl)pyrimidin-2-amine Chemical compound CC1=CC(Br)=CC(NC=2N=C(C=CN=2)C(F)F)=C1 UBVHBYRYYQOCPQ-UHFFFAOYSA-N 0.000 description 2
- BLCLNMBMMGCOAS-UHFFFAOYSA-N n-[1-[[1-[[1-[[1-[[1-[[1-[[1-[2-[(carbamoylamino)carbamoyl]pyrrolidin-1-yl]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-[(2-methylpropan-2-yl)oxy]-1-oxopropan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amin Chemical compound C1CCC(C(=O)NNC(N)=O)N1C(=O)C(CCCN=C(N)N)NC(=O)C(CC(C)C)NC(=O)C(COC(C)(C)C)NC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 BLCLNMBMMGCOAS-UHFFFAOYSA-N 0.000 description 2
- LOXPQOCJGVJSKQ-UHFFFAOYSA-N n-[3-(difluoromethyl)-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC(NC=2N=C(C=CN=2)C(F)(F)F)=CC(C(F)F)=C1 LOXPQOCJGVJSKQ-UHFFFAOYSA-N 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 230000004770 neurodegeneration Effects 0.000 description 2
- 208000015122 neurodegenerative disease Diseases 0.000 description 2
- PCHKPVIQAHNQLW-CQSZACIVSA-N niraparib Chemical compound N1=C2C(C(=O)N)=CC=CC2=CN1C(C=C1)=CC=C1[C@@H]1CCCNC1 PCHKPVIQAHNQLW-CQSZACIVSA-N 0.000 description 2
- 229910017604 nitric acid Inorganic materials 0.000 description 2
- 239000012038 nucleophile Substances 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- 239000010502 orange oil Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 description 2
- 229960001756 oxaliplatin Drugs 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 229960001592 paclitaxel Drugs 0.000 description 2
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 2
- WRUUGTRCQOWXEG-UHFFFAOYSA-N pamidronate Chemical compound NCCC(O)(P(O)(O)=O)P(O)(O)=O WRUUGTRCQOWXEG-UHFFFAOYSA-N 0.000 description 2
- 229940046231 pamidronate Drugs 0.000 description 2
- 229960001639 penicillamine Drugs 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 description 2
- 229960003171 plicamycin Drugs 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229940068917 polyethylene glycols Drugs 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- NROKBHXJSPEDAR-UHFFFAOYSA-M potassium fluoride Chemical compound [F-].[K+] NROKBHXJSPEDAR-UHFFFAOYSA-M 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 2
- 239000003207 proteasome inhibitor Substances 0.000 description 2
- 108060006633 protein kinase Proteins 0.000 description 2
- KWGRBVOPPLSCSI-WCBMZHEXSA-N pseudoephedrine Chemical compound CN[C@@H](C)[C@@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WCBMZHEXSA-N 0.000 description 2
- 238000005086 pumping Methods 0.000 description 2
- 239000012264 purified product Substances 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 2
- 229940044551 receptor antagonist Drugs 0.000 description 2
- 239000002464 receptor antagonist Substances 0.000 description 2
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 2
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000006722 reduction reaction Methods 0.000 description 2
- 208000023504 respiratory system disease Diseases 0.000 description 2
- 208000037803 restenosis Diseases 0.000 description 2
- 238000004007 reversed phase HPLC Methods 0.000 description 2
- 238000007142 ring opening reaction Methods 0.000 description 2
- 229960001860 salicylate Drugs 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 230000037390 scarring Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 150000003333 secondary alcohols Chemical class 0.000 description 2
- 238000009491 slugging Methods 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000012279 sodium borohydride Substances 0.000 description 2
- 229910000033 sodium borohydride Inorganic materials 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 208000010110 spontaneous platelet aggregation Diseases 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 230000000707 stereoselective effect Effects 0.000 description 2
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 2
- 229960001052 streptozocin Drugs 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 229940037128 systemic glucocorticoids Drugs 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 229960001603 tamoxifen Drugs 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 2
- QFJCIRLUMZQUOT-UHFFFAOYSA-N temsirolimus Natural products C1CC(O)C(OC)CC1CC(C)C1OC(=O)C2CCCCN2C(=O)C(=O)C(O)(O2)C(C)CCC2CC(OC)C(C)=CC=CC=CC(C)CC(C)C(=O)C(OC)C(O)C(C)=CC(C)C(=O)C1 QFJCIRLUMZQUOT-UHFFFAOYSA-N 0.000 description 2
- NRUKOCRGYNPUPR-QBPJDGROSA-N teniposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@@H](OC[C@H]4O3)C=3SC=CC=3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 NRUKOCRGYNPUPR-QBPJDGROSA-N 0.000 description 2
- YAPQBXQYLJRXSA-UHFFFAOYSA-N theobromine Chemical compound CN1C(=O)NC(=O)C2=C1N=CN2C YAPQBXQYLJRXSA-UHFFFAOYSA-N 0.000 description 2
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 2
- 150000001467 thiazolidinediones Chemical class 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 229960001196 thiotepa Drugs 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 229940044693 topoisomerase inhibitor Drugs 0.000 description 2
- 229960000303 topotecan Drugs 0.000 description 2
- 229960000575 trastuzumab Drugs 0.000 description 2
- 229960001727 tretinoin Drugs 0.000 description 2
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 229960001055 uracil mustard Drugs 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 2
- 229960004528 vincristine Drugs 0.000 description 2
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 2
- GBABOYUKABKIAF-GHYRFKGUSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-GHYRFKGUSA-N 0.000 description 2
- 229960002066 vinorelbine Drugs 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- VNDYJBBGRKZCSX-UHFFFAOYSA-L zinc bromide Chemical compound Br[Zn]Br VNDYJBBGRKZCSX-UHFFFAOYSA-L 0.000 description 2
- XRASPMIURGNCCH-UHFFFAOYSA-N zoledronic acid Chemical compound OP(=O)(O)C(P(O)(O)=O)(O)CN1C=CN=C1 XRASPMIURGNCCH-UHFFFAOYSA-N 0.000 description 2
- 229960004276 zoledronic acid Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- XWTYSIMOBUGWOL-UHFFFAOYSA-N (+-)-Terbutaline Chemical compound CC(C)(C)NCC(O)C1=CC(O)=CC(O)=C1 XWTYSIMOBUGWOL-UHFFFAOYSA-N 0.000 description 1
- DOWZPWBBZLFWLY-ZHPDPMBESA-N (1S)-1-(5-bromo-1,3-thiazol-2-yl)-1-[(1S,3R,4S)-4-ethyl-3-methylcyclohexyl]ethanol Chemical compound C(C)[C@@H]1[C@@H](C[C@H](CC1)[C@](C)(O)C=1SC(=CN=1)Br)C DOWZPWBBZLFWLY-ZHPDPMBESA-N 0.000 description 1
- KWGRBVOPPLSCSI-SCZZXKLOSA-N (1r,2r)-2-(methylamino)-1-phenylpropan-1-ol Chemical compound CN[C@H](C)[C@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-SCZZXKLOSA-N 0.000 description 1
- FVUHGTQDOMGZOT-RITPCOANSA-N (1r,3s)-3-methoxycarbonylcyclopentane-1-carboxylic acid Chemical compound COC(=O)[C@H]1CC[C@@H](C(O)=O)C1 FVUHGTQDOMGZOT-RITPCOANSA-N 0.000 description 1
- JKFZMIQMKFWJAY-RQJQXFIZSA-N (1r,3s,5z)-5-[(2e)-2-[(3as,7as)-1-[(2r)-6-hydroxy-6-methylhept-4-yn-2-yl]-7a-methyl-3a,5,6,7-tetrahydro-3h-inden-4-ylidene]ethylidene]-4-methylidenecyclohexane-1,3-diol Chemical compound C1(/[C@@H]2CC=C([C@]2(CCC1)C)[C@@H](CC#CC(C)(C)O)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C JKFZMIQMKFWJAY-RQJQXFIZSA-N 0.000 description 1
- SFUIGUOONHIVLG-UHFFFAOYSA-N (2-nitrophenyl)boronic acid Chemical class OB(O)C1=CC=CC=C1[N+]([O-])=O SFUIGUOONHIVLG-UHFFFAOYSA-N 0.000 description 1
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 1
- JTBVPIHWMWILJU-MHZLTWQESA-N (2s)-2-(2-acetylanilino)-3-[4-[2-(5-methyl-2-phenyl-1,3-oxazol-4-yl)ethoxy]phenyl]propanoic acid Chemical compound CC(=O)C1=CC=CC=C1N[C@H](C(O)=O)CC(C=C1)=CC=C1OCCC1=C(C)OC(C=2C=CC=CC=2)=N1 JTBVPIHWMWILJU-MHZLTWQESA-N 0.000 description 1
- VGSJXSLGVQINOL-MHZLTWQESA-N (2s)-2-[4-[2-[(2,4-difluorophenyl)carbamoyl-heptylamino]ethyl]phenoxy]-2-methylbutanoic acid Chemical compound C=1C=C(F)C=C(F)C=1NC(=O)N(CCCCCCC)CCC1=CC=C(O[C@@](C)(CC)C(O)=O)C=C1 VGSJXSLGVQINOL-MHZLTWQESA-N 0.000 description 1
- WMUIIGVAWPWQAW-DEOSSOPVSA-N (2s)-2-ethoxy-3-{4-[2-(10h-phenoxazin-10-yl)ethoxy]phenyl}propanoic acid Chemical compound C1=CC(C[C@H](OCC)C(O)=O)=CC=C1OCCN1C2=CC=CC=C2OC2=CC=CC=C21 WMUIIGVAWPWQAW-DEOSSOPVSA-N 0.000 description 1
- MHFUWOIXNMZFIW-WNQIDUERSA-N (2s)-2-hydroxypropanoic acid;n-[4-[4-(4-methylpiperazin-1-yl)-6-[(5-methyl-1h-pyrazol-3-yl)amino]pyrimidin-2-yl]sulfanylphenyl]cyclopropanecarboxamide Chemical compound C[C@H](O)C(O)=O.C1CN(C)CCN1C1=CC(NC2=NNC(C)=C2)=NC(SC=2C=CC(NC(=O)C3CC3)=CC=2)=N1 MHFUWOIXNMZFIW-WNQIDUERSA-N 0.000 description 1
- IRAAJHYKQDFNFO-SFHVURJKSA-N (2s)-3-[4-[2-[1,3-benzoxazol-2-yl(methyl)amino]ethoxy]phenyl]-2-(2,2,2-trifluoroethoxy)propanoic acid Chemical compound N=1C2=CC=CC=C2OC=1N(C)CCOC1=CC=C(C[C@H](OCC(F)(F)F)C(O)=O)C=C1 IRAAJHYKQDFNFO-SFHVURJKSA-N 0.000 description 1
- LJRDOKAZOAKLDU-UDXJMMFXSA-N (2s,3s,4r,5r,6r)-5-amino-2-(aminomethyl)-6-[(2r,3s,4r,5s)-5-[(1r,2r,3s,5r,6s)-3,5-diamino-2-[(2s,3r,4r,5s,6r)-3-amino-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-6-hydroxycyclohexyl]oxy-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl]oxyoxane-3,4-diol;sulfuric ac Chemical compound OS(O)(=O)=O.N[C@@H]1[C@@H](O)[C@H](O)[C@H](CN)O[C@@H]1O[C@H]1[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](N)C[C@@H](N)[C@@H]2O)O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)N)O[C@@H]1CO LJRDOKAZOAKLDU-UDXJMMFXSA-N 0.000 description 1
- ZGGHKIMDNBDHJB-NRFPMOEYSA-M (3R,5S)-fluvastatin sodium Chemical compound [Na+].C12=CC=CC=C2N(C(C)C)C(\C=C\[C@@H](O)C[C@@H](O)CC([O-])=O)=C1C1=CC=C(F)C=C1 ZGGHKIMDNBDHJB-NRFPMOEYSA-M 0.000 description 1
- OQANPHBRHBJGNZ-FYJGNVAPSA-N (3e)-6-oxo-3-[[4-(pyridin-2-ylsulfamoyl)phenyl]hydrazinylidene]cyclohexa-1,4-diene-1-carboxylic acid Chemical compound C1=CC(=O)C(C(=O)O)=C\C1=N\NC1=CC=C(S(=O)(=O)NC=2N=CC=CC=2)C=C1 OQANPHBRHBJGNZ-FYJGNVAPSA-N 0.000 description 1
- ZKSNZYLCOXUJIR-VOKUKXJJSA-N (5s,5ar,8ar,9r)-5-[[(2r,4ar,6r,7r,8r,8as)-7-(dimethylamino)-8-hydroxy-2-methyl-4,4a,6,7,8,8a-hexahydropyrano[3,2-d][1,3]dioxin-6-yl]oxy]-9-(4-hydroxy-3,5-dimethoxyphenyl)-5a,6,8a,9-tetrahydro-5h-[2]benzofuro[6,5-f][1,3]benzodioxol-8-one Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)N(C)C)[C@@H]3[C@@H]2C(OC3)=O)=C1 ZKSNZYLCOXUJIR-VOKUKXJJSA-N 0.000 description 1
- DLROLUIVVKTFPW-LVEBQJTPSA-N (5s,5as,8ar,9r)-9-(4-hydroxy-3,5-dimethoxyphenyl)-5-(4-nitroanilino)-5a,6,8a,9-tetrahydro-5h-[2]benzofuro[5,6-f][1,3]benzodioxol-8-one Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](NC=3C=CC(=CC=3)[N+]([O-])=O)[C@@H]3[C@@H]2C(OC3)=O)=C1 DLROLUIVVKTFPW-LVEBQJTPSA-N 0.000 description 1
- OMJKFYKNWZZKTK-POHAHGRESA-N (5z)-5-(dimethylaminohydrazinylidene)imidazole-4-carboxamide Chemical compound CN(C)N\N=C1/N=CN=C1C(N)=O OMJKFYKNWZZKTK-POHAHGRESA-N 0.000 description 1
- BSRQHWFOFMAZRL-BODGVHBXSA-N (7s,9s)-7-[(2r,4s,5s,6s)-5-[(2s,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-4-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-8,10-dihydro-7h-tetracene-5,12-dione;hydron;chloride Chemical compound Cl.C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@H]1[C@@H](O)C[C@H](O[C@@H]2C3=C(O)C=4C(=O)C5=CC=CC=C5C(=O)C=4C(O)=C3C[C@](O)(C2)C(=O)CO)O[C@H]1C BSRQHWFOFMAZRL-BODGVHBXSA-N 0.000 description 1
- LKJPYSCBVHEWIU-KRWDZBQOSA-N (R)-bicalutamide Chemical compound C([C@@](O)(C)C(=O)NC=1C=C(C(C#N)=CC=1)C(F)(F)F)S(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-KRWDZBQOSA-N 0.000 description 1
- DCSCXTJOXBUFGB-JGVFFNPUSA-N (S)-(-)-verbenone Chemical compound CC1=CC(=O)[C@@H]2C(C)(C)[C@H]1C2 DCSCXTJOXBUFGB-JGVFFNPUSA-N 0.000 description 1
- OBRNDARFFFHCGE-PERKLWIXSA-N (S,S)-formoterol fumarate Chemical compound OC(=O)\C=C\C(O)=O.C1=CC(OC)=CC=C1C[C@H](C)NC[C@@H](O)C1=CC=C(O)C(NC=O)=C1.C1=CC(OC)=CC=C1C[C@H](C)NC[C@@H](O)C1=CC=C(O)C(NC=O)=C1 OBRNDARFFFHCGE-PERKLWIXSA-N 0.000 description 1
- KGQQKBSALJNKEH-ONEGZZNKSA-N (e)-4-ethoxy-1,1-difluorobut-3-en-2-one Chemical compound CCO\C=C\C(=O)C(F)F KGQQKBSALJNKEH-ONEGZZNKSA-N 0.000 description 1
- XGQXULJHBWKUJY-LYIKAWCPSA-N (z)-but-2-enedioic acid;n-[2-(diethylamino)ethyl]-5-[(z)-(5-fluoro-2-oxo-1h-indol-3-ylidene)methyl]-2,4-dimethyl-1h-pyrrole-3-carboxamide Chemical compound OC(=O)\C=C/C(O)=O.CCN(CC)CCNC(=O)C1=C(C)NC(\C=C/2C3=CC(F)=CC=C3NC\2=O)=C1C XGQXULJHBWKUJY-LYIKAWCPSA-N 0.000 description 1
- YFMFNYKEUDLDTL-UHFFFAOYSA-N 1,1,1,2,3,3,3-heptafluoropropane Chemical compound FC(F)(F)C(F)C(F)(F)F YFMFNYKEUDLDTL-UHFFFAOYSA-N 0.000 description 1
- LVGUZGTVOIAKKC-UHFFFAOYSA-N 1,1,1,2-tetrafluoroethane Chemical compound FCC(F)(F)F LVGUZGTVOIAKKC-UHFFFAOYSA-N 0.000 description 1
- AEBWATHAIVJLTA-UHFFFAOYSA-N 1,2,3,3a,4,5,6,6a-octahydropentalene Chemical compound C1CCC2CCCC21 AEBWATHAIVJLTA-UHFFFAOYSA-N 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical group ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- KPZGRMZPZLOPBS-UHFFFAOYSA-N 1,3-dichloro-2,2-bis(chloromethyl)propane Chemical compound ClCC(CCl)(CCl)CCl KPZGRMZPZLOPBS-UHFFFAOYSA-N 0.000 description 1
- DDGHBOLOCQWPKE-UHFFFAOYSA-N 1,3-thiazole;hydrobromide Chemical compound [Br-].C1=CSC=[NH+]1 DDGHBOLOCQWPKE-UHFFFAOYSA-N 0.000 description 1
- ZOBPZXTWZATXDG-UHFFFAOYSA-N 1,3-thiazolidine-2,4-dione Chemical compound O=C1CSC(=O)N1 ZOBPZXTWZATXDG-UHFFFAOYSA-N 0.000 description 1
- XGIKJBAZJQQPHD-UHFFFAOYSA-N 1,4-dioxaspiro[4.5]decan-8-yl-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methanone Chemical compound C=1C(C=2SC(=NC=2)C(=O)C2CCC3(CC2)OCCO3)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 XGIKJBAZJQQPHD-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical group C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- MZNMZWZGUGFQJP-UHFFFAOYSA-N 1-[11-(dodecylamino)-10-hydroxyundecyl]-3,7-dimethylpurine-2,6-dione Chemical compound O=C1N(CCCCCCCCCC(O)CNCCCCCCCCCCCC)C(=O)N(C)C2=C1N(C)C=N2 MZNMZWZGUGFQJP-UHFFFAOYSA-N 0.000 description 1
- DRBFPGWFRLHXNY-UHFFFAOYSA-N 1-[4-(hydroxymethyl)cyclohexyl]-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethanol Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CO)CC2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 DRBFPGWFRLHXNY-UHFFFAOYSA-N 0.000 description 1
- KVWZRIJJNXGLDX-UHFFFAOYSA-N 1-azabicyclo[2.2.2]octan-3-yl 2,2-diphenylpropanoate;hydrochloride Chemical compound Cl.C1N(CC2)CCC2C1OC(=O)C(C)(C=1C=CC=CC=1)C1=CC=CC=C1 KVWZRIJJNXGLDX-UHFFFAOYSA-N 0.000 description 1
- NSBBFZZSXMQBJJ-UHFFFAOYSA-N 1-cyclopent-3-en-1-ylethanone Chemical compound CC(=O)C1CC=CC1 NSBBFZZSXMQBJJ-UHFFFAOYSA-N 0.000 description 1
- UOWIYNWMROWVDG-UHFFFAOYSA-N 1-dimethoxyphosphorylpropan-2-one Chemical compound COP(=O)(OC)CC(C)=O UOWIYNWMROWVDG-UHFFFAOYSA-N 0.000 description 1
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 description 1
- WNWHHMBRJJOGFJ-UHFFFAOYSA-N 16-methylheptadecan-1-ol Chemical class CC(C)CCCCCCCCCCCCCCCO WNWHHMBRJJOGFJ-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- RVCKCEDKBVEEHL-UHFFFAOYSA-N 2,3,4,5,6-pentachlorobenzyl alcohol Chemical compound OCC1=C(Cl)C(Cl)=C(Cl)C(Cl)=C1Cl RVCKCEDKBVEEHL-UHFFFAOYSA-N 0.000 description 1
- IPDWABJNXLNLRA-UHFFFAOYSA-N 2,3-dihydroxybutanedioic acid;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)C(O)C(O)C(O)=O.OC(=O)CC(O)(C(O)=O)CC(O)=O IPDWABJNXLNLRA-UHFFFAOYSA-N 0.000 description 1
- WHPFEQUEHBULBW-UHFFFAOYSA-N 2,4-dichloro-5-fluoropyrimidine Chemical compound FC1=CN=C(Cl)N=C1Cl WHPFEQUEHBULBW-UHFFFAOYSA-N 0.000 description 1
- STMIIPIFODONDC-UHFFFAOYSA-N 2-(2,4-dichlorophenyl)-1-(1H-1,2,4-triazol-1-yl)hexan-2-ol Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(O)(CCCC)CN1C=NC=N1 STMIIPIFODONDC-UHFFFAOYSA-N 0.000 description 1
- UEJJHQNACJXSKW-UHFFFAOYSA-N 2-(2,6-dioxopiperidin-3-yl)-1H-isoindole-1,3(2H)-dione Chemical compound O=C1C2=CC=CC=C2C(=O)N1C1CCC(=O)NC1=O UEJJHQNACJXSKW-UHFFFAOYSA-N 0.000 description 1
- GFMMXOIFOQCCGU-UHFFFAOYSA-N 2-(2-chloro-4-iodoanilino)-N-(cyclopropylmethoxy)-3,4-difluorobenzamide Chemical compound C=1C=C(I)C=C(Cl)C=1NC1=C(F)C(F)=CC=C1C(=O)NOCC1CC1 GFMMXOIFOQCCGU-UHFFFAOYSA-N 0.000 description 1
- ZUJVUCJJHKUMNN-UHFFFAOYSA-N 2-(3-bromo-5-methylphenyl)guanidine;nitric acid Chemical compound O[N+]([O-])=O.CC1=CC(Br)=CC(N=C(N)N)=C1 ZUJVUCJJHKUMNN-UHFFFAOYSA-N 0.000 description 1
- XWNJMSJGJFSGRY-UHFFFAOYSA-N 2-(benzylamino)-3,7-dihydropurin-6-one Chemical compound N1C=2N=CNC=2C(=O)N=C1NCC1=CC=CC=C1 XWNJMSJGJFSGRY-UHFFFAOYSA-N 0.000 description 1
- DSBSVDCHFMEYBX-FFXKMJQXSA-N 2-[(2r)-2-methylpyrrolidin-2-yl]-1h-benzimidazole-4-carboxamide;dihydrochloride Chemical compound Cl.Cl.N=1C2=C(C(N)=O)C=CC=C2NC=1[C@@]1(C)CCCN1 DSBSVDCHFMEYBX-FFXKMJQXSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- ORFBIYUBCXIHMN-UHFFFAOYSA-N 2-[2-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclopropyl]-2-methylpropanoic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2C(C2)C(C)(C)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 ORFBIYUBCXIHMN-UHFFFAOYSA-N 0.000 description 1
- ZKLPARSLTMPFCP-OAQYLSRUSA-N 2-[2-[4-[(R)-(4-chlorophenyl)-phenylmethyl]-1-piperazinyl]ethoxy]acetic acid Chemical compound C1CN(CCOCC(=O)O)CCN1[C@@H](C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-OAQYLSRUSA-N 0.000 description 1
- JVPFMUKVMZTQNA-UHFFFAOYSA-N 2-[3-[1-[5-[3-[(5-fluoro-4-methylpyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]-2,2-dimethylcyclobutyl]acetic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2C(C(CC(O)=O)C2)(C)C)=CC(C)=CC=1NC1=NC=C(F)C(C)=N1 JVPFMUKVMZTQNA-UHFFFAOYSA-N 0.000 description 1
- ROTPRZBMPVLUNA-UHFFFAOYSA-N 2-[3-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2,2-dimethylcyclobutyl]acetic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2C(C(CC(O)=O)C2)(C)C)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 ROTPRZBMPVLUNA-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-IVMDWMLBSA-N 2-amino-2-deoxy-D-glucopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O MSWZFWKMSRAUBD-IVMDWMLBSA-N 0.000 description 1
- RXNZFHIEDZEUQM-UHFFFAOYSA-N 2-bromo-1,3-thiazole Chemical compound BrC1=NC=CS1 RXNZFHIEDZEUQM-UHFFFAOYSA-N 0.000 description 1
- UZJYZAYUNDJTTM-UHFFFAOYSA-N 2-chloro-4-cyclopropyl-5-fluoropyrimidine Chemical compound FC1=CN=C(Cl)N=C1C1CC1 UZJYZAYUNDJTTM-UHFFFAOYSA-N 0.000 description 1
- HLVJKADQILYNGE-UHFFFAOYSA-N 2-chloro-5-fluoro-4-methoxypyrimidine Chemical compound COC1=NC(Cl)=NC=C1F HLVJKADQILYNGE-UHFFFAOYSA-N 0.000 description 1
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 1
- 229940013085 2-diethylaminoethanol Drugs 0.000 description 1
- VZWOXDYRBDIHMA-UHFFFAOYSA-N 2-methyl-1,3-thiazole Chemical compound CC1=NC=CS1 VZWOXDYRBDIHMA-UHFFFAOYSA-N 0.000 description 1
- VSKXJRZPVDLHFY-UHFFFAOYSA-N 2-methylcyclohexane-1-carboxylic acid Chemical compound CC1CCCCC1C(O)=O VSKXJRZPVDLHFY-UHFFFAOYSA-N 0.000 description 1
- AFXKCBFBGDUFAM-UHFFFAOYSA-N 2-methylpropan-2-amine;hydrofluoride Chemical compound [F-].CC(C)(C)[NH3+] AFXKCBFBGDUFAM-UHFFFAOYSA-N 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- NDMPLJNOPCLANR-UHFFFAOYSA-N 3,4-dihydroxy-15-(4-hydroxy-18-methoxycarbonyl-5,18-seco-ibogamin-18-yl)-16-methoxy-1-methyl-6,7-didehydro-aspidospermidine-3-carboxylic acid methyl ester Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 NDMPLJNOPCLANR-UHFFFAOYSA-N 0.000 description 1
- RVNUUWJGSOHMRR-UHFFFAOYSA-N 3,5-dibromoaniline Chemical compound NC1=CC(Br)=CC(Br)=C1 RVNUUWJGSOHMRR-UHFFFAOYSA-N 0.000 description 1
- JEFDRZNBQYMGKG-UHFFFAOYSA-N 3-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2,2-dimethylcyclobutane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2C(C(C(O)=O)C2)(C)C)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 JEFDRZNBQYMGKG-UHFFFAOYSA-N 0.000 description 1
- SJCXBNAWDXYOFX-UHFFFAOYSA-N 3-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]adamantane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C23CC4(CC(CC(C4)C2)C3)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 SJCXBNAWDXYOFX-UHFFFAOYSA-N 0.000 description 1
- VBVMPVBFMNEDIV-UHFFFAOYSA-N 3-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]bicyclo[3.1.0]hexane-6-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CC3C(C3C(O)=O)C2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 VBVMPVBFMNEDIV-UHFFFAOYSA-N 0.000 description 1
- LGBNVIQVVULXPV-UHFFFAOYSA-N 3-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclopentane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 LGBNVIQVVULXPV-UHFFFAOYSA-N 0.000 description 1
- QNJCRBZVUFRESB-UHFFFAOYSA-N 3-aminopyridine-2-carbaldehyde Chemical compound NC1=CC=CN=C1C=O QNJCRBZVUFRESB-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- OUDCOMBHRXKPIJ-UHFFFAOYSA-N 3-bromo-5-nitrobenzaldehyde Chemical compound [O-][N+](=O)C1=CC(Br)=CC(C=O)=C1 OUDCOMBHRXKPIJ-UHFFFAOYSA-N 0.000 description 1
- DHYHYLGCQVVLOQ-UHFFFAOYSA-N 3-bromoaniline Chemical compound NC1=CC=CC(Br)=C1 DHYHYLGCQVVLOQ-UHFFFAOYSA-N 0.000 description 1
- VQRPRRMKMAREJT-UHFFFAOYSA-N 3-fluoro-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)aniline Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC(N)=CC(F)=C1 VQRPRRMKMAREJT-UHFFFAOYSA-N 0.000 description 1
- RCNTYSJFQLDZAI-UHFFFAOYSA-N 3-methyl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)aniline Chemical compound CC1=CC(N)=CC(B2OC(C)(C)C(C)(C)O2)=C1 RCNTYSJFQLDZAI-UHFFFAOYSA-N 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- UCFSYHMCKWNKAH-UHFFFAOYSA-N 4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound CC1(C)OBOC1(C)C UCFSYHMCKWNKAH-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- ABHUJSHJKQHQTK-UHFFFAOYSA-N 4-(difluoromethyl)-n-[3-methyl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]pyrimidin-2-amine Chemical compound C=1C(B2OC(C)(C)C(C)(C)O2)=CC(C)=CC=1NC1=NC=CC(C(F)F)=N1 ABHUJSHJKQHQTK-UHFFFAOYSA-N 0.000 description 1
- NKOTXYPTXKUCDL-UHFFFAOYSA-N 4-(trifluoromethyl)pyrimidin-2-amine Chemical compound NC1=NC=CC(C(F)(F)F)=N1 NKOTXYPTXKUCDL-UHFFFAOYSA-N 0.000 description 1
- BKDUWMJFLCNPKP-UHFFFAOYSA-N 4-(trifluoromethyl)pyrimidine Chemical compound FC(F)(F)C1=CC=NC=N1 BKDUWMJFLCNPKP-UHFFFAOYSA-N 0.000 description 1
- MGQSNNBKPWYKBK-HHQIGMCSSA-N 4-[(1r)-1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)[C@](C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 MGQSNNBKPWYKBK-HHQIGMCSSA-N 0.000 description 1
- MGQSNNBKPWYKBK-DWFFKFSKSA-N 4-[(1s)-1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)[C@@](C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 MGQSNNBKPWYKBK-DWFFKFSKSA-N 0.000 description 1
- WQXNIJWETNFCKI-UHFFFAOYSA-N 4-[1,2-dihydroxy-1-[5-[3-[(4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound COC1=CC=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(O)(CO)C2CCC(CC2)C(O)=O)=N1 WQXNIJWETNFCKI-UHFFFAOYSA-N 0.000 description 1
- ZZLNYARSYNMNJW-UHFFFAOYSA-N 4-[1,2-dihydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(CO)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C)=N1 ZZLNYARSYNMNJW-UHFFFAOYSA-N 0.000 description 1
- IVJGSCPSOOUQQE-UHFFFAOYSA-N 4-[1,2-dihydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(CO)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 IVJGSCPSOOUQQE-UHFFFAOYSA-N 0.000 description 1
- UFMOLBGLCSDNFU-UHFFFAOYSA-N 4-[1-[5-[2-bromo-3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound CC1=CC=NC(NC=2C=C(C(Br)=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 UFMOLBGLCSDNFU-UHFFFAOYSA-N 0.000 description 1
- QUYPJAZQYHPUKY-UHFFFAOYSA-N 4-[1-[5-[3-[(4-cyclopropyl-5-fluoropyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC(N=1)=NC=C(F)C=1C1CC1 QUYPJAZQYHPUKY-UHFFFAOYSA-N 0.000 description 1
- AZJRKCZUVVLVLL-UHFFFAOYSA-N 4-[1-[5-[3-[(4-cyclopropylpyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC(N=1)=NC=CC=1C1CC1 AZJRKCZUVVLVLL-UHFFFAOYSA-N 0.000 description 1
- RSCLFOAUBJGMBA-UHFFFAOYSA-N 4-[1-[5-[3-[(5-chloro-4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C1=C(Cl)C(OC)=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 RSCLFOAUBJGMBA-UHFFFAOYSA-N 0.000 description 1
- JPZCDLWCZLNXKN-UHFFFAOYSA-N 4-[1-[5-[3-[(5-fluoro-4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C1=C(F)C(OC)=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 JPZCDLWCZLNXKN-UHFFFAOYSA-N 0.000 description 1
- NGTDTLVCPZGNBK-UHFFFAOYSA-N 4-[1-[5-[3-[(5-fluoro-4-methylpyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1,2-dihydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(CO)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=C(F)C(C)=N1 NGTDTLVCPZGNBK-UHFFFAOYSA-N 0.000 description 1
- FFYGKIBTMLDZEM-UHFFFAOYSA-N 4-[1-[5-[3-[(5-fluoro-4-methylpyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=C(F)C(C)=N1 FFYGKIBTMLDZEM-UHFFFAOYSA-N 0.000 description 1
- MHFLPFCZEYOKRW-UHFFFAOYSA-N 4-[1-[5-[3-[[4-(difluoromethyl)pyrimidin-2-yl]amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylic acid Chemical compound C1CC(C(O)=O)C(C)CC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C=CN=3)C(F)F)C=C(C)C=2)S1 MHFLPFCZEYOKRW-UHFFFAOYSA-N 0.000 description 1
- FQWMJZQSAYUTRZ-UHFFFAOYSA-N 4-[1-[5-[3-[[4-(difluoromethyl)pyrimidin-2-yl]amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)F)=N1 FQWMJZQSAYUTRZ-UHFFFAOYSA-N 0.000 description 1
- NQDPVMWALVUAFX-UHFFFAOYSA-N 4-[1-[5-[3-[[4-(difluoromethyl)pyrimidin-2-yl]amino]-5-methylphenyl]-1,3-thiazol-2-yl]-2,2,2-trifluoro-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(C2CCC(CC2)C(O)=O)C(F)(F)F)=CC(C)=CC=1NC1=NC=CC(C(F)F)=N1 NQDPVMWALVUAFX-UHFFFAOYSA-N 0.000 description 1
- XWZIXSGZKFPTEC-UHFFFAOYSA-N 4-[1-[5-[3-cyclopropyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=2)C2CC2)SC=1C(O)(C)C1CCC(C(O)=O)CC1 XWZIXSGZKFPTEC-UHFFFAOYSA-N 0.000 description 1
- XFSBUXXXANIIGC-UHFFFAOYSA-N 4-[1-[5-[3-fluoro-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(F)C=2)SC=1C(O)(C)C1CCC(C(O)=O)CC1 XFSBUXXXANIIGC-UHFFFAOYSA-N 0.000 description 1
- DPKVFUJQKKNMFB-UHFFFAOYSA-N 4-[1-fluoro-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(F)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 DPKVFUJQKKNMFB-UHFFFAOYSA-N 0.000 description 1
- ARQOCRFKRGQCAJ-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-(hydroxymethyl)-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(CO)C=2)SC=1C(O)(C)C1CCC(C(O)=O)CC1 ARQOCRFKRGQCAJ-UHFFFAOYSA-N 0.000 description 1
- WGFYTKUCMSJMMN-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-[(4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]ethyl]-2-methylcyclohexane-1-carboxylic acid Chemical compound COC1=CC=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CC(C)C(CC2)C(O)=O)=N1 WGFYTKUCMSJMMN-UHFFFAOYSA-N 0.000 description 1
- BDYOIWWTHSEGBN-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-[(4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound COC1=CC=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 BDYOIWWTHSEGBN-UHFFFAOYSA-N 0.000 description 1
- OFJJFQSKZJIGII-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2-methylcyclohexane-1-carboxylic acid Chemical compound C1CC(C(O)=O)C(C)CC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C)C=CN=3)C=C(C)C=2)S1 OFJJFQSKZJIGII-UHFFFAOYSA-N 0.000 description 1
- MMBDNZOWCKKOLU-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carbonitrile Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C#N)=CC(C)=CC=1NC1=NC=CC(C)=N1 MMBDNZOWCKKOLU-UHFFFAOYSA-N 0.000 description 1
- QEPRCONRQVQCKN-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C)=N1 QEPRCONRQVQCKN-UHFFFAOYSA-N 0.000 description 1
- JSQZBYMDMRVRSY-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]propyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C)C=CN=3)C=C(C)C=2)SC=1C(O)(CC)C1CCC(C(O)=O)CC1 JSQZBYMDMRVRSY-UHFFFAOYSA-N 0.000 description 1
- MAYFIMMTGLLCAX-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-propan-2-yloxypyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound CC(C)OC1=CC=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 MAYFIMMTGLLCAX-UHFFFAOYSA-N 0.000 description 1
- AHAJLJLVEORGRX-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-propan-2-ylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound CC(C)C1=CC=NC(NC=2C=C(C=C(C)C=2)C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=N1 AHAJLJLVEORGRX-UHFFFAOYSA-N 0.000 description 1
- BXCQWSSQZOINQB-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2-methylcyclohexane-1-carboxylic acid Chemical compound C1CC(C(O)=O)C(C)CC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)S1 BXCQWSSQZOINQB-UHFFFAOYSA-N 0.000 description 1
- DBNAMAIVNVDFOH-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carbonitrile Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C#N)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 DBNAMAIVNVDFOH-UHFFFAOYSA-N 0.000 description 1
- MGQSNNBKPWYKBK-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 MGQSNNBKPWYKBK-UHFFFAOYSA-N 0.000 description 1
- ZIROHOYPZLZQIS-UHFFFAOYSA-N 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]propyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)SC=1C(O)(CC)C1CCC(C(O)=O)CC1 ZIROHOYPZLZQIS-UHFFFAOYSA-N 0.000 description 1
- SSGXQCOZBVDPGK-UHFFFAOYSA-N 4-[1-hydroxy-2-methyl-1-[5-[3-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]propyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=CC=2)SC=1C(O)(C(C)C)C1CCC(C(O)=O)CC1 SSGXQCOZBVDPGK-UHFFFAOYSA-N 0.000 description 1
- FRLDHARHIUKPDQ-UHFFFAOYSA-N 4-[1-hydroxy-2-methyl-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]propyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)SC=1C(O)(C(C)C)C1CCC(C(O)=O)CC1 FRLDHARHIUKPDQ-UHFFFAOYSA-N 0.000 description 1
- DRVGGLFFFXUBGU-UHFFFAOYSA-N 4-[1-methoxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound N=1C=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)SC=1C(C)(OC)C1CCC(C(O)=O)CC1 DRVGGLFFFXUBGU-UHFFFAOYSA-N 0.000 description 1
- DCCGKHRGTGLYCO-UHFFFAOYSA-N 4-[2,2,2-trifluoro-1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(C2CCC(CC2)C(O)=O)C(F)(F)F)=CC(C)=CC=1NC1=NC=CC(C)=N1 DCCGKHRGTGLYCO-UHFFFAOYSA-N 0.000 description 1
- IXFISEFLNBHMBN-UHFFFAOYSA-N 4-[2,2,2-trifluoro-1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)(C2CCC(CC2)C(O)=O)C(F)(F)F)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 IXFISEFLNBHMBN-UHFFFAOYSA-N 0.000 description 1
- RJZRNLJOIFTXME-UHFFFAOYSA-N 4-[2-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(CO)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 RJZRNLJOIFTXME-UHFFFAOYSA-N 0.000 description 1
- PUXJQBBFELZSDC-UHFFFAOYSA-N 4-[3,4-dihydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]butyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(CC(O)CO)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C)=N1 PUXJQBBFELZSDC-UHFFFAOYSA-N 0.000 description 1
- QBQLYIISSRXYKL-UHFFFAOYSA-N 4-[[4-[2-(5-methyl-2-phenyl-1,3-oxazol-4-yl)ethoxy]phenyl]methyl]-1,2-oxazolidine-3,5-dione Chemical compound CC=1OC(C=2C=CC=CC=2)=NC=1CCOC(C=C1)=CC=C1CC1C(=O)NOC1=O QBQLYIISSRXYKL-UHFFFAOYSA-N 0.000 description 1
- CQJHORVWHNTQJP-UHFFFAOYSA-N 4-[amino-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(N)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 CQJHORVWHNTQJP-UHFFFAOYSA-N 0.000 description 1
- OHQHGRYHFAMFJU-UHFFFAOYSA-N 4-[fluoro-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(F)C2CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 OHQHGRYHFAMFJU-UHFFFAOYSA-N 0.000 description 1
- GFFXZLZWLOBBLO-BWVDBABLSA-N 4-amino-1-[(2r,4s,5r)-3-(fluoromethylidene)-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]pyrimidin-2-one Chemical compound O=C1N=C(N)C=CN1[C@H]1C(=CF)[C@H](O)[C@@H](CO)O1 GFFXZLZWLOBBLO-BWVDBABLSA-N 0.000 description 1
- PULHLIOPJXPGJN-BWVDBABLSA-N 4-amino-1-[(2r,4s,5r)-4-hydroxy-5-(hydroxymethyl)-3-methylideneoxolan-2-yl]pyrimidin-2-one Chemical compound O=C1N=C(N)C=CN1[C@H]1C(=C)[C@H](O)[C@@H](CO)O1 PULHLIOPJXPGJN-BWVDBABLSA-N 0.000 description 1
- WBOSBXUVXRYGKG-UHFFFAOYSA-N 4-butoxycarbonylcyclohexane-1-carboxylic acid Chemical compound CCCCOC(=O)C1CCC(C(O)=O)CC1 WBOSBXUVXRYGKG-UHFFFAOYSA-N 0.000 description 1
- 125000000242 4-chlorobenzoyl group Chemical group ClC1=CC=C(C(=O)*)C=C1 0.000 description 1
- XTNVLEVPXCVDTB-UHFFFAOYSA-N 4-cyanocyclohexane-1-carbonyl chloride Chemical compound ClC(=O)C1CCC(C#N)CC1 XTNVLEVPXCVDTB-UHFFFAOYSA-N 0.000 description 1
- KJZWYCAIEUYAIW-UHFFFAOYSA-N 4-cyanocyclohexane-1-carboxylic acid Chemical compound OC(=O)C1CCC(C#N)CC1 KJZWYCAIEUYAIW-UHFFFAOYSA-N 0.000 description 1
- HVCNXQOWACZAFN-UHFFFAOYSA-N 4-ethylmorpholine Chemical compound CCN1CCOCC1 HVCNXQOWACZAFN-UHFFFAOYSA-N 0.000 description 1
- WGYDYLZIYRHXPS-UHFFFAOYSA-N 4-hydroxy-4-[[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(CC3(O)CCC(CC3)C(O)=O)=NC=2)=CC(C)=CC=1NC1=NC=CC(C)=N1 WGYDYLZIYRHXPS-UHFFFAOYSA-N 0.000 description 1
- FPMVQMQBZXFGLE-UHFFFAOYSA-N 4-hydroxy-4-[hydroxy-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(O)C2(O)CCC(CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 FPMVQMQBZXFGLE-UHFFFAOYSA-N 0.000 description 1
- PJJGZPJJTHBVMX-UHFFFAOYSA-N 5,7-Dihydroxyisoflavone Chemical compound C=1C(O)=CC(O)=C(C2=O)C=1OC=C2C1=CC=CC=C1 PJJGZPJJTHBVMX-UHFFFAOYSA-N 0.000 description 1
- 102000004023 5-Lipoxygenase-Activating Proteins Human genes 0.000 description 1
- 108090000411 5-Lipoxygenase-Activating Proteins Proteins 0.000 description 1
- NFFXEUUOMTXWCX-UHFFFAOYSA-N 5-[(2,4-dioxo-1,3-thiazolidin-5-yl)methyl]-2-methoxy-n-[[4-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound C1=C(C(=O)NCC=2C=CC(=CC=2)C(F)(F)F)C(OC)=CC=C1CC1SC(=O)NC1=O NFFXEUUOMTXWCX-UHFFFAOYSA-N 0.000 description 1
- LGZKGOGODCLQHG-CYBMUJFWSA-N 5-[(2r)-2-hydroxy-2-(3,4,5-trimethoxyphenyl)ethyl]-2-methoxyphenol Chemical compound C1=C(O)C(OC)=CC=C1C[C@@H](O)C1=CC(OC)=C(OC)C(OC)=C1 LGZKGOGODCLQHG-CYBMUJFWSA-N 0.000 description 1
- IETKPTYAGKZLKY-UHFFFAOYSA-N 5-[[4-[(3-methyl-4-oxoquinazolin-2-yl)methoxy]phenyl]methyl]-1,3-thiazolidine-2,4-dione Chemical compound N=1C2=CC=CC=C2C(=O)N(C)C=1COC(C=C1)=CC=C1CC1SC(=O)NC1=O IETKPTYAGKZLKY-UHFFFAOYSA-N 0.000 description 1
- 239000002677 5-alpha reductase inhibitor Substances 0.000 description 1
- NMUSYJAQQFHJEW-KVTDHHQDSA-N 5-azacytidine Chemical compound O=C1N=C(N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 NMUSYJAQQFHJEW-KVTDHHQDSA-N 0.000 description 1
- HMVGGGOWCWNMNY-UHFFFAOYSA-N 5-bromo-2-methyl-1,3-thiazole Chemical compound CC1=NC=C(Br)S1 HMVGGGOWCWNMNY-UHFFFAOYSA-N 0.000 description 1
- SRXKXMHCYITMQF-UHFFFAOYSA-N 5-fluoro-4-methoxy-n-[3-methyl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]pyrimidin-2-amine Chemical compound C1=C(F)C(OC)=NC(NC=2C=C(C=C(C)C=2)B2OC(C)(C)C(C)(C)O2)=N1 SRXKXMHCYITMQF-UHFFFAOYSA-N 0.000 description 1
- MMRCWWRFYLZGAE-ZBZRSYSASA-N 533u947v6q Chemical compound O([C@]12[C@H](OC(C)=O)[C@]3(CC)C=CCN4CC[C@@]5([C@H]34)[C@H]1N(C)C1=C5C=C(C(=C1)OC)[C@]1(C(=O)OC)C3=C(C4=CC=CC=C4N3)CCN3C[C@H](C1)C[C@@](C3)(O)CC)C(=O)N(CCCl)C2=O MMRCWWRFYLZGAE-ZBZRSYSASA-N 0.000 description 1
- JTDYUFSDZATMKU-UHFFFAOYSA-N 6-(1,3-dioxo-2-benzo[de]isoquinolinyl)-N-hydroxyhexanamide Chemical compound C1=CC(C(N(CCCCCC(=O)NO)C2=O)=O)=C3C2=CC=CC3=C1 JTDYUFSDZATMKU-UHFFFAOYSA-N 0.000 description 1
- PBYBPOJEDUTZSM-UHFFFAOYSA-N 6-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]bicyclo[3.1.0]hexane-3-carboxylic acid Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2C3CC(CC32)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 PBYBPOJEDUTZSM-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- VVIAGPKUTFNRDU-UHFFFAOYSA-N 6S-folinic acid Natural products C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-UHFFFAOYSA-N 0.000 description 1
- RGVRUQHYQSORBY-UHFFFAOYSA-N 7-(4-amino-5-hydroxy-6-methyloxan-2-yl)oxy-6,9,11-trihydroxy-9-(2-hydroxyethyl)-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione Chemical compound C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(CCO)CC1OC1CC(N)C(O)C(C)O1 RGVRUQHYQSORBY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- PBCZSGKMGDDXIJ-UHFFFAOYSA-N 7beta-hydroxystaurosporine Natural products C12=C3N4C5=CC=CC=C5C3=C3C(O)NC(=O)C3=C2C2=CC=CC=C2N1C1CC(NC)C(OC)C4(C)O1 PBCZSGKMGDDXIJ-UHFFFAOYSA-N 0.000 description 1
- MROJXXOCABQVEF-UHFFFAOYSA-N Actarit Chemical compound CC(=O)NC1=CC=C(CC(O)=O)C=C1 MROJXXOCABQVEF-UHFFFAOYSA-N 0.000 description 1
- 208000004476 Acute Coronary Syndrome Diseases 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- 208000000884 Airway Obstruction Diseases 0.000 description 1
- OGSPWJRAVKPPFI-UHFFFAOYSA-N Alendronic Acid Chemical compound NCCCC(O)(P(O)(O)=O)P(O)(O)=O OGSPWJRAVKPPFI-UHFFFAOYSA-N 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- KFYRPLNVJVHZGT-UHFFFAOYSA-N Amitriptyline hydrochloride Chemical compound Cl.C1CC2=CC=CC=C2C(=CCCN(C)C)C2=CC=CC=C21 KFYRPLNVJVHZGT-UHFFFAOYSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 206010002198 Anaphylactic reaction Diseases 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 206010002388 Angina unstable Diseases 0.000 description 1
- 208000028185 Angioedema Diseases 0.000 description 1
- 102400000068 Angiostatin Human genes 0.000 description 1
- 108010079709 Angiostatins Proteins 0.000 description 1
- 229940123413 Angiotensin II antagonist Drugs 0.000 description 1
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010003210 Arteriosclerosis Diseases 0.000 description 1
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 108010004586 Ataxia Telangiectasia Mutated Proteins Proteins 0.000 description 1
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 1
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 1
- 208000004300 Atrophic Gastritis Diseases 0.000 description 1
- 229940123877 Aurora kinase inhibitor Drugs 0.000 description 1
- 102000003989 Aurora kinases Human genes 0.000 description 1
- 108090000433 Aurora kinases Proteins 0.000 description 1
- 208000030767 Autoimmune encephalitis Diseases 0.000 description 1
- 206010050245 Autoimmune thrombocytopenia Diseases 0.000 description 1
- MBUVEWMHONZEQD-UHFFFAOYSA-N Azeptin Chemical compound C1CN(C)CCCC1N1C(=O)C2=CC=CC=C2C(CC=2C=CC(Cl)=CC=2)=N1 MBUVEWMHONZEQD-UHFFFAOYSA-N 0.000 description 1
- 208000036170 B-Cell Marginal Zone Lymphoma Diseases 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 208000025321 B-lymphoblastic leukemia/lymphoma Diseases 0.000 description 1
- MLDQJTXFUGDVEO-UHFFFAOYSA-N BAY-43-9006 Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 MLDQJTXFUGDVEO-UHFFFAOYSA-N 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 229940124291 BTK inhibitor Drugs 0.000 description 1
- 208000023328 Basedow disease Diseases 0.000 description 1
- KUVIULQEHSCUHY-XYWKZLDCSA-N Beclometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)COC(=O)CC)(OC(=O)CC)[C@@]1(C)C[C@@H]2O KUVIULQEHSCUHY-XYWKZLDCSA-N 0.000 description 1
- 208000009137 Behcet syndrome Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-DCSYEGIMSA-N Beta-Lactose Chemical compound OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-DCSYEGIMSA-N 0.000 description 1
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 description 1
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 1
- 229940122361 Bisphosphonate Drugs 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 206010048396 Bone marrow transplant rejection Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 201000006474 Brain Ischemia Diseases 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 238000006418 Brown reaction Methods 0.000 description 1
- PJFHZKIDENOSJB-UHFFFAOYSA-N Budesonide/formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1.C1CC2=CC(=O)C=CC2(C)C2C1C1CC3OC(CCC)OC3(C(=O)CO)C1(C)CC2O PJFHZKIDENOSJB-UHFFFAOYSA-N 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- DPKVFUJQKKNMFB-ZBVLSHQLSA-N C=1C(C=2SC(=NC=2)C(C)(F)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)C(C)(F)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 DPKVFUJQKKNMFB-ZBVLSHQLSA-N 0.000 description 1
- MGQSNNBKPWYKBK-UBMNLSNXSA-N C=1C(C=2SC(=NC=2)[C@@](C)(O)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 Chemical compound C=1C(C=2SC(=NC=2)[C@@](C)(O)[C@@H]2CC[C@H](CC2)C(O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 MGQSNNBKPWYKBK-UBMNLSNXSA-N 0.000 description 1
- KYYIFVGLZAJMDL-QAQDUYKDSA-N C=1C(C=2SC(C[C@@H]3CC[C@H](CC3)C(O)=O)=NC=2)=CC(C)=CC=1NC1=NC=CC(C)=N1 Chemical compound C=1C(C=2SC(C[C@@H]3CC[C@H](CC3)C(O)=O)=NC=2)=CC(C)=CC=1NC1=NC=CC(C)=N1 KYYIFVGLZAJMDL-QAQDUYKDSA-N 0.000 description 1
- QEPRCONRQVQCKN-IDWQXUTKSA-N CC([C@H](CC1)CC[C@@H]1C(O)=O)(c1ncc(-c2cc(C)cc(Nc3nc(C)ccn3)c2)[s]1)O Chemical compound CC([C@H](CC1)CC[C@@H]1C(O)=O)(c1ncc(-c2cc(C)cc(Nc3nc(C)ccn3)c2)[s]1)O QEPRCONRQVQCKN-IDWQXUTKSA-N 0.000 description 1
- FGBLYXFZBWFKQV-UHFFFAOYSA-N CC1CC(CCC1C(=O)O)C=O Chemical compound CC1CC(CCC1C(=O)O)C=O FGBLYXFZBWFKQV-UHFFFAOYSA-N 0.000 description 1
- RJHYPMSSAKYVAE-SXYIOBQASA-N CCOC([C@H](CC1)CC[C@@H]1C(CO)c([s]1)ncc1Br)=O Chemical compound CCOC([C@H](CC1)CC[C@@H]1C(CO)c([s]1)ncc1Br)=O RJHYPMSSAKYVAE-SXYIOBQASA-N 0.000 description 1
- 101150006084 CHKB gene Proteins 0.000 description 1
- 0 C[C@]1(CC[C@@](*)CC1)C(*)(c1ncc(-c2cc(*)cc(Nc3nc(*)ccn3)c2)[s]1)O Chemical compound C[C@]1(CC[C@@](*)CC1)C(*)(c1ncc(-c2cc(*)cc(Nc3nc(*)ccn3)c2)[s]1)O 0.000 description 1
- LERNTVKEWCAPOY-VOGVJGKGSA-N C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 Chemical compound C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 LERNTVKEWCAPOY-VOGVJGKGSA-N 0.000 description 1
- 101100381481 Caenorhabditis elegans baz-2 gene Proteins 0.000 description 1
- 101100326430 Caenorhabditis elegans bub-1 gene Proteins 0.000 description 1
- 101100220616 Caenorhabditis elegans chk-2 gene Proteins 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- KLWPJMFMVPTNCC-UHFFFAOYSA-N Camptothecin Natural products CCC1(O)C(=O)OCC2=C1C=C3C4Nc5ccccc5C=C4CN3C2=O KLWPJMFMVPTNCC-UHFFFAOYSA-N 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 102000003847 Carboxypeptidase B2 Human genes 0.000 description 1
- 108090000201 Carboxypeptidase B2 Proteins 0.000 description 1
- 206010007572 Cardiac hypertrophy Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- AOCCBINRVIKJHY-UHFFFAOYSA-N Carmofur Chemical compound CCCCCCNC(=O)N1C=C(F)C(=O)NC1=O AOCCBINRVIKJHY-UHFFFAOYSA-N 0.000 description 1
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 1
- 102100025832 Centromere-associated protein E Human genes 0.000 description 1
- ZKLPARSLTMPFCP-UHFFFAOYSA-N Cetirizine Chemical compound C1CN(CCOCC(=O)O)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-UHFFFAOYSA-N 0.000 description 1
- JWBOIMRXGHLCPP-UHFFFAOYSA-N Chloditan Chemical compound C=1C=CC=C(Cl)C=1C(C(Cl)Cl)C1=CC=C(Cl)C=C1 JWBOIMRXGHLCPP-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 1
- 206010053567 Coagulopathies Diseases 0.000 description 1
- 208000015943 Coeliac disease Diseases 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- HVXBOLULGPECHP-WAYWQWQTSA-N Combretastatin A4 Chemical compound C1=C(O)C(OC)=CC=C1\C=C/C1=CC(OC)=C(OC)C(OC)=C1 HVXBOLULGPECHP-WAYWQWQTSA-N 0.000 description 1
- 206010069781 Complications associated with device Diseases 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- XZMCDFZZKTWFGF-UHFFFAOYSA-N Cyanamide Chemical compound NC#N XZMCDFZZKTWFGF-UHFFFAOYSA-N 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 229930105110 Cyclosporin A Natural products 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- 102000010918 Cysteinyl leukotriene receptors Human genes 0.000 description 1
- 108050001116 Cysteinyl leukotriene receptors Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- VVNCNSJFMMFHPL-VKHMYHEASA-N D-penicillamine Chemical compound CC(C)(S)[C@@H](N)C(O)=O VVNCNSJFMMFHPL-VKHMYHEASA-N 0.000 description 1
- ZBNZXTGUTAYRHI-UHFFFAOYSA-N Dasatinib Chemical compound C=1C(N2CCN(CCO)CC2)=NC(C)=NC=1NC(S1)=NC=C1C(=O)NC1=C(C)C=CC=C1Cl ZBNZXTGUTAYRHI-UHFFFAOYSA-N 0.000 description 1
- 206010051055 Deep vein thrombosis Diseases 0.000 description 1
- 206010012434 Dermatitis allergic Diseases 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 238000006646 Dess-Martin oxidation reaction Methods 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 206010012689 Diabetic retinopathy Diseases 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 208000003556 Dry Eye Syndromes Diseases 0.000 description 1
- 206010013774 Dry eye Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 239000012824 ERK inhibitor Substances 0.000 description 1
- 206010014498 Embolic stroke Diseases 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 206010014561 Emphysema Diseases 0.000 description 1
- 206010060742 Endocrine ophthalmopathy Diseases 0.000 description 1
- 102400001047 Endostatin Human genes 0.000 description 1
- 108010079505 Endostatins Proteins 0.000 description 1
- SAMRUMKYXPVKPA-VFKOLLTISA-N Enocitabine Chemical compound O=C1N=C(NC(=O)CCCCCCCCCCCCCCCCCCCCC)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 SAMRUMKYXPVKPA-VFKOLLTISA-N 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- 108010074604 Epoetin Alfa Proteins 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- DBVJJBKOTRCVKF-UHFFFAOYSA-N Etidronic acid Chemical compound OP(=O)(O)C(O)(C)P(O)(O)=O DBVJJBKOTRCVKF-UHFFFAOYSA-N 0.000 description 1
- 244000166102 Eucalyptus leucoxylon Species 0.000 description 1
- 235000004694 Eucalyptus leucoxylon Nutrition 0.000 description 1
- 206010051841 Exposure to allergen Diseases 0.000 description 1
- RSCIYYHIBVZXDI-UHFFFAOYSA-O Fagaridine Chemical compound C1=C2OCOC2=CC2=CC=C3C4=CC=C(OC)C(O)=C4C=[N+](C)C3=C21 RSCIYYHIBVZXDI-UHFFFAOYSA-O 0.000 description 1
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 1
- VTLYFUHAOXGGBS-UHFFFAOYSA-N Fe3+ Chemical compound [Fe+3] VTLYFUHAOXGGBS-UHFFFAOYSA-N 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- GGUVRMBIEPYOKL-WMVCGJOFSA-N GW 409544 Chemical compound C([C@H](NC(/C)=C\C(=O)C=1C=CC=CC=1)C(O)=O)C(C=C1)=CC=C1OCCC(=C(O1)C)N=C1C1=CC=CC=C1 GGUVRMBIEPYOKL-WMVCGJOFSA-N 0.000 description 1
- 208000036495 Gastritis atrophic Diseases 0.000 description 1
- 206010017993 Gastrointestinal neoplasms Diseases 0.000 description 1
- 241000237858 Gastropoda Species 0.000 description 1
- 241000206672 Gelidium Species 0.000 description 1
- HEMJJKBWTPKOJG-UHFFFAOYSA-N Gemfibrozil Chemical compound CC1=CC=C(C)C(OCCCC(C)(C)C(O)=O)=C1 HEMJJKBWTPKOJG-UHFFFAOYSA-N 0.000 description 1
- 206010018364 Glomerulonephritis Diseases 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- VPNYRYCIDCJBOM-UHFFFAOYSA-M Glycopyrronium bromide Chemical compound [Br-].C1[N+](C)(C)CCC1OC(=O)C(O)(C=1C=CC=CC=1)C1CCCC1 VPNYRYCIDCJBOM-UHFFFAOYSA-M 0.000 description 1
- 208000024869 Goodpasture syndrome Diseases 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 206010072579 Granulomatosis with polyangiitis Diseases 0.000 description 1
- 208000015023 Graves' disease Diseases 0.000 description 1
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 1
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 1
- 238000007341 Heck reaction Methods 0.000 description 1
- 208000035186 Hemolytic Autoimmune Anemia Diseases 0.000 description 1
- 206010062506 Heparin-induced thrombocytopenia Diseases 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 102000003834 Histamine H1 Receptors Human genes 0.000 description 1
- 108090000110 Histamine H1 Receptors Proteins 0.000 description 1
- 102000003964 Histone deacetylase Human genes 0.000 description 1
- 108090000353 Histone deacetylase Proteins 0.000 description 1
- 101001034652 Homo sapiens Insulin-like growth factor 1 receptor Proteins 0.000 description 1
- 101000605743 Homo sapiens Kinesin-like protein KIF23 Proteins 0.000 description 1
- 101000844245 Homo sapiens Non-receptor tyrosine-protein kinase TYK2 Proteins 0.000 description 1
- 101001059454 Homo sapiens Serine/threonine-protein kinase MARK2 Proteins 0.000 description 1
- 101000997832 Homo sapiens Tyrosine-protein kinase JAK2 Proteins 0.000 description 1
- 101000851007 Homo sapiens Vascular endothelial growth factor receptor 2 Proteins 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- VSNHCAURESNICA-UHFFFAOYSA-N Hydroxyurea Chemical compound NC(=O)NO VSNHCAURESNICA-UHFFFAOYSA-N 0.000 description 1
- 206010020649 Hyperkeratosis Diseases 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- 229940124790 IL-6 inhibitor Drugs 0.000 description 1
- MPBVHIBUJCELCL-UHFFFAOYSA-N Ibandronate Chemical compound CCCCCN(C)CCC(O)(P(O)(O)=O)P(O)(O)=O MPBVHIBUJCELCL-UHFFFAOYSA-N 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 description 1
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 description 1
- 102000009438 IgE Receptors Human genes 0.000 description 1
- 108010073816 IgE Receptors Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 102100021854 Inhibitor of nuclear factor kappa-B kinase subunit beta Human genes 0.000 description 1
- 101710205525 Inhibitor of nuclear factor kappa-B kinase subunit beta Proteins 0.000 description 1
- 102000014429 Insulin-like growth factor Human genes 0.000 description 1
- 102100039688 Insulin-like growth factor 1 receptor Human genes 0.000 description 1
- 102100040018 Interferon alpha-2 Human genes 0.000 description 1
- 108010079944 Interferon-alpha2b Proteins 0.000 description 1
- 102000051628 Interleukin-1 receptor antagonist Human genes 0.000 description 1
- 108700021006 Interleukin-1 receptor antagonist Proteins 0.000 description 1
- 102100026018 Interleukin-1 receptor antagonist protein Human genes 0.000 description 1
- 101710144554 Interleukin-1 receptor antagonist protein Proteins 0.000 description 1
- 102100030694 Interleukin-11 Human genes 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 102100039064 Interleukin-3 Human genes 0.000 description 1
- 206010022941 Iridocyclitis Diseases 0.000 description 1
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 1
- SHGAZHPCJJPHSC-NUEINMDLSA-N Isotretinoin Chemical compound OC(=O)C=C(C)/C=C/C=C(C)C=CC1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-NUEINMDLSA-N 0.000 description 1
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 1
- 108010024121 Janus Kinases Proteins 0.000 description 1
- 102000015617 Janus Kinases Human genes 0.000 description 1
- 208000007766 Kaposi sarcoma Diseases 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- 206010023330 Keloid scar Diseases 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 102100038406 Kinesin-like protein KIF23 Human genes 0.000 description 1
- 102100023424 Kinesin-like protein KIF2C Human genes 0.000 description 1
- 101710134369 Kinesin-like protein KIF2C Proteins 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- 239000004395 L-leucine Substances 0.000 description 1
- 235000019454 L-leucine Nutrition 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 239000002067 L01XE06 - Dasatinib Substances 0.000 description 1
- 239000002136 L01XE07 - Lapatinib Substances 0.000 description 1
- 239000005536 L01XE08 - Nilotinib Substances 0.000 description 1
- 239000002177 L01XE27 - Ibrutinib Substances 0.000 description 1
- CZQHHVNHHHRRDU-UHFFFAOYSA-N LY294002 Chemical compound C1=CC=C2C(=O)C=C(N3CCOCC3)OC2=C1C1=CC=CC=C1 CZQHHVNHHHRRDU-UHFFFAOYSA-N 0.000 description 1
- DAQAKHDKYAWHCG-UHFFFAOYSA-N Lactacystin Natural products CC(=O)NC(C(O)=O)CSC(=O)C1(C(O)C(C)C)NC(=O)C(C)C1O DAQAKHDKYAWHCG-UHFFFAOYSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- XNRVGTHNYCNCFF-UHFFFAOYSA-N Lapatinib ditosylate monohydrate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1.CC1=CC=C(S(O)(=O)=O)C=C1.O1C(CNCCS(=O)(=O)C)=CC=C1C1=CC=C(N=CN=C2NC=3C=C(Cl)C(OCC=4C=C(F)C=CC=4)=CC=3)C2=C1 XNRVGTHNYCNCFF-UHFFFAOYSA-N 0.000 description 1
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 1
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 description 1
- 229940113306 Ligase inhibitor Drugs 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 229940124761 MMP inhibitor Drugs 0.000 description 1
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 1
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 description 1
- 108010047230 Member 1 Subfamily B ATP Binding Cassette Transporter Proteins 0.000 description 1
- XOGTZOOQQBDUSI-UHFFFAOYSA-M Mesna Chemical compound [Na+].[O-]S(=O)(=O)CCS XOGTZOOQQBDUSI-UHFFFAOYSA-M 0.000 description 1
- 206010027480 Metastatic malignant melanoma Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- QXKHYNVANLEOEG-UHFFFAOYSA-N Methoxsalen Chemical compound C1=CC(=O)OC2=C1C=C1C=COC1=C2OC QXKHYNVANLEOEG-UHFFFAOYSA-N 0.000 description 1
- 208000019695 Migraine disease Diseases 0.000 description 1
- PCZOHLXUXFIOCF-UHFFFAOYSA-N Monacolin X Natural products C12C(OC(=O)C(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 PCZOHLXUXFIOCF-UHFFFAOYSA-N 0.000 description 1
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical compound CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 1
- 101100073787 Mus musculus Kif20b gene Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 229940121948 Muscarinic receptor antagonist Drugs 0.000 description 1
- 208000007101 Muscle Cramp Diseases 0.000 description 1
- 208000002231 Muscle Neoplasms Diseases 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- 208000014767 Myeloproliferative disease Diseases 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 1
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- ZMGFEKDSJROBLW-BXHJMNKNSA-N N=1C=C(Br)SC=1C(N)[C@H]1CC[C@H](C(O)=O)CC1 Chemical compound N=1C=C(Br)SC=1C(N)[C@H]1CC[C@H](C(O)=O)CC1 ZMGFEKDSJROBLW-BXHJMNKNSA-N 0.000 description 1
- VLDFRESMBCRDBK-IWTGGTBMSA-N N=1C=C(Br)SC=1C(O)(C)[C@H]1CC[C@H](C(O)=O)CC1 Chemical compound N=1C=C(Br)SC=1C(O)(C)[C@H]1CC[C@H](C(O)=O)CC1 VLDFRESMBCRDBK-IWTGGTBMSA-N 0.000 description 1
- OMTRTTACTDRJAT-JALUVWQTSA-N N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](N)CC1 Chemical compound N=1C=CSC=1C(O)(C)[C@H]1CC[C@H](N)CC1 OMTRTTACTDRJAT-JALUVWQTSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 1
- JAUOIFJMECXRGI-UHFFFAOYSA-N Neoclaritin Chemical compound C=1C(Cl)=CC=C2C=1CCC1=CC=CN=C1C2=C1CCNCC1 JAUOIFJMECXRGI-UHFFFAOYSA-N 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 206010029350 Neurotoxicity Diseases 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 1
- 102100032028 Non-receptor tyrosine-protein kinase TYK2 Human genes 0.000 description 1
- 229920000305 Nylon 6,10 Polymers 0.000 description 1
- QSSYUVGWWQBOBQ-YXSASFKJSA-N OC144-093 Chemical compound CCO/C=C\CC(C=C1)=CC=C1C1=NC(C(C=C2)=CC=C2NC(C)C)=C(C(C=C2)=CC=C2NC(C)C)N1 QSSYUVGWWQBOBQ-YXSASFKJSA-N 0.000 description 1
- REYJJPSVUYRZGE-UHFFFAOYSA-N Octadecylamine Chemical compound CCCCCCCCCCCCCCCCCCN REYJJPSVUYRZGE-UHFFFAOYSA-N 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 239000012661 PARP inhibitor Substances 0.000 description 1
- 102000038030 PI3Ks Human genes 0.000 description 1
- 108091007960 PI3Ks Proteins 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 206010034277 Pemphigoid Diseases 0.000 description 1
- 229940080774 Peroxisome proliferator-activated receptor gamma agonist Drugs 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- 229940123932 Phosphodiesterase 4 inhibitor Drugs 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229940121906 Poly ADP ribose polymerase inhibitor Drugs 0.000 description 1
- 229920001710 Polyorthoester Polymers 0.000 description 1
- TUZYXOIXSAXUGO-UHFFFAOYSA-N Pravastatin Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(O)C=C21 TUZYXOIXSAXUGO-UHFFFAOYSA-N 0.000 description 1
- HFVNWDWLWUCIHC-GUPDPFMOSA-N Prednimustine Chemical compound O=C([C@@]1(O)CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)[C@@H](O)C[C@@]21C)COC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 HFVNWDWLWUCIHC-GUPDPFMOSA-N 0.000 description 1
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 description 1
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- 208000010378 Pulmonary Embolism Diseases 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- AHHFEZNOXOZZQA-ZEBDFXRSSA-N Ranimustine Chemical compound CO[C@H]1O[C@H](CNC(=O)N(CCCl)N=O)[C@@H](O)[C@H](O)[C@H]1O AHHFEZNOXOZZQA-ZEBDFXRSSA-N 0.000 description 1
- 101100372762 Rattus norvegicus Flt1 gene Proteins 0.000 description 1
- 108090000873 Receptor Protein-Tyrosine Kinases Proteins 0.000 description 1
- 102000004278 Receptor Protein-Tyrosine Kinases Human genes 0.000 description 1
- 208000033464 Reiter syndrome Diseases 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 206010063897 Renal ischaemia Diseases 0.000 description 1
- IIDJRNMFWXDHID-UHFFFAOYSA-N Risedronic acid Chemical compound OP(=O)(O)C(P(O)(O)=O)(O)CC1=CC=CN=C1 IIDJRNMFWXDHID-UHFFFAOYSA-N 0.000 description 1
- YJDYDFNKCBANTM-QCWCSKBGSA-N SDZ PSC 833 Chemical compound C\C=C\C[C@@H](C)C(=O)[C@@H]1N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C(=O)[C@H](C(C)C)NC1=O YJDYDFNKCBANTM-QCWCSKBGSA-N 0.000 description 1
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 1
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 1
- 102100031463 Serine/threonine-protein kinase PLK1 Human genes 0.000 description 1
- 101710183160 Serine/threonine-protein kinase PLK1 Proteins 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 229910004298 SiO 2 Inorganic materials 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 239000004280 Sodium formate Substances 0.000 description 1
- BCKXLBQYZLBQEK-KVVVOXFISA-M Sodium oleate Chemical compound [Na+].CCCCCCCC\C=C/CCCCCCCC([O-])=O BCKXLBQYZLBQEK-KVVVOXFISA-M 0.000 description 1
- UIRKNQLZZXALBI-MSVGPLKSSA-N Squalamine Chemical compound C([C@@H]1C[C@H]2O)[C@@H](NCCCNCCCCN)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@H](C)CC[C@H](C(C)C)OS(O)(=O)=O)[C@@]2(C)CC1 UIRKNQLZZXALBI-MSVGPLKSSA-N 0.000 description 1
- UIRKNQLZZXALBI-UHFFFAOYSA-N Squalamine Natural products OC1CC2CC(NCCCNCCCCN)CCC2(C)C2C1C1CCC(C(C)CCC(C(C)C)OS(O)(=O)=O)C1(C)CC2 UIRKNQLZZXALBI-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- 108091008874 T cell receptors Proteins 0.000 description 1
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 1
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 1
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 1
- LGGHDPFKSSRQNS-UHFFFAOYSA-N Tariquidar Chemical compound C1=CC=CC2=CC(C(=O)NC3=CC(OC)=C(OC)C=C3C(=O)NC3=CC=C(C=C3)CCN3CCC=4C=C(C(=CC=4C3)OC)OC)=CN=C21 LGGHDPFKSSRQNS-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- 206010043647 Thrombotic Stroke Diseases 0.000 description 1
- 201000007023 Thrombotic Thrombocytopenic Purpura Diseases 0.000 description 1
- IVTVGDXNLFLDRM-HNNXBMFYSA-N Tomudex Chemical compound C=1C=C2NC(C)=NC(=O)C2=CC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)S1 IVTVGDXNLFLDRM-HNNXBMFYSA-N 0.000 description 1
- 206010044221 Toxic encephalopathy Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 208000032109 Transient ischaemic attack Diseases 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- RTKIYFITIVXBLE-UHFFFAOYSA-N Trichostatin A Natural products ONC(=O)C=CC(C)=CC(C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-UHFFFAOYSA-N 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 102100033444 Tyrosine-protein kinase JAK2 Human genes 0.000 description 1
- 102000006275 Ubiquitin-Protein Ligases Human genes 0.000 description 1
- 108010083111 Ubiquitin-Protein Ligases Proteins 0.000 description 1
- 208000007814 Unstable Angina Diseases 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 102000016549 Vascular Endothelial Growth Factor Receptor-2 Human genes 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 1
- 208000024248 Vascular System injury Diseases 0.000 description 1
- 208000012339 Vascular injury Diseases 0.000 description 1
- GXBMIBRIOWHPDT-UHFFFAOYSA-N Vasopressin Natural products N1C(=O)C(CC=2C=C(O)C=CC=2)NC(=O)C(N)CSSCC(C(=O)N2C(CCC2)C(=O)NC(CCCN=C(N)N)C(=O)NCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(CCC(N)=O)NC(=O)C1CC1=CC=CC=C1 GXBMIBRIOWHPDT-UHFFFAOYSA-N 0.000 description 1
- 108010004977 Vasopressins Proteins 0.000 description 1
- 102000002852 Vasopressins Human genes 0.000 description 1
- 206010047163 Vasospasm Diseases 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- PCWZKQSKUXXDDJ-UHFFFAOYSA-N Xanthotoxin Natural products COCc1c2OC(=O)C=Cc2cc3ccoc13 PCWZKQSKUXXDDJ-UHFFFAOYSA-N 0.000 description 1
- HUCJFAOMUPXHDK-UHFFFAOYSA-N Xylometazoline Chemical compound CC1=CC(C(C)(C)C)=CC(C)=C1CC1=NCCN1 HUCJFAOMUPXHDK-UHFFFAOYSA-N 0.000 description 1
- YEEZWCHGZNKEEK-UHFFFAOYSA-N Zafirlukast Chemical compound COC1=CC(C(=O)NS(=O)(=O)C=2C(=CC=CC=2)C)=CC=C1CC(C1=C2)=CN(C)C1=CC=C2NC(=O)OC1CCCC1 YEEZWCHGZNKEEK-UHFFFAOYSA-N 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- VPNYRYCIDCJBOM-ZFNKBKEPSA-M [(3r)-1,1-dimethylpyrrolidin-1-ium-3-yl] (2r)-2-cyclopentyl-2-hydroxy-2-phenylacetate;bromide Chemical compound [Br-].C1[N+](C)(C)CC[C@H]1OC(=O)[C@](O)(C=1C=CC=CC=1)C1CCCC1 VPNYRYCIDCJBOM-ZFNKBKEPSA-M 0.000 description 1
- YYAZJTUGSQOFHG-IAVNQIGZSA-N [(6s,8s,10s,11s,13s,14s,16r,17r)-6,9-difluoro-17-(fluoromethylsulfanylcarbonyl)-11-hydroxy-10,13,16-trimethyl-3-oxo-6,7,8,11,12,14,15,16-octahydrocyclopenta[a]phenanthren-17-yl] propanoate;2-(hydroxymethyl)-4-[1-hydroxy-2-[6-(4-phenylbutoxy)hexylamino]eth Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1.C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)C1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O YYAZJTUGSQOFHG-IAVNQIGZSA-N 0.000 description 1
- CKXIPXAIFMTQCS-LRDUUELOSA-N [2-[(2s,4s)-4-[(2r,3r,4r,5s,6s)-3-fluoro-4,5-dihydroxy-6-methyloxan-2-yl]oxy-2,5,12-trihydroxy-7-methoxy-6,11-dioxo-3,4-dihydro-1h-tetracen-2-yl]-2-oxoethyl] 3-aminopropanoate Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)COC(=O)CCN)[C@@H]1O[C@@H](C)[C@@H](O)[C@@H](O)[C@H]1F CKXIPXAIFMTQCS-LRDUUELOSA-N 0.000 description 1
- JEQZBROLGZVPFD-UHFFFAOYSA-N [3-(aminomethyl)-5-iodophenyl]methanol Chemical compound NCC1=CC(I)=CC(CO)=C1 JEQZBROLGZVPFD-UHFFFAOYSA-N 0.000 description 1
- XKMJQGPUCURYIM-UHFFFAOYSA-N [3-iodo-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]methanol Chemical compound OCC1=CC(I)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 XKMJQGPUCURYIM-UHFFFAOYSA-N 0.000 description 1
- ILWQPVXNQPKQPO-UHFFFAOYSA-N [5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methanol Chemical compound C=1C(C=2SC(CO)=NC=2)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 ILWQPVXNQPKQPO-UHFFFAOYSA-N 0.000 description 1
- MXRQMVJXZTTXCN-FKJYKYSXSA-N [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)C(C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 Chemical compound [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)C(C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 MXRQMVJXZTTXCN-FKJYKYSXSA-N 0.000 description 1
- MXRQMVJXZTTXCN-WDSHCNNQSA-N [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)[C@](C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 Chemical compound [O-]C(=O)C(F)(F)F.C=1C(C=2SC(=NC=2)[C@](C)(O)[C@@H]2CC[C@H](CC2)C2=NNN=N2)=CC(C)=CC=1NC1=NC(C(F)(F)F)=CC=[NH+]1 MXRQMVJXZTTXCN-WDSHCNNQSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 229940124532 absorption promoter Drugs 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 229960005012 aclidinium bromide Drugs 0.000 description 1
- XLAKJQPTOJHYDR-QTQXQZBYSA-M aclidinium bromide Chemical compound [Br-].C([C@@H](C(CC1)CC2)OC(=O)C(O)(C=3SC=CC=3)C=3SC=CC=3)[N+]21CCCOC1=CC=CC=C1 XLAKJQPTOJHYDR-QTQXQZBYSA-M 0.000 description 1
- 229950003218 actarit Drugs 0.000 description 1
- 229940119059 actemra Drugs 0.000 description 1
- 150000001263 acyl chlorides Chemical class 0.000 description 1
- 229960002964 adalimumab Drugs 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 239000000808 adrenergic beta-agonist Substances 0.000 description 1
- 229940090167 advair Drugs 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 238000005054 agglomeration Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 229960000548 alemtuzumab Drugs 0.000 description 1
- 229940062527 alendronate Drugs 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- 201000010435 allergic urticaria Diseases 0.000 description 1
- OFCNXPDARWKPPY-UHFFFAOYSA-N allopurinol Chemical compound OC1=NC=NC2=C1C=NN2 OFCNXPDARWKPPY-UHFFFAOYSA-N 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- 102000030619 alpha-1 Adrenergic Receptor Human genes 0.000 description 1
- 108020004102 alpha-1 Adrenergic Receptor Proteins 0.000 description 1
- 102000030484 alpha-2 Adrenergic Receptor Human genes 0.000 description 1
- 108020004101 alpha-2 Adrenergic Receptor Proteins 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- BIIVYFLTOXDAOV-YVEFUNNKSA-N alvocidib Chemical compound O[C@@H]1CN(C)CC[C@@H]1C1=C(O)C=C(O)C2=C1OC(C=1C(=CC=CC=1)Cl)=CC2=O BIIVYFLTOXDAOV-YVEFUNNKSA-N 0.000 description 1
- 229950010817 alvocidib Drugs 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229960003437 aminoglutethimide Drugs 0.000 description 1
- ROBVIMPUHSLWNV-UHFFFAOYSA-N aminoglutethimide Chemical compound C=1C=C(N)C=CC=1C1(CC)CCC(=O)NC1=O ROBVIMPUHSLWNV-UHFFFAOYSA-N 0.000 description 1
- PECIYKGSSMCNHN-UHFFFAOYSA-N aminophylline Chemical compound NCCN.O=C1N(C)C(=O)N(C)C2=NC=N[C]21.O=C1N(C)C(=O)N(C)C2=NC=N[C]21 PECIYKGSSMCNHN-UHFFFAOYSA-N 0.000 description 1
- 229960003556 aminophylline Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- VJZITPJGSQKZMX-XDPRQOKASA-N amrubicin Chemical compound O([C@H]1C[C@](CC2=C(O)C=3C(=O)C4=CC=CC=C4C(=O)C=3C(O)=C21)(N)C(=O)C)[C@H]1C[C@H](O)[C@H](O)CO1 VJZITPJGSQKZMX-XDPRQOKASA-N 0.000 description 1
- 229960002550 amrubicin Drugs 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 230000036783 anaphylactic response Effects 0.000 description 1
- 208000003455 anaphylaxis Diseases 0.000 description 1
- 229960002932 anastrozole Drugs 0.000 description 1
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000004037 angiogenesis inhibitor Substances 0.000 description 1
- 229940121369 angiogenesis inhibitor Drugs 0.000 description 1
- 239000002333 angiotensin II receptor antagonist Substances 0.000 description 1
- CIDNKDMVSINJCG-GKXONYSUSA-N annamycin Chemical compound I[C@@H]1[C@H](O)[C@@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(=O)CO)C1 CIDNKDMVSINJCG-GKXONYSUSA-N 0.000 description 1
- 201000004612 anterior uveitis Diseases 0.000 description 1
- 230000001387 anti-histamine Effects 0.000 description 1
- 230000003388 anti-hormonal effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960003121 arginine Drugs 0.000 description 1
- KBZOIRJILGZLEJ-LGYYRGKSSA-N argipressin Chemical compound C([C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSC[C@@H](C(N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)=O)N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)NCC(N)=O)C1=CC=CC=C1 KBZOIRJILGZLEJ-LGYYRGKSSA-N 0.000 description 1
- 239000003886 aromatase inhibitor Substances 0.000 description 1
- 229940046844 aromatase inhibitors Drugs 0.000 description 1
- 208000011775 arteriosclerosis disease Diseases 0.000 description 1
- 239000008122 artificial sweetener Substances 0.000 description 1
- 235000021311 artificial sweeteners Nutrition 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- MCGDSOGUHLTADD-UHFFFAOYSA-N arzoxifene Chemical compound C1=CC(OC)=CC=C1C1=C(OC=2C=CC(OCCN3CCCCC3)=CC=2)C2=CC=C(O)C=C2S1 MCGDSOGUHLTADD-UHFFFAOYSA-N 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- FZCSTZYAHCUGEM-UHFFFAOYSA-N aspergillomarasmine B Natural products OC(=O)CNC(C(O)=O)CNC(C(O)=O)CC(O)=O FZCSTZYAHCUGEM-UHFFFAOYSA-N 0.000 description 1
- GXDALQBWZGODGZ-UHFFFAOYSA-N astemizole Chemical compound C1=CC(OC)=CC=C1CCN1CCC(NC=2N(C3=CC=CC=C3N=2)CC=2C=CC(F)=CC=2)CC1 GXDALQBWZGODGZ-UHFFFAOYSA-N 0.000 description 1
- TWHSQQYCDVSBRK-UHFFFAOYSA-N asulacrine Chemical compound C12=CC=CC(C)=C2N=C2C(C(=O)NC)=CC=CC2=C1NC1=CC=C(NS(C)(=O)=O)C=C1OC TWHSQQYCDVSBRK-UHFFFAOYSA-N 0.000 description 1
- 229950011088 asulacrine Drugs 0.000 description 1
- 229960005370 atorvastatin Drugs 0.000 description 1
- 239000003719 aurora kinase inhibitor Substances 0.000 description 1
- 229940009100 aurothiomalate Drugs 0.000 description 1
- XJHSMFDIQHVMCY-UHFFFAOYSA-M aurothiomalic acid Chemical compound OC(=O)CC(S[Au])C(O)=O XJHSMFDIQHVMCY-UHFFFAOYSA-M 0.000 description 1
- 201000000448 autoimmune hemolytic anemia Diseases 0.000 description 1
- 229960002756 azacitidine Drugs 0.000 description 1
- WOIIIUDZSOLAIW-NSHDSACASA-N azapropazone Chemical compound C1=C(C)C=C2N3C(=O)[C@H](CC=C)C(=O)N3C(N(C)C)=NC2=C1 WOIIIUDZSOLAIW-NSHDSACASA-N 0.000 description 1
- 229960001671 azapropazone Drugs 0.000 description 1
- 229960002170 azathioprine Drugs 0.000 description 1
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 1
- 229960004574 azelastine Drugs 0.000 description 1
- HNYOPLTXPVRDBG-UHFFFAOYSA-N barbituric acid Chemical compound O=C1CC(=O)NC(=O)N1 HNYOPLTXPVRDBG-UHFFFAOYSA-N 0.000 description 1
- 229950000210 beclometasone dipropionate Drugs 0.000 description 1
- NBMKJKDGKREAPL-DVTGEIKXSA-N beclomethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O NBMKJKDGKREAPL-DVTGEIKXSA-N 0.000 description 1
- 229960003094 belinostat Drugs 0.000 description 1
- NCNRHFGMJRPRSK-MDZDMXLPSA-N belinostat Chemical compound ONC(=O)\C=C\C1=CC=CC(S(=O)(=O)NC=2C=CC=CC=2)=C1 NCNRHFGMJRPRSK-MDZDMXLPSA-N 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- ABSXPNGWJFAPRT-UHFFFAOYSA-N benzenesulfonic acid;n-[3-[[5-fluoro-2-[4-(2-methoxyethoxy)anilino]pyrimidin-4-yl]amino]phenyl]prop-2-enamide Chemical compound OS(=O)(=O)C1=CC=CC=C1.C1=CC(OCCOC)=CC=C1NC1=NC=C(F)C(NC=2C=C(NC(=O)C=C)C=CC=2)=N1 ABSXPNGWJFAPRT-UHFFFAOYSA-N 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- KEPVPNRFMVTTKV-UHFFFAOYSA-N benzyl n-[4-[methoxy(methyl)carbamoyl]cyclohexyl]carbamate Chemical compound C1CC(C(=O)N(C)OC)CCC1NC(=O)OCC1=CC=CC=C1 KEPVPNRFMVTTKV-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 229960003237 betaine Drugs 0.000 description 1
- 229960000397 bevacizumab Drugs 0.000 description 1
- 150000005347 biaryls Chemical class 0.000 description 1
- 229960000997 bicalutamide Drugs 0.000 description 1
- JAPMJSVZDUYFKL-UHFFFAOYSA-N bicyclo[3.1.0]hexane Chemical compound C1CCC2CC21 JAPMJSVZDUYFKL-UHFFFAOYSA-N 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- HTJWUNNIRKDDIV-UHFFFAOYSA-N bis(1-adamantyl)-butylphosphane Chemical compound C1C(C2)CC(C3)CC2CC13P(CCCC)C1(C2)CC(C3)CC2CC3C1 HTJWUNNIRKDDIV-UHFFFAOYSA-N 0.000 description 1
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 1
- 229950008548 bisantrene Drugs 0.000 description 1
- 150000004663 bisphosphonates Chemical class 0.000 description 1
- HODFCFXCOMKRCG-UHFFFAOYSA-N bitolterol mesylate Chemical compound CS([O-])(=O)=O.C1=CC(C)=CC=C1C(=O)OC1=CC=C(C(O)C[NH2+]C(C)(C)C)C=C1OC(=O)C1=CC=C(C)C=C1 HODFCFXCOMKRCG-UHFFFAOYSA-N 0.000 description 1
- 229960000585 bitolterol mesylate Drugs 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 208000015294 blood coagulation disease Diseases 0.000 description 1
- GMJWGJSDPOAZTP-MIDYMNAOSA-N bms-188797 Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](OC(C)=O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)C=4C=CC=CC=4)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)OC)C(=O)C1=CC=CC=C1 GMJWGJSDPOAZTP-MIDYMNAOSA-N 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 208000000594 bullous pemphigoid Diseases 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 210000001217 buttock Anatomy 0.000 description 1
- 229960001948 caffeine Drugs 0.000 description 1
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical compound C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 1
- 229940127093 camptothecin Drugs 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- WNRZHQBJSXRYJK-UHFFFAOYSA-N carboxyamidotriazole Chemical compound NC1=C(C(=O)N)N=NN1CC(C=C1Cl)=CC(Cl)=C1C(=O)C1=CC=C(Cl)C=C1 WNRZHQBJSXRYJK-UHFFFAOYSA-N 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229940105329 carboxymethylcellulose Drugs 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 229960003261 carmofur Drugs 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- 229960000590 celecoxib Drugs 0.000 description 1
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 230000012820 cell cycle checkpoint Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000011712 cell development Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000011748 cell maturation Effects 0.000 description 1
- 230000012292 cell migration Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 108010031379 centromere protein E Proteins 0.000 description 1
- 229960001803 cetirizine Drugs 0.000 description 1
- 229960005395 cetuximab Drugs 0.000 description 1
- IQCIQDNWBGEGRL-UHFFFAOYSA-N chembl1614651 Chemical compound O=C1C2=C(O)C=CC(O)=C2N2N=C(CNCCO)C3=CC=C(NCCCN)C1=C32 IQCIQDNWBGEGRL-UHFFFAOYSA-N 0.000 description 1
- CFBUZOUXXHZCFB-OYOVHJISSA-N chembl511115 Chemical compound COC1=CC=C([C@@]2(CC[C@H](CC2)C(O)=O)C#N)C=C1OC1CCCC1 CFBUZOUXXHZCFB-OYOVHJISSA-N 0.000 description 1
- 239000013043 chemical agent Substances 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 239000000812 cholinergic antagonist Substances 0.000 description 1
- 208000023819 chronic asthma Diseases 0.000 description 1
- 208000016644 chronic atrophic gastritis Diseases 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 229950001653 cilomilast Drugs 0.000 description 1
- 229940090100 cimzia Drugs 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- ACSIXWWBWUQEHA-UHFFFAOYSA-N clodronic acid Chemical compound OP(O)(=O)C(Cl)(Cl)P(O)(O)=O ACSIXWWBWUQEHA-UHFFFAOYSA-N 0.000 description 1
- 229960002286 clodronic acid Drugs 0.000 description 1
- WDDPHFBMKLOVOX-AYQXTPAHSA-N clofarabine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1F WDDPHFBMKLOVOX-AYQXTPAHSA-N 0.000 description 1
- 229960000928 clofarabine Drugs 0.000 description 1
- 229960001214 clofibrate Drugs 0.000 description 1
- KNHUKKLJHYUCFP-UHFFFAOYSA-N clofibrate Chemical compound CCOC(=O)C(C)(C)OC1=CC=C(Cl)C=C1 KNHUKKLJHYUCFP-UHFFFAOYSA-N 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- LGZKGOGODCLQHG-UHFFFAOYSA-N combretastatin Natural products C1=C(O)C(OC)=CC=C1CC(O)C1=CC(OC)=C(OC)C(OC)=C1 LGZKGOGODCLQHG-UHFFFAOYSA-N 0.000 description 1
- 229960005537 combretastatin A-4 Drugs 0.000 description 1
- HVXBOLULGPECHP-UHFFFAOYSA-N combretastatin A4 Natural products C1=C(O)C(OC)=CC=C1C=CC1=CC(OC)=C(OC)C(OC)=C1 HVXBOLULGPECHP-UHFFFAOYSA-N 0.000 description 1
- 238000010668 complexation reaction Methods 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- GBRBMTNGQBKBQE-UHFFFAOYSA-L copper;diiodide Chemical compound I[Cu]I GBRBMTNGQBKBQE-UHFFFAOYSA-L 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 210000004087 cornea Anatomy 0.000 description 1
- 238000007887 coronary angioplasty Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- POADTFBBIXOWFJ-VWLOTQADSA-N cositecan Chemical compound C1=CC=C2C(CC[Si](C)(C)C)=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 POADTFBBIXOWFJ-VWLOTQADSA-N 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- COFJBSXICYYSKG-OAUVCNBTSA-N cph2u7dndy Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(N)=O)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 COFJBSXICYYSKG-OAUVCNBTSA-N 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 1
- JCWIWBWXCVGEAN-UHFFFAOYSA-L cyclopentyl(diphenyl)phosphane;dichloropalladium;iron Chemical compound [Fe].Cl[Pd]Cl.[CH]1[CH][CH][CH][C]1P(C=1C=CC=CC=1)C1=CC=CC=C1.[CH]1[CH][CH][CH][C]1P(C=1C=CC=CC=1)C1=CC=CC=C1 JCWIWBWXCVGEAN-UHFFFAOYSA-L 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 108010057085 cytokine receptors Proteins 0.000 description 1
- 102000003675 cytokine receptors Human genes 0.000 description 1
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 description 1
- 229960003901 dacarbazine Drugs 0.000 description 1
- 229960004969 dalteparin Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 229960002448 dasatinib Drugs 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 201000001981 dermatomyositis Diseases 0.000 description 1
- 229960001271 desloratadine Drugs 0.000 description 1
- NKLCNNUWBJBICK-UHFFFAOYSA-N dess–martin periodinane Chemical compound C1=CC=C2I(OC(=O)C)(OC(C)=O)(OC(C)=O)OC(=O)C2=C1 NKLCNNUWBJBICK-UHFFFAOYSA-N 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- NIJJYAXOARWZEE-UHFFFAOYSA-N di-n-propyl-acetic acid Natural products CCCC(C(O)=O)CCC NIJJYAXOARWZEE-UHFFFAOYSA-N 0.000 description 1
- 150000004985 diamines Chemical class 0.000 description 1
- WMKGGPCROCCUDY-PHEQNACWSA-N dibenzylideneacetone Chemical compound C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 WMKGGPCROCCUDY-PHEQNACWSA-N 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 1
- 229960001259 diclofenac Drugs 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- LFQCJSBXBZRMTN-OAQYLSRUSA-N diflomotecan Chemical compound CC[C@@]1(O)CC(=O)OCC(C2=O)=C1C=C1N2CC2=CC3=CC(F)=C(F)C=C3N=C21 LFQCJSBXBZRMTN-OAQYLSRUSA-N 0.000 description 1
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- NYDXNILOWQXUOF-UHFFFAOYSA-L disodium;2-[[4-[2-(2-amino-4-oxo-1,7-dihydropyrrolo[2,3-d]pyrimidin-5-yl)ethyl]benzoyl]amino]pentanedioate Chemical compound [Na+].[Na+].C=1NC=2NC(N)=NC(=O)C=2C=1CCC1=CC=C(C(=O)NC(CCC([O-])=O)C([O-])=O)C=C1 NYDXNILOWQXUOF-UHFFFAOYSA-L 0.000 description 1
- IWLDTXOHXPDPQG-UHFFFAOYSA-L disodium;hydroxy-[1-hydroxy-1-[hydroxy(oxido)phosphoryl]-3-pyrrolidin-1-ylpropyl]phosphinate Chemical compound [Na+].[Na+].OP(=O)(O)C(P([O-])([O-])=O)(O)CCN1CCCC1 IWLDTXOHXPDPQG-UHFFFAOYSA-L 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 208000009190 disseminated intravascular coagulation Diseases 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- VSJKWCGYPAHWDS-UHFFFAOYSA-N dl-camptothecin Natural products C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)C5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-UHFFFAOYSA-N 0.000 description 1
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 1
- 229960003668 docetaxel Drugs 0.000 description 1
- AMRJKAQTDDKMCE-UHFFFAOYSA-N dolastatin Chemical compound CC(C)C(N(C)C)C(=O)NC(C(C)C)C(=O)N(C)C(C(C)C)C(OC)CC(=O)N1CCCC1C(OC)C(C)C(=O)NC(C=1SC=CN=1)CC1=CC=CC=C1 AMRJKAQTDDKMCE-UHFFFAOYSA-N 0.000 description 1
- 229930188854 dolastatin Natural products 0.000 description 1
- 238000011143 downstream manufacturing Methods 0.000 description 1
- 230000007783 downstream signaling Effects 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 229940103439 dulera Drugs 0.000 description 1
- XHQZXHMRBXBPEL-UHFFFAOYSA-N eaton reagent Chemical compound CS(O)(=O)=O.O1P(O2)(=O)OP3(=O)OP1(=O)OP2(=O)O3 XHQZXHMRBXBPEL-UHFFFAOYSA-N 0.000 description 1
- 229960002224 eculizumab Drugs 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000003821 enantio-separation Methods 0.000 description 1
- 229940073621 enbrel Drugs 0.000 description 1
- 229950011487 enocitabine Drugs 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 201000001564 eosinophilic gastroenteritis Diseases 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- 229960003388 epoetin alfa Drugs 0.000 description 1
- 229930013356 epothilone Natural products 0.000 description 1
- 150000003883 epothilone derivatives Chemical class 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 229960001842 estramustine Drugs 0.000 description 1
- FRPJXPJMRWBBIH-RBRWEJTLSA-N estramustine Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 FRPJXPJMRWBBIH-RBRWEJTLSA-N 0.000 description 1
- 239000002834 estrogen receptor modulator Substances 0.000 description 1
- 229960000403 etanercept Drugs 0.000 description 1
- DGKKLYPEMLTKGS-SQYUCLKFSA-N ethyl (1r,2s,4r)-4-[(1s)-1-(5-bromo-1,3-thiazol-2-yl)-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1[C@H](C)[C@H](C(=O)OCC)CC[C@H]1[C@](C)(O)C1=NC=C(Br)S1 DGKKLYPEMLTKGS-SQYUCLKFSA-N 0.000 description 1
- DGKKLYPEMLTKGS-LMCGPQHNSA-N ethyl (1s,2r,4s)-4-[(1s)-1-(5-bromo-1,3-thiazol-2-yl)-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1[C@@H](C)[C@@H](C(=O)OCC)CC[C@@H]1[C@](C)(O)C1=NC=C(Br)S1 DGKKLYPEMLTKGS-LMCGPQHNSA-N 0.000 description 1
- JQJQTTXAAMWPPA-UHFFFAOYSA-N ethyl 4-[1-[5-[3-[(5-fluoro-4-methoxypyrimidin-2-yl)amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1C(C)C(C(=O)OCC)CCC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(OC)C(F)=CN=3)C=C(C)C=2)S1 JQJQTTXAAMWPPA-UHFFFAOYSA-N 0.000 description 1
- HMOKOQHEAJIIIR-UHFFFAOYSA-N ethyl 4-[1-[5-[3-[[4-(difluoromethyl)pyrimidin-2-yl]amino]-5-methylphenyl]-1,3-thiazol-2-yl]-1-hydroxyethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1C(C)C(C(=O)OCC)CCC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C=CN=3)C(F)F)C=C(C)C=2)S1 HMOKOQHEAJIIIR-UHFFFAOYSA-N 0.000 description 1
- FRKUBDMYYRVQIW-UHFFFAOYSA-N ethyl 4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1C(C)C(C(=O)OCC)CCC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C)C=CN=3)C=C(C)C=2)S1 FRKUBDMYYRVQIW-UHFFFAOYSA-N 0.000 description 1
- MYAANBSJJKAHEZ-UHFFFAOYSA-N ethyl 4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]-2-methylcyclohexane-1-carboxylate Chemical compound C1C(C)C(C(=O)OCC)CCC1C(C)(O)C1=NC=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)S1 MYAANBSJJKAHEZ-UHFFFAOYSA-N 0.000 description 1
- FEJZEWHBENYUPP-UHFFFAOYSA-N ethyl 4-[[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OCC)CCC1CC1=NC=C(C=2C=C(NC=3N=C(C)C=CN=3)C=C(C)C=2)S1 FEJZEWHBENYUPP-UHFFFAOYSA-N 0.000 description 1
- YVPJCJLMRRTDMQ-UHFFFAOYSA-N ethyl diazoacetate Chemical compound CCOC(=O)C=[N+]=[N-] YVPJCJLMRRTDMQ-UHFFFAOYSA-N 0.000 description 1
- 229960000745 ethylnorepinephrine hydrochloride Drugs 0.000 description 1
- 229940009626 etidronate Drugs 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960004945 etoricoxib Drugs 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 210000003414 extremity Anatomy 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- ZZCHHVUQYRMYLW-HKBQPEDESA-N farglitazar Chemical compound N([C@@H](CC1=CC=C(C=C1)OCCC=1N=C(OC=1C)C=1C=CC=CC=1)C(O)=O)C1=CC=CC=C1C(=O)C1=CC=CC=C1 ZZCHHVUQYRMYLW-HKBQPEDESA-N 0.000 description 1
- 229960002297 fenofibrate Drugs 0.000 description 1
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 description 1
- LSLYOANBFKQKPT-UHFFFAOYSA-N fenoterol Chemical compound C=1C(O)=CC(O)=CC=1C(O)CNC(C)CC1=CC=C(O)C=C1 LSLYOANBFKQKPT-UHFFFAOYSA-N 0.000 description 1
- 229960001022 fenoterol Drugs 0.000 description 1
- RWTNPBWLLIMQHL-UHFFFAOYSA-N fexofenadine Chemical compound C1=CC(C(C)(C(O)=O)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 RWTNPBWLLIMQHL-UHFFFAOYSA-N 0.000 description 1
- 229960003592 fexofenadine Drugs 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 229960005304 fludarabine phosphate Drugs 0.000 description 1
- 239000012025 fluorinating agent Substances 0.000 description 1
- SYTBZMRGLBWNTM-UHFFFAOYSA-N flurbiprofen Chemical compound FC1=CC(C(C(O)=O)C)=CC=C1C1=CC=CC=C1 SYTBZMRGLBWNTM-UHFFFAOYSA-N 0.000 description 1
- 238000011010 flushing procedure Methods 0.000 description 1
- 229960002074 flutamide Drugs 0.000 description 1
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 description 1
- 229960003765 fluvastatin Drugs 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- VVIAGPKUTFNRDU-ABLWVSNPSA-N folinic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-ABLWVSNPSA-N 0.000 description 1
- 235000008191 folinic acid Nutrition 0.000 description 1
- 239000011672 folinic acid Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 229960000193 formoterol fumarate Drugs 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 238000007306 functionalization reaction Methods 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 229950011325 galarubicin Drugs 0.000 description 1
- 229940083124 ganglion-blocking antiadrenergic secondary and tertiary amines Drugs 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 229960003627 gemfibrozil Drugs 0.000 description 1
- 229960002442 glucosamine Drugs 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 229940015042 glycopyrrolate Drugs 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229960001743 golimumab Drugs 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- NDEMNVPZDAFUKN-UHFFFAOYSA-N guanidine;nitric acid Chemical compound NC(N)=N.O[N+]([O-])=O.O[N+]([O-])=O NDEMNVPZDAFUKN-UHFFFAOYSA-N 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 210000003709 heart valve Anatomy 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical class CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 229940121372 histone deacetylase inhibitor Drugs 0.000 description 1
- 239000003276 histone deacetylase inhibitor Substances 0.000 description 1
- 229940125697 hormonal agent Drugs 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940048921 humira Drugs 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 229960001330 hydroxycarbamide Drugs 0.000 description 1
- XXSMGPRMXLTPCZ-UHFFFAOYSA-N hydroxychloroquine Chemical compound ClC1=CC=C2C(NC(C)CCCN(CCO)CC)=CC=NC2=C1 XXSMGPRMXLTPCZ-UHFFFAOYSA-N 0.000 description 1
- 229960004171 hydroxychloroquine Drugs 0.000 description 1
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- 230000001146 hypoxic effect Effects 0.000 description 1
- 229940015872 ibandronate Drugs 0.000 description 1
- 229960001507 ibrutinib Drugs 0.000 description 1
- XYFPWWZEPKGCCK-GOSISDBHSA-N ibrutinib Chemical compound C1=2C(N)=NC=NC=2N([C@H]2CN(CCC2)C(=O)C=C)N=C1C(C=C1)=CC=C1OC1=CC=CC=C1 XYFPWWZEPKGCCK-GOSISDBHSA-N 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 229960000908 idarubicin Drugs 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- 229960001101 ifosfamide Drugs 0.000 description 1
- 229960003685 imatinib mesylate Drugs 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 239000000367 immunologic factor Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229940046732 interleukin inhibitors Drugs 0.000 description 1
- 229940117681 interleukin-12 Drugs 0.000 description 1
- UEXQBEVWFZKHNB-UHFFFAOYSA-N intermediate 29 Natural products C1=CC(N)=CC=C1NC1=NC=CC=N1 UEXQBEVWFZKHNB-UHFFFAOYSA-N 0.000 description 1
- 201000004332 intermediate coronary syndrome Diseases 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 229960001361 ipratropium bromide Drugs 0.000 description 1
- KEWHKYJURDBRMN-ZEODDXGYSA-M ipratropium bromide hydrate Chemical compound O.[Br-].O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 KEWHKYJURDBRMN-ZEODDXGYSA-M 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 210000004153 islets of langerhan Anatomy 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 229940039009 isoproterenol Drugs 0.000 description 1
- 229960005280 isotretinoin Drugs 0.000 description 1
- FABUFPQFXZVHFB-CFWQTKTJSA-N ixabepilone Chemical compound C/C([C@@H]1C[C@@H]2O[C@]2(C)CCC[C@@H]([C@@H]([C@H](C)C(=O)C(C)(C)[C@H](O)CC(=O)N1)O)C)=C\C1=CSC(C)=N1 FABUFPQFXZVHFB-CFWQTKTJSA-N 0.000 description 1
- 229960002014 ixabepilone Drugs 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 201000010666 keratoconjunctivitis Diseases 0.000 description 1
- 229960004125 ketoconazole Drugs 0.000 description 1
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 1
- 229960000991 ketoprofen Drugs 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 229940054136 kineret Drugs 0.000 description 1
- DAQAKHDKYAWHCG-RWTHQLGUSA-N lactacystin Chemical compound CC(=O)N[C@H](C(O)=O)CSC(=O)[C@]1([C@@H](O)C(C)C)NC(=O)[C@H](C)[C@@H]1O DAQAKHDKYAWHCG-RWTHQLGUSA-N 0.000 description 1
- 229940001447 lactate Drugs 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 229960001021 lactose monohydrate Drugs 0.000 description 1
- 229960004891 lapatinib Drugs 0.000 description 1
- VHOGYURTWQBHIL-UHFFFAOYSA-N leflunomide Chemical compound O1N=CC(C(=O)NC=2C=CC(=CC=2)C(F)(F)F)=C1C VHOGYURTWQBHIL-UHFFFAOYSA-N 0.000 description 1
- 229960000681 leflunomide Drugs 0.000 description 1
- 229960003136 leucine Drugs 0.000 description 1
- 229960001691 leucovorin Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 229960001614 levamisole Drugs 0.000 description 1
- ZCGOMHNNNFPNMX-KYTRFIICSA-N levocabastine Chemical compound C1([C@@]2(C(O)=O)CCN(C[C@H]2C)[C@@H]2CC[C@@](CC2)(C#N)C=2C=CC(F)=CC=2)=CC=CC=C1 ZCGOMHNNNFPNMX-KYTRFIICSA-N 0.000 description 1
- 229960001120 levocabastine Drugs 0.000 description 1
- 229960001508 levocetirizine Drugs 0.000 description 1
- 239000000436 ligase inhibitor Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 229960003088 loratadine Drugs 0.000 description 1
- JCCNYMKQOSZNPW-UHFFFAOYSA-N loratadine Chemical compound C1CN(C(=O)OCC)CCC1=C1C2=NC=CC=C2CCC2=CC(Cl)=CC=C21 JCCNYMKQOSZNPW-UHFFFAOYSA-N 0.000 description 1
- 229960004844 lovastatin Drugs 0.000 description 1
- PCZOHLXUXFIOCF-BXMDZJJMSA-N lovastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 PCZOHLXUXFIOCF-BXMDZJJMSA-N 0.000 description 1
- QLJODMDSTUBWDW-UHFFFAOYSA-N lovastatin hydroxy acid Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(C)C=C21 QLJODMDSTUBWDW-UHFFFAOYSA-N 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 229940124302 mTOR inhibitor Drugs 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- OTCKOJUMXQWKQG-UHFFFAOYSA-L magnesium bromide Chemical compound [Mg+2].[Br-].[Br-] OTCKOJUMXQWKQG-UHFFFAOYSA-L 0.000 description 1
- 229910001623 magnesium bromide Inorganic materials 0.000 description 1
- FRIJBUGBVQZNTB-UHFFFAOYSA-M magnesium;ethane;bromide Chemical compound [Mg+2].[Br-].[CH2-]C FRIJBUGBVQZNTB-UHFFFAOYSA-M 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 239000003628 mammalian target of rapamycin inhibitor Substances 0.000 description 1
- 150000002696 manganese Chemical class 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 201000007924 marginal zone B-cell lymphoma Diseases 0.000 description 1
- 208000021937 marginal zone lymphoma Diseases 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 201000006512 mast cell neoplasm Diseases 0.000 description 1
- 208000008585 mastocytosis Diseases 0.000 description 1
- 210000003519 mature b lymphocyte Anatomy 0.000 description 1
- 229960003464 mefenamic acid Drugs 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 229960001929 meloxicam Drugs 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000001525 mentha piperita l. herb oil Substances 0.000 description 1
- 229960000901 mepacrine Drugs 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- 229960004635 mesna Drugs 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- LULAYUGMBFYYEX-UHFFFAOYSA-N metachloroperbenzoic acid Natural products OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- LMOINURANNBYCM-UHFFFAOYSA-N metaproterenol Chemical compound CC(C)NCC(O)C1=CC(O)=CC(O)=C1 LMOINURANNBYCM-UHFFFAOYSA-N 0.000 description 1
- 208000021039 metastatic melanoma Diseases 0.000 description 1
- 229940071648 metered dose inhaler Drugs 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- HNJJXZKZRAWDPF-UHFFFAOYSA-N methapyrilene Chemical compound C=1C=CC=NC=1N(CCN(C)C)CC1=CC=CS1 HNJJXZKZRAWDPF-UHFFFAOYSA-N 0.000 description 1
- 229960001869 methapyrilene Drugs 0.000 description 1
- 229960004469 methoxsalen Drugs 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- QRXXFLLOPHGEAR-SFYZADRCSA-N methyl (1r,3s)-3-acetyl-2,2-dimethylcyclobutane-1-carboxylate Chemical compound COC(=O)[C@@H]1C[C@H](C(C)=O)C1(C)C QRXXFLLOPHGEAR-SFYZADRCSA-N 0.000 description 1
- WOETYOHHXCXCBM-JIMHFIIXSA-N methyl (1s,3r)-3-[1-hydroxy-1-(1,3-thiazol-2-yl)ethyl]cyclopentane-1-carboxylate Chemical compound C1[C@@H](C(=O)OC)CC[C@H]1C(C)(O)C1=NC=CS1 WOETYOHHXCXCBM-JIMHFIIXSA-N 0.000 description 1
- QRXXFLLOPHGEAR-JGVFFNPUSA-N methyl (1s,3r)-3-acetyl-2,2-dimethylcyclobutane-1-carboxylate Chemical compound COC(=O)[C@H]1C[C@@H](C(C)=O)C1(C)C QRXXFLLOPHGEAR-JGVFFNPUSA-N 0.000 description 1
- XFKYUMYFILZJGG-UHFFFAOYSA-N methyl 2,2-dimethyl-3-oxopropanoate Chemical compound COC(=O)C(C)(C)C=O XFKYUMYFILZJGG-UHFFFAOYSA-N 0.000 description 1
- VNJMCDQYRCNFIM-UHFFFAOYSA-N methyl 2,2-dimethyl-4-oxocyclohexane-1-carboxylate Chemical compound COC(=O)C1CCC(=O)CC1(C)C VNJMCDQYRCNFIM-UHFFFAOYSA-N 0.000 description 1
- RFXKJNIWKOHLFF-UHFFFAOYSA-N methyl 3-amino-5-iodobenzoate Chemical compound COC(=O)C1=CC(N)=CC(I)=C1 RFXKJNIWKOHLFF-UHFFFAOYSA-N 0.000 description 1
- VLPZZYBYQXJMME-UHFFFAOYSA-N methyl 4-[1-hydroxy-1-(1,3-thiazol-2-yl)ethyl]-1-methylcyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OC)(C)CCC1C(C)(O)C1=NC=CS1 VLPZZYBYQXJMME-UHFFFAOYSA-N 0.000 description 1
- XZSNNJMHDKWVGJ-UHFFFAOYSA-N methyl 4-[hydroxy-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]methyl]cyclohexane-1-carboxylate Chemical compound C1CC(C(=O)OC)CCC1C(O)C1=NC=C(C=2C=C(NC=3N=C(C=CN=3)C(F)(F)F)C=C(C)C=2)S1 XZSNNJMHDKWVGJ-UHFFFAOYSA-N 0.000 description 1
- LARSGJZNVQJRMD-UHFFFAOYSA-N methyl 4-formylcyclohexane-1-carboxylate Chemical compound COC(=O)C1CCC(C=O)CC1 LARSGJZNVQJRMD-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- DVSDBMFJEQPWNO-UHFFFAOYSA-N methyllithium Chemical compound C[Li] DVSDBMFJEQPWNO-UHFFFAOYSA-N 0.000 description 1
- PQIOSYKVBBWRRI-UHFFFAOYSA-N methylphosphonyl difluoride Chemical group CP(F)(F)=O PQIOSYKVBBWRRI-UHFFFAOYSA-N 0.000 description 1
- VKHAHZOOUSRJNA-GCNJZUOMSA-N mifepristone Chemical compound C1([C@@H]2C3=C4CCC(=O)C=C4CC[C@H]3[C@@H]3CC[C@@]([C@]3(C2)C)(O)C#CC)=CC=C(N(C)C)C=C1 VKHAHZOOUSRJNA-GCNJZUOMSA-N 0.000 description 1
- 229960003248 mifepristone Drugs 0.000 description 1
- 206010027599 migraine Diseases 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- VMMKGHQPQIEGSQ-UHFFFAOYSA-N minodronic acid Chemical compound C1=CC=CN2C(CC(O)(P(O)(O)=O)P(O)(O)=O)=CN=C21 VMMKGHQPQIEGSQ-UHFFFAOYSA-N 0.000 description 1
- 229950011129 minodronic acid Drugs 0.000 description 1
- 239000003595 mist Substances 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 229960000350 mitotane Drugs 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 229960005127 montelukast Drugs 0.000 description 1
- 208000005264 motor neuron disease Diseases 0.000 description 1
- 210000003097 mucus Anatomy 0.000 description 1
- 230000036457 multidrug resistance Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 201000002077 muscle cancer Diseases 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 210000003098 myoblast Anatomy 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- OFIIMRVYFDVZAF-UHFFFAOYSA-N n-(3,5-dibromophenyl)-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound FC(F)(F)C1=CC=NC(NC=2C=C(Br)C=C(Br)C=2)=N1 OFIIMRVYFDVZAF-UHFFFAOYSA-N 0.000 description 1
- DPHDSIQHVGSITN-UHFFFAOYSA-N n-(3,5-dichloropyridin-4-yl)-2-[1-[(4-fluorophenyl)methyl]-5-hydroxyindol-3-yl]-2-oxoacetamide Chemical compound C1=C(C(=O)C(=O)NC=2C(=CN=CC=2Cl)Cl)C2=CC(O)=CC=C2N1CC1=CC=C(F)C=C1 DPHDSIQHVGSITN-UHFFFAOYSA-N 0.000 description 1
- NAQGTLCPZGXUQL-UHFFFAOYSA-N n-(3-bromophenyl)pyrimidin-2-amine Chemical compound BrC1=CC=CC(NC=2N=CC=CN=2)=C1 NAQGTLCPZGXUQL-UHFFFAOYSA-N 0.000 description 1
- NJSMWLQOCQIOPE-OCHFTUDZSA-N n-[(e)-[10-[(e)-(4,5-dihydro-1h-imidazol-2-ylhydrazinylidene)methyl]anthracen-9-yl]methylideneamino]-4,5-dihydro-1h-imidazol-2-amine Chemical compound N1CCN=C1N\N=C\C(C1=CC=CC=C11)=C(C=CC=C2)C2=C1\C=N\NC1=NCCN1 NJSMWLQOCQIOPE-OCHFTUDZSA-N 0.000 description 1
- ZDUZYDDAHVZGCI-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]-9-hydroxy-5,6-dimethylpyrido[4,3-b]carbazole-1-carboxamide Chemical compound CN1C2=CC=C(O)C=C2C2=C1C(C)=C1C=CN=C(C(=O)NCCN(C)C)C1=C2 ZDUZYDDAHVZGCI-UHFFFAOYSA-N 0.000 description 1
- XBGNERSKEKDZDS-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]acridine-4-carboxamide Chemical compound C1=CC=C2N=C3C(C(=O)NCCN(C)C)=CC=CC3=CC2=C1 XBGNERSKEKDZDS-UHFFFAOYSA-N 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- KBFAZZRAQXNRIO-UHFFFAOYSA-N n-[3-[[tert-butyl(dimethyl)silyl]oxymethyl]-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound C=1C(B2OC(C)(C)C(C)(C)O2)=CC(CO[Si](C)(C)C(C)(C)C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 KBFAZZRAQXNRIO-UHFFFAOYSA-N 0.000 description 1
- WQXKVFHALQKVAT-UHFFFAOYSA-N n-[3-[[tert-butyl(dimethyl)silyl]oxymethyl]-5-iodophenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound CC(C)(C)[Si](C)(C)OCC1=CC(I)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 WQXKVFHALQKVAT-UHFFFAOYSA-N 0.000 description 1
- IINXJTWOYSHZOL-UHFFFAOYSA-N n-[3-bromo-5-(1,3-thiazol-5-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound FC(F)(F)C1=CC=NC(NC=2C=C(C=C(Br)C=2)C=2SC=NC=2)=N1 IINXJTWOYSHZOL-UHFFFAOYSA-N 0.000 description 1
- NEGKMFUWJNRJKO-UHFFFAOYSA-N n-[3-bromo-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC(Br)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 NEGKMFUWJNRJKO-UHFFFAOYSA-N 0.000 description 1
- XMJXBQNZJIBYRK-UHFFFAOYSA-N n-[3-bromo-5-(difluoromethyl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound FC(F)C1=CC(Br)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 XMJXBQNZJIBYRK-UHFFFAOYSA-N 0.000 description 1
- IRMHXVUERTUKBK-UHFFFAOYSA-N n-[3-cyclopropyl-5-(1,3-thiazol-5-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound FC(F)(F)C1=CC=NC(NC=2C=C(C=C(C=2)C2CC2)C=2SC=NC=2)=N1 IRMHXVUERTUKBK-UHFFFAOYSA-N 0.000 description 1
- FQVCEZZUIDTVMR-UHFFFAOYSA-N n-[3-fluoro-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-4-(trifluoromethyl)pyrimidin-2-amine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC(F)=CC(NC=2N=C(C=CN=2)C(F)(F)F)=C1 FQVCEZZUIDTVMR-UHFFFAOYSA-N 0.000 description 1
- GPHVXYBDEIEYHU-UHFFFAOYSA-N n-[4-[1-hydroxy-1-[5-[3-methyl-5-[(4-methylpyrimidin-2-yl)amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexyl]methanesulfonamide Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)NS(C)(=O)=O)=CC(C)=CC=1NC1=NC=CC(C)=N1 GPHVXYBDEIEYHU-UHFFFAOYSA-N 0.000 description 1
- OPXKZHWBUDZONQ-UHFFFAOYSA-N n-[4-[1-hydroxy-1-[5-[3-methyl-5-[[4-(trifluoromethyl)pyrimidin-2-yl]amino]phenyl]-1,3-thiazol-2-yl]ethyl]cyclohexyl]methanesulfonamide Chemical compound C=1C(C=2SC(=NC=2)C(C)(O)C2CCC(CC2)NS(C)(=O)=O)=CC(C)=CC=1NC1=NC=CC(C(F)(F)F)=N1 OPXKZHWBUDZONQ-UHFFFAOYSA-N 0.000 description 1
- GWLFIMOOGVXSMZ-UHFFFAOYSA-N n-[[1-[2-(diethylamino)ethylamino]-7-methoxy-9-oxothioxanthen-4-yl]methyl]formamide Chemical compound S1C2=CC=C(OC)C=C2C(=O)C2=C1C(CNC=O)=CC=C2NCCN(CC)CC GWLFIMOOGVXSMZ-UHFFFAOYSA-N 0.000 description 1
- ILCQYORZHHFLNL-UHFFFAOYSA-N n-bromoaniline Chemical class BrNC1=CC=CC=C1 ILCQYORZHHFLNL-UHFFFAOYSA-N 0.000 description 1
- OYSBVBIAZACMHG-UHFFFAOYSA-N n-methoxy-n-methyl-1,4-dioxaspiro[4.5]decane-8-carboxamide Chemical compound C1CC(C(=O)N(C)OC)CCC21OCCO2 OYSBVBIAZACMHG-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- NPAGDVCDWIYMMC-IZPLOLCNSA-N nandrolone Chemical compound O=C1CC[C@@H]2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 NPAGDVCDWIYMMC-IZPLOLCNSA-N 0.000 description 1
- 229960004719 nandrolone Drugs 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-M naphthalene-1-sulfonate Chemical compound C1=CC=C2C(S(=O)(=O)[O-])=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-M 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-N naphthalene-1-sulfonic acid Chemical compound C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-N 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 229960002009 naproxen Drugs 0.000 description 1
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 1
- 210000003928 nasal cavity Anatomy 0.000 description 1
- 239000007923 nasal drop Substances 0.000 description 1
- 229940100662 nasal drops Drugs 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 235000021096 natural sweeteners Nutrition 0.000 description 1
- IXOXBSCIXZEQEQ-UHTZMRCNSA-N nelarabine Chemical compound C1=NC=2C(OC)=NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1O IXOXBSCIXZEQEQ-UHTZMRCNSA-N 0.000 description 1
- 229960000801 nelarabine Drugs 0.000 description 1
- PUUSSSIBPPTKTP-UHFFFAOYSA-N neridronic acid Chemical compound NCCCCCC(O)(P(O)(O)=O)P(O)(O)=O PUUSSSIBPPTKTP-UHFFFAOYSA-N 0.000 description 1
- 229950010733 neridronic acid Drugs 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- PKWDZWYVIHVNKS-UHFFFAOYSA-N netoglitazone Chemical compound FC1=CC=CC=C1COC1=CC=C(C=C(CC2C(NC(=O)S2)=O)C=C2)C2=C1 PKWDZWYVIHVNKS-UHFFFAOYSA-N 0.000 description 1
- 230000007135 neurotoxicity Effects 0.000 description 1
- 231100000228 neurotoxicity Toxicity 0.000 description 1
- HHZIURLSWUIHRB-UHFFFAOYSA-N nilotinib Chemical compound C1=NC(C)=CN1C1=CC(NC(=O)C=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)=CC(C(F)(F)F)=C1 HHZIURLSWUIHRB-UHFFFAOYSA-N 0.000 description 1
- 229960001346 nilotinib Drugs 0.000 description 1
- 229960002653 nilutamide Drugs 0.000 description 1
- XWXYUMMDTVBTOU-UHFFFAOYSA-N nilutamide Chemical compound O=C1C(C)(C)NC(=O)N1C1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 XWXYUMMDTVBTOU-UHFFFAOYSA-N 0.000 description 1
- 229960001420 nimustine Drugs 0.000 description 1
- VFEDRRNHLBGPNN-UHFFFAOYSA-N nimustine Chemical compound CC1=NC=C(CNC(=O)N(CCCl)N=O)C(N)=N1 VFEDRRNHLBGPNN-UHFFFAOYSA-N 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 108010046821 oprelvekin Proteins 0.000 description 1
- 229960001840 oprelvekin Drugs 0.000 description 1
- 229960002657 orciprenaline Drugs 0.000 description 1
- 229940035567 orencia Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- NVOYVOBDTVTBDX-PMEUIYRNSA-N oxitropium Chemical compound CC[N+]1(C)[C@H]2C[C@@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)[C@H](CO)C1=CC=CC=C1 NVOYVOBDTVTBDX-PMEUIYRNSA-N 0.000 description 1
- 229960000797 oxitropium Drugs 0.000 description 1
- BEEDODBODQVSIM-UHFFFAOYSA-N oxymetazoline hydrochloride Chemical compound Cl.CC1=CC(C(C)(C)C)=C(O)C(C)=C1CC1=NCCN1 BEEDODBODQVSIM-UHFFFAOYSA-N 0.000 description 1
- 229960005162 oxymetazoline hydrochloride Drugs 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 1
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 1
- 125000001312 palmitoyl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000011236 particulate material Substances 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 229960005079 pemetrexed Drugs 0.000 description 1
- QOFFJEBXNKRSPX-ZDUSSCGKSA-N pemetrexed Chemical compound C1=N[C]2NC(N)=NC(=O)C2=C1CCC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 QOFFJEBXNKRSPX-ZDUSSCGKSA-N 0.000 description 1
- 229960003349 pemetrexed disodium Drugs 0.000 description 1
- 235000019477 peppermint oil Nutrition 0.000 description 1
- 208000015385 phacoanaphylactic uveitis Diseases 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 238000009521 phase II clinical trial Methods 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- 229960002895 phenylbutazone Drugs 0.000 description 1
- VYMDGNCVAMGZFE-UHFFFAOYSA-N phenylbutazonum Chemical compound O=C1C(CCCC)C(=O)N(C=2C=CC=CC=2)N1C1=CC=CC=C1 VYMDGNCVAMGZFE-UHFFFAOYSA-N 0.000 description 1
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 1
- 229960000395 phenylpropanolamine Drugs 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 1
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 1
- 239000002587 phosphodiesterase IV inhibitor Substances 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 229960005095 pioglitazone Drugs 0.000 description 1
- 229960000952 pipobroman Drugs 0.000 description 1
- NJBFOOCLYDNZJN-UHFFFAOYSA-N pipobroman Chemical compound BrCCC(=O)N1CCN(C(=O)CCBr)CC1 NJBFOOCLYDNZJN-UHFFFAOYSA-N 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 229940096701 plain lipid modifying drug hmg coa reductase inhibitors Drugs 0.000 description 1
- 230000010118 platelet activation Effects 0.000 description 1
- HRGDZIGMBDGFTC-UHFFFAOYSA-N platinum(2+) Chemical compound [Pt+2] HRGDZIGMBDGFTC-UHFFFAOYSA-N 0.000 description 1
- 229950008499 plitidepsin Drugs 0.000 description 1
- UUSZLLQJYRSZIS-LXNNNBEUSA-N plitidepsin Chemical compound CN([C@H](CC(C)C)C(=O)N[C@@H]1C(=O)N[C@@H]([C@H](CC(=O)O[C@H](C(=O)[C@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N2CCC[C@H]2C(=O)N(C)[C@@H](CC=2C=CC(OC)=CC=2)C(=O)O[C@@H]1C)C(C)C)O)[C@@H](C)CC)C(=O)[C@@H]1CCCN1C(=O)C(C)=O UUSZLLQJYRSZIS-LXNNNBEUSA-N 0.000 description 1
- 108010049948 plitidepsin Proteins 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 229920001610 polycaprolactone Polymers 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 208000005987 polymyositis Diseases 0.000 description 1
- 229920006324 polyoxymethylene Polymers 0.000 description 1
- 239000011698 potassium fluoride Substances 0.000 description 1
- 235000003270 potassium fluoride Nutrition 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 1
- 229960004583 pranlukast Drugs 0.000 description 1
- 229960002965 pravastatin Drugs 0.000 description 1
- TUZYXOIXSAXUGO-PZAWKZKUSA-N pravastatin Chemical compound C1=C[C@H](C)[C@H](CC[C@@H](O)C[C@@H](O)CC(O)=O)[C@H]2[C@@H](OC(=O)[C@@H](C)CC)C[C@H](O)C=C21 TUZYXOIXSAXUGO-PZAWKZKUSA-N 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 208000017426 precursor B-cell acute lymphoblastic leukemia Diseases 0.000 description 1
- 229960004694 prednimustine Drugs 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- 238000002953 preparative HPLC Methods 0.000 description 1
- 150000003138 primary alcohols Chemical class 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 description 1
- 229960000624 procarbazine Drugs 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 201000007914 proliferative diabetic retinopathy Diseases 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- JCRIVQIOJSSCQD-UHFFFAOYSA-N propylhexedrine Chemical compound CNC(C)CC1CCCCC1 JCRIVQIOJSSCQD-UHFFFAOYSA-N 0.000 description 1
- 229960000786 propylhexedrine Drugs 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 201000001475 prostate lymphoma Diseases 0.000 description 1
- 239000011253 protective coating Substances 0.000 description 1
- 239000003528 protein farnesyltransferase inhibitor Substances 0.000 description 1
- 229960003908 pseudoephedrine Drugs 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- JEXVQSWXXUJEMA-UHFFFAOYSA-N pyrazol-3-one Chemical compound O=C1C=CN=N1 JEXVQSWXXUJEMA-UHFFFAOYSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- GPKJTRJOBQGKQK-UHFFFAOYSA-N quinacrine Chemical compound C1=C(OC)C=C2C(NC(C)CCCN(CC)CC)=C(C=CC(Cl)=C3)C3=NC2=C1 GPKJTRJOBQGKQK-UHFFFAOYSA-N 0.000 description 1
- 102000009929 raf Kinases Human genes 0.000 description 1
- 108010077182 raf Kinases Proteins 0.000 description 1
- GZUITABIAKMVPG-UHFFFAOYSA-N raloxifene Chemical compound C1=CC(O)=CC=C1C1=C(C(=O)C=2C=CC(OCCN3CCCCC3)=CC=2)C2=CC=C(O)C=C2S1 GZUITABIAKMVPG-UHFFFAOYSA-N 0.000 description 1
- 229960004622 raloxifene Drugs 0.000 description 1
- BKXVVCILCIUCLG-UHFFFAOYSA-N raloxifene hydrochloride Chemical compound [H+].[Cl-].C1=CC(O)=CC=C1C1=C(C(=O)C=2C=CC(OCCN3CCCCC3)=CC=2)C2=CC=C(O)C=C2S1 BKXVVCILCIUCLG-UHFFFAOYSA-N 0.000 description 1
- 229960002119 raloxifene hydrochloride Drugs 0.000 description 1
- 229960004432 raltitrexed Drugs 0.000 description 1
- 229960002185 ranimustine Drugs 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 208000002574 reactive arthritis Diseases 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 238000006268 reductive amination reaction Methods 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 230000019254 respiratory burst Effects 0.000 description 1
- 229940100552 retinamide Drugs 0.000 description 1
- 102000027483 retinoid hormone receptors Human genes 0.000 description 1
- 108091008679 retinoid hormone receptors Proteins 0.000 description 1
- VUPQHSHTKBZVML-UHFFFAOYSA-J rhodium(3+);tetraacetate Chemical compound [Rh+3].[Rh+3].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O VUPQHSHTKBZVML-UHFFFAOYSA-J 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229940089617 risedronate Drugs 0.000 description 1
- XMSXOLDPMGMWTH-UHFFFAOYSA-N rivoglitazone Chemical compound CN1C2=CC(OC)=CC=C2N=C1COC(C=C1)=CC=C1CC1SC(=O)NC1=O XMSXOLDPMGMWTH-UHFFFAOYSA-N 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 1
- MNDBXUUTURYVHR-UHFFFAOYSA-N roflumilast Chemical compound FC(F)OC1=CC=C(C(=O)NC=2C(=CN=CC=2Cl)Cl)C=C1OCC1CC1 MNDBXUUTURYVHR-UHFFFAOYSA-N 0.000 description 1
- 229960002586 roflumilast Drugs 0.000 description 1
- 229960004586 rosiglitazone Drugs 0.000 description 1
- 229960000672 rosuvastatin Drugs 0.000 description 1
- BIXNGBXQRRXPLM-UHFFFAOYSA-K ruthenium(3+);trichloride;hydrate Chemical compound O.Cl[Ru](Cl)Cl BIXNGBXQRRXPLM-UHFFFAOYSA-K 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 229960002052 salbutamol Drugs 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 201000000306 sarcoidosis Diseases 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000000849 selective androgen receptor modulator Substances 0.000 description 1
- BTIHMVBBUGXLCJ-OAHLLOKOSA-N seliciclib Chemical compound C=12N=CN(C(C)C)C2=NC(N[C@@H](CO)CC)=NC=1NCC1=CC=CC=C1 BTIHMVBBUGXLCJ-OAHLLOKOSA-N 0.000 description 1
- 229950003647 semaxanib Drugs 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 229940068638 simponi Drugs 0.000 description 1
- 229960002855 simvastatin Drugs 0.000 description 1
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 235000015424 sodium Nutrition 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- HLBBKKJFGFRGMU-UHFFFAOYSA-M sodium formate Chemical compound [Na+].[O-]C=O HLBBKKJFGFRGMU-UHFFFAOYSA-M 0.000 description 1
- 235000019254 sodium formate Nutrition 0.000 description 1
- RYYKJJJTJZKILX-UHFFFAOYSA-M sodium octadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC([O-])=O RYYKJJJTJZKILX-UHFFFAOYSA-M 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 229960003787 sorafenib Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- LBJQKYPPYSCCBH-UHFFFAOYSA-N spiro[3.3]heptane Chemical compound C1CCC21CCC2 LBJQKYPPYSCCBH-UHFFFAOYSA-N 0.000 description 1
- 229950001248 squalamine Drugs 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 102000009076 src-Family Kinases Human genes 0.000 description 1
- 108010087686 src-Family Kinases Proteins 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 229960001940 sulfasalazine Drugs 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- MLKXDPUZXIRXEP-MFOYZWKCSA-N sulindac Chemical compound CC1=C(CC(O)=O)C2=CC(F)=CC=C2\C1=C/C1=CC=C(S(C)=O)C=C1 MLKXDPUZXIRXEP-MFOYZWKCSA-N 0.000 description 1
- 229960000894 sulindac Drugs 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000007755 survival signaling Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 229940035073 symbicort Drugs 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 229960001967 tacrolimus Drugs 0.000 description 1
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229960001674 tegafur Drugs 0.000 description 1
- WFWLQNSHRPWKFK-ZCFIWIBFSA-N tegafur Chemical compound O=C1NC(=O)C(F)=CN1[C@@H]1OCCC1 WFWLQNSHRPWKFK-ZCFIWIBFSA-N 0.000 description 1
- 229960004964 temozolomide Drugs 0.000 description 1
- 229960001278 teniposide Drugs 0.000 description 1
- 229960000195 terbutaline Drugs 0.000 description 1
- HYNBSBAWGATECV-UHFFFAOYSA-N tert-butyl 4-oxocyclohexane-1-carboxylate Chemical compound CC(C)(C)OC(=O)C1CCC(=O)CC1 HYNBSBAWGATECV-UHFFFAOYSA-N 0.000 description 1
- ILMRJRBKQSSXGY-UHFFFAOYSA-N tert-butyl(dimethyl)silicon Chemical group C[Si](C)C(C)(C)C ILMRJRBKQSSXGY-UHFFFAOYSA-N 0.000 description 1
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 1
- 229960005353 testolactone Drugs 0.000 description 1
- BPEWUONYVDABNZ-DZBHQSCQSA-N testolactone Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(OC(=O)CC4)[C@@H]4[C@@H]3CCC2=C1 BPEWUONYVDABNZ-DZBHQSCQSA-N 0.000 description 1
- MRXQMNWIADOAJY-UHFFFAOYSA-M tetrabutylazanium;fluoride;dihydrofluoride Chemical compound F.F.[F-].CCCC[N+](CCCC)(CCCC)CCCC MRXQMNWIADOAJY-UHFFFAOYSA-M 0.000 description 1
- BJORNXNYWNIWEY-UHFFFAOYSA-N tetrahydrozoline hydrochloride Chemical compound Cl.N1CCN=C1C1C2=CC=CC=C2CCC1 BJORNXNYWNIWEY-UHFFFAOYSA-N 0.000 description 1
- 229940021790 tetrahydrozoline hydrochloride Drugs 0.000 description 1
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 1
- 229960003433 thalidomide Drugs 0.000 description 1
- 229960004559 theobromine Drugs 0.000 description 1
- 229960000278 theophylline Drugs 0.000 description 1
- 125000000437 thiazol-2-yl group Chemical group [H]C1=C([H])N=C(*)S1 0.000 description 1
- 150000003557 thiazoles Chemical class 0.000 description 1
- SRVJKTDHMYAMHA-WUXMJOGZSA-N thioacetazone Chemical compound CC(=O)NC1=CC=C(\C=N\NC(N)=S)C=C1 SRVJKTDHMYAMHA-WUXMJOGZSA-N 0.000 description 1
- 230000002537 thrombolytic effect Effects 0.000 description 1
- 206010043778 thyroiditis Diseases 0.000 description 1
- 229960000257 tiotropium bromide Drugs 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 125000005147 toluenesulfonyl group Chemical group C=1(C(=CC=CC1)S(=O)(=O)*)C 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- XFCLJVABOIYOMF-QPLCGJKRSA-N toremifene Chemical compound C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 XFCLJVABOIYOMF-QPLCGJKRSA-N 0.000 description 1
- 229960005026 toremifene Drugs 0.000 description 1
- 229960005267 tositumomab Drugs 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 201000010875 transient cerebral ischemia Diseases 0.000 description 1
- 230000008736 traumatic injury Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- YNDXUCZADRHECN-JNQJZLCISA-N triamcinolone acetonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O YNDXUCZADRHECN-JNQJZLCISA-N 0.000 description 1
- 229960002117 triamcinolone acetonide Drugs 0.000 description 1
- RTKIYFITIVXBLE-QEQCGCAPSA-N trichostatin A Chemical compound ONC(=O)/C=C/C(/C)=C/[C@@H](C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-QEQCGCAPSA-N 0.000 description 1
- WLPUWLXVBWGYMZ-UHFFFAOYSA-N tricyclohexylphosphine Chemical compound C1CCCCC1P(C1CCCCC1)C1CCCCC1 WLPUWLXVBWGYMZ-UHFFFAOYSA-N 0.000 description 1
- PQDJYEQOELDLCP-UHFFFAOYSA-N trimethylsilane Chemical compound C[SiH](C)C PQDJYEQOELDLCP-UHFFFAOYSA-N 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- NOYPYLRCIDNJJB-UHFFFAOYSA-N trimetrexate Chemical compound COC1=C(OC)C(OC)=CC(NCC=2C(=C3C(N)=NC(N)=NC3=CC=2)C)=C1 NOYPYLRCIDNJJB-UHFFFAOYSA-N 0.000 description 1
- 229960001099 trimetrexate Drugs 0.000 description 1
- GXPHKUHSUJUWKP-UHFFFAOYSA-N troglitazone Chemical compound C1CC=2C(C)=C(O)C(C)=C(C)C=2OC1(C)COC(C=C1)=CC=C1CC1SC(=O)NC1=O GXPHKUHSUJUWKP-UHFFFAOYSA-N 0.000 description 1
- 229960001641 troglitazone Drugs 0.000 description 1
- GXPHKUHSUJUWKP-NTKDMRAZSA-N troglitazone Natural products C([C@@]1(OC=2C(C)=C(C(=C(C)C=2CC1)O)C)C)OC(C=C1)=CC=C1C[C@H]1SC(=O)NC1=O GXPHKUHSUJUWKP-NTKDMRAZSA-N 0.000 description 1
- 229960000281 trometamol Drugs 0.000 description 1
- 102000003390 tumor necrosis factor Human genes 0.000 description 1
- 229940046728 tumor necrosis factor alpha inhibitor Drugs 0.000 description 1
- 239000002452 tumor necrosis factor alpha inhibitor Substances 0.000 description 1
- 239000002691 unilamellar liposome Substances 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 125000005500 uronium group Chemical group 0.000 description 1
- 229960002004 valdecoxib Drugs 0.000 description 1
- LNPDTQAFDNKSHK-UHFFFAOYSA-N valdecoxib Chemical compound CC=1ON=C(C=2C=CC=CC=2)C=1C1=CC=C(S(N)(=O)=O)C=C1 LNPDTQAFDNKSHK-UHFFFAOYSA-N 0.000 description 1
- MSRILKIQRXUYCT-UHFFFAOYSA-M valproate semisodium Chemical compound [Na+].CCCC(C(O)=O)CCC.CCCC(C([O-])=O)CCC MSRILKIQRXUYCT-UHFFFAOYSA-M 0.000 description 1
- 229960000604 valproic acid Drugs 0.000 description 1
- 229950010938 valspodar Drugs 0.000 description 1
- 108010082372 valspodar Proteins 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 229960003726 vasopressin Drugs 0.000 description 1
- 229950011257 veliparib Drugs 0.000 description 1
- DCSCXTJOXBUFGB-UHFFFAOYSA-N verbenone Natural products CC1=CC(=O)C2C(C)(C)C1C2 DCSCXTJOXBUFGB-UHFFFAOYSA-N 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- UGGWPQSBPIFKDZ-KOTLKJBCSA-N vindesine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(N)=O)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1N=C1[C]2C=CC=C1 UGGWPQSBPIFKDZ-KOTLKJBCSA-N 0.000 description 1
- 229960004355 vindesine Drugs 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229950005839 vinzolidine Drugs 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 229960004764 zafirlukast Drugs 0.000 description 1
- MWLSOWXNZPKENC-SSDOTTSWSA-N zileuton Chemical compound C1=CC=C2SC([C@H](N(O)C(N)=O)C)=CC2=C1 MWLSOWXNZPKENC-SSDOTTSWSA-N 0.000 description 1
- 229960005332 zileuton Drugs 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 229940102001 zinc bromide Drugs 0.000 description 1
- FBTUMDXHSRTGRV-ALTNURHMSA-N zorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(\C)=N\NC(=O)C=1C=CC=CC=1)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 FBTUMDXHSRTGRV-ALTNURHMSA-N 0.000 description 1
- 229960000641 zorubicin Drugs 0.000 description 1
- IHOVFYSQUDPMCN-QKUIIBHLSA-N zosuquidar Chemical compound C([C@H](COC=1C2=CC=CN=C2C=CC=1)O)N(CC1)CCN1C1C2=CC=CC=C2C2C(F)(F)C2C2=CC=CC=C12 IHOVFYSQUDPMCN-QKUIIBHLSA-N 0.000 description 1
- 229950005752 zosuquidar Drugs 0.000 description 1
- 238000011911 α-alkylation Methods 0.000 description 1
- 229930195724 β-lactose Natural products 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pulmonology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
본 발명은 비장 티로신 키나제의 강력한 억제제이고, 상기 효소에 의해 매개되는 질환, 예컨대 천식, COPD 및 류마티스 관절염 및 암의 치료 및 예방에 유용한 화학식 I의 신규 피리미딘 아민을 제공한다.
Description
비장 티로신 키나제 (Syk)는 비만 세포, B-세포, 대식세포 및 호중구를 비롯한 다수의 염증 세포에서 면역수용체 신호전달의 주요 매개자로서 설명되어 온 단백질 티로신 키나제이다. Fc 수용체 및 B-세포 수용체를 비롯한 이러한 면역수용체는 알레르기성 질환 및 항체-매개 자가면역 질환 둘 다에 중요하며, 따라서 Syk를 약리학적으로 방해하는 것이 이러한 장애를 치료할 수 있을 것으로 생각할 수 있다.
알레르기성 비염 및 천식은 비만 세포, 호산구, T 세포 및 수지상 세포를 비롯한 다수의 세포 유형이 관련된 과민 반응 및 염증성 사례와 연관된 질환이다. 알레르겐에 노출 후, 비만 세포 및 기타 세포 유형에서 IgE 및 IgG에 대한 고친화성 이뮤노글로불린 수용체들이 가교되고 하류 과정이 활성화되어, 염증유발 매개자 및 기도 연축유발물질의 방출이 야기된다. 예를 들어, 비만 세포에서, 알레르겐에 의한 IgE 수용체 가교는 미리 형성된 과립으로부터 히스타민을 비롯한 매개자의 방출을 야기할 뿐만 아니라, 프로스타글란딘 및 류코트리엔을 비롯한 새롭게 합성된 지질 매개자의 합성 및 방출을 야기한다.
Syk 키나제는 Fc엡실론R1 및 또는 Fc엡실론R1 수용체의 가교와 연관된 하류 세포 신호를 전달하는데 중요한, 신호전달 캐스케이드에서 초기에 위치하는 비-수용체 연결 티로신 키나제이다. 예를 들어, 비만 세포에서, 수용체-IgE 복합체의 알레르겐 가교 후의 Fc엡실론R1 신호전달의 초기 순서는 먼저 Lyn (Src 패밀리 티로신 키나제) 및 그 후 Syk가 관련된다. 따라서, Syk 활성의 억제제는 모든 하류 신호전달 캐스케이드를 억제하여, 염증유발 매개자 및 연축유발물질의 방출에 의해 개시되는 즉각적 알레르기 반응 및 유해 사례를 완화시킬 것으로 예상된다 (문헌 [Wong et al. 2004, Expert Opin. Investig. Drugs (2004) 13 (7) 743-762]).
최근, 알레르기성 비염의 치료를 위한 I/II상 연구에서 비강내로 투여된 Syk 키나제 억제제 R112 (리겔(Rigel))가, 알레르기성 비루의 개선과 크게 상관있는, 주요 면역 매개자인 PGD2의 통계적으로 유의한 감소를 제공할 뿐만 아니라, 다양한 지시자에 걸쳐서 안전한 것으로 나타났으며, 따라서 국소 Syk 키나제 억제제의 임상적 안전성 및 효능에 대한 제1 증거를 제공한다. (문헌 [Meltzer, Eli O.; Berkowitz, Robert B.; Grossbard, Elliott B, Journal of Allergy and Clinical Immunology (2005), 115(4), 791-796]). 알레르기성 비염에 대한 보다 최근의 II상 임상 시험에서 (Clinical Trials.gov Identifier NCT0015089), R112는 위약에 대해 효능이 부족한 것으로 나타났다.
류마티스 관절염 (RA)은 인구의 대략 1%에 영향을 미치는 자가면역 질환이다. 이는 골 및 연골의 약화 파괴를 야기하는 관절의 염증에 의해 특성화된다. 가역적 B 세포 고갈을 유발하는 리툭시맙에 대한 최근의 임상 연구 (문헌 [J. C. W. Edwards et al. 2004, New Eng. J. Med. 350: 2572-2581])는 B 세포 기능을 표적화하는 것이 자가면역 질환, 예컨대 RA에서 적절한 치료 전략임을 나타내었다. 임상적 이익은 자동-반응성 항체 (또는 류마티스 인자)의 감소와 상관관계가 있고, 이들 연구는 B 세포 기능 및 실제 자가-항체 생산이 질환에서 진행 중인 병리상태에 있어서 중요함을 제시한다.
비장 티로신 키나제 (Syk)가 결핍된 마우스로부터의 세포를 이용한 연구는 B 세포 기능에서 상기 키나제의 비-중복 역할을 입증하였다. Syk의 결핍은 B 세포 발생에서의 차단에 의해 특성화된다 (문헌 [M. Turner et al. 1995 Nature 379: 298-302 및 Cheng et al. 1995, Nature 378: 303-306]). 이들 연구는, Syk가 결핍된 성숙 B 세포에 대한 연구 (문헌 [Kurasaki et al. 2000, Immunol. Rev. 176:19-29])와 함께, Syk가 B 세포의 분화 및 활성화에 요구됨을 입증한다. 따라서, RA 환자에서 Syk를 억제하는 것은 B 세포 기능을 차단하여 류마티스 인자 생성을 감소시킬 가능성이 있다. B 세포 기능에서 Syk의 역할, 및 RA의 치료에의 추가 관련성의 역할에 더하여, Fc 수용체 (FcR) 신호전달에서 Syk 활성이 필요하다. RA에서 면역 복합체에 의한 FcR 활성화는 다수의 염증유발 매개자의 방출에 기여하는 것으로 제시되었다.
미국 특허 번호 7,803,801은 하기 화학식을 갖는 Syk 억제제를 개시하고 있다.
상기 식에서, 가변기는 상기 문헌에 정의된 바와 같다.
본 발명은 Syk 키나제 활성의 억제제인 신규 화합물에 관한 것이다. 따라서, 이들 화합물은 부적절한 Syk 활성과 연관된 장애의 치료에서, 특히 Syk에 의해 매개되는 질환 상태의 치료 및 예방에서 잠재적 치료 이익을 갖는다. 이러한 질환 상태는 염증성, 알레르기성 및 자가면역 질환, 예를 들어 천식, 만성 폐쇄성 폐 질환 (COPD), 성인 호흡 곤란 증후군 (ARDS), 궤양성 결장염, 크론병, 기관지염, 피부염, 알레르기성 비염, 건선, 경피증, 두드러기, 류마티스 관절염, 특발성 혈소판감소성 자반증 (ITP), 다발성 경화증, 암, HIV 및 루푸스를 포함할 수 있다.
본 발명은 Syk의 강력한 억제제인 신규 화합물 뿐만 아니라 그를 함유하는 제약 조성물을 제공한다. Syk 억제제로서 본 발명의 화합물은 Syk 단백질에 의해 매개되는 질환 및 장애의 치료 및 예방에 유용하고; 이러한 질환 및 장애는 천식, COPD, 류마티스 관절염, 암 및 특발성 혈소판감소성 자반증을 포함하나, 이에 제한되는 것은 아니다.
본 발명은 하기 화학식 I의 화합물 또는 그의 제약상 허용되는 염을 제공한다.
<화학식 I>
상기 식에서,
A는 카르보사이클이거나, 또는
모이어티 A-(R7)n(R8)은 1,4-디옥사스피로[4.5]데실을 나타내고;
n은 0, 1, 2 또는 3이고;
R1은 C1 - 4알킬, C1 - 4플루오로알킬, C3 - 6시클로알킬 또는 C1 - 4알콕시이고;
R2는 H 또는 할로겐이고;
R3은 H, 할로겐, C1 - 4알킬, C1 - 4할로알킬, C3 - 6시클로알킬 또는 C1 - 4히드록시알킬이고;
R4는 H 또는 할로겐이고;
R5는 H, OH, C1 - 4알콕시, 할로겐 또는 NH2이고;
R6은 H, C1 - 4알킬, C1 - 4할로알킬, C3 - 6시클로알킬 또는 C1 - 4히드록시알킬이거나; 또는
R5 및 R6은 함께 옥소이고;
R7은 OH 및 C1 - 4알킬로부터 선택되고;
R8은 (CRaRb)nCO2Rc, CONRdRe, 테트라졸릴, OH, CH2OH, 옥소, CN, NHCO2Rf 및 NHSO2Rf로부터 선택되며; 단 R8 및 -C(R5)(R6)-은 동일한 고리 탄소 원자에 부착되지 않고;
Ra 및 Rb는 각각 독립적으로 H 및 메틸로부터 선택되고;
Rc는 H 또는 C1 - 4알킬이고;
Rd 및 Re는 각각 독립적으로 H 및 C1 - 4알킬로부터 선택되고;
Rf는 C1 - 4알킬 또는 벤질이다.
화학식 I의 한 군에서, 화합물은 고리 A가 카르보사이클인 화합물이다. 그의 한 하위군에서, A는 C3 - 6시클로알킬, 아다만틸 및 비시클로[3.1.0]헥실로부터 선택된다. 한 실시양태에서, A는 시클로프로필, 시클로부틸, 시클로펜틸 및 시클로헥실로부터 선택된다. 제2 실시양태에서, A는 시클로헥실이다.
화학식 I의 또 다른 군에서, 화합물은 R1이 C1 - 4알킬 또는 C1 - 4플루오로알킬인 화합물이다. 그의 한 하위군에서, R1은 C1 - 3알킬, 예컨대 메틸, 에틸, n-프로필 또는 이소프로필이다. 그의 제2 하위세트에서, R1은 C1 - 3플루오로알킬, 예컨대 디플루오로메틸 또는 트리플루오로메틸이다. 한 실시양태에서, R1은 메틸이다. 제2 실시양태에서, R1은 트리플루오로메틸이다. 제3 실시양태에서, R1은 디플루오로메틸이다.
화학식 I의 또 다른 군에서, 화합물은 R3이 C1 - 4알킬, C1 - 4할로알킬 또는 C3 - 6시클로알킬인 화합물이다. 한 실시양태에서, R3은 메틸, 디플루오로메틸 및 시클로프로필로부터 선택된다. 제2 실시양태에서, R3은 메틸이다.
화학식 I의 또 다른 군에서, 화합물은 R5가 OH인 화합물이다.
화학식 I의 또 다른 군에서, 화합물은 R6이 H, C1 - 4알킬 또는 C1 - 4할로알킬인 화합물이다. 그의 한 하위군에서, R6은 H, C1 - 3알킬, 및 플루오로-, 디플루오로- 및 트리플루오로메틸로부터 선택된다. 한 실시양태에서, R6은 메틸이다. 제2 실시양태에서, R6은 트리플루오로메틸이다.
화학식 I의 또 다른 군에서, 화합물은 A가 카르보사이클이고, R8이 (CRaRb)nCO2Rc 및 C(O)NRdRe로부터 선택된 것인 화합물이다. 그의 한 하위군에서, R8은 CO2Rc 및 C(O)NRdRe로부터 선택된다. 한 실시양태에서, A는 C3 - 6시클로알킬이고, R8은 CO2Rc이다. 제2 실시양태에서, A는 C3-6시클로알킬이고, R8은 C(O)NRdRe이다.
화학식 I의 또 다른 군에서, 화합물은 하기 화학식 Ia를 갖는 화합물 또는 그의 제약상 허용되는 염이다.
<화학식 Ia>
상기 식에서,
A는 카르보사이클이고;
n은 0, 1 또는 2이고;
R1은 C1 - 4알킬 또는 C1 - 4플루오로알킬이고;
R3은 C1 - 4알킬, C1 - 4할로알킬 또는 C3 - 6시클로알킬이고;
R6은 H, C1 - 4알킬 또는 C1 - 4할로알킬이고;
R7은 C1 - 4알킬이고;
R8은 CO2Rc 또는 CONRdRe이고;
Rc는 H 또는 C1 - 4알킬이고;
Rd 및 Re는 각각 독립적으로 H 및 C1 - 4알킬로부터 선택된다.
화학식 I의 또 다른 군에서, 화합물은 하기 화학식 Ib를 갖는 화합물 또는 그의 제약상 허용되는 염이다.
<화학식 Ib>
상기 식에서,
n은 0, 1 또는 2이고;
R1은 C1 - 4알킬 또는 C1 - 4플루오로알킬이고;
R3은 C1 - 4알킬, C1 - 4할로알킬 또는 C3 - 6시클로알킬이고;
R6은 H, C1 - 4알킬 또는 C1 - 4할로알킬이고;
R7은 C1 - 4알킬이고;
R8은 CO2Rc 또는 CONRdRe이고;
Rc는 H 또는 C1 - 4알킬이고;
Rd 및 Re는 각각 독립적으로 H 및 C1 - 4알킬로부터 선택된다.
화학식 I의 또 다른 군에서, 화합물은 하기 화학식 Ic를 갖는 화합물 또는 그의 제약상 허용되는 염이다.
<화학식 Ic>
상기 식에서, n, R1, R3, R6, R7, R8, Rc, Rd 및 Re는 화학식 Ib를 갖는 화합물에 대해 상기 기재된 바와 같다.
화학식 Ic를 갖는 화합물의 한 하위군에서, R8은 CO2Rc로부터 선택된다.
본 발명의 대표적 화합물은 하기와 같으며, 여기서 각각의 명명된 화합물은 그의 개별 이성질체, 이들의 혼합물 (라세미체 및 부분입체이성질체 혼합물 포함), 뿐만 아니라 그의 제약상 허용되는 염을 포괄하도록 한다:
4-{1-[5-(2-브로모-5-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-3-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산;
tert-부틸 4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트;
3-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-2,2-디메틸시클로부탄카르복실산;
3-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}트리시클로[3.3.1.13,7]데칸-1-카르복실산;
6-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}비시클로[3.1.0]헥산-3-카르복실산;
메틸 4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실레이트;
4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산;
(3-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-2,2-디메틸시클로부틸)아세트산;
4-[1-(5-{3-[(4-시클로프로필-5-플루오로피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
에틸 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-2-메틸시클로헥산카르복실레이트;
4-{1-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-2,2,2-트리플루오로-1-히드록시에틸}시클로헥산카르복실산;
4-{2,2,2-트리플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-[1,2-디히드록시-1-(5-{3-[(4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
4-[1-(5-{3-[(5-플루오로-4-메틸피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1,2-디히드록시에틸]시클로헥산카르복실산;
N-(4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥실)메탄술폰아미드;
N-{4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥실}메탄술폰아미드;
에틸 4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]-2-메틸시클로헥산카르복실레이트;
4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]-2-메틸시클로헥산카르복실산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-2-메틸시클로헥산카르복실산;
부틸 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트;
1,4-디옥사스피로[4.5]데스-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메탄올;
4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)프로필]시클로헥산카르복실산;
에틸 4-{1-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}-2-메틸시클로헥산카르복실레이트;
4-{1-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}-2-메틸시클로헥산카르복실산;
1,4-디옥사스피로[4.5]데스-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메타논;
에틸 4-[1-(5-{3-[(5-플루오로-4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트;
4-1-(5-{3-[(5-플루오로-4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실산;
4-[1-히드록시-1-(5-{3-[(4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)에틸]-2-메틸시클로헥산카르복실산;
3-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]-2,2-디메틸시클로부틸}아세트산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산올;
{3-[1-(5-{3-[(5-플루오로-4-메틸피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]-2,2-디메틸시클로부틸}아세트산;
4-히드록시-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산;
1-[4-(히드록시메틸)시클로헥실]-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에탄올;
에틸 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]프로필}시클로헥산카르복실레이트;
부틸 4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트;
4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(1-메틸에틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-[1-(5-{3-[(4-시클로프로필피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
4-[1-히드록시-1-(5-{3-[(4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(1-메틸에톡시)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-[1-(5-{3-[(5-플루오로-4-메틸피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
4-[1-(5-{3-[(5-클로로-4-메틸피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
4-[1-(5-{3-[(5-플루오로-4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
4-[1-(5-{3-[(5-클로로-4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
부틸 4-[1-히드록시-1-(5-{3-[(4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트;
부틸 4-[1-(5-{3-[(5-플루오로-4-메톡시피리미딘-2-일)아미노]-5-메틸페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트;
부틸 4-[1-히드록시-1-(5-{3-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트;
4-[1-히드록시-1-(5-{3-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
부틸 4-{1-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실레이트;
4-{1-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]프로필}시클로헥산카르복실산;
4-{1-히드록시-2-메틸-1-[5-(3-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]프로필}시클로헥산카르복실산;
4-{1-히드록시-2-메틸-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]프로필}시클로헥산카르복실산;
4-{1,2-디히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-[2,2,2-트리플루오로-1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
4-[1,2-디히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산;
벤질 {4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥실}카르바메이트;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르보니트릴;
4-{1-메톡시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-{2-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-{아미노[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산;
4-[3,4-디히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)부틸]시클로헥산카르복실산;
4-[1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르보니트릴;
2-[2-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로프로필]-2-메틸프로판산;
3-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}비시클로[3.1.0]헥산-6-카르복실산;
3-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로펜탄카르복실산;
4-{플루오로[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산;
1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-[4-(2H-테트라졸-5-일)시클로헥실]에탄올;
1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)-1-[4-(2H-테트라졸-5-일)시클로헥실]에탄올;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-{시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산;
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산카르복실산;
4-{1-플루오로-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산;
1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-[4-(2H-테트라졸-5-일)시클로헥실]에탄올;
4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복스아미드;
4-[1-(5-{2-브로모-3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산;
4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산;
3,3-디메틸-4-{[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]카르보닐}시클로헥사논;
4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}-3,3-디메틸시클로헥산올;
4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산;
메틸 (1,3-시스, 1,4-트랜스)-3-히드록시-2,2-디메틸-4-{[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]카르보닐}시클로펜탄카르복실레이트;
4-[1-히드록시-1-{5-[3-(히드록시메틸)-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐]-1,3-티아졸-2-일}에틸]시클로헥산카르복실산;
4-{1-[5-(3-시클로프로필-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산;
4-{1-[5-(3-플루오로-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산;
4-(1-{5-[3-(디플루오로메틸)-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐]-1,3-티아졸-2-일}-1-히드록시에틸)시클로헥산카르복실산.
본원에서, 다양한 용어는 하기 정의된 바와 같다:
"알킬"은 명시된 개수의 탄소 원자를 갖는 직쇄 또는 분지쇄 탄화수소 라디칼을 지칭한다. "알킬"의 예는 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, t-부틸, n-펜틸, 이소펜틸 등을 포함하나, 이에 제한되는 것은 아니다.
"카르보사이클"은 모든 고리 원자가 탄소인 비-방향족 포화 또는 부분 불포화 모노시클릭 고리를 지칭하며, 고리는 단리되어 있거나, 1 또는 2개의 이러한 고리 또는 벤젠 고리에 융합 (오르토-융합, 스피로-융합 및 가교 포함)된다. 폴리시클릭 카르보사이클의 경우에, 부착 지점은 임의의 고리 상에 존재할 수 있다. 카르보사이클의 예는 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헥세닐, 시클로헵틸, 시클로헵테닐, 비시클로[3.3.0]옥탄, 인단, 비시클로[3.3.1]노난, 데칼린, 테트라히드로나프탈렌, 스피로[3.3]헵탄, 비시클로[3.1.0]헥산, 아다만탄, 트리시클로[2.2.1.02,6]헵탄, 디스피로[2.1.2.3]데칸을 포함하나, 이에 제한되는 것은 아니다.
"시클로알킬"은 고리 탄소 원자의 명시된 개수를 함유하고 헤테로원자는 함유하지 않는 포화 고리를 지칭한다. 유사한 방식으로, 용어 "C3 -6 시클로알킬"은 3 내지 6개의 고리 탄소 원자를 갖는 포화 고리를 지칭한다. 본 발명에 유용한 예시적인 "시클로알킬" 기는 시클로프로필, 시클로부틸, 시클로펜틸 및 시클로헥실을 포함하나, 이에 제한되는 것은 아니다.
"할로겐" 또는 "할로"는 플루오린, 염소, 브로민 또는 아이오딘을 지칭한다.
"할로알킬"은 1개 내지 모든 수소 원자까지 할로겐에 의해 대체되고; 할로겐은 본원에 정의된 바와 같은 것인, 상기 정의된 바와 같은 알킬 기를 지칭한다. 본 발명에 유용한 이러한 분지형 또는 직쇄형 할로알킬 기의 예는 1개 이상의 할로, 예를 들어 플루오로, 클로로, 브로모 및 아이오도로 독립적으로 치환된, 메틸, 에틸, 프로필, 이소프로필, 이소부틸 및 n-부틸을 포함하나, 이에 제한되는 것은 아니다. 유사하게, 용어 "플루오로알킬"은 1개 및 모든 수소 원자까지 플루오린에 의해 대체된 것인 상기 정의된 바와 같은 알킬 기를 지칭한다. "할로알킬"의 예는 플루오로메틸, 디플루오로메틸, 트리플루오로메틸, 1-플루오로에틸, 2-플루오로에틸, 2,2-디플루오로에틸, 2,2,2-트리플루오로에틸 및 퍼플루오로-n-프로필을 포함하나, 이에 제한되는 것은 아니다. "플루오로알킬"의 예는 플루오로메틸, 디플루오로메틸, 트리플루오로메틸, 1-플루오로에틸, 2-플루오로에틸, 2,2-디플루오로에틸, 2,2,2-트리플루오로에틸 및 퍼플루오로-n-프로필을 포함하나, 이에 제한되는 것은 아니다.
"히드록시알킬"은 각 탄소 원자 상의 1개의 수소 원자가 히드록시 기에 의해 대체된 것인 상기 정의된 바와 같은 알킬 기를 지칭한다. "히드록시알킬"의 예는 히드록시메틸, 히드록시에틸, 프로판-1,2-디올을 포함하나, 이에 제한되는 것은 아니다.
제약 조성물에서와 같이 용어 "조성물"은 활성 성분(들), 및 담체를 구성하는 불활성 성분(들) (제약상 허용되는 부형제)을 포함하는 생성물, 뿐만 아니라 임의의 2종 이상의 성분의 조합, 착화 또는 응집으로부터, 또는 하나 이상의 성분의 해리로부터, 또는 하나 이상의 성분의 다른 유형의 반응 또는 상호작용으로부터 직접 또는 간접적으로 생성되는 임의의 생성물을 포괄하는 것으로 의도된다. 따라서, 본 발명의 제약 조성물은 화학식 I의 화합물 및 제약상 허용되는 부형제를 혼합함으로써 제조된 임의의 조성물을 포괄한다.
본원에 사용된 용어 "임의로"는 후속적으로 기재되는 사건(들)이 일어날 수 있거나 일어나지 않을 수 있음을 의미하며, 일어난 사건(들) 및 일어나지 않은 사건들 둘 다를 포함한다.
본원에 사용된 용어 "1개 이상의 기로 치환된"은 지명된 치환기 또는 치환기들, 다수의 치환도로의 치환을 지칭하며, 치환기의 수가 명확하게 언급되지 않는 한 동일하거나 상이한 치환기로 모든 수소 원자를 대체하는 것까지 허용된다. 치환기의 수가 명확하게 언급되지 않은 경우, 1개 이상을 의도한다.
각각의 가변기는 일반적 구조 화학식 정의 내에서 발생할 때마다 독립적으로 정의된다. 예를 들어, "A" 고리 상의 1개 초과의 R7 치환기가 있는 경우, 각각의 치환기는 각 경우에 독립적으로 선택되고, 각각의 치환기는 다른 치환기(들)와 동일하거나 상이할 수 있다.
용어 "Syk 억제제"는 Syk 효소를 억제하는 화합물을 의미하는데 사용된다.
용어 "Syk 매개 질환" 또는 "부적절한 Syk 활성에 의해 매개되는 장애 또는 질환 또는 상태"는 Syk 키나제 메카니즘에 의해 매개 또는 조정되는 임의의 질환 상태를 의미하는데 사용된다. 이러한 질환 상태는 염증성, 알레르기성 및 자가면역 질환, 예를 들어 천식, 만성 폐쇄성 폐 질환 (COPD), 성인 호흡 곤란 증후군 (ARDS), 궤양성 결장염, 크론병, 기관지염, 피부염, 알레르기성 비염, 건선, 경피증, 두드러기, 류마티스 관절염, 다발성 경화증, 암, HIV 및 루푸스, 특히 천식, 만성 폐쇄성 폐 질환 (COPD), 성인 호흡 곤란 증후군 (ARDS), 알레르기성 비염 및 류마티스 관절염을 포함할 수 있다.
본원에 사용된 "본 발명의 화합물"은 화학식 I의 화합물, 또는 그의 염, 용매화물 또는 생리학상 기능적 유도체를 의미한다.
본원에 사용된 용어 "용매화물"은 용질 (본 발명에서는, 화학식 I의 화합물 또는 그의 염) 및 용매에 의해 형성된 다양한 화학양론의 복합체를 지칭한다. 본 발명의 목적을 위한 이러한 용매는 용질의 생물학적 활성을 방해하지 않을 수 있다. 적합한 용매의 예는 물, 아세톤, 메탄올, 에탄올 및 아세트산을 포함하나, 이에 제한되는 것은 아니다. 바람직하게는, 사용된 용매는 제약상 허용되는 용매이다. 적합한 제약상 허용되는 용매의 예는 물, 에탄올 및 아세트산을 포함한다. 가장 바람직하게는, 용매는 물이다.
본원에 사용된 용어 "생리학상 기능적 유도체"는 생체내에서 변환되어 화학식 I의 화합물, 또는 상기 화합물의 제약상 허용되는 염, 수화물 또는 용매화물을 제공하는 화합물 (예를 들어, 약물 전구체)을 지칭한다. 변환은 다양한 메카니즘에 의해 (예를 들어, 대사 또는 화학적 과정에 의해), 예컨대 예를 들어 혈액 중에서의 가수분해를 통해 발생할 수 있다. 전구약물은 이러한 유도체이고, 전구약물의 사용에 대한 논의는 문헌 [T. Higuchi and W. Stella, "Pro-drugs as Novel Delivery Systems," Vol. 14 of the A.C.S. Symposium Series, 및 Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987]에 제공된다.
화학식 I의 화합물은 하나 초과의 형태 (다형성으로서 공지된 특성)로 결정화될 수 있으며, 이러한 다형체 형태 ("다형체")가 화학식 I의 범주 내에 있는 것으로 이해해야 한다. 다형성은 일반적으로 온도 또는 압력 또는 둘 다의 변화에 대한 반응으로서 발생할 수 있고, 또한 결정화 과정에서의 변화로부터 야기될 수 있다. 다형체는 당업계에 공지된 다양한 물리적 특성, 예컨대 X선 회절 패턴, 용해도 및 융점에 의해 구별될 수 있다.
화학식 I의 화합물은 비대칭 또는 키랄 중심을 함유할 수 있고, 따라서 다양한 입체이성질체 형태로 존재할 수 있다. 화학식 I의 화합물의 모든 입체이성질체 형태 뿐만 아니라 그의 혼합물, 예컨대 라세미 혼합물이 본 발명의 일부를 형성하는 것으로 의도된다. 부분입체이성질체 혼합물은 당업자에게 널리 공지된 방법, 예컨대 예를 들어 크로마토그래피 및/또는 분별 결정화에 의해, 그의 물리적 화학적 차이에 기반하여 그의 개별 부분입체이성질체로 분리될 수 있다. 거울상이성질체는 거울상이성질체 혼합물을 적절한 광학 활성 화합물 (예를 들어, 키랄 보조제, 예컨대 키랄 알콜 또는 모셔(Mosher) 산 클로라이드)과 반응시켜 부분입체이성질체 혼합물로 전환시키고, 부분입체이성질체를 분리하고, 개별 부분입체이성질체들을 상응하는 순수한 거울상이성질체로 전환 (예를 들어, 가수분해)시킴으로써 분리될 수 있다. 거울상이성질체는 또한 키랄 고정상을 갖는 칼럼을 사용하는 크로마토그래피에 의해 분리될 수 있다. 또한, 화학식 I의 화합물의 일부는 회전장애이성질체 (예를 들어, 치환된 비아릴)일 수 있고, 본 발명의 일부로서 간주된다.
화학식 I의 화합물이 호변이성질체를 형성할 수 있다는 것이 또한 주목된다. 본 발명의 화합물의 모든 호변이성질체 및 호변이성질체의 혼합물이 본 발명의 화합물의 범주 내에 포함되는 것으로 이해해야 한다. 본원에 기재된 화합물 중 일부는 올레핀계 이중 결합을 함유하고, 달리 명시되지 않는 한, E 및 Z 기하 이성질체를 둘 다 포함하도록 한다.
각각의 가변기에 대한 실시양태는 일반적으로 각각의 가변기에 대해 상기에 개별적으로 열거되어 있으며, 본 발명은 또한 화학식 I의 여러 또는 각각의 실시양태가 상기 열거된 각각의 실시양태로부터 선택된 그러한 화합물을 포함한다. 따라서, 본 발명은 각각의 가변기에 대한 실시양태의 모든 조합을 포함하는 것으로 의도된다.
본 발명의 화합물은 제약상 허용되는 염의 형태일 수 있고/거나 제약상 허용되는 염으로서 투여될 수 있다. 적합한 염에 대한 개관을 위해 문헌 [Berge et al., J. Pharm. Sci. 1977, 66, 1-19]를 참조한다. 전형적으로, 본 발명의 염은 제약상 허용되는 염이다. 용어 "제약상 허용되는 염" 내에 포괄된 염은 본 발명의 화합물의 비-독성 염을 지칭한다. 적합한 제약상 허용되는 염은 산 또는 염기 부가염을 포함할 수 있다.
제약상 허용되는 산 부가염은, 임의로 적합한 용매, 예컨대 유기 용매 중에서 화학식 I의 화합물을 적합한 무기 또는 유기 산 (예컨대, 브로민화수소산, 염산, 황산, 질산, 인산, 숙신산, 말레산, 포름산, 아세트산, 프로피온산, 푸마르산, 시트르산, 타르타르산, 락트산, 벤조산, 살리실산, 글루탐산, 아스파르트산, p-톨루엔술폰산, 벤젠술폰산, 메탄술폰산, 에탄술폰산, 나프탈렌술폰산, 예컨대 2-나프탈렌술폰산 또는 헥산)과 반응시켜 염을 수득하고 이를 통상적으로 예를 들어 결정화 및 여과에 의해 단리함으로써 형성될 수 있다. 화학식 I의 화합물의 제약상 허용되는 산 부가염은 예를 들어 히드로브로마이드, 히드로클로라이드, 술페이트, 니트레이트, 포스페이트, 숙시네이트, 말레에이트, 포르메이트, 아세테이트, 프로피오네이트, 푸마레이트, 시트레이트, 타르트레이트, 락테이트, 벤조에이트, 살리실레이트, 글루타메이트, 아스파르테이트, p-톨루엔술포네이트, 벤젠술포네이트, 메탄술포네이트, 에탄술포네이트, 나프탈렌술포네이트 (예를 들어, 2-나프탈렌술포네이트) 또는 헥사노에이트 염이거나 이들을 포함할 수 있다.
제약상 허용되는 염기 염은 화학식 I의 화합물을 적합한 무기 또는 유기 염기와 반응시켜 형성될 수 있다. 무기 염기로부터 유도된 염은 알루미늄, 암모늄, 칼슘, 구리, 제2철, 제1철, 리튬, 마그네슘, 제2망가니즈 염, 제1망가니즈, 칼륨, 나트륨, 아연 등을 포함한다. 암모늄, 칼슘, 마그네슘, 칼륨 및 나트륨 염이 특히 바람직하다. 제약상 허용되는 유기 비-독성 염기로부터 유도된 염은 1급, 2급 및 3급 아민, 자연 발생 치환된 아민을 비롯한 치환된 아민, 시클릭 아민, 및 염기성 이온 교환 수지, 예컨대 아르기닌, 베타인, 카페인, 콜린, N,N'-디벤질에틸렌디아민, 디에틸아민, 2-디에틸아미노에탄올, 2-디메틸아미노에탄올, 에탄올아민, 에틸렌디아민, N-에틸-모르폴린, N-에틸피페리딘, 글루카민, 글루코사민, 히스티딘, 히드라바민, 이소프로필아민, 리신, 메틸글루카민, 모르폴린, 피페라진, 피페리딘, 폴리아민 수지, 프로카인, 퓨린, 테오브로민, 트리에틸아민, 트리메틸아민, 트리프로필아민, 트로메타민 등의 염을 포함한다.
또한, 다른 비-제약상 허용되는 염, 예를 들어 옥살레이트 또는 트리플루오로아세테이트가 예를 들어 본 발명의 화합물의 단리에 사용될 수 있으며, 이는 본 발명의 범주 내에 포함된다.
본 발명은 화합물이 모노- 또는 디-히드레이트, 또는 모노 - 또는 디히드로클로라이드로서 존재하는 경우와 같이 화학식 I의 화합물의 모든 가능한 화학량론적 및 비-화학량론적 형태를 그 범주 내에 포함한다.
화학식 I의 화합물에서, 원자는 그의 천연 동위원소 존재비를 나타낼 수 있거나, 또는 원자 중 1개 이상은, 동일한 원자 번호를 갖지만 자연에서 주로 발견되는 원자 질량 또는 질량수와 상이한 원자 질량 또는 질량수를 갖는 특정한 동위원소로 인공적으로 농축될 수 있다. 본 발명은 화학식 I의 화합물의 모든 적합한 동위원소 변형을 포함하도록 한다. 예를 들어, 수소 (H)의 다양한 동위원소 형태는 경수소 (1H) 및 중수소 (2H)를 포함한다. 경수소는 자연에서 발견되는 우세한 수소 동위원소이다. 중수소를 농축시키는 것은 특정의 치료 이점, 예컨대 생체내 반감기의 증가 또는 투여량 요건의 감소를 제공할 수 있거나, 또는 생물학적 샘플의 특성화를 위한 표준물로서 유용한 화합물을 제공할 수 있다. 화학식 I에 속하는 동위원소-농축된 화합물은 당업자에게 널리 공지된 통상의 기술에 의해, 또는 적절한 동위원소-농축된 시약 및/또는 중간체를 사용하여 본원의 반응식 및 실시예에 기재된 것과 유사한 방법에 의해 과도한 실험 없이 제조될 수 있다.
화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체는 Syk 활성의 억제제이며, 따라서 부적절한 Syk 활성과 연관된 질환 및 상태의 치료에 잠재적으로 유용할 것으로 여겨진다.
화학식 I의 화합물 또는 그의 제약상 허용되는 염, 및 제약 조성물은 비장 티로신 키나제 (Syk)에 의해 매개되는 다양한 상태 또는 질환을 치료 또는 예방하는데 사용될 수 있다. 이러한 상태 및 질환은 하기를 포함하나, 이에 제한되는 것은 아니다: (1) 관절염, 예컨대 류마티스 관절염, 소아 관절염, 건선성 관절염 및 골관절염; (2) 천식 및 다른 폐쇄성 기도 질환, 예컨대 만성 천식, 후기 천식, 기도 과민반응, 기관지염, 기관지 천식, 알레르기성 천식, 본태성 천식, 외인성 천식, 먼지 천식, 성인 호흡 곤란 증후군, 재발성 기도 폐쇄 및 만성 폐쇄 폐 질환, 예컨대 기종; (3) 자가면역 질환 또는 장애, 예컨대 단일 기관 또는 단일 세포-유형 자가면역 장애로 명시된 것들, 예를 들어 하시모토 갑상선염, 자가면역 용혈성 빈혈, 악성 빈혈의 자가면역 위축성 위염, 자가면역 뇌척수염, 자가면역 고환염, 굿패스쳐병, 자가면역 혈소판감소증, 예컨대 특발성 혈소판감소성 자반증, 교감신경성 안염, 중증 근무력증, 그레이브스병, 원발성 담즙성 간경변증, 만성 공격성 간염, 궤양성 결장염 및 막 사구체병증, 전신 자가면역 장애를 수반하는 것으로 명시된 것들, 예를 들어 전신 홍반성 루푸스, 면역 혈소판감소성 자반증, 류마티스 관절염, 쇼그렌 증후군, 라이터 증후군, 다발근염-피부근염, 전신 경화증, 결절성 다발동맥염, 다발성 경화증 및 수포성 유천포창, 및 B-세포 (체액) 기반 또는 T-세포 기반일 수 있는 추가의 자가면역 질환, 예컨대 코간 증후군, 강직성 척추염, 베게너 육아종증, 자가면역 탈모증, 제I형 또는 소아 발병 당뇨병, 및 갑상선염; (4) 암 또는 종양, 예컨대 소화관암/위장관암, 결장암, 간암, 피부암, 예컨대 비만 세포 종양 및 편평 세포 암종, 유방암 및 유암, 난소암, 전립선암, 림프종 및 백혈병 (비제한적으로 급성 골수성 백혈병, 만성 골수성 백혈병, 외투 세포 림프종, NHL B 세포 림프종 (예를 들어, 전구 B-ALL, 변연부 B 세포 림프종, 만성 림프구성 백혈병, 미만성 거대 B 세포 림프종, 버킷 림프종, 종격 거대 B-세포 림프종), 호지킨 림프종, NK 및 T 세포 림프종; TEL-Syk 및 ITK-Syk 융합 유래된 종양 포함), 골수종, 예컨대 다발성 골수종, 골수증식성 장애, 신장암, 폐암, 근육 암, 골암, 방광암, 뇌암, 흑색종, 예컨대 경구 및 전이성 흑색종, 카포시 육종, 증식성 당뇨병성 망막병증, 및 혈관신생-연관 장애, 예컨대 고형 종양, 및 췌장암; (5) 당뇨병, 예컨대 제I형 당뇨병 및 당뇨병으로부터의 합병증; (6) 안 질환, 장애 또는 상태, 예컨대 눈의 자가면역 질환, 각결막염, 춘계 결막염, 포도막염, 예컨대 베체트병과 연관된 포도막염 및 렌즈-유발 포도막염, 각막염, 포진성 각막염, 원추 각막염, 각막 상피 이영양증, 각막백반, 안구 천포창, 무렌 궤양, 공막염, 그레이브스 안병증, 보그트-코야나기-하라다 증후군, 건성 각결막염 (안구 건조), 플릭테뉼, 홍채모양체염, 사르코이드증, 내분비 안병증, 교감신경성 안염, 알레르기성 결막염 및 안구 신생혈관화; (7) 장 염증, 알레르기 또는 상태, 예컨대 크론병 및/또는 궤양성 결장염, 염증성 장 질환, 복강 질환, 직장염, 호산구성 위장염 및 비만세포증; (8) 신경변성 질환, 예컨대 운동 뉴런 질환, 알츠하이머병, 파킨슨병, 근위축성 측삭 경화증, 헌팅톤병, 뇌 허혈, 또는 외상성 손상, 타격, 글루타메이트 신경독성 또는 저산소증에 의해 유발되는 신경변성 질환; 졸중에서의 허혈성/재관류 손상, 심근 허혈, 신장 허혈, 심장 발작, 심장 비대증, 아테롬성동맥경화증 및 동맥경화증, 기관 저산소증; (9) 혈소판 응집 및 혈소판 활성화와 연관되거나 또는 그에 의해 유발되는 질환, 예컨대 동맥경화증, 혈전증, 내막 증식증 및 혈관 손상 후 재협착; (10) 심혈관 질환과 연관된 상태, 예컨대 재협착, 급성 관상동맥 증후군, 심근경색, 불안정형 협심증, 불응성 협심증, 혈전용해 요법후 또는 관상동맥 혈관성형술 후 발생하는 폐쇄성 관상동맥 혈전, 혈전성 매개 뇌혈관 증후군, 색전성 졸중, 혈전성 졸중, 일과성 허혈 발작, 정맥 혈전증, 심부 정맥 혈전증, 폐 색전, 응고병증, 파종성 혈관내 응고, 혈전성 혈소판감소성 자반증, 폐쇄성 혈전혈관염, 헤파린-유발 혈소판감소증과 연관된 혈전성 질환, 체외 순환과 연관된 혈전성 합병증, 심장 또는 다른 혈관내 카테터삽입과 같은 기기와 연관된 혈전성 합병증, 대동맥내 풍선 펌프, 관상동맥 스텐트 또는 심장 판막, 보철 장치의 조정이 필요한 상태 등; (11) 피부 질환, 상태 또는 장애, 예컨대 아토피성 피부염, 습진, 건선, 경피증, 소양증 및 다른 소양성 상태; (12) 알레르기 반응, 예컨대 아나필락시스, 알레르기성 비염, 알레르기성 피부염, 알레르기성 두드러기, 혈관부종, 알레르기성 천식, 또는 곤충 교상, 식품, 약물 또는 화분에 대한 알레르기 반응; (13) 이식 거부, 예컨대 췌장섬 이식 거부, 골수 이식 거부, 이식편-대-숙주 질환, 골수, 연골, 각막, 심장, 추간판, 섬, 신장, 사지, 간, 폐, 근육, 근모세포, 신경, 췌장, 피부, 소장 또는 기도와 같은 기관 및 세포 이식 거부 및 이종 이식; (14) 저등급 반흔형성, 예컨대 경피증, 증가된 섬유증, 켈로이드, 수술후 반흔, 폐 섬유증, 혈관 연축, 편두통, 재관류 손상 및 심근경색후.
따라서, 본 발명은 부적절한 Syk 활성에 의해 매개되는 질환 및 상태의 요법에서, 특히 그의 치료에 사용하기 위한 화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체를 제공한다. 본원에 지칭된 부적절한 Syk 활성은 특정의 포유동물 대상체에서 예상되는 정상 Syk 활성에서 벗어난 임의의 Syk 활성이다. 부적절한 Syk 활성은, 예를 들어 활성의 비정상적 증가, 또는 Syk 활성의 시기 및 또는 제어에서의 이상의 형태로 나타날 수 있다. 이러한 부적절한 활성은 이후에 예를 들어, 부적절한 또는 탈제어된 활성화를 야기하는 단백질 키나제의 과다발현 또는 돌연변이로부터 유발될 수 있다.
추가 실시양태에서, 본 발명은 탈조절된 Syk 활성과 관련된 장애의 예방 및/또는 치료를 위해 Syk를 조절하거나, 조정하거나 또는 억제하는 방법에 관한 것이다.
추가 실시양태에서, 본 발명은 Syk 활성에 의해 매개되는 장애를 앓는 포유동물에게 유효량의 화학식 I의 화합물, 또는 그의 제약상 허용되는 염, 용매화물 또는 생리학상 기능적 유도체를 투여하는 것을 포함하는, 상기 포유동물의 치료 방법을 제공한다.
추가 실시양태에서, 본 발명은 Syk 활성에 의해 매개되는 장애의 치료를 위한 의약의 제조에서의 화학식 I의 화합물, 또는 그의 제약상 허용되는 염 또는 용매화물 또는 그의 생리학상 기능적 유도체의 용도를 제공한다.
추가 실시양태에서, 상기 Syk 활성에 의해 매개되는 장애는 천식이다. 추가 실시양태에서, 상기 장애는 류마티스 관절염이다. 또 다른 실시양태에서, 상기 장애는 암이다. 추가 실시양태에서, 상기 장애는 안구 결막염이다.
본 발명의 또 다른 측면은, Fc 수용체 신호전달 캐스케이드 또는 탈과립화의 화학적 매개자의 방출 또는 합성에 의해 특성화되고/거나 그에 의해 유발되고/거나 그와 연관된 질환의 치료 또는 예방에 대한 치료 접근법으로서, FceRI 및/또는 FcgRI-매개 탈과립화를 비롯한 상기 Fc 수용체 신호전달 캐스케이드에 의해 유발되거나 그와 연관된 질환을 치료하는 방법을 제공한다. 또한, Syk는 이뮤노티로신-기재 활성화 모티프 (ITAM) 신호전달, B 세포 수용체 신호전달, T 세포 수용체 신호전달에서 중요한 역할을 하는 것으로 공지되어 있으며, 호중구에서 인테그린 베타 (1), 베타 (2) 및 베타 (3) 신호전달의 필수적 성분이다. 따라서, 본 발명의 화합물은 Fc 수용체, ITAM, B 세포 수용체 및 인테그린 신호전달 캐스케이드, 뿐만 아니라 이러한 신호전달 캐스케이드를 통하여 유도되는 세포 반응을 조절하는데 사용될 수 있다. 조절되거나 억제될 수 있는 세포 반응의 비제한적 예는 호흡 폭발, 세포 접착, 세포 탈과립화, 세포 확산, 세포 이동, 식세포작용, 칼슘 이온 플럭스, 혈소판 응집 및 세포 성숙을 포함한다.
요법에 사용하기 위해, 화학식 I의 화합물, 뿐만 아니라 그의 염, 용매화물 및 생리학상 기능적 유도체를 미가공 화학물질로서 투여할 수 있는 것이 가능한 한편, 활성 성분을 제약 조성물로서 제공하는 것이 가능하다. 따라서, 본 발명은 또한 화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체, 및 하나 이상의 제약상 허용되는 담체, 희석제 또는 부형제를 포함하는 제약 조성물을 추가로 제공한다. 화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체는 상기 기재된 바와 같다. 담체(들), 희석제(들) 또는 부형제(들)는 제제의 다른 성분과 상용성이어야 하고 그의 수용자에게 유해하지 않아야 한다는 점에서 허용되는 것이어야 한다. 본 발명의 또 다른 측면에 따라, 화학식 I의 화합물, 또는 그의 염, 용매화물 및 생리학상 기능적 유도체를 하나 이상의 제약상 허용되는 담체, 희석제 또는 부형제와 혼합하는 것을 포함하는, 제약 조성물의 제조 방법이 또한 제공된다.
본 발명의 제약 조성물은 단위 용량당 소정량의 활성 성분을 함유하는 단위 투여 형태로 제공될 수 있다. 이러한 단위는 치료되는 상태, 투여 경로, 및 환자의 연령, 체중 및 상태에 따라, 예를 들어 5 μg 내지 1 g, 바람직하게는 1 mg 내지 700 mg, 보다 바람직하게는 5 mg 내지 100 mg의 화학식 I의 화합물을 함유할 수 있다. 따라서, 이러한 단위 용량은 1일 1회 초과로 투여될 수 있다. 바람직한 단위 투여량 조성물은 활성 성분의 상기 본원에 언급된 바와 같은 1일 용량 또는 하위-용량 (1일 1회 초과의 투여를 위해), 또는 그의 적절한 분획을 함유하는 것이다. 또한, 이러한 제약 조성물은 제약 업계에 널리 공지된 임의의 방법에 의해 제조될 수 있다.
본 발명의 제약 조성물은 임의의 적절한 경로, 예를 들어 경구 (협측 또는 설하 포함), 직장, 국소, 흡입, 비강, 안구 또는 비경구 (정맥내 및 근육내 포함) 경로로 투여에 적합화될 수 있다. 이러한 조성물은 제약학 업계에 공지된 임의의 방법에 의해, 예를 들어 활성 성분을 담체(들) 또는 부형제(들)와 회합시킴으로써 제조될 수 있다. 투여 형태는 정제, 트로키, 분산액, 현탁액, 용액, 캡슐, 크림, 연고, 에어로졸 등을 포함한다.
추가 실시양태에서, 본 발명은, 예를 들어 류마티스 관절염을 치료하기 위한, 경구 경로에 의한 투여에 적합화된 제약 조성물을 제공한다.
추가 실시양태에서, 본 발명은, 예를 들어 알레르기성 비염을 치료하기 위한, 비강 경로에 의한 투여에 적합화된 제약 조성물을 제공한다.
추가 실시양태에서, 본 발명은, 예를 들어 천식, COPD 또는 ARDS를 치료하기 위한, 흡입 경로에 의한 투여에 적합화된 제약 조성물을 제공한다.
추가 실시양태에서, 본 발명은, 안 질환, 예를 들어 결막염을 치료하기 위한, 안구 경로에 의한 투여에 적합화된 제약 조성물을 제공한다.
추가 실시양태에서, 본 발명은, 예를 들어 암을 치료하기 위한, 비경구 (정맥내 포함) 경로에 의한 투여에 적합화된 제약 조성물을 제공한다.
경구 투여에 적합화된 본 발명의 제약 조성물은 이산 단위, 예컨대 캡슐 또는 정제; 분말 또는 과립; 수성 또는 비-수성 액체 중의 용액 또는 현탁액; 식용 폼 또는 휩; 또는 수중유 액체 에멀젼 또는 유중수 액체 에멀젼으로 제공될 수 있다.
예를 들어, 정제 또는 캡슐 형태로 경구 투여하는 경우, 활성 약물 성분은 경구 비-독성 제약상 허용되는 불활성 담체, 예컨대 에탄올, 글리세롤, 물 등과 조합될 수 있다. 분말은, 화합물을 적합한 미세 크기로 분쇄하고, 예를 들어 전분 또는 만니톨로서의 식용 탄수화물과 같은 유사하게 분쇄된 제약 담체와 혼합하여 제조된다. 향미제, 보존제, 분산제 및 착색제가 또한 존재할 수 있다.
캡슐은 상기 기재된 바와 같이 분말 혼합물을 제조하고, 형성된 젤라틴 외피에 충전시킴으로써 제조된다. 활택제 및 윤활제, 예컨대 콜로이드성 실리카, 활석, 스테아르산마그네슘, 스테아르산칼슘 또는 고체 폴리에틸렌 글리콜이 충전 작업 이전에 분말 혼합물에 첨가될 수 있다. 캡슐이 섭취되는 경우에 의약의 이용성을 개선하기 위해 붕해제 또는 가용화제, 예컨대 한천-한천, 탄산칼슘 또는 탄산나트륨이 또한 첨가될 수 있다.
또한, 원하거나 필요한 경우에, 적합한 결합제, 윤활제, 붕해제 및 착색제가 또한 혼합물에 혼입될 수 있다. 적합한 결합제는 전분, 젤라틴, 천연 당, 예컨대 글루코스 또는 베타-락토스, 옥수수 감미제, 천연 및 합성 검, 예컨대 아카시아, 트라가칸트 또는 알긴산나트륨, 카르복시메틸셀룰로스, 폴리에틸렌 글리콜, 왁스 등을 포함한다. 이들 투여 형태에 사용되는 윤활제는 올레산나트륨, 스테아르산나트륨, 스테아르산마그네슘, 벤조산나트륨, 아세트산나트륨 등을 포함한다. 붕해제는 비제한적으로 전분, 메틸 셀룰로스, 한천, 벤토나이트, 크산탄 검 등을 포함한다. 정제는, 예를 들어 분말 혼합물의 제조, 과립화 또는 슬러깅, 윤활제 및 붕해제의 첨가, 및 정제로의 압축에 의해 제제화된다. 분말 혼합물은 적합하게 분쇄된 화합물을 상기 기재된 바와 같은 희석제 또는 염기, 및 임의로 결합제, 예컨대 카르복시메틸셀룰로스, 알기네이트, 젤라틴 또는 폴리비닐 피롤리돈, 용해 지연제, 예컨대 파라핀, 흡수 촉진제, 예컨대 4급 염, 및/또는 흡수 작용제, 예컨대 벤토나이트, 카올린 또는 인산이칼슘과 혼합하여 제조된다. 분말 혼합물은 결합제, 예컨대 시럽, 전분 페이스트, 아카시아 점액, 또는 셀룰로스 또는 중합체 물질의 용액으로 습윤시키고, 스크린을 통해 통과시켜 과립화될 수 있다. 과립화에 대한 대안으로서, 분말 혼합물을 타정기에 통과시킬 수 있으며, 그 결과물은 과립으로 부수어지는 불완전하게 형성된 슬러그이다. 정제 형성 다이에 점착되는 것을 방지하기 위해, 스테아르산, 스테아레이트 염, 활석 또는 미네랄 오일을 첨가함으로써 과립을 윤활시킬 수 있다. 이어서, 윤활된 혼합물은 정제로 압축된다. 본 발명의 화합물은 또한 자유 유동 불활성 담체와 배합되어, 과립화 또는 슬러깅 단계를 거치지 않고 직접 정제로 압축될 수 있다. 쉘락의 실링 코트, 당 또는 중합체 물질의 코팅, 및 왁스의 광택 코팅으로 이루어진 투명 또는 불투명 보호 코팅이 제공될 수 있다. 상이한 단위 투여량을 구별하기 위해 이들 코팅에 염료가 첨가될 수 있다.
경구용 유동액, 예컨대 용액, 시럽 및 엘릭시르는 주어진 양이 소정량의 화합물을 함유하도록 하는 투여 단위 형태로 제조될 수 있다. 시럽은 화합물을 적합한 향미 수용액 중에 용해시킴으로써 제조될 수 있는 한편, 엘릭시르는 비-독성 알콜성 비히클을 사용하여 제조된다. 현탁액은 화합물을 비-독성 비히클 중에 분산시킴으로써 제제화될 수 있다. 가용화제 및 유화제, 예컨대 에톡실화 이소스테아릴 알콜 및 폴리옥시 에틸렌 소르비톨 에테르, 보존제, 향미 첨가제, 예컨대 페퍼민트 오일 또는 천연 감미제 또는 사카린 또는 다른 인공 감미제 등이 또한 첨가될 수 있다.
적절한 경우, 경구 투여용 투여 단위 조성물은 마이크로캡슐화될 수 있다. 제제는 또한, 예를 들어 중합체, 왁스 등에 미립자 물질을 코팅 또는 포매시켜 연장 또는 지속 방출되도록 제조될 수 있다.
화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체는 또한 리포솜 전달 시스템, 예컨대 소형 단층 소포, 대형 단층 소포 및 다층 소포의 형태로 투여될 수 있다. 리포솜은 다양한 인지질, 예컨대 콜레스테롤, 스테아릴아민 또는 포스파티딜콜린으로부터 형성될 수 있다.
화학식 I의 화합물, 및 그의 염, 용매화물 및 생리학상 기능적 유도체는 또한 화합물 분자가 커플링된 개별 담체로서의 모노클로날 항체를 사용함으로써 전달될 수 있다. 화합물은 또한 표적화가능한 약물 담체로서의 가용성 중합체와 커플링될 수 있다. 이러한 중합체는 폴리비닐피롤리돈, 피란 공중합체, 폴리히드록시프로필메타크릴아미드-페놀, 폴리히드록시에틸아스파르트아미드페놀 또는 폴리에틸렌옥시드폴리리신 (팔미토일 잔기로 치환됨)을 포함할 수 있다. 또한, 화합물은 약물의 제어 방출을 달성하는데 유용한 생분해성 중합체의 부류, 예를 들어 폴리락트산, 폴리엡실론 카프로락톤, 폴리히드록시 부티르산, 폴리오르토에스테르, 폴리아세탈, 폴리디히드로피란, 폴리시아노아크릴레이트, 및 히드로겔의 가교된 또는 양친매성의 블록 공중합체에 커플링될 수 있다.
흡입 투여를 위한 투여 형태는 편리하게는 에어로졸 또는 건조 분말로서 제제화될 수 있다.
흡입 투여에 적합하고/거나 적합화된 조성물의 경우, 화학식 I의 화합물 또는 염이 입자-크기-감소된 형태인 것이 바람직하고, 크기-감소된 형태가 마이크로화에 의해 수득되거나 또는 수득가능한 것이 보다 바람직하다. 크기-감소된 (예를 들어, 마이크로화) 화합물 또는 염 또는 용매화물의 바람직한 입자 크기는 약 0.5 내지 약 10 마이크로미터의 D50 값 (예를 들어, 레이저 회절을 사용하여 측정된 바와 같음)에 의해 규정된다.
예를 들어 흡입 투여를 위한 에어로졸 제제는 제약상 허용되는 수성 또는 비-수성 용매 중의 활성 물질의 용액 또는 미세 현탁액을 포함할 수 있다. 에어로졸 제제는 분무 장치 또는 흡입기와 함께 사용하기 위한 카트리지 또는 리필의 형태를 취할 수 있는 밀봉된 용기 내에 멸균 형태로 단일 또는 다중 용량으로 제공될 수 있다. 대안적으로, 밀봉된 용기는, 일단 용기의 내용물이 소진된 후에 폐기되도록 하는 일체형 분배 장치, 예컨대 계량 밸브 (계량 용량 흡입기)가 장착된 단일 용량 비강 흡입기 또는 에어로졸 분배기일 수 있다.
투여 형태가 에어로졸 분배기를 포함하는 경우에, 이는 바람직하게는 압력, 예컨대 압축 공기, 이산화탄소 하에 적합한 추진제 또는 유기 추진제, 예컨대 히드로플루오로카본 (HFC)을 함유한다. 적합한 HFC 추진제는 1,1,1,2,3,3,3-헵타플루오로프로판 및 1,1,1,2-테트라플루오로에탄을 포함한다. 에어로졸 투여 형태는 또한 펌프-분무기의 형태를 취할 수 있다. 가압된 에어로졸은 활성 화합물의 용액 또는 현탁액을 함유할 수 있다. 이는 현탁액 제제의 분산 특성 및 균질성을 개선시키기 위해 추가의 부형제, 예를 들어 공-용매 및/또는 계면활성제의 혼입이 필요할 수 있다. 용액 제제는 또한 공-용매, 예컨대 에탄올의 첨가가 필요할 수 있다. 예를 들어 제제의 안정성 및/또는 맛 및/또는 미립자 질량 특성 (양 및/또는 프로파일)을 개선시키기 위해 다른 부형제 개질제가 또한 혼입될 수 있다.
흡입 투여에 적합하고/거나 적합화된 제약 조성물의 경우, 제약 조성물이 건조 분말 흡입성 조성물인 것이 바람직하다. 이러한 조성물은 분말 베이스, 예컨대 락토스, 글루코스, 트레할로스, 만니톨 또는 전분, 화학식 I의 화합물, 또는 그의 염 또는 용매화물 (바람직하게는 입자-크기-감소된 형태, 예를 들어 마이크로화 형태), 및 임의로 성능 개질제, 예컨대 L-류신 또는 또 다른 아미노산 및/또는 스테아르산의 금속 염, 예컨대 스테아르산마그네슘 또는 스테아르산칼슘을 포함할 수 있다. 바람직하게는, 건조 분말 흡입성 조성물은 락토스 및 화학식 I의 화합물 또는 그의 염의 건조 분말 블렌드를 포함한다. 락토스는 바람직하게는 락토스 수화물, 예를 들어 락토스 1수화물이고/거나 바람직하게는 흡입-등급 및/또는 미세-등급 락토스이다. 바람직하게는, 락토스의 입자 크기는, 락토스 입자의 90% 이상 (중량 기준 또는 부피 기준)이 직경에서 1000 마이크로미터 (μm) 미만 (예를 들어, 10-1000 마이크로미터, 예를 들어 30-1000 마이크로미터), 및/또는 락토스 입자의 50% 이상이 직경에서 500 마이크로미터 미만 (예를 들어, 10-500 마이크로미터)인 것으로 규정된다. 보다 바람직하게는, 락토스의 입자 크기는, 락토스 입자의 90% 이상이 직경에서 300 마이크로미터 미만 (예를 들어, 10-300 마이크로미터, 예를 들어 50-300 마이크로미터), 및/또는 락토스 입자의 50% 이상이 직경에서 100 마이크로미터 미만인 것으로 규정된다. 임의로, 락토스의 입자 크기는, 락토스 입자의 90% 이상이 직경에서 100-200 마이크로미터 미만, 및/또는 락토스 입자의 50% 이상이 직경에서 40-70 마이크로미터 미만인 것으로 규정된다. 입자의 약 3 내지 약 30% (예를 들어, 약 10%) (중량 기준 또는 부피 기준)가 직경에서 50 마이크로미터 미만 또는 20 마이크로미터 미만인 것이 바람직하다. 예를 들어, 비제한적으로, 적합한 흡입-등급 락토스는 E9334 락토스 (10% 미세물) (보르쿨로 도모 인그리디언츠(Borculo Domo Ingredients), 네덜란드 8017 J D 츠볼레 한체플라인 25)이다.
임의로, 특히 건조 분말 흡입성 조성물의 경우, 흡입 투여를 위한 제약 조성물은 적합한 흡입 장치 내 스트립 또는 리본에 세로로 탑재된 다수의 밀봉된 용량 용기 (예를 들어, 건조 분말 조성물을 함유함)에 혼입될 수 있다. 용기는 필요 시 파열될 수 있거나 벗겨져 개봉될 수 있으며, 예를 들어 건조 분말 조성물의 용량은 디스쿠스(DISKUS)® 장치 (글락소스미스클라인(GlaxoSmithKline))와 같은 장치를 통해 흡입에 의해 투여될 수 있다. 다른 건조 분말 흡입기는 통상의 당업자에게 널리 공지되어 있으며, 다수의 이러한 장치는 상업적으로 입수가능하며, 대표적인 장치는 에어로라이저(Aerolizer)® (노파르티스(Novartis)), 에어맥스(Airmax)™ (이백스(IVAX)), 클릭할러(ClickHaler)® (이노바타 바이오메드(Innovata Biomed)), 디스크할러(Diskhaler)® (글락소스미스클라인), 아큐할러(Accuhaler) (글락소스미스클라인), 이지할러(Easyhaler)® (오리온 파마(Orion Pharma)), 이클립스(Eclipse)™ (아벤티스(Aventis)), 플로우캡스(FlowCaps)® (호비온(Hovione)), 핸디할러(Handihaler)® (베링거 잉겔하임(Boehringer Ingelheim)), 풀비날(Pulvinal)® (키에시(Chiesi)), 로타할러(Rotahaler)® (글락소스미스클라인), 스카이할러(SkyeHaler)™ 또는 서티할러(Certihaler)™ (스카이파마(SkyePharma)), 트위스트할러(Twisthaler)® (쉐링 코포레이션(Schering Corp.)), 터부할러(Turbuhaler)® (아스트라제네카(AstraZeneca)), 울트라할러(Ultrahaler)® (아벤티스) 등을 포함한다.
안구 투여를 위한 투여 형태는 안과적 사용에 적합한 부형제와 함께 용액 또는 현탁액으로서 제제화될 수 있다.
비강 투여를 위한 투여 형태는 편리하게는 에어로졸, 용액, 점비제, 겔 또는 건조 분말로서 제제화될 수 있다.
흡입에 의한 투여에 적합화된 제약 조성물은 다양한 유형의 계량된, 용량 가압된 에어로졸, 네뷸라이저 또는 취입기를 사용하여 생성될 수 있는, 미립자 분진 또는 미스트를 포함한다.
비내 투여에 적합하고/거나 적합화된 제약 조성물의 경우, 화학식 I의 화합물, 또는 그의 제약상 허용되는 염 또는 용매화물은 유동액 분배기로부터의 전달을 위한 유동액 제제로서 제제화될 수 있다. 이러한 유동액 분배기는 예를 들어, 유동액 제제의 계량된 용량이 유동액 분배기의 펌프 메카니즘에 사용자-적용 힘을 적용할 때 분배되는 분배 노즐 또는 분배 오리피스를 가질 수 있다. 이러한 유동액 분배기는 일반적으로, 용량이 순차적 펌프 작용 시에 분배가능한 유동액 제제의 다중 계량된 용량의 저장소가 제공된다. 분배 노즐 또는 오리피스는 비강으로의 유동액 제제의 분사 분배를 위한, 사용자의 비공으로의 삽입을 위해 형성될 수 있다. 상기 언급된 유형의 유동액 분배기는 전문이 본원에 참조로 포함되는 WO-A-2005/044354에 기재 및 예시되어 있다. 분배기는, 유동액 제제를 수용하기 위한 용기 상에 탑재된 압축 펌프를 갖는 유동액 배출 장치를 수용하는 하우징을 갖는다. 하우징은, 하우징에 대해 안으로 움직일 수 있어 하우징에서 용기를 위로 움직이게 하여, 펌프를 압축되도록 하고, 하우징의 비강 노즐을 통하여 펌프 스템 밖으로 제제의 계량된 용량을 펌핑하는, 하나 이상의 손가락-작동가능한 측면 레버를 갖는다. 특히 바람직한 유동액 분배기는 WO-A-2005/044354의 도 30-40에 예시된 일반적 유형의 유동액 분배기이다.
다음은 본 발명의 화합물에 대한 대표적인 제약 투여 형태의 예이다:
본 발명의 화합물이 흡입, 정맥내, 경구 또는 비강내 경로에 의해 정상적으로 투여되는 다른 치료제와 조합으로 투여되는 경우, 생성된 제약 조성물이 동일한 경로에 의해 투여될 수 있음을 알 것이다.
특히 상기 언급된 성분 이외에, 조성물은 해당 제제의 유형과 관련된 분야에서 통상적인 다른 작용제를 포함할 수 있는 것으로 이해해야 하며, 예를 들어 경구 투여에 적합한 조성물은 향미제를 포함할 수 있다.
본 발명의 화합물의 치료 유효량은, 예를 들어 동물의 연령 및 체중, 치료가 필요한 정확한 상태 및 그의 중증도, 제제의 특성 및 투여 경로를 비롯한 다수의 요인에 따라 달라질 것이며, 궁극적으로 의사 또는 수의사가 판단할 것이다. 그러나, 부적절한 Syk 활성과 연관된 질환 또는 상태의 치료를 위한 화학식 I의 화합물의 유효량은 일반적으로 1일에 5 μg 내지 100 mg/수용자 (포유동물) 체중 1 kg의 범위, 보다 통상적으로는 1일에 5 μg 내지 10 mg/체중 1 kg의 범위일 것이다. 이 양은 1일 단일 용량, 또는 보다 통상적으로는 총 1일 용량이 동일하도록 하는 1일 수회 (예컨대, 2, 3, 4, 5 또는 6회)의 하위-용량으로 주어질 수 있다. 그의 염 또는 용매화물의 유효량은 화학식 I의 화합물 그 자체의 유효량의 비율로서 결정될 수 있다.
본 발명의 화합물, 및 그의 염 및 용매화물 및 그의 생리학상 기능적 유도체는 부적절한 Syk 활성과 연관된 질환 및 상태의 치료를 위해 단독으로 또는 다른 치료제와 조합하여 사용될 수 있다. 따라서, 본 발명에 따른 조합 요법은 화학식 I의 하나 이상의 화합물, 또는 그의 제약상 허용되는 염 또는 용매화물 또는 그의 생리학상 기능적 유도체의 투여 및 하나 이상의 다른 제약 활성제의 사용을 포함한다. 화학식 I의 화합물(들) 및 다른 제약 활성제(들)는 함께 또는 개별적으로 투여될 수 있고, 개별적으로 투여되는 경우에 이는 동시에 또는 임의의 순서로 순차적으로 투여될 수 있다. 화학식 I의 화합물(들) 및 다른 제약 활성제(들)의 양 및 상대적 투여 시점은 목적하는 조합 치료 효과가 달성되도록 선택될 것이다.
염증성 질환, 류마티스 관절염, 건선, 염증성 장 질환, COPD, 천식 및 알레르기성 비염의 치료를 위해 화학식 I의 화합물은 하기 하나 이상의 다른 활성제와 조합될 수 있다: (1) TNF-α 억제제, 예컨대 인플릭시맙 (레미케이드(Remicade)®), 에타네르셉트 (엔브렐(Enbrel)®), 아달리무맙 (휴미라(Humira)®), 세르톨리주맙 페골 (심지아(Cimzia)®) 및 골리무맙 (심포니(Simponi)®); (2) 비-선택적 COX-I/COX-2 억제제 (예컨대, 피록시캄, 디클로페낙, 프로피온산, 예컨대 나프록센, 플루비프로펜, 페노프로펜, 케토프로펜 및 이부프로펜, 페나메이트, 예컨대 메페남산, 인도메타신, 술린닥, 에토돌락, 아자프로파존, 피라졸론, 예컨대 페닐부타존, 살리실레이트, 예컨대 아스피린); (3) COX-2 억제제 (예컨대, 멜록시캄, 셀레콕시브, 로페콕시브, 발데콕시브 및 에토리콕시브); (4) 류마티스 관절염의 치료를 위한 기타 작용제, 예컨대 메토트렉세이트, 레플루노미드, 술파살라진, 아자티오프린, 시클로스포린, 타크롤리무스, 페니실라민, 부실라민, 아크타리트, 미조리빈, 로벤자리트, 시클레소니드, 히드록시클로로퀸, d-페니실라민, 아우로티오말레이트, 아우라노핀, 또는 비경구 또는 경구 금, 시클로포스파미드, 림포스타트-B, BAFF/APRIL 억제제 및 CTLA-4-Ig 또는 그의 모방체; (5) 류코트리엔 생합성 억제제, 5-리폭시게나제 (5-LO) 억제제 또는 5-리폭시게나제 활성화 단백질 (FLAP) 길항제, 예컨대 질류톤; (6) LTD4 수용체 길항제, 예컨대 자피르루카스트, 몬테루카스트 및 프란루카스트; (7) PDE4 억제제, 예컨대 로플루밀라스트, 실로밀라스트, AWD-12-281 (엘비온(Elbion)) 및 PD-168787 (화이자(Pfizer)); (8) 항히스타민성 H1 수용체 길항제, 예컨대 세티리진, 레보세티리진, 로라타딘, 데스로라타딘, 펙소페나딘, 아스테미졸, 아젤라스틴, 레보카바스틴, 올로파티딘, 메타피릴렌 및 클로르페니라민; (9) α1- 및 α2-아드레날린수용체 효능제 혈관수축제 교감신경흥분제, 예컨대 프로필헥세드린, 페닐에프린, 페닐프로판올아민, 슈도에페드린, 나파졸린 히드로클로라이드, 옥시메타졸린 히드로클로라이드, 테트라히드로졸린 히드로클로라이드, 크실로메타졸린 히드로클로라이드 및 에틸노르에피네프린 히드로클로라이드; (10) 항콜린제, 예컨대 이프라트로피움 브로마이드, 티오트로피움 브로마이드, 옥시트로피움 브로마이드, 아클린디늄 브로마이드, 글리코피롤레이트, (R,R)-글리코피롤레이트, 피렌제핀 및 텔렌제핀; (11) β-아드레날린수용체 효능제, 예컨대 메타프로테레놀, 이소프로테레놀, 이소프레날린, 알부테롤, 포르모테롤 (특히 푸마레이트 염), 살메테롤 (특히 크시나포에이트 염), 테르부탈린, 오르시프레날린, 비톨테롤 메실레이트, 페노테롤, 및 피르부테롤, 또는 메틸크산타닌, 예컨대 테오필린 및 아미노필린, 나트륨 크로모글리케이트; (12) 인슐린-유사 성장 인자 유형 I (IGF-I) 모방체; (13) 글루코코르티코스테로이드, 특히 감소된 전신 부작용을 갖는 흡입된 글루코코르티코이드, 예컨대 프레드니손, 프레드니솔론, 플루니솔리드, 트리암시놀론 아세토니드, 베클로메타손 디프로피오네이트, 부데소니드, 플루티카손 프로피오네이트, 시클레소니드 및 모메타손 푸로에이트; (14) 키나제 억제제, 예컨대 야누스 키나제 (JAK 1 및/또는 JAK2 및/또는 JAK 3 및/또는 TYK2), p38 MAPK 및 IKK2의 억제제; (15) B-세포 표적화 생물제제, 예컨대 리툭시맙 (리툭산(Rituxan)®); (16) 선택적 공동자극 조절제, 예컨대 아바타셉트 (오렌시아(Orencia)); (17) 인터류킨 억제제, 예컨대 IL-1 억제제 아나킨라 (키네레트(Kineret)) 및 IL-6 억제제 토실리주맙 (악템라(Actemra)).
본 발명은 또한 화학식 I의 화합물 또는 그의 제약상 허용되는 염을 베타2-아드레날린수용체 효능제 및 항염증 코르티코스테로이드와 함께 포함하는, 소위 "3중 조합" 요법을 제공한다. 바람직하게는 이 조합은 천식, COPD 또는 알레르기성 비염의 치료 및/또는 예방을 위한 것이다. 베타2-아드레날린수용체 효능제 및/또는 항염증 코르티코스테로이드는 상기 기재된 바와 같고/거나 WO 03/030939 A1에 기재된 바와 같을 수 있다. 이러한 "3중" 조합의 대표적 예는 애드베어(Advair)®의 성분 (살메테롤 크시나포에이트 및 플루티카손 프로피오네이트), 심비코르트(Symbicort)® (부데소니드 및 포르모테롤 푸마레이트) 또는 둘레라(Dulera)® (모메타손 푸로에이트 및 포르모테롤). 푸마레이트).살메테롤 또는 그의 제약상 허용되는 염 (예를 들어, 살메테롤 크시나포에이트) 및 플루티카손 프로피오네이트와 조합된 화학식 I의 화합물 또는 그의 제약상 허용되는 염이다.
암의 치료를 위해, 화학식 I의 화합물은 하나 이상의 항암제와 조합될 수 있다. 이러한 작용제의 예는 문헌 [Cancer Principles and Practice of Oncology by V.T. Devita and S. Hellman (editors), 6th edition (February 15, 2001), Lippincott Williams & Wilkins Publishers]에서 찾을 수 있다. 당업자는 작용제의 조합이 약물 및 관련된 암의 특정한 특성에 기초하여 유용할 것인지를 인지할 수 있을 것이다. 이러한 항암제는 하기를 포함하나, 이에 제한되는 것은 아니다: (1) 에스트로겐 수용체 조절제, 예컨대 디에틸스티베스트랄, 타목시펜, 랄록시펜, 이독시펜, LY353381, LY117081, 토레미펜, 플루옥시메스테로 및 SH646; (2) 다른 호르몬제, 예컨대 아로마타제 억제제 (예를 들어, 아미노글루테티미드, 테트라졸 아나스트로졸, 레트로졸 및 엑세메스탄), 황체화 호르몬 방출 호르몬 (LHRH) 유사체, 케토코나졸, 고세렐린 아세테이트, 류프롤리드, 메게스트롤 아세테이트 및 미페프리스톤; (3) 안드로겐 수용체 조절제, 예컨대 피나스테리드 및 다른 5α-리덕타제 억제제, 닐루타미드, 플루타미드, 비칼루타미드, 리아로졸 및 아비라테론 아세테이트; (4) 레티노이드 수용체 조절제, 예컨대 벡사로텐, 트레티노인, 13-시스-레티노산, 9-시스-레티노산, α-디플루오로메틸오르니틴, ILX23-7553, 트랜스-N-(4'-히드록시페닐) 레틴아미드 및 N-4-카르복시페닐 레틴아미드; (5) 항증식제, 예컨대 안티센스 RNA 및 DNA 올리고뉴클레오티드, 예컨대 G3139, ODN698, RVASKRAS, GEM231 및 INX3001, 및 항대사물, 예컨대 에노시타빈, 카르모푸르, 테가푸르, 펜토스타틴, 독시플루리딘, 트리메트렉세이트, 플루다라빈, 카페시타빈, 갈로시타빈, 시타라빈 옥포스페이트, 포스테아빈 나트륨 수화물, 랄티트렉세드, 팔티트렉시드, 에미테푸르, 티아조푸린, 데시타빈, 놀라트렉세드, 페메트렉세드, 넬자라빈, 2'-데옥시-2'-메틸리덴시티딘, 2'-플루오로메틸렌-2'-데옥시시티딘, N6-[4-데옥시-4-[N2-[2(E),4(E)-테트라데카디에노일]글리실아미노]-L-글리세로-B-L-만노-헵타피라노실]아데닌, 아플리딘, 엑테이나시딘, 트록사시타빈, 아미노프테린, 5-플루오로우라실, 플록수리딘, 메토트렉세이트, 류코바린, 히드록시우레아, 티오구아닌 (6-TG), 메르캅토퓨린 (6-MP), 시타라빈, 펜토스타틴, 플루다라빈 포스페이트, 클라드리빈 (2-CDA), 아스파라기나제, 겜시타빈, 알라노신, 스와인소닌, 로메트렉솔, 덱스라족산, 메티오니나제 및 3-아미노피리딘-2-카르복스알데히드 티오세미카르바존; (6) 파르네실-단백질 트랜스퍼라제 억제제, 예컨대 파르네실-단백질 트랜스퍼라제 (FPTase), 게라닐게라닐-단백질 트랜스퍼라제 유형 I (GGPTase-I) 및 게라닐게라닐-단백질 트랜스퍼라제 유형-II (GGPTase-II, Rab GGPTase로도 또한 명명됨); (7) HMG-CoA 리덕타제 억제제, 예컨대 로바스타틴, 심바스타틴, 프라바스타틴, 아토르바스타틴, 플루바스타틴 및 로수바스타틴; (8) 혈관신생 억제제, 예컨대 티로신 키나제 수용체 Flt-1 (VEGFR1) 및 Flk-1/KDR (VEGFR2)의 억제제, 표피-유래, 섬유모세포-유래 또는 혈소판 유래 성장 인자의 억제제, MMP (매트릭스 메탈로프로테아제) 억제제, 인테그린 차단제, 인터페론-α, 인터류킨-12, 에리트로포이에틴 (에포이에틴-α), 과립구-CSF (필그라스틴), 과립구, 대식세포-CSF (사르그라모스팀), 펜토산 폴리술페이트, 시클로옥시게나제 억제제, 스테로이드성 항염증제, 카르복시아미도트리아졸, 콤브레타스타틴 A-4, 스쿠알라민, 6-O-클로로아세틸-카르보닐)-푸마길롤, 탈리도미드, 안지오스타틴, 트로포닌-1, 안지오텐신 II 길항제, 헤파린, 카르복시펩티다제 U 억제제, 및 VEGF에 대한 항체, 엔도스타틴, 우크라인, 란피르나제, IM862, 아세틸디나날린, 5-아미노-1-[[3,5-디클로로-4-(4-클로로벤조일)페닐]메틸]-1H-1,2,3-트리아졸-4-카르복스마이드, CM101, 스쿠알라민, 콤브레타스타틴, RPI4610, NX31838, 황산화 만노펜타오스 포스페이트 및 3-[(2,4-디메틸피롤-5-일)메틸렌]-2-인돌린 (SU5416); (9) PPAR-γ 효능제, PPAR-δ 효능제, 티아졸리딘디온 (예컨대, DRF2725, CS-011, 트로글리타존, 로시글리타존 및 피오글리타존), 페노피브레이트, 겜피브로질, 클로피브레이트, GW2570, SB219994, AR-H039242, JTT-501, MCC-555, GW2331, GW409544, NN2344, KRP297, NP0110, DRF4158, NN622, GI262570, PNU182716, DRF552926, 2-[(5,7-디프로필-3-트리플루오로메틸-1,2-벤즈이속사졸-6-일)옥시]-2-메틸프로피온산 (USSN 09/782,856에 개시됨) 및 (2R)-7-(3-(2-클로로-4-(4-플루오로페녹시)페녹시)프로폭시)-2-에틸크로만-2-카르복실산 (USSN 60/235,708 및 60/244,697에 개시됨); (9) 고유 다중약물 내성의 억제제, 예컨대 p-당단백질 (P-gp)의 억제제, 예컨대 LY335979, XR9576, OC144-093, R101922, VX853 및 PSC833 (발스포다르); (10) 세포 증식 및 생존 신호전달의 억제제, 예컨대 EGFR의 억제제 (예를 들어, 게피티닙 및 에를로티닙), ERB-2의 억제제 (예를 들어, 트라스투주맙), IGF1R의 억제제, 예컨대 MK-0646 (달로투주맙), CD20의 억제제 (리툭시맙), 시토카인 수용체의 억제제, MET의 억제제, PI3K 패밀리 키나제의 억제제 (예를 들어, LY294002), 세린/트레오닌 키나제 (WO 03/086404, WO 03/086403, WO 03/086394, WO 03/086279, WO 02/083675, WO 02/083139, WO 02/083140 및 WO 02/083138에 기재된 바와 같은 Akt의 억제제를 포함하나 이에 제한되지는 않음), Raf 키나제의 억제제 (예를 들어, BAY-43-9006), MEK의 억제제 (예를 들어, CI-1040 및 PD-098059) 및 mTOR의 억제제 (예를 들어, 와이어쓰(Wyeth) CCI-779 및 아리아드(Ariad) AP23573); (11) 비스포스포네이트, 예컨대 에티드로네이트, 파미드로네이트, 알렌드로네이트, 리세드로네이트, 졸레드로네이트, 이반드로네이트, 인카드로네이트 또는 시마드로네이트, 클로드로네이트, EB-1053, 미노드로네이트, 네리드로네이트, 피리드로네이트 및 틸루드로네이트; (12) γ-세크레타제 억제제; (13) 수용체 티로신 키나제 (RTK)를 방해하는 작용제, 예컨대 c-Kit, Eph, PDGF, Flt3 및 c-Met의 억제제; (14) 세포 주기 체크포인트를 방해하는 작용제, 예컨대 ATR, ATM, Chk1 및 Chk2 키나제의 억제제, 및 cdk 및 cdc 키나제 억제제 (7-히드록시스타우로스포린, 플라보피리돌, CYC202 (시클라셀(Cyclacel)) 및 BMS-387032에 의해 구체적으로 예시됨); (15) BTK 억제제, 예컨대 PCI32765, AVL-292 및 AVL-101; (16) PARP 억제제, 예컨대 이니파립, 올라파립, AGO14699, ABT888 및 MK4827; (16) ERK 억제제; (17) mTOR 억제제, 예컨대 시롤리무스, 리다포롤리무스, 템시롤리무스, 에베롤리무스; (18) 세포독성제/세포증식억제제.
"세포독성제/세포증식억제제"는 세포 사멸을 유발하거나, 세포의 기능을 직접 방해하여 우선적으로 세포 증식을 억제하거나, 세포 유사분열을 억제 또는 방해하는 화합물, 예컨대 알킬화제, 종양 괴사 인자, 삽입제, 저산소증 활성화 화합물, 미세관 억제제/미세관-안정화제, 유사분열 키네신의 억제제, 히스톤 데아세틸라제의 억제제, 유사분열 진행에 관련된 키나제의 억제제, 항대사물; 생물학적 반응 개질제; 호르몬/항-호르몬 치료제, 조혈 성장 인자, 모노클로날 항체 표적화 치료제, 토포이소머라제 억제제, 프로테아솜 억제제 및 유비퀴틴 리가제 억제제를 지칭한다.
세포독성제의 예는 세르테네프, 카켁틴, 클로람부실, 시클로포스파미드, 이포스파미드, 메클로레타민, 멜팔란, 우라실 머스타드, 티오테파, 부술판, 카르무스틴, 로무스틴, 스트렙토조신, 타소네르민, 로니다민, 카르보플라틴, 알트레타민, 다카르바진, 프로카르바진, 프레드니무스틴, 디브로모둘시톨, 라니무스틴, 포테무스틴, 네다플라틴, 옥살리플라틴, 테모졸로미드, 헵타플라틴, 에스트라무스틴, 임프로술판 토실레이트, 트로포스파미드, 니무스틴, 디브로스피듐 클로라이드, 푸미테파, 로바플라틴, 사트라플라틴, 프로피로마이신, 시스플라틴, 이로풀벤, 덱스이포스파미드, 시스-아민디클로로(2-메틸-피리딘)백금, 벤질구아닌, 글루포스파미드, GPX100, (트랜스, 트랜스, 트랜스)-비스-뮤-(헥산-1,6-디아민)-뮤-[디아민-백금(II)]비스[디아민(클로로)백금 (II)]테트라클로라이드, 디아리지디닐스페르민, 삼산화비소, 1-(11-도데실아미노-10-히드록시운데실)-3,7-디메틸크산틴, 조루비신, 독소루비신, 다우노루비신, 이다루비신, 안트라센디온, 블레오마이신, 미토마이신 C, 닥티노마이신, 플리카토마이신, 비산트렌, 미톡산트론, 피라루비신, 피나피드, 발루비신, 암루비신, 안티네오플라스톤, 3'-데아미노-3'-모르폴리노-13-데옥소-10-히드록시카르미노마이신, 안나마이신, 갈라루비신, 엘리나피드, MEN10755 및 4-데메톡시-3-데아미노-3-아지리디닐-4-메틸술포닐-다우노루비신을 포함하나, 이에 제한되는 것은 아니다.
저산소증 활성화가능 화합물의 한 예는 티라파자민이다.
프로테아솜 억제제의 예는 락타시스틴 및 보르테조밉을 포함하나, 이에 제한되는 것은 아니다.
미세관 억제제/미세관-안정화제의 예는 빈크리스틴, 빈블라스틴, 빈데신, 빈졸리딘, 비노렐빈, 빈데신 술페이트, 3',4'-디데히드로-4'-데옥시-8'-노르빈카류코블라스틴, 포도필로톡신 (예를 들어, 에토포시드 (VP-16) 및 테니포시드 (VM-26)), 파클리탁셀, 도세탁솔, 리족신, 돌라스타틴, 미보불린 이세티오네이트, 아우리스타틴, 세마도틴, RPR109881, BMS184476, 빈플루닌, 크립토피신, 안히드로빈블라스틴, N,N-디메틸-L-발릴-L-발릴-N-메틸-L-발릴-L-프롤릴-L-프롤린-t-부틸아미드, TDX258, 에포틸론 (예를 들어, 미국 특허 번호 6,284,781 및 6,288,237 참조) 및 BMS188797을 포함한다.
토포이소머라제 억제제의 몇몇 예는 토포테칸, 하이캅타민, 이리노테칸, 루비테칸, 6-에톡시프로피오닐-3',4'-O-엑소-벤질리덴-카르트레우신, 루르토테칸, 7-[2-(N-이소프로필아미노)에틸]-(20S)캄프토테신, BNP1350, BNPI1100, BN80915, BN80942, 에토포시드 포스페이트, 테니포시드, 소부족산, 2'-디메틸아미노-2'-데옥시-에토포시드, GL331, N-[2-(디메틸아미노)에틸]-9-히드록시-5,6-디메틸-6H-피리도[4,3-b]카르바졸-1-카르복스아미드, 아술라크린, 2,3-(메틸렌디옥시)-5-메틸-7-히드록시-8-메톡시벤조[c]-페난트리디늄, 5-(3-아미노프로필아미노)-7,10-디히드록시-2-(2-히드록시에틸아미노메틸)-6H-피라졸로[4,5,1-데]아크리딘-6-온, N-[1-[2-(디에틸아미노)에틸아미노]-7-메톡시-9-옥소-9H-티오크산텐-4-일메틸]포름아미드, N-(2-(디메틸아미노)에틸)아크리딘-4-카르복스아미드, 6-[[2-(디메틸아미노)에틸]아미노]-3-히드록시-7H-인데노[2,1-c]퀴놀린-7-온 및 디메스나이다.
유사분열 키네신의 억제제의 예는 KSP의 억제제, MKLP1의 억제제, CENP-E의 억제제, MCAK의 억제제, Kif14의 억제제, Mphosph1의 억제제 및 Rab6-KIFL의 억제제를 포함하나, 이에 제한되는 것은 아니다.
"히스톤 데아세틸라제 억제제"의 예는 보리노스타트, 트리코스타틴 A, 옥삼플라틴, PXD101, MG98, 발프로산 및 스크립타이드를 포함하나, 이에 제한되는 것은 아니다.
"유사분열 진행과 관련된 키나제의 억제제"는 오로라 키나제의 억제제, Polo-유사 키나제 (PLK)의 억제제 (특히, PLK-1의 억제제), bub-1의 억제제 및 bub-R1의 억제제를 포함하나, 이에 제한되는 것은 아니다. "오로라 키나제 억제제"의 한 예는 VX-680이다.
"항증식제"는 안티센스 RNA 및 DNA 올리고뉴클레오티드, 예컨대 G3139, ODN698, RVASKRAS, GEM231 및 INX3001, 및 항대사물, 예컨대 에노시타빈, 카르모푸르, 테가푸르, 펜토스타틴, 독시플루리딘, 트리메트렉세이트, 플루다라빈, 카페시타빈, 갈로시타빈, 시타라빈 옥포스페이트, 포스테아빈 나트륨 수화물, 랄티트렉세드, 팔티트렉시드, 에미테푸르, 티아조푸린, 데시타빈, 놀라트렉세드, 페메트렉세드, 넬자라빈, 2'-데옥시-2'-메틸리덴시티딘, 2'-플루오로메틸렌-2'-데옥시시티딘, N6-[4-데옥시-4-[N2-[2,4-테트라데카디에노일]글리실아미노]-L-글리세로-B-L-만노-헵타피라노실]아데닌, 아플리딘, 엑테이나시딘, 트록사시타빈, 아미노프테린, 5-플루오로우라실, 플록수리딘, 메토트렉세이트, 류코바린, 히드록시우레아, 티오구아닌 (6-TG), 메르캅토퓨린 (6-MP), 시타라빈, 펜토스타틴, 플루다라빈 포스페이트, 클라드리빈 (2-CDA), 아스파라기나제, 겜시타빈, 알라노신, 스와인소닌, 로메트렉솔, 덱스라족산, 메티오니나제 및 3-아미노피리딘-2-카르복스알데히드 티오세미카르바존을 포함한다.
화학식 I의 화합물과 조합될 수 있는, 암 요법에 사용되는 적합한 작용제의 비제한적 예는 아바렐릭스; 알데스류킨; 알렘투주맙; 알리트레티노인; 알로퓨리놀; 알트레타민; 아미포스틴; 아나스트로졸; 삼산화비소; 아스파라기나제; 아자시티딘; 벤다무스틴; 베바시주맙; 벡사로텐; 블레오마이신; 보르테조밉; 부술판; 칼루스테론; 카페시타빈; 카르보플라틴; 카르무스틴; 세툭시맙; 클로람부실; 시스플라틴; 클라드리빈; 클로파라빈; 시클로포스파미드; 시타라빈; 다카르바진; 닥티노마이신, 악티노마이신 D; 달테파린; 다르베포에틴 알파; 다사티닙; 다우노루비신; 데가렐릭스; 데니류킨 디프티톡스; 덱스라족산; 도세탁셀; 독소루비신; 드로모스타놀론 프로피오네이트; 에쿨리주맙; 엘리엇(Elliott) B 용액; 엘트롬보파그; 에피루비신; 에포에틴 알파; 에를로티닙; 에스트라무스틴; 에토포시드 포스페이트; 에토포시드; 에베롤리무스; 엑세메스탄; 필그라스팀; 플록수리딘; 플루다라빈; 플루오로우라실; 풀베스트란트; 게피티닙; 겜시타빈; 겜투주맙 오조가미신; 고세렐린 아세테이트; 히스트렐린 아세테이트; 히드록시우레아; 이브리투모맙 티욱세탄; 이다루비신; 이포스파미드; 이마티닙 메실레이트; 인터페론 알파 2a; 인터페론 알파-2b; 이리노테칸; 익사베필론; 라파티닙; 레날리도미드; 레트로졸; 류코보린; 류프롤리드 아세테이트; 레바미솔; 로무스틴; 메클로레타민, 질소 머스타드; 메게스트롤 아세테이트; 멜팔란, L-PAM; 메르캅토퓨린; 메스나; 메토트렉세이트; 메톡살렌; 미토마이신 C; 미토탄; 미톡산트론; 난드롤론 펜프로피오네이트; 넬라라빈; 닐로티닙; 노페투모맙; 오파투무맙; 오프렐베킨; 옥살리플라틴; 파클리탁셀; 팔리페르민; 파미드로네이트; 파니투무맙; 파조파닙; 페가데마제; 페가스파르가제; 페그필그라스팀; 페메트렉세드 이나트륨; 펜토스타틴; 피포브로만; 플레릭사포르; 플리카마이신, 미트라마이신; 포르피머 나트륨; 프랄라트렉세이트; 프로카르바진; 퀴나크린; 라스부리카제; 랄록시펜 히드로클로라이드; 리툭시맙; 로미뎁신; 로미프롤스팀; 사르그라모스팀; 사르그라모스팀; 사트라플라틴; 소라페닙; 스트렙토조신; 수니티닙 말레에이트; 타목시펜; 테모졸로미드; 템시롤리무스; 테니포시드; 테스토락톤; 티오구아닌; 티오테파; 토포테칸; 토레미펜; 토시투모맙; 트라스투주맙; 트레티노인; 우라실 머스타드; 발루비신; 빈블라스틴; 빈크리스틴; 비노렐빈; 보리노스타트; 및 졸레드로네이트를 포함하나, 이에 제한되는 것은 아니다.
적절한 경우에 다른 치료 성분(들)이 염의 형태로, 예를 들어 알칼리 금속 또는 아민 염으로서, 또는 산 부가염 또는 전구약물로서, 또는 에스테르, 예를 들어 저급 알킬 에스테르로서, 또는 용매화물, 예를 들어 수화물로서 사용되어, 치료 성분의 활성 및/또는 안정성 및/또는 물리적 특성, 예컨대 용해도를 최적화할 수 있음이 당업자에게 명백할 것이다. 또한 적절한 경우에 치료 성분이 광학적으로 순수한 형태로 사용될 수 있음이 명백할 것이다.
상기 지칭된 조합물은 편리하게는 제약 조성물의 형태로 사용하기 위해 제공될 수 있으며, 따라서 상기 정의된 바와 같은 조합물을 제약상 허용되는 희석제 또는 담체와 함께 포함하는 제약 조성물이 본 발명의 추가 측면을 나타낸다. 이러한 조합물은 호흡기 질환에서 특히 흥미로우며, 편리하게는 흡입 또는 비강내 전달에 적합화된다.
이러한 조합물의 개별 화합물은 별도의 또는 조합된 제약 조성물로 순차적으로 또는 동시에 투여될 수 있다. 바람직하게는, 개별 화합물은 조합된 제약 조성물로 동시에 투여될 것이다. 공지된 치료제의 적절한 용량은 당업자에 의해 용이하게 인지될 것이다.
Syk 억제는 하기 검정 프로토콜을 사용하여 결정될 수 있다:
생물학적 검정
재조합 인간 Syk 효소에 대한 균질 시간-분해 형광 (HTRF) 검정: 재조합 GST-hSyk 융합 단백질을 인간 Syk 활성을 억제하는 화합물의 효능을 측정하는데 사용하였다. 재조합 인간 GST-Syk (카르나 바이오사이언시스(Carna Biosciences) #08-176) (5pM 최종 농도)를 DMSO (0.1% 최종 농도) 중에 희석된 다양한 농도의 억제제와 함께 384 웰 플레이트 포맷 중 15 mM 트리스(Tris)-HCl (pH 7.5), 0.01% 트윈 20, 2 mM DTT에서 10분 동안 실온에서 인큐베이션하였다. 반응을 개시하기 위해, Syk에 대한 인산화 부위를 함유하는 비오티닐화 기질 펩티드 (250 nM 최종 농도)를 마그네슘 (5 mM 최종 농도) 및 ATP (25 μM 최종 농도)와 함께 첨가하였다. 반응물의 최종 부피는 10 μL였다. 펩티드의 인산화를 실온에서 45' 동안 진행되도록 하였다. 반응을 켄칭하고 인산화 생성물을 검출하기 위해, 2 nM 유로퓸-항-포스포티로신 항체 (퍼킨 엘머(Perkin Elmer) #AD0161) 및 70 nM SA-APC (퍼킨-엘머 #CR130-100)를 15 mM 트리스 pH 7.5, 40 mM EDTA, 0.01% 트윈 20에 함께 첨가하였다. 켄칭 용액의 최종 부피는 10 μL였다. 생성된 HTRF 신호를 시간-분해 형광 프로토콜을 사용하는 엔비전(EnVision) (퍼킨-엘머) 판독기 상에서 30분 후에 측정하였다. 10-용량 적정 (10 μM 내지 0.508 nM) 및 머크 검정 데이터 애널라이저(Merck Assay Data Analyzer)를 이용하는 4 파라미터 로지스틱 곡선 피팅에 따라 IC50을 결정하였다. rhSyk 활성 (IC50)을 +++ (100 nM 이하), ++ (100 내지 1000 nM), + (1 내지 10 μM)로 나타내었다. IC50 값은 또한 하기 대표적 화합물에 대하여 제공된다:
본 발명의 화합물은 표준 화학을 비롯한 다양한 방법에 의해 제조될 수 있다. 예시적인 일반적 합성 방법이 하기에 제시되고, 이어서 본 발명의 구체적 화합물이 실시예에서 제조된다. 임의의 상기 정의된 가변기는 달리 나타내지 않는 한 이전에 정의된 의미를 계속 가질 것이다.
화학식 I의 화합물은 하기 합성 반응식에 의해 부분적으로 제시된 바와 같은, 유기 합성 업계에 공지된 방법에 의해 제조될 수 있다. 하기 기재된 모든 반응식에서, 일반적인 화학 원리에 따라 필요한 경우에 민감성 또는 반응성 기에 대한 보호기가 사용되는 것으로 널리 이해된다. 보호기는 유기 합성의 표준 방법에 따라 조작된다 (문헌 [T. W. Green and P. G. M. Wuts (1991) Protecting Groups in Organic Synthesis, John Wiley & Sons]). 이들 기는 당업자에게 용이하게 명백한 방법을 이용하여 화합물 합성 중 편리한 단계에서 제거된다. 보호기 뿐만 아니라 반응 조건 및 반응 단계의 순서의 선택은 화학식 I의 화합물의 제조와 일관되는 것이어야 한다. 당업자는 입체중심이 화학식 I의 화합물에 존재하는지 인지할 것이다. 따라서, 본 발명은 모든 가능한 입체이성질체를 포함하고, 입체이성질체의 혼합물 (예컨대, 라세미 화합물) 뿐만 아니라 개별 입체이성질체를 포함한다. 화합물이 단일 거울상이성질체로서 요구되는 경우에, 이는 입체특이적 또는 입체선택적 합성에 의해, 또는 최종 생성물 또는 임의의 편리한 중간체의 분할에 의해 수득될 수 있다. 최종 생성물, 중간체 또는 출발 물질의 분할은 당업계에 공지된 임의의 적합한 방법에 의해 수행될 수 있다. 예를 들어, 문헌 [Stereochemistry of Organic Compounds by E. L. Eliel, S. H. Wilen, and L. N. Mander (Wiley-Interscience, 1994)]를 참조한다.
하기 약어가 반응식 및 실시예에 사용된다: Ac=아세틸; AcOH=아세트산; Bn=벤질; Boc (t-Boc)=t-부틸옥시카르보닐; BOP=(벤조트리아졸-1-일옥시)트리스(디메틸아미노)포스포늄 헥사플루오로포스페이트; DAST=(디에틸아미노)황 트리플루오라이드; dba=디벤질리덴아세톤; DCE=1,2-디클로로에탄; DCM=디클로로메탄; Dibal/Dibal-H=디이소부틸알루미늄 히드라이드; DIPEA/DIEA=디이소프로필에틸아민; DMAP=N,N-디메틸아미노피리딘; DME=1,2-디메톡시에탄; DMF=디메틸 포름아미드; DMSO=디메틸술폭시드; Dppf=1,1'-비스(디페닐포스피노)페로센; EDC=N-(3-디메틸아미노프로필)-N'-에틸카르보디이미드; EtOAc=에틸 아세테이트; HATU=N,N,N',N'-테트라메틸-O-(7-아자벤조트리아졸-1-일)우로늄 헥사플루오로포스페이트; HMDS=헥사메틸디실라잔; HOBT=1-히드록시벤조트리아졸; HPLC=고압력 액체 크로마토그래피; IPA=이소프로필 알콜; LDA=리튬 디이소프로필아미드; mCPBA=메타-클로로퍼옥시벤조산; Ms=메탄술포닐 (메실); MTBE=메틸 t-부틸 에테르; NBS=N-브로모숙신이미드; Ph=페닐; SFC=초임계 유체 크로마토그래피; TBAF=t-부틸암모늄 플루오라이드; TBDMS/TBS=t-부틸 디메틸실릴; TFA=트리플루오로아세트산/트리플루오로아세테이트; THF=테트라히드로푸란; TLC=박층 크로마토그래피; TMS=트리메틸실릴; Ts=톨루엔술포닐 (톨릴); TSA=p-톨루엔술폰산. 알킬/시클로알킬 기에 대한 약어: Me = 메틸, Et = 에틸, nPr = n-프로필, iPr = 이소프로필, nBu = n-부틸, t-Bu = 3급 부틸, cPr = 시클로프로필, cBu = 시클로부틸, cPen = 시클로펜틸, cHex = 시클로헥실, cHept = 시클로헵틸.
<반응식 1>
화학식 I의 화합물은 보론산 에스테르 (1)의 티아졸 브로마이드 (2)와의 스즈키 커플링에 의해 제조될 수 있다. 보론산 에스테르 (1)은 2-클로로피리미딘 (3) 및 3-브로모아닐린 (5)를 반응시켜 상응하는 N-(3-브로모페닐)-피리미딘-2-아민 (6)을 형성하고, 이어서 비스(피나콜레이토)디보론과의 미야우라 커플링에 의해 수득될 수 있다. 화학식 I의 화합물은 또한 Pd 촉매의 존재 하에 2-클로로피리미딘 (3) 및 티아졸-치환된 아닐린 (4)를 반응시킴으로써 또는 대안적으로 SNAr 반응에 의해 수득될 수 있다. 그 다음, 티아졸-치환된 아닐린 (4)는 스즈키 커플링 조건 하에 브로모티아졸 및 니트로페닐 보론산 에스테르를 사용하고, 이어서 니트로방향족 화합물을 아닐린으로 환원시키는 것으로 공지된 표준 조건, 예컨대 Pd-촉매화된 수소화를 이용하는 니트로 기의 아미노 기로의 환원에 의해 형성될 수 있다. 화학식 I의 화합물은 또한 브로모-치환된 아닐린 (6)과 치환된 티아졸 (7) 사이의 헤크 반응에 의해 형성될 수 있다. 브로모-치환된 아닐린 (6)은 2-클로로피리미딘 (3)과 치환된 브로모-아닐린 (5) 사이의 SNAr 반응에 의해 제조될 수 있다.
<반응식 2>
화학식 7a의 화합물은 LDA로 탈양성자화될 수 있고, 카르보닐 함유 화합물의 첨가로 알콜 (8)이 수득된다. 알콜 (8)은 플루오린화제, 예컨대 DAST를 사용하여 플루오라이드 (9)로 전환될 수 있다. 대안적으로, NBS를 사용한 (8)의 브로민화로 (10)이 수득된다.
<반응식 3>
카르복실산, 예컨대 (11)은 아민 및 표준 아미드 커플링 시약을 사용하여 아미드 (12)로 전환될 수 있다.
<반응식 4>
2,4-디클로로피리미딘 (13)으로 출발하는 2-클로로피리미딘 빌딩 블록의 제조를 반응식 4에 예시한다. 스즈키 커플링을 통한 피리미딘 관능화로, 치환된 2-클로로피리미딘 (15)가 수득되는 한편, 치환된 알콜 친핵체와의 염기 매개 SNAr 반응으로 에테르 (14)가 제공된다.
다양한 티아졸 빌딩 블록의 제조는 하기 반응식 5, 6 및 7에 예시된다.
<반응식 5>
반응식 5에 도시된 바와 같이, 티아졸의 탈양성자화에 이어서 알데히드 (16)의 첨가로 알콜 (17)이 수득된다. 알콜 (17)의 산화에 이어서 NBS를 사용한 브로민화로 (18)이 수득된다. 케톤 (18)로의 친핵체 첨가는 치환된 알콜 (19)를 제공한다. 대안적으로, 케톤 (18)의 환원적 아미노화로 아민 (20)이 수득된다.
<반응식 6>
반응식 6에 도시된 바와 같이, 케톤 (18)은 비티히 반응에 이어서 디히드록실화에 의해 디올 (21)로 전환될 수 있다. 대안적으로, (18)은 비티히 반응을 통해 1,1'-이치환된 올레핀 (22)로 전환될 수 있다. 올레핀 (22)의 디히드록실화로 디올 (23)이 수득되는 한편, (22)의 산화는 에폭시드 (24)를 제공한다. 에폭시드 (24)의 TFA 및 트리에틸실란으로의 개환으로 1급 알콜 (25)가 수득되는 한편, TBAF로의 개환으로 (26)이 수득된다.
<반응식 7>
반응식 7 에 도시된 바와 같이, 1급 브로마이드 (27)의 트리에틸포스파이트와의 반응으로 (28)이 수득된다. 수소화나트륨을 사용한 28의 탈양성자화에 이어서 케톤 첨가로, 치환된 올레핀 (29)가 수득된다. 올레핀 (29)의 디히드록실화로 디올 (30)이 생성된다.
<반응식 8>
치환된 시클로헥실 유도체의 제조는 반응식 8에 예시된다. (31)의 α-알킬화로 (32)가 수득된다. 카르복실산 (32)는 티오닐 클로라이드를 사용하여 아실 클로라이드로 전환될 수 있다. Pd(OAc)2 및 디메틸아연과의 즉각적 반응으로 케톤 (33)이 수득되며, 이는 반응식 2에 나타난 바와 같이 사용될 수 있다.
화학식 I의 화합물은 적절한 물질을 사용하여 본원의 반응식 및 실시예에 기재된 절차에 따라 제조될 수 있으며, 이들은 하기 구체적 실시예에 의해 추가로 예시된다. 그러나, 예시된 화합물은 본 발명에 대한 예시일 뿐, 어떤 방식으로든 본 발명의 범주를 제한하는 것으로 해석되어서는 안된다. 실시예는 본 발명의 화합물의 제조를 위한 상세사항을 추가로 예시한다. 당업자는 하기 제조 절차의 보호기, 시약, 뿐만 아니라 조건 및 방법에 대한 공지된 변형을 이용하여 이들 화합물을 제조할 수 있다는 것을 용이하게 이해할 것이다. 화학 시약이 상업적으로 입수가능하지 않은 경우, 이러한 화학 시약은 문헌에서 기재된 공지된 방법에 따라 또는 이를 적용함으로써 당업자에 의해 용이하게 제조될 수 있다는 것이 또한 이해된다. 모든 온도는 달리 나타내지 않는 한 섭씨 온도이다. 질량 스펙트럼 (MS)은 전기분무 이온-질량 분광분석법 (ESI) 또는 대기압 화학적 이온화 질량 분광분석법 (APCI)에 의해 측정하였다.
중간체 1: 3-메틸-5-(1,3-티아졸-5-일)아닐린
단계 1: 1 L 3구 둥근 바닥 플라스크 중 디옥산 (720 mL)을 30분 동안 탈기하였다. 3-브로모-5-메틸아닐린 (60 g, 193 mmol), (비스피나콜레이토)디보론 (96 g, 377 mmol), 아세트산칼륨 (42.7 g, 435 mmol), X-Phos (8.3 g, 17.41 mmol) 및 Pd2dba3 (3.99 g, 4.35 mmol)을 탈기된 용매에 N2(g) 하에 첨가하였다. 실온에서 10분 동안 교반한 후, 반응 혼합물을 80℃의 내부 온도로 가열하였다. 약 4시간 후, 가열 맨틀을 제거하고, 빙수조로 대체하였다. 반응 혼합물을 30℃로 냉각시킨 다음, 셀라이트(CELITE)의 패드를 통해 (MTBE 500 mL로 세척하면서) 여과하였다. 이것을 500 mL pH 8 인산염 완충액, 500 mL 염수 및 추가의 MTBE 500 mL가 들은 4 L 분리 깔때기로 옮겼다. 층을 분리하고, 유기 층을 염수 및 물의 1:1 v:v 혼합물 1 L로 세척하였다. 수성 층을 합하고, 순차적으로 MTBE의 제2의 500 mL 부분으로 역추출하였다. 합한 유기부를 MgSO4 100 g으로 처리하고, 생성된 혼합물을 20분 동안 교반하였다. 이어서, 생성된 현탁액을 여과하고, 진공 하에 농축시켰다. 생성된 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0-25% 에틸 아세테이트)에 의해 정제하여 3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)아닐린을 담오렌지색 고체로서 수득하였다.
단계 2: 3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)아닐린 (20.98 g, 90 mmol), 5-브로모티아졸 (8.85 mL, 99 mmol) 및 탄산나트륨 (90 mL, 180 mmol)을 플라스크에서 합하였다. 2-메틸-THF (326 mL)를 첨가하고, 혼합물을 N2로 1.5시간 동안 탈기한 후, 1,1'-비스(디페닐포스피노)페로센-팔라듐(II)디클로라이드 디클로로메탄 착체 (3.67 g, 4.50 mmol)를 첨가하였다. 반응물을 100℃로 밤새 가열한 다음, 실온으로 냉각시켰다. 반응 혼합물을 에틸 아세테이트로 세척하면서 셀라이트의 패드를 통해 여과하였다. 층을 분리하고, 수성 층을 에틸 아세테이트로 역추출하고, Na2SO4 상에서 건조시키고, 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0-40% 에틸 아세테이트)에 의해 정제하였다. 3-메틸-5-(1,3-티아졸-5-일)아닐린을 황색빛 갈색 고체로서 단리하였다.
중간체 2: 4-시클로프로필-5-플루오로-N-[3-메틸-5-(1,3-티아졸-5-일)페닐]피리미딘-2-아민
단계 1: 5-플루오로-2,4-디클로로피리미딘 (5 g, 29.9 mmol), 시클로프로필 보론산 (2.57 g, 29.9 mmol), 제3 인산칼륨 (15.89 g, 74.9 mmol) 및 PdCl2(dppf)-디클로로메탄 부가물 (1.22 g, 1.50 mmol)을 건조 플라스크에 첨가하였다. 플라스크를 아르곤으로 탈기한 다음, 테트라히드로푸란 (150 ml)을 첨가하였다. 반응 혼합물을 아르곤으로 5분 동안 탈기한 다음, 67℃로 가열하였다. 12시간 후, 반응 혼합물을 실온으로 냉각시킨 후, 에틸 아세테이트 (1000 mL)로 희석하고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켰다. 잔류물을 실리카 겔 상에서 플래쉬 크로마토그래피 (EtOAc/헥산 구배)에 의해 정제하여 2-클로로-4-시클로프로필-5-플루오로피리미딘을 수득하였다.
단계 2: 3-메틸-5-(1,3-티아졸-5-일)아닐린 (0.250 g, 1.31 mmol), 단계 1의 생성물 (0.227 g, 1.31 mmol), 아세트산팔라듐(II) (0.0295 g, 0.131 mmol), 크산트포스 (0.114 g, 0.197 mmol) 및 탄산세슘 (0.856 g, 2.63 mmol)을 건조 플라스크에 첨가하였다. 플라스크를 아르곤으로 탈기한 다음, 디옥산 (4.4 ml)을 첨가하였다. 반응 혼합물을 아르곤으로 5분 동안 탈기한 다음, 100℃로 가열하였다. 2시간 후, 반응 혼합물을 실온으로 냉각시킨 후, 에틸 아세테이트로 희석하고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켰다. 잔류물을 실리카 겔 상에서 플래쉬 크로마토그래피 (EtOAc/디클로로메탄 구배)에 의해 정제하여 4-시클로프로필-5-플루오로-N-[3-메틸-5-(1,3-티아졸-5-일)페닐]피리미딘-2-아민을 수득하였다.
중간체 3: 메틸 (1S,3R)-3-아세틸-2,2-디메틸시클로부탄카르복실레이트
단계 1: (-)-버베논 (615 mg, 4.09 mmol)을 아세토니트릴 (2.0 mL), CCl4 (2.0 mL) 및 물 (3.0 mL)의 혼합물 중에 용해시켰다. 과아이오딘산나트륨 (3.59 g, 16.79 mmol) 및 염화루테늄(III) 수화물 (18.68 mg, 0.090 mmol)을 첨가하고, 생성된 2상 혼합물을 실온에서 24시간 동안 격렬히 교반하였다. 이어서, 반응 혼합물을 DCM으로 희석하고, H2O로 세척하고, DCM (3x)으로 추출하였다. 합한 유기 층을 건조 (Na2SO4)시키고, 여과하고, 감압 하에 농축시켜 (1R,3S)-3-아세틸-2,2-디메틸시클로부탄카르복실산을 연황색 오일로서 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 2: 아세틸 클로라이드 (1.02 ml, 14.32 mmol)를 MeOH (10 mL)에 0℃에서 적가하고, 생성된 혼합물을 0℃에서 30분 동안 교반하였다. 단계 1로부터의 (1R,3S)-3-아세틸-2,2-디메틸시클로부탄카르복실산 (696 mg, 4.09 mmol)을 MeOH (2 mL) 중 용액으로서 첨가하고, 반응 혼합물을 실온까지 가온하면서 밤새 교반하였다. 이어서, 휘발성 물질을 감압 하에 제거하고, 잔류물을 실리카 겔 상에서 플래쉬 크로마토그래피 (구배 용리, 헥산 중 2% → 20% EtOAc)에 의해 정제하여 메틸 (1R,3S)-3-아세틸-2,2-디메틸시클로부탄카르복실레이트를 무색 오일로서 수득하였다.
중간체 4: 메틸 2-(2-아세틸시클로프로필)-2-메틸프로파노에이트
단계 1: 0℃에서 테트라히드로푸란 (200 mL) 중 디메틸 (2-옥소프로필)포스포네이트 (4.09 mL, 30.0 mmol)의 용액에 칼륨 tert-부톡시드 (3.22 g, 28.7 mmol)를 첨가하였다. 15분 후, 반응 혼합물을 실온으로 이동시키고, 추가로 15분 후 메틸 2,2-디메틸-3-옥소프로파노에이트 (3.39 g, 26.0 mmol)를 첨가하였다. 불투명한 반응 혼합물을 21시간 동안 교반한 다음, 디에틸 에테르 (100 ml)와 물 (100 mL) 사이에 분배하였다. 층을 분리하고, 수성 층을 디에틸 에테르 (100 mL, 50 mL)로 추출하였다. 합한 유기 층을 수성 포화 중탄산나트륨 용액 및 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (0-4% 메탄올/디클로로메탄)에 의해 정제하여 메틸 (3E)-2,2-디메틸-5-옥소헥스-3-에노에이트를 수득하였다.
단계 2: 디메틸술폭시드 (6 mL) 중 트리메틸술폭슘 아이오다이드 (506 mg, 2.297 mmol) 및 칼륨 tert-부톡시드 (258 mg, 2.297 mmol)의 용액을 1.5시간 동안 교반한 다음, 테트라히드로푸란 (6 mL) 중 메틸 (3E)-2,2-디메틸-5-옥소헥스-3-에노에이트 (340 mg, 1.998 mmol)의 용액에 시린지를 통해 옮겼다. 반응 혼합물을 14시간 동안 교반한 다음, 디에틸 에테르 (25 mL)와 물:포화 수성 중탄산나트륨 용액의 5:1 v:v 혼합물 (12 mL) 사이에 분배하였다. 층을 분리하고, 수성 층을 디에틸 에테르 (20 mL, 10 mL)로 추출하였다. 합한 유기부를 물 (3x10 mL) 및 염수 (10 mL)로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 메틸 2-(2-아세틸시클로프로필)-2-메틸프로파노에이트를 수득하였으며, 이를 추가의 정제 없이 사용하였다.
중간체 5: 에틸 3-아세틸비시클로[3.1.0]헥산-6-카르복실레이트
디클로로메탄 (6 mL) 중 에틸 디아조아세테이트 (0.266 mL, 2.179 mmol)의 용액을 디클로로메탄 (6 mL) 중 1-(시클로펜트-3-엔-1-일)에타논 (200 mg, 1.816 mmol) 및 아세트산로듐(II) 이량체 (16.1 mg, 0.036 mmol)의 용액에 시린지 펌프를 통해 6시간에 걸쳐 첨가하였다. 추가로 11시간 후, 반응 혼합물을 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (10-30% 에틸 아세테이트/헥산)에 의해 정제하여 에틸 3-아세틸비시클로[3.1.0]헥산-6-카르복실레이트를 수득하였다.
중간체 6: 2-클로로-4-디플루오로메틸-피리미딘
-20℃로 냉각된 CH2Cl2 (300 mL) 중 디플루오로아세트산 무수물 (50 g, 287 mmol)의 용액에 DMAP (0.351 g, 2.87 mmol)를 첨가하고, 이어서 에틸 비닐 에테르 (13.8 mL, 144 mmol)를 내부 온도가 -10℃를 초과하지 않도록 하는 속도로 첨가하였다. 첨가가 완결된 후, 플라스크를 0℃에서 12시간 동안 교반한 후, 6시간에 걸쳐 실온으로 천천히 가온하였다. CH2Cl2와 함께 물을 첨가하고, 층을 분리하고, 유기부를 수성 포화 NaHCO3에 이어서 염수로 순차적으로 세척하였다. 유기 층을 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 후속적으로 EtOH (162 mL) 중에 녹이고, 빙수조에 담근 다음, 우레아 (17.25 g, 287 mmol)를 첨가하고, 이어서 진한 HCl (43 mL)을 내부 온도가 20℃를 초과하지 않도록 하는 속도로 첨가하였다. 첨가가 완결되었을 때, 냉각 조를 제거하고, 생성된 혼합물을 18시간 동안 교반한 후, 진공 하에 농축시켰다. EtOH를 첨가하고, 혼합물을 재차 농축시킨 다음, EtOAc를 첨가하고, 혼합물을 다시 농축시켰다 (2x). 잔류물을 EtOAc (100 mL)로 희석하고, 생성된 불균질 혼합물을 10분 동안 교반한 다음, 용매를 가만히 따랐다. 이것을 2회 더 반복한 다음, 담갈색 고체를 여과에 의해 수집하고, 48시간 동안 진공 하에 건조시킨 후, 옥시염화인 (215 mL, 2310 mmol)으로 희석하였다. 생성된 현탁액을 105℃로 90분 동안 가열하였으며, 이 시간 동안 이것이 균질하게 되는 것으로 관찰되었다. 반응 혼합물을 실온으로 냉각시키고, 2 L 얼음 및 온도 탐침이 들은 4 L의 냉각된 플라스크에 조심스럽게 부었다. 혼합물을 발열이 중단될 때까지 1시간 동안 교반하고, 발열이 중단되면 내용물을 추가의 CH2Cl2가 들은 분리 깔때기로 옮겼다. 층을 분리하고, 수성 층을 CH2Cl2 (2x)로 추출한 다음, 합한 유기부를 MgSO4로 건조시키고, 여과하고, 진공 (200 Torr, 40℃) 하에 오렌지색 오일로 농축시켰다. 생성물을 진공 하에 1분 동안 두어 2-클로로-4-디플루오로메틸-피리미딘을 CH2Cl2 중 62.5 중량% 용액으로서 수득하였다 (1H NMR에 의해 판단된 바와 같음).
중간체 7: 2-클로로-4-(프로판-2-일옥시)피리미딘
2-프로판올 (84 mL) 중 2,4-디클로로피리미딘 (5.0 g, 34 mmol)의 용액에 Cs2CO3 (12 g, 37 mmol)을 첨가하고, 혼합물을 실온에서 16시간 동안 교반하였다. 이어서, 반응물을 65℃로 3시간 동안 가열한 후, 반응물을 여과하고, 농축시켰다. 실리카 겔 상에서 0-10% EtOAc/헥산의 구배 용매계를 사용하여 정제하여 2-클로로-4-(프로판-2-일옥시)피리미딘을 무색 오일로서 수득하였다.
중간체 8: N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민
단계 1: 1,4-디옥산 (2 L) 중 3-브로모-5-메틸아닐린 (162.5 g, 873.66 mmol)의 용액을 제조하고, 2-클로로-4-(트리플루오로메틸)피리미딘 (182 g, 994.54 mmol) 및 메탄술폰산 (97.5 g, 1.02 mol)을 순차적으로 첨가하였다. 생성된 용액을 환류 하에 밤새 가열하였다. 생성된 혼합물을 냉각시키고, 진공 하에 농축시켰다. 잔류물을 물 2 L로 희석한 다음, 수성 포화 중탄산나트륨 용액을 사용하여 pH 7-8로 조정하고, 이어서 EtOAc (2x2 L)로 추출하였다. 유기 층을 합하고, 물 (2x 2 L)로 세척하고, 무수 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 N-(3-브로모-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아민을 담황색 고체로서 수득하였다.
단계 2: 1,4-디옥산 (3 L) 중 N-(3-브로모-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아민 (250 g, 753.01 mmol)의 용액에 4,4,5,5-테트라메틸-2-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-1,3,2-디옥사보롤란 (225 g, 885.83 mmol), KOAc (225 g, 2.30 mol) 및 Pd(dppf)Cl2 (19 g, 25.23 mmol)를 첨가하였다. 생성된 용액을 환류 하에 밤새 가열하였다. 고체를 여과하고, 여과물을 실리카 겔 칼럼을 통과시켜 탈색시켰다. 분획을 수집하고, 진공 하에 농축시켰다. 이것으로, 정제된 생성물의 1 부분 및 조 생성물의 1 부분을 수득하였다. 조 생성물을 활성탄을 사용하여 다시 탈색시켜 생성물의 추가 분취액을 수득하였다. 정제된 생성물의 2 부분을 합하여 N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 백색 고체로서 수득하였다.
중간체 9: 5-플루오로-4-메톡시-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민
2-클로로-5-플루오로-4-메톡시피리미딘 (0.32 g, 1.97 mmol) 및 3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)아닐린 (0.40 g, 1.72 mmol)이 들은 플라스크에 디옥산 (17 mL) 및 메탄술폰산 (0.13 mL, 1.97 mmol)을 첨가하였다. 반응물을 100℃에서 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 에틸 아세테이트로 희석하고, 물로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켰다. 정제를 위해 플래쉬 크로마토그래피를 사용하여 5-플루오로-4-메톡시-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민을 수득하였다.
하기 중간체를 중간체 8 또는 중간체 9에 나타낸 경로를 이용하여 제조하였다. 일부 경우에, SNAR 반응에 사용된 산을 변화시켰다.
중간체 21: N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민
1,4-디옥산 (800 mL) 중 N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (80 g, 211.08 mmol)의 용액에 5-브로모-1,3-티아졸 (28 g, 171.78 mmol), Pd(dppf)Cl2 (8 g, 10.62 mmol) 및 물 (447 mL) 중 탄산나트륨 (44.7 g, 421.70 mmol)의 용액을 첨가하였다. 생성된 용액을 환류 하에 1시간 동안 가열하였다. 이어서, 이것을 실온으로 냉각되도록 하고, 진공 하에 농축시켰다. 잔류물을 EtOAc (500 mL)로 희석하고, 여과하였다. 여과물을 염수 (2x300 mL) 및 물 (2x300 mL)로 세척하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 조 생성물을 1:5 비의 EtOAc:DCM으로부터 재결정화하여 생성물 1 부분을 수득하였다. 모액을 실리카 겔 칼럼 상에 적용하고, 디클로로메탄/에틸 아세테이트 (2:1)로 용리시켜 N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 연황색 고체로서 수득하였다.
중간체 22: 에틸 (1S,2R,4S)-4-[1(R)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트; 에틸 (1S,2R,4S)-4-[1(S)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트; 에틸 (1R,2S,4R)-4-[1(R)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트; 에틸 (1R,2S,4R)-4-[1(S)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트
단계 1: THF (250 mL) 중 (메톡시메틸)트리페닐포스포늄 클로라이드 (55.8 g, 163 mmol)의 냉각된 (0℃) 용액에 KOtBu (THF 중 1 M, 163 mL, 163 mmol)를 내부 온도가 5℃를 초과하지 않도록 하는 속도로 첨가하였다. 첨가가 완결되었을 때, 생성된 혼합물을 1시간 동안 교반하였으며, 이 시점에 에틸 (1,2-시스)-2-메틸-4-옥소시클로헥산카르복실레이트 (20 g, 109 mmol)를 THF (200 mL) 중 용액으로서 도입하였다. 반응 혼합물을 실온으로 천천히 가온되도록 하고, 18시간 동안 교반하였다. 이어서, 용기를 빙조에 담그고, 물 (100 mL)을 첨가하고, 이어서 6N HCl (250 mL)을 첨가하였다. 냉각 조를 제거하고, 반응물을 가수분해가 TLC에 의해 완결될 때까지 (~2 h) 교반하고, 가수분해가 완결되면 이것을 물 및 EtOAc로 희석하였다. 층을 분리하고, 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켜 에틸 (1,2-시스)4-포르밀-2-메틸시클로헥산카르복실레이트 (23 g)를 이성질체의 혼합물로서 수득하였다. 이 무색 오일을 직접 후속 단계에 추가의 조작 없이 사용하였다.
단계 2: 500 mL 둥근 바닥 플라스크에 iPrMgCl-LiCl (THF 중 1.3 M, 92 mL, 119 mmol)을 첨가하고, 용액을 빙조에서 냉각시켰다. 이어서, 티아졸 (8.9 mL, 125 mmol)을 내부 온도가 5℃를 초과하지 않도록 하는 속도로 도입한 다음, 농후한 슬러리를 1시간 동안 교반하였다. THF 100 mL를 도입하고, 반응 혼합물을 -50℃로 냉각시키고, 이 시점에 에틸 (1,2-시스)-4-포르밀-2-메틸시클로헥산카르복실레이트 (이성질체의 혼합물, 23 g)를 캐뉼라를 통해 THF (100 mL) 중 용액으로서 첨가하였다. 완결되었을 때, 반응 혼합물을 5℃로 천천히 가온되도록 하고, 30분 동안 교반한 다음, 물 및 EtOAc를 첨가하여 켄칭하였다. 층을 분리하고, 유기 혼합물을 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켜 에틸 (1,2-시스)-4-[히드록시(1,3-티아졸-2-일)메틸]-2-메틸시클로헥산카르복실레이트 (34 g)를 이성질체의 혼합물로서 수득하였다. 이 갈색 오일을 직접 후속 단계에 추가의 조작 없이 사용하였다.
단계 3: 에틸 (1,2-시스)-4-[히드록시(1,3-티아졸-2-일)메틸]-2-메틸시클로헥산카르복실레이트 (34 g)의 조 혼합물을 DMF (200 mL)로 희석하고, NBS (21.2 g, 119 mmol)를 첨가하였다. 생성된 혼합물을 55℃로 가열하고, 출발 물질이 소모될 때까지 교반한 다음, 가열 맨틀을 제거하였다. 아황산나트륨 (10 g)을 함유하는 물 (220 mL)을 첨가하고, 이어서 EtOAc를 첨가하였다. 층을 분리하고, 유기부를 물로 재차 세척한 다음, MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 에틸 (1,2-시스)-(1,4-트랜스)-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-2-메틸시클로헥산 카르복실레이트를 황색 오일 (2급 알콜 입체중심에서의 부분입체이성질체의 1:1 혼합물)로서 및 에틸 (1,2-시스)-(1,4-시스)-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-2-메틸시클로헥산카르복실레이트를 황색 오일 (2급 알콜 입체중심에서의 부분입체이성질체의 3:2 혼합물)로서 수득하였다.
단계 4: 에틸 (1,2-시스)-(1,2-트랜스)-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-2-메틸시클로헥산 카르복실레이트 (16.0 g, 44.2 mmol)를 CH2Cl2 (160 mL)로 희석하고, 실온 수조에 담갔다. 여기에 데스-마르틴(Dess-Martin) 퍼아이오디난 (20.6 g, 48.6 mmol)을 첨가하여 현저한 발열을 생성시켰다. 60분 후, 5% NaHCO3 및 5% 아황산나트륨의 수용액을 첨가하고, 생성된 2상 혼합물을 두 층이 분명해질 때까지 교반하고, 두 층이 분명해지면 이들을 분리하고, 수성 층을 CH2Cl2로 역추출하고, 합한 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 실리카 겔 상에서 플래쉬 크로마토그래피에 의해 에틸 (1,2-시스)-(1,4-트랜스)-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]-2-메틸시클로헥산카르복실레이트를 담황색 오일로서 수득하였다.
단계 5: 에틸 (1,2-시스)-(1,4-트랜스)-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]-2-메틸시클로헥산 카르복실레이트 (6.7 g, 18.7 mmol)를 THF (67 mL)로 희석하고, 드라이아이스/아세톤 조에서 냉각시켰다. 이 용액에 MeMgBr (Et2O 중 3 M, 6.23 mL, 18.7 mmol)을 내부 온도가 -60℃를 초과하지 않도록 하는 속도로 첨가하였다. 이러한 첨가 후, 반응 혼합물을 ≤60℃에서 1시간 동안 교반한 다음, 물에 이어서 EtOAc 및 추가의 물로 희석하였다. 층을 분리하고, 수성 층을 EtOAc로 재추출하였다. 합한 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 겔 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 에틸 (1,2-시스)-(1,4-트랜스)4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산 카르복실레이트를 부분입체이성질체 1:1 혼합물의 담황색 오일로서 수득한 다음, 이를 키랄 SFC에 의해 분리하여 모든 4종의 입체이성질체: 에틸 (1S,2R,4S)-4-[(1R)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트, 에틸 (1S,2R,4S)-4-[(1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산 카르복실레이트, 에틸 (1R,2S,4R)-4-[(1R)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트 및 에틸 (1R,2S,4R)-4-[(1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]-2-메틸시클로헥산카르복실레이트를 수득하였다.
중간체 23: 시스-메틸-3-아세틸시클로펜탄카르복실레이트
단계 1: DCM (20 ml) 중 시스-3-(메톡시카르보닐)시클로펜탄카르복실산 (2 g, 11.62 mmol)의 용액에 DMF (0.05 mL)를 첨가하고, 이어서 옥살릴 클로라이드 (1.118 ml, 12.78 mmol)를 적가하였다. 반응 혼합물을 기체 발생이 중단된 후 2시간 동안 실온에서 교반하였다. 이어서, 휘발성 물질을 감압 하에 제거하고, 유성 잔류물을 다음 단계에 추가의 정제 없이 사용하였다.
단계 2: 메틸리튬의 용액 (Et2O 중 1.6 M, 55.2 ml, 88 mmol)을 THF (97 ml) 중 아이오딘화구리(I) (8.85 g, 46.5 mmol)의 현탁액에 0℃에서 적가하였다. 실온에서 10분 동안 교반한 후, 혼합물을 -78℃로 냉각시키고, 단계 1로부터의 조 산 클로라이드 (2.215 g, 11.62 mmol)를 THF (1 mL) 중 용액으로서 적가하였다. 반응 혼합물을 -78℃에서 30분 동안 교반하고, MeOH로 켄칭하고, 실온으로 가온되도록 하였다. 포화 수성 NH4Cl을 첨가하고, 혼합물을 Et2O로 추출하였다. 유기 층을 분리하고, 염수로 세척하고, Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 SiO2 겔 (헥산 중 10% → 80% Et2O 구배 용리)에 의해 정제하여 시스-메틸-3-아세틸시클로펜탄카르복실레이트를 무색 오일로서 수득하였다.
중간체 24: 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트
단계 1: THF (250 mL) 중 (메톡시메틸)트리페닐포스포늄 클로라이드 (60.4 g, 176 mmol)의 냉각된 (0℃) 용액에 KOtBu (THF 중 1 M, 176 mL, 176 mmol)를 내부 온도가 5℃를 초과하지 않도록 하는 속도로 첨가하였다. 첨가가 완결되었을 때, 생성된 혼합물을 1시간 동안 교반하였으며, 이 시점에 에틸 4-옥소시클로헥산카르복실레이트 (20 g, 118 mmol)를 THF (200 mL) 중 용액으로서 도입하였다. 반응 혼합물을 실온으로 천천히 가온되도록 하며, 실온에서 18시간 동안 교반하였다. 이어서, 용기를 빙조에 담그고, 물 (100 mL)을 첨가하고, 이어서 6N HCl (250 mL)을 첨가하였다. 냉각 조를 제거하고, 반응물을 가수분해가 TLC에 의해 완결될 때까지 (~2 h) 교반하고, 가수분해가 완결되면 이것을 물 및 EtOAc로 희석하였다. 층을 분리하고, 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켜 에틸 4-포르밀시클로헥산카르복실레이트 (23 g)를 트랜스:시스 이성질체의 3:2 혼합물로서 수득하였다. 이 무색 오일을 직접 후속 단계에 추가의 조작 없이 사용하였다.
단계 2: 500 mL 둥근 바닥 플라스크에 iPrMgCl-LiCl (THF 중 1.3 M, 99 mL, 129 mmol)을 첨가하고, 용액을 빙조에서 냉각시켰다. 이어서, 티아졸 (9.7 mL, 135 mmol)을 내부 온도가 5℃를 초과하지 않도록 하는 속도로 도입한 다음, 농후한 슬러리를 1시간 동안 교반하였다. THF 100 mL를 도입하고, 반응 혼합물을 -50℃로 냉각시키고, 이 시점에 에틸 4-포르밀시클로헥산카르복실레이트 (23 g)를 캐뉼라를 통해 THF (100 mL) 중 용액으로서 첨가하였다. 완결되었을 때, 반응 혼합물을 5℃로 천천히 가온되도록 하고, 이 온도에서 30분 동안 교반한 다음, 물 및 EtOAc를 첨가하여 켄칭하였다. 층을 분리하고, 유기 혼합물을 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켜 에틸 4-[히드록시(1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트를 트랜스:시스 이성질체 (둘 다 라세미 혼합물임)의 3:2 혼합물로서 수득하였다. 이 갈색 오일을 직접 후속 단계에 추가의 조작 없이 사용하였다.
단계 3: 에틸 4-[히드록시(1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트 (34 g)의 조 혼합물을 DMF (220 mL)로 희석하고, NBS (23 g, 129 mmol)를 첨가하였다. 생성된 혼합물을 55℃로 가열하고, 출발 물질이 소모될 때까지 교반하고, 이 시점에 가열 맨틀을 제거하였다. 아황산나트륨 (10 g)을 함유하는 물 (220 mL)을 첨가하고, 이어서 EtOAc를 첨가하였다. 층을 분리하고, 유기부를 물로 재차 세척한 다음, MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 라세미 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]시클로헥산카르복실레이트를 백색 고체로서 및 라세미 에틸 시스-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]시클로헥산카르복실레이트를 황색 오일로서 수득하였다. 트랜스 이성질체에 대한 특성화 데이터:
단계 4: 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]시클로헥산카르복실레이트 (11.5 g, 33 mmol)를 CH2Cl2 (115 mL)로 희석하고, 실온 수조에 담갔다. 여기에 데스-마르틴 퍼아이오디난 (15.4 g, 36.3 mmol)을 첨가하여 현저한 발열을 발생시켰다. 30분 후, 5% NaHCO3 및 5% 아황산나트륨의 수용액을 첨가하고, 생성된 2상 혼합물을 두 층이 분명해질 때까지 교반하였다. 층을 분리하고, 수성 층을 CH2Cl2로 역추출하고, 합한 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (11.1 g, 32 mmol)를 황색 오일로서 수득하였다.
중간체 25: N-{트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥실}메탄술폰아미드
단계 1: 0℃에서 THF (107 mL) 중 벤질 {트랜스-4-[메톡시(메틸)카르바모일]시클로헥실}카르바메이트 (3.43 g, 10.71 mmol)의 용액에 메틸마그네슘 브로마이드 (디에틸 에테르 중 3.0 M, 5.35 mL, 16.06 mmol)를 첨가하고, 반응물을 0℃에서 1시간 동안 교반하였다. 이어서, 메틸마그네슘 브로마이드 (디에틸 에테르 중 3.0 M, 5.35 mL, 16.06 mmol)의 추가 부분을 첨가하고, 반응물을 실온으로 가온되도록 한 다음, 1시간 동안 교반하였다. 반응물을 수성 포화 염화암모늄으로 천천히 켄칭하였다. 물 및 에틸 아세테이트를 첨가하고, 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켜 벤질 (트랜스-4-아세틸시클로헥실)카르바메이트를 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 2: -78℃에서 THF (87 mL) 중 티아졸 (740 mg, 8.72 mmol)의 용액에 n-BuLi (헥산 중 2.5 M, 3.84 mL, 9.59 mmol)를 첨가하고, 용액을 -78℃에서 30분 동안 교반하였다. THF (5 mL) 중 벤질 (트랜스-4-아세틸시클로헥실)카르바메이트 (1.20 g, 4.36 mmol)의 용액을 첨가하고, 반응물을 -78℃에서 1시간 동안 교반하였다. 반응물을 물로 희석하고, 실온으로 가온하였다. 혼합물을 에틸 아세테이트로 추출하고, 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 실리카 겔 상에서 칼럼 크로마토그래피 (디클로로메탄 중 0-10% 메탄올 구배)하여 벤질 {트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥실}카르바메이트를 수득하였다.
단계 3: -78℃에서 디클로로메탄 중 벤질 {트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥실}카르바메이트 (895 mg, 2.48 mmol)의 용액에 삼브로민화붕소 (디클로로메탄 중 1.0 M, 2.7 mL, 2.7 mmol)를 적가하였다. 1시간 후, 용액을 0℃로 가온하였다. 이어서, 삼브로민화붕소 (디클로로메탄 중 1.0 M, 2.7 mL, 2.7 mmol)의 또 다른 부분을 적가하고, 반응물을 실온으로 가온되도록 하였다. 이어서, 용액을 조심스럽게 메탄올로 희석하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 1-(트랜스-4-아미노시클로헥실)-1-(1,3-티아졸-2-일)에탄올을 수득하였다.
단계 4: 0℃에서 디클로로메탄 (2.9 mL) 및 트리에틸아민 (0.31 mL, 2.21 mmol) 중 1-(트랜스-4-아미노시클로헥실)-1-(1,3-티아졸-2-일)에탄올 (100 mg, 0.44 mmol)의 용액에 메탄술포닐 클로라이드 (34 μL, 0.44 mmol)를 첨가하고, 반응물을 0℃에서 10분 동안 교반되도록 한 다음, 물, 디클로로메탄 및 수성 포화 중탄산나트륨으로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 칼럼 크로마토그래피 (헥산 중 0-100% 에틸 아세테이트 구배)에 의해 정제하여 N-{트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥실}메탄술폰아미드를 수득하였다.
단계 5: DMF (4.0 mL) 중 N-{트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥실}메탄술폰아미드 (178 mg, 0.59 mmol)의 용액에 N-브로모숙신이미드 (104 mg, 0.585 mmol)를 첨가하고, 반응물을 50℃에서 1시간 동안 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 또 다른 부분의 N-브로모숙신이미드 (52 mg, 0.292 mmol)를 첨가하였다. 이어서, 반응물을 50℃에서 1시간 동안 가열하였다. 이어서, 용액을 실온으로 냉각시키고, 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 칼럼 크로마토그래피에 의해 정제하여 N-{트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥실}메탄술폰아미드를 수득하였다.
중간체 26: 트랜스-4-아세틸시클로헥산카르보니트릴
단계 1: 디클로로메탄 (7.7 mL) 중 트랜스-4-시아노시클로헥산카르복실산 (1.29 g, 8.42 mmol)의 용액에 티오닐 클로라이드 (디클로로메탄 중 2.0 M, 10.11 mL, 20.21 mmol)를 첨가하고, 반응물을 38℃에서 밤새 가열하였다. 이어서, 반응물을 농축시켜 트랜스-4-시아노시클로헥산카르보닐 클로라이드를 수득하였으며, 이를 후속 단계에 추가의 정제 없이 사용하였다.
단계 2: 단계 1로부터의 생성물 (1.44 g, 8.42 mmol)에 디옥산 (56 mL)을 첨가하고, 용액을 30분 동안 표면하 버블링을 통해 아르곤으로 탈기하였다. Pd(OAc)2 (95 mg, 0.42 mmol)를 첨가하고, 아르곤을 용액을 통해 15분 동안 버블링하였다. 디메틸아연 (톨루엔 중 2.0 M, 4.21 mL, 8.42 mmol)을 첨가하고, 용액을 배기시킨 다음, 아르곤으로 5회 퍼징하였다. 반응물을 38℃에서 밤새 가열하였다. 이어서, 혼합물을 실온으로 냉각시키고, 물 및 에틸 아세테이트로 조심스럽게 희석하고, 셀라이트의 패드를 통해 여과하고, 에틸 아세테이트로 세척하였다. 여과물의 유기 층을 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 칼럼 크로마토그래피에 의해 정제하여 트랜스-4-아세틸시클로헥산카르보니트릴을 수득하였다.
중간체 27: 트랜스-에틸 4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시프로필]시클로헥산카르복실레이트
THF (6 mL) 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (500 mg, 1.444 mmol)의 용액을 -60℃로 냉각시켰다. 에틸마그네슘 브로마이드 (THF 중 3.0 M, 481 μl, 1.444 mmol)를 적가하고, 생성된 혼합물을 1시간 동안 교반하였다. 혼합물을 물 및 EtOAc로 희석하고, 층을 분리하였다. 유기 층을 포화 중탄산나트륨, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (5-80% EtOAc/헥산)에 의해 정제하여 라세미-트랜스-에틸 4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시프로필]시클로헥산카르복실레이트를 황색 고체로서 수득하였다. 라세미 혼합물을 초임계 유체 크로마토그래피 (키랄 테크놀로지(Chiral Technology) AD-H 2.1 X 25cm, 5uM, 30% / 70% 메탄올/CO2, 14분 실행시간)에 의해 정제하여 거울상이성질체 1 및 거울상이성질체 2를 투명한 오일로서 수득하였다.
중간체 28: 에틸 트랜스-4-[(S)-(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트
에틸 트랜스-4-[(R)-(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트
무수 THF (16 ml) 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (518 mg, 1.49 mmol)의 용액을 시클로프로필마그네슘 브로마이드 (1.49 mmol, 테트라히드로푸란 중 0.5 M, 2.99 mL)로 0℃에서 질소 분위기 하에 20분에 걸쳐 적가 처리하였다. 실온에서 1시간 교반한 후, 추가의 시클로프로필마그네슘 브로마이드 (2.23 mmol, 테트라히드로푸란 중 0.5 M, 4.48 mL)를 0℃에서 20분에 걸쳐 적가한 다음, 혼합물을 실온에 도달하도록 하였다. 4시간 후, 혼합물을 포화 염화암모늄 및 에틸 아세테이트로 희석하고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 20% EtOAc)에 의해 정제하여 라세미 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트를 백색 고체로서 수득하였다. 2종의 거울상이성질체를 키랄 초임계 유체 크로마토그래피 (키랄 테크놀로지 AS, 2.1 x 25 cm, 10 uM, 45/55 MeOH/CO2, 유량: 70 mL/분, 14분 실행시간, WL: 220 nm)에 의해 분리하였다. 용리를 7.91분 및 10.78분에서 관찰하였다. 각 피크의 합한 분획을 감압 하에 농축시켰다.
거울상이성질체 1 (체류시간 = 7.91 min): 에틸 트랜스-4-[(S 또는 R)-(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트.
거울상이성질체 2 (체류시간 = 10.78 min): 에틸 트랜스-4-[(R 또는 S)-(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트.
중간체 29: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시-2-메틸프로필]시클로헥산카르복실레이트
무수 THF (16 ml) 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (800 mg, 2.31 mmol)의 용액을 이소프로필마그네슘 브로마이드 (2.31 mmol, 2 M, 1.15 mL)로 0℃에서 질소 분위기 하에 1시간에 걸쳐 적가 처리하였다. 0℃에서 15분 동안 교반한 후, 반응물을 실온에 도달하도록 하였다. 1시간 후, 반응 혼합물을 포화 염화암모늄으로 켄칭하고, 에틸 아세테이트 중에 녹이고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 20% EtOAc)에 이어서 정제용 HPLC 역상 (C-18)에 의해 아세토니트릴 중 55% → 100% 물 (0.1% 트리플루오로아세트산)로 용리시키면서 정제하였다. 수집된 분획을 에틸 아세테이트로 희석하고, 포화 중탄산나트륨, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시-2-메틸프로필]시클로헥산카르복실레이트를 백색 고체로서 수득하였다.
중간체 30: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2-히드록시에틸]시클로헥산카르복실레이트
단계 1: 메틸(트리페닐)포스포늄 브로마이드 (774 mg, 2.166 mmol)를 무수 디에틸 에테르 (5 mL) 중에 현탁시키고, 칼륨 tert-부톡시드 (2.311 mmol, THF 중 1.78 M, 1.29 mL)를 0℃에서 적가하였다. 현탁액을 동일한 온도에서 25분 방치하였다 (용액은 오렌지색-갈색이 됨). 디에틸 에테르 (1 ml) 및 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (500 mg, 1.444 mmol)의 용액을 0℃에서 적가하였다. 혼합물을 동일한 온도에서 30분 동안 방치하고, 실온으로 도달하도록 하고, 추가 90분 동안 교반 하에 방치하고, 물로 희석하고, 에틸 아세테이트 중에 녹였다. 유기 상을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 10% EtOAc)에 의해 정제하여 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)에테닐]시클로헥산카르복실레이트 (62%)를 오일로서 수득하였다.
단계 2: 디클로로메탄 (10 mL) 중 단계 1로부터의 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)에테닐]시클로헥산카르복실레이트 (308 mg, 0.895 mmol)의 용액을 0℃에서 메타-클로로퍼벤조산 (261 mg, 1.163 mmol, 77%)으로 조금씩 처리하였다. 혼합물을 실온에서 16시간 동안 교반하고, 디클로로메탄으로 희석하고, 2N 수산화나트륨으로 세척하였다. 수성 상을 디클로로메탄으로 추출하고, 합한 유기 층을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하였다. 휘발성 물질을 감압 하에 제거하고, 조 생성물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 20% EtOAc)에 의해 정제하여 에틸 트랜스-4-[2-(5-브로모-1,3-티아졸-2-일)옥시란-2-일]시클로헥산카르복실레이트를 무색 오일로서 수득하였다.
단계 3: 단계 2로부터의 에틸 트랜스-4-[2-(5-브로모-1,3-티아졸-2-일)옥시란-2-일]시클로헥산카르복실레이트 (30 mg, 0.082 mmol)의 DCM (0.7 mL) 중 용액을 트리플루오로아세트산 (0.266 mL, 1.665 mmol) 및 트리에틸실란 (0.128 mL, 1.665 mmol)으로 처리하고, 45℃에서 16시간 동안 방치하였다. 휘발성 물질을 감압 하에 제거하고, 잔류물을 디클로로메탄 중에 녹이고, 포화 중탄산나트륨, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2-히드록시에틸]시클로헥산카르복실레이트를 수득하였으며, 이를 추가의 특성화 없이 그 자체로 사용하였다.
중간체 31: 트랜스-4-[아미노(5-브로모-1,3-티아졸-2-일)메틸]시클로헥산카르복실산
단계 1: 트랜스-에틸 4-(5-브로모티아졸-2-카르보닐)시클로헥산카르복실레이트 (150 mg, 0.433 mmol), 나트륨 시아노보로히드라이드 (63 mg, 1.00 mmol), 아세트산암모늄 (83 mg, 1.08 mmol), THF (0.6 mL) 및 메탄올 (1.8 mL)을 밀봉된 바이알에서 합하고, 80℃의 온도로 16시간 동안 가열하였다. 혼합물을 23℃로 냉각시키고, 후속적으로 EtOAc가 들은 분리 깔때기로 옮겼다. 유기 층을 포화 수성 중탄산나트륨으로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 농축시켜 조 트랜스-에틸 4-(아미노(5-브로모티아졸-2-일)메틸)시클로헥산카르복실레이트를 수득하였으며, 이를 직접 후속 합성 변환에 정제 없이 사용하였다.
단계 2: 단계 1로부터의 조 혼합물을 메탄올 (3 mL) 중에 용해시키고, 수산화나트륨 (물 중 1.0 M, 0.950 mL, 0.950 mmol)을 생성된 용액에 첨가하였다. 이어서, 반응 혼합물을 50℃의 온도로 30분 동안 가열하였다. 반응물을 후속적으로 냉각시키고, TFA (0.1 mL)를 사용하여 산성화시키고, 농축시켜 라세미 트랜스-4-[아미노(5-브로모-1,3-티아졸-2-일)메틸]시클로헥산카르복실산을 수득하였으며, 이를 후속 합성 변환에 정제 없이 사용하였다.
중간체 32: 부틸 트랜스-4-[(1S 또는 1R)-1-(5-브로모-1,3-티아졸-2-일)-1-메톡시에틸]시클로헥산카르복실레이트
DMF (1 mL) 중 부틸 트랜스-4-[(1S 또는 1R)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (실시예 19, 단계 3, Rt = 7.86 min) (50 mg, 0.128 mmol)의 무수 용액을 0℃에서 수소화나트륨 (7 mg, 0.179 mmol, 미네랄 오일 중 60%)로 처리한 다음, 실온에서 10분 동안 교반하였다. 아이오도메탄 (9 uL, 0.141 mmol)을 반응 혼합물에 적가하였다. 1시간 후, 추가의 NaH (4.5 mg, 0.128 mmol, 미네랄 오일 중 60%)를 0℃에서 첨가하고, 이어서 아이오도메탄 (9 uL, 0.141 mmol)을 첨가하였다. 생성된 혼합물을 실온에서 20분 동안 교반 하에 방치하고, 1N 염산으로 켄칭하고, 에틸 아세테이트 중에 녹였다. 유기 상을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 15% EtOAc)에 의해 정제하여 부틸 트랜스-4-[(1S 또는 1R)-1-(5-브로모-1,3-티아졸-2-일)-1-메톡시에틸]시클로헥산카르복실레이트를 오일로서 수득하였다.
중간체 33: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1,2-디히드록시에틸]시클로헥산카르복실레이트
에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)에테닐]시클로헥산카르복실레이트 (40 mg, 0.12 mmol), 4-메틸모르폴린 N-옥시드 (31 mg, 0.27 mmol), THF (0.8 ml), 물 (0.4 ml) 및 사산화오스뮴 (0.22 ml, 0.028 mmol)을 합하고, 혼합물을 실온에서 40분 동안 교반하였다. 이어서, 혼합물을 포화 티오황산나트륨으로 희석하고, EtOAc로 추출하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (EtOAc/헥산=1/1) 상에서 정제하여 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1,2-디히드록시에틸]시클로헥산-카르복실레이트를 수득하였다.
중간체 34: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2,2,2-트리플루오로-1-히드록시에틸]시클로헥산카르복실레이트
THF (15 ml) 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산-카르복실레이트 (608 mg, 1.756 mmol)의 용액에 트리플루오로메틸 트리메틸실란 (0.520 ml, 3.51 mmol)을 첨가하였다. 이어서, 테트라부틸암모늄 플루오라이드 (7.0 ml, 7.00 mmol)를 혼합물에 천천히 첨가하였다. 1시간 후, 혼합물을 물로 희석하고, EtOAc로 추출하였다. 유기 상을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (헥산 중 0-20% EtOAc) 상에서 정제하여 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2,2,2-트리플루오로-1-히드록시에틸]시클로헥산카르복실레이트를 수득하였다.
중간체 35: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-3,4-디히드록시부틸]시클로헥산카르복실레이트
단계 1: 메틸트리페닐포스포늄 브로마이드 (2.58 g, 7.22 mmol), 칼륨 tert-부톡시드 (0.8248 g, 7.35 mmol) 및 톨루엔 (24 ml)을 합하고, 환류 하에 1시간 동안 가열하였다. 이어서, 혼합물을 -10℃로 냉각시키고, 톨루엔 2 ml 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산-카르복실레이트 (1.022 g, 2.95 mmol)를 적가하였다. 혼합물을 2℃ 내지 3℃에서 1.5시간 동안 교반하였다. 반응물을 수성 포화 염화암모늄으로 희석하고, EtOAc (2x)로 추출하고, 합한 유기 상을 물, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (헥산 중 0-8% EtOAc) 상에서 정제하여 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)부트-3-엔-1-일]시클로헥산카르복실레이트를 수득하였다.
단계 2: 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)부트-3-엔-1-일]시클로헥산카르복실레이트 (40 mg, 0.107 mmol), 4-메틸모르폴린 N-옥시드 (14 mg, 0.120 mmol), THF (0.8 ml), 물 (0.4 ml) 및 사산화오스뮴 (0.2 ml, 0.025 mmol). 혼합물을 실온에서 15분 동안 교반하였다. 혼합물을 티오황산나트륨으로 희석하고, EtOAc로 추출하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (헥산 중 0-100% EtOAc) 상에서 정제하여 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-3,4-디히드록시부틸]시클로헥산카르복실레이트를 수득하였다.
중간체 36: 트랜스- 및 시스-에틸 4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-4-히드록시시클로헥산카르복실레이트
단계 1: 5-브로모-2-메틸티아졸 (2.00 g, 11.23 mmol)을 사염화탄소 (40 mL) 중 N-브로모숙신이미드 (2.199 g, 12.36 mmol) 및 벤조일 퍼옥시드 (0.136 g, 0.562 mmol)와 합하였다. 혼합물을 환류 하에 밤새 교반하였다. 반응물을 실온으로 냉각시키고, 갈색 용액을 여과하여 고체를 제거하고, 필터 케이크를 사염화탄소로 1회 세척하였다. 합한 여과물을 갈색 잔류물로 농축시키고, 실리카 겔 상에서 크로마토그래피 (헥산 중 0-25% 에테르)에 의해 정제하여 5-브로모-2-(브로모메틸)-1,3-티아졸을 황색 오일로서 수득하였다.
단계 2: 5-브로모-2-(브로모메틸)-1,3-티아졸 (1.02 g, 3.97 mmol) 및 트리에틸 포스파이트 (1.389 mL, 7.94 mmol)를 톨루엔 (8 mL) 중에서 합하고, 환류 하에 밤새 교반하였다. 반응물을 실온으로 냉각시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (에틸 아세테이트 중 0-5% 메탄올)에 의해 정제하여 디에틸 [(5-브로모-1,3-티아졸-2-일)메틸]포스포네이트를 황색 오일로서 수득하였다.
단계 3: THF (10 mL) 중 수소화나트륨 (미네랄 오일 중 60%, 122 mg, 3.06 mmol)의 현탁액을 0℃로 냉각시키고, THF (2 mL) 중 디에틸 [(5-브로모-1,3-티아졸-2-일)메틸]포스포네이트 (769 mg, 2.448 mmol)를 적가하고, 후속적으로 0℃에서 30분 동안 교반하였다. 이어서, THF (2 mL) 중 에틸 4-옥소시클로헥산카르복실레이트 (417 mg, 2.448 mmol)를 첨가하고, 2시간에 걸쳐 실온으로 가온되도록 하였다. 이어서, 반응물을 포화 염화암모늄으로 희석하고, 에틸 아세테이트 (2x)로 추출하였다. 합한 유기 층을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0-10% 에틸 아세테이트)에 의해 정제하여 에틸 4-[(5-브로모-1,3-티아졸-2-일)메틸리덴]시클로헥산카르복실레이트를 황색 오일로서 수득하였다.
단계 4: 에틸 4-[(5-브로모-1,3-티아졸-2-일)메틸리덴]시클로헥산카르복실레이트 (415 mg, 1.257 mmol)에 이어서 4-메틸모르폴린 N-옥시드 (294 mg, 2.51 mmol)를 아세톤 (8 mL) 및 물 (1 mL) 중에 녹이고, 사산화오스뮴 (물 중 4 중량%, 0.986 mL, 0.126 mmol)을 첨가하였다. 반응물을 실온에서 3시간 동안 교반한 다음, 10% Na2S2O3으로 희석하고, 에틸 아세테이트 (2x)로 추출하였다. 합한 유기 층을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 역상 HPLC (물 중 35-70% 아세토니트릴 (0.1% TFA 함유))에 의해 정제하여 에틸 4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-4-히드록시시클로헥산카르복실레이트의 부분입체이성질체를 분리하였다. 각각의 단리된 부분입체이성질체의 합한 분획을 따로 합하고, 농축시켜 아세토니트릴을 제거하고, 수성 포화 중탄산나트륨으로 희석하고, 디클로로메탄 (2x)으로 추출하였다. 각각의 부분입체이성질체에 대해 독립적으로, 합한 유기 층을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켰다. HPLC에 의해 단리된 보다 빠른 용리 피크는 중간체 36-A: 트랜스-에틸 4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-4-히드록시시클로헥산카르복실레이트였다.
HPLC에 의해 단리된 보다 느린 용리 피크는 중간체 36-B: 시스-에틸 4-[(5-브로모-1,3-티아졸-2-일)(히드록시)메틸]-4-히드록시시클로헥산카르복실레이트였다.
중간체 37:
메틸 (1S,3R)-3-[(1R)-1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로펜탄카르복실레이트,
메틸 (1S,3R)-3-[(1S)-1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로펜탄카르복실레이트,
메틸 (1R,3S)-3-[(1R)-1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로펜탄카르복실레이트, 및
메틸 (1R,3S)-3-[(1S)-1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로펜탄카르복실레이트
티아졸 (501 mg, 5.88 mmol)을 THF (1.2 mL) 중에 용해시키고, 이소프로필마그네슘 클로라이드 리튬 클로라이드 착체 (THF 중 1.3 M 용액, 5.88 mL, 7.64 mmol)를 적가하고, 생성된 혼합물을 실온에서 1시간 동안 교반하였다. 이어서, 시스-메틸 3-아세틸시클로펜탄카르복실레이트 (1.2 g, 7.05 mmol)를 THF (2 mL) 중 용액으로서 첨가하고, 반응 혼합물을 실온에서 3시간 동안 교반하였다. 반응 혼합물을 포화 NH4Cl 및 디에틸 에테르로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 12% → 100% Et2O)에 의해 정제하여 시스-메틸 3-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로펜탄카르복실레이트를 무색 오일로서 수득하였다;
이어서, 상기 생성물을 SFC (칼럼: 키랄 테크놀로지 AD-H 2.1 X 25cm, 5uM. 이동상: 10% / 90% 에탄올/CO2. 유량: 70 mL/분. 파장: 220 nm)에 의해 4종의 단일 거울상이성질체적으로 순수한 표제 화합물로 분리하였다.
중간체 38: 1-[트랜스-4-(히드록시메틸)시클로헥실]-1-(1,3-티아졸-2-일)에탄올
단계 1: 티아졸 (100 mg, 1.175 mmol)을 THF (11 mL) 중에 용해시키고, -78℃의 온도로 냉각시켰다. N-부틸리튬 (헥산 중 2 M, 0.587 mL, 1.175 mmol)을 첨가하고, 혼합물을 -78℃에서 30분 동안 교반되도록 하였다. 이어서, THF (1 mL) 중 트랜스-부틸 4-아세틸시클로헥산카르복실레이트 (319 mg, 1.410 mmol)의 용액을 혼합물에 첨가하고, 합한 용액을 -78℃에서 1시간 동안 교반되도록 하였다. 반응물을 물로 희석하고, 23℃로 가온하고, EtOAc가 들은 분리 깔때기로 옮겼다. 층을 분리하고, 유기 층을 물로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 부틸 트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트를 수득하였다.
단계 2: 부틸 트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트 (150 mg, 0.482 mmol)를 질소 분위기 하에 바이알에 넣고, THF (2 mL)를 첨가하였다. 수소화알루미늄리튬 (THF 중 3.5 M, 0.270 mL, 0.945 mmol)을 첨가하였다. 23℃에서 20분 동안 교반한 후, 반응물을 적가를 통해 메탄올 (5 mL)로 조심스럽게 희석하였다. 생성된 백색 현탁액을 셀라이트를 통해 여과하고, 여과물을 농축시켜 1-[트랜스-4-(히드록시메틸)시클로헥실]-1-(1,3-티아졸-2-일)에탄올을 수득하였으며, 이를 후속 합성 변환에 정제 없이 사용하였다.
중간체 39: 메틸 4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]-1-메틸시클로헥산카르복실레이트
단계 1: -78℃에서 리튬 디이소프로필 아미드 (테트라히드로푸란/헵탄/에틸벤젠 중 1.8 M, 46.2 mL, 83 mmol)의 용액에 테트라히드로푸란 (80 mL) 중 4-(메톡시카르보닐)시클로헥산카르복실산 (6.2 g, 33.3 mmol)의 용액을 캐뉼라 니들을 통해 15분에 걸쳐 첨가하였다. 40분 동안 교반한 후, 아이오도메탄 (3.12 mL, 49.9 mmol)을 갈색 반응 혼합물에 30초에 걸쳐 첨가하였다. 45분 후, 반응 조를 4시간에 걸쳐 실온으로 가온되도록 한 다음, 반응 혼합물을 0℃로 냉각시킨 후, 염산 (물 중 2.0 M, 100 mL)을 첨가하였다. 반응 혼합물을 헥산 (50 mL)으로 희석하고, 층을 분리하였다. 수성 층을 에틸 아세테이트 (2x100mL)로 추출하였다. 합한 유기 층을 염수 (3x50 mL)로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 농축시켜 4-(메톡시카르보닐)-4-메틸시클로헥산카르복실산을 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 2: 디클로로메탄 (30 mL) 중 4-(메톡시카르보닐)-4-메틸시클로헥산카르복실산 (6.67 g, 33.3 mmol)의 용액에 티오닐 클로라이드 (40 mL, 80 mmol)를 채운 다음, 38℃로 17시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 다음, 감압 하에 농축시켜 메틸 4-(클로로카르보닐)-1-메틸시클로헥산카르복실레이트를 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 3: 1,4-디옥산 (200 mL) 중 메틸 4-(클로로카르보닐)-1-메틸시클로헥산카르복실레이트 (7.282 g, 33.3 mmol) 및 아세트산팔라듐(II) (374 mg, 1.665 mmol)의 탈산소화된 용액에 디메틸아연 (톨루엔 중 2.0 M, 16.65 mL, 33.3 mmol)을 첨가하였다. 흑색 반응 혼합물을 불활성 분위기 하에 38℃에서 15시간 동안 가열한 후, 물 (30 mL)로 희석하였다. 생성된 현탁액을 셀라이트를 통해 2회 여과하였다. 여과물을 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (5-45% 에틸 아세테이트/헥산)에 의해 정제하여 메틸 4-아세틸-1-메틸시클로헥산카르복실레이트를 수득하였다.
단계 4: 테트라히드로푸란 (5 mL) 중 티아졸 (0.309 mL, 4.36 mmol)의 용액에 이소프로필마그네슘 클로라이드 리튬 클로라이드 착체의 용액 (테트라히드로푸란 중 1.0 M, 3.36 mL, 4.36 mmol)을 첨가하였다. 20분 후, 생성된 용액을 테트라히드로푸란 (10 mL) 중 메틸 4-아세틸-1-메틸시클로헥산카르복실레이트 (864.9 mg, 4.36 mmol)의 용액에 시린지를 통해 6분에 걸쳐 첨가하였다. 90분 후, 포화 수성 염화암모늄 용액 (5 mL)을 반응 혼합물에 첨가하고, 생성된 현탁액을 물 (5 mL)과 에틸 아세테이트 (30 mL) 사이에 분배하였다. 유기 층을 포화 수성 중탄산나트륨 용액 및 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 키랄 크로마토그래피 (메탄올/초임계 CO2)에 의해 정제하여 메틸 4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]-1-메틸시클로헥산카르복실레이트의 4종의 분리 입체이성질체 (피크 1, 피크 2, 피크 3, 피크 4)를 수득하였다.
중간체 40: (1S,2S)-1-히드록시-N-메틸-1-페닐프로판-2-아미늄 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트
단계 1: 수산화나트륨 (H2O 중 3.0 M, 5.98 mL, 17.93 mmol)을 메탄올 (6 mL) 중 라세미 부틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (2.0 g, 5.12 mmol)의 용액에 첨가하고, 70℃로 3시간 동안 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 염산 (H2O 중 3.0 M)으로 산성화시켰다. 물 (10 mL)을 첨가하고, 혼합물을 밤새 교반하였으며, 이 시점에 결정화가 발생하였다. 반응물을 여과하고, 필터 케이크를 물로 세척한 다음, 질소 백 하에 건조시켜 라세미 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산을 백색 고체로서 수득하였다.
단계 2: (1R,2R)-2-(메틸아미노)-1-페닐프로판-1-올 (0.25 g, 1.50 mmol)을 라세미 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산 (500 mg, 1.50 mmol)의 용액에 첨가하고, 생성된 용액을 실온에서 밤새 교반하였으며, 이 시점에 결정화가 발생하였다. 생성된 고체를 여과에 의해 수집하고, 1:1 EtOAc:헥산으로 세척하였다. 생성된 모액을 진공 하에 농축시킨 다음, 이소프로판올 (3.5 mL) 및 (1S,2S)-2-(메틸아미노)-1-페닐프로판-1-올을 첨가하였다. 반응물을 밤새 교반하였으며, 이 시점에 결정화가 발생하였다. 이어서, EtOAc (3 mL)를 첨가하고, 20분 후, 고체를 여과에 의해 수집하고, 필터 케이크를 EtOAc로 세척한 다음, 질소 백 하에 건조시켜 (1S,2S)-1-히드록시-N-메틸-1-페닐프로판-2-아미늄 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트를 백색 고체로서 수득하였다.
실시예 1
트랜스-4-{(1R)-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
트랜스-4-{(1S)-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
단계 1: THF (78 mL)가 들은 플라스크를 -78℃로 냉각시켰다. LDA (THF/헵탄/에틸벤젠 중 1.8 M, 21.7 mL, 39.1 mmol)를 첨가하고, 이어서 THF (25 mL) 중 N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (2.63 g, 7.82 mmol)의 용액을 첨가하였다. 생성된 용액을 -78℃에서 30분 동안 교반되도록 하였다. THF (10 mL) 중 부틸 트랜스-4-아세틸시클로헥산카르복실레이트 (2.65 g, 11.73 mmol)의 용액을 한 번에 첨가하고, 용액을 -78℃에서 1시간 동안 교반하였다. 이어서, 반응물을 물로 희석하고, 실온으로 가온되도록 하였다. 이어서, 혼합물을 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 라세미 부틸 트랜스-4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트를 수득하였다.
단계 2: 메탄올 (10.7 mL) 중 부틸 트랜스-4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트 (600 mg, 1.066 mmol)의 용액에 수산화나트륨 (H2O 중 1.0 M, 2.13 mL, 2.13 mmol)을 첨가하고, 반응물을 100℃에서 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, HCl (H2O 중 1.0 M)을 사용하여 ~3의 pH로 산성화시킨 다음, 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켰다. 잔류물을 정제하고, 동시에 거울상이성질체를 초임계 유체 크로마토그래피 (키랄 OJ(Chiral OJ) 칼럼, 35%:75% 메탄올/CO2, 5.0분 실행시간)에 의해 분리하여 트랜스-4-{(1R)-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산 및 트랜스-4-{(1S)-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산을 수득하였다. 보다 빠른 용리 거울상이성질체 (Rt = 3.22 min)에 대한 특성화 데이터:
하기 화합물을 적절한 중간체를 사용하여 실시예 1에 기재된 바와 유사한 방식으로 제조하였다. 달리 명시하지 않는 한, 용어 시스 및 트랜스는 시클로알킬 고리 주위의 입체화학을 지칭한다.
실시예 2
트랜스-4-{(R)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산
트랜스-4-{(S)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산
단계 1: (4-트리플루오로메틸-피리미딘-2-일)-[3-메틸-5-(4,4,5,5-테트라메틸-[1,3,2]디옥사보롤란-2-일)-페닐]-아민 (29 mg, 0.077 mmol), 에틸 트랜스-4-[(R 또는 S)-(5-브로모-1,3-티아졸-2-일)(시클로프로필)히드록시메틸]시클로헥산카르복실레이트 (중간체 28, 보다 빠른 용리 거울상이성질체, Rt = 7.91 min) (30 mg, 0.077 mmol) 및 PdCl2(dppf)2-CH2Cl2 부가물 (3 mg, 0.05 mmol)의 혼합물을 탈기된 2-메틸테트라히드로푸란 (1 mL) 및 탄산나트륨 (물 중 2 M, 77 uL) 중에 녹였다. 반응 플라스크를 질소로 퍼징하고, 80℃로 16시간 동안 가열하였다. 혼합물을 실온으로 냉각시키고, 에틸 아세테이트로 희석하고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 50% EtOAc)에 의해 정제하여 에틸 트랜스-4-{(S 또는 R)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실레이트를 무색 오일 30 mg (69%)으로서 수득하였다.
단계 2: THF:메탄올:물의 1:1:1 혼합물 (1.5 mL) 중 단계 1로부터의 트랜스-4-{(S 또는 R)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실레이트 (30 mg, 0.054 mmol)의 용액에 수산화나트륨 (1M, 0.214 mL)을 첨가하고, 16시간 동안 실온에서 방치하였다. 반응 혼합물을 염산 (물 중 1M)으로 켄칭하고, 에틸 아세테이트로 추출하였다. 유기 상을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 역상 정제용 HPLC (C-18, 아세토니트릴 중 50% → 100% 물 (0.1% 트리플루오로아세트산 함유)로 용리)에 의해 정제하여 트랜스-4-{(R 또는 S)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산을 연황색 고체로서 수득하였다.
또한 단계 1에서 중간체 28 (보다 느린 용리 거울상이성질체, Rt = 10.78 min)을 사용한 트랜스-4-{(R 또는 S)-시클로프로필(히드록시)[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산의 제조도 이러한 반응 순서를 따른다. rhSyk = +++.
적절한 중간체를 사용하여 실시예 2에 나타낸 경로를 이용하여 하기 화합물을 제조하였다. 달리 명시하지 않는 한, 용어 시스 및 트랜스는 시클로알킬 고리 주위의 입체화학을 지칭한다.
실시예 3
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산카르복실산
단계 1: 디메틸아세트아미드 (0.55 mL) 중 N-(3-브로모-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아민 (41 mg, 0.123 mmol), 카탁슘 A(Cataxium A) (8.9 mg, 0.025 mmol), 트리스(디벤질리덴아세톤)디팔라듐(0) (5.7 mg, 0.0062 mmol), 피발산 (0.006 mL, 0.049 mmol) 및 메틸 4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]-1-메틸시클로헥산카르복실레이트 (피크 3) (51.2 mg, 0.370 mmol)의 용액을 125℃에서 24시간 동안 가열하였다. 이어서, 반응 혼합물을 실온으로 냉각되도록 하고, 디에틸 에테르 (10 mL), 에틸 아세테이트 (20 mL) 및 포화 수성 중탄산나트륨 용액 (10 mL)으로 희석하였다. 층을 분리하고, 유기 층을 물 (3x 10 mL) 및 염수 (10 mL)로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (20-50% 에틸 아세테이트/헥산)에 의해 정제하여 메틸 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산카르복실레이트를 수득하였다.
단계 2: 테트라히드로푸란 (0.6 mL) 및 메탄올 (1.2 mL) 중 메틸 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산카르복실레이트 (37.8 mg, 0.071 mmol)의 용액에 수산화나트륨 (물 중 1.0 M, 0.283 mL, 0.283 mmol)을 첨가하였다. 반응 혼합물을 마이크로웨이브 오븐에서 160℃로 5분 동안 조사하였다. 실온으로 냉각시킨 후, 염산 (물 중 2.0 M, 0.145 mL, 0.290 mmol)을 첨가하였다. 혼합물을 10% IPA:CHCl3과 염수 사이에 분배한 다음, 층을 분리하였다. 수성 층을 10% IPA:CHCl3으로 추출하고, 합한 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 감압 하에 농축시켜 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산카르복실산을 수득하였다.
적절한 중간체를 사용하여 실시예 3에 나타낸 경로를 이용하여 하기 화합물을 제조하였다. 달리 명시하지 않는 한, 용어 시스 및 트랜스는 시클로알킬 고리 주위의 입체화학을 지칭한다.
실시예 4
트랜스-4-{1-플루오로-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
단계 1: 디클로로메탄 (1.8 mL) 중 부틸 트랜스-4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트 (200 mg, 0.355 mmol) 및 촉매량의 에탄올 (1.0 μL, 0.018 mmol)의 용액에 데옥소플루오르 (0.33 mL, 1.78 mmol)를 적가하였다. 반응물을 20분 동안 교반한 다음, 반응물을 조심스럽게 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 부틸 트랜스-4-{1-플루오로-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트를 수득하였다.
단계 2: 메탄올 (1.5 mL) 중 부틸 트랜스-4-{1-플루오로-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트 (80 mg, 0.14 mmol)의 용액에 수산화나트륨 (H2O 중 1.0 M, 0.28 mL, 0.28 mmol)을 첨가하고, 반응물을 60℃로 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, HCl (물 중 1.0 M)을 사용하여 ~3의 pH로 산성화시키고, 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 라세미 트랜스-4-{1-플루오로-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산을 수득하였다.
적절한 중간체를 사용하여 실시예 4에 나타낸 경로를 이용하여 하기 화합물을 제조하였다. 달리 명시하지 않는 한, 용어 시스 및 트랜스는 시클로알킬 고리 주위의 입체화학을 지칭한다.
실시예 5
트랜스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산
시스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산
단계 1: -78℃에서 THF (101 mL) 중 2-메틸티아졸 (1.0 g, 10.1 mmol)의 용액에 n-부틸리튬 (헥산 중 2.5 M, 6.05 mL, 15.1 mmol)을 첨가하고, 용액을 -78℃에서 30분 동안 교반하였다. THF (5 mL) 중 tert-부틸 4-옥소시클로헥산카르복실레이트 (2.4 g, 12.1 mmol)의 용액을 한 번에 첨가하고, 반응물을 -78℃에서 1시간 동안 유지하였다. 이어서, 반응물을 물로 희석하고, 실온으로 가온되도록 하였다. 이어서, 혼합물을 물로 추가로 희석하고, 에틸 아세테이트 및 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 tert-부틸 트랜스-4-히드록시-4-(1,3-티아졸-2-일메틸)시클로헥산카르복실레이트 및 tert-부틸 시스-4-히드록시-4-(1,3-티아졸-2-일메틸)시클로헥산카르복실레이트를 수득하였다. 시스 이성질체에 대한 특성화:
트랜스 이성질체에 대한 특성화:
단계 2: DMF (6.5 mL) 중 tert-부틸 트랜스-4-히드록시-4-(1,3-티아졸-2-일메틸)시클로헥산카르복실레이트 (192 mg, 0.646 mmol)의 용액에 N-브로모숙신이미드 (149 mg, 0.839 mmol)를 첨가하고, 반응물을 실온에서 1시간 동안 교반하였다. 이 때, 추가량의 N-브로모숙신이미드 (149 mg, 0.839 mmol)를 첨가하고, 반응물을 3시간 동안 교반하였다. 이어서, 반응물을 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 칼럼 크로마토그래피에 의해 정제하여 tert-부틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)메틸]-4-히드록시시클로헥산카르복실레이트를 수득하였다.
단계 3: 4-메틸-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민 (145 mg, 0.446 mmol), tert-부틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)메틸]-4-히드록시시클로헥산카르복실레이트 (168 mg, 0.446 mmol), 1,1'-비스(디페닐포스피노)페로센디클로로 팔라듐 (II) 디클로로메탄 착체 (16 mg, 0.022 mmol)가 들은 플라스크에 탈기된 2-메틸테트라히드로푸란 및 탄산나트륨 (물 중 2 M, 0.45 mL, 0.90 mmol)을 첨가하였다. 이어서, 혼합물을 배기시키고, 아르곤으로 5회 퍼징하였다. 이어서, 반응물을 80℃에서 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 tert-부틸 트랜스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트를 수득하였다.
상기와 유사한 방식으로, tert-부틸 시스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트를 제조하였다.
단계 4: 메탄올 (1.0 mL) 중 tert-부틸 트랜스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트 (103 mg, 0.208 mmol)의 용액에 수산화나트륨 (H2O 중 1.0 M, 1.0 mL, 1.0 mmol)을 첨가하고, 반응물을 80℃로 밤새 가열하였다. 이어서, 반응물을 냉각시키고, HCl (H2O 중 1.0 M)을 사용하여 ~3의 pH로 산성화시킨 다음, 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 생성물의 에피머 혼합물이 관찰되었다. 이성질체를 초임계 유체 크로마토그래피 (키랄 OJ 칼럼, 4:6 메탄올/CO2, 4.5분 실행시간)에 의해 분리하여 트랜스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산 (Rt = 2.53 min) 및 시스-4-히드록시-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산 (Rt = 3.43 min)을 수득하였다. 트랜스 이성질체에 대한 특성화 데이터:
시스 이성질체에 대한 특성화 데이터:
실시예 6
2-{[3-(2-{(1R)-1-히드록시-1-[트랜스-4-(2H-테트라졸-5-일)시클로헥실]에틸}-1,3-티아졸-5-일)-5-메틸페닐]아미노}-4-(트리플루오로메틸)피리미딘-1-이움 트리플루오로아세테이트
2-{[3-(2-{(1S)-1-히드록시-1-[트랜스-4-(2H-테트라졸-5-일)시클로헥실]에틸}-1,3-티아졸-5-일)-5-메틸페닐]아미노}-4-(트리플루오로메틸)피리미딘-1-이움 트리플루오로아세테이트
DMF (4.4 mL) 중 트랜스-4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르보니트릴 (214 mg, 0.439 mmol)의 용액에 브로민화아연 (99 mg, 0.439 mmol) 및 나트륨 아지드 (29 mg, 0.439 mmol)를 첨가하고, 반응물을 130℃로 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 소량의 물로 희석하였다. DMSO (2 mL)를 첨가하고, 용액을 역상 HPLC에 의해 정제하여 라세미 2-{[3-(2-{1-히드록시-1-[트랜스-4-(2H-테트라졸-5-일)시클로헥실]에틸}-1,3-티아졸-5-일)-5-메틸페닐]아미노}-4-(트리플루오로메틸)피리미딘-1-이움 트리플루오로아세테이트를 수득하였다. 거울상이성질체를 초임계 유체 크로마토그래피 (키랄 OJ 칼럼, 2:8 메탄올/CO2, 12분 실행시간)에 의해 분리하여 2-{[3-(2-{(1R)-1-히드록시-1-[트랜스-4-(2H-테트라졸-5-일)시클로헥실]에틸}-1,3-티아졸-5-일)-5-메틸페닐]아미노}-4-(트리플루오로메틸)피리미딘-1-이움 트리플루오로아세테이트 및 2-{[3-(2-{(1S)-1-히드록시-1-[트랜스-4-(2H-테트라졸-5-일)시클로헥실]에틸}-1,3-티아졸-5-일)-5-메틸페닐]아미노}-4-(트리플루오로메틸)피리미딘-1-이움 트리플루오로아세테이트를 수득하였다. 보다 빠른 용리 거울상이성질체 (Rt = 6.38 min)에 대한 특성화:
적절한 중간체를 사용하여 실시예 6에 나타낸 경로를 이용하여 하기 화합물을 제조하였다:
실시예 7
시스-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복스아미드
트랜스-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복스아미드
단계 1: THF (5 mL)가 들은 플라스크를 -78℃로 냉각시켰다. LDA (THF/헵탄/에틸벤젠 중 1.8 M, 3.3 mL, 5.95 mmol)를 첨가하고, 이어서 THF (5 mL) 중 N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (0.50 g, 1.49 mmol)의 용액을 한 번에 첨가하고, 생성된 용액을 -78℃에서 30분 동안 교반되도록 하였다. 이어서, THF (5 mL) 중 메틸 4-포르밀시클로헥산카르복실레이트 (336 mg, 1.93 mmol)의 용액을 한 번에 첨가하고, 생성된 용액을 -78℃에서 1시간 동안 교반하였다. 이어서, 반응물을 물로 희석하고, 실온으로 가온되도록 하였다. 이어서, 혼합물을 물 및 에틸 아세테이트로 추가로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 메틸 4-{히드록실[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실레이트를 4종의 이성질체의 혼합물로서 수득하였다.
단계 2: 메탄올 (1.96 mL) 중 메틸 4-{히드록실[5-(3-메틸-5-{[4-(트리플루오로메틸)-피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실레이트의 용액에 1N NaOH (0.79 mL, 0.79 mmol)를 첨가하고, 혼합물을 실온에서 16시간 동안 교반하였다. THF (1.96 mL)를 첨가하고, 혼합물을 60℃에서 6시간 동안 교반한 다음, 실온으로 냉각시키고, pH = 3일 때까지 HCl (H2O 중 1M)을 첨가하였다. 혼합물을 3:1 CHCl3:이소프로판올로 희석하고, 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 농축시켰다. 잔류물을 칼럼 크로마토그래피에 의해 정제하여 4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산을 백색 고체로서 수득하였다. 시스 및 트랜스 이성질체를 초임계 유체 크로마토그래피 (키랄 OJ 칼럼, 1:3 메탄올/CO2, 11분 실행시간)에 의해 분리하였다. 시스 이성질체 (Rt = 5.15 min)에 대한 특성화 데이터:
제2 용리 거울상이성질체 Rt = 8.26 min.
단계 3: DMF (1 mL) 중 시스-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복실산 (24 mg, 0.049 mmol), EDC (19 mg, 0.097 mmol), HOBt (13 mg, 0.097 mmol) 및 디이소프로필에틸 아민 (51 uL, 0.292 mmol)의 용액에 염화암모늄 (7.8 mg, 0.15 mmol)을 첨가하고, 혼합물을 실온에서 16시간 동안 교반하였다. 이어서, 용액을 물로 희석하고, 에틸 아세테이트 (3x)로 추출하였다. 유기 층을 합하고, 황산마그네슘으로 건조시키고, 여과하고, 농축시켰다. 잔류물을 칼럼 크로마토그래피에 의해 정제하여 시스-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복스아미드를 백색 고체로서 수득하였다.
상기와 유사한 방식으로, 트랜스-4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}시클로헥산카르복스아미드를 제조하였다.
실시예 8
트랜스-4-[(1R 또는 1S)-1-(5-{2-브로모-3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산
N-브로모숙신이미드 (21.9 mg, 0.123 mmol)를 트랜스-4-[(1R 또는 1S)-1-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산 (50 mg, 0.110 mmol) 및 DMF (1.2 ml)의 용액에 첨가하였다. 혼합물을 실온에서 20분 동안 교반하였다. 이어서, CHCl3 중 포화 티오황산나트륨 용액 및 10% IPA를 첨가하였다. 유기 상을 물로 세척하고, 황산나트륨으로 건조시키고, 진공 하에 농축시켰다. 잔류물을 역상 HPLC 상에서 정제하였다. 생성물 분획을 수집하고, pH=8로 염기성화시킨 다음, EtOAc로 추출하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨으로 건조시키고, 농축시켜 트랜스-4-[(1R 또는 1S)-1-(5-{2-브로모-3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산을 수득하였다.
적절한 중간체를 사용하여 실시예 8에 나타낸 경로를 이용하여 하기 실시예를 제조하였다:
실시예 9
트랜스-4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
단계 1: 메틸(트리페닐)포스포늄 브로마이드 (774 mg, 2.166 mmol)를 디에틸 에테르 (5 ml) 중에 현탁시키고, 칼륨 tert-부톡시드 (THF 중 1.78 M, 1.3 ml, 2.314 mmol)를 0℃에서 적가하고, 현탁액을 동일한 온도에서 30분 동안 교반하였다. 디에틸 에테르 (1 ml) 중 에틸 트랜스-4-[(5-브로모-1,3-티아졸-2-일)카르보닐]시클로헥산카르복실레이트 (500 mg, 1.444 mmol)의 용액을 0℃에서 적가하고, 혼합물을 0℃ 내지 5℃에서 1시간 20분 동안 교반하였다. 혼합물을 포화 염화암모늄으로 희석하고, EtOAc로 추출하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨으로 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 0% → 8% EtOAc)에 의해 정제하여 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)에테닐]시클로헥산카르복실레이트를 담황색 오일로서 수득하였다.
단계 2: mCPBA (130 mg, 0.582 mmol)를 0℃에서 DCM (3 ml) 중 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)에테닐]시클로헥산카르복실레이트 (182 mg, 0.529 mmol)의 용액에 첨가하였다. 이어서, 혼합물을 실온에서 17시간 동안 교반되도록 하고, 디클로로메탄으로 희석하고, 수산화나트륨 (H2O 중 2M)으로 세척하였다. 수성 층을 DCM으로 추출하고, 합한 유기 층을 염수로 세척하고, 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (헥산 중 0-15% EtOAc)에 의해 정제하여 에틸 트랜스-4-[2-(5-브로모-1,3-티아졸-2-일)옥시란-2-일]시클로헥산카르복실레이트를 수득하였다.
단계 3: 바이알에 에틸 트랜스-4-[2-(5-브로모-1,3-티아졸-2-일)옥시란-2-일]시클로헥산카르복실레이트 (101 mg, 0.28 mmol) 및 테트라-N-부틸암모늄 디수소트리플루오라이드 (422 mg, 1.34 mmol)를 첨가하였다. 혼합물을 120℃에서 3시간 45분 동안 가열하였다. 혼합물을 물로 희석하고, EtOAc로 추출하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 농축시켜 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2-플루오로-1-히드록시에틸]시클로헥산-카르복실레이트를 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 4: 라세미 에틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-2-플루오로-1-히드록시에틸]시클로헥산-카르복실레이트 (107 mg, 0.281 mmol), N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (231 mg, 0.610 mmol), X-Phos (56 mg, 0.120 mmol), Pd2(dba)3 (52 mg, 0.056 mmol), 탄산세슘 (429 mg, 1.32 mmol), 1,4-디옥산 (3.0 ml) 및 물 (0.3 ml)을 합하고, 바이알을 배기시키고, 질소로 3회 퍼징한 다음, 100℃로 2시간 동안 가열하였다. 이어서, 혼합물을 여과하고, EtOAc로 희석하였다. 유기 상을 물, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (DCM 중 0-10% MeOH) 상에서 정제하여 라세미 에틸 트랜스-4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트를 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 5: 에틸 트랜스-4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)-피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트 (72 mg, 0.130 mmol)를 HCl (물 중 10 M, 2 ml, 20.0 mmol) 중에 용해시키고, 환류 하에 20분 동안 가열하였다. 반응물을 DMSO로 희석하고, 역상 HPLC (아세토니트릴/물 (0.1% TFA 개질제 함유)) 상에서 정제하여 라세미 트랜스-4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산을 수득하였다.
실시예 10
트랜스-4-{(1S)-2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
트랜스-4-{(1R)-2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산
트랜스-4-{2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산 (34.3 mg)을 키랄 테크놀로지 AD-H 2.1 X 25cm, 5uM (이동상: 45% / 55% 에탄올/CO2, 유량: 65 mL/분, 파장: 275 nm, 19.5분 실행시간) 상에서 분할하여 제1 용리 거울상이성질체 (Rt = 6.96 min) 및 제2 용리 거울상이성질체 (Rt = 16.40 min)를 수득하였으며, 이는 트랜스-4-{(1S)-2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산 및 트랜스-4-{(1R)-2-플루오로-1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산이었다.
실시예 11
N-(3-{2-[(2,2-디메틸-4-옥소시클로헥실)카르보닐]-1,3-티아졸-5-일}-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아미늄 트리플루오로아세테이트
THF (55 mL) 중 N,N-디이소프로필아민 (13.98 mL, 98 mmol)의 용액을 -78℃로 냉각시켰다. 내부 온도를 -65℃ 미만으로 유지하면서 -78℃에서 n-부틸리튬 (61.3 mL, 헥산 중 1.6 M, 98 mmol)을 시린지를 통해 조금씩 용액에 첨가하였다. 반응 혼합물을 -60℃로 가온하고, 45분 동안 에이징시킨 다음, -78℃로 다시 냉각시켰다. THF 55 mL 중 N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (2.113 g, 6.28 mmol)의 용액을 내부 온도를 -70℃ 미만으로 유지하면서 캐뉼라 (정압 사용)를 통해 30분의 기간에 걸쳐 앞서 기재된 새롭게 제조된 LDA 용액으로 옮겼다. 반응물을 -78℃에서 35분 동안 에이징시키고, -50℃로 가온하고, 추가로 15분 동안 에이징시켰다. 혼합물을 -70℃로 냉각시키고, THF (50 mL) 중 메틸 2,2-디메틸-4-옥소시클로헥산카르복실레이트 (9.04 g, 49.1 mmol)의 용액을 내부 온도를 -65℃ 미만으로 유지하면서 캐뉼라 (정압 사용)를 통해 45분의 기간에 걸쳐 리튬 염이 들은 플라스크로 옮긴 다음, -65℃에서 20분 동안 에이징시켰다. 차가운 조를 제거하고, 반응물을 실온으로 가온되도록 하였다. 혼합물을 0℃로 냉각시키고, 반응물을 에탄올 (1 mL) 및 물 (1 mL)로 희석하였다. 혼합물을 EtOAc (1 L)로 희석하고, 포화 염화암모늄 (세척액 전체 부피 1.5 L)으로 3회 세척하였다. 유기 층을 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시키고, 실리카 겔 칼럼 크로마토그래피 (0-30% EtOAc:헥산)에 이어서 역상 고압 액체 크로마토그래피 (아세토니트릴/물 (0.1% TFA 개질제 함유))에 의해 정제하여 라세미 N-(3-{2-[(2,2-디메틸-4-옥소시클로헥실)카르보닐]-1,3-티아졸-5-일}-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아미늄 트리플루오로아세테이트를 수득하였다.
실시예 12
4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}-3,3-디메틸시클로헥산올
N-(3-{2-[(2,2-디메틸-4-옥소시클로헥실)카르보닐]-1,3-티아졸-5-일}-5-메틸페닐)-4-(트리플루오로메틸)피리미딘-2-아미늄 트리플루오로아세테이트 (100 mg, 0.166 mmol)를 메탄올 (1.66 mL) 중에 용해시키고, 0℃로 냉각시켰다. 수소화붕소나트륨 (18.8 mg, 0.498 mmol)을 반응물에 첨가하고, 생성된 혼합물을 0℃에서 30분 동안 에이징시켰다. 반응물을 물로 켄칭하고, EtOAc (3x)로 추출하였다. 합한 유기 층을 진공 하에 농축시키고, 실리카 겔 칼럼 크로마토그래피에 의해 정제하여 4-{히드록시[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메틸}-3,3-디메틸시클로헥산올을 수득하였다.
혼합물은 부분입체이성질체의 ~4:1 혼합물로서 존재한다.
실시예 13
트랜스- 및 시스-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산
단계 1: 에틸 4-[(5-브로모-1,3-티아졸-2-일)메틸리덴]시클로헥산카르복실레이트 (223 mg, 0.676 mmol), 4-메틸-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민 (220 mg, 0.676 mmol) 및 1,1'-비스(디페닐포스피노)페로센디클로로 팔라듐(II) 디클로로메탄 착체 (49.5 mg, 0.068 mmol)를 플라스크에서 합한 다음, 이를 밀봉하고, 질소 (2x)로 플러싱하였다. 디옥산 (4 mL) 및 탄산나트륨 (물 중 2 M, 1.015 mL, 2.029 mmol)을 첨가하고, 반응물을 질소 (2x)로 다시 플러싱하였다. 혼합물을 80℃로 1시간 동안 가열한 다음, 실온으로 냉각시키고, 물로 희석하고, EtOAc (2x)로 추출하였다. 합한 유기 층을 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피 (헥산 중 5-60% EtOAc)에 의해 정제하여 에틸 4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸리덴]시클로헥산카르복실레이트를 황색 발포체로서 수득하였다.
단계 2: 에틸 4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸리덴]시클로헥산카르복실레이트 (175 mg, 0.390 mmol)를 에탄올 (5 mL) 중에 녹이고, 탄소 상 팔라듐 (10% 로딩, 104 mg, 0.098 mmol)을 첨가하였다. 반응물을 수소 기체 (3x)로 퍼징하고, 수소 분위기 (풍선을 통함) 하에 실온에서 밤새 교반하였다. 이어서, 혼합물을 셀라이트를 통해 여과하고, 감압 하에 농축시키고, 잔류물을 실리카 겔 상에서 플래쉬 크로마토그래피 (헥산 중 0-50% 에틸 아세테이트)에 의해 정제하여 에틸 4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트 (황색 검)를 부분입체이성질체의 3:1 혼합물로서 수득하였다.
단계 3: 에틸 4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실레이트 (147 mg, 0.326 mmol)를 마이크로웨이브 바이알 내 메탄올 (2.0 mL) 중에 현탁시키고, 수산화나트륨 (물 중 1M, 0.652 mL, 0.652 mmol)을 첨가하였다. 반응물을 110℃로 30분 동안 마이크로웨이브 조사를 통해 가열하였다. 반응물을 수성 1M HCl을 사용하여 pH = 3-4로 산성화시키고, 클로로포름 중 15% 이소프로필 알콜 (2x)로 추출하였다. 합한 유기 층을 황산마그네슘 상에서 건조시키고, 감압 하에 농축시켜 4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산을 부분입체이성질체의 2.5:1 혼합물로 회백색 고체로서 수득하였다.
부분입체이성질체를 키랄 SFC (키랄 테크놀로지 AS, 2.1 x 25 cm, 10 uM, 25/75 MeOH/CO2, 유량: 70 mL/분, 10.5분 실행시간, WL: 220 nm)에 의해 분리하였다. 용리가 7.26분 및 8.55분에서 관찰되었다. 각 피크의 합한 분획을 따로 감압 하에 농축시켰다.
보다 빠른 용리 이성질체: 시스-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산.
보다 느린 용리 이성질체: 트랜스-4-[(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)메틸]시클로헥산카르복실산.
실시예 14
메틸 (1,3-시스, 1,4-트랜스)-3-히드록시-2,2-디메틸-4-{[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]카르보닐}시클로펜탄카르복실레이트
단계 1: 메틸 시스-4-히드록시-2,2-디메틸-4-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]시클로헥산카르복실레이트 (570 mg, 1.095 mmol)를 이튼(Eaton) 시약 (4.14 mL, 21.9 mmol) 중에 현탁시키고, 60℃로 1.5시간 동안 가열하였다. 이어서, 반응물을 실온으로 냉각되도록 하고, 수성 포화 중탄산나트륨을 천천히 첨가하여 희석하고, EtOAc (3x)로 추출하였다. 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 진공 하에 농축시켰다. 실리카 겔 칼럼 크로마토그래피 (10%-35% EtOAc:헥산)에 의해 정제하고, 부분입체이성질체를 역상 고압 액체 크로마토그래피 (아세토니트릴/물 (0.1% TFA 개질제 함유))에 의해 분리하여 목적 생성물을 TFA 염으로서 수득하였다. 잔류물을 포화 수성 중탄산나트륨으로 희석하고, EtOAc (3x)로 추출하였다. 합한 유기 층을 Na2SO4 상에서 건조시키고, 진공 하에 농축시켜 메틸 2,2-디메틸-4-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]시클로헥스-3-엔-1-카르복실레이트를 수득하였다.
단계 2: 단계 1로부터의 2,2-디메틸-4-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]시클로헥스-3-엔-1-카르복실레이트 (34 mg, 0.068 mmol)를 아세톤 (800 μL) 및 물 (100 μL) 중에 용해시켰다. 사산화오스뮴 (165 μL, 0.027 mmol, 물 중 4%) 및 4-메틸모르폴린 N-옥시드 (32 mg, 0.271 mmol)를 반응물에 순차적으로 첨가하고, 현탁액을 실온에서 40시간 동안 교반하였다. 반응물을 5% 수성 Na2S2O5로 희석하고, 15분 동안 교반하였다. 혼합물을 EtOAc (3x)로 추출하고, Na2SO4 상에서 건조시키고, 진공 하에 농축시켰다. 실리카 겔 칼럼 크로마토그래피 (20%-75% EtOAc:헥산)에 의해 정제하여 메틸 (1,3-시스, 1,4-트랜스)-3-히드록시-2,2-디메틸-4-{[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]카르보닐}시클로펜탄카르복실레이트를 수득하였다.
실시예 15
트랜스-4-[(1R 또는 1S)-1-히드록시-1-{5-[3-(히드록시메틸)-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐]-1,3-티아졸-2-일}에틸]시클로헥산카르복실산
단계 1: 메틸 3-아미노-5-아이오도벤조에이트 (250 mg, 0.90 mmol)가 들은 플라스크에 THF (9.0 mL)를 첨가하였다. 용액을 0℃로 냉각시키고, 수소화알루미늄리튬 (THF 중 1.0M, 1.8 mL, 1.8 mmol)을 천천히 첨가하고, 반응물을 실온으로 가온되도록 하였다. TLC에 의해 완결되면, 반응물을 물에 이어서 에틸 아세테이트로 조심스럽게 희석하였다. 유기 층을 추출하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 실리카 겔 상에서 플래쉬 크로마토그래피하여 [3-(아미노메틸)-5-아이오도페닐]메탄올을 수득하였다.
단계 2: 단계 1의 생성물 (109 mg, 0.44 mmol)이 들은 플라스크에 디옥산 (1.4 mL) 중 2-클로로-4-(트리플루오로메틸)피리미딘 (92 mg, 0.50 mmol)의 용액을 첨가하였다. 메탄술폰산 (0.02 mL, 0.37 mmol)을 첨가하고, 반응물을 100℃에서 밤새 가열하였다. 이어서, 반응물을 실온으로 냉각시키고, 에틸 아세테이트로 희석하고, 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 실리카 겔 상에서 플래쉬 크로마토그래피하여 (3-아이오도-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)메탄올을 수득하였다.
단계 3: DMF (71 mL) 중 단계 2의 생성물 (2.79 g, 7.06 mmol)이 들은 플라스크에 tert-부틸디메틸실릴 클로라이드 (1.60 g, 10.59 mmol), 이미다졸 (0.96 g, 14.12 mmol) 및 DMAP (86 mg, 0.71 mmol)를 첨가하였다. 2시간 후, 반응물을 물 및 에틸 아세테이트로 희석하였다. 유기 층을 분리하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 실리카 겔 상에서 칼럼 크로마토그래피하여 N-[3-({[tert-부틸(디메틸)실릴]옥시}메틸)-5-아이오도페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 4: 탈기된 디옥산 (68 mL)을 단계 3의 생성물 (3.46 g, 6.79 mmol), (비스피나콜레이토)디보론 (2.59 g, 10.19 mmol), 디시클로헥실[2',4',6'-트리(프로판-2-일)비페닐-2-일]포스판 (324 mg, 0.68 mmol), Pd(OAc)2 (76 mg, 0.34 mmol) 및 아세트산칼륨 (1.33 g, 13.59 mmol)이 들은 플라스크에 첨가하였다. 용액을 배기시킨 다음, 아르곤으로 5회 퍼징한 다음, 85℃로 밤새 가열하였다. 용액을 냉각시키고, 에틸 아세테이트로 희석하고, 물로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 정제를 위해 실리카 겔 상에서 플래쉬 크로마토그래피를 사용하여 N-[3-({[tert-부틸(디메틸)실릴]옥시}메틸)-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 5: N-(3-((Tert-부틸디메틸실릴옥시)메틸)-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐)-4-(트리플루오로메틸)피리미딘-2-아민 (30.0 mg, 0.059 mmol), 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산 - (1S,2S)-2-(메틸아미노)-1-페닐프로판-1-올 (1:1) (35.3 mg, 0.071 mmol), 탄산칼륨 (24.4 mg, 0.177 mmol) 및 PdCl2(dppf) (8.62 mg, 0.012 mmol)를 4-mL 바이알에 넣었다. 바이알을 배기시키고, 질소로 재충전하였다. 1,4-디옥산 (1 mL) 및 물 (0.2 mL)을 첨가하고, 반응 혼합물을 80℃로 2시간 동안 가열하였다. TFA (0.5 mL)를 첨가하고, 기체 발생이 중단된 후, 반응 혼합물을 마이크로필터에 통과시키고, 여과물을 정제용 역상 HPLC [(C-18), 아세토니트릴/물 + 0.1% TFA (0 → 100% MeCN으로 용리)]에 의해 직접 정제하여 트랜스-4-((R 또는 S)-1-히드록시-1-(5-(3-(히드록시메틸)-5-(4-(트리플루오로메틸)피리미딘-2-일아미노)페닐)티아졸-2-일)에틸)시클로헥산카르복실산 TFA 염을 황색 고체로서 수득하였다.
실시예 16
트랜스-4-{(1R 또는 1S)-[5-(3-시클로프로필-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산
단계 1: 3,5-디브로모아닐린 (4.47 g, 17.8 mmol) 및 2-클로로-4-(트리플루오로메틸)피리미딘 (2.36 mL, 19.6 mmol)의 용액에 p-톨루엔술폰산 (4.06 g, 21.4 mmol)을 첨가하였고, 이는 농후한 현탁액의 형성을 유발하였다. 이 혼합물을 100℃로 밤새 가열하고, 이 시점 동안 이것은 짙은 적색 용액이 되었다. 혼합물을 EtOAc (200 mL)로 희석하고, 포화 수성 NaHCO3 (200 mL) 및 염수 (200 mL)로 세척하였다. 유기 층을 건조 (Na2SO4)시키고, 여과하고, 진공 하에 농축시켰다. 이어서, 잔류물을 실리카 겔 상에서 크로마토그래피 (100:0 → 85:15 헥산:EtOAc)에 의해 정제하여 N-(3,5-디브로모페닐)-4-(트리플루오로메틸)피리미딘-2-아민을 담황색 고체로서 수득하였다.
단계 2: DMSO (10.1 mL) 중 단계 1로부터의 생성물 (2.0g, 5.0 mmol)의 용액에 4,4,5,5-테트라메틸-2-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-1,3,2-디옥사보롤란 (1.4 g, 5.5 mmol), 아세트산칼륨 (1.48 g, 15.1 mmol) 및 1,1'-비스(디페닐포스피노)페로센]디클로로팔라듐(II) (123 mg, 0.151 mmol)을 첨가하고, 혼합물을 마이크로웨이브 장치에서 125℃로 30분 동안 가열하였다. 혼합물을 EtOAc (100 mL)로 희석하고, 1:1 H2O:염수 (2 x 100 mL)로 세척하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 이어서, 잔류물을 실리카 겔 상에서 크로마토그래피 (100:0 → 70:30 헥산:EtOAc)에 의해 정제하여 N-[3-브로모-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 회백색 고체로서 수득하였다.
단계 3: THF (12.8 mL) 중 아세트산팔라듐 (19 mg, 0.085 mmol) 및 부틸 디-1-아다만틸 포스핀 (61 mg, 0.18 mmol)의 용액을 15분 동안 교반하였다. 이어서, 단계 2로부터의 생성물 (755 mg, 1.70 mmol), 5-브로모-1,3-티아졸 (0.760 ml, 8.50 mmol), 플루오린화칼륨 (296 mg, 5.10 mmol) 및 물 (4.25 mL)을 첨가하고, 혼합물을 75℃로 밤새 가열하였다. 실온으로 냉각시킨 후, 혼합물을 EtOAc (100 mL)로 희석하고, 염수 (100 mL)로 세척하였다. 담황색 고체가 분리 깔때기의 벽 상에 용해되지 않은 상태로 남아있었으며, 따라서 이를 THF (100 ml)로 헹구었다. 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 이어서, 잔류물을 실리카 겔 상에서 크로마토그래피 (100:0 → 50:50 헥산:EtOAc)에 의해 정제하여 N-[3-브로모-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 회백색 고체로서 수득하였다.
단계 4: 플라스크에 단계 3으로부터의 생성물 (523 mg, 1.30 mmol), 시클로프로필 보론산 (336 mg, 3.91 mmol), 인산칼륨 (968 mg, 4.56 mmol), 아세트산팔라듐 (15 mg, 0.07 mmol) 및 트리시클로헥실포스핀 (37 mg, 0.13 mmol)을 첨가하였다. 탈기된 톨루엔 (10 mL) 및 물 (0.5 mL)을 첨가하고, 용액을 배기시킨 다음, 아르곤으로 5회 퍼징하였다. 이어서, 혼합물을 마이크로웨이브 장치에서 130℃의 온도로 30분 동안 가열하였다. 반응물을 EtOAc로 희석하고, 물로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 이어서, 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 N-[3-시클로프로필-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 5: THF (2.8 ml) 중 단계 4로부터의 생성물 (100 mg, 0.276 mmol)의 용액을 -78℃의 온도로 냉각시켰다. LDA (THF/헵탄/에틸벤젠 중 2.0 M, 550 μl, 1.100 mmol)를 첨가하고, 용액을 상기 온도에서 30분 동안 교반하였다. 이어서, THF (1 mL) 중 트랜스-부틸 4-아세틸시클로헥산카르복실레이트 (94 mg, 0.414 mmol)의 용액을 반응 혼합물에 첨가하고, 합한 용액을 -78℃에서 1.5시간 동안 교반되도록 하였으며, 이 시점에 반응물을 MeOH (1 mL)로 희석하였다. 혼합물을 농축시켜 조 트랜스-부틸 4-((1R 또는 1S)-(5-(3-시클로프로필-5-(4-(트리플루오로메틸)피리미딘-2-일아미노)페닐)티아졸-2-일)-1-히드록시에틸)시클로헥산카르복실레이트를 수득하였으며, 이를 단계 6에 정제 없이 사용하였다.
단계 6: 메탄올 (2 ml) 중 단계 5로부터의 생성물 (120 mg, 0.204 mmol)의 용액에 수산화나트륨 (물 중 1.0 M, 1.0 ml, 1.0 mmol)을 첨가하였다. 혼합물을 80℃의 온도로 45분 동안 가열하였다. 이어서, 혼합물을 23℃로 냉각시키고, TFA (0.1 ml)를 첨가하였다. 이어서, 용액을 농축시키고, DMSO (2 ml) 중에 재현탁시켰다. 생성된 잔류물을 역상 HPLC (아세토니트릴/물 (0.1% TFA 개질제 함유))에 의해 정제하여 트랜스-4-((1R 또는 1S)-(5-(3-시클로프로필-5-(4-(트리플루오로메틸)피리미딘-2-일아미노)페닐)티아졸-2-일)-1-히드록시에틸)시클로헥산카르복실산을 TFA 염으로서 수득하였다.
실시예 17
트랜스-4-{(1R 또는 1S)-1-[5-(3-플루오로-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산
단계 1: 3-플루오로-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)아닐린 (3.3 g, 14.00 mmol) 및 2-클로로-4-(트리플루오로메틸)피리미딘 (2.94 g, 16.10 mmol)이 들은 플라스크에 디옥산 (44 mL) 및 메탄술폰산 (1.55 g, 16.10 mmol)을 첨가하였다. 반응 혼합물을 100℃에서 밤새 가열하였다. 이어서, 반응 혼합물을 실온으로 냉각시키고, 에틸 아세테이트로 희석하고, 물로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 감압 하에 농축시켰다. 잔류물을 실리카 겔 상에서 크로마토그래피에 의해 정제하여 N-[3-플루오로-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 2: 2-5 mL 마이크로웨이브 바이알에 N-[3-플루오로-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (20 mg, 0.052 mmol), 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산 - (1S,2S)-2-(메틸아미노)-1-페닐프로판-1-올 (1:1) (26.1 mg, 0.052 mmol), PdCl2(dppf) (7.64 mg, 10.44 μmol), 탄산칼륨 (21.64 mg, 0.157 mmol), 디옥산 (870 μl) 및 물 (174 μl)을 첨가하였다. 바이알을 밀봉하고, 3 주기의 배기 및 아르곤 플러싱을 통해 아르곤을 넣은 다음, 80℃로 2시간 동안 가열하였다. 생성된 혼합물을 셀라이트 플러그를 통해 여과한 다음, 고체를 EtOAc로 세척하였다. 여과물을 농축시켜 갈색 고체를 수득하였다. 잔류물을 고압 액체 크로마토그래피 (물/아세토니트릴 (0.1% TFA 개질제 함유))에 의해 정제한 다음, 동결건조시켜 트랜스-4-{(1R 또는 1S)-1-[5-(3-플루오로-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산의 TFA 염을 담갈색 분말로서 수득하였다.
실시예 18
트랜스-4-((1R 또는 1S)-{5-[3-(디플루오로메틸)-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐]-1,3-티아졸-2-일}-1-히드록시에틸)시클로헥산카르복실산
단계 1: 3-브로모-5-니트로벤즈알데히드 (501 mg, 2.178 mmol)를 DCM (1.7 ml) 중에 용해시키고, 0℃로 냉각시켰다. 데옥소플루오르 (2ml, 10.85 mmol)를 적가하고, 반응물을 실온으로 가온되도록 하고, 실온에서 18시간 동안 교반하였다. 생성된 용액을 포화 중탄산나트륨에 붓고, 디클로로메탄으로 추출하였다. 유기 상을 농축시키고, 실리카 겔 상에서 정제하여 1-브로모-3-(디플루오로메틸)-5-니트로벤젠을 수득하였다.
단계 2: EtOH (7 ml) 중 1-브로모-3-(디플루오로메틸)-5-니트로벤젠 (418.4 mg, 1.660 mmol)의 용액에 물 (3.5 ml), 철 (500 mg, 8.95 mmol) 및 염화암모늄 (46 mg, 0.860 mmol)을 첨가하였다. 이어서, 혼합물을 95℃로 6시간 동안 가열하고, 물로 희석하고, EtOAc로 추출하였다. 유기 상을 농축시켜 잔류물을 수득하였으며, 이를 실리카 겔 (헥산/EtOAc=8/2) 상에서 정제하여 3-브로모-5-(디플루오로메틸)아닐린을 수득하였다.
단계 3: 디옥산 (4 ml) 중 2-클로로-4-(트리플루오로메틸)피리미딘 (0.297 g, 1.626 mmol)의 용액을 3-브로모-5-(디플루오로메틸)아닐린 (0.314 g, 1.414 mmol)에 첨가하고, 이어서 메탄술폰산 (0.11 ml, 1.694 mmol)을 첨가하고, 생성된 용액을 100℃로 밤새 가열하였다. 반응물을 물로 희석하고, EtOAc로 추출하였다. 유기 상을 포화 중탄산나트륨, 물로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (EtOAc/헥산=2/8)에 의해 정제하여 N-[3-브로모-5-(디플루오로메틸)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 4: N-[3-브로모-5-(디플루오로메틸)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (443 mg, 1.203 mmol), 4,4,4',4',5,5,5',5'-옥타메틸-2,2'-비-1,3,2-디옥사보롤란 (458 mg, 1.805 mmol), 아세트산칼륨 (354 mg, 3.61 mmol) 및 PdCl2(dppf)-CH2Cl2 부가물 (197 mg, 0.241 mmol)을 디옥산 (5 ml) 중에 용해시켰다. 혼합물을 배기시키고, 질소로 5회 퍼징한 다음, 100℃로 밤새 가열하였다. 혼합물을 여과하고, EtOAc 및 물로 세척하였다. 유기 상을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 (헥산/EtOAc=7/3) 상에서 정제하여 N-[3-(디플루오로메틸)-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 5: 바이알에 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실산 - (1S,2S)-2-(메틸아미노)-1-페닐프로판-1-올 (1:1) (115 mg, 0.231 mmol), N-[3-(디플루오로메틸)-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (80 mg, 0.193 mmol), PdCl2(dppf) (24.4 mg, 0.033 mmol), 1,4-디옥산 (2 ml) 및 탄산나트륨 (물 중 2 M, 0.3 ml, 0.600 mmol)을 첨가하였다. 혼합물을 배기시키고, 질소로 5회 퍼징한 다음, 80℃로 2시간 동안 가열하였다. 혼합물을 여과하고, 역상 HPLC (아세토니트릴/물 (0.1% TFA 개질제 함유)) 상에서 정제하여 트랜스-4-((1R 또는 1S-{5-[3-(디플루오로메틸)-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐]-1,3-티아졸-2-일}-1-히드록시에틸)시클로헥산카르복실산의 TFA 염을 수득하였다.
실시예 19
트랜스-4-{(1R 또는 S)-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산 (실시예 1, 보다 빠른 용리 이성질체)
단계 1: CH2Cl2 (150 mL) 중 트랜스-4-(부톡시카르보닐)시클로헥산카르복실산 (문헌 [J. Chem. Soc., Perkin Trans. 1, 1999, 20, 3023]) (18.9 g, 83 mmol)의 질소 하에 환기 및 냉각된 용액 (0℃)에 촉매량의 DMF (30 μL)에 이어서 옥살릴 클로라이드 (7.97 mL, 91 mmol)를 첨가하였다. 이어서, 반응 혼합물을 실온으로 천천히 가온되도록 하고, 이 온도에서 이것을 14시간 동안 교반하였으며, 이 시점에 이것을 황색 오일로 농축시키고, 진공 하에 3시간 동안 건조시켰다. 주로 부틸 트랜스-4-(클로로카르보닐)시클로헥산카르복실레이트로 이루어진 잔류물을 THF (200 mL)로 희석하고, 빙조에서 냉각시켰다. 이 용액에 PdCl2(dppf)-CH2Cl2 (3.38 g, 4.14 mmol, 5 mol%)에 이어서 디메틸 아연 (PhCH3 중 2 M, 29 mL, 58 mmol, 0.7 당량)을 내부 온도가 15℃를 초과하지 않도록 하는 속도로 첨가하였다. 이어서, 냉각 조를 제거하고, 실온에서 2시간 동안 교반한 후, 반응 혼합물을 0℃로 재냉각시키고, 이 온도에서 이것을 H2O로 조심스럽게 희석하였다. 초기 발열이 진정된 후, 충분한 1N HCl 및 EtOAc를 도입하여 균질한 2상 혼합물이 형성되도록 하였다. 층을 분리하고, 유기부를 H2O로 재차 세척한 다음, MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 부틸 트랜스-4-아세틸시클로헥산카르복실레이트를 비-점성 오렌지색 오일로서 수득하였다.
단계 2: iPrMgCl-LiCl (THF 중 1.3 M, 55.2 mL, 71.8 mmol)이 들은 질소 하에 냉각된 (0℃) 플라스크에 내부 온도를 < 10℃로 유지하면서 티아졸 (5.10 mL, 71.8 mmol)을 첨가하였다. 생성된 불균질 혼합물을 실온으로 가온하고, 이 온도에서 이것을 10분 동안 교반한 다음, -20℃로 재냉각시켰다. 이어서, THF (20 + 5 mL) 중 부틸 트랜스-4-아세틸시클로헥산카르복실레이트 (12.5 g, 55.2 mmol)의 용액을 시린지를 통해 첨가하였다. 이어서, 냉각 조를 제거하고, 반응 혼합물을 10℃로 천천히 가온하였고, 이 동안 이것은 거의 완전히 균질화되는 것으로 관찰되었다. 40분 후, 포화 수성 NH4Cl에 이어서 EtOAc를 첨가하고, 층을 분리하고, 유기부를 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 부틸 트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트를 담황색 오일로서 수득하였다.
단계 3: DMF (84 mL) 중 부틸 트랜스-4-[1-히드록시-1-(1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트 (10.5 g, 33.7 mmol)의 용액에 NBS (6.90 g, 38.8 mmol)를 첨가하고, 생성된 혼합물을 55℃로 60분 동안 가열하였다. 이어서, 가열을 중단하고, 아황산나트륨 (2 g)을 함유하는 물 (30 mL)을 첨가하여 반응 혼합물을 탈색시켰으며, 이를 후속적으로 물 및 EtOAc로 추가로 희석하였다. 층을 분리하고, 유기부를 물로 재차 세척한 다음, MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 라세미 부틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트를 무색 오일로서 수득하였다. 이어서, 부틸 트랜스-4-[1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트를 키랄 초임계 유체 크로마토그래피 (키랄 AD-H 칼럼, 40:60% 메탄올:CO2, 12분 실행시간)에 의해 분리하여 99% ee 초과로 부틸 트랜스-4-[(1R)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸] 시클로헥산카르복실레이트 및 부틸 트랜스-4-[(1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (Rt = 5.57 min 및 7.86 min) 둘 다를 수득하였다. 이어서, 단리된 보다 느린 용리 거울상이성질체 (Rt = 7.86 min)를 나머지 합성 동안 사용하였다 (절대 입체화학은 알려지지 않음).
단계 4: 2-메틸-THF (70 mL) 및 수성 Na2CO3 (2 M, 17.9 mL, 35.9 mmol)을 플라스크에 첨가하고, N2로 탈기하였다. 상기 혼합물에 N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (7.48 g, 19.7 mmol), 부틸 트랜스-4-[(1R 또는 1S)-1-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (Rt = 7.86 min, 7 g, 17.9 mmol) 및 PdCl2(dppf)-CH2Cl2 (0.73 g, 0.90 mmol, 5 mol%)를 첨가하였다. 생성된 혼합물을 75℃로 가열하였으며, 이 온도에서 이것을 18시간 동안 교반한 다음, 실온으로 냉각시키고, H2O 및 EtOAc로 희석하고, H2O 및 EtOAc 둘 다로 세척하면서 셀라이트의 패드를 통해 여과하였다. 층을 분리하고, 수성 층을 EtOAc로 역추출한 다음, 합한 유기부를 MgSO4로 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 부틸 트랜스-4-{(1R 또는 S)-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트를 점성 황색 오일로서 수득하였다.
단계 5: MeOH (88 mL) 중 부틸 트랜스-4-{(1R 또는 S)-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실레이트 (8.8 g, 15.6 mmol)에 NaOH (H2O 중 1.0M, 54.7 mL, 54.7 mmol)를 첨가하고, 생성된 불균질 혼합물을 70℃로 가열하였다. 1.5시간 후, 반응 혼합물에서 열을 제거하고, 냉각시켰다. 55℃에 도달 시, HCl (H2O 중 1.0M, 55 mL, 55 mmol)을 적가하여 결정화를 유발하였다. 불균질 혼합물을 실온에서 3시간 동안 교반한 다음, 여과하고, 물로 2회 세척하였다. 목적 생성물을 질소 백 하에 14시간 동안 건조시켜 트랜스-4-{(1R 또는 S)-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}-페닐)-1,3-티아졸-2-일]에틸}시클로헥산카르복실산을 담황색 고체로서 수득하였다.
실시예 20
트랜스-4-[(1R 또는 S)-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산 (화합물 2-52)
단계 1: 2-메틸-THF (150 mL) 및 수성 Na2CO3 (2 M, 38.4 mL, 77 mmol)을 플라스크에 첨가하고, N2로 탈기하였다. 상기 혼합물에 4-메틸-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민 (13.75 g, 42.3 mmol), 부틸 트랜스-4-[(1R 또는 S)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (실시예 19, 단계 3, Rt = 7.86 min) (15 g, 38.4 mmol) 및 PdCl2(dppf)-CH2Cl2 (1.57 g, 1.92 mmol, 5 mol%)를 첨가하였다. 생성된 혼합물을 75℃로 가열하고, 5시간 동안 교반한 다음, 실온으로 냉각시키고, H2O 및 EtOAc로 희석한 다음, H2O 및 EtOAc 둘 다로 세척하면서 셀라이트의 패드를 통해 여과하였다. 층을 분리하고, 수성 층을 EtOAc로 역추출한 다음, 합한 유기부를 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 부틸 트랜스-4-[(1R 또는 S)-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트 (84 중량%)를 점성 황색 오일로서 수득하였다.
단계 2: MeOH (212 mL) 중 부틸 트랜스-4-[(1R 또는 S)-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실레이트 (21.8 g, 84 중량%, 35 mmol)의 용액에 1N NaOH (122 mL, 122 mmol)를 첨가하고, 생성된 불균질 혼합물을 70℃로 가열하였다. 1.5시간 후, 반응 혼합물에서 열을 제거하고, 55℃로 냉각시켰다. 이어서, 1N HCl (122 mL, 122 mmol)을 적가하여 결정화의 유발을 개시하였다. 불균질 혼합물을 실온에서 2시간 동안 교반한 다음, 여과하고, 물로 2회 세척하였다. 목적 생성물을 질소 백 하에 14시간 동안 건조시켜 트랜스-4-[(1R 또는 S)-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산을 백색 고체로서 수득하였다. 이 물질을 EtOAc (300 mL) 중에 녹이고, 생성된 슬러리를 55℃로 가열하고, 1시간 동안 교반하였다. 실온으로 냉각시킨 후, 혼합물을 여과하고, 케이크를 헥산으로 세척한 다음, 질소 백 하에 18시간 동안 건조시켜 트랜스-4-[(1R 또는 S)-히드록시-1-(5-{3-메틸-5-[(4-메틸피리미딘-2-일)아미노]페닐}-1,3-티아졸-2-일)에틸]시클로헥산카르복실산을 백색 고체로서 수득하였다.
실시예 21
트랜스-4-{(1R 또는 S)-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산 (화합물 2-77)
단계 1: 디플루오로아세트산 무수물 (72.9 mL, 586 mmol) 및 디클로로메탄 (488 mL)이 들은 3구 플라스크를 -30℃로 냉각시켰다. 피리딘 (52.1 ml, 645 mmol) 및 에틸 비닐 에테르 (64.8 ml, 674 mmol)의 혼합물을 첨가 깔때기를 통해 적가하여 내부 온도를 -20℃ 초과가 되지 않도록 유지하였다. 첨가가 완결된 후, 혼합물을 주위 온도로 밤새 천천히 가온하였다. 이어서, 반응물을 디클로로메탄 (500 mL)으로 물 (500 mL)과 함께 희석하였다. 디클로로메탄 층을 건조시키고, 여과하고, 감압 (30℃에서 300 mbar) 하에 약 150 mL의 부피로 농축시킨 다음, 단계 3에 직접 사용하였다.
단계 2: EtOH (760 mL) 중 3-브로모-5-메틸아닐린 (170 g, 914 mmol)에 시아나미드 (물 중 50 중량%, 82 mL, 1050 mmol) 및 질산 (70%, 64.2 mL, 1005 mmol)을 첨가하였다. 혼합물을 90℃에서 밤새 환류한 다음, 주위 온도로 냉각시켰다. 반응물을 진공 하에 약 600 mL로 농축시킨 다음, 차가운 에테르 (1500 mL)를 격렬히 교반하면서 첨가하였다. 생성된 침전물을 여과하고, 150 mL 에테르로 세척하여 1-(3-브로모-5-메틸페닐)구아니딘 니트레이트를 수득하였다.
단계 3: EtOH (604 ml) 중 단계 1로부터의 (3E)-4-에톡시-1,1-디플루오로부트-3-엔-2-온 (79 g, 527 mmol, DCM 함유), 1-(3-브로모-5-메틸페닐)구아니딘 니트레이트 (123 g, 423 mmol) 및 탄산칼륨 (117 g, 845 mmol)의 혼합물을 85℃에서 1시간 동안 가열한 다음, 주위 온도로 천천히 냉각시켰다. 얼음 물 (2L)을 혼합물에 첨가하고, 15분 동안 교반하였다. 생성된 침전물을 여과하고, 밤새 건조시켜 N-(3-브로모-5-메틸페닐)-4-(디플루오로메틸)피리미딘-2-아민을 수득하였다.
단계 4: 디옥산 (520 mL) 중 N-(3-브로모-5-메틸페닐)-4-(디플루오로메틸)피리미딘-2-아민 (98 g, 312 mmol), 비스(피나콜로에이토)디보론 (91 g, 359 mmol), Pd(dppf)Cl2·CH2Cl2 (12.74 g, 15.6 mmol) 및 아세트산칼륨 (77 g, 780 mmol)의 혼합물을 N2로 10분 동안 탈기한 다음, 85℃로 22시간 동안 가열하였다. 실온으로 냉각시킨 후, 물 및 EtOAc를 첨가하였다. 유기 층을 물 및 염수로 세척하고, 황산마그네슘 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 상에서 칼럼 크로마토그래피 (750 g, hex 중 0-50% EtOAc)에 의해 정제하여 4-(디플루오로메틸)-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민을 수득하였다.
단계 5: 2-메틸-THF (964 mL) 및 수성 탄산나트륨 (2 M, 247 mL, 494 mmol)을 플라스크에 첨가하고, N2로 탈기하였다. 상기 혼합물에 4-(디플루오로메틸)-N-[3-메틸-5-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]피리미딘-2-아민 (94 g, 259 mmol), 부틸 트랜스-4-[(1R 또는 S)-(5-브로모-1,3-티아졸-2-일)-1-히드록시에틸]시클로헥산카르복실레이트 (실시예 19, 단계 3, Rt = 7.86 min) (96.3 g, 247 mmol) 및 PdCl2(dppf)-CH2Cl2 (10.1 g, 12.3 mmol, 5 mol%)를 첨가하였다. 생성된 혼합물을 75℃로 가열하고, 3시간 동안 교반한 다음, 실온으로 냉각시키고, H2O 및 EtOAc로 희석한 다음, H2O 및 EtOAc 둘 다로 세척하면서 셀라이트의 패드를 통해 여과하였다. 층을 분리하고, 수성 층을 EtOAc로 역추출한 다음, 합한 유기부를 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 잔류물을 실리카 상에 흡착시키고, 플래쉬 크로마토그래피에 의해 정제하여 부틸 트랜스-4-{(1R 또는 S)-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실레이트를 점성 황색 오일로서 수득하였다.
단계 6: MeOH (1493 mL) 중 부틸 트랜스-4-{(1R 또는 S)-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실레이트 (113 g, 208 mmol)의 용액에 NaOH (H2O 중 1 M, 726 mL, 726 mmol)를 첨가하고, 생성된 불균질 혼합물을 70℃로 가열하였다. 1시간 후, 반응 혼합물에서 열을 제거하고, 냉각시켰다. 55℃에 도달 시, HCl (H2O 중 1 M, 726 mL, 726 mmol)을 적가하여 결정화의 유발을 개시하였다. 불균질 혼합물을 실온에서 1시간 동안 교반한 다음, 여과하고, 물로 2회 세척하였다. 필터 케이크를 질소 백 하에 14시간 동안 건조시킨 다음, EtOAc (1.8 L) 중에 녹이고, 생성된 슬러리를 환류 하에 가열하고, 2시간 동안 교반하였다. 60℃로 냉각시킨 후, 헥산 (1.8 L)을 20분에 걸쳐 첨가한 다음, 반응 혼합물을 실온으로 냉각시키고, 여과하고, 케이크를 헥산 (2x 400 mL)으로 세척한 다음, 질소 백 하에 18시간 동안 건조시켜 트랜스-4-{(1R 또는 S)-[5-(3-{[4-(디플루오로메틸)피리미딘-2-일]아미노}-5-메틸페닐)-1,3-티아졸-2-일]-1-히드록시에틸}시클로헥산카르복실산을 담황색 고체로서 수득하였다.
실시예 22
1,4-디옥사스피로[4.5]데크-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메탄올
메탄올 (5 mL) 중 1,4-디옥사스피로[4.5]데크-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메타논 (실시예 1-20) (100 mg, 0.20 mmol)의 용액에 수소화붕소나트륨 (22.5 mg, 0.60 mmol)을 첨가하였다. 1시간 후, 물을 조심스럽게 첨가한 다음, 에틸 아세테이트 및 물로 희석하였다. 유기 층을 분리하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 실리카 겔 상에서 플래쉬 크로마토그래피 (헥산을 사용한 0-100% 에틸 아세테이트 구배)하여 1,4-디옥사스피로[4.5]데크-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메탄올을 수득하였다.
실시예 23
4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산올
단계 1: 리튬 디이소프로필 아미드 (테트라히드로푸란/헵탄/에틸벤젠 중 1.8 M, 3.96 mL, 7.14 mmol)를 -78℃에서 THF (5 mL) 중 N-[3-메틸-5-(1,3-티아졸-5-일)페닐]-4-(트리플루오로메틸)피리미딘-2-아민 (800 mg, 2.38 mmol)의 용액에 첨가하였다. -78℃에서 30분 후, THF (8 mL) 중 N-메톡시-N-메틸-1,4-디옥사스피로[4.5]데칸-8-카르복스아미드 (1.09 g, 4.76 mmol)의 용액을 천천히 첨가하고, 반응물을 실온으로 가온되도록 한 다음, 16시간 동안 교반하였다. 반응물을 물에 이어서 에틸 아세테이트 및 염수로 조심스럽게 희석하였다. 유기 층을 분리하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. HPLC (아세토니트릴/물 (0.1% TFA 개질제 함유))에 의해 정제하여 1,4-디옥사스피로[4.5]데크-8-일[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]메타논 및 4-{[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]카르보닐}시클로헥사논의 혼합물을 수득하였으며, 이를 추가의 정제 없이 후속 단계에 사용하였다.
단계 2: 메틸마그네슘 브로마이드 (디에틸 에테르 중 3.0 M, 0.2 mL, 0.60 mmol)를 0℃에서 디클로로메탄 (5 mL) 중 단계 1로부터의 생성물 (190 mg, 0.42 mmol)의 용액에 첨가하였다. 이어서, 반응물을 실온으로 가온하고, 3일 동안 교반하였다. 이어서, 반응물을 0℃로 냉각시키고, 추가량의 메틸마그네슘 브로마이드 (디에틸 에테르 중 3.0 M, 0.2 mL, 0.60 mmol)를 첨가하였다. 이어서, 반응물을 물에 이어서 디클로로메탄 및 포화 수성 염화암모늄으로 조심스럽게 희석하였다. 유기 층을 분리하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. HPLC (아세토니트릴/물 (개질제로서 0.1% TFA 함유))에 의해 정제하여 목적 분획을 수득하였으며, 이를 합한 다음, 에틸 아세테이트 및 포화 수성 중탄산나트륨으로 희석하였다. 유기 층을 분리하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 4-{1-히드록시-1-[5-(3-메틸-5-{[4-(트리플루오로메틸)피리미딘-2-일]아미노}페닐)-1,3-티아졸-2-일]에틸}-1-메틸시클로헥산올을 이성질체의 혼합물로서 수득하였다.
Claims (14)
- 하기 화학식 I의 화합물 또는 그의 제약상 허용되는 염.
<화학식 I>
상기 식에서,
A는 카르보사이클이거나, 또는
모이어티 A-(R7)n(R8)은 1,4-디옥사스피로[4.5]데실을 나타내고;
n은 0, 1, 2 또는 3이고;
R1은 C1 - 4알킬, C1 - 4플루오로알킬, C3 - 6시클로알킬 또는 C1 - 4알콕시이고;
R2는 H 또는 할로겐이고;
R3은 H, 할로겐, C1 - 4알킬, C1 - 4할로알킬, C3 - 6시클로알킬 또는 C1 - 4히드록시알킬이고;
R4는 H 또는 할로겐이고;
R5는 H, OH, C1 - 4알콕시, 할로겐 또는 NH2이고;
R6은 H, C1 - 4알킬, C1 - 4할로알킬, C3 - 6시클로알킬 또는 C1 - 4히드록시알킬이거나; 또는
R5 및 R6은 함께 옥소이고;
R7은 OH 및 C1 - 4알킬로부터 선택되고;
R8은 (CRaRb)nCO2Rc, CONRdRe, 테트라졸릴, OH, CH2OH, 옥소, CN, NHCO2Rf 및 NHSO2Rf로부터 선택되며; 단 R8 및 -C(R5)(R6)-은 동일한 고리 탄소 원자에 부착되지 않고;
Ra 및 Rb는 각각 독립적으로 H 및 메틸로부터 선택되고;
Rc는 H 또는 C1 - 4알킬이고;
Rd 및 Re는 각각 독립적으로 H 및 C1 - 4알킬로부터 선택되고;
Rf는 C1 - 4알킬 또는 벤질이다. - 제1항에 있어서, 고리 A가 카르보사이클인 화합물 또는 그의 제약상 허용되는 염.
- 제1항에 있어서, R1이 C1 - 4알킬 또는 C1 - 4플루오로알킬인 화합물 또는 그의 제약상 허용되는 염.
- 제1항에 있어서, R5가 OH인 화합물 또는 그의 제약상 허용되는 염.
- 제1항에 있어서, A가 카르보사이클이고, R8이 (CRaRb)nCO2Rc 및 C(O)NRdRe로부터 선택된 것인 화합물 또는 그의 제약상 허용되는 염.
- 제7항에 있어서, R8이 CO2Rc인 화합물 또는 그의 제약상 허용되는 염.
- 치료 유효량의 제1항의 화합물 또는 그의 제약상 허용되는 염 및 제약상 허용되는 담체를 포함하는 제약 조성물.
- Syk-매개 질환의 치료 또는 예방이 필요한 환자에게 치료 유효량의 제1항의 화합물 또는 그의 제약상 허용되는 염을 투여하는 것을 포함하는, Syk-매개 질환의 치료 또는 예방을 위한 방법.
- 제11항에 있어서, 상기 질환이 천식 또는 COPD인 방법.
- 제11항에 있어서, 상기 질환이 류마티스 관절염인 방법.
- 제11항에 있어서, 상기 질환이 암인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161484418P | 2011-05-10 | 2011-05-10 | |
| US61/484,418 | 2011-05-10 | ||
| PCT/US2012/036423 WO2012154519A1 (en) | 2011-05-10 | 2012-05-04 | Aminopyrimidines as syk inhibitors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140028062A true KR20140028062A (ko) | 2014-03-07 |
Family
ID=47139531
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137032289A Withdrawn KR20140028062A (ko) | 2011-05-10 | 2012-05-04 | Syk 억제제로서의 아미노피리미딘 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9290490B2 (ko) |
| EP (1) | EP2706853B1 (ko) |
| JP (1) | JP2014513686A (ko) |
| KR (1) | KR20140028062A (ko) |
| CN (1) | CN103619172A (ko) |
| AU (1) | AU2012253885A1 (ko) |
| BR (1) | BR112013028900A2 (ko) |
| CA (1) | CA2834604A1 (ko) |
| MX (1) | MX2013013090A (ko) |
| RU (1) | RU2013154412A (ko) |
| WO (1) | WO2012154519A1 (ko) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2612217C2 (ru) | 2011-05-04 | 2017-03-03 | Мерк Шарп И Доум Корп. | Аминопиридинсодержащие ингибиторы тирозинкиназы селезенки (syk) |
| WO2012154518A1 (en) | 2011-05-10 | 2012-11-15 | Merck Sharp & Dohme Corp. | Bipyridylaminopyridines as syk inhibitors |
| KR20140028062A (ko) | 2011-05-10 | 2014-03-07 | 머크 샤프 앤드 돔 코포레이션 | Syk 억제제로서의 아미노피리미딘 |
| US9120785B2 (en) | 2011-05-10 | 2015-09-01 | Merck Sharp & Dohme Corp. | Pyridyl aminopyridines as Syk inhibitors |
| WO2013192128A1 (en) | 2012-06-20 | 2013-12-27 | Merck Sharp & Dohme Corp. | Imidazolyl analogs as syk inhibitors |
| EP2863914B1 (en) | 2012-06-20 | 2018-10-03 | Merck Sharp & Dohme Corp. | Pyrazolyl derivatives as syk inhibitors |
| WO2013192098A1 (en) | 2012-06-22 | 2013-12-27 | Merck Sharp & Dohme Corp. | SUBSTITUTED PYRIDINE SPLEEN TYROSINE KINASE (Syk) INHIBITORS |
| US9416111B2 (en) | 2012-06-22 | 2016-08-16 | Merck Sharp & Dohme Corp. | Substituted diazine and triazine spleen tyrosine kinease (Syk) inhibitors |
| WO2014031438A2 (en) | 2012-08-20 | 2014-02-27 | Merck Sharp & Dohme Corp. | SUBSTITUTED PHENYL SPLEEN TYROSINE KINASE (Syk) INHIBITORS |
| US9586931B2 (en) | 2012-09-28 | 2017-03-07 | Merck Sharp & Dohme Corp. | Triazolyl derivatives as Syk inhibitors |
| US9624210B2 (en) | 2012-12-12 | 2017-04-18 | Merck Sharp & Dohme Corp. | Amino-pyrimidine-containing spleen tyrosine kinase (Syk) inhibitors |
| EP2934525B1 (en) | 2012-12-21 | 2019-05-08 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminopyridines as spleen tyrosine kinase inhibitors |
| US9499534B2 (en) | 2013-04-26 | 2016-11-22 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminopyrimidines as spleen tyrosine kinase inhibitors |
| EP2988744A4 (en) * | 2013-04-26 | 2016-11-02 | Merck Sharp & Dohme | THIAZOLSUBSTITUTED AMINOHETEROARYLE AS MILZTYROSINKINASE INHIBITOR |
| SG11201600373YA (en) * | 2013-07-31 | 2016-02-26 | Gilead Sciences Inc | Syk inhibitors |
| EP3082807B1 (en) | 2013-12-20 | 2018-07-04 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors |
| US9670196B2 (en) | 2013-12-20 | 2017-06-06 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminoheteroaryls as Spleen Tyrosine Kinase inhibitors |
| WO2015095445A1 (en) | 2013-12-20 | 2015-06-25 | Merck Sharp & Dohme Corp. | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors |
| US9775839B2 (en) | 2014-03-13 | 2017-10-03 | Merck Sharp & Dohme Corp. | 2-pyrazine carboxamides as spleen tyrosine kinase inhibitors |
| CN104262157B (zh) * | 2014-09-19 | 2016-01-13 | 江西仁明医药化工有限公司 | 3-乙酰基环戊烷羧酸甲酯顺、反异构体的控制方法 |
| TW201822764A (zh) | 2016-09-14 | 2018-07-01 | 美商基利科學股份有限公司 | Syk抑制劑 |
| CA3036384A1 (en) | 2016-09-14 | 2018-03-22 | Gilead Sciences, Inc. | Syk inhibitors |
| WO2018195471A1 (en) | 2017-04-21 | 2018-10-25 | Gilead Sciences, Inc. | Syk inhibitors in combination with hypomethylating agents |
| CN108794331A (zh) * | 2018-07-23 | 2018-11-13 | 蚌埠中实化学技术有限公司 | 一种3-乙酰基环戊基甲酸甲酯的制备方法 |
| JP2022526713A (ja) | 2019-03-21 | 2022-05-26 | オンクセオ | がんの処置のための、キナーゼ阻害剤と組み合わせたDbait分子 |
| JP2023500906A (ja) | 2019-11-08 | 2023-01-11 | インサーム(インスティテュ ナシオナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシェ メディカル) | キナーゼ阻害剤に対する獲得抵抗性を有するがんの処置方法 |
| WO2021148581A1 (en) | 2020-01-22 | 2021-07-29 | Onxeo | Novel dbait molecule and its use |
Family Cites Families (83)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5710129A (en) | 1995-02-23 | 1998-01-20 | Ariad Pharmaceuticals, Inc. | Inhibitors of SH2-mediated processes |
| AU3578695A (en) | 1995-10-02 | 1997-04-28 | Eisai Co. Ltd. | Acridone derivative |
| US5958957A (en) * | 1996-04-19 | 1999-09-28 | Novo Nordisk A/S | Modulators of molecules with phosphotyrosine recognition units |
| EP0920426B9 (de) * | 1996-08-26 | 2005-04-06 | ALTANA Pharma AG | Neue thiazol-derivate mit phosphodiesterase inhibierender wirkung |
| ATE401312T1 (de) | 1997-12-15 | 2008-08-15 | Astellas Pharma Inc | Pyrimidin-5-carboxamid-derivate |
| ES2391550T3 (es) | 1999-04-15 | 2012-11-27 | Bristol-Myers Squibb Company | Inhibidores cíclicos de la proteína tirosina quinasa |
| WO2000075113A1 (en) | 1999-06-09 | 2000-12-14 | Yamanouchi Pharmaceutical Co., Ltd. | Novel heterocyclic carboxamide derivatives |
| GB9918035D0 (en) | 1999-07-30 | 1999-09-29 | Novartis Ag | Organic compounds |
| CN1615873A (zh) | 1999-12-24 | 2005-05-18 | 阿文蒂斯药物有限公司 | 氮杂吲哚类化合物 |
| JP2001302667A (ja) | 2000-04-28 | 2001-10-31 | Bayer Ag | イミダゾピリミジン誘導体およびトリアゾロピリミジン誘導体 |
| US6248790B1 (en) | 2000-06-29 | 2001-06-19 | Parker Hughes Institute | Treatment of inflammation with 2,4,6-trihydroxy-alpha-rho-methoxyphenylacetophenone, or its pharmaceutically acceptable derivatives |
| WO2002096905A1 (en) | 2001-06-01 | 2002-12-05 | Vertex Pharmaceuticals Incorporated | Thiazole compounds useful as inhibitors of protein kinases |
| EP1397142A4 (en) | 2001-06-19 | 2004-11-03 | Bristol Myers Squibb Co | PYRIMIDINE PHOSPHODIESTERASE (PDE) INHIBITORS 7 |
| GB0115109D0 (en) | 2001-06-21 | 2001-08-15 | Aventis Pharma Ltd | Chemical compounds |
| MXPA03011998A (es) | 2001-06-23 | 2005-07-01 | Aventis Pharma Inc | Pirrolopirimidinas como inhibidores de protein cinasa. |
| US6897208B2 (en) | 2001-10-26 | 2005-05-24 | Aventis Pharmaceuticals Inc. | Benzimidazoles |
| JP2005247690A (ja) | 2002-01-08 | 2005-09-15 | Nippon Nohyaku Co Ltd | 6,6,6−トリフルオロ−3,5−ジオキソヘキサン酸エステル及びその互変異性体の製造方法 |
| TWI329105B (en) | 2002-02-01 | 2010-08-21 | Rigel Pharmaceuticals Inc | 2,4-pyrimidinediamine compounds and their uses |
| GB0206215D0 (en) | 2002-03-15 | 2002-05-01 | Novartis Ag | Organic compounds |
| EP1554269A1 (en) | 2002-07-09 | 2005-07-20 | Vertex Pharmaceuticals Incorporated | Imidazoles, oxazoles and thiazoles with protein kinase inhibiting activities |
| JP2004203748A (ja) | 2002-12-24 | 2004-07-22 | Kissei Pharmaceut Co Ltd | 新規なイミダゾ[1,2−c]ピリミジン誘導体、それを含有する医薬組成物およびそれらの用途 |
| JP2006519846A (ja) | 2003-03-10 | 2006-08-31 | シェーリング コーポレイション | 複素環式キナーゼインヒビター:使用および合成の方法 |
| JP2006524688A (ja) | 2003-03-25 | 2006-11-02 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼのインヒビターとして有用なチアゾール |
| ATE396731T1 (de) | 2003-03-25 | 2008-06-15 | Vertex Pharma | Thiazole zur verwendung als inhibitoren von protein-kinasen |
| MXPA05012281A (es) * | 2003-05-14 | 2006-05-19 | Torreypines Therapeutics Inc | Compuestos y uso de los mismos en la modulacion beta amiloide. |
| JP4886511B2 (ja) | 2003-07-30 | 2012-02-29 | ライジェル ファーマシューティカルズ, インコーポレイテッド | 2,4−ピリミジンジアミン化合物による自己免疫疾患の治療または予防方法 |
| DE602004032446D1 (de) | 2003-08-07 | 2011-06-09 | Rigel Pharmaceuticals Inc | 2,4-pyrimidindiamin-verbindungen und verwendungen als antiproliferative mittel |
| TWI339206B (en) | 2003-09-04 | 2011-03-21 | Vertex Pharma | Compositions useful as inhibitors of protein kinases |
| ATE399165T1 (de) | 2003-09-12 | 2008-07-15 | Rigel Pharmaceuticals Inc | Chinolinverbindungen und deren verwendungen |
| GB0321710D0 (en) | 2003-09-16 | 2003-10-15 | Novartis Ag | Organic compounds |
| AU2004297235A1 (en) | 2003-12-04 | 2005-06-23 | Vertex Pharmaceuticals Incorporated | Quinoxalines useful as inhibitors of protein kinases |
| US7345043B2 (en) | 2004-04-01 | 2008-03-18 | Miikana Therapeutics | Inhibitors of histone deacetylase |
| WO2006004865A1 (en) | 2004-06-29 | 2006-01-12 | Rigel Pharmaceuticals, Inc. | 2-substituted quinoline compounds and their uses as inhibitors of the ige receptor signaling cascade |
| CN101044127A (zh) | 2004-08-23 | 2007-09-26 | 惠氏公司 | 用作纤溶酶原激活剂抑制剂-1的噻唑基-萘基酸 |
| EP1786783A1 (en) | 2004-09-01 | 2007-05-23 | Rigel Pharmaceuticals, Inc. | Synthesis of 2,4-pyrimidinediamine compounds |
| EP1817303A2 (en) | 2004-10-29 | 2007-08-15 | Rigel Pharmaceuticals, Inc. | Substituted pyridines with activity on syk kinase |
| DK1814878T3 (da) | 2004-11-24 | 2012-05-07 | Rigel Pharmaceuticals Inc | Spiro-2, 4-pyrimidindiamin-forbindelser og anvendelser deraf |
| US8604055B2 (en) | 2004-12-31 | 2013-12-10 | Dr. Reddy's Laboratories Ltd. | Substituted benzylamino quinolines as cholesterol ester-transfer protein inhibitors |
| KR101278397B1 (ko) | 2005-01-19 | 2013-06-25 | 리겔 파마슈티칼스, 인크. | 2,4-피리미딘디아민 화합물의 전구약물 및 이의 용도 |
| CN101166734A (zh) * | 2005-02-28 | 2008-04-23 | 日本烟草产业株式会社 | 具有Syk抑制活性的新型的氨基吡啶化合物 |
| WO2006093247A1 (ja) | 2005-02-28 | 2006-09-08 | Japan Tobacco Inc. | Syk阻害活性を有する新規なアミノピリジン化合物 |
| US7530158B2 (en) | 2005-04-19 | 2009-05-12 | Hitachi Global Storage Technologies Netherlands B.V. | CPP read sensor fabrication using heat resistant photomask |
| WO2006129100A1 (en) | 2005-06-03 | 2006-12-07 | Glaxo Group Limited | Novel compounds |
| SG137989A1 (en) | 2005-06-08 | 2008-01-28 | Rigel Pharmaceuticals Inc | Compositions and methods for inhibition of the JAK pathway |
| CA2607901C (en) | 2005-06-13 | 2016-08-16 | Rigel Pharmaceuticals, Inc. | Methods and compositions for treating degenerative bone disorders using a syk inhibitory 2,4-pyrimidinediamine |
| WO2007028445A1 (en) | 2005-07-15 | 2007-03-15 | Glaxo Group Limited | 6-indolyl-4-yl-amino-5-halogeno-2-pyrimidinyl-amino derivatives |
| WO2007009681A1 (en) | 2005-07-15 | 2007-01-25 | Glaxo Group Limited | 1 , 1-DIOXID0-2 , 3-DIHYDRO-l , 2-BENZISOTHIAZ0L-6-YL-1H-INDAZOL-4-YL-2 , 4-PYRIMIDINEDI AMINE DERIVATIVES |
| GB0515026D0 (en) | 2005-07-21 | 2005-08-31 | Novartis Ag | Organic compounds |
| JP2009511528A (ja) | 2005-10-13 | 2009-03-19 | グラクソ グループ リミテッド | Syk阻害物質としてのピロロピリミジン誘導体群 |
| US7713987B2 (en) | 2005-12-06 | 2010-05-11 | Rigel Pharmaceuticals, Inc. | Pyrimidine-2,4-diamines and their uses |
| EP1960372B1 (en) | 2005-12-15 | 2015-12-09 | Rigel Pharmaceuticals, Inc. | Kinase inhibitors and their uses |
| WO2007085540A1 (en) | 2006-01-27 | 2007-08-02 | Glaxo Group Limited | 1h-indaz0l-4-yl-2 , 4-pyrimidinediamine derivatives |
| CA2642211C (en) | 2006-02-17 | 2012-01-24 | Rigel Pharmaceuticals, Inc. | 2,4-pyrimidinediamine compounds for treating or preventing autoimmune diseases |
| JP2009530342A (ja) | 2006-03-20 | 2009-08-27 | エフ.ホフマン−ラ ロシュ アーゲー | Btkおよびsyk蛋白キナーゼを阻害する方法 |
| WO2007117692A2 (en) | 2006-04-11 | 2007-10-18 | Vertex Pharmaceuticals Incorporated | Thiazoles, imidazoles, and pyrazoles useful as inhibitors of protein kinases |
| NZ574621A (en) * | 2006-07-07 | 2012-03-30 | Boehringer Ingelheim Int | Phenyl substituted heteroaryl-derivatives and use thereof as anti-tumour agents |
| WO2008024634A1 (en) | 2006-08-25 | 2008-02-28 | Smithkline Beecham Corporation | Pyrimdine compounds useful as kinase inhibitors |
| PL2091918T3 (pl) | 2006-12-08 | 2015-02-27 | Novartis Ag | Związki i kompozycje jako inhibitory kinazy białkowej |
| US8268850B2 (en) | 2007-05-04 | 2012-09-18 | Irm Llc | Pyrimidine derivatives and compositions as C-kit and PDGFR kinase inhibitors |
| BRPI0814432A2 (pt) | 2007-07-17 | 2017-05-09 | Rigel Pharmaceuticals Inc | pirimidinadiaminas substituídas por amina cíclica como inibidores de pkc |
| CA2698511C (en) | 2007-09-04 | 2016-10-11 | The Scripps Research Institute | Substituted pyrimidinyl-amines as protein kinase inhibitors |
| WO2009031011A2 (en) | 2007-09-05 | 2009-03-12 | Pfizer Limited | Xinafoate salt of n4-(2, 2-difluoro-4h-benz0 [1,4] 0xazin-3-one) -6-yl] -5-fluoro-n2- [3- (methylaminocar bonylmethyleneoxy) phenyl] 2, 4-pyrimidinediamine |
| JPWO2009084695A1 (ja) | 2007-12-28 | 2011-05-19 | カルナバイオサイエンス株式会社 | 2−アミノキナゾリン誘導体 |
| TW200942537A (en) | 2008-02-01 | 2009-10-16 | Irm Llc | Compounds and compositions as kinase inhibitors |
| NZ587039A (en) | 2008-02-13 | 2013-01-25 | Gilead Connecticut Inc | 6-aryl-imidazo[1, 2-a]pyrazine derivatives, method of making, and method of use thereof |
| ES2617622T3 (es) | 2008-02-15 | 2017-06-19 | Rigel Pharmaceuticals, Inc. | Compuestos de pirimidin-2-amina y su uso como inhibidores de JAK cinasas |
| SG165655A1 (en) | 2008-04-16 | 2010-11-29 | Portola Pharm Inc | 2, 6-diamino- pyrimidin- 5-yl-carboxamides as syk or JAK kinases inhibitors |
| KR101623997B1 (ko) | 2008-04-16 | 2016-05-24 | 포톨라 파마슈티컬스, 인코포레이티드 | syk 또는 JAK 키나제 억제제로서의 2,6-디아미노-피리미딘-5-일-카르복스아미드 |
| JP2011518219A (ja) | 2008-04-22 | 2011-06-23 | ポートラ ファーマシューティカルズ, インコーポレイテッド | タンパク質キナーゼの阻害剤 |
| TWI453207B (zh) | 2008-09-08 | 2014-09-21 | Signal Pharm Llc | 胺基三唑并吡啶,其組合物及使用其之治療方法 |
| JP5412804B2 (ja) | 2008-11-19 | 2014-02-12 | 日産自動車株式会社 | 燃料電池スタック |
| JP5567587B2 (ja) | 2008-12-08 | 2014-08-06 | ギリアード コネチカット, インコーポレイテッド | イミダゾピラジンSyk阻害剤 |
| TW201105669A (en) * | 2009-07-30 | 2011-02-16 | Irm Llc | Compounds and compositions as Syk kinase inhibitors |
| EP2512246B1 (en) | 2009-12-17 | 2015-09-30 | Merck Sharp & Dohme Corp. | Aminopyrimidines as syk inhibitors |
| US8759366B2 (en) | 2009-12-17 | 2014-06-24 | Merck Sharp & Dohme Corp. | Aminopyrimidines as SYK inhibitors |
| AU2011206621B2 (en) | 2010-01-12 | 2016-04-14 | Ab Science | Thiazole and oxazole kinase inhibitors |
| EP2593107A1 (en) * | 2010-07-12 | 2013-05-22 | Merck Sharp & Dohme Corp. | Tyrosine kinase inhibitors |
| EP2441755A1 (en) | 2010-09-30 | 2012-04-18 | Almirall, S.A. | Pyridine- and isoquinoline-derivatives as Syk and JAK kinase inhibitors |
| CN103298788A (zh) | 2010-10-28 | 2013-09-11 | 日本新药株式会社 | 吡啶衍生物及医药 |
| RU2612217C2 (ru) | 2011-05-04 | 2017-03-03 | Мерк Шарп И Доум Корп. | Аминопиридинсодержащие ингибиторы тирозинкиназы селезенки (syk) |
| WO2012154518A1 (en) | 2011-05-10 | 2012-11-15 | Merck Sharp & Dohme Corp. | Bipyridylaminopyridines as syk inhibitors |
| US9120785B2 (en) | 2011-05-10 | 2015-09-01 | Merck Sharp & Dohme Corp. | Pyridyl aminopyridines as Syk inhibitors |
| KR20140028062A (ko) | 2011-05-10 | 2014-03-07 | 머크 샤프 앤드 돔 코포레이션 | Syk 억제제로서의 아미노피리미딘 |
-
2012
- 2012-05-04 KR KR1020137032289A patent/KR20140028062A/ko not_active Withdrawn
- 2012-05-04 CN CN201280032430.0A patent/CN103619172A/zh active Pending
- 2012-05-04 US US14/116,207 patent/US9290490B2/en active Active
- 2012-05-04 JP JP2014510371A patent/JP2014513686A/ja active Pending
- 2012-05-04 RU RU2013154412/04A patent/RU2013154412A/ru not_active Application Discontinuation
- 2012-05-04 WO PCT/US2012/036423 patent/WO2012154519A1/en not_active Ceased
- 2012-05-04 CA CA2834604A patent/CA2834604A1/en not_active Abandoned
- 2012-05-04 MX MX2013013090A patent/MX2013013090A/es not_active Application Discontinuation
- 2012-05-04 BR BR112013028900A patent/BR112013028900A2/pt not_active IP Right Cessation
- 2012-05-04 EP EP12782298.9A patent/EP2706853B1/en active Active
- 2012-05-04 AU AU2012253885A patent/AU2012253885A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CA2834604A1 (en) | 2012-11-15 |
| BR112013028900A2 (pt) | 2017-01-03 |
| WO2012154519A1 (en) | 2012-11-15 |
| EP2706853A1 (en) | 2014-03-19 |
| MX2013013090A (es) | 2013-12-16 |
| RU2013154412A (ru) | 2015-06-20 |
| EP2706853A4 (en) | 2014-11-05 |
| US20140148474A1 (en) | 2014-05-29 |
| JP2014513686A (ja) | 2014-06-05 |
| AU2012253885A1 (en) | 2013-10-31 |
| EP2706853B1 (en) | 2017-06-14 |
| CN103619172A (zh) | 2014-03-05 |
| US9290490B2 (en) | 2016-03-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20140028062A (ko) | Syk 억제제로서의 아미노피리미딘 | |
| EP2707357B1 (en) | Pyridyl aminopyridines as syk inhibitors | |
| JP5242857B2 (ja) | Syk阻害剤としてのアミノピリミジン類 | |
| US9145391B2 (en) | Bipyridylaminopyridines as Syk inhibitors | |
| US9487504B2 (en) | Imidazolyl analogs as syk inhibitors | |
| EP3083559B1 (en) | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors | |
| US9745295B2 (en) | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors | |
| US9598405B2 (en) | Thiazole-substituted aminopyridines as spleen tyrosine kinase inhibitors | |
| EP2988749B1 (en) | Thiazole-substituted aminopyrimidines as spleen tyrosine kinase inhibitors | |
| US20150166486A1 (en) | Substituted diazine and triazine spleen tyrosine kinease (syk) inhibitors | |
| EP3116506B1 (en) | 2-pyrazine carboxamides as spleen tyrosine kinase inhibitors | |
| US20150299125A1 (en) | Prodrug bipyridylaminopyridines as syk inhibitors | |
| EP3082807B1 (en) | Thiazole-substituted aminoheteroaryls as spleen tyrosine kinase inhibitors | |
| US9670196B2 (en) | Thiazole-substituted aminoheteroaryls as Spleen Tyrosine Kinase inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20131205 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |