-
Hintergrund der Erfindung
-
Gebiet der Erfindung
-
Die
vorliegende Erfindung betrifft pharmazeutische Formulierungen zur
Verwendung in der Verabreichung von Medikamenten durch Inhalation.
Insbesondere betrifft diese Erfindung pharmazeutische Formulierungen
von Fluticasonpropionat und Salmeterol oder einem pharmazeutisch
akzeptablen Salz davon (wie das Xinafoat) zur Verwendung in Druckdosierinhalatoren
("pressurised metered
dose inhalers",
MDIs). Die Erfindung betrifft ebenfalls Verfahren zu ihrer Herstellung
und ihre Verwendung in der Therapie.
-
Beschreibung des Standes
der Technik
-
Inhalatoren
sind allgemein bekannte Vorrichtungen zur Verabreichung von pharmazeutisch
aktiven Stoffen in die Atemwege durch Inhalation. Solche aktiven
Stoffe, die üblicherweise
durch Inhalation übertragen werden,
schließen
Bronchodilatatoren, wie β2-Agonisten
und Anticholinergika, Kortikosteroide, Antiallergika und andere
Stoffe ein, die effizient durch Inhalation verabreicht werden können, wodurch
die therapeutische Breite vergrößert und
Nebenwirkungen des aktiven Stoffes reduziert werden.
-
4-Hydroxy-α1-[[[6-(4-phenylbutoxy)hexyl]amino]methyl]-1,3-benzoldimethanol
wurde als einer einer weiten Reihe von Bronchodilatatoren in GB-A-2
140 800 beschrieben. Diese Verbindung ist ebenfalls unter dem generischen
Namen Salmeterol bekannt, dessen Xinafoatsalz weithin als hochwirksame
Behandlung von inflammatorischen Krankheiten, wie Asthma und chronisch-obstruktive
Lungenkrankheit (COPD), bekannt geworden ist.
-
(6a,11b,16a,17a)-6,9-Difluor-11-hydroxy-16-methyl-3-oxo-17-(1-oxopropoxy)androsta-1,4-dien-l7-thiocarbonsäure-S-fluormethylester
wurde als ein antiinflammatorisches Steroid in
US-PS 4,335,121 beschrieben. Diese Verbindung
ist ebenfalls unter dem generischen Namen Fluticasonpropionat bekannt
und ist seitdem als ein hocheffektives Steroid in der Behandlung
von inflammatorischen Krankheiten, wie Asthma und chronisch-obstruktive
Lungenkrankheit (COPD), bekannt geworden.
-
Es
wird angenommen, dass die gleichzeitige Verabreichung von Salmeterol
und Fluticasonpropionat signifikante Vorteile in der Behandlung
und Bekämpfung
dieser inflammatorischen Krankheiten hat.
-
Dosierinhalatoren
(MDIs) sind der häufigste
Typ eines weiten Bereichs von Inhalatortypen und verwenden ein verflüssigtes
Treibmittel, um Tröpfchen,
die das pharmazeutische Produkt enthalten, in die Atemwege als Aerosol
auszustoßen.
MDI-Formulierungen werden allgemein als Lösungsformulierungen oder Suspensionsformulierungen
charakterisiert.
-
Die
am häufigsten
verwendeten Aerosoltreibmittel für
Medikamente waren Freon 11 (CCl3F) im Gemisch
mit Freon 12 (CCl2F2)
und Freon 114 (CF2Cl·CF2Cl).
Jedoch wird jetzt angenommen, dass diese Treibmittel den Abbau von
Ozon in der Stratosphäre
hervorrufen, und ihre Verwendung wird jetzt eingestellt, um die Verwendung
aller CFK-haltigen Aerosoltreibmittel zu eliminieren. Es besteht
deshalb ein Bedarf an der Bereitstellung einer Aerosolformulierung
für Medikamente,
die sogenannte "ozonfreundliche" Treibmittel einsetzen.
-
Hydrofluoralkane
(HFAs); ebenfalls bekannt als Fluorkohlenwasserstoffe oder FKWs)
enthalten kein Chlor und werden als weniger zerstörerisch
gegenüber
Ozon betrachtet, und diese sind vorgeschlagene Ersatzstoffe für CFKs.
Insbesondere werden 1,1,1,2-Tetrafluorethan
(HFA 134a) und 1,1,1,2,3,3,3-Heptafluorpropan (HFA 227) als die
besten Kandidaten für
Nicht-CFK-Treibmittel anerkannt.
-
Die
Wirksamkeit einer Aerosolvorrichtung, wie eines MDI, ist eine Funktion
der am geeigneten Ort in der Lunge abgeschiedenen Dosis. Die Abscheidung
wird durch verschiedene Faktoren beeinflusst, von denen der wichtigste
die aerodynamische Partikelgröße ist.
Feste Partikel und/oder Tröpfchen
in einer Aerosolformulierung können
durch ihren Massenmedianwert des aerodynamischen Durchmessers (MMAD,
der Durchmesser, um den die aerodynamischen Massendurchmesser gleich
verteilt sind) gekennzeichnet werden.
-
Die
Partikelabscheidung in der Lunge hängt weitgehend von drei physikalischen
Mechanismen ab:
- 1. Aufprall, eine Funktion
der Partikelträgheit;
- 2. Sedimentation aufgrund von Schwerkraft; und
- 3. Diffusion, die aus der Brown'schen Bewegung von feinen Partikeln
im Submikrometerbereich (<1 μm) resultiert.
-
Die
Masse der Partikel bestimmt, welcher der drei Hauptmechanismen vorherrscht.
-
Der
effektive aerodynamische Durchmesser ist eine Funktion der Größe, Form
und Dichte der Partikel und wird die Größe der auf sie wirkenden Kräfte beeinflussen.
Obwohl Trägheits-
und Schwerkrafteffekte mit zunehmender Partikelgröße und Partikeldichte
zunehmen, nehmen z.B. die durch Diffusion erzeugten Verschiebungen
ab. In der Praxis spielt Diffusion eine geringe Rolle in der Abscheidung
aus pharmazeutischen Aerosolen. Aufprall und Sedimentation können aus
einer Messung des MMAD bewertet werden, der die Verschiebung über Stromlinien
unter dem Einfluss von Trägheit
bzw. Schwerkraft bestimmt.
-
Aerosolpartikel
mit äquivalentem
MMAD und GSD (geometrische Standardabweichung) weisen eine ähnliche
Abscheidung in der Lunge auf, unabhängig von ihrer Zusammensetzung.
Die GSD ist ein Maß für die Variabilität der aerodynamischen
Partikeldurchmesser.
-
Zur
Inhalationstherapie gibt es einen Vorzug für Aerosole, in denen die Partikel
zur Inhalation einen Durchmesser von ca. 0,5 bis 5 μm haben.
Partikel, die größer als
5 μm im
Durchmesser sind, werden primär durch
Trägheitsaufprall
in der Mundrachenhöhe
abgeschieden, Partikel mit 0,5 bis 5 μm Durchmesser, die hauptsächlich durch
die Schwerkraft beeinflusst werden, sind ideal zur Abscheidung in
den leitenden Atemwegen, und Partikel mit 0,5 bis 3 μm Durchmesser
sind wünschenswert
zur Aerosolübertragung
in die Lungenperipherie. Partikel von weniger als 0,5 μm können ausgeatmet
werden.
-
Atembare
Partikel werden allgemein als diejenigen mit aerodynamischen Durchmessern
von weniger als 5 μm
betrachtet. Diese Partikel, insbesondere diejenigen mit einem Durchmesser
von ca. 3 μm,
werden effizient in den unteren Atemwegen durch Sedimentation abgeschieden.
-
Es
wurde kürzlich
bei Patienten mit milder und schwerer Atemwegsobstruktion gezeigt,
dass die Partikelgröße der Wahl
für ein β2-Agonist-
oder anticholinerges Aerosol ca. 3 μm sein sollte (P. Zaanen et
al., Int. J. Pharm. 107, 211–217
(1994), Int. J. Pharm. 114, 111–115
(1995), Thorax, 51, 977–980
(1996).
-
Viele
der für
den MMAD von Partikeln relevanten Faktoren sind relevant für Tröpfchen,
und die zusätzlichen
Faktoren der Geschwindigkeit der Lösungsmittelverdampfung und
der Oberflächenspannung
sind ebenfalls wichtig.
-
In
Suspensionsformulierungen wird die Partikelgröße im Prinzip während der
Herstellung durch die Größe gesteuert,
auf die das feste Medikament reduziert wird, gewöhnlich durch Mikronisierung.
Falls jedoch der suspendierte Wirkstoff die geringste Löslichkeit
im Treibmittel hat, kann ein als Ostwald-Reifung bekannter Prozess
zu Partikelgrößenwachstum
führen.
Ebenfalls können
Partikel eine Tendenz zu Aggregation aufweisen oder an Teilen des
MDI anhaften, z.B. an der Dose oder am Ventil. Die Wirkung der Ostwald-Reifung
und insbesondere der Wirkstoffabscheidung kann besonders schwerwiegend
für hochwirksame
Wirkstoffe (einschließlich
Salmeterolxinafoat und Fluticasonpropionat) sein, die in geringen
Dosen formuliert werden müssen. Lösungsformulierungen
leiden nicht an diesen Nachteilen, aber leiden an anderen, indem
die Partikel- oder Tröpfchengröße eine
Funktion sowohl der Geschwindigkeit der Verdampfung des Treibmittels
aus der Formulierung als auch der Zeit zwischen der Freisetzung
der Formulierung aus der Dose und dem Moment der Inhalation ist.
Daher kann sie einer beträchtlichen
Variabilität
unterliegen und ist allgemein schwierig zu steuern.
-
Neben
ihrem Einfluss auf das therapeutische Profil eines Wirkstoffs hat
die Größe von Aerosolpartikeln einen
wichtigen Einfluss auf das Nebenwirkungsprofils eines Wirkstoffs.
Zum Beispiel ist es allgemein bekannt, dass die Mundrachenhöhlenabscheidung
von Aerosolformulierungen von Steroiden zu Nebenwirkungen führen kann,
wie Candidiasis von Mund und Rachen. Außerdem kann ein höherer systemischer
Kontakt mit den Aerosolpartikeln aufgrund einer tiefen Lungenpenetration
die ungewünschten
systemischen Wirkungen bestimmter Wirkstoffe steigern. Zum Beispiel
kann der systemische Kontakt mit bestimmten Steroiden Nebenwirkungen
auf den Knochenmetabolismus und das Knochenwachstum erzeugen.
-
Suspensionsaerosolformulierungen,
die Salmeterol und Fluticasonpropionat enthalten, werden in EP-A-0
416 951 und
US-PS 5 653 962 beschrieben.
-
-
Lösungsformulierungen
von Medikamenten werden in WO 98/56349, WO 94/13262, WO 98/24420 und
WO 00/30607 offenbart.
-
Wir
haben jetzt eine Formulierung von Salmeterol oder einem pharmazeutisch
akzeptablen Salz davon und Fluticasonpropionat erfunden, die einige
oder alle der oben genannten Nachteile eliminiert oder substantiell
abmildert.
-
Zusammenfassung der Erfindung
-
So
stellen wir erfindungsgemäß eine pharmazeutische
Aerosolformulierung bereit, die (i) Salmeterol oder ein pharmazeutisch
akzeptables Salz davon, (ii) Fluticasonpropionat, (iii) ein Hydrofluoralkan-(HFA)-Treibmittel,
(iv) eine Komponente mit geringer Flüchtigkeit, ausgewählt aus
Glycerin und Polyethylenglykol, um den Massenmedianwert des aerodynamischen
Durchmessers (MMAD) der Aerosolpartikel bei Auslösung des Inhalators zu erhöhen; und
(v) Ethanol als Solubilisierungsmittel in ausreichender Menge umfasst,
um das Salmeterol oder pharmazeutisch akzeptable Salz davon und
Fluticasonpropionat in der Formulierung zu solubilisieren; und dadurch
gekennzeichnet, dass das Salmeterol oder pharmazeutisch akzeptable Salz
davon und das Fluticasonpropionat vollständig in der Formulierung gelöst sind.
-
Ausführliche Beschreibung der Erfindung
-
Die
Gegenwart der Komponente mit geringer Flüchtigkeit in der Lösungsformulierung
erhöht
die feine Partikelmasse (FPM), wie sie durch den Inhalt der Stufen
3–5 eines
Andersen Cascade Impactor bei Auslösung der Formulierung definiert
wird, relativ zu Lösungsformulierungen,
die diese Komponente auslassen. Lösungsformulierungen, die die
Komponente mit geringer Flüchtigkeit
auslassen, führen
allgemein zu einer Partikelgrößenverteilung,
die einen höheren
Gehalt feiner Partikel aufweist; solche Verteilungen stimmen allgemein
nicht mit der Verteilung von Suspensionsformulierungen überein und
mögen deshalb
nicht bioäquivalent sein.
-
Beispiele
für HFA-Treibmittel
schließen
1,1,1,2-Tetrafluorethan (HFA134) und 1,1,1,2,3,3,3-Heptafluor-n-propan
(HFA227) und Mischungen daraus ein. Das bevorzugte Treibmittel ist
1,1,1,2-Tetrafluorethan (HFA134a). Ein alternatives bevorzugtes
Treibmittel ist 1,1,1,2,3,3,3-Heptafluor-n-propan
(HFA227).
-
Die
Komponente mit geringer Flüchtigkeit
ist Glycerin oder Polyethylenglykol (z.B. PEG200 oder PEG400). Bevorzugt
ist die Komponente mit geringer Flüchtigkeit in einer Menge von
0,5 bis 3 % (G/G) vorhanden.
-
Das
bevorzugte Solubilisierungsmittel ist Ethanol.
-
In
einer ersten Ausführungsform
der Erfindung bevorzugten wir, dass Salmeterol in Form des Xinafoatsalzes
verwendet wird. Salmeterolxinafoat kann in zwei als Form I und Form
II bekannten polymorphen Formen hergestellt werden. Form I, die
eine Schmelzendotherme bei 140°C
aufweist, kann durch Ausfällung
aus einer heißen
methanolischen Lösung
von Salmeterolxinafoat bei Zugabe zu kaltem Isopropanol hergestellt werden,
wie in WO 93/16031 beschrieben. Form II, die eine Schmelzendotherme
bei 125°C
hat, kann durch Umkristallisation aus überkritischer Flüssigkeit
hergestellt werden, wie in WO 95/01324 beschrieben. Bevorzugt wird
Salmeterolxinafoat als Form II-Polymorph eingesetzt, da von dieser
Form vorhergesagt wird, dass sie eine höhere Löslichkeit hat. Alternativ kann
Salmeterolxinafoat als Form I-Polymorph eingesetzt werden.
-
Insbesondere
bevorzugen wir, Salmeterolxinafoat in Form des gereinigten Enantiomers
R-Salmeterolxinafoat zu verwenden. Überraschend haben wir festgestellt,
dass R-Salmeterolxinafoat in einer polymorphen Form, die durch Kristallisation
aus Ether erhältlich
ist, signifikant löslicher
in Mischungen aus Ethanol/HFA134a und Ethanol/HFA227 als racemisches
Salmeterolxinafoat ist. Ohne durch die Theorie gebunden zu sein,
kann diese höhere
Löslichkeit
der geringen Kristallgitterenergie zugeschrieben werden, wie sie
durch eine Schmelzendotherme bei 95°C gezeigt wird (die beträchtlich
niedriger als diejenige der oben genannten zwei Formen von Salmeterolxinafoat
ist).
-
In
einer zweiten Ausführungsform
der Erfindung bevorzugen wir, Salmeterol als freie Base zu verwenden.
-
Überrascht
haben wir festgestellt, dass Salmeterolbase substantiell löslicher
in Mischungen aus Ethanol/HFA134a und Ethanol/HFA227 als racemisches
Salmeterolxinafoat oder sogar R-Salmeterolxinafoat ist. Es ist ebenfalls
von Interesse, Salmeterolbase als R-Salmeterolbase zu verwenden.
-
Die
Verwendung von R-Salmeterolxinafoat oder -base hat den weiteren
Vorteil, dass sie den Vorteil der höheren Wirksamkeit von R-Salmeterol
relativ zu racemischem Salmeterol mit dem Ergebnis nutzt, dass eine
geringere Konzentration des Wirkstoffs in Lösung erforderlich ist.
-
In
einer dritten, weniger bevorzugten Ausführungsform wird Salmeterol
als Sulfatsalz verwendet. Das bevorzugte Solubilisierungsmittel
für Salmeterolsulfat
ist Propylenglykol.
-
Wie
aus den Beispielen ersichtlich ist, zeigen Formulierungen aus Salmeterolbase
und Fluticasonpropionat in Ethanol und HFA134a oder HFA227, insbesondere
zusammen mit der Komponente geringer Flüchtigkeit, wie Glycerin oder
Polyethylenglykol, besonders ausgezeichnete Übertragungseigenschaften.
-
Im
Vorhergehenden, außer
wenn anders angegeben, werden Wirkstoffmengen von Salmeterol als
geeignet für
Salmeterolbase angegeben, aber es versteht sich, dass für Salmeterolxinafoat
oder ein anderes pharmazeutisch akzeptables Salz davon eine geeignete
Umwandlung vorgenommen werden kann, um eine geeignete Masse von
Wirkstoff in der übertragenen
Dosis zu ergeben. Zum Beispiel entspricht eine Dosis von 25 μg Salmeterol
einer Dosis von 36,3 μg
Salmeterolxinafoat. Es versteht sich ebenfalls, dass Salmeterol
als Racemat (wie es bevorzugt ist) oder in Form eines enantiomerangereicherten
(oder gereinigten) einzelnen R- oder S-Enantiomers verwendet werden
kann. Im Vorhergehenden werden Wirkstoffmengen als angemessen für den racemischen
Wirkstoff angegeben, aber es versteht sich, dass die Einstellung
der Dosierungsmasse angemessen sein kann, wenn ein unterschiedliches
Verhältnis
von Enantiomeren eingesetzt wird. Zum Beispiel kann R-Salmeterol
wünschenswert
mit der Hälfte
der normalen Dosis von racemischem Salmeterol eingesetzt werden.
-
Wir
bevorzugen, dass die Formulierung geeignet zur Übertragung einer therapeutischen
Menge von Salmeterol und Fluticasonpropionat in einer oder zwei
Auslösungen
ist. Bevorzugt wird die Formulierung geeignet zur Übertragung
von 25–50 μg Salmeterol
pro Auslösung
sein, speziell von 25 μg
pro Auslösung
von Salmeterol (z.B. als Xinafoat). Bevorzugt wird die Formulierung
geeignet zur Übertragung
von 25–250 μg Fluticasonpropionat
pro Auslösung
sein, insbesondere 25 μg,
50 μg, 125 μg oder 250 μg, speziell
25 μg oder
50 μg pro
Auslösung
von Fluticasonpropionat.
-
Die
erfindungsgemäße Formulierung
wird in Verbindung mit einem geeigneten Dosierventil verwendet werden.
Wir bevorzugen, dass die Formulierung durch ein Dosierventil ausgelöst wird,
das ein Volumen von 50 bis 100 μl übertragen
kann, z.B. 50 oder 63 μl
oder besonders bevorzugt 100 μl.
-
Wenn
ein 25 μl-Dosiervolumen
verwendet wird, wäre
die Endkonzentration von Salmeterol, das pro Auslösung übertragen
wird, für
eine 25 μg-Dosis
0,05 % (G/V) oder 0,042 % (G/G). Wenn ein 63 μl-Dosiervolumen verwendet wird, wäre die Endkonzentration
von Salmeterol, das pro Auslösung übertragen
wird, 0,04 % (G/V) oder 0,033 % (G/G). Falls ein 100 μl-Dosierventil
verwendet würde,
wäre die
Endkonzentration von Salmeterol, das pro Auslösung übertragen wird, 0,025 % (G/V)
oder 0,021 % (G/G) für
eine 25 μg-Dosis.
-
Wenn
ein 50 μl-Dosiervolumen
verwendet wird, wäre
die Endkonzentration von Fluticasonpropionat, die pro Auslösung übertragen
wird, 0,1 % G/V (was 0,1 g Fluticasonpropionat auf 100 ml Formulierung
entspricht) oder ca. 0,083 % G/G (was 0,083 g Fluticasonpropionat
auf 100 g Formulierung entspricht) für eine 50 μg-Dosis, 0,25 % (G/V) oder ca.
0,21 % (G/G) für
eine 125 μg-Dosis,
0,5 % (G/V) oder ca. 0,42 % (G/G) für eine 250 μg-Dosis und 0,05 % (G/V) oder
ca. 0,042 % (G/G) für
eine 25 μg-Dosis.
Wenn ein 63 μl-Dosiervolumen
verwendet wird, wäre
die Endkonzentration von Fluticasonpropionat, das pro Auslösung übertragen
wird, 0,079 % (G/V) oder ca. 0,067 % (G/G) für eine 50 μg-Dosis, 0,198 % (G/V) oder
ca. 0,167 % (G/G) für
eine 125 μg-Dosis,
0,397 % (G/V) oder ca. 0,333 % (G/G) für eine 250 μg-Dosis und 0,04 % (G/V) oder
ca. 0,033 % (G/G) für
eine 25 μg-Dosis.
Wenn ein 100 μl-Dosiervolumen
verwendet wird, wäre
die Endkonzentration von Fluticasonpropionat, das pro Auslösung übertragen
wird, 0,05 % G/V oder ca. 0,042 % G/G für eine 50 μg-Dosis, 0,13 % (G/V) oder ca.
0,10 % (G/G) für
eine 125 μg-Dosis,
0,25 % (G/V) oder ca. 0,21 % (G/G) für eine 250 μg-Dosis und 0,025 % (G/V) oder
ca. 0,021 % (G/G) für
eine 25 μg-Dosis.
-
Die
zuvor bezeichneten Zahlen in G/G sind insoweit ungefähr, als
dass sie nicht den Dichteunterschied zwischen HF134a und Ethanol
berücksichtigen,
jedoch können
die genauen Zahlen leicht bestimmt werden.
-
Die
Verwendung eines größeren Dosierkammervolumens,
z.B. 100 μl,
ist allgemein bevorzugt.
-
Wir
bevorzugen, dass die Formulierung zwischen 0,5 und 2 % (G/G) der
Komponente mit geringer Flüchtigkeit
enthält,
besonders bevorzugt zwischen 0,8 und 1,6 % (G/G), insbesondere zwischen
1,0 und 1,6 % (G/G). Wir bevorzugen speziell, 1,3 % (G/G) zu verwenden.
Wir bevorzugen ebenfalls speziell, 1,0 % (G/G) der Komponente mit
geringer Flüchtigkeit
zu verwenden. Jedoch ist der am meisten bevorzugte Bereich 0,5–1 % (G/G),
z.B. 0,5 %, 0,75 % oder 1 % (G/G).
-
Es
ist notwendig, die Komponente mit geringer Flüchtigkeit, das Solubilisierungsmittel
und das Treibmittel in relativen Anteilen einzusetzen, so dass die
Komponenten frei mischbar sind.
-
Abhängig von
der Endkonzentration von Salmeterol oder pharmazeutisch akzeptablem
Salz davon und Fluticasonpropionat in der Formulierung werden das
Treibmittel und die genaue Menge von Komponente mit geringer Flüchtigkeit
und die erforderliche Konzentration von Solubilisierungsmittel (z.B.
Ethanol) variieren. Um nicht den Dampfdruck des Treibmittels auf
ein nicht wünschenswertes
Ausmaß abzusenken,
sollte die Ethanolmenge bevorzugt etwa 35 % nicht übersteigen.
Die Ethanolmenge wird besonders bevorzugt im Bereich von 5 bis 30
%, insbesondere 5–15
%, speziell 6–12
%, z.B. 7–10
% G/G, sein.
-
Wenn
die Konzentration von Salmeterolxinafoat ca. 0,025 % G/V ist, die
Konzentration von Fluticasonpropionat ca. 0,05 % G/V ist und das
Treibmittel 1,1,1,2-Tetrafluorethan ist, ist eine Ethanolmenge von
21–24 %
G/V, speziell ca. 22 % G/G besonders geeignet. Wenn die Konzentration
von Salmeterolxinafoat ca. 0,025 % G/V ist, die Konzentration von
Fluticasonpropionat ca. 0,025 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist,
ist eine Ethanolmenge von 17–20
% G/G, speziell ca. 18 % G/G, besonders geeignet.
-
Wenn
die Konzentration von Salmeterol (als Xinafoat) ca. 0,025 % G/V
ist, die Konzentration von Fluticasonpropionat ca. 0,025 % G/V ist
und das Treibmittel 1,1,1,2-Tetrafluorethan ist, ist eine Ethanolmenge
von 23–26
% G/G, speziell ca. 25 % G/G, besonders geeignet. Wenn die Konzentration
von Salmeterol (als Xinafoat) ca. 0,025 % G/V ist, die Konzentration
von Fluticasonpropionat ca. 0,05 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist,
ist eine Ethanolmenge von 21–24
% G/G, speziell ca. 23 % G/G, besonders geeignet. Wenn die Konzentration
von Salmeterol (als Xinafoat) ca. 0,025 % G/V ist, die Konzentration
von Fluticasonpropionat ca. 0,13 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan
ist, ist eine Ethanolmenge von 20–23 % G/G, speziell ca. 21
% G/G besonders geeignet. Wenn die Konzentration von Salmeterol
(als Xinafoat) ca. 0,025 % G/V ist, die Konzentration von Fluticasonpropionat
ca. 0,25 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist,
ist eine Ethanolmenge von 39–42
% G/G, speziell ca. 41 % G/G, besonders geeignet.
-
Die
Konzentration von Salmeterol, ausgedrückt aus Gewicht von Xinafoat,
wird bevorzugt im Bereich von 0,02–0,05 % G/V sein, speziell
0,02–0,03
% G/V, z.B. ca. 0,025 % G/V (entsprechend 0,014 %–0,035 % G/V,
speziell 0,014 %–0,021
% G/V, z.B. ca. 0,017 % G/V, ausgedrückt als Gewicht von Base).
Ein anderer Bereich von Interesse ist 0,017–0,028 % G/V, z.B. ca. 0,025
% G/V, ausgedrückt
als Gewicht von Base. Die Konzentration von Fluticasonpropionat
wird bevorzugt im Bereich von 0,02–0,2 % G/V sein, speziell 0,02–0,15 %
G/V, z.B. 0,025–0,13
% G/V, speziell 0,025–0,05
% G/V.
-
Für eine Salmeterolkonzentration
von 0,025 % G/V (als Xinafoat) haben wir überraschend festgestellt, dass
die erforderliche Ethanolmenge zur Solubilisierung von Salmeterolxinafoat
und Fluticasonpropionat in einer Formulierung in HFA134a abnimmt,
wenn die Fluticasonpropionatkonzentration von 0,025 % G/V auf 0,13 %
G/V zunimmt. Dies impliziert, dass es eine gewisse Wechselwirkung
zwischen Salmeterol (als Xinafoat) und Fluticasonpropionat in der
Formulierung geben kann. Angesichts dieser Beobachtung haben wir
eingesehen, dass die Formulierungen, die eine höhere Konzentration von Fluticasonpropionat
einsetzen, mit einer geringeren Ethanolmenge formuliert werden können, als
man ansonsten erwarten könnte.
Dies führt
zu einer Anzahl von Vorteilen, z.B. dass solche Formulierungen eine
feine Partikelmasse (FPM) haben, die höher als angenommen ist.
-
So
bevorzugen wir, dass das Verhältnis
der Konzentration von Salmeterol (insbesondere als Xinafoat) zu
Fluticasonpropionat, ausgedrückt
als G/V, wobei das Gewicht von Salmeterol als Gewicht der freien
Base ausgedrückt
ist, im Bereich von 1:1 bis 1:6 ist, insbesondere 1:2 bis 1:6, z.B.
ca. 1:5. In Konzentrationswerten werden diese Verhältnisse
bevorzugt eingesetzt, wenn die Zahl "1" einer
Konzentration von ca. 0,025 % G/V entspricht.
-
Die
obigen Ethanolkonzentrationen sind angemessen für Salmeterolxinafoat in Form
des Form I-Polymorphs. Eine etwas geringere Konzentration würde als
notwendig für
den Form II-Polymorph erwartet werden.
-
Wenn
die Konzentration von R-Salmeterol (vorhanden als Xinafoat) 0,04
% G/V ist (bezogen auf das Gewicht von R-Salmeterolbase), die Konzentration
von Fluticasonpropionat weniger als ca. 0,05 % G/V ist (z.B. 0,025
%, 0,04 % oder 0,05 % G/V) und das Treibmittel 1,1,1,2-Tetrafluorethan
ist, ist eine Ethanolmenge von 12–19 % G/G, z.B. 13 % G/G, geeignet.
Wenn die Konzentration von R-Salmeterol (vorhanden als Xinafoat)
0,025 % G/V ist (bezogen auf das Gewicht von R-Salmeterolbase),
die Konzentration von Fluticasonpropionat weniger als ca. 0,05 %
G/V ist (z.B. 0,025 %, 0,04 % oder 0,05 % G/V) und das Treibmittel
1,1,1,2-Tetrafluorethan ist, ist eine Ethanolmenge von 9–11 % G/G,
z.B. 10 % G/G, geeignet. Wenn die Konzentration von R-Salmeterol
(vorhanden als Xinafoat) 0,025 % G/V ist (bezogen auf das Gewicht
von R-Salmeterolbase), die Konzentration von Fluticasonpropionat
ca. 0,025 % G/V ist und das Treibmittel 1,1,1,2,3,3,3-Heptafluor-n-propan
ist, ist eine Ethanolmenge von 13–15 % G/G, z.B. 14 % G/G, geeignet.
-
Wenn
die Konzentration von Salmeterol (vorhanden als freie Base) 0,05
% G/V ist, die Konzentration von Fluticasonpropionat ca. 0,05 %
G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist, ist eine
Ethanolmenge von ca. 9–11
% G/G, z.B. 10 % G/G, geeignet. Wenn die Konzentration von Salmeterol
(vorhanden als freie Base) 0,04 % G/V ist, die Konzentration von
Fluticasonpropionat ca. 0,04 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan
ist, ist eine Ethanolmenge von ca. 8–10 % G/G, z.B. 9 % G/G, geeignet.
Wenn die Konzentration von Salmeterol (vorhanden als freie Base)
0,025 % G/V ist, die Konzentration von Fluticasonpropionat ca. 0,05
% G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist, ist eine
Ethanolmenge von ca. 9–11
% G/G, z.B. 10 % G/G, geeignet. Wenn die Konzentration von Salmeterol
(vorhanden als freie Base) 0,025 % G/V ist, die Konzentration von
Fluticasonpropionat ca. 0,025 % G/V ist und das Treibmittel 1,1,1,2-Tetrafluorethan ist,
ist eine Ethanolmenge von ca. 6–10
%, bevorzugt 6–8
% G/G, z.B. 7 % G/G, geeignet.
-
Wenn
die Konzentration von Salmeterol (vorhanden als freie Base) ca.
0,025 % G/V ist, die Konzentration von Fluticasonpropionat ca. 0,025
% G/V ist und das Treibmittel 1,1,1,2,3,3,3-Heptafluor-n-propan
ist, ist eine Ethanolmenge von 13–15 %, bevorzugt ca. 14 % G/G,
geeignet.
-
Die
bevorzugte Konzentration von Salmeterol (vorhanden als freie Base)
in der Formulierung ist 0,025–0,05
% G/V. Die bevorzugte Konzentration von Fluticasonpropionat in der
Formulierung ist 0,025–0,13 %
G/V, besonders bevorzugt 0,025–0,05
% G/V, insbesondere ca. 0,025 % G/V. Wenn 1,1,1,2-Tetrafluorethan das
Treibmittel ist, ist die bevorzugte Konzentration von Ethanol als
Solubilisierungsmittel in der Formulierung ca. 6–12 %, z.B. 7–10 % G/G.
Wenn 1,1,1,2,3,3,3-Heptafluor-n-propan das Treibmittel ist, ist
die bevorzugte Konzentration von Ethanol als Solubilisierungsmittel
in der Formulierung 13–15
%, z.B. ca. 14 % G/G.
-
Erfindungsgemäße Formulierungen,
die frei von Tensid sind, sind bevorzugt. Erfindungsgemäße Formulierungen,
die frei von allen Exzipienten neben dem Solubilisierungsmittel
(Ethanol), der Komponente mit geringer Flüchtigkeit (Glycerin oder Polyethylenglykol)
und dem Treibmittel sind, sind besonders bevorzugt.
-
Wir
haben ebenfalls überraschend
festgestellt, dass, obwohl Fluticasonpropionat stabil gegen chemischen
Abbau bei Lagerung in einer Ethanol/HFA134a-Lösung zu sein scheint, Salmeterol
(z.B. als freie Base oder Xinafoat) eine Tendenz zu chemischem Abbau
zeigt. Ohne durch die Theorie beschränkt zu sein, nehmen wir an,
dass dieser chemische Abbau auf einer säurekatalysierten Dimerisierung
des Salmeterols beruhen kann. Es kann deshalb bevorzugt sein, ein
Mittel in einer Menge, die den chemischen Abbau von Salmeterol unterdrücken kann,
in die Formulierung einzuführen.
Zum Beispiel schließen
Mittel, die die säurekatalysierte Dimerisierung
verhindern können,
Basen ein, wie Natrium- oder Kaliumhydroxid oder Natriumcarbonat
oder ein organisches Amin. Es kann notwendig sein, ebenfalls eine
geringe Menge Wasser in die Formulierung einzuführen, z.B. 0,05–2 % G/G
Wasser oder besonders bevorzugt 0,1–1 % G/G Wasser. Der chemische
Abbau kann ebenfalls durch Oxidation gefördert werden, die z.B. aus
Spuren von Peroxid herrührt,
das in Ventilkomponenten (wie Peroxidvulkanisierte Kautschuke) oder
Exzipienten vorhanden ist. Bevorzugt wird eine Peroxidkontamination
z.B. durch Verwendung geeignet gereinigter Ventilkomponenten und
dergl. vermieden. Alternativ kann ein Antioxidationsmittel eingesetzt
werden (bevorzugt eines, das keine Säure ist). Erfindungsgemäße Formulierungen,
die frei von allen Exzipienten neben dem Solubilisierungsmittel
(Ethanol), der Komponente mit geringer Flüchtigkeit (Glycerin oder Polyethylenglykol),
dem Mittel, das den chemischen Abbau von Salmeterol unterdrücken kann,
und etwaigem Wasser in der Formulierung und dem Treibmittel sind,
sind ebenfalls bevorzugt.
-
Die
erfindungsgemäße pharmazeutische
Zusammensetzung kann in Dosen ("Kanister") gefüllt werden,
die zur Übertragung
pharmazeutischer Aerosolformulierungen geeignet sind. Dosen umfassen
allgemein einen Behälter,
der dem Dampfdruck des HFA-Treibmittels widerstehen kann, wie eine
Kunststoff- oder kunststoffbeschichtete Glasflasche oder bevorzugt
eine Metalldose, z.B. eine Aluminiumdose, die gegebenenfalls eloxiert,
lackbeschichtet und/oder kunststoffbeschichtet sein kann, wobei
der Behälter
mit einem Dosierventil verschlossen ist. Dosen können mit einem Polymer beschichtet
sein, wie in WO 96/32151 beschrieben, z.B. mit einem Copolymer aus
Polyethersulfon (PES) und Polytetrafluorethylen (PTFE). Ein anderes
Polymer zur Beschichtung, das erwogen werden kann, ist FEP (fluoriertes
Ethylenpropylen). Die Dosierventile werden konstruiert, um eine
abgemessene Menge der Formulierung pro Auslösung abzugeben, und beinhalten
eine Dichtung, um Leckage von Treibmittel durch das Ventil zu verhindern.
Die Dichtung kann jedes geeignete elastomere Material umfassen,
wie z.B. niederdichtes Polyethylen, Chlorbutyl, schwarze und weiße Butadien-Acrylnitril-Kautschuke,
Butylkautschuk, Neopren, EPDM (z.B. wie in WO 95/02651 beschrieben)
und TPE (thermoplastisches Elastomer, z.B. wie in WO 92/11190 beschrieben).
EPDM- und TPE-Kautschuke sind bevorzugt. Geeignete Ventile sind
gewerblich erhältlich
von allgemein in der Aerosolindustrie bekannten Herstellern, z.B. von
Valois, Frankreich (z.B. DF10, DF30, DF60), Bespak plc, GB (z.B.
BK300, BK356, BK357) und 3M-Neotechnic
Ltd., GB (z.B. SpraymiserTM). Das DF31-Ventil
von Valois, Frankreich, ist ebenfalls geeignet.
-
Ventildichtungen,
speziell die Gehäusedichtung,
und ebenfalls die Abdichtungen um die Dosierkammer, werden bevorzugt
aus einem Material hergestellt, das inert und resistent gegenüber Extraktion
in den Inhalten der Formulierung ist, speziell wenn der Inhalt Ethanol
einschließt.
-
Ventilmaterialien,
speziell das Herstellungsmaterial der Dosierkammer, werden bevorzugt
aus einem Material hergestellt, das inert und resistent gegenüber Verformung
durch den Inhalt der Formulierung ist, speziell wenn der Inhalt
Ethanol einschließt.
Besonders geeignete Materialien zur Verwendung in der Herstellung der
Dosierkammer schließen
Polyester, z.B. Polybutylenterephthalat (PBT), und Acetale, speziell
PBT, ein.
-
Herstellungsmaterialien
für die
Dosierkammer und/oder den Ventilschaft können wünschenswert fluoriert, teilweise
fluoriert oder mit fluorhaltigen Stoffen imprägniert sein, um der Wirkstoffabscheidung
zu widerstehen.
-
Ventile,
die vollständig
oder im wesentlichen aus Metallkomponenten zusammengesetzt sind
(z.B. Spraymiser, 3M-Neotechnic), sind speziell zur erfindungsgemäßen Verwendung
bevorzugt.
-
Herkömmliche
Masseherstellungsverfahren und Ausrüstung, die den Fachleuten auf
dem Gebiet der pharmazeutischen Aerosolherstellung allgemein bekannt
sind, können
zur Herstellung von Chargen im großen Maßstab für die gewerbliche Herstellung
gefüllter
Dosen eingesetzt werden. So wird z.B. in einem Masseherstellungsverfahren
ein Dosierventil auf eine Aluminiumdose aufgequetscht, um eine leere
Dose zu bilden. Das Medikament wird in ein Füllgefäß gegeben, und eine Mischung
aus Ethanol, Komponente mit geringer Flüchtigkeit und verflüssigtem
Treibmittel wird unter Druck durch das Füllgefäß in ein Herstellungsgefäß gefüllt. Eine Teilmenge
der Formulierung wird dann durch das Dosierventil in die Dose gefüllt.
-
In
einem alternativen Verfahren wird eine Teilmenge der verflüssigten
Formulierung in eine offene Dose unter Bedingungen gegeben, die
ausreichend kalt sind, so dass die Formulierung nicht verdampft,
und dann wird ein Dosierventil auf die Dose aufgequetscht.
-
In
einem alternativen Verfahren wird eine Teilmenge des Medikaments,
das im Solubilisierungsmittel und etwaiger Komponente mit geringer
Flüchtigkeit
gelöst
ist, in eine leere Dose abgegeben, ein Dosierventil wird aufgequetscht,
und dann wird das Treibmittel in die Dose durch das Ventil gefüllt.
-
Typischerweise
wird in Chargen, die zur pharmazeutischen Verwendung hergestellt
werden, jede gefüllte
Dose auf Gewicht überprüft, mit
einer Chargennummer codiert und in einem Gestell zur Lagerung vor
der Freisetzungsuntersuchung verpackt.
-
Jede
gefüllte
Dose wird zweckmäßig in eine
geeignete Kanalisierungsvorrichtung vor der Verwendung eingepasst,
um einen Dosierinhalator zur Verabreichung des Medikaments in die
Lungen oder Nasenhöhle
eines Patienten zu bilden. Geeignete Kanalisierungsvorrichtungen umfassen
z.B. einen Ventilauslöser
und einen zylindrischen oder konusartigen Durchtritt, durch den
Medikament aus der gefüllten
Dose über
das Dosierventil in die Nase oder den Mund eines Patienten übertragen
werden kann, z.B. einen Mundstückauslöser.
-
In
einer typischen Anordnung sitzt der Ventilschaft in einem Düsenblock,
der eine in eine Expansionskammer führende Öffnung aufweist. Die Expansionskammer
hat eine Ausgangsöffnung,
die sich in das Mundstück
erstreckt. Durchmesser der Auslöser-(Ausgangs-)Öffnung im
Bereich von 0,15–0,45
mm, insbesondere 0,2–0,45
mm, sind allgemein geeignet, z.B. 0,25, 0,30, 0,33 oder 0,42 mm.
Wir haben festgestellt, dass es vorteilhaft ist, einen kleinen Durchmesser
zu verwenden, z.B. 0,25 mm oder weniger, insbesondere 0,22 mm, da dies
zu einem höheren
FPM und einer geringeren Rachenabscheidung zu führen neigt. 0,15 mm ist ebenfalls besonders
geeignet. Die Abmessungen der Öffnung
sollten nicht so klein sein, dass eine Blockade des Strahls auftritt.
-
Auslöserstrahllängen sind
typischerweise im Bereich von 0,30–1,7 mm, z.B. 0,30, 0,65 oder
1,50 mm. Kleinere Abmessungen sind bevorzugt, z.B. 0,65 mm oder
0,30 mm.
-
Zur
Vermeidung von Wassereintritt in die Formulierung kann es wünschenswert
sein, das MDI-Erzeugnis in einer flexiblen Packung zu umhüllen, die
dem Wassereintritt widerstehen und die Absorption oder Freisetzung
von etwaigem Treibmittel, das aus der Dose austreten kann, erlauben
kann. Es kann ebenfalls wünschenswert
sein, ein Trockenmittel in die Verpackung aufzunehmen. Exemplarische
Umhüllungen
werden in
US-PS 6 119 853 beschrieben.
-
Dosierinhalatoren
werden konstruiert, um eine feste Einheitsdosierung von Medikament
pro Auslösung
oder "Sprühstoß" zu übertragen,
z.B. im Bereich von 10 bis 5000 μg
Medikament pro Sprühstoß.
-
Die
Verabreichung von Medikament kann zur Behandlung von milden, moderaten
oder schweren, akuten oder chronischen Symptomen oder zur prophylaktischen
Behandlung indiziert sein. Die Behandlung kann von Asthma, chronisch-obstruktiver
Lungenkrankheit (COPD) oder einer anderen respiratorischen Störung sein.
Man wird einsehen, dass die präzise
Verabreichungsdosis vom Alter und Zustand des Patienten abhängen wird,
und die Menge und Häufigkeit
der Verabreichung wird letztlich in der Verantwortung des behandelnden
Arztes liegen. Typischerweise kann eine Verabreichung ein- oder
mehrmals erfolgen, z.B. 1- bis 8-mal pro Tag, was z.B. 1, 2, 3 oder
4 Sprühstöße jedes
Mal ergibt.
-
Das
bevorzugte Behandlungsschema beträgt 2 Sprühstöße von 25 μg/Sprühstoß Salmeterol (z.B. als Xinafoat)
und 25, 50, 125 oder 250 μg/Sprühstoß (insbesondere
25 oder 50 μg/Sprühstoß) Fluticasonpropionat,
zweimal pro Tag.
-
Die
hier beschriebenen gefüllten
Dosen und Dosierinhalatoren umfassen weitere Aspekte der vorliegenden
Erfindung.
-
Ein
weiterer Aspekt der vorliegenden Erfindung umfasst die Verwendung
einer hier zuvor beschriebenen Formulierung in der Herstellung eines
Medikaments zur Behandlung von Atemwegsstörungen, z.B. Asthma oder chronisch-obstruktiver
Lungenkrankheit (COPD).
-
Wie
oben erwähnt
wurde, schließen
die Vorteile der Erfindung in einigen oder allen ihrer Ausführungsformen
die Tatsache ein, dass erfindungsgemäße Formulierungen umweltfreundlicher,
stabiler, weniger anfällig
für Ostwald-Reifung
oder Wirkstoffabscheidung auf den Innenoberflächen eines Dosierinhalators
sein können,
eine bessere Dosierungseinheitlichkeit aufweisen können, ein
höheres
FPM übertragen
können,
eine niedrigere Rachenabscheidung ergeben können, leichter oder wirtschaftlicher
hergestellt werden können
oder in anderer Weise vorteilhaft gegenüber bekannten Formulierungen
sein können.
-
Die
Erfindung wird unter Bezugnahme auf die folgenden Beispiele veranschaulicht.
-
Beispiele 1 und 2
-
Formulierungen
können
mit einer Zusammensetzung wie folgt hergestellt werden:
| Salmeterolxinafoat: | 0,025
% G/V |
| Fluticasonpropionat: | 0,05
% G/V |
| Ethanol: | 22
% G/G |
| Glycerin: | 1,3
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierung
kann in eine Aluminiumdose unter Druck gefüllt und mit einem Dosierventil mit
einer 100 μl-Dosierkammer
versehen werden.
| Salmeterolxinafoat: | 0,025
% G/V |
| Fluticasonpropionat: | 0,025
% G/V |
| Ethanol: | 18
% G/G |
| Glycerin: | 1,3
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierung
kann in eine Aluminiumdose unter Druck gefüllt und mit einem Dosierventil mit
einer 100 μl-Dosierkammer
versehen werden.
-
Beispiel 3
-
Eine
Formulierung wurde mit Zusammensetzungen wie folgt hergestellt:
| Salmeterol
(als Xinafoat): | 0,025
% G/V (bezogen auf Gewicht von Salmeterolbase) |
| Fluticasonpropionat: | 0,025
% G/V |
| Ethanol: | 25
% G/G |
| Glycerin: | 1,0
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierung
wurde in eine Aluminiumdose (120 Auslösungen/Dose; Durchschnitt von 40
Auslösungen)
unter Druck gefüllt
und mit einem Dosierventil (Valois DF60) mit einer Dosierkammer
mit einem Volumen von 100 μl
versehen. Diese Formulierung ist geeignet zur Abgabe von 25 μg Salmeterol
und 25 μg
Fluticasonpropionat pro Auslösung.
-
Beispiel 4
-
Eine
Formulierung wurde mit Zusammensetzungen wie folgt hergestellt:
| Salmeterol
(als Xinafoat): | 0,025
% G/V (bezogen auf Gewicht von Salmeterolbase) |
| Fluticasonpropionat: | 0,05
% G/V |
| Ethanol: | 23
% G/G |
| Glycerin: | 1,0
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierung
wurde in eine Aluminiumdose (120 Auslösungen/Dose; Durchschnitt von 40
Auslösungen)
unter Druck gefüllt
und mit einem Dosierventil (Valois DF60) mit einer Dosierkammer
mit einem Volumen von 100 μl
versehen. Diese Formulierung ist geeignet zur Abgabe von 25 μg Salmeterol
und 50 μg
Fluticasonpropionat pro Auslösung.
-
Beispiel 5
-
Eine
Formulierung wurde mit Zusammensetzungen wie folgt hergestellt:
| Salmeterol
(als Xinafoat): | 0,025
% G/V (bezogen auf Gewicht von Salmeterolbase) |
| Fluticasonpropionat: | 0,13
% G/V |
| Ethanol: | 21
% G/G |
| Glycerin: | 1,0
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierung
wurde in eine Aluminiumdose (120 Auslösungen/Dose; Durchschnitt von 40
Auslösungen)
unter Druck gefüllt
und mit einem Dosierventil (Valois DF60) mit einer Dosierkammer
mit einem Volumen von 100 μl
versehen. Diese Formulierung ist zur Abgabe von 25 μg Salmeterol
und 125 μg
Fluticasonpropionat pro Auslösung
geeignet.
-
Beispiele 6–8
-
Formulierungen
wurden mit Zusammensetzungen wie folgt hergestellt:
| Salmeterol
(als freie Base): | 0,025
% G/V |
| Fluticasonpropionat: | 0,025
% G/V |
| Ethanol: | 7
% G/G |
| Glycerin
oder PEG200 oder PEG400: | 0,5
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierungen
wurden in eine Aluminiumdose (120 Auslösungen/Dose; Durchschnitt von
40 Auslösungen)
unter Druck gefüllt
und mit einem Dosierventil (Valois DF60) mit einer Dosierkammer
mit einem Volumen von 100 μl
versehen. Diese Formulierungen sind zur Abgabe von 25 μg Salmeterol
und 25 μg Fluticasonpropionat
pro Auslösung
geeignet.
-
Beispiele 9–11
-
Formulierungen
wurden mit Zusammensetzungen wie folgt hergestellt:
| Salmeterol
(als freie Base): | 0,025
% G/V |
| Fluticasonpropionat: | 0,05
% G/V |
| Ethanol: | 10
% G/G |
| Glycerin
oder PEG200 oder PEG400: | 0,5
% G/G |
| 1,1,1,2-Tetrafluorethan: | auf
100 % |
-
Diese
Lösungsformulierungen
wurden in eine Aluminiumdose (120 Auslösungen/Dose; Durchschnitt von
40 Auslösungen)
unter Druck gefüllt
und mit einem Dosierventil (Valois DF60) mit einer Dosierkammer
mit einem Volumen von 100 μl
versehen. Diese Formulierungen sind zur Abgabe von 25 μg Salmeterol
und 50 μg Fluticasonpropionat
pro Auslösung
geeignet.
-
Daten der "Andersen Cascade
Impaction"
-
Formulierungen
wie in den Beispielen 6 bis 11 beschrieben wurden unter Verwendung
eines Andersen Cascade Impactor untersucht, wobei ein Auslöser von
Bespak (Variante BK621) mit 0,22 mm (Öffnung) × 0,65 mm (Strahllänge) verwendet
wurde. Die Untersuchung wurde an Dosen zu "Beginn der Verwendung" ("beginning of use", BoU) durchgeführt, und
abgegebener Wirkstoff aus 10 Auslösungen wurde im Instrument
aufgefangen, nachdem 4 Vorbereitungsauslösungen zum Verwerfen abgefeuert
waren. Die Ergebnisse sind in den Tabellen 1 bis 4 und 1 und 2 gezeigt.
Produkt in den individuellen Stufen des Cascade Impactor wurde in
wässrigem
Methanol gelöst
und durch eine HPLC-Säule
(stationäre
Phase: 20 cm C18 reverse Phase (Hypersil); mobile Phase: Methanol/MeCN,
gepuffert mit Ammoniumacetat) eluiert, um die Bestimmung der jeweiligen
Mengen von Salmeterol und Fluticasonpropionat zu erlauben (diese
Mengen sind separat in den nachfolgenden Tabellen und Figuren gezeigt).
-
Kurze Beschreibung der
Tabellen:
-
Tabelle
1: Cascade Impaction-Analyse von Lösungsaerosolen von Salmeterol
und Fluticasonpropionat/HFA134a, die 7 % Ethanol mit 0,5 % von verschiedenen
Komponenten geringer Flüchtigkeit
enthalten (gemäß Beispielen
6–8) (Mikrogramm-Daten)
-
Tabelle
2: Cascade Impaction-Analyse von Lösungsaerosolen von Salmeterol
und Fluticasonpropionat/HFA134a, die 7 % Ethanol mit 0,5 % von verschiedenen
Komponenten geringer Flüchtigkeit
enthalten (gemäß Beispielen
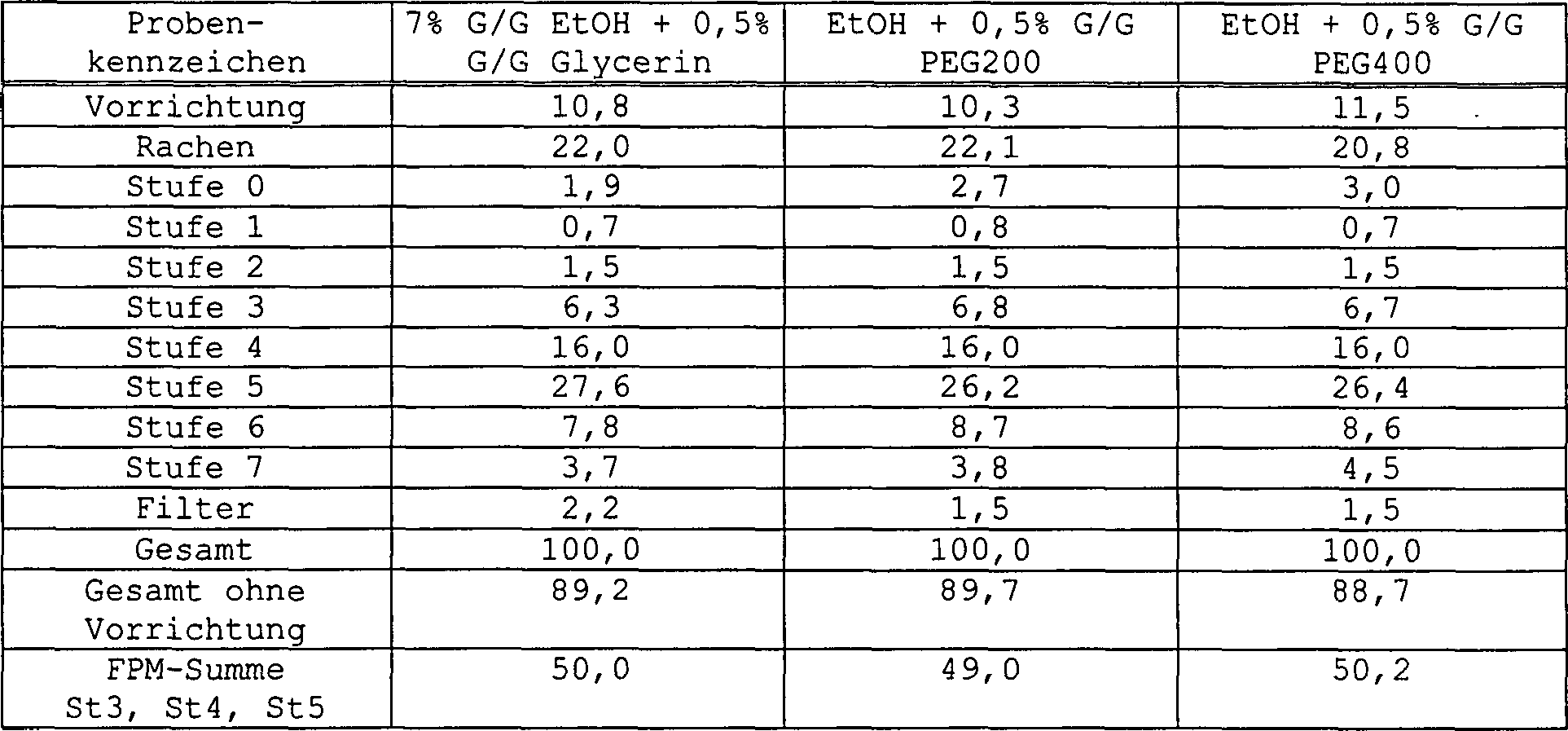
6–8) (Prozent-Daten)
-
Tabelle
3: Cascade Impaction-Analyse von Lösungsaerosolen von Salmeterol
und Fluticasonpropionat/HFA134a, die 10 % Ethanol mit 0,5 % von
verschiedenen Komponenten geringer Flüchtigkeit enthalten (gemäß Beispielen
9–11)
(Mikrogramm-Daten)
-
Tabelle
4: Cascade Impaction-Analyse von Lösungsaerosolen von Salmeterol
und Fluticasonpropionat/HFA134a, die 10 % Ethanol mit 0,5 % von
verschiedenen Komponenten geringer Flüchtigkeit enthalten (gemäß Beispielen
9–11)
(Prozent-Daten)
-
Kurze Beschreibung der
Figuren:
-
1:
Cascade Impaction-Analyse von Lösungsaerosolen
von Salmeterol und Fluticasonpropionat/HFA134, die 7 % Ethanol mit
0,5 % von verschiedenen Komponenten mit geringer Flüchtigkeit
enthalten (Mikrogramm-Daten) (Daten gemäß Tabelle 1)
-
2:
Cascade Impaction-Analyse von Lösungsaerosolen
von Salmeterol und Fluticasonpropionat/HFA134, die 10 % Ethanol
mit 0,5 % von verschiedenen Komponenten mit geringer Flüchtigkeit
enthalten (Mikrogramm-Daten)
(Daten gemäß Tabelle
3)
-
Aus
den Tabellen und Figuren kann abgeleitet werden, dass außergewöhnlich gute
Daten in Bezug auf die feine Partikelmasse aus der Verwendung von
Salmeterolbase und Fluticasonpropionat unter Verwendung von Ethanol
als Solubilisierungsmittel und HFA134a als Treibmittel mit Glycerin
oder Polyethylenglykol (PEG200, PEG400) als Komponente mit geringer
Flüchtigkeit
erhalten werden. Außerdem
sind diese Daten zu Salmeterol und Fluticasonpropionat in einer
Lösungsformulierung
zusammen sehr ähnlich
den Daten zu Salmeterol und Fluticasonpropionat in einer Lösungsformulierung
individuell. Sie sind ebenfalls ähnlich
entsprechenden Daten zur derzeit vermarkteten exzipientenfreien
Suspensionsformulierung von Salmeterolxinafoat und Fluticasonpropionat
in HFA134a ("Seretide
Evohaler") ähnlich.
-
Durchgehend
in der Beschreibung und in den nachfolgenden Ansprüchen, wenn
der Zusammenhang nichts anderes erfordert, verstehen sich das Wort "umfassen" und Variationen
wie "umfasst" und "umfassend" als Implizieren
des Einschlusses einer angegebenen Zahl oder eines angegebenen Schrittes
oder einer angegebenen Gruppe von Zahlen, aber nicht als Ausschluss
jeder anderen Zahl oder jedes anderen Schrittes oder jeder anderen
Gruppe von Zahlen oder Schritten.
-
Tabelle
1 Ergebnisse
der Cascade Impaction mit Salmeterolbase (μg)
-
Ergebnisse
der Cascade Impaction mit Fluticasonpropionat (μg)
-
Tabelle
2 Ergebnisse
der Cascade Impaction mit Salmeterolbase (μg)
-
Ergebnisse
der Cascade Impaction mit Fluticasonpropionat (μg)
-
Tabelle
3 Ergebnisse
der Cascade Impaction mit Salmeterolbase (μg)
-
Ergebnisse
der Cascade Impaction mit Fluticasonpropionat (μg)
-
Tabelle
4 Ergebnisse
der Cascade Impaction mit Salmeterolbase (%)
-
Ergebnisse
der Cascade Impaction mit Fluticasonpropionat (%)