DE102012022880B4 - Electronic devices containing organic layers - Google Patents
Electronic devices containing organic layers Download PDFInfo
- Publication number
- DE102012022880B4 DE102012022880B4 DE102012022880.5A DE102012022880A DE102012022880B4 DE 102012022880 B4 DE102012022880 B4 DE 102012022880B4 DE 102012022880 A DE102012022880 A DE 102012022880A DE 102012022880 B4 DE102012022880 B4 DE 102012022880B4
- Authority
- DE
- Germany
- Prior art keywords
- atoms
- group
- radicals
- substituted
- organic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/10—Apparatus or processes specially adapted to the manufacture of electroluminescent light sources
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1033—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1037—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
- H10K2102/10—Transparent electrodes, e.g. using graphene
- H10K2102/101—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO]
- H10K2102/103—Transparent electrodes, e.g. using graphene comprising transparent conductive oxides [TCO] comprising indium oxides, e.g. ITO
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/113—Heteroaromatic compounds comprising sulfur or selene, e.g. polythiophene
- H10K85/1135—Polyethylene dioxythiophene [PEDOT]; Derivatives thereof
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Manufacturing & Machinery (AREA)
- Plural Heterocyclic Compounds (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
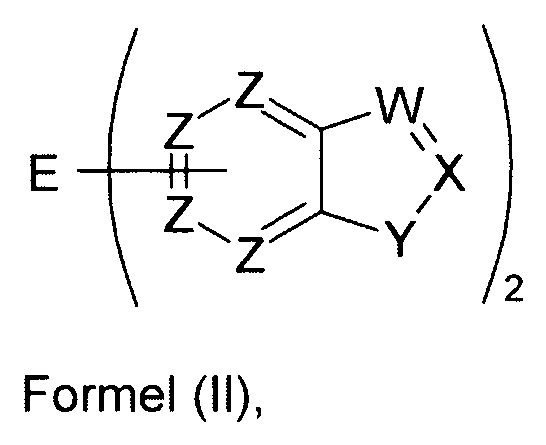
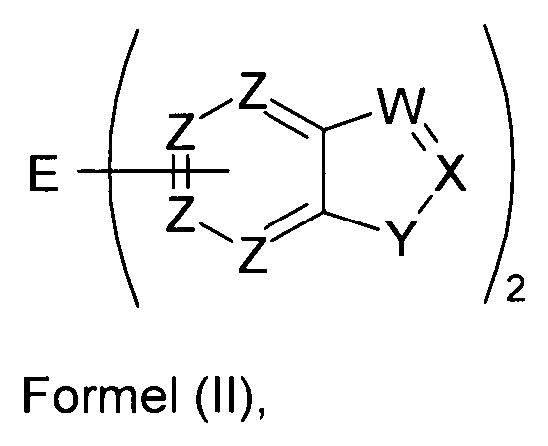
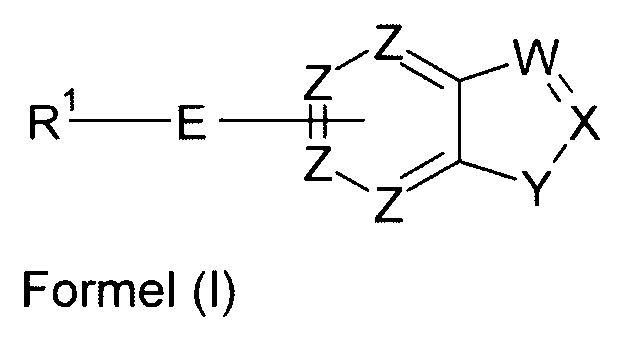
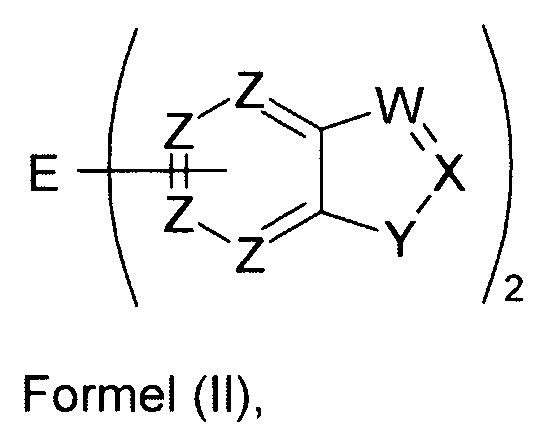
Elektronische Vorrichtung enthaltend mindestens eine organische Schicht, wobei die organische Schicht eine oder mehrere Verbindungen einer Formel (I) oder (II) umfasst
E ist eine divalente Gruppe gewählt aus S=O und S(=O)2;
W, X sind bei jedem Auftreten gleich oder verschieden N, P oder CR1;
Y ist bei jedem Auftreten gleich oder verschieden NR1, PR1, O oder S;
Z ist gleich C, wenn ein Substituent gebunden ist, und ist anderenfalls bei jedem Auftreten gleich oder verschieden CR1 oder N;
R1 ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, C(=O)R2, CN, Si(R2)3, N(R2)2, NO2, P(=O)(R2)2, S(=O)R2, S(=O)2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen, wobei die oben genannten Gruppen jeweils mit einem oder mehreren Resten R2 substituiert sein können und wobei eine oder mehrere CH2-Gruppen in den oben genannten Gruppen durch -R2C=CR2-, -C=C-, Si(R2)2, C=O, C=S, C=NR2, -C(=O)O-, -C(=O)NR2-, NR2, P(=O)(R2), -O-, -S-, SO oder SO2 ersetzt sein können und wobei ein oder mehrere H-Atome in den oben genannten Gruppen durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 30 aromatischen Ring-atomen, die durch einen oder mehrere Reste R2 substituiert sein kann, wobei zwei oder mehr Reste R1 miteinander verknüpft sein können und einen Ring bilden können; wobei die Gruppe R1, die an die Gruppe E gebunden ist, gewählt ist aus aromatischen oder heteroaromatischen Ringsystemen mit 5 bis 30 aromatischen Ringatomen, welche jeweils mit einem oder mehreren Resten R2 substituiert sein können;
R2 ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, C(=O)R3, CN, Si(R3)3, N(R3)2 , NO2, P(=O)(R3)2, S(=O)R3, S(=O)2R3, eine geradkettige Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen, wobei die oben genannten Gruppen jeweils mit einem oder mehreren Resten R3 substituiert sein können und wobei eine oder mehrere CH2-Gruppen in den oben genannten Gruppen durch -R3C=CR3-, -C≡C-, Si(R3)2, C=O, C=S, C=NR3, -C(=O)O-, -C(=O)NR3-, NR3, P(=O)(R3), -O-, -S-, SO oder SO2 ersetzt sein können und wobei ein oder mehrere H-Atome in den oben genannten Gruppen durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R3 substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 30 aromatischen Ring-atomen, die durch einen oder mehrere Reste R3 substituiert sein kann, wobei zwei oder mehr Reste R2 miteinander verknüpft sein können und einen Ring bilden können;
R3 ist bei jedem Auftreten gleich oder verschieden H, D, F oder ein aliphatischer, aromatischer oder heteroaromatischer organischer Rest mit 1 bis 20 C-Atomen, in dem auch ein oder mehrere H-Atome durch D oder F ersetzt sein können; dabei können zwei oder mehr Substituenten R3 miteinander verknüpft sein und einen Ring bilden.Electronic device containing at least one organic layer, wherein the organic layer comprises one or more compounds of formula (I) or (II)
E is a divalent group chosen from S=O and S(=O) 2 ;
W, X are the same or different at each occurrence as N, P or CR 1 ;
Y is the same or different at each occurrence: NR 1 , PR 1 , O or S;
Z is equal to C when a substituent is attached and is otherwise the same or different at each occurrence and is CR 1 or N;
R 1 is, identically or differently at each occurrence, H, D, F, Cl, Br, I, C(=O)R 2 , CN, Si(R 2 ) 3 , N(R 2 ) 2 , NO 2 , P(=O)(R 2 ) 2 , S(=O)R 2 , S(=O) 2 R 2 , a straight-chain alkyl, alkoxy or thioalkyl group having 1 to 20 C atoms or a branched or cyclic alkyl, alkoxy or thioalkyl group having 3 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms, where the abovementioned groups can each be substituted by one or more radicals R 2 and where one or more CH 2 groups in the abovementioned groups can be replaced by -R 2 C=CR 2 -, -C=C-, Si(R 2 ) 2 , C=O, C=S, C=NR 2 , -C(=O)O-, -C(=O)NR 2 -, NR 2 , P(=O)(R 2 ), -O-, -S-, SO or SO 2 and wherein one or more H atoms in the abovementioned groups can be replaced by D, F, Cl, Br, I, CN or NO 2 , or an aromatic or heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 2 , or an aryloxy or heteroaryloxy group having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 2 , wherein two or more radicals R 1 can be linked to one another and can form a ring; wherein the group R 1 which is bonded to the group E is selected from aromatic or heteroaromatic ring systems having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 2 ;
R 2 is, identically or differently on each occurrence, H, D, F, Cl, Br, I, C(=O)R 3 , CN, Si(R 3 ) 3 , N(R 3 ) 2 , NO 2 , P(=O)(R 3 ) 2 , S(=O)R 3 , S(=O) 2 R 3 , a straight-chain alkyl, alkoxy or thioalkyl group having 1 to 20 C atoms or a branched or cyclic alkyl, alkoxy or thioalkyl group having 3 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms, where the abovementioned groups may each be substituted by one or more radicals R 3 and where one or more CH 2 groups in the abovementioned groups are replaced by -R 3 C=CR 3 -, -C≡C-, Si(R 3 ) 2 , C=O, C=S, C=NR 3 , -C(=O)O-, -C(=O)NR 3 -, NR 3 , P(=O)(R 3 ), -O-, -S-, SO or SO 2 and where one or more H atoms in the abovementioned groups can be replaced by D, F, Cl, Br, I, CN or NO 2 , or an aromatic or heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 3 , or an aryloxy or heteroaryloxy group having 5 to 30 aromatic ring atoms, which can be substituted by one or more radicals R 3 , where two or more radicals R 2 can be linked to one another and can form a ring;
R 3 is, identically or differently at each occurrence, H, D, F or an aliphatic, aromatic or heteroaromatic organic radical having 1 to 20 C atoms, in which one or more H atoms may be replaced by D or F; two or more R 3 substituents may be linked to one another to form a ring.
Description
Die vorliegende Erfindung betrifft eine elektronische Vorrichtung enthaltend eine oder mehrere Verbindungen einer Formel (I) oder (II). Weiterhin betrifft die Erfindung die Verwendung einer Verbindung einer Formel (I) oder (II) in einer elektronischen Vorrichtung, bevorzugt in einer organischen Elektrolumineszenzvorrichtung, besonders bevorzugt als Matrixmaterial in einer emittierenden Schicht. Nochmals weiterhin betrifft die Erfindung bestimmte Verbindungen der Formel (I) oder (II), welche sich zur Verwendung in der erfindungsgemäßen Vorrichtung eignen.The present invention relates to an electronic device containing one or more compounds of formula (I) or (II). The invention further relates to the use of a compound of formula (I) or (II) in an electronic device, preferably in an organic electroluminescent device, particularly preferably as matrix material in an emitting layer. The invention further relates to certain compounds of formula (I) or (II) which are suitable for use in the device according to the invention.
Die Entwicklung von funktionellen Verbindungen zur Verwendung in elektronischen Vorrichtungen ist aktuell Gegenstand intensiver Forschung. Ziel ist hierbei unter anderem die Entwicklung von Verbindungen, welche ein verbessertes Eigenschaftsprofil der Vorrichtungen ermöglichen. Ebenfalls von Interesse ist die Bereitstellung von alternativen Verbindungen zur Verwendung in elektronischen Vorrichtungen.The development of functional compounds for use in electronic devices is currently the subject of intensive research. One of the aims is to develop compounds that enable an improved property profile of the devices. Also of interest is the provision of alternative compounds for use in electronic devices.
Unter dem Begriff elektronische Vorrichtung werden gemäß der vorliegenden Erfindung unter anderem organische integrierte Schaltungen (OICs), organische Feld-Effekt-Transistoren (OFETs), organische Dünnfilmtransistoren (OTFTs), organische lichtemittierende Transistoren (OLETs), organische Solarzellen (OSCs), organische optische Detektoren, organische Photorezeptoren, organische Feld-Quench-Devices (OFQDs), organische lichtemittierende elektrochemische Zellen (OLECs), organische Laserdioden (O-Laser), organische plasmonemittierende Dioden und organische Elektrolumineszenzvorrichtungen (OLEDs) verstanden.According to the present invention, the term electronic device includes, inter alia, organic integrated circuits (OICs), organic field-effect transistors (OFETs), organic thin-film transistors (OTFTs), organic light-emitting transistors (OLETs), organic solar cells (OSCs), organic optical detectors, organic photoreceptors, organic field quench devices (OFQDs), organic light-emitting electrochemical cells (OLECs), organic laser diodes (O-lasers), organic plasmon-emitting diodes and organic electroluminescent devices (OLEDs).
Der Aufbau der oben genannten organischen Elektrolumineszenzvorrichtungen (OLEDs) ist dem Fachmann bekannt und unter anderem in
Betreffend die Leistungsdaten der organischen Elektrolumineszenzvorrichtungen sind, insbesondere in Hinblick auf eine breite kommerzielle Verwendung, noch weitere Verbesserungen erforderlich. Von besonderer Bedeutung sind in diesem Zusammenhang die Lebensdauer, die Effizienz und die Betriebsspannung der organischen Elektrolumineszenzvorrichtungen sowie die realisierten Farbwerte. Insbesondere bei blau emittierenden Elektrolumineszenzvorrichtungen besteht Verbesserungspotential bezüglich der Lebensdauer der Vorrichtungen. Zudem ist es wünschenswert, dass die Verbindungen zur Verwendung als Funktionsmaterialien in elektronischen Vorrichtungen eine hohe thermische Stabilität und eine hohe Glasübergangstemperatur aufweisen und sich unzersetzt sublimieren lassen.With regard to the performance data of the organic electroluminescent devices, further improvements are required, particularly with regard to broad commercial use. Of particular importance in this context are the service life, efficiency and operating voltage of the organic electroluminescent devices as well as the color values achieved. There is potential for improvement in the service life of blue-emitting electroluminescent devices in particular. It is also desirable that the compounds for use as functional materials in electronic devices have high thermal stability and a high glass transition temperature and can be sublimated without decomposition.
Weiterhin besteht Bedarf an Matrixmaterialien, insbesondere an Matrixmaterialien für phosphoreszierende Emitter, die gleichzeitig zu guter Effizienz, hoher Lebensdauer und geringer Betriebsspannung der elektronischen Vorrichtungen führen. Nochmals insbesondere besteht Interesse an der Bereitstellung von Matrixmaterialien für grün emittierende phosphoreszierende Dotanden. Gerade die Eigenschaften der Matrixmaterialien sind häufig limitierend für die Lebensdauer und die Effizienz der organischen Elektrolumineszenzvorrichtung. Bei Matrixmaterialien für phosphoreszierende Emitter ist es wünschenswert, dass diese ein hochliegendes T1-Niveau (Triplettniveau) aufweisen. Besonders relevant ist dies bei Matrixmaterialien für blau emittierende phosphoreszierende Emitter.There is also a need for matrix materials, particularly matrix materials for phosphorescent emitters, which simultaneously lead to good efficiency, a long service life and a low operating voltage of the electronic devices. There is also particular interest in the provision of matrix materials for green-emitting phosphorescent dopants. The properties of the matrix materials in particular are often limiting for the service life and efficiency of the organic electroluminescent device. In the case of matrix materials for phosphorescent emitters, it is desirable that they have a high T 1 level (triplet level). This is particularly relevant for matrix materials for blue-emitting phosphorescent emitters.
Weiterhin ist die Bereitstellung neuer Elektronentransportmaterialien wünschenswert, da gerade auch die Eigenschaften des Elektronentransportmaterials einen wesentlichen Einfluss auf die oben genannten Eigenschaften der organischen Elektrolumineszenzvorrichtung ausüben. Insbesondere besteht Bedarf an Elektronentransportmaterialien, welche gleichzeitig zu guter Effizienz, hoher Lebensdauer und geringer Betriebsspannung führen.Furthermore, the provision of new electron transport materials is desirable, since the properties of the electron transport material have a significant influence on the above-mentioned properties of the organic electroluminescent device. In particular, there is a need for electron transport materials that simultaneously lead to good efficiency, a long service life and a low operating voltage.
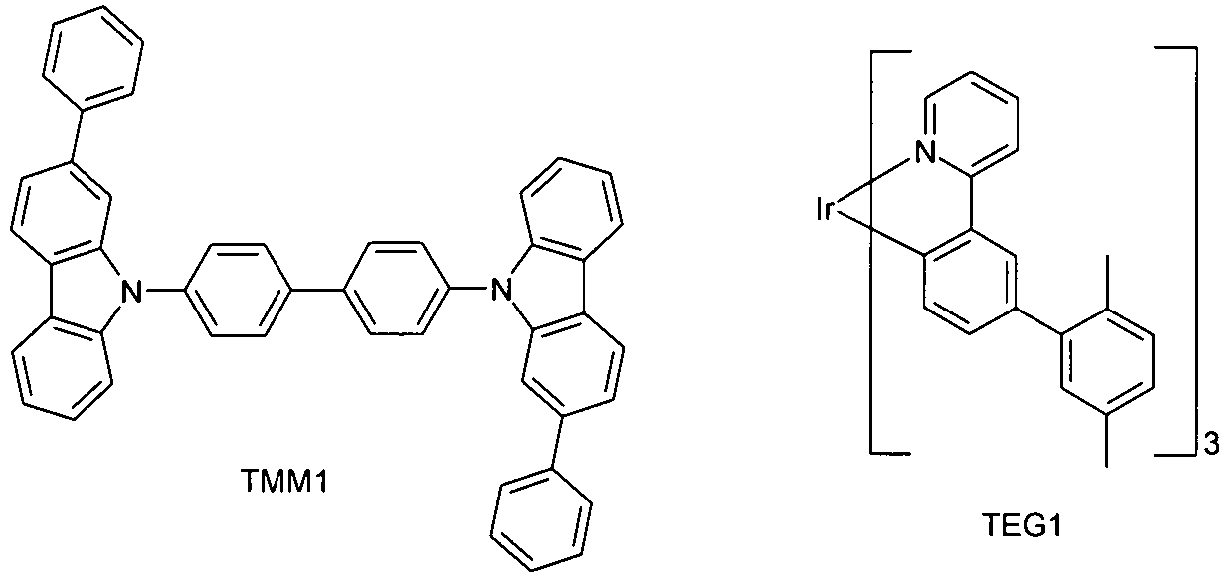
Gemäß dem Stand der Technik werden häufig Carbazolderivate, z. B. Bis(carbazolyl)biphenyl, als Matrixmaterialien für phosphoreszierende Emitter verwendet. Ebenfalls werden in dieser Funktion Ketone (
Im Stand der Technik bekannt ist die Verwendung von Benzimidazolverbindungen, welche mit Arylgruppen substituiert sind, in OLEDs (
In
Benzimidazolverbindungen, welche mit einem Sulfoxid oder Sulfon substituiert sind, werden auch im folgenden Stand der Technik offenbart:
- -
Korshak et al. : Synthesis and investigation of poly(benzimidazole imides) based on new di-imidodicarboxylic acids, Polymer Science U.S.S.R. 1980, Vol. 22, No 6, S. 1325-1333 - -
Jouanneau et al. : Synthesis and characterization of ionic conducting sulfonated polybenzimidazoles, J. Polym. Sci. Part A, 2010, Vol. 48, No. 8, S. 1732-1742 - -
Korshak et al. : Two-stage synthesis of poly(N-phenylbenzimidazoles, Macromolecules 1972, Vol. 5, No. 6, S. 807-812 - -
WO 2011/076323 A1
- -
Korshak et al. : Synthesis and investigation of poly(benzimidazole imides) based on new di-imidodicarboxylic acids, Polymer Science USSR 1980, Vol. 22, No 6, pp. 1325-1333 - -
Jouanneau et al. : Synthesis and characterization of ionic conducting sulfonated polybenzimidazoles, J. Polym. Sci. Part A, 2010, Vol. 48, No. 8, pp. 1732-1742 - -
Korshak et al. : Two-stage synthesis of poly(N-phenylbenzimidazoles, Macromolecules 1972, Vol. 5, No. 6, pp. 807-812 - -
WO 2011/076323 A1
Der vorliegenden Erfindung liegt somit die technische Aufgabe zu Grunde, alternative Verbindungen bereitzustellen, welche sich zur Verwendung in elektronischen Vorrichtungen wie beispielsweise OLEDs eignen, und welche insbesondere als Matrixmaterialien für phosphoreszierende Emitter und/oder als Elektronentransportmaterialien eingesetzt werden können.The present invention is therefore based on the technical object of providing alternative compounds which are suitable for use in electronic devices such as OLEDs and which can be used in particular as matrix materials for phosphorescent emitters and/or as electron transport materials.
Im Rahmen der vorliegenden Erfindung wurde nun gefunden, dass sich Verbindungen der unten angegebenen Formel (I) oder (II) ausgezeichnet zur Verwendung in elektronischen Vorrichtungen eignen, besonders als Matrixmaterialien für phosphoreszierende Emitter und/oder als Elektronentransportmaterialien.Within the scope of the present invention, it has now been found that compounds of the formula (I) or (II) given below are excellently suitable for use in electronic devices, in particular as matrix materials for phosphorescent emitters and/or as electron transport materials.
Gegenstand der Erfindung ist somit eine elektronische Vorrichtung enthaltend mindestens eine organische Schicht, wobei die organische Schicht eine oder mehrere Verbindungen einer Formel (I) oder (II) umfasst
- E
- ist eine divalente Gruppe gewählt aus S=O und S(=O)2;
- W, X
- sind bei jedem Auftreten gleich oder verschieden N, P oder CR1;
- Y
- ist bei jedem Auftreten gleich oder verschieden NR1, PR1, O oder S;
- Z
- ist gleich C, wenn ein Substituent gebunden ist, und ist anderenfalls bei jedem Auftreten gleich oder verschieden CR1 oder N;
- R1
- ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, C(=O)R2, CN, Si(R2)3, N(R2)2, NO2, P(=O)(R2)2, S(=O)R2, S(=O)2R2, eine geradkettige Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen, wobei die obengenannten Gruppen jeweils mit einem oder mehreren Resten R2 substituiert sein können und wobei eine oder mehrere CH2-Gruppen in den oben genannten Gruppen durch -R2C=CR2-, -C≡C- , Si(R2)2, C=O, C=S, C=NR2, -C(=O)O-, -C(=O)NR2-, NR2, P(=O)(R2), -O-, -S-, SO oder SO2 ersetzt sein können und wobei ein oder mehrere H-Atome in den oben genannten Gruppen durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R2 substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 30 aromatischen Ringatomen, die durch einen oder mehrere Reste R2 substituiert sein kann, wobei zwei oder mehr Reste R1 miteinander verknüpft sein können und einen Ring bilden können; wobei die Gruppe R1, die an die Gruppe E gebunden ist, gewählt ist aus aromatischen oder heteroaromatischen Ringsystemen mit 5 bis 30 aromatischen Ringatomen, welche jeweils mit einem oder mehreren Resten R2 substituiert sein können;
- R2
- ist bei jedem Auftreten gleich oder verschieden H, D, F, Cl, Br, I, C(=O)R3, CN, Si(R3)3, N(R3)2, NO2, P(=O)(R3)2, S(=O)R3, S(=O)2R3, eine geradkettige Alkyl-, Alkoxy- oder Thioalkylgruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkylgruppe mit 3 bis 20 C-Atomen oder eine Alkenyl- oder Alkinylgruppe mit 2 bis 20 C-Atomen, wobei die oben genannten Gruppen jeweils mit einem oder mehreren Resten R3 substituiert sein können und wobei eine oder mehrere CH2-Gruppen in den oben genannten Gruppen durch -R3C=CR3-, -C≡C- , Si(R3)2, C=O, C=S, C=NR3, -C(=O)O-, -C(=O)NR3-, NR3, P(=O)(R3), -O-, -S-, SO oder SO2 ersetzt sein können und wobei ein oder mehrere H-Atome in den oben genannten Gruppen durch D, F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 30 aromatischen Ringatomen, das jeweils durch einen oder mehrere Reste R3 substituiert sein kann, oder eine Aryloxy- oder Heteroaryloxygruppe mit 5 bis 30 aromatischen Ringatomen, diedurch einen oder mehrere Reste R3 substituiert sein kann, wobei zwei oder mehr Reste R2 miteinander verknüpft sein können und einen Ring bilden können;
- R3
- ist bei jedem Auftreten gleich oder verschieden H, D, F oder ein aliphatischer, aromatischer oder heteroaromatischer organischer Rest mit 1 bis 20 C-Atomen, in dem auch ein oder mehrere H-Atome durch D oder F ersetzt sein können; dabei können zwei oder mehr Substituenten R3 miteinander verknüpft sein und einen Ring bilden.
- E
- is a divalent group chosen from S=O and S(=O) 2 ;
- W, X
- are the same or different at each occurrence: N, P or CR 1 ;
- Y
- is the same or different at each occurrence: NR 1 , PR 1 , O or S;
- Z
- is equal to C when a substituent is attached and is otherwise the same or different at each occurrence and is CR 1 or N;
- R1
- is on each occurrence, identically or differently, H, D, F, Cl, Br, I, C(=O)R 2 , CN, Si(R 2 ) 3 , N(R 2 ) 2 , NO 2 , P(=O)(R 2 ) 2 , S(=O)R 2 , S(=O) 2 R 2 , a straight-chain alkyl, alkoxy or thioalkyl group having 1 to 20 C atoms or a branched or cyclic alkyl, alkoxy or thioalkyl group having 3 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms, where the abovementioned groups may each be substituted by one or more radicals R 2 and where one or more CH 2 groups in the abovementioned groups are substituted by -R 2 C=CR 2 -, -C≡C- , Si(R 2 ) 2 , C=O, C=S, C=NR 2 , -C(=O)O-, -C(=O)NR 2 -, NR 2 , P(=O)(R 2 ), -O-, -S-, SO or SO 2 and where one or more H atoms in the abovementioned groups can be replaced by D, F, Cl, Br, I, CN or NO 2 , or an aromatic or heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 2 , or an aryloxy or heteroaryloxy group having 5 to 30 aromatic ring atoms, which can be substituted by one or more radicals R 2 , where two or more radicals R 1 can be linked to one another and can form a ring; wherein the group R 1 which is bonded to the group E is selected from aromatic or heteroaromatic ring systems having 5 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 ;
- R2
- is, identically or differently on each occurrence, H, D, F, Cl, Br, I, C(=O)R 3 , CN, Si(R 3 ) 3 , N(R 3 ) 2 , NO 2 , P(=O)(R 3 )2, S(=O)R 3 , S(=O) 2 R 3 , a straight-chain alkyl, alkoxy or thioalkyl group having 1 to 20 C atoms or a branched or cyclic alkyl, alkoxy or thioalkyl group having 3 to 20 C atoms or an alkenyl or alkynyl group having 2 to 20 C atoms, where the abovementioned groups may each be substituted by one or more radicals R 3 and where one or more CH 2 groups in the abovementioned groups are -R 3 C=CR 3 -, -C≡C-, Si(R 3 ) 2 , C=O, C=S, C=NR 3 , -C(=O)O-, -C(=O)NR 3 -, NR 3 , P(=O)(R 3 ), -O-, -S-, SO or SO 2 and where one or more H atoms in the abovementioned groups can be replaced by D, F, Cl, Br, I, CN or NO 2 , or an aromatic or heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which can be substituted by one or more radicals R 3 , or an aryloxy or heteroaryloxy group having 5 to 30 aromatic ring atoms, which can be substituted by one or more radicals R 3 , where two or more radicals R 2 can be linked to one another and can form a ring;
- R3
- is on each occurrence, identically or differently, H, D, F or an aliphatic, aromatic or heteroaromatic organic radical having 1 to 20 C atoms, in which one or more H atoms may be replaced by D or F; two or more substituents R 3 may be linked to one another to form a ring.
Folgende allgemeine Definitionen gelten in der vorliegenden Anmeldung:
- Eine Arylgruppe im Sinne dieser Erfindung enthält 6 bis 60 aromatische Ringatome; eine Heteroarylgruppe im Sinne dieser Erfindung enthält 5 bis 60 aromatische Ringatome, von denen mindestens eines ein Heteroatom darstellt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und S. Dies stellt die grundlegende Definition dar. Werden in der Beschreibung der vorliegenden Erfindung andere Bevorzugungen angegeben, beispielsweise bezüglich der Zahl der aromatischen Ringatome oder der enthaltenen Heteroatome, so gelten diese.
- An aryl group in the sense of this invention contains 6 to 60 aromatic ring atoms; a heteroaryl group in the sense of this invention contains 5 to 60 aromatic ring atoms, of which at least one is a heteroatom. The heteroatoms are preferably selected from N, O and S. This represents the basic definition. If other preferences are given in the description of the present invention, for example with regard to the number of aromatic ring atoms or the heteroatoms contained, these apply.
Dabei wird unter einer Arylgruppe bzw. Heteroarylgruppe entweder ein einfacher aromatischer Cyclus, also Benzol, bzw. ein einfacher heteroaromatischer Cyclus, beispielsweise Pyridin, Pyrimidin oder Thiophen, oder ein kondensierter (annellierter) aromatischer bzw. heteroaromatischer Polycyclus, beispielsweise Naphthalin, Phenanthren, Chinolin oder Carbazol verstanden. Ein kondensierter (annellierter) aromatischer bzw. heteroaromatischer Polycyclus besteht im Sinne der vorliegenden Anmeldung aus zwei oder mehr miteinander kondensierten einfachen aromatischen bzw. heteroaromatischen Cyclen. Eine solche Gruppe wird im Rahmen der vorliegenden Erfindung auch als kondensierte Arylgruppe bzw. Heteroarylgruppe bezeichnet.An aryl group or heteroaryl group is understood to be either a simple aromatic cycle, i.e. benzene, or a simple heteroaromatic cycle, for example pyridine, pyrimidine or thiophene, or a condensed (fused) aromatic or heteroaromatic polycycle, for example naphthalene, phenanthrene, quinoline or carbazole. A condensed (fused) aromatic or heteroaromatic polycycle in the sense of the present application consists of two or more simple aromatic or heteroaromatic cycles condensed together. Such a group is also referred to as a condensed aryl group or heteroaryl group in the context of the present invention.
Unter einer Aryl- oder Heteroarylgruppe, die jeweils mit den oben genannten Resten substituiert sein kann und die über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, welche abgeleitet sind von Benzol, Naphthalin, Anthracen, Phenanthren, Pyren, Dihydropyren, Chrysen, Perylen, Fluoranthen, Benzanthracen, Benzphenanthren, Tetracen, Pentacen, Benzpyren, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, Pyrazin, Phenazin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol.An aryl or heteroaryl group, which can be substituted by the above-mentioned radicals and which can be linked to the aromatic or heteroaromatic via any position, is understood to mean in particular groups which are derived from benzene, naphthalene, anthracene, phenanthrene, pyrene, dihydropyrene, chrysene, perylene, fluoranthene, benzanthracene, benzphenanthrene, tetracene, pentacene, benzopyrene, furan, benzofuran, isobenzofuran, dibenzofuran, thiophene, benzothiophene, isobenzothiophene, dibenzothiophene, pyrrole, indole, isoindole, carbazole, pyridine, quinoline, isoquinoline, acridine, phenanthridine, benzo-5,6-quinoline, benzo-6,7-quinoline, benzo-7,8-quinoline, phenothiazine, phenoxazine, pyrazole, indazole, imidazole, benzimidazole, Naphthimidazole, phenanthrimidazole, pyridimidazole, pyrazinimidazole, quinoxalinimi dazol, oxazole, benzopyridazine, naphthoxazole, anthroxazole, phenanthroxazole, isoxazole, 1,2-thiazole, 1,3-thiazole, benzothiazole, pyridazine, benzopyridazine, pyrimidine, benzopyrimidine, quinoxaline, pyrazine, phenazine, naphthyridine, azacarbazole, benzocarboline, phenanthroline, 1,2,3-triazole, 1,2,4-triazole, benzotriazole, 1,2,3-oxadiazole, 1,2,4-oxadiazole, 1,2,5-oxadiazole, 1,3,4-oxadiazole, 1,2,3-thiadiazole, 1,2,4-thiadiazole, 1,2,5-thiadiazole, 1,3,4-thiadiazole, 1,3,5-triazine, 1,2,4-triazine, 1,2,3-triazine, tetrazole, 1,2,4,5-tetrazine, 1,2,3,4-tetrazine, 1,2,3,5-tetrazine, purine, pteridine, indolizine and benzothiadiazole.
Unter einer Aryloxygruppe gemäß der Definition der vorliegenden Erfindung wird eine Arylgruppe, wie oben definiert, verstanden, welche über ein Sauerstoffatom gebunden ist. Eine analoge Definition gilt für Heteroaryloxygruppen.An aryloxy group according to the definition of the present invention is understood to mean an aryl group as defined above which is bonded via an oxygen atom. An analogous definition applies to heteroaryloxy groups.
Ein aromatisches Ringsystem im Sinne dieser Erfindung enthält 6 bis 60 C-Atome im Ringsystem. Ein heteroaromatisches Ringsystem im Sinne dieser Erfindung enthält 5 bis 60 aromatische Ringatome, von denen mindestens eines ein Heteroatom darstellt. Die Heteroatome sind bevorzugt ausgewählt aus N, O und/oder S. Unter einem aromatischen oder heteroaromatischen Ringsystem im Sinne dieser Erfindung soll ein System verstanden werden, das nicht notwendigerweise nur Aryl- oder Heteroarylgruppen enthält, sondern in dem auch mehrere Aryl- oder Heteroarylgruppen durch eine nicht-aromatische Einheit (bevorzugt weniger als 10 % der von H verschiedenen Atome), wie z. B. ein sp3-hybridisiertes C-, Si-, N- oder O-Atom, ein sp2-hybridisiertes C- oder N-Atom oder ein sp-hybridisiertes C-Atom, verbunden sein können. So sollen beispielsweise auch Systeme wie 9,9'-Spirobifluoren, 9,9'-Diarylfluoren, Triarylamin, Diarylether, Stilben, etc. als aromatische Ringsysteme im Sinne dieser Erfindung verstanden werden, und ebenso Systeme, in denen zwei oder mehrere Arylgruppen beispielsweise durch eine lineare oder cyclische Alkyl-, Alkenyl- oder Alkinylgruppe oder durch eine Silylgruppe verbunden sind. Weiterhin werden auch Systeme, in denen zwei oder mehr Aryl- oder Heteroarylgruppen über Einfachbindungen miteinander verknüpft sind, als aromatische oder heteroaromatische Ringsysteme im Sinne dieser Erfindung verstanden, wie beispielsweise Systeme wie Biphenyl, Terphenyl oder Diphenyltriazin.An aromatic ring system in the sense of this invention contains 6 to 60 C atoms in the ring system. A heteroaromatic ring system in the sense of this invention contains 5 to 60 aromatic ring atoms, of which at least one is a heteroatom. The heteroatoms are preferably selected from N, O and/or S. An aromatic or heteroaromatic ring system in the sense of this invention is to be understood as a system which does not necessarily only contain aryl or heteroaryl groups, but in which several aryl or heteroaryl groups can also be connected by a non-aromatic unit (preferably less than 10% of the atoms other than H), such as an sp 3 -hybridized C, Si, N or O atom, an sp 2 -hybridized C or N atom or an sp-hybridized C atom. For example, systems such as 9,9'-spirobifluorene, 9,9'-diarylfluorene, triarylamine, diaryl ether, stilbene, etc. are to be understood as aromatic ring systems within the meaning of this invention, as are systems in which two or more aryl groups are linked, for example, by a linear or cyclic alkyl, alkenyl or alkynyl group or by a silyl group. Furthermore, systems in which two or more aryl or heteroaryl groups are linked to one another via single bonds are also to be understood as aromatic or heteroaromatic ring systems within the meaning of this invention, for example systems such as biphenyl, terphenyl or diphenyltriazine.
Unter einem aromatischen oder heteroaromatischen Ringsystem mit 5 - 60 aromatischen Ringatomen, welches noch jeweils mit Resten wie oben definiert substituiert sein kann und welches über beliebige Positionen am Aromaten bzw. Heteroaromaten verknüpft sein kann, werden insbesondere Gruppen verstanden, die abgeleitet sind von Benzol, Naphthalin, Anthracen, Benzanthracen, Phenanthren, Benzphenanthren, Pyren, Chrysen, Perylen, Fluoranthen, Naphthacen, Pentacen, Benzpyren, Biphenyl, Biphenylen, Terphenyl, Terphenylen, Quaterphenyl, Fluoren, Spirobifluoren, Dihydrophenanthren, Dihydropyren, Tetrahydropyren, cis- oder trans-Indenofluoren, Truxen, Isotruxen, Spirotruxen, Spiroisotruxen, Furan, Benzofuran, Isobenzofuran, Dibenzofuran, Thiophen, Benzothiophen, Isobenzothiophen, Dibenzothiophen, Pyrrol, Indol, Isoindol, Carbazol, Indolocarbazol, Indenocarbazol, Pyridin, Chinolin, Isochinolin, Acridin, Phenanthridin, Benzo-5,6-chinolin, Benzo-6,7-chinolin, Benzo-7,8-chinolin, Phenothiazin, Phenoxazin, Pyrazol, Indazol, Imidazol, Benzimidazol, Naphthimidazol, Phenanthrimidazol, Pyridimidazol, Pyrazinimidazol, Chinoxalinimidazol, Oxazol, Benzoxazol, Naphthoxazol, Anthroxazol, Phenanthroxazol, Isoxazol, 1,2-Thiazol, 1,3-Thiazol, Benzothiazol, Pyridazin, Benzopyridazin, Pyrimidin, Benzpyrimidin, Chinoxalin, 1,5-Diazaanthracen, 2,7-Diazapyren, 2,3-Diazapyren, 1,6-Diazapyren, 1,8-Diazapyren, 4,5-Diazapyren, 4,5,9,10-Tetraazaperylen, Pyrazin, Phenazin, Phenoxazin, Phenothiazin, Fluorubin, Naphthyridin, Azacarbazol, Benzocarbolin, Phenanthrolin, 1,2,3-Triazol, 1,2,4-Triazol, Benzotriazol, 1,2,3-Oxadiazol, 1,2,4-Oxadiazol, 1,2,5-Oxadiazol, 1,3,4-Oxadiazol, 1,2,3-Thiadiazol, 1,2,4-Thiadiazol, 1,2,5-Thiadiazol, 1,3,4-Thiadiazol, 1,3,5-Triazin, 1,2,4-Triazin, 1,2,3-Triazin, Tetrazol, 1,2,4,5-Tetrazin, 1,2,3,4-Tetrazin, 1,2,3,5-Tetrazin, Purin, Pteridin, Indolizin und Benzothiadiazol oder Kombinationen dieser Gruppen.An aromatic or heteroaromatic ring system with 5 - 60 aromatic ring atoms, which can be substituted with residues as defined above and which can be linked to the aromatic or heteroaromatic ring via any position, is understood to mean in particular groups which are derived from benzene, naphthalene, anthracene, benzanthracene, phenanthrene, benzphenanthrene, pyrene, chrysene, perylene, fluoranthene, naphthacene, pentacene, benzopyrene, biphenyl, biphenylene, terphenyl, terphenylene, quaterphenyl, fluorene, spirobifluorene, dihydrophenanthrene, dihydropyrene, cis- or trans-indenofluorene, truxene, isotruxene, spirotruxene, spiroisotruxene, furan, benzofuran, isobenzofuran, dibenzofuran, thiophene, benzothiophene, isobenzothiophene, dibenzothiophene, pyrrole, indole, Isoindole, carbazole, indolocarbazole, indenocarbazole, pyridine, quinoline, isoquinoline, acridine, phenanthridine, benzo-5,6-quinoline, benzo-6,7-quinoline, benzo-7,8-quinoline, phenothiazine, phenoxazine, pyrazole, indazole, imidazole, benzimidazole, naphthimidazole, Phenanthrimidazole, Pyridimidazole, Pyrazinimidazole, Quinoxalinimidazole, Oxazole, Benzoxazole, Naphthoxazole, Anthroxazole, Phenanthroxazole, Isoxazole, 1,2-thiazole, 1,3-thiazole, Benzothiazole, Pyridazine, Benzopyridazine, Pyrimidine, Benzpyrimidine, Quinoxaline, 1,5-diazaanthracene, 2,7-diazapyrene, 2,3-diazapyrene, 1,6-diazapyrene, 1,8-diazapyrene, 4,5-diazapyrene, 4,5,9,10-tetraazaperylene, pyrazine, phenazine, phenoxazine, phenothiazine, fluorubin, naphthyridine, azacarbazole, benzocarboline, phenanthroline, 1,2,3-triazole, 1,2,4-triazole, benzotriazole, 1,2,3-oxadiazole, 1,2,4-oxadiazole, 1,2,5-oxadiazole, 1,3,4-oxadiazole, 1,2,3-thiadiazole, 1,2,4-thiadiazole, 1,2,5-thiadiazole, 1,3,4-thiadiazole, 1,3,5-triazine, 1,2,4-triazine, 1,2,3-triazine, tetrazole, 1,2,4,5-tetrazine, 1,2,3,4-tetrazine, 1,2,3,5-tetrazine, purine, pteridine, indolizine and benzothiadiazole or combinations of these groups.
Im Rahmen der vorliegenden Erfindung werden unter einer geradkettigen Alkylgruppe mit 1 bis 40 C-Atomen bzw. einer verzweigten oder cyclischen Alkylgruppe mit 3 bis 40 C-Atomen bzw. einer Alkenyl- oder Alkinylgruppe mit 2 bis 40 C-Atomen, in der auch einzelne H-Atome oder CH2-Gruppen durch die oben bei der Definition der Reste genannten Gruppen substituiert sein können, bevorzugt die Reste Methyl, Ethyl, n-Propyl, i-Propyl, n-Butyl, i-Butyl, s-Butyl, t-Butyl, 2-Methylbutyl, n-Pentyl, s-Pentyl, Cyclopentyl, neoPentyl, n-Hexyl, Cyclohexyl, neo-Hexyl, n-Heptyl, Cycloheptyl, n-Octyl, Cyclooctyl, 2-Ethylhexyl, Trifluormethyl, Pentafluorethyl, 2,2,2-Trifluorethyl, Ethenyl, Propenyl, Butenyl, Pentenyl, Cyclopentenyl, Hexenyl, Cyclohexenyl, Heptenyl, Cycloheptenyl, Octenyl, Cyclooctenyl, Ethinyl, Propinyl, Butinyl, Pentinyl, Hexinyl oder Octinyl verstanden. Unter einer Alkoxy- oder Thioalkylgruppe mit 1 bis 40 C-Atomen werden bevorzugt Methoxy, Trifluormethoxy, Ethoxy, n-Propoxy, i-Propoxy, n-Butoxy, i-Butoxy, s-Butoxy, t-Butoxy, n-Pentoxy, s-Pentoxy, 2-Methylbutoxy, n-Hexoxy, Cyclohexyloxy, n-Heptoxy, Cycloheptyloxy, n-Octyloxy, Cyclooctyloxy, 2-Ethylhexyloxy, Pentafluorethoxy, 2,2,2-Trifluorethoxy, Methylthio, Ethylthio, n-Propylthio, i-Propylthio, n-Butylthio, i-Butylthio, s-Butylthio, t-Butylthio, n-Pentylthio, s-Pentylthio, n-Hexylthio, Cyclohexylthio, n-Heptylthio, Cycloheptylthio, n-Octylthio, Cyclooctylthio, 2-Ethylhexylthio, Trifluormethylthio, Pentafluorethylthio, 2,2,2-Trifluorethylthio, Ethenylthio, Propenylthio, Butenylthio, Pentenylthio, Cyclopentenylthio, Hexenylthio, Cyclohexenylthio, Heptenylthio, Cycloheptenylthio, Octenylthio, Cyclooctenylthio, Ethinylthio, Propinylthio, Butinylthio, Pentinylthio, Hexinylthio, Heptinylthio oder Octinylthio verstanden.In the context of the present invention, a straight-chain alkyl group having 1 to 40 C atoms or a branched or cyclic alkyl group having 3 to 40 C atoms or an alkenyl or alkynyl group having 2 to 40 C atoms, in which individual H atoms or CH 2 groups can also be substituted by the groups mentioned above in the definition of the radicals, preferably the radicals methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, s-butyl, t-butyl, 2-methylbutyl, n-pentyl, s-pentyl, cyclopentyl, neopentyl, n-hexyl, cyclohexyl, neo-hexyl, n-heptyl, cycloheptyl, n-octyl, cyclooctyl, 2-ethylhexyl, Trifluoromethyl, pentafluoroethyl, 2,2,2-trifluoroethyl, ethenyl, propenyl, butenyl, pentenyl, cyclopentenyl, hexenyl, cyclohexenyl, heptenyl, cycloheptenyl, octenyl, cyclooctenyl, ethynyl, propynyl, butynyl, pentinyl, hexynyl or octynyl. Among an alkoxy or thioalkyl group with 1 to 40 carbon atoms, preference is given to methoxy, trifluoromethoxy, ethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, n-pentoxy, s-pentoxy, 2-methylbutoxy, n-hexoxy, cyclohexyloxy, n-Heptoxy, Cycloheptyloxy, n-Octyloxy, Cyclooctyloxy, 2-Ethylhexyloxy, Pentafluorethoxy, 2,2,2-Trifluorethoxy, Methylthio, Ethylthio, n-Propylthio, i-Propylthio, n-Butylthio, i-Butylthio, s-Butylthio, t-Butylthio, n-pentylthio, s-pentylthio, n-hexylthio, cyclohexylthio, n-Heptylthio, Cyclo heptylthio, n-octylthio, cyclooctylthio, 2-ethylhexylthio, trifluoromethylthio, pentafluoroethylthio, 2,2,2-trifluoroethylthio, ethenylthio, propenylthio, butenylthio, pentenylthio, cyclopentenylthio, hexenylthio, cyclohexenylthio, heptenylthio, Cycloheptenylthio, octenylthio, cyclooctenylthio, ethynylthio, propynylthio, butynylthio, pentinylthio, hexynylthio, heptynylthio or octynylthio are understood.
Unter der Formulierung, dass zwei oder mehr Reste miteinander einen Ring bilden können, soll im Rahmen der vorliegenden Anmeldung unter anderem verstanden werden, dass die beiden Reste miteinander durch eine chemische Bindung verknüpft sind. Dies wird durch das folgende Schema verdeutlicht:
Weiterhin soll unter der oben genannten Formulierung aber auch verstanden werden, dass für den Fall, dass einer der beiden Reste Wasserstoff darstellt, der zweite Rest unter Bildung eines Rings an die Position, an die das Wasserstoffatom gebunden war, bindet. Dies soll durch das folgende Schema verdeutlicht werden:
Es gelten die folgenden bevorzugten Ausführungsformen für die Verbindungen der Formel (I) und (II).The following preferred embodiments apply to the compounds of formula (I) and (II).
Bevorzugt ist E gleich S(=O)2.Preferably, E is S(=O) 2 .
Die Gruppe E kann an einer beliebigen Position am Sechsring gebunden sein und ist bevorzugt in meta- oder in para-Position zur Gruppe Y gebunden.The group E can be bonded to any position on the six-membered ring and is preferably bonded in meta- or para-position to the group Y.
Bevorzugt ist W bei jedem Auftreten gleich oder verschieden N oder CR1. Besonders bevorzugt ist W gleich N.Preferably, W is the same or different at each occurrence from N or CR 1 . Particularly preferably, W is N.
Bevorzugt ist X bei jedem Auftreten gleich oder verschieden N oder CR1. Besonders bevorzugt ist X gleich CR1.Preferably, X is the same or different on each occurrence and is N or CR 1 . Particularly preferably, X is CR 1 .
Bevorzugt ist Y bei jedem Auftreten gleich oder verschieden NR1, O oder S, besonders bevorzugt NR1.Preferably, Y is the same or different on each occurrence and is NR 1 , O or S, particularly preferably NR 1 .
Ganz besonders bevorzugt ist eine Ausführungsform, in der W gleich N ist, X gleich CR1 ist und Y gleich NR1 ist.Very particularly preferred is an embodiment in which W is N, X is CR 1 and Y is NR 1 .
Bevorzugt weist die Verbindung der Formel (I) oder (II) keine kondensierte Arylgruppe mit mehr als 13 aromatischen Ringatomen auf. Es wurde gefunden, dass ohne das Vorhandensein einer kondensierten Arylgruppe mit mehr als 13 aromatischen Ringatomen in der Verbindung OLEDs mit deutlich verbesserten Eigenschaften bezüglich der Effizienz und der Lebensdauer erhalten werden können. Insbesondere gilt dies für OLEDs enthaltend die Verbindung in einer Schicht, welche einen oder mehrere phosphoreszierende Emitter enthält. Besonders bevorzugt weist die Verbindung der Formel (I) oder (II) keine kondensierte Arylgruppe mit mehr als 10 aromatischen Ringatomen auf.The compound of formula (I) or (II) preferably does not have a condensed aryl group with more than 13 aromatic ring atoms. It has been found that without the presence of a condensed aryl group with more than 13 aromatic ring atoms in the compound, OLEDs with significantly improved properties in terms of efficiency and lifetime can be obtained. This applies in particular to OLEDs containing the compound in a layer which contains one or more phosphorescent emitters. The compound of formula (I) or (II) particularly preferably does not have a condensed aryl group with more than 10 aromatic ring atoms.
Bevorzugt ist für den Fall dass an eine Gruppe Z kein Substituent gebunden ist, diese Gruppe Z gleich CR1. Weiterhin ist es bevorzugt, dass 0, 1 oder 2 Gruppen Z pro aromatischem Sechsring gleich N sind und die restlichen Gruppen Z, an die kein Substituent gebunden ist, gleich CR1 sind. Weiterhin ist es bevorzugt, dass nicht mehr als zwei benachbarte Gruppen Z gleich N sind.In the case where no substituent is bonded to a group Z, this group Z is preferably CR 1 . It is furthermore preferred that 0, 1 or 2 groups Z per aromatic six-membered ring are N and the remaining groups Z to which no substituent is bonded are CR 1 . It is furthermore preferred that no more than two adjacent groups Z are N.
Bevorzugt ist R1 bei jedem Auftreten gleich oder verschieden H, D, F, CN, Si(R2)3, N(R2)2, eine geradkettige Alkyl- oder Alkoxygruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl- oder Alkoxygruppe mit 3 bis 20 C-Atomen, wobei die oben genannten Gruppen jeweils mit einem oder mehreren Resten R2 substituiert sein können und wobei in den oben genannten Gruppen eine oder mehrere CH2-Gruppen durch -C=C-, -R2C=CR2-, Si(R2)2, C=O, C=NR2, -NR2-, -O-, -S-, -C(=O)O- oder -C(=O)NR2- ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 20 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R2 substituiert sein kann, wobei zwei oder mehr Reste R1 miteinander verknüpft sein können und einen Ring bilden können; wobei die Gruppe R1, die an die Gruppe E gebunden ist, gewählt ist aus aromatischen oder heteroaromatischen Ringsystemen mit 5 bis 30 aromatischen Ringatomen, welche jeweils mit einem oder mehreren Resten R2 substituiert sein können. Bevorzugt ist die Gruppe R1, die an die Gruppe E gebunden ist, gewählt aus aromatischen Ringsystemen mit 6 bis 18 aromatischen Ringatomen, welche mit einem oder mehreren Resten R2 substituiert sein können.Preferably, R 1 is, identically or differently on each occurrence, H, D, F, CN, Si(R 2 ) 3 , N(R 2 ) 2 , a straight-chain alkyl or alkoxy group having 1 to 20 C atoms or a branched or cyclic alkyl or alkoxy group having 3 to 20 C atoms, where the abovementioned groups may each be substituted by one or more radicals R 2 and where in the abovementioned groups one or more CH 2 groups may be replaced by -C=C-, -R 2 C=CR 2 -, Si(R 2 ) 2 , C=O, C=NR 2 , -NR 2 -, -O-, -S-, -C(=O)O- or -C(=O)NR 2 -, or an aromatic or heteroaromatic ring system having 5 to 20 aromatic ring atoms, each of which may be substituted by one or more R 2 radicals, where two or more R 1 radicals can be linked to one another and can form a ring; where the group R 1 which is bonded to the group E is selected from aromatic or heteroaromatic ring systems having 5 to 30 aromatic ring atoms, which can each be substituted by one or more R 2 radicals. Preferably, the group R 1 which is bonded to the group E is selected from aromatic ring systems having 6 to 18 aromatic ring atoms, which can be substituted by one or more R 2 radicals.
Bevorzugt ist R2 bei jedem Auftreten gleich oder verschieden H, D, F, CN, Si(R3)3, N(R3)2, eine geradkettige Alkyl- oder Alkoxygruppe mit 1 bis 20 C-Atomen oder eine verzweigte oder cyclische Alkyl- oder Alkoxygruppe mit 3 bis 20 C-Atomen, wobei die oben genannten Gruppen jeweils mit einem oder mehreren Resten R3 substituiert sein können und wobei in den oben genannten Gruppen eine oder mehrere CH2-Gruppen durch -C≡C-, -R3C=CR3-, Si(R3)2, C=O, C=NR3, -NR3-, -O-, -S-, -C(=O)O- oder -C(=O)NR3- ersetzt sein können, oder ein aromatisches oder heteroaromatisches Ringsystem mit 5 bis 20 aromatischen Ringatomen, das jeweils mit einem oder mehreren Resten R3 substituiert sein kann, wobei zwei oder mehr Reste R2 miteinander verknüpft sein können und einen Ring bilden können.Preferably, R 2 is, identically or differently on each occurrence, H, D, F, CN, Si(R 3 ) 3 , N(R 3 ) 2 , a straight-chain alkyl or alkoxy group having 1 to 20 C atoms or a branched or cyclic alkyl or alkoxy group having 3 to 20 C atoms, where the abovementioned groups may each be substituted by one or more radicals R 3 and where in the abovementioned groups one or more CH 2 groups may be replaced by -C≡C-, -R 3 C=CR 3 -, Si(R 3 ) 2 , C=O, C=NR 3 , -NR 3 -, -O-, -S-, -C(=O)O- or -C(=O)NR 3 -, or an aromatic or heteroaromatic ring system having 5 to 20 aromatic ring atoms, each substituted by one or more several radicals R 3 , where two or more radicals R 2 can be linked together to form a ring.
Bevorzugt ist an den Grundkörper der Verbindung der Formel (I) oder (II) mindestens eine Gruppe gebunden, welche gewählt ist aus aromatischen Ringsystemen mit 6 bis 18 aromatischen Ringatomen, bevorzugt 12 bis 18 aromatischen Ringatomen, und heteroaromatischen Ringsystemen mit 5 bis 18 aromatischen Ringatomen, welche mit jeweils mit einem oder mehreren Resten R2 substituiert sein können.Preferably, at least one group selected from aromatic ring systems having 6 to 18 aromatic ring atoms, preferably 12 to 18 aromatic ring atoms, and heteroaromatic ring systems having 5 to 18 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , is bonded to the base body of the compound of formula (I) or (II).
Besonders bevorzugt enthält die Verbindung der Formel (I) oder (II) mindestens eine Gruppe R1, welche gewählt ist aus
- - Heteroarylgruppen mit 5 bis 20 aromatischen Ringatomen, die mit einem oder mehreren Resten R2 substituiert sein können und die mindestens einen heteroaromatischen Fünfring mit zwei oder mehr Heteroatomen gewählt aus N, O und S enthalten;
- - Heteroarylgruppen mit 5 bis 20 aromatischen Ringatomen, die mit einem oder mehreren Resten R2 substituiert sein können und die mindestens einen heteroaromatischen Sechsring mit einem oder mehreren Heteroatomen gewählt aus N, O und S enthalten; und
- - Carbazolderivaten, die mit einem oder mehreren Resten R2 substituiert sein können.
- - heteroaryl groups having 5 to 20 aromatic ring atoms which may be substituted by one or more radicals R 2 and which contain at least one heteroaromatic five-membered ring with two or more heteroatoms selected from N, O and S;
- - heteroaryl groups having 5 to 20 aromatic ring atoms, which may be substituted by one or more radicals R 2 and which contain at least one heteroaromatic six-membered ring with one or more heteroatoms selected from N, O and S; and
- - Carbazole derivatives which may be substituted by one or more radicals R 2 .
Unter Carbazolderivaten werden im Sinne der vorliegenden Erfindung auch Carbazolderivate mit ankondensierten Gruppen, wie beispielsweise Indenocarbazole oder Indolocarbazole, sowie Carbazolderivate, in denen ein oder mehrere Kohlenstoffatome in den aromatischen Sechsringen durch Stickstoff ersetzt sind, verstanden.For the purposes of the present invention, carbazole derivatives also include carbazole derivatives with fused groups, such as indenocarbazoles or indolocarbazoles, as well as carbazole derivatives in which one or more carbon atoms in the aromatic six-membered rings are replaced by nitrogen.
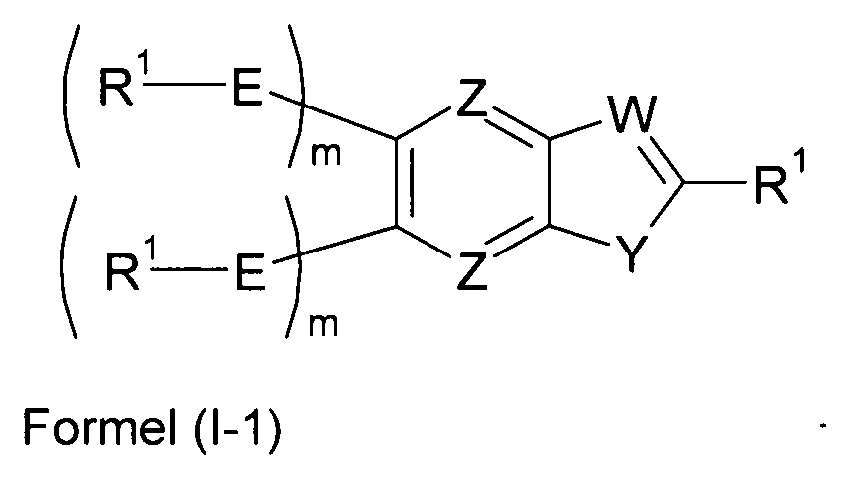
Bevorzugte Ausführungsformen der Verbindung gemäß Formel (I) entsprechen der folgenden Formel
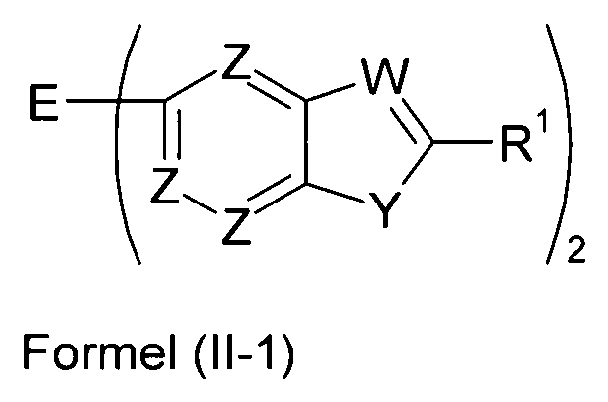
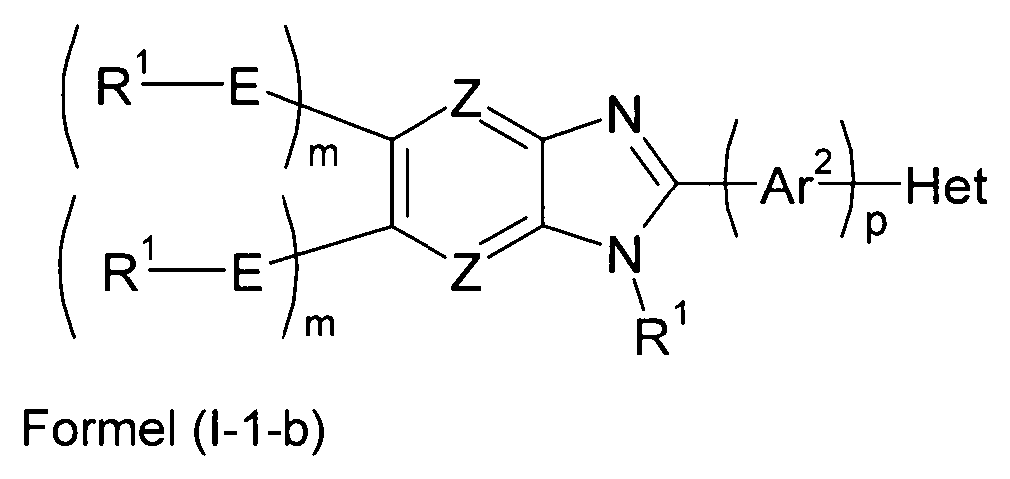
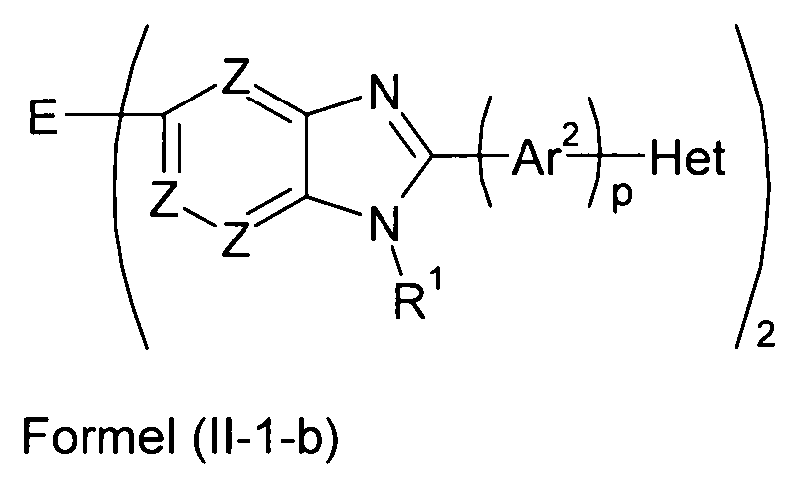
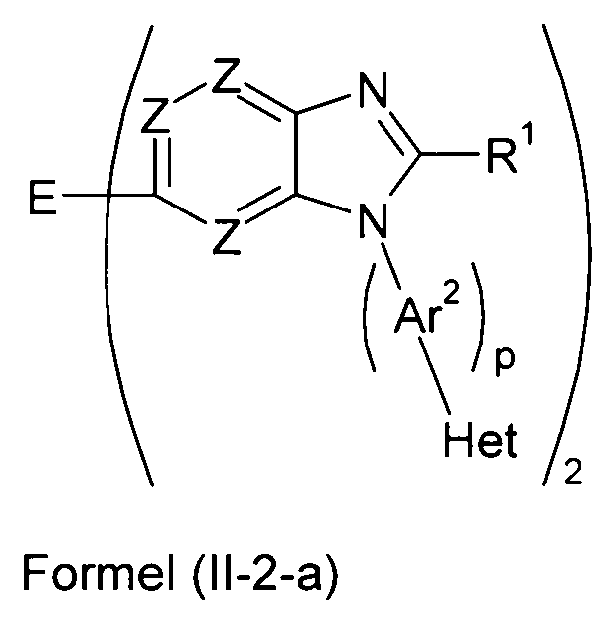
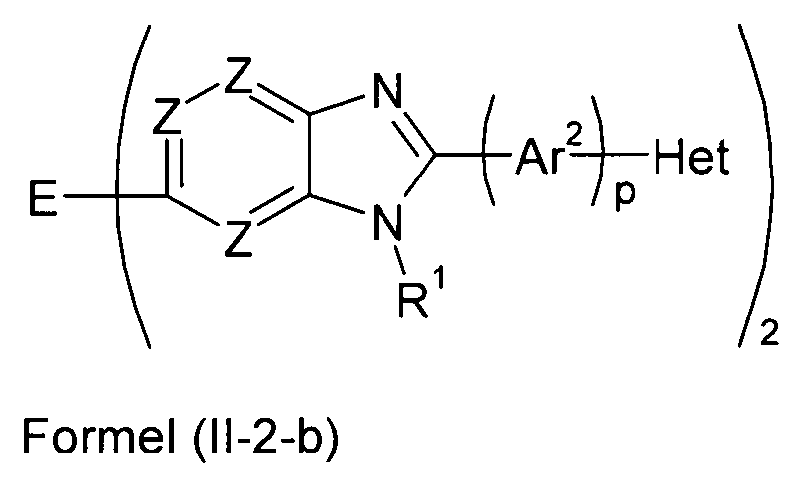
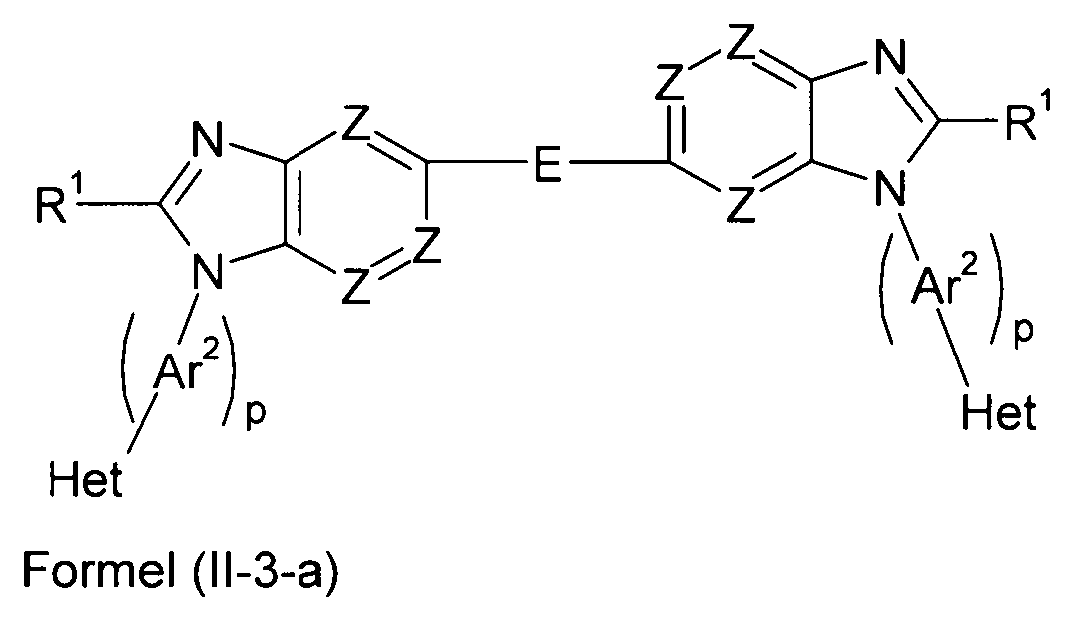
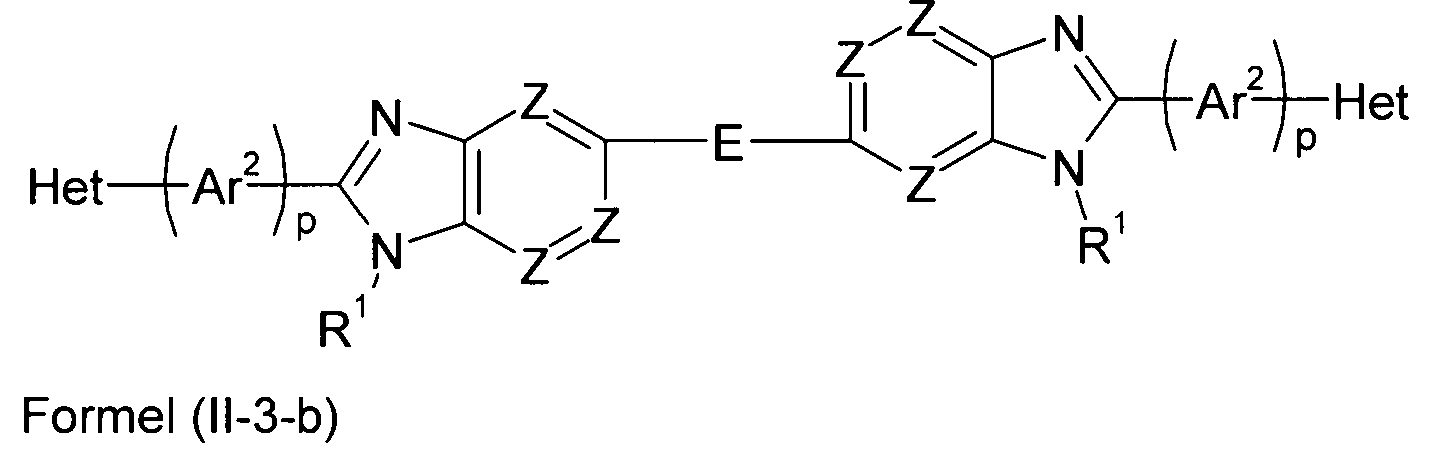
Bevorzugte Ausführungsformen der Verbindung gemäß Formel (II) entsprechen den folgenden Formeln
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (I) entspricht der folgenden Formel:
m bei jedem Auftreten gleich 0 oder 1 ist, wobei die Summe der Indices m gleich 1 ist, und
p gleich 0, 1 oder 2 ist; und
Ar2 eine Aryl- oder Heteroarylgruppe mit 5 bis 10 aromatischen Ringatomen darstellt, welche mit einem oder mehreren Resten R2 substituiert sein kann, und
Het eine Gruppe der Formel (Het-a) darstellt
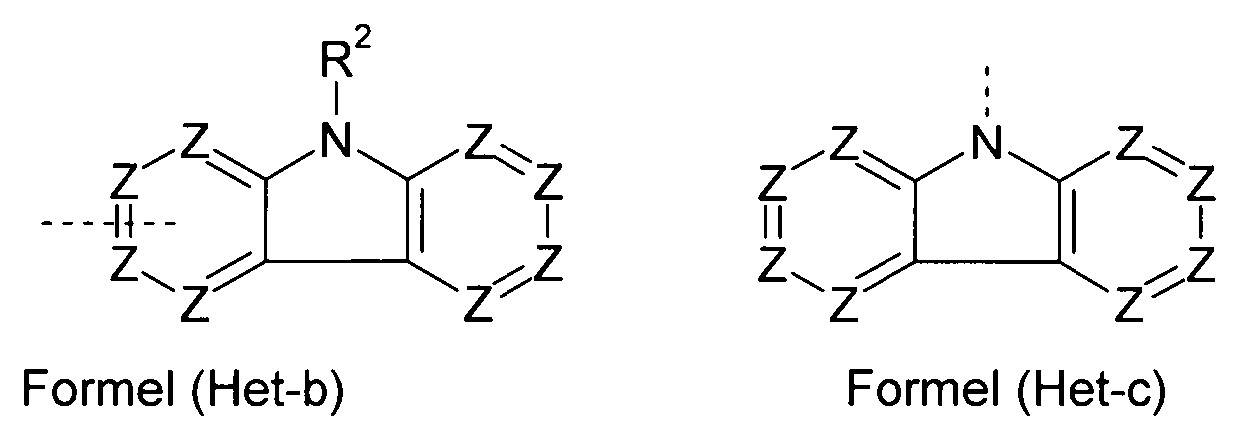
oder Het eine Gruppe der Formel (Het-b) oder (Het-c) darstellt
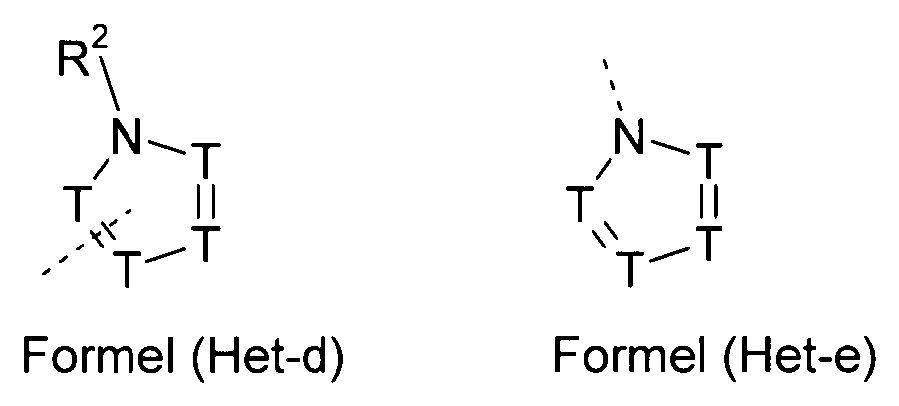
oder Het eine Gruppe der Formel (Het-d) oder (Het-e) darstellt
m is equal to 0 or 1 at each occurrence, where the sum of the indices m is equal to 1, and
p is 0, 1 or 2; and
Ar 2 represents an aryl or heteroaryl group having 5 to 10 aromatic ring atoms, which may be substituted by one or more radicals R 2 , and
Het represents a group of the formula (Het-a)
or Het represents a group of the formula (Het-b) or (Het-c)
or Het represents a group of the formula (Het-d) or (Het-e)
Eine weitere besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (I) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Eine besonders bevorzugte Ausführungsform der Verbindung gemäß Formel (II) entspricht der folgenden Formel:
Bevorzugt ist für Verbindungen der Formel (I-1-a), (1-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) und (II-3-b) Z gleich CR1 und E gleich S(=O)2. Bevorzugt ist p gleich 0.Preferably, for compounds of the formula (I-1-a), (1-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) and (II-3-b), Z is CR 1 and E is S(=O) 2 . Preferably, p is 0.
Bevorzugt sind in Gruppen der Formel (Het-a) zwei oder drei Gruppen T gleich N. Besonders bevorzugt sind Gruppen (Het-a) gewählt aus Pyrimidyl, Pyridazinyl, Pyrazinyl und Triazinyl, welche wahlweise mit Resten R2 substituiert sein können.Preferably, in groups of the formula (Het-a), two or three groups T are equal to N. Particularly preferred groups (Het-a) are selected from pyrimidyl, pyridazinyl, pyrazinyl and triazinyl, which can optionally be substituted by radicals R 2 .
Die Verbindungen der Formel (I-1-a), (1-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) und (II-3-b) sind als solche Gegenstand der vorliegenden Erfindung.The compounds of the formula (I-1-a), (I-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) and (II-3-b) are as such the subject of the present invention.
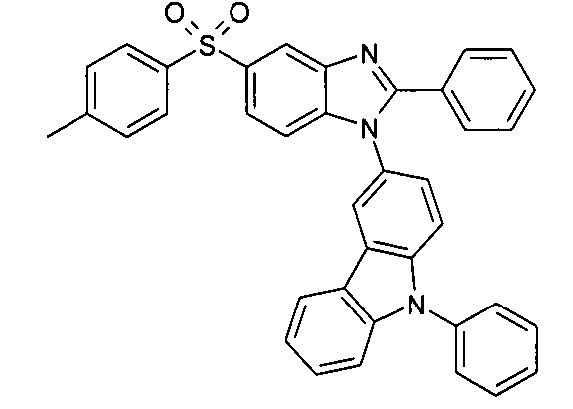
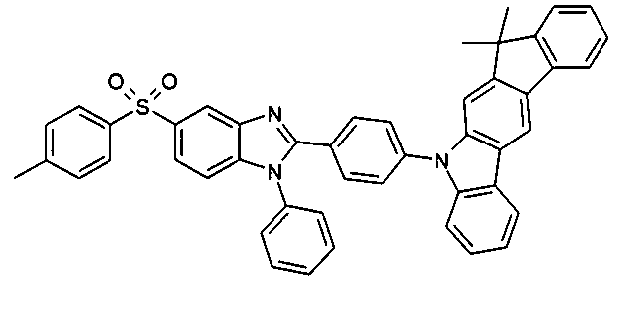
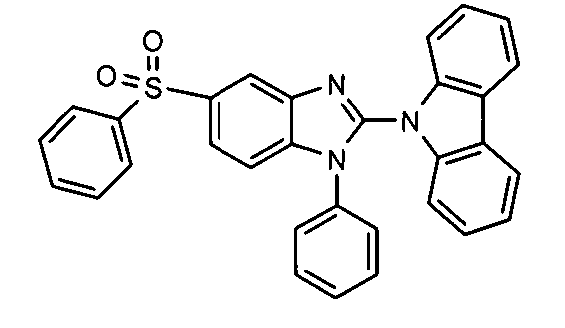
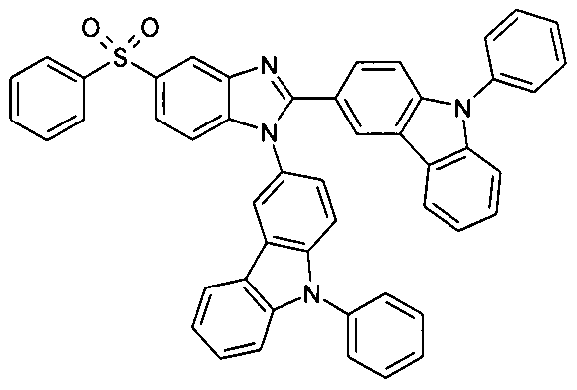
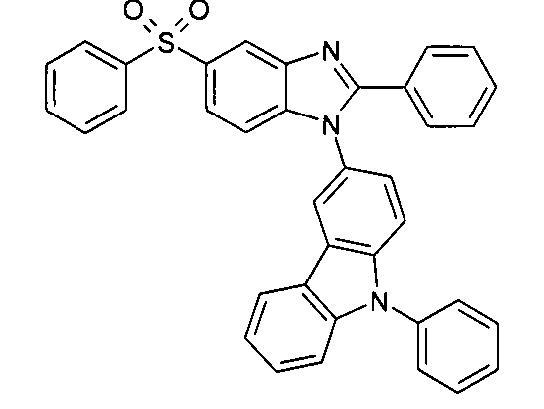
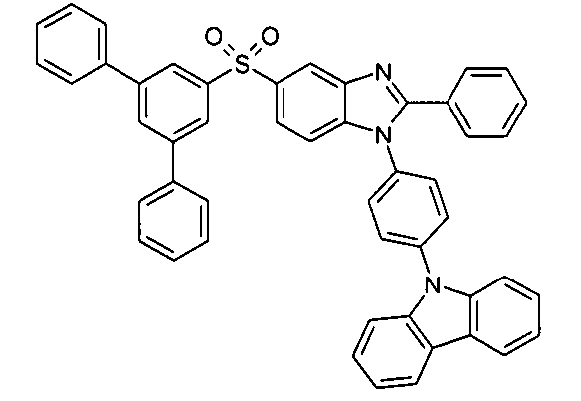
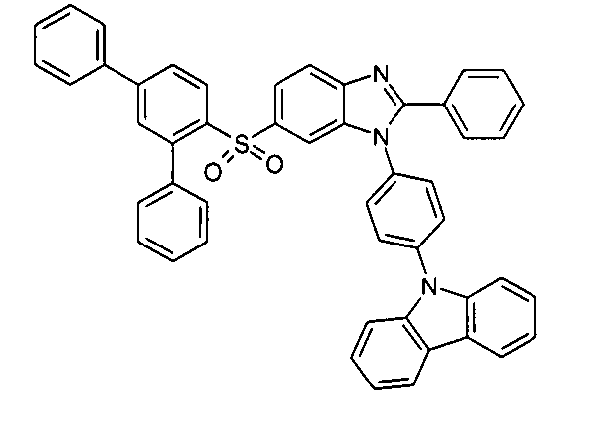
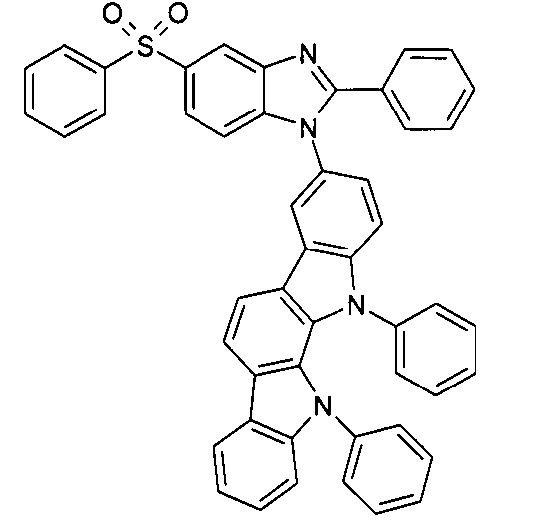
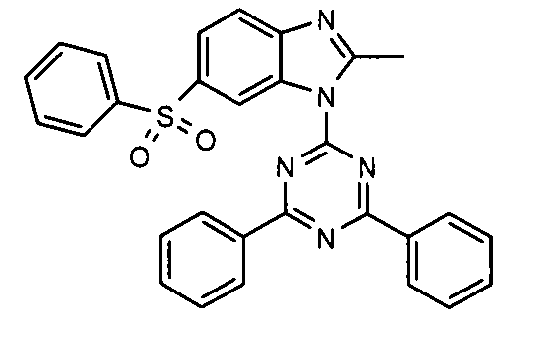
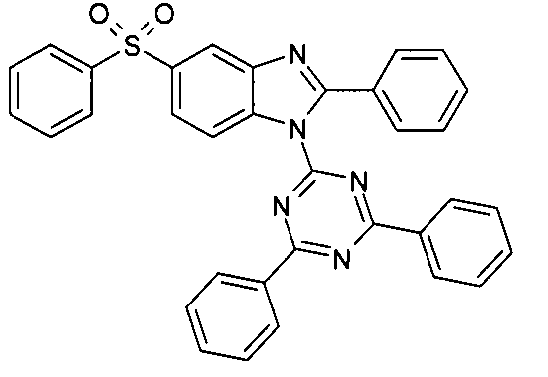
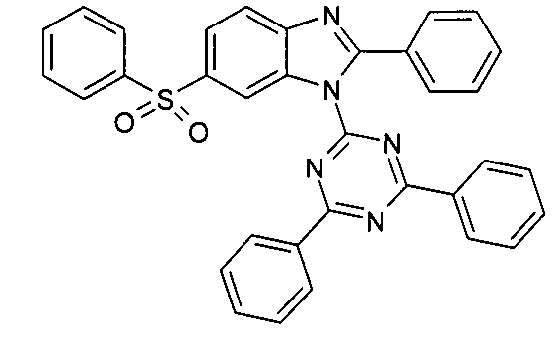
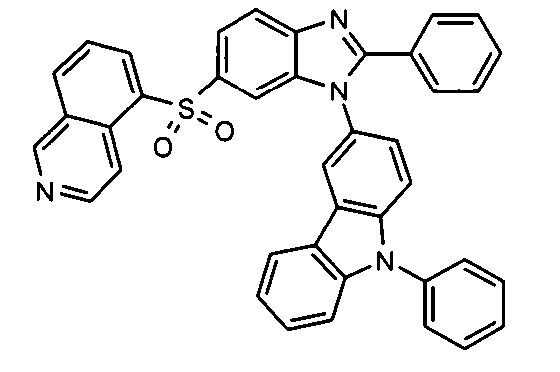
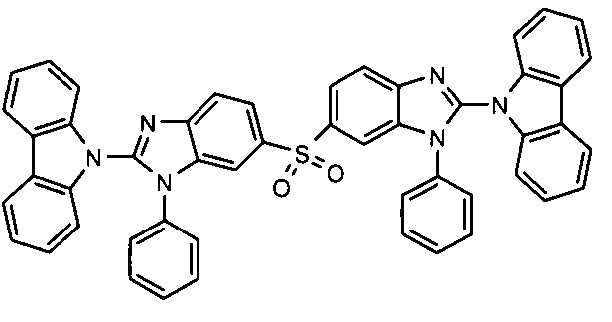
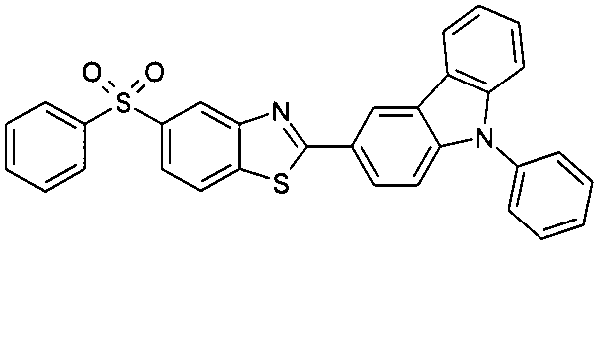
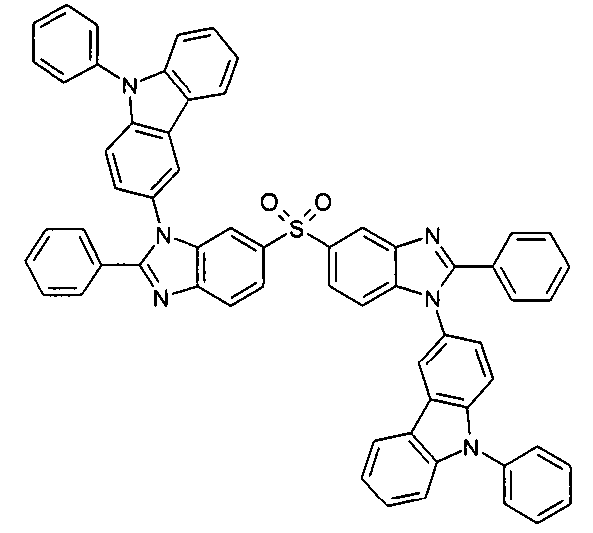
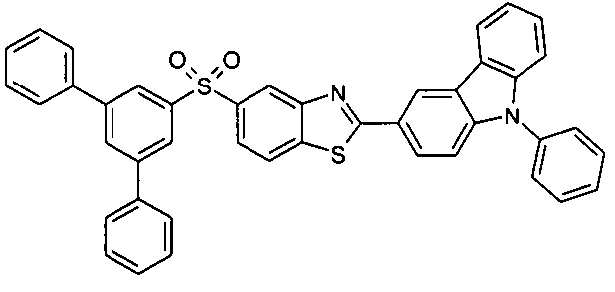
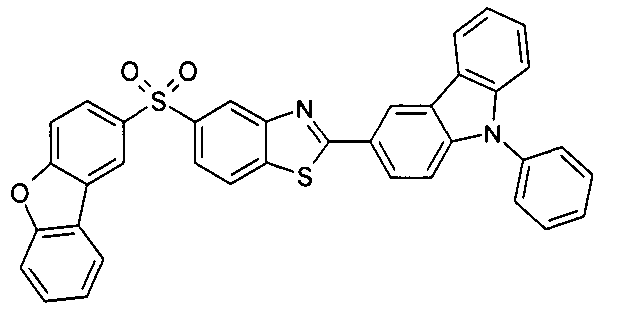
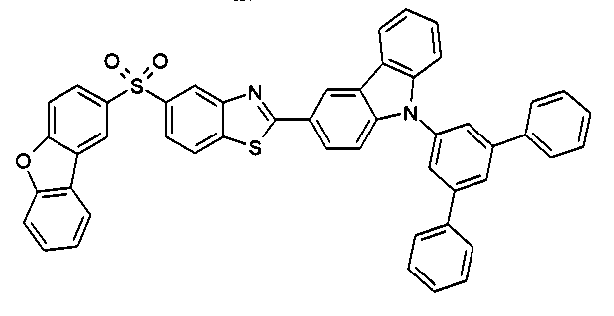
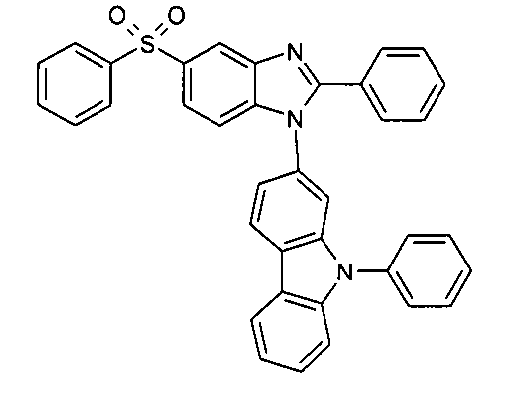
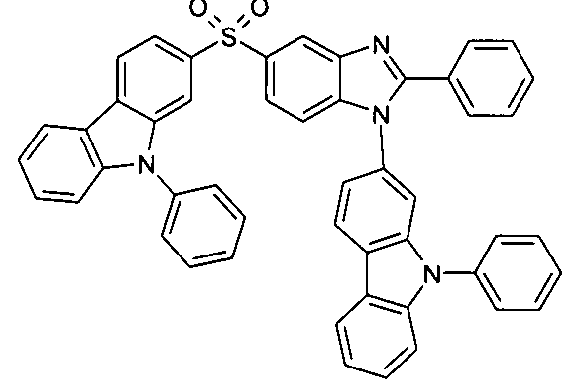
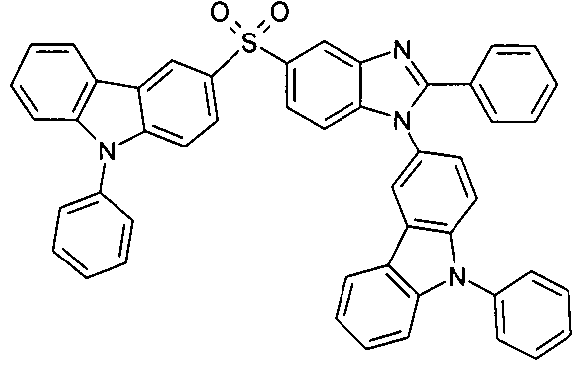
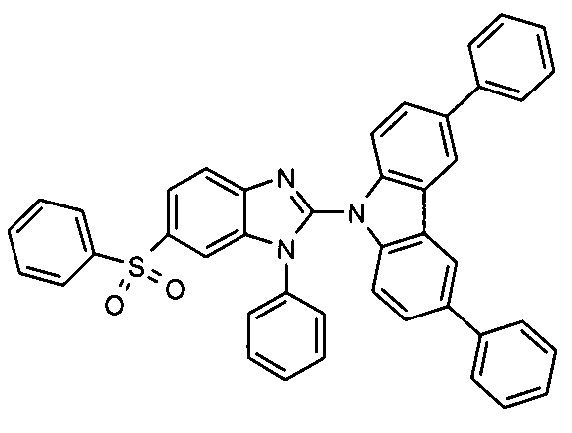
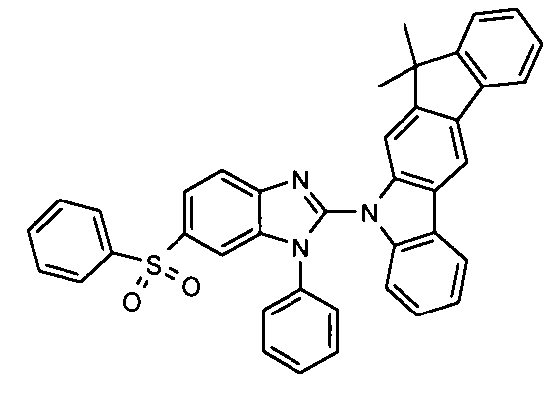
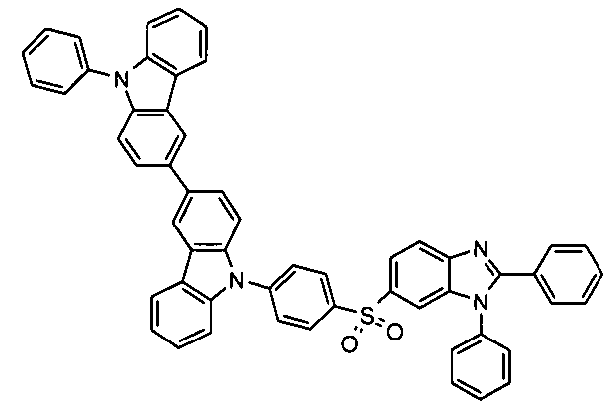
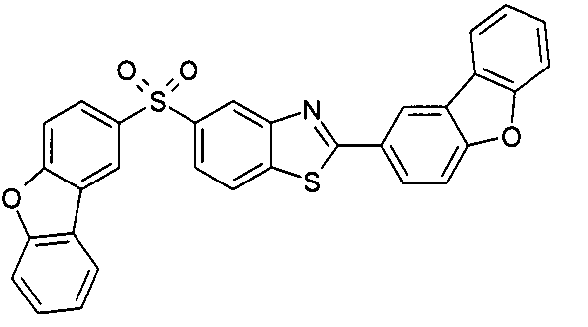
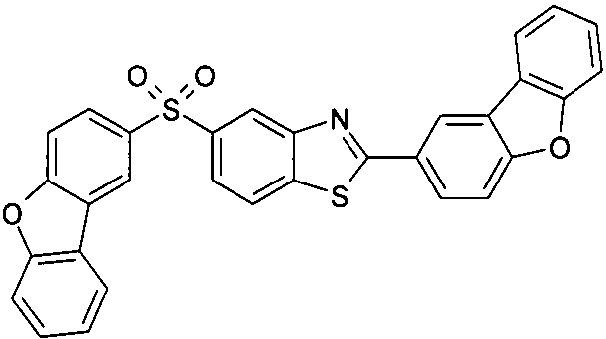
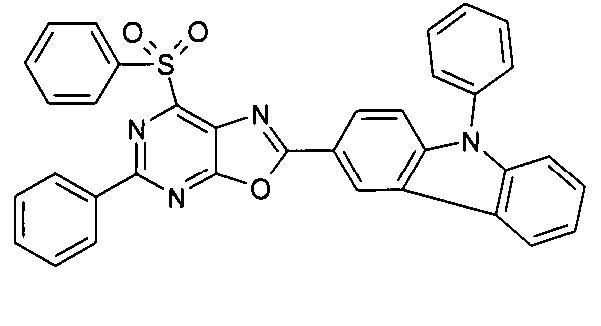
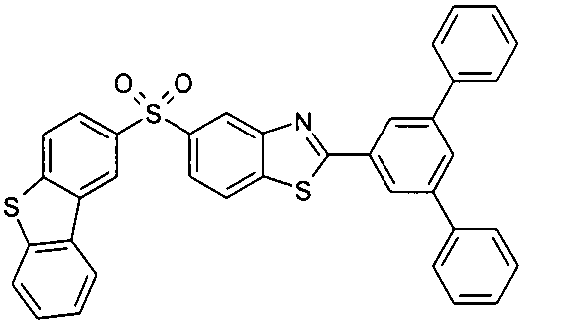
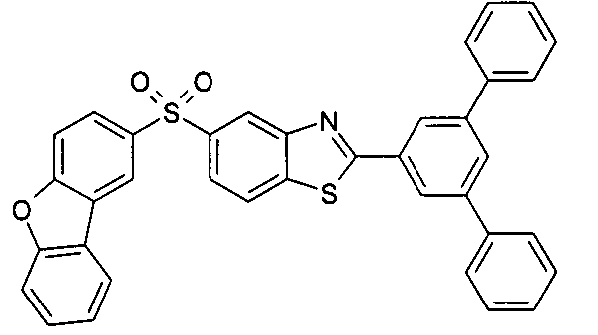
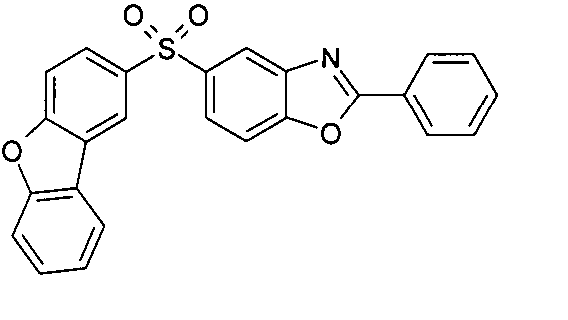
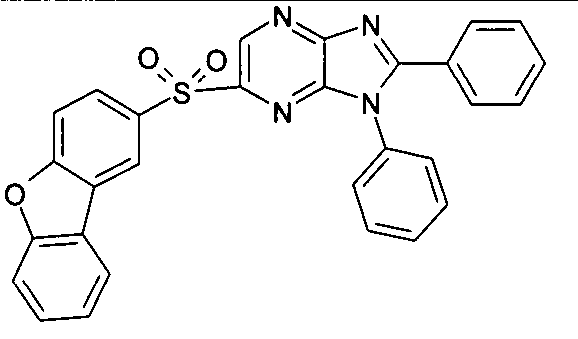
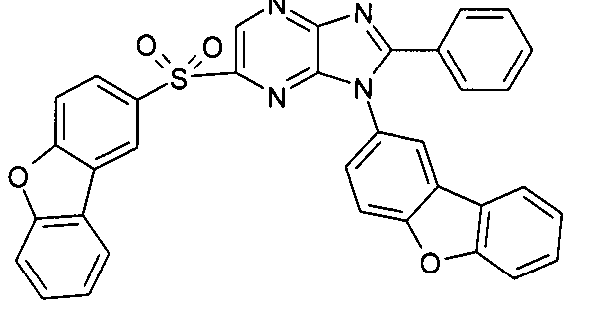
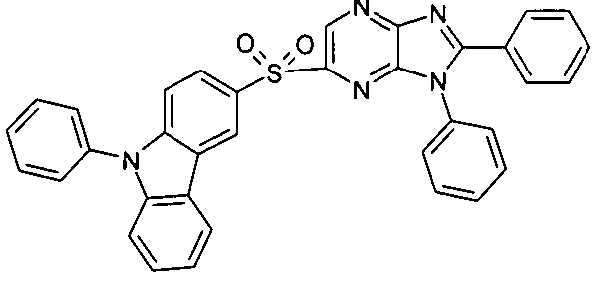
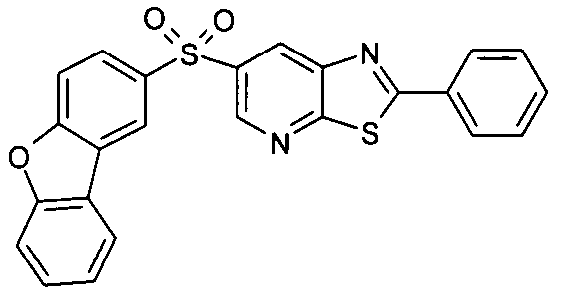
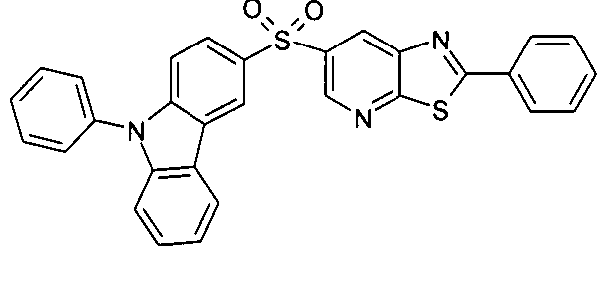
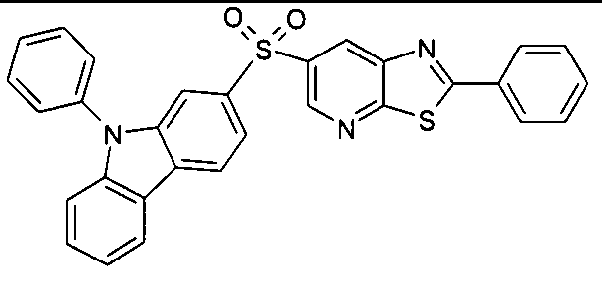
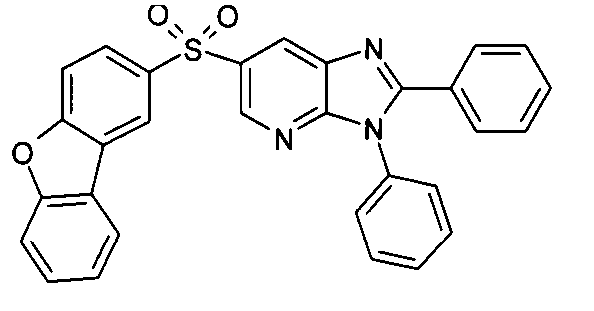
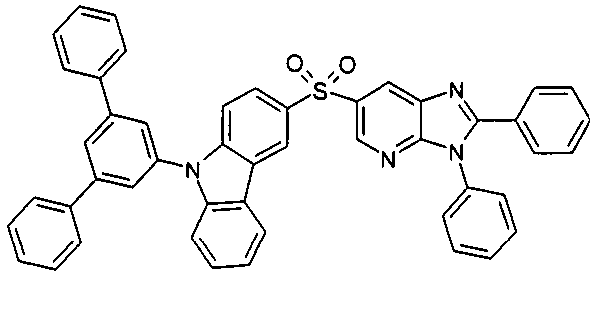
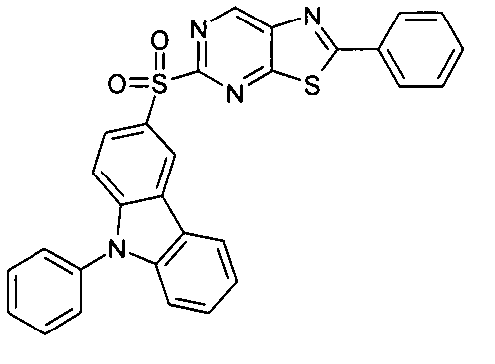
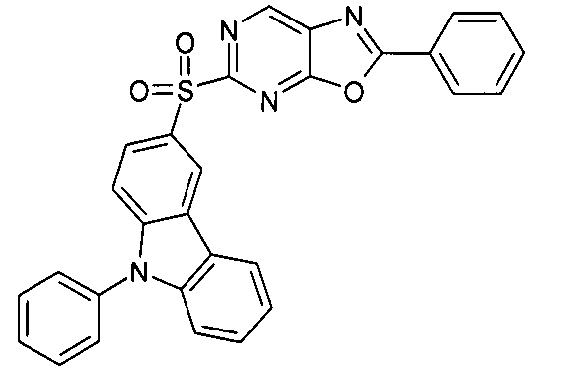
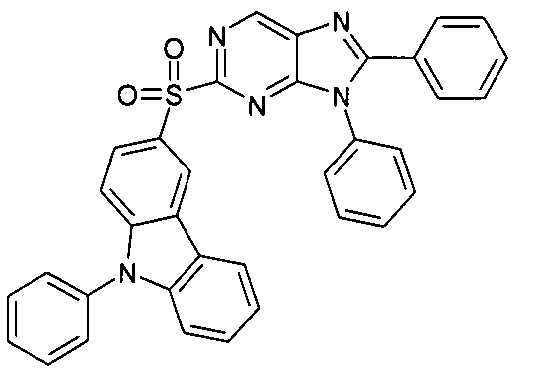
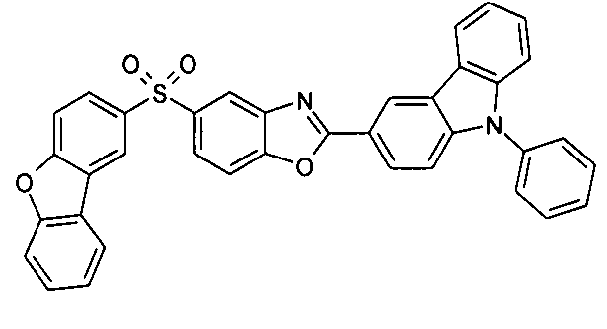
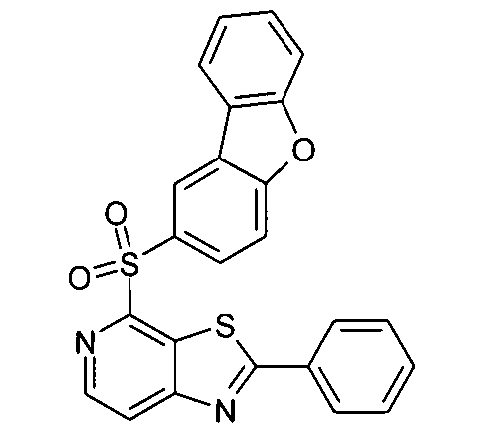
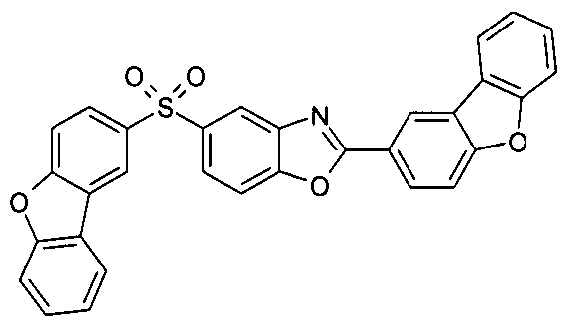
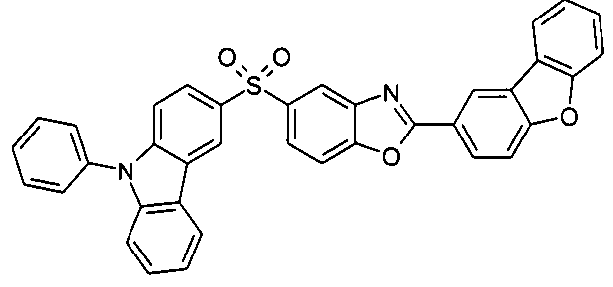
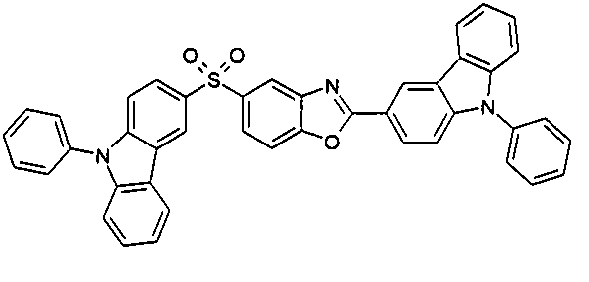
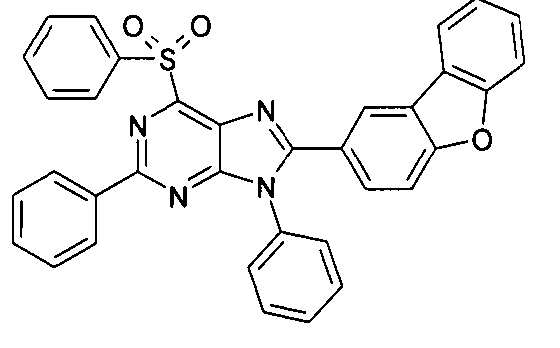
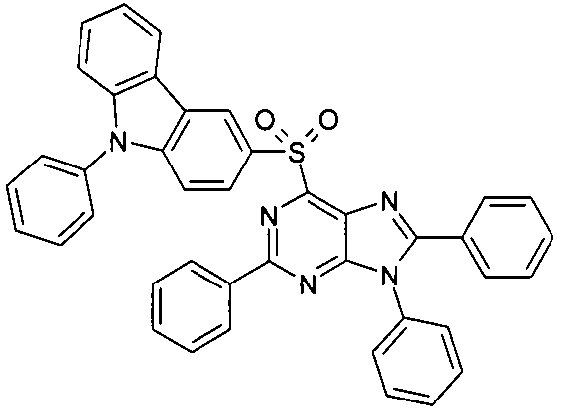
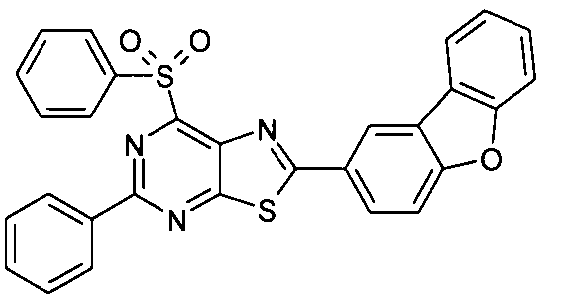
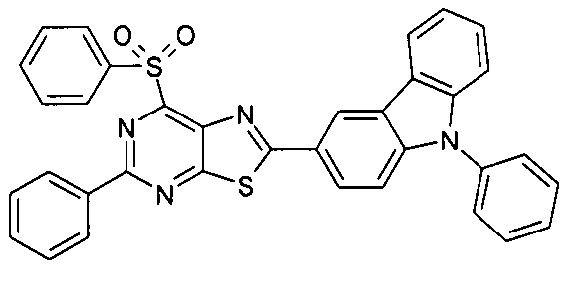
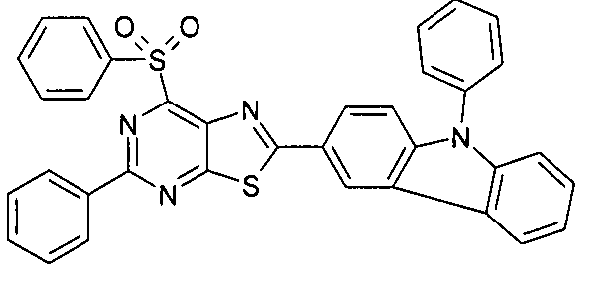
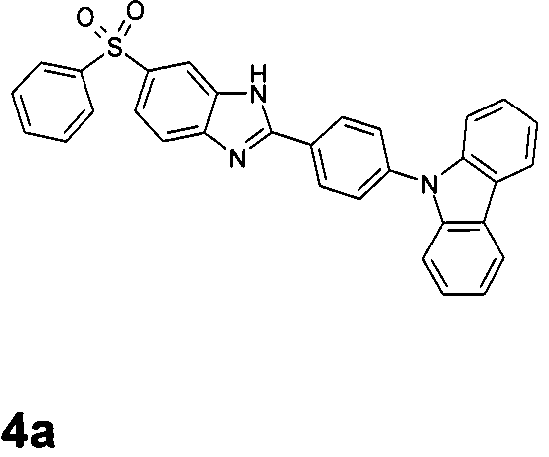
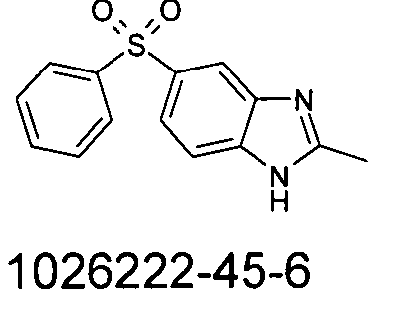
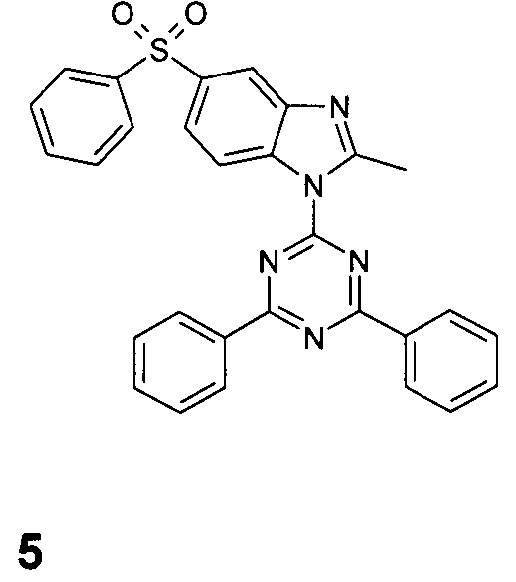
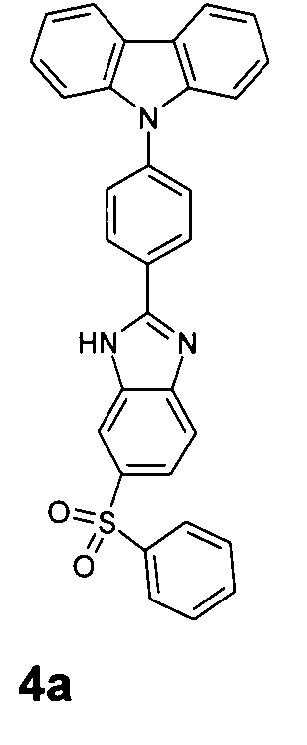
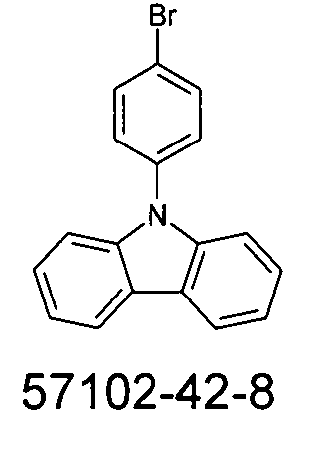
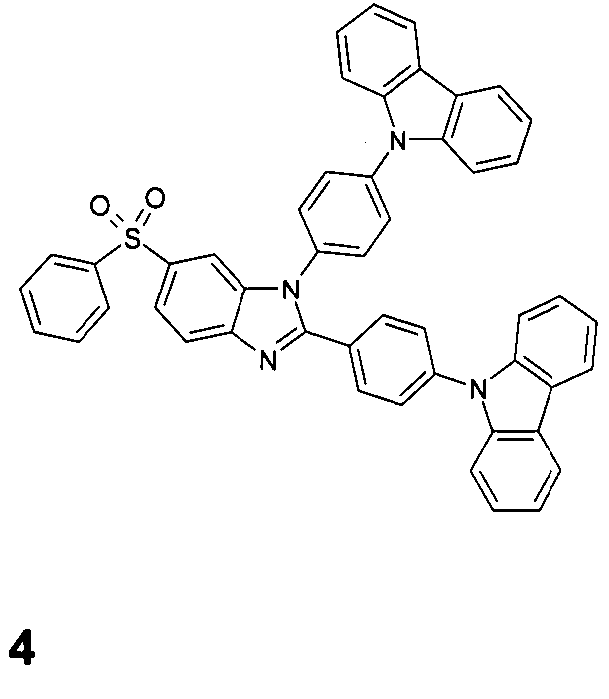
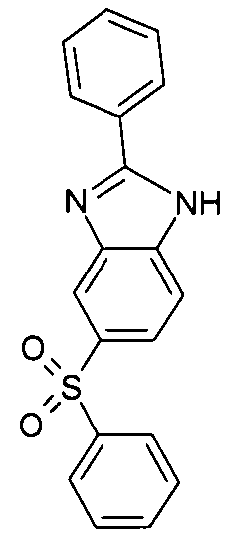
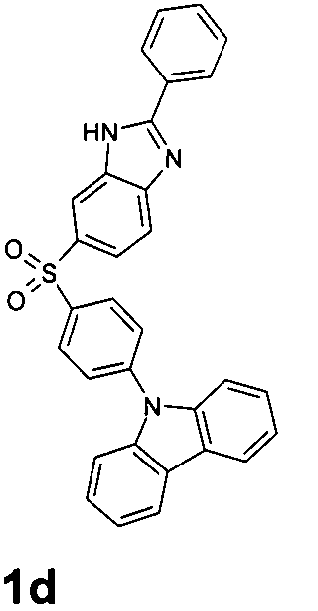
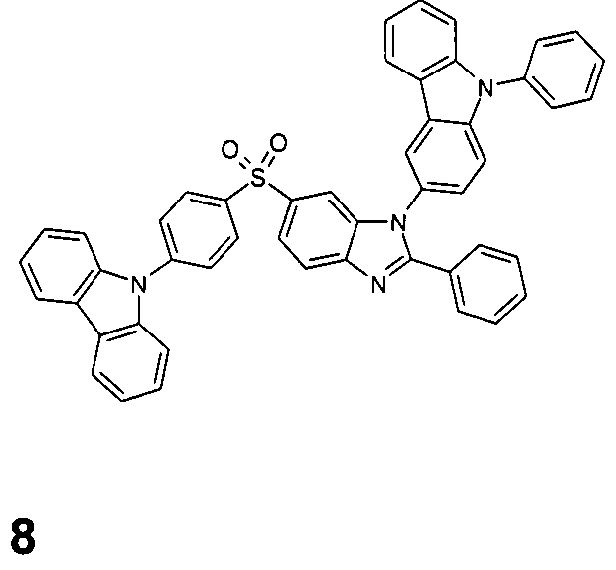
Die folgenden Verbindungen stellen Beispiele für Verbindungen gemäß Formel (I) oder (II) dar.
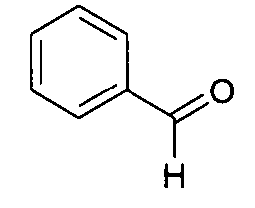
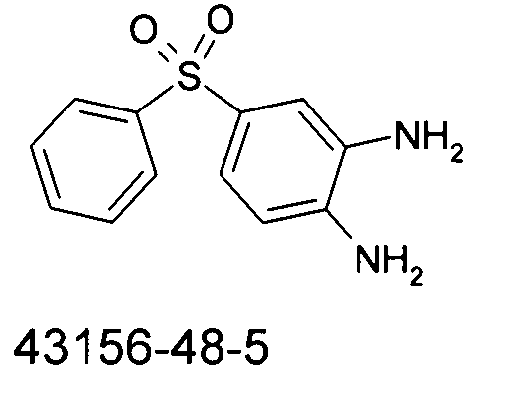
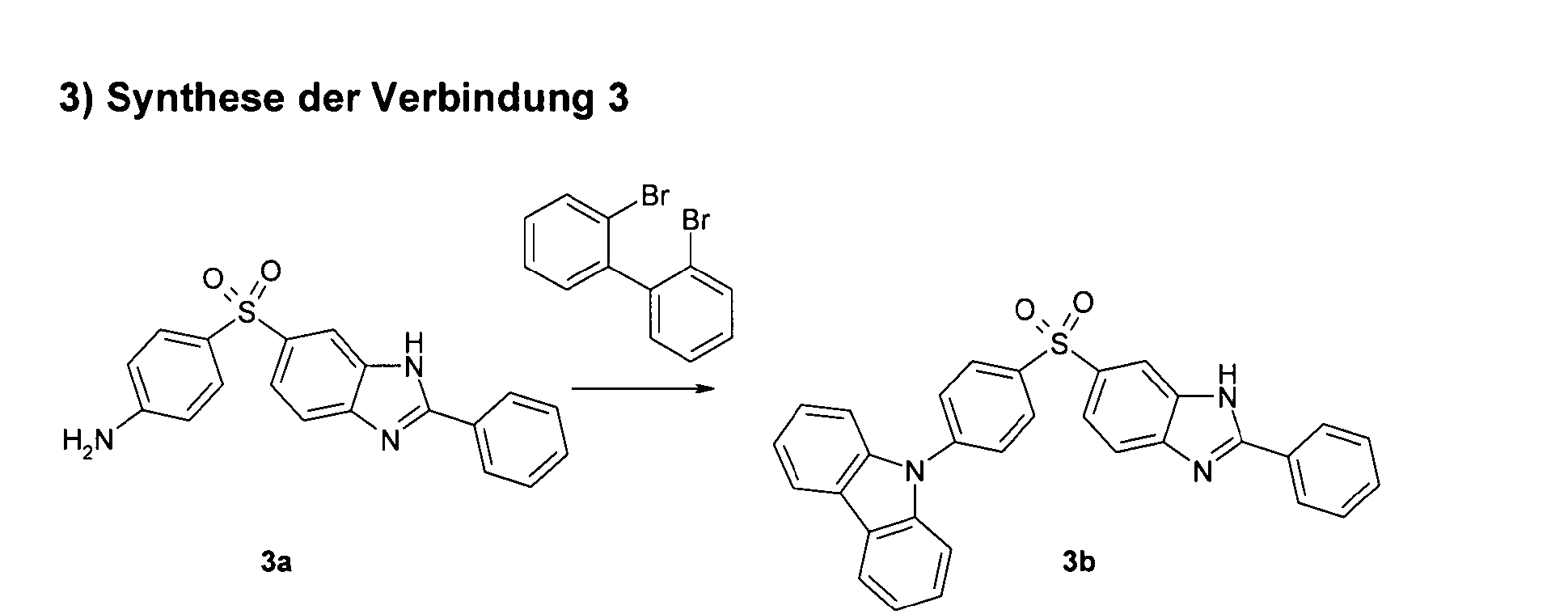
Die Verbindungen gemäß Formel (I) und (II) können durch geeignete Kombination von dem Fachmann bekannten organischen Reaktionen hergestellt werden, beispielsweise Buchwald-Kupplung und Kondensationsreaktionen zwischen Aminen und Aldehyden.The compounds according to formula (I) and (II) can be prepared by suitable combination of organic reactions known to the person skilled in the art, for example Buchwald coupling and condensation reactions between amines and aldehydes.
Im Folgenden werden exemplarische Reaktionswege zur Herstellung der Verbindungen gezeigt. Der Fachmann kann im Rahmen seines allgemeinen Fachwissens von diesen Reaktionswegen abweichen bzw. sie modifizieren, um weitere unter den Umfang der Formeln (I) und (II) fallende Verbindungen herzustellen.
- Ar: Aryl- oder Heteroarylgruppe
- R: organischer Rest
- L: Abgangsgruppe, beispielsweise Halogenid, Tosylat oder Mesylat
- Ar: aryl or heteroaryl group
- R: organic residue
- L: leaving group, for example halide, tosylate or mesylate
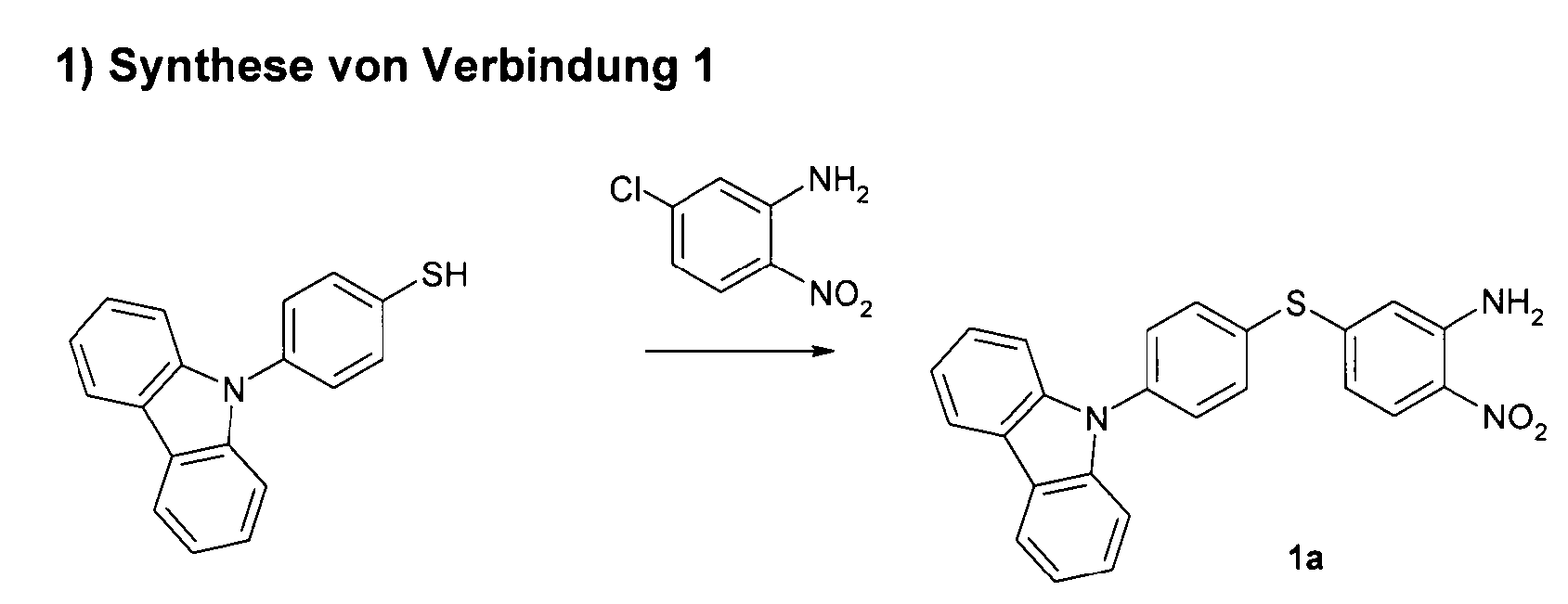
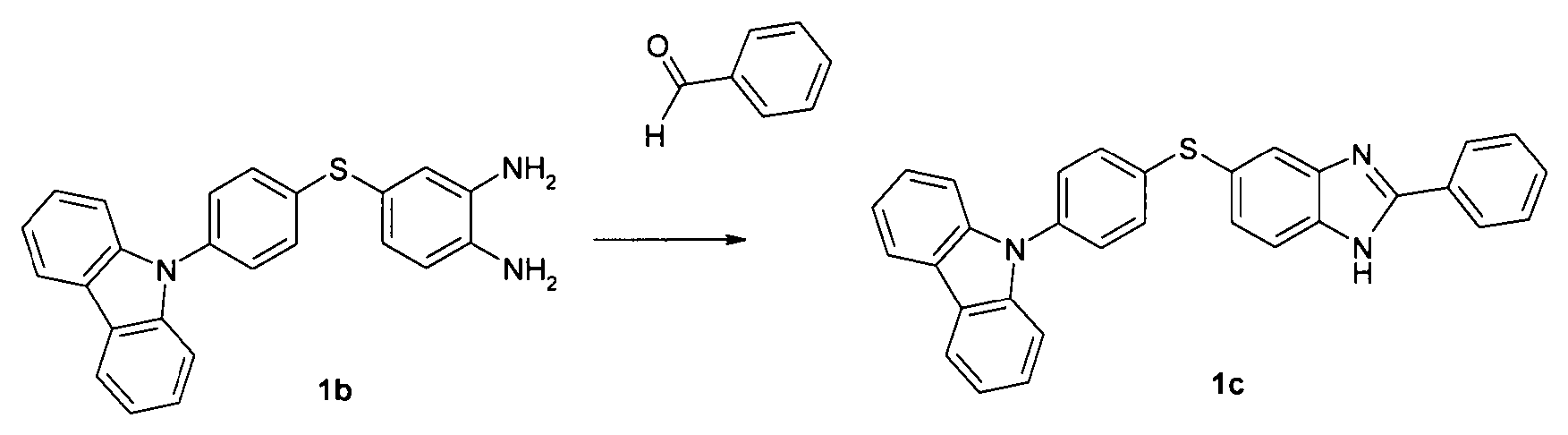
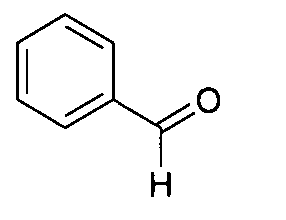
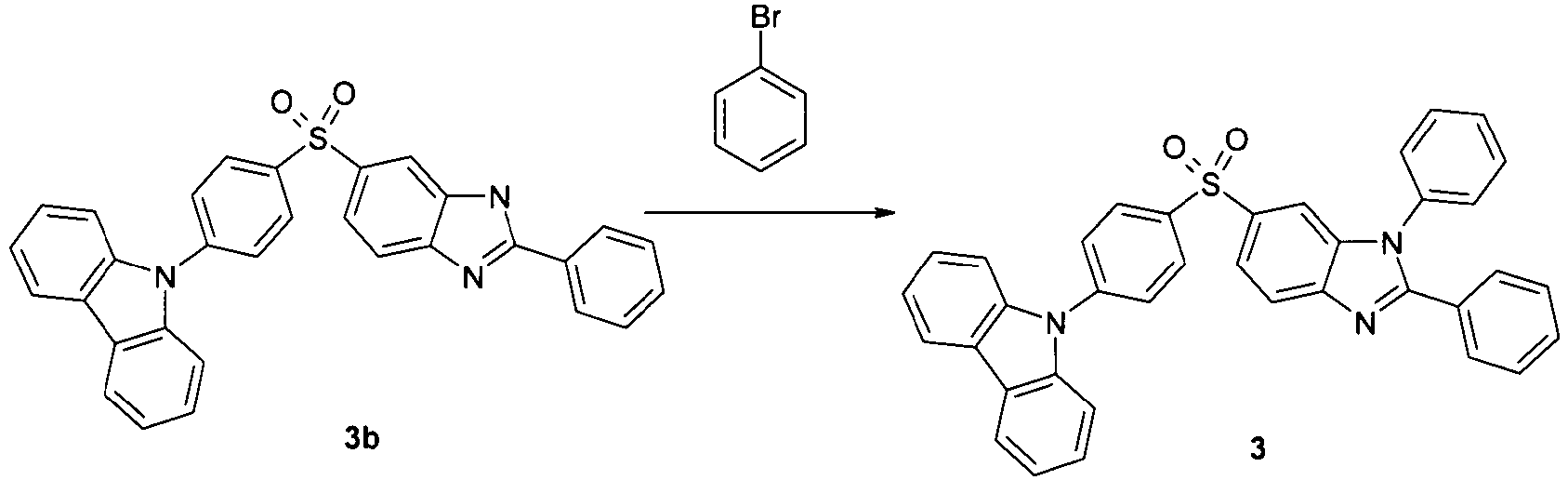
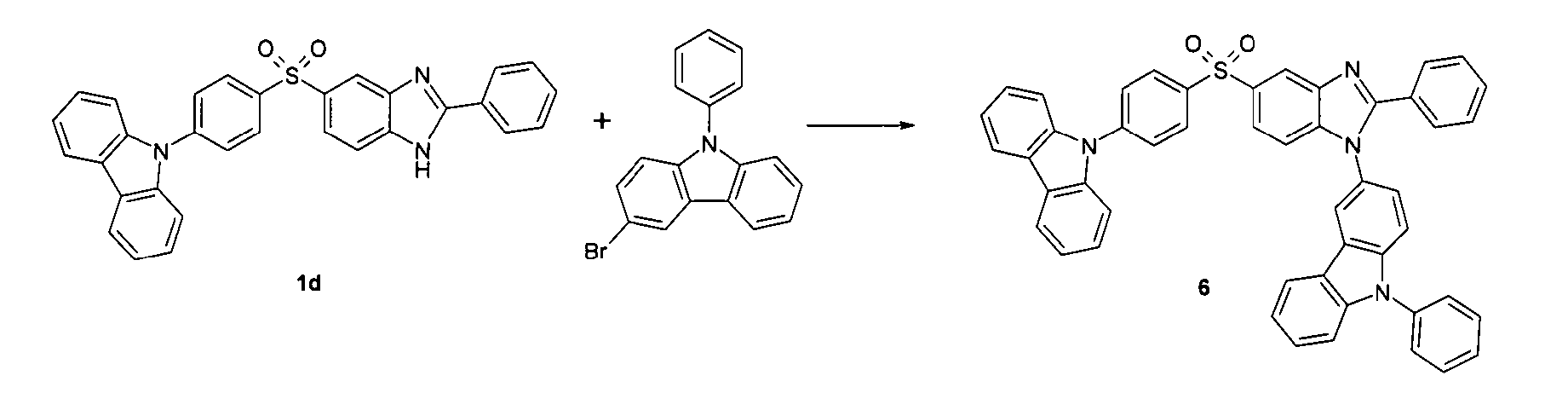
Gemäß dem in Schema 1 gezeigten Reaktionsweg wird aus einem 1,2-Diaminobenzol mit einer Thiogruppe über eine Kondensationsreaktion mit einem Aldehyd eine thiosubstituierte Benzimidazolgruppe hergestellt. Über eine Oxidationsreaktion wird daraus das entsprechende Sulfoxid-Derivat hergestellt. Die freie N-H-Gruppe des Benzimidazols wird anschließend mit einer Aryl- oder Heteroarylgruppe substituiert, beispielsweise über eine Buchwald-Kupplung.
- Ar: Aryl- oder Heteroarylgruppe
- R: organischer Rest
- L: Abgangsgruppe, beispielsweise Halogenid, Tosylat oder Mesylat
- Ar: aryl or heteroaryl group
- R: organic residue
- L: leaving group, for example halide, tosylate or mesylate
In Schema 2 ist ein analoger Reaktionsweg zur Herstellung von Derivaten gemäß Formel (II) gezeigt. Die Reaktionen entsprechen den bei Schema 1 Diskutierten.Scheme 2 shows an analogous reaction pathway for the preparation of derivatives according to formula (II). The reactions correspond to those discussed in Scheme 1.
Gegenstand der Erfindung ist somit ein Verfahren zur Herstellung von Verbindungen der (I-1-a), (1-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) und (II-3-b), dadurch gekennzeichnet, dass mindestens eine Kondensations-Reaktion zwischen einem Aldehyd und einer Arylverbindung, welche mindestens eine Aminogruppe enthält, umfasst ist.The invention thus relates to a process for preparing compounds of (I-1-a), (1-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) and (II-3-b), characterized in that at least one condensation reaction between an aldehyde and an aryl compound which contains at least one amino group is involved.
Bevorzugt umfasst das Verfahren weiterhin mindestens eine Oxidationsreaktion. Ebenfalls bevorzugt umfasst das Verfahren weiterhin mindestens eine übergangsmetallkatalysierte Kupplungsreaktion, bevorzugt eine Buchwald-Kupplungsreaktion.The process preferably further comprises at least one oxidation reaction. The process also preferably further comprises at least one transition metal-catalyzed coupling reaction, preferably a Buchwald coupling reaction.
Die oben beschriebenen erfindungsgemäßen Verbindungen, insbesondere Verbindungen, welche mit reaktiven Abgangsgruppen, wie Brom, lod, Chlor, Boronsäure oder Boronsäureester, substituiert sind, können als Monomere zur Erzeugung entsprechender Oligomere, Dendrimere oder Polymere Verwendung finden. Geeignete reaktive Abgangsgruppen sind beispielsweise Brom, lod, Chlor, Boronsäuren, Boronsäureester, Amine, Alkenyl- oder Alkinylgruppen mit endständiger C-C-Doppelbindung bzw. C-C-Dreifachbindung, Oxirane, Oxetane, Gruppen, die eine Cycloaddition, beispielsweise eine 1,3-dipolare Cycloaddition, eingehen, wie beispielsweise Diene oder Azide, Carbonsäurederivate, Alkohole und Silane.The compounds according to the invention described above, in particular compounds which are substituted with reactive leaving groups such as bromine, iodine, chlorine, boronic acid or boronic acid esters, can be used as monomers for producing corresponding oligomers, dendrimers or polymers. Suitable reactive leaving groups are, for example, bromine, iodine, chlorine, boronic acids, boronic acid esters, amines, alkenyl or alkynyl groups with a terminal C-C double bond or C-C triple bond, oxiranes, oxetanes, groups which undergo a cycloaddition, for example a 1,3-dipolar cycloaddition, such as dienes or azides, carboxylic acid derivatives, alcohols and silanes.
Weiterer Gegenstand der Erfindung sind daher Oligomere, Polymere oder Dendrimere enthaltend eine oder mehrere Verbindungen gemäß Formel (I-1-a), (I-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) und (II-3-b), wobei die Bindung(en) zum Polymer, Oligomer oder Dendrimer an beliebigen, mit R1 oder R2 substituierten Positionen lokalisiert sein können. Je nach Verknüpfung der erfindungsgemäßen Verbindung ist die Verbindung Bestandteil einer Seitenkette des Oligomers oder Polymers oder Bestandteil der Hauptkette. Unter einem Oligomer im Sinne dieser Erfindung wird eine Verbindung verstanden, welche aus mindestens drei Monomereinheiten aufgebaut ist. Unter einem Polymer im Sinne der Erfindung wird eine Verbindung verstanden, die aus mindestens zehn Monomereinheiten aufgebaut ist. Die erfindungsgemäßen Polymere, Oligomere oder Dendrimere können konjugiert, teilkonjugiert oder nichtkonjugiert sein. Die erfindungsgemäßen Oligomere oder Polymere können linear, verzweigt oder dendritisch sein. In den linear verknüpften Strukturen können die Einheiten gemäß den oben genannten Formeln direkt miteinander verknüpft sein oder sie können über eine bivalente Gruppe, beispielsweise über eine substituierte oder unsubstituierte Alkylengruppe, über ein Heteroatom oder über eine bivalente aromatische oder heteroaromatische Gruppe miteinander verknüpft sein. In verzweigten und dendritischen Strukturen können beispielsweise drei oder mehrere Einheiten gemäß den oben genannten Formeln über eine trivalente oder höhervalente Gruppe, beispielsweise über eine trivalente oder höhervalente aromatische oder heteroaromatische Gruppe, zu einem verzweigten bzw. dendritischen Oligomer oder Polymer verknüpft sein.The invention therefore further relates to oligomers, polymers or dendrimers containing one or more compounds according to formula (I-1-a), (I-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) and (II-3-b), where the bond(s) to the polymer, oligomer or dendrimer can be located at any position substituted with R 1 or R 2. Depending on the linkage of the compound according to the invention, the compound is part of a side chain of the oligomer or polymer or part of the main chain. An oligomer in the sense of this invention is understood to mean a compound which is made up of at least three monomer units. A polymer in the sense of the invention is understood to mean a compound which is made up of at least ten monomer units. The polymers, oligomers or dendrimers according to the invention can be conjugated, partially conjugated or non-conjugated. The oligomers or polymers according to the invention can be linear, branched or dendritic. In the linearly linked structures, the units according to the abovementioned formulas can be linked directly to one another or they can be linked to one another via a bivalent group, for example via a substituted or unsubstituted alkylene group, via a heteroatom or via a bivalent aromatic or heteroaromatic group. In branched and dendritic structures, for example, three or more units according to the abovementioned formulas can be linked to form a branched or dendritic oligomer or polymer via a trivalent or higher-valent group, for example via a trivalent or higher-valent aromatic or heteroaromatic group.
Für die Wiederholeinheiten in Oligomeren, Dendrimeren und Polymeren gelten dieselben Bevorzugungen wie oben für die erfindungsgemäßen Verbindungen beschrieben.The same preferences apply to the repeat units in oligomers, dendrimers and polymers as described above for the compounds according to the invention.
Zur Herstellung der Oligomere oder Polymere werden die erfindungsgemäßen Monomere homopolymerisiert oder mit weiteren Monomeren copolymerisiert. Geeignete und bevorzugte Comonomere sind gewählt aus Fluorenen (z. B. gemäß
Die erfindungsgemäßen Polymere, Oligomere und Dendrimere weisen vorteilhafte Eigenschaften, insbesondere hohe Lebensdauern, hohe Effizienzen und gute Farbkoordinaten auf.The polymers, oligomers and dendrimers according to the invention have advantageous properties, in particular long lifetimes, high efficiencies and good color coordinates.
Die erfindungsgemäßen Polymere und Oligomere werden in der Regel durch Polymerisation von einer oder mehreren Monomersorten hergestellt, von denen mindestens ein Monomer im Polymer zu Wiederholungseinheiten der oben genannten Formeln führt. Geeignete Polymerisationsreaktionen sind dem Fachmann bekannt und in der Literatur beschrieben. Besonders geeignete und bevorzugte Polymerisationsreaktionen, die zu C-C- bzw. C-N-Verknüpfungen führen, sind folgende:
- (A) SUZUKI-Polymerisation;
- (B) YAMAMOTO-Polymerisation;
- (C) STILLE-Polymerisation; und
- (D) HARTWIG-BUCHWALD-Polymerisation.
- (A) SUZUKI polymerization;
- (B) YAMAMOTO polymerization;
- (C) STILLE polymerization; and
- (D) HARTWIG-BUCHWALD polymerization.
Wie die Polymerisation nach diesen Methoden durchgeführt werden kann und wie die Polymere dann vom Reaktionsmedium abgetrennt und aufgereinigt werden können, ist dem Fachmann bekannt und in der Literatur, beispielsweise in
Gegenstand der vorliegenden Erfindung ist somit auch ein Verfahren zur Herstellung der erfindungsgemäßen Polymere, Oligomere und Dendrimere, das dadurch gekennzeichnet ist, dass sie durch Polymerisation gemäß SUZUKI, Polymerisation gemäß YAMAMOTO, Polymerisation gemäß STILLE oder Polymerisation gemäß HARTWIG-BUCHWALD hergestellt werden. Die erfindungsgemäßen Dendrimere können gemäß dem Fachmann bekannten Verfahren oder in Analogie dazu hergestellt werden. Geeignete Verfahren sind in der Literatur beschrieben, wie z. B. in
Für die Verarbeitung der erfindungsgemäßen Verbindungen aus flüssiger Phase, beispielsweise durch Spin-Coating oder durch Druckverfahren, sind Formulierungen der erfindungsgemäßen Verbindungen erforderlich. Diese Formulierungen können beispielsweise Lösungen, Dispersionen oder Miniemulsionen sein. Es kann bevorzugt sein, hierfür Mischungen aus zwei oder mehr Lösemitteln zu verwenden. Geeignete und bevorzugte Lösemittel sind beispielsweise Toluol, Anisol, o-, m- oder p-Xylol, Methylbenzoat, Dimethylanisol, Mesitylen, Tetralin, Veratrol, THF, Methyl-THF, THP, Chlorbenzol, Dioxan oder Mischungen dieser Lösemittel.For processing the compounds according to the invention from the liquid phase, for example by spin coating or by printing processes, formulations of the compounds according to the invention are required. These formulations can be, for example, solutions, dispersions or miniemulsions. It may be preferable to use mixtures of two or more solvents for this purpose. Suitable and preferred solvents are, for example, toluene, anisole, o-, m- or p-xylene, methyl benzoate, dimethylanisole, mesitylene, tetralin, veratrole, THF, methyl-THF, THP, chlorobenzene, dioxane or mixtures of these solvents.
Gegenstand der Erfindung ist daher weiterhin eine Formulierung, insbesondere eine Lösung, Dispersion oder Miniemulsion, enthaltend mindestens eine Verbindung gemäß Formel (I-1-a), (I-1-b), (II-1-a), (II-1-b), (II-2-a), (II-2-b), (II-3-a) und (II-3-b) oder mindestens ein Polymer, Oligomer oder Dendrimer enthaltend mindestens eine Einheit gemäß diesen Formeln sowie mindestens ein Lösungsmittel, bevorzugt ein organisches Lösungsmittel. Wie solche Lösungen hergestellt werden können, ist dem Fachmann bekannt und beispielsweise in
Die Verbindungen gemäß Formel (I) oder (II) eignen sich für den Einsatz in elektronischen Vorrichtungen, insbesondere in organischen Elektrolumineszenzvorrichtungen (OLEDs). Abhängig von der Substitution werden die Verbindungen in unterschiedlichen Funktionen und in unterschiedlichen Schichten der organischen Elektrolumineszenzvorrichtung eingesetzt. The compounds according to formula (I) or (II) are suitable for use in electronic devices, in particular in organic electroluminescent devices (OLEDs). Depending on the substitution, the compounds are used in different functions and in different layers of the organic electroluminescent device.
Bevorzugt ist allgemein die Verwendung der Verbindungen in einer elektronentransportierenden Schicht oder in einer emittierenden Schicht.In general, the use of the compounds in an electron-transporting layer or in an emitting layer is preferred.
Ein weiterer Gegenstand der Erfindung ist daher die Verwendung der Verbindungen gemäß Formel (I) oder (II) in elektronischen Vorrichtungen. Dabei sind die elektronischen Vorrichtungen bevorzugt ausgewählt aus der Gruppe bestehend aus organischen integrierten Schaltungen (O-ICs), organischen Feld-Effekt-Transistoren (O-FETs), organischen Dünnfilmtransistoren (O-TFTs), organischen lichtemittierenden Transistoren (O-LETs), organischen Solarzellen (O-SCs), organischen optischen Detektoren, organischen Photorezeptoren, organischen Feld-Quench-Devices (O-FQDs), organischen lichtemittierenden elektrochemischen Zellen (OLECs), organischen Laserdioden (O-Laser), organischen plasmonemittierenden Dioden und besonders bevorzugt organischen Elektrolumineszenzvorrichtungen (OLEDs).The invention therefore further relates to the use of the compounds according to formula (I) or (II) in electronic devices. The electronic devices are preferably selected from the group consisting of organic integrated circuits (O-ICs), organic field-effect transistors (O-FETs), organic thin-film transistors (O-TFTs), organic light-emitting transistors (O-LETs), organic solar cells (O-SCs), organic optical detectors, organic photoreceptors, organic field quench devices (O-FQDs), organic light-emitting electrochemical cells (OLECs), organic laser diodes (O-lasers), organic plasmon-emitting diodes and particularly preferably organic electroluminescent devices (OLEDs).
Die erfindungsgemäße organische Elektrolumineszenzvorrichtung enthält bevorzugt eine Anode, eine Kathode sowie eine oder mehrere organische Schichten, wobei mindestens eine organische Schicht eine oder mehrere Verbindungen der Formel (I) oder (II) enthält. Die organische Elektrolumineszenzvorrichtung enthält weiterhin bevorzugt mindestens eine elektrolumineszierende Schicht. Die elektrolumineszierende Schicht kann eine Verbindung der Formel (I) oder (II) enthalten, die Verbindung der Formel (I) oder (II) kann jedoch auch ausschließlich in einer anderen Schicht der Vorrichtung vorliegen, beispielsweise in einer Elektronentransportschicht.The organic electroluminescent device according to the invention preferably contains an anode, a cathode and one or more organic layers, wherein at least one organic layer contains one or more compounds of the formula (I) or (II). The organic electroluminescent device further preferably contains at least one electroluminescent layer. The electroluminescent layer can contain a compound of the formula (I) or (II), the compound of the formula (I) or (II) can but may also be present exclusively in another layer of the device, for example in an electron transport layer.
Diese anderen Schichten, welche wahlweise in der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung vorliegen können, sind beispielsweise ausgewählt aus jeweils einer oder mehreren Lochinjektionsschichten, Lochtransportschichten, Lochblockierschichten, Elektronentransportschichten, Elektroneninjektionsschichten, Elektronenblockierschichten, Excitonenblockierschichten, Zwischenschichten (Interlayers), Ladungserzeugungsschichten (Charge-Generation Layers, (
Die organische Elektrolumineszenzvorrichtung kann auch mehrere emittierende Schichten enthalten. Besonders bevorzugt weisen diese Emissionsschichten in diesem Fall insgesamt mehrere Emissionsmaxima zwischen 380 nm und 750 nm auf, so dass insgesamt weiße Emission resultiert, d. h. in den emittierenden Schichten werden verschiedene emittierende Verbindungen verwendet, die fluoreszieren oder phosphoreszieren können und die blaues und gelbes, orangefarbenes oder rotes Licht emittieren. Insbesondere bevorzugt sind Systeme mit drei emittierenden Schichten, wobei die drei Schichten blaue, grüne und orangefarbene oder rote Emission zeigen (für den prinzipiellen Aufbau siehe z. B.
Es ist bevorzugt, dass die erfindungsgemäße Vorrichtung einen oder mehrere phosphoreszierende Dotanden aufweist. Weiterhin kann die Verbindung auch einen oder mehrere fluoreszierende Dotanden aufweisen. Gemäß einer möglichen Ausführungsform weist die erfindungsgemäße Vorrichtung mindestens einen phosphoreszierenden Dotanden und mindestens einen fluoreszierenden Dotanden auf. Die erfindungsgemäße Vorrichtung kann jedoch auch ausschließlich einen oder mehrere fluoreszierende Dotanden aufweisen.It is preferred that the device according to the invention has one or more phosphorescent dopants. Furthermore, the compound can also have one or more fluorescent dopants. According to one possible embodiment, the device according to the invention has at least one phosphorescent dopant and at least one fluorescent dopant. However, the device according to the invention can also have exclusively one or more fluorescent dopants.
Als phosphoreszierende Dotanden (= Triplettemitter) eignen sich insbesondere Verbindungen, die bei geeigneter Anregung Licht, vorzugsweise im sichtbaren Bereich, emittieren und außerdem mindestens ein Atom der Ordnungszahl größer 20, bevorzugt größer 38 und kleiner 84, besonders bevorzugt größer 56 und kleiner 80 enthalten. Bevorzugt werden als Phosphoreszenzemitter Verbindungen, die Kupfer, Molybdän, Wolfram, Rhenium, Ruthenium, Osmium, Rhodium, Iridium, Palladium, Platin, Silber, Gold oder Europium enthalten, verwendet, insbesondere Verbindungen, die Iridium, Platin oder Kupfer enthalten.Particularly suitable as phosphorescent dopants (= triplet emitters) are compounds which emit light, preferably in the visible range, when suitably excited and which also contain at least one atom with an atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80. Preferably, compounds containing copper, molybdenum, tungsten, rhenium, ruthenium, osmium, rhodium, iridium, palladium, platinum, silver, gold or europium are used as phosphorescent emitters, in particular compounds containing iridium, platinum or copper.
Dabei werden im Sinne der vorliegenden Erfindung alle lumineszierenden Iridium-, Platin- oder Kupferkomplexe als phosphoreszierende Verbindungen angesehen.For the purposes of the present invention, all luminescent iridium, platinum or copper complexes are considered to be phosphorescent compounds.
In einer bevorzugten Ausführungsform der vorliegenden Erfindung werden die erfindungsgemäßen Verbindungen als Matrixmaterial in Kombination mit einem oder mehreren Dotanden, vorzugsweise phosphoreszierenden Dotanden, eingesetzt.In a preferred embodiment of the present invention, the compounds according to the invention are used as matrix material in combination with one or more dopants, preferably phosphorescent dopants.
Unter einem Dotanden wird in einem System enthaltend ein Matrixmaterial und einen Dotanden diejenige Komponente verstanden, deren Anteil in der Mischung der kleinere ist. Entsprechend wird unter einem Matrixmaterial in einem System enthaltend ein Matrixmaterial und einen Dotanden diejenige Komponente verstanden, deren Anteil in der Mischung der größere ist.In a system containing a matrix material and a dopant, a dopant is understood to be the component whose proportion in the mixture is the smaller. Accordingly, in a system containing a matrix material and a dopant, a matrix material is understood to be the component whose proportion in the mixture is the larger.
Der Anteil des Matrixmaterials in der emittierenden Schicht beträgt typischerweise zwischen 50.0 und 99.9 Vol.-%, bevorzugt zwischen 80.0 und 99.5 Vol.-% und besonders bevorzugt für fluoreszierende emittierende Schichten zwischen 92.0 und 99.5 Vol.-% sowie für phosphoreszierende emittierende Schichten zwischen 85.0 und 97.0 Vol.-%. Entsprechend beträgt der Anteil des Dotanden zwischen 0.1 und 50.0 Vol.-%, bevorzugt zwischen 0.5 und 20.0 Vol.-% und besonders bevorzugt für fluoreszierende emittierende Schichten zwischen 0.5 und 8.0 Vol.-% sowie für phosphoreszierende emittierende Schichten zwischen 3.0 und 15.0 Vol.-%.The proportion of the matrix material in the emitting layer is typically between 50.0 and 99.9 vol.%, preferably between 80.0 and 99.5 vol.% and particularly preferably for fluorescent emitting layers between 92.0 and 99.5 vol.% and for phosphorescent emitting layers between 85.0 and 97.0 vol.%. Accordingly, the proportion of the dopant is between 0.1 and 50.0 vol.%, preferably between 0.5 and 20.0 vol.% and particularly preferably for fluorescent emitting layers between 0.5 and 8.0 vol.% and for phosphorescent emitting layers between 3.0 and 15.0 vol.%.
Eine emittierende Schicht einer organischen Elektrolumineszenzvorrichtung kann auch Systeme umfassend mehrere Matrixmaterialien (Mixed-Matrix-Systeme) und/oder mehrere Dotanden enthalten. Bevorzugt werden Mixed-Matrix-Systeme in phosphoreszierenden organischen Elektrolumineszenzvorrichtungen eingesetzt. Auch im Fall von mixed-Matrix-Systemen sind die Dotanden im Allgemeinen diejenigen Materialien, deren Anteil im System der kleinere ist und die Matrixmaterialien sind diejenigen Materialien, deren Anteil im System der größere ist. In Einzelfällen kann jedoch der Anteil eines einzelnen Matrixmaterials im System kleiner sein als der Anteil eines einzelnen Dotanden.An emitting layer of an organic electroluminescent device can also contain systems comprising several matrix materials (mixed matrix systems) and/or several dopants. Mixed matrix systems are preferably used in phosphorescent organic electroluminescent devices. In the case of mixed matrix systems too, the dopants are generally those materials whose proportion in the system is the smaller and the matrix materials are those materials whose proportion in the system is the larger. In individual cases, however, the proportion of an individual matrix material in the system can be smaller than the proportion of an individual dopant.
In einer bevorzugten Ausführungsform der Erfindung werden die erfindungsgemäßen Verbindungen als eine Komponente von Mixed-Matrix-Systemen verwendet. Die Mixed-Matrix-Systeme umfassen bevorzugt zwei oder drei verschiedene Matrixmaterialien, besonders bevorzugt zwei verschiedene Matrixmaterialien. Bevorzugt stellt dabei eines der beiden Materialien ein Material mit lochtransportierenden Eigenschaften und das andere ein Material mit elektronentransportierenden Eigenschaften dar. Bevorzugt stellen die erfindungsgemäßen Verbindungen dabei das Material mit elektronentransportierenden Eigenschaften dar.In a preferred embodiment of the invention, the compounds according to the invention are used as a component of mixed matrix systems. The mixed matrix systems preferably comprise two or three different matrix materials, particularly preferably two different matrix materials. Preferably, one of the two materials is a material with hole-transporting properties and the other is a material with electron-transporting properties. Preferably, the compounds according to the invention are the material with electron-transporting properties.
Die beiden unterschiedlichen Matrixmaterialien können in einem Verhältnis von 1:50 bis 1:1, bevorzugt 1:20 bis 1:1, besonders bevorzugt 1:10 bis 1:1 und ganz besonders bevorzugt 1:4 bis 1:1 vorliegen.The two different matrix materials can be present in a ratio of 1:50 to 1:1, preferably 1:20 to 1:1, particularly preferably 1:10 to 1:1 and most preferably 1:4 to 1:1.
Die Mixed-Matrix-Systeme können einen oder mehrere Dotanden umfassen. Die Dotandverbindung bzw. die Dotandverbindungen zusammen haben erfindungsgemäß einen Anteil von 0.1 bis 50.0 Vol.-% an der Gesamtmischung und bevorzugt einen Anteil von 0.5 bis 20.0 Vol.-% an der Gesamtmischung. Entsprechend haben die Matrixkomponenten zusammen einen Anteil von 50.0 bis 99.9 Vol-% an der Gesamtmischung und bevorzugt einen Anteil von 80.0 bis 99.5 Vol.-% an der Gesamtmischung.The mixed matrix systems can comprise one or more dopants. According to the invention, the dopant compound or the dopant compounds together have a proportion of 0.1 to 50.0 vol.% of the total mixture and preferably a proportion of 0.5 to 20.0 vol.% of the total mixture. Accordingly, the matrix components together have a proportion of 50.0 to 99.9 vol.% of the total mixture and preferably a proportion of 80.0 to 99.5 vol.% of the total mixture.
Besonders geeignete Matrixmaterialien, welche in Kombination mit den erfindungsgemäßen Verbindungen als Matrixkomponenten eines Mixed-Matrix-Systems eingesetzt werden können, sind aromatische Amine, insbesondere Triarylamine, z. B. gemäß
Für phosphoreszierende Dotanden zur Verwendung in Mixed-Matrix-Systemen gelten dieselben Bevorzugungen wie oben angegeben.For phosphorescent dopants for use in mixed-matrix systems, the same preferences as stated above apply.
In einer weiteren bevorzugten Ausführungsform der Erfindung werden die erfindungsgemäßen Verbindungen als Elektronentransportmaterial in einer Elektronentransport- oder Elektroneninjektionsschicht eingesetzt. Dabei kann die emittierende Schicht fluoreszierende und/oder phosphoreszierende Emitter enthalten. Wenn die Verbindungen als Elektronentransportmaterial eingesetzt werden, kann es bevorzugt sein, wenn sie dotiert sind, beispielsweise mit Alkalimetallkomplexen, wie z. B. Liq (Lithiumhydroxychinolinat). Auch eignet sich die Kombination der erfindungsgemäßen Verbindung in einer Elektronentransportschicht mit einer Elektroneninjektionsschicht. Als Materialien für die Elektroneninjektionsschicht eignen sich beispielsweise Alkali- oder Erdalkalifluoride, wie z. B. LiF.In a further preferred embodiment of the invention, the compounds according to the invention are used as electron transport material in an electron transport or electron injection layer. The emitting layer can contain fluorescent and/or phosphorescent emitters. If the compounds are used as electron transport material, it can be preferred if they are doped, for example with alkali metal complexes, such as Liq (lithium hydroxyquinolinate). The combination of the compound according to the invention in an electron transport layer with an electron injection layer is also suitable. Suitable materials for the electron injection layer are, for example, alkali or alkaline earth fluorides, such as LiF.
In nochmals einer weiteren bevorzugten Ausführungsform der Erfindung werden die erfindungsgemäßen Verbindungen als Lochblockiermaterial in einer Lochblockierschicht eingesetzt. Unter einer Lochblockierschicht wird eine Schicht verstanden, die auf Kathodenseite direkt an eine emittierende Schicht angrenzt.In yet another preferred embodiment of the invention, the compounds according to the invention are used as hole-blocking material in a hole-blocking layer. A hole-blocking layer is understood to be a layer which directly adjoins an emitting layer on the cathode side.
Im Folgenden werden die in den erfindungsgemäßen elektronischen Vorrichtungen für die jeweiligen Funktionen bevorzugt eingesetzten Materialien aufgeführt.The materials preferably used in the electronic devices according to the invention for the respective functions are listed below.
Bevorzugte fluoreszierende Dotanden sind ausgewählt aus der Klasse der Arylamine. Unter einem Arylamin bzw. einem aromatischen Amin im Sinne dieser Erfindung wird eine Verbindung verstanden, die drei substituierte oder unsubstituierte aromatische oder heteroaromatische Ringsysteme direkt an den Stickstoff gebunden enthält. Bevorzugt ist mindestens eines dieser aromatischen oder heteroaromatischen Ringsysteme ein kondensiertes Ringsystem, besonders bevorzugt mit mindestens 14 aromatischen Ringatomen. Bevorzugte Beispiele hierfür sind aromatische Anthracenamine, aromatische Anthracendiamine, aromatische Pyrenamine, aromatische Pyrendiamine, aromatische Chrysenamine oder aromatische Chrysendiamine. Unter einem aromatischen Anthracenamin wird eine Verbindung verstanden, in der eine Diarylaminogruppe direkt an eine Anthracengruppe gebunden ist, vorzugsweise in 9-Position. Unter einem aromatischen Anthracendiamin wird eine Verbindung verstanden, in der zwei Diarylaminogruppen direkt an eine Anthracengruppe gebunden sind, vorzugsweise in 9,10-Position. Aromatische Pyrenamine, Pyrendiamine, Chrysenamine und Chrysendiamine sind analog dazu definiert, wobei die Diarylaminogruppen am Pyren bevorzugt in 1-Position bzw. in 1,6-Position gebunden sind.Preferred fluorescent dopants are selected from the class of arylamines. An arylamine or an aromatic amine in the sense of this invention is understood to mean a compound which contains three substituted or unsubstituted aromatic or heteroaromatic ring systems directly bonded to the nitrogen. Preferably, at least one of these aromatic or heteroaromatic ring systems is a condensed ring system, particularly preferably with at least 14 aromatic ring atoms. Preferred examples of these are aromatic anthraceneamines, aromatic anthracenediamines, aromatic pyreneamines, aromatic pyrenediamines, aromatic chrysenamines or aromatic chrysenediamines. An aromatic anthraceneamine is understood to mean a compound in which a diarylamino group is bonded directly to an anthracene group, preferably in the 9-position. An aromatic anthracenediamine is understood to mean a compound in which two diarylamino groups are bonded directly to an anthracene group, preferably in the 9,10-position. Aromatic pyrenamines, pyrenediamines, chrysenamines and chrysenediamines are defined analogously, whereby the diarylamino groups on the pyrene are preferably bonded in the 1-position or in the 1,6-position.
Bevorzugte phosphoreszierende Dotanden können den Anmeldungen
Bevorzugte Matrixmaterialien für fluoreszierende Dotanden sind ausgewählt aus den Klassen der Oligoarylene (z. B. 2,2',7,7'-Tetraphenylspirobifluoren gemäß
Bevorzugte Matrixmaterialien für phosphoreszierende Dotanden, zur Verwendung als Einzelmatrix oder als Mixed-Matrix, wurden oben angegeben.Preferred matrix materials for phosphorescent dopants, for use as single matrix or mixed matrix, have been given above.
Geeignete Ladungstransportmaterialien, wie sie in der Lochinjektions- bzw. Lochtransportschicht bzw. Elektronenblockierschicht oder in der Elektronentransportschicht der erfindungsgemäßen organischen Elektrolumineszenzvorrichtung verwendet werden können, sind neben den erfindungsgemäßen Verbindungen beispielsweise die in
Beispiele für bevorzugte Lochtransportmaterialien, die in einer Lochtransport-, Lochinjektions- oder Elektronenblockierschicht in der erfindungsgemäßen Elektrolumineszenzvorrichtung verwendet werden können, sind Indenofluorenamine und Derivate (z. B. gemäß
Als Kathode der organischen Elektrolumineszenzvorrichtung sind Metalle mit geringer Austrittsarbeit, Metalllegierungen oder mehrlagige Strukturen aus verschiedenen Metallen bevorzugt, wie beispielsweise Erdalkalimetalle, Alkalimetalle, Hauptgruppenmetalle oder Lanthanoide (z. B. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Weiterhin eignen sich Legierungen aus einem Alkali- oder Erdalkalimetall und Silber, beispielsweise eine Legierung aus Magnesium und Silber. Bei mehrlagigen Strukturen können auch zusätzlich zu den genannten Metallen weitere Metalle verwendet werden, die eine relativ hohe Austrittsarbeit aufweisen, wie z. B. Ag oder Al, wobei dann in der Regel Kombinationen der Metalle, wie beispielsweise Ca/Ag, Mg/Ag oder Ba/Ag verwendet werden. Es kann auch bevorzugt sein, zwischen einer metallischen Kathode und dem organischen Halbleiter eine dünne Zwischenschicht eines Materials mit einer hohen Dielektrizitätskonstante einzubringen. Hierfür kommen beispielsweise Alkalimetall- oder Erdalkalimetallfluoride, aber auch die entsprechenden Oxide oder Carbonate in Frage (z. B. LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3, etc.). Weiterhin kann dafür Lithiumchinolinat (LiQ) verwendet werden. Die Schichtdicke dieser Schicht beträgt bevorzugt zwischen 0.5 und 5 nm.Metals with a low work function, metal alloys or multilayer structures made of different metals are preferred as the cathode of the organic electroluminescent device, such as alkaline earth metals, alkali metals, main group metals or lanthanides (e.g. Ca, Ba, Mg, Al, In, Mg, Yb, Sm, etc.). Alloys made of an alkali or alkaline earth metal and silver are also suitable, for example an alloy of magnesium and silver. In the case of multilayer structures, other metals that have a relatively high work function can also be used in addition to the metals mentioned, such as. B. Ag or Al, whereby combinations of metals such as Ca/Ag, Mg/Ag or Ba/Ag are generally used. It may also be preferable to introduce a thin intermediate layer of a material with a high dielectric constant between a metallic cathode and the organic semiconductor. For example, alkali metal or alkaline earth metal fluorides are suitable for this, but also the corresponding oxides or carbonates (e.g. LiF, Li 2 O, BaF 2 , MgO, NaF, CsF, Cs 2 CO 3 , etc.). Lithium quinolinate (LiQ) can also be used for this purpose. The layer thickness is preferably between 0.5 and 5 nm.
Als Anode sind Materialien mit hoher Austrittsarbeit bevorzugt. Bevorzugt weist die Anode eine Austrittsarbeit größer 4.5 eV vs. Vakuum auf. Hierfür sind einerseits Metalle mit hohem Redoxpotential geeignet, wie beispielsweise Ag, Pt oder Au. Es können andererseits auch Metall/Metalloxid-Elektroden (z. B. Al/Ni/NiOx, Al/PtOx) bevorzugt sein. Für einige Anwendungen muss mindestens eine der Elektroden transparent oder teiltransparent sein, um entweder die Bestrahlung des organischen Materials (organische Solarzelle) oder die Auskopplung von Licht (OLED, O-LASER) zu ermöglichen. Bevorzugte Anodenmaterialien sind hier leitfähige gemischte Metalloxide. Besonders bevorzugt sind Indium-ZinnOxid (ITO) oder Indium-Zink Oxid (IZO). Bevorzugt sind weiterhin leitfähige, dotierte organische Materialien, insbesondere leitfähige dotierte Polymere.Materials with a high work function are preferred as anode. The anode preferably has a work function greater than 4.5 eV vs. vacuum. On the one hand, metals with a high redox potential are suitable for this, such as Ag, Pt or Au. On the other hand, metal/metal oxide electrodes (e.g. Al/Ni/NiO x , Al/PtO x ) may also be preferred. For some applications, at least one of the electrodes must be transparent or partially transparent in order to enable either the irradiation of the organic material (organic solar cell) or the coupling out of light (OLED, O-LASER). Preferred anode materials here are conductive mixed metal oxides. Indium tin oxide (ITO) or indium zinc oxide (IZO) are particularly preferred. Also preferred are conductive, doped organic materials, in particular conductive doped polymers.
Die Vorrichtung wird entsprechend (je nach Anwendung) strukturiert, kontaktiert und schließlich versiegelt, da sich die Lebensdauer der erfindungsgemäßen Vorrichtungen bei Anwesenheit von Wasser und/oder Luft verkürzt.The device is structured, contacted and finally sealed accordingly (depending on the application), since the service life of the devices according to the invention is shortened in the presence of water and/or air.
In einer bevorzugten Ausführungsform ist die erfindungsgemäße organische Elektrolumineszenzvorrichtung dadurch gekennzeichnet, dass eine oder mehrere Schichten mit einem Sublimationsverfahren beschichtet werden. Dabei werden die Materialien in Vakuum-Sublimationsanlagen bei einem Anfangsdruck kleiner 10-5 mbar, bevorzugt kleiner 10-6 mbar aufgedampft. Dabei ist es jedoch auch möglich, dass der Anfangsdruck noch geringer ist, beispielsweise kleiner 10-7 mbar.In a preferred embodiment, the organic electroluminescent device according to the invention is characterized in that one or more layers are coated using a sublimation process. The materials are vapor-deposited in vacuum sublimation systems at an initial pressure of less than 10 -5 mbar, preferably less than 10 -6 mbar. However, it is also possible for the initial pressure to be even lower, for example less than 10 -7 mbar.
Bevorzugt ist ebenfalls eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten mit dem OVPD (Organic Vapour Phase Deposition) Verfahren oder mit Hilfe einer Trägergassublimation beschichtet werden. Dabei werden die Materialien bei einem Druck zwischen 10-5 mbar und 1 bar aufgebracht. Ein Spezialfall dieses Verfahrens ist das OVJP (Organic Vapour Jet Printing) Verfahren, bei dem die Materialien direkt durch eine Düse aufgebracht und so strukturiert werden (z. B.
Weiterhin bevorzugt ist eine organische Elektrolumineszenzvorrichtung, dadurch gekennzeichnet, dass eine oder mehrere Schichten aus Lösung, wie z. B. durch Spincoating, oder mit einem beliebigen Druckverfahren, wie z. B. Siebdruck, Flexodruck, Tiefdruck (Gravur), Slot-Die-Printing, Slot-Die-Coating, Nozzle Printing oder Offsetdruck, besonders bevorzugt aber LITI (Light Induced Thermal Imaging, Thermotransferdruck) oder Ink-Jet Druck (Tintenstrahldruck), hergestellt werden. Hierfür sind lösliche Verbindungen gemäß Formel (I) oder Formel (II) nötig. Hohe Löslichkeit lässt sich durch geeignete Substitution der Verbindungen erreichen.Also preferred is an organic electroluminescent device, characterized in that one or more layers are produced from solution, such as by spin coating, or using any printing method, such as screen printing, flexographic printing, gravure printing (engraving), slot-die printing, slot-die coating, nozzle printing or offset printing, but particularly preferably LITI (light induced thermal imaging, thermal transfer printing) or ink-jet printing. Soluble compounds according to formula (I) or formula (II) are required for this. High solubility can be achieved by suitable substitution of the compounds.
Weiterhin bevorzugt ist es, dass zur Herstellung einer erfindungsgemäßen organischen Elektrolumineszenzvorrichtung eine oder mehrere Schichten aus Lösung und eine oder mehrere Schichten durch ein Sublimationsverfahren aufgetragen werden.It is further preferred that, in order to produce an organic electroluminescent device according to the invention, one or more layers are applied from solution and one or more layers are applied by a sublimation process.
Erfindungsgemäß können die elektronischen Vorrichtungen enthaltend eine oder mehrere Verbindungen gemäß Formel (I) oder (II) in Displays, als Lichtquellen in Beleuchtungsanwendungen sowie als Lichtquellen in medizinischen und/oder kosmetischen Anwendungen (z.B. Lichttherapie) eingesetzt werden.According to the invention, the electronic devices comprising one or more compounds according to formula (I) or (II) can be used in displays, as light sources in lighting applications and as light sources in medical and/or cosmetic applications (e.g. light therapy).
Die erfindungsgemäßen Vorrichtungen weisen bevorzugt einen oder mehrere der unten angegebenen Vorteile auf:
- - bei Verwendung der Verbindungen gemäß Formel (I) oder (II) in den Vorrichtungen, insbesondere als Matrixmaterialien für phosphoreszierende Emitter, können eine hohe Leistungseffizienz und eine niedrige Betriebsspannung der Vorrichtungen erreicht werden
- - bei Verwendung der Verbindungen gemäß Formel (I) oder (II) wird eine lange Lebensdauer der elektronischen Vorrichtung erhalten.
- - die Verbindungen gemäß Formel (I) oder (II) weisen deutlich bessere Löslichkeit und Filmbildungseigenschaften auf im Vergleich zu im Stand der Technik bekannten Materialien, insbesondere im Vergleich zu carbazolbasierten Matrixmaterialien
- - when using the compounds according to formula (I) or (II) in the devices, in particular as matrix materials for phosphorescent emitters, a high power efficiency and a low operating voltage of the devices can be achieved
- - when using the compounds according to formula (I) or (II), a long lifetime of the electronic device is obtained.
- - the compounds according to formula (I) or (II) have significantly better solubility and film-forming properties compared to materials known in the prior art, in particular compared to carbazole-based matrix materials
Die Erfindung wird durch die nachfolgenden Ausführungsbeispiele näher erläutert. Die Erfindung ist nicht auf den Umfang der explizit offenbarten Beispiele beschränkt.The invention is explained in more detail by the following embodiments. The invention is not limited to the scope of the explicitly disclosed examples.
Ausführungsbeispieleimplementation examples
Unter Schutzgas werden 22.9 g (49 mmol) 5[(2-Phenyl-1 H-benzimidazol-5-yl)thio]-9-phenyl-N-carbazol in 0.3 L Eisessig vorgelegt. Zu dieser Lösung werden 33 mL (619 mmol) 30% H2O2-Lösung zugetropft und über Nacht gerührt. Das Gemisch wird mit Na2SO3 Lösung versetzt, die Phasen werden getrennt und das Lösungsmittel im Vakuum entfernt. Der Gehalt an Produkt beträgt gemäß 1H-NMR ca. 98 % bei einer Gesamtausbeute von 23.2 g (95 %).
2) Synthesen von Vorstufen analog zu Schritt 3 in Beispiel 12) Synthesis of precursors analogous to step 3 in Example 1
4) Synthese von Verbindung 54) Synthesis of compound 5
Analog zum letzten Schritt in Beispiel 1 kann die folgende Verbindung 5 erhalten werden:
5) Synthese von Verbindung 65) Synthesis of compound 6
6) Synthesen der Verbindungen 2, 4, 7, 8 und 96) Syntheses of compounds 2, 4, 7, 8 and 9
Analog zum oben beschriebenen Schritt können folgende Verbindungen erhalten werden:
7) Synthese der Verbindung 107) Synthesis of compound 10
Entsprechend dem ersten Schritt der Synthese von Verbindung 3 wird aus der Zwischenstufe 10b die Verbindung 10 erhalten:
8) Synthese der Verbindung 118) Synthesis of compound 11
Entsprechend dem ersten Schritt der Synthese von Verbindung 3 kann die Verbindung 11 erhalten werden:
Als Referenz-Materialien werden verwendet:
Beispiel 9: Lösungen und Zusammensetzungen enthaltend Matrixmaterialen und TEG1 für OLEDsExample 9: Solutions and compositions containing matrix materials and TEG1 for OLEDs
Lösungen Ref sowie A bis K, wie sie in Tabelle 1 zusammengefasst sind, werden wie folgt hergestellt: Zunächst werden 200 mg des TMM und 50 mg TEG1 in 10 mL Chlorbenzol gelöst und so lange gerührt, bis die Lösung klar ist. Die Lösung wird filtriert unter Verwendung eines Filters Millipore Millex LS, Hydrophobic PTFE 5.0 µm. Tabelle 1: Zusammensetzung der Lösungen
Die Lösungen werden verwendet, um die emittierende Schicht von OLEDs zu beschichten. Die entsprechende Feststoffzusammensetzung kann erhalten werden, indem das Lösemittel der Lösungen verdampft wird. Diese kann für die Herstellung weiterer Formulierungen verwendet werden.The solutions are used to coat the emitting layer of OLEDs. The corresponding solid composition can be obtained by evaporating the solvent of the solutions. This can be used to prepare further formulations.
Beispiel 10: Herstellung der OLEDsExample 10: Production of OLEDs
OLED-Ref sowie die erfindungsgemäßen OLED-A bis OLED-K, welche alle den Aufbau IOT/PEDOT/Interlayer/EML/Kathode aufweisen, werden unter Verwendung der entsprechenden Lösungen, wie in Tabelle 2 zusammengefasst, gemäß der folgenden Vorschrift hergestellt:
- 1) Beschichtung von 80 nm PEDOT (Baytron P Al 4083) auf ein ITObeschichtetes Glassubstrat durch Spin-Coating, und 10 Minuten bei 180°C ausheizen.
- 2) Beschichtung einer 20 nm Interlayer durch Spin-Coating einer Toluollösung von HIL-012 (Merck KGaA) (Konzentration 0.5 Gew.%) in einer Glovebox.
- 3) Ausheizen der Interlayer bei 180 °C für 1 h in einer Glovebox.
- 4) Beschichtung einer 80 nm emittierenden Schicht durch Spin-Coating einer entsprechenden Lösung gemäß Tabelle 1.
- 5) Ausheizen der Vorrichtung bei 180 °C für 10 min.
- 6) Aufdampfen einer Ba/Al-Kathode (3 nm + 150 nm).
- 7) Verkapselung der Vorrichtung.
- 1) Coating of 80 nm PEDOT (Baytron P Al 4083) on an ITO coated glass substrate by spin coating and annealing for 10 minutes at 180°C.
- 2) Coating of a 20 nm interlayer by spin-coating a toluene solution of HIL-012 (Merck KGaA) (concentration 0.5 wt%) in a glove box.
- 3) Bake the interlayer at 180 °C for 1 h in a glove box.
- 4) Coating of an 80 nm emitting layer by spin-coating an appropriate solution according to Table 1.
- 5) Bake the device at 180 °C for 10 min.
- 6) Evaporation of a Ba/Al cathode (3 nm + 150 nm).
- 7) Encapsulation of the device.
Beispiel 11: Messungen und Vergleich der ErgebnisseExample 11: Measurements and comparison of results
Die so erhaltenen OLEDs werden nach Standardmethoden charakterisiert. Dabei werden die folgenden Eigenschaften gemessen: UIL-Charakteristik, Elektrolumineszenzspektrum, Farbkoordinaten (CIEx und CIEy), Effizienz und Betriebsspannung. Die Ergebnisse sind in Tabelle 3 zusammengefasst, wobei OLED-Ref als Vergleich gemäß dem Stand der Technik dient. In Tabelle 3 steht Uon für die Einsatzspannung, und U(100) für die Spannung bei 100 cd/m2. Tabelle 3: Messergebnisse mit OLED-Ref sowie OLED-A bis OLED-K
Wie aus Tabelle 3 ersichtlich ist, werden unter Verwendung der erfindungsgemäßen Matrixmaterialien deutlich verbesserte phosphoreszierende OLEDs in Bezug auf Betriebsspannung und Effizienz erhalten. Alle OLEDs zeigen vergleichbare Farbkoordinaten.As can be seen from Table 3, using the matrix materials according to the invention, significantly improved phosphorescent OLEDs are obtained in terms of operating voltage and efficiency. All OLEDs show comparable color coordinates.
Es ist ebenfalls möglich (nicht explizit gezeigt), die erfindungsgemäßen Verbindungen als Triplett-Matrixmaterialien in Kombination mit einem weiteren Matrixmaterial (Mixed-Matrix) zu verwenden.It is also possible (not explicitly shown) to use the compounds according to the invention as triplet matrix materials in combination with another matrix material (mixed matrix).
Weiterhin ergibt auch die Verwendung mit anderen Triplett-Emittern als TEG1 gute Ergebnisse.Furthermore, the use with triplet emitters other than TEG1 also produces good results.
Claims (9)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11010151.6 | 2011-12-22 | ||
| EP11010151 | 2011-12-22 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE102012022880A1 DE102012022880A1 (en) | 2013-06-27 |
| DE102012022880B4 true DE102012022880B4 (en) | 2024-12-24 |
Family
ID=48575694
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102012022880.5A Active DE102012022880B4 (en) | 2011-12-22 | 2012-11-23 | Electronic devices containing organic layers |
Country Status (1)
| Country | Link |
|---|---|
| DE (1) | DE102012022880B4 (en) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103483332B (en) * | 2013-09-11 | 2016-08-10 | 中山大学 | Piezoluminescent material with thermally activated delayed fluorescence and aggregation-induced luminescent properties, its synthesis method and application |
| CN103694992B (en) * | 2013-12-26 | 2016-03-16 | 深圳市华星光电技术有限公司 | Hot activation delayed fluorescence material, its synthetic method and use the OLED of this hot activation delayed fluorescence material |
| KR101577121B1 (en) * | 2013-12-27 | 2015-12-14 | 주식회사 두산 | Organic compounds and organic electro luminescence device comprising the same |
| CN103833754B (en) * | 2014-01-02 | 2016-03-23 | 山东大学 | There is the carbazole of diaza aromatic condensed ring structure and phenanthridines compounds and synthetic method thereof |
| CN103887447B (en) * | 2014-04-01 | 2016-02-10 | 上海道亦化工科技有限公司 | A kind of organic electroluminescence device |
| EP3015469B1 (en) | 2014-10-30 | 2018-12-19 | Idemitsu Kosan Co., Ltd. | 5-(benzimidazol-2-yl)benzimidazo[1,2-a]benzimidazoles for electronic applications |
| EP3053918B1 (en) | 2015-02-06 | 2018-04-11 | Idemitsu Kosan Co., Ltd. | 2-carbazole substituted benzimidazoles for electronic applications |
| CN114342103B (en) * | 2019-09-19 | 2025-12-23 | 默克专利有限公司 | A mixture of two host materials and an organic electroluminescent device containing the mixture |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
Family Cites Families (87)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US4780536A (en) | 1986-09-05 | 1988-10-25 | The Ohio State University Research Foundation | Hexaazatriphenylene hexanitrile and its derivatives and their preparations |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| DE4111878A1 (en) | 1991-04-11 | 1992-10-15 | Wacker Chemie Gmbh | LADDER POLYMERS WITH CONJUGATED DOUBLE BINDINGS |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| DE69432054T2 (en) | 1993-09-29 | 2003-10-09 | Idemitsu Kosan Co | ORGANIC ELECTROLUMINESCENT ELEMENTS AND ARYLENE DIAMINE DERIVATIVES |
| DE69412567T2 (en) | 1993-11-01 | 1999-02-04 | Hodogaya Chemical Co., Ltd., Tokio/Tokyo | Amine compound and electroluminescent device containing it |
| JPH07133483A (en) | 1993-11-09 | 1995-05-23 | Shinko Electric Ind Co Ltd | Organic light emitting material for EL device and EL device |
| EP0676461B1 (en) | 1994-04-07 | 2002-08-14 | Covion Organic Semiconductors GmbH | Spiro compounds and their application as electroluminescence materials |
| DE4436773A1 (en) | 1994-10-14 | 1996-04-18 | Hoechst Ag | Conjugated polymers with spirocenters and their use as electroluminescent materials |
| WO1997005184A1 (en) | 1995-07-28 | 1997-02-13 | The Dow Chemical Company | 2,7-aryl-9-substituted fluorenes and 9-substituted fluorene oligomers and polymers |
| DE19614971A1 (en) | 1996-04-17 | 1997-10-23 | Hoechst Ag | Polymers with spiro atoms and their use as electroluminescent materials |
| DE19652261A1 (en) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Aryl-substituted poly (p-arylenevinylenes), process for their preparation and their use in electroluminescent devices |
| US6344283B1 (en) | 1996-12-28 | 2002-02-05 | Tdk Corporation | Organic electroluminescent elements |
| DE19846766A1 (en) | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | A conjugated fluorene-based polymer useful as an organic semiconductor, electroluminescence material, and for display elements |
| US6166172A (en) | 1999-02-10 | 2000-12-26 | Carnegie Mellon University | Method of forming poly-(3-substituted) thiophenes |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| KR100946314B1 (en) | 1999-12-01 | 2010-03-09 | 더 트러스티즈 오브 프린스턴 유니버시티 | Organic light emitting device comprising a phosphorescent organo metallic compound |
| KR100377321B1 (en) | 1999-12-31 | 2003-03-26 | 주식회사 엘지화학 | Electronic device comprising organic compound having p-type semiconducting characteristics |
| JP4220644B2 (en) | 2000-02-14 | 2009-02-04 | 三井化学株式会社 | Amine compound and organic electroluminescent device containing the compound |
| US6660410B2 (en) | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| CN101924190B (en) | 2000-08-11 | 2012-07-04 | 普林斯顿大学理事会 | Organometallic compounds and emission-shifting organic electrophosphorescence |
| JP4154140B2 (en) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | Metal coordination compounds |
| JP4154138B2 (en) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | Light emitting element, display device and metal coordination compound |
| JP4154139B2 (en) | 2000-09-26 | 2008-09-24 | キヤノン株式会社 | Light emitting element |
| GB0104177D0 (en) | 2001-02-20 | 2001-04-11 | Isis Innovation | Aryl-aryl dendrimers |
| EP1370619B1 (en) | 2001-03-10 | 2006-06-21 | MERCK PATENT GmbH | Solutions and dispersions of organic semiconductors |
| DE10141624A1 (en) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors | Solutions of polymeric semiconductors |
| DE10159946A1 (en) | 2001-12-06 | 2003-06-18 | Covion Organic Semiconductors | Process for the production of aryl-aryl coupled compounds |
| DE10249723A1 (en) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Conjugated polymers containing arylamine units, their preparation and use |
| GB0226010D0 (en) | 2002-11-08 | 2002-12-18 | Cambridge Display Tech Ltd | Polymers for use in organic electroluminescent devices |
| JP2006511939A (en) | 2002-12-23 | 2006-04-06 | コビオン・オーガニック・セミコンダクターズ・ゲーエムベーハー | Organic electroluminescence device |
| DE10304819A1 (en) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazole-containing conjugated polymers and blends, their preparation and use |
| DE10310887A1 (en) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| US7851071B2 (en) | 2003-03-13 | 2010-12-14 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| JP4411851B2 (en) | 2003-03-19 | 2010-02-10 | コニカミノルタホールディングス株式会社 | Organic electroluminescence device |
| JP5318347B2 (en) | 2003-04-15 | 2013-10-16 | メルク パテント ゲーエムベーハー | Mixture of matrix material and organic semiconductor capable of emitting light, use thereof, and electronic component comprising said mixture |
| EP2236579B1 (en) | 2003-04-23 | 2014-04-09 | Konica Minolta Holdings, Inc. | Organic electroluminescent element and display |
| EP1491568A1 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors GmbH | Semiconductive Polymers |
| DE10328627A1 (en) | 2003-06-26 | 2005-02-17 | Covion Organic Semiconductors Gmbh | New materials for electroluminescence |
| KR101105619B1 (en) | 2003-07-07 | 2012-01-18 | 메르크 파텐트 게엠베하 | Mixtures of organic emissive semiconductors and matrix materials, their use and electronic components comprising said materials |
| DE10333232A1 (en) | 2003-07-21 | 2007-10-11 | Merck Patent Gmbh | Organic electroluminescent element |
| DE10337346A1 (en) | 2003-08-12 | 2005-03-31 | Covion Organic Semiconductors Gmbh | Conjugated polymers containing dihydrophenanthrene units and their use |
| DE10338550A1 (en) | 2003-08-19 | 2005-03-31 | Basf Ag | Transition metal complexes with carbene ligands as emitters for organic light-emitting diodes (OLEDs) |
| WO2005026144A1 (en) | 2003-09-12 | 2005-03-24 | Sumitomo Chemical Company, Limited | Dendrimer compound and organic luminescent element employing the same |
| DE10345572A1 (en) | 2003-09-29 | 2005-05-19 | Covion Organic Semiconductors Gmbh | metal complexes |
| US7795801B2 (en) | 2003-09-30 | 2010-09-14 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| US7659540B2 (en) | 2003-10-22 | 2010-02-09 | Merck Patent Gmbh | Materials for electroluminescence and the utilization thereof |
| DE102004008304A1 (en) | 2004-02-20 | 2005-09-08 | Covion Organic Semiconductors Gmbh | Organic electronic devices |
| US7790890B2 (en) | 2004-03-31 | 2010-09-07 | Konica Minolta Holdings, Inc. | Organic electroluminescence element material, organic electroluminescence element, display device and illumination device |
| KR100787425B1 (en) | 2004-11-29 | 2007-12-26 | 삼성에스디아이 주식회사 | Phenylcarbazole compound and organic electroluminescent device using same |
| DE102004020298A1 (en) | 2004-04-26 | 2005-11-10 | Covion Organic Semiconductors Gmbh | Electroluminescent polymers and their use |
| DE102004023277A1 (en) | 2004-05-11 | 2005-12-01 | Covion Organic Semiconductors Gmbh | New material mixtures for electroluminescence |
| US7598388B2 (en) | 2004-05-18 | 2009-10-06 | The University Of Southern California | Carbene containing metal complexes as OLEDs |
| JP4862248B2 (en) | 2004-06-04 | 2012-01-25 | コニカミノルタホールディングス株式会社 | Organic electroluminescence element, lighting device and display device |
| DE102004032527A1 (en) | 2004-07-06 | 2006-02-02 | Covion Organic Semiconductors Gmbh | Electroluminescent polymers |
| EP1655359A1 (en) | 2004-11-06 | 2006-05-10 | Covion Organic Semiconductors GmbH | Organic electroluminescent device |
| JP2006156847A (en) | 2004-11-30 | 2006-06-15 | Fuji Photo Film Co Ltd | Organic electroluminescent element |
| EP1669386A1 (en) | 2004-12-06 | 2006-06-14 | Covion Organic Semiconductors GmbH | Conjugated polymers, representation thereof, and use |
| EP2371810A1 (en) | 2005-01-05 | 2011-10-05 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescent device using same |
| JP2006253445A (en) | 2005-03-11 | 2006-09-21 | Toyo Ink Mfg Co Ltd | Organic electroluminescence device |
| WO2006100896A1 (en) | 2005-03-18 | 2006-09-28 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescence device utilizing the same |
| CN101171320B (en) | 2005-05-03 | 2013-04-10 | 默克专利有限公司 | Organic electroluminescent device |
| DE102005023437A1 (en) | 2005-05-20 | 2006-11-30 | Merck Patent Gmbh | Connections for organic electronic devices |
| BRPI0613785A2 (en) | 2005-07-08 | 2011-02-01 | Unilever Nv | starch-containing food product, process for preparing intact starch-containing plant cells and process for preparing starch-containing food product |
| DE102005037734B4 (en) | 2005-08-10 | 2018-02-08 | Merck Patent Gmbh | Electroluminescent polymers, their use and bifunctional monomeric compounds |
| EP1956022B1 (en) | 2005-12-01 | 2012-07-25 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent element and organic electroluminescent element |
| DE102005060473A1 (en) | 2005-12-17 | 2007-06-28 | Merck Patent Gmbh | Conjugated polymers, their preparation and use |
| DE102006025777A1 (en) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| DE102006025846A1 (en) | 2006-06-02 | 2007-12-06 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| DE102006031990A1 (en) | 2006-07-11 | 2008-01-17 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| US8062769B2 (en) | 2006-11-09 | 2011-11-22 | Nippon Steel Chemical Co., Ltd. | Indolocarbazole compound for use in organic electroluminescent device and organic electroluminescent device |
| JP2008130754A (en) | 2006-11-20 | 2008-06-05 | Fujifilm Corp | Organic electroluminescence device |
| DE102007002714A1 (en) | 2007-01-18 | 2008-07-31 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| DE102007024850A1 (en) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| DE102007053771A1 (en) | 2007-11-12 | 2009-05-14 | Merck Patent Gmbh | Organic electroluminescent devices |
| US8815412B2 (en) | 2007-12-21 | 2014-08-26 | Semiconductor Energy Laboratory Co., Ltd. | Quinoxaline derivative, and light-emitting element, light-emitting device, and electronic appliance using the quinoxaline derivative |
| DE102008033943A1 (en) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | New materials for organic electroluminescent devices |
| DE102008036982A1 (en) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organic electroluminescent device |
| WO2010027181A2 (en) | 2008-09-02 | 2010-03-11 | 주식회사 두산 | Anthracene derivative and organic electroluminescence element using the same |
| KR20110097612A (en) | 2008-11-11 | 2011-08-31 | 메르크 파텐트 게엠베하 | Organic electroluminescent devices |
| DE102008056688A1 (en) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| DE102009023155A1 (en) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| DE102009031021A1 (en) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| DE102010005697A1 (en) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Connections for electronic devices |
| DE102010014933A1 (en) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materials for electronic devices |
-
2012
- 2012-11-23 DE DE102012022880.5A patent/DE102012022880B4/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
Non-Patent Citations (3)
| Title |
|---|
| JOUANNEAU, Julien [et al.]: Synthesis and characterization of ionic conducting sulfonated polybenzimidazoles. In: Journal of polymer science. Part A, Vol. 48, 2010, No. 8, S. 1732-1742. – ISSN 0024-9297 |
| KORSHAK, V. V. [et al.]: Synthesis and investigation of poly(benzimidazole imides) based on new di-imidodicarboxylic acids. In: Polymer science U.S.S.R., Vol. 22, 1980, No. 6, S. 1325-1333. – ISSN 0032-3950 |
| KORSHAK, V. V. [et al.]: Two-stage synthesis of poly(N-phenylbenzimidazoles). In: Macromolecules, Vol. 5, 1972, No. 6, S. 807-812. – ISSN 0024-9297 |
Also Published As
| Publication number | Publication date |
|---|---|
| DE102012022880A1 (en) | 2013-06-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2705552B1 (en) | Compounds for electronic devices | |
| EP3424907B1 (en) | Connections and organic electronic devices | |
| DE112010004381B4 (en) | materials for electronic devices | |
| EP2875092B1 (en) | Compounds and organic electroluminescent devices | |
| EP3114102B1 (en) | Materials for electronic devices | |
| EP3439065B1 (en) | Materials for electronic devices | |
| EP2705550B1 (en) | Compounds for electronic devices | |
| EP3378857B1 (en) | Materials for electronic devices | |
| EP2791105B1 (en) | Compounds for electronic devices | |
| EP2737554B1 (en) | Compounds for electronic devices | |
| EP2875699B1 (en) | Derivates of 2-diarylaminofluoren and organic electronic devices comprising the same | |
| EP2858980B1 (en) | Phenanthrenes for use in organic electronic devices | |
| EP2926385B1 (en) | Electronic device | |
| DE102010024542A1 (en) | Materials for electronic devices | |
| WO2012048780A1 (en) | Compounds for electronic devices | |
| WO2012143079A1 (en) | Compounds for electronic devices | |
| WO2014079527A1 (en) | Materials for electronic devices | |
| DE102012022880B4 (en) | Electronic devices containing organic layers | |
| EP3615542B1 (en) | Compounds for electronic devices | |
| WO2014106524A2 (en) | Materials for electronic devices | |
| EP3679023A1 (en) | Materials for electronic devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| R012 | Request for examination validly filed | ||
| R016 | Response to examination communication | ||
| R016 | Response to examination communication | ||
| R018 | Grant decision by examination section/examining division | ||
| R020 | Patent grant now final |