요약
한 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
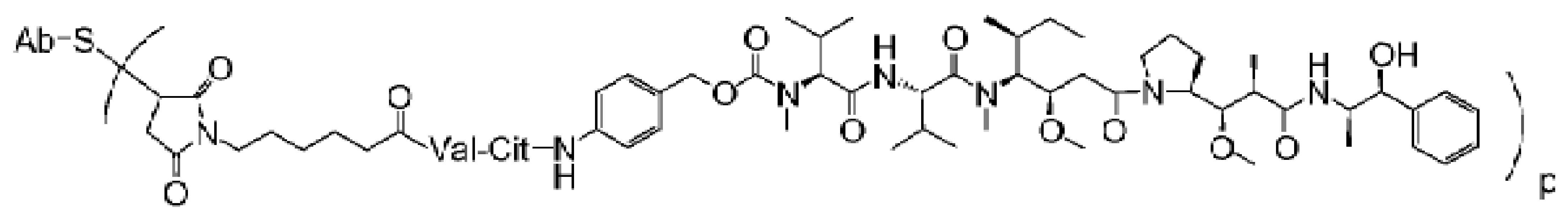
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴이다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 2이다.
일부 구체예들에서, 면역접합체는 약 1 mg/kg 내지 약 5 mg/kg인 용량으로 투여된다.. 일부 구체예들에서, 면역접합체는 약 1.2 mg/kg, 약 1.8 mg/kg, 약 2.4 mg/kg, 약 3.6 mg/kg, 또는 약 4.8 mg/kg의 용량으로 투여된다. 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 1회 이상의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체는 각 사이클에 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 각 사이클에 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 각 사이클에 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 각 사이클에 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체 및 리툭시맙은 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 특정 구체예들에서, 리툭시맙은 면역접합체 전에 투여된다. 특정 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 2회, 적어도 3회, 적어도 4회, 적어도 5회, 적어도 6회, 또는 적어도 7회 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 리툭시맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 전신 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 특정 구체예들에서, 달리 명시되지 않는 한 (NOS), DLBCL은 조직학적으로 확인된 DLBCL이고, 인간은 무통성 질환이 DLBCL로 전환된 병력이 있다. 특정 구체예들에서, DLBCL은 재발성 또는 불응성 DLBCL이다. 특정 구체예들에서, 인간은 동부 종양학 협력 그룹(ECOG) 전신 활동도 점수 0, 1, 또는 2를 가진다. 특정 구체예들에서, 인간은 자가 또는 동종 줄기 세포 이식 (SCT)이 예정되어 있지 않다. 특정 구체예들에서, 인간은 젬시타빈과 백금 기반 제제를 병용한 선행 요법을 받은 적이 없다. 특정 구체예들에서, 인간은 이상 반응에 대한 국립 암 연구소(National Cancer Institute) 공통 용어 기준, 버전 5.0에 따라 1등급보다 높은 말초 신경병증이 없다. 특정 구체예들에서, 인간은 1차 또는 2차 중추신경계 림프종이 없다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 자가 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 DLBCL에 대해 적어도 2가지 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대해 폴라투주맙 베도틴-피이크를 사용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 성인 인간은 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종을 가진다.
특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다. 특정 구체예들에서, 치료받은 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 특정 구체예들에서, 치료받은 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수 중 33% 이하의 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 신경독성을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 신경독성을 경험하지 않는다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 33% 이하의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 40% 미만의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 8% 미만의 인간이 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 6% 미만의 인간이 말초 신경병증을 경험하여, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하게 된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 치료받는 다수의 인간 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체는 각 사이클에 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 각 사이클에 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 각 사이클에 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 각 사이클에 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체 및 리툭시맙은 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 특정 구체예들에서, 리툭시맙은 면역접합체 전에 투여된다. 특정 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 14일 이내 인간에서 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 14일 이내 인간에서 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 상기 다수 중 33% 이하의 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 상기 다수 중 33% 이하의 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 상기 다수의 인간 중 33% 이하가 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 상기 다수의 인간 중 33% 이하가 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 2회, 적어도 3회, 적어도 4회, 적어도 5회, 적어도 6회, 또는 적어도 7회 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 리툭시맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴이다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 2이다.
일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 전신 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 특정 구체예들에서, 달리 명시되지 않는 한 (NOS), DLBCL은 조직학적으로 확인된 DLBCL이고, 인간은 무통성 질환이 DLBCL로 전환된 병력이 있다. 특정 구체예들에서, DLBCL은 재발성 또는 불응성 DLBCL이다. 특정 구체예들에서, 인간은 동부 종양학 협력 그룹(ECOG) 전신 활동도 점수 0, 1, 또는 2를 가진다. 특정 구체예들에서, 인간은 자가 또는 동종 줄기 세포 이식 (SCT)이 예정되어 있지 않다. 특정 구체예들에서, 인간은 젬시타빈과 백금 기반 제제를 병용한 선행 요법을 받은 적이 없다. 특정 구체예들에서, 인간은 이상 반응에 대한 국립 암 연구소(National Cancer Institute) 공통 용어 기준, 버전 5.0에 따라 1등급보다 높은 말초 신경병증이 없다. 특정 구체예들에서, 인간은 1차 또는 2차 중추신경계 림프종이 없다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 자가 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대해 폴라투주맙 베도틴-피이크를 사용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 성인 인간은 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종을 가진다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 신경독성을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 신경독성을 경험하지 않는다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 33% 이하의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 40% 미만의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 8% 미만의 인간이 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 6% 미만의 인간이 말초 신경병증을 경험하여, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 완전 반응을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 부분 반응을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 무진행 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 무진행 생존 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 무사건 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 무사건 생존 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 시작 후 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상 동안 인간을 생존하게 한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 이러한 다수의 인간의 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상의 전체 생존 중앙값을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 전체 생존 중앙값의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 종양 용해 증후군을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 종양 용해 증후군에 대한 예방적 치료를 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 감염을 일으키지 않는다. 일부 구체예들에서, 감염은 폐포자충 감염 또는 헤르페스 바이러스 감염이다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 감염에 대한 예방적 치료를 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 호중구 감소증을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 호중구 감소증에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 호중구 감소증에 대한 예방적 치료는 G-CSF를 인간에게 투여하는 것을 포함한다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여 후 인간에서 3등급 또는 등급 4 호중구감소증이 발생하는 경우 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴 치료를 중단하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 인간에서 절대 호중구 수치 (ANC)가 >1000/μL로 증가하는 경우, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 호중구 감소증을 치료하기 위해 하나 이상의 성장 인자를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 하나 이상의 성장 인자는 G-CSF를 포함한다. 일부 구체예들에서, 상기 방법은 ANC가 인간에서 21일 사이클의 7일차에 또는 이전에 > 1000/μL로 회복되는 경우, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 용량 감소없이 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 ANC가 인간에서 21일 사이클의 7일차 이후에 > 1000/μL로 회복되는 경우, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함하며, 이때 면역접합체의 용량은 1.4 mg/kg로 감소된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 용량 감소가 이전에 있었던 경우, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 B형 간염 재활성화를 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 B형 간염 재활성화에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 본원에 제공된 방법은 B형 간염 재활성화가 인간에서 검출되는 경우 항바이러스 약물을 인간에게 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 약물-유발 간 손상, 진행성 다초점 백질뇌병증, 전신 과민 반응, 아나필락시스 반응, 아나필락시양 반응, 및 2차 악성 종양으로 구성된 그룹에서 선택된 하나 이상의 이상 반응을 일으키지 않는다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 완전 반응율 (CRR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 객관적 반응율 (ORR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 최적의 전체 반응율 (BOR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 반응 기간 (DOR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 63% 이상, 적어도 약 65% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 14% 이상, 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무진행 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 42% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 67% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 38% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 3.5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 전체 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무사건 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무사건 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 객관적 반응율을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 35% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 완전 반응율을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 10% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 부분 반응율을 초래한다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 부분 반응율의 증가를 초래한다.
또 다른 양상에서, 본원은 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위해 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 포함하는 키트를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위해 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 사용하기 위한 폴라투주맙 베도틴-피이크를 포함하는 키트를 제공한다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간 중 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
한 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴이다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 2이다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체는 각 사이클에 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 각 사이클에 약 1000 mg의 용량으로 투여되고, 젬시타빈은 각 사이클에 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 각 사이클에 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 오비누투주맙은 면역접합체 전에 투여된다. 특정 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다:
다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.4 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 75 mg/m2의 용량으로 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 2회, 적어도 3회, 적어도 4회, 적어도 5회, 적어도 6회, 또는 적어도 7회 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 오비누투주맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 전신 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 특정 구체예들에서, 달리 명시되지 않는 한 (NOS), DLBCL은 조직학적으로 확인된 DLBCL이고, 인간은 무통성 질환이 DLBCL로 전환된 병력이 있다. 특정 구체예들에서, DLBCL은 재발성 또는 불응성 DLBCL이다. 특정 구체예들에서, 인간은 동부 종양학 협력 그룹(ECOG) 전신 활동도 점수 0, 1, 또는 2를 가진다. 특정 구체예들에서, 인간은 자가 또는 동종 줄기 세포 이식 (SCT)이 예정되어 있지 않다. 특정 구체예들에서, 인간은 젬시타빈과 백금 기반 제제를 병용한 선행 요법을 받은 적이 없다. 특정 구체예들에서, 인간은 이상 반응에 대한 국립 암 연구소(National Cancer Institute) 공통 용어 기준, 버전 5.0에 따라 1등급보다 높은 말초 신경병증이 없다. 특정 구체예들에서, 인간은 1차 또는 2차 중추신경계 림프종이 없다. 일부 구체예들에서, 인간은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 자가 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대해 폴라투주맙 베도틴-피이크를 사용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 성인 인간은 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종을 가진다.
특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다. 특정 구체예들에서, 치료받은 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 특정 구체예들에서, 치료받은 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수 중 33% 이하의 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 신경독성을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 신경독성을 경험하지 않는다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 33% 이하의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 40% 미만의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 8% 미만의 인간이 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 6% 미만의 인간이 말초 신경병증을 경험하여, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하게 된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 치료받는 다수의 인간 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
특정 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함한다. 일부 구체예들에서, 항-CD79b 항체는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 3 내지 4이다. 특정 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체는 각 사이클에 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 각 사이클에 약 1000 mg의 용량으로 투여되고, 젬시타빈은 각 사이클에 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 각 사이클에 약 100 mg/m2의 용량으로 투여된다. 특정 구체예들에서, 오비누투주맙은 면역접합체 전에 투여된다. 특정 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여된다. 특정 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증이 일어나지 않게 한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증이 일어나지 않게 한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간 중 33% 이하는 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간 중 33% 이하는 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간 중 33% 이하가 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 치료를 필요로 하는 인간에게 유효량의 다음을 투여하는 것을 포함하는 인간의 미만성 거대 B-세포 림프종 (DLBCL) 치료 방법이 본원에 제공된다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 오비누투주맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간 중 33% 이하가 14일 이내 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 2회, 적어도 3회, 적어도 4회, 적어도 5회, 적어도 6회, 또는 적어도 7회 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 오비누투주맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴이다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 2이다.
일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 전신 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 특정 구체예들에서, 달리 명시되지 않는 한 (NOS), DLBCL은 조직학적으로 확인된 DLBCL이고, 인간은 무통성 질환이 DLBCL로 전환된 병력이 있다. 특정 구체예들에서, DLBCL은 재발성 또는 불응성 DLBCL이다. 특정 구체예들에서, 인간은 동부 종양학 협력 그룹(ECOG) 전신 활동도 점수 0, 1, 또는 2를 가진다. 특정 구체예들에서, 인간은 자가 또는 동종 줄기 세포 이식 (SCT)이 예정되어 있지 않다. 특정 구체예들에서, 인간은 젬시타빈과 백금 기반 제제를 병용한 선행 요법을 받은 적이 없다. 특정 구체예들에서, 인간은 이상 반응에 대한 국립 암 연구소(National Cancer Institute) 공통 용어 기준, 버전 5.0에 따라 1등급보다 높은 말초 신경병증이 없다. 특정 구체예들에서, 인간은 1차 또는 2차 중추신경계 림프종이 없다. 일부 구체예들에서, 인간은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 자가 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대해 폴라투주맙 베도틴-피이크를 사용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 성인 인간은 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종을 가진다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 말초 신경병증을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 등급 4 이상의 신경독성을 일으키지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 등급 4 이상의 신경독성을 경험하지 않는다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 33% 이하의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 40% 미만의 인간이 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 8% 미만의 인간이 3등급 이상의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 6% 미만의 인간이 말초 신경병증을 경험하여, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하게 된다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 완전 반응을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 부분 반응을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 무진행 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 무진행 생존 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 무사건 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 무사건 생존 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 시작 후 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상 동안 인간을 생존하게 한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 이러한 다수의 인간의 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상의 전체 생존 중앙값을 초래한다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 생존 증가를 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 전체 생존 중앙값의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 종양 용해 증후군을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 종양 용해 증후군에 대한 예방적 치료를 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 감염을 일으키지 않는다. 일부 구체예들에서, 감염은 폐포자충 감염 또는 헤르페스 바이러스 감염이다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 감염에 대한 예방적 치료를 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 호중구 감소증을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 호중구 감소증에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 호중구 감소증에 대한 예방적 치료는 G-CSF를 인간에게 투여하는 것을 포함한다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴의 투여 후 인간에서 3등급 또는 등급 4 호중구감소증이 발생하는 경우 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴 치료를 중단하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 인간에서 절대 호중구 수치 (ANC)가 >1000/μL로 증가하는 경우, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 호중구 감소증을 치료하기 위해 하나 이상의 성장 인자를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 하나 이상의 성장 인자는 G-CSF를 포함한다. 일부 구체예들에서, 상기 방법은 ANC가 인간에서 21일 사이클의 7일차에 또는 이전에 > 1000/μL로 회복되는 경우, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 용량 감소없이 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함한다. 일부 구체예들에서, 상기 방법은 ANC가 인간에서 21일 사이클의 7일차 이후에 > 1000/μL로 회복되는 경우, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 재개하는 것을 추가로 포함하며, 이때 면역접합체의 용량은 1.4 mg/kg로 감소된다. 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 용량 감소가 이전에 있었던 경우, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 B형 간염 재활성화를 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 B형 간염 재활성화에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 본원에 제공된 방법은 B형 간염 재활성화가 인간에서 검출되는 경우 항바이러스 약물을 인간에게 투여하는 것을 추가로 포함한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈 및 옥살리플라틴의 투여는 약물-유발 간 손상, 진행성 다초점 백질뇌병증, 전신 과민 반응, 아나필락시스 반응, 아나필락시양 반응, 및 2차 악성 종양으로 구성된 그룹에서 선택된 하나 이상의 이상 반응을 일으키지 않는다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 완전 반응율 (CRR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 객관적 반응율 (ORR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 최적의 전체 반응율 (BOR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 반응 기간 (DOR)의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 63% 이상, 적어도 약 65% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 14% 이상, 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무진행 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 42% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 67% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 38% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 3.5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 전체 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무사건 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무사건 생존율의 증가를 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 객관적 반응율을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 35% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 완전 반응율을 초래한다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 10% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 부분 반응율을 초래한다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 다수의 인간에게 투여하면 상응하는 다수의 인간에게 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 부분 반응의 증가를 초래한다.
또 다른 양상에서, 본원은 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위해 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 포함하는 키트를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위해 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 사용하기 위한 폴라투주맙 베도틴-피이크를 포함하는 키트를 제공한다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간 중 33% 이하는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험한다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에게 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않는다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 치료받는 다수의 인간 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, 이때, 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 상기 다수의 인간 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 1.8 mg/kg 용량의 폴라투주맙 베도틴-피이크, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 1.8 mg/kg 용량의 폴라투주맙 베도틴-피이크, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 폴라투주맙 베도틴-피이크, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 폴라투주맙 베도틴-피이크 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 4.8 mg/kg 용량의 일라다투주맙 베도틴, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 3.6 mg/kg 용량의 일라다투주맙 베도틴, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 4.8 mg/kg 용량의 일라다투주맙 베도틴, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 일라다투주맙 베도틴, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 일라다투주맙 베도틴 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 3.6 mg/kg 용량의 일라다투주맙 베도틴, 375 mg/m2 용량의 리툭시맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 일라다투주맙 베도틴, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 일라다투주맙 베도틴 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 1.8 mg/kg 용량의 폴라투주맙 베도틴-피이크, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 1.8 mg/kg 용량의 폴라투주맙 베도틴-피이크, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 폴라투주맙 베도틴-피이크, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 폴라투주맙 베도틴-피이크 및 오비누투주맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 4.8 mg/kg 용량의 일라다투주맙 베도틴, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 3.6 mg/kg 용량의 일라다투주맙 베도틴, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함한다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 4.8 mg/kg 용량의 일라다투주맙 베도틴, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 일라다투주맙 베도틴, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 일라다투주맙 베도틴 및 오비누투주맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 치료를 필요로하는 인간에서 재발성 또는 불응성 미만성 거대 B-세포 림프종 (R/R DLBCL)을 치료하는 방법을 제공하며, 이 방법은 인간에게 3.6 mg/kg 용량의 일라다투주맙 베도틴, 1000 mg 용량의 오비누투주맙, 1000 mg/m2 용량의 젬시타빈, 및 100 mg/m2 용량의 옥살리플라틴을 투여하는 것을 포함하고, 이때 일라다투주맙 베도틴, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 일라다투주맙 베도틴 및 오비누투주맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 리툭시맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 리툭시맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 리툭시맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 오비누투주맙, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 제공하고:
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 오비누투주맙을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 오비누투주맙, 및 옥살리플라틴과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 젬시타빈을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여는, 인간에서 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 일으키지 않으며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
또 다른 양상에서, 본원은 전술한 구체예들 중 어느 하나에 따라 면역접합체, 젬시타빈, 및 오비누투주맙과 병용하여 미만성 거대 B-세포 림프종 (DLBCL)을 치료하는 방법에서 사용하기 위한 옥살리플라틴을 제공하며, 이때 면역접합체는 다음 화학식을 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 다수의 인간에 대한 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴의 투여는, 이러한 다수의 인간들 중 33% 이하가 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상의 말초 신경병증을 경험하게 하며; 그리고 이때 면역접합체, 오비누투주맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 오비누투주맙은 약 1000 mg의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
상세한 설명
본원에서 사용되는 용어 “폴라투주맙 베도틴-피이크”는 IUPHAR/BPS 번호 8404, KEGG 번호 D10761, 또는 CAS 등록 번호 1313206-42-6을 갖는 항-CD79b 면역접합체를 지칭한다. 폴라투주맙 베도틴-피이크는 또한 호환적으로 “폴라투주맙 베도틴”, “huMA79bv28-MC-vc-PAB-MMAE”, “DCDS4501A”, 또는 “RG7596”로도 지칭된다.
본원은 유효량의 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 제제 (예를 들어, 항-CD20 항체, 예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 개체 (예를 들어, 인간)에게 투여하는 것을 포함하는, 만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL)을 치료 또는 이의 진행을 지연시키는 방법을 제공한다.
일부 구체예들에서, 상기 방법은 미만성 거대 B-세포 림프종 (DLBCL), 예를 들어, 재발성/불응성 DLBCL이 있는 개체에게 (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) GYTFSSYWIE (서열 번호: 21)의 아미노산 서열을 포함하는 HVR-H1; (ii) GEILPGGGDTNYNEIFKG(서열 번호: 22)의 아미노산 서열을 포함하는 HVR-H2; (iii) TRRVPIRLDY (서열 번호: 23)의 아미노산 서열을 포함하는 HVR-H3; (iv) KASQSVDYEGDSFLN (서열 번호: 24)의 아미노산 서열을 포함하는 HVR-L1; (v) AASNLES (서열 번호: 25)의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) QQSNEDPLT (서열 번호: 26)의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8 (예를 들어, 2 내지 5, 또는 3 내지 4)이고, (b) 항-CD20 제제 (예를 들어, 리툭시맙), 및 (c) 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여함으로써 이러한 개체를 치료하는 것을 포함한다. 일부 구체예들에서, 면역접합체는 약 1.4 mg/kg 내지 약 1.8 mg/kg의 용량으로 투여되고, 항-CD20 제제 (예를 들어, 리툭시맙)는 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
I. 일반적인 기술
본 발명의 실시는 달리 지시되지 않는 한, 해당 분야의 기술에 속하는 분자 생물학 (재조합 기술 포함), 미생물학, 세포 생물학, 생화학 및 면역학의 통상적인 기술을 사용할 것이다. 이러한 기술들은 문헌들, 예를 들어, “Molecular Cloning: A Laboratory Manual”, second edition (Sambrook 외, 1989); “Oligonucleotide Synthesis” (M. J. Gait, ed., 1984); “Animal Cell Culture” (R. I. Freshney, ed., 1987); “Methods in Enzymology” (Academic Press, Inc.); “Current Protocols in Molecular Biology” (F. M. Ausubel 외, eds., 1987, and periodic updates); “PCR: The Polymerase Chain Reaction”, (Mullis 외, ed., 1994); “A Practical Guide to Molecular Cloning” (Perbal Bernard V., 1988); “Phage Display: A Laboratory Manual” (Barbas 외, 2001)에 상세히 설명되어 있다.
II. 정의
본 발명을 상세히 설명하기 전에, 본 발명은 특정 조성물 또는 생물학적 시스템에 제한되지 않으며, 이는 물론 달라질 수 있는 것으로 이해되어야 한다. 또한, 본 명세서에서 사용된 용어는 특정 구체예를 설명하기 위한 것이며, 제한하고자 하는 것이 아님을 이해해야 한다.
본 명세서 및 첨부된 청구범위에 사용되는 단수형 '하나' 및 '그것'은 내용에서 달리 명백하게 지시하지 않는 한 복수의 지시 대상을 포함한다. 따라서, 예를 들어 “분자”에 대한 지칭은 선택적으로 이러한 분자의 2개 이상의 조합 등을 포함한다.
본원에서 사용되는 용어 “약”은 본 발명의 기술 분야의 숙련된 기술자에게 널리 공지된 바와 같이, 각각의 값에 대한 통상적인 오차 범위를 지칭한다. 본원의 값 또는 매개변수에 대한 “약”의 지칭은 그 값 또는 매개변수 그 자체(per se)에 관한 구체예들을 포함 (및 설명)한다.
본원에 기재된 본 발명의 양태 및 구체예는 “포함하는(comprising)”, “구성되는(consisting) 및 “~로 본질적으로 구성되는”의 양상 및 구체예를 포함하는 것으로 이해된다.
본원에서 사용되는 용어 “CD79b”는 달리 명시되지 않는 한 영장류 (예를 들어, 인간, 사이노몰구스 원숭이(“cyno”)) 및 설치류 (예를 들어, 마우스 및 래트)와 같은 포유동물을 비롯한 임의의 척추동물 출처로부터 얻은 임의의 천연 CD79b를 지칭한다. 인간 CD79b는 또한 본원에서 “Igβ”, “B29”, “DNA225786” 또는 “PRO36249”로 지칭된다. 신호 서열을 포함하는 예시적인 CD79b 서열은 서열 번호: 1에 제시된다. 신호 서열이 없는 예시적인 CD79b 서열은 서열 번호: 2에 제시된다. 용어 “CD79b”는 “전장 (full-length)의” 가공되지 않은 CD79b 뿐만 아니라 세포에서의 가공으로 인해 발생되는 CD79b의 모든 형태를 포함한다. 이 용어는 또한 CD79b의 자연 발생 변이체, 예를 들어 스플라이스 변이체, 대립유전자 변이체 및 이소형을 포함한다. 본원에 기재된 CD79b 폴리펩티드는 다양한 출처, 예를 들어, 인간 조직 유형 또는 다른 출처로부터 단리되거나 재조합 또는 합성 방법에 의해 제조될 수 있다. “천연 서열 CD79b 폴리펩티드”는 자연 유래의 상응하는 CD79b 폴리펩티드와 동일한 아미노산 서열을 갖는 폴리펩티드를 포함한다. 이러한 천연 서열 CD79b 폴리펩티드는 자연으로부터 단리될 수 있거나 재조합 또는 합성 수단에 의해 생산될 수 있다. 용어 “천연 서열 CD79b 폴리펩티드”는 구체적으로 특정 CD79b 폴리펩티드의 자연 발생 절두 또는 분비된 형태 (예를 들어, 세포외 도메인 서열), 상기 폴리펩티드의 자연 발생 변이체 형태 (예를 들어, 선택적으로 스플라이싱된 형태) 및 자연 발생 대립유전자 변이체를 포함한다.
본원에서 사용되는 “CD20”은 인간 B-림프구 항원 CD20 (CD20, B-림프구 표면 항원 B1, Leu-16, Bp35, BM5 및 LF5로도 공지됨; 서열은 SwissProt 데이터베이스 항목 P11836에 특성화되어 있음)을 지칭하며, pre-B 및 성숙한 B 림프구에 위치한 약 35kD의 분자량을 갖는 소수성 막횡단 단백질이다. (Valentine, M.A., 외, J. Biol. Chem. 264(19) (1989 11282-11287; Tedder, T.F., 외, Proc. Natl. Acad. Sci. U.S.A. 85 (1988) 208-12; Stamenkovic, I., 외, J. Exp. Med. 167 (1988) 1975-80; Einfeld, D.A. 외, EMBO J. 7 (1988) 711-7; Tedder, T.F., 외, J. Immunol. 142 (1989) 2560-8). 이에 상응하는 인간 유전자는 막-스패닝 4-도메인, 서브패밀리 A, 구성원 1 (Membrane-spanning 4-domains, subfamily A, member 1)로서, MS4A1로도 공지되어 있다. 이 유전자는 막-스패닝 4A 유전자 패밀리의 구성원을 인코딩한다. 이 초기 단백질 패밀리의 구성원은 공통적인 구조적 특성 및 유사한 인트론/엑손 스플라이스 경계를 특징으로 하며 조혈 세포 및 비림프 조직들 사이에서 독특한 발현 패턴을 나타낸다. 이 유전자는 B 세포의 형질 세포로의 발달 및 분화에 일정한 역할을 하는 B 림프구 표면 분자를 인코딩한다. 이 패밀리 구성원은 패밀리 구성원들의 클러스터에서 11q12에 국재화되어 있다. 이 유전자의 선택적 스플라이싱은 동일한 단백질을 인코딩하는 두 개의 전사체 변이체를 생성한다.
용어 “CD20” 및 “CD20 항원”은 본원에서 호환적으로 사용되며, 세포에 의해 자연적으로 발현되거나 CD20 유전자로 형질감염된 세포 상에서 발현되는 인간 CD20의 임의의 변이체, 이소형 및 종 상동체를 포함한다. CD20 항원에 대한 본 발명의 항체의 결합은 CD20을 비활성화함으로써 CD20을 발현하는 세포 (예를 들어, 종양 세포)의 사멸을 매개한다. CD20을 발현하는 세포의 사멸은 다음 메커니즘 중 하나 이상에 의해 발생할 수 있다: 세포 사멸/아폽토시스 유도, ADCC 및 CDC. 해당 분야에 알려진 바와 같이 CD20의 동의어는 B-림프구 항원 CD20, B-림프구 표면 항원 B1, Leu-16, Bp35, BM5 및 LF5를 포함한다.
용어 “CD20 항원의 발현”은 세포, 예를 들어 T- 또는 B-세포에서 CD20 항원의 유의한 수준의 발현을 나타내고자 하는 것이다. 한 구체예에서, 본 발명의 방법에 따라 치료받는 환자는 B-세포 종양 또는 암에 대해 유의한 수준의 CD20을 발현한다. “CD20 발현 암”을 갖는 환자는 해당 분야에 공지된 표준 분석법에 의해 결정될 수 있다. 예를 들어, CD20 항원 발현은 면역조직화학 (IHC) 검출, FACS를 사용하여 또는 상응하는 mRNA의 PCR 기반 검출을 통해 측정된다.
“친화도”는 분자 (예를 들어, 항체)의 단일 결합 부위와 이의 결합 짝 (예를 들어, 항원) 사이의 비공유 상호작용의 총합 강도를 지칭한다. 다른 언급이 없는 한, 본원에서 사용되는 “결합 친화도”란 결합 쌍의 구성요소들간 (예컨대, 항체와 항원)의 1:1 상호작용을 반영한 고유한 결합 친화도를 지칭한다. 분자 X의 그 짝 Y에 대한 친화도는 일반적으로 해리 상수 (Kd)로 나타낼 수 있다. 친화도는 본원에 기재된 것을 포함하여 해당 분야에 공지된 일반적인 방법에 의해 측정 될 수 있다. 결합 친화도를 측정하기 위한 구체적인 설명적 및 예시적 구체예는 아래에 기재되어 있다.
“친화도 성숙된” 항체는 하나 이상의 초가변 영역(HVR)에 하나 이상의 변경을 보유하지 않는 모 항체와 비교하여 이러한 변경이 있는 항체를 지칭하며, 이러한 변경은 항원에 대한 항체의 친화도를 개선한다.
본원에서 용어 “항체”는 가장 넓은 의미로 사용되며 원하는 항원 결합 활성을 나타내는 한 모노클로날 항체, 폴리클로날 항체, 다중특이성 항체 (예를 들어, 이중특이성 항체) 및 항체 단편을 포함하는 (그러나 이에 제한되지 않음) 다양한 항체 구조를 포함한다.
“항체 단편”은 무손상 항체가 결합하는 항원에 결합하는 무손상 항체의 일부를 포함하는 무손상 항체 이외의 분자를 지칭한다. 항체 단편의 예는 Fv, Fab, Fab', Fab'-SH, F(ab')2; 디아바디; 선형 항체; 단일쇄 항체 분자 (예를 들어, scFv); 및 항체 단편들로부터 형성된 다중특이적 항체를 포함하나 이에 제한되는 것은 아니다.
참조 항체와 “동일한 에피토프에 결합하는 항체”는 경쟁 분석에서 참조 항체의 그 항원에 대한 결합을 50% 이상 차단하는 항체를 지칭하며, 반대로, 참조 항체는 경쟁 분석에서 이러한 항체의 그 항원에 대한 결합을 50% 이상 차단한다. 예시적인 경쟁 분석이 본원에 제공된다.
용어 “에피토프”는 항체가 결합하는 항원 분자 상의 특정 부위를 지칭한다.
용어 “키메라” 항체는 중쇄 및/또는 경쇄의 일부가 특정 출처 또는 종들로부터 유래되는 반면, 중쇄 및/또는 경쇄의 나머지는 상이한 출처 또는 종들로부터 유래되는 항체를 지칭한다.
항체의 “클래스(class)”란 항체의 중쇄가 보유하는 불변 도메인 또는 불변 영역의 유형을 지칭한다. 항체에는 5가지 주요 클래스가 있다: IgA, IgD, IgE, IgG, 및 IgM, 그리고 이들중 몇몇은 서브클래스(이소형), 예컨대, IgG1, IgG2, IgG3, IgG4, IgA1, 및 IgA2로 더욱 세분될 수 있다. 상이한 클래스의 면역글로불린에 해당하는 중쇄 불변 도메인들은 각각 α, δ, ε, γ, 및 μ로 불린다.
용어 “항-CD79b 항체” 또는 “CD79b에 결합하는 항체”는 항체가 CD79b를 표적함에 있어서 진단제 및/또는 치료제로서 유용하도록 충분한 친화도로 CD79b에 결합할 수 있는 항체를 지칭한다. 바람직하게는, 관련되지 않은 비-CD79b 단백질에 대한 항-CD79b 항체의 결합 정도는, 예를 들어, 방사성면역분석법(RIA)으로 측정시 CD79b에 대한 항체의 결합의 약 10% 미만이다. 특정 구체예들에서, CD79b에 결합하는 항체는 ≤ 1 μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, 또는 ≤ 0.1 nM의 해리 상수 (Kd)를 가진다. 특정 구체예들에서, 항-CD79b 항체는 상이한 종들의 CD79b 사이에 보존되는 CD79b의 에피토프에 결합한다.
본 발명에 따른 용어 “항-CD20 항체”는 항체가 CD20을 표적함에 있어서 진단제 및/또는 치료제로서 유용하도록 충분한 친화도로 CD20에 결합할 수 있는 항체를 지칭한다. 바람직하게는, 관련되지 않은 비-CD20 단백질에 대한 항-CD20 항체의 결합 정도는, 예를 들어, 방사성면역분석법(RIA)으로 측정시 CD20에 대한 항체의 결합의 약 10% 미만이다. 특정 구체예들에서, CD20에 결합하는 항체는 ≤ 1 μM, ≤ 100 nM, ≤ 10 nM, ≤ 1 nM, 또는 ≤ 0.1 nM의 해리 상수 (Kd)를 가진다. 특정 구체예들에서, 항-CD20 항체는 상이한 종들의 CD20 사이에 보존되는 CD20의 에피토프에 결합한다.
“단리된” 항체는 자연 환경의 구성요소에서 분리된 항체이다. 일부 구체예들에서, 항체는 예를 들어 전기영동 (예를 들어, SDS-PAGE, 등전점 (IEF), 모세관 전기영동) 또는 크로마토그래피 (예를 들어, 이온 교환 또는 역상 HPLC)로 결정하였을 때 95% 또는 99% 초과의 순도로 정제된다. 항체 순도 평가 방법의 검토는, 예를 들어, Flatman 외, J. Chromatogr. B 848:79-87 (2007)를 참고하라. 항체의 “가변 영역” 또는 “가변 도메인”은 항체의 중쇄 또는 경쇄의 아미노-말단 도메인을 지칭한다. 중쇄의 가변 도메인은 “VH”로 지칭될 수 있다. 경쇄의 가변 도메인은 “VL”로 지칭될 수 있다. 이러한 도메인은 일반적으로 항체의 가장 가변적인 부분이며 항원 결합 부위를 포함한다.
“항-CD79b 항체를 인코딩하는 단리된 핵산”은, 단일 벡터 또는 별도의 벡터에 있는 이러한 핵산 분자를 포함하는, 항체 중쇄 및 경쇄 (또는 이의 단편)를 인코딩하는 하나 이상의 핵산 분자, 및 숙주 세포의 하나 이상의 위치에 존재하는 이러한 핵산 분자(들)을 지칭한다.
용어 “모노클로날 항체(monoclonal antibody)”는 본원에서 이용된 바와 같이 실질적으로 동질 항체의 모집단으로부터 수득한 항체, 예를 들어, 이러한 모집단을 포함하는 개별 항체는 동일하거나 및/또는 동일한 에피토프에 결합하지만, 예로써, 자연 발생적 돌연변이를 포함하는 또는 모노클로날 항체 제재를 제조하는 동안 발생되는 가능한 변이체 항체의 경우는 제외되며, 이러한 변이체들은 일반적으로 소량 존재한다. 상이한 결정요소 (에피토프)에 대항하는 상이한 항체를 일반적으로 함유하는 폴리클로날 항체 제재들과 대조적으로, 모노클로날 항체 제재들의 각 모노클로날 항체는 항원에 있는 단일 결정요소에 대해 지시된다. 따라서, 수식어 “모노클로날(monoclonal)”은 실질적으로 동질성 항체 모집단으로부터 수득되는 항체의 특성을 나타내며, 임의의 특정 방법에 의한 항체 제조를 필요로 하는 것으로 해석되어서는 안된다. 예를 들면, 본 발명에 따라 사용되는 모노클로날 항체는 하이브리도마 방법, 재조합 DNA 방법, 파지-디스플레이 방법 그리고 인간 면역 글로불린 좌위의 전부 또는 일부를 포함하는 유전자삽입 동물을 이용하는 방법들을 비롯한 (그러나 이에 제한되지 않음) 다양한 기술에 의해 제조 될 수 있으며, 이러한 방법 및 모노클로날 항체를 제조하는 다른 예시적인 방법이 본원에 기재되어 있다.
“네이키드(naked) 항체”는 이질성 모이어티 (예로써, 세포독성 모이어티) 또는 방사능라벨에 접합되지 않은 항체를 말한다. 상기 네이키드 항체는 약학 제제에 존재할 수 있다.
“고유 항체”는 변하는 구조를 갖는 자연 발생 면역글로불린 분자를 지칭한다. 예를 들면, 고유 IgG 항체는 이종사량체 당단백질로써, 약 150,000 달톤이며, 2개의 동일한 경쇄와 2개의 동일한 중쇄를 포함하며, 이들은 이황화 결합에 의해 연결되어 있다. 도메인 N-말단으로부터 C-말단으로, 각각의 중쇄는 가변 중쇄 도메인 또는 중쇄 가변 도메인이라고도 불리는 가변 영역 (VH), 이어서 3개의 불변 도메인(CH1, CH2, 및 CH3)을 갖는다. 유사하게, N-말단으로부터 C-말단으로, 각각의 경쇄는 가변 경쇄 도메인 또는 경쇄 가변 도메인이라고도 불리는 가변 영역 (VL), 이어서 불변 경쇄 (CL) 도메인을 갖는다. 항체의 경쇄는 불변 도메인의 아미노산 서열에 따라 카파 (κ) 및 람다 (λ)라고 하는 두 가지 유형 중 하나로 지정될 수 있다.
본원에서 용어 “Fc 영역”은 불변 영역의 적어도 일부를 함유하는 면역글로불린 중쇄의 C-말단 영역을 정의하는데 사용된다. 상기 용어는 천연 서열 Fc 영역 및 변이체 Fc 영역을 포함한다. 한 구체예에서, 인간 IgG 중쇄 Fc 영역은 Cys226, 또는 Pro230에서 중쇄의 카르복실-말단까지 연장된다. 그러나, Fc 영역의 C-말단 리신(Lys447)은 존재하거나 존재하지 않을 수 있다. 명시적으로 다른 언급이 없는 한, Fc 영역 또는 불변 영역에서 아미노산 잔기의 넘버링은 EU 넘버링 체계, Kabat 외, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991에서 설명된 소위 EU 색인에 따른다.
“프레임워크” 또는 “FR”은 초가변 영역 (HVR) 잔기들 이외의 가변 도메인 잔기를 지칭한다. 가변 도메인의 FR은 일반적으로 4개의 FR 도메인들로 구성된다: FR1, FR2, FR3, 및 FR4. 따라서, HVR 및 FR 서열들은 일반적으로 VH (또는 VL)에서 다음의 순서로 나타난다: FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
본원의 목적과 관련하여 “수용체 인간 프레임워크”는 하기 정의된 바와 같이, 인간 면역글로불린 프레임워크 또는 인간 공통 프레임워크로부터 유래된 경쇄 가변 도메인(VL) 프레임워크 또는 중쇄 가변 도메인(VH) 프레임워크의 아미노산 서열을 포함하는 프레임워크이다. 인간 면역글로불린 프레임워크 또는 인간 공통 프레임워크로부터 “유래된” 수용체 인간 프레임워크는 이의 동일한 아미노산 서열을 포함할 수 있거나, 아미노산 서열 변화를 함유할 수 있다. 일부 구체예들에서, 아미노산 변화의 수는 10개 이하, 9개 이하, 8개 이하, 7개 이하, 6개 이하, 5개 이하, 4개 이하, 3개 이하 또는 2개 이하이다. 일부 구체예들에서, VL 수용체 인간 프레임워크는 VL 인간 면역글로불린 프레임워크 서열 또는 인간 공통 프레임워크 서열과 서열이 동일하다.
용어 “전장 항체”, “무손상 항체” 및 “전 항체 (whole antibody)”는 천연 항체 구조와 실질적으로 유사한 구조를 갖거나 본원에 정의된 바와 같은 Fc 영역을 함유하는 중쇄를 갖는 항체를 지칭하기 위해 본원에서 호환적으로 사용된다.
“숙주 세포”, “숙주 세포주” 및 “숙주 세포 배양물”이라는 용어는 상호교환적으로 사용되며 외인성 핵산이 도입된 세포를 지칭하며, 이러한 세포의 자손을 포함한다. 숙주 세포는 “형질전환체” 및 “형질전환된 세포”를 포함하며, 이는 계대 수에 관계없이 1차 형질전환된 세포 및 이로부터 유래된 자손을 포함한다. 자손은 핵산 함량이 모 세포와 완전히 동일하지 않을 수 있지만 돌연변이를 포함할 수 있다. 최초로 형질전환된 세포에서 스크리닝되거나 선별된 것과 동일한 기능 또는 생물학적 활성을 갖는 돌연변이 자손이 본원에 포함된다.
“인간 항체”는 인간 또는 인간 세포에 의해 생성되거나 인간 항체 레퍼토리 또는 다른 인간 항체-인코딩 서열을 이용하는 비-인간 출처로부터 유래된 항체의 아미노산 서열에 상응하는 아미노산 서열을 갖는 항체이다. 이러한 인간 항체의 정의는 비인간 항원 결합 잔기를 포함하는 인간화 항체를 명확하게 배제한다.
"인간 공통 프레임워크"는 인간 면역글로불린 VL 또는 VH 프레임워크 서열의 선별에 있어서 가장 일반적으로 발생하는 아미노산 잔기를 나타내는 프레임워크이다. 일반적으로, 인간 면역글로불린 VL 또는 VH 서열은 가변 도메인 서열의 하위그룹으로부터 선택된다. 일반적으로, 서열들의 하위그룹들은 Kabat 외, Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols. 1-3에서와 같은 하위그룹이다. 한 구체예에서, VL의 경우, 하위그룹은 상기 Kabat 외의 문헌에서와 같은 하위그룹 카파 I이다. 한 구체예에서, VH의 경우, 하위그룹은 상기 Kabat 외의 문헌에서와 같은 하위그룹 III이다.
“인간화” 항체는 비인간 HVR로부터의 아미노산 잔기 및 인간 FR로부터의 아미노산 잔기를 포함하는 키메라 항체를 지칭한다. 특정 구체예들에서, 인간화 항체는 적어도 하나, 및 전형적으로 2개의 가변 도메인을 실질적으로 모두 포함할 것이고, 여기서 모든 또는 실질적으로 모든 HVR(예를 들어, CDR)은 비-인간 항체의 것에 상응하고, 그리고 모든 또는 실질적으로 모든 FR은 인간 항체의 것에 상응한다. 인간화 항체는 선택적으로 인간 항체로부터 유래된 항체 불변 영역의 적어도 일부를 포함할 수 있다. 항체의 “인간화 형태”, 예를 들어, 비-인간 항체는 인간화를 거친 항체를 지칭한다.
본원에서 사용되는 용어 “초가변 영역” 또는 “HVR”은 서열이 초가변이고 및/또는 구조적으로 정의된 루프 (“초가변 루프”)를 형성하는 항체 가변 도메인의 영역들 각각을 지칭한다. 일반적으로 천연 4쇄 항체는 6개의 HVR을 포함한다: VH에 3개 (H1, H2, H3), 그리고 VL에 3개 (L1, L2, L3). HVR은 일반적으로 초가변 루프 및/또는 “상보성 결정 영역” (CDR)의 아미노산 잔기를 포함하며, 후자는 가장 높은 서열 가변성을 가지며 및/또는 항원 인식에 관여한다. 아미노산 잔기 26-32 (L1), 50-52 (L2), 91-96 (L3), 26-32 (H1), 53-55 (H2), 및 96-101 (H3)에서 나타나는 예시적인 초가변 루프 (Chothia 및 Lesk, J. Mol. Biol. 196:901-917 (1987)); 예시적인 CDR들 (CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2, 및 CDR-H3)은 L1의 아미노산 잔기 24-34, L2의 50-56, L3의 89-97, H1의 31-35B, H2의 50-65, 및 H3의 95-102에서 나타난다. (Kabat 외, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991).) VH의 CDR1을 제외하고, CDR은 일반적으로 초가변 루프를 형성하는 아미노산 잔기를 포함한다. CDR은 또한 항원과 접촉하는 잔기인 “특이성 결정 잔기” 또는 “SDR”을 포함한다. SDR은, 축약된-CDR 또는 a-CDR이라 불리는 CDR들의 영역 내에 포함된다. 예시적인 a-CDR들 (a-CDR-L1, a-CDR-L2, a-CDR-L3, a-CDR-H1, a-CDR-H2, 및 a-CDR-H3)은 L1의 아미노산 잔기 31-34, L2의 50-55, L3의 89-96, H1의 31-35B, H2의 50-58, 및 H3의 95-102에서 발생한다. (Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008) 참조.) 달리 명시되지 않는 한, 가변 도메인의 HVR 잔기 및 기타 잔기 (예를 들어, FR 잔기)는 상기 Kabat 외,에 따라 넘버링된다.
“가변 영역” 또는 “가변 도메인”은 항체가 항원에 결합하는데 관여하는 항체 중쇄 또는 경쇄 도메인을 지칭한다. 고유 항체의 중쇄와 경쇄 (차례로 VH 및 VL)의 가변 도메인은 일반적으로 유사한 구조를 가지며, 각 도메인은 4개의 보존된 프레임워크 영역 (FRs)과 3개의 초가변 영역 (HVR들)을 포함한다. (예를 들어, Kindt 외, Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007).참조) 단일 VH 또는 VL 도메인은 항원-결합 특이성을 부여하기에 충분할 수 있다. 더욱이, 특정 항원에 결합하는 항체는 상보성 VH 또는 VL 도메인의 라이브러리를 스크린하기 위하여 항원에 결합하는 항체의 VH 또는 VL 도메인을 이용하여 분리될 수 있다. 예를 들어, Portolano 외, J. Immunol. 150:880-887 (1993); Clarkson 외, Nature 352:624-628 (1991) 참조.
“이펙터 기능”은 항체의 Fc 영역에 기인하는 생물학적 활성을 지칭하며, 이는 항체 이소형에 따라 달라진다. 항체 이펙터 기능들의 예에는 다음이 포함된다: C1q 결합 및 보체 의존성 세포독성 (CDC); Fc 수용체 결합; 항체 의존성 세포-매개 세포독성(ADCC); 식균 작용; 세포 표면 수용체 (예를 들어, B-세포 수용체)의 하향조절; 및 B-세포 활성화.
“CD79b 폴리펩티드 변이체”는 본원에 개시된 전장 천연 서열 CD79b 폴리펩티드 서열, 본원에 개시된 신호 펩티드가 없는 CD79b 폴리펩티드 서열, 본원에 개시된 신호 펩티드가 있거나 없는 CD79b 폴리펩티드의 세포외 도메인, 또는 본원에 개시된 전장 CD79b 폴리펩티드 서열의 임의의 기타 단편 (예를 들어, 전장 CD79b 폴리펩티드에 대한 완전 코딩 서열의 일 부분만을 나타내는 핵산에 의해 인코딩되는 단편들)에 적어도 약 80% 아미노산 서열 동일성을 가지는 본원에 정의된 CD79b 폴리펩티드, 바람직하게는 활성 CD79b 폴리펩티드를 의미한다. 이러한 CD79b 폴리펩티드 변이체는 예를 들어, 전장 천연 아미노산 서열의 N- 또는 C-말단에서 하나 이상의 아미노산 잔기가 추가되거나 결실된 CD79b 폴리펩티드를 포함한다. 보통, CD79b 폴리펩티드 변이체는 본원에 개시된 전장 천연 서열 CD79b 폴리펩티드 서열, 본원에 개시된 신호 펩티드가 없는 CD79b 폴리펩티드 서열, 본원에 개시된 신호 펩티드가 있거나 없는 CD79b 폴리펩티드의 세포외 도메인, 또는 본원에 개시된 전장 CD79b 폴리펩티드 서열의 임의의 다른 구체적으로 정의된 단편에 적어도 약 80% 아미노산 서열 동일성, 대안적으로 적어도 약 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 또는 99% 아미노산 서열 동일성을 가질 것이다. 보통, CD79b 변이체 폴리펩티드는 적어도 약 10 아미노산 길이, 대안적으로, 적어도 약 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250, 260, 270, 280, 290, 300, 310, 320, 330, 340, 350, 360, 370, 380, 390, 400, 410, 420, 430, 440, 450, 460, 470, 480, 490, 500, 510, 520, 530, 540, 550, 560, 570, 580, 590, 600 또는 그 이상의 아미노산 길이이다. 선택적으로, CD79b 변이체 폴리펩티드는 천연 CD79b 폴리펩티드 서열과 비교하여 1개 이하의 보존적 아미노산 치환, 대안적으로 천연 CD79b 폴리펩티드 서열과 비교하여 2, 3, 4, 5, 6, 7, 8, 9 또는 10개 이하의 보존적 아미노산 치환을 가질 것이다.
참조 폴리펩티드 서열에 대한 “아미노산 서열 동일성 퍼센트 (%)”는, 서열들을 정렬하고 필요에 따라 최대 퍼센트 서열 동일성을 달성하기 위해 갭을 도입한 후 참조 폴리펩티드 서열의 아미노산 잔기들과 동일한, 후보 서열의 아미노산 잔기들의 백분율로 정의되며, 보존적 치환은 서열 동일성의 일부로 고려하지 않는다. 아미노산 서열 동일성 퍼센트를 결정하기 위한 정렬은 해당 분야의 기술 범위에 속하는 다양한 방식으로, 예를 들어, BLAST, BLAST-2, ALIGN 또는 Megalign(DNASTAR) 소프트웨어와 같은 공개적으로 이용가능한 컴퓨터 소프트웨어를 사용하여 이루어질 수 있다. 당업자는 비교되는 서열들의 전체 길이에 걸쳐 최대 정렬을 구현하는 데 필요한 임의의 알고리즘을 포함하여 서열들을 정렬하기 위한 적절한 매개변수를 결정할 수 있다. 그러나, 본원의 목적을 위해, 아미노산 서열 동일성 % 값은 서열 비교 컴퓨터 프로그램 ALIGN-2를 사용하여 생성된다. ALIGN-2 서열 비교 컴퓨터 프로그램은 Genentech, Inc.에서 제작되었으며 소스 코드는 미국 워싱턴 D.C., 20559에 소재한 미국 저작권청에 사용자 문서와 함께 제출되었으며, 미국 저작권 등록 번호 TXU510087로 등록되었다. ALIGN-2 프로그램은 캘리포니아주 사우스 샌프란시스코에 소재한 Genentech, Inc.사로부터 공개적으로 이용가능하거나 소스 코드로부터 컴파일될 수 있다. ALIGN-2 프로그램은 디지털 UNIX V4.0D를 포함한 UNIX 운영 체제에서 사용되도록 컴파일해야 한다. 모든 서열 비교 매개변수는 ALIGN-2 프로그램에 의해 설정되며 변경되지 않는다.
ALIGN-2가 아미노산 서열 비교에 사용되는 경우, 주어진 아미노산 서열 B에, 이와 관련한, 또는 이에 대한 주어진 아미노산 서열 A의 아미노산 서열 동일성 %는 (다른 방식으로, 주어진 아미노산 서열 B에, 이와 관련한, 또는 이에 대한 특정 아미노산 서열 동일성 %를 가지는 또는 포함하는 주어진 아미노산 서열 A로 표현될 수 있음) 다음과 같이 계산된다:
100 x 분율 X/Y
이때 X는 A와 B의 프로그램 정렬에서 서열 정렬 프로그램 ALIGN-2에 의해 동일한 매치로 기록되는 아미노산 잔기의 수를 말하며, Y는 B의 전체 아미노산 잔기 수가 된다. 아미노산 서열 A의 길이는 아미노산 서열 B의 길이와 동일하지 않는 경우, B에 대한 A의 아미노산 서열 동일성 %는 A에 대한 B의 아미노산 서열 동일성 %와 동일하지 않은 것으로 인정된다. 달리 특정 언급이 없는 한, 본원에서 이용된 모든 아미노산 서열 동일성 % 값은 ALIGN-2 컴퓨터 프로그램을 이용하여 바로 전 단락에서 설명된 바와 같이 수득된다.
본원에 사용된 용어 “벡터”는 이것이 연결되는 다른 핵산을 증식시킬 수 있는 핵산 분자를 지칭한다. 이 용어에는 자가-복제 핵산 구조체로서의 벡터 그리고 그것이 도입되는 숙주 세포의 게놈에 통합된 벡터가 포함된다. 특정 벡터는 작동가능하게 연결된 핵산의 발현을 지시할 수 있다. 이러한 벡터는 본원에서 “발현 벡터”로 지칭된다.
“면역접합체”는, 비제한적으로 세포독성제를 포함한, 하나 이상의 이종성 분자(들)에 접합된 항체이다.
본원에 제공된 화학식들과 관련하여, “p”는 항체 당 약물 모이어티의 평균 수를 나타내며, 이는 예를 들어, 항체 당 약 1 내지 약 20개의 약물 모이어티, 특정 구체예에서는 항체당 1 내지 약 8개의 약물 모이어티 범위일 수 있다. 본 발명은, 항체당 평균 약물 로딩이 약 2 내지 약 5, 또는 약 3 내지 약 4 (예를 들어, 약 3.5)인 화학식 I의 항체-약물 화합물의 혼합물을 포함하는 조성물을 포함한다.
본원에 사용된 용어 “세포독성제”는 세포 기능을 억제 또는 방지하고/하거나 세포 사멸 또는 파괴를 유발하는 물질을 지칭한다. 세포독성제는 방사성 동위원소(예를 들어, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 및 Lu의 방사성 동위원소); 화학요법제 또는 약물(예를 들어, 메토트렉세이트, 아드리아마이신, 빈카 알칼로이드(빈크리스틴, 빈블라스틴, 에토포사이드), 독소루비신, 멜팔란, 미토마이신 C, 클로람부실, 다우노루비신 또는 기타 삽입 물질); 성장 억제제; 효소, 예를 들어, 핵산분해효소 및 이의 단편; 항생제; 독소, 예를 들어, 박테리아, 진균, 식물 또는 동물 기원의 효소적으로 활성인 독소 또는 소분자 독소, 이의 단편 및/또는 변이체 포함; 그리고 아래에 개시되는 다양한 항종양제 또는 항암제를 포함하나, 이에 제한되는 것은 아니다.
“암” 및 “암성”이라는 용어는 전형적으로 조절되지 않은 세포 성장을 특징으로 하는 포유동물의 생리학적 병태를 지칭하거나 설명한다. 암의 예는 B 세포 림프종 (낮은 등급/소포 비호지킨 림프종(NHL), 소 림프구성(SL) NHL, 중간 등급/소포 NHL, 중간 등급 미만성 NHL, 높은 등급 면역모세포 NHL, 높은 등급 림프모구 NHL, 높은 등급 소형 비절단 세포 NHL, 거대 종양 NHL; 외투 세포 림프종, AIDS 관련 림프종 및 발덴스트롬 마크로글로불린혈증); 만성 림프구성 백혈병(CLL); 급성 림프구성 백혈병(ALL); 털 세포 백혈병; 만성 골수성 백혈병; 및 이식후 림프증식성 장애 (PTLD), 뿐만 아니라 식세포종과 관련된 비정상적인 혈관 증식, 부종 (예를 들어, 뇌종양과 관련된 것) 및 메이그 증후군을 포함하나, 이에 제한되는 것은 아니다. 보다 구체적인 예에는 재발성 또는 불응성 NHL, 일차 (front line) 낮은 등급 NHL, III/IV기 NHL, 화학요법 내성 NHL, 전구체 B 림프구성 백혈병 및/또는 림프종, 소 림프구성 림프종, B 세포 만성 림프구성 백혈병 및/또는 전림프구성 백혈병 및/또는 소 림프구성 림프종, B 세포 전림프구성 림프종, 면역세포종 및/또는 림프형질구성 림프종, 림프형질구성 림프종, 변연부 B 세포 림프종, 비장 변연부 림프종, 림프절외 변연부 - MALT 림프종, 림프절 변연부 림프종, 모세포 백혈병, 형질세포종 및/또는 형질 세포 골수종, 낮은 등급/여포성 림프종, 중간 등급/여포성 NHL, 외투 세포 림프종, 여포 중심 림프종(여포성), 소포 림프종 (예를 들어, 재발성/불응성 소포 림프종) 중간 등급 미만성 NHL, 미만성 거대 B 세포 림프종 (DLBCL), 재발성 DLBCL, 불응성 DLBCL, 재발성/불응성 DLBCL, 공격성 NHL (공격적인 최전선 NHL 및 공격적인 재발성 NHL 포함), 자가 줄기 세포 이식 후 재발성 또는 이러한 이식에 대한 불응성, 원발성 종격동 거대 B 세포 림프종, 원발성 삼출성 림프종, 높은 등급의 면역모세포성 NHL, 높은 등급의 림프모세포성 NHL, 높은 등급의 소형 비절단 세포 NHL, 거대 종양 NHL, 버킷 림프종, 전구체 (말초) 거대 과립 림프구성 백혈병, 균상 식육종 및/또는 세자리 증후군, 표피 (피부) 림프종, 역형성 거대 세포 림프종, 혈관 중심성 림프종이 포함되나 이에 제한되는 것은 아니다.
“개체” 또는 “대상체”는 포유동물이다. 포유동물에는 가축 (예를 들어, 소, 양, 고양이, 개 및 말), 영장류 (예를 들어, 인간 및 비인간 영장류, 예를 들어, 원숭이), 토끼 및 설치류 (예를 들어, 마우스 및 랫트)가 포함되나 이에 제한되는 것은 아니다. 특정 구체예들에서, 개체 또는 대상체는 인간이다.
제제, 예를 들어, 약학 제제의 “유효량”은 원하는 치료 또는 예방 결과를 달성하기 위해 필요한 투여량으로 그리고 기간 동안 효과적인 양을 지칭한다.
용어 “약학 제제 (pharmaceutical formulation)”란 이 조성물 안에 포함된 활성 성분의 생물학적 활성이 효과가 있도록 하기 위한 형태의 제재를 지칭하며, 이러한 제제가 투여되는 대상체에게 수용불가능한 독성을 주는 추가 성분들은 포함하지 않는다.
약학적으로 허용되는 담체는 활성 성분 이외에 약학 제제 안에 있는 성분을 말하며, 대상체에게 비독성이다. 약학적으로 허용되는 담체는 완충액, 부형제, 안정화제, 또는 보존제다.
본원에서 사용되는 “치료” (및 “치료하다” 또는 “치료하는”과 같은 이의 문법적 변형)는 치료를 받는 개체의 자연적 과정을 변경하려는 시도에 있어서의 임상적 개입을 의미하며, 예방을 위해 또는 임상 병리학 과정 중에 수행될 수 있다. 치료의 바람직한 효과에는 유리 경쇄의 감소, 질환의 발생 또는 재발 방지, 증상의 완화, 질환의 직간접적인 병리학적 결과의 감소, 질환 진행 속도 감소, 질환 상태의 개선 또는 완화, 및 관해 또는 개선된 예후가 포함되나 이에 제한되는 것은 아니다. 일부 구체예들에서, 본원에 기재된 항체는 질환의 발병을 지연시키거나 질환의 진행을 늦추는 데 사용된다.
용어 “CD79b-양성 암”은 표면에 CD79b를 발현하는 세포를 포함하는 암을 지칭한다. 일부 구체예들에서, 세포 표면에서 CD79b의 발현은 예를 들어 면역조직화학, FACS 등과 같은 방법에서 CD79b에 대한 항체를 사용하여 결정된다. 대안적으로, CD79b mRNA 발현은 세포 표면 상의 CD79b 발현과 상관관계가 있는 것으로 간주되며, 인시튜 혼성화 및 RT-PCR(정량적 RT-PCR 포함)로부터 선택된 방법에 의해 결정될 수 있다.
본원에서 사용되는 “~와 함께” 또는 “~와 병용하여”는 또 다른 치료 방식에 더하여 하나의 치료 방식을 투여하는 것을 지칭한다. 따라서, “~와 함께” 또는 “~와 병용하여”는 개체에게 하나의 치료 방식을 기타 치료 방식의 투여 전, 동안, 또는 후에 투여하는 것을 지칭한다.
“화학요법제”는 암 치료에 유용한 화합물이다. 화학요법제의 예는 엘로티닙 (TARCEVA®, Genentech/OSI Pharm.), 보르테조밉(VELCADE®, Millennium Pharm.), 디설피람, 에피갈로카테킨 갈레이트, 살리노스포라미드 A, 카르필조밉, 17-AAG(겔다나마이신), 라디시콜, 젖산 탈수소효소 A (LDH-A), 풀베스트란트(FASLODEX®, AstraZeneca), 수니티브(SUTENT®, Pfizer/Sugen), 레트로졸(FEMARA®, Novartis), 이마티닙 메실레이트(GLEEVEC®, Novartis), 피나수네이트(VATALANIB®, Novartis), 옥살리플라틴(ELOXATIN®, Sanofi), 5-FU(5-플루오로우라실), 류코보린, 라파마이신(Sirolimus, RAPAMUNE®, Wyeth), 라파티닙(TYKERB®, GSK572016, Glaxo Smith Kline), 로나파밉 (SCH 66336), 소라페닙 (NEXAVAR®, Bayer Labs), 게피티닙 (IRESSA®, AstraZeneca), AG1478, 알킬화제, 예를 들어, 티오테파 및 CYTOXAN® 사이클로포스파미드; 알킬 술포네이트, 예를 들어, 부술판, 임프로술판 및 피포술판; 아지리딘, 예를 들어, 벤조도파, 카르보쿠온, 메투레도파, 우레도파; 알트레타민, 트리에틸렌멜라민, 트리에틸렌포스포르아미드, 트리에틸렌티오포스포르아미드 및 트리메틸로멜라민을 포함하는 에틸렌이민 및 메틸라멜라민; 아세토게닌 (특히 불라타신 및 불라타시논); 캄토테신 (토포테칸 및 이리노테칸 포함); 브리오스타틴; 칼리스타틴; CC-1065 (아도젤레신, 카르젤레신 및 비젤레신 합성 유사체 포함); 크립토피신 (특히 크립토파이신 1 및 크립토파이신 8); 부신피질호르몬제 (프레드니손 및 프레드니솔론 포함); 사이프로테론 아세테이트; 피나스테리드 및 두타스테리드를 포함하는 5a-환원효소); 보리노스타트, 로미뎁신, 파노비노스타트, 발프로산, 모세티노스타트 돌라스타틴; 알데스류킨, 탈크 듀오카르마이신 (합성 유사체, KW-2189 및 CB1-TM1 포함); 엘류테로빈; 판크라티스타틴; 사르코딕틴; 스폰지스타틴; 질소 머스타드, 예를 들어, 클로람부실, 클로마파진, 클로로포스파미드, 에스트라무스틴, 이포스파미드, 메클로레타민, 메클로레타민 옥사이드 하이드로클로라이드, 멜팔란, 노벤비친, 페네스테린, 프레드니무스틴, 트로포스파미드, 우라실 머스타드; 니트로소우레아, 예를 들어, 카르무스틴, 클로로조토신, 포테무스틴, 로무스틴, 니무스틴 및 라님누스틴; 항생제, 예를 들어, 에네다이인 항생제 (예를 들어, 칼리케아마이신, 특히, 칼리케아마이신 γ 및 칼리케아마이신 ω(Angew Chem. Intl. Ed. Engl. 1994 33:183-186); 다이네미신 A를 포함하는 다이네미신; 클로드로네이트와 같은 비스포스포네이트; 에스페라미신; 뿐만 아니라 네오카르지노스타틴 발색단 및 관련 발색단백 엔디인 항생제 발색단), 아클라시노마이신, 악티노마이신, 아우트라마이신, 아자세린, 블레오마이신, 칵티노마이신, 카라비신, 카미노마이신, 카르지노필린, 크로모마이신, 닥티노마이신, 다우노루비신, 데토루비신, 6-디아조-5-옥소-L-노르류신, ADRIAMYCIN® (독소루비신), 모르폴리노-독소루비신, 시아노모르폴리노-독소루비신, 2-피롤리노-독소루비신 및 데옥시독소루비신), 에피루비신, 에소루비신, 에베롤리무스, 소트라타우린, 이다루비신, 마르셀로마이신, 미토마이신, 예를 들어, 미토마이신 C, 마이코페놀산, 노갈라마이신, 올리보마이신, 페플로마이신, 포르피로마이신, 퓨로마이신, 켈라마이신, 로도루비신, 스트렙토니그린, 스트렙토조신, 투베르시딘, 우베니멕스, 지노스타틴, 조루비신; 메토트렉세이트 및 5-플루오로우라실(5-FU)과 같은 항대사물질; 데놉테린, 메토트렉세이트, 프테롭테린, 트리메트렉세이트와 같은 엽산 유사체; 플루다라빈, 6-메르캅토퓨린, 티아미프린, 티오구아닌과 같은 퓨린 유사체; 안시타빈, 아자시티딘, 6-아자우리딘, 카르모푸르, 시타라빈, 디데옥시우리딘, 독시플루리딘, 에노시타빈, 플록수리딘과 같은 피리미딘 유사체; 칼루스테론, 드로모스타놀론 프로피오네이트, 에피티오스타놀, 메피티오스탄, 테스토락톤과 같은 안드로겐; 아미노글루테티미드, 미토탄, 트리로스탄과 같은 항부신; 프롤린산과 같은 엽산 보충제; 아세글라톤; 알도포스파미드 글리코시드; 아미노레불린산; 에닐루라실; 암사크린; 베스트라부실; 비산트렌; 에다트락세이트; 데포파민; 데메콜신; 디아지쿠온; 엘포미틴; 엘립티늄 아세테이트; 에포틸론; 에토글루시드; 갈륨 니트레이트; 하이드록시우레아; 렌티난; 로니다이닌; 메이탄신 및 안사미토신과 같은 메이탄시노이드; 미토구아존; 미톡산트론; 모피담놀; 니트라에린; 펜토스타틴; 페나멧; 피라루비신; 로속산트론; 포도필린산; 2-에틸하이드라지드; 프로카바진; PSK® 다당류 복합체 (JHS Natural Products, Eugene, Oreg.); 라족산; 리족신; 시조푸란; 스피로게르마늄; 테누아존산; 트리아지쿠온; 2,2',2''-트리클로로트리에틸아민; 트리코테센 (특히 T-2 독소, 베라쿠린 A, 로리딘 A 및 안구이딘); 우레탄; 빈데신; 다카르바진; 만노무스틴; 미토브로니톨; 미토락톨; 피포브로만; 가시토신; 아라비노사이드(“Ara-C”); 사이클로포스파미드; 티오테파; 탁소이드, 예를 들어, TAXOL (파클리탁셀; Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANE® (무-크레모포어), 파클리탁셀의 알부민-조작된 나노입자 제제 (American Pharmaceutical Partners, Schaumberg, Ill.), 및 TAXOTERE® (도세탁셀, 독세탁셀; Sanofi-Aventis); 클로람부실; GEMZAR® (젬시타빈); 6-티오구아닌; 머캅토퓨린; 메토트렉세이트; 시스플라틴 및 카르보플라틴과 같은 백금 유사체; 빈블라스틴; 에토포시드 (VP-16); 이포스파미드; 미톡산트론; 빈크리스틴; NAVELBINE® (비노렐빈); 노반트론; 테니포사이드; 에다트렉세이트; 다우노마이신; 아미노프테린; 카페시타빈 (XELODA®); 이반드로네이트; CPT-11; 토포이소머라제 억제제 RFS 2000; 디플루오로메틸오르니틴 (DMFO); 레티노산과 같은 레티노이드; 및 상기 어느 하나의 약학상 허용되는 염, 산 및 유도체; 뿐만 아니라 상기 둘 이상의 복합물, 예를 들어, 사이클로포스파미드, 독소루비신, 빈크리스틴, 및 프레드니솔론의 복합 요법의 약어 CHOP, 및 옥살리플라틴 (ELOXATINTM)을 5-FU 및 류코보린과 복합하여 사용하는 치료 요법의 약어 FOLFOX를 포함하나 이에 제한되는 것은 아니다. 화학요법제의 또 다른 예에는 벤다무스틴 (또는 벤다무스틴-HCl) (TREANDA®), 이브루티닙, 레날리도마이드 및/또는 이델랄리십 (GS-1101)이 포함된다.
화학요법제의 또 다른 예는 암의 성장을 촉진할 수 있는 호르몬의 효과를 조절, 감소, 차단 또는 억제하는 작용을 하는 항호르몬제를 포함하며, 이는 종종 전신 또는 신체 전체 치료의 형태이다. 화학요법제는 호르몬 자체일 수 있다. 예에는, 예를 들어 타목시펜 (NOLVADEX® 타목시펜 포함), 랄록시펜 (EVISTA®), 드롤록시펜, 4-하이드록시타목시펜, 트리옥시펜, 케옥시펜, LY117018, 오나프리스톤, 및 토레미펜 (FARESTON®)을 비롯한, 항에스트로겐 및 선택적 에스트로겐 수용체 조절제(SERM); 항프로게스테론; 에스트로겐 수용체 하향 조절제(ERD); 풀베스트란트 (FASLODEX®)와 같은 에스트로겐 수용체 길항제; 난소를 억제하거나 폐쇄하는 기능을 하는 제제, 예를 들어, 류프롤리드 아세테이트 (LUPRON® 및 ELIGARD®), 고세렐린 아세테이트, 부세렐린 아세테이트 및 트립테렐린과 같은 황체형성 호르몬 방출 호르몬 (LHRH) 효능제; 플루타미드, 닐루타미드 및 비칼루타미드와 같은 항안드로겐; 및 부신에서 에스트로겐 생성을 조절하는 효소 아로마타제를 억제하는 아로마타제 억제제, 예를 들어, 4(5)-이미다졸, 아미노글루테티미드, 메게스트롤 아세테이트 (MEGASE®), 엑세메스탄 (AROMASIN®), 포르메스타니, 파드로졸, 보로졸 (RIVISOR®), 레트로졸 (FEMARA®) 및 아나스트로졸 (ARIMIDEX®)이 포함된다. 또한, 화학요법제의 이러한 정의에는 비스포스포네이트, 예를 들어, 클로드로네이트 (예를 들어, BONEFOS® 또는 OSTAC®), 에티드로네이트 (DIDROCAL®), NE-58095, 졸레드론산/졸레드로네이트 (ZOMETA®), 알렌드로네이트 (FOSAMAX®), 파미드로네이트 (AREDIA®), 틸루드로네이트 (SKELID®), 또는 리세드로네이트 (ACTONEL®); 뿐만 아니라 트록사시타빈(1,3-디옥솔란 뉴클레오시드 시토신 유사체); 안티센스 올리고뉴클레오티드, 특히, 특히, 예를 들어 PKC-알파, Raf, H-Ras 및 표피 성장 요소 수용체(EGF-R)와 같은 비정상적인 세포 증식과 관련된 신호 전달 경로에서 유전자의 발현을 억제하는 것들; 백신, 예를 들어, THERATOPE® 백신 및 유전자 요법 백신, 예를 들어, ALLOVECTIN® 백신, LEUVECTIN® 백신, 및 VAXID® 백신이 포함된다.
일부 구체예들에서, 화학요법제는 토포이소머라제 1 억제제 (예를 들어, LURTOTECAN®); 풀베스트란트와 같은 항에스트로겐; 이마티닙 또는 EXEL-0862 (티로신 키나제 억제제)와 같은 키트 억제제; 에를로티닙 또는 세툭시맙과 같은 EGFR 억제제; 베바시주맙과 같은 항-VEGF 억제제; 아리노테칸; rmRH (예를 들어, ABAELIX®); 라파티닙 및 라파티닙 디토실레이트(ErbB-2 및 EGFR 이중 티로신 키나제 소분자 억제제는 GW572016로도 알려짐); 17AAG(열 충격 단백질(Hsp) 90 독(poison)인 겔다나마이신 유도체), 및 상기 어느 하나의 약학적으로 허용되는 염, 산 또는 유도체를 포함한다.
화학요법제는 또한 항체, 예를 들어, 알렘투주맙 (Campath), 베바시주맙 (AVASTIN®, Genentech); 세툭시맙 (ERBITUX®, Imclone); 파니투무맙 (VECTIBIX®, Amgen), 리툭시맙 (RITUXAN®, Genentech/Biogen Idec), 유블리툭시맙, 오파투무맙, 이브리투모맙 티욱세탄, 퍼투주맙 (OMNITARG®, 2C4, Genentech), 트라스투주맙 (HERCEPTIN®, Genentech), 토시투모맙 (Bexxar, Corixia), 및 항체 약물 접합체, 젬투주맙 오조가미신 (MYLOTARG®, Wyeth)을 포함한다. 상기 화합물과 조합되는 제제들로서 치료 가능성이 있는 추가 인간화 모노클로날 항체들은 다음을 포함한다: 아폴리주맙, 아셀리주맙, 아틀리주맙, 바피네우주맙, 비바투주맙 메르탄신, 칸투주맙 메르탄신, 세델리주맙, 세르톨리주맙 페골, 시드푸시투주맙, 시드투주맙, 다클리주맙, 에쿨리주맙, 에팔리주맙, 에프라투주맙, 에를리주맙, 펠비주맙, 폰톨리주맙, 겜투주맙 오조가마이신, 이노투주맙 오조가마이신, 이필리무맙, 라베투주맙, 린투주맙, 마투주맙,메폴리주맙, 모타비주맙, 모토비주맙, 나탈리주맙, 니모투주맙, 놀로비주맙, 누마비주맙, 오크렐리주맙, 오말리주맙, 팔리비주맙, 파스콜리주맙, 펙푸시투주맙, 펙투주맙, 펙셀리주맙, 랄리비주맙, 라니비주맙, 레슬리비주맙, 레슬리주맙, 레시비주맙, 로벨리주맙, 루플리주맙, 시브로투주맙, 시플리주맙, 손투주맙, 타카투주맙 테트락세탄, 타도시주맙, 탈리주맙, 테피바주맙, 토실리주맙, 토랄리주맙, 투코투주맙 셀모류킨, 투쿠시투주맙, 우마비주맙, 우르톡사주맙, 우스테키누맙, 비실리주맙, 및 인터루킨-12 p40 단백질을 인식하도록 유전적으로 변형된 재조합의 전적인 인간-서열, 전장 IgG1 λ항체인 항-인터루킨-12 (ABT-874/J695, Wyeth Research and Abbott Laboratories).
“패키지 삽입물”이라는 용어는 치료 제품의 사용에 관한 적응증, 사용법, 투여량, 투여, 병용 요법, 금기 및/또는 경고에 대한 정보를 포함하는 치료 제품의 상용 패키지에 관례적으로 포함된 지침을 지칭하는 데 사용된다.
“알킬”은 노말, 2차, 3차 또는 환형 탄소 원자를 함유하는 C1-C18 탄화수소이다. 예에는 메틸 (Me, -CH3), 에틸 (Et, -CH2CH3), 1-프로필 (n-Pr, n-프로필, -CH2CH2CH3), 2-프로필 (i-Pr, i-프로필, -CH(CH3)2), 1-부틸 (n-Bu, n-부틸, -CH2CH2CH2CH3), 2-메틸-1-프로필 (i-Bu, i-부틸, -CH2CH(CH3)2), 2-부틸 (s-Bu, s-부틸, -CH(CH3)CH2CH3), 2-메틸-2-프로필 (t-Bu, t-부틸, -C(CH3) 3), 1-펜틸 (n-펜틸, -CH2CH2CH2CH2CH3), 2-펜틸 (-CH(CH3)CH2CH2CH3), 3-펜틸 (-CH(CH2CH3)2), 2-메틸-2-부틸 (-C(CH3)2CH2CH3), 3-메틸-2-부틸 (-CH(CH3)CH(CH3)2), 3-메틸-1-부틸 (-CH2CH2CH(CH3)2), 2-메틸-1-부틸 (-CH2CH(CH3)CH2CH3), 1-헥실 (-CH2CH2CH2CH2CH2CH3), 2-헥실 (-CH(CH3)CH2CH2CH2CH3), 3-헥실 (-CH(CH2CH3)(CH2CH2CH3)), 2-메틸-2-펜틸 (-C(CH3)2CH2CH2CH3), 3-메틸-2-펜틸 (-CH(CH3)CH(CH3)CH2CH3), 4-메틸-2-펜틸 (-CH(CH3)CH2CH(CH3)2), 3-메틸-3-펜틸 (-C(CH3)(CH2CH3)2), 2-메틸-3-펜틸 (-CH(CH2CH3)CH(CH3)2), 2,3-다이메틸-2-부틸 (-C(CH3)2CH(CH3)2), 3,3-다이메틸-2-부틸 (-CH(CH3)C(CH3)3이 있다.
본원에 사용된 용어 “C1-C8 알킬”은 1 내지 8개의 탄소 원자를 갖는 직쇄 또는 분지형, 포화 또는 불포화 탄화수소를 지칭한다. 대표적인 “C1-C8 알킬” 그룹에는, -메틸, -에틸, -n-프로필, -n-부틸, -n-펜틸, -n-헥실, -n-헵틸, -n-옥틸, -n-노닐 및 -n-데실이 포함되나 이에 제한되는 것은 아니며; 한편 분지형 C1-C8 알킬에는, -이소프로필, -sec-부틸, -이소부틸, -tert-부틸, -이소펜틸, 2-메틸부틸이 포함되나 이에 제한되는 것은 아니며, 불포화 C1-C8 알킬에는 -비닐, -알릴, -1-부테닐, -2-부테닐, -이소부틸레닐, -1-펜테닐, -2-펜테닐, -3-메틸-1-부테닐, -2-메틸-2-부테닐, -2,3-다이메틸-2-부테닐, 1-헥실, 2-헥실, 3-헥실, -아세틸레닐, -프로피닐, -1-부티닐, -2-부티닐, -1-펜티닐, -2-펜티닐, -3-메틸-1 부티닐이 포함되나 이에 제한되는 것은 아니다. C1-C8 알킬 그룹은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -SO3R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 하나 이상의 작용기들로 치환되거나 치환되지 않을 수 있으며; 이때 각R'은 독립적으로 H, -C1-C8 알킬 및 아릴에서 선택된다.
본원에 사용된 용어 “C1-C12 알킬”은 1 내지 12개의 탄소 원자를 갖는 직쇄 또는 분지형, 포화 또는 불포화 탄화수소를 지칭한다. C1-C12 알킬 그룹은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -SO3R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 하나 이상의 작용기들로 치환되거나 치환되지 않을 수 있으며; 이때 각R'은 독립적으로 H, -C1-C8 알킬 및 아릴에서 선택된다.
본원에 사용된 용어 “C1-C6 알킬”은 1 내지 6개의 탄소 원자를 갖는 직쇄 또는 분지형, 포화 또는 불포화 탄화수소를 지칭한다. 대표적인 “C1-C6 알킬” 그룹에는, -메틸, -에틸, -n-프로필, -n-부틸, -n-펜틸, 및 n-헥실이 포함되나 이에 제한되는 것은 아니며; 한편 분지형 C1-C6 알킬에는, -이소프로필, -sec-부틸, -이소부틸, -tert-부틸, -이소펜틸, 및 2-메틸부틸이 포함되나 이에 제한되는 것은 아니고; 불포화 C1-C6 알킬에는, -비닐, -알릴, -1-부테닐, -2-부테닐, 및 -이소부틸레닐, -1-펜테닐, -2-펜테닐, -3-메틸-1-부테닐, -2-메틸-2-부테닐, -2,3-다이메틸-2-부테닐, 1-헥실, 2-헥실, 및 3-헥실이 포함되나 이에 제한되는 것은 아니다. C1-C6 알킬 그룹은 C1-C8 알킬 그룹에 대해 상기 기재된 바와 같이 하나 이상의 작용기로 치환되거나 치환되지 않을 수 있다.
본원에 사용된 용어 “C1-C4 알킬”은 1 내지 4개의 탄소 원자를 갖는 직쇄 또는 분지형, 포화 또는 불포화 탄화수소를 지칭한다. 대표적인 “C1-C4 알킬” 그룹에는, -메틸, -에틸, -n-프로필, -n-부틸이 포함되나 이에 제한되는 것은 아니며; 한편 분지형 C1-C4 알킬에는, -이소프로필, -sec-부틸, -이소부틸, -tert-부틸이 포함되나 이에 제한되는 것은 아니고; 불포화 C1-C4 알킬에는, -비닐, -알릴, -1-부테닐, -2-부테닐, 및 -이소부틸레닐이 포함되나 이에 제한되는 것은 아니다. C1-C4 알킬 그룹에는 C1-C8 알킬 그룹에 대해 상기 기재된 바와 같이 하나 이상의 작용기로 치환되거나 치환되지 않을 수 있다.
“알콕시”는 산소에 단일 결합된 알킬 그룹이다. 예시적인 알콕시 그룹에는, 메톡시 (-OCH3) 및 에톡시 (-OCH2CH3)가 포함되나 이에 제한되는 것은 아니다. “C1-C5 알콕시”는 1 내지 5개 탄소 원자를 가지는 알콕시 그룹이다. 알콕시 그룹은 알킬 그룹에 대해 상기 기재된 바와 같이 비치환되거나 하나 이상의 작용기로 치환될 수 있다.
“알케닐”은 하나 이상의 불포화 부위, 즉 탄소-탄소 sp 2 이중 결합을 갖는 노말, 2차, 3차 또는 환형 탄소 원자를 함유하는 C2-C18 탄화수소이다. 예에는, 에틸렌 또는 비닐 (-CH=CH2), 알릴 (-CH2CH=CH2), 사이클로펜테닐 (-C5H7), 및 5-헥세닐 (-CH2 CH2CH2CH2CH=CH2)이 포함되나 이에 제한되는 것은 아니다. “C2-C8 알케닐”은 하나 이상의 불포화 부위, 즉 탄소-탄소 sp 2 이중 결합을 갖는 2 내지 8개 노말, 2차, 3차 또는 환형 탄소 원자를 함유하는 탄화수소이다.
“알키닐”은 하나 이상의 불포화 부위, 즉 탄소-탄소 sp 삼중 결합을 갖는 노말, 2차, 3차 또는 환형 탄소 원자를 함유하는 C2-C18 탄화수소이다. 예에는, 아세틸레닉 (-C≡CH) 및 프로파길 (-CH2C≡CH)이 포함되나 이에 제한되는 것은 아니다. “C2-C8 알키닐”은 하나 이상의 불포화 부위, 즉 탄소-탄소 sp 삼중 결합을 갖는 2 내지 8개 노말, 2차, 3차 또는 환형 탄소 원자를 함유하는 탄화수소이다.
“알킬렌”은 1-18개의 탄소 원자의 포화, 분지쇄 또는 직쇄 또는 고리형 탄화수소 라디칼을 나타내며, 모 알칸의 동일하거나 2개의 상이한 탄소 원자로부터 2개의 수소 원자를 제거함으로써 유도된 2개의 1가 라디칼 중심을 갖는다. 전형적인 알킬렌 라디칼에는, 메틸렌 (-CH2-) 1,2-에틸 (-CH2CH2-), 1,3-프로필 (-CH2CH2CH2-), 1,4-부틸 (-CH2CH2CH2CH2-) 등이 포함되나 이에 제한되는 것은 아니다.
“C1-C10 알킬렌”은 화학식 -(CH2)1-10-의 직쇄, 포화 탄화수소 그룹이다. C1-C10 알킬렌의 예에는 메틸렌, 에틸렌, 프로필렌, 부틸렌, 펜틸렌, 헥실렌, 헵틸렌, 옥시틸렌, 노닐렌 및 데칼렌이 포함된다.
“알케닐렌”은 2-18개의 탄소 원자의 불포화, 분지쇄 또는 직쇄 또는 고리형 탄화수소 라디칼을 나타내며, 모 알켄의 동일하거나 2개의 상이한 탄소 원자로부터 2개의 수소 원자를 제거함으로써 유도된 2개의 1가 라디칼 중심을 갖는다. 전형적인 알케닐렌 라디칼은, 1,2-에틸렌 (-CH=CH-)을 포함하나 이에 제한되지 않는다.
“알키닐렌”은 2-18개의 탄소 원자의 불포화, 분지쇄 또는 직쇄 또는 고리형 탄화수소 라디칼을 나타내며, 모 알킨의 동일하거나 2개의 상이한 탄소 원자로부터 2개의 수소 원자를 제거함으로써 유도된 2개의 1가 라디칼 중심을 갖는다. 전형적인 알키닐렌 라디칼에는, 아세틸렌 (-C≡C-), 프로파길 (-CH2C≡C-), 및 4-펜티닐 (-CH2CH2CH2C≡C-)이 포함되나 이에 제한되는 것은 아니다.
“아릴”은 카보사이클릭 방향족 그룹을 지칭한다. 아릴 그룹의 예는 페닐, 나프틸 및 안트라세닐을 포함하지만 이에 제한되지는 않는다. 카보사이클릭 방향족 그룹 또는 헤테로고리형 방향족 그룹은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 하나 이상의 작용기들로 치환되거나 치환되지 않을 수 있으며; 이때 각 R'은 독립적으로 H, -C1-C8 알킬 및 아릴에서 선택된다.
“C5-C20 아릴”은 카보사이클릭 방향족 고리에 5 내지 20개의 탄소 원자를 가지는 아릴 그룹이다. C5-C20 아릴 그룹의 예는 페닐, 나프틸 및 안트라세닐을 포함하지만 이에 제한되지는 않는다. C5-C20 아릴 그룹은 아릴 그룹에 대해 상기 기재된 바와 같이 치환되거나 치환되지 않을 수 있다. “C5-C14 아릴”은 카보사이클릭 방향족 고리에 5 내지 14개의 탄소 원자를 가지는 아릴 그룹이다. C5-C14 아릴 그룹의 예는 페닐, 나프틸 및 안트라세닐을 포함하지만 이에 제한되지는 않는다. C5-C14 아릴 그룹은 아릴 그룹에 대해 상기 기재된 바와 같이 치환되거나 치환되지 않을 수 있다.
“아릴렌”은 2개의 공유 결합을 갖고 다음 구조에서 보는 바와 같이 오르토, 메타 또는 파라 배열일 수 있는 아릴 그룹이다:
여기서 페닐 그룹은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 최대 4개 작용기로 치환되거나 치환되지 않을 수 있고; 이때 각 R'은 H, -C1-C8 알킬 및 아릴에서 독립적으로 선택된다.
“아릴알킬”은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자에 결합된 수소 원자 중 하나가 아릴 라디칼로 대체된 비환형 알킬 라디칼을 지칭한다. 전형적인 아릴알킬 그룹에는, 벤질, 2-페닐에탄-1-일, 2-페닐에텐-1-일, 나프틸메틸, 2-나프틸에탄-1-일, 2-나프틸에텐-1-일, 나프토벤질, 2-나프토페닐에탄-1-일 등이 포함되나 이에 제한되는 것은 아니다. 아릴알킬 그룹은 6 내지 20개의 탄소 원자를 포함하고, 예를 들어, 아릴알킬 그룹의 알칸일, 알케닐 또는 알키닐 그룹을 포함하는 알킬 모이어티는 1 내지 6개의 탄소 원자이고 아릴 모이어티는 5 내지 14개의 탄소 원자이다.
“헤테로아릴알킬” 은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자에 결합된 수소 원자 중 하나가 헤테로아릴 라디칼로 대체된 비환형 알킬 라디칼을 지칭한다. 전형적인 헤테로아릴알킬 그룹에는, 2-벤즈이미다졸릴메틸, 2-퓨릴에틸 등이 포함되나 이에 제한되는 것은 아니다. 헤테로아릴알킬 그룹은 6 내지 20개 탄소 원자를 포함하고, 예를 들어, 헤테로아릴알킬 그룹의 알칸일, 알케닐 또는 알키닐 그룹을 포함하는 알킬 모이어티는 1 내지 6개 탄소 원자이고 헤테로아릴 모이어티는 is 5 내지 14개 탄소 원자 및 N, O, P, 및 S에서 선택된 1 내지 3개 헤테로원자이다. 헤테로아릴알킬 그룹의 헤테로아릴 모이어티는 3 내지 7개 고리원 (2 내지 6개 탄소 원자)을 가지는 모노사이클 또는 7 내지 10개 고리원 (4 내지 9개 탄소 원자 및 N, O, P, 및 S에서 선택된 1 내지 3개 헤테로원자)을 가지는 바이사이클, 예를 들어: 바이사이클로 [4,5], [5,5], [5,6], 또는 [6,6] 시스템 일 수 있다.
“치환된 알킬,” “치환된 아릴,” 및 “치환된 아릴알킬”은 각각, 하나 이상의 수소 원자들이 각각 독립적으로 치환기로 대체된 알킬, 아릴, 및 아릴알킬을 의미한다. 전형적인 치환기들에는, -X, -R, -O-, -OR, -SR, -S-, -NR2, -NR3, =NR, -CX3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, NC(=O)R, -C(=O)R, -C(=O)NR2, -SO3 -, -SO3H, -S(=O)2R, -OS(=O)2OR, -S(=O)2NR, -S(=O)R, -OP(=O)(OR)2, -P(=O)(OR)2, -PO- 3, -PO3H2, -C(=O)R, -C(=O)X, -C(=S)R, -CO2R, -CO2 -, -C(=S)OR, -C(=O)SR, -C(=S)SR, -C(=O)NR2, -C(=S)NR2, -C(=NR)NR2이 포함되나 이에 제한되는 것은 아니며, 여기서 각 X는 독립적으로 독립적으로 할로겐: F, Cl, Br, 또는 I이고; 각 R은 독립적으로 -H, C2-C18 알킬, C6-C20 아릴, C3-C14 헤테로사이클, 보호기 또는 전구약물 모이어티이다. 상기 기재된 알킬렌, 알케닐렌, 및 알키닐렌 그룹 또한 유사하게 치환될 수 있다.
“헤테로아릴” 및 “헤테로사이클”은 하나 이상의 고리 원자가 헤테로원자, 예를 들어 질소, 산소 및 황인 고리 시스템을 지칭한다. 헤테로사이클 라디칼은 3 내지 20개 탄소 원자 및 N, O, P, 및 S에서 선택된 1 내지 3개 헤테로원자를 포함한다. 헤테로사이클은 3 내지 7개 고리원 (2 내지 6개 탄소 원자 및 N, O, P, 및 S에서 선택된 1 내지 3개 헤테로원자)을 가지는 모노사이클 또는 7 내지 10개 고리원 (4 내지 9 탄소 원자 및 N, O, P, 및 S에서 선택된 1 내지 3개 헤테로원자)을 가지는 바이사이클, 예를 들어, 바이사이클로 [4,5], [5,5], [5,6], 또는 [6,6] 시스템 일 수 있다.
헤테로사이클의 예는, 예를 들어, Paquette, Leo A., “Principles of Modern Heterocyclic Chemistry” (W.A. Benjamin, New York, 1968), 특히, 1, 3, 4, 6, 7, 및 9장; “The Chemistry of Heterocyclic Compounds, A series of Monographs” (John Wiley & Sons, New York, 1950 to present), 특히 13, 14, 16, 19, 및 28권; and J. Am. Chem. Soc. (1960) 82:5566에 기재되어 있다.
헤테로사이클의 예에는, 예로서 그리고 제한없이 피리딜, 다이하이드로피리딜, 테트라하이드로피리딜(피페리딜), 티아졸릴, 테트라하이드로티오페닐, 황산화된 테트라하이드로티오페닐, 피리미디닐, 푸라닐, 티에닐, 피롤릴, 피라졸릴, 이미다졸릴, 테트라졸릴, 벤조푸라닐, 티아나프탈레닐, 인돌릴, 인돌레닐, 퀴놀리닐, 이소퀴놀리닐, 벤즈이미다졸릴, 피페리디닐, 4-피페리도닐, 피롤리디닐, 2-피롤리도닐, 피롤리닐, 테트라하이드로푸라닐, 비스-테트라하이드로푸라닐, 테트라하이드로피라닐, 비스-테트라하이드로피라닐, 테트라하이드로퀴놀리닐, 테트라하이드로이소퀴놀리닐, 데카하이드로퀴놀리닐, 옥타하이드로이소퀴놀리닐, 아조시닐, 트리아지닐, 6H-1,2,5-티아디아지닐, 2H,6H-1,5,2-디티아지닐, 티에닐, 티안트레닐, 피라닐, 이소벤조푸라닐, 크로메닐, 잔테닐, 페녹사티닐, 2H-피롤릴, 이소티아졸릴, 이속사졸릴, 피라지닐, 피리다지닐, 인돌리지닐, 이소인돌릴, 3H-인돌릴, 1H-인다졸릴, 퓨리닐, 4H-퀴놀리지닐, 프탈라지닐, 나프티리디닐, 퀴녹살리닐, 퀴나졸리닐, 신놀리닐, 프테리디닐, 4aH-카바졸릴, 카바졸릴, β-카르보리닐, 페난트리디닐, 아크리디닐, 피리미디닐, 페난트롤리닐, 페나지닐, 페노티아지닐, 푸라자닐, 페녹사지닐, 이소크로마닐, 크로마닐, 이미다졸리디닐, 이미다졸리닐, 피라졸리디닐, 피라졸리닐, 피페라지닐, 인돌리닐, 이소인돌리닐, 퀴누클리디닐, 모르폴리닐, 옥사졸리디닐, 벤조트리아졸릴, 벤즈이속사졸릴, 옥스인돌릴, 벤족사졸리닐, 및 이사티노일이 포함된다.
예로서 그리고 제한없이, 탄소 결합된 헤테로사이클은 피리딘의 위치 2, 3, 4, 5, 또는 6, 피리다진의 위치 3, 4, 5, 또는 6, 피리미딘의 위치 2, 4, 5, 또는 6, 피라진의 위치 2, 3, 5, 또는 6, 푸란, 테트라하이드로푸란, 티오푸란, 티오펜, 피롤 또는 테트라하이드로피롤의 위치 2, 3, 4, 또는 5, 옥사졸, 이미다졸 또는 티아졸의 위치 2, 4, 또는 5, 이속사졸, 피라졸, 또는 이소티아졸의 위치 3, 4, 또는 5, 아지리딘의 위치 2 또는 3, 아제티딘의 위치 2, 3, 또는 4, 퀴놀린의 위치 2, 3, 4, 5, 6, 7, 또는 8 또는 이소퀴놀린의 위치 1, 3, 4, 5, 6, 7, 또는 8에서 결합된다. 더욱 더 전형적으로, 탄소 결합된 헤테로사이클은 2-피리딜, 3-피리딜, 4-피리딜, 5-피리딜, 6-피리딜, 3-피리다지닐, 4-피리다지닐, 5-피리다지닐, 6-피리다지닐, 2-피리미디닐, 4-피리미디닐, 5-피리미디닐, 6-피리미디닐, 2-피라지닐, 3-피라지닐, 5-피라지닐, 6-피라지닐, 2-티아졸릴, 4-티아졸릴, 또는 5-티아졸릴을 포함한다.
비제한적인 예로서, 질소 결합된 헤테로사이클은 아지리딘, 아제티딘, 피롤, 피롤리딘, 2-피롤린, 3-피롤린, 이미다졸, 이미다졸리딘, 2-이미다졸린, 3-이미다졸린, 피라졸, 피라졸린, 2-피라졸린, 3-피라졸린, 피페리딘, 피페라진, 인돌, 인돌린, 1H-인다졸의 위치 1, 이소인돌 또는 이소인돌린의 위치 2, 모르폴린의 위치 4 및 카바졸 또는 β-카볼린의 위치 9에서 결합된다. 더욱 더 전형적으로, 질소 결합된 헤테로사이클은 1-아지리딜, 1-아제테딜, 1-피롤릴, 1-이미다졸릴, 1-피라졸릴, 및 1-피페리디닐을 포함한다.
“C3-C8 헤테로사이클”은 고리 탄소 원자들의 1 내지 4개가 독립적으로 O, S 및 N으로 구성된 그룹의 헤테로원자로 대체된, 방향족 또는 비-방향족 C3-C8 카보사이클을 지칭한다. C3-C8헤테로사이클의 대표적인 예에는 벤조푸라닐, 벤조티오펜, 인돌릴, 벤조피라졸릴, 쿠마리닐, 이소퀴놀리닐, 피롤릴, 티오페닐, 푸라닐, 티아졸릴, 이미다졸릴, 피라졸릴, 트리아졸릴, 퀴놀리닐, 피리미디닐, 피리디닐, 피리도닐, 피라지닐, 피리다지닐, 이소티아졸릴, 이속사졸릴 및 테트라졸릴이 포함되나 이에 제한되는 것은 아니다. C3-C8 헤테로사이클은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3 , -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 최대 7개 작용기로 치환되거나 치환되지 않을 수 있고; 이때 각 R'은 H, -C1-C8 알킬 및 아릴에서 독립적으로 선택된다.
“C3-C8 헤테로사이클로”는 헤테로사이클 그룹의 수소 원자 중 하나가 결합으로 대체된, 상기 정의된 C3-C8 헤테로사이클 그룹을 지칭한다. C3-C8 헤테로사이클로는, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 최대 6개 작용기로 치환되거나 치환되지 않을 수 있고; 이때 각 R'은 H, -C1-C8 알킬 및 아릴에서 독립적으로 선택된다.
“C3-C20 헤테로사이클”은 고리 탄소 원자들의 1 내지 4개가 독립적으로 O, S 및 N으로 구성된 그룹의 헤테로원자로 대체된, 방향족 또는 비-방향족 C3-C8 카보사이클을 지칭한다. C3-C20 헤테로사이클은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 최대 7개 작용기로 치환되거나 치환되지 않을 수 있고; 이때 각 R'은 H, -C1-C8 알킬 및 아릴에서 독립적으로 선택된다.
“C3-C20 헤테로사이클로”는 헤테로사이클 그룹의 수소 원자 중 하나가 결합으로 대체된, 상기 정의된 C3-C20 헤테로사이클 그룹을 지칭한다.
“카보사이클”은 모노사이클로서 3 내지 7개의 탄소 원자 또는 바이사이클로서 7 내지 12개의 탄소 원자를 갖는 포화 또는 불포화 고리를 의미한다. 모노사이클릭 카보사이클은 3 내지 6개의 고리 원자, 더욱 더 전형적으로 5 또는 6개의 고리 원자를 갖는다. 바이사이클릭 카보사이클은 예를 들어, 바이사이클로 [4,5], [5,5], [5,6] 또는 [6,6] 시스템으로 배열된 7 내지 12개 고리 원자, 또는 바이사이클로 [5,6] 또는 [6,6] 시스템으로 배열된 9 또는 10개 고리 원자를 가진다. 모노사이클릭 카보사이클의 예는 사이클로프로필, 사이클로부틸, 사이클로펜틸, 1-사이클로펜트-1-에닐, 1-사이클로펜트-2-에닐, 1-사이클로펜트-3-에닐, 사이클로헥실, 1-사이클로헥스-1-에닐, 1-사이클로헥스-2-에닐, 1-사이클로헥스-3-에닐, 사이클로헵틸, 및 사이클로옥틸을 포함한다.
“C3-C8 카보사이클”은 3-, 4-, 5-, 6-, 7- 또는 8-원의 포화 또는 불포화 비-방향족 카보사이클릭 고리이다. 대표적인 C3-C8 카보사이클에는, -사이클로프로필, -사이클로부틸, -사이클로펜틸, -사이클로펜타다이에닐, -사이클로헥실, -사이클로헥세닐, -1,3-사이클로헥사다이에닐, -1,4-사이클로헥사다이에닐, -사이클로헵틸, -1,3-사이클로헵타다이에닐, -1,3,5-사이클로헵타트라이에닐, -사이클로옥틸, 및 -사이클로옥타다이에닐이 포함되나 이에 제한되는 것은 아니다. C3-C8 카보사이클 그룹은, -C1-C8 알킬, -O-(C1-C8 알킬), -아릴, -C(O)R', -OC(O)R', -C(O)OR', -C(O)NH2, -C(O)NHR', -C(O)N(R')2 -NHC(O)R', -S(O)2R', -S(O)R', -OH, -할로겐, -N3, -NH2, -NH(R'), -N(R')2 및 -CN을 비롯한 (그러나 이에 제한되는 것은 아님) 하나 이상의 작용기들로 치환되거나 치환되지 않을 수 있으며; 이때 각R'은 독립적으로 H, -C1-C8 알킬 및 아릴에서 선택된다.
“C3-C8 카보사이클로”는 카보사이클 그룹의 수소 원자 중 하나가 결합으로 대체된, 상기 정의된 C3-C8 카보사이클 그룹을 지칭한다.
“링커”는 약물 모이어티에 항체를 공유적으로 부착시키는 원자들의 사슬 또는 공유 결합을 포함하는 화학적 모이어티를 지칭한다. 다양한 구체예들에서, 링커는 2가 라디칼, 예를 들어, 알킬디일, 아릴디일, 헤테로아릴디일, 모이어티, 예를 들어: -(CR2)nO(CR2)n-, 알킬옥시의 반복 단위 (예를 들어, 폴리에틸렌옥시, PEG, 폴리메틸렌옥시) 및 알킬아미노 (예를 들어, 폴리에틸렌아미노, 제파민™); 및 숙시네이트, 숙신아미드, 디글리콜레이트, 말로네이트, 및 카프로아미드를 포함하는 이산 에스터와 아미드를 포함한다. 다양한 구체예들에서, 링커는 하나 이상의 아미노산 잔기, 예를 들어, 발린, 페닐알라닌, 리신 및 호모리신을 포함할 수 있다.
“키랄”이라는 용어는 거울상 짝과 중첩되지 않는 특성을 갖는 분자를 나타내고, 용어 “아키랄”은 거울상 짝에 중첩될 수 있는 분자를 나타낸다.
“입체이성질체”라는 용어는 화학적 구성이 동일하지만 공간에서 원자 또는 그룹의 배열과 관련하여 다른 화합물을 지칭한다.
“부분입체이성질체”는 2개 이상의 키랄 중심을 갖고 분자가 서로 거울상이 아닌 입체이성질체를 지칭한다. 부분입체이성질체는 물리적 특성, 녹는점, 끓는점, 스펙트럼 특성 및 반응성이 상이하다. 부분입체이성질체의 혼합물은 전기영동 및 크로마토그래피와 같은 고해상도 분석 절차에서 분리될 수 있다.
“거울상 이성질체”는 서로 중첩될 수 없는 거울상인 화합물의 두 입체이성질체를 지칭한다.
본원에서 사용되는 입체화학 정의 및 관례는 일반적으로 S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; and Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (1994) John Wiley & Sons, Inc., New York에 따른다. 많은 유기 화합물은 광학 활성 형태로 존재한다, 즉, 평면 편광면을 회전시키는 능력이 있다. 광학 활성 화합물을 설명할 때 접두사 D와 L, 또는 R과 S는 키랄 중심(들)에 대한 분자의 절대 배열을 나타내는 데 사용된다. 접두사 d 및 l 또는 (+) 및 (-)는 화합물에 의한 평면 편광의 회전 기호를 지정하는 데 사용되며, (-) 또는 1은 화합물이 좌회전성임을 의미한다. (+) 또는 d가 접두사로 붙은 화합물은 우회전성이다. 주어진 화학 구조에 있어서, 이러한 입체이성질체는 서로 거울상이라는 점을 제외하고는 동일하다. 특정 입체이성질체는 또한 거울상 이성질체로 지칭될 수 있으며, 이러한 이성질체의 혼합물은 종종 거울상 이성질체 혼합물로 지칭된다. 거울상 이성질체의 50:50 혼합물은 라세미 혼합물 또는 라세미체로 지칭되며, 이는 화학 반응 또는 공정에서 입체선택성 또는 입체특이성이 없는 경우에 발생할 수 있다. 용어 “라세미 혼합물” 및 “라세미체”는 광학 활성이 없는 2개의 거울상 이성질체 종의 등몰 혼합물을 지칭한다.
“이탈기”는 다른 작용기로 치환될 수 있는 작용기를 지칭한다. 특정 이탈기는 해당 분야에 잘 알려져 있으며, 예에는 할로겐화물 (예를 들어, 염화물, 브롬화물, 또는 요오드화물), 메탄술포닐 (메실), p-톨루엔술포닐 (토실), 트리플루오로메틸술포닐 (트리플레이트) 및 트리플루오로메틸술포네이트가 포함되나 이에 제한되는 것은 아니다.
용어 “보호기”는 화합물 상의 특정 작용기를 차단 또는 보호하면서 다른 작용기를 반응시키기 위해 일반적으로 사용되는 치환기를 지칭한다. 예를 들어, “아미노-보호기”는 화합물에서 아미노 작용기를 차단하거나 보호하는, 아미노기에 부착되는 치환기이다. 적합한 아미노-보호기는 아세틸, 트리플루오로아세틸, t-부톡시카르보닐 (BOC), 벤질옥시카르보닐 (CBZ) 및 9-플루오레닐메틸렌옥시카르보닐 (Fmoc)을 포함하나 이에 제한되지는 않는다. 보호기 및 이의 용도에 관한 일반적인 설명에 관하여, T. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, New York, 1991, 또는 최신판을 참조하라.
III. 방법
본원은 치료를 필요로 하는 개체 (예를 들어, 인간 개체)에게 유효량의 (a) 세포독성제에 연결된 CD79b에 결합하는 항체를 포함하는 면역접합체, (b) 항-CD20 항체, 및 (c) 하나 이상의 화학요법제를 투여하는 것을 포함하는, 개체에서 B-세포 증식성 장애 (예를 들어, 미만성 거대 B-세포 림프종 (DLBCL), 예를 들어, 재발성/불응성 DLBCL)를 치료하는 방법을 제공한다.
일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 옥살리플라틴을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴이다.
용어 “공동-투여” 또는 “공동-투여하는 것”은 항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제를 두 개 (또는 그 이상)의 별도 제제로서 (또는 항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제를 포함하는 하나의 단일 제제로서) 투여하는 것을 지칭한다. 별도의 제제가 사용되는 경우, 공동-투여는 동시 또는 어느 순서로든 순차적일 수 있으며, 여기서 바람직하게는 모든 활성 제제가 동시에 생물학적 활성을 발휘하는 시기가 있다. 일부 구체예들에서, 항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제는 동시에 또는 순차적으로 공동-투여된다. 일부 구체예들에서, 모든 치료제가 순차적으로 공동-투여되는 경우, 용량은 동일한 날에 2회 이상의 별도 투여로 투여되거나 하나 이상의 제제가 1일차에 (예를 들어, 21일 사이클의 1일차에) 투여되고, 다른 약제(들)는 약 2일차(예를 들어, 21일 사이클의 2일차)에 공동-투여된다. 일부 구체예들에서, 용어 “순차적으로”는 제1 성분의 투여 후 7일 이내, 예를 들어, 제1 성분의 투여 후 4일, 3일, 2일, 또는 1일 이내를 의미하고; “동시에”라는 용어는 동일한 시간에를 의미한다. 일부 구체예들에서, 용어 “순차적으로”는 제1 성분의 투여 후 1일 미만 이내, 예를 들어, 제1 성분의 투약 후 24시간 미만, 20시간 미만, 15시간 미만, 10시간 미만, 12시간 미만, 8시간 미만, 6시간 미만, 3시간 미만, 2시간 미만, 또는 1시간 미만 이내를 의미한다. 일부 구체예들에서, 항-CD79b 면역접합체 및 항-CD20 항체는 각 21일 사이클의 약 1일차에 순차적으로 공동-투여되고 하나 이상의 화학요법제는 각 21일 사이클의 약 2일차에 순차적으로 공동-투여된다.
본원에 기재된 임의의 치료 방법에 사용하기 위해 본원에 제공된 항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제는 우수한 의료 관행과 일치하는 방식으로 제제화, 투약 및 투여될 것이다. 이와 관련하여 고려해야 할 요소에는 치료 중인 특정 장애, 치료 중인 특정 포유동물, 개별 환자의 임상 병태, 장애의 원인, 제제 전달 부위, 투여 방법, 투여 일정, 및 의료 종사자에게 알려진 기타 요소가 포함된다. 면역접합체는 꼭 그럴 필요는 없지만, 문제의 장애를 예방하거나 치료하기 위해 현재 사용되는 하나 이상의 제제와 함께 선택적으로 제제화된다.
항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제의 공동-투여량 및 공동-투여 시점은 치료받는 환자의 유형(인종, 성별, 연령, 체중 등) 및 병태 및 치료 중인 질환 또는 병태의 중증도에 따라 달라질 것이다. 항-CD79b 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제는 한 번에 또는 일련의 치료에 걸쳐, 예를 들어 같은 날 또는 다음 날에 환자에게 적합하게 공동-투여된다.
일부 구체예들에서, 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)의 투여량은 대략 1.4-5 mg/kg, 1.4-4 mg/kg, 1.4-3.2 mg/kg, 1.4-2.4 mg/kg, 또는 1.4-1.8 mg/kg 중 어느 하나이다. 상기 방법들 중 어느 하나의 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 1.4 mg/kg, 1.5 mg/kg. 1.6 mg/kg. 1.7 mg/kg, 1.8 mg/kg, 1.9 mg/kg, 2.0 mg/kg, 2.2 mg/kg, 2.4 mg/kg, 2.6 mg/kg, 2.8 mg/kg, 3.0 mg/kg, 3.2 mg/kg, 3.4 mg/kg, 3.6 mg/kg, 3.8 mg/kg, 4.0 mg/kg, 4.2 mg/kg, 4.4 mg/kg, 4.6 mg/kg, 및/또는 4.8 mg/kg 중 어느 하나이다. 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 1.4 mg/kg이다. 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 1.8 mg/kg이다. 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 2.4 mg/kg이다. 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 3.2 mg/kg이다. 일부 구체예들에서, 항-CD79b 면역접합체의 투여량은 약 3.6 mg/kg이다. 상기 방법들 중 어느 하나의 일부 구체예들에서, 항-CD79b 면역접합체는 q3wk 투여된다. 상기 방법들 중 어느 하나의 일부 구체예들에서, 항-CD79b 면역접합체는 각 21일 사이클에 1회 투여된다. 상기 방법들 중 어느 하나의 일부 구체예들에서, 항-CD79b 면역접합체는 각 21일 사이클의 약 1일차에 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체는 정맥내 주입을 통해 투여된다. 일부 구체예들에서, 주입을 통해 투여되는 투여량은 일반적으로 3주 마다 (예를 들어, 각 21일 사이클의 1일차에) 총 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16회 이상의 투약 동안 투약 당 약 1 mg 내지 약 2,000 mg 범위이다. 일부 구체예들에서, 주입을 통해 투여되는 투여량은 일반적으로 각 21일 사이클의 약 1일차에 최대 8회의 21일 사이클 동안 투약 당 약 1 mg 내지 약 2,000 mg 범위이다. 대안적으로, 투여량 범위는 약 1 mg 내지 약 2,000 mg, 약 1 mg 내지 약 1,800 mg, 약 400 mg 내지 약 1200 mg, 약 600 mg 내지 약 1000 mg, 약 10 mg 내지 약 500 mg, 약 10 mg 내지 약 300 mg, 약 10mg 내지 약 200 mg, 및 약 1 mg 내지 약 200 mg이다. 일부 구체예들에서, 주입을 통해 투여되는 투여량은 일반적으로 각 21일 사이클의 1일차에 총 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16회 이상의 투약 동안 투약 당 약 1 μg/m2 내지 약 10,000 μg/m2 범위이다. 일부 구체예들에서, 주입을 통해 투여되는 투여량은 일반적으로 3주 마다 1회 투약으로 최대 8회의 21일 사이클 동안 투약 당 약 1 μg/m2 내지 약 10,000 μg/m2 범위이다. 대안적으로, 투여량 범위는 약 1 μg/m2 내지 약 1000 μg/m2, 약 1 μg/m2 내지 약 800 μg/m2, 약 1 μg/m2 내지 약 600 μg/m2, 약 1 μg/m2 내지 약 400 μg/m2, 약 10 μg/m2 내지 약 500 μg/m2, 약 10 μg/m2 내지 약 300 μg/m2, 약 10 μg/m2 내지 약 200 μg/m2, 및 약 1 μg/m2 내지 약 200 μg/m2이다. 투여량은 질환의 증상을 완화하거나 완화하기 위해 1주 1회, 1주 수 회, 그러나 1일 1회 미만, 1개월 수 회 그러나 1일 1회 미만, 1개월 수 회 그러나 1주 1회 미만, 1개월 1회, 3주 마다 1회, 21일마다 1회, 각 21일 사이클에 1회, 각 21일 사이클의 1일차에, 또는 간헐적으로 투여될 수 있다. 투여는 최대 8회의 21일 사이클 동안 또는 치료 중인 B 세포 증식성 장애(예를 들어, DLBCL)의 종양 또는 증상이 완화될 때까지 상기 개시된 간격들 중 어느 하나로 계속될 수 있다. 증상의 관해 또는 완화가 달성된 후, 이러한 지속 투여에 의해 이러한 관해 또는 완화가 연장되는 경우, 투여를 계속할 수 있다.
일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)의 투여량은 약 300-1600 mg/m2 내지/또는 300-2000 mg 이다. 일부 구체예들에서, 항-CD20 항체의 투여량은 약 300 mg/m2, 375 mg/m2, 600 mg/m2, 1000 mg/m2, 또는 1250 mg/m2 및/또는 300 mg, 1000 mg, 또는 2000 mg이다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이고 투여되는 투여량은 375 mg/m2이다. 일부 구체예들에서, 항-CD20 항체는 q3w (즉, 3주 마다) 투여된다. 일부 구체예들에서, 항-CD20 항체는 각 21일 사이클에 1회 (예를 들어, 각 21일 사이클의 1일차에) 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 리툭시맙의 투여량은 각 21일 사이클의 1일차에 375 mg/m2 일 수 있다. 일부 구체예들에서, 리툭시맙의 투여량은 최대 8회의 21일 사이클 동안 각 21일 사이클의 1일차에 375 mg/m2 일 수 있다. 일부 구체예들에서, 리툭시맙의 투여량은 8회의 21일 사이클 동안 각 21일 사이클의 1일차에 375 mg/m2 일 수 있다.
일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)는 질환의 증상을 완화하거나 경감시키기 위해 1주 1회, 1개월 수 회 그러나 1주 1회 미만, 1개월 1회, 3주 마다 1회, 21일마다 1회, 각 21일 사이클에 1회, 각 21일 사이클의 1일차에, 또는 간헐적으로 투여될 수 있다. 투여는 최대 8회의 21일 사이클 동안 또는 치료 중인 B 세포 증식성 장애(예를 들어, DLBCL)의 종양 또는 증상이 완화될 때까지 상기 개시된 간격들 중 어느 하나로 계속될 수 있다. 증상의 관해 또는 완화가 달성된 후, 이러한 지속 투여에 의해 이러한 관해 또는 완화가 연장되는 경우, 투여를 계속할 수 있다.
일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 50 mg/m2 내지 약 2000 mg/m2 이다. 일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 50 mg/m2 내지 약 100 mg/m2, 약 100 mg/m2 내지 약 200 mg/m2, 약 200 mg/m2 내지 약 300 mg/m2, 약 300 mg/m2 내지 약 400 mg/m2, 약 400 mg/m2 내지 약 500 mg/m2, 약 500 mg/m2 내지 약 600 mg/m2, 약 600 mg/m2 내지 약 700 mg/m2, 약 700 mg/m2 내지 약 800 mg/m2, 약 800 mg/m2 내지 약 900 mg/m2, 약 900 mg/m2 내지 약 1000 mg/m2, 약 1000 mg/m2 내지 약 1100 mg/m2, 약 1100 mg/m2 내지 약 1200 mg/m2, 약 1200 mg/m2 내지 약 1300 mg/m2, 약 1300 mg/m2 내지 약 1400 mg/m2, 약 1400 mg/m2 내지 약 1500 mg/m2, 또는 약 1500 mg/m2 내지 약 2000 mg/m2이다.
일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 500 mg/m2 내지 약 1500 mg/m2 (예를 들어, 약 500 mg/m2 내지 약 600 mg/m2, 약 600 mg/m2 내지 약 700 mg/m2, 약 700 mg/m2 내지 약 800 mg/m2, 약 800 mg/m2 내지 약 900 mg/m2, 약 900 mg/m2 내지 약 1000 mg/m2, 약 1000 mg/m2 내지 약 1100 mg/m2, 약 1100 mg/m2 내지 약 1200 mg/m2, 약 1200 mg/m2 내지 약 1300 mg/m2, 약 1300 mg/m2 내지 약 1400 mg/m2, 약 1400 mg/m2 내지 약 1500 mg/m2)의 젬시타빈 용량을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 1000 mg/m2의 젬시타빈 용량을 포함한다. 일부 구체예들에서, 젬시타빈 용량은 q3w 또는 각 21일 사이클에 약 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 젬시타빈 용량은 최대 8회의 21일 사이클 동안 각 21일 사이클에 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 젬시타빈 용량은 8회의 21일 사이클 동안 각 21일 사이클에 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 50 mg/m2 내지 약 200 mg/m2 (예를 들어, 50 mg/m2 내지 약 100 mg/m2 또는 약 100 mg/m2 내지 약 200 mg/m2)의 옥살리플라틴 용량을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제의 투여량은 약 100 mg/m2의 옥살리플라틴 용량을 포함한다. 일부 구체예들에서, 옥살리플라틴 용량은 q3w 또는 각 21일 사이클에 약 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 옥살리플라틴 용량은 최대 8회의 21일 사이클 동안 각 21일 사이클에 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 젬시타빈 용량은 8회의 21일 사이클 동안 각 21일 사이클에 1회 (예를 들어, 각 21일 사이클의 2일차에) 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴을 포함하고, 젬시타빈 및옥살리플라틴은 각 21일 사이클의 약 2일차에 정맥내 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴을 포함하고, 젬시타빈 및옥살리플라틴은 최대 약 8회의 사이클 동안 각 21일 사이클의 2일차에 정맥내 투여된다.
일부 구체예들에서, 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)은 질환의 증상을 완화하거나 완화하기 위해 1주 1회, 1주 수 회, 그러나 1일 1회 미만, 1개월 수 회 그러나 1일 1회 미만, 1개월 수 회 그러나 1주 1회 미만, 1개월 1회, 3주 마다 1회, 각 21일 사이클에 1회, 각 21일 사이클의 약 2일차에, 또는 간헐적으로 투여될 수 있다. 투여는 최대 약 8회의 21일 사이클 동안 또는 치료 중인 B 세포 증식성 장애의 종양 또는 증상이 완화될 때까지 상기 개시된 간격들 중 어느 하나로 계속될 수 있다. 증상의 관해 또는 완화가 달성된 후, 이러한 지속 투여에 의해 이러한 관해 또는 완화가 연장되는 경우, 투여를 계속할 수 있다.
항-CD79b 면역접합체(예를 들어, 폴라투주맙 베도틴-피이크) 및 기타 제제의 병용 요법을 위한 예시적인 투약 요법은, 각 21일 사이클의 약 1일차에 약 1.4-5 mg/kg로 투여되는 항-CD79b 면역접합체 (예를 들어 huMA79bv28-MC-vc-PAB-MMAE), + 각 21일 사이클의 약 1일차에 약 300-1600 mg/m2 로 투여되는 항-CD20 항체 (예를 들어, 리툭시맙), + 각 21일 사이클의 약 2일차에 약 50 mg/m2 내지 약 2000 mg/m2로 투여되는 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) (예를 들어, 약 500 mg/m2 내지 약 2000 mg/m2로 투여되는 젬시타빈 및 약 50 mg/m2 내지 약 200 mg/m2로 투여되는 옥살리플라틴)를 포함하나, 이에 제한되는 것은 아니다. 일부 구체예들에서, 항-CD79b 면역접합체 (예를 들어 폴라투주맙 베도틴-피이크)는 각 21일 사이클의 약 1일차에 약 1.8 mg/kg로 투여되고, 항-CD20 항체 (예를 들어, 리툭시맙)는 각 21일 사이클의 약 1일차에 약 375 mg/m2로 투여되고, 그리고 하나 이상의 화학요법제 (예를 들어, 약 1000 mg/m2로 투여되는 젬시타빈 및 약 100 mg/m2로 투여되는 옥살리플라틴)는 각 21일 사이클의 약 2일차에 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체는 약 1.8 mg/kg로 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이고 약 1.8 mg/kg로 투여된다. 일부 구체예들에서, 항-CD20 항체는 약 375 mg/m2로 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이고 약 375 mg/m2로 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 약 1000 mg/m2로 투여되는 젬시타빈 및 약 100 mg/m2로 투여되는 옥살리플라틴을 포함한다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이고 약 1.8 mg/kg로 투여되고, 항-CD20 항체는 리툭시맙이고 약 375 mg/m2로 투여되고, 그리고 하나 이상의 화학요법제는 약 1000 mg/m2로 투여되는 젬시타빈 및 약 100 mg/m2로 투여되는 옥살리플라틴이다.
본원에 기재된 치료 방법에 사용하기 위한 본원에 제공된 면역접합체, 본원에 제공된 항-CD20 항체, 및 본원에 제공된 하나 이상의 화학요법제는 비경구, 폐내 및 비강내, 그리고, 국소 치료가 필요한 경우 병변내 투여를 비롯한 임의의 적합한 수단에 의해 투여될 수 있다. 비경구 주입에는 근육내, 정맥내 (예를 들어, 정맥내 주입), 동맥내, 복강내 또는 피하 투여가 포함된다. 투약은 부분적으로는 투약이 단기인지 만성인지에 따라 임의의 적합한 경로, 예를 들어, 주사, 가령, 정맥내 또는 피하 주사에 의해 이루어질 수 있다. 단일 또는 다양한 시점에 걸친 다중 투여, 일시 투여 및 펄스 주입을 비롯한 (그러나 이에 제한되지 않는) 다양한 투약 일정이 본원에서 고려된다.
본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고; (b) 항-CD20 항체, 및 (c) 하나 이상의 화학요법제. 일부 구체예들에서, 면역접합체는 서열 번호: 19의 아미노산 서열을 포함하는 중쇄 가변 도메인(VH) 및 서열 번호: 20의 아미노산 서열을 포함하는 경쇄 가변 도메인(VL)을 포함하는 항-CD79b 항체를 포함한다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 인간은 14 일 이내에 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는, 14 일 이내에 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 이러한 다수의 인간들 중 33% 이하 (
예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)가 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 이러한 다수의 인간들 중 약 40% 미만 (
예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이며, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수의 인간들 중 33% 이하 (
예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)가 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 40% 미만 (
예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 면역접합체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, p는 2 내지 7, 2 내지 6, 2 내지 5, 3 내지 5, 또는 3 내지 4이다. 일부 구체예들에서, p는 2 내지 5이다. 일부 구체예들에서, p는 3 내지 4이다. 일부 구체예들에서, p는 3.5이다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 하나 이상의 화학요법제는 본원에 제공된 화학요법제를 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 옥살리플라틴을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴이다.
일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴이다. 특정 구체예들에서, p는 2 내지 5이다. 특정 구체예들에서, p는 2이다. 일부 구체예들에서, 면역접합체는 약 1 mg/kg 내지 약 5 mg/kg인 용량으로 투여된다.. 일부 구체예들에서, 면역접합체는 약 1.2 mg/kg, 약 1.8 mg/kg, 약 2.4 mg/kg, 약 3.6 mg/kg, 또는 약 4.8 mg/kg의 용량으로 투여된다. 일부 구체예들에서, 면역접합체는 약 1.8 mg/kg의 용량으로 투여된다.
본원에서 사용되는 용어 “일라다투주맙 베도틴”은 약물에 관한 국제 일반명 (INN) 번호 10647, 또는 CAS 등록 번호 1906205-77-3을 가지는 항-CD79b 면역접합체를 지칭한다. 일라다투주맙 베도틴은 또한 호환적으로 “DCDS0780A” 또는 “RO7032005”로도 지칭된다.
항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 동일한 투여 경로로 또는 상이한 투여 경로로 투여될 수 있다. 일부 구체예들에서, 항-CD79b 면역접합체는 정맥내, 근육내, 피하, 국소, 경구, 경피, 복강내, 안와내, 이식, 흡입, 척추강내, 뇌실내 또는 비강내 투여된다. 일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)는 정맥내, 근육내, 피하, 국소, 경구, 경피, 복강내, 안와내, 이식, 흡입, 척추강내, 뇌실내 또는 비강내 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 정맥내, 근육내, 피하, 국소, 경구, 경피, 복강내, 안와내, 이식, 흡입, 척추강내, 뇌실내 또는 비강내 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체, 항-CD20 항체 (예를 들어 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 각각 정맥내 주입을 통해 투여된다. 질환의 예방 또는 치료를 위해 유효량의 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)가 투여될 수 있다.
일부 구체예들에서, 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)는 약 1.4 mg/kg 내지 약 2 mg/kg (예를 들어, 약 1.4 mg/kg 내지 약 1.6 mg/kg, 약 1.6 mg/kg 내지 약 1.8 mg/kg, 또는 약 1.8 mg/kg 내지 약 2 mg/kg)의 용량으로 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체는 1.8 mg/kg의 용량으로 투여된다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크는 1.8 mg/kg의 용량으로 투여된다. 대안적으로 또는 추가적으로, 일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)는 약 300-1800 mg/m2 (예를 들어, 약 300 mg/m2 내지 약 600 mg/m2, 약 600 mg/m2 내지 약 900 mg/m2, 약 900 mg/m2 내지 약 1200 mg/m2, 약 1200 mg/m2 내지 약 1500 mg/m2, 또는 약 1500 mg/m2 내지 약 1800 mg/m2) 및/또는 약 300-2000 mg (예를 들어, 약 300 mg 내지 약 600 mg, 약 600 mg 내지 약 900 mg, 약 900 mg 내지 약 1200 mg, 약 1200 mg 내지 약 1500 mg, 약 1500 mg 내지 약 1750 mg, 또는 약 1750 mg 내지 약 2000 mg)의 용량이 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 리툭시맙은 약 375 mg/m2의 투여량으로 투여된다. 대안적으로 또는 추가적으로, 일부 구체예들에서, 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 약 50 mg/m2 내지 약 2000 mg/m2 (예를 들어, 약 50 mg/m2 내지 약 100 mg/m2, 약 100 mg/m2 내지 약 200 mg/m2, 약 200 mg/m2 내지 약 400 mg/m2, 약 400 mg/m2 내지 약 600 mg/m2, 약 600 mg/m2 내지 약 800 mg/m2, 약 800 mg/m2 내지 약 1000 mg/m2, 약 1000 mg/m2 내지 약 1200 mg/m2, 약 1200 mg/m2 내지 약 1400 mg/m2, 약 1400 mg/m2 내지 약 1600 mg/m2, 약 1600 mg/m2 내지 약 1800 mg/m2, 또는 약 1800 mg/m2 내지 약 2000 mg/m2)의 용량으로 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈을 포함한다. 일부 구체예들에서, 젬시타빈은 약 1000 mg/m2의 용량으로 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 옥살리플라틴을 포함한다. 일부 구체예들에서, 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴이고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 그리고 옥살리플라틴은 약 100 mg/m2의 용량으로 투여된다.
일부 구체예들에서, 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 적어도 1회의 21일 사이클 (예를 들어, 약 1, 약 2, 약 3, 약 4, 약 5, 약 6, 약 7, 또는 약 8회, 또는 그 이상의 21일 사이클) 동안 투여된다.
일부 구체예들에서, 항-CD79b 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 최대 8회의 21일 사이클 (예를 들어, 약 1, 약 2, 약 3, 약 4, 약 5, 약 6, 약 7, 또는 약 8회의 21일 사이클) 동안 투여된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)는 각 21일 사이클의 약 1일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이고 폴라투주맙 베도틴-피이크는 각 21일 사이클의 약 1일차에 정맥내 투여된다. 대안적으로 또는 추가적으로, 일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)는 각 21일 사이클의 약 1일차에 정맥내 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이고, 리툭시맙은 각 21일 사이클의 약 1일차에 투여된다. 대안적으로 또는 추가적으로, 일부 구체예들에서, 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 각 21일 사이클의 약 2일차에 정맥내 투여된다. 일부 구체예들에서, 화학요법제는 젬시타빈 및 옥살리플라틴이고, 젬시타빈 및옥살리플라틴은 각 21일 사이클의 약 2일차에 정맥내 투여된다.
일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 적어도 1회의 21일 사이클 동안 투여되고, 이때 면역접합체 및 항-CD20 항체는 각 21일 사이클의 약 1일차에 정맥내 투여되고, 그리고 하나 이상의 화학요법제는 각 21일 사이클의 약 2일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 최대 8회의 21일 사이클 동안 투여되고, 이때, 면역접합체 및 항-CD20 항체는 각 21일 사이클의 약 1일차에 정맥내 투여되고, 그리고 하나 이상의 화학요법제는 각 21일 사이클의 약 2일차에 정맥내 투여된다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴이다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 약 약 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 그리고 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 투여되고 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 투여된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 약 약 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고, 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 그리고 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 투여되고 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 투여된다.
본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m2의 용량으로 투여되고; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14 일 이내 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내)에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 14 일 이내 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내)에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 14 일 이내 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내)에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 14 일 이내 (
예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내)에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 이러한 다수의 인간들 중 33% 이하 (
예를 들어, any of 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, or 약 0.5% 이하)가 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 5 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다. 일부 구체예들에서, 치료받는 다수의 인간들 중에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 후, 이러한 다수의 인간들 중 약 40% 미만 (
예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 최대 8회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 33% 이하 (예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)가 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 5 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 40% 미만 (
예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
또한 본원은 치료를 필요로 하는 개체에게 다음을 유효량 투여하는 것을 포함하는 개체의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL) 치료 방법을 제공한다: (a) 다음 화학식을 포함하는 면역접합체
, 이때 Ab는 (i) 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 (ii) 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 이때 p는 2 내지 5이고, (b) 리툭시맙, (c) 젬시타빈, 및 (d) 옥살리플라틴; 이때 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 1회의 21일 사이클 동안 투여되고, 이때 각 사이클 동안 면역접합체는 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 약 375 mg/m
2의 용량으로 투여되고, 젬시타빈은 약 1000 mg/m
2의 용량으로 투여되고, 및 옥살리플라틴은 약 100 mg/m
2의 용량으로 투여되고; 그리고 이때 면역접합체 및 리툭시맙은 각 21일 사이클의 1일차에 정맥내 투여되고, 젬시타빈 및 옥살리플라틴은 각 21일 사이클의 2일차에 정맥내 투여되며; 그리고 이때 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 33% 이하 (예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)가 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 40% 미만 (
예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 항-CD20 항체 (예를 들어, 리툭시맙)는 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크) 전 (예를 들어, 최대 약 1 시간, 최대 약 2 시간, 최대 약 4 시간, 최대 약 6 시간, 최대 약 12 시간, 최대 약 16 시간, 최대 약 18 시간, 최대 약 22 시간, 최대 약 24 시간, 또는 최대 약 1 일, 최대 약 2 일, 최대 약 3 일, 또는 그 이상 전)에 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이고, 리툭시맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 면역접합체는 항-CD20 항체 전 (예를 들어, 최대 약 1 시간, 최대 약 2 시간, 최대 약 4 시간, 최대 약 6 시간, 최대 약 12 시간, 최대 약 16 시간, 최대 약 18 시간, 최대 약 22 시간, 최대 약 24 시간, 또는 최대 약 1 일, 최대 약 2 일, 최대 약 3 일, 또는 그 이상 전)에 투여된다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이고, 면역접합체는 리툭시맙 전에 투여된다.
일부 구체예들에서, 하나 이상의 화학요법제는 순차적으로 투여된다. 일부 구체예들에서, 화학요법제는 젬시타빈 및 옥살리플라틴이다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전 (예를 들어, 최대 약 1 시간, 최대 약 2 시간, 최대 약 4 시간, 최대 약 6 시간, 최대 약 12 시간, 최대 약 16 시간, 최대 약 18 시간, 최대 약 22 시간, 최대 약 24 시간, 또는 최대 약 1 일, 최대 약 2 일, 최대 약 3 일, 또는 그 이상 전)에 투여된다. 일부 구체예들에서, 옥살리플라틴은 젬시타빈 전 (예를 들어, 최대 약 1 시간, 최대 약 2 시간, 최대 약 4 시간, 최대 약 6 시간, 최대 약 12 시간, 최대 약 16 시간, 최대 약 18 시간, 최대 약 22 시간, 최대 약 24 시간, 또는 최대 약 1 일, 최대 약 2 일, 최대 약 3 일, 또는 그 이상 전)에 투여된다.
일부 구체예들에서, 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제는 1, 2, 3, 4, 5, 6, 7, 또는 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 화학요법제는 젬시타빈 및 옥살리플라틴이다. 일부 구체예들에서, 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 1, 2, 3, 4, 5, 6, 7, 또는 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다.
전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 2회, 적어도 3회, 적어도 4회, 적어도 5회, 적어도 6회, 또는 적어도 7회 21일 사이클 동안 투여된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 8회의 21일 사이클 동안 투여된다. 일부 구체예들에서, 리툭시맙은 면역접합체 전에 투여된다. 일부 구체예들에서, 젬시타빈은 옥살리플라틴 전에 투여된다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 요법을 받았다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 인간은 달리 명시되지 않는 한 (NOS), 조직학적으로 확인된 미만성 거대 B-세포 림프종이 있거나, 또는 인간은 무통성 질환이 DLBCL로 전환된 병력이 있다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 하나의 선행 전신 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 예를 들어, 일부 경우, 인간은 이전에 자가 조혈모세포 이식 (HSCT)을 받은 적이 있다 (화학요법에 이은 공고 자가 HSCT는 한 차수의 요법으로 간주된다). 또 다른 예에서, 인간은 이전에 동종 HSCT를 받았고 인간은 더 이상 면역억제 요법을 받지 않고 있으며 활동성 이식편 대 숙주병(GVHD)이 없다 (화학요법에 이은 동종 HSCT는 한 차수의 요법으로 간주된다). 일부 구체예들에서, 인간은 선행 국소 요법, 예를 들어, 방사선요법을 받았다. 일부 구체예들에서, DLBCL은 재발성 또는 불응성이다. 일부 구체예들에서, 마지막 요법 완료 후 반응이 ≥ 6 개월 지속된 후 DLBCL이 재발하는 경우 이는 재발성이다. 일부 구체예들에서, DLBCL이 선행 요법 동안 진행하거나 또는 선행 요법 후 6 개월 이내 (< 6 개월) 진행하는 경우 이는 불응성이다. 일부 구체예들에서, 인간은 적어도 하나의 2차원적으로 측정가능한 병변, 예를 들어 컴퓨터 단층촬영(CT) 또는 자기공명영상(MRI)에 의해 측정된 가장 긴 치수가 1.5cm보다 큰 병변을 갖는다. 일부 구체예들에서, 인간은 0, 1, 또는 2의 동부 종양학 협력 그룹 (ECOG) 전신 활동도 점수를 가진다. 일부 구체예들에서, 인간은 자가 또는 동종 줄기 세포 이식 (SCT)이 예정되어 있지 않다. 일부 구체예들에서, 인간은 젬시타빈과 백금 기반 제제를 병용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 이상 반응에 대한 국립 암 연구소(National Cancer Institute) 공통 용어 기준, 버전 5.0에 따라 1등급보다 높은 말초 신경병증이 없다. 일부 구체예들에서, 인간은 1차 또는 2차 중추신경계 (CNS) 림프종이 없다. 일부 구체예들에서, 인간은 리히터 변환 또는 이전의 모세관 누출 증후군(CLL)이 없다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 전에 자가 조혈모세포 이식(HSCT) 대상이 아니다. 일부 구체예들에서, 인간은 DLBCL에 대한 적어도 2가지 선행 요법을 받았다. 일부 구체예들에서, 인간은 DLBCL에 대해 폴라투주맙 베도틴-피이크를 사용한 선행 요법을 받은 적이 없다. 일부 구체예들에서, 인간은 성인이다. 일부 구체예들에서, 성인 인간은 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종을 가진다.
일부 구체예들에서, 달리 명시되지 않는 한 (NOS), 미만성 거대 B-세포 림프종 (DLBCL) (예를 들어, 달리 명시되지 않는 한, 재발성 또는 불응성 미만성 거대 B-세포 림프종)은 독특한 임상 표현, 조직 형태, 신생물 세포 표현형, 및/또는 기타 DLBCL 하위유형들에 대한 병원체 관련 기준에 적합하지 않은 DLBCL을 지칭한다. DLBC NOS는 일반적으로 모든 DLBCL 사례의 약 80-85%를 나타내는 공격적인 질환이다. 표준 화학 요법으로 치료받은 DLBCL NOS 환자의 전체 장기 생존율은 약 65%이다. 예를 들어, Grimm 외 (2019) Annals of Diagnostic Pathology, 38:6-10를 참조하라.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 14일 이내에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 33% 미만 (예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 40% 미만 (예를 들어, 약 40% 미만, 약 39% 이하, 약 38% 이하, 약 37% 이하, 약 36% 이하, 약 35% 이하, 약 34% 이하, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 8% 미만 (예를 들어, 약 8%, 7%, 6%, 5%, 4%, 3%, 2%, 또는 1% 미만)의 인간이 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 6% 미만 (예를 들어, 약 6%, 5%, 4%, 3%, 2%, 또는 1% 미만)의 인간이 말초 신경병증을 경험하여, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료를 중단하게 된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 신경독성을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 신경독성을 인간에서 일으키지 않는다. 일부 구체예들에서, 신경독성은 감각 및/또는 운동 말초 신경병증을 지칭한다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여 시작 후 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상 동안 인간을 생존하게 한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 이러한 다수의 인간의 적어도 약 10 개월 이상, 적어도 약 11 개월 이상, 적어도 약 12 개월 이상, 적어도 약 13 개월 이상, 적어도 약 14 개월 이상, 또는 적어도 약 15 개월 이상의 전체 생존 중앙값을 초래한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 전체 생존 (OS) 시간을 증가시킨다. OS는 면역접합체, 항-CD20 항체, 및 하나 이상의 화학요법제의 최초 투여시로부터 임의의 원인으로 인한 사망이 발생한 시점까지 측정된다. 일부 구체예들에서, OS, 예를 들어, OS 중앙값은, 일, 주, 월, 또는 년 단위로 측정된다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, OS, 예를 들어, OS 중앙값을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. OS, 예를 들어, OS 중앙값은 해당 분야에 공지된 방법에 따라 추정될 수 있다. 일부 경우 OS, 예를 들어, OS 중앙값은 카플란-마이어 방법을 사용하여 추정된다. 일부 구체예들에서, 치료 효과의 추정치는 계층화된 Cox 비례 위험 분석(예를 들어, 95% 신뢰 한계 포함)을 사용하여 사망에 대한 위험 비율로 표현된다. 일부 구체예들에서, 브룩메이어-크로울리 방법론은 OS 중앙값에 대한 95% 신뢰 구간을 구성하는 데 사용된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 생존을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 전체 생존을 예를 들어, OS 중앙값을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 42% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 67% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 38% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 3.5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 전체 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 전체 생존율을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 1년 전체 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 1년시에 어떠한 원인으로도 사망하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 2년 전체 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 2년시에 어떠한 원인으로도 사망하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 3.5년 전체 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 3.5년시에 어떠한 원인으로도 사망하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 5년 전체 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 5년시에 어떠한 원인으로도 사망하지 않은 인간의 비율을 지칭한다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무진행 생존을 초래한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 무진행 생존 (PFS) 시간을 증가시킨다. 일부 구체예들에서, PFS는 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 1차 투여시부터 Lugano 2014 반응 기준 (Cheson 외, (2014) J Clin Oncol 32:3059-3068)에 따른 첫 번째 질환 진행 발생시, 또는 임의의 원인으로 인한 사망시까지로 측정된다. 일부 구체예들에서, PFS는, 일, 주, 월, 또는 년 단위로 측정된다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, PFS를, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, PFS는 카플란-마이어 방법을 사용하여 계산된다. 일부 구체예들에서, 치료 효과의 추정치는 계층화된 Cox 비례 위험 분석(예를 들어, 95% 신뢰 한계 포함)을 사용하여 위험 비율로 표현된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 무진행 생존을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여받은 상응하는 다수 인간의 무진행 생존 (예를 들어, 무진행 생존 중앙값)과 비교하여 상기 다수에서 인간의 무진행 생존 (예를 들어, 무진행 생존 중앙값)을 예를 들어, OS 중앙값을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 무진행 생존은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 1차 투여시부터 Lugano 2014 반응 기준에 따른 첫 번째 질환 질행 발생시 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반) 또는 임의의 원인으로 인한 사망시까지 측정된다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 1년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 63% 이상, 적어도 약 65% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 14% 이상, 적어도 약 15% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 5년 무진행 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무진행 생존율을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 1년 무진행 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 1년시에 Lugano 2014 반응 기준에 따른 질환 진행 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망이 발생하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 2년 무진행 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 2년시에 Lugano 2014 반응 기준에 따른 질환 진행 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망이 발생하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 3.5년 무진행 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 3.5년시에 Lugano 2014 반응 기준에 따른 질환 진행 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망이 발생하지 않은 인간의 비율을 지칭한다. 일부 구체예들에서, 5년 무진행 생존율은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여받은 다수의 인간 중 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴으로 치료 시작 후 5년시에 Lugano 2014 반응 기준에 따른 질환 진행 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망이 발생하지 않은 인간의 비율을 지칭한다.
일부 구체예들에서, OS 및 PFS는 HSCT를 받은 환자에서 평가된다.
일부 구체예들에서, 본원에 제공된 방법에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여에 대한 반응은 해당 분야에 공지된 임의의 방법으로 측정된다. 일부 구체예들에서, 본원에 제공된 방법에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여에 대한 반응은 양전자 방출 단층촬영(PET) 및/또는 컴퓨터 단층촬영(CT) 스캔으로 측정된다. 일부 구체예들에서, 본원에 제공된 방법에 따른 치료에 대한 반응은 2014 Lugano 기준 (Cheson 외, (2014) J Clin Oncol 32:3059-3068)을 사용하여 평가된다. 일부 구체예들에서, 본원에 제공된 방법에 따른 치료에 대한 반응은 치료 동안 또는 치료 종료 시에 평가된다. 일부 구체예들에서, 본원에 제공된 방법에 따른 치료에 대한 반응은 본원에 제공된 방법에 따른 치료의 투여 전 평가와 비교하여 환자에서 평가된다. 일부 구체예들에서, CT 스캔은 6개월마다 수행된다. 일부 구체예들에서, PET 스캔은 본원에 제공된 방법에 따라 치료 투여 전 및 종료 시에 수행된다. 일부 구체예들에서, PET 및/또는 CT (예를 들어, PET-CT) 스캔은 두개골 기저부에서 허벅지 중간까지 포함된다. 일부 구체예들에서, 전신 PET-CT 스캔이 수행된다. 일부 구체예들에서, CT 스캔에는 흉부, 목, 복부 및 골반 스캔이 포함되지만 이에 제한되지 않는 정맥내 조영이 포함된다. 일부 구체예들에서, 종양의 방사선학적 평가는 예를 들어 질환 진행 또는 재발이 의심되는 경우 수행된다. 일부 구체예들에서, 본원에 제공된 방법에 따른 치료에 대한 골 반응은 골수 생검을 사용하여 평가되며, 이는 해당 분야에 공지된 임의의 방법에 따라 수행될 수 있다. 일부 경우, PET-CT에서 골 신호가 음성인 환자에서 골수 생검이 수행된다. 일부 구체예들에서, PET-CT 및/또는 CT 스캔은 본원에 제공된 방법에 따른 치료의 투여 전에 그리고 본원에 제공된 방법에 따른 치료의 투여 동안 및 이후에 임상적으로 지시된 바와 같이 수득된다. 일부 구체예들에서, PET-CT 및/또는 CT 스캔은 본원에 제공된 방법에 따라 치료를 투여한 후 최대 2년 동안 수행된다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 완전 반응을 초래한다. 일부 구체예들에서, 완전 반응은 Lugano 2014 반응 기준에 따라 (Cheson 외, (2014) J Clin Oncol 32:3059-3068) PET-CT를 기반으로 한 완전한 대사 반응을 포함한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 완전 반응율 (CRR)을 증가시킨다. 일부 구체예들에서, CRR은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 이용한 치료 종료시, 예를 들어, Lugano 2014 반응 기준에 따라 양전자 방출 단층촬영 및 컴퓨터 단층촬영 (PET-CT) 분석에 기반하여 완전한 대사 반응에 도달한 환자들의 비율을 지칭한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, CRR을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, CRR은 PET 데이터를 포함하지 않고 결정된다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 완전 반응율 (CRR)을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 35% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 완전 반응율을 초래한다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 부분 반응을 초래한다. 일부 구체예들에서, 부분 반응은 Lugano 2014 반응 기준에 따라, PET CT 데이터를 포함하는 부분 대사 반응을 포함한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 객관적 반응율 (ORR)을 증가시킨다. 일부 구체예들에서, ORR은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 이용한 치료 종료시, 예를 들어, Lugano 2014 반응 기준에 따라 양전자 방출 단층촬영 및 컴퓨터 단층촬영 (PET-CT) 분석에 기반하여 완전한 또는 부분 대사 반응에 도달한 환자들의 비율을 지칭한다. 일부 구체예들에서, ORR은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 이용한 치료 종료시, 예를 들어, Lugano 2014 반응 기준에 따라 완전한 또는 부분 대사 반응에 도달한 환자들의 비율을 지칭한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, ORR을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, ORR은 PET 데이터를 포함하지 않고 결정된다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 객관적 반응율 (ORR)을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 객관적 반응율을 초래한다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 10% 이상, 적어도 약 20% 이상, 적어도 약 30% 이상, 적어도 약 40% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 부분 반응율을 초래한다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 부분 반응율을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 부분 반응율은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 이용한 치료 종료시, 예를 들어, Lugano 2014 반응 기준에 따라 양전자 방출 단층촬영 및 컴퓨터 단층촬영 (PET-CT) 분석에 기반하여 부분 대사 반응에 도달한 환자들의 비율을 지칭한다. 일부 구체예들에서, 부분 반응율은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 이용한 치료 종료시, 예를 들어, Lugano 2014 반응 기준에 따라 부분 대사 반응에 도달한 환자들의 비율을 지칭한다.
일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 최적의 전체 반응 (BOR) 비율을 증가시킨다. 일부 구체예들에서, BOR은, 예를 들어, Lugano 2014 반응 기준에 따라 양전자 방출 단층촬영 및 컴퓨터 단층촬영 (PET-CT) 또는 CT 분석에 기반하여, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)로 치료하는 동안 최적의 반응을 지칭한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, BOR의 비율을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 최적의 전체 반응율 (BOR)을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월, 적어도 약 5 개월, 적어도 약 6 개월, 적어도 약 7 개월, 적어도 약 8 개월, 적어도 9 개월, 적어도 약 10 개월, 적어도 약 11 개월, 적어도 약 12 개월, 적어도 약 13 개월, 적어도 약 14 개월, 적어도 약 15 개월, 적어도 약 16 개월, 적어도 약 17 개월, 적어도 약 18 개월, 적어도 약 19 개월, 적어도 약 20 개월, 적어도 약 21 개월, 적어도 약 22 개월, 적어도 약 23 개월, 적어도 약 24 개월, 또는 적어도 약 25 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 4 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 6 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 9.5 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 11 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴으로 치료 시작 후 적어도 약 14 개월 동안 인간의 무사건 생존을 초래한다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 무사건 생존 (EFSeff) 시간을 증가시킨다. 일부 구체예들에서, EFSeff는 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 1차 투여시부터 임의의 질환 진행 또는 재발, 임의의 원인으로 인한 사망, 또는 또 다른 항-림프종 치료 개시의 발생시까지의 시간을 지칭한다. 일부 구체예들에서, EFSeff는, 일, 주, 월, 또는 년 단위로 측정된다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, EFSeff을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, (예를 들어, 상기 기재된) PFS 분석에 사용되는 방법들을 사용하여 EFSeff를 분석한다. 일부 구체예들에서, 무사건 생존은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 1차 투여시부터 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반); (ii) 임의의 원인으로 인한 사망; 또는 (iii) 새로운 항-림프종 치료 (NALT) 개시의 발생시까지의 시간으로 측정된다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 상응하는 인간에게 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하는 것과 비교하여 인간의 무사건 생존을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 상기 다수에서 인간의 무사건 생존을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 전술한 구체예들 중 어느 하나와 조합될 수 있는 일부 구체예들에서, 다수의 인간에 대한 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 이러한 다수의 인간 중 적어도 약 44% 이상, 적어도 약 45% 이상, 적어도 약 50% 이상, 적어도 약 60% 이상, 적어도 약 70% 이상, 적어도 약 80% 이상, 적어도 약 90% 이상, 적어도 약 95% 이상, 또는 약 100%의 2년 무사건 생존율을 초래한다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 상응하는 다수의 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 1년, 2년, 3.5년, 또는 5년 무사건 생존율을 예를 들어, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, 1년 무사건 생존율은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여받은 다수의 인간들에서 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료 시작 후 1년시에 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), (ii) 임의의 원인으로 인한 사망, 또는 (iii) 새로운 항-림프종 치료 (NALT)의 개시가 발생하지 않는 인간의 비율을 지칭한다. 일부 구체예들에서, 2년 무사건 생존율은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여받은 다수의 인간들에서 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료 시작 후 2년시에 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), (ii) 임의의 원인으로 인한 사망, 또는 (iii) 새로운 항-림프종 치료 (NALT)의 개시가 발생하지 않는 인간의 비율을 지칭한다. 일부 구체예들에서, 3.5년 무사건 생존율은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여받은 다수의 인간들에서 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료 시작 후 3.5년시에 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), (ii) 임의의 원인으로 인한 사망, 또는 (iii) 새로운 항-림프종 치료 (NALT)의 개시가 발생하지 않는 인간의 비율을 지칭한다. 일부 구체예들에서, 5년 무사건 생존율은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여받은 다수의 인간들에서 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료 시작 후 5년시에 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), (ii) 임의의 원인으로 인한 사망, 또는 (iii) 새로운 항-림프종 치료 (NALT)의 개시가 발생하지 않는 인간의 비율을 지칭한다.
일부 구체예들에서, 무사건 생존은 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 1차 투여시부터, 또는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 치료 시작시부터 (i) 질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반); (ii) 임의의 원인으로 인한 사망; 또는 (iii) 새로운 항-림프종 치료 (NALT) 개시의 발생시까지의 시간으로 측정된다.
일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해 반응 기간 (DOR)의 시간을 증가시킨다. 일부 구체예들에서, DOR은 Lugano 2014 기준을 사용하여 객관적 반응이 있는, 본원에 제공된 방법에 따른 치료를 투여받은 환자에서 완전 또는 부분 반응의 최초 발생 일자부터 진행성 질환 또는 사망이 발생한 최초 일자까지로 측정된다. 일부 구체예들에서, DOR은 일, 주, 월, 또는 년 단위로 측정된다. 일부 구체예들에서, 본원에 제공된 방법들에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 투여는, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여에 비해, DOR을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다. 일부 구체예들에서, (예를 들어, 상기 기재된) PFS 분석에 사용되는 방법들을 사용하여 DOR을 분석하지만, DOR 분석은 계층화되지 않는다. 일부 구체예들에서, 다수의 인간에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 상응하는 인간에게 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하는 것과 비교하여 반응 기간 (DOR)을, 적어도 약 1.1 배, 적어도 약 1.5 배, 적어도 약 2 배, 적어도 약 2.5 배, 적어도 약 3 배, 적어도 약 3.5 배, 적어도 약 4 배, 적어도 약 4.5 배, 적어도 약 5 배, 적어도 약 5.5 배, 또는 적어도 약 6 배, 또는 그 이상 증가시킨다.
일부 구체예들에서, 본원에 제공된 방법에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료에 대한 반응을 환자 보고 결과 (PRO) 도구를 사용하여 평가한다. PRO 도구의 예에는, 제한 없이, FACT/GOG-Ntx12 신경병증 (Kopec 외, (2006) J Supportive Oncol, 4:W1-W8; Calhoun 외, (2003) Int J Gynecol Cancer, 13:741-748), EQ-5D-5L (EuroQol (1990) Health Policy, 16:199-208; Brooks (1996) Health Policy, 37:53-72; Herdman 외, (2011) 20:1727-1736; Janssen 외, (2013) Qual Life Res, 22:1717-1727; http://www(dot)euroqol(dot)org/about-eq-5d/valuation-of-eq-5d; Devlin 외, (2017) Health Economics, 1-16), EORTC QLQ-C30 (Aaronson 외, (1993) J Natl Cancer Inst, 85:365-376; Fitzsimmons 외, (1999) 35:939-941), 및 FACT/Lym (Cella 외, (1993) J Clin ONcol, 11:570-579; Cella 외, (2005) Blood, 106:750; Carter 외, (2008) Blood, 112:2376; Hlubocky 외, (2013) Lymphoma, ID147176; Webster 외, (2003) Health Qual Life Outcomes, 1:79)가 포함된다.
일부 구체예들에서, 본원에 제공된 방법에 따른 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 투여 후 이상 반응은 미국 국립 암 연구소 이상 반응 표준 용어 기준, 버전 5 (NCI CTCAE v5.0), 암 요법/부인과 종양 그룹의 기능적 평가-신경독성 12-문항 척도 (FACT/GOG-Ntx12), 임상 실험실 검사 결과, 심전도 (ECG), 및/또는 활력 징후에 따라 평가된다. 일부 구체예들에서, 치료 철회를 초래하는 이상 반응, 용량 감소 또는 중단을 초래하는 이상 반응, 등급 3의 이상 반응, 사망을 초래하는 이상 반응, 심각한 이상 반응, 및/또는 특정한 관심 이상 반응을 분석한다. 일부 구체예들에서, 본원에 제공된 이상 반응은 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및/또는 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)에 대한 노출과 관련하여 분석된다.
일부 구체예들에서, 본원에 제공된 방법에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자들에서 말초 신경병증의 발생을 FACT/GOG-Ntx12 점수 및/또는 NCI CTCAE v5.0으로 평가한다. 말초 신경병증(감각 및/또는 운동)의 증상에는 감각 저하, 감각 과민, 이상감각, 감각 이상, 불편함, 작열감, 쇠약, 보행 장애 또는 신경병증 통증이 포함되지만 이에 제한되지 않는다. 일부 구체예들에서, 예를 들어, 이상 반응 분석에 기반한 말초 신경병증의 발생율이 계산된다. 일부 구체예들에서, 말초 신경병증이 발생한 모든 환자는 본원에 제공된 방법에 따른 치료 종료 후 해소 또는 안정화시까지 추적 관찰된다. 일부 구체예들에서, 본원에 제공된 방법들에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자들의 50% 미만 (예를 들어, 약 50%, 45%, 40%, 35%, 34%, 33%, 32%, 31%, 30%, 29%, 28%, 27%, 26%, 25%, 24%, 23%, 22%, 21%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 또는 0.5% 미만)은 14 일 이내 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1일 이내) ≤ 1등급으로 해소되지 않는 ≥ 3등급 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 본원에 제공된 방법들에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자들의 40% 미만은 14 일 이내 ≤ 1등급으로 해소되지 않는 ≥ 3등급 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 본원에 제공된 방법들에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자들의 33% 미만은 14 일 이내 ≤ 1등급으로 해소되지 않는 ≥ 3등급 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 본원에 제공된 방법들에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자들의 30% 미만은 14 일 이내 ≤ 1등급으로 해소되지 않는 ≥ 3등급 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여는 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 인간에서 일으키지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하지 않는다. 일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 투여 후, 인간은 4등급 이상 (예를 들어, 4등급 이상, 또는 5등급 이상)의 신경독성을 경험하지 않는다. 일부 구체예들에서, 신경독성은 감각 및/또는 운동 말초 신경병증을 지칭한다. 일부 구체예들에서, 다수의 인간들에게, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면, 이러한 다수의 인간들 중 약 33% 미만 (예를 들어, 약 33% 이하, 약 32% 이하, 약 31% 이하, 약 30% 이하, 약 29% 이하, 약 28% 이하, 약 27% 이하, 약 26% 이하, 약 25% 이하, 약 24% 이하, 약 23% 이하, 약 22% 이하, 약 21% 이하, 약 20% 이하, 약 19% 이하, 약 18% 이하, 약 17% 이하, 약 16% 이하, 약 15% 이하, 약 14% 이하, 약 13% 이하, 약 12% 이하, 약 11% 이하, 약 10% 이하, 약 9% 이하, 약 8% 이하, 약 7% 이하, 약 6% 이하, 약 5% 이하, 약 4% 이하, 약 3% 이하, 약 2% 이하, 약 1% 이하, 또는 약 0.5% 이하)이 14 일 이내에 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내에) 1등급 이하로 해소되지 않는 3 등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험하게 된다. 일부 구체예들에서, 다수의 인간들에게 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하면 이러한 다수 중 약 40% 미만 (예를 들어, 약 40%, 35%, 34%, 33%, 32%, 31%, 30%, 29%, 28%, 27%, 26%, 25%, 24%, 23%, 22%, 21%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 또는 0.5% 미만)의 인간이 14 일 이내 (예를 들어, 14 일, 13 일, 12 일, 11 일, 10 일, 9 일, 8 일, 7 일, 6 일, 5 일, 4 일, 3 일, 2 일, 또는 1 일 이내)에 1등급 이하로 해소되지 않는 3등급 이상 (예를 들어, 3등급 이상, 4등급 이상, 또는 5등급 이상)의 말초 신경병증을 경험한다. 특정 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴은 적어도 4회의 21일 사이클 동안 투여되었다.
일부 구체예들에서, 약물-유발 간 손상의 발생이 평가된다.
일부 구체예들에서, 본원에 제공된 방법에 따라 투여될 때 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)의 면역원성이 평가된다. 일부 구체예들에서, 본원에 제공된 방법에 따라 투여될 때 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크)의 면역원성은 면역접합체에 대한 항-약물 항체(ADA)를 측정함으로써 평가된다. 일부 구체예들에서, ADA는 환자 혈청 샘플에서 검증된 항체-가교 효소-결합 면역흡착 분석(ELISA)을 사용하여 측정된다.
일부 구체예들에서, 본원에 제공된 방법에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자에서 이상 반응의 발생율은 적어도 1회의 21일 치료 사이클이 완료된 후 평가된다. 일부 구체예들에서, 본원에 제공된 방법에 따라 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여받은 환자에서 이상 반응의 발생율은 적어도 2회의 21일 치료 사이클이 완료된 후 평가된다.
일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및/또는 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 용량은 이상 반응의 발생에 따라 변경된다. 일부 구체예들에서, 이상 반응은 한 사이클의 1일차에 주입 전 72시간 이내에 얻은 실험실 검사 결과에 기반한다. 특정 구체예들에서, 증상들은 미국 국립 암 연구소 이상 반응 표준 용어 기준, 버전 5 (NCI CTCAE v5.0)에 따라 등급화된다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 호중구 감소증을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 호중구 감소증에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 호중구 감소증에 대한 예방 치료는 G-CSF, 예를 들어, 각 치료 사이클에서 G-CSF의 투여를 포함한다. 일부 구체예들에서, 3 또는 4등급등급 호중구 감소증이 발생하는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)의 치료는 절대 호중구 수 (ANC)가 >1000/μL로 회복될 때까지 보류된다. 일부 구체예들에서, 호중구 감소증을 관리하기 위해 필요한 경우 성장 인자(예를 들어, G-CSF)가 투여된다. 예를 들어, Smith 외 (2016) J Clin Oncol, 24:3187-205를 참조하라. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는, ANC가 7일차 또는 그 이전에 인간에서 > 1000/μL로 회복되는 경우 추가 용량 감소 없이 재개된다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크의 용량은, ANC가 7일차 이후 인간에서 > 1000/μL로 회복되는 경우 1.4 mg/kg까지 감소된다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크의 선행 용량 감소가 있었던 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 3 또는 4등급등급 혈소판감소증이 발생한 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 혈소판이 > 75,000/μL로 회복될 때까지 보류된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는, 혈소판이 7일차 또는 그 이전에 > 75,000/μL로 회복되는 경우 추가 용량 감소 없이 재개된다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크의 용량은, 혈소판이 7일차 이후 > 75,000/μL로 회복되는 경우 1.4 mg/kg로 감소된다. 일부 구체예들에서, 폴라투주맙 베도틴-피이크의 선행 용량 감소가 있었던 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 2등급 또는 3등급 말초 신경병증이 발생한 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 ≤ 1등급으로 개선될 때까지 지연된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는, 2등급 또는 3등급 말초 신경병증이 ≤ 14 일 이내에 등급 ≤ 1로 회복되는 경우, 영구적으로 감소된 1.4 mg/kg 용량의 폴라투주맙 베도틴-피이크 및 75 mg/m2 용량의 옥살리플라틴으로 재시작된다. 일부 구체예들에서, 환자가 이전에 2등급 말초 신경병증이 있었던 경우 2등급 또는 3등급 말초 신경병증이 14일차 또는 그 이전에 등급 ≤ 1로 회복되지 않는 경우 및/또는 이전에 용량을 폴라투주맙 베도틴-피이크를 1.4 mg/kg으로 또는 옥살리플라틴을 75 mg/m2으로 감소시켰던 경우, 폴라투주맙 베도틴-피이크 단독 치료는 중단된다. 일부 구체예들에서, 대상체에게 이전에 3등급 말초 신경병증이 있었던 경우 치료는 중단된다. 일부 구체예들에서, 2등급 또는 3등급 말초 신경병증이 > 14 일차까지 또는 예정된 다음 사이클 일자 이후까지 ≤ 1등급으로 회복되지 않는 경우 옥살리플라틴 및 폴라투주맙 베도틴-피이크는 영구적으로 중단된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 4등급 말초 신경병증이 발생하는 경우 중단된다.
일부 구체예들에서, 인후두 감각 이상이 발생하는 경우, 옥살리플라틴 주입은 6시간까지 연장된다.
일부 구체예들에서, 1-2등급 주입 관련 반응(IRR)이 발생하면 주입의 속도를 늦추거나 이를 보류한다. 일부 구체예들에서, 대상체들은 지지 치료를 받는다. 일부 구체예들에서, 지지 치료에는 아세트아미노펜/파라세타몰 및 항히스타민제(예를 들어, 디펜히드라민 및/또는 정맥내 식염수)가 포함된다. 일부 구체예들에서, 기관지 경련, 두드러기 또는 호흡곤란에 대한 지지 치료에는 항히스타민제, 산소, 코르티코스테로이드(예를 들어, 100mg IV 프레드니솔론 또는 등가물) 및/또는 기관지 확장제가 포함된다. 일부 구체예들에서, 증상이 해소되면 주입 속도 상승이 재개된다. 일부 구체예들에서, 재개시 후 주입 속도 상승에 있어서, 증상이 완전히 해소되었을 때 중단 전에 달성된 속도의 50%로 주입을 재개한다. 일부 구체예들에서, 주입 관련 증상이 없는 경우 주입 속도는 30분 마다 50 mg/시간의 증가분으로 상승된다. 일부 구체예들에서, 1-2등급 IRR이 발생한 경우, 폴라투주맙 베도틴은 다음 사이클에서 90분에 걸쳐 주입된다. 일부 구체예들에서, 주입 관련 반응이 발생하지 않으면 폴라투주맙 베도틴의 후속 주입이 30분에 걸쳐 투여된다. 일부 구체예들에서, 모든 사이클에서 사전투약을 투여한다. 일부 구체예들에서, 천명이나 두드러기 증상이 재발되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 3등급 IRR이 발생한 경우, 주입은 중단된다. 일부 구체예들에서, 대상체들은 지지 치료를 받는다. 일부 구체예들에서, 지지 치료에는 아세트아미노펜/파라세타몰 및 항히스타민제(예를 들어, 디펜히드라민 및/또는 정맥내 식염수)가 포함된다. 일부 구체예들에서, 기관지 경련, 두드러기 또는 호흡곤란에 대한 지지 치료에는 항히스타민제, 산소, 코르티코스테로이드(예를 들어, 100mg IV 프레드니솔론 또는 등가물) 및/또는 기관지 확장제가 포함된다. 일부 구체예들에서, 증상이 해소되면 주입 속도 상승이 재개된다. 일부 구체예들에서, 재개시 후 주입 속도 상승에 있어서, 증상이 완전히 해소되었을 때 중단 전에 달성된 속도의 50%로 주입을 재개한다. 일부 구체예들에서, 주입 관련 증상이 없는 경우 주입 속도는 30분 마다 50 mg/시간의 증가분으로 상승된다. 일부 구체예들에서, 동일한 이상 반응이 동일한 중증도로 재발되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 4등급 IRR이 발생하는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 총 빌리루빈 > 3.0 mg/dL이 관찰되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 ≤ 14 일 이내에 ≤ 1.5 mg/dL로 해소될 때까지 지연된다. 일부 구체예들에서, 담즙정체, 황달 또는 간 기능 장애의 징후가 없고 다른 기여 요인(예를 들어, 전이성 질환의 악화 또는 공지의 간독성 물질 또는 보고된 감염 병인에 대한 동시 노출)이 없이, 간 트랜스아미나제 > 3 x 기준선의 간 트랜스아미나제 증가 및 >2 x ULN의 직접 빌리루빈 증가가 관찰되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 종양 용해 증후군을 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 종양 용해 증후군에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 예방적 치료는 예를 들어, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 약 1일 또는 2일 전에 시작하는 수액, 예를 들어, 1일 3리터의 체액을 포함한다. 일부 구체예들에서, 예방적 치료는 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 약 48 내지 약 72시간 전에 시작하는 알로퓨리놀(예를 들어, 300mg/일 경구) 또는 적합한 대체 치료(예를 들어, 라스부리카제)를 포함한다. 일부 구체예들에서, 예방적 치료는 예를 들어, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴을 투여하기 약 1 또는 2일 전에 시작하는 수액, 예를 들어, 1일 3리터의 체액; 및 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 투여하기 약 48 내지 약 72시간 전에 시작하는 알로퓨리놀(예를 들어, 300mg/일 경구) 또는 적합한 대체 치료(예를 들어, 라스부리카제)를 포함한다. 일부 구체예들에서, 인간에게 종양 용해 증후군의 위험이 있는 경우, 예를 들어 인간에게 높은 종양 부하가 있는 경우(예를 들어, 림프구 수 ≥ 25 × 109/L 또는 부피가 큰 림프절병증) 종양 용해 증후군에 대한 예방적 치료가 인간에게 투여된다. 일부 구체예들에서, 종양 용해 증후군에 대한 예방적 치료는 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴 각각의 투여 전에 투여된다. 일부 구체예들에서, 3 또는 4등급등급 종양 용해 증후군 (TLS)이 발생하는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 보류된다. 일부 구체예들에서, 다음 투약은 최대 14일 동안 지연된다. 일부 구체예들에서, TLS이 완전히 해소되면, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 예방 요법과 함께 다음 예정된 주입 동안 총 용량(full dose)으로 재개된다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 감염을 일으키지 않는다. 일부 구체예들에서, 감염은 폐포자충 감염 또는 헤르페스 바이러스 감염이다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 감염에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, 감염에 대한 예방적 치료는 하나 이상의 적합한 항바이러스 약물을 포함한다. 일부 구체예들에서, 인간에게 B형 간염 재활성화를 위한 예방적 치료가, 예를 들어, Flowers 외, 2013; National Comprehensive Cancer Network (NCCN) 2017에 기재된 바와 같이 투여된다.
일부 구체예들에서, 3 또는 4등급의 비혈액학적 독성(탈모, 구역, 구토 제외)이 발생한 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 최대 14일 동안 지연된다. 일부 구체예들에서, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는, 등급 ≤ 1 또는 기준선으로의 개선이 관찰되는 경우 감소된 용량으로 또는 총 용량으로 재개된다.
일부 구체예들에서, 2등급의 비혈액학적 독성이 발생한 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 최대 14일 동안 지연된다. 일부 구체예들에서, 등급 ≤ 1 또는 기준선으로의 개선이 관찰되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료에 관한 이전의 용량들이 투여된다.
일부 구체예들에서, 1등급의 비혈액학적 독성이 발생한 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 변경되지 않는다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈, 및 옥살리플라틴의 투여는 인간에서 B형 간염 재활성화를 일으키지 않는다. 일부 구체예들에서, 본원에 제공된 방법은 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴을 인간에게 투여하기 전, 투여하는 동안 및/또는 투여한 후에 인간에게 B형 간염 재활성화에 대한 예방적 치료를 투여하는 것을 추가로 포함한다. 일부 구체예들에서, B형 간염 재활성화를 위한 예방적 치료는 예를 들어, Flowers 외, 2013; National Comprehensive Cancer Network (NCCN) 2017에 기재된 바와 같은 항-바이러스 약물을 포함한다. 일부 구체예들에서, 본원에 제공된 방법은 B형 간염 재활성화가 인간에서 검출되는 경우 항바이러스 약물, 예를 들어, 적합한 뉴클레오시드 유사체를 인간에게 투여하는 것을 추가로 포함한다. 일부 구체예들에서, B형 간염 재활성화는 새로운 검출 가능한 HBV-DNA 수준에 의해 결정된다. 일부 구체예들에서, HBV-DNA 수준이 세계보건기구(WHO) 권장 범위인 29IU/mL~100IU/mL 사이인 경우 2주 이내에 HBV-DNA 수준을 재검사한다. 일부 구체예들에서, HBV-DNA 수준이 양성인 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 보류되고 대상체는 뉴클레오시드 유사체로 치료된다. 일부 구체예들에서, > 100 IU/mL의 WHO-권장 컷오프의 HBV-DNA 수준이 관찰되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 보류되고 뉴클레오시드 유사체가 투여된다. 일부 구체예들에서, 적절한 항바이러스 요법을 받는 동안 증가하는 HBV-DNA 바이러스 부하(100IU/mL 초과)가 관찰되는 경우, 면역접합체 (예를 들어, 폴라투주맙 베도틴-피이크), 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴) 치료는 중단된다.
일부 구체예들에서, 면역접합체, 리툭시맙, 젬시타빈 및 옥살리플라틴의 투여는 약물-유발 간 손상, 진행성 다초점 백질뇌병증, 전신 과민 반응, 아나필락시스 반응, 아나필락시양 반응, 및 2차 악성 종양으로 구성된 그룹에서 선택된 하나 이상의 이상 반응을 일으키지 않는다. 일부 구체예들에서, 약물-유발 간 손상은 인간에서 Hy의 법칙에 의해 정의된 바와 같이 빌리루빈 상승 또는 임상 황달과 함께 ALT 또는 AST 상승을 포함한다. 일부 구체예들에서, 약물-유발 간 손상은 인간에서 치료시 발생하는 ALT 또는 AST > 3 x 기준선 값과 함께 총 빌리루빈 > 2 x ULN (이들 중 + 35%는 직접 빌리루빈임)을 포함한다. 일부 구체예들에서, 약물-유발 간 손상은 인간에서 치료시 발생하는 ALT 또는 AST > 3 x 기준선 값과 함께 임상 황달을 포함한다. 일부 구체예들에서, 전신 과민 반응, 아나필락시스 반응 및 아나필락시양 반응은 Sampson의 기준을 사용하여 평가된다.
치료를 필요로 하는 개체 (인간 개체)에서 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL)을 치료하는 방법에 사용하기 위한, 다음 화학식을 포함하는 면역접합체가 제공되며,
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다. 일부 구체예들에서, 면역접합체는 본원에 제공된 방법에 따라 사용하기 위한 것이다. 일부 구체예들에서, 면역접합체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
또한 치료를 필요로 하는 개체 (인간 개체)에서 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL)을 치료하기 위한 약제의 제조에서, 다음 화학식을 포함하는 면역접합체의 용도가 제공되며
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이고, 이때 약제는 항-CD20 항체 (예를 들어, 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)와 병용 투여하기 위한 것이다 (예를 들어, 이를 위해 제제화된다). 일부 구체예들에서, 약제 (즉, 면역접합체를 포함하는 약제)는 본원에 기재된 방법에서 사용하기 위한 것이다. 일부 구체예들에서, 면역접합체는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
치료를 필요로 하는 개체 (인간 개체)의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL)을 치료하는 방법에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체가 제공되며,
이때 Ab는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 항-CD79b 항체이고, 그리고 이때 p는 2 내지 5이고, 상기 방법은 개체에게 유효량의 (a) 면역접합체, (b) 리툭시맙 (c) 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)를 투여하는 것을 포함하고, 이때 면역접합체는 약 1.4 내지 약 1.8 mg/kg의 용량으로 투여되고, 리툭시맙은 375 mg/m2의 용량으로 투여되고, 및 하나 이상의 화학요법제는 50-2000 mg/m2의 용량으로 투여된다 (예를 들어, 젬시타빈은 1000 mg/m2의 용량으로 투여되고 옥살리플라틴은 100 mg/m2의 용량으로 투여된다). 일부 구체예들에서, 면역접합체는 본원에 기재된 방법에 따라 사용하기 위한 것이다. 일부 구체예들에서, p는 3 내지 4이다. 일부 구체예들에서, p는 3.5이다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
또한 치료를 필요로 하는 개체 (인간 개체)의 미만성 거대 B-세포 림프종 (DLBCL, 예를 들어, 재발성/불응성 DLBCL)을 치료하기 위한 약제의 제조에서 사용하기 위한, 다음 화학식을 포함하는 면역접합체가 제공되며
이때 Ab는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 항-CD79b 항체이고, 그리고 이때 p는 2 내지 5이고, 이때 상기 약제는 리툭시맙, 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)와 병용하여 투여하기 위한 것이며 (예를 들어, 이를 위해 제제화되며), 이때 약제는 약 1.4 내지 약 1.8 mg/kg 용량의 면역접합체 투여를 위하여 제제화되고, 리툭시맙은 375 mg/m2 용량의 투여를 위한 것이고, 및 하나 이상의 화학요법제는 50-2000 mg/m2 용량의 투여를 위한 것이다 (예를 들어, 젬시타빈은 1000 mg/m2 용량으로 투여 및 옥살리플라틴은 100 mg/m2 용량으로 투여). 일부 구체예들에서, 약제 (즉, 면역접합체를 포함하는 약제)는 본원에 기재된 방법에 따라 사용하기 위한 것이다. 일부 구체예들에서, p는 3 내지 4이다. 일부 구체예들에서, p는 3.5이다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크이다.
IV. 항-CD79b 항체 및 약물 / 세포독성제를 포함하는 면역접합체 (“항-CD79b 면역접합체”)
일부 구체예들에서, 항-CD79b 면역접합체는 암 세포 (예를 들어, 미만성 거대 B-세포 림프종 (DLBCL) 세포)를 표적하는 항-CD79b 항체 (Ab), 약물 모이어티 (D), 및 Ab를 D에 부착시키는 링커 모이어티 (L)를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 하나 이상의 아미노산 잔기, 예를 들어, 리신 및/또는 시스테인을 통해 링커 모이어티 (L)에 부착된다. 일부 구체예들에서, 면역접합체는 화학식 Ab-(L-D)p를 포함하고, 이때: (a) Ab는 항-CD79b 항체이고; (b) L은 링커이고; (c) D는 세포독성제이고; 그리고 (d) p는 1-8 범위이다.
예시적인 항-CD79b 면역접합체는 다음 화학식 I을 포함한다:
Ab-(L-D)p
이때 p는 1 내지 약 20 (예를 들어, 1 내지 15, 1 내지 10, 1 내지 8, 2 내지 5, 또는 3 내지 4)이다. 일부 구체예들에서, 항-CD79b 항체에 접합될 수 있는 약물 모이어티의 수는 유리 시스테인 잔기의 수에 의해 제한된다. 일부 구체예들에서, 유리 시스테인 잔기는 본원의 다른 곳에서 기술된 방법에 의해 항체 아미노산 서열 내로 도입된다. 화학식 I의 예시적인 항-CD79b 면역접합체는 1, 2, 3 또는 4개의 조작된 시스테인 아미노산을 포함하는 항-CD79b 항체를 포함하지만 이에 제한되지는 않는다 (Lyon, R. 외 (2012) Methods in Enzym. 502:123-138). 일부 구체예들에서, 하나 이상의 유리 시스테인 잔기가 조작 없이 항-CD79b 항체에 이미 존재하며, 이 경우 기존의 유리 시스테인 잔기를 사용하여 항-CD79b 항체를 약물/세포독성제에 접합시킬 수 있다. 일부 구체예들에서, 항-CD79b 항체는 하나 이상의 유리 시스테인 잔기를 생성하기 위해 약물/세포독성제에 항체가 접합하기 이전에 환원 조건에 노출된다.
A. 예시적인 링커
“링커”(L)는 하나 이상의 약물 모이어티 (D)를 항-CD79b 항체 (Ab)에 연결하여 화학식 I의 항-CD79b 면역접합체를 형성하는데 사용될 수 있는 이작용기 또는 다작용기 모이어티이다. 일부 구체예들에서, 항-CD79b 면역접합체는 약물 및 항-CD79b 항체에 공유 부착하기 위한 반응성 기능을 갖는 링커를 사용하여 제조될 수 있다. 예를 들어, 일부 구체예들에서, 항-CD79b 항체 (Ab)의 시스테인 티올은 링커 또는 약물-링커 중간체의 반응성 작용기와 결합을 형성하여 항-CD79b 면역접합체를 만들 수 있다.
한 양상에서, 링커는 항-CD79b 항체에 존재하는 유리 시스테인과 반응하여 공유 결합을 형성할 수 있는 작용기를 갖는다. 예시적인 반응성 작용기는 예를 들어 말레이미드, 할로아세트아미드, a-할로아세틸, 활성화된 에스테르, 예컨대 숙신이미드 에스테르, 4-니트로페닐 에스테르, 펜타플루오로페닐 에스테르, 테트라플루오로페닐 에스테르, 무수물, 산 염화물, 술포닐 클로라이드, 이소시아네이트, 이소티오시아네이트를 포함하나 이에 제한되지는 않는다. 예를 들어, Klussman, 외 (2004), Bioconjugate Chemistry 15(4):765-773의 766 페이지의 접합 방법, 및 이 문헌의 실시예를 참고하라.
일부 구체예들에서, 링커는 항-CD79b 항체 상에 존재하는 친전자성 그룹과 반응할 수 있는 작용기를 갖는다. 예시적인 친전자성 그룹은 제한 없이, 예를 들어, 알데히드 및 케톤 카르보닐 그룹을 포함한다. 일부 구체예들에서, 링커의 반응성 작용기의 헤테로원자는 항체의 친전자성 그룹과 반응하여 항체 단위에 공유 결합을 형성할 수 있다. 예시적인 반응성 작용기는 예를 들어, 하이드라지드, 옥심, 아미노, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트 및 아릴하이드라지드를 포함하지만 이에 제한되지는 않는다.
일부 구체예들에서, 링커는 하나 이상의 링커 성분들을 포함한다. 예시적인 링커 성분은 예를 들어, 6-말레이미도카프로일 (“MC”), 말레이미도프로파노일 (“MP”), 발린-시트룰린 (“val-cit” 또는 “vc”), 알라닌-페닐알라닌 (“ala-phe”), p -아미노벤질옥시카르보닐 (“PAB”), N-숙신이미딜 4-(2-피리딜티오) 펜타노에이트 (“SPP”), 및 4-(N-말레이미도메틸) 사이클로헥산-1 카르복실레이트 (“MCC”)를 포함한다. 다양한 링커 성분이 해당 분야에 공지되어 있으며, 그 중 일부는 아래 기재되어 있다.
일부 구체예들에서, 링커는 약물의 방출을 촉진하는 “절단가능한 링커”이다. 비제한적인 예시적 절단가능한 링커는 산-불안정성 링커 (예를 들어, 하이드라존 포함), 프로테아제-민감성 (예를 들어, 펩티다제-민감성) 링커, 광불안정성 링커, 또는 이황화물-함유 링커를 포함한다 (Chari 외, Cancer Research 52:127-131 (1992); US 5208020).
특정 구체예들에서, 링커 (L)은 다음 화학식 II를 가지며:
이때 A는 “스트레처 단위”이고, a는 0 내지 1의 정수이고; W는 “아미노산 단위”이고, w는 0 내지 12의 정수이고; Y는 “스페이서 단위”이고, y는 0, 1 또는 2이고; Ab, D, 및 p는 상기 화학식 I에서와 같이 정의된다. 이러한 링커의 예시적인 구체예들은 미국 특허 7,498,298에 기재되어 있으며, 이 문헌은 본원에 명시적으로 참고로 포함된다.
일부 구체예들에서, 링커 성분은 항체를 다른 링커 성분 또는 약물 모이어티에 연결하는 “스트레처 단위”를 포함한다. 비제한적인 예시적인 스트레처 단위가 아래에 제시되어 있다 (여기서 물결선은 항체, 약물 또는 추가 링커 성분에 대한 공유 부착 부위를 나타낸다):
일부 구체예들에서, 링커 성분은 “아미노산 단위”를 포함한다. 일부 이러한 구체예에서, 아미노산 단위는 프로테아제에 의한 링커의 절단을 허용함으로써, 리소좀 효소와 같은 세포내 프로테아제에 노출시 항-CD79b 면역접합체로부터 약물/세포독성제의 방출을 촉진시킨다 (Doronina 외, (2003) Nat. Biotechnol. 21:778-784). 예시적인 아미노산 단위는 디펩티드, 트리펩티드, 테트라펩티드, 및 펜타펩티드를 포함하지만 이에 제한되지 않는다. 예시적인 디펩티드에는 발린-시트룰린 (vc 또는 val-cit), 알라닌-페닐알라닌 (af 또는 ala-phe); 페닐알라닌-리신 (fk 또는 phe-lys); 페닐알라닌-호모리신 (phe-homolys); 및 N-메틸-발린-시트룰린 (Me-val-cit)이 포함되나 이에 제한되는 것은 아니다. 예시적인 트리펩티드에는 글리신-발린-시트룰린 (gly-val-cit) 및 글리신-글리신-글리신 (gly-gly-gly)이 포함되지만 이에 제한되는 것은 아니다. 아미노산 단위는 천연적으로 발생하는 아미노산 잔기 및/또는 소수 아미노산 및/또는 비-천연 발생 아미노산 유사체, 예를 들어, 시트룰린을 포함할 수 있다. 아미노산 단위는 특정 효소, 예를 들어 종양 관련 프로테아제, 카텝신 B, C 및 D, 또는 플라스민 프로테아제에 의한 효소적 절단을 위해 설계 및 최적화될 수 있다.
일부 구체예들에서, 링커 성분은 항체를 약물 모이어티에 직접적으로 또는 스트레처 단위 및/또는 아미노산 단위를 통해 연결하는 “스페이서” 단위를 포함한다. 스페이서 단위는 “자기-희생” 또는 “비-자기-희생” 일 수 있다. “비-자기 희생” 스페이서 단위는 ADC의 절단 시 스페이서 단위의 일부 또는 전부가 약물 모이어티에 결합된 채로 남아 있는 것이다. 비-자기 희생 스페이서 단위의 예는 글리신 스페이서 단위 및 글리신-글리신 스페이서 단위를 포함하지만 이에 제한되지 않는다. 일부 구체예들에서, 종양 세포 관련 프로테아제에 의한 글리신-글리신 스페이서 단위를 함유하는 ADC의 효소적 절단은 ADC의 잔부로부터 글리신-글리신-약물 모이어티의 방출을 초래한다. 일부 이러한 구체예에서, 글리신-글리신-약물 모이어티는 종양 세포에서 가수분해 단계를 거쳐 약물 모이어티로부터 글리신-글리신 스페이서 단위를 절단한다.
“자기-희생” 스페이서 단위는 약물 모이어티의 방출을 가능하게 한다. 특정 구체예들에서, 링커의 스페이서 단위는 p-아미노벤질 단위를 포함한다. 일부 이러한 구체예에서, p-아미노벤질 알콜은 아미드 결합을 통해 아미노산 단위에 부착되고, 벤질 알코올과 약물 사이에 카바메이트, 메틸카바메이트 또는 탄산염이 생성된다 (Hamann 외, (2005) Expert Opin. Ther. Patents (2005) 15:1087-1103). 일부 구체예들에서, 스페이서 단위는 p-아미노벤질옥시카르보닐 (PAB)이다. 일부 구체예들에서, 항-CD79b 면역접합체는 다음 구조를 포함하는 자기-희생 링커를 포함한다:
이때 Q는 -C1-C8 알킬, -O-(C1-C8 알킬), -할로겐, -니트로, 또는 -시아노이고; m은 0 내지 4 범위의 정수이고; p는 1 내지 약 20의 범위이다. 일부 구체예들에서, p는 1 내지 10, 1 내지 7, 1 내지 5, 또는 1 내지 4 범위이다.
자기-희생 스페이서의 다른 예에는, PAB 그룹과 전기적으로 유사한 방향족 화합물, 예를 들어, 2-아미노이미다졸-5-메탄올 유도체 (미국 특허 제 7,375,078; Hay 외, (1999) Bioorg. Med. Chem. Lett. 9:2237) 및 오르토- 또는 파라-아미노벤질아세탈이 포함되지만, 이에 제한되는 것은 아니다. 일부 구체예들에서, 아미드 결합 가수분해 시 고리화를 거치는 스페이서, 예를 들어 치환 및 비치환 4-아미노부티르산 아미드 (Rodrigues 외 (1995) Chemistry Biology 2:223), 적절하게 치환된 바이사이클로[2.2.1] 및 바이사이클로[2.2.2] 고리 시스템 (Storm 외 (1972) J. Amer. Chem. Soc. 94:5815) 및 2-아미노페닐프로피오닉 애시드 아미드 (Amsberry, 외 (1990) J. Org. Chem. 55:5867)가 사용될 수 있다. 글리신 잔기의 α-탄소에 대한 약물의 연결은 ADC에서 유용할 수 있는 자기-희생 스페이서의 또 다른 예이다 (Kingsbury 외 (1984) J. Med. Chem. 27:1447).
일부 구체예들에서, 링커 L은 분지형 다작용기 링커 모이어티를 통해 하나 이상의 약물 모이어티를 항체에 공유 부착하기 위한 수지상 유형의 링커일 수 있다 (Sun 외 (2002) Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun 외 (2003) Bioorganic & Medicinal Chemistry 11:1761-1768). 수지상 링커는 ADC의 효능과 관련된 약물 대 항체의 몰비, 즉 로딩을 증가시킬 수 있다. 따라서, 항체가 반응성 시스테인 티올기를 하나만 보유하는 경우, 다수의 약물 모이어티가 수지상 링커를 통해 부착될 수 있다.
화학식 III, IV, V의 항-CD79 면역접합체와 관련하여 비제한적인 예시적 링커가 하기에 제시되어 있다:
이때 (Ab)는 항-CD79b 항체이고, (D)는 약물/세포독성제이고, “Val-Cit”은 발린-시트룰린 디펩티드이고, MC는 6-말레이미도카프로일이고, PAB는 p-아미노벤질옥시카르보닐이고, 및 p는 1 내지 약 20 (예를 들어, 1 내지 15, 1 내지 10, 1 내지 8, 2 내지 5, 또는 3 내지 4)이다.
일부 구체예들에서, 항-CD79b 면역접합체는 하기 화학식 VI-V 중 어느 하나의 구조를 포함한다:
이때 X는:
Y는:
각 R은 독립적으로 H 또는 C1-C6 알킬이고; 그리고 n은 1 내지 12이다.
전형적으로, 펩티드-유형 링커는 2개 이상의 아미노산 및/또는 펩티드 단편 사이에 펩티드 결합을 형성함으로써 제조될 수 있다. 이러한 펩티드 결합은 예를 들어 액상 합성 방법 (예를 들어, E. Schroder and K. Lubke (1965) “The Peptides”, 1권, pp 76-136, Academic Press)에 따라 제조될 수 있다.
일부 구체예들에서, 링커는 용해도 및/또는 반응성을 조절하는 작용기로 치환된다. 비제한적인 예로서, 설포네이트(-SO3 -) 또는 암모늄과 같은 하전된 치환기는 링커 시약의 수용해도를 증가시키고 링커 시약과 항체 및/또는 약물 모이어티의 커플링 반응을 촉진하거나 또는 항-CD79b 면역접합체를 제조하기 위해 사용된 합성 경로에 따라 Ab-L (항-CD79b 항체-링커 중간체)과 D, 또는 D-L (약물 / 세포독성제-링커 중간체)과 Ab의 커플링 반응을 촉진시킬 수 있다. 링커의 일부는 항체에 결합되고 링커의 일부는 약물에 결합되며, 그 다음 항-CD79 Ab-(링커 부분)a는 약물/세포독성제-(링커 부분)b에 결합되어 화학식 I의 항-CD79b 면역접합체를 형성한다. 이러한 일부 구체예들에서, 항-CD79b 항체는 화학식 I의 항-CD79b 면역접합체에서 1개 초과의 약물 / 세포독성제가 항-CD79b 항체에 커플링되도록 1개 초과의 (링커 부분)a 치환기를 포함한다.
본원에 제공된 항-CD79b 면역접합체는 다음과 같은 링커 시약으로 제조된 항-CD79b 면역접합체를 명시적으로 고려하지만, 이에 제한되지는 않는다: 비스-말레이미도-트리옥시에틸렌 글리콜(BMPEO), N-(β-말레이미도프로필옥시)-N-하이드록시 숙신이미드 에스테르(BMPS), N-(ε말레이미도카프로일옥시) 숙신이미드 에스테르(EMCS), N-[γ말레이미도부티릴옥시]숙신이미드 에스테르( GMBS), 1,6-헥산-비스-비닐설폰(HBVS), 숙신이미딜 4-(N-말레이미도메틸)사이클로헥산-1-카복시-(6-아미도카프로에이트)(LC-SMCC), m-말레이미도벤조일-N-하이드록시숙신이미드 에스테르(MBS), 4-(4-N-말레이미도페닐)부티르산 하이드라지드(MPBH), 숙신이미딜 3-(브로모아세트아미도)프로피오네이트(SBAP), 숙신이미딜 아이오도아세테이트(SIA), 숙신이미딜(4-요오도아세틸)아미노벤조에이트(SIAB), N-숙신이미딜-3-(2-피리딜디티오)프로피오네이트(SPDP), N-숙신이미딜-4-(2-피리딜티오)펜타노에이트(SPP), 숙신이미딜 4-(N-말레이미도메틸) )시클로헥산-1-카르복실레이트(SMCC), 숙신이미딜 4-(p-말레이미도페닐)부티레이트(SMPB), 숙신이미딜 6-[(베타-말레이미도프로피온아미도)헥사노에이트](SMPH), 이미노티올란(IT), 설포-EMCS, 설포-GMBS, 설포-KMUS, 설포-MBS, 설포-SIAB, 설포-SMCC 및 설포-SMPB, 및 숙신이미딜-(4-비닐설폰)벤조에이트(SVSB), 및 다음과 같은 비스-말레이미드 시약들: 디티오비스말레이미도에탄(DTME), 1,4-비스말레이미도부탄(BMB), 1,4 비스말레이미딜-2,3-디하이드록시부탄(BMDB), 비스말레이미도헥산(BMH), 비스말레이미도에탄(BMOE), BM(PEG)2(아래 표시) 및 BM (PEG)3(아래에 표시됨); 이미도에스테르의 이작용기성 유도체(예를 들어, 디메틸 아디피미데이트 HCl), 활성 에스테르(예를 들어, 디숙신이미딜 수베레이트), 알데히드(예를 들어, 글루타르알데히드), 비스-아지도 화합물(예를 들어, 비스(p-아지도벤조일) 헥산디아민), 비스-디아조늄 유도체(예를 들어, 비스-(p-디아조늄벤조일)-에틸렌디아민), 디이소시아네이트(예를 들어, 톨루엔 2,6-디이소시아네이트) 및 비스-활성 불소 화합물(예를 들어, 1,5-디플루오로-2,4-디니트로벤젠). 일부 구체예들에서, 비스-말레이미드 시약은 항체 내 시스테인의 티올기가 티올 함유 약물 모이어티, 링커 또는 링커-약물 중간체에 부착될 수 있게 한다. 티올기와 반응성인 다른 작용기는 아이오도아세트아미드, 브로모아세트아미드, 비닐 피리딘, 디설파이드, 피리딜 디설파이드, 이소시아네이트, 및 이소티오시아네이트를 포함하지만 이에 제한되지 않는다.
특정한 유용한 링커 시약은, 예를 들어, Pierce Biotechnology, Inc. (Rockford, IL), Molecular Biosciences Inc.(Boulder, CO)와 같은 다양한 상업적 공급원으로부터 얻거나, 다음과 같이 해당 분야; 예를 들어, Toki 외 (2002) J. Org. Chem. 67:1866-1872; Dubowchik, 외, (1997) Tetrahedron Letters, 38:5257-60; Walker, M.A. (1995) J. Org. Chem. 60:5352-5355; Frisch 외 (1996) Bioconjugate Chem. 7:180-186; US 6214345; WO 02/088172; US 2003130189; US2003096743; WO 03/026577; WO 03/043583; 및 WO 04/032828에 기재된 절차에 따라 합성될 수 있다.
탄소-14-표지된 1-이소티오시아나토벤질-3-메틸디에틸렌 트리아민펜타아세트산 (MX-DTPA)은 방사성뉴클레오티드를 항체에 접합시키기 위한 예시적인 킬레이트제이다. 예를 들어, WO94/11026을 참조하라.
B. 항-CD79b 항체
일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (f) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 적어도 1, 2, 3, 4, 5, 또는 6개 HVR들을 포함하는 항-CD79b 항체를 포함한다. 일부 이러한 구체예들에서, 면역접합체는 (i) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3 및/또는 (ii) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1을 적어도 하나 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (i) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3 및/또는 (ii) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1을 적어도 하나 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; 및 (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3에서 선택된 적어도 하나, 적어도 2, 또는 적어도 3개의 VH HVR 서열들을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3 및 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3, 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3, 및 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; 및 (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 적어도 하나, 적어도 2, 또는 적어도 3개의 VL HVR 서열들을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 VL HVR 서열들을 적어도 하나, 적어도 2, 또는 3개 모두 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1, (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2, 및 (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3에서 선택된 VH HVR 서열들을 적어도 하나, 적어도 2, 또는 3개 모두 포함하는 VH 도메인; 및 (b) (i) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1, (ii) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2, 및 (iii) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 VL HVR 서열들을 적어도 하나, 적어도 2, 또는 3개 모두 포함하는 VL 도메인을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (i) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3 및/또는 (ii) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1을 적어도 하나 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (f) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체를 포함한다 (표 A 참조). 일부 구체예들에서, 면역접합체는 (i) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3 및/또는 (ii) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1을 적어도 하나 포함한다 (표 A 참조). 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (f) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체를 포함한다 (표 A 참조).
표 A: HVR 아미노산 서열.
일부 구체예들에서, 면역접합체는 Kabat 외의 문헌의 넘버링에 따라 폴라투주맙 베도틴-피이크에서 항-CD79b 항체의 CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2, 및 CDR-L3을 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 항-CD79b 면역접합체는 인간화 항-CD79b 항체를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 본원에 제공된 임의의 구체예에서와 같은 HVR을 포함하고, 인간 수용체 프레임워크, 예를 들어 인간 면역글로불린 프레임워크 또는 인간 공통 프레임워크를 추가로 포함한다. 일부 구체예들에서, 인간 수용체 프레임워크는 인간 VL 카파 1 (VLKI) 프레임워크 및/또는 VH 프레임워크 VHIII이다. 일부 구체예들에서, 인간화 항-CD79b 항체는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (c) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (d) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (e) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (f) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함한다.
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 27의 아미노산 서열을 포함하는 중쇄 FR (HC FR) 1; (b) 서열 번호: 28의 아미노산 서열을 포함하는 HC FR2; (c) 서열 번호: 29의 아미노산 서열을 포함하는 HC FR3; (d) 서열 번호: 30의 아미노산 서열을 포함하는 HC FR4; (e) 서열 번호: 31의 아미노산 서열을 포함하는 경쇄 FR (LC FR) 1; (f) 서열 번호: 32의 아미노산 서열을 포함하는 LC FR2; (g) 서열 번호: 33의 아미노산 서열을 포함하는 LC FR3; 및 (h) 서열 번호: 34의 아미노산 서열을 포함하는 LC FR4에서 선택된 적어도 1, 2, 3, 4, 5, 6, 7, 또는 8개의 프레임워크 영역(FR)들을 포함하는 항-CD79b 항체를 포함한다 (표 B 참조).
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 27의 아미노산 서열을 포함하는 HC FR1; (b) 서열 번호: 28의 아미노산 서열을 포함하는 HC FR2; (c) 서열 번호: 29의 아미노산 서열을 포함하는 HC FR3; 및 (d) 서열 번호: 30의 아미노산 서열을 포함하는 HC FR4에서 선택된 적어도 1, 적어도 2, 적어도 3개, 또는 4개의 HC FR 모두를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 31의 아미노산 서열을 포함하는 LC FR1; (b) 서열 번호: 32의 아미노산 서열을 포함하는 LC FR2; (c) 서열 번호: 33의 아미노산 서열을 포함하는 LC FR3; 및 (d) 서열 번호: 34의 아미노산 서열을 포함하는 LC FR4에서 선택된 적어도 1, 적어도 2, 적어도 3개, 또는 4개의 LC FR 모두를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 27의 아미노산 서열을 포함하는 HC FR1; (b) 서열 번호: 28의 아미노산 서열을 포함하는 HC FR2; (c) 서열 번호: 29의 아미노산 서열을 포함하는 HC FR3; 및 (d) 서열 번호: 30의 아미노산 서열을 포함하는 HC FR4를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 (a) 서열 번호: 31의 아미노산 서열을 포함하는 LC FR1; (b) 서열 번호: 32의 아미노산 서열을 포함하는 LC FR2; (c) 서열 번호: 33의 아미노산 서열을 포함하는 LC FR3; 및 (d) 서열 번호: 34의 아미노산 서열을 포함하는 LC FR4를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) (i) 서열 번호: 27의 아미노산 서열을 포함하는 HC FR1; (ii) 서열 번호: 28의 아미노산 서열을 포함하는 HC FR2; (iii) 서열 번호: 29의 아미노산 서열을 포함하는 HC FR3; 및 (iv) 서열 번호: 30의 아미노산 서열을 포함하는 HC FR4에서 선택된 적어도 1개, 적어도 2개, 적어도 3개, 또는 4개의 HC FR 모두를 포함하는 VH 도메인; 및 (b) (i) 서열 번호: 31의 아미노산 서열을 포함하는 LC FR1; (ii) 서열 번호: 32의 아미노산 서열을 포함하는 LC FR2; (iii) 서열 번호: 33의 아미노산 서열을 포함하는 LC FR3; 및 (iv) 서열 번호: 34의 아미노산 서열을 포함하는 LC FR4에서 선택된 적어도 1개, 적어도 2개, 적어도 3개, 또는 4개의 LC FR 모두를 포함하는 VL 도메인을 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 (a) 서열 번호: 27의 아미노산 서열을 포함하는 HC FR1; (b) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (c) 서열 번호: 28의 아미노산 서열을 포함하는 HC FR2; (d) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (e) 서열 번호: 29의 아미노산 서열을 포함하는 HC FR3; (f) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (g) 서열 번호: 30의 아미노산 서열을 포함하는 HC FR4; (h) 서열 번호: 31의 아미노산 서열을 포함하는 LC FR1; (i) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (j) 서열 번호: 32의 아미노산 서열을 포함하는 LC FR2; (k) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; (l) 서열 번호: 33의 아미노산 서열을 포함하는 LC FR3; (m) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3; 및 (n) 서열 번호: 34의 아미노산 서열을 포함하는 LC FR4를 포함하는 항-CD79b 항체를 포함한다.
표 B: 중쇄 및 경쇄 프레임워크 영역 아미노산 서열.
일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 서열 번호: 19의 아미노산 서열에 적어도 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100% 서열 동일성을 가지는 중쇄 가변 도메인(VH) 서열을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 서열 번호: 19의 아미노산 서열에 적어도 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 동일성을 갖는 VH 서열은 참조 서열에 비해 치환 (예를 들어, 보존적 치환), 삽입 또는 결실을 포함하지만, 해당 서열을 포함하는 항-CD79b 면역접합체는 CD79b에 결합하는 능력을 보유한다. 일부 구체예들에서, 서열 번호: 19에서 총 1 내지 10개의 아미노산이 치환, 삽입 및/또는 결실되었다. 일부 구체예들에서, 서열 번호: 19에서 총 1 내지 5개의 아미노산이 치환, 삽입 및/또는 결실되었다. 일부 구체예들에서, HVR 외부 영역에서 (즉, FR에서) 치환, 삽입 또는 결실이 발생한다. 일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 서열 번호: 19의 VH 서열을 포함하며, 이 서열의 번역후 변형도 포함된다. 일부 구체예들에서, VH는 (a) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1, (b) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2, 및 (c) 서열 번호: 17 또는 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3에서 선택된 1, 2 또는 3개의 HVR을 포함한다.
EVQLVESGGG LVQPGGSLRL SCAASGYTFS SYWIEWVRQA PGKGLEWIGE ILPGGGDTNY NEIFKGRATF SADTSKNTAY LQMNSLRAED TAVYYCTRRV PIRLDYWGQG TLVTVSS (서열 번호: 19)
일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 서열 번호: 20의 아미노산 서열에 적어도 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 또는 100% 서열 동일성을 가지는 경쇄 가변 도메인(VL) 서열을 포함하는 항-CD79b 항체를 포함한다. 특정 구체예들에서, 서열 번호: 20의 아미노산 서열에 적어도 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 동일성을 갖는 VL 서열은 참조 서열에 비해 치환 (예를 들어, 보존적 치환), 삽입 또는 결실을 포함하지만, 해당 서열을 포함하는 항-CD79b 면역접합체는 CD79b에 결합하는 능력을 보유한다. 특정 구체예들에서, 서열 번호: 20에서 총 1 내지 10개의 아미노산이 치환, 삽입 및/또는 결실되었다. 특정 구체예들에서, 서열 번호: 20에서 총 1 내지 5개의 아미노산이 치환, 삽입 및/또는 결실되었다. 특정 구체예들에서, HVR 외부 영역에서 (즉, FR에서) 치환, 삽입 또는 결실이 발생한다. 일부 구체예들에서, 항-CD79b 면역접합체는 서열 번호: 20의 VL 서열을 포함하는 항-CD79b 항체를 포함하며, 이 서열의 번역후 변형도 포함된다. 일부 구체예들에서, VL은 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 1, 2, 또는 3개 HVR들을 포함한다. 일부 구체예들에서, VL은 (a) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (b) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (c) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3에서 선택된 1, 2, 또는 3개 HVR들을 포함한다.
DIQLTQSPSS LSASVGDRVT ITCKASQSVD YEGDSFLNWY QQKPGKAPKL LIYAASNLES GVPSRFSGSG SGTDFTLTIS SLQPEDFATY YCQQSNEDPL TFGQGTKVEI KR (서열 번호: 20)
일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 본원에 제공된 임의의 구체예에서와 같은 VH 및 본원에 제공된 임의의 구체예에서와 같은 VL을 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 각각 서열 번호: 19 및 서열 번호: 20의 VH 및 VL 서열을 포함하는 항-CD79b 항체를 포함하며, 이들 서열의 번역후 변형도 포함한다.
일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크에서 항-CD79b 항체의 VH 및 VL을 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체(예를 들어, 항-CD79b 면역접합체)는 본원에 기재된 항-CD79b 항체와 동일한 에피토프에 결합하는 항-CD79b 항체를 포함한다. 예를 들어, 일부 구체예들에서, 면역접합체 (예를 들어, 항-CD79b 면역접합체)는 서열 번호: 19의 VH 서열 및 서열 번호: 20의 VL 서열을 포함하는 항-CD79b 항체와 동일한 에피토프에 결합하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 모노클로날 항체, 키메라 항체, 인간화 항체, 또는 인간 항체인 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 본원에 기재된 항-CD79b 항체의 항원-결합 단편, 예를 들어 Fv, Fab, Fab', scFv, 디아바디 또는 F(ab')2 단편을 포함한다. 일부 구체예들에서, 면역접합체는 실질적으로 전장 항-CD79b 항체, 예를 들어, IgG1 항체 또는 본원의 다른 곳에 기재된 바와 같은 다른 항체 부류 또는 이소형을 포함한다.
일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및/또는 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및/또는 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및/또는 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 38의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 폴라투주맙 베도틴-피이크에서 항-CD79b 항체의 중쇄 및 경쇄를 포함하는 항-CD79b 항체를 포함한다.
일부 구체예들에서, 면역접합체는 일라다투주맙 베도틴에서 항-CD79b 항체의 중쇄 및 경쇄를 포함하는 항-CD79b 항체를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 서열 번호: 37의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다.
C. 약물 / 세포독성제
항-CD79 면역접합체는 하나 이상의 약물 / 세포독성제, 예컨대 화학요법제 또는 약물, 성장 억제제, 독소 (예를 들어, 단백질 독소, 박테리아, 진균, 식물 또는 동물 기원의 효소적 활성 독소, 또는 이의 단편), 또는 방사성 동위원소 (즉, 방사성접합체)에 접합된 항-CD79b 항체 (예를 들어, 본원에 기재된 항-CD79b 항체)를 포함한다. 이러한 면역접합체는 강력한 세포독성 약물을 항원-발현 암세포 (예를 들어, 종양 세포)에 표적화함으로써 항체 및 세포독성 약물 모두의 특성을 결합함으로써, (Teicher, B.A. (2009) Current Cancer Drug Targets 9:982-1004), 효능을 최대화하고 표적외 독성을 최소화하여 치료 지수를 향상시킨 (Carter, P.J. and Senter P.D. (2008) The Cancer Jour. 14(3):154-169; Chari, R.V. (2008) Acc. Chem. Res. 41:98-107) 표적화된 화학요법 분자이다. 즉, 항-CD79 면역접합체는 암 세포/조직에 유효 투여량의 약물을 선택적으로 전달하여 치료 지수 (“치료 구간”)를 증가시키면서 더 큰 선택성, 즉, 더 낮은 유효 투여량을 달성할 수 있다 (Polakis P. (2005) Current Opinion in Pharmacology 5:382-387).
본원에 제공된 방법에 사용된 항-CD79 면역접합체는 항암 활성을 갖는 것들을 포함한다. 일부 구체예들에서, 항-CD79 면역접합체는 약물 모이어티에 접합된, 즉 공유 부착된 항-CD79b 항체를 포함한다. 일부 구체예들에서, 항-CD79b 항체는 링커를 통해 약물 모이어티에 공유적으로 부착된다. 항-CD79 면역접합체의 약물 모이어티(D)는 세포독성 또는 세포증식억제(cytostatic) 효과를 갖는 임의의 화합물, 모이어티 또는 작용기를 포함할 수 있다. 약물 모이어티는 튜불린 결합, DNA 결합 또는 삽입, 그리고 RNA 폴리머라제, 단백질 합성 및/또는 토포이소머라제의 억제를 비롯한 (그러나 이에 제한되지 않는) 메커니즘에 의해 세포독성 및 세포증식억제 효과를 부여할 수 있다. 예시적인 약물 모이어티에는 메이탄시노이드, 돌라스타틴, 아우리스타틴, 칼리케아마이신, 안트라사이클린, 듀오카르마이신, 빈카 알칼로이드, 탁산, 트리코테센, CC1065, 캄프토테신, 엘리나피드, 및 세포독성 활성을 갖는 이들의 입체이성질체, 동배체, 유사체 및 유도체가 포함되나 이에 제한되지는 않는다.
(i) 메이탄신 및 메이탄시노이드
일부 구체예들에서, 항-CD79b 면역접합체는 하나 이상의 메이탄시노이드 분자에 접합된 항-CD79b 항체를 포함한다. 메이탄시노이드는 메이탄신의 유도체이며, 튜불린 중합을 억제함으로써 작용하는 유사분열 억제제이다. 메이탄신은 동아프리카 관목인 메이테누스 세라타(Maytenus serrata)에서 처음으로 분리되었다 (미국 특허 제 3896111). 후속하여, 특정 미생물들이 메이탄시놀 및 C-3 메이탄시놀 에스테르와 같은 메이탄시노이드도 생산한다는 것이 발견되었다 (미국 특허 제 4,151,042). 합성 메이탄시노이드는, 예를 들어, 미국 특허 제 4,137,230; 4,248,870; 4,256,746; 4,260,608; 4,265,814; 4,294,757; 4,307,016; 4,308,268; 4,308,269; 4,309,428; 4,313,946; 4,315,929; 4,317,821; 4,322,348; 4,331,598; 4,361,650; 4,364,866; 4,424,219; 4,450,254; 4,362,663; 및 4,371,533에 개시되어 있다.
메이탄시노이드 약물 모이어티는 항체-약물 접합체에서 흥미로운 약물 모이어티인데, 그 이유는 다음과 같다: (i) 발효 또는 발효 생성물의 화학적 변형 또는 유도체화에 의한 제조가 비교적 용이함, (ii) 항체에 대한 비-이황화물 링커를 통한 접합에 적합한 작용기로 유도체화 가능함, (iii) 혈장에서 안정함, 및 (iv) 다양한 종양 세포주에 대해 효과적임.
메이탄시노이드 약물 모이어티로서 사용하기에 적합한 특정 메이탄시노이드는 해당 분야에 공지되어 있고 공지된 방법에 따라 천연 공급원으로부터 단리되거나 유전 공학 기술을 사용하여 생성될 수 있다 (예를 들어, Yu 외 (2002) PNAS 99:7968-7973 참조). 메이탄시노이드는 또한 공지된 방법에 따라 합성적으로 제조될 수 있다.
예시적인 메이탄시노이드 약물 모이어티는 변형된 방향족 고리, 예를 들어: C-19-데클로로 (미국 특허 4256746) (예를 들어, 안사마이토신 P2의 리튬 알루미늄 하이드라이드 환원에 의해 제조됨); C-20-하이드록시 (또는 C-20-데메틸) +/-C-19-데클로로 (미국 특허 제 4361650 및 4307016) (예를 들어, 스트렙토마이세스 또는 악티노마이세스를 사용한 LAH를 사용한 탈메틸화 또는 탈염소화에 의해 제조됨); 및 C-20-데메톡시, C-20-아실옥시 (-OCOR), +/-데클로로 (미국 특허 제 4,294,757) (예를 들어, 아실 클로라이드를 사용한 아실화에 의해 제조됨)를 가진 것들, 및 상기 방향족 고리의 다른 위치들에 변형을 가지는 것들을 포함하나 이에 제한되는 것은 아니다.
예시적인 메이탄시노이드 약물 모이어티는 또한 변형들, 예를 들어: C-9-SH (미국 특허 제 4424219) (예를 들어, 메이탄시놀과 H2S 또는 P2S5의 반응에 의해 제조됨); C-14-알콕시메틸(데메톡시/CH2OR)(US 4331598); C-14-하이드록시메틸 또는 아실옥시메틸 (CH2OH 또는 CH2OAc) (미국 특허 제 4450254) (예를 들어, 노카르디아 (Nocardia)속으로부터 제조됨); C-15-하이드록시/아실옥시 (US 4364866) (예를 들어, 스트렙토마이세스(Streptomyces)에 의한 메이탄시놀의 전환에 의해 제조됨); C-15-메톡시 (미국 특허 제 4313946 및 4315929) (예를 들어, 트레위아 누들플로라(Trewia nudlflora)로부터 단리됨); C-18-N-데메틸 (미국 특허 제 4362663 및 4322348) (예를 들어, 스트렙토마이세스(Streptomyces)에 의한 메이탄시놀의 탈메틸화에 의해 제조됨); 및 4,5-데옥시 (US 4371533) (예를 들어, 메이탄시놀의 티타늄 트리클로라이드/LAH 환원에 의해 제조됨)를 가지는 것들을 포함한다.
메이탄시노이드 화합물의 많은 위치가 연결 위치로 유용하다. 예를 들어, 에스테르 링키지(linkage)는 통상적인 커플링 기술을 사용하여 하이드록실기와의 반응에 의해 형성될 수 있다. 일부 구체예들에서, 반응은 하이드록실기를 갖는 C-3 위치, 하이드록시메틸로 변형된 C-14 위치, 하이드록실기로 변형된 C-15 위치, 및 하이드록실기를 갖는 C-20 위치에서 일어날 수 있다. 일부 구체예들에서, 링키지는 메이탄시놀 또는 메이탄시놀 유사체의 C-3 위치에서 형성된다.
메이탄시노이드 약물 모이어티는 다음 구조를 갖는 것들을 포함한다:
여기서 물결선은 항-CD79b 면역접합체의 링커에 대한 메이탄시노이드 약물 모이어티의 황 원자의 공유 부착을 나타낸다. 각 R은 독립적으로 H 또는 C1-C6 알킬 일 수 있다. 아미드 기를 황 원자에 부착시키는 알킬렌 사슬은 메탄일, 에탄일 또는 프로필 일 수 있다, 즉, m은 1, 2 또는 3이다 (US 633410; US 5208020; Chari 외 (1992) Cancer Res. 52:127-131; Liu 외 (1996) Proc. Natl. Acad. Sci USA 93:8618-8623).
메이탄시노이드 약물 모이어티의 모든 입체이성질체는 본원에 제공된 방법, 즉, 키랄 탄소에서 R 및 S 배열의 임의의 조합에 사용되는 항-CD79b 면역접합체로 고려된다 (US 7276497; US 6913748; US 6441163; US 633410 (RE39151); US 5208020; Widdison 외 (2006) J. Med. Chem. 49:4392-4408, 이들 문헌은 그 전문이 참고로 포함됨). 일부 구체예들에서, 메이탄시노이드 약물 모이어티는 다음과 같은 입체화학을 갖는다:
메이탄시노이드 약물 모이어티의 예시적인 구체예는, 다음 구조를 가지는 DM1; DM3; 및 DM4를 포함하나 이에 제한되는 것은 아니다:
이때 물결선은 항-CD79b 면역접합체의 링커 (L)에 대한 약물의 황 원자의 공유 부착을 나타낸다.
다른 예시적인 메이탄시노이드 항-CD79b 면역접합체는 다음 구조 및 약어를 갖는다 (여기서, Ab는 항-CD79b 항체이고 p는 1 내지 약 20임. 일부 구체예들에서, p는 1 내지 10, p는 1 내지 7, p는 1 내지 5, 또는 p는 1 내지 4임):
DM1이 BMPEO 링커를 통해 항체의 티올기에 연결된 예시적인 항체-약물 접합체는 다음 구조 및 약어를 갖는다:
이때 Ab는 항-CD79b 항체이고; n은 0, 1 또는 2이고; p는 1 내지 약 20이다. 일부 구체예들에서, p는 1 내지 10, p는 1 내지 7, p는 1 내지 5, 또는 p는 1 내지 4이다.
메이탄시노이드를 함유하는 면역접합체, 이의 제조 방법, 및 이의 치료 용도는 예를 들어 미국 특허 제 5,208,020호 및 제 5,416,064호; US 2005/0276812 A1; 및 유럽 특허 EP 0 425 235 B1에 기술되어 있으며, 이들 문헌의 개시 내용은 본원에 명시적으로 참고로 포함된다. 또한 Liu 외, Proc. Natl. Acad. Sci. USA 93:8618-8623 (1996); 및 Chari 외, Cancer Research 52:127-131 (1992) 참조.
일부 구체예들에서, 항-CD79b 항체-메이탄시노이드 접합체는 항체 또는 메이탄시노이드 분자의 생물학적 활성을 유의하게 감소시키지 않으면서 항-CD79b 항체를 메이탄시노이드 분자에 화학적으로 연결함으로써 제조될 수 있다. 예를 들어, 미국 특허 제 5,208,020 참조 (이의 개시내용은 본원에 명시적으로 참고로 포함된다). 일부 구체예들에서, 항체 분자당 평균 3-4개의 메이탄시노이드 분자가 접합된 항-CD79b 면역접합체는 항체의 기능 또는 용해도에 부정적인 영향을 미치지 않으면서 표적 세포들의 세포독성을 향상시키는 효능을 보여주었다. 어떤 경우에는 한 분자의 독소/항체 조차도 네이키드 항-CD79b 항체를 사용하는 것보다 세포독성을 향상시킬 것으로 예상된다.
항체-메이탄시노이드 접합체를 제조하기 위한 예시적인 연결기는, 예를 들어 본원에 기재된 것 그리고 미국 특허 제 5208020; EP 특허 0 425 235 B1; Chari 외, Cancer Research 52:127-131 (1992); US 2005/0276812 A1; 및 US 2005/016993 A1에 기재된 것들을 포함하고, 이들 문헌의 개시 내용은 본원에 명시적으로 참고로 포함된다.
(2) 아우리스타틴과 돌라스타틴
약물 모이어티에는 돌라스타틴, 아우리스타틴 및 이들의 유사체 및 유도체가 포함된다 (US 5635483; US 5780588; US 5767237; US 6124431). 아우리스타틴은 해양 연체동물 화합물 돌라스타틴-10의 유도체이다. 특정 이론에 한정하고자 하는 것은 아니지만 돌라스타틴과 아우리스타틴은 미세소관 역학, GTP 가수분해, 핵 및 세포 분열을 방해하고 (Woyke 외 (2001) Antimicrob. Agents and Chemother. 45(12):3580-3584) 항암 (US 5663149) 및 항진균 활성 (Pettit 외 (1998) Antimicrob. Agents Chemother. 42:2961-2965)을 가지는 것으로 나타났다. 돌라스타틴/아우리스타틴 약물 모이어티는 펩티드 약물 모이어티의 N (아미노) 말단 또는 C (카르복실) 말단을 통해 항체에 부착될 수 있다 (WO 02/088172; Doronina 외 (2003) Nature Biotechnology 21(7):778-784; Francisco 외 (2003) Blood 102(4):1458-1465).
예시적인 아우리스타틴 구체예는 US 7498298 및 US 7659241에 개시된 N-말단 연결된 모노메틸아우리스타틴 약물 모이어티 DE 및 DF를 포함하며, 이들 문헌의 개시내용은 그 전문이 명시적으로 참고로 포함된다:
이때 DE 및 DF의 물결선은 항체 또는 항체-링커 성분에 대한 공유 부착 부위를 나타내며, 각 위치에서 독립적으로 다음과 같다:
R2는 H 및 C1-C8 알킬에서 선택되고;
R3는 H, C1-C8 알킬, C3-C8 카보사이클, 아릴, C1-C8 알킬-아릴, C1-C8 알킬-(C3-C8 카보사이클), C3-C8 헤테로사이클 및 C1-C8 알킬-(C3-C8 헤테로사이클)에서 선택되고;
R4는 H, C1-C8 알킬, C3-C8 카보사이클, 아릴, C1-C8 알킬-아릴, C1-C8 알킬-(C3-C8 카보사이클), C3-C8 헤테로사이클 및 C1-C8 알킬-(C3-C8 헤테로사이클)에서 선택되고;
R5는 H 및 메틸에서 선택되고;
또는 R4 및 R5는 결합하여 카보사이클릭 고리를 형성하고 화학식 -(CRaRb)n-를 가지며 이때 Ra 및 Rb는 독립적으로 H, C1-C8 알킬 및 C3-C8 카보사이클에서 선택되고 n은 2, 3, 4, 5 및 6에서 선택되고;
R6는 H 및 C1-C8 알킬에서 선택되고;
R7은 H, C1-C8 알킬, C3-C8 카보사이클, 아릴, C1-C8 알킬-아릴, C1-C8 알킬-(C3-C8 카보사이클), C3-C8 헤테로사이클 및 C1-C8 알킬-(C3-C8 헤테로사이클)에서 선택되고;
각 R8은 독립적으로 H, OH, C1-C8 알킬, C3-C8 카보사이클 및 O-(C1-C8 알킬)에서 선택되고;
R9은 H 및 C1-C8 알킬에서 선택되고;
R10은 아릴 또는 C3-C8 헤테로사이클에서 선택되고;
Z는 O, S, NH, 또는 NR12이고, 이때 R12는 C1-C8 알킬이고;
R11은 H, C1-C20 알킬, 아릴, C3-C8 헤테로사이클, -(R13O)m-R14, 또는 -(R13O)m-CH(R15)2에서 선택되고;
m은 1-1000 범위의 정수이고;
R13은 C2-C8 알킬이고;
R14는 H 또는 C1-C8 알킬이고;
각 경우 R15는 독립적으로 H, COOH, -(CH2)n-N(R16)2, -(CH2)n-SO3H, 또는 -(CH2)n-SO3-C1-C8 알킬이고;
각 경우 R16은 독립적으로 H, C1-C8 알킬, 또는 -(CH2)n-COOH이고;
R18은 -C(R8)2-C(R8)2-아릴, -C(R8)2-C(R8)2-(C3-C8 헤테로사이클), 및 -C(R8)2-C(R8)2-(C3-C8 카보사이클)에서 선택되고; 그리고
n은 0 내지 6 범위의 정수이다.
한 구체예에서, R3, R4 및 R7은 독립적으로 이소프로필 또는 sec-부틸이고 R5는 -H 또는 메틸이다. 한 예시적 구체예에서, R3 및 R4는 각각 이소프로필이고, R5는 -H이고, 그리고 R7은 sec-부틸이다.
또한 또 다른 구체예에서, R2 및 R6는 각각 메틸이고, 그리고 R9은 -H이다.
또한 또 다른 구체예에서, 각 경우 R8은 -OCH3이다.
한 예시적 구체예에서, R3 및 R4는 각각 이소프로필이고, R2 및 R6는 각각 메틸이고, R5는 -H이고, R7은 sec-부틸이고, 각 경우 R8은 -OCH3이고, 그리고 R9은 -H이다.
한 구체예에서, Z는 -O- 또는 -NH-이다.
한 구체예에서, R10은 아릴이다.
한 예시적 구체예에서, R10은 -페닐이다.
한 예시적 구체예에서, Z가 -O-일 때, R11은 -H, 메틸 또는 t-부틸이다.
한 구체예에서, Z가 -NH일 때, R11은 -CH(R15)2이고, 이때 R15는 -(CH2)n-N(R16)2이고, 그리고 R16은 -C1-C8 알킬 또는 -(CH2)n-COOH이다.
또 다른 구체예에서, Z가 -NH일 때, R11은 -CH(R15)2이고, 이때 R15는 -(CH2)n-SO3H이다.
화학식 DE의 예시적인 아우리스타틴 구체예는 MMAE이고, 이때 물결선은 항-CD79b 면역접합체의 링커 (L)에 대한 공유 부착을 나타낸다:
화학식 DF의 예시적인 아우리스타틴 구체예는 MMAF이고, 이때 물결선은 항-CD79b 면역접합체의 링커 (L)에 대한 공유 부착을 나타낸다:
다른 예시적인 구체예는 펜타펩티드 아우리스타틴 약물 모이어티의 C-말단에 페닐알라닌 카르복시 변형을 갖는 모노메틸발린 화합물 (WO 2007/008848) 및 펜타펩티드 아우리스타틴 약물 모이어티의 C-말단에 페닐알라닌 측쇄 변형을 갖는 모노메틸발린 화합물 (WO 2007/008603)을 포함한다.
MMAE 또는 MMAF 및 다양한 링커 성분을 포함하는 화학식 I의 항-CD79b 면역접합체의 비제한적인 예시적 구체예는 다음 구조 및 약어를 갖는다 (여기서 “Ab”는 항-CD79b 항체이고, p는 1 내지 약 8이고, “Val-Cit”은 발린-시트룰린 디펩티드이고 “S”는 황 원자이다).
Ab-MC-vc-PAB-MMAF
Ab-MC-vc-PAB-MMAE
Ab-MC-MMAE
Ab-MC-MMAF
특정 구체예들에서, 항-CD79b 면역접합체는 Ab-MC-vc-PAB-MMAE의 구조를 포함하고, 이때 p는, 예를 들어, 약 1 내지 약 8; 약 2 내지 약 7; 약 3 내지 약 5; 약 3 내지 약 4; 또는 약 3.5이다. 일부 구체예들에서, 항-CD79b 면역접합체는 huMA79bv28-MC-vc-PAB-MMAE, 예를 들어, Ab-MC-vc-PAB-MMAE의 구조를 포함하는 항-CD79b 면역접합체이고, 이때 p는, 예를 들어, 약 1 내지 약 8; 약 2 내지 약 7; 약 3 내지 약 5; 약 3 내지 약 4; 또는 약 3.5이고, 이때 항-CD79b 항체(Ab)는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄, 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함한다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 폴라투주맙 베도틴-피이크는 IUPHAR/BPS 번호 8404, KEGG 번호 D10761을 가지며, “DCDS4501A” 또는 “RG7596”로도 지칭될 수 있다.
MMAF 및 다양한 링커 성분을 포함하는 화학식 I의 항-CD79b 면역접합체의 비제한적인 예시적 구체예는 Ab-MC-PAB-MMAF 및 Ab-PAB-MMAF를 추가로 포함한다. 단백질분해적으로 절단될 수 없는 링커에 의해 항체에 부착된 MMAF를 포함하는 면역접합체는 단백질분해적으로 절단가능한 링커에 의해 항체에 부착된 MMAF를 포함하는 면역접합체에 필적하는 활성을 갖는 것으로 밝혀진 바 있다 (Doronina 외, (2006) Bioconjugate Chem. 17:114-124). 이러한 일부 구체예들에서, 약물 방출은 세포에서 항체 분해에 의해 영향을 받는 것으로 여겨진다.
MMAE 및 다양한 링커 성분을 포함하는 화학식 I의 항-CD79b 면역접합체의 비제한적인 예시적 구체예는 Ab-MC-PAB-MMAF 및 Ab-PAB-MMAF를 추가로 포함한다.
전형적으로, 펩티드-기반 약물 모이어티는 2개 이상의 아미노산 및/또는 펩티드 단편 사이에 펩티드 결합을 형성함으로써 제조될 수 있다. 이러한 펩티드 결합은 예를 들어 액상 합성 방법 (예를 들어, E. Schroder and K. Lubke“The Peptides”, 1권, pp 76-136, 1965, Academic Press 참조)에 따라 제조될 수 있다. 아우리스타틴/돌라스타틴 약물 모이어티는 일부 구체예에서 다음과 같은 방법에 따라 제조될 수 있다: US 7498298; US 5635483; US 5780588; Pettit 외 (1989) J. Am. Chem. Soc. 111:5463-5465; Pettit 외 (1998) Anti-Cancer Drug Design 13:243-277; Pettit, G.R., 외, Synthesis, 1996, 719-725; Pettit 외 (1996) J. Chem. Soc. Perkin Trans. 1 5:859-863; 및 Doronina (2003) Nat. Biotechnol. 21(7):778-784.
일부 구체예들에서, 화학식 DE, 예를 들어, MMAE, 및 DF, 예를 들어, MMAF의 아우리스타틴/돌라스타틴 약물 모이어티, 및 약물-링커 중간체 및 이의 유도체, 예를 들어, MC-MMAF, MC-MMAE, MC-vc-PAB-MMAF, 및 MC-vc-PAB-MMAE는, US 7498298; Doronina 외, (2006) Bioconjugate Chem. 17:114-124; 및 Doronina 외, (2003) Nat. Biotech. 21:778-784에 기재된 방법을 사용하여 제조된 다음 관심 항체에 접합될 수 있다.
(3) 칼리케아마이신
일부 구체예들에서, 항-CD79b 면역접합체는 하나 이상의 칼리케아마이신 분자에 접합된 항-CD79b 항체를 포함한다. 칼리케아마이신 계열의 항생제 및 이의 유사체는 서브피코몰 농도에서 이중 가닥 DNA 절단을 생성할 수 있다 (Hinman 외, (1993) Cancer Research 53:3336-3342; Lode 외, (1998) Cancer Research 58:2925-2928). 칼리케아마이신은 세포내 작용 부위를 가지고 있지만 어떤 경우에는 원형질막을 쉽게 통과하지 못한다. 따라서, 항체-매개 내재화를 통한 이들 제제의 세포 흡수는 일부 구체예에서 이들 0제제의 세포독성 효과를 크게 향상시킬 수 있다. 칼리케아마이신 약물 모이어티를 갖는 항-CD79b 항체 면역접합체를 제조하는 비제한적인 예시적인 방법은 예를 들어 US 5712374; US 5714586; US 5739116; 및 US 5767285에 기재되어 있다.
(4) 기타 약물 모이어티
일부 구체예들에서, 항-CD79b 면역접합체는 젤다나마이신 (Mandler 외 (2000) J. Nat. Cancer Inst. 92(19):1573-1581; Mandler 외 (2000) Bioorganic & Med. Chem. Letters 10:1025-1028; Mandler 외 (2002) Bioconjugate Chem. 13:786-791); 및/또는 디프테리아 A 사슬, 디프테리아 독소의 비결합 활성 단편, 외독소 A 사슬 (수도모나스 아에루기노사 (Pseudomonas aeruginosa)로부터 얻음), 리신(ricin) A 사슬, 아브린 A 사슬, 모데신 A 사슬, 알파-사르신, 알레우리테스 포르디이 (Aleurites fordii) 단백질, 디안틴 단백질, 파이토라카 아메리카나 단백질 (PAPI, PAPII, 및 PAP-S), 모모르디카 카란티아 (momordica charantia) 억제제, 쿠르신, 크로틴, 사파오나리아 오피시날리스(sapaonaria officinalis) 억제제, 젤로닌, 미토젤린, 레스트릭토신(restrictocin), 페노마이신(phenomycin), 에노마이신(enomycin) 및 트리코테세네스(tricothecenes)를 포함한 (그러나 이에 제한되는 것은 아님) 효소적 활성 독소 및 이의 단편을 포함한다. 예를 들어, WO 93/21232 참조.
약물 모이어티에는 또한 핵분해 활성을 갖는 화합물 (예를 들어, 리보뉴클레아제 또는 DNA 엔도뉴클레아제)이 포함된다.
특정 구체예들에서, 항-CD79b 면역접합체는 고 방사성 원자를 포함한다. 다양한 방사성 동위원소를 방사성접합 항체 생산에 이용할 수 있다. 예에는 At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 및 Lu의 방사성 동위원소가 포함된다. 일부 구체예들에서, 항-CD79b 면역접합체가 검출에 사용되는 경우, 섬광학 연구를 위한 방사성 원자, 예를 들어 Tc99 또는 I123, 또는 핵 자기 공명 (NMR) 영상 (자기 공명 영상, MRI로도 알려짐)를 위한 스핀 라벨, 예를 들어, 지르코늄-89, 요오드-123, 요오드-131, 인듐-111, 불소-19, 탄소-13, 질소-15, 산소-17, 가돌리늄, 망간 또는 철을 포함할 수 있다. 예를 들어 PET 영상화를 위해 지르코늄-89는 다양한 금속 킬레이트제와 착물화될 수 있고, 항체에 접합될 수 있다 (WO 2011/056983).
방사성- 또는 기타 표지는 공지된 방식으로 항-CD79b 면역접합체에 혼입될 수 있다. 예를 들어, 펩티드는 예를 들어 하나 이상의 수소 대신에 하나 이상의 불소-19 원자를 포함하는 적합한 아미노산 전구체를 사용하여 생합성되거나 화학적으로 합성될 수 있다. 일부 구체예들에서, 표지, 예를 들어, Tc99, I123, Re186, Re188 및 In111은 항-CD79b 항체에서 시스테인 잔기를 통해 부착될 수 있다. 일부 구체예들에서, 이트륨-90은 항-CD79b 항체의 리신 잔기를 통해 부착될 수 있다. 일부 구체예들에서, IODOGEN 방법 (Fraker 외 (1978) Biochem. Biophys. Res. Commun. 80: 49-57)을 사용하여 아이오딘-123을 혼입시킬 수 있다. “Monoclonal Antibodies in Immunoscintigraphy” (Chatal, CRC Press 1989)는 특정한 다른 방법들을 기재하고 있다.
특정 구체예들에서, 항-CD79b 면역접합체는 전구약물-활성화 효소에 접합된 항-CD79b 항체를 포함할 수 있다. 이러한 일부 구체예들에서, 전구약물-활성화 효소는 전구약물 (예를 들어, 펩티딜 화학요법제, WO 81/01145 참조)을 활성 약물, 예를 들어, 항암 약물로 전환시킨다. 이러한 면역접합체는 일부 구체예에서 항체-의존성 효소-매개 전구약물 요법(“ADEPT”)에 유용하다. 항-CD79b 항체에 접합될 수 있는 효소에는 포스페이트-함유 전구약물을 유리 약물로 전환시키는 데 유용한 알칼리성 포스파타제; 설페이트-함유 전구약물을 유리 약물로 전환시키는데 유용한 아릴설파타제; 무독성 5-플루오로시토신을 항암제인 5-플루오로우라실로 전환하는데 유용한 시토신 데아미나제; 펩티드 함유 전구약물을 유리 약물로 전환시키는데 유용한 세라티아 프로테아제, 써모리신, 서브틸리신, 카르복시펩티다제 및 카텝신(예컨대 카텝신 B 및 L)과 같은 프로테아제; D-아미노산 치환체를 함유하는 전구약물 전환에 유용한 D-알라닐카르복시펩티다제; 당화된 전구약물을 유리 약물로 전환하는데 유용한 β-갈락토시다제 및 뉴라미니다제와 같은 탄수화물 절단 효소; β-락탐으로 유도체화된 약물을 유리 약물로 전환시키는 데 유용한 β-락타마제; 및 이는 각각 페녹시아세틸 또는 페닐아세틸 기를 사용하여 아민 질소에서 유도체화된 약물을 유리 약물로 전환하는 데 유용한 페니실린 V 아미다제 및 페니실린 G 아미다제와 같은 페니실린 아미다제가 포함되나, 이에 제한되는 것은 아니다. 일부 구체예들에서, 효소는 해당 분야에 잘 알려진 재조합 DNA 기술에 의해 항체에 공유 결합될 수 있다. 예를 들어, Neuberger 외, Nature 312:604-608 (1984) 참조.
D. 약물 로딩
약물 로딩은 화학식 I의 분자에서 항-CD79b 항체당 약물 모이어티의 평균 수인 p로 표시된다. 약물 로딩은 항체당 1 내지 20개의 약물 모이어티(D) 범위일 수 있다. 화학식 I의 항-CD79b 면역접합체는 1 내지 20개의 범위의 약물 모이어티와 접합된 항-CD79b 항체의 집합체를 포함한다. 접합 반응으로부터의 항-CD79b 면역접합체 제조에서 항-CD79b 항체당 약물 모이어티의 평균 수는 질량 분광법, ELISA 분석법 및 HPLC와 같은 통상적인 수단에 의해 특성화될 수 있다. p와 관련하여 항-CD79b 면역접합체의 정량적 분포 또한 결정될 수 있다. 일부 예에서, p가 다른 약물 로딩을 사용하여 항-CD79b 면역접합체로부터 얻은 특정 값일 때 균질한 항-CD79b 면역접합체의 분리, 정제 및 특성화는 역상 HPLC 또는 전기영동과 같은 수단에 의해 달성될 수 있다.
일부 항-CD79b 면역접합체의 경우, p는 항-CD79b 항체의 부착 부위 수에 의해 제한될 수 있다. 예를 들어, 부착이 시스테인 티올인 경우, 상기 특정 예시적 구체예에서와 같이, 항-CD79b 항체는 하나 또는 여러 개의 시스테인 티올 기를 가질 수 있고, 또는 링커가 부착될 수 있는 단 하나 또는 여러 개의 충분히 반응성인 티올 기를 가질 수 있다. 특정 구체예들에서, 더 높은 약물 로딩, 예를 들어, p >5는 특정 항-CD79b 면역접합체의 응집, 불용성, 독성 또는 세포 투과성의 손실을 유발할 수 있다. 특정 구체예들에서, 항-CD79b 면역접합체에 대한 평균 약물 로딩 범위는 1 내지 약 8; 약 2 내지 약 6; 약 3 내지 약 5; 또는 약 3 내지 약 4이다. 실제로, 특정 항체-약물 접합체의 경우, 항체당 약물 모이어티의 최적 비율은 8 미만일 수 있고 약 2 내지 약 5일 수 있는 것으로 나타났다 (US 7498298). 특정 구체예들에서, 항체당 약물 모이어티의 최적 비율은 약 3 내지 약 4이다. 특정 구체예들에서, 항체당 약물 모이어티의 최적 비율은 약 3.5이다.
특정 구체예들에서, 접합 반응 중에 이론상 최대값 보다 적은 수의 약물 모이어티들이 항-CD79b 항체에 접합된다. 항체는, 예를 들어, 이하에서 논의되는 바와 같이 약물-링커 중간체 또는 링커 시약과 반응하지 않는 리신 잔기를 함유할 수 있다. 일반적으로, 항체는 약물 모이어티에 연결될 수 있는 많은 유리 및 반응성 시스테인 티올기를 포함하지 않으며; 실제로 항체의 대부분의 시스테인 티올 잔기는 이황화물 다리로 존재한다. 특정 구체예들에서, 항-CD79b 항체는 부분 또는 전체 환원 조건 하에 디티오트레이톨(DTT) 또는 트리카르보닐에틸포스핀(TCEP)과 같은 환원제로 환원되어, 반응성 시스테인 티올 기를 생성할 수 있다. 특정 구체예들에서, 항-CD79b 항체는 리신 또는 시스테인과 같은 반응성 친핵성 작용기를 드러내기 위해 변성 조건에 적용된다.
항-CD79b 면역접합체의 로딩 (약물/항체 비율)은 상이한 방식으로, 예를 들어, 예를 들어, 다음에 의해 조절될 수 있다: (i) 항체에 대한 약물-링커 중간체 또는 링커 시약의 몰 과량을 제한, (ii) 접합 반응 시간 또는 온도를 제한, (iii) 시스테인 티올 변형을 위한 환원 조건을 부분적으로 또는 제한.
하나 이상의 친핵성 그룹이 약물-링커 중간체 또는 링커 시약과 반응하는 경우, 생성된 생성물은 항-CD79b 항체에 부착된 하나 이상의 약물 모이어티의 분포를 가지는 항-CD79b 면역접합체 화합물들의 혼합물임을 이해하여야 한다. 항체 당 약물의 평균 수는 항체에 특이적이고 약물에 특이적인 이중 ELISA 항체 분석에 의해 혼합물로부터 계산될 수 있다. 개개의 항-CD79b 면역접합체 분자들은 질량 분광법에 의해 혼합물 중에서 확인되어 HPLC, 예를 들어, 소수성 상호작용 크로마토그래피에 의해 분리될 수 있다 (예를 들어, McDonagh 외 (2006) Prot. Engr. Design & Selection 19(7):299-307; Hamblett 외 (2004) Clin. Cancer Res. 10:7063-7070; Hamblett, K.J., 외, “Effect of drug loading on the pharmacology, pharmacokinetics, and toxicity of an anti-CD30 antibody-drug conjugate,” Abstract No. 624, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004; Alley, S.C., 외, “Controlling the location of drug attachment in antibody-drug conjugates,” Abstract No. 627, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004 참조). 특정 구체예들에서, 단일 로딩 값을 갖는 균질한 항-CD79b 면역접합체는 전기영동 또는 크로마토그래피에 의해 접합 혼합물로부터 단리될 수 있다.
E. 항-CD79b 면역접합체의 제조 방법
화학식 I의 항-CD79b 면역접합체는 예를 들어, (1) 항-CD79b 항체의 친핵성 그룹과 2가 링커 시약의 반응으로 공유 결합을 통해 Ab-L을 형성한 후 약물 모이어티 D와 반응; 및 (2) 약물 모이어티의 친핵성 그룹과 2가 링커 시약의 반응으로, 공유 결합을 통해 D-L을 형성한 후 항-CD79b 항체의 친핵성 그룹과 반응을 포함하는 (그러나 이에 제한되는 것은 아님), 당업자에게 공지된 유기 화학 반응, 조건, 및 시약들을 사용하는 몇 가지 경로들에 의해 제조될 수 있다. 후자의 경로를 통해 화학식 I의 항-CD79b 면역접합체를 제조하는 예시적인 방법은 US 7498298에 기재되어 있으며, 이는 본원에 참조로 명시적으로 포함된다.
항체의 친핵성 그룹에는 다음이 포함되나 이에 제한되는 것은 아니다: (i) N-말단 아민 그룹, (ii) 측쇄 아민 그룹, 예를 들어, 리신, (iii) 측쇄 티올 그룹, 예를 들어 시스테인, 및 (iv) 당 하이드록실 그룹 또는 항체가 당화된 아미노 그룹. 아민, 티올 및 하이드록실 그룹은 친핵성이며 다음을 포함하는, 링커 모이어티 및 링커 시약 상의 친전자성 그룹과 반응하여 공유 결합을 형성할 수 있다: (i) 활성 에스테르, 예를 들어, NHS 에스테르, HOBt 에스테르, 할로포르메이트 및 산 할로겐화물; (ii) 알킬 및 벤질 할라이드, 예를 들어, 할로아세트아미드; 및 (iii) 알데히드, 케톤, 카르복실 및 말레이미드 그룹. 특정 항체는, 환원가능한 사슬간 이황화물, 즉 시스테인 다리를 가진다. 항-CD79b 항체는 항-CD79b 항체가 완전히 또는 부분적으로 환원되도록 DTT(디티오트레이톨) 또는 트리카르보닐에틸포스핀 (TCEP)과 같은 환원제로 처리함으로써 링커 시약과의 접합에 대해 반응성이 되게 할 수 있다. 따라서 각 시스테인 다리는 이론적으로 두 개의 반응성 티올 친핵체를 형성한다. 추가의 친핵성 그룹들은, 예를 들어, 리신 잔기를 2-이미노티올란과 반응시켜 아민을 티올로 전환시키는 것과 같은 리신 잔기의 변형을 통해 항-CD79b 항체에 도입될 수 있다. 반응성 티올 그룹들은 또한 1개, 2개, 3개, 4개 또는 그 이상의 시스테인 잔기를 도입함으로써 (예를 들어, 하나 이상의 비-천연 시스테인 아미노산 잔기를 포함하는 변이체 항체를 제조함으로써) 항-CD79b 항체에 도입될 수 있다.
본원에 기재된 항-CD79b 면역접합체는 또한 항-CD79b 항체 상의 친전자성 그룹, 예컨대 알데히드 또는 케톤 카르보닐 그룹과 링커 시약 또는 약물 상의 친핵성 그룹 사이의 반응에 의해 생성될 수 있다. 링커 시약 상의 유용한 친핵성 그룹은 하이드라지드, 옥심, 아미노, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트 및 아릴하이드라지드를 포함하지만 이에 제한되지는 않는다. 한 구체예에서, 항-CD79b 항체는 링커 시약 또는 약물의 친핵성 치환기와 반응할 수 있는 친전자성 모이어티들을 도입하도록 변형된다. 또 다른 구체예에서, 당화된 항-CD79b 항체의 당은 링커 시약 또는 약물 모이어티의 아민 그룹과 반응할 수 있는 알데히드 또는 케톤 그룹을 형성하기 위해 예를 들어 과요오드산염 산화 시약으로 산화될 수 있다. 생성된 이민 쉬프 염기 그룹은 안정한 결합을 형성할 수 있거나, 예를 들어, 보로하이드라이드 시약에 의해 환원되어 안정한 아민 링키지를 형성할 수 있다. 한 구체예에서, 당화된 항-CD79b 항체의 탄수화물 부분과 갈락토스 산화효소 또는 메타과요오드산 나트륨의 반응은 항-CD79b 항체에 카르보닐 (알데히드 및 케톤) 그룹을 생성할 수 있으며, 이는 약물 상의 적절한 그룹과 반응할 수 있다 (Hermanson, Bioconjugate Techniques). 또 다른 구체예에서, N-말단 세린 또는 트레오닌 잔기를 포함하는 항-CD79b 항체는 메타-과요오드산 나트륨과 반응하여 일차 아미노산 대신 알데하이드를 생성할 수 있다 (Geoghegan & Stroh, (1992) Bioconjugate Chem. 3:138-146; US 5362852). 이러한 알데하이드는 약물 모이어티 또는 링커 친핵체와 반응할 수 있다.
약물 모이어티 상의 예시적인 친핵성 그룹은, (i) 활성 에스테르, 예를 들어, NHS 에스테르, HOBt 에스테르, 할로포르메이트 및 산 할로겐화물; (ii) 알킬 및 벤질 할라이드, 예를 들어, 할로아세트아미드; (iii) 알데히드, 케톤, 카르복실 및 말레이미드 그룹을 포함하는, 링커 모이어티 및 링커 상의 친전자성 그룹과 공유 결합을 형성하도록 반응할 수 있는 아민, 티올, 하이드록실, 하이드라지드, 옥심, 하이드라진, 티오세미카르바존, 하이드라진 카르복실레이트, 및 아릴하이드라지드 그룹을 포함하지만 이에 제한되지는 않는다.
항-CD79b 면역접합체를 제조하기 위해 사용될 수 있는 비제한적인 예시적인 가교제 시약은 본원에 “예시적 링커”라는 제목의 섹션에 기술되어 있다. 이러한 가교제 시약을 사용하여 단백질 모이어티 및 화학적 모이어티를 포함하는 2개의 모이어티를 연결하는 방법은 해당 분야에 공지되어 있다. 일부 구체예들에서, 항-CD79b 항체 및 세포독성제를 포함하는 융합 단백질은 예를 들어 재조합 기술 또는 펩티드 합성에 의해 제조될 수 있다. 재조합 DNA 분자는 항체를 인코딩하는 영역 및 접합체의 원하는 특성을 파괴하지 않는 링커 펩티드를 인코딩하는 영역에 의해 분리된 또는 서로 인접한 접합체의 세포독성 부분들을 포함할 수 있다. 또한 또 다른 구체예에서, 항체-수용체 접합체를 환자에게 투여한 후 정화제를 사용하여 결합되지 않은 접합체를 순환계에서 제거한 다음, 세포독성제 (예를 들어, 약물 또는 방사성 뉴클레오티드)에 접합된 “리간드” (예를 들어, 아비딘)를 투여하는 종양 예비-표적화에서 사용하기 위해 항-CD79b 항체는 “수용체” (예를 들어, 스트렙타비딘)에 접합될 수 있다. 항-CD79b 면역접합체에 관한 추가 세부사항은 미국 특허 제 8545850 및 WO/2016/049214에 제공되며, 이 문헌들의 내용은 그 전문이 본원에 참조로 명시적으로 포함된다.
VI. 항-CD20 제제
CD20 항원에 대한 항-CD20 항체의 결합 특성 및 생물학적 활성에 따라 2가지 유형의 항-CD20 항체(유형 I 및 유형 II 항-CD20 항체)가 Cragg, M.S., 외, Blood 103 (2004) 2738-2743; and Cragg, M.S., 외, Blood 101 (2003) 1045-1052에 따라 구분 될 수 있다, 표 C를 참조하라.
표 C: 유형 I 및 유형 II 항-CD20 항체들의 특성
유형 I 항-CD20 항체의 예에는 예를 들어, 리툭시맙, HI47 IgG3 (ECACC, 하이브리도마), 2C6 IgG1 (WO 2005/103081에 개시됨), 2F2 IgG1 (WO 2004/035607 및 WO 2005/103081에 개시됨) 및 2H7 IgG1 (WO 2004/056312에 개시됨)이 포함된다.
일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 리툭시맙이다. 일부 구체예들에서, 리툭시맙(참조 항체, 유형 I 항-CD20 항체의 예)은 인간 CD20 항원에 대해 지시된 모노클로날 항체를 함유하는 유전적으로 조작된 키메라 인간 감마 1 뮤린 불변 도메인이다. 그러나 이 항체는 당조작 (glycoengineered) 및 어푸코실화(afucosylated)되지 않으므로 적어도 85%의 푸코스 양을 가진다. 이 키메라 항체는 인간 감마 1 불변 도메인을 포함하고 I1998년 4월 17일자로 등록되고 DEC Pharmaceuticals Corporation에 양도된 US 5,736,137 (Andersen, 외)에서 명칭 “C2B8”으로 확인된다. 리툭시맙은 미만성 거대 B-세포 림프종 (DLBCL), 재발성 또는 불응성 저 등급 또는 소포 CD20 양성 B세포 비호지킨 림프종 환자의 치료에 승인되었다. 시험관 내 작용 메커니즘 연구에서 리툭시맙이 인간 보체 의존성 세포독성 (CDC)을 나타내는 것으로 나타났다 (Reff, M.E., 외 Blood 83(2) (1994) 435-445). 또한, 항체 의존성 세포 독성 (ADCC)을 측정하는 분석에서 활성을 나타낸다.
일부 구체예들에서, 일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 Kabat 등의 넘버링에 따라, 리툭시맙의 CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2, 및 CDR-L3를 포함한다. 일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항-CD20 항체는 리툭시맙의 VH 및 VL을 포함한다. 일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항-CD20 항체는 리툭시맙의 중쇄 및 경쇄를 포함한다. 본원에서 사용되는 용어 “리툭시맙”은 CAS 등록 번호 174722-31-7을 가지는 항-CD20 항체를 지칭한다.
일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 어푸코실화된 항-CD20 항체이다.
유형 II 항-CD20 항체의 예에는 예를 들어, 인간화 B-Ly1 항체 IgG1 (WO 2005/044859에 개시된 키메라 인간화 IgG1 항체), 11B8 IgG1 (WO 2004/035607에 개시됨), 및 AT80 IgG1이 포함된다. 전형적으로 IgG1 이소형의 유형 II 항-CD20 항체는 특징적인 CDC 성질들을 보여준다. 유형 II 항-CD20 항체는 IgG1 이소형의 유형 I 항체에 비해 감소된 CDC (IgG1 이소형의 경우)를 가진다. 일부 구체예들에서 유형 II 항-CD20 항체, 예를 들어, GA101 항체는 증가된 항체 의존성 세포 세포독성 (ADCC)을 가진다. 일부 구체예들에서, 유형 II 항-CD20 항체, 더욱 바람직하게는 어푸코실화된 인간화 B-Ly1 항체는 WO 2005/044859 및 WO 2007/031875에 기재되어 있다.
일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 GA101 항체이다. 일부 구체예들에서, 본 발명에서 사용되는 GA101 항체는 인간 CD20에 결합하는 다음 항체 중 어느 하나를 지칭한다: (1) 서열 번호:5의 아미노산 서열을 포함하는 HVR-H1, 서열 번호:6의 아미노산 서열을 포함하는 HVR-H2, 서열 번호:7의 아미노산 서열을 포함하는 HVR-H3, 서열 번호:8의 아미노산 서열을 포함하는 HVR-L1, 서열 번호:9의 아미노산 서열을 포함하는 HVR-L2, 및 서열 번호:10의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항체; (2) 서열 번호:11의 아미노산 서열을 포함하는 VH 도메인 및 서열 번호:12의 아미노산 서열을 포함하는 VL 도메인을 포함하는 항체, (3) 서열 번호:13의 아미노산 서열 및 서열 번호: 14의 아미노산 서열을 포함하는 항체; (4) 오비누투주맙으로 공지된 항체, 또는 (5) 서열 번호:13의 아미노산 서열에 적어도 95%, 96%, 97%, 98% 또는 99% 서열 동일성을 가지는 아미노산 서열을 포함하고 서열 번호: 14의 아미노산 서열에 적어도 95%, 96%, 97%, 98% 또는 99% 서열 동일성을 가지는 아미노산 서열을 포함하는 항체. 한 구체예에서, GA101 항체는 IgG1 이소형 항체이다.
일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 인간화 B-Ly1 항체이다. 일부 구체예들에서, 인간화 B-Ly1 항체는 WO 2005/044859 및 WO 2007/031875에 개시된 인간화 B-Ly1 항체를 지칭하며, 이는 뮤린 모노클로날 항-CD20 항체 B-Ly1 (뮤린 중쇄 (VH)의 가변 영역: 서열 번호: 3; 뮤린 경쇄 (VL)의 가변 영역: 서열 번호: 4- Poppema, S. and Visser, L., Biotest Bulletin 3 (1987) 131-139 참조)로부터 IgG1의 인간 불변 도메인의 키메라화 이후 인간화에 의해 얻었다 (WO 2005/044859 및 WO 2007/031875 참조). 인간화 B-Ly1 항체는 WO 2005/044859 및 WO 2007/031875에 상세히 개시되어 있다.
일부 구체예들에서, 인간화 B-Ly1 항체는 서열 번호: 15-16 및 40-55의 그룹에서 선택된 중쇄의 가변 영역 (VH)을 가진다 (WO 2005/044859 및 WO 2007/031875의 B-HH2 내지 B-HH9 및 B-HL8 내지 B-HL17에 해당). 일부 구체예들에서, 가변 도메인은 서열 번호: 15, 16, 42, 44, 46, 48 및 50으로 구성된 그룹에서 선택된다 (WO 2005/044859 및 WO 2007/031875의 B-HH2, BHH-3, B-HH6, B-HH8, B-HL8, B-HL11 및 B-HL13에 해당). 일부 구체예들에서, 인간화 B-Ly1 항체는 서열 번호: 55의 경쇄 가변 영역(VL)을 갖는다 (WO 2005/044859 및 WO 2007/031875의 B-KV1에 해당). 일부 구체예들에서, 인간화 B-Ly1 항체는 서열 번호: 42의 중쇄 가변 영역 (VH) (WO 2005/044859 및 WO 2007/031875의 B-HH6에 해당) 및 서열 번호: 55의 경쇄 가변 영역 (VL) (WO 2005/044859 및 WO 2007/031875의 B-KV1에 해당)을 가진다. 일부 구체예들에서, 인간화 B-Ly1 항체는 IgG1 항체이다. 이러한 어푸코실화된 인간화 B-Ly1 항체는 WO 2005/044859, WO 2004/065540, WO 2007/031875, Umana, P. 외, Nature Biotechnol. 17 (1999) 176-180 및 WO 99/154342에 기재된 절차에 따라 Fc 영역에서 당조작 (glycoengineered, GE)된다. 일부 구체예들에서, 어푸코실화된 당조작 인간화 B-Ly1은 B-HH6-B-KV1 GE이다. 일부 구체예들에서, 항-CD20 항체는 오비누투주맙 (권장 INN, WHO Drug Information, Vol. 26, No. 4, 2012, p. 453)이다. 본원에서 사용되는, 오비누투주맙은 GA101 또는 RO5072759와 동의어이다. 이는 상표명 GAZYVA®로 치료 용도로 상업적으로 이용 가능하며 1000mg/40mL (25mg/mL) 단일 투여량 바이알로 제공된다. 이것은 모든 선행 버전들 (예를 들어, Vol. 25, No. 1, 2011, p.75-76)을 대체하며 이전에는 아푸투주맙으로 알려져 있었다 (권장 INN, WHO Drug Information, Vol. 23, No. 2, 2009, p. 176;Vol. 22, No. 2, 2008, p. 124). 일부 구체예들에서, 인간화 B-Ly1 항체는 서열 번호: 17의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 18의 아미노산 서열을 포함하는 경쇄를 포함하는 항체, 또는 이러한 항체의 항원-결합 단편이다. 일부 구체예들에서, 인간화 B-Ly1 항체는 서열 번호: 17의 3개의 중쇄 CDR을 포함하는 중쇄 가변 영역 및 서열 번호: 18의 3개의 경쇄 CDR을 포함하는 경쇄 가변 영역을 포함한다.
일부 구체예들에서, 일부 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항-CD20 항체는 Kabat 등의 넘버링에 따라, 오비누투주맙의 CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2, 및 CDR-L3를 포함한다. 일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항-CD20 항체는 오비누투주맙의 VH 및 VL을 포함한다. 일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항-CD20 항체는 오비누투주맙의 중쇄 및 경쇄를 포함한다.
일부 구체예들에서, 인간화 B-Ly1 항체는 어푸코실화된 당조작된 인간화 B-Ly1이다. 이러한 당조작된 인간화 B-Ly1 항체는 Fc 영역에서 변경된 당화 패턴을 가지며, 바람직하게는 감소된 수준의 푸코스 잔기를 갖는다. 일부 구체예들에서, 푸코스의 양은 Asn297에서 올리고당의 총량의 약 60% 이하이다 (한 구체예에서 푸코스의 양은 약 40% 내지 약 60%이고, 다른 구체예에서 푸코스의 양은 약 50% 이하이고, 또 다른 구체예에서 푸코스의 양은 약 30% 이하이다). 일부 구체예들에서, Fc 영역의 올리고당은 이등분된다. 이러한 당조작된 인간화 B-Ly1 항체는 증가된 ADCC를 가진다.
“리툭시맙과 비교한, 항-CD20 항체의 Raji 세포(ATCC-번호 CCL-86) 상의 CD20에 대한 결합능의 비율”은 실시예 2에 기재된 바와 같이 Raji 세포 (ATCC-번호 CCL-86)가 있는 FACSArray (Becton Dickinson)에서 상기 Cy5와 접합된 항-CD20 항체 및 Cy5와 접합된 리툭시맙을 사용하여 직접 면역형광 측정 (평균 형광 강도(MFI)가 측정됨)에 의해 결정되며, 다음과 같이 계산된다:
Raji 세포 (ATCC-번호 CCL-86) 상의 CD20에 대한 결합능의 비율 =
MFI는 평균 형광 강도이다. 본 명세서에서 “Cy5-표지 비율”은 항체 한 분자당 Cy5-표지 분자의 수를 의미한다.
통상적으로 상기 유형 II 항-CD20 항체는 상기 두 번째 항-CD20 항체의 Raji 세포 (ATCC-번호 CCL-86) 상의 CD20에 대한 결합능의 비율이 리툭시맙과 비교하여 0.3 내지 0.6이며, 그리고 한 구체예에서, 0.35 내지 0.55이고, 또한 또 다른 구체예에서, 0.4 내지 0.5이다.
“증가된 항체 의존성 세포 세포독성 (ADCC)을 갖는 항체”는, 본원에 정의된 바와 같이 당업자에게 공지된 임의의 적합한 방법에 의해 측정시 증가된 ADCC를 갖는 항체를 의미한다.
예시적으로 허용되는 시험관내 ADCC 분석은 아래에 설명되어 있다:
1) 이러한 분석은 항체의 항원 결합 영역에 의해 인식되는 표적 항원을 발현하는 것으로 알려진 표적 세포를 사용하고;
2) 이러한 분석은 무작위로 선택된 건강한 기증자의 혈액에서 단리된 인간 말초 혈액 단핵 세포 (PBMC)를 이펙터 세포로 사용하며;
3) 이러한 분석은 다음 프로토콜에 따라 수행된다:
i) PBMC를 표준 밀도 원심분리 절차를 사용하여 단리하고 RPMI 세포 배양 배지에서 5 x 106개 세포/ml로 현탁시킨다;
ii) 표적 세포들을 표준 조직 배양 방법으로 성장시키고, 생존력이 90% 이상인 지수 성장 단계에서 수확하고, RPMI 세포 배양 배지에서 세척하고, 51Cr의 100 마이크로-Curies로 표지시키고, 세포 배양 배지로 2회 세척하고, 105개 세포/ml의 밀도로 세포 배양 배지에 재현탁시키고;
iii) 100 마이크로리터의 상기 최종 표적 세포 현탁액을 96-웰 마이크로타이터 플레이트의 각 웰에 옮기고;
iv) 항체를 세포 배양 배지에서 4000ng/ml로부터 0.04ng/ml로 연속 희석하고 생성된 항체 용액 50마이크로리터를 96-웰 마이크로타이터 플레이트의 표적 세포에 첨가하여 상기 전체 농도 범위에 걸쳐 다양한 항체 농도를 3번 반복으로 검사하고;
v) 최대 방출(MR) 대조군의 경우, 상기 표지된 표적 세포들을 포함하는 플레이트의 3개 추가 웰들은 항체 용액 대신 50 마이크로리터의 2% (VN) 비-이온성 세제 수용액 (Nonidet, Sigma, St. Louis)을 제공받고 (상기 iv);
vi) 자발적 방출 (SR) 대조군의 경우, 표지된 표적 세포들을 포함하는 플레이트의 3개의 추가 웰들은 항체 용액 대신 50 마이크로리터의 RPMI 세포 배양 배지를 제공받고 (상기 iv);
vii) 그 후 96-웰 마이크로타이터 플레이트를 1분 동안 50 x g에서 원심분리하고 4°C에서 1시간 동안 인큐베이션하고;
viii) 50 마이크로리터의 PBMC 현탁액 (상기 i)을 각 웰에 첨가하여 25:1의 이펙터:표적 세포 비율을 생성하고 플레이트를 37℃에서 4시간 동안 5% CO2 대기 하의 인큐베이터에 두었으며;
ix) 각 웰의 무세포 상층액을 수확하고 감마 계수기를 사용하여 실험적으로 방출된 방사능(ER)을 정량하고;
x) 각 항체 농도에서 특이적 용해 백분율을 식 (ER-MR)/(MR-SR) x 100에 따라 계산하며, 여기서 ER은 해당 항체 농도에 대해 정량화된 (상기 ix 참조) 평균 방사능이고, MR은 MR 대조군 (상기 V 참조)에 대해 정량화된 (상기 ix 참조) 평균 방사능, SR은 SR 대조군 (위의 vi 참조)에 대해 정량화된 (상기 ix 참조) 평균 방사능이며;
4) “증가된 ADCC”는 상기 검사한 항체 농도 범위 내에서 관찰된 특이적 용해의 최대 백분율 증가 및 상기 검사한 항체 농도 범위 내에서 관찰된 특이적 용해의 최대 백분율의 1/2을 달성하는 데 필요한 항체 농도 감소로 정의된다. 한 구체예에서, ADCC의 증가는, 당업자에게 공지된 동일한 표준 생산, 정제, 제형 및 저장 방법을 사용하여 동일한 유형의 숙주 세포에 의해 생성된 동일한 항체에 의해 매개되는 상기 분석법으로 측정된 ADCC와 비교되며, 단, 비교 항체 (증가된 ADCC 결여)는 GnTIII을 과발현하도록 조작되거나 푸코실트랜스퍼라제 8 (FUT8) 유전자 (예를 들어, FUT8 녹아웃을 위해 조작된 것을 포함)로부터 발현이 감소되도록 조작된 숙주 세포에 의해 생산되지 않았다.
일부 구체예들에서, “증가된 ADCC”는 예를 들어, 상기 항체의 돌연변이 및/또는 당조작에 의해 얻을 수 있다. 일부 구체예들에서, 항-CD20 항체는 GlcNAc에 의해 이등분되는 항체의 Fc 영역에 부착된 바이안테나형 (biantennary) 올리고당을 갖도록 당조작된다. 일부 구체예들에서, 항-CD20 항체는 이러한 항체를 단백질 푸코실화가 결핍된 숙주 세포 (예를 들어, Lec13 CHO 세포 또는 알파-1,6-푸코실트랜스퍼라제 유전자 (FUT8)가 결실되거나 FUT 유전자 발현이 녹다운된 세포)에서 발현시킴으로써 Fc 영역에 부착된 탄수화물 상의 푸코스가 결핍되도록 당조작된다. 일부 구체예들에서, 항-CD20 항체 서열은 ADCC를 향상시키도록 Fc 영역이 조작되었다. 일부 구체예들에서, 이러한 조작된 항-CD20 항체 변이체는 Fc 영역의 위치 298, 333, 및/또는 334 (잔기는 EU 넘버링)에서 하나 이상의 아미노산 치환을 갖는 Fc 영역을 포함한다.
일부 구체예들에서, 용어 “보체 의존성 세포독성(CDC)”은 보체의 존재 하에서 본 발명에 따른 항체에 의한 인간 암 표적 세포의 용해를 지칭한다. CDC는 보체의 존재 하에 본 발명에 따른 항-CD20 항체로 CD20 발현 세포들의 제제를 처리함으로써 측정될 수 있다. CDC는 항체가 100nM의 농도에서 4시간 후 종양 세포의 20% 이상의 용해 (세포 사멸)를 유도하는 경우 발견된다. 일부 구체예들에서, 분석은 51Cr 또는 Eu 표지된 종양 세포 그리고 방출된 51Cr 또는 Eu의 측정으로 수행된다. 대조군은 표적 세포를 보체와 함께 그러나 항체 없이 인큐베이션 하는 것을 포함한다.
일부 구체예들에서, 항-CD20 항체는 모노클로날 항체, 예를 들어, 인간 항체이다. 일부 구체예들에서, 항-CD20 항체는 항체 단편, 예를 들어, Fv, Fab, Fab', scFv, 디아바디, 또는 F(ab')2 단편이다. 일부 구체예들에서, 항-CD20 항체는 실질적으로 전장 항체, 예를 들어, IgG1 항체, IgG2a 항체 또는 본원에 정의된 기타 항체 부류 또는 이소형이다.
일부 구체예들에서, 항-CD20 항체는 ABP 798 (Amgen, 미국), Zytux (AryoGen Pharmed, 이란), AcellBia/Usmal (Biocad, Russia), BI 695500 (Boehringer Ingelheim, 독일), Truxima (Celltrion, 한국), Blitzima (Celltrion, 한국), Ritemvia (Celltrion, 한국), Rituzena/ Tuxella (Celltrion, 한국), CT-P10 (Celltrion, 한국), Reditux (Dr Reddy's Laboratories, 인도), Maball (Hetero Group, 인도), MabTas (Intas Biopharmaceuticals, 인도), JHL1101 (JHL Biotech, 대만), Novex (RTXM83) (mAbxience/Laboratorio Elea, 스페인/아르헨티나), MabionCD20 (Mabion, 폴란드; Mylan, 인도), PF-05280586 (Pfizer, 미국), Kikuzubam (Probiomed, 멕시코), 리툭시맙 (Zenotech Laboratories), RituxiRel (Reliance Life Sciences, 인도), SAIT101 (Samsung BioLogics, 한국), Rixathon/ Riximyo (GP2013) (Sandoz, 스위스), HLX01 (Shanghai Henlius Biotech, 중국), TL011 (Teva Pharmaceutical Industries, 이스라엘; Lonza, 스위스), 또는 Redditux (TRPharma, 터키)이다.
VI. 항체
일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 아래 기재된 특징들을 단독으로 또는 조합하여 포함할 수 있다.
A. 항체 친화도
특정 구체예들에서, 본원에서 제공되는 치료 방법에서 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 ≤ 1μM, ≤ 100 nM, ≤ 50 nM, ≤ 10 nM, ≤ 5 nM, ≤ 1 nM, ≤ 0.1 nM, ≤ 0.01 nM, 또는 ≤ 0.001 nM의 해리 상수 (Kd)를 가지며, 선택적으로 ≥ 10-13 M이다. (예를 들어, 10-8 M 이하, 예를 들어, 10-8 M 내지 10-13 M, 예를 들어, 10-9 M 내지 10-13 M).
한 구체예에서, Kd는 다음과 같은 분석에 의해 설명된 바와 같이 관심 항체의 Fab 버전 및 이의 항원으로 수행된 방사성 표지된 항원 결합 분석(RIA)에 의해 측정된다. 항원에 대한 Fab의 용액 결합 친화도는 표지되지 않은 항원의 적정 시리즈 (a titration series) 존재하에 Fab를 최소 농도의 (125I) 표지된 항원으로 평형화한 다음, 결합된 항원을 항-Fab 항체 코팅된 플레이트로 포획하여 측정한다 (예를 들어, Chen 외, J. Mol. Biol. 293:865-881(1999) 참조). 분석 조건을 설정하기 위해 MICROTITER® 다중 웰 플레이트 (Thermo Scientific)를 50mM 탄산나트륨 (pH 9.6) 중 5 μg/ml의 포획 항-Fab 항체(Cappel Labs)로 밤새 코팅한 다음, PBS 중 2%(w/v) 소 혈청 알부민으로 실온 (약 23°C)에서 2~5시간 동안 차단시켰다. 비흡착 플레이트 (Nunc #269620)에서 100pM 또는 26pM [125I]-항원을 관심 Fab의 연속 희석액과 혼합한다 (예를 들어, Presta 외, Cancer Res. 57:4593-4599 (1997)의 항-VEGF 항체, Fab-12의 평가와 일치). 그런 다음 관심 Fab를 밤새 인큐베이션한다. 그러나 인큐베이션은 평형에 도달하도록 더 오랜 기간 (예를 들어, 약 65시간) 동안 계속될 수 있다. 그 후, 혼합물을 실온에서의 인큐베이션 (예를 들어, 1시간 동안)을 위해 포획 플레이트로 옮긴다. 그런 다음 용액을 제거하고 플레이트를 PBS 중 0.1% 폴리소르베이트 20 (TWEEN-20®) 으로 8회 세척한다. 플레이트가 건조되면 150 μl/웰의 섬광제 (MICROSCINT-20 TM; Packard)를 추가하고 플레이트를 TOPCOUNT™감마 카운터(Packard)에서 10분 동안 계수한다. 경쟁 결합 분석에 사용하기 위해 최대 결합의 20% 이하를 제공하는 각 Fab의 농도가 선택된다.
또 다른 구체예에 따르면, Kd는 ~10 반응 단위 (RU)에서 고정된 항원 CM5 칩과 함께 25℃에서 BIACORE®-2000 또는 BIACORE®-3000을 사용하여 표면 플라즈몬 공명 분석을 사용하여 측정된다. 간단히 말해서, 카르복시메틸화된 덱스트란 바이오센서 칩(CM5, BIACORE, Inc.)은 공급업체의 지침에 따라 N-에틸-N'-(3-디메틸아미노프로필)-카르보디이미드 하이드로클로라이드 (EDC) 및 N-하이드록시숙신이미드(NHS)로 활성화된다. 항원은 10 mM 소듐 아세테이트, pH 4.8을 이용하여 5 μg/ml (~0.2 μM)으로 희석시킨 후, 5 μl/분의 유속으로 주사하여 결합된 단백질의 대략 10 반응 단위 (RU)를 얻는다. 항원 주사 후, 1M 에탄올아민을 주사하여 반응하지 않은 그룹을 차단한다. 운동성 측정을 위하여, 2-배 연속 희석된 Fab (예를 들어, 0.78 nM 내지 500 nM)는 25°C, 대략적으로 25 μl/분의 유속에서 0.05% 폴리소르베이트 20 (TWEEN-20TM) 계면활성제가 포함된 PBS (PBST)에 주사된다. 결합(association)과 해리(dissociation) 센서그램을 동시에 피팅함으로써, 단순 일대일 Langmuir 결합 모델 (BIAcore Evaluation Software 버전 3.2)을 이용하여 결합 속도 (kon)와 해리 속도 (koff)가 산출된다. 평형 해리 상수 (Kd)는 비율 kon/koff로 계산된다. 예를 들어, Chen 등, J. Mol. Biol. 293:865-881 (1999) 참조. 상기 표면 플라스몬 공명 분석에 의한 결합 속도(on-rate)가 106 M-1s-1를 초과한다면, 그 다음 분광계, 이를 테면 정지-유동(stop-flow) 장착된 분광광도계 (Aviv Instruments) 또는 교반 큐벳(stirred cuvette)이 있는 8000-일련의 SLM-Aminco TM 분광광도계 (ThermoSpectronic)에서 측정되었을 때, 항원 농도를 증가시킨 상태하에서, PBS, pH 7.2안에 20 nM 항-항원 항체 (Fab 형태)의 25°C 형광 방출 강도 (여기(excitation)= 295 nm; 방출 = 340 nm, 16 nm 밴드-대역)을 측정하는 형광 퀀칭 기술을 이용하여 결합이 결정될 수 있다.
B. 항체 단편
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 항체 단편이다. 항체 단편은, Fab, Fab', Fab'-SH, F(ab')2, Fv, 및 scFv 단편, 및 하기 기재된 기타 단편들을 포함하지만 이에 제한되지는 않는다. 특정 항체 단편의 검토는, Hudson 외, Nat. Med. 9:129-134 (2003)를 참조하라. scFv 단편의 검토를 위해, 예를 들어, Pluckthun, in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994)를 참조하라; 또한 WO 93/16185; 및 미국 특허 제 5,571,894 및 5,587,458을 참조하라. 구난 수용체 결합 에피토프 잔기를 포함하고 생체내 반감기가 증가된 Fab 및 F(ab')2 단편에 대한 논의는 미국 특허 제 5,869,046을 참조하라.
디아바디는 2가 또는 이중 특이적일 수 있는 2개의 항원 결합 부위가 있는 항체 단편이다. 예를 들어, EP 404,097; WO 1993/01161; Hudson 외, Nat. Med. 9:129-134 (2003); 및 Hollinger 외, Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993)를 참조하라. 트리아바디 및 테트라바디 또한 Hudson 외, Nat. Med. 9:129-134 (2003)에 기재되어 있다.
단일-도메인 항체는 항체의 중쇄 가변 도메인의 전부 또는 일부 또는 경쇄 가변 도메인의 전부 또는 일부를 포함하는 항체 단편이다. 특정 구체예들에서, 단일 도메인 항체는 인간 단일 도메인 항체이다 (Domantis, Inc., Waltham, MA; 예를 들어, 미국 특허 제 6,248,516 B1 참조).
항체 단편은 본원에 기재된 바와 같이, 무손상 항체의 단백질분해 소화, 뿐만 아니라 재조합 숙주 세포 (예를 들어, 대장균 또는 파지)에 의한 생산을 포함한 (그러나 이에 제한되지 않음) 다양한 기술에 의해 제조될 수 있다.
C. 키메라 및 인간화 항체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 키메라 항체이다. 특정 키메라 항체는, 예를 들어, 미국 특허 제 4,816,567; 및 Morrison 외, Proc. Natl. Acad. Sci. USA, 81:6851-6855 (1984))에 기재되어 있다. 한 예에서, 키메라 항체는 비인간 가변 영역 (예를 들어, 마우스, 래트, 햄스터, 토끼, 또는 원숭이와 같은 비인간 영장류로부터 유래된 가변 영역) 및 인간 불변 영역을 포함한다. 추가 예에서, 키메라 항체는 클래스 또는 서브클래스가 모 항체의 그것로부터 변경된 “클래스 전환된” 항체이다. 키메라 항체는 이의 항원-결합 단편을 포함한다.
특정 구체예들에서, 키메라 항체는 인간화 항체이다. 전형적으로, 비-인간 항체는 비-인간 모 항체의 특이성 및 친화도를 유지하면서 인간에 대한 면역원성을 감소시키기 위해 인간화된다. 일반적으로, 인간화 항체는 HVR, 예를 들어 CDR, (또는 이의 일부)이 비-인간 항체로부터 유래되고 FR (또는 이의 일부)이 인간 항체 서열로부터 유래되는 하나 이상의 가변 도메인을 포함한다. 인간화 항체는 선택적으로 인간 불변 영역의 적어도 일부를 또한 포함할 것이다. 일부 구체예들에 있어서, 인간화된 항체에서 일부 FR 잔기는 비-인간 항체 (예로써, HVR 잔기가 유도된 항체)의 대응 잔기로 대체되어, 예로써, 항체 특이성 또는 친화도가 복원 또는 개선된다.
인간화 항체 및 이의 제조 방법은, 예를 들어, Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008)에 논의되어 있으며, 예를 들어, Riechmann 외, Nature 332:323-329 (1988); Queen 외, Proc. Nat'l Acad. Sci. USA 86:10029-10033 (1989); 미국 특허 제 5, 821,337, 7,527,791, 6,982,321, 및 7,087,409; Kashmiri 외, Methods 36:25-34 (2005) (SDR (a-CDR) 이식을 기재); Padlan, Mol. Immunol. 28:489-498 (1991) (“표면노출잔기변형(resurfacing)”을 기재); Dall'Acqua 외, Methods 36:43-60 (2005) (“FR 셔플링”을 기재); 및 Osbourn 외, Methods 36:61-68 (2005) 및 Klimka 외, Br. J. Cancer, 83:252-260 (2000) (FR 셔플링으로의 “유도된 선별” 접근법을 기재)에 상세히 기재되어 있다.
인간화에 사용될 수 있는 인간 프레임워크 영역은 다음을 포함하나 이에 제한되는 것은 아니다: “최적화” 방법을 사용하여 선택된 프레임워크 영역 (예를 들어, Sims 외, J. Immunol. 151:2296 (1993) 참조); 경쇄 또는 중쇄 가변 영역의 특정 하위그룹의 인간 항체의 공통 서열로부터 유래된 프레임워크 영역 (예를 들어, Carter 외, Proc. Natl. Acad. Sci. USA, 89:4285 (1992); 및 Presta 외, J. Immunol., 151:2623 (1993) 참조); 인간 성숙 (체세포 돌연변이) 프레임워크 영역 또는 인간 생식계열 프레임워크 영역 (예를 들어, Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008) 참조); 그리고 스크리닝 FR 라이브러리로부터 유래된 프레임워크 영역 (예를 들어, Baca 외, J. Biol. Chem. 272:10678-10684 (1997) 및 Rosok 외, J. Biol. Chem. 271:22611-22618 (1996) 참조).
D. 인간 항체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 인간 항체이다. 인간 항체는 해당 분야에 공지된 다양한 기술을 사용하여 생산될 수 있다. 인간 항체는 일반적으로 van Dijk and van de Winkel, Curr. Opin. Pharmacol. 5: 368-74 (2001) 및 Lonberg, Curr. Opin. Immunol. 20:450-459 (2008)에 기재되어 있다.
인간 항체는 항원 공격에 반응하여 무손상 인간 항체 또는 인간 가변 영역을 갖는 무손상 항체를 생산하도록 변형된 형질전환 동물에 면역원을 투여함으로써 제조될 수 있다. 이러한 동물은 일반적으로 내인성 면역글로불린 유전자좌를 대체하는, 또는 염색체외에 존재하거나 동물의 염색체에 무작위로 통합된, 인간 면역글로불린 유전자좌의 전체 또는 일부를 포함한다. 이러한 유전자삽입 마우스에서 상기 내인성 면역글로불린 좌위는 일반적으로 비활성화 되어 있다. 형질전환 동물로부터 인간 항체를 얻는 방법에 대한 검토는 Lonberg, Nat. Biotech. 23:1117-1125 (2005)를 참조하라. 또한, 예를 들어, XENOMOUSETM 기술을 기재하는 미국 특허 제 6,075,181 및 6,150,584; HuMab® 기술을 기재하는 미국 특허 제 5,770,429; K-M MOUSE® 기술을 기재하는 미국 특허 제 7,041,870, 그리고 VelociMouse® 기술을 기재하는 미국 특허출원 공개공보 US 2007/0061900)를 참조하라. 이러한 동물에 의해 생성된 무손상 항체로부터의 인간 가변 영역은 예를 들어 상이한 인간 불변 영역과 조합함으로써 추가로 변형될 수 있다.
인간 항체는 하이브리도마 기반 방법으로도 만들 수 있다. 인간 모노클로날 항체의 생산을 위한 인간 골수종 및 마우스-인간 이종골수종 세포주가 기재되어 있다. (예를 들어, Kozbor J. Immunol., 133: 3001 (1984); Brodeur 외, Monoclonal Antibody Production Techniques and Applications, pp. 51-63 (Marcel Dekker, Inc., New York, 1987); and Boerner 외, J. Immunol., 147: 86 (1991). 참조) 인간 B-세포 하이브리도마 기술을 통해 생성된 인간 항체는 또한 Li 외, Proc. Natl. Acad. Sci. USA, 103:3557-3562 (2006)에 기재되어 있다. 또 다른 방법에는 예를 들어 미국 특허 제 7,189,826 (하이브리도마 세포주로부터 모노클로날 인간 IgM 항체의 생산 설명) 및 Ni, Xiandai Mianyixue, 26(4):265-268 (2006) (인간-인간 하이브리도마 설명)에 기재된 방법들이 포함된다. 인간 하이브리도마 기술 (Trioma 기술)은 또한 Vollmers and Brandlein, Histology and Histopathology, 20(3):927-937 (2005) 및 Vollmers and Brandlein, Methods and Findings in Experimental and Clinical Pharmacology, 27(3):185-91 (2005)에 기재되어 있다.
인간 항체는 또한 인간 유래 파지 디스플레이 라이브러리로부터 선별된 Fv 클론 가변 도메인 서열을 단리함으로써 생성될 수 있다. 그런 다음 이러한 가변 도메인 서열은 원하는 인간 불변 도메인과 조합될 수 있다. 항체 라이브러리에서 인간 항체를 선별하는 기술이 아래에 설명되어 있다.
E. 라이브러리-유래 항체
일부 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 조합 라이브러리들을 원하는 활성 또는 활성들을 갖는 항체들에 대해 스크리닝함으로써 단리될 수 있다. 예를 들어, 파지 디스플레이 라이브러리들을 생성하고 이러한 라이브러리들을 원하는 결합 특성을 갖는 항체에 대해 스크리닝하기 위한 다양한 방법이 해당 분야에 공지되어 있다. 이러한 방법들은, 예를 들어, Hoogenboom 외, in Methods in Molecular Biology 178:1-37 (O'Brien 외, ed., Human Press, Totowa, NJ, 2001)에 검토되어 있으며, 예를 들어, McCafferty 외, Nature 348:552-554; Clackson 외, Nature 352: 624-628 (1991); Marks 외, J. Mol. Biol. 222: 581-597 (1992); Marks and Bradbury, in Methods in Molecular Biology 248:161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu 외, J. Mol. Biol. 338(2): 299-310 (2004); Lee 외, J. Mol. Biol. 340(5): 1073-1093 (2004); Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004); 및 Lee 외, J. Immunol. Methods 284(1-2): 119-132(2004)에 더 상세히 설명되어 있다.
특정 파지 디스플레이 방법에서, VH 및 VL 유전자의 레퍼토리들은, Winter 외, Ann. Rev. Immunol., 12: 433-455 (1994)에 기재된 바와 같이 중합효소 연쇄 반응(PCR)에 의해 개별적으로 클로닝되고 파지 라이브러리들에서 무작위로 재조합된 후, 항원-결합 파지에 대해 스크리닝 될 수 있다. 파지는 일반적으로 항체 단편들을 단일 사슬 Fv(scFv) 단편 또는 Fab 단편으로 표시한다. 면역화된 공급원으로부터의 라이브러리는 하이브리도마를 제작할 필요없이 면역원에 대한 고-친화도 항체를 제공한다. 대안적으로, 나이브 레퍼토리는 Griffiths 외, EMBO J, 12: 725-734 (1993)에 기재된 바와 같이 (예를 들어, 인간으로부터) 복제되어, 면역화 없이 광범위한 자가 항원 및 자가 항원들에 대한 하나의 항체 공급원을 제공할 수 있다. 마지막으로, 나이브 라이브러리는 Hoogenboom and Winter, J. Mol. Biol., 227: 381-388 (1992)에 기재된 바와 같이 줄기 세포로부터 재배열되지 않은 V-유전자 절편들을 복제하고 무작위 서열을 포함하는 PCR 프라이머를 사용하여 고도로 가변적인 CDR3 영역을 인코딩하고 시험관내 재배열을 수행함으로써 합성적으로 제조될 수도 있다. 인간 항체 파지 라이브러리들을 설명하는 특허 문헌들에는, 예를 들어: 미국 특허 제 5,750,373, 및 미국 특허출원 공개공보 제 2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936, 및 2009/0002360을 포함한다.
인간 항체 라이브러리로부터 단리된 항체 또는 항체 단편은 본원에서 인간 항체 또는 인간 항체 단편으로 간주된다.
F. 다중특이적 항체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 다중특이적 항체, 예를 들어, 이중특이적 항체이다. 다중특이적 항체는 적어도 2개의 상이한 부위에 대한 결합 특이성을 갖는 모노클로날 항체이다. 특정 구체예들에서, 결합 특이성 중 하나는 하나의 항원 (예를 들어, CD79b 또는 CD20)에 대한 것이고 다른 하나는 임의의 다른 항원에 대한 것이다. 특정 구체예들에서, 결합 특이성 중 하나는 하나의 항원 (예를 들어, CD79b 또는 CD20)에 대한 것이고 다른 하나는 CD3에 대한 것이다. 예를 들어, 미국 특허 제 5,821,337 참조. 특정 구체예들에서, 이중특이적 항체는 단일 항원 (예를 들어, CD79b 또는 CD20)의 2개의 상이한 에피토프에 결합할 수 있다. 이중특이적 항체는 또한 세포독성제를 항원 (예를 들어, CD79b 또는 CD20)을 발현하는 세포에 국재화하는데 사용될 수 있다. 이중특이적 항체는 전장 항체 또는 항체 단편으로 제조될 수 있다.
다중특이성 항체를 제조하기 위한 기술에는 상이한 특이성을 갖는 2개의 면역글로불린 중쇄-경쇄 쌍의 재조합 공동 발현 (Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, 및 Traunecker 외, EMBO J. 10: 3655 (1991) 참조), 및 “놉-인-홀” 조작 (예를 들어, 미국 특허 제 5,731,168 참조)이 포함되지만 이에 제한되지는 않는다. 다중특이성 항체는 또한 항체 Fc-이종이량체 분자를 만들기 위해 정전기 조정 효과를 조작하여 (WO 2009/089004A1); 2개 이상의 항체 또는 단편을 가교하여 (예를 들어, 미국 특허 제 4,676,980, 및 Brennan 외, Science, 229: 81 (1985) 참조); 류신 지퍼를 사용하여 이중특이적 항체를 생산하여 (예를 들어, Kostelny 외, J. Immunol., 148(5):1547-1553 (1992) 참조); “디아바디” 기술을 사용하여 이중특이적 항체 단편들을 제조하여 (예를 들어, Hollinger 외, Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993) 참조); 그리고 단일-사슬 Fv (sFv) 이량체들을 사용하여 (예를 들어, Gruber 외, J. Immunol., 152:5368 (1994) 참조); 그리고 예를 들어, Tutt 외, J. Immunol. 147: 60 (1991)에 기재된 바와 같이 삼중특이성 항체를 제조하여 제조될 수 있다.
“옥토퍼스 항체”를 포함하여 3개 이상의 기능적 항원 결합 부위를 갖는 조작된 항체도 본 발명에 포함된다 (예를 들어, US 2006/0025576A1 참조).
본원의 항체 또는 단편은 또한 CD79b 뿐만 아니라 다른 상이한 항원에 결합하는 항원 결합 부위를 포함하는 “이중 작용 FAb” 또는 “DAF”를 포함한다 (예를 들어, US 2008/0069820 참조).
G. 항체 변이체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)의 아미노산 서열 변이체가 고려된다. 예를 들어, 항-CD79b 항체 또는 항-CD20 항체의 결합 친화도 및/또는 기타 생물학적 특성을 개선하는 것이 바람직할 수 있다. 항체의 아미노산 서열 변이체는 항체를 인코딩하는 뉴클레오티드 서열에 적절한 변형을 도입함으로써 또는 펩티드 합성에 의해 제조될 수 있다. 이러한 변형은 예를 들어 항체의 아미노산 서열 내의 잔기들로부터의 결실 및/또는 이들 내부로의 삽입 및/또는 이들의 치환을 포함한다. 최종 구조체가 원하는 특성, 예를 들어, 항원 결합을 보유하는 한, 최종 구조체에 도달하기 위한 어떠한 결실, 삽입 및 치환의 조합이라도 이루어질 수 있다.
(i) 치환, 삽입, 및 결실 변이체
특정 구체예들에서, 하나 이상의 아미노산 치환을 갖는 항체 변이체가 제공된다. 치환 돌연변이유발에 대한 관심 부위는 HVR 및 FR을 포함한다. 보존적 치환들을 표 D 에서 “바람직한 치환”이라는 제목으로 나타낸다. 더 많은 실질적인 변화가 표 D 의 “예시적 치환”이라는 제목하에 제시되며, 이는 아미노산 측쇄 클래스를 참조하여 이하에서 추가로 설명된다. 아미노산 치환을 관심 항체에 도입하고 원하는 활성, 예를 들어 유지/개선 항원 결합, 감소된 면역원성, 또는 개선된 ADCC 또는 CDC에 대해 생성물을 스크리닝할 수 있다.
표 D
아미노산은 공통적인 측쇄 특성에 따라 다음과 같이 그룹화될 수 있다:
(1) 소수성: 노르류신, Met, Ala, Val, Leu, Ile;
(2) 중성 친수성: Cys, Ser, Thr, Asn, Gln;
(3) 산성: Asp, Glu;
(4) 염기성: His, Lys, Arg;
(5) 측쇄 방향에 영향을 주는 잔기: Gly, Pro;
(6) 방향족: Trp, Tyr, Phe.
비-보존적 치환은 이들 분류들 중 하나의 구성원을 또 다른 분류로 바꾸게 될 것이다.
치환 변이체의 한 유형은 모 항체 (예를 들어, 인간화 또는 인간 항체)의 하나 이상의 초가변 영역 잔기를 치환하는 것을 포함한다. 일반적으로, 추가 연구를 위해 선택된 생성된 변이체(들)는 모 항체에 비해 특정 생물학적 특성(예를 들어, 증가된 친화도, 감소된 면역원성)에서 변형 (예를 들어, 개선)을 가질 것이고 및/또는 모 항체의 특정 생물학적 특성을 실질적으로 보유할 것이다. 예시적인 치환 변이체는 친화도 성숙 항체이며, 이는 예를 들어 본원에 기재된 것과 같은 파지 디스플레이 기반 친화도 성숙 기술을 사용하여 편리하게 생성될 수 있다. 간단히 말해서, 하나 이상의 HVR 잔기를 돌연변이시키고 변이체 항체가 파지 상에 제시되고 특정 생물학적 활성 (예를 들어, 결합 친화도)에 대해 스크리닝된다.
예를 들어, 항체 친화성을 개선하기 위해 HVR에서 변경 (예를 들어, 치환)이 이루어질 수 있다. 이러한 변경은 HVR “핫스팟”, 즉, 체세포 성숙 과정 동안 높은 빈도로 돌연변이를 거치는 코돈들에 의해 인코딩되는 잔기 (예를 들어, Chowdhury, Methods Mol. Biol. 207:179-196 (2008) 참고), 및/또는 SDR (a-CDR)에서 이루어질 수 있으며, 생성된 변이체 VH 또는 VL을 결합 친화도에 대해 검사한다. 보조 라이브러리를 구성하고 재선택함에 의한 친화도 성숙은, 예를 들어, Hoogenboom 외, Methods in Molecular Biology 178:1-37에 기재되어 있다 (O'Brien 외, ed., Human Press, Totowa, NJ, (2001).) 친화도 성숙의 일부 구체예에서, 다양성은 성숙을 위해 선택된 가변 유전자 내부로 임의의 다양한 방법 (예를 들어, 에러-프론 PCR, 사슬 셔플링, 또는 올리고뉴클레오티드-지정 돌연변이유발)에 의해 도입된다. 그런 다음 보조 라이브러리가 생성된다. 그런 다음 라이브러리를 스크리닝하여 원하는 친화도를 가진 항체 변이체를 식별한다. 다양성을 도입하는 또 다른 방법은 여러 HVR 잔기 (예를 들어, 한 번에 4-6개 잔기)를 무작위화하는 HVR-지시형 접근 방식(HVR-directed approaches)을 포함한다. 항원 결합에 관여하는 HVR 잔기는 예를 들어 알라닌 스캐닝 돌연변이유발 또는 모델링을 사용하여 구체적으로 확인될 수 있다. 특히 CDR-H3 및 CDR-L3이 표적이 되는 경우가 많다.
특정 구체예들에서, 치환, 삽입 또는 결실은 그러한 변경이 항원에 결합하는 항체의 능력을 실질적으로 감소시키지 않는 한 하나 이상의 HVR 내에서 발생할 수 있다. 예를 들어, 결합 친화도를 실질적으로 감소시키지 않는 보존적 변경 (예를 들어, 본원에 제공된 보존적 치환)이 HVR에서 이루어질 수 있다. 이러한 변경은 HVR “핫스팟” 또는 SDR 외부에 있을 수 있다. 상기 제공된 변이체 VH 및 VL 서열의 특정 구체예에서, 각각의 HVR은 변경되지 않거나 1개, 2개 또는 3개 이하의 아미노산 치환을 포함한다.
돌연변이유발을 위해 표적화될 수 있는 항체의 잔기 또는 영역을 식별하는데 유용한 방법은 “알라닌 스캐닝 돌연변이유발”로 지칭되며, Cunningham and Wells (1989) Science, 244:1081-1085에 기재되어 있다. 이 방법에서, 표적 잔기 또는 표적 잔기들의 그룹 (예컨대, 하전된 잔기, 가령 Arg, Asp, His, Lys, 및 Glu)이 식별되고, 중성 또는 음으로 하전된 아미노산 (예컨대, 알라닌 또는 폴리알라닌)으로 대체되어, 항원과 항체의 상호작용이 영향을 받았는지를 판단한다. 초기 치환에 대한 기능적 민감성을 나타내는 아미노산 위치에 추가 치환이 도입될 수 있다. 대안적으로, 또는 추가적으로, 항원-항체 복합체의 결정 구조를 사용하여 항체와 항원 사이의 접촉점을 식별한다. 이러한 접촉 잔기 및 인접 잔기는 치환 후보로서 표적화되거나 제거될 수 있다. 변이체들이 원하는 성질을 포함하는지 여부를 결정하기 위해 이들을 스크리닝할 수 있다.
아미노산 서열 삽입은 1개 잔기에서 100개 이상의 잔기를 함유하는 폴리펩티드에 이르는 길이 범위의 아미노- 및/또는 카르복실-말단 융합, 뿐만 아니라 단일 또는 다중 아미노산 잔기의 서열내 삽입을 포함한다. 말단 삽입의 예는 N-말단 메티오닐 잔기를 갖는 항체를 포함한다. 항체 분자의 다른 삽입 변이체는 항체의 혈청 반감기를 증가시키는 효소(예를 들어, ADEPT의 경우) 또는 폴리펩티드에 대한 항체의 N- 또는 C-말단에 대한 융합을 포함한다.
(ii) 당화 변이체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 항체가 당화되는 정도를 증가 또는 감소시키도록 변경된다. 항체에 대한 당화 부위의 부가 또는 결실은 하나 이상의 당화 부위가 생성되거나 제거되도록 아미노산 서열을 변경함으로써 편리하게 이루어질 수 있다.
항체가 Fc 영역을 포함하는 경우, 이에 부착된 탄수화물이 변경될 수 있다. 포유동물 세포에 의해 생산된 천연 항체는 일반적으로 Fc 영역의 CH2 도메인의 Asn297에 대한 N-링키지에 의해 부착되는 분지형 바이안테나형 올리고당을 포함한다. 예를 들어, Wright 외, TIBTECH 15:26-32 (1997) 참조. 올리고당은 바이안테나형 올리고당 구조의 “줄기”에 다양한 탄수화물, 예를 들어 만노오스, N-아세틸 글루코사민(GlcNAc), 갈락토오스 및 시알산을 포함할 수 있을 뿐만 아니라 GlcNAc에 부착된 푸코스를 포함할 수 있다. 일부 구체예들에서, 특정 개선된 특성을 갖는 항체 변이체를 생성하기 위해 본 발명의 항체에서 올리고당의 변형이 이루어질 수 있다.
한 구체예에서, Fc 영역에 (직접적으로 또는 간접적으로) 부착된 푸코스가 없는 탄수화물 구조를 갖는 항체 변이체가 제공된다. 예를 들어, 이러한 항체에서 푸코스의 양은 1% 내지 80%, 1% 내지 65%, 5% 내지 65% 또는 20% 내지 40%일 수 있다. 푸코스의 양은 예를 들면, WO 2008/077546에서 설명된 바와 같이 MALDI-TOF 질량 분광분석에 의해 측정하여, Asn 297에 부착된 모든 당구조 (예컨대, 복합체, 하이브리드 및 높은 만노스 구조)의 합에 대한, Asn297에서 당 사슬 내부의 평균 푸코스 양을 계산함으로써 결정된다. Asn297은 Fc 영역의 약 297번 위치에 위치한 아스파라긴 잔기 (Fc 영역 잔기는 Eu 넘버링)를 나타내며; 그러나 Asn297은 또한 항체의 경미한 서열 변이로 인해 위치 297의 약 ± 3 아미노산 상류 또는 하류, 즉, 위치 294 내지 300에 위치할 수 있다. 이러한 푸코실화 변이체는 개선된 ADCC 기능을 가질 수 있다. 예를 들어, 미국 특허출원 공개공보 제 US 2003/0157108 (Presta, L.); US 2004/0093621 (Kyowa Hakko Kogyo Co., Ltd) 참조. “탈푸코실화” 또는 “푸코스-결핍” 항체 변이체들과 관련된 문헌들의 예는 다음을 포함한다: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki 외, J. Mol. Biol. 336:1239-1249 (2004); Yamane-Ohnuki 외, Biotech. Bioeng. 87: 614 (2004). 탈푸코실화 항체를 생산할 수 있는 세포주의 예에는 단백질 푸코실화가 결핍된 Lec13 CHO 세포 (Ripka 외, Arch. Biochem. Biophys. 249:533-545 (1986); 미국 특허출원 US 2003/0157108 A1, Presta, L; 및 WO 2004/056312 A1, Adams 외, 특히 실시예 11), 및 녹아웃 세포주, 예를 들어, 알파-1,6-푸코실트랜스퍼라제 유전자, FUT8, 녹아웃 CHO 세포 (예를 들어, Yamane-Ohnuki 외, Biotech. Bioeng. 87: 614 (2004); Kanda, Y. 외, Biotechnol. Bioeng., 94(4):680-688 (2006); 및 WO2003/085107 참조)가 포함된다.
항체의 Fc 영역의 이촉각성 올리고당이 GlcNAc에 의해 양분되어 있는, 양분된 올리고당을 가진 항체 변이체들이 추가로 제공된다. 이러한 항체 변이체는 감소된 푸코실화 및/또는 개선된 ADCC 기능을 가질 수 있다. 이러한 항체 변이체의 예는, 예를 들어, WO 2003/011878 (Jean-Mairet 외,); 미국 특허 제 6,602,684 (Umana 외,); 및 US 2005/0123546 (Umana 외,)에 기재되어 있다. Fc 영역에 부착된 올리고당에 적어도 하나의 갈락토스 잔기를 갖는 항체 변이체가 또한 제공된다. 이러한 항체 변이체는 개선된 CDC 기능을 가질 수 있다. 이러한 항체 변이체는 예를 들어, WO 1997/30087 (Patel 외,); WO 1998/58964 (Raju, S.); 및 WO 1999/22764 (Raju, S.)에 기재되어 있다.
(iii) Fc 변이체
특정 구체예에서, 하나 이상의 아미노산 변형이 본원에 제공된 치료 방법에 사용되는 항체(예를 들어, 항-CD79b 항체 또는 항-CD20 항체)의 Fc 영역 내로 도입되어 Fc 영역 변이체를 생성할 수 있다. Fc 영역 변이체는 하나 이상의 아미노산 위치에서 아미노산 변형(예를 들어, 치환)을 포함하는 인간 Fc 영역 서열(예를 들어, 인간 IgG1, IgG2, IgG3 또는 IgG4 Fc 영역)을 포함할 수 있다.
특정 구체예들에서, 본 발명은 모든 이펙터 기능이 아닌 일부를 보유하는 항체 변이체를 고려하는데, 이는 생체내에서 항체의 반감기가 중요하지만 또한 특정 이펙터 기능 (가령, 보체 및 ADCC)이 불필요하거나 유해한 응용분야에 있어서 바람직한 후보가 되게 한다. 시험관내 및/또는 생체내 세포독성 분석을 실행하여 CDC 및/또는 ADCC 활성의 감소/고갈을 확인할 수 있다. 예를 들면, Fc 수용체 (FcR) 결합 분석을 수행하여 상기 항체가 FcgR 결합은 없으나 (그리하여 ADCC 활성이 없을 수 있음), FcRn 결합 능력은 유지함을 확인할 수 있다. ADCC를 조정하는 주요 세포, NK 세포들은 오직 Fc(RIII만을 발현시키지만, 단핵구는 Fc(RI, Fc(RII 및 Fc(RIII를 발현시킨다. 조혈 세포들에서 FcR 발현은 Ravetch and Kinet, Annu. Rev. Immunol. 9:457-492 (1991)의 페이지 464의 표 3에 요약되어 있다. 관심 분자의 ADCC 활성을 평가하기 위한 시험관내 분석의 비제한적 실시예는 미국 특허 제 5,500,362 (예컨대, Hellstrom, I. 외. Proc. Nat'l Acad. Sci. USA 83:7059-7063 (1986) 참고) 및 Hellstrom, I 외, Proc. Nat'l Acad. Sci. USA 82:1499-1502 (1985); 5,821,337 (Bruggemann, M. 외, J. Exp. Med. 166:1351-1361 (1987) 참고)에 설명되어 있다. 대안으로, 비-방사능활성 분석 방법들이 이용될 수 있다 (예를 들면, 유동 세포측정을 위한 ACTI™ 비-방사능활성 세포독성 분석 (CellTechnology, Inc. Mountain View, CA); 그리고 CytoTox 96® 비-방사능활성 세포독성 분석 (Promega, Madison, WI) 참고). 이러한 분석에 유용한 이펙터 세포들은 말초 혈액 단핵 세포들 (PBMC) 및 자연 살해 (NK) 세포들을 포함한다. 대안으로, 또는 추가적으로, 관심 분자의 ADCC 활성은, 예컨대, Clynes 외. Proc. Nat'l Acad. Sci. USA 95:652-656 (1998)에서 공개된 바와 같은 동물 모델에서 생체내에서 평가될 수 있다. 상기 항체가 C1q에 결합할 수 없고, 이로 인하여 CDC 활성이 결여된다는 것을 확인하기 위하여 C1q 결합 분석이 또한 실행될 수 있다. 예로써, WO 2006/029879와 WO 2005/100402에서 C1q 및 C3c 결합 ELISA 참조. 보체 활성화를 평가하기 위하여, CDC 분석이 실행될 수 있다 (예를 들면, Gazzano-Santoro 외. J. Immunol. Methods 202:163 (1996); Cragg, M.S. 외. Blood. 101:1045-1052 (2003); 그리고 Cragg, M.S. 및 M.J. Glennie Blood. 103:2738-2743 (2004) 참고). 또한 FcRn 결합과 생체내 제거/반감기 결정은 해당 분야에 공지된 방법들을 이용하여 또한 실시될 수 있다 (예컨대, Petkova, S.B. 외. Int'l. Immunol. 18(12):1759-1769 (2006) 참고).
감소된 이펙터 기능를 가진 항체들은 Fc 영역 잔기 238, 265, 269, 270, 297, 327 및 329 중 하나 또는 그 이상의 치환을 가진 것들을 포함한다 (미국 특허 제 6,737,056). 이러한 Fc 돌연변이체들은 잔기 265 및 297의 잔기가 알라닌으로 치환된 소위 “DANA” Fc 돌연변이체를 포함하는, 아미노산 위치 265, 269, 270, 297 및 327중 2개 또는 그 이상에서 치환을 가진 Fc 돌연변이체를 포함한다 (미국 특허 제 7,332,581 참고).
FcRs에 대한 결합이 개선된 또는 감소된 특정 항체 변이체들이 설명된다. (가령, 미국 특허 제 6,737,056; WO 2004/056312, 및 Shields 외, J. Biol. Chem. 9(2): 6591-6604 (2001). 참조)
특정 구체예들에 있어서, 항체 변이체는 ADCC를 개선시키는 하나 또는 그 이상의 아미노산 치환들, 예로써, Fc 영역의 위치 298, 333, 및/또는 334 (잔기는 EU 넘버링)에서 치환을 가진 Fc 영역을 포함한다.
일부 구체예들에 있어서, Fc 영역 안에 예로써, 미국 특허 제 6,194,551, WO 99/51642, 및 Idusogie 외 J. Immunol. 164: 4178-4184 (2000)에서 설명된 바와 같이, 변경된 (가령, 개선된 또는 감소된) C1q 결합 및/또는 보체 의존적 세포독성 (CDC)을 초래하는 변경이 만들어진다.
태아로 모계 IgGs의 전달을 담당하는, 반감기가 증가되고 신생아의 Fc 수용체 (FcRn)에 대한 결합이 개선된 항체들 (Guyer 외, J. Immunol. 117:587 (1976) 그리고 Kim 외, J. Immunol. 24:249 (1994))은 US2005/0014934A1 (Hinton 외)에 기재되어 있다. 이들 항체는 FcRn에 대한 Fc 영역의 결합을 개선시키는 하나 또는 그 이상의 치환들을 가진 Fc 영역을 내부에 포함한다. 이러한 Fc 변이체들은 Fc 영역 잔기의 하나 또는 그 이상에서 치환을 가진 것들을 포함한다: 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 또는 434, 예로써, Fc 영역 잔기 434의 치환 (미국 특허 제 7,371,826).
Fc 영역 변이체들의 다른 예들에 관하여 Duncan & Winter, Nature 322:738-40 (1988); 미국 특허 제 5,648,260; 미국 특허 제 5,624,821; 그리고 WO 94/29351 참조.
(iv) 시스테인
조작된 항체 변이체
특정 구체예들에 있어서, 본원에 제공된 치료 방법에 사용되는 항-CD79b 항체 또는 항-CD20 항체의 하나 이상의 잔기가 시스테인 잔기로 치환된, 시스테인 조작된 항-PD-L1 항체, 가령, “thioMAbs”를 만드는 것이 바람직할 수 있다. 특정 구체예에서, 상기 치환된 잔기는 항체의 접근가능한 부위에서 나타난다. 이들 잔기를 시스테인으로 치환함으로써, 반응성 티올기는 이러한 항체의 접근가능한 부위에 위치하게 되고, 다른 모이어티, 가령, 하기에서 설명되는 약물 모이어티 또는 연결기-약물 모이어티에 이 항체가 접합되어 면역접합체가 생성될 수 있다. 특정 구체예들에 있어서, 다음과 같은 임의의 하나 또는 그 이상의 잔기는 시스테인으로 치환될 수 있다: 경쇄의 V205 (Kabat 넘버링); 중쇄의 A118 (EU 넘버링); 그리고 중쇄 Fc 영역의 S400 (EU 넘버링). 본원에 기재된 방법에 사용하기 위한 예시적인 시스테인 조작된 항-CD79b 항체에 대해서는 예를 들어 WO 2009/012268을 참조하라. 시스테인 조작된 항체는 예를 들면, 미국 특허 제 7,521,541에서 설명된 것과 같이 생성될 수 있다.
(v) 항체 유도체
특정 구체예들에서, 본원에 제공된 치료 방법에 사용되는 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체) 는 해당 분야에 공지되어 있고, 쉽게 입수할 수 있는 추가의 비단백질성 모이어티를 함유하도록 추가로 변형될 수 있다. 상기 항체의 유도체화에 적합한 모이어티들은 수용성 중합체들을 포함하나, 이에 제한되지 않는다. 수용성 중합체들의 비-제한적 예들에는, 폴리에틸렌 글리콜 (PEG), 에틸렌 글리콜/프로필렌 글리콜의 공중합체, 카르복시메틸셀룰로스, 덱스트란, 폴리비닐 알콜, 폴리비닐 피롤리돈, 폴리-1, 3-디옥솔란, 폴리-1,3,6-트라이옥세인, 에틸렌/말레산 무수물 공중합체, 폴리아미노산 (동종중합체 또는 무작위 공중합체), 및 덱스트란 또는 폴리(n-비닐 피롤리돈)폴리에틸렌 글리콜, 프로프로필렌 글리콜 동종중합체, 폴리프로필렌 옥사이드/에틸렌 옥사이드 공중합체, 폴리옥시에틸화 폴리올 (예를 들어, 글리세롤), 폴리비닐 알콜, 및 이의 혼합물이 포함되나 이에 제한되는 것은 아니다. 폴리에틸렌 글리콜 프로피온알데히드는 물에서의 안정성으로 인하여 제조에 있어 장점을 가질 수 있다. 중합체는 임의의 분자량일 수 있고, 분지형 또는 비-분지형일 수 있다. 상기 항체에 부착된 폴리머의 수는 가변적일 수 있으며, 하나 이상의 폴리머가 부착된 경우, 이들은 동일하거나 또는 상이한 분자들일 수 있다. 일반적으로, 유도체화에 이용된 중합체의 수 및/또는 유형은 개선되는 항체의 특정 성질들 또는 기능들, 상기 항체 유도체가 특정 조건하에서 치료에 이용되는지의 여부를 포함하는 고려사항들에 근거하여 결정될 수 있다.
또 다른 구체예에서, 방사선에 노출시켜 선별적으로 가열될 수 있는 항체와 비단백질성 모이어티의 접합체들이 제공된다. 한 구체예에서, 상기 비단백질성 모이어티는 탄소 나노튜브다 (Kam 외, Proc. Natl. Acad. Sci. USA 102: 11600-11605 (2005)). 방사능은 임의의 파장일 수 있으며, 정상 세포들에게 해를 주지 않지만, 그러나 상기 항체-비단백질성 모이어티에 근접한 세포들은 사멸되는 온도에서 비단백질성 모이어티에 열을 가하는 파장이 포함되나, 이에 제한되는 것은 아니다.
H. 재조합 방법 및 조성물
항체는 예를 들어 미국 특허 제4,816,567호에 기재된 바와 같은 재조합 방법 및 조성물을 사용하여 생성될 수 있다. 한 구체예에서, 본원에 기재된 항체를 코딩하는 단리된 핵산이 제공된다. 이러한 핵산은 항체의 VL을 포함하는 아미노산 서열 및/또는 VH를 포함하는 아미노산 서열(예를 들어, 항체의 경쇄 및/또는 중쇄)을 인코딩할 수 있다. 다른 구체예에서, 이러한 핵산을 포함하는 하나 이상의 벡터(예를 들어, 발현 벡터)가 제공된다. 또 다른 구체예에서, 이러한 핵산을 포함하는 숙주 세포가 제공된다. 이러한 한 구체예에서, 숙주 세포는 다음을 포함한다 (예를 들어, 다음에 의해 형질전환되어 있다): (1) 항체의 VL을 포함하는 아미노산 서열 및 항체의 VH를 포함하는 아미노산 서열을 인코딩하는 핵산을 포함하는 벡터, 또는 (2) 항체의 VL을 포함하는 아미노산 서열을 코딩하는 핵산을 포함하는 제1 벡터 및 항체의 VH를 포함하는 아미노산 서열을 코딩하는 핵산을 포함하는 제2 벡터. 한 구체예에서, 숙주 세포는 진핵생물, 예를 들어 중국 햄스터 난소(CHO) 세포 또는 림프구양 세포 (예를 들어, Y0, NS0, Sp20 세포)이다. 한 구체예에서, 항체의 발현에 적합한 조건 하에 상기 제공된 바와 같은 항체를 인코딩하는 핵산을 포함하는 숙주 세포를 배양하는 단계, 및 선택적으로 숙주 세포 (또는 숙주 세포 배양 배지)로부터 항체를 회수하는 단계를 포함한다.
항체의 재조합 생산을 위하여, 예컨대, 상기 기재한 항체를 인코드하는 핵산이 단리되고, 숙주 세포 안에서 추가 클로닝 및/또는 발현을 위하여 하나 이상의 벡터 안으로 삽입된다. 이러한 핵산은 통상적인 과정에 의해 (가령, 항체의 중쇄 및 경쇄를 인코드하는 유전자에 특이적으로 결합할 수 있는 올리고뉴클레오티드 프로브를 사용함으로써) 용이하게 단리되고, 시퀀싱된다.
항체-인코딩 벡터의 클로닝 또는 발현에 적합한 숙주 세포는 본원에 기재된 원핵 또는 진핵 세포를 포함한다. 예를 들어, 항체는 특히 당화 및 Fc 이펙터 기능이 필요하지 않은 경우 박테리아에서 생성될 수 있다. 박테리아에서 항체 단편 및 폴리펩티드의 발현에 관해서는, 예를 들어 미국 특허 제 5,648,237, 5,789,199 및 5,840,523을 참조하라. (또한 Charlton, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ, 2003), pp. 245-254의 대장균에서의 항체 단편의 발현에 관한 설명 참조). 발현 후, 항체는 가용성 분획 중의 박테리아 세포 페이스트로부터 단리될 수 있으며 추가로 정제될 수 있다.
원핵세포 이외에도, 진핵 미생물, 이를 테면 섬유성 곰팡이 또는 효모는 항체-인코딩 벡터의 적절한 클로닝 또는 발현 숙주이며, 당화 경로가 “인간화되고”, 결과적으로 부분적으로 또는 온전하게 인간 당화 패턴을 가진 항체가 생산되는 곰팡이 및 효모 균주가 포함된다. Gerngross, Nat. Biotech. 22:1409-1414 (2004), 및 Li 외, Nat. Biotech. 24:210-215 (2006) 참고.
당화된 항체의 발현에 적합한 숙주 세포들은 다세포 유기체 (무척추동물 및 척추동물)로부터 또한 유도된다. 무척추동물 세포들의 예로는 식물 및 곤충 세포들이 포함된다. 스포도프테라 푸르기페르다(Spodoptera frugiperda) 세포들의 형질감염을 위하여 곤충 세포들과 병용될 수 있는 많은 베큘로바이러스 균주들이 확인되었다.
식물 세포 배양물 또한 숙주로 이용될 수 있다. 예컨대, 미국 특허 제 5,959,177, 6,040,498, 6,420,548, 7,125,978, 및 6,417,429호를 참고하라 (유전자삽입 식물에서 항체를 생산하기 위한 PLANTIBODIESTM 을 설명).
척추동물 세포들 또한 숙주로 이용될 수 있다. 예를 들면, 현탁액에서 성장하도록 개조시킨 포유동물 세포주들이 유용할 수 있다. 유용한 포유동물 숙주 세포주의 다른 예는 SV40에 의해 형질전환된 원숭이 신장 CV1 세포주 (COS-7); 인간 배아 신장 세포주 (예를 들면, Graham 외, J. Gen Virol. 36:59 (1977)에 설명된 293 또는 293 세포); 아기 햄스터 신장 세포 (BHK); 마우스 세르톨리 세포 (예를 들면, Mather, Biol. Reprod. 23:243-251 (1980)에 설명된 TM4 세포); 원숭이 신장 세포 (CV1); 아프리카 녹색 원숭이 신장 세포 (VERO-76); 인간 경부 암종 세포 (HELA); 개 신장 세포 (MDCK; 버팔로 래트 간 세포 (BRL 3A); 인간 폐 세포 (W138); 인간 간 세포 (Hep G2), 생쥐 유방 종양 (MMT 060562); 예를 들면, Mather 외, Annals N.Y. Acad. Sci. 383:44-68 (1982)에 설명된 TRI 세포; MRC 5 세포; 및 FS4 세포이다. 다른 유용한 포유동물 숙주 세포주는 DHFR-CHO 세포를 포함하는 차이니즈 햄스터 난소(CHO) 세포 (Urlaub 외, Proc. Natl. Acad. Sci. USA 77:4216 (1980)); 및 Y0, NS0 및 Sp2/0과 같은 골수종 세포주를 포함한다. 항체 생산에 적합한 특정 포유동물 숙주 세포주의 검토는 예컨대, Yazaki 및 Wu, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ), pp. 255-268 (2003)를 참고하라.
I. 분석
본원에 제공된 치료 방법에 사용되는 항체(예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 해당 분야에 공지된 다양한 분석법에 의해 그 물리적/화학적 특성 및/또는 생물학적 활성에 대해 확인, 스크리닝 또는 특성화될 수 있다.
한 양상에서, 본원에 제공된 치료 방법에 사용된 항체 (예를 들어, 항-CD79b 항체 또는 항-CD20 항체)는 그 항원 결합 활성에 대해, 예를 들어 ELISA, BIACore®, FACS, 또는 웨스턴 블롯과 같은 공지된 방법으로 검사한다.
또 다른 양상에서, 경쟁 분석법을 사용하여 표적 항원에 대한 결합에 대해 본원에 기재된 임의의 항체와 경쟁하는 항체를 식별할 수 있다. 특정 구체예에서, 이러한 경쟁 항체는 본원에 기재된 항체에 의해 결합되는 동일한 에피토프(예를 들어, 선형 또는 입체형태 에피토프)에 결합한다. 항체가 결합하는 에피토프를 맵핑하기 위한 상세한 예시적 방법이 Morris (1996) “Epitope Mapping Protocols,” in Methods in Molecular Biology vol. 66 (Humana Press, Totowa, NJ)에 제공된다.
예시적인 경쟁 분석에서, 고정된 항원은 항원에 결합하는 표지된 제1 항체 (예를 들어, 본원에 기재된 임의의 항체) 및 항원에 결합하기 위해 제1 항체와 경쟁하는 능력에 대해 검사할, 표지되지 않은 제2 항체를 포함하는 용액에서 인큐베이션된다. 제2 항체는 하이브리도마 상청액에 존재할 수 있다. 대조군으로서, 고정된 항원은 표지된 제1 항체를 포함하지만 표지되지 않은 제2 항체는 포함하지 않는 용액에서 인큐베이션된다. 항원에 대한 제1 항체의 결합을 허용하는 조건하에서 인큐베이션한 후, 과량의 결합되지 않은 항체를 제거하고, 고정된 항원과 결합된 표지의 양을 측정한다. 고정된 항원과 결합된 표지의 양이 대조 샘플에 비해 테스트 샘플에서 실질적으로 감소하면, 이는 제2 항체가 항원에 대한 결합을 위해 제1 항체와 경쟁하고 있음을 나타낸다. Harlow and Lane (1988) Antibodies: A Laboratory Manual ch.14 (Cold Spring Harbor Laboratory, Cold Spring Harbor, NY) 참조.
VII. 화학요법제
일부 구체예들에서, 하나 이상의 화학요법제는 암 치료에 유용한 화학적 화합물을 포함한다. 화학요법제의 예들에는 에를로티닙 (TARCEVA®, Genentech/OSI Pharm.), 보르테조밉 (VELCADE®, Millennium Pharm.), 디설피람, 에피갈로카테킨 갈레이트, 살리노스포라미드 A, 카르필조밉, 17-AAG (겔다나마이신), 라디시콜, 젖산 탈수소효소 A (LDH-A), 풀베스트란트 (FASLODEX®, AstraZeneca), 수니팁 (SUTENT®, Pfizer/Sugen), 레트로졸 (FEMARA®, Novartis), 이마티닙 메실레이트 (GLEEVEC®, Novartis), 피나수네이트 (VATALANIB®, Novartis), 옥살리플라틴 (ELOXATIN®, Sanofi), 5-FU (5-플루오로우라실), 류코보린, 라파마이신 (시롤리무스, RAPAMUNE®, Wyeth), 파라티닙 (TYKERB®, GSK572016, Glaxo Smith Kline), 로나파밉 (SCH 66336), 소라페닙 (NEXAVAR®, Bayer Labs), 게피티닙 (IRESSA®, AstraZeneca), AG1478, 알킬화제, 가령, 티오테파 및 CYTOXAN® 사이클로포스파미드; 알킬 설포네이트, 가령, 부설판, 임프로설판 및 피포설판; 아지리딘, 가령, 벤조도파, 카르보쿠온, 메투레도파, 및 우레도파; 알트레타민, 트라이에틸렌멜라민, 트라이에틸렌포스포라미드, 트라이에틸렌티오포스포라미드 및 트라이메틸로멜라민을 포함한 에틸렌이민 및 메틸라멜라민; 아세토게닌 (특히 불라타신 및 불라타시논); 캄토테신 (토포테칸 및 이리노테칸 포함); 브리오스타틴; 칼리스타틴; CC-1065 (이의 아도젤레신, 카르젤레신 및 바이젤레신 합성 유사체 포함); 크립토피신 (특히 크립토피신 1 및 크립토피신 8); 아드레노코르티코스테로이드 (프레드니손 및 프레드니솔론 포함); 사이프로테론 아세테이트; 피라스테리드 및 두타스테리드를 포함한 5a-환원효소; 보리노스타트, 로미뎁신, 파노비노스타트, 발프로익 애시드, 모세티노스타트 돌라스타틴; 알데스류킨, 탈크 듀오카르마이신 (합성 유사체, KW-2189 및 CB1-TM1 포함); 엘레우테로빈; 판크라티스타틴; 사르코딕티인; 스폰지스타틴; 질소 머스터드, 가령, 클로람부실, 클로마파진, 클로로포스파미드, 에스트라무스틴, 이포스파미드, 메클로레타민, 메클로레타민 옥사이드 하이드로클로라이드, 멜팔란, 노벰비친, 페네스테린, 프레드니무스틴, 트로포스파미드, 우라실 머스터드; 니트로소우레아, 가령, 카르무스틴, 클로로조토신, 포테무스틴, 로무스틴, 니무스틴, 및 라님무스틴; 항생제, 가령, 에네다이인 항생제 (예컨대, 칼리키아마이신, 특히 칼리키아마이신 γ및 칼리키아마이신 ω(Angew Chem. Intl. Ed. Engl. 1994 33:183-186); 다이네미신 A를 포함한 다이네미신; 바이포스포네이트, 가령, 클로드로네이트; 에스페라미신; 뿐만 아니라 네오카르지노스타틴 발색단 및 관련 크로모프로테인 에네다이인 항생 발색단), 아클라시노마이신, 악티노마이신, 아우트라마이신, 아자세린, 블레오마이신, 칵티노마이신, 카라비신, 카미노마이신, 카르지노필린, 크로모마이시니스, 닥티노마이신, 다우노루비신, 데토루비신, 6-다이아조-5-옥소- L-노르류신, ADRIAMYCIN® (독소루비신), 모르폴리노-독소루비신, 시아노모르폴리노-독소루비신, 2-피롤리노-독소루비신 및 데옥시독소루비신), 에피루비신, 에소루비신, 에베롤리무스, 소트라타우린, 이다루비신, 마르셀로마이신, 미토마이신, 가령, 미토마이신 C, 마이코페놀릭 애시드, 노갈라마이신, 올리보마이신, 페플로마이신, 포르피로마이신, 퓨로마이신, 쿠엘라마이신, 로도루비신, 스트렙토니그린, 스트렙토조신, 투베르시딘, 우베니멕스, 지노스타틴, 조루비신; 항-대사산물, 가령, 메토트렉세이트 및 5-플루오로우라실 (5-FU); 엽산 유사체, 가령, 데노프테린, 메토트렉세이트, 프테로프테린, 트라이메트렉세이트; 퓨린 유사체, 가령, 플루다라빈, 6-머캅토퓨린, 티아미프린, 티오구아닌; 피리미딘 유사체, 가령, 안시타빈, 아자시티딘, 6-아자우리딘, 카르모푸르, 시타라빈, 다이데옥시우리딘, 독시플루리딘, 에노시타빈, 플록수리딘; 안드로겐, 가령, 칼루스테론, 드로모스타놀론 프로피오네이트, 에피티오스타놀, 메피티오스테인, 테스토락톤; 항-아드레날, 가령, 미노글루테티미드, 미토테인, 트릴로스테인; 엽산 보충제, 가령, 프롤리닉 애시드; 아세글라톤; 알도포스파미드 글리코시드; 아미노레불리닉 애시드; 에닐우라실; 암사크린; 베스트라부실; 비산트렌; 에다트락세이트; 데포파민; 데메콜신; 디아지쿠온; 엘포미틴; 엘립티늄 아세테이트; 에포틸론; 에토글루시드; 갈륨 니트레이트; 하이드록시우레아; 렌티난; 로니다이닌; 마이탄시노이드, 가령, 마이탄신 및 안사미토신; 미토구아존; 미톡산트론; 모피담놀; 니트라에린; 펜토스타틴; 페나메트; 피라루비신; 로속산트론; 포도필리닉 애시드; 2-에틸하이드라지드; 프로카르바진; PSK® 다당류 복합체 (JHS Natural Products, Eugene, Oreg.); 라족산; 리족신; 시조퓨란; 스피로게르마늄; 테누아조닉 애시드; 트라이아지쿠온; 2,2',2''-트라이클로로트라이에틸아민; 트라이코 트라이코쎄신 (특히 T-2 톡신, 베라큐린 A, 로리딘 A 및 안구이딘); 우레탄; 빈데신; 다카르바진; 만노무스틴; 미토브로니톨; 미토락톨; 피포브로만; 가시토신; 아라비노시드 (“Ara-C”); 사이클로포스파미드; 티오테파; 탁소이드, 예컨대, TAXOL (파클리탁셀; Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANE® (무-크레모포르), 파클리탁셀의 알부민-조작된 나노입자 제제 (American Pharmaceutical Partners, Schaumberg, Ill.), 및 TAXOTERE® (도세탁셀, 독세탁셀; Sanofi-Aventis); 클로람부실; GEMZAR® (젬시타빈); 6-싸이오구아닌; 머캅토퓨린; 메토트렉세이트; 백금 유사체, 가령, 시스플라틴 및 카르보플라틴; 빈블라스틴; 에토포시드 (VP-16); 이포스파미드; 미톡산트론; 빈크리스틴; NAVELBINE® (비노렐빈); 노반트로네솜(novantronesom); 테니포시드; 에다트렉세이트; 다우노마이신; 아미노프테린; 카페시타빈 (XELODA®);이반드로네이트; CPT-11; 국소이성화효소 억제제 RFS 2000; 다이플루오로메틸오르니틴 (DMFO); 레티노이드, 가령, 레티노익 애시드; 및 상기 어느 하나의 약학적으로 허용가능한 염, 산 및 유도체; 뿐만 아니라 상기 둘 이상의 조합, 예를 들어, CHOP (사이클로포스파미드, 독소루비신, 빈크리스틴 및 프레드니솔론의 병용 요법에 대한 약어) 및 FOLFOX(5-FU 및 류코보린과 옥살리플라틴(ELOXATINTM)을 병용하는 치료 요법에 대한 약어)가 포함된다. 화학요법제의 또 다른 예에는 벤다무스틴 (또는 벤다무스틴-HCl) (TREANDA®), 이브루티닙, 레날리도마이드 및/또는 이델랄리십 (GS-1101)이 포함된다.
일부 구체예들에서, 하나 이상의 화학요법제는 암의 성장을 촉진할 수 있는 호르몬의 효과를 조절, 감소, 차단 또는 억제하는 작용을 하는 항호르몬제를 포함하며, 이는 종종 전신 또는 신체 전체 치료의 형태이다. 화학요법제는 호르몬 자체일 수 있다. 예에는, 예를 들어 타목시펜 (NOLVADEX® 타목시펜 포함), 랄록시펜 (EVISTA®), 드롤록시펜, 4-하이드록시타목시펜, 트리옥시펜, 케옥시펜, LY117018, 오나프리스톤, 및 토레미펜 (FARESTON®)을 비롯한, 항에스트로겐 및 선택적 에스트로겐 수용체 조절제(SERM); 항프로게스테론; 에스트로겐 수용체 하향 조절제(ERD); 풀베스트란트 (FASLODEX®)와 같은 에스트로겐 수용체 길항제; 난소를 억제하거나 폐쇄하는 기능을 하는 제제, 예를 들어, 류프롤리드 아세테이트 (LUPRON® 및 ELIGARD®), 고세렐린 아세테이트, 부세렐린 아세테이트 및 트립테렐린과 같은 황체형성 호르몬 방출 호르몬 (LHRH) 효능제; 플루타미드, 닐루타미드 및 비칼루타미드와 같은 항안드로겐; 및 부신에서 에스트로겐 생성을 조절하는 효소 아로마타제를 억제하는 아로마타제 억제제, 예를 들어, 4(5)-이미다졸, 아미노글루테티미드, 메게스트롤 아세테이트 (MEGASE®), 엑세메스탄 (AROMASIN®), 포르메스타니, 파드로졸, 보로졸 (RIVISOR®), 레트로졸 (FEMARA®) 및 아나스트로졸 (ARIMIDEX®)이 포함된다. 또한, 화학요법제의 이러한 정의에는 비스포스포네이트, 예를 들어, 클로드로네이트 (예를 들어, BONEFOS® 또는 OSTAC®), 에티드로네이트 (DIDROCAL®), NE-58095, 졸레드론산/졸레드로네이트 (ZOMETA®), 알렌드로네이트 (FOSAMAX®), 파미드로네이트 (AREDIA®), 틸루드로네이트 (SKELID®), 또는 리세드로네이트 (ACTONEL®); 뿐만 아니라 트록사시타빈(1,3-디옥솔란 뉴클레오시드 시토신 유사체); 안티센스 올리고뉴클레오티드, 특히, 특히, 예를 들어 PKC-알파, Raf, H-Ras 및 표피 성장 요소 수용체(EGF-R)와 같은 비정상적인 세포 증식과 관련된 신호 전달 경로에서 유전자의 발현을 억제하는 것들; 백신, 예를 들어, THERATOPE® 백신 및 유전자 요법 백신, 예를 들어, ALLOVECTIN® 백신, LEUVECTIN® 백신, 및 VAXID® 백신이 포함된다.
일부 구체예들에서, 하나 이상의 화학요법제는 토포이소머라제 1 억제제 (예를 들어, LURTOTECAN®); 풀베스트란트와 같은 항에스트로겐; 이마티닙 또는 EXEL-0862 (티로신 키나제 억제제)와 같은 키트 억제제; 에를로티닙 또는 세툭시맙과 같은 EGFR 억제제; 베바시주맙과 같은 항-VEGF 억제제; 아리노테칸; rmRH (예를 들어, ABAELIX®); 라파티닙 및 라파티닙 디토실레이트(ErbB-2 및 EGFR 이중 티로신 키나제 소분자 억제제는 GW572016로도 알려짐); 17AAG(열 충격 단백질(Hsp) 90 독(poison)인 겔다나마이신 유도체), 및 상기 어느 하나의 약학적으로 허용되는 염, 산 또는 유도체를 포함한다.
일부 구체예들에서, 하나 이상의 화학요법제는 또한 항체, 예를 들어, 알렘투주맙 (Campath), 베바시주맙 (AVASTIN®, Genentech); 세툭시맙 (ERBITUX®, Imclone); 파니투무맙 (VECTIBIX®, Amgen), 리툭시맙 (RITUXAN®, Genentech/Biogen Idec), 유블리툭시맙, 오파투무맙, 이브리투모맙 티욱세탄, 퍼투주맙 (OMNITARG®, 2C4, Genentech), 트라스투주맙 (HERCEPTIN®, Genentech), 토시투모맙 (Bexxar, Corixia), 및 항체 약물 접합체, 젬투주맙 오조가미신 (MYLOTARG®, Wyeth)을 포함한다. 상기 화합물과 조합되는 제제들로서 치료 가능성이 있는 추가 인간화 모노클로날 항체들은 다음을 포함한다: 아폴리주맙, 아셀리주맙, 아틀리주맙, 바피네우주맙, 비바투주맙 메르탄신, 칸투주맙 메르탄신, 세델리주맙, 세르톨리주맙 페골, 시드푸시투주맙, 시드투주맙, 다클리주맙, 에쿨리주맙, 에팔리주맙, 에프라투주맙, 에를리주맙, 펠비주맙, 폰톨리주맙, 겜투주맙 오조가마이신, 이노투주맙 오조가마이신, 이필리무맙, 라베투주맙, 린투주맙, 마투주맙,메폴리주맙, 모타비주맙, 모토비주맙, 나탈리주맙, 니모투주맙, 놀로비주맙, 누마비주맙, 오크렐리주맙, 오말리주맙, 팔리비주맙, 파스콜리주맙, 펙푸시투주맙, 펙투주맙, 펙셀리주맙, 랄리비주맙, 라니비주맙, 레슬리비주맙, 레슬리주맙, 레시비주맙, 로벨리주맙, 루플리주맙, 시브로투주맙, 시플리주맙, 손투주맙, 타카투주맙 테트락세탄, 타도시주맙, 탈리주맙, 테피바주맙, 토실리주맙, 토랄리주맙, 투코투주맙 셀모류킨, 투쿠시투주맙, 우마비주맙, 우르톡사주맙, 우스테키누맙, 비실리주맙, 및 인터루킨-12 p40 단백질을 인식하도록 유전적으로 변형된 재조합의 전적인 인간-서열, 전장 IgG1 λ 항체인 항-인터루킨-12 (ABT-874/J695, Wyeth Research and Abbott Laboratories).
일부 구체예들에서, 하나 이상의 화학요법제는 알킬화제를 포함한다. 알킬화제는 DNA가 RNA로 전사되는 것을 억제하여 단백질 합성을 중단시키는 작용을 하는 항종양 또는 항암제의 일종이다. 알킬화제는 DNA의 수소 원자를 알킬기(CnH2n+1)로 대체하여 DNA 사슬 내에 가교를 형성하여 DNA 가닥 절단을 유발하여 비정상적 염기 페어링, 세포 분열의 억제, 및, 궁극적으로, 세포 사멸을 초래한다. 이 작용은 모든 세포에서 발생하지만 암세포와 같이 빠르게 분열하는 세포는 일반적으로 알킬화제의 영향에 가장 민감하다.
알킬화제는 일반적으로 6가지 클래스로 구분된다: (1) 제한 없이, 예를 들어, 메클로레타민, 시클로포스파미드, 이포스파미드, 벤다무스틴, 멜팔란 및 클로람부실을 포함하는 질소 머스타드; (2) 제한없이, 알트레타민 및 티오테파를 포함하는 에틸렌아민 및 메틸렌아민 유도체; (3) 제한없이, 예를 들어 부설판을 포함하는 알킬 설포네이트; (4) 제한 없이 예를 들어 카르무스틴 및 로무스틴을 포함하는 니트로소우레아; (5) 제한 없이 예를 들어 다카르바진 및 프로카르바진, 테모졸로미드를 포함하는 트리아젠; 및 (6) 예를 들어, 제한 없이, 시스플라틴, 카보플라틴 및 옥살리플라틴을 포함하는 백금-함유 항종양제. 임의의 공지된 알킬화제(상기 열거된 것들을 포함하나 이에 제한되지 않음)가 본원에서 제공되는 치료 방법에 사용될 수 있다. 벤다무스틴은 본원에 기재된 방법에 사용되는 예시적인 알킬화제이다. 벤다무스틴의 화학명은 4-(5-(비스(2-클로로에틸)아미노)-1-메틸-1H-벤조[d]이미다졸-2-일)부타노익 애시드이며, C16H21Cl2N3O2의 분자식 및 358.263 g/mol의 분자량을 가진다. 벤다무스틴 (CAS 등록 #16506-27-7)은 퓨린-유사 벤즈이미다졸 고리를 포함하는 이작용기성 메클로레타민 유도체이다. 벤다무스틴은 용액 및 용액 제형용 분말로 제공된다. 일부 구체예들에서, 본원에 기재된 방법에 사용된 알킬화제는 벤다무스틴의 염 또는 용매화물이다. 일부 구체예들에서, 벤다무스틴 염은 벤다무스틴-HCl (CAS # 3543-75-7)로서, C16H21Cl2N3O2.HCl의 분자식 및 394.72 g/mol의 분자량을 가진다. 벤다무스틴-HCl은 BENDEKA, TREANDA, TREAKISYM, RIBOMUSTIN, LEVACT, MUSTIN, 등으로 시판되고 있다.
일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 (예를 들어, GEMZAR®)을 포함한다. 젬시타빈은 항대사물질 뉴클레오시드 유사체 (2',2'-다이플루오로데옥시시티딘)이다. 이의 디- 및 트리-포스페이트 형태들만이 세포독성 활성을 가지므로, 데옥시시티딘 키나제에 의한 세포내 인산화 이후 활성이 된다. 구체적으로, 트리포스페이트 형태는 비활성 염기로서 DNA에 통합되기 위하여 데옥시시티딘 트라이포스페이트와 경쟁하고, 디포스페이트 형태는 inhibits 정상적인 DNA 합성에 필수적인 리보뉴클레오티드 환원효소를 억제한다. 젬시타빈은 IUPAC 명명법에 따라 “2'-데옥시-2',2'-디플루오로시티딘 모노하이드로클로라이드” (β-이성질체)라고도 하며 다음 구조를 가진다:
용어 “2'-데옥시-2',2'-디플루오로시티딘 모노하이드로클로라이드 (β-이성질체)” 또는 “젬시타빈”의 사용은 (달리 지시되지 않는 한) 약상 허용되는 용매화물 (수화물 포함) 및 이의 다형체 또는 약학상 허용되는 염을 포괄한다. 2'-데옥시-2',2'-디플루오로시티딘 모노하이드로클로라이드 (β-이성질체)의 약학 조성물은 하나 이상의 희석제, 비히클 및/또는 부형제를 포함할 수 있다. 2'-데옥시-2',2'-디플루오로시티딘 모노히드로클로라이드(β-이성질체)를 포함하는 약제학적 조성물의 한 예는 GEMZAR® (젬시타빈 HCl)이다. GEMZAR®는 활성 성분으로 2'-데옥시-2',2'-디플루오로시티딘 모노하이드로클로라이드 (β-이성질체)를 그리고 정맥 주사 전용 멸균 형태의 기타 불활성 성분을 포함한다. GEMZAR®의 바이얼은 만니톨(각각 200mg 또는 1g) 및 아세트산나트륨(각각 12.5mg 또는 62.5mg)으로 제제화된, 젬시타빈 HCl (유리 염기로 표시) 200mg 또는 1g을 멸균 동결건조 분말로서 함유한다. pH 조정을 위해 염산 및/또는 수산화나트륨을 첨가했을 수 있다.
일부 구체예들에서, 하나 이상의 화학요법제는 옥살리플라틴 (예를 들어, ELOXATIN®)을 포함한다. 옥살리플라틴은 분자식이 C8H14N2O4Pt이고 화학명이 시스-[(1R,2 R)-1,2-사이클로헥산디아민-N,N][옥살라토(2-)-O,O] 백금인 화학요법제이다. 이의 화학구조를 하기에 나타낸다:
용어 “시스-[(1R,2 R)-1,2-사이클로헥산디아민-N,N][옥살라토(2-)-O,O] 백금” 또는 “옥살리플라틴”의 사용은 (달리 지시되지 않는 한) 약상 허용되는 용매화물 (수화물 포함) 및 이의 다형체 또는 약학상 허용되는 염을 포괄한다. 옥살리플라틴의 백금 원자는 두 개의 인접한 구아노신 잔기 사이에 1,2-가닥내 가교를 형성하여 이중 나선을 주 홈 쪽으로 약 30도 구부러지게 한다. 옥살리플라틴은 약물의 최종 세포독성 대사산물에서 유지되는 비가수분해성 디아미노시클로헥산(DACH) 운반체 리간드를 가지고 있다. DNA 및 다른 거대분자와의 반응은 옥살레이트의 카르복실 에스테르기 중 하나 또는 둘 모두의 가수분해에 의해 진행되어 DACH 백금 단일 부가물 또는 이중 기능 DACH-백금 가교를 남긴다. DACH-백금 부가물의 고유한 화학적 및 입체적 특성은 시스플라틴과의 교차 내성 결여로 인한 것으로 보인다 (Di Francesco 외, (2002) Cell Mol Life Sci, 59(11):1914-27에서 검토됨). 옥살리플라틴은 알칼리 가수분해되어 두 개의 연속 단계에서 옥살라토 모노덴테이트 (pKa 7.23) 및 이수화된 옥살리플라틴 복합체를 생성한다. 모노덴테이트 중간체는 내인성 화합물과 빠르게 반응하는 것으로 가정된다 (Jerremalm 외, (2003) J Pharm Sci, 92(2):436-438). 서열 5'-d(CCTCTGGTCTCC)를 갖는 DNA 12량체 이중체에 결합된 옥살리플라틴의 결정 구조가 보고된 바 있는데; 백금 원자는 두 개의 인접한 구아노신 잔기들 사이에 1,2-가닥내 가교를 형성하고, 그리하여 이중 나선을 주 홈을 향해 약 30도 구부리러지게 한다. 결정학은 옥살리플라틴과 이중체 DNA 사이의 상호작용을 매개하는 키랄성의 중요성에 대한 구조적 증거를 제공했다 (Spingler 외, (2001) Inorg Chem, 40(22):5596-602). 그러므로, 옥살리플라틴의 성공은 벌크 부가물 뿐만 아니라 가닥내 및 가닥간 가교로 인한 DNA 손상 유도 능력 (Takahara 외, (1995) Nature, 377(6550):649-52), 그리고 세포자멸사를 유도하는 능력 (Boulikas and Vougiouka, (2003) Oncol Rep, 10(6):1663-82)에 있다.
일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴 (예를 들어, GEMZAR® 및 ELOXATIN®)을 포함한다. 일부 구체예들에서, 하나 이상의 화학요법제는 젬시타빈 및 옥살리플라틴 (예를 들어, GEMZAR® 및 ELOXATIN®)이다.
VIII. 약학 제제
본원에 기재된 임의의 방법에 사용하기 위한 본원에 기재된 임의의 제제(예를 들어, 항-CD79b 면역접합체, 항-CD20 제제, 및 하나 이상의 화학요법제)의 약학 제제는 원하는 정도의 순도를 가지는 이러한 제제(들)을 선택적인 약학적으로 허용가능한 희석제, 담체, 부형제 또는 안정화제 (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980))와 혼합하여, 동결 건조된 제제 또는 수용액의 형태로 제조된다. 약학적으로 허용가능한 담체는 이용되는 투여량 및 농도에서 수용자에 비독성이며, 다음을 포함하나, 이에 제한되지 않는다: 완충액, 가령, 포스페이트, 시트레이트 및 다른 유기산; 아스코르브산 및 메티오닌을 포함하는 항산화제; 보존제 (가령, 옥타데실디메틸벤질 암모늄 클로라이드; 헥사메토니움 클로라이드; 벤잘코니움 클로라이드; 벤제토늄 클로라이드; 페놀, 부탈 또는 벤질 알코올; 알킬 파라벤 가령, 메틸 또는 프로필 파라벤; 카테콜; 레소르치놀; 시클로헥사놀; 3-펜타놀; 그리고 m-크레졸); 낮은 분자량의 (약 10개 잔기 미만) 폴리펩티드; 단백질, 가령, 혈청 알부민, 젤라틴, 또는 면역글로블린; 친수성 중합체 가령, 폴리비닐피롤리돈; 아미노산 가령, 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌, 또는 리신; 모노사카라이드, 디사카라이드, 그리고 글루코스, 만노스, 또는 덱스트린을 포함하는 기타 탄수화물; 킬레이트 물질 가령, EDTA; 당, 가령, 슈크로스, 만니톨, 트레할로스 또는 소르비톨; 염-형성 카운터-이온, 가령, 나트륨; 금속 복합체 (예컨대 Zn-단백질 복합체); 및/또는 비-이온성 계면활성제 가령, 폴리에틸렌 글리콜 (PEG). 본 명세서에서 예시적인 약학적으로 허용되는 담체는 세포간(insterstitial) 약물 분산 물질, 가령, 가용성 중성-활성 히알루로니다제 당단백질 (sHASEGP), 예를 들면, 인간 가용성 PH-20 히알루로니다제 당단백질, 이를 테면, rHuPH20 (HYLENEX®, Baxter International, Inc.)을 포함한다. rHuPH20를 포함하는 특정 예시적인 sHASEGPs 및 이를 이용하는 방법은 미국 공개 특허 출원 제 2005/0260186 및 2006/0104968에 기재되어 있다. 한 양상에서, sHASEGP는 하나 또는 그 이상의 추가 글리코사미노글리카나제 가령, 콘드로이티나제와 조합된다.
예시적인 동결건조된 항체 또는 면역접합체 제제는 미국 특허 제 6,267,958에서 기재된다. 수용액 항체 또는 면역접합체 제제는 미국 특허 제 6,171,586 및 WO2006/044908에서 기재된 것들을 포함하며, 후자 제제는 히스티딘-아세테이트 완충액을 포함한다.
본원의 제형은 또한 치료되는 특정 적응증에 필요한 둘 이상의 활성 성분, 바람직하게는 서로 불리하게 영향을 미치지 않는 상보적 활성을 갖는 성분을 함유 할 수 있다.
활성 성분은 콜로이드성 약물 전달 시스템 (예를 들어, 리포좀, 알부민 미소구, 마이크로에멀젼, 나노입자 및 나노캡슐)에서 각각 코아세르베이션 기술에 의해 또는 계면 중합, 예를 들어 하이드록시메틸셀룰로스 또는 젤라틴-마이크로캡슐 및 폴리-(메틸메타크릴레이트) 마이크로캡슐에 의해 준비된 마이크로캡슐 또는 마크로에멀젼 (macroemulsions)안에 포집될 수 있다. 이런 기술은 Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)에서 개시된다.
서방형 제재가 제조될 수 있다. 서방형 제재의 적합한 예들에는 상기 항체 또는 면역접합체를 함유하는 고체 소수성 폴리머의 반투과성 매트릭스가 포함되며, 이러한 매트릭스는 성형된 제품 형태, 예컨대 필름, 또는 마이크로캡슐 형태로 존재한다.
생체내 투여에 사용되는 제제는 일반적으로 무균이다. 무균은 예컨대, 무균 여과막을 통한 여과에 의해 용이하게 구현 될 수 있다.
항-CD79 면역접합체를 포함하는 약학 제제에 관한 추가 세부사항은 WO 2009/099728에 제공되며, 이의 내용은 그 전체가 본원에 참조로 명백하게 포함된다.
IX. 키트 및 제조 물품
또 다른 구체예에서, (예를 들어, 본원에 기재된) 항-CD79b 면역접합체 및 적어도 하나의 추가 제제를 포함하는 제조 물품 또는 키트가 제공된다. 일부 구체예들에서 적어도 하나의 추가 제제는 항-CD20 항체 (예를 들어 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)이다. 일부 구체예들에서, 이러한 제조 물품 또는 키트는 개체에서 B-세포 증식성 장애 (예를 들어, DLBCL, 예를 들어 재발성/불응성 DLBCL)를 치료하거나 이의 진행을 지연시키기 위해 항-CD79b 면역접합체를 적어도 하나의 추가 제제, 예를 들어, 항-CD20 항체 (예를 들어, 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)와 함께 사용하는 것에 관한 지침을 포함하는 패키지 삽입물을 추가로 포함한다. 해당 분야에 공지된 임의의 항-CD79b 면역접합체 및 항암제가 제조 물품 또는 키트에 포함될 수 있다. 일부 구체예들에서, 키트는 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위하여 항-CD20 항체 (예를 들어 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)와 병용하여 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다. 일부 구체예들에서, 키트는 본원에 제공된 방법에 따라 사용하기 위한 것이다.
일부 구체예들에서, 키트는 미만성 거대 B-세포 림프종 (DLBCL)이 있는, 치료를 필요로 하는 인간을 치료하기 위해 리툭시맙, 젬시타빈, 및 옥살리플라틴과 병용하여 사용하기 위한, 다음 화학식을 포함하는 면역접합체를 포함하고
이때 Ab는 (i) 서열 번호: 21의 아미노산 서열을 포함하는 HVR-H1; (ii) 서열 번호: 22의 아미노산 서열을 포함하는 HVR-H2; (iii) 서열 번호: 23의 아미노산 서열을 포함하는 HVR-H3; (iv) 서열 번호: 24의 아미노산 서열을 포함하는 HVR-L1; (v) 서열 번호: 25의 아미노산 서열을 포함하는 HVR-L2; 및 (vi) 서열 번호: 26의 아미노산 서열을 포함하는 HVR-L3를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 1 내지 8이다. 일부 구체예들에서, 키트는 본원에 제공된 방법에 따라 사용하기 위한 것이다.
일부 구체예들에서, 키트는 다음 화학식을 포함하는 면역접합체를 포함하고
이때 Ab는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH를 포함하는 중쇄 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 2 내지 5이다. 일부 구체예들에서, p는 3 내지 4, 예를 들어, 3.5이다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 특정 구체예들에서, 항-CD79b 면역접합체는 Ab-MC-vc-PAB-MMAE의 구조를 포함한다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 일부 구체예들에서 적어도 하나의 추가 제제는 항-CD20 항체 (예를 들어 리툭시맙) 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)이다. 일부 구체예에서, 키트는 본원에 제공된 방법에 따라 개체 (예를 들어, 본원에 기재된 하나 이상의 특징을 갖는 개체)의 DLBCL 치료에 사용하기 위한 것이다.
일부 구체예들에서, 키트는 다음 화학식을 포함하는 면역접합체를 포함하고
이때 Ab는 (i) 서열 번호: 19의 아미노산 서열을 포함하는 VH를 포함하는 중쇄 및 (ii) 서열 번호: 20의 아미노산 서열을 포함하는 VL을 포함하는 경쇄를 포함하는 항-CD79b 항체이고, 그리고 이때 p는 2 내지 5이다. 일부 구체예들에서, p는 3 내지 4, 예를 들어, 3.5이다. 일부 구체예들에서, 면역접합체는 서열 번호: 36의 아미노산 서열을 포함하는 중쇄 및 서열 번호: 35의 아미노산 서열을 포함하는 경쇄를 포함하는 항-CD79b 항체를 포함한다. 특정 구체예들에서, 항-CD79b 면역접합체는 Ab-MC-vc-PAB-MMAE의 구조를 포함한다. 일부 구체예들에서, 항-CD79b 면역접합체는 폴라투주맙 베도틴-피이크이다. 일부 구체예들에서, 적어도 하나의 추라 제제는 리툭시맙, 젬시타빈 및 옥살리플라틴이다. 일부 구체예에서, 키트는 본원에 제공된 방법에 따라 개체 (예를 들어, 본원에 기재된 하나 이상의 특징을 갖는 개체)의 DLBCL 치료에 사용하기 위한 것이다.
일부 구체예들에서, 항-CD79b 면역접합체, 항-CD20 항체 (예를 들어 리툭시맙), 및 하나 이상의 화학요법제 (예를 들어, 젬시타빈 및 옥살리플라틴)는 동일한 용기 또는 별도의 용기에 존재한다. 적합한 용기는, 예를 들어, 병, 바이얼, 백 및 주사기를 포함한다. 용기는 다양한 재료, 가령, 유리, 플라스틱 (예컨대, 폴리비닐 클로라이드 또는 폴리올레핀) 또는 금속 합금 (예컨대, 스테인리스 강 또는 하스텔로이)으로 형성 될 수 있다. 일부 구체예들에서, 용기는 제제를 보유하며 용기 위의 라벨 또는 용기와 관련된 라벨은 사용지침을 표시할 수 있다. 제조 물품 또는 키트는 다른 완충제, 희석제, 필터, 바늘, 주사기 및 사용 지침서가 있는 포장 삽입물을 비롯하여, 상업적 및 사용자 관점에서 필요한 다른 물질을 추가로 포함 할 수 있다. 일부 구체예들에서, 제조 물품은 하나 이상의 또 다른 제제 (예컨대, 화학요법제, 및 항-종양제)를 추가로 포함한다. 하나 이상의 제제에 적합한 용기는, 예를 들어, 병, 바이얼, 백, 및 주사기를 포함한다.
표 E: 아미노산 서열.
본 명세서는 해당 분야의 당업자가 본 발명을 실시하기에 충분한 것으로 간주된다. 전술한 설명으로부터 본 명세서에 제시되고 기재된 것 이외에 본 발명의 다양한 변형들이 해당 분야의 당업자들에게 명확해질 것이며 첨부된 청구범위에 속할 것이다. 본 명세서에 인용된 모든 간행물, 특허 및 특허 출원은 모든 목적을 위해 그 전문이 본원의 참고자료로 포함된다.
실시예
다음은 본 발명의 방법 및 조성물의 예이다. 다양한 다른 실시예가 전술한 일반적인 설명에 따라 실시될 수 있는 것으로 이해된다.
실시예 1: 재발성/불응성 미만성 거대 B 세포 림프종 환자에서 폴라투주맙 베도틴과 리툭시맙 + 젬시타빈 + 옥살리플라틴 병용 (Pola-R-GemOx) 대 R-GemOx 단독의 안전성 및 효능을 평가하는 III상, 공개 라벨, 다기관, 무작위배정 연구
본 실시예는 재발성/불응성 미만성 거대 B 세포 림프종 (DLBCL) 환자에서 폴라투주맙 베도틴과 리툭시맙, 젬시타빈 및 옥살리플라틴 병용 (Pola-R-GemOx)의 안전성 및 효능을 리툭시맙, 젬시타빈 및 옥살리플라틴 단독 (R-GemOx)과 비교하여 평가하는 III상, 공개-라벨, 다기관, 무작위배정 연구를 설명한다. 본 연구에서, 치료는 2 단계로 이루어진다: 1) Pola-R-GemOx 병용의 안전성을 평가하는 초기 안전성 도입 단계 (1단계); 및 2) Pola-R-GemOx 대 R-GemOx의 안전성 및 효능을 비교하는 무작위배정 대조 시험 (RCT) 단계 (2단계).
I. 연구 목표
A. 1단계: 안전성 도입
안전성 목표 및 평가변수
1차 안전성 목표
이 연구의 1단계의 1차 안전성 목표는 병용 요법으로서 Pola-R-GemOx의 안전성과 내약성을 평가하는 것이다.
1차 안전성 평가변수
이 연구 1단계의 1차 안전성 평가변수는 미국 국립 암 연구소 이상 반응 표준 용어 기준, 버전 5 (NCI CTCAE v5.0)에 따른, 신체 소견 및 이상 반응 (AE)의 발생, 특성 및 중증도이며, 특히 말초 신경병증에 중점을 둔다.
2차 안전성 목표
본 연구 1단계의 2차 안전성 목표는 병용 요법으로서 Pola-R-GemOx의 안전성 및 내약성을 평가하고 폴라투주맙 베도틴의 면역원성을 평가하는 것이다.
2차 안전성 평가변수
말초 신경병증, 이 연구의 1단계의 2차 안전성 평가변수는 암 치료/부인과 종양 그룹의 기능적 평가-신경독성 12-항목 척도(FACT-GOG/Ntx12)에 의해 측정된 말초 신경병증의 발생률 및 평가; 투약 중단, 용량 감소 및 용량 강도로 측정된 Pola-R-GemOx의 내약성; 및 기준선에서의 항-약물 항체 (ADA)의 존재량 및 연구 중 ADA의 발생률이다.
효능 목표 및 평가변수
2차 효능 목표
본 연구 1단계의 2차 효능 목표는 Pola-R-GemOx의 효능을 평가하는 것이다.
2차 효능 평가변수
본 연구 1단계의 2차 효능 평가변수는 다음과 같다:
●
완전 반응(CR), 치료 종료시 PET-CT에 기반하여 Lugano 2014 반응 기준에 따라 (Cheson 외, (2014) J Clin Oncol 32:3059-3068) 완전한 대사 반응에 도달한 환자들의 비율로 정의됨.
●
객관적 반응율 (ORR), 치료 종료시 Lugano 2014 반응 기준에 따라 (PET CT 데이터를 포함한 반응에 기반) 완전한 또는 부분 대사 반응에 도달한 환자들의 비율로 정의됨.
●
최적의 전체 반응 (BOR), 치료 시작시부터 치료 종료시까지, Lugano 2014 반응 기준에 따라 기록된 최적 반응으로 정의됨.
●
무진행 생존 (PFS), 연구 치료제의 첫 투약시부터 Lugano 2014 반응 기준에 따른 첫 번째 질환 진행 발생시 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망시까지의 시간으로 정의됨.
●
전체 생존(OS), 연구 치료제 첫 투약시부터 임의의 원인으로 인한 사망시까지의 시간으로 정의됨.
●
무사건 생존 (EFSeff), 연구 치료제 첫 투약시부터 다음 중 어느 하나의 최초 발생시까지의 시간으로 정의됨:
o
질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반).
o
임의의 원인으로 인한 사망.
o
프로토콜에 명시되지 않은 임의의 항-림프종 치료 (NALT) 개시.
약동학 목표 및 평가변수
약동학 목표
본 연구 1단계의 약동학 목표는 폴라투주맙 베도틴의 약동학(PK) 프로파일을 평가하는 것이다.
약동학 평가변수
본 연구 1단계의 약동학적 평가변수는 재발성 또는 불응성 DLBCL 환자에서 R-GemOx와 폴라투주맙 베도틴 병용의 PK 프로파일과 폴라투주맙 베도틴과 R-GemOx 사이의 잠재적 PK 상호작용이다.
B. 2단계: 무작위배정 대조 시험 (RCT)
효능 목표 및 평가변수
1차 및 2차 효능 목표
본 연구 2단계의 1차 및 2차 효능 목표는 Pola-R-GemOx의 효능을 R-GemOx 단독과 비교하여 평가하는 것이다.
1차 효능 평가변수
본 연구 2단계의 1차 효능 평가변수는 무작위 배정시부터 임의의 원인으로 인한 사망시까지의 시간으로 정의되는 전체 생존(OS)이다.
2차 효능 평가변수
본 연구 2단계의 2차 효능 평가변수는 다음과 같다:
●
계층적 검사 절차에 포함된 주요 2차 평가변수(아래 섹션 V 참조):
o
PFS, 무작위배정시부터 Lugano 2014 반응 기준에 따른 첫 번째 질환 진행 발생시, 또는 임의의 원인으로 인한 사망시까지의 시간으로 정의됨.
o
CRR, 치료 종료시 PET-CT에 기반하여 Lugano 2014 반응 기준에 따라 완전한 대사 반응에 도달한 환자들의 비율로 정의됨.
o
ORR, 치료 종료시 Lugano 2014 반응 기준에 따라 완전한 또는 부분 대사 반응에 도달한 환자들의 비율로 정의됨.
●
다중성 절차 검사를 위해 조정되지 않은 2차 평가변수:
o
BOR, 무작위배정시부터 치료 종료시까지, Lugano 2014 반응 기준에 따라 기록된 최적 반응으로 정의됨.
o
CRR, 치료 종료시 PET-CT에 기반하여 Lugano 2014 반응 기준에 따라 완전한 대사 반응에 도달한 환자들의 비율로 정의됨.
o
ORR, 치료 종료시 Lugano 2014 반응 기준에 따라 (PET CT 데이터를 포함한 반응에 기반) 완전한 또는 부분 대사 반응에 도달한 환자들의 비율로 정의됨.
o
객관적 반응 기간 (DoR), 기록된 첫 객관적 반응 발생시 (PET CT 데이터를 포함한 반응에 기반)부터, Lugano 2014 반응 기준에 따른 질환 진행 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반), 또는 임의의 원인으로 인한 사망시 (어느 것이든 먼저 발생하는 시점)까지의 시간으로 정의됨.
o
EFSeff, 무작위배정시부터 다음 중 어느 하나의 최초 발생시까지의 시간으로 정의됨:
●
질환 진행 또는 재발 (PET CT 데이터를 포함하거나 임의의 PET 데이터를 포함하지 않는 반응에 기반).
●
임의의 원인으로 인한 사망.
●
NALT 개시.
환자 보고 결과 (PRO) 목표 및 평가변수
2차 및 탐색적 PRO 목표
본 연구 2단계의 2차 PRO 목표는 건강 관련 삶의 질 측면에 대한 치료 및 질환의 영향을 평가하는 것이다.
2차 PRO 평가변수
본 연구 2단계의 2차 PRO 평가변수는 다음과 같다:
●
유럽 암 연구 및 치료 기구 삶의 질 설문지, Core 30 (EORTC QLQ-C30)으로 측정한 신체 기능 악화 및 피로시까지의 시간.
●
암 치료 림프종의 기능 평가 (FACT-Lym) 하위척도로 측정한 림프종 증상의 진행시까지의 시간.
●
FACT/GOG-NTX-12 하위 척도 점수로 측정한 말초 신경병증의 기준선으로부터의 변화.
탐색적 PRO 평가변수
●
본 연구 2단계의 탐색적 PRO 평가변수는 EORTC QLQ-C30, FACT-Lym 하위척도, FACT/GOG-NTX-12, 및 EQ-5D-5L의 모든 척도에 대한 기준선으로부터의 변화 및 기술 요약 통계이다.
안전성 목표 및 평가변수
안전성 목표
본 연구 2단계의 안전성 목표는 병용 요법으로서 Pola-R-GemOx의 안전성 및 내약성을 R-GemOx와 비교하여 평가하고 폴라투주맙 베도틴의 면역원성을 평가하는 것이다.
안전성 평가변수
본 연구 2단계의 안전성 평가변수는 다음과 같다:
●
NCI CTCAE v5.0 및 신체 소견에 따른 AE(말초 신경병증 포함)의 발생율, 특성 및 중증도.
●
투약 중단, 용량 감소 및 용량 강도에 의해 평가된 내약성.
●
FACT-GOG/Ntx12로 측정된 말초 신경병증의 발생율 및 평가.
●
기준선에서의 항-약물 항체(ADA)의 존재량 및 연구 중 ADA의 발생율.
바이오마커 목표 및 평가변수
탐색적 바이오마커 목표
본 연구 2단계의 탐색적 바이오마커 평가변수는 다음 기준을 충족하는 바이오마커를 식별하는 것이다:
●
폴라투주맙 베도틴에 대한 반응의 예후가 존재(즉, 예측 바이오마커).
●
더 심각한 질환으로의 진행과의 관련 존재(즉, 예후 바이오마커).
●
폴라투주맙 베도틴 활성의 증거를 제공하거나 질환 생물학에 대한 지식과 이해를 높임.
탐색적 바이오마커 평가변수
이 연구 2단계의 탐색적 바이오마커 목표는 전체 생존(OS), 무진행 생존(PFS), 완전 반응(CR) 비율을 포함한 효능 평가변수와, 탐색적 바이오마커, 예를 들어 분자 DLBCL 기원 하위유형 예후 세포, BCL2 및 MYC 이중 발현자, 주요 림프종 돌연변이 사이의 관련성이다.
약동학 목표 및 평가변수
약동학 목표
본 연구 2단계의 약동학 목표는 폴라투주맙 베도틴의 약동학(PK) 프로파일을 평가하는 것이다.
약동학 평가변수
본 연구 2단계의 약동학 평가변수는 다음과 같다:
재발성 또는 불응성 DLBCL 환자에서 R-GemOx와 폴라투주맙 베도틴 병용의 PK 프로파일.
폴라투주맙 베도틴과 R-GemOx 사이의 잠재적 PK 상호작용.
II. 환자
총 약 216명의 환자들에서, 약 10명의 환자가 안전성 도입기 (1단계)에 등록되고, 약 206명의 환자가 무작위배정 부분 (2단계)에 등록된다.
A. 포함 기준
환자가 다음 기준을 충족하는 경우 본 연구에 포함된다:
●
연령 ≥ 18세.
●
달리 명시되지 않는 한 (NOS), 조직학적으로 확인된 미만성 거대 B-세포 림프종 또는 무통성 질환이 DLBCL로 전환된 병력.
●
적어도 1 (≥ 1)차의 선행 전신 요법.
o
이전에 자가 조혈모세포 이식 (HSCT)이 허용됨; 화학요법에 이은 공고 자가 HSCT는 한 차수의 요법으로 간주된다..
o
환자가 모든 면역억제 요법을 받지 않고 활동성 이식편 대 숙주병(GVHD)이 없는 한 이전에 동종 HSCT가 허용됨; 화학요법에 이은 동종 HSCT는 한 차수의 요법으로 간주된다.
o
국소 요법(예를 들어, 방사선요법)은 치료 차수로 간주되지 않는다.
●
다음과 같이 정의되는, 재발성 또는 불응성 질환:
o
재발성: 마지막 요법 완료 후 반응이 ≥ 6 개월 지속된 후 질환이 재발.
o
불응성: 질환이 요법 동안 진행하거나 선행 요법 후 6 개월 이내 (< 6 개월) 진행.
●
CT 또는 MRI로 측정할 때 가장 긴 치수가 >1.5cm로 정의되는 적어도 하나의 2차원 측정가능한 병변.
●
0, 1 또는 2의 동부 종양학 협력 그룹 (ECOG) 전신 활동도 점수.
o
3의 ECOG 전신 활동도 점수를 가지며, 이러한 활동도가 DLBCL-관련이고 스크리닝 단계 중 7일의 스테로이드 치료 사전단계(예를 들어, 1 mg/kg 프레드니손) 이후인 경우에만 RCT 단계 (2단계)에 포함되는 것으로 간주된다. 연구 등록 적격이기 위해서는 후속하여 2 이하로의 ECOG 전신 활동도 점수 개선이 관찰되어야 한다.
●
다음과 같이 정의된 적절한 혈액학적 기능:
o
헤모글로빈 ≥ 8 g/dL.
o
호중구 감소증이 기저 질환으로 인한 것이고 스테로이드 투여 전인 경우 절대 호중구 수 (ANC) ≥ 1.5 x 109/L 또는 ≥ 0.5 x 109.
o
혈소판감소증이 기저 질환으로 인한 것인 경우 혈소판 수 ≥ 75 x 109/L 또는 ≥ 50 x 109.
●
가임 여성의 경우: 금욕 유지 또는 피임 방법 사용에 대한 동의 및 난자 기증 자제에 대한 동의
●
남성의 경우: 금욕을 유지하기로 동의 또는 피임 방법을 사용하기로 동의하고 정자 기증을 자제하기로 동의.
B. 제외 기준
환자가 다음 기준을 충족하는 경우 본 연구에서 제외된다:
●
인간화 또는 뮤린 모노클로날 항체(또는 재조합 항체 관련 융합 단백질)에 대한 중증 알레르기 또는 아나필락시스 반응의 병력, 또는 뮤린 제품에 대한 민감성 또는 알레르기 공지.
●
리툭시맙, 젬시타빈 또는 옥살리플라틴에 대한 금기.
●
등록 시 NCI CTCAE v5.0에 따라 > 1등급으로 평가된 말초 신경병증.
●
폴라투주맙 베도틴 또는 젬시타빈 + 백금 기반 제제 조합을 이전에 사용.
●
이전 또는 진행 중인 폴라투주맙 베도틴 시험에 등록.
●
사이클 1의 1일차 전 2주 이내 암 치료 목적으로 방사선요법, 화학요법, 면역요법, 면역억제 요법, 또는 임의의 연구용 제제로 치료.
o
탈모증을 제외하고 선행 요법의 모든 급성, 임상적으로 유의한 치료 관련 독성은 사이클 1의 1일차 이전에 ≤ 2등급으로 해소되어야 함.
●
모집시 자가 또는 동종 줄기 세포 이식이 예정됨.
o
하나의 선행 요법만 받은, 줄기 세포 이식에 적합한 환자들은 본 시험에서 제외됨. 이식 부적격 사유에는 연령, 전신활동도 점수, 동반 질환, 이식 실패 또는 실패한 절차, 구제 요법에 대한 불충분한 반응, 환자 거부 또는 논리적 이유가 포함됨.
●
모집시 1차 또는 2차 중추신경계(CNS) 림프종.
●
리히터 변환 또는 이전의 모세관 누출 증후군(CLL).
●
이상 실험실 값들이 기저 림프종으로 인한 경우를 제외하고, 다음과 같은 이상 실험실 값들 중 하나:
o
크레아티닌 > 1.5 x 정상 상한(ULN) 또는 측정된 크레아티닌 제거율 < 30 mL/분.
o
아스파르테이트 아미노전이효소 (AST) 또는 알라닌 아미노전이효소 (ALT) > 2.5 x ULN.
o
총 빌리루빈 ≥ 1.5 x ULN; 총 빌리루빈이 ≤ 3 x ULN인 경우 보고된 길버트 질환이 있는 환자는 등록됨.
o
치료용 항응고제 부재시 국제 국제 표준화 비율(INR) 또는 프로트롬빈 시간 (PT) > 1.5 x ULN.
o
루푸스 항응고제 부재시 부분 트롬보플라스틴 시간 (PTT) 또는 활성화 부분 트롬보플라스틴 시간 (aPTT) > 1.5 x ULN.
●
프로토콜 준수 또는 결과 해석에 영향을 미칠 수 있는 기타 악성 종양의 병력. 다음은 예외이다:
o
연구 이전 임의의 시점에서 피부의 기저 또는 편평 세포 암종 또는 자궁경부의 제자리 암종을 완치한 병력이 있는 환자는 적격이다.
o
치료 의향이 있는, 적절하게 치료된 기타 악성 종양 (및 등록 전 ≥ 2년 동안 치료 없이 관해 상태에 있었던 악성 종양)이 있는 환자는 적격이다.
o
연구 전 임의의 시점에서 치료가 필요하지 않은 저등급, 초기 단계 전립선암(글리슨 점수 6 이하, 1기 또는 2기)이 있는 환자는 적격이다.
●
중증 심혈관 질환(예를 들어, 뉴욕 심장학회[NYHA] 분류 III 또는 IV 심장 질환, 지난 6개월 이내의 심근 경색증, 불안정한 부정맥, 또는 불안정 협심증) 또는 중증 폐 질환(폐쇄성 폐 질환 및 기관지 경련의 병력 포함)을 비롯한, 프로토콜 준수 또는 결과 해석에 영향을 미칠 수 있는 중요하고 통제되지 않는 수반 질환의 증거.
●
연구 등록 시 알려진 활성 박테리아, 바이러스, 진균, 마이코박테리아, 기생충 또는 기타 감염(손발톱 바닥의 진균 감염 제외), 또는 사이클 1의 1일차 전 4주 이내에 주요 감염 발생.
●
결핵이 의심되는 또는 잠복 결핵 환자; 잠복 결핵은 인터페론-감마 방출 분석 양성으로 확인됨.
●
만성 B형 간염 바이러스(HBV) 감염에 대한 검사 결과 양성 (B형 간염 표면 항원[HBsAg] 혈청학 양성으로 정의됨).
o
잠재성 또는 이전 HBV 감염 (HBsAg 음성 및 B형 간염 코어 항체 [HBcAb] 양성으로 정의) 환자는 HBV DNA가 검출되지 않는 경우 포함되며, 단, 연구 치료제의 마지막 사이클 후 적어도 12개월 동안 매 사이클의 1일차에 매월 DNA 검사를 받아야 함.
●
C형 간염 바이러스(HCV) 항체 검사 결과 양성.
o
HCV 항체에 양성인 환자는 중합효소 연쇄 반응 (PCR)이 HCV RNA에 대해 음성인 경우에만 적격임.
●
공지된 인간 면역 결핍 바이러스(HIV) 혈청양성 상태 병력. HIV 상태를 알 수 없는 환자의 경우 지역 규정에서 요구하는 경우 스크리닝시 HIV 검사를 수행한다.
●
치료 전 4주 이내에 생백신 접종.
●
진단용 이외의 최근의 주요 수술 (이클 1 1일차 시작 전 6주 이내).
●
연구용 약물의 사용을 금하거나 결과 해석에 영향을 미칠 수 있거나 환자를 치료 합병증으로 인한 고위험에 빠뜨릴 수 있는 질환 또는 병태에 대한 합리적인 의심을 제공하는 기타 질환, 대사 기능장애, 신체 검사 소견 또는 임상 실험실 소견.
●
연구 중 또는 연구 약물의 마지막 투여 후 12개월 이내에 임신 또는 수유 중이거나, 임신을 계획.
III. 연구 설계
본 연구는 재발성 또는 불응성 DLBCL 환자들에서 III상, 다기관, 공개 라벨, 무작위배정 연구이다. 연구는 스크리닝 기간, 치료 기간(1단계 및 2단계) 및 치료 후 기간으로 구성된다. 치료 후 기간에는 연구 치료의 마지막 투여 후 28일에 발생하는 치료 방문 종료 및 추적 기간이 포함된다. 이상 반응, 중증 이상 반응 및 특별한 관심대상의 이상 반응은 연구 약물의 마지막 투여 후 90일까지 또는 프로토콜에 명시되지 않은 항림프종 치료(NALT) 시작시까지 보고된다.
연구의 전체 설계는 도 1에 제시되어 있다.
A. 스크리닝 기간
이 연구에 적격이려면 환자가 조직학적으로 확인된, 재발 또는 불응성 DLBCL이 있어야 한다.
환자는 모집 전에 자가 조혈모세포 이식 (HSCT)을 받았을 수 있다; 화학요법에 이은 공고 자가 HSCT는 한 차수의 요법으로 간주된다. 모든 면역억제 요법을 받지 않고 활동성 이식편 대 숙주병(GVHD)이 없는 한 이전에 동종 HSCT 받은 환자는 등록됨; 화학요법에 이은 동종 HSCT는 하나의 요법차수로 간주된다. 국소 요법(예를 들어, 방사선요법)은 치료 차수로 간주되지 않는다. NCI CTCAE v5.0에 따라 1 초과인 것으로 평가된 말초 신경병증 환자들은 등록에서 제외된다. 기타 포함 및 제외 기준은 상기 섹션 II에 제시된다.
B. 치료 기간
치료 기간은 안전성 도입 단계(1단계)와 무작위배정 대조 시험(2단계)의 두 단계로 진행된다.
안전성 도입인 1단계에서 10명의 환자가 Pola-R-GemOx로 실험 연구 치료를 받는다.
무작위배정 대조 시험(RCT)인 2단계에서 환자는 Pola-R-GemOx를 사용한 실험 연구 치료 또는 R-GemOx를 사용한 대조 연구 치료를 받도록 1:1 비율로 무작위로 할당된다.
본 연구의 무작위 배정 부분(2단계)의 주요 목적은 OS로 측정한 재발성 또는 불응성 DLBCL 환자에서 Pola-R-GemOx 대 R-GemOx의 효능을 평가하는 것이다. R-GemOx 군 (Mounier 외, (2013) Haematologica, 98:1726-1731)에서 OS 중앙값을 9.5개월 그리고 무작위배정 비율을 1:1로 가정할 때, 80% 검정력 및 0.05의 양측 α로 OS 중앙값에서 6.3개월의 그룹간 차이를 검출하기 위해서는 121건의 사례가 필요하다(위험비 [HR] = 0.60). 위의 통계적 가정을 바탕으로 모집 기간 약 11개월(월 18명)과 마지막 환자를 무작위 배정한 후 14개월의 추적 관찰을 예상하고, 10%의 예상 탈락률을 고려하여 총 약 206명의 환자가 본 연구의 2단계에 포함된다. 환자는 Pola-R-GemOx 및 R-GemOx 치료에 1:1의 비율로 무작위 배정된다.
치료 기간의 두 단계 모두에서 환자는 각각 최대 8 사이클의 Pola-R-GemOx 또는 8 사이클의 R-GemOx를 21일 사이클로 투여받는다.
1단계:
안전성 도입
총 10명의 환자가 Pola-R-GemOx로 치료된다. 10명의 환자는 3개의 코호트에 걸쳐 배정된다:
● 코호트 1: 첫 3명의 환자.
● 코호트 2: 두 번째 3명의 환자.
● 코호트 3: 마지막 4명의 환자.
각 코호트 내에서 급성 말초 신경병증 독성에 중점을 두고 모든 대상체에서 제4 사이클 종료시 안전성을 평가한다. 코호트 내에서 모든 안전성 평가가 수행되고 추가 대상체 발생이 정리되면 다음 코호트에서 모집이 시작된다. 이 절차를 3개 코호트 모두가 완전히 모집될 때까지 계속한다.
코호트 2 및 코호트 3은 각각 코호트 1 및 코호트 2에서 모든 안전성 평가가 완료되고 다음 코호트 모집이 승인될 때까지 등록되지 않는다. 코호트 내의 환자가 질환 진행, 사망 또는 직접적으로 말초 신경병증으로 인한 것이 아닌 기타 이유 때문에 치료 사이클 4 이전에 중단하는 경우, 환자가 교체된다.
코호트의 전체 모집단이 적어도 4회 사이클을 완료시, 특히 말초 신경병증에 중점을 둔 Pola-R-GemOx의 총 안전성 프로파일이 평가되고 다음 코호트가 열릴지 여부에 대한 권장 사항이 제공된다 (진행/중단 결정). 다음 코호트에 대한 추가 등록을 중단할 수 있는 잠재적 근거는, 코호트 내 환자의 > 33.33%가 14일 이내에 ≤ 1등급으로 해소되지 않는 ≥ 3등급 말초 신경병증을 가지는지 여부이다. 용량 조절의 잠재적인 유익한 효과, 말초 신경병증 발생의 해소에 관한 시간 경과 등이 진행/중단 결정에서 고려된다. 또한, 코호트 2 및 코호트 3에 대한 안전성 평가에서 제4 치료 사이클 이후에 진행하는 이전 코호트들의 모든 환자를 재평가하여 Pola-R-GemOx의 누적 신경독성 가능성과 말초 신경병증 해소 과정을 평가한다.
1단계는 또한 ADA 및 R-GemOx와 병용되는 폴라투주맙 베도틴의 희박 PK 프로파일을 평가한다.
본 연구의 안전성 도입 (1단계)에 관한 요약을 도 2에 제공한다.
열 번째 대상체가 전체 치료 기간을 완료한 후(도 2), Pola-R-GemOx 요법의 안전성과 내약성이 평가되고 열 번째 환자에 대한 치료 종료 시 본 연구의 2단계 (RCT 단계)를 계속할지 여부를 결정(진행/중단 결정)(도 2)한다. 1단계 종료 시 공식적인 진행/중단 결정은 다음과 같이 결정된다:
●
1단계의 치료 기간에 마지막으로 남은 환자가 Pola-R-GemOx의 마지막 용량을 투여받았을 때, 특히 등급 ≥ 3의 말초 신경병증 발생 빈도, 경과 및 가역성에 초점을 두어 1단계 연구 모집단의 전체 안전성 프로파일을 검토한다.
o
1단계(n = 10)의 3명 이하의 환자가 치료 기간 동안 ≥ 3등급의 말초 신경병증이 있었고 14일 이내에 ≤ 1등급으로 해소되지 않으면 연구는 2단계인 무작위배정 대조 시험(RCT) 단계로 계속된다.
o
1단계(n = 10)의 4명 이하의 환자가 치료 기간 동안 ≥ 3등급의 말초 신경병증이 있었고 14일 이내에 ≤ 1등급으로 해소되지 않으면 연구는 보류된다.
o
최초 연구 치료 용량에서 말초 신경병증의 위험이 용량 조절 후 만족스럽게 완화되는 것으로 확인되었는지 여부를 평가한다.
이전 정보를 기반으로 RCT 단계인 2단계로 계속 진행할 것인지에 대한 권장 사항이 제공된다.
2단계:
무작위배정 대조 시험
Pola-R-GemOx 병용 요법이 안전성 도입(1단계)에서 허용가능한 것으로 간주되면 RCT 단계로의 등록이 시작된다. 총 206명의 적격 환자가 1:1 비율로 무작위배정되어 Pola-R-GemOx(실험 치료) 또는 R-GemOx(대조)를 받는다.
무작위배정은 계층화된 순열 블록을 사용하여 IxRS에 의해 수행된다. 계층화 요인에는 다음이 포함된다: 1) 선행 전신 치료 또는 요법의 차수 (1 vs. ≥ 2); 2) 마지막 전신 치료 또는 요법의 결과 (재발성 vs. 불응성); 및 3) 연령 (≤ 70세 vs. > 70세). 선행 전신 치료 또는 요법의 라인 수를 기반으로 계층화하는 경우: 화학 요법에 이은 공고 자가 HSCT는 한 라인의 요법으로 계산된다; 화학 요법에 이은 동종 HSCT는 한 라인의 요법으로 계산된다; 국소 요법(예를 들어, 방사선 요법)은 치료 라인으로 간주되지 않는다. 마지막 전신 요법 또는 치료 결과를 기반으로 계층화하는 경우: 재발성 질환은 마지막 라인의 치료 완료 후 ≥ 6개월 후 재발하는 질환으로 정의되고; 불응성 질환은 치료 중 진행되거나 또는 선행 치료로부터 6개월 이내 (< 6개월)에 진행되는 질환으로 정의된다.
계층화는 질환 진행 및 질환 상태 측면에서 거의 동등한 치료 그룹을 생성함으로써, 실험 (Pola-R-GemOx) 및 대조 (R-GemOx) 그룹들 간 비교를 확실하게 할 수 있게 한다.
중간 안전성 분석은 RCT 단계중에 수행된다. 1차 및 2차 안전성 중간 분석은 각각 처음 10명 및 20명의 환자를 각 군에 무작위배정하고 적어도 2사이클의 치료를 완료한 후 수행된다. 그 후, 중간 안전성 평가의 빈도는 2차 안전성 중간 평가 동안 관찰된 ≥ 3등급 말초 신경병증 발생 수에 따라 달라진다. 14 일 이내 ≤ 1등급로 회복되는 ≥ 3등급의 말초 신경병증은 중단 규칙에 고려되지 않는다.
안전성은 NCI CTCAE v5.0, FACT/GOG-Ntx12 점수, 임상 실험실 검사 결과, 심전도(ECG) 및 활력 징후에 따른 이상 반응으로 평가된다. 반응 평가는 치료 종료 시 양전자 방출 단층촬영-컴퓨터 단층촬영(PET-CT) 스캔을 기반으로 한 Lugano 2014 기준에 따른다.
2단계는 ADA 및 R-GemOx와 병용되는 폴라투주맙 베도틴의 희박 PK 프로파일을 평가한다. 또한 2단계는 바이오마커와 환자 보고 결과를 평가한다.
C. 연구 종료 및 연구 기간
초기 안전성 도입 후 무작위배정 단계에 대한 모집이 약 11개월에 걸쳐 이루어진다.
이는 사례-기반 시험이다. 최종 OS 분석을 위한 임상시험 마감일은 목표 사망건 수(121명 사망) 발생시 확정되며, 이는 본 연구의 RCT 단계에서 첫 번째 환자([FPI]의 첫 번째 환자)가 무작위배정된 후 약 25개월로 예상된다.
연구 기간과 최종 분석 시간은 모집률과 사건 발생 수에 따라 다르다. 사망 사건을 연구 과정 전반에 걸쳐 모니터링하고, 연구 일정을 업데이트한다.
IV. 임상시험용 의약품의 용량 및 투여 시기
이 연구의 임상시험용 의약품(IMP)은 Pola-R-GemOx이다. 대조 요법은 R-GemOx이다.
Pola-R-GemOx 실험 치료 요법의 요약을 도 3A에 제공한다.
R-GemOx 대조군 치료 요법의 요약을 도 3B에 제공한다.
A. 폴라투주맙 베도틴
폴라투주맙 베도틴 1.8mg/kg은 실험 치료 그룹 (Pola-R-GemOx)에서만 최대 8사이클 동안 각 21일 사이클의 1일차에 정맥내 투여된다.
폴라투주맙 베도틴은 리툭시맙 투여 후 같은 날 투여하거나, 리툭시맙 투여가 지연된 경우 다음 날 투여된다.
스크리닝 동안 (-28일 ~ -1일) 얻은 환자 체중은 모든 치료 사이클에 대한 용량 결정에 사용된다; 해당 치료 사이클의 1일차 이전 96시간 이내의 환자 체중이 스크리닝 동안 얻은 체중의 10%보다 크거나 작으면 새로운 체중을 사용하여 용량을 계산한다. 용량 조정을 촉발한 체중은 향후 용량 조정시 새로운 참조 체중으로 사용된다. 모든 후속 용량은 그에 따라 수정된다. 10% 미만의 체중 변화에 대한 용량 조정 또한 로컬 표준 치료인 경우 허용된다.
초기 용량은 90 (+/- 10)분에 걸쳐 (로컬 지침에 따름) 수분을 충분히 섭취한 환자에게 투여된다. 사전투약 (예를 들어, 기관 표준 관행에 따라 경구 아세트아미노펜 또는 파라세타몰 500-1000 mg 및 디펜하이드라민 50-100 mg)을 폴라투주맙 베도틴을 투여하기 전 ≥30분에 개별 환자에게 투여할 수 있다. 코르티코스테로이드의 투여는 담당 의사의 재량에 따라 허용되었다. 사전투약 없이 1차 주입에서 주입 관련 반응 (IRR)이 관찰된 경우, 후속 투약 전에 예비약물을 투여한다.
주입 관련 증상을 경험하는 환자의 경우 폴라투주맙 베도틴 주입이 느려지거나 중단된다. 초기 투약 후, 환자는 열, 오한, 경직, 저혈압, 메스꺼움 또는 기타 주입 관련 증상에 대해 90분 동안 관찰된다. 선행 주입이 내약성이 좋지 않은 경우, 후속 투여량의 폴라투주맙 베도틴을 30 ± 10분에 걸쳐 투여한 후, 주입 후 30분의 관찰 기간이 후속되었다.
폴라투주맙 베도틴 투여 동안, 주입 시작 전, 주입하는 동안 15 ± 5 분 마다, 주입 종료시, 사이클 1의 투약 완료 후 90분 동안 30 ± 10분 마다, 및 후속 사이클에서 투약 완료 후 30 ± 10 분에 활력 징후를 평가한다.
폴라투주맙 베도틴은 동결건조 제형 (140 mg/바이얼)이다. 투여 전에, 동결건조된 분말을 주사용 멸균수로 7.2mL 부피로 재구성한다.
B. 리툭시맙
리툭시맙 (Mabthera/Rituxan®) 375 mg/m2를 최대 8 사이클 동안 각 21일 사이클의 1일차에 정맥내 투여한다. 리툭시맙은 같은 날 폴라투주맙 베도틴 전에 투여된다; 리툭시맙의 투약 지연이 있는 경우 폴라투주맙 베도틴은 다음날 투여된다.
사이클 1에서 리툭시맙을 투여하는 동안 활력징후는 주입 전, 주입 시작 후 90분 동안 약 15 ± 5분마다, 주입 종료 후 1시간까지 30 ± 10분마다 얻는다. 후속 주기에서 리툭시맙을 투여하는 동안 활력 징후는 주입 전, 주입 시작 후, 및 주입 종료 후 1시간까지 약 30 ± 10분마다 기록된다.
스크리닝시 계산된 환자의 체표면적(BSA)은 연구 전반에 걸쳐 리툭시맙의 용량을 계산하는데 사용되며, 환자의 체중이 스크리닝에서 > 10% 증가하거나 감소한 경우 BSA를 다시 계산하여 후속 투약에 사용한다. 비만 환자의 경우 BSA 상한선이 없으며 조정 체중이 아닌 실제 체중을 권장한다. 비만 환자(비만은 체질량 지수 ≥ 30으로 정의됨, 킬로그램을 제곱미터로 나누어 측정)에 대한 경험적 용량 조정은 기관 지침에 따라 시행된다.
리툭시맙 투여는 다른 연구 치료제 투여 최소 30분 전에 완료된다. 환자에게 IRR 위험이 증가하는 경우 (높은 종양 부담, 높은 말초 림프구 수), 리툭시맙 주입을 2일에 걸쳐 분할한다. 리툭시맙 주입 중 이상반응을 경험한 환자에 대해 필요한 경우 다음 날에도 리툭시맙 투여를 계속한다. 리툭시맙의 용량을 2일에 걸쳐 분할하는 경우, 두 번의 주입 모두 적절한 사전투약과 첫 번째 주입 속도로 이루어진다.
모든 리툭시맙 주입은 경구 아세트아미노펜 (예를 들어, 650-1000 mg)과 항히스타민제(예를 들어, 디펜히드라민 하이드로클로라이드(50-100 mg))를 사전투약한 후 각 주입을 시작하기 30분 이상 전에 환자에게 투여한다 (금기가 없는 경우). 추가 글루코코르티코이드(예를 들어, 100mg IV 프레드니손 또는 프레드니솔론 또는 등가물)가 허용된다. 이전 주입 시 주입 관련 증상을 경험하지 않은 환자의 경우 후속 주입 시 사전투약을 생략할 수 있다.
리툭시맙은 전용 라인을 통해 느린 IV 주입으로 투여된다. IV 주입 펌프(예를 들어, Braun Infusomat Space)를 사용하여 리툭시맙의 주입 속도를 조절한다. 폴리염화비닐(PVC), 폴리우레탄(PUR) 또는 폴리에틸렌(PE)을 제품 접촉면으로 사용하는 투여 세트와 폴리올레핀, 폴리프로필렌(PP), PVC 또는 PE를 제품 접촉면으로 사용하는 IV 백은 호환된다. 흡착 가능성으로 인해 추가 인라인 필터는 사용되지 않는다. 폴라투주맙 베도틴 투여에 사용되는 인라인 필터는 리툭시맙 투여에 사용되지 않는다.
환자가 유의한 주입 반응 없이 연구 치료의 제1 사이클을 견디면, 리툭시맙은 로컬 기관 지침에 따라 급속 주입으로 투여된다.
리툭시맙의 1차 및 후속 주입의 투여에 대한 요약이 표 1에 제공된다.
표 1: 리툭시맙의 1차 및 후속 주입의 투여.
C. 젬시타빈
젬시타빈 1000 mg/m2 를 최대 8 사이클 동안 각 21일 사이클의 2일차에 정맥내 투여한다. 젬시타빈은 같은 날 옥살리플라틴 전에 투여된다. 리툭시맙 투약이 2일에 걸쳐 분할되는 경우, 젬시타빈은 2일차(즉, 리툭시맙 투약이 완료된 당일) 또는 다음 날에 투여된다.
혈액학적 독성이 있는 경우 사이클은 연기된다.
젬시타빈을 투여하는 방법은 El Gnaoui 외, (2007) Ann Oncol, 18:1363-1368에 설명되어 있다. 간단히 말해서, (500mL의 생리 식염수 중) 젬시타빈 1000 mg/m2을 10 mg/m2/분의 고정 투약 속도로 투여한다. 이러한 연장된 투여 일정은 표준 30분 IV 일정과 비교하여 우수한 세포내 약물 농도를 달성하는 것으로 나타났다.
D. 옥살리플라틴
옥살리플라틴 100 mg/m2를 최대 8 사이클 동안 각 21일 사이클의 2일차에 정맥내 투여한다. 옥살리플라틴은 같은 날 젬시타빈 후에 투여된다. 리툭시맙 투약이 2일에 걸쳐 분할되는 경우, 옥살리플라틴은 2일차(즉, 리툭시맙 투약이 완료된 당일) 또는 다음 날에 투여된다.
옥살리플라틴을 투여하는 방법은 로컬 처방 정보에 설명되어 있다.
E. 용량 변경
용량 변경 또는 감소는 표 2에 명시된 바와 같이 수행된다. 모든 이상 반응은 해당 사이클의 1일차에 주입 전 72시간 이내에 얻은 실험실 검사 결과에 기반한다. 증상 등급의 결정은 NCI-CTCAE v5.0에 따른다. 지지 치료를 위해, 환자는 이전 4시간 동안 투여받지 않은 경우 아세트아미노펜/파라세타몰 및 항히스타민제, 예를 들어, 디펜히드라민으로 치료받는다. IV 식염수가 지시될 수 있다. 기관지 경련, 두드러기 또는 호흡 곤란의 경우 환자는 항히스타민제, 산소, 코르티코스테로이드 (예를 들어, 100mg IV 프레드니솔론 또는 등가물) 및/또는 기관지 확장제가 필요할 수 있다. 승압제 지원이 필요한 저혈압 환자는 연구 약물을 영구적으로 중단한다. 재개시 후 주입 속도 상승에 있어서, 증상이 완전히 해소되었을 때, 중단 전에 달성된 속도의 50%로 주입을 재개한다. 주입 관련 증상이 없는 경우 주입 속도는 30분 마다 50 mg/시간의 증가분으로 상승된다.
표 2: 이상반응을 경험한 환자의 관리를 위한 지침.
F. 병용 요법
병용 요법은 연구 치료 시작 7일 전부터 연구 완료/중단 방문시까지 프로토콜-필수 치료 외에 환자가 사용한 모든 약물(예를 들어, 처방약, 일반의약품, 백신, 약초 또는 동종 요법 치료제, 영양 보조제)로 구성된다. 이러한 모든 약물이 기록된다.
환자는 연구 동안 다음 요법을 사용할 수 있다: 경구 피임약, 호르몬 대체 요법 및/또는 기타 유지 요법.
일반적으로 연구자는 로컬 표준 관행에 따라 임상적으로 제시되는 지지 요법으로 환자의 치료를 관리했다. 임상적으로 필요한 경우 성장 인자(예를 들어, 에리트로포이에틴)의 사용을 포함하여 기관 표준에 따라 연구 전반에 걸쳐 최적의 의료 관리에 필요한 지원 조치가 제공된다. 임상적으로 필요한 경우 모든 환자에 대해 항구토 요법이 시행된다. 암 치료가 목적이 아닌 한약 요법은 연구 동안 조사자의 재량에 따라 사용된다.
G. 사전투약
폴라투주맙 베도틴 전 사전투약
폴라투주맙 베도틴 주입은 리툭시맙 주입 직후에 이루어진다. 결과적으로, 모든 리툭시맙 주입 전에 사전투약이 필요하므로(아래 참조), 폴라투주맙 베도틴에 대한 추가 사전투약은 필요하지 않다.
그러나 폴라투주맙 베도틴의 투약이 지연되는 경우에는 사전투약 후에 폴라투주맙 베도틴을 투여한다. 사전투약은, 폴라투주맙 베도틴 투여 시작 전 ≥30분에 투여되는 (기관 표준 관행에 따라) 경구 아세트아미노펜 또는 파라세타몰 500-1000 mg 및 디펜하이드라민 50-100 mg으로 구성된다. 코르티코스테로이드의 투여는 담당 의사의 재량에 따라 허용되었다.
리툭시맙 전 사전투약
모든 리툭시맙 주입은 사전투약 후 환자에게 투여된다. 리툭시맙 요법 전에 다음과 같은 사전투약이 필요하다:
●
모든 주입 시작 ≥ 30분 전에 아세트아미노펜/파라세타몰(650-1000 mg)을 경구 투여한다.
●
항히스타민제, 예를 들어 디펜히드라민 (25-50 mg), 각 주입 시작 ≥ 30분 전 (금기가 아닌 경우).
고 위험의 종양 용해 증후군 환자에 대한 사전투약
높은 종양 부담을 갖고 조사자가 종양 용해의 위험이 있는 것으로 간주하는 환자는 또한 치료 시작 전에 종양 용해 예방처치를 받는다.
환자는 수분을 잘 섭취한다. 연구 치료 첫 투약 1-2일 전부터 시작하여, 대략 3 L/일의 수분 섭취를 유지하는 것이 바람직하다.
또한, 종양 부담이 크고 종양 용해의 위험이 있는 것으로 간주되는 환자는 치료의 사이클 1의 1일차 및 수분공급 전 48-72시간 전에 시작하여 300 mg/일의 알로퓨리놀 경구 또는 적절한 대체 치료제(예를 들어, 라스부리카제)로 치료받는다. 연구자가 적절하다고 판단하는 경우 환자는 각 후속 치료 사이클 전에 적절한 수분공급과 함께 반복적으로 예방처치를 계속 받는다.
감염 예방
기포포자충 및 헤르페스바이러스 감염에 대한 항감염 예방요법은 개별 환자 위험 요인에 기반하여 기관 관행 또는 연구자 선호도에 따라 구성된다. B형 간염 재활성화를 위한 예방적 항바이러스 약물이 치료의 표준인 국가에서 환자는 이러한 약물들로 치료받는다 (Flowers 외, 2013; NCCN 2017).
호중구 감소증의 예방 및 치료
각 요법 사이클에서 1차 예방요법으로서 G-CSF의 투여는 로컬/기관 지침에 따라 투여된다. G-CSF의 용량과 형태는 연구자의 재량이다. 추가 G-CSF의 사용은 조사자의 재량에 따라 호중구감소증의 치료를 위해 허용된다.
B형 간염 재활성화 모니터링 및 치료
잠재성 또는 이전 HBV 감염 (HBsAg 음성 및 B형 간염 코어 항체 [HBcAb] 양성으로 정의) 환자는 HBV DNA가 검출되지 않는 경우 본 연구에 포함된다. 이들 환자들은 연구 치료의 매 사이클의 1일차에 그리고 마지막 사이클 후 적어도 12개월 동안 실시간 PCR로 얻은 HBV DNA 수준을 가지며, 적어도 10 IU/mL의 민감도를 가지는 분석을 사용한다.
HBV-DNA 분석이 양성이 되고 세계보건기구(WHO)의 100IU/mL 컷오프를 초과하는 경우, 연구 치료가 보류되고 환자는 (리툭시맙 마지막 투약 후 적어도 1년 동안) 적절한 뉴클레오시드 유사체로 치료받으며, 관리를 위해 즉시 위장병 전문의 또는 간 전문의에게 의뢰된다. 환자는 HBV DNA 수준이 감지할 수 없는 수준으로 감소하면 연구 치료를 재개한다.
HBV DNA 검사가 양성이고 ≤ 100IU/mL인 경우 환자는 2주 이내에 재검사를 받는다. 분석 결과가 여전히 양성이면 연구 치료를 보류하고 환자를 적절한 뉴클레오시드 유사체로 치료하고(리툭시맙의 마지막 투여 후 적어도 1년 동안) 즉시 위장병 전문의 또는 간 전문의에게 진료를 의뢰한다. 환자는 HBV DNA 수준이 감지할 수 없는 수준으로 감소하면 연구 치료를 재개한다.
환자가 항바이러스제를 투여받는 동안 환자의 HBV DNA 수준이 100 IU/mL를 초과하면 연구 치료가 영구적으로 중단된다.
B형 간염 재활성화를 위한 예방적 항바이러스제가 치료의 표준인 국가의 환자는 예방적으로 치료받는다.
주의 요법
QT 연장 병력이 있거나 소인이 있는 환자, QT 간격을 연장하는 것으로 알려진 약물을 복용 중인 환자, 저칼륨혈증, 저칼슘혈증 또는 저마그네슘혈증과 같은 전해질 장애가 있는 환자의 경우 옥살리플라틴 투여에 주의가 필요하다. QT 간격은 옥살리플라틴 투여 전후에 정기적으로 면밀히 모니터된다. ECG 기록은 임상적으로 필요한 경우 특정 시점들에서 얻는다. QT 연장의 경우, 옥살리플라틴 치료를 중단한다.
강력한 CYP3A 억제제를 투여받는 환자를 폴라투주맙 베도틴 투여 시 이상반응에 대해 면밀히 모니터한다 (Han 외, (2013) J Clin Pharmacol, 53:866-77).
P-gp 억제제인 병용 약물은 면밀한 모니터링이 필요한 부작용을 유발할 수 있으므로 주의해야 한다. 환자가 P-gp 억제제 범주의 약물을 복용하는 경우 조사자는 해당 범주에 속하는 것으로 알려지거나 의심되는 약물의 사용을 평가하고 문서화한다. 강력한 P-gp 억제제를 vc-MMAE ADC (예를 들어, 폴라투주맙 베도틴)와 동시에 투여받는 환자는 이상반응에 대해 면밀히 모니터링한다.
금기 요법
이 프로토콜에서 연구 치료제, 방사선요법 또는 임의의 유형의 기타 동시 연구 제제로 정의되지 않은 다른 병용 항종양제로 치료하면 환자가 연구 치료로부터 철회된다.
● 다음과 같은 병용 요법의 사용은 하기와 같이 금지된다:
●
연구 치료 시작 전 2주 이내 및 연구 치료 기간 동안 (프로토콜-필수 연구 치료 이외의) 조사 요법은 금지된다.
●
젬시타빈, 옥살리플라틴 및 CNS 예방을 위한 척수강내 화학요법 이외의 세포독성 화학요법.
●
연구 치료제 이외의 면역요법 또는 면역억제 요법.
●
방사선 면역요법.
●
피임약 이외의 호르몬 요법, 안정한 호르몬-대체 요법 또는 메게스트롤 아세테이트.
●
림프종 치료용 생물학적 제제.
o
임상적으로 필요한 경우, 조혈 성장 인자와 같은 지지 요법인 생물학적 제제는 허용된다.
●
림프종 치료를 위한 모든 요법(척수강내 CNS 예방요법 제외).
●
방사선요법.
●
예방접종.
o
이 연구에 참여하는 환자는 리툭시맙 시작 전 적어도 28일 동안, 연구 치료 중 임의의 시점에 또는 B 세포가 회복될 때까지 생 바이러스 백신으로 1차 또는 추가 백신접종을 받을 수 없다.
이러한 제제의 사용이 필요한 환자는 연구 치료를 중단한다.
V. 연구 평가
A. 환자 및 질환 특성
임상적으로 중요한 질환, 수술, 암 이력(이전 암 요법, 이식 부적격 사유, 2016년 WHO 분류, 현재 앤아버 병기 및 절차 포함), ECOG 전신활동도 점수 및 생식 상태를 포함한 병력이 기록된다. 또한 연구 치료 시작 전 7일 이내에 환자가 사용한 모든 약물 (예를 들어, 처방약, 일반의약품, 백신, 약초 또는 동종 요법 치료제, 영양 보조제)가 기록된다.
완전한 신체 검사가 수행되고 기준선에서 확인된 모든 이상이 기록된다.
종양 평가의 일부로 신체 검사에는 림프절 비대, 간비대 및 비장 비대의 존재 및 정도에 대한 평가가 포함된다.
연구 동안, 제한된 증상-지향적 신체 검사가 수행되며 이는 주로 관련성이 있는 계통 (즉, 심혈관, 호흡기, 증상과 관련된 계통, 종양 평가와 관련된 계통 [림프절, 간 및 비장])에 제한된다. 제한된 신체 검사는 또한 감각 저하, 감각 과민, 이상감각, 감각 이상, 불편함, 작열감, 쇠약, 보행 장애, 균형 상실, 기립성 저혈압, 실신 또는 신경병증 통증을 포함한 신경병증의 증상을 모니터한다. 기준선으로부터의 이상(abnormalities) 변화가 기록된다.
활력 징후, 체중, 신장 및 BSA가 기록된다. 신장과 BSA는 스크리닝 시에만 필요하며, 마지막 BSA 평가 이후 체중에 > 10% 변화가 있는 경우 BSA를다시 계산한다. ECG 기록을 얻는다.
실험 치료 및 대조군 그룹의 비교가 수행된다. 연령, 성별, 인종/민족 및 기준선 특성(특히, 계층화 변수)과 같은 인구통계 변수는 모든 무작위배정된 환자들에 대하여 치료군 별로 요약된다. 연속 변수는 평균, 표준 편차, 중앙값, 범위 및 사분위수 범위를 사용하여 요약된다. 범주형 변수는 비율로 요약된다.
누적 연구 약물 용량, 투여량 변경/중단 및 노출 기간에 대한 기술 통계가 제공된다. ECG는 기술적으로 분석된다. 활력 징후의 변화는 연속 변수에 대한 기술 통계를 사용하여 분석된다.
다음 평가가 수행된다:
●
국제 예후 지수 (IPI): NHL 환자에서 OS를 예후하는 임상 평가 도구 (국제 비-호지킨 림프종 예후 인자 1993). 이 도구는 연령, 혈청 및 젖산 탈수소효소(LDH) 수준, ECOG 전신 활동도 점수, 암 단계 및 림프절 외 부위 침범을 비롯한 5가지 임상 요인의 측정값을 기반으로 한다.
●
동부 종양학 협력 그룹 전신활동도 (ECOG): 자신을 돌볼 수 있는 능력, 일상 활동 및 신체 능력(걷기, 일하기 등) 측면에서 환자의 기능 수준을 설명하는 임상 평가 도구 (ECOG ACRIN 암 연구 그룹 2018).
다음과 같은 실험실 검사가 수행된다:
●
혈액학: 백혈구 (WBC) 수, 적혈구 (RBC) 수, 헤모글로빈, 헤마토크릿, 혈소판 수 및 감별 검사 (호중구, 호산구, 호염기구, 단핵구 및 림프구).
●
혈청 또는 혈장 화학: 나트륨, 칼륨, 염화물, 중탄산염 (또는 CO2), 포도당, 혈액 요소 질소(BUN) 또는 요소, 크레아티닌, 총 단백질, 알부민, 인, 칼슘, 총 및 (가능한 경우) 직접 빌리루빈, 알칼리성 포스파타제, 알라닌 아미노전이효소(ALT), 아스파테이트 아미노전이효소(AST), 요산 및 젖산 탈수소효소(LDH).
●
응집: 국제 표준화 비율(INR) 또는 프로트롬빈 시간 (PT), 및 부분 트롬보플라스틴 시간 (PTT) 또는 활성화 부분 트롬보플라스틴 시간 (aPTT).
●
바이러스 혈청학: HIV; B형 간염 표면 항체(HBsAb), HBsAg 및 총 HBcAb; 환자가 HBcAb 양성인 경우 PCR에 의한 HBV-DNA; HCV 항체; 환자가 HCV 항체 양성인 경우 PCR에 의한 HCV RNA.
정상 범위를 벗어난 값을 가진 실험실 데이터는 다음과 같다. 또한 선택된 실험실 데이터 및 활력 징후의 변화를 요약한다.
B. 통계적 평가
분석 모집단은 다음과 같이 정의된다:
●
치료 의향 (ITT) 모집단: 할당된 연구 치료를 받았는지 여부에 관계없이 할당된 치료 군에 따라 그룹화된 모든 무작위배정된 환자.
●
안전성 도입 모집단: 안전성 도입기 (1단계) 동안 임의의 양의 연구 약물을 투여받는 환자.
●
안전성 모집단: 무작위배정 대조 시험 (2단계) 동안 임의의 양의 연구 약물을 투여받는 환자.
●
PRO-평가가능 모집단: PRO-평가가능 모집단에는 기준선 및 적어도 1회의 기준선 이후 평가를 한 모든 무작위배정된 환자가 포함된다. 모든 PRO 분석은 무작위배정시 할당된 치료 군을 기반으로 수행된다.
●
약동학-평가가능 모집단: PK 모집단은 적어도 1회의 연구 약물 용량을 투여받고 적어도 1회의 투약 후 농도 결과가 있는 모든 환자를 포함한다.
모든 효능 분석에서 환자는 무작위배정시 할당된 치료에 따라 그룹화된다. 모든 안전성 분석에서 환자는 실제로 받은 치료에 따라 그룹화된다.
가설 검정은 달리 명시되지 않는 한 양측이다. 본 연구의 제1종 오류(α)는 0.05(양측)이다.
C. 안전성
안전성은 NCI CTCAE v5.0, FACT/GOG-Ntx12 점수, 임상 실험실 검사 결과, 심전도(ECG) 및 활력 징후에 따른 이상 반응으로 평가된다.
안전성 평가는 중증 이상 사례 및 특정 관심대상의 이상 사례를 포함한 이상 사례 모니터링 및 보고, 안전 실험실 평가 수행, 활력 징후 측정 및 연구의 안전성 평가에 중요하다고 간주되는 기타 검사 수행으로 구성된다. 연구 약물 시작 후 모든 이상 반응은 연구 약물의 마지막 투여 후 90일 또는 NALT 시작시까지 보고된다.
안전성은 이상 반응 및 연구 치료제 노출의 요약을 통해 평가되고 치료 군 별로 제시된다.
이상 반응의 축어 설명은 맵핑된 용어, 적절한 시소러스 수준, 및 독성 등급 별로 요약되어 있다. 각 환자에 대해 동일한 이상 반응이 여러 번 발생하는 경우 보고된 최대 중증도가 요약에 사용된다.
다음 치료 관련 이상 반응은 별도로 요약된다: 연구 약물 철회를 초래하는 이상 반응, 용량 감소 또는 중단을 초래하는 이상 반응, 등급 + 3의 이상 반응, 사망을 초래하는 이상 반응, 심각한 이상 반응, 및 특정 관심 이상 반응. 또한 노출 조정 분석과 재발성 AE 분석이 적절하게 제공된다.
모든 사망 및 사망 원인이 요약되어 있다.
적절한 경우 식별된 NCI CTCAE v5.0 3등급 및 4등급 값과 함께 관련 실험실 값이 시간별로 요약된다. NCI CTCAE 등급 변화를 치료 군 별로 표로 작성한다.
연구 전반에 걸쳐 FACT/GOG-Ntx12 점수 및 NCI CTCAE v5.0으로 측정한 말초 신경병증이 요약되어 있다. 또한, 모든 환자가 사이클 2를 완료하거나 이전에 이러한 유형의 사건을 보고하는 것을 비롯하여 AE를 기반으로 한 말초 신경병증의 비율이 계산된다.
환자 보고 결과는 악화까지의 시간과 다양한 PRO 도구의 선택된 질문에 대한 기준선에서의 변화를 조사하고 요약하여 분석된다.
누적 연구 약물 용량, 투여량 변경/중단 및 노출 기간에 대한 기술 통계가 제공된다. ECG는 기술적으로 분석된다. 활력 징후의 변화는 연속 변수에 대한 기술 통계를 사용하여 분석된다.
본 연구에서 특정 관심 대상의 이상 반응은 다음과 같다:
●
말초 신경병증 ≥ 3등급.
●
Hy의 법칙에 의해 정의된, 빌리루빈 상승 또는 임상 황달과 함께 ALT 또는 AST 상승을 포함하는, 잠재적인 약물-유발 간 손상 사례. 다음은 이상 반응으로 보고된다:
o
치료시 발생하는 ALT 또는 AST > 3 x 기준선 값과 함께 총 빌리루빈 > 2 x ULN (이들 중 ≥ 35%는 직접 빌리루빈임).
o
치료시 발생하는 ALT 또는 AST > 3 x 기준선 값과 함께 임상 황달.
●
모든 등급의 종양 용해 증후군(인과성과 무관).
●
진행성 다초점 백질뇌병증.
●
Sampson의 기준에 의해 정의된 전신 과민 반응/아나필락시스 및 아나필락시스양 반응
●
두 번째 악성 종양.
기저 질환의 예상 진행 패턴과 명확하게 일치하는 사례들은 이상 사례로 보고되지 않는다. 이상 반응 보고서는 PRO 데이터에서 유래한 것이 아니다.
연구자는 각 이상 반응이 기준선 등급 또는 그 보다 우수한 등급으로 해소되거나, 이상 반응이 연구자에 의해 안정한 것으로 평가되거나, 환자가 추적관찰에서 누락되거나, 환자가 동의를 철회할 때까지 각 이상 반응을 추적관찰한다.
이상 반응 보고 기간 종료 후(연구 약물의 마지막 투여 또는 NALT 시작 후 90일로 정의됨), 원인에 관계없이 모든 사망 및 연구 약물에 대한 사전 노출과 관련이 있다고 여겨지는 중증 AE가 보고된다.
말초 신경병증의 AE가 있는 모든 환자는 가능한 악화로 인한 연구 치료 중단 후 (코스팅 현상) 그리고 그 후 해소 또는 안정화될 때까지 추적 관찰된다.
투약 중단, 용량 감소 및 용량 강도를 사용하여 내약성을 결정한다.
D. 효능
1차 효능 평가변수
이 연구의 무작위 배정 부분에 대한 주요 효능 목표는 다음 평가변수를 기반으로 재발성 또는 불응성 DLBCL 환자에서 R-GemOx와 비교한 Pola-R-GemOx의 효능을 평가하는 것이다:
●
전체 생존 (OS), 무작위배정시부터 연구 중 임의의 원인으로 인한 사망시까지의 시간으로 정의됨.
ITT 모집단에 대한 1차 효능 분석이 완료되며, 환자는 무작위배정으로 할당된 치료에 따라 그룹화된다. 사망하지 않은 환자에 대한 데이터는 환자가 마지막으로 생존한 것으로 알려진 날짜에 중도절단된다. 그렇지 않으면 데이터는 무작위배정일 + 1일에 중도절단된다.
카플란-마이어 방법론을 사용하여 각 치료 부문의 OS 중앙값을 추정하고 카플란-마이어 곡선을 생성한다. 치료 군들 간 OS를 계층화된 로그 순위 검정으로 비교한다. 사망에 대한 위험비(HR)는 계층화된 Cox 비례 위험 모델을 사용하여 추정된다. 계층화 요인은 상기 기재한 바와 같이 IxRS 별 무작위배정 계층화 요인과 동일하다. HR에 95% 신뢰 구간 (CI)이 제공된다. Brookmeyer-Crowley 방법론은 각 치료군의 OS 중앙값에 대한 95% CI를 구성하는 데 사용된다.
본 연구의 제1종 오류(α)는 0.05(양측)이다.
환자가 HSCT에 적격이되어 이식 (최적의 이익)을 받는 경우, 이것이 미칠 수 있는 영향을 평가하기 위해 OS 및 PFS에 대한 민감도 분석이 수행된다. 이를 위해 이식 시 환자 데이터가 중도절단된다.
2차 효능 평가변수
다음 섹션에서는 연구의 무작위배정 부분(2단계)의 2차 평가변수에 대한 분석을 자세히 설명한다. 안전성 도입 단계(1단계)에 대해 유사한 분석이 수행되지만 기술 통계에 제한된다.
PET-CT 및 CT 스캔은 스크리닝시, 치료 중 및 치료 후 임상적으로 지시된 바에 따라, 연구 약물의 마지막 투약 후 28 일, 그 후 추적기간 중 최대 2년 동안 2 (PET-CT) 및 6 (CT) 개월 마다 얻는다.
양측 0.05 유의 수준에서 전체 제1종 오류율을 제어하기 위해, 계층적 검사 절차를 사용하여 1차 및 주요 2차 효능 평가변수의 다중 통계 검정을 조정한다. 주요 2차 평가변수는 다음 순서로 검정된다:
●
PFS.
●
치료 종료시 완전 반응율 (CRR) (PET-CT 데이터를 포함한 반응에 기반).
●
치료 종료시 객관적 반응율 (ORR) (PET-CT 데이터를 포함한 반응에 기반).
주어진 가설은 모든 이전 가설이 양측 유의 수준 0.05에서 기각되었을 때에만 기각된다.
다중도 조정은 기타 평가변수의 검정에 있어서는 수행되지 않으며 주의하여 해석된다.
반응은 신체 검사 및 치료 종료 시 Lugano 2014 반응 기준을 사용한 PET-CT 스캔을 기반으로 평가된다. 종양 평가는 스크리닝, 치료 중간 (사이클 4, 15일차부터 사이클 5, 1일차까지) 및 치료 종료 시에 이루어진다. 초기 및 치료 종료 평가에는 PET가 포함된다. CT 스캔은 장기 추적 관찰에서 또는 연구 종료시까지 2년 동안 6개월마다 완료된다. 종양 평가에 사용된 모든 1차 영상 데이터가 수집된다.
PET-CT 스캔에는 두개골 기저부에서 허벅지 중간까지 포함된다. 전신 PET-CT 스캔은 임상적으로 적절할 때 수행된다. 이미지 향상 시스템(예를 들어, GE Healthcare의 Q.Clear 또는 이와 유사한 것)은 사용되지 않는다. IV 조영제를 사용한 CT 스캔에는 흉부, 복부 및 골반 스캔이 포함된다; 임상적으로 필요한 경우 목의 CT 스캔이 포함된다. 반응 평가를 위한 CT 스캔은 로컬 규제 당국에서 요구하는 경우에만 사전 관련 영역에 제한된다. 진행성 질환이 의심되는 경우 조사자의 재량에 따라 언제든지 CT 스캔을 반복한다. 방사선 사진 평가를 포함한 전체 종양 평가는 질환 진행 또는 재발이 의심될 때마다 수행된다. PET-CT는 스크리닝 및 치료 종료 평가에서 필수이다.
ET-CT에서 골 신호가 음성인 환자에서 골수 생검이 수행된다.
조영제가 금기인 환자(예를 들어, 조영제 알레르기 또는 신장 청소율 장애가 있는 환자)의 경우 연구 치료 기간 동안 표적 병변을 일관되고 정확하게 측정할 수 있는 한 조영제 없이 CT 또는 PET-CT 조합 스캔이 허용된다.
후속 요법(예를 들어, CAR-T 요법 또는 자가 줄기 세포 이식)이 필요한 PR 또는 CR 반응이 있는 환자는 연구를 계속하고 평가할 수 있다.
완전 반응율
완전 반응율 (CRR)은 치료 종료시 Lugano 2014 반응 기준에 따라 (PET-CT 데이터를 비롯한 반응에 기반하여) 완전한 대사 반응이 있는 환자들의 비율로 정의된다. 기준선 이후 종양 평가가 없는 환자를 포함하여 이들 기준을 충족하지 않는 환자는 무반응자로 간주된다.
CRR은 ITT 모집단을 사용하여 분석된다.
CRR의 추정치는 각 치료군에 대해 계산되며, 이의 95% 신회 구간 (CI)은 Cloper-Pearson 방법을 사용하여 계산된다. 치료 군들 간의 CRR 차이가 계산되며, 이의 95% CI는 이상 분포에 대한 정규 근사치를 사용하여 계산된다. 계층화된 Cochran-Mantel-Haenszel 검사를 사용하여 두 치료군 간의 CRR을 비교한다. 계층화 요인은 1차 평가변수 OS 분석에 대해 설명한 것과 동일하다.
PET 데이터를 포함하지 않는 반응을 사용하여 CRR에 대해 동일한 분석을 반복하므로 완전 대사 반응 대신 완전 반응을 갖는 환자를 고려한다.
객관적 반응율
객관적 반응은 치료 종료시 Lugano 2014 반응 기준에 따라 (PET-CT 데이터를 포함한 반응에 기반한) 완전 또는 부분 대사 반응으로 정의된다. 기준선 이후 종양 평가가 없는 환자를 포함하여 이들 기준을 충족하지 않는 환자는 무반응자로 간주된다.
ORR은 객관적인 반응을 보이는 환자의 비율로 정의된다.
ORR은 ITT 모집단을 사용하여 분석된다.
ORR의 추정치가 각 치료군에 대해 계산되고 95% CI는 Cloper-Pearson 방법을 사용하여 계산된다. 치료 군들 간의 ORR 차이가 계산되며, 이의 95% CI는 이상 분포에 대한 정규 근사치를 사용하여 계산된다. 계층화된 Cochran-Mantel-Haenszel 검사를 사용하여 두 치료군 간의 ORR을 비교한다. 계층화 요인은 1차 평가변수 OS 분석에 대해 설명한 것과 동일하다.
PET 데이터를 포함하지 않는 반응을 사용하여 ORR에 대해 동일한 분석을 반복한 다음, 객관적 반응(PET 데이터를 포함하지 않는 반응에 기반)은 치료 종료 시 완전 또는 부분 반응(PET 데이터를 포함하지 않는 반응에 기반)으로 정의된다.
최적의 전체 반응
최적의 전체 반응 (BOR)은 Lugano 2014 반응 기준에 따라 (PET-CT 또는 CT 데이터를 포함하는 반응에 기반하여) 연구 중 최적의 반응으로 정의된다.
BOR은 ITT 모집단을 사용하여 분석된다.
BOR 비율의 추정치가 각 치료군에 대해 계산되고 95% CI는 Cloper-Pearson 방법을 사용하여 계산된다.
무진행 생존
무진행 생존 (PFS)은 무작위배정시부터 질환 진행의 첫 발생 또는 임의의 원인으로 인한 사망시 (둘 중 먼저 발생하는 것)까지의 시간으로 정의된다. 보고된 질환 진행 없이 사망한 환자는 사망 일자에 사건으로 간주된다. 분석 시점(임상시험 마감)에 진행되지도 않고 사망하지도 않은 환자 및 추적 관찰에 실패한 환자는 마지막 평가가능한 종양 평가 일자에 중도절단된다. 기준선 후 종양 평가를 받지 않은 환자는 무작위배정 시점 +1일차에 중도절단된다. 카플란-마이어 추정치 및 중앙값, 25번째 및 75번째 백분위수의 관련 95% CI가 표시된다. 카플란-마이어 곡선은 치료 군들 전반의 차이에 관한 시각적 설명을 제공한다. 치료 효과의 추정치는 95% 신뢰 한계 포함하는 계층화된 Cox 비례 위험 분석을 사용하여 위험 비율로 표현된다.
반응 기간
반응 기간(DOR)은 Lugano 2014 반응 기준을 사용하여 객관적인 반응을 보이는 환자에서 평가된다. DOR은 완전 또는 부분 반응 (둘 중 먼저 기록된 상태)의 최초 발생 일자부터 진행성 질환 또는 사망이 기록된 최초 일자 중 먼저 발생하는 날짜까지의 시간 간격으로 정의된다. 분석시 질환진행이 없었고 사망하지 않은 환자는 마지막 종양 평가일에 중도절단된다. 완전 또는 부분 반응이 처음 발생한 일자 이후에 종양 평가가 수행되지 않으면 DOR은 완전 또는 부분 반응이 처음 발생한 일자 +1일차에 중도절단된다. DOR은 무작위배정되지 않은 환자 하위집합 (특히 객관적인 반응을 달성한 환자)을 기반으로 하므로, 치료군 간의 비교는 설명을 위해 이루어진다. 분석이 계층화되지 않는다는 점을 제외하고, PFS 분석에 대해 자세히 설명된 방법을 DOR 분석에 사용한다.
무사건 생존
무사건 생존 (EFSeff)은 무작위배정시부터 다음 사례들의 최초 발생시까지의 시간으로 정의된다:
●
질환 진행 또는 재발.
●
임의의 원인으로 인한 사망.
●
NALT 개시.
EFSeff 사건이 없는 환자들은 마지막 평가가능한 종양 평가시에 중도절단된다. 기준선 후 종양 평가를 받지 않은 환자는 무작위배정 시점에 중도절단된다. PFS 분석에 대해 자세히 설명된 방법론을 EFSeff 분석에 사용한다.
E. 환자 보고 결과
치료 효과를 평가하고 폴라투주맙 베도틴의 안전성 프로파일을 보다 완전히 특성화하기 위해 환자 보고 결과 (PRO) 도구가 완성되었다. 또한 PRO 도구를 사용하면 폴라투주맙 베도틴에 대한 각 환자의 직접적인 경험을 포착할 수 있다.
PRO 평가가능 모집단은 달리 명시되지 않는 한 방문 요약 및 기준선에서의 변화, 응답자 분석 및 혼합 효과 모델 반복 측정(MMRM) 모델링에 대한 기술적 분석에 사용된다. ITT 모집단은 완료 분석 및 악화 시간 분석에 사용된다.
PRO 데이터는 다음 도구를 사용하여 수집된다: FACT/GOG-Ntx12, EQ-5D-5L, EORTC QLQ-C30 및 FACT/Lym.
FACT/GOG-Ntx12
FACT/GOG-Ntx12는 화학 요법으로 유발된 말초 신경병증을 측정하기 위해 설계된 12개 문항의 환자 보고 결과 도구이다 (Kopec 외, (2006) J Supportive Oncol, 4:W1-W8). FACT/GOG-Ntx 점수는 1단계 (안전성 도입) 및 2단계 (RCT) 동안을 포함하여 시험 전반에 걸쳐 보고된다. FACT/GOG-Ntx-12 설문지 척도 각각에 대해 각 방문 시 기술 통계 및 기준선으로부터의 변화가 치료 군 별로 보고된다. 설문지 내 누락된 문항의 경우 개발자 지침에 따라 일할 점수가 계산된다 (Calhoun 외, (2003) Int J Gynecol Cancer, 13:741-748). PRO 완료율은 치료 군 별로 각 시점에서 요약된다. 신경독성 하위척도의 경우, 각 방문 시 기술 통계 및 기준선으로부터의 변화는 안전성 도입 모집단에 대해 보고된다.
EQ-5D-5L
EuroQol 5-차원 설문지, [5-수준 버전 (EQ-5D-5L])는 검증된 자가 보고 건강 상태 설문지로서, 5차원을 통해 건강 상태 효용 점수를 계산하는 데 사용된다 (EuroQol (1990) Health Policy, 16:199-208; Brooks (1996) Health Policy, 37:53-72; Herdman 외, (2011) 20:1727-1736; Janssen 외, (2013) Qual Life Res, 22:1717-1727). 5가지 차원은 모두 환자의 건강 상태를 설명하는 5자리 숫자로 조합될 수 있다. 이러한 기술적 숫자는 게시된 가중치를 사용하여 단일 요약 지수 효용 점수로 변환된다. 본 연구에서, 영국의 크로스웍 수치 세트 (crosswalk value set) (EuroQol Research Foundation at http://www(dot)euroqol(dot)org/about-eq-5d/valuation-of-eq-5d에 EuroQol Research Foundation이 게시; Devlin 외, (2017) Health Economics, 1-16)가 사용된다. 또한, 설문지의 두번째 부분에서는, 현재의 건강 상태를 0 내지 100 범위 값의 시각 아날로그 척도 (VAS)로 측정한다.
시간 경과에 따른 각 EQ-5D-5L 평가의 경우, 각 설문에 대하여 각각 5개 범주의 환자들의 수 및 백분율을 평가한다. 각 방문 시 EQ-5D-5L 지수 효용 점수 및 기준선으로부터의 관련 변화에 대한 요약을 치료 군 별로 제공한다. EuroQoL 시각 아날로그 척도 (EQ-VAS)에 대해 유사한 분석을 수행한다.
지수 효용 점수와 VAS는 혼합 선형 모델로 분석된다. 또한 EQ-5D-5L 지수 및 EQ-VAS 점수에서 임상적으로 의미 있는 임계값을 초과하는 변화를 보고한 환자의 비율이 보고된다. 임상적으로 의미 있는 개선 임계값은 + 0.07점의 지수 효용 점수, +7점의 VAS 점수 변화로 정의된다.
EORTC QLQ-C30
EORTC QLQ-C30은 검증되고 신뢰할 수 있는 자가 보고 측정이다 (Aaronson 외, (1993) J Natl Cancer Inst, 85:365-376; Fitzsimmons 외, (1999) 35:939-941). 이는 지난 주차의 리콜 기간에 있어서 환자 기능의 5가지 측면(신체적, 정서적, 역할, 인지적, 사회적), 3가지 증상 척도(피로, 메스꺼움 및 구토, 통증), 전반적인 건강/삶의 질, 6개의 단일 문항(호흡곤란, 불면증, 식욕 상실, 변비, 설사, 금전적 어려움)을 평가하는 30개 설문으로 구성된다.
EORTC QLQ-C30 설문지의 경우, 모든 항목 및 하위 척도에 대해 각 방문 시 요약 통계 및 선형 변환 점수 기준선으로부터의 변화가 보고된다.
악화까지의 시간은 무작위배정 시로부터 기준선에서 EORTC QLQ-C30 신체 기능 척도의 10점 감소가 처음 기록될 때까지의 시간으로 정의된다. 피로의 경우 악화까지의 시간은 무작위배정 시로부터 기준선에서 10점 증가가 처음 기록될 때까지의 시간으로 정의된다. 임상 데이터 마감 시점에 악화가 관찰되지 않은 환자는 기준선 이후 평가의 경우 누락되지 않은 마지막 평가 일자에, 기준선 이후 평가가 없는 경우 무작위 배정일 + 1일차에 중도절단된다. 악화까지의 시간에 대한 위험비는 계층화된 Cox 비례 위험 모델을 사용하여 추정된다. 위험비에 대해 95% CI가 제공된다. 카플란-마이어 방법론을 사용하여 각 치료 군의 악화까지의 시간 중앙값을 추정하고 카플란-마이어 곡선을 생성한다.
EORTC QLQ-C30 데이터를 EORTC 채점 매뉴얼에 따라 채점한다 (Fayers 외, (2001) 유럽 암 연구 및 치료 기구, 브뤼셀). 누락된 데이터는 시점 별로 평가 및 보고된다. 데이터가 불완전한 경우, 모든 설문지 하위 척도에 대해, 구성 문항들의 50% 이상이 완료된 경우, 채점 매뉴얼 및 게시된 검증 보고서에 따라 일할 점수가 계산된다. 문항들의 50% 미만이 완료된 하위척도의 경우, 하위척도는 누락된 것으로 간주된다. 완료율은 각 시점에서 EORTC QLQ-C30을 완료할 것으로 예상되는 환자의 수와 비율로 요약된다.
FACT-Lym
FACT-Lym은 특히 림프종 환자에게 사용되는 검증된 건강 관련 삶의 질 (HRQoL) 도구이다. 이는 FACT-일반 설문 (FACT-G), 및 림프종-특이적 하위척도 (FACT-Lym LYMS; 0-60 범위)로 구성된다 (Cella 외, (1993) J Clin ONcol, 11:570-579; Cella 외, (2005) Blood, 106:750). 세 가지 요약 척도, FACT-Lym 시험 결과 지수, FACT-G 및 FACT-Lym 총점을 계산한다. 점수가 높을 수록 보다 우수한 HRQoL을 반영한다.
FACT-Lym 설문지 척도 각각에 대해 각 방문 시 기술 통계 및 기준선으로부터의 변화가 치료 군 별로 보고된다.
개별 하위척도 및 FACT-Lym TOT 수준에서 임상적으로 의미 있는 최소한으로 중요한 차이(즉, 환자에게 중요한 것으로 간주되는 가장 작은 변화량)가 사전에 지정되고 이를 이용하여 치료 결과로서 FACT-Lym LYMS (≥ 3 점), FACT-Lym TOI (≥ 6 점), 및 FACT-Lym TOT (≥ 7 점) 척도에서 의미있는 변화를 보고하는 환자들의 비율을 정의한다 (Carter 외, (2008) Blood, 112:2376).
악화까지의 시간은 무작위 배정시부터 기준선에서 + 3-점 감소가 처음 기록될 때까지의 시간으로 정의된다 (Carter 외, (2008) Blood, 112: 2376; Hlubocky 외, (2013) Lymphoma, ID147176). 임상 데이터 마감 시점에 악화가 관찰되지 않은 환자는 기준선 이후 평가의 경우 누락되지 않은 마지막 평가 일자에, 기준선 이후 평가가 없는 경우 무작위 배정일자 + 1일차에 중도절단된다. 악화까지의 시간에 대한 위험비는 계층화된 Cox 비례 위험 모델을 사용하여 추정된다. 위험비에 대해 95% CI가 제공된다. 카플란-마이어 방법론을 사용하여 각 치료 군의 악화까지의 시간 중앙값을 추정하고 카플란-마이어 곡선을 생성한다. 보충 문항-수준 분석은 FACT-Lym LYMS의 개별 B-증상 문항들로 원시 1-점 악화를 사용하여 수행된다. 설문지 내 누락된 문항의 경우 개발자 지침에 따라 일할 점수가 계산된다 (Webster 외, (2003) Health Qual Life Outcomes, 1:79). PRO 완료율은 치료 군 별로 각 시점에서 요약된다.
F. 약동학 분석
1단계 및 2단계 동안 혈액 샘플에 대해 폴라투주맙 베도틴의 PK 분석이 수행된다. 혈청 폴라투주맙 베도틴 총 항체 (DAR 0 및 DAR ≥ 1을 포함한 모든 약물 대 항체 비율[DAR] 종 포함), 혈장 폴라투주맙 베도틴 접합체(acMMAE로 평가됨) 및 혈장 비접합 MMAE 농도는 검증된 방법을 사용하여 정량화된다. 샘플은 또한 다른 잠재적인 이화 산물에 대해 분석된다.
폴라투주맙 베도틴, 젬시타빈 및 옥살리플라틴 대 시간 데이터의 개별 및 평균 혈청 및 혈장 농도를 표로 작성하고 플롯한다. 농도 데이터의 요약 통계는 각 분석물에 대한 각 샘플링시 계산된다. (수집된 데이터에 대해 적절하게) PK 매개변수, 최대 농도 (Cmax), 최저 농도 (Ctrough)가 추정된다. 이러한 매개변수에 대한 추정치를 표로 작성하고 요약한다 (평균 및 SD). PK 매개변수는 사용 가능한 데이터를 기반으로 적절한 기술을 사용하여 결정된다. PK 매개변수 추정에는 모집단 PK 분석 방법이 적용된다. 잠재적인 약물 상호작용은 현재 연구의 PK를 과거 데이터와 비교하여 평가한다. PK 변동성과 인구통계학적 및 병태생리학적 공변량 사이의 잠재적 상관관계는 모집단 PK 분석에 의해 조사된다. PK 변동성과 약력학, 효능 및 안전성 결과 간의 잠재적 상관관계는 탐색적 그래픽 분석 및 PK-약력학 모델링에 의해 조사된다.
G. 면역원성 분석
1단계 및 2단계 동안 검증된 항체-가교 ELISA를 사용하여 환자 혈청 샘플에서 항-폴라투주맙 베도틴 항체의 존재를 스크리닝 및 확인하고 확인된 ADA-양성 샘플의 역가를 특성화하고 결정한다.
면역원성 분석 모집단은 적어도 1개의 평가가능한 기준선 이후 ADA 샘플과 함께 적어도 1회 용량의 폴라투주맙 베도틴을 투여받은 모든 환자로 구성된다. 환자는 받은 치료에 따라, 또는 연구 중단 전에 치료를 받지 않은 경우 할당된 치료에 따라 그룹화된다.
기준선에서 (기준선 유병률) 및 기준선 이후에서 (기준선 이후 발생율) ADA-양성 및 ADA-음성 환자의 수 및 비율을 치료 그룹 별로 요약한다. 기준선 이후 발생율을 결정할 때, 환자가 기준선에서 ADA 음성이거나 데이터가 누락되었지만 연구 약물 노출 후 ADA에 대해 양성인 경우 (치료 유도 ADA 반응); 또는 기준선에서 ADA 양성이고 하나 이상의 기준선 이후 샘플의 역가가 기준선 샘플의 역가보다 0.60 역가 단위 이상 큰 경우 (치료 강화 ADA 반응), 환자는 ADA 양성인 것으로 간주된다. 환자가 기준선에서 ADA 음성이거나 데이터가 누락되었고 기준선 이후의 모든 샘플들이 음성인 경우, 또는 기준선에서 ADA 양성이지만 역가가 기준선 샘플의 역가보다 0.60 역가 단위 이상 큰 기준선 이후 샘플들을 가지지 않는 경우 (치료에 영향받지 않음), 환자는 ADA 음성으로 간주된다.
ADA 상태와 안전성, 효능, PK 및 바이오마커 결과변수 간의 관계는 표준 언어 및/또는 용어를 사용하여 분석 및 보고된다.
H. 바이오마커 분석
생물표지자2단계에서는 종양 조직 및 혈장 샘플에 대한 바이오마커 테스트 분석이 수행된다.
비침습적 단순 혈장 수집을 통해 순환 종양 DNA(ctDNA)를 평가할 수 있으며, 이는 종양 세포의 세포자멸사 잔해에서 유래하는 것으로 여겨진다. ctDNA를 정량하고 게놈 돌연변이에 대해 평가한다. 기준선에서 이 정보를 예후 및 치료 효과 평가를 위한 임상 효능과 연관시키는 것 외에도 이 정보는 분자 수준에서 잔류 질환을 모니터링하고 클론 진화를 추적할 수 있다.
종양생물학과 관련된 바이오마커들 및 폴라투주맙 베도틴 및 리툭시맙의 작용기전에 대한 분석을 수행한다.
분석은 후보 바이오마커의 예후 및/또는 예측 가치를 평가한다. 후보 바이오마커와 OS, PFS 및 PET-CT CR 비율 사이의 연관성, 및 치료에 따른 및 치료와 무관한, 효능 및 안전성에 대한 기타 척도를 각각 잠재적 예측 및 예후 가치를 평가하기 위해 조사한다. 효능에 대한 DLBCL 하위유형(즉, COO) 및 돌연변이 프로파일을 포함한 기준선 예후 특성의 효과는 단변량 및/또는 다변량 통계 방법을 사용하여 평가된다.
현재까지 가장 잘 확립된 DLBCL 바이오마커 서브세트는 B 세포 기원 종양의 발달 단계 또는 기원 세포(COO)와 일치하는` 분자적으로 정의된 프로파일, 즉, 활성화 B-세포-유사 (ABC) 프로파일, 배 중심 B-세포-유사 (GCB) 또는 미분류 프로파일, BCL2/MYC 이중 발현자 프로파일 (MYC 및 BCL2 모두의 발현 증가를 특징으로 함), 및 BCL2/MYC 이중-적중 프로파일 (BCL2 및 MYC 모두에서의 전위)이다. WHO 분류의 최근 개정판에서 새로운 분자 하위 그룹인, MYC 및 BCL2 및/또는 BCL6 재배열이 있는 고도 B세포 림프종 (HGBL DH/TH)이 정의되었다 (Swerdlow 외, (2016) Blood, 127:2375-2390). 보다 최근에, 별개의 유전형, 후성유전학 및 임상 특징을 갖는 전술한 범주를 초월하는 분자 하위유형이 확인되었다. 예에는 Schmitz 외, (2018) N Engl J Med, 378:1396-1407에 의해 설명된 4가지 유전자 하위유형과, Chapuy 외, (2018) Nat Med, 24:679-690에 의해 설명된 5가지 DLBCL 하위집합이 포함된다.
이 연구의 바이오마커에는 위에서 논의한 바이오마커, 폴라투주맙 베도틴 표적(CD79b), 차세대 시퀀싱(NGS)에 의한 종양 돌연변이 프로파일링, 및 DLBCL에서 확립된 예후 바이오마커들 (기원 세포, BCL2/MYC 이중 발현 및 BCL2/MYC 이중-전위)이 포함되나 이에 제한되는 것은 아니다. 예시적인 탐색적 바이오마커들을 표 3에 요약하여 제공한다.
표 3: 후향적 탐색 연구를 위한 바이오마커(2단계).
ctDNA = 순환 종양 DNA; IHC = 면역조직화학; NGS = 차세대 시퀀싱.
하위그룹 분석
인구통계학 및 관련 기준선 특성에 의해 정의된 하위그룹에서 치료-유익 연구 결과의 일관성을 평가하기 위해 이러한 하위그룹의 OS 및 PFS를 평가한다.
치료 이익의 일관성을 계층화된 Cox 비례 위험 모델을 사용하여 평가하고 95% CI로 위험비가 추정된다. 숲 도표를 사용하여 결과를 요약한다.
중간 안전성 분석
FACT/GOG-Ntx12 검사를 비롯한, 안전성 데이터에 대한 여러 중간 분석이 수행된다. 안전성 도입 (1단계) 동안, 안전성 데이터는 적어도 3번 분석된다. RCT 단계 동안, 안전성 데이터는 각 치료 군에서 처음 10명과 20명의 환자가 무작위배정된 후 분석된다; RCT 단계 동안 후속 중간 분석의 빈도는 2차 중간 분석에서 ≥ 3등급 말초 신경병증 사건의 수에 따라 달라진다. 이러한 중간 안전성 분석은 필요한 경우 연구 치료를 완료할 때까지 모집된 모든 환자를 평가한다.