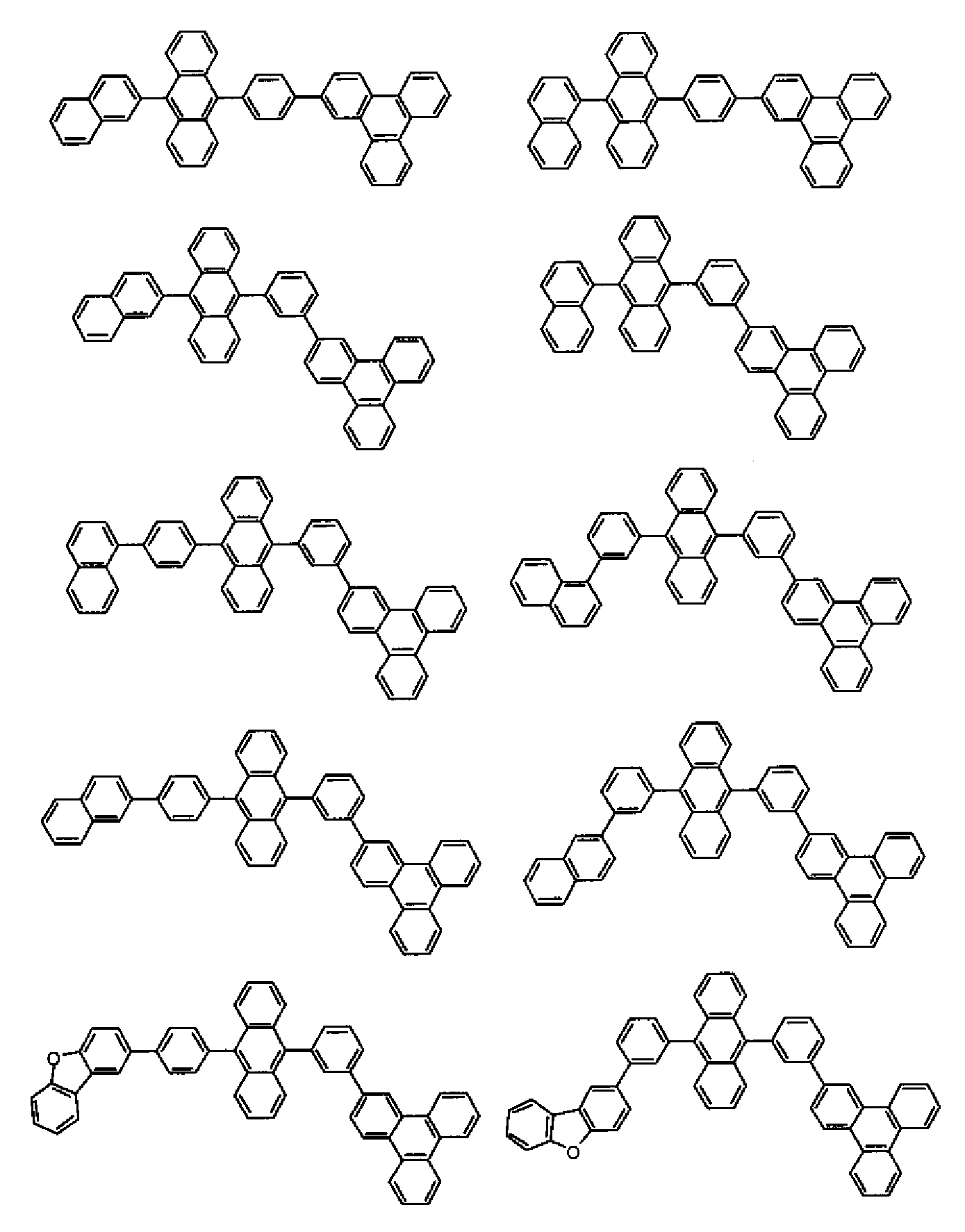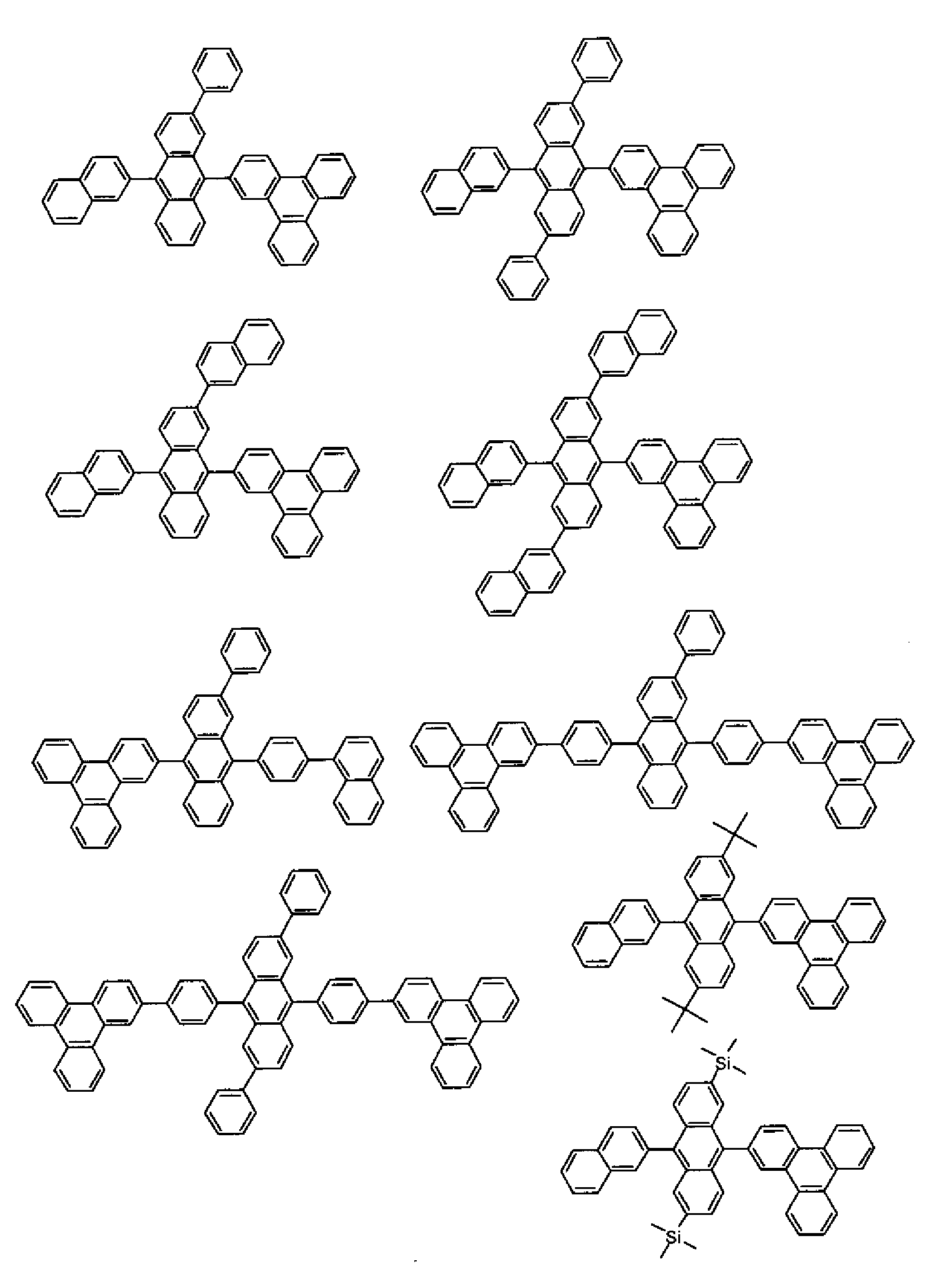KR20100090269A - 축합 방향족 유도체 및 이것을 사용한 유기 전계 발광 소자 - Google Patents
축합 방향족 유도체 및 이것을 사용한 유기 전계 발광 소자 Download PDFInfo
- Publication number
- KR20100090269A KR20100090269A KR1020107011034A KR20107011034A KR20100090269A KR 20100090269 A KR20100090269 A KR 20100090269A KR 1020107011034 A KR1020107011034 A KR 1020107011034A KR 20107011034 A KR20107011034 A KR 20107011034A KR 20100090269 A KR20100090269 A KR 20100090269A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- formula
- unsubstituted
- condensed aromatic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 C(C1)C=Cc2c1c1cc(-c3cccc(-c4c(cccc5)c5c(-c5cccc(-c6cc*(c(C=CCC7)c7c7c8cccc7)c8c6)c5)c5c4cccc5)c3)ccc1[o]2 Chemical compound C(C1)C=Cc2c1c1cc(-c3cccc(-c4c(cccc5)c5c(-c5cccc(-c6cc*(c(C=CCC7)c7c7c8cccc7)c8c6)c5)c5c4cccc5)c3)ccc1[o]2 0.000 description 5
- MWPLVEDNUUSJAV-UHFFFAOYSA-N c1cc2cc(cccc3)c3cc2cc1 Chemical compound c1cc2cc(cccc3)c3cc2cc1 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 1
- NKGZKFFMGSACJZ-UHFFFAOYSA-N c1ccc2[o]c(ccc(-c(cc3)ccc3-c3c(cccc4)c4c(-c4cc(-c5ccc(c6ccccc6c6c7cccc6)c7c5)ccc4)c4c3cccc4)c3)c3c2c1 Chemical compound c1ccc2[o]c(ccc(-c(cc3)ccc3-c3c(cccc4)c4c(-c4cc(-c5ccc(c6ccccc6c6c7cccc6)c7c5)ccc4)c4c3cccc4)c3)c3c2c1 NKGZKFFMGSACJZ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
- C07C15/20—Polycyclic condensed hydrocarbons
- C07C15/38—Polycyclic condensed hydrocarbons containing four rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/0805—Compounds with Si-C or Si-Si linkages comprising only Si, C or H atoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B1/00—Dyes with anthracene nucleus not condensed with any other ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
- C09B57/001—Pyrene dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/22—Ortho- or ortho- and peri-condensed systems containing three rings containing only six-membered rings
- C07C2603/24—Anthracenes; Hydrogenated anthracenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/22—Ortho- or ortho- and peri-condensed systems containing three rings containing only six-membered rings
- C07C2603/26—Phenanthrenes; Hydrogenated phenanthrenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/40—Ortho- or ortho- and peri-condensed systems containing four condensed rings
- C07C2603/42—Ortho- or ortho- and peri-condensed systems containing four condensed rings containing only six-membered rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Furan Compounds (AREA)
Abstract
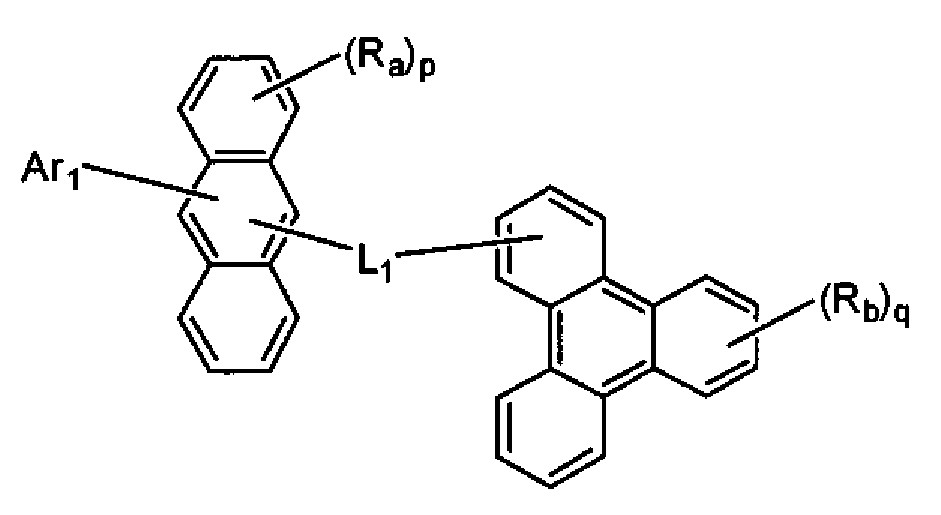
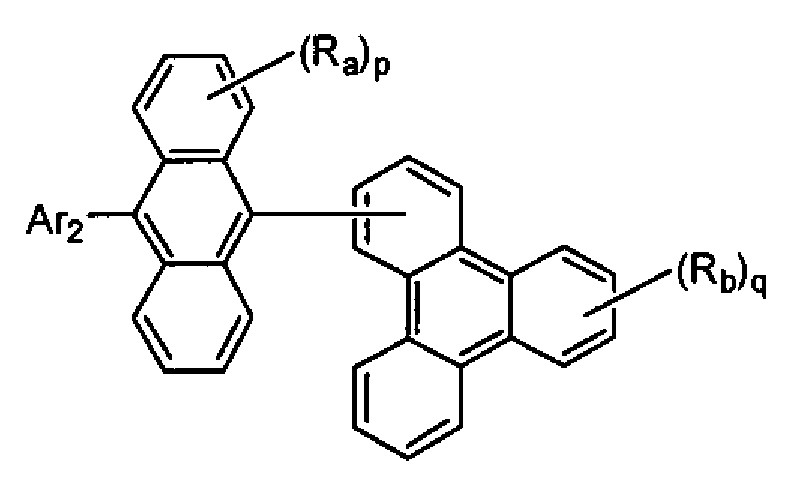
<화학식 1>
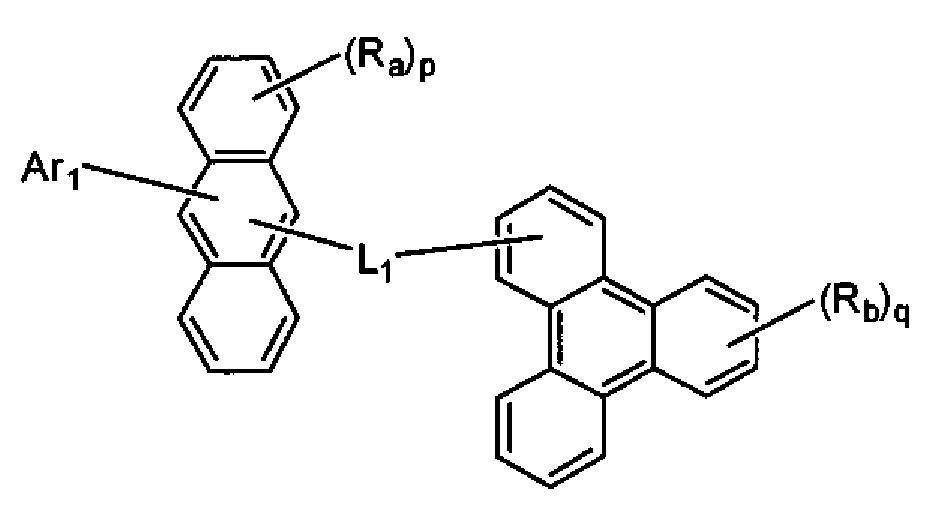
(화학식 1에서, Ra 및 Rb는 각각 수소 원자 또는 치환기를 나타내고, p는 1 내지 8의 정수, q는 1 내지 11의 정수를 나타내고, p 및 q가 2 이상인 경우, Ra 및 Rb는 각각 동일하거나 상이할 수 있고, Ra는 인접하는 치환기끼리 환을 형성할 수도 있고, L1은 단결합, 또는 치환 또는 비치환된 2가의 연결기를 나타내고, Ar1은 치환 또는 비치환된 핵탄소수 6 내지 50의 아릴기, 또는 치환 또는 비치환된 핵원자수 5 내지 50의 헤테로아릴기를 나타내되, 단 L1이 단결합이며, Ra 중 적어도 하나가 수소 원자가 아닌 경우, Ar1은 트리페닐레닐기가 아니고, L1 및 Ar1의 치환기, 및 Ra 및 Rb는 아미노기를 포함하지 않음)
Description
Claims (18)
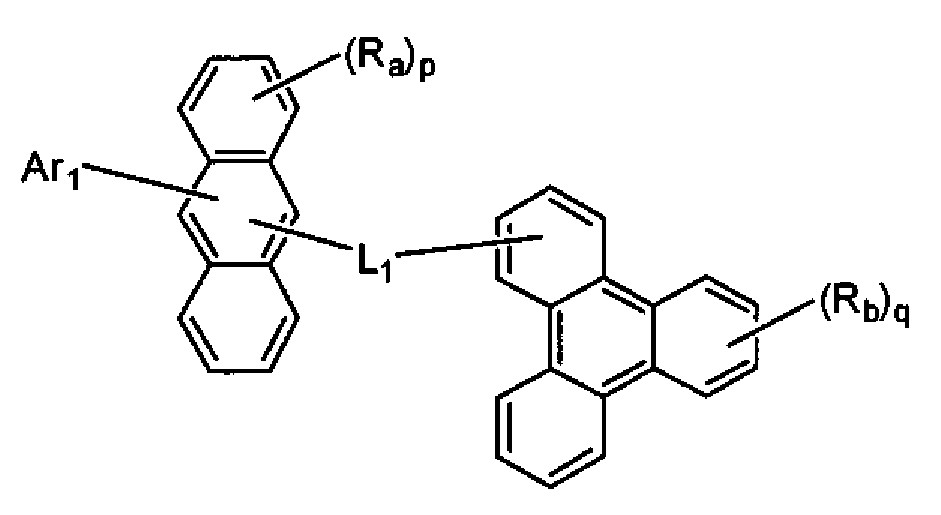
- 하기 화학식 1로 표시되는 축합 방향족 유도체.
<화학식 1>
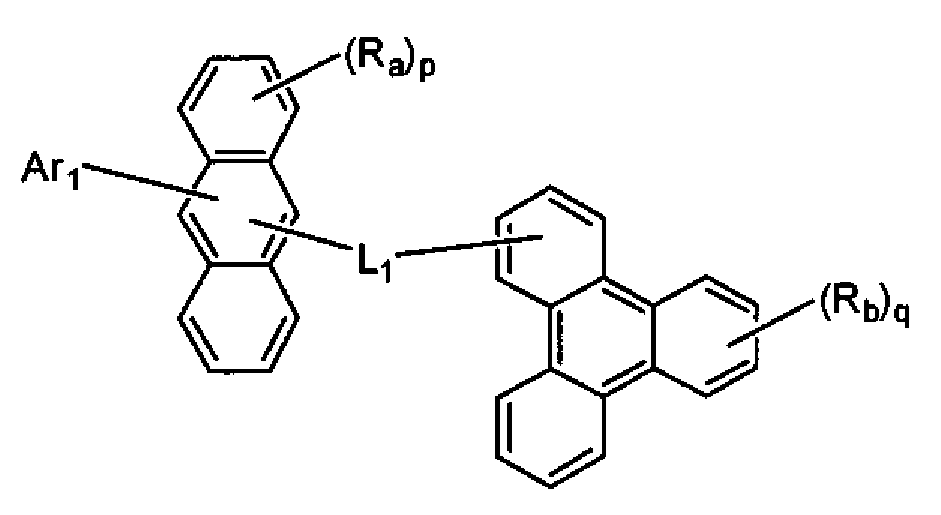
(화학식 1에서, Ra 및 Rb는 각각 수소 원자 또는 치환기를 나타내고, p는 1 내지 8의 정수, q는 1 내지 11의 정수를 나타내며, p 또는 q가 2 이상인 경우, Ra 또는 Rb는 각각 동일하거나 상이할 수 있고, Ra는 인접하는 치환기끼리 환을 형성할 수도 있고, L1은 단결합, 또는 치환 또는 비치환된 2가의 연결기를 나타내고, Ar1은 치환 또는 비치환된 핵탄소수 6 내지 50의 아릴기, 또는 치환 또는 비치환된 핵원자수 5 내지 50의 헤테로아릴기를 나타내되, 단 트리페닐렌기가 안트라센 골격의 9 위치 또는 10 위치에 결합하고 있고, L1이 단결합이며, Ra 중 적어도 하나가 수소 원자가 아닌 경우, Ar1은 트리페닐레닐기가 아니고, L1 및 Ar1의 치환기, 및 Ra 및 Rb는 아미노기를 포함하지 않음) - 제1항에 있어서, 하기 화학식 1로 표시되는 축합 방향족 유도체.
<화학식 1>
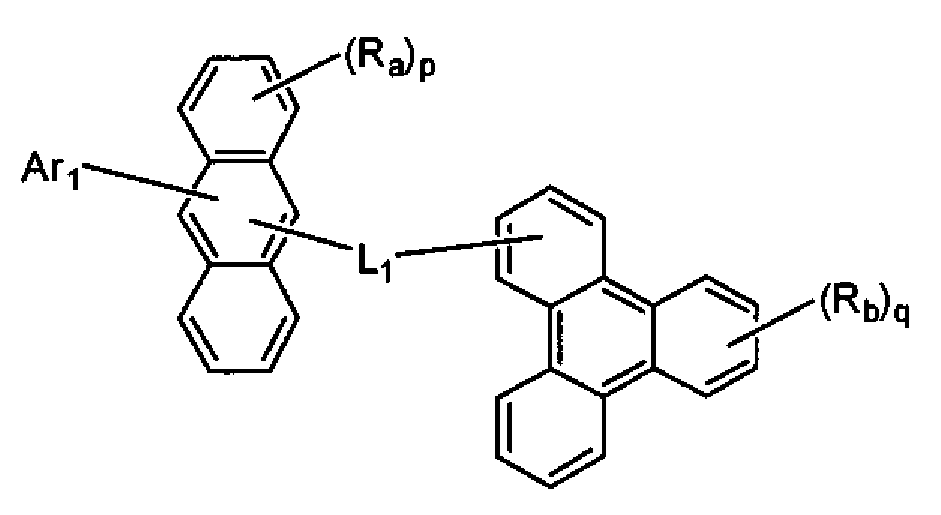
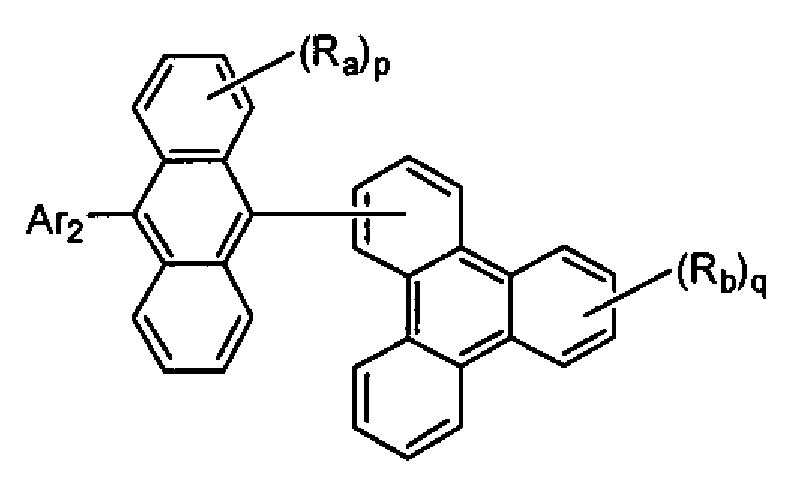
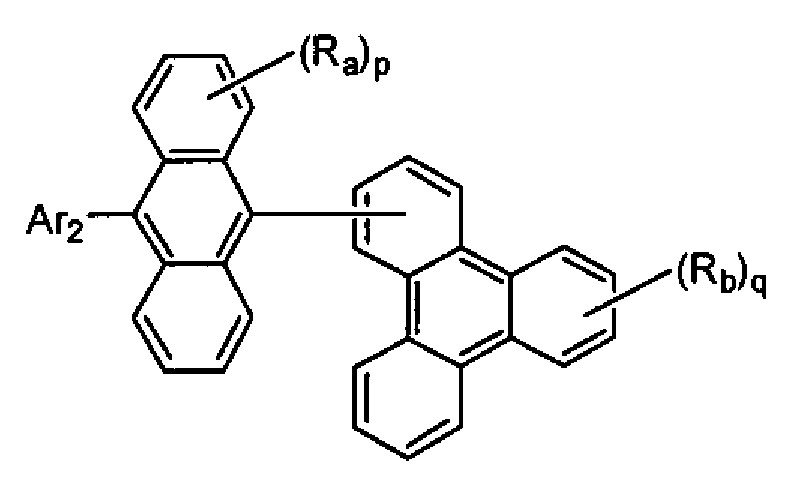
(화학식 1에서, Ra 및 Rb는 각각 수소 원자 또는 치환기를 나타내고, p는 1 내지 8의 정수, q는 1 내지 11의 정수를 나타내며, p 또는 q가 2 이상인 경우, Ra 또는 Rb는 각각 동일하거나 상이할 수 있고, Ra는 인접하는 치환기끼리 환을 형성할 수도 있고, L1은 단결합, 또는 치환 또는 비치환된 2가의 연결기를 나타내고, Ar1은 치환 또는 비치환된 핵탄소수 6 내지 50의 아릴기, 또는 치환 또는 비치환된 핵원자수 5 내지 50의 헤테로아릴기를 나타내되, 단 L1이 단결합이며, Ra 중 적어도 하나가 수소 원자가 아닌 경우, Ar1은 트리페닐레닐기가 아니고, L1 및 Ar1의 치환기, 및 Ra 및 Rb는 아미노기를 포함하지 않음) - 제3항에 있어서, 상기 화학식 2의 Ar2가 치환 또는 비치환된 핵탄소수 10 내지 20의 축합 방향족환인 축합 방향족 유도체.
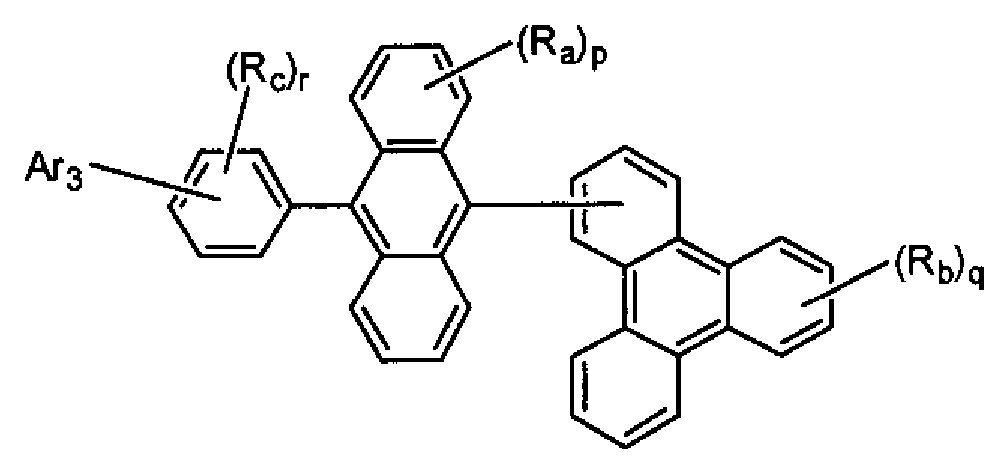
- 제5항에 있어서, 상기 화학식 3의 Ar3이 치환 또는 비치환된 핵탄소수 10 내지 20의 축합 방향족환인 축합 방향족 유도체.
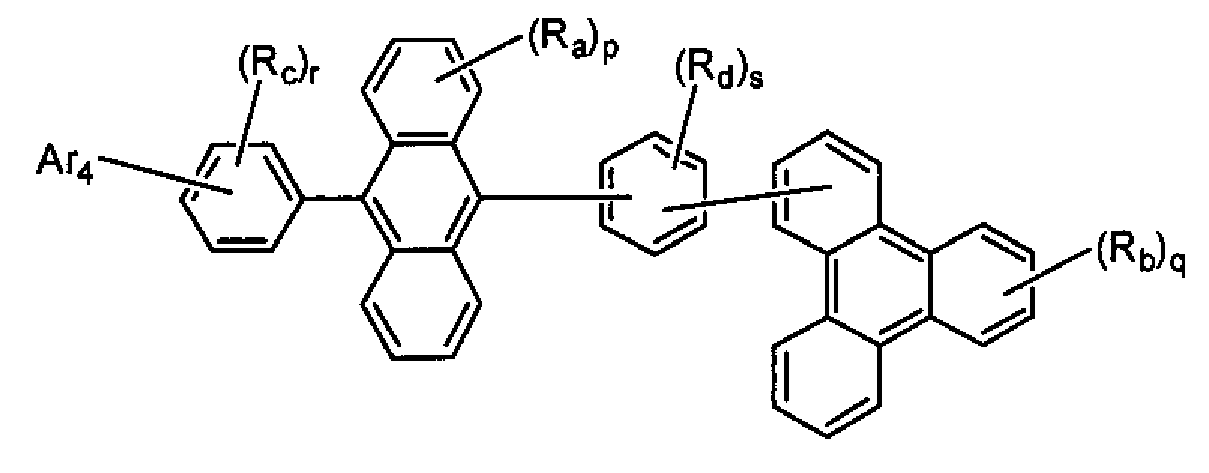
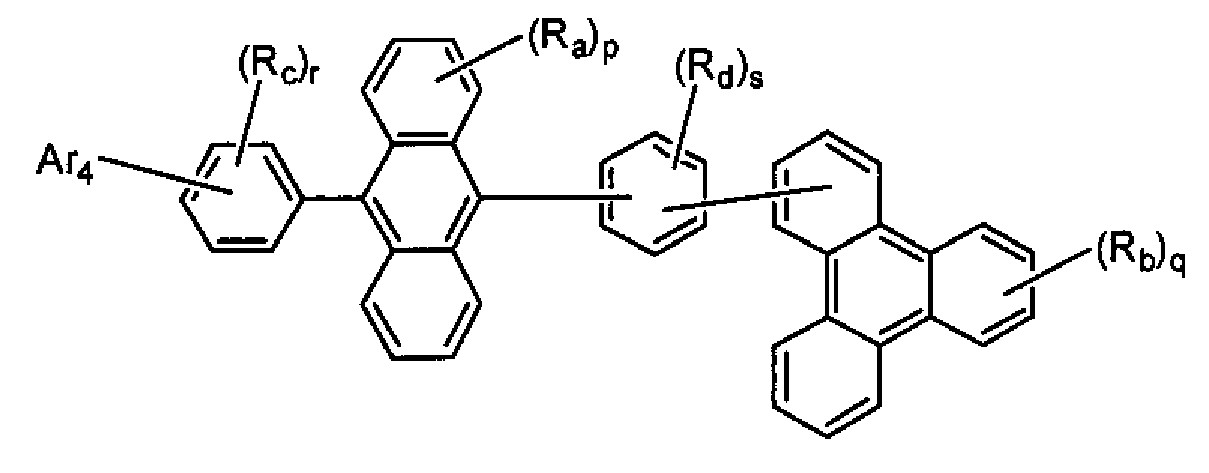
- 제7항에 있어서, 상기 화학식 4의 Ar4가 치환 또는 비치환된 핵탄소수 10 내지 20의 축합 방향족환인 축합 방향족 유도체.
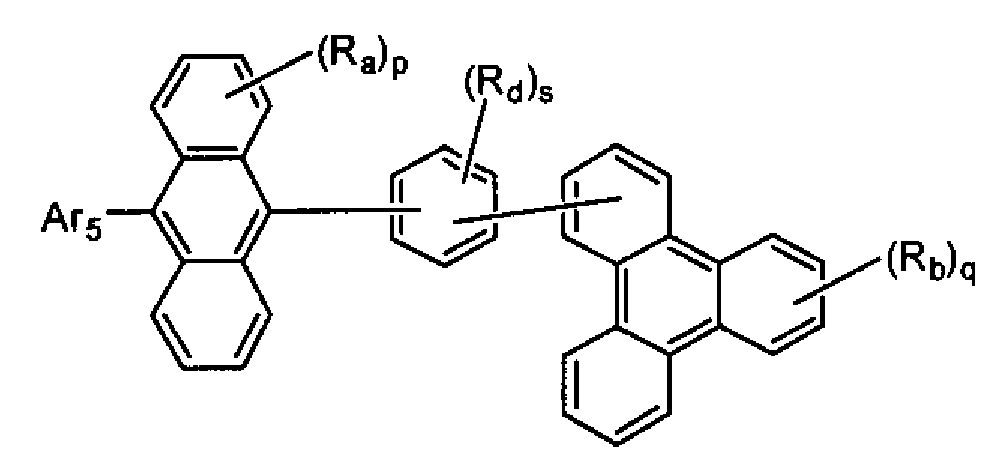
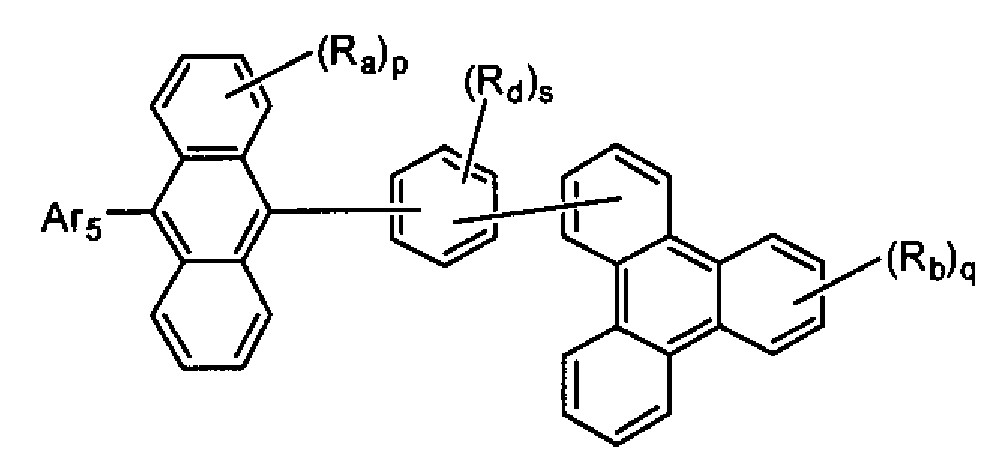
- 제9항에 있어서, 상기 화학식 5의 Ar5가 치환 또는 비치환된 나프틸기인 축합 방향족 유도체.
- 제1항 내지 제10항 중 어느 한 항에 기재된 축합 방향족 유도체를 함유하는 유기 전계 발광 소자용 재료.
- 제11항에 있어서, 발광 재료인 유기 전계 발광 소자용 재료.
- 양극 및 음극과,
상기 양극 및 음극의 사이에 협지되어 있는 발광층을 포함하는 하나 이상의 유기 박막층을 갖고,
상기 유기 박막층 중 적어도 한층이 제1항 내지 제10항 중 어느 한 항에 기재된 축합 방향족 유도체를 함유하는 유기 전계 발광 소자. - 제13항에 있어서, 상기 발광층이 상기 축합 방향족 유도체를 함유하는 유기 전계 발광 소자.
- 제14항에 있어서, 상기 발광층이 상기 축합 방향족 유도체를 호스트 재료로서 함유하는 유기 전계 발광 소자.
- 제13항 내지 제15항 중 어느 한 항에 있어서, 상기 발광층이 형광성 도펀트 및 인광성 도펀트 중 적어도 하나를 추가로 함유하는 유기 전계 발광 소자.
- 제16항에 있어서, 상기 형광성 도펀트가 아릴아민 화합물인 유기 전계 발광 소자.
- 제16항에 있어서, 상기 형광성 도펀트가 스티릴아민 화합물인 유기 전계 발광 소자.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007301837 | 2007-11-21 | ||
| JPJP-P-2007-301837 | 2007-11-21 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20100090269A true KR20100090269A (ko) | 2010-08-13 |
| KR101477844B1 KR101477844B1 (ko) | 2014-12-30 |
Family
ID=40667463
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107011034A Active KR101477844B1 (ko) | 2007-11-21 | 2008-11-17 | 축합 방향족 유도체 및 이것을 사용한 유기 전계 발광 소자 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US8623520B2 (ko) |
| EP (1) | EP2213641B1 (ko) |
| JP (1) | JP5399920B2 (ko) |
| KR (1) | KR101477844B1 (ko) |
| TW (1) | TW200927880A (ko) |
| WO (1) | WO2009066641A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9627628B2 (en) | 2013-06-17 | 2017-04-18 | Samsung Display Co., Ld. | Organic light emitting diode device |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8623520B2 (en) * | 2007-11-21 | 2014-01-07 | Idemitsu Kosan Co., Ltd. | Fused aromatic derivative and organic electroluminescence device using the same |
| JP5378397B2 (ja) * | 2007-11-22 | 2013-12-25 | グレイセル・ディスプレイ・インコーポレーテッド | 高効率の青色電界発光化合物およびこれを使用する表示素子 |
| EP2239259B1 (en) | 2007-12-28 | 2016-04-13 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and use of the same in an organic electroluminescent device |
| CA2713949C (en) | 2008-04-11 | 2016-10-11 | Board Of Regents The University Of Texas System | Method and apparatus for nanoparticle electrogenerated chemiluminescence amplification |
| EP2626692A3 (en) | 2008-05-08 | 2014-10-01 | Board of Regents of the University of Texas System | Luminescent nanostructured materials for use in electrogenerated chemiluminescence |
| KR20110043625A (ko) * | 2008-07-28 | 2011-04-27 | 이데미쓰 고산 가부시키가이샤 | 유기 발광 매체 및 유기 el 소자 |
| WO2010013675A1 (ja) * | 2008-07-28 | 2010-02-04 | 出光興産株式会社 | 有機発光媒体及び有機el素子 |
| CN104795495B (zh) | 2009-04-24 | 2017-09-29 | 出光兴产株式会社 | 芳香族胺衍生物和使用其的有机电致发光元件 |
| DE102009053191A1 (de) * | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| CN102239141A (zh) | 2009-12-16 | 2011-11-09 | 出光兴产株式会社 | 芳香族胺衍生物和使用其的有机电致发光元件 |
| TWI397516B (zh) * | 2010-02-03 | 2013-06-01 | Nat Univ Tsing Hua | 含聯三伸苯基之芳香族化合物及有機發光二極體 |
| US8288015B2 (en) * | 2010-04-18 | 2012-10-16 | National Tsing Hua University | Triphenylene based aromatic compounds and OLEDs utilizing the same |
| US8968887B2 (en) * | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| CN102241620B (zh) * | 2010-05-14 | 2013-07-17 | 国立清华大学 | 含苯并[9,10]菲基的芳香族化合物及利用其的有机发光二极管 |
| JP5778407B2 (ja) * | 2010-07-29 | 2015-09-16 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子及び電荷輸送材料 |
| JP5973762B2 (ja) * | 2011-03-31 | 2016-08-23 | ユー・ディー・シー アイルランド リミテッド | 電荷輸送材料、有機電界発光素子及び該素子を用いたことを特徴とする発光装置、表示装置または照明装置 |
| KR101535824B1 (ko) * | 2011-12-16 | 2015-07-13 | 엘지디스플레이 주식회사 | 유기 발광 소자 |
| WO2015139808A1 (de) * | 2014-03-18 | 2015-09-24 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| KR101780605B1 (ko) | 2014-09-19 | 2017-09-21 | 이데미쓰 고산 가부시키가이샤 | 신규의 화합물 |
| JP2020518107A (ja) | 2017-04-26 | 2020-06-18 | オーティーアイ ルミオニクス インコーポレーテッドOti Lumionics Inc. | 表面上のコーティングをパターン化する方法およびパターン化されたコーティングを含むデバイス |
| US11751415B2 (en) | 2018-02-02 | 2023-09-05 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating same |
| CN116456753A (zh) | 2019-03-07 | 2023-07-18 | Oti照明公司 | 一种光电子器件 |
| WO2020212953A1 (en) | 2019-04-18 | 2020-10-22 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating the same |
| JP7576337B2 (ja) | 2019-05-08 | 2024-11-01 | オーティーアイ ルミオニクス インコーポレーテッド | 核生成抑制コーティングを形成するための材料およびそれを組み込んだデバイス |
| WO2022123431A1 (en) | 2020-12-07 | 2022-06-16 | Oti Lumionics Inc. | Patterning a conductive deposited layer using a nucleation inhibiting coating and an underlying metallic coating |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6150042A (en) * | 1996-12-09 | 2000-11-21 | Toyo Ink Manufacturing Co., Ltd. | Material for organoelectro-luminescence device and use thereof |
| KR100799799B1 (ko) * | 1999-09-21 | 2008-02-01 | 이데미쓰 고산 가부시키가이샤 | 유기 전자발광 소자 및 유기 발광 매체 |
| JP2003109765A (ja) * | 2001-09-28 | 2003-04-11 | Canon Inc | 有機発光素子 |
| JP2004002351A (ja) * | 2002-03-27 | 2004-01-08 | Tdk Corp | 有機el素子 |
| JP4170655B2 (ja) * | 2002-04-17 | 2008-10-22 | 出光興産株式会社 | 新規芳香族化合物及びそれを利用した有機エレクトロルミネッセンス素子 |
| TWI314947B (en) * | 2002-04-24 | 2009-09-21 | Eastman Kodak Compan | Organic light emitting diode devices with improved operational stability |
| JP4025136B2 (ja) | 2002-07-31 | 2007-12-19 | 出光興産株式会社 | アントラセン誘導体、有機エレクトロルミネッセンス素子用発光材料及び有機エレクトロルミネッセンス素子 |
| KR100924462B1 (ko) | 2002-08-23 | 2009-11-03 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자 및 안트라센 유도체 |
| TW593624B (en) * | 2002-10-16 | 2004-06-21 | Univ Tsinghua | Aromatic compounds and organic LED |
| JP4035482B2 (ja) * | 2003-06-27 | 2008-01-23 | キヤノン株式会社 | 置換アントリル誘導体およびそれを使用した有機発光素子 |
| JP4070676B2 (ja) | 2003-07-25 | 2008-04-02 | 三井化学株式会社 | 非対称置換アントラセン化合物、および該非対称置換アントラセン化合物を含有する有機電界発光素子 |
| JP4984891B2 (ja) * | 2004-07-02 | 2012-07-25 | Jnc株式会社 | 発光材料およびこれを用いた有機電界発光素子 |
| JP4677221B2 (ja) | 2004-11-26 | 2011-04-27 | キヤノン株式会社 | 有機発光素子 |
| US20060204783A1 (en) * | 2005-03-10 | 2006-09-14 | Conley Scott R | Organic electroluminescent device |
| US20060286405A1 (en) * | 2005-06-17 | 2006-12-21 | Eastman Kodak Company | Organic element for low voltage electroluminescent devices |
| JP4726584B2 (ja) * | 2005-09-15 | 2011-07-20 | 三井化学株式会社 | 芳香族化合物、該芳香族化合物を含有する有機電界発光素子 |
| US9666826B2 (en) * | 2005-11-30 | 2017-05-30 | Global Oled Technology Llc | Electroluminescent device including an anthracene derivative |
| JP4979247B2 (ja) * | 2006-03-08 | 2012-07-18 | 三井化学株式会社 | アントラセン化合物および該化合物を含有する有機電界発光素子 |
| KR100833218B1 (ko) | 2006-04-14 | 2008-05-28 | 주식회사 이엘엠 | 트리페닐렌 유도체 및 이를 이용한 유기 발광 다이오드 |
| KR100857025B1 (ko) * | 2006-05-22 | 2008-09-05 | (주)그라쎌 | 고성능의 청색 발광 화합물 및 이를 함유하는 표시소자 |
| US8795855B2 (en) | 2007-01-30 | 2014-08-05 | Global Oled Technology Llc | OLEDs having high efficiency and excellent lifetime |
| US8623520B2 (en) * | 2007-11-21 | 2014-01-07 | Idemitsu Kosan Co., Ltd. | Fused aromatic derivative and organic electroluminescence device using the same |
| JP5378397B2 (ja) * | 2007-11-22 | 2013-12-25 | グレイセル・ディスプレイ・インコーポレーテッド | 高効率の青色電界発光化合物およびこれを使用する表示素子 |
| JP2009209127A (ja) * | 2008-02-08 | 2009-09-17 | Toyo Ink Mfg Co Ltd | カルバゾリル基を有する化合物およびその用途 |
| KR100910150B1 (ko) * | 2008-04-02 | 2009-08-03 | (주)그라쎌 | 신규한 유기 발광 화합물 및 이를 발광재료로서 채용하고있는 유기 발광 소자 |
-
2008
- 2008-11-17 US US12/743,815 patent/US8623520B2/en active Active
- 2008-11-17 WO PCT/JP2008/070882 patent/WO2009066641A1/ja not_active Ceased
- 2008-11-17 JP JP2009542548A patent/JP5399920B2/ja not_active Expired - Fee Related
- 2008-11-17 EP EP08851689.3A patent/EP2213641B1/en not_active Not-in-force
- 2008-11-17 KR KR1020107011034A patent/KR101477844B1/ko active Active
- 2008-11-20 TW TW097144854A patent/TW200927880A/zh unknown
-
2013
- 2013-10-28 US US14/065,096 patent/US10153450B2/en active Active
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9627628B2 (en) | 2013-06-17 | 2017-04-18 | Samsung Display Co., Ld. | Organic light emitting diode device |
| US10418560B2 (en) | 2013-06-17 | 2019-09-17 | Samsung Display Co., Ltd. | Organic light emitting diode device |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5399920B2 (ja) | 2014-01-29 |
| KR101477844B1 (ko) | 2014-12-30 |
| JPWO2009066641A1 (ja) | 2011-04-07 |
| TW200927880A (en) | 2009-07-01 |
| EP2213641A1 (en) | 2010-08-04 |
| WO2009066641A1 (ja) | 2009-05-28 |
| US10153450B2 (en) | 2018-12-11 |
| EP2213641A4 (en) | 2011-01-26 |
| US20100295030A1 (en) | 2010-11-25 |
| US8623520B2 (en) | 2014-01-07 |
| US20140061628A1 (en) | 2014-03-06 |
| EP2213641B1 (en) | 2018-05-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101477844B1 (ko) | 축합 방향족 유도체 및 이것을 사용한 유기 전계 발광 소자 | |
| JP5473600B2 (ja) | クリセン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 | |
| JP5443996B2 (ja) | ベンゾフェナントレン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 | |
| KR101419101B1 (ko) | 벤조크리센 유도체 및 이것을 사용한 유기 전계 발광 소자 | |
| KR101353635B1 (ko) | 벤조크리센 유도체 및 이것을 사용한 유기 전계 발광 소자 | |
| EP2085382B1 (en) | Aromatic amine derivative and organic electroluminescent element using the same | |
| KR101379133B1 (ko) | 방향족 아민 유도체 및 그들을 사용한 유기 전기발광 소자 | |
| KR101420475B1 (ko) | 모노벤조크리센 유도체, 이것을 포함하는 유기 전계 발광 소자용 재료, 및 이것을 사용한 유기 전계 발광 소자 | |
| JP5335691B2 (ja) | ベンズアントラセン化合物及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2010098458A1 (ja) | 有機エレクトロルミネッセンス素子 | |
| KR20110097784A (ko) | 방향족 아민 유도체 및 유기 전기발광 소자 | |
| KR20100017854A (ko) | 다환계 환집합 화합물 및 그것을 이용한 유기 전기 발광 소자 | |
| KR20100097189A (ko) | 질소 함유 헤테로환 유도체 및 그것을 이용한 유기 전기발광 소자 | |
| WO2009154207A1 (ja) | アントラセン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2009133917A1 (ja) | アントラセン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2009081776A1 (ja) | ベンズアントラセン化合物及びそれを用いた有機エレクトロルミネッセンス素子 | |
| WO2009142230A1 (ja) | アントラセン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
St.27 status event code: N-2-6-B10-B15-exm-PE0601 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| J201 | Request for trial against refusal decision | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PJ0201 | Trial against decision of rejection |
St.27 status event code: A-3-3-V10-V11-apl-PJ0201 |
|
| PB0901 | Examination by re-examination before a trial |
St.27 status event code: A-6-3-E10-E12-rex-PB0901 |
|
| B701 | Decision to grant | ||
| PB0701 | Decision of registration after re-examination before a trial |
St.27 status event code: A-3-4-F10-F13-rex-PB0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| FPAY | Annual fee payment |
Payment date: 20171114 Year of fee payment: 4 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20181129 Year of fee payment: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 8 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 9 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 10 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 11 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 12 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 12 |