KR102079249B1 - 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 - Google Patents
신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 Download PDFInfo
- Publication number
- KR102079249B1 KR102079249B1 KR1020120062860A KR20120062860A KR102079249B1 KR 102079249 B1 KR102079249 B1 KR 102079249B1 KR 1020120062860 A KR1020120062860 A KR 1020120062860A KR 20120062860 A KR20120062860 A KR 20120062860A KR 102079249 B1 KR102079249 B1 KR 102079249B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- compound
- carbon atoms
- layer
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 165
- 239000010410 layer Substances 0.000 claims description 172
- 125000004432 carbon atom Chemical group C* 0.000 claims description 108
- 238000002347 injection Methods 0.000 claims description 94
- 239000007924 injection Substances 0.000 claims description 94
- 230000005525 hole transport Effects 0.000 claims description 70
- 238000000034 method Methods 0.000 claims description 53
- 239000000463 material Substances 0.000 claims description 52
- 125000003118 aryl group Chemical group 0.000 claims description 38
- 239000012044 organic layer Substances 0.000 claims description 31
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 30
- 125000001072 heteroaryl group Chemical group 0.000 claims description 29
- -1 R 21 Chemical compound 0.000 claims description 28
- 125000000217 alkyl group Chemical group 0.000 claims description 27
- 125000005843 halogen group Chemical group 0.000 claims description 27
- 239000002346 layers by function Substances 0.000 claims description 27
- 150000003839 salts Chemical class 0.000 claims description 24
- 229910052805 deuterium Inorganic materials 0.000 claims description 23
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 22
- 125000003367 polycyclic group Chemical group 0.000 claims description 22
- 125000005647 linker group Chemical group 0.000 claims description 18
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 17
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 16
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 16
- 239000002019 doping agent Substances 0.000 claims description 15
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 15
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 15
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 claims description 12
- 125000000732 arylene group Chemical group 0.000 claims description 12
- 229910052739 hydrogen Inorganic materials 0.000 claims description 12
- 239000001257 hydrogen Substances 0.000 claims description 12
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 11
- 125000005549 heteroarylene group Chemical group 0.000 claims description 10
- 229910052799 carbon Inorganic materials 0.000 claims description 9
- 150000002431 hydrogen Chemical class 0.000 claims description 9
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 8
- 150000007857 hydrazones Chemical class 0.000 claims description 8
- 125000000542 sulfonic acid group Chemical group 0.000 claims description 8
- 150000001721 carbon Chemical class 0.000 claims description 7
- 125000003342 alkenyl group Chemical group 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 5
- 150000004696 coordination complex Chemical class 0.000 claims description 5
- 239000010409 thin film Substances 0.000 claims description 5
- 125000000304 alkynyl group Chemical group 0.000 claims description 4
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical group [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 claims description 4
- 229910044991 metal oxide Inorganic materials 0.000 claims description 4
- 150000004706 metal oxides Chemical class 0.000 claims description 4
- 150000002894 organic compounds Chemical class 0.000 claims description 4
- 150000004059 quinone derivatives Chemical group 0.000 claims description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 3
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 3
- 150000004982 aromatic amines Chemical class 0.000 claims description 2
- 150000001975 deuterium Chemical group 0.000 claims description 2
- 125000005504 styryl group Chemical group 0.000 claims description 2
- SWGZHHCRMZDRSN-BTJKTKAUSA-N (Z)-but-2-enedioic acid 1-phenoxypropan-2-ylhydrazine Chemical compound OC(=O)\C=C/C(O)=O.NNC(C)COC1=CC=CC=C1 SWGZHHCRMZDRSN-BTJKTKAUSA-N 0.000 claims 1
- 125000003107 substituted aryl group Chemical group 0.000 claims 1
- 230000015572 biosynthetic process Effects 0.000 description 174
- 238000003786 synthesis reaction Methods 0.000 description 169
- 239000000543 intermediate Substances 0.000 description 165
- 229940125904 compound 1 Drugs 0.000 description 41
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 38
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 37
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 20
- 125000001424 substituent group Chemical group 0.000 description 20
- 239000000243 solution Substances 0.000 description 18
- 238000006243 chemical reaction Methods 0.000 description 17
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 14
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 14
- 125000001624 naphthyl group Chemical group 0.000 description 13
- 239000002904 solvent Substances 0.000 description 13
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 12
- 238000004528 spin coating Methods 0.000 description 12
- 238000001771 vacuum deposition Methods 0.000 description 11
- UCCUXODGPMAHRL-UHFFFAOYSA-N 1-bromo-4-iodobenzene Chemical compound BrC1=CC=C(I)C=C1 UCCUXODGPMAHRL-UHFFFAOYSA-N 0.000 description 10
- 230000008020 evaporation Effects 0.000 description 10
- 238000001704 evaporation Methods 0.000 description 10
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 10
- 235000019341 magnesium sulphate Nutrition 0.000 description 10
- 239000000758 substrate Substances 0.000 description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 10
- WDBQJSCPCGTAFG-QHCPKHFHSA-N 4,4-difluoro-N-[(1S)-3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-pyridin-3-ylpropyl]cyclohexane-1-carboxamide Chemical compound FC1(CCC(CC1)C(=O)N[C@@H](CCN1CCC(CC1)N1C(=NN=C1C)C(C)C)C=1C=NC=CC=1)F WDBQJSCPCGTAFG-QHCPKHFHSA-N 0.000 description 9
- MINMDCMSHDBHKG-UHFFFAOYSA-N 4-[4-[[6-methoxy-2-(2-methoxyimidazo[2,1-b][1,3,4]thiadiazol-6-yl)-1-benzofuran-4-yl]oxymethyl]-5-methyl-1,3-thiazol-2-yl]morpholine Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(=C(S1)C)N=C1N1CCOCC1 MINMDCMSHDBHKG-UHFFFAOYSA-N 0.000 description 9
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 125000003277 amino group Chemical group 0.000 description 9
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 9
- 230000000903 blocking effect Effects 0.000 description 9
- 238000000151 deposition Methods 0.000 description 9
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 9
- 239000000872 buffer Substances 0.000 description 8
- 229910052757 nitrogen Inorganic materials 0.000 description 8
- 238000010898 silica gel chromatography Methods 0.000 description 8
- 125000003739 carbamimidoyl group Chemical group C(N)(=N)* 0.000 description 7
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- XQVWYOYUZDUNRW-UHFFFAOYSA-N N-Phenyl-1-naphthylamine Chemical compound C=1C=CC2=CC=CC=C2C=1NC1=CC=CC=C1 XQVWYOYUZDUNRW-UHFFFAOYSA-N 0.000 description 6
- 230000008021 deposition Effects 0.000 description 6
- 229920000767 polyaniline Polymers 0.000 description 6
- 125000001725 pyrenyl group Chemical group 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 5
- VCUXVXLUOHDHKK-UHFFFAOYSA-N 2-(2-aminopyrimidin-4-yl)-4-(2-chloro-4-methoxyphenyl)-1,3-thiazole-5-carboxamide Chemical compound ClC1=CC(OC)=CC=C1C1=C(C(N)=O)SC(C=2N=C(N)N=CC=2)=N1 VCUXVXLUOHDHKK-UHFFFAOYSA-N 0.000 description 5
- HCCNBKFJYUWLEX-UHFFFAOYSA-N 7-(6-methoxypyridin-3-yl)-1-(2-propoxyethyl)-3-(pyrazin-2-ylmethylamino)pyrido[3,4-b]pyrazin-2-one Chemical compound O=C1N(CCOCCC)C2=CC(C=3C=NC(OC)=CC=3)=NC=C2N=C1NCC1=CN=CC=N1 HCCNBKFJYUWLEX-UHFFFAOYSA-N 0.000 description 5
- 239000011248 coating agent Substances 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 229940126142 compound 16 Drugs 0.000 description 5
- 229940126545 compound 53 Drugs 0.000 description 5
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 5
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 5
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 4
- QEBYEVQKHRUYPE-UHFFFAOYSA-N 2-(2-chlorophenyl)-5-[(1-methylpyrazol-3-yl)methyl]-4-[[methyl(pyridin-3-ylmethyl)amino]methyl]-1h-pyrazolo[4,3-c]pyridine-3,6-dione Chemical compound C1=CN(C)N=C1CN1C(=O)C=C2NN(C=3C(=CC=CC=3)Cl)C(=O)C2=C1CN(C)CC1=CC=CN=C1 QEBYEVQKHRUYPE-UHFFFAOYSA-N 0.000 description 4
- MAGFQRLKWCCTQJ-UHFFFAOYSA-M 4-ethenylbenzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=C(C=C)C=C1 MAGFQRLKWCCTQJ-UHFFFAOYSA-M 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 125000005110 aryl thio group Chemical group 0.000 description 4
- 125000004104 aryloxy group Chemical group 0.000 description 4
- 125000006267 biphenyl group Chemical group 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- 239000011777 magnesium Substances 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- YGNUPJXMDOFFDO-UHFFFAOYSA-N n,4-diphenylaniline Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1NC1=CC=CC=C1 YGNUPJXMDOFFDO-UHFFFAOYSA-N 0.000 description 4
- 125000000027 (C1-C10) alkoxy group Chemical group 0.000 description 3
- 125000006743 (C1-C60) alkyl group Chemical group 0.000 description 3
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 3
- KZSDTBVDHCKNBY-UHFFFAOYSA-N 2-bromo-cyclopenta[def]phenanthren-4-one Chemical compound C1=CC=C2C=CC3=CC(Br)=CC4=C3C2=C1C4=O KZSDTBVDHCKNBY-UHFFFAOYSA-N 0.000 description 3
- DFRAKBCRUYUFNT-UHFFFAOYSA-N 3,8-dicyclohexyl-2,4,7,9-tetrahydro-[1,3]oxazino[5,6-h][1,3]benzoxazine Chemical compound C1CCCCC1N1CC(C=CC2=C3OCN(C2)C2CCCCC2)=C3OC1 DFRAKBCRUYUFNT-UHFFFAOYSA-N 0.000 description 3
- ISMDILRWKSYCOD-GNKBHMEESA-N C(C1=CC=CC=C1)[C@@H]1NC(OCCCCCCCCCCCNC([C@@H](NC(C[C@@H]1O)=O)C(C)C)=O)=O Chemical compound C(C1=CC=CC=C1)[C@@H]1NC(OCCCCCCCCCCCNC([C@@H](NC(C[C@@H]1O)=O)C(C)C)=O)=O ISMDILRWKSYCOD-GNKBHMEESA-N 0.000 description 3
- 229940126639 Compound 33 Drugs 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- LVDRREOUMKACNJ-BKMJKUGQSA-N N-[(2R,3S)-2-(4-chlorophenyl)-1-(1,4-dimethyl-2-oxoquinolin-7-yl)-6-oxopiperidin-3-yl]-2-methylpropane-1-sulfonamide Chemical compound CC(C)CS(=O)(=O)N[C@H]1CCC(=O)N([C@@H]1c1ccc(Cl)cc1)c1ccc2c(C)cc(=O)n(C)c2c1 LVDRREOUMKACNJ-BKMJKUGQSA-N 0.000 description 3
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 3
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 3
- JHISZOPVKQMFQE-UHFFFAOYSA-M [Br-].C1=CC([Mg+])=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 Chemical compound [Br-].C1=CC([Mg+])=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 JHISZOPVKQMFQE-UHFFFAOYSA-M 0.000 description 3
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 3
- 229940126086 compound 21 Drugs 0.000 description 3
- 229940035423 ethyl ether Drugs 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 3
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000004076 pyridyl group Chemical group 0.000 description 3
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- YJLIKUSWRSEPSM-WGQQHEPDSA-N (2r,3r,4s,5r)-2-[6-amino-8-[(4-phenylphenyl)methylamino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CNC1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O YJLIKUSWRSEPSM-WGQQHEPDSA-N 0.000 description 2
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 2
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 2
- 125000006746 (C1-C60) alkoxy group Chemical group 0.000 description 2
- 125000006745 (C2-C60) alkynyl group Chemical group 0.000 description 2
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 2
- GWOAJJWBCSUGHH-UHFFFAOYSA-N 1-bromo-4-(4-iodophenyl)benzene Chemical group C1=CC(Br)=CC=C1C1=CC=C(I)C=C1 GWOAJJWBCSUGHH-UHFFFAOYSA-N 0.000 description 2
- HQHHKYXPFKHLBF-UHFFFAOYSA-N 1-bromo-4-iodonaphthalene Chemical compound C1=CC=C2C(Br)=CC=C(I)C2=C1 HQHHKYXPFKHLBF-UHFFFAOYSA-N 0.000 description 2
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 2
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 2
- VYMNCOOEVDIPTL-UHFFFAOYSA-N 2-bromo-6-iodonaphthalene Chemical compound C1=C(I)C=CC2=CC(Br)=CC=C21 VYMNCOOEVDIPTL-UHFFFAOYSA-N 0.000 description 2
- WBIQQQGBSDOWNP-UHFFFAOYSA-N 2-dodecylbenzenesulfonic acid Chemical compound CCCCCCCCCCCCC1=CC=CC=C1S(O)(=O)=O WBIQQQGBSDOWNP-UHFFFAOYSA-N 0.000 description 2
- LFOIDLOIBZFWDO-UHFFFAOYSA-N 2-methoxy-6-[6-methoxy-4-[(3-phenylmethoxyphenyl)methoxy]-1-benzofuran-2-yl]imidazo[2,1-b][1,3,4]thiadiazole Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(C=1)=CC=CC=1OCC1=CC=CC=C1 LFOIDLOIBZFWDO-UHFFFAOYSA-N 0.000 description 2
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical group C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 2
- OBAJPWYDYFEBTF-UHFFFAOYSA-N 2-tert-butyl-9,10-dinaphthalen-2-ylanthracene Chemical compound C1=CC=CC2=CC(C3=C4C=CC=CC4=C(C=4C=C5C=CC=CC5=CC=4)C4=CC=C(C=C43)C(C)(C)C)=CC=C21 OBAJPWYDYFEBTF-UHFFFAOYSA-N 0.000 description 2
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 2
- JAUCIDPGGHZXRP-UHFFFAOYSA-N 4-phenyl-n-(4-phenylphenyl)aniline Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1NC(C=C1)=CC=C1C1=CC=CC=C1 JAUCIDPGGHZXRP-UHFFFAOYSA-N 0.000 description 2
- WPQJQVZDUZXMTO-UHFFFAOYSA-N 4-phenyl-n-[4-(9-phenylcarbazol-3-yl)phenyl]aniline Chemical compound C=1C=C(C=2C=C3C4=CC=CC=C4N(C=4C=CC=CC=4)C3=CC=2)C=CC=1NC(C=C1)=CC=C1C1=CC=CC=C1 WPQJQVZDUZXMTO-UHFFFAOYSA-N 0.000 description 2
- RKZDZWJDQTZDLD-UHFFFAOYSA-N 4h-cyclopenta[def]phenanthrene Chemical compound C1=CC=C2CC3=CC=CC4=CC=C1C2=C34 RKZDZWJDQTZDLD-UHFFFAOYSA-N 0.000 description 2
- RSIWALKZYXPAGW-NSHDSACASA-N 6-(3-fluorophenyl)-3-methyl-7-[(1s)-1-(7h-purin-6-ylamino)ethyl]-[1,3]thiazolo[3,2-a]pyrimidin-5-one Chemical compound C=1([C@@H](NC=2C=3N=CNC=3N=CN=2)C)N=C2SC=C(C)N2C(=O)C=1C1=CC=CC(F)=C1 RSIWALKZYXPAGW-NSHDSACASA-N 0.000 description 2
- XASOHFCUIQARJT-UHFFFAOYSA-N 8-methoxy-6-[7-(2-morpholin-4-ylethoxy)imidazo[1,2-a]pyridin-3-yl]-2-(2,2,2-trifluoroethyl)-3,4-dihydroisoquinolin-1-one Chemical compound C(N1C(=O)C2=C(OC)C=C(C=3N4C(=NC=3)C=C(C=C4)OCCN3CCOCC3)C=C2CC1)C(F)(F)F XASOHFCUIQARJT-UHFFFAOYSA-N 0.000 description 2
- VIZUPBYFLORCRA-UHFFFAOYSA-N 9,10-dinaphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=C(C=CC=C2)C2=C1 VIZUPBYFLORCRA-UHFFFAOYSA-N 0.000 description 2
- RFTRFDMRINNTSI-UHFFFAOYSA-N 9,9-dimethyl-n-phenylfluoren-2-amine Chemical compound C1=C2C(C)(C)C3=CC=CC=C3C2=CC=C1NC1=CC=CC=C1 RFTRFDMRINNTSI-UHFFFAOYSA-N 0.000 description 2
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 229910001148 Al-Li alloy Inorganic materials 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- UEXCJVNBTNXOEH-UHFFFAOYSA-N Ethynylbenzene Chemical group C#CC1=CC=CC=C1 UEXCJVNBTNXOEH-UHFFFAOYSA-N 0.000 description 2
- 101000837344 Homo sapiens T-cell leukemia translocation-altered gene protein Proteins 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102100028692 T-cell leukemia translocation-altered gene protein Human genes 0.000 description 2
- JHYLKGDXMUDNEO-UHFFFAOYSA-N [Mg].[In] Chemical compound [Mg].[In] JHYLKGDXMUDNEO-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- DMVOXQPQNTYEKQ-UHFFFAOYSA-N biphenyl-4-amine Chemical compound C1=CC(N)=CC=C1C1=CC=CC=C1 DMVOXQPQNTYEKQ-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 229940126208 compound 22 Drugs 0.000 description 2
- 229940125851 compound 27 Drugs 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 229940125844 compound 46 Drugs 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 2
- 229940060296 dodecylbenzenesulfonic acid Drugs 0.000 description 2
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- SJCKRGFTWFGHGZ-UHFFFAOYSA-N magnesium silver Chemical compound [Mg].[Ag] SJCKRGFTWFGHGZ-UHFFFAOYSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- KLZHUQDVWUXWEZ-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1.C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 KLZHUQDVWUXWEZ-UHFFFAOYSA-N 0.000 description 2
- 125000004957 naphthylene group Chemical group 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 2
- 125000005560 phenanthrenylene group Chemical group 0.000 description 2
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 125000005548 pyrenylene group Chemical group 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 2
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- 125000000923 (C1-C30) alkyl group Chemical group 0.000 description 1
- 125000006744 (C2-C60) alkenyl group Chemical group 0.000 description 1
- 125000006818 (C3-C60) cycloalkyl group Chemical group 0.000 description 1
- 0 *C1(*)C(C=C(*)CC2C=C3)=C2C2=C3C=C(*N(*)[Al])CC12 Chemical compound *C1(*)C(C=C(*)CC2C=C3)=C2C2=C3C=C(*N(*)[Al])CC12 0.000 description 1
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 1
- UHXOHPVVEHBKKT-UHFFFAOYSA-N 1-(2,2-diphenylethenyl)-4-[4-(2,2-diphenylethenyl)phenyl]benzene Chemical compound C=1C=C(C=2C=CC(C=C(C=3C=CC=CC=3)C=3C=CC=CC=3)=CC=2)C=CC=1C=C(C=1C=CC=CC=1)C1=CC=CC=C1 UHXOHPVVEHBKKT-UHFFFAOYSA-N 0.000 description 1
- KTADSLDAUJLZGL-UHFFFAOYSA-N 1-bromo-2-phenylbenzene Chemical group BrC1=CC=CC=C1C1=CC=CC=C1 KTADSLDAUJLZGL-UHFFFAOYSA-N 0.000 description 1
- XUPYWKAKDZRRGW-UHFFFAOYSA-N 1-bromo-5-iodonaphthalene Chemical compound C1=CC=C2C(Br)=CC=CC2=C1I XUPYWKAKDZRRGW-UHFFFAOYSA-N 0.000 description 1
- MCZUXEWWARACSP-UHFFFAOYSA-N 1-ethynylnaphthalene Chemical group C1=CC=C2C(C#C)=CC=CC2=C1 MCZUXEWWARACSP-UHFFFAOYSA-N 0.000 description 1
- IYZMXHQDXZKNCY-UHFFFAOYSA-N 1-n,1-n-diphenyl-4-n,4-n-bis[4-(n-phenylanilino)phenyl]benzene-1,4-diamine Chemical compound C1=CC=CC=C1N(C=1C=CC(=CC=1)N(C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 IYZMXHQDXZKNCY-UHFFFAOYSA-N 0.000 description 1
- SPDPTFAJSFKAMT-UHFFFAOYSA-N 1-n-[4-[4-(n-[4-(3-methyl-n-(3-methylphenyl)anilino)phenyl]anilino)phenyl]phenyl]-4-n,4-n-bis(3-methylphenyl)-1-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=C(C)C=CC=2)C=2C=C(C)C=CC=2)C=2C=C(C)C=CC=2)=C1 SPDPTFAJSFKAMT-UHFFFAOYSA-N 0.000 description 1
- YQDSWSPIWVQKBC-UHFFFAOYSA-N 1h-cyclopenta[l]phenanthrene Chemical compound C12=CC=CC=C2C2=CC=CC=C2C2=C1CC=C2 YQDSWSPIWVQKBC-UHFFFAOYSA-N 0.000 description 1
- LDHICRTVVSISIW-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1.C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 LDHICRTVVSISIW-UHFFFAOYSA-N 0.000 description 1
- GEQBRULPNIVQPP-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 GEQBRULPNIVQPP-UHFFFAOYSA-N 0.000 description 1
- LLKRSJVPTKFSLS-UHFFFAOYSA-N 2-bromo-5-iodopyridine Chemical compound BrC1=CC=C(I)C=N1 LLKRSJVPTKFSLS-UHFFFAOYSA-N 0.000 description 1
- UIZYADPAFMRMIH-UHFFFAOYSA-N 2-bromo-8,9-dihydro-4h-cyclopenta[def]phenanthrene Chemical compound C1CC2=CC(Br)=CC3=C2C2=C1C=CC=C2C3 UIZYADPAFMRMIH-UHFFFAOYSA-N 0.000 description 1
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 description 1
- WLPATYNQCGVFFH-UHFFFAOYSA-N 2-phenylbenzonitrile Chemical group N#CC1=CC=CC=C1C1=CC=CC=C1 WLPATYNQCGVFFH-UHFFFAOYSA-N 0.000 description 1
- PPWNCLVNXGCGAF-UHFFFAOYSA-N 3,3-dimethylbut-1-yne Chemical group CC(C)(C)C#C PPWNCLVNXGCGAF-UHFFFAOYSA-N 0.000 description 1
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 description 1
- USCSRAJGJYMJFZ-UHFFFAOYSA-N 3-methyl-1-butyne Chemical group CC(C)C#C USCSRAJGJYMJFZ-UHFFFAOYSA-N 0.000 description 1
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 1
- LXOCTSJQHHCASE-UHFFFAOYSA-N 3-phenyl-n-(3-phenylphenyl)aniline Chemical compound C=1C=CC(C=2C=CC=CC=2)=CC=1NC(C=1)=CC=CC=1C1=CC=CC=C1 LXOCTSJQHHCASE-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- BUYWHAXNANPEKG-UHFFFAOYSA-N 4-carbazol-9-yl-n-(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C(C=C1)=CC=C1NC1=CC=C(N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 BUYWHAXNANPEKG-UHFFFAOYSA-N 0.000 description 1
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 description 1
- OSQXTXTYKAEHQV-WXUKJITCSA-N 4-methyl-n-[4-[(e)-2-[4-[4-[(e)-2-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]ethenyl]phenyl]phenyl]ethenyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(\C=C\C=2C=CC(=CC=2)C=2C=CC(\C=C\C=3C=CC(=CC=3)N(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)=CC=2)=CC=1)C1=CC=C(C)C=C1 OSQXTXTYKAEHQV-WXUKJITCSA-N 0.000 description 1
- DIVZFUBWFAOMCW-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n,1-n-bis[4-(n-(3-methylphenyl)anilino)phenyl]-4-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 DIVZFUBWFAOMCW-UHFFFAOYSA-N 0.000 description 1
- QYNTUCBQEHUHCS-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n-[4-[4-(n-[4-(n-(3-methylphenyl)anilino)phenyl]anilino)phenyl]phenyl]-1-n,4-n-diphenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 QYNTUCBQEHUHCS-UHFFFAOYSA-N 0.000 description 1
- HSNBRDZXJMPDGH-UHFFFAOYSA-N 5-bromo-2-iodopyridine Chemical compound BrC1=CC=C(I)N=C1 HSNBRDZXJMPDGH-UHFFFAOYSA-N 0.000 description 1
- QBMIPMOSKSYZNU-UHFFFAOYSA-N 8,9-dihydrocyclopenta[def]phenanthrene Chemical compound C1CC2=CC=CC3=C2C2=C1C=CC=C2C3 QBMIPMOSKSYZNU-UHFFFAOYSA-N 0.000 description 1
- QRMLAMCEPKEKHS-UHFFFAOYSA-N 9,9-dimethyl-n-(4-phenylphenyl)fluoren-2-amine Chemical compound C1=C2C(C)(C)C3=CC=CC=C3C2=CC=C1NC(C=C1)=CC=C1C1=CC=CC=C1 QRMLAMCEPKEKHS-UHFFFAOYSA-N 0.000 description 1
- VIJYEGDOKCKUOL-UHFFFAOYSA-N 9-phenylcarbazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 VIJYEGDOKCKUOL-UHFFFAOYSA-N 0.000 description 1
- LSUNPIIMDFFXTL-UHFFFAOYSA-N BrC1=CC=2CCC=3C=C(C=C4C3C2C(=C1)C4)Br.BrC4=CC=1CCC=2C=C(C=C3C2C1C(=C4)C3)Br Chemical compound BrC1=CC=2CCC=3C=C(C=C4C3C2C(=C1)C4)Br.BrC4=CC=1CCC=2C=C(C=C3C2C1C(=C4)C3)Br LSUNPIIMDFFXTL-UHFFFAOYSA-N 0.000 description 1
- JBVPGCANLQOVEA-UHFFFAOYSA-N BrC1=CC=2CCC=3C=CC=C4C3C2C(=C1)C4.BrC4=CC=1CCC=2C=CC=C3C2C1C(=C4)C3 Chemical compound BrC1=CC=2CCC=3C=CC=C4C3C2C(=C1)C4.BrC4=CC=1CCC=2C=CC=C3C2C1C(=C4)C3 JBVPGCANLQOVEA-UHFFFAOYSA-N 0.000 description 1
- 125000003860 C1-C20 alkoxy group Chemical group 0.000 description 1
- CEYFTVIZUNSJBW-UHFFFAOYSA-N C1=CC=C2C=3C=4C(=CC=CC4CCC13)C2.C2=CC=C1C=3C=4C(=CC=CC4CCC23)C1 Chemical compound C1=CC=C2C=3C=4C(=CC=CC4CCC13)C2.C2=CC=C1C=3C=4C(=CC=CC4CCC23)C1 CEYFTVIZUNSJBW-UHFFFAOYSA-N 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- KEQFTVQCIQJIQW-UHFFFAOYSA-N N-Phenyl-2-naphthylamine Chemical compound C=1C=C2C=CC=CC2=CC=1NC1=CC=CC=C1 KEQFTVQCIQJIQW-UHFFFAOYSA-N 0.000 description 1
- TZYWCYJVHRLUCT-VABKMULXSA-N N-benzyloxycarbonyl-L-leucyl-L-leucyl-L-leucinal Chemical compound CC(C)C[C@@H](C=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)OCC1=CC=CC=C1 TZYWCYJVHRLUCT-VABKMULXSA-N 0.000 description 1
- QBUMWEJYTMMJIG-UHFFFAOYSA-N N-naphthalen-2-yldibenzofuran-3-amine Chemical compound C1=CC=CC2=CC(NC=3C=C4C(C5=CC=CC=C5O4)=CC=3)=CC=C21 QBUMWEJYTMMJIG-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910006404 SnO 2 Inorganic materials 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- 229910001508 alkali metal halide Inorganic materials 0.000 description 1
- 150000008045 alkali metal halides Chemical class 0.000 description 1
- 125000005037 alkyl phenyl group Chemical group 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 125000005577 anthracene group Chemical group 0.000 description 1
- 229940027991 antiseptic and disinfectant quinoline derivative Drugs 0.000 description 1
- 125000005264 aryl amine group Chemical group 0.000 description 1
- QVQLCTNNEUAWMS-UHFFFAOYSA-N barium oxide Inorganic materials [Ba]=O QVQLCTNNEUAWMS-UHFFFAOYSA-N 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229910052790 beryllium Inorganic materials 0.000 description 1
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- JRXXLCKWQFKACW-UHFFFAOYSA-N biphenylacetylene Chemical group C1=CC=CC=C1C#CC1=CC=CC=C1 JRXXLCKWQFKACW-UHFFFAOYSA-N 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Inorganic materials [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 150000001716 carbazoles Chemical class 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 125000002676 chrysenyl group Chemical group C1(=CC=CC=2C3=CC=C4C=CC=CC4=C3C=CC12)* 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004802 cyanophenyl group Chemical group 0.000 description 1
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 1
- 125000004188 dichlorophenyl group Chemical group 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000007772 electrode material Substances 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- OAYLNYINCPYISS-UHFFFAOYSA-N ethyl acetate;hexane Chemical compound CCCCCC.CCOC(C)=O OAYLNYINCPYISS-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000005281 excited state Effects 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- JVZRCNQLWOELDU-UHFFFAOYSA-N gamma-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=NC=C1 JVZRCNQLWOELDU-UHFFFAOYSA-N 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000005059 halophenyl group Chemical group 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 1
- 125000003824 heptacenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC5=CC6=CC7=CC=CC=C7C=C6C=C5C=C4C=C3C=C12)* 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- GNOIPBMMFNIUFM-UHFFFAOYSA-N hexamethylphosphoric triamide Chemical compound CN(C)P(=O)(N(C)C)N(C)C GNOIPBMMFNIUFM-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Inorganic materials [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 229910001623 magnesium bromide Inorganic materials 0.000 description 1
- QUZNVZUTDKEPBJ-UHFFFAOYSA-M magnesium;3h-pyridin-3-ide;bromide Chemical compound [Mg+2].[Br-].C1=C[C-]=CN=C1 QUZNVZUTDKEPBJ-UHFFFAOYSA-M 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 1
- JWTJIFMXLBCLPV-UHFFFAOYSA-N n,9,9-triphenylfluoren-2-amine Chemical compound C=1C=C2C3=CC=CC=C3C(C=3C=CC=CC=3)(C=3C=CC=CC=3)C2=CC=1NC1=CC=CC=C1 JWTJIFMXLBCLPV-UHFFFAOYSA-N 0.000 description 1
- 125000005029 naphthylthio group Chemical group C1(=CC=CC2=CC=CC=C12)S* 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- QGLKJKCYBOYXKC-UHFFFAOYSA-N nonaoxidotritungsten Chemical compound O=[W]1(=O)O[W](=O)(=O)O[W](=O)(=O)O1 QGLKJKCYBOYXKC-UHFFFAOYSA-N 0.000 description 1
- 125000003261 o-tolyl group Chemical group [H]C1=C([H])C(*)=C(C([H])=C1[H])C([H])([H])[H] 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000004866 oxadiazoles Chemical class 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 125000003933 pentacenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C12)* 0.000 description 1
- JQQSUOJIMKJQHS-UHFFFAOYSA-N pentaphenyl group Chemical group C1=CC=CC2=CC3=CC=C4C=C5C=CC=CC5=CC4=C3C=C12 JQQSUOJIMKJQHS-UHFFFAOYSA-N 0.000 description 1
- 125000004115 pentoxy group Chemical group [*]OC([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- 150000005041 phenanthrolines Chemical class 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 150000003248 quinolines Chemical class 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 229940042055 systemic antimycotics triazole derivative Drugs 0.000 description 1
- UGNWTBMOAKPKBL-UHFFFAOYSA-N tetrachloro-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(Cl)=C(Cl)C1=O UGNWTBMOAKPKBL-UHFFFAOYSA-N 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 1
- 229910001887 tin oxide Inorganic materials 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- 229910001930 tungsten oxide Inorganic materials 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
- C07C211/56—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings the carbon skeleton being further substituted by halogen atoms or by nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/57—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton
- C07C211/58—Naphthylamines; N-substituted derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/57—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton
- C07C211/61—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings being part of condensed ring systems of the carbon skeleton with at least one of the condensed ring systems formed by three or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/58—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/36—Radicals substituted by singly-bound nitrogen atoms
- C07D213/38—Radicals substituted by singly-bound nitrogen atoms having only hydrogen or hydrocarbon radicals attached to the substituent nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/76—Dibenzothiophenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/06—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members
- C07C2603/10—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings
- C07C2603/12—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings only one five-membered ring
- C07C2603/18—Fluorenes; Hydrogenated fluorenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/40—Ortho- or ortho- and peri-condensed systems containing four condensed rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/93—Spiro compounds
- C07C2603/94—Spiro compounds containing "free" spiro atoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
| 정공수송 재료 | 구동전압 (V) |
전류밀도 (㎃/㎠) |
휘도 (cd/㎡) |
효율 (cd/A) |
발광색 | 반감수명 (hr @100㎃/㎠) | |
| 실시예 1 | 화합물 1 | 6.63 | 50 | 2,540 | 5.08 | 청색 | 314hr |
| 실시예 2 | 화합물 6 | 6.77 | 50 | 2,225 | 4.45 | 청색 | 292hr |
| 실시예 3 | 화합물 13 | 7.05 | 50 | 2,264 | 4.52 | 청색 | 326hr |
| 실시예 4 | 화합물 40 | 6.96 | 50 | 2,461 | 4.92 | 청색 | 347hr |
| 실시예 5 | 화합물 53 | 6.72 | 50 | 2,580 | 5.16 | 청색 | 312hr |
| 실시예 6 | 화합물 77 | 6.58 | 50 | 2,495 | 4.99 | 청색 | 226hr |
| 실시예 7 | 화합물 80 | 6.39 | 50 | 2,339 | 4.67 | 청색 | 297hr |
| 실시예 8 | 화합물 87 | 6.55 | 50 | 2,695 | 5.39 | 청색 | 332hr |
| 비교예 1 | NPB | 7.35 | 50 | 2,065 | 4.13 | 청색 | 145hr |
| 비교예 2 | 비교화합물 | 6.99 | 50 | 2,022 | 4.04 | 청색 | 308 hr |
Claims (20)
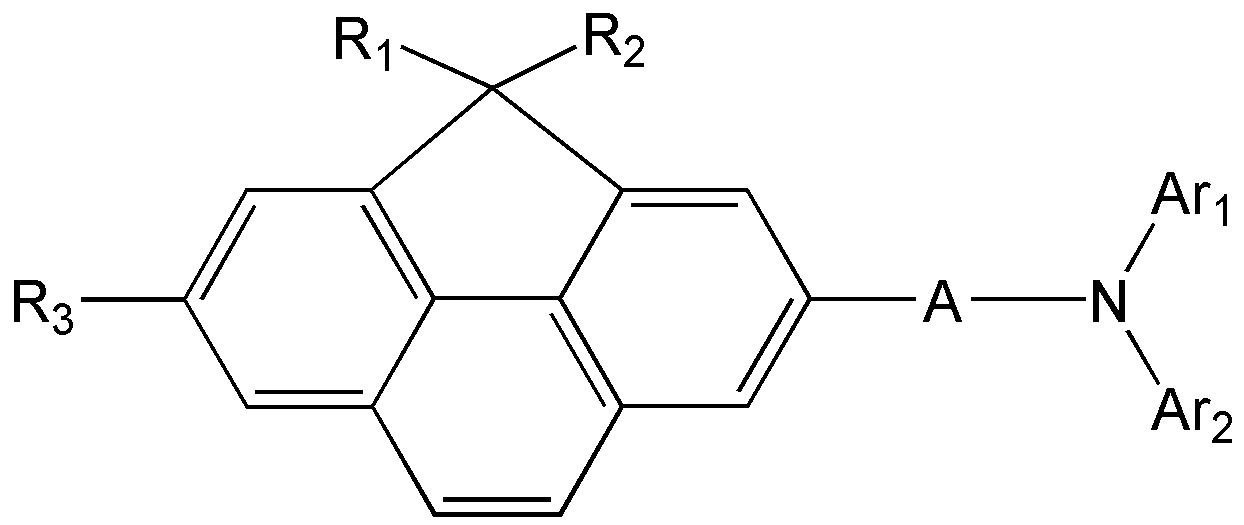
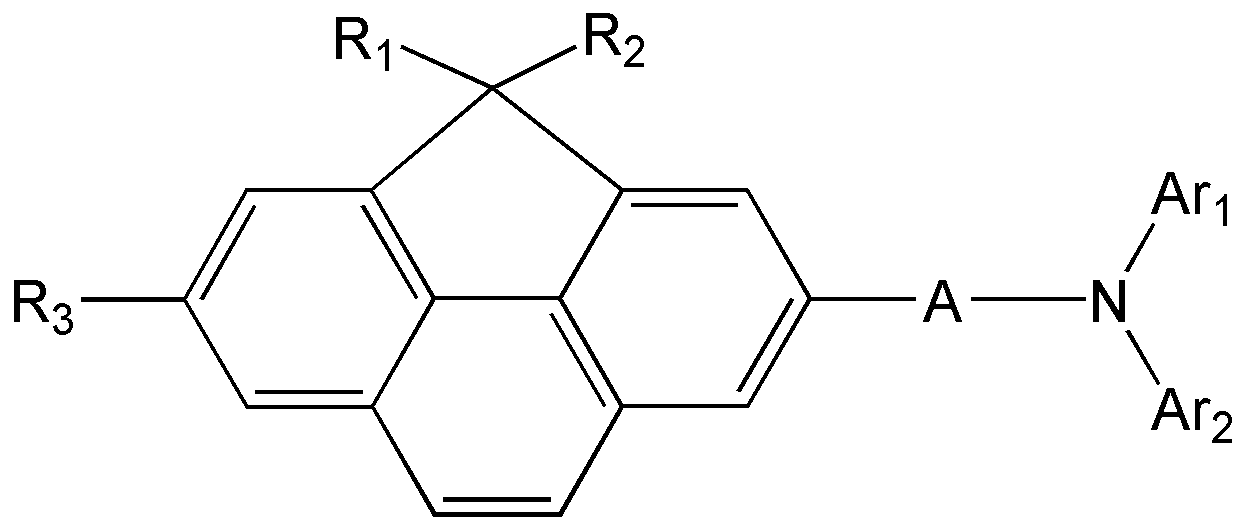
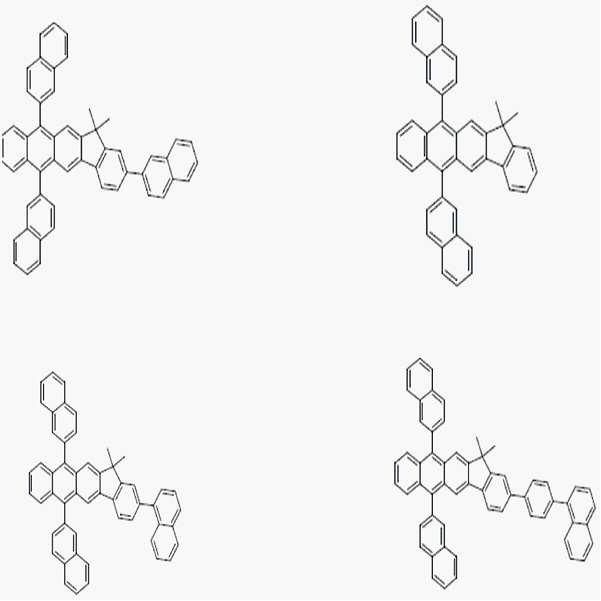
- 하기 화학식 1로 표시되는 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물:
<화학식 1>
상기 식 중, R1 및 R2 는 각각 독립적으로 할로겐기, 시아노기, 치환 또는 비치환된 탄소수 1 내지 30의 알킬기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴기, 치환 또는 비치환된 탄소수 3 내지 30의 헤테로아릴기, 또는 치환 또는 비치환된 탄소수 6 내지 30의 축합다환기를 나타내고, 선택적으로 R1 및 R2는 연결되어 고리를 형성할 수 있으며,
R3은 수소, 중수소, 할로겐기, 시아노기, 치환 또는 비치환된 탄소수 5 내지 30의 아릴기, 치환 또는 비치환된 탄소수 3 내지 30의 헤테로아릴기, 또는 치환 또는 비치환된 탄소수 6 내지 30의 축합다환기를 나타내고,
A는 비치환된 탄소수 6 내지 10의 아릴렌기, 비치환된 탄소수 2 내지 11의 헤테로아릴렌기, 또는 상기 아릴렌기 및/또는 상기 헤테로아릴렌기가 2 이상 연결된 연결기이고,
Ar1 및 Ar2는 각각 독립적으로 치환 또는 비치환된 탄소수 5 내지 30의 아릴기, 치환 또는 비치환된 탄소수 3 내지 30의 헤테로아릴기, 또는 치환 또는 비치환된 탄소수 6 내지 30의 축합다환기를 나타내며,
상기 치환된 알킬기, 치환된 아릴기, 치환된 헤테로아릴기 및 치환된 축합다환기의 하나 이상의 수소는 중수소 원자, 할로겐 원자, 히드록시기, 니트로기, 시아노기, 드라진, 히드라존, 카르복실기나 그의 염, 술폰산기나 그의 염, 인산이나 그의 염, 또는 탄소수 1 내지 10의 알킬기, 탄소수 1 내지 10의 알콕시기, 탄소수 2 내지 10의 알케닐기, 탄소수 2 내지 10의 알키닐기, 탄소수 6 내지 16의 아릴기, 또는 탄소수 4 내지 16의 헤테로아릴기로 치환될 수 있다. - 삭제
- 제 1 항에 있어서,
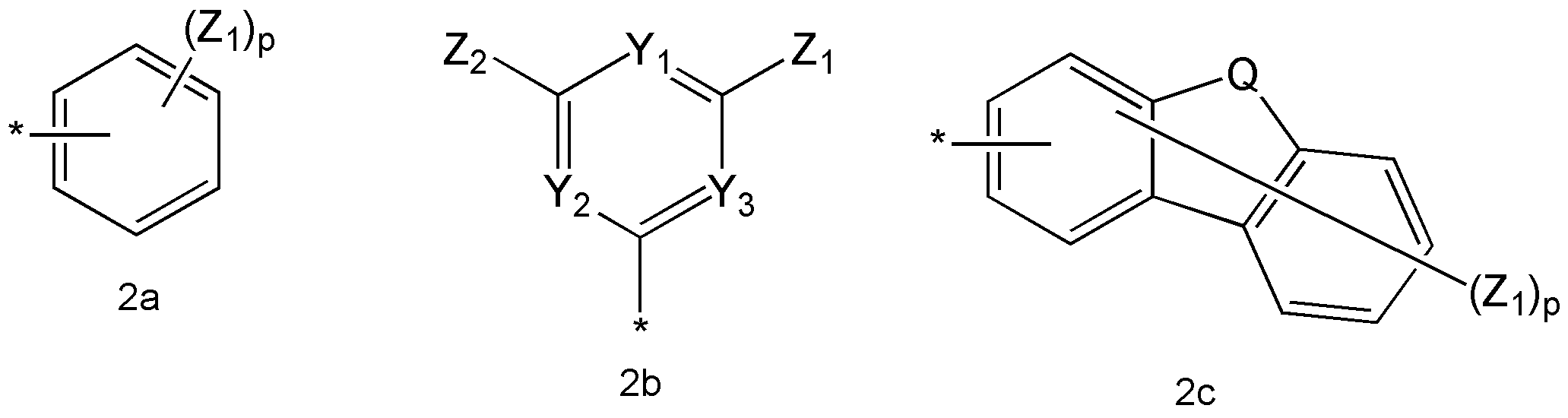
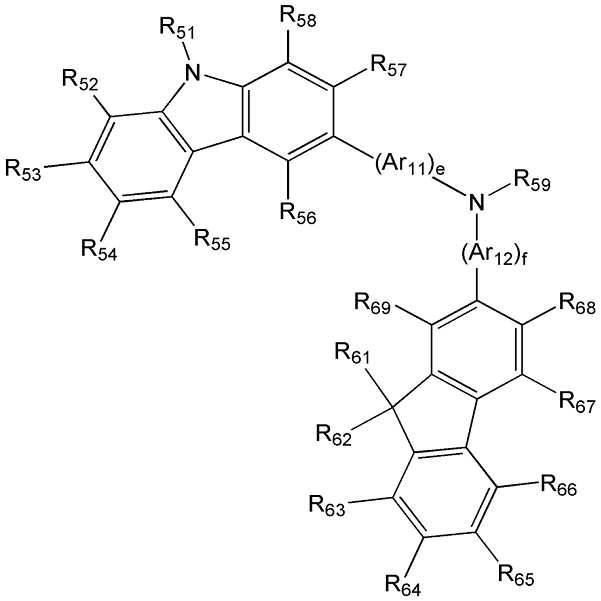
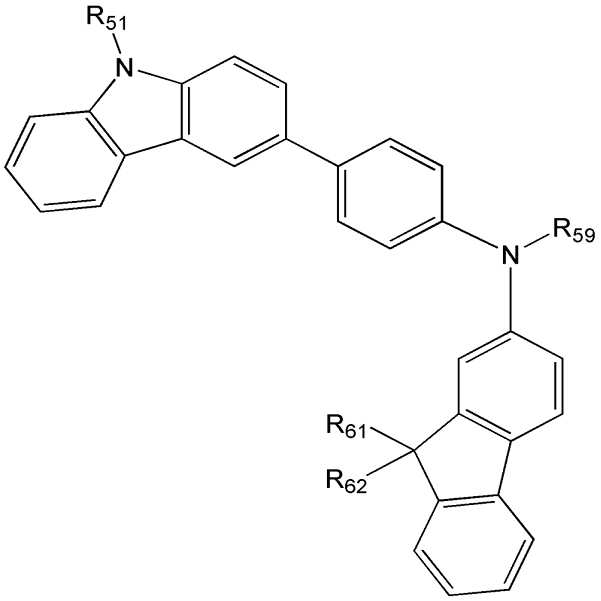
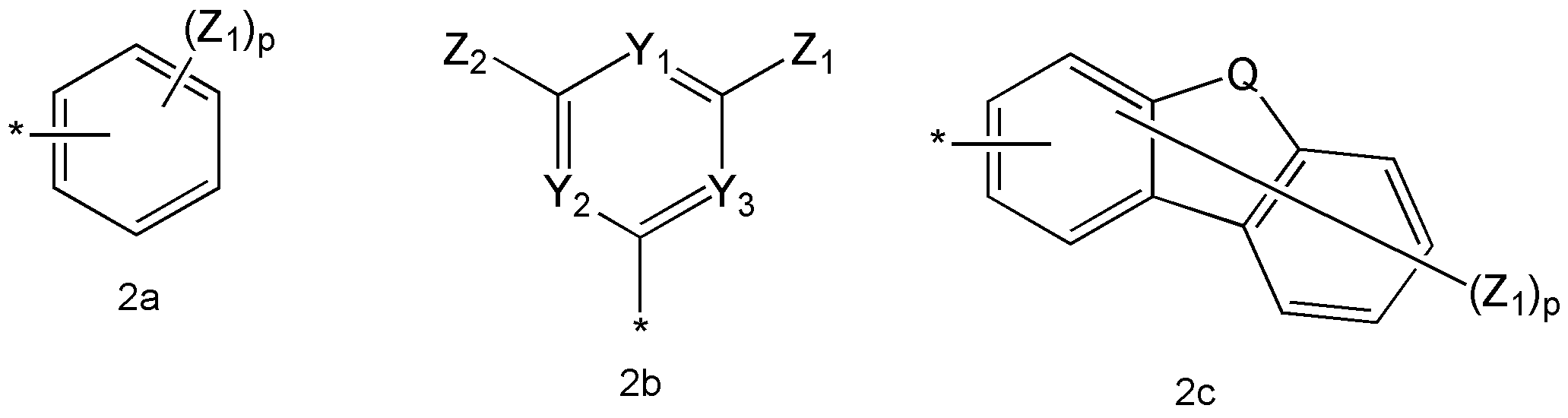
상기 화학식 1 식 중, R1 및 R2 는 각각 독립적으로 수소, 중수소, 할로겐기, 시아노기, 탄소수 탄소수 1 내지 20의 알킬기 또는 하기 화학식 2a 내지 2c 중 어느 하나인 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물:
상기 화학식 2a 내지 2c 중,
Y1, Y2 및 Y3는 각각 독립적으로, -N=, -N(R20)- 또는 -C(R21)=로 표시되는 연결기들이고;
Q는 -C(R30)(R31)-, -N(R32)-, -S- 또는 -O-로 표시되는 연결기들이고;
Z1, Z2, R20, R21, R30, R31 및 R32는 서로 독립적으로, 수소 원자, 중수소, 탄소수 1 내지 20의 알킬기, 탄소수 5 내지 20의 아릴기, 탄소수 3 내지 20의 헤테로아릴기, 탄소수 6 내지 20의 축합 다환기, 할로겐기, 시아노기, 니트로기, 하이드록시기 또는 카르복시기이고;
p는 1 내지 7의 정수이고;
*는 결합을 나타낸다. - 제 1 항에 있어서,
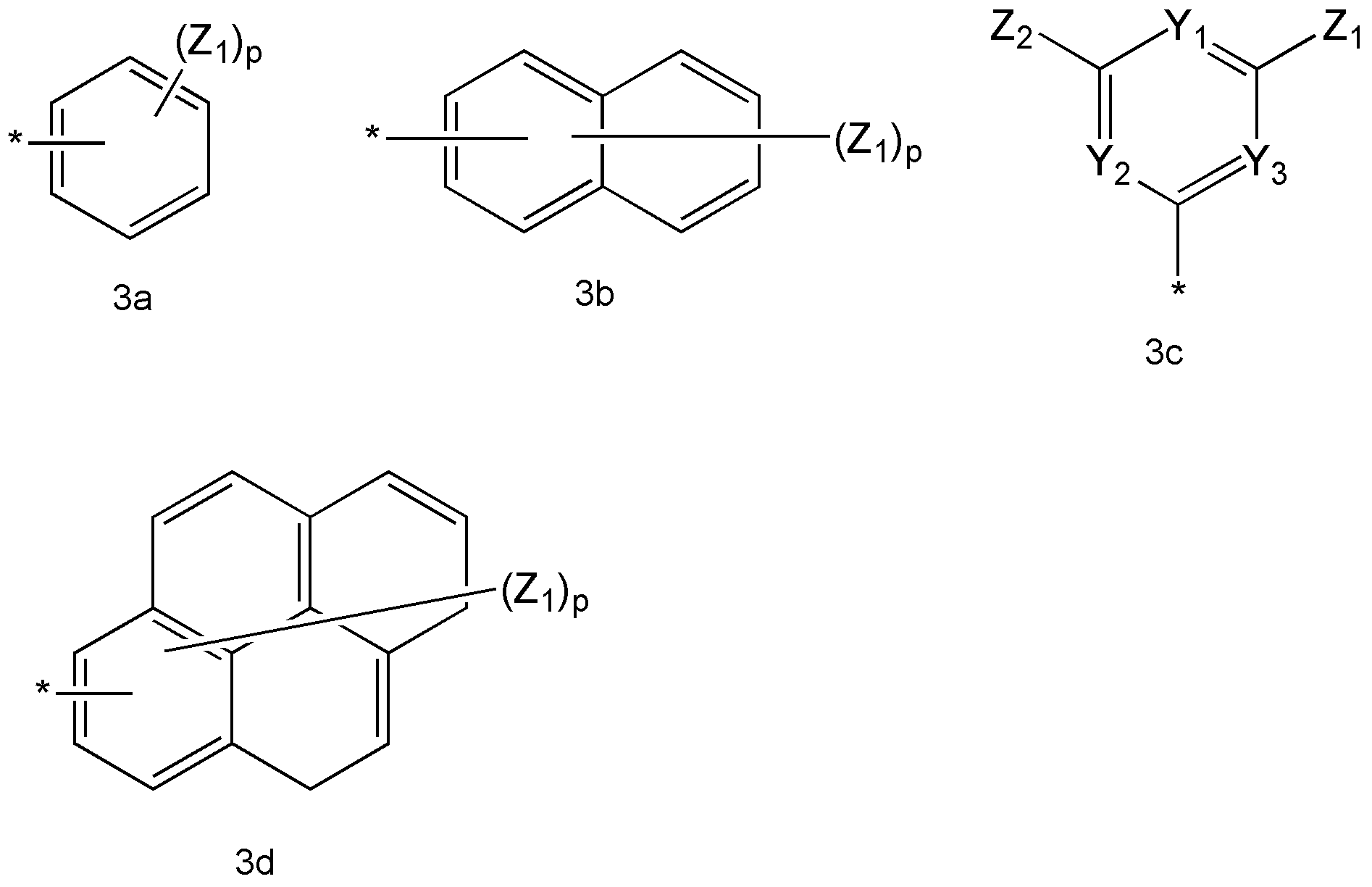
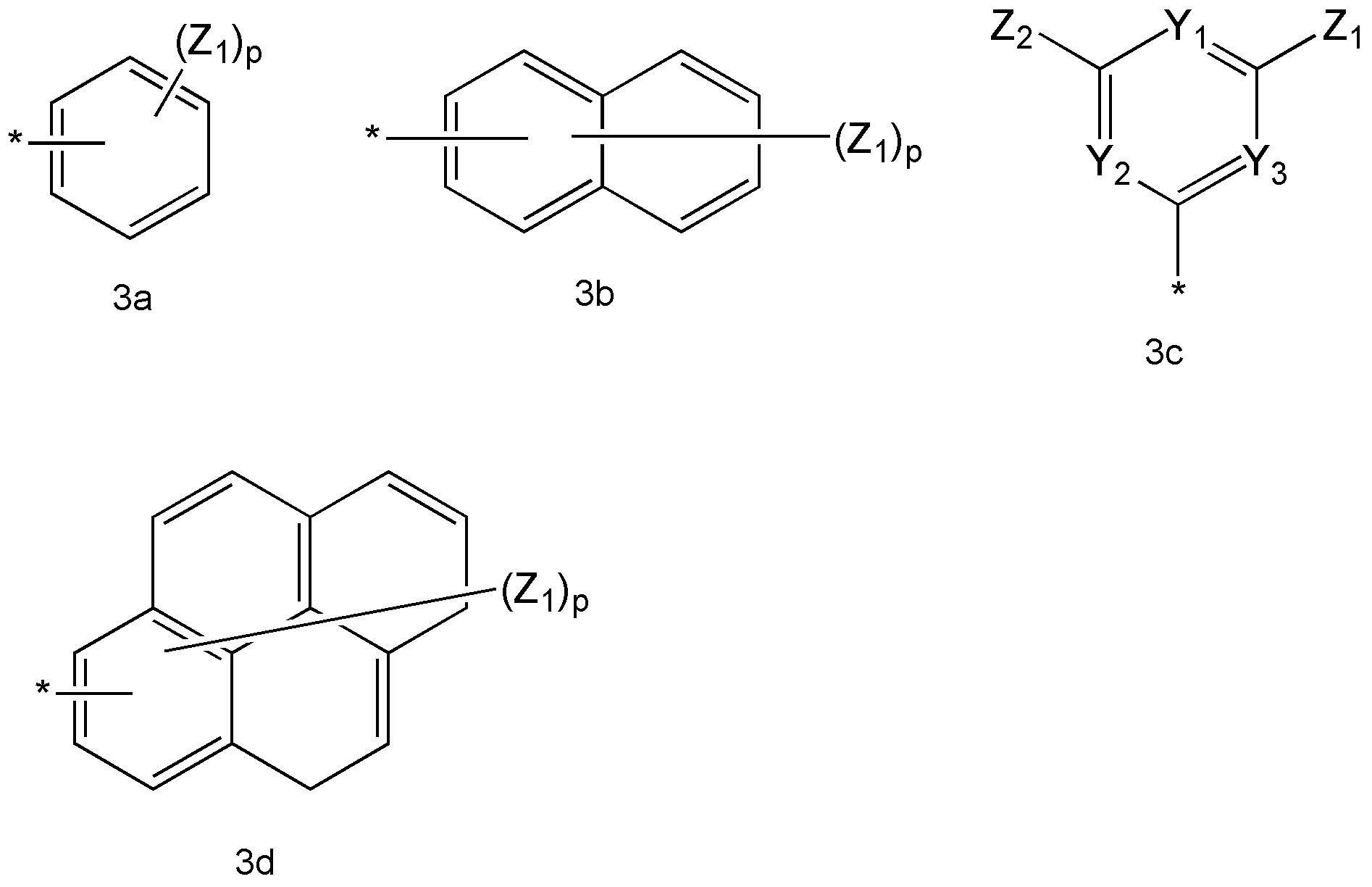
상기 화학식 1 식 중, R3은 수소, 중수소, 할로겐기, 또는 화학식 3a 내지 3d 중 하나 이상인 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물:
상기 화학식 3a 내지 3d 중,
Y1, Y2 및 Y3는 각각 독립적으로, -N=, -N(R20)- 또는 -C(R21)=로 표시되는 연결기들이고;
Z1, Z2, R20 및 R21은 서로 독립적으로, 수소 원자, 중수소, 탄소수 1 내지 20의 알킬기, 탄소수 5 내지 20의 아릴기, 탄소수 3 내지 20의 헤테로아릴기, 탄소수 6 내지 20의 축합 다환기, 할로겐기, 시아노기, 니트로기, 하이드록시기 또는 카르복시기이고;
p는 1 내지 9의 정수이고;
*는 결합을 나타낸다. - 제 1 항에 있어서,
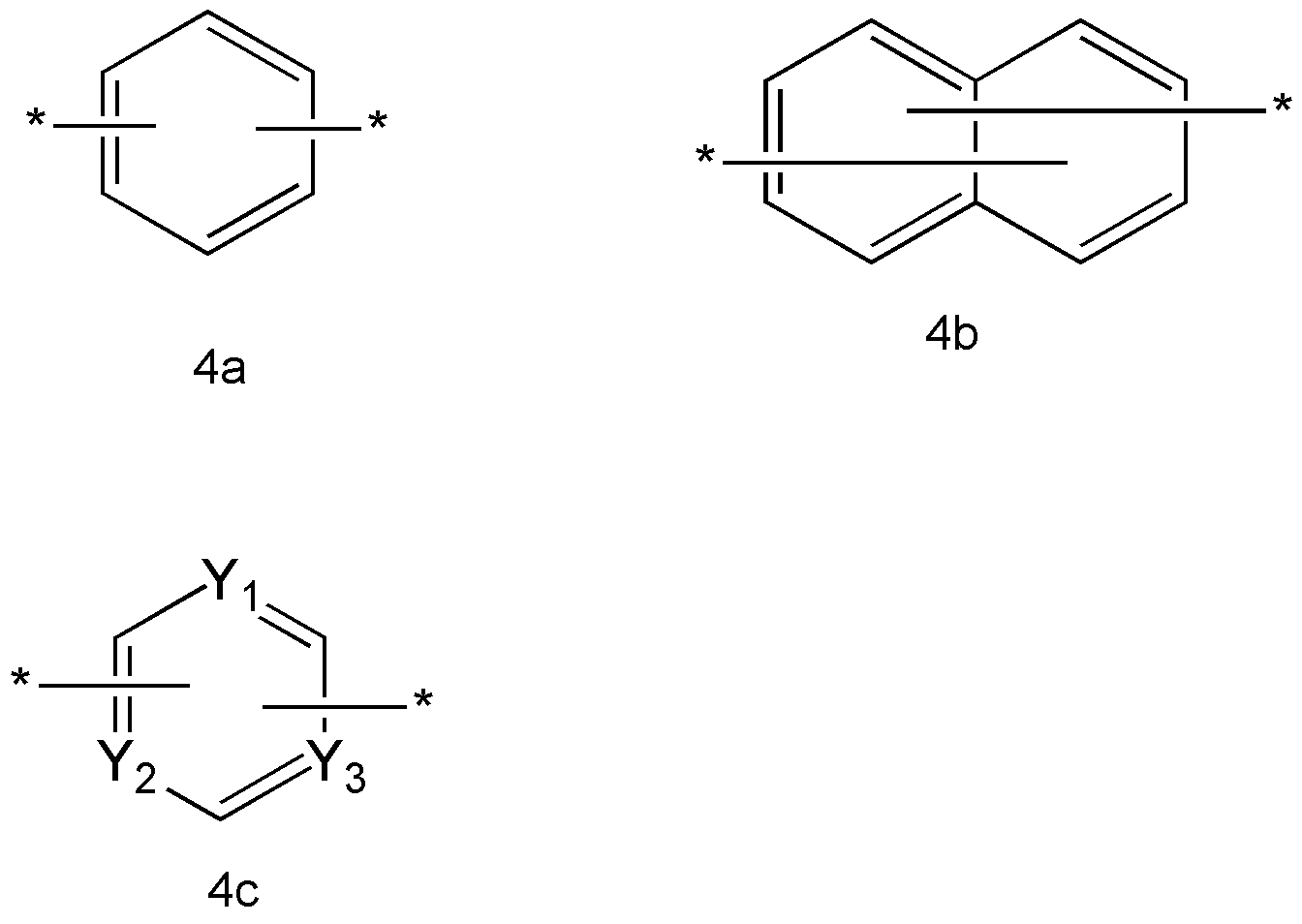
상기 화학식 1 식 중, A는 화학식 4a 내지 화학식 4c 중 어느 하나, 또는 화학식 4a 내지 4c 중 하나 이상이 서로 연결된 연결기인 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물:
상기 화학식 4a 내지 4c 중,
Y1, Y2 및 Y3는 각각 독립적으로, -N= 또는 -C(R21)=로 표시되는 연결기들이고;
R21은 수소 원자, 중수소, 탄소수 1 내지 20의 알킬기, 탄소수 5 내지 20의 아릴기, 탄소수 3 내지 20의 헤테로아릴기, 탄소수 6 내지 20의 축합 다환기, 할로겐기, 시아노기, 니트로기, 하이드록시기 또는 카르복시기를 나타낸다. - 제 1 항에 있어서,
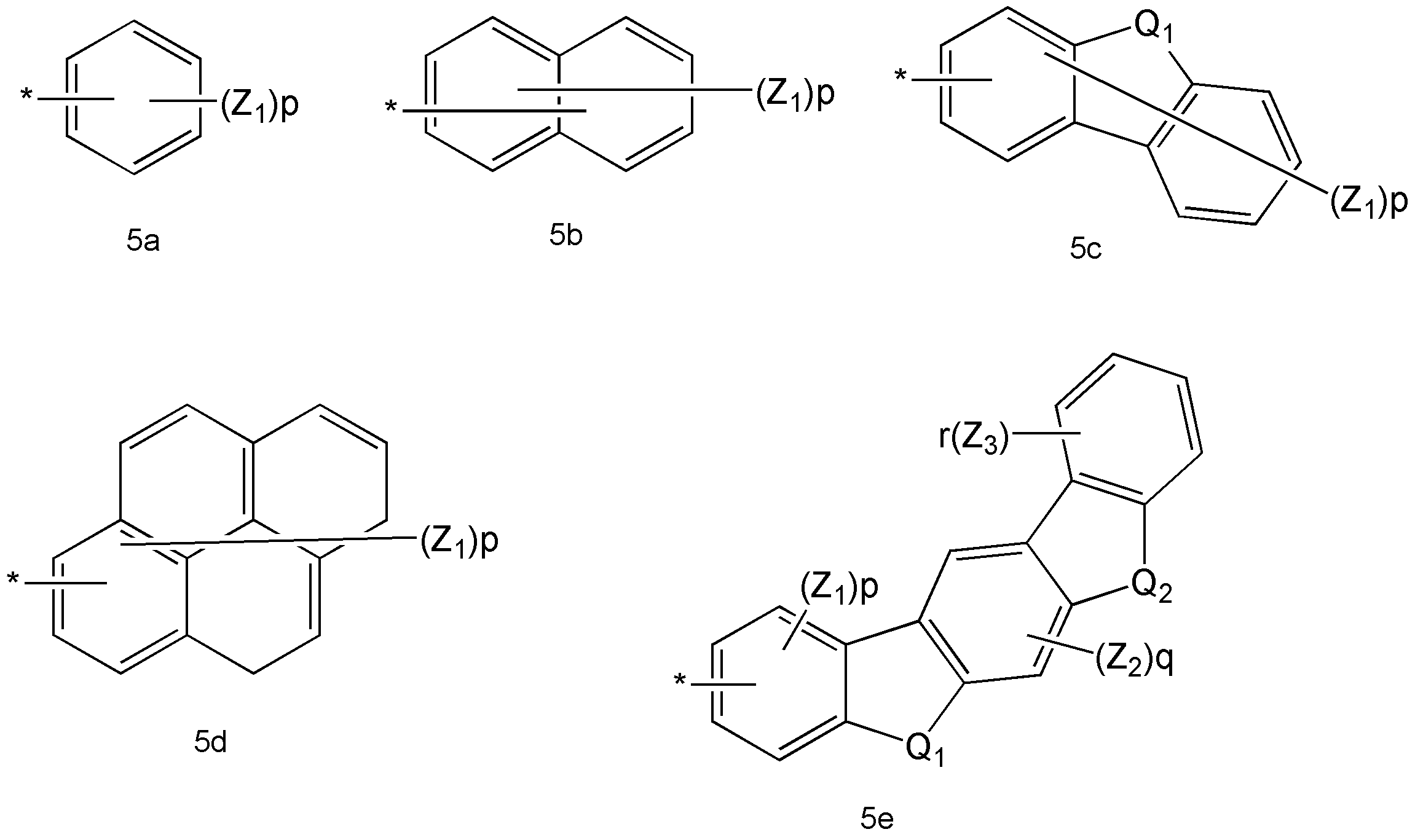
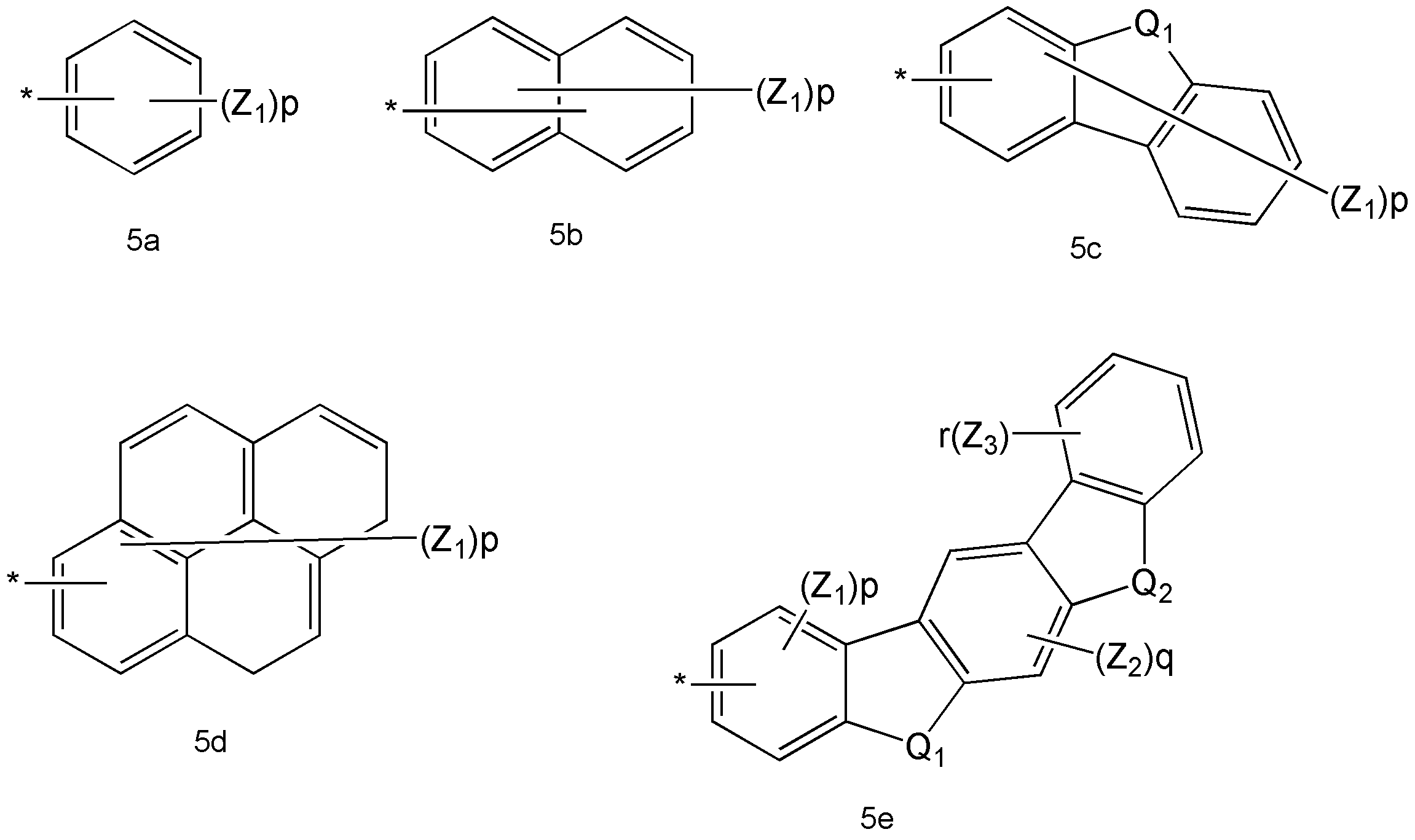
상기 화학식 1 식 중, Ar1 및 Ar2는 화학식 5a 내지 5e 중 어느 하나인 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물:
상기 화학식 5a 내지 5e 중,
Q1 및 Q2는 각각 독립적으로 -C(R30)(R31)-, -N(R32)-, -S- 또는 -O-로 표시되는 연결기들이고;
Z1, Z2, Z3, R30, R31 및 R32는 서로 독립적으로, 수소 원자, 중수소, 탄소수 1 내지 20의 알킬기, 탄소수 5 내지 20의 아릴기, 탄소수 3 내지 20의 헤테로아릴기, 탄소수 6 내지 20의 축합 다환기, 할로겐기, 시아노기, 니트로기, 하이드록시기 또는 카르복시기이고;
p는 1 내지 9의 정수이고;
q는 1 또는 2이고;
r은 1 내지 4의 정수이고;
*는 결합을 나타낸다. - 삭제
- 제 1 전극;
제 2 전극; 및
상기 제 1 전극 및 제 2 전극 사이에 개재된 유기층을 구비한 유기 발광 소자로서,
상기 유기층이 제 1 항, 제 3 항 내지 제 6 항 및 제 8 항 중 어느 한 항의 화합물을 포함하는 유기 발광 소자. - 제 9 항에 있어서,
상기 유기층이 정공 주입층, 정공 수송층, 또는 정공 주입 및 정공 수송기능을 동시에 갖는 기능층인 유기 발광 소자. - 제 9 항에 있어서,
상기 유기층이 정공 수송층 또는 정공 주입층인 유기 발광 소자. - 제 9 항에 있어서,
상기 유기 발광 소자가 발광층, 정공 주입층, 정공 수송층, 또는 정공 주입 및 정공 수송기능을 동시에 갖는 기능층을 포함하고,
상기 정공 주입층, 정공 수송층, 또는 정공 주입 및 정공 수송기능을 동시에 갖는 기능층은 제 1 항의 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물을 포함하며,
상기 발광층은 안트라센계 화합물, 아릴아민계 화합물 또는 스티릴계 화합물을 포함하는 유기 발광 소자. - 제 9 항에 있어서,
상기 유기 발광 소자가 발광층, 정공 주입층, 정공 수송층, 또는 정공 주입 및 정공 수송기능을 동시에 갖는 기능층을 포함하고,
상기 정공 주입층, 정공 수송층, 또는 정공 주입 및 정공 수송기능을 동시에 갖는 기능층은 제 1 항의 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물을 포함하며,
상기 발광층의 적색층, 녹색층, 청색층 또는 흰색층의 어느 한 층은 인광 화합물을 포함하는 유기 발광 소자. - 제 13 항에 있어서,
상기 정공 주입층, 정공 수송층, 또는 정공 주입 기능 및 정공 수송 기능을 동시에 갖는 기능층이 전하 생성 물질을 포함하는 유기 발광 소자. - 제 14 항에 있어서,
상기 전하 생성 물질이 p-도펀트이고, 상기 p-도펀트가 퀴논 유도체, 금속 산화물 및 시아노기-함유 화합물인 유기 발광 소자. - 제 9 항에 있어서,
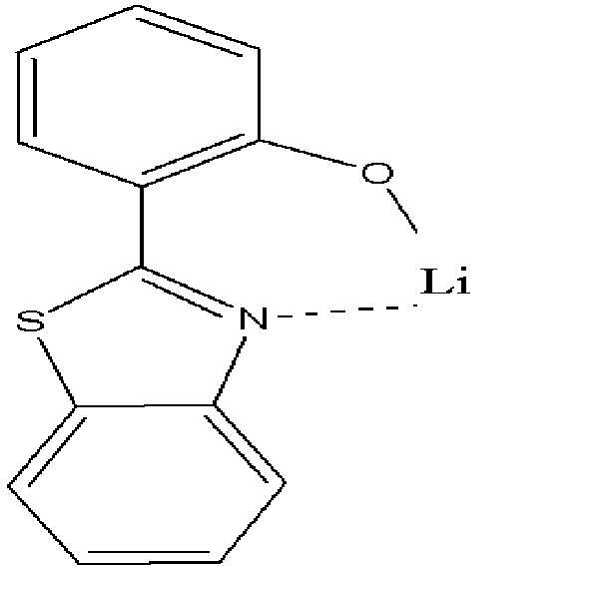
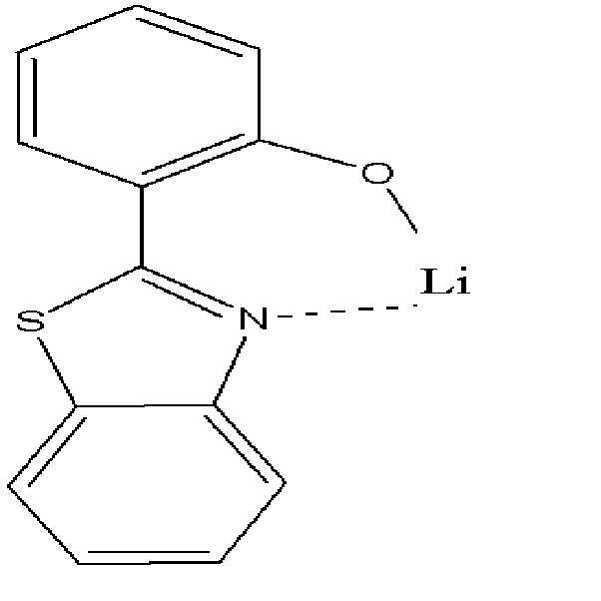
상기 유기층이 전자 수송층을 포함하고, 상기 전자 수송층이 전자 수송성 유기 화합물 및 금속 착체를 포함하는 유기 발광 소자. - 제 16 항에 있어서,
상기 금속 착체가 Li 착제인 유기 발광 소자. - 제 9 항에 있어서,
상기 유기층이 상기 정공 주입 능력 및/또는 정공 수송 능력을 가지는 화합물을 사용하여 습식 공정으로 형성되는 유기 발광 소자. - 제 9 항의 유기 발광 소자를 구비하고, 상기 유기 발광 소자의 제 1 전극이 박막 트랜지스터의 소스 전극 또는 드레인 전극과 전기적으로 연결된 평판 표시 장치.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120062860A KR102079249B1 (ko) | 2012-06-12 | 2012-06-12 | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 |
| US13/675,973 US9371270B2 (en) | 2012-06-12 | 2012-11-13 | Compound for organic light-emitting device and organic light-emitting device including the same |
| TW102103240A TW201350462A (zh) | 2012-06-12 | 2013-01-29 | 用於有機發光裝置之化合物以及包含其之有機發光裝置 |
| CN201310053295.4A CN103483208A (zh) | 2012-06-12 | 2013-02-19 | 用于有机发光装置的化合物和包含该化合物的有机发光装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120062860A KR102079249B1 (ko) | 2012-06-12 | 2012-06-12 | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20130139105A KR20130139105A (ko) | 2013-12-20 |
| KR102079249B1 true KR102079249B1 (ko) | 2020-02-20 |
Family
ID=49714546
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120062860A Active KR102079249B1 (ko) | 2012-06-12 | 2012-06-12 | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9371270B2 (ko) |
| KR (1) | KR102079249B1 (ko) |
| CN (1) | CN103483208A (ko) |
| TW (1) | TW201350462A (ko) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102357439B1 (ko) | 2012-02-14 | 2022-02-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 스피로비플루오렌 화합물 |
| KR101475118B1 (ko) * | 2012-09-26 | 2014-12-22 | 엘지디스플레이 주식회사 | 유기전계발광소자 및 그 제조방법 |
| KR20140096662A (ko) * | 2013-01-28 | 2014-08-06 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| KR102038969B1 (ko) * | 2013-04-12 | 2019-11-01 | 삼성디스플레이 주식회사 | 유기 화합물 및 이를 포함하는 유기 발광 장치 |
| KR101476231B1 (ko) * | 2013-10-02 | 2014-12-24 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102177212B1 (ko) * | 2013-12-11 | 2020-11-11 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| WO2015108325A1 (ko) * | 2014-01-16 | 2015-07-23 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR101680093B1 (ko) | 2014-01-16 | 2016-11-28 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102278600B1 (ko) * | 2014-03-06 | 2021-07-19 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| KR102253440B1 (ko) * | 2014-06-02 | 2021-05-20 | 삼성디스플레이 주식회사 | 아민계 화합물 및 이를 포함한 유기 발광 소자 |
| KR102388727B1 (ko) * | 2015-03-30 | 2022-04-21 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 유기 발광 소자 |
| JP6804201B2 (ja) * | 2015-06-17 | 2020-12-23 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | モノアミン誘導体、及び有機電界発光素子 |
| KR102560940B1 (ko) | 2015-06-17 | 2023-08-01 | 삼성디스플레이 주식회사 | 모노 아민 유도체 및 이를 포함하는 유기 전계 발광 소자 |
| KR102675680B1 (ko) * | 2015-12-15 | 2024-06-18 | 삼성디스플레이 주식회사 | 아민 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102620119B1 (ko) * | 2016-02-15 | 2024-01-03 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102573815B1 (ko) * | 2016-05-09 | 2023-09-04 | 삼성디스플레이 주식회사 | 다환 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| CN108117508A (zh) * | 2016-11-30 | 2018-06-05 | 北京鼎材科技有限公司 | 螺芴环化合物、其应用及采用其的空穴传输材料和有机电致发光器件 |
| KR102032955B1 (ko) | 2017-06-07 | 2019-10-16 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR102559469B1 (ko) * | 2017-07-07 | 2023-07-25 | 주식회사 동진쎄미켐 | 신규 화합물 및 이를 포함하는 유기 발광 소자 |
| US11778909B2 (en) | 2018-05-03 | 2023-10-03 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| CN111384273B (zh) * | 2018-12-29 | 2021-07-16 | Tcl科技集团股份有限公司 | 一种量子点发光二极管及其制备方法 |
| KR102853323B1 (ko) | 2020-06-19 | 2025-09-01 | 삼성디스플레이 주식회사 | 발광 소자, 이의 제조 방법 및 이를 포함한 전자 장치 |
| KR20220037808A (ko) | 2020-09-18 | 2022-03-25 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| CN112341343B (zh) * | 2020-11-04 | 2023-04-25 | 陕西莱特光电材料股份有限公司 | 一种有机化合物及包含其的电子元件和电子装置 |
| CN114075117B (zh) * | 2021-06-04 | 2023-07-21 | 陕西莱特迈思光电材料有限公司 | 一种有机化合物以及使用其的电子元件和电子装置 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101990553B1 (ko) * | 2012-04-17 | 2019-06-19 | 삼성디스플레이 주식회사 | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4356429A (en) | 1980-07-17 | 1982-10-26 | Eastman Kodak Company | Organic electroluminescent cell |
| US4885211A (en) | 1987-02-11 | 1989-12-05 | Eastman Kodak Company | Electroluminescent device with improved cathode |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| DE69511755T2 (de) | 1994-04-26 | 2000-01-13 | Tdk Corp | Phenylanthracenderivat und organisches EL-Element |
| JP3816969B2 (ja) | 1994-04-26 | 2006-08-30 | Tdk株式会社 | 有機el素子 |
| JP3588978B2 (ja) | 1997-06-12 | 2004-11-17 | 凸版印刷株式会社 | 有機薄膜el素子 |
| JPH11135261A (ja) | 1997-10-27 | 1999-05-21 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料およびそれを使用した有機エレクトロルミネッセンス素子 |
| US5972247A (en) | 1998-03-20 | 1999-10-26 | Eastman Kodak Company | Organic electroluminescent elements for stable blue electroluminescent devices |
| JP2000003782A (ja) | 1998-06-12 | 2000-01-07 | Casio Comput Co Ltd | 電界発光素子 |
| EP1009043A3 (en) | 1998-12-09 | 2002-07-03 | Eastman Kodak Company | Electroluminescent device with polyphenyl hydrocarbon hole transport layer |
| US6465115B2 (en) | 1998-12-09 | 2002-10-15 | Eastman Kodak Company | Electroluminescent device with anthracene derivatives hole transport layer |
| US6355756B1 (en) | 1999-05-18 | 2002-03-12 | International Business Machines Corporation | Dual purpose electroactive copolymers, preparation thereof, and use in opto-electronic devices |
| KR100560778B1 (ko) * | 2003-04-17 | 2006-03-13 | 삼성에스디아이 주식회사 | 유기 전계 발광 디스플레이 장치 |
| KR100773522B1 (ko) | 2003-10-02 | 2007-11-07 | 삼성에스디아이 주식회사 | 사이클로펜타페난트렌계 화합물 및 이를 이용한 유기 전계발광 소자 |
| US7554121B2 (en) * | 2003-12-26 | 2009-06-30 | Semiconductor Energy Laboratory Co., Ltd. | Organic semiconductor device |
| KR100718104B1 (ko) | 2004-01-15 | 2007-05-14 | 삼성에스디아이 주식회사 | 스피로사이클로펜타페난트렌플루오렌계 화합물 및 이를이용한 유기 전계 발광 소자 |
| KR101338253B1 (ko) | 2006-06-15 | 2013-12-09 | 삼성디스플레이 주식회사 | 사이클로펜타페난트렌계 화합물 및 이를 이용한 유기 전계발광 소자 |
| JP5221061B2 (ja) * | 2006-06-15 | 2013-06-26 | 三星ディスプレイ株式會社 | シクロペンタフェナントレン系化合物及びそれを利用した有機電界発光素子 |
| KR101321500B1 (ko) | 2006-09-29 | 2013-10-30 | 삼성디스플레이 주식회사 | 유기 전계 발광 화합물 및 이를 이용한 유기 전계 발광소자 |
| KR101359630B1 (ko) | 2006-10-23 | 2014-02-10 | 삼성디스플레이 주식회사 | 유기 전계 발광 화합물 및 이를 이용한 유기 전계 발광소자 |
| KR101328974B1 (ko) | 2006-10-31 | 2013-11-13 | 삼성디스플레이 주식회사 | 유기 전계 발광 화합물 및 이를 이용한 유기 전계 발광소자 |
| KR100867134B1 (ko) | 2007-02-26 | 2008-11-06 | 부산대학교 산학협력단 | 발광 물질 및 이를 이용한 전기 발광 소자 |
| KR101453873B1 (ko) * | 2007-10-08 | 2014-10-24 | 삼성디스플레이 주식회사 | 사이클로펜타페난트렌계 화합물 및 이를 이용한 유기 발광소자 |
| KR100964223B1 (ko) * | 2008-02-11 | 2010-06-17 | 삼성모바일디스플레이주식회사 | 유기 발광 소자 및 이를 구비한 평판 표시 장치 |
| KR102129241B1 (ko) * | 2008-05-16 | 2020-07-02 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 트리아릴아민 유도체, 발광 물질, 발광 소자, 발광 장치 및 전자 기기 |
| KR100967801B1 (ko) | 2008-08-29 | 2010-07-05 | 부산대학교 산학협력단 | 4H―사이클로펜타[def]페난트렌의 골격을 갖는 공중합체 및 이를 포함하는 유기 고분자 박막 태양 전지 소자 |
| KR101328978B1 (ko) * | 2010-10-26 | 2013-11-13 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
-
2012
- 2012-06-12 KR KR1020120062860A patent/KR102079249B1/ko active Active
- 2012-11-13 US US13/675,973 patent/US9371270B2/en active Active
-
2013
- 2013-01-29 TW TW102103240A patent/TW201350462A/zh unknown
- 2013-02-19 CN CN201310053295.4A patent/CN103483208A/zh active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101990553B1 (ko) * | 2012-04-17 | 2019-06-19 | 삼성디스플레이 주식회사 | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| TW201350462A (zh) | 2013-12-16 |
| US9371270B2 (en) | 2016-06-21 |
| CN103483208A (zh) | 2014-01-01 |
| KR20130139105A (ko) | 2013-12-20 |
| US20130328021A1 (en) | 2013-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102079249B1 (ko) | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 | |
| KR101990553B1 (ko) | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102096047B1 (ko) | 신규 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102117610B1 (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102059939B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102191994B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102098736B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20150106501A (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102203102B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20150025259A (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102086546B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102102350B1 (ko) | 아릴아민 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20140058755A (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20140063300A (ko) | 유기 발광 소자 | |
| KR101952707B1 (ko) | 신규한 화합물 및 이를 포함한 유기발광 소자 | |
| KR102159148B1 (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102040871B1 (ko) | 신규한 유기 발광 소자용 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102120891B1 (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102098740B1 (ko) | 전자 주입 능력 및/또는 전자 수송 능력을 가지는 신규한 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102232690B1 (ko) | 신규 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20140096662A (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102044866B1 (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20140055140A (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR102177212B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20150022288A (ko) | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20120612 |
|
| N231 | Notification of change of applicant | ||
| PN2301 | Change of applicant |
Patent event date: 20120725 Comment text: Notification of Change of Applicant Patent event code: PN23011R01D |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20170612 Comment text: Request for Examination of Application Patent event code: PA02011R01I Patent event date: 20120612 Comment text: Patent Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20190321 Patent event code: PE09021S01D |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20190916 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20191121 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20200213 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20200214 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| PR1001 | Payment of annual fee |
Payment date: 20230125 Start annual number: 4 End annual number: 4 |
|
| PR1001 | Payment of annual fee |
Payment date: 20240125 Start annual number: 5 End annual number: 5 |
|
| PR1001 | Payment of annual fee |
Payment date: 20250122 Start annual number: 6 End annual number: 6 |