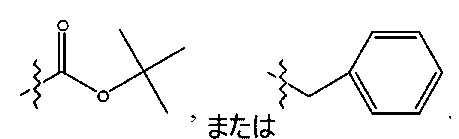JP7246309B2 - 免疫応答を調節するためのオキサビシクロヘプタン - Google Patents
免疫応答を調節するためのオキサビシクロヘプタン Download PDFInfo
- Publication number
- JP7246309B2 JP7246309B2 JP2019530702A JP2019530702A JP7246309B2 JP 7246309 B2 JP7246309 B2 JP 7246309B2 JP 2019530702 A JP2019530702 A JP 2019530702A JP 2019530702 A JP2019530702 A JP 2019530702A JP 7246309 B2 JP7246309 B2 JP 7246309B2
- Authority
- JP
- Japan
- Prior art keywords
- combination
- alkyl
- inhibitor
- alkynyl
- alkenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4525—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Endocrinology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Steroid Compounds (AREA)
Description
この出願は、2016年12月8日に出願された米国仮特許出願第62/497,949号、2017年2月28日に出願された米国仮特許出願第62/465,001号および2017年8月14日に出願された米国仮特許出願第62/545,373号(これらの全体は、参考として本明細書に援用される)の利益を主張する。
ツチハンミョウ抽出物(Mylabris)の主な活性成分であるカンタリジンは、PP2Aの強力な阻害剤であることが示されている伝統的な漢方薬に由来する化合物である(Efferth, T.ら、2005年)。カンタリジンはヘパトーマの処置においてこれまで使用されており、多剤耐性の白血病細胞株に対する有効性を示しているが(Efferth, T.ら、2002年)、その重度の毒性によりその臨床的有用性は制限される。LB-100は、毒性が大幅に少ない、カンタリジンの小分子誘導体である。これまでの前臨床研究によって、LB-100が、神経膠芽腫(GBM)、転移性褐色細胞腫、および膵臓がんに対するテモゾロミド、ドキソルビシン、および放射線療法の細胞傷害性効果を増強させ得ることが示されている(Wei, D.ら、2013年;Lu, J.ら、2009年;Zhang, C.ら、2010年;Martiniova, L.ら、2011年)。LB-100では、充実性腫瘍の処置のための、ドセタキセルと組み合わせた第1相研究も行われている(Chung, V.、2013年)。
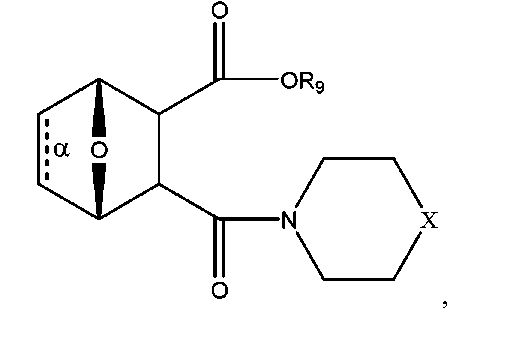
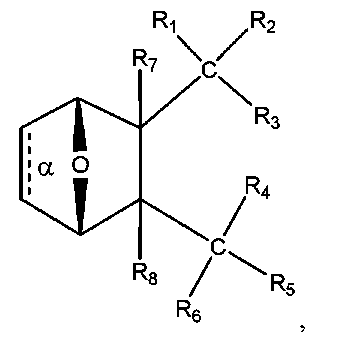
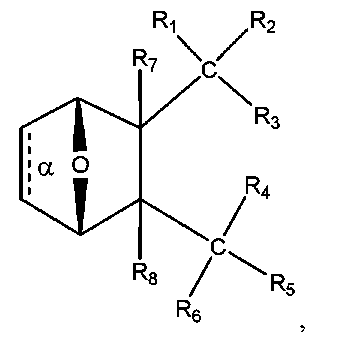
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
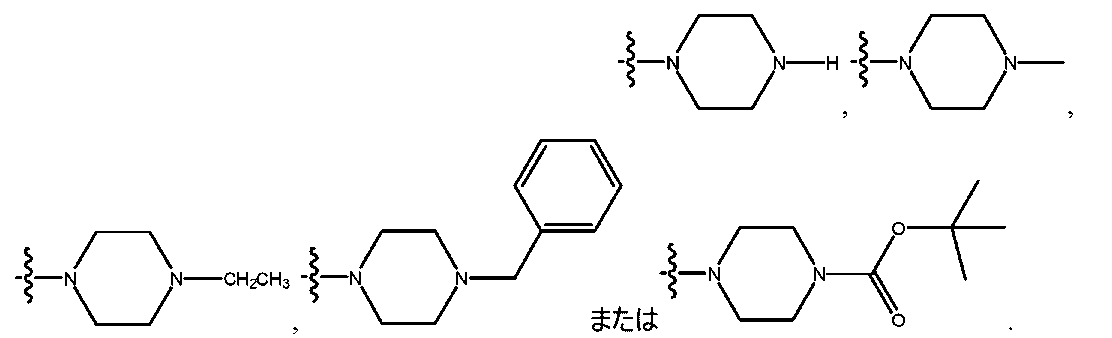
R4が、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
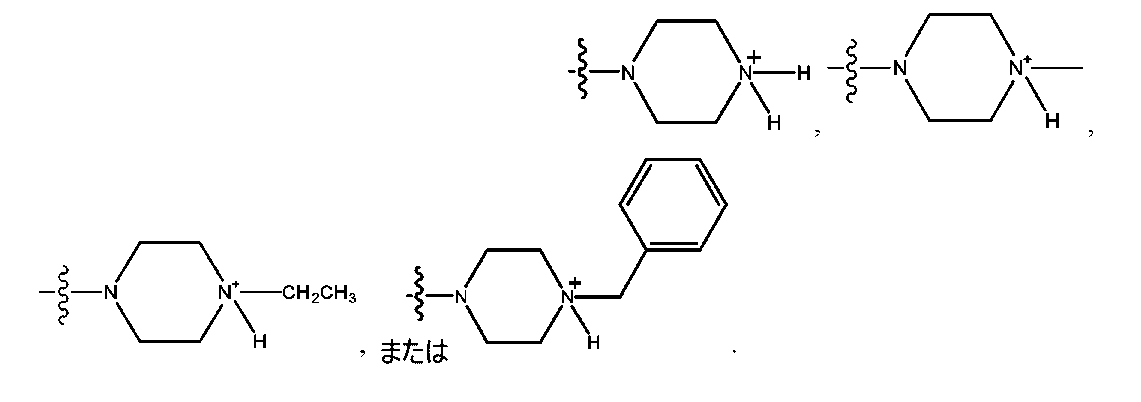
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hである。
ここで、R9は、アルキル、アルケニル、アルキニル、またはアリールであり、
R4は、
式中、Xは、O、S、NR10、N+HR10、またはN+R10R10であり、
ここで、各R10は、独立して、H、アルキル、アルケニル、アルキニル、アリール、
結合αが、存在しているかもしくは存在せず、
R9が、存在しているかもしくは存在せず、存在している場合には、H、アルキル、アルケニル、アルキニル、もしくはフェニルであり、かつ
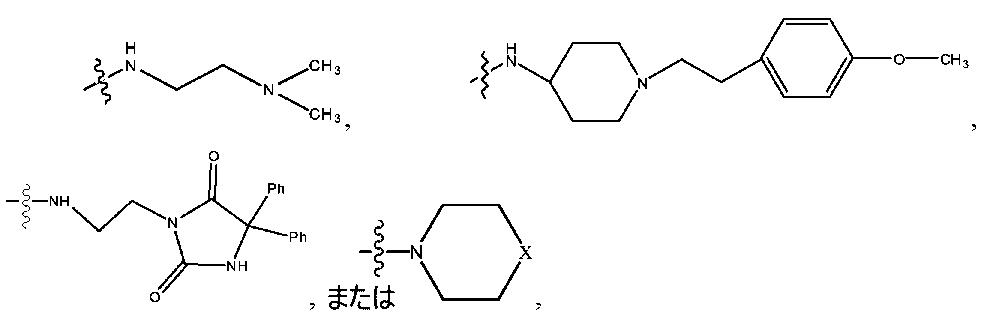
Xが、O、NR10、NH+R10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
ここで、R12が、Hもしくはアルキルである。
結合αが、存在しているかもしくは存在せず、
Xが、OもしくはNR10であり、
ここで、各R10が、独立して、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
ここで、R12が、Hもしくはアルキルである。
結合αが、存在しているかもしくは存在せず、
Xが、OもしくはNH+R10であり、
ここで、R10が、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
ここで、R12が、Hもしくはアルキルである。
を含む方法を提供する。
黒色腫などの所与の状態を処置するための2つの薬物の投与は、いくつかの潜在的な問題を生じさせる。2つの薬物の間でのin vivoでの相互作用は、複雑である。任意の単一の薬物の効果は、その吸収、分布、および排出に関連する。2つの薬物が体内に導入されると、各薬物は、他方の薬物の吸収、分布、および排出に影響し得、したがって他方の薬物の効果を改変し得る。例えば、1つの薬物は、他方の薬物の排出の代謝経路に関与する酵素の生産を阻害、活性化、または誘発し得る(Guidance for Industry、1999年)。したがって、2つの薬物を、同一の状態を処置するために投与する場合、各薬物が、ヒト被験体における他方の薬物の治療的活性を補う、他方の薬物の治療的活性に対して影響を有さない、または他方の薬物の治療的活性に干渉するかどうかは、予測不可能である。
(実施例1 PP2A阻害およびCTLA-4活性)
化合物LB-100および本明細書において開示されるLB-100のその他の同族体は、CTLA-4およびPP2Aの相互作用を変更し、それによって、T細胞活性化のCTLA-4媒介性阻害を遮断することによって、T細胞においてCTLA-4の機能を阻害する。このような相互作用は、T細胞活性化の増大をもたらす。
初代ヒトT細胞およびジャーカットT細胞をLB-100を用いて処置し、T細胞活性化レベルを測定する。LB-100は、T細胞の活性化を増大する。
ある量の化合物LB-100を、がんに罹患した被験体に投与する。化合物の量は、被験体において細胞傷害性T細胞の数を増大することによってがんを処置するのに有効である。
CTLA-4チェックポイント阻害剤と組み合わせたある量の化合物LB-100を、がんに罹患した被験体に投与する。化合物および阻害剤の量は、被験体を処置するのに有効である。
追加療法は、相乗作用を提供し、副作用が低減したより低い用量を可能にする。
がんとの関連で、免疫系の重要性は、がん免疫療法の開発とともにますます認識されるようになった。自己免疫を防ぐ免疫系の天然制御機序が、免疫監視を逃れるために腫瘍によって利用されることが多い。プログラム細胞死-1(PD-1)および細胞傷害性Tリンパ球関連タンパク質4(CTLA-4)などのチェックポイント分子は、腫瘍のネオ抗原を認識する細胞傷害性T細胞の活性を抑制するように腫瘍によって構成的に活性化される免疫系の負の調節因子である(Topalianら、2015年)。免疫抑制性制御性T細胞(Treg)もまた、CD8T細胞の有効性を低減するために腫瘍微小環境(TME)に動員される。PD-1またはCTLA-4シグナル伝達を遮断するモノクローナル抗体は、転移性黒色腫を有する一部の患者において耐久性のある長期間応答を誘導し得る。これは、進行した黒色腫の処置のための米国食品医薬品局による2011年のイピリムマブ(抗CTLA-4)の承認および2014年のニボルマブ(抗PD-1)の承認につながった。複数のその他のがんにチェックポイント阻害剤の使用を拡大するために現在の臨床治験が進行中であり、がん療法へのアプローチにおいてパラダイムシフトの先駆けとなっている。しかし、患者のサブセットのみが、単剤では、チェックポイント阻害に有効に応答し、これは、免疫抑制TMEを作り出すことに複数の重複した機序が関与しているという事実を強調する。したがって、研究の活性領域は、チェックポイント阻害の効果を増大し得る組み合わせ戦略を同定することである。
PP2Aは、細胞分裂、DNA損傷応答、相同組換え修復および有糸分裂停止におけるその調節性役割のために、がん療法のための潜在的に重要な標的として長く認識されているが、この酵素の阻害は、臨床使用には毒性が高すぎる可能性が高いと考えられてきた。この研究は、難治性固形腫瘍を有する患者におけるPP2Aの阻害剤LB-100の安全性、耐容性、および潜在的抗がん活性を示す。PP2A活性は、多数の種類のがんにおいて変異によって直接的にまたは間接的に変更される。PP2Aの臨床上安全な阻害剤の利用可能性は、がん療法にとって有望な新規手段、すなわち、PP2A機能において、および/またはDNA-損傷-修復経路において変異により獲得された異常を有するがんにおけるPP2Aの薬理学的阻害を開く。この研究の結果は、単独およびがんの処置のためのその他の薬剤と組み合わせたLB-100のさらなる開発を支援する。
適格な患者は、進行性固形腫瘍を有すると証明された、標準治療が失敗した18歳またはそれよりも年長とした。患者は、少なくとも12週間の平均余命、0または1のECOGパフォーマンスステータスを有さなくてはならず、インフォームドコンセントを得ることができなければならなかった。参加前に、患者は、先の処置からベースラインまたはグレード1未満の毒性に回復していなければならず、適当な骨髄(絶対好中球数>1.5×109個/Lおよび血小板数>100×109個/L)、腎臓(血清クレアチニン<1.2mg/dLおよび>1.2mg/dLである場合には、クレアチニンクリアランス[Cockcroft-Gault法]>60mL/分/1.73m2)および肝機能(血漿総ビリルビン<1.5mg/dL、アラニントランスアミナーゼ(ALT)およびアスパラギン酸トランスアミナーゼ(AST)<2.5×正常の上限)を有さなくてはならない。患者は、いかなる他の制御されない全身性疾患も有してはならない。妊娠可能性のある女性は、陰性の血清または尿妊娠検査結果を有さなくてはならなかった。
オープンラベル、用量漸増、第I相研究を実施して、3週間毎に3日間連続投与したLB-100の安全性、耐容性および活性を評価した。薬物動態研究を最大耐容用量(MTD)でデザインした。出発用量、0.25mg/m2、イヌにおいて最も高い非重度毒性用量の1/15および用量漸増のデザインは、FDAによって指定されたものである。研究は、各研究センターでヒト調査委員会によって承認され、clinicaltrials.gov:NCT01837667に登録されている。
LB-100の用量を、3人の患者の群において漸増した。新規用量レベルの第1の患者を3週間観察し、その後、次の2人をその用量で処置した。潜在的なDLTが生じた場合には、3人の新規患者をその用量に入れた。別のDLTが生じた場合には、3人のさらなる患者を、以前の非DLT用量で処置して、第2相治験のためにそのレベルの安全性を決定した。
主目的は、3週間毎に、3日間連続で静脈内に毎日投与されたLB-100の安全性、耐容性および最大耐容用量を決定することであった。二次的目的は、潜在的な抗腫瘍活性のいかなる証拠も文書に記録し、LB-100をMTDで受けている患者における、LB-100および代謝産物、エンドタールに関する薬物動態データを得ることであった(Quangら、2016年)。
7回の用量漸増にわたり29人の患者のエントリーがあった。1人の患者は、急性感染のために1回の用量後に処置を停止し、回復後に再登録した。両経過は、別個の患者エントリーとして解析した。2人の患者は、3.1mg/m2レベルで用量制限毒性を有していた(血清クレアチニンまたは算出された血清クレアチニンクリアランスにおける可逆的増大)。6人(20.7%)の患者において研究薬物が関連することがほぼ確実なまたは可能性があるグレード3の有害事象が発生した[貧血(n=2)、クレアチニンクリアランスの減少、呼吸困難、低ナトリウム血症、リンパ球減少症]。応答が評価可能である20人の患者のうち10人(50%)が、4またはそれより多いサイクルの間、安定病態を有していた。膵臓癌を有する1人の患者は、10サイクル後に記載された部分応答を有しており、それは、さらに5サイクルの間維持された。安定病態に達しているその他の患者は、以下のうちの1つを有していた:線維肉腫、軟骨肉腫、胸腺腫、非定型肺カルチノイドまたは卵巣がん、精巣がん、乳がん(n=2)および前立腺がん。LB-100の推奨第2相用量は、2.33mg/m2、3週間毎に3日間の間、毎日である。
進行した固形腫瘍を有する28人の患者が4つの臨床現場で登録された。患者の人口統計学的特徴が表1に列挙されている。4人の患者は、毒性について評価可能ではなかった。これらの患者のうち3人は、サイクル1を完了する前に疾患関連合併症を有していた。非定型肺カルチノイドを有する4番目の患者を、急性感染のために1回の用量のLB-100の後に研究から除外した;該患者を7週間後に研究に再度入れ、5サイクルの間安定病態に達した。両経過を解析に含めた。これらの有害な事象のうち、薬物投与と関連していると考えられるものはなかった。
24人の患者が、LB-100の3日サイクルの少なくとも1つを完了した。試験した用量レベルは、0.25、0.50、0.83、1.25、1.75、2.33および3.1mg/m2であった。最初の6用量レベルの間、DLTはなかった。3.1mg/m2用量レベルで、前立腺がんを有する患者および軟骨肉腫を有する患者は、それぞれ、4および9サイクルの処置の間、DLTを有していなかった。卵巣がんを有する第3の患者は、サイクル1後に算出されたクレアチニンクリアランスにおいてグレード3の増大を有しており、8日目までに正常に戻り、腫瘍進行前に2.33mg/m2の低減された用量でさらに3つのサイクルを受けた。線維肉腫を有する第4の患者は、第1の経過後に算出されたクレアチニンクリアランスにおいてグレード3の増大を有していた。クレアチニンは、21日目までに処置前の値に戻り、2.33mg/m2での第2の経過は、クレアチニンクリアランスにおいてグレード2の増大をもたらし、その他の毒性は伴わなかった。用量は1.75mg/m2に低下し、さらに10のサイクルが投与され、36週後の進行まで毒性を伴わなかった。3.1mg/m2で2/4人の患者が、サイクル1の間にクレアチニンクリアランスにおいてグレード3の増大を有していたので、3人のさらなる患者は、2.33mg/m2の先行用量レベルで評価した。該患者は制限毒性を有さず、それによって、そのレベルでMTDを確立した。可逆性の軽度から中程度の疲労以外の症候性毒性はなかった。薬物投与と関連している可能性がある有害事象を、表2に列挙する。
1人の患者において1日目に、ならびに2人の患者において1日目および3日目に2.33mg/m2のLB-100のMTDで2時間注入の前および完了後4時間かけてLB-100およびエンドタールの血漿中濃度を測定した(Quangら、2016年)。LB-100の薬物動態は、1日目および3日目で同様であり、低クリアランス、低分布体積および短い半減期を特徴とした。エンドタールの血漿中濃度は注入を通じて低く、1人の患者では検出の下限(5ng/mL)未満であった。その他の2人の患者では、最後のサンプリング時点(4時間)でエンドタールの最大濃度(34.7ng/mL)が観察され、これは、その排出半減期の決定を妨げた(表3)。
測定可能な疾患を有する20人の患者のうち、膵臓がんを有する1人の患者が、10サイクル後に認められ、さらに5サイクル持続する部分応答を有しており、16人の患者では、その指標病変(複数可)の進行はなかった。該患者は、新規病変の出現または臨床進行を表すと判断された症状のいずれかのために研究から除外した。十二指腸腺癌を有する1人および結腸腺癌を有する2人の、3人の患者のみが、RECIST判定基準によるその指標病変(複数可)の大きさの有意な増加を有していた(図1)。
LB-100、PP2Aの強力な阻害剤のMTDを、固形腫瘍を有する患者において決定した。推奨第2相開始用量は、腎毒性の非存在下では3.1mg/m2までの漸増、および疾患が安定または退縮している場合、腎毒性があるなら1.75mg/m2またはそれより低いものへの漸減を伴って、2.33mg/m2、3週間毎に3日間毎日である。患者は、疾患の安定性を有しており、膵臓がんを有する1人の患者は、3週間毎に3日間毎日、0.83mg/m2ほどの低い用量で膵臓がんの客観的退縮があったので、ヒトにおける最適抗がん活性は、MTDよりもかなり低い可能性がある。
抗がん療法と組み合わせたある量の化合物LB-100を、がんに罹患した被験体に投与する。化合物および抗がん療法の量は、被験体を処置するのに有効である。
PP2Aの薬理学的阻害は、免疫活性化およびがん免疫療法を増強し得る。PP2Aの阻害は、従来のCD4およびCD8T細胞の増殖を直接的に増大することによって、およびTregの免疫抑制機能を損なうことによって、がん免疫療法を増強するはずである。LB-100は、免疫チェックポイント遮断の効果を増大し得ると仮定した。これは、前臨床モデルにおいて、PP2Aの薬理学的阻害が免疫療法と相乗作用し得ることを実証する最初の研究である。
LB-100を用いるPP2Aの阻害は免疫媒介性抗腫瘍応答を増強し得るという仮説を試験するために、マウスにCT26腫瘍細胞を移植した。CT26は、低レベルのPD-L1を発現するマウス結腸腺癌であり、抗PD1療法に対して耐性である。約13日後、30~100mm3の間の腫瘍サイズを有するマウスを、4つの処置群(PBS対照、LB-100のみ - 0.16mg/kg、抗PD-1のみ - 10mg/kgまたは両方の組み合わせ)に無作為化した。処置は、合計28日間2日毎に行った。2日毎に腫瘍サイズを評価した(図20A~C)。抗PD1を用いる単剤処置は、腫瘍負荷の低減または生存の増大において有効ではなかった。LB-100単独は、メジアン生存を21から33日に増大できた(p=0.02)。組み合わせ処置は、処置後14日目に対照と比較して(p<0.01)平均腫瘍体積を70%有意に低下させた。メジアン生存はまた、21から72日に増大した(p<0.01)。より著しくは、マウスの50%が、腫瘍の完全退縮(CR)に達し、疾患の証拠はなかった。この応答は、処置の完了後に耐久性のあるものであった。
試薬-LB-100は、Lixte Biotechnologyによって提供された。抗マウスPD-1、クローンRMP1-14、抗体は、BioXcellから購入した。フローサイトメトリーに以下のモノクローナル抗体(mAb)を使用した:ラット抗マウスCD4-BV421、ラット抗マウスCD3-PE、ラット抗マウスCD8a-Alexa647、ラット抗マウスCD45-BV785、ラット抗マウスIFNg-FITC、ラット抗マウスFOXP3-Alexa647。これらの抗体は、Biolegendから購入した。
処置効果を、腫瘍浸潤リンパ球で評価した(図23A~B)。CT26腫瘍を有するマウスを、上記のようにLB-100および/または抗PD-1抗体を用いて処置した。処置の12日後、腫瘍をFACSによって解析した。LB-100および抗PD-1抗体の組み合わせを用いて処置したマウスから得た腫瘍浸潤CD8+T細胞は、対照動物および抗PD-1単独を用いて処置した動物から得た細胞と比較してIFNg+CD8+T細胞の有意な増大を示した(それぞれ11.0%および10.5%と比較して25.3%、p=0.05)。IFNγは、抗腫瘍応答を媒介する最も重大なサイトカインであるので、この結果は、組み合わせで処置されたマウスが、移植された腫瘍に対して増強された免疫を有することの機能的確認である。さらに、TregにおけるPP2Aの公知の重要性を考慮し、LB-100および/または抗PD-1処置の効果を腫瘍中に存在するTregの量に関して調べた。LB-100単独は、腫瘍環境中のTregを有意に枯渇させた(対照における14.7%と比較して2.1%)。この効果は、抗PD-1または組み合わせによるTreg枯渇に対する効果に対して同程度である。LB-100単独がTregを枯渇させることができるという事実は、LB-100単独処置群において観察された、小さいが有意な生存利益を説明する、可能性のある機序を示唆する。
PD-1および/またはPD-L1チェックポイント阻害剤との組み合わせで、ある量の化合物LB-100をがんに罹患した被験体に投与する。化合物および阻害剤の量は、被験体を処置するのに有効である。
追加療法は、相乗作用を提供し、低減された副作用しか伴わないより少ない用量を可能にする。
本実施例は、とりわけ、小分子PP2A阻害剤、LB-100が、抗PD1(aPD-1)遮断と組み合わせた場合に、CT26結腸がんモデルにおいて耐久性のある免疫媒介性抗腫瘍応答を相乗的に誘発することを実証する。この効果は、T細胞依存性であり、腫瘍の相当な割合の著しい退縮につながった。腫瘍リンパ球の解析は、エフェクター対制御性T細胞比の著しい増大をもたらすエフェクターT細胞の浸潤の増強および抑制性制御性T細胞の枯渇を実証した。腫瘍のクリアランスは、抗原特異的二次防御免疫を確立した。LB-100およびaPD-1遮断の相乗作用はまた、B16黒色腫モデルにおいても観察された。さらに、本明細書において、LB-100によってmTORC1シグナル伝達経路が特異的に活性化され、ナイーブCD4細胞の制御性T細胞への分化の減少がもたらされたという知見が記載される。Th1の発現の増大およびTh2サイトカインの発現の減少も見られた。これらのデータは、チェックポイント阻害と組み合わせたPP2A阻害の橋渡しの可能性を強調する。
参考
本発明は、例えば、以下の項目を提供する。
(項目1)
がんに罹患した被験体を処置する方法であって、有効量のPP2A阻害剤を有効量のチェックポイント阻害剤と組み合わせて前記被験体に投与することを含み、合わせた場合の前記量が、前記被験体を処置するのに有効である、方法。
(項目2)
がんに罹患しておりチェックポイント阻害剤を受容している被験体を処置する方法であって、前記チェックポイント阻害剤単独と比較して処置を増強するのに有効な量のPP2A阻害剤を前記被験体に投与することを含む、方法。
(項目3)
被験体における腫瘍またはがんを処置する方法であって、有効量のPP2A阻害剤を有効量のチェックポイント阻害剤と組み合わせて前記被験体に投与することを含み、合わせた場合の前記量が、前記腫瘍または前記がんを処置するのに有効である、方法。
(項目4)
がんに罹患した被験体におけるがん細胞に対するT細胞応答を増大させる方法であって、ある量のPP2A阻害剤を前記がん細胞に対する前記T細胞応答を増大させるのに有効な有効量のチェックポイント阻害剤と組み合わせて前記被験体に投与することを含む、方法。
(項目5)
がんに罹患した被験体におけるT細胞の活性化を増大させる方法であって、有効量のPP2A阻害剤を有効量のチェックポイント阻害剤と組み合わせて前記被験体に投与し、それによって、前記T細胞の活性化を増大させることを含む、方法。
(項目6)
前記量の前記化合物および前記量の前記チェックポイント阻害剤が、各々定期的に前記被験体に投与される、項目1~5のいずれか一項に記載の方法。
(項目7)
前記量の前記化合物および前記量の前記チェックポイント阻害剤が、同時に、個別に、または逐次的に投与される、項目1~6のいずれか一項に記載の方法。
(項目8)
前記チェックポイント阻害剤が、前記PP2A阻害剤と同時に、前記PP2A阻害剤の前に、または前記PP2A阻害剤の後に投与される、項目1~7のいずれか一項に記載の方法。
(項目9)
一緒に投与される場合の前記量のチェックポイント阻害剤および前記量の化合物が、同量の各薬剤が単独で投与される場合よりも、前記被験体を処置するのに有効である、項目1~8のいずれか一項に記載の方法。
(項目10)
一緒に投与される場合の前記量の前記化合物および前記量の前記チェックポイント阻害剤が、前記被験体における前記がんの臨床症状を低減させるのに有効である、項目1~9のいずれか一項に記載の方法。
(項目11)
前記化合物が、前記チェックポイント阻害剤の免疫療法的効果を増強させる、項目1~10のいずれか一項に記載の方法。
(項目12)
前記がんが、免疫応答による処置に対して感受性である、項目1~11のいずれか一項に記載の方法。
(項目13)
前記免疫チェックポイント阻害剤がCTLA-4剤である、項目1~12のいずれか一項に記載の方法。
(項目14)
前記CTLA-4チェックポイント阻害剤が、イピリムマブまたはトレメリムマブである、項目13に記載の方法。
(項目15)
前記免疫チェックポイント阻害剤が、抗PD-1または抗PD-L1剤である、項目1~12のいずれか一項に記載の方法。
(項目16)
前記PD-1および/またはPD-L1チェックポイント阻害剤が、アテゾリズマブ、ニボルマブ、またはペムブロリズマブである、項目15に記載の方法。
(項目17)
前記がんが、黒色腫、腎細胞癌、前立腺がん、尿路上皮癌、または卵巣がんである、項目1~16のいずれか一項に記載の方法。
(項目18)
前記がんが黒色腫である、項目17に記載の方法。
(項目19)
前記化合物が、0.25mg/m 2 、0.5mg/m 2 、0.83mg/m 2 、1.25mg/m 2 、1.75mg/m 2 、2.33mg/m 2 、または3.1mg/m 2 の用量で投与される、項目1~16のいずれか一項に記載の方法。
(項目20)
前記化合物が、2.33mg/m 2 の用量で投与される、項目19に記載の方法。
(項目21)
前記化合物が3週間毎に3日間投与される、項目1~16のいずれか一項に記載の方法。
(項目22)
前記イピリムマブが、0.5mg/kg~10mg/kgまたはそれ未満の用量で静脈内に投与される、項目14に記載の方法。
(項目23)
前記イピリムマブが、3週間毎またはそれより少なく、90分にわたり静脈内に投与される、項目22に記載の方法。
(項目24)
前記アテゾリズマブが、0.1mg/kg~20mg/kgまたはそれ未満の用量で静脈内に投与される、項目14に記載の方法。
(項目25)
前記アテゾリズマブが、3週間毎またはそれより少なく、60分にわたり静脈内に投与される、項目22に記載の方法。
(項目26)
前記ニボルマブが、0.1mg/kg~10mg/kgまたはそれ未満の用量で静脈内に投与される、項目16に記載の方法。
(項目27)
前記ニボルマブが、2週間毎またはそれより少なく、60分にわたり静脈内に投与される、項目26に記載の方法。
(項目28)
前記ペムブロリズマブが、1mg/kg~10mg/kgまたはそれ未満の用量で静脈内に投与される、項目16に記載の方法。
(項目29)
前記ペムブロリズマブが、3週間毎またはそれより少なく、30分にわたり静脈内に投与される、項目28に記載の方法。
(項目30)
T細胞におけるCTLA-4の機能を阻害する方法であって、前記T細胞にPP2A阻害剤を投与し、それによって前記CTLA-4の機能を阻害することを含む、方法。
(項目31)
T細胞におけるPD-1:PD-L1相互作用を阻害する方法であって、前記T細胞にPP2A阻害剤を投与し、それによってPD-1:PD-L1の相互作用を阻害することを含む、方法。
(項目32)
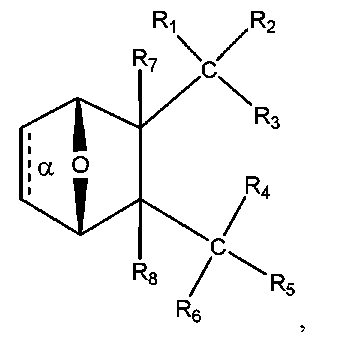
前記PP2A阻害剤が、構造:
を有するか、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR 1 およびR 2 が=Oであり、
R 3 が、OH、O - 、OR 9 、O(CH 2 ) 1~6 R 9 、SH、S - 、もしくはSR 9 であり、
ここで、R 9 が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R 4 が、
であり、
式中、Xが、O、S、NR 10 、N + HR 10 、もしくはN + R 10 R 10 であり、
ここで、各R 10 が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
、-CH 2 CN、-CH 2 CO 2 R 11 、もしくは-CH 2 COR 11 であり、
ここで、各R 11 が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R 5 およびR 6 が、一緒になって=Oであり、
R 7 およびR 8 が、それぞれHである、
項目1~23のいずれか1項に記載の方法。
(項目33)
前記化合物が、構造:
を有する、項目32に記載の方法。
(項目34)
前記化合物内の結合αが存在する、項目32または33に記載の方法。
(項目35)
前記化合物内の結合αが存在しない、項目32または33に記載の方法。
(項目36)
R 3 が、OH、O - 、またはOR 9 であり、
ここで、R 9 が、アルキル、アルケニル、アルキニル、またはアリールであり、
R 4 が、
であり、
式中、Xが、O、S、NR 10 、N + HR 10 、またはN + R 10 R 10 であり、
ここで、各R 10 が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
である、
項目32または33に記載の方法。
(項目37)
R 3 が、OH、O - 、またはOR 9 であり、ここで、R 9 が、H、メチル、エチル、またはフェニルである、項目36に記載の方法。
(項目38)
R 3 が、OH、O - 、またはOR 9 であり、ここで、R 9 がメチルである、項目37に記載の方法。
(項目39)
R 4 が、
である、項目36に記載の方法。
(項目40)
R 4 が、
であり、式中、R 10 が、H、アルキル、アルケニル、アルキニル、アリール、または
である、項目36に記載の方法。
(項目41)
R 4 が、
であり、式中、R 10 が、-H、-CH 3 、-CH 2 CH 3 、または
である、項目40に記載の方法。
(項目42)
R 4 が、
である、項目41に記載の方法。
(項目43)
R 4 が、
であり、式中、R 10 が、H、アルキル、アルケニル、アルキニル、アリール、
である、項目36に記載の方法。
(項目44)
R 4 が、
である、項目43に記載の方法。
(項目45)
R 4 が、
である、項目36に記載の方法。
(項目46)
前記化合物が、構造
を有するか、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
R 9 が、存在しているかもしくは存在せず、存在している場合には、H、アルキル、アルケニル、アルキニル、もしくはフェニルであり、かつ
Xが、O、NR 10 、NH + R 10 、もしくはN + R 10 R 10 であり、
ここで、各R 10 が、独立して、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
、-CH 2 CN、-CH 2 CO 2 R 12 、もしくは-CH 2 COR 12 であり、
ここで、R 12 が、Hもしくはアルキルである、
項目34または35に記載の方法。
(項目47)
前記化合物が、構造
を有するか、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
Xが、OもしくはNR 10 であり、
ここで、各R 10 が、独立して、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
、-CH 2 CN、-CH 2 CO 2 R 12 、もしくは-CH 2 COR 12 であり、
ここで、R 12 が、Hもしくはアルキルである、
項目46に記載の方法。
(項目48)
前記化合物が、構造
を有するか、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
Xが、OもしくはNH + R 10 であり、
ここで、R 10 が、H、アルキル、置換されたアルキル、アルケニル、置換されたアルケニル、アルキニル、置換されたアルキニル、アリール、
、-CH 2 CN、-CH 2 CO 2 R 12 、もしくは-CH 2 COR 12 であり、
ここで、R 12 が、Hもしくはアルキルである、
項目46に記載の方法。
(項目49)
前記化合物が、構造
を有するか、またはその塩もしくはエステルである、項目40に記載の方法。
Claims (53)
- がんに罹患した被験体を処置するための組み合わせ物であって、前記組み合わせ物がPP2A阻害剤およびチェックポイント阻害剤を含み、合わせた場合の量が、前記組み合わせ物が前記被験体に投与される場合に前記被験体を処置するのに有効であり、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組み合わせ物。 - がんに罹患しておりチェックポイント阻害剤を受容している被験体を処置するための、PP2A阻害剤を含む組成物であって、前記組成物の量が、前記組成物が前記被験体に投与される場合に、前記PP2A阻害剤の不在下での前記チェックポイント阻害剤と比較して処置を増強するのに有効であり、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - 被験体における腫瘍またはがんを処置するための組み合わせ物であって、前記組み合わせ物がPP2A阻害剤およびチェックポイント阻害剤を含み、合わせた場合の量が、前記組み合わせ物が前記被験体に投与される場合に前記腫瘍または前記がんを処置するのに有効であり、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組み合わせ物。 - がんに罹患した被験体におけるがん細胞に対するT細胞応答を増大させるための組み合わせ物であって、前記組み合わせ物がある量のPP2A阻害剤およびある量のチェックポイント阻害剤を含み、合わせた場合の前記量が、前記組み合わせ物が前記被験体に投与される場合に前記がん細胞に対する前記T細胞応答を増大させるのに有効であり、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組み合わせ物。 - がんに罹患した被験体におけるT細胞の活性化を増大させるための組み合わせ物であって、前記組み合わせ物がある量のPP2A阻害剤およびある量のチェックポイント阻害剤を含み、合わせた場合の前記量が、前記組み合わせ物が前記被験体に投与される場合にT細胞の活性化を増大させるのに有効であり、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組み合わせ物。 - 前記量の前記PP2A阻害剤および前記量の前記チェックポイント阻害剤が、各々定期的に前記被験体に投与されることを特徴とする、請求項1および3~5のいずれか一項に記載の組み合わせ物、または請求項2に記載の組成物。
- 前記量の前記PP2A阻害剤および前記量の前記チェックポイント阻害剤が、同時に、個別に、または逐次的に投与されることを特徴とする、請求項1および3~6のいずれか一項に記載の組み合わせ物、または請求項2もしくは6に記載の組成物。
- 前記チェックポイント阻害剤が、前記PP2A阻害剤と同時に、前記PP2A阻害剤の前に、または前記PP2A阻害剤の後に投与されることを特徴とする、請求項1および3~7のいずれか一項に記載の組み合わせ物、または請求項2、6および7のいずれか一項に記載の組成物。
- 一緒に投与される場合の前記量の前記チェックポイント阻害剤および前記量の前記PP2A阻害剤が、同量の各薬剤が単独で投与される場合よりも、前記被験体を処置するのに有効である、請求項1および3~8のいずれか一項に記載の組み合わせ物、または請求項2および6~8のいずれか一項に記載の組成物。
- 一緒に投与される場合の前記量の前記PP2A阻害剤および前記量の前記チェックポイント阻害剤が、前記被験体における前記がんの臨床症状を低減させるのに有効である、請求項1および3~9のいずれか一項に記載の組み合わせ物、または請求項2および6~9のいずれか一項に記載の組成物。
- 前記PP2A阻害剤が、前記チェックポイント阻害剤の免疫療法的効果を増強させる、請求項1および3~10のいずれか一項に記載の組み合わせ物、または請求項2および6~10のいずれか一項に記載の組成物。
- 前記がんが、免疫応答による処置に対して感受性である、請求項1および3~11のいずれか一項に記載の組み合わせ物、または請求項2および6~11のいずれか一項に記載の組成物。
- 前記抗PD-1抗体または抗PD-L1抗体が、アテゾリズマブ、ニボルマブ、またはペムブロリズマブである、請求項1および3~12のいずれか一項に記載の組み合わせ物、または請求項2および6~12のいずれか一項に記載の組成物。
- 前記がんが、黒色腫、腎細胞癌、前立腺がん、尿路上皮癌、神経膠芽腫または卵巣がんである、請求項1および3~13のいずれか一項に記載の組み合わせ物、または請求項2および6~13のいずれか一項に記載の組成物。
- 前記がんが黒色腫である、請求項14に記載の組み合わせ物または組成物。
- 前記PP2A阻害剤が、0.25mg/m2、0.5mg/m2、0.83mg/m2、1.25mg/m2、1.75mg/m2、2.33mg/m2、または3.1mg/m2の用量で投与されることを特徴とする、請求項1および3~15のいずれか一項に記載の組み合わせ物、または請求項2および6~15のいずれか一項に記載の組成物。
- 前記PP2A阻害剤が、2.33mg/m2の用量で投与されることを特徴とする、請求項16に記載の組み合わせ物または組成物。
- 前記PP2A阻害剤が3週間毎に3日間投与されることを特徴とする、請求項1および3~17のいずれか一項に記載の組み合わせ物、または請求項2および6~17のいずれか一項に記載の組成物。
- 前記抗PD-1抗体および/または抗PD-L1抗体がアテゾリズマブであり、前記アテゾリズマブが、0.1mg/kg~20mg/kgまたはそれ未満の用量で静脈内に投与されることを特徴とする、請求項13に記載の組み合わせ物または組成物。
- 前記アテゾリズマブが、3週間毎またはそれより少なく、60分にわたり静脈内に投与されることを特徴とする、請求項19に記載の組み合わせ物または組成物。
- 前記抗PD-1抗体および/または抗PD-L1抗体がニボルマブであり、前記ニボルマブが、0.1mg/kg~10mg/kgまたはそれ未満の用量で静脈内に投与されることを特徴とする、請求項13に記載の組み合わせ物または組成物。
- 前記ニボルマブが、2週間毎またはそれより少なく、60分にわたり静脈内に投与されることを特徴とする、請求項21に記載の組み合わせ物または組成物。
- 前記抗PD-1抗体および/または抗PD-L1抗体がペムブロリズマブであり、前記ペムブロリズマブが、1mg/kg~10mg/kgまたはそれ未満の用量で静脈内に投与されることを特徴とする、請求項13に記載の組み合わせ物または組成物。
- 前記ペムブロリズマブが、3週間毎またはそれより少なく、30分にわたり静脈内に投与されることを特徴とする、請求項23に記載の組み合わせ物または組成物。
- 前記PP2A阻害剤内の結合αが存在する、請求項25に記載の組み合わせ物または組成物。
- 前記PP2A阻害剤内の結合αが存在しない、請求項25に記載の組み合わせ物または組成物。
- R3が、OH、O-、またはOR9であり、ここで、R9が、H、メチル、エチル、またはフェニルである、請求項28に記載の組み合わせ物または組成物。
- R3が、OH、O-、またはOR9であり、ここで、R9がメチルである、請求項29に記載の組み合わせ物または組成物。
- 前記PP2A阻害剤が、構造
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
R9が、存在しているかもしくは存在せず、存在している場合には、H、アルキル、アルケニル、アルキニル、もしくはフェニルであり、かつ
Xが、O、NR10、NH+R10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
、-CH2CN、-CH2CO2R12、もしくは-CH2COR12であり、
ここで、R12が、Hもしくはアルキルである、
請求項1および3~24のいずれか一項に記載の組み合わせ物または請求項2および6~24のいずれか一項に記載の組成物。 - がんに罹患した被験体を処置するための、PP2A阻害剤を含む組成物であって、前記組成物がチェックポイント阻害剤と組み合わせて前記被験体に投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - がんに罹患した被験体を処置するための、チェックポイント阻害剤を含む組成物であって、前記組成物がPP2A阻害剤と組み合わせて前記被験体に投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - 被験体における腫瘍またはがんを処置するための、PP2A阻害剤を含む組成物であって、前記組成物がチェックポイント阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - 被験体における腫瘍またはがんを処置するための、チェックポイント阻害剤を含む組成物であって、前記組成物がPP2A阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - がんに罹患した被験体におけるがん細胞に対するT細胞応答を増大させるための、PP2A阻害剤を含む組成物であって、前記組成物がチェックポイント阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - がんに罹患した被験体におけるがん細胞に対するT細胞応答を増大させるための、チェックポイント阻害剤を含む組成物であって、前記組成物がPP2A阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - がんに罹患した被験体におけるT細胞の活性化を増大させるための、PP2A阻害剤を含む組成物であって、前記組成物がチェックポイント阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - がんに罹患した被験体におけるT細胞の活性化を増大させるための、チェックポイント阻害剤を含む組成物であって、前記組成物がPP2A阻害剤と組み合わせて投与されることを特徴とし、
前記PP2A阻害剤が、構造:
を有する化合物、またはその塩、両性イオン、もしくはエステルであり、式中、
結合αが、存在しているかもしくは存在せず、
一緒になったR1およびR2が、=Oであり、
R3が、OH、O-、OR9、O(CH2)1~6R9、SH、S-、もしくはSR9であり、
ここで、R9が、H、アルキル、アルケニル、アルキニル、もしくはアリールであり、
R4が、
であり、
式中、Xが、O、S、NR10、N+HR10、もしくはN+R10R10であり、
ここで、各R10が、独立して、H、アルキル、アルケニル、アルキニル、アリール、
であり、
ここで、各R11が、独立して、H、アルキル、アルケニル、もしくはアルキニルであり、
R5およびR6が、一緒になって=Oであり、
R7およびR8が、各々Hであり;かつ
前記チェックポイント阻害剤が、抗PD-1抗体または抗PD-L1抗体である、組成物。 - 前記組み合わせ物または組成物は、前記がんの阻害、退縮、または静止を誘発する、請求項1、3~41および51のいずれか一項に記載の組み合わせ物または請求項2および6~52のいずれか一項に記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023003205A JP2023036999A (ja) | 2016-12-08 | 2023-01-12 | 免疫応答を調節するためのオキサビシクロヘプタン |
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662497949P | 2016-12-08 | 2016-12-08 | |
| US62/497,949 | 2016-12-08 | ||
| US201762465001P | 2017-02-28 | 2017-02-28 | |
| US62/465,001 | 2017-02-28 | ||
| US201762545373P | 2017-08-14 | 2017-08-14 | |
| US62/545,373 | 2017-08-14 | ||
| PCT/US2017/065270 WO2018107004A1 (en) | 2016-12-08 | 2017-12-08 | Oxabicycloheptanes for modulation of immune response |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023003205A Division JP2023036999A (ja) | 2016-12-08 | 2023-01-12 | 免疫応答を調節するためのオキサビシクロヘプタン |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020502094A JP2020502094A (ja) | 2020-01-23 |
| JP2020502094A5 JP2020502094A5 (ja) | 2021-01-21 |
| JP7246309B2 true JP7246309B2 (ja) | 2023-03-27 |
Family
ID=62491355
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019530702A Active JP7246309B2 (ja) | 2016-12-08 | 2017-12-08 | 免疫応答を調節するためのオキサビシクロヘプタン |
| JP2023003205A Pending JP2023036999A (ja) | 2016-12-08 | 2023-01-12 | 免疫応答を調節するためのオキサビシクロヘプタン |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023003205A Pending JP2023036999A (ja) | 2016-12-08 | 2023-01-12 | 免疫応答を調節するためのオキサビシクロヘプタン |
Country Status (14)
| Country | Link |
|---|---|
| US (2) | US12168008B2 (ja) |
| EP (2) | EP4324477A3 (ja) |
| JP (2) | JP7246309B2 (ja) |
| KR (2) | KR20240042151A (ja) |
| CN (2) | CN116585480A (ja) |
| AU (1) | AU2017370731B2 (ja) |
| BR (1) | BR112019011627A2 (ja) |
| CA (1) | CA3046515A1 (ja) |
| DK (1) | DK3551629T3 (ja) |
| ES (1) | ES2970913T3 (ja) |
| IL (2) | IL290857B2 (ja) |
| MX (1) | MX2019006694A (ja) |
| NZ (1) | NZ754522A (ja) |
| WO (1) | WO2018107004A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MX2015014249A (es) | 2013-04-09 | 2016-06-02 | Lixte Biotechnology Inc | Formulaciones de oxabicicloheptanos y oxabicicloheptenos. |
| ES2985668T3 (es) | 2015-05-15 | 2024-11-06 | Lixte Biotechnology Inc | Profármacos de oxabicicloheptano para uso en el tratamiento del cáncer |
| DK3551629T3 (da) | 2016-12-08 | 2024-02-12 | Lixte Biotechnology Inc | Oxabicycloheptaner til modulering af immunrespons |
| KR102723511B1 (ko) | 2019-08-13 | 2024-10-28 | 주식회사 엘지에너지솔루션 | 전극 스크랩 재활용 방법 및 이를 이용한 전극 제조 방법 |
| WO2022128546A1 (en) * | 2020-12-16 | 2022-06-23 | Merus N.V. | Multispecific antibodies for the treatment of cancer |
| JP2024504586A (ja) * | 2021-01-19 | 2024-02-01 | リクスト・バイオテクノロジー,インコーポレイテッド | 小細胞肺がんの処置のためのオキサビシクロヘプタン |
| WO2024097784A2 (en) * | 2022-11-03 | 2024-05-10 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes for treating refractory cancers |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010518081A (ja) | 2007-02-06 | 2010-05-27 | リクスト・バイオテクノロジー・ホールディングス,インコーポレイテッド | オキサビシクロヘプタンおよびオキサビシクロヘプテン、それらの製造および使用 |
| WO2016168716A1 (en) | 2015-04-17 | 2016-10-20 | Bristol-Myers Squibb Company | Compositions comprising a combination of an anti-pd-1 antibody and another antibody |
Family Cites Families (185)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2957906A (en) | 1955-10-25 | 1960-10-25 | Monsanto Chemicals | Ketones |
| US3227473A (en) | 1963-12-12 | 1966-01-04 | Julian S Halbern | Check identification |
| JPS5752354B2 (ja) | 1973-10-22 | 1982-11-06 | ||
| JPS5069091U (ja) | 1973-10-25 | 1975-06-19 | ||
| US3980674A (en) | 1974-01-28 | 1976-09-14 | Delmar Chemicals Limited | 2,3-Disubstituted 7-oxabicyclo-[2.2.1]-5-heptene |
| JPS5132733A (en) | 1974-09-10 | 1976-03-19 | Kyowa Hakko Kogyo Kk | Josozai |
| US3954913A (en) | 1975-01-06 | 1976-05-04 | The Standard Oil Company | Stabilized nitrile polymers |
| JPS5188631U (ja) | 1975-01-10 | 1976-07-15 | ||
| JPS5188631A (en) | 1975-01-31 | 1976-08-03 | Hiiryoyosatsukinzai oyobi sonoseizoho | |
| US4143054A (en) | 1977-11-04 | 1979-03-06 | E. R. Squibb & Sons, Inc. | 7-oxabicycloheptane- and 7-oxabicycloheptene compounds |
| US4218478A (en) | 1979-01-05 | 1980-08-19 | Ruiko Oiwa | Trichostatin as an antiprotozoal agent |
| US4760067A (en) | 1979-08-15 | 1988-07-26 | Merck & Co., Inc. | Allylsulfoxide enzyme inhibitors |
| US4298752A (en) | 1980-09-19 | 1981-11-03 | Regents Of The University Of California | Cycloadduct precursors of cantharidin and method |
| US4614825A (en) | 1982-05-17 | 1986-09-30 | E. R. Squibb & Sons, Inc. | 7-oxabicycloheptane and 7-oxabicycloheptene compounds |
| US4463015A (en) | 1982-08-18 | 1984-07-31 | E. R. Squibb & Sons, Inc. | Aryl substituted 7-oxabicycloheptane compounds, useful in inhibiting platelet aggregation |
| US4518696A (en) | 1983-01-11 | 1985-05-21 | Chr. Hansen's Laboratory, Inc. | Stabilized liquid bacterial suspension for oral administration to animals |
| US4524151A (en) | 1983-11-14 | 1985-06-18 | E. R. Squibb & Sons, Inc. | 7-Oxabicycloheptane thio ethers useful as cardiovascular agents |
| JPS61176523A (ja) | 1985-01-30 | 1986-08-08 | Teruhiko Beppu | 制癌剤 |
| US4654355A (en) | 1985-08-01 | 1987-03-31 | E. R. Squibb & Sons, Inc. | 7-oxabicycloheptane substituted amide-thioamide prostaglandin analogs |
| US4816579A (en) | 1986-06-04 | 1989-03-28 | E. R. Squibb & Sons, Inc. | 7-oxabicycloheptane amino-alcohol intermediates useful in making thromboxane A2 receptor antagonists |
| US4851553A (en) | 1986-06-04 | 1989-07-25 | E. R. Squibb & Sons, Inc. | 7-oxabicycloheptane amido-carboxylic acids |
| US4851423A (en) | 1986-12-10 | 1989-07-25 | Schering Corporation | Pharmaceutically active compounds |
| SU1553533A1 (ru) | 1988-01-28 | 1990-03-30 | Военная Краснознаменная академия химической защиты им.Маршала Советского Союза С.К.Тимошенко | Способ получени 1,4-бисполифторалкил-7-оксбицикло [2.2.1]гептанов |
| JP2789365B2 (ja) | 1988-12-14 | 1998-08-20 | 塩野義製薬株式会社 | ジカルボン酸モノエステルおよびその製造法 |
| RU2015980C1 (ru) | 1990-02-06 | 1994-07-15 | Е.Р.Сквибб энд Санз, Инк. | 7-оксабициклогептилзамещенные гетероциклические амиды или их стереоизомеры в качестве антагонистов рецепторов тромбоксана |
| US5763647A (en) | 1990-03-30 | 1998-06-09 | Shionogi & Co., Ltd. | Preparation of optically active 1,4-bridged-cyclohexane carboxylic acid derivatives |
| WO1991018891A1 (en) | 1990-06-04 | 1991-12-12 | Pfizer Inc. | Aromatic pyrrolidine and thiazolidine amides |
| US5229115A (en) | 1990-07-26 | 1993-07-20 | Immunex Corporation | Adoptive immunotherapy with interleukin-7 |
| US5266710A (en) | 1990-12-18 | 1993-11-30 | Patel Ramesh N | (Exo,exo)-7-oxabicyclo[2.2.1]heptane-2,3-dimethanol; monoacyl ester and diacyl ester |
| US5206386A (en) | 1991-03-20 | 1993-04-27 | Isp Investments Inc. | Controlled release N-substituted pyrrolidone esters and process for the use thereof |
| US5580858A (en) | 1991-06-10 | 1996-12-03 | Alberta Research Council | Immunosuppressive and tolerogenic modified Lewisx compounds |
| JP3134233B2 (ja) | 1991-07-26 | 2001-02-13 | 株式会社林原生物化学研究所 | α−グリコシル ケルセチンとその製造方法並びに用途 |
| US5326898A (en) | 1992-02-11 | 1994-07-05 | Allergan, Inc. | Substituted phenylethenyl compounds having retinoid-like biological activity |
| US6602713B1 (en) | 2001-02-09 | 2003-08-05 | Isis Pharmaceuticals, Inc. | Antisense modulation of protein phosphatase 2 catalytic subunit beta expression |
| US5580856A (en) | 1994-07-15 | 1996-12-03 | Prestrelski; Steven J. | Formulation of a reconstituted protein, and method and kit for the production thereof |
| US5518993A (en) | 1994-08-12 | 1996-05-21 | Buckman Laboratories International, Inc. | Pesticidal compositions containing ethoxylated fatty amines for increasing the effectiveness of endothal and salts thereof |
| US5770382A (en) | 1994-12-30 | 1998-06-23 | Ligand Pharmaceuticals, Inc. | Tricyclic retinoids, methods for their production and use |
| US6222055B1 (en) | 1995-07-06 | 2001-04-24 | Fraunhofer-Gesellschaft Zur Foerderung Der Angwandten Forschung E.V. | Hydrolyzable and polymerizable and/or polyadditive silanes |
| DE19600707B4 (de) | 1996-01-11 | 2004-02-19 | Glüsenkamp, Karl-Heinz, Dr. | Biyclische Anhydrid-Wirkstoff-Verbindungen, Verfahren zur Herstellung und Verwendung derselben |
| US5968965A (en) | 1996-01-30 | 1999-10-19 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6777217B1 (en) | 1996-03-26 | 2004-08-17 | President And Fellows Of Harvard College | Histone deacetylases, and uses related thereto |
| US5925651A (en) | 1996-04-03 | 1999-07-20 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6387673B1 (en) | 1997-05-01 | 2002-05-14 | The Salk Institute For Biological Studies | Compounds useful for the modulation of processes mediated by nuclear hormone receptors, methods for the identification and use of such compounds |
| DK2018858T3 (da) | 1997-10-15 | 2013-01-07 | Polarx Biopharmaceuticals Inc | Sammensætninger og fremgangsmåder til behandlingen af primære og metastatiske neoplastiske sygdomme ved anvendelse af arsentrioxid |
| US6632823B1 (en) | 1997-12-22 | 2003-10-14 | Merck & Co., Inc. | Substituted pyridine compounds useful as modulators of acetylcholine receptors |
| US6262116B1 (en) | 1998-01-23 | 2001-07-17 | Sloan-Kettering Institute For Cancer Research | Transcription therapy for cancers |
| JP2002516880A (ja) | 1998-06-05 | 2002-06-11 | テクニオン リサーチ アンド デベロップメント ファウンデーション リミテッド | インスリンを補った乳児用調製乳 |
| AUPP466598A0 (en) | 1998-07-14 | 1998-08-06 | University Of Newcastle Research Associates Limited, The | Product and process |
| US20040110822A1 (en) | 1998-07-14 | 2004-06-10 | The University Of Newcastle Research Associates | Anhydride modified cantharidin analogues useful in the treatment of cancer |
| JP4511042B2 (ja) | 1998-08-07 | 2010-07-28 | メルク セローノ ソシエテ アノニム | 不妊症の治療のためのfsh模倣物 |
| US20020151515A1 (en) | 1999-06-18 | 2002-10-17 | Roberts Bruce L. | Preparation and use of superior vaccines |
| US6949624B1 (en) | 1999-08-03 | 2005-09-27 | The United States Of America As Represented By The Department Of Health And Human Services | Cloning of the human nuclear receptor co-repressor gene |
| EA200601252A1 (ru) | 1999-09-08 | 2006-10-27 | Слоан-Кеттеринг Инститьют Фор Кэнсер Рисёч | Новый класс веществ, вызывающих дифференцировку клеток и являющихся ингибиторами гистондеацетилазы, и способы их применения |
| US7605185B2 (en) | 1999-11-23 | 2009-10-20 | Gerhart Graupner | Treatment of arrhythmia by retinoids affecting signal transduction |
| WO2001062242A1 (en) | 2000-02-24 | 2001-08-30 | Biocryst Pharmaceuticals, Inc. | Prodrugs of substituted cyclopentane and cyclopentene compounds useful as neuraminidase inhibitors |
| JP4518627B2 (ja) | 2000-03-14 | 2010-08-04 | 旭化成イーマテリアルズ株式会社 | ヒドロキシポリアミド |
| EP1280764B1 (en) | 2000-03-24 | 2010-11-24 | Methylgene, Inc. | Inhibitors of histone deacetylase |
| DE10038043B4 (de) | 2000-08-02 | 2006-09-07 | Walter, Michael, Dr. | Phamakologisch wirksame Substanz zur Behandlung kardiovaskulärer Erkrankungen |
| PE20020354A1 (es) | 2000-09-01 | 2002-06-12 | Novartis Ag | Compuestos de hidroxamato como inhibidores de histona-desacetilasa (hda) |
| US7199137B2 (en) | 2000-09-21 | 2007-04-03 | Smithkline Beecham Plc | Imidazole derivatives as Raf kinase inhibitors |
| US6696483B2 (en) | 2000-10-03 | 2004-02-24 | Oncopharmaceutical, Inc. | Inhibitors of angiogenesis and tumor growth for local and systemic administration |
| US7154022B2 (en) | 2000-10-06 | 2006-12-26 | Board Of Trustees Operating Michigan State University | Divinyl ether synthase gene, and protein and uses thereof |
| CN1213050C (zh) | 2000-11-23 | 2005-08-03 | 拜尔公司 | 氧杂双环[2.2.1]庚烷衍生物,其制备方法和作为农药的用途 |
| US20020177692A1 (en) | 2001-04-16 | 2002-11-28 | Myriad Genetics, Incorporated | BCL-XL-interacting protein and use thereof |
| AU2002242175A1 (en) | 2001-02-16 | 2002-09-04 | Brigham And Women's Hospital | Methods for modulating an immune response by modulating the interaction between ctla4 and pp2a |
| AUPR392301A0 (en) | 2001-03-23 | 2001-04-26 | University Of Newcastle Research Associates Limited, The | Protein phosphatase inhibitors |
| US20040253637A1 (en) | 2001-04-13 | 2004-12-16 | Biosite Incorporated | Markers for differential diagnosis and methods of use thereof |
| US6905669B2 (en) | 2001-04-24 | 2005-06-14 | Supergen, Inc. | Compositions and methods for reestablishing gene transcription through inhibition of DNA methylation and histone deacetylase |
| DE10122898A1 (de) | 2001-05-11 | 2002-11-14 | Haarmann & Reimer Gmbh | Verwendung von Hydroxyflavanonen zur Maskierung des bitteren Geschmacks |
| US20070015144A9 (en) | 2001-05-25 | 2007-01-18 | Genset, S.A. | Human cDNAs and proteins and uses thereof |
| AU2002322721B2 (en) | 2001-08-03 | 2009-01-08 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Acylthiols and component thiol compositions as anti-HIV and anti-retroviral agents |
| US20040010045A1 (en) | 2001-09-07 | 2004-01-15 | Taolin Yi | Therapeutic compositions comprised of pentamidine and methods of using same to treat cancer |
| US7179450B2 (en) | 2001-09-20 | 2007-02-20 | Medi-Physics, Inc. | Methods for in vivo evaluation of pulmonary physiology and/or function using NMR signals of polarized Xe |
| US20040087657A1 (en) | 2001-10-16 | 2004-05-06 | Richon Victoria M. | Treatment of neurodegenerative diseases and cancer of the brain using histone deacetylase inhibitors |
| CN100457183C (zh) | 2001-11-06 | 2009-02-04 | 诺瓦提斯公司 | 环氧酶-2抑制剂/组蛋白脱乙酰酶抑制剂的组合 |
| EP1463713A1 (en) | 2001-11-23 | 2004-10-06 | Eli Lilly And Company | Prodrugs of excitatory amino acids |
| JP2004035408A (ja) | 2002-02-15 | 2004-02-05 | Chiron Corp | テザシタビンを含有する安定な組成物 |
| WO2003070754A1 (fr) | 2002-02-20 | 2003-08-28 | Minoru Yoshida | Inhibiteurs d'histone desacetylase et procede de production de ces inhibiteurs |
| US7456219B2 (en) | 2002-03-04 | 2008-11-25 | Merck Hdac Research, Llc | Polymorphs of suberoylanilide hydroxamic acid |
| US7148257B2 (en) | 2002-03-04 | 2006-12-12 | Merck Hdac Research, Llc | Methods of treating mesothelioma with suberoylanilide hydroxamic acid |
| EA013642B1 (ru) | 2002-03-08 | 2010-06-30 | Басф Акциенгезельшафт | Фунгицидная смесь на базе протиоконазола с хлорпирифосом |
| US6809118B2 (en) | 2002-07-25 | 2004-10-26 | Yih-Lin Chung | Methods for therapy of radiation cutaneous syndrome |
| IL149404A0 (en) | 2002-04-29 | 2002-11-10 | Yissum Res Dev Co | METHODS AND COMPOSITIONS FOR MODULATING β-CATENIN PHOSPHORYLATION |
| WO2003092616A2 (en) | 2002-05-01 | 2003-11-13 | The Cleveland Clinic Foundation | Therapeutic compositions comprised of pentamidine and methods of using same to treat cancer |
| US20040087531A1 (en) | 2002-05-16 | 2004-05-06 | Adam Telerman | Compositions and methods for the treatment of cancer |
| NZ538686A (en) | 2002-09-23 | 2008-01-31 | Schering Corp | Novel imidazopyrazines as cyclin dependent kinase inhibitors |
| US7154002B1 (en) | 2002-10-08 | 2006-12-26 | Takeda San Diego, Inc. | Histone deacetylase inhibitors |
| US7189740B2 (en) | 2002-10-15 | 2007-03-13 | Celgene Corporation | Methods of using 3-(4-amino-oxo-1,3-dihydro-isoindol-2-yl)-piperidine-2,6-dione for the treatment and management of myelodysplastic syndromes |
| US8404716B2 (en) | 2002-10-15 | 2013-03-26 | Celgene Corporation | Methods of treating myelodysplastic syndromes with a combination therapy using lenalidomide and azacitidine |
| DE03768629T1 (de) | 2002-11-05 | 2006-01-26 | The Regents Of The University Of California, Oakland | Verfahren und materialien zur untersuchung von mit glioblastomprogression assoziierten wegen |
| GB0226855D0 (en) | 2002-11-18 | 2002-12-24 | Queen Mary & Westfield College | Histone deacetylase inhibitors |
| CN1753912B (zh) | 2002-12-23 | 2011-11-02 | 惠氏公司 | 抗pd-1抗体及其用途 |
| US20040197888A1 (en) | 2002-12-31 | 2004-10-07 | Armour Christopher D. | Alternatively spliced isoforms of histone deacetylase 3 (HDAC3) |
| US20050222013A1 (en) | 2003-01-16 | 2005-10-06 | Georgetown University | Methods for the use of inhibitors of histone deacetylase as synergistic agents in cancer therapy |
| US8802116B2 (en) | 2003-02-27 | 2014-08-12 | Novasel Australia Pty. Ltd. | Poloxamer emulsion preparations |
| CA2518407A1 (en) | 2003-03-12 | 2004-09-23 | Samaritan Pharmaceuticals, Inc. | Animal model simulating neurologic disease |
| ES2423800T3 (es) | 2003-03-28 | 2013-09-24 | Novartis Vaccines And Diagnostics, Inc. | Uso de compuestos orgánicos para la inmunopotenciación |
| US7842835B2 (en) | 2003-07-07 | 2010-11-30 | Georgetown University | Histone deacetylase inhibitors and methods of use thereof |
| WO2005025620A2 (en) | 2003-08-13 | 2005-03-24 | Pharmacia Corporation | Combination therapy with inhibitors of inducible nitric oxide synthase and alkylating agents |
| US7514438B2 (en) | 2003-08-13 | 2009-04-07 | Amgen, Inc. | Melanin concentrating hormone receptor antagonist |
| CA2535585A1 (en) | 2003-08-21 | 2005-03-03 | Osaka University | Pharmaceutical composition for preventing or remedying cardiac hypertrophy and cardiocascular disease caused thereby |
| US7378409B2 (en) | 2003-08-21 | 2008-05-27 | Bristol-Myers Squibb Company | Substituted cycloalkylamine derivatives as modulators of chemokine receptor activity |
| US7094193B2 (en) | 2003-08-28 | 2006-08-22 | Philip Morris Usa Inc. | High speed laser perforation of cigarette tipping paper |
| EP1670466A4 (en) | 2003-10-06 | 2007-04-25 | Glaxo Group Ltd | PREPARATION OF 1,6,7-TRISUBSTITUTED AZABENIC ZIMIDAZOLES AS KINASE-INHIBITORS |
| EP1678121A4 (en) | 2003-10-24 | 2007-07-25 | Exelixis Inc | MODULATORS OF TAO KINASES AND METHODS OF USE |
| US20050182011A1 (en) | 2003-11-13 | 2005-08-18 | Eric Olson | Inhibition of TRP channels as a treatment for cardiac hypertrophy and heart failure |
| GB0328157D0 (en) | 2003-12-04 | 2004-01-07 | Imp College Innovations Ltd | Compounds |
| EP1699436A2 (en) | 2003-12-12 | 2006-09-13 | Myogen, Inc. | Enoximone formulations and their use in the treatment of cardiac hypertrophy and heart failure |
| US8652502B2 (en) | 2003-12-19 | 2014-02-18 | Cordis Corporation | Local vascular delivery of trichostatin A alone or in combination with sirolimus to prevent restenosis following vascular injury |
| US20050282893A1 (en) | 2004-01-30 | 2005-12-22 | Au Jessie L | Methods and compositions for using suramin, pentosan, polysulfate, telomerase antisense and telomerase inhibitors |
| US20050283841A1 (en) | 2004-02-02 | 2005-12-22 | Mckinsey Timothy A | Inhibition of protein kinase C-related kinase (PRK) as a treatment for cardiac hypertrophy and heart failure |
| US7253204B2 (en) | 2004-03-26 | 2007-08-07 | Methylgene Inc. | Inhibitors of histone deacetylase |
| FR2872704B1 (fr) | 2004-07-12 | 2007-11-02 | Laurent Schwartz | Pluritherapie contre le cancer |
| CN1586500A (zh) | 2004-07-19 | 2005-03-02 | 俞锋 | 治疗肿瘤的斑蝥酸钠注射剂及其制备方法 |
| EP1786428B1 (en) | 2004-08-17 | 2012-05-16 | The Johns Hopkins University | Pde5 inhibitor compositions and methods for treating cardiac indications |
| WO2006052842A2 (en) | 2004-11-09 | 2006-05-18 | The Trustees Of The University Of Pennsylvania | Methods for diagnosis of myelodysplastic syndromes (mds) |
| KR100677149B1 (ko) | 2004-11-12 | 2007-02-02 | 삼성전자주식회사 | 잉크 조성물 |
| WO2006102760A1 (en) | 2005-04-01 | 2006-10-05 | Methylgene Inc. | Inhibitors of histone deacetylase |
| CN1304396C (zh) | 2005-04-08 | 2007-03-14 | 中山大学 | 斑蝥素衍生物及其制备方法 |
| MX2007013978A (es) | 2005-05-09 | 2008-02-22 | Ono Pharmaceutical Co | Anticuerpos monoclonales humanos a muerte programada 1 (pd-1) y metodos para tratamiento de cancer utilizando anticuerpos anti-pd-1 solos o en combinacion con otros inmunoterapeuticos. |
| GB0511266D0 (en) | 2005-06-02 | 2005-07-13 | Trust | Chemical compounds |
| CN105330741B (zh) | 2005-07-01 | 2023-01-31 | E.R.施贵宝&圣斯有限责任公司 | 抗程序性死亡配体1(pd-l1)的人单克隆抗体 |
| WO2007014029A2 (en) | 2005-07-22 | 2007-02-01 | The Regents Of The University Of Colorado, A Body Corporate | Yin yang 1 as a treatment for cardiac hypertrophy and heart failure |
| AU2006280062A1 (en) | 2005-08-10 | 2007-02-22 | Novartis Ag | Method of use of deacetylase inhibitors |
| EP2275096A3 (en) | 2005-08-26 | 2011-07-13 | Braincells, Inc. | Neurogenesis via modulation of the muscarinic receptors |
| US20070092553A1 (en) | 2005-10-21 | 2007-04-26 | Pfab Lp | Compositions and methods of making rapidly dissolving lonically masked formulations |
| BRPI0620040A2 (pt) | 2005-12-19 | 2011-10-25 | Methylgene Inc | inibidores de histona desacetilase para realçar a atividade de agentes antifúngicos |
| WO2007092414A2 (en) | 2006-02-06 | 2007-08-16 | Lixte Biotechnology Holdings, Inc. | Use of phosphatases to treat tumors overexpressing n-cor |
| AU2007234843B2 (en) | 2006-04-07 | 2013-07-11 | Methylgene Inc. | Inhibitors of histone deacetylase |
| PE20080695A1 (es) | 2006-04-27 | 2008-06-28 | Banyu Pharma Co Ltd | Derivados de dihidropirazolopirimidinona como inhibidores de quinasa weel |
| US20090018142A9 (en) | 2006-05-02 | 2009-01-15 | Zhengping Zhuang | Use of phosphatases to treat tumors overexpressing N-CoR |
| US20080267947A1 (en) | 2006-09-07 | 2008-10-30 | Cirrito Thomas P | Cancer therapy with cantharidin and cantharidin analogs |
| US8129340B2 (en) | 2006-09-08 | 2012-03-06 | Institut Gustave Roussy | Inhibitors of protein phosphatase 1, GADD34 and protein phosphatase 1/GADD34 complex, preparation and uses thereof |
| US20080097561A1 (en) | 2006-10-18 | 2008-04-24 | Medcool, Inc. | Dual cycle thermal system and method of use |
| AU2007321720A1 (en) | 2006-11-15 | 2008-05-22 | Genetic Technologies Limited | Compounds, compositions and methods for controlling invertebrate pests |
| US8413445B2 (en) | 2007-05-11 | 2013-04-09 | General Electric Company | Method and system for porous flame holder for hydrogen and syngas combustion |
| KR101562580B1 (ko) | 2007-06-18 | 2015-10-22 | 머크 샤프 앤 도메 비.브이. | 사람 프로그램된 사멸 수용체 pd-1에 대한 항체 |
| EP2185173A4 (en) | 2007-08-03 | 2011-01-12 | Lixte Biotechnology Inc | USE OF PHOSPHATASES FOR THE TREATMENT OF NEUROBLASTOMES AND MEDULLOGASTOMES |
| CN101854804B (zh) | 2007-10-01 | 2014-07-23 | 利克斯特生物技术公司 | Hdac抑制剂 |
| JP5069091B2 (ja) | 2007-12-12 | 2012-11-07 | 三菱電機株式会社 | 監視カメラおよび監視カメラシステム |
| ES2639857T3 (es) | 2008-02-11 | 2017-10-30 | Cure Tech Ltd. | Anticuerpos monoclonales para el tratamiento del tumor |
| WO2009114335A2 (en) | 2008-03-12 | 2009-09-17 | Merck & Co., Inc. | Pd-1 binding proteins |
| WO2010147612A1 (en) | 2009-06-18 | 2010-12-23 | Lixte Biotechnology, Inc. | Methods of modulating cell regulation by inhibiting p53 |
| CA2730428A1 (en) | 2008-08-01 | 2010-02-04 | Lixte Biotechnology, Inc. | Methods for regulating cell mitosis by inhibiting serine/threonine phosphatase |
| US8227473B2 (en) | 2008-08-01 | 2012-07-24 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes, their preparation and use |
| AU2009277086B2 (en) | 2008-08-01 | 2015-12-10 | Lixte Biotechnology, Inc. | Neuroprotective agents for the prevention and treatment of neurodegenerative diseases |
| NZ591130A (en) | 2008-08-25 | 2012-09-28 | Amplimmune Inc | Compositions comprising a PD-1 antagonists and cyclophosphamide and methods of use thereof |
| WO2010027827A2 (en) | 2008-08-25 | 2010-03-11 | Amplimmune, Inc. | Targeted costimulatory polypeptides and methods of use to treat cancer |
| CN101367783A (zh) | 2008-10-10 | 2009-02-18 | 中国科学技术大学 | 5-羟甲基糠醛的制备方法 |
| BRPI0917592B1 (pt) | 2008-12-09 | 2021-08-17 | Genentech, Inc | Anticorpo anti-pd-l1, composição, artigos manufaturados e usos de uma composição |
| US8741295B2 (en) | 2009-02-09 | 2014-06-03 | Universite De La Mediterranee | PD-1 antibodies and PD-L1 antibodies and uses thereof |
| GB0903325D0 (en) | 2009-02-26 | 2009-04-08 | Univ Aberdeen | Antibody molecules |
| US20120135522A1 (en) | 2009-06-18 | 2012-05-31 | Kovach John S | Methods of modulating cell regulation by inhibiting p53 |
| US20130017199A1 (en) | 2009-11-24 | 2013-01-17 | AMPLIMMUNE ,Inc. a corporation | Simultaneous inhibition of pd-l1/pd-l2 |
| WO2011094683A2 (en) | 2010-01-29 | 2011-08-04 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Method of identifying myelodysplastic syndromes |
| CA2796963A1 (en) | 2010-04-23 | 2011-10-27 | Piramal Enterprises Limited | Nitric oxide releasing prodrugs of therapeutic agents |
| EP2714924B1 (en) | 2011-05-24 | 2018-03-21 | Lixte Biotechnology, Inc. | HDAC Inhibitors for use in the treatment of Gaucher's disease, von Hippel-Lindau disease, phaeochromocytoma and paragangliomas. |
| US9345705B2 (en) | 2011-09-15 | 2016-05-24 | Merck Sharp & Dohme Corp. | Compositions and methods for treating cancer |
| WO2013056211A2 (en) | 2011-10-13 | 2013-04-18 | H. Lee Moffitt Cancer Center & Research Institute, Inc. | Telomerase reverse transcriptase deficience as diagnostic marker of myelodysplastic syndrome |
| NZ702237A (en) | 2012-06-01 | 2016-08-26 | Taisho Pharmaceutical Co Ltd | Prodrug of fluorine-containing amino acid |
| WO2014005080A1 (en) | 2012-06-29 | 2014-01-03 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes for the treatment of reperfusion injury |
| CA2877167A1 (en) | 2012-06-29 | 2014-01-03 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes for the treatment of diabetes |
| US9738933B2 (en) | 2012-12-05 | 2017-08-22 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | RNF41 as a biomarker predicting response to lenalidomide in non-del(5q) MDS |
| WO2014137741A1 (en) | 2013-03-05 | 2014-09-12 | Lixte Biotechnology, Inc. | Hdac inhibitors for treating traumatic brain injury |
| EP2968279A4 (en) | 2013-03-15 | 2016-09-28 | Lixte Biotechnology Inc | SANGUINARIN ANALOG PPC2 HEMMER FOR CANCER TREATMENT |
| MX2015014249A (es) * | 2013-04-09 | 2016-06-02 | Lixte Biotechnology Inc | Formulaciones de oxabicicloheptanos y oxabicicloheptenos. |
| JP2016538281A (ja) | 2013-11-15 | 2016-12-08 | リクスト・バイオテクノロジー,インコーポレイテッド | 血液脳関門を通過するタンパク質ホスファターゼ阻害剤 |
| US9051332B1 (en) | 2013-11-20 | 2015-06-09 | Transitions Optical, Inc. | Photochromic indeno-fused ring pyran compounds |
| JOP20200094A1 (ar) | 2014-01-24 | 2017-06-16 | Dana Farber Cancer Inst Inc | جزيئات جسم مضاد لـ pd-1 واستخداماتها |
| CA2940097A1 (en) | 2014-04-28 | 2015-11-05 | Alembic Pharmaceuticals Limited | Novel polymorphic forms of vortioxetine and its pharmaceutically acceptable salts |
| EP3157336A4 (en) | 2014-06-20 | 2018-01-24 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes for the treatment of ovarian cancer |
| WO2016014783A1 (en) | 2014-07-24 | 2016-01-28 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Protein phosphatase 2a inhibitors for treating myelodysplastic syndromes |
| WO2016040877A1 (en) | 2014-09-12 | 2016-03-17 | Lixte Biotechnology, Inc. | Human dosing of phosphatase inhibitor |
| US9994584B2 (en) | 2014-10-15 | 2018-06-12 | Lixte Biotechnology, Inc. | Process of synthesizing 3-(4-methylpiperazine-1-carbonyl)-7-oxabicyclo[2.2.1] heptane-2-carboxylic acid |
| EP3258930B1 (en) | 2015-02-19 | 2020-12-09 | Lixte Biotechnology, Inc. | Oxabicycloheptanes and oxabicycloheptenes for the treatment of depressive and stress disorders |
| ES2985668T3 (es) | 2015-05-15 | 2024-11-06 | Lixte Biotechnology Inc | Profármacos de oxabicicloheptano para uso en el tratamiento del cáncer |
| IL297003A (en) | 2015-09-17 | 2022-12-01 | Novartis Ag | car-t cell treatments with improved efficacy |
| CA3051828A1 (en) | 2016-01-27 | 2017-08-03 | Lixte Biotechnology, Inc. | Clinical regimen for treating myelodysplastic syndrome with phosphatase inhibitor |
| WO2017176289A1 (en) | 2016-04-08 | 2017-10-12 | Celgene Corporation | Uses of lenalidomide and car t-cells |
| DK3551629T3 (da) | 2016-12-08 | 2024-02-12 | Lixte Biotechnology Inc | Oxabicycloheptaner til modulering af immunrespons |
| WO2019113155A1 (en) | 2017-12-05 | 2019-06-13 | Lixte Biotechnology, Inc. | Oxabicycloheptanes for treatment of secondary acute myeloid leukemia |
| WO2019241536A1 (en) | 2018-06-14 | 2019-12-19 | Lixte Biotechnology, Inc. | Oxabicycloheptanes for enhancing car t cell function |
| RU201598U1 (ru) | 2020-05-14 | 2020-12-22 | Андрей Владимирович Дмитриев | Безреагентная испарительная градирня |
| JP2024504586A (ja) | 2021-01-19 | 2024-02-01 | リクスト・バイオテクノロジー,インコーポレイテッド | 小細胞肺がんの処置のためのオキサビシクロヘプタン |
| WO2023133371A2 (en) | 2022-01-04 | 2023-07-13 | Lixte Biotechnology, Inc. | Compositions and methods for treating cancer or preventing, inhibiting or reducing risk of metastasis of a cancer |
-
2017
- 2017-12-08 DK DK17879038.2T patent/DK3551629T3/da active
- 2017-12-08 EP EP23202240.0A patent/EP4324477A3/en active Pending
- 2017-12-08 NZ NZ754522A patent/NZ754522A/en unknown
- 2017-12-08 ES ES17879038T patent/ES2970913T3/es active Active
- 2017-12-08 CN CN202310498623.5A patent/CN116585480A/zh active Pending
- 2017-12-08 US US16/467,721 patent/US12168008B2/en active Active
- 2017-12-08 MX MX2019006694A patent/MX2019006694A/es unknown
- 2017-12-08 CA CA3046515A patent/CA3046515A1/en active Pending
- 2017-12-08 KR KR1020247008982A patent/KR20240042151A/ko not_active Withdrawn
- 2017-12-08 AU AU2017370731A patent/AU2017370731B2/en active Active
- 2017-12-08 WO PCT/US2017/065270 patent/WO2018107004A1/en not_active Ceased
- 2017-12-08 KR KR1020197019763A patent/KR20190098995A/ko not_active Ceased
- 2017-12-08 BR BR112019011627-3A patent/BR112019011627A2/pt unknown
- 2017-12-08 EP EP17879038.2A patent/EP3551629B1/en active Active
- 2017-12-08 JP JP2019530702A patent/JP7246309B2/ja active Active
- 2017-12-08 CN CN201780084881.1A patent/CN110234647B/zh active Active
- 2017-12-08 IL IL290857A patent/IL290857B2/en unknown
-
2019
- 2019-06-06 IL IL267134A patent/IL267134B/en unknown
-
2023
- 2023-01-12 JP JP2023003205A patent/JP2023036999A/ja active Pending
-
2024
- 2024-12-13 US US18/979,811 patent/US20250221985A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010518081A (ja) | 2007-02-06 | 2010-05-27 | リクスト・バイオテクノロジー・ホールディングス,インコーポレイテッド | オキサビシクロヘプタンおよびオキサビシクロヘプテン、それらの製造および使用 |
| WO2016168716A1 (en) | 2015-04-17 | 2016-10-20 | Bristol-Myers Squibb Company | Compositions comprising a combination of an anti-pd-1 antibody and another antibody |
Non-Patent Citations (2)
| Title |
|---|
| INTLEKOFER, A.M. et al.,J leukoc Biol,2013年,Vol. 94,p. 25-39 |
| PARRY, R.V. et al.,Mol Cell Biol,2005年,Vol. 25, No. 21,p. 9543-9553 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023036999A (ja) | 2023-03-14 |
| JP2020502094A (ja) | 2020-01-23 |
| KR20240042151A (ko) | 2024-04-01 |
| AU2017370731B2 (en) | 2022-06-02 |
| BR112019011627A2 (pt) | 2019-11-12 |
| CN110234647A (zh) | 2019-09-13 |
| EP3551629B1 (en) | 2023-11-15 |
| EP3551629A4 (en) | 2020-07-29 |
| NZ754522A (en) | 2025-11-28 |
| CA3046515A1 (en) | 2018-06-14 |
| US20250221985A1 (en) | 2025-07-10 |
| US12168008B2 (en) | 2024-12-17 |
| EP3551629A1 (en) | 2019-10-16 |
| IL290857A (en) | 2022-04-01 |
| CN116585480A (zh) | 2023-08-15 |
| CN110234647B (zh) | 2023-05-23 |
| US20200069680A1 (en) | 2020-03-05 |
| ES2970913T3 (es) | 2024-05-31 |
| WO2018107004A1 (en) | 2018-06-14 |
| AU2017370731A1 (en) | 2019-07-04 |
| IL290857B2 (en) | 2023-03-01 |
| IL267134A (en) | 2019-08-29 |
| IL290857B (en) | 2022-11-01 |
| EP4324477A2 (en) | 2024-02-21 |
| KR20190098995A (ko) | 2019-08-23 |
| MX2019006694A (es) | 2019-08-21 |
| EP4324477A3 (en) | 2024-05-22 |
| IL267134B (en) | 2022-04-01 |
| DK3551629T3 (da) | 2024-02-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7246309B2 (ja) | 免疫応答を調節するためのオキサビシクロヘプタン | |
| US20180028531A1 (en) | Use of plinabulin in combination with immune checkpoint inhibitors | |
| US20210379106A1 (en) | Oxabicycloheptanes for enhancing car t cell function | |
| KR20180100652A (ko) | 크로멘 화합물 및 제2활성제의 조합물 | |
| US20250073230A1 (en) | Use of plinabulin in combination with immune checkpoint inhibitors | |
| US20220226281A1 (en) | Compounds for use in anti-cancer immunotherapy | |
| WO2023053142A1 (en) | Novel combination of serotonin receptor (5-htr2b) antagonist and an immunomodulator and chemotherapeutic drugs for inhibition of cancer | |
| CN113316449A (zh) | 胍那苄作为免疫疗法的佐剂 | |
| CN110891944B (zh) | 用于治疗癌症的化合物、组合物及其用途 | |
| AU2020343329C1 (en) | Methods of treatment | |
| CA3214753A1 (en) | Dosing of bispecific t cell engager | |
| HK40015901A (en) | Oxabicycloheptanes for modulation of immune response | |
| HK40015901B (en) | Oxabicycloheptanes for modulation of immune response | |
| BR112017016902B1 (pt) | Composição farmacêutica, respectivo uso e uso de plinabulina | |
| NZ750444B2 (en) | Use of plinabulin in combination with immune checkpoint inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201207 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201207 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211210 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220309 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220510 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220510 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20220929 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230112 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20230112 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20230120 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20230123 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230310 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230314 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7246309 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |