JP2022546400A - 高濃度の薬理学的に活性な抗体の新規製剤 - Google Patents
高濃度の薬理学的に活性な抗体の新規製剤 Download PDFInfo
- Publication number
- JP2022546400A JP2022546400A JP2022513090A JP2022513090A JP2022546400A JP 2022546400 A JP2022546400 A JP 2022546400A JP 2022513090 A JP2022513090 A JP 2022513090A JP 2022513090 A JP2022513090 A JP 2022513090A JP 2022546400 A JP2022546400 A JP 2022546400A
- Authority
- JP
- Japan
- Prior art keywords
- pharmaceutical
- formulation
- lysine
- antibody
- omalizumab
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/42—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against immunoglobulins
- C07K16/4283—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an allotypic or isotypic determinant on Ig
- C07K16/4291—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an allotypic or isotypic determinant on Ig against IgE
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Dermatology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Inorganic Chemistry (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Description
a.IgEに結合する薬理学的に活性な抗体;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含み、
抗体濃度が少なくとも100mg/mlである医薬安定液体製剤を提供する。
a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのリジン又はリジンHCl;
d.0.02%~約0.04%のポロキサマー188;
e.pH6.0を含む医薬液体製剤を提供する。
a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのアルギニン又はアルギニンHCl;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0を含む医薬液体製剤を提供する。
a.IgEに結合する薬理学的に活性な抗体;
b.ヒスチジンバッファー;
c.凝集阻害剤としてのリジン又その好適な塩;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含み、
抗体濃度が少なくとも100mg/mlである医薬液体製剤を提供する。
本明細書で使用される用語は、一般に、本発明の文脈において、及び各用語が使用される特定の文脈において、当技術分野におけるそれらの通常の意味を有する。本発明を説明するために使用される特定の用語は、本発明の説明に関して実務者に更なるガイダンスを提供するために、以下又は本明細書の他の箇所で論じられる。特定の用語の同義語が与えられる。1以上の同義語の記載は、他の同義語の使用を排除しない。本明細書で論じられる任意の用語の例を含む本明細書の任意の箇所での例の使用は、例示に過ぎず、本発明又は任意の例示された用語の範囲及び意味を何ら限定しない。本発明は、本明細書に与えられる様々な実施形態に限定されない。特段の断りがない限り、本明細書で使用される技術的及び科学的用語はいずれも、本発明が関連する技術分野における通常の知識を有する者によって通常理解される意味と同一の意味を有する。矛盾が生じる場合には、定義を含む本明細書が優先される。
a.IgEに結合する薬理学的に活性な抗体;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含み、
抗体濃度が少なくとも100mg/mlである医薬安定液体製剤を提供する。
a.125mg/ml~約160mg/mlのオマリズマブ;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.125mg/ml~約160mg/mlのオマリズマブ;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.150mg/ml~約160mg/mlのオマリズマブ;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.オマリズマブ;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される、約1mM~約200mMの濃度の好適な凝集阻害剤;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.オマリズマブ;
b.5mg/ml~約20mg/mlのリン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される、約1mM~約200mMの濃度の好適な凝集阻害剤;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.オマリズマブ;
b.5mg/ml~約20mg/mlのリン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される、約1mM~約200mMの濃度の好適な凝集阻害剤;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0~7.0を含む医薬安定液体製剤を提供する。
a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのリジン又はリジンHCl;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0を含む医薬安定液体製剤を提供する。
a.約150mg/mlのオマリズマブ抗体;
b.約20mMのリン酸バッファー;
c.凝集阻害剤としての約200mMのリジン又はリジンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む医薬安定液体製剤を提供する。
a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのアルギニン又はアルギニンHCl;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0を含む医薬安定液体製剤を提供する。
a.約150mg/mlのオマリズマブ抗体;
b.約20mMのリン酸バッファー;
c.凝集阻害剤としての約200mMのアルギニン又はアルギニンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む医薬安定液体製剤を提供する。
a.約50mg/ml~150mg/mlの量の高濃度の薬理学的に活性な抗IgE抗体;
b.少なくとも約8mM又は20mMの量のヒスチジン又はヒスチジンHClを含む好適なバッファー;
c.好適な凝集阻害剤としてリジン又はリジンHCL;
d.ポリソルベート又はポロキサマー188;及び
e.pH6.0~7.0を含む新規医薬安定製剤を提供する。
a.高濃度の薬理学的に活性な抗体;
b.好適なバッファーとしてメチオニン;
c.好適な凝集阻害剤としてアルギニン又はアルギニンHCl;
d.ポリソルベート又はポロキサマー188;及び
e.pH6.0~7.0を含む新規医薬安定製剤を提供する。
a.高濃度の薬理学的に活性な抗体;
b.好適なバッファーとしてメチオニン及びリン酸塩;
c.好適な凝集阻害剤としてアルギニン又はアルギニンHCl;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む新規医薬安定製剤を提供する。
a.高濃度の薬理学的に活性な抗体;
b.好適なバッファーとしてヒスチジン;
c.好適な凝集阻害剤としてリジン又はリジンHCl;
d.ポロキサマー188;及び
e.pH6.0~7.0を含む新規医薬安定製剤を提供する。
a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのヒスチジンバッファー;
c.凝集阻害剤としての100mM~約200mMのリジン又はリジンHCl;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0を含む新規医薬安定製剤を提供する。
a.約150mg/mlのオマリズマブ抗体;
b.約20mMのヒスチジンバッファー;
c.凝集阻害剤としての約200mMのリジン又はリジンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む新規医薬安定製剤を提供する。
オマリズマブ注射用製剤を、皮下投与用に150mg/mLの抗体濃度で調製した。
オマリズマブ注射用製剤を、皮下投与用に150mg/mLの抗体濃度で調製した。
オマリズマブ注射用製剤を、皮下投与用に150mg/mLの抗体濃度で調製した。
実施例1、実施例2、及び実施例3に記載される3種類の製剤はいずれも、タンパク質のフォールディング状態及び熱安定性を分析するために、示差走査蛍光定量法(DSF)によって更に評価される。これは、温度上昇範囲(例えば、25℃~95℃)におけるタンパク質の安定性、タンパク質の制御された加熱(例えば、0.5℃/分)による熱タンパク質アンフォールディングを調べるための高速で高信頼性の強力なツールである。サンプルのタンパク質濃度を分析前に規格化した。
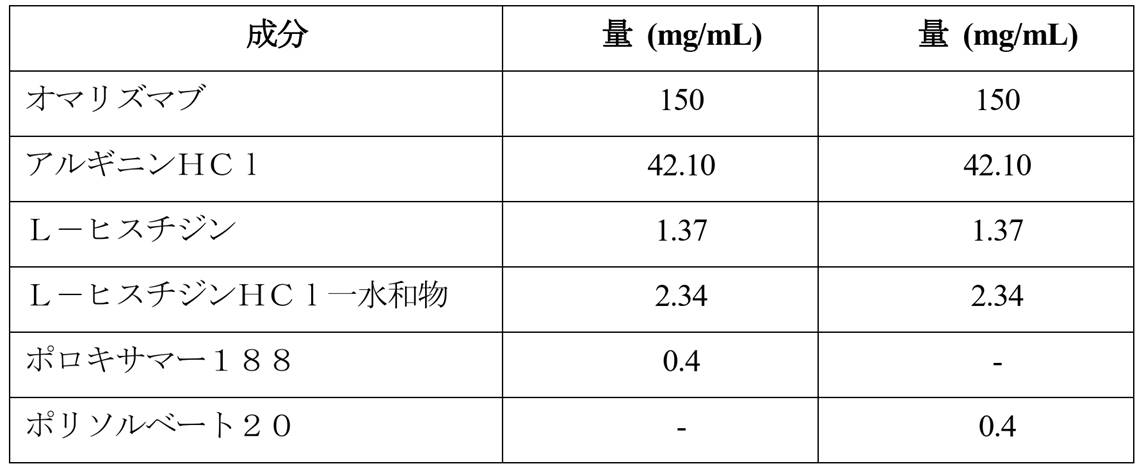
製剤は、20mMのヒスチジンバッファー、200mMのリジンHCl、及びポロキサマー188をpH6.0で添加して調製した。バルク溶液を、0.2μmのPVDFフィルターでろ過してろ過溶液を得、1mLのろ過溶液を1mLのガラス製PFSに充填した。
F2製剤を、20mMのヒスチジンバッファー、200mMのアルギニンHCl、及びポロキサマー188をpH6.0で添加して調製した。バルク溶液を、0.2μmのPVDFフィルターでろ過してろ過溶液を得、1mLのろ過溶液を1mLのガラス製PFSに充填した。
Claims (36)
- 医薬安定液体製剤であって、
a.IgEに結合する薬理学的に活性な抗体;
b.リン酸バッファー;
c.アルギニン若しくはリジン又はそれらの好適な塩から選択される好適な凝集阻害剤;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含み、
抗体濃度が少なくとも100mg/mlであることを特徴とする、医薬安定液体製剤。 - 前記IgEに結合する薬理学的に活性な抗体が、オマリズマブである、請求項1に記載の医薬製剤。
- 前記オマリズマブが、少なくとも約100mg/ml~約200mg/mlで存在する、請求項2に記載の医薬製剤。
- 前記オマリズマブが、少なくとも約150mg/mlで存在する、請求項3に記載の医薬製剤。
- 前記リン酸バッファーが、約5mg/ml~約20mg/mlで存在する、請求項1に記載の医薬製剤。
- 凝集阻害剤としての前記アルギニンが、約100mM~約200mMで存在する、請求項1に記載の医薬製剤。
- 凝集阻害剤としての前記アルギニンが、約200mMで存在する、請求項6に記載の医薬製剤。
- 凝集阻害剤としての前記リジンが、約100mM~約200mMで存在する、請求項1に記載の医薬製剤。
- 凝集阻害剤としての前記リジンが、約200mMで存在する、請求項8に記載の医薬製剤。
- 前記アルギニン若しくはリジンの好適な塩が、アルギニンHCl若しくはリジンHClである、請求項1に記載の医薬製剤。
- 前記界面活性剤が、約0.02%~約0.04%で存在する、請求項1に記載の医薬製剤。
- 前記界面活性剤が、ポリソルベート又はポロキサマー188から選択される、請求項11に記載の医薬製剤。
- 前記界面活性剤が、ポロキサマー188である、請求項11に記載の医薬製剤。
- 前記pHが、6.0である、請求項11に記載の医薬製剤。
- a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのリジン又はリジンHCl;
d.0.02%~約0.04%のポロキサマー188;
e.pH6.0を含む、請求項1に記載の医薬液体製剤。 - a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのリン酸バッファー;
c.凝集阻害剤としての100mM~約200mMのアルギニン又はアルギニンHCl;
d.0.02%~約0.04%のポロキサマー188;
e.pH6.0を含む、請求項1に記載の医薬液体製剤。 - a.約150mg/mlのオマリズマブ抗体;
b.約20mMのリン酸バッファー;
c.凝集阻害剤としての約200mMのリジン又はリジンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む、請求項15に記載の医薬液体製剤。 - a.約150mg/mlのオマリズマブ抗体;
b.約20mMのリン酸バッファー;
c.凝集阻害剤としての約200mMのアルギニン又はアルギニンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む、請求項16に記載の医薬液体製剤。 - ヒスチジンバッファーを含まない、請求項1に記載の医薬液体製剤。
- 請求項1に記載の医薬液体製剤を含むことを特徴とする、薬物送達デバイス。
- 喘息、蕁麻疹、アレルギー、慢性特発性蕁麻疹から選択される疾患を有する患者に請求項1に記載の医薬液体製剤を投与して、前記患者の前記疾患を治療することを含む、治療方法。
- 約20cs以下の動粘度を有する、請求項1に記載の医薬液体製剤。
- 約10csの動粘度を有する、請求項22に記載の医薬液体製剤。
- 医薬安定液体製剤であって、
a.IgEに結合する薬理学的に活性な抗体;
b.ヒスチジンバッファー;
c.凝集阻害剤としてのリジン又はその好適な塩;
d.好適な界面活性剤;及び
e.pH6.0~7.0を含み、
抗体濃度が少なくとも100mg/mlであることを特徴とする、医薬安定液体製剤。 - 前記IgEに結合する薬理学的に活性な抗体が、オマリズマブである、請求項24に記載の医薬製剤。
- 前記オマリズマブが、少なくとも約100mg/ml~約200mg/mlで存在する、請求項25に記載の医薬製剤。
- 前記オマリズマブが、少なくとも約150mg/mlで存在する、請求項26に記載の医薬製剤。
- 前記ヒスチジンバッファーが、約5mg/ml~約20mg/mlで存在する、請求項27に記載の医薬製剤。
- 凝集阻害剤としての前記リジンが、約100mM~約200mMで存在する、請求項28に記載の医薬製剤。
- 凝集阻害剤としての前記リジンが、約200mMで存在する、請求項29に記載の医薬製剤。
- a.100~160mg/mlのオマリズマブ抗体;
b.5mM~20mMのヒスチジンバッファー;
c.凝集阻害剤としての100mM~約200mMのリジン又はリジンHCl;
d.0.02%~約0.04%のポロキサマー188;及び
e.pH6.0を含む、請求項24に記載の医薬液体製剤。 - a.約150mg/mlのオマリズマブ抗体;
b.約20mMのヒスチジンバッファー;
c.凝集阻害剤としての約200mMのリジン又はリジンHCl;
d.約0.04%のポロキサマー188;及び
e.pH6.0を含む、請求項31に記載の医薬液体製剤。 - アルギニンを含まない、請求項24に記載の医薬液体製剤。
- 請求項24に記載の医薬液体製剤を含むことを特徴とする、薬物送達デバイス。
- 喘息、蕁麻疹、アレルギー、慢性特発性蕁麻疹から選択される疾患を有する患者に請求項24に記載の医薬液体製剤を投与して、前記患者の前記疾患を治療することを含む、治療方法。
- 約10csの動粘度を有する、請求項24に記載の医薬液体製剤。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN201921035059 | 2019-08-30 | ||
| IN201921035059 | 2019-08-30 | ||
| PCT/IB2020/058080 WO2021038532A1 (en) | 2019-08-30 | 2020-08-29 | Novel formulation of highly concentrated pharmacologically active antibody |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2022546400A true JP2022546400A (ja) | 2022-11-04 |
| JPWO2021038532A5 JPWO2021038532A5 (ja) | 2023-11-24 |
| JP7792137B2 JP7792137B2 (ja) | 2025-12-25 |
Family
ID=74684124
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022513090A Active JP7792137B2 (ja) | 2019-08-30 | 2020-08-29 | 高濃度の薬理学的に活性な抗体の新規製剤 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US20220267473A1 (ja) |
| EP (1) | EP4021497A4 (ja) |
| JP (1) | JP7792137B2 (ja) |
| AU (1) | AU2020337093B2 (ja) |
| CA (1) | CA3152838A1 (ja) |
| WO (1) | WO2021038532A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2021262609A1 (en) | 2020-05-01 | 2022-12-22 | Kashiv Biosciences, Llc | An improved process of purification of protein |
| CA3237624A1 (en) * | 2023-07-28 | 2025-04-24 | Genentech, Inc. | NEW USES FOR OMALIZUMAB |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007524602A (ja) * | 2003-04-04 | 2007-08-30 | ジェネンテック・インコーポレーテッド | 高濃度抗体及びタンパク質製剤 |
| JP2010529999A (ja) * | 2007-06-14 | 2010-09-02 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | 抗体製剤 |
| JP2015509526A (ja) * | 2012-03-07 | 2015-03-30 | カディラ ヘルスケア リミティド | 医薬製剤 |
| JP2016515120A (ja) * | 2013-03-15 | 2016-05-26 | バイオジェン・エムエイ・インコーポレイテッドBiogen MA Inc. | 抗アルファvベータ5抗体を用いた急性腎損傷の治療及び予防 |
| WO2017104778A1 (ja) * | 2015-12-18 | 2017-06-22 | アステラス製薬株式会社 | 抗ヒトtslp受容体抗体含有医薬組成物 |
| JP2018500380A (ja) * | 2014-12-31 | 2018-01-11 | ノベルメド セラピューティクス,インコーポレーテッド | アグリコシル化治療用抗体の製剤 |
| WO2019023564A1 (en) * | 2017-07-27 | 2019-01-31 | Alexion Pharmaceutical, Inc. | ANTI-C5 ANTIBODY FORMULATIONS WITH HIGH CONCENTRATION |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE60139944D1 (de) * | 2000-10-12 | 2009-10-29 | Genentech Inc | Niederviskose konzentrierte proteinformulierungen |
| US8703126B2 (en) | 2000-10-12 | 2014-04-22 | Genentech, Inc. | Reduced-viscosity concentrated protein formulations |
| SG10201500871TA (en) * | 2009-11-13 | 2015-04-29 | Sanofi Aventis Deutschland | Pharmaceutical composition comprising a glp-1 agonist and methionine |
| WO2013096791A1 (en) * | 2011-12-23 | 2013-06-27 | Genentech, Inc. | Process for making high concentration protein formulations |
| PE20150964A1 (es) * | 2012-09-07 | 2015-07-25 | Coherus Biosciences Inc | Formulaciones acuosas estables de adalimumab |
| RS57864B1 (sr) * | 2013-06-17 | 2018-12-31 | De Staat Der Nederlanden Vert Door De Minister Van Vws Ministerie Van Volksgezondheid Welzijn En Spo | Postupci za sprečavanje agregacije virusnih komponenti |
| ES2962373T3 (es) * | 2016-04-13 | 2024-03-18 | Medimmune Llc | Uso de aminoácidos como compuestos estabilizadores en composiciones farmacéuticas que contienen altas concentraciones de agentes terapéuticos basados en proteínas |
| CA3063324A1 (en) * | 2017-05-16 | 2018-11-22 | Bhami's Research Laboratory, Pvt. Ltd. | High concentration protein formulations with reduced viscosity |
-
2020
- 2020-08-29 AU AU2020337093A patent/AU2020337093B2/en active Active
- 2020-08-29 JP JP2022513090A patent/JP7792137B2/ja active Active
- 2020-08-29 WO PCT/IB2020/058080 patent/WO2021038532A1/en not_active Ceased
- 2020-08-29 EP EP20858260.1A patent/EP4021497A4/en active Pending
- 2020-08-29 CA CA3152838A patent/CA3152838A1/en active Pending
-
2022
- 2022-02-28 US US17/682,314 patent/US20220267473A1/en active Pending
-
2024
- 2024-10-25 US US18/926,965 patent/US20250043027A1/en active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007524602A (ja) * | 2003-04-04 | 2007-08-30 | ジェネンテック・インコーポレーテッド | 高濃度抗体及びタンパク質製剤 |
| JP2010529999A (ja) * | 2007-06-14 | 2010-09-02 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | 抗体製剤 |
| JP2015509526A (ja) * | 2012-03-07 | 2015-03-30 | カディラ ヘルスケア リミティド | 医薬製剤 |
| JP2016515120A (ja) * | 2013-03-15 | 2016-05-26 | バイオジェン・エムエイ・インコーポレイテッドBiogen MA Inc. | 抗アルファvベータ5抗体を用いた急性腎損傷の治療及び予防 |
| JP2018500380A (ja) * | 2014-12-31 | 2018-01-11 | ノベルメド セラピューティクス,インコーポレーテッド | アグリコシル化治療用抗体の製剤 |
| WO2017104778A1 (ja) * | 2015-12-18 | 2017-06-22 | アステラス製薬株式会社 | 抗ヒトtslp受容体抗体含有医薬組成物 |
| WO2019023564A1 (en) * | 2017-07-27 | 2019-01-31 | Alexion Pharmaceutical, Inc. | ANTI-C5 ANTIBODY FORMULATIONS WITH HIGH CONCENTRATION |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4021497A1 (en) | 2022-07-06 |
| US20220267473A1 (en) | 2022-08-25 |
| EP4021497A4 (en) | 2023-09-06 |
| JP7792137B2 (ja) | 2025-12-25 |
| CA3152838A1 (en) | 2021-03-04 |
| US20250043027A1 (en) | 2025-02-06 |
| AU2020337093A1 (en) | 2022-04-21 |
| WO2021038532A1 (en) | 2021-03-04 |
| AU2020337093B2 (en) | 2025-02-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7235770B2 (ja) | 高濃度vegf受容体融合タンパク質を含む製剤 | |
| CN102946861B (zh) | 浓缩蛋白制剂及其用途 | |
| RU2664691C2 (ru) | Стабильная фармацевтическая композиция на основе слитого белка tnfr:fc | |
| BRPI0620316A2 (pt) | formulações de proteìnas com viscosidades reduzida e seus usos | |
| US20250043027A1 (en) | Formulation of highly concentrated pharmacologically active antibody | |
| US20240182554A1 (en) | Protein solution formulation containing high concentration of an anti-vegf antibody | |
| KR20190071760A (ko) | 약학적 제형 및 그의 제조 방법 | |
| JP2024510480A (ja) | 融合タンパク質の新規製剤 | |
| CN111375057B (zh) | 一种包含抗Her2单克隆抗体的药物配制剂 | |
| US10959939B2 (en) | Liquid pharmaceutical composition of etanercept with lysine and proline |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220318 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20220527 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230829 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230829 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231114 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240730 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240731 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241016 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241204 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250124 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20250430 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250829 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20251202 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20251208 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7792137 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |