JP2013524169A - 液滴によるアッセイ用の検出システム - Google Patents
液滴によるアッセイ用の検出システム Download PDFInfo
- Publication number
- JP2013524169A JP2013524169A JP2013501528A JP2013501528A JP2013524169A JP 2013524169 A JP2013524169 A JP 2013524169A JP 2013501528 A JP2013501528 A JP 2013501528A JP 2013501528 A JP2013501528 A JP 2013501528A JP 2013524169 A JP2013524169 A JP 2013524169A
- Authority
- JP
- Japan
- Prior art keywords
- light
- pulse
- signal
- droplet
- flow path
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000001514 detection method Methods 0.000 title claims abstract description 181
- 238000003556 assay Methods 0.000 title abstract description 33
- 238000000034 method Methods 0.000 claims abstract description 154
- 238000012545 processing Methods 0.000 claims abstract description 20
- 238000005286 illumination Methods 0.000 claims description 169
- 239000000975 dye Substances 0.000 claims description 156
- 238000007689 inspection Methods 0.000 claims description 70
- 230000003287 optical effect Effects 0.000 claims description 70
- 230000005284 excitation Effects 0.000 claims description 40
- 238000002156 mixing Methods 0.000 claims description 38
- 238000005070 sampling Methods 0.000 claims description 27
- 230000000737 periodic effect Effects 0.000 claims description 25
- 239000012530 fluid Substances 0.000 claims description 22
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 19
- 238000007843 droplet-based assay Methods 0.000 claims description 19
- 238000000295 emission spectrum Methods 0.000 claims description 17
- 238000000862 absorption spectrum Methods 0.000 claims description 13
- 230000005540 biological transmission Effects 0.000 claims description 13
- 230000008859 change Effects 0.000 claims description 12
- 238000012544 monitoring process Methods 0.000 claims description 12
- 238000001914 filtration Methods 0.000 claims description 10
- 238000006243 chemical reaction Methods 0.000 claims description 9
- 238000001228 spectrum Methods 0.000 claims description 9
- 238000010521 absorption reaction Methods 0.000 claims description 8
- 238000005259 measurement Methods 0.000 claims description 8
- 230000008569 process Effects 0.000 claims description 8
- 230000003321 amplification Effects 0.000 claims description 7
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 7
- 230000035945 sensitivity Effects 0.000 claims description 7
- 230000004044 response Effects 0.000 claims description 5
- 230000005855 radiation Effects 0.000 description 27
- 238000012360 testing method Methods 0.000 description 16
- 239000000839 emulsion Substances 0.000 description 14
- 238000010586 diagram Methods 0.000 description 10
- 108020004707 nucleic acids Proteins 0.000 description 10
- 102000039446 nucleic acids Human genes 0.000 description 10
- 150000007523 nucleic acids Chemical class 0.000 description 10
- 239000000523 sample Substances 0.000 description 9
- 230000003595 spectral effect Effects 0.000 description 9
- 239000011248 coating agent Substances 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- 230000007274 generation of a signal involved in cell-cell signaling Effects 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 230000001360 synchronised effect Effects 0.000 description 5
- 230000000712 assembly Effects 0.000 description 4
- 238000000429 assembly Methods 0.000 description 4
- 238000003752 polymerase chain reaction Methods 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 3
- 230000001351 cycling effect Effects 0.000 description 3
- 238000007405 data analysis Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 238000005530 etching Methods 0.000 description 3
- 238000000695 excitation spectrum Methods 0.000 description 3
- 239000007850 fluorescent dye Substances 0.000 description 3
- 238000004020 luminiscence type Methods 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- BZTDTCNHAFUJOG-UHFFFAOYSA-N 6-carboxyfluorescein Chemical compound C12=CC=C(O)C=C2OC2=CC(O)=CC=C2C11OC(=O)C2=CC=C(C(=O)O)C=C21 BZTDTCNHAFUJOG-UHFFFAOYSA-N 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 238000002060 fluorescence correlation spectroscopy Methods 0.000 description 2
- 238000002376 fluorescence recovery after photobleaching Methods 0.000 description 2
- 238000002866 fluorescence resonance energy transfer Methods 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 238000012203 high throughput assay Methods 0.000 description 2
- 239000013307 optical fiber Substances 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000011144 upstream manufacturing Methods 0.000 description 2
- 0 *CC[C@@](*)[C@@]1(**CC1)*1CCCC1 Chemical compound *CC[C@@](*)[C@@]1(**CC1)*1CCCC1 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 108020005187 Oligonucleotide Probes Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 239000011358 absorbing material Substances 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 238000004164 analytical calibration Methods 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 238000005842 biochemical reaction Methods 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000003759 clinical diagnosis Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 238000003271 compound fluorescence assay Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 238000013500 data storage Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000007847 digital PCR Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000000198 fluorescence anisotropy Methods 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 238000002875 fluorescence polarization Methods 0.000 description 1
- 238000001506 fluorescence spectroscopy Methods 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000012447 hatching Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000002751 oligonucleotide probe Substances 0.000 description 1
- 238000000206 photolithography Methods 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007493 shaping process Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- ABZLKHKQJHEPAX-UHFFFAOYSA-N tetramethylrhodamine Chemical compound C=12C=CC(N(C)C)=CC2=[O+]C2=CC(N(C)C)=CC=C2C=1C1=CC=CC=C1C([O-])=O ABZLKHKQJHEPAX-UHFFFAOYSA-N 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Optical investigation techniques, e.g. flow cytometry
- G01N15/1456—Optical investigation techniques, e.g. flow cytometry without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/01—Arrangements or apparatus for facilitating the optical investigation
- G01N21/03—Cuvette constructions
- G01N21/05—Flow-through cuvettes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/25—Colour; Spectral properties, i.e. comparison of effect of material on the light at two or more different wavelengths or wavelength bands
- G01N21/31—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/55—Specular reflectivity
- G01N21/552—Attenuated total reflection
- G01N21/553—Attenuated total reflection and using surface plasmons
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6486—Measuring fluorescence of biological material, e.g. DNA, RNA, cells
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502769—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by multiphase flow arrangements
- B01L3/502784—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by multiphase flow arrangements specially adapted for droplet or plug flow, e.g. digital microfluidics
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/01—Arrangements or apparatus for facilitating the optical investigation
- G01N21/03—Cuvette constructions
- G01N2021/0346—Capillary cells; Microcells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/01—Arrangements or apparatus for facilitating the optical investigation
- G01N21/03—Cuvette constructions
- G01N21/05—Flow-through cuvettes
- G01N2021/052—Tubular type; cavity type; multireflective
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N2021/6417—Spectrofluorimetric devices
- G01N2021/6419—Excitation at two or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N2021/6417—Spectrofluorimetric devices
- G01N2021/6421—Measuring at two or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
- G01N2021/6441—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks with two or more labels
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/84—Systems specially adapted for particular applications
- G01N21/85—Investigating moving fluids or granular solids
- G01N2021/8557—Special shaping of flow, e.g. using a by-pass line, jet flow, curtain flow
- G01N2021/8564—Sample as drops
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/062—LED's
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/062—LED's
- G01N2201/0627—Use of several LED's for spectral resolution
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/069—Supply of sources
- G01N2201/0696—Pulsed
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Dispersion Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Optics & Photonics (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
Abstract
Description
本出願は、2010年3月25日に出願された米国仮特許出願第61/317684号に基づくものであり、米国特許法第119条(e)項により該仮出願の権利を主張し、参照によりそのすべてをすべての目的において本明細書に組み込む。
本出願は、2006年5月9日に発行された米国特許第7041481号、2010年7月8日に公開された米国特許出願公開第2010/0173394 A1号、およびJoseph R. Lakowicz著、「PRINCIPLES OF FLUORESCENCE SPECTROSCOPY」(第2版、1999年)を参照により、それらすべてをすべての目的において組み込む。
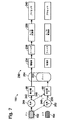
図1に、液滴によるアッセイまたは他の手段で区画したものによるアッセイを実施するためのシステムの例50を示す。簡単には、このシステムは、試料調製ステップ52、液滴生成ステップ54、反応(例えば増幅)ステップ56、検出ステップ58、およびデータ解析ステップ60を含み得る。このシステムを用いてデジタルPCR(ポリメラーゼ連鎖反応)解析を実施することができる。より具体的には、試料調製ステップ52は、臨床用または環境用などの試料を収集し、試料を処理して関連する核酸を放出させ、(例えば標的核酸を増幅するために)核酸を含む反応混合物を形成することを含み得る。液滴生成ステップ54は、核酸を液滴中に封入することを含み得る。このステップでは、例えば、液滴1個につきほぼ1つの各標的核酸のコピーがあり、液滴はそれと混ざらない搬送流体、例えば油などの中に懸濁し乳剤を形成している。反応ステップ56は、これらの液滴を適切に反応させ、例えば、温度サイクリングを実施してPCR増幅を誘起し、それによって、液滴中に標的核酸がもし存在すれば、その核酸を増幅してさらなるコピーを形成することを含み得る。検出ステップ58は、液滴からの放射など、増幅があったか否かを示す何らかの1つ(または複数)の信号を検出することを含み得る。最後に、データ解析ステップ60は、増幅が生じた液滴の割合(液滴の部分)に基づいて試料中の標的核酸の濃度を推定することを含み得る。本明細書で開示する検出システムは、図1のステップの任意の適切な組合せを任意の適切な順序で、ただし特に検出ステップ58および/またはデータ解析ステップ60を実施すればよい。本開示の検出システムに適したものとなり得る液滴によるアッセイシステムのさらなる態様は、先に列記した相互参照の項に記載されており、特に、2010年3月25日に出願された米国仮特許出願第61/317684号、2006年5月9日に発行された米国特許第7041481号、2010年7月8日に公開された米国特許出願公開第2010/0173394 A1号を参照により本明細書に組み込む。
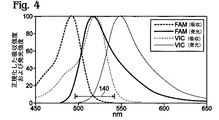
この節では、励起光の時間多重(例えば、パルス照明)および/または発光読取値の時間多重を利用して、吸収および発光のスペクトルが重なり合う状態で、蛍光色素からの光の「単一点」検出を行う検出システムの例を図4〜8を参照して説明する(蛍光色素とは蛍光体を含む化合物である)。
本節では、本明細書で開示する検出システムのいずれかの照明光学素子および/または集光光学素子に組み込むことができるスリットを図9および図10A〜10Cを参照して説明する。
本節では、混合信号を用いることによって液滴を識別する手法の例を図11を参照して説明する。
Y=aX1+bX2
式中、Yは混合信号の混合値であり、aおよびbは定数である。X1およびX2は、2つの別個の信号からの互いに対応する個々の信号値である。他の別個の信号からの追加の信号値(例えば、cX3、dX4など)も含めることができる。これらの定数は互いに同じとしてもよいし、異なってもよい。実施形態の例では、これらの定数は、少なくともほぼ同じものとし、そのため、別個の信号の同じ割合の部分を用いて混合信号を生成する。したがって、得られた混合信号は、別個の信号210、212の平均に対応し得る。
本節では、本明細書で開示する検出システムで用いる検出ユニットの例440、特にその光学配置の例を図12および図13を参照して説明する。検出ユニット440は、例えば、検出システム150(図5参照)に組み込むことができる。
本節では、励起/発光体積を空間的に離して離間した検査部位を画定する検出システムの例を図14〜16を参照して説明する。
本節では、液滴によるアッセイ用の検出システムの追加の態様および特徴について説明する。これらを一連の番号を振ったパラグラフとして提示するが、追加の態様および特徴はこれらに制限されるものではない。これらのパラグラフはそれぞれ、1つまたは複数の他のパラグラフ、および/または、本出願の他の箇所で開示したものと任意の適切なやり方で組み合わせることができる。以下では、これらのパラグラフの一部は、特に他のパラグラフを参照しさらに制限を加えることによって上記の適切な組合せの一部の例が示されるが、これらに限定されるものではない。
1. 液滴を検出する方法であって、(A)流路の検査領域を、液滴が前記検査領域を通過するときに第1の光パルスに対して第2の光パルスが交互に配置された光パルスで照明するステップであって、前記第1のパルスは前記第2のパルスとスペクトル的に異なる、ステップと、(B)前記検査領域が前記第1のパルスおよび前記第2のパルスで照明される期間に検出される光を表すデータを収集するステップとを含む、方法。
2. 前記第1のパルスは第1の範囲の波長の光を画定し、前記第2のパルスは第2の範囲の波長の光を画定し、前記第1の範囲は前記第2の範囲と異なる、パラグラフ1に記載の方法。
3. 前記第1のパルスのみが単一波長の光によって生成されるか、または、前記第1のパルスおよび前記第2のパルスがともにそれぞれの単一波長の光によって生成される、パラグラフ1に記載の方法。
4. 前記第1のパルスはパルス化された光源によって生成される、パラグラフ1から3のいずれかに記載の方法。
5. 前記第1のパルスおよび前記第2のパルスは、それぞれのパルス化された光源によって生成される、パラグラフ1から4のいずれかに記載の方法。
6. 前記第1のパルスまたは前記第2のパルス、あるいは前記第1のパルスおよび前記第2のパルスの両方は、前記検査領域まで間欠的に伝達される少なくとも1つの連続光ビームによって生成される、パラグラフ1に記載の方法。
7. 前記第1のパルスおよび前記第2のパルスは、少なくとも1つのLEDから放出される光を含む、パラグラフ1に記載の方法。
8. 前記第1のパルスおよび前記第2のパルスは、それぞれのパルス化されたLEDから放出される、パラグラフ7に記載の方法。
9. 前記検査領域のうちそれぞれ重なり合う体積が、前記第1のパルスおよび前記第2のパルスによって照明される、パラグラフ1に記載の方法。
10. 前記第1のパルスおよび前記第2のパルスの期間に、前記検査領域の重なり合う体積からの光を検出するステップをさらに含む、パラグラフ1に記載の方法。
11. 少なくとも1つの第1のパルスおよび少なくとも1つの第2のパルスで各液滴が照明される、パラグラフ1に記載の方法。
12. 複数の第1のパルスおよび複数の第2のパルスで各液滴が照明される、パラグラフ11に記載の方法。
13. 各液滴は、前記液滴の直径よりも狭い光ビームで照明される、パラグラフ1に記載の方法。
14. 前記第1のパルスおよび前記第2のパルスは、それぞれ第1および第2の光源によって放出される光を含み、前記方法は、前記第1および第2の光源によって放出される前記光を、前記光が前記検査領域を照明する前にスリットを通過させるステップをさらに含む、パラグラフ1に記載の方法。
15. データを収集する前記ステップは、前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光をそれぞれ表す第1の信号および第2の信号を生成するステップを含む、パラグラフ1に記載の方法。
16. 前記液滴は第1の色素および第2の色素を含み、前記第1の信号は第1の検出構成から生成され、前記第2の信号は第2の検出構成から生成され、前記第1の検出構成の前記第1および第2の色素に対する感度は、前記第2の検出構成の前記第1および第2の色素に対する感度と相対的に異なる、パラグラフ15に記載の方法。
17. 第1の検出器および第2の検出器で前記検査領域からの光を検出するステップをさらに含み、前記第1の信号は前記第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は前記第2の検出器によって少なくとも他に優先して検出される光を表す、パラグラフ15に記載の方法。
18. 各検出器は、前記第1のパルスおよび前記第2のパルスの期間に光を検出する、パラグラフ17に記載の方法。
19. 各検出器の利得は、第1のパルスまたは第2のパルスが前記流路の前記検査領域を照明しているかどうかに従って、経時的に調整される、パラグラフ17に記載の方法。
20. 前記第1の信号および前記第2の信号は周期信号である、パラグラフ15に記載の方法。
21. 前記データは、前記検査領域が前記第1のパルスおよび前記第2のパルスで照明される期間に同じ検出器で検出される光を表す、パラグラフ1に記載の方法。
22. 前記第1のパルスおよび前記第2のパルスの期間に前記検査領域からの光を検出するステップをさらに含み、光を検出する前記ステップでは、第1の信号および第2の信号が生成され、データを収集する前記ステップは、前記第1のパルスおよび前記第2のパルスに対応して前記第1の信号および前記第2の信号をそれぞれ周期的にゲーティングするステップを含む、パラグラフ1に記載の方法。
23. 前記照明ステップは、前記流路によって画定される長軸に対して横方向に細長い断面を有する光ビームを前記流路と交差させるステップを含む、パラグラフ1に記載の方法。
24. 前記照明ステップは、前記流路の円盤状の体積を照明するステップを含む、パラグラフ1に記載の方法。
25. 前記照明ステップは、前記第1のパルスおよび前記第2のパルスとスペクトル的に異なる第3の光パルスで前記流路の前記検査領域を照明するステップを含む、パラグラフ1に記載の方法。
26. 液滴を検出する方法であって、(A)流路の検査領域を、液滴が前記検査領域を通過するときに第1の光源および第2の光源によって放出される光パルスで交互に照明するステップと、(B)前記光パルスによって照明される前記検査領域からの光を検出するステップと、(C)第1の信号および第2の信号を生成するステップとを含み、前記第1の信号は、第1の領域が前記第1の光源からの光パルスで照明されるときに少なくとも他に優先して検出される光を表し、前記第2の信号は、第2の領域が前記第2の光源からの光パルスで照明されるときに少なくとも他に優先して検出される光を表す、方法。
27. 前記第1の信号および前記第2の信号に基づいて、前記液滴中の第1の標的および第2の標的の濃度を推定するステップをさらに含む、パラグラフ26に記載の方法。
28. 個々の液滴中で増幅反応が起こったかどうかを判断するステップをさらに含む、パラグラフ26に記載の方法。
29. 液滴に基づくアッセイ用の検出システムであって、(A)流路と、(B)前記流路の検査領域を、液滴が前記検査領域を通過するときに第1の光パルスに対して第2の光パルスが交互に配置された光パルスで照明するように構成された照明アセンブリであって、前記第1のパルスは前記第2のパルスとスペクトル的に異なる、照明アセンブリと、(C)前記検査領域からの光を検出するように構成された1つまたは複数の検出器と、(D)前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光を表すデータを収集する制御部とを備える、システム。
30. 前記第1のパルスは第1の範囲の波長の光を画定し、前記第2のパルスは第2の範囲の波長の光を画定し、前記第1の範囲は前記第2の範囲と異なる、パラグラフ29に記載のシステム。
31. 前記第1のパルスのみが単一波長の光によって生成されるか、または、前記第1のパルスおよび前記第2のパルスがともにそれぞれの単一波長の光によって生成される、パラグラフ29に記載のシステム。
32. 前記照明アセンブリは少なくとも1つのパルス化された光源を備える、パラグラフ29に記載のシステム。
33. 前記照明アセンブリは1対のパルス化されたLEDを備える、パラグラフ29に記載のシステム。
34. 前記照明アセンブリは、前記検査領域に間欠的に伝達される光ビームを放出するように構成された少なくとも1つの連続光源を備える、パラグラフ29に記載のシステム。
35. 前記第1のパルスおよび前記第2のパルスは、前記検査領域の重なり合う体積を照明するように構成される、パラグラフ29に記載のシステム。
36. 前記1つまたは複数の検出器は、前記第1のパルスおよび前記第2のパルスの期間に前記検査領域の重なり合う体積からの光を検出するように構成される、パラグラフ29に記載のシステム。
37. 前記照明アセンブリは、前記流路によって画定される長軸に対して横方向に細長い断面を有する光ビームで前記検査領域を照明するように構成される、パラグラフ29に記載のシステム。
38. 前記照明アセンブリは、光が前記検査領域を照明する前に通過する少なくとも1つのスリットを備える、パラグラフ29に記載のシステム。
39. 前記制御部は、前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光をそれぞれ表す第1の信号および第2の信号を生成するように構成される、パラグラフ29に記載のシステム。
40. 前記1つまたは複数の検出器は、第1の検出器および第2の検出器を含み、前記第1の信号は前記第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は前記第2の検出器によって少なくとも他に優先して検出される光を表す、パラグラフ39に記載のシステム。
41. 各検出器は、前記第1のパルスおよび前記第2のパルスの期間に光を検出するように構成される、パラグラフ40に記載のシステム。
42. 前記第1の信号および前記第2の信号は周期信号である、パラグラフ39に記載のシステム。
43. 前記制御部は、第1のパルスまたは第2のパルスが前記流路の前記検査領域を照明しているかどうかに従って、経時的に各検出器の利得を調整するように構成される、パラグラフ29に記載のシステム。
44. 前記1つまたは複数の検出器は、それぞれ少なくともほぼ連続な第1の信号および第2の信号を生成し、前記制御部は、前記第1のパルスおよび前記第2のパルスに対応して前記第1の信号および前記第2の信号をそれぞれ周期的にゲートして前記信号を周期的にするように構成される、パラグラフ29に記載のシステム。
45. 前記照明アセンブリは、前記流路によって画定される長軸に対して横に細長い断面を有する光ビームを形成する、パラグラフ29に記載のシステム。
46. 前記照明アセンブリは、前記流路の円盤状の体積を照明するように構成される、パラグラフ29に記載のシステム。
47. 前記照明アセンブリは、第1の光源および第2の光源を備え、前記システムは、前記光源が前記流路の重なり合う体積を照明するときに、前記液滴を前記検査領域に通過させるように構成された少なくとも1つのポンプをさらに備える、パラグラフ29に記載のシステム。
48. 液滴に基づくアッセイにおける検出システムであって、(A)流路と、(B)前記流路の検査領域を、液滴が前記領域を通過するときに照明する光ビームを生成するように構成された照明アセンブリと、(C)前記検査領域から受け取った光を検出するように構成された検出器と、(D)前記検出器によって検出される光を表すデータを収集する制御部とを備え、前記光ビームは、前記流路と交差する断面が細長い、システム。
49. 前記照明アセンブリは光源およびスリットを備え、前記光源によって放射される光は、前記検査領域に到達する前に前記スリットを通過する、パラグラフ48に記載のシステム。
50. 前記光ビームは、前記流路によって画定される長軸に対して横方向に細長い断面を有する、パラグラフ48に記載のシステム。
51. 前記ビームの断面は、前記流路全体の半分の位置で、前記流路の対向する面から外側に延びる、パラグラフ48に記載のシステム。
52. 前記流路はチューブによって画定され、前記ビームの断面は、前記流路全体の半分の位置で、前記チューブの直径よりも長い、パラグラフ51に記載のシステム。
53. 前記断面は、前記流路全体の半分の位置で、前記チューブと交差しない対向する端部を有する、パラグラフ52に記載のシステム。
54. 前記光ビームは、前記流路の円盤状の体積を照明する、パラグラフ48に記載のシステム。
55. 前記光ビームは対向する平坦な側面を有する、パラグラフ48に記載のシステム。
56. 前記光ビームは前記流路の長軸に平行な寸法を有し、前記寸法にわたって前記ビームが前記流路と交差し、前記寸法は前記流路の直径よりも短い、パラグラフ48に記載のシステム。
57. 液滴に基づくアッセイにおける検出システムであって、(A)流路と、(B)前記流路の検査領域を、液滴が前記領域を通過するときに照明する光源と、(C)前記検査領域から受け取った光を検出するように構成された検出器と、(D)前記検出器によって検出される光を表すデータを収集する制御部とを備え、前記光源が放出する光は、前記光源と前記検出器との間の少なくとも1つのスリットを通過して進む、システム。
58. 前記少なくとも1つのスリットは、前記光源から前記検査領域への光路上に配設されるスリットを含む、パラグラフ57に記載のシステム。
59. 前記少なくとも1つのスリットは、集光光学素子と前記流路との間に配設されるスリットを含む、パラグラフ57に記載のシステム。
60. 液滴を検出する方法であって、(A)断面が細長い光ビームで流路の検査領域を照明するステップと、(B)複数の液滴が前記検査領域を通過するときに、前記領域から経時的に検出される光を表すデータを収集するステップとを含む、方法。
61. 前記照明ステップは、光源と前記検査領域との間の光路上に配設されたスリットを通して光を送るステップを含む、パラグラフ60に記載の方法。
62. 前記検査領域の円盤状の体積を照明する、パラグラフ60に記載の方法。
63. 前記光ビームは、前記流路によって画定される長軸に対して横方向に細長い断面を有する、パラグラフ60に記載の方法。
64. 前記照明ステップは、液滴を、前記液滴の直径よりも薄い光ビームで照明するステップを含む、パラグラフ60に記載の方法。
65. 液滴に基づくアッセイ用の検出方法であって、(A)液滴を運ぶ流体の流れから一連の期間に、それぞれ異なる検出構成で検出される光を表す少なくとも2つの別個の信号を生成するステップと、(B)前記少なくとも2つの別個の信号を混合して混合信号を形成するステップと、(C)前記混合信号を処理して液滴に対応する期間を特定するステップとを含む、方法。
66. 前記混合ステップは、個々の期間ごとに前記別個の信号からの値の線形結合を形成するステップを含む、パラグラフ65に記載の方法。
67. 線形結合を形成する前記ステップは、前記値を同じ割合で含む線形結合を形成するステップを含む、パラグラフ66に記載の方法。
68. 前記混合ステップは、前記少なくとも2つの信号によるデジタル形式で行われる、パラグラフ65に記載の方法。
69. 前記混合ステップは、前記少なくとも2つの信号が生成されているときに、少なくとも部分的に行われる、パラグラフ65に記載の方法。
70. 前記混合ステップは、個々の期間ごとに前記別個の信号からの値を混合するステップを含み、所与の期間ごとに混合される値の各々は、前記所与の期間のそれぞれ異なる部分で検出される光を表す、パラグラフ65に記載の方法。
71. 所与の期間ごとに混合される値の各々は、前記所与の期間の互いに重なり合わない部分で検出器される光を表す、パラグラフ70に記載の方法。
72. 前記混合ステップは、個々の期間ごとに前記別個の信号からの値を混合するステップを含み、所与の期間ごとに混合される値の各々は、前記所与の期間の同じ部分またはすべての部分で検出される光を表す、パラグラフ65に記載の方法。
73. 前記別個の信号は、流体の流れを保持する流路のある領域から、第1の光源および第2の光源からの交互に配置された光パルスで前記領域が照明される期間に検出される光を表す第1の信号および第2の信号を含む、パラグラフ65に記載の方法。
74. 前記第1の信号は、前記第1の光源からのパルス期間に第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は、前記第2の光源からのパルス期間に第2の検出器によって少なくとも他に優先して検出される光を表す、パラグラフ73に記載の方法。
75. それぞれの異なる色素は蛍光体を含む、パラグラフ65に記載の方法。
76. 液滴に基づくアッセイ用の検出方法であって、(A)液滴を運ぶ流体の流れから一連の期間に検出されるそれぞれ異なる波長または波長帯の光を表す少なくとも2つの別個の信号を生成するステップであって、それぞれの波長または波長帯から検出される光は個々の液滴中の異なる標的の存在の有無を示す、ステップと、(B)前記少なくとも2つの別個の信号を混合して混合信号を形成するステップと、(C)前記混合信号を処理して液滴に対応する期間を識別するステップと、(D)前記識別された期間に検出された別個の信号の各々の値に基づいて、液滴が異なる標的の各々を含むかを判断するステップとを含む、方法。
77. 液滴に基づくアッセイ用の検出方法であって、(A)液滴を含む流体の流れから一連の期間に検出されるそれぞれ異なる波長帯の光を表す少なくとも2つの信号を生成するステップと、(B)前記少なくとも2つの信号の複数の値を混合して混合信号を形成するステップと、(C)前記混合信号の液滴に対応する部分を識別するステップと、(D)前記識別された部分に対応する前記少なくとも2つの信号の値を処理して、どの液滴がどの標的を含むかを判断するステップとを含む、方法。
78. 液滴に基づくアッセイ用の検出システムであって、(A)少なくとも2つの異なる色素を含む液滴を運ぶ流体の流れからの光を検出するように構成された1つまたは複数の検出器と、(B)液滴を運ぶ流体の流れから一連の期間に、それぞれ異なる検出構成で検出される光を表す別個の信号を生成し、前記少なくとも2つの別個の信号を混合して混合信号を形成し、前記混合信号を処理して液滴に対応する期間を識別するように構成された制御部とを備える、システム。
79. 液滴用の検出方法であって、(A)第1の色素および第2の色素を含む液滴を準備するステップであって、前記第1の色素の発光スペクトルおよび前記第2の色素の吸収スペクトルが重なり合う波長帯を画定し、前記重なり合いは、前記第1の色素が前記第2の色素の最大吸収波長で励起された場合に前記第1の色素からその発光最大値の少なくとも半分が生成される程度に大きい、ステップと、(B)前記第1の色素および前記第2の色素をともに励起し得る励起光で前記液滴を照明するステップであって、前記励起光は1つまたは複数のLEDによって放出され、前記重なり合う波長帯の短波長側の区域のみを含む、ステップと、(C)前記第1の色素および前記第2の色素が放出する光を検出するステップとを含み、前記第2の色素が放出する光は、前記短波長側の区域から離れた前記重なり合う波長帯の長波長側の区域のみを含む波長域で検出される、方法。
80. 前記吸収スペクトルおよび前記発光スペクトルが、それぞれ約20nm以内である波長でそれぞれ最大値を有する、パラグラフ79に記載の方法。
81. 前記1つまたは複数のLEDは、前記第1の色素を選択的に励起する第1のLEDおよび前記第2の色素を選択的に励起する第2のLEDを含む、パラグラフ79に記載の方法。
82. 前記第1の色素および前記第2の色素からそれぞれ選択的に検出される光を表す第1の組のデータおよび第2の組のデータを収集するステップをさらに含む、パラグラフ79に記載の方法。
83. 前記第1の色素はFAM色素であり、前記第2の色素はVIC色素である、パラグラフ79に記載の方法。
84. 前記重なり合う波長帯は、前記それぞれのスペクトルがその吸収または発光の最大値の20%以上の値で重なり合うところとして定義され、前記重なり合う波長帯の幅は少なくとも25nmである、パラグラフ79に記載の方法。
85. 液滴に基づくアッセイにおける検出システムであって、(A)第1の色素および第2の色素を含む液滴を受け取るように構成された流路であって、前記第1の色素の発光スペクトルおよび前記第2の色素の吸収スペクトルにより重なり合う波長帯が画定され、前記重なり合いは、前記第1の色素が前記第2の色素の最大吸収波長で励起された場合に前記第1の色素からその最大発光値の少なくとも半分が生成される程度に大きい、流路と、(B)1つまたは複数のLEDを含み、前記第1および第2の色素をともに励起し得る励起光で前記液滴を照明するように構成された照明アセンブリであって、前記励起光は、前記LEDから放出され、前記重なり合う波長帯の短波長側の区域のみを含む、照明アセンブリと、(C)前記第1の色素および前記第2の色素が放出する光を検出するように構成された1つまたは複数の検出器であって、前記第2の色素からの前記光は、前記短波長側の区域から離れた前記重なり合う波長帯の長波長側の区域のみを含む波長域で検出される、検出器と、を備えるシステム。
86. 前記照明アセンブリは、前記短波長側の区域を画定する1つまたは複数のフィルタを備える、パラグラフ85に記載のシステム。
87. 前記1つまたは複数の検出器を含む集光アセンブリをさらに備え、前記集光アセンブリは、前記長波長側の区域を画定する1つまたは複数のフィルタを含む、パラグラフ85に記載のシステム。
88. 液滴用の検出方法であって、(A)光ビームを生成するステップと、(B)前記光ビームを主ビームおよび少なくとも1つのサンプリングビームに分岐するステップと、(C)前記サンプリングビームの強度を監視するステップと、(D)前記監視ステップから得られる1つまたは複数の測定値に基づいて、前記光ビームの強度を調整するステップと、(E)流路の検査領域を、液滴が前記検査領域を通過するときに前記主ビームで照明するステップと、(F)前記検査領域から検出される光を表すデータを収集するステップとを含む、方法。
89. 光ビームを生成する前記ステップは、光源から放出される光をフィルタリングして前記放出される光のスペクトルを変化させるステップを含み、前記分岐ステップは、前記フィルタリングステップの後で実施される、パラグラフ88に記載の方法。
90. 前記フィルタリングステップは、特定波長域透過波長フィルタ、長波長透過フィルタ、短波長透過フィルタ、またはこれらの組合せを用いて実施される、パラグラフ88に記載の方法。
91. 光ビームを生成する前記ステップは、少なくとも2つの光源から放出される光ビームを混合するステップを含み、前記混合ステップは、前記フィルタリングステップの後で実施される、パラグラフ88に記載の方法。
92. 光ビームを生成する前記ステップは、LEDを用いて光を放出させるステップを含む、パラグラフ88に記載の方法。
93. 光ビームを生成する前記ステップは、第1の光源および第2の光源からの光を混合するステップを含み、前記分岐ステップは、前記光ビームを第1のサンプリングビームおよび第2のサンプリングビームに分岐するステップを含み、前記第1のサンプリングビームは前記第1の光源に対応し、前記第2のサンプリングビームは前記第2の光源に対応する、パラグラフ88に記載の方法。
94. 前記調整ステップにより、前記主ビームの各光源に対応する部分の強度がほぼ一定に保たれる、パラグラフ93に記載の方法。
72 光
74 液滴
76 流路
78 照明アセンブリ
80 集光アセンブリ
82、84 光源
85 照明光学素子
86、88 検出器
90 集光光学素子
92 検査領域
96 乳剤
98 連続相
100 乳剤、液滴の動き
102 集光
104 入射光
106 集光光路
108 入射光路
Claims (94)
- 液滴を検出する方法であって、
流路の検査領域を、液滴が前記検査領域を通過するときに第1の光パルスに対して第2の光パルスが交互に配置された光パルスで照明するステップであって、前記第1のパルスは前記第2のパルスとスペクトル的に異なる、ステップと、
前記検査領域が前記第1のパルスおよび前記第2のパルスで照明される期間に検出される光を表すデータを収集するステップとを含む、方法。 - 前記第1のパルスは第1の範囲の波長の光を画定し、前記第2のパルスは第2の範囲の波長の光を画定し、前記第1の範囲は前記第2の範囲と異なる、請求項1に記載の方法。
- 前記第1のパルスのみが単一波長の光によって生成されるか、または、前記第1のパルスおよび前記第2のパルスがともにそれぞれの単一波長の光によって生成される、請求項1に記載の方法。
- 前記第1のパルスはパルス化された光源によって生成される、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスは、それぞれのパルス化された光源によって生成される、請求項1に記載の方法。
- 前記第1のパルスまたは前記第2のパルス、あるいは前記第1のパルスおよび前記第2のパルスの両方は、前記検査領域まで間欠的に伝達される少なくとも1つの連続光ビームによって生成される、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスは、少なくとも1つのLEDから放出される光を含む、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスは、それぞれのパルス化されたLEDから放出される、請求項7に記載の方法。
- 前記検査領域のうちそれぞれ重なり合う体積が、前記第1のパルスおよび前記第2のパルスによって照明される、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスの期間に、前記検査領域の重なり合う体積からの光を検出するステップをさらに含む、請求項1に記載の方法。
- 少なくとも1つの第1のパルスおよび少なくとも1つの第2のパルスで各液滴が照明される、請求項1に記載の方法。
- 複数の第1のパルスおよび複数の第2のパルスで各液滴が照明される、請求項11に記載の方法。
- 各液滴は、前記液滴の直径よりも狭い光ビームで照明される、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスは、それぞれ第1および第2の光源によって放出される光を含み、前記方法は、前記第1および第2の光源によって放出される前記光を、前記光が前記検査領域を照明する前にスリットを通過させるステップをさらに含む、請求項1に記載の方法。
- データを収集する前記ステップは、前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光をそれぞれ表す第1の信号および第2の信号を生成するステップを含む、請求項1に記載の方法。
- 前記液滴は第1の色素および第2の色素を含み、前記第1の信号は第1の検出構成から生成され、前記第2の信号は第2の検出構成から生成され、前記第1の検出構成の前記第1および第2の色素に対する感度は、前記第2の検出構成の前記第1および第2の色素に対する感度と相対的に異なる、請求項15に記載の方法。
- 第1の検出器および第2の検出器で前記検査領域からの光を検出するステップをさらに含み、前記第1の信号は前記第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は前記第2の検出器によって少なくとも他に優先して検出される光を表す、請求項15に記載の方法。
- 各検出器は、前記第1のパルスおよび前記第2のパルスの期間に光を検出する、請求項17に記載の方法。
- 各検出器の利得は、第1のパルスまたは第2のパルスが前記流路の前記検査領域を照明しているかどうかに従って経時的に調整される、請求項17に記載の方法。
- 前記第1の信号および前記第2の信号は周期信号である、請求項15に記載の方法。
- 前記データは、前記検査領域が前記第1のパルスおよび前記第2のパルスで照明される期間に同じ検出器で検出される光を表す、請求項1に記載の方法。
- 前記第1のパルスおよび前記第2のパルスの期間に前記検査領域からの光を検出するステップをさらに含み、光を検出する前記ステップでは、第1の信号および第2の信号が生成され、データを収集する前記ステップは、前記第1のパルスおよび前記第2のパルスに対応して前記第1の信号および前記第2の信号をそれぞれ周期的にゲーティングするステップを含む、請求項1に記載の方法。
- 前記照明ステップは、前記流路によって画定される長軸に対して横方向に細長い断面を有する光ビームを前記流路と交差させるステップを含む、請求項1に記載の方法。
- 前記照明ステップは、前記流路の円盤状の体積を照明するステップを含む、請求項1に記載の方法。
- 前記照明ステップは、前記第1のパルスおよび前記第2のパルスとスペクトル的に異なる第3の光パルスで前記流路の前記検査領域を照明するステップを含む、請求項1に記載の方法。
- 液滴を検出する方法であって、
流路の検査領域を、液滴が前記検査領域を通過するときに第1の光源および第2の光源によって放出される光パルスで交互に照明するステップと、
前記光パルスによって照明される前記検査領域からの光を検出するステップと、
第1の信号および第2の信号を生成するステップとを含み、
前記第1の信号は、第1の領域が前記第1の光源からの光パルスで照明されるときに少なくとも他に優先して検出される光を表し、前記第2の信号は、第2の領域が前記第2の光源からの光パルスで照明されるときに少なくとも他に優先して検出される光を表す、方法。 - 前記第1の信号および前記第2の信号に基づいて、前記液滴中の第1の標的および第2の標的の濃度を推定するステップをさらに含む、請求項26に記載の方法。
- 個々の液滴中で増幅反応が起こったかどうかを判断するステップをさらに含む、請求項26に記載の方法。
- 液滴に基づくアッセイ用の検出システムであって、
流路と、
前記流路の検査領域を、液滴が前記検査領域を通過するときに第1の光パルスに対して第2の光パルスが交互に配置された光パルスで照明するように構成された照明アセンブリであって、前記第1のパルスは前記第2のパルスとスペクトル的に異なる、照明アセンブリと、
前記検査領域からの光を検出するように構成された1つまたは複数の検出器と、
前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光を表すデータを収集する制御部とを備える、システム。 - 前記第1のパルスは第1の範囲の波長の光を画定し、前記第2のパルスは第2の範囲の波長の光を画定し、前記第1の範囲は前記第2の範囲と異なる、請求項29に記載のシステム。
- 前記第1のパルスのみが単一波長の光によって生成されるか、または、前記第1のパルスおよび前記第2のパルスがともにそれぞれの単一波長の光によって生成される、請求項29に記載のシステム。
- 前記照明アセンブリは少なくとも1つのパルス化された光源を備える、請求項29に記載のシステム。
- 前記照明アセンブリは1対のパルス化されたLEDを備える、請求項29に記載のシステム。
- 前記照明アセンブリは、前記検査領域に間欠的に伝達される光ビームを放出するように構成された少なくとも1つの連続光源を備える、請求項29に記載のシステム。
- 前記第1のパルスおよび前記第2のパルスは、前記検査領域の重なり合う体積を照明するように構成される、請求項29に記載のシステム。
- 前記1つまたは複数の検出器は、前記第1のパルスおよび前記第2のパルスの期間に前記検査領域の重なり合う体積からの光を検出するように構成される、請求項29に記載のシステム。
- 前記照明アセンブリは、前記流路によって画定される長軸に対して横方向に細長い断面を有する光ビームで前記検査領域を照明するように構成される、請求項29に記載のシステム。
- 前記照明アセンブリは、光が前記検査領域を照明する前に通過する少なくとも1つのスリットを備える、請求項29に記載のシステム。
- 前記制御部は、前記第1のパルスおよび前記第2のパルスで前記検査領域が照明される期間に検出される光をそれぞれ表す第1の信号および第2の信号を生成するように構成される、請求項29に記載のシステム。
- 前記1つまたは複数の検出器は、第1の検出器および第2の検出器を含み、前記第1の信号は前記第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は前記第2の検出器によって少なくとも他に優先して検出される光を表す、請求項39に記載のシステム。
- 各検出器は、前記第1のパルスおよび前記第2のパルスの期間に光を検出するように構成される、請求項40に記載のシステム。
- 前記第1の信号および前記第2の信号は周期信号である、請求項39に記載のシステム。
- 前記制御部は、第1のパルスまたは第2のパルスが前記流路の前記検査領域を照明しているかどうかに従って、経時的に各検出器の利得を調整するように構成される、請求項29に記載のシステム。
- 前記1つまたは複数の検出器は、それぞれ少なくともほぼ連続な第1の信号および第2の信号を生成し、前記制御部は、前記第1のパルスおよび前記第2のパルスに対応して前記第1の信号および前記第2の信号をそれぞれ周期的にゲートして前記信号を周期的にするように構成される、請求項29に記載のシステム。
- 前記照明アセンブリは、前記流路によって画定される長軸に対して横に細長い断面を有する光ビームを形成する、請求項29に記載のシステム。
- 前記照明アセンブリは、前記流路の円盤状の体積を照明するように構成される、請求項29に記載のシステム。
- 前記照明アセンブリは、第1の光源および第2の光源を備え、前記システムは、前記光源が前記流路の重なり合う体積を照明するときに、前記液滴を前記検査領域に通過させるように構成された少なくとも1つのポンプをさらに備える、請求項29に記載のシステム。
- 液滴に基づくアッセイにおける検出システムであって、
流路と、
前記流路の検査領域を、液滴が前記領域を通過するときに照明する光ビームを生成するように構成された照明アセンブリと、
前記検査領域から受け取った光を検出するように構成された検出器と、
前記検出器によって検出される光を表すデータを収集する制御部とを備え、
前記光ビームは、前記流路と交差する断面が細長い、システム。 - 前記照明アセンブリは光源およびスリットを備え、前記光源によって放射される光は、前記検査領域に到達する前に前記スリットを通過する、請求項48に記載のシステム。
- 前記光ビームは、前記流路によって画定される長軸に対して横方向に細長い断面を有する、請求項48に記載のシステム。
- 前記ビームの断面は、前記流路全体の半分の位置で、前記流路の対向する面から外側に延びる、請求項48に記載のシステム。
- 前記流路はチューブによって画定され、前記ビームの断面は、前記流路全体の半分の位置で、前記チューブの直径よりも長い、請求項51に記載のシステム。
- 前記断面は、前記流路全体の半分の位置で、前記チューブと交差しない対向する端部を有する、請求項52に記載のシステム。
- 前記光ビームは、前記流路の円盤状の体積を照明する、請求項48に記載のシステム。
- 前記光ビームは対向する平坦な側面を有する、請求項48に記載のシステム。
- 前記光ビームは前記流路の長軸に平行な寸法を有し、前記寸法にわたって前記ビームが前記流路と交差し、前記寸法は前記流路の直径よりも短い、請求項48に記載のシステム。
- 液滴に基づくアッセイにおける検出システムであって、
流路と、
前記流路の検査領域を、液滴が前記領域を通過するときに照明する光源と、
前記検査領域から受け取った光を検出するように構成された検出器と、
前記検出器によって検出される光を表すデータを収集する制御部とを備え、
前記光源が放出する光は、前記光源と前記検出器との間の少なくとも1つのスリットを通過して進む、システム。 - 前記少なくとも1つのスリットは、前記光源から前記検査領域への光路上に配設されるスリットを含む、請求項57に記載のシステム。
- 前記少なくとも1つのスリットは、集光光学素子と前記流路との間に配設されるスリットを含む、請求項57に記載のシステム。
- 液滴を検出する方法であって、
断面が細長い光ビームで流路の検査領域を照明するステップと、
複数の液滴が前記検査領域を通過するときに、前記領域から経時的に検出される光を表すデータを収集するステップとを含む、方法。 - 前記照明ステップは、光源と前記検査領域との間の光路上に配設されたスリットを通して光を送るステップを含む、請求項60に記載の方法。
- 前記検査領域の円盤状の体積を照明する、請求項60に記載の方法。
- 前記光ビームは、前記流路によって画定される長軸に対して横方向に細長い断面を有する、請求項60に記載の方法。
- 前記照明ステップは、液滴を、前記液滴の直径よりも薄い光ビームで照明するステップを含む、請求項60に記載の方法。
- 液滴に基づくアッセイ用の検出方法であって、
液滴を運ぶ流体の流れから一連の期間に、それぞれ異なる検出構成で検出される光を表す少なくとも2つの別個の信号を生成するステップと、
前記少なくとも2つの別個の信号を混合して混合信号を形成するステップと、
前記混合信号を処理して液滴に対応する期間を特定するステップとを含む、方法。 - 前記混合ステップは、個々の期間ごとに前記別個の信号からの値の線形結合を形成するステップを含む、請求項65に記載の方法。
- 線形結合を形成する前記ステップは、前記値を同じ割合で含む線形結合を形成するステップを含む、請求項66に記載の方法。
- 前記混合ステップは、前記少なくとも2つの信号によるデジタル形式で行われる、請求項65に記載の方法。
- 前記混合ステップは、前記少なくとも2つの信号が生成されているときに、少なくとも部分的に行われる、請求項65に記載の方法。
- 前記混合ステップは、個々の期間ごとに前記別個の信号からの値を混合するステップを含み、所与の期間ごとに混合される値の各々は、前記所与の期間のそれぞれ異なる部分で検出される光を表す、請求項65に記載の方法。
- 所与の期間ごとに混合される値の各々は、前記所与の期間の互いに重なり合わない部分で検出器される光を表す、請求項70に記載の方法。
- 前記混合ステップは、個々の期間ごとに前記別個の信号からの値を混合するステップを含み、所与の期間ごとに混合される値の各々は、前記所与の期間の同じ部分またはすべての部分で検出される光を表す、請求項65に記載の方法。
- 前記別個の信号は、流体の流れを保持する流路のある領域から、第1の光源および第2の光源からの交互に配置された光パルスで前記領域が照明される期間に検出される光を表す第1の信号および第2の信号を含む、請求項65に記載の方法。
- 前記第1の信号は、前記第1の光源からのパルス期間に第1の検出器によって少なくとも他に優先して検出される光を表し、前記第2の信号は、前記第2の光源からのパルス期間に第2の検出器によって少なくとも他に優先して検出される光を表す、請求項73に記載の方法。
- それぞれの異なる色素は蛍光体を含む、請求項65に記載の方法。
- 液滴に基づくアッセイ用の検出方法であって、
液滴を運ぶ流体の流れから一連の期間に検出されるそれぞれ異なる波長または波長帯の光を表す少なくとも2つの別個の信号を生成するステップであって、それぞれの波長または波長帯から検出される光は個々の液滴中の異なる標的の存在の有無を示す、ステップと、
前記少なくとも2つの別個の信号を混合して混合信号を形成するステップと、
前記混合信号を処理して液滴に対応する期間を識別するステップと、
前記識別された期間に検出された別個の信号の各々の値に基づいて、液滴が異なる標的の各々を含むかを判断するステップとを含む、方法。 - 液滴に基づくアッセイ用の検出方法であって、
液滴を含む流体の流れから一連の期間に検出されるそれぞれ異なる波長帯の光を表す少なくとも2つの信号を生成するステップと、
前記少なくとも2つの信号の複数の値を混合して混合信号を形成するステップと、
前記混合信号の液滴に対応する部分を識別するステップと、
前記識別された部分に対応する前記少なくとも2つの信号の値を処理して、どの液滴がどの標的を含むかを判断するステップとを含む、方法。 - 液滴に基づくアッセイ用の検出システムであって、
少なくとも2つの異なる色素を含む液滴を運ぶ流体の流れからの光を検出するように構成された1つまたは複数の検出器と、
液滴を運ぶ流体の流れから一連の期間に、それぞれ異なる検出構成で検出される光を表す別個の信号を生成し、前記少なくとも2つの別個の信号を混合して混合信号を形成し、前記混合信号を処理して液滴に対応する期間を識別するように構成された制御部とを備える、システム。 - 液滴用の検出方法であって、
第1の色素および第2の色素を含む液滴を準備するステップであって、前記第1の色素の発光スペクトルおよび前記第2の色素の吸収スペクトルが、重なり合う波長帯を画定し、前記重なり合いは、前記第1の色素が前記第2の色素の最大吸収波長で励起された場合に前記第1の色素からその発光最大値の少なくとも半分が生成される程度に大きい、ステップと、
前記第1の色素および前記第2の色素をともに励起し得る励起光で前記液滴を照明するステップであって、前記励起光は1つまたは複数のLEDによって放出され、前記重なり合う波長帯の短波長側の区域のみを含む、ステップと、
前記第1の色素および前記第2の色素が放出する光を検出するステップとを含み、前記第2の色素が放出する光は、前記短波長側の区域から離れた前記重なり合う波長帯の長波長側の区域のみを含む波長域で検出される、方法。 - 前記吸収スペクトルおよび前記発光スペクトルが、それぞれ約20nm以内である波長でそれぞれ最大値を有する、請求項79に記載の方法。
- 前記1つまたは複数のLEDは、前記第1の色素を選択的に励起する第1のLEDおよび前記第2の色素を選択的に励起する第2のLEDを含む、請求項79に記載の方法。
- 前記第1の色素および前記第2の色素からそれぞれ選択的に検出される光を表す第1の組のデータおよび第2の組のデータを収集するステップをさらに含む、請求項79に記載の方法。
- 前記第1の色素はFAM色素であり、前記第2の色素はVIC色素である、請求項79に記載の方法。
- 前記重なり合う波長帯は、前記それぞれのスペクトルがその吸収または発光の最大値の20%以上の値で重なり合うところとして定義され、前記重なり合う波長帯の幅は少なくとも25nmである、請求項79に記載の方法。
- 液滴に基づくアッセイにおける検出システムであって、
第1の色素および第2の色素を含む液滴を受け取るように構成された流路であって、前記第1の色素の発光スペクトルおよび前記第2の色素の吸収スペクトルにより重なり合う波長帯が画定され、前記重なり合いは、前記第1の色素が前記第2の色素の最大吸収波長で励起された場合に前記第1の色素からその最大発光値の少なくとも半分が生成される程度に大きい、流路と、
1つまたは複数のLEDを含み、前記第1および第2の色素をともに励起し得る励起光で前記液滴を照明するように構成された照明アセンブリであって、前記励起光は、前記LEDから放出され、前記重なり合う波長帯の短波長側の区域のみを含む、照明アセンブリと、
前記第1の色素および前記第2の色素が放出する光を検出するように構成された1つまたは複数の検出器であって、前記第2の色素からの前記光は、前記短波長側の区域から離れた前記重なり合う波長帯の長波長側の区域のみを含む波長域で検出される、検出器と、を備えるシステム。 - 前記照明アセンブリは、前記短波長側の区域を画定する1つまたは複数のフィルタを備える、請求項85に記載のシステム。
- 前記1つまたは複数の検出器を含む集光アセンブリをさらに備え、前記集光アセンブリは、前記長波長側の区域を画定する1つまたは複数のフィルタを含む、請求項85に記載のシステム。
- 液滴用の検出方法であって、
光ビームを生成するステップと、
前記光ビームを主ビームおよび少なくとも1つのサンプリングビームに分岐するステップと、
前記サンプリングビームの強度を監視するステップと、
前記監視ステップから得られる1つまたは複数の測定値に基づいて、前記光ビームの強度を調整するステップと、
流路の検査領域を、液滴が前記検査領域を通過するときに前記主ビームで照明するステップと、
前記検査領域から検出される光を表すデータを収集するステップとを含む、方法。 - 光ビームを生成する前記ステップは、光源から放出される光をフィルタリングして前記放出される光のスペクトルを変化させるステップを含み、前記分岐ステップは、前記フィルタリングステップの後で実施される、請求項88に記載の方法。
- 前記フィルタリングステップは、特定波長域透過波長フィルタ、長波長透過フィルタ、短波長透過フィルタ、またはこれらの組合せを用いて実施される、請求項88に記載の方法。
- 光ビームを生成する前記ステップは、少なくとも2つの光源から放出される光ビームを混合するステップを含み、前記混合ステップは、前記フィルタリングステップの後で実施される、請求項88に記載の方法。
- 光ビームを生成する前記ステップは、LEDを用いて光を放出させるステップを含む、請求項88に記載の方法。
- 光ビームを生成する前記ステップは、第1の光源および第2の光源からの光を混合するステップを含み、前記分岐ステップは、前記光ビームを第1のサンプリングビームおよび第2のサンプリングビームに分岐するステップを含み、前記第1のサンプリングビームは前記第1の光源に対応し、前記第2のサンプリングビームは前記第2の光源に対応する、請求項88に記載の方法。
- 前記調整ステップにより、前記主ビームの各光源に対応する部分の強度がほぼ一定に保たれる、請求項93に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US31768410P | 2010-03-25 | 2010-03-25 | |
| US61/317,684 | 2010-03-25 | ||
| PCT/US2011/030077 WO2011120006A1 (en) | 2010-03-25 | 2011-03-25 | Detection system for droplet-based assays |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013524169A true JP2013524169A (ja) | 2013-06-17 |
| JP2013524169A5 JP2013524169A5 (ja) | 2014-05-15 |
Family
ID=44673665
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013501528A Pending JP2013524169A (ja) | 2010-03-25 | 2011-03-25 | 液滴によるアッセイ用の検出システム |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US8730479B2 (ja) |
| EP (1) | EP2550351A4 (ja) |
| JP (1) | JP2013524169A (ja) |
| CA (1) | CA2767113A1 (ja) |
| WO (1) | WO2011120006A1 (ja) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016038208A (ja) * | 2014-08-05 | 2016-03-22 | 株式会社島津製作所 | 光学的検出器 |
| CN105936930A (zh) * | 2015-03-04 | 2016-09-14 | 松下知识产权经营株式会社 | Dna检测方法和dna检测装置 |
| JP2016168043A (ja) * | 2015-03-10 | 2016-09-23 | パナソニックIpマネジメント株式会社 | 複数の核酸ターゲットの解析方法 |
| WO2017187490A1 (ja) * | 2016-04-26 | 2017-11-02 | 株式会社日立ハイテクノロジーズ | 分析装置 |
| WO2019244358A1 (ja) * | 2018-06-22 | 2019-12-26 | 株式会社日立ハイテクノロジーズ | 電気泳動装置 |
| WO2020008972A1 (ja) * | 2018-07-06 | 2020-01-09 | 日本板硝子株式会社 | 反応処理装置 |
| JP2020073912A (ja) * | 2020-01-20 | 2020-05-14 | 日本板硝子株式会社 | 反応処理装置 |
| KR20210062596A (ko) * | 2019-11-21 | 2021-05-31 | 주식회사 바이오티엔에스 | 형광 검출 장치 및 이를 이용한 형광 검출 방법 |
| JP2022063291A (ja) * | 2018-06-22 | 2022-04-21 | 株式会社日立ハイテク | 電気泳動装置 |
| JP2022545093A (ja) * | 2019-08-23 | 2022-10-25 | ミダイアグノスティクス・エヌブイ | リアルタイムpcr検出のためのマルチカラーシステム |
Families Citing this family (73)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9417190B2 (en) | 2008-09-23 | 2016-08-16 | Bio-Rad Laboratories, Inc. | Calibrations and controls for droplet-based assays |
| US12162008B2 (en) | 2008-09-23 | 2024-12-10 | Bio-Rad Laboratories, Inc. | Partition-based method of analysis |
| GB2502409B8 (en) | 2008-09-23 | 2014-10-15 | Bio Rad Laboratories | Droplet-based assay system |
| US10512910B2 (en) | 2008-09-23 | 2019-12-24 | Bio-Rad Laboratories, Inc. | Droplet-based analysis method |
| US8633015B2 (en) | 2008-09-23 | 2014-01-21 | Bio-Rad Laboratories, Inc. | Flow-based thermocycling system with thermoelectric cooler |
| US11130128B2 (en) | 2008-09-23 | 2021-09-28 | Bio-Rad Laboratories, Inc. | Detection method for a target nucleic acid |
| US9492797B2 (en) | 2008-09-23 | 2016-11-15 | Bio-Rad Laboratories, Inc. | System for detection of spaced droplets |
| US9132394B2 (en) | 2008-09-23 | 2015-09-15 | Bio-Rad Laboratories, Inc. | System for detection of spaced droplets |
| US8709762B2 (en) | 2010-03-02 | 2014-04-29 | Bio-Rad Laboratories, Inc. | System for hot-start amplification via a multiple emulsion |
| US12090480B2 (en) | 2008-09-23 | 2024-09-17 | Bio-Rad Laboratories, Inc. | Partition-based method of analysis |
| US9764322B2 (en) | 2008-09-23 | 2017-09-19 | Bio-Rad Laboratories, Inc. | System for generating droplets with pressure monitoring |
| WO2011120024A1 (en) | 2010-03-25 | 2011-09-29 | Quantalife, Inc. | Droplet generation for droplet-based assays |
| US9156010B2 (en) | 2008-09-23 | 2015-10-13 | Bio-Rad Laboratories, Inc. | Droplet-based assay system |
| US9598725B2 (en) | 2010-03-02 | 2017-03-21 | Bio-Rad Laboratories, Inc. | Emulsion chemistry for encapsulated droplets |
| US8951939B2 (en) | 2011-07-12 | 2015-02-10 | Bio-Rad Laboratories, Inc. | Digital assays with multiplexed detection of two or more targets in the same optical channel |
| EP2940153B1 (en) | 2009-09-02 | 2020-05-13 | Bio-Rad Laboratories, Inc. | System for mixing fluids by coalescence of multiple emulsions |
| EP2556170A4 (en) | 2010-03-25 | 2014-01-01 | Quantalife Inc | TRAPPING TRANSPORT AND DETECTION SYSTEM |
| EP4016086A1 (en) | 2010-11-01 | 2022-06-22 | Bio-Rad Laboratories, Inc. | System for forming emulsions |
| US12097495B2 (en) | 2011-02-18 | 2024-09-24 | Bio-Rad Laboratories, Inc. | Methods and compositions for detecting genetic material |
| CN103534360A (zh) | 2011-03-18 | 2014-01-22 | 伯乐生命医学产品有限公司 | 借助对信号的组合使用进行的多重数字分析 |
| WO2012149042A2 (en) | 2011-04-25 | 2012-11-01 | Bio-Rad Laboratories, Inc. | Methods and compositions for nucleic acid analysis |
| EP2737089B1 (en) | 2011-07-29 | 2017-09-06 | Bio-rad Laboratories, Inc. | Library characterization by digital assay |
| EP2739587B1 (en) | 2011-08-01 | 2020-05-27 | Denovo Sciences | Cell capture system |
| US10466160B2 (en) | 2011-08-01 | 2019-11-05 | Celsee Diagnostics, Inc. | System and method for retrieving and analyzing particles |
| US9404864B2 (en) | 2013-03-13 | 2016-08-02 | Denovo Sciences, Inc. | System for imaging captured cells |
| US9174216B2 (en) | 2013-03-13 | 2015-11-03 | DeNovo Science, Inc. | System for capturing and analyzing cells |
| WO2013155531A2 (en) | 2012-04-13 | 2013-10-17 | Bio-Rad Laboratories, Inc. | Sample holder with a well having a wicking promoter |
| US9427737B2 (en) | 2012-12-14 | 2016-08-30 | Bio-Rad Laboratories, Inc. | Methods and compositions for using oils for analysis and detection of molecules |
| US9752181B2 (en) | 2013-01-26 | 2017-09-05 | Denovo Sciences, Inc. | System and method for capturing and analyzing cells |
| CN105492890B (zh) | 2013-02-22 | 2020-05-01 | 生命技术公司 | 校准用于执行生物分析的仪器的方法 |
| US9707562B2 (en) | 2013-03-13 | 2017-07-18 | Denovo Sciences, Inc. | System for capturing and analyzing cells |
| WO2014152048A2 (en) * | 2013-03-14 | 2014-09-25 | Cytonome/St, Llc | Assemblies and methods for reducing optical crosstalk in particle processing systems |
| JP2016114356A (ja) * | 2013-04-10 | 2016-06-23 | パナソニック株式会社 | 蛍光検出装置、及び蛍光検出方法 |
| US9856535B2 (en) | 2013-05-31 | 2018-01-02 | Denovo Sciences, Inc. | System for isolating cells |
| US10391490B2 (en) | 2013-05-31 | 2019-08-27 | Celsee Diagnostics, Inc. | System and method for isolating and analyzing cells |
| CN105518439B (zh) * | 2013-08-27 | 2018-02-16 | 株式会社日立高新技术 | 核酸分析装置及其装置诊断方法 |
| JP6632525B2 (ja) | 2013-11-06 | 2020-01-22 | ベクトン・ディキンソン・アンド・カンパニーBecton, Dickinson And Company | マイクロ流体デバイスならびにその製造方法および使用方法 |
| CN105899936B (zh) * | 2013-11-13 | 2019-12-24 | 贝克顿·迪金森公司 | 光学成像系统及使用其的方法 |
| KR102189845B1 (ko) * | 2014-06-03 | 2020-12-14 | 한국전자통신연구원 | 유체의 성질을 측정하는 장치 및 방법 |
| US10274428B2 (en) | 2014-11-25 | 2019-04-30 | Ge Healthcare Bio-Sciences Ab | Intergration of fluorescence detection capability into light absorbance measurement apparatus |
| US11123740B2 (en) | 2015-06-29 | 2021-09-21 | Arizona Board Of Regents On Behalf Of Arizona State University | Systems and methods for continuous flow digital droplet polymerase chain reaction bioanalysis |
| CN107923070A (zh) * | 2015-08-25 | 2018-04-17 | 生物辐射实验室股份有限公司 | 数字式免疫测定 |
| US10379047B2 (en) * | 2016-11-30 | 2019-08-13 | Scientific Industries, Inc. | Apparatus for detecting pH and dissolved oxygen |
| US10060847B2 (en) | 2015-12-30 | 2018-08-28 | Bio-Rad Laboratories, Inc. | Detection and signal processing system for particle assays |
| CN108700500B (zh) | 2015-12-30 | 2021-10-29 | 生物辐射实验室股份有限公司 | 用于颗粒的光学检测系统 |
| US10088468B2 (en) | 2016-02-04 | 2018-10-02 | Nova Biomedical Corporation | Analyte system and method for determining hemoglobin parameters in whole blood |
| EP3472591B1 (en) * | 2016-06-20 | 2023-08-30 | Plair SA | Device and method for detecting and/or characterizing fluid-borne particles |
| EP3544737B1 (en) | 2016-11-28 | 2025-04-23 | Arizona Board of Regents on behalf of Arizona State University | Methods related to continuous flow droplet reaction |
| EP3586094B1 (en) * | 2017-02-23 | 2023-08-16 | Phoseon Technology, Inc. | Integrated illumination-detection flow cell for liquid chromatography and corresponding method |
| DE102017113194B4 (de) * | 2017-06-14 | 2019-06-19 | Deutsches Zentrum für Luft- und Raumfahrt e.V. | Verfahren zum Verfolgen einer Vielzahl von punktförmigen Objekten im Raum |
| CN112980667B (zh) | 2017-08-29 | 2024-09-17 | 伯乐实验室有限公司 | 用于分离和分析细胞的系统和方法 |
| CN107860701A (zh) * | 2017-12-22 | 2018-03-30 | 广东顺德墨赛生物科技有限公司 | 微滴式进样荧光检测控制系统 |
| WO2019159109A1 (en) * | 2018-02-15 | 2019-08-22 | Societe Des Produits Nestle S.A. | Analyzer |
| CN112236218B (zh) * | 2018-04-02 | 2022-04-26 | 滴管公司 | 用于连续流乳液处理的系统和方法 |
| US11040347B2 (en) | 2018-06-14 | 2021-06-22 | Owl biomedical, Inc. | Microfabricated droplet dispensor with immiscible fluid |
| US12440841B2 (en) | 2018-06-14 | 2025-10-14 | Owl biomedical, Inc. | Microfabricated droplet dispensor with immiscible fluid and genetic sequencer |
| WO2020013811A1 (en) * | 2018-07-10 | 2020-01-16 | Xinova, LLC | Assessment of water quality using rainbow patterns |
| WO2020190641A1 (en) * | 2019-03-21 | 2020-09-24 | Becton, Dickinson And Company | Light detection systems and methods of use thereof |
| CN110118758B (zh) * | 2019-04-01 | 2022-06-03 | 深圳市趣方科技有限公司 | 一种散射荧光双模态流式成像系统 |
| US10633693B1 (en) | 2019-04-16 | 2020-04-28 | Celsee Diagnostics, Inc. | System and method for leakage control in a particle capture system |
| US11273439B2 (en) | 2019-05-07 | 2022-03-15 | Bio-Rad Laboratories, Inc. | System and method for target material retrieval from microwells |
| WO2020227309A1 (en) | 2019-05-07 | 2020-11-12 | Bio-Rad Laboratories, Inc. | System and method for automated single cell processing |
| CN114207407A (zh) | 2019-05-31 | 2022-03-18 | 安伯斯顿生物科学股份有限公司 | 低丰度事件的微流体确定 |
| EP3980754A1 (en) * | 2019-06-07 | 2022-04-13 | Helmholtz Zentrum München - Deutsches Forschungszentrum für Gesundheit und Umwelt (GmbH) | System and method for real-time multicolor shortwave infrared fluorescence imaging |
| KR20250084977A (ko) | 2019-06-14 | 2025-06-11 | 바이오 래드 래버러토리스 인코오포레이티드 | 자동화된 단일 세포 처리 및 분석을 위한 시스템 및 방법 |
| US11504719B2 (en) | 2020-03-12 | 2022-11-22 | Bio-Rad Laboratories, Inc. | System and method for receiving and delivering a fluid for sample processing |
| JP6962628B1 (ja) * | 2021-03-15 | 2021-11-05 | 株式会社ピーアンドエム | 検出装置 |
| WO2023003547A1 (en) * | 2021-07-21 | 2023-01-26 | Hewlett-Packard Development Company, L.P. | Fluidic devices with multiple interface properties |
| KR20240132441A (ko) * | 2021-10-28 | 2024-09-03 | 피티티 엑스플러레이션 앤드 프로덕션 퍼블릭 컴퍼니 리미티드 | 유체 내 입자 검출 장치 및 상기 입자의 검출 방법 |
| EP4444910A4 (en) | 2021-12-10 | 2025-11-05 | Bio Rad Laboratories Inc | Compositions, processes and systems for the treatment of samples with functionalized particles of adjustable morphology |
| EP4453246A4 (en) * | 2021-12-20 | 2025-12-24 | Countable Labs Inc | DIGITAL DETECTION AND QUANTIFICATION OF MULTIPLE TARGETS |
| CN119053846A (zh) * | 2022-02-28 | 2024-11-29 | 生物辐射实验室股份有限公司 | 宽谱分析系统 |
| EP4306929A1 (en) * | 2022-07-11 | 2024-01-17 | Ecole Polytechnique Fédérale de Lausanne | Fluorometer system, fluorescene analysis method, and use thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0465654A (ja) * | 1990-07-05 | 1992-03-02 | Hitachi Ltd | 細胞分析装置 |
| JP2007046947A (ja) * | 2005-08-08 | 2007-02-22 | Bay Bioscience Kk | フローサイトメータおよびフローサイトメトリ方法 |
| JP2008256712A (ja) * | 2008-06-12 | 2008-10-23 | Onchip Cellomics Consortium | 液滴分光システムと分光法 |
Family Cites Families (258)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3575220A (en) | 1968-08-12 | 1971-04-20 | Scientific Industries | Apparatus for dispensing liquid sample |
| BR7500831A (pt) | 1974-02-11 | 1975-12-02 | Fmc Corp | Aparelho de separacao de bolhas de gas corpo de transmissao de gas para uso no aparelho processo para fabricacao do dito corpo e para difusao de bolhas finas de gas em um corpo de liquido |
| US4051025A (en) | 1976-09-29 | 1977-09-27 | The United States Of America As Represented By The Department Of Health, Education And Welfare | Preparative countercurrent chromatography with a slowly rotating helical tube array |
| US4201691A (en) | 1978-01-16 | 1980-05-06 | Exxon Research & Engineering Co. | Liquid membrane generator |
| GB2040443B (en) * | 1978-12-07 | 1983-01-12 | English Electric Co Ltd | Optical particle size analyser |
| US4283262A (en) | 1980-07-01 | 1981-08-11 | Instrumentation Laboratory Inc. | Analysis system |
| GB2097692B (en) | 1981-01-10 | 1985-05-22 | Shaw Stewart P D | Combining chemical reagents |
| US4636075A (en) * | 1984-08-22 | 1987-01-13 | Particle Measuring Systems, Inc. | Particle measurement utilizing orthogonally polarized components of a laser beam |
| US4948961A (en) | 1985-08-05 | 1990-08-14 | Biotrack, Inc. | Capillary flow device |
| US5225332A (en) | 1988-04-22 | 1993-07-06 | Massachusetts Institute Of Technology | Process for manipulation of non-aqueous surrounded microdroplets |
| US5055390A (en) | 1988-04-22 | 1991-10-08 | Massachusetts Institute Of Technology | Process for chemical manipulation of non-aqueous surrounded microdroplets |
| DE69002767T2 (de) | 1989-06-22 | 1994-03-17 | Atta | Fluor- und phosphorhaltige amphiphilische moleküle mit oberflächenaktiven eigenschaften. |
| GB8917963D0 (en) | 1989-08-05 | 1989-09-20 | Scras | Apparatus for repeated automatic execution of a thermal cycle for treatment of biological samples |
| KR100236506B1 (ko) | 1990-11-29 | 2000-01-15 | 퍼킨-엘머시터스인스트루먼츠 | 폴리머라제 연쇄 반응 수행 장치 |
| US5270183A (en) | 1991-02-08 | 1993-12-14 | Beckman Research Institute Of The City Of Hope | Device and method for the automated cycling of solutions between two or more temperatures |
| US5994056A (en) | 1991-05-02 | 1999-11-30 | Roche Molecular Systems, Inc. | Homogeneous methods for nucleic acid amplification and detection |
| EP0519338B1 (en) | 1991-06-20 | 1996-08-28 | F. Hoffmann-La Roche Ag | Improved methods for nucleic acid amplification |
| US5422277A (en) | 1992-03-27 | 1995-06-06 | Ortho Diagnostic Systems Inc. | Cell fixative composition and method of staining cells without destroying the cell surface |
| US5587128A (en) | 1992-05-01 | 1996-12-24 | The Trustees Of The University Of Pennsylvania | Mesoscale polynucleotide amplification devices |
| US5637469A (en) | 1992-05-01 | 1997-06-10 | Trustees Of The University Of Pennsylvania | Methods and apparatus for the detection of an analyte utilizing mesoscale flow systems |
| EP0636413B1 (en) | 1993-07-28 | 2001-11-14 | PE Corporation (NY) | Nucleic acid amplification reaction apparatus and method |
| US5538667A (en) | 1993-10-28 | 1996-07-23 | Whitehill Oral Technologies, Inc. | Ultramulsions |
| US5538848A (en) | 1994-11-16 | 1996-07-23 | Applied Biosystems Division, Perkin-Elmer Corp. | Method for detecting nucleic acid amplification using self-quenching fluorescence probe |
| JP2909216B2 (ja) | 1994-04-29 | 1999-06-23 | パーキン‐エルマー コーポレイション | 核酸増幅生成物のリアルタイム検出装置 |
| US5972716A (en) | 1994-04-29 | 1999-10-26 | The Perkin-Elmer Corporation | Fluorescence monitoring device with textured optical tube and method for reducing background fluorescence |
| EP0695941B1 (en) | 1994-06-08 | 2002-07-31 | Affymetrix, Inc. | Method and apparatus for packaging a chip |
| US5555191A (en) | 1994-10-12 | 1996-09-10 | Trustees Of Columbia University In The City Of New York | Automated statistical tracker |
| US5585069A (en) | 1994-11-10 | 1996-12-17 | David Sarnoff Research Center, Inc. | Partitioned microelectronic and fluidic device array for clinical diagnostics and chemical synthesis |
| FR2733766B1 (fr) | 1995-05-03 | 1997-06-06 | Rhone Poulenc Rorer Sa | Methode de diagnostic de la schizophrenie |
| US20020022261A1 (en) | 1995-06-29 | 2002-02-21 | Anderson Rolfe C. | Miniaturized genetic analysis systems and methods |
| US5856174A (en) | 1995-06-29 | 1999-01-05 | Affymetrix, Inc. | Integrated nucleic acid diagnostic device |
| US6130098A (en) | 1995-09-15 | 2000-10-10 | The Regents Of The University Of Michigan | Moving microdroplets |
| US6057149A (en) | 1995-09-15 | 2000-05-02 | The University Of Michigan | Microscale devices and reactions in microscale devices |
| US20020068357A1 (en) | 1995-09-28 | 2002-06-06 | Mathies Richard A. | Miniaturized integrated nucleic acid processing and analysis device and method |
| US6562605B1 (en) | 1995-11-13 | 2003-05-13 | Genencor International, Inc. | Extraction of water soluble biomaterials from fluids using a carbon dioxide/surfactant mixture |
| US5736314A (en) | 1995-11-16 | 1998-04-07 | Microfab Technologies, Inc. | Inline thermo-cycler |
| WO1997036681A1 (en) | 1996-04-03 | 1997-10-09 | The Perkin-Elmer Corporation | Device and method for multiple analyte detection |
| NZ333346A (en) | 1996-06-28 | 2000-03-27 | Caliper Techn Corp | High-throughput screening assay systems in microscale fluidic devices |
| EP0909385B1 (en) | 1996-06-28 | 2008-09-10 | Caliper Life Sciences, Inc. | Method of transporting fluid samples within a microfluidic channel |
| US7026468B2 (en) | 1996-07-19 | 2006-04-11 | Valentis, Inc. | Process and equipment for plasmid purification |
| US6558916B2 (en) | 1996-08-02 | 2003-05-06 | Axiom Biotechnologies, Inc. | Cell flow apparatus and method for real-time measurements of patient cellular responses |
| US7268179B2 (en) | 1997-02-03 | 2007-09-11 | Cytonix Corporation | Hydrophobic coating compositions, articles coated with said compositions, and processes for manufacturing same |
| US6391622B1 (en) | 1997-04-04 | 2002-05-21 | Caliper Technologies Corp. | Closed-loop biochemical analyzers |
| US6143496A (en) | 1997-04-17 | 2000-11-07 | Cytonix Corporation | Method of sampling, amplifying and quantifying segment of nucleic acid, polymerase chain reaction assembly having nanoliter-sized sample chambers, and method of filling assembly |
| WO1998052691A1 (en) | 1997-05-16 | 1998-11-26 | Alberta Research Council | Microfluidic system and methods of use |
| JP3120453B2 (ja) | 1997-06-19 | 2000-12-25 | トヨタ自動車株式会社 | 微小液滴の保持方法、反応方法 |
| US5912945A (en) | 1997-06-23 | 1999-06-15 | Regents Of The University Of California | X-ray compass for determining device orientation |
| DE69838521T2 (de) | 1997-07-07 | 2008-05-21 | Medical Research Council | Methode zur Erhöhung der Konzentration von Nucleinsäuremolekülen |
| US5980936A (en) | 1997-08-07 | 1999-11-09 | Alliance Pharmaceutical Corp. | Multiple emulsions comprising a hydrophobic continuous phase |
| ATE294860T1 (de) | 1997-09-16 | 2005-05-15 | Egea Biosciences Llc | Methoden zur kompletten chemischen synthese und zusammensetzung von genen und genomen |
| US6833242B2 (en) | 1997-09-23 | 2004-12-21 | California Institute Of Technology | Methods for detecting and sorting polynucleotides based on size |
| US6540895B1 (en) | 1997-09-23 | 2003-04-01 | California Institute Of Technology | Microfabricated cell sorter for chemical and biological materials |
| US6074725A (en) | 1997-12-10 | 2000-06-13 | Caliper Technologies Corp. | Fabrication of microfluidic circuits by printing techniques |
| EP1059873B1 (en) | 1998-03-04 | 2006-08-16 | Visx Incorporated | System for laser treatment of presbyopia |
| US6175669B1 (en) | 1998-03-30 | 2001-01-16 | The Regents Of The Universtiy Of California | Optical coherence domain reflectometry guidewire |
| JP3081880B2 (ja) | 1998-03-30 | 2000-08-28 | 農林水産省食品総合研究所長 | マイクロスフィアの連続製造装置 |
| US6384915B1 (en) | 1998-03-30 | 2002-05-07 | The Regents Of The University Of California | Catheter guided by optical coherence domain reflectometry |
| JP3012608B1 (ja) | 1998-09-17 | 2000-02-28 | 農林水産省食品総合研究所長 | マイクロチャネル装置及び同装置を用いたエマルションの製造方法 |
| US6146103A (en) | 1998-10-09 | 2000-11-14 | The Regents Of The University Of California | Micromachined magnetohydrodynamic actuators and sensors |
| US6637463B1 (en) | 1998-10-13 | 2003-10-28 | Biomicro Systems, Inc. | Multi-channel microfluidic system design with balanced fluid flow distribution |
| US6176609B1 (en) | 1998-10-13 | 2001-01-23 | V & P Scientific, Inc. | Magnetic tumble stirring method, devices and machines for mixing in vessels |
| US6086740A (en) | 1998-10-29 | 2000-07-11 | Caliper Technologies Corp. | Multiplexed microfluidic devices and systems |
| US6261431B1 (en) | 1998-12-28 | 2001-07-17 | Affymetrix, Inc. | Process for microfabrication of an integrated PCR-CE device and products produced by the same |
| GB9900298D0 (en) | 1999-01-07 | 1999-02-24 | Medical Res Council | Optical sorting method |
| US6522407B2 (en) | 1999-01-22 | 2003-02-18 | The Regents Of The University Of California | Optical detection dental disease using polarized light |
| US6326083B1 (en) | 1999-03-08 | 2001-12-04 | Calipher Technologies Corp. | Surface coating for microfluidic devices that incorporate a biopolymer resistant moiety |
| US6303343B1 (en) | 1999-04-06 | 2001-10-16 | Caliper Technologies Corp. | Inefficient fast PCR |
| US6964846B1 (en) | 1999-04-09 | 2005-11-15 | Exact Sciences Corporation | Methods for detecting nucleic acids indicative of cancer |
| US6357907B1 (en) | 1999-06-15 | 2002-03-19 | V & P Scientific, Inc. | Magnetic levitation stirring devices and machines for mixing in vessels |
| US6440706B1 (en) | 1999-08-02 | 2002-08-27 | Johns Hopkins University | Digital amplification |
| US6524456B1 (en) | 1999-08-12 | 2003-02-25 | Ut-Battelle, Llc | Microfluidic devices for the controlled manipulation of small volumes |
| DE19964337B4 (de) | 1999-10-01 | 2004-09-16 | Agilent Technologies, Inc. (n.d.Ges.d.Staates Delaware), Palo Alto | Mikrofluidischer Mikrochip mit abbiegbarem Ansaugrohr |
| AU4714201A (en) | 1999-12-07 | 2001-06-18 | Exact Sciences Corporation | Supracolonic aerodigestive neoplasm detection |
| ATE340025T1 (de) | 2000-01-06 | 2006-10-15 | Caliper Life Sciences Inc | Vorrichtungen und verfahren für hochdurchsatz- probenentnahme und analyse |
| US20020151040A1 (en) | 2000-02-18 | 2002-10-17 | Matthew O' Keefe | Apparatus and methods for parallel processing of microvolume liquid reactions |
| US20020058329A1 (en) | 2000-02-18 | 2002-05-16 | Sharat Singh | Multiple-site reaction device and method |
| JP3282619B2 (ja) | 2000-03-22 | 2002-05-20 | 住友電装株式会社 | ワイヤーハーネスの屈曲試験方法及び電線の屈曲試験装置 |
| US7279146B2 (en) | 2003-04-17 | 2007-10-09 | Fluidigm Corporation | Crystal growth devices and systems, and methods for using same |
| EP1286913A2 (en) | 2000-05-24 | 2003-03-05 | Micronics, Inc. | Microfluidic concentration gradient loop |
| US7351376B1 (en) | 2000-06-05 | 2008-04-01 | California Institute Of Technology | Integrated active flux microfluidic devices and methods |
| US6466713B2 (en) | 2000-08-18 | 2002-10-15 | The Regents Of The University Of California | Optical fiber head for providing lateral viewing |
| US6773566B2 (en) | 2000-08-31 | 2004-08-10 | Nanolytics, Inc. | Electrostatic actuators for microfluidics and methods for using same |
| WO2002022878A1 (en) | 2000-09-14 | 2002-03-21 | Caliper Technologies Corp. | Microfluidic devices and methods for performing temperature mediated reactions |
| AU2001290879A1 (en) | 2000-09-15 | 2002-03-26 | California Institute Of Technology | Microfabricated crossflow devices and methods |
| KR100649342B1 (ko) | 2000-10-30 | 2006-11-27 | 시쿼넘, 인코포레이티드 | 기판 상으로 서브마이크로리터 볼륨들을 전달하기 위한 방법 및 장치 |
| KR100435921B1 (ko) | 2000-12-29 | 2004-06-12 | 주식회사 태평양 | 동수역학적 이중 안정화에 의한 안정한 수-유-수 다중에멀젼 시스템 및 이의 제조방법 |
| US7567596B2 (en) * | 2001-01-30 | 2009-07-28 | Board Of Trustees Of Michigan State University | Control system and apparatus for use with ultra-fast laser |
| DE60211857T2 (de) | 2001-02-23 | 2006-12-21 | Japan Science And Technology Agency, Kawaguchi | Verfahren zur herstellung einer emulsion und vorrichtung dafür |
| US6949176B2 (en) | 2001-02-28 | 2005-09-27 | Lightwave Microsystems Corporation | Microfluidic control using dielectric pumping |
| US7192557B2 (en) | 2001-03-28 | 2007-03-20 | Handylab, Inc. | Methods and systems for releasing intracellular material from cells within microfluidic samples of fluids |
| US6575188B2 (en) | 2001-07-26 | 2003-06-10 | Handylab, Inc. | Methods and systems for fluid control in microfluidic devices |
| US7010391B2 (en) | 2001-03-28 | 2006-03-07 | Handylab, Inc. | Methods and systems for control of microfluidic devices |
| US7270786B2 (en) | 2001-03-28 | 2007-09-18 | Handylab, Inc. | Methods and systems for processing microfluidic samples of particle containing fluids |
| EP1384022A4 (en) | 2001-04-06 | 2004-08-04 | California Inst Of Techn | NUCLEIC ACID AMPLIFICATION USING MICROFLUID DEVICES |
| US6793723B2 (en) * | 2001-05-10 | 2004-09-21 | Pitney Bowes Inc. | Homogeneous photosensitive optically variable ink compositions for ink jet printing |
| US20030049659A1 (en) | 2001-05-29 | 2003-03-13 | Lapidus Stanley N. | Devices and methods for isolating samples into subsamples for analysis |
| NZ530037A (en) | 2001-06-12 | 2006-03-31 | Keryx Biopharmaceuticals Inc | Use of glycosaminoglycans for the treatment of HIV-associated nephropathy |
| US6905885B2 (en) | 2001-06-12 | 2005-06-14 | The Regents Of The University Of California | Portable pathogen detection system |
| US6808683B2 (en) | 2001-09-25 | 2004-10-26 | Cytonome, Inc. | Droplet dispensing system |
| CA2451614C (en) | 2001-06-25 | 2011-01-04 | Georgia Tech Research Corporation | Dual resonance energy transfer nucleic acid probes |
| US6797257B2 (en) | 2001-06-26 | 2004-09-28 | The Board Of Trustees Of The University Of Illinois | Paramagnetic polymerized protein microspheres and methods of preparation thereof |
| US6573490B2 (en) * | 2001-06-28 | 2003-06-03 | Valeo Electrical Systems, Inc. | Interleaved mosaic imaging rain sensor |
| US20030032172A1 (en) | 2001-07-06 | 2003-02-13 | The Regents Of The University Of California | Automated nucleic acid assay system |
| US7297778B2 (en) | 2001-07-25 | 2007-11-20 | Affymetrix, Inc. | Complexity management of genomic DNA |
| US20030027150A1 (en) | 2001-08-03 | 2003-02-06 | Katz David A. | Method of haplotyping and kit therefor |
| AUPR707101A0 (en) | 2001-08-16 | 2001-09-06 | Corbett Research Pty Ltd | Continuous flow thermal device |
| US7094379B2 (en) | 2001-10-24 | 2006-08-22 | Commissariat A L'energie Atomique | Device for parallel and synchronous injection for sequential injection of different reagents |
| GB0127564D0 (en) | 2001-11-16 | 2002-01-09 | Medical Res Council | Emulsion compositions |
| JP4355210B2 (ja) | 2001-11-30 | 2009-10-28 | フルイディグム コーポレイション | 微小流体デバイスおよび微小流体デバイスの使用方法 |
| US7198897B2 (en) | 2001-12-19 | 2007-04-03 | Brandeis University | Late-PCR |
| US20030170698A1 (en) | 2002-01-04 | 2003-09-11 | Peter Gascoyne | Droplet-based microfluidic oligonucleotide synthesis engine |
| US20030180765A1 (en) | 2002-02-01 | 2003-09-25 | The Johns Hopkins University | Digital amplification for detection of mismatch repair deficient tumor cells |
| ATE397096T1 (de) | 2002-03-20 | 2008-06-15 | Innovativebio Biz | Mikrokapseln mit kontrollierter durchlässigkeit die ein nukleinsäureamplifizierungsreaktionsgemisch enthalten und deren benutzung als reaktionsgefäss für parallele reaktionen |
| US7312085B2 (en) | 2002-04-01 | 2007-12-25 | Fluidigm Corporation | Microfluidic particle-analysis systems |
| US7993266B2 (en) | 2002-04-26 | 2011-08-09 | Lawrence Livermore National Security, Llc | Early detection of contagious diseases |
| EP2302389B1 (en) | 2002-05-09 | 2018-01-24 | The University of Chicago | Device and method for pressure-driven plug transport and reaction |
| FR2841063B1 (fr) | 2002-06-18 | 2004-09-17 | Commissariat Energie Atomique | Dispositif de deplacement de petits volumes de liquide le long d'un micro-catenaire par des forces electrostatiques |
| JP2006507921A (ja) | 2002-06-28 | 2006-03-09 | プレジデント・アンド・フェロウズ・オブ・ハーバード・カレッジ | 流体分散のための方法および装置 |
| US6794671B2 (en) * | 2002-07-17 | 2004-09-21 | Particle Sizing Systems, Inc. | Sensors and methods for high-sensitivity optical particle counting and sizing |
| US20040038385A1 (en) | 2002-08-26 | 2004-02-26 | Langlois Richard G. | System for autonomous monitoring of bioagents |
| US7188731B2 (en) | 2002-08-26 | 2007-03-13 | The Regents Of The University Of California | Variable flexure-based fluid filter |
| WO2004040001A2 (en) | 2002-10-02 | 2004-05-13 | California Institute Of Technology | Microfluidic nucleic acid analysis |
| US20060094108A1 (en) | 2002-12-20 | 2006-05-04 | Karl Yoder | Thermal cycler for microfluidic array assays |
| EP1587940A4 (en) | 2002-12-20 | 2006-06-07 | Caliper Life Sciences Inc | SINGLE MOLECULAR AMPLIFICATION AND DNA PROOF |
| US20050042639A1 (en) | 2002-12-20 | 2005-02-24 | Caliper Life Sciences, Inc. | Single molecule amplification and detection of DNA length |
| CA2521999A1 (en) | 2002-12-20 | 2004-09-02 | Biotrove, Inc. | Assay apparatus and method using microfluidic arrays |
| CA2513535C (en) | 2003-01-29 | 2012-06-12 | 454 Corporation | Bead emulsion nucleic acid amplification |
| WO2004071638A2 (en) | 2003-02-11 | 2004-08-26 | Regents Of The University Of California, The | Microfluidic devices and method for controlled viscous shearing and formation of amphiphilic vesicles |
| US7041481B2 (en) | 2003-03-14 | 2006-05-09 | The Regents Of The University Of California | Chemical amplification based on fluid partitioning |
| EP3511693B1 (en) * | 2003-03-28 | 2022-08-24 | Inguran, LLC | Apparatus for detecting the breakoff point of a droplet generation system |
| US8828663B2 (en) | 2005-03-18 | 2014-09-09 | Fluidigm Corporation | Thermal reaction device and method for using the same |
| US7604965B2 (en) | 2003-04-03 | 2009-10-20 | Fluidigm Corporation | Thermal reaction device and method for using the same |
| DE10315640A1 (de) | 2003-04-04 | 2004-10-14 | Ignatov, Konstantin | Verfahren zur kontrollierten Freisetzung von Komponenten in eine Lösung |
| DE602004028837D1 (de) | 2003-07-03 | 2010-10-07 | Univ New Jersey Med | Gene als diagnostische werkzeuge für autismus |
| US7629123B2 (en) | 2003-07-03 | 2009-12-08 | University Of Medicine And Dentistry Of New Jersey | Compositions and methods for diagnosing autism |
| US8048627B2 (en) | 2003-07-05 | 2011-11-01 | The Johns Hopkins University | Method and compositions for detection and enumeration of genetic variations |
| EP1654527A4 (en) | 2003-08-01 | 2012-01-04 | Ge Healthcare Bio Sciences Ab | OPTICAL RESONANCE ANALYSIS UNIT |
| EP2662136A3 (en) | 2003-08-27 | 2013-12-25 | President and Fellows of Harvard College | Method for handling and mixing droplets |
| JP4474870B2 (ja) * | 2003-08-27 | 2010-06-09 | セイコーエプソン株式会社 | 液滴視認方法、液滴吐出ヘッド検査装置および液滴吐出装置 |
| WO2005023091A2 (en) | 2003-09-05 | 2005-03-17 | The Trustees Of Boston University | Method for non-invasive prenatal diagnosis |
| US20050277125A1 (en) | 2003-10-27 | 2005-12-15 | Massachusetts Institute Of Technology | High-density reaction chambers and methods of use |
| US7141537B2 (en) | 2003-10-30 | 2006-11-28 | 3M Innovative Properties Company | Mixture of fluorinated polyethers and use thereof as surfactant |
| ES2355242T3 (es) | 2003-12-05 | 2011-03-24 | Beatrice And Samuel A. Seaver Foundation | Procedimiento de evaluación del riesgo genético relativo al autismo. |
| CA2553833C (en) | 2004-01-28 | 2012-10-02 | 454 Corporation | Nucleic acid amplification with continuous flow emulsion |
| US8293471B2 (en) | 2004-01-28 | 2012-10-23 | Marshall University Research Corporation | Apparatus and method for a continuous rapid thermal cycle system |
| WO2005075683A1 (en) | 2004-02-03 | 2005-08-18 | Postech Foundation | High throughput device for performing continuous-flow reactions |
| KR100552706B1 (ko) | 2004-03-12 | 2006-02-20 | 삼성전자주식회사 | 핵산 증폭 방법 및 장치 |
| CN100431679C (zh) | 2004-03-23 | 2008-11-12 | 独立行政法人科学技术振兴机构 | 微小液滴的生成方法及装置 |
| US7432106B2 (en) | 2004-03-24 | 2008-10-07 | Applied Biosystems Inc. | Liquid processing device including gas trap, and system and method |
| EP2439285B1 (en) | 2004-03-31 | 2019-05-08 | The General Hospital Corporation | Method to determine responsiveness of cancer to epidermal growth factor receptor targeting treatments |
| US20050221279A1 (en) | 2004-04-05 | 2005-10-06 | The Regents Of The University Of California | Method for creating chemical sensors using contact-based microdispensing technology |
| HU227246B1 (en) | 2004-04-30 | 2010-12-28 | Szegedi Biolog Koezpont | Use of genes as molecular markers in diagnosis of schizophrenia and diagnostic kit |
| WO2005110395A1 (en) | 2004-05-19 | 2005-11-24 | University Of South Carolina | System and device for magnetic drug targeting with magnetic drug carrier particles |
| US8652851B2 (en) | 2004-06-17 | 2014-02-18 | University Of Florida Research Foundation, Inc. | Multi-acceptor molecular probes and applications thereof |
| ATE425264T1 (de) | 2004-06-29 | 2009-03-15 | Hoffmann La Roche | Assoziation von snps in ppar gamma mit osteoporose |
| US20080268436A1 (en) | 2004-08-20 | 2008-10-30 | Jubao Duan | Schizophrenia, Schizoaffective Disorder and Bipolar Disorder Susceptibility Gene Mutation and Applications to Their Diagnosis and Treatment |
| WO2006027757A2 (en) | 2004-09-09 | 2006-03-16 | Institut Curie | Microfluidic device using a collinear electric field |
| US7968287B2 (en) | 2004-10-08 | 2011-06-28 | Medical Research Council Harvard University | In vitro evolution in microfluidic systems |
| WO2006047787A2 (en) | 2004-10-27 | 2006-05-04 | Exact Sciences Corporation | Method for monitoring disease progression or recurrence |
| US8951746B2 (en) | 2004-11-05 | 2015-02-10 | Southwest Research Institute | Method and devices for screening cervical cancer |
| US20090098044A1 (en) | 2004-11-15 | 2009-04-16 | Australian Nuclear Science And Technology Organisation | Solid particles from controlled destabilisation of microemulsions |
| US20060166223A1 (en) | 2005-01-26 | 2006-07-27 | Reed Michael W | DNA purification and analysis on nanoengineered surfaces |
| US7423751B2 (en) * | 2005-02-08 | 2008-09-09 | Northrop Grumman Corporation | Systems and methods for use in detecting harmful aerosol particles |
| CN101193905B (zh) | 2005-02-11 | 2014-06-25 | 纪念斯隆-凯特林癌症中心 | 用于检测抗药egfr突变体的方法和组合物 |
| WO2006096571A2 (en) | 2005-03-04 | 2006-09-14 | President And Fellows Of Harvard College | Method and apparatus for forming multiple emulsions |
| KR20100099333A (ko) | 2005-03-05 | 2010-09-10 | 주식회사 씨젠 | 이중 특이성 올리고뉴클레오타이드를 사용한 방법 및 이중 특이성 올리고뉴클레오타이드 |
| WO2006099579A2 (en) | 2005-03-16 | 2006-09-21 | Applera Corporation | Compositions and methods for clonal amplification and analysis of polynucleotides |
| US20070048756A1 (en) | 2005-04-18 | 2007-03-01 | Affymetrix, Inc. | Methods for whole genome association studies |
| US20070024658A1 (en) * | 2005-07-28 | 2007-02-01 | Eastman Kodak Company | Apparatus and method for detection of liquid droplets |
| DE102005037401B4 (de) | 2005-08-08 | 2007-09-27 | MAX-PLANCK-Gesellschaft zur Förderung der Wissenschaften e.V. | Bildung einer Emulsion in einem fluidischen Mikrosystem |
| WO2007038670A2 (en) | 2005-09-30 | 2007-04-05 | Perlegen Sciences, Inc. | Methods and compositions for screening and treatment of disorders of blood glucose regulation |
| DE102005062174C5 (de) * | 2005-12-23 | 2010-05-06 | INSTITUT FüR MIKROTECHNIK MAINZ GMBH | Meßchip |
| WO2007081386A2 (en) | 2006-01-11 | 2007-07-19 | Raindance Technologies, Inc. | Microfluidic devices and methods of use |
| US7976795B2 (en) | 2006-01-19 | 2011-07-12 | Rheonix, Inc. | Microfluidic systems |
| WO2007089541A2 (en) | 2006-01-27 | 2007-08-09 | President And Fellows Of Harvard College | Fluidic droplet coalescence |
| SI1981995T2 (sl) | 2006-02-02 | 2019-08-30 | The Board Of Trustees Of The Leland Stanford Junior University | Neinvazivni genetski presejalni test ploda z digitalno analizo |
| US20100304446A1 (en) | 2006-02-07 | 2010-12-02 | Stokes Bio Limited | Devices, systems, and methods for amplifying nucleic acids |
| EP1991357B1 (en) | 2006-02-07 | 2016-09-14 | Stokes Bio Limited | A microfluidic analysis system |
| ATE523244T1 (de) | 2006-02-07 | 2011-09-15 | Stokes Bio Ltd | Flüssigkeitsbrückesystem und verfahren |
| WO2007120745A2 (en) | 2006-04-11 | 2007-10-25 | Optiscan Biomedical Corporation | Noise reduction for analyte detection system |
| US7815871B2 (en) | 2006-04-18 | 2010-10-19 | Advanced Liquid Logic, Inc. | Droplet microactuator system |
| US7816121B2 (en) | 2006-04-18 | 2010-10-19 | Advanced Liquid Logic, Inc. | Droplet actuation system and method |
| EP2021113A2 (en) | 2006-05-11 | 2009-02-11 | Raindance Technologies, Inc. | Microfluidic devices |
| US7608399B2 (en) | 2006-06-26 | 2009-10-27 | Blood Cell Storage, Inc. | Device and method for extraction and analysis of nucleic acids from biological samples |
| EP1881079A1 (en) | 2006-07-20 | 2008-01-23 | Pangaea Biotech, S.A. | Method for the detection of EGFR mutations in blood samples |
| EP3536396B1 (en) | 2006-08-07 | 2022-03-30 | The President and Fellows of Harvard College | Fluorocarbon emulsion stabilizing surfactants |
| WO2008024114A1 (en) | 2006-08-24 | 2008-02-28 | Genizon Biosciences Inc. | Genemap of the human genes associated with schizophrenia |
| US20080166720A1 (en) * | 2006-10-06 | 2008-07-10 | The Regents Of The University Of California | Method and apparatus for rapid nucleic acid analysis |
| EP1912067A1 (en) | 2006-10-12 | 2008-04-16 | Eppendorf Array Technologies S.A. | Method for quantification of a target compound obtained from a biological sample upon chips |
| WO2008052138A2 (en) | 2006-10-25 | 2008-05-02 | The Regents Of The University Of California | Inline-injection microdevice and microfabricated integrated dna analysis system using same |
| WO2008070074A2 (en) | 2006-12-04 | 2008-06-12 | Pgxhealth Llc | Genetic markers of schizophrenia |
| US20080176237A1 (en) | 2006-12-07 | 2008-07-24 | Biocept, Inc. | Non-invasive prenatal genetic screen |
| US8262900B2 (en) | 2006-12-14 | 2012-09-11 | Life Technologies Corporation | Methods and apparatus for measuring analytes using large scale FET arrays |
| US8338166B2 (en) | 2007-01-04 | 2012-12-25 | Lawrence Livermore National Security, Llc | Sorting, amplification, detection, and identification of nucleic acid subsequences in a complex mixture |
| US8228657B2 (en) | 2007-01-17 | 2012-07-24 | University Of Rochester | Frequency-addressable apparatus and methods for actuation of liquids |
| WO2008109878A2 (en) | 2007-03-07 | 2008-09-12 | California Institute Of Technology | Testing device |
| US9029085B2 (en) | 2007-03-07 | 2015-05-12 | President And Fellows Of Harvard College | Assays and other reactions involving droplets |
| CA2679091A1 (en) | 2007-03-08 | 2008-09-18 | Abdelmajid Belouchi | Genemap of the human genes associated with schizophrenia |
| US7776927B2 (en) | 2007-03-28 | 2010-08-17 | President And Fellows Of Harvard College | Emulsions and techniques for formation |
| EP2479552B1 (en) * | 2007-04-02 | 2015-09-02 | Acoustic Cytometry Systems, Inc. | Methods for enhanced analysis of acoustic field focused cells and particles |
| JP5666763B2 (ja) | 2007-04-11 | 2015-02-12 | 味の素株式会社 | 油中水型乳化組成物 |
| US8951732B2 (en) | 2007-06-22 | 2015-02-10 | Advanced Liquid Logic, Inc. | Droplet-based nucleic acid amplification in a temperature gradient |
| WO2009011808A1 (en) | 2007-07-13 | 2009-01-22 | President And Fellows Of Harvard College | Droplet-based selection |
| US20100086913A1 (en) | 2007-07-30 | 2010-04-08 | Roche Molecular Systems, Inc. | Methods of Identification Using Methylation of CPG |
| US20090053719A1 (en) | 2007-08-03 | 2009-02-26 | The Chinese University Of Hong Kong | Analysis of nucleic acids by digital pcr |
| GB2452057A (en) * | 2007-08-23 | 2009-02-25 | Shaw Stewart P D | A microfluidic device for thermal assays |
| EP2198293B1 (en) | 2007-09-07 | 2012-01-18 | Fluidigm Corporation | Copy number variation determination, methods and systems |
| CN102124125A (zh) | 2007-10-16 | 2011-07-13 | 霍夫曼-拉罗奇有限公司 | 通过克隆性测序的高分辨率、高通量hla基因分型 |
| US7807920B2 (en) | 2007-10-30 | 2010-10-05 | Opel, Inc. | Concentrated solar photovoltaic module |
| US8603566B2 (en) | 2007-12-20 | 2013-12-10 | University Of Massachusetts | Cross-linked biopolymers, related compounds and methods of use |
| JP5224801B2 (ja) | 2007-12-21 | 2013-07-03 | キヤノン株式会社 | 核酸増幅装置 |
| US8367370B2 (en) | 2008-02-11 | 2013-02-05 | Wheeler Aaron R | Droplet-based cell culture and cell assays using digital microfluidics |
| US20090220434A1 (en) | 2008-02-29 | 2009-09-03 | Florida State University Research Foundation | Nanoparticles that facilitate imaging of biological tissue and methods of forming the same |
| US8062903B2 (en) | 2008-03-03 | 2011-11-22 | University Of Washington | Droplet compartmentalization for chemical separation and on-line sampling |
| US9487822B2 (en) | 2008-03-19 | 2016-11-08 | Fluidigm Corporation | Method and apparatus for determining copy number variation using digital PCR |
| US9011777B2 (en) | 2008-03-21 | 2015-04-21 | Lawrence Livermore National Security, Llc | Monodisperse microdroplet generation and stopping without coalescence |
| DK2279405T3 (da) | 2008-05-13 | 2014-01-13 | Advanced Liquid Logic Inc | Dråbeaktuatorindretninger, -systemer og -fremgangsmåder |
| EP2313520B1 (en) | 2008-07-04 | 2014-08-27 | Decode Genetics EHF | Copy number variations predictive of risk of schizophrenia |
| EP4047367A1 (en) | 2008-07-18 | 2022-08-24 | Bio-Rad Laboratories, Inc. | Method for detecting target analytes with droplet libraries |
| US8256931B2 (en) | 2008-07-24 | 2012-09-04 | Seward George H | Achromatic homogenizer and collimator for LEDs |
| JP2011530305A (ja) | 2008-08-12 | 2011-12-22 | ストークス バイオ リミテッド | デジタルpcrのための方法 |
| US9180453B2 (en) | 2008-08-15 | 2015-11-10 | University Of Washington | Method and apparatus for the discretization and manipulation of sample volumes |
| WO2010021936A1 (en) | 2008-08-16 | 2010-02-25 | The Board Of Trustees Of The Leland Stanford Junior University | Digital pcr calibration for high throughput sequencing |
| US8383345B2 (en) | 2008-09-12 | 2013-02-26 | University Of Washington | Sequence tag directed subassembly of short sequencing reads into long sequencing reads |
| WO2010033200A2 (en) | 2008-09-19 | 2010-03-25 | President And Fellows Of Harvard College | Creation of libraries of droplets and related species |
| US9598725B2 (en) | 2010-03-02 | 2017-03-21 | Bio-Rad Laboratories, Inc. | Emulsion chemistry for encapsulated droplets |
| US9156010B2 (en) | 2008-09-23 | 2015-10-13 | Bio-Rad Laboratories, Inc. | Droplet-based assay system |
| US8951939B2 (en) | 2011-07-12 | 2015-02-10 | Bio-Rad Laboratories, Inc. | Digital assays with multiplexed detection of two or more targets in the same optical channel |
| US20120171683A1 (en) | 2010-03-02 | 2012-07-05 | Ness Kevin D | Analysis of fragmented genomic dna in droplets |
| US8633015B2 (en) | 2008-09-23 | 2014-01-21 | Bio-Rad Laboratories, Inc. | Flow-based thermocycling system with thermoelectric cooler |
| US20130059754A1 (en) | 2011-09-01 | 2013-03-07 | Bio-Rad Laboratories, Inc. | Digital assays with reduced measurement uncertainty |
| US20130017551A1 (en) | 2011-07-13 | 2013-01-17 | Bio-Rad Laboratories, Inc. | Computation of real-world error using meta-analysis of replicates |
| WO2011120024A1 (en) | 2010-03-25 | 2011-09-29 | Quantalife, Inc. | Droplet generation for droplet-based assays |
| US9132394B2 (en) | 2008-09-23 | 2015-09-15 | Bio-Rad Laboratories, Inc. | System for detection of spaced droplets |
| US8709762B2 (en) | 2010-03-02 | 2014-04-29 | Bio-Rad Laboratories, Inc. | System for hot-start amplification via a multiple emulsion |
| US20130084572A1 (en) | 2011-09-30 | 2013-04-04 | Quantalife, Inc. | Calibrations and controls for droplet-based assays |
| US20100304978A1 (en) | 2009-01-26 | 2010-12-02 | David Xingfei Deng | Methods and compositions for identifying a fetal cell |
| EP3415235B1 (en) | 2009-03-23 | 2025-11-12 | Bio-Rad Laboratories, Inc. | Manipulation of microfluidic droplets |
| US20100261230A1 (en) | 2009-04-08 | 2010-10-14 | Applied Biosystems, Llc | System comprising dual-sided thermal cycler and emulsion pcr in pouch |
| EP2940153B1 (en) | 2009-09-02 | 2020-05-13 | Bio-Rad Laboratories, Inc. | System for mixing fluids by coalescence of multiple emulsions |
| ES2709123T3 (es) | 2009-09-21 | 2019-04-15 | Akonni Biosystems | Método y dispositivo para lisis magnética |
| WO2011042564A1 (en) | 2009-10-09 | 2011-04-14 | Universite De Strasbourg | Labelled silica-based nanomaterial with enhanced properties and uses thereof |
| EP2488656B1 (en) | 2009-10-15 | 2015-06-03 | Ibis Biosciences, Inc. | Multiple displacement amplification |
| US8835358B2 (en) | 2009-12-15 | 2014-09-16 | Cellular Research, Inc. | Digital counting of individual molecules by stochastic attachment of diverse labels |
| WO2011079176A2 (en) | 2009-12-23 | 2011-06-30 | Raindance Technologies, Inc. | Microfluidic systems and methods for reducing the exchange of molecules between droplets |
| US9399797B2 (en) | 2010-02-12 | 2016-07-26 | Raindance Technologies, Inc. | Digital analyte analysis |
| JP5934657B2 (ja) | 2010-02-12 | 2016-06-15 | レインダンス テクノロジーズ, インコーポレイテッド | デジタル検体分析 |
| EP2556170A4 (en) | 2010-03-25 | 2014-01-01 | Quantalife Inc | TRAPPING TRANSPORT AND DETECTION SYSTEM |
| EP2622103B2 (en) | 2010-09-30 | 2022-11-16 | Bio-Rad Laboratories, Inc. | Sandwich assays in droplets |
| EP4016086A1 (en) | 2010-11-01 | 2022-06-22 | Bio-Rad Laboratories, Inc. | System for forming emulsions |
| WO2012109604A1 (en) | 2011-02-11 | 2012-08-16 | Raindance Technologies, Inc. | Thermocycling device for nucleic acid amplification and methods of use |
| EP3859011A1 (en) | 2011-02-11 | 2021-08-04 | Bio-Rad Laboratories, Inc. | Methods for forming mixed droplets |
| EP3736281A1 (en) | 2011-02-18 | 2020-11-11 | Bio-Rad Laboratories, Inc. | Compositions and methods for molecular labeling |
| CN103534360A (zh) | 2011-03-18 | 2014-01-22 | 伯乐生命医学产品有限公司 | 借助对信号的组合使用进行的多重数字分析 |
| US8841071B2 (en) | 2011-06-02 | 2014-09-23 | Raindance Technologies, Inc. | Sample multiplexing |
| US9556470B2 (en) | 2011-06-02 | 2017-01-31 | Raindance Technologies, Inc. | Enzyme quantification |
| US8658430B2 (en) | 2011-07-20 | 2014-02-25 | Raindance Technologies, Inc. | Manipulating droplet size |
| EP2737089B1 (en) | 2011-07-29 | 2017-09-06 | Bio-rad Laboratories, Inc. | Library characterization by digital assay |
-
2011
- 2011-03-25 JP JP2013501528A patent/JP2013524169A/ja active Pending
- 2011-03-25 CA CA2767113A patent/CA2767113A1/en not_active Abandoned
- 2011-03-25 WO PCT/US2011/030077 patent/WO2011120006A1/en not_active Ceased
- 2011-03-25 EP EP11760347.2A patent/EP2550351A4/en not_active Withdrawn
- 2011-12-30 US US13/341,678 patent/US8730479B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0465654A (ja) * | 1990-07-05 | 1992-03-02 | Hitachi Ltd | 細胞分析装置 |
| JP2007046947A (ja) * | 2005-08-08 | 2007-02-22 | Bay Bioscience Kk | フローサイトメータおよびフローサイトメトリ方法 |
| JP2008256712A (ja) * | 2008-06-12 | 2008-10-23 | Onchip Cellomics Consortium | 液滴分光システムと分光法 |
Cited By (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016038208A (ja) * | 2014-08-05 | 2016-03-22 | 株式会社島津製作所 | 光学的検出器 |
| CN105936930A (zh) * | 2015-03-04 | 2016-09-14 | 松下知识产权经营株式会社 | Dna检测方法和dna检测装置 |
| JP2016165276A (ja) * | 2015-03-04 | 2016-09-15 | パナソニックIpマネジメント株式会社 | Dna検出方法、およびdna検出装置 |
| US9523123B2 (en) | 2015-03-04 | 2016-12-20 | Panasonic Intellectual Property Management Co., Ltd. | DNA detection method and DNA detection device |
| JP2016168043A (ja) * | 2015-03-10 | 2016-09-23 | パナソニックIpマネジメント株式会社 | 複数の核酸ターゲットの解析方法 |
| US9528149B2 (en) | 2015-03-10 | 2016-12-27 | Panasonic Intellectual Property Management Co., Ltd. | Method for analyzing multiple nucleic acid targets |
| WO2017187490A1 (ja) * | 2016-04-26 | 2017-11-02 | 株式会社日立ハイテクノロジーズ | 分析装置 |
| JP2022063291A (ja) * | 2018-06-22 | 2022-04-21 | 株式会社日立ハイテク | 電気泳動装置 |
| JP7228060B2 (ja) | 2018-06-22 | 2023-02-22 | 株式会社日立ハイテク | 電気泳動装置 |
| US12092607B2 (en) | 2018-06-22 | 2024-09-17 | Hitachi High-Tech Corporation | Electrophoresis apparatus |
| US11733205B2 (en) | 2018-06-22 | 2023-08-22 | Hitachi High-Tech Corporation | Electrophoresis apparatus |
| WO2019244358A1 (ja) * | 2018-06-22 | 2019-12-26 | 株式会社日立ハイテクノロジーズ | 電気泳動装置 |
| JPWO2019244358A1 (ja) * | 2018-06-22 | 2021-07-01 | 株式会社日立ハイテク | 電気泳動装置 |
| JP7023358B2 (ja) | 2018-06-22 | 2022-02-21 | 株式会社日立ハイテク | 電気泳動装置 |
| WO2020008972A1 (ja) * | 2018-07-06 | 2020-01-09 | 日本板硝子株式会社 | 反応処理装置 |
| JP2020008405A (ja) * | 2018-07-06 | 2020-01-16 | 日本板硝子株式会社 | 反応処理装置 |
| US12222289B2 (en) | 2018-07-06 | 2025-02-11 | Go!Foton, Inc. | Reaction processor |
| JP2022545093A (ja) * | 2019-08-23 | 2022-10-25 | ミダイアグノスティクス・エヌブイ | リアルタイムpcr検出のためのマルチカラーシステム |
| KR102278427B1 (ko) | 2019-11-21 | 2021-07-16 | 주식회사 바이오티엔에스 | 형광 검출 장치 및 이를 이용한 형광 검출 방법 |
| KR20210062596A (ko) * | 2019-11-21 | 2021-05-31 | 주식회사 바이오티엔에스 | 형광 검출 장치 및 이를 이용한 형광 검출 방법 |
| JP7233385B2 (ja) | 2020-01-20 | 2023-03-06 | 日本板硝子株式会社 | 反応処理装置 |
| JP2020073912A (ja) * | 2020-01-20 | 2020-05-14 | 日本板硝子株式会社 | 反応処理装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20120194805A1 (en) | 2012-08-02 |
| WO2011120006A8 (en) | 2011-12-15 |
| CA2767113A1 (en) | 2011-09-29 |
| US8730479B2 (en) | 2014-05-20 |
| EP2550351A1 (en) | 2013-01-30 |
| WO2011120006A1 (en) | 2011-09-29 |
| EP2550351A4 (en) | 2014-07-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2013524169A (ja) | 液滴によるアッセイ用の検出システム | |
| US9029800B2 (en) | Compact analyzer with spatial modulation and multiple intensity modulated excitation sources | |
| US10371621B2 (en) | Assemblies and methods for reducing optical crosstalk in particle processing systems | |
| KR100647317B1 (ko) | 다채널 형광 측정용 광학계 및 이를 채용한 다채널 형광시료 분석 장치 | |
| JP6501714B2 (ja) | 光学調査装置 | |
| US20070098594A1 (en) | Analytical multi-spectral optical detection system | |
| US20240027325A1 (en) | Method and apparatus for flow-based, single-particle and/or single-molecule analysis | |
| US11828697B2 (en) | Multichannel excitation and emission for miniaturized, planar fluorescence activated cell sorting | |
| JP2013033008A (ja) | 光学分析装置及び光学分析方法 | |
| CN103221806A (zh) | 使用两个以上的波长带的光的测量的光学分析方法 | |
| CN110226082B (zh) | 具有多个强度峰值设计的流式细胞仪 | |
| US10137479B2 (en) | Temporal multiplexed excitation for miniaturized, planar fluorescence activated cell sorting | |
| US12449360B2 (en) | Apparatus and method for fluorescence excitation and detection | |
| KR102719550B1 (ko) | 1차원 광센서를 이용한 다중 웰 pcr 형광 측정 장치 | |
| WO2013021984A1 (ja) | 共焦点顕微鏡又は多光子顕微鏡の光学系を用いた光分析装置及び光分析方法 | |
| WO2015189298A1 (en) | An optical system for detecting fluorescent or luminescent signals of at least two samples | |
| JP2005321347A (ja) | 光検出装置 | |
| US9110023B2 (en) | Optical system | |
| JP2010117287A (ja) | 蛍光偏光検出装置 | |
| EP3317643B1 (en) | Modulation of luminescent dyes | |
| KR20210083489A (ko) | 현장형 분자진단 장치 및 기기에 사용 가능한 소형이며 저가의 형광 광학 장치 | |
| HK1125695A (zh) | 分析多光谱光学探测系统 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140325 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140325 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20141225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150126 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150713 |