DE10349033A1 - Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter - Google Patents
Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter Download PDFInfo
- Publication number
- DE10349033A1 DE10349033A1 DE10349033A DE10349033A DE10349033A1 DE 10349033 A1 DE10349033 A1 DE 10349033A1 DE 10349033 A DE10349033 A DE 10349033A DE 10349033 A DE10349033 A DE 10349033A DE 10349033 A1 DE10349033 A1 DE 10349033A1
- Authority
- DE
- Germany
- Prior art keywords
- mixtures
- conjugated
- polymer
- polymers
- triplet
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L65/00—Compositions of macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain; Compositions of derivatives of such polymers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/655—Aromatic compounds comprising a hetero atom comprising only sulfur as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Die vorliegende Erfindung betrifft Mischungen und Polymere, die Struktureinheiten der Formel (1) bis (5) enthalten und außerdem Struktureinheiten, die aus dem Triplett-Zustand Licht emittieren. Die erfindungsgemäßen Materialien sind besser löslich und leichter chemisch zugänglich und sind daher für den Einsatz in organischen Leuchtdioden besser geeignet als Vergleichsmaterialien gemäß dem Stand der Technik.The present invention relates to mixtures and polymers containing structural units of the formulas (1) to (5) and also to structural units which emit light from the triplet state. The materials according to the invention are more soluble and more readily chemically accessible and are therefore more suitable for use in organic light-emitting diodes than comparative materials according to the prior art.
Description
Die vorliegende Erfindung beschreibt neue Materialien und Materialmischungen für die Verwendung in organischen elektronischen Bauteilen, wie Elektrolumineszenzelementen, und deren Verwendung in darauf basierenden Displays.The The present invention describes new materials and material blends for the Use in organic electronic components, such as electroluminescent elements, and their use in displays based thereon.
Seit
ca. 12 Jahren läuft
eine breit angelegte Forschung zur Kommerzialisierung von Anzeige-
und Beleuchtungselementen auf Basis polymerer (organischer) Leuchtdioden
(PLEDs). Ausgelöst
wurde diese Entwicklung durch die Grundlagenentwicklungen, welche
in
Eine Entwicklung, die sich seit einigen Jahren vor allem auf dem Gebiet der „Small molecule"-Displays abzeichnet, ist der Einsatz von Materialien, die aus dem Triplett-Zustand Licht emittieren können und die somit Phosphoreszenz statt Fluoreszenz zeigen (M. A. Baldo, S. Lamansky, P. E. Burrows, M. E. Thompson, S. R. Forrest, Appl. Phys. Lett. 1999, 75, 4–6). Diese Verbindungen werden im Folgenden als „Triplett-Emitter" bezeichnet.A Development, which for some years mainly in the field the "Small molecule "displays appear, is the use of materials that emit light from the triplet state can and thus show phosphorescence instead of fluorescence (M.A. Baldo, S. Lamansky, P.E. Burrows, M.E. Thompson, S.R. Forrest, Appl. Phys. Lett. 1999, 75, 4-6). These compounds are referred to below as "triplet emitters".
Aus theoretischen Überlegungen ist unter Verwendung solcher Triplett-Emitter eine bis zu vierfache Energie- und Leistungseffizienz möglich. Ob sich diese Entwicklung allerdings durchsetzen wird, hängt stark davon ab, ob entsprechende Device-Kompositionen gefunden werden können, die diese Vorteile auch in OLEDs umsetzen können. Als wesentliche Bedingungen für die praktische Anwendbarkeit sind hier insbesondere effizienter Energieübertrag auf den Triplett-Emitter (und damit verbunden effiziente Lichtemission), eine hohe operative Lebensdauer und eine niedrige Einsatz- und Betriebsspannung, um mobile Applikationen zu ermöglichen, zu nennen.Out theoretical considerations using such triplet emitters, up to four times the energy and power efficiency possible. However, whether this development will prevail depends heavily on it from, if appropriate device compositions can be found which can also implement these advantages in OLEDs. As essential conditions for the Practical applicability here is especially efficient energy transfer to the triplet emitter (and associated efficient light emission), a high operating life and low operating and operating voltage, to enable mobile applications to call.
Um
dies zu erreichen, sind außer
den Eigenschaften des Triplett-Emitters selbst auch die Eigenschaften
des Matrixmaterials von herausragender Bedeutung. Während hierfür lange
Zeit vor allem Materialien, basierend auf Carbazolverbindungen,
in Betracht gezogen wurden und erste gute Ergebnisse zeigten, wurden vor
kurzem mit neuen Matrixmaterialien, basierend auf Keto- und Iminverbindungen
(vgl.
In letzter Zeit gibt es zunehmend Bemühungen, sich die oben genannten Vorteile aufdampfbarer Triplett-Emitter auch für Polymeranwendungen zu Nutze zu machen. So werden so genannte Hybrid-Device-Strukturen erwogen, die die Vorteile der "Small-molecule"-OLEDs mit denen der Polymer-OLEDs (= PLEDs) verbinden und durch Mischen des Triplett-Emitters in das Polymer entstehen. Andererseits kann der Triplett-Emitter selber auch kovalent an das Polymer gebunden werden. Beide Methoden haben den Vorteil, dass die Verbindungen aus Lösung verarbeitet werden können und dass kein teurer und aufwändiger Aufdampfprozess wie für Devices auf Basis niedermolekularer Verbindungen erforderlich ist. Das Aufbringen aus Lösung (z. B. mit Hilfe hochauflösender Druckverfahren) wird langfristig deutliche Vorteile gegenüber dem heute gängigen Vakuum-Verdampfungsprozess aufweisen, v. a. hinsichtlich Skalierbarkeit, Strukturierbarkeit, Beschichtungseffizienz und Ökonomie. Auch hier ist ein geeignetes Matrix-Material notwendig, das einen effizienten Energietransfer auf den Triplett-Emitter ermöglicht und das in Verbindung mit diesem gute Lebensdauern bei niedrigen Betriebsspannungen aufweist.In Recently, there are increasing efforts to become the above Benefits of evaporable triplet emitter also for polymer applications to use close. Thus, so-called hybrid device structures are considered the benefits of the "small-molecule" OLEDs with those connect the polymer OLEDs (= PLEDs) and by mixing the triplet emitter arise in the polymer. On the other hand, the triplet emitter itself also covalently bound to the polymer. Both methods have the advantage that the connections can be processed from solution and that no more expensive and elaborate Vapor deposition process as for Devices based on low molecular weight compounds is required. The application from solution (eg with the help of high-resolution Printing process) will have significant long-term advantages over the today common Have vacuum evaporation process, v. a. in terms of scalability, Structurability, coating efficiency and economy. Again, here is one suitable matrix material necessary for an efficient energy transfer allows for the triplet emitter and that in conjunction with this good life at low Operating voltages.
In
der nicht offen gelegten Anmeldeschrift
Trotz der in den o. g. Publikationen und Anmeldeschriften zitierten Fortschritte gibt es also immer noch erhebliches Verbessungspotential für entsprechende Materialien auf dem Gebiet der aus Lösung verarbeitbaren Triplett-Emitter. U. a. auf folgenden Feldern ist weiterhin ein deutlicher Verbesserungsbedarf zu sehen:
- (1) Die Löslichkeit der Polymere und Blends mit den oben beschriebenen überbrückten Carbazol-Einheiten, die den nächst liegenden Stand der Technik darstellen, ist noch nicht immer zufriedenstellend. So ist es beispielsweise nicht möglich, einen hohen Anteil der dort beschriebenen überbrückten Carbazol-Einheiten einzupolymerisieren, da dies zu unlöslichen Polymeren führt. Für die Anwendung ist es jedoch notwendig, lösliche Polymere zur Verfügung zu haben.
- (2) Die oben beschriebenen überbrückten Carbazol-Einheiten zeigen zwar in der Anwendung schon recht gute Ergebnisse. Ein weiterer Nachteil dieser Einheiten, außer der eingeschränkten Löslichkeit, ist jedoch der teilweise sehr aufwändige chemische Zugang zu diesen Verbindungen. Hier wäre es wünschenswert, Verbindungen und Monomere zur Verfügung zu haben, deren Device-Eigenschaften vergleichbar oder besser sind, die aber leichter bzw. in weniger Schritten chemisch zugänglich sind.
- (3) Die Polymere und Mischungen gemäß Stand der Technik zeigen eine hohe Sauerstoffempfindlichkeit. So lassen sich diese nur unter sorgfältigem Ausschluss von Sauerstoff verarbeiten. Hier wären weniger empfindliche Substanzen deutlich von Vorteil.
- (1) The solubility of the polymers and blends with the above-described bridged carbazole units, which are the closest prior art, is still not always satisfactory. Thus, for example, it is not possible to copolymerize a high proportion of the bridged carbazole units described therein, since this leads to insoluble polymers. For the application, however, it is necessary to have soluble polymers available.
- (2) Although the bridged carbazole units described above show quite good results in the application. Another disadvantage of these units, apart from the limited solubility, however, is the sometimes very complicated chemical access to these compounds. Here it would be desirable to have available compounds and monomers whose device properties are comparable or better, but which are chemically accessible more easily or in fewer steps.
- (3) The polymers and blends of the prior art show high oxygen sensitivity. Thus, they can only be processed with careful exclusion of oxygen. Here, less sensitive substances would be clearly beneficial.
Es ist also offensichtlich, dass hier weiterhin großer Verbesserungsbedarf besteht.It It is therefore obvious that there is still a great need for improvement here.
Überraschend wurde gefunden, dass – bisher unbekannte – Polymere und Mischungen, die bestimmte Struktureinheiten enthalten, in Kombination mit Triplett-Emittern deutliche Verbesserungen bei diesen Problemen im Vergleich zu Mischungen oder Polymeren gemäß Stand der Technik ergeben. Die Device-Eigenschaften bleiben dabei vergleichbar gut. Diese Polymere und Mischungen sind durch Standardreaktionen leichter chemisch zugänglich oder teilweise sogar kommerziell erhältlich und führen im Allgemeinen auch bei hohem Anteil immer noch zu gut löslichen Polymeren. Außerdem zeigen sie eine geringere Sauerstoffempfindlichkeit, was ihre Herstellung und Verarbeitung deutlich erleichtert. Sie sind daher Gegenstand der vorliegenden Anmeldung.Surprised was found that - so far unknown - polymers and mixtures containing certain structural units in combination with triplet emitters significant improvements in these problems compared to blends or polymers according to the state of technology. The device properties stay comparably good. These polymers and mixtures are more readily chemically accessible or even partially accessible by standard reactions commercially available and lead generally still too soluble even at high levels Polymers. Furthermore show a lower sensitivity to oxygen, what their production and processing significantly easier. They are therefore subject of the present application.
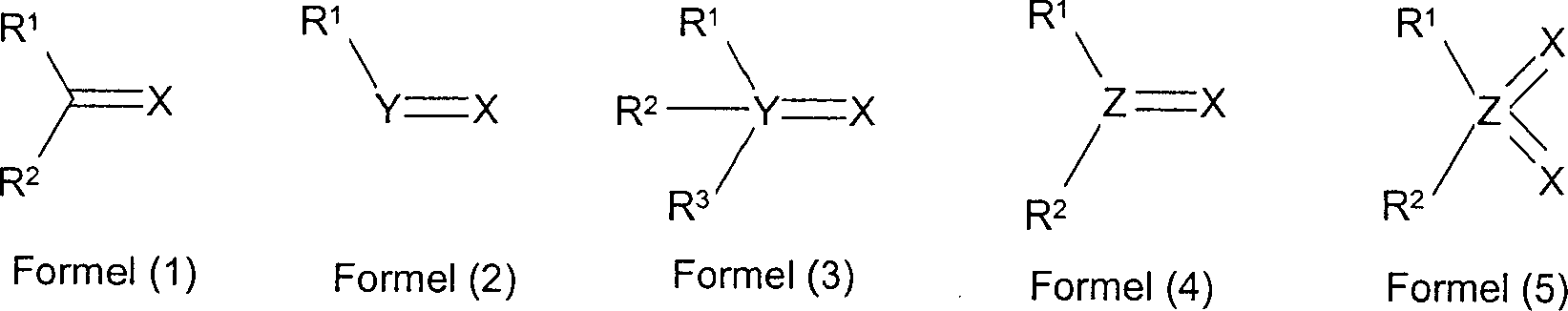
Gegenstand der Erfindung sind Mischungen (Blends), enthaltend
- (A) mindestens ein Polymer,
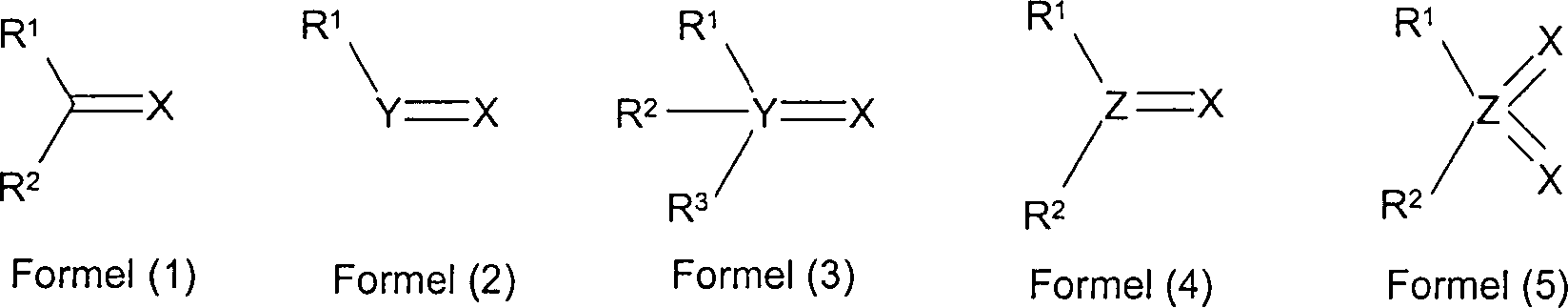
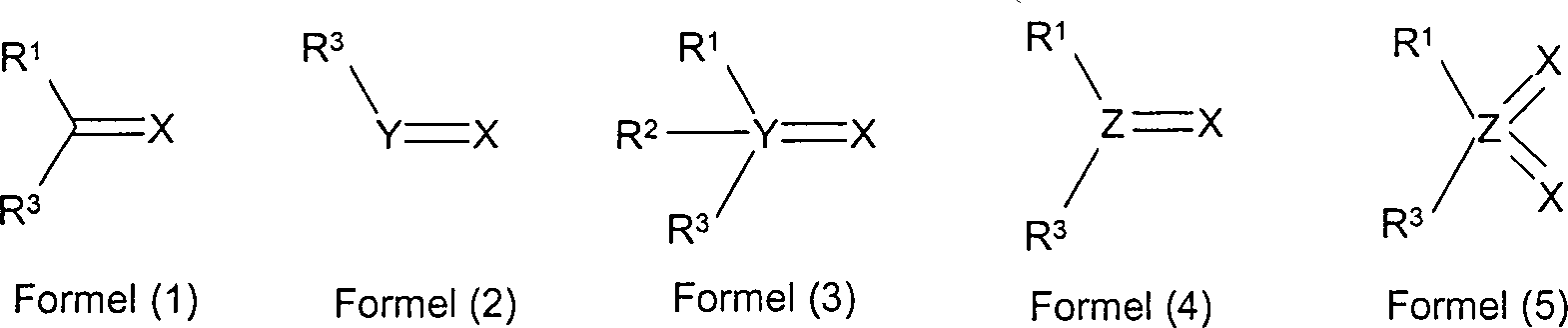
- (B) mindestens eine Struktureinheit, ausgewählt aus den Formeln (1) bis (5), wobei die verwendeten Symbole folgende Bedeutung haben: X steht für O, S, Se oder N-R4, mit der Maßgabe, dass X für Formel (4) und Formel (5) nicht S oder Se sein darf; Y steht für P, As, Sb oder Bi; Z steht für S, Se oder Te; R1, R2, R3 ist bei jedem Auftreten gleich oder verschieden H, F, CN, N(R4)2, eine geradkettige, verzweigte oder cyclische Alkyl-, Alkoxy- oder Thioalkoxygruppe mit 1 bis 40 C-Atomen, die mit R5 substituiert oder auch unsubstituiert sein kann, wobei ein oder mehrere nicht benachbarte CH2-Gruppen durch -R6C=CR6-, -C≡C-, Si(R6)2, Ge(R6)2, Sn(R6)2, C=O, C=S, C=Se, C=NR6, -O-, -S-, -NR6- oder -CONR6- ersetzt sein können und wobei ein oder mehrere H-Atome durch F, Cl, Br, I, CN oder NO2 ersetzt sein können, oder eine Aryl-, Aryloxy- oder Heteroarylgruppe mit 1 bis 40 C-Atomen, die durch ein oder mehrere Reste R5 substituiert sein können, wobei mehrere Substituenten R1, R2 und/oder R3 miteinander ein mono- oder polycyclisches, aliphatisches oder aromatisches Ringsystem bilden können; dabei dürfen nicht alle Substituenten R1 bis R3 an einer Struktureinheit H oder F sein; R4 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch -R6C=CR6-, -C≡C-, Si(R6)2, Ge(R6)2, Sn(R6)2, -NR6-, -O-, -S-, -CO-O-, -O-CO-O- ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl-, Heteroaryl- oder Aryloxygruppe mit 1 bis 40 C-Atomen, welche auch durch ein oder mehrere Reste R6 substituiert sein können oder OH oder N(R5)2; R5 ist bei jedem Auftreten gleich oder verschieden R4 oder CN, B(R6)2 oder Si(R6)3. R6 ist bei jedem Auftreten gleich oder verschieden H oder ein aliphatischer oder aromatischer Kohlenwasserstoffrest mit 1 bis 20 C-Atomen; und außerdem
- (C) mindestens einen Triplett-Emitter.
- (A) at least one polymer,
- (B) at least one structural unit selected from the formulas (1) to (5), wherein the symbols used have the following meaning: X is O, S, Se or NR 4 , with the proviso that X for formula (4) and formula (5) may not be S or Se; Y stands for P, As, Sb or Bi; Z stands for S, Se or Te; R 1 , R 2 , R 3 are each the same or different at each occurrence, H, F, CN, N (R 4 ) 2 , a straight, branched or cyclic alkyl, alkoxy or thioalkoxy group having 1 to 40 carbon atoms, which R 5 may be substituted or unsubstituted, where one or more non-adjacent CH 2 groups is replaced by -R 6 C = CR 6 -, -C≡C-, Si (R 6 ) 2 , Ge (R 6 ) 2 , Sn (R 6 ) 2 , C = O, C = S, C = Se, C = NR 6 , -O-, -S-, -NR 6 - or -CONR 6 - may be replaced and wherein one or more H Atoms can be replaced by F, Cl, Br, I, CN or NO 2 , or an aryl, aryloxy or heteroaryl group having 1 to 40 C atoms, which may be substituted by one or more R 5 radicals, where several Substituents R 1 , R 2 and / or R 3 may together form a mono- or polycyclic, aliphatic or aromatic ring system; not all substituents R 1 to R 3 on a structural unit may be H or F; R 4 is the same or different at each occurrence as a straight-chain, branched or cyclic alkyl or alkoxy chain having 1 to 22 C atoms, in which also one or more non-adjacent C atoms is replaced by -R 6 C = CR 6 -, -C ≡C-, Si (R 6 ) 2 , Ge (R 6 ) 2 , Sn (R 6 ) 2 , -NR 6 -, -O-, -S-, -CO-O-, -O-CO-O - may be replaced, wherein also one or more H atoms may be replaced by fluorine, an aryl, heteroaryl or aryloxy group having 1 to 40 carbon atoms, which may also be substituted by one or more radicals R 6 or OH or N (R 5 ) 2 ; R 5 is the same or different at each occurrence as R 4 or CN, B (R 6 ) 2 or Si (R 6 ) 3 . R 6 is the same or different at each occurrence, H or an aliphatic or aromatic hydrocarbon radical having 1 to 20 carbon atoms; and also
- (C) at least one triplet emitter.
Das oben und im Folgenden verwendete Symbol „=" steht für eine Doppelbindung im Sinne der Lewis-Schreibweise von Zwei-Elektronen-Zwei-Zentren-Bindungen.The The symbol "=" used above and below denotes a double bond in the sense the Lewis notation of two-electron two-center bonds.
Die erfindungsgemäßen Mischungen liegen vorzugsweise als amorphe Mischungen vor.The mixtures according to the invention are preferably present as amorphous mixtures.
In
WO 03/046108 werden Polymere beschrieben, die 9-Oxo-9-phosphafluoren-Bausteine in Kombination
mit Arylen-Bausteinen enthalten. In der nicht offen gelegten Anmeldung
Unter einem Triplett-Emitter im Sinne der Erfindung soll eine Verbindung verstanden werden, die aus dem Triplett-Zustand Licht emittiert, also in der Elektrolumineszenz Phosphoreszenz statt Fluoreszenz zeigt, bevorzugt ein metallorganischer Triplett-Emitter. Diese Verbindung kann prinzipiell niedermolekular, oligomer, dendrimer oder polymer sein. Dies sind vor allem Verbindungen, welche Schweratome, d. h. Atome aus dem Periodensystem der Elemente mit einer Ordnungszahl von mehr als 36, enthalten. Besonders geeignet sind hierfür Verbindungen, welche d- und f-Übergangsmetalle enthalten, die die o. g. Bedingung erfüllen. Ganz besonders geeignet sind hier entsprechende Struktureinheiten, welche Elemente der Gruppe 8 bis 10 (d. h. Ru, Os, Rh, Ir, Pd, Pt) enthalten. Ohne an eine spezielle Theorie gebunden sein zu wollen, werden im Sinne dieser Anmeldung alle emittierenden Verbindungen, die diese Elemente der Gruppe 8 bis 10 enthalten, als Triplett-Emitter bezeichnet.Under a triplet emitter in the context of the invention is intended to be a compound which emits light from the triplet state, So in electroluminescence phosphorescence instead of fluorescence shows, preferably an organometallic triplet emitter. This connection can in principle be low molecular weight, oligomer, dendrimer or polymer. these are especially compounds which are heavy atoms, d. H. Atoms from the periodic table of elements with an atomic number greater than 36. Particularly suitable for this purpose Compounds which are d and f transition metals contain the o. g. Fulfill condition. Especially suitable here are corresponding structural units, which elements of the group 8 to 10 (i.e., Ru, Os, Rh, Ir, Pd, Pt). Without one To be bound to special theory, in the sense of this application all emitting compounds containing these elements of group 8 to contain 10, as a triplet emitter designated.
Bei den erfindungsgemäßen Mischungen, die alle mindestens ein Polymer enthalten, gibt es nun verschiedene Ausführungsformen, bei denen die Einheiten gemäß Formel (1) bis (5) und/oder der Triplett-Emitter entweder eingemischt oder kovalent an das Polymer gebunden sind.at the mixtures according to the invention, all contain at least one polymer, there are now different Embodiments, where the units according to formula (1) to (5) and / or the triplet emitter either mixed or covalently bonded to the polymer.
Eine Ausführungsform der Erfindung sind Mischungen BLEND1, enthaltend
- (A) 5–99,5 Gew.% mindestens eines Polymers POLY1; POLY1 enthält 1–100 mol%, bevorzugt 5–80 mol%, besonders bevorzugt 10–50 mol% einer oder mehrerer Wiederholeinheiten MONO1, wobei MONO1 mindestens eine Struktureinheit gemäß Formel (1) bis (5) enthält, und außerdem
- (B) 0,5–95 Gew.%, bevorzugt 0,5–80 Gew.%, besonders bevorzugt 1–50 Gew.%, insbesondere 2–25 Gew.% eines oder mehrerer Triplett-Emitter (TRIP1).
- (A) 5-99.5% by weight of at least one polymer POLY1; POLY1 contains 1-100 mol%, preferably 5-80 mol%, particularly preferably 10-50 mol% of one or more repeat units MONO1, wherein MONO1 contains at least one structural unit of the formula (1) to (5), and also
- (B) 0.5-95% by weight, preferably 0.5-80% by weight, particularly preferably 1-50% by weight, in particular 2-25% by weight of one or more triplet emitters (TRIP1).
Auch wenn dies aus der Beschreibung hervorgeht, sei hier ausdrücklich darauf hingewiesen, dass die Wiederholeinheit MONO1, die Struktureinheiten gemäß Formel (1) bis (5) enthält, auch mehr als eine dieser Einheiten enthalten kann.Also if this is clear from the description, it is explicitly stated here noted that the repeating unit MONO1, the structural units according to formula (1) to (5) contains can also contain more than one of these units.
In der Ausführungsform BLEND1 ist der Triplett-Emitter (TRIP1) nicht-kovalent zu dem Polymer POLY1 gemischt. Die Wiederholeinheiten MONO1, enthaltend Strukturelemente gemäß Formel (1) bis (5), sind kovalent an das Polymer gebunden. Dabei kann die Bindung prinzipiell an jeder beliebigen Position stattfinden, d. h. diese Einheiten können über eine oder mehrere Positionen an R1 bis R3 bzw. gegebenenfalls über R4, R5 oder R6 in Formel (1) bis (5) eingebaut werden. Je nach Verknüpfung sind diese Struktureinheiten dann in die Haupt- oder Seitenkette des Polymers eingebaut.In the embodiment BLEND1, the triplet emitter (TRIP1) is non-covalently mixed with the polymer POLY1. The repeating units MONO1 containing structural elements according to formulas (1) to (5) are covalently bonded to the polymer. In this case, the bond can in principle take place at any desired position, ie these units can be incorporated via one or more positions on R 1 to R 3 or optionally via R 4 , R 5 or R 6 in formula (1) to (5). Depending on the linkage, these structural units are then incorporated into the main or side chain of the polymer.
Eine weitere Ausführungsform der Erfindung sind Mischungen BLEND2, enthaltend
- (A) 0,5–99 Gew.% mindestens eines Polymers POLY2; POLY2 enthält 0,5–100 mol% eines oder mehrerer Triplett-Emitter (TRIP2) kovalent gebunden, und außerdem
- (B) 1–99,5 Gew.% mindestens einer Verbindung VERB1, die mindestens eine Struktureinheit gemäß Formel (1) bis (5) enthält und die in der Lage ist, bei Raumtemperatur glasartige Schichten zu bilden, bevorzugt mit einer Glastemperatur größer 70°C.
- (A) 0.5-99% by weight of at least one polymer POLY2; POLY2 contains 0.5-100 mol% of one or more triplet emitters (TRIP2) covalently bound, as well as
- (B) 1-99.5% by weight of at least one compound VERB1 which contains at least one structural unit of the formula (1) to (5) and which is capable of forming vitreous layers at room temperature, preferably with a glass transition temperature greater than 70 ° C.
Auch wenn das aus der Beschreibung für BLEND2 hervorgeht, sei hier ausdrücklich darauf hingewiesen, dass die Verbindung VERB1, die Struktureinheiten gemäß Formel (1) bis (5) enthält, auch mehr als eine dieser Einheiten enthalten kann.Also if that's from the description for BLEND2, it should be noted that that the compound VERB1, the structural units according to formula (1) to (5) contains can also contain more than one of these units.
Der Triplett-Emitter TRIP2 kann dabei in die Haupt- und/oder in die Seitenkette des Polymers POLY2 eingebaut werden.Of the Triplet Emitter TRIP2 can be in the main and / or in the Side chain of the polymer POLY2 be incorporated.
Ein weiterer Aspekt dieser Erfindung sind Mischungen BLEND3, enthaltend
- (A) 0,5–98,5 Gew.% mindestens eines Polymers POLY3;
- (B) 1–99 Gew.% mindestens einer Verbindung VERB1, die mindestens eine Struktureinheit der Formel (1) bis (5) enthält und in der Lage ist, bei Raumtemperatur glasartige Schichten zu bilden, bevorzugt mit einer Glastemperatur größer 70°C; und außerdem
- (C) 0,5–95 Gew.%, bevorzugt 0,5–80 Gew.%, besonders bevorzugt 1–50 Gew.%, insbesondere 2–25 Gew.% eines oder mehrerer Triplett-Emitter (TRIP1).
- (A) 0.5-98.5% by weight of at least one polymer POLY3;
- (B) 1-99% by weight of at least one compound VERB1 which contains at least one structural unit of the formula (1) to (5) and is capable of forming vitreous layers at room temperature, preferably with a glass transition temperature greater than 70 ° C .; and also
- (C) 0.5-95% by weight, preferably 0.5-80% by weight, more preferably 1-50% by weight, in particular 2-25% by weight, of one or more triplet emitters (TRIP1).
Ein weiterer Aspekt dieser Erfindung sind Mischungen BLEND4, enthaltend
- (A) 0,5–98,5 Gew.% mindestens eines Polymers POLY3; und außerdem
- (B) 1,5–99,5 Gew.% einer Verbindung TRIP3; TRIP3 enthält eine oder mehrere Struktureinheiten der Formel (1) bis (5) kovalent an einen oder mehrere Triplett-Emitter gebunden enthält, wobei mindestens eine Gruppe X frei, d. h. nicht an ein Metallatom koordiniert, vorliegen muss; dies schließt nicht aus, dass weitere Struktureinheiten der Formel (1) bis (5) vorhanden sein können, deren Atom X an ein Metallatom koordiniert ist (beispielsweise Acetylacetonat-Liganden).
- (A) 0.5-98.5% by weight of at least one polymer POLY3; and also
- (B) 1.5-99.5% by weight of a compound TRIP3; TRIP3 contains one or more structural units of the formula (1) to (5) covalently bonded to one or more triplet emitters, wherein at least one group X must be free, ie not coordinated to a metal atom; this does not exclude that further structural units of formula (1) to (5) may be present whose atom X is coordinated to a metal atom (for example acetylacetonate ligands).
Die Polymere (A) (POLY1 bis POLY3) können konjugiert, teilkonjugiert, gekreuzt-konjugiert oder nicht-konjugiert sein.The Polymers (A) (POLY1 to POLY3) can conjugated, partially conjugated, crossed-conjugated or non-conjugated.
Derartige konjugierte Polymere im Sinne dieser Erfindung sind Polymere, die in der Hauptkette hauptsächlich sp2-hybridisierte (bzw. teilweise auch sp-hybridisierte) Kohlenstoffatome enthalten, die auch durch entsprechende Heteroatome ersetzt sein können, und deren Einheiten miteinander in Konjugation stehen. Dies bedeutet im einfachsten Fall abwechselndes Vorliegen von Doppel- und Einfachbindungen in der Hauptkette. Hauptsächlich meint, dass natürlich (ohne weiteres Zutun) auftretende Defekte, die zu Konjugationsunterbrechungen führen, den Begriff "konjugiertes Polymer" nicht entwerten. Des Weiteren wird in diesem Anmeldetext ebenfalls als konjugiert bezeichnet, wenn sich in der Hauptkette Arylamineinheiten, Arylphosphineinheiten und/oder bestimmte Heterocyclen (d. h. Konjugation über N-, O-, S- oder P-Atome) und/oder metallorganische Komplexe, wie beispielsweise Einheiten gemäß TRIP2 (Konjugation über das Metallatom), befinden. Teilkonjugierten Polymere im Sinne dieser Erfindung sind Polymere, die entweder in der Hauptkette längere konjugierte Abschnitte enthalten, die durch nicht-konjugierte Abschnitte unterbrochen werden, oder die in den Seitenketten eines in der Hauptkette nicht-konjugierten Polymers längere konjugierte Abschnitte enthalten. Gekreuzt-konjugierte Polymere im Sinne dieser Erfindung sind Polymere, in denen zwei konjugierte Abschnitte nicht miteinander in Konjugation treten, jeder einzelne dieser Abschnitte aber mit einer dritten Einheit konjugiert ist. Dies ist beispielsweise der Fall, wenn zwei konjugierte Abschnitte direkt über eine Ketogruppe, eine Sulfoxidgruppe, eine Sulfongruppe oder eine Phosphinoxidgruppe verknüpft sind, aber beispielsweise auch bei geminaler Verknüpfung zweier konjugierter Abschnitte über eine substituierte oder unsubstituierte Alkengruppe oder bei Verknüpfung zweier konjugierter Abschnitte über beispielsweise eine meta-Phenylengruppe. Hingegen würden Einheiten, wie beispielsweise einfache (Thio)Etherbrücken, Esterverknüpfungen, Amid- oder Imidverknüpfungen eindeutig als nicht-konjugierte Segmente definiert.Such conjugated polymers in the context of this invention are polymers which contain in the main chain mainly sp 2 -hybridized (or in part also sp-hybridized) carbon atoms, which may also be replaced by corresponding heteroatoms, and whose units are in conjugation with one another. In the simplest case this means alternating presence of double and single bonds in the main chain. Mainly, of course, that of course (without further action) occurring defects that lead to conjugation interruptions, do not devalue the term "conjugated polymer". Furthermore, in this application text is also referred to as conjugated when in the main chain Arylamineinheiten, Arylphosphineinheiten and / or certain heterocycles (ie conjugation of N, O, S or P atoms) and / or organometallic complexes, such as units according to TRIP2 (conjugation via the metal atom). Partially conjugated polymers for the purposes of this invention are polymers which either contain longer conjugated portions in the main chain which are interrupted by non-conjugated portions or which contain longer conjugated portions in the side chains of a polymer which is not conjugated in the main chain. Cross-conjugated polymers in the sense of this invention are polymers in which two conjugated sections do not conjugate with each other, but each of these sections is conjugated to a third unit. This is the case, for example, when two conjugated segments are linked directly via a keto group, a sulfoxide group, a sulfone group or a phosphine oxide group, but also for example when two conjugated segments are geminally linked via a substituted or unsubstituted alkene group or when two conjugated segments are linked via, for example, one meta-phenylene group. By contrast, units such as simple (thio) ether bridges, ester linkages, amide or imide linkages are clearly defined as non-conjugated segments.
In einer bevorzugten Ausführungsform ist das Polymer konjugiert. In diesem Fall ist für POLY1 die Struktureinheit gemäß Formel (1) bis (5) in die Seitenkette gebunden. Wenn der Triplett-Emitter TRIP2 in POLY2 in die Hauptkette gebunden ist, erfolgt die Verknüpfung in der Weise, dass die Konjugation des Polymers entweder über den Liganden eines metallorganischen Triplett-Emitters oder über das Zentralatom eines metallorganischen Triplett-Emitters erhalten bleibt.In a preferred embodiment the polymer is conjugated. In this case, the structural unit is for POLY1 according to formula (1) to (5) bound in the side chain. When the triplet emitter TRIP2 is bound to the main chain in POLY2, the link is made in the way that the conjugation of the polymer either over the Ligands of an organometallic triplet emitter or over the Central atom of a metallocene triplet emitter is maintained.
In einer weiteren bevorzugten Ausführungsform ist das Polymer gekreuzt-konjugiert. Für Polymer POLY1 ist es dabei besonders bevorzugt, wenn die gekreuzt-konjugierten Abschnitte durch die Einheiten gemäß Formel (1) bis (5) gebildet werden.In a further preferred embodiment the polymer is crossed-conjugated. It is included for polymer POLY1 particularly preferred when the crossed-conjugated sections are through the units according to formula (1) to (5) are formed.
Die Polymere POLY1, POLY2 und POLY3 können außer den Einheiten MONO1 (in POLY1) und dem Triplett-Emitter TRIP2 (in POLY2) verschiedene weitere Strukturelemente enthalten. Bei konjugierten, teilkonjugierten oder gekreuzt-konjugierten Polymeren können die weiteren Struktureinheiten beispielsweise aus den im Folgenden beschriebenen Klassen stammen:
- 1. Struktureinheiten,
die das Polymergrundgerüst
bilden können:
Hier sind zunächst
Poly-Phenylene und davon abgeleitete Strukturen bildende Einheiten
zu nennen. Dies sind beispielsweise (jeweils substituierte oder
unsubstituierte) ortho-, meta- oder para-Phenylene, 1,4-Naphthylene,
9,10-Anthracenylene, 2,7-Phenanthrenylene,
2,7-(9,10-Dihydro)phenanthrenylene (
DE 10337346.2 DE 10143353 GB 0226010.7 EP 03014042.0 - 2. Struktureinheiten, die die Ladungsinjektions- bzw. Ladungstransporteigenschaften
beeinflussen. Dies kann sich sowohl auf die Elektroneninjektions-
oder -transporteigenschaften (wie beispielsweise Oxadiazol- oder
Triazineinheiten) wie auch auf die Lochinjektions- oder -transporteigenschaften
(wie beispielsweise Triarylamineinheiten) beziehen. Hier sei auf
die umfangreiche Auflistung derartiger Struktureinheiten in WO 02/077060
verwiesen. Ebenso kommen für
diesen Zweck die in den nicht offen gelegten Anmeldeschriften beschriebenen
Naphthylarylamine (
DE 10249723.0 DE 10304819.7 DE 10328627.6 EP 03018832.0
- 1. Structural units which can form the polymer backbone: Poly-phenylenes and structures derived therefrom must first be mentioned here. These are for example (in each case substituted or unsubstituted) ortho, meta or para-phenylenes, 1,4-naphthylenes, 9,10-anthracenylenes, 2,7-phenanthrenylenes, 2,7- (9,10-dihydro) -phenanthrenylenes (
DE 10337346.2 DE 10143353 GB 0226010.7 EP 03014042.0 - 2. Structural units that influence the charge injection or charge transport properties. This may relate to both electron injection or transport properties (such as oxadiazole or triazine units) as well as hole injection or transport properties (such as triarylamine units). Reference should be made here to the extensive listing of such structural units in WO 02/077060. Likewise, for this purpose the naphthylarylamines described in the unpublished application patents (
DE 10249723.0 DE 10304819.7 DE 10328627.6 EP 03018832.0
Eine weitere geeignete Verbindungsklasse für gekreuzt-konjugierte Polymere POLY1 sind aromatische Polyketone und aromatische Polysulfone, die jeweils zur besseren Löslichkeit noch substituiert sein können. Einen Überblick über diese Verbindungsklassen geben P. A. Staniland in „Comprehensive Polymer Science", Ed. G. Allen, Volume 5, Kapitel 29, 483–497 und F. Parodi, ibid., Kapitel 33, 561–591.A another suitable class of compounds for crossed-conjugated polymers POLY1 are aromatic polyketones and aromatic polysulfones which each for better solubility still be substituted. An overview of this Link classes give P.A. Staniland in "Comprehensive Polymer Science," Ed 5, chapter 29, 483-497 and F. Parodi, ibid., chapter 33, 561-591.
Wenn es sich bei den Polymeren POLY1, POLY2 oder POLY3 um nicht-konjugierte Polymere handelt, kommen hierfür prinzipiell beliebige Verbindungsklassen in Frage, sofern die Polymere ausreichend löslich sind in einem Lösungsmittel oder einem Lösungsmittelgemisch, in dem auch die anderen Blendbestandteile löslich sind, so dass alle Komponenten aus Lösung gemeinsam verarbeitet werden können. Beispiele für nicht-konjugierte Polymere, die hier verwendet werden können, sind beispielsweise Polystyrol, Polycarbonate, PMMA (Polymethylmethacrylat), Polyvinylbutyral, aber auch elektronisch aktive, nicht-konjugierte Polymere, wie beispielsweise PVK (Polyvinylcarbazol) oder Derivate davon.If the polymers POLY1, POLY2 or POLY3 are non-conjugated Polymers come, come for this In principle, any classes of compounds in question, provided that the polymers are sufficiently soluble in a solvent or a solvent mixture, in which the other blend components are soluble, so that all components out of solution can be processed together. Examples of non-conjugated Polymers which can be used here are, for example, polystyrene, Polycarbonates, PMMA (polymethyl methacrylate), polyvinyl butyral, but also electronically active, non-conjugated Polymers such as PVK (polyvinylcarbazole) or derivatives from that.
Die
Polymere POLY1, POLY2 und POLY3 sind entweder Homopolymere, d. h.
sie enthalten dann nur eine einzelne Monomerstruktur, oder es sind
Copolymere. Die Copolymere können
statistische, alternierende oder auch blockartige Strukturen aufweisen
oder auch mehrere dieser Strukturen abwechselnd besitzen. Wie konjugierte
Copolymere mit blockartigen Strukturen erhalten werden können, ist
beispielsweise ausführlich
beschrieben in der nicht offen gelegten Anmeldung
Die
Polymere POLY1, POLY2 und POLY3 werden durch Polymerisation von
einem oder mehreren Monomeren hergestellt. Insbesondere für die Synthese
konjugierter oder gekreuzt-konjugierter Polymere haben sich hier
einige Typen bewährt,
die zu C-C-Verknüpfungen
(SUZUKI-Kupplung, YAMAMOTO-Kupplung, STILLE-Kupplung) oder zu C-N-Verknüpfungen
(HARTWIG-BUCHWALD-Kupplung) führen.
Wie die Polymerisation nach diesen Methoden durchgeführt werden
kann und wie die Polymere dann vom Reaktionsmedium abgetrennt und
aufgereinigt werden können,
ist beispielsweise im Detail beschrieben in der nicht offen gelegten Anmeldeschrift
Nach diesen Methoden kann auch die Synthese teilkonjugierter oder nicht-konjugierter Polymere durchgeführt werden, indem entsprechende Monomere verwendet werden, die nicht durchgängig konjugiert sind. Für teilkonjugierte oder nicht-konjugierte Polymere kommen aber auch andere Synthesemethoden in Frage, wie sie allgemein aus der Polymerchemie geläufig sind, wie beispielsweise Polykondensationen, die z. B. zu Ester- oder Amidverknüpfungen führen, oder Polymerisationen, die beispielsweise über die Reaktion von Alkenen ablaufen und zu Polyethylen-Derivaten im weitesten Sinne führen, die dann die Chromophore in den Seitenketten gebunden enthalten.By these methods, the synthesis of partially conjugated or non-conjugated polymers can also be carried out by using appropriate monomers that are not consistently conjugated. For partially conjugated or non-conjugated polymers but other synthetic methods in question, as they are commonly known in polymer chemistry, such as polycondensations, the z. B. lead to ester or amide linkages, or polymerizations, for example, via the reaction of Alkenes run off and lead to polyethylene derivatives in the broadest sense, which then contain the chromophores bound in the side chains.
Für bevorzugte
Struktureinheiten gemäß Formel
(1) bis (5) gilt Folgendes:
X steht für O, S oder N-R4;
Y
steht für
P oder As;
Z steht für
S oder Se;
R1 bis R6 sind
wie oben definiert.For preferred structural units according to formulas (1) to (5), the following applies:
X is O, S or NR 4 ;
Y stands for P or As;
Z stands for S or Se;
R 1 to R 6 are as defined above.
Für besonders
bevorzugte Strukturen gemäß Formel
(1) bis (5) gilt Folgendes:
X steht für O oder N-R4;
Y
steht für
P;
Z steht für
S;
R1 bis R6 sind
wie oben definiert, wobei an jeder Struktureinheit gemäß Formel
(1) bis (5) mindestens einer der Substituenten R1 bis
R3 eine Aryl- oder Heteroarylgruppe mit
1 bis 40 C-Atomen darstellt, die mit einem oder mehreren Substituenten
R4 substituiert oder unsubstituiert sein
kann.For particularly preferred structures according to formulas (1) to (5), the following applies:
X is O or NR 4 ;
Y stands for P;
Z stands for S;
R 1 to R 6 are as defined above, wherein at each structural unit according to formula (1) to (5) at least one of the substituents R 1 to R 3 represents an aryl or heteroaryl group having 1 to 40 carbon atoms, with one or a plurality of substituents R 4 may be substituted or unsubstituted.
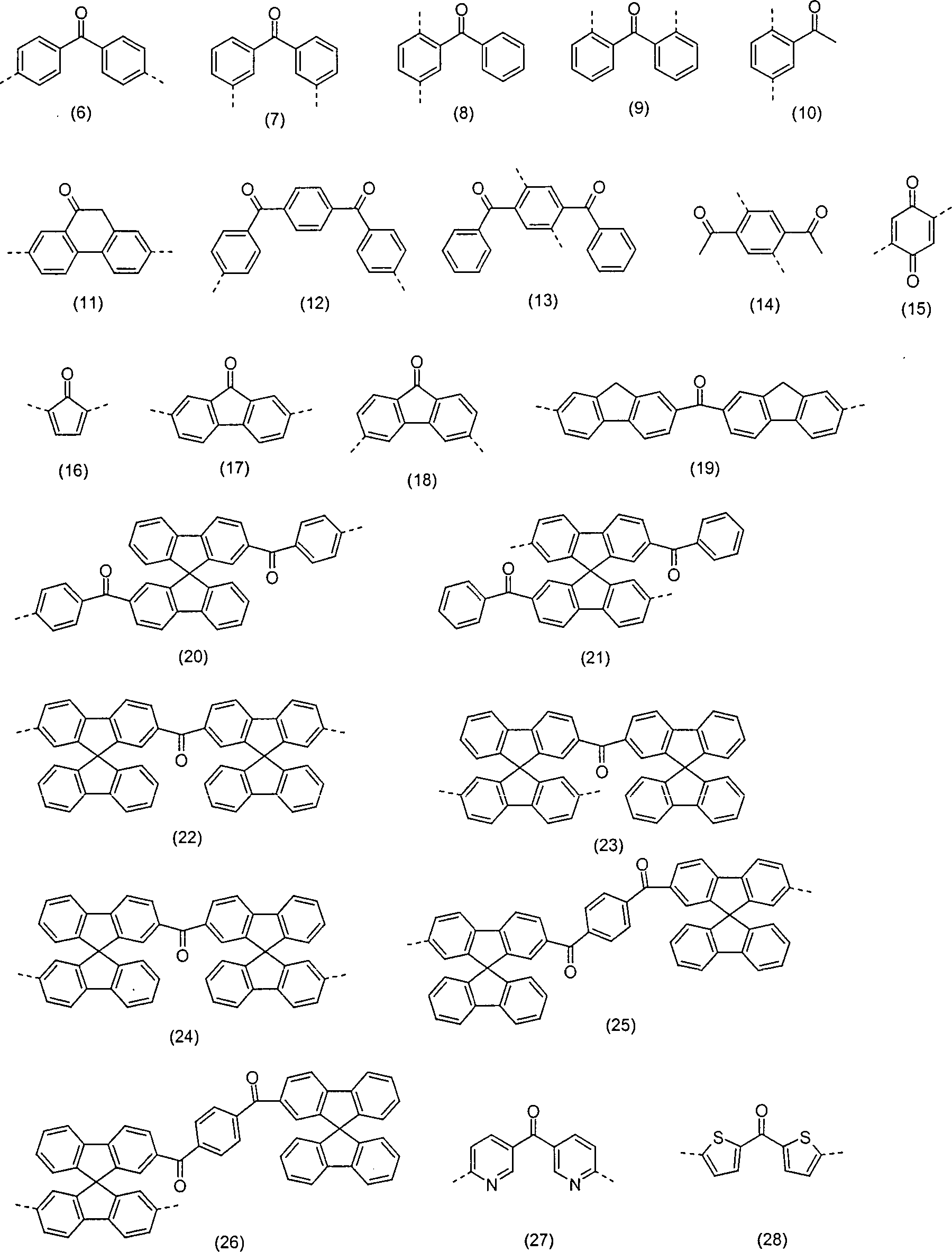
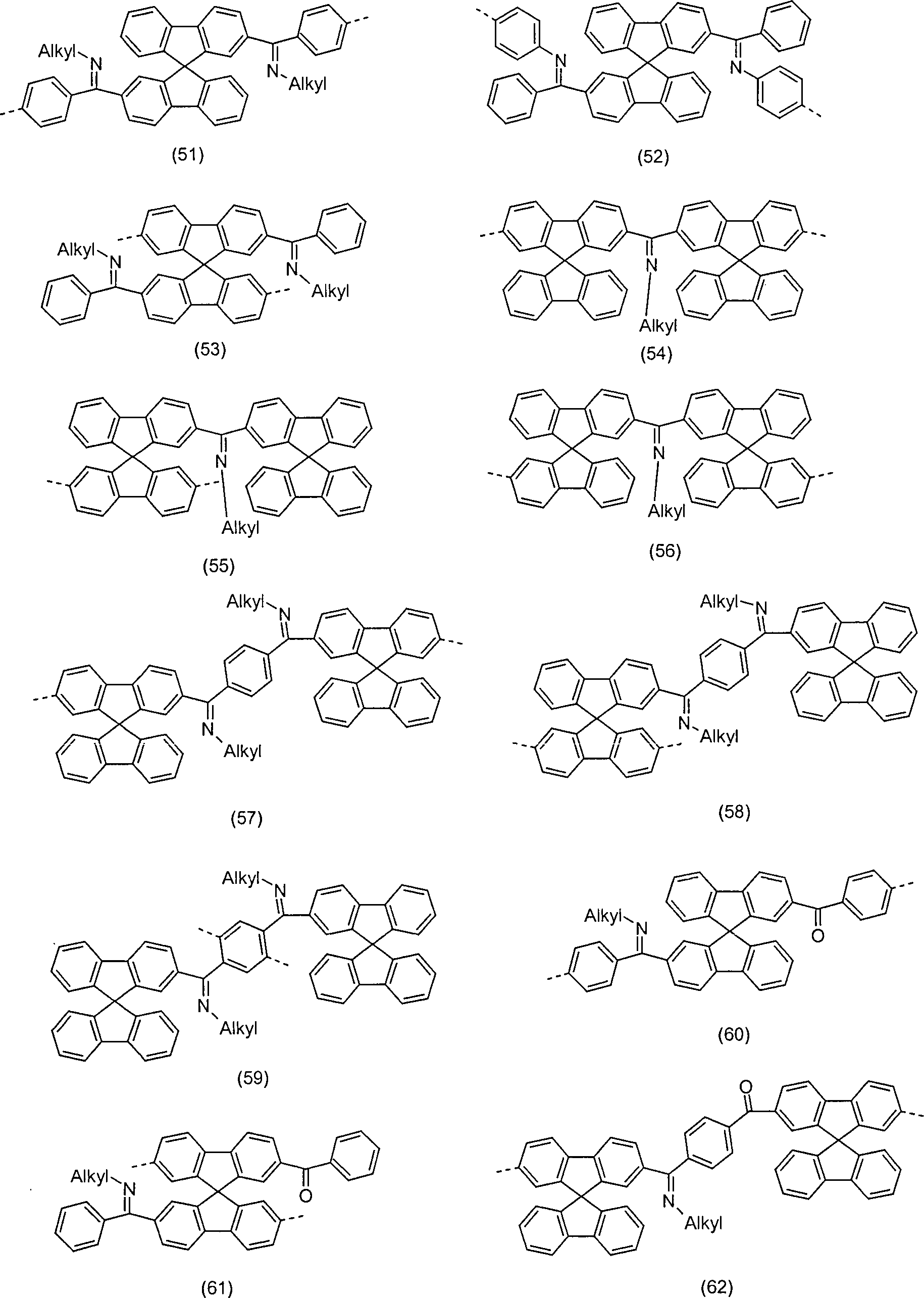
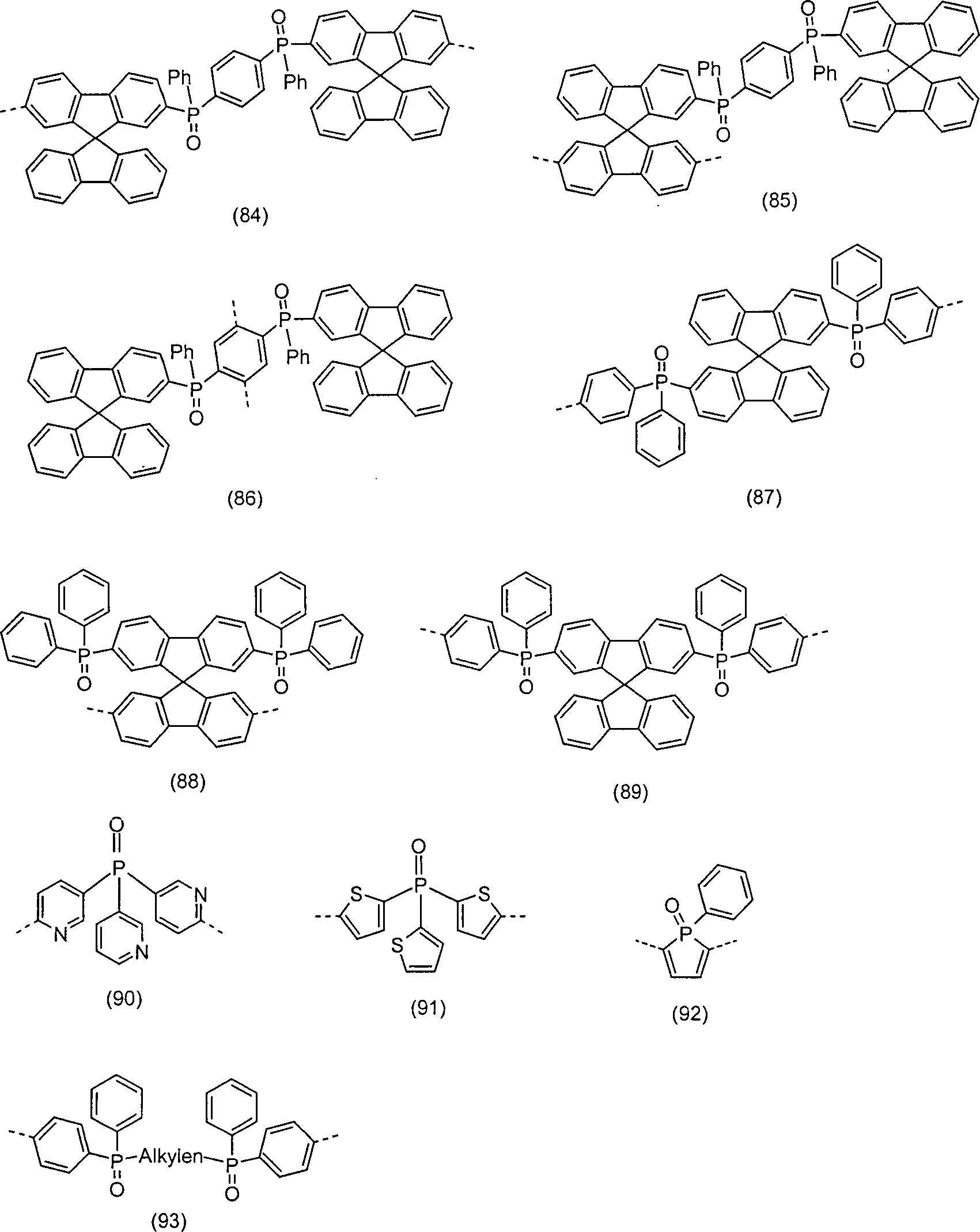
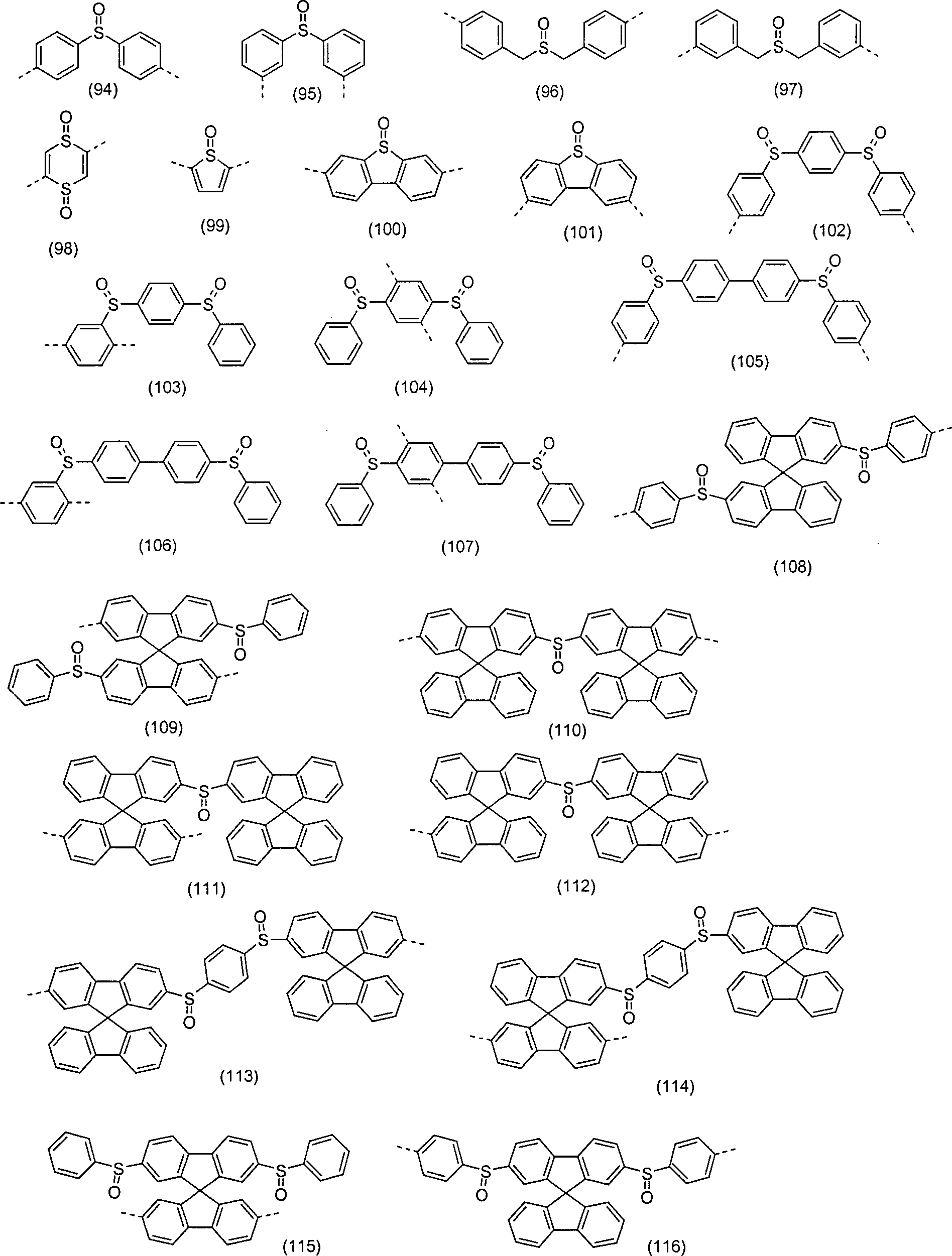
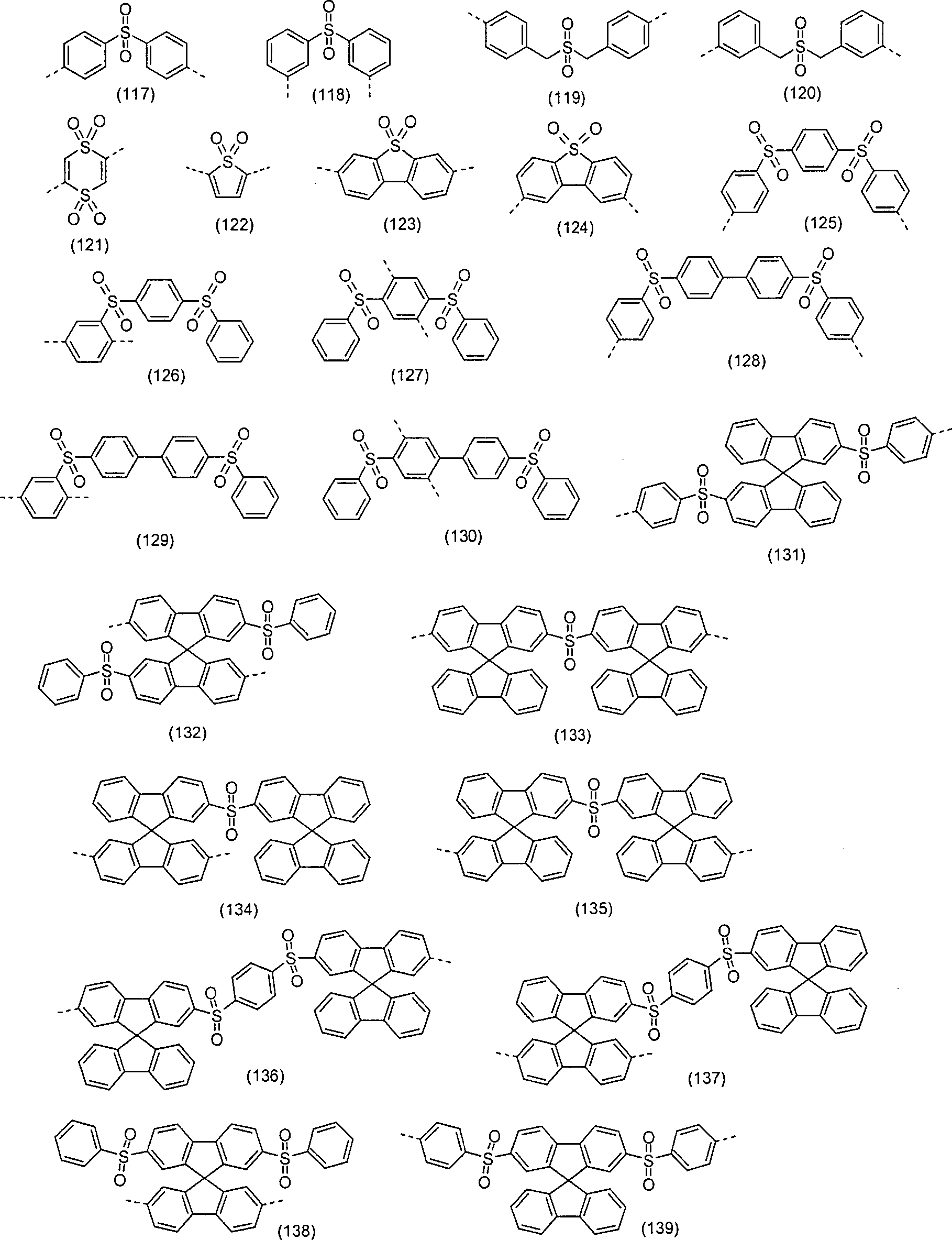
Beispiele für besonders bevorzugte Wiederholeinheiten MONO1 bzw. Verbindungen VERB1, die Struktureinheiten gemäß den Formeln (1) bis (5) enthalten, sind substituierte oder unsubstituierte Strukturen gemäß den abgebildeten Formeln (6) bis (139), wobei die gestrichelten Einfachbindungen eine mögliche Verknüpfung im Polymer (MONO1) oder Verknüpfungen zur Molekülverlängerung (VERB1) bedeuten; Ph steht für eine substituierte oder unsubstituierte Phenylgruppe und Alkyl für eine geradkettige, verzweigte oder cyclische Alkylkette, die substituiert oder unsubstituiert sein kann und in der ein oder mehrere H-Atome durch Fluor ersetzt sein können. Diese Strukturelemente gemäß Formeln (6) bis (139) sind auch bevorzugt Bestandteil der Verbindungen TRIP3, die eine Kombination aus Triplett-Emitter und Einheiten gemäß Formel (1) bis (5) darstellen. Potentielle Substituenten sind wegen der besseren Übersichtlichkeit in der Regel nicht abgebildet: Examples of particularly preferred repeat units MONO1 or compounds VERB1 which contain structural units according to the formulas (1) to (5) are substituted or unsubstituted structures according to the depicted formulas (6) to (139), where the dashed single bonds represent a possible linkage in the Polymer (MONO1) or molecular extension linkages (VERB1); Ph is a substituted or unsubstituted phenyl group and alkyl is a straight, branched or cyclic alkyl chain which may be substituted or unsubstituted and in which one or more H atoms may be replaced by fluorine. These structural elements according to formulas (6) to (139) are also preferably constituents of the compounds TRIP3 which represent a combination of triplet emitters and units of the formula (1) to (5). Potential substituents are usually not shown because of the better clarity:
Auch wenn dies aus der Beschreibung hervorgeht, sei hier nochmals explizit darauf verwiesen, dass die Struktureinheiten gemäß den Formeln (6) bis (139) auch unsymmetrisch substituiert sein können, d. h. dass an einer Einheit unterschiedliche Substituenten R4 vorhanden sein können, bzw. diese auch an unterschiedliche Positionen gebunden sein können.Although this is evident from the description, it should again be explicitly stated here that the structural units according to the formulas (6) to (139) can also be unsymmetrically substituted, ie that different substituents R 4 can be present on one unit, or these can also be tied to different positions.
Die Wiederholeinheiten MONO1 sind kovalenter Bestandteil von POLY1. Es hat sich gezeigt, dass ein Anteil im Bereich von 5–99 mol% dieser Wiederholeinheiten (bezogen auf alle Wiederholeinheiten im Polymer) hier gute Ergebnisse erzielt. Bevorzugt ist für POLY1 also ein Anteil von 5–99 mol% Wiederholeinheiten MONO1. Besonders bevorzugt ist ein Anteil von 10–80 mol% Wiederholeinheiten MONO1, ganz besonders bevorzugt ist ein Anteil von 10–50 mol% Wiederholeinheiten MONO1.The Repeat units MONO1 are a covalent constituent of POLY1. It has been found that a proportion in the range of 5-99 mol% of these repeat units (referring to all repeat units in Polymer) achieved good results here. Preferred is for POLY1 So a share of 5-99 mol% repetition units MONO1. Particularly preferred is a proportion from 10-80 mol% repeat units MONO1, very particularly preferred is a Share of 10-50 mol% repetition units MONO1.
Verbindungen VERB1 sind Mischungs-Bestandteil von BLEND2 und BLEND3. Es hat sich gezeigt, dass ein Anteil im Bereich von 5–99 Gew.% dieser Verbindungen hier gute Ergebnisse erzielt. Bevorzugt ist für BLEND2 und BLEND3 also ein Anteil von 5–99 Gew.% Verbindungen VERB1. Besonders bevorzugt ist ein Anteil von 10–80 Gew.% VERB1, ganz besonders bevorzugt ist ein Anteil von 10–50 Gew.% VERB1.VERB1 compounds are a blend component of BLEND2 and BLEND3. It has shown, that a proportion in the range of 5-99 wt.% Of these compounds gives good results here. For BLEND2 and BLEND3, therefore, a proportion of 5-99% by weight of compounds VERB1 is preferred. Particularly preferred is a proportion of 10-80 wt.% VERB1, most preferably a proportion of 10-50 wt.% VERB1.
Eine weitere bevorzugte Ausführungsform ist die Mischung BLEND5, die durch Einmischen von Verbindungen VERB1 in BLEND1 entsteht, so dass hier Struktureinheiten gemäß Formel (1) bis (5) sowohl kovalent an das Polymer gebunden als auch eingemischt vorliegen. Hier hat sich gezeigt, dass ein Gesamtanteil von 5–99 mol% Struktureinheiten gemäß dieser Formeln gute Ergebnisse erzielt, unabhängig davon, ob diese Einheiten kovalent an das Polymer gebunden sind oder eingemischt sind. Bevorzugt ist hier also ein Gesamtanteil von 5–99 mol% Struktureinheiten gemäß Formeln (1) bis (5). Besonders bevorzugt ist ein Gesamtanteil von 10–80 mol% Struktureinheiten gemäß Formeln (1) bis (5), ganz besonders bevorzugt ist ein Gesamtanteil von 10–50 mol% Struktureinheiten gemäß Formeln (1) bis (5).A further preferred embodiment is the blend BLEND5, which by mixing compounds VERB1 in BLEND1 arises, so that here structural units according to formula (1) to (5) both covalently bound to the polymer and mixed available. Here it has been shown that a total proportion of 5-99 mol% Structural units according to this Formulas achieved good results, regardless of whether these units are covalently bound to the polymer or are mixed. Prefers So here is a total of 5-99 mol% of structural units according to formulas (1) to (5). Particularly preferred is a total proportion of 10-80 mol% Structural units according to formulas (1) to (5), very particularly preferably a total proportion of 10-50 mol% Structural units according to formulas (1) to (5).
Eine weitere bevorzugte Ausführungsform ist die Mischung BLEND6, die durch Einmischen von Verbindungen VERB1 in BLEND4 entsteht, so dass hier Struktureinheiten gemäß Formel (1) bis (5) sowohl kovalent an den Triplett-Emitter gebunden wie auch eingemischt vorliegen. Auch hier hat sich gezeigt, dass ein Gesamtanteil von 5–99 mol% dieser Struktureinheiten gute Ergebnisse erzielt, unabhängig davon, ob diese Einheiten kovalent an den Triplett-Emitter gebunden sind oder eingemischt sind. Bevorzugt ist hier also ein Gesamtanteil von 5–99 mol% Struktureinheiten gemäß Formeln (1) bis (5). Besonders bevorzugt ist ein Gesamtanteil von 10–80 mol% Struktureinheiten gemäß Formeln (1) bis (5), ganz besonders bevorzugt ist ein Gesamtanteil von 10–50 mol% Struktureinheiten gemäß Formeln (1) bis (5).A further preferred embodiment is the mixture BLEND6, which by mixing compounds VERB1 in BLEND4 arises, so that here structural units according to formula (1) to (5) both covalently bonded to the triplet emitter as also mixed. Again, it has been shown that one Total share of 5-99 mol% of these structural units achieved good results, regardless of whether these units are covalently bound to the triplet emitter or mixed in. Preference is thus here a total share from 5-99 mol% Structural units according to formulas (1) to (5). Particularly preferred is a total proportion of 10-80 mol% Structural units according to formulas (1) to (5), very particularly preferably a total proportion of 10-50 mol% Structural units according to formulas (1) to (5).
Die in BLEND1 und BLEND3 eingemischten Triplett-Emitter TRIP1, bzw. die in POLY2 (= BLEND2) einpolymerisierten Triplett-Emitter TRIP2, bzw. die in BLEND4 eingemischten Triplett-Emitter TRIP3 können aus beliebigen organischen, metallorganischen bzw. anorganischen Substanzklassen ausgewählt werden, die bei Raumtemperatur aus dem Triplett-Zustand Licht emittieren können, also Phosphoreszenz statt Fluoreszenz zeigen: Dies sind zunächst vor allem Verbindungen, welche Schweratome, d. h. Atome aus dem Periodensystem der Elemente mit einer Ordnungszahl von mehr als 36, enthalten. Besonders geeignet sind hierfür Verbindungen, welche d- und f-Übergangsmetalle enthalten, die die o. g. Bedingung erfüllen. Ganz besonders bevorzugt sind hier entsprechende Struktureinheiten, welche Elemente der Gruppe 8 bis 10 (d. h. Ru, Os, Rh, Ir, Pd, Pt) enthalten. Solche Verbindungen sind für alle Emissionsfarben (Blau, Grün, Rot) bekannt, die benötigt werden, um Full Colour Displays zu bauen.The triplet emitters TRIP1, blended in BLEND1 and BLEND3, respectively the triplet emitter TRIP2 copolymerized in POLY2 (= BLEND2), or the TRIP3 triplet emitters mixed in BLEND4 can turn off any organic, organometallic or inorganic substance classes selected which emit light at room temperature from the triplet state can, So phosphorescence instead of fluorescence show: These are first all compounds which are heavy atoms, d. H. Atoms from the periodic table of elements with an atomic number greater than 36. Particularly suitable for this are compounds, which d and f transition metals contain the o. g. Fulfill condition. Very particularly preferred here are corresponding structural units, which elements of the group 8 to 10 (i.e., Ru, Os, Rh, Ir, Pd, Pt). Such compounds are for all emission colors (blue, green, Red) that are needed to build full color displays.
Die
Triplett-Emitter TRIP1 bzw. TRIP3 können niedermolekulare, oligomere,
dendrimere oder polymere Verbindungen sein. Da diese als Mischungsbestandteil
(BLEND1, BLEND3 bzw. BLEND4) verarbeitet wird, muss eine ausreichende
Löslichkeit
in geeigneten Lösungsmitteln
(z. B. Toluol, Xylol, Anisol, THF, Methylanisol, Methylnaphthalin
oder Mischungen dieser Lösemittel)
gegeben sein, damit die Verarbeitung aus Lösung möglich ist. Als niedermolekulare
Struktureinheiten kommen hier z. B. verschiedene Komplexe in Frage,
welche beispielsweise in den Anmeldeschriften WO 02/068435, WO 02/081488,
Der Triplett-Emitter TRIP2 wird kovalent in die Polymerkette von POLY2 (BLEND2) eingebaut. Um den Einbau von TRIP2 in POLY2 zu ermöglichen, müssen an TRIP2 funktionelle polymerisierbare Gruppen vorhanden sein. Beispiele für entsprechende bromierte Komplexe, die als Monomere in Polymerisationsreaktionen eingesetzt werden können, werden beschrieben in WO 02/068435. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet.Of the Triplet emitter TRIP2 is covalently inserted in the polymer chain of POLY2 (BLEND2) installed. To enable the installation of TRIP2 in POLY2, have to TRIP2 functional polymerizable groups may be present. Examples for corresponding brominated complexes used as monomers in polymerization reactions can be used are described in WO 02/068435. The corresponding descriptions will be hereby considered as part of the application via citation.
Die erfindungsgemäße Mischung BLEND1 wird nun erhalten, indem dem Polymer POLY1 ein Triplett-Emitter TRIP1 zugemischt werden.The inventive mixture BLEND1 is now obtained by giving the polymer POLY1 a triplet emitter TRIP1 be mixed.
Die erfindungsgemäße Mischung BLEND2 wird erhalten, indem dem Polymer POLY2 Verbindung VERB1, enthaltend Struktureinheiten gemäß Formel (1) bis (5), zugemischt wird.The inventive mixture BLEND2 is obtained by adding to the polymer POLY2 compound VERB1, containing structural units of the formula (1) to (5) is mixed.
Die erfindungsgemäße Mischung BLEND3 wird erhalten, indem dem Polymer POLY3 Verbindung VERB1, enthaltend Struktureinheiten gemäß Formel (1) bis (5), sowie ein Triplett-Emitter TRIP1 zugemischt werden.The mixture BLEND3 according to the invention is obtained by admixing the polymer POLY3 with compound VERB1 containing structural units of the formula (1) to (5) and a triplet emitter TRIP1 become.
Die erfindungsgemäße Mischung BLEND4 wird erhalten, indem dem Polymer POLY3 Einheiten TRIP3 zugemischt werden.The inventive mixture BLEND4 is obtained by adding POLY3 units TRIP3 to the polymer become.
Es kann außerdem bevorzugt sein, in BLEND1 bis BLEND4 noch beliebige weitere konjugierte, gekreuzt-konjugierte oder nicht-konjugierte Polymere, Oligomere, Dendrimere oder beliebige weitere niedermolekulare Verbindungen einzumischen. Die Zugabe weiterer Komponenten kann sich für manche Anwendungen als sinnvoll erweisen: So kann beispielsweise durch Zugabe einer elektronisch aktiven Substanz die Loch- bzw. Elektroneninjektion, der Loch- bzw. Elektronentransport oder das Ladungsgleichgewicht im entsprechenden Blend reguliert werden. Die Zusatzkomponente kann auch den Singulett-Triplett-Transfer erleichtern. Jedoch auch die Zugabe elektronisch inerter Verbindungen kann hilfreich sein, um beispielsweise die Viskosität einer Lösung oder die Morphologie des gebildeten Films zu kontrollieren. Die so erhaltenen Blends sind ebenfalls Gegenstand der Erfindung.It can also be preferred, in BLEND1 to BLEND4 any further conjugated, crossed-conjugated or non-conjugated polymers, oligomers, Dendrimers or any other low molecular weight compounds interfere. The addition of additional components may be for some Applications prove useful: For example, by Addition of an electronically active substance, the hole or electron injection, the hole or electron transport or the charge balance be regulated in the corresponding blend. The additional component can also facilitate the singlet-triplet transfer. But also the Adding electronically inert compounds may be helpful for example, the viscosity of a solution or to control the morphology of the formed film. The Blends thus obtained are also the subject of the invention.
Weiterhin Gegenstand der Erfindung sind Polymere POLY4, enthaltend
- (A) 1–99,5 mol%, bevorzugt 5–80 mol%, besonders bevorzugt 10–50 mol% einer oder mehrerer Wiederholeinheiten MONO1 mit mindestens einer Struktureinheit gemäß Formel (1) bis (5), wobei die Symbole X, Y, Z und R1–R6 dieselbe Bedeutung besitzen, wie oben beschrieben, und
- (B) 0,5–95 mol%, bevorzugt 1–50 mol%, besonders bevorzugt 2–25 mol%, eines oder mehrerer Triplett-Emitter TRIP2.
- (A) 1-99.5 mol%, preferably 5-80 mol%, particularly preferably 10-50 mol% of one or more repeat units MONO1 having at least one structural unit of the formula (1) to (5), wherein the symbols X, Y, Z and R 1 -R 6 have the same meaning as described above, and
- (B) 0.5-95 mol%, preferably 1-50 mol%, particularly preferably 2-25 mol%, of one or more triplet emitters TRIP2.
Dabei erfolgt der Einbau der Wiederholeinheiten MONO1, wie für das Polymer POLY1 beschrieben, in die Haupt- und/oder Seitenkette von POLY4. Ebenso erfolgt der Einbau des Triplett-Emitters TRIP2, wie für POLY2 beschrieben, in die Haupt- und/oder Seitenkette von POLY4.there the incorporation of repeat units MONO1, as for the polymer POLY1, in the main and / or side chain of POLY4. Likewise, the installation of the triplet emitter TRIP2, as for POLY2 described in the main and / or Side chain of POLY4.
Das Polymer POLY4 kann konjugiert, teilkonjugiert, gekreuzt-konjugiert oder nicht-konjugiert sein. In einer bevorzugten Ausführungsform ist POLY4 konjugiert oder gekreuzt-konjugiert. Wenn POLY4 gekreuzt-konjugiert ist, ist es bevorzugt, wenn die gekreuzt-konjugierten Abschnitte durch Wiederholeinheiten gemäß Formel (1) bis (5) erzeugt werden.The Polymer POLY4 can be conjugated, partially conjugated, cross-conjugated or non-conjugated be. In a preferred embodiment POLY4 is conjugated or crossed-conjugated. When POLY4 is crossed-conjugated is, it is preferred if the crossed-conjugated sections by repeating units according to formula (1) to (5) are generated.
POLY4 kann weitere Strukturelemente (z. B. Polymer-Grundgerüst-Bausteine, Ladungsinjektions- oder -transportbausteine) enthalten, wie für POLY1 bis POLY3 beschrieben. Ebenso kann es statistisch, alternierend oder blockartig aufgebaut, kann linear oder verzweigt sein. Eine weitere bevorzugte Ausführungsform von POLY4 ist ein dendritischer Aufbau des Polymers. Die Synthese von POLY4 erfolgt wie für POLY1 bis POLY3 beschrieben. Besonders bevorzugte Wiederholeinheiten MONO1 sind auch hier Strukturen gemäß Formel (6) bis (139).POLY4 may contain further structural elements (eg polymer backbone building blocks, Charge injection or transport devices), as for POLY1 to POLY3 described. Likewise, it can be statistical, alternating or block-like, can be linear or branched. A Another preferred embodiment of POLY4 is a dendritic structure of the polymer. The synthesis of POLY4 takes place as for POLY1 to POLY3 described. Particularly preferred repeat units MONO1 are also structures according to formulas (6) to (139).
Des Weiteren kann bevorzugt sein, in POLY4 noch beliebige weitere konjugierte, teilkonjugierte, gekreuzt-konjugierte oder nicht-konjugierte Polymere, Oligomere, Dendrimere oder beliebige weitere niedermolekulare Verbindungen einzumischen, so dass auch hier eine Mischung entsteht. Hier kann es bevorzugt sein, zusätzliche Verbindungen VERB1 einzumischen, so dass der Gesamtanteil an Strukturen gemäß Formel (1) bis (5) erhöht wird. Ebenso kann das zusätzliche Einmischen weiterer Triplett-Emitter TRIP1 bevorzugt sein. Aber auch die Zugabe anderer Komponenten kann sich für manche Anwendungen als sinnvoll erweisen. So kann beispielsweise durch Zugabe einer elektronisch aktiven Substanz die Loch- bzw. Elektroneninjektion, der Loch- bzw. Elektronentransport oder das Ladungsgleichgewicht des so entstandenen Blends reguliert werden. Die Zusatzkomponente kann auch den Singulett-Triplett-Transfer erleichtern. Jedoch auch die Zugabe elektronisch inerter Verbindungen kann hilfreich sein, um beispielsweise die Viskosität einer Lösung oder die Morphologie des gebildeten Films zu kontrollieren. Die so aus POLY4 erhaltenen Mischungen sind ebenfalls Gegenstand der Erfindung.Of Furthermore, it may be preferable to have any further conjugated in POLY4, partially conjugated, crossed-conjugated or non-conjugated polymers, Oligomers, dendrimers or any other low molecular weight compounds to intervene, so that here too a mixture arises. Here can it prefers extra Intermix compounds VERB1, giving the total share of structures according to formula (1) to (5) increased becomes. Likewise, the additional Mixing in of further triplet emitters TRIP1 may be preferred. But The addition of other components may also be useful for some applications prove. For example, by adding an electronic active substance, the hole or electron injection, the hole or Electron transport or the charge balance of the resulting Blends are regulated. The additional component can also be the singlet-triplet transfer facilitate. However, the addition of electronically inert compounds can be helpful, for example, the viscosity of a solution or to control the morphology of the formed film. The so obtained from POLY4 mixtures are also the subject of Invention.
Die Darstellung von BLEND1 bis BLEND6 erfolgt folgendermaßen: Die Einzelbestandteile des Blends werden in einem geeigneten Mischungsverhältnis zusammengegeben und in einem geeigneten Lösungsmittel gelöst. Geeignete Lösemittel sind beispielsweise Toluol, Anisol, Xylole, Methylanisol, Methylnaphthalin, Chlorbenzol, cyclische Ether (z. B. Dioxan, THF, Methyldioxan) oder auch Amide (z. B. NMP, DMF) oder Mischungen dieser Lösemittel. Alternativ können die Bestandteile des Blends auch einzeln gelöst werden. Die Lösung des Blends erhält man in diesem Fall durch Zusammenfügen der Einzellösungen im geeigneten Mischungsverhältnis. Dabei findet der Lösevorgang bevorzugt in einer inerten Atmosphäre statt. Der Blend wird üblicherweise nicht als Feststoff (durch nochmaliges Ausfällen) isoliert, sondern direkt aus Lösung weiter verarbeitet; jedoch sind auch Blends, die noch einmal ausgefällt wurden, Gegenstand der Erfindung. Ein geeignetes Verhältnis der einzelnen Komponenten ist beispielsweise eine Mischung, die insgesamt 1–99,5 mol%, bevorzugt 5–99 mol%, besonders bevorzugt 10–80 mol%, insbesondere 10–50 mol% Einheiten gemäß Formel (1) bis (5) (MONO1 in POLY1 bzw. VERB1) enthält und 0,5–95 mol%, bevorzugt 0,5–80 mol%, besonders bevorzugt 1–50 mol%, insbesondere 2–25 mol% TRIP1, TRIP2 und TRIP3 enthält, wobei sich die Angaben auf die gesamt vorhandenen Einheiten (Blendbestandteile bzw. Wiederholeinheiten im Polymer) beziehen. Dies ist unabhängig davon, ob die Komponenten kovalent an ein Polymer gebunden sind oder eingemischt sind.The representation of BLEND1 to BLEND6 is as follows: The individual components of the blend are combined in a suitable mixing ratio and dissolved in a suitable solvent. Suitable solvents are, for example, toluene, anisole, xylenes, methylanisole, methylnaphthalene, chlorobenzene, cyclic ethers (eg dioxane, THF, methyldioxane) or else amides (eg NMP, DMF) or mixtures of these solvents. Alternatively, the components of the blend can also be solved individually. The solution of the blend is obtained in this case by combining the individual solutions in a suitable mixing ratio. The dissolution process preferably takes place in an inert atmosphere. The blend is usually not isolated as a solid (by reprecipitation), but further processed directly from solution; However, blends that have been precipitated again, the subject of the invention. A suitable ratio of the individual components is, for example, a mixture which comprises a total of 1-99.5 mol%, preferably 5-99 mol%, particularly preferably 10-80 mol%, in particular 10-50 mol% of units of the formula (1) to ( 5) (MONO1 in POLY1 or VERB1) and contains 0.5-95 mol%, preferably 0.5-80 mol%, particularly preferably 1-50 mol%, in particular 2-25 mol% TRIP1, TRIP2 and TRIP3, wherein the data refer to the total existing units (blend components or repeating units in the polymer). This is independent of whether the components are covalently bound to a polymer or blended.
Die erfindungsgemäßen Mischungen BLEND1 bis BLENDE und Polymere POLY4 weisen gegenüber dem o. g. Stand der Technik u. a. folgende überraschenden Vorteile auf:
- • Die Löslichkeit in organischen Lösemitteln ist im Allgemeinen besser als die Löslichkeit der Polymere und Mischungen gemäß Stand der Technik. Die bessere Löslichkeit bietet einen Vorteil beispielsweise gegenüber überbrückten Carbazol-Einheiten, die als nächst liegender Stand der Technik angeführt werden, da dort häufig der maximale Carbazolanteil durch die schlechte Löslichkeit festgelegt wird, jedoch in manchen Fällen ein höherer Carbazolanteil für die weitere Verbesserung der Device-Eigenschaften wünschenswert wäre.
- • Die
chemische Zugänglichkeit
der Einheiten gemäß Formel
(1) bis (5), sowohl als Blendbestandteil wie auch als Monomer, ist
unproblematisch. Teilweise sind diese Blendbestandteile und Monomere
auch kommerziell erhältlich.
Dies ist ein entscheidender Vorteil gegenüber beispielsweise den überbrückten Carbazol-Einheiten (
DE 10328627.6 - • Die erfindungsgemäßen Mischungen und Polymere zeigen eine höhere Sauerstoffstabilität als Mischungen und Polymere gemäß Stand der Technik. Dadurch vereinfacht sich die Herstellung dieser Verbindungen und Mischung auch auch deren Verarbeitung, was einen erheblichen praktischen Vorteil darstellt.
- • Die Effizienz der Lichtemission des Triplett-Emitters ist in erfindungsgemäßen Mischungen BLEND1 bis BLEND6 bzw. Polymeren POLY4 vergleichbar zu Polymeren und Mischungen gemäß Stand der Technik. Dies stellt zwar keinen unmittelbaren Vorteil dieser Verbindungen dar, jedoch ist es essentiell, dass diese Eigenschaft bei der Verbesserung der anderen Eigenschaften erhalten bleibt.
- Solubility in organic solvents is generally better than the solubility of the polymers and blends of the prior art. The better solubility offers an advantage, for example, over bridged carbazole units, which are considered to be the closest prior art, since the maximum carbazole content is often determined by the poor solubility, but in some cases a higher carbazole content for the further improvement of the device Properties would be desirable.
- • The chemical accessibility of the units according to formula (1) to (5), both as a blend component as well as a monomer, is not a problem. In part, these blend components and monomers are also commercially available. This is a decisive advantage over, for example, the bridged carbazole units (
DE 10328627.6 - The mixtures and polymers according to the invention show a higher oxygen stability than mixtures and polymers according to the prior art. This simplifies the preparation of these compounds and mixture and their processing, which represents a significant practical advantage.
- The efficiency of the light emission of the triplet emitter in blends according to the invention BLEND1 to BLEND6 or polymers POLY4 is comparable to polymers and mixtures according to the prior art. While this is not an immediate benefit of these compounds, it is essential that this property be preserved while improving the other properties.
Die
Mischungen BLEND1 bis BLEND6 bzw. die Polymere POLY4 können in
PLEDs verwendet werden. Für
den Bau von PLEDs wird in der Regel ein allgemeines Verfahren verwendet,
das entsprechend für den
Einzelfall anzupassen ist. Ein solches Verfahren wurde beispielsweise
in
Wie oben beschrieben, eignen sich die erfindungsgemäßen Mischungen BLEND1 bis BLEND6 bzw. die erfindungsgemäßen Polymere POLY4 ganz besonders als Elektrolumineszenzmaterialien in derart hergestellten PLEDs oder Displays. Als Elektrolumineszenzmaterialien im Sinne dieser Erfindung gelten Materialien, die als aktive Schicht in einer PLED bei Anlegen eines elektrischen Feldes Licht abstrahlen (lichtemittierende Schicht).As described above, mixtures BLEND1 to BLEND6 according to the invention are suitable or the polymers according to the invention POLY4 especially as electroluminescent materials in such manufactured PLEDs or displays. As electroluminescent materials For the purposes of this invention, materials that act as an active layer emit light in a PLED when an electric field is applied (light-emitting layer).
Gegenstand der Erfindung ist daher auch die Verwendung einer erfindungsgemäßen Mischung BLEND1 bis BLEND6 bzw. eines erfindungsgemäßen Polymers POLY4 in einer PLED als Elektrolumineszenzmaterial.object The invention therefore also relates to the use of a blend BLEND1 according to the invention to BLEND6 or a polymer according to the invention POLY4 in one PLED as electroluminescent material.
Gegenstand der Erfindung ist somit ebenfalls eine PLED mit einer oder mehreren aktiven Schichten, wobei mindestens eine dieser aktiven Schichten ein oder mehrere erfindungsgemäße Mischungen BLEND1 bis BLEND6 bzw. erfindungsgemäße Polymere POLY4 enthält.object The invention is therefore also a PLED with one or more active layers, wherein at least one of these active layers one or more mixtures according to the invention BLEND1 to BLEND6 or polymers according to the invention POLY4 contains.
PLEDs finden z. B. Anwendung als selbstleuchtende Anzeigeelemente, wie Kontrolllampen, alphanumerische Displays, mehr- oder vollfarbige Displays, Hinweisschilder und in optoelektronischen Kopplern.PLEDs find z. B. Application as self-luminous display elements, such as Indicator lights, alphanumeric displays, multicolor or full color Displays, information signs and in optoelectronic couplers.
Im vorliegenden Anmeldetext und auch in den im Weiteren folgenden Beispielen wird auf die Verwendung erfindungsgemäßer Mischungen BLEND1 bis BLEND6 bzw. erfindungsgemäßer Polymere POLY4 in Bezug auf PLEDs und die entsprechenden Displays abgezielt. Trotz dieser Beschränkung der Beschreibung ist es für den Fachmann ohne weiteres erfinderisches Zutun möglich, die erfindungsgemäßen Polymere oder Blends auch für weitere Verwendungen in anderen elektronischen Devices (Vorrichtungen) zu benutzen, z. B. für organische Solarzellen (O-SCs), nicht-lineare Optik oder auch organische Laserdioden (O-Laser), um nur einige Anwendungen zu nennen.In the present application text and also in the examples below, the use of mixtures according to the invention BLEND1 to BLEND6 or polymers POLY4 according to the invention with respect to PLEDs and the corresponding displays is aimed at. Despite this restriction the description is It is possible for the skilled artisan without further inventive step to use the polymers or blends of the invention for other uses in other electronic devices (devices), eg. As for organic solar cells (O-SCs), non-linear optics or organic laser diodes (O-laser), to name only a few applications.
Die Erfindung wird durch die nachfolgenden Beispiele näher erläutert, ohne sie dadurch einschränken zu wollen.The Invention is illustrated by the following examples, without thereby restricting them want.
Beispiel 1: Synthese der Co-Monomere für die PolymereExample 1: Synthesis of Co-monomers for the polymers
Die
Synthese weiterer Co-Monomere, die für konjugierte Polymere verwendet
wurden, ist bereits in WO 02/077060 und der darin zitierten Literatur,
sowie in
Beispiel 2: 4,4'-Dibrombenzophenon (Monomer M6 gemäß Formel (1))Example 2: 4,4'-Dibromobenzophenone (Monomer M6 according to formula (1))
4,4'-Dibrombenzophenon wurde von Fluka in einer Reinheit von 98% erhalten und durch weitere Umkristallisation aus Ethanol bis zu einer Reinheit von 99,7% (gemäß HPLC) aufgereinigt.4,4'-dibromobenzophenone was obtained by Fluka in a purity of 98% and by more Recrystallization from ethanol to a purity of 99.7% (according to HPLC) purified.
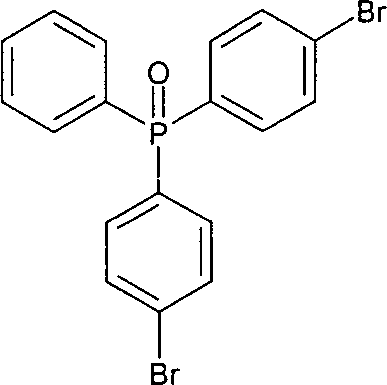
Beispiel 3: Synthese von Bis(4-bromphenyl)-phenylphosphanoxid (Monomer M7 gemäß Formel (3))Example 3: Synthesis of Bis (4-bromophenyl) -phenylphosphine oxide (monomer M7 according to formula (3))
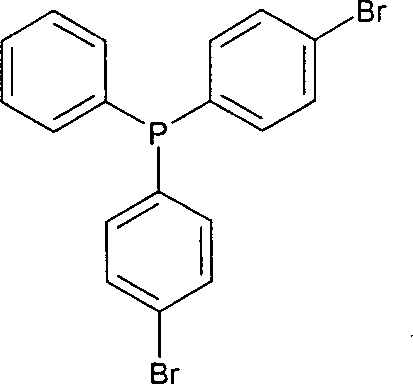
a) Synthese von Bis(4-bromphenyl)-phenylphosphan a) Synthesis of bis (4-bromophenyl) phenylphosphine
In einem trockenen 1000 mL Vierhalskolben mit Innenthermometer, Rührkern, Argon-Überlagerung und 2 Tropftrichtern wurden 33,9 g (144 mmol) Dibrombenzol in 300 mL trockenem THF gelöst und auf –70°C gekühlt. Innerhalb 30 min. wurden 90 mL (144 mmol) n-Butyllithium (1,6M in Hexan) zugetropft und 1 h bei dieser Temperatur nachgerührt. Dann wurden bei dieser Temperatur 12,9 g (9,75 ml, 72 mmol) Dichlorphenylphosphan in 60 mL trockenem THF zugetropft. Über Nacht ließ man auf Raumtemperatur kommen. Es wurden 20 mL Methanol zugegeben, und der Ansatz wurde zur Trockene eingedampft. Der Rückstand wurde in Dichlormethan aufgenommen, filtriert und das Lösungsmittel im Vakuum entfernt. Die Verbindung wurde ohne weitere Aufreinigung für die folgende Umsetzung eingesetzt.In a dry 1000 mL four-necked flask with internal thermometer, stirrer, Argon overlay and 2 dropping funnels were 33.9 g (144 mmol) of dibromobenzene in 300 mL dissolved dry THF and cooled to -70 ° C. Within 30 min. 90 mL (144 mmol) n-butyllithium (1.6 M in hexane) was added dropwise and stirred for 1 h at this temperature. Then at this Temperature 12.9 g (9.75 ml, 72 mmol) of dichlorophenylphosphine in 60 added dropwise to dry THF. about Night was left come to room temperature. 20 mL of methanol were added, and the reaction was evaporated to dryness. The residue was in dichloromethane taken up, filtered and the solvent removed in a vacuum. The compound was without further purification for the following implementation used.
b) Synthese von Bis(4-bromphenyl)-pfienylphosphanoxid b) Synthesis of bis (4-bromophenyl) -pfienylphosphine oxide
In einem 500 mL Vierhalskolben mit Innenthermometer, mechanischem Rührer, Rückflusskühler und Tropftrichter wurden 10,05 g (24 mmol) Bis(4-bromphenyl)-phenylphophan in 200 mL Ethylacetat gelöst und auf 5°C Innentemperatur abgekühlt. Dazu wurde innerhalb 30 min. eine Lösung von 2,25 mL (26,4 mmol) H2O2 (35%ig) in 17,5 mL Wasser getropft und weitere 12 h bei Raumtemperatur gerührt. Anschließend wurden 25 mL gesättigte Natriumsulfit-Lösung zugegeben, die organische Phase abgetrennt, zweimal mit gesättigter Natriumsulfit-Lösung gewaschen und über Natriumsulfat getrocknet. Das Lösungsmittel wurde im Vakuum entfernt. Die Aufreinigung erfolgte zunächst durch Säulenchromatographie auf Silica mit einem Lösemittelgemisch von anfangs Hexan:Ethylacetat 2:1 zu Hexan:Ethylacetat 1:1. Weitere Reinigung erfolgte durch Umkristallisation aus Heptan/Toluol. Es wurden 6,5 g Produkt in einer Reinheit von 99,7% (gemäß HPLC) erhalten. 1H-NMR (500 MHz, CDCl3): [ppm] 7,46–7,66 (m). 31P-NMR (CDCl3): [ppm] 28,40.In a 500 ml four-necked flask with internal thermometer, mechanical stirrer, reflux condenser and dropping funnel, 10.05 g (24 mmol) of bis (4-bromophenyl) phenylphosphine were dissolved in 200 ml of ethyl acetate and cooled to 5 ° C. internal temperature. This was within 30 min. a solution of 2.25 mL (26.4 mmol) of H 2 O 2 (35%) in 17.5 mL of water was added dropwise and stirred for a further 12 h at room temperature. Subsequently, 25 mL of saturated sodium sulfite solution were added, the organic phase separated, washed twice with saturated sodium sulfite solution and dried over sodium sulfate. The solvent was removed in vacuo. The purification was carried out first by column chromatography on silica with a solvent mixture of initially hexane: ethyl acetate 2: 1 to hexane: ethyl acetate 1: 1. Further purification was carried out by recrystallization from heptane / toluene. There were obtained 6.5 g of product in a purity of 99.7% (according to HPLC). 1 H-NMR (500 MHz, CDCl3): [ppm] 7.46 to 7.66 (m). 31 P-NMR (CDCl3): [ppm] 28,40.
Beispiel 4: Blendbestandteil V1 (VERB1 gemäß Formel (1))Example 4: Blend component V1 (VERB1 according to formula (1))
Als
Blendbestandteil V1 wurde beispielhaft das folgende Keton verwendet,
dessen Synthese bereits in
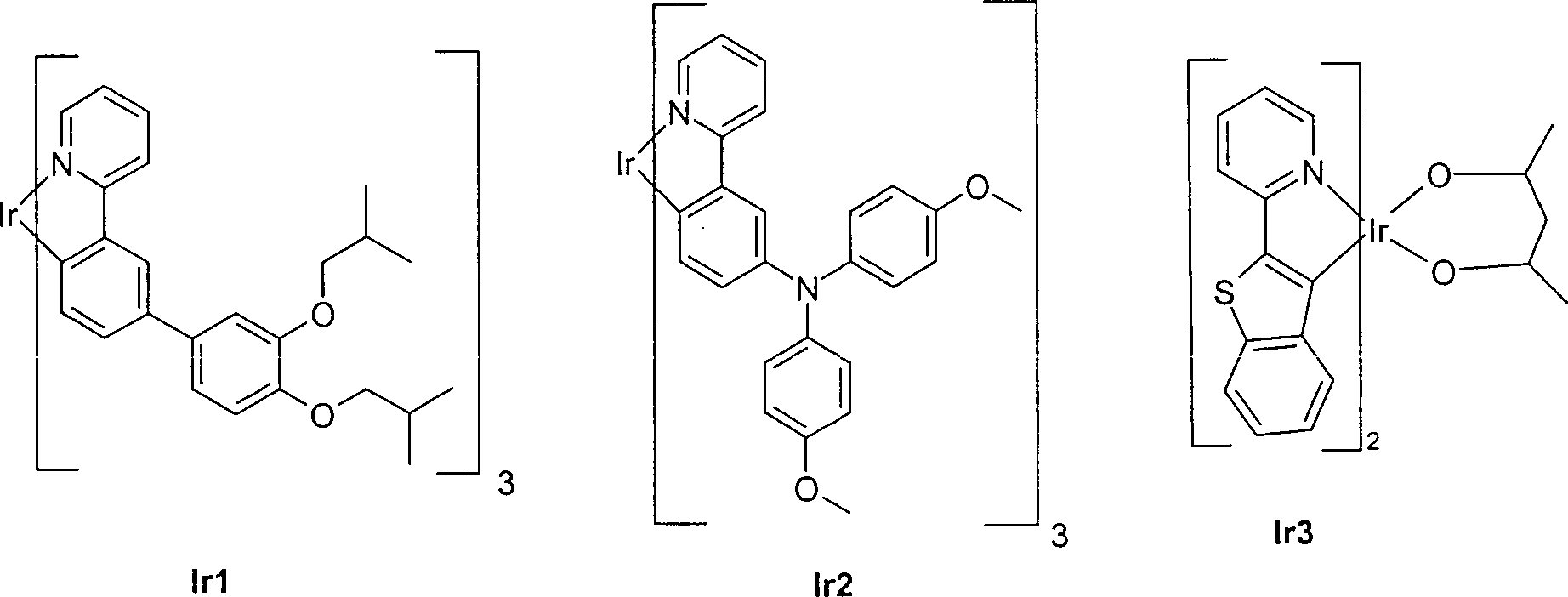
Beispiel 5: Struktureinheiten TRIP1 zur Verwendung in BlendsExample 5: Structural units TRIP1 for use in blends
Bei
den hier beispielhaft verwendeten Verbindungen TRIP1 handelt es
sich um Derivate von tris-(Phenylpyridyl)-Iridium(III). Die Synthese
dieser Verbindungen ist bereits beschrieben in der Anmeldeschrift
WO 02/081488 und in der nicht offen gelegten Patentanmeldung
Beispiel 6: Synthese konjugierter Polymere POLY3Example 6: Synthesis of conjugated Polymers POLY3
Die
Synthese konjugierter Polymere POLY3, die keine Einheiten gemäß Formel
(I) und keine Verbindungen TRIP2 enthalten, ist bereits beispielsweise
in den Anmeldeschriften WO 02/077060,
Beispiel 7: Synthese von Polymer P1Example 7: Synthesis of Polymer P1
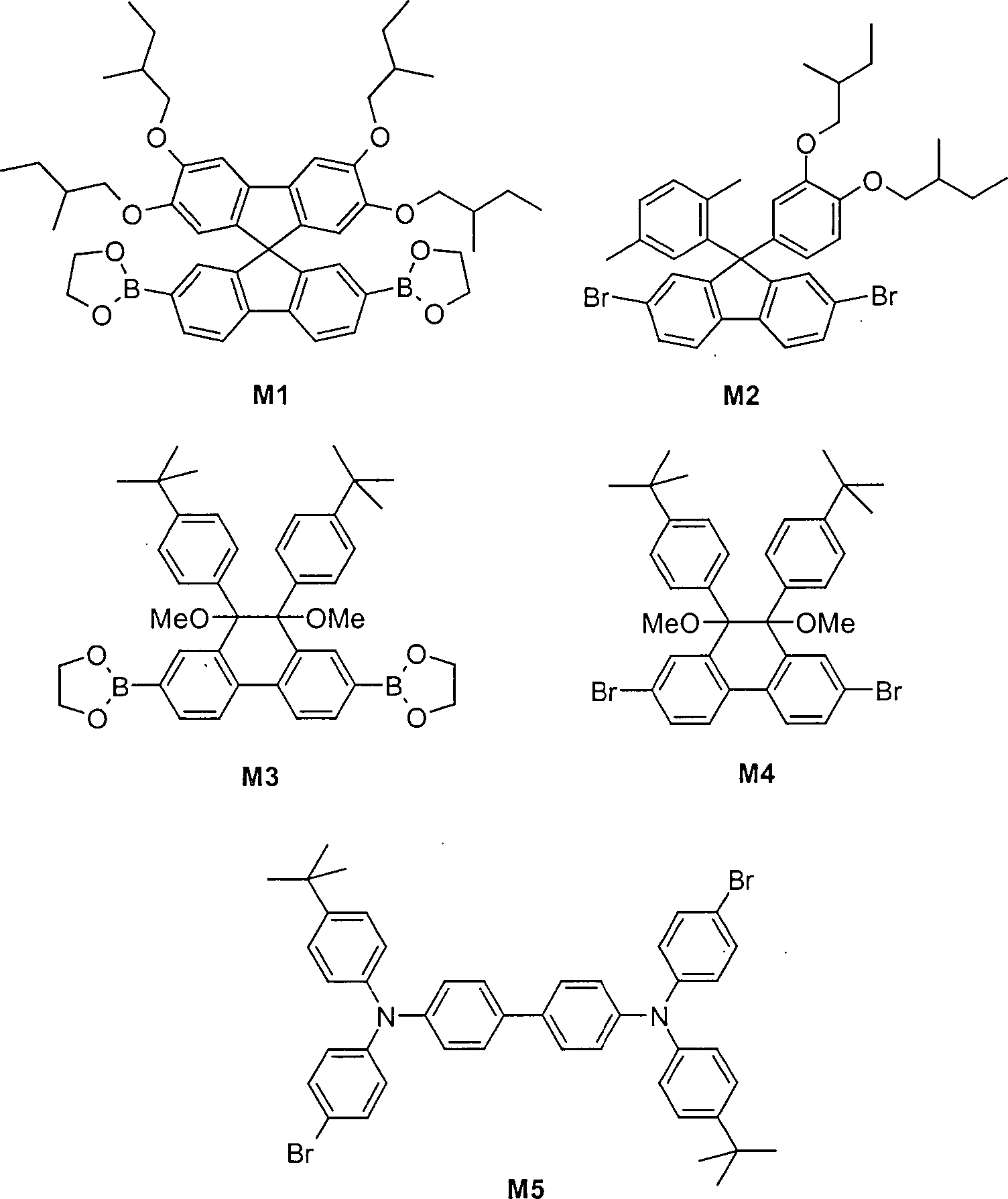
Die Synthese erfolgte gemäß dem in WO 03/048224 beschriebenen Verfahren. Es wurden eingesetzt: 1,6013 g (2 mmol) Monomer M1, 0,8118 g (1,2 mmol) Monomer M2, 0,3035 g (0,4 mmol) Monomer M5, 0,1744 g (0,1 mmol) Monomer M7 und 2,03 g (2,2 Äquivalente) Kaliumphosphat Hydrat in 19 mL Dioxan, 6 mL Toluol und 12 mL H2O. Als Katalysator wurden verwendet: 0,45 mg Pd(OAc)2 und 3,65 mg P(o-tolyl)3. Nach Aufarbeitung wurden 1,57 g Polymer erhalten, das ein Molekulargewicht Mn 58000 und Mw 185000 aufwies (GPC in THF mit Polystyrol-Standard).The synthesis was carried out according to the method described in WO 03/048224. The following were used: 1.6013 g (2 mmol) of monomer M1, 0.8118 g (1.2 mmol) of monomer M2, 0.3035 g (0.4 mmol) of monomer M5, 0.1744 g (0.1 mmol ) Monomer M7 and 2.03 g (2.2 equivalents) of potassium phosphate hydrate in 19 mL dioxane, 6 mL toluene and 12 mL H 2 O. The catalyst used was: 0.45 mg Pd (OAc) 2 and 3.65 mg P (o-tolyl) 3 . After working up, 1.57 g of polymer were obtained which had a molecular weight M n 58,000 and M w 185,000 (GPC in THF with polystyrene standard).
Beispiel 8: Synthese von Polymer P2:Example 8: Synthesis of Polymer P2:
Die Synthese erfolgte gemäß dem in WO 03/048224 beschriebenen Verfahren. Es wurden eingesetzt: 1,2889 g (2 mmol) Monomer M3, 0,7951 g (1,2 mmol) Monomer M4, 0,3035 g (0,4 mmol) Monomer M5, 0,1360 g (0,1 mmol) Monomer M6 und 2,03 g (2,2 Äquivalente) Kaliumphosphat Hydrat in 19 mL Dioxan, 6 mL Toluol und 12 mL H2O. Als Katalysator wurden verwendet: 0,45 mg Pd(OAc)2 und 3,65 mg P(o-tolyl)3. Nach Aufarbeitung wurden 1,72 g Polymer erhalten, das ein Molekulargewicht Mn 87000 und Mw 219000 aufwies (GPC in THF mit Polystyrol-Standard).The synthesis was carried out according to the method described in WO 03/048224. The following were used: 1.2889 g (2 mmol) of monomer M3, 0.7951 g (1.2 mmol) of monomer M4, 0.3035 g (0.4 mmol) of monomer M5, 0.1360 g (0.1 mmol ) Monomer M6 and 2.03 g (2.2 equivalents) of potassium phosphate hydrate in 19 mL dioxane, 6 mL toluene, and 12 mL H 2 O. The catalyst used was: 0.45 mg Pd (OAc) 2 and 3.65 mg P (o-tolyl) 3 . After work-up, 1.72 g of polymer were obtained which had a molecular weight M n 87,000 and M w 219,000 (GPC in THF with polystyrene standard).
Beispiel 10: Herstellung der BlendsExample 10: Production the blends
Die Herstellung der Mischungen erfolgte durch Lösen der Blendbestandteile im gewünschten Verhältnis und in der gewünschten Konzentration in einem geeigneten Lösemittel. Als Lösemittel wurde hier Toluol verwendet. Dabei wurde der Lösevorgang in einer inerten Atmosphäre bei 60°C durchgeführt. Die Lösung wurde ohne Isolierung der Mischung (nochmaliges Ausfällen der Feststoffanteile) direkt verarbeitet.The Preparation of the mixtures was carried out by dissolving the blend components in desired relationship and in the desired Concentration in a suitable solvent. As a solvent toluene was used here. The dissolution process was in an inert the atmosphere at 60 ° C carried out. The solution was without isolation of the mixture (repeated precipitation of the Solids) directly processed.
Beispiel 11: Herstellung der polymeren Leuchtdioden (PLEDs)Example 11: Preparation polymeric light-emitting diodes (PLEDs)
Wie
PLEDs dargestellt werden können,
ist bereits in
Claims (31)
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10349033A DE10349033A1 (en) | 2003-10-22 | 2003-10-22 | Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter |
| EP04790695.3A EP1675930B1 (en) | 2003-10-22 | 2004-10-21 | New materials for electroluminescence and the utilization thereof |
| EP10015929.2A EP2366752B1 (en) | 2003-10-22 | 2004-10-21 | New materials for electroluminescence and use of same |
| US10/576,920 US7659540B2 (en) | 2003-10-22 | 2004-10-21 | Materials for electroluminescence and the utilization thereof |
| CN200480031198.4A CN1894357A (en) | 2003-10-22 | 2004-10-21 | Novel materials for electroluminescence, and their uses |
| JP2006536042A JP2007517079A (en) | 2003-10-22 | 2004-10-21 | Novel materials for electroluminescence and their use |
| PCT/EP2004/011888 WO2005040302A1 (en) | 2003-10-22 | 2004-10-21 | New materials for electroluminescence and the utilization thereof |
| KR1020067007587A KR101215160B1 (en) | 2003-10-22 | 2006-04-20 | New materials and their uses for electroluminescence |
| US12/639,591 US8173276B2 (en) | 2003-10-22 | 2009-12-16 | Materials for electroluminescence and the utilization thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10349033A DE10349033A1 (en) | 2003-10-22 | 2003-10-22 | Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE10349033A1 true DE10349033A1 (en) | 2005-05-25 |
Family
ID=34484893
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE10349033A Withdrawn DE10349033A1 (en) | 2003-10-22 | 2003-10-22 | Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter |
Country Status (2)
| Country | Link |
|---|---|
| CN (1) | CN1894357A (en) |
| DE (1) | DE10349033A1 (en) |
Cited By (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102008049037A1 (en) | 2008-09-25 | 2010-04-22 | Merck Patent Gmbh | New polymers with low polydispersity |
| EP1961780A4 (en) * | 2005-12-02 | 2010-06-30 | Sumitomo Chemical Co | POLYMERIC COMPOUND AND POLYMERIC ELECTROLUMINESCENT DEVICE USING THE SAME |
| US7790057B2 (en) | 2006-07-11 | 2010-09-07 | Merck Patent Gmbh | Electroluminescent polymers and use thereof |
| US7820305B2 (en) | 2004-07-06 | 2010-10-26 | Merck Patent Gmbh | Electroluminescent polymers |
| WO2011015265A2 (en) | 2009-08-04 | 2011-02-10 | Merck Patent Gmbh | Electronic devices comprising multi cyclic hydrocarbons |
| US7947382B2 (en) | 2004-04-26 | 2011-05-24 | Merck Patent Gmbh | Electroluminescent polymers and the use thereof |
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
| WO2011076314A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent formulations |
| WO2011076326A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent functional surfactants |
| WO2011110277A1 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Fibers in therapy and cosmetics |
| WO2011110275A2 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Radiative fibers |
| WO2011147522A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Compositions comprising quantum dots |
| WO2011147521A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Down conversion |
| WO2012007102A1 (en) * | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Polymer materials for organic electroluminescent devices |
| US8580395B2 (en) | 2008-08-29 | 2013-11-12 | Merck Patent Gmbh | Electroluminescent polymers, method for the production thereof, and use thereof |
| US8679644B2 (en) | 2004-04-26 | 2014-03-25 | Merck Patent Gmbh | Electroluminescent polymers containing planar arylamine units, the preparation and use thereof |
| WO2016034262A1 (en) | 2014-09-05 | 2016-03-10 | Merck Patent Gmbh | Formulations and electronic devices |
| WO2016107663A1 (en) | 2014-12-30 | 2016-07-07 | Merck Patent Gmbh | Formulations and electronic devices |
| WO2016155866A1 (en) | 2015-03-30 | 2016-10-06 | Merck Patent Gmbh | Formulation of an organic functional material comprising a siloxane solvent |
| WO2016198141A1 (en) | 2015-06-12 | 2016-12-15 | Merck Patent Gmbh | Esters containing non-aromatic cycles as solvents for oled formulations |
| WO2017036572A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Formulation of an organic functional material comprising an epoxy group containing solvent |
| WO2017097391A1 (en) | 2015-12-10 | 2017-06-15 | Merck Patent Gmbh | Formulations containing ketones comprising non-aromatic cycles |
| WO2017102049A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a mixture of at least two different solvents |
| WO2017102048A1 (en) | 2015-12-15 | 2017-06-22 | Merck Patent Gmbh | Esters containing aromatic groups as solvents for organic electronic formulations |
| WO2017102052A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a solid solvent |
| WO2017140404A1 (en) | 2016-02-17 | 2017-08-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017157783A1 (en) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Receptacle comprising a formulation containing at least one organic semiconductor |
| WO2017216128A1 (en) | 2016-06-17 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017216129A1 (en) | 2016-06-16 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018001928A1 (en) | 2016-06-28 | 2018-01-04 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018024719A1 (en) | 2016-08-04 | 2018-02-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077662A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077660A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018104202A1 (en) | 2016-12-06 | 2018-06-14 | Merck Patent Gmbh | Preparation process for an electronic device |
| WO2018108760A1 (en) | 2016-12-13 | 2018-06-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018138319A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic electroluminescence (el) element |
| WO2018138318A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2018178136A1 (en) | 2017-03-31 | 2018-10-04 | Merck Patent Gmbh | Printing method for an organic light emitting diode (oled) |
| WO2018189050A1 (en) | 2017-04-10 | 2018-10-18 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018202603A1 (en) | 2017-05-03 | 2018-11-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019016184A1 (en) | 2017-07-18 | 2019-01-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019115573A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019162483A1 (en) | 2018-02-26 | 2019-08-29 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019238782A1 (en) | 2018-06-15 | 2019-12-19 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2020094538A1 (en) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2021213917A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Emulsions comprising organic functional materials |
| WO2021213918A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2022122607A1 (en) | 2020-12-08 | 2022-06-16 | Merck Patent Gmbh | An ink system and a method for inkjet printing |
| WO2022223675A1 (en) | 2021-04-23 | 2022-10-27 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2023012084A1 (en) | 2021-08-02 | 2023-02-09 | Merck Patent Gmbh | A printing method by combining inks |
| WO2023057327A1 (en) | 2021-10-05 | 2023-04-13 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2023237458A1 (en) | 2022-06-07 | 2023-12-14 | Merck Patent Gmbh | Method of printing a functional layer of an electronic device by combining inks |
| WO2024126635A1 (en) | 2022-12-16 | 2024-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2025032039A1 (en) | 2023-08-07 | 2025-02-13 | Merck Patent Gmbh | Process for the preparation of an electronic device |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8174000B2 (en) * | 2009-02-11 | 2012-05-08 | Universal Display Corporation | Liquid compositions for inkjet printing of organic layers or other uses |
| DE102010048498A1 (en) * | 2010-10-14 | 2012-04-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2012085982A1 (en) | 2010-12-24 | 2012-06-28 | パナソニック株式会社 | Organic el element and method for producing same |
-
2003
- 2003-10-22 DE DE10349033A patent/DE10349033A1/en not_active Withdrawn
-
2004
- 2004-10-21 CN CN200480031198.4A patent/CN1894357A/en active Pending
Cited By (60)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7947382B2 (en) | 2004-04-26 | 2011-05-24 | Merck Patent Gmbh | Electroluminescent polymers and the use thereof |
| US8679644B2 (en) | 2004-04-26 | 2014-03-25 | Merck Patent Gmbh | Electroluminescent polymers containing planar arylamine units, the preparation and use thereof |
| US7820305B2 (en) | 2004-07-06 | 2010-10-26 | Merck Patent Gmbh | Electroluminescent polymers |
| US7985810B2 (en) | 2005-12-02 | 2011-07-26 | Sumitomo Chemical Company, Limited | Polymer compound and polymer light emitting device using the same |
| EP1961780A4 (en) * | 2005-12-02 | 2010-06-30 | Sumitomo Chemical Co | POLYMERIC COMPOUND AND POLYMERIC ELECTROLUMINESCENT DEVICE USING THE SAME |
| US7790057B2 (en) | 2006-07-11 | 2010-09-07 | Merck Patent Gmbh | Electroluminescent polymers and use thereof |
| US8580395B2 (en) | 2008-08-29 | 2013-11-12 | Merck Patent Gmbh | Electroluminescent polymers, method for the production thereof, and use thereof |
| DE102008049037A1 (en) | 2008-09-25 | 2010-04-22 | Merck Patent Gmbh | New polymers with low polydispersity |
| WO2011015265A2 (en) | 2009-08-04 | 2011-02-10 | Merck Patent Gmbh | Electronic devices comprising multi cyclic hydrocarbons |
| WO2011076326A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent functional surfactants |
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
| WO2011076314A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent formulations |
| WO2011110275A2 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Radiative fibers |
| WO2011110277A1 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Fibers in therapy and cosmetics |
| WO2011147522A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Compositions comprising quantum dots |
| WO2011147521A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Down conversion |
| EP3309236A1 (en) | 2010-05-27 | 2018-04-18 | Merck Patent GmbH | Compositions comprising quantum dots |
| WO2012007102A1 (en) * | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Polymer materials for organic electroluminescent devices |
| US9236571B2 (en) | 2010-07-16 | 2016-01-12 | Merck Patent Gmbh | Polymer materials for organic electroluminescent devices |
| WO2016034262A1 (en) | 2014-09-05 | 2016-03-10 | Merck Patent Gmbh | Formulations and electronic devices |
| WO2016107663A1 (en) | 2014-12-30 | 2016-07-07 | Merck Patent Gmbh | Formulations and electronic devices |
| WO2016155866A1 (en) | 2015-03-30 | 2016-10-06 | Merck Patent Gmbh | Formulation of an organic functional material comprising a siloxane solvent |
| WO2016198141A1 (en) | 2015-06-12 | 2016-12-15 | Merck Patent Gmbh | Esters containing non-aromatic cycles as solvents for oled formulations |
| EP3581633A1 (en) | 2015-06-12 | 2019-12-18 | Merck Patent GmbH | Esters containing non-aromatic cycles as solvents for oled formulations |
| WO2017036572A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Formulation of an organic functional material comprising an epoxy group containing solvent |
| WO2017097391A1 (en) | 2015-12-10 | 2017-06-15 | Merck Patent Gmbh | Formulations containing ketones comprising non-aromatic cycles |
| WO2017102048A1 (en) | 2015-12-15 | 2017-06-22 | Merck Patent Gmbh | Esters containing aromatic groups as solvents for organic electronic formulations |
| EP4084109A1 (en) | 2015-12-15 | 2022-11-02 | Merck Patent GmbH | Esters containing aromatic groups as solvents for organic electronic formulations |
| WO2017102049A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a mixture of at least two different solvents |
| WO2017102052A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a solid solvent |
| WO2017140404A1 (en) | 2016-02-17 | 2017-08-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017157783A1 (en) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Receptacle comprising a formulation containing at least one organic semiconductor |
| DE102016003104A1 (en) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Container comprising a formulation containing at least one organic semiconductor |
| WO2017216129A1 (en) | 2016-06-16 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017216128A1 (en) | 2016-06-17 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018001928A1 (en) | 2016-06-28 | 2018-01-04 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018024719A1 (en) | 2016-08-04 | 2018-02-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077662A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077660A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018104202A1 (en) | 2016-12-06 | 2018-06-14 | Merck Patent Gmbh | Preparation process for an electronic device |
| WO2018108760A1 (en) | 2016-12-13 | 2018-06-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018138318A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2018138319A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic electroluminescence (el) element |
| WO2018178136A1 (en) | 2017-03-31 | 2018-10-04 | Merck Patent Gmbh | Printing method for an organic light emitting diode (oled) |
| WO2018189050A1 (en) | 2017-04-10 | 2018-10-18 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018202603A1 (en) | 2017-05-03 | 2018-11-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019016184A1 (en) | 2017-07-18 | 2019-01-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019115573A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019162483A1 (en) | 2018-02-26 | 2019-08-29 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019238782A1 (en) | 2018-06-15 | 2019-12-19 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2020094538A1 (en) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2021213917A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Emulsions comprising organic functional materials |
| WO2021213918A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2022122607A1 (en) | 2020-12-08 | 2022-06-16 | Merck Patent Gmbh | An ink system and a method for inkjet printing |
| WO2022223675A1 (en) | 2021-04-23 | 2022-10-27 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2023012084A1 (en) | 2021-08-02 | 2023-02-09 | Merck Patent Gmbh | A printing method by combining inks |
| WO2023057327A1 (en) | 2021-10-05 | 2023-04-13 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2023237458A1 (en) | 2022-06-07 | 2023-12-14 | Merck Patent Gmbh | Method of printing a functional layer of an electronic device by combining inks |
| WO2024126635A1 (en) | 2022-12-16 | 2024-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2025032039A1 (en) | 2023-08-07 | 2025-02-13 | Merck Patent Gmbh | Process for the preparation of an electronic device |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1894357A (en) | 2007-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE10349033A1 (en) | Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter | |
| EP1675930B1 (en) | New materials for electroluminescence and the utilization thereof | |
| EP1763566B1 (en) | Electroluminescent polymers | |
| EP1670844B2 (en) | White-emitting copolymers, representation and use thereof | |
| EP1932866B1 (en) | Blends comprising conjugated carbazole polymers, synthesis and usage thereof | |
| EP1641894B1 (en) | Novel materials for electroluminescence | |
| DE60108726T2 (en) | LUMINESCENT POLYMER | |
| DE60103442T3 (en) | Polymeric fluorescent material, process for its preparation, and luminescent polymer device in which it is used | |
| EP1927610B1 (en) | Process for the synthesis of aryl- or heteroarylamine boronic acid derivatives | |
| DE102005037734B4 (en) | Electroluminescent polymers, their use and bifunctional monomeric compounds | |
| DE102004023277A1 (en) | New material mixtures for electroluminescence | |
| DE112009000181B4 (en) | Process for the production of white light emitting material | |
| EP2038241B1 (en) | Electroluminescent polymers and use thereof | |
| DE10249723A1 (en) | Conjugated polymers containing arylamine units, their preparation and use | |
| DE102004020298A1 (en) | Electroluminescent polymers and their use | |
| DE102004023278A1 (en) | Electroluminescent polymers | |
| EP2318473B1 (en) | Fluorine-bridged associations for optoelectronic applications | |
| DE112005003006T5 (en) | Phosphorescent OLED | |
| DE102004003008A1 (en) | Organic semiconductor, for use in organic LEDs and solar cells and laser diodes, contains a polymer and structural units which emit light from the triplet state and a triplet emitter |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8139 | Disposal/non-payment of the annual fee |