DE102004024364A1 - Process for the preparation of polymers - Google Patents
Process for the preparation of polymers Download PDFInfo
- Publication number
- DE102004024364A1 DE102004024364A1 DE200410024364 DE102004024364A DE102004024364A1 DE 102004024364 A1 DE102004024364 A1 DE 102004024364A1 DE 200410024364 DE200410024364 DE 200410024364 DE 102004024364 A DE102004024364 A DE 102004024364A DE 102004024364 A1 DE102004024364 A1 DE 102004024364A1
- Authority
- DE
- Germany
- Prior art keywords
- polymer
- solvent
- solution
- synthesis
- microdroplet
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 229920000642 polymer Polymers 0.000 title claims abstract description 72
- 238000000034 method Methods 0.000 title claims abstract description 54
- 230000008569 process Effects 0.000 title claims abstract description 11
- 239000002904 solvent Substances 0.000 claims abstract description 57
- 230000015572 biosynthetic process Effects 0.000 claims abstract description 40
- 238000003786 synthesis reaction Methods 0.000 claims abstract description 40
- 239000007787 solid Substances 0.000 claims abstract description 12
- 238000000018 DNA microarray Methods 0.000 claims abstract description 7
- 108091034117 Oligonucleotide Proteins 0.000 claims description 26
- 229920001940 conductive polymer Polymers 0.000 claims description 19
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 claims description 16
- 239000000758 substrate Substances 0.000 claims description 16
- 239000002773 nucleotide Substances 0.000 claims description 14
- 125000003729 nucleotide group Chemical group 0.000 claims description 14
- 239000002253 acid Substances 0.000 claims description 9
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 9
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 9
- 150000001720 carbohydrates Chemical class 0.000 claims description 7
- 235000014633 carbohydrates Nutrition 0.000 claims description 7
- 239000002777 nucleoside Substances 0.000 claims description 7
- 239000000126 substance Substances 0.000 claims description 7
- 150000001413 amino acids Chemical class 0.000 claims description 6
- 238000011065 in-situ storage Methods 0.000 claims description 6
- 125000003835 nucleoside group Chemical group 0.000 claims description 5
- 108090000623 proteins and genes Proteins 0.000 claims description 5
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims description 4
- 108020004707 nucleic acids Proteins 0.000 claims description 4
- 102000039446 nucleic acids Human genes 0.000 claims description 4
- 150000007523 nucleic acids Chemical class 0.000 claims description 4
- 108010038807 Oligopeptides Proteins 0.000 claims description 3
- 102000015636 Oligopeptides Human genes 0.000 claims description 3
- 102000004169 proteins and genes Human genes 0.000 claims description 3
- 125000005907 alkyl ester group Chemical group 0.000 claims description 2
- 238000004891 communication Methods 0.000 claims description 2
- 239000000539 dimer Substances 0.000 claims description 2
- 239000013638 trimer Substances 0.000 claims description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 claims 2
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical compound OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 claims 2
- 239000004480 active ingredient Substances 0.000 claims 1
- 230000001404 mediated effect Effects 0.000 claims 1
- 239000007921 spray Substances 0.000 claims 1
- 229920001222 biopolymer Polymers 0.000 abstract description 3
- 230000002194 synthesizing effect Effects 0.000 abstract description 2
- 238000006243 chemical reaction Methods 0.000 description 28
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 27
- 239000000243 solution Substances 0.000 description 26
- -1 dimethoxytrityl Chemical group 0.000 description 21
- 125000006239 protecting group Chemical group 0.000 description 11
- 238000005859 coupling reaction Methods 0.000 description 10
- 150000008300 phosphoramidites Chemical class 0.000 description 10
- 125000000217 alkyl group Chemical group 0.000 description 9
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 8
- 239000000178 monomer Substances 0.000 description 8
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- 239000012190 activator Substances 0.000 description 6
- 238000009835 boiling Methods 0.000 description 6
- 125000000524 functional group Chemical group 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 229910052698 phosphorus Inorganic materials 0.000 description 6
- 239000011574 phosphorus Substances 0.000 description 6
- 239000007790 solid phase Substances 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 4
- 102000053602 DNA Human genes 0.000 description 4
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 4
- VAYOSLLFUXYJDT-RDTXWAMCSA-N Lysergic acid diethylamide Chemical compound C1=CC(C=2[C@H](N(C)C[C@@H](C=2)C(=O)N(CC)CC)C2)=C3C2=CNC3=C1 VAYOSLLFUXYJDT-RDTXWAMCSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 4
- 150000001875 compounds Chemical group 0.000 description 4
- 238000010276 construction Methods 0.000 description 4
- 230000008878 coupling Effects 0.000 description 4
- 238000010168 coupling process Methods 0.000 description 4
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 4
- 125000000623 heterocyclic group Chemical group 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 125000000304 alkynyl group Chemical group 0.000 description 3
- 239000000010 aprotic solvent Substances 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000004140 cleaning Methods 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 150000003833 nucleoside derivatives Chemical class 0.000 description 3
- 238000010647 peptide synthesis reaction Methods 0.000 description 3
- 238000006116 polymerization reaction Methods 0.000 description 3
- 229920001184 polypeptide Polymers 0.000 description 3
- 229920002477 rna polymer Polymers 0.000 description 3
- 125000006850 spacer group Chemical group 0.000 description 3
- 235000000346 sugar Nutrition 0.000 description 3
- 150000008163 sugars Chemical class 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000011593 sulfur Chemical group 0.000 description 3
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical group OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 2
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- GONFBOIJNUKKST-UHFFFAOYSA-N 5-ethylsulfanyl-2h-tetrazole Chemical compound CCSC=1N=NNN=1 GONFBOIJNUKKST-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- PYGXAGIECVVIOZ-UHFFFAOYSA-N Dibutyl decanedioate Chemical compound CCCCOC(=O)CCCCCCCCC(=O)OCCCC PYGXAGIECVVIOZ-UHFFFAOYSA-N 0.000 description 2
- NIQCNGHVCWTJSM-UHFFFAOYSA-N Dimethyl phthalate Chemical compound COC(=O)C1=CC=CC=C1C(=O)OC NIQCNGHVCWTJSM-UHFFFAOYSA-N 0.000 description 2
- 108091093037 Peptide nucleic acid Proteins 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 206010039509 Scab Diseases 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- PYMYPHUHKUWMLA-LMVFSUKVSA-N aldehydo-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 150000005829 chemical entities Chemical class 0.000 description 2
- 238000000970 chrono-amperometry Methods 0.000 description 2
- 238000004769 chrono-potentiometry Methods 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- DOIRQSBPFJWKBE-UHFFFAOYSA-N dibutyl phthalate Chemical compound CCCCOC(=O)C1=CC=CC=C1C(=O)OCCCC DOIRQSBPFJWKBE-UHFFFAOYSA-N 0.000 description 2
- JXTHNDFMNIQAHM-UHFFFAOYSA-N dichloroacetic acid Chemical compound OC(=O)C(Cl)Cl JXTHNDFMNIQAHM-UHFFFAOYSA-N 0.000 description 2
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 2
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 238000011066 ex-situ storage Methods 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 125000005647 linker group Chemical group 0.000 description 2
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 2
- 238000001668 nucleic acid synthesis Methods 0.000 description 2
- 238000002515 oligonucleotide synthesis Methods 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical class CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 150000003536 tetrazoles Chemical class 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- DKZRLCHWDNEKRH-UHFFFAOYSA-N 1-nonoxynonane Chemical compound CCCCCCCCCOCCCCCCCCC DKZRLCHWDNEKRH-UHFFFAOYSA-N 0.000 description 1
- CDAISMWEOUEBRE-LKPKBOIGSA-N 1D-chiro-inositol Chemical compound O[C@H]1[C@@H](O)[C@H](O)[C@H](O)[C@@H](O)[C@@H]1O CDAISMWEOUEBRE-LKPKBOIGSA-N 0.000 description 1
- SVUOLADPCWQTTE-UHFFFAOYSA-N 1h-1,2-benzodiazepine Chemical compound N1N=CC=CC2=CC=CC=C12 SVUOLADPCWQTTE-UHFFFAOYSA-N 0.000 description 1
- NTFJXDRAVMOYBG-UHFFFAOYSA-N 2-(2,2-dicyanoethoxymethyl)propanedinitrile Chemical compound N#CC(C#N)COCC(C#N)C#N NTFJXDRAVMOYBG-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- WDQJOZMFBREMOF-UHFFFAOYSA-N 2-hexylnaphthalen-1-ol Chemical compound C1=CC=CC2=C(O)C(CCCCCC)=CC=C21 WDQJOZMFBREMOF-UHFFFAOYSA-N 0.000 description 1
- DGMOBVGABMBZSB-UHFFFAOYSA-N 2-methylpropanoyl chloride Chemical compound CC(C)C(Cl)=O DGMOBVGABMBZSB-UHFFFAOYSA-N 0.000 description 1
- MTJGVAJYTOXFJH-UHFFFAOYSA-N 3-aminonaphthalene-1,5-disulfonic acid Chemical compound C1=CC=C(S(O)(=O)=O)C2=CC(N)=CC(S(O)(=O)=O)=C21 MTJGVAJYTOXFJH-UHFFFAOYSA-N 0.000 description 1
- ZBXNFTFKKOSPLD-UHFFFAOYSA-N 5-methylsulfanyl-2h-tetrazole Chemical compound CSC1=NN=NN1 ZBXNFTFKKOSPLD-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- JAPCXGFREZPNHK-UHFFFAOYSA-N 9-phenyl-9h-xanthene Chemical compound C12=CC=CC=C2OC2=CC=CC=C2C1C1=CC=CC=C1 JAPCXGFREZPNHK-UHFFFAOYSA-N 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- MQIUGAXCHLFZKX-UHFFFAOYSA-N Di-n-octyl phthalate Natural products CCCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC MQIUGAXCHLFZKX-UHFFFAOYSA-N 0.000 description 1
- ZVFDTKUVRCTHQE-UHFFFAOYSA-N Diisodecyl phthalate Chemical compound CC(C)CCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC(C)C ZVFDTKUVRCTHQE-UHFFFAOYSA-N 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 108010043958 Peptoids Proteins 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 229920002396 Polyurea Polymers 0.000 description 1
- 230000006819 RNA synthesis Effects 0.000 description 1
- 108091028664 Ribonucleotide Chemical group 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- BTGRAWJCKBQKAO-UHFFFAOYSA-N adiponitrile Chemical compound N#CCCCCC#N BTGRAWJCKBQKAO-UHFFFAOYSA-N 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 125000002723 alicyclic group Chemical group 0.000 description 1
- 125000005233 alkylalcohol group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003276 anti-hypertensive effect Effects 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 239000003699 antiulcer agent Substances 0.000 description 1
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 1
- 238000003491 array Methods 0.000 description 1
- 229910052785 arsenic Inorganic materials 0.000 description 1
- RQNWIZPPADIBDY-UHFFFAOYSA-N arsenic atom Chemical group [As] RQNWIZPPADIBDY-UHFFFAOYSA-N 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 229940049706 benzodiazepine Drugs 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 description 1
- 229940073608 benzyl chloride Drugs 0.000 description 1
- ZYIPABRMGYNQKB-UHFFFAOYSA-N benzyl n-(5-phenyl-1,3-oxazol-2-yl)carbamate Chemical compound C=1C=CC=CC=1COC(=O)NC(O1)=NC=C1C1=CC=CC=C1 ZYIPABRMGYNQKB-UHFFFAOYSA-N 0.000 description 1
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 125000000319 biphenyl-4-yl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- BJQHLKABXJIVAM-UHFFFAOYSA-N bis(2-ethylhexyl) phthalate Chemical compound CCCCC(CC)COC(=O)C1=CC=CC=C1C(=O)OCC(CC)CCCC BJQHLKABXJIVAM-UHFFFAOYSA-N 0.000 description 1
- SNAMIIGIIUQQSP-UHFFFAOYSA-N bis(6-methylheptyl) hydrogen phosphate Chemical compound CC(C)CCCCCOP(O)(=O)OCCCCCC(C)C SNAMIIGIIUQQSP-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ULBTUVJTXULMLP-UHFFFAOYSA-N butyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCCC ULBTUVJTXULMLP-UHFFFAOYSA-N 0.000 description 1
- YTIVTFGABIZHHX-UHFFFAOYSA-N butynedioic acid Chemical compound OC(=O)C#CC(O)=O YTIVTFGABIZHHX-UHFFFAOYSA-N 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000002144 chemical decomposition reaction Methods 0.000 description 1
- 239000007806 chemical reaction intermediate Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- DMSZORWOGDLWGN-UHFFFAOYSA-N ctk1a3526 Chemical compound NP(N)(N)=O DMSZORWOGDLWGN-UHFFFAOYSA-N 0.000 description 1
- 238000002484 cyclic voltammetry Methods 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- KZPXREABEBSAQM-UHFFFAOYSA-N cyclopenta-1,3-diene;nickel(2+) Chemical compound [Ni+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KZPXREABEBSAQM-UHFFFAOYSA-N 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 239000005549 deoxyribonucleoside Substances 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 239000012351 deprotecting agent Substances 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 229960005215 dichloroacetic acid Drugs 0.000 description 1
- FBSAITBEAPNWJG-UHFFFAOYSA-N dimethyl phthalate Natural products CC(=O)OC1=CC=CC=C1OC(C)=O FBSAITBEAPNWJG-UHFFFAOYSA-N 0.000 description 1
- 229960001826 dimethylphthalate Drugs 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- QYDYPVFESGNLHU-UHFFFAOYSA-N elaidic acid methyl ester Natural products CCCCCCCCC=CCCCCCCCC(=O)OC QYDYPVFESGNLHU-UHFFFAOYSA-N 0.000 description 1
- 238000002848 electrochemical method Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 150000002243 furanoses Chemical class 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 150000002333 glycines Chemical class 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- VUNCWTMEJYMOOR-UHFFFAOYSA-N hexachlorocyclopentadiene Chemical compound ClC1=C(Cl)C(Cl)(Cl)C(Cl)=C1Cl VUNCWTMEJYMOOR-UHFFFAOYSA-N 0.000 description 1
- YUMSFAHUVUYTKV-UHFFFAOYSA-N hexadecylcyclopentane Chemical compound CCCCCCCCCCCCCCCCC1CCCC1 YUMSFAHUVUYTKV-UHFFFAOYSA-N 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- QYDYPVFESGNLHU-KHPPLWFESA-N methyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC QYDYPVFESGNLHU-KHPPLWFESA-N 0.000 description 1
- 229940073769 methyl oleate Drugs 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- BDJRBEYXGGNYIS-UHFFFAOYSA-N nonanedioic acid Chemical compound OC(=O)CCCCCCCC(O)=O BDJRBEYXGGNYIS-UHFFFAOYSA-N 0.000 description 1
- 238000002966 oligonucleotide array Methods 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Chemical group 0.000 description 1
- JIRNEODMTPGRGV-UHFFFAOYSA-N pentadecylbenzene Chemical compound CCCCCCCCCCCCCCCC1=CC=CC=C1 JIRNEODMTPGRGV-UHFFFAOYSA-N 0.000 description 1
- HENJCAULAAJZLZ-UHFFFAOYSA-N pentadecylcyclopentane Chemical compound CCCCCCCCCCCCCCCC1CCCC1 HENJCAULAAJZLZ-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 238000005731 phosphitylation reaction Methods 0.000 description 1
- SXADIBFZNXBEGI-UHFFFAOYSA-N phosphoramidous acid Chemical group NP(O)O SXADIBFZNXBEGI-UHFFFAOYSA-N 0.000 description 1
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 1
- 125000002743 phosphorus functional group Chemical group 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- XXRYFVCIMARHRS-UHFFFAOYSA-N propan-2-yl n-dimethoxyphosphorylcarbamate Chemical compound COP(=O)(OC)NC(=O)OC(C)C XXRYFVCIMARHRS-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 239000002342 ribonucleoside Substances 0.000 description 1
- 239000002336 ribonucleotide Chemical group 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 150000003291 riboses Chemical class 0.000 description 1
- FZHCFNGSGGGXEH-UHFFFAOYSA-N ruthenocene Chemical compound [Ru+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 FZHCFNGSGGGXEH-UHFFFAOYSA-N 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- JZALLXAUNPOCEU-UHFFFAOYSA-N tetradecylbenzene Chemical compound CCCCCCCCCCCCCCC1=CC=CC=C1 JZALLXAUNPOCEU-UHFFFAOYSA-N 0.000 description 1
- NQAVPKIJZCHUNS-UHFFFAOYSA-N tetradecylcyclohexane Chemical compound CCCCCCCCCCCCCCC1CCCCC1 NQAVPKIJZCHUNS-UHFFFAOYSA-N 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- DKRUJKKWJGNYQN-UHFFFAOYSA-N tridecylcyclohexane Chemical compound CCCCCCCCCCCCCC1CCCCC1 DKRUJKKWJGNYQN-UHFFFAOYSA-N 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 229940035893 uracil Drugs 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 238000007704 wet chemistry method Methods 0.000 description 1
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/0046—Sequential or parallel reactions, e.g. for the synthesis of polypeptides or polynucleotides; Apparatus and devices for combinatorial chemistry or for making molecular arrays
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00277—Apparatus
- B01J2219/00351—Means for dispensing and evacuation of reagents
- B01J2219/00378—Piezoelectric or ink jet dispensers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00277—Apparatus
- B01J2219/00497—Features relating to the solid phase supports
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00277—Apparatus
- B01J2219/00497—Features relating to the solid phase supports
- B01J2219/00527—Sheets
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00585—Parallel processes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00596—Solid-phase processes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00605—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00605—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports
- B01J2219/0061—The surface being organic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00605—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports
- B01J2219/00612—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports the surface being inorganic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00605—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports
- B01J2219/00614—Delimitation of the attachment areas
- B01J2219/00617—Delimitation of the attachment areas by chemical means
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00605—Making arrays on substantially continuous surfaces the compounds being directly bound or immobilised to solid supports
- B01J2219/00632—Introduction of reactive groups to the surface
- B01J2219/00637—Introduction of reactive groups to the surface by coating it with another layer
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00653—Making arrays on substantially continuous surfaces the compounds being bound to electrodes embedded in or on the solid supports
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00659—Two-dimensional arrays
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00675—In-situ synthesis on the substrate
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/0068—Means for controlling the apparatus of the process
- B01J2219/00686—Automatic
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00709—Type of synthesis
- B01J2219/00713—Electrochemical synthesis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00718—Type of compounds synthesised
- B01J2219/0072—Organic compounds
- B01J2219/00722—Nucleotides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00718—Type of compounds synthesised
- B01J2219/0072—Organic compounds
- B01J2219/00725—Peptides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00718—Type of compounds synthesised
- B01J2219/0072—Organic compounds
- B01J2219/00731—Saccharides
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/06—Libraries containing nucleotides or polynucleotides, or derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/10—Libraries containing peptides or polypeptides, or derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/12—Libraries containing saccharides or polysaccharides, or derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B50/00—Methods of creating libraries, e.g. combinatorial synthesis
- C40B50/14—Solid phase synthesis, i.e. wherein one or more library building blocks are bound to a solid support during library creation; Particular methods of cleavage from the solid support
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B60/00—Apparatus specially adapted for use in combinatorial chemistry or with libraries
- C40B60/14—Apparatus specially adapted for use in combinatorial chemistry or with libraries for creating libraries
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Nanotechnology (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Composite Materials (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Saccharide Compounds (AREA)
- Application Of Or Painting With Fluid Materials (AREA)
Abstract
Die vorliegende Erfindung betrifft ein Verfahren zur schrittweisen Synthese von Polymeren, insbesondere Biopolymeren, auf einer festen Trägeroberfläche, umfassend die Schritte des Bereitstellens einer festen Trägeroberfläche mit einer Bindungsstelle, Aufbringen eines ersten Mikrotröpfchens einer Lösung, umfassend einen ersten Polymerbaustein auf die Bindungsstelle zur Befestigung des ersten Polymerbausteins auf der Bindungsstelle und des Anwendens der modifizierten Bindungsstelle des vorhergehenden Schrittes eines zweiten Mikrotröpfchens einer Lösung, umfassend den gleichen oder einen verschiedenen Polymerbaustein, worin die Lösung ein Lösungsmittel mit einer Viskosität von mehr als 7 mPaÈs enthält. Die vorliegende Erfindung betrifft weiter einen Biochip, der durch ein Verfahren gemäß der Erfindung erhalten wird und in einem weiteren Aspekt ein automatisiertes Polymersynthesesystem zur Synthese einer Polymerkette auf einem festen Träger durch sequenzielle Zugabe von Polymerbausteinen, umfassend einen Tintenstrahldruckkopf, eine Behandlungszelle, Transportmittel und einen Behälter, umfassend eine Lösung und einen Polymerbaustein.The present invention relates to a process for the stepwise synthesis of polymers, in particular biopolymers, on a solid support surface, comprising the steps of providing a solid support surface with a binding site, applying a first microdroplet of a solution comprising a first polymer building block to the attachment site for attachment of the first Polymer building blocks on the binding site and applying the modified binding site of the previous step a second microdroplet of a solution comprising the same or a different polymer building block, wherein the solution contains a solvent having a viscosity of more than 7 mPaÈs. The present invention further relates to a biochip obtained by a method according to the invention and in another aspect to an automated polymer synthesis system for synthesizing a polymer chain on a solid support by sequential addition of polymer building blocks comprising an ink jet printhead, a treatment cell, transport means and a container comprising a solution and a polymer building block.
Description
Die vorliegende Erfindung betrifft ein Verfahren für die schrittweise Synthese von Polymeren auf einer festen Trägeroberfläche und die Verwendung eines derartigen Verfahrens zur Herstellung von Biochips. Weiterhin betrifft die vorliegende Erfindung ein System zur automatisierten Polymersynthese zur Synthese eines Polymers einer Polymerkette auf einem festen Träger durch sequenzielle Zugabe von Polymerbaustein an spezifische Orte auf der Oberfläche eines Substrats.The The present invention relates to a process for the stepwise synthesis of polymers on a solid support surface and the use of a such process for the production of biochips. Furthermore the present invention is a system for automated polymer synthesis for the synthesis of a polymer of a polymer chain on a solid carrier by sequential addition of polymer building block to specific locations on the surface a substrate.
Heutzutage nimmt der Bedarf an Systemen, die für die Synthese von Polymeren geeignet sind, insbesondere auf dem Gebiet der Herstellung von Oligonukleotiden oder Polypeptidpolymeren zu. Verschiedene synthetische Methodologien wurden für diesen Zweck entwickelt. Die zwei wichtigsten synthetischen Methodologien sind i) die schrittweise photochemische Synthese und ii) die klassische chemische Synthese derartiger Polymere. Beide Methodologien umfassen die Umwandlung von wenigstens einer funktionellen Gruppe von Bausteinen des gewünschten Polymers durch aufeinanderfolgendes Umsetzen dieser Bausteine zur schrittweisen Bildung des gewünschten Polymers.nowadays the need for systems responsible for the synthesis of polymers decreases are suitable, in particular in the field of production of oligonucleotides or polypeptide polymers. Various synthetic methodologies were for developed this purpose. The two most important synthetic methodologies i) the stepwise photochemical synthesis and ii) the classical one chemical synthesis of such polymers. Both methodologies include the conversion of at least one functional group of building blocks of the desired Polymers by successively converting these building blocks to step by step Education of the desired Polymer.
Die funktionellen Gruppen (üblicherweise endständige OH-Gruppen) der Bausteine werden zeitweise durch intermediäre Schutzgruppen geschützt, die nach Behandlung mit geeigneten Reagenzien entfernt werden. Diese Schutzgruppen sind üblicherweise entweder säurelabile Gruppen wie beispielsweise DMT (Dimethoxytrityl) und seine Derivate oder photolabile Gruppen wie beispielsweise NPPOC (2-Nitrophenyl-propyloxycarbonyl).The functional groups (usually terminal OH groups) the Building blocks are temporarily protected by intermediate protecting groups, the after treatment with suitable reagents. These Protecting groups are common either acid labile Groups such as DMT (dimethoxytrityl) and its derivatives or photolabile groups such as NPPOC (2-nitrophenyl-propyloxycarbonyl).
Es wurden viele Anstrengungen unternommen, um diese Schutzgruppen zu variieren. Beispielsweise beschreibt das US-Patent Nr. 6,222,030 die Verwendung von carbonatgeschützten Hydroxylgruppen in einem 3'-5' Oligonukleotid.It Many efforts have been made to protect these groups vary. For example, U.S. Patent No. 6,222,030 describes the use of carbonate-protected Hydroxyl groups in a 3'-5 'oligonucleotide.
Die Polymere wie Oligonukleotide oder Polypeptide sind zur Herstellung sogenannter Biochips oder Genchips nützlich, wobei die Polymere auf ein Array eines üblicherweise planaren Substrats befestigt sind. Die Polymere werden auf das Substrat entweder durch direkte in situ oder nach einer ex situ Synthese aufgetragen. Die in situ Synthese auf dem Substrat ist oftmals bevorzugt, da es den leichten Aufbau verschiedener oder identischer Polymerketten direkt auf dem entsprechenden Substrat ohne aufwändige Zwischenschritte nach der ex situ Synthese der Polymere vor der Befestigung der Polymerketten auf dem Substrat erfordert.The Polymers such as oligonucleotides or polypeptides are for production so-called biochips or gene chips, the polymers on an array of one usually planar substrate are attached. The polymers are on the substrate either by direct in situ or after an ex situ synthesis applied. In situ synthesis on the substrate is often preferred as it is the easy construction of different or identical polymer chains directly on the corresponding substrate without elaborate intermediate steps after the ex situ synthesis of the polymers prior to attachment of the polymer chains on the substrate requires.
Jedoch haben die meisten der bekannten synthetischen Methodologien für die photochemische in situ Synthese, ernsthafte Nachteile aufgrund eines erforderlichen ausgefeilten Aufbaus um die Reaktionsstelle genau zu definieren, wo die Polymerkette aufgebaut werden muss. Dies umfasst u.a. die Verwendung einer Mehrzahl von Masken oder einer Mehrzahl von Mikrospiegeln für die genaue Auswahl der Reaktionsstelle.however have most of the known synthetic methodologies for the photochemical In situ synthesis, serious disadvantages due to a required sophisticated construction to precisely define the reaction site, where the polymer chain has to be built up. This includes i.a. the Use of a plurality of masks or a plurality of micromirrors for the exact selection of the reaction site.
Ebenso hat die chemische synthetische Methodologie unter Verwendung der klassischen "Nasschemie" ernsthafte Nachteile in Bezug auf die in diesen Reaktionen verwendeten Lösungsmittel, die eine Anzahl von Erfordernissen erfüllen müssen, damit sie beispielsweise für Tintenstrahldruckköpfe geeignet sind.As well has the chemical synthetic methodology using the classic "wet chemistry" serious disadvantages with respect to the solvents used in these reactions, which must meet a number of requirements, for example suitable for inkjet printheads are.
Diese Anforderungen sind beispielsweise
- a) ausreichende Löslichkeit der Mischung Base/Aktivator
- b) Unterstützen der Kopplungsreaktion zwischen beispielsweise einem Phosphoramiditderivat und dem Träger/Nukleosideinheit (Lösungsmitteleffekt, polar und aprotisch zur gleichen Zeit)
- c) einen hohen Siedepunkt zur Vermeidung einer Verflüchtigung des Tröpfchens auf der Oberfläche
- d) sie dürfen nicht zu teuer sein und müssen eine geringe Toxizität aufweisen
- e) sie sollen wasserfrei sein
- f) sie sollen chemisch kompatibel mit der Mischung Base/Aktivator sein
- g) und sollen durch einen Tintenstrahldruckkopf aufspritzbar sein, insbesondere im Hinblick auf die Dimension der Düsen des Druckkopfes.
- a) sufficient solubility of the mixture base / activator
- b) Assisting the coupling reaction between, for example, a phosphoramidite derivative and the carrier / nucleoside unit (solvent effect, polar and aprotic at the same time)
- c) a high boiling point to avoid volatilization of the droplet on the surface
- d) they must not be too expensive and have low toxicity
- e) they should be anhydrous
- f) they should be chemically compatible with the mixture base / activator
- g) and are to be sprayed by an ink jet print head, in particular with regard to the dimension of the nozzles of the print head.
Typischerweise wird Acetonitril insbesondere in der Oligonukleotidsynthese aufgrund seiner hohen Polarität verwendet, was die Lösung des entsprechenden Reaktionspartners ermöglicht. Weiterhin ist eine typische Reaktion bei der Synthese von Oligonukleotiden die Kopplungsreaktion zwischen einem Phosphoramidit und einer Hydroxygruppe, beispielsweise einer alkoholischen Hydroxygruppe der 5'-OH- oder 3'-OH der Desoxyriboseeinheit. Diese Reaktion erfordert ein polares und ein aprotisches Lösungsmittel wie Acetonitril.typically, acetonitrile is due in particular in the oligonucleotide synthesis its high polarity used what the solution the corresponding reaction partner allows. Furthermore, one is typical reaction in the synthesis of oligonucleotides the coupling reaction between a phosphoramidite and a hydroxy group, for example an alcoholic hydroxy group of the 5'-OH or 3'-OH of the deoxyribose unit. This reaction requires a polar and an aprotic solvent such as acetonitrile.
Jedoch weist Acetonitril verschiedene Nachteile auf, wie beispielsweise seinen geringen Siedepunkt (81°C), seine Inkompatibilität mit vielen Materialien, die in kommerziell erhältlichen Tintenstrahldruckköpfen etc. verwendet werden wie Klebstoffen, Plastik. Aufgrund seines geringen Siedepunkts, verdampfen die Acetonitriltropfen quasi sofort nachdem sie aus dem Druckkopf versprüht wurden.however For example, acetonitrile has several disadvantages, such as its low boiling point (81 ° C), its incompatibility with many materials used in commercially available inkjet printheads etc. be used as adhesives, plastics. Because of its low Boiling point, the acetonitrile drops evaporate almost immediately after sprayed it out of the printhead were.
Deswegen war es ein Ziel im Stand der Technik, Acetonitril durch andere Lösungsmittel zu ersetzen, die besser die vorstehend erwähnten Anforderungen erfüllen.therefore It was an objective in the art to use acetonitrile with other solvents which better meet the above-mentioned requirements.
Das US-Patent Nr. 6,028,129 schlägt Ethylen- und Propylencarbonatderivate zur Verwendung bei der automatisierten Synthese von zweidimensionalen Oligonukleotidarrays vor. Diese Verbindungen werden dazu verwendet, um die gut bekannten Nachteile, die durch die Verwendung von Acetonitril entstehen zu überwinden.The U.S. Patent No. 6,028,129 Ethylene and propylene carbonate derivatives for use in automated Synthesis of two-dimensional oligonucleotide arrays. These connections are used to overcome the well-known disadvantages caused by to overcome the use of acetonitrile.
Die Offenbarung des US-Patents Nr. 6,177,558 betrifft ebenfalls den Ersatz von Acetonitril insbesondere im Hinblick auf das Problem der Verdampfung. Demgemäß, umfasst die Reagenslösung die auf die Oberfläche aufgespritzt wird, beispielsweise auf einem Biochip, weitere Reaktanden, die in wenigstens Lösungsmittel mit einem relativ hohen Siedepunkt enthalten sind, welches vorzugsweise ein polares, aprotisches Lösungsmittel ist, das einen Siedepunkt von wenigstens ungefähr 140°C aufweist und ausgewählt ist aus der Gruppe bestehend aus Dinitrilen, Glymen, Diglyme und deren Derivaten.The Revelation of US Pat. No. 6,177,558 also relates to Replacement of acetonitrile especially with regard to the problem the evaporation. Accordingly, includes the reagent solution the on the surface sprayed on, for example on a biochip, further reactants, in at least solvent are contained with a relatively high boiling point, which preferably a polar, aprotic solvent which has a boiling point of at least about 140 ° C and is selected from the group consisting of dinitriles, glymes, diglyme and theirs Derivatives.
Weiterhin schlägt das US-Patent 6,419,883 die Verwendung von Mikrotröpfchen einer Lösung vor, die ein Lösungsmittel umfasst, das einen Siedepunkt von 150°C oder höher aufweist, eine Oberflächenspannung von 30 dyne/cm oder höher und eine Viskosität von 0,015 g/cm/sek. Die Lösungsmittel, die in diesem Patent offenbart sind, sind N-Methyl-2-pyrolidon, Propylencarbonat oder γ-Butyrolacton.Farther beats U.S. Patent 6,419,883 discloses the use of microdroplets of a solution ago, which is a solvent which has a boiling point of 150 ° C or higher, a surface tension of 30 dyne / cm or higher and a viscosity of 0.015 g / cm / sec. The solvents, disclosed in this patent are N-methyl-2-pyrolidone, Propylene carbonate or γ-butyrolactone.
Jedoch sind die vorgeschlagenen Lösungsmittel aus dem Stand der Technik nicht immer mit Tintenstrahldruckköpfen mit einer Vielzahl von Düsen kompatibel, insbesondere wenn die Dimensionen der Düsen klein sind und Mikrotröpfchen erzeugen können, die keine einheitliche Größe aufweisen. Daher ist es unmöglich, eine genaue Reaktionskontrolle aufrechtzuerhalten und ein Reaktionsprotokoll insbesondere mit Hinblick auf die Konzentration der Polymerbausteine.however are the proposed solvents from the prior art is not always with ink jet print heads with a variety of nozzles compatible, especially if the dimensions of the nozzles are small are and microdroplets can generate which do not have a uniform size. Therefore, it is impossible to maintain a precise reaction control and a reaction protocol in particular with regard to the concentration of the polymer building blocks.
Daher war das der Erfindung zugrundeliegende Problem die zur Verfügungstellung eines Lösungsmittels, das allgemein in einem Verfahren für die schrittweise Synthese von Polymeren anwendbar ist unabhängig von spezifischen Systemen, wie die Art des Tintenstrahldruckkopfs etc. zur Durchführung des Verfahrens.Therefore was the underlying problem of the invention, the provision a solvent, generally in a stepwise synthesis process of polymers is applicable regardless of specific systems, such as the type of ink jet print head, etc. for performing the Process.
Das der Erfindung zugrundeliegende Problem wird daher durch ein Verfahren zur schrittweisen Synthese von Polymeren auf einer festen Trägeroberfläche gelöst, umfassend die Schritte des:
- a) zur Verfügungstellens einer festen Trägeroberfläche, die eine chemische funktionalisierte Bindungsstelle aufweist
- b) Auftragen eines ersten Mikrotröpfchens einer Lösung umfassend einen ersten Polymerbaustein auf dieser Bindungsstelle zur Befestigung des ersten Polymerbausteins an die Bindungsstelle
- c) des Auftragens auf die modifizierte Bindungsstelle aus Schritt b) eines zweiten Mikrotröpfchens einer Lösung umfassend den gleichen oder einen verschiedenen Polymerbaustein
- a) providing a solid support surface having a chemical functionalized binding site
- b) applying a first microdroplet of a solution comprising a first polymer building block on this binding site for attaching the first polymer building block to the binding site
- c) applying to the modified binding site from step b) a second microdroplet of a solution comprising the same or a different polymer building block
In einer bevorzugten Ausführungsform hat das Lösungsmittel eine Viskosität im Bereich von 8 bis 30, vorzugsweise im Bereich von 8 bis 20 mPa·Sekunde. Weniger als 7 mPa·Sekunde sind nicht bevorzugt, weil in diesem Fall das Lösungsmittel nicht mit einem Tintenstrahldruckkopf verwendet werden kann, der Düsendurchmesser aufweist, die so klein sind wie nachstehend angegeben. Mehr als 30 mPa·Sekunde resultiert in einer zu viskosen Flüssigkeit, die nicht mit üblichen Tintenstrahldruckköpfen verwendet werden kann. Weiterhin wird die Reakti vität auf der Stelle, wo das Lösungsmitteltröpfchen aufgetragen wird, aufgrund der zunehmenden Viskosität des Lösungsmittels abnehmen. Es wurde überraschenderweise gefunden, dass der ausgewählte Bereich der Viskosität die Verwendung des Lösungsmittels in einem Verfahren gemäß der Erfindung erlaubt, ohne dass das Lösungsmittel in größerem Ausmaß verdampft. Daher wird das Verkrusten der Düsen etc. der verwendeten Vorrichtung zum Aufsprühen der Lösung, die die polymeren Bausteine enthält (ebenfalls als "Synthons" bezeichnet) oder das sogenannte "Blooming" des Tröpfchens, sobald es auf der Oberfläche des Substrats aufgetragen ist, erfolgreich vermieden.In a preferred embodiment has the solvent a viscosity in the range of 8 to 30, preferably in the range of 8 to 20 mPa · second. Less than 7 mPa · second are not preferred because in this case the solvent is not with a Inkjet printhead can be used, the nozzle diameter which are as small as indicated below. More than 30 mPa · second results in too viscous liquid that is not usual Inkjet printheads can be used. Furthermore, the reactivity on the Place where the solvent droplet applied will decrease due to the increasing viscosity of the solvent. It was surprisingly found that the selected Range of viscosity the use of the solvent in a method according to the invention, without the solvent evaporated to a greater extent. Therefore, the crusting of the nozzles, etc. the device used for spraying the solution containing the polymeric building blocks contains (also referred to as "synthons") or the so-called "blooming" of the droplet, once it's on the surface of the substrate is successfully avoided.
Die Bildung von Krusten um die Düsen aufgrund der Verdampfung des Lösungsmittels vermindert nicht nur die Konzentration des Reagens in dem Tröpfchen und damit beeinflusst es auch das Ergebnis der Kopplungsreaktion und die Bildung von unerwünschten Nebenprodukten auf der Oberfläche. Außerdem resultiert eine Verkrustung in einem chemischen Abbau des Materials, das die Kruste bildet, das sogar die nachfolgenden Tröpfchen kontaminieren kann. Die meisten der im der Stand der Technik verwendeten Lösungsmittel erfordern ein regelmäßiges Säubern der Vorrichtung, insbesondere der Düsen des Tintenstrahldruckkopfes. Die vorliegende Erfindung ermöglicht ebenfalls beträchtlich verlängerte Reinigungsintervalle, d.h. die Reinigung wird zwei- oder selbst dreimal weniger oft als im Stand der Technik durchgeführt.The Formation of crusts around the nozzles due to the evaporation of the solvent not only decreases the concentration of the reagent in the droplet and It also influences the result of the coupling reaction and the formation of unwanted By-products on the surface. Furthermore crusting results in chemical degradation of the material, that forms the crust that even contaminate the subsequent droplets can. Most of the solvents used in the prior art require a regular cleaning of the Device, in particular the nozzles of the inkjet printhead. The present invention also allows considerably extended Cleaning intervals, i. the cleaning will be two or even three times less often than in the prior art.
Weiterhin ist es bevorzugt, dass das Lösungsmittel eine Oberflächenspannung von mehr als 26 bis 32 dyne/cm aufweist. Diese erhöhte Oberflächenspannung in Kombination mit der ausgewählten Viskosität gemäß der Erfindung des Lösungsmittels vermeidet effizient das "Blooming" eines Tröpfchens der Lösung, die auf die Oberfläche aufgebracht wurde.Farther it is preferred that the solvent a surface tension of more than 26 to 32 dyne / cm. This increased surface tension in combination with the selected one viscosity according to the invention of the solvent efficiently avoids the "blooming" of a droplet the solution, the on the surface was applied.
Spezifische bevorzugte Beispiele eines Lösungsmittels gemäß der Erfindung umfassen, sind aber nicht beschränkt auf Methyloleat, 1-Phenyltetradecan, 1-Cyclopentylpentadecan, 1-Cyclohexyltridecan, Hexylnaphthol, Dinonylether, Dibutylsebazat, 1-Phenylpentadecan, 1-Cyclopentylhexadecan, Hexachlorocyclopentadien, Biscyanoethylether, 1-Cyclohexyltetradecan, Benzylbenzoat, N-Butylstearat, Diethylphthalat, 3-Methylsulfolan, 2-Pyrrolidon, 1-Decylnaphthol, Dimethylphthalat, Dibutylphathalat, Diisooctylphathalt, Dioctylphthalat, Diisodecylphthalat.specific preferred examples of a solvent according to the invention include, but are not limited to on methyl oleate, 1-phenyl tetradecane, 1-cyclopentyl pentadecane, 1-cyclohexyl tridecane, Hexylnaphthol, dinonyl ether, dibutyl sebacate, 1-phenylpentadecane, 1-cyclopentylhexadecane, hexachlorocyclopentadiene, biscyanoethyl ether, 1-cyclohexyltetradecane, benzyl benzoate, N-butyl stearate, diethyl phthalate, 3-methyl, 2-pyrrolidone, 1-decylnaphthol, dimethyl phthalate, dibutyl phthalate, Diisooctyl phosphate, dioctyl phthalate, diisodecyl phthalate.
Diese Verbindungen stellen die erforderliche Polarität bereit, die in einen ersten Aspekt nötig ist zum Lösen der meisten polymeren Bausteine und in einem zweiten Aspekt zur Unterstützung der Kopplungsreaktion, die dazu tendieren, polare und aprotische Lösungsmittel aufgrund der Reaktionszwischenprodukte in den Kopplungsreaktionen zu bevorzugen.These Connections provide the required polarity, which in a first Aspect necessary is to solve most polymeric building blocks and in a second aspect to support the coupling reaction, which tend to be polar and aprotic solvent due to the reaction intermediates in the coupling reactions to prefer.
In einer besonders vorteilhaften Ausführungsform der Erfindung umfasst das Lösungsmittel oder ist eine chemische Verbindung, die eine derivatisierte Carboxylgruppe enthält. Es wurde überraschenderweise gefunden, dass insbesondere Polycarbonsäurederivate, d.h. Verbindungen die zwei oder mehr derivatisierte Carboxylfunktionen umfassen und die die vorstehend erwähnten physikalischen Eigenschaften aufweisen, besonders geeignet sind und ein bevorzugtes Lösungsmittel insbesondere auf dem Gebiet der Synthese von Biopolymeren darstellen. Der Ausdruck "derivatisierte Carbonsäure oder Funktion" bedeutet, dass das saure Proton (oder in anderen Worten die saure OH-Einheit) der COOH-Gruppen durch eine nichtprotische Einheit substituiert wurde. Beispiele derartiger Derivate umfassen sind aber nicht beschränkt auf Alkyl, Aryl, Aralkylester und dergleichen.In a particularly advantageous embodiment of the invention the solvent or is a chemical compound that is a derivatized carboxyl group contains. It has surprisingly been found in particular polycarboxylic acid derivatives, i.e. Compounds the two or more derivatized carboxylic functions and which include the aforementioned physical properties have, are particularly suitable and a preferred solvent especially in the field of synthesis of biopolymers. The term "derivatized carboxylic acid or function "means that the acid proton (or in other words the acidic OH unit) the COOH groups substituted by a non-protic moiety has been. Examples of such derivatives include, but are not limited to Alkyl, aryl, aralkyl esters and the like.
Die carboxylischen Funktionen sind normalerweise an ein Gerüst befestigt, das beispielsweise ein aromatisches, heteroaromatisches, Alkyl, Alkenyl oder Alkynylgerüst oder dergleichen ist.The carboxylic functions are usually attached to a scaffold, for example, an aromatic, heteroaromatic, alkyl, Alkenyl or alkynyl skeleton or the like.
Die
am meisten bevorzugten chemischen Verbindungen weisen die Formel
R1, R2 sind
gleich oder verschieden und stellen eine lineare oder verzweigte
C1-C10 Alkyl, Alkenyl-
oder Alkynylgruppe dar, B ist eine lineare oder verzweigte C1-C10-Alkyl-, Alkenyl-,
Alkynylgruppe, ein substituierter oder unsubstituierter aromatischer,
heteroaromatischer, alicyclischer oder heterocyclischer Ring.The most preferred chemical compounds have the formula
R 1 , R 2 are the same or different and represent a linear or branched C 1 -C 10 alkyl, alkenyl or alkynyl group, B is a linear or branched C 1 -C 10 alkyl, alkenyl, alkynyl, a substituted or unsubstituted aromatic, heteroaromatic, alicyclic or heterocyclic ring.
Bevorzugte Beispiele sind bevorzugt ausgewählt aus der Gruppe bestehend aus Alkyldiestern der Oxalsäure, Malonsäure, Succinsäure, Glutarsäure, Adipinsäure, Suberinsäure, Acelainsäure, Sebacinsäure, Maleinsäure, Fumarsäure, Muconsäure, Acetylendicarbonsäure, Phthalsäure, Isophthalsäure, Terephthalsäure.preferred Examples are preferably selected from the group consisting of alkyl diesters of oxalic, malonic, succinic, glutaric, adipic, suberic, azelaic, sebacic, maleic, fumaric, muconic, acetylenedicarboxylic, phthalic, isophthalic, terephthalic.
Am meisten bevorzugt sind die Alkylester der polycarboxylischen, am meisten bevorzugt der Dicarbonsäuren, worin die Alkylgruppe bevorzugt eine verzweigte lineare C1-C10-Alkyl, bevorzugt eine C1-C6-Alkylgruppe, insbesondere Methyl, Ethyl, Propyl, Butyl, Pentyl ist.Most preferred are the alkyl esters of the polycarboxylic, most preferably the dicarboxylic acids wherein the alkyl group is preferably a branched linear C 1 -C 10 alkyl, preferably a C 1 -C 6 alkyl group, especially methyl, ethyl, propyl, butyl, pentyl is.
In einer anderen bevorzugten Ausführungsform wird nicht nur ein Lösungsmittel verwendet, sondern die Lösung enthält ein zweites Lösungsmittel (das erste Lösungsmittel ist das Carbonsäurederivat). Die Verwendung eines zweiten Lösungsmittels er höht die Gesamtausbeute der Reaktion, insbesondere für die einzelnen Kopplungsschritte. Die Verwendung eines zweiten Lösungsmittels ermöglicht weiterhin das Feintuning der Viskosität, die Oberflächenspannung und der Polarität und der aprotischen Eigenschaften der Lösung. Weiterhin erhöht das zweite Lösungsmittel die Löslichkeit der Phosphorverbindung, vorzugsweise ein Phosphoramidit und/oder des Aktivators in der Reaktionsmischung.In another preferred embodiment not only one solvent is used, but the solution contains a second solvent (the first solvent is the carboxylic acid derivative). The use of a second solvent he heightens the overall yield of the reaction, especially for the individual NEN coupling steps. The use of a second solvent further allows fine tuning of the viscosity, surface tension, and polarity and aprotic properties of the solution. Furthermore, the second solvent increases the solubility of the phosphorus compound, preferably a phosphoramidite and / or the activator in the reaction mixture.
In dieser Hinsicht ist es für den Erfolg der Erfindung wichtig, dass die Menge des zweiten Lösungsmittels in der Lösung niedriger ist als die Menge des ersten Lösungsmittels. Wenn das zweite Lösungsmittel im Überschuss vorliegen würde, würde die Art dieses zweiten Lösungsmittels vorherrschen. Vorzugsweise liegt daher die Menge des zweiten Lösungsmittels im Bereich von 1 bis 30 Vol.-%, vorzugsweise 5 bis 30 Vol.-%, am meisten bevorzugt von 10 bis 30 Vol.-% in Bezug auf das Gesamtvolumen der Lösung. Weiterhin ist es bevorzugt, dass das zweite Lösungsmittel eine Viskosität von weniger als 6 mPa·Sekunde aufweist. Bevorzugte Lösungsmittel sind beispielsweise Glyme wie Triglyme, Diglyme, Adiponitril, Acetonitril und dergleichen.In In that sense it is for the success of the invention important that the amount of the second solvent in the solution is lower than the amount of the first solvent. If the second solvent in excess would be present would the Type of this second solvent prevalence. Preferably, therefore, the amount of the second solvent in the range of 1 to 30% by volume, preferably 5 to 30% by volume, on most preferably from 10 to 30% by volume with respect to the total volume the solution. Furthermore, it is preferable that the second solvent has a viscosity of less as 6 mPa · second having. Preferred solvents For example, glymes such as triglyme, diglyme, adiponitrile, acetonitrile and the same.
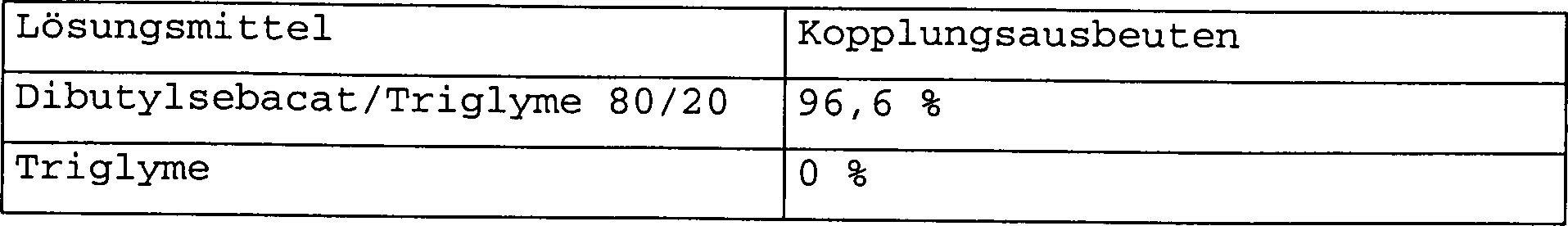
Tabelle 1 zeigt in einem Fluss des zweiten Lösungsmittels auf die Kopplungsausbeute für jeden Reaktionsschritt bei der schrittweisen Synthese von Oligonukleotiden.table Figure 1 shows in a flow of the second solvent on the coupling yield for each Reaction step in the stepwise synthesis of oligonucleotides.
Wenn das zweite Lösungsmittel allein verwendet wird (Triglyme) findet keine Reaktion statt, aber die Lösung bestehend aus einer Mischung aus 80 Vol.-% Dibutylsebacat und 20 Vol.-% Triglyme erbringt hohe Reaktionsausbeuten.If the second solvent is used alone (triglyme), no reaction takes place, however the solution consisting of a mixture of 80% by volume dibutyl sebacate and 20% Vol .-% triglyme yields high reaction yields.
Die relative Viskosität μrel = μzweites Lösungsmittel/μerstes Lösungsmittel der Lösung ist vorzugsweise niedriger als 0,95. Es wurde überraschenderweise gefunden, dass der Wert für die relative Viskosität von niedriger als 0,95 zu einer Erhöhung der Reaktionsgeschwindigkeit im Bereich von einem Faktor 2 bis 10, vorzugsweise 3 bis 8 und zu einer Zunahme in der Ausbeute (bis zu 15 bis 20 % höhere Ausbeute) von jedem der aufeinanderfolgenden Kopplungsschritte führt.The relative viscosity μ rel = μ second solvent / μ first solvent of the solution is preferably lower than 0.95. It has surprisingly been found that the value of the relative viscosity of less than 0.95 leads to an increase in the reaction rate in the range of a factor of 2 to 10, preferably 3 to 8 and an increase in the yield (up to 15 to 20%). higher yield) of each of the consecutive coupling steps.
Der Begriff "Substrat" umfasst jedes geeignete Substrat wie Glas, Siliciumdioxid, Siliconmaterialien, aber ebenso Polymermaterialien wie Poylethylen, Polypropylen, Polystyrol und dergleichen, die funktionalisiert werden können oder nicht und die entsprechenden Verbundmaterialien.Of the The term "substrate" includes any suitable one Substrate such as glass, silica, silicone materials, but as well Polymer materials such as polyethylene, polypropylene, polystyrene and the like, which may or may not be functionalized and the corresponding ones Composite materials.
In einer besonders bevorzugten Ausführungsform der Erfindung wird das Substrat mit einem Array metallischer Elektroden versehen. Vor der Durchführung des Schrittes a) wird ein elektrisch leitfähiges Polymer an die metallischen Elektroden aufgebracht, worin das elektrisch leitfähige Polymer gleich oder verschieden ist für jede Elektrode des Arrays.In a particularly preferred embodiment The invention relates to the substrate with an array of metallic electrodes Mistake. Before the implementation of step a) is an electrically conductive polymer to the metallic Electrodes applied, wherein the electrically conductive polymer the same or different is for every electrode of the array.
Es ist besonders bevorzugt, dass das elektrisch leitende Polymer in situ auf der metallischen Elektrode synthetisiert wird. Die Synthese des elektrisch leitenden Polymers ist in einer besonders bevorzugten Ausführungsform eine elektrochemische Synthese. In einer Ausführungsform der Erfindung, sind polymere Bausteine deshalb außerdem neben biomolekulare Bausteine wie Nukleotide, Oligonukleotide, Aminosäuren, Oligopeptide, Kohlenhydrate ebenfalls vorzugsweise elektropolymerisierbare Monomere oder Makromere (Oligomere), Polymere, etc. Es ist weiter bevorzugt, dass die vorstehend erwähnten Biomoleküle schon chemisch an die elektropolymerisierbaren Monomere oder Oligomere oder selbst Polymere gebunden sind bevor sie auf die Oberfläche aufgebracht werden. Die Verfahren zur elektrochemischen Polymerisation, die üblicherweise für die Herstellung von ECPs (elektrisch leitfähige Polymere) verwendet werden, wie eine Polymerisation auf den eingestellten Strom (Chronopotentiometrie) oder bei einem eingestellten Potenzial (Chronoamperometrie) sind ebenfalls im Verfahren gemäß der Erfindung anwendbar.It is particularly preferred that the electrically conductive polymer in situ is synthesized on the metallic electrode. The synthesis of the electrically conductive polymer is in a particularly preferred embodiment an electrochemical synthesis. In one embodiment of the invention polymeric building blocks therefore also in addition to biomolecular building blocks such as nucleotides, oligonucleotides, amino acids, oligopeptides, Carbohydrates also preferably electropolymerizable monomers or macromers (oligomers), polymers, etc. It is further preferred that the above mentioned biomolecules already chemically to the electropolymerisierbaren monomers or oligomers or even polymers are bound before being applied to the surface become. The methods of electrochemical polymerization, usually for the Production of ECPs (electrically conductive polymers) can be used like a polymerization on the set current (chronopotentiometry) or at a set potential (chronoamperometry) are also in the process according to the invention applicable.
Die Qualität der Ablagerung des elektrisch leitfähigen Polymers kann durch die Wahl der experimentellen Bedingungen kontrolliert werden: die Konzentration des Monomers, beispielsweise Pyrrol, THF und dergleichen, des Verhältnisses von Oligonukleotid-Monomer/Monomers, die Art des Lösungsmittels, die verwendete elektrochemische Methode (cyclische Voltametrie, Chronoamperometrie oder Chronopotentiometrie). Das erhaltene Copolymer kann daher verschiedene Qualitäten der Porosität und der Zugänglichkeit in Abhängigkeit von gewünschten nachfolgenden Verwendung haben und wenn die Menge des gebundenen Oligonukleotids modifiziert werden kann.The quality the deposition of the electrically conductive polymer can by the Choice of experimental conditions to be controlled: the concentration of the monomer, for example pyrrole, THF and the like, of the ratio of oligonucleotide monomer / monomers, the type of solvent, the electrochemical method used (cyclic voltammetry, Chronoamperometry or chronopotentiometry). The obtained copolymer can therefore different qualities the porosity and accessibility dependent on of desired have subsequent use and if the amount of bound Oligonucleotide can be modified.
Durch das Messen des während der Reaktion gelieferten Stroms, macht es die Elektrode effektiv möglich, den Fortschritt der Polymerisationsreaktion zu verfolgen (beispielsweise über die Dicke des gebildeten Polymers) oder den Fortschritt der nachfolgenden Reaktion, die auf dem Copolymer durchgeführt werden.By measuring the while In response to the reaction current, it makes the electrode effective possible, to follow the progress of the polymerization reaction (for example, via the Thickness of the polymer formed) or the progress of the following Reaction carried out on the copolymer.
Gemäß einer bevorzugten Ausführungsform des erfindungsgemäßen Verfahrens in einem oder anderen seiner Varianten, umfasst es weiterhin die Verlängerung einer Oligonukleotidkette über mehrere sukzessive Schritte, wobei jeder dieser Schritte aus dem Binden eines oder mehrerer Nukleotide oder Oligonukleotide besteht.According to one preferred embodiment the method according to the invention in one or other of its variants, it still includes the renewal an oligonucleotide chain via several successive steps, each of these steps being taken from the Binding of one or more nucleotides or oligonucleotides.
Die Verlängerung des Oligonukleotids wird auf der Oberfläche des Trägers durch Zusammenstellen der geschützten Monomere durchgeführt, beginnend mit wenigstens einem Nukleotid oder Oligonukleotid des auf der Oberfläche des elektrisch leitfähigen Polymers gebunden ist. Die Standardverfahren zur chemischen Synthese von Nukleinsäuren können zur Durchführung dieser Ausführungsform verwendet werden.The renewal of the oligonucleotide is deposited on the surface of the support by assembling the protected Monomers performed, starting with at least one nucleotide or oligonucleotide of the surface of the electrically conductive Polymers is bound. The standard methods for chemical synthesis of nucleic acids can to carry out this embodiment be used.
Um eine gute Adhäsion von weiteren Polymerbausteinen auf dem elektrisch leitenden Polymer zu ermöglichen, ist es bevorzugt, dass das elektrisch leitende Polymer eine chemische Funktionalität aufweist, die die Befestigung eines Polymerbausteins ermöglicht. Der Begriff "chemische Funktionalität" bezeichnet eine chemisch reaktive Gruppe (maskiert oder unmaskiert) wie beispielsweise eine Amino-, Acetyl-, Carboxyl-, Hydroxylgruppe etc.Around a good adhesion of further polymer building blocks on the electrically conductive polymer to enable it is preferred that the electrically conductive polymer is a chemical functionality has, which allows the attachment of a polymer block. The term "chemical Functionality "refers to a chemical reactive group (masked or unmasked) such as a Amino, acetyl, carboxyl, hydroxyl, etc.
Vorzugsweise werden die Polymerbausteine aus der Gruppe ausgewählt, umfassend Nukleoside, Nukleotide, Oligonukleotide, Aminosäuren, Oligopeptide, Kohlenhydrate, Dimere und Trimere davon. Diese Auswahl erleichtert die Herstellung von sogenannten Bio- oder Genchips beträchtlich. In einer weiter bevorzugten Ausführungsform der Erfindung wird ein Redoxpaar wie organometallische Komplexe wie Ferrocen, Nickelocen, Ruthenocen in das Polymer vor, während oder nach der elektrochemischen Synthese des Polymers eingebaut. Die Einführung eines Redoxpaars vergrößert die elektrisch leitenden Eigenschaften des elektrisch leitfähigen Polymers.Preferably the polymer building blocks are selected from the group comprising Nucleosides, nucleotides, oligonucleotides, amino acids, oligopeptides, carbohydrates, Dimers and trimers thereof. This selection facilitates the production of so-called bio or gene chips considerably. In a further preferred embodiment The invention provides a redox couple such as organometallic complexes such as ferrocene, nickelocene, ruthenocene in the polymer before, during or incorporated after the electrochemical synthesis of the polymer. The introduction a redox couple enlarges the electrically conductive properties of the electrically conductive polymer.
Das der Erfindung zugrundeliegende Problem wird weiter durch einen Biochip gelöst, der ein Substrat, eine Elektrode umfasst, wobei an die Elektrode elektrisch leitendes Polymer befestigt ist und an das leitende Polymer ein Biomolekül gebunden ist, das ausgewählt ist aus Nukleinsäuren und ihren Derivaten, Peptiden, Proteinen und Kohlenhydraten, erhältlich durch ein Verfahren gemäß der Erfindung.The The problem underlying the invention is further by a biochip solved, which comprises a substrate, an electrode, wherein the electrode electrically conductive polymer is attached and to the conductive polymer a biomolecule is bound, the selected is from nucleic acids and their derivatives, peptides, proteins and carbohydrates, obtainable by a method according to the invention.
In noch einem weiteren Aspekt wird das Problem der Erfindung durch ein automatisiertes Polymersynthesesystem zur Synthese einer Polymerkette auf einem festen Träger durch sequenzielle Zugabe von Polymerbausteinen gelöst, umfassend die folgenden Elemente:
- a) einen Tintenstrahldruckkopf umfassend eine Mehrzahl von Düsen zum Aufsprühen eines Mikrotröpfchens auf einen ausgewählten Platz auf dem Träger
- b) eine Behandlungseinheit zur Behandlung des Trägers auf dem ein Mikrotröpfchen abgelagert wurde mit einem Reagens
- c) Transportmittel zu Bewegung des Trägers benachbart zum Druckkopf und/oder zur Behandlungseinheit
- d) ein Gefäß umfassend eine Lösung enthaltend einen Polymerbaustein
- a) an ink jet printhead comprising a plurality of nozzles for spraying a microdroplet to a selected location on the support
- b) a treatment unit for treating the carrier on which a microdroplet has been deposited with a reagent
- c) transport means for movement of the carrier adjacent to the print head and / or the treatment unit
- d) a vessel comprising a solution containing a polymer building block
In einer bevorzugten Ausführungsform ist jede einzelne Düse einzeln ansteuerbar, was damit die Konstruktion einer Mehrzahl von verschiedenen Polymerketten oder einer vorher definierten Anzahl enthaltend verschiedene Bausteine erlaubt, bevor die Reaktion gestartet wird.In a preferred embodiment is every single nozzle individually controllable, what with the construction of a plurality of different polymer chains or a pre-defined number containing different building blocks allowed before the reaction started becomes.
Vorzugsweise ist der Abstand der Düsen im Bereich von 0,02 bis 0,005 μm, mehr bevorzugt im Bereich von 0,015 bis 0,1 μm. Diese enge Anordnung erleichtert es die Mikrotröpfchen in komplexen Strukturen auf der Oberfläche des Biochips aufzubringen.Preferably is the distance of the nozzles in the range of 0.02 to 0.005 μm, more preferably in the range of 0.015 to 0.1 microns. This close arrangement facilitates it's the microdroplets in complex structures on the surface of the biochip.
Der Durchmesser der Düsen ist vorzugsweise im Bereich von 30 bis 70 Mikrons, um kleine Mikrotröpfchen mit einer einheitlichen Größe und Volumen zu erzeugen. Das Volumen eines Mikrotröpfchens liegt bevorzugt im Bereich von 60 bis 100 Pikoliter zur Kontrolle der Menge des aufgetragenen Polymerbausteins.Of the Diameter of the nozzles is preferably in the range of 30 to 70 microns, with small microdroplets a uniform size and volume to create. The volume of a microdroplet is preferably in the Range of 60 to 100 picoliters to control the amount of applied Polymer block.
In einer weiteren bevorzugten Ausführungsform umfasst der Tintenstrahlkopf einen Tank in Verbindung mit jeder Düse. Dies vereinfacht den Aufbau des Systems, weil im Stand der Technik jede Düse mit einem Reservoir verbunden sein musste, und damit kompliziertere Kontrollmittel erforderte.In another preferred embodiment, the ink jet head includes a tank in communication with each nozzle. This simplifies the construction of the system, because in the prior art each nozzle with a Reservoir had to be connected, and thus required more complicated means of control.
Definitionen und Abkürzungendefinitions and abbreviations
Polymerbaustein: Der Begriff Polymerbaustein (alternativ auch als Synton bezeichnet) bezeichnet eine chemische Einheit, die innerhalb des Endpolymers umfasst ist. Die chemische Einheit kann daher funktionelle Gruppen vor dem Einbau in das Endpolymer umfassen. Nicht einschränkende Beispiele geeigneter polymerer Bausteine entsprechend der Erfindung sind substituierte und nichtsubstituierte Phosphoramidite, Mono-, Oligo- und Polynukleotide, Aminosäuren, Peptide, Zucker (Furanosen, Ribosen, etc.), Biotin, Avidin, Streptavidin, Antikörper und dergleichen.Polymer: The term polymer building block (alternatively also called Synton) denotes a chemical entity within the final polymer is included. The chemical entity can therefore be functional groups prior to incorporation into the final polymer. Non-limiting examples suitable polymeric building blocks according to the invention are substituted and unsubstituted phosphoramidites, mono-, oligo and polynucleotides, Amino acids, Peptides, sugars (furanoses, riboses, etc.), biotin, avidin, streptavidin, antibodies and like.
Mikrotröpfchen: ein Mikrotröpfchen ist eine getrennte und diskrete Einheit vorzugsweise mit einem Volumen von ungefähr 100 bis 200 Pikolitern, am meisten bevorzugt zwischen 5 und 70 Pikolitern.Microdroplets: a microdroplet is a separate and discrete unit, preferably with one volume of about 100 to 200 picoliters, most preferably between 5 and 70 picoliters.
Es versteht sich, dass der Begriff "Lösung" wie er hier verwendet wird, das Lösungsmittel per se bezeichnet und das gelöste Produkt oder mehrere gelöste Produkte.It It is understood that the term "solution" as used here becomes, the solvent designated per se and the solved Product or more dissolved Products.
Die Mikrotröpfchen bilden, wenn sie auf der Oberfläche reagieren, sogenannte Spots oder Mikropunkte. Die Arrays der erhaltenen Polymere gemäß der vorliegenden Erfindung sind in diesen Mikropunkte oder Spots angeordnet, die getrennte und diskrete Einheiten sind. Der Durchmesser jedes Mikrodots kann größer als 1000 μm sein, aber liegt typischerweise im Bereich von 5 μm bis 8 μm, vorzugsweise von 10 μm bis ungefähr 500 μm und am meisten bevorzugt von 20 bis 200 μm.The microdroplets form when on the surface react, so-called spots or microdots. The arrays of the obtained Polymers according to the present invention Invention are arranged in these microdots or spots, the separate and discrete units. The diameter of each microdot can be bigger than 1000 μm but is typically in the range of 5 microns to 8 microns, preferably of 10 μm until about 500 μm and most preferably from 20 to 200 microns.
Der Abstand zwischen den einzelnen Mikropunkte ist typischerweise ungefähr 1 μm bis ungefähr 500 μm, bevorzugt von 20 μm bis ungefähr 400 μm. Im Allgemeinen sollte der Abstand zwischen den Mikropunkte vorzugsweise im Bereich der entsprechenden Stelle der Mikrotröpfchen sein, um die Verwendung von benachbarten Spots zu vermeiden.Of the Distance between the individual microdots is typically about 1 μm to about 500 μm, preferably of 20 μm until about 400 μm. In general, the distance between the microdots should preferably be be in the area of the appropriate spot of the microdroplets to use to avoid from neighboring spots.
Die physische Trennung der Mikrospots wird durch die Reaktion der verbleibenden funktionellen Gruppen mit einer nicht entfernbaren Schutzgruppe, vorzugsweise umfassend Phosphor erreicht. Diese Gebiete bilden eine nicht reaktive Schutzoberfläche, die chemisch inert ist.The physical separation of the microspots is determined by the reaction of the remaining functional groups with a non-removable protecting group, preferably comprising phosphorus. These areas form one non-reactive protective surface, which is chemically inert.
Der Begriff "Biomolekül" oder "Biopolymer" wie er hier verwendet wird, bedeutet jegliches biologische Molekül in Form eines Polymers, wie Oligonukleotide, Aminosäuren, Peptide, Proteine, Kohlenhydrate, Antikörper etc. Der Begriff "Nukleosid" wie er hier verwendet wird, umfasst sowohl Desoxyribonukleoside und Ribonukleoside. Der Begriff "Oligonukleotid" bezieht sich auf ein Oligonukleotid, das Desoxyribonukleotid- oder Ribonukleotideinheiten aufweist.Of the Term "biomolecule" or "biopolymer" as used herein means any biological molecule in the form of a polymer, such as Oligonucleotides, amino acids, Peptides, proteins, carbohydrates, antibodies, etc. The term "nucleoside" as used herein includes both deoxyribonucleosides and ribonucleosides. Of the The term "oligonucleotide" refers to an oligonucleotide, the deoxyribonucleotide or ribonucleotide units having.
Geeignete Nukleotide, geeignet zur Synthese von Oligonukleotiden gemäß der vorliegenden Erfindung sind diejenigen Nukleotide, die aktive Phosphor enthaltende Gruppen enthalten, wie Phosphortriester, H-Phosphonat und Phosphoramiditgruppen.suitable Nucleotides suitable for the synthesis of oligonucleotides according to the present invention Invention are those nucleotides containing active phosphorus Groups such as phosphorus triester, H-phosphonate and phosphoramidite groups.
Der Begriff "Aktivator" bedeutet üblicherweise einen Katalysator, der im Falle eine Oligonukleotidsynthese ein Katalysator ist, der die Reaktion zwischen der 3'-Phosphoramiditgruppe eines Nukleosids und der Hydroxylgruppe des nächsten Nukleosids oder Nukleotids begünstigt. Dies kann 5-Methylthiotetrazol, Tetrazol oder 5-Ethylthiotetrazol, DCI oder Pyridiniumchlorid sein.Of the The term "activator" usually means a catalyst which in the case of oligonucleotide synthesis a Catalyst is the reaction between the 3'-phosphoramidite group of a nucleoside and the hydroxyl group of the next Nucleosides or nucleotides favored. This may be 5-methylthiotetrazole, tetrazole or 5-ethylthiotetrazole, DCI or pyridinium chloride.
Der Begriff "Alkyl" wie er hier verwendet wird, bezieht sich auf jede gesättigte gerade Kette, verzweigte oder cyclische Kohlenwasserstoffgruppe von 1 bis 1 Kohlenstoffatomen, wie Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, etc. Der Begriff Alkyl umfasst ebenfalls Cycloalkylgrupen wie Cyclopentyl, Cyclohexyl, Cycloheptyl etc.Of the Term "alkyl" as used herein is, refers to any saturated straight chain, branched or cyclic hydrocarbon group from 1 to 1 carbon atoms, such as methyl, ethyl, n-propyl, isopropyl, n-butyl, etc. The term alkyl also includes cycloalkyl groups such as cyclopentyl, Cyclohexyl, cycloheptyl, etc.
Der Begriff "Niederalkyl" bezeichnet eine Alkylgruppe von 1 bis 4 Kohlenstoffatomen und schließt Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, t-Butyl ein.Of the Term "lower alkyl" refers to a Alkyl group of 1 to 4 carbon atoms and includes methyl, Ethyl, n -propyl, isopropyl, n -butyl, isobutyl, t -butyl.
Der Ausdruck "heterocyclisch" bezieht sich auf jegliche fünfgliedrige oder sechsgliedrige monocyclische Strukturen oder auf eine achtgliedrige bis elfgliedrige bicyclische Struktur, die entweder ungesättigt oder gesättigt ist. Die Heterocyclen umfassen wenigstens ein Heteroatom ausgebildet aus der Gruppe bestehend aus Stickstoff, Sauerstoff, Schwefel, Phosphor, Arsen und dergleichen. Die Begriffe "Stickstoffheteroatome" und "Schwefelheteroatome" ebenso wie "Phosphorheteroatome" umfassen jegliche oxidierte Form von Stickstoff, Schwefel und Phosphor, ebenso wie die quaternisierte Form jeglichen basischen Stickstoffs. Beispiele von "heterocyclischen Verbindungen" umfassen Piperidinyl, Morpholinyl und Pyrrolidinyl.The term "heterocyclic" refers to any five-membered or six-membered monocyclic structure or an eight-membered to eleven-membered bicyclic structure which is either unsaturated or saturated. The heterocycles comprise at least one heteroatom selected from the group consisting of nitrogen, oxygen, sulfur, phosphorus, arsenic and the like. The terms "nitrogen heteroatoms" and "sulfur heteroatoms" as well as "phosphorus heteroatoms" include any oxidized form of nitrogen, sulfur and phosphorus as well as the quaternized form of any basic nitrogen. Examples of "heterocyclic compounds" include piperidinyl, morpholinyl and pyrrolidinyl.
Der Begriff "Oligonukleotid" wie er hier verwendet wird bezeichnet Polydesoxynukleotide (enthaltend 2-Desoxy-D-ribose), Polyribonukleotide (enthaltend D-Ribose) oder jede andere Art eines Polynukleotids, welches ein n-Glykosid einer Purin- der Pyridiminbase ist oder andere Polymere, die nicht nukleotidische Gerüste enthalten, vorausgesetzt dass die polymere Nukleobasen eine Konfiguration enthalten, die die Basenpaarung und Basenstapelung ermöglicht, wie es der Fall bei DNA und RNA ist.Of the Term "oligonucleotide" as used herein is called polydeoxynucleotides (containing 2-deoxy-D-ribose), Polyribonucleotides (containing D-ribose) or any other type of one Polynucleotide, which is an n-glycoside of a purine of pyridimine base or other polymers containing non-nucleotide scaffolds, provided that the polymeric nucleobases contain a configuration, which allows the base pairing and base stacking, as is the case with DNA and RNA is.
Mit dem Begriff "Schutzgruppe" wie er hier verwendet wird, wird eine Spezies bezeichnet, die verhindert, dass ein Segment eines Moleküls eine spezifische chemische Reaktion eingeht, aber die vom Molekül nach Vervollständigung dieser Reaktion entfernt werden kann. Dies ist im Kontrast zu einer "Cappinggruppe", die permanent an ein Segment oder eine funktionelle Gruppe eines Moleküls bindet oder an funktionelle Gruppen auf der Oberfläche des Substrats zur Verhinderung von jeglicher weiteren Umwandlung dieses Segments.With the term "protecting group" as used herein is called a species that prevents a segment of a molecule a specific chemical reaction is received, but that of the molecule after completion this reaction can be removed. This is in contrast to a "capping group" that is constantly on a segment or a functional group of a molecule binds or to functional groups on the surface of the substrate for prevention from any further transformation of this segment.
Das Verfahren der vorliegenden Erfindung kann ebenfalls dazu verwendet werden, Peptide durch Standardfestphasen-Peptidsynthesemethodologien zu synthetisieren.The Method of the present invention may also be used be synthesized peptides by standard solid-phase peptide synthesis methodologies.
Typischerweise wird eine Festphasenpeptidsynthese in C- zu N-Richtung durchgeführt. Daher sind Linkergruppen erforderlich, so dass die Spaltung am Ende des synthetischen Protokolls eine C-ständige Säure oder Amid erzeugt. In bevorzugten Ausführungsformen, wird ein Linker, der eine Aktive der Carboxylgruppe enthält an Aminogruppen gebunden, wie an die aktivierte Oberfläche eines Trägers gemäß der Erfindung binden können. Jeder der üblichen "temporären" Schutzgruppen, die üblicherweise in der Polypeptidsynthesechemie verwendet werden, sind geeignet zur Verwendung der vorliegenden Erfindung. Nicht einschränkende Beispiele unter diesen sind beispielsweise BOC (t-Butoxycarbonyl) und FMOC (Nα9-Fluorenylmethoxycarbonyl) Gruppen.Typically, solid phase peptide synthesis is performed in C to N direction. Therefore, linker groups are required such that cleavage at the end of the synthetic protocol produces a C-acid or amide. In preferred embodiments, a linker containing an active of the carboxyl group is attached to amino groups, as can bind to the activated surface of a carrier according to the invention. Any of the common "temporary" protecting groups commonly used in polypeptide synthesis chemistry are suitable for use with the present invention. Non-limiting examples of these are, for example, BOC (t-butoxycarbonyl) and FMOC (N α9 -fluorenylmethoxycarbonyl) groups.
Andere geeignete Aminoschutzgruppen umfassen sind aber nicht beschränkt auf 2-(4-Biphenyl)propyl[2]oxycarbonyl (BPOC), 1-1-1-Adamantyl-1-methylethoxycarbonyl (ADPOC) und dergleichen. Repräsentative Aktivatoren oder sogenannte in situ Kopplungs reagenzien geeignet zur Verwendung der vorliegenden Erfindung umfassen sind aber nicht beschränkt auf N,N'-Dicyclohexylcarbodiimid (DCC) und dergleichen. Ihre Verwendung ist in Verbindung mit der Verwendung weiterer Beschleuniger oder Additive wie 1-Hydroxybenzotriazol (HoBt), Benzotriazol-1-yl-oxy-tris-(Dimethylamino)phosphoniumhexafluorophosphat (BOP) und dergleichen bevorzugt.Other suitable amino protecting groups include, but are not limited to 2- (4-biphenyl) propyl [2] oxycarbonyl (BPOC), 1-1-1-adamantyl-1-methylethoxycarbonyl (ADPOC) and the same. Representative Activators or so-called in situ coupling reagents suitable but do not include for use in the present invention limited on N, N'-dicyclohexylcarbodiimide (DCC) and the like. Their use is in conjunction with the Use of other accelerators or additives such as 1-hydroxybenzotriazole (HoBt), benzotriazol-1-yl-oxy-tris (dimethylamino) phosphonium hexafluorophosphate (BOP) and the like are preferable.
Das erfindungsgemäße Verfahren wird vorzugsweise dazu verwendet, Desoxyribonukleinsäure (DNA) oder Ribonukleinsäure (RNA) Polymerspezies herzustellen (sogenannte Oligonukleotide), aber jede der bekannten Chemien für Festphasen-DNA oder RNA-Synthese umfassend Phosphittriester, Phosphoramiditsynthese und H-Phosphonatsynthese kann ebenfalls verwendet werden.The inventive method is preferably used to deoxyribonucleic acid (DNA) or ribonucleic acid (RNA) to produce polymer species (so-called oligonucleotides), but comprising any of the known chemistries for solid phase DNA or RNA synthesis Phosphite triester, phosphoramidite synthesis and H-phosphonate synthesis can also be used.
Prinzipiell ist das Verfahren der vorliegenden Erfindung nützlich zur Durchführung jeder iterativer Nukleinsäure-Synthesetechnik. In einer bevorzugten Ausführungsform der Erfindung werden Oligonukleotide durch die Phosphoramiditverfahren hergestellt. Für die Phosphoramiditsynthese gemäß der Erfindung werden die reaktiven Stellen auf der Oberfläche des Substrats manchmal mit einem weiteren Spacermolekül entsprechend aus dem Stand der Technik bekannter Verbindungen funktionalisiert. Die Einführung der Spacer kann vor dem Beginn der Erzeugung der Polymerkette stattfinden oder, beispielsweise nach Schritt a) des Verfahrens gemäß der Erfindung. Die Spacergruppen können ebenfalls an zuvor ausgewählte Stellen des Reaktionsträgers aufgetragen sein.in principle For example, the process of the present invention is useful for carrying out each iterative nucleic acid synthesis technique. In a preferred embodiment The invention provides oligonucleotides by the phosphoramidite method produced. For the phosphoramidite synthesis according to the invention sometimes the reactive sites on the surface of the substrate become with another spacer molecule functionalized according to known from the prior art compounds. The introduction the spacer can take place before the beginning of the production of the polymer chain or, for example, after step a) of the method according to the invention. The spacer groups can also to previously selected ones Make the reaction carrier be applied.
Typischerweise haben monomere Nukleotid- und Nukleosidpolymerbausteine (oder ebenso Syntons genannt) temporäre Schutzgruppen an entsprechenden Nukleobasen oder 2'-O-Stellungen.typically, have monomeric nucleotide and Nukleosidpolymerbausteine (or as well Called syntons) temporary Protecting groups at corresponding nucleobases or 2'-O-positions.
Festphasennukleinsäure-Synthesetechniken verwenden die sogenannten temporären und permanenten Schutzgruppen in analoger Weise wie Festphasenpeptidsynthese. Basenlabile Schutzgruppen werden verwendet, um exocyclische Aminogruppen der heterocyclischen Nukleobasen während der Synthese zu schützen. Diese Art des Schutzes wird üblicherweise durch Acylierung mit Acylierungreagenzien wie Benzylchlorid und Isobutrylchlorid erzielt. Säurelabile Schutzgruppen werden zum Schutz des Nukleotid 5'-Hydroxyls während der Synthese verwendet. Repräsentative Hydroxylschutzgruppen sind dem Durchschnittsfachmann bekannt. Diese umfassen sind aber nicht beschränkt auf Dimethoxytrityl, Monomethoxytrityl, Trityl und 9-Phenylxanthen (Pixyl) Gruppen. Dimethoxytrityl-(DNP)-Schutzgruppen sind weithin verwendet aufgrund der großen Säurelabilität, welche die effiziente Entfernung selbst durch sehr verdünnte Säuren ermöglicht.Solid phase nucleic acid synthesis techniques use the so-called temporary and permanent protecting groups in a manner analogous to solid phase peptide synthesis. Base-labile protecting groups are used to protect exocyclic amino groups of heterocyclic nucleobases during synthesis. This type of protection is usually achieved by acylation with acylating reagents such as benzyl chloride and isobutyryl chloride. Acid labile protecting groups are used to protect the nucleotide 5'-hydroxyl during synthesis. Representative hydroxyl protecting groups are known to one of ordinary skill in the art. These include but are not limited to dimethoxytrityl, monomethoxytrityl, trityl and 9-phe nylxanthene (pixyl) groups. Dimethoxytrityl (DNP) protecting groups are widely used because of the high acid lability which enables efficient removal even by very dilute acids.
Der erste Schritt des iterativen Kettenverlängerungszyklus gemäß der Phosphoramidittechnik ist die Entfernung der 5'-O-chutzgruppe (Entschützung) des ursprünglichen Monomers durch Eintauchen des Reaktionsträgers in eine Lösung des Entschützungsmittels. Dies ist gefolgt durch Zugabe eines Spülmittels. Geeignete Reagenzien zur Entschützung umfassen Lewissäuren wie ZnBa2, AlCl3, BF3 und TiCl4 in verschiedenen Lösungsmitteln wie Dichlormethan, Nitromethan, Tetrahydrofuran und gemischte Lösungsmittel wie Nitromethan und Niederalkylalkohole wie Methanol, Ethanol oder Mischungen davon. Protische Säuren, allein oder in Verbindung, wie Essigsäure, Dichloressigsäure, Trichloressigsäure, Trifluoressigsäure und Toluolsulfonsäure können ebenfalls verwendet werden. Die Ketten werden durch Zugabe und Reaktion aktivierter 5'-O-geschützter monomerer Syntone verlängert. Bei der Phosphoramidittechnik wird eine 5'-DMTA-Desoxynukleosid-3'-O-(N,N-diisopropylamino)-β-cyanoethylphosphit auf dem Reaktionsträger aufgebracht. Phosphoramidite zahlreicher Nukleoside sind kommerziell erhältlich.The first step of the iterative chain extension cycle according to the phosphoramide technique is the removal of the 5'-O-protecting group (deprotection) of the original monomer by immersing the reaction carrier in a solution of the deprotecting agent. This is followed by the addition of a rinse. Suitable reagents for deprotection include Lewis acids such as ZnBa 2 , AlCl 3 , BF 3 and TiCl 4 in various solvents such as dichloromethane, nitromethane, tetrahydrofuran and mixed solvents such as nitromethane and lower alkyl alcohols such as methanol, ethanol or mixtures thereof. Protic acids, alone or in combination, such as acetic acid, dichloroacetic acid, trichloroacetic acid, trifluoroacetic acid and toluenesulfonic acid can also be used. The chains are extended by addition and reaction of activated 5'-O-protected monomeric syntons. In the phosphoramidite technique, a 5'-DMTA-deoxynucleoside-3'-O- (N, N-diisopropylamino) -β-cyanoethyl phosphite is applied to the reaction support. Phosphoramidites of numerous nucleosides are commercially available.
Ein milder organischer Katalyator oder Aktivator, typischerweise Tetrazol, Ethylthiotetrazol der Metyhlthiotetrazol wird auf dem Reaktionsträger mit dem Phosphoramidit aufgebracht. Die Kopplungsreaktion wird durch die Zugabe eines Spüllösungsmittels, typischerweise trockenem Acetonitril gefolgt.One mild organic catalyst or activator, typically tetrazole, Ethylthiotetrazole of Metylthiotetrazole is on the reaction medium with applied to the phosphoramidite. The coupling reaction is through the addition of a rinse solvent, typically followed by dry acetonitrile.
Nach dem Spülen wird ein Cappingmittel zugegeben, beispielsweise durch Eintauchen des Substrats in einer Lösung des Cappingmittels auf den vorausgewählten Stellen des Reaktionsträgers zur Kappung von freien Hydroxylspezies, die aufgrund einer unvollständigen Reaktion der Phosphitmonomere verblieben (Capping 1). Im Kontext der vorliegenden Erfindung wird festgestellt, dass ein fundamentaler Unterschied zwischen dem Capping nicht reagierter reaktiver Gruppen auf der Oberfläche des festen Trägers existiert (ebenso als "Oberflächenkappung" oder Kappung 1 bezeichnet) und des Nukleotids/Nukleosids selber (Kappung 2). Beide Reaktionen werden als "Kappung" bezeichnet, jedoch sollten sie nicht miteinander verwechselt werden. Das Kappungsmittel für das "zweite Kappen", das typischerweise eine Lösung eines Säureanhydrids ist, fungiert ebenfalls zur Umkehrung der unerwünschten Phosphitylierung von Guanin O-6-Stellungen.To the rinse a capping agent is added, for example by immersion of the substrate in a solution of the capping agent on the preselected positions of the reaction carrier for Capping of free hydroxyl species due to an incomplete reaction the phosphite monomers remained (capping 1). In the context of the present Invention is found to be a fundamental difference between the capping of unreacted reactive groups on the surface of the solid support exists (also referred to as "surface capping" or capping 1) and the nucleotide / nucleoside itself (capping 2). Both reactions are referred to as "capping", however they should not be confused with each other. The capping agent for the "second caps," that typically a solution an acid anhydride also acts to reverse the unwanted phosphitylation of Guanin O-6 positions.
Die Oxidierung des entstehenden Phosphittriesters zum entsprechenden Phosphattriester kann durch Zugabe eines aus dem Stand der Technik bekannten Oxidationsmittels, das dafür geeignet ist, erreicht werden, wie etwa einer Lösung von alkalischen Iod in Wasser.The Oxidation of the resulting Phosphittriesters to the corresponding Phosphate triesters can be made by adding one from the prior art known oxidizing agent, which is suitable to be achieved, such as about a solution of alkaline iodine in water.
Einem Durchschnittsfachmann ist es klar, dass die Synthese der Oligonukleotide entweder in 3'-5'- oder 5'-3'-Richtun erfolgen kann.a One of ordinary skill in the art will appreciate that the synthesis of the oligonucleotides either in 3'-5 'or 5'-3' direction can.
Das erfindungsgemäße Verfahren kann bei der Synthese von Oligonukleotiden verwendet werden, die natürlich vorkommende Nukleobasen Avenin (A), Thymin (T), Guanin (G), Cytosin (C) und Uracil (U) haben, ebenso bei nicht natürlicherweise vorkommenden Nukleobasen. Nicht natürlicherweise vorkommende Nukleobasen sind molekulare Einheiten, die aus dem Stand der Technik bekannt sind, dass sie die Funktion von natürlich vorkommenden Nukleobasen in ihrer biologischen Rolle das Bestandteile von Nukleinsäuren nachahmen.The inventive method can be used in the synthesis of oligonucleotides, the naturally occurring nucleobases Avenin (A), Thymine (T), Guanine (G), Cytosine (C) and Uracil (U) have, as well not natural occurring nucleobases. Non-naturally occurring nucleobases are molecular entities known in the art are that they have the function of naturally occurring nucleobases imitate the components of nucleic acids in their biological role.
Oligonukleotide Spezies haben eine große Anzahl von Modifikationen für Nukleobasen, Zuckern oder Zwischenzuckerverknüpfungen und können gemäß den Verfahren der Erfindung hergestellt werden, das allgemein für die Synthese jeglicher Oligomere, die durch Festphasentechniken synthetisierbar sind, wie beispielsweise ebenfalls auf Polykohlenhydrate.oligonucleotides Species have a big one Number of modifications for Nucleobases, sugars or intersugar linkages and may be prepared according to the methods of the invention, generally for synthesis any oligomers synthesizable by solid-phase techniques are, for example, also on polycarbohydrates.
Beispielsweise kann das Verfahren gemäß der vorliegenden Erfindung bei der Synthese von S-Phosphordithioaten, Phosphorthioaten, etc. ebenso verwendet werden.For example can the method according to the present Invention in the synthesis of S-phosphorodithioates, phosphorothioates, etc. are also used.
Die erfindungsgemäß hergestellten Polymere können aus mehr als einer Art einer monomeren Untereinheit zusammengesetzt sein (beispielsweise Aminosäuren, Peptidnukleinsäuren, Nukleotide, Zucker (Kohlenhydrate) etc.) und können mehr als eine Art der Zwischenuntereinheitverknüpfung aufweisen. Illustrative Polymere, die gemäß den Verfahren der Erfindung hergestellt wurden, umfassen Peptide, Peptoide (n-alkylierte Glycine), Alphapolyester, Polythioamide, n-Hydroxyaminosäuren, Betaester, POlysulfonamide, n-Alkylatpolysulfonamide, Polyharnstoffe, Peptidnukleinsäuren, Nukleotide, Polysaccharide, Polycarbonate, Oligonukleotide, Oligonukleoside und dergleichen und chimäre Moleküle, die einen oder mehrere dieser Polymere zusammen als ein einziges Makromolekül aufweisen.The produced according to the invention Polymers can composed of more than one kind of a monomeric subunit be (for example, amino acids, Peptide nucleic acids, Nucleotides, sugars (carbohydrates) etc.) and can be more than one type of Between subunit link exhibit. Illustrative polymers made according to the methods of the invention include peptides, peptoids (n-alkylated glycines), Alpha polyesters, polythioamides, n-hydroxyamino acids, beta esters, polysulfonamides, n-alkylate polysulfonamides, polyureas, peptide nucleic acids, nucleotides, Polysaccharides, polycarbonates, oligonucleotides, oligonucleosides and the like and chimera molecules the one or more of these polymers together as a single macromolecule exhibit.
Bibliotheken monomerer Spezies können ebenfalls durch das Verfahren der Erfindung hergestellt werden. Diese umfassen Benzo diazepin-Bibliotheken und andere derartiger analoger Bibliotheken, umfassend aber beschränkt auf Anti-Hypertensinwirkstoffe, Anti-Magengeschwürwirkstoffe, Fungizide, Antibiotika, Entzündungshemmer, etc.libraries monomeric species can also be prepared by the process of the invention. These include benzodiazepine libraries and others analog libraries, but limited to anti-hypertensives, Anti-ulcer agents, Fungicides, antibiotics, anti-inflammatories, Etc.
Einem Durchschnittsfachmann ist es klar, dass der Umfang der Erfindung nicht nur die vorstehend erwähnten Merkmale umfasst, sondern auch Kombinationen davon und dass der Umfang der Erfindung ebenfalls jedes einzelnen Merkmals in Bezug zur der Erfindung, wie sie vorstehend beschrieben, umfasst.a One of ordinary skill in the art will appreciate that the scope of the invention not just the ones mentioned above Features includes, but also combinations thereof and that of Scope of the invention also with respect to each individual feature to the invention as described above comprises.
Claims (26)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE200410024364 DE102004024364A1 (en) | 2004-05-17 | 2004-05-17 | Process for the preparation of polymers |
| PCT/EP2005/005359 WO2005110593A2 (en) | 2004-05-17 | 2005-05-17 | Process and automated system for the synthesis of polymers |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE200410024364 DE102004024364A1 (en) | 2004-05-17 | 2004-05-17 | Process for the preparation of polymers |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102004024364A1 true DE102004024364A1 (en) | 2005-12-15 |
Family
ID=34968373
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE200410024364 Ceased DE102004024364A1 (en) | 2004-05-17 | 2004-05-17 | Process for the preparation of polymers |
Country Status (2)
| Country | Link |
|---|---|
| DE (1) | DE102004024364A1 (en) |
| WO (1) | WO2005110593A2 (en) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8580201B2 (en) | 2010-02-22 | 2013-11-12 | Oligoco, Inc. | Wicking-based reagent-solution draining in an automated system |
| WO2011102914A2 (en) * | 2010-02-22 | 2011-08-25 | Oligoco | Automated polymer-synthesis system |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69404657T2 (en) * | 1993-05-27 | 1997-12-18 | Protogene Laboratories, Inc., Palo Alto, Calif. | METHOD AND DEVICE FOR CARRYING OUT A VARIETY OF CHEMICAL REACTIONS ON A CARRIER SURFACE |
| US6384210B1 (en) * | 1997-03-20 | 2002-05-07 | University Of Washington | Solvent for biopolymer synthesis, solvent microdroplets and methods of use |
| DE10065278A1 (en) * | 2000-12-29 | 2002-07-11 | Aventis Res & Tech Gmbh & Co | Biochip accelerating macromolecule immobilization electrically, for detection or recognition, has electrically-conductive polymer coated onto electrodes |
| DE10308931A1 (en) * | 2003-02-28 | 2004-09-23 | Apibio Sas | System and method for the synthesis of polymers |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5156810A (en) * | 1989-06-15 | 1992-10-20 | Biocircuits Corporation | Biosensors employing electrical, optical and mechanical signals |
| US5874554A (en) * | 1996-12-13 | 1999-02-23 | Incyte Pharmaceuticals, Inc. | Methods and solvent vehicles for reagent delivery in oligonucleotide synthesis using automated pulse jetting devices |
| US6177558B1 (en) * | 1997-11-13 | 2001-01-23 | Protogene Laboratories, Inc. | Method and composition for chemical synthesis using high boiling point organic solvents to control evaporation |
| FR2781886B1 (en) * | 1998-07-31 | 2001-02-16 | Commissariat Energie Atomique | MULTIPLE POINT CHEMICAL OR BIOLOGICAL ANALYSIS MICROSYSTEM |
| WO2001017670A1 (en) * | 1999-09-09 | 2001-03-15 | Ben-Gurion University Of The Negev | Matrices of probes and their preparation |
| WO2001062377A2 (en) * | 2000-02-22 | 2001-08-30 | Genospectra, Inc. | Microarray fabrication techniques and apparatus |
| US20030059846A1 (en) * | 2001-08-17 | 2003-03-27 | Diamond Scott L. | Drug interaction assay chip |
| US20040152081A1 (en) * | 2003-01-31 | 2004-08-05 | Leproust Eric M. | Viscosity control during polynucleotide synthesis |
| DE10311315A1 (en) * | 2003-03-14 | 2004-09-30 | Apibio Sas | Method and device for the detection of biomolecules |
-
2004
- 2004-05-17 DE DE200410024364 patent/DE102004024364A1/en not_active Ceased
-
2005
- 2005-05-17 WO PCT/EP2005/005359 patent/WO2005110593A2/en not_active Ceased
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69404657T2 (en) * | 1993-05-27 | 1997-12-18 | Protogene Laboratories, Inc., Palo Alto, Calif. | METHOD AND DEVICE FOR CARRYING OUT A VARIETY OF CHEMICAL REACTIONS ON A CARRIER SURFACE |
| US6384210B1 (en) * | 1997-03-20 | 2002-05-07 | University Of Washington | Solvent for biopolymer synthesis, solvent microdroplets and methods of use |
| DE10065278A1 (en) * | 2000-12-29 | 2002-07-11 | Aventis Res & Tech Gmbh & Co | Biochip accelerating macromolecule immobilization electrically, for detection or recognition, has electrically-conductive polymer coated onto electrodes |
| DE10308931A1 (en) * | 2003-02-28 | 2004-09-23 | Apibio Sas | System and method for the synthesis of polymers |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2005110593A2 (en) | 2005-11-24 |
| WO2005110593A3 (en) | 2006-04-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69406119T2 (en) | NUCLEOTID / ELECTRONIC CONDUCTIVE POLYMER COPOLYMERISAT, METHOD FOR THE PRODUCTION THEREOF AND ITS USE | |
| US6337393B1 (en) | Method and composition for chemical synthesis on an open environment support surface using high boiling point organic solvents to control evaporation | |
| DE69632989T2 (en) | Template for the synthesis of combinatorial libraries in solution | |
| DE60013777T2 (en) | METHOD FOR PRODUCING ADDRESSED LIGAND MATRICES ON A SURFACE | |
| US6852850B2 (en) | Use of ionic liquids for fabrication of polynucleotide arrays | |
| DE60024181T2 (en) | Macromolecular arrays of polymer branches and processes for their preparation | |
| DE69430006T2 (en) | CONNECTIONS AND PROCEDURE | |
| DE10308931A1 (en) | System and method for the synthesis of polymers | |
| DE69621836T2 (en) | REUSABLE SOLID SUPPORT FOR OLIGONUCLEOTID SYNTHESIS, METHOD FOR PRODUCING IT AND METHOD FOR USE THEREOF | |
| EP1212338A2 (en) | Nucleoside derivatives with photo-unstable protective groups | |
| EP0983290B1 (en) | Method for producing polymers having nucleo-bases as side-groups | |
| DE102004024364A1 (en) | Process for the preparation of polymers | |
| EP1114186B1 (en) | Method for controlling quality in the construction of oligomer grids | |
| DE19853242B4 (en) | Derivatization of carrier surfaces | |
| DE69328693T2 (en) | BIOPOLYMERSYNTHESIS BY SURFACE-ACTIVATED ORGANIC POLYMERS | |
| DE602005001414T2 (en) | Photolabile protecting groups | |
| EP0728768B1 (en) | Phosphine groups linked to polymer side chains and their metal complexes | |
| WO2000053309A1 (en) | Method for photolytically deprotecting immobilized nucleoside derivatives, especially in the production of dna chips | |
| DE60200886T2 (en) | POLYMERS | |
| WO1997049714A1 (en) | Process for combining parallel oligonucleotide synthesis and preparation of oligomer chips | |
| WO2002016022A2 (en) | Novel strategie for synthesising polymers on surfaces | |
| DE10003631A1 (en) | Mask-free nucleoside derivatives with 3`-O-photolabile protecting groups of the o-nitrobenzyl type for the synthesis of "inverse" DNA chips | |
| DE10133779A1 (en) | Preparation of polynucleotides useful in gene technology involves reacting free 5'-hydroxy group of a oligonucleotide with a hydroxy group | |
| EP1079920A1 (en) | Device and method for producing a system of chain molecules on a support material | |
| DE10247790A1 (en) | Solid phase synthesis of labelled oligonucleotide conjugate, by nucleophilic substitution of labile protecting group on terminal hydroxy group with labeling reagent |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OP8 | Request for examination as to paragraph 44 patent law | ||
| 8131 | Rejection |