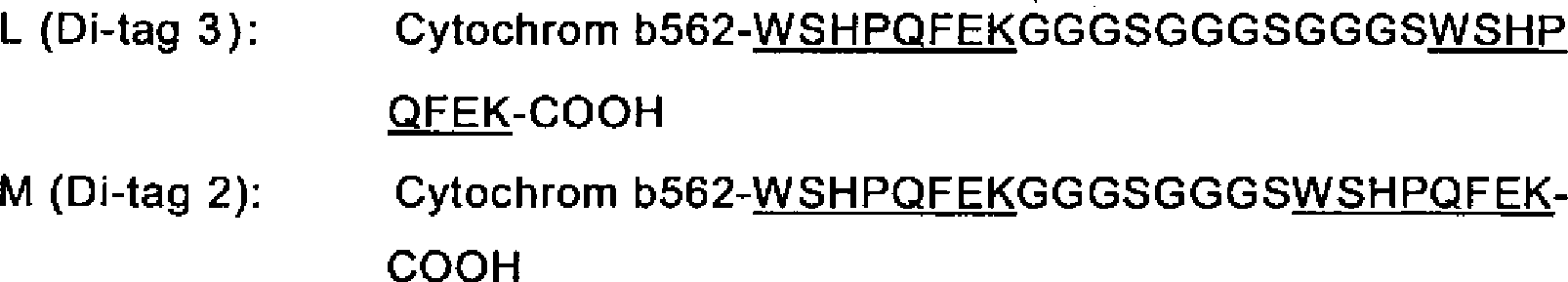DE10113776B4 - Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein - Google Patents
Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein Download PDFInfo
- Publication number
- DE10113776B4 DE10113776B4 DE10113776A DE10113776A DE10113776B4 DE 10113776 B4 DE10113776 B4 DE 10113776B4 DE 10113776 A DE10113776 A DE 10113776A DE 10113776 A DE10113776 A DE 10113776A DE 10113776 B4 DE10113776 B4 DE 10113776B4
- Authority
- DE
- Germany
- Prior art keywords
- streptavidin
- protein
- binding
- peptide
- fusion protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 108010090804 Streptavidin Proteins 0.000 title claims abstract description 134
- 230000027455 binding Effects 0.000 title claims abstract description 102
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 86
- 102000037865 fusion proteins Human genes 0.000 title claims description 56
- 108020001507 fusion proteins Proteins 0.000 title claims description 56
- 150000007523 nucleic acids Chemical class 0.000 title claims description 29
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 title claims description 21
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 title claims description 21
- 238000000034 method Methods 0.000 title claims description 18
- 239000013604 expression vector Substances 0.000 title claims description 10
- 108020004707 nucleic acids Proteins 0.000 title claims description 8
- 102000039446 nucleic acids Human genes 0.000 title claims description 8
- 230000004927 fusion Effects 0.000 title description 4
- 235000001014 amino acid Nutrition 0.000 claims abstract description 57
- 229940024606 amino acid Drugs 0.000 claims abstract description 54
- 150000001413 amino acids Chemical class 0.000 claims abstract description 41
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 claims abstract description 4
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 claims abstract description 3
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 claims abstract description 3
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims abstract description 3
- 229960001230 asparagine Drugs 0.000 claims abstract description 3
- 235000009582 asparagine Nutrition 0.000 claims abstract description 3
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 claims abstract description 3
- 229930182817 methionine Natural products 0.000 claims abstract description 3
- 108090000623 proteins and genes Proteins 0.000 claims description 62
- 102000004169 proteins and genes Human genes 0.000 claims description 60
- 235000018102 proteins Nutrition 0.000 claims description 52
- 108020003175 receptors Proteins 0.000 claims description 33
- 102000005962 receptors Human genes 0.000 claims description 33
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 24
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 claims description 22
- 238000010828 elution Methods 0.000 claims description 16
- 229960002685 biotin Drugs 0.000 claims description 11
- 235000020958 biotin Nutrition 0.000 claims description 11
- 239000011616 biotin Substances 0.000 claims description 11
- AUTOLBMXDDTRRT-JGVFFNPUSA-N (4R,5S)-dethiobiotin Chemical compound C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O AUTOLBMXDDTRRT-JGVFFNPUSA-N 0.000 claims description 7
- 102000002260 Alkaline Phosphatase Human genes 0.000 claims description 7
- 108020004774 Alkaline Phosphatase Proteins 0.000 claims description 7
- 238000003776 cleavage reaction Methods 0.000 claims description 7
- 230000007017 scission Effects 0.000 claims description 7
- 102000004190 Enzymes Human genes 0.000 claims description 6
- 108090000790 Enzymes Proteins 0.000 claims description 6
- 238000001042 affinity chromatography Methods 0.000 claims description 6
- 239000003446 ligand Substances 0.000 claims description 6
- AHFHSGZOVWHIQQ-UHFFFAOYSA-N 3-hydroxy-2-phenyldiazenylbenzoic acid Chemical compound OC(=O)C1=CC=CC(O)=C1N=NC1=CC=CC=C1 AHFHSGZOVWHIQQ-UHFFFAOYSA-N 0.000 claims description 4
- 108010028230 Trp-Ser- His-Pro-Gln-Phe-Glu-Lys Proteins 0.000 claims description 4
- 239000013592 cell lysate Substances 0.000 claims description 3
- 238000012217 deletion Methods 0.000 claims description 3
- 230000037430 deletion Effects 0.000 claims description 3
- AGBQKNBQESQNJD-UHFFFAOYSA-M lipoate Chemical compound [O-]C(=O)CCCCC1CCSS1 AGBQKNBQESQNJD-UHFFFAOYSA-M 0.000 claims description 3
- 235000019136 lipoic acid Nutrition 0.000 claims description 3
- 238000006467 substitution reaction Methods 0.000 claims description 3
- 229960002663 thioctic acid Drugs 0.000 claims description 3
- WWVANQJRLPIHNS-BKPPORCPSA-N 2-iminobiotin Chemical compound N1C(=N)N[C@H]2[C@H](CCCCC(=O)O)SC[C@H]21 WWVANQJRLPIHNS-BKPPORCPSA-N 0.000 claims description 2
- 108010001336 Horseradish Peroxidase Proteins 0.000 claims description 2
- 239000012876 carrier material Substances 0.000 claims description 2
- 239000007850 fluorescent dye Substances 0.000 claims description 2
- 238000002360 preparation method Methods 0.000 claims description 2
- 230000008569 process Effects 0.000 claims description 2
- 108020001775 protein parts Proteins 0.000 claims description 2
- NMJVVXMKAZVOCO-CAGKOAJJSA-N NN1C(N([C@H]2CS[C@@H](CCCCC(O)=O)[C@@H]12)N)=O.CC=1C(=C(C(=C(C(=O)O)C1)N=NC1=CC=CC=C1)O)C Chemical compound NN1C(N([C@H]2CS[C@@H](CCCCC(O)=O)[C@@H]12)N)=O.CC=1C(=C(C(=C(C(=O)O)C1)N=NC1=CC=CC=C1)O)C NMJVVXMKAZVOCO-CAGKOAJJSA-N 0.000 claims 1
- 125000000539 amino acid group Chemical group 0.000 claims 1
- 239000013598 vector Substances 0.000 claims 1
- 230000002860 competitive effect Effects 0.000 description 20
- 102000004196 processed proteins & peptides Human genes 0.000 description 18
- -1 s Chemical class 0.000 description 16
- 238000000746 purification Methods 0.000 description 13
- 125000003275 alpha amino acid group Chemical group 0.000 description 9
- 230000036963 noncompetitive effect Effects 0.000 description 9
- 101710205889 Cytochrome b562 Proteins 0.000 description 8
- 229920001184 polypeptide Polymers 0.000 description 8
- 238000001514 detection method Methods 0.000 description 7
- 238000010494 dissociation reaction Methods 0.000 description 7
- 230000005593 dissociations Effects 0.000 description 7
- 239000007790 solid phase Substances 0.000 description 7
- 229920002684 Sepharose Polymers 0.000 description 6
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 210000004899 c-terminal region Anatomy 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- 108010011170 Ala-Trp-Arg-His-Pro-Gln-Phe-Gly-Gly Proteins 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 241000588724 Escherichia coli Species 0.000 description 3
- 150000001615 biotins Chemical class 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 238000006073 displacement reaction Methods 0.000 description 3
- 229910001385 heavy metal Inorganic materials 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 108010018381 streptavidin-binding peptide Proteins 0.000 description 3
- JKNCSZDPWAVQAI-ZKWXMUAHSA-N 5-[(2s,3s,4r)-3,4-diaminothiolan-2-yl]pentanoic acid Chemical compound N[C@H]1CS[C@@H](CCCCC(O)=O)[C@H]1N JKNCSZDPWAVQAI-ZKWXMUAHSA-N 0.000 description 2
- 108010052832 Cytochromes Proteins 0.000 description 2
- 102000018832 Cytochromes Human genes 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 230000010799 Receptor Interactions Effects 0.000 description 2
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 238000011097 chromatography purification Methods 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000009146 cooperative binding Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 239000005090 green fluorescent protein Substances 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000002427 irreversible effect Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 125000006850 spacer group Chemical group 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- DEQPBRIACBATHE-FXQIFTODSA-N 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]-2-iminopentanoic acid Chemical compound N1C(=O)N[C@@H]2[C@H](CCCC(=N)C(=O)O)SC[C@@H]21 DEQPBRIACBATHE-FXQIFTODSA-N 0.000 description 1
- 241000242764 Aequorea victoria Species 0.000 description 1
- 241000006382 Bacillus halodurans Species 0.000 description 1
- 244000063299 Bacillus subtilis Species 0.000 description 1
- 235000014469 Bacillus subtilis Nutrition 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 102100029727 Enteropeptidase Human genes 0.000 description 1
- 108010013369 Enteropeptidase Proteins 0.000 description 1
- JRDYDYXZKFNNRQ-XPUUQOCRSA-N Gly-Ala-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)CN JRDYDYXZKFNNRQ-XPUUQOCRSA-N 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 108010085220 Multiprotein Complexes Proteins 0.000 description 1
- 102000007474 Multiprotein Complexes Human genes 0.000 description 1
- PSKRILMFHNIUAO-JYJNAYRXSA-N Phe-Glu-Lys Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H](CCCCN)C(=O)O)N PSKRILMFHNIUAO-JYJNAYRXSA-N 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 108010026552 Proteome Proteins 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- 238000003491 array Methods 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 238000010923 batch production Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 150000007942 carboxylates Chemical group 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 230000009920 chelation Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000012875 competitive assay Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000008846 dynamic interplay Effects 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000012846 protein folding Effects 0.000 description 1
- 230000004853 protein function Effects 0.000 description 1
- 239000012460 protein solution Substances 0.000 description 1
- 230000012743 protein tagging Effects 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000003381 solubilizing effect Effects 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 108010051423 streptavidin-agarose Proteins 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 230000036964 tight binding Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/36—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Actinomyces; from Streptomyces (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Peptides Or Proteins (AREA)
Abstract
Isoliertes streptavidinbindendes, kompetitiv eluierbares Peptid, umfassend mindestens zwei streptavidinbindende Einzelmodule, wobei der Abstand zwischen den zwei Einzelmodulen 0 und maximal 50 Aminosäuren beträgt und wobei ein Einzelmodul mindestens die Sequenz -His-Pro-Baa- beinhaltet, worin Baa entweder Glutamin, Asparagin oder Methionin darstellt und wobei mindestens das andere Einzelmodul mindestens die Sequenz -Oaa-Xaa-His- Pro-Gln-Phe-Yaa-Zaa- beinhaltet, wobei Oaa entweder Trp, Lys oder Arg darstellt, Xaa eine beliebige Aminosäure darstellt und wobei Yaa und Zaa entweder beide Gly darstellen oder Yaa Glu und Zaa Lys oder Arg darstellt.An isolated streptavidin-binding, competitively-elutable peptide comprising at least two streptavidin-binding single modules, wherein the distance between the two individual modules is 0 and at most 50 amino acids and wherein a single module contains at least the sequence -His-Pro-Baa, wherein Baa is either glutamine, asparagine or methionine and wherein at least the other single moiety includes at least the sequence -Oaa-Xaa-His-Pro-Gln-Phe-Yaa-Zaa, where Oaa is either Trp, Lys or Arg, Xaa is any amino acid and Yaa and Zaa are either both represent Gly or Yaa represents Glu and Zaa represents Lys or Arg.
Description
Die vorliegende Erfindung betrifft ein isoliertes streptavidinbindendes, kompetitiv eluierbares Peptid, ein dieses umfassendes Fusionspeptid, eine dafür codierende Nukleinsäure, einen Expressionsvektor, Verfahren zur Herstellung eines rekombinanten Fusionsproteins und Verfahren zum Nachweis und/oder zur Gewinnung des Fusionsproteins gemäß den Patentansprüchen. Die vorliegende Erfindung betrifft somit sequenziell angeordnete streptavidinbindende Peptid-Bindungsmodule, die insbesondere als Affinitätsanhängsel eingesetzt werden können. Die Affinitätsanhängsel umfassen mindestens zwei Einzelmodule, die eine avide Bindung an Streptavidin vermitteln können.The present invention relates to an isolated streptavidin-binding, competitively elutable peptide, a fusion peptide comprising this, a nucleic acid coding therefor, an expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or recovering the fusion protein according to the claims. The present invention thus relates to sequentially arranged streptavidin binding peptide binding modules, which can be used in particular as Affinitätsanhängsel. The affinity tags comprise at least two single modules capable of mediating avid binding to streptavidin.
Viele Projekte zur Aufklärung von Genomen von verschiedenen Organismen stehen kurz vor der Fertigstellung. So wurde das menschliche Genom kürzlich fast vollständig sequenziert und die Sequenzdaten zugeordnet und aufgearbeitet (erschienen in i) Nature, Vol. 409, 15. Februar 2001, ii) Science, Vol. 291, Nr. 5507, 16. Februar 2001). Eine der nächsten Herausforderungen wird die Aufklärung der jeweils zugehörigen Proteome sein, d. h. die Aufklärung der dem Genom zugehörigen Proteinfunktionen und ihr dynamisches Wechselspiel zum Aufbau von zellulären Funktionen.Many projects to unravel genomes from different organisms are nearing completion. Thus, the human genome has recently been almost completely sequenced and sequenced and processed (published in i) Nature, Vol. 409, Feb. 15, 2001, ii) Science, Vol. 291, No. 5507, Feb. 16, 2001). One of the next challenges will be the elucidation of the respective proteomes. H. the elucidation of the protein functions associated with the genome and their dynamic interplay to build up cellular functions.
Mit Hilfe moderner gentechnischer Methoden ist es möglich, fast jedes natürliche Gen zu klonieren und das zugehörige Protein rekombinant in Mikroorganismen oder Gewebekulturen zu produzieren. Damit wird zum einen der Zugang zu Proteinen geschaffen, die in ihrem natürlichen Produzenten nur in verschwindend geringen Mengen vorkommen und daher aus dieser Quelle nicht oder nur schwer zu gewinnen sind. Zum anderen schafft der rekombinante Ansatz aber auch eine große Vielfalt an gentechnischen Möglichkeiten, das Zielprotein zu verändern, um es dadurch genau zu charakterisieren und/oder um es dadurch leichter handhaben zu können.With the help of modern genetic engineering methods, it is possible to clone almost any natural gene and produce the associated protein recombinantly in microorganisms or tissue cultures. On the one hand, this provides access to proteins that are found in their natural producers only in minuscule quantities and therefore are difficult or impossible to obtain from this source. On the other hand, the recombinant approach also creates a wide variety of genetic engineering possibilities for altering the target protein in order to accurately characterize it and / or make it easier to handle.
Ein erster Schritt zur Charakterisierung des Zielproteins ist in der Regel dessen Reinigung von den Wirtsproteinen, die klassisch nur durch die empirische Entwicklung eines für jedes Protein speziellen Verfahrens erreicht werden kann. Um ein Detektionsverfahren zu etablieren, das z. B. wichtig für die Optimierung von Herstellungsprozessen, aber auch „downstream” für die weitere Charakterisierung des Zielproteins hilfreich sein kann, war es früher notwendig, ein spezifisches Antiserum gegen das gewünschte Protein herzustellen, wozu aber wiederum das Zielprotein zunächst als Reinsubstanz dargestellt werden musste. Weitere Verfahren zur „downstream”-Analyse von rekombinanten Proteinen bedingen oft die möglichst irreversible Immobilisierung an einer festen Phase wie z. B. in den Vertiefungen einer Mikrotiterplatte oder in Form von sogenannten „Arrays” auf Chips (Proteinchips). Da jedes Protein eine Substanz mit individuellen Eigenschaften ist und deswegen jedes Protein bei der direkten Immobilisierung anders beeinflusst wird, ist es zur Präsentierung von Proteinen in nativer, authentischer Form von Vorteil, wenn die Immobilisierung durch ein unabhängiges Modul auf standardisierte Weise erreicht werden kann.A first step in characterizing the target protein is usually its purification from the host proteins, which can be achieved classically only by the empirical development of a procedure specific to each protein. To establish a detection method, the z. B. important for the optimization of manufacturing processes, but also "downstream" for the further characterization of the target protein may be helpful, it was previously necessary to produce a specific antiserum to the desired protein, but in turn the target protein first had to be presented as a pure substance. Other methods for "downstream" analysis of recombinant proteins often require the most irreversible immobilization on a solid phase such. B. in the wells of a microtiter plate or in the form of so-called "arrays" on chips (protein chips). Since each protein is a substance with individual properties and therefore each protein is differently influenced by direct immobilization, it is advantageous to present proteins in native, authentic form if immobilization can be achieved by an independent module in a standardized manner.
Eine universelle Lösung für diese Fragestellungen beruht prinzipiell auf der geringfügigen Modifikation eines rekombinanten Gens während der Klonierung mit Nukleotidsequenzen, die für sogenannte Peptidanhängsel (Peptid-Tags) codieren. Dabei ist es wichtig, dass das Peptidanhängsel geeignete Bindungseigenschaften für einen Rezeptor hat. In der Praxis sieht die Ausnutzung eines solchen Peptidanhängsels folgendermaßen aus:
Nach oder während der Expression wird das beliebige Zielprotein durch ein Peptidanhängsel modifiziert. Die bekannten und gut charakterisierten Bindungseigenschaften des Peptidanhängsels in verschiedenen Testverfahren für seinen Rezeptor stehen jetzt für die weitere Analyse des Zielproteins zur Verfügung. In der Regel wird das Affinitätsanhängsel zunächst zur Reinigung des fusionierten Proteins mittels eines immobilisierten Rezeptors genutzt. Für die Reinigung durch Affinitätschromatographie ist es wichtig, dass das rekombinante Fusionsprotein unter milden Bedingungen wieder von der festen Phase eluiert werden kann. Nach der Reinigung ist es unter Umständen wünschenswert, dass das Peptidanhängsel zur Immobilisierung des rekombinanten Zielproteins an einer festen Phase wie z. B. an der Wand einer Mikrotiterplattenvertiefung ausgenutzt werden kann. Hier ist in der Regel die besonders feste Anbindung gewünscht, d. h., dass sich das Fusionsprotein unter keinen Umständen wieder von der festen Phase während des Testverfahrens ablöst.A universal solution to these problems is based in principle on the slight modification of a recombinant gene during the cloning with nucleotide sequences that code for so-called peptide tags (peptide tags). It is important that the peptide tag has suitable binding properties for a receptor. In practice, the use of such a peptide tag looks like this:
After or during expression, any target protein is modified by a peptide tag. The known and well-characterized binding properties of the peptide tag in various assays for its receptor are now available for further analysis of the target protein. In general, the affinity tag is first used to purify the fused protein by means of an immobilized receptor. For purification by affinity chromatography, it is important that the recombinant fusion protein can be eluted from the solid phase under mild conditions. After purification, it may be desirable for the peptide tag to immobilize the recombinant target protein on a solid phase, e.g. B. can be exploited on the wall of a microtiter plate well. As a rule, the particularly strong binding is desired here, ie, under no circumstances should the fusion protein detach from the solid phase during the test procedure.
Ein häufig verwendetes Peptidanhängsel ist der His6-Tag. Dieser bindet an Schwermetallionen, wie etwa Nickel unter Bildung eines Chelats. Ein Problem, das bei der Verwendung dieses Tags bei der Reinigung von Proteinen auftritt, ist die Kontamination des gewünschten Proteins mit den als Rezeptor verwendeten Schwermetallen. Weiterhin handelt es sich bei der Chelatbildung zwischen Schwermetall-Rezeptor und His6-Tag um eine Bindung mit nur geringer Spezifität. Zur Loslösung des Tags sind hohe Konzentrationen an Imidazol erforderlich, welche in vielen Anwendungen ebenfalls problematisch sein können. Insgesamt können unter Verwendung von His6-Tags bisher Reinheitsgrade von etwa 80% des gewünschten Proteins erhalten werden. Ebenfalls ist bekannt, dass Affinitätsanhängsel wie das His6-Tag oder das FLAG-Tag auch zum Nachweis von entsprechenden Fusionsproteinen mittels „Epitop-Tagging” verwendet werden können. Siehe Jarvik & Telmer, Ann. Rev. Genet. 1998, 32, 601–18 und Hernan et al., Biotechniques, 2000, 28, 789–793. Jarvik & Telmer sowie Hernan et al. berichten dabei, dass zur Erhöhung der Nachweissensitivität im Western Blot z. B. auch Tandem- oder Triple-Tags verwendet werden können.A commonly used peptide tag is the His 6 tag. This binds to heavy metal ions, such as nickel to form a chelate. A problem that occurs when using this tag in the purification of proteins is the contamination of the desired protein with the heavy metals used as a receptor. Furthermore, the chelation between heavy metal receptor and His 6 tag is a binding with only low specificity. Detachment of the tag requires high concentrations of imidazole, which can also be problematic in many applications. Overall, under Use of His 6 tags so far purity levels of about 80% of the desired protein can be obtained. It is also known that affinity tags such as the His6 tag or the FLAG tag can also be used to detect corresponding fusion proteins by means of "epitope tagging". See Jarvik & Telmer, Ann. Rev. Genet. 1998, 32, 601-18 and Hernan et al., Biotechniques, 2000, 28, 789-793. Jarvik & Telmer and Hernan et al. report that to increase the detection sensitivity in the Western Blot z. As well as tandem or triple tags can be used.
Eine weitere Klasse von Peptidanhängseln mit einer spezifischen Bindungseigenschaft für Streptavidin als Rezeptor wurden z. B. im
Die Entwicklung dieser Affinitätsanhängsel hatte ihren Ursprung in der Beobachtung von Devlin et al. (1990) und Lam et al. (1991), dass Streptavidin überhaupt in der Lage ist, Peptide zu binden. Als Mindestmotiv für Streptavidinbindung wurde von den Autoren die aus 3 Aminosäuren bestehende Peptidsequenz NH2-His-Pro-Gln(Met, Asn)-COOH erachtet. Solche Peptide alleine konnten jedoch nicht für praktische Anwendungen herangezogen werden, da die Bindungsaffinität zu gering war (Weber et al., 1992). Erst nachdem Schmidt und Skerra (1993) die Affinität optimierten, wurden praktische Anwendungen möglich (siehe auch
Trotz der Optimierung von Schmidt und Skerra (1993) gab es immer noch Probleme in bestimmten Anwendungsformaten und/oder wegen des unterschiedlichen Einflusses von verschiedenen Fusionsproteinen auf die Bindungsaffinität zu Streptavidin (Schmidt und Skerra, 1994). Insbesondere zeigte sich, dass das zunächst am stärksten bevorzugte streptavidinbindende Peptid mit der Sequenz NH2-Trp-Arg-His-Pro-Gln-Phe-Gly-Gly-COOH (Strep-tag®) nur am freien C-terminalen Ende des rekombinanten Protein-Fusionspartners eingesetzt werden konnte, da die C-terminale Carboxylat-Gruppe eine ionische Wechselwirkung zu einem Argininrest des Streptavidins einging (Schmidt et al., 1996, J. Mol. Biol. 255, 753–766). Für die allgemeinere Anwendung erwies sich die erstmals von Schmidt et al., in J. Mol. Biol., 1996, 255, 753–766 beschriebene Peptidsequenz NH2-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-COOH (Strep-tag® II) als geeigneter, da diese unabhängig von der Platzierung am rekombinanten Fusionsproteinpartner genutzt werden konnte. Siehe auch Skerra & Schmidt, Biomolecular Engineering, 1999, 16, 79–86, die die praktischen Anwendungen des Strep-tag® II einschließlich dessen Verwendung zum immunchemischen Nachweis von Proteinen in Western Blot und ELISA-Verfahren zusammenfassen. Allerdings war die Affinität des Strep-tag® II:Streptavidin-Komplexes niedriger als die Affinität des Strep-tag®:Streptavidin-Komplexes (Schmidt et al., 1996).Despite the optimization of Schmidt and Skerra (1993), there were still problems in certain application formats and / or because of the differential influence of different fusion proteins on the binding affinity to streptavidin (Schmidt and Skerra, 1994). In particular, it was found that the first most preferred streptavidin-binding peptide with the sequence NH 2 -Trp-Arg-His-Pro-Gln-Phe-Gly-Gly-COOH (Strep- tag® ) only at the free C-terminal end of the recombinant Protein fusion partner could be used since the C-terminal carboxylate group an ionic interaction with an arginine residue of streptavidin received (Schmidt et al., 1996, J. Mol. Biol. 255, 753-766). For the more general application, the peptide sequence NH 2 -Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-, described for the first time by Schmidt et al., J. Mol. Biol., 1996, 255, 753-766, proved to be more suitable. COOH (Strep- tag® II), since it could be used independently of the placement on the recombinant fusion protein partner. See also Skerra & Schmidt, Biomolecular Engineering, 1999, 16, 79-86, which summarizes the practical applications of Strep- tag® II including its use for immunochemical detection of proteins in Western blotting and ELISA procedures. However, the affinity of the Strep- tag® II: streptavidin complex was lower than the affinity of the Strep- tag® : streptavidin complex (Schmidt et al., 1996).
Deshalb wurde der Rezeptor Streptavidin hinsichtlich besserer Strep-tag® II-Bindung optimiert. Streptavidinmuteine mit deutlich höherer Strep-tag® II-Affinität konnten generiert werden und sind im
Die unterschiedlichen Anforderungen, die an eine solche Peptidanhängsel:Rezeptor-Interaktion gestellt werden, d. h. eine möglichst reversible Bindung zur schonenden Reinigung sowie eine möglichst irreversible Bindung zur Immobilisierung in diagnostischen Testsystemen im Mikrotiterplattenformat oder auf Proteinchips können somit nicht oder nicht optimal durch ein und dieselbe Interaktion erfüllt werden.The different demands placed on such a peptide tag: receptor interaction, d. H. a reversible binding as possible for gentle cleaning and an irreversible binding as possible for immobilization in diagnostic test systems in microtiter plate format or on protein chips can thus not or not optimally be met by one and the same interaction.
Versucht man also das Problem durch Generierung einer allgemein optimal funktionierenden Peptidanhängsel:Rezeptor-Interaktion auf monovalenter Basis zu lösen, gerät man in ein Dilemma: Wird die Bindung stark genug für die feste Bindung an Oberflächen, dann kann unter Umständen keine effiziente Elution unter kompetitiven Bedingungen während der affinitätschromatographischen Reinigung durchgeführt werden. Die kompetitive Elution ist aber eine elementare Bedingung, dass die Elution der Affinitätschromatographie spezifisch, effizient und schonend durchgeführt werden kann (siehe z. B. Skerra und Schmidt, 1999). Der Grund des Dilemmas liegt darin dass jede Wechselwirkung durch eine Bindungsrate und eine Dissoziationsrate kinetisch determiniert ist. Es ist ein allgemeines Prinzip, dass für die Immobilisierung an Oberflächen sehr langsame Dissoziationsraten bevorzugt werden, während bei der affinitätschromatographischen Elution durch ein kompetitiv (kompetitiv bedeutet, dass beide Liganden isoliert, jedoch nicht gleichzeitig binden können) bindendes Agens vergleichsweise schnelle Dissoziationsraten bevorzugt werden. Das heißt also, ein ideales Affinitätsanhängsel müsste sich unter kompetitiven Bedingungen so verhalten, als hätte es eine schnelle Dissoziationsrate zum Rezeptor, und unter nicht kompetitiven Bedingungen sollte es eine sehr langsame Dissoziationsrate aufweisen.Thus, attempting to solve the problem by generating a generally optimally functioning peptide tag: receptor interaction on a monovalent basis poses a dilemma: if binding becomes strong enough for tight binding to surfaces, then efficient elution under competitive conditions may not be possible during the affinity chromatographic purification. However, the competitive elution is an elementary condition that the elution of affinity chromatography can be carried out specifically, efficiently and gently (see, for example, Skerra and Schmidt, 1999). The reason of the dilemma is that each interaction is kinetically linked by a rate of binding and a dissociation rate is determined. It is a general principle that very slow dissociation rates are preferred for immobilization on surfaces, whereas in affinity chromatographic elution by competitively (competitively means that both ligands can be isolated but not simultaneously bind) binding agent comparatively fast dissociation rates are preferred. That is, an ideal affinity tag would have to behave under competitive conditions as if it had a fast dissociation rate to the receptor, and under non-competitive conditions it should have a very slow dissociation rate.
Weiterer Stand der Technik findet sich in
Eine Aufgabe der Erfindung war es deshalb, kurze Peptidsequenzen zu entwickeln, die mit einem rekombinanten Protein verbunden werden können, ohne mit dessen Funktion zu interferieren, die den Nachweis mit einem leicht verfügbaren Reagenz ermöglichen, die leicht kontrollierbare Bindungseigenschaften zeigen und welche trotz starker Bindeaffinität an Oberflächen unter kompetitiven Bedingungen leicht eluiert werden können.An object of the invention, therefore, was to develop short peptide sequences that can be linked to a recombinant protein without interfering with its function, allowing detection with a readily available reagent, showing readily controllable binding properties, and which, despite strong binding affinity Surfaces under competitive conditions can be easily eluted.
Diese Aufgabe wird erfindungsgemäß gelöst durch ein streptavidinbindendes, kompetitiv eluierbares Peptid, umfassend mindestens zwei streptavidinbindende Einzelmodule oder Epitope, wobei der Abstand zwischen den zwei Einzelmodulen 0 und maximal 50 Aminosäuren beträgt und wobei ein Einzelmodul mindestens die Sequenz -His-Pro-Baa-beinhaltet, worin Baa entweder Glutamin, Asparagin oder Methionin darstellt und wobei mindestens das andere Einzelmodul mindestens die Sequenz -Oaa-Xaa-His- Pro-Gln-Phe-Yaa-Zaa- beinhaltet, wobei Oaa entweder Trp, Lys oder Arg darstellt, Xaa eine beliebige Aminosäure darstellt und wobei Yaa und Zaa entweder beide Gly darstellen oder Yaa Glu und Zaa Lys oder Arg darstellt..This object is achieved according to the invention by a streptavidin-binding, competitively elutable peptide comprising at least two streptavidin-binding individual modules or epitopes, the distance between the two individual modules being 0 and a maximum of 50 amino acids and a single module containing at least the sequence -His-Pro-Baa, wherein Baa is either glutamine, asparagine or methionine and wherein at least the other single moiety includes at least the sequence -Oaa-Xaa-His-Pro-Gln-Phe-Yaa-Zaa, where Oaa is either Trp, Lys or Arg, Xaa is any one Wherein Yaa and Zaa are either both Gly or Yaa Glu and Zaa Lys or Arg.
Eine erfindungsgemäße Lösung besteht somit in der Verwendung von streptavidinbindenden Dianhängseln (Ditags) oder Multianhängseln (Multitags). Damit ist die sequenzielle Anordnung von mindestens zwei unterschiedlichen oder identischen, streptavidinbindenden oder/und streptavidinmuteinebindenden Modulen (Epitopen) gemeint, welche als Fusionspartner zu dem rekombinanten Zielprotein eingesetzt werden können. Überraschenderweise kann durch eine solche Anordnung ein Aviditätseffekt durch divalente oder multivalente Bindung eines Ditags oder Multitags an ein homotetrameres Strep-Tactin®- oder Streptavidin- oder anderes Muteinmolekül von Streptavidin erzielt werden. Solche Aviditätseffekte sind bisher in erster Linie für Immunglobuline bekannt, da diese sich durch ihre flexible „hinge”-Region an die sterischen Anforderungen des bivalenten Bindens an zwei Epitope gleichzeitig anpassen können. Die Struktur des tetrameren Streptavidins (Weber et al., 1989) ist demgegenüber im Vergleich zu Antikörpern eher starr und kaum flexibel.A solution according to the invention thus consists in the use of streptavidin-binding Dianags (Ditags) or Multianags (Multitags). By this is meant the sequential arrangement of at least two different or identical streptavidin-binding or / and streptavidin muteins binding modules (epitopes) which can be used as fusion partners to the recombinant target protein. Surprisingly, an avidity can be achieved by such an arrangement by divalent or multivalent binding of ditags or multiple tags on a homotetrameric Strep-Tactin ® - or streptavidin or other Muteinmolekül of streptavidin be achieved. Such avidity effects have hitherto been known primarily for immunoglobulins, since they can adapt to the steric requirements of bivalent binding to two epitopes simultaneously by virtue of their flexible "hinge" region. In contrast, the structure of tetrameric streptavidin (Weber et al., 1989) is rather rigid and barely flexible compared to antibodies.
Die erfindungsgemäßen Ditags oder Multitags sind insbesondere zur kooperativen Bindung an jeweils ein einziges Streptavidintetramer oder Streptavidindimer fähig. Durch die kooperative Bindung wird ein Aviditätseffekt erzielt, also eine verstärkte Bindung der Peptidanhängsel an einen Streptavidin-Rezeptor. Es wird vermutet, dass bei Inkontaktbringen der erfindungsgemäßen Peptide, welche mindestens 2 streptavidinbindende Einzelmodule oder Epitope umfassen, mit einem Streptavidin-Rezeptor zunächst in üblicher Weise eine Wechselwirkung zwischen den Einzelepitopen und den Streptavidin-Rezeptor-Bindestellen erfolgt. Die Ausbildung der Einzelbindung unterliegt dabei jeweils dem Masse-Wirkungs-Gesetz, wobei die Stärke der Bindung durch die jeweiligen Dissoziationskonstanten (Kd) bestimmt wird. Bei Losung einer Bindung zwischen einem Einzelmodul und einem Streptavidin-Rezeptor erfolgt jedoch keine Loslösung des Peptids vom Streptavidin-Rezeptor, da das Peptid immer noch durch wenigstens ein weiteres Einzelmodul an den Streptavidin-Rezeptor gebunden ist. Aufgrund der räumlichen Nähe zum Streptavidin-Rezeptor, in der sich das losgelöste Einzelmodul befindet, erfolgt dann eine Rückbindung des losgelösten Einzelmoduls an den Streptavidin-Rezeptor. Unter nicht kompetitiven Bedingungen ist somit ein synergistischer bzw. avider Effekt zu beobachten, da immer wieder eine Rückbindung erfolgt.The ditags or multitags according to the invention are in particular capable of cooperative binding to a single streptavidin tetramer or streptavidin dimer. The cooperative binding results in an avidity effect, ie an increased binding of the peptide appendages to a streptavidin receptor. It is assumed that upon contacting the peptides according to the invention, which comprise at least 2 streptavidin-binding individual modules or epitopes, an interaction between the individual epitopes and the streptavidin receptor binding sites first takes place in a customary manner with a streptavidin receptor. The formation of the single bond is in each case subject to the law of mass-action, the strength of the bond being determined by the respective dissociation constants (K d ). However, when solving for binding between a single module and a streptavidin receptor, there is no detachment of the peptide from the streptavidin receptor because the peptide is still bound to the streptavidin receptor by at least one other single module. Due to the close proximity to the streptavidin receptor, in which the detached single module is located, there is then a return of the detached single module to the streptavidin receptor. Under non-competitive conditions, a synergistic or avid effect can be observed, as it is always tied back.
Unter kompetitiven Bedingungen wird eine frei gewordene Streptavidin-Bindestelle durch einen zumeist im Überschuss zugegebenen anderen Liganden bzw. Kompetitor belegt, so dass aufgrund von Verdrängungseffekten keine Rückbindung erfolgen kann. Dadurch kann die Aufgabe gelöst werden, 2 verschiedene Bindeaffinitätsstärken bei unterschiedlichen Umgebungsbedingungen bereitzustellen (wobei sich die avide Bindungsstärke unter nicht kompetitiven Bedingungen stärker von den monovalenten Bindungsstärken unterscheidet als unter kompetitiven Bedingungen).Under competitive conditions, a vacated streptavidin binding site is occupied by another ligand or competitor, which is usually added in excess, so that no backbonding can take place due to displacement effects. Thus, the problem can be solved by providing 2 different binding affinity strengths under different environmental conditions (with the avide bond strength under non-competitive conditions being more different than monovalent bond strengths than under competitive conditions).
Die erfindungsgemäßen Peptide umfassen bevorzugt 2, 3 oder 4 Streptavidin-bindende Einzelmodule, besonders bevorzugt 2 oder 4 Streptavidin-bindende Einzelmodule und am meisten bevorzugt 2 Streptavidin-bindende Einzelmodule. The peptides of the invention preferably comprise 2, 3 or 4 streptavidin-binding single modules, more preferably 2 or 4 streptavidin-binding single modules, and most preferably 2 streptavidin-binding single modules.
Ein wesentliches Merkmal der erfindungsgemäßen Peptide besteht darin, dass es sich nicht um 2 separate Anhängsel oder Tags handelt, sondern um eine sequenzielle Anordnung von mindestens 2 Streptavidin-bindenden Einzelmodulen. Auf diese Weise werden die Bindeeigenschaften durch das Streptavidin-bindende Dianhängsel bzw. Multianhängsel festgelegt und sind unabhängig von einem damit zu fusionierenden Protein. Im Gegensatz dazu sind bei Verwendung von 2 unabhängigen Tags am C-Terminus und am N-Terminus eines Proteins oder an gleichen oder verschiedenen Termini von dimeren oder multimeren Proteinkomplexen die Bindeeigenschaften von dem oder den jeweiligen Fusionsprotein (den Domänen), insbesondere von dessen Proteinfaltung abhängig.An essential feature of the peptides according to the invention is that they are not separate tags or tags but a sequential arrangement of at least 2 streptavidin-binding single modules. In this way, the binding properties are determined by the streptavidin-binding Dianhängsel or multi-appendage and are independent of a protein to be fused with it. In contrast, when using two independent tags at the C-terminus and at the N-terminus of a protein, or at the same or different termini of dimeric or multimeric protein complexes, the binding properties are dependent on the particular fusion protein (s), particularly its protein folding ,
Mit den erfindungsgemäßen Peptid-Tags lässt sich i) durch die sequenzielle Anordnung von mindestens zwei streptavidinbindenden Peptiden eine wesentlich stärkere Anbindung an immobilisiertes Streptavidin oder Streptavidinmuteine generieren, sodass das Affinitätspeptid ii) den gängigen Standards für diagnostische immunologische Testverfahren im Mikrotiterplattenformat genügt und das gleiche Fusionsprotein mit dem gleichen Ditag lässt sich iii) noch effizient im affinitätschromatographischen Reinigungsverfahren kompetitiv eluieren. Anders ausgedrückt: Das Ditag verhält sich im Hinblick auf seine Bindungseigenschaften, insbesondere Bindungsfestigkeit in den unter i) und ii) beschriebenen Verfahren wie ein Monotag mit wesentlich höherer Bindungsaffinität und in dem unter iii) beschriebenen Verfahren ähnlich wie die einzelnen Monotags, aus dem das Ditag zusammengesetzt ist, separat betrachtet.With the peptide tags according to the invention i) can be generated by the sequential arrangement of at least two streptavidinbindenden peptides a much stronger binding to immobilized streptavidin or Streptavidinmuteine so that the affinity peptide ii) meets the usual standards for diagnostic immunological test in microtiter plate format and the same fusion protein On the same day, iii) can be eluted competitively in the affinity chromatographic purification process. In other words, the ditag behaves in terms of its binding properties, in particular bond strength in the methods described under i) and ii) as a monotag with significantly higher binding affinity and in the method described under iii) similar to the individual Monotags from the Ditag is composed, considered separately.
Des Weiteren ist das Ditag:Streptavidin-System besonders interessant, da es eine ganze Reihe von streptavidinbindenden Bindungspeptiden aber auch von Streptavidinmuteinen gibt und da dadurch – durch die Ausnutzung aller möglichen Kombinationen – eine besonders große und dennoch fein unterteilte Bandbreite an Bindungsaktivitäten erzeugt werden kann.Furthermore, the Ditag: streptavidin system is of particular interest, as there is a whole range of streptavidin-binding binding peptides as well as streptavidin muteins and, by exploiting all possible combinations, a particularly large and yet finely divided range of binding activities can be generated.
Verwendet man z. B. die Sequenz NH2-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-COOH bindet das Fusionsprotein besonders stark an Strep-Tactin®, in jedem Fall stärker als NH2-Trp-Ser-His-Pro-Gin-Phe-Glu-Lys-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-His-Pro-Gln-Xaa-Xaa-Xaa-COOH, welches wiederum stärker als NH2-His-Pro-Gln-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-His-Pro-Gln-COOH bindet. Die gleichen Peptide binden wiederum schlechter an Streptavidin. Durch diese Kombinationsmöglichkeiten kann für jede beabsichtigte Anwendung die Kombination ausgesucht werden, die eine Affinität zu Streptavidin oder Strep-Tactin® oder anderem Streptavidinmutein herstellt, die für den beabsichtigten Einsatzzweck ideal ist.If one uses z. For example, the sequence NH 2 -Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Trp-Ser-His-Pro-Gln-Phe Glu-Lys-COOH particularly strongly bind the fusion protein to Strep-tactin ®, in any case stronger than NH 2 -Trp-Ser-His-Pro-Gin-Phe-Glu-Lys-Xaa-Xaa-Xaa-Xaa-Xaa -Xaa-Xaa-Xaa-Xaa-Xaa-His-Pro-Gln-Xaa-Xaa-Xaa-COOH, which in turn is more powerful than NH 2 -His-Pro-Gln-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa. Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-Xaa-His-Pro-Gln-COOH binds. The same peptides in turn bind worse to streptavidin. With these combinations, the combination can be chosen for each intended use, which produces an affinity to streptavidin or Strep-Tactin ® or other streptavidin, which is ideal for the intended purpose.
Der Ausdruck ”Streptavidin”, wie hierin verwendet, umfasst Wildtyp-Streptavidin, Streptavidinmuteine und Streptavidin-artige Polypeptide, soweit nicht im Einzelfall anders angegeben. Unter Wildtyp-Streptavidin (wt-Streptavidin) wird auf die bei Argarana et al., Nucleic Acids Res. 14 (1986) 1871–1882 offenbarte Aminosäuresequenz Bezug genommen. Streptavidinmuteine sind Polypeptide, welche sich von der Sequenz des Wildtyp-Streptavidins durch eine oder mehrere Aminosäuresubstitutionen, -deletionen oder -additionen auszeichnen, wobei sie die Bindungseigenschaften von wt-Streptavidin beibehalten haben. Streptavidin-artige Polypeptide sowie Streptavidinmuteine sind Polypeptide, welche im Wesentlichen immunologisch äquivalent zu Wildtyp-Streptavidin sind und insbesondere in der Lage sind, Biotin, Biotinderivate oder Biotinanaloga mit gleicher oder unterschiedlicher Affinität wie wt-Streptavidin zu binden. Streptavidin-artige Polypeptide oder Streptavidinmuteine können Aminosäuren enthalten, die nicht Teil des Wildtyp-Streptavidins sind oder sie können lediglich einen Teil des Wildtyp-Streptavidins umfassen. Streptavidin-artige Polypeptide sind auch Polypeptide die zu Wildtyp-Streptavidin nicht identisch sind, da der Wirt nicht über erforderliche Enzyme verfügt, die erforderlich sind, um das Wirthergestellte Polypeptid in die Struktur von Wildtyp-Streptavidin zu transformieren.The term "streptavidin" as used herein includes wild-type streptavidin, streptavidin muteins, and streptavidin-like polypeptides, unless otherwise indicated in a particular case. Wildtype streptavidin (wt-streptavidin) refers to the amino acid sequence disclosed in Argarana et al., Nucleic Acids Res. 14 (1986) 1871-1882. Streptavidin muteins are polypeptides that are distinguished from the wild-type streptavidin sequence by one or more amino acid substitutions, deletions or additions while retaining the binding properties of wt-streptavidin. Streptavidin-like polypeptides as well as streptavidin muteins are polypeptides which are substantially immunologically equivalent to wild-type streptavidin and, in particular, are capable of binding biotin, biotin derivatives or biotin analogs with the same or different affinity as wt-streptavidin. Streptavidin-like polypeptides or streptavidin muteins may contain amino acids that are not part of the wild-type streptavidin or may comprise only part of the wild-type streptavidin. Streptavidin-like polypeptides are also polypeptides that are not identical to wild-type streptavidin because the host does not have the necessary enzymes necessary to transform the host-produced polypeptide into the structure of wild-type streptavidin.
Unter den Begriff Streptavidin fallen auch Streptavidintetramere sowie Streptavidindimere, insbesondere Streptavidinhomotetramere, Streptavidinhomodimere, Streptavidinheterotetramere und Streptavidinheterodimere. Jede Untereinheit hat in der Regel eine Bindungsstelle für Biotin oder Biotinanaloga oder für streptavidinbindende Peptide.The term streptavidin also includes streptavidin tetramers and streptavidin dimemers, in particular streptavidin homotetramers, streptavidin homodimers, streptavidin heterotetramers and streptavidin heterodimers. Each subunit typically has a binding site for biotin or biotin analogs or for streptavidin-binding peptides.
Beispiele für Streptavidine bzw. Streptavidinmuteine sind beispielsweise in
Ein weiterer für ein Ditag zu bevorzugender Anwendungsfall ist die besonders effiziente Reinigung von rekombinanten Fusionsproteinen aus verdünnten Lösungen im „Batchformat” (im Gegensatz zum Säulenchromatographieformat). Wegen der signifikant erhöhten apparenten Affinität im Vergleich zum Monotag reichert sich das Protein in der verdünnten Lösung stärker an der immobilen Phase an und es geht bei den sequentiellen Waschschritten, während derer sich das Gleichgewicht ja immer wieder neu einstellt, wesentlich weniger rekombinantes Fusionsprotein verloren. Sobald dann das kompetitiv bindende Agens im Überschuss zugesetzt wird, kann das Ditag tragende rekombinante Protein auch im „Batchformat” effizient eluiert werden. Another preferred application for a Ditag is the particularly efficient purification of recombinant fusion proteins from dilute solutions in "batch format" (in contrast to the column chromatography format). Because of the significantly increased apparent affinity compared to the monotag, the protein in the dilute solution accumulates more strongly on the immobile phase and it is lost in the sequential washing steps, during which the equilibrium yes again and again, much less recombinant fusion protein. Then, as soon as the competitively binding agent is added in excess, the recombinant protein carrying the ditag can also be efficiently eluted in the "batch format".
Unter Batchformat sind insbesondere solche Testformate zu verstehen, bei denen keine Durchwanderung von Elutionsmittel durch eine Säule oder ein Bett stattfindet, sondern Rezeptoren auf einer Festphase fixiert sind und bei jedem Waschschritt praktisch die gesamte flüssige Phase entfernt wird. Beispiele für ein Batchformat sind magnetische Beads, welche an ihrer Oberfläche Rezeptoren tragen und bei einem Waschschritt jeweils mit Flüssigkeit in Kontakt gebracht werden, wobei diese Flüssigkeit dann in jedem Waschschritt wieder vollständig oder nahezu vollständig abgetrennt werden kann. Ein weiteres Beispiel für Batchformat sind Protein-Chips bzw. auf Mikrotiterplatten oder ähnlichen Platten aufgebrachte Rezeptoren.Batch format is to be understood in particular as those test formats in which no migration of eluent through a column or a bed takes place, but receptors are fixed on a solid phase and in each washing step virtually the entire liquid phase is removed. Examples of a batch format are magnetic beads which carry receptors on their surface and in each case are brought into contact with liquid in a washing step, whereby this liquid can then be completely or almost completely separated off in each washing step. Another example of batch format are protein chips or receptors applied to microtiter plates or similar plates.
Erfindungsgemäß umfasst ein Minimalbindungsditag ein isoliertes Peptid, das aus mindestens 2 Einzelmodulen (Epitopen) wie in Anspruch 1 definiert zusammengesetzt ist, wobei der Abstand zwischen den beiden Modulen 0 und maximal 50 Aminosäuren beträgt.According to the invention, a minimal binding tag comprises an isolated peptide composed of at least 2 single modules (epitopes) as defined in claim 1, wherein the distance between the two modules is 0 and a maximum of 50 amino acids.
Mit solchen „Ditags” oder ”Multitags” können höhere Affinitäten zu dem jeweiligen Streptavidin oder Streptavidinmutein als mit einem einzelnen (z. B. dem besser bindenden, falls zwei verschiedene benutzt wurden) „Monotag” erzielt werden, auch wenn das besser bindende Modul der zwei Einzelmodule als Monotag eingesetzt wird. Zusätzlich besteht noch die Möglichkeit, eine feinere Abstufung in dem Affinitätsbereich zu erzeugen als dies durch Monotags möglich ist. Trotzdem lassen sich Ditag oder Multitag tragende rekombinante Fusionsproteine effizient kompetitiv von mit einem Rezeptor beschichteten festen Phasen eluieren. Eine hohe Flexibilität bei der Abstufung des Affinitätsbereichs der erfindungsgemäßen Tags lässt sich auf einfache Weise erreichen und kann insbesondere durch die Wahl des Peptid-Tag (das durch eine Reihe von verschiedenen oder/und identischen Einzelmodulen zusammengesetzt werden kann), durch die Wahl des Rezeptor-Streptavidin und durch die Wahl des Kompetitors zur Elution unter kompetitiven Bedingungen erhalten werden.With such "ditags" or "multitags", higher affinities for the particular streptavidin or streptavidin mutein than for a single (eg the better binding if two different ones were used) "monotag" can be achieved, even though the better binding modulus of the two individual modules is used as a single day. In addition, there is still the possibility of producing a finer gradation in the affinity region than is possible by monotags. Nevertheless, Ditag or multitag recombinant fusion proteins can be efficiently competitively eluted from receptor coated solid phases. A high degree of flexibility in the gradation of the affinity region of the tags according to the invention can be achieved in a simple manner and can be achieved in particular by the choice of the peptide tag (which can be composed by a number of different or / and identical individual modules), by the choice of the receptor Streptavidin and be obtained by the choice of the competitor for elution under competitive conditions.
Des Weiteren ist die Herstellung von stabilen dimeren rekombinanten Proteinen in der folgenden Anordung möglich: Rekombinantes Protein-Ditag-Streptavidin(mutein) mit insgesamt vier Bindungsstellen-Ditag-rekombinantes Protein. Auch können zwei verschiedene rekombinante Proteine über eine solche Anordnung stabil verbunden werden.Furthermore, the production of stable dimeric recombinant proteins in the following arrangement is possible: recombinant protein-ditag-streptavidin (mutein) with a total of four binding sites-Ditag recombinant protein. Also, two different recombinant proteins can be stably linked via such an arrangement.
Eine bevorzugte Anwendung von Ditag-Fusionsproteinen ist a) die stabile Anbindung des Fusionspartners an mit Streptavidin(mutein) beschichteten Oberflächen und/oder b) die effiziente Reinigung von Ditag-Fusionsproteinen aus verdünnten Lösungen, insbesondere im Batchformat (im Gegensatz zum Säulenchromatographieformat). Gerade die hochparallele Reinigung im kleinen Maßstab, jedoch mit hohen Ausbeuten und hohen Reinheitsgraden und aus komplexen Gemischen ist eine große Herausforderung für Affinitätsanhängselsysteme in „high throughput”-Formaten, die durch den Ditag-Ansatz für streptavidinbindende Affinitätsanhängsel gelöst wurde.A preferred application of Ditag fusion proteins is a) stable attachment of the fusion partner to streptavidin (mutein) coated surfaces and / or b) efficient purification of Ditag fusion proteins from dilute solutions, especially in batch format (as opposed to column chromatography format). High-level purification on a small scale, but with high yields and high levels of purity and complex mixtures, is a major challenge for high-throughput affinity tagging systems, which were solved by the Ditag approach to streptavidin-binding affinity tags.
In dem erfindungsgemäßen Peptid liegen die beiden Module, die eine Bindung an Streptavidin vermitteln, in einem Abstand von 0 und maximal 50, bevorzugt in einem Abstand von mindestens 4, mehr bevorzugt mindestens 8 und bis zu bevorzugt höchstens 30, mehr bevorzugt höchstens 20 Aminosäuren vor. Besonders bevorzugt beträgt der Abstand zwischen den beiden eine Bindung an Streptavidin vermittelnden Einzelmodulen 8 oder 12 Aminosäuren. Die Länge der Bindungsmodule beträgt bevorzugt mindestens 3, mehr bevorzugt mindestens 4 und am meisten bevorzugt mindestens 6 und bevorzugt höchstens 15, mehr bevorzugt höchstens 12 und am meisten bevorzugt höchstens 8 Aminosäuren.In the peptide according to the invention, the two modules which mediate binding to streptavidin are at a distance of 0 and at most 50, preferably at a distance of at least 4, more preferably at least 8 and up to preferably at most 30, more preferably at most 20 amino acids , The distance between the two individual modules mediating a binding to streptavidin is particularly preferably 8 or 12 amino acids. The length of the binding moieties is preferably at least 3, more preferably at least 4 and most preferably at least 6 and preferably at most 15, more preferably at most 12 and most preferably at most 8 amino acids.
Die zwischen den Einzelmodulen vorliegenden Aminosäuren können beliebige Aminosäuren sein. Es handelt sich bevorzugt um natürlich vorkommende Aminosäuren, es können jedoch auch chemisch modifizierte Aminosäuren vorliegen. Solche chemisch modifizierten Aminosäuren können insbesondere bei einem in vitro Expressionssystem eingebaut werden.The amino acids present between the individual modules can be any desired amino acids. They are preferably naturally occurring amino acids, but chemically modified amino acids may also be present. Such chemically modified amino acids can be incorporated in particular in an in vitro expression system.
In dem erfindungsgemäßen Peptid liegen die streptavidinbindenden Einzelmodule sequenziell vor, d. h. es ist kein Protein mit einer biologischen Funktion zwischen den Einzelmodulen angeordnet, sondern gegebenenfalls lediglich eine gewisse Anzahl an Linker-Aminosäuren. Bevorzugte Linker-Aminosäuren sind Gly und Ser, insbesondere Ketten, welche ausschließlich oder hauptsächlich, z. B. > 60%, Gly und Ser enthalten. Die Linkerlänge kann an die Entferung der Bindungszentren in den jeweiligen Streptavidin-Rezeptor angepasst werden. Bei einem tetrameren Streptavidin liegen beispielsweise zwei Bindungsstellen auf der Vorderseite und zwei Bindungsstellen auf der Rückseite vor. Bevorzugt sind deshalb Peptidanhängsel, welche 2 oder 4 (2 + 2) Bindungsstellen aufweisen und dazwischen Linker, welche gerade zur Überbrückung der Entfernung der Bindungszentren geeignet sind. Besonders bevorzugt sind deshalb Peptide mit folgendem Aufbau:
Gegebenenfalls keine oder 1 bis 50 Linker-Aminosäure(n)/Bindemodul mit 3 bis 15 Aminosäuren, insbesondere 3 bis 8 Aminosäuren/Linkerbereich mit bis 20, insbesondere 8 bis 12 Linker-Aminosäuren/Bindemodul mit 3 bis 5, insbesondere 3 bis 8 Aminosäuren/ggf. ein weiterer nichtfunktioneller Peptidbereich mit keiner oder 1 bis 50 Linker-Aminosäure(n) oder gegebenenfalls keine oder 1 bis 50 Linker-Aminosäuren/Bindemodul mit 3 bis 15 Aminosäuren, insbesondere 3 bis 8 Aminosäuren/Linkerbereich mit 0 bis 20, insbesondere 8 bis 12 Linker-Aminosäuren/Bindemodul mit 3 bis 15, insbesondere 3 bis 8 Aminosäuren/Linkerbereich mit 15 bis 40, insbesondere 18 bis 25 Linker-Aminosäuren/Bindemodul mit 3 bis 15, bevorzugt 3 bis 8 Aminosäuren/Linkerabschnitt mit 0 bis 20, insbesondere 8 bis 12 Linker-Aminosäuren/Bindemodul mit 3 bis 15, insbesondere 3 bis 8 Aminosäuren/ggf. Linkerabschnitt mit keiner oder 1 bis 50 Linker-Aminosäure(n).In the peptide according to the invention, the streptavidin-binding individual modules are present in sequence, ie there is no protein with a biological function between the individual modules, but optionally only a certain number of linker amino acids. Preferred linker amino acids are Gly and Ser, in particular chains, which are exclusively or mainly, for. > 60%, Gly and Ser. The linker length can be adapted to the distance of the binding sites to the respective streptavidin receptor. For example, in a tetrameric streptavidin, there are two binding sites on the front and two binding sites on the back. Peptide tags are therefore preferred which have 2 or 4 (2 + 2) binding sites and intervening linkers which are currently suitable for bridging the removal of the binding centers. Therefore, peptides with the following structure are particularly preferred:
Optionally no or 1 to 50 linker amino acid (s) / binding moiety having 3 to 15 amino acids, in particular 3 to 8 amino acids / linker region containing up to 20, in particular 8 to 12 linker amino acids / binding moiety having 3 to 5, in particular 3 to 8 amino acids /possibly. a further non-functional peptide region having no or 1 to 50 linker amino acid (s) or optionally no or 1 to 50 linker amino acids / binding moiety having 3 to 15 amino acids, in particular 3 to 8 amino acids / linker region having 0 to 20, in particular 8 to 12 Linker amino acids / binding module with 3 to 15, in particular 3 to 8 amino acids / linker region with 15 to 40, in particular 18 to 25 linker amino acids / binding moiety with 3 to 15, preferably 3 to 8 amino acids / linker section with 0 to 20, in particular 8 to 12 linker amino acids / binding module with 3 to 15, in particular 3 to 8 amino acids / if necessary Linker section with no or 1 to 50 linker amino acid (s).
Das erfindungsgemäße Peptid kann neben den beiden Einzelmodulen und den Aminosäuren, die zwischen den Einzelmodulen liegen, noch weitere Aminosäuren enthalten, die sich an einer Seite an mindestens eines der Einzelmodule anschließen. Die Gesamtlänge des erfindungsgemäßen isolierten Peptids beträgt mindestens 11 Aminosäuren, mehr bevorzugt mindestens 20 Aminosäuren und kann bevorzugt bis zu 500 Aminosäuren, mehr bevorzugt bis zu 100 Aminosäuren und am meisten bevorzugt bis zu 56 Aminosäuren und insbesondere bis zu 40 Aminosäuren betragen.In addition to the two individual modules and the amino acids which lie between the individual modules, the peptide according to the invention may contain further amino acids which adjoin at least one of the individual modules on one side. The total length of the isolated peptide of the invention is at least 11 amino acids, more preferably at least 20 amino acids, and may preferably be up to 500 amino acids, more preferably up to 100 amino acids, and most preferably up to 56 amino acids, and most preferably up to 40 amino acids.
Das eine der zwei Einzelmodule, welche eine Bindung an Streptavidin vermitteln, wird bevorzugt ausgewählt aus einer der Sequenzen: -His-Pro-Gln-, -His-Pro-Gln-Phe-, -Oaa-Xaa-His-Pro-Gln-Phe-Yaa-Zaa-, wobei Oaa entweder Trp, Lys oder Arg darstellt, Xaa eine beliebige Aminosäure und bevorzugt eine natürlich vorkommende Aminosäure darstellt und wobei Yaa und Zaa entweder beide Gly darstellen oder Yaa Glu und Zaa Lys oder Arg darstellt, -Trp-Xaa-His-Pro-Gln-Phe-Yaa-Zaa, wobei Xaa eine beliebige Aminosäure darstellt und wobei Yaa und Zaa entweder beide Gly darstellen oder Yaa Glu und Zaa Lys oder Arg darstellt oder -Trp-Ser-His-Pro-Gln-Phe-Glu-Lys.One of the two individual modules which mediate binding to streptavidin is preferably selected from one of the following sequences: -His-Pro-Gln-, -His-Pro-Gln-Phe-, -Oaa-Xaa-His-Pro-Gln- Phe-Yaa-Zaa, wherein Oaa is either Trp, Lys or Arg, Xaa is any amino acid and preferably a naturally occurring amino acid and wherein Yaa and Zaa are either both Gly or Yaa is Glu and Zaa is Lys or Arg, -Trp- Xaa-His-Pro-Gln-Phe-Yaa-Zaa, wherein Xaa represents any amino acid and wherein Yaa and Zaa are either both Gly or Yaa is Glu and Zaa is Lys or Arg or -Trp-Ser-His-Pro-Gln Phe-Glu-Lys.
Die bevorzugten, sequenziell angeordneten Bindemodule verleihen eine erhöhte Affinität zu Streptavidin, können jedoch im kompetitiven Testformat noch ausreichend losgelöst werden.The preferred, sequentially arranged binding modules confer an increased affinity for streptavidin, but can still be sufficiently separated in the competitive assay format.
Besonders bevorzugt weist das erfindungsgemäße Peptid die Sequenz Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-(Xaa)n-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys auf, wobei Xaa eine beliebige Aminosäure darstellt und n eine ganze Zahl von 5 bis 20, insbesondere von 8 bis 12 ist, sowie die Sequenz Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-(GlyGlyGlySer)n-Trp-Ser-His-Pro-Gln-Phe -Glu-Lys, wobei n eine ganze Zahl von 1 bis 5 und bevorzugt 2 oder 3 darstellt.The peptide according to the invention particularly preferably has the sequence Trp-Ser-His-Pro-Gln-Phe-Glu-Lys- (Xaa) n -Trp-Ser-His-Pro-Gln-Phe-Glu-Lys, where Xaa is any one of And n is an integer from 5 to 20, especially from 8 to 12, and the sequence Trp-Ser-His-Pro-Gln-Phe-Glu-Lys- (GlyGlyGlySer) n -Trp-Ser-His-Pro -Gln-Phe -Glu-Lys, wherein n represents an integer of 1 to 5 and preferably 2 or 3.
Im Rahmen der Erfindung wurde festgestellt, dass die erfindungsgemäßen Peptidsequenzen eine hohe Bindungsaffinität für Streptavidin bzw. Kern-Streptavidin (ein proteolytisches Spaltprodukt von Streptavidin) (Bayer, E. A. et al., Biochem. J. 259 (1989), 369–376) sowie für Streptavidinmuteine aufweisen, die insbesondere höher als die Bindungsaffinitäten der einzelnen Bindungsmodule ist und gleichzeitig bei kompetitiven Bedingungen leicht eluiert werden können.In the context of the invention it has been found that the peptide sequences according to the invention have a high binding affinity for streptavidin or nuclear streptavidin (a proteolytic cleavage product of streptavidin) (Bayer, EA et al., Biochem J. 259 (1989), 369-376) and for Streptavidinmuteine, in particular, is higher than the binding affinities of the individual binding modules and can be easily eluted at the same time under competitive conditions.
Die einzelnen Bindungsmodule des erfindungsgemäßen Peptids weisen bevorzugt eine Bindeaffinität zum jeweiligen Streptavidin-Rezeptor Kd von höchstens 10–2, mehr bevorzugt höchstens 10–3, noch mehr bevorzugt höchstens 10–5 und mindestens 10–13, mehr bevorzugt mindestens 10–10, noch mehr bevorzugt mindestens 10–6 und am meisten bevorzugt mindestens 10–6 M auf. Die Elution unter kompetitiven Bedingungen wird dann bevorzugt mit einem Kompetitor durchgeführt, der eine höhere Affinität zum jeweiligen Streptavidinrezeptor aufweist, bevorzugt eine Affinität, welche mindestens eine Größenordnung, mehr bevorzugt mindestens zwei Größenordnungen und am meisten bevorzugt mindestens 3 Größenordnungen größer ist. Die Bindungsaffinität von Streptavidin:Biotin beträgt beispielsweise 4 × 10–14 M. Aufgrund der sequenziellen Anordnung der erfindungsgemäßen Ditags und des damit verbundenen Aviditätseffektes ist insbesondere die Verwendung von 2 Bindemodulen, die jeweils eine Bindeaffinität von 10–6 M oder höher, insbesondere 10–5 M oder höher aufweisen möglich, wobei unter nicht kompetitiven Bedingungen trotz der geringen Bindeaffinitäten der einzelnen Bindemodule eine starke Bindung zum Streptavidin-Rezeptor erhalten wird.The individual binding modules of the peptide according to the invention preferably have a binding affinity for the respective streptavidin receptor K d of at most 10 -2 , more preferably at most 10 -3 , even more preferably at most 10 -5 and at least 10 -13 , more preferably at least 10 -10 . even more preferably at least 10 -6, and most preferably at least 10 -6 M. The elution under competitive conditions is then preferably carried out with a competitor having a higher affinity for the respective streptavidin receptor, preferably an affinity which is at least one order of magnitude, more preferably at least two orders of magnitude and most preferably at least three orders of magnitude larger. The binding affinity of streptavidin: biotin is, for example, 4 × 10 -14 M. Due to the sequential arrangement of the ditags according to the invention and the avidity effect associated therewith, the use of 2 binding modules, each having a binding affinity of 10 -6 M or higher, in particular 10 - 5 M or higher are possible, whereby a strong binding to the streptavidin receptor is obtained under non-competitive conditions despite the low binding affinities of the individual binding modules.
Besonders bevorzugte Streptavidinmuteine sind solche, die im
Das erfindungsgemäße isolierte Peptid wird bevorzugt als Tag oder Affinitätsanhängsel eingesetzt. Deshalb ist ein weiterer Gegenstand der Erfindung ein Fusionsprotein, umfassend ein wie oben beschriebenes erfindungsgemäßes Peptid mit mindestens zwei an Streptavidin oder Streptavidinmuteine bindenden Einzelmodulen verbunden mit einem Protein. Wenn die erfindungsgemäße Peptidsequenz in einem Fusionsprotein vorhanden ist, so weist auch dieses Fusionsprotein eine hohe Affinität für Streptavidin auf und kann gleichzeitig unter kompetitiven Bedingungen leicht eluiert werden.The isolated peptide according to the invention is preferably used as a tag or affinity tag. Therefore, a further subject of the invention is a fusion protein comprising a peptide according to the invention as described above having at least two individual modules binding to streptavidin or streptavidin muteins bound to a protein. If the peptide sequence according to the invention is present in a fusion protein, then this fusion protein also has a high affinity for streptavidin and can at the same time easily be eluted under competitive conditions.
Neben einer Elution bei kompetitiven Bedingungen, also in Gegenwart eines weiteren Streptavidinliganden, kann die Rezeptor-Affinitätsanhängsel-Bindung auch durch Veränderung des pH-Wertes (pH-Shift) gelöst werden, wodurch eine einfache Elution erfolgen kann. Bei Einstellen von sauren Bedingungen wird mindestens ein Histidinrest des erfindungsgemäßen Peptids protoniert, wodurch die Rezeptor-Affinitätsanhängsel-Bindung gelöst wird.In addition to elution in competitive conditions, ie in the presence of another streptavidin ligand, the receptor-affinity tag binding can also be solved by changing the pH (pH shift), whereby a simple elution can take place. When acid conditions are set, at least one histidine residue of the peptide of the invention is protonated, thereby solubilizing the receptor affinity tag binding.
Die erfindungsgemäße Peptidsequenz kann am carboxyterminalen Ende, am aminoterminalen Ende oder innerhalb der Aminosäuresequenz des Proteins liegen, solange hiermit keine negativen Eigenschaften verbunden sind, wie z. B. eine Hinderung oder Zerstörung der biologischen Aktvität, wenn deren Erhaltung erwünscht ist.The peptide sequence according to the invention may be at the carboxy-terminal end, at the amino-terminal end or within the amino acid sequence of the protein, as long as no negative properties are associated therewith, such as e.g. B. a hindrance or destruction of biological activity, if their conservation is desired.
Das im Fusionsprotein vorhandene Protein kann sowohl ein vollständiges Protein sowie eine Mutante eines Proteins, wie z. B. eine Deletionsmutante oder Substitutionsmutante, sein oder auch nur ein Teil eines Proteins. Das erfindungsgemäße Peptid kann direkt oder über Linker- oder Spacersequenzen mit dem gewünschten Protein verbunden sein.The protein present in the fusion protein can be both a complete protein and a mutant of a protein, such. A deletion mutant or substitution mutant, or even part of a protein. The peptide according to the invention can be linked directly or via linker or spacer sequences with the desired protein.
Ein weiterer Gegenstand der Erfindung ist ein Expressionsvektor, der eine Nukleinsäure-Sequenz, insbesondere eine DNA-Sequenz enthält, welche für ein erfindungsgemäßes Peptid codiert, sowie eine oder mehrere Restriktionsschnittstellen in 5'- oder/und 3'-Richtung von dieser Nukleinsäuresequenz aufweist, welche die Einbringung einer weiteren Nukleinsäuresequenz, insbesondere einer DNA-Sequenz erlaubt, die für das zu exprimierende Protein oder einen Proteinteil codiert. Die Nukleinsäuresequenz ist bevorzugt unter der Kontrolle eines geeigneten Promotors und gegebenenfalls eines Operators. Bevorzugt schließt sich wenigstens eine Restriktionsschnittstelle unmittelbar an die für das erfindungsgemäße Peptid codierende Nukleinsäuresequenz an. Es ist aber auch möglich, die Schnittstellen in einiger Entfernung vorzusehen, so dass zwischen dem erfindungsgemäßen Peptid und dem damit zu fusionierenden Protein ein Spacer- bzw. Linkerbereich bereitgestellt wird. Der Linkerbereich kann auch eine Spaltstelle für eine sequenzspezifische Protease, wie z. B. Enterokinase oder Faktor Xα, umfassen oder darstellen, so dass das Affinitätsanhängsel nach Expression und ggf. Reinigung des Fusionsproteins von dem gewünschten Protein abgespalten werden kann.A further subject of the invention is an expression vector which contains a nucleic acid sequence, in particular a DNA sequence, which codes for a peptide according to the invention and has one or more restriction sites in the 5 'or / and 3' direction of this nucleic acid sequence, which allows the introduction of a further nucleic acid sequence, in particular a DNA sequence coding for the protein to be expressed or a protein part. The nucleic acid sequence is preferably under the control of a suitable promoter and optionally an operator. At least one restriction cleavage site preferably directly adjoins the nucleic acid sequence coding for the peptide according to the invention. However, it is also possible to provide the interfaces at some distance, so that a spacer or linker region is provided between the peptide according to the invention and the protein to be fused thereto. The linker region can also be a cleavage site for a sequence-specific protease, such. Enterokinase or factor Xα, so that the affinity tag can be cleaved from the desired protein after expression and, optionally, purification of the fusion protein.
Mit Hilfe des erfindungsgemäßen Expressionsvektors wird es ermöglicht, die Nukleinsäuresequenz für ein interessierendes Protein in einfacher Weise mit einer Nukleinsäuresequenz für das erfindungsgemäße Peptid anzuordnen und nach Expression ein erfindungsgemäßes Fusionsprotein zu erhalten. Wird z. B. in eine Restriktionsschnittstelle in 5'-Richtung von der Nukleinsäuresequenz für das erfindungsgemäße Peptid die Nukleinsäuresequenz für das damit zu fusionierende Protein insertiert, wird ein Fusionsprotein erhalten, welches das die Streptavidin-Affinität vermittelnde erfindungsgemäße Ditag- oder Multitag-Peptid am Carboxy-Terminus aufweist. Entsprechend liegt das erfindungsgemäße Affinitätsanhängsel am Aminoterminus vor, wenn die Nukleinsäuresequenz des zu fusionierenden Peptids in eine Restriktionsschnittstelle in 3'-Richtung insertiert wird.With the aid of the expression vector according to the invention, it is possible to arrange the nucleic acid sequence for a protein of interest in a simple manner with a nucleic acid sequence for the peptide according to the invention and to obtain after expression a fusion protein according to the invention. If z. For example, if the nucleic acid sequence for the protein to be fused with it is inserted into a restriction cleavage site in the 5 'direction of the nucleic acid sequence for the peptide according to the invention, a fusion protein is obtained which contains the streptavidin-affinity-mediating ditag or multitagged peptide according to the invention at the carboxy terminus having. Accordingly, the affinity tag according to the invention is present at the amino terminus when the nucleic acid sequence of the peptide to be fused is inserted into a restriction cleavage site in the 3 'direction.
Die Restriktionsschnittstelle muss im erfindungsgemäßen Expressionsvektor nicht unbedingt unmittelbar neben der ersten oder letzten Base der für das Peptid codierenden Nukleinsäuresequenz liegen. Vorzugsweise sollte sie jedoch so hegen, dass bei der Translation das Leseraster nicht beeinträchtigt wird und eine Verbindung von nur wenigen, vorzugsweise höchstens 10 zusätzlichen Aminosäuren zwischen dem Peptid und der Aminosäuresequenz des Proteins entsteht.The restriction site does not necessarily have to lie directly next to the first or last base of the nucleic acid sequence coding for the peptide in the expression vector according to the invention. Preferably, however, it should be such that during translation the reading frame is not affected and a Compound of only a few, preferably at most 10 additional amino acids between the peptide and the amino acid sequence of the protein is formed.
Ein weiterer Gegenstand der Erfindung ist ein Verfahren zur Herstellung eines rekombinanten Fusionsproteins, bei dem man eine für das oben genannte Fusionsprotein codierende Nukleinsäuresequenz in eine geeignete Wirtszelle einbringt. Die Herstellung kann auch als in vitro Expression durchgeführt werden, wobei man eine für das Fusionsprotein codierende Nukleinsäuresequenz in einen Zellextrakt oder ein Zelllysat einbringt. Durch Expression der Nukleinsäuresequenz kann das erfindungsgemäße Fusionsprotein erhalten werden. Die Anwesenheit des Expressionsproduktes kann über ein Konjugat von Streptavidin oder einer Streptavidinmutante und einer Markierung oder/und einer Festphase leicht nachgewiesen werden. Weiterhin ist die Isolierung bzw. Aufreinigung des gewünschten Proteins als Fusionsprotein unter Verwendung der Streptavidin-bindenden Eigenschaften des erfindungsgemäßen Ditags oder Multitags auf einfache Weise möglich, wobei beispielsweise eine Streptavidin-Affinitäts-Chromatographie eingesetzt werden kann.Another object of the invention is a method for producing a recombinant fusion protein, wherein introducing a coding for the above-mentioned fusion protein nucleic acid sequence in a suitable host cell. The preparation can also be carried out as in vitro expression, wherein a coding for the fusion protein nucleic acid sequence is introduced into a cell extract or a cell lysate. By expression of the nucleic acid sequence, the fusion protein according to the invention can be obtained. The presence of the expression product can be readily detected via a conjugate of streptavidin or a streptavidin mutant and a label or / and a solid phase. Furthermore, the isolation or purification of the desired protein as a fusion protein using the streptavidin-binding properties of the ditag or multiday according to the invention is possible in a simple manner, for example, a streptavidin-affinity chromatography can be used.
Das Einbringen der Nukleinsäuresequenz in eine geeignete Wirtszelle oder in Zelllysat erfolgt bevorzugt mit einem erfindungsgemäßen Expressionsvektor, welcher eine Nukleinsäure enthält, die für das gewünschte Fusionsprotein codiert.The introduction of the nucleic acid sequence into a suitable host cell or in cell lysate is preferably carried out with an expression vector according to the invention which contains a nucleic acid which codes for the desired fusion protein.
Das Konjugat aus Streptavidin und Markierung umfasst bevorzugt eine Fluoreszenzmarkierung oder/und eine Enzymmarkierung, insbesondere alkalische Phosphatase oder Meerrettich-Peroxidase. Grundsätzlich kann jedoch jede beliebige Markierung eingesetzt werden, die einen Nachweis erlaubt, beispielsweise auch Direktmarkierungen, wie etwa Gold- oder Latexpartikel, oder andere dem Fachmann bekannte Markierungen.The conjugate of streptavidin and label preferably comprises a fluorescent label and / or an enzyme label, in particular alkaline phosphatase or horseradish peroxidase. In principle, however, any desired label can be used which allows detection, for example also direct markings, such as, for example, gold or latex particles, or other labels known to the person skilled in the art.
Ein wesentlicher Vorteil der erfindungsgemäßen Peptide und des erfindungsgemäßen Verfahrens zur Herstellung von rekombinanten Fusionsproteinen liegt darin, dass die Aufreinigung des exprimierten Fusionsproteins leicht durch Affinitätschromatographie über eine Säule mit immobilisiertem Streptavidin oder eine immobilisierte Streptavidinmutante oder im Batch-Verfahren durchgeführt werden kann. Während die erfindungsgemäßen Ditags oder Multitags eine hohe Affinität zu dem Rezeptor zeigen, kann die Elution trotzdem vorteilhaft unter sehr milden kompetitiven Bedingungen durchgeführt werden, z. B. durch Zugabe von Biotin oder Biotin-ähnlichen Verbindungen, und insbesondere durch Zugabe von 2-Iminobiotin, Liponsäure, Hydroxyphenylazobenzoesäure (HABA), Dimetylhydroxyphenylazobenzoesäure(DM-HABA), Diaminobiotin oder/und Desthiobiotin. Durch eine kompetitive Elution mit Streptavidin-Liganden kann das gewünschte Fusionsprotein somit auf einfache Weise und unter schonenden Bedingungen wieder freigesetzt werden. Besonders bevorzugt ist die Elution im Kleinstmaßstab (von Mikrogrammmengen) im Batchformat mit Biotin.A significant advantage of the peptides according to the invention and of the method according to the invention for the production of recombinant fusion proteins is that the purification of the expressed fusion protein can easily be carried out by affinity chromatography on a column with immobilized streptavidin or an immobilized streptavidin mutant or in a batch process. While the ditags or multitags of the present invention show high affinity for the receptor, elution can still be advantageously performed under very mild competitive conditions, e.g. Example by adding biotin or biotin-like compounds, and in particular by adding 2-iminobiotin, lipoic acid, hydroxyphenylazobenzoic acid (HABA), Dimetylhydroxyphenylazobenzoesäure (DM-HABA), diaminobiotin or / and Desthiobiotin. By a competitive elution with streptavidin ligands, the desired fusion protein can thus be released again in a simple manner and under mild conditions. Particularly preferred is the elution on the smallest scale (of microgram quantities) in batch format with biotin.
Aufgrund der sehr starken Wechselwirkung zwischen Biotin und Streptavidin ist bei der Verwendung von Biotin als Kompetitor die Elution besonders effizient. Allerdings kann eine Regenerierung des Streptavidin-Rezeptors bei Verwendung von Biotin als Kompetitor nicht oder nur schwierig erfolgen. Deshalb ist die Verwendung von Biotin insbesondere dann bevorzugt, wenn eine Regenerierung nicht notwendig ist, beispielsweise bei kleinen Maßstäben (Mikrogrammmengen Streptavidin).Due to the very strong interaction between biotin and streptavidin, elution is particularly efficient when using biotin as the competitor. However, regeneration of the streptavidin receptor when using biotin as a competitor is difficult or impossible. Therefore, the use of biotin is particularly preferred when regeneration is not necessary, for example at small scales (microgram quantities of streptavidin).
Bei Durchführung der Elution in größerem, auch industriellem Maßstab (mg-bis kg-Mengen Streptavidin) wird hingegen vorzugsweise ein Kompetitor verwendet, welcher eine ausreichend hohe Bindungsaffinität zum Streptavidin-Rezeptor hat, um eine effektive Elution zu bewirken, welcher aber trotzdem von dem Streptavidin-Rezeptor wieder losgelöst werden kann, um ein regenerierbares System bereitzustellen. Besonders bevorzugt wird im großen Maßstab deshalb Desthiobiotin, Iminobiotin, Diaminobiotin, Liponsäure, HABA, oder/und DM-HABA als Kompetitor eingesetzt. Im großen Maßstab ist auch die pH-Erniedrigung eine interessante Alternative zur Kompetitionselution.When carrying out the elution on a larger, industrial scale (mg to kg quantities of streptavidin), however, a competitor is preferably used, which has a sufficiently high binding affinity to the streptavidin receptor to effect an effective elution, but which nevertheless from the streptavidin Receptor can be detached again to provide a regenerable system. Desthiobiotin, iminobiotin, diaminobiotin, lipoic acid, HABA, or / and DM-HABA is therefore particularly preferably used on a large scale as a competitor. On a large scale, pH reduction is also an interesting alternative to competition elution.
Für die Streptavidin-Affinitäts-Chromatographie kann z. B. eine Streptavidin-Agarose-Matrix eingesetzt werden. Bevorzugt wird Sepharose Polysaccharid (Pharmacia) oder Macro Prep(Poly-Methacrylat; Bio Rad) oder POROS (Polystyrol (OH-modifiziert); PE Biosystems) als Trägermaterial verwendet.For streptavidin affinity chromatography, for. As a streptavidin-agarose matrix can be used. Sepharose polysaccharide (Pharmacia) or Macro Prep (poly-methacrylate, Bio Rad) or POROS (polystyrene (OH-modified), PE Biosystems) is preferably used as carrier material.
Ein weiterer Gegenstand der Erfindung ist eine Nukleinsäure, die für ein erfindungsgemäßes Ditag- oder Multitagpeptid codiert.Another object of the invention is a nucleic acid encoding a Ditag- or multitag peptide according to the invention.
Weiterhin umfasst die Erfindung die Verwendung von Streptavidin oder/und eines Streptavidinmuteins als Rezeptor zur Bindung eines erfindungsgemäßen Peptids.Furthermore, the invention encompasses the use of streptavidin or / and a streptavidin mutein as a receptor for binding a peptide according to the invention.
Mit dem erfindungsgemäßen Ditag oder Multitag ist ein schneller und sicherer Nachweis von Fusionsproteinen, die beispielsweise als Expressionsprodukte erhalten werden, möglich. Weiterhin weist das Fusionsprotein genau einstellbare und vorteilhafte Bindungseigenschaften an Streptavidin auf, sodass eine leichte Aufreinigung des Expressionsproduktes ermöglicht wird, die auch in großtechnischem Maßstab durchführbar ist. With the Ditag or multitag according to the invention, rapid and reliable detection of fusion proteins obtained, for example, as expression products is possible. Furthermore, the fusion protein has precisely adjustable and advantageous binding properties to streptavidin, so that an easy purification of the expression product is made possible, which can also be carried out on an industrial scale.
Mit Hilfe des erfindungsgemäßen Expressionsvektors wird die Expression eines erfindungsgemäßen Fusionsproteins erleichtert, wobei ein solcher Expressionsvektor universell für alle zu exprimierenden Proteine anwendbar ist. Das erfindungsgemäße Peptid stört im Fusionsprotein die biologische Aktivität des übrigen Proteinanteils nicht und muss daher nicht unbedingt vor einer Weiterverwendung abgespalten werden. Sollte jedoch aus bestimmten Gründen eine Abspaltung erwünscht sein, so kann der erfindungsgemäße Expressionsvektor auch derart aufgebaut sein, dass er zwischen der Restriktionsschnittstelle zur Einbringung der Nukleinsäuresequenz für das Protein und der für das Protein codierenden Sequenz noch eine Nukleinsäuresequenz aufweist, welche für eine spezifische Proteaseschnittstelle codiert. Somit kann nach Expression und gegebenenfalls Aufreinigung oder Nachweis des Expressionsproduktes eine leichte Abspaltung der Peptidsequenz durchgeführt werden.With the aid of the expression vector according to the invention, the expression of a fusion protein according to the invention is facilitated, wherein such an expression vector is universally applicable for all proteins to be expressed. The peptide according to the invention does not interfere with the biological activity of the remaining protein portion in the fusion protein and therefore does not necessarily have to be cleaved off from further use. However, if cleavage is desired for some reason, the expression vector of the invention may also be constructed such that it has, between the restriction site for introducing the nucleic acid sequence for the protein and the sequence coding for the protein, a nucleic acid sequence encoding a specific protease site , Thus, after expression and optionally purification or detection of the expression product, an easy cleavage of the peptide sequence can be carried out.
Die Erfindung wird durch die folgenden Beispiele und die beigefügte Figur weiter erläutert.The invention will be further elucidated by the following examples and the attached figure.
Wie aus den
BeispieleExamples
Beispiel 1example 1
Es wurden drei verschiedene rekombinante Proteine mit einem Monotag der Sequenz Trp-Ser-His-Pro-Gln-Phe-Glu-Lys, einem Ditag 1 der Sequenz Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-(GlyGlyGlySer)2-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys und einem Ditag 2 mit der Sequenz Trp-Ser-His-Pro-Gln-Phe-Glu-Lys-(GlyGlyGlySer)3-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys hergestellt, so dass insgesamt 9 verschiedene rekombinante Fusionsproteine erhalten wurden.Three different recombinant proteins with a monotag of the sequence Trp-Ser-His-Pro-Gln-Phe-Glu-Lys, a Ditag 1 of the sequence Trp-Ser-His-Pro-Gln-Phe-Glu-Lys (GlyGlyGlySer ) 2-Trp-Ser-His-Pro-Gln-Phe-Glu-Lys and a
Für dieses Experiment wurden zwei gefärbte Proteine (Green Fluorescent Protein (GFP) aus A. victoria, grün, und Cytochrom b562 aus E. coli, rot) und ein Enzym (alkalische Phosphatase aus E. coli) verwendet, um die Anwesenheit des Fusionsproteins jeweils ohne Weiteres direkt oder nach Zugabe eines chromogenen Enzymsubstrats anhand der Farbe beobachten zu können.For this experiment, two stained proteins (Green Fluorescent Protein (GFP) from A. victoria, green, and cytochrome b562 from E. coli, red) and an enzyme (alkaline phosphatase from E. coli) were used to detect the presence of the fusion protein, respectively be able to observe directly on the basis of the color directly or after addition of a chromogenic enzyme substrate.
Die Bindungseigenschaften aller 9 Proteine wurden in einem Biacore-Gerät kinetisch untersucht, wobei als Rezeptor Streptavidin (Wildtyp mit der Sequenz Glu-Ser-Ala-Val an den Positionen 44 bis 47), Streptavidinmutein ml (mit der Sequenz Val-Thr-Ala-Arg an den Positionen 44 bis 47) und Streptavidinmutein m2 (mit der Sequenz Ile-Gly-Ala-Arg an den Positionen 44 bis 47) eingesetzt wurden.The binding properties of all 9 proteins were kinetically assayed in a Biacore device using as receptor Streptavidin (wild type with the sequence Glu-Ser-Ala-Val at the positions 44 to 47), Streptavidin mutein (with the sequence Val-Thr-Ala-Arg at positions 44-47) and streptavidin mutein m 2 (with the sequence Ile-Gly-Ala-Arg at positions 44-47).
Zur Dissoziationskinetikbestimmung wurde einmal mit Kompetitor (z. B. Desthiobiotin) und einmal ohne Kompetitor gemessen.Dissociation kinetics were measured once with competitor (eg desthiobiotin) and once without competitor.
Der Verbleib der alkalischen Phosphatase (AP) in einer Mikrotiterplatte kann leicht durch die Färbung mit einem Enzymsubstrat indirekt nachgewiesen werden. Es wurde festgestellt, dass mit Ditags versehene AP eine deutlich stärkere Anbindung an mit Strep-Tactin® beschichtete Wände von Mikrotiterplatten als die mit einem Monotag versehene AP zeigt.The fate of alkaline phosphatase (AP) in a microtiter plate can easily be detected indirectly by staining with an enzyme substrate. It has been found that with ditags AP provided a significantly stronger connection to coated with Strep-Tactin ® walls of microtiter plates provided with a Monotag than the AP shows.
Beispiel 2Example 2
Anhand von magnetischen, mit Strep-Tactin® beschichteten Beads wurde eine Reinigung von Fusionsproteinen mit Ditags im Batch-Format in verschiedenen Verdünnungsstufen durchgeführt. Es gelang eine Reinigung der Fusionsproteine in kleinem Maßstab mit hoher Ausbeute und hohem Reinheitsgrad.Using magnetic, coated with Strep-Tactin ® beads purification of fusion proteins with ditags in batch format was conducted in various dilutions. It was possible to purify the fusion proteins on a small scale with high yield and high purity.
Beispiel 3Example 3
Bindung von Cytochrom b562 mit verachiedenen Affinitätsanhängseln an Strep-Tactin® SepharoseBinding of cytochrome b562 with verachiedenen affinity appendages of Strep-Tactin ® Sepharose
Von E. coli Cytochrom b562, rot, mit C-terminalem Strep-tag® ist bekannt, dass es im Vergleich zu anderen Strep-tag® Fusionsproteinen besonders schlecht an immobilisiertes Streptavidin bindet (Schmidt und Skerra, 1994).E. coli cytochrome b562, red, with C-terminal Strep- tag® is known to bind particularly poorly to immobilized streptavidin compared to other Strep- tag® fusion proteins (Schmidt and Skerra, 1994).
In diesem Experiment wurden die Bindung von Cytochrom b562 – mit verschiedenen Affinitätsanhängseln am C-Terminus (Di-tag 3; Di-tag 2; Mono-tag) – an 3 Säulen (L, M, R) mit identischem Strep-Tactin®-Sepharosematerial verglichen: In this experiment, the binding of cytochrome b562 were - with different affinity appendages at the C-terminus (Di-
(Die unterstrichenen Bereiche sind die streptavidinbindenden Module)(The underlined areas are the streptavidin binding modules)
Definierte gereinigte Mengen der 3 unterschiedlichen Fusionsproteine (700 μg mit Di-tag 3; 800 μg mit Di-tag 2; 950 μg mit Mono-tag) wurden auf eine Strep-Tactin® Sepharose-Säule mit 2 ml Bettvolumen und einer Biotin-Bindungskapazität von ca. 350 nmol pro ml gegeben. Nachdem die Proteinlösung vollkommen eingedrungen war, wurde die Säule mit Puffer W (100 mM Tris-Cl pH 8,0; 150 mM NaCl; nicht kompetitive Bedingungen) gewaschen.
LITERATURLITERATURE
- Devlin, J. J., Panganiban, L. C. & Devlin, P. E. (1990), Random peptide libraries: A source of specific protein binding molecules. Science 249, 404–406.Devlin, J.J., Panganiban, L.C. & Devlin, P.E. (1990), Random peptide libraries: A source of specific protein binding molecules. Science 249, 404-406.
- Lam, K. S., Salmon, E. S., Hersh, E. M., Hruby, V. J., Kazmierski, W. M. & Knapp, R. J. (1991). A new type of synthetic peptide library for identifying ligand-binding activity. Nature 354, 82–84.Lam, K.S., Salmon, E.S., Hersh, E.M., Hruby, V.J., Kazmierski, W.M. & Knapp, R.J. (1991). Ligand-binding activity. Nature 354, 82-84.
- Schmidt, T. G. M. & Skerra, A. (1993). The random peptide library-assisted engineering of a C-terminal affinity peptide, useful for the detection and purification of a functional Ig Fv fragment. Prot. Engineering 6, 109–122.Schmidt, TGM & Skerra, A. (1993). The random peptide library-assisted engineering of a C-terminal affinity peptide, useful for the detection and purification of a functional Ig Fv fragment. Prot. Engineering 6, 109-122.
- Schmidt, T. G. M. & Skerra, A. (1994). One-step affinity purification of bacterially produced proteins by means of the ”Strep tag” and immobilized recominant core streptavidin. J. Cromatogr. A676, 337–345.Schmidt, T.G.M. & Skerra, A. (1994). One-step affinity purification of bacterially produced proteins by means of the "strep tag" and immobilized recominant core streptavidin. J. Cromatogr. A676, 337-345.
- Schmidt, T. G. M., Koepke, J., Frank, R. & Skerra, A. (1996). Molecular interaction between the Strep-tag affinity peptide and its cognate target streptavidin. J. Mol. Biol. 255, 753–766.Schmidt, T.G.M., Koepke, J., Frank, R. & Skerra, A. (1996). Molecular interaction between the strep-tag affinity peptide and its cognate target streptavidin. J. Mol. Biol. 255, 753-766.
- Skerra, A. & Schmidt, T. G. M. (1999). Applications of a Peptide Ligand for streptavidin: the Strep-tag. Biomolecular Engineering 16, 79–86.Skerra, A. & Schmidt, T.G.M. (1999). Applications of a peptide ligand for streptavidin: the strep-tag. Biomolecular Engineering 16, 79-86.
- Voss, S. & Skerra, a. (1997) Mutagenesis of a flexible loop in streptavidin leads to higher affinity for the Strep-tag II peptide and improved Performance in recombinant protein purification. Protein Eng. 10, 975–982.Voss, S. & Skerra, a. (1997) Mutagenesis of a flexible loop in streptavidin leads to higher affinity for the Strep-tag II peptide and improved performance in recombinant protein purification. Protein Eng. 10, 975-982.
- Weber, P. C., Pantoliano, M. W. & Thompson, L. D. (1992). Crystal structure and ligand-binding studies of a screened peptide complexed with streptavidin. Biochemistry 31, 9350–9354.Weber, P.C., Pantoliano, M.W. & Thompson, L.D. (1992). Crystal structure and ligand-binding studies of a screened peptide complexed with streptavidin. Biochemistry 31, 9350-9354.
- Weber, P. C., M. W. Pantoliano and F. R. Salemme (1995). Crystallographic and thermodynamic comparison of structurally diverse molecules binding to streptavidin. Acta Cryst. D51: 590–596.Weber, P.C., M.W. Pantoliano and F.R. Salemme (1995). Crystallographic and thermodynamic comparison of structurally diverse molecules binding to streptavidin. Acta Cryst. D51: 590-596.
Claims (18)
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10113776A DE10113776B4 (en) | 2001-03-21 | 2001-03-21 | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein |
| PCT/EP2001/011846 WO2002077018A1 (en) | 2001-03-21 | 2001-10-12 | Sequentially arranged streptavidin-binding modules as affinity tags |
| EP01274019.7A EP1370574B1 (en) | 2001-03-21 | 2001-10-12 | Sequentially arranged streptavidin-binding modules as affinity tags |
| US10/026,578 US7981632B2 (en) | 2001-03-21 | 2001-12-17 | Sequentially arranged streptavidin-binding modules as affinity tags |
| US13/185,070 US8735540B2 (en) | 2001-03-21 | 2011-07-18 | Peptides with sequentially arranged streptavidin binding modules |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10113776A DE10113776B4 (en) | 2001-03-21 | 2001-03-21 | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE10113776A1 DE10113776A1 (en) | 2002-10-02 |
| DE10113776B4 true DE10113776B4 (en) | 2012-08-09 |
Family
ID=7678401
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE10113776A Expired - Fee Related DE10113776B4 (en) | 2001-03-21 | 2001-03-21 | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein |
Country Status (4)
| Country | Link |
|---|---|
| US (2) | US7981632B2 (en) |
| EP (1) | EP1370574B1 (en) |
| DE (1) | DE10113776B4 (en) |
| WO (1) | WO2002077018A1 (en) |
Families Citing this family (97)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10113776B4 (en) | 2001-03-21 | 2012-08-09 | "Iba Gmbh" | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein |
| US20040067532A1 (en) | 2002-08-12 | 2004-04-08 | Genetastix Corporation | High throughput generation and affinity maturation of humanized antibody |
| DE102004014983A1 (en) | 2004-03-26 | 2005-10-20 | Univ Stuttgart | Recombinant polypeptides of the members of the TNF ligand family and their use |
| DE102005011579B4 (en) * | 2005-03-14 | 2011-12-15 | Helmholtz Zentrum München Deutsches Forschungszentrum Für Gesundheit Und Umwelt (Gmbh) | Affinity tags for protein purification, its production and use, and methods for purifying a protein |
| WO2007094739A1 (en) | 2006-02-13 | 2007-08-23 | Agency For Science, Technology And Research | Method of processing a biological and/or chemical sample |
| US8261598B2 (en) * | 2006-03-09 | 2012-09-11 | Agency For Science, Technology And Research | Apparatus for performing a reaction in a droplet and method of using the same |
| US9874501B2 (en) | 2006-11-24 | 2018-01-23 | Curiox Biosystems Pte Ltd. | Use of chemically patterned substrate for liquid handling, chemical and biological reactions |
| WO2008063135A1 (en) * | 2006-11-24 | 2008-05-29 | Agency For Science, Technology And Research | Apparatus for processing a sample in a liquid droplet and method of using the same |
| WO2008136769A1 (en) | 2007-05-03 | 2008-11-13 | Nanyang Technological University | Online contaminant detection and removal system |
| US20090263870A1 (en) * | 2007-09-10 | 2009-10-22 | Agency For Science, Technology And Research | System and method for amplifying a nucleic acid molecule |
| US8877688B2 (en) | 2007-09-14 | 2014-11-04 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| CN101855242B (en) | 2007-09-14 | 2014-07-30 | 阿迪马布有限责任公司 | Rationally designed, synthetic antibody libraries and uses therefor |
| US12529164B2 (en) | 2007-09-14 | 2026-01-20 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| WO2013114217A1 (en) | 2012-02-05 | 2013-08-08 | Curiox Biosystems Pte Ltd. | Array plates and methods for making and using same |
| US10725020B2 (en) | 2007-11-14 | 2020-07-28 | Curiox Biosystems Pte Ltd. | High throughput miniaturized assay system and methods |
| US8784752B2 (en) | 2009-04-17 | 2014-07-22 | Curiox Biosystems Pte Ltd | Use of chemically patterned substrate for liquid handling, chemical and biological reactions |
| WO2012011877A2 (en) | 2010-07-23 | 2012-01-26 | Curiox Biosystems Pte Ltd | Apparatus and method for multiple reactions in small volumes |
| ES2682750T5 (en) | 2011-07-18 | 2025-02-04 | Iba Lifesciences Gmbh | Method of reversibly staining a target cell |
| AU2012325013A1 (en) | 2011-10-17 | 2014-03-27 | Westfaelische Wilhelms-Universitaet Muenster | Methods of risk assessment of PML and related apparatus |
| TWI425096B (en) * | 2012-02-10 | 2014-02-01 | Nat Applied Res Laboratories | Modifying surface of a substrate with bio-molecules |
| CN106940268B (en) | 2012-02-23 | 2021-09-21 | 朱诺治疗有限公司 | Chromatographic separation of cells and other complex biological materials |
| EP2841446A2 (en) | 2012-04-26 | 2015-03-04 | IBA GmbH | Adapter molecule capable of reversibly equipping a fusion protein carrying an oligohistidine affinity tag with a further affinity tag and methods of using the same |
| JP6475630B2 (en) | 2012-11-16 | 2019-02-27 | イーベーアー ゲーエムベーハー | Streptavidin muteins and methods of using them |
| US9708656B2 (en) | 2013-05-06 | 2017-07-18 | Pacific Biosciences Of California, Inc. | Real-time electronic sequencing |
| WO2014201265A1 (en) | 2013-06-14 | 2014-12-18 | Pacific Biosciences Of California, Inc. | Bis-biotinylation tags |
| US10544449B2 (en) | 2013-06-14 | 2020-01-28 | Pacific Biosciences Of California, Inc. | Bis-biotinylation tags |
| US9557318B2 (en) | 2013-07-09 | 2017-01-31 | Curiox Biosystems Pte Ltd. | Array plates for washing samples |
| ES2837856T3 (en) * | 2013-12-20 | 2021-07-01 | Hutchinson Fred Cancer Res | Labeled Chimeric Effector Molecules and Receptors |
| LU92409B1 (en) | 2014-03-21 | 2015-09-22 | Philipps Universit T Marburg | Means and methods for itaconic acid production |
| RU2735640C9 (en) | 2014-04-16 | 2021-02-08 | Юно Терепьютикс Гмбх | Methods, sets and device for cell population multiplication |
| CN113046321A (en) | 2014-04-23 | 2021-06-29 | 朱诺治疗学股份有限公司 | Methods of isolating, culturing and genetically engineering immune cell populations for adoptive therapy |
| EP3137905B1 (en) | 2014-04-30 | 2021-01-13 | IBA GmbH | Method of isolating a target cell |
| US10300452B2 (en) | 2015-03-24 | 2019-05-28 | Pacific Biosciences Of California, Inc. | Methods and compositions for single molecule composition loading |
| EP3075389A1 (en) | 2015-03-31 | 2016-10-05 | Technische Universität München | T cell receptors and peptides derived by mutations for the treatment of cancer |
| WO2016166568A1 (en) | 2015-04-16 | 2016-10-20 | Juno Therapeutics Gmbh | Methods, kits and apparatus for expanding a population of cells |
| EP3288569A4 (en) | 2015-04-29 | 2018-12-19 | Fred Hutchinson Cancer Research Center | Modified hematopoietic stem/progenitor and non-t effector cells, and uses thereof |
| US11827904B2 (en) | 2015-04-29 | 2023-11-28 | Fred Hutchinson Cancer Center | Modified stem cells and uses thereof |
| US10545139B2 (en) | 2015-06-16 | 2020-01-28 | Curiox Biosystems Pte Ltd. | Methods and devices for performing biological assays using magnetic components |
| CN108139345B (en) | 2015-08-06 | 2021-04-20 | 加利福尼亚太平洋生物科学股份有限公司 | System and method for selectively addressing sparsely arranged electronic measurement devices |
| MA45488A (en) | 2015-10-22 | 2018-08-29 | Juno Therapeutics Gmbh | CELL CULTURE PROCESSES, KITS AND APPARATUS |
| MA45489A (en) | 2015-10-22 | 2018-08-29 | Juno Therapeutics Gmbh | CELL CULTURE PROCESSES, ASSOCIATED KITS AND APPARATUS |
| RU2761555C2 (en) | 2015-10-22 | 2021-12-09 | Джуно Терапьютикс Гмбх | Methods, sets, means and devices for transduction |
| KR20190003938A (en) | 2016-02-25 | 2019-01-10 | 셀 메디카 스위처란트 아게 | Modified cells for immunotherapy |
| AU2017257203B2 (en) * | 2016-04-25 | 2019-08-22 | Iba Gmbh | Streptavidin muteins and methods of using them |
| EP3452517A4 (en) * | 2016-05-04 | 2019-12-18 | The Children's Medical Center Corporation | METHODS OF PURIFYING AVIDIN-LIKE PROTEINS AND FUSION PROTEINS THEREFROM |
| CN109983133B (en) | 2016-06-28 | 2023-09-08 | 慕尼黑工业大学 | Combination of reversible and irreversible cell labels for analysis of receptor-ligand Koff rates |
| PL240585B1 (en) | 2016-07-18 | 2022-05-02 | Helix Biopharma Corp | Immunological CAR cells for treatment of tumours |
| US10294454B2 (en) | 2016-08-24 | 2019-05-21 | General Electric Company | Methods and kits for cell activation |
| MX2019008538A (en) | 2017-01-20 | 2019-11-05 | Juno Therapeutics Gmbh | Cell surface conjugates and related cell compositions and methods. |
| BR112019017120A8 (en) | 2017-02-17 | 2023-05-02 | Hutchinson Fred Cancer Res | COMBINATION THERAPIES FOR TREATMENT OF CANCER AND BCMA-RELATED AUTOIMMUNE DISORDERS |
| CN110709979B (en) | 2017-04-05 | 2024-04-09 | 科睿思生物科技(私人)有限公司 | Method, device and apparatus for cleaning samples on an array plate |
| JP7339160B2 (en) | 2017-04-27 | 2023-09-05 | ジュノ セラピューティクス ゲーエムベーハー | Oligomeric particle reagents and methods of use thereof |
| KR20200064060A (en) | 2017-07-29 | 2020-06-05 | 주노 쎄러퓨티크스 인코퍼레이티드 | Reagent for cell amplification expressing a recombinant receptor |
| PT3661968T (en) | 2017-08-04 | 2022-07-04 | Governing Council Univ Toronto | Nanoparticle platform for antibody and vaccine delivery |
| CN111065409A (en) | 2017-09-06 | 2020-04-24 | 弗雷德哈钦森癌症研究中心 | STREP-TAG specific binding protein and application thereof |
| JP7407701B2 (en) | 2017-09-06 | 2024-01-04 | フレッド ハッチンソン キャンサー センター | strep tag-specific chimeric receptors and their uses |
| CN111479916B (en) * | 2017-10-20 | 2024-10-22 | 弗莱德哈钦森癌症中心 | Systems and methods for generating B cells genetically modified to express selected antibodies |
| US11162138B2 (en) | 2017-10-30 | 2021-11-02 | Pacific Biosciences Of California, Inc. | Multi-amplitude modular labeled compounds |
| WO2019102265A1 (en) | 2017-11-23 | 2019-05-31 | Theraphage Inc. | Peptide displaying bacteriophage nanoparticles and related compositions and methods |
| BR112020011215A2 (en) | 2017-12-08 | 2020-11-17 | Juno Therapeutics Inc | process for producing a modified t-cell composition |
| US10655168B2 (en) | 2017-12-22 | 2020-05-19 | Pacific Biosciences Of California, Inc. | Modified biotin-binding proteins for immobilization |
| US20210079061A1 (en) | 2018-02-26 | 2021-03-18 | Fred Hutchinson Cancer Research Center | Compositions and methods for cellular immunotherapy |
| EP3833742A2 (en) | 2018-08-09 | 2021-06-16 | Juno Therapeutics, Inc. | Processes for generating engineered cells and compositions thereof |
| WO2020048876A1 (en) | 2018-09-03 | 2020-03-12 | Technische Universitaet Muenchen | A double peptide tag combining reversibility and flexible functionalization |
| US12366580B2 (en) | 2018-09-11 | 2025-07-22 | Juno Therapeutics, Inc. | Methods for mass spectrometry analysis of engineered cell compositions |
| US20240165232A1 (en) | 2018-09-24 | 2024-05-23 | Fred Hutchinson Cancer Research Center | Chimeric receptor proteins and uses thereof |
| AU2019370705B2 (en) | 2018-10-31 | 2026-01-22 | Juno Therapeutics Gmbh | Methods for selection and stimulation of cells and apparatus for same |
| CN113272018A (en) | 2018-11-06 | 2021-08-17 | 朱诺治疗学股份有限公司 | Method for producing genetically engineered T cells |
| CA3139965A1 (en) | 2019-06-07 | 2020-12-10 | Ivie AIFUWA | Automated t cell culture |
| CN114929360A (en) | 2019-10-30 | 2022-08-19 | 朱诺治疗学有限公司 | Cell selection and/or stimulation devices and methods of use |
| KR102826762B1 (en) | 2019-11-30 | 2025-07-01 | 강마-헬스코드 (상하이) 바이오테크 컴퍼니 리미티드 | Biomagnetic microspheres and their manufacturing method and use |
| EP4097218A1 (en) | 2020-01-28 | 2022-12-07 | Juno Therapeutics, Inc. | Methods for t cell transduction |
| CA3163761C (en) | 2020-01-31 | 2023-07-11 | Herbert Stadler | Methods of isolating a biological entity |
| CN115361955A (en) | 2020-02-12 | 2022-11-18 | 朱诺治疗学股份有限公司 | Chimeric antigen receptor T cell compositions directed against BCMA and methods and uses thereof |
| EP4103204A1 (en) | 2020-02-12 | 2022-12-21 | Juno Therapeutics, Inc. | Cd19-directed chimeric antigen receptor t cell compositions and methods and uses thereof |
| CN115835873A (en) | 2020-05-13 | 2023-03-21 | 朱诺治疗学股份有限公司 | Method for producing donor batch cells expressing recombinant receptors |
| EP4240756A1 (en) | 2020-11-04 | 2023-09-13 | Juno Therapeutics, Inc. | Cells expressing a chimeric receptor from a modified invariant cd3 immunoglobulin superfamily chain locus and related polynucleotides and methods |
| KR20240018454A (en) | 2021-05-06 | 2024-02-13 | 주노 테라퓨틱스 게엠베하 | Methods for stimulating and transducing T cells |
| TW202317602A (en) | 2021-07-15 | 2023-05-01 | 福瑞德哈金森腫瘤中心 | Chimeric polypeptides |
| WO2023017115A1 (en) | 2021-08-11 | 2023-02-16 | Iba Lifesciences Gmbh | Fractionation of cells based on a marker protein |
| AR126900A1 (en) | 2021-08-27 | 2023-11-29 | Humabs Biomed Sa | GENETICALLY MODIFIED CORONAVIRUS POLYPEPTIDES, POLYNUCLEOTIDES, VECTORS AND HOST CELLS, AND RELATED COMPOSITIONS |
| JP2024537397A (en) | 2021-10-16 | 2024-10-10 | ザ・ホスピタル・フォー・シック・チルドレン | Modified Multibody Constructs, Compositions, and Methods |
| WO2023060359A1 (en) | 2021-10-16 | 2023-04-20 | The Hospital For Sick Children | Modified multabody constructs, compositions, and methods targeting sars-cov-2 |
| WO2023147510A1 (en) | 2022-01-28 | 2023-08-03 | Juno Therapeutics, Inc. | Chromatography arrays and related methods and kits |
| CN119256003A (en) | 2022-04-14 | 2025-01-03 | 儿童医院 | PFCSP-based immunogens and related compositions and methods |
| WO2023215725A1 (en) | 2022-05-02 | 2023-11-09 | Fred Hutchinson Cancer Center | Compositions and methods for cellular immunotherapy |
| WO2023213969A1 (en) | 2022-05-05 | 2023-11-09 | Juno Therapeutics Gmbh | Viral-binding protein and related reagents, articles, and methods of use |
| EP4532695A1 (en) | 2022-05-25 | 2025-04-09 | Celgene Corporation | Methods of manufacturing t cell therapies |
| EP4615960A1 (en) | 2022-11-09 | 2025-09-17 | C3S2 GmbH | Methods for manufacturing engineered immune cells |
| EP4658675A1 (en) | 2023-02-03 | 2025-12-10 | C3S2 GmbH | Methods for non-viral manufacturing of engineered immune cells |
| WO2024182516A1 (en) | 2023-02-28 | 2024-09-06 | Juno Therapeutics, Inc. | Cell therapy for treating systemic autoimmune diseases |
| WO2024182781A1 (en) | 2023-03-02 | 2024-09-06 | Vir Biotechnology, Inc. | Coronavirus compositions and uses thereof |
| EP4688826A1 (en) | 2023-04-04 | 2026-02-11 | Innate Pharma | Modular chimeric antigen receptor |
| EP4484441A1 (en) | 2023-06-26 | 2025-01-01 | Eberhard-Karls-Universität Tübingen | Mhc-class i derived polypeptide |
| WO2025083196A1 (en) | 2023-10-18 | 2025-04-24 | Tq Therapeutics Gmbh | A method of manufacturing a cellular therapy product and respective kits and devices |
| WO2025101820A1 (en) | 2023-11-08 | 2025-05-15 | Fred Hutchinson Cancer Center | Compositions and methods for cellular immunotherapy |
| WO2025238197A1 (en) | 2024-05-16 | 2025-11-20 | Iba Lifesciences Gmbh | Functionalized three-dimensional (3d) polymer scaffold for affinity chromatography |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19641876A1 (en) * | 1996-10-10 | 1998-04-16 | Inst Bioanalytik Gmbh | Streptavidin muteins |
| EP0965597A1 (en) * | 1996-12-27 | 1999-12-22 | Mochida Pharmaceutical Co., Ltd. | Cell membrane-directed drugs |
| WO2001098366A2 (en) * | 2000-06-19 | 2001-12-27 | Dyax Corp. | Enterokinase cleavage sequences and their use |
| WO2002038580A1 (en) * | 2000-10-31 | 2002-05-16 | The General Hospital Corporation | Streptavidin-binding peptides and uses thereof |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0198015B2 (en) | 1984-10-02 | 1995-07-19 | Biogen, Inc. | Production of streptavidin-like polypeptides |
| CA1340522C (en) * | 1987-03-10 | 1999-05-04 | Heinz Dobeli | Fusion proteins containing neighbouring histidines for improved purification |
| US5654176A (en) * | 1987-05-28 | 1997-08-05 | Amrad Corporation Limited | Fusion proteins containing glutathione-s-transferase |
| US5292646A (en) * | 1991-02-06 | 1994-03-08 | Genetics Institute, Inc. | Peptide and protein fusions to thioredoxin and thioredoxin-like molecules |
| DE4237113B4 (en) * | 1992-11-03 | 2006-10-12 | "Iba Gmbh" | Peptides and their fusion proteins, expression vector and method of producing a fusion protein |
| WO1996024606A1 (en) | 1995-02-09 | 1996-08-15 | University Of Washington | Modified-affinity streptavidin |
| CA2222035A1 (en) | 1995-04-11 | 1997-03-27 | Trustees Of Boston University | Streptavidin mutants |
| CA2241849A1 (en) * | 1996-01-05 | 1997-07-17 | Eli Lilly And Company | Fusion proteins comprising cell cycle regulatory proteins |
| WO1998040396A1 (en) | 1997-03-14 | 1998-09-17 | Trustees Of Boston University | Multiflavor streptavidin |
| US6841359B2 (en) * | 2000-10-31 | 2005-01-11 | The General Hospital Corporation | Streptavidin-binding peptides and uses thereof |
| DE10113776B4 (en) | 2001-03-21 | 2012-08-09 | "Iba Gmbh" | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein |
| AR059851A1 (en) * | 2006-03-16 | 2008-04-30 | Genentech Inc | ANTIBODIES OF EGFL7 AND METHODS OF USE |
-
2001
- 2001-03-21 DE DE10113776A patent/DE10113776B4/en not_active Expired - Fee Related
- 2001-10-12 EP EP01274019.7A patent/EP1370574B1/en not_active Expired - Lifetime
- 2001-10-12 WO PCT/EP2001/011846 patent/WO2002077018A1/en not_active Ceased
- 2001-12-17 US US10/026,578 patent/US7981632B2/en not_active Expired - Lifetime
-
2011
- 2011-07-18 US US13/185,070 patent/US8735540B2/en not_active Expired - Lifetime
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19641876A1 (en) * | 1996-10-10 | 1998-04-16 | Inst Bioanalytik Gmbh | Streptavidin muteins |
| US6103493A (en) * | 1996-10-10 | 2000-08-15 | Institut Fur Bioanalytic | Streptavidin muteins |
| EP0965597A1 (en) * | 1996-12-27 | 1999-12-22 | Mochida Pharmaceutical Co., Ltd. | Cell membrane-directed drugs |
| WO2001098366A2 (en) * | 2000-06-19 | 2001-12-27 | Dyax Corp. | Enterokinase cleavage sequences and their use |
| WO2002038580A1 (en) * | 2000-10-31 | 2002-05-16 | The General Hospital Corporation | Streptavidin-binding peptides and uses thereof |
Non-Patent Citations (5)
| Title |
|---|
| A. Skerra et.al., "Applications of a peptide ligand for streptavidin: the Strep-tag". In: Biomolecular Engineering, ISSN: 1389-0344, 1999, 16, 79-86 * |
| H. Takami, et.al., "Complete genome sequence of the alkaliphilic bacterium Bacillus halodurans and genomic sequence comparison with Bacillus subtilis". In: Nucleic Acids Res., ISSN 0305-1048, 2000, 28, 4317 - 4331 * |
| J.W. Jarvik, et.al., "Epitope Tagging". In: Annu. Rev. Genet., ISSN 0066-4197, 1998, 32, 601 - 618 * |
| R. Hernan, et.al., "Multiple epitope tagging of expressed proteins for enhanced detection". In: BioTechniques, ISSN 0736-6205, 2000, 28, 789 -793 * |
| T.G.M. Schmidt et.al., "Molecular Interaction between the Strep-tag affinity peptide and its cognate target, streptavidin". In: Journal of Molecular Biology, ISSN: 0022-2836, 1996, 255, 753-766 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1370574B1 (en) | 2018-05-09 |
| US20030083474A1 (en) | 2003-05-01 |
| US8735540B2 (en) | 2014-05-27 |
| DE10113776A1 (en) | 2002-10-02 |
| US7981632B2 (en) | 2011-07-19 |
| US20120149870A1 (en) | 2012-06-14 |
| WO2002077018A1 (en) | 2002-10-03 |
| EP1370574A1 (en) | 2003-12-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE10113776B4 (en) | Isolated streptavidin-binding, competitively elutable peptide, this comprehensive fusion peptide, nucleic acid coding therefor, expression vector, methods for producing a recombinant fusion protein and methods for detecting and / or obtaining the fusion protein | |
| DE19641876B4 (en) | streptavidin muteins | |
| EP0799890B1 (en) | Recombinant inactive core streptavidin mutants | |
| DE3650055T2 (en) | FIBROBLAST GROWTH FACTOR. | |
| DE68916537T2 (en) | PRODUCTION OF AN INSULIN-LIKE GROWTH FACTOR-BINDING PROTEIN. | |
| DE69006100T2 (en) | Fibronectin derivatives. | |
| DE4237113B4 (en) | Peptides and their fusion proteins, expression vector and method of producing a fusion protein | |
| DE69716905T2 (en) | ANALOGS OF THE GLUCAGON-LIKE PEPTIDES -2 | |
| DE68929096T2 (en) | Human rhinovirus receptor protein that inhibits susceptibility to virus infection | |
| EP0600372B1 (en) | Process for the preparation of proinsulin with correctly linked cystin bridges | |
| EP1481004B1 (en) | Streptavidin-binding peptide | |
| DE570027T1 (en) | T cell receptor, specific for antigen polypeptides and related polynucleotides. | |
| WO1996035718A1 (en) | Process for producing erythropoietin containing no animal proteins | |
| DE3689620T2 (en) | DNA MODIFIED BY CYS CODON. | |
| DE3650276T2 (en) | PROTEIN CLEANING. | |
| CA2385444A1 (en) | Humanin, a polypeptide suppressing neuronal death | |
| EP1353948B1 (en) | Soluble cyclic analogues of the beta amyloide peptide | |
| DD298948A5 (en) | NEW CYTOKINE | |
| EP1330655B1 (en) | Method for analyzing proteins | |
| DE69120409T2 (en) | METHOD FOR CLEANING RECOMBINANT PROTEINS AND PRODUCTS USEFUL FOR THIS | |
| DE19740310A1 (en) | Peptide with affinity for coagulation factor VIII | |
| DE3587721T2 (en) | Hormones and methods of making, using and testing the same. | |
| WO1989001485A1 (en) | Purification of raw peptides by preparative medium-pressure liquid chromatography | |
| DE69320961T2 (en) | Glutathione analog and paralogue series made of substances imitating glutathione | |
| DE102005011579B4 (en) | Affinity tags for protein purification, its production and use, and methods for purifying a protein |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OM8 | Search report available as to paragraph 43 lit. 1 sentence 1 patent law | ||
| 8127 | New person/name/address of the applicant |
Owner name: "IBA GMBH", 37079 GOETTINGEN, DE |
|
| 8110 | Request for examination paragraph 44 | ||
| R016 | Response to examination communication | ||
| R016 | Response to examination communication | ||
| R018 | Grant decision by examination section/examining division | ||
| R020 | Patent grant now final |
Effective date: 20121110 |
|
| R119 | Application deemed withdrawn, or ip right lapsed, due to non-payment of renewal fee |