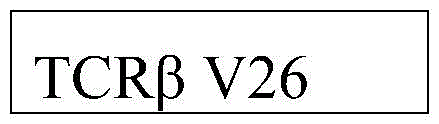CN116249718A - 结合至钙网蛋白的多功能性分子及其用途 - Google Patents
结合至钙网蛋白的多功能性分子及其用途 Download PDFInfo
- Publication number
- CN116249718A CN116249718A CN202180073493.XA CN202180073493A CN116249718A CN 116249718 A CN116249718 A CN 116249718A CN 202180073493 A CN202180073493 A CN 202180073493A CN 116249718 A CN116249718 A CN 116249718A
- Authority
- CN
- China
- Prior art keywords
- amino acid
- acid sequence
- seq
- sequence
- deletions
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
公开了多功能性分子,其包括i)结合至钙网蛋白的抗原结合结构域;以及以下中的一种、两种或全部:(ii)免疫细胞接合物(例如,选自NK细胞接合物、T细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物);(iii)细胞因子分子;和/或(iv)基质修饰部分。另外公开了编码多功能性分子的核酸、产生上述分子的方法以及使用上述分子治疗癌症的方法。
Description
相关申请
本申请要求于2020年8月26日提交的美国临时申请第63/070,769号的权益,其全部内容在此通过引用并入。
背景技术
骨髓增生性赘生物(MPN)是一组导致骨髓中血细胞异常生长的病况。常见的骨髓增生性赘生物包括原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)和慢性髓性白血病(CML)。原发性骨髓纤维化是一种慢性血癌,其中过多的瘢痕组织在骨髓中形成并损害骨髓产生正常血细胞的能力。考虑到对改进骨髓增生性赘生物(例如骨髓纤维化)治疗的持续需求,高度期望靶向骨髓增生性赘生物的新组合物和治疗。
发明内容
在一方面,本文尤其提供了一种包含多肽分子的组合物,其包含:(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,例如,表4、表5、表6、表24、表25、表16、表17、表18或表19的任一者中公开的钙网蛋白靶向性抗原结合结构域,以及(ii)结合至TCRβV的第二抗原结合结构域,例如,表30、表31、表32、表10、表11、表12或表13的任一者中公开的抗TCRβV抗原结合结构域,或结合至NKp30的第二抗原结合结构域,例如,表7、表8、表35、表36、表9、表10或表34中公开的抗NKp30抗原结合结构域。
在一些实施方案中,多肽分子是多功能性多肽分子。
在一些实施方案中,多肽分子是多特异性多肽分子。
在一些实施方案中,第二抗原结合结构域结合至TCRβV。
在一些实施方案中,第二抗原结合结构域激活T细胞,或第二抗原结合结构域不激活T细胞。
在一些实施方案中,第二抗原结合结构域结合至TCRβV12或TCRβV6(例如,包含SEQID NO:1044的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含如表30、表31、表32、表10、表11、表12或表13中所列的一个或多个氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含具有表30、表31、表10、表11、表12或表13中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表30、表31、表10、表11、表12或表13中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表30、表31、表10、表11、表12或表13中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,(ii)VL包含具有表30、表31、表10、表11、表12或表13中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表30、表31、表10、表11、表12或表13中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表30、表31、表10、表11、表12或表13中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:3A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:4A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:5A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQID NO:6A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:8A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:45A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:46A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:47A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:51A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:52A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:53A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(d)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:48A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:49A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:50A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:54A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:55A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:56A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含表30、表31、表10、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含表30、表31、表10、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),(iii)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(iv)VL包含SEQ ID NO:10A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:11A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:1312A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:1314A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:17A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:18A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:19A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:20A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:21A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:22A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:57A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:58A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:59A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:63A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:64A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:65A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:60A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:61A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:62A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:66A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:67A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:68A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:15A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:16A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含:SEQ ID NO:23A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:24A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或SEQ ID NO:25A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(ii)VL包含:SEQ ID NO:26A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:27A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:28A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:29A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或SEQ IDNO:30A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,如本文所述的组合物包含:第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL;第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRVβ)的第一部分(例如,结合至TCR(例如,TCRVβ)的第一scFv);第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRVβ)的任选第二部分(例如,结合至TCR(例如,TCRVβ)的第二scFv);第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,第二抗原结合结构域结合至NKp30。
在一些实施方案中,第二抗原结合结构域选自结合至(例如,激活)NKp30的抗体分子(例如,抗原结合结构域)或配体,例如,第二抗原结合结构域是结合至(例如,激活)NKp30的抗体分子或配体。
在一些实施方案中,第二抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表7、表35、表9、表10或表34的VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表7、表35、表9、表10或表34的VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,和/或(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表8、表36、表9、表10或表34的VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表8、表36、表9、表10或表34的VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3。
在一些实施方案中,第二抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7315的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7327的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7329的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)VH,该VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQ ID NO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(ii)VL,该VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQ ID NO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或(ii)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(1)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR4,和/或(2)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR4。
在一些实施方案中,第二抗原结合结构域包含:(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(i)VH,该VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL,该VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含轻链,该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链和轻链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
在一些实施方案中,如本文所述的组合物包含:第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL;第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体);第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体);第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合至位于钙网蛋白的C-末端内的表位,任选地其中第一抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,如本文所述的组合物进一步包含结合至第二钙网蛋白的第三抗原结合结构域,例如,其中第二钙网蛋白突变型蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中:(i)第三抗原结合结构域不同于第一抗原结合结构域,或(ii)第三抗原结合结构域与第一抗原结合结构域相同。
在一些实施方案中,第二钙网蛋白分子与第一抗原结合结构域结合的钙网蛋白分子相同。
在一些实施方案中,第二钙网蛋白分子不同于第一抗原结合结构域结合的钙网蛋白分子。
在一些实施方案中,第二钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中第二钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合的钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第三抗原结合结构域结合至位于第二钙网蛋白的C-末端内的表位,任选地其中第三抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,第一抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表4、表24、表25或表17中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3;(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表5、表24、表25或表18中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(iii)VH,该VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);(iv)VL,该VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);(v)VH,该VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR4,和/或(vi)VL,该VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR4。
在一些实施方案中,多功能性分子进一步包含肿瘤靶向部分。
在一些实施方案中,肿瘤靶向部分结合至肿瘤抗原。
在一些实施方案中,肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一些实施方案中,肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
在一些实施方案中,肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
在一些实施方案中,多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中多功能性分子与骨髓增生性赘生物细胞之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
在一些实施方案中,骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:骨髓增生性赘生物细胞不包含JAK2 V617F突变,或骨髓增生性赘生物细胞不包含MPL突变。
在一些实施方案中,如本文所述的组合物进一步包含接头,例如,第一抗原结合结构域和第二抗原结合结构域之间的接头。
在一些实施方案中,接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
在一些实施方案中,接头是肽接头。
在一些实施方案中,肽接头包含Gly和Ser。
在一些实施方案中,肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
在另一方面,本文提供了一种多功能性分子,其包含:(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,例如,表4、表5、表6、表24、表25、表16、表17、表18或表19的任一者中公开的钙网蛋白靶向性抗原结合结构域,以及(ii)结合至TCRβV的第二抗原结合结构域,例如,表30、表31、表32、表10、表11、表12或表13的任一者中公开的抗TCRβV抗原结合结构域,或结合至NKp30的第二抗原结合结构域,例如,表7、表8、表35、表36、表9、表10或表34中公开的抗NKp30抗原结合结构域。
在一些实施方案中,第二抗原结合结构域结合至TCRβV。
在一些实施方案中,第二抗原结合结构域激活T细胞,或第二抗原结合结构域不激活T细胞。
在一些实施方案中,第二抗原结合结构域结合至TCRβV12或TCRβV6(例如,包含SEQID NO:1044的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含如表30、表31、表32、表10、表11、表12或表13中所列的一个或多个氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含具有表30、表31、表10、表11、表12或表13中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表30、表31、表10、表11、表12或表13中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表30、表31、表10、表11、表12或表13中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,(ii)VL包含具有表30、表31、表10、表11、表12或表13中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表30、表31、表10、表11、表12或表13中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表30、表31、表10、表11、表12或表13中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:3A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:4A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:5A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQID NO:6A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:8A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:45A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:46A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:47A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:51A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:52A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:53A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(d)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:48A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:49A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:50A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:54A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:55A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:56A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含表30、表31、表10、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含表30、表31、表10、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),(iii)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(iv)VL包含SEQ ID NO:10A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:11A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:1312A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:1314A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:17A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:18A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:19A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:20A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:21A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:22A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:57A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:58A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:59A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:63A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:64A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:65A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:60A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:61A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:62A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或(ii)VL包含SEQ ID NO:66A的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:67A的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:68A的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(a)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:15A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL包含SEQ ID NO:16A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(b)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含:SEQ ID NO:23A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:24A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或SEQ ID NO:25A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(ii)VL包含:SEQ ID NO:26A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:27A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:28A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)、SEQ ID NO:29A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或SEQ IDNO:30A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,如本文所述的多功能性分子包含:第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL;第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRVβ)的第一部分(例如,结合至TCR(例如,TCRVβ)的第一scFv);第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRVβ)的任选第二部分(例如,结合至TCR(例如,TCRVβ)的第二scFv);第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ IDNO:6314的氨基酸序列的分子,任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,第二抗原结合结构域结合至NKp30。
在一些实施方案中,第二抗原结合结构域选自结合至(例如,激活)NKp30的抗体分子(例如,抗原结合结构域)或配体,例如,第二抗原结合结构域是结合至(例如,激活)NKp30的抗体分子或配体。
在一些实施方案中,第二抗原结合结构域包含:重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表7、表35、表9、表10或表34的VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表7、表35、表9、表10或表34的VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,和/或(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表8、表36、表9、表10或表34的VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表8、表36、表9、表10或表34的VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3。
在一些实施方案中,第二抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7315的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7327的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7329的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)VH,该VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQ ID NO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或(ii)VL,该VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQ ID NO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或(ii)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(1)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR4,和/或(2)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR4。
在一些实施方案中,第二抗原结合结构域包含:(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:(i)VH,该VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(ii)VL,该VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含轻链,该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链和轻链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
在一些实施方案中,如本文所述的多功能性分子包含:第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL;第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体);第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体);第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合至位于钙网蛋白的C-末端内的表位,任选地其中第一抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,如本文所述的多功能性分子进一步包含结合至第二钙网蛋白的第三抗原结合结构域,例如,其中第二钙网蛋白突变型蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中:(i)第三抗原结合结构域不同于第一抗原结合结构域,或(ii)第三抗原结合结构域与第一抗原结合结构域相同。
在一些实施方案中,第二钙网蛋白分子与第一抗原结合结构域结合的钙网蛋白分子相同。
在一些实施方案中,第二钙网蛋白分子不同于第一抗原结合结构域结合的钙网蛋白分子。
在一些实施方案中,第二钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中第二钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合的钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第三抗原结合结构域结合至位于第二钙网蛋白的C-末端内的表位,任选地其中第三抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,第一抗原结合结构域包含:(i)重链可变区(VH),该重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表4、表24、表25或表17中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3;(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表5、表24、表25或表18中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(iii)VH,该VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);(iv)VL,该VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);(v)VH,该VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR4,和/或(vi)VL,该VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR4。
在一些实施方案中,多功能性分子进一步包含肿瘤靶向部分。
在一些实施方案中,肿瘤靶向部分结合至肿瘤抗原。
在一些实施方案中,肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一些实施方案中,肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
在一些实施方案中,肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
在一些实施方案中,多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中多功能性分子与骨髓增生性赘生物细胞之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
在一些实施方案中,骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:骨髓增生性赘生物细胞不包含JAK2 V617F突变,或骨髓增生性赘生物细胞不包含MPL突变。
在一些实施方案中,如本文所述的多功能性分子进一步包含接头,例如,第一抗原结合结构域和第二抗原结合结构域之间的接头。
在一些实施方案中,接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
在一些实施方案中,接头是肽接头。
在一些实施方案中,肽接头包含Gly和Ser。
在一些实施方案中,肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
在另一方面,本文提供了一种核酸分子,其编码如本文所述的多功能性分子。
在另一方面,本文提供了一种载体,例如,表达载体,其包含如本文所述的核酸分子。
在另一方面,本文提供了一种细胞,其包含如本文所述的核酸分子或如本文所述的载体。
在另一方面,本文提供了一种制备(例如,产生)如本文所述的多功能性分子的方法,其包括在合适的条件(例如,适于基因表达和/或同源或异源二聚化的条件)下,培养如本文所述的细胞。
在另一方面,本文提供了一种药物组合物,其包含如本文所述的组合物、如本文所述的多功能性分子、如本文所述的核酸分子、如本文所述的载体或如本文所述的细胞以及药学上可接受的载剂、赋形剂、稀释剂或稳定剂。
在另一方面,本文提供了一种治疗癌症的方法,其包括向有需要的对象施用如本文所述的组合物、如本文所述的多功能性分子、如本文所述的核酸分子、如本文所述的载体、如本文所述的细胞或如本文所述的药物组合物,其中多功能性分子以有效治疗癌症的量施用。
在另一方面,本文提供了如本文所述的组合物、如本文所述的多功能性分子、如本文所述的核酸分子、如本文所述的载体或如本文所述的细胞在制造用于治疗癌症的药物中的用途。
在一些实施方案中,对象具有表达第一和/或第二钙网蛋白的癌细胞。
在一些实施方案中,对象具有JAK2 V617F突变。
在一些实施方案中,对象不具有JAK2 V617F突变。
在一些实施方案中,对象具有MPL突变。
在一些实施方案中,对象不具有MPL突变。
在一些实施方案中,癌症是血液癌症,任选地其中癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML),任选地其中癌症是骨髓纤维化。
在一些实施方案中,癌症是实体瘤癌症。
在一些实施方案中,如本文所述的方法或如本文所述的用途进一步包括施用第二种治疗性处理。
在一些实施方案中,第二种治疗性处理包括治疗性药剂(例如,化疗药剂、生物药剂、激素疗法)、放射或手术。
在一些实施方案中,治疗性药剂选自:化疗药剂或生物药剂。
在另一方面,本文提供了一种检测样品或对象中的钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法,其包括:使样品或对象与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及检测抗体分子与样品或对象之间复合物的形成,从而检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
在一些实施方案中,在体外或体内检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
在一些实施方案中,如本文所述的方法进一步包括使参考样品或对象与抗体分子接触;以及检测抗体分子与参考样品或对象之间复合物的形成,其中样品或对象中复合物的形成相对于参考样品或对象的变化(例如,统计学上显著的变化)指示样品或对象中存在钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
在一些实施方案中,如本文所述的方法进一步包括从对象获得样品。
在一些实施方案中,样品包含血浆、组织(例如,癌性组织)、活检、血液(例如,全血)、PBMC、骨髓和/或淋巴组织(例如,淋巴结)中的一种或多种。
在一些实施方案中,样品未经冷冻和/或固定。
在一些实施方案中,样品已经冷冻(例如,快速冷冻)和/或固定(例如,福尔马林固定石蜡包埋(FFPE))。
在一些实施方案中,对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
在一些实施方案中,如本文所述的方法进一步包括例如使用多面板方法进行流式分析。
在一些实施方案中,如本文所述的方法进一步包括评估T细胞克隆形成能力,例如,以确定T细胞恶性肿瘤的存在和/或水平。
在一些实施方案中,如本文所述的方法进一步包括测量来自生物样品的钙网蛋白+(例如,野生型钙网蛋白+和/或突变型钙网蛋白+)细胞的水平(例如,确定钙网蛋白+细胞例如相对于参考样品或对象是否耗尽)。
在一些实施方案中,如本文所述的方法进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的胞内水平。
在一些实施方案中,如本文所述的方法进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的膜水平。
在一些实施方案中,如本文所述的方法进一步包括例如在(例如,用本文所述的抗体分子)治疗后,评估对象的预后、严重程度或疾病或病症(例如,癌症,例如,骨髓纤维化)存在或不存在的变化。
在一些实施方案中,抗体分子被可检测地标记。
在另一方面,本文提供了一种评估对象的方法,其包括:使来自对象的样品(例如,本文所述的样品)与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及检测抗体分子与样品之间复合物的形成,从而评估对象。
在一些实施方案中,对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
在一些实施方案中,对象尚未用本文所述的抗体分子治疗。
在一些实施方案中,对象已用本文所述的抗体分子治疗。
在另一方面,本文提供了一种试剂盒,其包含本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子和针对用于检测样品或对象中钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法的说明书。
本领域技术人员将认识到或仅使用常规实验的方法就能够确定本文所述的本发明具体实施方案的许多等效物。这些等效物旨在被以下实施方案涵盖。
除非另有定义,否则本文所用的所有技术和科学术语具有与本发明所属领域的普通技术人员的通常理解相同的含义。尽管在本发明的实践或测试中可以使用与本文所述的方法和材料相似或等效的那些,但下文描述了合适的方法和材料。本文提及的所有出版物、专利申请、专利和其他参考文献通过引用以它们的整体并入。在冲突的情况下,以本说明书(包括定义)为准。另外,材料、方法和实施例仅是说明性的,而非限制性的。
本发明的其他特征和优点将从以下详细描述和权利要求中显而易见。
附图说明
本专利或申请文件含有至少一张彩色附图。带有彩色附图的本专利或专利申请公开的副本将在收到请求并支付必要费用后由专利局提供。
图1A-1B示出了抗体A源小鼠VH和VL框架1、CDR1、框架2、CDR2、框架3、CDR3和框架4区与它们各自的人源化序列的比对。Kabat CDR以粗体示出,Chothia CDR以斜体示出,组合CDR以方框示出。回复突变的框架位置用双下划线表示。图1A示出了鼠抗体A的VH序列(SEQID NO:1A)和人源化抗体A-H的VH序列(SEQ ID NO:9A)。图1B示出了鼠抗体A(SEQ ID NO:2A)的VL序列和人源化抗体A-H的VL序列(SEQ ID NO:10A和SEQ ID NO:11A)。
图2A-2B示出了抗体B源小鼠VH和VL框架1、CDR1、框架2、CDR2、框架3、CDR3和框架4区与它们各自的人源化序列的比对。Kabat CDR以粗体示出,Chothia CDR以斜体示出,组合CDR以方框示出。回复突变的框架位置用双下划线表示。图2A示出了鼠抗体B的VH序列(SEQID NO:15A)和人源化VH序列B-H.1A至B-H.1C(SEQ ID NO:23A-25A)。图2B示出了鼠抗体B的VL序列(SEQ ID NO:16A)和人源化VL序列B-H.1D至B-H.1H(SEQ ID NO:26A-30A)。
图3描绘了TCRBV基因家族和亚家族的系统发生树,其中相应的抗体被绘图。亚家族身份如下:亚家族A:TCRβV6;亚家族B:TCRβV10;亚家族C:TCRβV12;亚家族D:TCRβV5;亚家族E:TCRβV7;亚家族F:TCRβV11;亚家族G:TCRβV14;亚家族H:TCRβV16;亚家族I:TCRβV18;亚家族J:TCRβV9;亚家族K:TCRβV13;亚家族L:TCRβV4;亚家族M:TCRβV3;亚家族N:TCRβV2;亚家族O:TCRβV15;亚家族P:TCRβV30;亚家族Q:TCRβV19;亚家族R:TCRβV27;亚家族S:TCRβV28;亚家族T:TCRβV24;亚家族U:TCRβV20;亚家族V:TCRβV25;以及亚家族W:TCRβV29亚家族。亚家族成员在本文标题为“TCRβV”的部分中详细描述。
图4A-4C示出了抗TCR Vβ13.1抗体(A-H.1)激活6天的人CD3+T细胞。使用磁珠分离(阴性选择)来分离人CD3+T细胞,并用100nM的固定化(板包被)抗TCR Vβ13.1(A-H.1)或抗CD3ε(OKT3)抗体激活6天。图4A示出了扩增的T细胞的两个散点图(左图:用OKT3激活;右图:用A-H.1激活),使用抗TCR Vβ13.1(A-H.1)和随后的二级荧光染料缀合抗体的流式细胞术分析评估了该T细胞的TCR Vβ13.1表面表达。图4B示出了抗TCR Vβ13.1(A-H.1)或抗CD3e(OKT3)激活的TCR Vβ13.1阳性T细胞相对于总T细胞(CD3+)的百分比(%)。图4C示出了通过以60μl/min的恒定速率对每个T细胞亚群门控(CD3或TCR Vβ13.1)中的事件数进行20秒计数获得的相对细胞计数。数据显示为3个供体的平均值。
图5A-5B示出了抗TCR Vβ13.1抗体(A-H.1)激活的人CD3+T细胞对转化细胞系RPMI8226的细胞溶解活性。图5A描绘了用A-H.1或OKT3激活的人CD3+T细胞的靶细胞裂解。使用磁珠分离(阴性选择)来分离人CD3+T细胞,并用指定浓度的固定化(板包被)A-H.1或OKT3激活4天,然后以5∶1的比率(E∶T)与RPMI 8226细胞共培养2天。接着使用流式细胞术分析,通过FACS染色CFSE/CD138-标记的和膜不可渗透的DNA染料(DRAQ7)来分析样品RPMI 8226细胞的细胞裂解。图5B示出了用A-H.1或OKT3激活的人CD3+T细胞的靶细胞裂解,其以5∶1的比率(E∶T)与RPMI-8226一起孵育6天,随后如上所述分析RPMI 8226细胞的细胞裂解。靶细胞裂解百分比(%)通过使用以下公式:[(x-基础)/(100%-基础),其中x是样品的细胞裂解]标准化为基础靶细胞裂解(即无抗体处理)来确定。所示数据代表n=1个供体。
图6A-6B示出了用指定抗体激活的人PBMC产生IFNg。从指定数量供体的全血中分离人PBMC,随后用100Nm的所示抗体进行固相(板包被)刺激。在第1、2、3、5或6天收集上清液。图6A是比较在激活后第1、2、3、5或6天用抗TCR Vβ13.1抗体(A-H.1或A-H.2)或抗CD3e抗体(OKT3或SP34-2)激活的指定抗体激活的人PBMC中IFNg产生的图。图6B示出了在激活后第1、2、3、5或6天用指定抗TCR Vβ13.1抗体或抗CD3e抗体(OKT3)激活的指定抗体激活的人PBMC中的IFNg产生。
图7A-7B示出了用指定抗体激活的人PBMC产生IL-2。使用与图6A-6B所述相似的实验设置。
图8A-8B示出了用指定抗体激活的人PBMC产生IL-6。使用与图6A-6B所述相似的实验设置。
图9A-9B示出了用指定抗体激活的人PBMC产生TNF-α。使用与图6A-6B所述相似的实验设置。
图10A-10B示出了用指定抗体激活的人PBMC产生IL-1β。使用与图6A-6B所述相似的实验设置。
图11A-11B是显示当与抗CD3e抗体OKT3激活的PBMC相比时,抗TCR Vβ13.1抗体A-H.1激活的人PMBC中IFNg分泌的延迟动力学的图。
图11A示出了来自4个供体的IFNg分泌数据。图11B示出了来自4个另外供体的IFNg分泌数据。所示数据代表n=8个供体。
图12描绘了与抗CD3e抗体(OKT3或SP34-2)激活的PBMC相比,抗TCR Vβ13.1抗体(A-H.1或A-H.2)激活的人PBMC中增加的CD8+TSCM和Temra T细胞亚群。
图13A-13F示出了抗TCRVb抗体的表征。图13A是描绘用抗CD3(OKT3)抗体或抗TCRVb抗体激活的T细胞增殖的图。图13B示出了用抗TCRVb抗体选择性扩增CD45RA+效应记忆CD8+和CD4+T细胞(TEMRA)细胞。Tn=幼稚T细胞;Tscm=干细胞记忆T细胞;Tcm=中央记忆T细胞;Tem=效应记忆T细胞;Temra=效应记忆CD45RA+T细胞。图13C是显示用抗TCRVb抗体或抗CD3抗体刺激的PBMC分泌IFN-g的图。图13D示出了用抗TCRVb抗体或抗CD3抗体刺激的T细胞的靶细胞裂解。刺激细胞4天,随后与多发性骨髓瘤靶细胞一起孵育2天,用于评估细胞杀伤。图13E是显示用抗TCRVb抗体或抗CD3抗体刺激的T细胞分泌穿孔素的图。用100ng/ml结合板的抗体刺激5天后,通过FACS染色分析PBMC中TCRVB阳性和TCRVB阴性T细胞中的穿孔素。图13F是显示用抗TCRVb抗体或抗CD3抗体刺激的T细胞的粒酶B的图。用100ng/ml结合板的抗体刺激5天后,通过FACS染色分析PBMC中TCRVB阳性和TCRVB阴性T细胞中的粒酶B。
图14A-14B示出了通过用抗TCRVb抗体以100nM的剂量刺激PBMC 6天的IL-2和IL-15产生和人NK细胞扩增。图14A示出了用抗TCRVb抗体或抗CD3抗体刺激的T细胞中IL-2或IL-15的分泌。图14B描绘了显示用抗TCRVb抗体或抗CD3抗体或对照样品刺激的细胞中NKp46染色对比CD56抗体染色的流式细胞术点图。
图15A-15C示出了用抗TCRVb抗体或抗CD3抗体刺激的PBMC中细胞因子的分泌。
图16A-16B示出了双重靶向性BCMA-TCRvb抗体分子对MM细胞的杀伤。图16A示出了以下双重靶向性抗体分子中的一种的体外杀伤:BCMA-TCRVb、BCMA-CD3,或对照-TCRVb;或同种型对照。图16B示出了双重靶向性BCM-TCRVb抗体对MM细胞的体内杀伤。
图17示出了用识别一个臂上的FcRH5和另一个臂上的TCRVb的双重靶向性抗体裂解MM靶细胞。
图18A-18C是附接至二聚化模块(例如,免疫球蛋白恒定区)的功能性部分的示例性形式和构型的示意图。图18A描绘了与异源二聚体Fc结构域共价连接的部分A、B、C和D。图18B描绘了与同源二聚体Fc结构域共价连接的部分A、B、C和D。图18C描绘了与异源二聚体重链和轻链恒定结构域(例如,Fab CH1和Fab CL)共价连接的部分A、B、C和D。在一些实施方案中,功能性部分是结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的抗原结合结构域。在一些实施方案中,功能性部分是以大致相同的亲和力结合至野生型钙网蛋白和钙网蛋白突变型蛋白的抗原结合结构域。在一些实施方案中,功能性部分是优先结合至钙网蛋白突变型蛋白而非野生型钙网蛋白的抗原结合结构域,例如,其中第一钙网蛋白突变型蛋白包含SEQ ID NO:6286的氨基酸序列,并且野生型钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。在一些实施方案中,功能性部分是免疫细胞接合物,其选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物。在一些实施方案中,功能性部分是细胞因子分子。在一些实施方案中,功能性部分是基质修饰部分。
图19A和19B是包含结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第一抗原结合结构域(例如,第一Fab)、结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第二抗原结合结构域(例如,第二Fab)以及结合至CD3的一个或多个部分(例如,结合至CD3的scFv)的多功能性分子的示例性形式和构型的示意图。在一个实施方案中,第一抗原结合结构域(例如,第一Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQ ID NO:6113或6314的氨基酸序列的钙网蛋白突变型蛋白。在一个实施方案中,第二抗原结合结构域(例如,第二Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQ ID NO:6313或6314的氨基酸序列的钙网蛋白突变型蛋白。
图20A和20B是包含结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第一抗原结合结构域(例如,第一Fab)、结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第二抗原结合结构域(例如,第二Fab)以及结合至TCR(例如,TCRβ)的一个或多个部分(例如,结合至TCR(例如,TCRβ)的scFv)的多功能性分子的示例性形式和构型的示意图。在一个实施方案中,第一抗原结合结构域(例如,第一Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQID NO:6313或6314的氨基酸序列的钙网蛋白突变型蛋白。在一个实施方案中,第二抗原结合结构域(例如,第二Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQ ID NO:6313或6314的氨基酸序列的钙网蛋白突变型蛋白。
图21A和21B是包含结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第一抗原结合结构域(例如,第一Fab)、结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的第二抗原结合结构域(例如,第二Fab)以及结合至NKp30的一个或多个部分(例如,结合至NKp30的抗体分子或配体)的多功能性分子的示例性形式和构型的示意图。在一个实施方案中,第一抗原结合结构域(例如,第一Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQ IDNO:6313或6314的氨基酸序列的钙网蛋白突变型蛋白。在一个实施方案中,第二抗原结合结构域(例如,第二Fab)结合至本文公开的钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白),例如,表2或3中公开的钙网蛋白突变型蛋白,例如,表2或3中公开的1型或2型钙网蛋白突变型蛋白,例如,包含SEQ ID NO:6313或6314的氨基酸序列的钙网蛋白突变型蛋白。
图22是显示NKp30抗体与NK92细胞结合的图。数据计算为百分比-AF747阳性群体。
图23是显示NKp30抗体激活NK92细胞的图。使用仓鼠抗NKp30mAb生成数据。
图24A-24D是显示包含TGFβ抑制剂的示例性多特异性分子的示意图。在一些实施方案中,TGFβ抑制剂包含TGF-β受体ECD同源二聚体。在一些实施方案中,TGFβ抑制剂包含TGFBR2 ECD异源二聚体。在图24A和24B中,两个TGFBR ECD结构域与两个Fc区的C-末端连接。在一些实施方案中,图24A或24B中所示的CH1-Fc-TGFBR ECD区包含SEQ ID NO:6405或3193的氨基酸序列。在一些实施方案中,图24A或24B中所示的Fc-TGFBR ECD区包含SEQ IDNO:6407或6408的氨基酸序列。在图24C和24D中,两个TGFBR ECD结构域分别与CH1和CL连接。在一些实施方案中,图24C或24D中所示的TGFBR ECD-CH1-Fc区包含SEQ ID NO:6409或6410的氨基酸序列。在一些实施方案中,图24C或24D中所示的TGFBR ECD-CL区包含SEQ IDNO:6411或6412的氨基酸序列。在一些实施方案中,多特异性分子包含结合部分A和结合部分B。在一些实施方案中,结合部分A或结合部分B是本文公开的钙网蛋白靶向性抗原结合结构域。
图25A-25B是一系列显示酶联免疫吸附测定(ELISA)结果的图,其显示亲本IgG形式的抗体6C10(BKM0106)与野生型钙网蛋白(CALR WT)和两种钙网蛋白突变体(CALR ins和CALR del,如本文所述)的结合水平。图25A示出了在板上包被指定抗原(CALR WT、CALR ins或CALR del)时的ELISA结果。图25B示出了在板上包被BKM0106抗体时的ELISA结果。
图26A-26B是一系列显示亲本IgG形式的抗体6C10(BKM0106)与表达两种钙网蛋白突变体(CALR ins和CALR del,如本文所述)中的一种的细胞的结合的图,如通过FACS所评估的。
图27是显示各种抗体分子在体内鼠骨髓纤维化模型中的治疗效果的图。测试的抗体分子包括针对突变型钙网蛋白(mtCalR)的ADCC启用抗体分子、包含mtCalR结合结构域和对另一种靶(即,TCRvβ或CD3)具有特异性的第二结合结构域以及LALAPG变体Fc区的双特异性抗体。将初始小鼠脾和媒介物用作对照。
图28是显示如本文所述的示例性抗CD3抗体分子BKM0020、BKM0025、BKM0028、BKM0038与人CD3e(huCD3e)和食蟹猴CD3e(cCD3e)的体外结合的表。
图29是显示如本文所述的示例性抗CD3抗体分子BKM0020与表达人CD3e(huCD3e)的Jurkat细胞的结合的图。
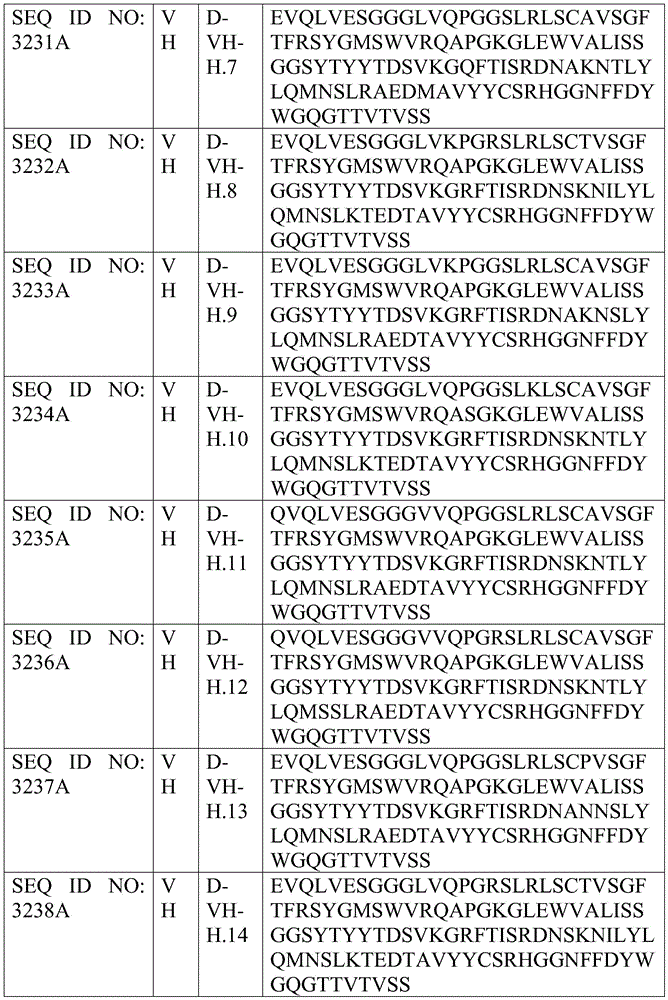
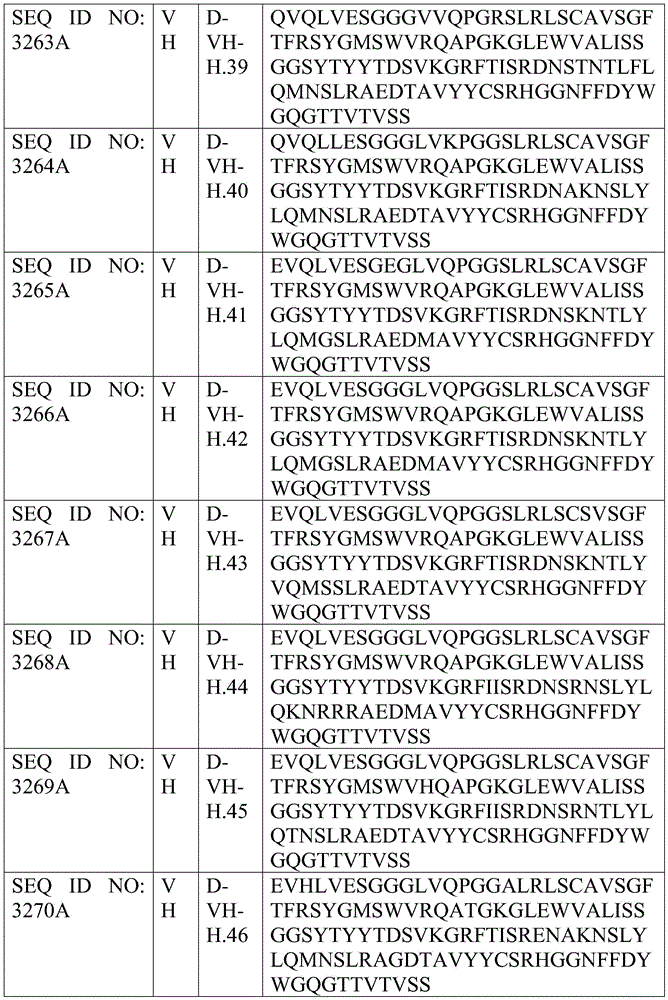
图30A和30B是显示亲和力成熟的人源化抗体A-H序列的比对的示意图。图30A示出了亲和力成熟的人源化抗体A-H VL序列的比对(按照出现的顺序分别为SEQ ID NO:3377A-3389A)。图30B示出了亲和力成熟的人源化抗体A-H VH序列的比对(按照出现的顺序分别为SEQ ID NO:3390A-3436A)。
具体实施方案
本文公开了包含多种(例如,两种或更多种)功能性(或结合特异性)的多功能性分子(本文也称为“多特异性分子”),其包含(i)结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的抗原结合结构域,例如,其中钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,以及(ii)以下中的一种、两种或全部:(a)免疫细胞接合物,其选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物;(b)细胞因子分子;(c)基质修饰部分,以及(d)肿瘤靶向部分(例如,其结合至选自以下的肿瘤抗原:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1)。在一些实施方案中,抗原结合结构域结合至钙网蛋白(例如,野生型钙网蛋白或突变型钙网蛋白,例如,如本文所述的)。在一些实施方案中,抗原结合结构域结合至表2或表3中公开的钙网蛋白突变型蛋白。在一些实施方案中,抗原结合结构域结合至表2或表3中公开的1型钙网蛋白突变型蛋白。在一些实施方案中,抗原结合结构域结合至表2或表3中公开的2型钙网蛋白突变型蛋白。在一些实施方案中,抗原结合结构域结合至表2或表3中公开的1型和2型钙网蛋白突变型蛋白。在一些实施方案中,T细胞接合物包含结合至TCRβ亚基可变链(TCRβV)(例如,TCRβV6或TCRβV12)的另外的抗原结合结构域。
在实施方案中,多特异性或多功能性分子是双特异性(或双功能性)分子、三特异性(或三功能性)分子或四特异性(或四功能性)分子。在实施方案中,多特异性或多功能性分子是双特异性分子。
不受理论束缚,预期本文公开的多特异性或多功能性分子在表达钙网蛋白的细胞存在下,例如在表面上定位(例如,桥接)和/或激活免疫细胞(例如,选自T细胞、NK细胞、B细胞、树突细胞或巨噬细胞的免疫效应细胞)。在表达钙网蛋白的细胞存在下,预期使用本文所述的多特异性或多功能性分子增加免疫细胞的接近度和/或活性增强了针对靶细胞的免疫应答,从而提供更有效的疗法。
公开了包括(i)基质修饰部分和(ii)结合至钙网蛋白(例如,野生型钙网蛋白和/或钙网蛋白突变型蛋白)的抗原结合结构域的新型多功能性(例如,多特异性)分子,例如,其中钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列。不受理论束缚,认为本文公开的多功能性分子尤其靶向(例如,定位于)癌症部位,并改变肿瘤基质,例如,改变癌症部位附近的肿瘤微环境。多功能性分子可以进一步包括以下中的一种或两种:免疫细胞接合物(例如,选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物中的一种、两种、三种或全部);和/或细胞因子分子。因此,本文尤其提供了包括上述部分的多功能性(例如,多特异性)分子、编码其的核酸、产生上述分子的方法,以及使用上述分子治疗癌症的方法。
因此,本文尤其提供了包括上述部分的多特异性或多功能性分子(例如;多特异性或多功能性抗体分子)、编码其的核酸、产生上述分子的方法,以及使用上述分子治疗疾病或病症(例如,癌症)的方法。
定义
在一些实施方案中,多功能性分子包括免疫细胞接合物。“免疫细胞接合物”是指结合和/或激活免疫细胞(例如,参与免疫应答的细胞)的一种或多种结合特异性。在一些实施方案中,免疫细胞选自T细胞、NK细胞、B细胞、树突细胞和/或巨噬细胞。免疫细胞接合物可以是结合至免疫细胞抗原(例如,T细胞、NK细胞抗原、B细胞抗原、树突细胞抗原和/或巨噬细胞抗原)的抗体分子、受体分子(例如,全长受体、受体片段或其融合体(例如,受体-Fc融合体))或配体分子(例如,全长配体、配体片段或其融合体(例如,配体-Fc融合体))。在一些实施方案中,免疫细胞接合物特异性结合至靶免疫细胞,例如,优先结合至靶免疫细胞。例如,当免疫细胞接合物是抗体分子时,其以小于约10nM的解离常数结合至免疫细胞抗原(例如,T细胞抗原、NK细胞抗原、B细胞抗原、树突细胞抗原和/或巨噬细胞抗原)。
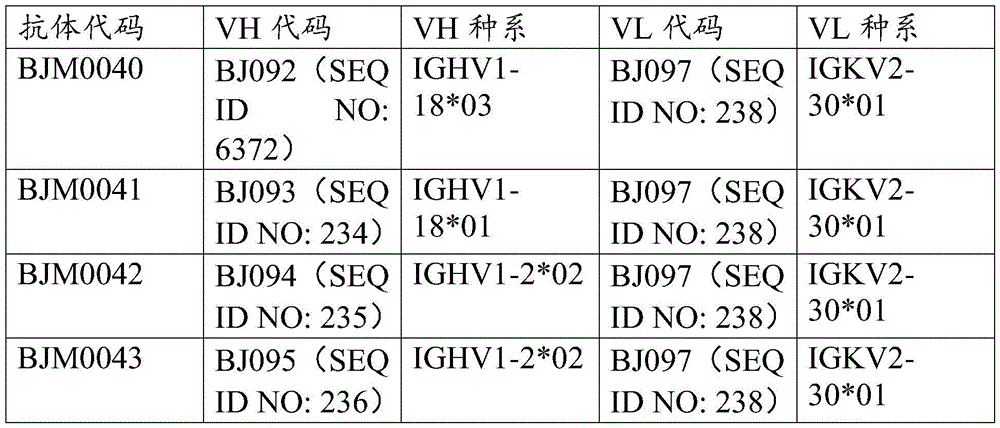
如本文所用,术语“T细胞受体β可变链”、“TCRVβ”、“TCRVb”和“TCRβV”可互换使用,是指包含T细胞受体抗原识别结构域的T细胞受体β链胞外区。术语TCRVβ或TCRβV包括哺乳动物同种型,例如,人TCRβV,人的物种同源物和包含至少一个与TCRβV共同表位的类似物。人TCRβV包含基因家族,该基因家族包含亚家族,包括但不限于:TCRβV6亚家族、TCRβV10亚家族、TCRβV12亚家族、TCRβV5亚家族、TCRβV7亚家族、TCRβV11亚家族、TCRβV14亚家族、TCRβV16亚家族、TCRβV18亚家族、TCRβV9亚家族、TCRβV13亚家族、TCRβV4亚家族、TCRβV3亚家族、TCRβV2亚家族、TCRβV15亚家族、TCRβV30亚家族、TCRβV19亚家族、TCRβV27亚家族、TCRβV28亚家族、TCRβV24亚家族、TCRβV20亚家族、TCRβV25亚家族,或TCRβV29亚家族。在一些实施方案中,TCRβV6亚家族包含:TCRβV6-4*01、TCRβV6-4*02、TCRβV6-9*01、TCRβV6-8*01、TCRβV6-5*01、TCRβV6-6*02、TCRβV6-6*01、TCRβV6-2*01、TCRβV6-3*01或TCRβV6-1*01在一些实施方案中,TCRβV包含TCRβV6-5*01。TCRβV6-5*01也称为TRBV65;TCRBV6S5;TCRBV13S1或TCRβV13.1。TCRβV6-5*01(例如,人TCRβV6-5*01)的氨基酸序列是本领域已知的,例如,由IMGTID L36092提供。在一些实施方案中,TCRβV6-5*01由SEQ ID NO:1043的核酸序列或与其具有85%、90%、95%、99%或更多同一性的序列编码。在一些实施方案中,TCRβV6-5*01包含SEQ ID NO:1044的氨基酸序列,或与其具有85%、90%、95%、99%或更多同一性的序列。
在一些实施方案中,多功能性分子包括细胞因子分子。如本文所用,“细胞因子分子”是指细胞因子的全长、片段或变体;细胞因子进一步包含受体结构域,例如,细胞因子受体二聚化结构域;或细胞因子受体的激动剂,例如,细胞因子受体的抗体分子(例如,激动性抗体),其引发天然存在的细胞因子的至少一种活性。在一些实施方案中,细胞因子分子选自白介素-2(IL-2)、白介素-7(IL-7)、白介素-12(IL-12)、白介素-15(IL-15)、白介素-18(IL-18)、白介素-21(IL-21)或干扰素γ,或其片段或变体,或上述细胞因子中任一种的组合。细胞因子分子可以是单体或二聚体。在一些实施方案中,细胞因子分子可进一步包括细胞因子受体二聚化结构域。在其他实施方案中,细胞因子分子是细胞因子受体的激动剂,例如,选自IL-15Ra或IL-21R的细胞因子受体的抗体分子(例如,激动性抗体)。
如本文所用,如在例如抗体分子、细胞因子分子、受体分子中使用的术语“分子”包括全长天然存在的分子以及变体,例如,功能性变体(例如,截短、片段、突变(例如,基本上相似的序列)或其衍生形式),只要未修饰的(例如,天然存在的)分子的至少一种功能和/或活性仍保留。
在一些实施方案中,多功能性分子包括基质修饰部分。如本文所用,“基质修饰部分”是指能够改变(例如,降解)基质组分的试剂,例如,蛋白质(例如,酶)。在一些实施方案中,基质组分选自例如ECM组分,例如,糖胺聚糖,例如,透明质酸(也称为玻尿酸或HA)、硫酸软骨素、软骨素、硫酸皮肤素、硫酸肝素、肝素、巢蛋白、腱生蛋白、聚集蛋白聚糖和硫酸角蛋白;或胞外蛋白,例如,胶原、层粘连蛋白、弹性蛋白、纤维蛋白原、纤连蛋白和玻连蛋白。
某些术语定义如下。
如本文所用,冠词“一个”和“一种”是指一个或多于一个(例如,至少一个)该冠词的语法对象。当在本文中与术语“包含”结合使用时,词语“一个”的使用可以表示“一个”,但它也符合“一个或多个”、“至少一个”和“一个或多于一个”的含义。
如本文所用,“约”和“大致”通常是指在给定测量的性质或精度的情况下测量量的可接受的误差程度。示例性误差程度在给定值范围的20%内,通常在10%内,更通常在5%内。
如本文所用,“抗体分子”是指包含至少一个免疫球蛋白可变结构域序列的蛋白质,例如,免疫球蛋白链或其片段。抗体分子包括抗体(例如,全长抗体)和抗体片段。在实施方案中,抗体分子包含全长抗体的抗原结合片段或功能性片段,或全长免疫球蛋白链。例如,全长抗体是天然存在的或通过正常免疫球蛋白基因片段重组过程形成的免疫球蛋白(Ig)分子(例如,IgG抗体)。在一些实施方案中,抗体分子是指免疫球蛋白分子的免疫活性抗原结合部分,例如抗体片段。抗体片段(例如,功能性片段)是抗体的一部分,例如,Fab、Fab’、Fab’、F(ab’)2、F(ab)2、可变片段(Fv)、结构域抗体(dAb)或单链可变片段(scFv)。功能性抗体片段结合至与由完整(例如,全长)抗体识别的抗原相同的抗原。术语“抗体片段”或“功能性片段”还包括由可变区组成的分离的片段,例如由重链和轻链可变区组成的“Fv”片段或其中轻链和重链可变区通过肽接头连接的重组单链多肽分子(“scFv蛋白”)。在一些实施方案中,抗体片段不包括无抗原结合活性的抗体部分,例如Fc片段或单个氨基酸残基。示例性抗体分子包括全长抗体和抗体片段,例如,dAb(结构域抗体)、单链、Fab、Fab’和F(ab’)2片段,以及单链可变片段(scFv)。
如本文所用,“免疫球蛋白可变结构域序列”是指可形成免疫球蛋白可变结构域结构的氨基酸序列。例如,该序列可包括天然存在的可变结构域的全部或部分氨基酸序列。例如,该序列可包括或可不包括一个、两个或更多个N-或C-末端氨基酸,或者可包括与蛋白质结构的形成相容的其他改变。
在一些实施方案中,抗体分子是单特异性的,例如,其包含对单个表位的结合特异性。在一些实施方案中,抗体分子是多特异性的,例如,其包含多个免疫球蛋白可变结构域序列,其中第一免疫球蛋白可变结构域序列对第一表位具有结合特异性,第二免疫球蛋白可变结构域序列对第二表位具有结合特异性。在一些实施方案中,抗体分子是双特异性抗体分子。如本文所用,“双特异性抗体分子”是指对多于一个(例如,两个、三个、四个或更多个)表位和/或抗原具有特异性的抗体分子。
如本文所用,“抗原”(Ag)是指可激发免疫应答的分子,例如,涉及某些免疫细胞的激活和/或抗体生成。任何大分子(包括几乎所有的蛋白质或肽)都可以是抗原。抗原也可以来源于基因组重组体或DNA。例如,包含编码能够引发免疫应答的蛋白质的核苷酸序列或部分核苷酸序列的任何DNA编码“抗原”。在一些实施方案中,抗原不需要仅由基因的全长核苷酸序列编码,抗原也根本不需要由基因编码。在一些实施方案中,抗原可以是合成的或可以来源于生物样品,例如,组织样品、肿瘤样品、细胞或具有其他生物组分的流体。如本文所用,“肿瘤抗原”或可互换的“癌症抗原”包括存在于癌症(例如,可激发免疫应答的癌细胞或肿瘤微环境)上或与其相关的任何分子。如本文所用,“免疫细胞抗原”包括存在于可激发免疫应答的免疫细胞上或与其相关的任何分子。
抗体分子的“抗原结合位点”或“结合部分”是指参与抗原结合的抗体分子(例如免疫球蛋白(Ig)分子)的一部分。在一些实施方案中,抗原结合位点由重(H)链和轻(L)链可变(V)区的氨基酸残基形成。重链和轻链可变区内的三个高度不同的区段被称为高变区,设置在称为“框架区”(FR)的更保守的侧翼区段之间。FR是天然存在于免疫球蛋白高变区之间和与其相邻的氨基酸序列。在一些实施方案中,在抗体分子中,轻链的三个高变区和重链的三个高变区在三维空间中彼此相对设置,以形成抗原结合表面,其与被结合抗原的三维表面互补。重链和轻链中每一条的三个高变区被称为“互补决定区”或“CDR”。框架区和CDR已在例如Kabat,E.A.,等人,(1991)Sequences of Proteins of Immunological Interest,第5版,U.S.Department of Health and Human Services,NIH公布第91-3242号和Chothia,C.等人,(1987)J.Mol.Biol.196:901-917中定义和描述。每条可变链(例如,可变重链和可变轻链)通常由三个CDR和四个FR组成,从氨基末端至羧基末端按氨基酸顺序排列:FR1、CDR1、FR2、CDR2、FR3、CDR3和FR4。
如本文所用,“癌症”可以包括所有类型的致癌过程和/或癌性生长。在一些实施方案中,癌症包括原发性肿瘤以及转移性组织或恶性转化细胞、组织或器官。在一些实施方案中,癌症包括癌症的所有组织病理学和阶段,例如,侵袭性/严重性的阶段。在一些实施方案中,癌症包括复发性和/或抗性癌症。术语“癌症”和“肿瘤”可互换使用。例如,这两个术语都包括实体和液体肿瘤。如本文所用,术语“癌症”或“肿瘤”包括恶化前以及恶性癌症和肿瘤。
如本文所用,“免疫细胞”是指在免疫系统中起作用的各种细胞中的任一种,例如,以抵御感染剂和外来物质。在一些实施方案中,该术语包括白细胞,例如,嗜中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、淋巴细胞和单核细胞。先天的白细胞包括吞噬细胞(例如,巨噬细胞、嗜中性粒细胞和树突细胞)、肥大细胞、嗜酸性粒细胞、嗜碱性粒细胞和自然杀伤细胞。先天的白细胞通过接触攻击较大的病原体或通过吞噬然后杀死微生物来鉴定和消除病原体,并且是适应性免疫应答激活的介质。适应性免疫系统的细胞是特殊类型的白细胞,称为淋巴细胞。B细胞和T细胞是淋巴细胞的重要类型,来源于骨髓中的造血干细胞。B细胞参与体液免疫应答,而T细胞参与细胞介导的免疫应答。术语“免疫细胞”包括免疫效应细胞。
如本文所用,术语“免疫效应细胞”是指参与免疫应答(例如,促进免疫效应应答)的细胞。免疫效应细胞的实例包括但不限于T细胞,例如,α/βT细胞和γ/δT细胞、B细胞、自然杀伤(NK)细胞、自然杀伤T(NK T)细胞和肥大细胞。
术语“效应功能”或“效应应答”是指细胞的特定功能。例如,T细胞的效应功能可以是细胞溶解活性或辅助活性,包括细胞因子的分泌。
本发明的组合物和方法包括多肽和核酸,该多肽和核酸具有指定序列或与其基本上相同或相似的序列,例如,与指定序列至少80%、85%、90%、95%相同或更高的序列。在氨基酸序列的背景下,术语“基本上相同”在本文中用于指含有足够或最小数量的氨基酸残基的第一氨基酸,该氨基酸残基i)与第二氨基酸序列中的比对氨基酸残基相同,或ii)保守置换,使得第一和第二氨基酸序列可具有共同的结构结构域和/或共同的功能活性。例如,含有共同结构结构域的与参考序列(例如,本文提供的序列)具有至少约80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列。
在核苷酸序列的背景下,术语“基本上相同”在本文中用于指含有足够或最小数量的核苷酸的第一核酸序列,该核苷酸与第二核酸序列中的比对核苷酸相同,使得第一和第二核苷酸序列编码具有共同功能活性的多肽,或编码共同结构多肽结构域或共同功能性多肽活性。例如,与参考序列(例如,本文提供的序列)具有至少约80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的核苷酸序列。
术语“变体”是指具有与参考氨基酸序列基本上相同的氨基酸序列或由基本上相同的核苷酸序列编码的多肽。在一些实施方案中,变体是功能性变体。
术语“功能性变体”是指具有与参考氨基酸序列基本上相同的氨基酸序列或由基本上相同的核苷酸序列编码,并且能够具有参考氨基酸序列的一种或多种活性的多肽。
序列之间的同源性或序列同一性(该术语在本文中可互换使用)的计算如下进行。
为了确定两个氨基酸序列或两个核酸序列的同一性百分比,对序列进行比对用于最佳比较(例如,可以在第一和第二氨基酸或核酸序列中的一个或两个中引入空位(gap)用于最佳比对,并且可以忽略非同源性序列用于比较)。在优选实施方案中,用于比较的比对的参考序列长度为参考序列长度的至少30%,优选至少40%,更优选至少50%、60%,甚至更优选至少70%、80%、90%、100%。然后比较相应氨基酸位置或核苷酸位置处的氨基酸残基或核苷酸。当第一序列中的位置被与第二序列中相应位置相同的氨基酸残基或核苷酸占据时,则分子在该位置是相同的(如本文所用,氨基酸或核酸“同一性”等同于氨基酸或核酸“同源性”)。
考虑到空位的数量和每个空位的长度,两个序列之间的同一性百分比是序列共有的相同位置数的函数,这些空位是为了两个序列的最佳比对而需要引入的。
可以使用数学算法来完成序列的比较和两个序列之间同一性百分比的确定。在优选实施方案中,使用已并入GCG软件包(可在http://www.gcg.com上获得)中GAP程序的Needleman和Wunsch((1970)J.Mol.Biol.48:444-453)算法、使用Blossum 62矩阵或PAM250矩阵,以及空位权重16、14、12、10、8、6或4和长度权重1、2、3、4、5或6来确定两个氨基酸序列之间的同一性百分比。在另一优选实施方案中,使用GCG软件包(可在http://www.gcg.com上获得)中的GAP程序、使用NWSgapdna.CMP矩阵,以及空位权重40、50、60、70或80和长度权重1、2、3、4、5或6来确定两个核苷酸序列之间的同一性百分比。一组特别优选的参数(以及除非另有说明应使用的参数)是空位罚分为12、空位扩展罚分为4和移码空位罚分为5的Blossum 62评分矩阵。
可以使用已并入ALIGN程序(2.0版本)的E.Meyers和W.Miller((1989)CABIOS,4:11-17)的算法、使用PAM120权重残基表、空位长度罚分12和空位罚分4来确定两个氨基酸或核苷酸序列之间的同一性百分比。
本文所述的核酸和蛋白质序列可以用作“查询序列”,以对公共数据库进行搜索来例如鉴定其他家族成员或相关序列。可以使用Altschul,等人,(1990)J.Mol.Biol.215:403-10的NBLAST和XBLAST程序(2.0版本)来进行这种搜素。可以用NBLAST程序进行BLAST核苷酸搜索,评分=100,字长=12,以获得与本发明的核酸分子同源的核苷酸序列。可以用XBLAST程序进行BLAST蛋白质搜索,评分=50,字长=3,以获得与本发明的蛋白质分子同源的氨基酸序列。为了获得空位比对用于比较,可以使用如Altschul等人,(1997)NucleicAcids Res.25:3389-3402中所述的Gapped BLAST。当使用BLAST和Gapped BLAST程序时,可以使用相应程序(例如,XBLAST和NBLAST)的默认参数。参见http://www.ncbi.nlm.nih.gov。
应理解,本发明的分子可具有另外的保守或非必需氨基酸置换,其对它们的功能没有实质性影响。
术语“氨基酸”旨在包括所有分子,无论是天然的还是合成的,其包括氨基官能团和酸官能团,并且能够包括在天然存在的氨基酸的聚合物中。示例性氨基酸包括天然存在的氨基酸;其类似物、衍生物和同系物;具有变体侧链的氨基酸类似物;以及前述中任一种的所有立体异构体。如本文所用,术语“氨基酸”包括D-或L-光学异构体和肽模拟物。
“保守氨基酸置换”是其中氨基酸残基被具有相似侧链的氨基酸残基替换的置换。具有相似侧链的氨基酸残基家族已在本领域中定义。这些家族包括具有碱性侧链(例如,赖氨酸、精氨酸、组氨酸)、酸性侧链(例如,天冬氨酸、谷氨酸)、不带电荷的极性侧链(例如,甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸)、非极性侧链(例如,丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)、β-分支侧链(例如,苏氨酸、缬氨酸、异亮氨酸)和芳香族侧链(例如,酪氨酸、苯丙氨酸、色氨酸、组氨酸)的氨基酸。
术语“多肽”、“肽”和“蛋白质”(如果是单链)在本文中可互换使用,是指任何长度的氨基酸的聚合物。聚合物可以是线性或分支的,它可包含修饰的氨基酸,并且它可被非氨基酸中断。该术语还包括已修饰的氨基酸聚合物;例如,二硫键形成、糖基化、脂化、乙酰化、磷酸化或任何其他操作,例如与标记组分缀合。多肽可以从天然来源分离,可以通过重组技术从真核或原核宿主产生,或者可以是合成程序的产物。
术语“核酸”、“核酸序列”、“核苷酸序列”或“多核苷酸序列”和“多核苷酸”可互换使用。它们是指任何长度的核苷酸的聚合形式,脱氧核糖核苷酸或核糖核苷酸或其类似物。多核苷酸可以是单链的或双链的,如果是单链的,可以是编码链或非编码(反义)链。多核苷酸可包含修饰的核苷酸,例如甲基化核苷酸和核苷酸类似物。核苷酸的序列可被非核苷酸组分中断。在聚合之后可以进一步修饰多核苷酸,例如通过与标记组分缀合。核酸可以是重组多核苷酸,或者基因组、cDNA、半合成或合成来源的多核苷酸,其在自然界中不存在或以非天然排列与另一多核苷酸连接。
如本文所用,术语“分离的”是指从其最初或天然环境(例如,天然环境,如果它是天然存在的)中除去的材料。例如,存在于活体动物中的天然存在的多核苷酸或多肽不是分离的,但是通过人为干预从天然系统共存材料中的一些或全部中分离的相同多核苷酸或多肽是分离的。这种多核苷酸可以是载体的一部分和/或这种多核苷酸或多肽可以是组合物的一部分,并且仍然是分离的,因为这种载体或组合物不是自然界中存在的环境的一部分。
如本文所用,术语“转化生长因子β-1(TGF-β1)”是指在人中由基因TGFB1或其直系同源物编码的蛋白质。Swiss-Prot登录号P01137提供了示例性人TGF-β1氨基酸序列。SEQID NO:6378中提供了示例性未成熟的人TGF-β1氨基酸序列。SEQ ID NO:6395中提供了示例性成熟人TGF-β1氨基酸序列。
如本文所用,术语“转化生长因子β-2(TGF-β2)”是指在人中由基因TGFB2或其直系同源物编码的蛋白质。Swiss-Prot登录号P61812提供了示例性人TGF-β2氨基酸序列。SEQID NO:6379中提供了示例性未成熟的人TGF-β2氨基酸序列。SEQ ID NO:6396中提供了示例性成熟人TGF-β2氨基酸序列。
如本文所用,术语“转化生长因子β-3(TGF-β3)”是指在人中由基因TGFB3或其直系同源物编码的蛋白质。Swiss-Prot登录号P10600提供了示例性人TGF-β3氨基酸序列。SEQID NO:6380中提供了示例性未成熟的人TGF-β3氨基酸序列。SEQ ID NO:6397中提供了示例性成熟人TGF-β3氨基酸序列。
如本文所用,“TGF-β受体多肽”是指TGF-β受体(例如,TGFBR1、TGFBR2或TGFBR3)或其片段或其变体。
如本文所用,术语“1型转化生长因子β受体(TGFBR1)”(也称为ALK-5或SKR4)是指在人中由基因TGFBR1或其直系同源物编码的蛋白质。Swiss-Prot登录号P36897提供了示例性人TGFBR1氨基酸序列。SEQ ID NO:6381、6382和6383中提供了示例性未成熟的人TGFBR1氨基酸序列。SEQ ID NO:6398、6399和6400中提供了示例性成熟人TGFBR1氨基酸序列。如本文所用,“TGFBR1多肽”是指TGFBR1或其片段或其变体。
如本文所用,术语“2型转化生长因子β受体(TGFBR2)”是指在人中由基因TGFBR2或其直系同源物编码的蛋白质。Swiss-Prot登录号P37173提供了示例性人TGFBR2氨基酸序列。SEQ ID NO:6384和6385中提供了示例性未成熟的人TGFBR2氨基酸序列。SEQ ID NO:6401和6402中提供了示例性成熟人TGFBR2氨基酸序列。如本文所用,“TGFBR2多肽”是指TGFBR2或其片段或其变体。
如本文所用,术语“3型转化生长因子β受体(TGFBR3)”是指在人中由基因TGFBR3或其直系同源物编码的蛋白质。Swiss-Prot登录号Q03167提供了示例性人TGFBR3氨基酸序列。SEQ ID NO:6392和6393中提供了示例性未成熟的人TGFBR3氨基酸序列。SEQ ID NO:6403和6404中提供了示例性成熟人TGFBR3氨基酸序列。如本文所用,“TGFBR3多肽”是指TGFBR3或其片段或其变体。
下文进一步详细地描述本发明的各个方面。在整个说明书中列出了另外的定义。
抗体分子
在一些实施方案中,如本文所述的多功能性分子、多特异性分子和/或抗原结合结构域包含抗体分子。在一个实施方案中,抗体分子结合至癌抗原,例如,肿瘤抗原或基质抗原。在一些实施方案中,癌抗原是例如哺乳动物(例如,人)癌抗原。在其他实施方案中,抗体分子结合至免疫细胞抗原,例如,哺乳动物(例如,人)免疫细胞抗原。例如,抗体分子特异性结合至癌抗原或免疫细胞抗原上的表位,例如,线性或构象表位。
在实施方案中,抗体分子是单特异性抗体分子并结合单个表位。例如,具有多个免疫球蛋白可变结构域序列的单特异性抗体分子,免疫球蛋白可变结构域序列中的每一个结合同一表位。
在实施方案中,抗体分子是多特异性或多功能性抗体分子,例如,其包含多个免疫球蛋白可变结构域序列,其中多个中的第一免疫球蛋白可变结构域序列对第一表位具有结合特异性,多个中的第二免疫球蛋白可变结构域序列对第二表位具有结合特异性。在实施方案中,第一和第二表位在同一抗原(例如,同一蛋白质(或多聚体蛋白质的亚基))上。在实施方案中,第一和第二表位重叠。在实施方案中,第一和第二表位不重叠。在实施方案中,第一和第二表位在不同抗原(例如,不同蛋白质(或多聚体蛋白质的不同亚基))上。在实施方案中,多特异性抗体分子包含第三、第四或第五免疫球蛋白可变结构域。在实施方案中,多特异性抗体分子是双特异性抗体分子、三特异性抗体分子或四特异性抗体分子。
在实施方案中,多特异性抗体分子是双特异性抗体分子。双特异性抗体对不超过两种抗原具有特异性。双特异性抗体分子的特征在于对第一表位具有结合特异性的第一免疫球蛋白可变结构域序列和对第二表位具有结合特异性的第二免疫球蛋白可变结构域序列。在实施方案中,第一和第二表位在同一抗原(例如,同一蛋白质(或多聚体蛋白质的亚基))上。在实施方案中,第一和第二表位重叠。在实施方案中,第一和第二表位不重叠。在实施方案中,第一和第二表位在不同抗原(例如,不同蛋白质(或多聚体蛋白质的不同亚基))上。在实施方案中,双特异性抗体分子包含对第一表位具有结合特异性的重链可变结构域序列和轻链可变结构域序列,以及对第二表位具有结合特异性的重链可变结构域序列和轻链可变结构域序列。在实施方案中,双特异性抗体分子包含对第一表位具有结合特异性的半抗体和对第二表位具有结合特异性的半抗体。在实施方案中,双特异性抗体分子包含对第一表位具有结合特异性的半抗体或其片段,以及对第二表位具有结合特异性的半抗体或其片段。在实施方案中,双特异性抗体分子包含对第一表位具有结合特异性的scFv或Fab或其片段,以及对第二表位具有结合特异性的scFv或Fab或其片段。
在实施方案中,抗体分子包含双抗体和单链分子,以及抗体的抗原结合片段(例如,Fab、F(ab’)2和Fv)。例如,抗体分子可以包括重(H)链可变结构域序列(本文缩写为VH)和轻(L)链可变结构域序列(本文缩写为VL)。在实施方案中,抗体分子包含重链和轻链或由重链和轻链组成(本文称为半抗体)。在另一实例中,抗体分子包括两个重(H)链可变结构域序列和两个轻(L)链可变结构域序列,从而形成两个抗原结合位点,例如Fab、Fab’、F(ab’)2、Fc、Fd、Fd’、Fv、单链抗体(例如scFv)、单可变结构域抗体、双抗体(Dab)(二价和双特异性)和嵌合(例如,人源化)抗体,其可通过修饰整个抗体或使用重组DNA技术从头合成的那些抗体来产生。这些功能性抗体片段保留了与它们相应抗原或受体选择性地结合的能力。抗体和抗体片段可以来自任何类型的抗体,包括但不限于IgG、IgA、IgM、IgD和IgE,以及来自任何亚类(例如,IgG1、IgG2、IgG3和IgG4)的抗体。抗体分子的制剂可以是单克隆或多克隆的。抗体分子也可以是人、人源化、CDR移植或体外生成的抗体。抗体可以具有重链恒定区,选自例如IgG1、IgG2、IgG3或IgG4。抗体还可以具有轻链,选自例如κ或λ。术语“免疫球蛋白”(Ig)在本文中可与术语“抗体”互换使用。
抗体分子的抗原结合片段的实例包括:(i)Fab片段,由VL、VH、CL和CH1结构域组成的单价片段;(ii)F(ab’)2片段,包含通过铰链区的二硫键连接的两个Fab片段的二价片段;(iii)由VH和CH1结构域组成的Fd片段;(iv)由抗体单臂的VL和VH结构域组成的Fv片段,(v)由VH结构域组成的双抗体(dAb)片段;(vi)骆驼或骆驼源化可变结构域;(vii)单链Fv(scFv),参见例如,Bird等人,(1988)Science 242:423-426;和Huston等人,(1988)Proc.Natl.Acad.Sci.USA 85:5879-5883);(viii)单结构域抗体。使用本领域技术人员已知的常规技术来获得这些抗体片段,并以与完整抗体相同的方式筛选片段的效用。
抗体分子包括完整分子以及其功能性片段。抗体分子的恒定区可以被改变(例如,突变),以修改抗体的特性(例如,增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能)。
抗体分子也可以是单结构域抗体。单结构域抗体可以包括其互补决定区是单结构域多肽的一部分的抗体。实例包括但不限于重链抗体、天然无轻链的抗体、来源于常规4-链抗体的单结构域抗体、工程化抗体和除来源于抗体的那些以外的单结构域支架。单结构域抗体可以是本领域中的任一种,或任何未来的单结构域抗体。单结构域抗体可来源于任何物种,包括但不限于小鼠、人、骆驼、美洲驼、鱼、鲨鱼、山羊、兔和牛。根据本发明的另一方面,单结构域抗体是天然存在的单结构域抗体,称为无轻链的重链抗体。例如,这种单结构域抗体公开于WO9404678中。为清楚起见,这种来源于天然无轻链的重链抗体的可变结构域在本文中称为VHH或纳米抗体,以将其与四条链免疫球蛋白的常规VH区分开。这种VHH分子可以来源于骆驼科物种(例如骆驼、美洲驼、单峰驼、羊驼和原驼)中产生的抗体。除骆驼科以外的其他物种可能会产生天然无轻链的重链抗体;这种VHH在本发明的范围内。
VH和VL区可以细分为高变区,称为“互补决定区”(CDR),中间散布着更保守的区域,称为“框架区”(FR或FW)。
框架区和CDR的范围已通过许多方法精确地定义(参见,Kabat,E.A.,等人,(1991)Sequences of Proteins of Immunological Interest,第5版,U.S.Department ofHealth and Human Services,NIH公布第91-3242号;Chothia,C.等人,(1987)J.Mol.Biol.196:901-917;以及由Oxford Molecular的AbM抗体建模软件使用的AbM定义。通常参见例如,Antibody Engineering Lab Manual中的Protein Sequence andStructure Analysis of Antibody Variable Domains.(编著:Duebel,S.和Kontermann,R.,Springer-Verlag,Heidelberg)。
如本文所用,术语“互补决定区”和“CDR”是指抗体可变区内赋予抗原特异性和结合亲和力的氨基酸序列。通常,在每个重链可变区中存在三个CDR(HCDR1、HCDR2、HCDR3),并且在每个轻链可变区中存在三个CDR(LCDR1、LCDR2、LCDR3)。
给定CDR的精确氨基酸序列边界可使用许多已知方案中的任一种来确定,包括Kabat等人,(1991),“Sequences of Proteins of Immunological Interest,”第5版,Public Health Service,National Institutes of Health,Bethesda,MD(“Kabat”编号方案)、Al-Lazikani等人,(1997)JMB 273,927-948(“Chothia”编号方案)描述的那些。如本文所用,根据“Chothia”编号方案定义的CDR有时也称为“高变环”。
例如,在Kabat下,重链可变结构域(VH)中的CDR氨基酸残基编号为31-35(HCDR1)、50-65(HCDR2)和95-102(HCDR3);并且轻链可变结构域(VL)中的CDR氨基酸残基编号为24-34(LCDR1)、50-56(LCDR2)和89-97(LCDR3)。在Chothia下,VH中的CDR氨基酸编号为26-32(HCDR1)、52-56(HCDR2)和95-102(HCDR3);并且VL中的氨基酸残基编号为26-32(LCDR1)、50-52(LCDR2)和91-96(LCDR3)。
每个VH和VL通常包括三个CDR和四个FR,从氨基末端至羧基末端按以下顺序排列:FR1、CDR1、FR2、CDR2、FR3、CDR3、FR4。
抗体分子可以是多克隆或单克隆抗体。
如本文所用,术语“单克隆抗体”或“单克隆抗体组合物”是指单分子组成的抗体分子的制剂。单克隆抗体组合物展示出对特定表位的单一结合特异性和亲和力。单克隆抗体可以通过杂交瘤技术或通过不使用杂交瘤技术的方法(例如,重组方法)制备。
抗体可以重组产生,例如,通过噬菌体展示或通过组合方法产生。
用于生成抗体的噬菌体展示和组合方法是本领域已知的(如例如,Ladner等人,美国专利第5,223,409号;Kang等人,国际公布WO92/18619号;Dower等人,国际公布第WO91/17271号;Winter等人,国际公布第WO92/20791号;Markland等人,国际公布第WO92/15679号;Breitling等人,国际公布第WO93/01288号;McCafferty等人,国际公布第WO92/01047号;Garrard等人,国际公布第WO92/09690号;Ladner等人,国际公布第WO90/02809号;Fuchs等人,(1991)Bio/Technology 9:1370-1372;Hay等人,(1992)Hum Antibod Hybridomas 3:81-85;Huse等人,(1989)Science 246:1275-1281;Griffths等人,(1993)EMBO J 12:725-734;Hawkins等人,(1992)J Mol Biol 226:889-896;Clackson等人,(1991)Nature 352:624-628;Gram等人,(1992)PNAS 89:3576-3580;Garrad等人,(1991)Bio/Technology 9:1373-1377;Hoogenboom等人,(1991)Nuc Acid Res19:4133-4137;和Barbas等人,(1991)PNAS 88:7978-7982中描述的,其全部内容通过引用并入本文)。
在一个实施方案中,抗体是完全人抗体(例如,在小鼠中制备的抗体,其已遗传工程化为从人免疫球蛋白序列产生抗体),或非人抗体,例如,啮齿动物(小鼠或大鼠)、山羊、灵长类动物(例如,猴)、骆驼抗体。优选地,非人抗体是啮齿动物(小鼠或大鼠抗体)。产生啮齿动物抗体的方法是本领域已知的。
可以使用携带人免疫球蛋白基因的转基因小鼠而非小鼠系统来生成人单克隆抗体。用目的抗原免疫的这些转基因小鼠的脾细胞用于产生杂交瘤,该杂交瘤分泌对来自人蛋白质的表位具有特异性亲和力的人mAb(参见例如,Wood等人,国际申请WO91/00906、Kucherlapati等人,PCT申请WO91/10741;Lonberg等人,国际申请WO92/03918;Kay等人,国际申请92/03917;Lonberg,N.等人,1994Nature 368:856-859;Green,L.L.等人,1994Nature Genet.7:13-21;Morrison,S.L.等人,1994Proc.Natl.Acad.Sci.USA 81:6851-6855;Bruggeman等人,1993Year Immunol 7:33-40;Tuaillon等人,1993PNAS 90:3720-3724;Bruggeman等人,1991Eur J Immunol 21:1323-1326)。
抗体分子可以是其中可变区或其一部分(例如,CDR)在非人生物体(例如,大鼠或小鼠)中生成的抗体分子。嵌合、CDR移植和人源化的抗体在本发明范围内。在非人生物体(例如,大鼠或小鼠)中生成,然后例如在可变框架或恒定区中修饰以降低人中抗原性的抗体分子在本发明范围内。
“有效的人”蛋白质是基本上不引起中和抗体应答(例如,人抗鼠抗体(HAMA)应答)的蛋白质。例如,在慢性或复发性疾病病况的治疗中,例如,如果重复施用抗体分子,HAMA在许多情况下可能是有问题的。HAMA应答可使重复的抗体施用可能无效,因为血清中的抗体清除率增加(参见例如,Saleh等人,Cancer Immunol.Immunother.,32:180-190(1990)),并且还因为可能的过敏反应(参见例如,LoBuglio等人,Hybridoma,5:5117-5123(1986))。
嵌合抗体可通过本领域已知的重组DNA技术产生(参见Robinson等人,国际专利申请PCT/US86/02269;Akira,等人,欧洲专利申请184,187;Taniguchi,M.,欧洲专利申请171,496;Morrison等人,欧洲专利申请173,494;Neuberger等人,国际申请WO86/01533;Cabilly等人,美国专利第4,816,567号;Cabilly等人,欧洲专利申请125,023;Better等人,(1988Science 240:1041-1043);Liu等人,(1987)PNAS 84:3439-3443;Liu等人,1987,J.Immunol.139:3521-3526;Sun等人,(1987)PNAS 84:214-218;Nishimura等人,1987,Canc.Res.47:999-1005;Wood等人,(1985)Nature314:446-449;和Shaw等人,1988,J.NatlCancer Inst.80:1553-1559)。
人源化或CDR移植抗体将具有(免疫球蛋白重链和/或轻链的)至少一个或两个但通常为所有三个受体CDR被供体CDR替换。抗体可用非人CDR的至少一部分替换,或者仅CDR中的一些可用非人CDR替换。仅需要替换结合至抗原所需数量的CDR。优选地,供体是啮齿动物抗体,例如,大鼠或小鼠抗体,受体将是人框架或人共有框架。通常,提供CDR的免疫球蛋白称为“供体”,提供框架的免疫球蛋白称为“受体”。在一个实施方案中,供体免疫球蛋白是非人(例如,啮齿动物)的。受体框架是天然存在的(例如,人)框架或共有框架,或与其约85%或更高,优选90%、95%、99%或更高相同的序列。
如本文所用,术语“共有序列”是指由相关序列家族中最频繁出现的氨基酸(或核苷酸)形成的序列(参见例如,Winnaker,From Genes to Clones(Verlagsgesellschaft,Weinheim,Germany 1987)。在蛋白质家族中,共有序列中的每个位置被该家族中该位置最频繁出现的氨基酸占据。如果两个氨基酸出现的频率相同,则在共有序列中可以包括任一个。“共有框架”是指共有免疫球蛋白序列中的框架区。
抗体分子可以通过本领域已知的方法人源化(参见例如,Morrison,S.L.,1985,Science 229:1202-1207、Oi等人,1986,BioTechniques 4:214,以及Queen等人,US 5,585,089、US 5,693,761和US 5,693,762,其全部内容在此通过引用并入)。
人源化或CDR移植的抗体分子可以通过CDR移植或CDR置换产生,其中免疫球蛋白链的一个、两个或所有CDR可以被替换。参见例如,美国专利5,225,539;Jones等人,1986Nature 321:552-525;Verhoeyan等人,1988Science 239:1534;Beidler等人,1988J.Immunol.141:4053-4060;Winter US 5,225,539,其全部内容在此明确地通过引用并入。Winter描述了可用于制备本发明的人源化抗体的CDR移植方法(1987年3月26日提交的UK专利申请GB 2188638A;Winter US 5,225,539),其内容明确地通过引用并入。
其中特定氨基酸已被置换、缺失或添加的人源化抗体分子也在本发明的范围内。在US 5,585,089(例如,US 5,585,089的第12-16栏)中描述了从供体中选择氨基酸的标准,其内容在此通过引用并入。1992年12月23日公布的Padlan等人,EP 519596A1中描述了使抗体人源化的其他技术。
抗体分子可以是单链抗体。单链抗体(scFv)可以是工程化的(参见例如,Colcher,D.等人,(1999)Ann N Y Acad Sci 880:263-80;和Reiter,Y.(1996)Clin Cancer Res 2:245-52)。单链抗体可以二聚化或多聚化,以生成对同一靶蛋白的不同表位具有特异性的多价抗体。
在其他实施方案中,抗体分子具有重链恒定区,选自例如IgG1、IgG2、IgG3、IgG4、IgM、IgA1、IgA2、IgD和IgE的重链恒定区;特别地,选自例如IgG1、IgG2、IgG3和IgG4的(例如,人)重链恒定区。在另一实施方案中,抗体分子具有轻链恒定区,选自例如κ或λ的(例如,人)轻链恒定区。恒定区可以被改变(例如,突变),以修改抗体的特性(例如,增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能和/或补体功能)。在一个实施方案中,抗体具有:效应功能;并且可以固定补体。在其他实施方案中,抗体不会:招募效应细胞;或固定补体。在另一实施方案中,抗体结合Fc受体的能力降低或无该能力。例如,它是同种型或亚型、片段或其他突变体,其不支持结合至Fc受体,例如,它具有诱变的或缺失的Fc受体结合区。
改变抗体恒定区的方法是本领域已知的。具有功能改变(例如,对效应配体(例如细胞上的FcR)或补体的C1组分的亲和力改变)的抗体可以通过用不同残基替换抗体恒定部分中的至少一个氨基酸残基来产生(参见例如,EP 388,151A1、美国专利第5,624,821号和美国专利第5,648,260号,其全部内容在此通过引用并入)。可以描述相似类型的改变,如果将其施加至鼠或其他物种免疫球蛋白,将减少或消除这些功能。
抗体分子可以衍生化或与另一功能性分子(例如,另一肽或蛋白质)连接。如本文所用,“衍生化”抗体分子是已被修饰的抗体分子。衍生化方法包括但不限于加入荧光部分、放射性核苷酸、毒素、酶或亲和配体,例如生物素。因此,本发明的抗体分子旨在包括本文所述抗体的衍生化形式和其他修饰形式,包括免疫粘附分子。例如,抗体分子可以(通过化学偶联、基因融合、非共价缔合或其他方式)功能性地连接至一个或多个其他分子实体,例如另一种抗体(例如,双特异性抗体或双抗体)、可检测剂、细胞毒性剂、药剂和/或可介导抗体或抗体部分与另一分子(例如链霉亲和素核心区或多组氨酸标签)缔合的蛋白质或肽。
一种类型的衍生化抗体分子通过将(相同类型或不同类型,例如,产生双特异性抗体的)两种或更多种抗体交联来产生。合适的交联剂包括具有由合适间隔区分开的两个明显反应性基团的异双功能性交联剂(例如,间马来酰亚胺苯甲酰基-N-羟基琥珀酰亚胺酯)或同双功能性交联剂(例如,辛二酸二琥珀酰亚胺酯)。这些接头可从Pierce ChemicalCompany,Rockford,Ill获得。
多特异性或多功能性抗体分子
本文定义的多特异性和多功能性分子的示例性结构在全文中描述。示例性结构进一步描述于:Weidle U等人,(2013)The Intriguing Options of MultispecificAntibody Formats for Treatment of Cancer.Cancer Genomics&Proteomics 10:1-18(2013);和Spiess C等人,(2015)Alternative molecular formats and therapeuticapplications for bispecific antibodies.Molecular Immunology 67:95-106;其中每一个的全部内容通过引用并入本文)。
在一些实施方案中,多特异性抗体分子可以包含多于一个抗原结合位点,其中不同位点对不同抗原具有特异性。在一些实施方案中,多特异性抗体分子可以结合同一抗原上的多于一个(例如,两个或更多个)表位。在一些实施方案中,多特异性抗体分子包含对靶细胞(例如,癌细胞)具有特异性的抗原结合位点和对免疫效应细胞具有特异性的不同抗原结合位点。在一些实施方案中,多特异性抗体分子是双特异性、三特异性或四特异性抗体分子。在一个实施方案中,多特异性抗体分子是双特异性抗体分子。双特异性抗体分子可分为五个不同的结构组:(i)双特异性免疫球蛋白G(BsIgG);(ii)附加有另外抗原结合部分的IgG;(iii)双特异性抗体片段;(iv)双特异性融合蛋白;以及(v)双特异性抗体缀合物。
BsIgG是每种抗原的单价形式。示例性BsIgG形式包括但不限于crossMab、DAF(二合一)、DAF(四合一)、DutaMab、DT-IgG、杵-臼共同LC、杵-臼组装件、电荷对、Fab臂交换、SEEDbody、triomab、LUZ-Y、Fcab、κλ体、正交Fab。参见Spiess等人,Mol.Immunol.67(2015):95-106。示例性BsIgG包括卡妥索单抗(Fresenius Biotech,Trion Pharma,Neopharm),其含有抗-CD3臂和抗-EpCAM臂;以及厄妥索单抗(Neovii Biotech,Fresenius Biotech),其靶向CD3和HER2。在一些实施方案中,BsIgG包含经工程化用于异源二聚化的重链。例如,可以使用“杵-臼”策略、SEED平台、(例如,κλ体内的)共同重链和使用异源二聚体Fc区将重链工程化用于异源二聚化。参见Spiess等人,Mol.Immunol.67(2015):95-106。已用于避免BsIgG中同源二聚体的重链配对的策略包括杵-臼、duobody、azymetric、电荷对、HA-TF、SEEDbody和差异蛋白A亲和力。参见同上。可以通过在不同宿主细胞中分开表达组分抗体并随后纯化/组装为BsIgG来产生BsIgG。也可以通过在单个宿主细胞中表达组分抗体来产生BsIgG。BsIgG可以使用亲和层析(例如,使用蛋白A和连续pH洗脱)来纯化。
附加有另外抗原结合部分的IgG是双特异性抗体分子的另一种形式。例如,通过将另外抗原结合单元附加至单特异性IgG上,例如,重链或轻链的N-或C-末端处,单特异性IgG可以工程化为具有双特异性。示例性另外抗原结合单元包括单结构域抗体(例如,可变重链或可变轻链)、工程化蛋白质支架和成对的抗体可变结构域(例如,单链可变片段或可变片段)。参见同上。附加IgG形式的实例包括双可变结构域IgG(DVD-Ig)、IgG(H)-scFv、scFv-(H)IgG、IgG(L)-scFv、scFv-(L)IgG、IgG(L,H)-Fv、IgG(H)-V、V(H)-IgG、IgG(L)-V、V(L)-IgG、KIH IgG-scFab、2scFv-IgG、IgG-2scFv、scFv4-Ig、zybody和DVI-IgG(四合一)。参见Spiess等人,Mol.Immunol.67(2015):95-106。IgG-scFv的实例是MM-141(MerrimackPharmaceuticals),其结合IGF-1R和HER3。DVD-Ig的实例包括ABT-981(AbbVie),其结合IL-1α和IL-1β;以及ABT-122(AbbVie),其结合TNF和IL-17A。
双特异性抗体片段(BsAb)是缺乏抗体恒定结构域中的一些或全部的双特异性抗体分子的形式。例如,一些BsAb缺乏Fc区。在一些实施方案中,双特异性抗体片段包括通过允许BsAb在单个宿主细胞中有效表达的肽接头连接的重链和轻链区。示例性双特异性抗体片段包括但不限于纳米抗体、纳米抗体-HAS、BiTE、双抗体、DART、TandAb、scDiabody、scDiabody-CH3、双抗体-CH3、三联体、微型抗体(miniantibody)、微抗体(minibody)、TriBi微抗体、scFv-CH3 KIH、Fab-scFv、scFv-CH-CL-scFv、F(ab’)2、F(ab’)2-scFv2、scFv-KIH、Fab-scFv-Fc、四价HCAb、scDiabody-Fc、双抗体-Fc、串联scFv-Fc和内抗体(intrabody)。参见同上。例如,BiTE形式包含串联scFv,其中组分scFv结合至T细胞上的CD3和癌细胞上的表面抗原。
双特异性融合蛋白包括与其他蛋白质连接的抗体片段,例如,以增加另外的特异性和/或功能性。双特异性融合蛋白的实例是immTAC,其包含与识别HLA呈递肽的亲和力成熟T细胞受体连接的抗CD3 scFv。在一些实施方案中,对接-锁定(DNL)方法可用于生成更高化合价的双特异性抗体分子。此外,与白蛋白结合蛋白或人血清白蛋白的融合可以延长抗体片段的血清半衰期。参见同上。
在一些实施方案中,化学缀合(例如,抗体和/或抗体片段的化学缀合)可以用于产生BsAb分子。参见同上。示例性双特异性抗体缀合物包括CovX-体形式,其中低分子量药物位点特异性缀合至每个Fab臂或抗体或其片段中的单个反应性赖氨酸。在一些实施方案中,缀合改善了低分子量药物的血清半衰期。示例性CovX-体是CVX-241(NCT01004822),其包含与抑制VEGF或Ang2的两个短肽缀合的抗体。参见同上。
抗体分子可以通过在宿主系统中(例如,至少一种或多种组分的)重组表达来产生。示例性宿主系统包括真核细胞(例如,哺乳动物细胞(例如,CHO细胞),或昆虫细胞(例如,SF9或S2细胞))和原核细胞(例如,大肠杆菌)。双特异性抗体分子可以通过在不同宿主细胞中分开表达组分并随后纯化/组装来产生。可替代地,抗体分子可以通过在单个宿主细胞中表达组分来产生。双特异性抗体分子的纯化可以通过各种方法进行,例如亲和层析,例如,使用蛋白A和连续pH洗脱。在其他实施方案中,亲和标签可用于纯化,例如,含组氨酸的标签、myc标签或链霉亲和素标签。
CDR移植支架
在一些实施方案中,抗体分子是CDR移植支架结构域。在一些实施方案中,支架结构域基于纤连蛋白结构域,例如,纤连蛋白III型结构域。纤连蛋白III型(Fn3)结构域的总折叠与最小功能性抗体片段(抗体重链的可变结构域)的总折叠密切相关。Fn3末端存在三个环;BC、DE和FG环的位置大致对应于抗体VH结构域的CDR1、2和3的位置。Fn3不具有二硫键;因此,与抗体及其片段不同,Fn3在还原条件下是稳定的(参见例如,WO98/56915;WO01/64942;WO00/34784)。Fn3结构域可以(例如,使用本文所述的CDR或高变环)修饰或改变,例如,以选择结合至本文所述的抗原/标记物/细胞的结构域。
在一些实施方案中,支架结构域(例如,折叠结构域)基于抗体,例如,通过从单克隆抗体的重链可变结构域缺失三条β链产生的“微抗体”支架(参见例如,Tramontano等人,1994,J Mol.Recognit.7:9;和Martin等人,1994,EMBO J.13:5303-5309)。“微抗体”可用于提供两个高变环。在一些实施方案中,支架结构域是V-样结构域(参见例如,Coia等人,WO99/45110)或来源于tendamistatin的结构域,其为通过两个二硫键保持在一起的74个残基六股β折叠片夹心(参见例如,McConnell和Hoess,1995,J Mol.Biol.250:460)。例如,tendamistatin的环可以(例如,使用CDR或高变环)修饰或改变,例如,以选择结合至本文所述的标记物/抗原/细胞的结构域。另一种示例性支架结构域是来源于CTLA-4胞外结构域的β-夹心结构(参见例如,WO00/60070)。
其他示例性支架结构域包括但不限于T细胞受体;MHC蛋白;胞外结构域(例如,纤连蛋白III型重复序列、EGF重复序列);蛋白酶抑制剂(例如,Kunitz结构域、ecotin、BPTI等);TPR重复序列;三叶草结构;锌指结构域;DNA结合蛋白;特别是单体DNA结合蛋白;RNA结合蛋白;酶,例如,蛋白酶(特别是灭活的蛋白酶)、RNA酶;伴侣蛋白,例如,硫氧还蛋白和热休克蛋白;以及胞内信号传导结构域(例如SH2和SH3结构域)。参见例如,US 20040009530和US 7,501,121,其通过引用并入本文。
在一些实施方案中,例如通过以下标准中的一个或多个评估和选择支架结构域:(1)氨基酸序列,(2)几个同源性结构域的序列,(3)三维结构,和/或(4)在pH、温度、盐度、有机溶剂、氧化剂浓度范围内的稳定性数据。在一些实施方案中,支架结构域是小的、稳定的蛋白质结构域,例如,少于100、70、50、40或30个氨基酸的蛋白质。结构域可包括一个或多个二硫键,或可螯合金属,例如,锌。
基于抗体的融合体
可以生成多种形式,其含有附接至抗体的N或C末端的另外结合实体。这些具有单链或二硫键稳定的Fv或Fab的融合体导致生成对每种抗原具有二价结合特异性的四价分子。scFv和scFab与IgG的组合使得能够产生可识别三种或更多种不同抗原的分子。
抗体-Fab融合体
抗体-Fab融合体是双特异性抗体,其包含与抗体重链C末端融合的第一靶的传统抗体和第二靶的Fab。通常,抗体和Fab将具有共同轻链。可以通过(1)使靶融合体的DNA序列工程化,和(2)将靶DNA转染至合适的宿主细胞中以表达融合蛋白来产生抗体融合体。如Coloma,J.等人,(1997)Nature Biotech 15:159所述,似乎抗体-scFv融合体可通过CH3结构域的C-末端和scFv的N-末端之间的(Gly)-Ser接头连接。
抗体-scFv融合体
抗体-scFv融合体是双特异性抗体,其包含传统抗体和与抗体重链C末端融合的唯一特异性的scFv。scFv可以通过scFv的重链直接或通过接头肽与C末端融合。可以通过(1)使靶融合体的DNA序列工程化,和(2)将靶DNA转染至合适的宿主细胞中以表达融合蛋白来产生抗体融合体。如Coloma,J.等人,(1997)Nature Biotech 15:159所述,似乎抗体-scFv融合体可通过CH3结构域的C-末端和scFv的N-末端之间的(Gly)-Ser接头连接。
可变结构域免疫球蛋白DVD
相关形式是双可变结构域免疫球蛋白(DVD),其由通过较短接头序列在V结构域N末端的第二特异性位置的VH和VL结构域组成。
其他示例性多特异性抗体形式包括例如以下US 20160114057A1、US20130243775A1、US 20140051833、US 20130022601、US 20150017187A1、US20120201746A1、US 20150133638A1、US 20130266568A1、US 20160145340A1、WO2015127158A1、US 20150203591A1、US 20140322221A1、US 20130303396A1、US20110293613、US 20130017200A1、US 20160102135A1、WO2015197598A2、WO2015197582A1、US 9359437、US 20150018529、WO2016115274A1、WO2016087416A1、US 20080069820A1、US9145588B、US 7919257和US 20150232560A1中描述的那些。利用全抗体-Fab/scFab形式的示例性多特异性分子包括以下US 9382323B2、US 20140072581A1、US 20140308285A1、US20130165638A1、US 20130267686A1、US 20140377269A1、US 7741446B2和WO1995009917A1中描述的那些。利用结构域交换形式的示例性多特异性分子包括以下US 20150315296A1、WO2016087650A1、US 20160075785A1、WO2016016299A1、US 20160130347A1、US20150166670、US 8703132B2、US 20100316645、US 8227577B2、US 20130078249中描述的那些。
含Fc的实体(微型抗体)
含Fc的实体(也称为微型抗体)可以通过将scFv与恒定重链区结构域3的C-末端(CH3-scFv)和/或与具有不同特异性的抗体的铰链区(scFv-铰链-Fc)融合来产生。还可以制备三价实体,其具有与IgG CH3结构域C-末端融合的二硫键稳定的可变结构域(无肽接头)。
含Fc的多特异性分子
在一些实施方案中,本文公开的多特异性分子包括免疫球蛋白恒定区(例如,Fc区)。示例性Fc区可以选自IgG1、IgG2、IgG3或IgG4的重链恒定区;更特别地,人IgG1、IgG2、IgG3或IgG4的重链恒定区。
在一些实施方案中,免疫球蛋白链恒定区(例如,Fc区)被改变(例如,突变),以增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能。
在其他实施方案中,第一和第二免疫球蛋白链恒定区(例如,第一和第二Fc区)的界面被改变(例如,突变),以例如相对于非工程化界面(例如,天然存在的界面)增加或减少二聚化。例如,免疫球蛋白链恒定区(例如,Fc区)的二聚化可以通过提供具有以下中的一种或多种的第一和第二Fc区的Fc界面来增强:成对突起-空腔(“杵-臼”)、静电相互作用或链交换,使得例如相对于非工程化界面形成更大比率的异源多聚体与同源多聚体。
在一些实施方案中,多特异性分子在选自例如人IgG1 Fc区的347、349、350、351、366、368、370、392、394、395、397、398、399、405、407或409中的一个或多个位置处包括配对的氨基酸置换。例如,免疫球蛋白链恒定区(例如,Fc区)可以包括选自以下的配对的氨基酸置换:T366S、L368A或Y407V(例如,对应于空腔或臼)和T366W(例如,对应于突起或杵)。
在其他实施方案中,多功能性分子包括半衰期延长剂,例如,人血清白蛋白或人血清白蛋白的抗体分子。
异源二聚化抗体分子及制备方法
已经公开了各种产生多特异性抗体的方法,以解决重链配对不正确的问题。下文描述了示例性方法。示例性多特异性抗体形式和制备所述多特异性抗体的方法也公开于例如Speiss等人,Molecular Immunology67(2015)95-106;和Klein等人,mAbs 4:6,653-663;2012年11月/12月;其中每一个的全部内容通过引用并入本文。
异源二聚化双特异性抗体基于天然IgG结构,其中两个结合臂识别不同抗原。通过强制重链异源二聚化,结合使轻链错配(例如,共同轻链)最小化的技术,生成能够限定单价(和同时)抗原结合的IgG衍生化形式。可以使用例如杵-臼或链交换工程化结构域(SEED)来获得强制重链异源二聚化。
杵-臼
如US 5,731,116、US 7,476,724和Ridgway,J.等人,(1996)Prot.Engineering 9(7):617-621中描述的杵-臼,广义上涉及:(1)突变一种或两种抗体的CH3结构域以促进异源二聚化;和(2)在促进异源二聚化的条件下组合突变的抗体。“杵”或“突起”通常通过用较大氨基酸替换亲本抗体中的小氨基酸(例如,T366Y或T366W)来产生;“臼”或“空腔”通过用较小氨基酸替换亲本抗体中的较大残基(例如,Y407T、T366S、L368A和/或Y407V)来产生。
对于包括Fc结构域的双特异性抗体,可以利用将特定突变引入重链的恒定区以促进Fc部分正确异源二聚化。Klein等(mAbs(2012)4:6,1-11)综述了几种这种技术,其内容通过引用以其整体并入本文。这些技术包括“杵-臼”(KiH)方法,其涉及将大残基引入抗体重链中的一条的CH3结构域中的一个。这种大残基纳入配对重链另一个CH3结构域中的互补“臼”中,以便促进重链正确配对(参见例如,US 7642228)。
示例性KiH突变包括“杵”重链中的S354C、T366W以及“臼”重链中的Y349C、T366S、L368A、Y407V。其他示例性KiH突变在表1中提供,具有另外任选的稳定化Fc半胱氨酸突变。
表1.示例性Fc KiH突变和任选的半胱氨酸突变
Igawa和Tsunoda提供了其他Fc突变,他们在一条链的CH3结构域中鉴定了三个带负电荷的残基,其与另一条链CH3结构域中的三个带正电荷的残基配对。这些特定的带电荷的残基对是:E356-K439、E357-K370、D399-K409,反之亦然。通过单独在链A中引入以下三种突变中的至少两种:E356K、E357K和D399K,以及链B中的K370E、K409D、K439E,或与新鉴定的二硫键结合,它们能够促进非常有效的异源二聚化,同时抑制同源二聚化(Martens T等人,A novel one-armed antic-Met antibody inhibits glioblastoma growth invivo.Clin Cancer Res 2006;12:6144-52;PMID:17062691)。Xencor基于结合结构计算和序列信息定义了41种变体对,随后筛选出最大异源二聚体,定义了链A上的S364H、F405A(HA)和链B上的Y349T、T394F(TF)的组合(Moore GL等人,A novel bispecific antibodyformat enables simultaneous bivalent and monovalent co-engagement of distincttarget antigens.MAbs 2011;3:546-57;PMID:22123055)。
促进多特异性抗体的异源二聚化的其他示例性Fc突变包括以下参考文献中描述的那些,其中每一个的内容通过引用并入本文,WO2016071377A1、US 20140079689A1、US20160194389A1、US 20160257763、WO2016071376A2、WO2015107026A1、WO2015107025A1、WO2015107015A1、US 20150353636A1、US 20140199294A1、US 7750128B2、US20160229915A1、US 20150344570A1、US 8003774A1、US 20150337049A1、US20150175707A1、US 20140242075A1、US 20130195849A1、US 20120149876A1、US20140200331A1、US 9309311B2、US 8586713、US 20140037621A1、US 20130178605A1、US20140363426A1、US 20140051835A1和US 20110054151A1。
稳定化半胱氨酸突变也已与KiH和其他Fc异源二聚化促进变体组合使用,参见例如,US 7183076。其他示例性半胱氨酸修饰包括例如US 20140348839A1、US 7855275B2和US9000130B2中公开的那些。
链交换工程化结构域(SEED)
通过发明链交换工程化结构域(SEED)C(H)3异源二聚体支持双特异性和不对称融合蛋白的设计的异源二聚体Fc平台是已知的。人IgG和IgA C(H)3结构域的这些衍生物产生互补的人SEED C(H)3异源二聚体,其由人IgA和IgG C(H)3序列的交替区段组成。当在哺乳动物细胞中表达时,所得SEED C(H)3结构域对优先缔合形成异源二聚体。SEEDbody(Sb)融合蛋白由[IgG1铰链]-C(H)2-[SEED C(H)3]组成,其可与一种或多种融合伴侣遗传连接(参见例如,Davis JH等人,SEEDbodies:fusion proteins based on strand exchangeengineered domain(SEED)CH3 heterodimers in an Fc analogue platform forasymmetric binders or immunofusions and bispecific antibodies.Protein Eng DesSel 2010;23:195-202;PMID:20299542和US 8871912。其中每一个的内容通过引用并入本文)。
Duobody
产生具有正确重链配对的双特异性抗体的“Duobody”技术是已知的。DuoBody技术涉及三个基本步骤,以在生产后的交换反应中生成稳定的双特异性人IgG1抗体。在第一步中,使用标准哺乳动物重组细胞系分别产生两个IgG1,每个IgG1在第三恒定(CH3)结构域中含有单一配对突变。随后,根据回收和纯化的标准过程纯化这些IgG1抗体。在生产和纯化之后(生产后),两种抗体在特制实验室条件下重组,产生产率非常高(通常>95%)的双特异性抗体产物(参见例如,Labrijn等人,PNAS 2013;110(13):5145-5150和Labrijn等人,NatureProtocols 2014;9(10):2450-63,其中每一个的内容通过引用并入本文)。
静电相互作用
公开了使用含带电荷的氨基酸的CH3氨基酸改变来制备多特异性抗体的方法,使得同源二聚体形成是静电上不利的。EP 1870459和WO2009089004描述了在宿主细胞中共表达不同抗体结构域时促进异源二聚体形成的其他策略。在这些方法中,用带电荷的氨基酸替换两个CH3结构域中构成重链恒定结构域3(CH3)、CH3-CH3界面的一个或多个残基,使得同源二聚体形成是静电上不利的,而异源二聚化是静电上有利的。使用静电相互作用来制备多特异性分子的另外的方法在以下参考文献中描述,其中每一个的内容通过引用并入本文,包括US 20100015133、US 8592562B2、US 9200060B2、US 20140154254A1和US9358286A1。
共同轻链
需要避免轻链错配,以生成双特异性IgG的均一制剂。实现其的一种方式是通过使用共同轻链原理,即组合共享一条轻链但仍具有单独特异性的两种结合物。提高从单体混合物形成所需双特异性抗体的示例性方法是通过提供与双特异性抗体的异聚化可变重链区中的每一个相互作用的共同可变轻链。如例如US 7183076B2、US 20110177073A1、EP2847231A1、WO2016079081A1和EP 3055329A1中公开的产生具有共同轻链的双特异性抗体的组合物和方法,其中每一个的内容通过引用并入本文。
CrossMab
减少轻链错配的另一种选择是CrossMab技术,其通过交换一半双特异性抗体的Fab中的CH1和CL结构域来避免非特异性L链错配。这种交叉变体保留了结合特异性和亲和力,但使两个臂如此不同以致防止了L链错配。CrossMab技术(如Klein等同上中综述的)涉及重链和轻链之间的结构域交换,以便促进形成正确配对。简言之,为了构建可通过使用两个不同的轻链-重链对结合至两种抗原的双特异性IgG样CrossMab抗体,应用两步修饰过程。首先,使用异源二聚化方法(例如,杵-臼(KiH)技术)将二聚化界面工程化为每条重链的C-末端,以确保仅有效地形成来自一个抗体(例如,抗体A)和第二抗体(例如,抗体B)的两条不同重链的异源二聚体。接着,交换一个抗体(抗体A)的恒定重链1(CH1)和恒定轻链(CL)结构域,保持可变重链(VH)和可变轻链(VL)结构域一致。CH1和CL结构域的交换确保修饰的抗体(抗体A)轻链仅有效地与修饰的抗体(抗体A)重链二聚化,而未修饰的抗体(抗体B)轻链仅有效地与未修饰的抗体(抗体B)重链二聚化;因此,只有所需的双特异性CrossMab才能有效地形成(参见例如,Cain,C.SciBX 4(28);doi:10.1038/scibx.2011.783,其内容通过引用并入本文)。
共同重链
提高从单体混合物形成所需双特异性抗体的示例性方法是通过提供与双特异性抗体的异聚化可变轻链区中的每一个相互作用的共同可变重链。例如US 20120184716、US20130317200和US 20160264685A1中公开了产生具有共同重链的双特异性抗体的组合物和方法,其中每一个的内容通过引用并入本文。
氨基酸修饰
产生具有正确轻链配对的多特异性抗体的替代组合物和方法包括各种氨基酸修饰。例如,Zymeworks描述了在CH1和/或CL结构域中具有一个或多个氨基酸修饰、在VH和/或VL结构域中具有一个或多个氨基酸修饰或其组合的异源二聚体,其是轻链和重链之间的界面的一部分,并且在每条重链和所需轻链之间产生优先配对,使得当异源二聚体对的两条重链和两条轻链在细胞中共表达时,第一异源二聚体的重链优先与轻链中的一条而不是另一条配对(参见例如,WO2015181805)。在WO2016026943(Argen-X)、US 20150211001、US20140072581A1、US 20160039947A1和US 20150368352中描述了其他示例性方法。
λ/κ形式
包括λ轻链多肽和κ轻链多肽的多特异性分子(例如,多特异性抗体分子)可用于允许异源二聚化。PCT公开第WO2018057955号(对应于2017年9月22日提交的PCT/US17/53053)中公开了生成包含λ轻链多肽和κ轻链多肽的双特异性抗体分子的方法),通过引用以其整体并入本文。
在一些实施方案中,多特异性分子包括多特异性抗体分子,例如,包含两种结合特异性的抗体分子,例如,双特异性抗体分子。多特异性抗体分子包括:
对第一表位具有特异性的λ轻链多肽1(LLCP1);
对第一表位具有特异性的重链多肽1(HCP1);
对第二表位具有特异性的κ轻链多肽2(KLCP2);以及
对第二表位具有特异性的重链多肽2(HCP2)。
如本文所用,术语“λ轻链多肽1(LLCP1)”是指包含足够轻链(LC)序列的多肽,使得当与同源重链可变区组合时,可以介导与其表位的特异性结合并与HCP1复合。在实施方案中,它包含CH1区的全部或片段。在实施方案中,LLCP1包含LC-CDR1、LC-CDR2、LC-CDR3、FR1、FR2、FR3、FR4和CH1,或足以介导其表位的特异性结合并与HCP1复合的序列。LLCP1与其HCP1一起提供对第一表位的特异性(而KLCP2与其HCP2一起提供对第二表位的特异性)。如本文别处所述,LLCP1对HCP1比对HCP2具有更高的亲和力。
如本文所用,术语“κ轻链多肽2(KLCP2)”是指包含足够轻链(LC)序列的多肽,使得当与同源重链可变区组合时,可以介导与其表位的特异性结合并与HCP2复合。在实施方案中,它包含CH1区的全部或片段。在实施方案中,KLCP2包含LC-CDR1、LC-CDR2、LC-CDR3、FR1、FR2、FR3、FR4和CH1,或足以介导其表位的特异性结合并与HCP2复合的序列。KLCP2与其HCP2一起提供对第二表位的特异性(而LLCP1与其HCP1一起提供对第一表位的特异性)。
如本文所用,术语“重链多肽1(HCP1)”是指包含足够重链(HC)序列(例如,HC可变区序列)的多肽,使得当与同源LLCP1组合时,可以介导与其表位的特异性结合并与HCP1复合。在实施方案中,它包含CH1区的全部或片段。在实施方案中,它包含CH2和/或CH3区的全部或片段。在实施方案中,HCP1包含HC-CDR1、HC-CDR2、HC-CDR3、FR1、FR2、FR3、FR4、CH1、CH2和CH3,或足以:(i)介导其表位的特异性结合并与LLCP1复合,(ii)如本文所述优先与LLCP1而不是KLCP2复合;以及(iii)如本文所述优先与HCP2而不是HCP1的另一分子复合的序列。HCP1与其LLCP1一起提供对第一表位的特异性(而KLCP2与其HCP2一起提供对第二表位的特异性)。
如本文所用,术语“重链多肽2(HCP2)”是指包含足够重链(HC)序列(例如,HC可变区序列)的多肽,使得当与同源LLCP1组合时,可以介导与其表位的特异性结合并与HCP1复合。在实施方案中,它包含CH1区的全部或片段。在实施方案中,它包含CH2和/或CH3区的全部或片段。在实施方案中,HCP1包含HC-CDR1、HC-CDR2、HC-CDR3、FR1、FR2、FR3、FR4、CH1、CH2和CH3,或足以:(i)介导其表位的特异性结合并与KLCP2复合,(ii)如本文所述优先与KLCP2而不是LLCP1复合;以及(iii)如本文所述优先与HCP1而不是HCP2的另一分子复合的序列。HCP2与其KLCP2一起提供对第二表位的特异性(而LLCP1与其HCP1一起提供对第一表位的特异性)。
在本文公开的多特异性抗体分子的一些实施方案中:
LLCP1对HCP1比对HCP2具有更高的亲和力;和/或
KLCP2对HCP2比对HCP1具有更高的亲和力。
在一些实施方案中,LLCP1对HCP1的亲和力充分大于其对HCP2的亲和力,使得在预选条件下,例如,在水性缓冲液中,例如,在pH 7的盐水中,例如,在pH 7或在生理条件下,至少75%、80%、90%、95%、98%、99%、99.5%或99.9%的多特异性抗体分子具有与HCP1复合或连接的LLCP1。
在本文公开的多特异性抗体分子的一些实施方案中:HCP1对HCP2比对HCP1的第二分子具有更大的亲和力;和/或
HCP2对HCP1比对HCP2的第二分子具有更大的亲和力。
在一些实施方案中,HCP1对HCP2的亲和力充分大于其对HCP1的第二分子的亲和力,使得在预选条件下,例如,在水性缓冲液中,例如,在pH 7的盐水中,例如,在pH 7或在生理条件下,至少75%、80%、90%、95%、98%、99%、99.5%或99.9%的多特异性抗体分子具有与HCP2复合或连接的HCP1。
在另一方面,本文公开了一种制备或产生多特异性抗体分子的方法。该方法包括:在(i)-(iv)缔合的条件下,
(i)提供第一重链多肽(例如,包含第一重链可变区(第一VH)、第一CH1、第一重链恒定区(例如,第一CH2、第一CH3或两者)中的一个、两个、三个或全部的重链多肽);
(ii)提供第二重链多肽(例如,包含第二重链可变区(第二VH)、第二CH1、第二重链恒定区(例如,第二CH2、第二CH3或两者)中的一个、两个、三个或全部的重链多肽);
(iii)提供优先与第一重链多肽(例如,第一VH)缔合的λ链多肽(例如,λ轻链可变区(VLλ)、λ轻链恒定链(VLλ)或两者);以及提供优先与第二重链多肽(例如,第二VH)缔合的κ链多肽(例如,λ轻链可变区(VLκ)、λ轻链恒定链(VLκ)或两者)。
在一些实施方案中,第一和第二重链多肽形成增强异源二聚化的Fc界面。
在一些实施方案中,将(i)-(iv)(例如,编码(i)-(iv)的核酸)导入单个细胞,例如,单个哺乳动物细胞,例如,CHO细胞。在一些实施方案中,(i)-(iv)在细胞中表达。
在一些实施方案中,将(i)-(iv)(例如,编码(i)-(iv)的核酸)导入不同细胞,例如,不同的哺乳动物细胞,例如,两种或更多种CHO细胞。在一些实施方案中,(i)-(iv)在细胞中表达。
在一个实施方案中,该方法进一步包括纯化细胞表达的抗体分子,例如,使用λ-和/或κ-特异性纯化,例如,亲和层析。
在一些实施方案中,该方法进一步包括评估细胞表达的多特异性抗体分子。例如,纯化的细胞表达的多特异性抗体分子可以通过本领域已知的技术进行分析,包括质谱。在一个实施方案中,纯化的细胞表达的抗体分子被裂解,例如,用木瓜蛋白酶消化以产生Fab部分,并使用质谱进行评估。
在一些实施方案中,该方法以高产率(例如,至少75%、80%、90%、95%、98%、99%、99.5%或99.9%)产生正确配对的κ/λ多特异性(例如,双特异性)抗体分子。
在其他实施方案中,多特异性(例如,双特异性)抗体分子包括:
(i)第一重链多肽(HCP1)(例如,包含第一重链可变区(第一VH)、第一CH1、第一重链恒定区(例如,第一CH2、第一CH3或两者)中的一个、两个、三个或全部的重链多肽),例如,其中HCP1结合至第一表位;
(ii)第二重链多肽(HCP2)(例如,包含第二重链可变区(第二VH)、第二CH1、第二重链恒定区(例如,第二CH2、第二CH3或两者)中的一个、两个、三个或全部的重链多肽),例如,其中HCP2结合至第二表位;
(iii)优先与第一重链多肽(例如,第一VH)缔合的λ轻链多肽(LLCP1)(例如,λ轻链可变区(VLl)、λ轻链恒定链(VLl)或两者),例如,其中LLCP1结合至第一表位;以及
(iv)提供优先与第二重链多肽(例如,第二VH)缔合的κ轻链多肽(KLCP2)(例如,λ轻链可变区(VLk)、λ轻链恒定链(VLk)或两者),例如,其中KLCP2结合至第二表位。
在一些实施方案中,第一和第二重链多肽形成增强异源二聚化的Fc界面。在一些实施方案中,多特异性抗体分子具有第一结合特异性和第二结合特异性,第一结合特异性包括与连接至Fc恒定区CH2-CH3结构域的第一重链可变区异源二聚化的杂合VLl-CLl(具有杵修饰),第二结合特异性包括与连接至Fc恒定区CH2-CH3结构域的第二重链可变区异源二聚化的杂合VLk-CLk(具有臼修饰)。
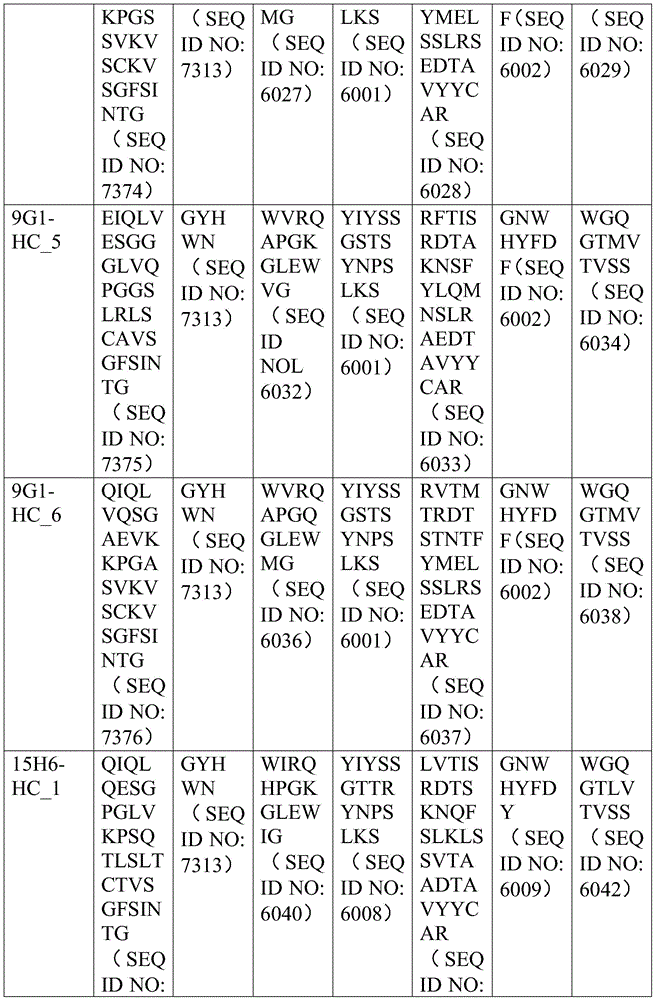
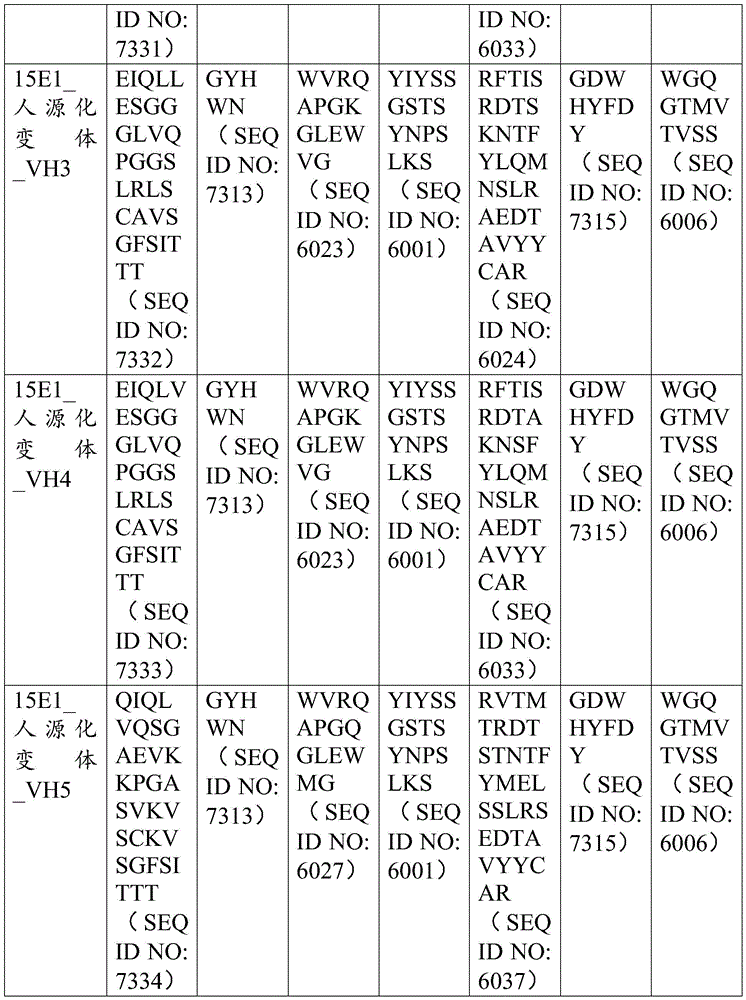
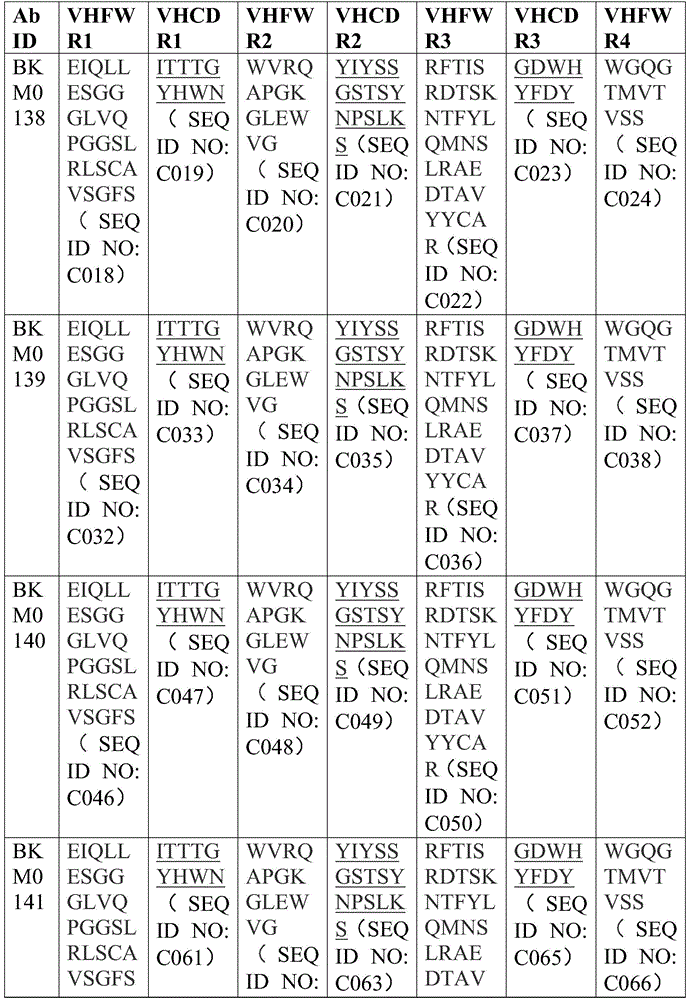
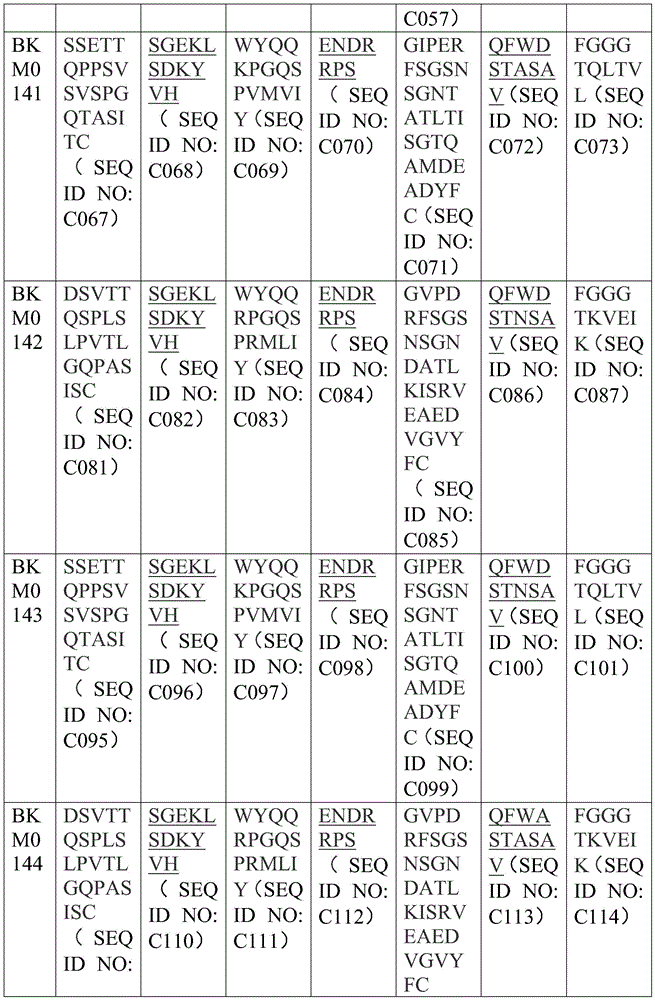
钙网蛋白靶向性抗原结合结构域
本发明尤其提供了多特异性(例如,双特异性、三特异性、四特异性)或多功能性分子,其包括例如工程化为含有一个或多个结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域。在一些实施方案中,多功能性分子以相似的亲和力结合至野生型钙网蛋白和钙网蛋白突变型蛋白。在一些实施方案中,多功能性分子优先结合至钙网蛋白突变型蛋白而非野生型钙网蛋白。
示例性野生型人钙网蛋白如SEQ ID NO:6285所示。
EPAVYFKEQFLDGDGWTSRWIESKHKSDFGKFVLSSGKFYGDEEKDKGLQTSQDARFYALSASFEPFSNKGQTLVVQFTVKHEQNIDCGGGYVKLFPNSLDQTDMHGDSEYNIMFGPDICGPGTKKVHVIFNYKGKNVLINKDIRCKDDEFTHLYTLIVRPDNTYEVKIDNSQVESGSLEDDWDFLPPKKIKDPDASKPEDWDERAKIDDPTDSKPEDWDKPEHIPDPDAKKPEDWDEEMDGEWEPPVIQNPEYKGEWKPRQIDNPDYKGTWIHPEIDNPEYSPDPSIYAYDNFGVLGLDLWQVKSGTIFDNFLITNDEAYAEEFGNETWGVTKAAEKQMKDKQDEEQRLKEEEEDKKRKEEEEAEDKEDDEDKDEDEEDEEDKEEDEEEDVPGQAKDEL(SEQ ID NO:6285)
另外的示例性野生型人钙网蛋白如SEQ ID NO:D1001所示:
MLLSVPLLLGLLGLAVAHHHHHHHHGGGGSEPAVYFKEQFLDGDGWTSRWIESKHKSDFGKFVLSSGKFYGDEEKDKGLQTSQDARFYALSASFEPFSNKGQTLVVQFTVKHEQNIDCGGGYVKLFPNSLDQTDMHGDSEYNIMFGPDICGPGTKKVHVIFNYKGKNVLINKDIRCKDDEFTHLYTLIVRPDNTYEVKIDNSQVESGSLEDDWDFLPPKKIKDPDASKPEDWDERAKIDDPTDSKPEDWDKPEHIPDPDAKKPEDWDEEMDGEWEPPVIQNPEYKGEWKPRQIDNPDYKGTWIHPEIDNPEYSPDPSIYAYDNFGVLGLDLWQVKSGTIFDNFLITNDEAYAEEFGNETWGVTKAAEKQMKDKQDEEQRLKEEEEDKKRKEEEEAEDKEDDEDKDEDEEDEEDKEEDEEEDVPGQA(SEQ ID NO:D1001)。
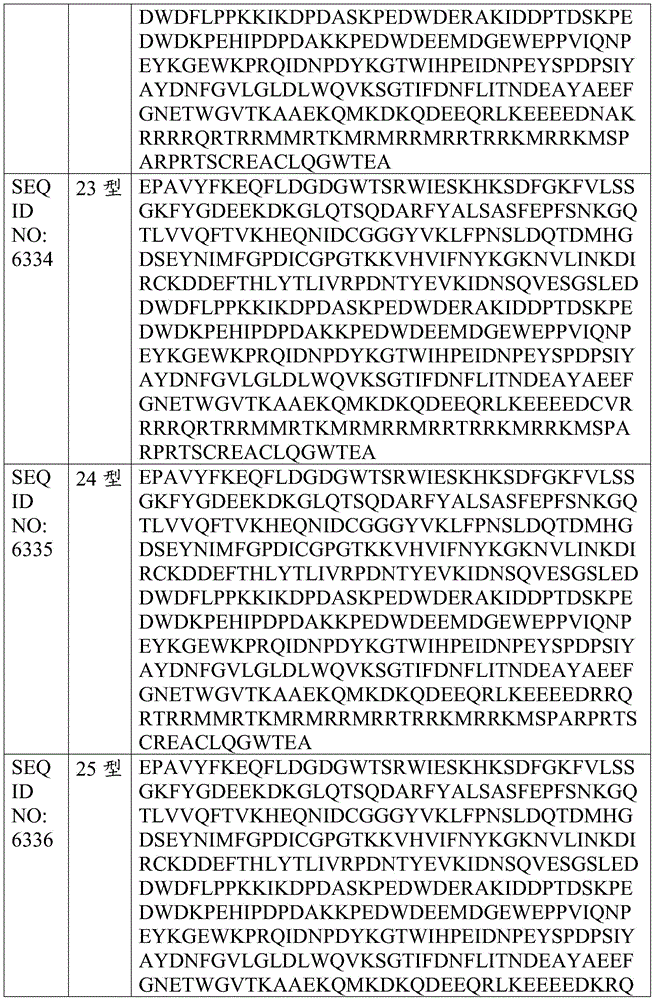
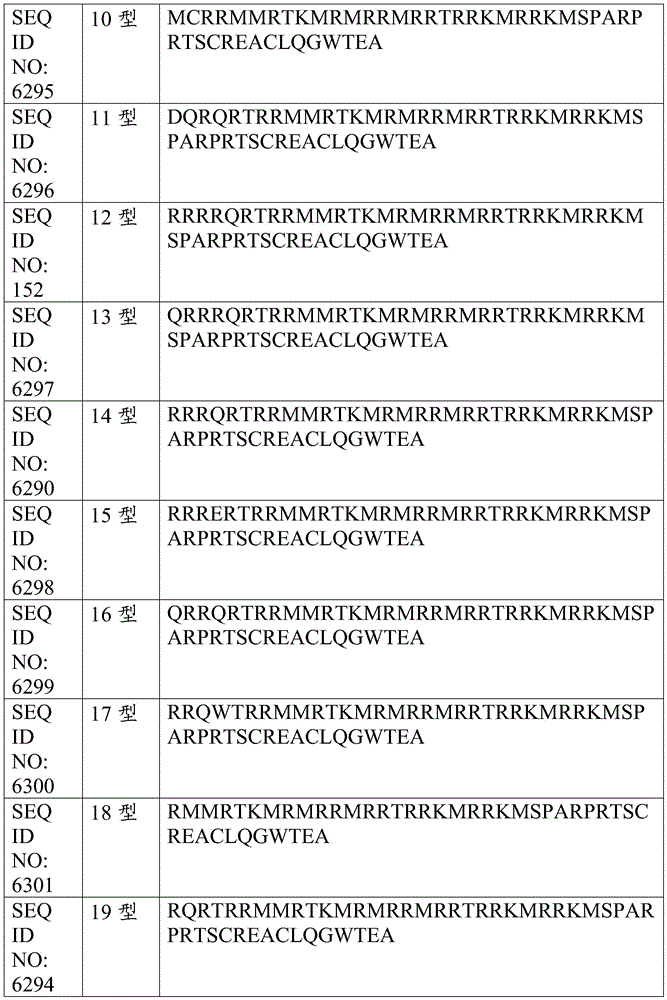
钙网蛋白突变型蛋白已被鉴定并发现与骨髓癌相关,例如,参见Nangalia等人,NEngl J Med.2013年12月19日;369(25):2391-2405、Klampfl等人,N Engl J Med.2013年12月19日;369(25):2379-90和US 20170269092,通过引用以其整体并入本文。突变型钙网蛋白在野生型钙网蛋白编码序列的外显子9中具有移码,导致野生型钙网蛋白C-末端带负电荷的氨基酸被主要带正电荷的多肽替换。表2公开了38种钙网蛋白突变型蛋白的全长氨基酸序列。表3公开了36种钙网蛋白突变型蛋白的C-末端氨基酸序列。所有38种钙网蛋白突变型蛋白包含RRKMSPARPRTSCREACLQGWTEA(SEQ ID NO:6286)的氨基酸序列。
钙网蛋白的主要突变是1型和2型突变(参见表2和3)。1型突变是52bp缺失(c.1092_1143del),而2型突变是5bp插入(c.1154_1155insTTGTC)。
表2.钙网蛋白突变体的全长氨基酸序列
表3.钙网蛋白突变体的C-末端氨基酸序列
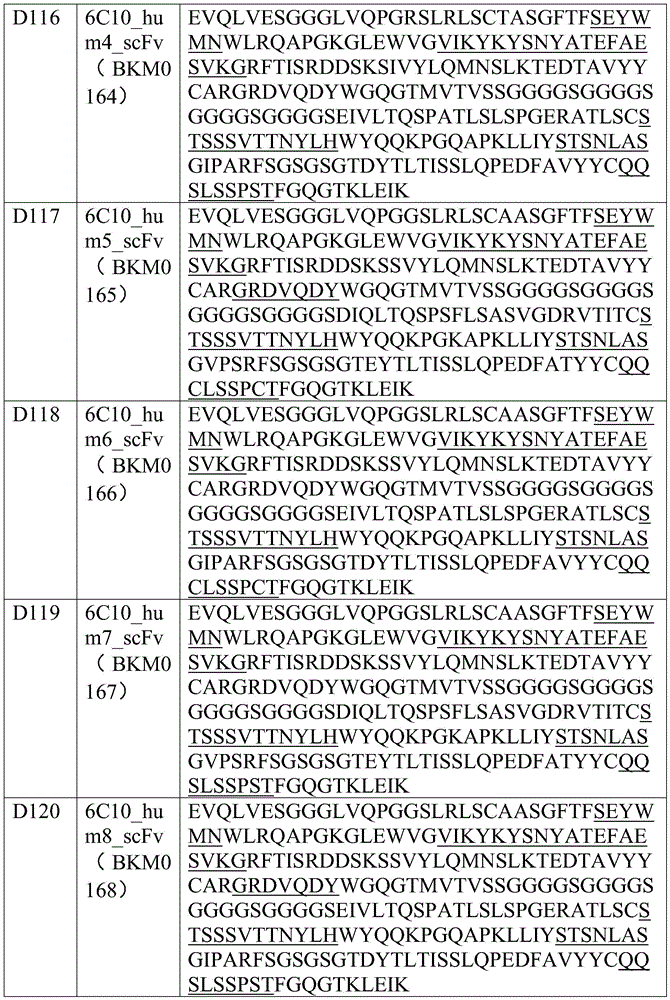
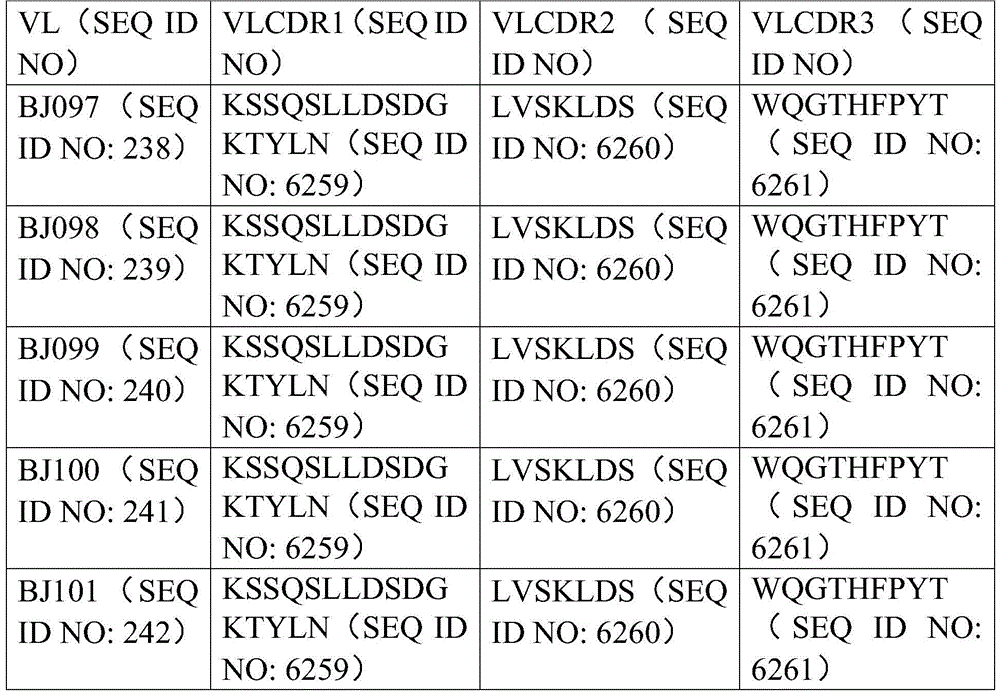
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含表4-7、表24和表25中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含来自鼠16B11.1抗体的一个、两个、三个CDR,例如,如表4中所述的。例如,在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6358的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6360的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:227的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6358的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6360的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:227的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6358的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6360的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:227的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6358的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6360的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:227的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
可替代地,或与包含含有来自鼠16B11.1抗体的一个、两个、三个CDR的VH的钙网蛋白靶向性抗原结合结构域组合,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含来源于鼠16B11.1抗体的一个、两个或三个CDR,例如,如表4中所述的。例如,在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:251的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:246的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:248的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:251的VLCDR1氨基酸序列、SEQ ID NO:253的VLCDR2氨基酸序列,以及SEQ ID NO:255的VLCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:258的VLCDR1氨基酸序列、SEQ ID NO:260的VLCDR2氨基酸序列,以及SEQ ID NO:262的VLCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:265的VLCDR1氨基酸序列、SEQ ID NO:267的VLCDR2氨基酸序列,以及SEQ ID NO:269的VLCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:272的VLCDR1氨基酸序列、SEQ IDNO:274的VLCDR2氨基酸序列,以及SEQ ID NO:276的VLCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:279的VLCDR1氨基酸序列、SEQ ID NO:281的VLCDR2氨基酸序列,以及SEQ ID NO:283的VLCDR3氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ IDNO:6253的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6254的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6255的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6253的VHCDR1氨基酸序列、SEQ IDNO:6254的VHCDR2氨基酸序列,和/或SEQ ID NO:6255的VHCDR3氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ IDNO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6259的VLCDR1氨基酸序列、SEQ IDNO:6260的VLCDR2氨基酸序列,以及SEQ ID NO:6261的VLCDR3氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含来自人源化16B11.1抗体的一个、两个、三个或四个框架区,例如,如表4中所述的。例如,在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6357的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6359的VHFWR2氨基酸序列、SEQ ID NO:6361的VHFWR3氨基酸序列,和/或SEQ ID NO:6273的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6362的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6363的VHFWR2氨基酸序列、SEQ ID NO:226的VHFWR3氨基酸序列,和/或SEQ IDNO:228的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:229的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6369的VHFWR2氨基酸序列、SEQ ID NO:6371的VHFWR3氨基酸序列,和/或SEQ ID NO:228的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6373的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6369的VHFWR2氨基酸序列、SEQ ID NO:6371的VHFWR3氨基酸序列,和/或SEQ ID NO:228的VHFWR4氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ IDNO:6374的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6375的VLFWR2氨基酸序列、SEQID NO:247的VLFWR3氨基酸序列,和/或SEQ ID NO:249的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:250的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:252的VLFWR2氨基酸序列、SEQ ID NO:254的VLFWR3氨基酸序列,和/或SEQ ID NO:256的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:257的轻链框架区1(VLFWR1)氨基酸序列、SEQID NO:259的VLFWR2氨基酸序列、SEQ ID NO:261的VLFWR3氨基酸序列,和/或SEQ ID NO:263的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:264的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:266的VLFWR2氨基酸序列、SEQ ID NO:268的VLFWR3氨基酸序列,和/或SEQ ID NO:270的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:271的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:273的VLFWR2氨基酸序列、SEQ ID NO:275的VLFWR3氨基酸序列,和/或SEQ ID NO:277的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:278的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:280的VLFWR2氨基酸序列、SEQ ID NO:282的VLFWR3氨基酸序列,和/或SEQID NO:284的VLFWR4氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ IDNO:6224的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6226的VHFWR2氨基酸序列、SEQID NO:6228的VHFWR3氨基酸序列,和/或SEQ ID NO:6230的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6240的VLFWR2氨基酸序列、SEQ ID NO:6242的VLFWR3氨基酸序列,和/或SEQ ID NO:6244的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6264的VHFWR2氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6265的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:228的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6278的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6279的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:6280的VLFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列、SEQ ID NO:6264的VHFWR2氨基酸序列、SEQ ID NO:6265的VHFWR3氨基酸序列,和/或SEQ ID NO:228的VHFWR4氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列、SEQ ID NO:6278的VLFWR2氨基酸序列、SEQ ID NO:6279的VLFWR3氨基酸序列,和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ IDNO:6347的氨基酸序列(或与SEQ ID NO:6347具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6348的氨基酸序列(或与SEQ ID NO:6348具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6349的氨基酸序列(或与SEQ ID NO:6349具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6350的氨基酸序列(或与SEQID NO:6350具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6351的氨基酸序列(或与SEQ ID NO:6351具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQID NO:6352的氨基酸序列(或与SEQ ID NO:6352具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQID NO:6353的氨基酸序列(或与SEQ ID NO:6353具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQID NO:6354的氨基酸序列(或与SEQ ID NO:6354具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQID NO:6355的氨基酸序列(或与SEQ ID NO:6355具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQID NO:6356的氨基酸序列(或与SEQ ID NO:6356具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ IDNO:6247的氨基酸序列(或与SEQ ID NO:6247具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列(或与SEQ ID NO:6249具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6247的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6247的氨基酸序列,该VL包含SEQ IDNO:6249的氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含如表4单行中所列的一个、两个或全部三个CDR序列,或与其(例如,与CDR序列中的一个、两个或全部三个)具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含如表5单行中所列的一个、两个或全部三个CDR序列,或与其(例如,与CDR序列中的一个、两个或全部三个)具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含:(i)VH,该VH包含如表4单行中所列的一个、两个或全部三个CDR序列,或与其(例如,与CDR序列中的一个、两个或全部三个)具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列;以及(ii)VL,该VL包含如表5单行中所列的一个、两个或全部三个CDR序列,或与其(例如,与CDR序列中的一个、两个或全部三个)具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
表4.钙网蛋白靶向性抗原结合结构域的示例性重链CDR和FWR
表5.钙网蛋白靶向性抗原结合结构域的示例性轻链CDR和FWR
表6.钙网蛋白靶向性抗原结合的示例性FWR
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含如表24中所列的VH氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含如表24中所列的VL氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含:(i)VH,该VH包含如表24中所列的VH氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,以及(ii)VL,该VL包含如表24中所列的VL氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
表24.钙网蛋白靶向性抗原结合的示例性可变区(下划线表示CDR序列)
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含scFv,该scFv包含如表25中所列的氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含scFv,该scFv包含如表25中所列的VH氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含scFv,该scFv包含如表25中所列的VL氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含scFv,该scFv包含如表25中所列的间隔区氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
表25.钙网蛋白靶向性抗原结合的示例性scFv序列(下划线表示CDR序列)
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含Fc区。在一些实施方案中,Fc区选自例如IgG1、IgG2、IgG3、IgG4、IgM、IgA1、IgA2、IgD和IgE的重链恒定区。在一些实施方案中,Fc区选自IgG1、IgG2、IgG3和IgG4的重链恒定区。在一些实施方案中,Fc区选自IgG1或IgG2(例如,人IgG1或IgG2)的重链恒定区。在一些实施方案中,重链恒定区是人IgG2a。在一些实施方案中,重链恒定区包含鼠IgG2a序列,例如,下文SEQ ID NO:D123,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列:
AKTTAPSVYPLAPVCGDTTGSSVTLGCLVKGYFPEPVTLTWNSGSLSSGVHTFPAVLQSDLYTLSSSVTVTSSTWPSQSITCNVAHPASSTKVDKKIEPRGPTIKPCPPCKCPAPNLLGGPSVFIFPPKIKDVLMISLSPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNKDLPAPIERTISKPKGSVRAPQVYVLPPPEEEMTKKQVTLTCMVTDFMPEDIYVEWTNNGKTELNYKNTEPVLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK(SEQ ID NO:D123)。
在一些实施方案中,Fc区包含Fc区变体,例如,如本文所述的。在一些实施方案中,Fc区包含一个或多个突变。在一些实施方案中,Fc区包含LALAPG突变。在一些实施方案中,Fc区包含鼠IgG2a-LALAPG变体的氨基酸序列,例如,下文SEQ ID NO:D124或D125的序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列:
AKTTAPSVYPLAPVCGDTTGSSVTLGCLVKGYFPEPVTLTWNSGSLSSGVHTFPAVLQSDLYTLSSSVTVTSSTWPSQSITCNVAHPASSTKVDKKIEPRGPTIKPCPPCKCPAPNAAGGPSVFIFPPKIKDVLMISLSPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNKDLGAPIERTISKPKGSVRAPQVYVLPPPEEEMTKKQVTLTCMVTDFMPEDIYVEWTNNGKTELNYKNTEPVLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK(SEQ ID NO:D124)
AKTTAPSVYPLAPVCGDTTGSSVTLGCLVKGYFPEPVTLTWNSGSLSSGVHTFPAVLQSDLYTLSSSVTVTSSTWPSQSITCNVAHPASSTKVDKKIEPRGPTIKPCPPCKCPAPNAAGGPSVFIFPPKIKDVLMISLSPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNKDLGAPIERTISKPKGSVRAPQVYVLPPCEEEMTKKQVTLWCMVTDFMPEDIYVEWTNNGKTELNYKNTEPVLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK(SEQ ID NO:D125)。
在一些实施方案中,Fc区包含人IgG2a N2976A变体的氨基酸序列,例如,下文SEQID NO:D130的序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列:
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYGSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:D130)。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含轻链恒定区,例如,CLκ区,例如,人CLκ区。在一些实施方案中,轻链恒定区包含下文SEQ ID NO:D126的氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列:
RADAAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC(SEQ ID NO:D126)。
在一些实施方案中,轻链恒定区包含下文SEQ ID NO:D131的氨基酸序列,或与其具有至少75%、80%、85%、90%、95%、96%、97%、98%或99%序列同一性的氨基酸序列:
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO:D131)。
另外的钙网蛋白靶向性抗原结合结构域
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含表16-19中公开的任何CDR氨基酸序列或可变区氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6253的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:243的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6255的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:6253的VHCDR1氨基酸序列、SEQ ID NO:243的VHCDR2氨基酸序列,和/或SEQ ID NO:6255的VHCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ IDNO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:6259的VLCDR1氨基酸序列、SEQ IDNO:6260的VLCDR2氨基酸序列,以及SEQ ID NO:6261的VLCDR3氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含SEQ ID NO:244的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含SEQ ID NO:245的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和/或VL,该VH包含SEQ ID NO:244的氨基酸序列,该VL包含SEQ ID NO:245的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH,该VH包含6372、234、235、236或237的氨基酸序列,或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VL,该VL包含238、239、240、241或242的氨基酸序列,或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:238的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:238的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:238的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:238的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:238的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:239的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列,该VL包含SEQ ID NO:239的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:239的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列,该VL包含SEQ ID NO:239的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:239的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列,该VL包含SEQ ID NO:239的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:239的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列,该VL包含SEQ ID NO:239的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:239的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列,该VL包含SEQ ID NO:239的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:240的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列,该VL包含SEQ ID NO:240的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:240的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列,该VL包含SEQ ID NO:240的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:240的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列,该VL包含SEQ ID NO:240的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:240的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列,该VL包含SEQ ID NO:240的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:240的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列,该VL包含SEQ ID NO:240的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:241的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列,该VL包含SEQ ID NO:241的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:241的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列,该VL包含SEQ ID NO:241的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:241的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列,该VL包含SEQ ID NO:241的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:241的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列,该VL包含SEQ ID NO:241的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:241的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列,该VL包含SEQ ID NO:241的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:242的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6372的氨基酸序列,该VL包含SEQ ID NO:242的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:242的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:234的氨基酸序列,该VL包含SEQ ID NO:242的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:242的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:235的氨基酸序列,该VL包含SEQ ID NO:242的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:242的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:236的氨基酸序列,该VL包含SEQ ID NO:242的氨基酸序列。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:242的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:237的氨基酸序列,该VL包含SEQ ID NO:242的氨基酸序列。
在一些实施方案中,钙网蛋白靶向性抗原结合结构域包含VH和VL,该VH包含SEQID NO:236的氨基酸序列,该VL包含SEQ ID NO:238的氨基酸序列。
表16.另外的钙网蛋白靶向性抗原结合结构域的示例性可变区
表17.钙网蛋白靶向性抗原结合结构域的示例性重链CDR
表18.钙网蛋白靶向性抗原结合结构域的示例性轻链CDR
表19.示例性钙网蛋白靶向性抗原结合结构域
免疫细胞接合物
本文公开的多特异性或多功能性分子的免疫细胞接合物可介导免疫细胞(例如,免疫效应细胞)的结合和/或激活。在一些实施方案中,免疫细胞选自T细胞、NK细胞、B细胞、树突细胞或巨噬细胞接合物或其组合。在一些实施方案中,免疫细胞接合物选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物或其组合中的一种、两种、三种或全部。免疫细胞接合物可以是免疫系统的激动剂。在一些实施方案中,免疫细胞接合物可以是抗体分子、配体分子(例如,进一步包含免疫球蛋白恒定区(例如,Fc区)的配体)、小分子或核苷酸分子。
T细胞接合物
本发明尤其提供了多特异性(例如,双特异性、三特异性、四特异性)或多功能性分子,其工程化为含有介导T细胞的结合和/或激活的一种或多种T细胞接合物。因此,在一些实施方案中,T细胞接合物选自抗原结合结构域或配体,其结合至(例如,并在一些实施方案中激活)TCR(例如,TCRβV)、CD3、TCRα、TCRβ、TCRγ、TCRζ、ICOS、CD28、CD27、HVEM、LIGHT、CD40、4-1BB、OX40、DR3、GITR、CD30、TIM1、SLAM、CD2或CD226的β亚基可变链中的一种或多种。在其他实施方案中,T细胞接合物选自抗原结合结构域或配体,其结合至但不激活TCRβV、CD3、TCRα、TCRβ、TCRγ、TCRζ、ICOS、CD28、CD27、HVEM、LIGHT、CD40、4-1BB、OX40、DR3、GITR、CD30、TIM1、SLAM、CD2或CD226中的一种或多种。在一些实施方案中,T细胞接合物结合至TCRβV。
在一些实施方案中,T细胞接合物结合至CD3(例如,包含结合至CD3的抗原结合结构域)。在一些实施方案中,多特异性或多功能性分子包含结合至CD3的T细胞接合物(例如,包含结合至CD3的抗原结合结构域)和钙网蛋白靶向性抗原结合结构域,例如,如本文所述的。
在一些实施方案中,多特异性或多功能性分子(例如,如本文所述的)包含结合至CD3的抗原结合结构域。在一些实施方案中,多特异性或多功能性分子包含结合至CD3的抗原结合结构域和钙网蛋白靶向性抗原结合结构域,例如,如本文所述的。
在一些实施方案中,结合至CD3的抗原结合结构域包含表26和/或表42中公开的一个或多个CDR(例如,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和/或VLCDR3),或与其具有至少85%、90%、95%或99%同一性的序列。在一些实施方案中,结合至CD3的抗原结合结构域包含表26和/或表42中公开的一个或多个框架区(例如,VHFWR1、VHFWR2、VHFWR3、VHFWR4、VLFWR1、VLFWR2、VLFWR3和/或VLFWR4),或与其具有至少85%、90%、95%或99%同一性的序列。在一些实施方案中,结合至CD3的抗原结合结构域包含表27中公开的VH和/或VL,或与其具有至少85%、90%、95%或99%同一性的序列。
表26.CD3靶向性抗原结合结构域的示例性重链CDR和FWR
表42.CD3靶向性抗原结合结构域的示例性轻链CDR和FWR
表27.CD3靶向性抗原结合结构域的示例性可变区
在一些实施方案中,多功能性分子(例如,scFv,例如,双特异性scFv)包含下文氨基酸序列(或其中包含的CDR、VH或VL序列),或与其具有至少85%、90%、95%或99%同一性的氨基酸序列:
EVQLVESGGGLVQPGKSLKLSCEASGFTFSGYGMHWVRQAPGRGLESVAYITSSSINIKYADAVKGRFTVSRDNAKNLLFLQMNILKSEDTAMYYCARFDWDKNYWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSSLPASLGDRVTINCQASQDISNYLNWYQQKPGKAPKLLIYYTNKLADGVPSRFSGSGSGRDSSFTISSLESEDIGSYYCQQYYNYPWTFGPGTKLEIKGGGGSTIKPCPPCKCPAPNAAGGPSVFIFPPKIKDVLMISLSPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNKDLGAPIERTISKPKGSVRAPQVCVLPPPEEEMTKKQVTLSCAVTDFMPEDIYVEWTNNGKTELNYKNTEPVLDSDGSYFMVSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK(SEQ ID NO:D127)。
在一些实施方案中,多功能性分子(例如,双特异性抗体分子)包含下文氨基酸序列(或其中包含的CDR(下划线)、VH或恒定区序列),或与其具有至少85%、90%、95%或99%同一性的氨基酸序列:
EVQLVESGGGLVQPGGSLRLSCAASGFTFSEYWMNWLRQAPGKGLEWVGVIKYKYSNYATEFAESVKGRFTISRDDSKSSVYLQMNSLKTEDTAVYYCARGRDVQDYWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCREEMTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:D212)。
在一些实施方案中,多功能性分子(例如,双特异性抗体分子)包含下文氨基酸序列(或其中包含的CDR(下划线)、VL或恒定区序列),或与其具有至少85%、90%、95%或99%同一性的氨基酸序列:DIQLTQSPSFLSASVGDRVTITCSTSSSVTTNYLHWYQQKPGKAPKLLIYSTSNLASGVPSRFSGSGSGTEYTLTISSLQPEDFATYYCQQCLSSPCTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO:D213)。
在一些实施方案中,多功能性分子(例如,scFv,例如,双特异性scFv)包含下文氨基酸序列(或其中包含的CDR(下划线)、VH或VL序列),或与其具有至少85%、90%、95%或99%同一性的氨基酸序列:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTTYWMHWVRQAPGQGLEWMGNFNPNNGDTNYNEKFKTRVTMTVDKSTSTAYMELRSLRSDDMAVYYCARDDYGRYYFDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSTLSASVGDRVTITCKSSQSLLNSRTRKNYLAWYQQKPGKAPKLLIYWAFTRESGVPSRFSGSGSGTEFTLTISSLQPDDFATYYCKQSFILRTFGGGTKVEIKDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSREEMTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:D214)。
人T细胞受体(TCR)复合物
T细胞受体(TCR)可以存在于T细胞表面。TCR识别细胞(例如,抗原呈递细胞)表面上的主要组织相容性复合物(MHC)分子上呈递(例如,结合)的抗原(例如,肽)。TCR是异源二聚体分子,并且可以包含α链、β链、γ链或δ链。包含α链和β链的TCR也称为TCRαβ。TCRβ链由以下区(也称为区段)组成:可变(V)、多样(D)、连接(J)和恒定(C)(参见Mayer G.和NylandJ.(2010)第10章:Major Histocompatibility Complex and T-cell Receptors-Role inImmune Responses.在:Microbiology and Immunology on-line,University of SouthCarolina School of Medicine)。TCRα链由V、J和C区组成。T细胞受体(TCR)通过V(可变)、D(多样)、J(连接)和C(恒定)区的体细胞重组的重排是T细胞发育和成熟中的决定性事件。TCR基因重排发生在胸腺中。
TCR可以包含受体复合物,称为TCR复合物,其包含由α链和β链组成的TCR异源二聚体和二聚体信号传导分子,例如,CD3共受体,例如,CD3δ/ε和/或CD3γ/ε。
TCRβV
免疫系统的多样性使得能够抵御大量病原体。由于种系基因组的大小有限,因此不仅通过V(D)J重组过程而且通过核苷酸的连接(V-D和D-J区段之间的连接)缺失和伪随机非模板核苷酸的添加来实现多样性。TCRβ基因经历基因排列,以产生多样性。
TCRVβ所有组分在个体和群体之间不同,这是因为例如在功能性基因区段中经常发生的7种失活多态性和包含2个Vβ基因区段的大片段插入/缺失相关多态性。
本发明尤其提供了抗体分子及其片段,其结合(例如,特异性结合)至人TCRβV链(TCRβV),例如,TCRβV基因家族(也称为组),例如,TCRβV亚家族(也称为亚组),例如,如本文所述的。TCRβV家族和亚家族是本领域已知的,例如,如Yassai等人,(2009)Immunogenetics61(7)第493-502页;Wei S.和Concannon P.(1994)Human Immunology 41(3)第201-206页中描述的。本文所述的抗体可以是重组抗体,例如,重组非鼠抗体,例如,重组人或人源化抗体。
在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV,例如,TCRβV家族,例如,基因家族或其变体。在一些实施方案中,TCRBV基因家族包含一个或多个(例如,如本文所述的,例如,图3、表28或29中的)亚家族。在一些实施方案中,TCRβV基因家族包含:TCRβV6亚家族、TCRβV10亚家族、TCRβV12亚家族、TCRβV5亚家族、TCRβV7亚家族、TCRβV11亚家族、TCRβV14亚家族、TCRβV16亚家族、TCRβV18亚家族、TCRβV9亚家族、TCRβV13亚家族、TCRβV4亚家族、TCRβV3亚家族、TCRβV2亚家族、TCRβV15亚家族、TCRβV30亚家族、TCRβV19亚家族、TCRβV27亚家族、TCRβV28亚家族、TCRβV24亚家族、TCRβV20亚家族、TCRβV25亚家族、TCRβV29亚家族、TCRβV1亚家族、TCRβV17亚家族、TCRβV21亚家族、TCRβV23亚家族,或TCRβV26亚家族。
在一些实施方案中,TCRβV6亚家族也称为TCRβV13.1。在一些实施方案中,TCRβV6亚家族包含:TCRβV6-4*01、TCRβV6-4*02、TCRβV6-9*01、TCRβV6-8*01、TCRβV6-5*01、TCRβV6-6*02、TCRβV6-6*01、TCRβV6-2*01、TCRβV6-3*01或TCRβV6-1*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-9*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-8*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-2*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-3*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-1*01或其变体。
在一些实施方案中,TCRβV6包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6(例如,TCRβV6-5*01)被SEQ ID NO:1A和/或SEQ ID NO:2A识别,例如,结合。在一些实施方案中,TCRβV6(例如,TCRβV6-5*01)被SEQ ID NO:9A和/或SEQ ID NO:10A识别,例如,结合。在一些实施方案中,TCRβV6被SEQ ID NO:9A和/或SEQ ID NO:11A识别,例如,结合。
在一些实施方案中,TCRβV10亚家族也称为TCRβV12。在一些实施方案中,TCRβV10亚家族包含:TCRβV10-1*01、TCRβV10-1*02、TCRβV10-3*01或TCRβV10-2*01或其变体。
在一些实施方案中,TCRβV12亚家族也称为TCRβV8.1。在一些实施方案中,TCRβV12亚家族包含:TCRβV12-4*01、TCRβV12-3*01或TCRβV12-5*01或其变体。在一些实施方案中,TCRβV12被SEQ ID NO:15A和/或SEQ ID NO:16A识别,例如,结合。在一些实施方案中,TCRβV12被SEQ ID NO:23A-25A中的任一者和/或SEQ ID NO:26A-30A中的任一者识别,例如,结合。
在一些实施方案中,TCRβV5亚家族选自:TCRβV5-5*01、TCRβV5-6*01、TCRβV5-4*01、TCRβV5-8*01、TCRβV5-1*01或其变体。
在一些实施方案中,TCRβV7亚家族包含TCRβV7-7*01、TCRβV7-6*01、TCRβV7-8*02、TCRβV7-4*01、TCRβV7-2*02、TCRβV7-2*03、TCRβV7-2*01、TCRβV7-3*01、TCRβV7-9*03或TCRβV7-9*01或其变体。
在一些实施方案中,TCRβV11亚家族包含:TCRβV11-1*01、TCRβV11-2*01或TCRβV11-3*01或其变体。
在一些实施方案中,TCRβV14亚家族包含TCRβV14*01或其变体。
在一些实施方案中,TCRβV16亚家族包含TCRβV16*01或其变体。
在一些实施方案中,TCRβV18亚家族包含TCRβV18*01或其变体。
在一些实施方案中,TCRβV9亚家族包含TCRβV9*01或TCRβV9*02或其变体。
在一些实施方案中,TCRβV13亚家族包含TCRβV13*01或其变体。
在一些实施方案中,TCRβV4亚家族包含TCRβV4-2*01、TCRβV4-3*01或TCRβV4-1*01或其变体。
在一些实施方案中,TCRβV3亚家族包含TCRβV3-1*01或其变体。
在一些实施方案中,TCRβV2亚家族包含TCRβV2*01或其变体。
在一些实施方案中,TCRβV15亚家族包含TCRβV15*01或其变体。
在一些实施方案中,TCRβV30亚家族包含TCRβV30*01或TCRβV30*02或其变体。
在一些实施方案中,TCRβV19亚家族包含TCRβV19*01或TCRβV19*02或其变体。
在一些实施方案中,TCRβV27亚家族包含TCRβV27*01或其变体。
在一些实施方案中,TCRβV28亚家族包含TCRβV28*01或其变体。
在一些实施方案中,TCRβV24亚家族包含TCRβV24-1*01或其变体。
在一些实施方案中,TCRβV20亚家族包含TCRβV20-1*01或TCRβV20-1*02或其变体。
在一些实施方案中,TCRβV25亚家族包含TCRβV25-1*01或其变体。
在一些实施方案中,TCRβV29亚家族包含TCRβV29-1*01或其变体。
表28:TCRβV亚家族和亚家族成员列表
表29:另外的TCRβV亚家族
抗TCRβV抗体
本文公开了一类新型抗体(即本文公开的抗TCRβV抗体分子)的发现,其尽管具有低序列相似性(例如,识别不同TCRβV亚家族的不同抗体分子之间的低序列同一性),但识别TCRβV蛋白上的结构保守区(例如,结构域)并具有相似的功能(例如,相似的细胞因子谱)。因此,本文公开的抗TCRβV抗体分子共享结构-功能关系。
在一些实施方案中,本文公开的抗TCRβV抗体分子不识别(例如,结合至)TCRβV:TCRα复合物的界面。
在一些实施方案中,本文公开的抗TCRβV抗体分子不识别(例如,结合至)TCRβV蛋白的恒定区。结合至TCRBV区的恒定区的示例性抗体是如Viney等(Hybridoma.1992Dec;11(6):701-13)中所述的JOVI.1。
在一些实施方案中,本文公开的抗TCRβV抗体分子不识别(例如,结合至)TCRβV蛋白互补决定区(例如,CDR1、CDR2和/或CDR3)中的一个或多个(例如,全部)。
在一些实施方案中,本文公开的抗TCRβV抗体分子结合(例如,特异性结合)至TCRβV区。在一些实施方案中,本文公开的抗TCRβV抗体分子的结合导致不同于结合至除TCRβV区以外的受体或分子的T细胞接合物(“非TCRβV结合T细胞接合物”)的细胞因子谱的细胞因子谱。在一些实施方案中,非TCRβV结合T细胞接合物包含结合至CD3分子(例如,CD3(CD3e)分子)或TCRα分子的抗体。在一些实施方案中,非TCRβV结合T细胞接合物是OKT3抗体或SP34-2抗体。
在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV,例如,TCRβV基因家族,例如,(例如,如本文所述的,例如,图3、表28或表29中的)TCRβV亚家族中的一个或多个。在一些实施方案中,抗TCRβV抗体分子结合至选自以下的一个或多个TCRβV亚家族:TCRβV6亚家族、TCRβV10亚家族、TCRβV12亚家族、TCRβV5亚家族、TCRβV7亚家族、TCRβV11亚家族、TCRβV14亚家族、TCRβV16亚家族、TCRβV18亚家族、TCRβV9亚家族、TCRβV13亚家族、TCRβV4亚家族、TCRβV3亚家族、TCRβV2亚家族、TCRβV15亚家族、TCRβV30亚家族、TCRβV19亚家族、TCRβV27亚家族、TCRβV28亚家族、TCRβV24亚家族、TCRβV20亚家族、TCRβV25亚家族、TCRβV29亚家族、TCRβV1亚家族、TCRβV17亚家族、TCRβV21亚家族、TCRβV23亚家族,或TCRβV26亚家族或其变体。
在一些实施方案中,抗TCRβV抗体分子结合至TCRβV6亚家族,其包含:TCRβV6-4*01、TCRβV6-4*02、TCRβV6-9*01、TCRβV6-8*01、TCRβV6-5*01、TCRβV6-6*02、TCRβV6-6*01、TCRβV6-2*01、TCRβV6-3*01或TCRβV6-1*01或其变体。在一些实施方案中,TCRβV6亚家族包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-9*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-8*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-2*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-3*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-1*01或其变体。
在一些实施方案中,抗TCRβV抗体分子结合至TCRβV10亚家族,其包含:TCRβV10-1*01、TCRβV10-1*02、TCRβV10-3*01或TCRβV10-2*01或其变体。
在一些实施方案中,抗TCRβV抗体分子结合至TCRβV12亚家族,其包含:TCRβV12-4*01、TCRβV12-3*01或TCRβV12-5*01或其变体。
在一些实施方案中,抗TCRβV抗体分子结合至TCRβV5亚家族,其包含:TCRβV5-5*01、TCRβV5-6*01、TCRβV5-4*01、TCRβV5-8*01、TCRβV5-1*01或其变体。
在一些实施方案中,抗TCRβV抗体分子不结合至TCRβV12,或以小于(例如,小于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的16G8鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至TCRβV12。
在一些实施方案中,抗TCRβV抗体分子以大于(例如,大于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的16G8鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至TCRβV12。
在一些实施方案中,抗TCRβV抗体分子以大于(例如,大于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的16G8鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至除TCRβV12以外的TCRβV区(例如,本文所述的TCRβV区,例如,TCRβV6亚家族(例如,TCRβV6-5*01))。
在一些实施方案中,抗TCRβV抗体分子不结合至TCRβV5-5*01或TCRβV5-1*01,或以小于(例如,小于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的TM23鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至TCRβV5-5*01或TCRβV5-1*01。
在一些实施方案中,抗TCRβV抗体分子以大于(例如,大于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的TM23鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至TCRβV5-5*01或TCRβV5-1*01。
在一些实施方案中,抗TCRβV抗体分子以大于(例如,大于约10%、20%、30%、40%、50%、60%、70%、80%、90%或约2、5或10倍)如美国专利5,861,155中所述的TM23鼠抗体或其人源化形式的亲和力和/或结合特异性的亲和力和/或结合特异性结合至除TCRβV5-5*01或TCRβV5-1*01以外的TCRβV区(例如,本文所述的TCRβV区,例如,TCRβV6亚家族(例如,TCRβV6-5*01))。
抗TCRβV6抗体
因此,在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV6,例如,TCRβV6亚家族,其包含:TCRβV6-4*01、TCRβV6-4*02、TCRβV6-9*01、TCRβV6-8*01、TCRβV6-5*01、TCRβV6-6*02、TCRβV6-6*01、TCRβV6-2*01、TCRβV6-3*01或TCRβV6-1*01。在一些实施方案中,TCRβV6亚家族包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-4*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-9*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-8*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-5*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*02或其变体。在一些实施方案中,TCRβV6包含TCRβV6-6*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-2*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-3*01或其变体。在一些实施方案中,TCRβV6包含TCRβV6-1*01或其变体。
在一些实施方案中,TCRβV6-5*01由SEQ ID NO:43A的核酸序列或与其具有85%、90%、95%、99%或更多同一性的序列编码。
SEQ ID NO:43A
ATGAGCATCGGCCTCCTGTGCTGTGCAGCCTTGTCTCTCCTGTGGGCAGGTCCAGTGAATGCTGGTGTCACTCAGACCCCAAAATTCCAGGTCCTGAAGACAGGACAGAGCATGACACTGCAGTGTGCCCAGGATATGAACCATGAATACATGTCCTGGTATCGACAAGACCCAGGCATGGGGCTGAGGCTGATTCATTACTCAGTTGGTGCTGGTATCACTGACCAAGGAGAAGTCCCCAATGGCTACAATGTCTCCAGATCAACCACAGAGGATTTCCCGCTCAGGCTGCTGTCGGCTGCTCCCTCCCAGACATCTGTGTACTTCTGTGCCAGCAGTTACTC
在一些实施方案中,TCRβV6-5*01包含SEQ ID NO:1044的氨基酸序列,或与其具有85%、90%、95%、99%或更多同一性的氨基酸序列。
SEQ ID NO:1044MSIGLLCCAALSLLWAGPVNAGVTQTPKFQVLKTGQSMTLQCAQDMNHEYMSWYRQDPGMGLRLIHYSVGAGITDQGEVPNGYNVSRSTTEDFPLRLLSAAPSQTSVYFCASSY
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是非鼠抗体分子,例如,人或人源化抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是人抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是人源化抗体分子。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是分离的或重组的。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含至少一个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的抗原结合区(例如,可变区或其抗原结合片段),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含至少一个、两个、三个或四个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含至少一个或两个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子包含具有SEQ ID NO:231A或3290A的共有序列的重链可变区(VH)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含至少一个或两个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的轻链可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子包含具有SEQ ID NO:230A或3289A的共有序列的轻链可变区(VL)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含IgG4(例如,人IgG4)的重链恒定区。在另一实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括IgG1(例如,人IgG1)的重链恒定区。在一个实施方案中,重链恒定区包含表32中所述的氨基序列,或与其基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括κ轻链恒定区,例如,人κ轻链恒定区。在一个实施方案中,轻链恒定区包含表32中所述的氨基序列,或与其基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链可变区(VH)的互补决定区(CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个(或统称为所有)来自重链可变区的CDR,该重链可变区包含表30中所示的氨基酸序列,或由表30中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表30中所示的或由表30中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的轻链可变区的互补决定区(CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个(或统称为所有)来自轻链可变区的CDR,该轻链可变区包含表30中所示的氨基酸序列,或由表30中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表30中所示的或由表30中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个、三个、四个、五个或六个(或统称为所有)来自重链和轻链可变区的CDR,该重链和轻链可变区包含表30中所示的氨基酸序列,或由表30中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表30中所示的或由表30中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的所有六个CDR,或密切相关的CDR,例如,相同或具有至少一个氨基酸改变但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)的CDR。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的抗体)的重链可变区的根据Kabat等的CDR(例如,如表30中所述的根据Kabat定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Kabat等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的抗体)的轻链可变区的根据Kabat等的CDR(例如,如表30中所述的根据Kabat定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Kabat等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个、三个、四个、五个或六个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Kabat等的CDR(例如,如表30中所述的根据Kabat定义的至少一个、两个、三个、四个、五个或六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Kabat等的一个、两个、三个、四个、五个或六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Kabat等的所有六个CDR(例如,如表30中所述的根据Kabat定义的所有六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Kabat等的所有六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。在一个实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个高变环,其具有与本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68)的相应高变环相同的标准结构,例如,与本文所述抗体的重链和/或轻链可变结构域的至少环1和/或环2相同的标准结构。参见例如,Chothia等人,(1992)J.Mol.Biol.227:799-817;Tomlinson等人,(1992)J.Mol.Biol.227:776-798对于高变环标准结构的描述。这些结构可以通过检查这些参考文献中所述的表格来确定。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或如表30中所述)的重链可变区的根据Chothia等的CDR(例如,如表30中所述的根据Chothia定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Chothia等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的抗体)的轻链可变区的根据Chothia等的CDR(例如,如表30中所述的根据Chothia定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Chothia等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括至少一个、两个、三个、四个、五个或六个来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Chothia等的CDR(例如,如表30中所述的根据Chothia定义的至少一个、两个、三个、四个、五个或六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Chothia等的一个、两个、三个、四个、五个或六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括来自本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或表30中所述的或由表30中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Chothia等的所有六个CDR(例如,如表30中所述的根据Chothia定义的所有六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表30中所示的根据Chothia等的所有六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。在一个实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括根据Kabat等、Chothia等或如表30中所述定义的CDR或高变环的组合。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)可以含有根据Kabat和Chothia定义的CDR或高变环的任何组合。
在一些实施方案中,如表30中所述的组合CDR是包含Kabat CDR和Chothia CDR的CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括表30中鉴定为组合CDR的CDR或高变环的组合。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)可以含有表30中所述的相应“组合”CDR的CDR或高变环的任何组合。
在实施方案中,例如,包含可变区、CDR(例如,组合CDR、Chothia CDR或Kabat CDR)或本文(例如,表30中)提及的其他序列的实施方案中,抗体分子是单特异性抗体分子、双特异性抗体分子、二价抗体分子、双互补位抗体分子或包含抗体的抗原结合片段的抗体分子,例如,半抗体或半抗体的抗原结合片段。在某些实施方案中,抗体分子包含多特异性分子,例如,双特异性分子,例如,如本文所述的。
在实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括:
(i)SEQ ID NO:2A、SEQ ID NO:10A或SEQ ID NO:11A的轻链互补决定区1(LCCDR1)、轻链互补决定区2(LC CDR2)和轻链互补决定区3(LC CDR3)中的一个、两个或全部,和/或
(ii)SEQ ID NO:1A或SEQ ID NO:9A的重链互补决定区1(HC CDR1)、重链互补决定区2(HC CDR2)和重链互补决定区3(HC CDR3)中的一个、两个或全部。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含SEQ ID NO:2A的LC CDR1、LC CDR2和LC CDR3以及SEQ ID NO:1A的HC CDR1、HCCDR2和HC CDR3。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含SEQ ID NO:10A的LC CDR1、LC CDR2和LC CDR3以及SEQ ID NO:9A的HC CDR1、HC CDR2和HC CDR3。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含SEQ ID NO:11A的LC CDR1、LC CDR2和LC CDR3以及SEQ ID NO:9A的HC CDR1、HC CDR2和HC CDR3。
在实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)SEQ ID NO:6的LC CDR1氨基酸序列、SEQ ID NO:7A的LC CDR2氨基酸序列,或SEQ ID NO:8A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:3的HC CDR1氨基酸序列、SEQ ID NO:4A的HC CDR2氨基酸序列,或SEQ ID NO:5A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:6A的LC CDR1氨基酸序列、SEQ ID NO:7A的LC CDR2氨基酸序列,或SEQ ID NO:8A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:3A的HC CDR1氨基酸序列、SEQ ID NO:4A的HC CDR2氨基酸序列,或SEQ ID NO:5A的HC CDR3氨基酸序列。
在实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)SEQ ID NO:51A的LC CDR1氨基酸序列、SEQ ID NO:52A的LC CDR2氨基酸序列,或SEQ ID NO:53A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:45的HC CDR1氨基酸序列、SEQ ID NO:46A的HC CDR2氨基酸序列,或SEQ ID NO:47A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:51A的LC CDR1氨基酸序列、SEQ ID NO:52A的LC CDR2氨基酸序列,或SEQ ID NO:53A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:45A的HC CDR1氨基酸序列、SEQ ID NO:46A的HC CDR2氨基酸序列,或SEQ ID NO:47A的HC CDR3氨基酸序列。
在实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)SEQ ID NO:54A的LC CDR1氨基酸序列、SEQ ID NO:55A的LC CDR2氨基酸序列,或SEQ ID NO:56A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:48A的HC CDR1氨基酸序列、SEQ ID NO:49A的HC CDR2氨基酸序列,或SEQ ID NO:50A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:54A的LC CDR1氨基酸序列、SEQ ID NO:55A的LC CDR2氨基酸序列,或SEQ ID NO:56A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:48A的HC CDR1氨基酸序列、SEQ ID NO:49A的HC CDR2氨基酸序列,或SEQ ID NO:50A的HC CDR3氨基酸序列。
在一个实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)的轻链或重链可变框架(例如,包括至少FR1、FR2、FR3和任选地FR4的区域)可以选自:(a)轻链或重链可变框架,其包括至少80%、85%、87%、90%、92%、93%、95%、97%、98%或100%的来自人轻链或重链可变框架的氨基酸残基,例如,来自人成熟抗体、人种系序列或人共有序列的轻链或重链可变框架残基;(b)轻链或重链可变框架,其包括20%至80%、40%至60%、60%至90%或70%至95%的来自人轻链或重链可变框架的氨基酸残基,例如,来自人成熟抗体、人种系序列或人共有序列的轻链或重链可变框架残基;(c)非人框架(例如,啮齿动物框架);或(d)已被修饰例如以去除抗原性或细胞毒性决定簇(例如,去免疫化或部分人源化)的非人框架。在一个实施方案中,轻链或重链可变框架区(特别是FR1、FR2和/或FR3)包括与人种系基因的VL或VH区段的框架至少70%、75%、80%、85%、87%、88%、90%、92%、94%、95%、96%、97%、98%、99%相同的或相同的轻链或重链可变框架序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含重链可变结构域,其具有至少一个、两个、三个、四个、五个、六个、七个、十个、十五个、二十个或更多个来自A-H.1至A-H.85中任一种(例如,A-H.1、A-H.2或A-H.68)的氨基酸序列(例如,图1A中或SEQ ID NO:9A中所示的整个可变区中FR区的氨基酸序列)的改变,例如,氨基酸置换或缺失。
可替代地,或者与本文所述的重链置换组合,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,其具有至少一个、两个、三个、四个、五个、六个、七个、十个、十五个、二十个或更多个来自A-H.1至A-H.85中任一种(例如,A-H.1、A-H.2或A-H.68)的氨基酸序列(例如,图1B中或SEQ ID NO:10A或SEQ ID NO:11A中所示的整个可变区中FR区的氨基酸序列)的氨基酸改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括图1A中所示的一个、两个、三个或四个重链框架区,或与其基本上相同的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括图1B中所示的一个、两个、三个或四个轻链框架区,或与其基本上相同的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的轻链框架区1,例如,如图1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的轻链框架区2,例如,如图1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的轻链框架区3,例如,如图1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的轻链框架区4,例如,如图1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含框架区,例如,框架区1(FR1),其包含改变,例如,根据Kabat编号的第10位处的置换(例如,保守置换)。在一些实施方案中,FR1在第10位处包含苯丙氨酸,例如,丝氨酸至苯丙氨酸的置换。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含框架区,例如,框架区2(FR2),其包含改变,例如,根据Kabat编号的本文公开位置处的置换(例如,保守置换)。在一些实施方案中,FR2在第36位处包含组氨酸,例如,根据Kabat编号的第36位处的置换,例如,酪氨酸至组氨酸的置换。在一些实施方案中,FR2在第46位处包含丙氨酸,例如,根据Kabat编号的第46位处的置换,例如,精氨酸至丙氨酸的置换。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含框架区,例如,框架区3(FR3),其包含改变,例如,根据Kabat编号的本文公开位置处的置换(例如,保守置换)。在一些实施方案中,FR3在第87位处包含苯丙氨酸,例如,根据Kabat编号的第87位处的置换,例如,酪氨酸至苯丙氨酸的置换。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含:(a)框架区1(FR1),其在第10位处包含苯丙氨酸,例如,根据Kabat编号的第10位处的置换,例如,丝氨酸至苯丙氨酸的置换;(b)框架区2(FR2),其在第36位处包含组氨酸,例如,根据Kabat编号的第36位处的置换,例如,酪氨酸至组氨酸的置换,并且在第46位处包含丙氨酸,例如,根据Kabat编号的第46位处的置换,例如,精氨酸至丙氨酸的置换;以及(c)框架区3(FR3),其在第87位处包含苯丙氨酸,例如,根据Kabat编号的第87位处的置换,例如,酪氨酸至苯丙氨酸的置换,例如,如SEQ IDNO:10A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含:(a)框架区2(FR2),其在第36位处包含组氨酸,例如,根据Kabat编号的第36位处的置换,例如,酪氨酸至组氨酸的置换,并且在第46位处包含丙氨酸,例如,根据Kabat编号的第46位处的置换,例如,精氨酸至丙氨酸的置换;以及(b)框架区3(FR3),其在第87位处包含苯丙氨酸,例如,根据Kabat编号的第87位处的置换,例如,酪氨酸至苯丙氨酸的置换,例如,如SEQ ID NO:11A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含轻链可变结构域,该轻链可变结构域包含:(a)框架区1(FR1),其包含改变,例如,根据Kabat编号的一个或多个(例如,所有)本文公开位置处的置换(例如,保守置换);(b)框架区2(FR2),其包含改变,例如,根据Kabat编号的一个或多个(例如,所有)本文公开位置处的置换(例如,保守置换),以及(c)框架区3(FR3),其包含改变,例如,根据Kabat编号的一个或多个(例如,所有)本文公开位置处的置换(例如,保守置换)。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的重链框架区1,例如,如图1A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的重链框架区2,例如,如图1A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的重链框架区3,例如,如图1A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的重链框架区4,例如,如图1A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含重链可变结构域,该重链可变结构域包含框架区,例如,框架区3(FR3),其包含改变,例如,根据Kabat编号的本文公开位置处的置换(例如,保守置换)。在一些实施方案中,FR3在第73位处包含苏氨酸,例如,根据Kabat编号的第73位处的置换,例如,谷氨酸至苏氨酸的置换。在一些实施方案中,FR3在第94位处包含甘氨酸,例如,根据Kabat编号的第94位处的置换,例如,精氨酸至甘氨酸的置换。在一些实施方案中,置换相对于人种系重链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含重链可变结构域,该重链可变结构域包含框架区3(FR3),其在第73位处包含苏氨酸,例如,根据Kabat编号的第73位处的置换,例如,谷氨酸至苏氨酸的置换,并且在第94位处包含甘氨酸,例如,根据Kabat编号的第94位处的置换,例如,精氨酸至甘氨酸的置换,例如,如SEQ ID NO:10A的氨基酸序列中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1或A-H.2的重链框架区1-4,例如,SEQ ID NO:9A,或如图1A和1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1的轻链框架区1-4,例如,SEQ ID NO:10A,或如图1A和1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.2的轻链框架区1-4,例如,SEQ ID NO:11A,或如图1A和1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1的重链框架区1-4,例如,SEQ ID NO:9A;以及A-H.1的轻链框架区1-4,例如,SEQ ID NO:10A,或如图1A和1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.2的重链框架区1-4,例如,SEQ ID NO:9A;以及A-H.2的轻链框架区1-4,例如,SEQ ID NO:11A,或如图1A和1B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)的重链或轻链可变结构域或两者包括与本文公开的氨基酸基本上相同(例如,与本文所述抗体(例如,选自A-H.1至A-H.85中任一种的抗体,例如,A-H.1、A-H.2或A-H.68,或如表30中所述的或由表30中的核苷酸序列编码的抗体)的可变区至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的氨基酸序列;或者其与本文所述抗体的可变区相差至少1或5个残基,但少于40、30、20或10个残基。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含至少一个、两个、三个或四个抗原结合区(例如,可变区),其具有如表30中所述的氨基酸序列,或与其基本上相同的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,或与表30中所示的序列相差不超过1、2、5、10或15个氨基酸残基的序列)。在另一实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包括VH和/或VL结构域,其由具有表30中所述的核苷酸序列或与其基本上相同的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,或与表30中所示的序列相差不超过3、6、15、30或45个核苷酸的序列)的核酸编码。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
VH结构域,其包含SEQ ID NO:9A的氨基酸序列、与SEQ ID NO:9A的氨基酸序列至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:9A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;和/或
VL结构域,其包含SEQ ID NO:10A的氨基酸序列、与SEQ ID NO:10A的氨基酸序列至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:10A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含:
VH结构域,其包含SEQ ID NO:9的氨基酸序列、与SEQ ID NO:9A的氨基酸序列至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:9A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;和/或
VL结构域,其包含SEQ ID NO:11A的氨基酸序列、与SEQ ID NO:11的氨基酸序列至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:11A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是全抗体或其片段(例如,Fab、F(ab’)2、Fv或单链Fv片段(scFv))。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是单克隆抗体或具有单特异性的抗体。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)也可以是人源化、嵌合、骆驼、鲨鱼或体外生成的抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是人源化抗体分子。抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)的重链和轻链可以是全长的(例如,抗体可以包括至少一条(优选两条)完整重链和至少一条(优选两条)完整轻链),或者可以包括抗原结合片段(例如,Fab、F(ab’)2、Fv、单链Fv片段、单结构域抗体、双抗体(dAb)、二价抗体,或双特异性抗体或其片段、其单结构域变体或骆驼抗体)。
在一些实施方案中,例如,如本文所述,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是多特异性分子(例如,双特异性分子)的形式。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)具有重链恒定区(Fc),其选自例如IgG1、IgG2、IgG3、IgG4、IgM、IgA1、IgA2、IgD和IgE的重链恒定区。在一些实施方案中,Fc区选自IgG1、IgG2、IgG3和IgG4的重链恒定区。在一些实施方案中,Fc区选自IgG1或IgG2(例如,人IgG1或IgG2)的重链恒定区。在一些实施方案中,重链恒定区是人IgG1。在一些实施方案中,Fc区包含Fc区变体,例如,如本文所述的。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)具有轻链恒定区,其选自例如κ或λ(优选κ(例如,人κ))的轻链恒定区。在一个实施方案中,恒定区被改变(例如,突变),以修改抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)的特性(例如,以增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能)。例如,恒定区在第296位(M至Y)、298位(S至T)、300位(T至E)、477位(H至K)和478位(N至F)处被突变,以改变Fc受体结合(例如,突变的位置例如相对于人IgG1对应于SEQ ID NO:212A或214A的第132位(M至Y)、134位(S至T)、136位(T至E)、313位(H至K)和314位(N至F);或SEQ ID NO:215A、216A、217A或218A的第135位(M至Y)、137位(S至T)、139位(T至E)、316位(H至K)和317位(N至F))。
抗体A-H.1包含重链和轻链,该重链包含SEQ ID NO:3278A的氨基酸序列,该轻链包含SEQ ID NO:72A的氨基酸序列。抗体A-H.2包含重链和轻链,该重链包含SEQ ID NO:3278A的氨基酸序列,该轻链包含SEQ ID NO:3279A的氨基酸序列。抗体A-H.68包含SEQ IDNO:1337A的氨基酸序列,或与其具有至少85%、90%、95%、96%、97%、98%或99%同一性的序列。
另外的示例性人源化抗TCRB V6抗体提供于表30中。在一些实施方案中,抗TCRβV6是抗体A,例如,人源化抗体A(抗体A-H),如表30中提供的。在一些实施方案中,抗TCRβV抗体包含表30中提供的LC CDR1、LC CDR2和LC CDR3中的一个或多个(例如,所有三个);和/或表30中提供的HC CDR1、HC CDR2和HC CDR3中的一个或多个(例如,所有三个),或与其具有至少85%、90%、95%、96%、97%、98%或99%同一性的序列。在一些实施方案中,抗体A包含表30中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少85%、90%、95%、96%、97%、98%或99%同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表1中所述抗体的VH和/或VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表1中所述抗体的VH,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表1中所述抗体的VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表1中所述抗体的VH和VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1、A-H.2、A-H.3、A-H.4、A-H.5、A-H.6、A-H.7、A-H.8、A-H.9、A-H.10、A-H.11、A-H.12、A-H.13、A-H.14、A-H.15、A-H.16、A-H.17、A-H.18、A-H.19、A-H.20、A-H.21、A-H.22、A-H.23、A-H.24、A-H.25、A-H.26、A-H.27、A-H.28、A-H.29、A-H.30、A-H.31、A-H.32、A-H.33、A-H.34、A-H.35、A-H.36、A-H.37、A-H.38、A-H.39、A-H.40、A-H.1、A-H.42、A-H.43、A-H.44、A-H.45、A-H.46、A-H.47、A-H.48、A-H.49、A-H.50、A-H.51、A-H.52、A-H.53、A-H.54、A-H.55、A-H.56、A-H.57、A-H.58、A-H.59、A-H.60、A-H.61、A-H.62、A-H.63、A-H.64、A-H.65、A-H.66、A-H.67、A-H.68、A-H.69、A-H.70、A-H.71、A-H.72、A-H.73、A-H.74、A-H.75、A-H.76、A-H.77、A-H.78、A-H.79、A-H.80、A-H.81、A-H.82、A-H.83、A-H.84或A-H.85的VH,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1、A-H.2、A-H.3、A-H.4、A-H.5、A-H.6、A-H.7、A-H.8、A-H.9、A-H.10、A-H.11、A-H.12、A-H.13、A-H.14、A-H.15、A-H.16、A-H.17、A-H.18、A-H.19、A-H.20、A-H.21、A-H.22、A-H.23、A-H.24、A-H.25、A-H.26、A-H.27、A-H.28、A-H.29、A-H.30、A-H.31、A-H.32、A-H.33、A-H.34、A-H.35、A-H.36、A-H.37、A-H.38、A-H.39、A-H.40、A-H.1、A-H.42、A-H.43、A-H.44、A-H.45、A-H.46、A-H.47、A-H.48、A-H.49、A-H.50、A-H.51、A-H.52、A-H.53、A-H.54、A-H.55、A-H.56、A-H.57、A-H.58、A-H.59、A-H.60、A-H.61、A-H.62、A-H.63、A-H.64、A-H.65、A-H.66、A-H.67、A-H.68、A-H.69、A-H.70、A-H.71、A-H.72、A-H.73、A-H.74、A-H.75、A-H.76、A-H.77、A-H.78、A-H.79、A-H.80、A-H.81、A-H.82、A-H.83、A-H.84或A-H.85的VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含A-H.1、A-H.2、A-H.3、A-H.4、A-H.5、A-H.6、A-H.7、A-H.8、A-H.9、A-H.10、A-H.11、A-H.12、A-H.13、A-H.14、A-H.15、A-H.16、A-H.17、A-H.18、A-H.19、A-H.20、A-H.21、A-H.22、A-H.23、A-H.24、A-H.25、A-H.26、A-H.27、A-H.28、A-H.29、A-H.30、A-H.31、A-H.32、A-H.33、A-H.34、A-H.35、A-H.36、A-H.37、A-H.38、A-H.39、A-H.40、A-H.1、A-H.42、A-H.43、A-H.44、A-H.45、A-H.46、A-H.47、A-H.48、A-H.49、A-H.50、A-H.51、A-H.52、A-H.53、A-H.54、A-H.55、A-H.56、A-H.57、A-H.58、A-H.59、A-H.60、A-H.61、A-H.62、A-H.63、A-H.64、A-H.65、A-H.66、A-H.67、A-H.68、A-H.69、A-H.70、A-H.71、A-H.72、A-H.73、A-H.74、A-H.75、A-H.76、A-H.77、A-H.78、A-H.79、A-H.80、A-H.81、A-H.82、A-H.83、A-H.84或A-H.85的VH,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列;以及A-H.1、A-H.2、A-H.3、A-H.4、A-H.5、A-H.6、A-H.7、A-H.8、A-H.9、A-H.10、A-H.11、A-H.12、A-H.13、A-H.14、A-H.15、A-H.16、A-H.17、A-H.18、A-H.19、A-H.20、A-H.21、A-H.22、A-H.23、A-H.24、A-H.25、A-H.26、A-H.27、A-H.28、A-H.29、A-H.30、A-H.31、A-H.32、A-H.33、A-H.34、A-H.35、A-H.36、A-H.37、A-H.38、A-H.39、A-H.40、A-H.1、A-H.42、A-H.43、A-H.44、A-H.45、A-H.46、A-H.47、A-H.48、A-H.49、A-H.50、A-H.51、A-H.52、A-H.53、A-H.54、A-H.55、A-H.56、A-H.57、A-H.58、A-H.59、A-H.60、A-H.61、A-H.62、A-H.63、A-H.64、A-H.65、A-H.66、A-H.67、A-H.68、A-H.69、A-H.70、A-H.71、A-H.72、A-H.73、A-H.74、A-H.75、A-H.76、A-H.77、A-H.78、A-H.79、A-H.80、A-H.81、A-H.82、A-H.83、A-H.84或A-H.85的VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
表30:结合至TCRVB6(例如,TCRVB6-5)的鼠、嵌合和人源化抗体分子的氨基酸和核苷酸序列。抗体分子包括鼠mAb抗体A,以及人源化mAb抗体A-H克隆A-H.1至A-H.85。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表30中所述抗体的VH和/或VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)包含表30中所述抗体的VH和VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,本文公开的抗TCRVb抗体具有抗原结合结构域,该抗原结合结构域具有VL,该VL具有SEQ ID NO:230A的共有序列,其中第30位是G、E、A或D;第31位是N或D;第32位是R或K;第36位是Y或H;和/或第56位是K或S。
在一些实施方案中,本文公开的抗TCRVb抗体具有抗原结合结构域,该抗原结合结构域具有VH,该VH具有SEQ ID NO:231A的共有序列,其中:第27位是H或T或G或Y;第28位是D或T或S;第30位是H或R或D或K或T;第31位是L或D或K或T或N;第32位是W或F或T或I或Y或G;第49位是R或W;第50位是V或I或F;第51位是F或S或Y;第52位是A或P;第56位是N或S;第57位是T或V或Y或I;第58位是K或R;第97位是G或V;第99位是Y或I;第102位是Y或A;和/或第103位是D或G。
抗TCRβV12抗体
因此,在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV12,例如,TCRβV12亚家族,其包含:TCRβV12-4*01、TCRβV12-3*01或TCRβV12-5*01。在一些实施方案中,TCRβV12亚家族包含TCRβV12-4*01。在一些实施方案中,TCRβV12亚家族包含TCRβV12-3*01。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是非鼠抗体分子,例如,人或人源化抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是人抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是人源化抗体分子。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是分离的或重组的。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含至少一个来自本文所述抗体(例如,表31中所述的,或由表31中的核苷酸序列编码的抗体)的抗原结合区(例如,可变区或其抗原结合片段),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含至少一个、两个、三个或四个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含至少一个或两个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含至少一个或两个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的轻链可变区,或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含IgG4(例如,人IgG4)的重链恒定区。在另一实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括IgG1(例如,人IgG1)的重链恒定区。在一个实施方案中,重链恒定区包含表32中所述的氨基序列,或与其基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括κ轻链恒定区,例如,人κ轻链恒定区。在一个实施方案中,轻链恒定区包含表32中所述的氨基序列,或与其基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链可变区的互补决定区(CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个(或统称为所有)来自重链可变区的CDR,该重链可变区包含表31中所示的氨基酸序列,或由表31中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表31中所示的或由表31中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的轻链可变区的互补决定区(CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个(或统称为所有)来自轻链可变区的CDR,该轻链可变区包含表31中所示的氨基酸序列,或由表31中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表31中所示的或由表31中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个、三个、四个、五个或六个(或统称为所有)来自重链和轻链可变区的CDR,该重链和轻链可变区包含表31中所示的氨基酸序列,或由表31中所示的核苷酸序列编码。在一个实施方案中,CDR中的一个或多个(或统称为所有CDR)相对于表31中所示的或由表31中所示的核苷酸序列编码的氨基酸序列具有一个、两个、三个、四个、五个、六个或更多个改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的所有六个CDR,或密切相关的CDR,例如,相同或具有至少一个氨基酸改变但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)的CDR。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自表31中所述的抗体)的重链可变区的根据Kabat等的CDR(例如,如表31中所述的根据Kabat定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Kabat等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,如表31中所述的抗体)的轻链可变区的根据Kabat等的CDR(例如,如表31中所述的根据Kabat定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Kabat等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个、三个、四个、五个或六个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Kabat等的CDR(例如,如表31中所述的根据Kabat定义的至少一个、两个、三个、四个、五个或六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Kabat等的一个、两个、三个、四个、五个或六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Kabat等的所有六个CDR(例如,如表31中所述的根据Kabat定义的所有六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Kabat等的所有六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个高变环,其具有与本文所述抗体(例如,表31中所述的抗体)的相应高变环相同的标准结构,例如,与本文所述抗体的重链和/或轻链可变结构域的至少环1和/或环2相同的标准结构。参见例如,Chothia等人,(1992)J.Mol.Biol.227:799-817;Tomlinson等人,(1992)J.Mol.Biol.227:776-798对于高变环标准结构的描述。这些结构可以通过检查这些参考文献中所述的表格来确定。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自表31中所述的抗体)的重链可变区的根据Chothia等的CDR(例如,如表31中所述的根据Chothia定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Chothia等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,如表31中所述的抗体)的轻链可变区的根据Chothia等的CDR(例如,如表31中所述的根据Chothia定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Chothia等的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个、三个、四个、五个或六个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Chothia等的CDR(例如,如表31中所述的根据Chothia定义的至少一个、两个、三个、四个、五个或六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Chothia等的一个、两个、三个、四个、五个或六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据Chothia等的所有六个CDR(例如,如表31中所述的根据Chothia定义的所有六个CDR);或由表31中的核苷酸序列编码;或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据Chothia等的所有六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,选自表31中所述的抗体)的重链可变区的根据组合CDR的CDR(例如,如表31中所述的根据组合CDR定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据组合CDR的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个或三个来自本文所述抗体(例如,如表31中所述的抗体)的轻链可变区的根据组合CDR的CDR(例如,如表31中所述的根据组合CDR定义的至少一个、两个或三个CDR),或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据组合CDR的一个、两个或三个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括至少一个、两个、三个、四个、五个或六个来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据组合CDR的CDR(例如,如表31中所述的根据组合CDR定义的至少一个、两个、三个、四个、五个或六个CDR);或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据组合CDR的一个、两个、三个、四个、五个或六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括来自本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的重链和轻链可变区的根据组合CDR的所有六个CDR(例如,如表31中所述的根据组合CDR定义的所有六个CDR);或由表31中的核苷酸序列编码;或与上述序列中任一者基本上相同(例如,至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的序列;或者其相对于表31中所示的根据组合CDR的所有六个CDR具有至少一个氨基酸改变,但不超过两个、三个或四个改变(例如,置换、缺失或插入,例如,保守置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可包括本文所述的任何CDR。
在一些实施方案中,如表31中所述的组合CDR是包含Kabat CDR和Chothia CDR的CDR。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括表31中鉴定为组合CDR的CDR或高变环的组合。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可以含有表31中所述的相应“组合”CDR的CDR或高变环的任何组合。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括根据Kabat等、Chothia等或如表31中所述定义的CDR或高变环的组合。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)可以含有根据Kabat和Chothia定义的CDR或高变环的任何组合。
在实施方案中,例如,包含可变区、CDR(例如,组合CDR、Chothia CDR或Kabat CDR)或本文(例如,表31中)提及的其他序列的实施方案中,抗体分子是单特异性抗体分子、双特异性抗体分子、二价抗体分子、双互补位抗体分子或包含抗体的抗原结合片段的抗体分子,例如,半抗体或半抗体的抗原结合片段。在一些实施方案中,抗体分子包含多特异性分子,例如,双特异性分子,例如,如本文所述的。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括:
(i)SEQ ID NO:16A、SEQ ID NO:26A、SEQ ID NO:27A、SEQ ID NO:28A、SEQ ID NO:29A或SEQ ID NO:30A的轻链互补决定区1(LC CDR1)、轻链互补决定区2(LC CDR2)和轻链互补决定区3(LC CDR3)中的一个、两个或全部,和/或
(ii)SEQ ID NO:15A、SEQ ID NO:23A、SEQ ID NO:24A或SEQ ID NO:25A的重链互补决定区1(HC CDR1)、重链互补决定区2(HC CDR2)和重链互补决定区3(HC CDR3)中的一个、两个或全部。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)SEQ ID NO:20A的LC CDR1氨基酸序列、SEQ ID NO:21A的LC CDR2氨基酸序列,或SEQ ID NO:22A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:17A的HC CDR1氨基酸序列、SEQ ID NO:18A的HC CDR2氨基酸序列,或SEQ ID NO:19A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:20A的LC CDR1氨基酸序列、SEQ ID NO:21A的LC CDR2氨基酸序列和SEQ ID NO:2A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:17A的HC CDR1氨基酸序列、SEQ ID NO:18A的HC CDR2氨基酸序列和SEQ ID NO:19A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)SEQ ID NO:63A的LC CDR1氨基酸序列、SEQ ID NO:64A的LC CDR2氨基酸序列,或SEQ ID NO:65A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:57A的HC CDR1氨基酸序列、SEQ ID NO:58A的HC CDR2氨基酸序列,或SEQ ID NO:59A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:63A的LC CDR1氨基酸序列、SEQ ID NO:64A的LC CDR2氨基酸序列,或SEQ ID NO:65A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:57A的HC CDR1氨基酸序列、SEQ ID NO:58A的HC CDR2氨基酸序列,或SEQ ID NO:59A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)SEQ ID NO:66A的LC CDR1氨基酸序列、SEQ ID NO:67A的LC CDR2氨基酸序列,或SEQ ID NO:68A的LC CDR3氨基酸序列;和/或
(ii)SEQ ID NO:60A的HC CDR1氨基酸序列、SEQ ID NO:61A的HC CDR2氨基酸序列,或SEQ ID NO:62A的HC CDR3氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
(i)轻链可变区(VL),其包含SEQ ID NO:63A的LC CDR1氨基酸序列、SEQ ID NO:64A的LC CDR2氨基酸序列,或SEQ ID NO:65A的LC CDR3氨基酸序列;和/或
(ii)重链可变区(VH),其包含SEQ ID NO:57A的HC CDR1氨基酸序列、SEQ ID NO:58A的HC CDR2氨基酸序列,或SEQ ID NO:59A的HC CDR3氨基酸序列。
在一个实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)的轻链或重链可变框架(例如,包括至少FR1、FR2、FR3和任选地FR4的区域)可以选自:(a)轻链或重链可变框架,其包括至少80%、85%、87%、90%、92%、93%、95%、97%、98%或100%的来自人轻链或重链可变框架的氨基酸残基,例如,来自人成熟抗体、人种系序列或人共有序列的轻链或重链可变框架残基;(b)轻链或重链可变框架,其包括20%至80%、40%至60%、60%至90%或70%至95%的来自人轻链或重链可变框架的氨基酸残基,例如,来自人成熟抗体、人种系序列或人共有序列的轻链或重链可变框架残基;(c)非人框架(例如,啮齿动物框架);或(d)已被修饰例如以去除抗原性或细胞毒性决定簇(例如,去免疫化或部分人源化)的非人框架。在一个实施方案中,轻链或重链可变框架区(特别是FR1、FR2和/或FR3)包括与人种系基因的VL或VH区段的框架至少70%、75%、80%、85%、87%、88%、90%、92%、94%、95%、96%、97%、98%、99%相同的或相同的轻链或重链可变框架序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链可变结构域,其具有至少一个、两个、三个、四个、五个、六个、七个、十个、十五个、二十个或更多个来自表31中所述的氨基酸序列(例如,图2A和2B中或SEQ ID NO:23A-25A中所示的整个可变区中FR区的氨基酸序列)的改变,例如,氨基酸置换或缺失。
可替代地,或者与本文所述的重链置换组合,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链可变结构域,其具有至少一个、两个、三个、四个、五个、六个、七个、十个、十五个、二十个或更多个来自本文所述抗体的氨基酸序列(例如,图2A和2B中或SEQ IDNO:26A-30A中所示的整个可变区中FR区的氨基酸序列)的氨基酸改变,例如,氨基酸置换或缺失。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括图2A中所示的一个、两个、三个或四个重链框架区,或与其基本上相同的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括图2B中所示的一个、两个、三个或四个轻链框架区,或与其基本上相同的序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链框架区1,例如,如图2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链框架区2,例如,如图2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链框架区3,例如,如图2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链框架区4,例如,如图2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区1(FR1),其包含改变,例如,根据Kabat编号的一个或多个(例如,所有)本文公开位置处的置换(例如,保守置换)。在一些实施方案中,FR1在第1位处包含天冬氨酸,例如,根据Kabat编号的第1位处的置换,例如,丙氨酸至天冬氨酸的置换。在一些实施方案中,FR1在第2位处包含天冬酰胺,例如,根据Kabat编号的第2位处的置换,例如,异亮氨酸至天冬酰胺的置换、丝氨酸至天冬酰胺的置换或酪氨酸至天冬酰胺的置换。在一些实施方案中,FR1在第4位处包含亮氨酸,例如,根据Kabat编号的第4位处的置换,例如,甲硫氨酸至亮氨酸的置换。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区1(FR1),其包含根据Kabat编号的第1位处的置换(例如,丙氨酸至天冬氨酸的置换)、根据Kabat编号的第2位处的置换(例如,异亮氨酸至天冬酰胺的置换、丝氨酸至天冬酰胺的置换或酪氨酸至天冬酰胺的置换),以及根据Kabat编号的第4位处的置换(例如,甲硫氨酸至亮氨酸的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区1(FR1),其包含根据Kabat编号的第1位处的置换(例如,丙氨酸至天冬氨酸的置换),以及根据Kabat编号的第2位处的置换(例如,异亮氨酸至天冬酰胺的置换、丝氨酸至天冬酰胺的置换或酪氨酸至天冬酰胺的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区1(FR1),其包含根据Kabat编号的第1位处的置换(例如,丙氨酸至天冬氨酸的置换),以及根据Kabat编号的第4位处的置换(例如,甲硫氨酸至亮氨酸的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区1(FR1),其包含根据Kabat编号的第2位处的置换(例如,异亮氨酸至天冬酰胺的置换、丝氨酸至天冬酰胺的置换或酪氨酸至天冬酰胺的置换),以及根据Kabat编号的第4位处的置换(例如,甲硫氨酸至亮氨酸的置换)。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区3(FR3),其包含改变,例如,根据Kabat编号的一个或多个(例如,所有)本文公开位置处的置换(例如,保守置换)。在一些实施方案中,FR3在第66位处包含甘氨酸,例如,根据Kabat编号的第66位处的置换,例如,赖氨酸至甘氨酸的置换或丝氨酸至甘氨酸的置换。在一些实施方案中,FR3在第69位处包含天冬酰胺,例如,根据Kabat编号的第69位处的置换,例如,酪氨酸至天冬酰胺的置换。在一些实施方案中,FR3在第71位处包含酪氨酸,例如,根据Kabat编号的第71位处的置换,例如,苯丙氨酸至酪氨酸的置换或丙氨酸至酪氨酸的置换。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区3(FR3),其包含根据Kabat编号的第66位处的置换(例如,赖氨酸至甘氨酸的置换或丝氨酸至甘氨酸的置换),以及根据Kabat编号的第69位处的置换(例如,酪氨酸至天冬酰胺的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区3(FR3),其包含根据Kabat编号的第66位处的置换(例如,赖氨酸至甘氨酸的置换或丝氨酸至甘氨酸的置换),以及根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换或丙氨酸至酪氨酸的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区3(FR3)其包含根据Kabat编号的第69位处的置换(例如,酪氨酸至天冬酰胺的置换),以及根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换或丙氨酸至酪氨酸的置换)。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含框架区,例如,框架区3(FR3),其包含根据Kabat编号的第66位处的置换(例如,赖氨酸至甘氨酸的置换或丝氨酸至甘氨酸的置换)、根据Kabat编号的第69位处的置换(例如,酪氨酸至天冬酰胺的置换),以及根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换或丙氨酸至酪氨酸的置换)。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含:框架区1(FR1),其包含根据Kabat编号的第2位处的置换,例如,异亮氨酸至天冬酰胺的置换;以及框架区3(FR3),其包含根据Kabat编号的第69位处的置换(例如,苏氨酸至天冬酰胺的置换)和根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换),例如,如SEQ ID NO:26A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含:(a)框架区1(FR1),其包含根据Kabat编号的第1位处的置换(例如,丙氨酸至天冬氨酸的置换)和根据Kabat编号的第2位处的置换(例如,异亮氨酸至天冬酰胺的置换);以及(b)框架区3(FR3),其包含根据Kabat编号的第69位处的置换(例如,苏氨酸至天冬酰胺的置换)和根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换),例如,如SEQ IDNO:27A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含:(a)框架区1(FR1),其包含根据Kabat编号的第2位处的置换,例如,丝氨酸至天冬酰胺的置换;和根据Kabat编号的第4位处的置换,例如,甲硫氨酸至亮氨酸的置换;以及(b)框架区3(FR3),其包含根据Kabat编号的第69位处的置换(例如,苏氨酸至天冬酰胺的置换)和根据Kabat编号的第71位处的置换(例如,苯丙氨酸至酪氨酸的置换),例如,如SEQ ID NO:28A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含:(a)框架区1(FR1),其包含根据Kabat编号的第2位处的置换,例如,丝氨酸至天冬酰胺的置换;以及(b)框架区3(FR3),其包含根据Kabat编号的第66位处的置换,例如,赖氨酸至甘氨酸的置换;根据Kabat编号的第69位处的置换,例如,苏氨酸至天冬酰胺的置换;和根据Kabat编号的第71位处的置换,例如,丙氨酸至酪氨酸的置换,例如,如SEQ ID NO:29A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链,该轻链包含:(a)框架区1(FR1),其包含根据Kabat编号的第2位处的置换,例如,酪氨酸至天冬酰胺的置换;以及(b)框架区3(FR3),其包含根据Kabat编号的第66位处的置换,例如,丝氨酸至甘氨酸的置换;根据Kabat编号的第69位处的置换,例如,苏氨酸至天冬酰胺的置换;和根据Kabat编号的第71位处的置换,例如,丙氨酸至酪氨酸的置换,例如,如SEQ ID NO:29A的氨基酸序列中所示。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链可变结构域,该轻链可变结构域包含:(a)框架区1(FR1),其包含改变,例如,根据Kabat编号的本文公开的一个或多个(例如,所有)位置处的置换(例如,保守置换),以及(b)框架区3(FR3),其包含改变,例如,根据Kabat编号的本文公开的一个或多个(例如,所有)位置处的置换(例如,保守置换)。在一些实施方案中,置换相对于人种系轻链框架区序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区1,例如,如图2A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区2,例如,如图2A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区3,例如,如图2A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区4,例如,如图2A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区1-4,例如,SEQ ID NO:20A-23A,或如图2A中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含轻链框架区1-4,例如,SEQ ID NO:26A-30A,或如图2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含重链框架区1-4,例如,SEQ ID NO:23A-25A;以及轻链框架区1-4,例如,SEQ ID NO:26A-30A,或如图2A和2B中所示。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)的重链或轻链可变结构域或两者包括与本文公开的氨基酸基本上相同(例如,与本文所述抗体(例如,如表31中所述的,或由表31中的核苷酸序列编码的抗体)的可变区至少80%、85%、90%、92%、95%、97%、98%、99%或更高相同)的氨基酸序列;或者其与本文所述抗体的可变区相差至少1或5个残基,但少于40、30、20或10个残基。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含至少一个、两个、三个或四个抗原结合区(例如,可变区),其具有如表31中所述的氨基酸序列,或与其基本上相同的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,或与表31中所示的序列相差不超过1、2、5、10或15个氨基酸残基的序列)。在另一实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包括VH和/或VL结构域,其由具有表31中所述的核苷酸序列或与其基本上相同的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,或与表31中所示的序列相差不超过3、6、15、30或45个核苷酸的序列)的核酸编码。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含选自SEQ ID NO:23A、SEQ ID NO:24A或SEQ ID NO:25A的氨基酸序列的氨基酸序列、与氨基酸序列SEQ ID NO:23A、SEQ ID NO:24A或SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A、SEQ ID NO:24A或SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;和/或
VL结构域,其包含选自SEQ ID NO:26A、SEQ ID NO:27A、SEQ ID NO:28A、SEQ IDNO:29A或SEQ ID NO:30A的氨基酸序列的氨基酸序列、与SEQ ID NO:26A、SEQ ID NO:27A、SEQ ID NO:28A、SEQ ID NO:29A或SEQ ID NO:30A的氨基酸序列至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:26A、SEQ ID NO:27A、SEQ ID NO:28A、SEQID NO:29A或SEQ ID NO:30A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:23A的氨基酸序列、与氨基酸序列SEQ ID NO:23A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:26A的氨基酸序列、与氨基酸序列SEQ ID NO:26A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:26A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:23A的氨基酸序列、与氨基酸序列SEQ ID NO:23A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:27A的氨基酸序列、与氨基酸序列SEQ ID NO:27A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:27A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:23A的氨基酸序列、与氨基酸序列SEQ ID NO:23A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:28A的氨基酸序列、与氨基酸序列SEQ ID NO:28A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:28A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:23A的氨基酸序列、与氨基酸序列SEQ ID NO:23A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:29A的氨基酸序列、与氨基酸序列SEQ ID NO:29A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:29A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:23A的氨基酸序列、与氨基酸序列SEQ ID NO:23A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:23A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:30A的氨基酸序列、与氨基酸序列SEQ ID NO:30A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:30A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:24A的氨基酸序列、与氨基酸序列SEQ ID NO:24A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:24A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:26A的氨基酸序列、与氨基酸序列SEQ ID NO:26A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:26A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:24A的氨基酸序列、与氨基酸序列SEQ ID NO:24A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:24A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:27A的氨基酸序列、与氨基酸序列SEQ ID NO:27A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:27A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:24A的氨基酸序列、与氨基酸序列SEQ ID NO:24A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:24A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:28A的氨基酸序列、与氨基酸序列SEQ ID NO:28A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:28A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:24A的氨基酸序列、与氨基酸序列SEQ ID NO:24A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:24A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:29A的氨基酸序列、与氨基酸序列SEQ ID NO:29A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:29A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:24A的氨基酸序列、与氨基酸序列SEQ ID NO:24A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:24A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:30A的氨基酸序列、与氨基酸序列SEQ ID NO:30A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:30A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:25A的氨基酸序列、与氨基酸序列SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:26A的氨基酸序列、与氨基酸序列SEQ ID NO:26A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:26A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:25A的氨基酸序列、与氨基酸序列SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:27A的氨基酸序列、与氨基酸序列SEQ ID NO:27A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:27A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:25A的氨基酸序列、与氨基酸序列SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:28A的氨基酸序列、与氨基酸序列SEQ ID NO:28A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:28A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:25A的氨基酸序列、与氨基酸序列SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:29A的氨基酸序列、与氨基酸序列SEQ ID NO:29A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:29A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)包含:
VH结构域,其包含SEQ ID NO:25A的氨基酸序列、与氨基酸序列SEQ ID NO:25A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:25A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列;以及
VL结构域,其包含SEQ ID NO:30A的氨基酸序列、与氨基酸序列SEQ ID NO:30A至少约85%、90%、95%、99%或更多相同的氨基酸序列,或与SEQ ID NO:30A的氨基酸序列相差不超过1、2、5、10或15个氨基酸残基的氨基酸序列。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是全抗体或其片段(例如,Fab、F(ab’)2、Fv或单链Fv片段(scFv))。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV6(例如,抗TCRβV6-5*01)抗体分子)是单克隆抗体或具有单特异性的抗体。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)也可以是人源化、嵌合、骆驼、鲨鱼或体外生成的抗体分子。在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是人源化抗体分子。抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)的重链和轻链可以是全长的(例如,抗体可以包括至少一条(优选两条)完整重链和至少一条(优选两条)完整轻链),或者可以包括抗原结合片段(例如,Fab、F(ab’)2、Fv、单链Fv片段、单结构域抗体、双抗体(dAb)、二价抗体,或双特异性抗体或其片段、其单结构域变体或骆驼抗体)。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)是多特异性分子(例如,双特异性分子)的形式,例如,如本文所述。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)具有重链恒定区(Fc),其选自例如IgG1、IgG2、IgG3、IgG4、IgM、IgA1、IgA2、IgD和IgE的重链恒定区。在一些实施方案中,Fc区选自IgG1、IgG2、IgG3和IgG4的重链恒定区。在一些实施方案中,Fc区选自IgG1或IgG2(例如,人IgG1或IgG2)的重链恒定区。在一些实施方案中,重链恒定区是人IgG1。
在一些实施方案中,抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)具有轻链恒定区,其选自例如κ或λ(优选κ(例如,人κ))的轻链恒定区。在一个实施方案中,恒定区被改变(例如,突变),以修改抗TCRβV抗体分子(例如,抗TCRβV12抗体分子)的特性(例如,以增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能)。例如,恒定区在第296位(M至Y)、298位(S至T)、300位(T至E)、477位(H至K)和478位(N至F)处被突变,以改变Fc受体结合(例如,突变的位置对应于SEQ ID NO:212A或214A的第132位(M至Y)、134位(S至T)、136位(T至E)、313位(H至K)和314位(N至F);或SEQ ID NO:215A、216A、217A或218A的第135位(M至Y)、137位(S至T)、139位(T至E)、316位(H至K)和317位(N至F))。
抗体B-H.1包含第一链和第二链,该第一链包含SEQ ID NO:3280A的氨基酸序列,该第二链包含SEQ ID NO:3281A的氨基酸序列。
本发明的另外的示例性抗TCRβV12抗体提供于表31中。在一些实施方案中,抗TCRβV12是抗体B,例如,人源化抗体B(抗体B-H),如表31中提供的。在一些实施方案中,抗TCRβV抗体包含表31中提供的LC CDR1、LC CDR2和LC CDR3中的一个或多个(例如,所有三个);和/或表31中提供的HC CDR1、HC CDR2和HC CDR3中的一个或多个(例如,所有三个),或与其具有至少95%同一性的序列。在一些实施方案中,抗体B包含表31中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少95%同一性的序列。
表31:结合至TCRVB12(例如,TCRVB12-3或TCRVB12-4)的鼠和人源化抗体分子的氨基酸和核苷酸序列。抗体分子包括鼠mAb抗体B以及人源化mAb抗体B-H.1至B-H.6。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。
表32.人IgG重链和人κ轻链的恒定区氨基酸序列
抗TCRβV5抗体
因此,在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV5。在一些实施方案中,TCRβV5亚家族包含TCRβV5-5*01、TCRβV5-6*01、TCRβV5-4*01、TCRβV5-8*01、TCRβV5-1*01或其变体。
本发明的示例性抗TCRβV5抗体提供于表33中。在一些实施方案中,抗TCRβV5是抗体C,例如,人源化抗体C(抗体C-H),如表33中提供的。在一些实施方案中,抗TCRβV抗体包含表33中提供的LC CDR1、LC CDR2和LC CDR3中的一个或多个(例如,所有三个);和/或表33中提供的HC CDR1、HC CDR2和HC CDR3中的一个或多个(例如,所有三个),或与其具有至少95%同一性的序列。在一些实施方案中,抗体C包含表33中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少95%同一性的序列。
表33:抗TCRβV5抗体的氨基酸序列
结合至TCRVB5(例如,TCRVB5-5或TCRVB5-6)的鼠和人源化抗体分子的氨基酸和核苷酸序列。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。
本发明的示例性抗TCRβV5抗体提供于表11中。在一些实施方案中,抗TCRβV5是抗体E,例如,人源化抗体E(抗体E-H),如表11中提供的。在一些实施方案中,抗TCRβV抗体包含表11中提供的LC CDR1、LC CDR2和LC CDR3中的一个或多个(例如,所有三个);和/或表11中提供的HC CDR1、HC CDR2和HC CDR3中的一个或多个(例如,所有三个),或与其具有至少95%同一性的序列。在一些实施方案中,抗体E包含表11中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少95%同一性的序列。
在一些实施方案中,抗体E包含重链和/或轻链,该重链包含SEQ ID NO:3284A的氨基酸序列,该轻链包含SEQ ID NO:3285A的氨基酸序列,或与其具有至少95%同一性的序列。
表11:抗TCRβV5抗体的氨基酸序列
结合至TCRVB5(例如,TCRVB5-5或TCRVB5-6)的鼠和人源化抗体分子的氨基酸和核苷酸序列。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。
在一些实施方案中,抗TCRβV5抗体分子包含表33中所述抗体的VH和/或VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV5抗体分子包含表33中所述抗体的VH和VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV5抗体分子包含表11中所述抗体的VH和/或VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV5抗体分子包含表11中所述抗体的VH和VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
抗TCRβV10抗体
因此,在一方面,本发明提供了一种抗TCRβV抗体分子,其结合至人TCRβV10亚家族成员。在一些实施方案中,TCRβV10亚家族也称为TCRβV12。在一些实施方案中,TCRβV10亚家族包含:TCRβV10-1*01、TCRβV10-1*02、TCRβV10-3*01或TCRβV10-2*01或其变体。
本发明的示例性抗TCRβV10抗体提供于表12中。在一些实施方案中,抗TCRβV10是抗体D,例如,人源化抗体D(抗体D-H),如表12中提供的。在一些实施方案中,抗体D包含表12中提供的一个或多个(例如,三个)轻链CDR和/或一个或多个(例如,三个)重链CDR,或与其具有至少95%同一性的序列。在一些实施方案中,抗体D包含表12中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少95%同一性的序列。
表12:抗TCRβV10抗体的氨基酸序列
结合至TCRBV10(例如,TCRBV10-1、TCRBV10-2或TCRBV10-3)的鼠和人源化抗体分子的氨基酸和核苷酸序列。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。
在一些实施方案中,抗TCRβV10抗体分子包含表12中所述抗体的VH或VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
在一些实施方案中,抗TCRβV10抗体分子包含表12中所述抗体的VH和VL,或与其具有至少80%、85%、90%、95%、96%、97%、98%、99%或更多同一性的序列。
另外的抗TCRVβ抗体
本发明的另外的示例性抗TCRβV抗体提供于表13中。在一些实施方案中,抗TCRβV抗体是人源化抗体,例如,如表13中提供的。在一些实施方案中,抗TCRβV抗体包含表13中提供的LC CDR1、LC CDR2和LC CDR3中的一个或多个(例如,所有三个);和/或表13中提供的HCCDR1、HC CDR2和HC CDR3中的一个或多个(例如,所有三个),或与其具有至少95%同一性的序列。在一些实施方案中,抗TCRβV抗体包含表13中提供的可变重链(VH)和/或可变轻链(VL),或与其具有至少95%同一性的序列。
表13:另外的抗TCRβV抗体的氨基酸序列
公开了结合至各种TCRVB家族的鼠和人源化抗体分子的氨基酸和核苷酸序列。显示了重链和轻链CDR的氨基酸、重链和轻链可变区的氨基酸和核苷酸序列,以及重链和轻链。表中公开的抗体包括MPB2D5、CAS1.1.3、IMMU222、REA1062、JOVI-3、IMMU546和MR5-2。MPB2D5结合人TCRβV20-1(按旧命名法为TCRβV2)。CAS1.1.3结合人TCRβV27(按旧命名法为TCRβV14)。IMMU222结合人TCRβV6-5、TCRβV6-6或TCRβV6-9(按旧命名法为TCRβV13.1)。REA1062结合人TCRβV5-1。JOVI-3结合人TCRβV28(按旧命名法为TCRβV3.1)。IMMU546结合人TCRβV2。MR5-2结合人TCRVβ13-2。
抗TCRVβ抗体效应功能和Fc变体
在一些实施方案中,例如,如本文所述,本文公开的抗TCRVβ抗体包含Fc区。在一些实施方案中,Fc区是野生型Fc区,例如,野生型人Fc区。在一些实施方案中,Fc区包含变体,例如,在Fc区中包含至少一个氨基酸残基的添加、置换或缺失的Fc区,其导致例如对至少一种Fc受体的亲和力降低或消除。
抗体的Fc区与许多受体或配体相互作用,包括Fc受体(例如,FcγRI、FcγRIIA、FcγRIIIA)、补体蛋白Clq和其他分子,例如蛋白A和G。这些相互作用对于各种效应功能和下游信号传导事件是必需的,包括:抗体依赖性细胞介导的细胞毒性(ADCC)、抗体依赖性细胞吞噬作用(ADCP)和补体依赖性细胞毒性(CDC)。
在一些实施方案中,包含变体Fc区的抗TCRVβ抗体对Fc受体(例如,本文所述的Fc受体)的亲和力降低(例如,消除)。在一些实施方案中,将降低的亲和力与具有野生型Fc区的其他方面相似的抗体进行比较。
在一些实施方案中,包含变体Fc区的抗TCRVβ抗体具有以下特性中的一种或多种:(1)效应功能降低(例如,ADCC、ADCP和/或CDC降低);(2)与一种或多种Fc受体的结合减少;和/或(3)与C1q补体的结合减少。在一些实施方案中,将特性(1)-(3)中任一个或全部的降低与具有野生型Fc区的其他方面相似的抗体进行比较。
在一些实施方案中,包含变体Fc区的抗TCRVβ抗体对人Fc受体(例如,FcγR I、FcγR II和/或FcγR III)的亲和力降低。在一些实施方案中,包含变体Fc区的抗TCRVβ抗体包含人IgG1区或人IgG4区。
在一些实施方案中,例如,如本文所述,包含变体Fc区的抗TCRVβ抗体激活和/或扩增T细胞。在一些实施方案中,包含变体Fc区的抗TCRVβ抗体具有本文所述的细胞因子谱,例如,不同于结合至除TCRβV区以外的受体或分子的T细胞接合物(“非TCRβV结合T细胞接合物”)的细胞因子谱的细胞因子谱。在一些实施方案中,非TCRβV结合T细胞接合物包含结合至CD3分子(例如,CD3(CD3e)分子)或TCRα分子的抗体。
示例性Fc区变体提供于表14中并且还公开于Saunders O,(2019)Frontiers inImmunology;第10卷,第1296条,其全部内容通过引用并入本文。
在一些实施方案中,抗TCRVβ抗体包含表14中公开的Fc区变体(例如,突变)中的任一个或全部或任何组合。在一些实施方案中,本文公开的抗TCRVβ抗体包含Asn297Ala(N297A)突变。在一些实施方案中,本文公开的抗TCRVβ抗体包含Leu234Ala/Leu235Ala(LALA)突变。
表14:示例性Fc修饰
自然杀伤细胞接合物
自然杀伤(NK)细胞以抗体非依赖性方式识别并破坏肿瘤和病毒感染的细胞。NK细胞的调控是通过激活和抑制NK细胞表面上的受体介导的。激活受体的一个家族是天然细胞毒性受体(NCR),其包括NKp30、NKp44和NKp46。NCR通过识别癌细胞上的硫酸乙酰肝素启动肿瘤靶向性。NKG2D是在活化的杀伤(NK)细胞上提供刺激和共刺激先天免疫应答的受体,导致细胞毒性活性。DNAM1是参与细胞间粘附、淋巴细胞信号传导、细胞毒性和由细胞毒性T淋巴细胞(CTL)和NK细胞介导的淋巴因子分泌的受体。DAP10(也称为HCST)是跨膜衔接蛋白,其与KLRK1缔合,以在淋巴和髓样细胞中形成激活受体KLRK1-HCST;该受体在触发针对表达细胞表面配体(例如MHC I类链相关MICA和MICB以及U(任选地L1)6结合蛋白(ULBP))的靶细胞的细胞毒性中起主要作用;KLRK1-HCST受体在针对肿瘤的免疫监视中起作用并且是肿瘤细胞的细胞溶解所必需的;实际上,不表达KLRK1配体的黑色素瘤细胞会逃脱由NK细胞介导的免疫监视。CD16是IgG Fc区的受体,其结合复合或聚集的IgG以及单体IgG,从而介导抗体依赖性细胞的细胞毒性(ADCC)和其他抗体依赖性应答,例如吞噬作用。
本发明尤其提供了多特异性(例如,双特异性、三特异性、四特异性)或多功能性分子,其工程化为含有介导NK细胞的结合和/或激活的一种或多种NK细胞接合物。因此,在一些实施方案中,NK细胞接合物选自抗原结合结构域或配体,其结合至(例如,激活):NKp30、NKp40、NKp44、NKp46、NKG2D、DNAM1、DAP10、CD16(例如,CD16a、CD16b或两者)、CRTAM、CD27、PSGL1、CD96、CD100(SEMA4D)、NKp80、CD244(也称为SLAMF4或2B4)、SLAMF6、SLAMF7、KIR2DS2、KIR2DS4、KIR3DS1、KIR2DS3、KIR2DS5、KIR2DS1、CD94、NKG2C、NKG2E或CD160。
在一些实施方案中,NK细胞接合物是结合至NKp30(例如,NK细胞表面上存在(例如,表达或展示)的NKp30)的抗原结合结构域,并且包含表7、8、35、36、9、10或34中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列。在一些实施方案中,NK细胞接合物是结合至NKp30(例如,NK细胞表面上存在(例如,表达或展示)的NKp30)的抗原结合结构域,并且包含美国专利第6,979,546号、美国专利第9,447,185号、PCT申请第WO2015121383A1号、PCT申请第WO2016110468A1号、PCT申请第WO2004056392A1号或美国申请公布第US 20070231322A1号中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列,这些序列在此通过引用并入。在一些实施方案中,NK细胞接合物(例如,结合至NKp30的抗原结合结构域)与NK细胞的结合激活NK细胞。结合至NKp30(例如,NK细胞表面上存在(例如,表达或展示)的NKp30)的抗原结合结构域可被称为靶向NKp30、NK细胞或两者。
在一些实施方案中,结合至NKp30的抗原结合结构域包含表7、表34或表8中公开的一个或多个CDR(例如,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和/或VLCDR3),或与其具有至少85%、90%、95%或99%同一性的序列。在一些实施方案中,结合至NKp30的抗原结合结构域包含表7、表34或表8中公开的一个或多个框架区(例如,VHFWR1、VHFWR2、VHFWR3、VHFWR4、VLFWR1、VLFWR2、VLFWR3和/或VLFWR4),或与其具有至少85%、90%、95%或99%同一性的序列。
在一些实施方案中,结合至NKP30的抗原结合结构域包含表35和/或表36中公开的一个或多个CDR(例如,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和/或VLCDR3),或与其具有至少85%、90%、95%或99%同一性的序列。在一些实施方案中,结合至NKP30的抗原结合结构域包含表35和/或表36中公开的一个或多个框架区(例如,VHFWR1、VHFWR2、VHFWR3、VHFWR4、VLFWR1、VLFWR2、VLFWR3和/或VLFWR4),或与其具有至少85%、90%、95%或99%同一性的序列。
在一些实施方案中,结合至NKp30的抗原结合结构域包含表9中公开的VH和/或VL,或与其具有至少85%、90%、95%或99%同一性的序列。在一些实施方案中,表9中公开的VH结构域中的任一个可与表9中公开的VL结构域中的任一个配对,以形成结合至NKp30的抗原结合结构域。在一些实施方案中,结合至NKp30的抗原结合结构域包含表10中公开的氨基酸序列,或与其具有至少85%、90%、95%或99%同一性的序列。
在一些实施方案中,结合至NKp30的抗原结合结构域包含VH和VL,该VH包含重链互补决定区1(VHCDR1)、VHCDR2和VHCDR3,该VL包含轻链互补决定区1(VLCDR1)、VLCDR2和VLCDR3。
在一些实施方案中,VHCDR1、VHCDR2和VHCDR3分别包含SEQ ID NO:7313、6001和7315的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2和VHCDR3分别包含SEQ ID NO:7313、6001和6002的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2和VHCDR3分别包含SEQ ID NO:7313、6008和6009的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2和VHCDR3分别包含SEQ IDNO:7313、7385和7315的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2和VHCDR3分别包含SEQ ID NO:7313、7318和6009的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7326、7327和7329的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:6063、6064和7293的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:6070、6071和6072的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VLCDR1、VLCDR2和VLCDR3分别包含SEQ IDNO:6070、6064和7321的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7313、6001、7315、7326、7327和7329的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7313、6001、6002、6063、6064和7293的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7313、6008、6009、6070、6071和6072的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7313、7385、7315、6070、6064和7321的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VHCDR1、VHCDR2、VHCDR3、VLCDR1、VLCDR2和VLCDR3分别包含SEQ ID NO:7313、7318、6009、6070、6064和7321的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,VH包含选自SEQ ID NO:7298或7300-7304的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列),和/或VL包含选自SEQ ID NO:7299或7305-7309的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH和VL分别包含SEQ ID NO:7302和7305的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH和VL分别包含SEQ ID NO:7302和7309的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,VH包含选自SEQ ID NO:6121或6123-6128的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列),和/或VL包含选自SEQ ID NO:7294或6137-6141的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH包含选自SEQ ID NO:6122或6129-6134的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列),和/或VL包含选自SEQ ID NO:6136或6142-6147的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH和VL分别包含SEQ ID NO:7295和7296的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH和VL分别包含SEQ ID NO:7297和7296的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,VH和VL分别包含SEQ ID NO:6122和6136的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,结合至NKp30的抗原结合结构域包含SEQ ID NO:7310的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,结合至NKp30的抗原结合结构域包含SEQ ID NO:7311的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。在一些实施方案中,结合至NKp30的抗原结合结构域包含SEQ ID NO:6187、6188、6189或6190的氨基酸序列(或与其具有至少85%、90%、95%或99%同一性的序列)。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6002的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,NKp30抗原结合结构域包含VH,该VH包含SEQ ID NO:6000的VHCDR1氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6064的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7293的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6063的VLCDR1氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列和SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6000的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6002的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),该VL包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6064的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7293的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,NKp30抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6000的VHCDR1氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,该VL包含SEQ ID NO:6063的VLCDR1氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列和SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6007的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6008的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6009的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,NKp30抗原结合结构域包含VH,该VH包含SEQ ID NO:6007的VHCDR1氨基酸序列、SEQ ID NO:6008的VHCDR2氨基酸序列,和/或SEQ ID NO:6009的VHCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6070的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6071的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6072的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6070的VLCDR1氨基酸序列、SEQ ID NO:6071的VLCDR2氨基酸序列和SEQ ID NO:6072的VLCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6007的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6008的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6009的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),该VL包含SEQ ID NO:6070的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6071的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6072的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,NKp30抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6007的VHCDR1氨基酸序列、SEQ ID NO:6008的VHCDR2氨基酸序列,和/或SEQ ID NO:6009的VHCDR3氨基酸序列,该VL包含SEQ ID NO:6070的VLCDR1氨基酸序列、SEQ ID NO:6071的VLCDR2氨基酸序列和SEQ ID NO:6072的VLCDR3氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ IDNO:6005的VHFWR3氨基酸序列,和/或SEQ ID NO:6006的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ IDNO:7292的VLFWR3氨基酸序列,和/或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQID NO:6005的VHFWR3氨基酸序列,和/或SEQ ID NO:6006的VHFWR4氨基酸序列,该VL包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,和/或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6003的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6004的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6005的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6006的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6066的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6067的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7292的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6003的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6004的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6005的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6006的VHFWR4氨基酸序列,该VL包含SEQ ID NO:6066的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6067的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7292的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6010的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6011的VHFWR2氨基酸序列、SEQ IDNO:6012的VHFWR3氨基酸序列,和/或SEQ ID NO:6013的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6073的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6074的VLFWR2氨基酸序列、SEQ IDNO:6075的VLFWR3氨基酸序列,和/或SEQ ID NO:6076的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6010的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6011的VHFWR2氨基酸序列、SEQID NO:6012的VHFWR3氨基酸序列,和/或SEQ ID NO:6013的VHFWR4氨基酸序列,该VL包含SEQ ID NO:6073的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6074的VLFWR2氨基酸序列、SEQ ID NO:6075的VLFWR3氨基酸序列,和/或SEQ ID NO:6076的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6010的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6011的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6012的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6013的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6073的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6074的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6075的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6076的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6010的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6011的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6012的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6013的VHFWR4氨基酸序列,该VL包含SEQ ID NO:6073的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6074的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6075的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6076的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6014的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6015的VHFWR2氨基酸序列、SEQ IDNO:6016的VHFWR3氨基酸序列,和/或SEQ ID NO:6017的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6014的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6015的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6016的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6017的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6077的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6078的VLFWR2氨基酸序列、SEQ IDNO:6079的VLFWR3氨基酸序列,和/或SEQ ID NO:6080的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6077的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6078的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6079的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6080的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6018的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6019的VHFWR2氨基酸序列、SEQ IDNO:6020的VHFWR3氨基酸序列,和/或SEQ ID NO:6021的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6018的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6019的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6020的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6021的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6081的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6082的VLFWR2氨基酸序列、SEQ IDNO:6083的VLFWR3氨基酸序列,和/或SEQ ID NO:6084的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6081的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6082的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6083的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6084的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6022的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6023的VHFWR2氨基酸序列、SEQ IDNO:6024的VHFWR3氨基酸序列,和/或SEQ ID NO:6025的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6022的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6023的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6024的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6025的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6085的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6086的VLFWR2氨基酸序列、SEQ IDNO:6087的VLFWR3氨基酸序列,和/或SEQ ID NO:6088的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6085的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6086的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6087的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6088的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6026的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6027的VHFWR2氨基酸序列、SEQ IDNO:6028的VHFWR3氨基酸序列,和/或SEQ ID NO:6029的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6026的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6027的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6028的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6029的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6089的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6090的VLFWR2氨基酸序列、SEQ IDNO:6091的VLFWR3氨基酸序列,和/或SEQ ID NO:6092的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6089的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6090的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6091的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6092的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6030的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6032的VHFWR2氨基酸序列、SEQ IDNO:6033的VHFWR3氨基酸序列,和/或SEQ ID NO:6034的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6030的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6032的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6033的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6034的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6093的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6094的VLFWR2氨基酸序列、SEQ IDNO:6095的VLFWR3氨基酸序列,和/或SEQ ID NO:6096的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6093的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6094的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6095的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6096的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6035的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6036的VHFWR2氨基酸序列、SEQ IDNO:6037的VHFWR3氨基酸序列,和/或SEQ ID NO:6038的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6035的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6036的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6037的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6038的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6039的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6040的VHFWR2氨基酸序列、SEQ IDNO:6041的VHFWR3氨基酸序列,和/或SEQ ID NO:6042的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6039的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6040的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6041的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6042的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6097的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6098的VLFWR2氨基酸序列、SEQ IDNO:6099的VLFWR3氨基酸序列,和/或SEQ ID NO:6100的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6097的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6098的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6099的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6100的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6043的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6044的VHFWR2氨基酸序列、SEQ IDNO:6045的VHFWR3氨基酸序列,和/或SEQ ID NO:6046的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6043的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6044的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6045的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6046的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6101的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6102的VLFWR2氨基酸序列、SEQ IDNO:6103的VLFWR3氨基酸序列,和/或SEQ ID NO:6104的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6101的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6102的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6103的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6104的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6047的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6048的VHFWR2氨基酸序列、SEQ IDNO:6049的VHFWR3氨基酸序列,和/或SEQ ID NO:6050的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6047的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6048的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6049的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6050的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6105的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6106的VLFWR2氨基酸序列、SEQ IDNO:6107的VLFWR3氨基酸序列,和/或SEQ ID NO:6108的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6105的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6106的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6107的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6108的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6051的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6052的VHFWR2氨基酸序列、SEQ IDNO:6053的VHFWR3氨基酸序列,和/或SEQ ID NO:6054的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6051的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6052的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6053的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6054的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6109的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6110的VLFWR2氨基酸序列、SEQ IDNO:6111的VLFWR3氨基酸序列,和/或SEQ ID NO:6112的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6109的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6110的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6111的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6112的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6055的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6056的VHFWR2氨基酸序列、SEQ IDNO:6057的VHFWR3氨基酸序列,和/或SEQ ID NO:6058的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6055的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6056的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6057的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6058的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6113的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6114的VLFWR2氨基酸序列、SEQ IDNO:6115的VLFWR3氨基酸序列,和/或SEQ ID NO:6116的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6113的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6114的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6115的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6116的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6059的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6060的VHFWR2氨基酸序列、SEQ IDNO:6061的VHFWR3氨基酸序列,和/或SEQ ID NO:6062的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6059的VHFWR1氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6060的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6061的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6062的VHFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6117的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6118的VLFWR2氨基酸序列、SEQ IDNO:6119的VLFWR3氨基酸序列,和/或SEQ ID NO:6120的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6117的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6118的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6119的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6120的VLFWR4氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6148的氨基酸序列(或与SEQ ID NO:6148具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6149的氨基酸序列(或与SEQ ID NO:6149具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6150的氨基酸序列(或与SEQ ID NO:6150具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6148的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6149的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6150的氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6148的氨基酸序列,该VL包含SEQ ID NO:6150的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6149的氨基酸序列,该VL包含SEQ ID NO:6150的氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6151的氨基酸序列(或与SEQ ID NO:6151具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6152的氨基酸序列(或与SEQ ID NO:6152具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6153的氨基酸序列(或与SEQ ID NO:6153具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6151的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH,该VH包含SEQ ID NO:6152的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VL,该VL包含SEQ ID NO:6153的氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ IDNO:6151的氨基酸序列,该VL包含SEQ ID NO:6153的氨基酸序列。在一些实施方案中,靶向NKp30的抗原结合结构域包含VH和VL,该VH包含SEQ ID NO:6152的氨基酸序列,该VL包含SEQ ID NO:6153的氨基酸序列。
在一些实施方案中,靶向NKp30的抗原结合结构域包含scFv。在一些实施方案中,scFv包含选自SEQ ID NO:6187-6190的氨基酸序列,或与其具有至少约93%、95%或99%序列同一性的氨基酸序列。
表7.NKp30靶向性抗原结合结构域的示例性重链CDR和FWR
表34.NKp30靶向性抗原结合结构域的示例性重链CDR和FWR(根据Kabat编号方案)
表8.NKp30靶向性抗原结合结构域的示例性轻链CDR和FWR
表35.NKp30靶向性抗原结合结构域的示例性重链CDR和FWR
表36.NKp30靶向性抗原结合结构域的示例性轻链CDR和FWR
表9.NKp30靶向性抗原结合结构域的示例性可变区
表10.示例性NKp30靶向性抗原结合结构域/抗体分子
在一些实施方案中,NK细胞接合物是结合至NKp46(例如,NK细胞表面上存在(例如,表达或展示)的NKp46)的抗原结合结构域,并且包含表15中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列。在一些实施方案中,NK细胞接合物(例如,结合至NKp46的抗原结合结构域)与NK细胞的结合激活NK细胞。结合至NKp46(例如,NK细胞表面上存在(例如,表达或展示)的NKp46)的抗原结合结构域可被称为靶向NKp46、NK细胞或两者。
在一些实施方案中,NK细胞接合物是结合至NKG2D(例如,NK细胞表面上存在(例如,表达或展示)的NKG2D)的抗原结合结构域,并且包含表15中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列。在一些实施方案中,NK细胞接合物(例如,结合至NKG2D的抗原结合结构域)与NK细胞的结合激活NK细胞。结合至NKG2D(例如,NK细胞表面上存在(例如,表达或展示)的NKG2D)的抗原结合结构域可被称为靶向NKG2D、NK细胞或两者。
在一些实施方案中,NK细胞接合物是结合至CD16(例如,NK细胞表面上存在(例如,表达或展示)的CD16)的抗原结合结构域,并且包含表15中公开的任何CDR氨基酸序列、框架区(FWR)氨基酸序列或可变区氨基酸序列。在一些实施方案中,NK细胞接合物(例如,结合至CD16的抗原结合结构域)与NK细胞的结合激活NK细胞。结合至CD16(例如,NK细胞表面上存在(例如,表达或展示)的CD16)的抗原结合结构域可被称为靶向CD16、NK细胞或两者。
表15.NKp46、NKG2D或CD16靶向性抗原结合结构域的示例性可变区
在一个实施方案中,NK细胞接合物是NKp30的配体,例如,是B7-6,例如,包含以下氨基酸序列:
DLKVEMMAGGTQITPLNDNVTIFCNIFYSQPLNITSMGITWFW KSLTFDKEVKVFEFFGDHQEAFRPGAIVSPWRLKSGDASLRLPGIQLEEAGEYRCEVVVTPLKAQGTVQLEVVASPASRLLLDQVGMKENEDKYMCESSGFYPEAINITWEKQTQKFPHPIEISEDVITGPTIKNMDGTFNVTSCLKLNSSQEDPGTVYQCVVRHASLHTPLRSNFTLTAARHSLSETEKTDNFS(SEQ ID NO:6198)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6198的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,NK细胞接合物是NKp44或NKp46的配体,其是病毒HA。病毒血凝素(HA)是病毒表面上的糖蛋白。HA蛋白允许病毒经由唾液酸糖部分结合至细胞膜,这有助于病毒膜与细胞膜的融合(参见例如,Eur J Immunol.2001年9月;31(9):2680-9“Recognition of viral hemagglutinins by NKp44 but not by NKp30”;和Nature.2001年2月22日;409(6823):1055-60“Recognition of haemagglutinins on virus-infectedcells by NKp46 activates lysis by human NK cells”,其中每一个的内容通过引用并入本文)。
在其他实施方案中,NK细胞接合物是NKG2D的配体,选自MICA、MICB或ULBP1,例如,其中:
(i)MICA包含以下氨基酸序列:
EPHSLRYNLTVLSWDGSVQSGFLTEVHLDGQPFLRCDRQKCRAKPQGQWAEDVLGNKTWDRETRDLTGNGKDLRMTLAHIKDQKEGLHSLQEIRVCEIHEDNSTRSSQHFYYDGELFLSQNLETKEWTMPQSSRAQTLAMNVRNFLKEDAMKTKTHYHAMHADCLQELRRYLKSGVVLRRTVPPMVNVTRSEASEGNITVTCRASGFYPWNITLSWRQDGVSLSHDTQQWGDVLPDGNGTYQTWVATRICQGEEQRFTCYMEHSGNHSTHPVPSGKVLVLQSHW(SEQ ID NO:6199)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6199的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列;
(ii)MICB包含以下氨基酸序列:
AEPHSLRYNLMVLSQDESVQSGFLAEGHLDGQPFLRYDRQKRRAKPQGQWAEDVLGAKTWDTETEDLTENGQDLRRTLTHIKDQKGGLHSLQEIRVCEIHEDSSTRGSRHFYYDGELFLSQNLETQESTVPQSSRAQTLAMNVTNFWKEDAMKTKTHYRAMQADCLQKLQRYLKSGVAIRRTVPPMVNVTCSEVSEGNITVTCRASSFYPRNITLTWRQDGVSLSHNTQQWGDVLPDGNGTYQTWVATRIRQGEEQRFTCYMEHSGNHGTHPVPSGKVLVLQSQRTD(SEQ IDNO:6200)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6200的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列;或
(iii)ULBP1包含以下氨基酸序列:
GWVDTHCLCYDFIITPKSRPEPQWCEVQGLVDERPFLHYDCVNHKAKAFASLGKKVNVTKTWEEQTETLRDVVDFLKGQLLDIQVENLIPIEPLTLQARMSCEHEAHGHGRGSWQFLFNGQKFLLFDSNNRKWTALHPGAKKMTEKWEKNRDVTMFFQKISLGDCKMWLEEFLMYWEQMLDPTKPPSLAPG(SEQ ID NO:6201)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6201的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是DNAM1的配体,选自NECTIN2或NECL5,例如,其中:
(i)NECTIN2包含以下氨基酸序列:
QDVRVQVLPEVRGQLGGTVELPCHLLPPVPGLYISLVTWQRPDAPANHQNVAAFHPKMGPSFPSPKPGSERLSFVSAKQSTGQDTEAELQDATLALHGLTVEDEGNYTCEFATFPKGSVRGMTWLRVIAKPKNQAEAQKVTFSQDPTTVALCISKEGRPPARISWLSSLDWEAKETQVSGTLAGTVTVTSRFTLVPSGRADGVTVTCKVEHESFEEPALIPVTLSVRYPPEVSISGYDDNWYLGRTDATLSCDVRSNPEPTGYDWSTTSGTFPTSAVAQGSQLVIHAVDSLFNTTFVCTVTNAVGMGRAEQVIFVRETPNTAGAGATGG(SEQ ID NO:6202)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6202的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列;或
(ii)NECL5包含以下氨基酸序列:
WPPPGTGDVVVQAPTQVPGFLGDSVTLPCYLQVPNMEVTHVSQLTWARHGESGSMAVFHQTQGPSYSESKRLEFVAARLGAELRNASLRMFGLRVEDEGNYTCLFVTFPQGSRSVDIWLRVLAKPQNTAEVQKVQLTGEPVPMARCVSTGGRPPAQITWHSDLGGMPNTSQVPGFLSGTVTVTSLWILVPSSQVDGKNVTCKVEHESFEKPQLLTVNLTVYYPPEVSISGYDNNWYLGQNEATLTCDARSNPEPTGYNWSTTMGPLPPFAVAQGAQLLIRPVDKPINTTLICNVTNALGARQAELTVQVKEGPPSEHSGISRN(SEQ ID NO:6203)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6203的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是DAP10的配体,其是NKG2D的衔接子(参见例如,Proc Natl Acad Sci U S A.2005年5月24日;102(21):7641-7646;和Blood,2011年9月15日,第118卷,第11期,其中每一个的全部内容通过引用并入本文)。
在其他实施方案中,NK细胞接合物是CD16的配体,其是CD16a/b配体,例如,进一步包含抗体Fc区的CD16a/b配体(参见例如,Front Immunol.2013;4:76讨论的抗体如何使用Fc通过CD16触发NK细胞,其全部内容并入本文)。
在其他实施方案中,NK细胞接合物是CRTAM的配体,其是NECL2,例如,其中NECL2包含以下氨基酸序列:
QNLFTKDVTVIEGEVATISCQVNKSDDSVIQLLNPNRQTIYFRDFRPLKDSRFQLLNFSSSELKVSLTNVSISDEGRYFCQLYTDPPQESYTTITVLVPPRNLMIDIQKDTAVEGEEIEVNCTAMASKPATTIRWFKGNTELKGKSEVEEWSDMYTVTSQLMLKVHKEDDGVPVICQVEHPAVTGNLQTQRYLEVQYKPQVHIQMTYPLQGLTREGDALELTCEAIGKPQPVMVTWVRVDDEMPQHAVLSGPNLFINNLNKTDNGTYRCEASNIVGKAHSDYMLYVYDPPTTIPPPTTTTTTTTTTTTTILTIITDSRAGEEGSIRAVDH(SEQ ID NO:6204)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6204的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是CD27的配体,其是CD70,例如,其中CD70包含以下氨基酸序列:
QRFAQAQQQLPLESLGWDVAELQLNHTGPQQDPRLYWQGGPALGRSFLHGPELDKGQLRIHRDGIYMVHIQVTLAICSSTTASRHHPTTLAVGICSPASRSISLLRLSFHQGCTIASQRLTPLARGDTLCTNLTGTLLPSRNTDETFFGVQWVRP(SEQ ID NO:6205)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6205的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是PSGL1的配体,其是L-选择素(CD62L),例如,其中L-选择素包含以下氨基酸序列:WTYHYSEKPMNWQRARRFCRDNYTDLVAIQNKAEIEYLEKTLPFSRSYYWIGIRKIGGIWTWVGTNKSLTEEAENWGDGEPNNKKNKEDCVEIYIKRNKDAGKWNDDACHKLKAALCYTASCQPWSCSGHGECVEIINNYTCNCDVGYYGPQCQFVIQCEPLEAPELGTMDCTHPLGNFSFSSQCAFSCSEGTNLTGIEETTCGPFGNWSSPEPTCQVIQCEPLSAPDLGIMNCSHPLASFSFTSACTFICSEGTELIGKKKTICESSGIWSNPSPICQKLDKSFSMIKEGDYN(SEQ ID NO:6206)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6206的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是CD96的配体,其是NECL5,例如,其中NECL5包含以下氨基酸序列:WPPPGTGDVVVQAPTQVPGFLGDSVTLPCYLQVPNMEVTHVSQLTWARHGESGSMAVFHQTQGPSYSESKRLEFVAARLGAELRNASLRMFGLRVEDEGNYTCLFVTFPQGSRSVDIWLRVLAKPQNTAEVQKVQLTGEPVPMARCVSTGGRPPAQITWHSDLGGMPNTSQVPGFLSGTVTVTSLWILVPSSQVDGKNVTCKVEHESFEKPQLLTVNLTVYYPPEVSISGYDNNWYLGQNEATLTCDARSNPEPTGYNWSTTMGPLPPFAVAQGAQLLIRPVDKPINTTLICNVTNALGARQAELTVQVKEGPPSEHSGISRN(SEQ ID NO:6203)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6203或6204的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是CD100(SEMA4D)的配体,其是CD72,例如,其中CD72包含以下氨基酸序列:RYLQVSQQLQQTNRVLEVTNSSLRQQLRLKITQLGQSAEDLQGSRRELAQSQEALQVEQRAHQAAEGQLQACQADRQKTKETLQSEEQQRRALEQKLSNMENRLKPFFTCGSADTCCPSGWIMHQKSCFYISLTSKNWQESQKQCETLSSKLATFSEIYPQSHSYYFLNSLLPNGGSGNSYWTGLSS NKDWKLTDDTQRTRTYAQSSKCNKVHKTWSWWTLESESCRSSLPYICEMTAFRFPD(SEQ ID NO:6207)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6207的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是NKp80的配体,其是CLEC2B(AICL),例如,其中CLEC2B(AICL)包含以下氨基酸序列:
KLTRDSQSLCPYDWIGFQNKCYYFSKEEGDWNSSKYNCSTQHADLTIIDNIEEMNFLRRYKCSSDHWIGLKMAKNRTGQWVDGATFTKSFGMRGSEGCAYLSDDGAATARCYTERKWICRKRIH(SEQ ID NO:6208)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于
SEQ ID NO:6208的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,NK细胞接合物是CD244的配体,其是CD48,例如,其中CD48包含以下氨基酸序列:
QGHLVHMTVVSGSNVTLNISESLPENYKQLTWFYTFDQKIVEWDSRKSKYFESKFKGRVRLDPQSGALYISKVQKEDNSTYIMRVLKKTGNEQEWKIKLQVLDPVPKPVIKIEKIEDMDDNCYLKLSCVIPGESVNYTWYGDKRPFPKELQNSVLETTLMPHNYSRCYTCQVSNSVSSKNGTVCLSPPCTLARS(SEQ ID NO:6209)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6209的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,NK细胞接合物是病毒血凝素(HA),HA是存在于流感病毒表面上的糖蛋白。它负责将病毒结合至膜上具有唾液酸的细胞,例如上呼吸道中的细胞或红细胞。HA具有至少18种不同的抗原。这些亚型被命名为H1至H18。NCR可以识别病毒蛋白。NKp46已显示出能够与流感的HA和副粘病毒(包括仙台病毒和新城疫病毒)的HA-NA相互作用。除NKp46以外,NKp44也可以与不同流感亚型的HA功能上相互作用。
在本文所述的多功能性分子中任一种的一些实施方案中,免疫细胞接合物是NK细胞接合物,例如,介导NK细胞的结合和激活的NK细胞接合物,或介导NK细胞的结合但不激活的NK细胞接合物。在某些实施方案中,NK细胞接合物选自结合至(例如,激活)以下的抗体分子(例如,抗原结合结构域)或配体:NKp30、NKp40、NKp44、NKp46、NKG2D、DNAM1、DAP10、CD16(例如,CD16a、CD16b或两者)、CRTAM、CD27、PSGL1、CD96、CD100(SEMA4D)、NKp80、CD244(也称为SLAMF4或2B4)、SLAMF6、SLAMF7、KIR2DS2、KIR2DS4、KIR3DS1、KIR2DS3、KIR2DS5、KIR2DS1、CD94、NKG2C、NKG2E或CD160,例如,NK细胞接合物是结合至(例如,激活)NKp30的抗体分子或配体。在一些实施方案中,NK细胞接合物是抗体分子,例如,抗原结合结构域。
在一些实施方案中,NK细胞接合物能够接合NK细胞。
在一些实施方案中,NK细胞接合物是结合至NKp30、NKp46、NKG2D或CD16的抗体分子,例如,抗原结合结构域。
在一些实施方案中,多功能性分子:
(i)特异性结合至NKp30、NKp46、NKG2D或CD16的表位,例如,与如本文所述的抗NKp30、抗NKp46、抗NKG2D或抗CD16抗体分子识别的表位相同或相似的表位;
(ii)表现出与如本文所述的抗NKp30、抗NKp46、抗NKG2D或抗CD16抗体分子相同或相似的结合亲和力或特异性,或两者;
(iii)抑制(例如,竞争性抑制)如本文所述的抗NKp30、抗NKp46、抗NKG2D或抗CD16抗体分子的结合;
(iv)与如本文所述的抗NKp30、抗NKp46、抗NKG2D或抗CD16抗体分子结合相同或重叠的表位;或
(v)与如本文所述的抗NKp30、抗NKp46、抗NKG2D或抗CD16分子竞争结合和/或结合相同的表位。
在一些实施方案中,抗NKp30、抗NKp46、抗NKG2D或抗CD16抗体分子包含一个或多个CDR、框架区、可变结构域、重链或轻链,或选自表7、8、35、36、9、10、15或34的抗原结合结构域,或与其基本相同的序列。在一些实施方案中,NK细胞接合物是结合至NKp30的抗体分子,例如,抗原结合结构域。在一些实施方案中,淋巴瘤细胞或淋巴细胞的裂解由NKp30介导。在一些实施方案中,当在淋巴瘤细胞上不存在肿瘤抗原或淋巴细胞上不存在TRBC1或TRBC2的情况下与NK细胞一起孵育时,多功能性分子不激活NK细胞。在一些实施方案中,当NK细胞是表达NKp30的NK细胞并且:(1)淋巴瘤细胞上还存在肿瘤抗原,或(2)淋巴细胞上还存在TRBC1或TRBC2时,多功能性分子激活NK细胞。在一些实施方案中,当NK细胞不是表达NKp30的NK细胞并且:(1)淋巴瘤细胞上还存在肿瘤抗原,或(2)淋巴细胞上还存在TRBC1或TRBC2时,多功能性分子不激活NK细胞。
在一些实施方案中,NK细胞接合物包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6002的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6064的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7293的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,NK细胞接合物包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,NK细胞接合物包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6004的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6005的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ ID NO:6006的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),和/或
(2)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6067的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:7292的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ ID NO:6069的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,NK细胞接合物包含:
(i)VH,该VH包含SEQ ID NO:6121的氨基酸序列(或与SEQ ID NO:6121具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,该VL包含SEQ ID NO:7294的氨基酸序列(或与SEQ ID NO:7294具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链,该重链包含SEQ ID NO:6148或6149的氨基酸序列(或与SEQ ID NO:6148或6149具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链,该轻链包含SEQ ID NO:6150的氨基酸序列(或与SEQ ID NO:6150具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链和轻链,该重链包含SEQ ID NO:6148或6149的氨基酸序列(或与SEQ ID NO:6148或6149具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含SEQ ID NO:6150的氨基酸序列(或与SEQ IDNO:6150具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6014的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6015的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6016的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6017的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6014的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6015的VHFWR2氨基酸序列、SEQ ID NO:6016的VHFWR3氨基酸序列,或SEQ ID NO:6017的VHFWR4氨基酸序列。
在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6123的氨基酸序列(或与SEQ ID NO:6123具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6018的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6019的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6020的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6021的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6018的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6019的VHFWR2氨基酸序列、SEQ ID NO:6020的VHFWR3氨基酸序列,或SEQ ID NO:6021的VHFWR4氨基酸序列。
在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6124的氨基酸序列(或与SEQ ID NO:6124具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6022的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6023的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6024的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6025的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6022的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6023的VHFWR2氨基酸序列、SEQ ID NO:6024的VHFWR3氨基酸序列,或SEQ ID NO:6025的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6125的氨基酸序列(或与SEQ IDNO:6125具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6026的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6027的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6028的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6029的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6026的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6027的VHFWR2氨基酸序列、SEQ ID NO:6028的VHFWR3氨基酸序列,或SEQ ID NO:6029的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6126的氨基酸序列(或与SEQ IDNO:6126具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6030的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6032的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6033的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6034的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6030的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6032的VHFWR2氨基酸序列、SEQ ID NO:6033的VHFWR3氨基酸序列,或SEQ ID NO:6034的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6127的氨基酸序列(或与SEQ IDNO:6127具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6035的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6036的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6037的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6038的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6035的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6036的VHFWR2氨基酸序列、SEQ ID NO:6037的VHFWR3氨基酸序列,或SEQ ID NO:6038的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6128的氨基酸序列(或与SEQ IDNO:6128具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6077的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6078的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6079的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6080的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6077的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6078的VLFWR2氨基酸序列、SEQ ID NO:6079的VLFWR3氨基酸序列,或SEQ ID NO:6080的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6137的氨基酸序列(或与SEQ IDNO:6137具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6081的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6082的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6083的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6084的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6081的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6082的VLFWR2氨基酸序列、SEQ ID NO:6083的VLFWR3氨基酸序列,或SEQ ID NO:6084的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6138的氨基酸序列(或与SEQ IDNO:6138具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6085的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6086的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6087的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6088的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6085的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6086的VLFWR2氨基酸序列、SEQ ID NO:6087的VLFWR3氨基酸序列,或SEQ ID NO:6088的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6139的氨基酸序列(或与SEQ IDNO:6139具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6089的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6090的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6091的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6092的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6089的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6090的VLFWR2氨基酸序列、SEQ ID NO:6091的VLFWR3氨基酸序列,或SEQ ID NO:6092的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6140的氨基酸序列(或与SEQ IDNO:6140具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6093的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6094的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6095的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6096的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6093的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6094的VLFWR2氨基酸序列、SEQ ID NO:6095的VLFWR3氨基酸序列,或SEQ ID NO:6096的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6141的氨基酸序列(或与SEQ IDNO:6141具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6007的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6008的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6009的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6070的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6071的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6072的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在某些实施方案中,NK细胞接合物包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6007的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6008的VHCDR2氨基酸序列,和/或SEQ ID NO:6009的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6070的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6071的VLCDR2氨基酸序列,和/或SEQ ID NO:6072的VLCDR3氨基酸序列。
在一些实施方案中,NK细胞接合物包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6010的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6011的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6012的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ ID NO:6013的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),和/或
(2)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6073的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6074的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6075的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ ID NO:6076的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6010的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6011的VHFWR2氨基酸序列、SEQ ID NO:6012的VHFWR3氨基酸序列,或SEQ ID NO:6013的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6073的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6074的VLFWR2氨基酸序列、SEQ ID NO:6075的VLFWR3氨基酸序列,或SEQ ID NO:6076的VLFWR4氨基酸序列。
在一些实施方案中,NK细胞接合物包含:
(i)VH,该VH包含SEQ ID NO:6122的氨基酸序列(或与SEQ ID NO:6122具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,该VL包含SEQ ID NO:6136的氨基酸序列(或与SEQ ID NO:6136具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链,该重链包含SEQ ID NO:6151或6152的氨基酸序列(或与SEQ ID NO:6151或6152具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链,该轻链包含SEQ ID NO:6153的氨基酸序列(或与SEQ ID NO:6153具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链和轻链,该重链包含SEQ ID NO:6151或6152的氨基酸序列(或与SEQ ID NO:6151或6152具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含SEQ ID NO:6153的氨基酸序列(或与SEQ IDNO:6153具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6039的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6040的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6041的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6042的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6039的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6040的VHFWR2氨基酸序列、SEQ ID NO:6041的VHFWR3氨基酸序列,或SEQ ID NO:6042的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6129的氨基酸序列(或与SEQ IDNO:6129具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6043的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6044的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6045的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6046的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6043的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6044的VHFWR2氨基酸序列、SEQ ID NO:6045的VHFWR3氨基酸序列,或SEQ ID NO:6046的VHFWR4氨基酸序列。
在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6130的氨基酸序列(或与SEQ ID NO:6130具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6047的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6048的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6049的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6050的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6047的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6048的VHFWR2氨基酸序列、SEQ ID NO:6049的VHFWR3氨基酸序列,或SEQ ID NO:6050的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6131的氨基酸序列(或与SEQ IDNO:6131具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6051的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6052的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6053的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6054的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6051的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6052的VHFWR2氨基酸序列、SEQ ID NO:6053的VHFWR3氨基酸序列,或SEQ ID NO:6054的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6132的氨基酸序列(或与SEQ IDNO:6132具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6055的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6056的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6057的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6058的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6055的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6056的VHFWR2氨基酸序列、SEQ ID NO:6057的VHFWR3氨基酸序列,或SEQ ID NO:6058的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6133的氨基酸序列(或与SEQ IDNO:6133具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6059的重链框架区1(VHFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6060的VHFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6061的VHFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6062的VHFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6059的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6060的VHFWR2氨基酸序列、SEQ ID NO:6061的VHFWR3氨基酸序列,或SEQ ID NO:6062的VHFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6134的氨基酸序列(或与SEQ IDNO:6134具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,其中NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6097的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6098的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6099的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6100的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6097的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6098的VLFWR2氨基酸序列、SEQ ID NO:6099的VLFWR3氨基酸序列,或SEQ ID NO:6100的VLFWR4氨基酸序列。在某些实施方案中,其中NK细胞接合物包含VL,该VL包含SEQ ID NO:6142的氨基酸序列(或与SEQ ID NO:6142具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6101的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6102的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6103的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6104的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6101的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6102的VLFWR2氨基酸序列、SEQ ID NO:6103的VLFWR3氨基酸序列,或SEQ ID NO:6104的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6143的氨基酸序列(或与SEQ IDNO:6143具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6105的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6106的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6107的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6108的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6105的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6106的VLFWR2氨基酸序列、SEQ ID NO:6107的VLFWR3氨基酸序列,或SEQ ID NO:6108的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6144的氨基酸序列(或与SEQ IDNO:6144具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6109的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6110的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6111的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6112的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6109的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6110的VLFWR2氨基酸序列、SEQ ID NO:6111的VLFWR3氨基酸序列,或SEQ ID NO:6112的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6145的氨基酸序列(或与SEQ IDNO:6145具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6113的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6114的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6115的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6116的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6113的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6114的VLFWR2氨基酸序列、SEQ ID NO:6115的VLFWR3氨基酸序列,或SEQ ID NO:6116的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6146的氨基酸序列(或与SEQ IDNO:6146具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6117的轻链框架区1(VLFWR1)氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6118的VLFWR2氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)、SEQ ID NO:6119的VLFWR3氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列),或SEQ IDNO:6120的VLFWR4氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)。在某些实施方案中,NK细胞接合物包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6117的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6118的VLFWR2氨基酸序列、SEQ ID NO:6119的VLFWR3氨基酸序列,或SEQ ID NO:6120的VLFWR4氨基酸序列。在某些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6147的氨基酸序列(或与SEQ IDNO:6147具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物是结合至NKp46的抗体分子,例如,抗原结合结构域。在某些实施方案中,淋巴瘤细胞的裂解由NKp46介导。在一些实施方案中,当在淋巴瘤细胞上不存在肿瘤抗原的情况下与NK细胞一起孵育时,多功能性分子不激活NK细胞。在一些实施方案中,当NK细胞是表达NKp46的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子激活NK细胞。在一些实施方案中,当NK细胞不是表达NKp46的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子不激活NK细胞。在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6182的氨基酸序列(或与SEQ ID NO:6182具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6183的氨基酸序列(或与SEQ ID NO:6183具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含scFv,该scFv包含SEQ ID NO:6181的氨基酸序列(或与SEQ ID NO:6181具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物是结合至NKG2D的抗体分子,例如,抗原结合结构域。在某些实施方案中,淋巴瘤细胞的裂解由NKG2D介导。在一些实施方案中,当在淋巴瘤细胞上不存在肿瘤抗原的情况下与NK细胞一起孵育时,多功能性分子不激活NK细胞。在一些实施方案中,当NK细胞是表达NKG2D的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子激活NK细胞。在一些实施方案中,当NK细胞不是表达NKG2D的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子不激活NK细胞。在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6176的氨基酸序列(或与SEQ ID NO:6176具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6177的氨基酸序列(或与SEQ ID NO:6177具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含scFv,该scFv包含SEQ ID NO:6175的氨基酸序列(或与SEQ ID NO:6175具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQID NO:6179的氨基酸序列(或与SEQ ID NO:6179具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含VL,该VL包含SEQID NO:6180的氨基酸序列(或与SEQ ID NO:6180具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含scFv,该scFv包含SEQ ID NO:6178的氨基酸序列(或与SEQ ID NO:6178具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物是结合至CD16的抗体分子,例如,抗原结合结构域。在一些实施方案中,淋巴瘤细胞的裂解由CD16介导。在一些实施方案中,当在淋巴瘤细胞上不存在肿瘤抗原的情况下与NK细胞一起孵育时,多功能性分子不激活NK细胞。在一些实施方案中,当NK细胞是表达CD16的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子激活NK细胞。在一些实施方案中,当NK细胞不是表达CD16的NK细胞并且淋巴瘤细胞上还存在肿瘤抗原时,多功能性分子不激活NK细胞。在一些实施方案中,NK细胞接合物包含VH,该VH包含SEQ ID NO:6185的氨基酸序列(或与SEQ ID NO:6185具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含VL,该VL包含SEQ ID NO:6186的氨基酸序列(或与SEQ ID NO:6186具有至少约93%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,NK细胞接合物包含scFv,该scFv包含SEQ ID NO:6184的氨基酸序列(或与SEQ ID NO:6184具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,NK细胞接合物是配体,任选地,该配体进一步包含免疫球蛋白恒定区,例如,Fc区。在某些实施方案中,NK细胞接合物是NKp44或NKp46的配体,例如,病毒HA。在某些实施方案中,NK细胞接合物是DAP10的配体,例如,NKG2D的辅助受体。在某些实施方案中,NK细胞接合物是CD16的配体,例如,CD16a/b配体,例如,进一步包含抗体Fc区的CD16a/b配体。
B细胞、巨噬细胞和树突细胞接合物
广泛地说,B细胞(也称为B淋巴细胞)是一类淋巴细胞亚型的白血细胞。它们通过分泌抗体在适应性免疫系统的体液免疫组分中起作用。另外,B细胞呈递抗原(它们也被分类为专职性抗原呈递细胞(APC))并分泌细胞因子。巨噬细胞是一类经由吞噬作用吞噬和消化细胞碎片、外来物质、微生物、癌细胞的白血细胞。除吞噬作用以外,它们在非特异性防御(先天免疫)中起重要作用,并且还通过募集其他免疫细胞(例如淋巴细胞)来帮助启动特异性防御机制(适应性免疫)。例如,它们作为T细胞的抗原呈递者是重要的。除增加炎症和刺激免疫系统以外,巨噬细胞还起到重要的抗炎作用,并且可以通过释放细胞因子来减少免疫反应。树突细胞(DC)是抗原呈递细胞,其在加工抗原材料中起作用,并将其呈递在免疫系统T细胞的细胞表面上。
本发明尤其提供了多特异性(例如,双特异性、三特异性、四特异性)或多功能性分子,其包括例如工程化为含有介导B细胞、巨噬细胞和/或树突细胞的结合和/或激活的一种或多种B细胞、巨噬细胞和/或树突细胞接合物。
因此,在一些实施方案中,免疫细胞接合物包含选自CD40配体(CD40L)或CD70配体中的一种或多种的B细胞、巨噬细胞和/或树突细胞接合物;结合至CD40或CD70的抗体分子;抗OX40的抗体分子;OX40配体(OX40L);Toll样受体的激动剂(例如,如本文所述的,例如,TLR4,例如,组成型活性TLR4(caTLR4)或TLR9激动剂);41BB;CD2;CD47;或STING激动剂,或其组合。
在一些实施方案中,B细胞接合物是CD40L、OX40L或CD70配体,或结合至OX40、CD40或CD70的抗体分子。
在一些实施方案中,巨噬细胞接合物是CD2激动剂。在一些实施方案中,巨噬细胞接合物是抗原结合结构域,其结合至:CD40L或结合CD40的抗原结合结构域或配体、(例如,如本文所述的)Toll样受体(TLR)激动剂,例如,TLR9或TLR4(例如,caTLR4(组成型活性TLR4)、CD47或STING激动剂。在一些实施方案中,STING激动剂是环状二核苷酸,例如,环状二-GMP(cdGMP)或环状二-AMP(cdAMP)。在一些实施方案中,STING激动剂是生物素化的。
在一些实施方案中,树突细胞接合物是CD2激动剂。在一些实施方案中,树突细胞接合物是配体、受体激动剂或抗体分子,其结合至以下中的一种或多种:OX40L、41BB、(例如,如本文所述的)TLR激动剂(例如,TLR9激动剂、TLR4(例如,caTLR4(组成型活性TLR4))、CD47或/和STING激动剂。在一些实施方案中,STING激动剂是环状二核苷酸,例如,环状二-GMP(cdGMP)或环状二-AMP(cdAMP)。在一些实施方案中,STING激动剂是生物素化的。
在其他实施方案中,免疫细胞接合物介导B细胞、巨噬细胞和/或树突细胞中的一种或多种的结合或激活。示例性B细胞、巨噬细胞和/或树突细胞接合物可以选自以下中的一种或多种:CD40配体(CD40L)或CD70配体;结合至CD40或CD70的抗体分子;抗OX40的抗体分子;OX40配体(OX40L);Toll样受体激动剂(例如,TLR4,例如,组成型活性TLR4(caTLR4)或TLR9激动剂);41BB激动剂;CD2;CD47;或STING激动剂,或其组合。
在一些实施方案中,B细胞接合物选自CD40L、OX40L或CD70配体,或结合至OX40、CD40或CD70的抗体分子中的一种或多种。
在其他实施方案中,巨噬细胞接合物选自以下中的一种或多种:CD2激动剂;CD40L;OX40L;结合至OX40、CD40或CD70的抗体分子;Toll样受体激动剂或其片段(例如,TLR4,例如,组成型活性TLR4(caTLR4));CD47激动剂;或STING激动剂。
在其他实施方案中,树突细胞接合物选自CD2激动剂、OX40抗体、OX40L、41BB激动剂、Toll样受体激动剂或其片段(例如,TLR4,例如,组成型活性TLR4(caTLR4))、CD47激动剂或STING激动剂中的一种或多种。
在一个实施方案中,OX40L包含以下氨基酸序列:
QVSHRYPRIQSIKVQFTEYKKEKGFILTSQKEDEIMKVQNNSVIINCDGFYLISLKGYFSQEVNISLHYQKDEEPLFQLKKVRSVNSLMVASLTYKDKVYLNVTTDNTSLDDFHVNGGELILIHQNPGEFCVL(SEQ ID NO:6210)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6210的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在另一实施方案中,CD40L包含以下氨基酸序列:
MQKGDQNPQIAAHVISEASSKTTSVLQWAEKGYYTMSNNLVTLENGKQLTVKRQGLYYIYAQVTFCSNREASSQAPFIASLCLKSPGRFERILLRAANTHSSAKPCGQQSIHLGGVFELQPGASVFVNVTDPSQVSHGTGFTSFGLLKL(SEQ ID NO:6211)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6211的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,STING激动剂包含环状二核苷酸,例如,环状二-GMP(cdGMP)、环状二-AMP(cdAMP)或其组合,任选地具有2’,5’或3’,5’磷酸酯键。
在一个实施方案中,免疫细胞接合物包括41BB配体,例如,包含以下氨基酸序列:
ACPWAVSGARASPGSAASPRLREGPELSPDDPAGLLDLRQGMFAQLVAQNVLLIDGPLSWYSDPGLAGVSLTGGLSYKEDTKELVVAKAGVYYVFFQLELRRVVAGEGSGSVSLALHLQPLRSAAGAAALALTVDLPPASSEARNSAFGFQGRLLHLSAGQRLGVHLHTEARARHAWQLTQGATVLGLFRVTPEIPAGLPSPRSE(SEQ ID NO:6212)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6212的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
Toll样受体
Toll样受体(TLR)是进化上保守的受体,是果蝇Toll蛋白的同源物,并且识别被称为病原体相关微生物模式(PAMP)(其仅由微生物病原体表达)或危险相关分子模式(DAMP)(其是从坏死或死亡细胞释放的内源性分子)的高度保守的结构基序。PAMP包括各种细菌细胞壁组分(例如脂多糖(LPS)、肽聚糖(PGN)和脂肽),以及鞭毛蛋白、细菌DNA和病毒双链RNA。DAMP包括胞内蛋白质(例如热休克蛋白)以及来自胞外基质的蛋白片段。通过相应的PAMP或DAMP对TLR的刺激启动信号级联放大,导致转录因子(例如AP-1、NF-κB和干扰素调控因子(IRF))的激活。TLR的信号传导导致各种细胞应答,包括指导适应性免疫应答的干扰素(IFN)、促炎性细胞因子和效应细胞因子的产生。TLR涉及许多炎性和免疫病症,并且在癌症中起作用(Rakoff-Nahoum S.和Medzhitov R.,2009.Toll-like receptors andcancer.Nat Revs Cancer 9:57-63)。
TLR是I型跨膜蛋白,其特征在于含有富亮氨酸重复序列(LRR)的胞外结构域和含有称为Toll/IL-1受体(TIR)结构域的保守区的胞质尾区。已表征了10种人和12种鼠TLR(人中TLR1至TLR10,小鼠中TLR1至TLR9、TLR11、TLR12和TLR13),TLR10的同源物是假基因。TLR2是识别来自革兰氏阳性细菌的各种PAMP(包括细菌脂蛋白、脂甘露聚糖和脂磷壁酸)所必需的。TLR3涉及病毒来源的双链RNA。TLR4主要由脂多糖激活。TLR5检测细菌鞭毛蛋白,TLR9是对未甲基化CpG DNA的应答所必需的。最后,TLR7和TLR8识别小的合成抗病毒分子,并且据报道单链RNA是它们的天然配体。已报道,TLR11识别尿路病原性大肠杆菌和来自刚地弓形虫(Toxoplasma gondii)的抑制蛋白(profilin)样蛋白。TLR彼此异源二聚化的能力明显扩展了TLR特异性的所有组成成分。例如,TLR2和TLR6的二聚体是对二酰化脂蛋白的应答所必需的,而TLR2和TLR1相互作用以识别三酰化脂蛋白。TLR的特异性也受到各种衔接子和辅助分子的影响,例如MD-2和CD14,它们响应于LPS与TLR4形成复合体。
TLR信号传导由至少两种不同的途径组成:导致炎性细胞因子产生的MyD88依赖性途径,以及与IFN-β的刺激和树突细胞的成熟相关的MyD88非依赖性途径。MyD88依赖性途径是所有TLR的共同途径,除了TLR3(Adachi O.等人,1998.Targeted disruption of theMyD88 gene results in loss of IL-1-and IL-18-mediated function.Immunity.9(1):143-50)。在由PAMP或DAMP激活时,TLR异源或同源二聚化,经由细胞质TIR结构域诱导衔接蛋白的募集。单独的TLR通过使用不同的衔接分子诱导不同的信号传导应答。TLR4和TLR2信号传导需要衔接子TIRAP/Mal,其涉及MyD88依赖性途径。TLR3通过衔接子TRIF/TICAM-1以MyD88非依赖性方式响应于双链RNA触发IFN-β的产生。TRAM/TICAM-2是另一种参与MyD88非依赖性途径的衔接分子,其功能限于TLR4途径。
TLR3、TLR7、TLR8和TLR9识别病毒核酸,并诱导I型IFN。导致诱导I型IFN的信号传导机制根据活化的TLR而不同。它们涉及干扰素调控因子、IRF、已知在抗病毒防御、细胞生长和免疫调控中起关键作用的转录因子家族。三种IRF(IRF3、IRF5和IRF7)充当病毒介导的TLR信号传导的直接转换器。TLR3和TLR4激活IRF3和IRF7,而TLR7和TLR8激活IRF5和IRF7(Doyle S.等人,2002.IRF3 mediates a TLR3/TLR4-specific antiviral geneprogram.Immunity.17(3):251-63)。此外,由TLR9配体CpG-A刺激的I型IFN生产已显示由PI(3)K和mTOR介导(Costa-Mattioli M.和Sonenberg N.2008.RAPping production of typeI interferon in pDCs through mTOR.Nature Immunol.9:1097-1099)。
TLR-9
TLR9识别DNA分子中未甲基化的CpG序列。与细菌基因组或病毒DNA相比,CpG位点在脊椎动物基因组上相对罕见(约1%)。TLR9由免疫系统的许多细胞表达,例如B淋巴细胞、单核细胞、自然杀伤(NK)细胞和浆细胞样树突细胞。TLR9在胞内内体区室中表达,并且通过与富含CpG基序的DNA结合而起到警示免疫系统病毒和细菌感染的作用。TLR9信号导致启动促炎性反应的细胞的激活,该促炎性反应导致细胞因子(例如I型干扰素和IL-12)的产生。
TLR激动剂
TLR激动剂可以激动一种或多种TLR,例如,人TLR-1、2、3、4、5、6、7、8、9或10中的一种或多种。在一些实施方案中,本文所述的辅助剂是TLR激动剂。在一些实施方案中,TLR激动剂特异性激动人TLR-9。在一些实施方案中,TLR-9激动剂是CpG部分。如本文所用,CpG部分是具有以下序列的线性二核苷酸:5’-C-磷酸酯-G-3’,即,胞嘧啶和鸟嘌呤仅由一个磷酸酯分开。
在一些实施方案中,CpG部分包含至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或更多个CpG二核苷酸。在一些实施方案中,CpG部分由1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个CpG二核苷酸组成。在一些实施方案中,CpG部分具有1-5、1-10、1-20、1-30、1-40、1-50、5-10、5-20、5-30、10-20、10-30、10-40或10-50个CpG二核苷酸。
在一些实施方案中,TLR-9激动剂是合成的ODN(寡脱氧核苷酸)。CpG ODN是短的合成单链DNA分子,其在特定的序列背景(CpG基序)中含有未甲基化的CpG二核苷酸。与存在于基因组细菌DNA中的天然磷酸二酯(PO)骨架相反,CPG ODN具有部分或完全硫代磷酸化(PS)骨架。CPG ODN有三大类:A、B和C类,它们的免疫刺激活性不同。CPG-A ODN的特征在于含PO中心CPG的回文基序和PS修饰的3’聚G串。它们诱导pDC高产量产生IFN-α,但是是TLR9依赖性NF-κB信号传导和促炎性细胞因子(例如,IL-6)产生的弱刺激物。CPG-B ODN含有具有一个或多个CPG二核苷酸的完整PS骨架。它们强烈激活B细胞和TLR9依赖性NF-κB信号传导,但弱刺激IFN-α分泌。CPG-C ODN组合了A类和B类两者的特征。它们含有完整的PS骨架和含CPG的回文基序。C类CPG ODN诱导强的pDC产生IFN-α以及B细胞刺激。
细胞因子分子
细胞因子通常是例如通过信号转导途径影响细胞活性的多肽。因此,多特异性或多功能性多肽的细胞因子是有用的,并且可以与受体介导的信号传导相关,该信号传导传递来自细胞膜外的信号,以调节细胞内的应答。细胞因子是蛋白质类信号传导化合物,其是免疫应答的介质。它们控制许多不同的细胞功能,包括增殖、分化和细胞存活/凋亡;细胞因子也参与几种病理生理学过程,包括病毒感染和自身免疫性疾病。细胞因子在各种刺激下由先天免疫系统(单核细胞、巨噬细胞、树突细胞)和适应性免疫系统(T细胞和B细胞)的各种细胞合成。细胞因子可分为两组:促炎性和抗炎性。促炎性细胞因子(包括IFNγ、IL-1、IL-6和TNF-α)主要来源于先天免疫细胞和Th1细胞。抗炎性细胞因子(包括IL-10、IL-4、IL-13和IL-5)由Th2免疫细胞合成。
本发明尤其提供了多特异性(例如,双特异性、三特异性、四特异性)或多功能性分子,其包括例如工程化为含有一种或多种细胞因子分子,例如,免疫调节(例如,促炎性)细胞因子及其变体,例如,功能性变体。因此,在一些实施方案中,细胞因子分子是白介素或其变体,例如,功能性变体。在一些实施方案中,白介素是促炎性白介素。在一些实施方案中,白介素选自白介素-2(IL-2)、白介素-12(IL-12)、白介素-15(IL-15)、白介素-18(IL-18)、白介素-21(IL-21)、白介素-7(IL-7)或干扰素γ。在一些实施方案中,细胞因子分子是促炎性细胞因子。
在某些实施方案中,细胞因子是单链细胞因子。在某些实施方案中,细胞因子是多链细胞因子(例如,细胞因子包含2条或更多条(例如,2条)多肽链)。示例性多链细胞因子是IL-12。
有用的细胞因子的实例包括但不限于GM-CSF、IL-1α、IL-1β、IL-2、IL-3、IL-4、IL-5、IL-6、IL-7、IL-8、IL-10、IL-12、IL-21、IFN-α、IFN-β、IFN-γ、MIP-1α、MIP-1β、TGF-β、TNF-α和TNFβ。在一个实施方案中,多特异性或多功能性多肽的细胞因子是选自GM-CSF、IL-2、IL-7、IL-8、IL-10、IL-12、IL-15、IL-21、IFN-α、IFN-γ、MIP-1α、MIP-1β和TGF-β的细胞因子。在一个实施方案中,多特异性或多功能性多肽的细胞因子是选自IL-2、IL-7、IL-10、IL-12、IL-15、IFN-α和IFN-γ的细胞因子。在某些实施方案中,细胞因子被突变,以除去N-和/或O-糖基化位点。糖基化的消除增加了可在重组生产中获得的产物的均一性。在某些实施方案中,细胞因子是TGF-β。在某些实施方案中,多特异性或多功能性多肽包含TGF-β抑制剂。
在一个实施方案中,多特异性或多功能性多肽的细胞因子是IL-2。在具体实施方案中,IL-2细胞因子可以引发选自以下细胞应答中的一种或多种:活化T淋巴细胞中的增殖、活化T淋巴细胞中的分化、细胞毒性T细胞(CTL)活性、活化B细胞中的增殖、活化B细胞中的分化、自然杀伤(NK)细胞中的增殖、NK细胞中的分化、活化T细胞或NK细胞的细胞因子分泌,以及NK/淋巴细胞活化的杀伤细胞(LAK)抗肿瘤细胞毒性。在另一具体实施方案中,IL-2细胞因子是对IL-2受体α-亚基的结合亲和力降低的突变型IL-2细胞因子。α-亚基(也称为CD25)与β-和γ-亚基(也分别称为CD122和CD132)一起形成异源三聚体高亲和力IL-2受体,而仅由β-和γ-亚基组成的二聚体受体被称为中间亲和力IL-2受体。如PCT专利申请第PCT/EP2012/051991号(其通过引用以其整体并入本文)中所述,与野生型IL-2多肽相比,与IL-2受体α-亚基结合降低的突变型IL-2多肽在调节性T细胞中诱导IL-2信号传导的能力降低,在T细胞中诱导较少的激活诱导的细胞死亡(AICD),并且体内毒性降低。使用这种毒性降低的细胞因子特别有利于根据本发明的多特异性或多功能性多肽,其因为Fc结构域的存在而具有长的血清半衰期。在一个实施方案中,根据本发明的多特异性或多功能性多肽的突变型IL-2细胞因子包含至少一个氨基酸突变,与未突变型IL-2细胞因子相比,其降低或消除突变型IL-2细胞因子对IL-2受体(CD25)α亚基的亲和力,但保留突变型IL-2细胞因子对中间亲和力IL-2受体(由IL-2受体的β和γ亚基组成)的亲和力。在一个实施方案中,一个或多个氨基酸突变是氨基酸置换。在具体实施方案中,突变型IL-2细胞因子在选自对应于人IL-2的42、45和72位残基位置的一个、两个或三个位置处包含一个、两个或三个氨基酸置换。在更具体实施方案中,突变型IL-2细胞因子在对应于人IL-2的42、45和72位残基的位置处包含三个氨基酸置换。在甚至更具体的实施方案中,突变型IL-2细胞因子是包含氨基酸置换F42A、Y45A和L72G的人IL-2。在一个实施方案中,突变型IL-2细胞因子在对应于人IL-2的第3位位置处另外包含氨基酸突变,其消除IL-2的O-糖基化位点。特别地,所述另外的氨基酸突变是用丙氨酸残基替换苏氨酸残基的氨基酸置换。可用于本发明的特定突变型IL-2细胞因子在对应于人IL-2的3、42、45和72位残基的位置处包含四个氨基酸置换。具体的氨基酸置换是T3A、F42A、Y45A和L72G。如PCT专利申请第PCT/EP2012/051991号和所附实施例中所证明的,所述四倍突变型IL-2多肽(IL-2qm)表现出与CD25无可检测到的结合、在T细胞中诱导凋亡的能力降低、在T.sub.reg细胞中诱导IL-2信号传导的能力降低,以及体内毒性分布降低。然而,它保留了激活效应细胞中的IL-2信号传导、诱导效应细胞增殖和由NK细胞生成作为次级细胞因子的IFN-γ的能力。
根据上述实施方案中任一项的IL-2或突变型IL-2细胞因子可包含另外的突变,该突变提供了进一步的优点,例如表达或稳定性增加。例如,第125位处的半胱氨酸可被中性氨基酸(例如丙氨酸)替换,以避免形成二硫键连接的IL-2二聚体。因此,在某些实施方案中,根据本发明的多特异性或多功能性多肽的IL-2或突变型IL-2细胞因子在对应于人IL-2的第125位残基的位置处包含另外的氨基酸突变。在一个实施方案中,所述另外的氨基酸突变是氨基酸置换C125A。
在具体实施方案中,多特异性或多功能性多肽的IL-2细胞因子包含SEQ ID NO:6364
[APTSSSTKKTQLQLEHLLLDLQMILNGINNYKNPKLTRMLTFKFYMPKKATELKHLQCLEEELKPLEEVLNLAQSKNFHLRPRDLISNINVIVLELKGSETTFMCEYADETATIVEFLNRWITFAQSIISTLT]的多肽序列。在另一具体实施方案中,多特异性或多功能性多肽的IL-2细胞因子包含
SEQ ID NO:6365
[APASSSTKKTQLQLEHLLLDLQMILNGINNYKNPKLTRMLTAKFAMPKKATELKHLQCLEEELKPLEEVLNGAQSKNFHLRPRDLISNINVIVLELKGSETTFMCEYADETATIVEFLNRWITFAQSIISTLT]的多肽序列。
在另一实施方案中,多特异性或多功能性多肽的细胞因子是IL-12。在具体实施方案中,所述IL-12细胞因子是单链IL-12细胞因子。在甚至更具体的实施方案中,单链IL-12细胞因子包含SEQ ID NO:6366
[IWELKKDVYVVELDWYPDAPGEMVVLTCDTPEEDGITWTLDQSSEVLGSGKTLTIQVKEFGDAGQYTCHKGGEVLSHSLLLLHKKEDGIWSTDILKDQKEPKNKTFLRCEAKNYSGRFTCWWLTTISTDLTFSVKSSRGSSDPQGVTCGAATLSAERVRGDNKEYEYSVECQEDSACPAAEESLPIEVMVDAVHKLKYENYTSSFFIRDIIKPDPPKNLQLKPLKNSRQVEVSWEYPDTWSTPHSYFSLTFCVQVQGKSKREKKDRVFTDKTSATVICRKNASISVRAQDRYYSSSWSEWASVPCSGGGGSGGGGSGGGGSRNLPVATPDPGMFPCLHHSQNLLRAVSNMLQKARQTLEFYPCTSEEIDHEDITKDKTSTVEACLPLELTKNESCLNSRETSFITNGSCLASRKTSFMMALCLSSIYEDLKMYQVEFKTMNAKLLMDPKRQIFLDQNMLAVIDELMQALNFNSETVPQKSSLEEPDFYKTKIKLCILLHAFRIRAVTIDRVMSYLNAS]的多肽序列。在一个实施方案中,IL-12细胞因子可以引发选自以下的细胞应答中的一种或多种:NK细胞中的增殖、NK细胞中的分化、T细胞中的增殖和T细胞中的分化。
在另一实施方案中,多特异性或多功能性多肽的细胞因子是IL-10。在具体实施方案中,所述IL-10细胞因子是单链IL-10细胞因子。在甚至更具体的实施方案中,单链IL-10细胞因子包含SEQ ID NO:6367
[SPGQGTQSENSCTHFPGNLPNMLRDLRDAFSRVKTFFQMKDQLDNLLLKESLLEDFKGYLGCQALSEMIQFYLEEVMPQAENQDPDIKAHVNSLGENLKTLRLRLRRCHRFLPCENKSKAVEQVKNAFNKLQEKGIYKAMSEFDIFINYIEAYMTMKIRNGGGGSGGGGSGGGGSGGGGSSPGQGTQSENSCTHFPGNLPNMLRDLRDAFSRVKTFFQMKDQLDNLLLKESLLEDFKGYLGCQALSEMIQFYLEEVMPQAENQDPDIKAHVNSLGENLKTLRLRLRRCHRFLPCENKSKAVEQVKNAFNKLQEKGIYKAMSEFDIFINYIEAYMTMKIRN]的多肽序列。在另一具体实施方案中,IL-10细胞因子是单体IL-10细胞因子。在更具体的实施方案中,单体IL-10细胞因子包含SEQ ID NO:6368
[SPGQGTQSENSCTHFPGNLPNMLRDLRDAFSRVKTFFQMKDQLDNLLLKESLLEDFKGYLGCQALSEMIQFYLEEVMPQAENQDPDIKAHVNSLGENLKTLRLRLRRCHRFLPCENGGGSGGKSKAVEQVKNAFNKLQEKGIYKAMSEFDIFINYIEAYMTMKIRN]的多肽序列。在一个实施方案中,IL-10细胞因子可以引发选自以下的细胞应答中的一种或多种:细胞因子分泌的抑制、抗原呈递细胞的抗原呈递的抑制、氧自由基释放的减少和T细胞增殖的抑制。根据本发明的多特异性或多功能性多肽,其中细胞因子是IL-10,特别用于下调炎症,例如,用于治疗炎性病症。
在另一实施方案中,多特异性或多功能性多肽的细胞因子是IL-15。在具体实施方案中,所述IL-15细胞因子是对IL-15受体α-亚基的结合亲和力降低的突变型IL-15细胞因子。不希望受理论束缚,与野生型IL-15多肽相比,与IL-15受体α-亚基结合降低的突变型IL-15多肽在全身结合至成纤维细胞的能力降低,导致药代动力学和毒性分布改善。使用毒性降低的细胞因子(例如所述的突变型IL-2和突变型IL-15效应部分)特别有利于根据本发明的多特异性或多功能性多肽,其因为Fc结构域的存在而具有长的血清半衰期。在一个实施方案中,根据本发明的多特异性或多功能性多肽的突变型IL-15细胞因子包含至少一个氨基酸突变,与未突变型IL-15细胞因子相比,其降低或消除突变型IL-15细胞因子对IL-15受体α-亚基的亲和力,但保留突变型IL-15细胞因子对中间亲和力IL-15/IL-2受体(由IL-15/IL-2受体的β-和γ-亚基组成)的亲和力。在一个实施方案中,氨基酸突变是氨基酸置换。在具体实施方案中,突变型IL-15细胞因子在对应于人IL-15的第53位残基的位置处包含氨基酸置换。在更具体实施方案中,突变型IL-15细胞因子是包含氨基酸置换E53A的人IL-15。在一个实施方案中,突变型IL-15细胞因子在对应于人IL-15的第79位位置处另外包含氨基酸突变,其消除IL-15的N-糖基化位点。特别地,所述另外的氨基酸突变是用丙氨酸残基替换天冬酰胺残基的氨基酸置换。在甚至更具体的实施方案中,IL-15细胞因子包含SEQ ID NO:6370
[NWVNVISDLKKIEDLIQSMHIDATLYTESDVHPSCKVTAMKCFLLELQVISLASGDASIHDTVENLIILANNSLSSNGAVTESGCKECEELEEKNIKEFLQSFVHIVQMFINTS]的多肽序列。在一个实施方案中,IL-15细胞因子可以引发选自以下的细胞应答中的一种或多种:活化T淋巴细胞中的增殖、活化T淋巴细胞中的分化、细胞毒性T细胞(CTL)活性、活化B细胞中的增殖、活化B细胞中的分化、自然杀伤(NK)细胞中的增殖、NK细胞中的分化、活化T细胞或NK细胞的细胞因子分泌,以及NK/淋巴细胞活化杀伤细胞(LAK)抗肿瘤细胞毒性。
可在多特异性或多功能性多肽中用作效应部分的突变型细胞因子分子可以通过使用本领域公知的遗传或化学方法进行缺失、置换、插入或修饰来制备。遗传方法可包括编码DNA序列的位点特异性诱变、PCR、基因合成等。可以例如通过测序验证正确的核苷酸改变。置换或插入可涉及天然以及非天然的氨基酸残基。氨基酸修饰包括公知的化学修饰方法,例如添加或去除糖基化位点或碳水化合物附着物等。
在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是GM-CSF。在具体实施方案中,GM-CSF细胞因子可以引发粒细胞、单核细胞或树突细胞中的增殖和/或分化。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是IFN-α。在具体实施方案中,IFN-α细胞因子可以引发选自以下的细胞应答中的一种或多种:抑制病毒感染细胞中的病毒复制,以及上调主要组织相容性复合体I(MHCI)的表达。在另一具体实施方案中,IFN-α细胞因子可以抑制肿瘤细胞中的增殖。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是IFNγ。在具体实施方案中,IFN-γ细胞因子可以引发选自以下的细胞应答中的一种或多种:巨噬细胞活性增加、MHC分子表达增加和NK细胞活性增加。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是IL-7。在具体实施方案中,IL-7细胞因子可以引发T和/或B淋巴细胞的增殖。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是IL-8。在具体实施方案中,IL-8细胞因子可以引发嗜中性粒细胞的趋化性。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是MIP-1α。在具体实施方案中,MIP-1α细胞因子可以引发单核细胞和T淋巴细胞中的趋化性。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是MIP-1β。在具体实施方案中,MIP-1β细胞因子可以引发单核细胞和T淋巴细胞中的趋化性。在一个实施方案中,多特异性或多功能性多肽的细胞因子(特别是单链细胞因子)是TGF-β。在具体实施方案中,TGF-β细胞因子可以引发选自以下的细胞应答中的一种或多种:单核细胞中的趋化性、巨噬细胞中的趋化性、活化的巨噬细胞中IL-1表达的上调和活化的B细胞中IgA表达的上调。
在一个实施方案中,本发明的多特异性或多功能性多肽以比对照细胞因子的解离常数(KD)大至少约1、1.5、2、2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5、8、8.5、9、9.5或10倍的解离常数(KD)结合至细胞因子受体。在另一实施方案中,多特异性或多功能性多肽以比包含两个或更多个效应部分的相应多特异性或多功能性多肽的KD大至少2、3、4、5、6、7、8、9或10倍的KD结合至细胞因子受体。在另一实施方案中,多特异性或多功能性多肽以比包含两种或更多种细胞因子的相应多特异性或多功能性多肽的解离常数KD大约10倍的解离常数KD结合至细胞因子受体。
在一些实施方案中,本文公开的多特异性分子包括细胞因子分子。在一些实施方案中,细胞因子分子包括细胞因子的全长、片段或变体;细胞因子受体结构域,例如,细胞因子受体二聚化结构域;或细胞因子受体的激动剂,例如,细胞因子受体的抗体分子(例如,激动性抗体)。
在一些实施方案中,细胞因子分子选自IL-2、IL-12、IL-15、IL-18、IL-7、IL-21或干扰素γ,或其片段或变体,或上述细胞因子中任一种的组合。细胞因子分子可以是单体或二聚体。在一些实施方案中,细胞因子分子可进一步包括细胞因子受体二聚化结构域。
在其他实施方案中,细胞因子分子是细胞因子受体的激动剂,例如,选自IL-15Ra或IL-21R的细胞因子受体的抗体分子(例如,激动性抗体)。
在一个实施方案中,细胞因子分子是IL-15,例如,人IL-15,例如,包含以下氨基酸序列:
NWVNVISDLKKIEDLIQSMHIDATLYTESDVHPSCKVTAMKCFLLELQVISLESGDASIHDTVENLIILANNSLSSNGNVTESGCKECEELEEKNIKEFLQSFVHIVQMFINTS(SEQ ID NO:6191)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6191的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,细胞因子分子包含受体二聚化结构域,例如,IL15Rα二聚化结构域。在一个实施方案中,IL15Rα二聚化结构域包含以下氨基酸序列:
MAPRRARGCRTLGLPALLLLLLLRPPATRGITCPPPMSVEHADIWVKSYSLYSRERYICNSGFKRKAGTSSLTECVL(SEQ ID NO:6192)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6192的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。在一些实施方案中,多特异性分子的细胞因子分子(例如,IL-15)和受体二聚化结构域(例如,IL15Rα二聚化结构域)例如经由接头(例如,Gly-Ser接头,例如,包含氨基酸序列
SGGSGGGGSGGGSGGGGSLQ(SEQ ID NO:6193)的接头)共价连接。在其他实施方案中,多特异性分子的细胞因子分子(例如,IL-15)和受体二聚化结构域(例如,IL15Rα二聚化结构域)不是共价连接的,例如,是非共价缔合的。
在其他实施方案中,细胞因子分子是IL-2,例如,人IL-2,例如,包含以下氨基酸序列:
APTSSSTKKTQLQLEHLLLDLQMILNGINNYKNPKLTRMLTFKFYMPKKATELKHLQCLEEELKPLEEVLNLAQSKNFHLRPRDLISNINVIVLELKGSETTFMCEYADETATIVEFLNRWITFCQSIISTLT(SEQ ID NO:6194)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6194的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,细胞因子分子是IL-18,例如,人IL-18,例如,包含以下氨基酸序列:YFGKLESKLSVIRNLNDQVLFIDQGNRPLFEDMTDSDCRDNAPRTIFIISMYKDSQPRGM
AVTISVKCEKISTLSCENKIISFKEMNPPDNIKDTKSDIIFFQRSVPGHDNKMQFESSSYEGYFLACEKERDLFKLILKKEDELGDRSIMFTVQNED(SEQ ID NO:6195)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6195的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,细胞因子分子是IL-21,例如,人IL-21,例如,包含以下氨基酸序列:
QGQDRHMIRMRQLIDIVDQLKNYVNDLVPEFLPAPEDVETNCEWSAFSCFQKAQLKSANTGNNERIINVSIKKLKRKPPSTNAGRRQKHRLTCPSCDSYEKKPPKEFLERFKSLLQKMIHQHLSSRTHGSEDS(SEQ ID NO:6196)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6196的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在其他实施方案中,细胞因子分子是干扰素γ,例如,人干扰素γ,例如,包含以下氨基酸序列:
QDPYVKEAENLKKYFNAGHSDVADNGTLFLGILKNWKEESDRKIMQSQIVSFYFKLFKNFKDDQSIQKSVETIKEDMNVKFFNSNKKKRDDFEKLTNYSVTDLNVQRKAIHELIQVMAELSPAAKTGKRKRSQMLFRG(SEQ IDNO:6197)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6197的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
TGF-β抑制剂
在一方面,本文提供了一种多特异性或多功能性多肽(例如,抗体分子),其包含TGF-β的调节剂(例如,TGF-β抑制剂)。在一些实施方案中,TGF-β抑制剂结合至并抑制TGF-β,例如,降低TGF-β的活性。在一些实施方案中,TGF-β抑制剂抑制TGF-β1(例如,降低其活性)。在一些实施方案中,TGF-β抑制剂抑制TGF-β2(例如,降低其活性)。在一些实施方案中,TGF-β抑制剂抑制TGF-β3(例如,降低其活性)。在一些实施方案中,TGF-β抑制剂抑制TGF-β1和TGF-β3(例如,降低其活性)。在一些实施方案中,TGF-β抑制剂抑制TGF-β1、TGF-β2和TGF-β3(例如,降低其活性)。
在一些实施方案中,TGF-β抑制剂包含TGF-β受体的一部分(例如,TGF-β受体的胞外结构域),其能够抑制TGF-β或其功能性片段或变体(例如,降低其活性)。在一些实施方案中,TGF-β抑制剂包含TGFBR1多肽(例如,TGFBR1的胞外结构域或其功能性变体)。在一些实施方案中,TGF-β抑制剂包含TGFBR2多肽(例如,TGFBR2的胞外结构域或其功能性变体)。在一些实施方案中,TGF-β抑制剂包含TGFBR3多肽(例如,TGFBR3的胞外结构域或其功能性变体)。在一些实施方案中,TGF-β抑制剂包含TGFBR1多肽(例如,TGFBR1的胞外结构域或其功能性变体)和TGFBR2多肽(例如,TGFBR2的胞外结构域或其功能性变体)。在一些实施方案中,TGF-β抑制剂包含TGFBR1多肽(例如,TGFBR1的胞外结构域或其功能性变体)和TGFBR3多肽(例如,TGFBR3的胞外结构域或其功能性变体)。在一些实施方案中,TGF-β抑制剂包含TGFBR2多肽(例如,TGFBR2的胞外结构域或其功能性变体)和TGFBR3多肽(例如,TGFBR3的胞外结构域或其功能性变体)。
可用作TGF-β抑制剂的示例性TGF-β受体多肽已公开于US 8993524、US 9676863、US 8658135、US 20150056199、US 20070184052和WO2017037634中,它们全部通过引用以其整体并入本文。
在一些实施方案中,TGF-β抑制剂包含TGFBR1的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6381的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6382的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6383的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6390的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6391的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。
在一些实施方案中,TGF-β抑制剂包含TGFBR2的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6384的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6385的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6386的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6387的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6388的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6389的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。
在一些实施方案中,TGF-β抑制剂包含TGFBR3的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6392的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6393的胞外结构域,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。在一些实施方案中,TGF-β抑制剂包含SEQ ID NO:6394的氨基酸序列,或与其基本上相同的序列(例如,与其至少80%、85%、90%或95%相同的序列)。
在一些实施方案中,TGF-β抑制剂包含不超过一个TGF-β受体胞外结构域。在一些实施方案中,TGF-β抑制剂包含两个或更多个(例如,两个、三个、四个、五个或更多个)例如经由接头连接在一起的TGF-β受体胞外结构域。
在一些实施方案中,多特异性分子包含图24A-24D中所示的构型。在一些实施方案中,TGFβ抑制剂包含TGF-β受体ECD同源二聚体。在一些实施方案中,TGFβ抑制剂包含TGF-β受体ECD异源二聚体。在一些实施方案中,两个TGFBR ECD结构域与两个Fc区(例如,两个Fc区的C-末端)连接。在一些实施方案中,两个TGFBR ECD结构域分别与CH1和CL连接。
表37.TGF-β多肽或TGF-β受体多肽的示例性氨基酸序列
基质修饰部分
实体瘤具有与正常组织相似的不同结构,并且包含两个不同但相互依赖的区室:赘生性细胞诱导的实质(赘生性细胞)和基质,它们分散于其中。所有肿瘤都具有基质,并且需要基质进行营养支持和去除废物。在作为细胞悬浮液生长的肿瘤(例如,白血病、腹水肿瘤)的情况下,血浆用作基质(Connolly JL等人,Tumor Structure and Tumor StromaGeneration.在:Kufe DW等编著的Holland-Frei Cancer Medicine.第6版.Hamilton:BCDecker;2003)。基质包括各种细胞类型,包括成纤维细胞/肌成纤维细胞、神经胶质细胞、上皮细胞、脂肪细胞、血管细胞、平滑肌细胞和免疫细胞,以及胞外基质(ECM)和胞外分子(LiHanchen等人,Tumor Microenvironment:The Role of the Tumor Stroma in Cancer.Jof Cellular Biochemistry 101:805-815(2007))。
本文所述的基质修饰部分包括能够降解基质组分的部分(例如,蛋白质,例如,酶),该基质组分例如ECM组分,例如,糖胺聚糖,例如,透明质酸(也称为玻尿酸或HA)、硫酸软骨素、软骨素、硫酸皮肤素、硫酸肝素、肝素、巢蛋白、腱生蛋白、聚集蛋白聚糖和硫酸角蛋白;或胞外蛋白,例如,胶原、层粘连蛋白、弹性蛋白、纤维蛋白原、纤连蛋白和玻连蛋白。
基质修饰酶
在一些实施方案中,基质修饰部分是酶。例如,基质修饰部分可以包括但不限于透明质酸酶、胶原酶、软骨素酶、基质金属蛋白酶(例如,巨噬细胞金属弹性蛋白酶)。
透明质酸酶
透明质酸酶是在整个动物界发现的一组中性和酸活性酶。透明质酸酶在底物特异性和作用机制方面不同。透明质酸酶有三大类:(1)哺乳动物型透明质酸酶(EC 3.2.1.35),其是以四糖和六糖为主要终产物的内切-β-N-乙酰己糖胺酶。它们具有水解和转糖苷酶活性,并且可以降解透明质酸和硫酸软骨素;(2)细菌透明质酸酶(EC 4.2.99.1)降解透明质酸,并在不同程度上降解硫酸软骨素和硫酸皮肤素。它们是内切-β-N-乙酰己糖胺酶,其通过β消除反应来操作,主要产生二糖终产物;(3)来自水蛭、其他寄生虫和甲壳类的透明质酸酶(EC 3.2.1.36)是内切-β-葡萄糖醛酸酶,其通过β1-3键的水解生成四糖和六糖终产物。
哺乳动物透明质酸酶可进一步分为两组:(1)中性活性酶和(2)酸活性酶。人基因组中有六种透明质酸酶样基因:HYAL1、HYAL2、HYAL3、HYAL4、HYALP1和PH20/SPAM1。HYALP1是假基因,HYAL3未显示出针对任何已知底物具有酶活性。HYAL4是软骨素酶,并且缺乏针对透明质酸的活性。HYAL1是原型酸活性酶,PH20是原型中性活性酶。酸活性透明质酸酶(例如HYAL1和HYAL2)在中性pH下缺乏催化活性。例如,HYAL1在体外pH超过4.5时无催化活性(Frost和Stern,“A Microtiter-Based Assay for Hyaluronidase Activity NotRequiring Specialized Reagents”,Analytical Biochemistry,第251卷,第263-269页(1997))。HYAL2是体外比活性非常低的酸活性酶。
在一些实施方案中,透明质酸酶是哺乳动物透明质酸酶。在一些实施方案中,透明质酸酶是重组人透明质酸酶。在一些实施方案中,透明质酸酶是中性活性透明质酸酶。在一些实施方案中,透明质酸酶是中性活性可溶性透明质酸酶。在一些实施方案中,透明质酸酶是重组PH20中性活性酶。在一些实施方案中,透明质酸酶是重组PH20中性活性可溶性酶。在一些实施方案中,透明质酸酶是糖基化的。在一些实施方案中,透明质酸酶具有至少一个N-连接的聚糖。可以使用本领域技术人员已知的常规方法来产生重组透明质酸酶,例如,US7767429,其全部内容通过引用并入本文。
在一些实施方案中,透明质酸酶是rHuPH20(也称为目前由Halozyme制造;2005年被FDA批准(参见例如,Scodeller P(2014)Hyaluronidase and otherExtracellular Matrix Degrading Enzymes for Cancer Therapy:New Uses and Nano-Formulations.J Carcinog Mutage 5:178;US 7767429;US 8202517;US 7431380;US8450470;US 8772246;US 8580252,其中每一个的全部内容通过引用并入本文)。rHuPH20由含有编码人透明质酸酶PH20可溶性片段的DNA质粒的遗传工程化CHO细胞产生。在一些实施方案中,透明质酸酶是糖基化的。在一些实施方案中,透明质酸酶具有至少一个N-连接的聚糖。可以使用本领域技术人员已知的常规方法来产生重组透明质酸酶,例如,US 7767429,其全部内容通过引用并入本文。在一些实施方案中,rHuPH20具有与LNFRAPPVIPNVPFLWAWNAPSEFCLGKFDEPLDMSLFSFIGSPRINATGQGVTIFYVDRLGYYPYIDSITGVTVNGGIPQKISLQDHLDKAKKDITFYMPVDNLGMAVIDWEEWRPTWARNWKPKDVYKNRSIELVQQQNVQLSLTEATEKAKQEFEKAGKDFLVETIKLGKLLRPNHLWGYYLFPDCYNHHYKKPGYNGSCFNVEIKRNDDLSWLWNESTALYPSIYLNTQQSPVAATLYVRNRVREAIRVSKIPDAKSPLPVFAYTRIVFTDQVLKFLSQDELVYTFGETVALGASGIVIWGTLSIMRSMKSCLLLDNYMETILNPYIINVTLAAKMCSQVLCQEQGVCIRKNWNSSDYLHLNPDNFAIQLEKGGKFTVRGKPTLEDLEQFSEKFYCSCYSTLSCKEKADVKDTDAVDVCIADGVCIDAFLKPPMETEEPQIFYNASPSTLS(SEQ ID NO:6213)的氨基酸序列至少95%(例如,至少96%、97%、98%、99%、100%)相同的序列。
在本文提供的方法中的任一种中,抗透明质酸剂可以是降解透明质酸的药剂,或者可以是抑制透明质酸合成的药剂。例如,抗透明质酸剂可以是透明质酸降解酶。在另一实例中,抗透明质酸剂是抑制透明质酸合成的药剂。例如,抗透明质酸剂是抑制透明质酸合成的药剂,例如针对HA合酶的有义或反义核酸分子,或是小分子药物。例如,抗透明质酸剂是4-甲基伞形酮(MU)或其衍生物,或来氟米特或其衍生物。这种衍生物包括例如4-甲基伞形酮(MU)的衍生物,即6,7-二羟基-4-甲基香豆素或5,7-二羟基-4-甲基香豆素。
在本文提供的方法的进一步实例中,透明质酸降解酶是透明质酸酶。在一些实例中,透明质酸降解酶是PH20透明质酸酶或其缺少C-末端糖基磷脂酰肌醇(GPI)附着位点或GPI附着位点的一部分的截短形式。在具体实例中,透明质酸酶是选自人、猴、牛、绵羊、大鼠、小鼠或豚鼠PH20的PH20。例如,透明质酸降解酶是中性活性和N-糖基化的人PH20透明质酸酶,并且选自(a)透明质酸酶多肽,其是全长PH20或PH20的C-末端截短形式,其中截短形式至少包括SEQ ID NO:6213的36-464位(例如36-481位、36-482位、36-483位)氨基酸残基,其中全长PH20具有SEQ ID NO:6213中所述的氨基酸序列;或(b)透明质酸酶多肽,其包含与SEQ ID NO:6213中所述的多肽或氨基酸序列的截短形式具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多序列同一性的氨基酸序列;或(c)包含氨基酸置换的(a)或(b)的透明质酸酶多肽,其中透明质酸酶多肽具有与SEQ ID NO:6213中所述的多肽或其相应截短形式具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多序列同一性的氨基酸序列。在示例性实例中,透明质酸降解酶是包含称为rHuPH20的组合物的PH20。
在其他实例中,抗透明质酸剂是通过与聚合物缀合而被修饰的透明质酸降解酶。聚合物可以是PEG,抗透明质酸剂可以是PEG化的透明质酸降解酶。因此,在本文提供的方法的一些实例中,透明质酸降解酶通过与聚合物缀合而被修饰。例如,透明质酸降解酶与PEG缀合,因此透明质酸降解酶是PEG化的。在示例性实例中,透明质酸降解酶是PEG化的PH20酶(PEGPH20)。在本文提供的方法中,皮质类固醇可以是糖皮质激素,其选自可的松、地塞米松、氢化可的松、甲基泼尼松龙、泼尼松龙和强的松。
软骨素酶
软骨素酶是在整个动物界发现的酶,其通过内切糖苷酶反应降解糖胺聚糖,特别是软骨素和硫酸软骨素。在一些实施方案中,软骨素酶是哺乳动物软骨素酶。在一些实施方案中,软骨素酶是重组人软骨素酶。在一些实施方案中,软骨素酶是HYAL4。其他示例性软骨素酶包括软骨素酶ABC(来源于普通变形杆菌(Proteus vulgaris);日本专利申请公开第6-153947号、T.Yamagata等人,J.Biol.Chem.,243,1523(1968)、S.Suzuki等人,J.Biol.Chem.,243,1543(1968))、软骨素酶AC(来源于肝素黄杆菌(Flavobacteriumheparinum);T.Yamagata等人,J.Biol.Chem.,243,1523(1968))、软骨素酶AC II(来源于金黄节杆菌(Arthrobacter aurescens);K.Hiyama和S.Okada,J.Biol.Chem.,250,1824(1975)、K.Hiyama和S.Okada,J.Biochem.(Tokyo),80,1201(1976))、透明质酸酶ACIII(来源于黄杆菌Hp102(Flavobacterium sp.Hp102);Hirofumi Miyazono等人,Seikagaku,61,1023(1989))、软骨素酶B(来源于肝素黄杆菌;Y.M.Michelacci和C.P.Dietrich,Biochem.Biophys.Res.Commun.,56,973(1974)、Y.M.Michelacci和C.P.Dietrich,Biochem.J.,151,121(1975)、Kenichi Maeyama等人,Seikagaku,57,1189(1985))、软骨素酶C(来源于黄杆菌Hp102;Hirofumi Miyazono等人,Seikagaku,61,1023(1939))等。
基质金属蛋白酶
基质金属蛋白酶(MMP)是锌依赖性内肽酶,其是参与胞外基质(ECM)降解的主要蛋白酶。MMP能够降解多种胞外分子和许多生物活性分子。人中已鉴定了24种MMP基因,其可以基于结构域组织和底物偏好组织化为六组:胶原酶(MMP-1、-8和-13)、明胶酶(MMP-2和MMP-9)、基质溶素(MMP-3、-10和-11)、基质溶解因子(MMP-7和MMP-26)、膜型(MT)-MMP(MMP-14、-15、-16、-17、-24和-25)和其他(MMP-12、-19、-20、-21、-23、-27和-28)。在一些实施方案中,基质修饰部分是人重组MMP(例如,MMP-1、-2、-3、-4、-5、-6、-7、-8、-9、10、-11、-12、-13、-14、15、-15、-17、-18、-19、20、-21、-22、-23或-24)。
胶原酶
三种哺乳动物胶原酶(MMP-1、-8和-13)是能够切割胶原性胞外基质的主要分泌型内肽酶。除原纤维胶原以外,胶原酶可以切割几种其他基质和非基质蛋白,包括生长因子。胶原酶以无活性的前体形式合成,一旦被激活,它们的活性就会被金属蛋白酶的特异性组织抑制剂TIMP以及非特异性蛋白酶抑制剂抑制(Ala-aho R等人,Biochimie.Collagenasesin cancer.2005年3月-4月;87(3-4):273-86)。在一些实施方案中,基质修饰部分是胶原酶。在一些实施方案中,胶原酶是人重组胶原酶。在一些实施方案中,胶原酶是MMP-1。在一些实施方案中,胶原酶是MMP-8。在一些实施方案中,胶原酶是MMP-13。
巨噬细胞金属弹性蛋白酶
巨噬细胞金属弹性蛋白酶(MME,也称为MMP-12)是MMP基质溶素亚群的成员,并且催化可溶性和不溶性弹性蛋白以及多种基质和非基质底物的水解,包括IV型胶原、纤连蛋白、层粘连蛋白、玻连蛋白、巢蛋白、乙酰肝素和硫酸软骨素(Erja 等人,Journalof Investigative Dermatology(2000)114,1113-1119;doi:10.1046/j.1523-1747.2000.00993)。在一些实施方案中,基质修饰部分是MME。在一些实施方案中,MME是人重组MME。在一些实施方案中,MME是MMP-12。
另外的基质修饰部分
在一些实施方案中,基质修饰部分导致以下中的一种或多种:减少基质或胞外基质(ECM)组分的水平或产生;减少肿瘤纤维化;增加间质肿瘤转运;改善肿瘤灌注;扩张肿瘤微脉管系统;降低肿瘤中的间质液压力(IFP);或者减少或增强药剂(例如,癌症治疗剂或细胞疗法)进入肿瘤或肿瘤脉管系统的渗透或扩散。
在一些实施方案中,减少的基质或ECM组分选自糖胺聚糖或胞外蛋白,或其组合。在一些实施方案中,糖胺聚糖选自透明质酸(也称为玻尿酸或HA)、硫酸软骨素、软骨素、硫酸皮肤素、肝素、硫酸肝素、巢蛋白、腱生蛋白、聚集蛋白聚糖和硫酸角蛋白。在一些实施方案中,胞外蛋白选自胶原、层粘连蛋白、弹性蛋白、纤维蛋白原、纤连蛋白或玻连蛋白。在一些实施方案中,基质修饰部分包括降解肿瘤基质或胞外基质(ECM)的酶分子。在一些实施方案中,酶分子选自透明质酸酶分子、胶原酶分子、软骨素酶分子、基质金属蛋白酶分子(例如,巨噬细胞金属弹性蛋白酶),或上述中任一种的变体(例如,片段)。术语“酶分子”包括酶的全长、片段或变体,例如,保留天然存在的酶的至少一个功能特性的酶变体。
在一些实施方案中,基质修饰部分减少玻尿酸的水平或产生。在其他实施方案中,基质修饰部分包含透明质酸降解酶、抑制透明质酸合成的药剂,或针对玻尿酸的抗体分子。
在一些实施方案中,透明质酸降解酶是透明质酸酶分子,例如,其全长或变体(例如,其片段)。在一些实施方案中,透明质酸降解酶在中性或酸性pH(例如,约pH 4-5)中具有活性。在一些实施方案中,透明质酸酶分子是哺乳动物透明质酸酶分子,例如,重组人透明质酸酶分子,例如,其全长或变体(例如,其片段,例如,截短形式)。在一些实施方案中,透明质酸酶分子选自HYAL1、HYAL2或PH-20/SPAM1,或其变体(例如,其截短形式)。在一些实施方案中,截短形式缺少C-末端糖基磷脂酰肌醇(GPI)附着位点或GPI附着位点的一部分。在一些实施方案中,透明质酸酶分子是糖基化的,例如,包含至少一个N-连接的聚糖。
在一些实施方案中,透明质酸酶分子包含以下氨基酸序列:LNFRAPPVIPNVPFLWAWNAPSEFCLGKFDEPLDMSLFSFIGSPRINATGQGVTIFYVDRLGYYPYIDSITGVTVNGGIPQKISLQDHLDKAKKDITFYMPVDNLGMAVIDWEEWRPTWARNWKPKDVYKNRSIELVQQQNVQLSLTEATEKAKQEFEKAGKDFLVETIKLGKLLRPNHLWGYYLFPD CYNHHYKKPGYNGSCFNVEIKRNDDLSWLWNESTALYPSIYLNTQQSPVAATLYVRNRVREAIRVSKIPDAKSPLPVFAYTRIVFTDQVLKFLSQDELVYTFGETVALGASGIVIWGTLSIMRSMKSCLLLDNYMETILNPYIINVTLAAKMCSQVLCQEQGVCIRKNWNSSDYLHLNPDNFAIQLEKGGKFTVRGKPTLEDLEQFSEKFYCSCYSTLSCKEKADVKDTDAVDVCIADGVCIDAFLKPPMETEEPQIFYNASPSTLS(SEQ ID NO:6213)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于
SEQ ID NO:6213的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,透明质酸酶分子包含:
(i)SEQ ID NO:6213的36-464位氨基酸序列;
(ii)PH20的36-481位、36-482位或36-483位氨基酸序列,其中PH20具有SEQ IDNO:6213中所述的氨基酸序列;或
(iii)与SEQ ID NO:6213中所述的多肽或氨基酸序列的截短形式具有至少95%至100%序列同一性的氨基酸序列;或
(iv)对于SEQ ID NO:6213中所述的氨基酸序列具有30、20、10、5或更少个氨基酸置换的氨基酸序列。在一些实施方案中,透明质酸酶分子包含与SEQ ID NO:6213的氨基酸序列至少95%(例如,至少95%、96%、97%、98%、99%、100%)相同的氨基酸序列。在一些实施方案中,透明质酸酶分子由与SEQ ID NO:6213的核苷酸序列至少95%(例如,至少96%、97%、98%、99%、100%)相同的核苷酸序列编码。
在一些实施方案中,透明质酸酶分子是PH20,例如,rHuPH20。在一些实施方案中,透明质酸酶分子是HYAL1,并且包含以下氨基酸序列:
FRGPLLPNRPFTTVWNANTQWCLERHGVDVDVSVFDVVANPGQTFRGPDMTIFYSSQGTYPYYTPTGEPVFGGLPQNASLIAHLARTFQDILAAIPAPDFSGLAVIDWEAWRPRWAFNWDTKDIYRQRSRALVQAQHPDWPAPQVEAVAQDQFQGAARAWMAGTLQLGRALRPRGLWGFYGFPDCYNYDFLSPNYTGQCPSGIRAQNDQLGWLWGQSRALYPSIYMPAVLEGTGKSQMYVQHRVAEAFRVAVAAGDPNLPVLPYVQIFYDTTNHFLPLDELEHSLGESAAQGAAGVVLWVSWENTRTKESCQAIKEYMDTTLGPFILNVTSGALLCSQALCSGHGRCVRRTSHPKALLLLNPASFSIQLTPGGGPLSLRGALSLEDQAQMAVEFKCRCYPGWQAPWCERKSMW(SEQ ID NO:6218)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6218的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)进一步包含聚合物,例如,与聚合物(例如,PEG)缀合。在一些实施方案中,透明质酸降解酶是PEG化的PH20酶(PEGPH20)。在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)进一步包含免疫球蛋白链恒定区(例如,Fc区),其选自例如IgG1、IgG2、IgG3和IgG4的重链恒定区,更特别是人IgG1、IgG2、IgG3或IgG4的重链恒定区。在一些实施方案中,免疫球蛋白恒定区(例如,Fc区)与透明质酸降解酶(例如,透明质酸酶分子)连接,例如,共价连接。在一些实施方案中,免疫球蛋白链恒定区(例如,Fc区)被改变(例如,突变),以增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能。在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)形成二聚体。
在一些实施方案中,基质修饰部分包含透明质酸合成的抑制剂,例如,HA合酶。在一些实施方案中,抑制剂包含针对HA合酶的有义或反义核酸分子,或是小分子药物。在一些实施方案中,抑制剂是4-甲基伞形酮(MU)或其衍生物(例如,6,7-二羟基-4-甲基香豆素或5,7-二羟基-4-甲基香豆素),或来氟米特或其衍生物。
在一些实施方案中,基质修饰部分包含针对玻尿酸的抗体分子。
在一些实施方案中,基质修饰部分包含胶原酶分子(例如,哺乳动物胶原酶分子),或其变体(例如,片段)。在一些实施方案中,胶原酶分子是胶原酶分子IV,例如,包含以下氨基酸序列:YNFFPRKPKWDKNQITYRIIGYTPDLDPETVDDAFARAFQVWSDVTPLRFSRIHDGEADIMINFGRWEHGDGYPFDGKDGLLAHAFAPGTGVGGDSHFDDDELWTLGEGQVVRVKYGNADGEYCKFPFLFNGKEYNSCTDTGRSDGFLWCSTTYNFEKDGKYGFCPHEALFTMGGNAEGQPCKFPFRFQGTSYDSCTTEGRTDGYRWCGTTEDYDRDKKYGFCPETAMSTVGGNSEGAPCVFPFTFLGNKYESCTSAGRSDGKMWCATTANYDDDRKWGFCPDQGYSLFLVAAHEFGHAMGLEHSQDPGALMAPIYTYTKNFRLSQDDIKGIQELYGASPDIDLGTGPTPTLGPVTPEICKQDIVFDGIAQIRGEIFFFKDRFIWRTVTPRDKPMGPLLVATFWPELPEKIDAVYEAPQEEKAVFFAGNEYWIYSASTLERGYPKPLTSLGLPPDVQRVDAAFNWSKNKKTYIFAGDKFWRYNEVKKKMDPGFPKLIADAWNAIPDNLDAVVDLQGGGHSYFFKGAYYLKLENQSLKSVKFGSIKSDWLGC(SEQ ID NO:6219)、其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6219的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
靶向部分
在一些实施方案中,本文公开的多特异性和/或多功能性分子包含肿瘤靶向部分。在一些实施方案中,肿瘤靶向部分靶向(例如,结合至)选自以下的肿瘤抗原:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。在一些实施方案中,肿瘤靶向部分靶向(例如,结合至)G6B。
G6B是指MPIG6B,也称为巨核细胞和血小板抑制性受体G6b或C6orf25。Swiss-Prot登录号O95866提供了示例性人G6B氨基酸序列。在一些实施方案中,G6B或G6B分子是天然存在的G6B或其功能性变体或片段。
CD34是指造血祖细胞抗原CD34。Swiss-Prot登录号P28906提供了示例性人CD34氨基酸序列。在一些实施方案中,CD34或CD34分子是天然存在的CD34或其功能性变体或片段。
CD41是指ITGA2B,也称为整合素α-IIb。Swiss-Prot登录号P08514提供了示例性人CD41氨基酸序列。在一些实施方案中,CD41或CD41分子是天然存在的CD41或其功能性变体或片段。
P-选择素是指SELP,也称为CD62P、GMP-140或LECAM3。Swiss-Prot登录号P16109提供了示例性人P-选择素氨基酸序列。在一些实施方案中,P-选择素或P-选择素分子是天然存在的P-选择素或其功能性变体或片段。
Clec2是指CLEC1B,也称为C型凝集素结构域家族1成员B。Swiss-Prot登录号Q9P126提供了示例性人Clec2氨基酸序列。在一些实施方案中,Clec2或Clec2分子是天然存在的Clec2或其功能性变体或片段。
cKIT是指肥大细胞/干细胞生长因子受体kit,也称为CD117。Swiss-Prot登录号P10721提供了示例性人cKIT氨基酸序列。在一些实施方案中,cKIT或cKIT分子是天然存在的cKIT或其功能性变体或片段。
FLT3是指受体型酪氨酸-蛋白激酶FLT3,也称为CD135。Swiss-Prot登录号P36888提供了示例性人FLT3氨基酸序列。在一些实施方案中,FLT3或FLT3分子是天然存在的FLT3或其功能性变体或片段。
MPL是指血小板生成素受体,也称为CD110。Swiss-Prot登录号P40238提供了示例性人MPL氨基酸序列。在一些实施方案中,MPL或MPL分子是天然存在的MPL或其功能性变体或片段。
ITGB3是指整合素β-3,也称为CD61。Swiss-Prot登录号P05106提供了示例性人ITGB3氨基酸序列。在一些实施方案中,ITGB3或ITGB3分子是天然存在的ITGB3或其功能性变体或片段。
ITGB2是指整合素β-2,也称为CD18。Swiss-Prot登录号P05107提供了示例性人ITGB2氨基酸序列。在一些实施方案中,ITGB2或ITGB2分子是天然存在的ITGB2或其功能性变体或片段。
GP5是指血小板糖蛋白V,也称为CD42d。Swiss-Prot登录号P40197提供了示例性人GP5氨基酸序列。在一些实施方案中,GP5或GP5分子是天然存在的GP5或其功能性变体或片段。
GP6是指血小板糖蛋白VI。Swiss-Prot登录号Q9HCN6提供了示例性人GP6氨基酸序列。在一些实施方案中,GP6或GP6分子是天然存在的GP6或其功能性变体或片段。
GP9是指血小板糖蛋白IX,也称为CD42a。Swiss-Prot登录号P14770提供了示例性人GP9氨基酸序列。在一些实施方案中,GP9或GP9分子是天然存在的GP9或其功能性变体或片段。
GP1BA是指血小板糖蛋白Ibα链,也称为CD42b。Swiss-Prot登录号P07359提供了示例性人GP1BA氨基酸序列。在一些实施方案中,GP1BA或GP1BA分子是天然存在的GP1BA或其功能性变体或片段。
DSC2是指桥粒芯胶蛋白-2,也称为钙粘蛋白家族成员2。Swiss-Prot登录号Q02487提供了示例性人DSC2氨基酸序列。在一些实施方案中,DSC2或DSC2分子是天然存在的DSC2或其功能性变体或片段。
FCGR2A指Fc-γ-RIIa,也称为CD32。Swiss-Prot登录号P12318提供了示例性人FCGR2A氨基酸序列。在一些实施方案中,FCGR2A或FCGR2A分子是天然存在的FCGR2A或其功能性变体或片段。
TNFRSF10A是指肿瘤坏死因子受体超家族成员10A,也称为死亡受体4、TNF相关凋亡诱导配体受体1、TRAIL-R1或CD261。Swiss-Prot登录号O00220提供了示例性人TNFRSF10A氨基酸序列。在一些实施方案中,TNFRSF10A或TNFRSF10A分子是天然存在的TNFRSF10A或其功能性变体或片段。
TNFRSF10B是指肿瘤坏死因子受体超家族成员10B,也称为死亡受体5、TNF相关凋亡诱导配体受体2、TRAIL-R2或CD262。Swiss-Prot登录号O14763提供了示例性人TNFRSF10B氨基酸序列。在一些实施方案中,TNFRSF10B或TNFRSF10B分子是天然存在的TNFRSF10B或其功能性变体或片段。
TM4SF1是指跨膜4L6家族成员1。Swiss-Prot登录号P30408提供了示例性人TM4SF1氨基酸序列。在一些实施方案中,TM4SF1或TM4SF1分子是天然存在的TM4SF1或其功能性变体或片段。
在一些实施方案中,多特异性和/或多功能性分子包含一个或多个另外的肿瘤靶向部分。在一些实施方案中,一个或多个另外的肿瘤靶向部分靶向(例如,结合至)与第一肿瘤靶向部分相同的肿瘤抗原。在一些实施方案中,一个或多个另外的肿瘤靶向部分靶向(例如,结合至)与第一肿瘤靶向部分不同的肿瘤抗原。在一些实施方案中,多特异性和/或多功能性分子包含靶向存在于同一细胞(例如,肿瘤细胞)上的不同肿瘤抗原的多个肿瘤靶向部分。在一些实施方案中,多特异性和/或多功能性分子包含靶向存在于不同细胞(例如,2、3、4、5、6、7、8、9、10或更多个不同肿瘤细胞)上的不同肿瘤抗原的多个肿瘤靶向部分。在一些实施方案中,肿瘤抗原中的每一种选自:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一些实施方案中,多特异性和/或多功能性分子包含第一肿瘤靶向部分(例如,靶向第一肿瘤抗原)和第二肿瘤靶向部分(例如,靶向第二肿瘤抗原)。在一些实施方案中,第一和第二肿瘤抗原存在于同一肿瘤细胞上。在一些实施方案中,第一和第三肿瘤抗原存在于同一肿瘤细胞上。在一些实施方案中,第二和第三肿瘤抗原存在于同一肿瘤细胞上。在一些实施方案中,第一、第二和第三肿瘤抗原存在于同一肿瘤细胞上。在一些实施方案中,第一和第二肿瘤抗原存在于不同肿瘤细胞上。在一些实施方案中,第一和第三肿瘤抗原存在于不同肿瘤细胞上。在一些实施方案中,第二和第三肿瘤抗原存在于不同肿瘤细胞上。在一些实施方案中,第一、第二和第三肿瘤抗原存在于不同肿瘤细胞上。
在一些实施方案中,第一、第二和/或第三肿瘤抗原在肿瘤细胞(例如,骨髓增生性赘生物细胞)中显示出比非肿瘤细胞更高的表达。在一些实施方案中,第一、第二和/或第三肿瘤抗原在肿瘤细胞(例如,骨髓增生性赘生物细胞)中的表达比第一、第二和/或第三肿瘤抗原在非肿瘤细胞中的表达高至少1.5、2、4、6、8或10倍。在一些实施方案中,多功能性分子优先结合至肿瘤细胞(例如,骨髓增生性赘生物细胞)而不是非肿瘤细胞。在一些实施方案中,多功能性分子与肿瘤细胞(例如,骨髓增生性赘生物细胞)之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。在一些实施方案中,第一和第二肿瘤靶向部分对肿瘤细胞(例如,骨髓增生性赘生物细胞)的亲和力(例如,组合亲和力)大于仅具有第一肿瘤靶向部分或第二肿瘤靶向部分中的一个的相似多功能性分子的亲和力。在一些实施方案中,第一和第二肿瘤靶向部分对肿瘤细胞(例如,骨髓增生性赘生物细胞)的亲和力(例如,组合亲和力)比仅具有第一肿瘤靶向部分或第二肿瘤靶向部分中的一个的相似多功能性分子的亲和力大至少2、5、10、20、30、40、50、75或100倍。
在一些实施方案中,第一、第二和第三肿瘤靶向部分对肿瘤细胞(例如,骨髓增生性赘生物细胞)的亲和力(例如,组合亲和力)大于仅具有第一肿瘤靶向部分、第二肿瘤靶向部分或第三肿瘤靶向部分中的一个的相似多功能性分子或仅具有第一肿瘤靶向部分、第二肿瘤靶向部分或第三肿瘤靶向部分中的两个的相似多功能性分子的亲和力。在一些实施方案中,第一、第二和第三肿瘤靶向部分对肿瘤细胞(例如,骨髓增生性赘生物细胞)的亲和力(例如,组合亲和力)比仅具有第一肿瘤靶向部分、第二肿瘤靶向部分或第三肿瘤靶向部分中的一个的相似多功能性分子或仅具有第一肿瘤靶向部分、第二肿瘤靶向部分或第三肿瘤靶向部分中的两个的相似多功能性分子的亲和力大至少2、5、10、20、30、40、50、75或100倍。
在一些实施方案中,第一肿瘤靶向部分和第二肿瘤靶向部分对第一和第二肿瘤抗原的亲和力(例如,组合亲和力)等于或大于(iii)、(iv)或(v)单独或作为多功能性分子的一部分对其相应结合成员的亲和力。在一些实施方案中,第一肿瘤靶向部分和第二肿瘤靶向部分对第一和第二肿瘤抗原的亲和力(例如,组合亲和力)比(iii)、(iv)或(v)单独或作为多功能性分子的一部分对其相应结合成员的亲和力大至少2、5、10、20、30、40、50、75或100倍。
在一些实施方案中,第一肿瘤靶向部分、第二肿瘤靶向部分和第三肿瘤靶向部分对第一、第二和第三肿瘤抗原的亲和力(例如,组合亲和力)等于或大于(iii)、(iv)或(v)单独或作为多功能性分子的一部分对其相应结合成员的亲和力。在一些实施方案中,第一肿瘤靶向部分、第二肿瘤靶向部分和第三肿瘤靶向部分对第一、第二和第三肿瘤抗原的亲和力(例如,组合亲和力)比(iii)、(iv)或(v)单独或作为多功能性分子的一部分对其相应结合成员的亲和力大至少2、5、10、20、30、40、50、75或100倍。
在上述方面的一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是CD41,并且第三肿瘤抗原是G6B。
在上述方面的一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是CD41,并且第三肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是G6B,并且第三肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD41,第二肿瘤抗原是G6B,并且第三肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是CD41,并且第三肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是G6B,并且第三肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD41,第二肿瘤抗原是G6B,并且第三肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD34,第二肿瘤抗原是P-选择素,并且第三肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD41,第二肿瘤抗原是P-选择素,并且第三肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是G6B,第二肿瘤抗原是P-选择素,并且第三肿瘤抗原是Clec2。
在上述方面的一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是CD34,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是CD41,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是G6B,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是P-选择素,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是Clec2,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是cKIT,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是FLT3,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是MPL,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是ITGB3,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是ITGB2,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是GP5,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是GP6,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是GP9,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是GP1BA,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是DSC2,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是FCGR2A,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是TNFRSF10A,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是TNFRSF10B,并且第二肿瘤抗原是TM4SF1。
在上述方面的一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是CD34。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是CD41。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是G6B。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是P-选择素。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是Clec2。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是cKIT。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是FLT3。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是MPL。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是ITGB3。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是ITGB2。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是GP5。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是GP6。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是GP9。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是GP1BA。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是DSC2。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是FCGR2A。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是TNFRSF10A。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是TNFRSF10B。在一些实施方案中,第一肿瘤抗原是TM4SF1,并且第二肿瘤抗原是TM4SF1。
靶向肿瘤抗原的抗体分子
在一些实施方案中,肿瘤靶向部分包含表38中所示的CDR、框架区或可变区序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
表38.能够结合至示例性靶分子的示例性抗体的序列
在一些实施方案中,第一、第二或第三肿瘤抗原是CD34。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2001的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2001的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2002的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2002的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,其中第一、第二或第三肿瘤抗原是CD41。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2007的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2007的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2008的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2008的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是P-选择素。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2013的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2013的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2014的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2014的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是cKIT。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2003的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2003的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2004的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2004的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是FLT3。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2005的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2005的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2006的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2006的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是MPL。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)(a)来自SEQ ID NO:2009的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2009的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2010的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2010的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);或
(ii)(a)来自SEQ ID NO:2011的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2011的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2012的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2012的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是DSC2。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)(a)来自SEQ ID NO:2015的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2015的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2016的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2016的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);或
(ii)(a)来自SEQ ID NO:2017的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2017的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2018的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2018的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是FCGR2A。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)(a)来自SEQ ID NO:2019的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2019的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2020的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2020的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);
(ii)(a)来自SEQ ID NO:2021的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2021的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2022的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2022的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),或
(iii)(a)来自SEQ ID NO:2023的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2023的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2024的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2024的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是TNFRSF10A或TNFRSF10B。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)(a)来自SEQ ID NO:2025的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2025的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2026的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2026的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);或
(ii)(a)来自SEQ ID NO:2027的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2027的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2028的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2028的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);
(iii)(a)来自SEQ ID NO:2029的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2029的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2030的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2030的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);
(ii)(a)来自SEQ ID NO:2031的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2031的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2032的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2032的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列);或
(v)(a)来自SEQ ID NO:2033的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(b)SEQ ID NO:2033的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(c)来自SEQ ID NO:2034的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(d)SEQ ID NO:2034的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,第一、第二或第三肿瘤抗原是TM4SF1。在一些实施方案中,第一、第二或第三肿瘤靶向部分包含:
(i)来自SEQ ID NO:2035的HCDR1、HCDR2和/或HCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),
(ii)SEQ ID NO:2035的VH(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列),
(iii)来自SEQ ID NO:2036的LCDR1、LCDR2和/或LCDR3(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(iv)SEQ ID NO:2036的VL(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
示例性抗CD34抗体序列
在一方面,本文提供了一种多特异性或多功能性分子,其包含肿瘤靶向部分,该肿瘤靶向部分包含CD34靶向部分。在另一方面,本文提供了一种抗CD34抗体分子(例如,单克隆抗CD34抗体分子)。
在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含表20或表21中公开的抗体或其抗原结合片段。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含表20或表21中公开的CDR、框架区或可变区序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的序列)。
在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH,该VH包含SEQ IDNO:6239的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6241的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6243的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH,该VH包含SEQ ID NO:6239的VHCDR1氨基酸序列、SEQ IDNO:6241的VHCDR2氨基酸序列,和/或SEQ ID NO:6243的VHCDR3氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VL,该VL包含SEQ ID NO:6245的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:1236的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6246的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VL,该VL包含SEQ ID NO:6245的VLCDR1氨基酸序列、SEQ ID NO:1236的VLCDR2氨基酸序列,以及SEQ ID NO:6246的VLCDR3氨基酸序列。
在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH,该VH包含SEQ IDNO:79、6225、6227或6229的氨基酸序列,或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VL,该VL包含SEQ ID NO:6231、6233、6235或6237的氨基酸序列,或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:79的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6231的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:79的氨基酸序列,该VL包含SEQ ID NO:6231的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6225的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6231的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:6225的氨基酸序列,该VL包含SEQ ID NO:6231的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6227的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6231的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:6227的氨基酸序列,该VL包含SEQ ID NO:6231的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6229的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6231的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:6229的氨基酸序列,该VL包含SEQ ID NO:6231的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:79的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6233的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:79的氨基酸序列,该VL包含SEQ ID NO:6233的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6225的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6233的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:6225的氨基酸序列,该VL包含SEQ ID NO:6233的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6227的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6233的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ ID NO:6227的氨基酸序列,该VL包含SEQ ID NO:6233的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6229的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6233的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQ IDNO:6229的氨基酸序列,该VL包含SEQ ID NO:6233的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:79的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:79的氨基酸序列,该VL包含SEQ ID NO:6235的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6225的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6225的氨基酸序列,该VL包含SEQ ID NO:6235的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6227的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ IDNO:6235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6227的氨基酸序列,该VL包含SEQ ID NO:6235的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6229的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ IDNO:6235的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6229的氨基酸序列,该VL包含SEQ ID NO:6235的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:79的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ IDNO:6237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:79的氨基酸序列,该VL包含SEQ ID NO:6237的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6225的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:6237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6225的氨基酸序列,该VL包含SEQ ID NO:6237的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6227的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ IDNO:6237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6227的氨基酸序列,该VL包含SEQ ID NO:6237的氨基酸序列。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和VL,该VH包含SEQ ID NO:6229的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ IDNO:6237的氨基酸序列(或与其具有至少约80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:6229的氨基酸序列,该VL包含SEQ ID NO:6237的氨基酸序列。
在一些实施方案中,CD34靶向部分或抗CD34抗体分子包含VH和或VL,该VH包含SEQID NO:79的氨基酸序列,该VL包含SEQ ID NO:6233的氨基酸序列。
表20.抗CD34抗体的示例性可变区序列
表21.抗CD34抗体的示例性CDR
接头
本文公开的多特异性或多功能性分子可以进一步包括接头,例如,在以下中的一个或多个之间的接头:抗原结合结构域和细胞因子分子、抗原结合结构域和免疫细胞接合物、抗原结合结构域和基质修饰部分、细胞因子分子和免疫细胞接合物、细胞因子分子和基质修饰部分、免疫细胞接合物和基质修饰部分、抗原结合结构域和免疫球蛋白链恒定区、细胞因子分子和免疫球蛋白链恒定区、免疫细胞接合物和免疫球蛋白链恒定区,或基质修饰部分和免疫球蛋白链恒定区。在一些实施方案中,接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头,或其组合。
在一个实施方案中,多特异性分子可以包括一个、两个、三个或四个接头,例如,肽接头。在一个实施方案中,肽接头包括Gly和Ser。在一些实施方案中,肽接头选自GGGGS(SEQID NO:6214);GGGGSGGGGS(SEQ ID NO:6215);GGGGSGGGGSGGGGS(SEQ ID NO:6216);以及DVPSGPGGGGGSGGGGS(SEQ ID NO:6217)。在一些实施方案中,肽接头是A(EAAAK)nA(SEQ IDNO:6413)家族的接头(例如,如Protein Eng.(2001)14(8):529-532中所述的)。这些是刚性螺旋接头,其中n为2-5。在一些实施方案中,肽接头选自AEAAAKEAAAKAAA(SEQ ID NO:6220);AEAAAKEAAAKEAAAKAAA(SEQ ID NO:6221);AEAAAKEAAAKEAAAKEAAAKAAA(SEQ ID NO:77);以及AEAAAKEAAAKEAAAKEAAAKEAAAKAAA(SEQ ID NO:78)。
核酸
还公开了编码上述多特异性或多功能性分子的核酸。
在某些实施方案中,如本文所述,本发明的特征在于核酸,其包含编码抗体分子的重链和轻链可变区以及CDR或高变环的核苷酸序列。例如,本发明的特征在于第一和第二核酸,它们分别编码选自本文公开的抗体分子中一种或多种抗体分子的重链和轻链可变区。核酸可以包含如本文表中所述的核苷酸序列,或与其基本上相同的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,或与本文表中所示的序列相差不超过3、6、15、30或45个核苷酸的序列)。
在某些实施方案中,核酸可以包含编码来自重链可变区的至少一个、两个或三个CDR或高变环的核苷酸序列,该重链可变区具有本文表中所述的氨基酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或具有一个或多个置换,例如,保守置换)。在其他实施方案中,核酸可以包含编码来自轻链可变区的至少一个、两个或三个CDR或高变环的核苷酸序列,该轻链可变区具有本文表中所述的氨基酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或具有一个或多个置换,例如,保守置换)。在另一实施方案中,核酸可以包含编码来自重链和轻链可变区的至少一个、两个、三个、四个、五个或六个CDR或高变环的核苷酸序列,该重链和轻链可变区具有本文表中所述的氨基酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或具有一个或多个置换,例如,保守置换)。
在某些实施方案中,核酸可以包含编码来自重链可变区的至少一个、两个或三个CDR或高变环的核苷酸序列,该重链可变区具有本文表中所述的核苷酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或能够在本文所述的严格条件下杂交)。在另一实施方案中,核酸可以包含编码来自轻链可变区的至少一个、两个或三个CDR或高变环的核苷酸序列,该轻链可变区具有本文表中所述的核苷酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或能够在本文所述的严格条件下杂交)。在另一实施方案中,核酸可以包含编码来自重链和轻链可变区的至少一个、两个、三个、四个、五个或六个CDR或高变环的核苷酸序列,该重链和轻链可变区具有本文表中所述的核苷酸序列,或与其基本上同源的序列(例如,与其至少约85%、90%、95%、99%或更多相同的序列,和/或能够在本文所述的严格条件下杂交)。
在某些实施方案中,核酸可以包含编码细胞因子分子、免疫细胞接合物或本文公开的基质修饰部分的核苷酸序列。
在另一方面,本申请的特征在于宿主细胞和载体,它们含有本文所述的核酸。如下文更详细描述,核酸可存在于单一载体中或存在于同一宿主细胞或不同宿主细胞中的不同载体中。
载体
本文进一步提供了载体,其包含编码本文所述的多特异性或多功能性分子的核苷酸序列。在一个实施方案中,载体包含编码本文所述的多特异性或多功能性分子的核苷酸。在一个实施方案中,载体包含本文所述的核苷酸序列。载体包括但不限于病毒、质粒、粘粒、λ噬菌体或酵母人工染色体(YAC)。
许多载体系统可以被使用。例如,一类载体利用来源于动物病毒(例如,牛乳头瘤病毒、多瘤病毒、腺病毒、牛痘病毒、杆状病毒、逆转录病毒(劳斯肉瘤病毒、MMTV或MOMLV)或SV40病毒)的DNA元件。另一类载体利用来源于RNA病毒(例如塞姆利基森林病毒、东方马脑炎病毒和黄病毒)的RNA元件。
另外,可通过引入一个或多个允许选择转染的宿主细胞的标记物来选择已将DNA稳定整合至其染色体中的细胞。标记可提供例如对营养缺陷型宿主的质子转移、杀生物剂抗性(例如,抗生素)或对重金属(例如铜)的抗性等。选择性标记基因可以直接与待表达的DNA序列连接,或通过共转化导入同一细胞。mRNA的最佳合成也可能需要另外的元件。这些元件可包括剪接信号,以及转录启动子、增强子和终止信号。
一旦制备了用于表达的表达载体或含有构建体的DNA序列,就可以将表达载体转染或导入合适的宿主细胞中。这可以使用各种技术来实现,例如,原生质体融合、磷酸钙沉淀、电穿孔、逆转录病毒转导、病毒转染、基因枪、基于脂质的转染或其他常规技术。在原生质体融合的情况下,细胞在培养基中生长并筛选合适的活性。用于培养所得转染的细胞和用于回收产生的抗体分子的方法和条件是本领域技术人员已知的,并且可基于本说明书根据所用的特定表达载体和哺乳动物宿主细胞而改变或优化。
细胞
在另一方面,本申请的特征在于宿主细胞和载体,它们含有本文所述的核酸。核酸可存在于单一载体中或存在于同一宿主细胞或不同宿主细胞中的不同载体中。宿主细胞可以是真核细胞,例如,哺乳动物细胞、昆虫细胞、酵母细胞或原核细胞,例如,大肠杆菌。例如,哺乳动物细胞可以是培养的细胞或细胞系。示例性哺乳动物细胞包括淋巴细胞系(例如,NSO)、中国仓鼠卵巢细胞(CHO)、COS细胞、卵母细胞和来自转基因动物的细胞,例如,乳腺上皮细胞。
本发明还提供了包含编码如本文所述的抗体分子的核酸的宿主细胞。
在一个实施方案中,宿主细胞遗传工程化为包含编码抗体分子的核酸。
在一个实施方案中,宿主细胞通过使用表达盒遗传工程化。短语“表达盒”是指核苷酸序列,其能够影响基因在与这种序列相容的宿主中表达。这种盒可包括启动子、含或不含内含子的开放阅读框,以及终止信号。也可以使用实现表达所需或有帮助的另外因子,例如,诱导型启动子。
本发明还提供了包含本文所述载体的宿主细胞。
细胞可以是但不限于真核细胞、细菌细胞、昆虫细胞或人细胞。合适的真核细胞包括但不限于Vero细胞、Hela细胞、COS细胞、CHO细胞、HEK293细胞、BHK细胞和MDCKII细胞。合适的昆虫细胞包括但不限于Sf9细胞。
用途和组合疗法
本文所述的方法包括通过使用本文所述的多特异性或多功能性分子(例如,使用本文所述的药物组合物)治疗对象的癌症。还提供了减少或改善对象癌症症状的方法,以及抑制癌症生长和/或杀伤一种或多种癌细胞的方法。在一些实施方案中,本文所述的方法在施用本文所述的或本文所述的药物组合物的对象中减小肿瘤的大小和/或减小癌细胞的数量。
在一些实施方案中,癌症是血液癌症。在一些实施方案中,血液癌症是白血病或淋巴瘤。如本文所用,“血液癌症”是指造血组织或淋巴组织的肿瘤,例如,影响血液、骨髓或淋巴结的肿瘤。示例性血液恶性肿瘤包括但不限于白血病(例如,急性成淋巴细胞性白血病(ALL)、急性髓样白血病(AML)、慢性淋巴细胞白血病(CLL)、慢性髓性白血病(CML)、毛细胞白血病、急性单核细胞性白血病(AMoL)、慢性骨髓单核细胞性白血病(CMML)、幼年型粒-单核细胞白血病(JMML)或大颗粒淋巴细胞性白血病)、淋巴瘤(例如,AIDS相关淋巴瘤、皮肤T细胞淋巴瘤、霍奇金淋巴瘤(例如,典型霍奇金淋巴瘤或结节性淋巴细胞主导型霍奇金淋巴瘤)、蕈样真菌病、非霍奇金淋巴瘤(例如,B细胞非霍奇金淋巴瘤(例如,伯基特淋巴瘤、小淋巴细胞性淋巴瘤(CLL/SLL)、弥漫性大B细胞淋巴瘤、滤泡性淋巴瘤、免疫母细胞性大细胞淋巴瘤、前体B成淋巴细胞性淋巴瘤或套细胞淋巴瘤)或T细胞非霍奇金淋巴瘤(蕈样真菌病、间变性大细胞淋巴瘤或前体T成淋巴细胞性淋巴瘤))、原发性中枢神经系统淋巴瘤、塞扎里综合征、瓦氏巨球蛋白血症)、慢性骨髓增生性赘生物、朗格汉斯细胞组织细胞增生症、多发性骨髓瘤/浆细胞赘生物、骨髓增生异常综合征或骨髓增生异常/骨髓增生性赘生物。
在一些实施方案中,癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML)。在一些实施方案中,癌症是骨髓纤维化。在一些实施方案中,对象患有骨髓纤维化。在一些实施方案中,对象具有钙网蛋白突变,例如,本文公开的钙网蛋白突变。在一些实施方案中,对象不具有JAK2-V617F突变。在一些实施方案中,对象具有JAK2-V617F突变。在一些实施方案中,对象具有MPL突变。在一些实施方案中,对象不具有MPL突变。
在一些实施方案中,癌症是实体癌。示例性实体癌包括但不限于卵巢癌、直肠癌、胃癌、睾丸癌、肛门区癌、子宫癌、结肠癌、直肠癌、肾细胞癌、肝癌、非小细胞肺癌、小肠癌、食管癌、黑色素瘤、卡波西肉瘤、内分泌系统癌、甲状腺癌、甲状旁腺癌、肾上腺癌、骨癌、胰癌、皮肤癌、头颈癌、皮肤或眼内恶性黑色素瘤、子宫癌、脑干神经胶质瘤、垂体腺瘤、表皮样癌、子宫颈鳞状细胞癌、输卵管癌、子宫内膜癌、阴道癌、软组织肉瘤、尿道癌、外阴癌、阴茎癌、膀胱癌、肾癌或输尿管癌、肾盂癌、脊髓轴肿瘤、中枢神经系统(CNS)赘生物、原发性CNS淋巴瘤、肿瘤血管生成、所述癌症的转移病变,或其组合。
在一些实施方案中,多特异性或多功能性分子(或药物组合物)以适于待治疗或预防的疾病的方式施用。施用的量和频率将由例如患者病况以及患者疾病类型和严重性等因素来确定。合适的剂量可通过临床试验来确定。例如,当指示“有效量”或“治疗量”时,医生可以考虑个体在肿瘤大小、感染或转移程度、对象的年龄、体重和病况方面的差异来确定待施用的药物组合物(或多特异性或多功能性分子)的精确量。在一些实施方案中,本文所述的药物组合物可以104至109个细胞/kg体重(例如,105至106个细胞/kg体重)的剂量施用,包括那些范围内的所有整数值。在一些实施方案中,本文所述的药物组合物可以以这些剂量施用多次。在一些实施方案中,本文所述的药物组合物可以使用免疫疗法中所述的输注技术来施用(参见例如,Rosenberg等人,New Eng.J.of Med.319:1676,1988)。
在一些实施方案中,将多特异性或多功能性分子或药物组合物肠胃外施用至对象。在一些实施方案中,将细胞静脉内、皮下、瘤内、结内、肌内、皮内或腹膜内施用至对象。在一些实施方案中,将细胞直接施用(例如,注射)至肿瘤或淋巴结中。在一些实施方案中,将细胞作为输注物(例如,如Rosenberg等人,New Eng.J.of Med.319:1676,1988中所述)或静脉内推注施用。在一些实施方案中,将细胞作为可注射的贮库制剂施用。
在一些实施方案中,对象是哺乳动物。在一些实施方案中,对象是人、猴、猪、狗、猫、牛、绵羊、山羊、兔、大鼠或小鼠。在实施方案中,对象是人。在一些实施方案中,对象是儿科对象,例如,小于18岁,例如,小于17、16、15、14、13、12、11、10、9、8、7、6、5、4、3、2、1岁或更小。在一些实施方案中,对象是成人,例如,至少18岁,例如,至少19、20、21、22、23、24、25、25-30、30-35、35-40、40-50、50-60、60-70、70-80或80-90岁。
组合疗法
本文公开的多特异性或多功能性分子可以与第二治疗性药剂或程序组合使用。
在一些实施方案中,多特异性或多功能性分子和第二治疗性药剂或程序在对象已被诊断患有癌症之后(例如,已消除对象的癌症之前)施用/进行。在一些实施方案中,多特异性或多功能性分子和第二治疗性药剂或程序同时或并行施用/进行。例如,当第二种治疗的递送开始时,一种治疗的递送仍在进行,例如,治疗的施用存在重叠。在其他实施方案中,多特异性或多功能性分子和第二治疗性药剂或程序依次施用/进行。例如,一种治疗的递送在另一种治疗的递送开始之前停止。
在一些实施方案中,组合疗法可以导致比单独用任一药剂的单一疗法更有效的治疗。在一些实施方案中,第一和第二治疗的组合比单独的第一或第二治疗更有效(例如,导致症状和/或癌细胞更大的减少)。在一些实施方案中,与作为单一疗法施用时实现相似作用通常所需的第一或第二治疗剂量相比,组合疗法允许使用较低剂量的第一或第二治疗。在一些实施方案中,组合疗法具有部分累加效应、完全累加效应或大于累加效应。
在一个实施方案中,多特异性或多功能性分子与疗法(例如,癌症疗法(例如,一种或多种抗癌药剂、免疫疗法、光动力疗法(PDT)、手术和/或放射))组合施用。术语“化疗”、“化疗药剂”和“抗癌药剂”在本文中可互换使用。多特异性或多功能性分子的施用和疗法(例如,癌症疗法)可以是依次发生的(有或无重叠)或同时发生的。在疗程(例如,癌症疗法)期间,多特异性或多功能性分子的施用可以是连续的或间歇的。本文所述的某些疗法可以用于治疗癌症和非癌性疾病。例如,使用本文所述的方法和组合物可以增强PDT在癌性和非癌性病况中的功效(例如,Agostinis,P.等人,(2011)CA Cancer J.Clin.61:250-281中综述的)。
抗癌疗法
在其他实施方案中,多特异性或多功能性分子与低或小分子量的化疗药剂组合施用。示例性低或小分子量的化疗药剂包括但不限于13-顺式视黄酸(异维甲酸,)、2-CdA(2-氯脱氧腺苷,克拉屈滨,LEUSTATINTM)、5-阿扎胞苷(阿扎胞苷,)、5-氟尿嘧啶(5-FU,氟尿嘧啶,)、6-巯基嘌呤(6-MP,巯基嘌呤,)、6-TG(6-硫代鸟嘌呤,硫代鸟嘌呤,THIOGUANINE)、abraxane(蛋白结合型紫杉醇)、放线菌素D(更生霉素,)、阿利维A酸全反式视黄酸(ATRA,维甲酸,)、六甲蜜胺(六甲嘧胺,HMM,)、氨甲蝶呤(甲氨蝶呤,甲氨蝶呤钠,MTX,TREXALLTM,)、氨磷汀阿糖胞嘧啶(Ara-C,阿糖胞苷,CYTOSAR-)、三氧化二砷天冬酰胺酶(欧文氏菌L-天冬氨酸酶,L-天冬氨酸酶,)、BCNU(卡莫斯汀,)、苯达莫司汀蓓萨罗丁博来霉素白消安 甲酰四氢叶酸钙(嗜橙菌因子,亚叶酸,甲酰四氢叶酸)、喜树碱-11(CPT-11,伊立替康,)、卡培他滨卡铂卡莫司汀晶片(具有卡莫司汀植入物的prolifeprospan 20,晶片)、CCI-779(坦罗莫司,)、CCNU(洛莫司汀,CeeNU)、CDDP(顺铂,PLATINOL-)、苯丁酸氮芥(瘤可宁)、环磷酰胺达卡巴嗪(DIC,DTIC,咪唑甲酰胺,DTIC-)、正定霉素(道诺霉素,盐酸道诺霉素,盐酸红比霉素,)、地西他滨右雷佐生DHAD(米托蒽醌,)、多西他赛多柔比星表柔比星(ELLENCETM)、雌莫司汀依托泊苷(VP-16,磷酸依托泊苷, )、氟尿苷、氟达拉滨氟尿嘧啶(霜剂)((CARACTM, )、吉西他滨羟基脲(DROXIATM,MYLOCELTM)、伊达比星异环磷酰胺伊沙匹隆(IXEMPRATM)、LCR(醛基长春碱,长春新碱,VCR,)、L-PAM(L-沙可来新,美法仑,苯丙氨酸氮芥,)、氮芥(盐酸氮芥,氮介,氮芥子气,)、美司钠(MESNEXTM)、丝裂霉素(丝裂霉素-C,MTC,)、奈拉滨奥沙利铂(ELOXATINTM)、紫杉醇(ONXALTM)、培门冬酶(PEG-L-天冬酰胺酶,)、培美曲塞喷司他汀甲苄肼链脲菌素替莫唑胺替尼泊苷(VM-26,)、TESPA(硫代磷酰胺,噻替派,TSPA,)、拓扑替康长春碱(硫酸长春碱,长春花碱,VLB,ALKABAN-)、长春瑞滨(酒石酸长春瑞滨,)和伏立诺他
在另一实施方案中,多特异性或多功能性分子与生物制剂联合施用。用于治疗癌症的生物制剂是本领域已知的,并且本发明的结合分子可例如与这些已知的生物制剂联合施用。例如,FDA已批准以下生物制剂用于治疗乳腺癌:(曲妥珠单抗,Genentech Inc.,加利福尼亚州南旧金山市;在HER2阳性乳腺癌中具有抗肿瘤活性的人源化单克隆抗体);(氟维司群,AstraZeneca Pharmaceuticals,LP,特拉华州威尔明顿市;用于治疗乳腺癌的雌激素受体拮抗剂;(阿那曲唑,AstraZeneca Pharmaceuticals,LP;阻断芳香酶(制备雌激素所需的酶)的非甾体芳香酶抑制剂;(依西美坦,Pfizer Inc.,纽约州纽约市;用于治疗乳腺癌的不可逆的甾体芳香酶灭活剂);(来曲唑,Novartis Pharmaceuticals,新泽西州东汉诺威市;FDA批准用于治疗乳腺癌的非甾体芳香酶抑制剂;以及(他莫昔芬,AstraZeneca Pharmaceuticals,LP;FDA批准用于治疗乳腺癌的非甾体抗雌激素)。可以与本发明的结合分子组合的其他生物制剂包括:(贝伐单抗,GenentechInc.;旨在抑制血管生成的第一个FDA批准的疗法);以及(替伊莫单抗,Biogen Idec,马萨诸塞州剑桥市;目前批准用于治疗B细胞淋巴瘤的放射性标记的单克隆抗体)。
另外,FDA已批准以下生物制剂用于治疗结肠直肠癌: (西妥昔单抗,ImClone Systems Inc.,纽约州纽约市,和Bristol-MyersSquibb,纽约州纽约市;是针对表皮生长因子受体(EGFR)的单克隆抗体);(甲磺酸伊马替尼;蛋白激酶抑制剂);以及(盐酸左旋咪唑,JanssenPharmaceutica Products,LP,新泽西州泰特斯维尔市;在Dukes’C期结肠癌患者手术切除后,FDA在1990年批准的与5-氟尿嘧啶组合作为辅助治疗的免疫调节剂)。
对于多发性骨髓瘤的治疗,示例性生物制剂包括万珂(硼替佐米,Millennium Pharmaceuticals,马萨诸塞州剑桥市;蛋白酶体抑制剂)。另外的生物制剂包括(沙利度胺,Clegene Corporation,新泽西州沃伦市;免疫调节药剂并且似乎具有多种作用,包括抑制骨髓瘤细胞生长和存活以及抗血管生成的能力。
另外的示例性癌症治疗性抗体包括但不限于3F8、阿巴伏单抗、阿德木单抗、阿夫土珠单抗、培戈-阿拉赛珠单抗、阿伦单抗( )、喷替酸阿妥莫单抗(HYBRI-)、马安那莫单抗、安芦组单抗(IMA-638)、阿泊珠单抗、阿西莫单抗(CEA-)、巴维昔单抗、贝妥莫单抗贝利木单抗(LYMPHOSTAT-)、贝索单抗贝伐珠单抗bivatuzumab mertansine、博纳吐单抗、本妥昔单抗、莫坎妥珠单抗、卡罗单抗喷地肽卡妥索单抗CC49、西妥昔单抗(C225,)、泊西他组单抗、西妥木单抗、泰坦-克利妥珠单抗、可那木单抗、达西组单抗、地诺单抗地莫单抗、依美昔单抗、依决洛单抗埃罗妥珠单抗、西依匹莫单抗、依帕珠单抗、厄妥索单抗埃达组单抗、法妥组单抗、芬妥木单抗、非苏木单抗、加利昔单抗、吉妥珠单抗吉妥昔单抗、glembatumumab vedotin、替伊莫单抗(ibritumomab tiuxetan,)、伊戈伏单抗(INDIMACIS-)、英妥木单抗、奥英妥珠单抗、伊匹木单抗、伊妥木单抗、拉贝珠单抗(CEA-)、来沙木单抗、林妥珠单抗、卢卡木单抗、鲁昔单抗、马帕木单抗、马妥珠单抗、米拉组单抗、明瑞莫单抗、米妥莫单抗、他那可单抗、埃托-那普妥莫单抗、耐昔妥珠单抗、尼妥珠单抗诺非妥莫单抗锝奥法木单抗奥拉单抗、莫妥组单抗、奥戈伏单抗帕尼单抗pemtumomab帕妥珠单抗平妥莫单抗、普林木单抗、雷莫芦单抗、雷珠单抗利妥木单抗、利妥昔单抗罗妥木单抗、沙妥莫单抗喷地肽、西罗珠单抗、司妥昔单抗、松妥组单抗、tacatuzumabtetraxetan(AFP-)、帕他莫单抗、替妥莫单抗、TGN1412、替西木单抗(曲美木单抗)、替加组单抗、TNX-650、托西莫单抗曲妥珠单抗曲美木单抗、西莫白介素单抗、维妥组单抗、伏洛昔单抗、伏妥莫单抗扎芦木单抗(HUMAX-)和扎木单抗(HUMAX-)。
在其他实施方案中,多特异性或多功能性分子与病毒癌症治疗性药剂组合施用。示例性病毒癌症治疗性药剂包括但不限于牛痘病毒(vvDD-CDSR)、表达癌胚抗原的麻疹病毒、重组牛痘病毒(TK-缺失加GM-CSF)、塞内卡谷病毒-001、新城疫病毒、柯萨奇病毒A21、GL-ONC1、EBNA1 C-末端/LMP2嵌合蛋白的重组修饰的牛痘安卡拉疫苗、表达癌胚抗原的麻疹病毒、G207溶瘤病毒、表达p53的修饰的牛痘病毒安卡拉疫苗、OncoVEX GM-CSF修饰的1型单纯疱疹病毒、禽痘病毒疫苗载体、重组牛痘前列腺特异性抗原疫苗、人乳头瘤病毒16/18L1病毒样颗粒/AS04疫苗、MVA-EBNA1/LMP2注射疫苗、四价HPV疫苗、四价人乳头瘤病毒(6、11、16、18型)重组疫苗重组禽痘-CEA(6D)/TRICOM疫苗;重组牛痘-CEA(6D)-TRICOM疫苗、重组修饰的牛痘安卡拉-5T4疫苗、重组禽痘-TRICOM疫苗、溶瘤性疱疹病毒NV1020、HPV L1 VLP疫苗V504、二价人乳头瘤病毒(16型和18型)疫苗单纯疱疹病毒HF10、Ad5CMV-p53基因、重组牛痘DF3/MUC1疫苗、重组牛痘-MUC-1疫苗、重组牛痘-TRICOM疫苗、ALVAC MART-1疫苗、表达人前脑啡肽原(NP2)的复制缺陷型I型单纯疱疹病毒(HSV-1)载体、野生型呼肠孤病毒、呼肠孤病毒3型Dearing溶瘤性病毒HSV1716、编码爱泼斯坦-巴尔病毒靶抗原的重组修饰的牛痘安卡拉(MVA)基疫苗、重组禽痘前列腺特异性抗原疫苗、重组牛痘前列腺特异性抗原疫苗、重组牛痘-B7.1疫苗、rAd-p53基因、Ad5-delta24RGD、HPV疫苗580299、JX-594(胸苷激酶缺失的牛痘病毒加GM-CSF)、HPV-16/18L1/AS04、禽痘病毒疫苗载体,牛痘-酪氨酸酶疫苗、MEDI-517HPV-16/18VLP AS04疫苗、含有单纯疱疹病毒TK99UN的胸苷激酶的腺病毒载体、HspE7、FP253/氟达拉滨、ALVAC(2)黑色素瘤多抗原治疗性疫苗、ALVAC-hB7.1、金丝雀痘-hIL-12黑色素瘤疫苗、Ad-REIC/Dkk-3、rAd-IFN SCH 721015、TIL-Ad-INFg、Ad-ISF35和柯萨奇病毒A21(CVA21,)。
在其他实施方案中,多特异性或多功能性分子与纳米药物组合施用。示例性癌症纳米药物包括但不限于(白蛋白结合型紫杉醇纳米颗粒)、CRLX101(与线性环糊精基聚合物缀合的CPT)、CRLX288(将多西他赛与可生物降解的聚合物聚(乳酸-co-乙醇酸)缀合)、阿糖胞苷脂质体(脂质体Ara-C,DEPOCYTTM)、道诺霉素脂质体多柔比星脂质体包封的道诺霉素柠檬酸盐脂质体和PEG抗-VEGF适体
在一些实施方案中,多特异性或多功能性分子与紫杉醇或紫杉醇制剂(例如,蛋白结合型紫杉醇(例如,))组合施用。示例性紫杉醇制剂包括但不限于白蛋白结合型紫杉醇纳米颗粒(由Abraxis Bioscience销售)、二十二碳六烯酸结合型紫杉醇(DHA-紫杉醇,Taxoprexin,由Protarga销售)、聚谷氨酸结合型紫杉醇(PG-紫杉醇,聚谷氨酸紫杉醇,CT-2103,XYOTAX,由Cell Therapeutic销售)、肿瘤激活的前药(TAP)、ANG105(与三个紫杉醇分子结合的血管肽-2,由ImmunoGen销售)、紫杉醇-EC-1(与erbB2识别肽EC-1结合的紫杉醇;参见Li等人,Biopolymers(2007)87:225-230),以及葡萄糖缀合的紫杉醇(例如,2’-紫杉醇甲基2-吡喃葡萄糖基琥珀酸酯,参见Liu等人,Bioorganic&Medicinal Chemistry Letters(2007)17:617-620)。
用于治疗癌症的示例性RNAi和反义RNA药剂包括但不限于CALAA-01、siG12DLODER(Local Drug EluteR)和ALN-VSP02。
其他癌症治疗性药剂包括但不限于细胞因子(例如,阿地白介素(IL-2,白介素-2,)、α干扰素(IFN-α,干扰素α,A(干扰素α-2b),ROFERON-(干扰素α-2a))、依泊汀α非格司亭(G-CSF,粒细胞集落刺激因子,)、GM-CSF(粒细胞巨噬细胞集落刺激因子,沙格司亭,LEUKINETM)、IL-11(白介素-11,奥普瑞白介素,)、干扰素α-2b(PEG缀合物)(PEG干扰素,PEG-INTRONTM)和培非格司亭(NEULASTATM))、激素疗法药剂(例如,氨鲁米特阿那曲唑比卡鲁胺依西美坦氟羟甲睾酮氟他胺氟维司群戈舍瑞林来曲唑亮丙瑞林(ELIGARDTM,VIADURTM)、甲地孕酮(醋酸甲地孕酮,)、尼鲁米特奥曲肽(醋酸奥曲肽,)、雷洛昔芬罗米司亭他莫昔芬和托瑞米芬)、磷脂酶A2抑制剂(例如,阿那格雷)、生物反应调节剂(例如,BCG和达依泊汀α)、靶向疗法药剂(例如,硼替佐米达沙替尼(SPRYCELTM)、denileukin diftitox埃罗替尼依维莫司吉非替尼甲磺酸伊马替尼(STI-571,GLEEVECTM)、拉帕替尼索拉菲尼和SU11248(舒尼替尼,)、免疫调节和抗血管生成药剂(例如,CC-5013(来那度胺,)和沙利度胺)、糖皮质激素(例如,可的松(氢化可的松,氢化可的松磷酸钠,氢化可的松琥珀酸钠,ALA-氢化可的松磷酸盐SOLU-)、Decadron(地塞米松,醋酸地塞米松,地塞米松磷酸钠,)、甲基泼尼松龙(6-甲基泼尼松龙,醋酸甲基泼尼松龙,甲基泼尼松龙琥珀酸钠, )、泼尼松龙(DELTA- )和强的松(LIQUID)),以及双膦酸盐类(例如,帕米膦酸盐和唑来膦酸)。
在一些实施方案中,多特异性或多功能性分子与酪氨酸激酶抑制剂(例如,受体酪氨酸激酶(RTK)抑制剂)组合使用。示例性酪氨酸激酶抑制剂包括但不限于表皮生长因子(EGF)途径抑制剂(例如,表皮生长因子受体(EGFR)抑制剂)、血管内皮生长因子(VEGF)途径抑制剂(例如,针对VEGF的抗体、VEGF捕获剂、血管内皮生长因子受体(VEGFR)抑制剂(例如,VEGFR-1抑制剂、VEGFR-2抑制剂、VEGFR-3抑制剂))、血小板衍生生长因子(PDGF)途径抑制剂(例如,血小板衍生生长因子受体(PDGFR)抑制剂(例如,PDGFR-β抑制剂))、RAF-1抑制剂、KIT抑制剂和RET抑制剂。在一些实施方案中,与AHCM药剂组合使用的抗癌药剂选自:阿昔替尼(AG013736)、博舒替尼(SKI-606)、西地尼布(RECENTINTM,AZD2171)、达沙替尼(BMS-354825)、厄洛替尼吉非替尼伊马替尼(CGP57148B,STI-571)、拉帕替尼 来他替尼(CEP-701)、来那替尼(HKI-272)、尼洛替尼semaxanib(塞马西尼,SU5416)、舒尼替尼(SU11248)、toceranib凡德他尼(ZD6474)、瓦他拉尼(PTK787,PTK/ZK)、曲妥珠单抗贝伐珠单抗利妥昔单抗西妥昔单抗帕尼单抗雷珠单抗尼洛替尼索拉非尼阿仑单抗吉妥珠单抗ENMD-2076、PCI-32765、AC220、多韦替尼乳酸盐(TKI258,CHIR-258)、BIBW 2992(TOVOKTM)、SGX523、PF-04217903、PF-02341066、PF-299804、BMS-777607、ABT-869、MP470、BIBF 1120AP24534、JNJ-26483327、MGCD265、DCC-2036、BMS-690154、CEP-11981、替沃扎尼(AV-951)、OSI-930、MM-121、XL-184、XL-647、XL228、AEE788、AG-490、AST-6、BMS-599626、CUDC-101、PD153035、培利替尼(EKB-569)、凡德他尼(zactima)、WZ3146、WZ4002、WZ8040、ABT-869(利尼伐尼)、AEE788、AP24534(普纳替尼)、AV-951(替沃扎尼)、阿昔替尼、BAY 73-4506(瑞戈非尼)、丙氨酸布立尼布(BMS-582664)、布立尼布(BMS-540215)、西地尼布(AZD2171)、CHIR-258(多韦替尼)、CP 673451、CYC116、E7080、Ki8751、马赛替尼(AB1010)、MGCD-265、二磷酸莫替沙尼(AMG-706)、MP-470、OSI-930、盐酸帕唑帕尼、PD173074、对甲苯磺酸索拉非尼(Bay43-9006)、SU 5402、TSU-68(SU6668)、瓦他拉尼、XL880(GSK1363089,EXEL-2880)。选定的酪氨酸激酶抑制剂选自舒尼替尼、埃罗替尼、吉非替尼或索拉非尼。在一个实施方案中,酪氨酸激酶抑制剂是舒尼替尼。
在一个实施方案中,多特异性或多功能性分子与以下中的一种或多种组合施用:抗血管生成药剂,或血管靶向药剂或血管破坏药剂。示例性抗血管生成药剂包括但不限于VEGF抑制剂(例如,抗VEGF抗体(例如,贝伐单抗);VEGF受体抑制剂(例如,伊曲康唑);细胞增殖和/或内皮细胞迁移的抑制剂(例如,羟酰胺基三唑、TNP-470);血管生成刺激物的抑制剂(例如,苏拉明)等。血管靶向药剂(VTA)或血管破坏药剂(VDA)旨在损伤癌瘤的脉管系统(血管),从而导致中枢性坏死(例如,Thorpe,P.E.(2004)Clin.Cancer Res.第10卷:415-427中综述的)。VTA可以是小分子。示例性小分子VTA包括但不限于微管去稳定药物(例如,康普瑞汀A-4磷酸二钠(CA4P)、ZD6126、AVE8062、Oxi4503);以及vadimezan(ASA404)。
免疫检查点抑制剂
在其他实施方案中,本文所述的方法包括免疫检查点抑制剂与多特异性或多功能性分子组合使用。该方法可以用于体内治疗性方案。
在一些实施方案中,免疫检查点抑制剂抑制检查点分子。示例性检查点分子包括但不限于CTLA4、PD1、PD-L1、PD-L2、TIM3、LAG3、CD160、2B4、CD80、CD86、B7-H3(CD276)、B7-H4(VTCN1)、HVEM(TNFRSF14或CD270)、BTLA、KIR、I类MHC、II类MHC、GAL9、VISTA、BTLA、TIGIT、LAIR1和A2aR。参见例如,Pardoll.Nat.Rev.Cancer12.4(2012):252-64,通过引用并入本文。
在一些实施方案中,免疫检查点抑制剂是PD-1抑制剂,例如,抗PD-1抗体,例如纳武单抗、派姆单抗或匹地利珠单抗。纳武单抗(也称为MDX-1106、MDX-1106-04、ONO-4538或BMS-936558)是特异性抑制PD1的完全人IgG4单克隆抗体。参见例如,US 8,008,449和WO2006/121168。派姆单抗(也称为Lambrolizumab、MK-3475、MK03475、SCH-900475或Merck)是结合至PD-1的人源化IgG4单克隆抗体。参见例如,Hamid,O.等人,(2013)New England Journal of Medicine369(2):134-44、US 8,354,509和WO2009/114335。匹地利珠单抗(也称为CT-011或Cure Tech)是结合至PD1的人源化IgG1k单克隆抗体。参见例如,WO2009/101611。在一个实施方案中,PD-1抑制剂是抗体分子,具有与其基本上相同或相似的序列,例如,与纳武单抗、派姆单抗或匹地利珠单抗的序列至少85%、90%、95%相同或更高的序列。另外的抗PD1抗体(例如,AMP514(Amplimmune))描述于例如US 8,609,089、US 2010028330和/或US 20120114649中。
在一些实施方案中,PD-1抑制剂是免疫粘附素,例如,包含与恒定区(例如,免疫球蛋白的Fc区)融合的PD-1配体(例如,PD-L1或PD-L2)胞外/PD-1结合部分的免疫粘附素。在一些实施方案中,PD-1抑制剂是AMP-224(B7-DCIg,例如,描述于WO2011/066342和WO2010/027827中),其是阻断B7-H1与PD-1之间相互作用的PD-L2 Fc融合可溶性受体。
在一些实施方案中,免疫检查点抑制剂是PD-L1抑制剂,例如,抗体分子。在一些实施方案中,PD-L1抑制剂是YW243.55.S70、MPDL3280A、MEDI-4736、MSB-0010718C或MDX-1105。在一些实施方案中,抗PD-L1抗体是MSB0010718C(也称为A09-246-2;Merck serono),其是结合至PD-L1的单克隆抗体。示例性人源化抗PD-L1抗体描述于例如WO2013/079174中。在一个实施方案中,PD-L1抑制剂是抗PD-L1抗体,例如,YW243.55.S70。YW243.55.S70抗体描述于例如WO2010/077634中。在一个实施方案中,PD-L1抑制剂是MDX-1105(也称为BMS-936559),其描述于例如WO2007/005874中。在一个实施方案中,PD-L1抑制剂是MDPL3280A(Genentech/Roche),其是针对PD-L1的人Fc-优化的IgG1单克隆抗体。参见例如,美国专利第7,943,743号和美国公布第20120039906号。在一个实施方案中,PD-L1抑制剂是抗体分子,具有与其基本上相同或相似的序列,例如,与YW243.55.S70、MPDL3280A、MEDI-4736、MSB-0010718C或MDX-1105的序列至少85%、90%、95%相同或更高的序列。
在一些实施方案中,免疫检查点抑制剂是PD-L2抑制剂,例如,AMP-224(其是阻断PD1和B7-H1之间相互作用的PD-L2 Fc融合可溶性受体)。参见例如,WO2010/027827和WO2011/066342。
在一个实施方案中,免疫检查点抑制剂是LAG-3抑制剂,例如,抗LAG-3抗体分子。在一些实施方案中,抗LAG-3抗体是BMS-986016(也称为BMS986016;Bristol-MyersSquibb)。BMS-986016和其他人源化抗LAG-3抗体描述于例如US 2011/0150892、WO2010/019570和WO2014/008218中。
在一些实施方案中,免疫检查点抑制剂是TIM-3抑制剂,例如,抗TIM3抗体分子,例如,美国专利第8,552,156号、WO2011/155607、EP 2581113和美国公布第2014/044728号中描述的。
在一些实施方案中,免疫检查点抑制剂是CTLA-4抑制剂,例如,抗CTLA-4抗体分子。示例性抗CTLA4抗体包括曲美木单抗(来自Pfizer的IgG2单克隆抗体,以前称为替西木单抗、CP-675、206);和伊匹木单抗(也称为MDX-010,CAS号477202-00-9)。其他示例性抗CTLA-4抗体描述于例如美国专利第5,811,097号中。
CRS分级
在一些实施方案中,与其他组合物相比,本文所述的组合物可诱导较低水平的细胞因子释放综合征(CRS)和/或可具有较低的引起CRS的机会(例如,可不引起CRS)。在一些实施方案中,CRS的严重程度可以如下分为1-5级。1-3级是低于重度CRS。4-5级是重度CRS。对于1级CRS,仅需要对症治疗(例如,恶心、发烧、疲劳、肌痛、不适、头痛),并且症状不危及生命。对于2级CRS,症状需要中度干预,并且通常响应于中度干预。患有2级CRS的对象出现响应于液体或一种低剂量血管加压药的低血压;或出现2级器官毒性或响应于低流量氧气(<40%氧气)的轻度呼吸道症状。在3级CRS对象中,低血压通常不能通过液体疗法或一种低剂量血管加压药逆转。这些对象通常需要多于低流量的氧气,并且具有3级器官毒性(例如,肾或心脏功能障碍或凝血障碍)和/或4级转氨酶升高。3级CRS对象需要更积极的干预,例如,40%或更高的氧、高剂量血管加压药和/或多种血管加压药。4级CRS对象患有立即危及生命的症状,包括4级器官毒性或需要机械通气。4级CRS对象通常不患具有转氨酶升高。在5级CRS对象中,毒性导致死亡。本文中CRS分级的标准集合如表39、表40和表41提供的。除非另有说明,否则如本文所用的CRS是指根据表40的标准的CRS。
在一些实施方案中,根据表39对CRS进行分级:
表39:CRS分级
表40:CTCAE v 4.0CRS分级量表
表41:NCI CRS分级量表
实施例
实施例1.α-TRBV6-5抗体克隆抗体A的人源化
小鼠α-TCRβ抗体克隆抗体A VH和VL的种系使用IMGT命名法指定,其中CDR区由组合Kabat和Chothia分类法定义。SEQ ID NO:1A和SEQ ID NO:2A分别是抗体A VH和VL序列,其中VH种系是小鼠IGHV1S12*01,并且VL种系是小鼠IGKV6-15*01。SEQ ID NO:3A-5A分别是抗体A VH CDR区1-3,并且SEQ ID NO:6A-8A对应于VL CDR区1-3(如表30中所述)。
使用相似的方法分别进行抗体A VH和VL序列的人源化。鉴定了框架区中对CDR移植成功至关重要的氨基酸位置。鉴定了人种系序列,其保留了必需的残基并含有大量的整体同一性。当人种系框架序列不含有匹配的重要氨基酸时,将其回复突变以匹配小鼠序列。将CDR区无改变地移植至人种系上。抗体A VH人源化为人IGHV1-69*01,并且抗体A VL人源化为IGKV1-17*01和IGKV1-27*01。作为人源化过程的结果,所有3种人源化序列被证实不含有引入的潜在负面的翻译后修饰位点,例如NG、DG、NS、NN、DS、NT、NXS或NXT。SEQ ID NO:9A是人源化抗体A-H.1VH,并且SEQ ID NO:10A和11A分别是人源化VL IGKV1-17*01和IGKV1-27*01种系(如表30中所述)。图1A和1B示出了鼠和人源化序列,注释描绘了CDR和框架区(FR)。
实施例2:α-TRBV12-3和TRBV12-4抗体克隆抗体B的人源化
小鼠α-TCRβ抗体克隆抗体B VH和VL的种系使用IMGT命名法指定,其中CDR区由组合Kabat和Chothia分类法定义。SEQ ID NO:15A和SEQ ID NO:16A分别是抗体B VH和VL序列,其中VH种系是小鼠IGHV5-17*02,并且VL种系是小鼠IGKV4-50*01。SEQ ID NO:17A-19A分别是B-H VH CDR区1-3,并且SEQ ID NO:20A-22A是B-H VL CDR区1-3(如表31中所述)。
将实施例1中所述的应用于人源化抗体A的方法用于将抗体B人源化。抗体B VH被人源化为人IGHV3-30*01、IGHV3-48*01和IGHV3-66*01,并且抗体B VL被人源化为人IGKV1-9*01、IGKV1-39*01、IGKV3-15*01、IGLV1-47*01和IGLV3-10*01。SEQ ID NO:23A-25A是B-H.1A、B-H.1B和B-H.1C人源化重链,并且SEQ ID NO:26A-30A是B-H.1D、B-H.1E、B-H.1F、B-H.1G和B-H.1H人源化轻链(如表31中所述)。图2A和2B示出了鼠和人源化序列,注释描绘了CDR和框架区(FR)。
实施例3:抗TCRβV抗体的表征
引言
目前用于癌症免疫疗法的设计为重定向T细胞以促进肿瘤细胞裂解的双特异性构建体通常利用单链可变片段(scFv),其衍生自针对T细胞受体(TCR)CD3e亚基的单克隆抗体(mAb)。然而,这种方法存在局限,该局限可能妨碍这种双特异性构建体完全实现治疗潜力。先前研究已表明,例如,低“激活”剂量的抗CD3e mAb可以引起长期T细胞功能障碍并发挥免疫抑制作用。另外,抗CD3e mAb结合至所有T细胞并因此同等地激活所有T细胞,这与大量T细胞激活引起的抗CD3e mAb的第一剂量副作用相关。这些大量活化的T细胞分泌大量细胞因子,其中最重要的是干扰素γ(IFNg)。这种过量的IFNg又例如激活巨噬细胞,然后其可以过量产生促炎性细胞因子,例如IL-1、IL-6和TNF-α,从而引起称为细胞因子释放综合征(CRS)的“细胞因子风暴”。因此,开发能够仅结合和激活必需的效应T细胞亚群以减少CRS的抗体可能是有利的。
结果
为此,鉴定了针对TCRβ亚基(TCR Vb)可变链的抗体。这些抗TCR Vb抗体结合并激活T细胞亚群,但例如没有CRS或CRS显著减少。使用板结合的抗TCR Vb13.1 mAb(A-H.1和A-H.2),显示出通过用A-H.1阳性染色定义的T细胞群体可以被扩增(从细胞培养的第0天约5%的T细胞至第6天几乎60%的总T细胞)(图4A-4C)。对于该实验,使用磁珠分离(阴性选择)来分离人CD3+T细胞,并用100nM的固定化(板包被)A-H.1或OKT3(抗CD3e)抗体激活6天。当与纯化的CD3+T细胞共培养时,扩增的Vb13.1+T细胞展示出针对经转化细胞系RPMI-8226的细胞溶解活性(图5A-5B)。
接着,评估PBMC由抗TCR VB抗体激活以产生细胞因子的能力。将用抗TCR VB抗体激活的PBMC的细胞因子产生与用以下激活的PBMC的细胞因子产生进行比较:(i)抗CD3e抗体(OKT3或SP34-2);(ii)抗TCR Vα(TCR VA)抗体,包括抗TCR VA12.1抗体6D6.6、抗TCRVA24JA18抗体6B11;(iii)抗TCRαβ抗体T10B9;和/或(iv)同种型对照(BGM0109)。测试的抗TCR VB抗体包括:人源化抗TCR VB13.1抗体(A-H.1或A-H.2)、鼠抗TCR VB5抗体E、鼠抗TCRVB8.1抗体B和鼠抗TCR VB12抗体D。BGM0109包含METDTLLLWVLLLWVPGSTGGLNDIFEAQKIEWHEGGGGSEPRTDTDTCPNPPDPCPTCPTPDLLGGPSVFIFPPKPKDVLMISLTPKITCVVVDVSEEEPDVQFNWYVNNVEDKTAQTETRQRQYNSTYRVVSVLPIKHQDWMSGKVFKCKVNNNALPSPIEKTISKPRGQVRVPQIYTFPPPIEQTVKKDVSVTCLVTGFLPQDIHVEWESNGQPQPEQNYKNTQPVLDSDGSYFLYSKLNVPKSRWDQGDSFTCSVIHEALHNHHMTKTISRSLGNGGGGS(SEQ ID NO:3282A)的氨基酸序列。
如图6A中所示,当板结合的A-H.1或A-H.2或抗CD3e抗体(OKT3或SP34-2)用于激活人PBMC时,诱导出T细胞的细胞因子IFNg(图6A)。所有测试的抗TCR VB抗体对IFNg的产生具有相似的作用(图6B)。抗TCR VA抗体不诱导相似的IFNg产生。
关于IL-2产生,与用抗CD3e抗体(OKT3或SP34-2)激活的PBMC相比,用A-H.1和A-H.2激活的PBMC导致IL-2产生增加(图7A),具有延迟的动力学(图7B)。图7B示出了抗TCR VB抗体激活的PBMC在激活(与板包被的抗体一起孵育)后第5天或第6天显示IL-2的峰值产生。相反,用OKT3激活的PBMC中的IL-2产生在激活后第2天达到峰值。与IFNG一样,所有测试的抗TCR VB抗体的IL-2作用(例如,IL-2的产生增强和动力学延迟)相似(图7B)。
也在相似条件下评估了与“细胞因子风暴”(以及相应的CRS)相关的细胞因子IL-6、IL-1β和TNF-α的产生。图8A、9A和10A示出了虽然用抗CD3e抗体激活的PBMC显示IL-6(图8A)、TNF-α(图9A)和IL-1β(图10A)的产生,但用A-H.1或A-H.2激活的PBMC没有或几乎没有观察到这些细胞因子的诱导。如图9B和10B中所示,用抗TCR VB抗体中任一种激活PBMC不诱导TNF-α和IL-1β产生。
进一步注意到,A-H.1激活的CD3+T细胞的IFNg产生的动力学相对于抗CD3e mAb(OKT3和SP34-2)激活的CD3+T细胞产生的动力学有延迟(图11A和11B)。
最后,观察到被称为TEMRA的记忆效应T细胞亚群优先在A-H.1或A-H.2激活的CD8+T细胞中扩增(图12)。分离的人PBMC用100nM的固定化(板包被)抗CD3e或抗TCR Vβ13.1激活6天。孵育6天后,通过对幼稚T细胞(CD8+、CD95-、CD45RA+、CCR7+)、干细胞记忆T细胞(TSCM;CD8+、CD95+、CD45RA+、CCF7+)、中央记忆T细胞(Tcm;CD8+,CD95+、CD45RA-、CCR7+)、效应记忆T细胞(Tem;CD8+、CD95+、CD45 RA-、CCR7-)和再表达CD45RA的效应记忆T细胞(Temra;CD8+、CD95+、CD45RA-、CCR7-)的表面标记物进行FACS染色来鉴定T细胞亚群。当与抗CD3e抗体(OKT3或SP34-2)激活的PBMC相比时,抗TCR Vβ13.1抗体(A-H.1或A-H.2)激活的人PBMC增加CD8+TSCM和Temra T细胞亚群。用CD4+T细胞观察到相似的扩增。
结论
本实施例中提供的数据显示出针对TCR Vb的抗体可以例如优先激活T细胞亚群,从而导致TEMRA扩增,TEMRA扩增可以例如促进肿瘤细胞裂解,但不促进CRS。因此,利用针对TCRVb的Fab或scFv或肽的双特异性构建体可以例如用于激活和重定向T细胞,以促进肿瘤细胞裂解,用于癌症免疫疗法而没有例如与抗CD3e靶向性相关的CRS的有害副作用。
实施例4:针对BCMA和T细胞接合物的双重靶向性抗体分子对多发性骨髓瘤(MM)细胞的在靶(on-target)T细胞介导的细胞毒性
本实施例示出了识别T细胞上的T细胞接合物(例如,TCRVb)和MM细胞上的BCMA的双重靶向性抗体分子对多发性骨髓瘤(MM)细胞的在靶T细胞介导的细胞毒性。
如图13A中所示,用板结合的抗TCRVb抗体激活5天的纯化的人T细胞以比用板结合的抗CD3(OKT3)抗体激活的纯化的人T细胞更高的速率增殖。T细胞的抗TCRVb抗体刺激导致CD45RA+效应记忆CD8+和CD4+T细胞(TEMRA)细胞的选择性扩增(图13B)。与未刺激的细胞或用抗CD3(SP34)抗体刺激的细胞相比,当用抗TCRVb抗体刺激时,CD8+和CD4+Temra细胞群体扩增更多。与用抗CD3抗体刺激的PBMC相比,抗TCRVb抗体导致用抗TCRVb抗体刺激的PMBC延迟分泌IFN-g(图13C)。另外,如图13D中所示,用抗TCRVb抗体或抗CD3抗体刺激的T细胞导致多发性骨髓瘤靶细胞的类似裂解。如图13E-13F中所示,用100ng/ml板结合的抗TCRVb抗体或抗CD3抗体刺激5天的T细胞分泌穿孔素和粒酶B。
与用抗OKT3抗体激活的PBMC相比,用抗TCRVb抗体激活PBMC导致更高的IL-2和/或IL-15产生和/或分泌(图14A)。PBMC的抗TCRVb抗体激活也导致扩增和/或存活,例如,自然杀伤(NK)细胞的增殖(图14B)。相比之下,用抗OKT3抗体激活的PBMC不导致NK细胞扩增。此外,如实施例3中所述,用抗TCRVb抗体激活的PBMC不导致与CRS相关的细胞因子IL-6、IL-1β和TNF-α的产生(图15)。这些体外表征研究显示,在一些实施方案中,如通过靶细胞裂解、穿孔素分泌和粒酶B分泌以及IFN-g分泌(例如,具有延迟的动力学)所证明的,抗TCRVb抗体例如激活和/或刺激T细胞,以促进T细胞杀伤。
接着,测试在一个臂上靶向BCMA且在另一臂上靶向TCRVb的双重靶向性抗体分子靶向并杀伤多发性骨髓瘤(MM)细胞的能力。健康供体PBMC与RMPI8226 MM细胞系和以下双重靶向性抗体分子中的一种共孵育:BCMA-TCRVb、BCMA-CD3或对照-TCRVb;或同种型对照。然后使用流式细胞术评估靶细胞裂解。如图16A中所示,双重靶向性BCMA-TCRVb抗体分子导致MM细胞的体外杀伤。
在MM小鼠模型中进一步体内测试双重靶向性BCMA-TCRVb抗体分子抑制MM肿瘤生长的能力。在第0天将NCI-H929细胞系注入NOD-scid IL2rγnull(NSG)受体小鼠中,随后在第9天递送PBMC。在第12、15、18和21天,经由腹膜内注射以0.5mg/kg的剂量施用双重靶向性BCMA-TCRVb抗体分子。图16B示出了用双重靶向性BCMA-TCRVb抗体分子体内对MM肿瘤生长的预防,例如,抑制。这些结果显示,在一些实施方案中,双重靶向性BCMA-TCRVb抗体分子例如可以体外和体内杀伤肿瘤细胞,例如,MM肿瘤细胞。因此,在一些实施方案中,双重靶向性BCMA-TCRVb抗体分子可以例如用作癌症(例如,血液癌症,例如,MM)的疗法。
实施例5:针对FcRH5和T细胞接合物的双重靶向性抗体分子的体外细胞毒性
本实施例示出了识别T细胞上的T细胞接合物(例如,TCRVb)和MM细胞上的FcRH5的双重靶向性抗体分子对多发性骨髓瘤(MM)细胞的体外细胞毒性。健康供体PBMC或纯化的T细胞与MOL8 MM细胞系以及在一个臂上靶向FcRH5且在另一臂上靶向TCRVb的双重靶向性抗体分子或与同种型对照抗体一起共孵育。然后使用流式细胞术评估靶细胞裂解。如图17中所示,双重靶向性FcRH5-TCRVb分子导致纯化的T细胞或PBMC杀伤MM细胞。这表明双重靶向性FcRH5-TCRVb分子可以靶向MM细胞,并促进免疫细胞(例如,PBMC,包括T细胞)杀伤MM细胞。
实施例6:免疫接种亚美尼亚仓鼠以生成抗NKp30抗体
简言之,用完全弗氏佐剂中的人NKp30蛋白胞外结构域对亚美尼亚仓鼠进行免疫,并在第14天和第28天用不完全弗氏佐剂(IFA)中的NKp30强化两次。在第56天,再给予一次IFA进行强化,三天后收获动物。收集脾,并与P3X63Ag8.653鼠骨髓瘤细胞系融合。将125ul的0.9×10^5个细胞/孔置于96孔板中,并在第7天、第11天以及之后根据需要,在用于选择的HAT或HT不存在或存在下,供应125μl的I-20+2ME+HAT(IMDM(4g/L葡萄糖)(补充有20%胎牛血清、4mM L-谷氨酰胺、1mM丙酮酸钠、50U青霉素、50μg链霉素和50μM 2-ME)以及杂交瘤克隆因子(最终1%)。融合后大致2周(细胞约50%融汇),收集上清液并测定结合。
实施例7:NKp30 mAb的杂交瘤筛选
在筛选前18小时用BG160(hNKp30细胞抗原)转染Expi293细胞。筛选当天,将转染的细胞稀释至0.05×10^6/mL,并加入抗亚美尼亚仓鼠Fc Alexa Fluor 488至终浓度为0.4ug/mL。将50uL(2,500个细胞)该混合物加入至384孔板的每个孔中。使用相同密度的未转染293细胞和次级细胞作为阴性对照。将5uL杂交瘤上清液加入至细胞混合物中,并将板在37℃下孵育1小时。然后该板在镜面球(Mirrorball)上进行成像。鉴定阳性克隆,并通过连续稀释亚克隆,以获得克隆选择的杂交瘤。使用相同方案再次确认之后,收获杂交瘤细胞,并回收相应的重链和轻链序列。将DNA亚克隆至pcDNA3.4中,随后表达相应的抗体并进一步验证。
实施例8:NKp30抗体与NK92细胞的结合
用含有0.5% BSA和0.1%叠氮化钠的PBS(染色缓冲液)洗涤NK-92细胞,并以200,000个细胞/孔加入至96孔V底板中。将仓鼠NKp30抗体加入至2.0倍连续稀释液的细胞中,并在室温下孵育1小时。用染色缓冲液洗涤板两次。以1∶100的稀释(1.4mg/ml储液)加入与AF647缀合的针对仓鼠Fc的第二抗体(Jackson,127-605-160),并与细胞在4℃下孵育30分钟,随后用染色缓冲液洗涤。随后在室温下用4%多聚甲醛将细胞固定10分钟。在CytoFLEXLS(Beckman Coulter)上读取板。数据计算为百分比-AF747阳性群体(图22)。
实施例9:使用NK92细胞系测量NKp30抗体活性的生物测定
在PBS中将NKp30抗体连续稀释三倍,并在平底96孔板中在2-8℃下孵育过夜。在PBS中将板洗涤两次,并将40,000个NK-92细胞加入含有IL-2的生长培养基中。将板在37℃、5% CO2的潮湿培养箱中孵育16-24小时,然后收集上清液。按照MSD测定说明来测量上清液中的IFNγ水平(图23)。从与仓鼠同种型IgG一起孵育的细胞中收集的上清液被用作阴性对照,并且来自与NKp30单克隆抗体(R&D,克隆210847)一起孵育的细胞的上清液用作阳性对照。使用仓鼠抗NKp30 mAB生成数据。
实施例10:抗钙网蛋白抗体的表征
将包含SEQ ID NO:6250的VH和SEQ ID NO:6252的VL的鼠抗钙网蛋白抗体AbM-1(也称为BIM0031)人源化。生成5个人源化VH(表16中所示的SEQ ID NO:6372和234-237)和5个人源化VL(表16中所示的SEQ ID NO:238-242)。所有人源化VH在HCDR2中包含半胱氨酸至丙氨酸的置换。合成如表19中公开的抗体BJM0040-BJM0064,并表征其生物化学和功能活性。
简言之,在蛋白A洗脱后,测量纯化蛋白质的表达水平。通过分析性SEC来分析蛋白质以评估聚集,并通过差示扫描荧光测定法(DSF)测试以鉴定更稳定的候选物。在ELISA测定中测量候选物针对与人Fc融合的突变型钙网蛋白C-末端肽的结合亲和力。表22中总结了结果。与亲本鼠抗体相比,在HCDR2中包含半胱氨酸至丙氨酸置换的人源化抗体表现出聚集减少。
表22.抗钙网蛋白抗体的表征总结
实施例11:人源化抗NKp30抗体的生成和表征
选择一系列仓鼠抗NKp30抗体。这些抗体显示出结合至人NKp30和食蟹猴NKp30,并诱导NK-90细胞产生IFNγ(数据未显示)。表9中公开了示例性仓鼠抗NKp30抗体15E1、9G1、15H6、9D9、3A12和12D10的VH和VL序列。表9中也公开了基于15E1、9G1和15H6的示例性人源化抗NKp30抗体的VH和VL序列。表34和表8中公开了这些抗体的Kabat CDR。
选择基于15E1的两种人源化构建体。第一种构建体BJM0407是包含重链可变区和λ轻链可变区的Fab,该重链可变区包含SEQ ID NO:7302的氨基酸序列,该λ轻链可变区包含SEQ ID NO:7305的氨基酸序列。它相应的scFv构建体BJM0859包含SEQ ID NO:7310的氨基酸序列。第二种构建体BJM0411是包含重链可变区和κ轻链可变区的Fab,该重链可变区包含SEQ ID NO:7302的氨基酸序列,该κ轻链可变区包含SEQ ID NO:7309的氨基酸序列。它相应的scFv构建体BJM0860包含SEQ ID NO:7311的氨基酸序列。BJM0407和BJM0411显示出类似的生物物理学特征,例如,与NKp30的结合亲和力和热稳定性。scFv构建体BJM0859和BJM0860也显示出类似的生物物理学特性。
实施例12:示例性抗钙网蛋白抗体分子与野生型或突变型钙网蛋白的结合
在本实施例中,测试了示例性抗钙网蛋白抗体分子BKM0106(亲本IgG形式的抗体6C10)与野生型钙网蛋白(CALR WT)的结合,并与两种钙网蛋白突变体(CALR ins和CALRdel,其序列分别以SEQ ID NO:D1002和D1003列于表2中)进行比较。进行两个ELISA试验,其中一个是在板上包被抗原,另一个是在板上包被抗体。
对于其中在板上包被抗原的实验,用CALR WT、CALR in或CALR del蛋白包被Maxisorp板。用3% BSA封闭板。将BKM0106稀释至100nM,并加入孔中。向每个孔中加入1∶20,000的抗人HRP(Jackson Immunoresearch 309-035-008)。加入一步式Turbo TMB-ELISA底物溶液,并通过加入1M HCl终止反应。在450nm处读板。
对于其中在板上包被抗体的实验,用BKM0106包被Maxisorp板。用3% BSA封闭板。将CALR WT、CALR ins和CALR del稀释至100nM,并加入单独的孔中。向每个孔中加入1∶5,000的抗His-Tag-HRP(Southern Biotech 4603-05)。加入一步式Turbo TMB-ELISA底物溶液,并通过加入1M HCl终止反应。在450nm处读板。
如图25A-25B中所示,示例性抗体BKM0106与CALR ins和CALR del突变体结合,但不与野生型钙网蛋白结合。
实施例13:示例性抗钙网蛋白抗体分子与表达突变型钙网蛋白的细胞的结合
在本实施例中,测试了示例性抗钙网蛋白抗体分子BKM0106(亲本IgG形式的抗体6C10)与表达突变型钙网蛋白(CALR ins和CALR del,其序列分别以SEQ ID NO:D1002和D1003列于表2中)的细胞的结合。简言之,用BH470(人TpoR)、BH472(人JAK2)和人CALR ins、人CALR del或BH800(人CALR WT)细胞抗原三重转染Expi293F细胞(Thermo FisherA14527)。向孔中加入0.78、1.56、3.125、6.25、12.5、25和50nM的BKM0106和hIgG1同种型对照。将细胞与二抗Alexa Fluor 488抗人IgG(Jackson ImmunoResearch 109-545-088)1∶200一起孵育。将Zombie Violet BV412(BioLegend 423114)活性染料1∶100加入细胞中。
如图26A-26B中所示,BKM0106以相似的应答与CALR ins和CALR del结合。
实施例14:通过经由双特异性抗体将mtCALR+细胞桥接至免疫效应细胞来靶向mtCALR+细胞
在本实施例中,在同基因鼠癌症模型中测试了一系列抗体分子的治疗效果。简言之,由示例性抗钙网蛋白抗体分子6C10和以下效应臂中的每一个生成了具有mIgG2a骨架的替代分子:
·BKM0201-mutCALR-6C10单克隆-ADCC启用
·BKM0202-mutCALR-6C10×TCRvB(2×2)双特异性-LALAPG
·BKM0204-mutCALR-6C10×CD3-2C11(1×1)双特异性-LALAPG
在使用表达mtCALR、hMPL和hJAK2的Ba/F3细胞工程化细胞生成的系统鼠模型中测试了上述分子的治疗效果。在研究的第1天,将2×10^6个悬浮于PBS中的工程化Ba/F3mtCALR、hMPL、hJAK2细胞静脉内注入雌性Balb/C小鼠中。每三天以1mg/kg或5mg/kg剂量的CALR×/TCRvB和对照双特异性分子通过静脉内快速浓注来处理小鼠,共4次给药(第4、7、10和13天)。对动物进行人道终点监测,并每周监测两次体重。在第15天对所有动物进行安乐死,切除脾,并监测脾重量作为疾病负担的替代。数据表明,与初始小鼠相比,Ba/F3mtCALR、hMPL、hJAK2细胞移植小鼠中媒介物处理的小鼠显示出脾重量增加近三倍,这表明疾病负担增加。
如图27中所示,与媒介物对照相比,所有三种抗体处理的小鼠显示出脾重量显著降低。
实施例15:示例性抗NKp30抗体分子的Biacore分析
在本实施例中,分析了一系列示例性抗NKp30抗体分子对NKp30的结合亲和力。简言之,通过使用BIAcore T200进行表面等离子体共振(SPR)测量。经由抗小鼠Fc抗体将人NKp30(BKM0179)固定在CM5芯片上至应答为50RU。将每种示例性抗体构建体以3.9、7.8、15.6、31.2、62.5和125nM的浓度以及20μl/min的流速注射到其上固定有人NKp30的表面上。使用1∶1结合模型拟合数据。
如表23中所示,与亲本抗体相比,示例性抗体中的大多数对人NKp30显示出保留的亲和力。
表23:Biacore结果
实施例16:示例性抗CD3抗体分子的产生和评估
抗CD3抗体分子的产生
用携带序列QDGNEEMGGITQTPYKVSISGTTVILTC(SEQ ID NO:D215)的KLH缀合的CD3e肽对四只C57/BL6小鼠进行免疫。在第四次免疫后三天对动物取血,以检查滴度。第四次免疫后,用抗原对动物进行两次强化免疫。最终强化后三至四天,处死动物,采集脾或淋巴结组织。使用产生20个杂交瘤细胞板的标准融合方法融合脾。使用ELISA通过检查与肽的结合和随后与CD3e蛋白的结合进行初步筛选。选择一个克隆4D4用于扩增,并按照亚克隆方案生成单克隆杂交瘤。
抗CD3抗体分子与CD3的体外结合
在本实施例中,使用表面等离振子共振(SPR)测试了示例性人源化抗CD3抗体分子BKM0020、BKM0025、BKM0028、BKM0038(如本文所述)对人或食蟹猴CD3e的结合亲和力。通过使用BIAcore T200进行SPR测量。经由抗人Fc抗体将每个构建体固定在CM5芯片上至应答为200RU。将人CD3e(Acro Biosystems CDE-H5223)稀释至500nM,然后稀释两倍。将每种分析物浓度以20μl/min的流速注入固定有每种抗体的表面上。使用1∶1结合模型拟合数据。图28中示出了结合亲和力结果。与亲本相比,保留了对人CD3e的亲和力,并且比亲本抗体相比,对食蟹猴CD3e的亲和力降低至1/2至1/3。
抗CD3抗体分子与细胞上表达的CD3的结合
使用FACS进行示例性人源化抗CD3抗体与表达CD3的Jurkat细胞的结合。从10ug/ml浓度开始在一系列3倍稀释液中测试了抗体,并使用与AF647缀合的抗人IgG二抗进行检测。如图29中所示,人源化抗CD3mAb显示出与表达CD3的Jurkat细胞的强结合。
实施例17:抗钙网蛋白(CALR)抗体的生成
用mutCALR 5bp ins(BJ028)抗原对两只亚美尼亚仓鼠(86和87)进行免疫。选择仓鼠#86,使用标准程序进行融合。融合产生12个杂交瘤板,其通过ELISA筛选与BJ028(mutCALR ins)、BJ027(野生型CALR)和BIM0167(与人Fc融合的CALR突变型肽)的结合。进一步选择15个克隆用于扩增和亚克隆。选择两个克隆用于进一步表征和测序,以获得V基因序列。通过将CDR移植至人框架上使仓鼠序列进一步人源化。使用例如如上所述的Biacore和FACS测试了所得人源化mAb的结合。
实施例18:α-TRBV6-5抗体的优化
优化抗TRBV6-5抗体,以改善对人和食蟹猴抗原的亲和力,改善热稳定性,并除去可能引起化学稳定性问题的序列基序。使用随机诱变(Caldwell等人,(1992)Randomization of genes by PCR mutagenesis.PCR Meth.Appl.2:28)或修改版Kunkel诱变(Kunkel TA.(1985)Rapid and efficient site-specific mutagenesis withoutphenotypic selection.PNAS 82(2):488-92)构建scFv文库。为了提高亲和力,使用标准噬菌体展示(Lee,CM等人,(2007)Selection of human antibody fragments by phagedisplay.Nature protocols 2,3001)和酵母展示技术(Chao G等人,(2006)Isolating andengineering human antibodies using yeast surface display.Nature Protocols.1(2):755-69)进行针对人和食蟹猴抗原的文库选择。噬菌体或酵母群体的热攻击用于选择热稳定性改善的克隆。选择后采用标准筛选方法(例如ELISA和流式细胞术)来鉴定具有改善特性的单个克隆。点击测序和突变-活性相关性分析后,使用相同的上述方法构建第二代文库。如上重复文库选择和单个克隆筛选,变化之处在于应用更严格的条件来选择具有最大活性的克隆。点击测序后,将scFv基因重新格式化为生物学相关的抗体形式,用于表达、纯化和分类。
援引并入
本文提及的所有出版物和专利在此通过引用以其整体并入,如同每个单独的出版物或专利被明确且单独地表明通过引用并入。
等效物
本领域技术人员将认识到或仅使用常规实验的方法就能够确定本文所述的本发明具体实施方案的许多等效物。这些等效物旨在被以下权利要求涵盖。
示例性实施方案
上述多功能性分子、核酸、载体、宿主细胞或方法中任一种的其他特征包括以下示例性实施方案中的一个或多个。
本领域技术人员将认识到或仅使用常规实验的方法就能够确定本文所述的本发明具体实施方案的许多等效物。这些等效物旨在被以下示例性实施方案涵盖。
示例性实施方案1
本发明尤其涉及新型多特异性或多功能性分子,其包括(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的抗原结合结构域;以及以下中的一种、两种或全部:(ii)免疫细胞接合物(例如,选自NK细胞接合物、T细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物);(iii)细胞因子分子;和/或(iv)基质修饰部分。术语“多特异性”或“多功能性”在本文中可互换使用。
不希望受理论束缚,预期本文公开的多特异性或多功能性分子使免疫细胞(例如,选自NK细胞、T细胞、B细胞、树突细胞或巨噬细胞的免疫效应细胞)靶向(例如,定位、桥接和/或激活)表达钙网蛋白(例如,野生型或突变型钙网蛋白)的靶细胞(例如,癌细胞),并且/或者改变肿瘤基质,例如,改变癌症部位附近的肿瘤微环境。预期使用本文所述的多特异性分子增加免疫细胞的接近度和/或活性增强了针对靶细胞(例如,癌细胞)的免疫应答,从而提供更有效的治疗(例如,更有效的癌症治疗)。不受理论的束缚,认为针对靶细胞(例如,癌细胞)的靶向、定位的免疫应答降低了本文所述的多特异性分子的全身毒性作用。
因此,本文尤其提供了包括上述部分的多特异性分子(例如,多特异性或多功能性抗体分子)、编码其的核酸、产生上述分子的方法,以及使用上述分子治疗癌症的方法。
在一方面,本发明的特征在于一种检测样品或对象中的钙网蛋白(例如,野生型或突变型钙网蛋白)的方法,其包括:使样品或对象与本文所述的抗钙网蛋白抗体分子接触;以及检测抗体分子与样品或对象之间复合物的形成,从而检测钙网蛋白(例如,野生型或突变型钙网蛋白)。
在一些实施方案中,在体外或体内检测钙网蛋白(例如,野生型或突变型钙网蛋白)。
在一些实施方案中,该方法进一步包括使参考样品或对象与抗体分子接触;以及检测抗体分子与参考样品或对象之间复合物的形成,其中样品或对象中复合物的形成相对于参考样品或对象的变化(例如,统计学上显著的变化)指示样品或对象中存在钙网蛋白(例如,野生型或突变型钙网蛋白)。
在一些实施方案中,该方法进一步包括从对象获得样品。
在一些实施方案中,样品包含血浆、组织(例如,癌性组织)、活检、血液(例如,全血)、PBMC、骨髓和/或淋巴组织(例如,淋巴结)中的一种或多种。在一些实施方案中,样品未经冷冻和/或固定。在一些实施方案中,样品已经福尔马林固定(例如,福尔马林固定石蜡包埋(FFPE))。在一些实施方案中,样品已经染色(例如,用于免疫组织化学分析)。在一些实施方案中,样品已经冷冻和/或固定。
在一些实施方案中,对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
在一些实施方案中,该方法进一步包括例如使用多面板方法进行流式细胞术分析。在一些实施方案中,该方法进一步包括进行免疫组织化学(IHC)分析,例如,单色或多重形式。在一些实施方案中,IHC方法包括明视野显色IHC。在实施方案中,明视野显色IHC方法包括通过一抗直接检测抗原,例如,该一抗用不同的发色团直接标记。在一些实施方案中,IHC方法包括荧光IHC。在实施方案中,荧光IHC方法包括通过一抗直接检测抗原,例如,该一抗用不同的荧光团直接标记。在一些实施方案中,该方法进一步包括对样品(例如,固定样品,例如,FFPE样品)进行免疫组织化学。在一些实施方案中,该方法进一步包括测量来自生物样品的钙网蛋白+(例如,野生型钙网蛋白+或突变型钙网蛋白+)细胞的水平(例如,确定钙网蛋白+(例如,野生型钙网蛋白+或突变型钙网蛋白+)细胞例如相对于参考样品或对象是否耗尽)。在一些实施方案中,该方法进一步包括测量钙网蛋白(例如,野生型或突变型钙网蛋白)的胞内水平。在一些实施方案中,该方法进一步包括测量钙网蛋白(例如,野生型或突变型钙网蛋白)的膜水平。
在一些实施方案中,该方法包括组合本文所述检测方法中的两种或更多种。在实施方案中,该方法包括基于核酸的方法和基于抗体的方法。
在一些实施方案中,该方法进一步包括例如在(例如,用本文所述的抗体分子)治疗后,评估对象的预后、严重程度或疾病或病症(例如,癌症,例如,骨髓纤维化)存在或不存在的变化。
在一些实施方案中,抗体分子被可检测地标记。在一些实施方案中,抗体分子是抗钙网蛋白(例如,野生型或突变型钙网蛋白)抗体分子。
在一方面,本发明的特征在于一种评估对象的方法,其包括:使来自对象的样品(例如,本文所述的样品)与本文所述的抗钙网蛋白(例如,野生型或突变型钙网蛋白)抗体分子接触;以及
检测抗体分子与样品之间复合物的形成,从而评估对象。
在一些实施方案中,对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。在一些实施方案中,对象尚未用本文所述的抗体分子治疗。在一些实施方案中,对象已用本文所述的抗体分子治疗。
在一方面,本发明的特征在于一种试剂盒,其包含本文所述的抗钙网蛋白(例如,野生型或突变型钙网蛋白)抗体分子和用于例如根据本文所述的方法检测样品或对象中钙网蛋白(例如,野生型或突变型钙网蛋白)的方法的说明书。
因此,在一方面,本发明的特征在于一种多功能性分子,其包括:(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,例如,表4、表5、表6、表24、表25、表16、表17、表18或表19的任一者中公开的钙网蛋白靶向性抗原结合结构域,
以及(ii)结合至TCRβV的第二抗原结合结构域,例如,表30、表31、表32、表33、表11、表12或表13的任一者中公开的抗TCRβV抗原结合结构域,或结合至NKp30的第二抗原结合结构域,例如,表7、表8、表35、表36、表9、表10或表34中公开的抗NKp30抗原结合结构域。
在一些实施方案中,第二抗原结合结构域结合至TCRβV。
在一些实施方案中,第二抗原结合结构域激活T细胞,或第二抗原结合结构域不激活T细胞。
在一些实施方案中,第二抗原结合结构域结合至TCRβV12或TCRβV6(例如,包含SEQID NO:1044的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含如表30、表31、表32、表33、表11、表12或表13中所列的一个或多个氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含具有表30、表31、表33、表11、表12或表13中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表30、表31、表33、表11、表12或表13中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表30、表31、表33、表11、表12或表13中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,(ii)VL包含具有表30、表31、表33、表11、表12或表13中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表30、表31、表33、表11、表12或表13中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表30、表31、表33、表11、表12或表13中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:3A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:4A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:5A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:6A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:8A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(c)重链可变区(VH)和/或轻链可变区(VL),其中:(i)VH包含SEQ ID NO:45A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:46A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:47A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:51A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:52A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:53A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(d)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:48A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:49A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:50A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:54A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:55A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:56A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含表30、表31、表33、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含表30、表31、表33、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)
(iii)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(iv)VL包含SEQ ID NO:10A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:11A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:1312A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:1314A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:17A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:18A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:19A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:20A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:21A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:22A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:57A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:58A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:59A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:63A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:64A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:65A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:60A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:61A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:62A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:66A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:67A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:68A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:15A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:16A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含:
SEQ ID NO:23A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:24A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:25A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL包含:
SEQ ID NO:26A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:27A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:28A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:29A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:30A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,多功能性分子包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRVβ)的第一部分(例如,结合至TCR(例如,TCRVβ)的第一scFv),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRVβ)的任选第二部分(例如,结合至TCR(例如,TCRVβ)的第二scFv),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:
第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,第二抗原结合结构域结合至NKp30。
在一些实施方案中,第二抗原结合结构域选自结合至(例如,激活)NKp30的抗体分子(例如,抗原结合结构域)或配体,例如,第二抗原结合结构域是结合至(例如,激活)NKp30的抗体分子或配体。
在一些实施方案中,第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表7、表35、表9、表10或表34的VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表7、表35、表9、表10或表34的VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,和/或
(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表8、表36、表9、表10或表34的VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表8、表36、表9、表10或表34的VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3。
在一些实施方案中,第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7315的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7327的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7329的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQID NO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL,该VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQID NO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:
(i)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:
(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
或(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:
(1)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR4,和/或
(2)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR4。
在一些实施方案中,第二抗原结合结构域包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
在一些实施方案中,第二抗原结合结构域包含:
(i)VH,该VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,该VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含轻链,该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第二抗原结合结构域包含重链和轻链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
在一些实施方案中,多特异性分子包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:
第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中多功能性分子包含图3A或3B的构型。
在一些实施方案中,钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合至位于钙网蛋白的C-末端内的表位,任选地其中第一抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,多特异性分子进一步包含:
结合至第二钙网蛋白的第三抗原结合结构域,例如,其中第二钙网蛋白突变型蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中:
(i)第三抗原结合结构域不同于第一抗原结合结构域,或
(ii)第三抗原结合结构域与第一抗原结合结构域相同。
在一些实施方案中,第二钙网蛋白分子与第一抗原结合结构域结合的钙网蛋白分子相同。
在一些实施方案中,第二钙网蛋白分子不同于第一抗原结合结构域结合的钙网蛋白分子。
在一些实施方案中,第二钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中第二钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
在一些实施方案中,第一抗原结合结构域结合的钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第三抗原结合结构域结合至位于第二钙网蛋白的C-末端内的表位,任选地其中第三抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
在一些实施方案中,第一抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表4、表24、表25或表17中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3;
(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表5、表24、表25或表18中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;
(iii)VH,该VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(ii)VL,该VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);
(v)VH,该VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR4,和/或
(vi)VL,该VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR4。
在一些实施方案中,多功能性分子进一步包含肿瘤靶向部分。
在一些实施方案中,肿瘤靶向部分结合至肿瘤抗原。
在一些实施方案中,肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一些实施方案中,肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
在一些实施方案中,肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
在一些实施方案中,多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中多功能性分子与骨髓增生性赘生物细胞之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
在一些实施方案中,骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:
骨髓增生性赘生物细胞不包含JAK2 V617F突变,或
骨髓增生性赘生物细胞不包含MPL突变。
在一些实施方案中,多特异性分子进一步包含接头,例如,第一抗原结合结构域和第二抗原结合结构域之间的接头。
在一些实施方案中,接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
在一些实施方案中,接头是肽接头。
在一些实施方案中,肽接头包含Gly和Ser。
在一些实施方案中,肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
在另一方面,本发明提供了一种核酸分子,其编码如本文所述的多功能性分子。
在另一方面,本发明提供了一种载体,例如,表达载体,其包含如本文所述的核酸分子。
在另一方面,本发明提供了一种宿主细胞,其包含如本文所述的核酸分子或载体。
在另一方面,本发明提供了一种制备(例如,产生)如本文所述的多功能性分子的方法,其包括在合适的条件(例如,适于基因表达和/或同源或异源二聚化的条件)下,培养本文所述的宿主细胞。
在另一方面,本发明提供了一种药物组合物,其包含如本文所述的多功能性分子以及药学上可接受的载剂、赋形剂或稳定剂。
在另一方面,本发明提供了一种治疗癌症的方法,其包括向有需要的对象施用如本文公开的多功能性分子,其中多功能性分子以有效治疗癌症的量施用。
在另一方面,本发明提供了一种如本文所述的多功能性分子在治疗癌症中的用途。在另一方面,本发明提供了一种本文公开的用于治疗癌症的多功能性分子。
在一些实施方案中,对象具有表达第一和/或第二钙网蛋白的癌细胞。
在一些实施方案中,其中对象具有JAK2 V617F突变。
在一些实施方案中,对象不具有JAK2 V617F突变。
在一些实施方案中,对象具有MPL突变。
在一些实施方案中,对象不具有MPL突变。
在一些实施方案中,癌症是血液癌症,任选地其中癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML),任选地其中癌症是骨髓纤维化。
在一些实施方案中,癌症是实体瘤癌症。
在一些实施方案中,该方法或用途进一步包括施用第二种治疗性处理。
在一些实施方案中,第二种治疗性处理包括治疗性药剂(例如,化疗药剂、生物药剂、激素疗法)、放射或手术。
在一些实施方案中,治疗性药剂选自:化疗药剂或生物药剂。
在另一方面,本发明的特征在于一种多功能性分子(例如,多肽或编码其的核酸),其包括:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,
以及
(ii)以下中的一种、两种或全部:
(a)免疫细胞接合物,其选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物;
(b)细胞因子分子;
(c)基质修饰部分;或
(d)结合至肿瘤抗原的肿瘤靶向部分,例如,选自:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一方面,本发明的特征在于一种多功能性分子(例如,多肽或编码其的核酸),其包括:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,以及
(ii)包含免疫细胞接合物的第二抗原结合结构域(例如,T细胞接合物,例如,结合至TCRβV的抗原结合结构域,例如,如本文所述的)。
在一方面,本发明的特征在于一种多功能性分子(例如,多肽或编码其的核酸),其包括:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,以及
(ii)包含肿瘤靶向部分的第二抗原结合结构域,例如,其结合至选自以下的肿瘤抗原:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一方面,本发明的特征在于一种多功能性分子(例如,多肽或编码其的核酸),其包括:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,
(ii)包含免疫细胞接合物的第二抗原结合结构域(例如,T细胞接合物,例如,结合至TCRβV的抗原结合结构域,例如,如本文所述的,例如,本文所述的抗TCRβV抗体分子),以及
(iii)包含肿瘤靶向部分的第三抗原结合结构域,例如,其结合至选自以下的肿瘤抗原:G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
在一些实施方案中,多功能性分子进一步包含细胞因子分子或细胞因子分子的调节剂,例如,TGF-β抑制剂,例如,如本文所述的。
在一些实施方案中,多功能性分子进一步包含NK细胞接合物,例如,结合至Nkp30的抗原结合结构域,例如,如本文所述的。
在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6285、D1001或6286的氨基酸序列。在一些实施方案中,野生型钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。在一些实施方案中,钙网蛋白突变型蛋白包含SEQ ID NO:6286的氨基酸序列。
在一些实施方案中,第一抗原结合结构域包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6224的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6226的VHFWR2氨基酸序列、SEQ ID NO:6228的VHFWR3氨基酸序列,或SEQ ID NO:6230的VHFWR4氨基酸序列。在一些实施方案中,第一抗原结合结构域包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6232的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6234的VHFWR2氨基酸序列、SEQ ID NO:6236的VHFWR3氨基酸序列,或SEQ ID NO:6230的VHFWR4氨基酸序列。在一些实施方案中,第一抗原结合结构域包含轻链可变区(VL),该轻链可变区(VL)包含SEQ IDNO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6240的VLFWR2氨基酸序列、SEQID NO:6242的VLFWR3氨基酸序列,或SEQ ID NO:6244的VLFWR4氨基酸序列。
在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含选自SEQ IDNO:6285-6312或D1001的氨基酸序列。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含选自SEQ ID NO:6313-6346或D002-D1003的氨基酸序列。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)是表2或3中公开的钙网蛋白(例如,野生型或突变型钙网蛋白)。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6287的氨基酸序列。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6313的氨基酸序列。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6288的氨基酸序列。在一些实施方案中,钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6314的氨基酸序列。
在一些实施方案中,多功能性分子进一步包含优先结合至第二钙网蛋白(例如,野生型或突变型钙网蛋白)的第二抗原结合结构域。在一些实施方案中,第二钙网蛋白(例如,野生型或突变型钙网蛋白)包含SEQ ID NO:6286的氨基酸序列。在一些实施方案中,第二抗原结合结构域不同于第一抗原结合结构域。在一些实施方案中,第二抗原结合结构域与第一抗原结合结构域相同。在一些实施方案中,第二钙网蛋白(例如,野生型或突变型钙网蛋白)包含选自SEQ ID NO:6287-6312的氨基酸序列。在一些实施方案中,第二钙网蛋白(例如,野生型或突变型钙网蛋白)包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。在一些实施方案中,第二钙网蛋白(例如,野生型或突变型钙网蛋白)是表2或3中公开的钙网蛋白(例如,野生型或突变型钙网蛋白)。在一些实施方案中,第二钙网蛋白包含SEQ IDNO:6287的氨基酸序列。在一些实施方案中,第二钙网蛋白包含SEQ ID NO:6313的氨基酸序列。在一些实施方案中,第二钙网蛋白包含SEQ ID NO:6288的氨基酸序列。在一些实施方案中,第二钙网蛋白包含SEQ ID NO:6314的氨基酸序列。
在一些实施方案中,第一钙网蛋白(例如,野生型或突变型钙网蛋白)是1型钙网蛋白(例如,野生型或突变型钙网蛋白),并且第二钙网蛋白(例如,野生型或突变型钙网蛋白)是2型钙网蛋白(例如,野生型或突变型钙网蛋白)。在一些实施方案中,第一钙网蛋白包含SEQ ID NO:6287的氨基酸序列,并且第二钙网蛋白包含SEQ ID NO:6288的氨基酸序列。在一些实施方案中,第一钙网蛋白包含SEQ ID NO:6313的氨基酸序列,并且第一钙网蛋白包含SEQ ID NO:6314的氨基酸序列。
在一些实施方案中,野生型钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,第一抗原结合结构域对第一钙网蛋白(例如,突变型钙网蛋白)和野生型钙网蛋白具有大约相同的亲和力(例如,相等的亲和力)。
在一些实施方案中,第二抗原结合结构域对第二钙网蛋白(例如,突变型钙网蛋白)和野生型钙网蛋白具有大约相同的亲和力(例如,相等的亲和力)。
在一些实施方案中,第一抗原结合结构域对第一钙网蛋白突变型蛋白比对野生型钙网蛋白具有更高的亲和力。在一些实施方案中,第一抗原结合结构域与第一钙网蛋白突变型蛋白之间结合的KD不超过第一抗原结合结构域与野生型钙网蛋白之间结合的KD的40%、30%、20%、10%、1%、0.1%或0.01%。在一些实施方案中,第一抗原结合结构域结合至位于第一钙网蛋白突变型蛋白的C-末端内的表位。在一些实施方案中,第一抗原结合结构域结合至位于SEQ ID NO:6286的氨基酸序列内的表位。在一些实施方案中,第一抗原结合结构域不结合至野生型钙网蛋白。在一些实施方案中,野生型钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,第二抗原结合结构域对第二钙网蛋白突变型蛋白比对野生型钙网蛋白具有更高的亲和力。在一些实施方案中,第二抗原结合结构域与第二钙网蛋白突变型蛋白之间结合的KD不超过第二抗原结合结构域与野生型钙网蛋白之间结合的KD的40%、30%、20%、10%、1%、0.1%或0.01%。在一些实施方案中,第二抗原结合结构域结合至位于第二钙网蛋白突变型蛋白的C-末端内的表位。在一些实施方案中,第二抗原结合结构域结合至位于SEQ ID NO:6286的氨基酸序列内的表位。在一些实施方案中,第二抗原结合结构域不结合至野生型钙网蛋白。在一些实施方案中,野生型钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
在一些实施方案中,多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞。在一些实施方案中,多功能性分子与骨髓增生性赘生物细胞之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。在一些实施方案中,骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞。在一些实施方案中,骨髓增生性赘生物细胞不包含JAK2 V617F突变。在一些实施方案中,骨髓增生性赘生物细胞不包含MPL突变。
在一些实施方案中,第一和/或第二抗原结合结构域包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6253的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6254的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6255的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,第一和/或第二抗原结合结构域包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6253的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6254的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6255的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),以及(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQID NO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6253的VHCDR1氨基酸序列、SEQ ID NO:6254的VHCDR2氨基酸序列,以及SEQ ID NO:6255的VHCDR3氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6259的VLCDR1氨基酸序列、SEQ ID NO:6260的VLCDR2氨基酸序列,以及SEQ IDNO:6261的VLCDR3氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6253的VHCDR1氨基酸序列、SEQ ID NO:6254的VHCDR2氨基酸序列,以及SEQ ID NO:6255的VHCDR3氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6259的VLCDR1氨基酸序列、SEQ ID NO:6260的VLCDR2氨基酸序列,以及SEQ ID NO:6261的VLCDR3氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6224的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6226的VHFWR2氨基酸序列、SEQ IDNO:6228的VHFWR3氨基酸序列,和/或SEQ ID NO:6230的VHFWR4氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6240的VLFWR2氨基酸序列、SEQ ID NO:6242的VLFWR3氨基酸序列,和/或SEQ ID NO:6244的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6224的重链框架区1(VHFWR1)氨基酸序列、SEQ IDNO:6226的VHFWR2氨基酸序列、SEQ ID NO:6228的VHFWR3氨基酸序列,和/或SEQ ID NO:6230的VHFWR4氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ IDNO:6240的VLFWR2氨基酸序列、SEQ ID NO:6242的VLFWR3氨基酸序列,和/或SEQ ID NO:6244的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6264的VHFWR2氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6265的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:228的VHFWR4氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ IDNO:6277的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6278的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6279的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6264的VHFWR2氨基酸序列(或具有不超过1、2、3、4、5或6个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6265的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:228的VHFWR4氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6278的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6279的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列、SEQ ID NO:6264的VHFWR2氨基酸序列、SEQ ID NO:6265的VHFWR3氨基酸序列,和/或SEQ ID NO:228的VHFWR4氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列、SEQ IDNO:6278的VLFWR2氨基酸序列、SEQ ID NO:6279的VLFWR3氨基酸序列,和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6263的VHFWR1氨基酸序列、SEQ ID NO:6264的VHFWR2氨基酸序列、SEQ ID NO:6265的VHFWR3氨基酸序列,和/或SEQ ID NO:228的VHFWR4氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列、SEQ ID NO:6278的VLFWR2氨基酸序列、SEQ ID NO:6279的VLFWR3氨基酸序列,和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6247的氨基酸序列(或与SEQ ID NO:6247具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列(或与SEQ ID NO:6249具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6247的氨基酸序列(或与SEQ ID NO:6247具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),以及
(ii)VL,该VL包含SEQ ID NO:6249的氨基酸序列(或与SEQ ID NO:6249具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6247的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含(i)VH,该VH包含SEQ ID NO:6247的氨基酸序列,以及(ii)VL,该VL包含SEQ ID NO:6249的氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含与SEQ IDNO:6250具有至少70%或75%序列同一性的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含与SEQ ID NO:6252具有至少85%或90%序列同一性的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含(i)VH,该VH包含与SEQ ID NO:6250具有至少70%或75%序列同一性的氨基酸序列,以及(ii)VL,该VL包含与SEQ ID NO:6252具有至少85%或90%序列同一性的氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6256的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6257的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6258或116的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。在一些实施方案中,第一和/或第二抗原结合结构域包含轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6256的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6257的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6258或116的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6259的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6260的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6261的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6232的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6234的VHFWR2氨基酸序列、SEQ IDNO:6236的VHFWR3氨基酸序列,和/或SEQ ID NO:6230的VHFWR4氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6240的VLFWR2氨基酸序列、SEQ ID NO:6242的VLFWR3氨基酸序列,和/或SEQ ID NO:6244的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6232的重链框架区1(VHFWR1)氨基酸序列、SEQ IDNO:6234的VHFWR2氨基酸序列、SEQ ID NO:6236的VHFWR3氨基酸序列,和/或SEQ ID NO:6230的VHFWR4氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6238的轻链框架区1(VLFWR1)氨基酸序列、SEQ IDNO:6240的VLFWR2氨基酸序列、SEQ ID NO:6242的VLFWR3氨基酸序列,和/或SEQ ID NO:6244的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6266的重链框架1(VHFWR1)氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6267的VHFWR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6268的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ IDNO:6269的VHFWR4氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6278的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6279的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:6266的重链框架1(VHFWR1)氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6267的VHFWR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQID NO:6268的VHFWR3氨基酸序列(或具有不超过1、2、3、4、5、6、7、8、9、10或11个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6269的VHFWR4氨基酸序列,以及
(ii)VL,该VL包含SEQ ID NO:6277的VLFWR1氨基酸序列(或具有不超过1、2或3个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6278的VLFWR2氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6279的VLFWR3氨基酸序列(或具有不超过1个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:6280的VLFWR4氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6248的氨基酸序列(或与SEQ ID NO:6248具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列(或与SEQ ID NO:6249具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含
(i)VH,该VH包含SEQ ID NO:6248的氨基酸序列(或与SEQ ID NO:6248具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),以及
(ii)VL,该VL包含SEQ ID NO:6249的氨基酸序列(或与SEQ ID NO:6249具有至少约93%、95%或99%序列同一性的氨基酸序列)。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含SEQ ID NO:6248的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含SEQ ID NO:6249的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含(i)VH,该VH包含SEQ ID NO:6248的氨基酸序列,以及(ii)VL,该VL包含SEQ ID NO:6249的氨基酸序列。
在一些实施方案中,第一和/或第二抗原结合结构域包含VH,该VH包含与SEQ IDNO:6251具有至少70%或74%序列同一性的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含VL,该VL包含与SEQ ID NO:6252具有至少85%或90%序列同一性的氨基酸序列。在一些实施方案中,第一和/或第二抗原结合结构域包含(i)VH,该VH包含与SEQ ID NO:6251具有至少70%或74%序列同一性的氨基酸序列,和/或(ii)VL,该VL包含与SEQ ID NO:6252具有至少85%或90%序列同一性的氨基酸序列。
在一些实施方案中,多功能性分子包含免疫细胞接合物,其选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物。在一些实施方案中,免疫细胞接合物结合至并激活免疫细胞,例如,效应细胞。在一些实施方案中,免疫细胞接合物结合至但不激活免疫细胞,例如,效应细胞。
在一些实施方案中,免疫细胞接合物是T细胞接合物,例如,介导对T细胞的结合和激活的T细胞接合物,或介导对T细胞的结合但不介导其激活的T细胞接合物。在一些实施方案中,T细胞接合物结合至CD3、TCRα、TCRβ、TCRγ、TCRζ、ICOS、CD28、CD27、HVEM、LIGHT、CD40、4-1BB、OX40、DR3、GITR、CD30、TIM1、SLAM、CD2或CD226。在一些实施方案中,T细胞接合物是抗CD3抗体分子。在一些实施方案中,T细胞接合物是抗TCRβ抗体分子,例如,本文所述的抗TCRβV抗体分子。
在一些实施方案中,免疫细胞接合物是NK细胞接合物,例如,介导对NK细胞的结合和激活的NK细胞接合物,或介导对NK细胞的结合但不介导其激活的NK细胞接合物。在一些实施方案中,NK细胞接合物选自结合至(例如,激活)以下的抗体分子(例如,抗原结合结构域)或配体:NKp30、NKp40、NKp44、NKp46、NKG2D、DNAM1、DAP10、CD16(例如,CD16a、CD16b或两者)、CRTAM、CD27、PSGL1、CD96、CD100(SEMA4D)、NKp80、CD244(也称为SLAMF4或2B4)、SLAMF6、SLAMF7、KIR2DS2、KIR2DS4、KIR3DS1、KIR2DS3、KIR2DS5、KIR2DS1、CD94、NKG2C、NKG2E或CD160。在一些实施方案中,NK细胞接合物是结合至(例如,激活)NKp30的抗体分子或配体。在一些实施方案中,NK细胞接合物是抗体分子,例如,抗原结合结构域。在一些实施方案中,NK细胞接合物是结合至NKp30或NKp46的抗体分子,例如,抗原结合结构域。在一些实施方案中,NK细胞接合物是配体,任选地,该配体进一步包含免疫球蛋白恒定区,例如,Fc区。在一些实施方案中,NK细胞接合物是NKp44或NKp46的配体,例如,病毒HA。在一些实施方案中,NK细胞接合物是DAP10的配体,例如,NKG2D的辅助受体。在一些实施方案中,NK细胞接合物是CD16的配体,例如,CD16a/b配体,例如,进一步包含抗体Fc区的CD16a/b配体。在一些实施方案中,免疫细胞接合物介导B细胞、巨噬细胞和/或树突细胞中的一种或多种的结合或激活或两者。
在一些实施方案中,免疫细胞接合物包含选自CD40配体(CD40L)或CD70配体中的一种或多种的B细胞、巨噬细胞和/或树突细胞接合物;结合至CD40或CD70的抗体分子;抗OX40的抗体分子;OX40配体(OX40L);Toll样受体的激动剂(例如,TLR4,例如,组成型活性TLR4(caTLR4)或TLR9激动剂);41BB;CD2激动剂;CD47;或STING激动剂,或其组合。在一些实施方案中,免疫细胞接合物是B细胞接合物,例如,CD40L、OX40L或CD70配体,或结合至OX40、CD40或CD70的抗体分子。在一些实施方案中,免疫细胞接合物是巨噬细胞接合物,例如,CD2激动剂;CD40L;OX40L;结合至OX40、CD40或CD70的抗体分子;Toll样受体(TLR)的激动剂(例如,TLR4,例如,组成型活性TLR4(caTLR4)或TLR9激动剂);CD47;或STING激动剂。在一些实施方案中,免疫细胞接合物是树突细胞接合物,例如,CD2激动剂、OX40抗体、OX40L、41BB激动剂、Toll样受体激动剂或其片段(例如,TLR4,例如,组成型活性TLR4(caTLR4))、CD47激动剂或STING激动剂。在一些实施方案中,STING激动剂包含环状二核苷酸,例如,环状二-GMP(cdGMP)、环状二-AMP(cdAMP)或其组合,任选地具有2’,5’或3’,5’磷酸酯键,例如,其中STING激动剂共价偶联至多功能性分子。
在一些实施方案中,多功能性分子包含细胞因子分子或其调节剂。在一些实施方案中,细胞因子分子选自TGF-β、白介素-2(IL-2)、白介素-7(IL-7)、白介素-12(IL-12)、白介素-15(IL-15)、白介素-18(IL-18)、白介素-21(IL-21)或干扰素γ,或其片段或变体,或上述细胞因子中任一种的组合。在一些实施方案中,细胞因子分子是单体或二聚体。在一些实施方案中,细胞因子分子进一步包含受体二聚化结构域,例如,IL15Rα二聚化结构域。在一些实施方案中,细胞因子分子(例如,IL-15)和受体二聚化结构域(例如,IL15Rα二聚化结构域)不是共价连接的,例如,是非共价缔合的。
在一些实施方案中,细胞因子分子的调节剂包含TGF-β抑制剂。
在一些实施方案中,多功能性分子包含基质修饰部分。在一些实施方案中,基质修饰部分导致以下中的一种或多种:减少基质或胞外基质(ECM)组分的水平或产生;减少肿瘤纤维化;增加间质肿瘤转运;改善肿瘤灌注;扩张肿瘤微脉管系统;降低肿瘤中的间质液压力(IFP);或者减少或增强药剂(例如,癌症治疗剂或细胞疗法)进入肿瘤或肿瘤脉管系统的渗透或扩散。在一些实施方案中,减少的基质或ECM组分选自糖胺聚糖或胞外蛋白,或其组合。在一些实施方案中,糖胺聚糖选自透明质酸(也称为玻尿酸或HA)、硫酸软骨素、软骨素、硫酸皮肤素、硫酸肝素、肝素、巢蛋白、腱生蛋白、聚集蛋白聚糖或硫酸角蛋白。在一些实施方案中,胞外蛋白选自胶原、层粘连蛋白、弹性蛋白、纤维蛋白原、纤连蛋白或玻连蛋白。在一些实施方案中,基质修饰部分包含降解肿瘤基质或胞外基质(ECM)的酶分子。在一些实施方案中,酶分子选自透明质酸酶分子、胶原酶分子、软骨素酶分子、基质金属蛋白酶分子(例如,巨噬细胞金属弹性蛋白酶),或上述中任一种的变体(例如,片段)。在一些实施方案中,基质修饰部分减少玻尿酸的水平或产生。在一些实施方案中,基质修饰部分包含透明质酸降解酶、抑制透明质酸合成的药剂,或针对玻尿酸的抗体分子。在一些实施方案中,透明质酸降解酶是透明质酸酶分子或其变体(例如,其片段)。在一些实施方案中,透明质酸降解酶在中性或酸性pH(例如,约pH 4-5)中具有活性。在一些实施方案中,透明质酸酶分子是哺乳动物透明质酸酶分子,例如,重组人透明质酸酶分子或其变体(例如,其截短形式)。在一些实施方案中,透明质酸酶分子选自HYAL1、HYAL2或PH-20/SPAM1,或其变体(例如,其截短形式)。在一些实施方案中,截短形式缺少C-末端糖基磷脂酰肌醇(GPI)附着位点或GPI附着位点的一部分。在一些实施方案中,透明质酸酶分子是糖基化的,例如,包含至少一个N-连接的聚糖。在一些实施方案中,透明质酸酶分子包含SEQ ID NO:6213的氨基酸序列或其片段,或与其基本相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6213的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。在一些实施方案中,透明质酸酶分子包含SEQ ID NO:6213的36-464位氨基酸残基。在一些实施方案中,透明质酸酶分子包含PH20的36-481位、36-482位或36-483位氨基酸残基,其中PH20具有SEQ ID NO:6213的氨基酸序列。在一些实施方案中,透明质酸酶分子包含与SEQ ID NO:6213的多肽或氨基酸序列的截短形式具有至少95%至100%序列同一性的氨基酸序列。在一些实施方案中,透明质酸酶分子包含对于SEQ ID NO:6213的氨基酸序列具有30、20、10、5或更少个氨基酸置换的氨基酸序列。在一些实施方案中,透明质酸酶分子包含与SEQ ID NO:6213的氨基酸序列至少95%(例如,至少95%、96%、97%、98%、99%、100%)相同的氨基酸序列。在一些实施方案中,透明质酸酶分子由与SEQID NO:6213的核苷酸序列至少95%(例如,至少96%、97%、98%、99%、100%)相同的核苷酸序列编码。在一些实施方案中,透明质酸酶分子是PH20,例如,rHuPH20。在一些实施方案中,透明质酸酶分子是HYAL1,并且包含SEQ ID NO:6218的氨基酸序列,或其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6218的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)进一步包含聚合物,例如,与聚合物(例如,PEG)缀合。在一些实施方案中,透明质酸降解酶是PEG化的PH20酶(PEGPH20)。在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)进一步包含免疫球蛋白链恒定区(例如,Fc区),其选自例如IgG1、IgG2、IgG3或IgG4的重链恒定区,更特别是人IgG1、IgG2、IgG3或IgG4的重链恒定区。在一些实施方案中,免疫球蛋白恒定区(例如,Fc区)与透明质酸降解酶(例如,透明质酸酶分子)连接,例如,共价连接。在一些实施方案中,免疫球蛋白链恒定区(例如,Fc区)被改变(例如,突变),以增加或减少以下中的一种或多种:Fc受体结合、抗体糖基化、半胱氨酸残基数量、效应细胞功能或补体功能。在一些实施方案中,透明质酸降解酶(例如,透明质酸酶分子)形成二聚体。在一些实施方案中,基质修饰部分包含透明质酸合成的抑制剂,例如,HA合酶。在一些实施方案中,抑制剂包含针对HA合酶的有义或反义核酸分子,或是小分子药物。在一些实施方案中,抑制剂是4-甲基伞形酮(MU)或其衍生物(例如,6,7-二羟基-4-甲基香豆素或5,7-二羟基-4-甲基香豆素),或来氟米特或其衍生物。在一些实施方案中,基质修饰部分包含胶原酶分子(例如,哺乳动物胶原酶分子),或其变体(例如,片段)。在一些实施方案中,胶原酶分子是胶原酶分子IV,例如,包含SEQ ID NO:6219的氨基酸序列,或其片段,或与其基本上相同(例如,与其95%至99.9%相同,或对于SEQ ID NO:6219的氨基酸序列具有至少一个氨基酸改变,但不超过五个、十个或十五个改变(例如,置换、缺失或插入,例如,保守置换))的氨基酸序列。
在一些实施方案中,多功能性分子包含免疫细胞接合物(例如,T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物)和细胞因子分子。在一些实施方案中,多功能性分子包含免疫细胞接合物(例如,T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物)和基质修饰部分。在一些实施方案中,多功能性分子包含细胞因子分子和基质修饰部分。在一些实施方案中,多功能性分子包含免疫细胞接合物(例如,T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物)、细胞因子分子和基质修饰部分。
在一些实施方案中,多功能性分子包含至少两条非连续多肽链。
在一些实施方案中,多功能性分子包含以下构型:
A,B-[二聚化模块]-C,-D
例如,图1A、1B和1C中所示的构型,其中:
(1)二聚化模块包含免疫球蛋白恒定结构域(例如,重链恒定结构域(例如,同源二聚体或异源二聚体重链恒定区,例如,Fc区))或免疫球蛋白可变区的恒定结构域(例如,Fab区);以及
(2)A、B、C和D独立地不存在;(i)结合钙网蛋白(例如,野生型钙网蛋白或突变型钙网蛋白)的抗原结合结构域,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列;(ii)免疫细胞接合物,其选自T细胞接合物、NK细胞接合物、B细胞接合物、树突细胞接合物或巨噬细胞接合物;(iii)细胞因子分子;或(iv)基质修饰部分,条件是:
A、B、C和D中的至少一个、两个或三个包含结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变体)的抗原结合结构域,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且剩余的A、B、C和D中的任一个不存在,或包含免疫细胞接合物、细胞因子分子或基质修饰部分中的一种。
在一些实施方案中,
(i)A包含结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含免疫细胞接合物,例如,T细胞接合物,例如,抗CD3抗体分子;
(ii)A包含结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含细胞因子分子;
(iii)A包含结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含基质修饰部分;
(iv)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含免疫细胞接合物,例如,T细胞接合物,例如,抗CD3抗体分子;
(v)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含细胞因子分子;
(vi)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含基质修饰部分;
(vii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含免疫细胞接合物,例如,T细胞接合物,例如,抗CD3抗体分子;
(viii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含细胞因子分子;
(ix)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含基质修饰部分;
(x)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)细胞因子分子;
(xi)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)基质修饰部分;
(xii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含(a)细胞因子分子和(b)基质修饰部分;
(xiii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)细胞因子分子;(xiv)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ IDNO:6286的氨基酸序列,并且C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)基质修饰部分;(xv)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含(a)细胞因子分子和(b)基质修饰部分;
(xvi)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)细胞因子分子;(xvii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ IDNO:6286的氨基酸序列,并且B或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)和(b)基质修饰部分;(xviii)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含(a)细胞因子分子和(b)基质修饰部分;
(xix)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B、C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)、(b)细胞因子分子和(c)基质修饰部分;
(xx)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,B包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且C或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)、(b)细胞因子分子和(c)基质修饰部分;或(xxi)A包含结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,其中第一钙网蛋白包含SEQ ID NO:6286的氨基酸序列,C包含结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,并且B或D包含(a)免疫细胞接合物(例如,T细胞接合物,例如,抗CD3抗体分子)、(b)细胞因子分子和(c)基质修饰部分。
在一些实施方案中,二聚化模块包含一个或多个免疫球蛋白链恒定区(例如,Fc区),该免疫球蛋白链恒定区包含以下中的一种或多种:成对的空腔-突起(“杵-臼”)、静电相互作用或链交换。在一些实施方案中,一个或多个免疫球蛋白链恒定区(例如,Fc区)在选自例如人IgG1Fc区的347、349、350、351、366、368、370、392、394、395、397、398、399、405、407或409中的一个或多个位置处包含氨基酸置换。在一些实施方案中,一个或多个免疫球蛋白链恒定区(例如,Fc区)包含选自以下的氨基酸置换:T366S、L368A或Y407V(例如,对应于空腔或臼),或T366W(例如,对应于突起或杵)或其组合。
在一些实施方案中,多功能性分子进一步包含接头,例如,在以下中的一个或多个之间的接头:抗原结合结构域和免疫细胞接合物、抗原结合结构域和细胞因子分子、抗原结合结构域和基质修饰部分、免疫细胞接合物和细胞因子分子、免疫细胞接合物和基质修饰部分、细胞因子分子和基质修饰部分、抗原结合结构域和二聚化模块、免疫细胞接合物和二聚化模块、细胞因子分子和二聚化模块,或基质修饰部分和二聚化模块。在一些实施方案中,接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。在一些实施方案中,接头是肽接头。在一些实施方案中,肽接头包含Gly和Ser。在一些实施方案中,肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
在一方面,本发明提供了一种多功能性分子,其包含:
(i)结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,例如,其中钙网蛋白突变型蛋白包含SEQ ID NO:6286的氨基酸序列,以及
(ii)结合至CD3的部分,例如,结合至CD3的抗体分子。
在一些实施方案中,多功能性分子包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至CD3的第一部分(例如,结合至CD3的第一scFv),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至CD3的任选第二部分(例如,结合至CD3的第二scFv),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第一和第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,任选地其中第一和第二钙网蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子。
在一些实施方案中,多功能性分子包含图2A或2B的构型。
在一方面,本发明提供了一种多功能性分子,其包含:
(i)结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,例如,其中钙网蛋白突变型蛋白包含SEQ ID NO:6286的氨基酸序列,以及
(ii)结合至TCR(例如,TCRβ)的部分,例如,结合至TCR(例如,TCRβ)的抗体分子。
在一些实施方案中,多功能性分子包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRβ)的第一部分(例如,结合至TCR(例如,TCRβ)的第一scFv),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRβ)的任选第二部分(例如,结合至TCR(例如,TCRβ)的第二scFv),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第一和第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,任选地其中第一和第二钙网蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子。
在一些实施方案中,多功能性分子包含图3A或3B的构型。
在一方面,本发明提供了一种多功能性分子,其包含:
(i)结合至钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的抗原结合结构域,例如,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列,以及
(ii)结合至NKp30的部分,例如,结合至(例如,激活)NKp30的抗体分子或配体。
在一些实施方案中,多功能性分子包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:第一VL和第一VH形成结合至第一钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白(例如,野生型钙网蛋白或钙网蛋白突变型蛋白)的第二抗原结合结构域,其中第一和第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列,任选地其中第一和第二钙网蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子。
在一些实施方案中,多功能性分子包含图4A或4B的构型。
在另一方面,本发明提供了一种分离的核酸分子,其编码本文所述的任何多特异性或多功能性分子。在另一方面,本发明提供了一种分离的核酸分子,其包含编码本文所述的多特异性或多功能性分子中任一种的核苷酸序列,或与其基本上同源(例如,与其至少80%、90%、95%至99.9%相同)的核苷酸序列。在另一方面,本发明提供了一种宿主细胞,其包含本文所述的核酸分子或载体。
在另一方面,本发明提供了一种制备(例如,产生)本文所述的多特异性或多功能性分子多肽的方法,其包括在合适的条件(例如,适于基因表达和/或同源或异源二聚化的条件)下,培养本文所述的宿主细胞。
在另一方面,本发明提供了一种药物组合物,其包含本文所述的多特异性或多功能性分子多肽以及药学上可接受的载剂、赋形剂或稳定剂。
在另一方面,本发明提供了一种治疗癌症的方法,其包括向有需要的对象施用本文所述的多特异性或多功能性分子多肽,其中多特异性抗体以有效治疗癌症的量施用。在一些实施方案中,对象具有表达第一和/或第二钙网蛋白突变体的癌细胞。在一些实施方案中,对象具有表达第一、第二或第三肿瘤抗原的肿瘤细胞,例如,对象具有表达选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的肿瘤细胞。在一些实施方案中,对象具有JAK2V617F突变。在一些实施方案中,对象不具有JAK2 V617F突变。在一些实施方案中,对象具有MPL突变。在一些实施方案中,对象不具有MPL突变。在一些实施方案中,癌症是血液癌症,任选地其中癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML)。在一些实施方案中,癌症是骨髓纤维化。在一些实施方案中,癌症是实体瘤癌症。在一些实施方案中,实体瘤癌症是胰癌(例如,胰腺癌)、乳腺癌、结肠直肠癌、肺癌(例如,小细胞或非小细胞肺癌)、皮肤癌、卵巢癌或肝癌中的一种或多种。
在一些实施方案中,癌细胞包含骨髓增生性赘生物细胞。在一些实施方案中,骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞。在一些实施方案中,骨髓增生性赘生物细胞是骨髓纤维化细胞。在一些实施方案中,骨髓增生性赘生物细胞是原发性血小板增多症细胞。在一些实施方案中,骨髓增生性赘生物细胞是真性红细胞增多症细胞。在一些实施方案中,骨髓增生性赘生物细胞是慢性髓性癌细胞。在一些实施方案中,骨髓增生性赘生物细胞包含JAK2突变(例如,JAK2 V617F突变)。在一些实施方案中,骨髓增生性赘生物细胞包含钙网蛋白突变。在一些实施方案中,骨髓增生性赘生物细胞包含MPL突变。
在一些实施方案中,该方法进一步包括施用第二种治疗性处理。在一些实施方案中,第二种治疗性处理包括治疗性药剂(例如,化疗药剂、生物药剂、激素疗法)、放射或手术。在一些实施方案中,治疗性药剂选自:化疗药剂或生物药剂。
示例性实施方案2
1.一种多功能性分子,其包含:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,例如,表4、表5、表6、表24、表25、表16、表17、表18或表19的任一者中公开的钙网蛋白靶向性抗原结合结构域,
以及
(ii)结合至TCRβV的第二抗原结合结构域,例如,表30、表31、表32、表33、表11、表12或表13的任一者中公开的抗TCRβV抗原结合结构域,或
结合至NKp30的第二抗原结合结构域,例如,表7、表8、表35、表36、表9、表10或表34中公开的抗NKp30抗原结合结构域。
2.根据实施方案1的多功能性分子,其中第二抗原结合结构域结合至TCRβV。
3.根据实施方案2的多功能性分子,其中第二抗原结合结构域激活T细胞,或第二抗原结合结构域不激活T细胞。
4.根据实施方案2或3的多功能性分子,其中第二抗原结合结构域结合至TCRβV12或TCRβV6(例如,包含SEQ ID NO:1044的氨基酸序列)。
5.根据实施方案2-4中任一项的多功能性分子,其中第二抗原结合结构域包含如表30、表31、表32、表33、表11、表12或表13中所列的一个或多个氨基酸序列。
6.根据实施方案2-5中任一项的多功能性分子,其中第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含具有表30、表31、表33、表11、表12或表13中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表30、表31、表33、表11、表12或表13中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表30、表31、表33、表11、表12或表13中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,(ii)VL包含具有表30、表31、表33、表11、表12或表13中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表30、表31、表33、表11、表12或表13中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表30、表31、表33、表11、表12或表13中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:3的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:4的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:5的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)VL包含SEQ ID NO:6的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:8的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:45的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:46的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:47的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或|
(ii)VL包含SEQ ID NO:51的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:52的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:53的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或|
(d)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:48的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:49的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:50的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或|
(ii)VL包含SEQ ID NO:54的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:55的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:56的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
7.根据实施方案2-5中任一项的多功能性分子,其中第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含表30、表31、表33、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含表30、表31、表33、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)
(iii)VH包含SEQ ID NO:9的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或(iv)VL包含SEQ ID NO:10的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:9的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:11的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:1312的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:1314的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
8.根据实施方案2-5中任一项的多功能性分子,其中第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:17的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:18的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:19的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或|
(ii)VL包含SEQ ID NO:20的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:21的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:22的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:57的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:58的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:59的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或|
(i)VL包含SEQ ID NO:63的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:64的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:65的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或|
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:60的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:61的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:62的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或|
(ii)VL包含SEQ ID NO:66的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:67的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:68的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
9.根据实施方案2-5中任一项的多功能性分子,其中第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含SEQ ID NO:15的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL包含SEQ ID NO:16的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)VH包含:
SEQ ID NO:23的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:24的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:25的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL包含:
SEQ ID NO:26的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:27的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:28的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:29的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:30的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
10.根据实施方案2-9中任一项的多功能性分子,其包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRVβ)的第一部分(例如,结合至TCR(例如,TCRVβ)的第一scFv),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRVβ)的任选第二部分(例如,结合至TCR(例如,TCRVβ)的第二scFv),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:
第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中多功能性分子包含图3A或3B的构型。
11.根据实施方案1的多功能性分子,其中第二抗原结合结构域结合至NKp30。
12.根据实施方案11的多功能性分子,其中第二抗原结合结构域选自结合至(例如,激活)NKp30的抗体分子(例如,抗原结合结构域)或配体,例如,第二抗原结合结构域是结合至(例如,激活)NKp30的抗体分子或配体。
13.根据实施方案11或12的多功能性分子,其中第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表7、表35、表9、表10或表34的VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表7、表35、表9、表10或表34的VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,和/或
(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表8、表36、表9、表10或表34的VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表8、表36、表9、表10或表34的VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3。
14.根据实施方案13的多功能性分子,其中第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7315的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7327的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7329的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
15.根据实施方案13或14的多功能性分子,其中第二抗原结合结构域包含:
(i)VH,该VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQID NO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL,该VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQID NO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
16.根据实施方案13-15中任一项的多功能性分子,其中第二抗原结合结构域包含:
(i)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)VH和VL,该VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
17.根据实施方案13-16中任一项的多功能性分子,其中第二抗原结合结构域包含:
(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
18.根据实施方案11或12的多功能性分子,其中第二抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
19.根据实施方案11、12或18中任一项的多功能性分子,其中第二抗原结合结构域包含:
(1)重链可变区(VH),该重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR4,和/或
(2)轻链可变区(VL),该轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR4。
20.根据实施方案19的多功能性分子,其中第二抗原结合结构域包含:
(1)重链可变区(VH),该重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),该轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
21.根据实施方案11、12或18-20中任一项的多功能性分子,其中第二抗原结合结构域包含:
(i)VH,该VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,该VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
22.根据实施方案11、12或18-21中任一项的多功能性分子,其中第二抗原结合结构域包含重链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
23.根据实施方案11、12或18-22中任一项的多功能性分子,其中第二抗原结合结构域包含轻链,该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
24.根据实施方案11、12或18-23中任一项的多功能性分子,其中第二抗原结合结构域包含重链和轻链,该重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),该轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或的99%序列同一性的氨基酸序列)。
25.根据实施方案11-24中任一项的多功能性分子,其包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,其中:
第一VL和第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且第二VL和第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,任选地其中第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中多功能性分子包含图3A或3B的构型。
26.根据前述实施方案中任一项的多功能性分子,其中钙网蛋白包含选自SEQ IDNO:6285-6312或D1001的氨基酸序列,任选地其中钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
27.根据前述实施方案中任一项的多功能性分子,其中钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
28.根据前述实施方案中任一项的多功能性分子,其中钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
29.根据前述实施方案中任一项的多功能性分子,其中第一抗原结合结构域结合至位于钙网蛋白的C-末端内的表位,任选地其中第一抗原结合结构域结合至位于SEQ IDNO:6285、D1001或6286的氨基酸序列内的表位。
30.根据前述实施方案中任一项的多功能性分子,其进一步包含结合至第二钙网蛋白的第三抗原结合结构域,例如,其中第二钙网蛋白突变型蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中:
(i)第三抗原结合结构域不同于第一抗原结合结构域,或
(ii)第三抗原结合结构域与第一抗原结合结构域相同。
31.根据实施方案30的多功能性分子,其中第二钙网蛋白分子与第一抗原结合结构域结合的钙网蛋白分子相同。
32.根据实施方案30的多功能性分子,其中第二钙网蛋白分子不同于第一抗原结合结构域结合的钙网蛋白分子。
33.根据实施方案30-32中任一项的多功能性分子,其中第二钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中第二钙网蛋白包含选自SEQ IDNO:6313-6346或D1002-D1003的氨基酸序列。
34.根据实施方案33的多功能性分子,其中第一抗原结合结构域结合的钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
35.根据实施方案30-34中任一项的多功能性分子,其中第三抗原结合结构域结合至位于第二钙网蛋白的C-末端内的表位,任选地其中第三抗原结合结构域结合至位于SEQID NO:6285、D1001或6286的氨基酸序列内的表位。
36.根据前述实施方案中任一项的多功能性分子,其中第一抗原结合结构域包含:
(i)重链可变区(VH),该重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表4、表24、表25或表17中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3;
(ii)轻链可变区(VL),该轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表5、表24、表25或表18中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;
(iii)VH,该VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(iv)VL,该VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);
(v)VH,该VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR4,和/或(vi)VL,该VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR4。
37.根据前述实施方案中任一项的多功能性分子,其中多功能性分子进一步包含肿瘤靶向部分。
38.根据实施方案37的多功能性分子,其中肿瘤靶向部分结合至肿瘤抗原。
39.根据实施方案38的多功能性分子,其中肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
40.根据实施方案37的多功能性分子,其中肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
41.根据实施方案40的多功能性分子,其中肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
42.根据前述实施方案中任一项的多功能性分子,其中多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中多功能性分子与骨髓增生性赘生物细胞之间的结合是多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
43.根据实施方案42的多功能性分子,其中骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:
骨髓增生性赘生物细胞不包含JAK2 V617F突变,或
骨髓增生性赘生物细胞不包含MPL突变。
44.根据前述实施方案中任一项的多功能性分子,其进一步包含接头,例如,第一抗原结合结构域和第二抗原结合结构域之间的接头。
45.根据实施方案44的多功能性分子,其中接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
46.根据实施方案44或45的多功能性分子,其中接头是肽接头。
47.根据实施方案46的多功能性分子,其中肽接头包含Gly和Ser。
48.根据实施方案46的多功能性分子,其中肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
49.一种核酸分子,其编码前述实施方案中任一项的多功能性分子。
50.一种载体,例如,表达载体,其包含实施方案49的核酸分子。
51.一种细胞,其包含实施方案49的核酸分子或实施方案50的载体。
52.一种制备(例如,产生)实施方案1-48中任一项的多功能性分子的方法,其包括在合适的条件(例如,适于基因表达和/或同源或异源二聚化的条件)下,培养实施方案51的细胞。
53.一种药物组合物,其包含实施方案1-48中任一项的多功能性分子以及药学上可接受的载剂、赋形剂或稳定剂。
54.一种治疗癌症的方法,其包括向有需要的对象施用实施方案1-48中任一项的多功能性分子,其中多功能性分子以有效治疗癌症的量施用。
55.实施方案1-48中任一项的多功能性分子在制造用于治疗癌症的药物中的用途。
56.根据实施方案54的方法或实施方案55的用途,其中对象具有表达第一和/或第二钙网蛋白的癌细胞。
57.根据实施方案54或56的方法或实施方案55或56的用途,其中对象具有JAK2V617F突变。
58.根据实施方案54或56的方法或实施方案55或56的用途,其中对象不具有JAK2V617F突变。
59.根据实施方案54或56-58中任一项的方法或实施方案55-58中任一项的用途,其中对象具有MPL突变。
60.根据实施方案54或56-58中任一项的方法或实施方案55-58中任一项的用途,其中对象不具有MPL突变。
61.根据实施方案54或56-60中任一项的方法或实施方案55-60中任一项的用途,其中癌症是血液癌症,任选地其中癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML),任选地其中癌症是骨髓纤维化。
62.根据实施方案54或56-60中任一项的方法或实施方案55-60中任一项的用途,癌症是实体瘤癌症。
63.根据实施方案54或56-62中任一项的方法或实施方案55-62中任一项的用途,其进一步包括施用第二种治疗性处理。
64.根据实施方案63的方法或实施方案63的用途,其中第二种治疗性处理包括治疗性药剂(例如,化疗药剂、生物药剂、激素疗法)、放射或手术。
65.根据实施方案64的方法或实施方案64的用途,其中治疗性药剂选自:化疗药剂或生物药剂。
66.一种检测样品或对象中的钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法,其包括:
使样品或对象与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及
检测抗体分子与样品或对象之间复合物的形成,
从而检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
67.根据实施方案66的方法,其中在体外或体内检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
68.根据实施方案66或67的方法,其进一步包括使参考样品或对象与抗体分子接触;以及检测抗体分子与参考样品或对象之间复合物的形成,其中样品或对象中复合物的形成相对于参考样品或对象的变化(例如,统计学上显著的变化)指示样品或对象中存在钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
69.根据实施方案66-68中任一项的方法,其进一步包括从对象获得样品。
70.根据实施方案66-69中任一项的方法,其中样品包含血浆、组织(例如,癌性组织)、活检、血液(例如,全血)、PBMC、骨髓和/或淋巴组织(例如,淋巴结)中的一种或多种。
71.根据实施方案66-70中任一项的方法,其中样品未经冷冻和/或固定。
72.根据实施方案66-70中任一项的方法,其中样品已经冷冻(例如,快速冷冻)和/或固定(例如,福尔马林固定石蜡包埋(FFPE))。
73.根据实施方案66-72中任一项的方法,其中对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
74.根据实施方案66-73中任一项的方法,其进一步包括例如使用多面板方法进行流式分析。
75.根据实施方案66-74中任一项的方法,其进一步包括评估T细胞克隆形成能力,例如,以确定T细胞恶性肿瘤的存在和/或水平。
76.根据实施方案66-75中任一项的方法,其进一步包括测量来自生物样品的钙网蛋白+(例如,野生型钙网蛋白+和/或突变型钙网蛋白+)细胞的水平(例如,确定钙网蛋白+细胞例如相对于参考样品或对象是否耗尽)。
77.根据实施方案66-76中任一项的方法,其进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的胞内水平。
78.根据实施方案66-77中任一项的方法,其进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的膜水平。
79.根据实施方案66-78中任一项的方法,其进一步包括例如在(例如,用本文所述的抗体分子)治疗后,评估对象的预后、严重程度或疾病或病症(例如,癌症,例如,骨髓纤维化)存在或不存在的变化。
80.根据实施方案66-79中任一项的方法,其中抗体分子被可检测地标记。
81.一种评估对象的方法,其包括:
使来自对象的样品(例如,本文所述的样品)与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及
检测抗体分子与样品之间复合物的形成,
从而评估对象。
82.根据实施方案81的方法,其中对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
83.根据实施方案81或82的方法,其中对象尚未用本文所述的抗体分子治疗。
84.根据实施方案81或82的方法,其中对象已用本文所述的抗体分子治疗。
85.一种试剂盒,其包含本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子和针对用于检测样品或对象中钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法的说明书。
Claims (135)
1.一种包含多肽分子的组合物,其包含:
(i)结合至野生型或突变型钙网蛋白的第一抗原结合结构域,以及
(ii)结合至TCRβV或NKp30的第二抗原结合结构域;
其中:
(A)所述第一抗原结合结构域包含:(i)重链可变区(VH),所述重链可变区(VH)包含分别具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)、VHCDR2和VHCDR3的氨基酸序列的VHCDR1、VHCDR2和VHCDR3;和/或(ii)轻链可变区(VL),所述轻链可变区(VL)包含分别具有表5、表24、表25或表18中轻链互补决定区1(VHCDR1)、VLCDR2和VLCDR3的氨基酸序列的VLCDR1、VLCDR2和VLCDR3;
(B)所述第二抗原结合结构域包含:(i)VH,所述VH包含分别具有表30、表31、表10、表11、表12或表13中VHCDR1、VHCDR2和VHCDR3的氨基酸序列的VHCDR1、VHCDR2和VHCDR3;和/或(ii)VL,所述VL包含分别具有表30、表31、表10、表11、表12或表13中VLCDR1、VLCDR2和VLCDR3的氨基酸序列的VLCDR1、VLCDR2和VLCDR3;或
(C)所述第二抗原结合结构域包含:(i)VH,所述VH包含分别具有表7、表35、表9、表10或表34中VHCDR1、VHCDR2和VHCDR3的氨基酸序列的VHCDR1、VHCDR2和VHCDR3;以及(ii)VL,所述VL包含分别具有表8、表36、表9、表10或表34中的VLCDR1、VLCDR2和VLCDR3的氨基酸序列的VLCDR1、VLCDR2和VLCDR3。
2.根据权利要求1所述的组合物,其中所述多肽分子是多功能性多肽分子。
3.根据权利要求1或2所述的组合物,其中所述多肽分子是多特异性多肽分子。
4.根据权利要求1-3中任一项所述的组合物,其中所述第二抗原结合结构域结合至TCRβV。
5.根据权利要求4所述的组合物,其中所述第二抗原结合结构域激活T细胞,或所述第二抗原结合结构域不激活T细胞。
6.根据权利要求4或5所述的组合物,其中所述第二抗原结合结构域结合至TCRβV12或TCRβV6。
7.根据权利要求4-6中任一项所述的组合物,其中所述第二抗原结合结构域包含如表30、表31、表32、表10、表11、表12或表13中所列的一个或多个氨基酸序列。
8.根据权利要求4-7中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(a)VH,所述VH包含分别具有表30、表31、表10、表11、表12或表13中VHCDR1、VHCDR2和VHCDR3的氨基酸序列的VHCDR1、VHCDR2和VHCDR3;和/或(ii)VL,所述VL包含分别具有表30、表31、表10、表11、表12或表13中VLCDR1、VLCDR2和VLCDR3的氨基酸序列的VLCDR1、VLCDR2和VLCDR3;
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:3A的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:4A的VHCDR2氨基酸序列,以及SEQ ID NO:5A的VHCDR3氨基酸序列,和/或
(ii)所述VL包含SEQ ID NO:6A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:7A的VLCDR2氨基酸序列,以及SEQ ID NO:8A的VLCDR3氨基酸序列;
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:45A的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:46A的VHCDR2氨基酸序列,以及SEQ ID NO:47A的VHCDR3氨基酸序列,
和/或
(ii)所述VL包含SEQ ID NO:51A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:52A的VLCDR2氨基酸序列,以及SEQ ID NO:53A的VLCDR3氨基酸序列;
和/或
(d)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:48A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个置换、添加或缺失的序列)、SEQ ID NO:49A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个置换、添加或缺失的序列),以及SEQ ID NO:50A的VHCDR3氨基酸序列,和/或
(ii)所述VL包含SEQ ID NO:54A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:55A的VLCDR2氨基酸序列,以及SEQ ID NO:56A的VLCDR3氨基酸序列。
9.根据权利要求4-7中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含表30、表31、表10、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含表30、表31、表10、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(iii)所述VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(iv)所述VL包含SEQ ID NO:10A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:11A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:1312A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:1314A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
10.根据权利要求4-7中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:17A的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:18A的VHCDR2氨基酸序列,以及SEQ ID NO:19A的VHCDR3氨基酸序列,
和/或
(ii)所述VL包含SEQ ID NO:20A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:21A的VLCDR2氨基酸序列,以及SEQ ID NO:22A的VLCDR3氨基酸序列;
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:57A的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:58A的VHCDR2氨基酸序列,以及SEQ ID NO:59A的VHCDR3氨基酸序列,
和/或
(ii)所述VL包含SEQ ID NO:63A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:64A的VLCDR2氨基酸序列,以及SEQ ID NO:65A的VLCDR3氨基酸序列;
和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:60A的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:61A的VHCDR2氨基酸序列,以及SEQ ID NO:62A的VHCDR3氨基酸序列,
和/或
(ii)所述VL包含SEQ ID NO:66A的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:67A的VLCDR2氨基酸序列,以及SEQ ID NO:68A的VLCDR3氨基酸序列。
11.根据权利要求4-7中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:15A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:16A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含:
SEQ ID NO:23A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:24A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:25A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)所述VL包含:
SEQ ID NO:26A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:27A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:28A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:29A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),或
SEQ ID NO:30A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
12.根据权利要求4-11中任一项所述的组合物,其包含:
第一多肽,其包含第一VL和第一CL,
第二多肽,其包含第一VH、第一CH1、第一二聚化结构域和结合至TCRVβ的第一部分,
第三多肽,其包含第二VH、第二CH1、第二二聚化结构域和结合至TCRVβ的任选第二部分,
第四多肽,其包含第二VL和第二CL,
其中:
所述第一VL和所述第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且所述第二VL和所述第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,
任选地其中所述第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中所述第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中所述多功能性分子包含图3A或3B的构型。
13.根据权利要求1-3中任一项所述的组合物,其中所述第二抗原结合结构域结合至NKp30。
14.根据权利要求13所述的组合物,其中所述第二抗原结合结构域选自结合至NKp30的抗体分子或配体。
15.根据权利要求13或14所述的组合物,其中所述第二抗原结合结构域包含:
(i)VH,所述VH包含分别具有表7、表35、表9、表10或表34中VHCDR1、VHCDR2和VHCDR3的氨基酸序列的VHCDR1、VHCDR2和VHCDR3;以及(ii)VL,所述VL包含分别具有表8、表36、表9、表10或表34中VLCDR1、VLCDR2和VLCDR3的氨基酸序列的VLCDR1、VLCDR2和VLCDR3。
16.根据权利要求15所述的组合物,其中所述第二抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,以及SEQ ID NO:7315的VHCDR3氨基酸序列;和/或
(ii)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:7327的VLCDR2氨基酸序列,以及SEQ ID NO:7329的VLCDR3氨基酸序列。
17.根据权利要求15或16所述的组合物,其中所述第二抗原结合结构域包含:
(i)VH,所述VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQ IDNO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL,所述VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQ IDNO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
18.根据权利要求15-17所述的组合物,其中所述第二抗原结合结构域包含:
(i)VH和VL,所述VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)VH和VL,所述VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
19.根据权利要求15-18所述的组合物,其中所述第二抗原结合结构域包含:
(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
20.根据权利要求13或14所述的组合物,其中所述第二抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,以及SEQ ID NO:6002的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,以及SEQ ID NO:7293的VLCDR3氨基酸序列。
21.根据权利要求13、14和20中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(1)重链可变区(VH),所述重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VHFWR4,和/或
(2)轻链可变区(VL),所述轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个置换、添加或缺失的序列)的VLFWR4。
22.根据权利要求21所述的组合物,其中所述第二抗原结合结构域包含:
(1)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
23.根据权利要求13、14和20-22中任一项所述的组合物,其中所述第二抗原结合结构域包含:
(i)VH,所述VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,所述VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
24.根据权利要求13、14和20-23中任一项所述的组合物,其中所述第二抗原结合结构域包含重链,所述重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
25.根据权利要求13、14和20-24中任一项所述的组合物,其中所述第二抗原结合结构域包含轻链,所述轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
26.根据权利要求13、14和20-25中任一项所述的组合物,其中所述第二抗原结合结构域包含重链和轻链,所述重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
27.根据权利要求13-26中任一项所述的组合物,其包含:
第一多肽,其包含第一VL和第一CL,
第二多肽,其包含第一VH、第一CH1、第一二聚化结构域和结合至NKp30的第一部分,
第三多肽,其包含第二VH、第二CH1、第二二聚化结构域和结合至NKp30的任选第二部分,
第四多肽,其包含第二VL和第二CL,
其中:
所述第一VL和所述第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且所述第二VL和所述第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,
任选地其中所述第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中所述第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中所述多功能性分子包含图3A或3B的构型。
28.根据权利要求1-27中任一项所述的组合物,其中所述钙网蛋白包含选自SEQ IDNO:6285-6312或D1001的氨基酸序列,任选地其中所述钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
29.根据权利要求1-28中任一项所述的组合物,其中所述钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列。
30.根据权利要求1-29中任一项所述的组合物,其中所述钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
31.根据权利要求1-30中任一项所述的组合物,其中所述第一抗原结合结构域结合至位于所述钙网蛋白的C-末端内的表位,任选地其中所述第一抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
32.根据权利要求1-31中任一项所述的组合物,其进一步包含结合至第二钙网蛋白的第三抗原结合结构域,任选地其中:
(i)所述第三抗原结合结构域不同于所述第一抗原结合结构域,或
(ii)所述第三抗原结合结构域与所述第一抗原结合结构域相同。
33.根据权利要求32所述的组合物,其中所述第二钙网蛋白分子与由所述第一抗原结合结构域结合的所述钙网蛋白分子相同。
34.根据权利要求32所述的组合物,其中所述第二钙网蛋白分子不同于由所述第一抗原结合结构域结合的所述钙网蛋白分子。
35.根据权利要求32-34中任一项所述的组合物,其中所述第二钙网蛋白包含选自SEQID NO:6285-6312或D1001的氨基酸序列,任选地其中所述第二钙网蛋白包含选自SEQ IDNO:6313-6346或D1002-D1003的氨基酸序列。
36.根据权利要求35所述的组合物,其中由所述第一抗原结合结构域结合的所述钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且所述第二钙网蛋白包含SEQ ID NO:6286的氨基酸序列。
37.根据权利要求32-36中任一项所述的组合物,其中所述第三抗原结合结构域结合至位于所述第二钙网蛋白的C-末端内的表位,任选地其中所述第三抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
38.根据权利要求1-37中任一项所述的组合物,其中所述第一抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列的VHCDR2,以及具有表4、表24、表25或表17中VHCDR3的氨基酸序列的VHCDR3;
(ii)轻链可变区(VL),所述轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VLCDR1)的氨基酸序列的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列的VLCDR2,以及具有表5、表24、表25或表18中VLCDR3的氨基酸序列的VLCDR3;
(iii)VH,所述VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(ii)VL,所述VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);
(v)VH,所述VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VHFWR4,和/或
(vi)VL,所述VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个置换、添加或缺失的序列)的VLFWR4。
39.根据权利要求1-38中任一项所述的组合物,其中所述多功能性分子进一步包含肿瘤靶向部分。
40.根据权利要求39所述的组合物,其中所述肿瘤靶向部分结合至肿瘤抗原。
41.根据权利要求40所述的组合物,其中所述肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
42.根据权利要求39所述的组合物,其中所述肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
43.根据权利要求42所述的组合物,其中所述肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
44.根据权利要求1-43中任一项所述的组合物,其中所述多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中所述多功能性分子与所述骨髓增生性赘生物细胞之间的结合是所述多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
45.根据权利要求44所述的组合物,其中所述骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:
所述骨髓增生性赘生物细胞不包含JAK2 V617F突变,或
所述骨髓增生性赘生物细胞不包含MPL突变。
46.根据权利要求1-45中任一项所述的组合物,其进一步包含接头,例如,所述第一抗原结合结构域和所述第二抗原结合结构域之间的接头。
47.根据权利要求46所述的组合物,其中所述接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
48.根据权利要求46或47所述的组合物,其中所述接头是肽接头。
49.根据权利要求48所述的组合物,其中所述肽接头包含Gly和Ser。
50.根据权利要求48所述的组合物,其中所述肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
51.一种多功能性分子,其包含:
(i)结合至钙网蛋白(例如,野生型或突变型钙网蛋白)的第一抗原结合结构域,例如,表4、表5、表6、表24、表25、表16、表17、表18或表19的任一者中公开的钙网蛋白靶向性抗原结合结构域,
以及
(ii)结合至TCRβV的第二抗原结合结构域,例如,表30、表31、表32、表10、表11、表12或表13的任一者中公开的抗TCRβV抗原结合结构域,或
结合至NKp30的第二抗原结合结构域,例如,表7、表8、表35、表36、表9、表10或表34中公开的抗NKp30抗原结合结构域。
52.根据权利要求51所述的多功能性分子,其中所述第二抗原结合结构域结合至TCRβV。
53.根据权利要求52所述的多功能性分子,其中所述第二抗原结合结构域激活T细胞,或所述第二抗原结合结构域不激活T细胞。
54.根据权利要求52或53所述的多功能性分子,其中所述第二抗原结合结构域结合至TCRβV12或TCRβV6(例如,包含SEQ ID NO:1044的氨基酸序列)。
55.根据权利要求52-54中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含如表30、表31、表32、表10、表11、表12或表13中所列的一个或多个氨基酸序列。
56.根据权利要求52-55中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含具有表30、表31、表10、表11、表12或表13中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表30、表31、表10、表11、表12或表13中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表30、表31、表10、表11、表12或表13中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,
(ii)所述VL包含具有表30、表31、表10、表11、表12或表13中轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表30、表31、表10、表11、表12或表13中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表30、表31、表10、表11、表12或表13中VLCDR3的氨基酸序列(或具有不超过1、
2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:3A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
4A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:5A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:6A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
7A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:8A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:45A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
46A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:47A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:51A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
52A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:53A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(d)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:48A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
49A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:50A的VHCDR3氨基酸序列(或具有不超过1、2、
3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:54A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
55A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:56A的VHCDR3氨基酸序列(或具有不超过1、2、
3或4个突变(例如,置换、添加或缺失)的序列)。
57.根据权利要求52-55中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含表30、表31、表10、表11、表12或表13中VH的氨基酸序列(或与其具有至少约77%、80%、
85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含表30、表31、表10、表11、表12或表13中VL的氨基酸序列(或与其具有至少约77%、80%、
85%、90%、95%或99%序列同一性的氨基酸序列)
(iii)所述VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(iv)所述VL包含SEQ ID NO:10A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:9A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:11A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:1312A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:1314A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
58.根据权利要求52-55中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:17A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
18A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:19A的VHCDR3氨基酸序列(或具有不超过1、2、
3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:20A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
21A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:22A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:57A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
58A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:59A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:63A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
64A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:65A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(c)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:60A的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
61A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:62A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或
(ii)所述VL包含SEQ ID NO:66A的轻链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:
67A的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQID NO:68A的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
59.根据权利要求52-55中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(a)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含SEQ ID NO:15A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)所述VL包含SEQ ID NO:16A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(b)重链可变区(VH)和/或轻链可变区(VL),其中:
(i)所述VH包含:
SEQ ID NO:23A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:24A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
或
SEQ ID NO:25A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
和/或
(ii)所述VL包含:
SEQ ID NO:26A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:27A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:28A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
SEQ ID NO:29A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),
或
SEQ ID NO:30A的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
60.根据权利要求52-59中任一项所述的多功能性分子,其包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至TCR(例如,TCRVβ)的第一部分(例如,结合至TCR(例如,TCRVβ)的第一scFv),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至TCR(例如,TCRVβ)的任选第二部分(例如,结合至TCR(例如,TCRVβ)的第二scFv),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,
其中:
所述第一VL和所述第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且所述第二VL和所述第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,
任选地其中所述第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中所述第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中所述多功能性分子包含图3A或3B的构型。
61.根据权利要求51所述的多功能性分子,其中所述第二抗原结合结构域结合至NKp30。
62.根据权利要求61所述的多功能性分子,其中所述第二抗原结合结构域选自结合至(例如,激活)NKp30的抗体分子(例如,抗原结合结构域)或配体,例如,所述第二抗原结合结构域是结合至(例如,激活)NKp30的抗体分子或配体。
63.根据权利要求61或62所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表7、表35、表9、表10或表34的VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表7、表35、表9、表10或表34的VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3,和/或
(ii)轻链可变区(VL),所述轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链互补决定区1(VLCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表8、表36、表9、表10或表34的VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表8、表36、表9、表10或表34的VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3。
64.根据权利要求63所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:7313的重链互补决定区1(VHCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:6001的VHCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7315的VHCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列);和/或
(ii)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:7326的轻链互补决定区1(VLCDR1)氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)、SEQ ID NO:7327的VLCDR2氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列),和/或SEQ ID NO:7329的VLCDR3氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)。
65.根据权利要求63或64所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)VH,所述VH包含SEQ ID NO:7298或7300-7304中任一者的氨基酸序列(或与SEQ IDNO:7298或7300-7304中任一者具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);和/或
(ii)VL,所述VL包含SEQ ID NO:7299或7305-7309中任一者的氨基酸序列(或与SEQ IDNO:7299或7305-7309中任一者具有至少约93%、95%或99%序列同一性的氨基酸序列)。
66.根据权利要求63-65中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)VH和VL,所述VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述VL包含SEQ ID NO:7305的氨基酸序列(或与7305具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)VH和VL,所述VH包含SEQ ID NO:7302的氨基酸序列(或与7302具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述VL包含SEQ ID NO:7309的氨基酸序列(或与7309具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
67.根据权利要求63-66中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)SEQ ID NO:7310的氨基酸序列(或与7310具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);或
(ii)SEQ ID NO:7311的氨基酸序列(或与7311具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
68.根据权利要求61或62所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:6000的重链互补决定区1(VHCDR1)氨基酸序列、SEQ ID NO:6001的VHCDR2氨基酸序列,和/或SEQ ID NO:6002的VHCDR3氨基酸序列,以及
(ii)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:6063的轻链互补决定区1(VLCDR1)氨基酸序列、SEQ ID NO:6064的VLCDR2氨基酸序列,和/或SEQ ID NO:7293的VLCDR3氨基酸序列。
69.根据权利要求61、62或68中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(1)重链可变区(VH),所述重链可变区(VH)包含具有表7、表35、表9、表10或表34的重链框架区1(VHFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR1、具有表7、表35、表9、表10或表34的VHFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR2、具有表7、表35、表9、表10或表34的VHFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR3,或具有表7、表35、表9、表10或表34的VHFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VHFWR4,和/或
(2)轻链可变区(VL),所述轻链可变区(VL)包含具有表8、表36、表9、表10或表34的轻链框架区1(VLFWR1)的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR1、具有表8、表36、表9、表10或表34的VLFWR2的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR2、具有表8、表36、表9、表10或表34的VLFWR3的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR3,或具有表8、表36、表9、表10或表34的VLFWR4的氨基酸序列(或较其具有不超过1、2、3、4、5或6个突变例如置换、添加或缺失的序列)的VLFWR4。
70.根据权利要求69所述的多功能性分子,其中所述第二抗原结合结构域包含:
(1)重链可变区(VH),所述重链可变区(VH)包含SEQ ID NO:6003的重链框架区1(VHFWR1)氨基酸序列、SEQ ID NO:6004的VHFWR2氨基酸序列、SEQ ID NO:6005的VHFWR3氨基酸序列,或SEQ ID NO:6006的VHFWR4氨基酸序列,以及
(3)轻链可变区(VL),所述轻链可变区(VL)包含SEQ ID NO:6066的轻链框架区1(VLFWR1)氨基酸序列、SEQ ID NO:6067的VLFWR2氨基酸序列、SEQ ID NO:7292的VLFWR3氨基酸序列,或SEQ ID NO:6069的VLFWR4氨基酸序列。
71.根据权利要求61、62和68-70中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含:
(i)VH,所述VH包含表7、表35、表9、表10或表34的VH的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),和/或
(ii)VL,所述VL包含表8、表36、表9、表10或表34的VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列)。
72.根据权利要求61、62和68-71中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含重链,所述重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
73.根据权利要求61、62和68-72中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含轻链,所述轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
74.根据权利要求61、62和68-73中任一项所述的多功能性分子,其中所述第二抗原结合结构域包含重链和轻链,所述重链包含表10的重链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列),所述轻链包含表10的轻链的氨基酸序列(或与其具有至少约75%、80%、85%、90%、95%或99%序列同一性的氨基酸序列)。
75.根据权利要求61-74中任一项所述的多功能性分子,其包含:
第一多肽,其包含例如从N-末端至C-末端的第一VL和第一CL,
第二多肽,其包含例如从N-末端至C-末端的第一VH、第一CH1、第一二聚化结构域(例如,第一Fc)和结合至NKp30的第一部分(例如,结合至NKp30的第一抗体分子或配体),
第三多肽,其包含例如从N-末端至C-末端的第二VH、第二CH1、第二二聚化结构域(例如,第二Fc)和结合至NKp30的任选第二部分(例如,结合至NKp30的第二抗体分子或配体),
第四多肽,其包含例如从N-末端至C-末端的第二VL和第二CL,
其中:
所述第一VL和所述第一VH形成结合至第一钙网蛋白的第一抗原结合结构域,并且所述第二VL和所述第二VH形成结合至第二钙网蛋白的第三抗原结合结构域,
任选地其中所述第一和第二钙网蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,
任选地其中所述第一和第二钙网蛋白突变型蛋白各自独立地选自:包含SEQ ID NO:6313的氨基酸序列的分子,或包含SEQ ID NO:6314的氨基酸序列的分子,
任选地其中所述多功能性分子包含图3A或3B的构型。
76.根据前述权利要求中任一项所述的多功能性分子,其中所述钙网蛋白包含选自SEQID NO:6285-6312或D1001的氨基酸序列,任选地其中所述钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
77.根据前述权利要求中任一项所述的多功能性分子,其中所述钙网蛋白包含SEQ IDNO:6285或D1001的氨基酸序列。
78.根据前述权利要求中任一项所述的多功能性分子,其中所述钙网蛋白包含SEQ IDNO:6286的氨基酸序列。
79.根据前述权利要求中任一项所述的多功能性分子,其中所述第一抗原结合结构域结合至位于所述钙网蛋白的C-末端内的表位,任选地其中所述第一抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
80.根据前述权利要求中任一项所述的多功能性分子,其进一步包含结合至第二钙网蛋白的第三抗原结合结构域,例如,其中所述第二钙网蛋白突变型蛋白包含SEQ ID NO:6285、D1001或6286的氨基酸序列,任选地其中:
(i)所述第三抗原结合结构域不同于所述第一抗原结合结构域,或
(ii)所述第三抗原结合结构域与所述第一抗原结合结构域相同。
81.根据权利要求80所述的多功能性分子,其中所述第二钙网蛋白分子与由所述第一抗原结合结构域结合的所述钙网蛋白分子相同。
82.根据权利要求80所述的多功能性分子,其中所述第二钙网蛋白分子不同于由所述第一抗原结合结构域结合的所述钙网蛋白分子。
83.根据权利要求80-82中任一项所述的多功能性分子,其中所述第二钙网蛋白包含选自SEQ ID NO:6285-6312或D1001的氨基酸序列,任选地其中所述第二钙网蛋白包含选自SEQ ID NO:6313-6346或D1002-D1003的氨基酸序列。
84.根据权利要求83所述的多功能性分子,其中由所述第一抗原结合结构域结合的所述钙网蛋白包含SEQ ID NO:6285或D1001的氨基酸序列,并且所述第二钙网蛋白包含SEQID NO:6286的氨基酸序列。
85.根据权利要求80-84中任一项所述的多功能性分子,其中所述第三抗原结合结构域结合至位于所述第二钙网蛋白的C-末端内的表位,任选地其中所述第三抗原结合结构域结合至位于SEQ ID NO:6285、D1001或6286的氨基酸序列内的表位。
86.根据前述权利要求中任一项所述的多功能性分子,其中所述第一抗原结合结构域包含:
(i)重链可变区(VH),所述重链可变区(VH)包含具有表4、表24、表25或表17中重链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR1、具有表4、表24、表25或表17中VHCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR2,和/或具有表4、表24、表25或表17中VHCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VHCDR3;
(ii)轻链可变区(VL),所述轻链可变区(VL)包含具有表5、表24、表25或表18中轻链互补决定区1(VHCDR1)的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR1、具有表5、表24、表25或表18中VLCDR2的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR2,和/或具有表5、表24、表25或表18中VLCDR3的氨基酸序列(或具有不超过1、2、3或4个突变(例如,置换、添加或缺失)的序列)的VLCDR3;
(iii)VH,所述VH包含表24、表25或表16中VH的氨基酸序列(或与其具有至少约77%、80%、85%、90%、95%或99%序列同一性的氨基酸序列);
(ii)VL,所述VL包含表24、表25或表16中VL的氨基酸序列(或与其具有至少约93%、95%或99%序列同一性的氨基酸序列);
(v)VH,所述VH包含具有表4或表6中重链框架区1(VHFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR1、具有表4或表6中VHFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR2、具有表4或表6中VHFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR3,和/或具有表4或表6中VHFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VHFWR4,和/或
(vi)VL,所述VL包含具有表5或表6中轻链框架区1(VLFWR1)的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR1、具有表5或表6中VLFWR2的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR2、具有表5或表6中VLFWR3的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR3,和/或具有表5或表6中VLFWR4的氨基酸序列(或具有不超过1、2、3、4、5、6、7、8或9个突变(例如,置换、添加或缺失)的序列)的VLFWR4。
87.根据前述权利要求中任一项所述的多功能性分子,其中所述多功能性分子进一步包含肿瘤靶向部分。
88.根据权利要求87所述的多功能性分子,其中所述肿瘤靶向部分结合至肿瘤抗原。
89.根据权利要求88所述的多功能性分子,其中所述肿瘤抗原选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1。
90.根据权利要求87所述的多功能性分子,其中所述肿瘤靶向部分包含例如结合至选自G6B、CD34、CD41、P-选择素、Clec2、cKIT、FLT3、MPL、ITGB3、ITGB2、GP5、GP6、GP9、GP1BA、DSC2、FCGR2A、TNFRSF10A、TNFRSF10B或TM4SF1的肿瘤抗原的抗体分子。
91.根据权利要求90所述的多功能性分子,其中所述肿瘤靶向部分包含VH和/或VL序列,例如,如表38或表20中所列的。
92.根据前述权利要求中任一项所述的多功能性分子,其中所述多功能性分子优先结合至骨髓增生性赘生物细胞而不是非肿瘤细胞,任选地其中所述多功能性分子与所述骨髓增生性赘生物细胞之间的结合是所述多功能性分子与非肿瘤细胞之间的结合的超过10、20、30、40、50倍。
93.根据权利要求92所述的多功能性分子,其中所述骨髓增生性赘生物细胞选自骨髓纤维化细胞、原发性血小板增多症细胞、真性红细胞增多症细胞或慢性髓性癌细胞,任选地其中:
所述骨髓增生性赘生物细胞不包含JAK2 V617F突变,或
所述骨髓增生性赘生物细胞不包含MPL突变。
94.根据前述权利要求中任一项所述的多功能性分子,其进一步包含接头,例如,所述第一抗原结合结构域和所述第二抗原结合结构域之间的接头。
95.根据权利要求94所述的多功能性分子,其中所述接头选自:可切割接头、不可切割接头、肽接头、柔性接头、刚性接头、螺旋接头或非螺旋接头。
96.根据权利要求94或95所述的多功能性分子,其中所述接头是肽接头。
97.根据权利要求96所述的多功能性分子,其中所述肽接头包含Gly和Ser。
98.根据权利要求96所述的多功能性分子,其中所述肽接头包含选自SEQ ID NO:6214-6217或6220-6221和77-78的氨基酸序列。
99.一种核酸分子,其编码前述权利要求中任一项所述的多功能性分子。
100.一种载体,例如,表达载体,其包含权利要求99所述的核酸分子。
101.一种细胞,其包含权利要求99所述的核酸分子或权利要求100所述的载体。
102.一种制备,例如,产生权利要求51-98中任一项所述的多功能性分子的方法,其包括在合适的条件,例如,适于基因表达和/或同源或异源二聚化的条件下,培养权利要求101所述的细胞。
103.一种药物组合物,其包含权利要求1-50中任一项所述的组合物、权利要求51-98中任一项所述的多功能性分子、权利要求99所述的核酸分子、权利要求100所述的载体或权利要求101所述的细胞以及药学上可接受的载剂、赋形剂、稀释剂或稳定剂。
104.一种治疗癌症的方法,其包括向有需要的对象施用权利要求1-50中任一项所述的组合物、权利要求51-98中任一项所述的多功能性分子、权利要求99所述的核酸分子、权利要求100所述的载体、权利要求101所述的细胞或权利要求103所述的药物组合物,其中所述多功能性分子以有效治疗所述癌症的量施用。
105.权利要求1-50中任一项所述的组合物、权利要求51-98中任一项所述的多功能性分子、权利要求99所述的核酸分子、权利要求100所述的载体或权利要求101所述的细胞在制造用于治疗癌症的药物中的用途。
106.根据权利要求104的方法或权利要求105的用途,其中所述对象具有表达所述第一和/或第二钙网蛋白的癌细胞。
107.根据权利要求104或106所述的方法或权利要求105或106所述的用途,其中所述对象具有JAK2 V617F突变。
108.根据权利要求104或106所述的方法或权利要求105或106所述的用途,其中所述对象不具有JAK2 V617F突变。
109.根据权利要求104或106-108中任一项所述的方法或权利要求105-108中任一项所述的用途,其中所述对象具有MPL突变。
110.根据权利要求104或106-108中任一项所述的方法或权利要求105-108中任一项所述的用途,其中所述对象不具有MPL突变。
111.根据权利要求104或106-110中任一项所述的方法或权利要求105-110中任一项所述的用途,其中所述癌症是血液癌症,
任选地其中所述癌症是骨髓增生性赘生物,例如,原发性或特发性骨髓纤维化(MF)、原发性血小板增多症(ET)、真性红细胞增多症(PV)或慢性髓性白血病(CML),任选地其中所述癌症是骨髓纤维化。
112.根据权利要求104或106-110中任一项所述的方法或权利要求105-110中任一项所述的用途,其中所述癌症是实体瘤癌症。
113.根据权利要求104或106-112中任一项所述的方法或权利要求105-112中任一项所述的用途,其进一步包括施用第二种治疗性处理。
114.根据权利要求113所述的方法或权利要求113所述的用途,其中所述第二种治疗性处理包括治疗性药剂(例如,化疗药剂、生物药剂、激素疗法)、放射或手术。
115.根据权利要求114所述的方法或权利要求114所述的用途,其中所述治疗性药剂选自:化疗药剂或生物药剂。
116.一种检测样品或对象中的钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法,其包括:
使所述样品或对象与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及
检测所述抗体分子与所述样品或对象之间复合物的形成,
从而检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
117.根据权利要求116所述的方法,其中在体外或体内检测钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
118.根据权利要求116或117所述的方法,其进一步包括使参考样品或对象与所述抗体分子接触;以及检测所述抗体分子与所述参考样品或对象之间复合物的形成,其中所述样品或对象中所述复合物的所述形成相对于所述参考样品或对象的变化,例如,统计学上显著的变化指示所述样品或对象中存在钙网蛋白(例如,野生型和/或突变型钙网蛋白)。
119.根据权利要求116-118中任一项所述的方法,其进一步包括从对象获得样品。
120.根据权利要求116-119中任一项所述的方法,其中所述样品包含血浆、组织(例如,癌性组织)、活检、血液(例如,全血)、PBMC、骨髓和/或淋巴组织例如淋巴结中的一种或多种。
121.根据权利要求116-120中任一项所述的方法,其中所述样品未经冷冻和/或固定。
122.根据权利要求116-120中任一项所述的方法,其中所述样品已经冷冻(例如,快速冷冻)和/或固定(例如,福尔马林固定石蜡包埋(FFPE))。
123.根据权利要求116-122中任一项所述的方法,其中所述对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
124.根据权利要求116-123中任一项所述的方法,其进一步包括例如使用多面板方法进行流式分析。
125.根据权利要求116-124中任一项所述的方法,其进一步包括评估T细胞克隆形成能力,例如,以确定T细胞恶性肿瘤的存在和/或水平。
126.根据权利要求116-125中任一项所述的方法,其进一步包括测量来自所述生物样品的钙网蛋白+(例如,野生型钙网蛋白+和/或突变型钙网蛋白+)细胞的水平(例如,确定所述钙网蛋白+细胞例如相对于参考样品或对象是否耗尽)。
127.根据权利要求116-126中任一项所述的方法,其进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的胞内水平。
128.根据权利要求116-127中任一项所述的方法,其进一步包括测量钙网蛋白(例如,野生型和/或突变型钙网蛋白)的膜水平。
129.根据权利要求116-128中任一项所述的方法,其进一步包括例如在(例如,用本文所述的抗体分子)治疗后,评估所述对象的预后、严重程度或疾病或病症(例如,癌症,例如,骨髓纤维化)存在或不存在的变化。
130.根据权利要求116-129中任一项所述的方法,其中所述抗体分子被可检测地标记。
131.一种评估对象的方法,其包括:
使来自所述对象的样品(例如,本文所述的样品)与本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子接触;以及
检测所述抗体分子与所述样品之间复合物的形成,
从而评估所述对象。
132.根据权利要求131所述的方法,其中所述对象患有本文所述的疾病或病症(例如,癌症,例如,骨髓纤维化)或处于患有本文所述的疾病或病症的风险中。
133.根据权利要求131或132所述的方法,其中所述对象尚未用本文所述的抗体分子治疗。
134.根据权利要求131或132所述的方法,其中所述对象已用本文所述的抗体分子治疗。
135.一种试剂盒,其包含本文所述的抗钙网蛋白(例如,野生型和/或突变型钙网蛋白)抗体分子和针对用于检测样品或对象中钙网蛋白(例如,野生型和/或突变型钙网蛋白)的方法的说明书。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063070769P | 2020-08-26 | 2020-08-26 | |
| US63/070,769 | 2020-08-26 | ||
| PCT/US2021/047571 WO2022046920A2 (en) | 2020-08-26 | 2021-08-25 | Multifunctional molecules that bind to calreticulin and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116249718A true CN116249718A (zh) | 2023-06-09 |
Family
ID=80352965
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180073493.XA Pending CN116249718A (zh) | 2020-08-26 | 2021-08-25 | 结合至钙网蛋白的多功能性分子及其用途 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20240002543A1 (zh) |
| EP (1) | EP4204450A4 (zh) |
| JP (1) | JP2023542080A (zh) |
| CN (1) | CN116249718A (zh) |
| AU (1) | AU2021331075A1 (zh) |
| CA (1) | CA3190755A1 (zh) |
| WO (1) | WO2022046920A2 (zh) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3737692A4 (en) | 2018-01-09 | 2021-09-29 | Elstar Therapeutics, Inc. | CALRETICULIN AND MODIFIED T-LYMPHOCYTES BINDING CONSTRUCTIONS FOR THE TREATMENT OF DISEASES |
| WO2019178362A1 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| CN112955465A (zh) | 2018-07-03 | 2021-06-11 | 马伦戈治疗公司 | 抗tcr抗体分子及其用途 |
| WO2020172605A1 (en) | 2019-02-21 | 2020-08-27 | Elstar Therapeutics, Inc. | Antibody molecules that bind to nkp30 and uses thereof |
| CN114026122B (zh) | 2019-02-21 | 2024-12-31 | 马伦戈治疗公司 | 结合t细胞相关癌细胞的多功能分子及其用途 |
| EP4084823A4 (en) | 2020-01-03 | 2024-05-15 | Marengo Therapeutics, Inc. | ANTI-TCR ANTIBODY MOLECULES AND THEIR USES |
| KR20240004937A (ko) | 2021-05-05 | 2024-01-11 | 이매틱스 바이오테크놀로지스 게엠베하 | Bma031 항원 결합 폴리펩타이드 |
| WO2023108201A1 (en) * | 2021-12-13 | 2023-06-22 | Central Adelaide Local Health Network Inc | Antibodies to mutant calreticulin and uses thereof |
| AU2023327927A1 (en) * | 2022-08-23 | 2025-02-20 | Imperial College Innovations Limited | Chimeric antigen receptor (car) to a tcr beta-chain variable region |
| WO2024081329A1 (en) * | 2022-10-12 | 2024-04-18 | Marengo Therapeutics, Inc. | Multifunctional molecules binding to tcr and uses thereof |
| WO2025075529A1 (en) * | 2023-10-04 | 2025-04-10 | Joint Stock Company "Biocad" | Antibody binds to trbv5-1 segment of human tor domain |
| WO2025109518A1 (en) * | 2023-11-21 | 2025-05-30 | Janssen Biotech, Inc. | Methods for treatment of myeloproliferative neoplasms |
Family Cites Families (153)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| JPS6147500A (ja) | 1984-08-15 | 1986-03-07 | Res Dev Corp Of Japan | キメラモノクロ−ナル抗体及びその製造法 |
| EP0173494A3 (en) | 1984-08-27 | 1987-11-25 | The Board Of Trustees Of The Leland Stanford Junior University | Chimeric receptors by dna splicing and expression |
| GB8422238D0 (en) | 1984-09-03 | 1984-10-10 | Neuberger M S | Chimeric proteins |
| JPS61134325A (ja) | 1984-12-04 | 1986-06-21 | Teijin Ltd | ハイブリツド抗体遺伝子の発現方法 |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| US5731116A (en) | 1989-05-17 | 1998-03-24 | Dai Nippon Printing Co., Ltd. | Electrostatic information recording medium and electrostatic information recording and reproducing method |
| DE768377T1 (de) | 1988-09-02 | 1998-01-02 | Dyax Corp | Herstellung und Auswahl von Rekombinantproteinen mit verschiedenen Bindestellen |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| GB8905669D0 (en) | 1989-03-13 | 1989-04-26 | Celltech Ltd | Modified antibodies |
| WO1991000906A1 (en) | 1989-07-12 | 1991-01-24 | Genetics Institute, Inc. | Chimeric and transgenic animals capable of producing human antibodies |
| DK0463151T3 (da) | 1990-01-12 | 1996-07-01 | Cell Genesys Inc | Frembringelse af xenogene antistoffer |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| ATE185601T1 (de) | 1990-07-10 | 1999-10-15 | Cambridge Antibody Tech | Verfahren zur herstellung von spezifischen bindungspaargliedern |
| CA2090473A1 (en) | 1990-08-29 | 1992-03-01 | Robert M. Kay | Homologous recombinatin in mammalian cells |
| JP2938569B2 (ja) | 1990-08-29 | 1999-08-23 | ジェンファーム インターナショナル,インコーポレイティド | 異種免疫グロブリンを作る方法及びトランスジェニックマウス |
| DE69129154T2 (de) | 1990-12-03 | 1998-08-20 | Genentech, Inc., South San Francisco, Calif. | Verfahren zur anreicherung von proteinvarianten mit geänderten bindungseigenschaften |
| DK1279731T3 (da) | 1991-03-01 | 2007-09-24 | Dyax Corp | Fremgangsmåde til udvikling af bindende miniproteiner |
| ATE269401T1 (de) | 1991-04-10 | 2004-07-15 | Scripps Research Inst | Bibliotheken heterodimerer rezeptoren mittels phagemiden |
| EP0519596B1 (en) | 1991-05-17 | 2005-02-23 | Merck & Co. Inc. | A method for reducing the immunogenicity of antibody variable domains |
| DE4122599C2 (de) | 1991-07-08 | 1993-11-11 | Deutsches Krebsforsch | Phagemid zum Screenen von Antikörpern |
| JP3980657B2 (ja) | 1992-06-26 | 2007-09-26 | 生化学工業株式会社 | コンドロイチナーゼabc、その製造法及び医薬組成物 |
| ATE420178T1 (de) | 1992-08-21 | 2009-01-15 | Univ Bruxelles | Immunoglobuline ohne leichtkette |
| WO1995009917A1 (en) | 1993-10-07 | 1995-04-13 | The Regents Of The University Of California | Genetically engineered bispecific tetravalent antibodies |
| GB9325182D0 (en) | 1993-12-08 | 1994-02-09 | T Cell Sciences Inc | Humanized antibodies or binding proteins thereof specific for t cell subpopulations exhibiting select beta chain variable regions |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US20020062010A1 (en) | 1997-05-02 | 2002-05-23 | Genentech, Inc. | Method for making multispecific antibodies having heteromultimeric and common components |
| DE69839147T2 (de) | 1997-06-12 | 2009-02-19 | Novartis International Pharmaceutical Ltd. | Künstliche antikörperpolypeptide |
| AUPP221098A0 (en) | 1998-03-06 | 1998-04-02 | Diatech Pty Ltd | V-like domain binding molecules |
| US6818418B1 (en) | 1998-12-10 | 2004-11-16 | Compound Therapeutics, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| AU775076B2 (en) | 1998-12-10 | 2004-07-15 | Bristol-Myers Squibb Company | Protein scaffolds for antibody mimics and other binding proteins |
| EP1163339A1 (en) | 1999-04-01 | 2001-12-19 | Innogenetics N.V. | A polypeptide structure for use as a scaffold |
| US6979546B2 (en) | 1999-11-15 | 2005-12-27 | Universita Di Genova | Triggering receptor involved in natural cytotoxicity mediated by human natural killer cells and antibodies that identify the same |
| DK2857516T3 (en) | 2000-04-11 | 2017-08-07 | Genentech Inc | Multivalent antibodies and uses thereof |
| AU2003209272A1 (en) | 2002-01-16 | 2003-09-02 | Zyomyx, Inc. | Engineered binding proteins |
| CA2872136C (en) | 2002-07-18 | 2017-06-20 | Merus B.V. | Recombinant production of mixtures of antibodies |
| AU2003294930B2 (en) | 2002-12-23 | 2008-12-04 | Innate Pharma | Pharmaceutical compositions having an effect on the proliferation of NK cells and a method using the same |
| AU2004204494B2 (en) | 2003-01-09 | 2011-09-29 | Macrogenics, Inc. | Identification and engineering of antibodies with variant Fc regions and methods of using same |
| EA009383B1 (ru) | 2003-03-05 | 2007-12-28 | Хэлозим, Инк. | РАСТВОРИМЫЙ ГЛИКОПРОТЕИН ГИАЛУРОНИДАЗЫ (sHASEGP), СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ЕГО СОДЕРЖАЩАЯ |
| US7871607B2 (en) | 2003-03-05 | 2011-01-18 | Halozyme, Inc. | Soluble glycosaminoglycanases and methods of preparing and using soluble glycosaminoglycanases |
| US20070184052A1 (en) | 2003-05-09 | 2007-08-09 | Lin Herbert Y | Soluble tgf-b type III receptor fusion proteins |
| AU2004242614B2 (en) | 2003-05-30 | 2011-09-22 | Merus N.V. | Fab library for the preparation of anti vegf and anti rabies virus fabs |
| JP2008502597A (ja) | 2004-04-30 | 2008-01-31 | イネイト・ファーマ | Nk型ldglのような免疫増殖性障害を処置するための組成物および方法 |
| US7501121B2 (en) | 2004-06-17 | 2009-03-10 | Wyeth | IL-13 binding agents |
| ES2344793T3 (es) | 2004-08-05 | 2010-09-07 | Genentech, Inc. | Antagonistas anti-cmet humanizados. |
| NZ553500A (en) | 2004-09-23 | 2009-11-27 | Genentech Inc Genentech Inc | Cysteine engineered antibodies and conjugates withCysteine engineered antibodies and conjugates with a free cysteine amino acid in the heavy chain a free cysteine amino acid in the heavy chain |
| CN101103045B (zh) | 2004-09-24 | 2015-11-25 | 安姆根有限公司 | 修饰的Fc分子 |
| US7431380B1 (en) | 2005-02-24 | 2008-10-07 | Theodore Allen Buresh | Louver kit |
| WO2006106905A1 (ja) | 2005-03-31 | 2006-10-12 | Chugai Seiyaku Kabushiki Kaisha | 会合制御によるポリペプチド製造方法 |
| EP2322557B1 (en) | 2005-10-14 | 2017-08-30 | Innate Pharma | Compositions and methods for treating proliferative disorders |
| PT1999154E (pt) | 2006-03-24 | 2013-01-24 | Merck Patent Gmbh | Domínios proteicos heterodiméricos modificados |
| AU2007285763B2 (en) | 2006-08-18 | 2011-12-15 | Armagen Technologies, Inc. | Agents for blood-brain barrier delivery |
| WO2008027236A2 (en) | 2006-08-30 | 2008-03-06 | Genentech, Inc. | Multispecific antibodies |
| US8227577B2 (en) | 2007-12-21 | 2012-07-24 | Hoffman-La Roche Inc. | Bivalent, bispecific antibodies |
| SI2235064T1 (sl) | 2008-01-07 | 2016-04-29 | Amgen Inc. | Metoda za izdelavo heterodimernih molekul - protitelesa fc z uporabo elektrostatičnih usmerjevalnih učinkov |
| UA121453C2 (uk) | 2008-04-11 | 2020-06-10 | Чугей Сейяку Кабусікі Кайся | Спосіб одержання фармацевтичної композиції, яка містить антитіло |
| CA2737271C (en) | 2008-09-17 | 2020-06-23 | National Research Council Of Canada | Hetero-multivalent binding agents for members of the tgf.beta. superfamily |
| KR101431318B1 (ko) | 2009-04-02 | 2014-08-20 | 로슈 글리카트 아게 | 전장 항체 및 단일쇄 fab 단편을 포함하는 다중특이성 항체 |
| JP5616428B2 (ja) | 2009-04-07 | 2014-10-29 | ロシュ グリクアート アクチェンゲゼルシャフト | 三価の二重特異性抗体 |
| WO2010129304A2 (en) | 2009-04-27 | 2010-11-11 | Oncomed Pharmaceuticals, Inc. | Method for making heteromultimeric molecules |
| US9676845B2 (en) | 2009-06-16 | 2017-06-13 | Hoffmann-La Roche, Inc. | Bispecific antigen binding proteins |
| US8703132B2 (en) | 2009-06-18 | 2014-04-22 | Hoffmann-La Roche, Inc. | Bispecific, tetravalent antigen binding proteins |
| CA2766220C (en) | 2009-06-26 | 2021-02-09 | Regeneron Pharmaceuticals, Inc. | Readily isolated bispecific antibodies with native immunoglobulin format |
| WO2011028952A1 (en) | 2009-09-02 | 2011-03-10 | Xencor, Inc. | Compositions and methods for simultaneous bivalent and monovalent co-engagement of antigens |
| IT1395574B1 (it) | 2009-09-14 | 2012-10-16 | Guala Dispensing Spa | Dispositivo di erogazione |
| CA2781539C (en) | 2009-11-23 | 2021-07-20 | Amgen Inc. | Monomeric antibody fc |
| EP3778917A3 (en) | 2009-12-04 | 2021-06-09 | F. Hoffmann-La Roche AG | Multispecific antibodies, antibody analogs, compositions, and methods |
| PL2542590T5 (pl) | 2010-03-05 | 2020-08-10 | The Johns Hopkins University | Kompozycje i sposoby dla ukierunkowanych immunomodulatorowych przeciwciał i białek fuzyjnych |
| TW201138821A (en) | 2010-03-26 | 2011-11-16 | Roche Glycart Ag | Bispecific antibodies |
| US9000130B2 (en) | 2010-06-08 | 2015-04-07 | Genentech, Inc. | Cysteine engineered antibodies and conjugates |
| CA2808482C (en) | 2010-08-16 | 2021-10-26 | Novimmune S.A. | Methods for the generation of multispecific and multivalent antibodies |
| EP2609111B1 (en) | 2010-08-24 | 2017-11-01 | F. Hoffmann-La Roche AG | Bispecific antibodies comprising a disulfide stabilized-fv fragment |
| KR101612999B1 (ko) | 2010-08-24 | 2016-04-15 | 로슈 글리카트 아게 | 활성화가능 이중특이적 항체 |
| AU2011325833C1 (en) | 2010-11-05 | 2017-07-13 | Zymeworks Bc Inc. | Stable heterodimeric antibody design with mutations in the Fc domain |
| US20120201746A1 (en) | 2010-12-22 | 2012-08-09 | Abbott Laboratories | Half immunoglobulin binding proteins and uses thereof |
| US10689447B2 (en) | 2011-02-04 | 2020-06-23 | Genentech, Inc. | Fc variants and methods for their production |
| EP2688909A2 (en) | 2011-03-25 | 2014-01-29 | Glenmark Pharmaceuticals S.A. | Hetero-dimeric immunoglobulins |
| RU2641256C2 (ru) | 2011-06-30 | 2018-01-16 | Чугаи Сейяку Кабусики Кайся | Гетеродимеризованный полипептид |
| UA117901C2 (uk) | 2011-07-06 | 2018-10-25 | Ґенмаб Б.В. | Спосіб посилення ефекторної функції вихідного поліпептиду, його варіанти та їх застосування |
| RS56879B1 (sr) | 2011-08-23 | 2018-04-30 | Roche Glycart Ag | Bispecifične molekule koje vezuju antigen za aktiviranje t ćelija |
| CA2791109C (en) | 2011-09-26 | 2021-02-16 | Merus B.V. | Generation of binding molecules |
| US10047144B2 (en) | 2011-10-19 | 2018-08-14 | Novimmune Sa | Methods of purifying antibodies |
| AU2012332021B8 (en) | 2011-11-04 | 2017-10-12 | Zymeworks Bc Inc. | Stable heterodimeric antibody design with mutations in the Fc domain |
| DK2794905T3 (da) | 2011-12-20 | 2020-07-06 | Medimmune Llc | Modificerede polypeptider til bispecifikke antistofgrundstrukturer |
| WO2013101909A1 (en) | 2011-12-27 | 2013-07-04 | Development Center For Biotechnology | Light chain-bridged bispecific antibody |
| EP2812357B1 (en) | 2012-02-10 | 2020-11-04 | F.Hoffmann-La Roche Ag | Single-chain antibodies and other heteromultimers |
| GB201203051D0 (en) | 2012-02-22 | 2012-04-04 | Ucb Pharma Sa | Biological products |
| CA2867020C (en) | 2012-03-13 | 2022-11-15 | Novimmune S.A. | Readily isolated bispecific antibodies with native immunoglobulin format |
| SG10201709018QA (en) | 2012-03-14 | 2017-11-29 | Regeneron Pharma | Multispecific antigen-binding molecules and uses thereof |
| CN114163530B (zh) | 2012-04-20 | 2025-04-29 | 美勒斯公司 | 用于产生免疫球蛋白样分子的方法和手段 |
| MX2019001355A (es) | 2012-05-10 | 2023-01-17 | Bioatla Llc | Anticuerpos monoclonales multiespecíficos. |
| WO2013166594A1 (en) | 2012-05-10 | 2013-11-14 | Zymeworks Inc. | Heteromultimer constructs of immunoglobulin heavy chains with mutations in the fc domain |
| EP2855531A1 (en) | 2012-05-24 | 2015-04-08 | F. Hoffmann-La Roche AG | Multispecific antibodies |
| US9499634B2 (en) | 2012-06-25 | 2016-11-22 | Zymeworks Inc. | Process and methods for efficient manufacturing of highly pure asymmetric antibodies in mammalian cells |
| WO2014001326A1 (en) | 2012-06-27 | 2014-01-03 | F. Hoffmann-La Roche Ag | Method for the selection and production of tailor-made, selective and multi-specific therapeutic molecules comprising at least two different targeting entities and uses thereof |
| BR112015000167B1 (pt) | 2012-07-06 | 2021-11-23 | Genmab B.V. | Proteína dimérica, proteína, composição, kit de partes e seus usos, bem como método para aumentar a oligomerização em solução de uma proteína dimérica compreendendo um primeiro e segundo polipeptídeo, cada um compreendendo pelo menos as regiões ch2 e ch3 de uma cadeia pesada de igg1 humana e proteína dimérica variante |
| WO2014018572A2 (en) | 2012-07-23 | 2014-01-30 | Zymeworks Inc. | Immunoglobulin constructs comprising selective pairing of the light and heavy chains |
| US9540442B2 (en) | 2012-08-02 | 2017-01-10 | Jn Biosciences Llc | Antibodies or fusion proteins multimerized via cysteine mutation and a mu tailpiece |
| US20150203591A1 (en) | 2012-08-02 | 2015-07-23 | Regeneron Pharmaceuticals, Inc. | Mutivalent antigen-binding proteins |
| EP2904093B1 (en) | 2012-10-03 | 2019-04-10 | Zymeworks Inc. | Methods of quantitating heavy and light chain polypeptide pairs |
| EP2904016B1 (en) | 2012-10-08 | 2018-11-14 | Roche Glycart AG | Fc-free antibodies comprising two fab-fragments and methods of use |
| UY35148A (es) | 2012-11-21 | 2014-05-30 | Amgen Inc | Immunoglobulinas heterodiméricas |
| US9914785B2 (en) | 2012-11-28 | 2018-03-13 | Zymeworks Inc. | Engineered immunoglobulin heavy chain-light chain pairs and uses thereof |
| WO2014100490A1 (en) | 2012-12-19 | 2014-06-26 | Adimab, Llc | Multivalent antibody analogs, and methods of their preparation and use |
| KR102249779B1 (ko) | 2012-12-27 | 2021-05-07 | 추가이 세이야쿠 가부시키가이샤 | 헤테로이량화 폴리펩티드 |
| EA201500741A1 (ru) | 2013-01-10 | 2016-01-29 | Генмаб Б.В. | ВАРИАНТЫ Fc-ОБЛАСТИ IGG1 ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ |
| TWI635098B (zh) | 2013-02-01 | 2018-09-11 | 再生元醫藥公司 | 含嵌合恆定區之抗體 |
| HK1218930A1 (zh) | 2013-02-08 | 2017-03-17 | Abbvie Stemcentrx Llc | 新型多特异性结构 |
| US20140308285A1 (en) | 2013-03-15 | 2014-10-16 | Amgen Inc. | Heterodimeric bispecific antibodies |
| ES2821753T3 (es) | 2013-03-15 | 2021-04-27 | Lilly Co Eli | Procedimientos de producción de Fab y de anticuerpos biespecíficos |
| US10858417B2 (en) | 2013-03-15 | 2020-12-08 | Xencor, Inc. | Heterodimeric proteins |
| US20140302037A1 (en) | 2013-03-15 | 2014-10-09 | Amgen Inc. | BISPECIFIC-Fc MOLECULES |
| CN118561989A (zh) | 2013-04-29 | 2024-08-30 | 豪夫迈·罗氏有限公司 | Fc-受体结合的修饰的非对称抗体及使用方法 |
| US20160114057A1 (en) | 2013-05-24 | 2016-04-28 | Zyeworks Inc. | Modular protein drug conjugate therapeutic |
| ES2736326T3 (es) | 2013-05-31 | 2019-12-27 | Zymeworks Inc | Heteromultímeros con función efectora reducida o silenciada |
| ES2658039T3 (es) | 2013-07-10 | 2018-03-08 | Sutro Biopharma, Inc. | Anticuerpos que comprenden múltiples residuos de aminoácidos no naturales sitio-específicos, métodos para su preparación y métodos de uso |
| EP3036262A4 (en) | 2013-08-22 | 2017-03-01 | Acceleron Pharma Inc. | Tgf-beta receptor type ii variants and uses thereof |
| SG10201803449VA (en) | 2013-09-27 | 2018-05-30 | Chugai Pharmaceutical Co Ltd | Method for producing polypeptide heteromultimer |
| KR20160044060A (ko) | 2013-10-11 | 2016-04-22 | 에프. 호프만-라 로슈 아게 | 다중특이적 도메인 교환된 통상의 가변 경쇄 항체 |
| CN105916880B (zh) | 2014-01-15 | 2020-01-17 | 豪夫迈·罗氏有限公司 | 具有改善的蛋白A结合作用的Fc区变体 |
| CN105873948B (zh) | 2014-01-15 | 2021-04-13 | 豪夫迈·罗氏有限公司 | 具有修饰的FCRN结合性质的Fc区变体 |
| CA2931986A1 (en) | 2014-01-15 | 2015-07-23 | F. Hoffmann-La Roche Ag | Fc-region variants with modified fcrn- and maintained protein a-binding properties |
| HUE054873T2 (hu) | 2014-02-10 | 2021-10-28 | Merck Patent Gmbh | Célzott TGF-béta-gátlás |
| US10106623B2 (en) | 2014-02-12 | 2018-10-23 | Michael Uhlin | Bispecific antibodies for use in stem cell transplantation |
| US20170058045A1 (en) | 2014-02-21 | 2017-03-02 | Regeneron Pharmaceuticals, Inc. | Methods, compositions and kits for cell specific modulation of target antigens |
| UA117289C2 (uk) | 2014-04-02 | 2018-07-10 | Ф. Хоффманн-Ля Рош Аг | Мультиспецифічне антитіло |
| HK1231490A1 (zh) | 2014-05-28 | 2017-12-22 | Zymeworks, Inc. | 修饰的抗原结合多肽构建体及其用途 |
| WO2015197582A1 (en) | 2014-06-27 | 2015-12-30 | Innate Pharma | Monomeric multispecific antigen binding proteins |
| AU2015279321B2 (en) | 2014-06-27 | 2021-03-04 | Innate Pharma, S.A. | Multispecific antigen binding proteins |
| JP6744292B2 (ja) | 2014-07-29 | 2020-08-19 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 多重特異性抗体 |
| PE20170263A1 (es) | 2014-08-04 | 2017-03-30 | Hoffmann La Roche | Moleculas biespecificas de union a antigeno activadoras de celulas t |
| GB201414823D0 (en) | 2014-08-20 | 2014-10-01 | Argen X Bv | Multispecific antibodies |
| RU2714116C2 (ru) | 2014-11-06 | 2020-02-11 | Ф. Хоффманн-Ля Рош Аг | ВАРИАНТЫ Fc-ОБЛАСТИ С МОДИФИЦИРОВАННЫМ СВЯЗЫВАНИЕМ FcRn И СПОСОБЫ ИХ ПРИМЕНЕНИЯ |
| AR102522A1 (es) | 2014-11-06 | 2017-03-08 | Hoffmann La Roche | Variantes de región fc con propiedades modificadas de unión a fcrn y proteína a |
| CA2968162A1 (en) | 2014-11-20 | 2016-05-26 | F. Hoffmann-La Roche Ag | Common light chains and methods of use |
| EP3227341A1 (en) | 2014-12-02 | 2017-10-11 | CeMM - Forschungszentrum für Molekulare Medizin GmbH | Anti-mutant calreticulin antibodies and their use in the diagnosis and therapy of myeloid malignancies |
| JP6721590B2 (ja) | 2014-12-03 | 2020-07-15 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 多重特異性抗体 |
| AU2015357053B2 (en) | 2014-12-05 | 2021-10-07 | Merck Patent Gmbh | Domain-exchanged antibody |
| US9767555B2 (en) | 2015-01-05 | 2017-09-19 | Case Western Reserve University | Disease characterization from fused pathology and radiology data |
| BR112017015136A2 (pt) | 2015-01-14 | 2018-01-30 | Compass Therapeutics Llc | polipeptídeo de construto de ligação ao antígeno imunomodulador multiespecífico, construto de ligação ao antígeno imunomodulador multiespecífico, conjugado, composição farmacêutica, método para tratar um indivíduo com câncer, método para inibir ou reduzir o crescimento de câncer, composição, célula, método de fazer um polipeptídeo de construto de ligação ao antígeno imunomodulador multiespecífico, vetor ou conjunto de vetores e kit |
| ES3006358T3 (en) | 2015-03-13 | 2025-03-18 | Novimmune Sa | Methods of purifying bispecific antibodies |
| ES3028883T3 (en) | 2015-08-31 | 2025-06-20 | Nat Res Council Canada | Tgf-beta-receptor ectodomain fusion molecules and uses thereof |
| WO2017165464A1 (en) * | 2016-03-21 | 2017-09-28 | Elstar Therapeutics, Inc. | Multispecific and multifunctional molecules and uses thereof |
| US11673971B2 (en) | 2016-09-23 | 2023-06-13 | Marengo Therapeutics, Inc. | Multispecific antibody molecules comprising lambda and kappa light chains |
| WO2019178362A1 (en) * | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| CN112955465A (zh) * | 2018-07-03 | 2021-06-11 | 马伦戈治疗公司 | 抗tcr抗体分子及其用途 |
| CN114026122B (zh) * | 2019-02-21 | 2024-12-31 | 马伦戈治疗公司 | 结合t细胞相关癌细胞的多功能分子及其用途 |
| CN114127113A (zh) * | 2019-02-21 | 2022-03-01 | 马伦戈治疗公司 | 与钙网蛋白结合的多功能分子及其用途 |
| EP4084821A4 (en) * | 2020-01-03 | 2024-04-24 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to cd33 and uses thereof |
-
2021
- 2021-08-25 CN CN202180073493.XA patent/CN116249718A/zh active Pending
- 2021-08-25 WO PCT/US2021/047571 patent/WO2022046920A2/en not_active Ceased
- 2021-08-25 CA CA3190755A patent/CA3190755A1/en active Pending
- 2021-08-25 AU AU2021331075A patent/AU2021331075A1/en not_active Abandoned
- 2021-08-25 JP JP2023513779A patent/JP2023542080A/ja active Pending
- 2021-08-25 EP EP21862666.1A patent/EP4204450A4/en active Pending
-
2023
- 2023-02-24 US US18/173,995 patent/US20240002543A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2021331075A1 (en) | 2023-04-06 |
| JP2023542080A (ja) | 2023-10-05 |
| WO2022046920A2 (en) | 2022-03-03 |
| EP4204450A4 (en) | 2024-11-13 |
| WO2022046920A3 (en) | 2022-04-07 |
| CA3190755A1 (en) | 2022-03-03 |
| EP4204450A2 (en) | 2023-07-05 |
| US20240002543A1 (en) | 2024-01-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20250340640A1 (en) | Anti-tcr antibody molecules and uses thereof | |
| CN114026122B (zh) | 结合t细胞相关癌细胞的多功能分子及其用途 | |
| CN116249718A (zh) | 结合至钙网蛋白的多功能性分子及其用途 | |
| JP7706373B2 (ja) | カルレティキュリンに結合する多機能性分子およびその使用 | |
| US20260022173A1 (en) | Anti-tcr antibody molecules and uses thereof | |
| CN110709422A (zh) | 多特异性分子及其用途 | |
| KR20230028242A (ko) | T 세포 관련 암 세포에 결합하는 다중기능성 분자 및 그것의 용도 | |
| US20230102344A1 (en) | Multifunctional molecules that bind to cd33 and uses thereof | |
| CN117597359A (zh) | 与tcr结合的多功能分子及其用途 | |
| CN118786150A (zh) | 与tcr结合的多功能分子及其用途 | |
| US20230333112A1 (en) | Methods of detecting trbc1 or trbc2 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |