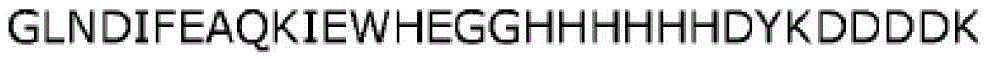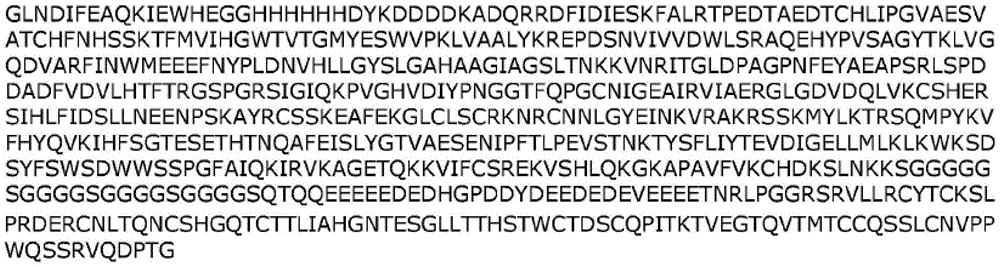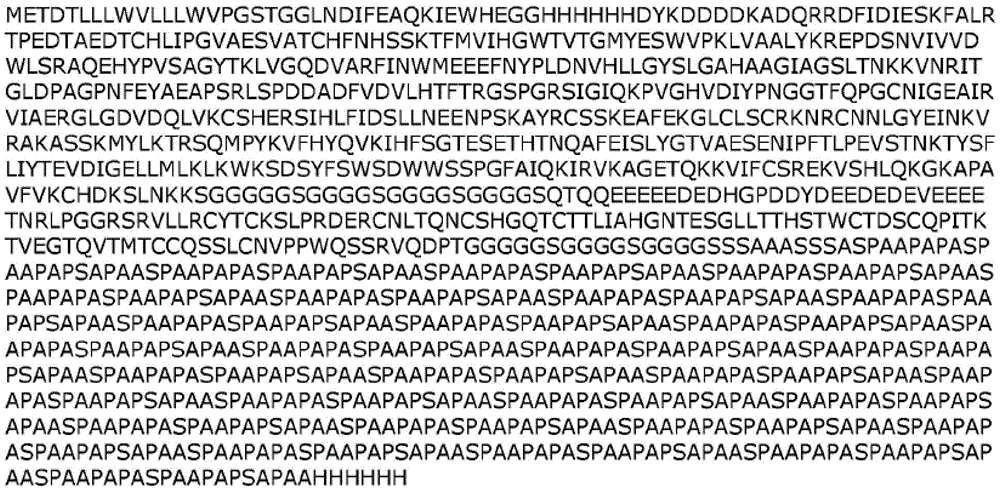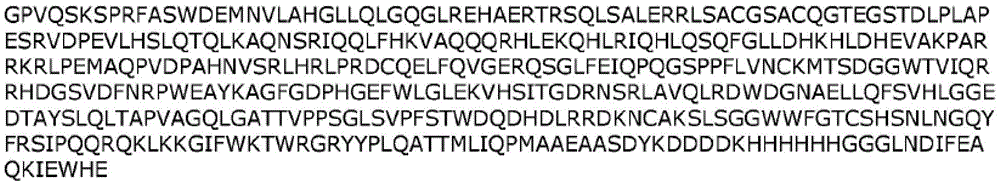CN113396158A - Lpl-gpihbp1融合多肽 - Google Patents
Lpl-gpihbp1融合多肽 Download PDFInfo
- Publication number
- CN113396158A CN113396158A CN201980089752.0A CN201980089752A CN113396158A CN 113396158 A CN113396158 A CN 113396158A CN 201980089752 A CN201980089752 A CN 201980089752A CN 113396158 A CN113396158 A CN 113396158A
- Authority
- CN
- China
- Prior art keywords
- seq
- lpl
- polypeptide
- fusion polypeptide
- gpihbp1
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/18—Carboxylic ester hydrolases (3.1.1)
- C12N9/20—Triglyceride splitting, e.g. by means of lipase
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y301/00—Hydrolases acting on ester bonds (3.1)
- C12Y301/01—Carboxylic ester hydrolases (3.1.1)
- C12Y301/01034—Lipoprotein lipase (3.1.1.34)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/20—Fusion polypeptide containing a tag with affinity for a non-protein ligand
- C07K2319/21—Fusion polypeptide containing a tag with affinity for a non-protein ligand containing a His-tag
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/35—Fusion polypeptide containing a fusion for enhanced stability/folding during expression, e.g. fusions with chaperones or thioredoxin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/40—Fusion polypeptide containing a tag for immunodetection, or an epitope for immunisation
- C07K2319/43—Fusion polypeptide containing a tag for immunodetection, or an epitope for immunisation containing a FLAG-tag
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Obesity (AREA)
- Veterinary Medicine (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Toxicology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本披露涉及包含脂蛋白脂肪酶(LPL)和糖基磷脂酰肌醇锚定高密度脂蛋白结合蛋白1(GPIHBP1)的融合多肽。本披露还涉及此类融合多肽在治疗诸如家族性乳糜微粒血症综合征(FCS)等疾病中的用途。
Description
技术领域
本披露涉及包含脂蛋白脂肪酶(LPL)和糖基磷脂酰肌醇锚定高密度脂蛋白结合蛋白1(GPIHBP1)的融合多肽。本披露还涉及此类融合多肽在治疗诸如家族性乳糜微粒血症综合征(FCS)等疾病中的用途。
背景技术
家族性乳糜微粒血症综合征(FCS)是一种由脂蛋白脂肪酶(LPL)缺陷引起并且特征在于异常高水平的血浆甘油三酯(TG)的罕见遗传性障碍。FCS患者表现为儿童期发病的严重高甘油三酯血症(>1,000mg/dL)、腹痛发作、复发性急性胰腺炎(AP)、发疹性皮肤黄色瘤、视网膜脂血症和肝脾大。AP是FCS的频繁且严重的表现(Davidson等人,2018,J.Clin.Lipidol[临床血脂学杂志],12(4):898-907.e2)。AP的风险随TG水平增加而逐渐增加(Nawaz等人,2015,Am J Gastroenterol[美国胃肠病学杂志]110:1497-1503)。高脂血症性胰腺炎(HTAP)的死亡率可以高达20%-30%(Gubensek等人,2014,PLoS One[公共科学图书馆·综合]9,e102748)。
脂蛋白脂肪酶(LPL)是脂肪酶基因家族成员。LPL是主要由脂肪细胞、骨骼肌细胞和心肌细胞分泌的甘油三酯脂肪酶。LPL折叠是由伴侣分子脂肪酶成熟因子1(LMF1)介导的。LPL分泌到内皮下空间,然后通过糖基磷脂酰肌醇HDL结合蛋白1(GPIHBP1)易位到毛细血管腔。易位后,LPL通过硫酸乙酰肝素蛋白多糖或GPIHBP1栓系到内皮细胞。栓系的LPL催化极低密度脂蛋白(VLDL)和乳糜微粒(CM)中携带的甘油三酯(TG)的水解(Savonen等人,2015,J Lipid Res[脂质研究杂志]56:588-598;Goulbourne等人,2014,Cell Metab[细胞代谢]18:389-396)。由LPL释放的游离脂肪酸被心脏和肌肉组织用作能量来源或被脂肪组织以TG的形式储存。LPL是受激动剂(ApoC2)刺激且受拮抗剂(ANGPTL3、ANGPTL 4、ANGPTL8)抑制的严格受控的酶(He等人,2018,Clin Chim Acta[临床化学学报]480:126-137)。LPL、GPIHBP1、LMF1的功能丧失突变导致LPL缺陷,从而引起血液中富含TG的CM的积累。
已证实尚无特效的经批准的药理学干预可改善高脂血症性胰腺炎(HTAP)的临床病程。用于将TG急剧降低至<1000mg/dL来治疗HTAP的治疗选择限于将患者转换为接受低热量肠胃外营养结合支持性护理。如果设备可用,则可以使用血浆置换(Chaudhry等人,2018,Expert Rev Clin Pharmacol[临床药理学专家评论]11:589-598;Gaudet等人,2013,JMedEcon[医学经济学杂志]16:657-666;Valaiyapathi和Ashraf,2017,Curr.Pediatr.Rev.[当代儿科研究]13(4):225-231),但是这非常昂贵。HTAP的预防也难以实现。FCS患者有很少选择来维持血浆TG低于1000mg/dL以避免腹痛发作和HTAP。此类患者在他们的整个生命中必须限制他们的膳食脂肪少于20g/天或15%的总能量摄入。百分之八十(80%)的FCS患者将这种依从性评价为“非常困难”(Stroes等人,2017,Atheroscler Suppl[动脉粥样硬化增刊]23:1-7)。
发明内容
我们出乎意料地发现当表达为与糖基磷脂酰肌醇锚定高密度脂蛋白结合蛋白1(GPIHBP1)的融合多肽时,脂蛋白脂肪酶(LPL)维持高比活性,不聚集,在PBS中稳定并且对被ANGPTL4活化有抗性。
因此,在一方面,本披露提供了融合多肽,所述融合多肽包含(i)脂蛋白脂肪酶(LPL)多肽或其功能性变体;以及(ii)糖基磷脂酰肌醇锚定高密度脂蛋白结合蛋白1(GPIHBP1)多肽或其功能性变体。所述GPIHBP1多肽(或其功能性变体)可以位于所述LPL多肽(或其功能性变体)的C末端或N末端。所述LPL多肽(或其功能性变体)和所述GPIHBP1多肽(或其功能性变体)可以直接融合在一起,或者可以通过接头连接。所述融合多肽可以进一步包含N末端或C末端氨基酸序列,例如以帮助纯化、以改善表达或以增加半衰期。此类N末端或C末端氨基酸序列可以被包括在所述多肽的表达中,但是随后(例如,在施用前)被去除。
在一个实施例中,本披露提供了一种从N末端至C末端具有式(I)或(II)之一的融合多肽:
A-B(n)-C-D(m)-E(I),或
A-D(m)-C-B(n)-E(II),其中
A=任选的N末端序列
B=LPL多肽或其功能性变体
C=任选的接头序列
D=GPIHBP1多肽或其功能性变体
E=任选的C末端序列,其中
n=从1至3的整数,并且
m=从1至3的整数。
在一些实施例中,n=1。在一些实施例中,m=1。在一些实施例中,n=1并且m=1。在某些实施例中,所述LPL多肽和/或所述GPIHBP1多肽是基于哺乳动物序列或其衍生物的。在特定的实施例中,所述LPL多肽和/或所述GPIHBP1多肽是基于人序列或其衍生物的。
在一些实施例中,所述LPL多肽的功能性变体包含与SEQ ID NO:1或SEQ ID NO:2的LPL多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。在一些实施例中,所述LPL多肽的功能性变体由与SEQ ID NO:1或SEQ ID NO:2的LPL多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列组成。在一些实施例中,所述LPL多肽的功能性变体包含以下的氨基酸序列:(i)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;或(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变的SEQ ID NO:1。在一些实施例中,所述LPL多肽的功能性变体由以下的氨基酸序列组成:(i)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;或(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变的SEQID NO:1。
在某些实施例中,所述LPL多肽的功能性变体是SEQ ID NO:1的截短形式。在某些实施例中,所述LPL多肽的功能性变体是SEQ ID NO:2的截短形式。在一些实施例中,所述LPL多肽的功能性变体是以下的截短形式:(i)与SEQ ID NO:1或SEQ ID NO:2具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;(iii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变的SEQ ID NO:1;(iv)SEQ ID NO:1;或(v)SEQ ID NO:2。在一些实施例中,所述LPL多肽的功能性变体是以下的截短形式:(i)与SEQ ID NO:1或SEQ IDNO:2具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;(iii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQID NO:1的氨基酸157-189中的任一个的点突变的SEQ ID NO:1;(iv)SEQ ID NO:1;或(v)SEQ ID NO:2,其中所述LPL多肽的截短形式对应于包含以下或由其组成的多肽的氨基酸序列:SEQ ID NO:1的氨基酸36-335、35-340、34-345、33-350、32-355、31-360、30-365、29-370、28-375、28-380、28-385、28-390、28-395、28-400、28-405、28-410、28-415、28-420、28-425、28-430、28-435、28-440、28-445、28-450、28-455、28-460、28-465或28-470。
在一些实施例中,所述LPL多肽的截短形式对应于包含以下或由其组成的多肽的氨基酸序列:SEQ ID NO:1的氨基酸36-335、35-340、34-345、33-350、32-355、31-360、30-365、29-370、28-375、28-380、28-385、28-390、28-395、28-400、28-405、28-410、28-415、28-420、28-425、28-430、28-435、28-440、28-445、28-450、28-455、28-460、28-465或28-470。在其某些实施例中,SEQ ID NO:1的所述截短形式与SEQ ID NO:1的对应区域具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性;任选地其中SEQ ID NO:1的所述截短形式具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变。
在一些实施例中,所述LPL多肽包含SEQ ID NO:1、2、3、4或45中的任一个或由其组成。
在一些实施例中,所述GPIHBP1多肽的功能性变体包含与SEQ ID NO:5、SEQ IDNO:6或SEQ ID NO:7的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。在一些实施例中,所述GPIHBP1多肽的功能性变体由与SEQ ID NO:5、SEQ ID NO:6或SEQ ID NO:7的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列组成。在某些实施例中,所述GPIHBP1多肽的功能性变体包含以下的氨基酸序列:具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:7的氨基酸中的任一个的点突变的SEQ ID NO:7。在某些实施例中,所述GPIHBP1多肽的功能性变体由以下的氨基酸序列组成:具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:7的氨基酸中的任一个的点突变的SEQ ID NO:7。
在一些实施例中,所述GPIHBP1多肽的功能性变体是以下的截短形式:(i)与SEQID NO:5的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;或(ii)SEQ ID NO:5。在一些实施例中,所述GPIHBP1多肽的功能性变体是以下的截短形式:(i)与SEQ ID NO:5的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;或(ii)SEQ ID NO:5,其中所述GPIHBP1多肽的截短形式对应于包含以下或由其组成的多肽的氨基酸序列:SEQ ID NO:5的氨基酸62-149、61-150、60-151、55-152、50-153、45-154、40-155、35-156、30-157、25-158或20-159。
在某些实施例中,所述GPIHBP1多肽的截短形式对应于包含以下或由其组成的多肽的氨基酸序列:SEQ ID NO:5的氨基酸62-149、61-150、60-151、55-152、50-153、45-154、40-155、35-156、30-157、25-158或20-159。在某些实施例中,SEQ ID NO:5的所述截短形式与SEQ ID NO:5的对应区域具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性。
在一些实施例中,所述GPIHBP1多肽包含SEQ ID NO:5、6、7、8、9或10中的任一个或由其组成。
在某些实施例中,所述LPL多肽和所述GPIHBP1多肽通过接头连接。在某些实施例中,所述LPL多肽和所述GPIHBP1多肽通过接头C连接。在一些实施例中,所述接头包含SEQID NO:11-27中的任一个所示的氨基酸序列或由其组成。在一些实施例中,所述接头包含SEQ ID NO:16或SEQ ID NO:17所示的氨基酸序列或由其组成。在一些实施例中,所述接头包含SEQ ID NO:11-27中的任一个所示的一个或多个氨基酸序列或由其组成。在一些实施例中,所述接头包含SEQ ID NO:16或SEQ ID NO:17所示的一个或多个氨基酸序列或由其组成。
在一些实施例中,所述融合多肽包含N末端序列。在一些实施例中,所述融合多肽包含N末端序列A。在一些实施例中,所述融合多肽包含C末端序列。在一些实施例中,所述融合多肽包含C末端序列E。在某些实施例中,所述N末端序列或所述C末端序列包含一个或多个选自下组的标签,该组由以下组成:His标签、FLAG标签、Arg标签、T7标签、Strep标签、S标签、AviTagTM和适配体标签。在一些实施例中,所述N末端序列或所述C末端序列包含His标签和AviTagTM。在一些实施例中,所述N末端序列或所述C末端序列由His标签和AviTagTM组成。在一些实施例中,所述N末端序列或所述C末端序列包含FLAG标签、His标签和AviTagTM。在一些实施例中,所述N末端序列或所述C末端序列由FLAG标签、His标签和AviTagTM组成。在某些实施例中,所述N末端序列或所述C末端序列包含SEQ ID NO:31或SEQ ID NO:32所示的氨基酸序列或由其组成。
在一些实施例中,所述N末端序列或所述C末端序列包含增加所述融合多肽在体内的半衰期的部分。在某些实施例中,所述N末端序列或所述C末端序列包含PEG序列、PAS序列或抗体序列。在一些实施例中,所述N末端序列或所述C末端序列包含增加所述融合多肽在体内的半衰期的部分,其中所述N末端序列或所述C末端序列包含PEG序列、PAS序列或任选地选自Fab或ScFv分子的抗体序列。在一些实施例中,所述抗体序列是Fab或ScFv分子。在一些实施例中,所述抗体Fab或ScFv结合白蛋白。在某些实施例中,所述抗体是CA645。
在一些实施例中,本文所述的融合多肽包含SEQ ID NO:33-40、46-48、51、53、54或55中的任一个的氨基酸序列或由其组成。在一些实施例中,本文所述的融合多肽包含表1中的氨基酸序列(任选地没有信号肽)中的任一个或由其组成。
在其他方面,本披露涉及一种编码如本文所述的融合多肽的核酸分子(例如,分离的核酸分子),包括DNA和RNA分子。
在一些实施例中,所述核酸分子包含与编码SEQ ID NO:33-40、46-48、51、53、54或55中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列。在一些实施例中,所述核酸分子包含与编码表1中的氨基酸序列中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列。
在一些实施例中,所述核酸分子包含与SEQ ID NO:44具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列。
在一些实施例中,所述核酸分子包含SEQ ID NO:44的核苷酸序列或由其组成。
还披露了包含本披露的核酸分子的载体,特别是表达载体。
本披露还提供了包含编码如本文所述的融合多肽的核酸和/或载体的宿主细胞。
本披露还提供了一种用于制备如本文所述的融合多肽的方法,所述方法包括将本披露的宿主细胞维持在适于表达核酸的条件下,从而表达重组核酸并且产生所述融合多肽。所述方法可以进一步包括分离和/或纯化所述融合多肽。
本披露还提供了一种药物组合物,所述药物组合物包含本披露的融合多肽、核酸分子、载体或宿主细胞,任选地进一步包含药学上或生理学上可接受的稀释剂和/或载体。本披露还提供了一种药物组合物,所述药物组合物包含本披露的融合多肽、核酸分子、载体或宿主细胞、以及药学上或生理学上可接受的稀释剂和/或载体。
本披露还提供了一种治疗患有病理学病症的患者的方法,所述方法包括向有需要的受试者施用本披露的融合多肽、核酸分子、载体、宿主细胞或药物组合物。在一个实施例中,所述受试者可以患有乳糜微粒血症综合征。
本披露还提供了根据本披露的融合多肽、核酸分子、载体、宿主细胞或药物组合物,(i)用于疗法和/或(ii)用于制造治疗本文披露的病理学障碍、疾病或病症的药物。在一些实施例中,本文提供了一种治疗患有病理学障碍、疾病或病症的患者的方法,所述方法包括向所述患者施用治疗有效量的本文所述的融合多肽、核酸、载体、宿主细胞或药物组合物。在一些实施例中,所述病理学障碍、疾病或病症可以选自乳糜微粒血症(包括家族性乳糜微粒血症综合征、多基因晚发性乳糜微粒血症和早发性乳糜微粒血症)、高脂血症性胰腺炎、高甘油三酯血症、腹痛、复发性急性胰腺炎、发疹性皮肤黄色瘤、视网膜脂血症、肝脾大、糖尿病、肥胖症、心血管疾病、慢性肾脏疾病、非酒精性脂肪性肝病、高甘油三酯血症性胰腺炎、肝脂肪变性、代谢综合征、缺血性心脏病和微血管病状。在一个实施例中,所述病症可以是乳糜微粒血症综合征(例如,家族性乳糜微粒血症综合征)。
附图说明
图1是显示多种LPL构建体的聚集水平、产率和脂肪酶活性的一系列图。图1小图(A)和(C)证明LPL成功表达(A),但是呈聚集形式(C)。当LPL与GPIHBP1共表达(B)时,未观察到聚集(C)。LPL和GPIHBP1的共表达导致更高的LPL活性(D),并且还保护LPL免于自发失活(E)。
图2是展示LPL-GPIHBP1融合多肽的聚集水平、活性和稳定性的一系列图。图1小图(A)和(B)证明LPL-GPIHBP1融合多肽稳定表达(A),并且没有聚集(B)。LPL-GPIHBP1融合多肽具有与共表达的构建体相当的活性(C),并且也是稳定的(D)。
图3示出了测试ANGPTL4是否能够从融合多肽中置换LPL的测定的示意图和结果(A)。ANGPTL4能够从共表达的LPL/GPIHBP1复合物中置换LPL(B)。展示了ANGPTL4与融合多肽和共表达的复合物二者的结合(C)。ANGPTL4和GPIHBP1二者均能够解离LPL/GPIHBP1复合物(D)。
图4是证明LPL/GPIHBP1复合物或LPL/GPIHBP1融合多肽对被ANGPTL4(A)或ANGPTL3(B)失活有抗性的一组图。
图5是展示对LPL/GPIHBP1融合多肽(A)和共表达的LPL/GPIHBP1复合物(B)二者的LPL的ANGPTL4结合表位定位的一组图。
图6是展示皮下施用的LPL/GPIHBP1融合多肽在C57BL/6小鼠中降低TG水平的能力的一组图。
图7是展示当静脉施用时LPL/GPIHBP1融合多肽在DBA/2小鼠中降低TG水平的能力的一系列图(A,B)。未观察到血浆游离脂肪酸的增加(C)。在5天内每日施用也始终降低血浆TG(D,E)。
图8是展示皮下施用的LPL/GPIHBP1融合多肽在DBA/2小鼠中降低TG水平的能力的一组图。
图9是证明在单次给药情况下接受正常饮食(A,B)或在重复给药情况下接受高脂肪饮食(C,D)的TALLYHO小鼠中皮下施用的LPL/GPIHBP1融合多肽对TG水平的剂量依赖性降低的一系列图。
图10是证明与白蛋白结合部分连接的LPL/GPIHBP1融合多肽降低TG的持续时间增加的一组图。
具体实施方式
脂蛋白脂肪酶(LPL)及其功能性变体
本文所述的融合多肽中使用的LPL多肽可以是哺乳动物的,诸如像人的。野生型人LPL是由具有UniProtKB/Swiss-Prot登录号P06858.1的氨基酸序列(SEQ ID NO:1)编码的。人LPL最初被翻译为具有475个氨基酸的前体蛋白。然后包含此前体蛋白的氨基酸1-27的信号肽被切割,留下包含氨基酸28-475的成熟形式(SEQ ID NO:2)。
在一个实施例中,本披露的融合多肽中使用的LPL多肽包含与SEQ ID NO:1或SEQID NO:2的LPL多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。在一个实施例中,本披露的融合多肽中使用的LPL多肽由与SEQ ID NO:1或SEQ ID NO:2的LPL多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列组成。在一个实施例中,本披露的融合多肽中使用的LPL多肽包含SEQ ID NO:1的氨基酸序列或由其组成。在一个实施例中,本披露的融合多肽中使用的LPL多肽包含SEQ ID NO:2的氨基酸序列或由其组成。
在另一个实施例中,本披露的融合多肽中使用的LPL多肽的功能性变体可以包含一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代成熟的人LPL多肽(SEQ ID NO:2)的氨基酸中的任一个的点突变。
如本文所用,“功能性变体”是指与亲本蛋白具有实质或显著序列同一性并且保留亲本蛋白的至少一种生物学活性的亲本蛋白变体。鉴于本披露,亲本蛋白的功能性变体可以通过本领域已知的手段制备。功能性变体可以包括对亲本蛋白的氨基酸的一个或多个修饰。所述修饰可以例如通过改善多肽的热稳定性、改变底物特异性、改变最适pH等改变多肽的物理化学特性。所述修饰还可以改变亲本蛋白的生物学活性,只要它们不破坏或消除亲本蛋白的所有生物学活性即可。
在一些实施例中,亲本蛋白的功能性变体包含不显著影响亲本蛋白的生物学活性的对亲本蛋白的取代,诸如保守氨基酸取代。保守取代包括但不限于在以下的组内的氨基酸取代:碱性氨基酸(精氨酸、赖氨酸和组氨酸)、酸性氨基酸(谷氨酸和天冬氨酸)、极性氨基酸(谷氨酰胺和天冬酰胺)、疏水性氨基酸(亮氨酸、异亮氨酸和缬氨酸)、芳香族氨基酸(苯丙氨酸、色氨酸和酪氨酸)以及小氨基酸(甘氨酸、丙氨酸、丝氨酸、苏氨酸和甲硫氨酸)。非标准或非天然氨基酸(诸如4-羟基脯氨酸、6-N-甲基赖氨酸、2-氨基异丁酸、异缬氨酸和α-甲基丝氨酸)也可以用于取代亲本蛋白中的标准氨基酸残基。
在一些实施例中,亲本蛋白的功能性变体包含对亲本蛋白的一个或多个氨基酸的缺失和/或插入。例如,LPL蛋白(例如,成熟LPL蛋白)的功能性变体可以包括对LPL蛋白(例如,成熟LPL蛋白)的1、2、3、4、5、6、7、8、9、10个或更多个氨基酸的缺失和/或插入。
在一些实施例中,亲本蛋白的功能性变体包含对亲本蛋白的氨基酸的取代(诸如保守氨基酸取代)和缺失和/或插入(诸如小缺失和/或插入)。
例如,在一个实施例中,可以对在SEQ ID NO:2的氨基酸294-297(SEQ ID NO:1的氨基酸321-324)处发现的RAKR序列进行一个或多个点突变。在一个实施例中,SEQ ID NO:2中的突变是R294A(如SEQ ID NO:45中所示)。RAKR序列是前蛋白转化酶的切割位点。因此,此位点的突变可以使多肽对蛋白质切割有抗性。可以对本披露的融合多肽中使用的LPL多肽进行可替代突变以抵抗蛋白水解切割,并且将所述可替代突变涵盖在本披露的范围内。
可以进行其他点突变以改善LPL多肽的功能。例如,在一个实施例中,本文所述的融合多肽中使用的功能性变体LPL多肽可以是所谓的“S447X”突变形式。此变体在LPL核苷酸序列的核苷酸1595处具有C到G的变化。这导致丝氨酸447到密码子的变化,产生缺乏最后两个C末端氨基酸(S和G)的LPL截短形式。此截短形式示于SEQ ID NO:3中。因此,在一个实施例中,本披露中使用的功能性变体LPL多肽包含SEQ ID NO:3或由其组成。
本披露的融合多肽中使用的LPL多肽可以在ANGPTL4结合位点中包含一个或多个点突变。因此,本披露的融合多肽中使用的LPL多肽可以在跨越SEQ ID NO:1的氨基酸157-189的区域中包含一个或多个点突变(缺失、添加或取代)。
LPL多肽的其他截短形式也可以用于本披露的融合多肽中。例如,仅包含氨基酸37-334的LPL截短形式(SEQ ID NO:4)(在本文中称为最小LPL催化结构域)可以用于本披露的融合多肽中。可用于本披露的融合多肽中的其他LPL截短形式包括对应于包含以下或由其组成的多肽的氨基酸序列的那些:氨基酸36-335、35-340、34-345、33-350、32-355、31-360、30-365、29-370、28-375、28-380、28-385、28-390、28-395、28-400、28-405、28-410、28-415、28-420、28-425、28-430、28-435、28-440、28-445、28-450、28-455、28-460、28-465或28-470(所有均参考SEQ ID NO:1)。
野生型LPL多肽的其他突变形式或截短形式也适用于本披露的融合多肽。在本披露中用作LPL多肽的功能性变体的任何此类突变形式或截短形式应当优选地保留SEQ IDNO:2中所示的野生型成熟多肽的至少一部分的活性。在一个实施例中,本披露的LPL多肽的功能性变体保留SEQ ID NO:2中所示的野生型成熟多肽的至少10%(例如20%、30%、40%、50%、60%、70%、80%、90%、95%、97%、98%、99%或更多)的活性。在某个实施例中,本披露的LPL多肽的功能性变体保留SEQ ID NO:2中所示的野生型成熟多肽的至少90%或更多的活性。在一个实施例中,可以使用三油酸甘油酯脂肪酶活性测定测量所述活性。参见例如,来自富士胶片和光诊断剂美国公司(FUJIFILM Wako DiagnosticsU.S.A.Corporation)或Hoppe和Theimer,1996,Phytochemistry[植物化学],42(4):973-978的HR系列NEFA-HR(2)测定。
糖基磷脂酰肌醇HDL结合蛋白1(GPIHBP1)及其功能性变体
本文所述的融合多肽中使用的GPIHBP1多肽可以是哺乳动物的,包括例如人的。野生型人GPIHBP1是由具有UniProtKB/Swiss-Prot登录号Q8IV16的氨基酸序列(SEQ ID NO:5)编码的。人GPIHBP1最初被翻译为具有184个氨基酸的前体蛋白。然后包含此前体蛋白的氨基酸1-20的信号肽被切割,产生包含氨基酸21-184的形式(SEQ ID NO:6)。当最初翻译时,人GPIHBP1还包含跨越氨基酸152-184的前肽。这也被去除,产生包含氨基酸21-151的成熟形式(SEQ ID NO:7)。
在一个实施例中,本披露的融合多肽中使用的GPIHBP1多肽包含与SEQ ID NO:5、SEQ ID NO:6或SEQ ID NO:7的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。在一个实施例中,本披露的融合多肽中使用的GPIHBP1多肽由与SEQ ID NO:5、SEQ ID NO:6或SEQ ID NO:7的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列组成。在一个实施例中,本披露的融合多肽中使用的GPIHBP1多肽包含SEQ ID NO:5的氨基酸序列或由其组成。在一个实施例中,本披露的融合多肽中使用的GPIHBP1多肽包含SEQ ID NO:6的氨基酸序列或由其组成。在一个实施例中,本披露的融合多肽中使用的GPIHBP1多肽包含SEQ ID NO:7的氨基酸序列或由其组成。
在另一个实施例中,本披露的融合多肽中使用的功能性变体GPIHBP1多肽可以包含一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代成熟的人GPIHBP1多肽(SEQ ID NO:7)的氨基酸中的任一个的点突变。
如本文所用,“功能性变体”是指与亲本蛋白具有实质或显著序列同一性并且保留亲本蛋白的至少一种生物学活性的亲本蛋白变体。鉴于本披露,亲本蛋白的功能性变体可以通过本领域已知的手段制备。功能性变体可以包括对亲本蛋白的氨基酸的一个或多个修饰。所述修饰可以例如通过改善多肽的热稳定性、改变底物特异性、改变最适pH等改变多肽的物理化学特性。所述修饰还可以改变亲本蛋白的生物学活性,只要它们不破坏或消除亲本蛋白的所有生物学活性即可。
在一些实施例中,亲本蛋白的功能性变体包含不显著影响亲本蛋白的生物学活性的对亲本蛋白的取代,诸如保守氨基酸取代。保守取代包括但不限于在以下的组内的氨基酸取代:碱性氨基酸(精氨酸、赖氨酸和组氨酸)、酸性氨基酸(谷氨酸和天冬氨酸)、极性氨基酸(谷氨酰胺和天冬酰胺)、疏水性氨基酸(亮氨酸、异亮氨酸和缬氨酸)、芳香族氨基酸(苯丙氨酸、色氨酸和酪氨酸)以及小氨基酸(甘氨酸、丙氨酸、丝氨酸、苏氨酸和甲硫氨酸)。非标准或非天然氨基酸(诸如4-羟基脯氨酸、6-N-甲基赖氨酸、2-氨基异丁酸、异缬氨酸和α-甲基丝氨酸)也可以用于取代亲本蛋白中的标准氨基酸残基。
在一些实施例中,亲本蛋白的功能性变体包含对亲本蛋白的一个或多个氨基酸的缺失和/或插入。例如,GPIHBP1蛋白(例如,成熟GPIHBP1蛋白)的功能性变体可以包括对GPIHBP1蛋白(例如,成熟GPIHBP1蛋白)的1、2、3、4、5、6、7、8、9、10个或更多个氨基酸的缺失和/或插入。
在一些实施例中,亲本蛋白的功能性变体包含对亲本蛋白的氨基酸的取代(诸如保守氨基酸取代)和缺失和/或插入(诸如小缺失和/或插入)。
GPIHBP1多肽的截短形式也可以用于本披露的融合多肽中。例如,缺乏前肽但是保留信号肽的GPIHBP1多肽的截短形式可以包含SEQ ID NO:5的氨基酸1-151(SEQ ID NO:8)。仅包含氨基酸63-148的可替代GPIHBP1截短形式(SEQ ID NO:9)(在本文中称为人GPIHBP1的最小功能结构域)可以用于本披露的融合多肽中。可用于本披露的融合多肽中的其他GPIHBP1截短形式包括包含氨基酸62-149、61-150、60-151、55-152、50-153、45-154、40-155、35-156、30-157、25-158、21-160、20-159(所有均参考SEQ ID NO:5)的那些。包含氨基酸21-160的截短形式在本文中称为SEQ ID NO:10。
野生型GPIHBP1多肽的其他突变形式或截短形式也适用于本披露的融合多肽。在本披露的融合多肽中用作GPIHBP1多肽的功能性变体的任何此类突变形式或截短形式应当优选地保留SEQ ID NO:7中所示的野生型成熟多肽的活性。在一个实施例中,本披露的GPIHBP1多肽的功能性变体保留SEQ ID NO:7中所示的野生型成熟多肽的至少10%(例如20%、30%、40%、50%、60%、70%、80%、90%、95%、97%、98%、99%或更多)的活性。在某个实施例中,本披露的GPIHBP1多肽的功能性变体保留SEQ ID NO:7中所示的野生型成熟多肽的至少90%或更多的活性。可以通过评估GPIHBP1的功能性变体保护LPL免于自发失活和免于被ANGPTL3和ANGPTL4失活的能力来测量所述功能性变体的活性。
LPL和GPIHBP1的示例性组合
本披露的融合多肽可以包含在本披露中所述的LPL和GPIHBP1部分中的任一种的组合。作为一组非限制性实例,LPL部分可以包含SEQ ID NO:1、2、3、4或45中的任一个或由其组成,并且GPIHBP1部分可以包含SEQ ID NO:5、6、7、8、9或10中的任一个或由其组成。
在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ ID NO:5的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ ID NO:6的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ ID NO:7的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ IDNO:8的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ IDNO:9的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:1的LPL部分和SEQ IDNO:10的GPIHBP1部分。
在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ ID NO:5的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ ID NO:6的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ ID NO:7的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ IDNO:8的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ IDNO:9的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:2的LPL部分和SEQ IDNO:10的GPIHBP1部分。
在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ ID NO:5的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ ID NO:6的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ ID NO:7的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ IDNO:8的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ IDNO:9的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:3的LPL部分和SEQ IDNO:10的GPIHBP1部分。
在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ ID NO:5的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ ID NO:6的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ ID NO:7的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ IDNO:8的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ IDNO:9的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:4的LPL部分和SEQ IDNO:10的GPIHBP1部分。
在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQ ID NO:5的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQ ID NO:6的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQ IDNO:7的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQID NO:8的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQ ID NO:9的GPIHBP1部分。在一个实施例中,融合蛋白可以包含SEQ ID NO:45的LPL部分和SEQ ID NO:10的GPIHBP1部分。
接头
在本披露中所述的LPL和GPIHBP1部分可以在连续的多肽链中与彼此直接键合,或通过合适的接头与彼此间接键合。接头可以是肽接头。肽接头通常用于融合多肽中,并且用于选择或设计接头的方法是众所周知的。(参见例如,Chen X等人Adv.Drug Deliv.Rev.[先进药物递送评论]65(10):135701369(2013)和Wriggers W等人,Biopolymers[生物聚合物]80:736-746(2005),将其各自的内容出于此目的并入本文)。
通常将肽接头分类为i)柔性接头,ii)螺旋形成接头,和iii)可切割接头,并且每种类型的实例是本领域已知的。在一个实例中,柔性接头被包括在本文所述的融合多肽中。柔性接头可以含有大部分的空间不受阻的氨基酸,诸如甘氨酸和丙氨酸。亲水性氨基酸Ser通常也用于柔性接头中。柔性接头的实例包括但不限于:聚甘氨酸(例如,(Gly)4和(Gly)5)、聚丙氨酸聚(Gly-Ala)和聚(Gly-Ser)(例如,(Glyn-Sern)n或(Sern-Glyn)n,其中每个n独立地是等于或大于1的整数)。
肽接头可以具有合适的长度。肽接头序列可以是至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、55、60、65、70、75个或更多个氨基酸残基的长度。例如,肽接头可以是从约5至约50个氨基酸的长度;从约10至约40个氨基酸的长度;从约15至约30个氨基酸的长度;或从约15至约20个氨基酸的长度。肽接头长度的变化可以保留或增强活性,从而在活性研究中产生优异的功效。肽接头序列可以由天然存在的氨基酸或非天然存在的氨基酸或者天然存在的氨基酸和非天然存在的氨基酸二者的混合物组成。
在一些方面,氨基酸甘氨酸和丝氨酸构成接头序列内的氨基酸。在某些方面,接头区包含甘氨酸重复的集合(GSG3)n(SEQ ID NO:11),其中n是等于或大于1的正整数(例如1至约20)。更具体地,接头序列可以是GSGGG(SEQ ID NO:12)。接头序列可以是GSGG(SEQ IDNO:13)。在某些其他方面,接头区取向包含甘氨酸重复的集合(SerGly3)n,其中n是等于或大于1的正整数(例如,1至约20)(SEQ ID NO:14)。
在其他实施例中,接头可以以随机或重复的方式含有甘氨酸(G)和丝氨酸(S)。例如,接头可以是(GGGGS)n(SEQ ID NO:15),其中n是范围从1至20的整数,例如1至4。在具体的实例中,n是4,并且接头是GGGGSGGGGSGGGGSGGGGS(SEQ ID NO:16)。在另一个具体的实例中,n是3,并且接头是GGGGSGGGGSGGGGS(SEQ ID NO:17)。
在其他实施例中,接头可以以随机或重复的方式含有甘氨酸(G)、丝氨酸(S)和脯氨酸(P)。例如,接头可以是(GPPGS)n,其中n是范围从1至20的整数,例如1-4。在具体的实例中,n是1,并且接头是GPPGS(SEQ ID NO:18)。
通常,当在患者或受试者(诸如人)中施用时,接头不是免疫原性的。因此,可以这样选择接头,使得它们具有低免疫原性或被认为具有低免疫原性。
本文所述的接头是示例性的,并且如果需要,接头可以包括其他氨基酸,诸如Glu和Lys。如果需要,肽接头可以包括例如(G3S)(SEQ ID NO:19)、(G4S)(SEQ ID NO:15)、(GYS)(SEQ ID NO:20)和/或(GlySer)(SEQ ID NO:21)的多个重复。在某些方面,肽接头可以包括例如(SG4)(SEQ ID NO:22)、(SG3)(SEQ ID NO:14)、(SG2)(SEQ ID NO:23)或(SerGly)(SEQID NO:24)的多个重复。
在其他方面,肽接头可以包括重复氨基酸序列单元的组合和倍数,诸如(G3S)+(G4S)+(GlySer)(SEQ ID NO:19+SEQ ID NO:15+SEQ ID NO:21)。在其他方面,Ser可以用Ala替代(例如,(G4A)(SEQ ID NO:25)或(G3A)(SEQ ID NO:26))。在又其他方面,接头包含基序(EAAAK)n,其中n是等于或大于1的正整数,例如1至约20(SEQ ID NO:27)。在某些方面,肽接头还可以包括可切割接头。
N末端序列和C末端序列
多种序列可以与本披露的融合多肽的N末端或C末端附接。这些可以是功能性的,诸如信号肽、纯化标签/序列或半衰期延长部分,或可以简单地包含间隔子序列。在一些实施例中,信号肽可以是METDTLLLWVLLLWVPGSTG(SEQ ID NO:52)。本文所述的融合多肽中的任一种均可以与或不与这种信号肽一起使用。
纯化标签和标记
多种标签或标记可以与本披露的融合多肽的N末端或C末端附接以帮助纯化。任何亲和标签均可以与本披露的融合多肽组合以帮助纯化。此类亲和标签的实例是His标签、FLAG标签、Arg标签、T7标签、Strep标签、S标签、适配体标签、AviTagTM或这些标签的任何组合。在一个实施例中,亲和标签是His标签(通常包含5-10个组氨酸残基),例如6His标签(即,HHHHHH)(SEQ ID NO:28)。在另一个实施例中,亲和标签是FLAG标签(即,DYKDDDDK)(SEQ ID NO:29)。在另一个实施例中,亲和标签是AviTagTM(即,GLNDIFEAQKIEWHE)(SEQ IDNO:30)。用于本披露的多种其他标签是本领域众所周知的。
也可以使用此类亲和标签的组合,包括在N末端的一个或多个标签、在C末端的一个或多个标签或在N末端和C末端中的每个末端的一个或多个标签。此类组合的实例包括与AviTag(A)组合的His标签(H)或与AviTag(A)和FLAG标签(F)二者组合的His标签(H)。标签可以处于任一取向,因此AviTag/His标签可以具有取向N-AH-C或N-HA-C,而Avi/His/FLAG标签可以具有取向N-AHF-C、N-FHA-C等。
在一个实施例中,根据本披露的融合多肽包含具有序列“GLNDIFEAQKIEWHEGGHHHHHHDYKDDDDK”(SEQ ID NO:31)的“AHF”标签。在另一个实施例中,根据本披露的融合多肽包含具有序列“DYKDDDDKHHHHHHGGGLNDIFEAQKIEWHE”(SEQ ID NO:32)的“FHA”标签。本文所述的融合多肽中的任一种均可以与或不与这种标签(例如,AHF或FHA标签)一起使用。
本文所述的融合多肽中的任一种均可以与或不与此类标签或标记一起使用。
半衰期延长
在其他实施例中,本披露的融合多肽可以在N末端或C末端处修饰以增加融合多肽在体内的半衰期。
多种策略可以用于延长融合多肽的半衰期。例如,可以通过以下方式延长半衰期:通过与聚乙二醇(PEG)、reCODE PEG、抗体支架、聚唾液酸(PSA)、羟乙基淀粉(HES)、白蛋白结合配体和碳水化合物屏蔽的化学连接;通过与结合至血清蛋白(诸如白蛋白、IgG、FcRn)的蛋白质的基因融合和转移;通过与结合至血清蛋白的其他结合部分(诸如纳米抗体、Fab、DARPin、亲合力多聚体(avimer)、亲和体和抗运载蛋白(anticalin))的偶联(遗传地或化学地);通过与rPEG、白蛋白、白蛋白结构域、白蛋白结合蛋白和Fc的基因融合;和/或通过掺入纳米载体、缓释配制品或医疗装置中。
为了延长融合多肽在体内的血清循环,可以通过PEG与融合多肽的N末端或C末端的位点特异性缀合或经由赖氨酸残基上存在的ε-氨基,将惰性聚合物分子(诸如高分子量PEG)附接到具有或不具有多功能接头的本文所述的融合多肽。为了使融合多肽聚乙二醇化,在一个或多个PEG基团附接到融合多肽的条件下,可以典型地使融合多肽与聚乙二醇(PEG)(诸如PEG的反应性酯或醛衍生物)反应。聚乙二醇化可以通过与反应性PEG分子(或类似的反应性水可溶性聚合物)的酰化反应或烷基化反应来进行。如本文所用,术语“聚乙二醇”旨在涵盖已用于衍生化其他蛋白质的任一种形式的PEG,诸如单(C1-C10)烷氧基-或芳氧基-聚乙二醇或聚乙二醇-马来酰亚胺。在一个实施例中,待聚乙二醇化的融合多肽是非糖基化的。可以使用导致最小生物学活性损失的直链或支链聚合物衍生化。可以通过SDS-PAGE和质谱法密切监测缀合程度,以确保PEG分子与融合多肽的正确缀合。可以通过尺寸排阻或通过离子交换色谱法从融合多肽-PEG缀合物中分离未反应的PEG。可以使用本领域技术人员众所周知的方法(例如,通过免疫测定)测试PEG衍生化融合多肽的活性以及体内功效。用于聚乙二醇化蛋白质的方法是本领域已知的,并且可以应用于本文公开的融合多肽,参见例如EP0154316和EP0401384,将其各自的内容出于此目的并入本文。
其他修改的聚乙二醇化技术可以与本文所述的融合多肽一起使用。在一个实施例中,本文所述的融合多肽可以包括重构化学正交定向工程技术(reconstitutingchemically orthogonal directed engineering technology,ReCODE PEG),其经由包括tRNA合成酶和tRNA的重构系统将化学上指定的侧链掺入生物合成蛋白中。此技术能够将超过30个新氨基酸掺入大肠杆菌、酵母和哺乳动物细胞中的生物合成蛋白中。tRNA在琥珀密码子所定位的任何位置掺入标准氨基酸,从而将琥珀从终止密码子转换成发出掺入化学上指定的氨基酸的信号的密码子。
在一个实施例中,本文所述的融合多肽可以包含用于血清半衰期延长的重组聚乙二醇化技术(rPEG)。此技术涉及将300-600个氨基酸的非结构化蛋白质尾与现有的药物蛋白的遗传地融合。由于这种非结构化蛋白质链的表观分子量是其实际分子量的约15倍,因此蛋白质的血清半衰期大大增加。与需要化学缀合和再纯化的传统的聚乙二醇化相比,大大简化了制造过程并且产物是均匀的。
聚乙二醇化的替代方案是(Schlapschy等人,2013,Protein EngDes Sel.[蛋白质工程设计与选择]26(8):489-501,将其内容出于此目的并入本文)。是基于多肽的无规卷曲结构域(RCD)技术(参见例如,WO 2011/144756和WO2008/155134,将其各自的内容出于此目的并入本文)。因此,在一个实施例中,本文所述的融合多肽可以是聚唾液酸化的。的多肽含有氨基酸脯氨酸、丙氨酸和任选的丝氨酸的序列(PA/S或PAS指示存在丝氨酸)。作为氨基酸残基组合的聚合物导致取消每个氨基酸残基的独特二级结构偏好以形成稳定的无序多肽。已观察到与缺乏这种加合物的处于其天然状态的蛋白质相比,与至少一种PAS多肽(其含有具有假定无规卷曲构象的氨基酸序列的结构域)附接的生物活性蛋白具有增加的体内和/或体外稳定性。
据说提供了某些优于聚乙二醇化的优势。例如,它维持高靶亲和力;迄今为止,它尚未在临床前试验中引起免疫原性;它是可生物降解的,使得它被肾脏酶有效降解;并且它在血流中是稳定的。PAS多肽没有显示出多分散性,并且不需要体外偶联步骤,从而不会负影响商品成本因素。对于相当分子量的PEG,PAS多肽具有更低的粘度,并且半衰期延长可以从10倍调节到大于300倍。这些优势可以使通过修饰的蛋白质更有效、更安全,并且通过降低剂量和施用频率的方式便利得多,提高了患者的依从性。
PAS200多肽链的流体动力学体积大致对应于分子量为20kDa的PEG聚合物,而PAS600多肽链的流体动力学体积大致对应于分子量为40kDa的PEG聚合物。数据提供了对于较高浓度下的相应流体动力学体积,PAS多肽的粘度比PEG聚合物的低三分之一至三倍。
聚唾液酸化使用天然聚合物聚唾液酸(PSA)来延长有效寿命并改善治疗性肽和蛋白质的稳定性。PSA是唾液酸的聚合物(糖)。当用于蛋白质和治疗性肽药物递送时,聚唾液酸在缀合时提供了保护性微环境。这增加了治疗性蛋白在循环中的有效寿命并且防止其被免疫系统识别。PSA聚合物天然存在于人体中。它被某些细菌采用,这些细菌已进化了数百万年以用它来包被它们的壁。然后,这些天然聚唾液酸化的细菌凭借分子模拟能够阻止机体的防御系统。PSA(大自然的终极秘密技术)可以容易地大量且具有预定的物理特征地产自此类细菌。即使当与蛋白质偶联时,细菌PSA也是完全非免疫原性的,因为它在化学上与人体中的PSA相同。在一个实施例中,本文所述的融合多肽可以是聚唾液酸化的。
另一种技术包括使用与融合多肽连接的羟乙基淀粉(“HES”)衍生物。在一个实施例中,本文披露的融合多肽可以是羟乙基淀粉化的。HES是一种源自蜡质玉米淀粉的改性天然聚合物,并且可以被人体的酶代谢。通常施用HES溶液以替代缺乏的血液体积并且改善血液的流变学特性。融合多肽的羟乙基淀粉化能够通过增加分子的稳定性以及通过降低肾清除率来延长循环半衰期,导致生物学活性增加。通过改变不同的参数(诸如HES的分子量),可以定制多种HES缀合物。
在一个实施例中,本披露的融合多肽可以与一种或多种人血清白蛋白(HSA)多肽或其部分融合。已在WO 93/15199、WO 93/15200和EP 0413622中描述了作为白蛋白融合多肽的组分的白蛋白作为多种蛋白质的载体的用途。还已提出使用HSA的N末端片段用于与多肽融合(EP 0399666)。因此,通过将本披露的融合多肽遗传地或化学地融合或缀合至白蛋白,可以稳定或延长保质期,和/或保留分子在溶液中、在体外和/或在体内的活性持续延长的时间段。可以例如在WO 2001/077137和WO 2003/006007中找到与HSA融合相关的另外的方法,将其各自的内容出于此目的并入本文。
在一个实施例中,本披露的融合多肽可以与结合至白蛋白(例如,人血清白蛋白(HSA))的抗体或其抗体片段融合。作为一组非限制性实例,白蛋白结合抗体或其抗体片段可以是Fab、scFv、Fv、scFab、(Fab’)2、单结构域抗体、骆驼科动物VHH结构域、VH或VL结构域、或全长单克隆抗体(mAb)。
在一个实施例中,本披露的融合多肽可以与脂肪酸融合以延长它们的半衰期。适于与生物分子连接的脂肪酸已在本领域中描述,例如WO 2015/200078、WO 2015/191781、US2013/0040884,将其各自的内容出于此目的并入本文。合适的半衰期延长性脂肪酸包括定义为C6-70烷基链、C6-70烯基链或C6-70炔基链的那些,其中的每个被至少一个羧酸(例如1、2、3或4个CO2H)取代,并且任选地进一步被羟基取代。例如,本文所述的蛋白质可以与具有下式A1、A2或A3中的任一个的脂肪酸:
其中R1是CO2H或H;
R2、R3和R4彼此独立地是H、OH、CO2H、-CH=CH2或-C=CH;
Ak是支链C6-C30亚烷基;
n、m和p彼此独立地是6与30之间的整数;或其酰胺、酯或药学上可接受的盐连接。
在一些实施例中,脂肪酸具有式A1,例如具有式A1的脂肪酸,其中n和m独立地是8至20,例如10至16。在另一个实施例中,脂肪酸部分具有式A1,并且其中R2和R3中的至少一个是CO2H。
在一些实施例中,脂肪酸选自下式:
其中Ak3、Ak4、Ak5、Ak6和Ak7独立地是(C8-20)亚烷基,并且R5和R6独立地是(C8-20)烷基。
在一些实施例中,脂肪酸选自下式:
在一些实施例中,脂肪酸选自下式:
在一些实施例中,脂肪酸具有式A2或A3。在具体的实施例中,缀合物包含具有式A2(其中p是8至20)的脂肪酸部分或具有式A3(其中Ak是C8-20亚烷基)的脂肪酸部分。
增加本披露的融合多肽的半衰期的方法包括和与白蛋白结合抗体融合。在一个实施例中,白蛋白结合抗体可以与人血清白蛋白结合。在一个实施例中,白蛋白结合抗体是Fab CA645(Adams等人,2016,MAbs[单克隆抗体],8(7):1336-1346,将其内容出于此目的并入本文)。在另一个实施例中,白蛋白结合抗体是CA645 ScFV。在一个实施例中,本披露的融合多肽包含PAS200或PAS600。
示例性构建体
本披露提供了表1中的以下示例性融合多肽构建体。在表1中所述的融合多肽可以与或不与信号肽(例如,METDTLLLWVLLLWVPGSTG(SEQ ID NO:52))一起使用。在表1中所述的融合多肽可以与或不与标签(例如,AHF标签诸如GLNDIFEAQKIEWHEGGHHHHHHDYKDDDDK(SEQID NO:31)或FHA诸如DYKDDDDKHHHHHHGGGLNDIFEAQKIEWHE(SEQ ID NO:32))一起使用。在一些情况下,在表1中所述的融合多肽可以与或不与信号肽和标签二者一起使用。
表1:示例性融合多肽构建体
编码本披露的融合多肽的核酸分子
本披露的另一方面涉及编码本披露的融合多肽的核酸分子。此类核酸分子可以是DNA或RNA。除非本文特别限定,否则所述术语涵盖含有已知的天然核苷酸类似物的核酸,这些核酸具有与参考核酸类似的结合特性并且以与天然存在的核苷酸类似的方式进行代谢。此类类似物的实例包括但不限于硫代磷酸酯、氨基磷酸酯、甲基膦酸酯、手性甲基磷酸酯、2-O-甲基核糖核苷酸、肽核酸(PNA)。除非另外指示,否则特定的核酸序列还隐含地涵盖其保守修饰的变体(例如,简并密码子取代)和互补序列以及明确指示的序列。具体地,如下文详述,简并密码子取代可以通过产生如下序列而实现,在这些序列中,一个或多个所选择的(或全部)密码子的第三位被混合碱基和/或脱氧肌苷残基取代(Batzer等人,Nucleic AcidRes.[核酸研究]19:5081,1991;Ohtsuka等人,J.Biol.Chem.[生物化学杂志]260:2605-2608,1985;和Rossolini等人,Mol.Cell.Probes[分子细胞探针]8:91-98,1994,将其各自的内容出于此目的并入本文)。
因此,本披露还提供了包含编码SEQ ID NO:33-40、46-48、51、53、54或55中的任何一个或多个的多肽序列的核苷酸序列的核酸。因此,本披露还提供了包含编码表1中的多肽序列(任选地没有信号肽和/或任选地没有标签或标记)中的任一个的核苷酸序列的核酸。
本披露进一步提供了包含与编码SEQ ID NO:33-40、46-48、51、53、54或55中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列的核酸。本披露进一步提供了包含与编码表1中的氨基酸序列(任选地没有信号肽和/或任选地没有标签或标记)中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列的核酸。典型地沿参考序列的全长测量序列同一性。
本披露进一步提供了包含与SEQ ID NO:44具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%或至少约99%序列同一性的核苷酸序列的核酸。
本披露还提供了包含SEQ ID NO:44的核苷酸序列的核酸。本披露还提供了由SEQID NO:44的核苷酸序列组成的核酸。
多核苷酸序列可以通过从头固相DNA合成或通过PCR诱变现有序列(例如,如以下实施例所述的序列)来产生。核酸的直接化学合成可以通过本领域已知的方法完成,诸如Narang等人,1979,Meth.Enzymol.[酶学方法]68:90的磷酸三酯方法;Brown等人,Meth.Enzymol.[酶学方法]68:109,1979的磷酸二酯方法;Beaucage等人,Tetra.Lett.[四面体快报],22:1859,1981的二乙基亚磷酰胺方法;和美国专利号4,458,066的固体支持方法,将其各自的内容出于此目的并入本文。通过PCR向多核苷酸序列中引入突变可以如以下文献中所述的进行,例如PCR Technology:Principles and Applications for DNAAmplification[PCR技术:用于DNA扩增的原理和应用],H.A.Erlich(编辑),弗里曼出版社(Freeman Press),纽约,纽约州,1992;PCRProtocols:A Guide to Methods andApplications[PCR方案:方法和应用指南],Innis等人(编辑),学术出版社(AcademicPress),圣地亚哥,加利福尼亚州,1990;Mattila等人,Nucleic Acids Res.[核酸研究]19:967,1991;以及Eckert等人,PCR Methods and Applications[PCR方法和应用]1:17,1991,将其各自的内容出于此目的并入本文。
载体
本披露还提供了包含本披露的一种或多种核酸分子的载体。
为了在宿主细胞中表达,编码融合多肽的核酸可以存在于合适的载体中,并且在引入合适的宿主中之后,可以根据本领域已知的标准克隆和表达技术表达序列以产生编码的融合多肽(例如,如Sambrook,J.,Fritsh,E.F.和Maniatis,T.Molecular Cloning:ALaboratory Manual[分子克隆:实验室手册]第2版,冷泉港实验室(Cold Spring HarborLaboratory),冷泉港实验室出版社(Cold Spring Harbor Laboratory Press),冷泉港,纽约州,1989中所述,将其各自的内容出于此目的并入本文)。本披露还涉及包含根据本披露的核酸序列的此类载体。
可以采用多种表达载体来表达编码本披露的融合多肽的多核苷酸。基于病毒的和非病毒的两种表达载体均可以用于在宿主细胞(诸如哺乳动物宿主细胞)中产生融合多肽。非病毒载体和系统包括质粒、附加型载体(典型地具有用于表达蛋白质或RNA的表达盒)以及人类人工染色体(参见例如,Harrington等人,Nat Genet.[自然·遗传学]15:345,1997,将其内容出于此目的并入本文)。例如,可用于在哺乳动物(例如,人)细胞中表达本披露的融合多肽的多核苷酸和多肽的非病毒载体包括pThioHis A、pThioHis B和pThioHis C,pcDNA3.1/His,pEBVHis A、pEBVHis B和pEBVHis C(英杰公司(Invitrogen),圣地亚哥,加利福尼亚州),MPS V载体和本领域已知用于表达其他蛋白质的多种其他载体。有用的病毒载体包括基于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒的载体,基于SV40、乳头瘤病毒、HBP EB病毒、痘苗病毒载体和塞姆利基森林病毒(SFV)的载体。参见,Brent等人,同上;Smith,Annu.Rev.Microbiol.[微生物学年度评论]49:807,1995;和Rosenfeld等人,Cell[细胞]68:143,1992,将其各自的内容出于此目的并入本文。
表达载体的选择取决于待表达载体的预期的宿主细胞。哺乳动物宿主细胞的表达载体可以包括表达控制序列,诸如复制起点、启动子和增强子(参见例如,Queen等人,Immunol.Rev.[免疫学评论]89:49-68,1986,将其内容出于此目的并入本文);以及必要的处理信息位点,诸如核糖体结合位点、RNA剪接位点、聚腺苷酸化位点和转录终止子序列。这些表达载体通常含有源自哺乳动物基因或源自哺乳动物病毒的启动子。合适的启动子可以是组成型的、细胞类型特异性的、阶段特异性的和/或可调节的或可调控的。有用的启动子包括但不限于金属硫蛋白启动子、组成型腺病毒主要晚期启动子、地塞米松诱导型MMTV启动子、SV40启动子、MRP polIII启动子、组成型MPS V启动子、四环素诱导型CMV启动子(诸如人立即早期CMV启动子)、组成型CMV启动子和本领域已知的启动子-增强子组合。
可以在非诱导条件下扩增转化生物体的培养物,而不使群体偏向于其表达产物被宿主细胞更好地耐受的编码序列。除了启动子之外,还可能需要或期望其他调节元件以高效表达本披露的抗体或其片段。这些元件典型地包括ATG起始密码子和相邻的核糖体结合位点或其他序列。此外,通过包含适合于使用中的细胞系统的增强子,可以提高表达效率(参见例如,Scharf等人,Results Probl.Cell Differ.[细胞分化的结果和问题]20:125,1994;和Bittner等人,Meth.Enzymol.[酶学方法],153:516,1987,将其各自的内容出于此目的并入本文)。例如,SV40增强子或CMV增强子可以用于增加哺乳动物宿主细胞中的表达。
因此,本披露提供了包含SEQ ID NO:44的核酸序列的克隆或表达载体。本披露还提供了包含含有与编码SEQ ID NO:33-40、46-48、51、53、54或55中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性的核苷酸序列的核酸的克隆或表达载体。本披露还提供了包含含有与编码表1中的氨基酸序列(任选地没有信号肽)中的任一个的核酸具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%或至少约99%序列同一性的核苷酸序列的核酸的克隆或表达载体。此外,本披露提供了包含编码SEQ ID NO:33-40、46-48、51、53或54中的一个或多个的核酸的克隆或表达载体。此外,本披露提供了包含编码表1中的氨基酸序列(任选地没有信号肽)中的一个或多个的核酸的克隆或表达载体。
宿主细胞
提供了包含本披露的核酸、本披露的载体或其任一种或两者的组合的重组细胞,包括原核细胞(例如,大肠杆菌)或真核细胞(例如,昆虫细胞、酵母细胞或哺乳动物细胞)。因此,提供了包含本披露的核酸、本披露的载体或其任一种或两者的组合的细胞,诸如酵母细胞、细菌细胞(例如,大肠杆菌)和哺乳动物细胞(例如,永生化哺乳动物细胞)。此类细胞通常用于表达根据本披露的融合多肽。可以通过标准技术将核酸或载体转染到宿主细胞中。
不同形式的术语“转染”旨在涵盖多种通常用于将外源DNA引入原核或真核宿主细胞中的技术,例如电穿孔、磷酸钙沉淀、DEAE-葡聚糖转染等。在原核或真核宿主细胞中表达本披露的融合多肽是可能的。代表性宿主细胞包括许多大肠杆菌菌株;哺乳动物细胞系,诸如CHO、CHO-K1和HEK293;昆虫细胞,诸如Sf9细胞;以及酵母细胞,诸如酿酒酵母和毕赤酵母。
用于表达本披露的融合多肽的哺乳动物宿主细胞可以包括中国仓鼠卵巢(CHO细胞)(包括dhfr-CHO细胞,由Urlaub和Chasin,1980 Proc.Natl.Acad.Sci.USA[美国国家科学院院刊]77:4216-4220描述并且与DH FR选择性标记一起使用,例如如描述于R.J.Kaufman和P.A.Sharp,1982Mol.Biol.[分子生物学]159:601-621中;将其各自的内容出于此目的并入本文)、NSO骨髓瘤细胞、COS细胞和SP2细胞。在一个实施例中,宿主细胞是CHO K1PD细胞。在另一个实施例中,宿主细胞是NSO1细胞。特别地,为了与NSO骨髓瘤细胞一起使用,另一种表达系统是WO 87/04462、WO 89/01036和EP 338,841中所示的GS基因表达系统,将其各自的内容出于此目的并入本文。在将编码融合多肽的重组表达载体引入哺乳动物宿主细胞中时,可以通过将宿主细胞培养足以允许在宿主细胞中表达融合多肽或将融合多肽分泌到宿主细胞生长的培养基中的时间段来产生融合多肽。可以使用标准蛋白质纯化方法从培养基中回收融合多肽。
药物组合物
本披露还提供了包含如本文所述的融合多肽、核酸、载体或宿主细胞的药物组合物。此类药物组合物可以包含治疗有效量的融合多肽、核酸、载体或宿主细胞和药学上或生理学上可接受的稀释剂和/或载体。通常选择载体以适于预期的施用方式,并且可以包括用于改变、维持或保持例如组合物的pH、摩尔渗透压浓度、黏度、澄清度、颜色、等渗性、气味、无菌性、稳定性、溶解或释放速率、吸附和/或渗透的试剂。典型地,这些载体包括水性或醇性/水性溶液、乳液或悬浮液,包括盐水和/或缓冲介质。
包含在药物组合物中的合适的试剂可以包括但不限于氨基酸(诸如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸)、抗微生物剂、抗氧化剂(诸如抗坏血酸、亚硫酸钠或亚硫酸氢钠)、缓冲剂(诸如硼酸盐、碳酸氢盐、Tris-HCl、柠檬酸盐、磷酸盐或其他有机酸)、疏松剂(诸如甘露糖醇或甘氨酸)、螯合剂(诸如乙二胺四乙酸(EDTA))、络合剂(诸如咖啡因、聚乙烯吡咯烷酮、β-环糊精或羟丙基-β-环糊精)、填充剂、单糖、二糖和其他碳水化合物(诸如葡萄糖、甘露糖或糊精)、蛋白质(诸如游离血清白蛋白、明胶或免疫球蛋白)、着色剂、调味剂和稀释剂、乳化剂、亲水性聚合物(诸如聚乙烯吡咯烷酮)、低分子量多肽、成盐抗衡离子(诸如钠)、防腐剂(诸如苯扎氯铵、苯甲酸、水杨酸、硫柳汞、苯乙醇、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、氯己定、山梨酸或过氧化氢)、溶剂(诸如甘油、丙二醇或聚乙二醇)、糖醇(诸如甘露糖醇或山梨糖醇)、悬浮剂、表面活性剂或润湿剂(诸如普郎尼克类(pluronics);PEG;脱水山梨糖醇酯;聚山梨醇酯(诸如聚山梨醇酯20或聚山梨醇酯80);Triton;氨丁三醇;卵磷脂;胆固醇或泰洛沙泊(tyloxapal))、稳定性增强剂(诸如蔗糖或山梨糖醇)、张力增强剂(诸如碱金属卤化物(诸如氯化钠或氯化钾)或甘露糖醇山梨糖醇)、递送媒介物、稀释剂、赋形剂和/或药物佐剂。
肠胃外媒介物可以包括但不限于氯化钠溶液、林格氏右旋糖、右旋糖和氯化钠以及乳酸林格氏液。可以包括合适的生理学上可接受的增稠剂,诸如羧甲基纤维素、聚乙烯吡咯烷酮、明胶和海藻酸盐。静脉内媒介物包括流体和营养补充物以及电解质补充物,诸如基于林格氏右旋糖的那些。在一些情况下,可以在药物组合物中包括调节组合物的张力的试剂,例如糖、多元醇(诸如甘露糖醇、山梨糖醇)或氯化钠。例如,在许多情况下,希望组合物是基本上等渗的。还可以存在防腐剂和其他添加剂,诸如抗微生物剂、抗氧化剂、螯合剂和惰性气体。精确的配制品将取决于施用途径。药物配制品的另外的相关原理、方法和组分是众所周知的(参见例如,Allen,Loyd V.编辑,(2012)Remington's PharmaceuticalSciences[雷明顿的药物科学],第22版,将其内容出于此目的并入本文)。
可以使用本领域已知的各种方法中的一种或多种,通过一种或多种施用途径施用本披露的药物组合物。如熟练技术人员将理解的,施用途经和/或方式将根据所希望的结果而变化。用于本披露的融合多肽的施用途径包括静脉内、肌内、皮内、腹膜内、皮下、脊柱或其他肠胃外施用途径,例如通过注射或输注。如本文所用的短语“肠胃外施用”意指除了肠道和局部施用以外的施用方式,通常通过注射施用,并且包括但不限于静脉内、肌内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊柱内、硬脑膜外以及胸骨内(intrastemal)注射和输注。当考虑肠胃外施用时,药物组合物通常呈无菌、无热原、肠胃外可接受的组合物的形式。用于肠胃外注射的特别合适的媒介物是正确保存的无菌等渗溶液。药物组合物可以呈冻干物的形式,诸如冻干饼。
可替代地,本文所述的融合多肽可以通过非肠胃外途径(诸如局部、表皮或粘膜施用途径,例如鼻内、口服、阴道、直肠、舌下或局部)施用。
在某些实施例中,药物组合物用于皮下施用。用于皮下施用多肽治疗剂(例如,抗体、融合多肽等)的合适的配制品组分和方法是本领域已知的,参见例如US 2011/0044977、US 8465739和US 8476239,将其各自的内容出于此目的并入本文。典型地,用于皮下施用的药物组合物含有合适的稳定剂(例如,氨基酸(诸如甲硫氨酸)和或糖(诸如蔗糖))、缓冲剂和/或张力剂。
用途和方法
本文所述的融合多肽具有治疗效用。例如,这些融合多肽可以施用给受试者,并且可以用于治疗疾病、预防和/或延迟疾病症状的发作。
因此,本披露提供了本披露的融合多肽、核酸、载体、宿主细胞或药物组合物,用于疗法或用作用于治疗疾病或障碍的药物。本披露进一步提供了本披露的融合多肽、核酸、载体、宿主细胞或药物组合物,用于治疗病理学障碍。本披露还提供了本披露的融合多肽、核酸、载体、宿主细胞或药物组合物在制造用于治疗病理学障碍的药物中的用途。本披露进一步提供了治疗患有病理学障碍的患者或受试者的方法,所述方法包括向所述患者或受试者施用治疗有效量的本披露的融合多肽、核酸、载体、宿主细胞或药物组合物。
在一个实施例中,正在被治疗的患者或受试者在治疗前可能具有150mg/dL或更高(例如,200mg/dL、250mg/dL、300mg/dL、350mg/dL、400mg/dL、500mg/dL、600mg/dL、700mg/dL、800mg/dL、900mg/dL、1000mg/dL、1100mg/dL、1200mg/dL、1300mg/dL、1400mg/dL、1500mg/dL或更高)的血液甘油三酯水平。
如本文所用,术语“病理学障碍”包括但不限于乳糜微粒血症(包括家族性乳糜微粒血症综合征、多基因晚发性乳糜微粒血症和早发性乳糜微粒血症)、高脂血症性胰腺炎、高甘油三酯血症、腹痛、复发性急性胰腺炎、发疹性皮肤黄色瘤、视网膜脂血症、肝脾大、糖尿病、肥胖症、心血管疾病、慢性肾脏疾病、非酒精性脂肪性肝病、高甘油三酯血症性胰腺炎、肝脂肪变性、代谢综合征、缺血性心脏病和微血管病状。
因此,在一个实施例中,本披露提供了本披露的融合多肽、核酸、载体、宿主细胞或药物组合物,用于治疗乳糜微粒血症(例如,家族性乳糜微粒血症综合征、多基因晚发性乳糜微粒血症和/或早发性乳糜微粒血症)。
综述
可以通过通常用于比较两种多肽的氨基酸位置相似性的标准方法来确定序列同一性。使用诸如BLAST或FASTA等计算机程序,对比两种多肽用于其各自的氨基酸的最佳匹配(沿着一个或两个序列的全长或沿着一个或两个序列的预定部分)。所述程序提供了默认的开放罚分和默认的空位罚分,并且评分矩阵诸如PAM 250[标准评分矩阵;参见Dayhoff等人,Atlas of Protein Sequence and Structure[蛋白质序列和结构图集],第5卷,增刊3(1978)]可以与计算机程序联合使用。例如,然后同一性百分比可以计算为:相同匹配的总数乘以100,然后除以在匹配跨度内较长序列的长度与引入较长序列中的空位的数量之和,以便比对两个序列。
在本说明书的整个说明书和权利要求书中,词语“包含(comprise)”和“含有”以及词语的变体(例如“包含(comprising和comprises)”)意指“包括但不限于”,并且不排除其他组分、整数或步骤。此外,除非上下文另外要求,否则单数涵盖复数:特别地,在使用不定冠词的情况下,除非上下文另外要求,否则说明书应被理解为考虑了复数以及单数。
关于数值x的术语“约”意指例如x+5%。
本披露的每个方面的特征可以如关于任何其他方面所述的。在本申请的范围内,明确的意图是,在前述段落、权利要求书和/或在以下描述和附图中阐述的各个方面、实施例、实例和替代方案、特别是其单独的特征可以独立地或以任何组合的方式采用。也就是说,除非此类特征不兼容,否则任何实施例的所有实施例和/或特征可以以任何方式和/或组合进行组合。
实例
通用方法
表达质粒
合成LPL、GPIHBP1、ANGPTL3和ANGPTL4的哺乳动物表达载体,并且开放阅读框的序列列于表2中。
表2重组人LPL、可溶性人GPIHBP1、人ANGPTL3、人ANGPTL4和人LPL-GPIHBP1融合多肽的氨基酸序列
酶和试剂
Amplex Red、试卤灵丁酸酯、Enzchek和DGGR底物购自生命技术公司(LifeTechnologies)。人VLDL和乳糜微粒分别来自EMD密理博公司(EMD Millipore)和雅典研究公司(Athens research)。BSA获自西格玛公司(Sigma)。HR系列NEFA-HR(2)显色剂A和HR系列NEFA-HR(2)显色剂B购自和光诊断剂公司(Wako Diagnostics)。洗涤剂获自西格玛公司。
重组蛋白的表达和纯化
人LPL:使用以下程序制备重组人LPL。使用标准聚乙烯亚胺转染方法,用编码全长人LPL多肽(匹配NCBI序列NM_000237.2)的哺乳动物表达质粒转染在FreeStyle 293表达培养基中培养的HEK293T细胞。转染后24小时,将肝素添加到培养基中至最终浓度为3U/mL,以增强分泌的LPL从细胞表面的释放。转染后60小时,收集培养基,使用0.2μm过滤器过滤,并且添加甘油至最终浓度为10%(v/v)。将所得溶液装载到5mL肝素琼脂糖HiTrap柱上,所述柱已用缓冲液A(50mM Tris-HCl、200mM NaCl,含有10%(v/v)甘油,pH 7.2)预平衡。用缓冲液A洗涤柱,然后用在缓冲液A中的500mM NaCl、1M NaCl和2MNaCl的阶梯梯度洗脱LPL。测定洗脱级分的LPL酶活性,并且通过SDS-PAGE评估蛋白质纯度。用1M NaCl洗脱催化活性最高且纯度最高的LPL。将纯化的人LPL的等分试样快速冷冻并且在-80℃下储存直到使用。
可溶性人GPIHBP1:使用标准聚乙烯亚胺(PEI)转染方法,将含有带有C末端FHA标签的GPIHBP1(solGPIHBP1)蛋白开放阅读框的可溶性结构域的质粒瞬时转染到HEK293T细胞中。使细胞在Freestyle293表达培养基中的悬浮培养中繁殖,并且在1升培养基中以1x106个细胞/mL最终细胞浓度进行转染。然后通过离心收集细胞,之后用0.22μm无菌过滤器过滤。使用切向流过滤(TFF)将澄清的上清液浓缩,并且缓冲液交换到50mM Tris.HCl pH8、150mM NaCl、10%甘油、20mM咪唑中。使浓缩的样品通过用含有50mM Tris.HCl pH 8、150mM NaCl、10%甘油和20mM咪唑的缓冲液平衡的5mL Ni-NTA亲和柱。装载样品后,将柱用相同的缓冲液洗涤,直到达到在280nm处的基线吸光度。然后通过运行咪唑梯度(20mM至500mM)洗脱结合的ANGPTL4蛋白。将相关级分合并,使用Amicon浓缩器(截留分子量10,000Da)浓缩,使用PD-10柱缓冲液交换到储存缓冲液(PBS)中,等分并且在液氮中快速冷冻。
人LPL-可溶性GPIHBP1复合物:使用标准聚乙烯亚胺(PEI)转染方法以3:1:1的摩尔比将编码人LPL(在N末端或C末端处未标签化或带有His或FHA纯化标签;hLPL)、可溶性人GPIHBP1(solGPIHBP1;在C末端处未标签化或带有FHA纯化标签)和人LMF1(hLMF1,登录号:Q96S06)的质粒瞬时转染到适应悬浮的HEK293T细胞中。将细胞在振荡培养箱中在37℃和5%CO2下维持72小时。然后通过离心收获细胞,并且通过0.22μm无菌过滤器过滤上清液。使用切向流过滤(TFF)将澄清的上清液浓缩,并且缓冲液交换到含有500mM NaCl、10%(v/v)甘油和20mM咪唑的20mM Tris-HCl(pH 7.5)中。然后将浓缩的样品施加到用含有500mMNaCl、10%(v/v)甘油和20mM咪唑的20mM Tris-HCl(pH 7.5)平衡的Ni-NTA亲和柱上,并且将柱用相同的缓冲液洗涤,直到达到在280nm处的基线吸光度。然后通过运行咪唑梯度(在含有500mM NaCl和10%(v/v)甘油的20mM Tris-HCl(pH 7.5)中的20mM至500mM咪唑)洗脱结合的hLPL-solGPIHBP1复合物,并且将含有hLPL-solGPIHBP1复合物的级分(通过SDS-PAGE鉴定)合并,浓缩(Amicon浓缩器,截留分子量30kDa)并且装载到用运行缓冲液(10mMTris,pH 7.5,含有300mM NaCl)平衡的Superdex200 16/60分级柱上。通过SDS PAGE分析峰级分,并且将含有LPL-solGPIHBP1复合物的级分合并,浓缩,等分,在液氮中快速冷冻,并且在-80℃下储存。
人LPL-可溶性GPIHBP1融合多肽:使用标准聚乙烯亚胺(PEI)转染方法以3:1的摩尔比将编码人LPL-(GGGGS)4接头-人GPIHBP1(在N末端或C末端处有FHA纯化标签)和人LMF1(hLMF1)的质粒瞬时转染到适应悬浮的HEK293T细胞中。将细胞在振荡培养箱中在37℃和5%CO2下维持72小时。然后通过离心收获细胞,并且通过0.22μm无菌过滤器过滤上清液。使用切向流过滤(TFF)将澄清的上清液浓缩,并且缓冲液交换到含有300mM NaCl、10%(v/v)甘油和30mM咪唑的50mM HEPES(pH 7.3)(缓冲液A)中。然后将浓缩的样品施加到用缓冲液A平衡的HiTrap Ni亲和柱(通用电气公司(GE))上,并且将柱用相同的缓冲液洗涤,直到达到在280nm处的基线吸光度。然后通过运行咪唑梯度(在缓冲液A中的30mM至300mM咪唑)洗脱结合的融合多肽,并且将含有融合多肽的级分(通过SDS-PAGE鉴定)合并,浓缩(Amicon浓缩器,截留分子量30kDa)并且装载到用含有300mM NaCl和10%甘油的10mM Tris(pH 7.5)平衡的Superdex 200 16/60分级柱(通用电气公司)上。通过SDS PAGE分析峰级分,并且将含有LPL-GPIHBP1融合多肽物的级分合并,浓缩,等分,在液氮中快速冷冻并且在-80℃下储存。
蛋白质的位点特异性生物素化
对带有AviTag的纯化的蛋白质如下进行生物素化:将在50mM Bicine pH 8.3缓冲液中的最终浓度为大约1mg/mL的纯化的蛋白质在10mM ATP、10mM乙酸镁、0.1mM生物素和BirA生物素连接酶(阿维迪蒂公司(Avidity))存在下在30℃下孵育1h,然后在4℃下放置过夜。然后将蛋白质使用Amicon浓缩器(截留分子量10,000)浓缩,使用PD-10柱缓冲液交换到储存缓冲液(50mM Tris.HCl pH 7.4、150mM NaCl、15%甘油)中,等分并且在液氮中快速冷冻。
生物化学测定
在替代底物EnzChek和试卤灵丁酸酯情况下的LPL酶活性。
EnzChek测定
在384孔黑板中进行测定。为了确定LPL活性,将变化量的LPL蛋白(单独的LPL、与GPIHBP1共纯化的LPL或LPL-GPIHBP1融合物)在含有以下的测定缓冲液中与1μM底物一起孵育:20mM Tris.Cl pH 8.0、150mM NaCl、1.5%BSA、0.05%为了确定ANGPTL4或ANGPTL3抑制LPL活性的能力,将固定量的LPL与ANGPTL4或3一起预孵育5min,之后添加Enzchek底物。使用Envision多孔板读取器(珀金埃尔默公司(Perkin Elmer))分别使用482和520nm的激发波长和发射波长监测活性。在反应的初始线性阶段计算水解速率。使用Microsoft Excel和GraphPad Prism软件进行数据分析。
试卤灵丁酸酯测定
与Enzchek类似地进行测定,除了以下例外:底物浓度为9μM,并且所使用的洗涤剂为0.025%Zwittergent。激发波长和发射波长如下:Ex.:500nm;Em.:593nm。
在VLDL和CM作为底物情况下的LPL酶活性
使用以下方案来评估纯化的LPL的活性。将LPL蛋白(单独的LPL、与GPIHBP1共纯化的LPL或LPL-GPIHBP1融合物;20μL/孔,使用测定缓冲液连续稀释2倍)与人VLDL或CM(20uL/孔,使用测定缓冲液稀释)在384孔Costar黑孔板中混合。向此混合物中添加含有偶联的酶系统(HR系列NEFA-HR(2),美国和光诊断剂公司(Wako Diagnostics USA))的Amplex Red混合物(20μL/孔,在PBS中稀释),并且使用Envision多孔板读取器(珀金埃尔默公司)分别使用531和590nm的激发波长和发射波长连续监测试卤灵的荧光30分钟。当阐明时,将固定浓度的LPL与ANGPTL3或4(使用测定缓冲液连续稀释2倍)以20μL的体积一起预孵育10min,然后添加VLDL。最终测定浓度为:变化的LPL,变化的ANGPTL3或4,2.3μg/mL人VLDL或10μg/ml人CM,0.75mM ATP,90μM辅酶A,0.5U/mL ACO,1.25U/mL ACS,1.2U/mL HRP,和10μM AmplexRed。使用Microsoft Excel和GraphPad Prism软件进行数据分析。
用于检测ANGPTL4对LPL/GPIHBP1复合物的破坏的ELISA测定。
将LPL-GPIHBP1复合物或LPL-GPIHBP1融合物(10nM,在GPIHBP1的C末端处位点特异性生物素化)与渐增浓度的ANGPTL4(12点2倍连续稀释液,最高浓度为100nM)一起孵育。然后将反应混合物施加到链霉亲和素包被的MSD上。使用LPL或ANGPTL4特异性Ab检测LPL和ANGPTL4的存在,随后将所述LPL或ANGPTL4特异性Ab使用磺基标签化的第二Ab进行定量。为了生成信号,添加1x MSD读取缓冲液T,并且使用Sector Imager 6000(MSD公司(MesoScale Discovery))来使板显影。
用于检测ANGPTL4对LPL/GPIHBP1复合物的破坏的SPR测定。
将带有C末端生物素标签的LPL-GPIHBP1复合物或融合物以1nM的浓度固定在链霉亲和素表面。使浓度为10nM的ANGPTL4在固定的复合物上流过,并且监测质量随时间的变化。
用于检测ANGPTL4与LPL/GPIHBP1复合物的结合的基于TR-FRET的测定
在384孔板(ProxiPlateTM 384孔白板,珀金埃尔默公司,美国)中以20μl的最终体积进行用于基于TR-FRET地检测ANGPTL4与LPL/GPIHBP1复合物的结合的测定。测定缓冲液的组成为20mM HEPES pH=7.4、100mM NaCl、10%HI-FBS、5mM CaCl2。测定程序如下:首先将4μL/孔的5x 6HIS-hLPL-HA-Flag/生物素化的hGPIHBP1-Avi复合物(在测定缓冲液中的50nM储液,10nM复合物最终浓度)添加到8μL/孔的缓冲液中。然后添加4μL/孔的5x非生物素化的ANGPTL4(26-406)-Flag-6HIS-Avi(最终浓度为1至1000nM),并且在室温下孵育1小时。孵育后,添加4μL的5x抗HA-Tb/抗myc-D2(浠思生物公司(Cisbio),在测定缓冲液中稀释至1.25nM抗HA-Tb/50nM链霉亲和素-D2储液浓度)(0.3125nM抗HA-Tb/10nM链霉亲和素-D2最终浓度),并且将混合物在室温下孵育3小时。最后,在Envision板读取器(Ex=320Em=665Em=615)上读取板。
用于检测LPL/ANGPTL4复合物破坏的基于TR-FRET的测定
在384孔板(ProxiPlateTM 384孔白板,珀金埃尔默公司,美国)中以20μl的最终体积进行用于基于TR-FRET地检测LPL/GPIHBP1复合物破坏的测定。测定缓冲液的组成为20mMHEPES pH=7.4、100mM NaCl、10%HI-FBS、5mM CaCl2。测定程序如下:首先将4μL/孔的5x6HIS-hLPL-HA-Flag/hGPIHBP1-Avi复合物(在测定缓冲液中的50nM储液,10nM复合物最终浓度)添加到8μL/孔的缓冲液中。然后添加4μL/孔的5xANGPTL4(26-406)-6HIS-myc(最终浓度为0.2至100nM),并且在室温下孵育1小时。孵育后,添加4μL的5x抗HA-Tb/抗myc-D2(浠思生物公司,在测定缓冲液中稀释至2.5nM抗HA-Tb/200nM抗myc-D2储液浓度)(0.5nM抗HA-Tb/40nM抗myc-D2最终浓度),并且将混合物在室温下孵育3小时。最后,在Envision板读取器(Ex=320Em=665Em=615)上读取板。
用于检测LPL/ANGPTL4复合物破坏的基于AlphaLISA的测定
在384孔板(ProxiPlateTM 384孔白板,珀金埃尔默公司,美国)中以20μl的最终体积进行用于基于地检测LPL/ANGPTL4复合物破坏的测定。测定缓冲液的组成为20mM HEPES pH=7.4、100mM NaCl、10%HI-FBS、5mM CaCl2。测定程序如下:首先添加4μL/孔的5x HA-hLPL/hGPIHBP1复合物(在测定缓冲液中的5nM储液)(1nM复合物最终浓度)。随后,添加4μL/孔的5x ANGPTL4(26-406)-6HIS-myc(在测定缓冲液中的50nM储液,10nM最终浓度)。孵育1小时后,添加4μL的5x抗HA受体珠(珀金埃尔默公司,在1x免疫测定缓冲液中的100μg/mL,20μg/mL最终浓度),并且将混合物在室温下再次孵育1小时。然后添加4μL的5x抗myc供体珠(珀金埃尔默公司定制珠包衣,在1x免疫测定缓冲液中的100μg/mL,20μg/mL最终浓度),并且将板用TOP Seal-A加透明板密封件(珀金埃尔默公司)密封。将板在室温下孵育过夜,随后使用默认的仪器设置在Envision板读取器上读取。根据移液技术,在添加后添加以1500RPM的短暂的离心脉冲以确保试剂到达孔的底部。
通过氢-氘交换/质谱法进行表位定位
使用氢-氘交换(HDx)与质谱法(MS)组合(Woods&Hamuro,2001,J Cell Biochem[细胞生物化学杂志],增刊37:89-98,将其内容出于此目的并入本文)来对LPL蛋白上的ANGPTL4结合表位定位。使用与文献(Chalmers,2006,将其内容出于此目的并入本文)中所述的那些类似的方法进行自动HDx/MS实验。在Waters HDx-MS平台上进行实验,所述平台包括LEAP自动进样器、纳米ACQUITY UPLC系统和Synapt G2质谱仪。在4℃下在pH 7的氘代Tris-HCl缓冲液中在不存在以及存在ANGPTL4(79.2μM)的情况下将LPL-GPIHBP1融合多肽(15.8μM)标记15分钟。然后将标记反应用冷冻的淬灭缓冲液在冰上淬灭三分钟。接下来,将淬灭的蛋白质溶液注入LC-MS系统中用于自动胃蛋白酶消化和肽分析。通过比较单独的和与ANGPTL4一起的LPL-GPIHBP1融合多肽的LC-MS数据来对融合多肽上的ANGPTL4结合表位定位。使用最少三个分析的一式三份重复进行所有测量。
动物研究
使用雄性的12周龄C57BL/6(泰康利公司(Taconic),伦斯勒,纽约州)、12-15周龄DBA/2J或15-24周龄TALLYHO/JngJ小鼠(杰克逊实验室(Jackson Lab),巴尔港,缅因州)进行研究。将动物饲养在正常的光周期中(6:00am-6:00pm),以正常的食物或高脂肪高蔗糖饮食(研究饮食目录号D12331i)喂养,并且在研究期间随意取水。所有程序均符合动物福利法(Animal Welfare Act)条例9CFR第1、2和3部分以及其他准则。在得到诺华生物医学研究所机构动物护理和使用委员会(Institutional Animal Care and Use Committee ofNovartis Institutes for BioMedical Research)批准的动物方案下进行研究。通过尾静脉抽血采集血液样品,将其收集在Microvette管(萨斯特德特股份有限两合公司(SarstedtAG&Co.),宁布雷希特,德国)中,并且在离心前在冰上保持。将动物随机分配到媒介物组或处理组(n=6-8只/组),并且使用WAKO Diagnostics试剂盒(山景城,加利福尼亚州)评估血清甘油三酯(TG)水平且在各组之间匹配。
在研究当天,向动物静脉内(IV)或皮下(SC)给药人血清白蛋白(HSA,作为阴性对照)或剂量从0.3至30mg/5ml/kg的在PBS中的LPL-GPIHBP1。在给药前以及在给药后的多个时间点采集尾部血液样品。如上所述的确定血清TG水平。
在DBA/2J小鼠中进行脂质耐受测试。静脉内注射英脱利匹特(磷脂稳定的大豆油作为20%脂肪乳剂,西格玛-奥德里奇公司(Sigma-Aldrich),圣路易斯,密苏里州)。通过尾静脉抽血获得血清样品,并且在英脱利匹特注射之前和在之后0.5、1和2小时测量TG。
使用GraphPad Prism 7.0(GraphPad软件公司(GraphPad Software),圣地亚哥,加利福尼亚州)进行统计学分析。通过双向方差分析(ANOVA)进行时间过程分析,之后对每个时间点使用邦费罗尼方法进行事后检验。数据表示为平均值±平均值的标准误差(SEM)。接受在p<0.05水平下的统计学显著性。
实例1:GPIHBP1稳定LPL,防止其聚集,并且增加脂肪酶活性
最初尝试自行纯化LPL蛋白。为了帮助这种纯化,合成了多种未标签化的或具有N末端或C末端标签的LPL构建体。将这些LPL构建体在哺乳动物细胞中表达,并且使用肝素色谱法或Ni亲和色谱法纯化。发现纯化的蛋白质具有活性,但是高度聚集(图1,小图A、C和D)。LPL与LMF1的共转染不改善LPL的产率,并且纯化的蛋白质仍然高度聚集(数据未显示)。GPIHBPI的纯化可溶性形式与LPL的共表达保护LPL免于自发失活(数据未显示)。然后,使GPIHBP1与LPL在LMF1的存在下以以下方式共表达:将N末端6-His标签化的LPL、未标签化的GPIHBP1和LMF1以3:1:1的比率共转染到HEK293T细胞中。使用Ni亲和色谱法捕获表达的蛋白质复合物。这种三重转染显著改善了LPL的纯度和产率(图1,小图B)。重要的是,GPIHBP1和LMF1的存在产生了LPL/GPIHBP1复合物,所述复合物是均质的并且在尺寸排阻色谱法期间洗脱为约75KDa复合物(图1,小图C)。这与1:1LPL/GPHBP1复合物的预测分子量非常吻合。LPL/GPHBP1复合物也具有是单独的LPL的约3-4倍的活性(图1,小图D),并且对LPL的自发失活有抗性(图1,小图E)。
实例2:LPL-GPIHBP1融合多肽是均质的,稳定的,并且具有高比活性
然后通过制备LPL-GPIHBP1融合构建体来产生LPL和GPIHBP1的非解离复合物。设计了具有经由20个氨基酸的丝氨酸/甘氨酸接头连接的LPL和可溶性GPIHBP1开放阅读框的哺乳动物表达载体。为了帮助纯化,将纯化标签添加到融合构建体的N末端或C末端。图2小图A示出了带有C末端FLAG-6-His-AviTagTM(FHA)标签的纯化的LPL-GPIHBP1复合物。使用Ni亲和色谱法和尺寸排阻色谱法获得大于95%纯的融合多肽(图2,小图A)。与LPL/GPIHBP1共表达的复合物类似,所产生的融合多肽不含聚集体,并且通过尺寸排阻色谱法以约75KDa的分子量拆分为单一均质物质(图2,小图B)。这些数据表明LPL/GPIHBP1复合物以及融合多肽由1个LPL和1个GPIHBP1分子组成。实际上,LPL/GPIHBP1复合物的晶体结构证实LPL和GPIHBP1形成了1:1的单体复合物(数据未显示)。融合多肽具有与共纯化的LPL/GPIHBP1复合物相当的活性(图2,小图C),从而证实融合不会对LPL的催化活性产生不利影响。此外,融合多肽是高度稳定的,并且在4度下维持活性持续7天的时间(图2,小图D)。
实例3:ANGPTL4解离LPL-GPIHBP1复合物
然后检查ANGPTL4/LPL/GPIHBP1相互作用以确定ANGPTL4与LPL的结合是否导致GPIHBP1的解离。
首先,将共表达的LPL/GPIHBP1复合物或LPL-GPIHBP1融合多肽通过C末端生物素化的GPIHBP1固定在链霉亲和素表面。然后将蛋白质与ANGPTL4一起孵育,并且用各自的高亲和力抗体监测结合的ANGPTL4和LPL的变化。在图3小图A顶上描绘了测定的示意图。当将复合物与ANGPTL4一起孵育时,观察到随ANGPTL4浓度的变化LPL从共表达的LPL/GPIHBP1复合物中的置换。另一方面,ANGPTL4不能从共价连接的LPL-GPIHBP1融合多肽中置换LPL(图3,小图A,左侧)。相应地,当探测结合的ANGPTL4时,ANGPTL4未被共表达的LPL/GPIHBP1复合物捕获。然而,随ANGPTL4浓度的变化ANGPTL4积累在与GPIHBP1共价连接的LPL上(图3,小图A,右侧)。
接下来,使用SPR分析ANGPTL与LPL和GPIHBP1的相互作用(图3,小图B)。证实了ANGPTL4从共表达的LPL/GPIHBP1复合物中置换LPL,但是未从融合多肽中置换LPL。
最后,在TR-FRET测定中,观察到ANGPTL4与LPL-GPIHBP1融合多肽结合(图3,小图C,左侧),并且解离LPL/GPIHBP1复合物(图3,小图C,右侧)。ANGPTL3也能够解离所述复合物,尽管不如ANGPTL4有效(数据未显示)。
这些数据表明ANGPTL4和GPIHBP1与LPL的结合是相互排斥的。实际上,当用游离的GPIHBP1或ANGPTL4攻击LPL/GPIHBP1复合物时,两种蛋白质均能够以类似的IC50值解离所述复合物(图3,小图D)。
这些观察结果与ANGPTL4和GPIHBP1对LPL的功能竞争一致。因此,我们推测LPL-GPIHBP1融合多肽可能比游离LPL和共表达的LPL/GPIHBP1复合物对ANGPTL4失活更具抗性。
实例4:LPL-GPIHBP1融合物对被ANGPTL4和ANGPTL3失活有抗性
研究了ANGPTL3和ANGPTL4对LPL的酶活性的影响。观察到LPL/GPIHBP1共表达的复合物对ANGPTL4失活的抗性是单独的LPL的6倍以上(IC50分别为19nM和3nM)(图4,小图A)。类似地,与单独的LPL相比,LPL/GPIHBP1共表达的复合物对ANGPTL3失活的抗性也更高(>37倍)(IC50分别为300nM和8nM)(图4,小图B)。这表明GPIHBP1不仅保护LPL免于自发失活,而且稳定它免于被ANGPTL失活。这种稳定作用在LPL-GPIHBP1融合多肽中甚至更明显。ANGPTL4介导的融合多肽失活的IC50是单独的LPL的35倍以上,并且是共表达的LPL/GPIHBP1复合物的5倍以上(分别为107nM、3nM和19nM)(图4,小图A)。GPIHBP1针对ANGPTL3失活的稳定作用对于融合多肽也更明显。单独的LPL和LPL/GPIHBP1共表达的复合物的IC50分别为7nM和300nM,而没有观察到LPL-GPIHBP1融合多肽对活性的损失(图4,小图B)。
实例5:HDx-MS实验定位LPL上的ANGPTL4结合表位
迄今为止,我们的研究证明ANGPTL4介导的融合多肽的失活弱于ANGPTL4介导的共表达的LPL/GPIHBP1复合物的失活,并且ANGPTL4与LPL保持结合。因此,使用融合多肽来定位LPL上的ANGPTL4结合位点。为此目的,将氢-氘交换(HDx)与质谱法(MS)组合使用。在此方法中,共价键合的氢原子被氘替代。用分离的蛋白质和蛋白质复合物进行交换反应。然后比较两种反应。如果将某个区域埋在蛋白质复合物中,则与分离的蛋白质相比,预期此区域中的酰胺交换更慢。使用此方法,在被ANGPTL4的存在屏蔽的LPL-GPIHBP1融合多肽中鉴定出了一段32个氨基酸(SEQ ID NO:1的氨基酸157至189)(图5,小图A)。在共表达的LPL/GPIHBP1复合物中相同的氨基酸段也得到了保护(图5,小图B)。这表明LPL与GPIHBP1的融合没有从根本上改变LPL和ANGPTL4的相互作用。参与LPL/ANGPTL4相互作用的氨基酸的知识为通过LPL定点诱变进一步稳定LPL-GPIHBP1融合多肽提供了路线图。
实例6:LPL-GPIHBP1融合多肽降低几种品系的小鼠中的甘油三酯水平
LPL-GPIHBP1融合多肽的改善的药理学特性(低聚集、对自发失活的抗性、高纯化产率)以及融合多肽对被LPL拮抗剂ANGPTL3和ANGPTL4失活的抗性使我们推测融合多肽可以作体内急剧TG降低的有效治疗剂。小鼠是用于此类研究的便利的动物模型,但是血浆TG在小鼠品系之间可能显著不同。因此在几种品系的小鼠中测试了LPL-GPIHBP1的TG降低作用以确保观察到的作用不是品系特异性的。
首先在C57BL/6小鼠中测试了TG降低。由于这些小鼠具有固有的低基础TG(约100mg/dL),因此它们的血浆TG因英脱利匹特大丸药而瞬时增加(脂质耐受性测试,图6)。如图6所指示的,这导致注射英脱利匹特大丸药后约30min TG水平的约5倍猛增(图6,HSA对照)。重要的是,皮下施用的LPL-GPIHBP1剂量依赖性地钝化了TG的增加,其中最高剂量使TG偏移的AUC降低约80%(图6,小图A和B)。
接下来,在DBA/2小鼠中测试了融合多肽对TG水平的影响,所述DBA/2小鼠具有约200mg/dL的较高的基础TG。由于小鼠血浆中的TG水平可能在一天的过程中发生实质性变化(在一些情况下证明在非喂养期间降低50%-60%),因此将融合多肽介导的TG水平降低相对于作为相同研究的一部分施用的HSA对照归一化。在这里同样,在静脉内施用后,LPL-GPIHBP1剂量依赖性地降低了DBA/2小鼠中的TG,其中在最高剂量下TG降低超过90%(图7,小图A和B)。担忧之一是,这种程度的快速TG降低可能会导致血浆中促炎性游离脂肪酸的增加。未观察到血浆游离脂肪酸的增加(图7,小图C),这表明组织利用了水解的TG。每天还向DBA/2小鼠施用LPL-GPIHBP1,持续5天。融合多肽始终降低血浆TG(图7,小图D和E),而在肝脏、心脏、骨骼肌或脂肪组织中没有明显的TG积累。
为了达到更高的血浆TG,在脂质耐受性测试期间向DBA/2小鼠皮下施用LPL-GPIHBP1。与C57BL/6研究的结果一致,LPL-GPIHBP1融合多肽剂量依赖性地钝化了TG的增加,其中最高剂量使TG偏移的AUC降低约90%(图8,小图A和B)。最后,在TALLYHO小鼠(具有约400mg/dL的基线TG的品系)中测试了LPL-GPIHBP1对TG降低的影响。在这种高脂血症品系中,皮下施用LPL-GPIHBP1剂量依赖性地降低了TG,其中最高剂量使TG降低约70%(图9,小图A和B)。为了达到甚至更高的基础血浆TG,将TALLYHO小鼠维持接受高脂肪/高蔗糖(HFHS)饮食。此方案使它们的TG增加到约1000mg/dL(接近与在患有FCS的人类患者中看到的类似水平)。重复皮下施用的LPL-GPIHBP1再次剂量依赖性地降低了血浆TG,其中最高剂量导致约90%的TG降低(图9,小图C和D)。这些数据令人信服地证明LPL-GPIHBP1融合多肽急剧降低了体内TG。
实例7:向LPL-GPIHBP1融合物中添加白蛋白结合部分延长了甘油三酯降低的持续
时间
确定LPL-GPIHBP1在静脉内施用后具有大约20min的血浆半衰期,并且当皮下施用时具有大约1.7小时的血浆半衰期(数据未显示),从而解释了在多种小鼠模型中在蛋白质施用后2-5小时TG的瞬时降低。为了延长TG降低作用,通过将CA645的Fab结构域(Adams等人,2016,同上)附接到LPL-GPIHBP1的N末端来产生LPL-GPIHBP1融合多肽的变体。在另一种构建体中,将CA645 scFv附接到LPL-GPIHBP1的C末端。两种构建体均结合白蛋白(数据未显示),并且通过使用酶的天然底物VLDL证实修饰不损害任一构建体的LPL酶活性。
然后测试了这些构建体在DBA/2小鼠中降低TG的能力。白蛋白结合部分的附接将最大TG降低的持续时间从大约3小时增加到24小时(图10)。
序列表
SEQ ID NO:1(人LPL;UniProtKB/Swiss-Prot:P06858.1)
SEQ ID NO:2(成熟的人LPL-氨基酸28-475)
SEQ ID NO:3(具有“S447X”突变的成熟的人LPL)
SEQ ID NO:4(SEQ ID NO:1的氨基酸37-334;最小LPL催化结构域)
SEQ ID NO:5(人GPIHBP1;UniProtKB:Q8IV16)
SEQ ID NO:6(成熟的人GPIHBP1-氨基酸21-184)
SEQ ID NO:7(人GPIHBP1-无信号序列、无前肽-氨基酸21-151)
SEQ ID NO:8(人GPIHBP1-无前肽-氨基酸1-151)
SEQ ID NO:9(最小功能结构域人GPIHBP1-氨基酸63-148)
SEQ ID NO:10(截短的人GPIHBP1-氨基酸21-160)
SEQ ID NO:11(接头)
SEQ ID NO:12(接头)
SEQ ID NO:13(接头)
SEQ ID NO:14(接头)
SEQ ID NO:15(接头)
SEQ ID NO:16(接头)
SEQ ID NO:17(接头)
SEQ ID NO:18(接头)
SEQ ID NO:19(接头)
SEQ ID NO:20(接头)
SEQ ID NO:21(接头)
SEQ ID NO:22(接头)
SEQ ID NO:23(接头)
SEQ ID NO:24(接头)
SEQ ID NO:25(接头)
SEQ ID NO:26(接头)
SEQ ID NO:27(接头)
SEQ ID NO:28(6His标签)
SEQ ID NO:29(FLAG标签)
SEQ ID NO:30(Avi标签)
SEQ ID NO:31(AHF标签)
SEQ ID NO:32(FHA标签)
SEQ ID NO:33(AHF-hLPL(28-475)-(GGGGS)4-hGPIHBP1(21-151))
SEQ ID NO:34(AHF-hLPL(28-475)-(GGGGS)4-hGPIHBP1(21-151)(无信号序列))
SEQ ID NO:35(AHF-hLPL(28-475)-(G4S)4-hGPIHBP1(21-151)-(G4S)3-PAS200)
SEQ ID NO:36(AHF-hLPL(28-475)-(G4S)4-hGPIHBP1(21-151)-(G4S)3-PAS600)
SEQ ID NO:37(AHF-hLPL(28-475)-(G4S)4-hGPIHBP1(21-151)-(G4S)3-CA645scFv-LV-HV)
SEQ ID NO:38(CA645Fab_HC(cotransf.CA645Fab_LC)-(G4S)3-hLPL(28-475)-(G4S)4-hGPIHBP1(21-151)-FHA)
SEQ ID NO:39(NOV2704Fab_HC(cotransf.NOV2704Fab_LC)-(G4S)3-hLPL(28-475)-(G4S)4-hGPIHBP1(21-151)-FHA)
SEQ ID NO:40(hLPL(28-475)-(GGGGS)4-hGPIHBP1(21-151))
SEQ ID NO:41(His6-hLPL(28-475))
SEQ ID NO:42(人LPL(28-475)-FHA)
SEQ ID NO:43(人ANGPTL4(26-406)-FLAG-6HIS-Avi)
SEQ ID NO:44(核苷酸序列:人LPL(28-475)-(G4S)4-人GPIHBP1(22-151)-FLAG-6HIS-Avi)
SEQ ID NO:45(成熟的人LPL R294A)
SEQ ID NO:46(AHF-hLPL(28-475)R294A-(GGGGS)4-hGPIHBP1(21-151))
SEQ ID NO:47(AHF-hLPL(28-475)R294A-(GGGGS)4-hGPIHBP1(21-151)(无信号序列))
SEQ ID NO:48(hLPL(28-475)R294A-(GGGGS)4-hGPIHBP1(21-151))
SEQ ID NO:49(人可溶性GPIHBP1(21-151)-FLAG-HIS6-Avi)
SEQ ID NO:50(人ANGPTL3(17-460)-FLAG-HIS6-Avi)
SEQ ID NO:51(LPL(28-475)-(G4S)4-hGPIHBP1(21-151)-FLAG-HIS6-Avi)
SEQ ID NO:52(信号序列)
SEQ ID NO:53(LPL(28-475)-(G4S)4-hGPIHBP1(21-151)-FLAG-HIS6-Avi)
SEQ ID NO:54(LPL(28-475)-(G4S)4-hGPIHBP1(21-151))
SEQ ID NO:55(hLPL(28-475)-(G4S)4-hGPIHBP1(21-151))
Claims (31)
1.一种融合多肽,所述融合多肽包含:
(i)脂蛋白脂肪酶(LPL)多肽或其功能性变体;以及
(ii)糖基磷脂酰肌醇锚定高密度脂蛋白结合蛋白1(GPIHBP1)多肽或其功能性变体。
2.根据权利要求1所述的融合多肽,所述融合多肽具有一个式(I)或(II)
A-B(n)-C-D(m)-E (I)A-D(m)-C-B(n)-E (II)
其中
A=任选的N末端序列
B=LPL多肽或其功能性变体
C=任选的接头序列
D=GPIHBP1多肽或其功能性变体
E=任选的C末端序列,其中
n=从1至3的整数,并且
m=从1至3的整数。
3.根据权利要求1或权利要求2所述的融合多肽,其中n=1和/或m=1。
4.根据前述权利要求中任一项所述的融合多肽,其中所述LPL多肽的功能性变体包含与SEQ ID NO:1或SEQ ID NO:2具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。
5.根据前述权利要求中任一项所述的融合多肽,其中所述LPL多肽的功能性变体包含以下的氨基酸序列:
(i)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;或
(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变的SEQ ID NO:1。
6.根据前述权利要求1至3中任一项所述的融合多肽,其中所述LPL多肽的功能性变体是以下的截短形式:
(i)与SEQ ID NO:1或SEQ ID NO:2具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;
(ii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:2的氨基酸中的任一个的点突变的SEQ ID NO:2;
(iii)具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:1的氨基酸157-189中的任一个的点突变的SEQ ID NO:1;
(iv)SEQ ID NO:1;或
(v)SEQ ID NO:2。
7.根据权利要求1至3中任一项所述的融合多肽,其中所述LPL多肽包含SEQ ID NO:1、2、3、4或45中的任一个或由其组成。
8.根据前述权利要求中任一项所述的融合多肽,其中所述GPIHBP1多肽的功能性变体包含与SEQ ID NO:5、SEQ ID NO:6或SEQ ID NO:7的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列。
9.根据前述权利要求中任一项所述的融合多肽,其中所述GPIHBP1多肽的功能性变体包含以下的氨基酸序列:具有一个或多个(例如,1、2、3、4、5、6、7、8、9、10个或更多个)添加到、缺失或取代SEQ ID NO:7的氨基酸中的任一个的点突变的SEQ ID NO:7。
10.根据前述权利要求1至7中任一项所述的融合多肽,其中所述GPIHBP1多肽的功能性变体是以下的截短形式:(i)与SEQ ID NO:5的GPIHBP1多肽具有至少约80%、至少约85%、至少约90%、至少约95%、至少约97%、至少约98%或至少约99%序列同一性的氨基酸序列;或
(ii)SEQ ID NO:5。
11.根据权利要求1至7中任一项所述的融合多肽,其中所述GPIHBP1多肽包含SEQ IDNO:5、6、7、8、9或10中的任一个或由其组成。
12.根据前述权利要求中任一项所述的融合多肽,其中所述LPL多肽和所述GPIHBP1多肽通过接头C连接。
13.根据权利要求12所述的融合多肽,其中所述接头包含SEQ ID NO:11-27中的任一个所示的一个或多个氨基酸序列或由其组成。
14.根据权利要求13所述的融合多肽,其中所述接头包含SEQ ID NO:16或SEQ ID NO:17所示的一个或多个氨基酸序列或由其组成。
15.根据前述权利要求中任一项所述的融合多肽,其中所述融合多肽包含N末端序列A。
16.根据前述权利要求中任一项所述的融合多肽,其中所述融合多肽包含C末端序列E。
17.根据权利要求15或权利要求16所述的融合多肽,其中所述N末端序列或所述C末端序列包含一个或多个选自下组的标签,该组由以下组成:His标签、FLAG标签、Arg标签、T7标签、Strep标签、S标签、AviTagTM和适配体标签。
18.根据权利要求17所述的融合多肽,其中所述N末端序列或所述C末端序列包含
(i)His标签和AviTagTM,或
(ii)FLAG标签、His标签和AviTagTM。
19.根据权利要求15或权利要求16所述的融合多肽,其中所述N末端序列或所述C末端序列包含SEQ ID NO:31或SEQ ID NO:32所示的氨基酸序列或由其组成。
20.根据前述权利要求中任一项所述的融合多肽,其中所述N末端序列或所述C末端序列包含增加所述融合多肽在体内的半衰期的部分,
并且其中所述N末端序列或所述C末端序列包含PEG序列、PAS序列或任选地选自Fab或ScFv分子的抗体序列。
21.根据权利要求20所述的融合多肽,其中所述抗体是CA645。
22.根据权利要求1-3中任一项所述的融合多肽,所述融合多肽包含SEQ ID NO:33-40、46-48、51、53、54或55中的任一个的氨基酸序列或由其组成。
23.一种分离的核酸序列,所述分离的核酸序列编码根据前述权利要求1至22中任一项所述的融合多肽。
24.一种载体,所述载体包含根据权利要求23所述的核酸。
25.一种宿主细胞,所述宿主细胞包含根据权利要求23所述的核酸或根据权利要求24所述的载体。
26.一种用于制备根据权利要求1至22中任一项所述的融合多肽的方法,所述方法包括将根据权利要求25所述的宿主细胞维持在适于表达核酸的条件下,从而表达核酸并且产生所述融合多肽,并且任选地分离和/或纯化所述融合多肽。
27.一种药物组合物,所述药物组合物包含根据权利要求1至22中任一项所述的融合多肽、根据权利要求23所述的核酸、根据权利要求24所述的载体或根据权利要求25所述的宿主细胞、以及药学上或生理学上可接受的稀释剂和/或载体。
28.根据权利要求1-22中任一项所述的融合多肽、根据权利要求23所述的核酸、根据权利要求24所述的载体、根据权利要求25所述的宿主细胞或根据权利要求27所述的药物组合物,用于疗法或用作用于治疗疾病或障碍的药物。
29.根据权利要求28所述的用于所述用途的融合多肽、核酸、载体、宿主细胞或药物组合物,其中所述疾病或障碍选自乳糜微粒血症(包括家族性乳糜微粒血症综合征、多基因晚发性乳糜微粒血症和早发性乳糜微粒血症)、高脂血症性胰腺炎、高甘油三酯血症、腹痛、复发性急性胰腺炎、发疹性皮肤黄色瘤、视网膜脂血症、肝脾大、糖尿病、肥胖症、心血管疾病、慢性肾脏疾病、非酒精性脂肪性肝病、高甘油三酯血症性胰腺炎、肝脂肪变性、代谢综合征、缺血性心脏病和微血管病状。
30.一种治疗患有疾病或障碍的患者的方法,所述方法包括向所述患者施用治疗有效量的根据权利要求1-22中任一项所述的融合多肽、根据权利要求23所述的核酸、根据权利要求24所述的载体、根据权利要求25所述的宿主细胞或根据权利要求27所述的药物组合物。
31.根据权利要求30所述的方法,其中所述疾病或障碍选自乳糜微粒血症(包括家族性乳糜微粒血症综合征、多基因晚发性乳糜微粒血症和早发性乳糜微粒血症)、高脂血症性胰腺炎、高甘油三酯血症、腹痛、复发性急性胰腺炎、发疹性皮肤黄色瘤、视网膜脂血症、肝脾大、糖尿病、肥胖症、心血管疾病、慢性肾脏疾病、非酒精性脂肪性肝病、高甘油三酯血症性胰腺炎、肝脂肪变性、代谢综合征、缺血性心脏病和微血管病状。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862771359P | 2018-11-26 | 2018-11-26 | |
| US62/771,359 | 2018-11-26 | ||
| PCT/IB2019/060140 WO2020109978A1 (en) | 2018-11-26 | 2019-11-25 | Lpl-gpihbp1 fusion polypeptides |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113396158A true CN113396158A (zh) | 2021-09-14 |
Family
ID=68807212
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201980089752.0A Pending CN113396158A (zh) | 2018-11-26 | 2019-11-25 | Lpl-gpihbp1融合多肽 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220025344A1 (zh) |
| EP (1) | EP3887393A1 (zh) |
| JP (1) | JP2022513626A (zh) |
| CN (1) | CN113396158A (zh) |
| WO (1) | WO2020109978A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117384912A (zh) * | 2023-12-13 | 2024-01-12 | 中国人民解放军东部战区总医院 | Gpihbp1突变型基因及其应用 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2025124559A1 (zh) * | 2023-12-13 | 2025-06-19 | 维亚臻生物技术(苏州)有限公司 | 捕获探针、含有其的家族性乳糜微粒血症综合征检测试剂盒及应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103732624A (zh) * | 2011-06-17 | 2014-04-16 | 瑞泽恩制药公司 | 抗angptl3抗体及其用途 |
| WO2018020477A1 (en) * | 2016-07-28 | 2018-02-01 | The Regents Of The University Of California | Methods and compositions for treating hypertriglyceridemia |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4458066A (en) | 1980-02-29 | 1984-07-03 | University Patents, Inc. | Process for preparing polynucleotides |
| DE3572982D1 (en) | 1984-03-06 | 1989-10-19 | Takeda Chemical Industries Ltd | Chemically modified lymphokine and production thereof |
| GB8601597D0 (en) | 1986-01-23 | 1986-02-26 | Wilson R H | Nucleotide sequences |
| GB8717430D0 (en) | 1987-07-23 | 1987-08-26 | Celltech Ltd | Recombinant dna product |
| GB8809129D0 (en) | 1988-04-18 | 1988-05-18 | Celltech Ltd | Recombinant dna methods vectors and host cells |
| CA2006596C (en) | 1988-12-22 | 2000-09-05 | Rika Ishikawa | Chemically-modified g-csf |
| ATE92107T1 (de) | 1989-04-29 | 1993-08-15 | Delta Biotechnology Ltd | N-terminale fragmente von menschliches serumalbumin enthaltenden fusionsproteinen. |
| FR2650598B1 (fr) | 1989-08-03 | 1994-06-03 | Rhone Poulenc Sante | Derives de l'albumine a fonction therapeutique |
| FR2686901A1 (fr) | 1992-01-31 | 1993-08-06 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides antithrombotiques, leur preparation et compositions pharmaceutiques les contenant. |
| FR2686899B1 (fr) | 1992-01-31 | 1995-09-01 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides biologiquement actifs, leur preparation et compositions pharmaceutiques les contenant. |
| WO2001077137A1 (en) | 2000-04-12 | 2001-10-18 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| ITMI20011483A1 (it) | 2001-07-11 | 2003-01-11 | Res & Innovation Soc Coop A R | Uso di composti come antagonisti funzionali ai recettori centrali deicannabinoidi |
| NZ532896A (en) | 2001-11-08 | 2007-08-31 | Pdl Biopharma Inc | Stable liquid pharmaceutical formulation of IGG antibodies including daclizumab and fontolizumab |
| WO2005027978A2 (en) | 2003-09-19 | 2005-03-31 | Novo Nordisk A/S | Albumin-binding derivatives of therapeutic peptides |
| TW200738261A (en) | 2005-12-20 | 2007-10-16 | Bristol Myers Squibb Co | Stable protein formulations |
| NZ580670A (en) | 2007-06-21 | 2011-09-30 | Univ Muenchen Tech | Biological active proteins having increased in vivo and/or vitro stability |
| US9345661B2 (en) | 2009-07-31 | 2016-05-24 | Genentech, Inc. | Subcutaneous anti-HER2 antibody formulations and uses thereof |
| BR112012029577B1 (pt) | 2010-05-21 | 2022-04-12 | Xl-Protein Gmbh | Conjugado de fármaco compreendendo polipeptídeos helicoidais randômicos prolina/alanina biossintéticos, e composição farmacêutica ou diagnóstica |
| WO2015191781A2 (en) | 2014-06-10 | 2015-12-17 | Amgen Inc. | Apelin polypeptides |
| US10588980B2 (en) | 2014-06-23 | 2020-03-17 | Novartis Ag | Fatty acids and their use in conjugation to biomolecules |
-
2019
- 2019-11-25 CN CN201980089752.0A patent/CN113396158A/zh active Pending
- 2019-11-25 JP JP2021529265A patent/JP2022513626A/ja active Pending
- 2019-11-25 EP EP19816456.8A patent/EP3887393A1/en not_active Withdrawn
- 2019-11-25 US US17/296,369 patent/US20220025344A1/en not_active Abandoned
- 2019-11-25 WO PCT/IB2019/060140 patent/WO2020109978A1/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103732624A (zh) * | 2011-06-17 | 2014-04-16 | 瑞泽恩制药公司 | 抗angptl3抗体及其用途 |
| WO2018020477A1 (en) * | 2016-07-28 | 2018-02-01 | The Regents Of The University Of California | Methods and compositions for treating hypertriglyceridemia |
Non-Patent Citations (1)
| Title |
|---|
| SIMON MYSLING等: "The acidic domain of the endothelial membrane protein GPIHBP1 stabilizes lipoprotein lipase activity by preventing unfolding of its catalytic domain", 《ELIFE》, vol. 5, pages 1 - 24 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117384912A (zh) * | 2023-12-13 | 2024-01-12 | 中国人民解放军东部战区总医院 | Gpihbp1突变型基因及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220025344A1 (en) | 2022-01-27 |
| JP2022513626A (ja) | 2022-02-09 |
| WO2020109978A1 (en) | 2020-06-04 |
| EP3887393A1 (en) | 2021-10-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102179392B1 (ko) | 글루카곤, glp-1 및 gip 수용체 모두에 활성을 갖는 삼중 활성체의 지속형 결합체 | |
| KR101993714B1 (ko) | 대사 장애를 치료하는데 이용하기 위한 조성물과 방법 | |
| US10610568B2 (en) | Compositions and methods of use for treating metabolic disorders | |
| CA3003115C (en) | DUAL-FUNCTION PROTEINS AND PHARMACEUTICAL COMPOSITION INCLUDING | |
| JP4344136B2 (ja) | アポリポタンパク質類似体 | |
| US20120093814A1 (en) | Fusion Proteins Comprising Canine FC Portions | |
| EA032727B1 (ru) | Мутантный резистентный к протеолизу полипептид fgf21 и его применение | |
| CN102272163A (zh) | 瘦素和瘦素类似物结合物及其用途 | |
| US20260022150A1 (en) | Gdnf fusion polypeptides and methods of use thereof | |
| TW201617364A (zh) | 用於治療代謝異常之組成物及方法 | |
| BR122020010972B1 (pt) | polipeptídeo isolado e de fusão, sua composição farmacêutica e multímero | |
| AU2016346864A1 (en) | Long-acting FGF21 fusion proteins and pharmaceutical composition comprising same | |
| JP2012529272A (ja) | Gdnfおよびbdnfを中枢神経系へ送達するための融合タンパク質 | |
| EP3672621A1 (en) | Glp-2 fusion polypeptides and uses for treating and preventing gastrointestinal conditions | |
| US12226451B2 (en) | FGF-21 formulations | |
| US20180280474A1 (en) | Treatment of bile acid disorders | |
| KR102569658B1 (ko) | 컨쥬게이트 c1 에스테라제 억제제 및 그의 용도 | |
| KR20240029769A (ko) | 융합단백질 및 이의 응용 | |
| CN113396158A (zh) | Lpl-gpihbp1融合多肽 | |
| KR20250167074A (ko) | 단백질 유사체 및 이의 응용 | |
| ES2356181T3 (es) | Construcción de apolipoproteínas. | |
| HK40015865A (zh) | Gdnf融合多肽及其使用方法 | |
| BR112016018721B1 (pt) | Proteína de fusão p97 (melanotransferrina), composição farmacêutica que compreende a dita proteína de fusão e uso da proteína de fusão para tratar uma doença de depósito lisossômico | |
| WO2014014816A2 (en) | Methods of treating glucose metabolism disorders |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20210914 |
|
| WD01 | Invention patent application deemed withdrawn after publication |