CN111848493B - 一种含有螺二芴的衍生物及其有机电致发光器件 - Google Patents
一种含有螺二芴的衍生物及其有机电致发光器件 Download PDFInfo
- Publication number
- CN111848493B CN111848493B CN202010889585.2A CN202010889585A CN111848493B CN 111848493 B CN111848493 B CN 111848493B CN 202010889585 A CN202010889585 A CN 202010889585A CN 111848493 B CN111848493 B CN 111848493B
- Authority
- CN
- China
- Prior art keywords
- compound
- group
- substituted
- unsubstituted
- spirobifluorene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- ICPSWZFVWAPUKF-UHFFFAOYSA-N 1,1'-spirobi[fluorene] Chemical compound C1=CC=C2C=C3C4(C=5C(C6=CC=CC=C6C=5)=CC=C4)C=CC=C3C2=C1 ICPSWZFVWAPUKF-UHFFFAOYSA-N 0.000 title claims abstract description 31
- 239000010410 layer Substances 0.000 claims abstract description 119
- 230000005525 hole transport Effects 0.000 claims abstract description 37
- 239000012044 organic layer Substances 0.000 claims abstract description 12
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 14
- 229910052805 deuterium Inorganic materials 0.000 claims description 14
- 229910052739 hydrogen Inorganic materials 0.000 claims description 10
- 239000001257 hydrogen Substances 0.000 claims description 10
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 9
- 150000002431 hydrogen Chemical class 0.000 claims description 7
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 6
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims 2
- 239000000463 material Substances 0.000 abstract description 106
- 238000004770 highest occupied molecular orbital Methods 0.000 abstract description 6
- UGPNGFWKKRUHPH-UHFFFAOYSA-N 9h-carbazole;1h-indene Chemical group C1=CC=C2CC=CC2=C1.C1=CC=C2C3=CC=CC=C3NC2=C1 UGPNGFWKKRUHPH-UHFFFAOYSA-N 0.000 abstract 1
- 239000011159 matrix material Substances 0.000 abstract 1
- 150000001875 compounds Chemical class 0.000 description 70
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 42
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical class ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 39
- 238000006243 chemical reaction Methods 0.000 description 37
- 238000002347 injection Methods 0.000 description 37
- 239000007924 injection Substances 0.000 description 37
- -1 isomers thereof) Chemical group 0.000 description 30
- 239000000047 product Substances 0.000 description 24
- 230000000903 blocking effect Effects 0.000 description 23
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 22
- 238000005481 NMR spectroscopy Methods 0.000 description 17
- 239000012074 organic phase Substances 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 125000003118 aryl group Chemical group 0.000 description 15
- 229910052757 nitrogen Inorganic materials 0.000 description 15
- 238000002360 preparation method Methods 0.000 description 14
- 125000000217 alkyl group Chemical group 0.000 description 13
- 239000007787 solid Substances 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 238000001704 evaporation Methods 0.000 description 11
- 239000010408 film Substances 0.000 description 11
- 238000004128 high performance liquid chromatography Methods 0.000 description 11
- 238000001819 mass spectrum Methods 0.000 description 11
- 238000003786 synthesis reaction Methods 0.000 description 11
- 125000004432 carbon atom Chemical group C* 0.000 description 10
- 229910052751 metal Inorganic materials 0.000 description 10
- 239000002184 metal Substances 0.000 description 10
- 125000001424 substituent group Chemical group 0.000 description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- 125000001072 heteroaryl group Chemical group 0.000 description 9
- 125000005549 heteroarylene group Chemical group 0.000 description 9
- 239000002346 layers by function Substances 0.000 description 9
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 8
- 125000000732 arylene group Chemical group 0.000 description 8
- 230000008020 evaporation Effects 0.000 description 8
- 238000000034 method Methods 0.000 description 8
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 8
- 239000000758 substrate Substances 0.000 description 8
- 230000004888 barrier function Effects 0.000 description 7
- 238000001514 detection method Methods 0.000 description 7
- 239000011521 glass Substances 0.000 description 7
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 7
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- 229940125904 compound 1 Drugs 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 239000011368 organic material Substances 0.000 description 6
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 6
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 6
- 125000000923 (C1-C30) alkyl group Chemical group 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 238000004440 column chromatography Methods 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 5
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 238000010992 reflux Methods 0.000 description 5
- 239000000741 silica gel Substances 0.000 description 5
- 229910002027 silica gel Inorganic materials 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 238000007738 vacuum evaporation Methods 0.000 description 5
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 4
- NJIAKNWTIVDSDA-FQEVSTJZSA-N 7-[4-(1-methylsulfonylpiperidin-4-yl)phenyl]-n-[[(2s)-morpholin-2-yl]methyl]pyrido[3,4-b]pyrazin-5-amine Chemical compound C1CN(S(=O)(=O)C)CCC1C1=CC=C(C=2N=C(NC[C@H]3OCCNC3)C3=NC=CN=C3C=2)C=C1 NJIAKNWTIVDSDA-FQEVSTJZSA-N 0.000 description 4
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 4
- TVIVIEFSHFOWTE-UHFFFAOYSA-N aluminum;quinolin-8-ol Chemical compound [Al+3].C1=CN=C2C(O)=CC=CC2=C1.C1=CN=C2C(O)=CC=CC2=C1.C1=CN=C2C(O)=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-N 0.000 description 4
- 239000010405 anode material Substances 0.000 description 4
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Chemical compound [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 4
- 239000010406 cathode material Substances 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 229940125797 compound 12 Drugs 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 4
- 125000005842 heteroatom Chemical group 0.000 description 4
- JKQOBWVOAYFWKG-UHFFFAOYSA-N molybdenum trioxide Chemical compound O=[Mo](=O)=O JKQOBWVOAYFWKG-UHFFFAOYSA-N 0.000 description 4
- 229910052763 palladium Inorganic materials 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 3
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 3
- IBXMKLPFLZYRQZ-UHFFFAOYSA-N 1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1C=CC(=O)C=CC1=CC=CC=C1 IBXMKLPFLZYRQZ-UHFFFAOYSA-N 0.000 description 3
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 3
- HCCNBKFJYUWLEX-UHFFFAOYSA-N 7-(6-methoxypyridin-3-yl)-1-(2-propoxyethyl)-3-(pyrazin-2-ylmethylamino)pyrido[3,4-b]pyrazin-2-one Chemical compound O=C1N(CCOCCC)C2=CC(C=3C=NC(OC)=CC=3)=NC=C2N=C1NCC1=CN=CC=N1 HCCNBKFJYUWLEX-UHFFFAOYSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 3
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 3
- 229940125877 compound 31 Drugs 0.000 description 3
- 229940126545 compound 53 Drugs 0.000 description 3
- 150000004696 coordination complex Chemical class 0.000 description 3
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- UEEXRMUCXBPYOV-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical compound [Ir].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 UEEXRMUCXBPYOV-UHFFFAOYSA-N 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 3
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 3
- 239000010453 quartz Substances 0.000 description 3
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- ZNOKGRXACCSDPY-UHFFFAOYSA-N tungsten trioxide Chemical compound O=[W](=O)=O ZNOKGRXACCSDPY-UHFFFAOYSA-N 0.000 description 3
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- XPEIJWZLPWNNOK-UHFFFAOYSA-N (4-phenylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=CC=C1 XPEIJWZLPWNNOK-UHFFFAOYSA-N 0.000 description 2
- XESMNQMWRSEIET-UHFFFAOYSA-N 2,9-dinaphthalen-2-yl-4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC(C=2C=C3C=CC=CC3=CC=2)=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=C(C=3C=C4C=CC=CC4=CC=3)N=C21 XESMNQMWRSEIET-UHFFFAOYSA-N 0.000 description 2
- MBHPOBSZPYEADG-UHFFFAOYSA-N 2-bromo-9,9-dimethylfluorene Chemical compound C1=C(Br)C=C2C(C)(C)C3=CC=CC=C3C2=C1 MBHPOBSZPYEADG-UHFFFAOYSA-N 0.000 description 2
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 2
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 2
- OSQXTXTYKAEHQV-WXUKJITCSA-N 4-methyl-n-[4-[(e)-2-[4-[4-[(e)-2-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]ethenyl]phenyl]phenyl]ethenyl]phenyl]-n-(4-methylphenyl)aniline Chemical group C1=CC(C)=CC=C1N(C=1C=CC(\C=C\C=2C=CC(=CC=2)C=2C=CC(\C=C\C=3C=CC(=CC=3)N(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)=CC=2)=CC=1)C1=CC=C(C)C=C1 OSQXTXTYKAEHQV-WXUKJITCSA-N 0.000 description 2
- VIZUPBYFLORCRA-UHFFFAOYSA-N 9,10-dinaphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=C(C=CC=C2)C2=C1 VIZUPBYFLORCRA-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- MSDMPJCOOXURQD-UHFFFAOYSA-N C545T Chemical compound C1=CC=C2SC(C3=CC=4C=C5C6=C(C=4OC3=O)C(C)(C)CCN6CCC5(C)C)=NC2=C1 MSDMPJCOOXURQD-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 150000001454 anthracenes Chemical class 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 2
- 229910052790 beryllium Inorganic materials 0.000 description 2
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N coumarin Chemical compound C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- GNTDGMZSJNCJKK-UHFFFAOYSA-N divanadium pentaoxide Chemical compound O=[V](=O)O[V](=O)=O GNTDGMZSJNCJKK-UHFFFAOYSA-N 0.000 description 2
- 239000007772 electrode material Substances 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 150000002220 fluorenes Chemical class 0.000 description 2
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 238000005286 illumination Methods 0.000 description 2
- 150000002460 imidazoles Chemical class 0.000 description 2
- 150000002503 iridium Chemical class 0.000 description 2
- 229910052741 iridium Inorganic materials 0.000 description 2
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 2
- 229910001092 metal group alloy Inorganic materials 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 229910000480 nickel oxide Inorganic materials 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 2
- 125000005561 phenanthryl group Chemical group 0.000 description 2
- 125000004437 phosphorous atom Chemical group 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 125000002098 pyridazinyl group Chemical group 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 125000005493 quinolyl group Chemical group 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- FOGKDYADEBOSPL-UHFFFAOYSA-M rubidium(1+);acetate Chemical compound [Rb+].CC([O-])=O FOGKDYADEBOSPL-UHFFFAOYSA-M 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 229910052709 silver Inorganic materials 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- NDVLTYZPCACLMA-UHFFFAOYSA-N silver oxide Chemical compound [O-2].[Ag+].[Ag+] NDVLTYZPCACLMA-UHFFFAOYSA-N 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 239000004408 titanium dioxide Substances 0.000 description 2
- 125000004306 triazinyl group Chemical group 0.000 description 2
- 125000005580 triphenylene group Chemical group 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical group C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 1
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 1
- UKSZBOKPHAQOMP-SVLSSHOZSA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 UKSZBOKPHAQOMP-SVLSSHOZSA-N 0.000 description 1
- SYSFTTYJTWPOOR-UHFFFAOYSA-N (2-diphenylphosphanyl-1-naphthalen-1-yl-3h-naphthalen-2-yl)-diphenylphosphane Chemical group C1C=C2C=CC=CC2=C(C=2C3=CC=CC=C3C=CC=2)C1(P(C=1C=CC=CC=1)C=1C=CC=CC=1)P(C=1C=CC=CC=1)C1=CC=CC=C1 SYSFTTYJTWPOOR-UHFFFAOYSA-N 0.000 description 1
- VIJSPAIQWVPKQZ-BLECARSGSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-4-methylpentanoyl]amino]-4,4-dimethylpentanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(C)=O VIJSPAIQWVPKQZ-BLECARSGSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- QBLFZIBJXUQVRF-UHFFFAOYSA-N (4-bromophenyl)boronic acid Chemical compound OB(O)C1=CC=C(Br)C=C1 QBLFZIBJXUQVRF-UHFFFAOYSA-N 0.000 description 1
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 1
- BGKHQCLJYVUKNB-UHFFFAOYSA-N (9,9-dimethylfluoren-1-yl)boronic acid Chemical compound C1=CC(B(O)O)=C2C(C)(C)C3=CC=CC=C3C2=C1 BGKHQCLJYVUKNB-UHFFFAOYSA-N 0.000 description 1
- 125000006749 (C6-C60) aryl group Chemical group 0.000 description 1
- UWRZIZXBOLBCON-VOTSOKGWSA-N (e)-2-phenylethenamine Chemical class N\C=C\C1=CC=CC=C1 UWRZIZXBOLBCON-VOTSOKGWSA-N 0.000 description 1
- IWZZBBJTIUYDPZ-DVACKJPTSA-N (z)-4-hydroxypent-3-en-2-one;iridium;2-phenylpyridine Chemical compound [Ir].C\C(O)=C\C(C)=O.[C-]1=CC=CC=C1C1=CC=CC=N1.[C-]1=CC=CC=C1C1=CC=CC=N1 IWZZBBJTIUYDPZ-DVACKJPTSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- PEIOJDSKZHVEQV-UHFFFAOYSA-N 1,3-diphenylpropane-1,3-dione europium(3+) 1,10-phenanthroline Chemical compound [Eu+3].N1=CC=CC2=CC=C3C=CC=NC3=C12.C(C1=CC=CC=C1)(=O)CC(C1=CC=CC=C1)=O.C(C1=CC=CC=C1)(=O)CC(C1=CC=CC=C1)=O.C(C1=CC=CC=C1)(=O)CC(C1=CC=CC=C1)=O PEIOJDSKZHVEQV-UHFFFAOYSA-N 0.000 description 1
- QXOGPTXQGKQSJT-UHFFFAOYSA-N 1-amino-4-[4-(3,4-dimethylphenyl)sulfanylanilino]-9,10-dioxoanthracene-2-sulfonic acid Chemical compound Cc1ccc(Sc2ccc(Nc3cc(c(N)c4C(=O)c5ccccc5C(=O)c34)S(O)(=O)=O)cc2)cc1C QXOGPTXQGKQSJT-UHFFFAOYSA-N 0.000 description 1
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 1
- KMZUUSFWPQLMQE-UHFFFAOYSA-N 1-bromo-9,9-dimethylfluorene Chemical compound C1=CC(Br)=C2C(C)(C)C3=CC=CC=C3C2=C1 KMZUUSFWPQLMQE-UHFFFAOYSA-N 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- VFMUXPQZKOKPOF-UHFFFAOYSA-N 2,3,7,8,12,13,17,18-octaethyl-21,23-dihydroporphyrin platinum Chemical compound [Pt].CCc1c(CC)c2cc3[nH]c(cc4nc(cc5[nH]c(cc1n2)c(CC)c5CC)c(CC)c4CC)c(CC)c3CC VFMUXPQZKOKPOF-UHFFFAOYSA-N 0.000 description 1
- BFTIPCRZWILUIY-UHFFFAOYSA-N 2,5,8,11-tetratert-butylperylene Chemical group CC(C)(C)C1=CC(C2=CC(C(C)(C)C)=CC=3C2=C2C=C(C=3)C(C)(C)C)=C3C2=CC(C(C)(C)C)=CC3=C1 BFTIPCRZWILUIY-UHFFFAOYSA-N 0.000 description 1
- STTGYIUESPWXOW-UHFFFAOYSA-N 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline Chemical compound C=12C=CC3=C(C=4C=CC=CC=4)C=C(C)N=C3C2=NC(C)=CC=1C1=CC=CC=C1 STTGYIUESPWXOW-UHFFFAOYSA-N 0.000 description 1
- MVVGSPCXHRFDDR-UHFFFAOYSA-N 2-(1,3-benzothiazol-2-yl)phenol Chemical compound OC1=CC=CC=C1C1=NC2=CC=CC=C2S1 MVVGSPCXHRFDDR-UHFFFAOYSA-N 0.000 description 1
- YLYPIBBGWLKELC-RMKNXTFCSA-N 2-[2-[(e)-2-[4-(dimethylamino)phenyl]ethenyl]-6-methylpyran-4-ylidene]propanedinitrile Chemical compound C1=CC(N(C)C)=CC=C1\C=C\C1=CC(=C(C#N)C#N)C=C(C)O1 YLYPIBBGWLKELC-RMKNXTFCSA-N 0.000 description 1
- IXHWGNYCZPISET-UHFFFAOYSA-N 2-[4-(dicyanomethylidene)-2,3,5,6-tetrafluorocyclohexa-2,5-dien-1-ylidene]propanedinitrile Chemical compound FC1=C(F)C(=C(C#N)C#N)C(F)=C(F)C1=C(C#N)C#N IXHWGNYCZPISET-UHFFFAOYSA-N 0.000 description 1
- VVCMGAUPZIKYTH-VGHSCWAPSA-N 2-acetyloxybenzoic acid;[(2s,3r)-4-(dimethylamino)-3-methyl-1,2-diphenylbutan-2-yl] propanoate;1,3,7-trimethylpurine-2,6-dione Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O.CN1C(=O)N(C)C(=O)C2=C1N=CN2C.C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 VVCMGAUPZIKYTH-VGHSCWAPSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- VFMAPIFSXMBTQP-UHFFFAOYSA-N 2-bromo-4-chloro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(Cl)C=C1Br VFMAPIFSXMBTQP-UHFFFAOYSA-N 0.000 description 1
- BEXOYZKPTUJSCZ-UHFFFAOYSA-N 2-chloro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)aniline Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(N)C(Cl)=C1 BEXOYZKPTUJSCZ-UHFFFAOYSA-N 0.000 description 1
- KHGJUVPQSMKNFA-UHFFFAOYSA-N 2-chloro-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)aniline Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(Cl)C(N)=C1 KHGJUVPQSMKNFA-UHFFFAOYSA-N 0.000 description 1
- POXIZPBFFUKMEQ-UHFFFAOYSA-N 2-cyanoethenylideneazanide Chemical group [N-]=C=[C+]C#N POXIZPBFFUKMEQ-UHFFFAOYSA-N 0.000 description 1
- NSMJMUQZRGZMQC-UHFFFAOYSA-N 2-naphthalen-1-yl-1H-imidazo[4,5-f][1,10]phenanthroline Chemical compound C12=CC=CN=C2C2=NC=CC=C2C2=C1NC(C=1C3=CC=CC=C3C=CC=1)=N2 NSMJMUQZRGZMQC-UHFFFAOYSA-N 0.000 description 1
- HPDNGBIRSIWOST-UHFFFAOYSA-N 2-pyridin-2-ylphenol Chemical compound OC1=CC=CC=C1C1=CC=CC=N1 HPDNGBIRSIWOST-UHFFFAOYSA-N 0.000 description 1
- CINYXYWQPZSTOT-UHFFFAOYSA-N 3-[3-[3,5-bis(3-pyridin-3-ylphenyl)phenyl]phenyl]pyridine Chemical compound C1=CN=CC(C=2C=C(C=CC=2)C=2C=C(C=C(C=2)C=2C=C(C=CC=2)C=2C=NC=CC=2)C=2C=C(C=CC=2)C=2C=NC=CC=2)=C1 CINYXYWQPZSTOT-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- HXWWMGJBPGRWRS-CMDGGOBGSA-N 4- -2-tert-butyl-6- -4h-pyran Chemical compound O1C(C(C)(C)C)=CC(=C(C#N)C#N)C=C1\C=C\C1=CC(C(CCN2CCC3(C)C)(C)C)=C2C3=C1 HXWWMGJBPGRWRS-CMDGGOBGSA-N 0.000 description 1
- PWFFDTZNRAEFIY-UHFFFAOYSA-N 4-(4-aminophenyl)-3-(4-methoxyphenyl)aniline Chemical compound C1=CC(OC)=CC=C1C1=CC(N)=CC=C1C1=CC=C(N)C=C1 PWFFDTZNRAEFIY-UHFFFAOYSA-N 0.000 description 1
- WPUSEOSICYGUEW-UHFFFAOYSA-N 4-[4-(4-methoxy-n-(4-methoxyphenyl)anilino)phenyl]-n,n-bis(4-methoxyphenyl)aniline Chemical compound C1=CC(OC)=CC=C1N(C=1C=CC(=CC=1)C=1C=CC(=CC=1)N(C=1C=CC(OC)=CC=1)C=1C=CC(OC)=CC=1)C1=CC=C(OC)C=C1 WPUSEOSICYGUEW-UHFFFAOYSA-N 0.000 description 1
- PBWATBVKPGTOTB-UHFFFAOYSA-N 4-bromo-9,9-diphenylfluorene Chemical compound BrC1=CC=CC2=C1C1=CC=CC=C1C2(C=1C=CC=CC=1)C1=CC=CC=C1 PBWATBVKPGTOTB-UHFFFAOYSA-N 0.000 description 1
- NGVPTMGYYAQJMS-UHFFFAOYSA-N 9,9-diethyl-N,N-diphenyl-7-[2-[4-(9-phenylfluoren-9-yl)phenyl]ethenyl]fluoren-2-amine Chemical compound C1(=CC=CC=C1)N(C1=CC=2C(C3=CC(=CC=C3C=2C=C1)C=CC1=CC=C(C=C1)C1(C2=CC=CC=C2C=2C=CC=CC1=2)C1=CC=CC=C1)(CC)CC)C1=CC=CC=C1 NGVPTMGYYAQJMS-UHFFFAOYSA-N 0.000 description 1
- DVNOWTJCOPZGQA-UHFFFAOYSA-N 9-[3,5-di(carbazol-9-yl)phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=C1 DVNOWTJCOPZGQA-UHFFFAOYSA-N 0.000 description 1
- 229910001316 Ag alloy Inorganic materials 0.000 description 1
- 229910000838 Al alloy Inorganic materials 0.000 description 1
- BGGALFIXXQOTPY-NRFANRHFSA-N C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC Chemical compound C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC BGGALFIXXQOTPY-NRFANRHFSA-N 0.000 description 1
- HFPKZKXVTHRNFZ-UHFFFAOYSA-N C1=CC(C)=CC=C1C1(C=2C=CC(C)=CC=2)C2=CC(C=3C=C4C(C5=CC(=CC=C5C4=CC=3)C=3C=C4C(C5=CC=CC=C5C4=CC=3)(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)=CC=C2C2=CC=CC=C21 Chemical compound C1=CC(C)=CC=C1C1(C=2C=CC(C)=CC=2)C2=CC(C=3C=C4C(C5=CC(=CC=C5C4=CC=3)C=3C=C4C(C5=CC=CC=C5C4=CC=3)(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)=CC=C2C2=CC=CC=C21 HFPKZKXVTHRNFZ-UHFFFAOYSA-N 0.000 description 1
- 229940127007 Compound 39 Drugs 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 150000000918 Europium Chemical class 0.000 description 1
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 1
- 229910000861 Mg alloy Inorganic materials 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 1
- AJWQKFXHSQQNPX-UHFFFAOYSA-N OC(C)(C)C(C)(C)O.NC=1C=C(C=CC1Cl)B(O)O Chemical compound OC(C)(C)C(C)(C)O.NC=1C=C(C=CC1Cl)B(O)O AJWQKFXHSQQNPX-UHFFFAOYSA-N 0.000 description 1
- YNPNZTXNASCQKK-UHFFFAOYSA-N Phenanthrene Natural products C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-IGMARMGPSA-N Protium Chemical compound [1H] YZCKVEUIGOORGS-IGMARMGPSA-N 0.000 description 1
- 241000720974 Protium Species 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- JFBZPFYRPYOZCQ-UHFFFAOYSA-N [Li].[Al] Chemical compound [Li].[Al] JFBZPFYRPYOZCQ-UHFFFAOYSA-N 0.000 description 1
- XCPQSHFJZZSKLG-UHFFFAOYSA-N [Li].[Mg].[Ca] Chemical compound [Li].[Mg].[Ca] XCPQSHFJZZSKLG-UHFFFAOYSA-N 0.000 description 1
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910001515 alkali metal fluoride Inorganic materials 0.000 description 1
- 229910000272 alkali metal oxide Inorganic materials 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- JYMITAMFTJDTAE-UHFFFAOYSA-N aluminum zinc oxygen(2-) Chemical compound [O-2].[Al+3].[Zn+2] JYMITAMFTJDTAE-UHFFFAOYSA-N 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000004653 anthracenylene group Chemical group 0.000 description 1
- XXLJGBGJDROPKW-UHFFFAOYSA-N antimony;oxotin Chemical compound [Sb].[Sn]=O XXLJGBGJDROPKW-UHFFFAOYSA-N 0.000 description 1
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- MUALRAIOVNYAIW-UHFFFAOYSA-N binap Chemical compound C1=CC=CC=C1P(C=1C(=C2C=CC=CC2=CC=1)C=1C2=CC=CC=C2C=CC=1P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MUALRAIOVNYAIW-UHFFFAOYSA-N 0.000 description 1
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 1
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 1
- 230000031709 bromination Effects 0.000 description 1
- 238000005893 bromination reaction Methods 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- 150000001716 carbazoles Chemical class 0.000 description 1
- CREMABGTGYGIQB-UHFFFAOYSA-N carbon carbon Chemical compound C.C CREMABGTGYGIQB-UHFFFAOYSA-N 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125844 compound 46 Drugs 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- XCJYREBRNVKWGJ-UHFFFAOYSA-N copper(II) phthalocyanine Chemical compound [Cu+2].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 XCJYREBRNVKWGJ-UHFFFAOYSA-N 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 229960000956 coumarin Drugs 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 150000004985 diamines Chemical class 0.000 description 1
- 125000004987 dibenzofuryl group Chemical group C1(=CC=CC=2OC3=C(C21)C=CC=C3)* 0.000 description 1
- 125000004988 dibenzothienyl group Chemical group C1(=CC=CC=2SC3=C(C21)C=CC=C3)* 0.000 description 1
- 125000005509 dibenzothiophenyl group Chemical group 0.000 description 1
- DKHNGUNXLDCATP-UHFFFAOYSA-N dipyrazino[2,3-f:2',3'-h]quinoxaline-2,3,6,7,10,11-hexacarbonitrile Chemical compound C12=NC(C#N)=C(C#N)N=C2C2=NC(C#N)=C(C#N)N=C2C2=C1N=C(C#N)C(C#N)=N2 DKHNGUNXLDCATP-UHFFFAOYSA-N 0.000 description 1
- BJXYHBKEQFQVES-NWDGAFQWSA-N enpatoran Chemical compound N[C@H]1CN(C[C@H](C1)C(F)(F)F)C1=C2C=CC=NC2=C(C=C1)C#N BJXYHBKEQFQVES-NWDGAFQWSA-N 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 description 1
- 125000005567 fluorenylene group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 1
- 238000004896 high resolution mass spectrometry Methods 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 229940079865 intestinal antiinfectives imidazole derivative Drugs 0.000 description 1
- KEQRPCPOINRCDB-UHFFFAOYSA-N iridium(3+);pentane-2,4-dione;1-phenylisoquinoline Chemical compound [Ir+3].CC(=O)CC(C)=O.C1=CC=CC=C1C1=NC=CC2=CC=CC=C12.C1=CC=CC=C1C1=NC=CC2=CC=CC=C12 KEQRPCPOINRCDB-UHFFFAOYSA-N 0.000 description 1
- DBNYWRKRZTXMCU-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical compound [Ir].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 DBNYWRKRZTXMCU-UHFFFAOYSA-N 0.000 description 1
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 229930192419 itoside Natural products 0.000 description 1
- FUJCRWPEOMXPAD-UHFFFAOYSA-N lithium oxide Chemical compound [Li+].[Li+].[O-2] FUJCRWPEOMXPAD-UHFFFAOYSA-N 0.000 description 1
- 229910001947 lithium oxide Inorganic materials 0.000 description 1
- MORCTKJOZRLKHC-UHFFFAOYSA-N lithium;oxoboron Chemical compound [Li].O=[B] MORCTKJOZRLKHC-UHFFFAOYSA-N 0.000 description 1
- SKEDXQSRJSUMRP-UHFFFAOYSA-N lithium;quinolin-8-ol Chemical compound [Li].C1=CN=C2C(O)=CC=CC2=C1 SKEDXQSRJSUMRP-UHFFFAOYSA-N 0.000 description 1
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- SJCKRGFTWFGHGZ-UHFFFAOYSA-N magnesium silver Chemical compound [Mg].[Ag] SJCKRGFTWFGHGZ-UHFFFAOYSA-N 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000005309 metal halides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- ZTLUNQYQSIQSFK-UHFFFAOYSA-N n-[4-(4-aminophenyl)phenyl]naphthalen-1-amine Chemical compound C1=CC(N)=CC=C1C(C=C1)=CC=C1NC1=CC=CC2=CC=CC=C12 ZTLUNQYQSIQSFK-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- MHJUNMARMFAUBI-UHFFFAOYSA-N n-phenyliminobenzamide Chemical compound C=1C=CC=CC=1C(=O)N=NC1=CC=CC=C1 MHJUNMARMFAUBI-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 238000000643 oven drying Methods 0.000 description 1
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 1
- GNRSAWUEBMWBQH-UHFFFAOYSA-N oxonickel Chemical compound [Ni]=O GNRSAWUEBMWBQH-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 150000005041 phenanthrolines Chemical class 0.000 description 1
- 125000005562 phenanthrylene group Chemical group 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical class N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 1
- SIOXPEMLGUPBBT-UHFFFAOYSA-M picolinate Chemical compound [O-]C(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-M 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920000172 poly(styrenesulfonic acid) Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000005550 pyrazinylene group Chemical group 0.000 description 1
- VLRICFVOGGIMKK-UHFFFAOYSA-N pyrazol-1-yloxyboronic acid Chemical compound OB(O)ON1C=CC=N1 VLRICFVOGGIMKK-UHFFFAOYSA-N 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 125000005548 pyrenylene group Chemical group 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 125000005551 pyridylene group Chemical group 0.000 description 1
- 125000005576 pyrimidinylene group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910001923 silver oxide Inorganic materials 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- PUZPDOWCWNUUKD-UHFFFAOYSA-M sodium fluoride Chemical compound [F-].[Na+] PUZPDOWCWNUUKD-UHFFFAOYSA-M 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 125000006836 terphenylene group Chemical group 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000005730 thiophenylene group Chemical group 0.000 description 1
- 238000010023 transfer printing Methods 0.000 description 1
- 125000005259 triarylamine group Chemical class 0.000 description 1
- 125000005558 triazinylene group Chemical group 0.000 description 1
- 125000003960 triphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)* 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 108010086502 tumor-derived adhesion factor Proteins 0.000 description 1
- 238000004506 ultrasonic cleaning Methods 0.000 description 1
- 238000001771 vacuum deposition Methods 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/94—[b, c]- or [b, d]-condensed containing carbocyclic rings other than six-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B59/00—Introduction of isotopes of elements into organic compounds ; Labelled organic compounds per se
- C07B59/002—Heterocyclic compounds
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/05—Isotopically modified compounds, e.g. labelled
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
本发明提供了一种含有螺二芴的衍生物及其有机电致发光器件,涉及有机光电材料技术领域。本发明所要解决的技术问题是目前有机电致发光器件中空穴传输类材料稳定性差以及有机电致发光器件寿命短的问题。本发明的含有螺二芴的衍生物以螺二芴类的基团为母体,通过单键或者桥与咔唑并茚类基团连接。本发明的有机电致发光器件包括阳极、有机物层和阴极,有机物层包括空穴传输层。本发明式I的含有螺二芴的衍生物具有较适合的HOMO能级以及更好的稳定性,将其用于有机电致发光器件的空穴传输层时,有机电致发光器件具有较高的发光效率、较低的驱动电压以及较长的使用寿命。
Description
技术领域
本发明涉及有机光电材料技术领域,具体涉及一种含有螺二芴的衍生物及其有机电致发光器件。
背景技术
有机电致发光器件(Organic Light-Emitting Diode,OLED)是一种由有机分子薄片组成的固态设备,施加电力之后就能发光。OLED因为效率高,对比度高,视角大,反应时间快,色彩饱和,结构相对简单,在显示和照明方面有非常广泛的应用前景,被称为梦幻显示技术。由于OLED可以在各式不同的基板上制造,使其成为柔性显示的关键技术。OLED器件由n型功能层、p型功能层、发光层、阴极以及阳极所构成。n型功能层包括空穴注入层(HoleInjection Layer,HIL)、空穴传输层(Hole Transporting Layer,HTL)、电子阻挡层(Electron Blocking Layer,EBL)等,p型功能层包括空穴阻挡层(Hole Blocking Layer,HBL),电子传输层(Electron Transporting Layer,ETL)和电子注入层(ElectronInjection Layer,EIL)等。
根据使用有机功能材料的不同,OLED器件可以分为两大类:小分子器件和高分子器件。小分子OLED技术发展的较早,而且技术已经达到商业化生产水平。高分子OLED又称为POLED,其发展始于1990年,由于聚合物可以采用旋涂、喷墨印刷等方法制备薄膜,从而有可能大大降低器件生产成本,但目前该技术远未成熟。根据驱动方式的不同,OLED器件也可以分为无源驱动型和有源驱动型两种。无源驱动型不采用薄膜晶体管(Thin FilmTransistor,TFT)基板,一般适用于中小尺寸显示;有源驱动型则采用TFT基板,适用于中大尺寸显示,特别是大尺寸全彩动态图像显示。目前,无源驱动型OLED和有源驱动型OLED技术已经比较成熟,已经推出大批商用产品。
对于用ITO玻璃透明电极作为阳极,不透明金属作为阴极,电子传输层、发光层、空穴传输层作为有机功能层的有机电致发光器件来说,在一定电压驱动下,电子和空穴分别从阴极和阳极注入到电子和空穴传输层,然后分别迁移到发光层,两者相遇形成激子使发光分子激发,后者经过辐射后发出可见光。辐射光可从ITO一侧观察到,金属电极膜同时也起了反射层的作用。
OLED器件要求从阳极注入的空穴与从阴极注入的电子能相对平衡的注入到发光层中,也就是要求空穴和电子的注入速率应该基本相同。空穴传输层紧邻发光层,空穴传输层在OLED器件中起着至关重要的作用,起到降低驱动电压和提高发光效率的作用,由此可见在制备OLED器件时有必要选择合适的空穴传输材料。空穴传输材料相对于电子传输材料和发光材料,空穴传输材料的稳定性较低,会导致OLED器件性能衰减,因而成为影响有机电致发光器件性能特别是使用寿命的主要因素,因此改善空穴传输材料的稳定性是研究的重点。
发明内容
为了解决目前有机电致发光器件中的有机功能层的材料稳定性差,尤其是空穴传输类材料稳定性差以及有机电致发光器件寿命短的问题,本发明提供了一种含有螺二芴的衍生物及其有机电致发光器件。
本发明通过使用下述式I所示的螺二芴的衍生物作为有机电致发光器件的有机功能层材料,可以实现上述目的,从而完成了本发明。
本发明提供了一种含有螺二芴的衍生物,具有如式I所示的结构通式,
所述Ar选自如下所示基团中的一种,
其中,所述X1、X2独立的选自单键或者C(R0)2,且X1、X2不同时为单键,所述R0选自取代或未取代的C1~C10的烷基、取代或未取代的C6~C30的芳基、取代或未取代的C3~C30的杂芳基中的一种;
所述m选自0~4中的整数,所述n选自0~3中的整数,所述k选自0~2中的整数,所述R选自氢、氘、取代或未取代的C1~C30的烷基中的一种,每个R相同或者不同;
所述L选自单键、取代或未取代的C6~C30的亚芳基、取代或未取代的C3~C30亚杂芳基中的一种;
所述Ar0选自取代或未取代的C1~C30的烷基、取代或未取代的C6~C30的芳基中的一种。
本发明还提供了一种有机电致发光器件,依次包括阳极、有机物层、阴极,所述有机物层含有上述本发明的含有螺二芴的衍生物。
有益效果:本发明式I的含有螺二芴的衍生物具有较适合的HOMO能级,能够有效的将空穴注入到发光层内,使发光层内产生更多的激子而发光,有效的提高了器件的发光效率,并且由于衍生物的HOMO能级与阳极和发光层更加的匹配,空穴的注入势垒较低,将式I的含有螺二芴的衍生物用作空穴传输层的器件的驱动电压较低。此外,本发明式I的含有螺二芴的衍生物具有更好的稳定性,器件在工作时含有式I的衍生物的有机薄膜不易变形,有效的改善了有机电致发光器件的使用寿命。
附图说明
图1为本发明化合物1的1H NMR图;图2为本发明化合物12的1H NMR图;
图3为本发明化合物184的1H NMR图;图4为本发明化合物194的1H NMR图;
图5为本发明化合物215的1H NMR图;图6为本发明化合物225的1H NMR图;
图7为本发明化合物232的1H NMR图;图8为本发明化合物240的1H NMR图。
具体实施方式
下面结合具体实施例,进一步阐明本发明,应理解这些实施例仅用于说明本发明而不用于限制本发明的范围,在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本申请所要求保护的范围内。
本发明所述的氢(H)包含其同位素,氕(P)、氘(D)、氚(T)。
本发明所述的烷基是指是指烷烃分子中少掉一个氢原子而成的一价基团,烷基是一类没有任何双键或者三键的饱和烃基。所述烷基包括直链烷基、支链烷基、环烷基。所述烷基的碳原子数为C1~C60,优选为C1~C30,进一步优选为C1~C15,还进一步优选为C1~C10。所述烷基实例包括但不限于如下基团,甲基、乙基、丙基(包括其异构体)、丁基(包括其异构体)、戊基(包括其异构体)、己基(包括其异构体)、庚基(包括其异构体)、辛基(包括其异构体)、壬基(包括其异构体)、癸基(包括其异构体)、十一烷基(包括其异构体)、十二烷基(包括其异构体)、十三烷基(包括其异构体)、十四烷基(包括其异构体)、十五烷基(包括其异构体),环丙基、环丁基、环戊基、环己基、金刚烷基、莰烷基、降冰片烷基等。上述烷基的同分异构体的实例如下,丙基包括正丙基、异丙基,丁基包括正丁基、异丁基、仲丁基、叔丁基,以此类推。
本发明所述的芳基是指芳香烃分子中少掉一个氢原子而成的一价基团。所述芳基包括单环芳基、多环芳基、稠环芳基。所述芳基的碳原子数为C6~C60,优选为C6~C30,进一步优选为C6~C20,还进一步优选为C6~C14。所述芳基实例包括但不限于如下基团,苯基、联苯基、三联苯基、四联苯基、萘基、菲基、蒽基、三亚苯基、芘基、苝基、荧蒽基、茚基、芴基、苯并芴基、螺二芴基、苯并螺二芴基等。
本发明所述的杂芳基是指芳基中的至少一个碳原子被杂原子取代的一价基团。所述杂原子包括但不限于如下所示原子,氧原子、硫原子、氮原子、硅原子、硼原子、磷原子等。所述杂芳基包括单环杂芳基、多环杂芳基、稠环杂芳基。所述杂芳基的碳原子数为C3~C60,优选为C3~C30,进一步优选为C3~C20,还进一步优选为C3~C10。所述杂芳基实例包括但不限于如下基团,呋喃基、苯并呋喃基、二苯并呋喃基、苯并二苯并呋喃基、噻吩基、苯并噻吩基、二苯并噻吩基、苯并二苯并噻吩基、咔唑基、苯并咔唑基、吖啶基、吩恶嗪基、吩噻嗪基、吡啶基、吡嗪基、哒嗪基、嘧啶基、三嗪基、喹啉基、异喹啉基、喹喔啉基、喹唑啉基、萘啶基等。
本发明所述的亚芳基是指芳香烃分子中少掉两个氢原子而成的二价基团。所述亚芳基包括单环亚芳基、多环亚芳基、稠环亚芳基或者其组合。所述亚芳基的碳原子数为C6~C60,优选为C6~C30,进一步优选为C6~C20,还进一步优选为C6~C14。所述亚芳基实例包括但不限于如下基团,亚苯基、亚联苯基、亚三联苯基、亚四联苯基、亚萘基、亚菲基、亚蒽基、亚三亚苯基、亚芘基、亚芴基、亚苯并芴基、亚螺二芴基、亚苯并螺二芴基等。
所述亚杂芳基是指亚芳基中的至少一个碳原子被杂原子取代的二价基团。所述杂原子包括但不限于如下所示原子,氧原子、硫原子、氮原子、硅原子、硼原子、磷原子等。所述亚杂芳基包括单环亚杂芳基、多环亚杂芳基、稠环亚杂芳基或者其组合。所述亚杂芳基的碳原子数为C3~C60,优选为C3~C30,进一步优选为C3~C20,还进一步优选为C3~C10。所述亚杂芳基实例包括但不限于如下基团,亚呋喃基、亚苯并呋喃基、亚二苯并呋喃基、亚苯并二苯并呋喃基、亚噻吩基、亚苯并噻吩基、亚二苯并噻吩基、亚苯并二苯并噻吩基、亚咔唑基、亚苯并咔唑基、亚吡啶基、亚嘧啶基、亚吡嗪基、亚三嗪基、亚喹啉基、亚异喹啉基等。
所述的“取代或未取代的C6~C30的芳基”中的“C6~C30”表示未取代的“芳基”中的碳原子数,不包含取代基中的碳原子数。所述的“取代或未取代的C3~C30的杂芳基”中的“C3~C30”表示未取代的“杂芳基”中的碳原子数,不包含取代基中的碳原子数。所述的“取代或未取代的C1~C30的烷基”中的“C1~C30”表示未取代的“烷基”中的碳原子数,不包含取代基中的碳原子数。其他情况不再赘述,以此类推。
本发明所述的“取代或未取代”中的“未取代”表示基团上的氢原子未被任何取代基替换的意思。
本发明所述的“取代或未取代”中的“取代”表示基团上的至少一个氢原子被取代基所替换的意思。当有多个氢被多个取代基替换时,所述多个取代基可以相同或者不同。上述被取代基所替换的氢的位置可以为任意位置。
上述“取代或未取代”中的“取代”所代表的取代基团选自如下所述基团中的一种,氘、卤素、氰基、硝基、取代或未取代的C1~C30的烷基、取代或未取代的C6~C60的芳基、取代或未取代的C3~C60的杂芳基。优选为氘、取代或未取代的甲基、取代或未取代的乙基、取代或未取代的丙基、取代或未取代的丁基、取代或未取代的戊基、取代或未取代的己基、取代或未取代的庚基、取代或未取代的辛基、取代或未取代的壬基、取代或未取代的癸基、取代或未取代的十一烷基、取代或未取代的十二烷基、取代或未取代的十三烷基、取代或未取代的十四烷基、取代或未取代的十五烷基、取代或未取代的环己基、取代或未取代的金刚烷基、取代或未取代的莰烷基,取代或未取代的苯基、取代或未取代的萘基、取代或未取代的菲基、取代或未取代的蒽基、取代或未取代的三亚苯基、取代或未取代的芴基、取代或未取代的苯并芴基、取代或未取代的螺二芴基、取代或未取代的二苯并呋喃基、取代或未取代的二苯并噻吩基、取代或未取代的咔唑基、取代或未取代的吡啶基、取代或未取代的嘧啶基、取代或未取代的哒嗪基、取代或未取代的三嗪基、取代或未取代的喹啉基、取代或未取代的喹喔啉基。
本发明所述的“选自0至M的整数”是指所述值选自0至M的整数中的任意一个,包括0,1,2…M-2,M-1,M。例如,“m选自0~4中的整数”是指m选自1,2,3,4;“n选自0~3中的整数”是指n选自0,1,2,3;以此类推。
本发明提供了一种含有螺二芴的衍生物,具有如式I所示的结构通式,
所述Ar选自如下所示基团中的一种,
其中,所述X1、X2独立的选自单键或者C(R0)2,且X1、X2不同时为单键,所述R0选自取代或未取代的C1~C10的烷基、取代或未取代的C6~C30的芳基、取代或未取代的C3~C30的杂芳基中的一种;
所述m选自0~4中的整数,所述n选自0~3中的整数,所述k选自0~2中的整数,所述R选自氢、氘、取代或未取代的C1~C30的烷基中的一种,每个R相同或者不同;
所述L选自单键、取代或未取代的C6~C30的亚芳基、取代或未取代的C3~C30亚杂芳基中的一种;
所述Ar0选自取代或未取代的C1~C30的烷基、取代或未取代的C6~C30的芳基中的一种。
优选的,所述含有螺二芴的衍生物具有如I-1~I-6所示的结构通式,
所述Ar0选自如下所示基团中的一种,
所述p选自0~5中的整数,所述q选自0~7中的整数,所述m选自0~4中的整数,所述R1选自氢、氘、取代或未取代的1~30的烷基中的一种,每个R1相同或者不同。
优选的,所述R选自氢、氘、取代或未取代的甲基、取代或未取代的乙基、取代或未取代的丙基、取代或未取代的丁基、取代或未取代的戊基、取代或未取代的己基、取代或未取代的庚基、取代或未取代的辛基、取代或未取代的壬基、取代或未取代的癸基、取代或未取代的十一烷基、取代或未取代的十二烷基、取代或未取代的十三烷基、取代或未取代的十四烷基、取代或未取代的十五烷基中的一种。
优选的,所述L选自单键或者如下所示基团中的一种,
所述X选自O、S、N(Rx)、C(Rx)2,所述Rx选自取代或未取代的C1~C10的烷基、取代或未取代的C6~C30的芳基中的一种;所述L1、L2独立的选自单键或者取代或未取代的亚苯基。
优选的,所述Ar0选自如下所述基团中的一种,
优选的,所述L选自单键或者如下所示基团中的一种,
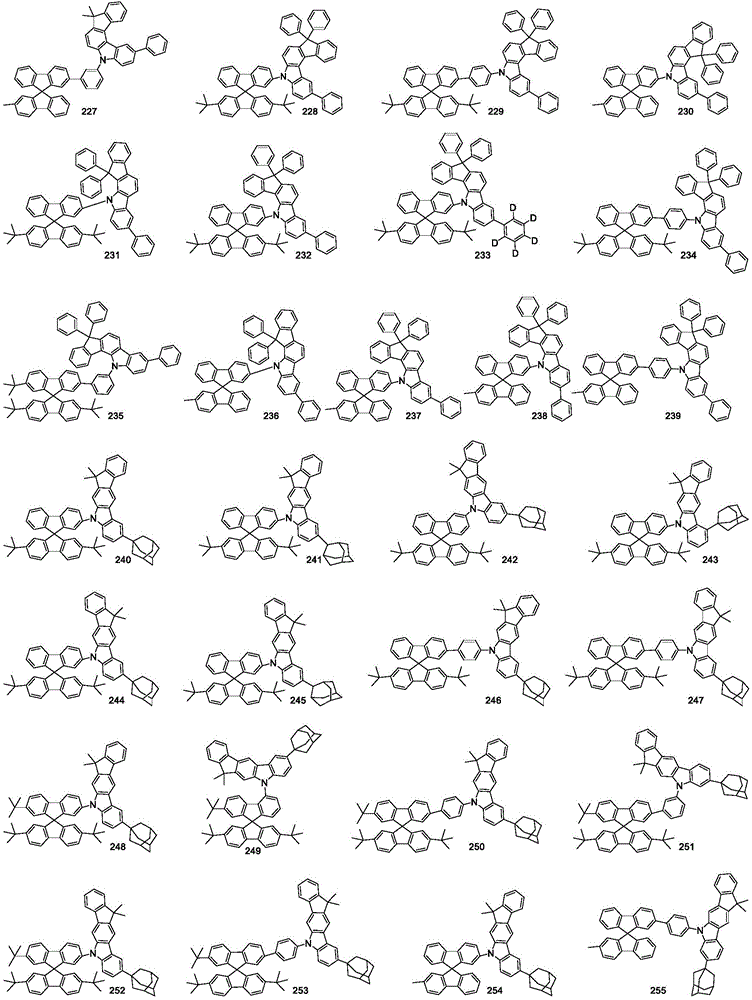
优选的,所述式I的含有螺二芴的衍生物选自如下所示结构中的一种,
以上列举了本发明所述的式I所示的含有螺二芴的衍生物的一些具体化学结构,但本发明不局限于所列的这些化学结构,凡是以式I所示结构为基础,取代基为如上所限定的基团都应包含在内。
本发明还提供了一种有机电致发光器件,依次包括阳极、有机物层、阴极,所述有机物层含有上述本发明的含有螺二芴的衍生物。
优选的,所述有机物层包括空穴传输层,所述空穴传输层含有上述本发明的含有螺二芴的衍生物。
本发明的有机物层除了含有空穴传输层外,还可以包含如下所述功能层中的一种或者多种,空穴注入层、电子阻挡层、发光层、空穴阻挡层、电子传输层、电子注入层等。还可以包含所述有机物层以外的功能层,例如,位于阳极或者阴极外侧的功能层。
本发明的有机电致发光器件的结构可以为如下所示的几种类型,但不仅限于所列举的有限结构:
阳极/空穴传输层/发光层/阴极
阳极/空穴传输层/发光层/电子传输层/阴极
阳极/空穴传输层/电子阻挡层/发光层/阴极
阳极/空穴注入层/空穴传输层/发光层/电子传输层/阴极
阳极/空穴传输层/发光层/电子传输层/电子注入层/阴极
阳极/空穴传输层/发光层/空穴阻挡层/电子传输层/阴极
阳极/空穴传输层/电子阻挡层/发光层/电子传输层/阴极
阳极/空穴注入层/空穴传输层/发光层/电子传输层/电子注入层/阴极
阳极/空穴注入层/空穴传输层/发光层/空穴阻挡层/电子传输层/电子注入层/阴极
阳极/空穴注入层/空穴传输层/电子阻挡层/发光层/电子传输层/电子注入层/阴极
阳极/空穴注入层/空穴传输层/电子阻挡层/发光层/空穴阻挡层/电子传输层/电子注入层/阴极
电极材料
为使载流子在器件中有效注入、传输与复合发光,电极材料要具有良好的导电性和稳定的化学性质;具有合适的功函数以减小注入势垒;最后作为出光电极还需要在可见光范围内具有较高的透明度。
阳极材料:本发明所述的阳极材料优选具有高功函数的材料,以便提高空穴的注入效率。所述阳极材料包括金属、金属氧化物、金属合金等,但不限于此。所述阳极材料的实例包括但不限于如下所述的材料,银(Ag)、铝(Al)、铂(Pt)、氧化铟锡(ITO)、氧化铟锌(IZO)、氧化锌:铝(ZnO:Al)或氧化锡:锑(SnO2:Sb)等。
阴极材料:本发明所述的阴极材料优选具有低功函数的材料,以便提高电子的注入效率。所述阴极材料包括金属、金属合金等,但不限于此。所述阴极材料的实例包括但不限于如下所述的材料,铝(Al)、银(Ag)、金(Au)、铅(Pb)、镁银合金(Mg:Al)、锂铝合金(Li:Al)、锂钙镁合金(Li:Ca:Mg)等。
注入材料
空穴注入材料:本发明所述的空穴注入材料优选能够有效降低阳极与空穴传输层之间的界面势垒的材料。所述空穴注入材料包括有机空穴注入材料和无机空穴注入材料。所述有机空穴注入材料包括酞菁类化合物、芳胺类化合物、含有多氰基的共轭有机材料等低分子有机化合物、高分子材料等,但不限于此;所述有机空穴注入材料的实例包括但不限于如下所述的材料,酞菁铜(CuPc),N4,N4,N4',N4'-四(4-甲氧基苯基)-[1,1'-联苯]-4,4'-二胺(MeO-TPD),1,4,5,8,9,11-六氮杂苯甲腈(HAT-CN)、2,3,5,6-四氟-7,7',8,8'-四氰二甲基对苯醌(F4-TCNQ),聚(N-乙烯基咔唑)(PVK)、聚(3,4-亚乙二氧基噻吩)/聚(苯乙烯磺酸)(PEDOT/PSS)等。所述无机空穴注入材料包括金属氧化物、金属卤化物等,但不限于此;所述无机空穴注入材料的实例包括但不限于如下所述的材料,三氧化钼(MoO3)、氧化银(AgO)、五氧化二钒(V2O5)、三氧化钨(WO3)、氧化镍(NiO)、二氧化钛(TiO2)、三氯化铁(FeCl3)等。
电子注入材料:本发明所述的电子注入材料优选能够有效降低阴极与电子注入层之间的界面势垒的材料。所述电子注入材料包括碱金属氧化物、碱金属氟化物、碱金属盐等,但不限于此。所述电子注入材料的实例包括但不限于如下所示的材料,氧化锂(Li2O)、氧化锂硼(LiBO2)、氟化锂(LiF)、氟化钠(NaF)、氟化铯(CsF)、8-羟基喹啉锂(Liq)、硅氧化钾(K2SiO3)、碳酸铯(Cs2CO3)、醋酸铷(CH3COORb)等。
传输材料
空穴传输材料:本发明所述的空穴传输材料优选具有较高的空穴迁移率、较好的稳定性的材料。所述空穴传输材料优选本发明式I的含有螺二芴的衍生物。
电子传输材料:本发明所述的电子传输材料优选具有较高的电子迁移率、适当的电子能级、较好的稳定性的材料。所述电子传输材料包括金属配合物、菲啰啉衍生物、咪唑衍生物、吡啶衍生物等,但不限于此。所述电子传输材料的实例包括但不限于如下所述的材料,三(8-羟基喹啉)合铝(III)(Alq3)、4,7-二苯基-1,10-菲罗啉(Bphen)、1,3,5-三(N-苯基-2-苯并咪唑)苯(TPBi)、3,3'-[5'-[3-(3-吡啶基)苯基](简称:TmPyPB)等。
阻挡材料
电子阻挡材料:本发明的电子阻挡层优选具有较高的LUMO能级、较高的空穴迁移率的材料。本发明的电子阻挡材料包括三芳胺衍生物、二胺衍生物等,但不限于此。本发明的电子传输材料的实例包括但不限于如下所述的材料,4,4',4”-三(咔唑-9-基)三苯胺(TCTA)、N,N'-二苯基-N,N'-(1-萘基)-1,1'-联苯-4,4'-二胺(NPB)等。
空穴阻挡材料:本发明的空穴阻挡层优选具有较低的HOMO能级、较高的电子迁移率的材料。本发明的空穴阻挡材料包括咪唑衍生物、菲啰啉衍生物、金属配合物等,但不限于此。本发明的空穴阻挡层的实例包括但不限于如下所述的材料,1,3,5-三(N-苯基-2-苯并咪唑)苯(TPBi)、4,7-二苯基-1,10-菲罗啉(Bphen)、2,9-二(萘-2-基)-4,7-二苯基-1,10-菲罗啉(NBphen)、2,9-二甲基-4,7-二苯基-1,10-菲啰啉(BCP)、二(8-羟基-2-甲基喹啉)-(4-苯基苯氧基)铝(BAlq)等。
发光材料
本发明所述的发光材料按照发光机理可以分为荧光材料和磷光材料,按照发光颜色有可以分为红光发光材料、绿光发光材料和蓝光发光材料。
荧光材料:本法的荧光材料包括红色荧光材料、绿色荧光材料和蓝色荧光材料。本发明的红色荧光材料包括DCM系列材料等,但不限于此。所述红色荧光材料的实例包括但不限于如下所述的材料,4-(二氰基亚甲基)-2-甲基-6-(4-二甲基氨基苯乙烯基)-4H-吡喃(DCM)、4-(二氰基甲撑)-2-叔丁基-6-(1,1,7,7-四甲基久洛尼啶-9-烯基)-4H-吡喃(DCJTB)等。本发明的绿色荧光材料包括金属配合物、香豆素染料等,但不限于此。所述绿色荧光材料的实例包括但不限于如下所述的材料,三(8-羟基喹啉)合铝(III)(Alq3)、香豆素545T(C-525T)等。所述蓝色荧光材料包括蒽衍生物、芴衍生物、苝衍生物、苯乙烯基胺衍生物等,但不限于此。所述蓝色荧光材料的实例包括但不限于如下所述的材料,9,10-二-(2-萘基)蒽(ADN)、9-[4-(2-(7-(N,N-二苯基氨基)-9,9-二乙基芴-2-基)乙烯基)苯基]-9-苯基-芴(DPAFVF)、2,5,8,11-四叔丁基苝(TBPe)、4,4'-二[4-(二对甲苯基氨基)苯乙烯基]联苯(DPAVBi)等。
磷光材料:本发明的磷光材料包括红色磷光材料、绿色磷光材料和蓝色磷光材料。本发明的红色磷光材料包括铱配合物、铂配合物、铕配合物等金属配合物,但不限于此。本发明的红色磷光材料的实例包括但不限于如下所述的材料,二(1-苯基异喹啉)(乙酰丙酮)铱(III)(Ir(piq)2(acac))、八乙基卟啉铂(PtOEP)、三(二苯甲酰基甲烷)单(菲罗啉)铕(III)(Eu(dbm)3(Phen))等,但不限于此。本发明的绿色磷光材料包括铝配合物、铱配合物、锌配合物等金属配合物,但不限于此。本发明的绿色磷光材料的实例包括但不限于如下所述的材料,三(8-羟基喹啉)合铝(III)(Alq3)、三(2-苯基吡啶)合铱(Ir(ppy)3)、乙酰丙酮酸二(2-苯基吡啶)铱(Ir(ppy)2(acac))、二[2-(2-苯并噻唑基)苯酚]锌(Zn(BTZ)2)等,但不限于此。本发明所述的蓝色磷光材料包括铱配合我、铍配合物等金属配合物,但不限于此。本发明的蓝色磷光材料的实例包括但不限于如下所示的材料,二(4,6-二氟苯基吡啶-C2,N)吡啶甲酰合铱(FIrpic)、二(2,4-二氟苯基吡啶)-四(1-吡唑基)硼酸铱(III)(Fir6)、二(2-羟基苯基吡啶)合铍(Bepp2)等,但不限于此。
上述荧光材料和磷光材料可以单独用于发光层,也可以作为客体材料与主体材料一起用于发光层。当荧光材料或者磷光材料与主体材料一起用于发光层时,其主体材料优选与客体材料相比最低未占轨道能级高、最高已占轨道能级低的材料。上述主体材料包括金属配合物、芴衍生物、蒽衍生物、咔唑衍生物等,但不限于此。所述主体材料的实例包括但不限于如下所述的材料,三(8-羟基喹啉)合铝(III)(Alq3)、2,7-二[9,9-二(4-甲基苯基)-芴-2-基]-9,9-二(4-甲基苯基)芴(TDAF)、9,10-二(2-萘基)蒽(ADN)、1,3,5-三(9-咔唑基)苯(TCP)、4,4'-二(9-咔唑)联苯(CBP)、4,4',4”-三(咔唑-9-基)三苯胺(TCTA)等。
本发明的阳极、阴极、空穴注入层、电子注入层、空穴传输层、电子传输层、空穴阻挡层、电子阻挡层、发光层等可以为单层结构也可以为叠层结构。当为叠层结构时,各层膜可以相同或者不同。每一层可以为单一材料形成的膜结构,也可以为多种材料相互混合形成的膜结构。所述阳极的膜厚为10nm~1μm,优选为50nm~500nm,进一步优选为50nm~200nm。所述阴极的膜厚为0.1nm~1μm,优选为5nm~500nm,进一步优选为5nm~200nm。所述空穴注入层的膜厚为0.1nm~500nm,优选为1nm~200nm,进一步优选为5nm~100nm。所述电子注入层的膜厚为0.001nm~500nm,优选为0.01nm~200nm,进一步优选为0.1nm~100nm。所述空穴传输层的膜厚优选为5nm~800nm,优选为10nm~500nm,进一步优选为10nm~200nm。所述电子传输层的膜厚为1nm~500nm,优选为5nm~200nm,进一步优选为5nm~100nm。所述空穴阻挡层的膜厚为0.1nm~200nm,优选为1nm~100nm,进一步优选为5nm~100nm。所述电子阻挡层的膜厚为0.1nm~200nm,优选为1nm~100nm,进一步优选为5nm~100nm。所述发光层的膜厚为5nm~400nm,优选为10nm~200nm,进一步优选为10nm~100nm。
对本发明有机电致发光器件中各层薄膜的制备方法没有特别限制,可以采用真空蒸镀法、溅射法、旋涂法、喷涂法、丝网印刷法、激光转印法等,但不限于此。
本发明的有机电致发光器件主要有两个应用领域,一是信息显示,二是固体照明。在信息显示方面被广泛应用于各种信息显示,如平板电脑、平板电视、手机、智能手表、数码照相机、VR、车载系统、可穿戴设备等。
合成实施例
对本发明式I所示的含有螺二芴的衍生物的制备方法没有特别限制,可以采用本领域的技术人员所熟知的常规方法。例如,溴代反应、合环反应、碳碳偶联反应、碳氮偶联反应等。
例如,本发明的含有螺二芴的衍生物可以采用如下所示的合成路线进行制备:
一、
二、
三、
四、
五、
六、
原料与试剂:本发明对以下实施例中所采用的原料或试剂没有特别的限制,可以为市售产品或采用本领域技术人员所熟知的制备方法制备得到。本发明所用的原料及试剂均为试剂纯。
仪器:由英国沃特斯公司生产的G2-Si四极杆串联飞行时间高分辨率质谱;由德国Elementar公司生产的Vario EL cube型有机元素分析仪;由德国Bruker公司生产的Bruker-510型核磁共振谱仪。
合成实施例1:化合物1的制备
向1L反应瓶中,依次加入化合物A-1(7.08g,25.0mmol)和N,N-二甲基甲酰胺(600ml),搅拌使化合物A-1溶解,随后在室温且避光的条件下向反应瓶中于30分钟内缓慢加入N-溴代琥珀酰亚胺(NBS)(4.45g,25.0mmol),将混合物搅拌8小时后倒入碳酸钠溶液(3M,1.2L)中。反应液用二氯甲烷进行萃取,合并有机相,将有机相依次进行干燥、浓缩,最后用甲醇进行重结晶,得到化合物B-1。质量8.33g,产率92%。
向500ml反应瓶中依次加入甲苯(69ml)、化合物B-1(7.97g,22.0mmol)、苯硼酸(3.22g,26.4mmol)、乙醇(34ml)、碳酸钾溶液(2M,34.0ml)、四三苯基膦钯(1.27mg,0.0011mmol),在氮气保护下回流4小时,反应结束后将反应液冷却至室温,反应液用水洗,随后用二氯甲烷进行萃取,合并有机相,将有机相进行干燥、浓缩,用甲苯进行重结晶,得到化合物C-1。质量5.46g,产率69%。
在氮气保护下,向500ml反应瓶中,依次加入化合物C-1(5.39g,15.0mmol)、化合物D-1(6.34g,12.5mmol)、叔丁醇钠(3.60g,37.5mmol)、甲苯(190ml)、三二亚苄基丙酮二钯(57.23mg,0.0625mmol)、三叔丁基膦(12.65mg,0.0625mmol),在回流的条件下反应24小时,反应结束后,将反应液冷却至室温。用二氯甲烷萃取反应液,合并有机相,将有机相依次用水洗、干燥、硅藻土过滤,将滤液浓缩,用乙醇重结晶,得到化合物1。质量7.76g,产率79%。HPLC检测固体纯度≧99.9%。质谱m/z:785.4117(理论值:785.4022)。理论元素含量(%)C60H51N:C,91.68;H,6.54;N,1.78,实测元素含量(%):C,91.86;H,6.32;N,1.82。1H NMR(600MHz,CDCl3)(δ,ppm):8.38(s,1H),8.34(s,1H),8.17(s,1H),8.09–8.00(m,4H),7.98–7.90(m,2H),7.82(dd,2H),7.73(d,1H),7.69–7.63(m,5H),7.62–7.56(m,3H),7.52–7.42(m,6H),7.33(t,1H),1.76(s,6H),1.27(s,18H)。上述结果证实获得产物为目标产品。
合成实施例2:化合物12的制备
向500ml反应瓶中加入9,9-二甲基-2-溴芴(27.3g,100mmol)、3-氨基-4-氯苯基硼酸频哪醇(30.4g,120mmol)、叔丁醇钠(19.2g,200mmol)、双(二亚苄基丙酮)钯(1.15g,2mmol)、2,2-双(二苯膦基)-1,1-联萘(BINAP)(2.49g,4mmol)、甲苯(320ml),在氮气保护下回流搅拌过夜。反应结束后,将反应液过滤,浓缩滤液,进行柱层析(硅胶,二氯甲烷)得到化合物b-1。质量35.2g,产率79%。
向500ml反应瓶中加入化合物b-1(26.7g,60mmol)、碳酸钾(16.6g,120mmol)、乙酸钯(135mg,0.6mmol)、三环己基膦四氟硼酸盐(220mg,0.6mmol)、N,N-二甲基乙酰胺(280ml),在氮气保护下回流过夜。反应结束后,将反应液冷却是室温,氯仿萃取,合并有机相,将有机相依次用水洗、无水硫酸镁干燥、浓缩,进行柱层析(硅胶,二氯甲烷:正己烷)得到化合物c-1。质量18.4g,产率75%。
向500ml反应瓶中依次加入甲苯(69ml)、氘带溴苯溴苯(3.56g,22.0mmol)、化合物c-1(10.8g,26.4mmol)、乙醇(34ml)、碳酸钾溶液(2M,34.0ml)、四三苯基膦钯(1.27mg,0.0011mmol),在氮气保护下回流4小时,反应结束后将反应液冷却至室温,反应液用水洗,随后用二氯甲烷进行萃取,合并有机相,将有机相进行干燥、浓缩,用甲苯进行重结晶,得到化合物C-2。质量5.61g,产率70%。
在氮气保护下,向500ml反应瓶中,依次加入化合物C-2(5.47g,15.0mmol)、化合物D-1(6.34g,12.5mmol)、叔丁醇钠(3.60g,37.5mmol)、甲苯(190ml)、三二亚苄基丙酮二钯(57.23mg,0.0625mmol)、三叔丁基膦(12.65mg,0.0625mmol),在回流的条件下反应24小时,反应结束后,将反应液冷却至室温。用二氯甲烷萃取反应液,合并有机相,将有机相依次用水洗、干燥、硅藻土过滤,将滤液浓缩,用乙醇重结晶,得到化合物12。质量7.12g,产率72%。HPLC检测固体纯度≧99.9%。质谱m/z:790.4429(理论值:790.4335)。理论元素含量(%)C60H46D5N:C,91.10;H,7.13;N,1.77,实测元素含量(%):C,91.26;H,7.25;N,1.49。1H NMR(600MHz,CDCl3)(δ,ppm):8.20(d,1H),8.03(d,1H),7.98(d,1H),7.90–7.85(m,2H),7.77–7.71(m,5H),7.67(s,1H),7.63(d,1H),7.57–7.52(m,2H),7.51–7.46(m,5H),7.41–7.37(m,1H),7.33–7.29(m,2H),1.72(s,6H),1.27(s,18H)。上述结果证实获得产物为目标产品。
合成实施例3:化合物31的制备
向250ml反应瓶中依次加入化合物C-1(5.39g,15mmol)、4-溴苯硼酸(3.61g,18mmol)、磷酸钾(9.55g,45mmol)、碘化亚铜(1.43g,7.5mmol)、乙二胺(1.00ml,15mmol)和甲苯(150ml),回流条件下反应12小时。反应结束后用乙酸乙酯进行萃取,合并有机相,将有机相进行水洗、干燥、浓缩,用甲苯重结晶,得到化合物E-1。质量4.67g,产率65%。
向反应瓶中依次加入化合物E-1(4.31g,9mmol)、化合物D-1(3.81g,7.5mmol)、甲苯(75ml)、乙醇(18.72ml)、碳酸钾溶液(7.5ml,2M)、四三苯基膦钯(43.3mg,0.0375mmol),在氮气保护下回流7小时。反应结束后,冷却至室温,将反应液倒入冷水中,并用二氯甲烷进行萃取,合并有机相,将有机相进行干燥、浓缩后,进行柱层析(硅胶,二氯甲烷:石油醚=2:1),得到化合物31。质量5.56g,产率86%。HPLC检测固体纯度≧99.9%。质谱m/z:861.4424(理论值:861.4335)。理论元素含量(%)C66H55N:C,91.95;H,6.43;N,1.62,实测元素含量(%):C,91.86;H,6.53;N,1.61。上述结果证实获得产物为目标产品。
合成实施例4:化合物53的制备
将合成实施例1中的化合物D-1换成等摩尔的化合物D-2,其他步骤相同,得到化合物53。质量8.00g,产率76%。HPLC检测固体纯度≧99.9%。质谱m/z:841.4731(理论值:841.4648)。理论元素含量(%)C64H59N:C,91.28;H,7.06;N,1.66,实测元素含量(%):C,91.45;H,7.01;N,1.54。上述结果证实获得产物为目标产品。
合成实施例5:化合物80的制备
将合成实施例1中的化合物D-1换成等摩尔的化合物D-3,其他步骤相同,得到化合物80。质量6.71g,产率78%。HPLC检测固体纯度≧99.9%。质谱m/z:687.3017(理论值:687.2926)。理论元素含量(%)C53H37N:C,92.54;H,5.42;N,2.04,实测元素含量(%):C,92.63;H,5.31;N,2.06。上述结果证实获得产物为目标产品。
合成实施例6:化合物184的制备
将合成实施例1中的化合物A-1换成等摩尔的化合物A-2,化合物D-1换成等摩尔的化合物D-3,其他步骤相同,得到化合物184。质量7.44g,产率69%。HPLC检测固体纯度≧99.9%。质谱m/z:861.3482(理论值:861.3396)。理论元素含量(%)C67H43N:C,93.35;H,5.03;N,1.62,实测元素含量(%):C,93.57;H,5.01;N,1.42。1H NMR(600MHz,CDCl3)(δ,ppm):8.20(d,1H),8.07–8.02(m,2H),7.98(d,1H),7.96–7.92(m,1H),7.89(s,1H),7.88–7.81(m,3H),7.78(d,1H),7.76–7.70(m,4H),7.67(s,1H),7.64(s,1H),7.58–7.47(m,7H),7.46–7.42(m,3H),7.41–7.36(m,2H),7.33(s,1H),7.28–7.21(m,6H),7.18–7.14(m,1H),7.12–7.08(m,4H),2.36(s,3H)。上述结果证实获得产物为目标产品。
合成实施例7:化合物194的制备
将合成实施例2中的9,9-二甲基-2-溴芴换成等摩尔的化合物1-溴-9,9-二甲基-9H-芴,其他步骤相同,得到化合物194。质量7.37g,产率75%。HPLC检测固体纯度≧99.9%。质谱m/z:实测值:785.4301(理论值:785.4022)。理论元素含量(%)C60H51N:C,91.68;H,6.54;N,1.78,实测元素含量(%):C,91.72;H,6.69;N,1.59。1H NMR(600MHz,CDCl3)(δ,ppm):8.28(d,1H),8.20–8.17(m,2H),8.06(d,1H),7.99–7.91(m,3H),7.84(d,2H),7.81(d,1H),7.75–7.62(m,9H),7.60–7.56(m,1H),7.51–7.46(m,3H),7.44(t,3H),7.35–7.31(m,1H),1.66(s,6H),1.27(s,18H)。上述结果证实获得产物为目标产品。
合成实施例8:化合物215的制备
向1L反应瓶中加入4-硼酸-9,9-二甲基芴(28.6g,120.0mmol)、2-溴-4-氯-1-硝基苯(23.6g,100.0mmol)、甲苯(250ml)、乙醇(80ml)、碳酸钾溶液(2M,75ml)、四(三苯基膦)钯(1.16g,1.00mmol),在氮气保护的条件下回流6小时。反应结束后,将反应液冷却至室温,过滤,滤液用氯仿进行萃取,蒸干有机相中的溶剂,然后进行柱层析(硅胶,乙酸乙酯),得到化合物b-3。质量24.5g,产率70%。
向500ml反应瓶中加入化合物b-3(21.0g,60mmol)、三苯基膦(47.2g,180mmol)、1,2-二氯苯(300ml),在氮气保护1下回流搅拌10小时。反应结束后,将反应液冷却至室温,过滤,滤液用氯仿进行萃取,蒸干有机相中的溶剂,进行柱层析(硅胶,二氯甲烷),得到化合物B-3。质量11.1g,产率58%。
向500ml反应瓶中依次加入甲苯(69ml)、化合物B-3(7.0g,22.0mmol)、4-联苯硼酸(5.23g,26.4mmol)、乙醇(34ml)、碳酸钾溶液(2M,34.0ml)、四三苯基膦钯(1.27mg,0.0011mmol),在氮气保护下回流4小时,反应结束后将反应液冷却至室温,反应液用水洗,随后用二氯甲烷进行萃取,合并有机相,将有机相进行干燥、浓缩,用甲苯进行重结晶,得到化合物C-5。质量6.42g,产率67%。
在氮气保护下,向500ml反应瓶中,依次加入化合物C-5(6.53g,15.0mmol)、化合物D-1(6.34g,12.5mmol)、叔丁醇钠(3.60g,37.5mmol)、甲苯(190ml)、三二亚苄基丙酮二钯(57.23mg,0.0625mmol)、三叔丁基膦(12.65mg,0.0625mmol),在回流的条件下反应24小时,反应结束后,将反应液冷却至室温。用二氯甲烷萃取反应液,合并有机相,将有机相依次用水洗、干燥、硅藻土过滤,将滤液浓缩,用乙醇重结晶,得到化合物215。质量8.30g,产率77%。HPLC检测固体纯度≧99.9%。质谱m/z:861.4427(理论值:861.4335)。理论元素含量(%)C66H55N:C,91.95;H,6.43;N,1.62,实测元素含量(%):C,91.84;H,6.57;N,1.59。1H NMR(600MHz,CDCl3)(δ,ppm):8.65(s,1H),8.47(d,1H),8.19(s,1H),8.06–8.02(m,2H),7.98(d,1H),7.96–7.90(m,3H),7.89–7.80(m,5H),7.75(d,1H),7.72–7.67(m,3H),7.65(d,2H),7.62–7.57(m,3H),7.53–7.49(m,3H),7.46–7.42(m,4H),7.35–7.31(m,1H),1.75(s,6H),1.27(s,18H)。上述结果证实获得产物为目标产品。
合成实施例9:化合物225的制备
将合成实施例8中的4-硼酸-9,9-二甲基芴换成等摩尔的9,9-二甲基芴-1-硼酸,4-联苯硼酸换成等摩尔的苯硼酸,化合物D-1换成等摩尔的化合物D-3,其他步骤相同,得到化合物225。质量6.36g,产率74%。HPLC检测固体纯度≧99.9%。质谱m/z:687.3014(理论值:687.2926)。理论元素含量(%)C53H37N:C,92.54;H,5.42;N,2.04,实测元素含量(%):C,92.62;H,5.36;N,2.02。1H NMR(600MHz,CDCl3)(δ,ppm):8.28(s,1H),8.18(s,1H),8.08–8.02(m,3H),7.98(d,1H),7.96–7.89(m,3H),7.83(d,1H),7.76–7.71(m,2H),7.68–7.62(m,4H),7.61–7.54(m,4H),7.51–7.46(m,3H),7.46–7.42(m,3H),7.36–7.31(m,1H),7.30–7.27(m,1H),2.36(s,3H),1.80(s,6H)。上述结果证实获得产物为目标产品。
合成实施例10:化合物232的制备
将合成实施例2中的9,9-二甲基-2-溴芴换成等摩尔的4-溴-9,9-二苯基芴,3-氨基-4-氯苯基硼酸频哪醇换成等摩尔的4-氨基-3-氯苯硼酸频那醇酯,其他步骤相同,得到化合物232。质量8.08g,产率71%。HPLC检测固体纯度≧99.9%。质谱m/z:909.4421(理论值:909.4335)。理论元素含量(%)C70H55N:C,92.37;H,6.09;N,1.54,实测元素含量(%):C,92.51;H,6.04;N,1.45。1H NMR(600MHz,CDCl3)(δ,ppm):8.20(d,1H),7.98(d,1H),7.89(s,1H),7.87–7.82(m,2H),7.77–7.69(m,6H),7.67(s,1H),7.62–7.57(m,2H),7.57–7.51(m,2H),7.52–7.46(m,4H),7.47–7.41(m,2H),7.42–7.36(m,1H),7.36–7.29(m,3H),7.28–7.20(m,6H),7.14–7.07(m,5H),1.27(s,18H)。上述结果证实获得产物为目标产品。
合成实施例11:化合物240的制备
将合成实施例1中的苯硼酸换成等摩尔的((1r,3r)-金刚烷-1-基)硼酸,其他步骤相同,得到化合物240。质量8.02g,产率71%。HPLC检测固体纯度≧99.9%。质谱m/z:843.4901(理论值:843.4804)。理论元素含量(%)C64H61N:C,91.06;H,7.28;N,1.66,实测元素含量(%):C,91.10;H,7.26;N,1.64。1H NMR(600MHz,CDCl3)(δ,ppm):8.38(s,1H),8.36(s,1H),8.15(s,1H),8.07–8.00(m,4H),7.94(d,1H),7.84–7.80(m,2H),7.76–7.71(m,2H),7.68–7.63(m,4H),7.61–7.57(m,1H),7.51–7.42(m,4H),7.06(d,1H),2.15–2.03(m,9H),1.91–1.82(m,4H),1.77(s,6H),1.74–1.70(m,2H),1.27(s,18H)。上述结果证实获得产物为目标产品。
器件实施例
有机材料的说明:有机材料都是经过升华,纯度都在99.99%以上。
基板的说明:ITO玻璃基板是从深圳南玻显示器件科技有限公司购买。ITO玻璃基板由5%的玻璃清洗液超声清洗2次,每次20分钟,再由去离子水超声清洗2次,每次10分钟。依次使用丙酮和异丙酮超声清洗20分钟,120℃烘干。
蒸镀系统的说明:器件的制备采用真空蒸镀系统,在真空不间断条件下连续蒸发制备完成。所用材料分别在不同的蒸发源石英坩埚中,蒸发源的温度可以单独控制。有机材料或掺杂母体有机材料的热蒸发速率一般定在0.1nm/s,掺杂材料蒸发速率调节按掺杂比率进行;电极金属蒸发速率在0.4~0.6nm/s。将处理好的玻璃基板放置到OLED真空镀膜机中,在薄膜制作过程中,系统真空度应该维持在5×10-5Pa以下,通过更换掩膜板分别来蒸镀有机层和金属电极,用Inficon的SQM160石英晶体膜厚检测仪检测蒸镀速度,用石英晶体振荡器检测薄膜厚度。
测试系统的说明:将测试软件、计算机、美国Keithley公司生产的K2400数字源表和美国Photo Research公司的PR788光谱扫描亮度计组成一个联合IVL测试系统来测试有机电致发光器件的驱动电压、发光效率、使用寿命、色坐标。
实施例1:有机电致发光器件1的制备
在玻璃基板上以ITO作为阳极;在阳极上真空蒸镀本发明的化合物1作为空穴传输层,蒸镀厚度为30nm;在空穴传输层上真空蒸镀CBP:Ir(ppy)3(95:5)作为发光层,蒸镀厚度为30nm;在发光层上真空蒸镀Bphen作为空穴阻挡层,蒸镀厚度为10nm;在空穴阻挡层上真空蒸镀Bphen作为电子传输层,蒸镀厚度为30nm;在电子传输层上真空蒸镀LiF作为电子注入层,蒸镀厚度为1nm;在电子注入层上真空蒸镀Al作为阴极,蒸镀厚度为100nm。
上述器件结构为:ITO/化合物1,30nm/CBP:Ir(ppy)3(95:5),30nm/Bphen,10nm/Bphen,30nm/LiF,1nm/Al,100nm
实施例2~31:有机电致发光器件2~31的制备
将实施例1空穴传输层中的化合物1分别换成化合物1、化合物2、化合物6、化合物12、化合物19、化合物26、化合物31、化合物36、化合物39、化合物40、化合物46、化合物51、化合物53、化合物61、化合物65、化合物73、化合物80、化合物94、化合物98、化合物111、化合物120、化合物123、化合物136、化合物148、化合物151、化合物184、化合物194、化合物215、化合物225、化合物232、化合物240,其他步骤相同,得到有机电致发光器件2~31。
比较例1~2:对比有机电致发光器件1~2的制备
将实施例1空穴传输层中的化合物1分别换成NPB、R-1,其他步骤相同,得到对比有机电致发光器件1~2。
本发明实施例1~31以及对比例1~2制备的有机电致发光器件的发光特性测试结果如表1所示。
表1有机电致发光器件的发光特性测试数据
从表1中可以看出,本发明的有机电致发光器件的驱动电压、发光效率以及使用寿命要比对比有机电致发光器件1~2的要高。这是由于相比于NPB或者R-1,本发明式I的含有螺二芴的衍生物具有更加合适的HOMO能级,即其HOMO能级与阳极以及发光层的更加匹配,空穴注入势垒较低,空穴能够有效的注入到发光层内实现空穴与电子的有效复合,因此空穴传输层含有本发明式I的衍生物的器件的驱动电压更低、发光效率更高。另外,由于本发明式I的含有螺二芴的衍生物具有较好的稳定性,因此含有本发明衍生物的器件的使用寿命较长。尤其是结构中含有叔丁基、异丙基、乙基、甲基、金刚烷基等烷基或者氘的化合物其稳定性要高于不含烷基和氘的化合物,器件的使用寿命也相对较长。
Claims (5)
1.一种含有螺二芴的衍生物,其特征在于,具有如I-1~I-6所示的结构通式,
其中,所述R0选自甲基、苯基中的一种;
所述m选自0~4中的整数,所述n选自0~3中的整数,所述k选自0~2中的整数,所述R选自氢、氘、甲基、异丙基、叔丁基中的一种,每个R相同或者不同,所述R'选自氢、氘中的一种,每个R'相同或者不同;当R选自甲基、异丙基或叔丁基时,(R)m中的m选自0或1;
所述L选自单键或者如下所示基团中的一种,
所述L1选自单键或者亚苯基;
所述Ar0选自如下所示基团中的一种,
所述p选自0~5中的整数,所述q选自0~7中的整数,所述m选自0~4中的整数,所述R1选自氢、氘中的一种,每个R1相同或者不同;所述R1'选自氢、氘、甲基、异丙基、叔丁基中的一种,每个R1'相同或者不同,当R1'选自甲基、异丙基、叔丁基时,(R1')p中的p选自1。
4.一种有机电致发光器件,其特征在于,依次包括阳极、有机物层、阴极,所述有机物层含有上述权利要求1~3任一项所述的含有螺二芴的衍生物。
5.根据权利要求4所述的一种有机电致发光器件,其特征在于,所述有机物层包括空穴传输层,所述空穴传输层含有权利要求1~3任一项所述的含有螺二芴的衍生物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010889585.2A CN111848493B (zh) | 2020-08-28 | 2020-08-28 | 一种含有螺二芴的衍生物及其有机电致发光器件 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202010889585.2A CN111848493B (zh) | 2020-08-28 | 2020-08-28 | 一种含有螺二芴的衍生物及其有机电致发光器件 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN111848493A CN111848493A (zh) | 2020-10-30 |
| CN111848493B true CN111848493B (zh) | 2022-10-14 |
Family
ID=72967321
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202010889585.2A Active CN111848493B (zh) | 2020-08-28 | 2020-08-28 | 一种含有螺二芴的衍生物及其有机电致发光器件 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN111848493B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114573592B (zh) * | 2022-02-06 | 2023-07-18 | 上海传勤新材料有限公司 | 一种含有螺吲哚和芳香胺的化合物及其制备方法和应用 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101832171B1 (ko) * | 2010-10-25 | 2018-04-16 | 삼성디스플레이 주식회사 | 축합환 화합물, 이를 포함한 유기 발광 소자 및 상기 유기 발광 소자를 포함한 평판 표시 장치 |
| KR20130084093A (ko) * | 2012-01-16 | 2013-07-24 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| KR102357439B1 (ko) * | 2012-02-14 | 2022-02-08 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 스피로비플루오렌 화합물 |
| KR20130127563A (ko) * | 2012-05-02 | 2013-11-25 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| CN107868090A (zh) * | 2016-09-28 | 2018-04-03 | 江苏三月光电科技有限公司 | 含有9,9’‑螺二芴的有机化合物及有机发光电致器件 |
| CN107868031A (zh) * | 2016-09-28 | 2018-04-03 | 江苏三月光电科技有限公司 | 一种以9,9’‑螺二芴为核心的有机化合物及其在有机电致发光器件上的应用 |
| TW201920070A (zh) * | 2017-06-28 | 2019-06-01 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| TWI779067B (zh) * | 2017-07-28 | 2022-10-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| CN110416422B (zh) * | 2018-04-28 | 2021-06-15 | 江苏三月科技股份有限公司 | 有机电致发光器件及包括其的显示器 |
| CN110551135A (zh) * | 2018-05-31 | 2019-12-10 | 江苏三月光电科技有限公司 | 一种含有氮杂五元并环的化合物及其在有机电致发光器件上的应用 |
| KR102322698B1 (ko) * | 2018-06-22 | 2021-11-09 | 엘티소재주식회사 | 헤테로고리 화합물, 이를 포함하는 유기 발광 소자, 유기 발광 소자의 유기물층용 조성물 및 유기 발광 소자의 제조 방법 |
| CN111377848A (zh) * | 2018-12-29 | 2020-07-07 | 江苏三月光电科技有限公司 | 一种以芴为核心的有机化合物及其制备方法和其应用 |
-
2020
- 2020-08-28 CN CN202010889585.2A patent/CN111848493B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN111848493A (zh) | 2020-10-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN112961147B (zh) | 一种含氮化合物及其有机电致发光器件 | |
| CN112661714B (zh) | 一种杂环化合物和包含该杂环化合物的有机电致发光器件 | |
| CN110256358B (zh) | 一种胺类衍生物及其有机电致发光器件 | |
| TWI608075B (zh) | 苯并吲哚并咔唑衍生物及使用其的發光元件材料及發光元件 | |
| CN115974806B (zh) | 一种杂环化合物及其有机电致发光器件 | |
| CN112341449A (zh) | 一种含螺芴的三芳胺类有机化合物及其有机发光器件 | |
| CN112028853B (zh) | 一种芳胺衍生物及其有机电致发光器件 | |
| CN113698340B (zh) | 一种咔唑衍生物及其有机电致发光器件 | |
| CN113735780B (zh) | 一种苯并五元杂环衍生物及其有机电致发光器件 | |
| CN114989021A (zh) | 一种含芴的三芳胺衍生物及其有机电致发光器件 | |
| CN116891477B (zh) | 一种吲哚并咔唑化合物及其有机电致发光器件 | |
| CN111606812B (zh) | 一种三芳胺衍生物及其有机电致发光器件 | |
| CN111808127B (zh) | 化合物、显示面板以及显示装置 | |
| CN114105891A (zh) | 一种芴衍生物及其有机电致发光器件 | |
| CN116903603A (zh) | 一种含有三嗪的杂环化合物及其有机电致发光器件 | |
| CN114656434B (zh) | 一种四胺化合物及其有机电致发光器件 | |
| CN114394949A (zh) | 一种联苯胺衍生物及其有机电致发光器件 | |
| CN111848493B (zh) | 一种含有螺二芴的衍生物及其有机电致发光器件 | |
| CN115835671B (zh) | 一种有机电致发光器件 | |
| CN111785849B (zh) | 一种含有覆盖层的顶发射有机电致发光器件 | |
| CN117126190A (zh) | 一种三芳胺衍生物及其有机电致发光器件 | |
| CN116554217A (zh) | 一种稠杂环化合物及其有机电致发光器件 | |
| CN117050103A (zh) | 一种杂环化合物及其有机电致发光器件 | |
| CN116903600A (zh) | 一种稠环化合物及其有机电致发光器件 | |
| CN117164574A (zh) | 一种含氮稠芳环的化合物及其有机电致发光器件 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| CB02 | Change of applicant information |
Address after: 130000 A5, North Lake Science and Technology Park, 3333 North Sheng street, Beihu science and Technology Development Zone, Jilin, Changchun Applicant after: Changchun hiprunsi Technology Co.,Ltd. Address before: 130000 A5, North Lake Science and Technology Park, 3333 North Sheng street, Beihu science and Technology Development Zone, Jilin, Changchun Applicant before: Changchun Hyperions Scientific Co.,Ltd. |
|
| CB02 | Change of applicant information | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |