WO2017095267A1 - Bispecific antibodies against cd3*cd19 - Google Patents
Bispecific antibodies against cd3*cd19 Download PDFInfo
- Publication number
- WO2017095267A1 WO2017095267A1 PCT/RU2016/000827 RU2016000827W WO2017095267A1 WO 2017095267 A1 WO2017095267 A1 WO 2017095267A1 RU 2016000827 W RU2016000827 W RU 2016000827W WO 2017095267 A1 WO2017095267 A1 WO 2017095267A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- cell
- lymphoma
- antibody
- cells
- leukemia
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
Definitions
- the invention relates to biotechnology and, in particular, can be used in medicine and the pharmaceutical industry for the manufacture of a medicament for the treatment of B-cell disease, depletion of B-cells or slowing the development of a pathological condition associated with B-cell disorders.
- Bispecific antibodies (BAPs) against CD3 * CD19 are currently being developed primarily for the treatment of malignant diseases of B cells or depletion of B cells, including non-Hodgkin’s lymphoma (WO2010037835, RU2228202), B-cell leukemia (RU2008129080), and acute lymphoblastic childhood leukemia (WO20100052013) H T.fl.
- BAPs act as adapters that physically connect T cells with tumor cells and trigger a powerful signaling cascade of the T-cell receptor complex by binding to the invariant component of the CD3 T-cell receptor.
- the second (target) antigen-specific fragment recognizes CD 19, i.e. BAP can connect a T cell and a cancer cell by simultaneously binding to CD3 and the target antigen.
- the activation and proliferation of T cells, the formation of a cytolytic synapse with the release of cytotoxic granules, and the secretion of cytokines occur.
- Targeted lysis of cancer cells includes perforation of the target cell membrane involving perforin and subsequent granzyme-induced apoptosis. It should be noted that after binding to T cells, BAPs recognize antigens on the surface of the cancer cell in the same way as conventional monospecific antibodies. Thus, it is possible to redirect cytotoxic function of T cells against tumor cells, and BAP activity is already observed at relatively low (picomolar) concentrations. Binding of BAT only to a T cell in the absence of a target cell does not cause T cell activation.
- bispecific antibodies known from the prior art (Blood, (ASH Annual Meeting Abstracts), 2009, 114: 840) indicate that the effective therapeutic concentration of drugs derived from the use of multivalent antibodies is significantly lower compared to classic anti-cancer antibodies drugs. This contributes to good tolerance, the possibility of implementing long-term courses of treatment and reducing the risk of side effects. In addition, the required volume and production cost of bespecifically antibodies is lower. Therefore, the creation of such antibodies will significantly reduce the scale and cost of producing drugs based on them and, most importantly, make these drugs available to all patients in need of such therapy.
- Blinatumomab consists of two domains: the anti-C019 scFv domain from the HD37 hybridoma and the anra-CD3 scFv domain from the OKTZ hybridoma. To obtain the antibody, the VLCD 19-VHCD 19-VHCD3-VLCD3 DNA fragment is expressed in DHFR-negative CHO cells (patent RU2228202).
- Blinatumomab in comparison with full-sized antibodies, has a relatively small molecular weight (55 kDa versus 155 kDa), which is why it is rapidly eliminated from the bloodstream. Therefore, to achieve stable concentrations of the drug in the blood, continuous intravenous administration of the drug is used for 2-4 weeks per cycle (in a two-week regimen - an dropper, two weeks - a break), which is quite difficult for the patient to tolerate.
- BiTE® antibodies demonstrate high efficacy of redirected lysis of cells expressing the tumor target antigen.
- EC50 values for BiTE® antibodies generally range from 0.1 to 50 pM (Bauerle P.A. and Reinhardt C. (2009) Cancer Res. 69 (12), pp. 4941-4944). Powerful cytolysis of tumor cells is necessary in order to cause a pharmacologically desired effect.
- Rader C Rader C.
- BiTE® format reports that the powerful lytic ability of the BiTE® format is explained by (1) its small size, which brings the target and effector cells in close proximity, allowing the formation of cytolytic synapses, and (2) its monovalent involvement of the TCR complex, which prevents systemic activation of effector cells in the absence of target cells (Rader C. (2011), Blood, 117 (17), pp. 4403-4404).
- the prior art describes that the BiTE® class of bispecific antibodies typically has 100-10000 times higher tumor cell lysis efficiencies relative to other bispecific formats and full IgGl monoclonal antibodies (Wolf et al. (2005) Drug Discov Today 10 ( 18), pp. 1237-1244).
- the present invention solves the problem of obtaining a bivalent antibody against CD3 * CD19, convenient to use and obtain compared with blinatumomab and at the same time highly effective in treating malignant diseases of B cells, depletion of B cells or slowing the development of pathological conditions associated with B- cellular disorders.
- bispecific molecules in comparison with the blinatumomab antibody (MT-103), are characterized by an increased half-life and are easy to obtain.
- properties of the indicated antibody as enhanced cytotoxic effect and high bioavailability even with subcutaneous administration at the level of 60% were even more unexpected for the team of authors.
- the latter characteristic is especially important, since until now, due to the low bioavailability, antibody preparations have been administered mainly via the intravenous route, which is more complex and less comfortable for the patient.
- the increased half-life, high efficiency and bioavailability with subcutaneous administration will reduce the frequency of administration of the drug and increase the convenience of its use.
- the first object of the present invention is a recombinant monoclonal bispecific anti-CD3 * CD19 antibody comprising two disulfide-linked chains, each of which consists of the following domains: VL (CD3) -Ll-VH (CD19) -L2-VL (CD19 ) -L3-VH (CD3) -H-CH2-CH3 (IgG), where VL (CD3), VL (CD19), VH (CD3) and VH (CD19) are the variable domains of the light and heavy chains of antibodies against CD3 and CD 19, respectively, LI, L2, L3 are linker sequences, H is the hinge region of IgG immunoglobulin and CH2-CH3 (IgG) is the constant region of the Ig immunoglobulin Fc domain G.
- said constant region of the IgG immunoglobulin Fc domain is preferably a constant region of the IgG2 immunoglobulin Fc domain and contains the sequence shown in SEQ ID NO: 5.
- the linker sequences LI, L2, L3 preferably have a length of 5-15 amino acids and have sequences according to essentially corresponding to the sequences presented in SEQ ID NO: 6, 7, 8, respectively.
- the hinge region of the IgG immunoglobulin essentially corresponds to the sequence shown in SEQ ID NO: 9.
- the specified antibody preferably has a half-life in blood, increased compared with the half-life of pancreatitis, measured in essentially similar conditions. Moreover, the half-life in blood of an antibody of the invention may be more than 40 hours. Moreover, the specified antibody preferably, but not necessarily has an amino acid sequence essentially corresponding to the sequence presented in SEQ ID NO: 10.
- the following objects of the present invention are a nucleic acid encoding a chain sequence of the specified bispecific anti-CD3 * CD19 antibody of the invention, and a vector containing it.
- the vector may be a vector for expressing a bispecific anti-CD3 * CD19 antibody in a host cell of the invention, comprising the aforementioned nucleic acid operably linked to nucleotide sequences enabling heterologous expression in the host cell.
- the specified vector may be a cloning vector containing the above nucleic acid, and flanking its restriction sites, allowing you to cut the specified nucleic acid using suitable restriction enzymes.
- the vector is an expression plasmid pRA1451 characterized by the following features:
- Accl 6490 IO
- Agel 460 IO
- Apal 995 IO
- BmgBI 3270 IO
- Bsml 7269 IO
- EcoRV 6457 i. O.
- Hindlll 1590 I.O.
- Notl 11146 I.O.
- Pfol 11021 I.O.
- Pmll 5699 I.O.
- Spel 4622 I.O.
- Swal 6466 acting
- Tthl 111 10585 acting).
- Another object of the present invention is a host cell containing a nucleic acid of the invention or a vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention in a host cell.
- the specified cell can be both prokaryotic and eukaryotic cells.
- said cell may be a mammalian cell, in particular a Chinese hamster cell.
- a further object of the present invention is a method for producing a bispecific anti-CD3 * CD19 antibody of the invention, comprising at least culturing a host cell of the invention under conditions that express the anti-CD3 * CD1 antibody of the invention and isolating the resulting product.
- Another object of the present invention is a method for purifying an anti-CD3 * CD19 antibody of the invention, comprising at least one chromatography step under conditions providing a preparation of an anti-CD3 * CD19 antibody of the invention, substantially free of host cell impurities.
- the specified method may further include a centrifugation step, preferably performed before the chromatography step, and another chromatography step.
- the first chromatography step is preferably, but not necessarily, performed using a protein A sorbent
- the second chromatography step is a cation exchange chromatography step.
- the next object of the present invention is the use of antibodies against CD3 * CD19 according to the invention for the treatment of b-cell diseases, depletion of b-cells or slow the development of pathological conditions associated with b-cell disorders.
- Said use comprises administering an antibody of the invention to a patient preferably, but not necessarily intravenously or subcutaneously.
- the antibody is administered to the patient in a therapeutically effective amount.
- Another object of the invention is a pharmaceutical composition for treating B-cell disease, depleting B-cells or slowing down the development of pathological conditions associated with B-cell disorders, comprising, as an active component, an anti-CD3 * CD19 antibody of the invention in a therapeutically effective amount and a pharmaceutically acceptable carrier.
- the next object of the present invention is a method of treating B-cell disease, depletion of B-cells or slowing the development of pathological conditions associated with B-cell disorders, comprising administering to a patient in need thereof an effective dose of an anti-CD3 * CD19 antibody of the invention, or an effective amount pharmaceutical compositions of the invention.
- B-lymphoblastic lymphoma B-cell acute lymphoblastic leukemia from progenitor cells
- B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT-type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma; mantle cell lymphoma; diffuse B-large cell lymphoma; media
- FIG. 1 Schematic representation of the construction of antibodies GNR-047
- FIG. 2. The design scheme of the expression vector
- FIG. 3 Map of expression vector pRA1451
- FIG. 4 Analysis of the ability of the GNR-047 antibody and MT-103 antibody to bind the native CD3 receptor on the Jurkat cell line and CD 19 receptor on the Raji cell line
- FIG. 5a Study of the pharmacokinetic characteristics of the GNR-047 antibody when administered intravenously at a dose of 0.5 mg / kg
- FIG. 56 The study of the pharmacokinetic characteristics of the MT-103 antibody when administered intravenously at a dose of 0.5 mg / kg
- FIG. 6a A study of the pharmacokinetic characteristics of the GNR-047 antibody when administered subcutaneously at a dose of 2.0 mg / kg
- FIG. 66 A study of the pharmacokinetic characteristics of the MT-103 antibody when administered subcutaneously at a dose of 2.0 mg / kg
- FIG. 7. Change in the average tumor volume during the study
- recombinant monoclonal bispecific anti-CD3 * CD19 antibody used in accordance with the present invention includes antibodies that specifically bind to both CD3 and CD 19, which are obtained using recombinant technologies.
- Antibody against CD3 * CD19 can be obtained on the basis of murine and / or human sequences and / or camel sequences and / or llama sequences and / or other suitable sequences, including artificial ones, including those created by modification of mouse and / or human sequences, for example, through the introduction of mutations.
- the anti-CD3 * CD19 antibody of the invention is chimeric. More preferably, the anti-CD3 * CD19 antibody of the invention is fully human.
- the recombinant monoclonal bispecific anti-CD3 * CD19 antibody of the invention contains the variable domains of the light and heavy chains of the anti-CD3 antibody, the variable domains of the light and heavy chains of the anti-CD 19 antibody, the linker sequence, the hinge region, the Fc sequence and has two chains connected by disulfide bonds .
- each chain preferably has the following structure: VL (CD3) -L1-VH (CD19) -L2-VL (CD19) -L3-VH (CD3) -H-CH2-
- VL (CD3), VL (CD19), VH (CD3) and VH (CD19) are the variable domains of the light and heavy chains of antibodies against CD3 and CD 19, respectively;
- LI, L2, L3 linker sequences
- H is a hinge region immunoglobulin IgG
- CH2-CH3 (IgG) is a constant region of the Fc domain of an IgG immunoglobulin.
- AHTH-CD3 antibodies are well known in the art.
- anti-POP antibodies include, but are not limited to, OKTZ, G4.18, 145-2C11, Leu4, NGH3, SCZ, SK7, SP34, RIV-9, and UCHT1.
- the anti-POP antibody binds to the same epitopes as OCTZ, G4.18, 145-2C11, Leu4, NGH3a, SCZ, SK7, SP34, RIV-9 and UCHT1.
- One of ordinary skill in the art can obtain additional anti-CD3 antibodies without undue experimentation and, inter alia, determine whether antibodies to the same epitopes are specific as anti-POP antibodies OKTZ, G4.18, 145-2C11, Leu4, NGGZa, VSZ , SK7, SP34, RTV-9, and UCHT1, finding out if the former prevent the binding of the latter to the CD3 antigenic polypeptide.
- variable domains of the anti-CD3 antibody light and heavy chains exhibiting high specificity and binding affinity for the CD3 antigenic polypeptide can be used within the scope of the present invention.
- AHTH-CD19 antibodies are also well known in the art, as are methods for their preparation.
- anti-C019 antibodies include, but are not limited to, HD37, HIB19, SJ25-C1, 4G7-2E3.
- these methods and antibodies are disclosed in Eurasian application EA200800094, published June 30, 2008.
- any variable domains of the anti-CD 19 antibody light and heavy chains that exhibit high specificity and binding strength to the CD 19 antigenic polypeptide can be used within the scope of the present invention. However, it is most preferred to use the variable light and heavy chain domains of the antibody in accordance with the present invention.
- anti-CD19 VL (CD3) and VH (CD3) characterized by the sequences shown in SEQ ID NO: 3 and SEQ ID NO: 4.
- Fc sequence is a term well known to those skilled in the art — this is the terminal portion of an immunoglobulin molecule that interacts with the Fc receptor on the cell surface and with some proteins of the complement system.
- immunoglobulins are divided into classes: IgA, IgD, IgE, IgG and IgM, and some of them can be further divided into subclasses (isotypes), for example, IgGl, IgG2, IgG3 and IgG4, IgAl and IgA2.
- the various classes of immunoglobulins are called [alpha], [delta], [epsilon], [gamma] and [mu], respectively.
- Four isotypes of human IgG bind various receptors, such as the neonatal Fc receptor, activating gamma Fc receptors, FcgRI, FcgRIIa and FcgRIIIa, inhibiting the FcgRIIb receptor and Clq with different affinities, obtaining different types of activity.
- the term "Fc sequence" in the framework of the present invention refers, inter alia, to Fc sequences modified to change the affinity for the corresponding receptor.
- the antibody of the present invention contains an Fc portion to extend the half-life.
- Such an Fc sequence is preferably of human origin, more preferably is the human Fc sequence of an IgG antibody, more preferably IgG2, even more preferably, is the sequence shown in SEQ ID NO: 5.
- the selection of an IgG2-type Fc sequence allows one to reduce the effector load due to the Fc sequence and thus reduce the directed toxicity of the antibody of the invention.
- linker refers to peptide linkers.
- the length and / or sequence of the linker affects the stability and / or solubility of the bispecific molecule.
- the linker can increase the flexibility of the resulting binding molecule and / or can improve its binding to the target antigen by reducing steric interference.
- the length and sequence of the linker depends on the sequence and length of the linked sequences. Methods for testing the suitability of various linkers are well known to the skilled person. For example, the properties of a binding molecule can be easily tested by analyzing its binding affinity using various types of linkers.
- the stability of the obtained molecule can be measured by methods known in the art, such as, for example, high-performance liquid chromatography, dividing the studied protein material into fractions, depending on the molecular weight of the protein and hydrodynamic characteristics.
- Linkers that are peptides consisting of at least 50%, at least 60%, at least 70%, at least 80%, at least 90%, or 100% of small amino acids, such as glycine, series and alanine. Linkers consisting solely of glycine and serine molecules are particularly preferred. Yu Preferably, the linker sequences of the invention are comprised of 5-15 amino acids. More preferably, the LI, L2, L3 linkers of the anti-CD3 * CD19 antibody of the invention are selected from the following sequences:
- hinge region refers to a sequence that in a natural immunoglobulin binds the CH1 domain to the region of the CH2-CH3 Fc fragment.
- the hinge region used in the antibody of the invention is preferably homologous to the natural region of the immunoglobulin and typically includes cysteine residues linking the two heavy chains via disulfide bonds, as in natural immunoglobulins.
- Typical hinge sequences of human and mouse immunoglobulins can be found in ANTIBODY ENGINEERING, a PRACTICAL GUIDE, (Borrebaeck, ed., W. H. Freeman and Co., 1992).
- Suitable hinge regions of the present invention may be derived from IgGl, IgG2, IgG3, IgG4 and other immunoglobulin isotypes. Most preferably, the IgGl hinge region with the sequence shown in SEQ ID NO: 9 is used in the antibody construct of the invention.
- variable regions in the construction of the antibody of the invention is of principle principle.
- the authors carried out work to assess in vitro toxicity for the release of pro-inflammatory cytokines and CD3-mediated antibody cytotoxicity against CD 19+ tumor cells (hereinafter, cytotoxic biological activity) of various variants of the bispecific BiMS format antibody:
- VH (CD3) -Ll-VH (CD19) -L2-VL (CD19) -L3-VL (CD3) -H-CH2-CH3 (IgG),
- an anti-CD3 * CD19 antibody is characterized by the sequence of SEQ ID NO: 10.
- the anti-CD3 * CD19 antibody of the invention is encoded by a nucleic acid, the structure of which can be derived by methods known in the art from the structure of the indicated antibody.
- the nucleic acid of the invention has a nucleotide sequence deduced from the amino acid sequence shown in SEQ ID NO: 10.
- the codon composition of the nucleic acid sequence of the invention is selected so that in the selected host cell maximum levels of its transcription and subsequent translation were achieved.
- the term "nucleic acid" as used in accordance with the present invention preferably refers to DNA. However, this term may also refer to RNA.
- the host cell may comprise a nucleic acid sequence of the invention stably integrated into the cellular genome.
- the host cell comprises a nucleic acid sequence of the invention operably integrated for expression in a vector type construct for expression or a linear expression element.
- expression of an anti-CD3 * CD19 antibody of the invention in a host cell is provided using a vector for expression.
- expression vector refers to any suitable vector, including chromosomal, extrachromosomal vectors and synthetic nucleic acid vectors containing a suitable set of expression control elements.
- the vector for expressing the bispecific anti-CD3 * CD19 antibody of the invention is preferably constructed to allow expression of the nucleic acid of the invention in mammalian cells.
- the specified vector without limitation can also be constructed to ensure expression of the nucleic acid according to the invention in the cells of plants, bacteria, yeast, animals other than mammals.
- examples of such vectors include derivatives of SV40, bacterial plasmids, phage DNA, baculoviruses, yeast plasmids, vectors derived from combinations of plasmids and phage DNA, and vectors from viral nucleic acid (RNA or DNA).
- Suitable immunoglobulin expression vectors are also disclosed, for example, in McLean et al., Mol. Immunol.
- a vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention may simultaneously be a cloning vector and have the ability to autonomously replicate in bacterial, yeast and other cells, and also be suitable for the production of a nucleic acid encoding an anti-CD3 * CD19 antibody of the invention, by treating said cloning vector with suitable restriction enzymes.
- the cloning vector containing a nucleic acid encoding an anti-CD3 * CD19 antibody of the invention does not additionally contain elements for expressing said nucleic acid to enhance its amplification in the host cell.
- the expression vector is a vector that is suitable for expression of an antibody in bacterial cells.
- examples of such vectors include BlueScript vectors (Stratagene), pIN vectors, pET vectors (Novagen, Madison WI), and others.
- the expression vector is a vector that is suitable for expression in the yeast system.
- Suitable vectors include, for example, vectors containing constitutive or inducible promoters such as alpha factor, alcohol oxidase and PGH.
- the expression vector is a vector that is suitable for expression of an antibody in a plant. Suitable vectors include, for example, vectors disclosed in RF patent RU2412251, published on 02.20.2011.
- the expression vector is a vector that is suitable for expression of an antibody in an insect.
- Suitable vectors include, for example, vectors disclosed in international application publication number WO 2010/025764 of 03/11/2010.
- the expression vector is a vector that is suitable for expression of the antibody in Chinese hamster cells.
- the nucleic acid encoding the antibody of the invention may be coupled to any suitable promoter, enhancer and other expression promoting elements. Moreover, these elements are selected based on the type of host cell.
- replication initiation site from plasmid pBR322 (Product No. 303-3s, New England Biolabs, Beverly, Mass) is applicable to most gram-negative bacteria, while the different replication initiation sites are from SV40, polyomavirus, adenovirus, and vesicular stomatitis virus (VSV) or papillomaviruses (such as HPV or BPV) can be used to clone vectors in mammalian cells.
- VSV vesicular stomatitis virus
- HPV or BPV papillomaviruses
- the transcription termination sequence is usually located 3 '(to the right) from the end of the coding regions of the polypeptide and serves to terminate the transcription. Transcription termination sequences in prokaryotic cells often contain a G-C-rich fragment, followed by a poly T-sequence. Transcription termination sequences can be cloned from a library purchased commercially as part of a vector.
- a selectable marker gene element encodes a protein necessary for the survival and growth of a host cell grown in a selective culture medium.
- Conventional selectable marker genes encode proteins that (a) confer resistance to antibiotics or other toxins, for example, ampicillin, tetracycline or kanamycin for prokaryotic host cells, (b) supplement auxotrophic cell deficiencies; or (c) supply the necessary nutrients.
- Preferred breeding markers are the kanamycin resistance gene, the ampicillin resistance gene, and the gene resistance to tetracycline.
- the neomycin resistance gene can also be used for selection in prokaryotic and eukaryotic host cells.
- Examples of breeding markers for mammalian cells include dihydrofolate reductase (DHFR) and thymidine kinase.
- DHFR dihydrofolate reductase
- Mammalian cell transformants are placed under selection pressure conditions, to which only transformants are adapted for survival, due to the marker present in the vector.
- the selection pressure is superimposed by culturing the transformed cells under conditions in which the concentration of the selection agent in the medium changes sequentially, which leads to amplification of both the selection gene and the target nucleic acid encoding the antibody of the invention.
- the amount of nucleic acid encoding the antibody of the invention amplified in this way will produce increased amounts of the antibody.
- the ribosome binding site is usually present to initiate translation of mRNA.
- a site is characterized by a Shine-Dalgarno sequence (prokaryotes) or a Kozak sequence (eukaryotes). This element is usually located 3 '(right) from the promoter and 5' (left) from the coding sequence of the expressed polypeptide.
- the Shine-Dalgarno sequence varies, but is usually polypurine (having a high A-G content). Many Shine-Dalgarno sequences have been identified, each of which can be easily synthesized using the methods presented above and used in the prokaryotic vector.
- An enhancer sequence can be inserted into a vector to increase transcription in eukaryotic host cells.
- enhancer sequences of mammalian genes are known (e.g., globin, elastase, albumin, alpha-fetoprotein and insulin). However, usually a virus enhancer should be used.
- the SV40 enhancer, cytomegalovirus early promoter enhancer, polyomavirus enhancer and adenovirus enhancers are examples of enhancer elements for activating eukaryotic promoters.
- the components of the vector can be homologous (from the same species and / or strain as the host cell), heterologous (from a species other than the species or strain of the host cell), hybrid (a combination of different sequences from more than one source ), synthetic or native sequences that typically act as regulators of immunoglobulin expression.
- the sources of the components of the vector can be any prokaryotic or eukaryotic organism, any a vertebrate or invertebrate organism, or any plant, provided that these components are functional in the mechanism of the host cell and can be activated by the mechanism of the host cell.
- the vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention is a vector for providing heterologous expression in Chinese hamster cells (CHO).
- a vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention may further comprise a nucleic acid sequence encoding a secretion / localization sequence that can direct the polypeptide into the periplasmic space or into the culture medium.
- sequences are known in the art and include secretion leaders or signal peptides, organelle targeting sequences (e.g., nuclear localization sequences, ER retention signals, mitochondrial transit sequences, chloroplast transit sequences), membrane localization / anchor sequences (e.g. stop sequences translocations, GPI anchor sequences), etc., which are well known in the field of the present invention.
- Recombinant expression of an anti-CD3 * CD19 antibody of the invention can be carried out in any suitable host cells known in the art. Moreover, the conditions for expression are selected individually for the type of the host cell and the elements used for heterologous expression.
- a host cell of the invention may be eukaryotic and prokaryotic.
- a prokaryotic host cell may be, inter alia, a bacterial cell.
- the eukaryotic host cell may be, inter alia, a yeast cell, a mammalian cell, a non-mammalian animal cell, for example, an insect cell, a plant cell.
- eukaryotic host cells of the present invention may be CHO cells, HEK-293 cells, HEK-294 cells, PER.C6 cells, NS0 cells and lymphocyte cells, as well as prokaryotic cells such as E. coli.
- Some embodiments of the present invention include the introduction of a vector to allow expression of the invention in an in vivo host cell, i.e. into a cell that is part of a living multicellular organism.
- the specified organism is preferably a person.
- expression host / vector combinations for expression can be used to express the antibody.
- a vector taking into account the preservation of its functionality in the host cell in which the specified vector will be introduced.
- the vector must be compatible with the mechanism of the host cell, so that amplification and expression are possible.
- expression vectors suitable for eukaryotic hosts include SV40, cattle papilloma virus, adenovirus, adeno-associated virus, cytomegalovirus and retrovirus.
- Expression vectors that can be used in bacterial hosts include bacterial plasmids such as pBluescript, pGEX2T, pUC, pCRl, pBR322, pMB9 and their derivatives, plasmids like RP4, characterized by a wide list of possible hosts, gtlO and ⁇ 1, phage DNA, represented by various lambda phage derivatives, such as ⁇ 989, and other phage DNAs, such as M13 and single-stranded filamentous phage.
- Expression vectors that can be used with yeast cells include plasmid 2 ⁇ and its derivatives.
- a vector that can be used in insect cells is pVL941.
- a vector combination is used to provide heterologous expression in Chinese hamster cells with cells of a commercially available CHO-M strain (Selexis).
- a host cell expressing a bispecific anti-CD3 * CD19 antibody of the invention can be obtained by transfection of a parent cell with a vector to allow expression of a bispecific anti-CD3 * CD19 antibody of the invention using any method known in the art, including electroporation, transduction, calcium -phosphate transfection, transfection with cationic lipids, scrape-loading (scraping load) and infection.
- a method for producing an anti-CD3 * CD19 antibody of the invention comprises culturing said host cell under conditions providing expression of a bispecific anti-CD3 * CD19 antibody of the invention and isolating the resulting product. Moreover, this expression can be carried out both under conditions of a small-scale or large-scale fermenter, and under incubation conditions in flasks, on a rocking chair. Incubation is carried out in a suitable nutrient medium containing sources of carbon and nitrogen and inorganic salts, one of the known methods. Suitable media are commercially available, but can also be prepared independently using components described, for example, in the catalog of the American Type Culture Collection (ATCC).
- ATCC American Type Culture Collection
- the term “medium” as used in accordance with the present invention includes any culture medium, solution, solid, semi-solid or solid support that can support or contain any host cell, including bacterial host cells, yeast host cells, cells - insect hosts, plant host cells, mammalian host cells, including CHO cells.
- An antibody of the invention may be isolated by any method known in the art. However, when choosing a method for isolating the antibody, it is necessary to take into account the features of the expression system used (host cell for expression / vector for expression). So, if the antibody mainly accumulates inside the host cell, it is necessary to choose a method of isolating the product that will ensure its extraction from the host cell. If the antibody accumulates predominantly in the culture fluid, the target product can be isolated from the culture fluid by methods designed to extract antibodies from the culture fluid. For example, an antibody of the invention can be isolated from the culture fluid by standard methods, including, without limitation, chromatography, centrifugation, filtration, extraction, drying, spraying, evaporation or precipitation.
- An antibody of the invention can be further purified using various techniques known in the art, including chromatography (e.g., ion exchange, affinity, hydrophobic or exclusion), electrophoresis, separation (e.g., ammonium sulfate precipitation), SDS-PAGE or extraction.
- chromatography e.g., ion exchange, affinity, hydrophobic or exclusion
- electrophoresis e.g., electrophoresis
- separation e.g., ammonium sulfate precipitation
- SDS-PAGE e.g., SDS-PAGE or extraction.
- the method for purifying an anti-CD3 * CD19 antibody of the invention comprises at least one chromatographic purification step. More preferably, a method for purifying an anti-CD3 * CD19 antibody of the invention comprises centrifugation, affinity chromatography using a protein A sorbent, and high resolution cation exchange chromatography.
- the anti-CD3 * CD19 antibody of the invention purified according to regulatory requirements is included in the pharmaceutical composition of the invention preferably together with pharmaceutically acceptable carriers and / or diluents.
- the mechanism of action of the proposed anti-CD3 * CD19 antibody is similar to that described for the anti-POP / anti-C019 antibody, Blinatumomab preparation (MT103); and consists in the activation of a multispecific T-cell cytological response against CD 19+ lymphoma cells.
- compositions based on antibodies against CD3 * CD19 can be used to treat all hematological cancers (lymphomas and leukemia) of B-cell nature, for example, such as B-cell tumors from precursors of B-lymphocytes, including: lymphoblastic lymphoma / B-cell acute lymphoblastic leukemia from progenitor cells; B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma
- composition according to the present invention can be applied directly to animals and humans (for example, locally in the form of injections, including subcutaneous injections).
- composition according to the present invention is administered parenterally, for example intravenously, intradermally, subcutaneously, intraperitoneally, intramuscularly, buccally, intraorbitally, intracerebrally, intraspinally, intraventricularly, intrathecally, intracerebrally
- the composition preferably comprises a portion of an aqueous or physiologically compatible solution or suspension of liquid does not adversely affect the balance of electrolytes and / or liquids in patients upon delivery of the target composition to patients.
- the pharmaceutical composition of the invention is prepared in a form suitable for parenteral administration, preferably for subcutaneous administration, including in the form of sterile aqueous a solution, suspension, emulsion, concentrate for the preparation of an aqueous solution, a lyophilized preparation for the preparation of an aqueous solution, a solution based on a non-aqueous solvent.
- Pharmaceutically acceptable agents for use in the pharmaceutical composition of the invention include carriers, excipients, diluents, antioxidants, preservatives, coloring, flavoring and diluting agents, emulsifying agents, suspending agents, solvents, fillers, bulking agents, buffers, delivery vehicles, tonicity agents, cosolvents , wetting agents, complexing agents, buffering agents, antimicrobial agents and surfactants, as shown, for example, in the "Handbook of Pharmace utical Excipients ”(2" d ed. London: The Pharmaceutical Press; 1994).
- a carrier or solvent to obtain a sterile aqueous solution in accordance with the present invention, for example, either Hank's solution, or Ringer's solution, or a suitable buffer solution, for example, physiological buffer solution, can be used.
- the buffers may be conventional buffers such as acetate, citrate, phosphate, bicarbonate buffers or Tris-HCl.
- Acetate buffer may have a pH of about 4-5.5
- Tris buffer may have a pH of about 7-8.5. Additional pharmaceutical agents are presented in Remington's Pharmaceutical Sciences, 18th Edition, A.R. Gennaro, ed., Mack Publishing Company, 1990.
- the anhydrous solvent may be propylene glycol, polyethylene glycol or olive oil or an ester suitable for injection, such as ethyl oleate.
- a suitable carrier for the purpose of preparing the pharmaceutical composition of the invention is a neutral buffered saline or saline mixed with serum albumin.
- the pharmaceutical composition of the invention may also contain ascorbic acid, low molecular weight polypeptides, hydrophilic polymers such as polyvinylpyrrolidone, amino acids such as glycine, glutamine, asparagine, arginine or lysine, monosaccharides, disaccharides and other carbohydrates including glucose, mannose dextrins, chelating agents such as EDTA, sugar alcohols such as mannitol or sorbitol; salt forming counterions, such as sodium; and / or nonionic surfactants such as tween, pluronic or polyethylene glycol (PEG), alkali metal halides (preferably sodium or potassium chloride), benzalkonium chloride, thimerosal, phenethyl alcohol, methyl paraben, propyl paraben, chlororexidine, sorbic acid, peroxide hydrogen, sorbitan esters, polysorbates such as polysorbate 80, tromethamine, lecit
- the most preferred adjuvants for use in the pharmaceutical composition of the invention are: sodium phosphate buffer, polysorbate 80 as a surfactant, mannitol as an isotonic agent, and histidine as a stabilizer.
- excipients can be used in combination with other active ingredients (for example, anti-cancer or anti-inflammatory drugs), provided that they do not cause unwanted effects.
- active ingredients for example, anti-cancer or anti-inflammatory drugs
- the pharmaceutical composition of the invention may further comprise one or more lyoprotectants disclosed, for example, in US Pat. Nos. 6,659,540, 6,566,329 and 6,373,716.
- a lyoprotectant which is a non-reducing sugar, such as sucrose, lactose or trehalose.
- the amount of lyoprotectant is preferably chosen so that after recovery, the resulting finished form is isotonic.
- the selected amount of lyoprotectant should be sufficient to prevent an unacceptable amount of protein degradation and / or aggregation after lyophilization.
- sugar lyoprotectant concentrations e.g., sucrose, lactose, trehalose
- sugar lyoprotectant concentrations are from about 10 mM to about 400 mM.
- composition according to the invention if obtained in lyophilized form, can be optionally completed with a pharmaceutically acceptable solvent and / or diluent, for example, physiological water solution and other commonly used pharmaceutically acceptable solvents.
- a pharmaceutically acceptable solvent and / or diluent for example, physiological water solution and other commonly used pharmaceutically acceptable solvents.
- compositions may contain a therapeutically effective amount of an antibody of the invention.
- therapeutically effective amount refers to that amount of an antibody of the invention that is effective for the necessary periods of time to achieve the desired therapeutic result, and any toxic or harmful effects of the antibody should be outweighed by therapeutically beneficial effects. from this antibody, which in a preferred embodiment of the present invention is at least one of leduyuschego: symptom relief, healing or increase the speed of recovery.
- the therapeutically effective amount of an antibody of the invention can vary according to factors such as the condition of the disease, age, gender, and weight of the individual, the ability of the antibody to induce the desired response specifically in the individual, the presence of concomitant diseases, route of administration, frequency of administration, individual treatment regimen.
- the attending physician can decide on the number of antibodies according to the invention, which it is advisable to treat each patient individually. Moreover, the attending physician may first administer small doses of the antibody of the invention and, according to the patient’s response, adjust its amount. Dosage ranges are from about 0.5 ⁇ g / kg to about 2 mg / kg, depending on the above factors. In this case, preferably, the pharmaceutical composition according to the invention contains 10-100 ⁇ g of antibody.
- composition according to the invention is prepared, dosed and administered in accordance with the principles of good medical practice. Standard pharmaceutical formulation methods are known to those skilled in the art (Remington 1995).
- a method of treating B-cell disease or B-cell depletion, or slowing the development of a pathological condition associated with B-cell disorders of the present invention includes administering to a patient in need thereof an effective amount of an antibody of the invention or a pharmaceutical composition of the invention. Moreover, in a preferred embodiment of the present of the invention, the antibody is administered subcutaneously to the patient. Moreover, the anti-CD3 * CD19 antibody of the invention can be administered to a patient in combination with another drug, including for at least one of the following purposes: to enhance the therapeutic effect against B-cell disease, to reduce side effects during treatment B-cell disease, to alleviate the symptoms of B-cell disease.
- the duration of therapy using the combination of the present invention varies depending on the severity of the disease to be treated and the condition, and also depending on the potential response of each individual patient. It is assumed that the duration of therapy is determined by the severity of the symptoms. Ultimately, the attending physician decides on the appropriate duration of therapy using the combination of the present invention.
- an antibody according to the invention can be obtained using technologically simple known recombinant methods, commercially available agents (vector, host cell, medium) and traditional methods for the isolation and purification of antibodies (Example 1);
- a pharmaceutical composition can be obtained in a technologically simple way, including in a lyophilized form suitable for subsequent reconstitution with traditional diluents (Example 2).
- the authors of the present invention also experimentally demonstrated, in comparison with MT103, a significantly increased half-life (T1 / 2) and exposure (AUC (O-inf)) of the anti-CD3 * CD19 antibody of the invention, while maintaining the maximum peak concentration (Cxx) when administered intravenously, and also increased bioavailability of antibodies against CD3 * CD19 according to the invention with both intravenous and subcutaneous administration (Example 4). Additionally, the authors of the present invention experimentally confirmed a higher affinity of the antibodies of the invention for CD3 and CD 19 and its higher antitumor activity when administered subcutaneously in comparison with MT103 (Examples 3 and 5).
- the gene encoding the anti-CD3 * CD19 antibody chain was constructed by annealing the overlapping chemically synthesized oligonucleotides.
- the sequence of the target gene was cloned into the commercially available vector pUC 19, whereby the vector pAPG_GNR047 was obtained, which was used for further work.
- pAPG_GNR047 vector After treating the pAPG_GNR047 vector with Hindlll, Xbal (New Ingland Biolabs) restriction endodesoxyribonucleases forming sticky ends, a 2235 bp fragment was then ligated, which was then ligated with the Hindlll and Xbal linearized pSTlOl expression vector.
- the resulting plasmid pRA1451 was verified by restriction mapping.
- the construction scheme of the expression vector pRA1451 is shown in FIG. 2.
- the resulting plasmid pRA1451 encoding a polypeptide with the sequence shown in SEQ ID NO: 10, is characterized by the following features:
- - pA is a synthetic polyadenylation signal.
- - contains unique recognition sites for the following restriction endonucleases: Accl (6490 no), Agel (460 no), Apal (995 no), BmgBI (3270 acting), Bsml (7269 acting), EcoRV (6457 no), Hindlll (1590 no), Notl ( 11146 no), Pfol (11021 no), Pmll (5699 no), Spel (4622 no), Swal (6466 no), Tthl 1 II (10585 no).
- Transfection was performed using a commercially available strain of CHO-M (Selexis).
- the selection of the producer cell line is due to the need to form an optimal glycosylation profile in the synthesis of human proteins, as well as their stability, safety and the possibility of using suspension culture conditions for this cell line, which are the most important parameters for the production of therapeutic antibodies.
- Cultivation was carried out in fed-batch mode using BalanCD CHO Growth A nutrient medium (Irvine Scientific) and CellBoost 3 (HyClone) nutrient supplement for 10 days at 37 ° ⁇ , 5% ⁇ 0 2 in the gas phase of the incubator. After cultivation, the culture fluid was clarified by centrifugation and transferred to the selection.
- BalanCD CHO Growth A nutrient medium Irvine Scientific
- CellBoost 3 HyClone
- Example 2 Pharmaceutical composition based on antibodies against CD3 * CD19.
- compositions of the following composition were used: 0.7 mg / ml anti-CD3 * CD19 antibody of the invention (hereinafter GNR-047), 150 mM sodium chloride, 1.8% mannitol, 20 mM sodium phosphate, 0.01% polysorbate 80.
- the purification conditions of the anti-CD3 * CD19 antibody of the invention at the last chromatographic stage of the process are selected so that the target protein is eluted from the sorbent in the form of a concentrated substance containing all the required components of the final formulation.
- an antibody solution with a concentration of about 5 mg / ml (the concentrated solution obtained in Example 1 after chromatographic purification) was diluted to the required concentration of 0.7 mg / ml using the buffer of the finished dosage form with stirring.
- the resulting solution was subjected to sterilizing filtration using a filter with a pore diameter of 0.22 ⁇ m and poured into sterile vials to store the composition and subsequent experiments.
- a solution containing anti-CD3 * CD19 antibodies of the invention in a finished buffer 150 mM sodium chloride, 1.8% mannitol, 20 mm sodium phosphate, 0.01% polysorbate 80
- a finished buffer 150 mM sodium chloride, 1.8% mannitol, 20 mm sodium phosphate, 0.01% polysorbate 80
- sodium chloride and mannitol were used as crystallizing components, the presence of which allows the formation of a tablet, and mannitol also played the role of a stabilizer during lyophilization.
- the resulting lyophilic preparation was stored at 4C in sealed vials.
- Water for injection was used as a solvent for reconstituting the lyophilized composition.
- 0.5 ml of the solvent was added to the vial containing the lyophilized antibody composition at room temperature and gently mixed by shaking until it was completely dissolved.
- Bacteriostatic water for injection can also serve as a solvent, dissolution in which allows the drug to be reused within 7 days.
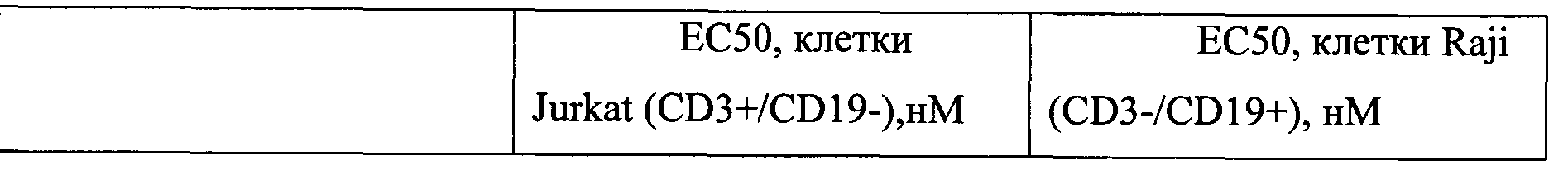
- the biological activity of the obtained antibody was evaluated by determining the binding constants in a competitive analysis on cells of the Raja line CD3- / CD19 + (Raji, ATCC® CCL-86) and Dzhurkat CD3 + / CD19- (Jurkat, ATCC® TIB-152) from the ATCC collection.
- Antibody MT-103 (blinatumomab) was used as a comparison drug. After incubation with the target molecules in successive 10-fold dilutions from 100 nM to 0.1 nM, a competing antibody (HD37 or OCTZ) was added to the cells at a concentration of 6 nM. Cells were washed with pH 7.0 sodium phosphate buffer and stained with anti-Human-FITS antibodies. Stained cells were analyzed by FACS Calibur.
- the table shows that the GNR-047 antibody binds to both CD3 and CD 19, and in both cases it is more effective than the MTUZ comparison drug. Such low, in comparison with the comparison drug, IC50 values can be explained by the presence of 2 valencies for each specificity (CD3 and CD 19
- rats of the Sprague Dawley line were used (Pushchino Kennel of Laboratory Animals, branch of the Institute of Bioorganic Chemistry named after Academicians MM Shemyakin and Yu. A. Ovchinnikov of the Russian Academy of Sciences) weighing about 400 g, 3 rats per group.
- test antibody GNR-047 or MT-103 was administered intravenously at a dose of 0.5 mg / kg or subcutaneously at a dose of 2.0 mg / kg to each rat. Blood samples were taken at certain intervals after injection, starting from 5 min, and the concentration of the drugs in the blood plasma was determined using enzyme-linked immunosorbent assay (ELISA).
- ELISA enzyme-linked immunosorbent assay
- the parameter is calculated taking into account the dose difference.
- TT necessary to reduce the concentration of the drug in blood plasma by 50% as a result of elimination;
- Sshah the highest concentration of the drug in the blood plasma;
- AUQo-t is the area bounded by the pharmacokinetic curve and the abscissa axis in the time interval from the moment of drug administration until the last blood sample is taken;
- AUQo-inf) the area bounded by the pharmacokinetic curve and the abscissa axis, extrapolated in time from the moment of drug administration to infinity; / a - part of the dose of the drug (in%), which reached the systemic circulation after extravascular administration.
- Example 5 Comparison of the antitumor activity of GNR-047 and MT 103 in a model of a tumor xenograft of Raji cells (Raji) in NOD / SCID mice during reconstitution of human PBMC
- the aim of the study was to compare the efficacy of GNR-047 and MT103 preparations in NOD / SCID mice (Taconic, Denmark) at several dose levels, on a Raja tumor cell xenograft model with simultaneous injections of human peripheral blood mononuclear cells (MCPC) to immunodeficient NOD / SCID mice .
- MCPC peripheral blood mononuclear cells
- Cells of the Raja line human Burkitt’s lymphoma
- Injected solutions were prepared by diluting the GNR-047 solution (composition) obtained in Example 2 (0.7 mg / ml) or MT103 (0.52 ⁇ g / ml) in 0.9% saline to obtain a concentration of 5 ⁇ g / ml (dose 1 ⁇ g) or 0.5 ⁇ g / ml (dose 0.1 ⁇ g).
- the experimental groups are described in table 3.
- Body weight was determined on day 0 and was subsequently recorded three times a week until day 48.
- Tumor volume was monitored 3 times a week from day 3 until the end of the study by measuring the large and small diameter of the tumor with a barbell. Based on the diameters, the tumor volume was calculated using the following formula:
- Tumor growth was significantly inhibited or suppressed in all study groups treated with GNR-047 or MT 103 (groups 3-9) compared with control group 2 treated with NPF. Moreover, in all the studied groups treated with GNR-047 or MT 103, inhibition of tumor growth was statistically significant (p ⁇ 0.05).
- Table 5 shows the tumor sizes for groups 1, 2, 4, 8, and 9, and the corresponding comparative graphs that allow us to estimate the size of the tumor during intravenous and subcutaneous administration (for groups 4, 8, and 9) are shown in Fig. 7.
- the present invention can be used in medicine for the treatment of B-cell diseases or depletion of B-cells, including B-lymphoblastic lymphoma / B-cell acute lymphoblastic leukemia from progenitor cells; B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT-type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma; mantle cell lymphoma; diffuse B-large cell lymphoma; mediastinal diffuse B-large cell lymphoma; primary exud
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Mycology (AREA)
- Biotechnology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- Veterinary Medicine (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ CD3*CD19 SPECIFIC ANTIBODIES AGAINST CD3 * CD19
ОБЛАСТЬ ТЕХНИКИ FIELD OF TECHNOLOGY
Изобретение относится к биотехнологии и, в частности, может быть использовано в медицине и фармацевтической промышленности для изготовления лекарственного средства для лечения В-клеточного заболевания, истощения В-клеток или замедления развития патологического состояния, ассоциированного с В-клеточными нарушениями. The invention relates to biotechnology and, in particular, can be used in medicine and the pharmaceutical industry for the manufacture of a medicament for the treatment of B-cell disease, depletion of B-cells or slowing the development of a pathological condition associated with B-cell disorders.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ BACKGROUND OF THE INVENTION
Биспецифические антитела (БАТ) против CD3*CD19 в настоящее время разрабатываются преимущественно для лечения злокачественных заболеваний В-клеток или истощения В-клеток, в том числе: неходжкинской лимфомы (WO2010037835, RU2228202), В-клеточного лейкоз (RU2008129080), детской острой лимфобластической лейкемии (WO20100052013) H T.fl. Bispecific antibodies (BAPs) against CD3 * CD19 are currently being developed primarily for the treatment of malignant diseases of B cells or depletion of B cells, including non-Hodgkin’s lymphoma (WO2010037835, RU2228202), B-cell leukemia (RU2008129080), and acute lymphoblastic childhood leukemia (WO20100052013) H T.fl.
Ряд завершенных и проводимых в настоящее время исследований (например, J Clin Oncol, 2011, 29: 2493-8; Cancer, 2010, 116: 5568-74; Science, 2008, 321: 974-7; BLINCYTO, AmGen Recearch GmbH (NCT00560794, NCT00274742, NCT01207388, NCT01209286, NCT01471782, NCT01466179, NCT01741792); AFM11, Affimed Therapeutics AG (NCT02106091)) дают все основания полагать, что лекарственные препараты на основе биспецифических антител против CD3* CD 19 обещают стать более эффективными в лечении упомянутых выше заболеваний. A number of studies completed and ongoing (e.g., J Clin Oncol, 2011, 29: 2493-8; Cancer, 2010, 116: 5568-74; Science, 2008, 321: 974-7; BLINCYTO, AmGen Recearch GmbH (NCT00560794 , NCT00274742, NCT01207388, NCT01209286, NCT01471782, NCT01466179, NCT01741792); AFM11, Affimed Therapeutics AG (NCT02106091)) give reason to believe that drugs based on bespecifically antibodies against CD3 * CD 19 promise to become more effective in the treatment.
Повышенная эффективность объясняется тем, что БАТ выполняют функцию адаптеров, которые физически соединяют Т-клетки с опухолевыми клетками и запускают мощный сигнальный каскад рецепторного комплекса Т-клеток посредством связывания с инвариантным компонентом CD3 Т-клеточного рецептора. При этом второй (целевой) антиген-специфичный фрагмент узнает CD 19, т.е. БАТ может соединить Т-клетку и раковую клетку за счет одновременного связывания с CD3 и антигеном-мишенью. В этом случае происходит активация и пролиферация Т-клеток, образование цитолитического синапса с высвобождением цитотоксических гранул и секреция цитокинов. Направленный лизис раковых клеток включает в себя перфорацию мембраны клетки-мишени с участием перфорина и последующий апоптоз, индуцированный гранзимами. Следует отметить, что после связывания с Т-клетками, БАТ распознают антигены на поверхности раковой клетки так же, как обычные моноспецифические антитела. Таким образом, удается перенаправить цитотоксическую функцию Т-клеток против опухолевых клеток, причем активность БАТ наблюдается уже при относительно низких (пикомолярных) концентрациях. Связывание же БАТ только с Т-клеткой в отсутствие клетки-мишени не вызывает Т-клеточную активацию. The increased efficiency is explained by the fact that BAPs act as adapters that physically connect T cells with tumor cells and trigger a powerful signaling cascade of the T-cell receptor complex by binding to the invariant component of the CD3 T-cell receptor. In this case, the second (target) antigen-specific fragment recognizes CD 19, i.e. BAP can connect a T cell and a cancer cell by simultaneously binding to CD3 and the target antigen. In this case, the activation and proliferation of T cells, the formation of a cytolytic synapse with the release of cytotoxic granules, and the secretion of cytokines occur. Targeted lysis of cancer cells includes perforation of the target cell membrane involving perforin and subsequent granzyme-induced apoptosis. It should be noted that after binding to T cells, BAPs recognize antigens on the surface of the cancer cell in the same way as conventional monospecific antibodies. Thus, it is possible to redirect cytotoxic function of T cells against tumor cells, and BAP activity is already observed at relatively low (picomolar) concentrations. Binding of BAT only to a T cell in the absence of a target cell does not cause T cell activation.
Примеры биспецифических антител, известных из уровня техники (Blood, (ASH Annual Meeting Abstracts), 2009, 114:840), свидетельствуют о том, что эффективная терапевтическая концентрация препаратов, полученных на основе использования мультивалентных антител, существенно ниже по сравнению с классическими антительными противораковыми препаратами. Это способствует хорошей переносимости, возможности осуществления длительных курсов лечения и уменьшению риска побочных эффектов. Кроме того, требуемый объем и стоимость производства биспецифических антител ниже. Поэтому создание таких антител позволит существенно сократить масштабы и расходы на производство препаратов на их основе и, что самое главное, сделать эти лекарства доступными для всех пациентов, нуждающихся в подобной терапии. Examples of bispecific antibodies known from the prior art (Blood, (ASH Annual Meeting Abstracts), 2009, 114: 840) indicate that the effective therapeutic concentration of drugs derived from the use of multivalent antibodies is significantly lower compared to classic anti-cancer antibodies drugs. This contributes to good tolerance, the possibility of implementing long-term courses of treatment and reducing the risk of side effects. In addition, the required volume and production cost of bespecifically antibodies is lower. Therefore, the creation of such antibodies will significantly reduce the scale and cost of producing drugs based on them and, most importantly, make these drugs available to all patients in need of such therapy.
В настоящее время было разработано и получено довольно много биспецифических антител против CD3*CD19. Наиболее перспективные из них представляют собой одноцепочечные молекулы как таковые, или нековалентные димеры, состоящие из одноцепочечных молекул. At present, quite a few bispecific antibodies against CD3 * CD19 have been developed and obtained. The most promising of them are single-chain molecules as such, or non-covalent dimers consisting of single-chain molecules.
Одним из одноцепочечных антител против CD3*CD1 является блинатумомаб (Blincyto, МТ103). Блинатумомаб состоит из двух доменов: домена анти-С019 scFv из гибридомы HD37 и домена anra-CD3 scFv из гибридомы ОКТЗ. Для получения антитела фрагмент ДНК VLCD 19-VHCD 19- VHCD3- VLCD3 экспрессируют в DHFR-отрицательных СНО клетках (патент RU2228202). One of the single chain antibodies against CD3 * CD1 is Blinatumomab (Blincyto, MT103). Blinatumomab consists of two domains: the anti-C019 scFv domain from the HD37 hybridoma and the anra-CD3 scFv domain from the OKTZ hybridoma. To obtain the antibody, the VLCD 19-VHCD 19-VHCD3-VLCD3 DNA fragment is expressed in DHFR-negative CHO cells (patent RU2228202).
Блинатумомаб, в сравнении с полноразмерными антителами, имеет относительно небольшую молекулярную массу (55 кДа против 155 кДа), из-за чего быстро элиминируется из кровотока. Поэтому для достижения стабильных концентраций препарата в крови используется непрерывное внутривенное введение препарата в течение 2-4 недель за один цикл (в режиме две недели - капельница, две недели - перерыв), что достаточно трудно переносимо для пациента. Blinatumomab, in comparison with full-sized antibodies, has a relatively small molecular weight (55 kDa versus 155 kDa), which is why it is rapidly eliminated from the bloodstream. Therefore, to achieve stable concentrations of the drug in the blood, continuous intravenous administration of the drug is used for 2-4 weeks per cycle (in a two-week regimen - an dropper, two weeks - a break), which is quite difficult for the patient to tolerate.
Кроме того, блинтомумаб сложно производить в промышленных масштабах, так как при производстве одноцепочечных антител могут образовываться гомо- и гетеродимеры, что приводит к усложнению процесса выделения и очистки таких антител. С другой стороны, возможен обратный процесс - нежелательная диссоциация димеров, как это было показано, например, в статье Glockshuber et al., Biochemistry, 1990, vol 29:1362-1367. Чтобы избежать этого, были предложены антитела, стабилизированные дисульфидными связями (Cell Oncol. (2012), 35:423-434), что позволило повысить как стабильность антитела в растворе, так и терапевтическую эффективность в сравнении с одноцепочечным антителом. In addition, blintomumab is difficult to produce on an industrial scale, since homo- and heterodimers can form in the production of single-chain antibodies, which complicates the process of isolation and purification of such antibodies. On the other hand, the opposite process is possible - undesired dissociation of dimers, as was shown, for example, in Glockshuber et al., Biochemistry, 1990, vol 29: 1362-1367. To avoid this, antibodies stabilized by disulfide bonds (Cell Oncol. (2012), 35: 423-434), which made it possible to increase both the stability of the antibody in solution and therapeutic efficacy in comparison with a single-chain antibody.
Несмотря на недостаточное удобство в применении и сложность получения блинатумомаб является одним из самых успешных антител против CD3*CD19. Despite the lack of ease of use and the difficulty of obtaining blinatumomab is one of the most successful antibodies against CD3 * CD19.
Блинатумомаб относится к антителам BiTE®. Антитела BiTE® демонстрируют высокую эффективность перенаправленного лизиса клеток, экспрессирующих опухолевый антиген-мишень. Значения ЕС50 для антител BiTE® в целом колеблются от 0,1 до 50 пМ (Bauerle Р.А. и Reinhardt С. (2009) Cancer Res. 69(12), рр.4941-4944). Мощный цитолиз опухолевых клеток необходим для того, чтобы вызвать фармакологически желательный эффект. В обзоре Rader С. сообщает, что мощная литическая способность формата BiTE® объясняется (1) его небольшим размером, который приводит мишень и эффекторные клетки в непосредственную близость, позволяя образовать цитолитические синапсы, и (2) его моновалентным задействованием комплекса TCR, что предупреждает системную активацию эффекторных клеток в отсутствие клеток-мишеней (Rader С. (2011), Blood, 117(17), pp. 4403- 4404). Кроме того, предшествующий уровень техники описывает, что класс BiTE® биспецифических антител имеет как правило в 100-10000 раз более высокую эффективность лизиса опухолевых клеток относительно других биспецифических форматов и полных моноклональных антител IgGl (Wolf и соавт. (2005) Drug Discov Today 10(18), pp. 1237-1244). Blinatumomab refers to BiTE® antibodies. BiTE® antibodies demonstrate high efficacy of redirected lysis of cells expressing the tumor target antigen. EC50 values for BiTE® antibodies generally range from 0.1 to 50 pM (Bauerle P.A. and Reinhardt C. (2009) Cancer Res. 69 (12), pp. 4941-4944). Powerful cytolysis of tumor cells is necessary in order to cause a pharmacologically desired effect. In a review, Rader C. reports that the powerful lytic ability of the BiTE® format is explained by (1) its small size, which brings the target and effector cells in close proximity, allowing the formation of cytolytic synapses, and (2) its monovalent involvement of the TCR complex, which prevents systemic activation of effector cells in the absence of target cells (Rader C. (2011), Blood, 117 (17), pp. 4403-4404). In addition, the prior art describes that the BiTE® class of bispecific antibodies typically has 100-10000 times higher tumor cell lysis efficiencies relative to other bispecific formats and full IgGl monoclonal antibodies (Wolf et al. (2005) Drug Discov Today 10 ( 18), pp. 1237-1244).
Таким образом, для специалиста из уровня техники следует, что небольшие моновалентные форматы биспецифических антител против CD3*CD19 формата BiTE® демонстрируют более мощную перенаправленную Т-клеточную литическую активность, чем крупные бивалентные CD3*CD19 биспецифические форматы, и использование крупных бивалентных CD3*CD19 биспецифических антител нецелесообразно. Thus, for a person skilled in the art, it follows that small monovalent formats of bispecific anti-CD3 * CD19 antibodies of the BiTE® format exhibit more powerful redirected T-cell lytic activity than large bivalent CD3 * CD19 bispecific formats, and the use of large bivalent CD3 * CD19 bispecific antibodies impractical.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ SUMMARY OF THE INVENTION
Настоящее изобретение решает задачу получения бивалентного антитела против CD3*CD19, удобного в применении и получении по сравнению с блинатумомабом и при этом обладающего высокой эффективностью в отношении лечения злокачественных заболеваний В-клеток, истощения В-клеток или замедления развития патологических состояний, ассоциированных с В-клеточными нарушениями. The present invention solves the problem of obtaining a bivalent antibody against CD3 * CD19, convenient to use and obtain compared with blinatumomab and at the same time highly effective in treating malignant diseases of B cells, depletion of B cells or slowing the development of pathological conditions associated with B- cellular disorders.
Работа коллектива авторов настоящего изобретения над улучшением фармакокинетических характеристик антител против CD3*CD19 привела к созданию новой конструкции антитела, представляющей собой биспецифическую двуцепочечную молекулу, каждая цепь которой содержит Fc-часть обычного IgG и четыре связывающих домена, з соединенных линкерами и расположенных в следующем порядке от Ν-конца к С-концу: VL(CD3)-L 1 - VH(CD 19)-L2- VL(CD 19)-L3 - VH(CD3)-H-CH2-CH3 (IgG), где VL(CD3), VL(CD19), VH(CD3) и VH(CD19) представляют собой вариабельные домены легкой и тяжелой цепей антител против CD3 и CD 19 соответственно, LI, L2, L3 - линкерные последовательности, Н - шарнирная область иммуноглобулина IgG и СН2-СНЗ (IgG) - константная область Fc-домена иммуноглобулина IgG. Две цепи соединены дисульфидными связями. The work of the team of the authors of the present invention to improve the pharmacokinetic characteristics of antibodies against CD3 * CD19 has led to the creation of a new antibody design, which is a bispecific double-stranded molecule, each chain of which contains the Fc part of normal IgG and four binding domains, connected by linkers and arranged in the following order from the конца-end to the C-end: VL (CD3) -L 1 - VH (CD 19) -L2-VL (CD 19) -L3 - VH (CD3) -H-CH2-CH3 (IgG), where VL (CD3), VL (CD19), VH (CD3) and VH (CD19) are the variable domains of the light and heavy chains of antibodies against CD3 and CD 19, respectively, LI, L2, L3 are linker sequences, N - the hinge region of IgG immunoglobulin and CH2-CH3 (IgG) is the constant region of the Fc domain of IgG immunoglobulin. The two chains are connected by disulfide bonds.
Неожиданно обнаружилось, что такие биспецифические молекулы в сравнении с антителом блинатумомаб (МТ-103) характеризуются увеличенным временем полужизни и просты в получении. При этом еще более неожиданными для коллектива авторов оказались такие свойства указанного антитела как усиленный цитотоксический эффект и высокая биодоступность даже при подкожном введении на уровне 60%. Последняя характеристика особенно важна, поскольку до настоящего времени, из-за малой биодоступности, препараты антител вводились преимущественно внутривенным путем, который более сложен и менее комфортен для пациента. Увеличенное время полувыведения, высокие эффективность и биодоступность при подкожном введении позволят уменьшить частоту введения препарата и увеличить удобство его применения. It was unexpectedly discovered that such bispecific molecules, in comparison with the blinatumomab antibody (MT-103), are characterized by an increased half-life and are easy to obtain. Moreover, such properties of the indicated antibody as enhanced cytotoxic effect and high bioavailability even with subcutaneous administration at the level of 60% were even more unexpected for the team of authors. The latter characteristic is especially important, since until now, due to the low bioavailability, antibody preparations have been administered mainly via the intravenous route, which is more complex and less comfortable for the patient. The increased half-life, high efficiency and bioavailability with subcutaneous administration will reduce the frequency of administration of the drug and increase the convenience of its use.
Таким образом, первый объект настоящего изобретения представляет собой рекомбинантное моноклональное биспецифическое антитело против CD3*CD19, включающее две соединенных дисульфидными связями цепи, каждая из которых состоит из следующих доменов: VL(CD3)-Ll-VH(CD19)-L2-VL(CD19)-L3-VH(CD3)-H-CH2-CH3(IgG), где VL(CD3), VL(CD19), VH(CD3) и VH(CD19) представляют собой вариабельные домены легкой и тяжелой цепей антител против CD3 и CD 19 соответственно, LI, L2, L3 - линкерные последовательности, Н - шарнирная область иммуноглобулина IgG и СН2-СНЗ (IgG) - константная область Fc-домена иммуноглобулина IgG. Thus, the first object of the present invention is a recombinant monoclonal bispecific anti-CD3 * CD19 antibody comprising two disulfide-linked chains, each of which consists of the following domains: VL (CD3) -Ll-VH (CD19) -L2-VL (CD19 ) -L3-VH (CD3) -H-CH2-CH3 (IgG), where VL (CD3), VL (CD19), VH (CD3) and VH (CD19) are the variable domains of the light and heavy chains of antibodies against CD3 and CD 19, respectively, LI, L2, L3 are linker sequences, H is the hinge region of IgG immunoglobulin and CH2-CH3 (IgG) is the constant region of the Ig immunoglobulin Fc domain G.
Причем указанная константная область Fc-домена иммуноглобулина IgG предпочтительно представляет собой константную область Fc-домена иммуноглобулина IgG2 и содержит последовательность, представленную в SEQ ID NO: 5. Линкерные последовательности LI, L2, L3 предпочтительно имеют длину 5-15 аминокислот и имеют последовательности, по существу соответствующие последовательностям, представленным в SEQ ID NO: 6, 7, 8 соответственно. Шарнирная область иммуноглобулина IgG по существу соответствует последовательности, представленной в SEQ ID NO:9. Moreover, said constant region of the IgG immunoglobulin Fc domain is preferably a constant region of the IgG2 immunoglobulin Fc domain and contains the sequence shown in SEQ ID NO: 5. The linker sequences LI, L2, L3 preferably have a length of 5-15 amino acids and have sequences according to essentially corresponding to the sequences presented in SEQ ID NO: 6, 7, 8, respectively. The hinge region of the IgG immunoglobulin essentially corresponds to the sequence shown in SEQ ID NO: 9.
Указанное антитело предпочтительно имеет время полужизни в крови, увеличенное по сравнению с временем полужизни блинатумомаба, измеренным в по существу аналогичных условиях. При этом время полужизни в крови антитела по изобретению может быть более 40 часов. При этом указанное антитело предпочтительно, но не обязательно имеет аминокислотную последовательность, по существу соответствующую последовательности, представленной в SEQ ID NO: 10. The specified antibody preferably has a half-life in blood, increased compared with the half-life of pancreatitis, measured in essentially similar conditions. Moreover, the half-life in blood of an antibody of the invention may be more than 40 hours. Moreover, the specified antibody preferably, but not necessarily has an amino acid sequence essentially corresponding to the sequence presented in SEQ ID NO: 10.
Следующими объектами настоящего изобретения являются нуклеиновая кислота, кодирующая последовательность цепи указанного биспецифического антитела против CD3*CD19 по изобретению, и содержащий ее вектор. Указанный вектор может быть вектором для обеспечения экспрессии биспецифического антитела против CD3*CD19 в клетке-хозяине, по изобретению, содержащим указанную выше нуклеиновую кислоту, функционально соединенную с нуклеотидными последовательностями, обеспечивающими возможность гетерологичной экспрессии в клетке-хозяине. Указанный вектор может быть вектором для клонирования, содержащим указанную выше нуклеиновую кислоту, и фланкирующие ее сайты рестрикции, позволяющие вырезать указанную нуклеиновую кислоту с помощью подходящих рестриктаз. Предпочтительно, но не обязательно указанный вектор является экспрессионной плазмидой pRA1451, характеризующейся следующими признаками: The following objects of the present invention are a nucleic acid encoding a chain sequence of the specified bispecific anti-CD3 * CD19 antibody of the invention, and a vector containing it. The vector may be a vector for expressing a bispecific anti-CD3 * CD19 antibody in a host cell of the invention, comprising the aforementioned nucleic acid operably linked to nucleotide sequences enabling heterologous expression in the host cell. The specified vector may be a cloning vector containing the above nucleic acid, and flanking its restriction sites, allowing you to cut the specified nucleic acid using suitable restriction enzymes. Preferably, but not necessarily, the vector is an expression plasmid pRA1451 characterized by the following features:
- состоит из 11308 п.о., - consists of 11308 bp
- имеет молекулярную массу 6.99 МДа, - has a molecular weight of 6.99 MDa,
содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность, представленную в SEQ ID NO: 10, contains the nucleotide sequence encoding the amino acid sequence shown in SEQ ID NO: 10,
- обеспечивает устойчивость клеток млекопитающих, трансфицированных указанной плазмидой, к пуромицину; - provides resistance of mammalian cells transfected with the indicated plasmid to puromycin;
- содержит следующие элементы: - contains the following elements:
- CMVe/EFla pro - энхансер вируса CMV и промотор транскрипции гена фактора элонгации альфа, - CMVe / EFla pro - enhancer of the CMV virus and promoter of transcription of the gene for elongation factor alpha,
- BGH рА - сигнал полиаденилирования бычьего гормона роста, - BGH pA - signal polyadenylation of bovine growth hormone,
- sv40 enh- энхансер вируса SV40, - sv40 enh- enhancer of the SV40 virus,
- SGE 1 - элемент прикрепления к ядерному матриксу, - SGE 1 - element of attachment to the nuclear matrix,
- Amp - ген β-лактамазы, - Amp - β-lactamase gene,
- sv40 pro - промотор вируса S V40, - sv40 pro - promoter of the virus S V40,
- риго— ген устойчивости к пуромицину, - rigo — puromycin resistance gene,
- рА - синтетический сигнал полиаденилирования, - pA - synthetic polyadenylation signal,
- содержит уникальные участки узнавания следующих эндонуклеаз рестрикции: Accl (6490 и.о.), Agel (460 и.о.), Apal (995 и.о.), BmgBI (3270 и.о.), Bsml (7269 и.о.), EcoRV (6457 и.о.), Hindlll (1590 и.о.), Notl (11146 и.о.), Pfol (11021 и.о.), Pmll (5699 и.о.), Spel (4622 и.о.), Swal (6466 и.о.), Tthl 111 (10585 и.о.). - contains unique recognition sites for the following restriction endonucleases: Accl (6490 IO), Agel (460 IO), Apal (995 IO), BmgBI (3270 IO), Bsml (7269 IO), EcoRV (6457 i. O.), Hindlll (1590 I.O.), Notl (11146 I.O.), Pfol (11021 I.O.), Pmll (5699 I.O.), Spel (4622 I.O.), Swal (6466 acting), Tthl 111 (10585 acting).
Еще одним объектом настоящего изобретения является клетка-хозяин, содержащая нуклеиновую кислоту по изобретению или вектор для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению в клетке-хозяине. Указанная клетка может быть, как прокариотической, так и эукариотической клеткой. Предпочтительно, но не обязательно указанная клетка может быть клеткой млекопитающего, в частности, клеткой китайского хомячка. Another object of the present invention is a host cell containing a nucleic acid of the invention or a vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention in a host cell. The specified cell can be both prokaryotic and eukaryotic cells. Preferably, but not necessarily, said cell may be a mammalian cell, in particular a Chinese hamster cell.
Следующим объектом настоящего изобретения является способ получения биспецифического антитела против CD3*CD19 по изобретению, включающий по меньшей мере культивирование клетки-хозяина по изобретению в условиях, обеспечивающих экспрессию антитела против CD3*CD1 по изобретению, и выделение полученного продукта. A further object of the present invention is a method for producing a bispecific anti-CD3 * CD19 antibody of the invention, comprising at least culturing a host cell of the invention under conditions that express the anti-CD3 * CD1 antibody of the invention and isolating the resulting product.
Также объектом настоящего изобретения является способ очистки антитела против CD3*CD19 по изобретению, включающий проведение по меньшей мере одной стадии хроматографии в условиях, обеспечивающих получение препарата антитела против CD3*CD19 по изобретению, по существу свободного от примесей клетки-хозяина. Указанный способ может дополнительно включать стадию центрифугирования, предпочтительно выполняемую до стадии хроматографии, и еще одну стадию хроматографии. Причем первая стадия хроматографии предпочтительно, но необязательно выполняется с использованием сорбента на основе протеина А, а вторая стадия хроматографии является стадией катионообменной хроматографии. Another object of the present invention is a method for purifying an anti-CD3 * CD19 antibody of the invention, comprising at least one chromatography step under conditions providing a preparation of an anti-CD3 * CD19 antibody of the invention, substantially free of host cell impurities. The specified method may further include a centrifugation step, preferably performed before the chromatography step, and another chromatography step. Moreover, the first chromatography step is preferably, but not necessarily, performed using a protein A sorbent, and the second chromatography step is a cation exchange chromatography step.
Следующим объектом настоящего изобретения является применение антитела против CD3*CD19 по изобретению для лечения В-клеточных заболевания, истощения В- клеток или замедления развития патологических состояний, ассоциированных с В- клеточными нарушения. The next object of the present invention is the use of antibodies against CD3 * CD19 according to the invention for the treatment of b-cell diseases, depletion of b-cells or slow the development of pathological conditions associated with b-cell disorders.
Указанное применение предусматривает введение антитела по изобретению пациенту предпочтительно, но не обязательно внутривенно или подкожно. При этом антитело вводят пациенту в терапевтически эффективном количестве. Еще одним объектом изобретения является фармацевтическая композиция для лечения В-клеточного заболевания, истощения В-клеток или замедления развития патологических состояний, ассоциированных с В-клеточными нарушения, содержащая в качестве активного компонента антитело против CD3*CD19 по изобретению в терапевтически эффективном количестве и фармацевтически приемлемый носитель. Said use comprises administering an antibody of the invention to a patient preferably, but not necessarily intravenously or subcutaneously. In this case, the antibody is administered to the patient in a therapeutically effective amount. Another object of the invention is a pharmaceutical composition for treating B-cell disease, depleting B-cells or slowing down the development of pathological conditions associated with B-cell disorders, comprising, as an active component, an anti-CD3 * CD19 antibody of the invention in a therapeutically effective amount and a pharmaceutically acceptable carrier.
Следующим объектом настоящего изобретения является способ лечения В- клеточного заболевания, истощения В-клеток или замедления развития патологических состояний, ассоциированных с В-клеточными нарушения, включающий введение пациенту, нуждающемуся в этом, эффективной дозы антитела против CD3*CD19 по изобретению, или эффективного количества фармацевтической композиции по изобретению. The next object of the present invention is a method of treating B-cell disease, depletion of B-cells or slowing the development of pathological conditions associated with B-cell disorders, comprising administering to a patient in need thereof an effective dose of an anti-CD3 * CD19 antibody of the invention, or an effective amount pharmaceutical compositions of the invention.
При этом указанным В-клеточным заболеванием, истощением В-клеток или замедлением развития патологического состояния, ассоциированного с В-клеточными нарушения, является одно из следующего: В-лимфобластная лимфома/В-клеточный острый лимфобластный лейкоз из клеток-предшественников; В-клеточные опухоли из периферических (зрелых) В-лимфоцитов, в том числе: В-клеточный хронический лимфоцитарный лейкоз/лимфома из малых лимфоцитов (лимфоцитарная лимфома); В- клеточный пролимфоцитарный лейкоз; лимфоплазмоцитарная лимфома; селезеночная лимфома маргинальной зоны; волосатоклеточный лейкоз; плазмоклеточная миелома/плазмоцитома; экстранодальная В-клеточная лимфома маргинальной зоны MALT- типа; нодальная В-клеточная лимфома маргинальной зоны; фолликулярная лимфома; лимфома из клеток мантийной зоны; диффузная В-крупноклеточная лимфома; медиастинальная диффузная В-крупноклеточная лимфома; первичная экссудативная лимфома; лимфома/лейкоз Беркитта, а также для лечения аутоиммунных заболеваний, вызванных патологической регуляцией В-клеток, таких как ревматоидный артрит, системная красная волчанка, гломерулонефрит, рассеянный склероз и миастения гравис. At the same time, the indicated B-cell disease, depletion of B-cells or a slowdown in the development of the pathological condition associated with B-cell disorders is one of the following: B-lymphoblastic lymphoma / B-cell acute lymphoblastic leukemia from progenitor cells; B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT-type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma; mantle cell lymphoma; diffuse B-large cell lymphoma; mediastinal diffuse B-large cell lymphoma; primary exudative lymphoma; Burkitt’s lymphoma / leukemia, as well as for the treatment of autoimmune diseases caused by pathological regulation of B cells, such as rheumatoid arthritis, systemic lupus erythematosus, glomerulonephritis, multiple sclerosis and myasthenia gravis.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ BRIEF DESCRIPTION OF THE DRAWINGS
Фиг. 1. Схематическое представление конструкции антитела GNR-047 FIG. 1. Schematic representation of the construction of antibodies GNR-047
Фиг. 2. Схема конструирования экспрессионного вектора FIG. 2. The design scheme of the expression vector
Фиг. 3. Карта экспрессионного вектора pRA1451 FIG. 3. Map of expression vector pRA1451
Фиг. 4. Анализ способности антитела GNR-047 и антитела МТ-103 связывать нативный рецептор CD3 на клеточной линии Jurkat и рецептор CD 19 на клеточной линии Raji FIG. 4. Analysis of the ability of the GNR-047 antibody and MT-103 antibody to bind the native CD3 receptor on the Jurkat cell line and CD 19 receptor on the Raji cell line
Фиг. 5а. Исследование фармакокинетических характеристик антитела GNR-047 при внутривенном введении в дозировке 0,5 мг/кг Фиг. 56. Исследование фармакокинетических характеристик антитела МТ-103 при внутривенном введении в дозировке 0,5 мг/кг FIG. 5a. Study of the pharmacokinetic characteristics of the GNR-047 antibody when administered intravenously at a dose of 0.5 mg / kg FIG. 56. The study of the pharmacokinetic characteristics of the MT-103 antibody when administered intravenously at a dose of 0.5 mg / kg
Фиг. 6а. Исследование фармакокинетических характеристик антитела GNR-047 при подкожном введении в дозировке 2,0 мг/кг FIG. 6a. A study of the pharmacokinetic characteristics of the GNR-047 antibody when administered subcutaneously at a dose of 2.0 mg / kg
Фиг. 66. Исследование фармакокинетических характеристик антитела МТ-103 при подкожном введении в дозировке 2,0 мг/кг FIG. 66. A study of the pharmacokinetic characteristics of the MT-103 antibody when administered subcutaneously at a dose of 2.0 mg / kg
Фиг. 7. Изменение среднего объема опухоли в процессе исследования FIG. 7. Change in the average tumor volume during the study
ЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ BEST MODE FOR CARRYING OUT THE INVENTION
Далее рассмотрены наиболее предпочтительные варианты осуществления настоящего изобретения, раскрыто смысловое содержание используемых в рамках настоящего изобретения терминов, а также представлены примеры, демонстрирующие осуществление настоящего изобретения и достигаемые при этом результаты. The following are the most preferred embodiments of the present invention, the semantic content of the terms used in the framework of the present invention is disclosed, and examples are presented that demonstrate the implementation of the present invention and the results achieved.
Термин "рекомбинантное моноклональное биспецифическое антитело против CD3*CD19", используемый в соответствии с настоящим изобретением, включает в себя антитела, специфически связывающиеся и с CD3, и с CD 19, которые получены с помощью рекомбинантных технологий. The term "recombinant monoclonal bispecific anti-CD3 * CD19 antibody" used in accordance with the present invention includes antibodies that specifically bind to both CD3 and CD 19, which are obtained using recombinant technologies.
Антитело против CD3*CD19 по изобретению может быть получено на основе мышиных, и/или человеческих последовательностей, и/или верблюжьих последовательностей, и/или последовательностей ламы, и/или иных подходящих последовательностей, включая искусственные, в том числе, созданные путем модификации мышиных и/или человеческих последовательностей, например, за счет введения мутаций. Предпочтительно антитело против CD3*CD19 по изобретению является химерным. Более предпочтительно антитело против CD3*CD19 по изобретению является полностью человеческим. Antibody against CD3 * CD19 according to the invention can be obtained on the basis of murine and / or human sequences and / or camel sequences and / or llama sequences and / or other suitable sequences, including artificial ones, including those created by modification of mouse and / or human sequences, for example, through the introduction of mutations. Preferably, the anti-CD3 * CD19 antibody of the invention is chimeric. More preferably, the anti-CD3 * CD19 antibody of the invention is fully human.
Рекомбинантное моноклональное биспецифическое антитело против CD3*CD19 по изобретению содержит вариабельные домены легкой и тяжелой цепей антитела против CD3, вариабельные домены легкой и тяжелой цепей антитела против CD 19, линкерные последовательности, шарнирную область, Fc последовательность и имеет две цепи, соединенные между собой дисульфидными связями. При этом каждая цепь предпочтительно имеет следующую структуру: VL(CD3) -L1-VH(CD19) -L2-VL(CD19) -L3-VH(CD3) -H-CH2- The recombinant monoclonal bispecific anti-CD3 * CD19 antibody of the invention contains the variable domains of the light and heavy chains of the anti-CD3 antibody, the variable domains of the light and heavy chains of the anti-CD 19 antibody, the linker sequence, the hinge region, the Fc sequence and has two chains connected by disulfide bonds . Moreover, each chain preferably has the following structure: VL (CD3) -L1-VH (CD19) -L2-VL (CD19) -L3-VH (CD3) -H-CH2-
CH3(IgG), где VL(CD3), VL(CD19), VH(CD3) и VH(CD19) представляют собой вариабельные домены легкой и тяжелой цепей антител против CD3 и CD 19 соответственно;CH3 (IgG), where VL (CD3), VL (CD19), VH (CD3) and VH (CD19) are the variable domains of the light and heavy chains of antibodies against CD3 and CD 19, respectively;
LI, L2, L3 - линкерные последовательности; Н представляет собой шарнирную область иммуноглобулина IgG; и CH2-CH3 (IgG) представляет собой константную область Fc-домена иммуноглобулина IgG. LI, L2, L3 — linker sequences; H is a hinge region immunoglobulin IgG; and CH2-CH3 (IgG) is a constant region of the Fc domain of an IgG immunoglobulin.
AHTH-CD3 антитела хорошо известны специалистам. Примеры анти-СОЗ антител включают, без ограничения, ОКТЗ, G4.18, 145-2С11, Leu4, НГГЗа, ВСЗ, SK7, SP34, RIV-9 и UCHT1. Предпочтительно анти-СОЗ антитело связывается с теми же эпитопами, что и ОКТЗ, G4.18, 145-2С11, Leu4, НГГЗа, ВСЗ, SK7, SP34, RIV-9 и UCHT1. AHTH-CD3 antibodies are well known in the art. Examples of anti-POP antibodies include, but are not limited to, OKTZ, G4.18, 145-2C11, Leu4, NGH3, SCZ, SK7, SP34, RIV-9, and UCHT1. Preferably, the anti-POP antibody binds to the same epitopes as OCTZ, G4.18, 145-2C11, Leu4, NGH3a, SCZ, SK7, SP34, RIV-9 and UCHT1.
Специалист в уровне техники без излишнего экспериментирования может получить дополнительные антитела против CD3 и, в том числе, определить, специфичны ли антитела к тем же эпитопам, что и анти-СОЗ антитела ОКТЗ, G4.18, 145-2С11 , Leu4, НГГЗа, ВСЗ, SK7, SP34, RTV-9 и UCHT1, выяснив, предотвращают ли первые связывание последних с антигенным полипептидом CD3. One of ordinary skill in the art can obtain additional anti-CD3 antibodies without undue experimentation and, inter alia, determine whether antibodies to the same epitopes are specific as anti-POP antibodies OKTZ, G4.18, 145-2C11, Leu4, NGGZa, VSZ , SK7, SP34, RTV-9, and UCHT1, finding out if the former prevent the binding of the latter to the CD3 antigenic polypeptide.
В целом, в рамках настоящего изобретения могут быть использованы любые вариабельные домены легкой и тяжелой цепей антитела против CD3, демонстрирующие высокую специфичность и аффинность связывания с антигенным полипептидом CD3. Однако наиболее предпочтительно в соответствии с настоящим изобретением использовать вариабельные домены легкой и тяжелой цепей антитела против CD3 VL(CD3) и VH(CD3), охарактеризованные последовательностями, представленными в SEQ ID ΝΟ:1 и SEQ ID NO:2. In general, any variable domains of the anti-CD3 antibody light and heavy chains exhibiting high specificity and binding affinity for the CD3 antigenic polypeptide can be used within the scope of the present invention. However, it is most preferable in accordance with the present invention to use the variable domains of the light and heavy chains of the antibodies against CD3 VL (CD3) and VH (CD3), characterized by the sequences shown in SEQ ID 1: 1 and SEQ ID NO: 2.
AHTH-CD19 антитела также хорошо известны специалистам, как и способы их получения. Примеры анти-С019 антител включают, без ограничения, HD37, HIB19, SJ25-C1, 4G7-2E3. Кроме того, указанные способы и антитела раскрыты в евразийской заявке ЕА200800094, опубликованной 30.06.2008. В целом, в рамках настоящего изобретения могут быть использованы любые вариабельные домены легкой и тяжелой цепей антитела против CD 19, демонстрирующие высокую специфичность и прочность связывания с антигенным полипептидом CD 19. Однако наиболее предпочтительно в соответствии с настоящим изобретением использовать вариабельные домены легкой и тяжелой цепей антитела против CD19 VL(CD3) и VH(CD3), охарактеризованные последовательностями, представленными в SEQ ID NO:3 и SEQ ID NO:4. AHTH-CD19 antibodies are also well known in the art, as are methods for their preparation. Examples of anti-C019 antibodies include, but are not limited to, HD37, HIB19, SJ25-C1, 4G7-2E3. In addition, these methods and antibodies are disclosed in Eurasian application EA200800094, published June 30, 2008. In general, any variable domains of the anti-CD 19 antibody light and heavy chains that exhibit high specificity and binding strength to the CD 19 antigenic polypeptide can be used within the scope of the present invention. However, it is most preferred to use the variable light and heavy chain domains of the antibody in accordance with the present invention. anti-CD19 VL (CD3) and VH (CD3), characterized by the sequences shown in SEQ ID NO: 3 and SEQ ID NO: 4.
Термин "Fc-последовательность" представляет собой термин, хорошо известный специалистам в данной области - это концевая часть молекулы иммуноглобулина, которая взаимодействует с Fc-рецептором на поверхности клетки и с некоторыми белками системы комплемента. В зависимости от аминокислотной последовательности константной области тяжелых цепей иммуноглобулины подразделяют на классы: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть дополнительно разделены на подклассы (изотипы), например, IgGl, IgG2, IgG3 и IgG4, IgAl и IgA2. В соответствии с константными областями тяжелых цепей различные классы иммуноглобулинов называют [альфа], [дельта], [эпсилон], [гамма] и [мю], соответственно. Четыре изотипа человеческого IgG связывают различные рецепторы, такие как неонатальный Fc-рецептор, активирующие Fc-рецепторы гамма, FcgRI, FcgRIIa и FcgRIIIa, ингибирующий рецептор FcgRIIb и Clq с различной аффинностью, получая разные виды активности. Однако термин "Fc-последовательность" в рамках настоящего изобретения относится, в том числе, к Fc-последовательностям, модифицированным для изменения сродства к соответствующему рецептору. The term “Fc sequence” is a term well known to those skilled in the art — this is the terminal portion of an immunoglobulin molecule that interacts with the Fc receptor on the cell surface and with some proteins of the complement system. Depending on the amino acid sequence of the constant region of the heavy chain, immunoglobulins are divided into classes: IgA, IgD, IgE, IgG and IgM, and some of them can be further divided into subclasses (isotypes), for example, IgGl, IgG2, IgG3 and IgG4, IgAl and IgA2. In accordance with the constant regions of the heavy chains, the various classes of immunoglobulins are called [alpha], [delta], [epsilon], [gamma] and [mu], respectively. Four isotypes of human IgG bind various receptors, such as the neonatal Fc receptor, activating gamma Fc receptors, FcgRI, FcgRIIa and FcgRIIIa, inhibiting the FcgRIIb receptor and Clq with different affinities, obtaining different types of activity. However, the term "Fc sequence" in the framework of the present invention refers, inter alia, to Fc sequences modified to change the affinity for the corresponding receptor.
Антитело по настоящему изобретению содержит Fc-часть, чтобы продлить период полураспада. Такая Fc-последовательность имеет предпочтительно человеческое происхождение, более предпочтительно, представляет собой человеческую Fc- последовательность антитела IgG, более предпочтительно IgG2, еще более предпочтительно, представляет собой последовательность, представленную в SEQ ID NO:5. При этом выбор Fc-последовательности типа IgG2 позволяет обеспечить снижение эффекторной нагрузки, обусловленной Fc-последовательностью и снизить таким образом направленную токсичность антитела по изобретению. The antibody of the present invention contains an Fc portion to extend the half-life. Such an Fc sequence is preferably of human origin, more preferably is the human Fc sequence of an IgG antibody, more preferably IgG2, even more preferably, is the sequence shown in SEQ ID NO: 5. In this case, the selection of an IgG2-type Fc sequence allows one to reduce the effector load due to the Fc sequence and thus reduce the directed toxicity of the antibody of the invention.
Термин "линкер", используемый в соответствии с настоящим изобретением, относится к пептидным линкерам. Длина и/или последовательность линкера влияет на стабильность и/или растворимость биспецифической молекулы. Линкер может повысить гибкость полученной связывающей молекулы и/или может улучшить связывание ее с антигеном-мишенью путем уменьшения стерических помех. Длина и последовательность линкера зависит от последовательности и длины связываемых последовательностей. Специалисту хорошо известны способы тестирования пригодности различных линкеров. Например, свойства связывающей молекулы можно легко протестировать путем анализа ее аффинности связывания при использовании различных типов линкеров. Стабильность полученной молекулы можно измерить способами, известными в данной области техники, такими как, например, высокоэффективная жидкостная храматография, разделяющая исследуемый белковый материал на фракции, в зависимости от молекулярной массы белка и гидродинамических характеристик. The term “linker” as used in accordance with the present invention refers to peptide linkers. The length and / or sequence of the linker affects the stability and / or solubility of the bispecific molecule. The linker can increase the flexibility of the resulting binding molecule and / or can improve its binding to the target antigen by reducing steric interference. The length and sequence of the linker depends on the sequence and length of the linked sequences. Methods for testing the suitability of various linkers are well known to the skilled person. For example, the properties of a binding molecule can be easily tested by analyzing its binding affinity using various types of linkers. The stability of the obtained molecule can be measured by methods known in the art, such as, for example, high-performance liquid chromatography, dividing the studied protein material into fractions, depending on the molecular weight of the protein and hydrodynamic characteristics.
Особенно предпочтительными являются линкеры, которые представляют собой пептиды, состоящие по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или 100% из небольших аминокислот, таких как глицин, серии и аланин. Особенно предпочтительными являются линкеры, состоящие только из молекул глицина и серина. ю Предпочтительно линкерные последовательности по изобретению состоят из 5-15 аминокислот. Более предпочтительно, чтобы линкеры LI, L2, L3 антитела против CD3*CD19 по изобретению были выбраны из следующих последовательностей: Linkers that are peptides consisting of at least 50%, at least 60%, at least 70%, at least 80%, at least 90%, or 100% of small amino acids, such as glycine, series and alanine. Linkers consisting solely of glycine and serine molecules are particularly preferred. Yu Preferably, the linker sequences of the invention are comprised of 5-15 amino acids. More preferably, the LI, L2, L3 linkers of the anti-CD3 * CD19 antibody of the invention are selected from the following sequences:
LI : (XXS)k, где k=2-3, L2: (XXS)n, где п =4-5, L3: (XXS)m, где m=2-3, X=G. LI: (XXS) k, where k = 2-3, L2: (XXS) n, where n = 4-5, L3: (XXS) m, where m = 2-3, X = G.
Еще более предпочтительно использовать в антителе по изобретению LI, L2, L3 с последовательностями, представленными в SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8. It is even more preferable to use LI, L2, L3 in the antibody of the invention with the sequences shown in SEQ ID NO: 6, SEQ ID NO: 7, SEQ ID NO: 8.
Термин "шарнирная область", используемый в соответствии с настоящим изобретением, относится к последовательности, которая в природном иммуноглобулине связывает СН1 -домен с областью СН2-СНЗ Fc-фрагмента. Шарнирная область, используемая в антителе по изобретению предпочтительно гомологична природной области иммуноглобулина и обычно включает цистеиновые остатки, связывающие две тяжелые цепи посредством дисульфидных связей, как в природных иммуноглобулинах. Типичные последовательности шарнирных областей иммуноглобулинов человека и мыши можно найти в ANTIBODY ENGINEERING, a PRACTICAL GUIDE, (Borrebaeck, ed., W. H. Freeman and Co., 1992). Подходящие шарнирные области по настоящему изобретению могут происходить от IgGl, IgG2, IgG3, IgG4 и других изотипов иммуноглобулинов. Наиболее предпочтительно в конструкции антитела по изобретению использовать шарнирную область IgGl с последовательностью, представленной в SEQ ID NO: 9. The term “hinge region”, used in accordance with the present invention, refers to a sequence that in a natural immunoglobulin binds the CH1 domain to the region of the CH2-CH3 Fc fragment. The hinge region used in the antibody of the invention is preferably homologous to the natural region of the immunoglobulin and typically includes cysteine residues linking the two heavy chains via disulfide bonds, as in natural immunoglobulins. Typical hinge sequences of human and mouse immunoglobulins can be found in ANTIBODY ENGINEERING, a PRACTICAL GUIDE, (Borrebaeck, ed., W. H. Freeman and Co., 1992). Suitable hinge regions of the present invention may be derived from IgGl, IgG2, IgG3, IgG4 and other immunoglobulin isotypes. Most preferably, the IgGl hinge region with the sequence shown in SEQ ID NO: 9 is used in the antibody construct of the invention.
Порядок расположения вариабельных областей в конструкции антитела по изобретению носит принцпиальный характер. Авторами была проведена работа по оценке in vitro токсичности по релизу провоспалительных цитокинов и CD3 опосредованной цитотоксичности антитела по отношению к CD 19+ опухолевым клеткам (здесь и далее цитотоксическая биологическая активность) различных вариантов биспецифического антитела формата BiMS: The arrangement of the variable regions in the construction of the antibody of the invention is of principle principle. The authors carried out work to assess in vitro toxicity for the release of pro-inflammatory cytokines and CD3-mediated antibody cytotoxicity against CD 19+ tumor cells (hereinafter, cytotoxic biological activity) of various variants of the bispecific BiMS format antibody:
VL(CD3)-Ll-VH(CD19)-L2-VL(CD19)-L3-VH(CD3)-H-CH2-CH3(IgG) (целевой), VH(CD19)-L1- VL(CD3) -L2- VH(CD3) -L3- VL(CD19) -H-CH2-CH3(IgG), VL (CD3) -Ll-VH (CD19) -L2-VL (CD19) -L3-VH (CD3) -H-CH2-CH3 (IgG) (target), VH (CD19) -L1-VL (CD3) - L2-VH (CD3) -L3-VL (CD19) -H-CH2-CH3 (IgG),
VH(CD3)-Ll-VH(CD19)-L2-VL(CD19)-L3-VL(CD3)-H-CH2-CH3(IgG), VH (CD3) -Ll-VH (CD19) -L2-VL (CD19) -L3-VL (CD3) -H-CH2-CH3 (IgG),
VH(CD19)-L1- VH(CD3) -L2- VL(CD3) -L3- VL(CD19) -H-CH2-CH3(IgG), в результате которых была установлена высокая цитотоксическая биологическая активность и низкая токсическая активность варианта биспецифического антитела VL(CD3)-L1- VH(CD19)-L2-VL(CD19)-L3-VH(CD3)-H-CH2-CH3(IgG), что может быть гипотетически связано с высокой аффинностью антитела из-за конформации вариабельных доменов по изобретению по отношению к CD3 специфичности. В наиболее предпочтительном варианте исполнения настоящего изобретения антитело против CD3*CD19 характеризуется последовательностью SEQ ID NO:10. Однако специалисту в данной области ясно, что без излишнего экспериментирования и затрат изобретательского творчества, руководствуясь раскрытыми выше сведениями, он может создать антитело по изобретению с другой последовательностью, но обладающее высокой эффективностью в отношении лечения злокачественных заболеваний В-клеток, истощения В-клеток или замедления развития патологических состояний, ассоциированных с В- клеточными нарушениями, и при этом удобное в применении и получении по сравнению с блинатумомабом. В качестве критерия отбора подходящих последовательностей антител по изобретению может быть использована специфичность/эффективность связывания с CD3 и CD 19, характерная для антитела с последовательностью, представленной в SEQ ID NO: 10 (см. Пример 3), время полужизни антитела в крови от около 40 ч., более предпочтительно от около 65 ч. VH (CD19) -L1- VH (CD3) -L2- VL (CD3) -L3- VL (CD19) -H-CH2-CH3 (IgG), as a result of which high cytotoxic biological activity and low toxicity of the bispecific variant were established antibodies VL (CD3) -L1-VH (CD19) -L2-VL (CD19) -L3-VH (CD3) -H-CH2-CH3 (IgG), which may be hypothetically associated with high affinity of the antibody due to the conformation of variable domains according to the invention in relation to CD3 specificity. In a most preferred embodiment of the present invention, an anti-CD3 * CD19 antibody is characterized by the sequence of SEQ ID NO: 10. However, the specialist in this field it is clear that without undue experimentation and the cost of inventive creativity, guided by the above disclosure, he can create an antibody according to the invention with a different sequence, but with high efficiency in the treatment of malignant diseases of b-cells, depletion of b-cells or slow development of pathological conditions associated with B-cell disorders, and at the same time convenient in use and preparation compared with blinatumomab. As a criterion for selecting suitable antibody sequences of the invention, specificity / binding efficiency of CD3 and CD 19, characteristic of an antibody with the sequence shown in SEQ ID NO: 10 (see Example 3), blood half-life from about 40, can be used hours, more preferably from about 65 hours
Антитело против CD3*CD19 по изобретению кодируется нуклеиновой кислотой, структура которой может быть выведена известными в данной области специалистам методами из структуры указанного антитела. В частности, в наиболее предпочтительном варианте осуществления настоящего изобретения нуклеиновая кислота по изобретению имеет нуклеотидную последовательность, выведенную из аминокислотной последовательности, представленной в SEQ ID NO: 10. При этом кодонный состав последовательности нуклеиновой кислоты по изобретению выбирается таким образом, чтобы в выбранной клетке-хозяине достигались максимальные уровни ее транскрипции и последующей трансляции. Термин «нуклеиновая кислота», используемый в соответствии с настоящим изобретением, относится предпочтительно к ДНК. Однако данный термин также может относится к РНК. The anti-CD3 * CD19 antibody of the invention is encoded by a nucleic acid, the structure of which can be derived by methods known in the art from the structure of the indicated antibody. In particular, in the most preferred embodiment of the present invention, the nucleic acid of the invention has a nucleotide sequence deduced from the amino acid sequence shown in SEQ ID NO: 10. The codon composition of the nucleic acid sequence of the invention is selected so that in the selected host cell maximum levels of its transcription and subsequent translation were achieved. The term "nucleic acid" as used in accordance with the present invention preferably refers to DNA. However, this term may also refer to RNA.
В одном варианте осуществления настоящего изобретения клетка-хозяин может содержать последовательность нуклеиновой кислоты по изобретению, стабильно встроенную в клеточный геном. В другом варианте осуществления настоящего изобретения клетка-хозяин содержит последовательность нуклеиновой кислоты по изобретению функционально встроенную для целей экспрессии в конструкции типа вектора для экспрессии или линейного экспрессирующего элемента. In one embodiment of the present invention, the host cell may comprise a nucleic acid sequence of the invention stably integrated into the cellular genome. In another embodiment of the present invention, the host cell comprises a nucleic acid sequence of the invention operably integrated for expression in a vector type construct for expression or a linear expression element.
В наиболее предпочтительном варианте осуществления настоящего изобретения экспрессия антитела против CD3*CD19 по изобретению в клетке-хозяине обеспечивается с помощью вектора для обеспечения экспрессии. Термин «вектор для обеспечения экспрессии», используемый в соответствии с настоящим изобретением, относится к любому подходящему вектору, включая хромосомные, внехромосомные векторы и векторы из синтетической нуклеиновой кислоты, содержащей подходящий набор контролирующих экспрессию элементов. In a most preferred embodiment of the present invention, expression of an anti-CD3 * CD19 antibody of the invention in a host cell is provided using a vector for expression. The term “expression vector” as used in accordance with the present invention refers to any suitable vector, including chromosomal, extrachromosomal vectors and synthetic nucleic acid vectors containing a suitable set of expression control elements.
Вектор для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению предпочтительно сконструирован таким образом, чтобы обеспечить экспрессию нуклеиновой кислоты по изобретению в клетках млекопитающих. Однако указанный вектор без ограничения может быть также быть сконструирован для обеспечения экспрессии нуклеиновой кислоты по изобретению в клетках растений, бактерий, дрожжей, животных, отличных от млекопитающих. Примеры таких векторов включают производные SV40, бактериальные плазмиды, фаговые ДНК, бакуловирусы, дрожжевые плазмиды, векторы, полученные из комбинаций плазмид и фаговых ДНК, и векторы из вирусной нуклеиновой кислоты (РНК или ДНК). Подходящие векторы экспрессии иммуноглобулина раскрыты также, например, в McLean et al., Mol. Immunol. 37: 837-45 (2000); Walls et al., Nucleic Acids Res., 21 : 2921-9 (1993) и Norderhaug et al., J. Immunol. Meth. 204: 77-87 (1997). The vector for expressing the bispecific anti-CD3 * CD19 antibody of the invention is preferably constructed to allow expression of the nucleic acid of the invention in mammalian cells. However, the specified vector without limitation can also be constructed to ensure expression of the nucleic acid according to the invention in the cells of plants, bacteria, yeast, animals other than mammals. Examples of such vectors include derivatives of SV40, bacterial plasmids, phage DNA, baculoviruses, yeast plasmids, vectors derived from combinations of plasmids and phage DNA, and vectors from viral nucleic acid (RNA or DNA). Suitable immunoglobulin expression vectors are also disclosed, for example, in McLean et al., Mol. Immunol. 37: 837-45 (2000); Walls et al., Nucleic Acids Res., 21: 2921-9 (1993) and Norderhaug et al., J. Immunol. Meth. 204: 77-87 (1997).
Вектор для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению может быть одновременно быть вектором для клонирования и обладать способностью автономно реплицироваться в бактериальных, дрожжевых и иных клетках, а также быть пригодным для получения нуклеиновой кислоты, кодирующей антитело против CD3*CD19 по изобретению, путем обработки указанного клонирующего вектора подходящими рестриктазами. Однако более предпочтительно, чтобы вектор для клонирования, содержащий нуклеиновую кислоту, кодирующую антитело против CD3*CD19 по изобретению, не содержал дополнительно элементов для обеспечения экспрессии указанной нуклеиновой кислоты для повышения эффективности его амплификации в клетке-хозяине. A vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention may simultaneously be a cloning vector and have the ability to autonomously replicate in bacterial, yeast and other cells, and also be suitable for the production of a nucleic acid encoding an anti-CD3 * CD19 antibody of the invention, by treating said cloning vector with suitable restriction enzymes. However, it is more preferable that the cloning vector containing a nucleic acid encoding an anti-CD3 * CD19 antibody of the invention does not additionally contain elements for expressing said nucleic acid to enhance its amplification in the host cell.
В одном варианте осуществления настоящего изобретения вектор для обеспечения экспрессии представляет собой вектор, который подходит для экспрессии антитела в бактериальных клетках. Примеры таких векторов включают векторы BlueScript (Stratagene), векторы pIN, векторы рЕТ (Novagen, Madison WI) и др. In one embodiment of the present invention, the expression vector is a vector that is suitable for expression of an antibody in bacterial cells. Examples of such vectors include BlueScript vectors (Stratagene), pIN vectors, pET vectors (Novagen, Madison WI), and others.
В другом варианте осуществления настоящего изобретения вектор для обеспечения экспрессии представляет собой вектор, который подходит для экспрессии в дрожжевой системе. Подходящие векторы включают, к примеру, векторы, содержащие конститутивные или индуцибельные промоторы типа альфа-фактора, алкоголь-оксидазы и PGH. В следующем варианте осуществления настоящего изобретения вектор для обеспечения экспрессии представляет собой вектор, который подходит для экспрессии антитела в растении. Подходящие векторы включают, например, векторы, раскрытые в патенте РФ RU2412251, опубликованном 20.02.2011. In another embodiment of the present invention, the expression vector is a vector that is suitable for expression in the yeast system. Suitable vectors include, for example, vectors containing constitutive or inducible promoters such as alpha factor, alcohol oxidase and PGH. In a further embodiment of the invention, the expression vector is a vector that is suitable for expression of an antibody in a plant. Suitable vectors include, for example, vectors disclosed in RF patent RU2412251, published on 02.20.2011.
В следующем варианте осуществления настоящего изобретения вектор для обеспечения экспрессии представляет собой вектор, который подходит для экспрессии антитела в насекомом. Подходящие векторы включают, например, векторы, раскрытые в международной заявке с номером публикации WO 2010/025764 от 11.03.2010. In a further embodiment of the invention, the expression vector is a vector that is suitable for expression of an antibody in an insect. Suitable vectors include, for example, vectors disclosed in international application publication number WO 2010/025764 of 03/11/2010.
В наиболее предпочтительном варианте осуществления настоящего изобретения вектор для обеспечения экспрессии представляет собой вектор, который подходит для экспрессии антитела в клетках китайского хомячка. In a most preferred embodiment of the present invention, the expression vector is a vector that is suitable for expression of the antibody in Chinese hamster cells.
В векторе для экспрессии по изобретению нуклеиновая кислота, кодирующая антитело по изобретению, может быть связана с любым подходящим промотором, энхансером и другими способствующими экспрессии элементами. При этом указанные элементы выбирают на основе типа клетки-хозяина. In the expression vector of the invention, the nucleic acid encoding the antibody of the invention may be coupled to any suitable promoter, enhancer and other expression promoting elements. Moreover, these elements are selected based on the type of host cell.
В частности, сайт инициации репликации из плазмиды pBR322 (Product No. 303-3s, New England Biolabs, Beverly, Mass) применим для большинства грамотрицательных бактерий, тогда как различные сайты инициации репликации из SV40, полиомавируса, аденовируса, вируса везикулярного стоматита (VSV) или папилломавирусов (таких как HPV или BPV) могут быть использованы для клонирования векторов в клетках млекопитающих. In particular, the replication initiation site from plasmid pBR322 (Product No. 303-3s, New England Biolabs, Beverly, Mass) is applicable to most gram-negative bacteria, while the different replication initiation sites are from SV40, polyomavirus, adenovirus, and vesicular stomatitis virus (VSV) or papillomaviruses (such as HPV or BPV) can be used to clone vectors in mammalian cells.
Последовательность терминации транскрипции обычно локализована 3' (справа) от конца кодирующих областей полипептида и служит для терминации транскрипции. Последовательности терминации транскрипции в прокариотических клетках часто содержат G-C-богатый фрагмент, за которым следует поли Т-последовательность. Последовательности терминации транскрипции могут быть клонированы из библиотеки, приобретенной коммерчески, в виде части вектора. The transcription termination sequence is usually located 3 '(to the right) from the end of the coding regions of the polypeptide and serves to terminate the transcription. Transcription termination sequences in prokaryotic cells often contain a G-C-rich fragment, followed by a poly T-sequence. Transcription termination sequences can be cloned from a library purchased commercially as part of a vector.
Элемент гена селектируемого маркера кодирует белок, необходимый для выживания и роста клетки-хозяина, выращиваемой в селективной культуральной среде. Обычные гены селектируемого маркера кодируют белки, которые (а) придают устойчивость к антибиотикам или другим токсинам, например, ампициллину, тетрациклину или канамицину для прокариотических клеток-хозяев, (Ь) дополняют ауксотрофные недостаточности клетки; или (с) поставляют необходимые питательные вещества. Предпочтительными селектируемыми маркерами являются ген устойчивости к канамицину, ген устойчивости к ампициллину и ген устойчивости к тетрациклину. Ген устойчивости к неомицину может быть также использован для отбора в прокариотических и эукариотических клетках-хозяевах. A selectable marker gene element encodes a protein necessary for the survival and growth of a host cell grown in a selective culture medium. Conventional selectable marker genes encode proteins that (a) confer resistance to antibiotics or other toxins, for example, ampicillin, tetracycline or kanamycin for prokaryotic host cells, (b) supplement auxotrophic cell deficiencies; or (c) supply the necessary nutrients. Preferred breeding markers are the kanamycin resistance gene, the ampicillin resistance gene, and the gene resistance to tetracycline. The neomycin resistance gene can also be used for selection in prokaryotic and eukaryotic host cells.
Примеры селектируемых маркеров для клеток млекопитающих включают дигидрофолатредуктазу (DHFR) и тимидинкиназу. Трансформанты клеток млекопитающих помещают в условия давления отбора, к которому адаптированы для выживания только трансформанты, благодаря маркеру, присутствующему в векторе. Давление отбора накладывается культивированием трансформированных клеток в условиях, в которых концентрация агента отбора в среде последовательно изменяется, что приводит к амплификации как гена отбора, так и целевой нуклеиновой кислоты, кодирующей антитело по изобретению. В результате амплифицированное таким образом количество нуклеиновой кислоты, кодирующей антитело по изобретению, позволит получить увеличенные количества указанного антитела. Examples of breeding markers for mammalian cells include dihydrofolate reductase (DHFR) and thymidine kinase. Mammalian cell transformants are placed under selection pressure conditions, to which only transformants are adapted for survival, due to the marker present in the vector. The selection pressure is superimposed by culturing the transformed cells under conditions in which the concentration of the selection agent in the medium changes sequentially, which leads to amplification of both the selection gene and the target nucleic acid encoding the antibody of the invention. As a result, the amount of nucleic acid encoding the antibody of the invention amplified in this way will produce increased amounts of the antibody.
Сайт связывания рибосом обычно присутствует для инициации трансляции мРНК. Например, такой сайт характеризуется последовательностью Шайна-Далгарно (прокариоты) или последовательностью Козака (эукариоты). Данный элемент обычно расположен 3' (справа) от промотора и 5' (слева) от кодирующей последовательности экспрессируемого полипептида. Последовательность Шайна-Дальгарно варьируется, но обычно представляет собой полипурин (имеющий высокое содержание A-G). Были идентифицированы многие последовательности Шайна-Дальгарно, каждая из которых может быть легко синтезирована с использованием способов, представленных выше и используемых в прокариотическом векторе. The ribosome binding site is usually present to initiate translation of mRNA. For example, such a site is characterized by a Shine-Dalgarno sequence (prokaryotes) or a Kozak sequence (eukaryotes). This element is usually located 3 '(right) from the promoter and 5' (left) from the coding sequence of the expressed polypeptide. The Shine-Dalgarno sequence varies, but is usually polypurine (having a high A-G content). Many Shine-Dalgarno sequences have been identified, each of which can be easily synthesized using the methods presented above and used in the prokaryotic vector.
Энхансерная последовательность может быть встроена в вектор для увеличения транскрипции в эукариотических клетках-хозяевах. Известны несколько энхансерных последовательностей генов млекопитающих (например, глобина, эластазы, альбумина, альфа-фетопротеина и инсулина). Однако обычно следует использовать энхансер из вируса. Энхансер SV40, энхансер раннего промотора цитомегаловируса, энхансер полиомавируса и энхансеры аденовируса являются примерами энхансерных элементов для активации эукариотических промоторов. An enhancer sequence can be inserted into a vector to increase transcription in eukaryotic host cells. Several enhancer sequences of mammalian genes are known (e.g., globin, elastase, albumin, alpha-fetoprotein and insulin). However, usually a virus enhancer should be used. The SV40 enhancer, cytomegalovirus early promoter enhancer, polyomavirus enhancer and adenovirus enhancers are examples of enhancer elements for activating eukaryotic promoters.
Компоненты вектора могут быть гомологичными (из одного и того же вида и/или штамма, что и клетка-хозяин), гетерологичными (из вида, иного, чем вид или штамм клетки- хозяина), гибридными (комбинацией различных последовательностей из более чем одного источника), синтетическими или нативными последовательностями, которые обычно действуют в качестве регуляторов экспрессии иммуноглобулина. Источниками компонентов вектора могут быть любой прокариотический или эукариотический организм, любой позвоночный или беспозвоночный организм, или любое растение, при условии, что данные компоненты являются функциональными в механизме клетки-хозяина и могут быть активированы механизмом клетки-хозяина. The components of the vector can be homologous (from the same species and / or strain as the host cell), heterologous (from a species other than the species or strain of the host cell), hybrid (a combination of different sequences from more than one source ), synthetic or native sequences that typically act as regulators of immunoglobulin expression. The sources of the components of the vector can be any prokaryotic or eukaryotic organism, any a vertebrate or invertebrate organism, or any plant, provided that these components are functional in the mechanism of the host cell and can be activated by the mechanism of the host cell.
В наиболее предпочтительном варианте осуществления настоящего изобретения вектор для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению представляет собой вектор для обеспечения гетерологичной экспрессии в клетках китайского хомячка (СНО). In a most preferred embodiment of the present invention, the vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention is a vector for providing heterologous expression in Chinese hamster cells (CHO).
Вектор для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению может дополнительно содержать последовательность нуклеиновой кислоты, кодирующую последовательность секреции/ локализации, которая может направлять полипептид в периплазматическое пространство или в культуральную среду. Такие последовательности известны в данной области и включают лидеры секреции или сигнальные пептиды, последовательности, нацеленные на органеллы (например, последовательности ядерной локализации, сигналы удержания в ER, митохондриальные транзитные последовательности, хлоропластные транзитные последовательности), последовательности мембранной локализации/якорные (например, последовательности остановки транслокации, якорные последовательности GPI) и др., которые хорошо известны в области настоящего изобретения. A vector for expressing a bispecific anti-CD3 * CD19 antibody of the invention may further comprise a nucleic acid sequence encoding a secretion / localization sequence that can direct the polypeptide into the periplasmic space or into the culture medium. Such sequences are known in the art and include secretion leaders or signal peptides, organelle targeting sequences (e.g., nuclear localization sequences, ER retention signals, mitochondrial transit sequences, chloroplast transit sequences), membrane localization / anchor sequences (e.g. stop sequences translocations, GPI anchor sequences), etc., which are well known in the field of the present invention.
Рекомбинантная экспрессия антитела против CD3*CD19 по изобретению может осуществляться в любых подходящих клетках-хозяевах, известных в данной области. При этом условия для экспрессии подбираются индивидуально для типа клетки-хозяина и используемых элементов для гетерологичной экспрессии. Recombinant expression of an anti-CD3 * CD19 antibody of the invention can be carried out in any suitable host cells known in the art. Moreover, the conditions for expression are selected individually for the type of the host cell and the elements used for heterologous expression.
Термин "клетка хозяина" в настоящем изобретении служит для обозначения клеток, в которые был введен экспрессирующий вектор по изобретению. Следует иметь в виду, что данный термин служит как для обозначения самих трансформантов, так и их потомства. При этом несмотря на то, что в последующих поколениях возможно появление модификаций вследствие воздействия окружающей среды или искусственного мутагенеза, то к такому потомству также должен быть применен термина "клетка-хозяин" в соответствии с настоящим изобретением. Клетка-хозяин по изобретению может быть эукариотической и прокариотической. Прокариотическая клетка-хозяин может быть, в том числе, бактериальной клеткой. Эукариотическая клетка-хозяин может быть, в том числе, дрожжевой клеткой, клеткой млекопитающего, клеткой животного, не являющегося млекопитающим, например, клеткой насекомого, клеткой растения. В частности, эукариотические клетки-хозяева по настоящему изобретению могут представлять собой клетки СНО, клетки НЕК-293, клетки НЕК-294, клетки PER.C6, клетки NS0 и клетки лимфоцитов, а также прокариотические клетки типа Е. coli. The term "host cell" in the present invention is used to refer to cells into which the expression vector of the invention has been introduced. It should be borne in mind that this term serves both to refer to the transformants themselves and their offspring. Moreover, although modifications may occur in subsequent generations due to environmental influences or artificial mutagenesis, the term “host cell” in accordance with the present invention should also be applied to such progeny. A host cell of the invention may be eukaryotic and prokaryotic. A prokaryotic host cell may be, inter alia, a bacterial cell. The eukaryotic host cell may be, inter alia, a yeast cell, a mammalian cell, a non-mammalian animal cell, for example, an insect cell, a plant cell. In particular, eukaryotic host cells of the present invention may be CHO cells, HEK-293 cells, HEK-294 cells, PER.C6 cells, NS0 cells and lymphocyte cells, as well as prokaryotic cells such as E. coli.
Некоторые варианты осуществления настоящего изобретения включают введение вектора для обеспечения экспрессии по изобретению в клетку-хозяина in vivo, т.е. в такую клетку, которая находится в составе живого многоклеточного организма. Указанным организмом предпочтительно является человек. Some embodiments of the present invention include the introduction of a vector to allow expression of the invention in an in vivo host cell, i.e. into a cell that is part of a living multicellular organism. The specified organism is preferably a person.
Согласно настоящему изобретению для экспрессии антитела можно использовать различные комбинации клетка-хозяин для экспрессии / вектор для обеспечения экспрессии. При этом необходимо выбирать вектор с учетом сохранения им функциональности в клетке- хозяине, в которой будет введен указанный вектор. Вектор должен быть совместим с механизмом клетки-хозяина, так чтобы была возможна амплификация и экспрессия. Например, к экспрессионным векторам, подходящим для эукариотических хозяев, относятся SV40, вирус папиломы крупного рогатого скота, аденовирус, аденоассоциированный вирус, цитомегаловирус и ретровирус. К экспрессионным векторам, которые можно применять в бактериальных хозяевах, относятся бактериальные плазмиды, такие как pBluescript, pGEX2T, pUC, pCRl , pBR322, pMB9 и их производные, плазмиды наподобие RP4, характеризующиеся широким списком возможных хозяев, gtlO и λΐ 1, фаговая ДНК, представленная различными производными фага лямбда, такими как ΝΜ989, и другие фаговые ДНК, такие как М13 и нитевидный фаг с одноцепочной ДНК. Экспрессионные векторы, которые можно использовать с дрожжевыми клетками, включают плазмиду 2μ и ее производные. Вектор, который можно применять в клетках насекомых, - pVL941. According to the present invention, various expression host / vector combinations for expression can be used to express the antibody. In this case, it is necessary to choose a vector taking into account the preservation of its functionality in the host cell in which the specified vector will be introduced. The vector must be compatible with the mechanism of the host cell, so that amplification and expression are possible. For example, expression vectors suitable for eukaryotic hosts include SV40, cattle papilloma virus, adenovirus, adeno-associated virus, cytomegalovirus and retrovirus. Expression vectors that can be used in bacterial hosts include bacterial plasmids such as pBluescript, pGEX2T, pUC, pCRl, pBR322, pMB9 and their derivatives, plasmids like RP4, characterized by a wide list of possible hosts, gtlO and λΐ 1, phage DNA, represented by various lambda phage derivatives, such as ΝΜ989, and other phage DNAs, such as M13 and single-stranded filamentous phage. Expression vectors that can be used with yeast cells include plasmid 2μ and its derivatives. A vector that can be used in insect cells is pVL941.
В наиболее предпочтительном варианте осуществления настоящего изобретения для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению используют комбинацию вектора для обеспечения гетерологичной экспрессии в клетках китайского хомячка с клетками коммерчески доступного штамма СНО-М (Selexis). In a most preferred embodiment of the present invention, to combine the expression of the bispecific anti-CD3 * CD19 antibody of the invention, a vector combination is used to provide heterologous expression in Chinese hamster cells with cells of a commercially available CHO-M strain (Selexis).
Клетка-хозяин, экспрессирующая биспецифическое антитело против CD3*CD19 по изобретению, может быть получена трансфекцией исходной клетки вектором для обеспечения экспрессии биспецифического антитела против CD3*CD19 по изобретению с помощью любого известного в данной области способа, в том числе, электропарацией, трансдукцией, кальций-фосфатной трансфекцией, трансфекцией с помощью катионных липидов, «scrape-loading» (соскоб-нагрузка) и инфицирования. A host cell expressing a bispecific anti-CD3 * CD19 antibody of the invention can be obtained by transfection of a parent cell with a vector to allow expression of a bispecific anti-CD3 * CD19 antibody of the invention using any method known in the art, including electroporation, transduction, calcium -phosphate transfection, transfection with cationic lipids, scrape-loading (scraping load) and infection.
Способ получения антитела против CD3*CD19 по изобретению включает культивирование указанной клетки-хозяина в условиях, обеспечивающих экспрессию биспецифического антитела против CD3*CD19 по изобретению и выделения полученного продукта. При этом указанная экспрессия может быть осуществлена, как в условиях мелкомасштабного или крупномасштабного ферментера, так и в условиях инкубации в колбах, на качалке. Инкубацию осуществляют в подходящей питательной среде, содержащей источники углерода и азота и неорганические соли, одним из известных способов. Подходящие среды являются коммерчески доступньми, но могут также быть приготовлены самостоятельно с использованием компонентов, описанных, например, в каталоге Американской Коллекции Типовых Культур (АТСС). В целом, используемый в соответствии с настоящим изобретением термин "среда" включает любую культуральную среду, раствор, твердое, полутвердое вещество или твердую подложку, которые могут поддерживать или содержать любую клетку-хозяина, включая бактериальные клетки-хозяева, дрожжевые клетки-хозяева, клетки-хозяева насекомых, растительные клетки-хозяева, клетки-хозяева млекопитающих, в том числе, клетки СНО. A method for producing an anti-CD3 * CD19 antibody of the invention comprises culturing said host cell under conditions providing expression of a bispecific anti-CD3 * CD19 antibody of the invention and isolating the resulting product. Moreover, this expression can be carried out both under conditions of a small-scale or large-scale fermenter, and under incubation conditions in flasks, on a rocking chair. Incubation is carried out in a suitable nutrient medium containing sources of carbon and nitrogen and inorganic salts, one of the known methods. Suitable media are commercially available, but can also be prepared independently using components described, for example, in the catalog of the American Type Culture Collection (ATCC). In general, the term “medium” as used in accordance with the present invention includes any culture medium, solution, solid, semi-solid or solid support that can support or contain any host cell, including bacterial host cells, yeast host cells, cells - insect hosts, plant host cells, mammalian host cells, including CHO cells.
Антитело по изобретению может быть выделено любым известным в данной области способом. Однако при выборе способа выделения антитела необходимо принимать во внимание особенности использованной системы экспрессии (клетка-хозяин для экспрессии/ вектор для экспрессии). Так, если антитело преимущественно накапливается внутри клетки- хозяина, необходимо выбрать такой способ выделения продукта, который обеспечит извлечение его из клетки-хозяина. Если антитело накапливается преимущественно в культуральную жидкости, то целевой продукт может быть выделен из культуральной жидкости способами, предназначенными для извлечения антител из культуральной жидкости. Например, антитело по изобретению может быть выделено из культуральной жидкости стандартными способами, включающими, без ограничений, хроматографию, центрифугирование, фильтрацию, экстракцию, сушку распыление, выпаривание или осаждение. Антитело по изобретению может быть дополнительно очищено с применением различных технологий, известных в данной области, включая хроматографию (например, ионообменную, аффинную, гидрофобную или эксклюзионную), электрофорез, разделение (например, осаждение сульфатом аммония), ДСН-ПААГ или экстракцию. An antibody of the invention may be isolated by any method known in the art. However, when choosing a method for isolating the antibody, it is necessary to take into account the features of the expression system used (host cell for expression / vector for expression). So, if the antibody mainly accumulates inside the host cell, it is necessary to choose a method of isolating the product that will ensure its extraction from the host cell. If the antibody accumulates predominantly in the culture fluid, the target product can be isolated from the culture fluid by methods designed to extract antibodies from the culture fluid. For example, an antibody of the invention can be isolated from the culture fluid by standard methods, including, without limitation, chromatography, centrifugation, filtration, extraction, drying, spraying, evaporation or precipitation. An antibody of the invention can be further purified using various techniques known in the art, including chromatography (e.g., ion exchange, affinity, hydrophobic or exclusion), electrophoresis, separation (e.g., ammonium sulfate precipitation), SDS-PAGE or extraction.
Предпочтительно способ очистки антитела против CD3*CD19 по изобретению включает по меньшей мере одну стадию хроматографической очистки. Более предпочтительно способ очистки антитела против CD3*CD19 по изобретению включает центрифугирование, аффинную хроматографию с использованием сорбента на основе протеина А и катионообменную хроматографию на сорбенте высокого разрешения. Preferably, the method for purifying an anti-CD3 * CD19 antibody of the invention comprises at least one chromatographic purification step. More preferably, a method for purifying an anti-CD3 * CD19 antibody of the invention comprises centrifugation, affinity chromatography using a protein A sorbent, and high resolution cation exchange chromatography.
Очищенное в соответствии с требованиями регуляторных органов антитело против CD3*CD19 по изобретению включают в фармацевтическую композицию по изобретению предпочтительно совместно с фармацевтически приемлемыми носителями и/или разбавителями. The anti-CD3 * CD19 antibody of the invention purified according to regulatory requirements is included in the pharmaceutical composition of the invention preferably together with pharmaceutically acceptable carriers and / or diluents.
Механизм действия предложенного антитела против CD3*CD19 аналогичен таковому, описанному для анти-СОЗ/анти-С019 антитела - препарата блинатумомаб (МТ103); и заключается в активации мультиспецифичного Т-клеточного цитологического ответа против CD 19+ клеток лимфомы. Поэтому фармацевтические композиции на основе антител против CD3*CD19 по изобретению могут применяться для лечения всех гематологических раковых заболеваний (лимфом и лейкозов) В-клеточной природы, например, таких как В-клеточные опухоли из предшественников В-лимфоцитов, в том числе: В-лимфобластная лимфома/В-клеточный острый лимфобластный лейкоз из клеток- предшественников; В-клеточные опухоли из периферических (зрелых) В-лимфоцитов, в том числе: В-клеточный хронический лимфоцитарный лейкоз/лимфома из малых лимфоцитов (лимфоцитарная лимфома); В-клеточный пролимфоцитарный лейкоз; лимфоплазмоцитарная лимфома; селезеночная лимфома маргинальной зоны; волосатоклеточный лейкоз; плазмоклеточная миелома/плазмоцитома; экстранодальная В- клеточная лимфома маргинальной зоны MALT-типа; нодальная В-клеточная лимфома маргинальной зоны; фолликулярная лимфома; лимфома из клеток мантийной зоны; диффузная В-крупноклеточная лимфома; медиастинальная диффузная В-крупноклеточная лимфома; первичная экссудативная лимфома; лимфома/лейкоз Беркитта, а также для лечения аутоиммунных заболеваний, вызванных патологической регуляцией В-клеток, таких как ревматоидный артрит, системная красная волчанка, гломерулонефрит, рассеянный склероз и миастения гравис. The mechanism of action of the proposed anti-CD3 * CD19 antibody is similar to that described for the anti-POP / anti-C019 antibody, Blinatumomab preparation (MT103); and consists in the activation of a multispecific T-cell cytological response against CD 19+ lymphoma cells. Therefore, pharmaceutical compositions based on antibodies against CD3 * CD19 according to the invention can be used to treat all hematological cancers (lymphomas and leukemia) of B-cell nature, for example, such as B-cell tumors from precursors of B-lymphocytes, including: lymphoblastic lymphoma / B-cell acute lymphoblastic leukemia from progenitor cells; B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma; mantle cell lymphoma; diffuse B-large cell lymphoma; mediastinal diffuse B-large cell lymphoma; primary exudative lymphoma; Burkitt’s lymphoma / leukemia, as well as for the treatment of autoimmune diseases caused by pathological regulation of B cells, such as rheumatoid arthritis, systemic lupus erythematosus, glomerulonephritis, multiple sclerosis and myasthenia gravis.
Фармацевтическая композиция согласно настоящему изобретению может быть применена у животных и человека, напрямую (например, локально в виде инъекций, в том числе, подкожных инъекций). Если композицию, согласно настоящему изобретению, вводят парентерально, например внутривенно, внутрикожно, подкожно, внутрибрюшинно, внутримышечно, буккально, интраорбитально, интрацеребрально, интраспинально, интравентрикулярно, интратекально, интрацеребрально, то композиция предпочтительно включает часть водной или физиологически совместимой жидкой суспензии или раствора, который не оказьшает негативного влияния на баланс электролитов и/или жидкостей у пациентов при доставке пациентам целевой композиции. The pharmaceutical composition according to the present invention can be applied directly to animals and humans (for example, locally in the form of injections, including subcutaneous injections). If the composition according to the present invention is administered parenterally, for example intravenously, intradermally, subcutaneously, intraperitoneally, intramuscularly, buccally, intraorbitally, intracerebrally, intraspinally, intraventricularly, intrathecally, intracerebrally, the composition preferably comprises a portion of an aqueous or physiologically compatible solution or suspension of liquid does not adversely affect the balance of electrolytes and / or liquids in patients upon delivery of the target composition to patients.
Согласно предпочтительному варианту исполнения, фармацевтическую композицию по изобретению получают в форме, пригодной для парентерального введения, предпочтительно для подкожного введения, в том числе, в виде стерильного водного раствора, суспензии, эмульсии, концентрата для приготовления водного раствора, лиофилизированного препарата для приготовления водного раствора, раствора на основе неводного растворителя. According to a preferred embodiment, the pharmaceutical composition of the invention is prepared in a form suitable for parenteral administration, preferably for subcutaneous administration, including in the form of sterile aqueous a solution, suspension, emulsion, concentrate for the preparation of an aqueous solution, a lyophilized preparation for the preparation of an aqueous solution, a solution based on a non-aqueous solvent.
Фармацевтически приемлемые агенты для использования в фармацевтической композиции по изобретению включают носители, эксципиенты, разбавители, антиоксиданты, консерванты, красящие, ароматизирующие и разбавляющие агенты, эмульгирующие агенты, суспендирующие агенты, растворители, наполнители, объемные агенты, буферы, носители доставки, агенты тоничности, сорастворители, увлажняющие агенты, комплексообразующие агенты, буферирующие агенты, антимикробные вещества и поверхностно-активные вещества, как это показано, например, в «Handbook of Pharmaceutical Excipients» (2"d ed. London: The Pharmaceutical Press; 1994). Pharmaceutically acceptable agents for use in the pharmaceutical composition of the invention include carriers, excipients, diluents, antioxidants, preservatives, coloring, flavoring and diluting agents, emulsifying agents, suspending agents, solvents, fillers, bulking agents, buffers, delivery vehicles, tonicity agents, cosolvents , wetting agents, complexing agents, buffering agents, antimicrobial agents and surfactants, as shown, for example, in the "Handbook of Pharmace utical Excipients ”(2" d ed. London: The Pharmaceutical Press; 1994).
При этом в качестве носителя или растворителя для получения стерильного водного раствора может быть использован в соответствии с настоящим изобретением, например, или раствор Хэнка, или раствор Рингера, или подходящий буферный раствор, например, физиологический буферный раствор. Буферы могут быть общепринятыми буферами, такими как ацетатный, цитратный, фосфатный, бикарбонатный буферы или Трис-HCl. Ацетатный буфер может иметь рН приблизительно 4-5,5, и Трис-буфер может иметь рН приблизительно 7-8,5. Дополнительные фармацевтические агенты представлены в Remington's Pharmaceutical Sciences, 18th Edition, A.R. Gennaro, ed., Mack Publishing Company, 1990. Безводным растворителем может быть пропиленгликоль, полиэтиленгликоль или оливковое масло или сложный эфир, пригодный для инъекций, такой как этилолеат. Также примером подходящего носителя для цели получения фармацевтической композиции по изобретению является нейтральный забуференный солевой раствор или солевой раствор, смешанный с сывороточным альбумином. In this case, as a carrier or solvent to obtain a sterile aqueous solution, in accordance with the present invention, for example, either Hank's solution, or Ringer's solution, or a suitable buffer solution, for example, physiological buffer solution, can be used. The buffers may be conventional buffers such as acetate, citrate, phosphate, bicarbonate buffers or Tris-HCl. Acetate buffer may have a pH of about 4-5.5, and Tris buffer may have a pH of about 7-8.5. Additional pharmaceutical agents are presented in Remington's Pharmaceutical Sciences, 18th Edition, A.R. Gennaro, ed., Mack Publishing Company, 1990. The anhydrous solvent may be propylene glycol, polyethylene glycol or olive oil or an ester suitable for injection, such as ethyl oleate. Also an example of a suitable carrier for the purpose of preparing the pharmaceutical composition of the invention is a neutral buffered saline or saline mixed with serum albumin.
В качестве вспомогательных веществ фармацевтическая композиция по изобретению может также содержать аскорбиновую кислоту, низкомолекулярные полипептиды, гидрофильные полимеры, такие как поливинилпирролидон, аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин, моносахариды, дисахариды и другие углеводы, включающие глюкозу, маннозу или декстрины, хелатообразующие агенты, такие как EDTA, сахароспирты, такие как маннит или сорбит; солеобразующие противоионы, такие как натрий; и/или неионогенные поверхностно-активные вещества, такие как Твин, плуроники или полиэтиленгликоль (ПЭГ), галогениды щелочных металлов (предпочтительно хлорид натрия или калия), бензалконийхлорид, тимеросал, фенетиловый спирт, метилпарабен, пропилпарабен, хлорексидин, сорбиновую кислоту, пероксид водорода, сложные эфиры сорбитана, полисорбаты, такие как полисорбат 80, трометамин, лецитин, холестерин, тилоксапал, высокомолекулярные структурные добавки (например, аравийскую камедь, альгиновую кислоту, фосфат кальция (двухосновный), целлюлозу, карбоксиметилцеллюлозу, натрийкарбоксиметилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, микрокристаллическую целлюлозу, декстран, декстрин, декстраты, сахарозу, тилозу, предварительно желатинизированный крахмал, сульфат кальция, амилозу, глицин, бентонит, мальтозу, сорбит, этилцеллюлозу, динатрийгидрофосфат, динатрийфосфат, динатрийпиросульфит, поливиниловый спирт, желатин, глюкозу, гуаровую камедь, жидкую глюкозу, прессуемый сахар, силикат магния-алюминия, мальтодекстрин, полиэтиленоксид, полиметакрилаты, повидон, альгинат натрия, трагакант, микрокристаллическую целлюлозу, крахмал и зеин). As adjuvants, the pharmaceutical composition of the invention may also contain ascorbic acid, low molecular weight polypeptides, hydrophilic polymers such as polyvinylpyrrolidone, amino acids such as glycine, glutamine, asparagine, arginine or lysine, monosaccharides, disaccharides and other carbohydrates including glucose, mannose dextrins, chelating agents such as EDTA, sugar alcohols such as mannitol or sorbitol; salt forming counterions, such as sodium; and / or nonionic surfactants such as tween, pluronic or polyethylene glycol (PEG), alkali metal halides (preferably sodium or potassium chloride), benzalkonium chloride, thimerosal, phenethyl alcohol, methyl paraben, propyl paraben, chlororexidine, sorbic acid, peroxide hydrogen, sorbitan esters, polysorbates such as polysorbate 80, tromethamine, lecithin, cholesterol, tyloxapal, high molecular weight structural additives (for example, gum arabic, alginic acid, calcium phosphate (dibasic), cellulose, carboxymethyl cellulose, hydroxyloxy cellulose cellulose cellulose cellulose cellulose microcrystalline cellulose, dextran, dextrin, dextrates, sucrose, tylose, pregelatinized starch, calcium sulfate, amylose, glycine, bentonite, maltose, sorbitol, ethyl cellulose, disodium hydrogen phosphate, disodium phosphate, disodium pyrosulphite, polyvinyl alcohol, gelatin, glucose, guar gum, liquid glucose, pressed sugar, magnesium-aluminum silicate, maltodextrin polyethylene glycol polyethylene glycol polyethylene glycol polyethylene glycol polyethylene glycol polyethylene glycol , starch and zein).
Наиболее предпочтительным вспомогательными веществами для использования в фармацевтической композиции по изобретению являются: натрий-фосфатный буфер, полисорбат 80 в качестве поверхностно-активного вещества, маннит в качестве изотонического агента и гистидин в качестве стабилизатора. The most preferred adjuvants for use in the pharmaceutical composition of the invention are: sodium phosphate buffer, polysorbate 80 as a surfactant, mannitol as an isotonic agent, and histidine as a stabilizer.
Указанные эксципиенты могут использоваться в комбинации с другими активными ингредиентами (например, противораковыми или противовоспалительными средствами) при условии, что они не вызывают нежелательных эффектов. These excipients can be used in combination with other active ingredients (for example, anti-cancer or anti-inflammatory drugs), provided that they do not cause unwanted effects.
Если фармацевтическая композиция по изобретению представляет собой лиофилизированную композицию, то она может дополнительно содержать один или несколько лиопротекторов, раскрытых, например, в патентах США 6685940, 6566329 и 6372716. В одном варианте осуществления настоящего изобретения в фармацевтической композиции используют лиопротектор, который является нередуцирующим сахаром, таким как сахароза, лактоза или трегалоза. Количество лиопротектора выбирается предпочтительно так, чтобы после восстановления полученная готовая форма являлась изотонической. При этом одновременно выбранное количество лиопротектора должно быть достаточным для предотвращения неприемлемого количества деградации и/или агрегации белка после лиофилизации. Примеры концентраций лиопротекторов для Сахаров (например, сахарозы, лактозы, трегалозы) в предварительно лиофилизированной композиции составляют приблизительно от 10 мМ до приблизительно 400 мМ. If the pharmaceutical composition of the invention is a lyophilized composition, it may further comprise one or more lyoprotectants disclosed, for example, in US Pat. Nos. 6,659,540, 6,566,329 and 6,373,716. In one embodiment of the present invention, a lyoprotectant, which is a non-reducing sugar, such as sucrose, lactose or trehalose. The amount of lyoprotectant is preferably chosen so that after recovery, the resulting finished form is isotonic. At the same time, the selected amount of lyoprotectant should be sufficient to prevent an unacceptable amount of protein degradation and / or aggregation after lyophilization. Examples of sugar lyoprotectant concentrations (e.g., sucrose, lactose, trehalose) in a pre-lyophilized composition are from about 10 mM to about 400 mM.
Фармацевтическая композиция по изобретению, если получена в лиофилизированной форме, может дополнительно комплектоваться фармацевтически приемлемым растворителем и/или разбавителем, например, водой, физиологическим раствором и другими обычно применяемыми фармацевтически приемлемыми растворителями . The pharmaceutical composition according to the invention, if obtained in lyophilized form, can be optionally completed with a pharmaceutically acceptable solvent and / or diluent, for example, physiological water solution and other commonly used pharmaceutically acceptable solvents.
Фармацевтические композиции могут содержать терапевтически эффективное количество количество антител по изобретению. Pharmaceutical compositions may contain a therapeutically effective amount of an antibody of the invention.
Термин «терапевтически эффективное количество», используемый в соответствии с настоящим изобретением, относится к такому количеству антитела по изобретению, которое является эффективным в течение необходимых периодов времени для достижения желаемого терапевтического результата, причем любые токсичные или вредные эффекты от данного антитела должны перевешиваться терапевтически благоприятными эффектами от данного антитела, которыми в предпочтительном варианте осуществления настоящего изобретения является по меньшей мере одно из следующего: ослабление симптомов, выздоровление или увеличение скорости выздоровления. Терапевтически эффективное количество антитела по изобретению может варьироваться в соответствии с такими факторами, как состояние болезни, возраст, пол и масса индивидуума, способность антитела индуцировать желаемую реакцию конкретно у данного индивидуума, наличие сопутствующих заболеваний, способ введения, частота введения, схема предварительного лечения индивидуума. The term “therapeutically effective amount” as used in accordance with the present invention refers to that amount of an antibody of the invention that is effective for the necessary periods of time to achieve the desired therapeutic result, and any toxic or harmful effects of the antibody should be outweighed by therapeutically beneficial effects. from this antibody, which in a preferred embodiment of the present invention is at least one of leduyuschego: symptom relief, healing or increase the speed of recovery. The therapeutically effective amount of an antibody of the invention can vary according to factors such as the condition of the disease, age, gender, and weight of the individual, the ability of the antibody to induce the desired response specifically in the individual, the presence of concomitant diseases, route of administration, frequency of administration, individual treatment regimen.
Специалисту в области техники не составит труда определить эффективное количество антитела по изобретению, исходя из известных правил и закономерностей. В конечном счете, лечащий врач, основываясь на личном опыте и практике, может принять решение по количеству антитела по изобретению, которым целесообразно лечить каждого пациента в отдельности. Более того, сначала лечащий врач может ввести малые дозы антитела по изобретению и по ответу организма пациента скорректировать его количество. Диапазоны доз составляют приблизительно от 0,5 мкг/кг до приблизительно 2 мг/кг в зависимости от вышеуказанных факторов. При этом предпочтительно, фармацевтическая композиция по изобретению содержит 10-100 мкг антитела. It will not be difficult for a person skilled in the art to determine an effective amount of an antibody of the invention based on known rules and patterns. Ultimately, the attending physician, based on personal experience and practice, can decide on the number of antibodies according to the invention, which it is advisable to treat each patient individually. Moreover, the attending physician may first administer small doses of the antibody of the invention and, according to the patient’s response, adjust its amount. Dosage ranges are from about 0.5 μg / kg to about 2 mg / kg, depending on the above factors. In this case, preferably, the pharmaceutical composition according to the invention contains 10-100 μg of antibody.
Фармацевтическую композицию по изобретению готовят, дозируют и вводят в соответствии с принципами надлежащей медицинской практики. Стандартные методы фармацевтических формуляций известны специалистам в данной области (Remington 1995). The pharmaceutical composition according to the invention is prepared, dosed and administered in accordance with the principles of good medical practice. Standard pharmaceutical formulation methods are known to those skilled in the art (Remington 1995).
Способ лечения В-клеточного заболеваня или истощения В-клеток, или замедления развития патологического состояния, ассоциированного с В-клеточными нарушения, по настоящему изобретению включает введение пациенту, нуждающемуся в этом, эффективного количества антитела по изобретению или фармацевтической композиции по изобретению. При этом в предпочтительном варианте осуществления настоящего изобретения антитело вводят пациенту подкожно. При этом антитело против CD3*CD19 по изобретению может быть введено пациенту в комбинации с другим лекарственным средством, в том числе, с по меньшей мере одной из следующих целей: для усиления терапевтического эффекта в отношении В-клеточного заболевания, для уменьшения побочных эффектов при лечении В-клеточного заболевания, для облегчения симптомов В- клеточного заболевания. A method of treating B-cell disease or B-cell depletion, or slowing the development of a pathological condition associated with B-cell disorders of the present invention includes administering to a patient in need thereof an effective amount of an antibody of the invention or a pharmaceutical composition of the invention. Moreover, in a preferred embodiment of the present of the invention, the antibody is administered subcutaneously to the patient. Moreover, the anti-CD3 * CD19 antibody of the invention can be administered to a patient in combination with another drug, including for at least one of the following purposes: to enhance the therapeutic effect against B-cell disease, to reduce side effects during treatment B-cell disease, to alleviate the symptoms of B-cell disease.
Длительность терапии с использованием комбинации по настоящему изобретению изменяется в зависимости от тяжести подлежащего лечению заболевания и состояния, а также в зависимости от потенциальной реакции каждого отдельного пациента. Предполагается, что длительность терапии определяется по выраженности симптомов. В конечном счете, лечащий врач принимает решение о подходящей длительности терапии с использованием комбинации по настоящему изобретению. The duration of therapy using the combination of the present invention varies depending on the severity of the disease to be treated and the condition, and also depending on the potential response of each individual patient. It is assumed that the duration of therapy is determined by the severity of the symptoms. Ultimately, the attending physician decides on the appropriate duration of therapy using the combination of the present invention.
Настоящее изобретение далее иллюстрируется приведенными ниже примерами. В частности, в подтверждение вышеизложенного авторы в эксперименте показали, что: The present invention is further illustrated by the following examples. In particular, in confirmation of the foregoing, the authors in the experiment showed that:
• антитело по изобретению может быть получено с использованием технологически несложных известных рекомбинантных методов, коммерчески доступных средств (вектора, клетки-хозяина, среды) и традиционных методов выделения и очистки антител (Пример 1); • an antibody according to the invention can be obtained using technologically simple known recombinant methods, commercially available agents (vector, host cell, medium) and traditional methods for the isolation and purification of antibodies (Example 1);
• на основе антитела против CD3*CD19 по изобретению может быть технологически простым способом получена фармацевтическая композиция, в том числе, в лиофилизированном виде, пригодном для последующего восстановления традиционными разбавителями (Пример 2). • based on antibodies against CD3 * CD19 according to the invention, a pharmaceutical composition can be obtained in a technologically simple way, including in a lyophilized form suitable for subsequent reconstitution with traditional diluents (Example 2).
Также авторами настоящего изобретения экспериментально продемонстрировано в сравнении с МТ103 значительно увеличенное время полувыведения (Т1/2) и экспозиции (AUC(O-inf)) антитела против CD3*CD19 по изобретению, при сохранении максимальной пиковой концентрации (Сшах) при внутривенном введении, а также повышенная биодоступность антитела против CD3*CD19 по изобретению как при внутривенном, так и при подкожном введении (Пример 4). Дополнительно авторами настоящего изобретения экспериментально подтверждено более высокое сродство антитела по изобретению к CD3 и CD 19 и его более высокая противоопухолевая активность при подкожном введении в сравнении с препаратом МТ103 (Примеры 3 и 5). The authors of the present invention also experimentally demonstrated, in comparison with MT103, a significantly increased half-life (T1 / 2) and exposure (AUC (O-inf)) of the anti-CD3 * CD19 antibody of the invention, while maintaining the maximum peak concentration (Cxx) when administered intravenously, and also increased bioavailability of antibodies against CD3 * CD19 according to the invention with both intravenous and subcutaneous administration (Example 4). Additionally, the authors of the present invention experimentally confirmed a higher affinity of the antibodies of the invention for CD3 and CD 19 and its higher antitumor activity when administered subcutaneously in comparison with MT103 (Examples 3 and 5).
Пример 1. Получение антитела против CD3*CD19 Example 1. Obtaining antibodies against CD3 * CD19
Конструирование рекомбинантных плазмидных ДНК Для клонирования были выбраны коммерчески доступный вектор фирмы Selexis, содержащий генетический элемент SGE1, способствующий усилению экспрессии в результате непосредственной близости целевого трансгена с высокоактивным ядерным транскрипционным комплексом. Construction of recombinant plasmid DNA For cloning, a commercially available Selexis vector containing the SGE1 genetic element was selected to enhance expression as a result of the close proximity of the target transgene with a highly active nuclear transcription complex.
Ген, кодирующий цепь антитела против CD3*CD19, был сконструирован в результате отжига перекрывающихся химически синтезированных олигонуклеотидов. Последовательность целевого гена бьша клонирована в коммерчески доступный вектор pUC 19, в результате чего бьш получен вектор pAPG_GNR047, который использовали для дальнейшей работы. После обработки вектора pAPG_GNR047 эндодезоксирибонуклеазами рестрикции Hindlll, Xbal (New Ingland Biolabs), образующими липкие концы, вьщеляли фрагмент размером 2235 п.о., который затем лигировали с линеаризованным по сайтам Hindlll и Xbal экспрессионным вектором pSTlOl. Полученная плазмида pRA1451 бьша верифицирована рестрикционным картированием. Схема конструирования экспрессионного вектора pRA1451 приведена на Фиг. 2. The gene encoding the anti-CD3 * CD19 antibody chain was constructed by annealing the overlapping chemically synthesized oligonucleotides. The sequence of the target gene was cloned into the commercially available vector pUC 19, whereby the vector pAPG_GNR047 was obtained, which was used for further work. After treating the pAPG_GNR047 vector with Hindlll, Xbal (New Ingland Biolabs) restriction endodesoxyribonucleases forming sticky ends, a 2235 bp fragment was then ligated, which was then ligated with the Hindlll and Xbal linearized pSTlOl expression vector. The resulting plasmid pRA1451 was verified by restriction mapping. The construction scheme of the expression vector pRA1451 is shown in FIG. 2.
После этого проводили последовательную двойную трансфекцию с последующей селекцией по резистентности к пуромицину с использованием стандартных методов. After that, sequential double transfection was carried out, followed by selection for puromycin resistance using standard methods.
Полученная плазмида pRA1451, кодирующая полипептид с последовательностью, представленной в SEQ ID NO: 10, характеризуется следующими признаками: The resulting plasmid pRA1451 encoding a polypeptide with the sequence shown in SEQ ID NO: 10, is characterized by the following features:
- состоит из 11308 п.о., - consists of 11308 bp
- имеет молекулярную массу 6.99 МДа, - has a molecular weight of 6.99 MDa,
- кодирует полипептид биспецифического антитела против CD3*CD19, GNR-047, - encodes a polypeptide bespecifically antibodies against CD3 * CD19, GNR-047,
- обеспечивает устойчивость клеток млекопитающих, трансфицированных указанной плазмидой, к пуромицину; - provides resistance of mammalian cells transfected with the indicated plasmid to puromycin;
- содержит следующие элементы: - contains the following elements:
- CMVe/EFla pro - энхансер вируса CMV и промотор транскрипции гена фактора элонгации альфа, - CMVe / EFla pro - enhancer of the CMV virus and promoter of transcription of the gene for elongation factor alpha,
- BGH рА - сигнал полиаденилирования бычьего гормона роста, - BGH pA - signal polyadenylation of bovine growth hormone,
- sv40 enh- энхансер вируса SV40, - sv40 enh- enhancer of the SV40 virus,
- SGE 1 - элемент прикрепления к ядерному матриксу, - SGE 1 - element of attachment to the nuclear matrix,
- Amp - ген β-лактамазы, - Amp - β-lactamase gene,
- sv40 pro - промотор вируса SV40, - sv40 pro - SV40 virus promoter,
- puro - ген устойчивости к пуромицину, - puro - puromycin resistance gene,
- рА - синтетический сигнал полиаденилирования. - pA is a synthetic polyadenylation signal.
- содержит уникальные участки узнавания следующих эндонуклеаз рестрикции: Accl (6490 n.o.), Agel (460 n.o.), Apal (995 n.o.), BmgBI (3270 и.о.), Bsml (7269 и.о.), EcoRV (6457 n.o.), Hindlll (1590 n.o.), Notl (11146 n.o.), Pfol (11021 n.o.), Pmll (5699 n.o.), Spel (4622 n.o.), Swal (6466 n.o.), Tthl 1 II (10585 n.o.). - contains unique recognition sites for the following restriction endonucleases: Accl (6490 no), Agel (460 no), Apal (995 no), BmgBI (3270 acting), Bsml (7269 acting), EcoRV (6457 no), Hindlll (1590 no), Notl ( 11146 no), Pfol (11021 no), Pmll (5699 no), Spel (4622 no), Swal (6466 no), Tthl 1 II (10585 no).
Генетическая конструкция экспрессионного вектора приведена на фиг.З. The genetic design of the expression vector is shown in Fig.Z.
Трансфекцию проводили с использованием коммерчески доступного штамма СНО- М (Selexis). Выбор линии клеток-продуцентов обусловлен необходимостью формирования оптимального профиля гликозилирования при синтезе человеческих белков, а также их стабильностью, безопасностью и возможностью применения суспензионных условий культивирования данной линии клеток, что является важнейшими параметрами для производства терапевтических антител. Transfection was performed using a commercially available strain of CHO-M (Selexis). The selection of the producer cell line is due to the need to form an optimal glycosylation profile in the synthesis of human proteins, as well as their stability, safety and the possibility of using suspension culture conditions for this cell line, which are the most important parameters for the production of therapeutic antibodies.
Культивирование проводилось в режиме fed-batch с использованием питательной среды BalanCD СНО Growth A (Irvine Scientific) и нутриентной добавки CellBoost 3 (HyClone) в течение 10 суток при температуре 37°С, 5% С02 в газовой фазе инкубатора. После культивирования культуральная жидкость осветлялась центрифугированием и передавалась на выделение. Cultivation was carried out in fed-batch mode using BalanCD CHO Growth A nutrient medium (Irvine Scientific) and CellBoost 3 (HyClone) nutrient supplement for 10 days at 37 ° С, 5% С0 2 in the gas phase of the incubator. After cultivation, the culture fluid was clarified by centrifugation and transferred to the selection.
Для выделения и очистки целевого продукта была разработана схема, включающая аффинную стадию с использованием сорбента на основе протеина А (с выходом продукта свыше 90%) и катионообменную хроматографию на сорбенте высокого разрешения, обеспечивающую эффективное разделение целевой формы белка и его олигомерных форм (выход целевой фракции более 80%). В результате были получены биспецифические антитела в количествах, достаточных для исследования их фармакокинетических и фармакодинамических свойств. To isolate and purify the target product, a scheme was developed that included the affinity step using a sorbent based on protein A (with a yield of more than 90%) and cation exchange chromatography on a high-resolution sorbent that effectively separated the target form of the protein and its oligomeric forms (yield of the target fraction more than 80%). As a result, bispecific antibodies were obtained in quantities sufficient to study their pharmacokinetic and pharmacodynamic properties.
Пример 2. Фармацевтическая композиция на основе антитела против CD3*CD19. Example 2. Pharmaceutical composition based on antibodies against CD3 * CD19.
Для проведения экспериментов на животных использовали фармацевтическую композицию следующего состава: 0,7 мг/мл антитела против CD3*CD19 по изобретению (далее GNR-047), 150 мМ хлорид натрия, 1,8% маннитол, 20мМ фосфат натрия, 0,01% полисорбат 80. For animal experiments, a pharmaceutical composition of the following composition was used: 0.7 mg / ml anti-CD3 * CD19 antibody of the invention (hereinafter GNR-047), 150 mM sodium chloride, 1.8% mannitol, 20 mM sodium phosphate, 0.01% polysorbate 80.
Условия очистки антитела против CD3*CD19 по изобретению на последней хроматографической стадии процесса подобраны таким образом, что целевой белок элюируется с сорбента в виде концентрированной субстанции, содержащей все требуемые компоненты финальной формуляции. Таким образом, для приготовления готовой лекарственной формы раствор антитела с концентрацией около 5 мг/мл (концентрированный раствор, полученный в Примере 1 после хроматографической очистки) разбавляли до требуемой концентрации 0,7 мг/мл с использованием буфера готовой лекарственной формы при перемешивании. Полученный раствор подвергали стерилизующей фильтрации с использованием фильтра с диаметром пор 0,22 мкм и разливали в стерильные флаконы для хранения композиции и последующих экспериментов. The purification conditions of the anti-CD3 * CD19 antibody of the invention at the last chromatographic stage of the process are selected so that the target protein is eluted from the sorbent in the form of a concentrated substance containing all the required components of the final formulation. Thus, to prepare the finished dosage form, an antibody solution with a concentration of about 5 mg / ml (the concentrated solution obtained in Example 1 after chromatographic purification) was diluted to the required concentration of 0.7 mg / ml using the buffer of the finished dosage form with stirring. The resulting solution was subjected to sterilizing filtration using a filter with a pore diameter of 0.22 μm and poured into sterile vials to store the composition and subsequent experiments.
Для получения лиофилизированной композиции, раствор, содержащий антитела против CD3*CD19 по изобретению в буфере готовой формы (150 мМ хлорид натрия, 1,8% маннитол, 20мМ фосфат натрия, 0,01% полисорбат 80), подвергали лиофилизации при стандартных условиях, включающих стадию замораживания и вакуумного обезвоживания. При этом хлорид натрия и маннит, использовали в качестве кристаллизующихся компонентов, наличие которых позволяет сформировать таблетку, а маннит также играл роль стабилизатора при лиофилизации. Полученный лиофильный препарат хранили при 4С в герметичных флаконах. To obtain a lyophilized composition, a solution containing anti-CD3 * CD19 antibodies of the invention in a finished buffer (150 mM sodium chloride, 1.8% mannitol, 20 mm sodium phosphate, 0.01% polysorbate 80) was lyophilized under standard conditions including stage of freezing and vacuum dehydration. In this case, sodium chloride and mannitol were used as crystallizing components, the presence of which allows the formation of a tablet, and mannitol also played the role of a stabilizer during lyophilization. The resulting lyophilic preparation was stored at 4C in sealed vials.
В качестве растворителя для восстановления лиофилизированной композиции использовали воду для инъекций. Для восстановления препарата к флакону, содержащему лиофилизированную композицию антитела, при комнатной температуре добавляли 0,5 мл растворителя и осторожно перемешивали покачиванием до полного растворения. В качестве растворителя также может выступать бактериостатическая вода для инъекций, растворение в которой позволяет многократно использовать препарат в течение 7 дней. Water for injection was used as a solvent for reconstituting the lyophilized composition. To restore the drug, 0.5 ml of the solvent was added to the vial containing the lyophilized antibody composition at room temperature and gently mixed by shaking until it was completely dissolved. Bacteriostatic water for injection can also serve as a solvent, dissolution in which allows the drug to be reused within 7 days.
Пример 3. Изучение биологической активности Example 3. The study of biological activity
Биологическую активность полученного антитела оценивали путем определения констант связывания в конкурентном анализе на клетках линии Раджи CD3-/CD19+ (Raji, АТСС® CCL-86) и Джуркат CD3+/CD19- (Jurkat, АТСС® TIB-152) из коллекции АТСС. The biological activity of the obtained antibody was evaluated by determining the binding constants in a competitive analysis on cells of the Raja line CD3- / CD19 + (Raji, ATCC® CCL-86) and Dzhurkat CD3 + / CD19- (Jurkat, ATCC® TIB-152) from the ATCC collection.
В качестве препарата сравнения использовали антитело МТ-103 (блинатумомаб). После инкубации с целевыми молекулами в последовательных 10-кратных разведениях от 100 нМ до 0,1 нМ, к клеткам добавляли конкурирующее антитело (HD37 или ОКТЗ) в концентрации 6 нМ. Клетки промывали натрий-фосфатным буферным раствором с рН 7,0 и прокрашивали anti-Human-FITS антителами. Прокрашенные клетки анализировали на FACS Calibur. Antibody MT-103 (blinatumomab) was used as a comparison drug. After incubation with the target molecules in successive 10-fold dilutions from 100 nM to 0.1 nM, a competing antibody (HD37 or OCTZ) was added to the cells at a concentration of 6 nM. Cells were washed with pH 7.0 sodium phosphate buffer and stained with anti-Human-FITS antibodies. Stained cells were analyzed by FACS Calibur.
Результаты связывания приведены в Таблице 1 и на Фиг. 4 The binding results are shown in Table 1 and in FIG. four
Таблица 1 Table 1
Из таблицы видно, что антитело GNR-047 связывается, как с CD3, так и с CD 19, причем в обоих случаях более эффективно, чем препарат сравнения МТЮЗ. Такие низкие, в сравнении с препаратом сравнения, значения IC50 могут объясняться наличием 2х валентностей для каждой специфичности (CD3 и CD 19 The table shows that the GNR-047 antibody binds to both CD3 and CD 19, and in both cases it is more effective than the MTUZ comparison drug. Such low, in comparison with the comparison drug, IC50 values can be explained by the presence of 2 valencies for each specificity (CD3 and CD 19
Пример 4. Сравнение фармакокинетических характеристик при внутривенном и подкожном введении Example 4. Comparison of pharmacokinetic characteristics with intravenous and subcutaneous administration
В виду того, что препарат GNR-047 показал улучшенные фармакокинетические характеристики при внутривенном введении по сравнению с МТЮЗ, целесообразным являлось определение фармакокинетических параметров при более удобном подкожном введении, при котором GNR-047 будет пролонгировано высвобождаться из депо в кровоток. In view of the fact that the GNR-047 preparation showed improved pharmacokinetic characteristics during intravenous administration compared with MTYuZ, it was advisable to determine the pharmacokinetic parameters with more convenient subcutaneous administration, in which GNR-047 will be prolonged to be released from the depot into the bloodstream.
Для проведения эксперимента использовались крысы линии Sprague Dawley (Питомник лабораторных животных «Пущино» филиала Института биорганической химии имени академиков М.М. Шемякина и Ю. А. Овчинникова Российской академии наук) массой около 400 г, 3 крысы на группу. For the experiment, rats of the Sprague Dawley line were used (Pushchino Kennel of Laboratory Animals, branch of the Institute of Bioorganic Chemistry named after Academicians MM Shemyakin and Yu. A. Ovchinnikov of the Russian Academy of Sciences) weighing about 400 g, 3 rats per group.
Каждой крысе вводили исследуемое антитело GNR-047 или МТ-103 внутривенно в дозировке 0,5 мг/кг или подкожно в дозировке 2,0 мг/кг. Образцы крови отбирали через определенные промежутки времени после инъекции, начиная с 5 мин, и определяли концентрации препаратов в плазме крови при помощи твердофазного иммуноферментного анализа (ELISA). The test antibody GNR-047 or MT-103 was administered intravenously at a dose of 0.5 mg / kg or subcutaneously at a dose of 2.0 mg / kg to each rat. Blood samples were taken at certain intervals after injection, starting from 5 min, and the concentration of the drugs in the blood plasma was determined using enzyme-linked immunosorbent assay (ELISA).
Полученные результаты представлены в таблице 2 и на Фиг. 5 и 6. The results obtained are presented in table 2 and in FIG. 5 and 6.
Таблица 2 table 2
**AUC(0-inf) в данном случае совпадает с AUC(O-t), так как в последней точке фармакокинетической кривой концентрация МТ103 близка к нулю. ** AUC (0-inf) in this case coincides with AUC (O-t), since at the last point of the pharmacokinetic curve the concentration of MT103 is close to zero.
*** Параметр рассчитан с учетом разницы доз. *** The parameter is calculated taking into account the dose difference.
Где, Where,
Тт - необходимое для снижения концентрации лекарственного препарата в плазме крови на 50% в результате элиминации; Сшах - наивысшее значение концентрации лекарственного препарата в плазме крови; AUQo-t) - площадь, ограниченная фармакокинетической кривой и осью абсцисс во временном интервале с момента введения лекарственного препарата до момента отбора последней пробы крови; AUQo-inf) - площадь, ограниченная фармакокинетической кривой и осью абсцисс, экстраполированная во времени с момента введения лекарственного препарата до бесконечности; /а - часть дозы лекарственного препарата (в %), достигшая системного кровотока после внесосудистого введения. TT - necessary to reduce the concentration of the drug in blood plasma by 50% as a result of elimination; Sshah - the highest concentration of the drug in the blood plasma; AUQo-t) is the area bounded by the pharmacokinetic curve and the abscissa axis in the time interval from the moment of drug administration until the last blood sample is taken; AUQo-inf) - the area bounded by the pharmacokinetic curve and the abscissa axis, extrapolated in time from the moment of drug administration to infinity; / a - part of the dose of the drug (in%), which reached the systemic circulation after extravascular administration.
В результате было показано значительное увеличение времени полувыведения (Т ) и экспозиция (AU o-mf) - площадь под фармакокинетической кривой) препарата GNR-047 в сравнении с препаратом МТ103, при сохранении максимальной пиковой концентрации (Стах) при внутривенном введении. As a result, a significant increase in half-life (T) and exposure (AU o-mf) - the area under the pharmacokinetic curve) of the GNR-047 preparation was shown in comparison with the MT103 preparation, while maintaining the maximum peak concentration (Stax) with intravenous administration.
При подкожном введении крысам абсолютная биодоступность препарата GNR-047 составила порядка 60%, в то время как МТ-103 показал очень низкую биодоступность - 6% (см. Фиг. 66). When administered subcutaneously to rats, the absolute bioavailability of GNR-047 was about 60%, while MT-103 showed a very low bioavailability of 6% (see Fig. 66).
Пример 5. Сравнение противоопухолевой активности GNR-047 и МТ 103 на модели опухолевого ксенотрансплантанта клеток линии Raji (Раджи) у мышей NOD/SCID при реконституции МКПК человека Example 5. Comparison of the antitumor activity of GNR-047 and MT 103 in a model of a tumor xenograft of Raji cells (Raji) in NOD / SCID mice during reconstitution of human PBMC
Цель исследования заключалась в сравнении эффективности препаратов GNR- 047 и МТ103 у мышей NOD/SCID (Taconic, Дания) при нескольких уровнях дозы, на модели ксенотрансплантата опухолевых клеток линии Раджи с одновременных инъекций мононуклеарных клеток периферической крови (МКПК) человека иммунодефицитным мышам NOD/SCID. Клетки линии Раджи (лимфома Беркитта человека) предварительно смешивали с МКПК человека и инокулировали подкожно с последующим внутривенным или подкожным введением исследуемых препаратов. Для этого девяти экспериментальным группам иммунодефицитных мышей NOD/SCID (9 животных на группу) подкожно вводили или клетки линии Раджи лимфомы Буркитта человека, или суспензию предварительно смешанных клеток линии Раджи и МКПК человека. По три животных из каждой группы получали МКПК человека от одного из трех отдельных здоровых доноров (когорты 1, 2 и 3). Через 2 часа после инокуляции клеток животным внутривенно или подкожно вводили, или НФБ (натрий-фосфатный буферный раствор), или исследуемые препараты GNR-047 или МТ 103 в различных дозах. Вводимый объем составлял 200 мкл. Во всех группах в течение 45 дней (дни с 3 по 48) оценивали объем опухоли. The aim of the study was to compare the efficacy of GNR-047 and MT103 preparations in NOD / SCID mice (Taconic, Denmark) at several dose levels, on a Raja tumor cell xenograft model with simultaneous injections of human peripheral blood mononuclear cells (MCPC) to immunodeficient NOD / SCID mice . Cells of the Raja line (human Burkitt’s lymphoma) were pre-mixed with human PBMC and inoculated subcutaneously, followed by intravenous or subcutaneous administration of the studied drugs. For this, nine experimental groups of immunodeficient NOD / SCID mice (9 animals per group) were subcutaneously injected with either human Raja line Burkitt lymphoma cells or a suspension of pre-mixed Raja line cells and human PBMC. Three animals from each group received human PBMC from one of three separate healthy donors (cohorts 1, 2, and 3). 2 hours after inoculation of the cells, the animals were injected intravenously or subcutaneously with either NFB (sodium phosphate buffer solution) or the studied preparations GNR-047 or MT 103 in various doses. The injection volume was 200 μl. In all groups, tumor volume was evaluated over 45 days (days 3 through 48).
Вводимые растворы готовили путем разведения раствора (композиции) GNR-047, полученного в Примере 2 (0,7 мг/мл), или МТ103 (0,52 мкг/мл) в 0,9% физиологическом растворе до получения концентрации 5 мкг/мл (доза 1 мкг) или 0,5 мкг/мл (доза 0,1 мкг). Экспериментальные группы описаны в таблице 3. Injected solutions were prepared by diluting the GNR-047 solution (composition) obtained in Example 2 (0.7 mg / ml) or MT103 (0.52 μg / ml) in 0.9% saline to obtain a concentration of 5 μg / ml (dose 1 μg) or 0.5 μg / ml (dose 0.1 μg). The experimental groups are described in table 3.
Таблица 3 Table 3
Исследуемый Researched
Клетки*, инокулированные Cells * Inoculated
Группа препарат (инъекция Group drug (injection
мыши путем п/к инъекции (д 0) mouse by sc injection (d 0)
1 раз/сутки) 1 time / day)
37 - 39 Клетки линии Раджи + МКПК 37 - 39 Cells of the Raji line + MCPC
40 - 42 (Донор 1) GNR-047 40 - 42 (Donor 1) GNR-047
5 43 - 45 Клетки линии Раджи + МКПК 1 5 43 - 45 Cells of the Raji line + MCPC 1
(Донор 2) мкг/животное, (Donor 2) mcg / animal,
Клетки линии Раджи + МКПК внутривенно Cells of the Raji line + MCPC intravenously
(Донор 3) (Donor 3)
46 - 48 Клетки линии Раджи + МКПК 46 - 48 Cells of the Raji line + MCPC
49 - 51 (Донор 1) GNR-047 49 - 51 (Donor 1) GNR-047
6 52 - 54 Клетки линии Раджи + МКПК 0,1 6 52 - 54 Cells of the Raji line + MCPC 0.1
(Донор 2) мкг/животное, (Donor 2) mcg / animal,
Клетки линии Раджи + МКПК внутривенно Cells of the Raji line + MCPC intravenously
(Донор 3) (Donor 3)
55 - 57 Клетки линии Раджи + МКПК 55 - 57 Cells of the Raji line + MCPC
58 - 60 (Донор 1) GNR-047 61 - 63 Клетки линии Раджи + МКПК 4 58 - 60 (Donor 1) GNR-047 61 - 63 Cells of the Raji line + MCPC 4
7 7
(Донор 2) мкг/животное, (Donor 2) mcg / animal,
Клетки линии Раджи + МКПК внутривенно Cells of the Raji line + MCPC intravenously
(Донор 3) (Donor 3)
64 - 66 Клетки линии Раджи + МКПК 64 - 66 Cells of the Raji line + MCPC
67 - 69 (Донор 1) GNR-047 70 - 72 Клетки линии Раджи + МКПК 67 - 69 (Donor 1) GNR-047 70 - 72 Cells of the Raji line + MCPC
8 1,7 8 1.7
(Донор 2) мкг/животное, (Donor 2) mcg / animal,
Клетки линии Раджи + МКПК подкожно Raji cells + PBMC subcutaneously
(Донор 3) (Donor 3)
73 - 75 Клетки линии Раджи + МКПК 73 - 75 Cells of the Raji line + MCPC
76 - 78 (Донор 1) GNR-047 79 - 81 Клетки линии Раджи + МКПК 76 - 78 (Donor 1) GNR-047 79 - 81 Cells of the Raji line + MCPC
9 0,17 9 0.17
(Донор 2) мкг/животное, (Donor 2) mcg / animal,
Клетки линии Раджи + МКПК подкожно Raji cells + PBMC subcutaneously
(Донор 3) (Donor 3)
*2,5*106 клеток линии Раджи, 1 *107 МКПК. * 2.5 * 10 6 cells of the Raji line, 1 * 10 7 MCPC.
У экспериментальных животных определяли следующие показатели: выживаемость, масса тела, объем опухоли, масса опухоли. The following indicators were determined in experimental animals: survival, body weight, tumor volume, tumor mass.
Массу тела определяли в день 0 и в последующем регистрировали три раза в неделю до дня 48. Объем опухоли контролировали 3 раза в неделю со дня 3 до окончания исследования путем измерения большого и малого диаметра опухоли штанге-циркулем. На основании диаметров вычисляли объем опухоли, используя следующую формулу: Body weight was determined on day 0 and was subsequently recorded three times a week until day 48. Tumor volume was monitored 3 times a week from day 3 until the end of the study by measuring the large and small diameter of the tumor with a barbell. Based on the diameters, the tumor volume was calculated using the following formula:
Объем = (малый диаметр)2 х большой диаметр х 0,5 В контрольной группе 1, получавшей НФБ (только клетки линии Раджи), до завершения исследования выжили 11% животных. Выживаемость у животных группы 2, получавших клетки линии Раджи и МКПК человека, не изменилась. В обеих группах смертность была обусловлена исключительно эвтаназией по этическим соображениям (вследствие большого объема опухоли). Volume = (small diameter) 2 x large diameter x 0.5 In control group 1 receiving NFB (only Raji cells), 11% of the animals survived until the study was completed. Survival in animals of group 2 treated with cells of the Raji line and human PBMC did not change. In both groups, mortality was due solely to euthanasia for ethical reasons (due to the large volume of the tumor).
Введение GNR-047 и МТ 103 повысило выживаемость в группах 3-9, что отражено в таблице 4, причем при большей дозе исследуемый препарат оказался более эффективным, чем препарат сравнения: The introduction of GNR-047 and MT 103 increased survival in groups 3-9, which is reflected in table 4, and with a higher dose, the studied drug was more effective than the comparison drug:
Таблица 4 Table 4
Выживаемость животных Animal survival
Критерии выведения экспериментальных животных из исследования: объем опухоли> 10% массы тела; изъязвление опухоли; снижение массы тела> 20%. Criteria for removing experimental animals from the study: tumor volume> 10% of body weight; tumor ulceration; weight loss> 20%.
Рост опухоли значительно ингибировался или подавлялся во всех исследуемых группах, получавших GNR-047 или МТ 103 (группы 3-9) по сравнению с контрольной группой 2, получавшей НФБ. При этом во всех исследуемых группах, получавших GNR-047 или МТ 103, ингибирование роста опухоли оказалось статистически значимым (р<0,05). Tumor growth was significantly inhibited or suppressed in all study groups treated with GNR-047 or MT 103 (groups 3-9) compared with control group 2 treated with NPF. Moreover, in all the studied groups treated with GNR-047 or MT 103, inhibition of tumor growth was statistically significant (p <0.05).
В таблице 5 приведены размеры опухоли для групп 1, 2, 4, 8 и 9, а соответствующие сравнительные графики, позволяющие оценить размер опухоли при внутривенном и подкожном введении (для групп 4, 8 и 9), приведены на Фиг.7. Table 5 shows the tumor sizes for groups 1, 2, 4, 8, and 9, and the corresponding comparative graphs that allow us to estimate the size of the tumor during intravenous and subcutaneous administration (for groups 4, 8, and 9) are shown in Fig. 7.
Таблица 5 Группа День исследования Table 5 Study Day Group
3 6 8 10 13 15 17 3 6 8 10 13 15 17
1 0,0 10,0 14,6 28,9 47,9 95,2 199,9 1 0.0 10.0 14.6 28.9 47.9 95.2 199.9
2 2,2 6,0 13,7 28,4 58,8 122,3 236,62 2.2 6.0 13.7 28.4 58.8 122.3 236.6
4 6 10,2 19,6 27,1 38,2 64,3 112,74 6 10.2 19.6 27.1 38.2 64.3 112.7
8 1,9 3,4 10,9 15,0 19,0 28,6 34,28 1.9 3.4 10.9 15.0 19.0 28.6 34.2
9 4,8 7,3 12,0 15,8 22,7 37,4 48,9 9 4.8 7.3 12.0 15.8 22.7 37.4 48.9
День исследования Study day
Группа Group
20 22 24 27 29 31 20 22 24 27 29 31
1 387,0 561,5 781,5 1046,5 1214,8 1559,2 1,387.0 561.5 781.5 1,046.5 1,214.8 1,559.2
2 443,9 598,8 745,0 1038,8 1243,7 1465,22 443.9 598.8 745.0 1038.8 1243.7 1465.2
4 149,8 176,4 254,5 377,1 465,4 589,6 4 149.8 176.4 254.5 377.1 465.4 589.6
8 37,2 33,5 45,1 92,3 108,4 187,9 8 37.2 33.5 45.1 92.3 108.4 187.9
9 75,9 94,8 190,8 259,8 320,3 409,9 9 75.9 94.8 190.8 259.8 320.3 409.9
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ INDUSTRIAL APPLICABILITY
Настоящее изобретение может быть использовано в медицине для лечения В- клеточных заболеваний или истощения В-клеток, в том числе, В-лимфобластная лимфома/В- клеточный острый лимфобластный лейкоз из клеток-предшественников; В-клеточные опухоли из периферических (зрелых) В-лимфоцитов, в том числе: В-клеточный хронический лимфоцитарный лейкоз/лимфома из малых лимфоцитов (лимфоцитарная лимфома); В- клеточный пролимфоцитарный лейкоз; лимфоплазмоцитарная лимфома; селезеночная лимфома маргинальной зоны; волосатоклеточный лейкоз; плазмоклеточная миелома/плазмоцитома; экстранодальная В-клеточная лимфома маргинальной зоны MALT- типа; нодальная В-клеточная лимфома маргинальной зоны; фолликулярная лимфома; лимфома из клеток мантийной зоны; диффузная В-крупноклеточная лимфома; медиастинальная диффузная В-крупноклеточная лимфома; первичная экссудативная лимфома; лимфома/лейкоз Беркитта, а также для лечения аутоиммунных заболеваний, вызванных патологической регуляцией В-клеток, таких как ревматоидный артрит, системная красная волчанка, гломерулонефрит, рассеянный склероз и миастения гравис. Настоящее изобретение также может быть использовано в фармацевтической промышленности для получения фармацевтических композиций, готовых лекарственных форм и наборов, содержащих антитело по изобретению, для лечения указанных выше заболеваний. The present invention can be used in medicine for the treatment of B-cell diseases or depletion of B-cells, including B-lymphoblastic lymphoma / B-cell acute lymphoblastic leukemia from progenitor cells; B-cell tumors from peripheral (mature) B-lymphocytes, including: B-cell chronic lymphocytic leukemia / lymphoma from small lymphocytes (lymphocytic lymphoma); B-cell prolymphocytic leukemia; lymphoplasmacytic lymphoma; splenic lymphoma of the marginal zone; hairy cell leukemia; plasma cell myeloma / plasmacytoma; extranodal B-cell lymphoma of the marginal zone of the MALT-type; nodal B-cell lymphoma of the marginal zone; follicular lymphoma; mantle cell lymphoma; diffuse B-large cell lymphoma; mediastinal diffuse B-large cell lymphoma; primary exudative lymphoma; Burkitt’s lymphoma / leukemia, as well as for the treatment of autoimmune diseases caused by pathological regulation of B cells, such as rheumatoid arthritis, systemic lupus erythematosus, glomerulonephritis, multiple sclerosis and myasthenia gravis. The present invention can also be used in the pharmaceutical industry for the preparation of pharmaceutical compositions, formulations and kits containing an antibody of the invention for the treatment of the above diseases.
СВОБОДНЫЙ ТЕКСТ ПЕРЕЧЕНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ SEQ ID N° 1 - вариабельный домен легкой цепи анти-СОЗ -антитела, FREE TEXT OF THE LIST OF SEQUENCES SEQ ID N ° 1 - the variable domain of the light chain anti-POP antibodies
SEQ ID 3 ° 2 - вариабельный домен тяжелой цепи анти-СОЗ антитела, SEQ ID j b 3 - вариабельный домен легкой цепи анти-С019 антитела,SEQ ID 3 ° 2 - the variable domain of the heavy chain anti-POP antibodies, SEQ ID jb 3 - the variable domain of the light chain of anti-C019 antibodies,
SEQ ID N° 4 - вариабельный домен тяжелой цепи анти-С019 антитела,SEQ ID N ° 4 - the variable domain of the heavy chain of anti-C019 antibodies,
SEQ ID ДО? 5 - константный домен СН2 СНЗ IG2, SEQ ID BEFORE? 5 - constant domain of CH2 SNZ IG2,
SEQ ID Jfe 6 -линкер L1 , SEQ ID Jfe 6 linker L1,
SEQ ID jVs 7 - линкер L2, SEQ ID jVs 7 - linker L2,
SEQ ID jVe 8 - линкер L3, SEQ ID jVe 8 - linker L3,
SEQ ID jV° 9 - шарнирная область H, SEQ ID jV ° 9 - hinge region H,
SEQ ID -4° 10 - антитело GNR-047. SEQ ID -4 ° 10 - antibody GNR-047.
Claims
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EA201890805A EA036905B1 (en) | 2015-12-01 | 2016-11-29 | Bispecific antibodies against cd3*cd19 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2015151459A RU2651776C2 (en) | 2015-12-01 | 2015-12-01 | Bispecific antibodies against cd3*cd19 |
| RU2015151459 | 2015-12-01 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017095267A1 true WO2017095267A1 (en) | 2017-06-08 |
Family
ID=58797475
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/RU2016/000827 Ceased WO2017095267A1 (en) | 2015-12-01 | 2016-11-29 | Bispecific antibodies against cd3*cd19 |
Country Status (3)
| Country | Link |
|---|---|
| EA (1) | EA036905B1 (en) |
| RU (1) | RU2651776C2 (en) |
| WO (1) | WO2017095267A1 (en) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112010982A (en) * | 2020-08-31 | 2020-12-01 | 重庆金迈博生物科技有限公司 | anti-GPC 3/CD3 bispecific antibody and application thereof |
| CN114364698A (en) * | 2019-08-21 | 2022-04-15 | 吉尼瑞姆股份公司 | Binding to the complementarity determining regions of CD3 and bispecific antigen binding molecules containing said CDRs |
| WO2022165171A1 (en) | 2021-01-28 | 2022-08-04 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for treating cytokine release syndrome |
| WO2023062188A1 (en) * | 2021-10-15 | 2023-04-20 | Amgen Research (Munich) Gmbh | Subcutaneous administration of cd19-binding t cell engaging antibodies |
| WO2023201226A1 (en) | 2022-04-11 | 2023-10-19 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for universal tumor cell killing |
| WO2024173830A2 (en) | 2023-02-17 | 2024-08-22 | Regeneron Pharmaceuticals, Inc. | Induced nk cells responsive to cd3/taa bispecific antibodies |
| US12221481B2 (en) | 2019-05-21 | 2025-02-11 | Novartis Ag | CD19 binding molecules and uses thereof |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102847350B1 (en) | 2015-11-25 | 2025-08-19 | 주식회사 리가켐바이오사이언스 | Antibody-drug conjugate comprising a branched linker and method for preparing the same |
| JP7664680B2 (en) | 2017-03-29 | 2025-04-18 | リガケム バイオサイエンシズ, インク. | Pyrrolobenzodiazepine dimer precursors and their ligand-linker conjugate compounds |
| SG11202010443WA (en) | 2018-05-09 | 2020-11-27 | Legochem Biosciences Inc | Compositions and methods related to anti-cd19 antibody drug conjugates |
| KR20210028544A (en) | 2019-09-04 | 2021-03-12 | 주식회사 레고켐 바이오사이언스 | Antibody-drug conjugate comprising antibody binding to antibody against human ROR1 and its use |
| IL298402A (en) | 2020-06-19 | 2023-01-01 | Hoffmann La Roche | Antibodies binding to cd3 and cd19 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7947646B2 (en) * | 2007-03-06 | 2011-05-24 | Amgen Inc. | Variant activin receptor polypeptides |
| US8658773B2 (en) * | 2011-05-02 | 2014-02-25 | Immunomedics, Inc. | Ultrafiltration concentration of allotype selected antibodies for small-volume administration |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2326389C (en) * | 1998-04-21 | 2007-01-23 | Micromet Gesellschaft Fur Biomedizinische Forschung Mbh | Novel cd19xcd3 specific polypeptides and uses thereof |
| DE60124912T2 (en) * | 2001-09-14 | 2007-06-14 | Affimed Therapeutics Ag | Multimeric, single chain, tandem Fv antibodies |
| EP2982696B1 (en) * | 2008-11-07 | 2019-03-27 | Amgen Research (Munich) GmbH | Treatment of acute lymphoblastic leukemia |
| KR102406407B1 (en) * | 2009-10-27 | 2022-06-08 | 암젠 리서치 (뮌헨) 게엠베하 | Dosage regimen for administering a CD19xCD3 bispecific antibody |
-
2015
- 2015-12-01 RU RU2015151459A patent/RU2651776C2/en active
-
2016
- 2016-11-29 WO PCT/RU2016/000827 patent/WO2017095267A1/en not_active Ceased
- 2016-11-29 EA EA201890805A patent/EA036905B1/en unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7947646B2 (en) * | 2007-03-06 | 2011-05-24 | Amgen Inc. | Variant activin receptor polypeptides |
| US8658773B2 (en) * | 2011-05-02 | 2014-02-25 | Immunomedics, Inc. | Ultrafiltration concentration of allotype selected antibodies for small-volume administration |
Non-Patent Citations (4)
| Title |
|---|
| NAGORSEN DIRK ET AL.: "Immunomodulatory therapy of cancer with T cell -engaging BiTE antibody blinatumomab", EXPERIMENTAL CELL RESEARCH, vol. 317, 2011, pages 1255 - 1260, XP028205663 * |
| REUSCH UWE ET AL.: "A tetravalent bispecific TandAb ( CD 19/ CD 3), AFM11, efficiently recruits T cells for the potent lysis of CD 19+ tumor cells.", MABS, vol. 7, no. 3, June 2015 (2015-06-01), pages 584 - 604, XP009184710 * |
| STEIN ANDREAS ET AL.: "Cation exchange chromatography in antibody purification: pH screening for optimised binding and HCP removal", JOURNAL OF CHROMATOGRAPHY B, vol. 848, 2007, pages 151 - 158, XP005922836 * |
| ULRICH H.WEIDLE ET AL.: "Tumor-antigen-binding bispecific antibodies for cancer treatment.", SEMINARS IN ONCOLOGY, vol. 41, no. 5, October 2014 (2014-10-01), pages 653 - 660, XP055250095 * |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12221481B2 (en) | 2019-05-21 | 2025-02-11 | Novartis Ag | CD19 binding molecules and uses thereof |
| CN114364698A (en) * | 2019-08-21 | 2022-04-15 | 吉尼瑞姆股份公司 | Binding to the complementarity determining regions of CD3 and bispecific antigen binding molecules containing said CDRs |
| CN114364698B (en) * | 2019-08-21 | 2024-05-28 | 吉尼瑞姆股份公司 | Complementarity determining regions binding to CD3 and bispecific antigen binding molecules containing said CDRs |
| CN112010982A (en) * | 2020-08-31 | 2020-12-01 | 重庆金迈博生物科技有限公司 | anti-GPC 3/CD3 bispecific antibody and application thereof |
| CN112010982B (en) * | 2020-08-31 | 2023-06-27 | 重庆金迈博生物科技有限公司 | A kind of anti-GPC3/CD3 bispecific antibody and its application |
| WO2022165171A1 (en) | 2021-01-28 | 2022-08-04 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for treating cytokine release syndrome |
| US12274747B2 (en) | 2021-01-28 | 2025-04-15 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for treating cytokine release syndrome |
| EP4538292A2 (en) | 2021-01-28 | 2025-04-16 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for treating cytokine release syndrome |
| WO2023062188A1 (en) * | 2021-10-15 | 2023-04-20 | Amgen Research (Munich) Gmbh | Subcutaneous administration of cd19-binding t cell engaging antibodies |
| WO2023201226A1 (en) | 2022-04-11 | 2023-10-19 | Regeneron Pharmaceuticals, Inc. | Compositions and methods for universal tumor cell killing |
| WO2024173830A2 (en) | 2023-02-17 | 2024-08-22 | Regeneron Pharmaceuticals, Inc. | Induced nk cells responsive to cd3/taa bispecific antibodies |
Also Published As
| Publication number | Publication date |
|---|---|
| EA201890805A1 (en) | 2018-08-31 |
| RU2651776C2 (en) | 2018-04-23 |
| RU2015151459A (en) | 2017-06-06 |
| EA036905B1 (en) | 2021-01-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2017095267A1 (en) | Bispecific antibodies against cd3*cd19 | |
| US12129309B2 (en) | Heterodimeric antibodies that bind CD3 and CD38 | |
| JP6484634B2 (en) | IL-15 heterodimeric protein and use thereof | |
| US11111305B2 (en) | Method of using a bispecific antibody to conditionally inhibit a receptor signaling complex | |
| JP2023056001A (en) | TGF-B-receptor ectodomain fusion molecule and uses thereof | |
| CN113166220A (en) | Novel cytokine prodrugs | |
| KR20200118080A (en) | Antibody variable domain targeting the NKG2D receptor | |
| JP2020529832A (en) | Targeted heterodimer Fc fusion protein containing IL-15 / IL-15Rα and antigen binding domain | |
| CN114222764A (en) | IL-2 fusion proteins that preferentially bind IL-2R alpha | |
| JP2019500862A (en) | Heterodimeric antibodies that bind to CD3 and PSMA | |
| AU2005248276A1 (en) | Glycosylated immunoglobulin and immunoadhesin comprising the same | |
| KR102399028B1 (en) | Bi-specific antigen-binding polypeptides | |
| KR102477536B1 (en) | Recombinant intravenous immunoglobulin (rIVIG) compositions and methods of making and using the same | |
| CA3193009A1 (en) | Methods and compositions for treating glioblastoma | |
| WO2023045977A1 (en) | Interleukin-2 mutant and fusion protein thereof | |
| JP2024513951A (en) | Anti-CD20 antibody and CAR-T structure | |
| KR20230160389A (en) | Dual specificity multifunctional fusion polypeptide | |
| CN119371526A (en) | Antibodies against human complement factor C2b and methods of use | |
| CN118451097A (en) | Novel IL27 receptor agonists and methods of use thereof | |
| JP2025532960A (en) | Fusions with CD8 antigen-binding molecules for treating chronic viral infections | |
| TW202334223A (en) | Cd20-pd1 binding molecules and methods of use thereof | |
| CN114712494B (en) | PD-1-targeting multifunctional antibody composition | |
| CN114712495B (en) | Multifunctional antibody composition | |
| WO2026016967A1 (en) | Fusion protein and use thereof | |
| KR20250075632A (en) | Antibodies targeting TNFα and IL-23 and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16871130 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 201890805 Country of ref document: EA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 16871130 Country of ref document: EP Kind code of ref document: A1 |