明細書
ル複素環誘導体および農園芸用殺菌剤および殺虫剤 技術分野:
本発明は新規なァリ一ル複素環誘導体、該化合物を有効成分として含有する農園芸用 殺菌剤および殺虫剤に関する。
背景技術:
農園芸作物の栽培に当り、作 の病害に対して多数の防除薬剤が使用されているが、 その防除効力が不十分であったり、薬剤耐性の病原菌の出現によりその使用が制限され たり、 また植物体に薬害や汚染を生じたり、 あるいは人畜魚類に対する毒性や環境への 影響の観点から、必ずしも満足すべき防除薬とは言い難いものが少なくない。従って、 かかる欠点の少ない安全に使用できる薬剤の出現が強く要請されている。
本発明化合物と類似した下記式に示すァリ -ル複素環化合物が、米国特許第 5 5 6 7 7 2 3号公報に殺ダニ活性を有する開示されている。
また、下記式に示す化合物が国際公開第 0 2 0 9 8 8 4 0号 卜に、糖尿病 治療薬としての作用を有することが開示されている。
また、 下記式に示す化合物が、 国際公開第 0 1 0 9 2 2 1 4号パンフレット、 国際公 開第 0 2 0 8 3 6 3 0号パンフレツ卜に、抗血栓薬としての作用を有することが開示さ れている。
発明の開示:
本発明の目的は、工業的に有利に合成でき効果が確実で安全に使用できる農園芸用殺
菌剤および殺虫剤となりうるァリ一ル複素環誘導体を提供することにある。
[式中、 は Ci-6アルキル基または、 Ci— 6アルコキシ基を表わす。
R
2は水素原子、 ハロゲン原子、 (:
6アルキル基、 — 6アルコキシ基、 Ci-eヒドロキ シアルキル基、 Ci—
6アルキN RIルォキシ d- 6アルキル基、 または アルキル力ルポ ニルォキシ Ci-6アルキル基を表N RIわす。 mは、 0または 1〜4の整数を表す。 Tは式 (2)、 式 (3)、 または式 (4) で表される基を表す。
R
(3)
— N = N— (4)
R3および R6は各々独立して、 水素原子、 Ci-eアルキル基、 または C^eアルキル 力ルポ二ル基を表わす。 R4および R 5は各々独立して、 水素原子、 または d— 6アルキ ル基を表わす。 nは、 1〜4の整数を表す。 Qは、 式 (5)、 式 (6)、 式 (7)、 式 (8) または式 (9) で表される基を表す。
X-N
(式中、 R7は C5_12アルキル基、 C^sハロアルキル基、 C3 8シクロアルキル基、 C
3-8シクロアルキル Ci— 6アルキル基、 C^eアルコキシ d_12アルキル基、 Gで置換 されてもよいフエニル基、 Gで置換されてもよいナフチル基、 アルキル基部分が アルコキシ基で置換されてもよくベンゼン環部分が Gで置換されてもよいフエ二ル^ -6アルキル基、 Gで置換されてもよいベンゾィル基、 ベンゼン環部分が Gで置換され てもよいフエニルァミノ基、 Gで置換されてもよいピリジル基、 ピリジン環部が Gで置 換されてもよいピリジル Ci-6アルキル基、 Gで置換されてもよいピラジニル基、 ビラ ジン環部が Gで置換されてもよいビラジニル Ci-6アルキル基、 Gで置換されてもよい ピリミジニル基、 Gで置換されてもよいキノリニル基、 Gで置換されてもよいフリル基、 Gで置換されてもよいべンゾフラニル基、 Gで置換されてもよいチェニル基、 Gで置換 されてもよいチアゾリル基、または Gで置換されてもよいテトラヒドロナフチル基を表 わす。 R8、 R9及び は各々独立して水素原子またはじい 6アルキル基を示す。 Ri
0は水素原子、' Ci-6アルキル基、 ハロゲン原子、 Ci-6アルキルカルポニル基、 Gで置 換されてもよいフエニル基、 ベンゼン環部分が Gで置換されてもよいフエニル Ci-6ァ ルキル基、 Gで置換されてもよいフエ二ルカルポニル基、 Gで置換されてもよいフエ二 ル Ci-6アルキルカルボニル基、 R7と結合した Ci_6アルキレン基またはシァノ基を表 わす。 、 Gはハロゲン原子、 Ci— 6アルキル基、 シァノ基で置換されてもよいじ: アル コキシ基、 Ci_6アルキルチオ基、 〇卜6アルキルスルホニル基、 ハロアルキル 基、 d— 6ハロアルコキシ基、 置換されてもよいフエニル基、 置換されてもよいフエノ キシ基、 置換されてもよいフエニル Ci—6アルコキシ基、 置換されてもよいピリジルォ キシ基、 Ci 6アルキルカルポニルォキシ基、 置換されてもよいフエ二ルカルポニルォ キシ基、 Ci-6アルキルスルホニルォキシ基、 Ci-6アルコキシカルボニルォキシ基、
C i 6アルコキシカルポニル C ^ 6アルコキシ基、 窒素原子が 1個もしくは 2個の同一 もしくは異なる アルキル基で置換されてもよい力ルバモイルォキシ基、 1個もし くは Ϊ個の同一もしくは異なる C i _6アルキル基で置換されてもよいアミノ基、 シァノ 基、 またはニトロ基を表す。 Xは酸素原子もしくは硫黄原子を表す。 kは 0または 1〜 3の整数を表す。 )]
で表されるァリール複素環誘導体および式 (1) で表されるァリール複素環誘導体また はその塩の 1種または 2種以上を有効成分として含有する農園芸用殺菌剤および殺虫剤 である。
発明を実施するための最良の形態:
前記式 (1) の定義において、
ω
は、 メチル、 ェチル、 プロピル、 イソプロピル、 ブチル、 s e c—ブチル、 イソ プチル、 t一ブチル等の Ci—
6アルキル基;またはメ卜キシ、 エトキシ、 プロピルォキ シ、 イソプロピルォキシ、 プチルォキシ、 s e c—プチルォキシ、 イソプチルォキシ、 t一ブチルォキシ等の d-6アルコキシ基を表わす。
R2は、 フッ素、 塩素、 臭素、 ヨウ素等のハロゲン原子; またはメチル、 ェチル、 プ 口ピル、 イソプロピル、 プチル、 s e c—ブチル、 イソプチル、 t一ブチル等の Cn アルキル基; またはメ卜キシ、 エトキシ等の Ci— 6アルコキシ基;またはヒドロキシメ チル、 1ーヒドロキシェチル、 2—ヒドロキシェチル等の ヒドロキシアルキル 基;またはメトキシメチル、 エトキシメチル、 1—メトキシェチル、 2—メトキシェチ ル等の Ci-6アルキルォキシ Ci-6アルキル基; またはァセ卜キシメチル、 プロポキシ メチル、 1—ァセトキシェチル、 2—ァセトキシェチル等の アルキルカルボニル ォキシ C i _ 6アルキル基を表わす。
mは 0、 1、 2、 3, 4の整数を表す。 mが 2、 3, 4のとき、 R2は同一でも相異なつ ていてもよい。
Tは前記式 (2)、 式 (3)、 式 (4) で表される基を表す。
式 (2)、 式 (3) において、 R3、 R6は各々独立して、 水素原子またはメチル、 ェチル、 プロピル、 イソプロピル、 プチル、 s e c—プチル、 イソプチル、 t一ブチル等のじ 丄 _6アルキル基; またはァセチル、 プロピオニル、 ノルマルプチリル、 イソプチリル等 の C卜6アルキル力ルポ二ル基を表わす。
式 (2、) において、 R4、 R5は各々独立して、 水素原子またはメチル、 ェチル、 プロピ ル、 イソプロピル、 プチル、 s e c—プチル、 イソプチル、 t—ブチル等の Ci-6アル キル基を表わす。
式 (2) において、 nは 1、 2、 3, 4の整数を表す。 nが 2、 3, 4のとき、 R4同士、 R5同士は同一でも相異なっていてもよい。
Qは、 前記式 (5)、 式 (6)、 式 (7)、 式 (8)、 式 (9) で表されるいずれかの基を 表す。
式 (5)、 式 (6)、 式 (7)、 式 (8)、 式 (9) において、 R7は、 ノルマルペンチル、 ノルマルへキシル、 ノルマルへプチル、 ノルマルォクチル、 ノルマルデシル等の Cs-i
2アルキル基; トリクロロメチル、 トリフルォロメチル、 トリブロモメチル等の Ci-e ハロアルキル基;シクロプロピル、 シクロブチル、 シクロペンチル、 シクロへキシル、 シクロへプチル等の C3— 8シクロアルキル基;シクロプロピルメチル、 シクロプロピル ェチル、 シクロブチルメチル、 シクロブチルェチル、 シクロペンチルメチル、 シクロべ ンチルェチル、 シクロへキシルメチル、 シクロへキシルェチル、 シクロへプチルメチル、 シクロへプチルェチル等の C3_8シクロアルキル C^ 6アルキル基; 1ーメトキシェチ ル、 1一エトキシェチル、 1—メトキシノルマルプロピル、 1—エトキシノルマルプロ ピル、 1ーメトキシ— 2—メチルノルマルプロピル、 1—エトキシ— 2—メチルノルマ ルプロピル、 1—メトキシ— 3—メチルノルマルプチル、 1—ェ卜キシ一 3—メチルノ
ルマルブチル、 1ーメ卜キシノルマルへキシル、 1一エトキシノルマルへキシル、 1— メトキシノルマルノニル、 1一エトキシノルマルノニル等の d - 6アルコキシ d _ 1 2 アルキル基; Gで置換されてもよいフエニル基; 2—メトキシー 1—ナフチル等の Gで 置換されてもよいナフチル基;ベンゼン環部が Gで置換されてもよいベンジル、 α—メ トキシベンジル、 1—フエニルェチル、 1—フエニルプロピル、 2—フエニルェチル、 2—フエ二ルー 1ーメトキシェチル、 3—フエニルプロピル、 3—フエニル— 1—メト キシプロピル等のアルキル基部分が C i - 6アルコキシ基で置換されてもよいフエニル
C 6アルキル基;ベンゼン環部が Gで置換されてもよいベンゾィル基; ベンゼン環部 が Gで置換されてもよいフエニルァミノ基; 2—ピリジル、 3—ピリジル、 4—ピリジ ル、 2—クロ口— 4—ピリジル等の Gで置換されてもよいピリジル基; 2—ピリジルメ チル、 3—ピリジルメチル、 4—ピリジルメチル、 1— ( 2—ピリジル)エヂル、 1一(3 一ピリジル)ェチル、 1一( 4—ピリジル)ェチル、 2—( 2—ピリジル)ェチル、 2— ( 3 一ピリジル)ェチル、 2 - ( 4一ピリジル)ェチル等のピリジン環部が Gで置換されても よいピリジル C i— 6アルキル基; Gで置換されてもよいピラジニル基; 2—ビラジニル メチル、 1— ( 2—ピラジニル)ェチル、 1— ( 2—ピラジニル)ェチル、 2—(2—ビラ ジニル)ェチル等のピラジン環部が Gで置換されてもよいビラジニル C! _ 6アルキル 基; 2—ピリミジル、 4 , 6—ジメトキシー 2 _ピリミジル等の Gで置換されてもよい ピリミジニル基; 2—キノリニル、 6—キノリニル等の Gで置換されてもよいキノリニ ル基; 5—メチル—2—フリル等の Gで置換されてもよいフリル基; Gで置換されても よいベンゾフラニル基; Gで置換されてもよいチェニル基; Gで置換されてもよいチア ゾリル基、 または Gで置換されてもよいテトラヒドロナフチル基を表す。
R 8 R 9及び は各々独立して水素原子またはメチル、 ェチル、 プロピル、 イソプ 口ピル、 プチル、 s e c—プチル、 イソプチル、 t _ブチル等の C i _ 6アルキル基を表 す。
R 1 0は水素原子またはメチル、 ェチル、 プロピル、 イソプロピル、 プチル、 s e c— プチル、 イソプチル、 t 一ブチル等の 6アルキル基; フッ素、 塩素、 臭素、 ヨウ素 等のハロゲン原子;ァセチル、 プロピオニル、 イソブチリル、 ノルマルプチリル、 ビバ ロイル等の d— 6アルキルカルボニル基; Gで置換されてもよいフエニル基; Gで置換 されてもよいフエ二ルカルポニル基;ベンゼン環部分が Gで置換されてもよいフエニル C i - eアルキル基;ベンゼン環部が Gで置換されてもよいフエ二ルァセチル、 1—フエ ニルプロピオニル、 2—フエニルプロピオニル等のフエ二ル^— 6アルキルカルボニル 基、 プロピレン、 ブチレン等の R 7と結合した アルキレン基、 またはシァノ基を 表わす。
Xは酸素原子または硫黄原子を表す。
Gは、 フッ素、 塩素、 臭素、 ヨウ素等のハロゲン原子;メチル、 ェチル、 プロピル、 イソプロピル、 プチル、 s e c—プチル、 イソプチル、 t 一ブチル等の アルキル 基;メ卜キシ、 ェ卜キシ、 プロボキシ、 イソプロボキシ、 ブ卜キシ、 s e c—ブトキシ、 イソブトキシ、 t 一ブトキシ、 シァノメトキシ、 1—シァノエトキシ、 2—シァノエ卜
キシ、 1 一シァノプロボキシ、 2—シァノプロポキシ等のシァノ基で置換されてもよい アルコキシ基; メチルチオ、 ェチルチオ、 プロピルチオ、 イソプロピルチオ、 ブ チルチオ、 s e c —プチルチオ、 イソプチルチオ等の C i _ 6アルキルチオ基;メタンス . ルホニル、 ェ夕ンスルホニル、 プロパンスルホニル等の C アルキルスルホニル基; クロロメチル、 フルォロメチル、 プロモメチル、 ジクロロメチル、 ジフルォロメチル、 ジブロモメチル、 トリクロロメチル、 トリフルォロメチル、 トリプロモメチル、 トリク ロロェチル、 トリフルォロェチル、 ペン夕フルォロェチル等の C i - 6ハロアルキル基; クロロメ卜キシ、 フルォロメトキシ、 プロモメトキシ、 ジクロロメ卜キシ、 ジフルォロ メ卜キシ、 ジブロモメトキシ、 トリクロロメトキシ、 トリフルォロメトキシ、 トリプロ モメトキシ、 トリクロ口エトキシ、 トリフルォロエトキシ、 ペン夕フルォロエトキシ等 の C ^ sハロアルコキシ基; フッ素、 塩素、 臭素、 ヨウ素等のハロゲン原子、 メチル、 ェチル、 プロピル等の アルキル基、 メトキシ、 エトキシ、 プロボキシ、 イソプロ ポキシ等の アルコキシ基、 メチルチオ、 ェチルチオ、 プロピルチオ等の C i— 6ァ ルキルチオ基、 トリクロロメチル、 卜リフルォロメチル等の ハロアルキル基、 ジ フルォロメ卜キシ、 トリクロロメトキシ、 トリフルォロメトキシ等の d— 6ハロアルコ キシ基で置換されてもよいフエニル基;フッ素、 塩素、 臭素、 ヨウ素等のハロゲン原子、 メチル、 ェチル、 プロピル等の 6アルキル基、 メトキシ、 エトキシ、 プロボキシ、 イソプロポキシ等の d - 6アルコキシ基、 メチルチオ、 ェチルチオ、 プロピルチオ等の じい 6アルキルチオ基、 トリクロロメチル、 トリフルォロメチル等の ハロアルキ ル基、 ジフルォロメトキシ、 トリクロロメ卜キシ、 トリフルォロメトキシ等の d— 6ノ、 口アルコキシ基で置換されてもよいフエノキシ基;そのフエニル部分がフッ素、 塩素、 臭素、 ヨウ素等のハロゲン原子、 メチル、 ェチル、 プロピル等の。, _ 6アルキル基、 メ トキシ、 エトキシ、 プロボキシ、 イソプロポキシ等の アルコキシ基、 メチルチオ、 ェチルチオ、 プロピルチオ等の C L - 6アルキルチオ基、 トリクロロメチル、 トリフルォ ロメチル等の d— 6ハロアルキル基、 ジフルォロメトギシ、 トリクロロメトキシ、 トリ フルォロメトキシ等の ハロアルコキシ基で置換されてもよいベンジル、 2—フエ ニルェチル、 3—フエニルプロピル等のフエニル C ^sアルコキシ基; 2 —ピリジルォ キシ、 3 —ピリジルォキシ、 4一ピリジルォキシ、 3 —メチル一 2 —ピリジルォキシ、 4—メチル— 2 —ピリジルォキシ、 5 —メチル— 2 —ピリジルォキシ、 6 _メチル— 2 —ピリジルォキシ、 3 —クロ口一 2 —ピリジルォキシ、 3, 5—ジクロロー 2 —ピリジ ルォキシ、 3 —クロロー 5 —トリフルォロメチル 2 —ピリジルォキシ等の置換されても よいピリジルォキシ基;ホルミルォキシ、 ァセトキシ、 プロピオニルォキシ、 プチリル ォキシ等の アルキルカルボニルォキシ基; フッ素、 塩素、 臭素、 ヨウ素等のハロ ゲン原子、 メチル、 ェチル、 プロピル等の C i _ 6アルキル基、 メトキシ、 エトキシ、 プ ロボキシ、 イソプロポキシ等の C i— 6アルコキシ基、 メチルチオ、 ェチルチオ、 プロピ ルチオ等の d— 6アルキルチオ基、 トリクロロメチル、 トリフルォロメチル等の d— 6 ハロアルキル基、 ジフルォロメ卜キシ、 トリクロロメトキシ、 トリフルォロメ卜キシ等 の C i— 6ハロアルコキシ基で置換されてもよいフエ二ルカルポニルォキシ基;メタンス
ルホニルォキシ、 ェ夕ンスルホニルォキシ、 プロパンスルホニルォキシ等の アル キルスルホニルォキシ基;メトキシカルボニルォキシ、 エトキシカルボニルォキシ、 プ 口ポキシカルボニルォキシ、 ブトキシカルポニルォキシ等の C アルコキシカルボ二 ルォキシ基;メトキシカルポニルメトキシ、 エトキシカルポニルメトキシ、 1—メトキ シカルポニルエトキシ、 1—エトキシカルボニルェトキシ、 2—メトキシカルボニルェ トキシ、 2—エトキシカルボニルエトキシ等の Cぃ6アルコキシ力ルポ二ルォキシじ i _ 6アルコキシ基; N—メチルカルバモイルォキシ、 N—ェチルカルバモイルォキシ、 N, N—ジメチルカルバモイルォキシ、 N—ェチル—メチルカルバモイルォキシ等の窒 素原子が 1個もしくは 2個の同一もしくは異なる Cぃ6アルキル基で置換されてもよい 力ルバモイルォキシ基;メチルァミノ、 ェチルァミノ、 ジメチルァミノ、 N—エヂルー N—メチルァミノ、 ジェチルァミノ等の 1個もしくは 2個の同一もしくは異なる C n アルキル基で置換されてもよいアミノ基;シァノ基;ニトロ基を表し、 これら Gは同一 または相異なって 2個から 5個置換してもよい。
式 (9 ) において、 kは 0、 1、 2、 3の整数を表す。
本発明における式 (1 ) で示されるァリール複素環誘導体の製造法について説明する。 式 ( 1 ) で示されるァリール複素環誘導体は例えば下記の方法で製造できるが、 該化合物の 製造法は、 これらの製造法に限定するものではない。
製造法例 1
式 (1 ) で示される本発明化合物は、 式(I)及び式(I I)で示される化合物から、 所望によ り塩基存在下に反応させることにより、下記の化学反応式に従って製造することができ
(I) (1)
(式中、 R ,、 R2、 T, Q、 mは前記と同じ意味を表し、 Yはハロゲン原子等の脱離基 を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセ卜二トリル、 プロピオン 二卜リル等の二卜リル系溶媒、 ジェチルェ一テル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 N, N-ジメチルホルムアミド、 ジメチルスルホキシド等の非プロト ン性極性溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 式(I I)で示される化合物の使用量は通常 1〜 5倍モルの範囲であり、好適には 1〜 2 倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力
リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [5. 4. 0]ゥンデ力一 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は。 式(I)で示される化合物に対し、 通 常 1〜 10倍モル、 好ましくは 1〜3倍モルである。
本反応の温度は、 — 78 :〜 200 の範囲で、 好適には— 20で〜 100での範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 30分〜 100時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 2 .
式 (1) で示されるァリール複素環誘導体のうち、 式(1— 1)で示される本発明化合 物は、 下記の化学反応式に従って、 式(III)で示される化合物から、 所望により塩基又 は酸の存在下に反応させることにより製造することができる。
(式中'、 R,、 R2、 R7、 T、 m は前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメ夕ン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニトリル等の二トリル系溶媒、 ジェチルェ —テル、 ジォキサン、 テトラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホ'ル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 卜リエチル ァミン、 N, N—ジメチルァニリン、 4ージメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [5. 4. 0]ゥンデカー 7—ェ ン等の有機塩基等が挙げられる。 用いられる塩基の使用量は、 式(III)で示される化合 物に対し、 通常 01〜10倍モル、 好ましくは 0. 1〜 3倍モルである。
酸としては、 塩酸、 硫酸等の無機酸、 トリフルォロ酢酸、 p—トルエンスルホン酸等 の有機酸等が挙げられる。用いられる酸の使用量は、 式(III)で示される化合物に対し、 通常 0. 01〜10倍モル、 好ましくは 0. 1〜3倍モルである。
本反応の温度は、 — 7 81:〜 2 0 0 の範囲で、 好適には— 2 0 〜 1 0 0 :の範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 3
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 一 2 )で示される本発明化合 物は、 下記の化学反応式に従って、 式(IV)で示される化合物から、 所望により塩基又は 酸の存在下に反応させることにより製造することができる。
(式中、 R !、 R2、 R 7、 T、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニトリル等の二トリル系溶媒、 ジェチルェ —テル、 ジォキサン、 テトラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 卜リエチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1 , 8—ジァザビシクロ [ 5 . 4 . 0 ]ゥンデカー 7—ェ ン等の有機塩基等が挙げられる。 用いられる塩基の使用量は、 式(IV)で示される化合物 に対し、 通常 0 . 0 1〜1 0倍モル、 好ましくは 0 . 1〜3倍モルである。
酸としては、 塩酸、 硫酸等の無機酸、 トリフルォロ酢酸、 p—トルエンスルホン酸等 の有機酸等が挙げられる。用いられる酸の使用量は、 式(IV)で示される化合物に対し、 通常 0 . 0 1〜 1 0倍モル、 好ましくは 0 . 1〜3倍モルである。
本反応の温度は、 — 7 8 〜 2 0 0での範囲で、 好適には— 2 0で〜 1 0 0での範囲 である。反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マ卜グラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 4
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1— 3 )で示される本発明化合
物は、 下記の化学反応式に従って、 式 (V)で示される化合物から、 所望により塩基又は 酸の存在下に反応させることにより製造することができる。
(式中、 R ,、 R2、 R 7、 R 1 0、 T、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1 , 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニトリル等の二トリル系溶媒、 ジェチルェ —テル、 ジォキサン、 テ卜ラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロ卜ン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
塩基としては、 例えば水酸化ナトリゥム、 水酸化力リゥム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン; N, N—ジメチルァニリン、 4ージメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [ 5 . 4 . 0 ]ゥンデ力— 7—ェ ン等の有機塩基等が挙げられる。 用いられる塩基の使用量は、 式 (V)で示される化合物 に対し、 通常 0 . 0 1〜 1 0倍モル、 好ましくは 0 . 1〜3倍モルである。
酸としては、 塩酸、 硫酸等の無機酸、 トリフルォロ酢酸、 p—トルエンスルホン酸等 の有機酸等が挙げられる。 用いられる酸の使用量は、 式 (V)で示される化合物に対し、 通常 0 . 0 1〜1 0倍モル、 好ましくは 0 . 1〜3倍モルである。
本反応の温度は、 —7 8で〜 2 0 0 °Cの範囲で、 好適には— 2 0 t:〜 1 0 0での範囲 である。反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 5
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 一 3 )で示される本発明化合 物は、 下記の化学反応式に従って、 式 (VI)及び式 (VI I)で示される化合物から、 所望に より塩基の存在下に反応させることにより製造することができる。
(式中、 R t、 R2、 R 7、 R 1 0、 T、 mは前記と同じ意味を表す。 Yは、 ハロゲン等の 脱離基を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニ卜リル等の二トリル系溶媒、 ジェチルェ 一テル、 ジォキサン、 テ卜ラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 卜リエチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [ 5 . 4 . 0 ]ゥンデ力一 7—ェ ン等の有機塩基等が挙げられる。 用いられる塩基の使用量は、 式 (VI)で示される化合物 に対し、 通常 1〜 1 0倍モル、 好ましくは 1 ~ 3倍モルである。
本反応の温度は、 — 7 8で〜 2 0 0での範囲で、 好適には— 2 0で〜 1 0 0 の範囲 である。反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 6
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 4 )で示される本発明化合物 は、 下記の化学反応式に従って、 式 (VI I I)で示されるァニリンから、 通常のジァゾ化及 び還元反応により、 式(IX)で示されるヒドラジンを製造した後、 製造法例 1で示した製 造法を用いて、 式 ( 1—4 )で示される本発明化合物を製造することができる。
(式中、 R 2、 Q、 Y、 mは前記と同じ意味を表す。)
製造法例 7
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 5 )で示される本発明化合物は、 下記の化学反応式に従って、 式(1一 4 )で示される本発明化合物から、 酸化剤の存在下、 所望により塩基の存在下に反応させることにより製造することができる。
(式中、 R 2、 Q、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1 , 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 酸化剤としては、 臭素などのハロゲン類、 過酸化水素等の過酸化物類、 パラジウム等 の金属類、 酸化水銀等の金属酸化物、 N—クロロサクシンイミド、 N—プロモサクシン イミド等が挙げられる。 用いられる酸化剤の使用量は、 式(1—4 )で示される化合物に 対し、 通常 1〜 1 0倍モル、 好ましくは 1〜3倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム'、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1 , 8—ジァザビシクロ [ 5 . 4 . 0 ]ゥンデ力— 7—ェ ン等の有機塩基等が挙げられる。 用いられる塩基の使用量は、 式 (VI)で示される化合物 に対し、 通常 1〜 1 0倍モル、 好ましくは 1〜 3倍モルである。
本反応の温度は、 一 7 8 〜 2 0 0 の範囲で、 好適には— 2 0 °C〜1 0 の範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 8
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 6 )で示される本発明化合物は、 下記の化学反応式に従って、 式 (XIV)で示される化合物から、 アミノ化剤の存在下に反 応させることにより製造することができる。
(式中、 R
2、 R
7、 T、 Q、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニトリル等の二トリル系溶媒、 ジェチルェ —テル、 ジォキサン、 テトラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
アミノ化剤としては、 O—(メシチレンスルホニル)ヒドロキシルァミン、 ヒドロキシ ルァミン— O—スルホン酸などのヒドロキシルァミン類等が挙げられる。用いられるァ ミノ化剤の使用量は、 式 (XIV)で示される化合物に対し、 通常 1〜 1 0倍モル、 好まし くは 1〜 2倍モルである。
本反応の温度は、 一 7 8で〜 2 0 0での範囲で、 好適には— 2 0で〜 1 0 0 の範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マ卜グラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 9
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 7 )で示される本発明化合物は、 下記の化学反応式に従って、 式 (XIV)及び式 (XV)で示される化合物から、 所望により酸 の存在下に反応させることにより製造することができる。
(式中、 R 1 ¾ R 2、 R 1 0、 T、 Υ、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トル.ェン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、、 ァセトニ卜リル、 プロピオ ンニ卜リル等の二トリル系溶媒、 ジェチルエーテル、 ジォキサン、 テトラヒドロフラン 等のエーテル系溶媒、 N, N—ジメチルホルムアミド、 ジメチルスルホキシド等の非プ 口トン性極性溶媒、 アセトン、 メチルェチルケトン等のケトン類、 水および、 これらの 溶媒を二つ以上混合した混合溶媒系が挙げられる。
酸としては、 蟻酸、 塩酸、 酢酸、 臭化水素酸等が挙げられる。 用いられる酸の使用量 は、 式 (XIV)で示される化合物に対し、 通常 1 ~ 1 0 0倍モル、 好ましくは 1〜 1 0倍 モルである。
本反応の温度は、 — 7 8 °C〜2 0 0 :の範囲で、 好適には— 2 0 °C〜 1 0 0での範 囲である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範 囲である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムク 口マトグラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 1 0
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 8 )で示される本発明化合物は、 下記の化学反応式に従って、 式 (XVI)で示される化合物から、 硫化剤の存在下に反応さ せることにより製造することができる。
(式中、 R 2、 R 7、 R 、 T、 Y、 m、 kは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセトニトリル、 プロピオン 二トリル等の二トリル系溶媒、 ジェチルエーテル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられ る。
硫化剤としては、 例えば五硫化二リン、 ローソン試薬等が挙げられる。 硫化剤の使用 量は、 式 (XVI)で示される化合物に対し、 通常 1〜 1 0倍モル、 好ましくは 1〜 3倍モ ルである。
本反応の温度は、 一 7 8 〜 2 0 0での範囲で、 好適には一 2 0 T:〜 1 0 0での範 囲である。反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範 囲である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムク ロマ卜グラフィ一等の公知慣用の製法により容易に精製できる。
製造法例 1 1
式 (1 ) で示されるァリール複素環誘導体のうち、 式(1 - 9 )で示される本発明化合物は、 下記の化学反応式に従って、 式 (XVI I)で示される化合物から、 所望により塩基の存在下 に反応させることにより製造することができる。
(式中、 R i、 R
2、 R
7、 R n、 T、 m、 kは前記と同じ意味を表す。 Lはアルキルス ルホニルォキシ、 トリフルォロメタンスルホニルォキシ、 ハロゲン等の脱離基を表す。) 本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニ卜リル、 プロピオンニ卜リル等の二トリル系溶媒、 ジェチルェ —テル、 ジォキサン、 テトラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 アセトン、 メチルェチル ケトン等のケトン類、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げら れる。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナ卜リウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [ 5 . 4. 0 ]ゥンデ力一 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は、 式 (XVII)で示される化合物に対し、 通常 1〜 1 0倍モル、 好ましくは 1〜 3倍モルである。
本反応の温度は、 — 7 8で〜 2 0 0での範囲で、 好適には— 2 O :〜 1 0 0 の範 囲である。反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範 囲である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムク 口マトグラフィ一等の公知慣用の製法により容易に精製できる。
参考として、本願記載の化合物の中間体化合物(II I)、 (IV)、 (V)、 (VI)、 (XIV)、 (XVI)、 (XVII)の製造法の例を示すが、 これらの製造法に限定するものではない。
中間体製造例 1
式 (XVIII) で示される中間体化合物は、 式 (X) で示される化合物とヒドロキシルアミ ン塩もしくはヒドロキシルァミン水溶液から、所望により塩基の存在下に反応させるこ とにより製造することができる。
(X) 2 (XVIII)
(式中、 I^、 R2、 T、 mは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ
ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1 , 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ジェチルエーテル、 ジォキサ ン、 テトラヒドロフラン等のエーテル系溶媒、 メタノール、 エタノール等のアルコール 類、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。
ヒドロキシルァミン塩もしくはヒドロキシルァミン水溶液の使用量は、 式 (X)で示さ れる化合物に対し、 純分換算で通常 1 ~ 1 0倍モルの範囲であり、 好適には 1〜 3倍モ ルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4ージメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [ 5. 4. 0 ]ゥンデカー 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は式 (X)で示される化合物に対し、 通常 1〜 1 0倍モル、 好ましくは 1〜3倍モルである。
本反応の温度は、 一 7 8 T:〜 2 0 0 の範囲で、 好適には一 2 0で〜 1 0 0 °Cの範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 2
式 (III) で示される中間体化合物は、 式 (XVI II) 及び式 (XI)で示される化合物から、 所 望により塩基あるいは脱水剤存在下に反応させることにより、下記の化学反応式に従つ て製造することができる。
(式中、 R ,、 R2、 T、 mは前記と同じ意味を表す。 Zは、 水酸基またはハロゲン等の 脱離基を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1 , 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセトニトリル、 プロピオン 二トリル等の二卜リル系溶媒、 ジェチルエーテル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 Ν, Ν-ジメチルホルムアミド、 ジメチルスルホキシド等の非プロトン 性極性溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 式 (XVI)で示される化合物の使用量は、 式 (XVI I I)で示される化合物に対し、 通常 1〜 5倍モルの範囲であり、 好適には 1〜 2倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力
リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4ージメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [5. 4. 0]ゥンデカー 7—ェ ン等の有機塩基等が挙げられる ό 塩基の使用量は式 (XVIII)で示される化合物に対し、 通常 1〜 10倍モル、 好ましくは 1〜3倍モルである。
脱水剤としては、 Ν, Ν—ジシクロへキシルカルポジイミド、 1一(3—ジメチルアミ ノプロピル)一 3一ェチルカルポジィミド塩酸塩等の カルポジィミド類ゃ光延反応法 (例えば、 J. Chem. S o c, Pe r k i n Tr an s 1., 1708、 (197 6)参照)を使用できる。
本反応の温度は、 — 78で〜 200 の範囲で、 好適には— 20 〜 100での範囲 である。反応時間は反応試剤の量及び温度により異なるが、 30分〜 100時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 3
式 (IV) で示される中間体化合物は、 式 (XII)及び式 (XIII)で示される化合物から、 所 望により塩基あるいは脱水剤存在下に反応させることにより、下記の化学反応式に従つ て製造することができる。
(式中、 R2、 R7、 T、 mは前記と同じ意味を表す。 Zは、 水酸基またはハロゲ ン等の脱離基を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロ口 エタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセ卜二卜リル、 プロピオン 二トリル等の二卜リル系溶媒、 ジェチルエーテル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 N,N-ジメチルホルムアミド、 ジメチルスルホキシド等の非プロトン 性極性溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 式 (XIII)で示される化合物の使用量は、 式 (XII)で示される化合物に対し、 通常 1〜 5倍モルの範囲であり、 好適には 1〜 2倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力
リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 N, N—ジメチルァニリン、 4—ジメチルァミノピリジン、 N—メチルピロリ ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [5. 4. 0]ゥンデカー 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は式 (XII)で示される化合物に対し、 通 常 1〜 10倍モル、 好ましくは 1〜3倍モルである。
脱水剤としては、 N, N—ジシクロへキシルカルポジイミド、 1— (3—ジメチルアミ ノプロピル) - 3一ェチルカルポジィミド塩酸塩等の カルポジィミド類ゃ光延反応法 (例えば、 J. Chem. Soc., Pe r k i n Tr an s 1., 1708、 (197 6)参照)を使用できる。
本反応の温度は、 — 78 :〜 200での範囲で、 好適には— 20で〜 100 Xの範囲 である。反応時間は反応試剤の量及び温度により異なるが、 30分〜 100時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マ卜グラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 4
式 (V) で示される中間体化合物は、 式 (VI)及び式 (VII)で示される化合物から、 所望に より塩基存在下に反応させることにより、下記の化学反応式に従つて製造することがで さる。
(式中、 1^、 R2、 R7、 R10、 T、 m、 Υは前記と同じ意味を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 メタノール、 エタノール等の アルコール類、 ァセトニトリル、 プロピオンニトリル等の二卜リル系溶媒、 ジェチルェ —テル、 ジォキサン、 テトラヒドロフラン等のエーテル系溶媒、 Ν, Ν—ジメチルホル ムアミド、 ジメチルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒 を二つ以上混合した混合溶媒系が挙げられる。
式 (VII)で示される化合物の使用量は、 式 (VI)で示される化合物に対し、 通常 1〜5 倍モルの範囲であり、 好適には 1〜 2倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 Ν, Ν—ジメチルァニリン、 4—ジメチルァミノピリジン、 Ν—メチルピロリ
ジン、 N—メチルモルホリン、 1, 8—ジァザビシクロ [ 5. 4. 0 ]ゥンデ力— 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は、 式 (VI)で示される化合物に対し、 通 常 1〜 1 0倍モル、 好ましくは 1〜3倍モルである。
本反応の温度は、 一 7 8で〜 2 0 0での範囲で、 好適には一 2 0 :〜 1 0 O :の範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マ卜グラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 5
式 (VI) で示される中間体化合物は、 式 (X)及び硫化水素、 もしくは式 (XIX)で示される チォアルキルアミドから、所望により塩基あるいは酸存在下に反応させることにより、 下記の化学反応式に従って製造することができる。
(式中、 R,、 R2、 T、 mは前記と同じ意味を表す。 R 1 2は d— 6アルキル基を表す。) 本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1 , 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ジェチルエーテル、 ジォキサ ン、 テトラヒドロフラン等のエーテル系溶媒、 N, N—ジメチルホルムアミド、 ジメチ ルスルホキシド等の非プロトン性極性溶媒、 水および、 これらの溶媒を二つ以上混合し た混合溶媒系が挙げられる。
硫化水素の使用量は、 式 (X)で示される化合物に対し、 通常 1〜 1 0 0倍モルの範囲 であり、 好適には 1 0 ~ 2 0倍モルである。 式 (XIX)で示されるチォアルキルアミドの 使用量は、 式 (X)で示される化合物に対し、 通常 1〜 5倍モルの範囲であり、 好適には
:!〜 3倍モルである。
塩基としては、 例えばピリジン、 トリェチルァミン、 N, N—ジメチルァニリン、 4 ージメチルァミノピリジン、 N—メチルピロリジン、 N—メチルモルホリン、 1 , 8— ジァザビシクロ [ 5 . 4. 0 ]ゥンデ力— 7—ェン等の有機塩基、 及びこれらの溶媒を二 つ以上混合した混合溶媒系が挙げられる。 塩基の使用量は式 (X)で示される化合物に対 し、 通常 1〜 1 0 0倍モル、 好ましくは 1〜 2 0倍モルである。
酸としては、 例えば蟻酸、 塩酸、 臭化水素酸等の無機酸等が挙げられる。 酸の使用量 は、 式 (X)で示される化合物に対し通常 1〜 1 0 0倍モル、 好ましくは 1〜 1 0倍モル である。
本反応の温度は、 0で〜 2 0 0 の範囲で、 好適には O t:〜 1 0 0での範囲である。
反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロマ卜ダラ フィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 6
式 (XIV) で示される中間体化合物は、 式 (VI)及び式 (XX)で示される化合物から、 下記 の化学反応式に従つて製造することができる。
(式中、 R,、 R2、 R 7、 T、 mは前記と同じ意味を表す。 R 1 2は d— 6アルキル基を表 す。) 本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロロ ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセトニ卜リル、 プロピオン 二トリル等の二トリル系溶媒、 ジェチルエーテル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 N, N—ジメチルホルムアミド、 ジメチルスルホキシド等の非プロ 卜ン性極性溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 式 (XX)で示される化合物の使用量は、式 (VI)で示される化合物に対し通常 1〜 5倍モ ルの範囲であり、 好適には 1〜 2倍モルである。
本反応の温度は、 一 7 8で〜 2 0 0での範囲で、 好適には一 2 0 〜 1 0 0での範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 3 0分〜 1 0 0時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 7
式 (XVI) で示される中間体化合物は、 式 (XI I)及び式 (XXI)で示される化合物から、 所 望により塩基あるいは脱水剤存在下に反応させることにより、下記の化学反応式に従づ て製造することができる。
(式中、 Ri、 R
2、 R
7、 Ru、 T、 m、 kは前記と同じ意味を表す。 Zは、 水酸基ま たはハロゲン等の脱離基を表す。)
本反応は溶媒存在下または無溶媒で行うことができる。使用できる溶媒としては、 反 応に不活性な溶媒であれば特に限定されず、 例えばペンタン、 へキサン、 ヘプタン、 ベ ンゼン、 トルエン、 キシレン等の炭化水素系溶媒、 ジクロロメタン、 1, 2—ジクロ口 ェタン、 クロ口ホルム、 四塩化炭素等のハロゲン系溶媒、 ァセトニ卜リル、 プロピオン 二卜リル等の二卜リル系溶媒、 ジェチルェ一テル、 ジォキサン、 テトラヒドロフラン等 のエーテル系溶媒、 Ν,Ν-ジメチルホルムアミド、 ジメチルスルホキシド等の非プロトン 性極性溶媒、 水および、 これらの溶媒を二つ以上混合した混合溶媒系が挙げられる。 式 (XXI)で示される化合物の使用量は、 式 (XII)で示される化合物に対し、 通常 1〜5 倍モルの範囲であり、 好適には 1〜 2倍モルである。
塩基としては、 例えば水酸化ナトリウム、 水酸化カリウム、 炭酸ナトリウム、 炭酸力 リウム、 炭酸水素ナトリウム、 炭酸水素カリウム等の無機塩基、 ピリジン、 トリェチル ァミン、 Ν, Ν—ジメチルァニリン、 4—ジメチルァミノピリジン、 Ν—メチルピロリ ジン、 Ν—メチルモルホリン、 1, 8—ジァザピシクロ [5. 4. 0]ゥンデ力一 7—ェ ン等の有機塩基等が挙げられる。 塩基の使用量は式 (XII)で示される化合物に対し、 通 常 1〜 10倍乇ル、 好ましくは 1〜3倍モルである。
脱水剤としては、 Ν, Ν—ジシクロへキシルカルポジイミド、 1— (3—ジメチルアミ ノプロピル)一 3一ェチルカルポジィミド塩酸塩等の カルポジィミド類ゃ光延反応法 (例えば、 J. Chem. S o c, Pe r k i n Tr an s 1., 1708、 (197 6)参照)を使用できる。
本反応の温度は、 一 78t:〜 200での範囲で、 好適には一 20で〜 100 の範囲 である。 反応時間は反応試剤の量及び温度により異なるが、 30分〜 100時間の範囲 である。 反応終了後は、 生成物の精製が必要であれば、 蒸留、 再結晶またはカラムクロ マトグラフィ一等の公知慣用の製法により容易に精製できる。
中間体製造例 8
式 (XVII) で示される中間体化合物のうち、 式 (XVII— 1) で示される中間体化合物あ るいは式 (XVII— 2) で示される中間体は、 下記の化学反応式に従って、 式 (XVI)で示 される中間体化合物から、 通常のハロゲン化反応により式 (XVII— 1) で示される中間 体化合物が製造でき、 通常の塩基を用いたスルホン化反応により式 (XVII— 2)で示さ れる中間体を製造することができる。
OS02R13
(式中、 R,、 R2、 R7、 Ru、 T、 m、 kは前記と同じ意味を表す。 Xは、 ハロゲン を表し、 3は低級アルキル基、 置換されてもよいフエ二ル基等を表す。)
農園芸用殺菌剤および殺虫剤
本発明化合物 (式 (1) で表される化合物またはその塩) は、 広範囲の種類の糸状菌、 例えば、 藻菌類 (Oomy c e t e s). 子のう (嚢) 菌類 (As c omy c e t e s), 不完全菌類 (Deu t e r omyc e t e s), 担子菌類 (Ba s i d i omyc e t e s) に属する菌に対しすぐれた殺菌力を有する。本発明化合物を有効成分とする組成 物は、 花卉、 芝、 牧草を含む農園芸作物の栽培に際し発生する種々の病害の防除に、 種 子処理、 茎葉散布、 土壌施用または水面施用等により使用することができる。
例えば、
テンサイ 掲斑病 (Ce r c o s po r a be t i c o l a)
ラッカセィ 褐斑病 (Myc o s phae r e l l a a r ach i d i s)
黒渋病 (Myc o s phae r e l l a be r ke l ey i) キュゥリ うどんこ病 (Spha e r o t he c a f u 1 i g i n e a)
つる枯病 (Myc o s ph ae r e l l a me 1 o n i s )
菌核病 (S c l e r o t i n i a s c l e r o t i o r um) 灰色力、び病 (Bo t ry t i s c i ne r e a)
黒星病 (C I ado s po r i um c u c ume r i n u m) トマト 灰色かび病 (Bo t r y t i s c i ne r e a)
葉力、び病 (C 1 ado s po r i um f u 1 v um)
ナス 灰色かび病 (Bo t r y t i s c i ne r e a)
黒枯病 (Co r yne s po r a me 1 onge n ae)
、 うどんこ病 (E r y s i p h e c i c ho r ac e a r um)
イチゴ 灰色力、び病 (Bo t r y t i s c i ne r e a)
うどんこ病 (Sohae r o t he c a humu l i )
夕マネギ 灰色腐敗病 (Bo t r y t i s a 1 1 i i )
灰色力、び病 (Bo t ry t i s c i ne r e a)
ィンゲン 菌核病 (S c l e r o t i n i a s c l e r o t i o r um)
灰色力、び病 (Bo t ry t i s c i ne r e a)
りんご うどんこ病 (Podo s phae r a l e uc o t r i c ha)
黒星病 (Ve n t u r i a i n a e q u a 1 i s
モニリア病 (M o n i 1 i n i a m a 1 i
カキ うどんこ病 (Phy l l ac t i n i a k a k i c o 1 a)
炭そ病 (G l oe o s po r i um k a k i )
角斑落葉病 (Ce r c o s po r a k a k i )
モモ ·ォゥトウ 灰星病 (Mo n i l i n i a f r uc t i c o l a)
ブドウ 灰色かび病 (Bo t r y t i s c i ne r e a)
うどんこ病 (Unc i nu l a ne c a t o r)
晚腐病 (G 1 ome r e 1 1 a c i n g u 1 a t a)
ナシ 黒星病 (Ve n t u r i a n a s h i c o 1 a)
赤星病 (Gymno s po r ang i um a s i a t i c um)
黒斑病 (A l t e r na r i a k i kuc h i an a)
チヤ 輪斑病 (Pe s t a l o t i a t he ae)
炭そ病 (Co l l e t o t r i c hum t h e a e— s i n e n s i s カンキッ そうか病 (E l s i n oe f awc e t t i)
青力、び病 (P e n i c i 1 1 i um i t a 1 i c um)
緑かび病 (Pen i c i 1 1 i um d i g i t a t um)
灰色力、び病 (B o t r y t i s c i ne r e a)
ォォムギ うどんこ病 (E r y s i phe g r ami n i s f . s p. ho r d e i) 裸黒穂病 (U s t i 1 a g o n u d a )
コムギの赤かび病 (G i b b e r e 1 1 a z e a e )
赤さび病 (Puc e i n i a r e c o n d i t a)
斑点病 (C o c h 1 i o b o 1 u s s a t i V u s )
眼紋病 (P s e u d o c e r c o s P o r e 1 1 a h e r P
1 d e 3 )
ふお病 (L e p t o s P h a e r i a n o d o r u m)
うどんこ病 (E r y s i P h e g r a m i n i s f . s P.
i)
紅色雪腐病 (M i c r o n e c t r i e 1 1 a n i v a 1 i
イネ いもち病 (P y r i c u 1 a r i a o r y z a e)
紋枯病 (Rh i z o c t o n i a s o 1 a n i )
馬鹿苗病 (G i b b e r e 1 1 a f u j i k u r o i)、
ごま葉枯病 (Co c h 1 i o b o 1 u s n i y a b e a n u
夕ノヾコ 菌核病 (Sc l e r o t i n i a s c l e r o t i o r um)
うどんこ病 (E ry s i phe c i c ho r a c e a r um)
チューリップ灰色力、び病 (Bo t ry t i s c i ne r e a)
ベントグラス 雪腐大粒菌核病 (S c l e r o t i n i a bo r e a l i s:)、 ォ一チヤ一ドグラスのうどんこ病 (E ry s i phe g r ami n i s)、 ダイズ 紫斑病 (Ce r c o s po r a k i kuc h i i)、
ジャガイモ ' トマトの疫病 (Phy t oph t ho r a i n f e s t an s), キユウリ ベと病 (P s e udo pe r ono s po r a c ube n s i s)、 ブドウ ベと病 (P l a smop a r a v i t i c o l a)
等の防除に使用することができる。
また、近年種々の病原菌においてべンズイミダゾール系殺菌剤ゃジカルポキシイミド 系殺菌剤等に対する耐性が発達し、 それらの薬剤の効力不足を生じており、 耐性菌にも 有効な薬剤が望まれている。本発明の化合物は、 それら薬剤に対し感受性の病原菌のみ ならず、 耐性菌にも優れた殺菌効果を有する薬剤である。
例えば、 チオファネ一トメチル、 べノミル、 カルベンダジム等のベンズイミダゾール
系殺菌剤に耐性を示す灰色かび病菌(Bo t ry t i s c i ne r e a)やテンサイ 褐斑病菌 (Ce r c o s po r a b e t i c o 1 a), リンゴ黒星病菌 (Ve n t u r i a i nae qua l i s), ナシ黒星炳菌 (V e n t u r i a na s h i c o
1 a) に対しても感受性菌と同様に本発明化合物は有効である。
さらに、 ジカルボキシイミド系殺菌剤 (例えば、 ビンクロゾリン、 プロシミドン、 ィ プロジオン) に耐性を示す灰色かび病菌 (B o t r y t i s c i n e r e a) に対し ても感受性菌と同様に本発明化合物は有効である。
適用がより好ましい病害としては、 テンサイの褐斑病、 コムギのうどんこ病、 イネの いもち病、 リンゴ黒星病、 キユウリの灰色かび病、 ラッカセィの褐斑病等が挙げられる。
(殺虫剤)
本発明化合物 (式 〔I〕 で表される化合物又はその塩) は農業上の有害生物、 衛生害虫、 貯殻害虫、 衣類害虫、 家屋害虫等の防除に使用でき、 殺成虫、 殺若虫、 殺幼虫、 殺卵作用 を有する。
鱗翅目害虫、 例えば、 ハスモンョトウ、 ョトウガ、 夕マナャガ、 ァォムシ、 夕マナギン ゥヮバ、 コナガ、 チヤノコカクモンハマキ、 チヤハマキ、 モモシンクィガ、 ナシヒメシン クイ、 ミカンハモグリガ、 チヤノホソガ、 キンモンホソガ、 マイマイガ、 チャドクガ、 二 カメィガ、 コプノメイガ、 ョ一口ピアンコ一ンボーラ一、 アメリカシロヒトリ、 スジマダ ラメィガ、 へリオティス属、 へリコベルパ属、 ァグロティス属、 ィガ、 コドリンガ、 ヮ夕 ァカミムシ等、
半翅目害虫、 例えば、 モモァカアブラムシ、 ヮ夕アブラムシ、 ニセダイコンアブラムシ、 ムギクピレアブラムシ、 ホソヘリカメムシ、 ァォクサカメムシ、 ャノネカイガラムシ、 ク ヮコナカィガラムシ、 オンシッコナジラミ、 タバココナジラミ、 ナシキジラミ、 ナシダン バイムシ、 トビイロゥン力、 ヒメ卜ピウンカ、 セジロウンカ、 ツマグロョコバイ等、 甲虫目害虫、 例えば、 キスジノミハムシ、 ゥリハムシ、 コロラドハムシ、 イネミズゾゥ ムシ、 コクゾゥムシ、 ァズキゾゥムシ、 マメコガネ、 ヒメコガネ、 ジアブロティカ属、 夕 バコシバンムシ、 ヒラタキクイムシ、 マツノマダラカミキリ、 ゴマダラカミキリ、 ァグリ ォティス属、 ニジユウャホシテントウ、 コクヌスト、 ヮタミゾゥムシ等、
双翅目害虫、 例えば、 イエバエ、 ォォクロバエ、 センチニクバエ、 ゥリミバエ、 ミカン コミバエ、 タネバエ、 イネハモグリバエ、 キイ口ショウジヨウバエ、 サシバエ、 コガ夕ァ カイエ力、 ネッ夕イシマ力、 シナハマダラ力等、
ァザミゥマ目害虫、 例えば、 ミナミキイロアザミゥマ、 チヤノキイロアザミゥマ等、 膜翅目害虫、 例えば、 イエヒメアリ、 キイロスズメバチ、 力ブラハバチ等、
直翅目害虫、 例えば、 トノサマバッ夕、 チヤパネゴキブリ、 ヮモンゴキブリ、 クロゴキブ リ等
シロアリ目害虫、 例えば、 イエシロアリ、 ャマトシロアリ等、
隠翅目害虫、 例えば、 ヒ卜ノミ、 ネコノミ等、 シラミ目害虫、 例えば、 ヒトジラミ等、 ダニ類、 例えば、 ナミハダ二、 ニセナミハダ二、 カンザヮハダ二、 ミカンハダニ、 リン ゴハダニ、 ミカンサビダ二、 リンゴサビダ二、 チヤノホコリダ二、 ブレビパルパス属、 ェ ォテトラニカス属、 ロビンネダニ、 ケナガコナダニ、 コナヒヨウヒダニ、 ォゥシマダニ、
フタトゲチマダニ等、
植物寄生性線虫類、 例えば、 サッマイモネコブセンチユウ、 ネグサレセンチユウ、 ダイ ズシストセンチユウ、 イネシンガレセンチユウ、 マツノザィセンチユウ等。
適用が好ましい有害生物としては、 鱗翅目害虫、 半翅目害虫、 甲虫目害虫、 ァザミゥマ 目害虫、 ハダ二類であり、 特に好ましくは鱗翅目害虫、 半翅目害虫、 ハダ二類 である。
又、 近年コナガ、 ゥン力、 ョコバイ、 アブラムシ等多くの害虫において有機リン剤、 力 一バメート剤ゃ殺ダニ剤に対する抵抗性が発達し、 それら薬剤の効力不足問題を生じてお り、 抵抗性系統の害虫やダニにも有効な薬剤が望まれている。 本発明化合物は感受性系統 のみならず、 有機リン剤、 カーバメ一卜剤、 ピレスロイド剤抵抗性系統の害虫や、 殺ダニ 剤抵抗性系統のダニにも優れた殺虫殺ダニ効果を有する薬剤である。
また本発明化合物は薬害が少なく、 魚類や温血動物への毒性が低く、 安全性の高い薬剤 である。
本発明化合物は、 水棲生物が船底、 魚網等の水中接触物に付着するのを防止するための 防汚剤として使用することもできる。
本発明殺菌剤および殺虫剤は本発明化合物の 1種または 2種以上を有効成分として 含有する。
本発明化合物を実際に施用する際には他成分を加えず純粋な形で使用できるし、また 農薬として使用する目的で一般の農薬のとり得る形態、 即ち、 水和剤、 粒剤、 粉剤、 乳 剤、 水溶剤、 懸濁剤、 顆粒水和剤等の形態で使用する'こともできる。
農薬製剤中に添加することのできる添加剤および担体としては、固型剤を目的とする 場合は、 大豆粉、 小麦粉等の植物性粉末、 珪藻土、 燐灰石、 石こう、 タルク、 ベントナ イト、 パイロフイライト、 クレー等の鉱物性微粉末、 安息香酸ソーダ、 尿素、 芒硝等の 有機及び無機化合物が使用される。
また、 液体の剤型を目的とする場合は、 ケロシン、 キシレンおよび石油系の芳香族炭 化水素、 シクロへキサン、 シクロへキサノン、 ジメチルホルムアミド、 ジメチルスルホ キシド、 アルコール、 アセトン、 トリクロルエチレン、 メチルイソプチルケトン、 鉱物 油、 植物油、 水等を溶剤として使用することができる。
さらに、 これらの製剤において均一かつ安定な形態をとるために、 必要に応じ界面活 性剤を添加することもできる。添加することができる界面活性剤としては特に限定はな いが、 例えば、 ポリオキシエチレンが付加したアルキルフエニルエーテル、 ポリオキシ エチレンが付加したアルキルエーテル、ポリオキシエチレンが付加した高級脂肪酸エス テル、 ポリオキシエチレンが付加したソルビタン高級脂肪酸エステル、 ポリオキシェチ レンが付加したトリスチリルフエニルエーテル等の非イオン性界面活性剤、ポリォキシ エチレンが付加したアルキルフエニルエーテルの硫酸エステル塩、アルキルベンゼンス ルホン酸塩、 高級アルコールの硫酸エステル塩、 アルキルナフ夕レンスルホン酸塩、 ポ リカルボン酸塩、 リグニンスルホン酸塩、 アルキルナフタレンスルホン酸塩のホルムァ ルデヒド縮合物、 ィソブチレン一無水マレイン酸の共重合物等が挙げられる。
このようにして得られた水和剤、 乳剤、 フロアブル剤, 水溶剤, 顆粒水和剤は水で所 定の濃度に希釈して溶解液, 懸濁液あるいは乳濁液として、 粉剤 ·粒剤はそのまま植物 に散布する方法で使用される。
また有効成分量は、 通常、 組成物 (製剤) 全体に対して好ましくは 0 . 0 1〜9 0重 量%であり、 より好ましくは 0 . 0 5〜8 5重量%でぁる。
製剤化された本発明の殺菌剤組成物は、 そのままで、 或いは水等で希釈して、 植物体、 種子、 水面または土壌に施用される。 施用量は、 気象条件、 製剤形態、 施用磁気、 施用 方法、 施用場所、 防除対象病害、 対象作物等により異なるが、 通常 1ヘクタール当たり 有効成分化合物量にして 1〜1 , 0 0 0 g、 好ましくは 1 0〜1 0 0 gである。
水和剤、 乳剤、 懸濁剤、 水溶剤、 顆粒水和剤等を水で希釈して施用する場合、 その施 用濃度は l〜1 0 0 0 p p m、 好ましくは 1 0〜2 5 0 p p mであり、 粒剤、 粉剤等の 場合は、 希釈することなくそのまま施用する。
なお、 本発明化合物は単独でも十分有効であることは言うまでもないが、 各種の殺菌剤 や殺虫'殺ダニ剤または共力剤の 1種または 2種以上と混合して使用することもできる。 本発明化合物と混合して使用できる殺菌剤、 殺虫剤、 殺ダニ剤、 植物生長調節剤の代 表例を以下に示す。
殺菌剤:
キヤプタン、 フオルペット、 チウラム、 ジラム、 ジネブ、 マンネブ、 マンコゼブ、 プロビネブ、 ポリカーバメート、 クロロタロニル、 キン! ゼン、 キヤプタホル、 ィプ ロジオン、 プロサイミドン、 ビンクロゾリン、 フルォロイミド、 サイモキサニル、 メプ ロニル、、 フルトラニル、 ペンシクロン、 ォキシカルボキシン、 ホセチルアルミニウム、 プロパモカーブ、 トリアジメホン、 トリアジメノール
、 プロピコナゾール、 ジクロブトラゾール、 ビテルタノール、 へキサコナゾール、 マイ クロブ夕ニル、 フルシラゾ一ル、 メトコナゾ一ル、 エタコナゾ一ル、 フルオトリマゾ一 ル、 シプロコナゾール、 エポキシコナゾール、 フルトリアフェン、 ベンコナゾール、 ジ ニコナゾ一ル、 サイプロコナゾ一ズ、 フエナリモール、 トリフルミゾール、 プロクロラ ズ、 イマザリル、 ぺフラゾェ一ト、 トリデモルフ、 フェンプロピモルフ、 トリホリン、 プチオベート、 ピリフエノックス、 ァニラジン、 ポリオキシン、 メタラキシル、 ォキサ ジキシル、 フララキシル、 イソプロチオラン、 プロべナゾール、 ピロ一ルニトリン、 ブ ラストサイジン S、 カスガマイシン、 バリダマイシン、 硫酸ジヒドロス卜レブトマイシ ン、 べノミル、 カルベンダジム、 チオファネ一トメチル、 ヒメキサゾ一ル、 塩基性塩化 銅、 塩基性硫酸銅、 フェンチンアセテート、 水酸化トリフエニル錫、 ジェ卜フェンカル ブ、 メタスルホカルプ、 キノメチオナー卜、 ピナパクリル、 レシチン、 重曹、 ジチアノ ン、 ジノカップ、 フエナミノスルフ、 ジクロメジン、 グァザチン、 ドジン、 I B P、 ェ ディフェンホス、 メパニピリム、 フェルムゾン、 トリクラミド、 メタスルホカルプ、 フ ルアジナム、 エトキノラック、 ジメトモルフ、 ピロキロン、 テクロフ夕ラム、 フサライ ド、 フエナジンォキシド、 チアベンダゾール、 トリシクラゾ一ル、 ビンクロゾリン、 シ モキサニル、 シクロブ夕ニル、 グァザチン、 プロパモカルプ塩酸塩、 ォキゾリニック酸、
ヒドロキシイソォキサゾ一ル、 ィミノクタジン酢酸塩等。
殺虫 ·殺ダニ剤:
有機燐およびカーバメート系殺虫剤:
フェンチオン、 フエニトロチオン、 ダイアジノン、 クロルピリホス、 E S P、 バミド チオン、 フェン卜ェ一卜、 ジメトエート、 ホルモチオン、 マラソン、 トリクロルホン、 チオメトン、 ホスメッ卜、 ジクロルボス、 ァセフェート、 E P B P、 メチルパラチオン、 ォキシジメトンメチル、 ェチオン、 サリチオン、 シァノホス、 イソキサチオン、 ピリダ フェンチオン、 ホサロン、 メチダチオン、 スルプロホス、 クロルフェンビンホス、 テト ラクロルビンホス、 ジメチルビンホス、 プロパホス、 イソフェンホス、 ェチルチオメト ン、 プロフエノホス、 ピラクロホス、 モノクロ卜ホス、 ァジンホスメチル、 アルディ力 ルブ、 メソミル、 チォジカルプ、 カルポフラン、 カルボスルファン、 ベンフラカルブ、 フラチォカルプ、 プロボキスル、 B P M C、 M T M C、 M I P C、 力ルバリル、 ピリミ カーブ、 ェチォフェンカルプ、 フエノキシカルプ、 E D D P等。
ピレスロイド系殺虫剤:
ペルメトリン、 シペルメトリン、 デル夕メスリン、 フェンバレレート、 フェンプロ パトリン、 ピレトリン、 アレスリン、 テトラメスリン、 レスメトリン、 ジメスリン、 プ 口パスリン、 フエノトリン、 プロトリン、 フルバリネート、 シフルトリン、 シハロトリ ン、 フルシトリネー卜、 エトフェンプロクス、 シクロプロトリン、 トロラメトリン、 シ ラフルォフェン、 プロフェンプロクス、 ァクリナスリン等。
ベンゾィルゥレア系その他の殺虫剤:
ジフルべンズロン、 クロルフルァズロン、 へキサフルムロン、 トリフルムロン、 テ卜 ラベンズロン、 フルフエノクスロン、 フルシクロクスロン、 ブプロフエジン、 ピリプロ キシフェン、 メトプレン、 ベンゾェピン、 ジァフェンチウロン、 ァセタミプリド、 イミ ダクロプリ ド、 二テンビラム、 フィプロニル、 カルタップ、 チオシクラム、 ベンスル夕 ップ、 硫酸ニコチン、 ロテノン、 メタアルデヒド、 機械油、 B Tや昆虫病原ウィルスな どの微生物農薬等。
殺線虫剤:
フエナミホス、 ホスチアゼート等。
殺ダニ剤:
クロルべンジレート、 フエ二ソブロモレ一卜、 ジコホル、 アミトラズ、 B P P S、 ベ ンゾメ一卜、 へキシチアゾクス、 酸化フェンブ夕スズ、 ポリナクチン、 キノメチォネ一 ト、 C P C B S、 テトラジホン、 アベルメクチン、 ミルべメクチン、 クロフエンテジン、 シへキサチン、 ピリダベン、 フェンピロキシメート、 テブフェンビラド、 ピリミジフエ ン、 フエノチォカルプ、 ジエノクロル等。
植物生長調節剤:
ジベレリン類 (例えばジベレリン A3 、 ジベレリン A4、 ジベレリン A7 ) I AA、 N AA。
次に実施例を挙げて本発明を更に詳細に説明する。
実施例 1
N— {2—ブロモー 5— [5— (2—クロ口フエニル)― 1, 2, 4一ォキサジァゾ一ルー 3—ィル] ベンジル } 力ルバミン酸メチル (化合物番号 2— 6) の製造
N- { 2—プロモー 5— [5— (2—クロ口フエニル)— 1, 2, 4—ォキサジァゾ一ル— 3—ィル] ベンジルァミン 0. 80 g (2. 2mmo 1 ), ピリジン 0. 21 g (2.. 6mmo 1) をテトラヒドロフラン 10mlに溶解し、 0T:にてクロロ蟮酸メチル 0. 23 g (0. 24mmo 1 ) を加えた後、 室温で反応させた。 1時間後反応液を氷水中 にあけ、 酢酸ェチルエステルにて抽出した。得られた有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 残留物をシリカゲル力 ラムクロマトグラフィー (溶媒:へキサン一酢酸ェチルエステル =7 : 3) にて精製し て、 目的とする N— {2—ブロモ一5— [5—(2—クロ口フエ二ル)一 1, 2, 4—ォキ サジァゾ一ルー 3—ィル]ベンジル }力ルバミン酸メチル 0. 48 gを得た。収率 52% 参考例 1
N- (2—ブロモ一 5—シァノベンジル)フタルイミドの製造
フタルイミドカリウム 4. 6 g (25mmo 1) を N, N—ジメチルホルムアミド 5 0m 1に懸濁させた溶液に、 2—プロモー 5—シァノベンジルクロリ ド 4. 8 g (20 mmo 1) を室温にて加え 1晚反応させた。 反応液を氷水中にあけ、 酢酸ェチルエステ ルにて抽出した。 有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残留物をジェチルエーテルにて洗浄し目的とす る N—(2—ブロモ一 5—シァノベンジル)フタルイミド 4. 7 gを得た。 収率 66%
N—ヒドロキシー 4ーブロモー 3—(フタルイミドメチル)ベンズアミジンの製造
N— (2—ブロモ一 5—シァノベンジル)フタルイミド 4. 7 g (14mmo l)、 ヒド ロキシルァミン塩酸塩 4. 8 g (42mmo 1 ) を含むエタノール溶液 60 m 1に、 0 - 10でにて炭酸ナトリウム 2. 2 g (2 lmmo 1 ) を溶解した水溶液 1 Om 1を滴 下したのち、 室温にて 30分、 次いで 3時間還流した。 エタノールを減圧留去後、 反応 液に飽和食塩水 5 Omlを加え、 酢酸ェチルエステルにて抽出した。 有機層を飽和食塩 水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得ら れた残留物をジェチルエーテルにて洗浄し目的とする N—ヒドロキシ— 4—プロモー 3— (フタルイミドメチル)ベンズアミジン 3. 9gを得た。 収率 75%
N— (2—クロ口べンゾィルォキシ)一4—プロモ一 3 - (フタルイミドメチル)ベンズ アミジンの製造
N—ヒドロキシ一 4—ブロモ一3— (フタルイミドメチル)ベンズアミジン 1. 2g (3. 2mmo l)、 ピリジン 0. 30 g (3. 8mmo 1 ) をテトラヒドロフラン 15ml に溶解し、 Ot:にて 2—クロ口べンゾイルクロリド 0. 64g (3. 7mmo 1 ) を加 えた後、 室温で反応させた。 1時間後反応液を氷水中にあけ、 酢酸ェチルエステルにて 抽出した。 得られた有機層を飽和食塩水で洗净した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し、 目的とする粗 N—(2—クロ口べンゾィルォキシ)一 4ーブ ロモ一 3— (フタルイミドメチル)ベンズアミジン 1. 6 gを得た。
N— { 2—ブロモー 5— [5— (2—クロ口フエニル) - 1, 2, 4—ォキサジァゾ一ルー 3—ィル] ベンジルフタルイミドの製造
N- (2—クロ口べンゾィルォキシ)一4—ブロモ—3—(フタルイミドメチル)ベンズ アミジン 1. 6 gを、 N, N—ジメチルホルムアミド 10m 1に溶解し、 140 で1 時間反応させた。 反応液を氷水中にあけ、 酢酸ェチルエステルにて抽出した。 有機層を 飽和食塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し た。 得られた残留物をシリカゲルカラムクロマトグラフィー (溶媒:へキサン—酢酸ェ チルエステル =7 : 3) にて精製して、 目的とする N— { 2—プロモー 5— [5 - (2 —クロ口フエ二ル)— 1, 2, 4—ォキサジァゾ一ル— 3—ィル] ベンジルフ夕ルイミド 1. 1 gを得た。
N— { 2—ブロモ— 5— [5—(2—クロ口フエニル) -1, 2, 4—ォキサジァゾ一ル— 3—ィル] ベンジルァミンの製造
N- { 2—ブロモー 5— [5—(2—クロ口フエニル) -1, 2, 4—ォキサジァゾ一ルー 3—ィル] ベンジルフタルイミド 1. 1 gをクロ口ホルム 2 Omlに溶解し、 抱水ヒド ラジン 0. 3 gを含むメタノール溶液 1 Om 1を室温にて加えた。 4 で 2日間反応 後、 不溶物をろ別し、 クロ口ホルムを減圧留去した。 得られた残留物にクロ口ホルム 1 Omlを加え、再度不溶物をろ別後、クロ口ホルムを減圧留去し、 目的とする粗 N— {2 —ブロモー 5— [5—(2—クロ口フエニル)— 1, 2, 4—才キサジァゾ一ル— 3—ィ ル] ベンジルァミン 0. 8 gを得た。
実施例 2
2— {2—クロロー 5— [5— (2—クロ口ベンジル)一 1, 2, 4—ォキサジァゾ一ルー
3—ィル] フエ二ル} カルバジン酸メチル (化合物番号 2— 68) の製造
2 - {2—クロ口一 5— [N— (2—クロ口フエ二ルァセトキシ)アミジノ] フエ二ル} カルバジン酸メチル 0. 8 gを、 N, N—ジメチルホルムアミド 10m 1に溶解し、 1 50でで 1時間反応させた。 反応液を氷水中にあけ、 酢酸ェチルエステルにて抽出した。 有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減 圧留去した。 得られた残留物をシリカゲルカラムクロマトグラフィー (溶媒; へキサ ン:酢酸ェチルエステル =6 : 4) にて精製して、 目的とする 2— {2—クロ口— 5— [5— (2—クロ口ベンジル)— 1, 2, 4—ォキサジァゾ一ル一 3—ィル] フエ二ル}力 ルバジン酸メチル 0. 7 gを得た。 参考例 2
ヒドロキシアミジノ)フエニル] カルバジン酸メチルの製 Me
2— (2—クロ口一 5—シァノフエニル)カルバジン酸メチル 4. 0 g (18mmo 1)、 ヒドロキシルァミン塩酸塩 4. 9 g (7 lmmo 1 ) を含むエタノール溶液 8 Om 1に、 0— 10でにて炭酸ナトリウム 3. 8 g (36mmo 1 ) を溶解した水溶液 15m 1を 滴下したのち、 室温にて 30分、 次いで 2時間還流した。 エタノールを減圧留去後、 反 応液に飽和食塩水 5 Omlを加え、 酢酸ェチルエステルにて抽出した。有機層を飽和食 塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得 られた残留物をジェチルェ一テルにて洗浄し目的とする 2— [2—クロ口— 5— (N— ヒドロキシアミジノ)フエニル] カルバジン酸メチル 4. l gを得た。 収率 89%
2 - {2—クロロー 5— [N— (2—クロ口フエ二ルァセトキシ)アミジノ] フエ二ル} カルバジン酸メチルの製造
2一 [2—クロ口一 5 - (N—ヒドロキシアミジノ)フエニル] カルバジン酸メチル 1. 2 g (4. 6mmo l)、 ピリジン 0. 44g (5. 6mmo 1 ) をテ卜ラヒドロフラ ン 2 Omlに溶解し、 0でにて 2—クロ口フエニルァセチルクロリド 0. 97 g (5. lmmo 1) を加えた後、 室温で反応させた。 1時間後反応液を氷水中にあけ、 酢酸ェ チルエステルにて抽出した。 得られた有機層を飽和食塩水で洗浄した後、 硫酸マグネシ ゥムを加えて乾燥、 ろ別後、 溶媒を減圧留去し、 シリカゲルカラムクロマトグラフィー (溶媒; へキサン:酢酸ェチルエステル =4: 6)にて精製して、 目的とする 2— {2 —クロ口一 5— [N- (2—クロ口フエ二ルァセトキシ)アミジノ] フエ二ル} カルバジ ン酸メチル 1. 4gを得た。 収率 80% 実施例 3
2 - { 2—クロ口— 5 - [3— (2—クロ口ベンジル) - 1, 2, 4一ォキサジァゾール— 5 - ィル] フエ二ル} カルバジン酸メチル (化合物番号 3— 37) の製造
N— {'[4—クロ口一 3— (2—メトキシカルボニルヒドラジノ)フエニル] カルボニル ォキシ } _ 2—クロ口べンジルアミジン 0. 32 gを、 N, N—ジメチルホルムアミド 1 Omlに溶解し、 15 Οΐ:で 1時間反応させた。 反応液を氷水中にあけ、 酢酸ェチル エステルにて抽出した。 有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加えて 乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残留物をシリカゲルカラムクロマトグラ フィ一 (溶媒; へキサン:酢酸ェチルエステル =6 : 4) にて精製して、 目的とする 2 - {2—クロ口一 5— [3—(2—クロ口ベンジル)一 1, 2, 4—ォキサジァゾ一ルー 5—ィル] フエ二ル} カルバジン酸メチル 0. 15gを得た。 収率 48% 参考例 3
N— {[4—クロ口一 3— (2—メトキシカルポニルヒドラジノ)フエニル] カルポニル ォキシ } _ 2—クロ口べンジルアミジンの製造
N—ヒドロキシー 2—クロ口べンジルアミジン 0. 38 g (2. lmmo l)、 4—ク ロロ一 3—(2—メトキシカルポニルヒドラジノ)安息香酸 0. 50 g (2. Immo 1 )> をジクロロメタン 1 Omlに溶解し、 室温にて 4ージメチルァミノピリジン 0. 27 g (2. 2mmo l)、 1一(3—ジメチルァミノプロピル)一 3—ェチルカルポジイミド 塩酸塩 0. 43 g (2. 2mmo 1) を加えた後、 室温で 1晚反応させた。 反応液を氷 水中にあけ、 酢酸ェチルエステルにて抽出した。 得られた有機層を飽和食塩水で洗浄し た後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し、 シリカゲルカラム クロマトグラフィー (溶媒; へキサン:酢酸ェチルエステル =4 : 6) にて精製して、 目的とする N— {[4—クロ口一 3— (2—メ卜キシカルボニルヒドラジノ)フエニル] カルボ二ルォキシ} — 2—クロ口べンジルアミジン 0. 32 gを得た。 収率 38% 実施例 4
2— {2—クロ口— 5— [4— (4—フルォロベンジル)— 2—チアゾリル] フエ二ル} カルバジン酸メチル (化合物番号 4一 88) の製造 zMe
2 - {2—クロ口一 5— [3— (4—フルオロフェニル) 一 2—プロパノニルチオイミ ドイル] フエ二ル} カルバジン酸メチル 0. 80 gを、 トルエン 1 Om 1中で 2時間反 応させた。 反応液を氷水中にあけ、 酢酸ェチルエステルにて抽出した。 有機層を飽和食 塩水で洗浄した後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得 られた残留物をシリカゲルカラムクロマトグラフィー (溶媒; へキサン:酢酸ェチル エステル =7 : 3) にて精製して、 目的とする 2— {2—クロロー 5— [4一(4ーフ ルォロベンジル)一 2—チアゾリル] フエ二ル} カルバジン酸メチル 0. 65 gを得た。 収率 86 % 参考例 4
2 - (2—クロ口— 5—チォカルバモイルフエ二ル)カルバジン酸メチルの製造 Me
ピリジン 20m 1中の 2— (2—クロ口一 5—シァノフエニル)カルバジン酸メチル 6 g (27mmo 1 ) に室温にてトリエチルァミン 3. 2 g (32mmo 1 ) を加えた後、 30でで硫化水素ガスを導入した。 約 3時間後、 窒素ガスで硫化水素ガスを置換後、 反 応液を氷水中にあけ、 得られた結晶をろ別後、 水洗、 n—へキサン洗することにより、 2— (2—クロロー 5 _チォカルバモイルフエニル)カルバジン酸メチル 6. 7 gを得た。 収率 97 %
2— {2—クロ口一 5— [3— (4—フルオロフェニル) 一 2—プロパノニルチオイミ ドイル] フエ二ル} カルバジン酸メチルの製造
2— (2—クロ口— 5—チォカルバモイルフエニル)カルバジン酸メチル 1. 4g (5. 4mmo 1 ) をテトヒドロフラン 15mlに溶解し、 0 にてピリジン 0. 64 g (8. lmmo l)、 1—ブロモ一 3—(4—フルオロフェニル)アセトン 1. 5 g (6. 5 m mo 1) を加えた後、 室温で 1晚反応させた。 反応液を氷水中にあけ、 酢酸ェチルエス テルにて抽出した。得られた有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加 えて乾燥、 ろ別後、 溶媒を減圧留去し、 シリカゲルカラムクロマトグラフィー (溶媒; へキサン:酢酸ェチルエステル = 1 : 1) にて精製して、 目的とする 2— { 2—クロ口 一 5— [3— (4—フルオロフェニル) —2—プロパノニルチオイミドイル] フエ二ル} カルバジン酸メチル 1. 5 gを得た。 収率 68% 実施例 5
2 - {2—クロ口— 5— [4— (2—トリフルォロメチルフエニル)一 2—チアゾリル] フエ二ル} カルバジン酸メチル (化合物番号 4一 68) の製造
2— (2—クロ口— 5—チォカルバモイルフエ二ル)カルバジン酸メチル 0. 50 g (1.
9mmo 1) をメタノール 10mlに溶解し、 室温にて 2—トリフルォロメチルフエナ シルブロミド 0. 63 g (2. 4mmo 1 ) を加えた後、 2時間還流した。 反応液を氷 水中にあけ、 酢酸ェチルエステルにて抽出した。 得られた有機層を飽和食塩水で洗浄し た後、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し、 シリカゲルカラム クロマトグラフィー (溶媒; へキサン:酢酸ェチルエステル =6 : 4) にて精製して、 目的とする 2— {2—クロ口一 5— [4— (2—トリフルォロメチルフエ二ル)一 2—チ ァゾリル] フエ二ル} カルバジン酸メチル 0. 53 gを得た。 収率 65%
実施例 6
2 - {2—クロ口一 5— [4— (2—クロ口フエ二ル)一 2—チアゾリル] フエ二ル} ジ ァゼンカルボン酸メチル (化合物番号 4— 109) の製造
2— {2—クロ口一 5— [4— (2—クロ口フエ二ル)一 2—チアゾリル] フエ二ル} 力 ルバジン酸メチル 0. 73 g (l. 9mmo 1 ) をクロ口ホルム 10m 1に溶解し、 室 温にてピリジン 0. 18 g (2. 3mmo l)、 N—クロロサクシンイミド 0. 27 g (2.、0mmo 1) を加えた後、 2時間攪拌した。 反応液を氷水中にあけ、 酢酸ェチル エステルにて抽出した。 得られた有機層を希塩酸、 ついで飽和食塩水で洗浄した後、 硫 酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残留物をシリカ ゲルカラムクロマトグラフィー (溶媒; へキサン:酢酸ェチルエステル = 5 : 1) に て精製して、 目的とする 2— {2—クロロー 5— [4— (2—クロ口フエニル)一 2—チ ァゾリル] フエ二ル} ジァゼンカルボン酸メチル 0. 60 gを得た。 収率 82% 実施例 7
2— {2—クロ口一 5— [3— (4—メチルフエニル)一 1, 2, 4—チアジアゾ一ル— 5—ィル] フエ二ル} カルバジン酸メチル (化合物番号 3— 90) の製造
2— {2—クロ口一 5— [N— (α—ジメチルァミノ一 4一メチルベンジリデン)チォカ ルバモイル] フエ二ル} カルバジン酸メチル 0. 35 g (0. 9mmo l)、 ピリジン 0. 14 g (1. 8mmo 1 ) をメチルアルコール 7 m 1に溶解し、 室温にて、 メチル アルコール 5m 1に溶解したヒドロキシルァミン— O—スルホン酸 0. l l g (l. 0 mmo 1) を加えた後、 1時間攪拌した。 反応液を希塩酸中にあけ、 酢酸ェチルエステ ルにて抽出後、 飽和食塩水で洗浄、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減 圧留去した。 得られた残留物をシリカゲルカラムクロマトグラフィー (溶媒; ベンゼ ン:酢酸ェチルエステル =4: 1) にて精製して、 目的とする 2 - { 2—クロ口— 5— [3— (4—メチルフエ二ル)— 1, 2, 4—チアジアゾ―ル—5—ィル] フエ二ル} 力 ルバジン酸メチル 0. 24 gを得た。 収率 75% 参考例 5
2 - {2—クロ口一 5— [N— (α—ジメチルァミノ一 4一メチルベンジリデン)チォカ ルバモイル] フエ二ル} カルバジン酸メチルの製造
2—(2—クロロー 5—チォカルバモイルフエニル)カルバジン酸メチル 0. 5g (1. 9 mmo 1) に室温にて、 N, N—ジメチルー 4一メチルベンズアミドジメチルァセタ ール 1. 6 g (7. 7 mmo 1 ) を加え室温にて 1時間、 60でで 4時間攪拌した。 室 温に冷却後、 反応混合物をシリカゲルカラムクロマトグラフィー (溶媒; ベンゼン: 酢酸ェチルエステル =3 : 7) にて精製して、 目的とする 2— {2—クロ口— 5— [N - (α—ジメチルァミノ— 4—メチルベンジリデン)チォカルバモイル] フエ二ル}カル バジン酸メチル 0. 7 gを得た。 収率 90% 実施例 8
2 - {2—クロ口一 5— [4— (2—クロ口フエ二ル)一 5—シァノ一 2—チアゾリル] フエ二ル} カルバジン酸メチル (化合物番号 4一 352) の製造
2— {2—クロ口一 5— [N- (α—ジメチルァミノ一 2—クロ口べンジリデン)チォカ ルバモイル] フエ二ル} カルバジン酸メチル 0. 4g (0. 9mmo l)、 プロモアセ 卜二トリル 0. 14g (l. 2mmo 1 ) をアセトン 20m 1に溶解し、 室温にて 1晚 反応させた。 反応液を減圧濃縮後、 酢酸 1 Omlを加え、 1時間還流した。 反応液を希 塩酸中にあけ、 酢酸ェチルエステルにて抽出後、 飽和食塩水で洗浄、 硫酸マグネシウム を加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残留物をシリカゲルカラムクロ マトグラフィ一 (溶媒; ベンゼン:酢酸ェチルエステル =7 : 3) にて精製して、 目 的とする 2— {2—クロ口一 5— [4— (2—クロ口フエ二ル)一 5—シァノ一2—チア ゾリル] フエ二ル} カルバジン酸メチル 0. 15 gを得た。 収率 39% 実施例 9
2— {2—クロ口一 5— [(4 S) -4, 5—ジヒドロ一 4—ベンジルォキサゾリン一 2 一ィル] フエ二ル} カルバジン酸メチル (化合物番号 5— 9) の製造 ,Me
2 - {2—クロ口一 5— [(1 S) —N— (2—メタンスルホニルォキシ)一 1一べンジ ルェチル] 力ルバモイルフエ二ル} カルバジン酸メチル 0. 65g (1. 4mmo l)、 トリ工チルァミン 0. 16 g (l. 6mmo 1 ) をジォキサン 1 Om 1に溶解し、 1. 5時間還流した。 反応液を希塩酸中にあけ、 酢酸ェチルエステルにて抽出後、 飽和食塩 水で洗浄、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残 留物をシリカゲルカラムクロマトグラフィー (溶媒; n—へキサン:酢酸ェチルエス テル =1 : 1) にて精製して、 目的とする 2— {2—クロ口— 5— [(4 S) -4, 5- ジヒドロ— 4—ベンジルォキサゾリン— 2—ィル] フエ二ル}カルバジン酸メチル 0. 42 gを得た。 収率 82 % 参考例 6
2 - {2—クロ口一 5— [(1 S) —N— (2—ヒドロキシ)— 1一ベンジルェチル] 力 ルバモイルフエ二ル} カルバジン酸メチルの製造
L—フエ二ルァラニノ一ル 0. 69g (4. 6mmo l)、 トリェチルァミン (5. 4 mmo 1) をテトラヒドロフラン 10mlに溶解し、 0 にてテトラヒドロフラン 5 m
1に溶解した 2— (2—クロロー 5—クロロカルポニルフエニル)カルバジン酸メチル 1. 2 g (4. 6mmo 1) を滴下した。 室温にて 2時間反応後、 反応液を希塩酸中に あけ、 酢酸ェチルエステルにて抽出後、 飽和食塩水で洗浄、 硫酸マグネシウムを加えて 乾燥、 ろ別後、 溶媒を減圧留去した。 得られた残留物をシリカゲルカラムクロマトダラ フィー (溶媒; n—へキサン:酢酸ェチルエステル = 1 : 9) にて精製して、 目的とす る 2— {2—クロ口一 5— [(1 S) —N— (2—ヒドロキシ)一 1一ベンジルェチル] 力ルバモイルフエ二ル} カルバジン酸メチル 1. l gを得た。 収率 65%
2 - {2—クロ口一 5— [(1 S) —N— (2—メタンスルホニルォキシ)一 1—ベンジ ルェチル] 力ルバモイルフエ二ル} カルバジン酸メチルの製造 zMe
H 0,M
2 - {2—クロ口一 5— [(1 S) — N— (2—ヒドロキシ)一 1—ベンジルェチル] 力 ルバモイルフエ二ル} カルバジン酸メチル 0. 5 g (1. 3mmo 1 ) をテトラヒドロ フラン 10mlに溶解し、 0でにてトリエチルァミン 0. 16 g (1. 6mmo l)、 次いでメタンスルホニルクロリド 0. 16 g (1. 4mmo 1 ) を滴下した。 室温にて 1時間反応後、 反応液を希塩酸中にあけ、 酢酸ェチルエステルにて抽出後、 飽和食塩水 で洗浄、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し、 目的とする 2— { 2—クロ口一 5— [(1 S) —N—(2—メタンスルホニルォキシ)一 1—ベンジルェ チル] 力ルバモイルフエ二ル} カルバジン酸メチル 0. 6 gを得た。 実施例 10
2 - {2—クロ口一 5— [(4 S) -4, 5—ジヒドロー 4—フエ二ルチアゾリンー 2— ィル] フエ二ル} カルバジン酸メチル (化合物番号 5— 2) のの製造 HCO
zMe
2 - {2—クロ口一 5— [(1 S) —N— (2—ヒドロキシ)一 1—フエニルェチル] 力 ルバモイルフエ二ル} カルバジン酸メチル 0. 7 g (l. 9mmo 1 ) をベンゼン 10 mlに溶解し、 ローソン試薬 1. 2 g (3. Ommo 1 ) を加えた後、 1時間還流した。 反応液を氷水中にあけ、 酢酸ェチルエステルにて抽出後、 10%炭酸ナトリウム水溶液、
次いで飽和食塩水で洗浄、 硫酸マグネシウムを加えて乾燥、 ろ別後、 溶媒を減圧留去し た。 得られた残留物をシリカゲルカラムクロマトグラフィー (溶媒; n—へキサン: 酢酸ェチルエステル =1 : 1) にて精製して、 目的とする 2— {2—クロ口— 5— [(4 S) -4, 5—ジヒドロー 4—フエ二ルチアゾリン— 2—ィル] フエ二ル} 力ルバジン 酸メチル 0. 33 gを得た。 収率 66%
実施例 1 1
2 - { 2—クロ口— 5— [5— (4—メ卜キシ一フエ二ル)—ォキサゾ一ル— 2—ィル] フエ二ル} カルバジン酸メチル (化合物番号 4一 398) の製造
2—クロ口一 5— [5— (4—メトキシフエ二ル)一 2—ォキサゾリル] ァニリン 1. 0 g (3. 6mmo 1 ) を THF 1 m 1に溶解させた後、 濃塩酸 4m 1を加えた。 あらかじめ 亜硝酸ナトリウム 0. 28 g (4. Ommo 1 ) を水 0. 5 m 1に溶解させた溶液を— 1 0°Cにて滴下した。 30分後、 反応液に塩化スズ 1. 5 g (7. 2 mm o 1 ) を濃塩酸 1. 5m lに溶解させた溶液を同じく一 10°Cにて加えた後、 30分反応させた。 析出物をろ 別後、 n—へキサンにて洗浄し、 粗生成物を THF 1 Om 1に溶解した。 — 1 0でにてク ロロ蟻酸メチル 0. 5 g (5. 3mmo l)、 卜リエチルァミン 1. l g (10. 9mmo 1 ) を加えた後、 室温で反応させた。 30分後、 反応液を氷水中にあけ、 酢酸ェチルエス テルにて抽出した。 得られた有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムを加え て乾燥、 ろ別後、 溶媒を減圧留去した。 残留物をシリカゲルカラムクロマトグラフィー (溶 媒:へキサン一酢酸ェチルエステル =4 : 1) にて精製して目的とする 2— { 2—クロ口 — 5— [5— (4—メトキシ—フエ二ル)—ォキサゾ一ル— 2—ィル] フエ二ル} 力ルバ ジン酸メチル 0. 4 gを得た。 収率 35% 参考例 7
2—クロロー 5— [5— (4—メトキシフエ二ル)— 2—ォキサゾリル] ァニリンの製造
鉄粉 5. 6 gと水 8 Om 1を 60でにて攪拌し、 酢酸 4m 1を加えた。 あらかじめ 2— (4—クロ口— 3—ニトロ一フエニル) 一 5— (4—メトキシ一フエニル) ーォキサゾ —ル 7. 5 g (22. 7mmo 1 ) をアセトン 4 Om 1に溶解させた溶液を 60でにて 滴下した。 3時間後、 反応液を放冷しセライトろ過を行い不溶物を除いた。 ろ液を酢酸ェ チルエステルにて抽出し、 得られた有機層を飽和食塩水で洗浄した後、 硫酸マグネシウム
を加えて乾燥、 ろ別後、 溶媒を減圧留去した。 残留物をシリカゲルカラムクロマトグラフ ィ一 (溶媒:へキサン—酢酸ェチルエステル =4 : 1) にて精製して目的とする 2—クロ ロー 5— [5— (4—メトキシフエ二ル)— 2—才キサゾリル] ァニリン 4. 5 gを得た。 収率 66 % 参考例 8
2— (4—クロロー 3—ニトロ一フエニル) 一 5— (4—メトキシ一フエニル) ーォキ サゾールの製造
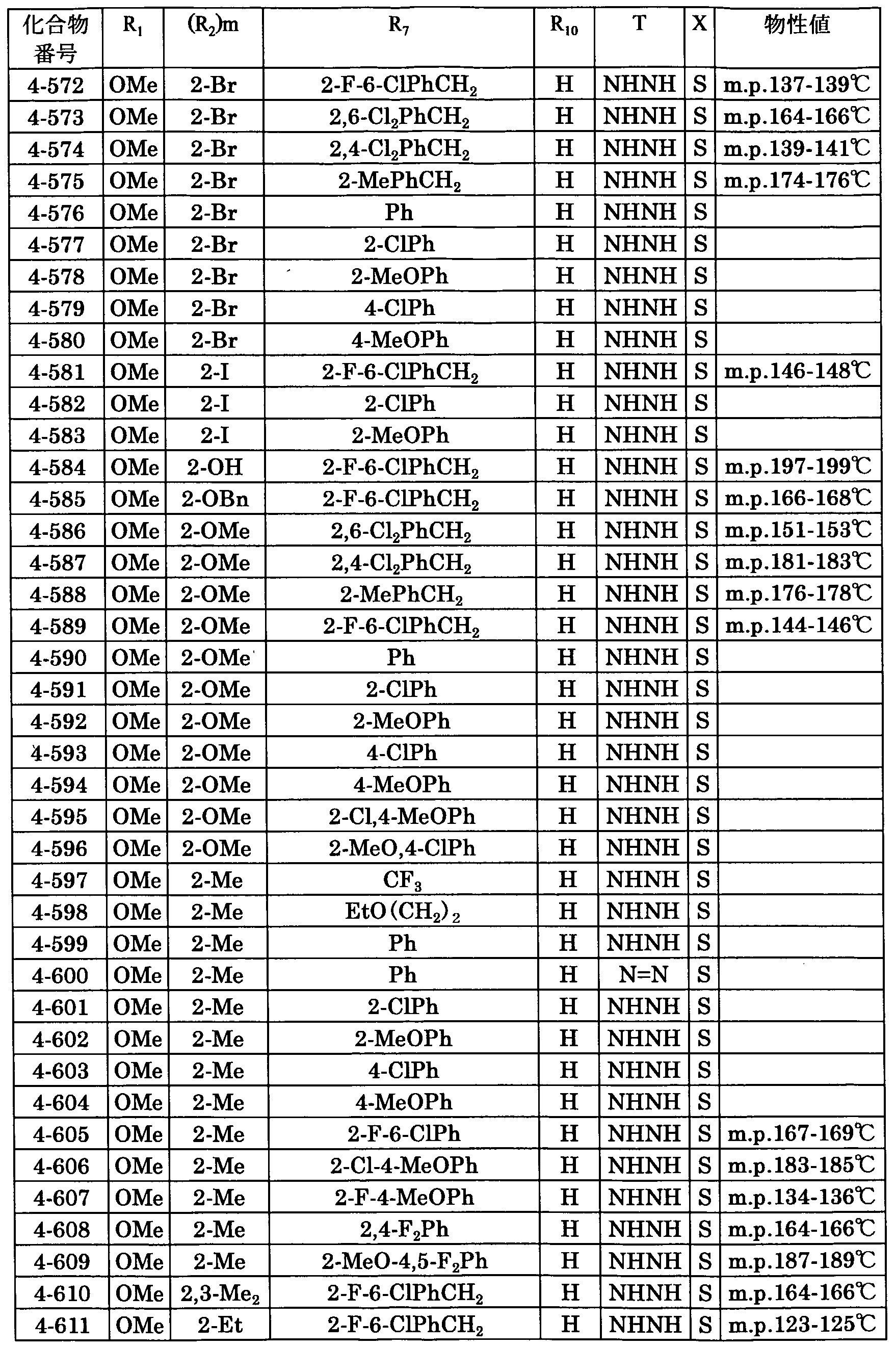
4—クロ口一 3—ニトロ一ベンゾイルク口ライド 5. 0 g (22. 7mmo 1 ) をべンゼ ン 100m lに溶解し、 2—アジド一 1— (4—メトキシフエ二ル) 一エタノン 4. 3 g (22. 7 mm o 1 ) , トリフエニルホスフィン 5. 9 g (22. 7mmo 1 ) を室温にて 加えた。 60でにて 1時間反応させた後、 反応溶媒を留去し残留物をシリカゲルカラムク 口マトグラフィ一 (溶媒:へキサン—酢酸ェチルエステル =4 : 1) にて精製して目的と する 2— (4—クロ口一 3—ニトロ一フエニル) 一 5— (4—メ卜キシ一フエニル) 一 ォキサゾ一ル 7. 5 gを得た。 収率 99 % 上記実施例を含め本発明化合物の具体例を第 1表〜第 4表に記載する。
ただし、 NHNMe *は *側の窒素原子がカルポニル炭素と結合する。
なお、 表中の略記号は以下の意味を示す。
Me ;メチル、 E t ;ェチル、 n P r ; ノルマルプロピル、 c P r ;シクロプロピル、 i P r ;イソプロピル、 i Bu ;イソブチル、 c P e n;シクロペンチル、 cHe x ; シクロへキシル、 Ph ; フエニル、 Bn;ベンジル、 Py; ピリジン、 P i v; ビバ ロイル、 Boc ;夕ーシャリ一ブトキシカルボニル、
JO請 Zdf/ェ:) d 6蘭 SOOZ OAV
化合物 R
7 T X 物性値 番号
2- 1 OMe H Ph NHNH O
2-2 OMe H 2-ClPh NHNH O
2-3 OMe H 2-ClPhCH2 NHNH O m.p.l38- 140°C
2-4 OMe H 2-ClPh CH2NH O m.p.H2- 114°C
2-5 OMe H 2-ClPhCH2 CH2NH O m.p.l23- 124°C
2-6 OMe 2-Br 2-ClPh CH2NH O m.p.l33- 135°C
2-7 OMe 2-Br 2-ClPhCH2 CH2NH O m.p.92-95°C
2-8 OMe 2-C1 2-ClPh CH2NH O
2-9 OMe 2-C1 2-ClPhCH2 CH2NH O
2- 10 OMe 2-F 2-ClPh CH2NH O
2-11 OMe 2-F 2-ClPhCH2 CH2NH O
2-12 OMe 2-Br 2-ClPhCH2 NHNH O m.p.l21-123°C
2- 13 OMe 2 -Me 2-ClPh NHNH O
2-14 OMe 2-Me 2-ClPhCH2 NHNH O m.p.l07- 110°C
2- 15 OMe 2-OMe 2-ClPh NHNH O
2- 16 OMe 2-OMe 2-ClPhCH2 NHNH O m.p.H3-115°C
2-17 OMe 2,4-Cl2-6-Me 2-ClPh NHNH O
2-18 OMe 2,4-Cl2-6-Me 2-ClPhCH2 NHNH O amorphous
2- 19 OMe 2,6-Cl2-4-Me 2-ClPh NHNH O
2-20 OMe 2,6-Cl2-4-Me 2-ClPhCH2 NHNH O amorphous
2-21 OMe 2,4,6-Clj 2-ClPh NHNH O
2-22 OMe 2,4,6-Clj 2-ClPhCH2 NHNH O amorphous
2-23 OMe 2,4,6-Me3 Ph NHNH O
2-24 OMe 2,4,6-Me3 PhCH2 NHNH o
2-25 OMe 2-C1 nC5H„ NHNH o m.p.85-87°C
2-26 OMe 2-C1 nC6H13 NHNH o m.p.53-56°C
2-27 OMe 2-C1 nC8H17 NHNH o m.p.53-55°C
2-28 OMe 2-C1 nCnH23 NHNH o m.p.60-62°C
2-29 OMe 2-C1 c-Pr NHNH 0 m.p.l42- 144°C
2-30 OMe 2-C1 c-PrCH2 NHNH o
2-31 OMe 2-C1 c-Pen NHNH o
2-32 OMe 2-C1 c-PenCH2 NHNH o
2-33 OMe 2-C1 c-Hex NHNH o m.p.l03- 104°C
2-34 OMe 2-C1 c-HexCH2 NHNH o η ·31.5472
2-35 OEt 2-C1 Ph NHNH o
2-36 OEt 2-C1 PhCH2 NHNH o
表 2の続き
化合物 R, R7 T X 物性値 番号
2-37 OiPr 2-C1 Ph NHNH O
2-38 OiPr 2-C1 PhCH2 NHNH O
2-39 OMe 2-C1 CC13 NHNH O nD 2391.5572
2-40 OMe 2-C1 CF3 NHNH O m.p.l38- 140°C
2-41 OMe 2-C1 2-ClPhNH NHNH O m.p.l87- 190°C
2-42 OMe 2-C1 3-ClPhNH NHNH O
2-43 OMe 2-C1 4-ClPhNH NHNH O m.p.200°C up
2-44 OMe 2-C1 2-ClPhCO NHNH O
2-45 OMe 2-C1 3-ClPhCO NHNH O
2-46 OMe 2-C1 4-ClPhCO NHNH O
2-47 OMe 2-C1 2-Cl-3-Py NHNH O m.p.l74-177°C
2-48 OMe 2-C1 2-Cl-4-Py NHNH O
2-49 OMe 2-C1 2-Cl-5-Py NHNH O m.p.68-70°C
2-50 OMe 2-C1 6-Me-2-Py NHNH O
2-51 OMe 2-C1 2-Me-5-Py NHNH O
2-52 OMe 2-C1 2-Me-3-Py NHNH O
2-53 OMe 2-C1 2-PyCH2 NHNH O m.p.l49-152°C
2-54 OMe 2-C1 3-PyCH2 NHNH O m.p.l60- 162°C
2-55 OMe 2-C1 4-PyCH2 NHNH O m.p.l75- 177°C
2-56 OMe 2-C1 6-Me-2-PyCH2 NHNH O m.p.l77-180°C
2-57 OMe 2-C1 Ph NHNH O m.p.l78-180°C
2-58 OMe 2-C1 2-ClPh NHNH O m.p.l44- 146°C
2-59 OMe 2-C1 3-ClPh NHNH O m.p.l78- 180°C
2-60 OMe 2-C1 4-ClPh NHNH O m.p.l85-186°C
2-61 OMe 2-C1 2-MePh NHNH O
2-62 OMe 2-C1 3-MePh NHNH O
2-63 OMe 2-C1 4-MePh NHNH o
2-64 OMe 2-C1 2,4- e2Ph NHNH o
2-65 OMe 2-C1 2,5-Me2Ph NHNH o m.p.l54-157°C
2-66 OMe 2-C1 3,5-Me2Ph NHNH o
2-67 OMe 2-C1 PhCH2 NHNH o m.p.l03- 105°C
2-68 OMe 2-C1 2-ClPhCH2 NHNH o nD 22 31.5892
2-69 OMe 2-C1 3-ClPhCH2 NHNH o m.p.H0-112°C
2-70 OMe 2-C1 4-ClPhCH2 NHNH o m.p.l30-132°C
2-71 OMe 2-C1 2-MePhCH2 NHNH o m.p.99-102°C
2-72 OMe 2-C1 3-MePhCH2 NHNH o
2-73 OMe 2-C1 4-MePhCH2 ΝΗΝΉ o
2-74 OMe 2-C1 2-MeOPhCH2 NHNH o m.p.H8-120°C
2-75 OMe 2-C1 3-MeOPhCH2 NHNH o
2-76 OMe 2- CI 4-MeOPhCH2 NHNH o m.p.l01- 103°C
2-77 OMe 2-C1 2-CF3PhCH2 NHNH o m.p.H8- 120°C
の続き
化合物番 R. R7 T X 物性値 号
2-78 OMe 2-C1 3-CF3PhCH2 NHNH O
2-79 OMe 2-C1 4-CF3PhCH2 NHNH O
2-80 OMe 2-C1 2-PhOPhCH2 NHNH O
2-81 OMe 2-C1 3-PhOPhCH2 NHNH O m.p.H0-113°C
2-82 OMe 2-C1 4-PhOPhCH2 NHNH O
2-83 OMe 2-C1 2-PhCH2OPhCH2 NHNH O amorphous
2-84 OMe 2-C1 3-PhCH2OPhCH2 NHNH O
2-85 OMe 2-C1 4-PhCH2OPhCH2 NHNH O
2-86 OMe 2-C1 2,6-Cl2PhCH2 NHNH O m.p.l63-166°C
2-87 OMe 2-C1 2,4-Cl2PhCH2 NHNH O
2-88 OMe 2-C1 2,6-F2PhCH2 ΝΗΝΉ O
2-89 OMe 2-C1 2-Cl-6-F-PhCH2 NHNH O m.p.l20- 122°C
2-90 OMe 2-C1 2-ClPhCH2 N=N O
2-91 OMe 2-C1 3-ClPhCH2 N=N O
2-92 OMe 2- CI 4-ClPhCH2 N=N O
2-93 OMe 2-C1 2-ClPhCH2 NHNMe O
2-94 OMe 2-C1 3-ClPhCH2 NHNMe O
2 - 95 OMe 2-C1 4-ClPhCH2 NHNMe O
2-96 OiPr 2-C1 2-ClPhCH2 NHNH O
2-97 OiPr 2-C1 3-ClPhCH2 NHNH O
2-98 OiPr 2-C1 4-ClPhCH2 NHNH o
2-99 Me 2-C1 2-ClPhCH2 NHNH o
2- 100 Me 2-C1 3-ClPhCH2 NHNH o
2-101 Me 2-C1 4-ClPhCH2 NHNH o
2- 102 OMe 2-C1 2-ClPhCH2 NHNH s
2-103 OMe 2-C1 3-ClPhCH2 NHNH s
2-104 OMe 2-C1 4-ClPhCH2 NHNH s
2- 105 OMe 2-C1 PhCH2 NHNH s
2-106 OMe 2-C1 PhCH2 N=N s
2- 107 OMe 2-C1 2-ClPhCH2 N=N s
2- 108 OMe 2-C1 2-F-4-MeOPh NHNH o
2- 109 OMe 2-C1 2-F-4-MeOPh N=N o
2- 110 OMe 2-C1 2-F-4-iPrOPh NHNH o
2- 111 OEt 2-C1 2-F-4-MeOPh NHNH o
2-112 OMe 2-C1 3-F-4-MeOPh NHNH o
2- 113 OMe 2-C1 4-F-2-MeOPh NHNH o
2- 114 OMe 2- CI 4-F-3-MeOPh NHNH o
2-115 OMe 2-C1 2-Me-4-MeOPh NHNH o
2- 116 OMe 2-C1 3-Me-4-MeOPh NHNH o
2-117 OMe 2-C1 2-Cl-3-MeOPhCH2 NHNH o
2- 118 OMe 2-C1 2-Cl-4-MeOPhCH
2 NHNH o
の続き
化合物番 R, (igm R7 T X 物性値 号
2-160 OMe 2-C1 4 - Cl-2- MeOPh NHNH S
2-161 OMe 2-C1 4-Cl-2-MeOPh N=N S
2-162 OMe 2-C1 4- CI- 3 -MeOPh NHNH s
2-163 OMe 2-C1 4-Cl-3-MeOPh N=N s
2-164 OMe 2-Cl 2,3-(MeO)2Ph NHNH s
2-165 OMe 2-C1 2,4-(MeO)2Ph NHNH s
2-166 OMe 2-Cl 2,5-(MeO)2Ph NHNH s
2-167 OMe 2-Cl 2,6-(MeO)2Ph NHNH s
2-168 OMe 2-Cl 3,4-(MeO)2Ph NHNH s
2-169 OMe 2-Cl 3,5-(MeO)2Ph NHNH s
2-170 OMe 2-Cl 2,3,4-(MeO)3Ph NHNH s
2-171 OMe 2-Cl 2,3,5 -(MeO)3Ph NHNH s
2-172 OMe 2-Cl 2,4,6-(MeO)3Ph NHNH s
2-173 OMe 2-Cl 2,6-F2-4-MeOPh NHNH s
2-174 OMe 2-Cl 2,3-F2-4-MeOPh NHNH s
2-175 OMe 2-Cl 2,4-F2-6-MeOPh NHNH s
2-176 OMe 2-Cl 2,5-F2 - 4 - MeOPh NHNH s
2-177 OMe 2-Cl 3,4-F2-2-MeOPh NHNH s
2-178 OMe 2-Cl 2,5-F2-4-MeOPh NHNH s
2-179 OMe 2-Cl 3,5-F2-4-MeOPh NHNH s
2-180 OMe 2-Cl 2,4,6-F3Ph NHNH s
表 3
化合物 R. (igm R
7 T X 物性値 番号
3- 1 OMe H Ph NHNH O
3-2 OMe H 2-ClPh NHNH O
3-3 OMe H 2-ClPhCH2 NHNH O
3-4 OMe H 2-ClPh CH2NH O
3-5 OMe H 2-ClPhCH2 CH2NH O
3-6 OMe 2-Br 2-ClPh CH2NH O
3-7 OMe 2-Br 2-ClPhCH2 CH2NH O
3-8 OMe 2-C1 2-ClPh CH2NH O
3-9 OMe 2-C1 2-ClPhCH2 CH2NH O
3- 10 OMe 2-F 2-ClPh CH2NH O
3-11 OMe 2-F 2-ClPhCH2 CH2NH O
3- 12 OMe 2-Br 2-ClPhCH2 NHNH O
3- 13 OMe 2-Me 2-ClPh NHNH O
3- 14 OMe 2-Me 2-ClPhCH2 NHNH O
3- 15 OMe 2-OMe 2-ClPh NHNH O
3- 16 OMe 2-OMe 2-ClPhCH2 NHNH O
3- 17 OMe 2,4-Cl2-6-Me 2-ClPh NHNH O
3- 18 OMe 2,4-Cl2-6-Me 2-ClPhCH2 NHNH O
3-19 OMe 2,6- Cl2-4- Me 2-ClPh NHNH O
3-20 OMe 2,6-Cl2-4-Me 2-ClPhCH2 NHNH O
3-21 OMe 2,4,6-Cl3 2-ClPh NHNH O
3-22 OMe 2,4,6-Clj 2-ClPhCH2 NHNH O
3-23 OMe 2,4,6-Me3 Ph NHNH O
3-24 OMe 2,4,6-Me3 PhCH2 NHNH o
3-25 OEt 2-C1 Ph NHNH o
3-26 OEt 2-C1 PhCH2 NHNH o
3-27 OiPr 2-C1 Ph NHNH o
3-28 OiPr 2-C1 PhCH2 NHNH o
3-29 OMe 2-C1 Ph NHNH o
3-30 OMe 2-C1 2-ClPh NHNH o
3-31 OMe 2-Cl 3-ClPh NHNH o
3-32 OMe 2-C1 4-ClPh NHNH o
3-33 OMe 2-Cl 2- ePh NHNH o
3-34 OMe 2-Cl 3-MePh NHNH o
3-35 OMe 2-Cl 4-MePh NHNH o
3-36 OMe 2-Cl PhCH2 NHNH o
の続き
化合物 R. (R i R7 T X 物性値 番号
3-37 OMe 2-C1 2-ClPhCH2 NHNH O m.p.l34- 137°C
3-38 OMe 2-C1 3-ClPhCH2 NHNH O
3-39 OMe 2-C1 4-ClPhCH2 NHNH O
3-40 OMe 2-C1 2-MePhCH2 NHNH O
3-41 OMe 2-C1 3-MePhCH2 NHNH O
3-42 OMe 2-C1 4-MePhCH2 NHNH O
3-43 OMe 2-C1 2-MeOPhCH2 NHNH O
3-44 OMe 2-C1 3-MeOPhCH2 NHNH O
3-45 OMe 2-C1 4-MeOPhCH2 NHNH O
3-46 OMe 2-C1 2-CF3PhCH2 NHNH O
3-47 OMe 2-C1 3-CF3PhCH2 NHNH O
3-48 OMe 2-C1 4-CF3PhCH2 NHNH O
3-49 OMe 2-C1 2,6-Cl2PhCH2 NHNH O
3-50 OMe 2-C1 2,4-Cl2PhCH2 NHNH O
3-51 OMe 2-C1 2,6-F2PhCH2 NHNH O
3-52 OMe 2-C1 2-Cl-6-F-PhCH2 NHNH O
3-53 OMe 2-C1 2-ClPhCH2 N=N O
3-54 OMe 2-C1 3-ClPhCH2 N=N O
3-55 OMe 2-C1 4-ClPhCH2 N=N O
3-56 OMe 2-C1 2-ClPhCH2 NHNMe O
3-57 OMe 2-C1 3-ClPhCH2 HNMe O
3-58 OMe 2-C1 4-ClPhCH2 NHNMe o
3-59 OiPr 2-C1 2-ClPhCH2 NHNH o
3-60 OiPr 2-C1 3-ClPhCH2 NHNH o
3-61 OiPr 2-C1 4-ClPhCH2 NHNH o
3-62 Me 2-C1 2-ClPhCH2 NHNH o
3-63 Me 2-C1 3-ClPhCH2 NHNH o
3-64 Me 2-C1 4-ClPhCH2 NHNH o
3-65 OMe 2-C1 2-ClPhCH2 NHNH s m.p.l48- 152°C
3-66 OMe 2-C1 3-ClPhCH2 NHNH s
3-67 OMe 2-C1 4-ClPhCH2 NHNH s
3-68 OMe 2-C1 PhCH2 NHNH s m.p.l65-168°C
3-69 OMe 2-C1 PhCH2 N=N s
3-70 OMe 2-C1 2-ClPhCH2 N=N s nD 22 81.6202
3-71 OMe 2-C1 2-F-4-MeOPh NHNH o m.p.l84-186°C
3-72 OMe 2-C1 2-F-4-MeOPh N=N 0
3-73 OMe 2-C1 2-F-4-iPrOPh NHNH o
3-74 OEt 2-C1 2-F-4-MeOPh NHNH o
3-75 OMe 2-C1 3.p-4-MeOPh NHNH o
3-76 OMe 2-C1 4-F-2-MeOPh NHNH 0
3-77 OMe 2-C1 4-F-3-MeOPh NHNH o
vu Oさ oifcld S6ls0AV
の続き
化合物 Ri (R2)m R7 T X 物性値 番号
3-119 OMe 2-C1 2-Cl-4-MeOPh NHNH S
3-120 OMe 2-C1 2-Cl-4-iPrOPh NHNH S
3-121 OMe 2-C1 3-Cl-4-iPrOPh NHNH S
3-122 OMe 2-C1 3-Cl-2-MeOPh NHNH S
3-123 OMe 2-C1 4-Cl-2-MeOPh NHNH S m.p.l88-190°C
3-124 OMe 2-C1 4-Cl-2-MeOPh N=N S m.p.l65-168°C
3-125 OMe 2-C1 4-Cl-3-MeOPh NHNH S
3-126 OMe 2-C1 4-Cl-3-MeOPh N=N S
3-127 OMe 2-C1 2,3-(MeO)2Ph NHNH S
3-128 OMe 2-C1 2,4-(MeO)2Ph NHNH S
3-129 OMe 2-C1 2,5-(MeO)2Ph NHNH S
3-130 OMe 2-C1 2,6-(MeO)2Ph NHNH S
3-131 OMe 2-C1 3,4-(MeO)2Ph NHNH s
3-132 OMe 2-C1 3,5-(MeO)2Ph NHNH s
3-133 OMe 2-C1 2,3,4-(MeO)3Ph NHNH s
3-134 OMe 2-C1 2,3,5 -(MeO)3Ph NHNH s
3-135 OMe 2-C1 2,4,6-(MeO)3Ph NHNH s
3-136 OMe 2-C1 2,6-F2-4-MeOPh NHNH s
3-137 OMe 2-C1 2,3-F2-4-MeOPh NHNH s
3-138 OMe 2-C1 2,4-F2-6-MeOPh NHNH s
3-139 OMe 2-C1 2,5-F2- 4-MeOPh NHNH s
3-140 OMe 2-C1 3,4-F2-2-MeOPh NHNH s
3-141 OMe 2-C1 2,5-F2-4-MeOPh NHNH s
3-142 OMe 2-C1 3,5—F2-4-MeOPh NHNH s
3-143 OMe 2-C1 2,4,6-F3Ph NHNH s
表 4の続き
化合物 R, (igm R7 Rio T X 物性値 番号
4-37 OMe 2-C1 PhCH2 nPr NHNH S
4-38 OiPr 2-C1 Ph H NHNH S
4-39 OiPr 2-C1 PhCH2 H NHNH s
4-40 OMe 2-C1 CC13 H NHNH s
4-41 OMe 2-C1 CF3 H NHNH s m.p.l49-151°C
4-42 OMe 2-C1 2-ClPhNH H NHNH s
4-43 OMe 2-C1 3-ClPhNH H NHNH s
4-44 OMe 2-C1 4-ClPhNH H NHNH s
4-45 OMe 2-C1 PhCO H NHNH s m.p.l58-161°C
4-46 OMe 2-C1 2-ClPhCO H NHNH s
4-47 OMe 2-C1 3-ClPhCO H NHNH s
4-48 OMe 2-C1 4-ClPhCO H NHNH s
4-49 OMe 2-C1 2-Py H NHNH s m.p.l59- 162°C
4-50 OMe 2-C1 3-Py H NHNH s m.p.l68- 1705°C
4-51 OMe 2-C1 4-Py H NHNH s m.p.205°C up
4-52 OMe 2-C1 2-Me-5-Py H NHNH s
4-53 OMe 2-C1 2-Me-3-Py H NHNH s
4-54 OMe 2-C1 2-PyCH2 H NHNH s
4-55 OMe 2-C1 3-PyCH2 H NHNH s
4-56 OMe 2-C1 4-PyCH2 H NHNH s
4-57 OMe 2-C1 6-Me-2-PyCH2 H NHNH s
4-58 OMe 2-C1 Ph H NHNH s m.p.l45- 150°C
4-59 OMe 2-C1 2-ClPh H NHNH s m.p.l63- 165°C
4-60 OMe 2-C1 3-ClPh H NHNH s m.p.l88-190°C
4-61 OMe 2-C1 4-ClPh H NHNH s m.p.l86- 188°C
4-62 OMe 2-C1 2-MePh H NHNH s m.p.l45-147°C
4-63 OMe 2-C1 3-MePh H NHNH s
4-64 OMe 2-C1 4-MePh H NHNH s m.p.l87-189°C
4-65 OMe 2-C1 2-MeOPh H NHNH s m.p.l63- 165°C
4-66 OMe 2-C1 3-MeOPh H NHNH s m.p. l63- 165°C
4-67 OMe 2-C1 4-MeOPh H NHNH s m.p.l85-187°C
4-68 OMe 2-C1 2-CFjPh H NHNH s m.p.l51 -153°C
4-69 OMe 2-C1 3-CFjPh H NHNH s m.p.l62- 165°C
4-70 OMe 2-C1 4-CFjPh H NHNH s m.p.l97- 199°C
4-71 OMe 2-C1 2-Ph-Ph H NHNH s
4-72 OMe 2-C1 4-Ph-Ph H NHNH s m.p.200°C up
4-73 OMe 2-C1 4-CNPh H NHNH s m.p.200°C up
4-74 OMe 2-C1 2-CF3OPh H NHNH s m.p.l53-154°C
4-75 OMe 2-C1 4-CFjOPh H NHNH s m.p.l85-186°C
4-76 OMe 2-C1 2,6-F2Ph H NHNH s m.p.l59-161°C
4-77 OMe 2-C1 2,4-F2Ph H NHNH s m.p.l74-176°C
表 4の続き
化合物 R, ( 2)m R7 Rio T X 物性値 番号
4-78 OMe 2-C1 2,6-Cl2Ph H NHNH S
4-79 OMe 2-C1 2,4-Cl2Ph H NHNH S m.p.l95-197°C
4-80 OMe 2-C1 1-naphtyl H NHNH S m.p.l70-171°C
4-81 OMe 2-C1 2-naphtyl H NHNH S m.p.l68-170°C
4-82 OMe 2-C1 2-BrPhCH2 H NHNH S m.p.l55-158°C
4-83 OMe 2-C1 2-ClPhCH2 H NHNH s m.p.l56-158°C
4-84 OMe 2-C1 3-ClPhCH2 H NHNH s m.p.l50-152°C
4-85 OMe 2-C1 4-ClPhCH2 H ΗΝΉ s m.p.l60-163°C
4-86 OMe 2-C1 2-FPhCH2 H NHNH s m.p.l39-142°C
4-87 OMe 2- CI 3-FPhCH2 H NHNH s m.p.l39-142°C
4-88 OMe 2-C1 4-FPhCH2 H NHNH s m.p.l89-191°C
4-89 OMe 2-C1 2-MePhCH2 H NHNH s m.p.l57-160°C
4-90 OMe 2- CI 3-MePhCH2 H NHNH s m.p.l42-144°C
4-91 OMe 2-C1 4-MePhCH2 H NHNH s m.p.l75-178°C
4-92 OMe 2-C1 2-MeOPhCH2 H NHNH s m.p.l59-164°C
4-93 OMe 2-C1 3-MeOPhCH2 H NHNH s
4-94 OMe 2-C1 4-MeOPhCH2 H NHNH s m.p.l78-180°C
4-95 OMe 2-C1 2-CF3PhCH2 H NHNH s m.p.l53-156°C
4-96 OMe 2-C1 3-CF3PhCH2 H NHNH s
4-97 OMe 2-C1 4-CF3PhCH2 H NHNH s
4-98 OMe 2-C1 2-PhOPhCH2 H NHNH s
4-99 OMe 2-C1 3-PhOPhCH2 H NHNH s
4-100 OMe 2-C1 4-PhOPhCH2 H NHNH s
4-101 OMe 2-C1 2-PhCH2OPhCH2 H NHNH s
4-102 OMe 2-C1 3-PhCH2OPhCH2 H NHNH s
4-103 OMe 2-C1 4-PhCH2OPhCH2 H NHNH s
4-104 OMe 2-C1 2,6-Cl2PhCH2 H NHNH s m.p.l66-168°C
4-105 OMe 2-C1 2,4-Cl2PhCH2 H NHNH s m.p.l45-146°C
4-106 OMe 2-C1 3,4-Cl2PhCH2 H NHNH s m.p.l82-184°C
4-107 OMe 2-C1 2,6-F2PhCH2 H NHNH s m.p.l65-168°C
4-108 OMe 2-C1 2-Cl-6-F-PhCH2 H NHNH s m.p.l54-156°C
4-109 OMe 2-C1 2-ClPh H N=N s m.p.99-102°C
4-110 OMe 2-C1 3-ClPh H N=N s
4-111 OMe 2-C1 4-ClPh H N=N s m.p.H0-113°C
4-112 OMe 2-C1 2-ClPhCH2 H N=N s m.p.H6-119°C
4-113 OMe 2-C1 3-ClPhCH2 H N=N s
4-114 OMe 2-C1 4-ClPhCH2 H N=N s m.p.l08-110°C
4-115 OMe 2-C1 2-FPhCH2 H N=N s nD 23"1.6224
4-116 OMe 2-C1 3-FPhCH2 H N=N s
4-117 OMe 2-C1 4-FPhCH2 H N=N s
4-118 OiPr 2-C1 2-ClPhCH2 H NHNH s
表 4の続き
/vu/ O 868/JOさ oifcld S6ls0S00iAV
4の続き
化合物 R, ( 2)m R7 Rio T X 物性値 番号
4-243 OMe 2-C1 2-Cl-6-MeOPhCH2 H N=N S
4-244 OMe 2-C1 2-Cl-3-MeOPhCH2 H NHNH s
4-245 OMe 2-C1 2-Cl-3-MeOPhCH2 H N=N s
4-246 OMe 2-C1 2-Cl-4-MeOPhCH2 H NHNH s m.p.l63- 165°C
4-247 OMe 2-C1 2-Cl-4-MeOPhCH2 H N=N s
4-248 OMe 2-C1 2-Br-3-MeOPh H NHNH s
4-249 OMe 2-C1 3.Br-4-MeOPh H NHNH s
4-250 OMe 2-C1 4-Br-2-MeOPh H NHNH s m.p.l98-200°C
4-251 OMe 2-C1 4-Br-3-MeOPh H NHNH s
4-252 OMe 2-C1 2,3-(MeO)2Ph H NHNH s
4-253 OMe 2- CI 2,3-(MeO)2Ph H N=N s
4-254 OMe 2-C1 2,4-(MeO)2Ph H NHNH s m.p.l75- 178°C
4-255 OMe 2-C1 2,4-(MeO)2Ph H N=N s
4-256 OMe 2-C1 2,5-(MeO)2Ph H NHNH s
4-257 OMe 2-C1 2,5-(MeO)2Ph H N=N s
4-258 OMe 2-C1 2,6-(MeO)2Ph H NHNH s m.p.l97- 199°C
4-259 OMe 2-C1 2,6-(MeO)2Ph H N=N s
4-260 OMe 2-C1 3,4-(MeO)2Ph H NHNH s m.p.l48-150°C
4-261 OMe 2-C1 3,4-(MeO)2Ph H N=N s
4-262 OMe 2-C1 3,5-(MeO)2Ph H NHNH s
4-263 OMe 2-C1 3,5-(MeO)2Ph H N=N s
4-264 OMe 2-C1 2,3,4-(MeO)3Ph H NHNH s amorphous
4-265 OMe 2-C1 2,3,4-(MeO)3Ph H N=N s
4-266 OMe 2-C1 2,3,5 -(MeO)3Ph H NHNH s
4-267 OMe 2-C1 2,3,5-(MeO)3Ph H N=N s
4-268 OMe 2-C1 2,4,6-(MeO)3Ph H NHNH s m.p.224-246°C
4-269 OMe 2-C1 2,4,6-(MeO)3Ph H N=N s
4-270 OMe 2-C1 2,3-(MeO)2PhCH2 H NHNH s
4-271 OMe 2-C1 2,3-(MeO)2PhCH2 H N=N s
4-272 OMe 2-C1 2,4-(MeO)2PhCH2 H NHNH s
4-273 OMe 2-C1 2,5-(MeO)2PhCH2 H NHNH s
4-274 OMe 2-C1 2,6-(MeO)2PhCH2 H NHNH s
4-275 OMe 2-C1 3,4-(MeO)2PhCH2 H NHNH s
4-276 OMe 2-C1 3,5-(MeO)2PhCH2 H NHNH s
4-277 OMe 2-C1 2,3,4-(MeO)3PhCH2 H NHNH s
4-278 OMe 2-C1 2,3,5-(MeO)3PhCH2 H NHNH s
4-279 OMe 2-C1 3,5-(MeO)2PhCH2 H NHNH s
4-280 OMe 2-C1 2,4,6-(MeO)3PhCH2 H NHNH s
4-281 OMe 2-C1 cHex H NHNH s m.p.l57-159°C
4-282 OMe 2-C1 3-NCPh H NHNH s m.p.l87-190°C
4-283 OMe 2-C1 (CH3)
2CHCH
2CH
2 H NHNH s m.p.81-83°C
4の続き
の続き
化合物番 R, ogm R7 Rio T X 物性値
4-338 OMe 2-C1 H 2-ClPhCO NHNH S m.p.l55- 157°C
4-339 OMe 2-C1 Me 2-ClPhCO NHNH s m.p.l85- 187°C
4-340 OMe 2-C1 H MeCO NHNH s m.p.l85- 187°C
4-341 OMe 2 - CI Me MeCO NHNH s m.p. l73- 175°C
4-342 OMe 2-C1 H MeOCO NHNH s m.p.205-208°C
4-343 OMe 2-C1 Me MeOCO NHNH s m.p.l76- 178°C
4-344 OMe 2-C1 H NC NHNH s m.p.l69- 172°C
4-345 OMe 2-C1 Me NC NHNH s m.p.207-209°C
4-346 OMe 2-C1 2-ClPh 2-ClPhCO NHNH s
4-347 OMe 2-C1 2-ClPh 2-ClPhCO N=N s
4-348 OMe 2-C1 2-ClPh MeCO NHNH s m.p.l65-168°C
4-349 OMe 2-C1 2-ClPh MeCO N=N s
4-350 OMe 2-C1 2-ClPh MeOCO NHNH s m.p.H2- 115°C
4-351 OMe 2-C1 2-ClPh MeOCO N=N s
4-352 OMe 2-C1 2-ClPh NC NHNH s m.p.l87-190°C
4-353 OMe 2-C1 2-ClPh NC N=N s
4-354 OMe 2- CI PhCH2 2-CIPhCO NHNH s
4-355 OMe 2-C1 PhCH2 2-ClPhCO N=N s
4-356 OMe 2-C1 PhCH2 MeCO NHNH s m.p.l58-160°C
4-357 OMe 2-C1 PhCH2 MeCO N=N s
4-358 OMe 2-C1 PhCH2 MeOCO NHNH s amorphous
4-359 OMe 2-C1 PhCH2 MeOCO N=N s
4-360 OMe 2-C1 PhCH2 NC NHNH s m.p.l79-181°C
4-361 OMe 2-C1 PhCH2 NC N=N s
4-362 OMe 2-C1 H 2-ClPhCH2CO NHNH s
4-363 OMe 2-C1 Me 2-ClPhCH2CO NHNH s m.p.l65-168°C
4-364 OMe 2-C1 2-ClPh 2-ClPhCH2CO NHNH s
4-365 OMe 2-C1 PhCH2 2-ClPhCH2CO NHNH s
4-366 OMe 2 -Me H 2-ClPhCO NHNH s
4-367 OMe 2-Me Me 2-ClPhCO NHNH s
4-368 OMe 2-Me H NC NHNH s
4-369 OMe 2-Me Me NC NHNH s
4-370 OMe 2-Me 2-ClPh 2-ClPhCO NHNH s
4-371 OMe 2-Me 2-ClPh NC NHNH s
4-372 OMe 2-Me 2-ClPh MeOCO NHNH s
4-373 OMe 2-C1 H Ph NHNH s m.p.174-1761:
4-374 OMe 2-C1 H 4-ClPh NHNH s πι.ρ.197-200Τ:
4-375 OMe 2-C1 H 2-MeOPh NHNH s m.p.l72-174'C
4-376 OMe 2-C1 H 2-MePh NHNH s m.p.l27-130tC
4-377 OMe 2-C1 H 4-MePh NHNH s
4-378 OMe 2-C1 H Ph N=N s m.p.152-1541:
4-379 OMe 2-C1 H 2-ClPh NHNH s
化合物 R. (R2)m R7 Rio T X 物性値 番号
4-421 OMe 2-C1 H NHNH s m. l62-164t:
4-422 OMe 2-C1 NHNH s Γη,ρ Ιδ Ι-ΙδΒ^
4-423 OMe 2-C1 O NHNH s .? 157-160^:
4-424 OMe 2-C1 H NHNH s m.pl01-103t
4-425 OMe 2-C1 2,6-Cl2Ph(CH2)2 H NHNH s m.p l40-142 :
4-426 OMe 2-C1 c-HexCHOMe H NHNH s amorphous
4-427 OMe 2-C1 PivO(CH2)2 H NHNH s nD 23 71.5531
4-428 OMe 2-C1 BnO(CH2)2 H NHNH s m.p.97-100t
4-429 OMe 2-C1 iPrO(CH2)2 H NHNH s m.p.83-85t
4-430 OMe 2-C1 MeC CH^ H NHNH s m.p.63-65t:
4-431 OMe 2-C1 EtO(CH2)2 H NHNH s amorphous
4-432 OMe 2-C1 nPrO(CH2)2 H NHNH s πι.ρ.93-95Τ
4-433 OMe 3-C1 nBuO(CH2)2 H NHNH s amorphous
4-434 OMe 3-C1 H NHNH s nD 22 81.5730
4-435 OMe 2-C1 BnOCH2 H NHNH s
4-436 OMe 2-C1 iPrOC¾ H NHNH s
4-437 OMe 2-C1 H NHNH s
4-438 OMe 2-C1 MeOCH2 H NHNH s
4-439 OMe 2-C1 EtOCH2 H NHNH s
4-440 OMe 2-C1 MeO(CH2)3 H NHNH s
4-441 OMe 2-C1 nPrO (CH2) 3 H NHNH s
4-442 OMe 2-C1 AcOCH2 H NHNH s m.p.l39-14r
4-443 OMe 2-C1 PivOCH2 H NHNH s m.p.87-89 :
4-444 OMe 2-C1 MeO(CR2)2 H N=N s m.p.58-60"C
4-445 OMe 2-C1 NHBoc H NHNH s
4-446 OMe 2-C1 PhNHCO H NHNH s m.p.200t:up
4-447 OMe 2-C1 Et02C H NHNH s m.p. l60-161t:
4-448 OMe 2-C1 C7H1502C H NHNH s m.p.H2-114 :
4-449 OMe 2-C1 Ph02C H NHNH s m.p.l98-199t:
4-450 OMe 2-C1 4-ClPh H NHNH 0 m.p .140-142^
4-451 OMe 2-C1 2-Cl-4-MeOPh H N=N s 0^.126-127
99
6 Ll0/t00Zd£/∑Jd 6蘭 SOOZ OAV
続き
化合物 R, (R2)m R7 Rio T X 物性値 ゥ
4-612 OMe 2-iPr 2-F-6-ClPhCH2 H NHNH S m.p.l59-161t:
4-613 OMe 2-Me 2-F-6-ClPhCH2 H NHNH S m.p.l39-141*C
4-614 OMe 2-Et 2,6-Cl2PhCH2 H NHNH S m-p-ioe-ios :
4-615 OMe 2-Me 2,6-Cl2PhCH2 H NHNH s ιη.ρ.134-136Τ:
4-616 OMe 2-Me 2,4-Cl2PhCH2 H NHNH s m.p.l39-141t:
4-617 OMe 2-iPr 2,4-Cl2PhCH2 H NHNH s m.p.152-154で
4-618 OMe 2-Et 2,4-Cl2PhCH2 H NHNH s m.p.l40-142 :
4-619 OMe 2-Et 2-MePhCH2 H NHNH s ιη.ρ.138-140Τ
4-620 OMe 2-Me 2-MePhCH2 H NHNH s m.p.l44-146'C
4-621 OMe 2-Me 2-FPhCH2 H NHNH s m.p.l24-126t:
5-1 OMe 2-C1 H 0 NHNH O amorphous
Q """
5-2 OMe 2-C1 H 0 NH H S amorphous
O """
5-3 OMe 2-C1 Cl H 0 NHNH o
5-4 OMe 2-C1 Cl H 0 NHNH s
5-5 OMe 2-C1 H 0 NHNH o amorphous
5-6 OMe 2-C1 H 0 NHNH s amorphous
5-7 OMe 2-C1 Cl H 0 NHNH o
5-8 OMe 2-C1 Cl H 0 NHNH s
5-9 OMe 2-C1 H 0 NHNH o amorphous
5-10 OMe 2-C1 H 0 NHNH s m.p.l64-165°C
5-11 OMe 2-C1 Cl H 0 NHNH o
5-12 OMe 2-C1 Cl H 0 NHNH s
5-13 OMe 2-C1 H 0 NHNH o amorphous
表 5の続き
化合物番 ogm R7 k T X 物性値 号
5- 14 OMe 2-C1 H 0 NHNH S m.p.l60-162°C
5-15 OMe 2-C1 C I H 0 NHNH o
5-16 OMe 2-C1 • cK Cl H 0 NHNH s
5- 17 OMe 2-C1 Me 0 NHNH o amorphous
5-18 OMe 2-C1 Me 0 NHNH s amorphous
5-19 OMe 2-C1 H 1 NHNH o
5-20 OMe 2-C1 H 1 NHNH s amorphous
5-21 OMe 2-C1 Cl H 0 NHNH s
5-22 OMe 2-C1 Cl H 0 NHNH s
5-23 OMe 2-C1 Cl H 0 NHNH s
5-24 OMe 2-C1 C l H 0 NHNH s
NMRデータ
'H-NMR(CDCl;i, δ (ppm) )
化合物番号 1一 26
0.90-1.84 (m, 13H) , 2.88 (dd, IH) , 3.38 (dd, IH) 4.82 (m, 1H) , 6.28 (br, IH) ,
6.57 (br, IH) , 7.03-7.34 (m, 3H)
化合物番号 2— 18
2.11 (s, 3H) , 3.68 (s, 3H), 4.46 (s, 2H) , 6.40 (br, IH) 6.91 (br, IH), 7.21-7.46 (m, 5H) 化合物番号 2— 20
2.19 (s, 3H), 3.69 (s, 3H) 4.46 (s, 2H) , 6.20 (br, IH), 6.59 (br, IH) , 7.23-7.45 (m, 5H) 化合物番号 2 -22
3.69 (s, 3H) , 4.48 (s, 2H) 6.43 (br, IH), 6.91 (br, IH) , 7.22-7.46 (m, 5H)
化合物番号 2 -83
3.74 (s, 3H) , 4.32 (s, 2H) 5.07 (s, 2H) , 6.33 (br, IH) , 6.62 (br, IH), 6.94-7.64 (m, 12H) 化合物番号 4 -146
3.37 (s, 3H) , 3.78 (s, 3H) 4.58 (s, 2H) , 6.57 (br, IH) , 7.03 (br, IH) 7.16-8.07 (m, 8H) 化合物番号 4 -179
1.37 (d, 6H) , 3.79 (s, 3H) 4.58 (m, IH), 6.33 (br, IH), 6.65 (br, IH) 6.66-8.24 (m, 7H) 化合物番号 4 -190
4.11 (s, 3H) , 7.08-8.26 (m, 7H)
化合物番号 4 -264
3.79 (s, 3H) , 3.92 (s, 6H) 3.93 (s, 3H) , 6.33 (br, IH) 6.61 (br, IH) 6.78-7.98 (m, 6H) 化合物番号 4 -290
1.40 (t, 3H) , 3.76 (s, 3H), 4.04 (Q, 2H) ' 6.31 (br, IH), 6.71 (br, IH), 6.50-7.61 (m, 6H) 化合物番号 4一 314
3.50 (s, 3H) , 3.76 (s, 3H), 6.16 (s, IH), 6.16 (br, IH), 6.62 (br, IH), 6.96-7.45 (m, 7H) 化合物番号 4一 315
3.45 (s, 3H) , 3.76 (s, 3H), 5.92 (s, IH), 6.30 (br, IH), 7.02 (br, IH), 7.02-7.62 (m, 8H) 化合物番号 4一 358
3.78 (s, 1H) , 3.89 (s, 3H) , 4.55 (s, 2H), 6, 32 (br, IH) , 6.59 (br, IH) , 7.16-7.53 (m, 8H) 化合物番号 4一 426
1.04〜1.93(m, 11H), 3.30 (s, 3H) , 3.75 (s, 3H) , 4.12 (m, IH) , 6.38 (br, IH),
7.00 (br, IH), 7.10 (s, IH), 7.28 (d, IH) , 7.38 (d, IH) , 7.53 (s, IH)
化合物番号 4一 431
1.23 (t, 3H), 3.08 (t, 2H), 3.54 (q, 2H) , 3.78 (s, 3H) , 3.80 (t, 2H), 6.31 (br, IH) 6.62 (br, IH), 7.00 (s, IH) , 7.31 (d, IH), 7.37 (d, IH) , 7.53 (s, IH)
化合物番号 4一 433
0.91 (t, 3H) 1.29 (m, 2H) , 1.54 (m, 2H) , 3.10 (t, 2H), 3.50 (t, 2H), 3.78 (5H, m) ,
6.3Kbr, IH), 6.61 (br, IH), 7.00 (s, IH) , 7.31 (d, IH), 7.36 (d, IH) , 7.53, (s, IH) 化合物番号 4一 483
3.76 (s, 3H) , 3.88 (s, 3H) , 6.34 (s, IH) , 6.34〜6· 80 (m, 2H) , 7.31〜7.40 (m, 2H),
7.54 (s, IH), 7.82 (t, IH), 8.10 (s, IH)
化合物番号 4一 503
1.80 (d, 3H) , 3.23 (s, 3H) , 4.96 (Q, IH) , 6.28 (br, IH), 6.6 (br, IH) , 6.89 (s, IH), 6.95 (m, IH), 7.11-7.37 (m, 4H) , 7.47 (s, IH)
化合物番号 5— 1 .
3.74 (s, 3H) , 4.26 (dd, IH), 4.78 (dd, IH) , 5.36 (dd, IH) , 6.28 (br, IH), 6.82 (br, IH), 7.27-7.64 (m, 8H)
化合物番号 5— 2
3.32 (s, 3H) , 3.74 (s, 3H) , 3.80 (dd, IH) , 5.68 (dd, IH) , 6.26 (br, IH), 6.72 (br, IH), 7.27-7.53 (m, 8H)
化合物番号 5— 5
3.73 (s, 3H) , 4.26 (dd, IH), 4.78 (dd, IH) , 5.36 (dd, IH) , 6.26 (br, IH), 6.91 (br, IH) 7.22-7.64 (m, 8H)
化合物番号 5— 6
3.32 (dd, IH), 3.74 (s, 3H), 3.80 (dd, 5.69 (dd, IH) , 6.27 (br, IH) , 6.72 (br, IH) 7.27-7.53 (m, 8H)
化合物番号 5— 9
2.72 (ad, IH), 3.21 (dd, 3.75 (s 3H), 4.14 (t, IH), 4.32 (t, IH), 4, 56 (m, IH), 6.28 (br, IH), 6.97 (br, 7.20-7.54 (m, 8H)
化合物番号 5— 13
2.72 (dd, IH), 3.23 (dd, 3.77 (s, 3H), 4.15 (t, IH), 4.33 (t, IH), 4.57 (m, IH),
6.29 (br, IH), 6.70 (br, 7.20-7.54 (m, 8H)
化合物番号 5— 17
1.41 (s, 3H), 2.97 (Q, 2H) , 3.77 (s, 3H) , 4.13 (Q, 2H), 6.29 (br, IH) , 6.60 (br, IH),
7.25-7.51 (m, 7H)
化合物番号 5— 18
1.44 (s, 3H) , 3.07 (s, 2H) , 3.21 (α, 2H), 3.77 (s, 3H) , 6.30 (br, IH), 6.62 (br, IH) , 7.22-7.54 (m, 7H)
化合物番号 5— 20
1.82 (m, IH) , 2.22 (m, IH) , 3. 01 (m, IH), 3.18(m, IH), 3.72 (s, 3H) 4.84 (m, IH) , 5.06 (s, 2H), 6. 4 (br, IH) 6.73 (br, IH), 6, 94-7.44 (m, 12H) 旋光度データ
化合物番号 5— 1 : [a]D 250 + 3,3 (c=0.89, CHCI3)
化合物番号 5— 2 : [a]D 250 +112.5 (c=1.10, CHCI3)
化合物番号 5— 5 ひ】。25.。 - 4.1 (C=0.97, cHcg 化合物番号 5— 6 ひ] D 25。 -110.8 (c=1.11, CHCI3) 化合物番号 5— 9 α]0 250 + 14.7 (c=0.99, CHc 化合物番号 5— 1 0 a]D 250 - 9.4 (c=0.96, CHc 化合物番号 5 - 1 3 a]D 250 - 13.6 (c=0.86, CHc 化合物番号 5— 14 a]D 250 + 9.4 (c=0.84, CHc
次に、 本発明の殺菌殺虫剤組成物の実施例を若干示すが、 添加物及び添加割合は、 こ れら実施例に限定されるべきものではなく、 広範囲に変化させることが可能である。 製剤実施例中の部は重量部を示す。 製剤実施例 1 水和剤
本発明化合物 4 0部
クレー 4 8部
ジォクチルスルホサクシネートナトリウム塩 4部
リグニンスルホン酸ナトリウム塩 8部
以上を均一に混合して微細に粉砕して、 有効成分 4 0 %の水和 ^ijを得た。 製剤実施例 2 乳剤
本発明化合物 1 0部
ソルべッソ 2 0 0 5 3部
シクロへキサノン 2 6部
ドデシルベンゼンスルホン酸カルシウム塩 1部
ポリオキシ: rチレンアルキルァリルエーテル 1 0部
以上を混合溶解して、 有効成分 1 0 %の乳剤を得た。 製剤実施例 3 粉剤
本発明化合物 1 0部
クレー 9 0部
以上を均一に混合、 微細に粉砕して、 有効成分 1 0 %の粉剤を得た。 製剤実施例 4 粒剤
本発明化合物 5部
クレー 7 3部
ベントナイト 2 0部
ジォクチルスルホサクシネートナトリウム塩 1部
リン酸カリウム 1部
以上をよく粉砕混合し、 水を加えてよく練り合せた後、 造粒乾燥して有効成分 5 %め 粒剤を得た。 製剤実施例 5 懸濁剤
本発明化合物 1 0部
ポリオキシエチレンアルキルァリルエーテル 4部
ポリカルボン酸ナトリウム塩 2部
グリセリン 1 0部
キサンタンガム 0. 2部
水 73. 8部
以上を混合し、粒度が 3ミクロン以下になるまで湿式粉碎して、有効成分 10%の懸 濁剤を得た。 製剤実施例 6 顆粒水和剤
本発明化合物 40
クレ一 , 36
塩化カリウム 10
アルキルベンゼンスルホン酸ナトリウム塩 1
リグニンスルホン酸ナトリウム塩 8
アルキルベンゼンスルホン酸ナトリゥム塩の
ホルムアルデヒド縮合物 5部
以上を均一に混合して微細に粉砕後, 適量の水を加えてから練り込んで粘土状にし た。 粘土状物を造粒した後乾燥し、 有効成分 40%の顆粒水和剤を得た。
次に、本発明化合物が各種植物病害防除剤および殺虫剤の有効成分として有用であるこ とを試験例で示す。
なお、本発明の効果を明確にするために、米国特許第 5567723号公報に記載の以 咅 Π ¾
下の対照化合物 Aとの比較試験も併せて行った。
対照化合物 A
試験例 1 リンゴ黒星病防除試験
素焼きポットで栽培したリンゴ幼苗 (品種 「国光」、 3 4葉期) に、 本発明化合物 の乳剤を有効成分 100 p pmの濃度で散布した。室温で自然乾燥した後、 リンゴ黒星 病菌 (Ve n t u r i a i n a e q u a 1 i s ) の分生胞子を接種し、 明暗を 1 2時 間毎にくりかえす 20で、高湿度の室内に 2週間保持した。葉上の病斑出現状態を無処 理と比較調査し、 防除効果を求めた結果、 1— 5 1— 3 1 2— 6 2— 7 2 - 1 2 2— 14 2— 25 2— 26 2— 27 2— 28 2— 29 2— 33 2 - 34 2— 39 2— 40 2 39 2 - 40 2 - 43 2— 49 2— 54 2 — 58 2— 59 2— 60 2— 65 2— 68 2— 69 2— 70 2— 7 1 2— 74 2— 76 2— 77 2— 8 1 2— 83 2— 86 2— 89 2- 12 2 3— 37 3— 65 3— 68 3— 70 3— 7 1 3— 88 3— 90 3 - 1 00 3— 101 3— 103 3— 104 3— 123 3— 124 4一 2 4一 3 4— 6 4—7 4一 8 4一 9 4— 10 4一 1 1 4-27, 4一 33 4— 34
4一 35、 4— 41、 4 -49、 4— 5 1、 4 - 58, 4 - 59、 4 -60、 4一 6 1、
4一 62. , 4-64, 4- -65、 4- -66、 4 - 67, 4- 68、 4- 69、 4一 70、
4一 72 、 4-73, 4 -74 、 4 — 75、 4一 76、 4 — 77、 4 - - 79、 4 - -80、
4一 81 、寸 4— 82、 4 -83 、 4 — 84、 4 -85, 4 - 86 、 4 -87 、 4 — 88、
4一 89 、 4— 90、 4. -9 1 、 4 -92, 4- -94、 4 - -95、 4 - 104 、 4 - 10
5、 4一 106、 4- - 1 07、 4一 108, 4 — 109、 4一 1 1 1 、 4 - 1 1 2、 4
— 1 14、
4— 1 1 5、 4— 1 27/ 4— 1 37、 4一 138、 4一 1 39、 4— 142、 4- 14 3、 4— 145、 4一 148、 4— 149、 4— 1 51、 4一 152、 4— 1 53、 4- 1 57、 4一 173、 4一 174、 4— 175、 4— 176、 4一 177、 4— 178、 4 - 1 79、 4一 182、 4— 183、 4一 185、 4— 186、 4— 190、 4一 199、 4
— 200、 4 - 203、 4— 207、 4一 208、 4— 210、 4一 2 1 2、 4 ― 222、
4-223 、 4- - 229. 4一 230、 4一 231、 4一 232、 4- 2 33、 4 — 237、
4-246 、 4 - 250, 4— 254、 4— 260、 4— 264、 4一 2 86、 4 — 287、
4-288 、 4- — 290、 4— 291、 4一 292、 4一 294、 4一 2 97、 4 - 307,
4-314 、 4- -315, 4— 3 16、 4一 318、 4一 321、 4— 3 28、 4 - 330,
4-332 、 4· — 334、 4一 336、 4一 348、 4— 373、 4— 3 74、 4 — 375、
4-399 、 4 -407 、 4— 408、 4— 409、 4— 410、 4 ― 41 1 、 4-41
3、 4-4 16 、 4-4 24、 4一 425、 4— 426、 4-427 、 4-4 2 8、 4—
429, 4一 4 30, 4一 435、 4— 438、 4— 439、 4-4 4 2、 4 ― 443、
4一 4、46 、 4 -449 、 4— 452、 4— 453、 4— 455、 4 ― 456 、 4-45
60 、 4-4 6 1、 4一 462、 4一 463、 4一 466 4-4 6 7、 4 -
468、 4一 4 69、 4 — 473、 4— 474、 4一 475、 4— 4 7 7、 4 ― 482、
4-483 、 4 -487 、 4— 49 1、 4— 492、 4一 493、 4 ― 494 、 4-49
5、 4— 4 96 、 4-4 99、 4- 501, 4— 51 3、 4— 51 5 、 4-5 2 5、 4一
526, 4一 5 27, 4 — 530、 4— 534、 4— 537、 4— 5 3 9、 4 ― 542、
4-544 、 4 -545 、 4— 546、 4— 547、 4— 549、 4 ― 550 4— 55
1、 4-5 52 , 4- 5 54、 4一 555、 4— 556、 4一 557 、 4-5 5 8、 4一
559, 4一 5 6 1, 4一 570、 4一 57 1、 4一 573、 4- 5 8 2、 4 ― 584、
4-587 、 4 -593 、 4— 594、 4— 603、 4— 604、 4 ― 605 、 4-60
6、 4-6 08 、 4-6 09、 4-6 1 1, 4— 6 1 2、 4-61 3 、 4-6 1 7、 4 -
6 18, 4一 6 19、 5一 1、 5-2, 5— 6、 5— 9、 5— 10、 5 13、 5 — 14、
5- 17, 5一 18の化合物が 7 5%以上の優れた防除価を示した。
一方、 対照化合物 Aの防除値は 0%であった。 試験例 2 インゲン灰色かび病防除試験
育苗バッ卜で栽培したインゲン (品種 「ながうずら」) の花を切除し、 本発明化合物 の乳剤を有効成分 1 O O P pmに調製した薬液に浸漬した。 浸漬後、 風乾し、 インゲン
灰色かび病菌 (Bo t r y t i s c i n e r e a) を噴霧接種した。 接種した花を無 処理のインゲン葉に乗せ、 恒温室 (20V) 〖こ 7日間保持した。 葉上の病斑直径を無処 理と比較調査し、 防除価を求めた。 その結果、 化合物番号 2— 39、 2— 58、 4-2 23、 4— 294、 4一 330、 5— 1の化合物が 75 %以上の優れた防除価を示した。 一方、 対照化合物 Aの防除値は 0%であった。 寸
試験例 3 コムギうどんこ病防除試験
素焼きポットで栽培した'コムギ幼苗 (品種 「チホク」、 1. 0〜1. 2葉期) に本発明化 合物の水和剤 100 p pmの濃度で散布した。葉を風乾させた後、 コムギうどんこ病菌 (E r y s i ph e g r am i n i寸s f . s p. t r i t i c i) の分生胞子を振り払い 接種し、 22〜25 °Cの温室で 7日間寸保持した。 葉上の病斑出現状態を無処理と比較調査 し、 防除効果を求めた。 その結果、 化合物番号 1一 5、 1 - -3 1、 2 - 4、 2-6 、 2 ―
7、 2— 12、 2- 14 、 2— 25、 2— 26、 2-27, 2-28, 2一 29、 2 ― 3
3、 2-34, 2 -40 、 2— 41、 2-59, 2-60, 2-67, 2一 68、 2 ― 7
1、 2— 77、 2-89 、 2— 122、 3— 65、 3-68 、 3-70, 3 - 7 1、 3 ― 1
00 、 3— 101、 3 - 103、 3— 104、 3 - - 123、 3— 124、 4 - 2、 4 ― 3 、
4-6, 4— 7、 4一 8、 4— 9、 4— 10、 4一 1 1、 4一 27、 4一 33、 4— 41、
4一 49、 4 -5 1, 4一 59、 4一 6 1、 4一 62、 4 — 64、 4 -65, 4 — 66、
4 - 67、 4 — 68、 4― 69、 4一 70、 4 _ 73、 4 _ 74、 4 -75, 4一 77、
4一 79、 4一 80、 4 - 81、 4一 82、 4一 83、 4 — 84、 4 -85. 4 — 86、
4 - 8'7、 4一 88、 4一 89、 4一 90、 4.一 92、 4- -94、 4- -95、 4- - 104,
4一 1 05 4- 10 6、 4- 1 07 、 4- - 1 08, 4- 109、 4 - 1 1 1, 4- 1 1
2、 4— 1 14、 4— 1 15、 4一 127、 4一 138、 4一 139, 4— 142、 4— 1 43、 4— 146、 4— 147、 4— 151、 4— 152、 4— 153、 4— 1 57、 4一
1 73 4— 1 74、 4— 1 75、 4 - - 17 6、 4- - 1 77、 4 - 1 78 、 4一 1 79, 4 一 18 0 、 4一 181、 4— 182、 4一 1 83, 4 — 185、 4一 18 6 、 4 ― 190、
4-2 0 0、 4— 203、 4— 207、 4 - 208、 4— 210、 4-2 1 2 、 4 - 222,
4-2 2 3、 4- 227, 4- 229, 4一 230、 4— 231、 4-2 4 6 、 4 — 250、
4-2 5 4、 4— 260、 4-264、 4- 286、 4— 287、 4-2 8 8 4 - 290.
4-2 9 1、 4- 292. 4— 294、 4 - 297、 4- 307, 4-3 1 4 、 4 — 3 1 5、
4-3 1 6、 4— 32 1、 4- 328、 4- 330、 4— 332、 4-3 3 4 , 4 — 374、
4- 3 9 9、 4— 407、 4-409 、 4 - -41 1 、 4-41 3 、 4一 4 1 6 、 4-42
4、 4 ― 426、 4— 427、 4-4 28、 4-4 29、 4-4 30、 4 ― 4 3 5、 4 -
438 、 4— 442、 4-449, 4一 4 52, 4 -453, 4 -45 6 、 4 ― 457、
4-4 6 、 4- -466 、 4-467 、 4一 4 6 9 、 4-47
3、 4 ― 475、 4一 477、 4— 4 81、 4-4 82、 4-4 83、 4 ― 4 8 7、 4—
49 1 、 4— 492、 4一 493、 4 -4 94, 4 -495, 4 -49 6 、 4 ― 499、
4-5 0 1、 4— 51 3、 4- 5 1 5 、 4 - - 524 、 4-526 、 4一 5 2 7 、 4- 53
0、 4 ― 537、 4- 539, 4— 5 42、 , 4-5 43、 4-5 46、 4一 5 4 7、 4-
549、 4— 550、 4— 55 1、 4— 5 5 5、 4一 5 56、 4— 55 7、 4一 5 58、 4— 56 1、 4一 570、 4— 57 1、 4— 57 2、 4一 57 3、 4— 584、 4- 58 7、 4一 593、 4一 594、 4— 60 3、 4— 604、 4— 60 5、 4一 606、 4一 608、 4一 609、 4一 6 1 0、 4— 6 1 1、 4一 6 1 2、 4- 6 1 3, 4— 6 1 4、 4一 6 1 7、 4一 6 1 8、 4一 6 1 9、 5— 1、 5— 2、 5— 6、 5— 9、 5— 1 0、 5— 1 3、 5— 14の化合物が 7 5 %以上の優れた防除価を示した。
一方、 対照化合物 Aの防除値は 0 %であった。 試験例 4 卜マト疫病防除試験
素焼きポットで栽培したトマト幼苗 (品種 「レジナ」、 4〜5葉期) に、 本発明化合 物の乳剤を有効成分 1 0 0 p pmの濃度で散布した。 散布後、 室温で自然乾燥し、 トマ ト疫病菌 (P h y t o p h t h o r a i n f e s t a n s) の遊走子嚢懸濁液を噴霧 接種し、 明暗を 12時間毎に繰り返す高湿度の恒温室 (20で) に 4日間保持した。 葉 寸
上の病斑出現状態を無処理と比較調査し、 防除効果を求めた。その結果、 化合物番号 1 一 2、 1一 1 2、 1一 2 2、 1一 2 6、 2 - 6、 2— 7、 2 - 1 2、 2— 14、 2 - 2 5、 2— 26、 2— 2 7、 2— 2 9、 2— 3 3、 2— 34、 2— 3 9、 2— 40、 2 - 4 1、 2— 43、 2— 5 3、 2— 5 7、 2 - 5 9、 2— 60、 2 - 6 7、 2 - 6 8、 2 一 6 9、 2— 70、 2— 7 1、 2— 74、 2 - 7 6、 2— 7 7、 2 - 8 1、 2— 8 3、
2— 86、 2— 8 9、 2— 1 22、 3— 37、 3— 6 5、 3— 68、 3— 70、 3— 7 1、
3 - 88, 3— 90、 3— 1 00、 3— 1 0 1、 3— 1 03、 3— 1 23、 3— 1 24、 4 一 7 、 - —8、 4— 9、 4- 1 0, 4- - 1 1、 4一 27、 4一 33、 4 - - 34、 4 - -41、
4一 49 、 4一 58、 4 - 59. 4一 6 0、 4— 6 1、 4— 62、 4 - - 64、 4- - 65、
4一 66, , 4 — 6 7、 4— 7 0、 4一 4 - - 77、 4 - - 79、
4一 8 1 、 4一 82、 4一 8 3、 4 - .84、 4— 8 5、 4 - 8 6 、 4 - 8 8, 4 — 89、
4 - 90' . 4 - — 9 1、 4— 92、 4一 94、 4— 95、 4- 1 04 、 4 - 1 0 5, 4 - 1
0 6 、 4一 1 07、 4— 1 0 8、 4一 - 1 0 9、 4— 1 1 1、 4— 1 1 2、 4- 1 14、
4一 1 1 5、 4— 1 3 8、 4一 1 39 、 4— 1 42、 4— 1 45、 4 - 1 46、 4 - 14
7、 4一 14 9、 4- 1 5 1、 4一 1 57、 4— 1 72、 4- 1 7 4、 4 - 1 7 5 , 4- 1
76、 4- 1 7 7、 4— 1 78、 4一 1 7 9、 4— 1 82、 4一 1 85 、 4- 1 8 6、 4一
1 9 1 、 4一 1 94、 4一 1 95、 4— 1 96、 4— 1 97、 4 - 1 9 9 、 4 - 2 00, 4
- 20 3、 4 — 207、 4 — 208、 4— 2 1 0、 4— 2 1 2、 4一 2 2 2、 4 ― 223、
4- 2 2 9、 4— 230、 4一 23 1、 4— 24 1、 4- 246, 4一 2 50、 4 — 2 54、
4- 2 60、 4— 264、 4— 286、 4— 287、 4- 288, 4 - 2 90、 4 — 29 1、
4- 2 92、 4— 294、 4— 297、 4— 307、 4— 3 14、 4 - 3 1 5、 4 — 3 1 6、
4- 3 2 1、 4- 332, 4- 336. 4— 34 1、 4一 343、 4一 3 60、 4 - 373,
4- 3 74、 4- 37 5、 4— 399、 4-407, 4-408, . 4 ― 40 9 、 4-4 1
1、 4一 4 1 3、 4一 4 1 6、 4-424, 4— 42 5、 4— 426、 4一 42 7、 4 - 429、 4— 430、 4— 43 5、 4— 446、 4— 449、 4一 452、 4一 45 3、 4— 455、 4一 45 6、 4一 459、 4— 46 1、 4一 462、 4一 46 3、 4— 46
6、 4― 46 7、 4一 469、 4- 473、 4-474, 4一 47 5、 4一 477、 4一
48 1 、 4一 4 8 2 、 4一 4 8 3、 4一 48 7、 4-49 1 、 4一 4 9 2 、 4一 4 93、
4-4 9 4 、 4 ― 4 9 5 、 4 -49 6、 4— 49 9、 4- 5 0 1 、 4一 5 1 3、 4一 5 1
5、 4 ― 5 24 、 4一 5 25 、 4 - 527、 4— 530、 4一 5 34 、 4 ― 53 7 、 4一
540 、 4 - 5 4 2 、 4一 5 43、 4- 544, 4- 545 、 4一 5 46 、 4一 5 47、
4- 5 4 8 、 4 ― 5 49 、 4 - 55 0、 4— 55 2、 4- 5 54 、 4一 5 5 5、 4 - 5 5
6、 4 ― 5 57 、 4一 5 58 、 4一 559、 4— 56 1、 4一 5 7 0 、 4 ― 57 1 、 4-
5 7 2 、 4一 5 7 3 、 4一 5 8 2、 4- 584, 4- 58 7 、 4一 6 03 、 4一 6 04、
4- 6 0 5 、 4 ― 6 06 、 4 - 60 8、 4- 60 9、 4- 6 1 1 、 4一 6 1 2、 4一 6 1
3、 4 ― 6 14 、 4 - 6 1 7, . 4一 6 1 8、 4— 6 1 9、 5 - -2、 5 - -6、 5一 9 、 5一 1
0、 5 ― 1 3、 5 ― 14, . 5 - - 1 7, , 5— 1 8、 5 - 20
の化合物が 7 5 %以上の優れた防除価を示した。
一方、 対照化合物 Aの防除値は 0 %であった。 試験例 5 コムギ赤さび病防除試験
素焼きポットで栽培したコムギ幼苗 (品種 「農林 6 1号」、 1. 0〜 1. 2葉期) に本発 明化合物の水和剤 1 O O p pmの濃度で散布した。 葉を風乾させた後、 コムギ赤さび病菌 (P u c c i n i a r e c.o n d i t a) の夏胞子を振り払い接種し、 22〜2 5°Cの 温室で 10日間保持した。 葉上の病斑出現状態を無処理と比較調査し、 防除効果を求めた。 その結果、 化合物番号 2一 1 2 、 2 - 14、 2一 2 5 、 2 - 2 6, 2一 2 7, 2一 3 9、
2— 40、 2 - 56, 2一 6 0 、 2一 7 7、 3一 6 5 、 3— 70、 3 - 7 1、 3一 90、
3— 1 00、 3 - 1 0 1 、 3 ― 1 03 、 3 - 1 04、 3一 1 2 3、 3一 1 24、 4- 2,
4— 3、 4一 6、 4- 7, . 4 8、 4. — 1 0、 , 4 - - 1 1、 4一 33、 4- - 34、 4-41 ,
4- 59, 4— 60、 4一 6 1 、 4- 6 2、 4- 64 、 4- 6 5, 4- 66、 4 _ 6 7、
4一 69、 4— 70、 4一 7 4 、 4一 7 5、 4一 7 7 4— 7 9、 4 - 8 1、 4一 8 2、
4- 83, 4— 8 5、 4一 8 6 、 4- 90、 4一 92 、 4- 1 04 、 4 - 1 0 5 、 4— 1
06、 4— 1 08、 4 - 1 0 9 、 4一 1 1 1 、 4一 1 1 2、 4— 1 14 、 4— 1 1 5、 4
- 1 27, 4一 1 38、 4- 1 39、 4- 1 42, , 4- 143、 4- - 148、 4 - - 1 5 1、
4一 1 5 2、 4- 1 53 、 4 ― 1 56 、 4一 1 5 7、 4 — 1 73、 4一 1 74、 4 - 1 7
5、 4— 1 7 6、 4一 1 77 、 4一 1 78、 4一 1 7 9 、 4— 1 8 0、 4- 1 8 1、 4 -
1 82、 4— 1 83、 4一 1 8 5、 4 - 1 8 6、 4一 1 90、 4 - 1 9 5、 4— 200、
4— 20 3、 4- 20 7 、 4 ― 208 、 4- 2 1 0、 4 — 2 1 2、 4 - 2 2 2、 4- 22
3、 4一 22 7、 4- 2 29 、 4- 2 30、 4一 2 3 1 、 4— 2 3 2、 4- 2 3 3、 4一
2 50、 4— 2 54、 4一 2 6 0、 4 - 26 4、 4一 2 86、 4— 28 7、 4 - 288、
4一 290、 4- 2 9 1 、 4 ― 29 2 、 4一 29 4、 4 - 2 97, 4一 300、 4- 30
7、 4— 3 1 4、 4- 3 1 5 、 4- 3 1 6、 4一 3 1 8 、 4- 32 1、 4- 32 8、 4—
3 30、 4— 332、 4一 3 3 4、 4 - 33 6、 4 - 3 44、 4一 37 4、 4 - 39 9、
4-40 7, 4-40 9 、 4 ― 4 1 0 、 4一 4 1 1、 4 — 4 1 2、 4一 4 1 6、 4-42
4、 4一 42 5、 4- 4 26 4-4 27、 4一 42 8 、 4-42 9、 4-43 0、 4一
43 5, 4― 438、 4-439、 4-442、 4 -446、 4― 449、 4-452、
4-45 3 、 4 ― 45 5, 4 ― 4 5 6、 4 - 4 5 7、 4 ― 4 6 3 、 4一 4 6 6、 4 -46
7、 4 -4 6 8 、 4- 469 、 4 ― 47 5、 4 ― 47 7 、 4 ― 4 8 1 , 4 ― 482 、 4一
48 3, 4 ― 4 8 7、 4-4 9 1 、 4-49 2 、 4 -4 9 3 4 ― 49 5 、 4-4 96、
4-499 、 4 ― 50 1 , 4 ― 5 1 3、 4一 5 1 5、 4 ― 5 2 4 、 4一 5 2 5、 4 - 5 2
6、 4- 5 3 0 、 4- 539 、 4 ― 547、 4 ― 549 、 4 ― 5 5 1、 4 ― 5 54 、 4 -
5 5 5, 4 ― 5 5 6、 4- 5 5 7 、 4- 55 8 、 4 - 5 5 9 、 4 ― 57 0 、 4- 5 7 1、
4 - 5 72 、 4 ― 57 3, 4 ― 5 8 4、 4 - 5 8 7、 4 ― 5 9 3 、 4一 5 9 4、 4 - 6 0
3、 4 - 6 0 4 、 4- 60 5 、 4 ― 606、 4 ― 6 08ヽ 4 ― 6 0 9、 4 ― 6 1 1 、 4一
6 1 2, 4 ― 6 1 3、 4-6 1 4 、 4- 6 1 7 、 4- 6 1 8ヽ 4 ― 6 1 9 、 5 - 2 、 5一
6、 5 - 9 、 5 ― 1 0、 5— 1 3 5 - 14. 5一 1 7
の化合物が 7 5 %以上の優れた防除価を示した。
一方、 対照化合物 Aの防除値は 0 %であった。 試験例 6 ァヮョトウに対する防除試験
前記の製剤実施例 1に示された水和剤の処方に従い,化合物濃度が 1 2 5 p pmに なるように水で希釈した。その薬液中にトウモロコシ葉を 30秒間浸潰し風乾後、ろ紙 を敷いたシャーレに入れァヮョトウ 2齢幼虫 5頭を接種した。ガラス蓋をして、温度 2 5で、湿度 6 5 %の恒温室内に置き > 6日後に殺虫率を調べた。 2反復である。その結果 > 化合物番号 2 ― 6 0 、 2 ― 6 5 、 2 ― 1 2 2、 3 ― 6 8 、 3 ― 90 、 3 ― 1 0 2、 3—
1 2 3'、 4— 2 7 、 4 ― 3 3、 4 ― 6 1 、 4 - 6 4 、 4 ― 6 5 、 4 ― 7 0 、 4 - 7 5,
4— 7 7、 4 ― 7 9 、 4 ― 8 1 、 4 ― 8 2 、 4— 8 4 、 4 ― 8 5、 4 ― 8 7 、 4— 9 1、
4— 9 5、 4 ― 1 0 4 、 4一 1 .0 5 、 4 ― 1 0 6 、 4 ― 1 0 7 、 4 ― 1 0 8 、 4— 14
2、 4 - 1 6 4 、 4一 1 7 2、 4 ― 1 7 3 、 4- 1 7 4 4 ― 1 7 5 、 4 ― 1 7 7、 4
- 1 7 8, 4 ― 1 7 9 、 4一 1 8 3 、 4 ― 1 8 5 、 4 ― 1 8 6 、 4 ― 1 9 5 、 4一 1 9
8、 4 - 1 9 9 、 4 ― 2 2 2、 4 ― 2 2 3 、 4 - 2 2 9 、 4 ― 2 3 0 4 ― 2 3 2, 4
- 2 3 3, 4 ― 2 3 7 、 4一 2 4 0 、 4 ― 246 、 4 ― 2 5 4 、 4 ― 2 9 4 , 4 - 3 2
8、 4 - 3 3 2 、 4 ― 3 4 1、 4 ― 3 7 4 、 4 - 4 2 2 、 4 ― 42 3 、 4一 424, 4 一 44 9、 4 ― 4 5 3 、 4一 4 5 4 、 4 ― 4 56 、 4 ― 4 5 7 、 4 ― 4 6 1 , 4 -46
3、 4 -46 7 、 4 ― 4 7 5、 4 ― 4 8 2 、 4一 4 9 5 、 4 ― 49 6 、 4 ― 49 7, 4 一 4 9 9、 4 ― 5 1 3 、 4一 5 1 5 、 4 ― 5 2 6 、 4 ― 5 3 9 、 4 ― 5 4 9 , 4 - 5 5
2、 4 - 5 5 3 4 ― 5 5 4、 4 ― 5 5 6 、 4 - 5 5 7 4 ― 5 5 9 、 4 ― 5 70, 4
— 5 7 1、 4 ― 5 7 2 、 4一 5 7 3 、 4 ― 6 04 、 4 ― 6 0 5 、 4 ― 6 0 6 、 4— 6 1
1、 4 - 6 1 3 4 ― 6 1 4、 4 ― 6 1 7 、 4 - 6 1 8 、 4 ― 6 1 9 、 5 ― 1 0, 5 -
1 8
の化合物が 1 00 %の殺虫率を示した。対照に用いたクロルジメフオルムの 1 2 5 p p mにおける殺虫率は 40 %であった。
試験例 7 ヮタァブラムシに対する効力試験
3寸鉢に播種した発芽 1 0日が経過したキユウリにヮ夕アブラムシ成虫を接種した。 1 日後に成虫を除去し,産下された若虫が寄生するキユウリに >前記製剤実施例 2に示 された乳剤の処方に従い、化合物濃度が 1 2 5 p pmになるように水で希釈した薬液を 散布した。温度 2 5で、湿度 6 5 %の恒温室内に置き, 6日後に殺虫率を調査した。試験 は 2反復である。その結果,化合物番号 1— 26、 2 - 6 、 2 - 2 5 、 2 ― 2 6 、 2 - 2
7、 2— 2 8、 2 - 33、 2 - 34、 2 - 4 1、 2 - 4 3 、 2 -4 9 、 2 ― 5 6 、 2 -
5 9、 2 - 60、 2— 6 5、 2 - 68、 2 - 6 9、 2— 7 0、 2 - 7 1 、 2 ― 7 6、 2 一 7 7、 2— 8 1、 2— 8 9、 2 - 1 2 2、 3— 7 0、 3 — 8 5、 3 ― 8 8 、 3 — 90、
3— 1 0 1、 3— 1 0 2、 3— 1 0 3、 3 - 1 04、 3 ― 1 2 3、 3 ― 1 2 4 、 4 - 1
0、 4一 1 1、 4一 1 6、 4一 2 7、 4一 33、 4 -4 5 、 4 -4 9 、 4 ― 5 8 、 4 -
59、 4一 6 0、 4一 6 1、 4一 6 2、 4- 64, 4一 6 5、 4一 6 6 、 4 ― 6 7、 4 一 6 9、 4一 7 0、 4— 7 5、 4一 7 6、 4一 7 7、 4 ― 7 9, 4 ― 8 1 、 4 ― 8 2、
4一 83、 4一 84、 4一 8 5、 4— 86、 4一 87、 4一 8 8、 4 ― 8 9 、 4一 9 1、
4— 9 2、 4一 9 5、 4一 1 04、 4一 1 0 5、 4— 1 0 6、 4一 1 0 7 、 4 ― 1 0 8、
4— 1 0 9、 4一 1 1 1、 4— 1 1 2、 4— 1 1 5、 4 ― 1 3 8、 4 ― 1 3 9 、 4 - 1
42、 4 - 148, 4一 149、 4- 1 5 1, 4一 1 5 2 , 4 - 1 5 3 、 4 ― 1 54、
4— 1 6 2、 4一 1 64、 4— 1 66、 4一 1 6 8、 4 ― 1 7 3、 4 ― 1 7 4 、 4 - 1
7 5、 4一 1 76、 4— 1 7 7、 4— 1 7 8、 4一 1 7 9 、 4— 1 8 2 、 4 ― 1 8 3、
4— 1 8 5、 4— 1 86、 4一 2 0 7、 4一 2 1 0、 4 ― 2 1 2、 4 ― 2 2 2 、 4 - 2
2 3、 、4— 2 2 7、 4— 2 2 9、 4— 2 30、 4— 2 3 2 、 4 - 2 3 3 、 4 ― 2 40、
4— 2 54、 4一 260、 4— 2 64、 4— 2 8 7、 4 ― 2 90、 4 ― 2 9 2 、 4 - 2
94、 4一 2 9 7、 4一 30 7、 4— 3 1 8、 4一 3 2 8 、 4 - 3 3 0 、 4 ― 3 3 2、
4一 3 34、 4— 3 74、 4— 40 7、 4— 409、 4 ― 4 1 6、 4 ― 4 2 2 4 -4
2 3、 4— 4 24、 4— 4 30、 4— 432、 4— 44 9 、 4 -4 5 3 、 4 ― 4 54、
4— 4 56、 4— 46 7、 4一 469、 4一 47 5、 4 ― 48 2、 4 ― 4 9 5 、 4 -4
96、 4一 497、 4一 5 1 3、 4— 5 1 5、 4— 5 2 4 、 4 - 5 2 6 、 4 ― 5 2 7、
4— 5 39、 4— 544、 4— 547、 4一 549、 4 ― 5 5 2、 4 ― 5 5 3 、 4 - 5
54、 4— 5 56、 4— 5 57、 4一 5 59、 4— 5 7 0 、 4— 5 7 2 、 4 ― 5 7 3、
4一 6 0 3、 4一 6 04、 4一 6 04、 4一 6 0 5、 4 ― 6 0 6、 4 ― 6 1 3 、 4 - 6
1 5、 4— 6 1 8、 4一 6 1 9、 5— 2、 5— 1 0、 5 ― 14、 5 ― 1 8 、 5一 1 9、
5 - 2 0の化合物が 1 0 0 %の殺虫率を示した。 なお、対照に用いたピリ 力 ブは 1
2 5 p pmで 6 %の殺虫率であった。 試験例 8 ナミハダ二に対する効力試験
3寸鉢に播種したインゲンの発芽後 7〜 1 0日を経過した第 1本葉上に、有機リン剤 抵抗性のナミハダ二雌成虫を 1 5頭接種したのち、 前記製剤実施例 1 に示された水和 剤の処方に従い、化合物濃度が 1 2 5 p pmになるように水で希釈した薬液を散布した。
温度 25t:、 湿度 65%の恒温室内に置き、 3日後に殺成虫率を調査した。試験は 2反 復である。 その結果,化合物番号 2— 77、 4— 68、 4— 79、 4— 109、 4— 1 74、 4—176、 4一 178、 4— 179、 4一 222、 4— 223、 4— 240、 4— 2.54、 4— 260、 4— 264、 4一 287、 4— 332、 4— 334、 4-4 13、 4— 554、 4一 593、 4一 594、 4— 609、 4一 610、 5— 14の化 合物が 100%の殺成虫率を示した。なお、対照に用いたクロルジメフオルムは 125 p pmで 13 %の殺成虫率であった。 産業上の利用可能性:
式 (1) で表されるァリール複素環誘導体またはその塩は農園芸用殺菌剤または農園芸 用殺虫剤として優れた効果を示す。