RU2772214C2 - Functionalized saccharides as anti-inflammatory agents - Google Patents
Functionalized saccharides as anti-inflammatory agents Download PDFInfo
- Publication number
- RU2772214C2 RU2772214C2 RU2019136874A RU2019136874A RU2772214C2 RU 2772214 C2 RU2772214 C2 RU 2772214C2 RU 2019136874 A RU2019136874 A RU 2019136874A RU 2019136874 A RU2019136874 A RU 2019136874A RU 2772214 C2 RU2772214 C2 RU 2772214C2
- Authority
- RU
- Russia
- Prior art keywords
- inflammatory
- group
- compound
- disease
- cytokine
- Prior art date
Links
- 229940121363 anti-inflammatory agent Drugs 0.000 title claims abstract description 10
- 239000002260 anti-inflammatory agent Substances 0.000 title claims abstract description 10
- 150000001720 carbohydrates Chemical class 0.000 title abstract description 19
- 150000001875 compounds Chemical class 0.000 claims abstract description 124
- 102000004127 Cytokines Human genes 0.000 claims abstract description 61
- 108090000695 Cytokines Proteins 0.000 claims abstract description 61
- 230000004054 inflammatory process Effects 0.000 claims abstract description 49
- 206010061218 Inflammation Diseases 0.000 claims abstract description 48
- 230000014509 gene expression Effects 0.000 claims abstract description 32
- 238000000034 method Methods 0.000 claims abstract description 25
- 241000124008 Mammalia Species 0.000 claims abstract description 19
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 19
- 230000007246 mechanism Effects 0.000 claims abstract description 9
- 238000001727 in vivo Methods 0.000 claims abstract description 5
- 230000003110 anti-inflammatory effect Effects 0.000 claims description 107
- -1 oncostatin Proteins 0.000 claims description 30
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 26
- 150000003839 salts Chemical class 0.000 claims description 25
- 201000010099 disease Diseases 0.000 claims description 24
- 102100037850 Interferon gamma Human genes 0.000 claims description 23
- 108010074328 Interferon-gamma Proteins 0.000 claims description 23
- 102000004890 Interleukin-8 Human genes 0.000 claims description 22
- 108090001007 Interleukin-8 Proteins 0.000 claims description 22
- 239000000203 mixture Substances 0.000 claims description 21
- 208000007882 Gastritis Diseases 0.000 claims description 20
- 208000007107 Stomach Ulcer Diseases 0.000 claims description 13
- 208000027866 inflammatory disease Diseases 0.000 claims description 13
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims description 10
- 102000003814 Interleukin-10 Human genes 0.000 claims description 10
- 108090000174 Interleukin-10 Proteins 0.000 claims description 10
- 102000013264 Interleukin-23 Human genes 0.000 claims description 10
- 108010065637 Interleukin-23 Proteins 0.000 claims description 10
- 102000004388 Interleukin-4 Human genes 0.000 claims description 10
- 108090000978 Interleukin-4 Proteins 0.000 claims description 10
- 102000004889 Interleukin-6 Human genes 0.000 claims description 10
- 108090001005 Interleukin-6 Proteins 0.000 claims description 10
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 10
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 10
- 230000002401 inhibitory effect Effects 0.000 claims description 10
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 9
- 102000013691 Interleukin-17 Human genes 0.000 claims description 9
- 108050003558 Interleukin-17 Proteins 0.000 claims description 9
- 208000023652 chronic gastritis Diseases 0.000 claims description 8
- 230000028709 inflammatory response Effects 0.000 claims description 8
- 239000002552 dosage form Substances 0.000 claims description 7
- 239000003937 drug carrier Substances 0.000 claims description 7
- 102100021943 C-C motif chemokine 2 Human genes 0.000 claims description 6
- 101710155857 C-C motif chemokine 2 Proteins 0.000 claims description 6
- 102100032367 C-C motif chemokine 5 Human genes 0.000 claims description 6
- 102100036150 C-X-C motif chemokine 5 Human genes 0.000 claims description 6
- 241000283707 Capra Species 0.000 claims description 6
- 108010055166 Chemokine CCL5 Proteins 0.000 claims description 6
- 108010014419 Chemokine CXCL1 Proteins 0.000 claims description 6
- 102000016950 Chemokine CXCL1 Human genes 0.000 claims description 6
- 102000019034 Chemokines Human genes 0.000 claims description 6
- 108010012236 Chemokines Proteins 0.000 claims description 6
- 101000947186 Homo sapiens C-X-C motif chemokine 5 Proteins 0.000 claims description 6
- 102100026720 Interferon beta Human genes 0.000 claims description 6
- 108090000467 Interferon-beta Proteins 0.000 claims description 6
- 102000003815 Interleukin-11 Human genes 0.000 claims description 6
- 108090000177 Interleukin-11 Proteins 0.000 claims description 6
- 102000013462 Interleukin-12 Human genes 0.000 claims description 6
- 108010065805 Interleukin-12 Proteins 0.000 claims description 6
- 102000000588 Interleukin-2 Human genes 0.000 claims description 6
- 108010002350 Interleukin-2 Proteins 0.000 claims description 6
- 102000000646 Interleukin-3 Human genes 0.000 claims description 6
- 108010002386 Interleukin-3 Proteins 0.000 claims description 6
- 102000000704 Interleukin-7 Human genes 0.000 claims description 6
- 108010002586 Interleukin-7 Proteins 0.000 claims description 6
- 102000000585 Interleukin-9 Human genes 0.000 claims description 6
- 108010002335 Interleukin-9 Proteins 0.000 claims description 6
- 241000283973 Oryctolagus cuniculus Species 0.000 claims description 6
- 201000005917 gastric ulcer Diseases 0.000 claims description 6
- 230000000770 proinflammatory effect Effects 0.000 claims description 6
- 239000000725 suspension Substances 0.000 claims description 6
- 201000000596 systemic lupus erythematosus Diseases 0.000 claims description 6
- 108010047761 Interferon-alpha Proteins 0.000 claims description 5
- 102000006992 Interferon-alpha Human genes 0.000 claims description 5
- 102000003810 Interleukin-18 Human genes 0.000 claims description 5
- 108090000171 Interleukin-18 Proteins 0.000 claims description 5
- 101710151805 Mitochondrial intermediate peptidase 1 Proteins 0.000 claims description 5
- 102000004887 Transforming Growth Factor beta Human genes 0.000 claims description 5
- 108090001012 Transforming Growth Factor beta Proteins 0.000 claims description 5
- 239000002775 capsule Substances 0.000 claims description 5
- 230000001404 mediated effect Effects 0.000 claims description 5
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 claims description 5
- 239000000843 powder Substances 0.000 claims description 5
- 239000003826 tablet Substances 0.000 claims description 5
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 claims description 5
- 208000011231 Crohn disease Diseases 0.000 claims description 4
- 102000004083 Lymphotoxin-alpha Human genes 0.000 claims description 4
- 108090000542 Lymphotoxin-alpha Proteins 0.000 claims description 4
- 208000001647 Renal Insufficiency Diseases 0.000 claims description 4
- 238000011161 development Methods 0.000 claims description 4
- 201000006370 kidney failure Diseases 0.000 claims description 4
- 206010002556 Ankylosing Spondylitis Diseases 0.000 claims description 3
- 208000003017 Aortic Valve Stenosis Diseases 0.000 claims description 3
- 201000001320 Atherosclerosis Diseases 0.000 claims description 3
- 206010007559 Cardiac failure congestive Diseases 0.000 claims description 3
- 206010009900 Colitis ulcerative Diseases 0.000 claims description 3
- 206010010744 Conjunctivitis allergic Diseases 0.000 claims description 3
- 201000004624 Dermatitis Diseases 0.000 claims description 3
- 206010012689 Diabetic retinopathy Diseases 0.000 claims description 3
- 208000001640 Fibromyalgia Diseases 0.000 claims description 3
- 206010016654 Fibrosis Diseases 0.000 claims description 3
- 208000018522 Gastrointestinal disease Diseases 0.000 claims description 3
- 206010018364 Glomerulonephritis Diseases 0.000 claims description 3
- 206010019280 Heart failures Diseases 0.000 claims description 3
- 206010020751 Hypersensitivity Diseases 0.000 claims description 3
- 206010024229 Leprosy Diseases 0.000 claims description 3
- 208000019693 Lung disease Diseases 0.000 claims description 3
- 206010033645 Pancreatitis Diseases 0.000 claims description 3
- 201000004681 Psoriasis Diseases 0.000 claims description 3
- 241000283984 Rodentia Species 0.000 claims description 3
- 206010039710 Scleroderma Diseases 0.000 claims description 3
- 208000021386 Sjogren Syndrome Diseases 0.000 claims description 3
- 208000006011 Stroke Diseases 0.000 claims description 3
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 claims description 3
- 201000006704 Ulcerative Colitis Diseases 0.000 claims description 3
- 206010046851 Uveitis Diseases 0.000 claims description 3
- 208000002205 allergic conjunctivitis Diseases 0.000 claims description 3
- 230000007815 allergy Effects 0.000 claims description 3
- 206010002906 aortic stenosis Diseases 0.000 claims description 3
- 206010003246 arthritis Diseases 0.000 claims description 3
- 208000024998 atopic conjunctivitis Diseases 0.000 claims description 3
- 238000002512 chemotherapy Methods 0.000 claims description 3
- 208000016097 disease of metabolism Diseases 0.000 claims description 3
- 230000004761 fibrosis Effects 0.000 claims description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 claims description 3
- 208000002551 irritable bowel syndrome Diseases 0.000 claims description 3
- 208000019423 liver disease Diseases 0.000 claims description 3
- 208000030159 metabolic disease Diseases 0.000 claims description 3
- 201000006417 multiple sclerosis Diseases 0.000 claims description 3
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 3
- 239000006187 pill Substances 0.000 claims description 3
- 238000001959 radiotherapy Methods 0.000 claims description 3
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 3
- 241000283690 Bos taurus Species 0.000 claims description 2
- 241000282836 Camelus dromedarius Species 0.000 claims description 2
- 241000282326 Felis catus Species 0.000 claims description 2
- 241000282849 Ruminantia Species 0.000 claims description 2
- 208000026935 allergic disease Diseases 0.000 claims description 2
- 239000007943 implant Substances 0.000 claims description 2
- 238000007911 parenteral administration Methods 0.000 claims description 2
- 239000000829 suppository Substances 0.000 claims description 2
- 230000000747 cardiac effect Effects 0.000 claims 1
- 208000019553 vascular disease Diseases 0.000 claims 1
- 241001465754 Metazoa Species 0.000 abstract description 31
- 239000003814 drug Substances 0.000 abstract description 19
- 230000000694 effects Effects 0.000 abstract description 14
- 239000000126 substance Substances 0.000 abstract description 6
- 230000004044 response Effects 0.000 abstract description 4
- 230000001629 suppression Effects 0.000 abstract description 3
- 230000005764 inhibitory process Effects 0.000 abstract 2
- 230000002884 effect on inflammation Effects 0.000 abstract 1
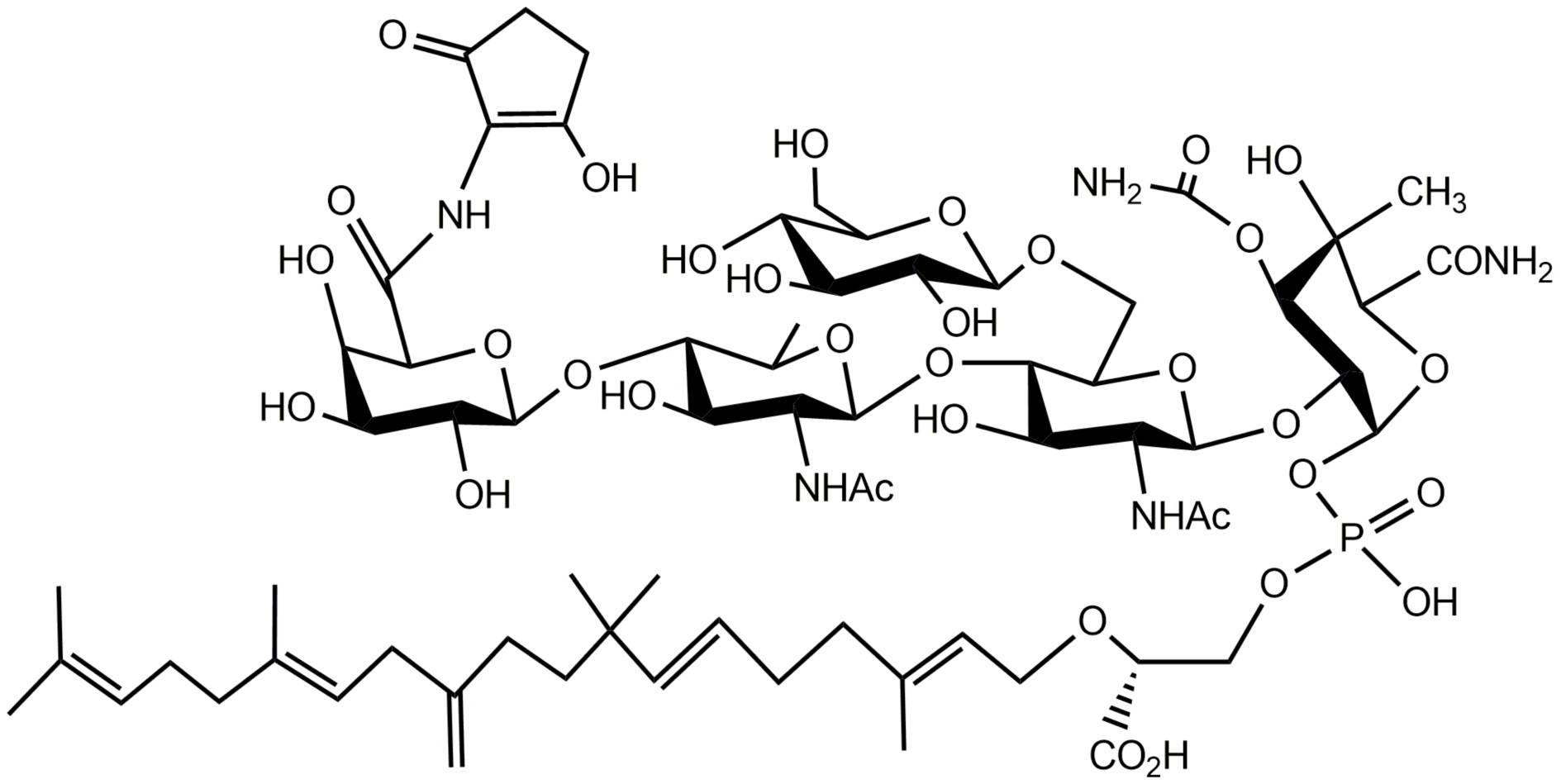
- PERZMHJGZKHNGU-JGYWJTCASA-N bambermycin Chemical compound O([C@H]1[C@H](NC(C)=O)[C@@H](O)[C@@H]([C@H](O1)CO[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@@H]1O[C@@H]([C@H]([C@H](O)[C@H]1NC(C)=O)O[C@H]1[C@@H]([C@@H](O)[C@@H](O)[C@H](O1)C(=O)NC=1C(CCC=1O)=O)O)C)[C@H]1[C@@H](OP(O)(=O)OC[C@@H](OC\C=C(/C)CC\C=C\C(C)(C)CCC(=C)C\C=C(/C)CCC=C(C)C)C(O)=O)O[C@H](C(O)=O)[C@@](C)(O)[C@@H]1OC(N)=O PERZMHJGZKHNGU-JGYWJTCASA-N 0.000 description 66
- 229910052739 hydrogen Inorganic materials 0.000 description 62
- 125000000217 alkyl group Chemical group 0.000 description 47
- 125000003118 aryl group Chemical group 0.000 description 44
- 125000001931 aliphatic group Chemical group 0.000 description 42
- 235000019374 flavomycin Nutrition 0.000 description 39
- 125000001072 heteroaryl group Chemical group 0.000 description 35
- 239000004181 Flavomycin Substances 0.000 description 34
- 241001490623 Helicobacter suis Species 0.000 description 28
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 28
- 125000006239 protecting group Chemical group 0.000 description 27
- 108020004414 DNA Proteins 0.000 description 21
- 241000699670 Mus sp. Species 0.000 description 19
- 230000000052 comparative effect Effects 0.000 description 19
- 125000004432 carbon atom Chemical group C* 0.000 description 18
- 210000004027 cell Anatomy 0.000 description 17
- 238000002474 experimental method Methods 0.000 description 17
- 108091034117 Oligonucleotide Proteins 0.000 description 15
- 125000003342 alkenyl group Chemical group 0.000 description 14
- 229910052799 carbon Inorganic materials 0.000 description 14
- 210000001744 T-lymphocyte Anatomy 0.000 description 13
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 13
- 235000005911 diet Nutrition 0.000 description 13
- 230000037213 diet Effects 0.000 description 13
- 208000015181 infectious disease Diseases 0.000 description 13
- 210000002540 macrophage Anatomy 0.000 description 12
- 210000001711 oxyntic cell Anatomy 0.000 description 12
- 230000002441 reversible effect Effects 0.000 description 12
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 11
- WQZGKKKJIJFFOK-SVZMEOIVSA-N (+)-Galactose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-SVZMEOIVSA-N 0.000 description 10
- 238000011529 RT qPCR Methods 0.000 description 10
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 10
- 125000000753 cycloalkyl group Chemical group 0.000 description 10
- 229940079593 drug Drugs 0.000 description 10
- 230000002055 immunohistochemical effect Effects 0.000 description 10
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 10
- 210000002784 stomach Anatomy 0.000 description 10
- 239000002253 acid Substances 0.000 description 9
- 210000003719 b-lymphocyte Anatomy 0.000 description 9
- 125000000304 alkynyl group Chemical group 0.000 description 8
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- SHZGCJCMOBCMKK-UHFFFAOYSA-N D-mannomethylose Natural products CC1OC(O)C(O)C(O)C1O SHZGCJCMOBCMKK-UHFFFAOYSA-N 0.000 description 7
- PNNNRSAQSRJVSB-UHFFFAOYSA-N L-rhamnose Natural products CC(O)C(O)C(O)C(O)C=O PNNNRSAQSRJVSB-UHFFFAOYSA-N 0.000 description 7
- 239000002585 base Substances 0.000 description 7
- 230000002496 gastric effect Effects 0.000 description 7
- 150000002430 hydrocarbons Chemical class 0.000 description 7
- 150000002632 lipids Chemical class 0.000 description 7
- 230000001338 necrotic effect Effects 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 239000012453 solvate Substances 0.000 description 7
- 239000004480 active ingredient Substances 0.000 description 6
- PYMYPHUHKUWMLA-LMVFSUKVSA-N aldehydo-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 6
- 125000003545 alkoxy group Chemical group 0.000 description 6
- 125000003277 amino group Chemical group 0.000 description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 6
- 230000037456 inflammatory mechanism Effects 0.000 description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 6
- 229910052757 nitrogen Inorganic materials 0.000 description 6
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 230000009469 supplementation Effects 0.000 description 6
- WQZGKKKJIJFFOK-IVMDWMLBSA-N D-allopyranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-IVMDWMLBSA-N 0.000 description 5
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 5
- 108010091358 Hypoxanthine Phosphoribosyltransferase Proteins 0.000 description 5
- 102100029098 Hypoxanthine-guanine phosphoribosyltransferase Human genes 0.000 description 5
- GZCGUPFRVQAUEE-ZXXMMSQZSA-N aldehydo-D-idose Chemical compound OC[C@@H](O)[C@H](O)[C@@H](O)[C@H](O)C=O GZCGUPFRVQAUEE-ZXXMMSQZSA-N 0.000 description 5
- GZCGUPFRVQAUEE-KAZBKCHUSA-N aldehydo-D-talose Chemical compound OC[C@@H](O)[C@H](O)[C@H](O)[C@H](O)C=O GZCGUPFRVQAUEE-KAZBKCHUSA-N 0.000 description 5
- 229950007118 bambermycin Drugs 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 235000000891 standard diet Nutrition 0.000 description 5
- 125000001424 substituent group Chemical group 0.000 description 5
- 229910052717 sulfur Inorganic materials 0.000 description 5
- 206010002091 Anaesthesia Diseases 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical group N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- WQZGKKKJIJFFOK-RSVSWTKNSA-N D-altro-hexose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-RSVSWTKNSA-N 0.000 description 4
- ZAQJHHRNXZUBTE-UHFFFAOYSA-N D-threo-2-Pentulose Natural products OCC(O)C(O)C(=O)CO ZAQJHHRNXZUBTE-UHFFFAOYSA-N 0.000 description 4
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 4
- SHZGCJCMOBCMKK-PQMKYFCFSA-N L-Fucose Natural products C[C@H]1O[C@H](O)[C@@H](O)[C@@H](O)[C@@H]1O SHZGCJCMOBCMKK-PQMKYFCFSA-N 0.000 description 4
- ZAQJHHRNXZUBTE-UCORVYFPSA-N L-ribulose Chemical compound OC[C@H](O)[C@H](O)C(=O)CO ZAQJHHRNXZUBTE-UCORVYFPSA-N 0.000 description 4
- 150000001299 aldehydes Chemical class 0.000 description 4
- 230000037005 anaesthesia Effects 0.000 description 4
- 239000000427 antigen Substances 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 150000004820 halides Chemical class 0.000 description 4
- 210000000987 immune system Anatomy 0.000 description 4
- 238000011532 immunohistochemical staining Methods 0.000 description 4
- 230000009545 invasion Effects 0.000 description 4
- 229960002725 isoflurane Drugs 0.000 description 4
- 150000002576 ketones Chemical class 0.000 description 4
- 230000007774 longterm Effects 0.000 description 4
- 230000007170 pathology Effects 0.000 description 4
- 238000011002 quantification Methods 0.000 description 4
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 3
- YTBSYETUWUMLBZ-UHFFFAOYSA-N D-Erythrose Natural products OCC(O)C(O)C=O YTBSYETUWUMLBZ-UHFFFAOYSA-N 0.000 description 3
- RFSUNEUAIZKAJO-VRPWFDPXSA-N D-Fructose Natural products OC[C@H]1OC(O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-VRPWFDPXSA-N 0.000 description 3
- WQZGKKKJIJFFOK-CBPJZXOFSA-N D-Gulose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-CBPJZXOFSA-N 0.000 description 3
- YTBSYETUWUMLBZ-IUYQGCFVSA-N D-erythrose Chemical compound OC[C@@H](O)[C@@H](O)C=O YTBSYETUWUMLBZ-IUYQGCFVSA-N 0.000 description 3
- UQPHVQVXLPRNCX-GSVOUGTGSA-N D-erythrulose Chemical compound OC[C@@H](O)C(=O)CO UQPHVQVXLPRNCX-GSVOUGTGSA-N 0.000 description 3
- SHZGCJCMOBCMKK-SVZMEOIVSA-N D-fucopyranose Chemical compound C[C@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O SHZGCJCMOBCMKK-SVZMEOIVSA-N 0.000 description 3
- 125000002353 D-glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 3
- BJHIKXHVCXFQLS-PUFIMZNGSA-N D-psicose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)C(=O)CO BJHIKXHVCXFQLS-PUFIMZNGSA-N 0.000 description 3
- LKDRXBCSQODPBY-IANNHFEVSA-N D-sorbose Chemical compound OCC1(O)OC[C@@H](O)[C@H](O)[C@H]1O LKDRXBCSQODPBY-IANNHFEVSA-N 0.000 description 3
- YTBSYETUWUMLBZ-QWWZWVQMSA-N D-threose Chemical compound OC[C@@H](O)[C@H](O)C=O YTBSYETUWUMLBZ-QWWZWVQMSA-N 0.000 description 3
- ZAQJHHRNXZUBTE-WUJLRWPWSA-N D-xylulose Chemical compound OC[C@@H](O)[C@H](O)C(=O)CO ZAQJHHRNXZUBTE-WUJLRWPWSA-N 0.000 description 3
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 3
- 101150059913 H2az1 gene Proteins 0.000 description 3
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 3
- SRBFZHDQGSBBOR-OWMBCFKOSA-N L-ribopyranose Chemical compound O[C@H]1COC(O)[C@@H](O)[C@H]1O SRBFZHDQGSBBOR-OWMBCFKOSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- BQDKZHDWNDUYAG-UHFFFAOYSA-N N-nitramidooxynitramide Chemical compound [O-][N+](=O)NON[N+]([O-])=O BQDKZHDWNDUYAG-UHFFFAOYSA-N 0.000 description 3
- 101150056612 PPIA gene Proteins 0.000 description 3
- 238000010240 RT-PCR analysis Methods 0.000 description 3
- 208000025865 Ulcer Diseases 0.000 description 3
- SRBFZHDQGSBBOR-STGXQOJASA-N alpha-D-lyxopyranose Chemical compound O[C@@H]1CO[C@H](O)[C@@H](O)[C@H]1O SRBFZHDQGSBBOR-STGXQOJASA-N 0.000 description 3
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 208000020832 chronic kidney disease Diseases 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000000392 cycloalkenyl group Chemical group 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 229910052736 halogen Inorganic materials 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 125000004404 heteroalkyl group Chemical group 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 3
- 230000008595 infiltration Effects 0.000 description 3
- 238000001764 infiltration Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 3
- 230000000813 microbial effect Effects 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 229940126409 proton pump inhibitor Drugs 0.000 description 3
- 239000000612 proton pump inhibitor Substances 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 238000012163 sequencing technique Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 231100000397 ulcer Toxicity 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- AQQSXKSWTNWXKR-UHFFFAOYSA-N 2-(2-phenylphenanthro[9,10-d]imidazol-3-yl)acetic acid Chemical compound C1(=CC=CC=C1)C1=NC2=C(N1CC(=O)O)C1=CC=CC=C1C=1C=CC=CC=12 AQQSXKSWTNWXKR-UHFFFAOYSA-N 0.000 description 2
- 108091006112 ATPases Proteins 0.000 description 2
- 102000057290 Adenosine Triphosphatases Human genes 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 108020000946 Bacterial DNA Proteins 0.000 description 2
- 208000024172 Cardiovascular disease Diseases 0.000 description 2
- 102000003952 Caspase 3 Human genes 0.000 description 2
- 108090000397 Caspase 3 Proteins 0.000 description 2
- LKDRXBCSQODPBY-OEXCPVAWSA-N D-tagatose Chemical compound OCC1(O)OC[C@@H](O)[C@H](O)[C@@H]1O LKDRXBCSQODPBY-OEXCPVAWSA-N 0.000 description 2
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 241000589989 Helicobacter Species 0.000 description 2
- 206010019375 Helicobacter infections Diseases 0.000 description 2
- 241000590002 Helicobacter pylori Species 0.000 description 2
- 102100023919 Histone H2A.Z Human genes 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000905054 Homo sapiens Histone H2A.Z Proteins 0.000 description 2
- 101001067833 Homo sapiens Peptidyl-prolyl cis-trans isomerase A Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 102100034539 Peptidyl-prolyl cis-trans isomerase A Human genes 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical group [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- 208000036142 Viral infection Diseases 0.000 description 2
- GPKUGWDQUVWHIC-UHFFFAOYSA-N [4-(4-hydrazinylphenyl)phenyl]hydrazine tetrahydrochloride Chemical compound Cl.Cl.Cl.Cl.NNC1=CC=C(C=C1)C1=CC=C(NN)C=C1 GPKUGWDQUVWHIC-UHFFFAOYSA-N 0.000 description 2
- LXKFVPKKRVKNIJ-MCDZGGTQSA-N [K].C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O Chemical compound [K].C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O LXKFVPKKRVKNIJ-MCDZGGTQSA-N 0.000 description 2
- 125000002015 acyclic group Chemical group 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 229940124599 anti-inflammatory drug Drugs 0.000 description 2
- 230000001640 apoptogenic effect Effects 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- GZUXJHMPEANEGY-UHFFFAOYSA-N bromomethane Chemical compound BrC GZUXJHMPEANEGY-UHFFFAOYSA-N 0.000 description 2
- 125000002843 carboxylic acid group Chemical group 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 208000037976 chronic inflammation Diseases 0.000 description 2
- 230000006020 chronic inflammation Effects 0.000 description 2
- 125000006165 cyclic alkyl group Chemical group 0.000 description 2
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 230000002526 effect on cardiovascular system Effects 0.000 description 2
- 230000008029 eradication Effects 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 238000011081 inoculation Methods 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 150000002892 organic cations Chemical class 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 239000011574 phosphorus Chemical group 0.000 description 2
- 238000003753 real-time PCR Methods 0.000 description 2
- 125000006413 ring segment Chemical group 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 229930195734 saturated hydrocarbon Natural products 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 239000011593 sulfur Chemical group 0.000 description 2
- 230000009385 viral infection Effects 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- CFXAVQUXSYFPDE-ZDVKUAOASA-N (2r,3r,4s,5s,6r)-2-[(2s,3s,4r,5r)-4-hydroxy-2,5-bis(hydroxymethyl)-2-[(2r,3r,4s,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxyoxolan-3-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol;hydrate Chemical compound O.O([C@@]1(O[C@@H]([C@H]([C@@H]1O[C@@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O)CO)CO)[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O CFXAVQUXSYFPDE-ZDVKUAOASA-N 0.000 description 1
- 125000006727 (C1-C6) alkenyl group Chemical group 0.000 description 1
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 description 1
- FTNJQNQLEGKTGD-UHFFFAOYSA-N 1,3-benzodioxole Chemical compound C1=CC=C2OCOC2=C1 FTNJQNQLEGKTGD-UHFFFAOYSA-N 0.000 description 1
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- ALKYHXVLJMQRLQ-UHFFFAOYSA-M 3-carboxynaphthalen-2-olate Chemical compound C1=CC=C2C=C(C([O-])=O)C(O)=CC2=C1 ALKYHXVLJMQRLQ-UHFFFAOYSA-M 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 108091093088 Amplicon Proteins 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 238000011725 BALB/c mouse Methods 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 208000027932 Collagen disease Diseases 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- SRBFZHDQGSBBOR-SOOFDHNKSA-N D-ribopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@@H]1O SRBFZHDQGSBBOR-SOOFDHNKSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 206010054272 Helicobacter gastritis Diseases 0.000 description 1
- 241000069681 Helicobacter suis HS5 Species 0.000 description 1
- 208000009889 Herpes Simplex Diseases 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- LKDRXBCSQODPBY-AMVSKUEXSA-N L-(-)-Sorbose Chemical compound OCC1(O)OC[C@H](O)[C@@H](O)[C@@H]1O LKDRXBCSQODPBY-AMVSKUEXSA-N 0.000 description 1
- YTBSYETUWUMLBZ-DMTCNVIQSA-N L-erythrose Chemical compound OC[C@H](O)[C@H](O)C=O YTBSYETUWUMLBZ-DMTCNVIQSA-N 0.000 description 1
- UQPHVQVXLPRNCX-VKHMYHEASA-N L-erythrulose Chemical compound OC[C@H](O)C(=O)CO UQPHVQVXLPRNCX-VKHMYHEASA-N 0.000 description 1
- LKDRXBCSQODPBY-NSHGFSBMSA-N L-fructose Chemical compound OCC1(O)OC[C@H](O)[C@H](O)[C@H]1O LKDRXBCSQODPBY-NSHGFSBMSA-N 0.000 description 1
- SHZGCJCMOBCMKK-DHVFOXMCSA-N L-fucopyranose Chemical compound C[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O SHZGCJCMOBCMKK-DHVFOXMCSA-N 0.000 description 1
- WQZGKKKJIJFFOK-DHVFOXMCSA-N L-galactose Chemical compound OC[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-DHVFOXMCSA-N 0.000 description 1
- WQZGKKKJIJFFOK-ZZWDRFIYSA-N L-glucose Chemical compound OC[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-ZZWDRFIYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-QRXFDPRISA-N L-gulose Chemical compound OC[C@@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QRXFDPRISA-N 0.000 description 1
- WQZGKKKJIJFFOK-ZNVMLXAYSA-N L-idopyranose Chemical compound OC[C@@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-ZNVMLXAYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-JFNONXLTSA-N L-mannopyranose Chemical compound OC[C@@H]1OC(O)[C@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-JFNONXLTSA-N 0.000 description 1
- BJHIKXHVCXFQLS-ZXEDONINSA-N L-psicose Chemical compound OC[C@H](O)[C@H](O)[C@H](O)C(=O)CO BJHIKXHVCXFQLS-ZXEDONINSA-N 0.000 description 1
- YTBSYETUWUMLBZ-IMJSIDKUSA-N L-threose Chemical compound OC[C@H](O)[C@@H](O)C=O YTBSYETUWUMLBZ-IMJSIDKUSA-N 0.000 description 1
- ZAQJHHRNXZUBTE-WVZVXSGGSA-N L-xylulose Chemical compound OC[C@H](O)[C@@H](O)C(=O)CO ZAQJHHRNXZUBTE-WVZVXSGGSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 101100117488 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) mip-1 gene Proteins 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 206010029719 Nonspecific reaction Diseases 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 208000037273 Pathologic Processes Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 208000008469 Peptic Ulcer Diseases 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 238000011530 RNeasy Mini Kit Methods 0.000 description 1
- MUPFEKGTMRGPLJ-RMMQSMQOSA-N Raffinose Natural products O(C[C@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](O[C@@]2(CO)[C@H](O)[C@@H](O)[C@@H](CO)O2)O1)[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 MUPFEKGTMRGPLJ-RMMQSMQOSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 241001646618 Streptomyces ederensis Species 0.000 description 1
- 241000971019 Streptomyces geysiriensis Species 0.000 description 1
- 241000946809 Streptomyces prasinus Species 0.000 description 1
- 241000948169 Streptomyces viridosporus Species 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 239000008049 TAE buffer Substances 0.000 description 1
- 229920002253 Tannate Polymers 0.000 description 1
- 108010006785 Taq Polymerase Proteins 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- MUPFEKGTMRGPLJ-UHFFFAOYSA-N UNPD196149 Natural products OC1C(O)C(CO)OC1(CO)OC1C(O)C(O)C(O)C(COC2C(C(O)C(O)C(CO)O2)O)O1 MUPFEKGTMRGPLJ-UHFFFAOYSA-N 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 1
- HGEVZDLYZYVYHD-UHFFFAOYSA-N acetic acid;2-amino-2-(hydroxymethyl)propane-1,3-diol;2-[2-[bis(carboxymethyl)amino]ethyl-(carboxymethyl)amino]acetic acid Chemical compound CC(O)=O.OCC(N)(CO)CO.OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O HGEVZDLYZYVYHD-UHFFFAOYSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 229920002877 acrylic styrene acrylonitrile Polymers 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 230000006022 acute inflammation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- PYMYPHUHKUWMLA-VPENINKCSA-N aldehydo-D-xylose Chemical compound OC[C@@H](O)[C@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-VPENINKCSA-N 0.000 description 1
- GZCGUPFRVQAUEE-MOJAZDJTSA-N aldehydo-L-allose Chemical compound OC[C@H](O)[C@H](O)[C@H](O)[C@H](O)C=O GZCGUPFRVQAUEE-MOJAZDJTSA-N 0.000 description 1
- GZCGUPFRVQAUEE-AZGQCCRYSA-N aldehydo-L-altrose Chemical compound OC[C@H](O)[C@H](O)[C@H](O)[C@@H](O)C=O GZCGUPFRVQAUEE-AZGQCCRYSA-N 0.000 description 1
- PYMYPHUHKUWMLA-YUPRTTJUSA-N aldehydo-L-lyxose Chemical compound OC[C@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-YUPRTTJUSA-N 0.000 description 1
- PNNNRSAQSRJVSB-BXKVDMCESA-N aldehydo-L-rhamnose Chemical compound C[C@H](O)[C@H](O)[C@@H](O)[C@@H](O)C=O PNNNRSAQSRJVSB-BXKVDMCESA-N 0.000 description 1
- PYMYPHUHKUWMLA-MROZADKFSA-N aldehydo-L-ribose Chemical compound OC[C@H](O)[C@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-MROZADKFSA-N 0.000 description 1
- GZCGUPFRVQAUEE-OMMKOOBNSA-N aldehydo-L-talose Chemical compound OC[C@H](O)[C@@H](O)[C@@H](O)[C@@H](O)C=O GZCGUPFRVQAUEE-OMMKOOBNSA-N 0.000 description 1
- PYMYPHUHKUWMLA-WISUUJSJSA-N aldehydo-L-xylose Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WISUUJSJSA-N 0.000 description 1
- 229930195726 aldehydo-L-xylose Natural products 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 239000003674 animal food additive Substances 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 230000004596 appetite loss Effects 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 210000000941 bile Anatomy 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 238000010805 cDNA synthesis kit Methods 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 239000002458 cell surface marker Substances 0.000 description 1
- 239000013043 chemical agent Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- VDANGULDQQJODZ-UHFFFAOYSA-N chloroprocaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1Cl VDANGULDQQJODZ-UHFFFAOYSA-N 0.000 description 1
- 229960002023 chloroprocaine Drugs 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000022831 chronic renal failure syndrome Diseases 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 235000020940 control diet Nutrition 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 125000002592 cumenyl group Chemical group C1(=C(C=CC=C1)*)C(C)C 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- GZCGUPFRVQAUEE-ARQDHWQXSA-N d-altrose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)[C@H](O)C=O GZCGUPFRVQAUEE-ARQDHWQXSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 229940043237 diethanolamine Drugs 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 208000010643 digestive system disease Diseases 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- XPPKVPWEQAFLFU-UHFFFAOYSA-J diphosphate(4-) Chemical compound [O-]P([O-])(=O)OP([O-])([O-])=O XPPKVPWEQAFLFU-UHFFFAOYSA-J 0.000 description 1
- 235000011180 diphosphates Nutrition 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 229950005627 embonate Drugs 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002327 eosinophilic effect Effects 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 229940012017 ethylenediamine Drugs 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 208000018685 gastrointestinal system disease Diseases 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 244000144993 groups of animals Species 0.000 description 1
- 229940037467 helicobacter pylori Drugs 0.000 description 1
- 125000005549 heteroarylene group Chemical group 0.000 description 1
- 125000004366 heterocycloalkenyl group Chemical group 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 239000002085 irritant Substances 0.000 description 1
- 231100000021 irritant Toxicity 0.000 description 1
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- BJHIKXHVCXFQLS-PQLUHFTBSA-N keto-D-tagatose Chemical compound OC[C@@H](O)[C@H](O)[C@H](O)C(=O)CO BJHIKXHVCXFQLS-PQLUHFTBSA-N 0.000 description 1
- BJHIKXHVCXFQLS-LFRDXLMFSA-N keto-L-tagatose Chemical compound OC[C@H](O)[C@@H](O)[C@@H](O)C(=O)CO BJHIKXHVCXFQLS-LFRDXLMFSA-N 0.000 description 1
- 229940001447 lactate Drugs 0.000 description 1
- 229940099584 lactobionate Drugs 0.000 description 1
- JYTUSYBCFIZPBE-AMTLMPIISA-N lactobionic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O JYTUSYBCFIZPBE-AMTLMPIISA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 235000021266 loss of appetite Nutrition 0.000 description 1
- 208000019017 loss of appetite Diseases 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-M mandelate Chemical compound [O-]C(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-M 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 229940102396 methyl bromide Drugs 0.000 description 1
- LRMHVVPPGGOAJQ-UHFFFAOYSA-N methyl nitrate Chemical compound CO[N+]([O-])=O LRMHVVPPGGOAJQ-UHFFFAOYSA-N 0.000 description 1
- JZMJDSHXVKJFKW-UHFFFAOYSA-M methyl sulfate(1-) Chemical compound COS([O-])(=O)=O JZMJDSHXVKJFKW-UHFFFAOYSA-M 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229950006327 napsilate Drugs 0.000 description 1
- 230000017074 necrotic cell death Effects 0.000 description 1
- 230000000474 nursing effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 230000000242 pagocytic effect Effects 0.000 description 1
- 210000001819 pancreatic juice Anatomy 0.000 description 1
- 229940014662 pantothenate Drugs 0.000 description 1
- 235000019161 pantothenic acid Nutrition 0.000 description 1
- 239000011713 pantothenic acid Substances 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000009054 pathological process Effects 0.000 description 1
- 239000003961 penetration enhancing agent Substances 0.000 description 1
- 235000019371 penicillin G benzathine Nutrition 0.000 description 1
- 208000011906 peptic ulcer disease Diseases 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- LYKMMUBOEFYJQG-UHFFFAOYSA-N piperoxan Chemical compound C1OC2=CC=CC=C2OC1CN1CCCCC1 LYKMMUBOEFYJQG-UHFFFAOYSA-N 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 239000006041 probiotic Substances 0.000 description 1
- 230000000529 probiotic effect Effects 0.000 description 1
- 235000018291 probiotics Nutrition 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- MUPFEKGTMRGPLJ-ZQSKZDJDSA-N raffinose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)O1 MUPFEKGTMRGPLJ-ZQSKZDJDSA-N 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 201000000306 sarcoidosis Diseases 0.000 description 1
- 230000037390 scarring Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 229910052710 silicon Chemical group 0.000 description 1
- 239000010703 silicon Chemical group 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 239000004575 stone Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 230000000451 tissue damage Effects 0.000 description 1
- 231100000827 tissue damage Toxicity 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- PIEPQKCYPFFYMG-UHFFFAOYSA-N tris acetate Chemical compound CC(O)=O.OCC(N)(CO)CO PIEPQKCYPFFYMG-UHFFFAOYSA-N 0.000 description 1
- 150000004043 trisaccharides Chemical class 0.000 description 1
- 101150004326 ureA gene Proteins 0.000 description 1
- 101150030895 ureAB gene Proteins 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 125000005023 xylyl group Chemical group 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Abstract
Description
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕFIELD OF TECHNOLOGY TO WHICH THE INVENTION RELATES
Настоящее изобретение относится к соединениям функционализированных сахаридов, применяемых в качестве противовоспалительных средств, которые оказывают воздействие на механизмы воспаления у млекопитающих.The present invention relates to compounds of functionalized saccharides used as anti-inflammatory agents that affect the mechanisms of inflammation in mammals.
УРОВЕНЬ ТЕХНИКИBACKGROUND OF THE INVENTION
Воспаление представляет собой сложную ответную биологическую реакцию иммунной системы, направленную на защиту организма от вредных для здоровья веществ, от повреждения и разрушения тканей. Ответная воспалительная реакция может быть инициирована физическими, химическими и инфекционными средствами, такими как бактерии, вирусы и другие патогенные микроорганизмы. Цель появления воспаления заключается в устранении первопричины повреждения, в очистке поврежденных клеток и тканей и в инициировании восстановления тканей.Inflammation is a complex biological response of the immune system, aimed at protecting the body from substances harmful to health, from tissue damage and destruction. The inflammatory response can be initiated by physical, chemical, and infectious agents such as bacteria, viruses, and other pathogens. The purpose of inflammation is to eliminate the root cause of damage, to clean up damaged cells and tissues, and to initiate tissue repair.
Воспаление может быть острым или хроническим. Острое воспаление относится к начальной ответной реакции иммунной системы организма на вредные раздражающие воздействия. Хроническое воспаление представляет собой форму длительного воспаления, которое приводит к рекрутменту макрофагов и Т-лимфоцитов. Макрофаги представляют собой крупные фагоцитарные лейкоциты, и вместе с Т-лимфоцитами, которые, как известно, продуцируют цитокины и ферменты, они вызывают более длительное повреждение клеток. Несмотря на то, что для организма необходимо иметь должным образом функционирующую иммунную систему, тем не менее, важно контролировать эти воспалительные механизмы, так как хроническое воспаление может приводить к различным патологиям и даже к раку.The inflammation can be acute or chronic. Acute inflammation refers to the initial response of the body's immune system to harmful irritants. Chronic inflammation is a form of long-term inflammation that leads to the recruitment of macrophages and T-lymphocytes. Macrophages are large phagocytic leukocytes, and together with T-lymphocytes, which are known to produce cytokines and enzymes, they cause longer-term cell damage. Although it is essential for the body to have a properly functioning immune system, it is nevertheless important to control these inflammatory mechanisms, as chronic inflammation can lead to various pathologies and even cancer.
Вместе с тем, термин "воспаление" не является синонимом термина "инфекция". Инфекция относится всего лишь к взаимодействию инвазии микроорганизма с ответной воспалительной реакцией организма на эту инвазию. С другой стороны, воспаление описывает воспалительный механизм, возникающий независимо от возбудителя. Несмотря на это, в медицине воспаление или органоспецифическое воспаление часто называют инфекцией, поскольку микробная инвазия обычно наблюдается во взаимосвязи с воспалением. Тем не менее, важно проводить различие между ними, поскольку многие патологические состояния включают воспалительные процессы, которые не обусловлены микробной или вирусной инвазией, и наоборот, не все микробные или вирусные инфекции приводят к воспалению.However, the term "inflammation" is not synonymous with the term "infection". Infection refers merely to the interaction of a microorganism invasion with the host's inflammatory response to that invasion. On the other hand, inflammation describes an inflammatory mechanism that occurs independently of the pathogen. Despite this, in medicine, inflammation or organ-specific inflammation is often referred to as infection because microbial invasion is commonly seen in association with inflammation. However, it is important to distinguish between the two because many pathological conditions involve inflammatory processes that are not due to microbial or viral invasion, and conversely, not all microbial or viral infections result in inflammation.
Смешение понятий инфекции и воспаления особенно характерно в случаях гастрита или наличия воспаления в желудке. Многие врачи считают хронический гастрит эквивалентным инфекции Helicobacter pylori (H. pylori). Однако известно, что существует множество других причин этого заболевания. Кроме того, желудочная патология также сохраняться даже после успешной эрадикации H. Pylori. В публикации Genta et al., American Journal of Gastroenterology, совсем недавно было сообщено, что примерно у 20% пациентов, у которых был взят гастробиоптат, был поставлен диагноз не связанного с инфекцией Helicobacter pylori гастрита. Учитывая его распространенность, в публикации Borkman et al., New England Journal Of Medicine было предложено рассматривать не связанный с инфекцией Helicobacter pylori гастрит как отдельную нозологическую форму. Известные причины воспаления желудка при отсутствии бактериальной инфекции, в частности, инфекции H. pylori, включают:The confusion between the concepts of infection and inflammation is especially characteristic in cases of gastritis or the presence of inflammation in the stomach. Many doctors consider chronic gastritis to be the equivalent of a Helicobacter pylori (H. pylori) infection. However, it is known that there are many other causes of this disease. In addition, gastric pathology also persists even after successful eradication of H. Pylori. In a publication by Genta et al., American Journal of Gastroenterology, it was most recently reported that approximately 20% of patients from whom a gastrobiopsy was taken were diagnosed with gastritis not associated with Helicobacter pylori infection. Given its prevalence, in the publication of Borkman et al., New England Journal Of Medicine, it was proposed to consider gastritis not associated with Helicobacter pylori infection as a separate nosological form. Known causes of stomach inflammation in the absence of a bacterial infection, particularly H. pylori infection, include:
(i) вирусную инфекцию (цитомегаловирус, простой герпес);(i) viral infection (cytomegalovirus, herpes simplex);
(ii) химическое или реактивное воспаление, вызванное рефлюксом желчи и панкреатического сока в желудок или экзогенными веществами, такими как NSAID (нестероидные противовоспалительные препараты), ASA (ацетилсалициловая кислота), алкоголь или химиотерапевтические препараты;(ii) chemical or reactive inflammation caused by reflux of bile and pancreatic juice into the stomach or by exogenous substances such as NSAIDs (non-steroidal anti-inflammatory drugs), ASAs (acetylsalicylic acid), alcohol or chemotherapy drugs;
(iii) аутоиммунное воспаление, характеризующееся наличием антител против париетальных клеток;(iii) autoimmune inflammation characterized by the presence of antibodies against parietal cells;
(iv) лучевое и эозинофильное воспаление;(iv) radiation and eosinophilic inflammation;
(v) воспаление в процессе коллагеноза;(v) inflammation during collagenosis;
(vi) воспаление при болезни Крона;(vi) inflammation in Crohn's disease;
(vii) воспаление при саркоидозе;(vii) inflammation in sarcoidosis;
(viii) вызванное стрессом воспаление;(viii) stress-induced inflammation;
(ix) желудочные виды бактерий у людей, не относящиеся к H. Pylori Helicobacter (NHPH), из которых H. Suis являются наиболее распространенными. Они связаны с хроническим гастритом, язвой желудка и другими патологическими изменениями желудка, как у животных, так и у людей (G. Zhang et al., Vet Res (2016) 47: 101, с. 1 1. 1 -3);(ix) human gastric bacterial species other than H. pylori Helicobacter (NHPH), of which H. suis is the most common. They are associated with chronic gastritis, gastric ulcer and other pathological changes in the stomach, both in animals and humans (G. Zhang et al., Vet Res (2016) 47: 101, p. 1 1. 1-3);
(x) идиопатические: все случаи гастрита, при которых не удается выявить причины заболевания.(x) idiopathic: all cases of gastritis in which no cause can be identified.
Помимо проблемы не связанного с бактериями Helicobacter гастрита, при лечении людей и сельскохозяйственных животных остается проблемой рецидив язвы желудка, даже после успешной эрадикации бактерий Helicobacter. Например, в случае свиней, несмотря на то, что у подвергнутых лечению животных может происходить рубцевания язвы, тем не менее, рецидив язвенной болезни у них является распространенной проблемой. Рецидив язвенной болезни вызывает у животного дискомфорт и потерю аппетита, что приводит к потере веса и к негативным экономическим последствиям. Но и при лечении людей, рецидив язвы желудка представляет собой серьезную угрозу для здоровья. В настоящее время, страдающие хроническим гастритом и/или язвенной болезнью желудка пациенты вынуждены длительно применять ингибиторы протонной помпы (PPI) для блокирования образования кислоты в желудке. Известно, что указанное длительное применение ингибиторов протонной помпы сопровождается многими побочными эффектами и повышает риск развития хронического заболевания почек, почечной недостаточности и повышенного риска сердечно-сосудистых осложнений.In addition to the problem of non-Helicobacter gastritis, gastric ulcer recurrence remains a problem in the treatment of humans and farm animals, even after successful eradication of Helicobacter bacteria. For example, in the case of pigs, although ulcer scarring may occur in treated animals, ulcer recurrence is still a common problem. A recurrence of peptic ulcer causes discomfort and loss of appetite in the animal, leading to weight loss and negative economic consequences. But even in the treatment of people, the recurrence of stomach ulcers is a serious threat to health. Currently, patients suffering from chronic gastritis and/or gastric ulcers are forced to use long-term proton pump inhibitors (PPI) to block the formation of acid in the stomach. It is known that this long-term use of proton pump inhibitors is accompanied by many side effects and increases the risk of developing chronic kidney disease, renal failure and an increased risk of cardiovascular complications.
В качестве варианта, вместо блокирования продукции кислоты в желудке, язву желудка и гастрит лечат путем целенаправленного воздействия на бактерии Helicobacter pylori.Alternatively, instead of blocking stomach acid production, gastric ulcers and gastritis are treated by targeting Helicobacter pylori bacteria.
Кроме того, для облегчения состояния воспаления желудка противопоказано применение нестероидных противовоспалительных препаратов (NSAID), поскольку известно, что эти препараты являются фактором риска возникновении патологии желудка.In addition, the use of non-steroidal anti-inflammatory drugs (NSAIDs) is contraindicated to alleviate the state of inflammation of the stomach, since these drugs are known to be a risk factor for the occurrence of gastric pathology.
На основании вышеизложенного, можно сделать вывод о том, что существует потребность в противовоспалительных средствах, в результате применения которых могут быть преодолены недостатки современных методов противовоспалительного лечения, такие как большое количество побочных эффектов, а именно повышенный риск возникновения хронического заболевания почек, почечной недостаточности, повышенный риск возникновения сердечно-сосудистых осложнений и другие подобные негативные побочные эффекты, ограниченная область применения, несоблюдение пациентом инструкций по приему препарата, и в результате применения которых могут быть преодолены проблемы рецидивов язвы, в частности, рецидивов язвы желудка.Based on the foregoing, it can be concluded that there is a need for anti-inflammatory drugs, as a result of which the disadvantages of modern methods of anti-inflammatory treatment can be overcome, such as a large number of side effects, namely an increased risk of chronic kidney disease, renal failure, increased the risk of cardiovascular complications and other similar negative side effects, limited scope, non-compliance by the patient with instructions for taking the drug, and as a result of the use of which problems of ulcer recurrence, in particular, recurrence of gastric ulcer, can be overcome.
СУЩНОСТЬ ИЗОБРЕТЕНИЯSUMMARY OF THE INVENTION
К удивлению заявителя настоящего изобретения, оказалось, что можно создать противовоспалительные лекарственные средства, которые бы удовлетворяли упомянутым выше требованиям.To the surprise of the applicant of the present invention, it turned out that it is possible to create anti-inflammatory drugs that would satisfy the requirements mentioned above.
Целью настоящего изобретения является создание альтернативного противовоспалительного средства вместо нестероидных противовоспалительных средств (NSAID) для устранения воспаления в желудке млекопитающих, страдающих от гастрита, язвы желудка, или млекопитающих с риском развития этих заболеваний.The aim of the present invention is to provide an alternative anti-inflammatory agent instead of non-steroidal anti-inflammatory drugs (NSAIDs) to eliminate inflammation in the stomach of mammals suffering from gastritis, gastric ulcer, or mammals at risk of developing these diseases.
Целью настоящего изобретения является создание альтернативы длительному применению ингибиторов протонной помпы (PPI) у субъектов, страдающих от язвенной болезни желудка и хронического гастрита.The aim of the present invention is to provide an alternative to the long-term use of proton pump inhibitors (PPIs) in subjects suffering from gastric ulcers and chronic gastritis.
Целью настоящего изобретения является создание противовоспалительного средства, которое может воздействовать на механизмы воспаления, лежащие в основе язвенной болезни желудка и гастрита у млекопитающих.The aim of the present invention is to provide an anti-inflammatory agent that can act on the inflammatory mechanisms underlying gastric ulcer and gastritis in mammals.
Настоящее изобретение относится к соединениям, применяемым в качестве противовоспалительного средства, которые воздействуют на механизмы воспаления у млекопитающих [обозначаемые далее как противовоспалительное соединение (C)], где указанное противовоспалительное соединение (C) представляет собой, по меньшей мере, одно из соединений, представленных общими формулами (I), (II), (III) или (IV), или его фармацевтически приемлемую соль, фармацевтически приемлемый сольват, изомер или их смесь:The present invention relates to compounds useful as an anti-inflammatory agent that act on the mechanisms of inflammation in mammals [hereinafter referred to as anti-inflammatory compound (C)], wherein said anti-inflammatory compound (C) is at least one of the compounds represented by the general formulas (I), (II), (III) or (IV), or a pharmaceutically acceptable salt, pharmaceutically acceptable solvate, isomer or mixture thereof:
формула (I)formula (I)
формула (II)formula (II)
гдеwhere
- каждый из R1 независимо выбирают из -OH или -N(R1a)(R1b), где каждый из R1a и R1b, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для аминогруппы, арильной, гетероарильной, алифатической и гетероалифатической группы,- each of R 1 is independently selected from -OH or -N(R 1a )(R 1b ), where each of R 1a and R 1b , independently of each other in each case of their presence, is selected from the group consisting of H, protective groups for amino group, aryl, heteroaryl, aliphatic and heteroaliphatic group,
- каждый из R2, R4, R5, R11 и R12, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, -ORz, -N(Rz)2, арильной, гетероарильной, алифатической и гетероалифатической группы, где Rz независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, защитной группы для аминогруппы, арильного, гетероарильного, алифатического, гетероалифатического и карбогидратного фрагмента,- each of R 2 , R 4 , R 5 , R 11 and R 12 , independently of each other in each case of their presence, is selected from the group consisting of H, -OR z , -N(R z ) 2 , aryl, a heteroaryl, aliphatic, and heteroaliphatic group, wherein R z is independently selected from the group consisting of H, a hydroxyl protecting group, an amino protecting group, an aryl, heteroaryl, aliphatic, heteroaliphatic, and carbohydrate moiety,
- каждый из R3 независимо выбирают из группы, состоящей из H, -OH, -NH2, -SH, ORw, -NH(Rw), -N(Rw)2, -SRw, -O(C=O)Rw, -NH(C=O)Rw, -O(C=NH)Rw, -NH(C=NH)Rw, -S(C=NH))Rw, -NH(C=S)Rw, -S(C=O)Rw, -O(C=S)Rw, -S(=S)Rw, арильной, гетероарильной, алифатической и гетероалифатической группы, где Rw выбирают из группы, состоящей из карбогидратного фрагмента, арильной, гетероарильной, алифатической и гетероалифатической группы,- each R 3 is independently selected from the group consisting of H, -OH, -NH 2 , -SH, OR w , -NH(R w ), -N(R w ) 2 , -SR w , -O(C =O)R w , -NH(C=O)R w , -O(C=NH)R w , -NH(C=NH)R w , -S(C=NH))R w , -NH( C=S)R w , -S(C=O)R w , -O(C=S)R w , -S(=S)R w , aryl, heteroaryl, aliphatic and heteroaliphatic group, where R w is selected from a group consisting of a carbohydrate fragment, an aryl, heteroaryl, aliphatic and heteroaliphatic group,
- каждый из R6, R14 и R15, независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, арильной, гетероарильной, алифатической, гетероалифатической группы и карбогидратного фрагмента,- each of R 6 , R 14 and R 15 , independently of each other and in each case of their presence, is selected from the group consisting of H, a protective group for a hydroxyl group, an aryl, heteroaryl, aliphatic, heteroaliphatic group and a carbohydrate moiety,
- каждый из R7 независимо выбирают из группы, состоящей из H, C(=O)N(Rz')2, -C(=O)ORz', защитной группы для гидроксильной группы, арильной, гетероарильной, алифатической, гетероалифатической группы и карбогидратного фрагмента, где Rz' независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, защитной группы для аминогруппы, арильной, гетероарильной, алифатической и гетероалифатической группы,- each R 7 is independently selected from the group consisting of H, C(=O)N(R z' ) 2 , -C(=O)OR z' , hydroxyl protecting group, aryl, heteroaryl, aliphatic, heteroaliphatic a group and a carbohydrate moiety, wherein R z' is independently selected from the group consisting of H, a hydroxyl protecting group, an amino protecting group, an aryl, a heteroaryl, an aliphatic, and a heteroaliphatic group,
- каждый из R10 независимо выбирают из группы, состоящей из -C(=O)N(Rl)(Rp), -C(=O)ORk и -CH2ORk, где Rl и Rp независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для аминогруппы, арильной, гетероарильной, алифатической, гетероалифатической группы и карбогидратного фрагмента, где Rk независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, арильной, гетероарильной, алифатической, гетероалифатической группы и карбогидратного фрагмента,- each R 10 is independently selected from the group consisting of -C(=O)N(R l )(R p ), -C(=O)OR k and -CH 2 OR k where R l and R p are independently from each other and in each case of their presence, is selected from the group consisting of H, a protective group for an amino group, an aryl, heteroaryl, aliphatic, heteroaliphatic group and a carbohydrate fragment, where R k is independently selected from the group consisting of H, a protective group for hydroxyl group, aryl, heteroaryl, aliphatic, heteroaliphatic group and carbohydrate moiety,
- каждый из R13 независимо выбирают из группы, состоящей из -OH и -N(Ro'')(Rm''), где Ro'' и Rm'', независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, -C(=O)Rh, защитной группы для аминогруппы, арильной, гетероарильной, алифатической и гетероалифатической группы, где Rh выбирают из группы, состоящей из карбогидратного фрагмента, арильной, гетероарильной, алифатической и гетероалифатической группы, - each of R 13 is independently selected from the group consisting of -OH and -N(R o'' )(R m'' ), where R o'' and R m'' , independently of each other in each case of their presence , is selected from the group consisting of H, -C(=O)R h , a protective group for the amino group, aryl, heteroaryl, aliphatic and heteroaliphatic group, where R h is selected from the group consisting of carbohydrate moiety, aryl, heteroaryl, aliphatic and heteroaliphatic group,
- каждый из (Ro) и (Rm), независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, -C(=O)Rw', защитной группы для аминогруппы, арильной, гетероарильной, алифатической и гетероалифатической группы, где Rw' выбирают из группы, состоящей из карбогидратного фрагмента, арильной, гетероарильной, алифатической и гетероалифатической группы;- each of (R o ) and (R m ), independently of each other in each case of their presence, is selected from the group consisting of H, -C(=O)R w' , a protective group for an amino group, aryl, heteroaryl, aliphatic and heteroaliphatic groups, where R w' is selected from the group consisting of carbohydrate fragment, aryl, heteroaryl, aliphatic and heteroaliphatic group;
- каждый из (Rs) и (Rt), независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, -C(=O)Rw'', защитной группы для аминогруппы, арильной, гетероарильной, алифатической и гетероалифатической группы, где Rw'' выбирают из группы, состоящей из карбогидратного фрагмента, арильной, гетероарильной, алифатической и гетероалифатической группы;- each of (R s ) and (R t ), independently of each other and in each case of their presence, is selected from the group consisting of H, -C(=O)R w'' , a protective group for an amino group, aryl, heteroaryl, aliphatic and heteroaliphatic groups, where R w'' is selected from the group consisting of carbohydrate fragment, aryl, heteroaryl, aliphatic and heteroaliphatic group;
- каждый из R6a и R6a', независимо друг от друга и в каждом случае их присутствия, выбирают из H или -OH, предпочтительно, чтобы R6a представлял собой H, и R6a' представлял собой -OH;- each of R 6a and R 6a' , independently of each other and in each case of their presence, is selected from H or -OH, preferably R 6a is H and R 6a' is -OH;
- каждый из Rc независимо выбирают из группы, состоящей из H, галогена, гетероарила, -ORq, -N(Rq)2, -SRq, NO2, -NC, -CN, -N3, -N(Rq)=NRq, -CHO, -C(=O)Rq, -C(=S)Rq, C(=NRq)Rq, -C(=O)ORq, -C(=NRq)ORq, -C(=NRq)N(Rq)2, -C(=O)N(Rq)2, -C(=S)ORq, -C(=O)SRq, -C(=S)SRq, -P(=O)(ORq)2, -S(=O)(ORq), -S(=O)2(ORq), -P(=O)N(Rq)2, -P(=O)2N(Rq)2, -C(=O)NR'S(=O)2Rq, -S(=O)N(Rq)2 and -S(=O)2N(Rq)2, где каждый из Rq независимо выбирают из группы, состоящей из H, алифатической, гетероалифатической группы, арильной, гетероарильной группы и защитной группы для гидроксильной группы,- each R c is independently selected from the group consisting of H, halogen, heteroaryl, -OR q , -N(R q ) 2 , -SR q , NO 2 , -NC, -CN, -N 3 , -N( R q )=NR q , -CHO, -C(=O)R q , -C(=S)R q , C(=NR q )R q , -C(=O)OR q , -C(= NR q )OR q , -C(=NR q )N(R q ) 2 , -C(=O)N(R q ) 2 , -C(=S)OR q , -C(=O)SR q , -C(=S)SR q , -P(=O)(OR q ) 2 , -S(=O)(OR q ), -S(=O) 2 (OR q ), -P(=O )N(R q ) 2 , -P(=O) 2 N(R q ) 2 , -C(=O)NR'S(=O) 2 R q , -S(=O)N(R q ) 2 and -S(=O) 2 N(R q ) 2 , where each R q is independently selected from the group consisting of H, an aliphatic, heteroaliphatic group, an aryl, a heteroaryl group, and a protecting group for a hydroxyl group,
- каждый из Ri независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, алифатической, гетероалифатической группы, арила и гетероарила,- each R i is independently selected from the group consisting of H, a protecting group for a hydroxyl group, an aliphatic, a heteroaliphatic group, an aryl and a heteroaryl,
- каждый Lipid независимо выбирают из H или C1–30 алифатического фрагмента, в котором от 0 до 10 метиленовых звеньев необязательно заменены на -O-, -NRx-, -S-, -C(=O)-, -C(=NRx)-, -S(=O)-, -S(=O)2-, -N=N-, -C=N-, -C(Ry)=C(Ry')-, -N–O–, арилен или гетероариленовый фрагмент, где каждый из Rx независимо выбирают из группы, состоящей из H, алифатической, гетероалифатической группы, арильной, гетероарильной группы или защитной группы для аминогруппы, и где каждый из Ry и Ry', независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, алифатической, гетероалифатической, арильной и гетероарильной группы.- each Lipid is independently selected from an H or C 1-30 aliphatic moiety in which 0 to 10 methylene units are optionally replaced by -O-, -NR x -, -S-, -C(=O)-, -C( =NR x )-, -S(=O)-, -S(=O) 2 -, -N=N-, -C=N-, -C(R y )=C(R y' )-, -N-O-, arylene, or heteroarylene moiety, wherein R x is each independently selected from the group consisting of H, an aliphatic, heteroaliphatic, aryl, heteroaryl, or amino protecting group, and wherein R y and R y' are each , independently of each other and in each case of their presence, is selected from the group consisting of H, aliphatic, heteroaliphatic, aryl and heteroaryl groups.
Кроме того, настоящее изобретение относится к фармацевтической композиции, применяемой в качестве противовоспалительного средства, которые воздействуют на механизмы воспаления у млекопитающих, которая включает носитель и, в качестве активного ингредиента, эффективное количество противовоспалительного соединения (C), определяемого в любом одном из представленных в изобретении вариантов осуществления.In addition, the present invention relates to a pharmaceutical composition for use as an anti-inflammatory agent that affects the mechanisms of inflammation in mammals, which comprises a carrier and, as an active ingredient, an effective amount of an anti-inflammatory compound (C) as defined in any one of the inventions. implementation options.
Кроме того, настоящее изобретение относится к способу приготовления указанной фармацевтической композиции.In addition, the present invention relates to a method for preparing said pharmaceutical composition.
Кроме того, настоящее изобретение относится к противовоспалительному соединению (C), определяемому в любом одном из представленных в изобретении вариантов осуществления, для применения в качестве лекарственного препарата.In addition, the present invention relates to an anti-inflammatory compound (C) defined in any one of the embodiments presented in the invention for use as a drug.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей носитель и, в качестве активного ингредиента, эффективное количество противовоспалительного соединения (C), определяемого в любом одном из представленных в изобретении вариантов осуществления, для применения в качестве лекарственного препарата.In addition, the present invention relates to a pharmaceutical composition comprising a carrier and, as an active ingredient, an effective amount of an anti-inflammatory compound (C) defined in any one of the embodiments presented in the invention, for use as a medicine.
Кроме того, настоящее изобретение относится к противовоспалительному соединению (C), определяемому в любом одном из представленных в изобретении вариантов осуществления, для применения при лечении воспалительных заболеваний или связанных с воспалением заболеваний.In addition, the present invention relates to an anti-inflammatory compound (C) as defined in any one of the embodiments of the invention for use in the treatment of inflammatory diseases or inflammation-related diseases.
Кроме того, настоящее изобретение относится к противовоспалительному соединению (C), определяемому в любом одном из представленных в изобретении вариантов осуществления, для применения при лечении заболевания, опосредованного, по меньшей мере, одним цитокином.In addition, the present invention relates to an anti-inflammatory compound (C) as defined in any one of the embodiments of the invention for use in the treatment of a disease mediated by at least one cytokine.
Кроме того, настоящее изобретение относится к in vivo способу подавления или торможения ответных воспалительных реакций путем применения противовоспалительного соединения (C), определяемого в любом одном из представленных в изобретении вариантов осуществления.In addition, the present invention relates to an in vivo method for suppressing or inhibiting inflammatory responses by using an anti-inflammatory compound (C) defined in any one of the embodiments presented in the invention.
Кроме того, настоящее изобретение относится к способу подавления или торможения экспрессии, по меньшей мере, одного цитокина у млекопитающего.In addition, the present invention relates to a method for suppressing or inhibiting the expression of at least one cytokine in a mammal.
Кроме того, настоящее изобретение относится к способу лечения связанных с воспалением заболеваний, ассоциированных с уровнями экспрессии цитокина у млекопитающих.In addition, the present invention relates to a method of treating inflammation-related diseases associated with cytokine expression levels in mammals.
ПРОТИВОВОСПАЛИТЕЛЬНОЕ СОЕДИНЕНИЕ (C) И ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬANTI-INFLAMMATORY COMPOUND (C) AND ITS PHARMACEUTICALLY ACCEPTABLE SALT
Далее следует иметь в виду, что все определения и преимущества, описанные выше для противовоспалительного соединения (C), в равной степени применимы к этому варианту осуществления и ко всем дополнительным вариантам осуществления, описанным ниже.Further, it should be understood that all definitions and advantages described above for the anti-inflammatory compound (C) apply equally to this embodiment and to all additional embodiments described below.
Используемые выше и ниже в изобретении определения имеют следующие значения, если не указано иное.Used above and below in the invention, the definitions have the following meanings, unless otherwise indicated.
Термин "алифатическая" включает как насыщенную, так и ненасыщенную, неароматическую линейную цепь (то есть, неразветвленную), разветвленную, ациклическую и циклическую углеводородную цепь, имеющую от 1 до 30 углеродных атомов, которые необязательно замещены с помощью одной или более групп, включающих, но этим не ограничивая, алкил, алкинил, алкенил, арил, галогенид, нитро, амино, эфир, кетон, альдегид, гидрокси, карбоновая кислота, или алкокси. Согласно конкретным вариантам осуществления, используемая в изобретении CF–G алифатическая группа определяет CF–G алифатическую группу, имеющую от F до G углеродных атомов, например C1–12 алифатическая группа определяет алифатическую группу, содержащую от 1 до 12 углеродных атомов, C1–10 алифатическая группа определяет алифатическую группу, содержащую от 1 до 12 углеродных атомов.The term "aliphatic" includes both saturated and unsaturated, non-aromatic straight chain (i.e. straight), branched, acyclic and cyclic hydrocarbon chain having from 1 to 30 carbon atoms, which are optionally substituted with one or more groups including, but not limited to, alkyl, alkynyl, alkenyl, aryl, halide, nitro, amino, ether, ketone, aldehyde, hydroxy, carboxylic acid, or alkoxy. In particular embodiments, the C F-G aliphatic group used in the invention defines a C F-G aliphatic group having F to G carbon atoms, e.g., C 1-12 aliphatic group defines an aliphatic group having 1 to 12 carbon atoms, C 1-10 aliphatic group defines an aliphatic group containing 1 to 12 carbon atoms.
Для обычного специалиста в этой области является очевидным, что "алифатический", как предполагается в изобретении, включает, но этим не ограничивая, алкильный, алкенильный и алкинильный фрагменты. Используемые в изобретении термины "алкил", "алкенил" и "алкинил" имеют обширный диапазон общепринятых значений, и они могут включать фрагмент, который представляет линейный, разветвленный, циклический (циклооалкильный, циклоалкенильный, циклоалкинильный) фрагменты или их комбинацию.It will be apparent to one of ordinary skill in the art that "aliphatic" as used herein includes, but is not limited to, alkyl, alkenyl, and alkynyl moieties. As used herein, the terms "alkyl", "alkenyl", and "alkynyl" have a wide range of conventional meanings and may include a moiety that is linear, branched, cyclic (cyclooalkyl, cycloalkenyl, cycloalkynyl) moieties, or a combination thereof.
Термин "алкил", применяемый отдельно или в комбинации, обозначает образованный из алкана радикал, который может представлять собой линейный алкил, разветвленный алкил или циклический алкил, содержащий от 1 до 30 углеродных атомов, если не указано иначе. Линейная или разветвленная алкильная группа присоединяется в любой доступной точке для получения стабильного соединения. Алкил также включает линейную или разветвленную алкильную группу, которая содержит циклоалкильную часть или прерывается циклоалкильной частью. Согласно конкретным вариантам осуществления, CA–B алкил обозначает линейный или разветвленный алкильный радикал, имеющий от A до B углеродных атомов, например C1–15 алкил обозначает линейный или разветвленный алкильный радикал, имеющий от 1 до 15 углеродных атомов, C1–12 алкил обозначает линейный или разветвленный алкильный радикал, имеющий от 1 до 12 углеродных атомов, C1–6 алкил обозначает линейный или разветвленный алкильный радикал, имеющий от 1 до 6 углеродных атомов, такой как, например, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-1-пропил. Согласно конкретным вариантам осуществления, циклический CC–D алкил обозначает циклический алкильный радикал, имеющий от C до D углеродных атомов, например C3–6 циклический алкил.The term "alkyl", used alone or in combination, denotes an alkane-derived radical which may be linear alkyl, branched alkyl or cyclic alkyl containing from 1 to 30 carbon atoms, unless otherwise indicated. A straight or branched alkyl group is attached at any available point to form a stable compound. Alkyl also includes a linear or branched alkyl group that contains a cycloalkyl moiety or is interrupted by a cycloalkyl moiety. In specific embodiments, C A-B alkyl denotes a linear or branched alkyl radical having from A to B carbon atoms, for example C 1-15 alkyl denotes a linear or branched alkyl radical having from 1 to 15 carbon atoms, C 1-12 alkyl denotes a linear or branched alkyl radical having 1 to 12 carbon atoms, C 1-6 alkyl denotes a linear or branched alkyl radical having 1 to 6 carbon atoms, such as, for example, methyl, ethyl, 1-propyl, 2 -propyl, 1-butyl, 2-butyl, 2-methyl-1-propyl. In specific embodiments, cyclic C C-D alkyl refers to a cyclic alkyl radical having C to D carbon atoms, such as C 3-6 cyclic alkyl.
Термин "алкенил", применяемый отдельно или в комбинации, обозначает линейный или разветвленный углеводород, содержащий 1-30 углеродных атомов, если не указано иначе, и, по меньшей мере, одну двойную связь углерод-углерод. Примеры алкенильных групп включают этенил, пропенил, изопропенил, бутенил, циклогексенил, циклогексенилалкил и другие подобные алкенильные группы. Алкенил также включает линейную или разветвленную алкенильную группу, которая содержит циклоалкильную часть или прерывается циклоалкильной частью. Двойные связи углерод-углерод могут содержаться или в циклоалкильной части, или в линейной цепи или в разветвленной части. Согласно конкретным вариантам осуществления, CH–I алкенил обозначает линейный или разветвленный алкенильный радикал, имеющий от H до I углеродных атомов, например, C1–6 алкенил обозначает линейный или разветвленный алкенильный радикал, имеющий от 1 до 6 углеродных атомов.The term "alkenyl", used alone or in combination, means a linear or branched hydrocarbon containing 1-30 carbon atoms, unless otherwise indicated, and at least one carbon-carbon double bond. Examples of alkenyl groups include ethenyl, propenyl, isopropenyl, butenyl, cyclohexenyl, cyclohexenylalkyl, and other similar alkenyl groups. Alkenyl also includes a linear or branched alkenyl group that contains a cycloalkyl moiety or is interrupted by a cycloalkyl moiety. The carbon-carbon double bonds may be present either in the cycloalkyl portion or in the straight chain or branched portion. In specific embodiments, C H-I alkenyl is a linear or branched alkenyl radical having H to I carbon atoms, for example, C 1-6 alkenyl is a linear or branched alkenyl radical having 1 to 6 carbon atoms.
Термин "алкинил", применяемый отдельно или в комбинации, обозначает линейный, разветвленный или циклический углеводород, содержащий от 1 до 30 углеродных атомов, содержащих, по меньшей мере, одну тройную связь углерод-углерод. Примеры алкинильных групп включают этинил, пропинил, бутинил и другие подобные алкинилы.The term "alkynyl", used alone or in combination, means a linear, branched or cyclic hydrocarbon containing from 1 to 30 carbon atoms containing at least one carbon-carbon triple bond. Examples of alkynyl groups include ethynyl, propynyl, butynyl, and the like.
Используемый в изобретении термин "гетероалифатический" относится к определенному в изобретении алифатическому фрагменту, который включает как насыщенные и ненасыщенные, неароматические, линейные (то есть, неразветвленные), разветвленные, ациклические, циклические (то есть, гетероциклические) или полициклические углеводороды, имеющие от 1 до 30 углеродных атомов, если не указано иначе, которые необязательно замещены с помощью одной или более групп, включающих, но этим не ограничивая, алкильную, алкинильную, алкенильную, арильную, галогенидную группы, нитрогруппу, аминогруппу, эфирную, кетоновую, альдегидную, гидроксильную группы, группу карбоновой кислоты или алкоксильную группу, и которые содержат один или более гетероатомов, таких как атомы кислорода, серы, азота, фосфора или кремния, например, вместо углеродных атомов. В конкретных вариантах осуществления, гетероалифатические фрагменты замещены путем независимой замены одного или более из атомов водорода в них на один или более заместителей. Для обычного специалиста в этой области является очевидным, что "гетероалифатический", как предполагается в изобретении, включает гетероалкильный, гетероциклоалкильный, гетероциклоалкенильный и гетероциклоалкинильный фрагменты. Поэтому, используемый в изобретении термин "гетероалкил" включает линейные, разветвленные и циклические алкильные группы, которые содержат один или более гетероатомов, таких как атомы кислорода, серы, азота, фосфора или кремния, например, вместо углеродных атомов. Аналогичное определение применяется к другим номенклатурным терминам, таким как "гетероалкенил", "гетероалкинил" и другим подобным терминам. Кроме того, используемые в изобретении термины "гетероалкил", "гетероалкенил", "гетероалкинил" и другие подобные термины охватывают как замещенные, так и незамещенные группы.As used herein, the term "heteroaliphatic" refers to an aliphatic moiety as defined herein, which includes both saturated and unsaturated, non-aromatic, linear (i.e., unbranched), branched, acyclic, cyclic (i.e., heterocyclic), or polycyclic hydrocarbons having from 1 up to 30 carbon atoms, unless otherwise indicated, which are optionally substituted with one or more groups including, but not limited to, alkyl, alkynyl, alkenyl, aryl, halide, nitro, amino, ether, ketone, aldehyde, hydroxyl groups , a carboxylic acid group or an alkoxy group, and which contain one or more heteroatoms such as oxygen, sulfur, nitrogen, phosphorus or silicon atoms, for example, instead of carbon atoms. In specific embodiments, the heteroaliphatic moieties are substituted by independently replacing one or more of their hydrogen atoms with one or more substituents. For a person of ordinary skill in this field, it is obvious that "heteroaliphatic", as intended in the invention, includes heteroalkyl, heterocycloalkyl, heterocycloalkenyl and heterocycloalkynyl fragments. Therefore, the term "heteroalkyl" as used herein includes linear, branched and cyclic alkyl groups which contain one or more heteroatoms such as oxygen, sulfur, nitrogen, phosphorus or silicon, for example, instead of carbon atoms. A similar definition applies to other nomenclature terms such as "heteroalkenyl", "heteroalkynyl" and other similar terms. In addition, as used herein, the terms "heteroalkyl", "heteroalkenyl", "heteroalkynyl", and the like, encompass both substituted and unsubstituted groups.
Используемый в изобретении термин "арил", применяемый отдельно или в комбинации, обозначает любую ароматическую группу на основе углеродных атомов, включающую, но этим не ограничивая, фенил, толил, ксилил, куменил, нафтил, антраценил и другие подобные группы, необязательно конденсированную с циклоалкилом или гетероциклилом, содержащими, предпочтительно, 5-7, более предпочтительно, 5-6, атомов в кольце, и/или необязательно замещенную с помощью от 1 до 5 групп или заместителей. Арил может быть необязательно замещен с помощью одной или более групп, включающих, но этим не ограничивая, алкильную, алкинильную, алкенильную, арильную, галогенидную группы, нитрогруппу, аминогруппу, эфирную, кетоновую, альдегидную, гидроксильную группы, группу карбоновой кислоты или алкоксильную группу, при условии, что заместитель присоединяют в одной точке к арилу, или при условии, что заместитель присоединяют в двух точках к арилу, с образованием бициклической системы, например, бензодиоксола, бензодиоксана, бензимидазола.As used herein, the term "aryl", used alone or in combination, means any aromatic group based on carbon atoms, including, but not limited to, phenyl, tolyl, xylyl, cumenyl, naphthyl, anthracenyl, and the like, optionally fused with cycloalkyl or heterocyclyl containing preferably 5-7, more preferably 5-6 ring atoms and/or optionally substituted with 1 to 5 groups or substituents. Aryl may be optionally substituted with one or more groups including, but not limited to, alkyl, alkynyl, alkenyl, aryl, halide, nitro, amino, ether, ketone, aldehyde, hydroxyl, carboxylic acid, or alkoxy groups, provided that the substituent is attached at one point to the aryl, or provided that the substituent is attached at two points to the aryl, to form a bicyclic system, for example, benzodioxole, benzodioxane, benzimidazole.
Термин "гетероарил", применяемый отдельно или в комбинации, обозначает моноциклическую ароматическую кольцевую структуру, содержащую 5 или 6 атомов в кольце, или бициклическую ароматическую группу, имеющую от 8 до 10 атомов, содержащую один или более, предпочтительно, 1-4, более предпочтительно 1-3, гетероатомов, независимо выбранных из группы O, S и N, и необязательно замещенную с помощью от 1 до 5 групп или заместителей, включающих, но этим не ограничивая, алкильную, алкинильную, алкенильную, арильную, галогенидную группы, нитрогруппу, аминогруппу, эфирную, кетоновую, альдегидную, гидроксильную группы, группу карбоновой кислоты или алкоксильную группу. Предполагается, что гетероарил также включает окисленные формы S или N, такие как сульфинил, сульфонил и N-оксид атома третичного азота в кольце. Атом углерода или азота присоединяют к гетероарильной кольцевой структуре таким образом, чтобы сохранялась стабильность ароматического кольца. Более конкретно, термин "гетероарил" включает, но этим не ограничивая, пиридил, фуранил, тиофенил, тиазолил, изотиазолил, триазолил, имидазолил, изоксазолил, пирролил, пиразолил, пиримидил, бензофуранил, изобензофуранил, бензотиазолил, бензоизотиазолил, бензотриазолил, индолил, изоиндолил, бензоксазолил, хинолил, изохинолил, бензимидазолил, бензизоксазолил, бензотиофенил, дибензофуран и бензодиазепин-2-он-5-ил и другие подобные гетероарильные группы.The term "heteroaryl", used alone or in combination, means a monocyclic aromatic ring structure containing 5 or 6 ring atoms, or a bicyclic aromatic group having 8 to 10 atoms, containing one or more, preferably 1-4, more preferably 1-3 heteroatoms independently selected from the group O, S and N and optionally substituted with 1 to 5 groups or substituents including, but not limited to, alkyl, alkynyl, alkenyl, aryl, halide, nitro, amino , an ether, a ketone, an aldehyde, a hydroxyl group, a carboxylic acid group, or an alkoxy group. It is contemplated that heteroaryl also includes oxidized S or N forms such as sulfinyl, sulfonyl and N-oxide of the tertiary nitrogen atom in the ring. A carbon or nitrogen atom is attached to the heteroaryl ring structure in such a way that the stability of the aromatic ring is maintained. More specifically, the term "heteroaryl" includes, but is not limited to, pyridyl, furanyl, thiophenyl, thiazolyl, isothiazolyl, triazolyl, imidazolyl, isoxazolyl, pyrrolyl, pyrazolyl, pyrimidyl, benzofuranyl, isobenzofuranyl, benzothiazolyl, benzoisothiazolyl, benzotriazolyl, indolyl, isoindolyl, benzoxazolyl, quinolyl, isoquinolyl, benzimidazolyl, benzisoxazolyl, benzothiophenyl, dibenzofuran and benzodiazepin-2-on-5-yl; and other similar heteroaryl groups.
Согласно конкретному варианту осуществления настоящего изобретения, Lipid представляет собой ненасыщенную C4–20 углеводородную цепь, в которой от 1 до 10 метиленовых звеньев заменены на -C(Ry)=C(Ry')-, где каждый из Ry и Ry', независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, алифатической, гетероалифатической, арильной или гетероарильной группы; и где указанная углеводородная цепь необязательно замещена с помощью C1–6 алкила, C3–6 циклического алкила, C1–6 алкенила или гидроксильной группы, предпочтительно, чтобы Lipid представлял собой C4–20 углеводородную цепь, в которой от 1 до 5 метиленовых звеньев заменены на -C(Ry)=C(Ry')-, где каждый из Ry и Ry', независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, C1–6 алкила и C1–6 алкенила, и где указанная углеводородная цепь необязательно замещена с помощью C1–6 алкила, C3–6 циклического алкила, C1–6 алкенила или гидроксильной группы, более предпочтительно, чтобы Lipid выбирали из фрагментов, имеющих следующие формулы:According to a specific embodiment of the present invention, Lipid is an unsaturated C 4-20 hydrocarbon chain in which 1 to 10 methylene units are replaced by -C(R y )=C(R y' )-, where each of R y and R y' , independently of each other in each case of their presence, is selected from the group consisting of H, aliphatic, heteroaliphatic, aryl or heteroaryl group; and wherein said hydrocarbon chain is optionally substituted with C 1-6 alkyl, C 3-6 cyclic alkyl, C 1-6 alkenyl or hydroxyl group, preferably Lipid is a C 4-20 hydrocarbon chain wherein 1 to 5 methylene units are replaced by -C(R y )=C(R y' )-, where each of R y and R y' , independently of each other in each case of their presence, is selected from the group consisting of H, C 1– 6 alkyl and C 1-6 alkenyl, and wherein said hydrocarbon chain is optionally substituted with C 1-6 alkyl, C 3-6 cyclic alkyl, C 1-6 alkenyl, or a hydroxyl group, more preferably Lipid is selected from moieties having the following formulas:
Еще более предпочтительно, чтобы Lipid выбирали из фрагментов, имеющих следующие формулы:Even more preferably, the Lipid is selected from moieties having the following formulas:
Согласно конкретному варианту осуществления настоящего изобретения, Lipid представляет собой насыщенную углеводородную цепь, имеющую общую Z: According to a specific embodiment of the present invention, Lipid is a saturated hydrocarbon chain having a common Z:
Формула ZFormula Z
гдеwhere
- каждый из R9' и R9'', независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, -OH и C1–6 алкила,- each of R 9' and R 9'' , independently of each other and in each case of their presence, is selected from the group consisting of H, -OH and C 1-6 alkyl,
- каждый из Rx' и Rx'', независимо друг от друга и в каждом случае их присутствия, выбирают из H, C1–15 алкила и арила, где указанный арил необязательно дополнительно замещен с помощью C1–15 алкила, и где n=4-30, и m=0 или 1- each of R x' and R x'' , independently of each other and in each case of their presence, is selected from H, C 1-15 alkyl and aryl, where the specified aryl is optionally additionally substituted with C 1-15 alkyl, and where n=4-30, and m=0 or 1
Предпочтительно, чтобы насыщенную углеводородную цепь выбирали из фрагментов, имеющих следующие формулы:Preferably, the saturated hydrocarbon chain is selected from moieties having the following formulas:
Согласно конкретному варианту осуществления настоящего изобретения, R1 независимо выбирают из -OH или -N(R1a)(R1b), где каждый из R1a и R1b, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, C1–20 алифатической и C1–20 гетероалифатической группы, предпочтительно, чтобы R1 представлял собой OH, NH2, или NH(R1b), где R1b представляет собой C1–10 циклоалкильную группу или C1–10 циклоалкенил, который необязательно замещен с помощью галогена, гидроксила или алкокси, более предпочтительно, чтобы R1 представлял собой -NH(R1b), где R1b имеет следующую формулу:According to a specific embodiment of the present invention, R 1 is independently selected from -OH or -N(R 1a )(R 1b ), where each of R 1a and R 1b , independently of each other in each case of their presence, is selected from the group consisting of H, C 1-20 aliphatic and C 1-20 heteroaliphatic, preferably R 1 is OH, NH 2 , or NH(R 1b ), where R1b is a C 1-10 cycloalkyl group or C 1-10 cycloalkenyl which is optionally substituted with halogen, hydroxyl or alkoxy, more preferably R 1 is -NH(R 1b ), where R 1b has the following formula:
Согласно конкретному варианту осуществления настоящего изобретения, R3 независимо выбирают из группы, состоящей из H, -OH и -ORw, где Rw выбирают из группы, состоящей из карбогидратного фрагмента, где указанный карбогидратный фрагмент независимо выбирают из группы, состоящей из D- и L- моносахаридов, таких как, в частности, D-эритроза, L-эритроза, D-треоза, L-треоза, L-эритрулоза, D-эритрулоза, D-арабиноза, L-арабиноза, D-дезоксирибоза, L-дезоксирибоза, D-ликсоза, L-ликсоза, D-рибоза, L-рибоза, D-рибулоза, L-рибулоза, D-ксилоза, L-ксилоза, D-ксилулоза, L-ксилулоза, D-аллоза, L-аллоза, D-альтроза, L-альтроза, D-галактоза, L-галактоза, D-глюкоза, L-глюкоза, D-гулоза, L-гулоза, D-идоза, L-идоза, D-манноза, L-манноза, D-талоза, L-талоза, D-фруктоза, L-фруктоза, D-псикоза, L-псикоза, D-сорбоза, L-сорбоза, D-тагатоза, L-тагатоза, D-фукоза, L-фукоза, D-рамноза и L-рамноза, дисахаридов, таких как, в частности, сахароза, лактоза, трегалоза и мальтоза, трисахаридов, таких как, в частности, акарбоза, рафиноза и мелицитоза, более предпочтительно, чтобы R3 представлял собой -ORw, где Rw представляет собой D-моносахарид, такой как, в частности, D-эритроза, D-треоза, D-эритрулоза, D-арабиноза, D-дезоксирибоза, D-ликсоза, D-рибоза, D-рибулоза, D-ксилоза, D-ксилулоза, D-аллоза, D-альтроза, D-галактоза, D-глюкоза, D-гулоза, D-идоза, D-манноза, D-талоза, D-фруктоза, D-псикоза, D-сорбоза D-тагатоза, D-фукоза и D-рамноза, еще более предпочтительно, чтобы R3 представлял собой -ORw, где Rw независимо выбирают из группы, состоящей из D-глюкозы, D-галактозы, D-аллозы, D-альтрозы, D-маннозы, D-идозы, D-галозы или D-талозы, наиболее предпочтительно, чтобы R3 представлял собой -ORw, где Rw представляет собой D-глюкозу.According to a particular embodiment of the present invention, R 3 is independently selected from the group consisting of H, -OH, and -OR w , where R w is selected from the group consisting of a carbohydrate moiety, wherein said carbohydrate moiety is independently selected from the group consisting of D- and L-monosaccharides, such as, in particular, D-erythrose, L-erythrose, D-threose, L-threose, L-erythrulose, D-erythrulose, D-arabinose, L-arabinose, D-deoxyribose, L-deoxyribose , D-lyxose, L-lyxose, D-ribose, L-ribose, D-ribulose, L-ribulose, D-xylose, L-xylose, D-xylulose, L-xylulose, D-allose, L-allose, D -altrose, L-altrose, D-galactose, L-galactose, D-glucose, L-glucose, D-gulose, L-gulose, D-idose, L-idose, D-mannose, L-mannose, D-talose , L-talose, D-fructose, L-fructose, D-psicose, L-psicose, D-sorbose, L-sorbose, D-tagatose, L-tagatose, D-fucose, L-fucose, D-rhamnose and L -rhamnose, disaccharides such as in particular sucrose, lactose, trehalose and maltose, trisaccharides such as in particular a carbose, raffinose and melicitose, more preferably R 3 is -OR w , where R w is a D-monosaccharide, such as, in particular, D-erythrose, D-threose, D-erythrulose, D-arabinose, D -deoxyribose, D-lyxose, D-ribose, D-ribulose, D-xylose, D-xylulose, D-allose, D-altrose, D-galactose, D-glucose, D-gulose, D-idose, D-mannose , D-talose, D-fructose, D-psicose, D-sorbose, D-tagatose, D-fucose and D-rhamnose, even more preferably R 3 is -OR w , where R w is independently selected from the group consisting of from D-glucose, D-galactose, D-allose, D-altrose, D-mannose, D-idose, D-halose or D-talose, most preferably R 3 is -OR w where R w is D-glucose.
Согласно конкретному варианту осуществления настоящего изобретения, каждый из R2, R4, R5, R11 и R12, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, ORz, C1–12 алифатического, C1–12 гетероалифатического и карбогидратного фрагмента, где Rz выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, C1–12 алифатической группы, C1–12 гетероалифатической группы, арила и гетероарила, и где указанный карбогидратный фрагмент выбирают из группы, состоящей из D-моносахаридов, таких как, в частности, D-эритроза, D-треоза, D-эритрулоза, D-арабиноза, D-дезоксирибоза, D-ликсоза, D-рибоза, D-рибулоза, D-ксилоза, D-ксилулоза, D-аллоза, D-альтроза, D-галактоза, D-глюкоза, D-гулоза, D-идоза, D-манноза, D-талоза, D-фруктоза, D-псикоза, D-сорбоза D-тагатоза, D-фукоза и D-рамноза, предпочтительно, чтобы каждый R2, R4, R5, R11 и R12, независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, ORz, защитной группы для гидроксильной группы, C1–6 алкила и карбогидратного фрагмента, где Rz выбирают из группы, состоящей из H, защитной группы для гидроксильной группы и C1–6 алкила, и где указанный карбогидратный фрагмент выбирают из группы, состоящей из D-глюкозы, D-галактозы, D-аллозы, D-альтрозы, D-маннозы, D-идозы, D-галозы и D-талозы, более предпочтительно, чтобы R2, R4, R11 и R12, независимо друг от друга и в каждом случае их присутствия, выбирали из H или ORz, где Rz выбирают из H или C1–6 алкила, более предпочтительно, чтобы R5 представлял собой C1–6 алкил, еще более предпочтительно, чтобы R2 представлял собой H, R4, R11, и R12 представлял собой -OH, и R5 представлял собой -CH3.According to a specific embodiment of the present invention, each of R 2 , R 4 , R 5 , R 11 and R 12 , independently of each other in each case of their presence, is selected from the group consisting of H, OR z , C 1-12 aliphatic , C 1-12 heteroaliphatic and carbohydrate fragment, where R z is selected from the group consisting of H, a protective group for the hydroxyl group, C 1-12 aliphatic group, C 1-12 heteroaliphatic group, aryl and heteroaryl, and where the specified carbohydrate fragment selected from the group consisting of D-monosaccharides, such as, in particular, D-erythrose, D-threose, D-erythrulose, D-arabinose, D-deoxyribose, D-lyxose, D-ribose, D-ribulose, D- xylose, D-xylulose, D-allose, D-altrose, D-galactose, D-glucose, D-gulose, D-idose, D-mannose, D-talose, D-fructose, D-psicose, D-sorbose D -tagatose, D-fucose and D-rhamnose, preferably each R 2 , R 4 , R 5 , R 11 and R 12 , independently of each other in each case of their presence, is selected from the group consisting from H, OR z , a hydroxyl protecting group, C 1-6 alkyl, and a carbohydrate moiety, wherein R z is selected from the group consisting of H, a hydroxyl protecting group, and C 1-6 alkyl, and wherein said carbohydrate moiety is selected from the group consisting of D-glucose, D-galactose, D-allose, D-altrose, D-mannose, D-idose, D-halose and D-talose, more preferably R 2 , R 4 , R 11 and R 12 , independently of one another and in each case present, is selected from H or OR z , where R z is selected from H or C 1-6 alkyl, more preferably R 5 is C 1-6 alkyl, even more preferably R 2 is H, R 4 , R 11 and R 12 is -OH and R 5 is -CH 3 .
Согласно конкретному варианту осуществления настоящего изобретения, каждый из R6, R14 и R15, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, C1–12 алифатической и C1–12 гетероалифатической группы, предпочтительно, чтобы R6, R14 и R15, независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H или защитной группы для гидроксильной группы, более предпочтительно, чтобы R6, R14 и R15, независимо друг от друга и в каждом случае их присутствия, представляли собой H.According to a specific embodiment of the present invention, each of R 6 , R 14 and R 15 , independently of each other in each case of their presence, is selected from the group consisting of H, a protecting group for a hydroxyl group, C 1-12 aliphatic and C 1 -12 heteroaliphatic group, preferably R 6 , R 14 and R 15 , independently of each other in each occurrence, are selected from the group consisting of H or a protecting group for a hydroxyl group, more preferably R 6 , R 14 and R 15 , independently of each other and in each case of their presence, were H.
Согласно конкретному варианту осуществления настоящего изобретения, R7 представляет собой группу -C(=O)N(Rz')2, где каждый из Rz' независимо выбирают из группы, состоящей из H, арила, гетероарила и C1–12 алкила, предпочтительно, чтобы каждый из Rz' независимо выбирали из H или C1–12 алкила, более предпочтительно, чтобы каждый из Rz' независимо выбирали из группы, состоящей из H, метила, этила и пропила, наиболее предпочтительно, чтобы каждый из Rz' независимо представлял собой H.According to a specific embodiment of the present invention, R 7 is a -C(=O)N(R z' ) 2 group, where each R z' is independently selected from the group consisting of H, aryl, heteroaryl, and C 1-12 alkyl , preferably each R z' is independently selected from H or C 1-12 alkyl, more preferably each R z' is independently selected from the group consisting of H, methyl, ethyl and propyl, most preferably each R z' is independently H.
Согласно конкретному варианту осуществления настоящего изобретения, каждый из R10 независимо выбирают из -C(=O)N(Rl)(Rp) или -C(=O)ORk, где Rl и Rp, независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для аминогруппы, арильной, гетероарильной, C1–12 алифатической и C1–12 гетероалифатической группы, и где Rk независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, арильной, гетероарильной, C1–30 алифатической и C1–30 гетероалифатической группы, предпочтительно, чтобы каждый из R10 независимо выбирали из -C(=O)N(Rl)(Rp) или -C(=O)ORk, где Rl и Rp, независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для аминогруппы, арила, гетероарила и C1–6 алкила, где каждый из Rk независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы и C1–6 алкила, более предпочтительно, чтобы каждый из R10 независимо выбирали из -C(=O)N(Rl)(Rp) или -C(=O)ORk, где Rl и Rp, независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, защитной группы для аминогруппы, метила, этила и пропила, где каждый из Rk независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, метила, этила и пропила, наиболее предпочтительно, чтобы R10 представлял собой -C(=O)NH2 или -C(=O)OH.According to a particular embodiment of the present invention, each R 10 is independently selected from -C(=O)N(R l )(R p ) or -C(=O)OR k , where R l and R p are independently and in each case present, is selected from the group consisting of H, an amino protecting group, aryl, heteroaryl, C 1-12 aliphatic, and C 1-12 heteroaliphatic, and where R k is independently selected from the group consisting of H, a protecting group for hydroxyl, aryl, heteroaryl, C 1-30 aliphatic and C 1-30 heteroaliphatic, preferably each R 10 is independently selected from -C(=O)N(R l )(R p ) or - C(=O)OR k , where R l and R p , independently of each other and in each case of their presence, are selected from the group consisting of H, an amino protecting group, aryl, heteroaryl and C 1-6 alkyl, where each R k is independently selected from the group consisting of H, a protecting group for a hydroxyl group and C 1-6 alkyl, more preferably each R 10 is not independently selected from -C(=O)N(R l )(R p ) or -C(=O)OR k , where R l and R p , independently of each other in each case of their presence, are selected from the group consisting of from H, an amino protecting group, methyl, ethyl and propyl, wherein each R k is independently selected from the group consisting of H, a hydroxyl protecting group, methyl, ethyl and propyl, most preferably R 10 is -C (=O)NH 2 or -C(=O)OH.
Согласно конкретному варианту осуществления настоящего изобретения, каждый из R13 независимо выбирают из группы, состоящей из -OH и -N(Ro'')(Rm''), где Ro'' и Rm'', независимо друг от друга в каждом случае их присутствия, выбирают из группы, состоящей из H, –C(=O)Rh, защитной группы для аминогруппы, C1–12 алифатической и C1–12 гетероалифатической группы, где Rh независимо выбирают из C1–12 алифатической или C1–12 гетероалифатической группы, предпочтительно, чтобы Ro'' и Rm', независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rh и C1–12 алкила, где Rh представляет собой C1–12 алкил, более предпочтительно, чтобы Ro'' и Rm'', независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rh и C1–6 алкила, где Rh представляет собой C1–6 алкил, наиболее предпочтительно, чтобы Ro'' представлял собой H, и Rm' представлял собой -C(=O)CH3.According to a specific embodiment of the present invention, each R 13 is independently selected from the group consisting of -OH and -N(R o'' )(R m'' ), where R o'' and R m'' , independently of each other each other in each occurrence is selected from the group consisting of H, -C(=O)R h , amino protecting group, C 1-12 aliphatic and C 1-12 heteroaliphatic, where R h is independently selected from C 1 -12 aliphatic or C 1-12 heteroaliphatic group, preferably R o'' and R m' , independently of each other in each occurrence, are selected from the group consisting of H, -C(=O)R h and C 1-12 alkyl, where R h is C 1-12 alkyl, more preferably R o'' and R m'' , independently of each other in each occurrence, are selected from the group consisting of H, - C(=O)R h and C 1-6 alkyl, where R h is C 1-6 alkyl, most preferably R o'' is H and R m' is -C(=O)CH 3 .
Согласно конкретному варианту осуществления настоящего изобретения, каждый из (Ro) и (Rm), независимо друг от друга в каждом случае их присутствия выбирают из группы, состоящей из H, -C(=O)Rw', защитной группы для аминогруппы, C1–12 алифатической и C1–12 гетероалифатической группы, где Rw' независимо выбирают из группы, состоящей из C1–12 алифатической и C1–12 гетероалифатической группы, предпочтительно, чтобы (Ro) и (Rm), независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rw', защитной группы для аминогруппы и C1–12 алкила, где Rw' представляет собой C1–12 алкил, более предпочтительно, чтобы (Ro) и (Rm), независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rw' и C1–6 алкила, где Rw' представляет собой C1–6 алкил, наиболее предпочтительно, чтобы (Ro) представлял собой H, и (Rm) представлял собой -C(=O)CH3.According to a specific embodiment of the present invention, each of (R o ) and (R m ), independently of each other in each case of their presence, is selected from the group consisting of H, -C(=O)R w' , a protective group for the amino group , C 1-12 aliphatic and C 1-12 heteroaliphatic, where R w' is independently selected from the group consisting of C 1-12 aliphatic and C 1-12 heteroaliphatic, preferably (R o ) and (R m ) , independently of each other in each occurrence, were selected from the group consisting of H, -C(=O)R w' , an amino protecting group, and C 1-12 alkyl, where R w' is C 1-12 alkyl, more preferably (R o ) and (R m ), independently of each other in each case of their presence, are selected from the group consisting of H, -C(=O)R w' and C 1-6 alkyl, where R w' is C 1-6 alkyl, most preferably (R o ) is H and (R m ) is -C(=O)CH 3 .
Согласно конкретному варианту осуществления настоящего изобретения, каждый из (Rs) и (Rt), независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, -C(=O)Rw'', защитной группы для аминогруппы, C1–12 алифатической и C1–12 гетероалифатической группы, где Rw'' независимо выбирают из C1–12 алифатической или C1–12 гетероалифатической группы, предпочтительно, чтобы (Rs) и (Rt), независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rw'', защитной группы для аминогруппы и C1–12 алкила, где Rw'' представляет собой C1–12 алкил, более предпочтительно, чтобы (Rs) и (Rt), независимо друг от друга в каждом случае их присутствия, выбирали из группы, состоящей из H, -C(=O)Rw'' и C1–6 алкила, где Rw'' представляет собой C1–6 алкил, наиболее предпочтительно, чтобы (Rs) представлял собой H, и (Rt) представляют собой -C(=O)CH3.According to a specific embodiment of the present invention, each of (R s ) and (R t ), independently of each other and in each case of their presence, is selected from the group consisting of H, -C(=O)R w'' , protective groups for amino, C 1-12 aliphatic and C 1-12 heteroaliphatic, where R w'' is independently selected from C 1-12 aliphatic or C 1-12 heteroaliphatic, preferably (R s ) and (R t ) , independently of each other in each occurrence, were selected from the group consisting of H, -C(=O)R w'' , an amino protecting group, and C 1-12 alkyl, where R w'' is C 1 –12 alkyl, more preferably (R s ) and (R t ), independently of each other in each occurrence, are selected from the group consisting of H, -C(=O)R w'' and C 1– 6 alkyl, where R w'' is C 1-6 alkyl, most preferably (R s ) is H and (R t ) is -C(=O)CH 3 .
Согласно конкретному варианту осуществления настоящего изобретения, каждый из Rc независимо выбирают из группы, состоящей из H, -C(=O)ORq, -C(=O)SRq, -C(=S)ORq, -C(=O)SRq, -C(=S)SRq, где каждый из Rq независимо выбирают из группы, состоящей из H, C1–12 алкила, арила, гетероарила и защитной группы для гидроксильной группы, предпочтительно, чтобы каждый из Rc независимо выбирали из группы, состоящей из H, -C(=O)ORq, -C(=O)SRq и -C(=O)SRq, где каждый из Rq независимо выбирают из группы, состоящей из H, C1–6 алкила и защитной группы для гидроксильной группы, более предпочтительно, чтобы каждый из Rc независимо выбирали из H или -C(=O)ORq, где каждый из Rq независимо выбирают из группы, состоящей из H, метила, этила и пропила, наиболее предпочтительно, чтобы Rc представлял собой -C(=O)OH.According to a particular embodiment of the present invention, each R c is independently selected from the group consisting of H, -C(=O)OR q , -C(=O)SR q , -C(=S)OR q , -C( =O)SR q , -C(=S)SR q , where each R q is independently selected from the group consisting of H, C 1-12 alkyl, aryl, heteroaryl and a hydroxyl protecting group, preferably each R c is independently selected from the group consisting of H, -C(=O)OR q , -C(=O)SR q and -C(=O)SR q , where each of R q is independently selected from the group consisting of H, C 1-6 alkyl and a protecting group for a hydroxyl group, more preferably each R c is independently selected from H or -C(=O)OR q where each R q is independently selected from the group consisting of H, methyl, ethyl and propyl, most preferably R c is -C(=O)OH.
Согласно конкретному варианту осуществления настоящего изобретения, каждый из Ri независимо выбирают из группы, состоящей из H, защитной группы для гидроксильной группы, C1–12 алифатической, C1–12 гетероалифатической группы, арила и гетероарила, предпочтительно, чтобы Ri независимо выбирали из группы, состоящей из H, защитной группы для гидроксильной группы, C1–12 алкила, арила и гетероарила, более предпочтительно, чтобы Ri независимо выбирали из группы, состоящей из H, защитной группы для гидроксильной группы и C1–6 алкила, еще более предпочтительно, чтобы Ri независимо выбирали из группы, состоящей из H, защитной группы для гидроксильной группы, метила, этила и пропила, наиболее предпочтительно, чтобы Ri представлял собой H.According to a specific embodiment of the present invention, each R i is independently selected from the group consisting of H, a protecting group for a hydroxyl group, C 1-12 aliphatic, C 1-12 heteroaliphatic, aryl and heteroaryl, preferably R i is independently selected from the group consisting of H, a hydroxyl protecting group, C 1-12 alkyl, aryl and heteroaryl, more preferably R i is independently selected from the group consisting of H, a hydroxyl protecting group and C 1-6 alkyl, even more preferably R i is independently selected from the group consisting of H, a hydroxyl protecting group, methyl, ethyl and propyl, most preferably R i is H.
Подробно описанные выше противовоспалительные соединения (C) по настоящему изобретению имеют несколько центров хиральности и существуют в стереохимически изомерных формах. Используемый в изобретении термин "стереохимически изомерные формы" обозначает все возможные соединения, состоящие из одних и тех же атомов, связанных одной и той же последовательностью химических связей, но имеющих различные пространственные структуры, которые не являются равнозначными, которыми могут обладать указанные в изобретении противовоспалительные соединения (C).The anti-inflammatory compounds (C) of the present invention described in detail above have multiple centers of chirality and exist in stereochemically isomeric forms. As used herein, the term "stereochemically isomeric forms" refers to all possible compounds consisting of the same atoms, linked by the same sequence of chemical bonds, but having different spatial structures that are not equivalent, which the anti-inflammatory compounds specified in the invention may have. (C).
Если не упомянуто или не указано иное, то химическое обозначение подробно описанных выше противовоспалительных соединений (C) охватывает смесь всех возможных стереохимически изомерных форм, которыми могут обладать указанные противовоспалительные соединения (C). Указанная смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанных противовоспалительных соединений (C). Предполагается, что все стереохимически изомерные формы соединений по настоящему изобретению, как в чистой форме, так и в смеси друг с другом, входят в объем настоящего изобретения.Unless otherwise mentioned or indicated, the chemical designation of the above detailed anti-inflammatory compounds (C) embraces the mixture of all possible stereochemically isomeric forms that said anti-inflammatory compounds (C) may have. Said mixture may contain all diastereomers and/or enantiomers of the basic molecular structure of said anti-inflammatory compounds (C). It is intended that all stereochemically isomeric forms of the compounds of the present invention, either in pure form or in admixture with each other, are within the scope of the present invention.
Предпочтительные противовоспалительные соединения (C) представляют собой соединения с формулой (Ia) [далее обозначаемые в изобретении как противовоспалительные соединения (C) класса I] или их фармацевтически приемлемую соль, фармацевтически приемлемый сольват, изомер или их смесь,Preferred anti-inflammatory compounds (C) are compounds of formula (Ia) [hereinafter referred to in the invention as class I anti-inflammatory compounds (C)] or a pharmaceutically acceptable salt, pharmaceutically acceptable solvate, isomer or mixture thereof,
Формула (Ia)Formula (Ia)
гдеwhere
- каждый из R1 независимо выбирают из OH, NH2 или NH(R1b), где R1b представляет собой C1-10 циклоалкильную группу или C1-10 циклоалкенил, который необязательно замещен с помощью галогена, гидроксила или алкокси, более предпочтительно, чтобы R1 представлял собой -NH(R1b), где R1b имеет следующую формулу:- each R 1 is independently selected from OH, NH 2 or NH(R 1b ), where R 1b is a C 1-10 cycloalkyl group or C 1-10 cycloalkenyl which is optionally substituted with halogen, hydroxyl or alkoxy, more preferably R 1 was -NH(R 1b ), where R 1b has the following formula:
- каждый из R3 независимо выбирают из группы, состоящей из H, -OH и -ORw, где Rw представляет собой D-глюкозу;- each R 3 is independently selected from the group consisting of H, -OH and -OR w , where R w represents D-glucose;
- каждый из R2 и R4, независимо друг от друга и в каждом случае их присутствия, выбирают из H или -OH;- each of R 2 and R 4 , independently of each other and in each case of their presence, is selected from H or -OH;
- каждый из R5 независимо выбирают из группы, состоящей из H, -OH и -CH3;- each R 5 is independently selected from the group consisting of H, -OH and -CH 3 ;
- Lipid выбирают из следующих фрагментов, имеющих формулу L1 или формулу L2:- Lipid is selected from the following fragments having formula L 1 or formula L 2 :
, ,
Формула L1 Formula L1
Формула L2 Formula L2
Более предпочтительно, чтобы противовоспалительное соединение (C) представляло собой смесь подробно описанных выше противовоспалительных соединений (C) класса I.More preferably, the anti-inflammatory compound (C) is a mixture of class I anti-inflammatory compounds (C) as detailed above.
Неограничивающие примеры выпускаемых промышленностью противовоспалительных соединений (C), подходящих для применения в изобретении, включают флавомицин®.Non-limiting examples of commercially available anti-inflammatory compounds (C) suitable for use in the invention include flavomycin ® .
Выпускаемый промышленностью флавомицин® также хорошо известен под его синонимическим названием бамбермицин.The commercially available flavomycin® is also well known by its synonymous name bambermycin.
Бамбермицин или Флавомицин® представляют собой известный комплекс соединений, в основном состоящий из моеномицина A и C, в частности, основным соединением является моеномицин A, имеющим формулу (Ib), описанную подробно ниже, а минорные соединения обозначают как A12, C1, C3 и C4. Моеномицин A и минорные соединения, обозначаемые как A12, C1, C3 и C4, представляют собой подробно описанные выше соединения формулы (Ia).Bambermycin or Flavomycin ® is a known complex of compounds mainly consisting of moenomycin A and C, in particular, the main compound is moenomycin A having the formula (Ib) described in detail below, and minor compounds are denoted as A 12 , C 1 , C 3 and C4 . Moenomycin A and minor compounds, referred to as A 12 , C 1 , C 3 and C4, are compounds of formula (Ia) described above in detail.
В моеномицине A, имеющим формулу (Ib), подробно описанную ниже, и в минорных соединения A12, C1, C3 и C4, Lipid имеет формулу L2, R2 представляет собой H, R1 представляет собой -NH(R1b), где R1b имеет следующую формулу:In moenomycin A having the formula (Ib) detailed below and in the minor compounds A 12 , C 1 , C 3 and C 4 , Lipid has the formula L 2 , R 2 is H, R 1 is -NH(R 1b ), where R 1b has the following formula:
В моеномицине A, R3 представляет собой ORw, где Rw представляет собой D-глюкозу, R4 представляет собой OH, и R5 представляет собой CH3. В моеномицине A12, R3 представляет собой ORw, где Rw представляет собой D-глюкозу, R4 представляет собой H, и R5 представляет собой OH.In moenomycin A, R 3 is OR w , where R w is D-glucose, R 4 is OH, and R 5 is CH 3 . In moenomycin A 12 , R 3 is OR w , where R w is D-glucose, R 4 is H, and R 5 is OH.
В моеномицине C1, R3 представляет собой H, R4 представляет собой H, и R5 представляет собой OH. В моеномицине C3, R3 представляет собой H, R4 представляет собой OH, и R5 представляет собой CH3. В моеномицине C4, R3 представляет собой OH, R4 представляет собой OH, и R5 представляет собой CH3.In moenomycin C 1 , R 3 is H, R 4 is H, and R 5 is OH. In moenomycin C 3 , R 3 is H, R 4 is OH, and R 5 is CH 3 . In moenomycin C 4 , R 3 is OH, R 4 is OH and R 5 is CH 3 .
Бамбермицин или флавомицин® может быть получен из стрептомицетов Streptomyces bambergiensis и Streptomyces ghanaensis, Streptomyces ederensis, Streptomyces geysiriensis и родственных штаммов, или биосинтезирован с образованием в результате описанного выше комплекса соединений. Так как комплекс не подвергают тщательной очистке, флавомицин® также содержит исходные используемые в биосинтезе компоненты и различные промежуточные соединения биосинтеза.Bambermycin or flavomycin® can be obtained from Streptomyces bambergiensis and Streptomyces ghanaensis, Streptomyces ederensis, Streptomyces geysiriensis and related strains, or biosynthesized to form the complex of compounds described above. Since the complex is not subjected to thorough purification, flavomycin® also contains the original components used in the biosynthesis and various intermediate compounds of the biosynthesis.
Бамбермицин также известен под названием флавофосфолипол. Бамбермицин, флавофосфолипол и флавомицин® в изобретении применяют взаимозаменяемо.Bambermycin is also known as flavophospholipol. Bambermycin, flavophospholipol and flavomycin® are used interchangeably in the invention.
Предпочтительным противовоспалительным соединением (C) класса I является, в частности, моеномицин A, имеющий формулу (Ib), или его фармацевтически приемлемую соль, фармацевтически приемлемый сольват, изомер или их смесь:A preferred class I anti-inflammatory compound (C) is in particular moenomycin A having the formula (Ib), or a pharmaceutically acceptable salt, a pharmaceutically acceptable solvate, an isomer or a mixture thereof:
Формула (Ib)Formula (IB)
Согласно альтернативному варианту осуществления настоящего изобретения, противовоспалительные соединения (C) представляют собой соединения формулы (IIa) [далее обозначаемые в изобретении как противовоспалительные соединения (C) класса II] или их фармацевтически приемлемую соль, фармацевтически приемлемый сольват, изомер или их смесь:According to an alternative embodiment of the present invention, the anti-inflammatory compounds (C) are compounds of formula (IIa) [hereinafter referred to in the invention as class II anti-inflammatory compounds (C)] or a pharmaceutically acceptable salt, a pharmaceutically acceptable solvate, an isomer or a mixture thereof:
Формула (IIa)Formula (IIa)
гдеwhere
- R3 представляет собой H или -OH;- R 3 represents H or -OH;
- каждый из R2 и R4, независимо друг от друга и в каждом случае их присутствия, выбирают из H или -OH;- each of R 2 and R 4 , independently of each other and in each case of their presence, is selected from H or -OH;
- каждый из R6a и R6a', независимо друг от друга и в каждом случае их присутствия, выбирают из H или -OH, предпочтительно, чтобы R6a представлял собой H, и R6a' представлял собой -OH;- each of R 6a and R 6a' , independently of each other and in each case of their presence, is selected from H or -OH, preferably R 6a is H and R 6a' is -OH;
- R5 представляет собой H, -OH или CH3;- R 5 represents H, -OH or CH 3 ;
- R13 представляет собой -OH или -NHC(=O)CH3;- R 13 represents -OH or -NHC(=O)CH 3 ;
- Lipid выбирают из следующих фрагментов, имеющих формулу L3, формулу L4 или формулу L5:- Lipid is selected from the following fragments having formula L 3 , formula L 4 or formula L 5 :
Согласно альтернативному варианту осуществления настоящего изобретения, противовоспалительные соединения (C) представляют собой соединения формулы (IIIa) [далее обозначаемые в изобретении как противовоспалительные соединения (C) класса III] или их фармацевтически приемлемую соль, фармацевтически приемлемый сольват, изомер их смесь:According to an alternative embodiment of the present invention, the anti-inflammatory compounds (C) are compounds of formula (IIIa) [hereinafter referred to in the invention as class III anti-inflammatory compounds (C)] or a pharmaceutically acceptable salt thereof, a pharmaceutically acceptable solvate, an isomer mixture thereof:
Формула (IIIa)Formula (IIIa)
гдеwhere
- каждый из R4 и R5, независимо друг от друга и в каждом случае их присутствия, выбирают из группы, состоящей из H, -CH3 и -OH;- each of R 4 and R 5 , independently of each other and in each case of their presence, is selected from the group consisting of H, -CH 3 and -OH;
- R7 независимо выбирают из H или -C(=O)NH2, предпочтительно, чтобы R7 представлял собой C(=O)NH2;- R 7 is independently selected from H or -C(=O)NH 2 , preferably R 7 is C(=O)NH 2 ;
- R10 независимо выбирают из -C(=O)NH2 или -C(=O)OH, предпочтительно, чтобы R10 представлял собой C(=O)NH2;- R 10 is independently selected from -C(=O)NH 2 or -C(=O)OH, preferably R 10 is C(=O)NH 2 ;
- R13 независимо выбирают из группы, состоящей из -OH или -NHC(=O)CH3, предпочтительно, чтобы R13 представлял собой --NHC(=O)CH3 - R 13 is independently selected from the group consisting of -OH or -NHC(=O)CH 3 , preferably R 13 is --NHC(=O)CH 3
- Lipid выбирают из следующих фрагментов, имеющих формулу L6, формулу L7 или формулу L8:- Lipid is selected from the following fragments having formula L 6 , formula L 7 or formula L 8 :
С точки зрения терапевтического применения, соли подробно описанного выше противовоспалительного соединения (C) по настоящему изобретению представляют собой соли, в которых противоион является фармацевтически приемлемым, и соли которого могут быть названы фармацевтически приемлемыми солями присоединения кислоты и присоединения основания. Однако, соли кислот и оснований, которые не являются фармацевтически приемлемыми, могут также находить применение, например, при получении или очистки фармацевтически приемлемого соединения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми, или нет, входят в объем настоящего изобретения.From the point of view of therapeutic use, the salts of the above-described anti-inflammatory compound (C) of the present invention are salts in which the counterion is pharmaceutically acceptable, and the salts of which may be referred to as pharmaceutically acceptable acid addition and base addition salts. However, salts of acids and bases which are not pharmaceutically acceptable may also find use, for example, in the preparation or purification of a pharmaceutically acceptable compound. All salts, whether or not they are pharmaceutically acceptable, are within the scope of the present invention.
Подразумевается, что фармацевтически приемлемые соли присоединения кислоты и основания включают активные нетоксичные формы солей присоединения кислоты и основания, которые способны образовывать подробно описанные выше противовоспалительные соединения (C) по настоящему изобретению. Фармацевтически приемлемые соли присоединения кислоты могут быть легко получены путем обработки основной формы с помощью такой соответствующей кислоты в анионной форме. Соответствующие анионы включают, например, трифторацетат, ацетат, бензолсульфонат, бензоат, бикарбонат, битартрат, бромид, кальция эдетат, камсилат, карбонат, хлорид, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эсилат, фумарат, глюцептат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изетионат, лактат, лактобионат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, памоат (эмбонат), пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, бумацетат, сукцинат, сульфат, таннат, тартрат, теоклат, триэтиодид и другие подобные анионы. Выбранный противоион сожет быть введен, используя ионообменные смолы. И наоборот, указанные солевые формы могут быть превращены в результате обработки соответствующим основанием в форму свободного основания.The pharmaceutically acceptable acid and base addition salts are intended to include the active non-toxic acid and base addition salt forms which are capable of forming the anti-inflammatory compounds (C) of the present invention described in detail above. Pharmaceutically acceptable acid addition salts can be easily obtained by treating the base form with such an appropriate acid in anionic form. Suitable anions include e.g. , hexylresorcinate, hydrabamine, hydrobromide, hydrochloride, hydroxynaphthoate, iodide, isethionate, lactate, lactobionate, malate, maleate, mandelate, mesylate, methyl bromide, methyl nitrate, methyl sulfate, mucat, napsilate, nitrate, pamoate (embonate), pantothenate, phosphate/diphosphate, polygalacturonate, salicylate, stearate, bumacetate, succinate, sulfate, tannate, tartrate, theoclate, triethiodide and other similar anions. The selected counterion can be introduced using ion exchange resins. Conversely, said salt forms may be converted by treatment with an appropriate base to the free base form.
Указанные в изобретении противовоспалительные соединения (C), содержащие кислотный протон, могут быть также превращены в их формы нетоксичных солей присоединения металла или амина путем обработки соответствующими органическими и неорганическими основаниями в катионной форме. Соответствующие основные соли включают соли, образованные органическими катионами, такими как бензатин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглюумин, прокаин и другие подобные органические катионы; и соли, образованные катионами металлов, таких как алюминий, кальций, литий, магний, калий, натрий, цинк и другие подобные металлы. И наоборот, указанные солевые формы могут быть превращены путем обработки соответствующей кислотой в свободную форму.The anti-inflammatory compounds (C) mentioned in the invention containing an acidic proton can also be converted into their non-toxic metal or amine addition salt forms by treatment with appropriate organic and inorganic bases in cationic form. Suitable base salts include salts formed with organic cations such as benzathine, chlorprocaine, choline, diethanolamine, ethylenediamine, megluumine, procaine and other similar organic cations; and salts formed by metal cations such as aluminum, calcium, lithium, magnesium, potassium, sodium, zinc and the like. Conversely, said salt forms can be converted by treatment with an appropriate acid to the free form.
Используемый выше термин "соль присоединения" также включает сольваты, которые способны образовывать указанное в изобретении противовоспалительное соединение (C), а также его соли. Такие сольваты представляют собой, например, гидраты, алкоголяты и другие подобные сольваты.As used above, the term "addition salt" also includes solvates which are capable of forming the anti-inflammatory compound (C) specified in the invention, as well as salts thereof. Such solvates are, for example, hydrates, alcoholates and the like.
Общеизвестно, что связанные с воспалением заболевания вовлекают в патологический процесс сложно организованную "систему" сети цитокинов, вследствие чего функционирование иммунной системы тонко сбалансирована за счет действия провоспалительных и противовоспалительных медиаторов или цитокинов.It is well known that inflammation-related diseases involve a complex "system" of cytokine networks in the pathological process, as a result of which the functioning of the immune system is finely balanced by the action of pro-inflammatory and anti-inflammatory mediators or cytokines.
Подробно описанное выше указанное противовоспалительное соединение (C) по настоящему изобретению воздействует на воспалительные механизмы у млекопитающих. Предпочтительно, чтобы подробно описанное выше противовоспалительное соединение (C) по настоящему изобретению воздействовало на воспалительные механизмы у не принадлежащих к человеческому роду млекопитающих. Не принадлежащее к человеческому роду млекопитающее может представлять собой свинью; жвачное животное, такое как, в частности, крупный рогатый скот, лошади; верблюда, овцу, козу, кошку, собаку; или грызуна, такого как, в частности, мышь, кролик или крыса, предпочтительно, свинью.As detailed above, said anti-inflammatory compound (C) of the present invention acts on inflammatory mechanisms in mammals. Preferably, the anti-inflammatory compound (C) of the present invention described in detail above acts on inflammatory mechanisms in non-human mammals. The non-human mammal may be a pig; a ruminant such as, in particular, cattle, horses; camel, sheep, goat, cat, dog; or a rodent such as, in particular, a mouse, a rabbit or a rat, preferably a pig.
Заявитель с удивлением обнаружил, что подробно описанное выше противовоспалительное соединение (C) по настоящему изобретению может воздействовать на экспрессию, по меньшей мере, одного цитокина путем подавления или торможения экспрессии, по меньшей мере, одного цитокина, где указанный цитокин выбирают из группы, состоящей из провоспалительных цитокинов, противовоспалительных цитокинов и хемокинов.The Applicant was surprised to find that the anti-inflammatory compound (C) of the present invention described in detail above can affect the expression of at least one cytokine by suppressing or inhibiting the expression of at least one cytokine, wherein said cytokine is selected from the group consisting of pro-inflammatory cytokines, anti-inflammatory cytokines and chemokines.
В контексте настоящего изобретения, предполагается, что выражения "по меньшей мере, один цитокин" означают один или более, чем один, цитокин. Другими словами, противовоспалительное соединение (C) по настоящему изобретению может подавлять или тормозить экспрессию одного, двух, трех или более цитокинов, и при этом в результате позволяет достигать более высокой терапевтической эффективности при меньшем количестве побочных эффектов.In the context of the present invention, it is intended that the expressions "at least one cytokine" mean one or more than one cytokine. In other words, the anti-inflammatory compound (C) of the present invention can suppress or inhibit the expression of one, two, three or more cytokines, and thereby achieve higher therapeutic efficacy with fewer side effects.
Кроме того, заявителем было обнаружено, что в результате подавления или торможения экспрессии, по меньшей мере, одного цитокина путем применения противовоспалительного соединения (C) по настоящему изобретению, наблюдается существенное снижение инфильтрации макрофагов, B-клеток и T-клеток. Это говорит о том, что противовоспалительное соединение (C) по настоящему изобретению обладает свойствами подавления или торможения воспаления.In addition, the Applicant has found that by suppressing or inhibiting the expression of at least one cytokine by using the anti-inflammatory compound (C) of the present invention, there is a significant reduction in the infiltration of macrophages, B cells and T cells. This indicates that the anti-inflammatory compound (C) of the present invention has the property of suppressing or inhibiting inflammation.
Примеры заболеваний, опосредуемых цитокинами (C), и которые поддаются лечению путем применения противовоспалительного соединения (C) по настоящему изобретению, в частности, включают воспалительные заболевания и связанные с воспалением заболевания.Examples of diseases mediated by cytokines (C) and which are treatable by using the anti-inflammatory compound (C) of the present invention specifically include inflammatory diseases and inflammation-related diseases.
Неограничивающие примеры воспалительных заболеваний, в частности, включают артрит, ревматоидный артрит, воспалительное заболевание кишечника, псориаз, множественный склероз, системную эритематозную волчанку (SLE), панкреатит, склеродермию, диабет типа I, воспалительное заболевание желудочно-кишечного тракта, аллергический конъюнктивит, гломерулонефрит, синдром Шегрена, увеит, дерматит, анкилозирующий спондилоартрит и фибромиалгию.Non-limiting examples of inflammatory diseases specifically include arthritis, rheumatoid arthritis, inflammatory bowel disease, psoriasis, multiple sclerosis, systemic lupus erythematosus (SLE), pancreatitis, scleroderma, type I diabetes, inflammatory bowel disease, allergic conjunctivitis, glomerulonephritis, Sjögren's syndrome, uveitis, dermatitis, ankylosing spondylitis and fibromyalgia.
Следует иметь в виду, что термин "воспалительное заболевание желудочно-кишечного тракта" относится к таким заболеваниям, как острый гастрит, хронический гастрит, развитие и рецидив язвы желудка, болезнь Крона, воспалительное заболевание кишечника, синдром раздраженного кишечника и язвенный колит.It should be understood that the term "inflammatory bowel disease" refers to diseases such as acute gastritis, chronic gastritis, development and recurrence of gastric ulcers, Crohn's disease, inflammatory bowel disease, irritable bowel syndrome and ulcerative colitis.
Неограничивающие примеры связанных с воспалением заболеваний, в частности, включают нейродегенеративное нарушение, застойная сердечная недостаточность, инсульт, стеноз аортального клапана, почечную недостаточность, аллергию, фиброз, атеросклероз, метаболическое заболевание, сердечно-сосудистое заболевание, осложнение, связанное с применением химиотерапии/лучевой терапии, заболевание печени, нарушение работы желудочно-кишечного тракта, офтальмологическое заболевание, диабетическую ретинопатию, легочное заболевание и проказу.Non-limiting examples of inflammation-related diseases include, but are not limited to, neurodegenerative disorder, congestive heart failure, stroke, aortic valve stenosis, renal failure, allergy, fibrosis, atherosclerosis, metabolic disease, cardiovascular disease, chemotherapy/radiotherapy complication , liver disease, gastrointestinal disorder, ophthalmic disease, diabetic retinopathy, pulmonary disease, and leprosy.
Провоспалительные цитокины, в частности, включают IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF, онкостатин и IFN-α, IFN-β и IFN-γ.Proinflammatory cytokines specifically include IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23 , TNF-α, LT, LIF, oncostatin and IFN-α, IFN-β and IFN-γ.
Противовоспалительные цитокины, в частности, включают IL-4, IL-10, IL-11, W-13 и TGF-β.Anti-inflammatory cytokines specifically include IL-4, IL-10, IL-11, W-13 and TGF-β.
Хемокины, в частности, включают IL-8, Gro-α, MIP-1, MCP-1, ENA-78 и RANTES (хемокин, экспрессируемый и секретируемый T-клетками при активации).Chemokines specifically include IL-8, Gro-α, MIP-1, MCP-1, ENA-78, and RANTES (a chemokine expressed and secreted by T cells upon activation).
Если не упомянуто или не указано иное, то подробно описанные выше обозначенные цитокины включают в себя все возможные гомологические формы, которые могут быть подавлены указанными противовоспалительными соединениями (C). Гомологию определяют как взаимную схожесть между биологическими структурами, белками или последовательностями ДНК, которая проистекают от общего предшественника. Например, термин "IL-8" относится к IL-8 и всем гомологам IL-8, в частности, таким как IL-8Kc, IL-8MIP, IL-8LIX и другие подобные цитокины.Unless otherwise noted or indicated, the designated cytokines detailed above include all possible homologous forms that can be suppressed by the indicated anti-inflammatory compounds (C). Homology is defined as the mutual similarity between biological structures, proteins, or DNA sequences that stems from a common ancestor. For example, the term "IL-8" refers to IL-8 and all IL-8 homologues, such as IL-8 Kc , IL-8 MIP, IL-8 LIX and other such cytokines in particular.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИPHARMACEUTICAL COMPOSITIONS
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей терапевтически эффективное количество противовоспалительного соединения (C), определенного выше и определенного в любом одном из представленных в изобретении вариантов осуществления, в частности, противовоспалительного соединения (C) любого из определенных выше классов (I) - (III), и фармацевтически приемлемый носитель.In addition, the present invention relates to a pharmaceutical composition comprising a therapeutically effective amount of an anti-inflammatory compound (C) as defined above and as defined in any one of the embodiments presented in the invention, in particular, an anti-inflammatory compound (C) of any of the classes (I) defined above - (III), and a pharmaceutically acceptable carrier.
Далее по тексту, выражение "противовоспалительное соединение (C)" подразумевает, применительно к целям настоящего изобретения, как множественное число, так и единственное число, то есть это означает, что композиция по изобретению может включать одно или более чем одно противовоспалительное соединение (C)"Hereinafter, the expression "anti-inflammatory compound (C)" means, in relation to the purposes of the present invention, both the plural and the singular, that is, it means that the composition according to the invention may include one or more than one anti-inflammatory compound (C) "
В еще одном аспекте, это изобретение относится к способу приготовления подробно описанной выше фармацевтической композиции, который включает тщательное смешение фармацевтически приемлемого носителя с терапевтически эффективным количеством противовоспалительного соединения (C), определенного выше и определенного в любом одном из представленных в изобретении вариантах осуществления, в частности, противовоспалительным соединением (C) любого из определенных выше классов (I) - (III).In yet another aspect, this invention relates to a method of preparing a pharmaceutical composition as detailed above, which comprises intimately mixing a pharmaceutically acceptable carrier with a therapeutically effective amount of an anti-inflammatory compound (C) as defined above and as defined in any one of the embodiments of the invention, in particular , anti-inflammatory compound (C) of any of the above-defined classes (I) - (III).
Поэтому, указанные противовоспалительные соединения (C) по настоящему изобретению, в частности, противовоспалительные соединения (C) любого из определенных выше классов (I) - (III), могут быть приготовлены с целью их введения в виде различных лекарственных форм. В качестве подходящих композиций могут быть упомянуты все композиции, обычно применяемые для системного введения лекарственных средств. Для приготовления фармацевтических композиций по этому изобретению, эффективное количество конкретного соединения, необязательно в форме соли присоединения или комплекса с металлом, в качестве активного ингредиента объединяют путем тщательного смешения с фармацевтически приемлемым носителем, который может принимать большое разнообразие форм, в зависимости от формы препарата, требуемой для введения. Желательно, чтобы эти фармацевтические композиции представляли собой лекарственную форму с разовой дозой, в частности, для перорального, ректального, чрескожного или парентерального введения. Например, при приготовлении композиций в лекарственной форме для перорального введения, могут быть использованы общепринятые фармацевтические среды, такие как, например, вода, гликоли, масла, спирта и другие подобные среды, в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазывающие вещества, связующие вещества, разрыхлители и другие подобные вещества в случае порошков, пилюль, капсул и таблеток.Therefore, said anti-inflammatory compounds (C) of the present invention, in particular, anti-inflammatory compounds (C) of any of the classes (I) to (III) defined above, can be prepared to be administered in various dosage forms. As suitable compositions there may be mentioned all compositions commonly used for the systemic administration of drugs. For the preparation of pharmaceutical compositions of this invention, an effective amount of a particular compound, optionally in the form of an addition salt or a metal complex, as the active ingredient is combined by intimate mixing with a pharmaceutically acceptable carrier which may take a wide variety of forms, depending on the formulation desired. for an introduction. Desirably, these pharmaceutical compositions are in unit dosage form, in particular for oral, rectal, transdermal or parenteral administration. For example, when preparing compositions in a dosage form for oral administration, conventional pharmaceutical media can be used, such as, for example, water, glycols, oils, alcohols and the like, in the case of oral liquid preparations, such as suspensions, syrups, elixirs, emulsions and solutions; or solid carriers such as starches, sugars, kaolin, lubricants, binders, disintegrants and the like in the case of powders, pills, capsules and tablets.
В силу легкости введения, таблетки и капсулы представляют собой наиболее удобные пероральные лекарственные формы с разовой дозой, в случае которых конечно используют твердые фармацевтические носители. Для парентеральных композиций, носитель обычно включает стерильную воду, по меньшей мере, в значительной степени, хотя могут быть включены в состав и другие ингредиенты, например, для улучшения растворимости. Могут быть приготовлены инъецируемые растворы, в которых, например, носитель включает физиологический раствор, раствор глюкозы или раствор смеси физиологического раствор и глюкозы. Могут быть приготовлены также инъецируемые суспензии, в случае которых могут использоваться соответствующие жидкие носители, суспендирующие средства и другие подобные вещества. Кроме того, к ним относятся препараты в твердой форме, которые предназначены для превращения, непосредственно перед применением, в препараты в жидкой форме. В композициях, применяемых для чрескожного введения, носитель необязательно включает вещество для усиления проникновения лекарственного средства, и/или подходящее увлажняющее средство, необязательно объединенные с подходящими добавками любой природы в минорных количествах, которые не оказывают существенного вредного воздействия на кожу.Because of their ease of administration, tablets and capsules are the most convenient single dose oral dosage forms, in which case, of course, solid pharmaceutical carriers are used. For parenteral compositions, the carrier will usually comprise sterile water, at least in large part, although other ingredients may be included, for example, to improve solubility. Injectable solutions may be prepared in which, for example, the carrier comprises saline, glucose solution, or a mixture of saline and glucose solution. Injectable suspensions may also be prepared in which case appropriate liquid carriers, suspending agents and the like may be used. They also include solid form preparations which are intended to be converted, shortly before use, to liquid form preparations. In compositions used for transdermal administration, the carrier optionally comprises a drug penetration enhancer and/or a suitable wetting agent, optionally combined with suitable additives of any nature in minor amounts that do not cause significant adverse effects on the skin.
Противовоспалительное соединение (C), определенное выше и определенное в любом одном из представленных в изобретении вариантов осуществления, в частности, противовоспалительные соединения (C) любого из определенных выше классов (I) - (III), могут быть также введены путем пероральной ингаляции или инсуффляции с помощью методов и препаратов, используемых в фармацевтике для введения таким путем. Так, обычно, указанное в изобретении противовоспалительное соединение (C), в частности, противовоспалительные соединения (C) любого из определенных выше классов (I) - (III), могут быть введены в легкие в форме раствора, суспензии или сухого порошка, причем раствор является предпочтительной формой. Для введения соединений по настоящему изобретению подходит любая система, разработанная для доставки растворов, суспензий или сухих порошков путем пероральной ингаляции или инсуффляции.The anti-inflammatory compound (C) as defined above and as defined in any one of the embodiments of the invention, in particular the anti-inflammatory compounds (C) of any of the classes (I) to (III) defined above, may also be administered by oral inhalation or insufflation using methods and preparations used in pharmaceuticals for administration in this way. Thus, in general, the anti-inflammatory compound (C) specified in the invention, in particular, anti-inflammatory compounds (C) of any of the classes (I) to (III) defined above, can be administered to the lungs in the form of a solution, suspension or dry powder, and the solution is the preferred form. Any system designed to deliver solutions, suspensions, or dry powders by oral inhalation or insufflation is suitable for administering the compounds of the present invention.
Особенно удобно приготавливать упомянутые выше фармацевтические композиции в виде лекарственной формы с разовой дозой с точки зрения простоты введения и равномерности дозирования. Используемая в изобретении лекарственная форма с разовой дозой относится к физически дискретным элементам, подходящим в качестве разовых доз, при этом каждый элемент содержит заданное количество активного ингредиента, рассчитанное для продуцирования требуемого терапевтического эффекта, вместе с требуемым фармацевтическим носителем. Примерами таких лекарственных форм с разовой дозой являются таблетки (включающие таблетки с насечкой или таблетки, покрытые оболочкой), капсулы, пилюли, суппозитории, пакетики с порошком, капсулы-имплантаты, инъецируемые растворы или суспензии и другие подобные формы, и их разделенные кратные количества.It is particularly advantageous to formulate the above-mentioned pharmaceutical compositions in single dose dosage form from the viewpoint of ease of administration and uniformity of dosing. As used herein, a single dose dosage form refers to physically discrete units suitable as unit doses, each unit containing a predetermined amount of the active ingredient calculated to produce the desired therapeutic effect, together with the required pharmaceutical carrier. Examples of such unit dose dosage forms are tablets (including scored or coated tablets), capsules, pills, suppositories, powder sachets, implant capsules, injectable solutions or suspensions, and the like, and divided multiples thereof.
Следует иметь в виду, что термин "терапевтически эффективное количество" обычно относится к количеству активного соединения или компонента или лекарственного средства, которое позволяет достигнуть биологического или лекарственного ответа в ткани, системе, у животного или у человека, искомого, в свете настоящего изобретения, исследователем, ветеринаром, лечащим врачом или другим клиническим врачом, который включает облегчение симптомов заболевания, подвергаемого лечению.It should be understood that the term "therapeutically effective amount" generally refers to the amount of an active compound or component or drug that allows a biological or drug response to be achieved in a tissue, system, animal or human being sought, in light of the present invention, by the researcher. , veterinarian, physician or other clinician, which includes alleviating the symptoms of the disease being treated.
В настоящем изобретении предполагается, что терапевтически эффективное количество определенного выше противовоспалительного соединения (C), в частности, противовоспалительного соединения (C) любого из определенных выше классов (I) - (III), относится к количеству, достаточному для профилактического действия, стабилизации или облегчения заболевания, опосредованного, по меньшей мере, одним цитокином, выбранным из группы, состоящей из подробно описанных выше провоспалительных цитокинов, противовоспалительных цитокинов и хемокинов, в частности, по меньшей мере, одного цитокина, выбранных из группы, состоящей из IL-8, Gro-α, MIP-1, MCP-1, ENA-78 и RANTES, IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL- 9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF, онкостатина, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 и TGF-β, более предпочтительно, чтобы, по меньшей мере, один цитокин выбирали из группы, состоящей из IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 и IFN-γ, еще более предпочтительно, чтобы, по меньшей мере, один из указанных цитокинов выбирали из группы, состоящей из IL-8, IL-1β и IFN-γ.The present invention contemplates that a therapeutically effective amount of an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, refers to an amount sufficient to prevent, stabilize or alleviate disease mediated by at least one cytokine selected from the group consisting of pro-inflammatory cytokines, anti-inflammatory cytokines and chemokines described above, in particular at least one cytokine selected from the group consisting of IL-8, Gro- α, MIP-1, MCP-1, ENA-78 and RANTES, IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL- 17, IL-18, IL-23, TNF-α, LT, LIF, oncostatin, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 and TGF- β, more preferably at least one cytokine is selected from the group consisting of IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 and IFN-γ, even more preferably S, at least one of these cytokines was selected from the group consisting of IL-8, IL-1β and IFN-γ.
ПРИМЕНЕНИЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СОЕДИНЕНИЙ (C) И ФАРМАЦЕВТИЧЕСКИХ КОМПОЗИЦИЙ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ И ПРИ ЛЕЧЕНИИ ЗАБОЛЕВАНИЙUSE OF ANTI-INFLAMMATORY COMPOUNDS (C) AND PHARMACEUTICAL COMPOSITIONS AS MEDICINES AND IN THE TREATMENT OF DISEASES
Настоящее изобретение относится к определенному выше противовоспалительному соединению (C), в частности, к противовоспалительному соединению (C) любого из определенных выше классов (I) - (III), которое применяют в качестве лекарственного препарата.The present invention relates to an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, which is used as a medicine.
Настоящее изобретение также относится к фармацевтической композиции, включающей терапевтически эффективное количество противовоспалительного соединения (C), определенного выше и определенного в любом одном из представленных в изобретении вариантах осуществления, в частности, противовоспалительного соединения (C) любого из определенных выше классов (I) - (III), и фармацевтически приемлемый носитель, которую применяют в качестве лекарственного препарата.The present invention also relates to a pharmaceutical composition comprising a therapeutically effective amount of an anti-inflammatory compound (C) as defined above and as defined in any one of the embodiments presented in the invention, in particular, an anti-inflammatory compound (C) of any of the classes (I) defined above - ( III), and a pharmaceutically acceptable carrier that is used as a drug.
Настоящее изобретение относится к определенному выше противовоспалительному соединению (C), в частности, к противовоспалительному соединению (C) любого из определенных выше классов (I) - (III), которое применяют при лечении воспалительных заболеваний, выбранных из группы артрита, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, множественного склероза, системной эритематозной волчанки (SLE), панкреатита, склеродермии, диабета типа I, воспалительного заболевания желудочно-кишечного тракта, аллергического конъюнктивита, гломерулонефрита, синдрома Шегрена, увеита, дерматита, анкилозирующего спондилоартрита и фибромиалгии, предпочтительно, для применения при лечении воспалительных заболеваний желудочно-кишечного тракта, таких как острый гастрит, хронический гастрит, развитие и рецидив язвы желудка, болезнь Крона, воспалительное заболевание кишечника, синдром раздраженного кишечника и язвенный колит, более предпочтительно, для применения при лечении острого гастрита, хронического гастрита, развития и рецидива язвы желудка.The present invention relates to an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, which is used in the treatment of inflammatory diseases selected from the group of arthritis, rheumatoid arthritis, inflammatory bowel disease, psoriasis, multiple sclerosis, systemic lupus erythematosus (SLE), pancreatitis, scleroderma, type I diabetes, inflammatory bowel disease, allergic conjunctivitis, glomerulonephritis, Sjögren's syndrome, uveitis, dermatitis, ankylosing spondylitis and fibromyalgia, preferably for use in the treatment of inflammatory diseases of the gastrointestinal tract, such as acute gastritis, chronic gastritis, development and recurrence of gastric ulcers, Crohn's disease, inflammatory bowel disease, irritable bowel syndrome and ulcerative colitis, more preferably for use in the treatment of acute gastritis, chronic gastritis, development and recurrence of stomach ulcers.
Настоящее изобретение относится к определенному выше противовоспалительному соединению (C), в частности, к противовоспалительному соединению (C) любого из определенных выше классов (I) - (III), которое применяют при лечении связанных с воспалением заболеваний, выбранных из группы нейродегенеративного нарушения, застойной сердечной недостаточности, инсульта, стеноза аортального клапана, почечной недостаточности, аллергии, фиброза, атеросклероза, метаболического заболевания, сердечно-сосудистого заболевания, осложнения, связанного с применением химиотерапии/лучевой терапии, заболевания печени, нарушения работы желудочно-кишечного тракта, офтальмологического заболевания, диабетической ретинопатии, легочного заболевания и проказы.The present invention relates to an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, which is used in the treatment of inflammation-related diseases selected from the group of neurodegenerative disorder, congestive heart failure, stroke, aortic valve stenosis, renal failure, allergies, fibrosis, atherosclerosis, metabolic disease, cardiovascular disease, chemotherapy/radiation therapy complications, liver disease, gastrointestinal disorders, eye disease, diabetic retinopathy, lung disease and leprosy.
Следовательно, определенное выше противовоспалительное соединение (C), в частности, противовоспалительное соединение (C) любого из определенных выше классов (I) - (III), и определенная выше фармацевтическая композиция могут использоваться при производстве лекарственного препарата, применяемого для лечения, профилактики или противодействия расстройству или заболеванию, ассоциированного с экспрессией цитокинов, включая определенные выше воспалительные заболевания и определенные выше связанные с воспалением заболевания.Therefore, the anti-inflammatory compound (C) as defined above, in particular the anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, and the pharmaceutical composition as defined above can be used in the manufacture of a medicament used for the treatment, prevention or counteracting a disorder or disease associated with cytokine expression, including inflammatory diseases as defined above and inflammation-associated diseases as defined above.
Настоящее изобретение относится к определенному выше противовоспалительному соединению (C), в частности, к противовоспалительному соединению (C) любого из определенных выше классов (I) - (III), которое применяют при лечении заболевания, опосредованного, по меньшей мере, одним цитокином.The present invention relates to an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, which is used in the treatment of a disease mediated by at least one cytokine.
По меньшей мере, один цитокин предпочтительно выбирать из группы, состоящей из подробно описанных выше провоспалительных цитокинов, противовоспалительных цитокинов и хемокинов, предпочтительно, чтобы, по меньшей мере, один цитокин выбирали из группы, состоящей из IL-8, Gro-α, MIP-1, MCP-1, ENA-78 и RANTES, IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL- 9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF, онкостатина, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 и TGF-β, более предпочтительно, чтобы, по меньшей мере, один цитокин выбирали из группы, состоящей из IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 и IFN-γ, еще более предпочтительно, чтобы, по меньшей мере, один из указанных цитокинов выбирали из группы, состоящей из IL-8, IL-1β и IFN-γ.At least one cytokine is preferably selected from the group consisting of pro-inflammatory cytokines, anti-inflammatory cytokines and chemokines as detailed above, preferably at least one cytokine is selected from the group consisting of IL-8, Gro-α, MIP- 1, MCP-1, ENA-78 and RANTES, IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL- 18, IL-23, TNF-α, LT, LIF, oncostatin, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 and TGF-β, more preferably that at least one cytokine is selected from the group consisting of IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 and IFN-γ , even more preferably, at least one of these cytokines is selected from the group consisting of IL-8, IL-1β and IFN-γ.
Для специалистов в области медицины хорошо известно, что величина точной дозы и частота введения зависят от используемого указанного в изобретении конкретного противовоспалительного соединения (C), конкретного состояния, подвергаемого лечению, тяжести состояния, подвергаемого лечению, возраста, массы тела, пола, степени расстройства и общего физического состояния конкретного пациента, а также от другого лекарственного препарата, который пациент может принимать. Кроме того, очевидно, что указанное эффективное суточное количество может быть уменьшено или увеличено в зависимости от ответа подвергаемого лечению субъекта и/или в зависимости от оценки лечащего врача, прописавшего применение соединений по настоящему изобретению.It is well known to those skilled in the art of medicine that the exact dosage and frequency of administration depend on the specific anti-inflammatory compound (C) used, the particular condition being treated, the severity of the condition being treated, age, body weight, sex, degree of disorder, and general physical condition of a particular patient, as well as from another drug that the patient may be taking. In addition, it is obvious that the specified effective daily amount can be reduced or increased depending on the response of the subject being treated and/or depending on the judgment of the attending physician who prescribed the use of the compounds of the present invention.
Как было указано выше, подробно описанное выше противовоспалительное соединение (C) по настоящему изобретению может воздействовать на воспалительные механизмы у животных.As mentioned above, the above-described anti-inflammatory compound (C) of the present invention can act on inflammatory mechanisms in animals.
В случае введения животным, определенное выше противовоспалительное соединение (C), в частности, противовоспалительное соединение (C) любого из определенных выше классов (I) - (III), и определенная выше фармацевтическая композиция, включающая, по меньшей мере, одно из указанных противовоспалительных соединений (C) в качестве активного ингредиента, могут быть добавлены в корм или питьевую воду для животного, могут быть введены путем обрызгивания в качестве пробиотика самке, кормящей молоком детенышей, могут быть введены в форме болюса с замедленным высвобождением или в форме камня для лизания.In the case of administration to animals, an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, and a pharmaceutical composition as defined above comprising at least one of said anti-inflammatory compounds (C) as an active ingredient, can be added to animal feed or drinking water, can be administered by spraying as a probiotic to a nursing female, can be administered in the form of a sustained release bolus or in the form of a lick stone.
Эффективное количество определенного выше противовоспалительного соединения (C), в частности, противовоспалительного соединения (C) любого из определенных выше (I) - (III), которое специфически подавляет или тормозит экспрессию, по меньшей мере, одного подробно описанного выше цитокина, для лечения животных составляет, предпочтительно, по меньшей мере, 1 ppm, предпочтительно, по меньшей мере, 2 ppm, более предпочтительно, по меньшей мере, 3 ppm, в расчете на суммарную массу корма для животного. С другой стороны, эффективное количество определенного выше противовоспалительного соединения (C), в частности, противовоспалительного соединения (C) любого из определенных выше (I) - (III), композиции (C) составляет, предпочтительно, менее чем 130 ppm, предпочтительно, менее чем 70 ppm, более предпочтительно, менее чем 35 ppm, в расчете на суммарную массу корма для животного, где животное в этом случае представляет собой грызуна, в частности, мышь. Следует иметь в виду, что, применительно к целям настоящего изобретения, величина верхнего предела не является критически важной, и эффективное количество зависит от конкретного вида животного, подвергаемого лечению. Изобретение, кроме того, относится к корму для животного, включающему определенное выше противовоспалительное соединение (C), в частности, противовоспалительное соединение (C) любого из определенных выше классов (I) - (III), фармацевтическую композицию, включающую указанное противовоспалительное соединение (C) в качестве активного ингредиента.An effective amount of an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of (I) to (III) as defined above, which specifically suppresses or inhibits the expression of at least one cytokine detailed above, for the treatment of animals is preferably at least 1 ppm, preferably at least 2 ppm, more preferably at least 3 ppm, based on the total weight of the animal feed. On the other hand, the effective amount of the anti-inflammatory compound (C) defined above, in particular the anti-inflammatory compound (C) of any of the above (I) to (III), composition (C) is preferably less than 130 ppm, preferably less than than 70 ppm, more preferably less than 35 ppm, based on the total weight of the animal feed, where the animal in this case is a rodent, in particular a mouse. It should be borne in mind that, in relation to the purposes of the present invention, the value of the upper limit is not critical, and the effective amount depends on the particular species of animal being treated. The invention further relates to an animal feed comprising an anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above, a pharmaceutical composition comprising said anti-inflammatory compound (C ) as the active ingredient.
СПОСОБЫ ЛЕЧЕНИЯ воспалительныХ заболеваниЙ С ПРИМЕНЕНИЕМ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СОЕДИНЕНИЙ (C) METHODS OF TREATMENT OF INFLAMMATORY DISEASES USING ANTI-INFLAMMATORY COMPOUNDS (C)
Настоящее изобретение относится к in vivo способу подавления или торможения ответных воспалительных реакций путем применения, по меньшей мере, одного определенного выше противовоспалительного соединения (C), в частности, противовоспалительного соединения (C) любого из классов (I) - (III), определенных выше и определенных в любом одном из представленных в изобретении вариантов осуществления.The present invention relates to an in vivo method for suppressing or inhibiting inflammatory responses by using at least one anti-inflammatory compound (C) as defined above, in particular an anti-inflammatory compound (C) of any of the classes (I) to (III) defined above. and defined in any one of the embodiments of the invention.
Кроме того, настоящее изобретение относится к способу подавления или торможения экспрессии, по меньшей мере, одного цитокина, у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в этом, количества противовоспалительного соединения (C), определенного выше и определенного в любом одном из представленных в изобретении вариантах осуществления, достаточного для торможения или подавления экспрессии, по меньшей мере, одного цитокина, где цитокин выбирают из группы, состоящей из IL-8, Gro-α, MIP-1, MCP-1, ENA-78 и RANTES, IL-1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23,TNF-α, LT, LIF, онкостатина, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 and TGF-β, более предпочтительно, чтобы, по меньшей мере, один цитокин выбирали из группы, состоящей из IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 и IFN-γ, еще более предпочтительно, чтобы, по меньшей мере, один из указанных цитокинов выбирали из группы, состоящей из IL-8, IL-1β и IFN-γ.In addition, the present invention relates to a method for suppressing or inhibiting the expression of at least one cytokine in a mammal, which method includes administering to a mammal in need thereof an amount of an anti-inflammatory compound (C) as defined above and as defined in any one of the following. in the invention embodiments, sufficient to inhibit or suppress the expression of at least one cytokine, where the cytokine is selected from the group consisting of IL-8, Gro-α, MIP-1, MCP-1, ENA-78 and RANTES, IL -1α, IL-1β, IL-2, IL-3, IL-6, IL-7, IL-9, IL-12, IL-17, IL-18, IL-23, TNF-α, LT, LIF , oncostatin, IFN-α, IFN-β, IFN-γ, IL-4, IL-10, IL-11, W-13 and TGF-β, more preferably at least one cytokine is selected from the group, consisting of IL-8, IL-4, IL-6, IL-10, TNF-α, TNF-β, IL-17, IL-23 and IFN-γ, even more preferably at least one of these cytokines were selected from the group consisting of IL-8, IL-1β and IFN-γ.
Кроме того, настоящее изобретение относится к способу лечения связанных с воспалением заболеваний, ассоциированных с уровнями экспрессии цитокинов у млекопитающих, где указанный способ включает введение млекопитающему, нуждающемуся в этом, количества противовоспалительного соединения (C), определенного выше и определенного в любом одном из представленных в изобретении вариантах осуществления, эффективного для лечения указанного связанного с воспалением заболевания.In addition, the present invention relates to a method of treating inflammation-related diseases associated with cytokine expression levels in a mammal, which method includes administering to a mammal in need thereof an amount of an anti-inflammatory compound (C) as defined above and as defined in any one of those presented in embodiments of the invention effective for treating said inflammation-related disease.
Приведенные далее примеры являются только иллюстрациями неограничивающих вариантов осуществления настоящего изобретения.The following examples are only illustrations of non-limiting embodiments of the present invention.
ПРИМЕРЫEXAMPLES
МАТЕРИАЛЫMATERIALS
а) Постановка экспериментаa) Setting up the experiment
Эксперименты проводили на экспериментальной модели на мышах с целью оценки влияния кормовых добавок с флавомицином® в качестве противовоспалительного соединения (C).Experiments were carried out in a mouse model to evaluate the effect of feed additives with flavomycin® as an anti-inflammatory compound (C).
Для in vivo экспериментов был выбран штамм мышей BALB/c в связи с тем, что у этого штамма мышей более выражена патология желудка по сравнению с другими штаммами мышей. Мышей подразделяли на 4 группы по 8 животных в каждой. 4 группы имеют следующие характеристики:For in vivo experiments, the BALB/c mouse strain was chosen due to the fact that this strain of mice has a more pronounced pathology of the stomach compared to other strains of mice. Mice were divided into 4 groups of 8 animals each. The 4 groups have the following characteristics:
1) инфицированная + стандартный рацион: сравнительный пример 11) infected + standard diet: comparative example 1
Мышам группы "сравнительного примера 1" дважды инокулировали внутрижелудочно 108 жизнеспособных бактерий штамма Helicobacter Suis (H.suis) HS1 в течение 48 часов (в день 8 и день 9). В день 17, мышам представляли неограниченный доступ к контрольному рациону (стандартному рациону без флавомицина®). Через 73 дня, мышей умерщвляли путем смещения шейных позвонков при глубокой анестезии с помощью изофлурана. Брали полоску желудочной ткани для выполнения описанных ниже экспериментальных процедур.Mice of the "comparative example 1" group were inoculated intragastrically with 108 viable Helicobacter suis (H. suis) HS1 strains twice for 48 hours (day 8 and day 9). On day 17, mice were given ad libitum access to the control diet (standard diet without flavomycin®). After 73 days, mice were sacrificed by dislocation of the cervical vertebrae under deep anesthesia with isoflurane. A strip of gastric tissue was taken to perform the experimental procedures described below.
2) инфицированная + рацион с добавлением флавомицина® (количество флавомицина® <100 ppm в расчете на суммарное количество предоставляемого рациона): пример 12) Infected + Flavomycin® Supplemented Diet (Amount of Flavomycin® <100 ppm based on total diet provided): Example 1
Мышам группы "примера 1" дважды инокулировали внутрижелудочно 108 жизнеспособных бактерий штамма Helicobacter Suis (H.suis) HS1 в течение 48 часов (в день 8 и день 9). В день 17, мышам представляли неограниченный доступ к рациону с добавкой флавомицина® (количество флавомицина® <100 ppm в расчете на суммарное количество предоставляемого рациона). Через 73 дня, мышей умерщвляли путем смещения шейных позвонков при глубокой анестезии с помощью изофлурана. Брали полоску желудочной ткани для выполнения описанных ниже экспериментальных процедур.Mice of the "Example 1" group were inoculated twice intragastrically with 108 viable Helicobacter Suis (H. suis) HS1 strain bacteria for 48 hours (Day 8 and Day 9). On day 17, mice were given ad libitum access to the flavomycin® supplemented diet (flavomycin® <100 ppm based on total diet provided). After 73 days, mice were sacrificed by dislocation of the cervical vertebrae under deep anesthesia with isoflurane. A strip of gastric tissue was taken to perform the experimental procedures described below.
3) неинфицированная + стандартный рацион: сравнительный пример 23) non-infected + standard diet: comparative example 2
Мышей группы "сравнительного примера 2" не подвергали внутрижелудочной инокуляции, и им представляли неограниченный доступ к контрольному корму, стандартному рациону без флавомицина®. Через 73 дня, мышей умерщвляли путем смещения шейных позвонков при глубокой анестезии с помощью изофлурана. Брали полоску желудочной ткани для выполнения описанных ниже экспериментальных процедур.The mice of the "comparative example 2" group were not subjected to intragastric inoculation and were given ad libitum access to the control chow, a standard diet without flavomycin®. After 73 days, mice were sacrificed by dislocation of the cervical vertebrae under deep anesthesia with isoflurane. A strip of gastric tissue was taken to perform the experimental procedures described below.
4) неинфицированная + рацион с добавлением флавомицина® (количество флавомицина® <100 ppm в расчете на суммарное количество предоставляемого корма): пример 24) Uninfected + Flavomycin® Supplemented Diet (Amount of Flavomycin® <100 ppm based on total feed provided): Example 2
Мышей группы "примера 2" не подвергали внутрижелудочной инокуляции, и им представляли неограниченный доступ к рациону с добавлением флавомицина® (количество флавомицина® <100 ppm в расчете на суммарное количество предоставляемого рациона). Через 73 дня, мышей умерщвляли путем смещения шейных позвонков при глубокой анестезии с помощью изофлурана. Брали полоску желудочной ткани для выполнения описанных ниже экспериментальных процедур.Mice of the "Example 2" group were not subjected to intragastric inoculation and were given ad libitum access to the diet supplemented with flavomycin® (amount of flavomycin® <100 ppm based on the total amount of diet provided). After 73 days, mice were sacrificed by dislocation of the cervical vertebrae under deep anesthesia with isoflurane. A strip of gastric tissue was taken to perform the experimental procedures described below.
b) Верификация постановки эксперимента - количественное определение H. suisb) Verification of the experimental setup - quantification of H. suis
Наличие инфекции H.suis определяли методом полимеразной цепной реакции в реальном времени (qRT-PCR). Эксперименты проводили так, как это подробно описано ниже. В таблице 1 показано, что группы "сравнительного примера 1" и "примера 1" инфицированы бактериями H.suis. Группы "сравнительного примера 2" и "примера 2" не инфицированы, как показано в таблице 1, поскольку у этих животных бактерии H.suis не были обнаружены.The presence of H. suis infection was determined by real-time polymerase chain reaction (qRT-PCR). Experiments were carried out as detailed below. Table 1 shows that the "Comparative Example 1" and "Example 1" groups were infected with H. suis bacteria. The "Comparative Example 2" and "Example 2" groups were not infected as shown in Table 1 because H. suis bacteria were not detected in these animals.
Таблица 1. Определение наличия инфекции H.suis методом qRT-PCR, выраженного в логарифмических соотношениях H. Suis на мг ткани (абсолютное количественное определение нуклеиновой кислоты (количество бактериальной ДНК) на данное количество образца (мг ткани).Table 1. Determination of the presence of H. suis infection by qRT-PCR expressed as logarithmic ratios of H. suis per mg of tissue (absolute nucleic acid quantitation (amount of bacterial DNA) per given amount of sample (mg of tissue).
МЕТОДЫMETHODS
Анализ методом полимеразной цепной реакции в реальном времени (qRT-PCR)Real-time polymerase chain reaction (qRT-PCR) analysis
1) Количественное определение H.suis1) Quantification of H.suis
Количественное определение образования колоний H. suis в желудке проводили в соответствии с публикациями Blaecher C. et al. (2013) и J.L. et al. (2004). Присутствие ДНК H.suis в экстрактах определяли с использованием специфичного для H. suis метода qRT-PCR с абсолютной количественной оценкой, основанной на гене ureA (Blaecher C. et al. (2013)). Сначала генерировали стандарт путем амплификации части кластера генов ureAB (1236 п.о.) из штамма H.suis HS5 с использованием праймеров U430F и U1735R ( J.L. et al. (2004)). Вкратце, реакции амплификации PCR включали 1 × реакционный буфер [67 мМ Tris/HCl, 16 мМ (NH4)2SO4, 0,45% Triton Х-100, 0,2% желатин], одну единицу ДНК-полимеразы Taq (Biotech International), 200 мкМ каждого дезоксинуклеотидтрифосфата, 2 мМ MgCl2, 10 пмоль каждого олигонуклеотидного праймера и 1 мкл разведенной ДНК (обычно разведение исходного образца в соотношении 1:10, содержащее приблизительно 20-100 нг/мкл) в конечном объеме 50 мкл. Условиями циклирования были начальная денатурация при 94°С в течение 3 минут, затем 35 циклов при 94°С в течение 10 секунд, 52°С в течение 30 секунд и 72°С в течение 1,5 минут с последующей конечной стадией элонгации при 72°С в течение 5 минут. Все реакции проводили с использованием термоциклера Perkin Elmer PE2400. Продукты PCR разделяли на мини-гелях с агарозой в буфере TAE (40 мМ Tris/ацетат, 1 мМ ЭДТА) и фотографировали при УФ-трансиллюминации после окрашивания бромидом этидия. Продукты PCR очищали перед секвенированием с помощью системы очистки Wizard PCR Preps DNA Purification System (Promega) или фильтров Centricon-100 (Amicon). Затем амплифицированную ДНК непосредственно секвенировали с использованием набора для секвенирования циклов ABI PRISM Ready Reaction DyeDeoxy Terminator Cycle Sequencing Kit (PE Applied Biosystems) и системы GeneAmp® PCR System 2400 (Perkin Elmer) в соответствии с протоколами фирм-производителей. Продукты секвенирования разделяли на секвенаторах model 377 DNA Sequencer и анализировали с использованием программ, содержащихся в прилагаемом пакете (PE Applied Biosystems). Во всех случаях, обе цепи ДНК секвенировали с помощью непрерывных перекрытий. После получения стандарта, были сделаны 10-кратные разведения, начиная с 108 ампликонов PCR, для каждого 9 мкл реакционной смеси. Один микролитр экстрагированной ДНК-матрицы добавляли к 9 мкл реакционной смеси, состоящей из 0,25 мкл обоих праймеров, расположенных внутри фрагмента 1236 п.о. (для получения продукта PCR 150 п.о.), 3,5 мкл воды хроматографической чистоты и 5 мкл SensiMix™ SYBR No-ROX (Bioline Reagents Ltd, London, UK). Смысловой праймер представлял собой BF_HsuisF1: 5'-AAA ACA MAG GCG ATC GCC CTG TA-3'. Антисмысловой праймер представлял собой BF_Hsuis R1: 5'-TTT CTT CGC CAG GTT CAA AGC G-3'. Температура отжига составила 62°С. Оба стандарта и образцы были подвергнуты двум параллельным анализам на системе CFX96™ RT-PCR System с термоциклером C1000 Thermal Cycler (Bio-Rad, Hercules, CA, USA). Результаты выражены в единицах абсолютного количества нуклеиновой кислоты (количества бактериальной ДНК) на данное количество образца (мг ткани).Quantification of the formation of H. suis colonies in the stomach was carried out in accordance with the publications of Blaecher C. et al. (2013) and JL et al. (2004). The presence of H. suis DNA in the extracts was determined using the H. suis-specific qRT-PCR method with absolute quantification based on the ureA gene (Blaecher C. et al. (2013)). First, a standard was generated by amplifying a portion of the ureAB gene cluster (1236 bp) from the H. suis HS5 strain using primers U430F and U1735R ( JL et al. (2004)). Briefly, PCR amplification reactions included 1× reaction buffer [67 mM Tris/HCl, 16 mM (NH 4 ) 2 SO 4 , 0.45% Triton X-100, 0.2% gelatin], one unit of Taq DNA polymerase ( Biotech International), 200 μM of each deoxynucleotide triphosphate, 2 mM MgCl 2 , 10 pmol of each oligonucleotide primer, and 1 μl of diluted DNA (typically a 1:10 dilution of the original sample containing approximately 20-100 ng/μl) in a final volume of 50 μl. Cycling conditions were initial denaturation at 94°C for 3 minutes followed by 35 cycles at 94°C for 10 seconds, 52°C for 30 seconds and 72°C for 1.5 minutes followed by a final elongation step at 72 °C for 5 minutes. All reactions were performed using a Perkin Elmer PE2400 thermal cycler. PCR products were resolved on agarose mini-gels in TAE buffer (40 mM Tris/acetate, 1 mM EDTA) and photographed under UV transillumination after staining with ethidium bromide. PCR products were purified prior to sequencing using the Wizard PCR Preps DNA Purification System (Promega) or Centricon-100 filters (Amicon). The amplified DNA was then directly sequenced using the ABI PRISM Ready Reaction DyeDeoxy Terminator Cycle Sequencing Kit (PE Applied Biosystems) and GeneAmp® PCR System 2400 (Perkin Elmer) according to the manufacturer's protocols. The sequencing products were separated on model 377 DNA Sequencers and analyzed using the programs contained in the attached package (PE Applied Biosystems). In all cases, both strands of DNA were sequenced using continuous overlaps. After obtaining the standard, 10-fold dilutions were made, starting with 108 PCR amplicons, for each 9 μl of the reaction mixture. One microliter of the extracted DNA template was added to 9 μl of the reaction mixture consisting of 0.25 μl of both primers located within the 1236 bp fragment. (to obtain a 150 bp PCR product), 3.5 µl chromatographic grade water, and 5 µl SensiMix™ SYBR No-ROX (Bioline Reagents Ltd, London, UK). The sense primer was BF_HsuisF1: 5'-AAA ACA MAG GCG ATC GCC CTG TA-3'. The antisense primer was BF_Hsuis R1: 5'-TTT CTT CGC CAG GTT CAA AGC G-3'. The annealing temperature was 62°C. Both standards and samples were run in duplicate on the CFX96™ RT-PCR System with C1000 Thermal Cycler (Bio-Rad, Hercules, CA, USA). The results are expressed in terms of the absolute amount of nucleic acid (amount of bacterial DNA) per given amount of sample (mg of tissue).
2). Уровни экспрессии цитокинов2). Cytokine expression levels
Оценку уровней экспрессии цитокинов проводили методом qRT-PCR в соответствии с публикациями Flahou B. et al. (2012) и Liu C. et al. (2016). РНК экстрагировали с использованием набора RNeasy Mini Kit® (Qiagen, Hilden, Germany) в соответствии с инструкциями фирмы-производителя. Полученные концентрации РНК измеряли с использованием спектрофотометра NanoDrop® (Isogen Life Science, Utrecht, The Netherlands)), после чего концентрацию всех образцов, взятых у всех мышей, принадлежащих к 4 группам, определенным выше в разделе постановка эксперимента, доводили до 1 мкг/мкл, затем синтезировали кДНК с использованием набора iScript™ cDNA Synthesis Kit (Bio-Rad, California, USA). Затем проводили анализ экспрессии для генов, кодирующих факторы хозяина, вовлеченные в воспаление. Конститутивные гены PPIa, H2afz и HPRT были включены в качестве эталонных генов. Все используемые последовательности праймеров приведены в таблице 2. Уровни экспрессии мРНК эталонного и целевого генов определяли количественно с использованием метода полимеразной цепной реакции с обратной транскриптазой (RT-PCR), описанного ранее (Flahou B. et al. (2012)). Использовали контролируемые без применения матрицы реакционные смеси, и все указанные образцы подвергали двум параллельным анализам. Значения порогового цикла (Ct) сначала нормализовали по среднему геометрическому значению Ct из эталонных генов. Кратность изменений рассчитывали методом ΔΔCT (72) по средним значениям Ct у мышей с отрицательным результатом на присутствие H. suis. И наконец, для каждого целевого гена, выражали результаты в виде кратности изменений уровней экспрессии мРНК у мышей, положительных по H.suis, относительно уровней экспрессии мРНК у мышей, отрицательных по H.suis. Результаты приведены в таблицах 3 и 4 ниже.Cytokine expression levels were assessed by qRT-PCR according to Flahou B. et al. (2012) and Liu C. et al. (2016). RNA was extracted using the RNeasy Mini Kit® (Qiagen, Hilden, Germany) according to the manufacturer's instructions. The resulting RNA concentrations were measured using a NanoDrop® spectrophotometer (Isogen Life Science, Utrecht, The Netherlands), after which the concentration of all samples taken from all mice belonging to the 4 groups defined above in the experimental setup section was adjusted to 1 µg/µl , then cDNA was synthesized using the iScript™ cDNA Synthesis Kit (Bio-Rad, California, USA). Then, expression analysis was performed for genes encoding host factors involved in inflammation. The constitutive genes PPIa, H2afz and HPRT were included as reference genes. All primer sequences used are shown in Table 2. mRNA expression levels of the reference and target genes were quantified using the reverse transcriptase polymerase chain reaction (RT-PCR) method described previously (Flahou B. et al. (2012)). Matrix-controlled reaction mixtures were used and all of these samples were subjected to two replicate analyses. Cycle threshold (Ct) values were first normalized to the geometric mean Ct of the reference genes. The multiplicity of changes was calculated by the ΔΔCT method (72) from the average Ct values in mice with a negative result for the presence of H. suis. Finally, for each target gene, the results were expressed as fold changes in mRNA expression levels in H. suis positive mice relative to mRNA expression levels in H. suis negative mice. The results are shown in tables 3 and 4 below.
Таблица 2. Последовательности праймеров, использованных в методе qRT-PCRTable 2. Primer sequences used in the qRT-PCR method
Иммуногистохимические исследования - определение иммуногистохимии Т-клеток, В-клеток, париетальных клеток, некротических клеток и инфильтрации макрофаговImmunohistochemical studies - determination of immunohistochemistry of T cells, B cells, parietal cells, necrotic cells and macrophage infiltration
Иммуногистохимические исследования проводили в соответствии с публикацией Flahou B. et al. (2010). Изготавливали следующие друг за другом гистологические срезы толщиной 5 мкм из залитых в парафин тканей. После регидратации и депарафинизации, проводили индуцированное нагреванием демаскирование антигена в цитратном буфере (рН 6,0) с использованием микроволновой печи. Микроскопические препараты инкубировали с 3% H2O2 в метаноле (5 минут) и 30% козьей сывороткой (30 минут) для блокирования активности эндогенной пероксидазы и неспецифических реакций, соответственно. Дифференцирование между Т- и В-лимфоцитами проводили путем окрашивания антигенов CD3 и CD20. Антигены CD3 обнаруживали с использованием поликлонального кроличьего антитела против CD3 (1/100; DakoCytomation). Антигены CD20 обнаруживали с использованием поликлонального кроличьего антитела против CD20 (1/100; Thermo Scientific, Fremont, USA), соответственно. За инкубацией с первичными антителами против CD3 и CD20, следовала инкубация с биотинилированным козьим анти-кроличьим антителом IgG (1/500; DakoCytomation). После промывания, срезы инкубировали с комплексом стрептавидин-биотин-HRP (DakoCytomation) и окрашивали с помощью тетрагидрохлорида диаминобензидина (DAB) и H2O2. Для выделения зрелых макрофагов использовали первичное антитело против маркера клеточной поверхности F4/80 (1/50; Santa Cruz Biotechnology, Inc., Santa Cruz, USA). Обнаружение проводили с использованием системы окрашивания ABC для крыс (Santa Cruz Biotechnology, Inc.). Апоптозные клетки идентифицировали путем иммуногистохимического окрашивания с использованием кроличьего поликлонального антитела против активной каспазы-3 и анти-кроличьего набора для окрашивания клеток и тканей HRP-AEC (R & D Systems, Minneapolis, USA). Париетальные клетки идентифицировали путем иммуногистохимического окрашивания для водородно-калиевой аденозинтрифосфатазы с использованием мышиного моноклонального антитела (1/200; Abcam Ltd, Кембридж, Великобритания) и биотинилированного козьего антимышиного IgG-антитела (1/200; DakoCytomation). Апоптозные клетки идентифицировали путем иммуногистохимического окрашивания с использованием кроличьего поликлонального антитела против активной каспазы-3 и анти-кроличьего набора для окрашивания клеток и тканей HRP-AEC (R & D Systems, Minneapolis, USA). Париетальные клетки идентифицировали путем иммуногистохимического окрашивания для водородно-калиевой аденозинтрифосфатазы с использованием мышиного моноклонального антитела (1/200; Abcam Ltd, Cambridge, UK) и биотинилированного козьего анти-мышиного IgG-антитела (1/200; DakoCytomation). И наконец, подсчитывали положительные клетки в пяти случайно выбранных полях зрения микроскопа под большим увеличением (увеличение: х400). Затем для каждой мыши определяли среднее число положительных клеток. Все результаты представлены в таблицах 5, 6, 7 и 8.Immunohistochemical studies were performed in accordance with the publication of Flahou B. et al. (2010). Histological sections successively 5 μm thick were made from paraffin-embedded tissues. After rehydration and deparaffinization, heat-induced antigen unmasking was performed in citrate buffer (pH 6.0) using a microwave oven. Slides were incubated with 3% H 2 O 2 in methanol (5 minutes) and 30% goat serum (30 minutes) to block endogenous peroxidase activity and non-specific reactions, respectively. Differentiation between T and B lymphocytes was performed by staining for CD3 and CD20 antigens. CD3 antigens were detected using a polyclonal rabbit anti-CD3 antibody (1/100; DakoCytomation). CD20 antigens were detected using a polyclonal anti-CD20 rabbit antibody (1/100; Thermo Scientific, Fremont, USA), respectively. Incubation with primary antibodies against CD3 and CD20 was followed by incubation with biotinylated goat anti-rabbit IgG (1/500; DakoCytomation). After washing, sections were incubated with streptavidin-biotin-HRP complex (DakoCytomation) and stained with diaminobenzidine tetrahydrochloride (DAB) and H 2 O 2 . Primary antibody against cell surface marker F4/80 (1/50; Santa Cruz Biotechnology, Inc., Santa Cruz, USA) was used to isolate mature macrophages. Detection was performed using a rat ABC staining system (Santa Cruz Biotechnology, Inc.). Apoptotic cells were identified by immunohistochemical staining using a rabbit polyclonal antibody against active caspase-3 and an anti-rabbit HRP-AEC cell and tissue staining kit (R&D Systems, Minneapolis, USA). Parietal cells were identified by immunohistochemical staining for hydrogen potassium adenosine triphosphatase using a mouse monoclonal antibody (1/200; Abcam Ltd, Cambridge, UK) and a biotinylated goat anti-mouse IgG antibody (1/200; DakoCytomation). Apoptotic cells were identified by immunohistochemical staining using a rabbit polyclonal antibody against active caspase-3 and an anti-rabbit HRP-AEC cell and tissue staining kit (R&D Systems, Minneapolis, USA). Parietal cells were identified by immunohistochemical staining for hydrogen potassium adenosine triphosphatase using a mouse monoclonal antibody (1/200; Abcam Ltd, Cambridge, UK) and a biotinylated goat anti-mouse IgG antibody (1/200; DakoCytomation). Finally, positive cells were counted in five randomly selected high magnification microscope fields (magnification: x400). The average number of positive cells was then determined for each mouse. All results are presented in tables 5, 6, 7 and 8.
РЕЗУЛЬТАТЫRESULTS
Эксперимент 1Experiment 1
Измерение уровней экспрессии цитокинов у H.suis инфицированных животных путем использования подробно описанного выше метода qRT-PCR.Measurement of cytokine expression levels in H. suis infected animals using the qRT-PCR method described in detail above.
Таблица 3. Результаты эксперимента по проведению исследования qRT-PCR для определения воздействия добавки флавомицинаи на уровни цитокинов у H.Suis инфицированных животных, выраженные в виде кратности изменения уровней экспрессии мРНК.Table 3. Results of a qRT-PCR experiment to determine the effects of flavomycin supplementation and on cytokine levels in H. Suis infected animals, expressed as fold change in mRNA expression levels.
В таблице 3 показано снижение уровней экспрессии IL-1β, IL-8MIP и IFN-γ у инфицированных животных, получавших рацион с добавкой флавомицина® (пример 1) по сравнению с контрольной группой, получавшей стандартный рацион (сравнительный пример 1). Table 3 shows the reduction in expression levels of IL-1β, IL-8MIP and IFN-γ in infected animals fed a diet supplemented with flavomycin® (Example 1) compared to a control group fed a standard diet (Comparative Example 1).
Эксперимент 2Experiment 2
Измерение уровней экспрессии цитокина в отсутствии инфекции H.suis путем использования подробно описанного выше метода qRT-PCR.Measurement of cytokine expression levels in the absence of H. suis infection using the qRT-PCR method detailed above.
Таблица 4. Результаты эксперимента по проведению исследования qRT-PCR для определения воздействия добавки флавомицина® на уровни цитокинов у неинфицированных животных, выраженные в виде кратности изменения уровней экспрессии мРНК.Table 4 Results of a qRT-PCR experiment to determine the effect of flavomycin® supplementation on cytokine levels in uninfected animals, expressed as fold change in mRNA expression levels.
В таблице 4 показано снижение экспрессии IL-1β даже в отсутствии инфекции. Уровни экспрессии IL-8MIP остаются стабильными, при этом наблюдается небольшое повышение экспрессии IFN-γ.Table 4 shows the decrease in IL-1β expression even in the absence of infection. IL-8MIP expression levels remain stable, with a slight increase in IFN-γ expression.
Эксперимент 3Experiment 3
Оценка ответной воспалительной реакции у H.suis инфицированных животных путем проведения подробно описанных выше иммуногистохимических исследований.Evaluation of the inflammatory response in H. suis infected animals by conducting the immunohistochemical studies described in detail above.
Таблица 5. Результаты иммуногистохимических исследований по определению воздействия добавки флавомицина® на число инфильтрирующих T-клеток, B-клеток и макрофагов у H.Suis инфицированных животных, выраженные в виде среднего числа подсчитанных положительных клеток.Table 5. Results of immunohistochemical studies to determine the effect of flavomycin® supplementation on the number of infiltrating T cells, B cells and macrophages in H. Suis infected animals, expressed as the mean number of positive cells counted.
В таблице 5 показано сильное уменьшение числа инфильтрирующих T-клеток, B-клеток и макрофагов у мышей, инфицированных H. suis и подвергнутых лечению с помощью флавомицина® (пример 1) по сравнению со сравнительным примером 1.Table 5 shows a strong decrease in the number of infiltrating T cells, B cells and macrophages in H. suis infected mice treated with flavomycin® (Example 1) compared to Comparative Example 1.
Эксперимент 4Experiment 4
Оценка ответной воспалительной реакции при отсутствии инфекции H.suis путем проведения подробно описанных выше иммуногистохимических исследований.Evaluation of the inflammatory response in the absence of H. suis infection by conducting the immunohistochemical studies described in detail above.
Таблица 6. Результаты иммуногистохимических исследований по определению воздействия добавки флавомицина® на число инфильтрирующих T-клеток, B-клеток и макрофагов у неинфицированных животных, выраженные в виде среднего числа подсчитанных положительных клеток.Table 6. Results of immunohistochemical studies to determine the effect of flavomycin® supplementation on the number of infiltrating T-cells, B-cells and macrophages in uninfected animals, expressed as the average number of positive cells counted.
В таблице 6 показан противовоспалительное действие флавомицина® в группе неинфицированных мышей, получавших рацион с добавкой (пример 2), по сравнению со сравнительным примером 2. В частности, наблюдалось снижение числа T-клеток и макрофагов.Table 6 shows the anti-inflammatory effect of flavomycin® in the group of non-infected mice fed a supplemented diet (Example 2) compared to Comparative Example 2. In particular, a decrease in the number of T cells and macrophages was observed.
На основании полученных результатов экспериментов 3 и 4, показано, что флавомицин® обладает противовоспалительным действием вне зависимости от наличия инфицирования H.suis.Based on the results of experiments 3 and 4, it is shown that flavomycin® has an anti-inflammatory effect, regardless of the presence of H. suis infection.
Эксперимент 5Experiment 5
Физиологическая оценка H.suis инфицированных животных путем проведения подробно описанных выше иммуногистохимических исследований.Physiological evaluation of H. suis infected animals by performing the immunohistochemical studies described in detail above.
Таблица 7. Результаты иммуногистохимических исследований по определению воздействия добавки флавомицина® на число некротических и париетальных клеток у H.Suis инфицированных животных, выраженные в виде среднего числа подсчитанных положительных клеток.Table 7. Results of immunohistochemical studies to determine the effect of flavomycin ® supplementation on the number of necrotic and parietal cells in H. Suis infected animals, expressed as the average number of positive cells counted.
В таблице 7 показано снижение числа некротических клеток для группы инфицированных животных, получавших рацион с добавкой флавомицина® (пример 1) по сравнению со сравнительным примером 1. Это указывает на то, что животные, получавшие рацион с добавкой флавомицина®, испытывают в меньшей степени клеточный некроз, чем тот, который можно было бы объяснить за счет подавления ответных воспалительных реакций. Что касается числа париетальных клеток, то обнаруживается более высокое число клеток, измеренное в группе животных, получавшие рацион с добавкой флавомицина®. Это можно объяснить тем фактом, что уменьшение воспаления в результате введения флавомицина®, вызывает меньшее повреждение париетальных клеток желудка.Table 7 shows the reduction in the number of necrotic cells for a group of infected animals fed a diet supplemented with flavomycin ® (Example 1) compared to comparative example 1. This indicates that animals fed a diet supplemented with flavomycin ® experience less cellular necrosis than that which could be explained by the suppression of inflammatory responses. As regards the number of parietal cells, a higher number of cells is found, measured in the group of animals treated with a diet supplemented with flavomycin ® . This can be explained by the fact that the reduction in inflammation resulting from the administration of flavomycin ® causes less damage to the parietal cells of the stomach.
Эксперимент 6Experiment 6
Физиологическая оценка H.suis не инфицированных животных путем проведения подробно описанных выше иммуногистохимических исследований.Physiological assessment of H. suis non-infected animals by performing the immunohistochemical studies described in detail above.
Таблица 8. Результаты иммуногистохимических исследований по определению воздействия добавки флавомицина® на число некротических и париетальных клеток у неинфицированных животных, выраженные в виде среднего числа подсчитанных положительных клеток.Table 8. Results of immunohistochemical studies to determine the effect of flavomycin ® supplementation on the number of necrotic and parietal cells in uninfected animals, expressed as the average number of positive cells counted.
В таблице 8 показано снижение числа некротических клеток, являющееся результатом уменьшения воспаления. Число париетальных клеток составляет приблизительно одну и ту же величину, как в примере 2, так и в сравнительном примере 2. Это указывает на то, что лечение с помощью флавомицина не оказывает негативного воздействия на число париетальных клеток. Table 8 shows the reduction in the number of necrotic cells resulting from the reduction in inflammation. The number of parietal cells is approximately the same value as in example 2 and in comparative example 2. This indicates that treatment with flavomycin does not adversely affect the number of parietal cells.
Принимая во внимание все полученные результаты, можно сделать вывод о том, что введение флавомицина® оказывает противовоспалительной действие, так как инфильтрация B-клеток, T-клеток и макрофагов, а также уровни IL-1β, IL-8MIP и IFN-γ понижались в группах животных, получавших рацион с добавкой флавомицина®. Более того, показано, что противовоспалительное действие не зависит от наличия H. suis инфицирования.Taking into account all the results obtained, it can be concluded that the administration of flavomycin ® has an anti-inflammatory effect, since the infiltration of B-cells, T-cells and macrophages, as well as the levels of IL-1β, IL-8MIP and IFN-γ decreased in groups of animals treated with a diet supplemented with flavomycin ® . Moreover, it has been shown that the anti-inflammatory effect is independent of the presence of H. suis infection.
--->--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙSEQUENCE LIST
<110> HuVePharma<110> HuVePharma
<120> Функционализированные сахариды в качестве противовоспалительных <120> Functionalized saccharides as anti-inflammatory
средствfunds
<130> PAT2523104EP01<130> PAT2523104EP01
<160> 14 <160> 14
<170> PatentIn version 3.5<170>PatentIn version 3.5
<210> 1<210> 1
<211> 23<211> 23
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> BF_HsuisF1 / SEQ ID NO: 1<400> BF_HsuisF1 / SEQ ID NO: 1
aaaacamagg cgatcgccct gta 23aaaacamagg cgatcgccct gta 23
<210> 2<210> 2
<211> 22<211> 22
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> BF_HsuisR1 / SEQ ID NO: 2<400> BF_HsuisR1 / SEQ ID NO: 2
tttcttcgcc aggttcaaag cg 22tttcttcgcc aggttcaaag cg 22
<210> 3<210> 3
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IFN-gamma - прямой / SEQ ID NO: 3<400> IFN-gamma - direct / SEQ ID NO: 3
ctgacctaga gaagacacat 20ctgacctaga gaagacacat 20
<210> 4<210> 4
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IFN-gamma - обратный / SEQ ID NO: 4<400> IFN-gamma - reverse / SEQ ID NO: 4
ggtcagtgaa gtaaaggtac 20ggtcagtgaa gtaaaggtac 20
<210> 5<210> 5
<211> 22<211> 22
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IL-1beta - прямой / SEQ ID NO: 5<400> IL-1beta - direct / SEQ ID NO: 5
cacctcacaa gcagagcaca ag 22cacctcacaa gcagagcaca ag 22
<210> 6<210> 6
<211> 25<211> 25
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IL-1beta - обратный / SEQ ID NO: 6<400> IL-1beta - reverse / SEQ ID NO: 6
gcattagaaa cagtccagcc catac 25gcattagaaa cagtccagcc catac 25
<210> 7<210> 7
<211> 21<211> 21
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IL-8MIP - прямой / SEQ ID NO: 7<400> IL-8MIP - straight / SEQ ID NO: 7
tgcctgaaga ccctgccaag g 21tgcctgaaga ccctgccaag g 21
<210> 8<210> 8
<211> 21<211> 21
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> IL-8MIP - обратный / SEQ ID NO: 8<400> IL-8MIP - reverse / SEQ ID NO: 8
gttagccttg cctttgttca g 21gttagccttg cctttgttca g 21
<210> 9<210> 9
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> H2AFZ - прямой / SEQ ID NO: 9<400> H2AFZ - straight / SEQ ID NO: 9
ggtatcaccc ctcgtcactt 20ggtatcaccc ctcgtcactt 20
<210> 10<210> 10
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> H2AFZ - обратный / SEQ ID NO: 10<400> H2AFZ - reverse / SEQ ID NO: 10
tcagcgattt gtggatgtgt 20tcagcgatt gtggatgtgt 20
<210> 11<210> 11
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> HPRT - прямой / SEQ ID NO: 11<400> HPRT - straight / SEQ ID NO: 11
caggccagac tttgttggat 20caggccagac tttgttggat 20
<210> 12<210> 12
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> HPRT - обратный / SEQ ID NO: 12<400> HPRT - reverse / SEQ ID NO: 12
ttgcgctcat cttaggcttt 20ttgcgctcat cttaggcttt 20
<210> 13<210> 13
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> PPIA - прямой / SEQ ID NO: 13<400> PPIA - straight / SEQ ID NO: 13
agcatacagg tcctggcatc 20agcatacagg tcctggcatc 20
<210> 14<210> 14
<211> 20<211> 20
<212> ДНК<212> DNA
<213> Искусственная последовательность<213> Artificial sequence
<220><220>
<223> Синтезированный олигонуклеотид<223> Synthesized oligonucleotide
<400> PPIA - обратный / SEQ ID NO: 14<400> PPIA - reverse / SEQ ID NO: 14
ttcaccttcc caaagaccac 20ttcaccttcc caaagaccac 20
<---<---
Claims (13)
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17169794.9 | 2017-05-05 | ||
| EP17169794 | 2017-05-05 | ||
| EP17173119.3 | 2017-05-26 | ||
| EP17173119 | 2017-05-26 | ||
| PCT/EP2018/061510 WO2018202855A1 (en) | 2017-05-05 | 2018-05-04 | Functionalized saccharides as anti-inflammatory agents |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2019136874A RU2019136874A (en) | 2021-06-07 |
| RU2019136874A3 RU2019136874A3 (en) | 2021-08-27 |
| RU2772214C2 true RU2772214C2 (en) | 2022-05-18 |
Family
ID=
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2289410C2 (en) * | 2001-04-04 | 2006-12-20 | Корикса Корпорейшн | Prophylaxis and treatment of infectious and other diseases by using compounds based on mono- n disaccharides |
| FR2908658A1 (en) * | 2006-11-20 | 2008-05-23 | Centre Nat Rech Scient | Composition useful to treat or prevent diseases associated with overexpression of tumor necrosis factor and/or interleukin-12, e.g. inflammatory diseases and neurodegenerative diseases, comprises phosphatidyl-myo-inositol mannoside |
| RU2346463C2 (en) * | 2007-03-20 | 2009-02-20 | Нина Александровна Ушакова | Method for production of dietary supplement |
| WO2009046314A2 (en) * | 2007-10-04 | 2009-04-09 | President And Fellows Of Harvard College | Moenomycin analogs, methods of synthesis, and uses thereof |
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2289410C2 (en) * | 2001-04-04 | 2006-12-20 | Корикса Корпорейшн | Prophylaxis and treatment of infectious and other diseases by using compounds based on mono- n disaccharides |
| FR2908658A1 (en) * | 2006-11-20 | 2008-05-23 | Centre Nat Rech Scient | Composition useful to treat or prevent diseases associated with overexpression of tumor necrosis factor and/or interleukin-12, e.g. inflammatory diseases and neurodegenerative diseases, comprises phosphatidyl-myo-inositol mannoside |
| RU2346463C2 (en) * | 2007-03-20 | 2009-02-20 | Нина Александровна Ушакова | Method for production of dietary supplement |
| WO2009046314A2 (en) * | 2007-10-04 | 2009-04-09 | President And Fellows Of Harvard College | Moenomycin analogs, methods of synthesis, and uses thereof |
Non-Patent Citations (1)
| Title |
|---|
| AINGE G D ET AL. Phosphatidylinositol mannosides: Synthesis and suppression of allergic airway disease, Bioorganic & Medicinal Chemistry,15.08.2006, Vol. 14, No. 16, page 5632-5642. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101622870B1 (en) | Boron-containing small molecules as anti-inflammatory agents | |
| CN110167918A (en) | Novel phenyl derivatives | |
| US20210246126A1 (en) | Compound for treatment or prevention of liver diseases | |
| JP7202892B2 (en) | Prophylactic and therapeutic agent for non-alcoholic fatty liver disease | |
| CZ80594A3 (en) | Derivatives of nucleosides or nucleoside analogs and pharmaceutical preparations in which they are comprised | |
| US20220387397A1 (en) | Compounds and compositions for treating conditions associated with nlrp activity | |
| US20230059136A1 (en) | The compounds and compositions for treating conditions associated with nlrp activity | |
| US20250387359A1 (en) | Compounds and methods for the treatment of parasitic infections | |
| US20050153985A1 (en) | Methods of treating acute inflammation in animals with p38 map kinase inhibitors | |
| KR102091464B1 (en) | Composition for anti-inflammation | |
| US12390441B2 (en) | Immunomodulating o-het/aryl azalides | |
| RU2772214C2 (en) | Functionalized saccharides as anti-inflammatory agents | |
| US11883421B2 (en) | Functionalized saccharides as anti-inflammatory agents | |
| JP2022502501A (en) | New use | |
| WO2024225368A1 (en) | Adenosine triphosphate secretion inhibitor, hepatic stellate cell activation inhibitor, hepatic stellate cell deactivator, hepatic fibrosis therapeutic agent, non-alcoholic steatohepatitis therapeutic agent, psoriasis therapeutic agent, and use of compound for producing adenosine triphosphate secretion inhibitor, hepatic stellate cell activation inhibitor, hepatic stellate cell deactivator, hepatic fibrosis therapeutic agent, non-alcoholic steatohepatitis therapeutic agent, and psoriasis therapeutic agent | |
| BR112019022686B1 (en) | Use of functionalized saccharide compounds for the treatment of an inflammatory disease. | |
| KR102625224B1 (en) | Composition for preventing, improving or treating autoimmune diseases comprising pyrazol-one derivatives | |
| JP2006509756A (en) | Use of the CRH (corticotropin releasing hormone) -UCN (urocortin) system in the treatment of inflammatory diseases | |
| CN113784713A (en) | Leukotriene synthesis inhibitors | |
| US20230355549A1 (en) | Method of preventing kidney injury disruption of intestinal lymphatics | |
| JP2021530512A (en) | Reutericyclin or Lactobacillus reuteri to control weight gain | |
| KR101192063B1 (en) | Pharmaceutical Composition for Treating Inflammatory Disease | |
| HK40120421A (en) | Methods of treating inflammation | |
| US20220242900A1 (en) | Substituted biphenyl or phenylheteroaryl-mannosides as antagonists of fimh | |
| TW202104204A (en) | Compounds for the treatment or prevention of liver disease |